Полимерный конъюгат координационного комплекса платины (ii) с производным сульфоксида - RU2721725C2
Код документа: RU2721725C2
Описание
ОБЛАСТЬ ТЕХНИКИ
[1] Настоящее изобретение относится к полимерному конъюгату комплекса платины (II), имеющему противоопухолевую активность, к которому посредством координационных связей присоединено производное сульфоксида, и к лекарственному средству, содержащему полимерный конъюгат в качестве активного ингредиента.
УРОВЕНЬ ТЕХНИКИ
[2] Как известно, комплексы платины, такие как цисплатин и оксалиплатин, оказывают противоопухолевое действие за счет ингибирования репликации ДНК и индуцирования апоптоза, и, таким образом, комплексы платины используют в клинической практике в качестве ключевого лекарственного средства при комбинированной терапии разнообразных раковых заболеваний. Тем не менее, известно, что в качестве побочных эффектов комплексы платины вызывают нарушения почек, тошноту и рвоту, расстройства периферической нервной системы и подавление функции костного мозга, и указанные побочные эффекты создают проблемы при клиническом применении комплексов платины.
[3] Для уменьшения указанных побочных эффектов и усиления терапевтических эффектов проводится разработка комплексов платины, в которых применяются технологии доставки лекарственных средств с использованием полимеров. Примеры препаратов DDS (система доставки лекарственных средств; англ. drug delivery system) для комплексов платины, которые на момент подачи заявки перешли на стадию клинических испытаний, включают координационное соединение диаминоциклогексанплатины (II) и блоксополимера (NC-4016; см. источник патентной литературы 1), липосомы направленного действия, в которые инкапсулирован оксалиплатин (МВР-426; см. источник патентной литературы 2) и координационное соединение цисплатина и блоксополимера (см. источник патентной литературы 3).
[4] С другой стороны, также проводятся исследования низкомолекулярных комплексов платины, и, что касается тетракоординированных комплексов платины (II), таких как цисплатин и оксалиплатин, то были описаны комплексы, содержащие в качестве лигандов производное сульфоксида, производное N-гетероцикла и производное тиомочевины, и т.д. (см. источник непатентной литературы 1).
[5] Если рассматривать тетракоординированный комплекс платины (II), содержащий производное сульфоксида в качестве лиганда, то были описаны комплексы, содержащие диметилсульфоксид, метилфенилсульфоксид, дифенилсульфоксид и т.д. в качестве производных сульфоксида, и было подтверждено, что указанные комплексы обладают противоопухолевым действием в животных моделях (см. источник непатентной литературы 2). Кроме того, также известен тетракоординированный комплекс платины (II), содержащий производное сульфоксида в качестве лиганда и еще два амино-лиганда в транс-конфигурации (см. источник непатентной литературы 3).
[6] Тем не менее, на момент подачи заявки не были описаны препараты DDS для комплекса платины, к которому посредством координационных связей присоединено полимерное производное сульфоксида, и ни один из препаратов DDS для комплекса платины, включая соединения, описанные в источниках патентной литературы 1-3, указанные выше, не поступил на рынок.
ДОКУМЕНТЫ, СОСТАВЛЯЮЩИЕ УРОВЕНЬ ТЕХНИКИ
ССЫЛКИ НА ПАТЕНТНУЮ ЛИТЕРАТУРУ
[7] Источник патентной литературы 1: патент Японии JP 3955992 В2
Источник патентной литературы 2: заявка на патент Японии JP 2008-538105 А
Источник патентной литературы 3: патент Японии JP 5458255 В2
ССЫЛКИ НА НЕПАТЕНТНУЮ ЛИТЕРАТУРУ
[8] Источник непатентной литературы 1: Chemical Reviews, 2014, 114, 4470-4495
Источник непатентной литературы 2: Inorganic Chemistry, 1990, 29, 397-403
Источник непатентной литературы 3: Inorganic Chemistry, 2001, 40, 1745-1750
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ПОСТАВЛЕННАЯ ЗАДАЧА
[9] Препарат DDS для комплекса платины, имеющий сильное противоопухолевое действие, для применения в качестве лекарственного средства недоступен, и требуется препарат DDS для комплекса платины, который можно применять в клинической практике, где комплекс платины конъюгирован с полимерным носителем, отличающимся от тех, что использовали в препаратах DDS, указанных выше. То есть, можно ожидать, что препарат DDS для комплекса платины, полученный путем образования координационных связей между платиной и полимерным производным сульфоксида и имеющий благодаря этому повышенную возможность поглощения комплекса платины клеткой, будет иметь сильное противоопухолевое действие и т.д.
СРЕДСТВА ДЛЯ РЕШЕНИЯ ПРОБЛЕМЫ
[10] Авторы настоящего изобретения провели тщательное исследование для решения проблем, описанных выше, в результате авторы обнаружили, что препарат DDS для комплекса платины, который может быть получен путем встраивания производного сульфоксида по карбоксильной группе боковой цепи в блоксополимер, содержащий структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, и образования координационных связей между сульфоксидной группой и платиной, имеет превосходные характеристики. Таким образом, авторы реализовали настоящее изобретение.
[11] То есть, настоящее изобретение относится к следующим объектам (1)-(12).
[12]
(1) Полимерный конъюгат комплекса платины (II), содержащий
блоксополимер, содержащий структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты;
производное сульфоксида, встроенное по карбоксильной группе боковой цепи в блоксополимер; и
комплекс платины (II), образующий координационные связи с сульфоксидной группой производного сульфоксида.
[13]
(2) Полимерный конъюгат комплекса платины (II) согласно (1), где полимерный конъюгат представлен следующей общей формулой (I):
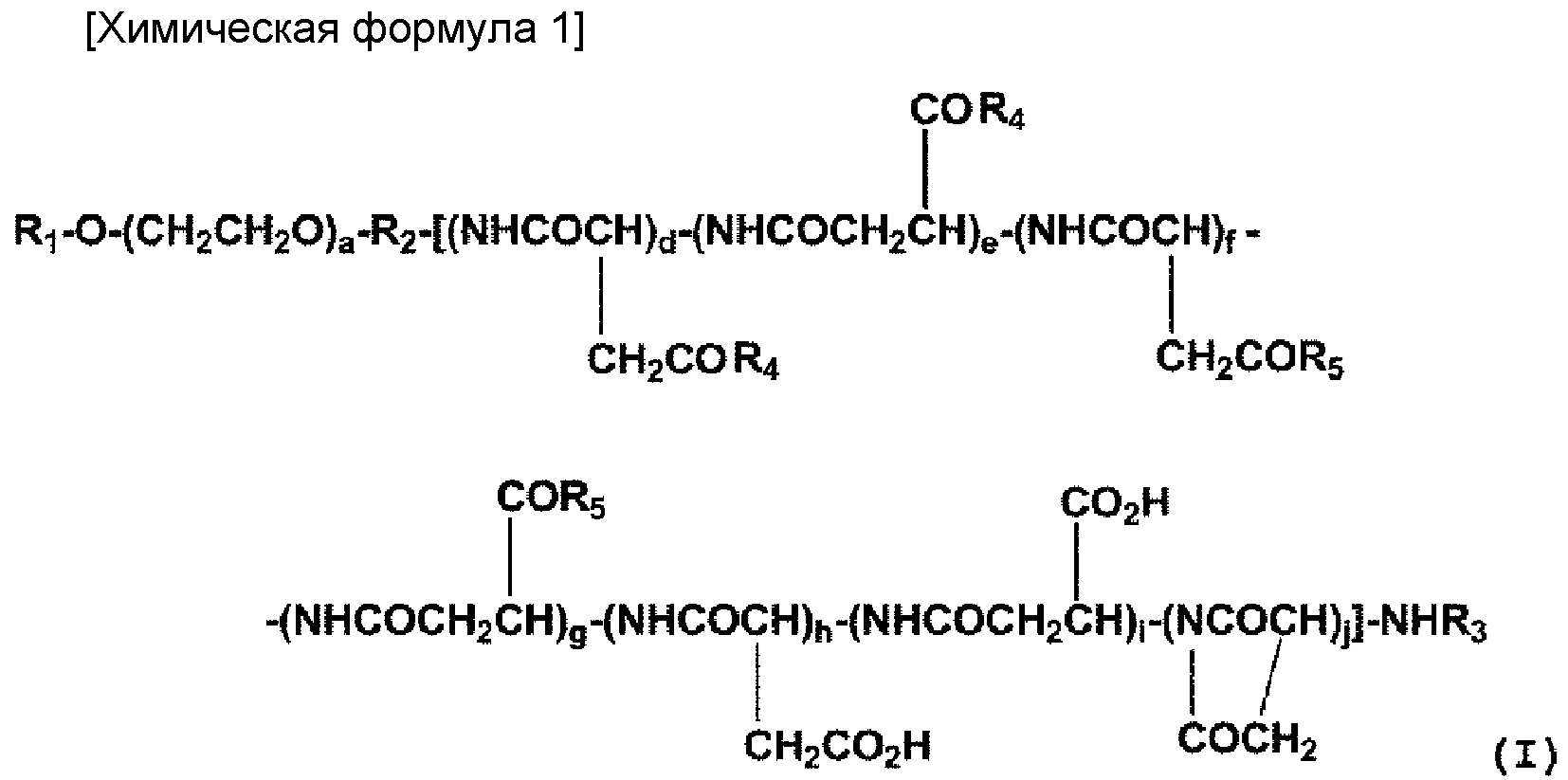
где R1 представляет собой атом водорода, (С1-С10) алкильную группу, необязательно имеющую заместитель, или (С6-С10) арильную группу, необязательно имеющую заместитель; R2 представляет собой связующую группу; R3 представляет собой атом водорода или (С1-С6) ацильную группу; R4 представляет собой заместитель, представленный на следующей общей формуле (II):
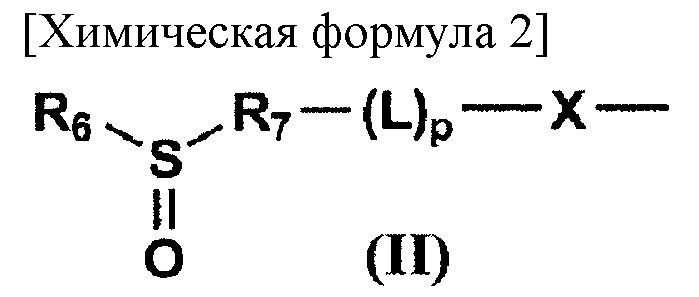
[где X представляет собой атом кислорода или NR8; R8 представляет собой атом водорода, (С1-С10) алкильную группу или (С6-С10) арильную группу, необязательно имеющую заместитель; L представляет собой линкер; р равен 0 или 1; R6 представляет собой (С1-С10) алкильную группу, необязательно имеющую заместитель, (С6-С10) арильную группу, необязательно имеющую заместитель, или (С7-С15) аралкильную группу, необязательно имеющую заместитель; и R7 представляет собой остаток, полученный в результате удаления Н из заместителя, представляющего собой R6, или циклическую структуру, образованную R6 и R7, связанными друг с другом], или на следующей общей формуле (III):
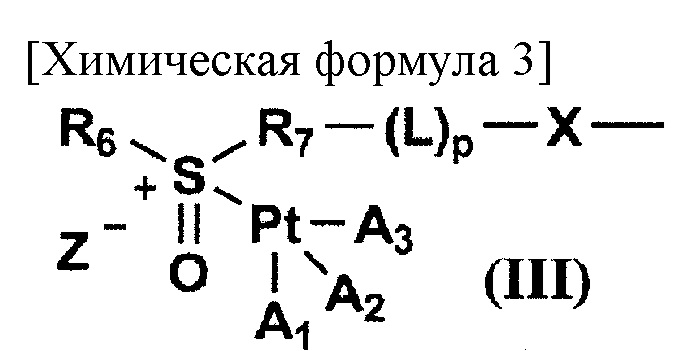
[где X представляет собой атом кислорода или NR8; R8 представляет собой атом водорода, (С1-С10) алкильную группу или (С6-С10) арильную группу, необязательно имеющую заместитель; L представляет собой линкер; р равен 0 или 1; R6 представляет собой (С1-С10) алкильную группу, необязательно имеющую заместитель, (С6-С10) арильную группу, необязательно имеющую заместитель, или (С7-С15) аралкильную группу, необязательно имеющую заместитель; R7 представляет собой остаток, полученный в результате удаления Н из заместителя, представляющего собой R6, или циклическую структуру, образованную R6 и R7, связанными друг с другом; каждый из A1, А2 и A3 представляет собой лиганд комплекса платины; и Z- представляет собой противоположно заряженный анион];
по меньшей мере один из R4 представляет собой заместитель, образующий координационные связи с комплексом платины, представленным на общей формуле (III); R5 представляет собой заместитель, выбранный из группы, состоящей из (С1-С30) алкоксигруппы, (С1-С30) аралкилоксигруппы, (С6-С10) арилоксигруппы, (С1-С30) алкиламиногруппы, необязательно имеющей заместитель, ди-(С1-С30) алкиламиногруппы, необязательно имеющей заместитель, заместитель, представленный на следующей общей формулое (IV), полученный в результате удаления Н из α-аминогруппы производного α-аминокислоты:
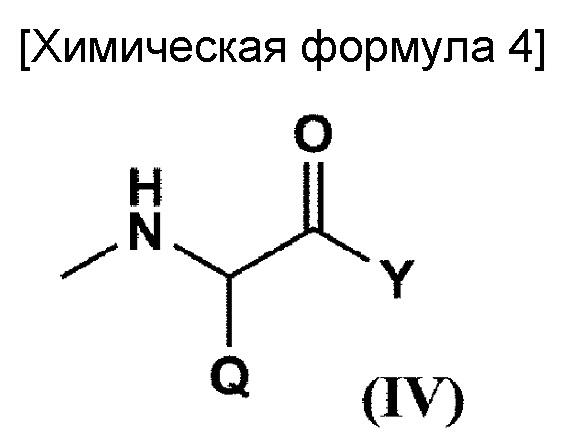
[где Q представляет собой остаток α-аминокислоты; Y представляет собой заместитель, выбранный из группы, состоящей из аминогруппы, содержащей (С1-С10) алкильную группу, необязательно имеющую заместитель, или бензильную группу, необязательно имеющую заместитель, (С1-С10) алкоксигруппы, необязательно содержащей фенильную группу, (С6-С10) арилоксигруппы и -NR12CONHR13; и каждый из R12 и R13, которые необязательно могут быть одинаковыми или различными, представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, необязательно замещенную третичной аминогруппой], и -NR9CONHR10;
каждый из R9 и R10, которые необязательно могут быть одинаковыми или различными, представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, необязательно замещенную третичной аминогруппой; а представляет собой целое число от 5 до 11500; каждый из d, е, f, g, h, i и j представляет собой целое число от 0 до 200; d+e представляет собой целое число от 1 до 200; d+e+f+g+h+i+j представляет собой целое число от 2 до 200; и порядок связывания различных составляющих звеньев полиаспарагиновой кислоты является случайным.
[14]
(3) Полимерный конъюгат комплекса платины (II) согласно (2), где R1 представляет собой (С1-С3) алкильную группу, необязательно имеющую заместитель; R2 представляет собой (С2-С6) алкиленовую группу; R3 представляет собой (С1-С3) ацильную группу; а представляет собой целое число от 10 до 2000; каждый из d, е, f, g, h, i и j представляет собой целое число от 0 до 100; d+e представляет собой целое число от 1 до 100; и d+e+f+g+h+i+j представляет собой целое число от 4 до 100.
[15]
(4) Полимерный конъюгат комплекса платины (II) согласно (2) или (3), где R1 представляет собой метальную группу; R2 представляет собой триметиленовую группу; R3 представляет собой ацетильную группу; R4 представляет собой заместитель, выбранный из группы, состоящей из заместителей, представленных на следующей формуле (V):
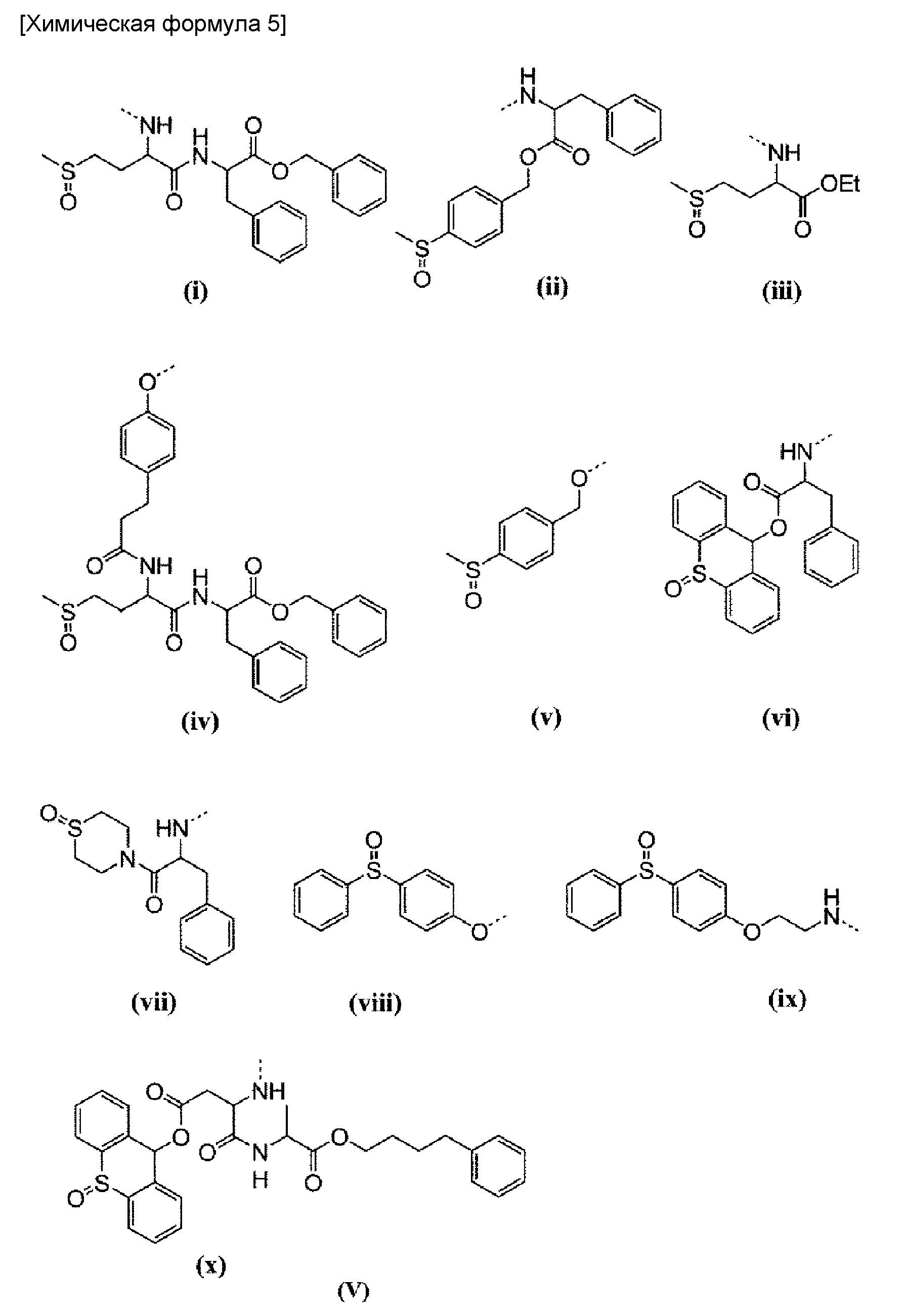
или заместитель, выбранный из группы заместителей, представленных на следующей формуле (VI):
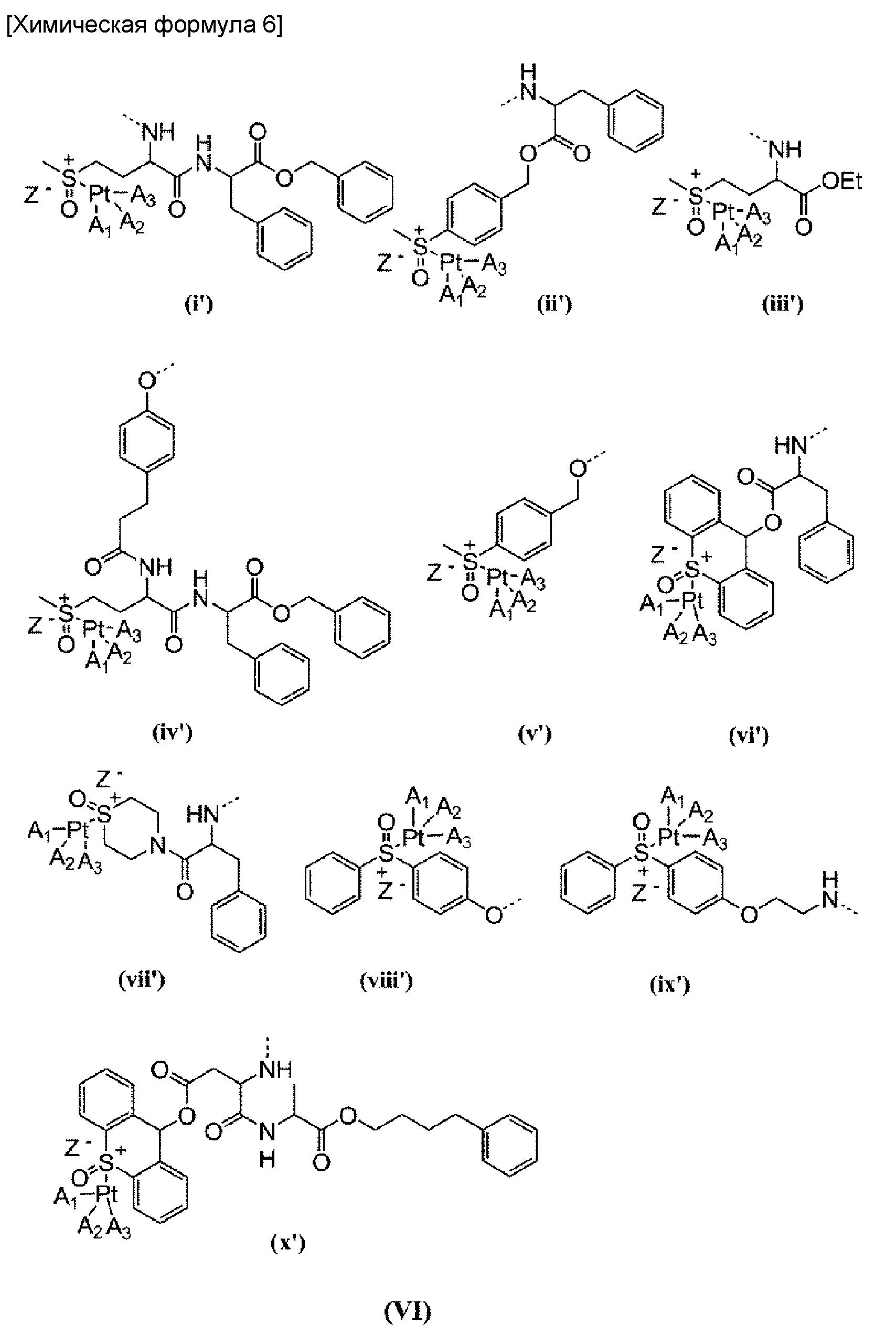
где A1, А2, A3 и Z-, соответственно, имеют такие же значения, что описаны выше;
по меньшей мере один из R4 представляет собой заместитель, образующий координационные связи с комплексом платины, представленным на формуле (VI); R5 представляет собой заместитель общей формулы (IV), в котором Q представляет собой бензильную группу, или -NR9CONHR10; и R9 и R10 оба представляют собой циклогексильную группу или изопропильную группу.
[16]
(5) Полимерный конъюгат комплекса платины (II) согласно (1), где полимерный конъюгат представлен следующей общей формулой (VII):
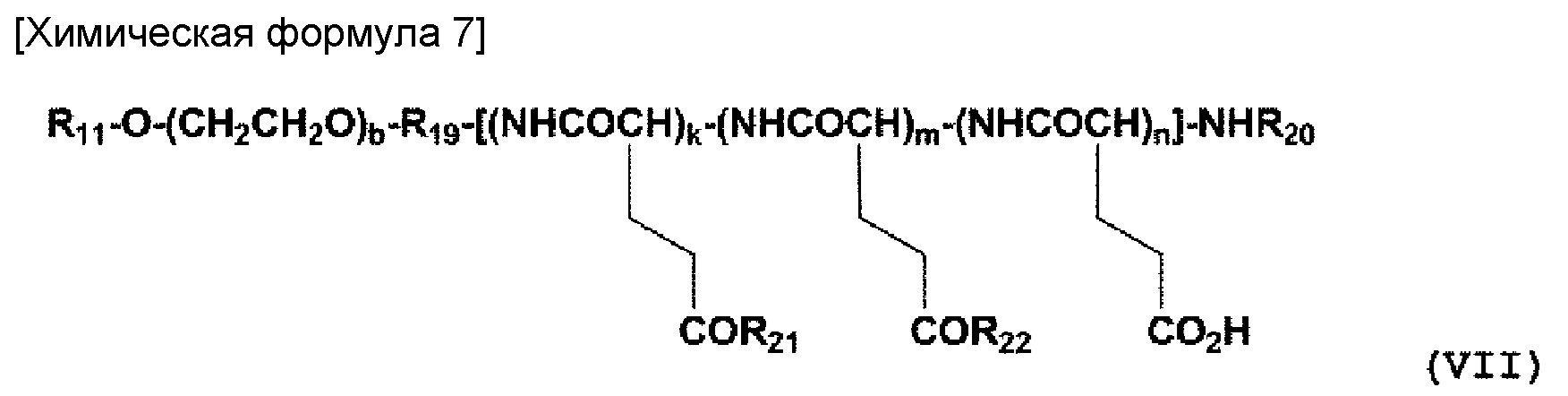
где R11 представляет собой атом водорода, (С1-С10) алкильную группу, необязательно имеющую заместитель, или (С6-С10) арильную группу, необязательно имеющую заместитель; R19 представляет собой связующую группу; R20 представляет собой атом водорода или (С1-С6) ацильную группу; R21 представляет собой заместитель, представленный на следующей общей формуле (VIII):
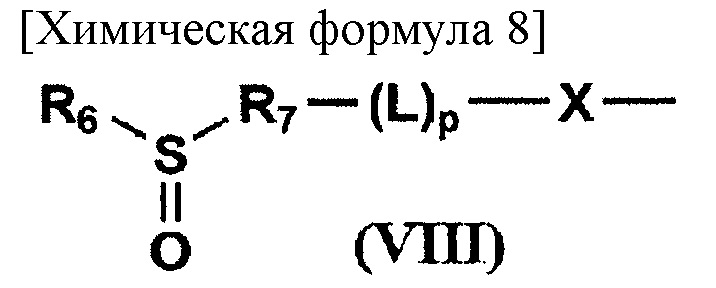
[где X представляет собой атом кислорода или NR8; R8 представляет собой атом водорода, (С1-С10) алкильную группу или (С6-С10) арильную группу, необязательно имеющую заместитель; L представляет собой линкер; р равен 0 или 1; R6 представляет собой (С1-С10) алкильную группу, необязательно имеющую заместитель, (С6-С10) арильную группу, необязательно имеющую заместитель, или (С7-С15) аралкильную группу, необязательно имеющую заместитель; и R7 представляет собой остаток, полученный в результате удаления Н из заместителя, представляющего собой R6, или циклическую структуру, образованную R6 и R7, связанными друг с другом], или на следующей общей формуле (IX):
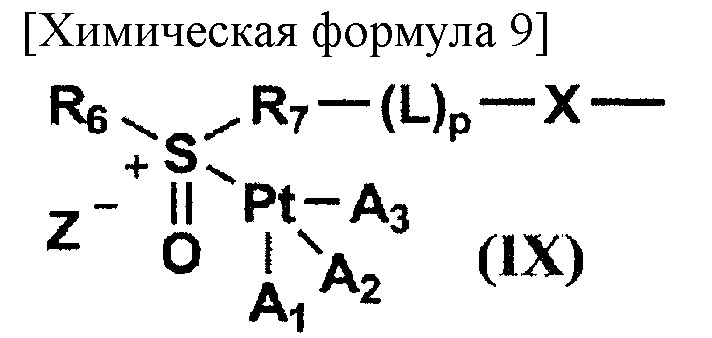
[где X представляет собой атом кислорода или NR8; R8 представляет собой атом водорода, (С1-С10) алкильную группу или (С6-С10) арильную группу, необязательно имеющую заместитель; L представляет собой линкер; р равен 0 или 1; R6 представляет собой (С1-С10) алкильную группу, необязательно имеющую заместитель, (С6-С10) арильную группу, необязательно имеющую заместитель, или (С7-С15) аралкильную группу, необязательно имеющую заместитель; R7 представляет собой остаток, полученный в результате удаления Н из заместителя, представляющего собой R6, или циклическую структуру, образованную R6 и R7, связанными друг с другом; каждый из A1, А2 и A3 представляет собой лиганд комплекса платины; и Z- представляет собой противоположно заряженный анион];
по меньшей мере один из R21 представляет собой заместитель, образующий координационные связи с комплексом платины, представленным на общей формуле (IX); R22 представляет собой заместитель, выбранный из группы, состоящей из (С1-С30) алкоксигруппы, (С1-С30) аралкилоксигруппы, (С6-С10) арилоксигруппы, (С1-С30) алкиламиногруппы, необязательно имеющей заместитель, ди-(С1-С30) алкиламиногруппы, необязательно имеющей заместитель, заместитель, представленный на следующей общей формуле (X), полученный в результате удаления Н из α-аминогруппы производного α-аминокислоты:
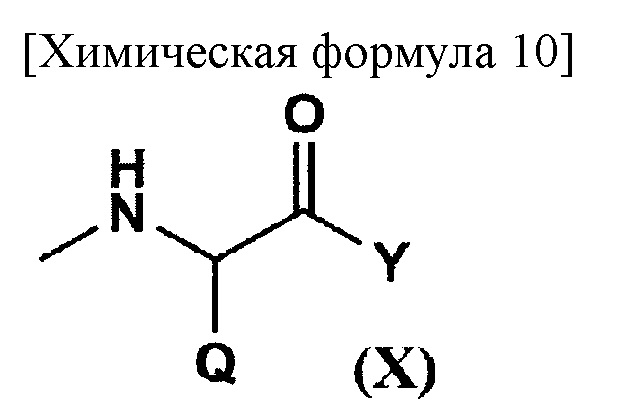
[где Q представляет собой остаток α-аминокислоты; Y представляет собой заместитель, выбранный из группы, состоящей из аминогруппы, содержащей (С1-С10) алкильную группу, необязательно имеющую заместитель, или бензильную группу, необязательно имеющую заместитель, (С1-С10) алкоксигруппы, необязательно содержащей фенильную группу, (С6-С10) арилоксигруппы и -NR12CONHR13; и каждый из R12 и R13, которые могут быть одинаковыми или различными, представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, необязательно замещенную третичной аминогруппой], и -NR9CONHR10;
каждый из R9 и R10, которые могут быть одинаковыми или различными, представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, необязательно замещенную третичной аминогруппой; b представляет собой целое число от 5 до 11500; k представляет собой целое число от 1 до 200; каждый m и n представляет собой целое число от 0 до 200; k+m+n представляет собой целое число от 2 до 200; и порядок связывания различных составляющих звеньев полиглутаминовой кислоты является случайным.
[17]
(6) Полимерный конъюгат комплекса платины (II) согласно (5), где R11 представляет собой (С1-С3) алкильную группу, необязательно имеющую заместитель; R19 представляет собой (С2-С6) алкиленовую группу, R20 представляет собой (С1-С3) ацильную группу; b представляет собой целое число от 10 до 2000; k представляет собой целое число от 1 до 100; каждый m и n представляет собой целое число от 0 до 100; и k+m+n представляет собой целое число от 3 до 100.
[18]
(7) Полимерный конъюгат комплекса платины (II) согласно (5) или (6), где R11 представляет собой метальную группу, R19 представляет собой триметиленовую группу, R20 представляет собой ацетильную группу, R21 представляет собой заместитель, выбранный из группы, состоящей из заместителей, представленных на следующей формуле (XI):
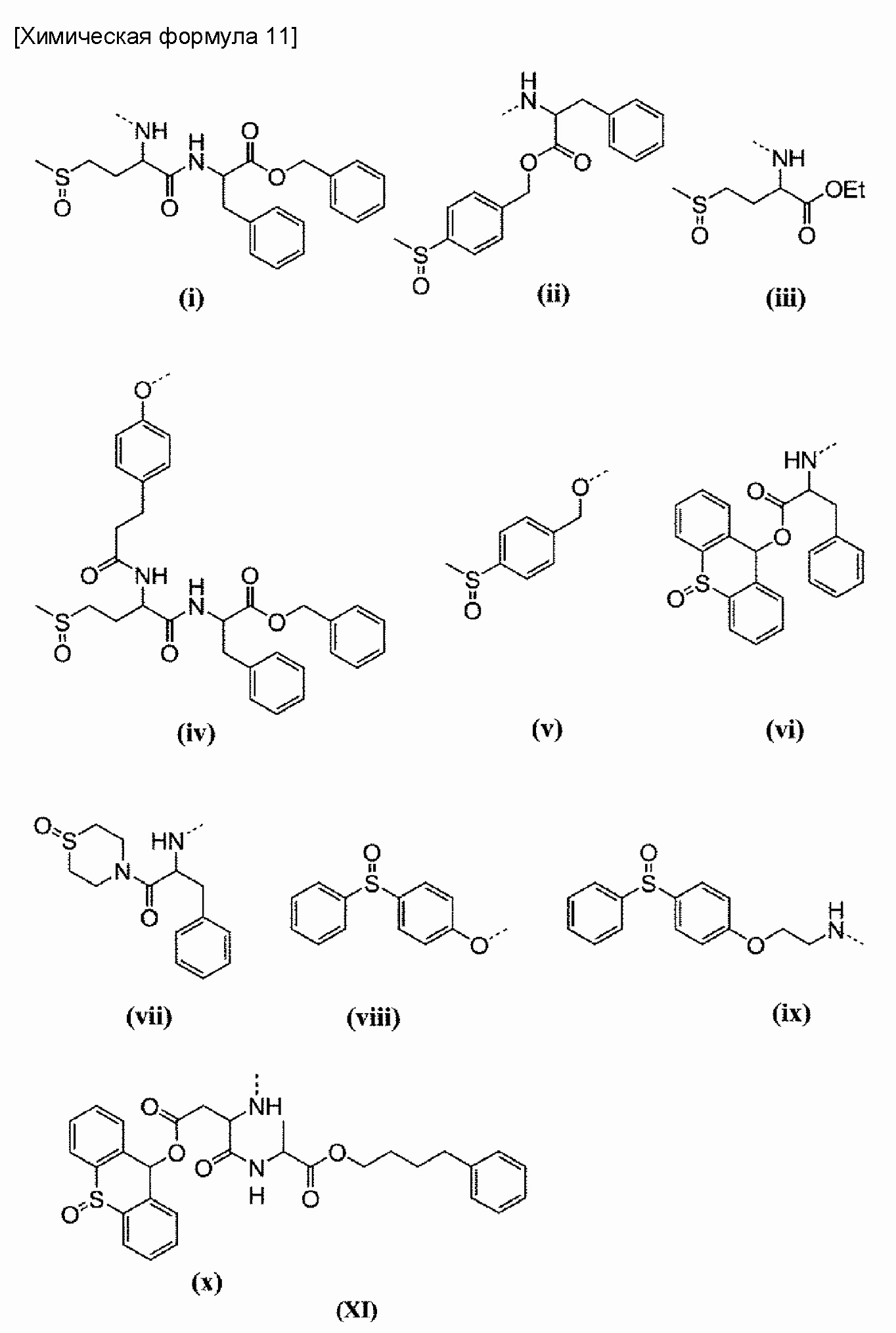
или заместитель, выбранный из группы заместителей, представленных на следующей формуле (XII):
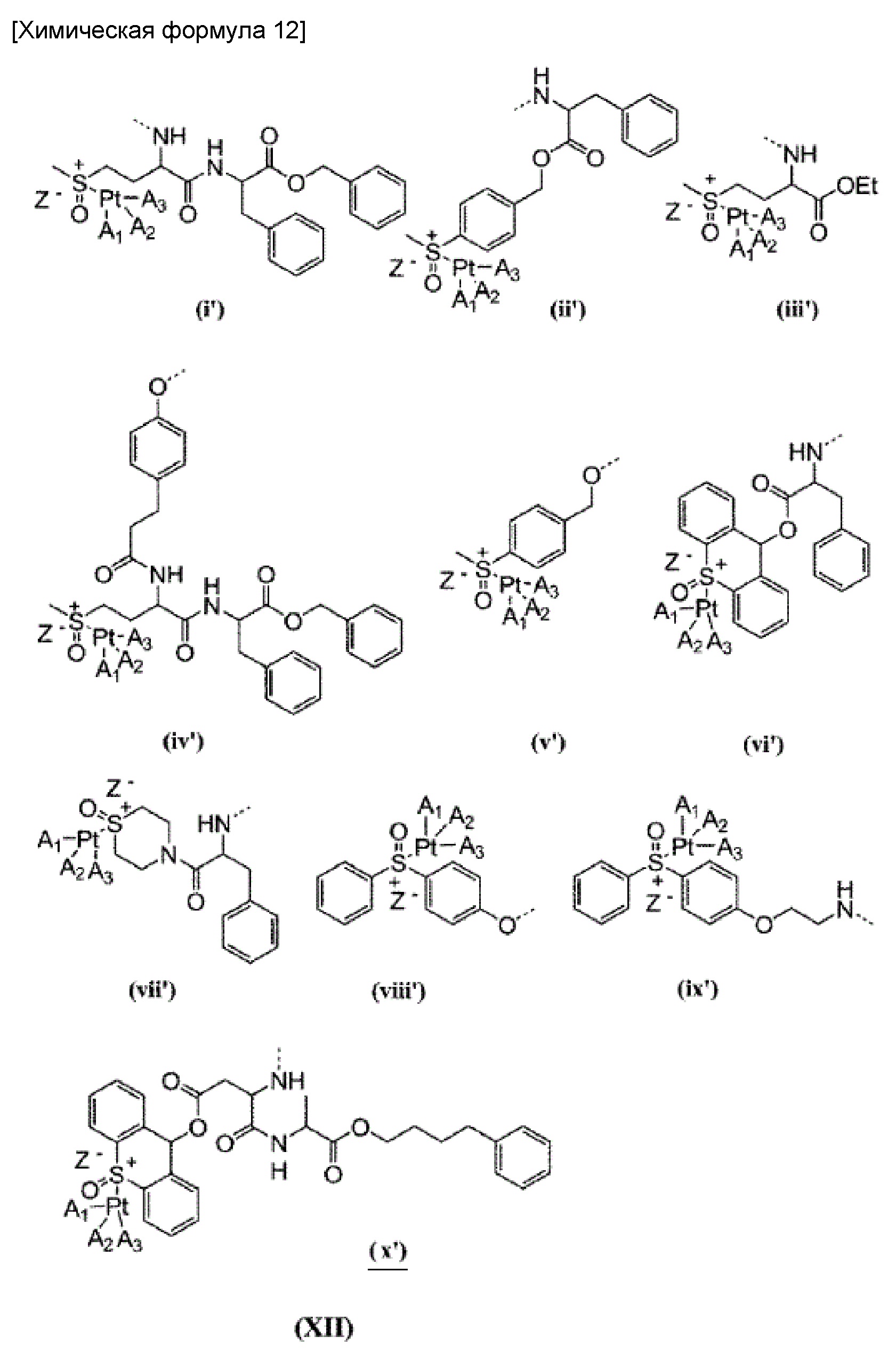
где A1, А2, A3 и Z- соответственно имеют такие же значения, что описаны выше;
при условии, что по меньшей мере один из R21 представляет собой заместитель, образующий координационные связи с комплексом платины, представленным на формуле (XII); R22 представляет собой заместитель общей формулы (X), в котором Q представляет собой бензильную группу, или -NR9CONHR10; и R9 и R10 оба представляют собой циклогексильную группу или изопропильную группу.
[19]
(8) Полимерный конъюгат комплекса платины (II) согласно любому из (2)-(7), где лиганды A1 и А2 в комплексе платины оба представляют собой аммиак или первичный, вторичный или третичный амин или объединены с образованием нециклического или циклического диамина, необязательно имеющего заместитель; и A3 представляет собой атом галогена, молекулу воды, амин, необязательно имеющий заместитель, гетероарильное соединение или сульфоксидное соединение.
[20]
(9) Полимерный конъюгат комплекса платины (II) согласно (8), где лиганды A1 и А2 в комплексе платины оба представляют собой аммиак или лиганд, выбранный из группы лигандов, представленных на следующей формуле (XIII):
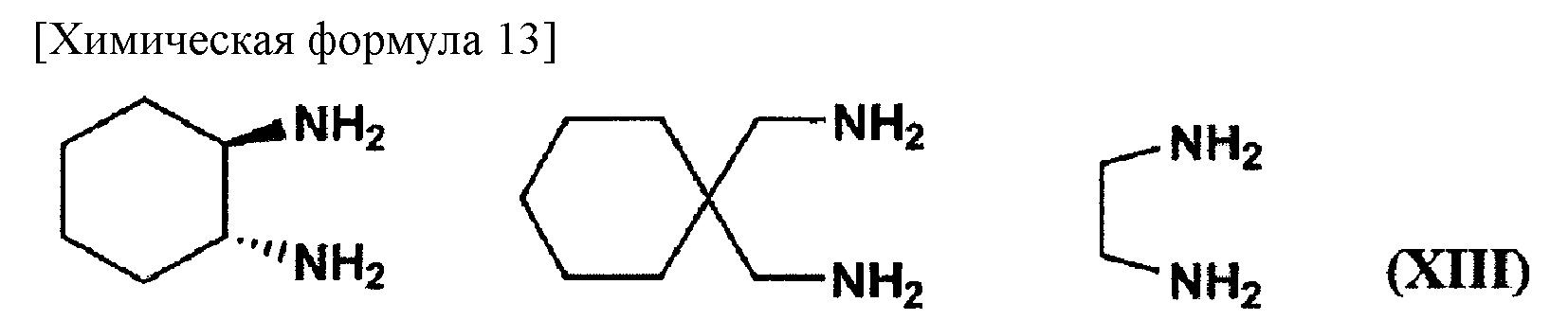
и A3 представляет собой атом хлора.
[21]
(10) Способ получения полимерного конъюгата комплекса платины (II) согласно любому из (1)-(9), включающий встраивание сульфоксидного производного по карбоксильной группе боковой цепи в блоксополимер, содержащий структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, и последующее образование координационной связи между сульфоксидной группой производного сульфоксида и комплексом платины за счет обмена лигандами.
[22]
(11) Лекарственное средство, содержащее полимерный конъюгат комплекса платины (II) согласно любому из (1)-(9) в качестве активного ингредиента.
(12) Противоопухолевый агент, содержащий полимерный конъюгат комплекса платины (II) согласно любому из (1)-(9) в качестве активного ингредиента.
ПРЕДПОЧТИТЕЛЬНЫЕ ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
[23] Полимерный конъюгат комплекса платины (II) согласно настоящему изобретению, в котором полимерное производное сульфоксида образует координационные связи с платиной, заряжен положительно и поэтому быстро захватывается клетками, которые заряжены отрицательно. Таким образом, лекарственное средство, содержащее полимерный конъюгат в качестве активного ингредиента, обеспечивает фармацевтический препарат, который обладает эффективной противоопухолевой активностью и пониженными побочными эффектами в клинических способах лечения. Кроме того, можно ожидать, что полимерный конъюгат комплекса платины (II) согласно настоящему изобретению будет иметь удовлетворительную стабильность в крови и высвобождать лекарственное средство в участке опухоли.
ОПИСАНИЕ ОСУЩЕСТВЛЕНИЯ ВАРИАНТОВ РЕАЛИЗАЦИИ
[24] Настоящее изобретение будет более подробно описано далее.
[25] Настоящее изобретение относится к полимерному конъюгату комплекса платины (II), в котором сульфоксидная группа производного сульфоксида, встроенного по карбоксильной группе боковой цепи в блоксополимер, содержащий структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты или структурный фрагмент полиэтиленгликоля и фрагмент полиглутаминовой кислоты, образует координационные связи с платиной.
[26] Структурный фрагмент полиэтиленгликоля согласно настоящему изобретению представляет собой полиэтиленгликоль, модифицированный по обоим концам или модифицированный по одному концу, где модифицирующие группы при двух концах могут быть одинаковыми или различными. Примеры терминальных модифицирующих групп включают метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, втор-бутильную группу, трет-бутильную группу, бензильную группу, 4-фенилбутильную группу, диметоксиэтильную группу, диэтоксиэтильную группу, аминоэтильную группу, аминопропильную группу и аминобутильную группу. Среди указанных групп предпочтительные примеры включают метильную группу, этильную группу, н-пропильную группу, изопропильную группу, диметоксиэтильную группу, аминоэтильную группу и аминопропильную группу.
[27] Молекулярная масса структурного фрагмента полиэтиленгликоля в блоксополимере, как правило, составляет от примерно 200 до 500000, предпочтительно от примерно 300 до 100000 и более предпочтительно от примерно 1000 до 90000.
[28] Количество карбоксильных групп боковой цепи во фрагменте полиаспарагиновой кислоты или фрагменте полиглутаминовой кислоты в блоксополимере составляет от примерно 1 до 300, предпочтительно от примерно 2 до 200 и более предпочтительно от примерно 4 до 100 в среднем на молекулу. Количество карбоксильных групп может быть определено, например, путем нейтрализационного титрования с использованием щелочей.
[29] Комплекс платины (II) согласно настоящему изобретению не ограничен каким-либо конкретным образом, если центральный атом металла представляет собой двухвалентную платину; тем не менее, предпочтителен цис-координированный комплекс. К комплексу платины (II) посредством координационных связей присоединена полимерная сульфоксидная группа. Фрагмент сульфоксидной группы, через который образуются координационные связи с платиной, представляет собой атом серы или атом кислорода.
[30] Фрагмент полиаспарагиновой кислоты согласно настоящему изобретению может представлять собой α-форму или β-форму полимера или может представлять собой смесь α-формы и β-формы полимера. Фрагмент полиаспарагиновой кислоты предпочтительно представляет собой смесь α-формы и β-формы полимера.
[31] Фрагмент полиглутаминовой кислоты согласно настоящему изобретению может представлять собой α-форму или γ-форму полимера или может представлять собой смесь α-формы и γ-формы полимера. Фрагмент полиглутаминовой кислоты предпочтительно представляет собой α-форму полимера.
[32] Фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты согласно настоящему изобретению может содержать только D-аминокислоты или только L-аминокислоты или может содержать произвольную смесь D-аминокислот и L-аминокислот.
[33] Степень конъюгации комплекса платины и блоксополимера, содержащего структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты или структурный фрагмент полиэтиленгликоля и фрагмент полиглутаминовой кислоты, в полимерном конъюгате комплекса платины (II) согласно настоящему изобретению не ограничена каким-либо конкретным образом, если указанная степень является достаточной для обеспечения эффективного действия; тем не менее, как правило, степень конъюгации составляет от 1% до 95% и предпочтительно от 5% до 80% от общей массы полимерного конъюгата.
[34] Атом галогена согласно настоящему изобретению представляет собой атом фтора, атом хлора, атом брома или атом йода.
[35] (С1-С10) алкильная группа в (С1-С10) алкильной группе, которая может иметь заместитель, согласно настоящему изобретению представляет собой линейную, разветвленную или циклическую (С1-С10) алкильную группу, и примеры (С1-С10) алкильной группы, которая может иметь заместитель, включают метальную группу, этильную группу, н-пропильную группу, н-бутильную группу, н-пентильную группу, н-гексильную группу, н-октильную группу, н-децильную группу, изопропильную группу, втор-бутильную группу, трет-бутильную группу, 2,2-диметилпропильную группу, циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, бензильную группу, фенэтильную группу, 4-фенилбутильную группу, диметоксиэтильную группу, диэтоксиэтильную группу, диметоксипропильную группу, диэтоксипропильную группу, аминоэтильную группу, диаминоэтильную группу, аминопропильную группу и аминобутильную группу. Кроме того, примеры (С1-С3) алкильной группы, - которая может иметь заместитель, включают метальную группу, этильную группу, н-пропильную группу, изопропильную группу, циклопропильную группу, бензильную группу, фенэтильную группу, диметоксиэтильную группу, диэтоксиэтильную группу, диметоксипропильную группу, диэтоксипропильную группу, аминоэтильную группу, диаминоэтильную группу и аминопропильную группу.
[36] Примеры (С6-С10) арильной группы, которая может иметь заместитель, согласно настоящему изобретению включают фенильную группу и нафтильную группу, которые могут иметь заместитель, и примеры заместителей включают атом галогена, гидроксильную группу, аминогруппу, алкоксигруппу, ацильную группу, амидную группу. Положение заместителя и количество заместителей не ограничено каким-либо конкретным образом.
Примеры аминогрупп включают аминогруппу, метиламиногруппу, этиламиногруппу, н-бутиламиногруппу, изопропиламиногруппу, циклогексиламиногруппу, бензиламиногруппу, 4-фенилбутиламиногруппу, диметиламиногруппу, диэтиламиногруппу, ди-н-бутиламиногруппу, диизопропиламиногруппу, дициклогексиламиногруппу, дибензиламиногруппу, бисфенилбутиламиногруппу, N-этилметиламинструппу, N-метилфениламиногруппу и N-метил-4-фенилбутиламиногруппу.
Примеры алкоксигрупп включают метоксигруппу, этоксигруппу, н-бутоксигруппу, трет-бутоксигруппу, циклопропилоксигруппу, циклогексилоксигруппу и адамантилоксигруппу.
Примеры ацильных групп включают формильную группу, ацетильную группу, пропионильную группу и пивалоильную группу.
Примеры амидных групп включают ацетамидную группу, бензамидную группу, N-метилацетамидную группу и N-метилбензамидную группу.
[37] Полимерный конъюгат комплекса платины (II) согласно настоящему изобретению, в котором сульфоксидная группа производного сульфоксида, встроенная по карбоксильной группе боковой цепи в блоксополимер, содержащий структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты, образует координационные связи с платиной, представлен, например, на общей формуле (I).
[38] Если рассматривать (С1-С10) алкильную группу, которая может иметь заместитель, в качестве R1 на общей формуле (I), то в числе примеров можно отметить группы, перечисленные выше, и среди них предпочтительной является (С1-С3) алкильная группа, которая может иметь заместитель, при этом особенно предпочтительной является метальная группа.
Если рассматривать (С6-С10) арильную группу, которая может иметь заместитель, в качестве R1 на общей формуле (I), то в числе примеров можно отметить группы, перечисленные выше.
[39] Примеры связующей группы, обозначенной R2 на общей формуле (I), включают линейную или разветвленную (С2-С6) алкиленовую группу. Среди прочих линейная (С2-С4) алкиленовая группа является предпочтительной, примеры включают этиленовую группу, триметиленовую группу и тетраметиленовую группу, при этом триметиленовая группа является особенно предпочтительной.
[40] Примеры (С1-С6) ацильной группы R3 на общей формуле (I) включают формильную группу, ацетильную группу, пропионильную группу и пивалоильную группу, и (С1-С3) ацильная группа является предпочтительной, при этом ацетильная группа является особенно предпочтительной.
[41] R4 на общей формуле (I) представляет собой заместитель общей формулы (II) или (III), и по меньшей мере один из R4 представляет собой заместитель, который образует координационные связи с комплексом платины (II), представленным на общей формуле (III).
[42] В случае, если атомы серы в сульфоксидных группах на общих формулах (II) и (III) являются асимметрическими центрами, соединение может представлять собой отдельное соединение или смесь стереоизомеров.
[43] X на общих формулах (II) и (III) представляет собой атом кислорода или NR8, и R8 представляет собой атом водорода, (С1-С10) алкильную группу или (С6-С10) арильную группу, которая может иметь заместитель.
[44] (С1-С10) алкильная группа R8 на общих формулах (II) и (III) представляет собой линейную, разветвленную или циклическую (С1-С10) алкильную группу, и примеры включают метильную группу, этильную группу, н-пропильную группу, н-бутильную группу, н-пентильную группу, н-гексильную группу, н-октильную группу, н-децильную группу, изопропильную группу, втор-бутильную группу и трет-бутильную группу. Среди прочих предпочтительными являются метальная группа, этильная группа, н-пропильная группа и н-бутильная группа.
[45] Если рассматривать (С6-С10) арильную группу, которая может иметь заместитель, в качестве R8 на общих формулах (II) и (III), то в числе примеров можно отметить группы, перечисленные выше, и среди прочих фенильная группа является предпочтительной.
[46] X на общих формулах (II) и (III) особенно предпочтительно представляет собой атом кислорода или NH, где R8 представляет собой атом водорода.
[47] L на общих формулах (II) и (III) представляет собой линкер, то есть группу, которая связывает R7 и X, группу, которая может иметь структуру линейного или циклического алкила, структуру сложного эфира, структуру амида, структуру простого эфира, структуру сульфида, структуру дисульфида и т.д. и может дополнительно иметь заместитель. Р равен 0 или 1, и если р равен 0, это означает, что R7 напрямую связан с X в отсутствие линкера.
Линкер не ограничен каким-либо конкретным образом; тем не менее, линкер представляет собой заместитель, с которым связаны R7 и X. Примеры включают ацетиламиногруппу, ацетоксигруппу, пропиониламиногруппу, пропионилоксигруппу, фенилпропиониламиногруппу, фенилпропионилоксигруппу, метальную группу, этильную группу, н-бутильную группу, циклопропильную группу, циклобутильную группу, циклогексильную группу, метоксигруппу, этоксигруппу, пропоксигруппу, н-бутоксигруппу, диметилсульфидную группу, диэтилсульфидную группу, этилметилсульфидную группу, диметилдисульфидную группу, диэтилдисульфидную группу, этилметилдисульфидную группу и производное янтарной кислоты.
[48] (С1-С10) алкильная группа в (С1-С10) алкильной группе, которая может иметь заместитель, в качестве R6 на общих формулах (II) и (III) может представлять собой линейную или разветвленную (С1-С10) алкильную группу, и примеры включают метальную группу, этильную группу, н-пропильную группу, н-бутильную группу, н-пентильную группу, н-гексильную группу, н-октильную группу, н-децильную группу, изопропильную группу, втор-бутильную группу, трет-бутильную группу и 2,2-диметилпропильную группу. Среди указанных групп предпочтительными являются метальная группа, этильная группа, н-пропильная группа и н-бутильная группа.
Заместитель не ограничен каким-либо конкретным образом; тем не менее, примеры включают (2-бензилоксикарбонил)фенэтиламинокарбонильную группу (группу, в которой сложный бензиловый эфир фенилаланина образует амидную связь с карбонильной группой) и этоксикарбонильную группу.
[49] Если рассматривать (С6-С10) арильную группу, которая может иметь заместитель, в качестве R6 на общих формулах (II) и (III), то в числе примеров можно отметить заместители, перечисленные выше, и среди прочих предпочтительными являются незамещенная фенильная группа и незамещенная нафтильная группа.
(С7-С15) аралкильная группа, которая может иметь заместитель, в качестве R6 на общих формулах (II) и (III) представляет собой линейную или разветвленную алкильную группу, с которой связана фенильная группа или нафтильная группа, примеры включают бензильную группу, фенэтильную группу, нафтилметильную группу и нафтилэтильную группу.
[50] R7 на общих формулах (II) и (III) представляет собой остаток, полученный в результате удаления Н (атом водорода) из заместителя, обозначенного R6, и предпочтительные группы являются схожими с R6. Положение, по которому удаляют Н, не ограничено каким-либо конкретным образом.
[51] Циклическая структура, образованная R6 и R7, связанными друг с другом, на общих формулах (II) и (III) предпочтительно представляет собой 3-8-членную кольцевую структуру и может содержать гетероатомы, такие как атом кислорода, атом серы, атом азота и атом фосфора, в качестве атомов, составляющих кольцевую структуру. Среди прочих предпочтительной является циклическая структура, представляющая собой 5-членную кольцевую, 6-членную кольцевую или 7-членную кольцевую структуру, которая не содержит гетероатомы, или 5-членную кольцевую или 6-членную кольцевую структуру, содержащую атом азота в качестве гетероатома. Гетероатом может представлять собой атом, который является частью линкера. Даже в случае, где используется кольцевая структура, R6 и R7 могут иметь заместители.
[52] Предпочтительным примером группы, представленной на общей формуле (II), может являться группа, имеющая структуру, представленную на следующей общей формуле (XIV). При этом, связь между группой (XIV) и карбоксильной группой боковой цепи блоксополимера обозначена пунктирной линией.
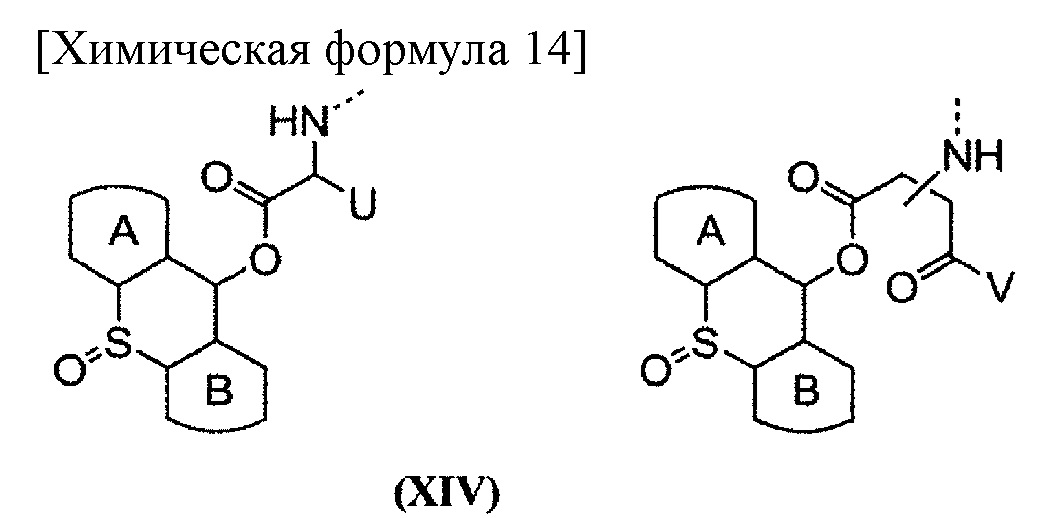
где кольцо А и кольцо В, которые могут быть одинаковыми или различными, представляют собой карбоциклическое кольцо, содержащее 5 или 7 членов в кольце, которое может иметь заместитель; U представляет собой остаток α-аминокислоты; и V представляет собой заместитель, полученный в результате удаления Н из аминогруппы α-аминокислоты, содержащей защищенную карбоксильную группу.
[53] Карбоциклическое кольцо в 5-7-членном кольце, которое может иметь заместитель, на общей формуле (XIV) может иметь ненасыщенную связь в кольце, которое конденсировано с оксидом тиопирана. Примеры заместителей включают низшую алкильную группу, ацильную группу и атом галогена; тем не менее, незамещенное карбоциклическое кольцо является предпочтительным. Оксид тиоксантена, в котором кольцо А и кольцо В оба представляют собой бензольное кольцо, является особенно предпочтительным.
U на общей формуле (XIV) представляет собой боковую цепь незаменимой аминокислоты, примеры включают атом водорода, метильную группу, бензильную группу и изобутильную группу. Бензильная группа является особенно предпочтительной, α-аминокислота может содержать только D-аминокислоты или только L-аминокислоты или может содержать произвольную смесь D-аминокислот и L-аминокислот в одной молекуле или в различных молекулах.
[54] Примеры α-аминокислот для получения V на общей формуле (XIV) включают глицин, аланин, фенилаланин и изолейцин, и примеры защитных групп для карбоксильной группы включают аминогруппу, содержащую бензильную группу, или (С1-С10) алкильную группу, которая может иметь заместитель, (С1-С10) алкоксигруппу, которая может содержать фенильную группу, и (С6-С10) арилоксигруппу. Среди указанных групп особенно предпочтительным является заместитель, полученный в результате удаления Н из аминогруппы сложного эфира 4-фенилбутилового спирта и аланина.
[55] При этом, -OCOCH-U и -OCOCH(1 или 2)СН(2 или 1)CO-V на общей формуле (XIV) соответствуют линкеру.
[56] Примеры групп, представленных на общей формуле (II), включают группы, обозначенные (i)-(x) на общей формуле (V), описанные выше. При этом, связь между группой (XIV) и карбоксильной группой боковой цепи в блоксополимере обозначена пунктирной линией.
[57] Предпочтительные примеры группы, представленной на общей формуле (III), включают группы, имеющие структуры, представленные на следующей общей формуле (XV). При этом связь между группой (XV) и карбоксильной группой боковой цепи в блоксополимере обозначена пунктирной линией.
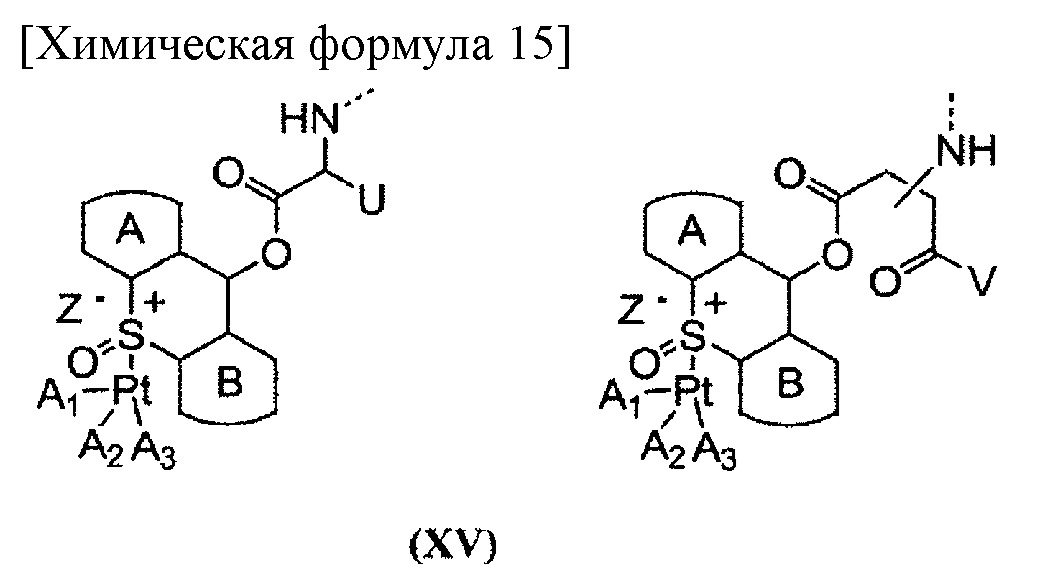
где кольцо А и кольцо В, которые могут быть одинаковыми или различными, представляют собой карбоциклическое кольцо, содержащее от 5 до 7 членов в кольце, которое может иметь заместитель; U представляет собой остаток α-аминокислоты; V представляет собой заместитель, полученный в результате удаления Н из аминогруппы α-аминокислоты, содержащей защищенную карбоксильную группу; каждый из A1, А2 и A3 представляет собой лиганд комплекса платины; и Z- представляет собой противоположно заряженный анион.
[58] Кольцо А, кольцо В, U и V на общей формуле (XV) схожи с кольцом А, кольцом В, U и V на общей формуле (XIV), и предпочтительные группы также являются схожими. Фрагмент, соответствующий линкеру, также является схожим.
[59] Каждый из A1, А2 и A3 на общей формуле (III) или общей формуле (XV) представляет собой лиганд в комплексе платины и не ограничен каким-либо конкретным образом. Тем не менее, каждый из A1 и А2, которые могут быть одинаковыми или различными, представляет собой аммиак или первичный, вторичный или третичный амин, или A1 и А2 могут быть объединены с образованием нециклического или циклического диамина, который может иметь заместитель, и A3 предпочтительно представляет собой атом галогена, молекулу воды, амин, который может иметь заместитель, гетероарильное соединение или сульфоксидное соединение. Примеры первичного, вторичного или третичного амина включают метиламин, этиламин, н-бутиламин, изопропиламин, циклогексиламин, бензиламин, 4-фенилбутиламин, диметиламин, диэтиламин, ди-н-бутиламин, диизопропиламин, дициклогексиламин, дибензиламин, бисфенилбутиламин, N-этилметиламин, N-метилизопропиламин и N-циклогексилметиламин.
Примеры гетероарильных соединений включают пиридин, хинолин и фенантридин, и атом азота в соединении образует координационные связи с платиной.
Примеры сульфоксидных соединений включают диметилсульфоксид, диэтилсульфоксид, дифенилсульфоксид, метилфенилсульфоксид, метилтолуилсульфоксид, бензилметилсульфоксид и дибензилсульфоксид.
Если рассматривать A1, А2 и A3 на общей формуле (III), то более предпочтительно A1 и А2 оба представляют собой аммиак или лиганд, выбранный из общей формулы (XIII), и A3 представляет собой атом хлора.
[60] Примеры групп, представленных на общей формуле (III), включают группы, обозначенные как (i')-(x') на общей формуле (VI). При этом, связь между группой (VI) и карбоксильной группой боковой цепи в блоксополимере обозначена пунктирной линией.
[61] Z- на общей формуле (III) или общей формуле (XV) представляет собой анион, имеющий противоположный заряд по сравнению с катионом платины, и не ограничен каким-либо конкретным образом. При необходимости можно применять различные ионы, получаемые в традиционных реакциях образования солей. Несмотря на то, что противоположно заряженный анион описан в настоящем изобретении как Z-, противоположно заряженный анион не ограничен одновалентным анионом и может представлять собой поливалентный анион. Примеры противоположно заряженных анионов включают трифторметилсульфонатный ион (-OSO2CF3), хлоридный ион (Cl-), нитратный ион (NO3-), фосфатный ион (HPO42-), сульфатный ион (SO42-) и гидрокарбонатный ион (HCO3-).
[62] R5 на общей формуле (I) представляет собой заместитель, выбранный из группы, состоящей из (С1-С30) алкоксигруппы, (С1-С30) аралкилоксигруппы, (С6-С10) арилоксигруппы, (С1-С30) алкиламиногруппы, которая может иметь заместитель, ди-(С1-С30) алкиламиногруппы, которая может иметь заместитель, производного α-аминокислоты, представленного на общей формуле (IV), и -NR9CONHR10, и каждый R9 и R10, которые могут быть одинаковыми или различными, представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой.
[63] Примеры (С1-С30) алкоксигрупп включают метоксигруппу, этоксигруппу, н-бутоксигруппу, трет-бутоксигруппу, циклопропилоксигруппу, циклогексилоксигруппу и адамантилоксигруппу, и среди прочих предпочтительными являются этоксигруппа и трет-бутоксигруппа.
Примеры (С1-С30) аралкилоксигрупп включают бензилоксигруппу, 2-фенилэтоксигруппу, 3-фенилпропоксигруппу и 4-фенилбутоксигруппу, и среди прочих предпочтительными являются бензилоксигруппа и 4-фенилбутоксигруппа.
Примеры (С6-С10) арилоксигрупп включают феноксигруппу и нафтоксигруппу.
[64] Примеры (С1-С30) алкиламиногруппы, которая может иметь заместитель, и ди-(С1-С30) алкиламиногруппы, которая может иметь заместитель, включают метиламиногруппу, этиламиногруппу, н-бутиламиногруппу, изопропиламиногруппу, циклогексиламиногруппу, бензиламиногруппу, 4-фенилбутиламиногруппу, диметиламиногруппу, диэтиламиногруппу, ди-н-бутиламиногруппу, диизопропиламиногруппу, дициклогексиламиногруппу, дибензиламиногруппу, бисфенилбутиламиногруппу, N-этилметиламиногруппу, N-метилфениламиногруппу и N-метил-4-фенилбутиламиногруппу. Среди прочих предпочтительными являются этиламиногруппу, бензиламиногруппа и 4-фенилбутиламиногруппа.
[65] Примеры (С3-С6) циклических алкильных групп включают циклопропильную группу, циклобутильную группу, циклопентильную группу и циклогексильную группу, и среди прочих предпочтительной является циклогексильная группа. Кроме того, примеры (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, включают метальную группу, этильную группу, н-пропильную группу, н-бутильную группу, н-пентильную группу, изопропильную группу, диметиламинопропильную группу и 2-морфолиноэтильную группу. Среди прочих предпочтительными являются изопропильная группа и диметиламинопропильная группа.
[66] Q в производном α-аминокислоты, представленном на общей формуле (IV), предпочтительно представляет собой боковую цепь незаменимой аминокислоты, и примеры включают атом водорода, метальную группу, бензильную группу и изобутильную группу. Бензильная группа, которая представляет собой боковую цепь фенилаланина, является особенно предпочтительной. Производное α-аминокислоты может содержать только D-аминокислоты или только L-аминокислоты или может содержать произвольную смесь D-аминокислот и L-аминокислот.
Примеры (С1-С10) алкильной группы, которая может иметь заместитель, в качестве Y включают заместители, перечисленные выше, и среди указанных групп предпочтительными являются метильная группа, этильная группа, фенильная группа, бензильная группа и 4-фенилбутильная группа.
Примеры (С1-С10) алкоксигруппы, которая может содержать фенильную группу, в качестве Y включают метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, трет-бутоксигруппу, бензилоксигруппу, фенэтилоксигруппу и 4-фенилбутоксигруппу.
Примеры (С6-С10) арилоксигруппы в качестве Y включают феноксигруппу и нафтоксигруппу.
В случае, если Y представляет собой -NR12CONHR13, примеры (С3-С6) циклической алкильной группы и (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, в качестве R12 и R13 включают группы, схожие с группами, перечисленными для R9 и R10 в R5 на общей формуле (I), описанной выше, и предпочтительные группы также являются схожими.
Среди указанных групп Y особенно предпочтительно представляет собой бензилоксигруппу.
[67] Заместители R4 и R5 на общей формуле (I) могут быть одинаковыми или различными в одной молекуле и могут представлять собой заместители одного вида или смесь заместителей в молекулах полимерного конъюгата комплекса платины.
Заместитель R5 на общей формуле (I) особенно предпочтительно представляет собой остаток, полученный в результате удаления Н из аминогруппы сложного бензилового эфира фенилаланина и/или -NR9CONHR10 (где R9 и R10 оба представляют собой циклогексильную группу или изопропильную группу).
[68] а на общей формуле (I) представляет собой целое число от 5 до 11500 и предпочтительно от 10 до 2000.
[69] Каждый из d, е, f, g, h, i и j на общей формуле (I) представляет собой целое число от 0 до 200, d+e представляет собой целое число от 1 до 200, и d+e+f+g+h+i+j представляет собой целое число от 2 до 200. Предпочтительно каждый из d, е, f, g, h, i и j представляет собой целое число от 0 до 100, d+e представляет собой целое число от 1 до 100, и d+e+f+g+h+i+j представляет собой целое число от 4 до 100.
Если рассматривать конъюгат комплекса платины (II), представленный на общей формуле (I) с полимерным производным сульфоксида, то порядок связей различных составляющих звеньев полиаспарагиновой кислоты является случайным.
[70] Полимерный конъюгат комплекса платины (II), в котором сульфоксидная группа производного сульфоксида, встроенная по карбоксильной группе боковой цепи в блокосполимер, содержащий структурный фрагмент полиэтиленгликоля и фрагмент полиглутаминовой кислоты, образует координационные связи с платиной, представлен, например, на общей формуле (VII), описанной выше.
[71] Примеры (С1-С10) алкильной группы, которая может иметь заместитель, в качестве R11 на общей формуле (VII) включают группы, схожие с (С1-С10) алкильной группой, которая может иметь заместитель, определенной для R1 на общей формуле (I), и предпочтительные группы также являются схожими.
Примеры (С6-С10) арильной группы, которая может иметь заместитель, в качестве R11 на общей формуле (VII) включают группы, схожие с (С6-С10) арильной группой, которая может иметь заместитель, определенной для R1 на общей формуле (I).
[72] Примеры связующих групп, представленных как R19 на общей формуле (VII), включают группы, схожие со связующей группой, определенной для R2 на общей формуле (I), и предпочтительные группы также являются схожими.
[73] Примеры (С1-С6) ацильных групп в качестве R20 на общей формуле (VII) включают группы, схожие с (С1-С6) ацильной группой, определенной для R3 на общей формуле (I), и предпочтительные группы также являются схожими.
[74] R21 на общей формуле (VII) представляет собой заместитель общей формулы (VIII) и (IX), и по меньшей мере один из R21 представляет собой заместитель, с которым образует координационные связи комплекс платины (II), представленный на общей формуле (IX).
[75] В случае, если атом серы в сульфоксидной группе на общих формулах (VIII) и (IX) представляет собой асимметрический центр, то соединение может представлять собой отдельное соединение или смесь стереоизомеров.
[76] Примеры X на общих формулах (VIII) и (IX) включают группы, схожие с X на общих формулах (II) и (III), и предпочтительные группы также являются схожими.
[77] Примеры R8 на общих формулах (VIII) и (IX) включают группы, схожие с R8 на общих формулах (II) и (III), и предпочтительные группы также являются схожими.
[78] L на общих формулах (VIII) и (IX) представляет собой линкер, и примеры включают группы, схожие с L на общих формулах (II) и (III). Кроме того, р также схож с р на общих формулах (II) и (III).
[79] Примеры (С1-С10) алкильной группы, которая может иметь заместитель, в качестве R6 на общих формулах (VIII) и (IX) включают группы, схожие с (С1-С10) алкильной группой, которая может иметь заместитель, определенной для R6 на общих формулах (II) и (III), и предпочтительные группы также являются схожими. Заместители также такие, как описано выше.
[80] Примеры (С6-С10) арильной группы, которая может иметь заместитель, в качестве R6 на общих формулах (VIII) и (IX) включают группы, схожие с (С6-С10) арильной группой, которая может иметь заместитель, определенной для R6 на общих формулах (II) и (III), и предпочтительные группы также являются схожими.
Примеры (С7-С15) аралкильной группы, которая может иметь заместитель, в качестве R6 на общих формулах (VIII) и (IX) включают группы, схожие с (С7-С15) аралкильной группой, которая может иметь заместитель, определенной для R6 на общих формулах (II) и (III), и предпочтительные группы также являются схожими.
[81] R7 на общих формулах (VIII) и (IX) схож с R7 на общих формулах (II) и (III), и предпочтительные группы также являются схожими.
[82] Циклическая структура, образованная R6 и R7, связанными друг с другом, на общих формулах (VIII) и (IX) предпочтительно представляет собой 3-8-членную кольцевую структуру и может содержать гетероатом, такой как атом кислорода, атом серы, атом азота или атом фосфора в качестве атома, составляющего кольцевую структуру. Среди прочих предпочтительной является циклическая структура, которая представляет собой 5-членную кольцевую, 6-членную кольцевую или 7-членную кольцевую структуру и не содержит гетероатом или 5-членную кольцевую или 6-членную кольцевую структуру, содержащую атом азота в качестве гетероатома. Гетероатом может представлять собой атом, который составляет часть линкера. Даже в случае, если R6 и R7 образуют кольцевую структуру, R6 и R7 могут иметь заместитель.
[83] Предпочтительный пример группы, представленной на общей формуле (VIII), может представлять собой группу, имеющую неполную структуру, представленную на общей формуле (XIV), и предпочтительный пример группы, представленной на общей формуле (IX), может представлять собой группу, имеющую неполную структуру, представленную на общей формуле (XV). В данном случае U, V, A1, А2, A3 и Z-, соответственно, имеют такие же значения, что описаны выше.
[84] Примеры групп, представленных на общей формуле (VIII), включают группы, обозначенные как (i)-(x) на общей формуле (XI), примеры, групп, представленных на общей формуле (IX), включают группы, обозначенные как (i')-(x') на общей формуле (XII). При этом, связь между группой (XII) и карбоксильной группой боковой цепи в блоксополимере обозначена пунктирной линией.
[85] A1, А2 и A3 на общей формуле (IX) представляют собой лиганды комплекса платины, и примеры включают группы, схожие с A1, А2 и A3 на общей формуле (III). Предпочтительные группы также являются схожими.
Примеры Z- на общей формуле (IX) включают ионы, схожие с Z- на общей формуле (III), и предпочтительные ионы также являются схожими.
[86] R22 на общей формуле (VII) представляет собой группу, выбранную из группы, состоящей из (С1-С30) алкоксигруппы, (С1-С30) аралкилоксигруппы, (С6-С10) арилоксигруппы, (С1-С30) алкиламиногруппы, которая может иметь заместитель, ди-(С1-С30) алкиламиногруппы, которая может иметь заместитель, производного α-аминокислоты, представленного на общей формуле (X), и -NR9CONHR10, и каждый из R9 и R10, которые могут быть одинаковыми или различными, представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой.
[87] В данном случае примеры (С1-С30) алкоксигруппы, (С1-С30) аралкилоксигруппы, (С6-С10) арилоксигруппы, (С1-С30) алкиламиногруппы, которая может иметь заместитель, ди-(С1-С30) алкиламиногруппы, которая может иметь заместитель, (С3-С6) циклической алкильной группы и (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, включают группы, схожие с (С1-С30) алкоксигруппой, (С1-С30) аралкилоксигруппой, (С6-С10) арилоксигруппой, (С1-С30) алкиламиногруппой, которая может иметь заместитель, ди-(С1-С30) алкиламиногруппой, которая может иметь заместитель, (С3-С6) циклической алкильной группой и (С1-С5) алкильной группой, которая может быть замещена третичной аминогруппой, определенными для R5 на общей формуле (I), соответственно. Предпочтительные группы также являются схожими.
[88] Примеры Q в производном α-аминокислоты, представленном на общей формуле (X), включают группы, схожие с Q в производном α-аминокислоты, представленном на общей формуле (IV), и предпочтительные группы также являются схожими. Кроме того, примеры (С3-С6) циклической алкильной группы и (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, в качестве R12 и R13 в случае, когда Y на общей формуле (X) представляет собой (С1-С10) алкильную группу, которая может иметь заместитель, (С1-С10) алкоксигруппу, которая может содержать фенильную группу, (С6-С10) арилоксигруппу и -NR12CONHR13, включают группы, схожие с (С3-С6) циклической алкильной группой и (С1-С5) алкильной группой, которая может быть замещена третичной аминогруппой, определенными для R12 и R13 в случаях, описанных выше, где Y на общей формуле (IV) представляет собой (С1-С10) алкильную группу, которая может иметь заместитель, (С1-С10) алкоксигруппу, которая может содержать фенильную группу, (С6-С10) арилоксигруппу и -NR12CONHR13. Предпочтительные группы также являются схожими. Среди указанных групп Y особенно предпочтительно представляет собой бензилоксигруппу.
[89] Заместители R21 и R22 на общей формуле (VII) могут быть одинаковыми или различными в одной молекуле, и заместители могут представлять собой заместители одного вида или их смесь в различных молекулах полимерного конъюгата комплекса платины.
Особенно предпочтительные примеры заместителей R22 на общей формуле (VII) включают остаток, полученный в результате удаления Н из аминогруппы сложного бензилового эфира фенилаланина и/или -NR9CONHR10 (где R9 и R10 оба представляют собой циклогексильную группу или изопропильную группу).
[90] b на общей формуле (VII) представляет собой целое число от 5 до 11500, и b предпочтительно равен от 10 до 2000.
[91] k на общей формуле (VII) представляет собой целое число от 1 до 200, каждый из m и n представляет собой целое число от 0 до 200, и k+m+n представляет собой целое число от 2 до 200. Предпочтительно к представляет собой целое число от 1 до 100, каждый из m и n представляет собой целое число от 0 до 100, и k+m+n равна от 3 до 100.
Если рассматривать конъюгат комплекса платины (II), представленного на общей формуле (VII), с полимерным производным сульфоксида, то порядок связей различных составляющих звеньев полиглутаминовой кислоты является случайным.
[92] Полимерный конъюгат комплекса платины (II) согласно настоящему изобретению, в котором полимерное производное сульфоксида образует координационные связи с платиной, может быть получен, например, путем встраивания производного сульфоксида по карбоксильной группе боковой цепи в блоксополимер, содержащий структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты или структурный фрагмент полиэтиленгликоля и фрагмент полиглутаминовой кислоты, и образования координационных связей между сульфоксидной группой и комплексом платины (II) путем обмена лигандами в органическом растворителе или водном растворе. Предложенный способ получения также включен в настоящее изобретение.
[93] Способ получения будет описан на примере соединения общей формулы (I) или общей формулы (VII). Если рассматривать способ встраивания структуры, представленной на общей формуле (II) или (III), в R4 на общей формуле (I), например, проводят взаимодействие блоксополимера, содержащего структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты, полученного способом, описанным в патенте Японии JP 3268913 В2, с производным сульфоксида, в котором защищены функциональные группы, отличные от гидроксильной группы, аминогруппы и т.д., которые могут вступать в соответствующие реакции, с использованием дегидратирующего конденсирующего агента, такого как дициклогексилкарбодиимид (DCC), диизопропилкарбодиимид (DIPC), гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (WSC) или 1-этоксикарбонил-2-этокси-1,2-дигидроксихинолинон (EEDQ), в растворителе, предпочтительно в апротонном полярном растворителе, таком как N,N-диметилформамид (ДМФ), 1,3-диметил-2-имидазолидинон (DMI) или N-метилпирролидон (NMP), при 0-180°C или предпочтительно при 5°C-50°C, в результате чего производное сульфоксида встраивается в блоксополимер. Полимерное производное сульфоксида получают традиционными способами разделения и очистки и т.д. Кроме того, во время реакции конденсации также можно применять вспомогательный реагент, такой как N,N-диметиламинопиридин (DMAP). Затем полученное таким образом производное сульфоксида растворяют в растворителе, предпочтительно в апротонном полярном растворителе, предпочтительно таком как N,N-диметилформамид (ДМФ), 1,3-диметил-2-имидазолидинон (DMI) или N-метилпирролидон (NMP), и в указанный раствор добавляют раствор, полученный в результате обработки DACH-платины (Pt(R,R-dach)Cl2) трифторметансульфонатом серебра (см. источник непатентной литературы: J. Am. Chem. Soc. 2014, 136, 2126-2134). Обмен лигандами проводят при 0°C-180°C и предпочтительно при 5°C-50°C, в результате чего сульфоксидная группа связывается с платиной. В случае использования защитных групп продукт можно обрабатывать по реакции элиминации в зависимости от применяемой защитной группы на такой стадии, где эта реакция не будет отрицательно влиять на основную реакцию.
[94] Кроме того, если рассматривать способ встраивания группы, представленной на общей формуле (VIII) или (IX), по R21 в соединении общей формулы (VII), например, указанную группу можно встраивать схожим способом с использованием блоксополимера, содержащего структурный фрагмент полиэтиленгликоля и фрагмент полиглутаминовой кислоты, полученного способом, описанным в патенте Японии JP 4745664 В2, вместо блоксополимера, содержащего структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты, описанного выше. Что касается защитных групп, то применяют тот же способ, что описан выше.
[95] Если рассматривать способ введения подходящего заместителя по R5 или R22 в соединение общей формулы (I) или (VII), то можно использовать способ активации карбоксильных групп блоксополимера, традиционно применяемый для синтеза сложных эфиров или синтеза амидов, и затем проводить взаимодействие по активированным карбоксильным группам с соответствующим спиртом, соответствующим амином, аминокислотой с защищенной карбоксильной группой и т.д. в количестве, которое требуется ввести в конъюгат, в основных условиях; способ активации соответствующего спирта, соответствующего амина, аминокислоты с защищенной карбоксильной группой и т.д., и затем проводить взаимодействие активированного соединения с карбоксильными группами блоксополимера; и т.д.
После очистки продукта также допускается повторная активация непрореагировавших карбоксильных групп в полимере и проведение конденсации по указанным повторно активированным карбоксильным группам с гидроксильной группой или аминогруппой производного сульфоксида. В качестве альтернативы, допускается повторное взаимодействие с различными спиртами, аминами и т.д., в результате чего образуется соединение, содержащее смесь различных заместителей R5 или R22, и затем проводят конденсацию по гидроксильной группе или аминогруппе производного сульфоксида с полученным таким образом соединением. Порядок указанных реакций может быть различным.
Способ получения комплекса платины (II) согласно настоящему изобретению, к которому посредством координационных связей присоединено полимерное производное сульфоксида, не ограничен указанными способами. Примеры способа получения также описаны ниже в разделе примеров.
[96] Лекарственное средство, содержащее в качестве активного ингредиента полимерный конъюгат комплекса платины (II), образующего координационные связи с полимерным производным сульфоксида, согласно настоящему изобретению, также включено в настоящее изобретение. Лекарственное средство предпочтительно применяют в качестве противоопухолевого агента.
Что касается применения в качестве противоопухолевого агента, то полимерный конъюгат можно использовать отдельно или в виде смеси с фармацевтически приемлемыми добавками, такими как носитель, вспомогательное вещество, разрыхлитель, связывающий агент, смазывающий агент, разжижающий агент, агент для нанесения покрытия, суспендирующий агент, эмульгатор, стабилизатор, консервант, корригент, вкусоароматическая добавка, разбавители и добавки для увеличения растворимости. Полимерный конъюгат можно вводить перорально или парентерально (системное введение, местное введение и т.д.) в виде препарата, такого как порошковый препарат, гранулированный препарат, таблетка, капсуловидная таблетка, капсула, инъекционный препарат, суппозиторий или мазь. Применение полимерного конъюгата в виде инъекционного препарата является особенно предпочтительным, и как правило, применяют, например, воду, 5% раствор глюкозы или маннита, водорастворимый органический растворитель (например, глицерин, этанол, N-метилпирролидон, полиэтиленгликоль, Cremophor или их смесь), смесь воды и водорастворимого органического растворителя и т.д.
[97] Количество полимерного конъюгата, вводимого в качестве противоракового агента, безусловно может быть различным в зависимости от пола, возраста, физиологического состояния, патологического состояния и т.д. пациента; тем не менее, как правило, противораковый агент вводят парентерально в дозе от 0,01 до 1500 мг/м2 и предпочтительно от 0,1 до 250 мг/м2 активного ингредиента в день взрослому. Введение путем инъекции проводят через вену, артерию, в болезненный участок (участок опухоли) и т.д.
ПРИМЕРЫ
[98] Далее настоящее изобретение будет описано более подробно при помощи примеров. Тем не менее, предполагается, что настоящее изобретение не ограничено указанными примерами.
В примерах настоящего изобретения используют следующие сокращения.
R,R-dach: (1R,2R)-циклогександиамин
1-ОНР: оксалиплатин
Boc: трет-бутоксикарбонильная группа
OTf: трифторметансульфонат
[99] Содержание лекарственного соединения в приведенных примерах определяют путем измерения содержания платины с использованием оптического эмиссионного спектрометра с индуктивно связанной плазмой, ИСП-ОЭС (производства Agilent Technologies, Inc.: модель 720-ES), и вычисления содержания в пересчете на Pt(R,R-dach)Cl2.
[100] Измерение размера частиц и дзета-потенциала соединения, применяемого в приведенных примерах, проводили с использованием устройства для измерения размера частиц-дзета потенциала (производства Malvern Instruments, Ltd.; ZETASIZER NANO ZS).
[101] Молекулярную массу соединения, применяемого в приведенном примере, измеряли путем ЖХ/МС (Shimadzu LCMS-2020).
Колонка: INERTSIL ODS-3 φ 2,1 мм × 100 мм
Подвижная фаза А: ацетонитрил/муравьиная кислота (99,9/0,1)
Подвижная фаза В: вода/муравьиная кислота (99,9/0,1)
Градиент:
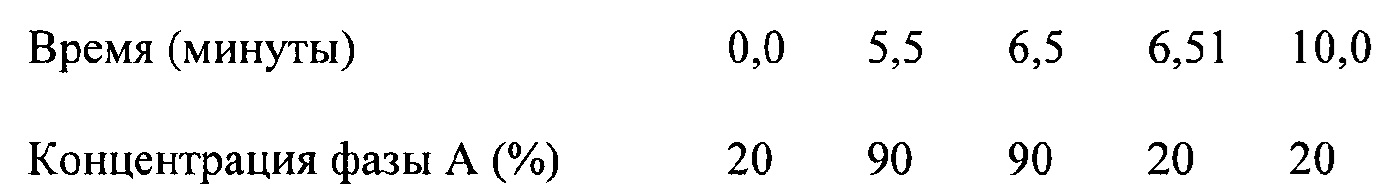
Расход: 0,3 мл/мин
[102] Справочный пример 1. Синтез производного сульфоксида (i)
Сульфоксид N-Boc-L-метионина (2,5 g; получали в Watanabe Chemical Industries, Ltd.) и гидрохлорид сложного бензилового эфира фенилаланина (3,0 г) суспендировали в дихлорметане (50 мл) и в суспензию добавляли DMAP (0,12 г) и триэтиламин (2,3 г). Смесь перемешивали при 0°C. В реакционный раствор добавляли WSC (2,17 г), затем постепенно повышали температуру до комнатной и перемешивали реакционный раствор в течение 46 часов. После завершения взаимодействия реакционный раствор последовательно промывали насыщенным водным раствором гидрокарбоната натрия, дистиллированной водой и насыщенным солевым раствором. В органический слой добавляли безводный сульфат натрия, отфильтровывали твердое вещество и затем концентрировали фильтрат при пониженном давлении. К полученному таким образом остатку добавляли смешанный раствор ацетона (50 мл) и гексана (450 мл), осаждалось твердое вещество. Твердое вещество собирали путем фильтрования и сушили при пониженном давлении, получали Вос-защищенную форму титульного соединения (3,0 г).
1Н ЯМР (CDCl3): δ 7,39-7,21 (10Н, m), 7,13-7,07 (2Н, m), 5,19-5,10 (2Н, m), 4,85-4,79 (1Н, m), 4,54-4,40 (1Н, m), 3,20-3,0 (3Н, m), 2,61 (1,5Н, s, SOMe), 2,54 (1,5Н, s, SOMe), 2,60-2,52 (1Н, m), 2,35-2,22 (1H, m), 2,18-2,08 (1H, m), 1,42 (9H, s).
Полученную таким образом Вос-защищенную форму (2,0 г) растворяли в дихлорметане (10 мл) и охлаждали раствор до 0°C. Затем медленно добавляли трифторуксусную кислоту (10 мл) и перемешивали смесь в течение 2 часов при указанной температуре. После завершения взаимодействия концентрировали реакционный раствор при пониженном давлении и получали трифторацетат титульного соединения (колич. выход).
[103] Справочный пример 2. Получение раствора Pt(R,R-dach)Cl(OTf) в ДМФ
Согласно способу, описанному в источнике непатентной литературы (J. Am. Chem. Soc., 2014, 136, 2126-2134), DACH-платину (Pt(R,R-dach)Cl2; 1,5 g), полученную способом, описанным в Bioorg. Med. Chem. Lett., 2006, 16, 1686-1691, суспендировали в ДМФ (50 мл) без доступа света и в суспензию добавляли раствор (25 мл) трифторметансульфоната серебра (1,0 г; получали в Tokyo Chemical Industry Co., Ltd.) в ДМФ. Затем перемешивали смесь в течение 20 часов при комнатной температуре. После завершения взаимодействия осаждали полученный хлорид серебра на центрифуге, фильтровали надосадочную жидкость, в результате чего получали раствор титульного соединения.
[104] Пример 1. Получение соединения согласно примеру 1 (конъюгат полимерного производного сульфоксида и комплекса платины (II), полученный путем встраивания производного сульфоксида (i) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43: на общей формуле (I), R1 = метальная группа, R2 = триметиленовая группа, R3 = ацетильная группа, R4 = производное сульфоксида (i) или (i'), R5 = изопропиламинокарбонилизопропиламиногруппа, Z = OTf, d+e+f+g+h+i+j = примерно 43, a = примерно 273)
Блоксополимер метоксиполиэтиленгликоля-полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 43; 2,65 г), полученный способом, описанным в патенте Японии JP 3268913 В2, и трифторацетат производного сульфоксида (i), полученного в справочном примере 1 (2,0 г), растворяли в ДМФ (70 мл) при 35°C и затем в раствор добавляли диизопропилэтиламин (1,6 мл) и DMAP (81 мг). Доводили температуру реакционного раствора до 25°C, затем добавляли DIPC (2,0 мл) и перемешивали смесь в течение 23 часов при указанной температуре. Затем добавляли DIPC (0,5 мл) и перемешивали смесь еще один час. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (70 мл), этанола (70 мл) и диизопропилового эфира (560 мл) и перемешивали смесь при комнатной температуре. Затем оставляли смесь отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Осажденное вещество собирали путем фильтрования и сушили при пониженном давлении. Таким образом получали полимерное производное сульфоксида (3,85 г). Полученное таким образом полимерное производное сульфоксида (3,7 г) растворяли в ДМФ (20 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (20 мг/мл, 58,6 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 24 часов при 25°C. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (80 мл), этанола (80 мл) и диизопропилового эфира (640 мг) и перемешивали смесь при комнатной температуре. Затем оставляли смесь отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Осажденное вещество собирали путем фильтрования и сушили при пониженном давлении. Таким образом получали неочищенную форму титульного соединения (4,72 г). Полученную таким образом неочищенную форму (2,2 г) очищали путем ультрафильтрации в перекрестном потоке, VIVAFLOW 200 (производства Sartorius AG, НОММ: 10 кДа), и лиофилизировали водный раствор, полученный после очистки. Таким образом получали титульное соединение (2,1 г). Содержание полученного таким образом лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 составляло 20,5% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 85 нм, титульное соединение образовывало мицеллы.
[105] Справочный пример 3. Получение блоксополимера, содержащего фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43
Блоксополимер метоксиполиэтитленгликоля-полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 43; 0,8 г), полученный способом, описанным в патенте Японии JP 3268913 В2, растворяли в ДМФ (8 мл) при 35°C и в раствор добавляли гидрохлорид сложного бензилового эфира фенилаланина (0,35 г), диизопропилэтиламин (0,21 мл) и DMAP (25 мг). Раствор охлаждали до 25°C и затем в раствор добавляли DIPC (0,22 мл). Смесь перемешивали в течение 5 часов при указанной температуре. После завершения взаимодействия смесь по каплям добавляли в перемешиваемый раствор гептанов (128 мл) и этанола (32 мл), и твердое вещество, осаждаемое из раствора, собирали путем фильтрования и сушили при пониженном давлении. Таким образом получали форму сложного бензилового эфира титульного соединения (1,0 г). Полученную таким образом форму сложного бензилового эфира (0,95 г) растворяли в ДМФ (19 мл) при 35°C, в раствор добавляли гидратированный Pd/C (10% 95 мг) и перемешивали смесь в течение 13 часов при комнатной температуре в атмосфере водорода. После завершения взаимодействия в реакционную смесь добавляли активированный уголь (0,95 г) и перемешивали смесь в течение одного часа и фильтровали. Полученный таким образом маточный раствор добавляли по каплям в перемешиваемый раствор этилацетата (40 мл) и диизопропилового эфира (160 мл), и твердое вещество, осажденное из раствора, собирали путем фильтрования и затем сушили при пониженном давлении. Таким образом получали титульное соединение (0,20 г).
[106] Справочный пример 4. Синтез (4-(метилсульфинил)фенил)метанола (производное сульфоксида (v))
Титульное соединение (0,49 г) синтезировали способом, описанным в Adv. Synth. Catal., 2007, 349, 2425-2430, с использованием (4-(метилтио)фенил)метанола (1,54 г). Спектр1Н ЯМР полученного таким образом соединения соответствовал данным, описанным в литературе.
[107] Пример 2. Получение соединения согласно примеру 2 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (ii) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43: на общей формуле (I) R1 = метальная группа, R2 = триметиленовая группа, R3 = ацетильная группа, R4 = производное сульфоксида (II) или (ii'), R5 = изопропиламинокарбонилизопропиламиногруппа или 2-амино-N-изопропил-N-(изопропилкарбамоил)-3-фенилпропанамид, Z = OTf, d+e+f+g+h+i+j = примерно 43, а = примерно 273)
Блоксополимер (0,65 г), содержащий фрагмент метоксиполиэтиленгликоля и структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, полученный в справочном примере 3, и производное сульфоксида (v) (0,14 г), полученное в справочном примере 4, растворяли в ДМФ (20 мл) при 35°C и затем в раствор добавляли DMAP (20 мг). Температуру реакционного раствора доводили до 25°C, затем добавляли DIPC (0,41 мл) и перемешивали смесь в течение 24,5 часа при указанной температуре. Затем добавляли DIPC (0,1 мл) и перемешивали смесь еще один час. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (20 мл), этанола (20 мл) и диизопропилового эфира (160 мл) и перемешивали смесь при комнатной температуре. Затем оставляли смесь отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Осажденный продукт собирали путем фильтрования и затем сушили при пониженном давлении, в результате чего получали полимерное производное сульфоксида (0,72 г). Полученное таким образом полимерное производное сульфоксида (0,7 г) растворяли в ДМФ (5 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (12,5 мг/мл, 15 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 23 часов при 25°C. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (20 мл), этанола (20 мл) и диизопропилового эфира (160 мл) и перемешивали смесь при комнатной температуре. Затем оставляли смесь отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Осажденный продукт собирали путем фильтрования и затем сушили при пониженном давлении, в результате чего получали неочищенную форму титульного соединения (0,85 г). Полученную таким образом неочищенную форму (0,84 г) очищали путем ультрафильтрации на центрифуге, VIVASPIN 20 (производства Sartorius AG, НОММ: 10 кДа), и лиофилизировали водный раствор, полученный после очистки. Таким образом получали титульное соединение (0,66 г). Содержание полученного таким образом лекарственного соединения в пересчете на количество Pt(R,R-dach)Cl2 составляло 15,0% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 60 нм, титульное соединение образовывало мицеллы.
[108] Справочный пример 5. Синтез сложного этилового эфира сульфоксида метионина (производное сульфоксида (iii))
Сульфоксид N-Boc-L-метионина (2,00 г) растворяли в дихлорметане (40 мл) и затем в раствор последовательно добавляли этанол (0,485 мл), DMAP (93,2 мг) и DIPC (1,32 мл). Смесь перемешивали в течение ночи и затем удаляли полученное в результате твердое вещество путем фильтрования. Концентрировали фильтрат при пониженном давлении. Затем неочищенную форму сложного этилового эфира сульфоксида N-Boc-L-метионина (2,84 г) растворяли в растворе хлороводорода в этаноле (2 моль/л, 12,4 мл) и перемешивали раствор в течение 4 часов. Концентрировали реакционный раствор при пониженном давлении и очищали остаток путем колоночной хроматографии на силикагеле (36 г силикагеля) с использованием смеси хлороформ : метанол = 15:1 (320 мл) для удаления любых нежелательных фракций. Затем продукт после очистки собирали в метаноле и очищали, таким образом получали титульное соединение (743 мг).
1Н ЯМР (CD3OD): δ 4,34 (2Н, q, J=7,0 Гц), 4,23 (1Н, t, J=6,0 Гц), 3,19-3,03 (1H, m), 3,00-2,85 (1Н, m), 2,70 (3Н, s), 2,54-2,27 (2Н, m), 1,34 (3Н, t, J=7,0 Гц).
[109] Пример 3. Получение соединения согласно примеру 3 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (iii) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43: на общей формуле (I) R1 = метильная группа, R2 = триметиленовая группа, R3 = ацетильная группа, R4 = производное сульфоксида (iii) или (iii'), R5 = изопропиламинокарбонилизопропиламиногруппа, Z = OTf, d+e+f+g+h+i+j = примерно 43, а = примерно 273)
Блоксополимер метоксиполиэтиленгликоля-полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 43; 742 мг), полученный способом, описанным в патенте Японии JP 3268913 В2, и сложный эфтиловый эфир сульфоксида метионина (516 мг), полученный в справочном примере 5, растворяли в ДМФ (11 мл) при 35°C и затем в раствор добавляли диизопропилэтиламин (0,49 мл). Температуру реакционного раствора доводили до 25°C, затем добавляли DIPC (0,60 мл) и по прошествии 22 часов 15 минут снова добавляли DIPC (0,15 мл). Смесь дополнительно перемешивали в течение 1 часа 50 минут. Реакционный раствор по каплям добавляли в диизопропиловый эфир (147 мл) и промывали контейнер реакционной смеси этилацетатом (14,7 мл) и добавляли в смесь. Смесь перемешивали в течение ночи при комнатной температуре и затем отфильтровывали полученный в результате порошок. Порошок дважды промывали диизопропиловым эфиром (15 мл) и получали неочищенную форму (1,24 г). Полученную таким образом неочищенную форму (1,24 г) растворяли в очищенной воде (14,7 мл) при обычной температуре, затем в раствор добавляли ионообменную смолу (производства Muromachi Chemicals, Inc., MUROMAC(r) XSC-1114-H; 10 мл) и перемешивали смесь в течение 1 часа 30 минут. Удаляли ионообменную смолу путем фильтрования и дважды промывали ионообменную смолу очищенной водой (10 мл) и добавляли в раствор. Лиофилизировали полученный водный раствор и таким образом получали полимерное производное сульфоксида (0,79 г). Полученное таким образом полимерное производное сульфоксида (740 мг) растворяли в ДМФ (3,7 мл) при 35°C и доводили температуру реакционного раствора до 25°C. Затем в реакционный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (23 мг/мл, 15 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 6 часов 30 минут. Реакционный раствор по каплям добавляли в диизопропиловый эфир (270 мл) и промывали контейнер реакционной смеси этилацетатом (27 мл) и добавляли в реакционный раствор. Наблюдали осаждение желтого твердого вещества, перемешивали реакционный раствор в течение 15 минут и затем оставляли отстаиваться, удаляли надосадочную жидкость. Затем к остатку добавляли диизопропиловый эфир (270 мл) и промывали остаток при перемешивании. Таким образом, собирали неочищенную форму титульного соединения (1,00 г) путем фильтрования. К неочищенной форме (1,00 г) добавляли очищенную воду (200 мл), перемешивали смесь и затем центрифугировали с получением надосадочной жидкости. Лиофилизировали раствор (100 мл), полученный в результате повторяющихся операций концентрирования на мембране (НОММ: 10 кДа) и разбавления, таким образом получали титульное соединение (691 мг). Содержание полученного таким образом лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 составляло 9,8% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Тем не менее, интенсивность рассеянного света была низкой, таким образом, было сделано предположение о том, что титульное соединение не образовывало наночастицы.
[110] Пример 4. Получение соединения согласно примеру 4 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (iii) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43: на общей формуле (I) R1 = метальная группа, R2 = триметиленовая группа, R3 = ацетильная группа, R4 = производное сульфоксида (iii) или (iii1), R5 = изопропиламинокарбонилизопропиламиногруппа или сложный бензиловый эфир фенилаланина, Z = OTf, d+e+f+g+h+i+j = примерно 43, а = примерно 273)
Блоксополимер метоксиполиэтиленгликоля-полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 43; 3,19 г), полученный способом, описанным в патенте Японии JP 3268913 В2, и сложный этиловый эфир сульфоксида метионина (743 мг), полученный в справочном примере 5, растворяли в ДМФ (64,0 мл) при 35°C и затем в раствор добавляли диизопропилэтиламин (2,1 мл). Температуру реакционного раствора доводили до 25°C и затем добавляли DIPC (0,585 мл). Через 3 часа в смесь добавляли гидрохлорид сложного бензилового эфира фенилаланина (944 мг) и DIPC (0,52 мл) и перемешивали смесь еще один час. Добавляли DIPC (0,52 мл) и перемешивали смесь один час. Затем добавляли гидрохлорид сложного бензилового эфира фенилаланина (944 мг) и DIPC (1,04 мл) и перемешивали смесь в течение 19 часов. Реакционный раствор по каплям добавляли в диизопропиловый эфир (640 мл) и промывали контейнер реакционной смеси этилацетатом (64 мл) и добавляли в реакционный раствор. Перемешивали смесь в течение ночи при комнатной температуре и затем отфильтровывали полученное в результате твердое вещество и промывали диизопропиловым эфиром (80 мл). Таким образом получали неочищенную форму (5,50 г). Полученную таким образом неочищенную форму (5,50 г) растворяли в смешанном растворе ацетонитрила (60 мл) и очищенной воды (6 мл) и затем пропускали раствор через ионообменную смолу (производства Muromachi Chemicals, Inc., MUROMAC(r) XSC-1114-H; 46 мл). Ионообменную смолу промывали смешанным раствором ацетонитрила (120 мл) и очищенной воды (12 мл) и добавляли в раствор и концентрировали в раствор при пониженном давлении. Добавляли очищенную воду (40 мл) и затем лиофилизировали смесь. Таким образом получали полимерное производное сульфоксида (4,43 г). Полученное таким образом полимерное производное сульфоксида (3,31 г) растворяли в ДМФ (16,6 мл) при 35°C и доводили температуру реакционного раствора до 25°C. Затем в реакционный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (12,5 мг/мл, 51 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 24 часов. Реакционный раствор разбавляли примерно в 20 раз очищенной водой и затем лиофилизировали раствор (60 мл), полученный после повторяющихся операций концентрирования на мембране (НОММ: 10 кДа) и разбавления. Таким образом получали титульное соединение (3,09 г). Содержание полученного таким образом лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 составляло 8,0% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 30 нм, титульное соединение образовывало мицеллы.
[111] Справочный пример 6. Синтез производного сульфоксида (iv)
В смешанный раствор трифторацетата производного сульфоксида (i) (0,5 г), синтезированного в справочном примере 1, дихлорметана (3 мл) и диизопропилэтиламина (0,25 мл) добавляли суспензию (4 мл) N-гидроксисукцинимидного эфира 3-(4'-гидроксифенил)пропановой кислоты (0,26 г), синтезированного согласно способу, описанному в непатентной литературе (Biomaterials, 2010, 31, 1148-1157), в дихлорметане и перемешивали смесь при комнатной температуре. Затем в смесь добавляли дополнительную порцию диизопропилэтиламина (0,5 мл) и перемешивали смесь в течение 19 часов. После завершения взаимодействия последовательно промывали реакционный раствор насыщенным водным раствором хлорида аммония и насыщенным солевым раствором и к органическому слою добавляли безводный сульфат натрия. Отфильтровывали твердое вещество и затем концентрировали фильтрат при пониженном давлении. К полученному таким образом остатку добавляли диэтиловый эфир, осаждалось твердое вещество. Твердое вещество собирали путем фильтрования и сушили при пониженном давлении, таким образом получали титульное соединение (0,55 г). ЖХ/МС (ИЭР, пол.): 551 [М+Н]+
[112] Пример 5. Получение соединения согласно примеру 5 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (iv) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиглутаминовой кислоты, имеющий степень полимеризации примерно 22: на общей формуле (VII) R11 = метальная группа, R19 = триметиленовая группа, R20 = ацетильная группа, R21 = производное сульфоксида (iv) или (iv'), R22 = изопропиламинокарбонилизопропиламиногруппа, Z = OTf, k+m+n = примерно 22, b = примерно 273)
Блоксополимер (0,6 г), содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиглутаминовой кислоты, имеющий степень полимеризации примерно 22, полученный способом, описанным в патенте Японии JP 4745664 В2, и производное сульфоксида (iv) (0,54 г), полученное в справочном примере 6, растворяли в ДМФ (20 мл) при 35°C и затем добавляли DMAP (11 мг). Температуру реакционного раствора доводили до 25°C, затем добавляли DIPC (0,27 мл) и перемешивали смесь в течение 23,5 часа при указанной температуре. Затем добавляли DIPC (0,06 мл) и перемешивали смесь еще один час. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (20 мл), этанола (20 мл) и диизопропилового эфира (160 мл) и перемешивали смесь при комнатной температуре. Затем оставляли смесь отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Осажденный продукт собирали путем фильтрования и затем сушили при пониженном давлении, таким образом получали полимерное производное сульфоксида (0,93 г). Полученное таким образом полимерное производное сульфоксида (0,9 г) растворяли в ДМФ (5 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (20 мг/мл, 16,7 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 24 часов при 25°C. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (20 мл), этанола (20 мл) и диизопропилового эфира (160 мл) и перемешивали смесь при комнатной температуре. Затем оставляли смесь отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Осажденный продукт собирали путем фильтрования и затем сушили при пониженном давлении, в результате чего получали неочищенную форму титульного соединения (1,1 г). Полученную таким образом неочищенную форму (1,0 г) очищали путем ультрафильтрации на центрифуге, VIVASPIN 20 (производства Sartorius AG, НОММ: 10 кДа), и лиофилизировали водный раствор, полученный после очистки. Таким образом получали титульное соединение (0,76 г). Содержание полученного таким образом лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 составляло 16,9% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 120 нм, титульное соединение образовывало мицеллы.
[113] Справочный пример 7. Синтез производного сульфоксида (vi)
Сульфоксид тиоксантенола (0,7 г), синтезированный способом, описанным в непатентной литературе (Tetrahedron Letters, 2010, 51, 6939-6941, и J. Org. Chem., 1967, 32, 3814-3817) и N-Boc-L-фенилаланин (0,97 г) суспендировали в дихлорметане (30 мл) и в суспензию добавляли DMAP (74 мг). Перемешивали смесь при 0°C. В реакционный раствор добавляли WSC (0,76 г) и затем медленно нагревали смесь до комнатной температуры. Перемешивали смесь в течение 2,5 часа. После завершения взаимодействия реакционный раствор последовательно промывали насыщенным водным раствором гидрокарбоната натрия, дистиллированной водой и насыщенным солевым раствором и к органическому слою добавляли безводный сульфат натрия. Отфильтровывали твердое вещество и концентрировали фильтрат при пониженном давлении. Полученный таким образом остаток сушили при пониженном давлении, в результате чего получали Вос-защищенную форму титульного соединения (1,45 г). Полученную таким образом Вос-защищенную форму (1,0 г) растворяли в дихлорметане (10 мл) и охлаждали раствор до 0°C. Затем в раствор медленно добавляли трифторуксусную кислоту (10 мл) и перемешивали смесь в течение одного часа при указанной температуре. После завершения взаимодействия концентрировали реакционный раствор при пониженном давлении и получали трифторацетат титульного соединения (0,75 г). ЖХ/МС (ИЭР, пол.): 475 [М+Н]+.
[114] Пример 6. Получение соединения согласно примеру 6 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (vi) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43: на общей формуле (I) R1 = метальная группа, R2 = триметиленовая группа, R3 = ацетильная группа, R4 = производное сульфоксида (vi) или (vi'), R5 = изопропиламинокарбонилизопропиламиногруппа, Z = OTf, d+e+f+g+h+i+j = примерно 43, а = примерно 273)
Блоксополимер метоксиполиэтиленгликоля-полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 43; 0,82 г), полученный способом, описанным в патенте Японии JP 3268913 В2, и производное сульфоксида (vi) (0,79 г), полученное в справочном примере 7, растворяли в ДМФ (15 мл) при 35°C и затем в раствор добавляли диизопропилэтиламин (0,16 мл) и DMAP (25 мг). Температуру реакционного раствора доводили до 25°C, затем добавляли DIPC (0,64 мл) и перемешивали смесь в течение 17 часов при указанной температуре. Затем добавляли DIPC (0,16 мл) и перемешивали смесь еще 2 часа. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (15 мл), этанола (15 мл) и диизопропилового эфира (120 мл) и перемешивали смесь при комнатной температуре. Затем оставляли смесь отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Осажденный продукт собирали путем фильтрования и затем сушили при пониженном давлении, в результате чего получали полимерное производное сульфоксида (1,27 г). Полученное таким образом полимерное производное сульфоксида (1,2 г) растворяли в ДМФ (10 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (20 мг/мл, 20,5 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 23 часов при 25°C. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (30 мл), этанола (30 мл) и диизопропилового эфира (240 мл) и перемешивали смесь при комнатной температуре. Затем оставляли смесь отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Осажденный продукт собирали путем фильтрования и затем сушили при пониженном давлении, в результате чего получали неочищенную форму титульного соединения (1,47 г). Полученную таким образом неочищенную форму (0,73 г) очищали путем ультрафильтрации на центрифуге, VIVASPIN 20 (производства Sartorius AG, НОММ: 10 кДа), и лиофилизировали водный раствор, полученный после очистки. Таким образом получали титульное соединение (0,6 г). Содержание полученного таким образом лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 составляло 13,6% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 126 нм, титульное соединение образовывало мицеллы.
[115] Справочный пример 8. Синтез трет-бутил-(S)-(1-оксо-3-фенил-1-тиоморфолинопропан-2-ил)карбамата
N-Boc-L-фенилаланин (265 мг), тиоморфолин (104 мкл) и моногидрат 1-гидроксибензотриазола (161 мг) суспендировали в смешанном растворе этилацетата (5 мл) и воды (2 мл) и в суспензию, охлажденную во льду, добавляли WSC (220 мг). Перемешивали смесь в течение 1,5 часа. Смесь нагревали до комнатной температуры и дополнительно перемешивали в течение 3 часов. Реакционный раствор разбавляли этилацетатом (20 мл) и последовательно промывали органический слой 5% водным раствором лимонной кислоты, насыщенным водным раствором гидрокарбоната натрия, водой и насыщенным солевым раствором. Затем органический слой сушили над безводным сульфатом натрия. Удаляли сульфат натрия путем фильтрования и отгоняли растворитель при пониженном давлении. Полученный таким образом остаток очищали путем колоночной хроматографии на силикагеле (гексан/этилацетат = 8/2) и получали титульное соединение в виде белого твердого вещества (294 мг, 84%).
1Н ЯМР (CDCl2): δ 7,189-7,321 (5Н, m), 5,364 (1Н, d), 4,804 (1Н, dd), 3,839 (1Н, m), 3,749 (1Н, ddd), 3,518 (1Н, ddd), 3,388 (1Н, ddd), 2,972 (2Н, d), 2,546 (1Н, ddd), 2,353-2,450 (2Н, m), 1,836 (1Н, m), 1,420 (9Н, s).
ЖХ/МС, время удерживания: 6,5 минуты; m/z (ИЭР, пол.): 351 [М+Н]+
[116] Справочный пример 9. Синтез трет-бутил-(S)-(1-(1-оксидотиоморфолино)-1-оксо-3-фенилпропан-2-ил)карбамата
В раствор соединения, полученного в справочном примере 8 (149 мг), в дихлорметане (3 мл) по каплям, охлаждая во льду, добавляли раствор 3-хлорпербензойной кислоты (104 мг; содержал примерно 30% воды) в дихлорметане (1 мл) и перемешивали смесь в течение одного часа. После завершения взаимодействия разбавляли реакционный раствор этилацетатом (25 мл) и последовательно промывали органический слой насыщенным водным раствором гидрокарбоната натрия, водой и насыщенным солевым раствором и затем сушили над безводным сульфатом натрия. Удаляли сульфат натрия путем фильтрования и отгоняли растворитель при пониженном давлении. Полученный таким образом остаток очищали путем колоночной хроматографии на силикагеле (этилацетат/метанол = 8/2) и получали титульное соединение в виде бесцветного маслянистого вещества (147 мг, 94%, смесь стереоизомеров примерно 1:1).
1Н ЯМР (CDCl2): δ 7,172-7,327 (10Н, m), 5,314 (2Н, q), 4,772-4,893 (2Н, m), 4,500 (1H, m), 4,406 (1Н, dt), 3,902 (1Н, ddd), 3,564-3,682 (5Н, m), 2,921-3,096 (4Н, m), 2,471-2,761 (5Н, m), 2,174-2,332 (2Н, m), 1,446 (9Н, s), 1,412 (9Н, s), 0,888 (1H, m).
ЖХ/МС, время удерживания: 4,9 минуты; m/z (ИЭР, пол.): 367 [М+Н]+
[117] Справочный пример 10. Синтез гидрохлорида (S)-2-амино-1-(1-оксидотиоморфолино)-3-фенилпропан-1-она (производное сульфоксида (vii))
В раствор соединения, полученного в справочном примере 9 (58 мг), в этаноле (0,5 мл) добавляли, охлаждая во льду, 2н. раствор хлороводородная кислота/этанол (2 мл) и перемешивали смесь в течение 10 минут. Нагревали смесь до комнатной температуры и перемешивали в течение 1 часа 10 минут. Затем добавляли 2н. раствор хлороводородная кислота/этанол (2 мл) и перемешивали смесь еще 17 часов. Отгоняли растворитель при пониженном давлении и получали титульное соединение в виде белого твердого вещества (44 мг). Титульное соединение использовали для последующего взаимодействия без очистки. ЖХ/МС, время удерживания: 0,8 минуты; m/z (ИЭР, пол.): 267 [М+Н]+
[118] Пример 7. Получение соединения согласно примеру 7 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (vii) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиглутаминовой кислоты, имеющий степень полимеризации примерно 22: на общей формуле (VII) R11 = метальная группа, R19 = триметиленовая группа, R20 = ацетильная группа, R21 = производное сульфоксида (vii) или (vii'), R22 = изопропиламинокарбонилизопропиламиногруппа или сложный бензиловый эфир фенилаланина, Z = OTf, k+m+n = примерно 22, b = примерно 273)
Блоксополимер метоксиполиэтиленгликоля-полиглутаминовой кислоты (степень полимеризации глутаминовой кислоты: примерно 22; 229 мг), полученный способом, описанным в патенте Японии JP 4745664 В2, и производное сульфоксида (vii) (41 мг), полученное в справочном примере 10, растворяли в ДМФ (3,5 мл) при 35°C и затем в раствор добавляли DMAP (4,1 мг). Температуру реакционного раствора доводили до 25°C и затем в реакционный раствор добавляли диизопропилэтиламин (23 мкл) и DIPC (26 мкл). Через 3 часа добавляли гидрохлорид сложного бензилового эфира фенилаланина (59 мг), диизопропилэтиламин (35 мкл) и DIPC (26 мкл). Через 19 часов добавляли DIPC (52 мкл) и перемешивали смесь еще 2 часа. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (7 мл), этанола (7 мл) и диизопропилового эфира (56 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Кроме того, к остатку добавляли смешанный раствор этилацетата (4 мл), этанола (4 мл) и диизопропилового эфира (32 мл), перемешивали смесь при комнатной температуре и затем оставляли отстаиваться, удаляли надосадочную жидкость. Полученное таким образом осажденное вещество дополнительно промывали этилацетатом (2 мл), этанолом (2 мл) и диизопропиловый эфиром (16 мл) и собирали твердое вещество путем фильтрования (266 мг). Полученную таким образом неочищенную форму (255 мг) растворяли в ацетонитриле (5 мл) и воде (10 мл), затем в раствор добавляли ионообменную смолу (DOWEX 50 (Н+) производства Dow Chemical Company; 3 мл) и смесь перемешивали и фильтровали. Отгоняли ацетонитрил из полученного фильтрата при пониженном давлении и затем лиофилизировали остаток. Таким образом получали полимерное производное сульфоксида (248 мг). Полученное таким образом полимерное производное сульфоксида (235 мг) растворяли в ДМФ (0,5 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (20 мг/мл, 1,5 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 23 часов. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (2 мл), этанола (2 мл) и диизопропилового эфира (16 мл) и перемешивали смесь при комнатной температуре. Смесь оставляли отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Кроме того, к остатку добавляли смешанный раствор этилацетата (1 мл), этанола (1 мл) и диизопропилового эфира (8 мл), перемешивали смесь при комнатной температуре и затем оставляли отстаиваться, удаляли надосадочную жидкость. Полученное в результате осажденное вещество промывали смешанным раствором этилацетата (0,5 мл), этанола (0,5 мл) и диизопропилового эфира (4 мл) и собирали осажденное вещество путем фильтрования (248 мг). Полученную таким образом неочищенную форму (235 мг) растворяли в метаноле (0,5 мл) и воде (14,5 мл) и затем очищали раствор путем ультрафильтрации на центрифуге с использованием VIVASPIN 20 (производства Sartorius AG, НОММ: 10 кДа) и лиофилизировали. Таким образом получали титульное соединение (220 мг). Содержание полученного таким образом лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 составляло 8,8% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 28 нм, титульное соединение образовывало мицеллы.
[119] Пример 8. Получение соединения согласно примеру 8 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (viii) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиглутаминовой кислоты, имеющий степень полимеризации примерно 22: на общей формуле (VII) R11 = метальная группа, R19 = триметиленовая группа, R20 = ацетильная группа, R21 = производное сульфоксида (viii) или (viii'), R22 = изопропиламинокарбонилизопропиламиногруппа или сложный бензиловый эфир фенилаланина, k+m+n = примерно 22, b = примерно 273)
Блоксополимер метоксиполиэтиленгликоля-полиглутаминовой кислоты (степень полимеризации глутаминовой кислоты: примерно 22; 500 мг), синтезированный способом, описанным в патенте Японии JP 4745664 В2; 4-(фенилсульфинил)фенол (113 мг), синтезированный способом, описанным в J. Org. Chem., 2011, 76, 4635-4644; и гидрохлорид сложного бензилового эфира фенилаланина (65 мг) растворяли в ДМФ (12,5 мл) при 35°C и затем доводили температуру реакционного раствора до 25°C. В реакционный раствор добавляли DMAP (14 мг) и диизопропилэтиламин (0,042 мл), после чего добавляли DIPC (0,213 мл). Через 19 часов добавляли DIPC (0,213 мл) и перемешивали смесь в течение 3 часов. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (37,5 мл) и диизопропилового эфира (150 мл) и перемешивали смесь при комнатной температуре. Смесь оставляли отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Полученное таким образом осажденное вещество дополнительно промывали смесью этилацетат/диизопропиловый эфир (1/4 (об./об.); 50 мл) и собирали неочищенную форму путем фильтрования. Полученную таким образом неочищенную форму растворяли в 50% водном растворе ацетонитрила (12 мл), охлажденном до 0°C и затем в раствор добавляли ионообменную смолу (DOWEX 50 (Н+) производства Dow Chemical Company; 3 мл). Встряхивали смесь в течение 45 минут. После отделения ионообменной смолы путем фильтрования концентрировали фильтрат и лиофилизировали, в результате чего получали полимерное производное сульфоксида (586 мг). Полученное таким образом полимерное производное сульфоксида (500 мг) растворяли в ДМФ (5 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (20 мг/мл, 3,4 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 24 часов. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (25 мл) и диизопропилового эфира (100 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли отстаиваться до осаждения и выделения целевого продукта и собирали осажденное вещество путем фильтрования. Полученную таким образом неочищенную форму растворяли в смеси метанол/вода (4/9 (об./об.); 13 мл) и затем раствор обрабатывали путем ультрафильтрации на центрифуге с использованием VIVASPIN 20 (производства Sartorius, НОММ: 10 кДа) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, лиофилизировали, таким образом получали титульное соединение (434 мг). Содержание полученного таким образом лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 составляло 9,3% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 28 нм, титульное соединение образовывало мицеллы.
[120] Справочный пример 11. Синтез гидрохлорида 2-(4-(фенилсульфинил)фенокси)-этиламина (производное сульфоксида (ix))
4-(фенилсульфинил)фенол (200 мг), который синтезировали способом, описанным в J. Org. Chem., 2011, 76, 4635-4644, карбонат калия (190 мг) и йодид калия (228 мг) суспендировали в ДМФ (1,8 мл) и в суспензию добавляли 2-бром-N-Вос-этиламин (308 мг). Смесь перемешивали при 50°C. Через 25 часов в смесь добавляли 2-бром-N-Boc-этиламин (103 мг) и карбонат калия (63 мг) и перемешивали смесь еще 25 часов. После завершения взаимодействия добавляли дистиллированную воду и дихлорметан и трижды экстрагировали водный слой дихлорметаном. Полученный в результате органический слой промывали 1н. водным раствором гидроксида натрия и насыщенным солевым раствором и затем сушили органический слой путем добавления безводного сульфата натрия. Фильтровали органический слой и затем концентрировали и получали неочищенную форму. Полученную таким образом неочищенную форму очищали путем колоночной хроматографии на силикагеле (гексан : этилацетат = 4:1 → 1:2 (об./об.)), получали N-Boc-2-(4-(фенилсульфинил)фенокси)этиламин (300 мг). Полученный таким образом N-Boc-2-(4-(фенилсульфинил)фенокси)этиламин (273 мг) растворяли в этаноле (1,9 мл) и в раствор добавляли 2н. раствор хлороводородная кислота/этанол (5,7 мл) при 0°C. Затем перемешивали смесь в течение 24 часов. После завершения взаимодействия концентрировали реакционный раствор, таким образом получали титульное соединение (216 мг).
1Н ЯМР (D2O): δ 7,55-7,75 (7Н, m), 7,17 (2Н, d, J=8,8 Гц), 4,35 (2Н, t, J=4,9 Гц), 3,46 (2Н, t, J=4,9 Гц).
[121] Пример 9. Получение соединения согласно примеру 9 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (ix) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43: на общей формуле (I) R1 = метальная группа, R2 = триметиленовая группа, R3 = ацетильная группа, R4 = производное сульфоксида (ix) или (ix'), R5 = изопропиламинокарбонилизопропиламиногруппа или сложный бензиловый эфир фенилаланина, d+e+f+g+h+i+j = примерно 43, а = примерно 273)
Блоксополимер метоксиполиэтиленгликоля-полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 43; 80 мг), синтезированный способом, описанным в патенте Японии JP 3268913 В2, гидрохлорид 2-(4-(фенилсульфинил)фенокси)этиламина (40 мг), описанный в справочном примере 11, и гидрохлорид сложного бензилового эфира фенилаланина (18 мг) растворяли в ДМФ (2 мл) при 35°C и затем доводили температуру реакционного раствора до 20°C. В реакционный раствор добавляли моногидрат 1-гидроксибензотриазола (34 мг) и диизопропилэтиламин (0,039 мл) и затем добавляли DIPC (0,058 мл). Смесь перемешивали в течение 25 часов. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этанола (8 мл) и диизопропилового эфира (32 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Полученный таким образом осажденный продукт дополнительно промывали смесью этанол/диизопропиловый эфир (1/4 (об./об.); 10 мл) и собирали неочищенную форму путем фильтрования. Полученную таким образом неочищенную форму растворяли в 50% водном растворе ацетонитрила (6 мл), охлажденном до 0°C, и затем в раствор добавляли ионообменную смолу (DOWEX 50 (Н+) производства Dow Chemical Company; 1 мл). Смесь встряхивали в течение одного часа. После отделения ионообменной смолы путем фильтрования концентрировали фильтрат и лиофилизировали, таким образом получали полимерное производное сульфоксида (111 мг). Полученное таким образом полимерное производное сульфоксида (88 мг) растворяли в ДМФ (0,9 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (20 мг/мл, 0,8 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 24 часов. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (5 мл) и диизопропилового эфира (20 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли отстаиваться до осаждения и выделения целевого продукта и собирали осажденный продукт путем фильтрования. Полученную таким образом неочищенную форму растворяли в смеси метанол/вода (2/7 (об./об.); 9 мл) и затем раствор обрабатывали путем ультрафильтрации на центрифуге с использованием VIVASPIN 20 (производства Sartorius AG, НОММ: 10 кДа) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, лиофилизировали, в результате чего получали титульное соединение (85 мг). Содержание полученного таким образом лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 составляло 11,3% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 28 нм, титульное соединение образовывало мицеллы.
[122] Пример 10. Получение соединения согласно примеру 10 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (viii) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 2000, и фрагмент полиглутаминовой кислоты, имеющий степень полимеризации примерно 8: на общей формуле (VII) R11 = метальная группа, R19 = триметиленовая группа, R20 = ацетильная группа, R21 = производное сульфоксида (viii) или (viii'), R22 = изопропиламинокарбонилизопропиламиногруппа или сложный бензиловый эфир фенилаланина, k+m+n = примерно 8, b = примерно 46)
Блоксополимер метоксиполиэтиленгликоля-полиглутаминовой кислоты (степень полимеризации глутаминовой кислоты: примерно 8; 600 мг), синтезированный согласно способу, описанному в патенте Японии JP 4745664 В2; 4-(фенилсульфинил)фенол (203 мг), синтезированный способом, описанным в J. Org. Chem., 2011, 76, 4635-4644; и гидрохлорид сложного бензилового эфира фенилаланина (181 мг) растворяли в ДМФ (18 мл) при 35°C и затем доводили температуру реакционного раствора до 25°C. В реакционный раствор добавляли DMAP (28 мг) и диизопропилэтиламин (0,118 мл) и затем добавляли DIPC (0,477 мл). Через 15,5 часа добавляли DIPC (0,477 мл) и смесь дополнительно перемешивали в течение 5 часов. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (18 мл) и диизопропилового эфира (162 мл) и перемешивали смесь при комнатной температуре. Смесь оставляли отстаиваться до осаждения и выделения продукта, удаляли надосадочную жидкость. Полученный таким образом осадок дополнительно дважды промывали диизопропиловым эфиром (180 мл) и сушили при пониженном давлении, в результате получали полимерное производное сульфоксида (953 мг). Полученное таким образом полимерное производное сульфоксида (953 мг) растворяли в диметилформамиде (10,9 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (20 мг/мл, 12,1 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 23 часов. После завершения взаимодействия реакционный раствор медленно добавляли в раствор диизопропилового эфира (230 мл) и перемешивали смесь при комнатной температуре. Смесь оставляли отстаиваться до осаждения целевого продукта, удаляли надосадочную жидкость. Полученный в результате осадок дополнительно дважды промывали диизопропиловым эфиром (230 мл) и сушили при пониженном давлении. Полученную таким образом неочищенную форму растворяли в воде (60 мл) и затем осаждали твердое вещество на центрифуге. Надосадочную жидкость обрабатывали путем ультрафильтрации на центрифуге с использованием VIVASPIN 20 (производства Sartorius AG, НОММ: 3 кДа) и удаляли низкомолекулярные соединения. В раствор, полученный после очистки, добавляли водный раствор мальтозы (40 мг/мл, 67,5 ммоль) и водный раствор Macrogol 4000 (20 мг/мл, 67,5 мл) и лиофилизировали смесь. В результате получали композицию, содержащую титульное соединение (4,62 г). Содержание лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 в композиции составляло 1,2% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 18 нм, титульное соединение образовывало мицеллы.
[123] Пример 11. Получение соединения согласно примеру 11 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (х) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43: на общей формуле (I) R1 = метальная группа, R2 = триметиленовая группа, R3 = ацетильная группа, R4 = производное сульфоксида (х) или (х'), R5 = изопропиламинокарбонилизопропиламиногруппа, d+e+f+g+h+i+j = примерно 43, а = примерно 273)
Блоксополимер (800 мг), содержащий фрагмент метоксиполиэтиленгликоля и фрагмент, имеющий структуру, на которой сложный эфир 4-(фенил-1-бутанола) и аланина-аспарагиновой кислоты связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, полученный способом, описанным в WO 2010/131675, и сульфоксид тиоксантенола (152 мг), синтезированный способом, описанным в непатентной литературе (Tetrahedron Letters, 2010, 51, 6939-6941, и J. Org. Chem., 1967, 32, 3814-3817), растворяли в ДМФ (10 мл) при 35°C и затем в раствор добавляли DMAP (13 мг). Температуру реакционного раствора доводили до 25°C и затем добавляли DIPC (0,227 мл). Через 23 часа добавляли DIPC (0,070 мл) и перемешивали смесь еще один час. После завершения взаимодействия реакционный раствор медленно добавляли в диизопропиловый эфир (160 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Полученный таким образом осажденный продукт собирали путем фильтрования и затем сушили при пониженном давлении. Таким образом получали полимерное производное сульфоксида (784 мг). Полученное таким образом полимерное производное сульфоксида (750 мг) растворяли в ДМФ (5 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (20 мг/мл, 9,3 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 24 часов. После завершения взаимодействия реакционный раствор медленно добавляли в смешанный раствор этилацетата (15 мл), этанола (15 мл) и диизопропилового эфира (120 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли отстаиваться до осаждения и выделения целевого продукта, осажденный продукт собирали путем фильтрования. Полученную таким образом неочищенную форму растворяли в смеси метанол/вода (1/8 (об./об.); 36 мл) и затем раствор обрабатывали путем ультрафильтрации на центрифуге с использованием VIVASPIN TURBO 15 (производства Sartorius AG, НОММ: 10 кДа) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, лиофилизировали, в результате получали титульное соединение (716 мг). Содержание полученного таким образом лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 составляло 10,5% (массовая доля). Кроме того, титульное соединение растворяли в очищенной воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 80 нм, титульное соединение образовывало мицеллы.
[124] Пример 12. Получение соединения согласно примеру 12 (конъюгат полимерного производного сульфоксида и комплекса платины, полученный путем встраивания производного сульфоксида (х) в блоксополимер, содержащий фрагмент метоксиполиэтиленгликоля, имеющий молекулярную массу 2000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 12: на общей формуле (I) R1 = метальная группа, R2 = триметиленовая группа, R3 = ацетильная группа, R4 = производное сульфоксида (х) или (х'), R5 = изопропиламинокарбонилизопропиламиногруппа, d+e+f+g+h+i+j = примерно 12, а = примерно 46)
Блоксополимер (700 мг), содержащий фрагмент метоксиполиэтиленгликоля и фрагмент, имеющий структуру, на которой сложный эфир (4-фенил-1-бутанола) и аспарагиновой кислоты-аланина связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, полученный способом, описанным в WO 2010/131675, и сульфоксид тиоксантенола(183 мг), синтезированный способом, описанным в непатентной литературе (Tetrahedron Letters, 2010, 51, 6939-6941, и J. Org. Chem., 1967, 32, 3814-3817), растворяли в ДМФ (9 мл) при 35°C и затем в раствор добавляли DMAP (16 мг). Температуру реакционного раствора доводили до 25°C и затем в реакционный раствор добавляли DIPC (0,344 мл). Через 24 часа добавляли DIPC (0,084 мл) и перемешивали смесь еще один час. После завершения взаимодействия смесь медленно добавляли в диизопропиловый эфир (300 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли отстаиваться до осаждения и выделения целевого продукта, удаляли надосадочную жидкость. Полученный в результате осажденный продукт собирали путем фильтрования и затем сушили при пониженном давлении. Таким образом получали полимерное производное сульфоксида (641 мг). Полученное таким образом полимерное производное сульфоксида (620 мг) растворяли в ДМФ (5 мл) при 35°C и затем охлаждали раствор до 25°C. Затем в полученный раствор добавляли раствор Pt(R,R-dach)Cl(OTf) (20 мг/мл, 7 мл), полученный способом, описанным в справочном примере 2, и перемешивали смесь в течение 24 часов. После завершения взаимодействия смесь медленно добавляли в диизопропиловый эфир (130 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли отстаиваться до осаждения и выделения целевого продукта, осажденный продукт собирали путем фильтрования. Полученную в результате неочищенную форму растворяли в смеси ацетонитрил/вода (1/19 (об./об.); 36 мл) и затем раствор обрабатывали путем ультрафильтрации на центрифуге с использованием VIVASPIN TURBO 15 (производства Sartorius AG, НОММ: 10 кДа) для удаления низкомолекулярных соединений. В полученный в результате водный раствор добавляли дигидрат трегалозы (2,4 г) и Macrogol 4000 (1,2 г) и лиофилизировали смесь. В результате получали смесь (3,8 г) титульного соединения, трегалозы и Macrogol 4000. Содержание лекарственного соединения в пересчете на Pt(R,R-dach)Cl2 в композиции составляло 0,85% (массовая доля).
[125] Пример исследования 1. Поверхностный заряд и размер частиц соединений, предложенных в примерах
Каждое из соединений, предложенных в примерах, растворяли в очищенной воде до концентрации 1 мг/мл и измеряли дзета-потенциал (поверхностный заряд) и размер частиц. Результаты приведены в таблице 1.
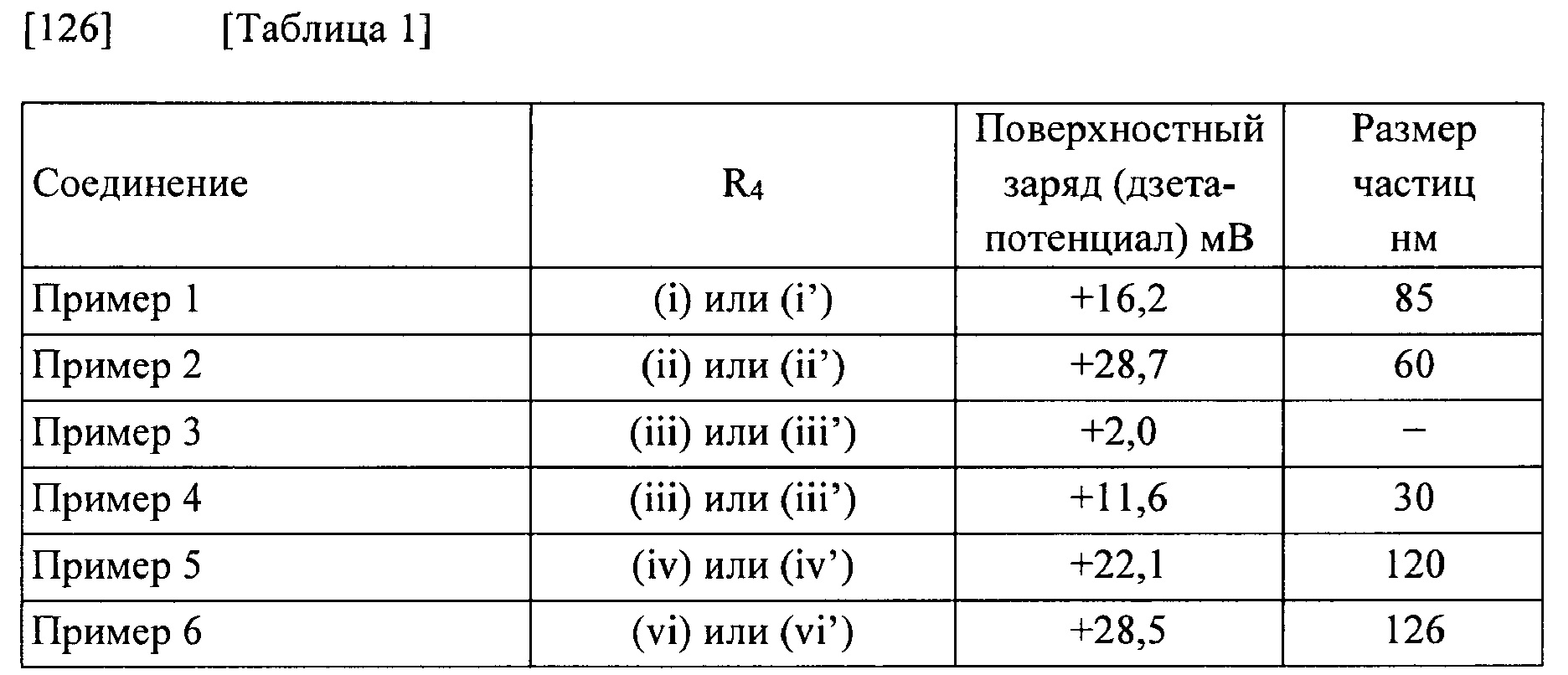

[127] Было подтверждено, что различные исследуемые соединения, предложенные в примерах, имели положительный (плюсовой) поверхностный заряд (дзета-потенциал). Кроме того, на основании результатов измерения размера частиц было сделано предположение, что все соединения, предложенные в примерах, за исключением примера 3, образовывали мицеллы с размером в нано-диапазоне.
[128] Пример исследования 2. Зависимость концентрация/время для ингибирующего действия в отношении пролиферации клеток DAN-G
<Клетки>
Клеточную линию рака поджелудочной железы человека, DAN-G, приобретали в Asta Medica GmbH, пролиферацию и пересев клеток проводили в рекомендованной среде, описанной в пояснительной брошюре.
<Исследование подавления пролиферации>
Из клеток DAN-G, которые выращивали и размножали в 10 см чашке для клеточных культур, удаляли питательную среду и промывали клетки один раз 5 мл ФБР (фосфатный буферный физиологический солевой раствор). Затем в клетки добавляли 1 мл смеси 0,25% трипсина/0,05% ЭДТА (этилендиаминтетрауксусная кислота)/ФБР и смесь оставляли отстаиваться на 5 минут при 37°C. После того, как было подтверждено, что клетки отставали от чашки, в чашку добавляли 9 мл среды для диспергирования клеток, дисперсию переносили в 15 мл пробирку (Corning, Inc.) и центрифугировали дисперсию в течение 5 минут при 1000 об./мин. Удаляли надосадочную жидкость, затем в пробирку добавляли 10 мл свежей среды и суспендировали клетки. Часть клеток окрашивали трипановым синим, количество жизнеспособных клеток измеряли на гемоцитометре. Суспендированные клетки разбавляли средой до концентрации 2,6×104 клеток/мл и инокулировали клетки в пять пластов в 96-луночных планшетах (планшеты А, В, С, D и Е) в объеме 190 мкл/лунка (5×103 клеток/лунка).
Клетки выращивали в течение ночи и затем в клетки добавляли 10 мкл/лунка соединения согласно примеру 1, растворенного в 5% растворе глюкозы, в концентрации (концентрация лекарственного соединения в пересчете на DACH-платину) 0, 0,024, 0,098, 0,39, 1,56, 6,25, 25 или 100 мкМ. Затем клетки выращивали при 37°C и 5% CO2. Каждую концентрацию исследовали в трех повторностях.
[129] Исследование проводили в пяти различных условиях, изменяя время добавления лекарственного средства.
В планшете А среду удаляли через 2 часа после добавления лекарственного средства, клетки трижды промывали 200 мкл среды, в планшет добавляли свежую среду, не содержащую лекарственное средство, в объеме 200 мкл/лунка и клетки дополнительно выращивали в течение 70 часов при 37°C и 5% CO2.
В планшете В среду удаляли через 6 часов после добавления лекарственного средства, клетки трижды промывали 200 мкл среды, в планшет добавляли свежую среду, не содержащую лекарственное средство, в объеме 200 мкл/лунка и клетки дополнительно выращивали в течение 66 часов при 37°C и 5% СО2.
В планшете С среду удаляли через 24 часа после добавления лекарственного средства, клетки трижды промывали 200 мкл среды, в планшет добавляли свежую среду, не содержащую лекарственное средство, в объеме 200 мкл/лунка и клетки дополнительно выращивали в течение 48 часов при 37°C и 5% СО2.
В планшете D среду удаляли через 48 часов после добавления лекарственного средства, клетки трижды промывали 200 мкл среды, в планшет добавляли свежую среду, не содержащую лекарственное средство, в объеме 200 мкл/лунка и клетки дополнительно выращивали в течение 24 часов при 37°C и 5% CO2.
В планшете Е среду удаляли через 72 часа после добавления лекарственного средства, клетки трижды промывали 200 мкл среды, в планшет добавляли свежую среду, не содержащую лекарственное средство, в объеме 200 мкл/лунка и немедленно проводили процедуру окрашивания, такую как описано ниже.
[130] В планшетах А, В, С, D и Е, в которых клетки выращивали в течение 72 часов, как описано выше, удаляли среду, затем в планшеты добавляли метанол, в результате клетки были иммобилизованы на планшетах. После удаления метанола в планшеты добавляли 0,05% раствор метиленового синего и клетки окрашивали в течение 30 минут. Удаляли метиленовый синий, избыток раствора красителя промывали водой, затем в планшеты добавляли 3% хлороводородную кислоту в объеме 200 мкл/лунка, таким образом экстрагировали метиленовый синий. Планшеты оставляли отстаиваться на 2 часа или дольше и измеряли поглощение при 660 нм на анализаторе микропланшетов (BENCHMARK PLUS производства Bio-Rad Laboratories, Inc.). Что касается измеренных значений, то брали среднее значение по трем лункам для каждой концентрации лекарственного средства. Относительное подавление пролиферации GI(x)% при концентрации лекарственного средства х вычисляли при помощи следующей формулы на основании измеренных значений поглощения.
GI(x)%=(1-(Ах-В)/(А0-В))×100
Ах представляет собой поглощение в лунках, содержащих лекарственное средство в концентрации х; А0 представляет собой поглощение в контрольных лунках с растворителем, в который не добавляли лекарственное средство; и В представляет собой поглощение в пустых лунках, которые не содержали клетки или лекарственное средство.
Схожее исследование также проводили для соединения согласно примеру 2 и 1-ОНР. Значения IC50 (концентрация лекарственного средства, при которой значение GI% равно 50%) для различных лекарственных средств приведены в таблице 2.
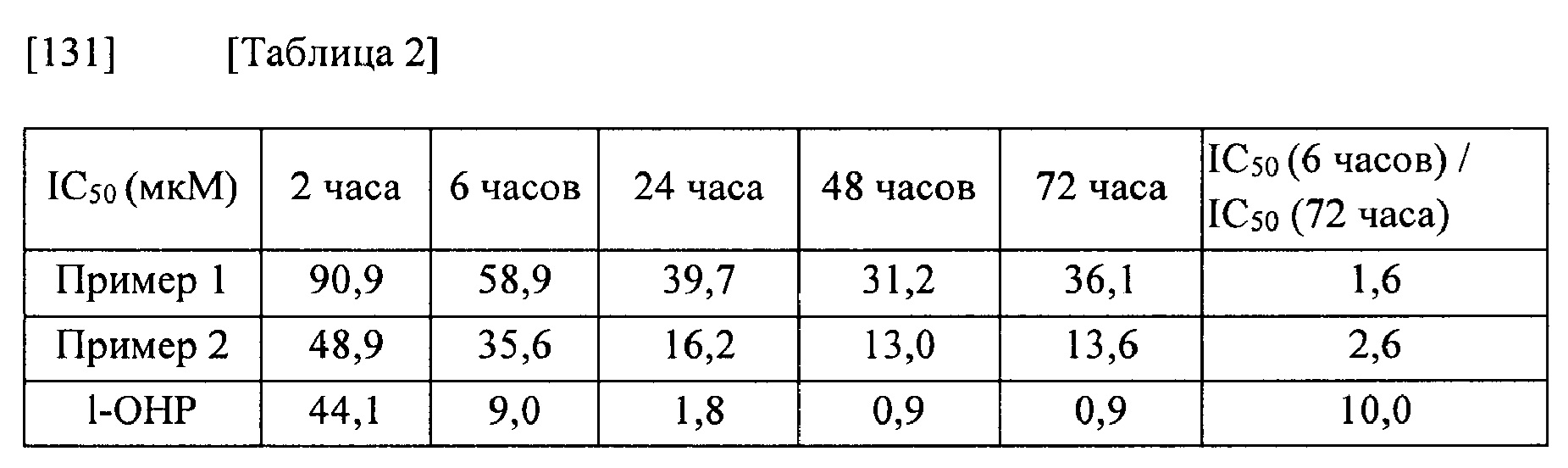
[132] Значение IC50 (6 часов) / IC50 (72 часа) для 1-ОНР составляло 10,0, это указывает на то, что при увеличении продолжительности действия лекарственного средства значение IC50 значительно уменьшалось. При этом значения IC50 (6 часов) / IC50 (72 часа) для соединения согласно примеру 1 и соединения согласно примеру 2 составляли 1,6 и 2,6, соответственно. Таким образом, даже при увеличении продолжительности действия лекарственного средства значения IC50 изменяли незначительно.
[133] На основании результатов примеров исследования 1 и 2, описанных выше, было сделано предположение о том, что, так как конъюгат комплекса платины, в котором полимерное производное сульфоксида образует координационные связи с платиной, имеет положительный заряд, то для конъюгата не требуется продолжительное время действия, конъюгат быстро поглощается клетками, в результате чего конъюгат обладает эффективным действием.
[134] Пример исследования 3. Противоопухолевое действие у мышей, которым трансплантировали клетки рака желудка человека 4-1ST
[135] <Животные и трансплантация опухоли>
Клетки рака желудка человека 4-1ST пересевали и выращивали под кожей мышей BALB/cA-nu/nu (далее бестимусные мыши). Клетки рака желудка человека 4-1ST проиобретали в Центральном институте экспериментальных животных.
[136] <Исследование противоопухолевого действия 1>
Клетки рака желудка 4-1ST собирали из участков под кожей бестимусных мышей, и опухоли тонко нарезали на блоки со стороной примерно 3 мм. Полученные в результате блоки опухолей подкожно трансплантировали в спину бестимусных мышей при помощи троакара. На 18й день после трансплантации, когда средний размер опухоли достигал примерно 100-200 мм3, внутривенно вводили различные лекарственные средства через хвостовую вену. Подготовку доз и введение различных лекарственных средств проводили следующим образом: соединение согласно примеру 1 растворяли в 5% растворе глюкозы для инъекций и раствор вводили один раз в дозах 75 мг/кг и 150 мг/кг. Соединение согласно примеру 2 растворяли в 5% растворе глюкозы для инъекций и раствор вводили один раз в дозах 75 мг/кг и 150 мг/кг. В качестве контрольных лекарственных средств 1-ОНР вводили один раз в дозе 20 мг/кг и цисплатин вводили один раз в дозе 10 мг/кг. Что касается количества вводимых 1-ОНР и цисплатина и высокого количества вводимых соединений согласно различным примерам, то во всех случаях вводили максимальную переносимую дозу (МПД дозу).
После введения различных лекарственных средств измеряли размеры опухолей по большой оси (L) и малой оси (W) в различные моменты времени при помощи штангенциркулей, вычисляли объем опухоли (L × W × W × 0,5). Исследование проводили с использованием четырех животных в группе во всех случаях в группе, в которой лекарственное средство не вводили, и в различных группах, в которых вводили лекарственные средства. В течение периода времени, начиная от первого введения до 20 го дня после введения в качестве показателя противоопухолевого действия вычисляли относительный объем опухоли (Т/С (%)) в каждой группе, в которой вводили лекарственное средство, при помощи следующей формулы, принимая относительный объем опухоли в группе, в которой не вводили лекарственное средство, за 100. Значения Т/С (%) в различных группах, в которых вводили лекарственное средство, приведены в таблице 3.
Формула: Т/С (%) = Относительный объем опухоли в группе, в которой вводили лекарственное средство / относительный объем опухоли в группе, в которой не вводили лекарственное средство × 100
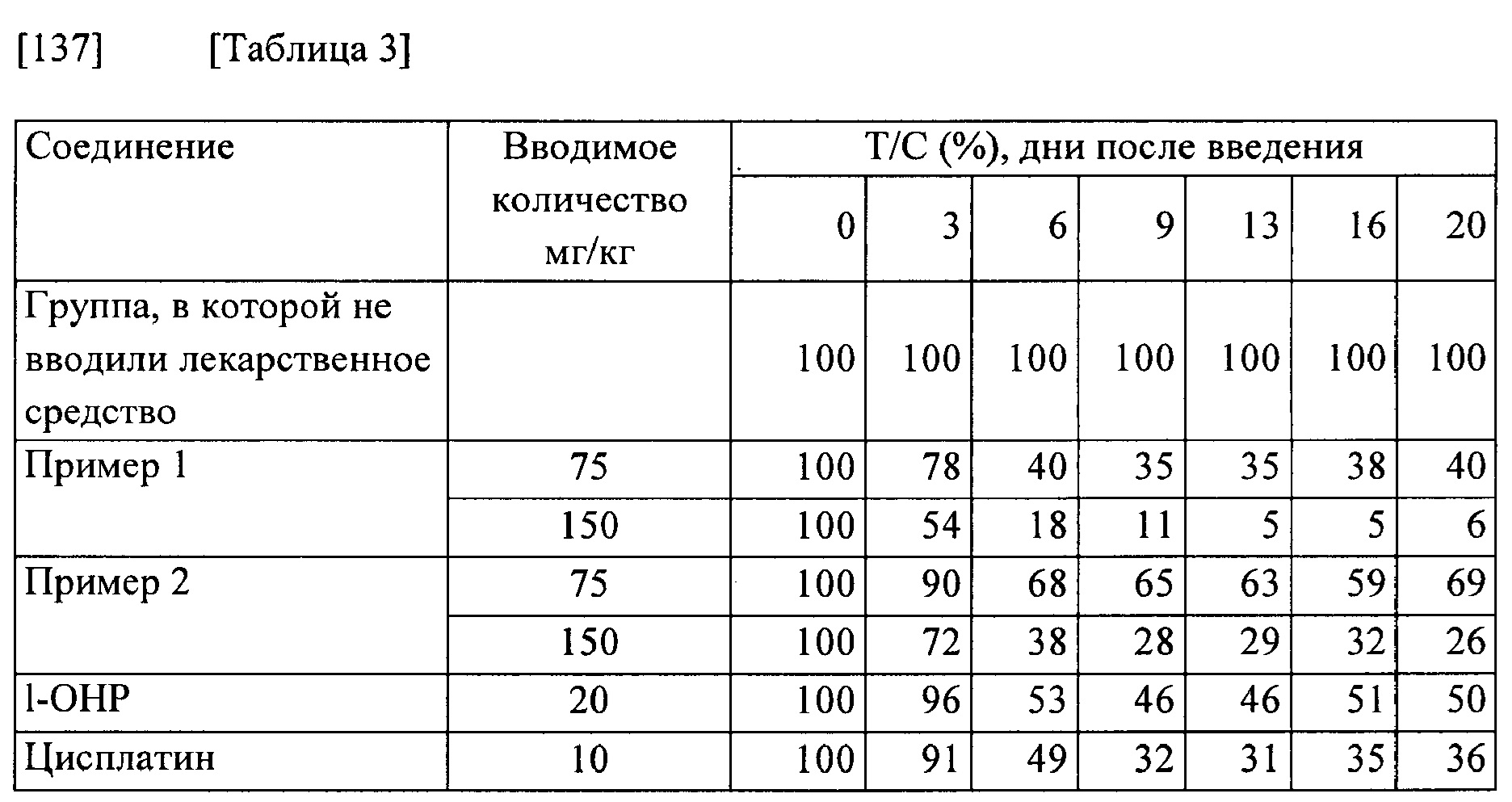
[138] <Исследование противоопухолевого действия 2>
Клетки рака желудка 4-1ST собирали из участков под кожей бестимусных мышей, и опухоли тонко нарезали на блоки со стороной примерно 3 мм. Полученные в результате блоки опухолей подкожно трансплантировали в спину бестимусных мышей при помощи троакара. На 18й день после трансплантации, когда средний размер опухоли достигал примерно 100-200 мм3, внутривенно вводили различные лекарственные средства через хвостовую вену. Подготовку доз и введение различных лекарственных средств проводили следующим образом: соединение согласно примеру 3 растворяли в 5% растворе глюкозы для инъекций и раствор вводили один раз в дозах 75 мг/кг и 150 мг/кг. Соединение согласно примеру 4 растворяли в 5% растворе глюкозы для инъекций и раствор вводили один раз в дозах 100 мг/кг и 200 мг/кг. В качестве контрольного лекарственного средства 1-ОНР вводили один раз в дозе 18 мг/кг. Что касается высоких вводимых количеств 1-ОНР и соединения согласно примеру 4, то в обоих случаях применяли максимальную переносимую дозу (МПД доза). Что касается соединения согласно примеру 3, то доза была равна МПД дозе или была ниже нее; тем не менее, вводимое количество соответствовало пределу растворимости. После введения различных лекарственных средств измеряли размеры опухолей по большой оси (L) и малой оси (W) в различные моменты времени при помощи штангенциркулей, вычисляли объем опухоли (L × W × W × 0,5). Исследование проводили с использованием четырех животных в группе во всех случаях в группе, в которой лекарственное средство не вводили, и в различных группах, в которых вводили лекарственные средства. Значения Т/С (%) для периода времени, начиная от первого введения до 21го дня после введения, в различных группах, в которых вводили лекарственное средство, приведены в таблице 4.
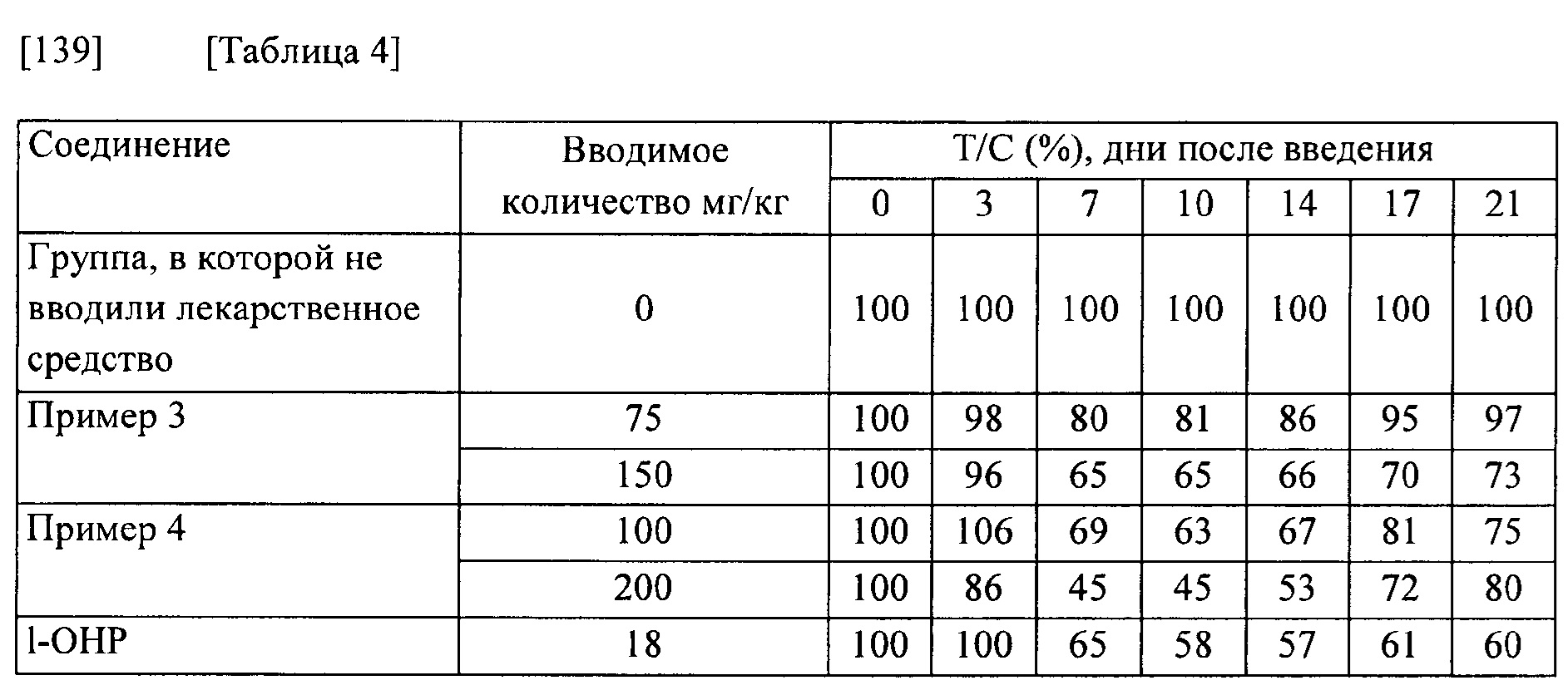
[140] Согласно результатам, описанным выше, соединение согласно примеру 1 и соединение согласно примеру 2, обладали улучшенным противоопухолевым действием по сравнению с 1-ОНР. В частности, соединение согласно примеру 1 имело противоопухолевое действие, равное или превосходящее 1-ОНР, даже в низких дозах, и при высоких дозах наблюдали значительное уменьшение опухолей. Соединение согласно примеру 3 и соединение согласно примеру 4 обладали таким же противоопухолевым действием, что и 1-ОНР.
[141] <Исследование противоопухолевого действия 3>
Клетки рака желудка 4-1ST собирали из участков под кожей бестимусных мышей, и опухоли тонко нарезали на блоки со стороной примерно 3 мм. Полученные в результате блоки опухолей подкожно трансплантировали в спину бестимусных мышей при помощи троакара. На 17й день после трансплантации, когда средний размер опухоли достигал примерно 100-200 мм3, внутривенно вводили различные лекарственные средства через хвостовую вену. Подготовку доз и введение различных лекарственных средств проводили следующим образом: соединение согласно примеру 6 растворяли в 5% растворе глюкозы для инъекций и раствор вводили один раз в дозах 12,5 мг/кг и 25 мг/кг. Соединение согласно примеру 11 растворяли в 5% растворе глюкозы для инъекций и раствор вводили один раз в дозах 5 мг/кг и 10 мг/кг. В качестве контрольного лекарственного средства 1-ОНР или цисплатин (CDDP) вводили один раз в дозе 18 мг/кг или 10 мг/кг. Что касается высоких вводимых количеств соединений, то во всех случаях применяли максимальную переносимую дозу (МПД доза). После введения различных лекарственных средств измеряли размеры опухолей по большой оси (L) и малой оси (W) в различные моменты времени при помощи штангенциркулей, вычисляли объем опухоли (L × W × W × 0,5). Исследование проводили с использованием четырех животных в группе во всех случаях в группе, в которой лекарственное средство не вводили, и в различных группах, в которых вводили лекарственные средства. Значения Т/С (%) для периода времени, начиная от первого введения до 21го дня после введения, в различных группах, в которых вводили лекарственное средство, приведены в таблице 5.
После введения измеряли массу тела мышей в различные моменты времени. Относительное изменение массы тела по сравнению с массой тела в день начала введения, которую принимали за 1, для периода, начиная от первого введения до 21го дня после введения, приведено в таблице 6.
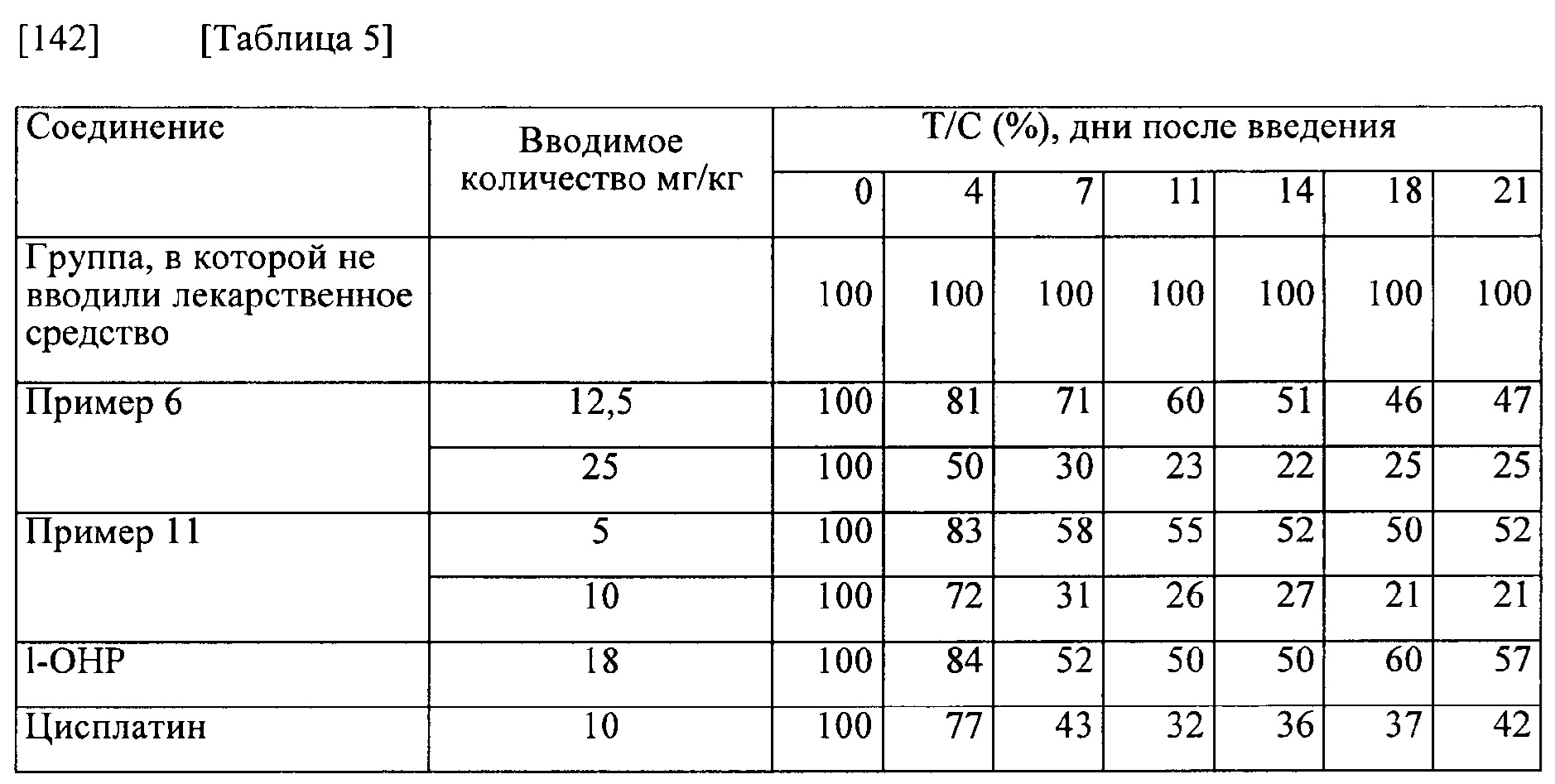
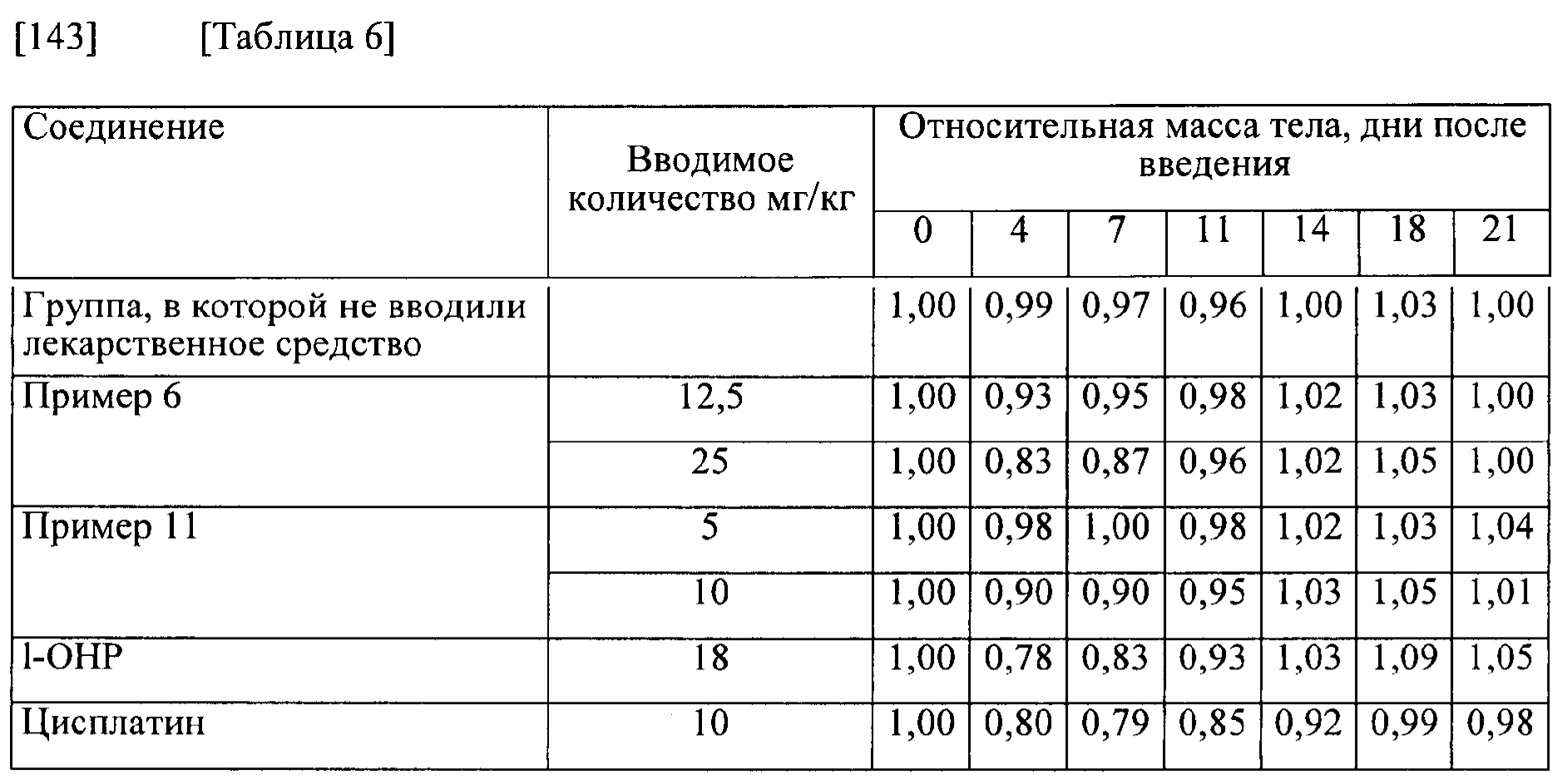
[144] Согласно результатам, описанным выше, соединение согласно примеру 6 и соединение согласно примеру 11 обладали противоопухолевым действием, значительно превосходящим 1-ОНР, и противоопухолевым действием, схожим с действием цисплатина или превышающим его, в МПД дозах. Кроме того, в дозах, равных 50% МПД, соединения, предложенные в примерах, сохраняли противоопухолевое действие, схожее с 1-ОНР или превышающее его. При этом, уменьшение массы тела на 4й день после введения в случае соединения согласно примеру 6 и соединения согласно примеру 11 было незначительным по сравнению с 1-ОНР и цисплатином, было показано, что побочные эффекты уменьшались.
Согласно результатам исследований противоопухолевого действия, описанным выше, было показано, что полимерные конъюгаты комплексов платины (II), в которых производное сульфоксида встроено по карбоксильной группе боковой цепи в блоксополимер, содержащий структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, и сульфоксидная группа образует координационные связи, обладают противоопухолевым действием, превосходящим 1-ОНР.
Реферат
Настоящее изобретение относится к полимерному конъюгату комплекса платины (II), а также к способу его получения. Полимерный конъюгат содержит блоксополимер, содержащий структурный фрагмент полиэтиленгликоля и фрагмент полиаспарагиновой или полиглутаминовой кислоты, производное сульфоксида, встроенное по карбоксильной группе боковой цепи в блоксополимер, и комплекс платины (II), образующий координационные связи с сульфоксидной группой производного сульфоксида. Комплекс платины (II) представляет собой цис-координированный комплекс. Полученный полимерный конъюгат относится к системе доставки лекарственных средств (препарат DDS) для комплекса платины и обладает повышенным противоопухолевым действием в качестве лекарственного средства и пониженными побочными эффектами. 2 н. и 1 з.п. ф-лы, 6 табл., 11 пр.
Формула
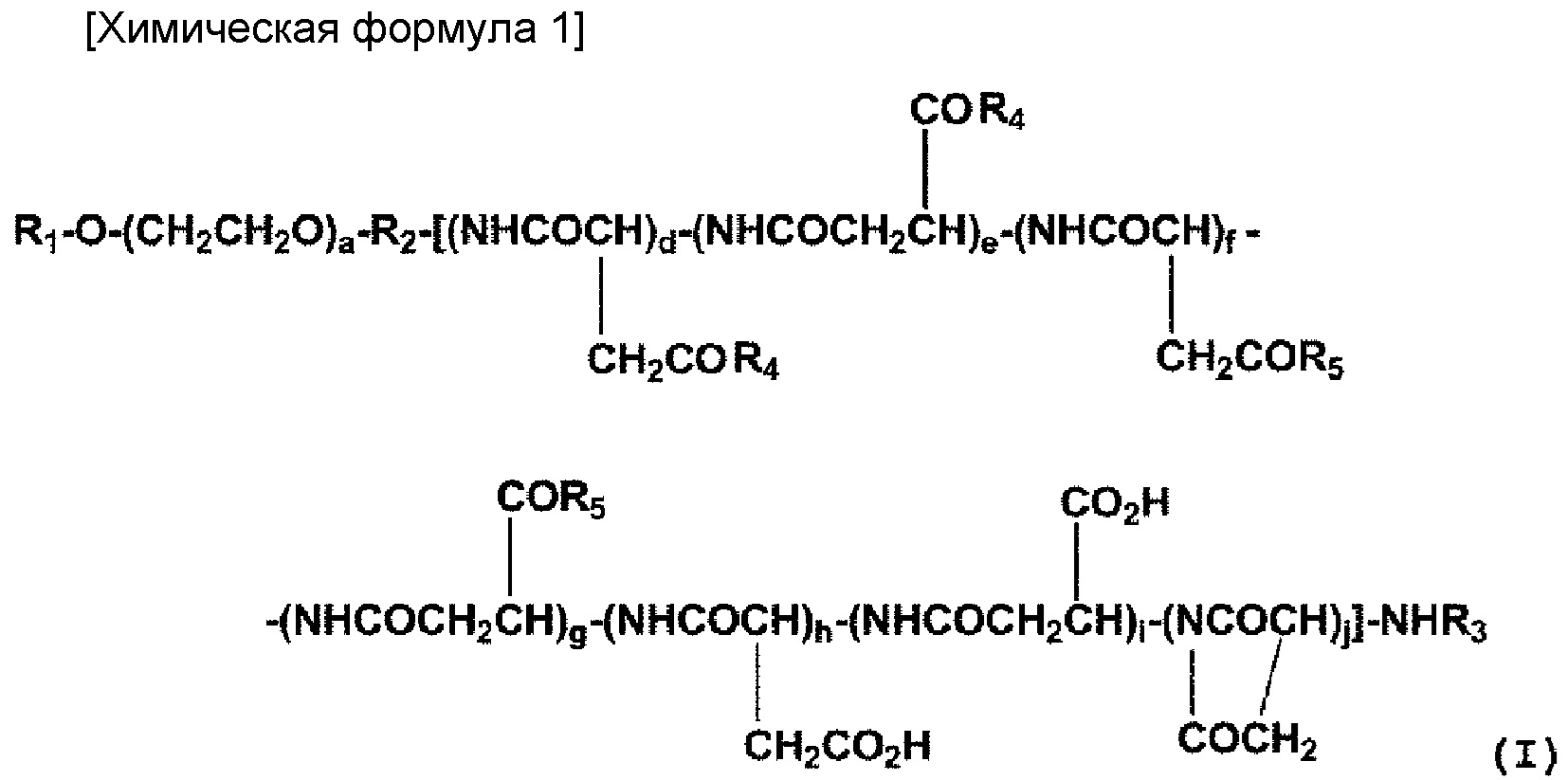
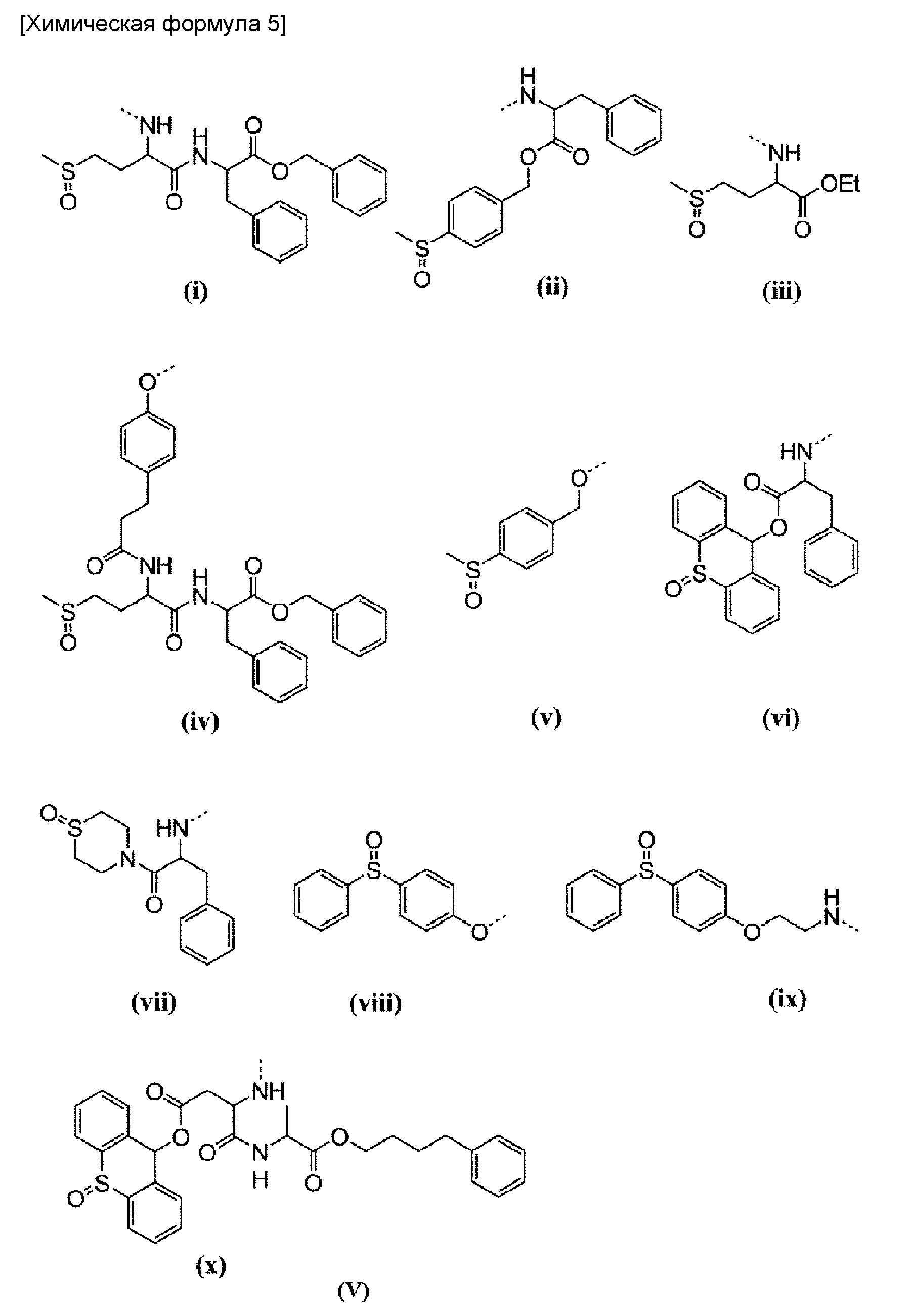
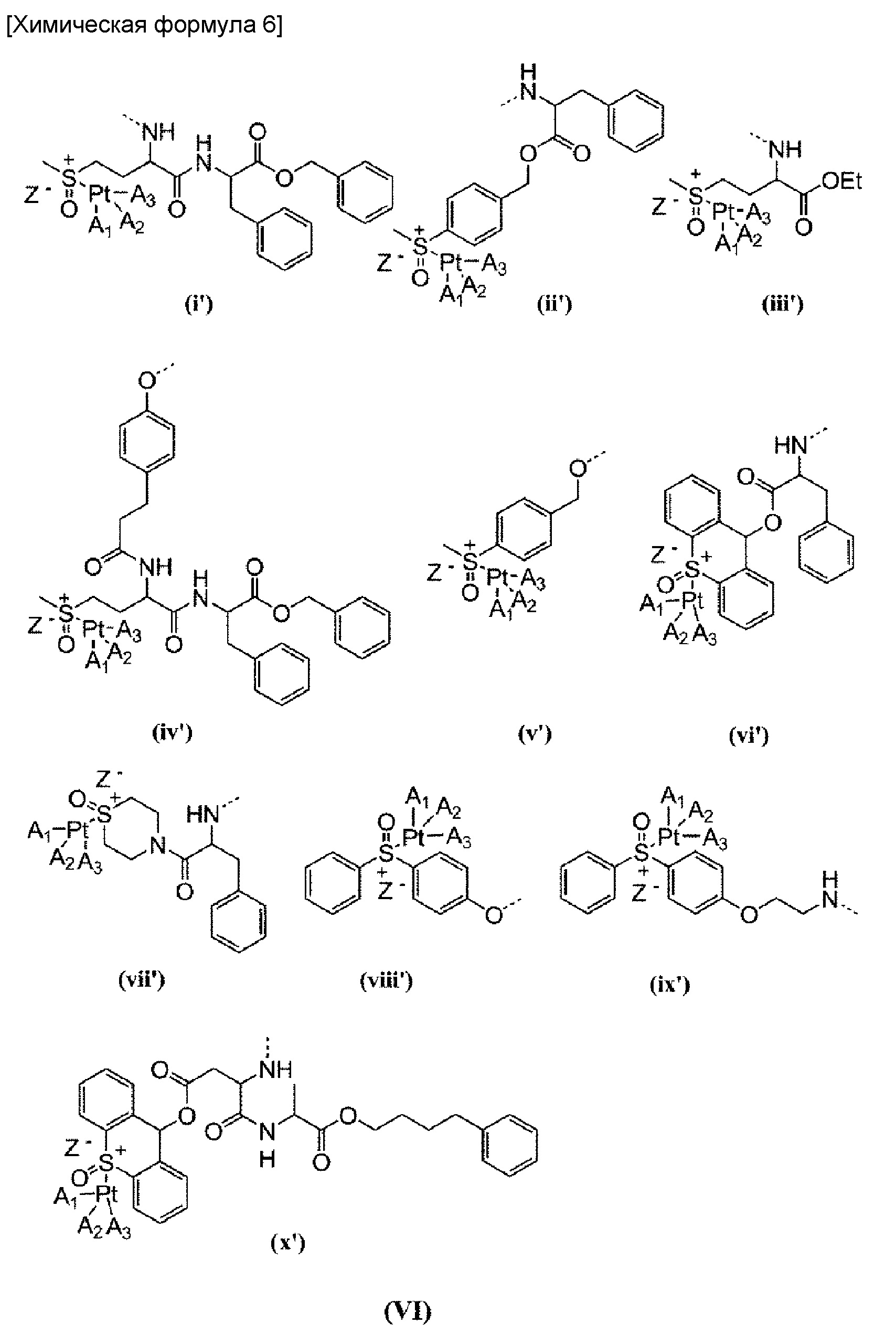
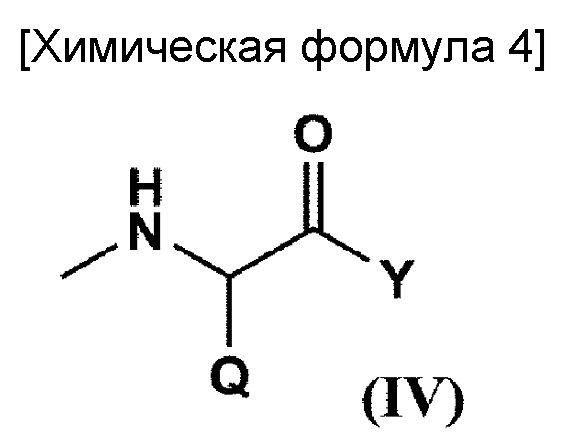
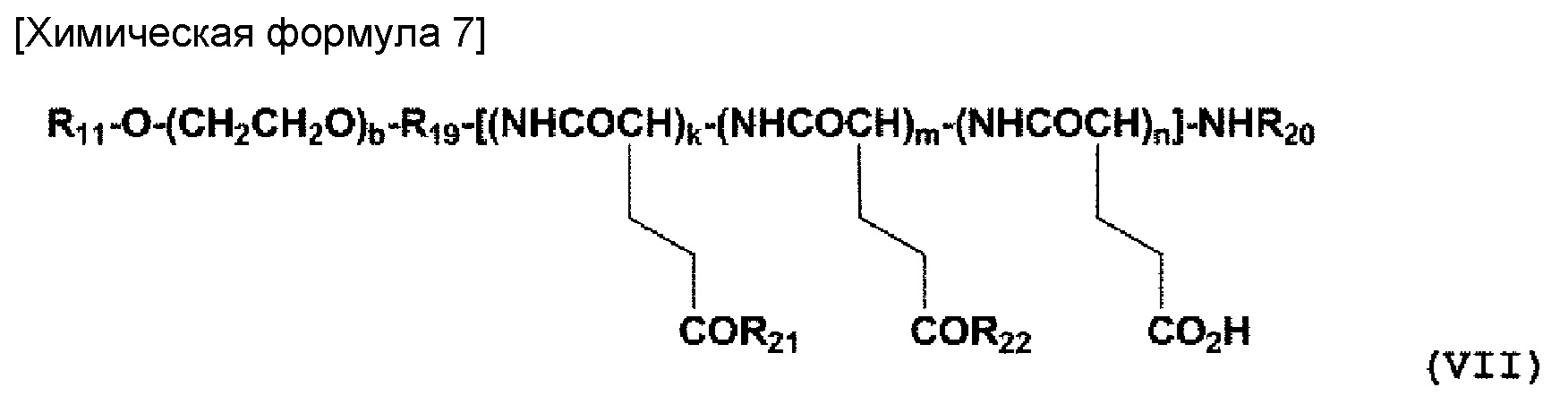
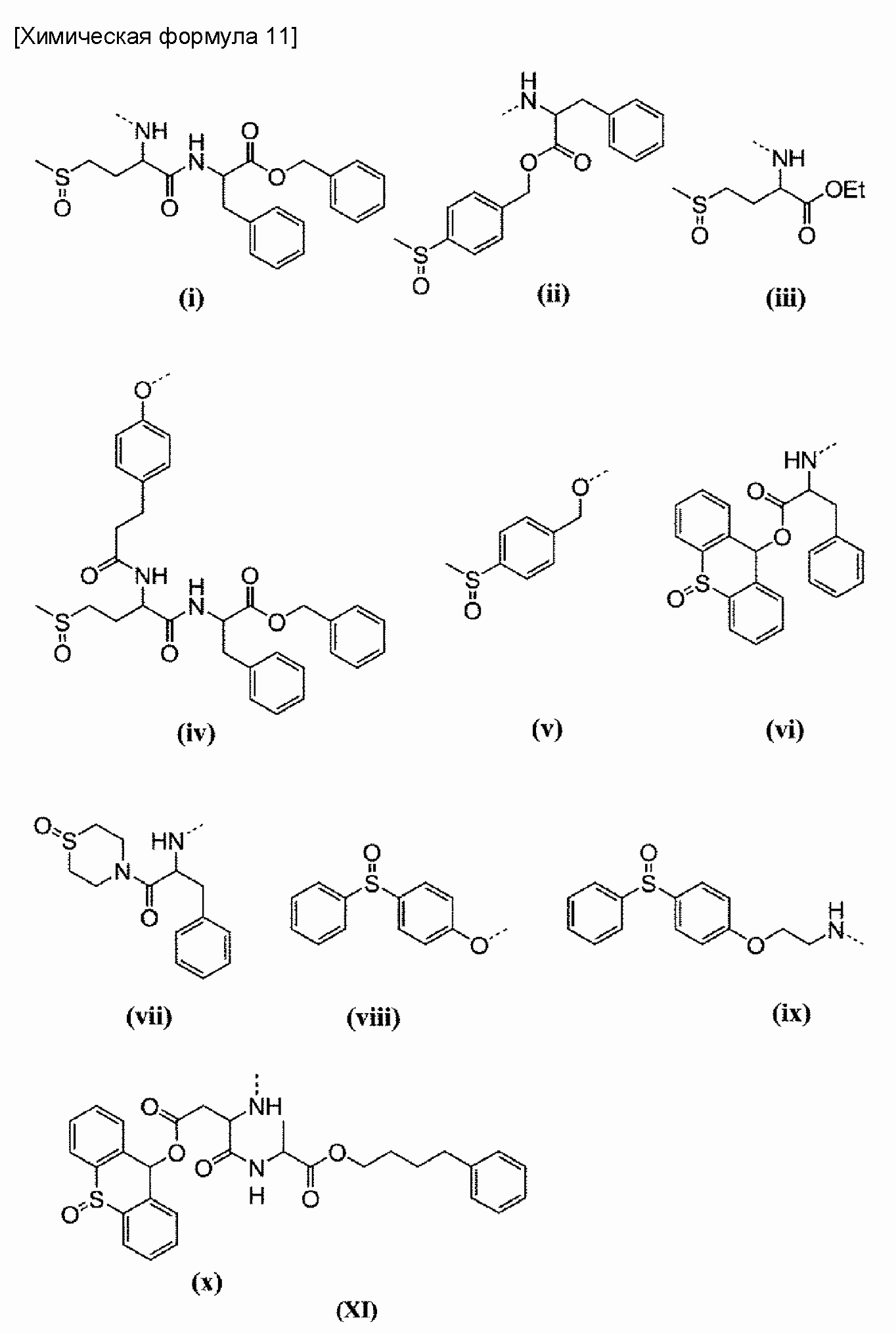
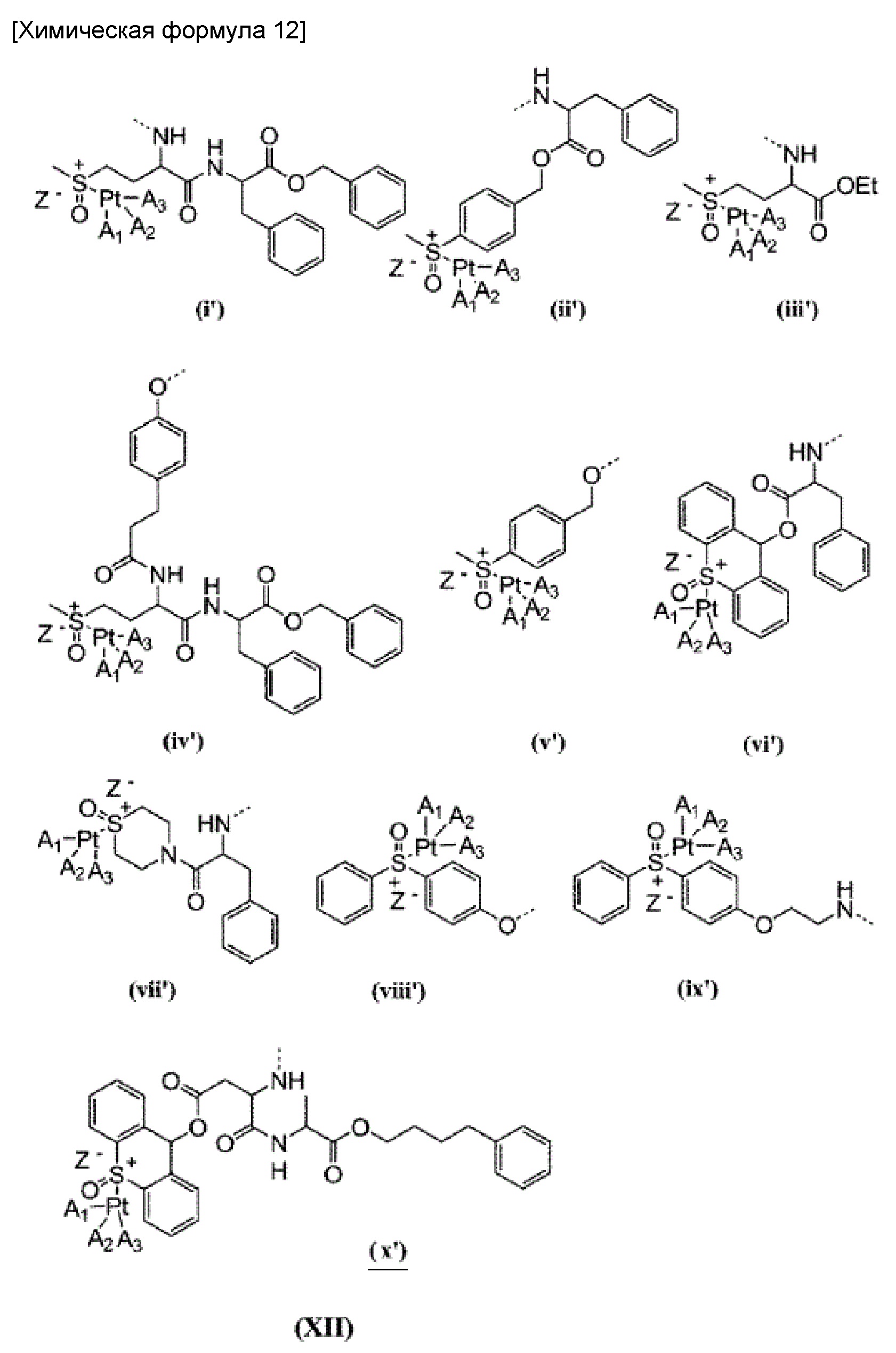
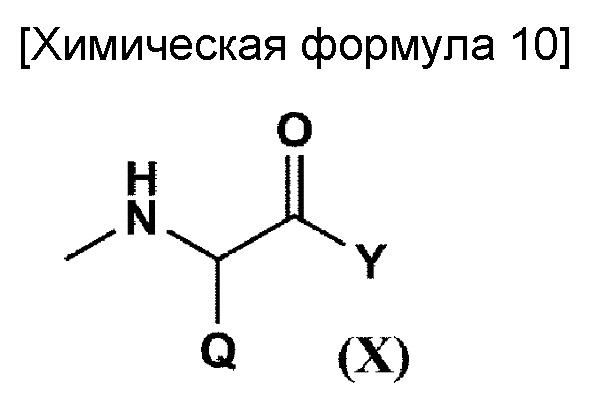
Документы, цитированные в отчёте о поиске
Способ получения полимеризованных координационных соединений комплекса платины
Координационный комплекс диаминоциклогексана платины (ii) с блоксополимером, содержащим сегмент поли(карбоновой кислоты), и включающий его противораковый агент
Высокомолекулярный конъюгат подофиллотоксинов

Комментарии