Способ очистки конъюгатов на основе il-15/il-15r-альфа - RU2701301C2
Код документа: RU2701301C2
Чертежи






























Описание
[0001] Настоящая международная заявка на патент испрашивает приоритет европейской заявки на патент EP 14000742.8, поданной 3 марта 2014 г., которая включена в данный документ с помощью ссылки.
Область изобретения
[0002] Настоящее изобретение относится к области биохимической инженерии. В частности, настоящее изобретение относится к улучшенному способу биохимического извлечения, при котором конъюгаты на основе IL-15/IL-15R-альфа могут быть подвергнуты рефолдингу и извлечены в мономерной форме. Данная композиция может быть использована в фармацевтических составах.
Предпосылки изобретения
[0003] Иммунотерапии, основанные на применении цитокинов, представляют особый интерес. Эти молекулы, которые представляют собой растворимые молекулы, участвуют в регуляции гуморального и/или клеточного иммунитета. Среди них, IL-2, IL-7, IL-12 и IL-15 еще в большей степени представляют особый интерес, поскольку они индуцируют выживаемость и/или пролиферацию NK-клеток и, таким образом, интересны в качестве вспомогательного лекарственного средства при лечении инфекционных или раковых заболеваний.
[0004] Цитокин интерлейкин-15 (IL-15) изначально идентифицировали в супернатантах культуры эпителиальных клеток почки обезьяны линии CV-1/EBNA и клеточной линии HuT-102 Т-клеточного лейкоза. Последовательность кДНК IL-15 кодирует белок-предшественник из 162 аминокислот (aa), состоящий из длинного лидерного пептида из 48-aa и зрелого белка из 114-aa. Несмотря на то, что гомологии последовательности с IL-2 не существует, анализ аминокислотной последовательности предполагает, что IL-15, подобно IL-2, является членом семейства цитокинов со структурой в виде четырехспирального пучка.
[0005] Интерлейкин-15 в настоящее время рассматривается как очень перспективное в будущем лекарственное средство. Тем не менее, ввиду короткого периода полужизни и других параметров, его продукция в клеточных линиях млекопитающих в действительности осуществляется в небольших количествах.
[0006] Новые конъюгаты на основе интерлейкина-15 и его рецептора IL-15 R-альфа или их фрагментов были описаны в патентах US 8124084 B2 и EP 1934353 B1.
[0007] На данный момент, даже если указанные коньюгаты имеют более длинный период полужизни, их очистка усложняется образованием димерных и мультимерных комплексов. Кроме того, в связи с образованием высоких долей димерных и олигомерных агрегатов, соответствующие очищенные композиции не могут быть использованы в качестве лекарственного препарата в связи с их возможным участием в реакциях иммуногенности/аллергенности против вводимых биопрепаратов (антитела к лекарственному средству, ADA).
[0008] Таким образом, существует потребность в новом способе очистки с тем, чтобы получить композицию конъюгата, которая может быть использована в качестве лекарственного препарата.
Краткое описание изобретения
[0009] Предусматривают способ очистки, применимый при приготовлении мономерного конъюгата. Данный способ обеспечивает жидкие фармацевтические композиции, содержащие такой мономерный конъюгат. Данный способ включает условия, которые вероятно улучшают рефолдинг указанного конъюгата в ходе процесса извлечения.
[00010] Авторы настоящего изобретения в настоящее время установили, что способ очистки с применением анионообменной хроматографии с последующей хроматографией гидрофобного взаимодействия позволяет получить конъюгат в мономерной форме, в то время как очистка с применением хроматографии гидрофобного взаимодействия с последующей анионообменной хроматографией не дает такой возможности. Кроме того, авторы настоящего изобретения неожиданно установили, что стадия загрузки хроматографии гидрофобного взаимодействия должна осуществляться путем перемешивания первого элюата и буфера для загрузки непосредственно в смесительной камере указанной хроматографической колонки. На самом деле, такая процедура загрузки является наиболее эффективной и позволяющей получать высокую концентрацию активного белка слияния в мономерной форме без соосаждения на хроматографической смоле.
[00011] Таким образом, в первом аспекте настоящее изобретение относится к способу получения композиции, содержащей мономерные конъюгаты из образца, при этом указанный конъюгат содержит:
[00012] a) полипептид, содержащий аминокислотную последовательность интерлейкина 15 или его производных, и
[00013] b) полипептид, содержащий аминокислотную последовательность домена sushi IL-15Rα или его производных,
[00014] где указанный способ предусматривает применение анионообменной хроматографии с последующей хроматографией гидрофобного взаимодействия указанного образца.
[00015] Во втором аспекте настоящее изобретение относится к фармацевтической композиции, содержащей упомянутый мономерный конъюгат.
[00016] В третьем аспекте настоящее изобретение относится к применению упомянутой композиции для лечения ракового и/или инфекционного заболевания у субъекта.
Краткое описание графических материалов
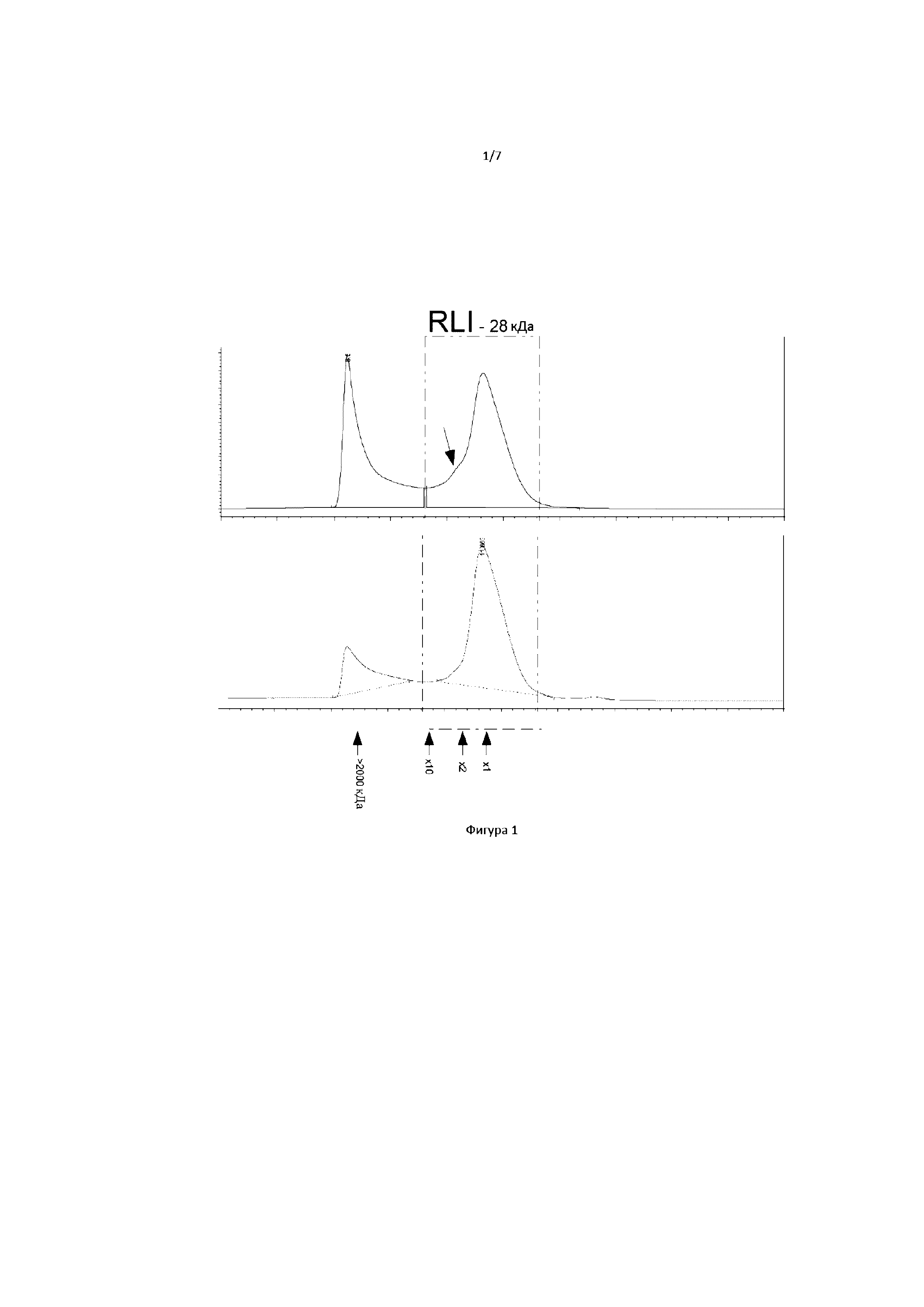
[00017] На Фигуре 1 показаны два профиля хроматографического элюирования продукции RLI в клеточных линиях CHO.
[00018] На Фигуре 2 показан профиль эксклюзионной хроматографии продукции RLI в клеточных линиях CHO.
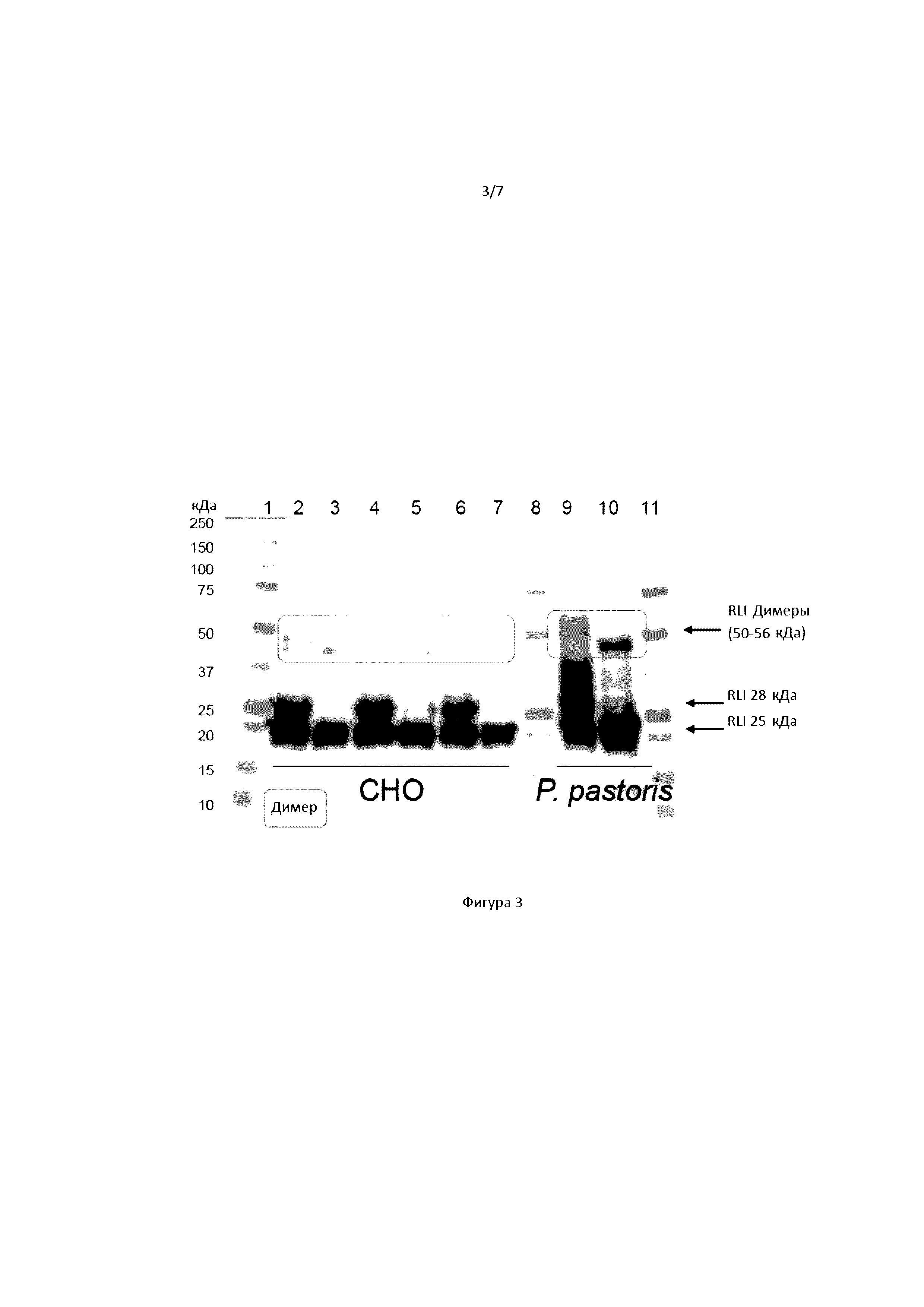
[00019] На Фигуре 3 показан вестерн-блоттинг с помощью антитела к IL-15 в отношении продуцируемого RLI в клеточных линиях CHO (дорожки 2-7) или в Pichia pastoris (дорожки 9 и10). Дегликозилирование RLI посредством PNGазы соответствует дорожкам 3, 5, 7 и 10.
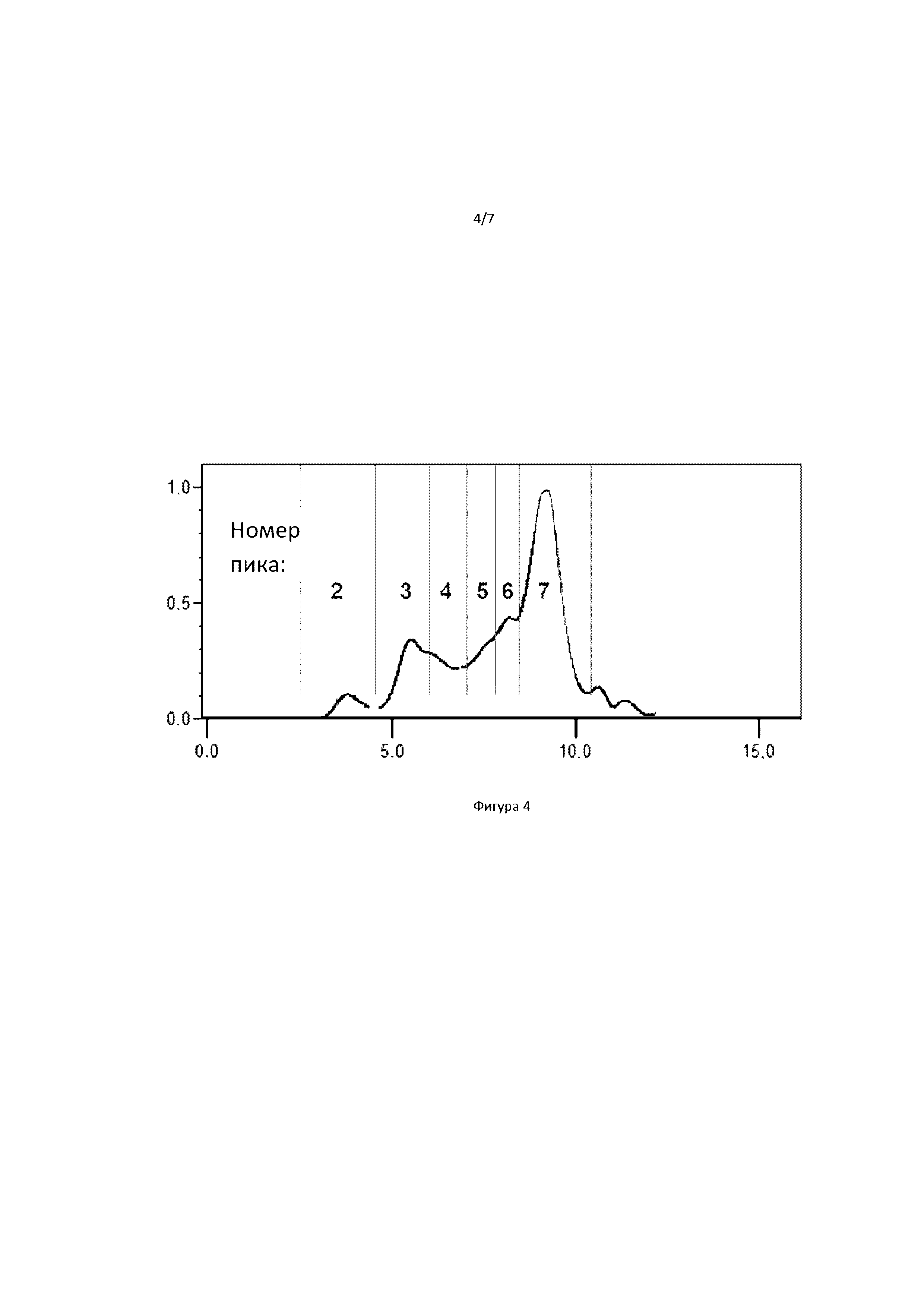
[00020] На фигуре 4 показана SEC-MALLS хроматограмма для RLI продукта (для рассеивания излучения).
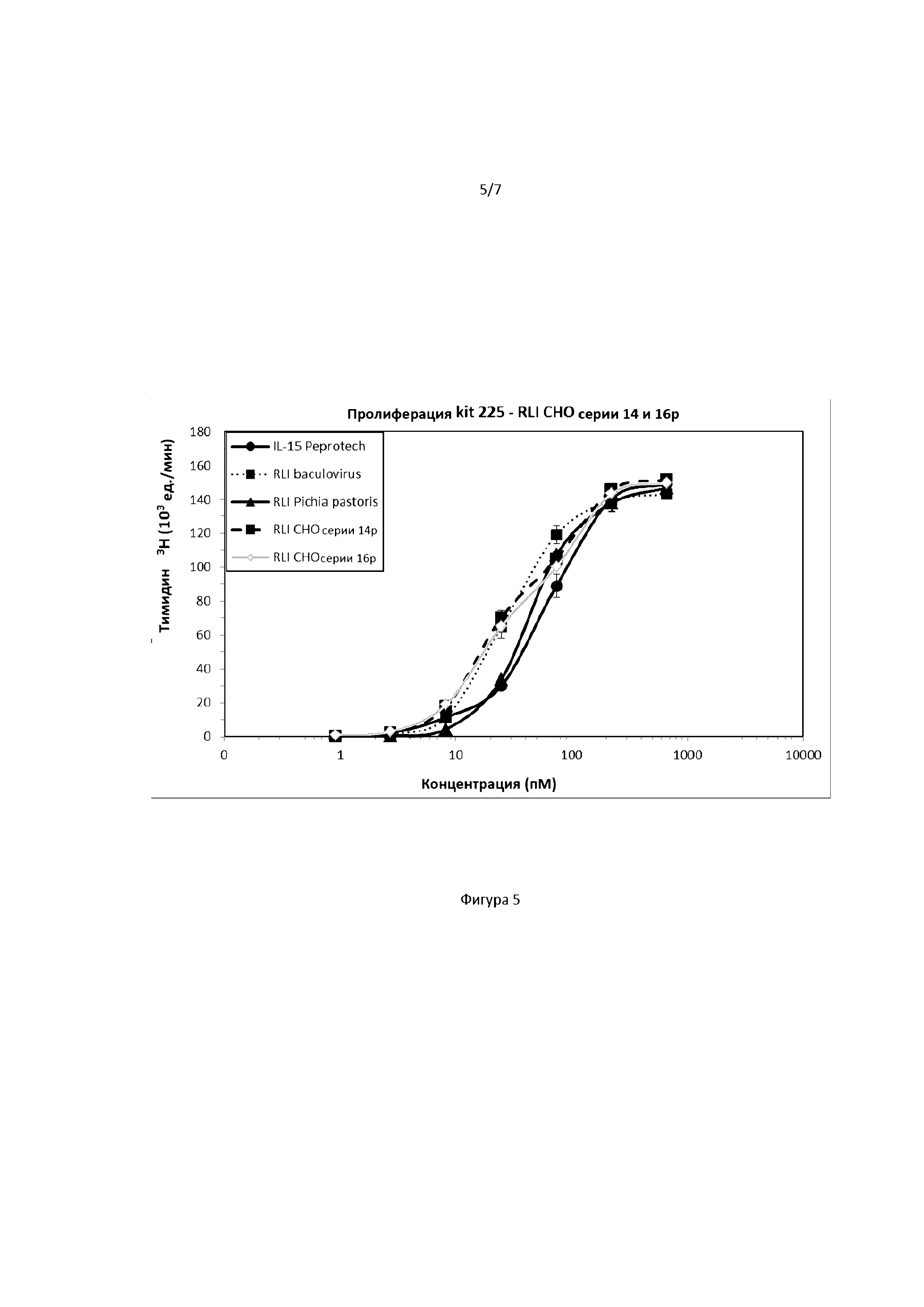
[00021] На фигуре 5 показана пролиферативная активность разной продукции RLI в отношении клеточных линий kit225.
[00022] На фигуре 6 показана пролиферативная активность разной продукции RLI в отношении клеточных линий 32DB.
[00023] На фигуре 7 показана пролиферация NK у мышей, наблюдаемая после введения мышам нескольких образцов RLI.
Подробное описание
[00024] Настоящее изобретение относится к новому способу получения фармацевтической композиции, содержащей мономерные конъюгаты.
[00025] Термин «мономерный» подразумевает, что большая часть конъюгата, присутствующего в композиции, представлена в мономерной, а не в агрегированной форме. Под термином «агрегированный» подразумевают физическое взаимодействие между молекулами полипептидов, которое приводит к образованию мультимеров, т.е. димеров или олигомеров, которые остаются растворимыми или которые могут выпадать в осадок из раствора. Большую часть времени указанное агрегированное состояние является необратимым и приводит к денатурации конъюгата. Следует отметить, что после денатурации конъюгат может быть связан с сильной иммуногенностью.
[00026] Процент конъюгата (по весу) в мономерной форме в данной композиции будет составлять по меньшей мере от 80% или более, т.е. по сравнению с агрегированной формой, предпочтительно по меньшей мере от 90% или более, и более предпочтительно по меньшей мере от 95% или более.
[00027] Термин «образец» относится к образцу среды для культивирования трансформированной клетки-хозяина, экспрессирующей указанный конъюгат. Клетки-хозяины, используемые в настоящем изобретении, представляют собой клетки млекопитающих, предпочтительно клетки CHO (Chinese Hamster Ovary (клетки яичника китайского хомячка)), такие как CHO K1 (ATCC номер CCL-31, CCL-61 или CRL-9618), CHO-DHFR (ATCC CRL-9096), CHO-DXB-11, клетки CHO с ATCC номером ATCC CRL 1610 или CHO DG44; HEK293 (Human Embryonic Kidney (человеческие эмбриональные клетки почек)), такие как 293 (ATCC номер CRL-1573) или HEK-293.2sus (ATCC номер CRL-1573.3); клетки COS, такие как COS-1 (ATCC номер CRL-1650) и COS-7 (ATCC номер CRL-1651); клетки PER.C6® (клеточные линии, производные человеческой сетчатки; DSM BIOLOGICS, CRUCELL); SP2O, такие как клетки SP2/0-Agl4 (ATCC номер доступа CRL-1851), клетки NSO или любые клетки, происходящие от них.
[00028] Предпочтительно, указанные клетки-хозяины представляют собой клеточные линии CHO.
[00029] В первом предпочтительном варианте осуществления, способ по настоящему изобретению включает стадии:
[00030] (a) осуществления анионообменной хроматографии (AEX) в отношении образца с получением первого элюата,
[00031] (b) осуществления хроматографии гидрофобного взаимодействия (HIC) в отношении первого элюата с получением второго элюата.
[00032] На первой стадии анионообменная хроматография (AEX) может быть осуществлена с применением AEX колонки или смолы, выбранной из группы, включающей или состоящей из Q Sepharose, (например, Q Sepharose Fast Flow, Q Sepharose XL, Q Sepharose big beads, Q sepharose high performance, Q sepharose XL), DEAE Sephadex A-25, DEAE Sephadex A-50, QAE Sephadex A-25, QAE Sephadex A-50, Sourse 15Q, Sourse 30Q, Resourse Q, Capto Q, Capto DEAE, Mono Q, Toyopearl Super Q, Toyopearl DEAE, Toyopearl QAE, Toyopearl Q, Toyopearl GigaCap Q. TSKgel SuperQ, TSKgel DEAE, Fractogel EMD TMAE, Fractogel EMD TMAE HiCap, Fractogel EMD DEAE, Fractogel EMD DMAE, Macroprep High Q, Macro-prep-DEAE, Unosphere Q, Nuvia Q, POROS HQ, POROS PI, DEAE Ceramic HyperD и Q Ceramic HyperD. DEAE Sepharose Fast Flow и ANX Sepharose 4 Fast Flow.
[00033] Преимущественно данная AEX смола или колонка представляет собой Q Sepharose или DEAE Sepharose, и более предпочтительно представляет собой сильный анионообменник, такой как Q Sepharose.
[00034] В настоящее время упомянутую стадию a) обычно выполняют в несколько стадий, включающих уравновешивание колонки или смолы, подбор образца и элюирование. После стадии загрузки или после стадии элюирования могут быть включены одна или несколько стадий отмывки.
[00035] Стадия уравновешивания выполняется просто в соответствии с инструкцией изготовителя.
[00036] Как было определено авторами изобретения, стадия подбора осуществляется с использованием буфера NaCl. В качестве примера, буфер для подбора содержит 0,5 M-1,5 M NaCl, предпочтительно 0,75 M-1,25 M и наиболее предпочтительно 1 M NaCl.
[00037] Указанная стадия подбора осуществляется предпочтительно на концентрированном или диафильтрованном культуральном супернатанте с применением ультрафильтрационной кассеты.
[00038] Разработчики анионообменной хроматографии (AEX) предлагают использовать pH по меньшей мере на одну единицу pH ниже, чем изоэлектрическая точка белка, который должен быть очищен.
[00039] Неожиданно авторы настоящего изобретения установили, что поскольку RLI1 (SEQ id n 16) или RLI2 (SEQ id n 17) имеет изоэлектрическую точку примерно 5,5, стадию a) необходимо осуществлять при pH равном или выше, чем 7,0 и предпочтительно равном или выше 7,5.
[00040] Стадию элюирования для анионообменной хроматографии (AEX) проводят в градиенте с применением солевого буфера от 1 до 0 M NaCl и предпочтительно от 0,75 до 0 M NaCl.
[00041] Стадию b) хроматографии гидрофобного взаимодействия (HIC) можно осуществлять с применением HIC колонки или смолы, выбранной из группы, включающей или состоящей из Phenyl Sepharose, Butyl Sepharose, Octyl Sepharose, ToyoPearl Hexyl-650, ToyoPearl Ether-650, Hydrocell C3, Hydreocell Phenyl 1500 или Hydrocell C4 1500.
[00042] Преимущественно, HIC смола или колонка представляет собой Phenyl Sepharose.
[00043] Как и в случае стадии a), указанная стадия b), как правило, предусматривает несколько стадий, включающих уравновешивание колонки или смолы, загрузку образца и элюирование. После стадии загрузки или после стадии элюирования могут быть включены одна или несколько стадий отмывки.
[00044] Как и в предыдущем случае, стадия уравновешивания выполняется просто в соответствии с инструкцией изготовителя.
[00045] Для стадии подбора буферный раствор содержит соль аммония, такую как сульфат аммония или ацетат аммония, предпочтительно сульфат аммония. В качестве примера, буфер для подбора содержит 0,75 M-2,5 M сульфата аммония, предпочтительно 1 M-2 M сульфата аммония и наиболее предпочтительно 1,5 M-2 M сульфата аммония.
[00046] Такая стадия подбора является решающей. В предыдущих экспериментах, реализованных авторами настоящего изобретения, все результаты очистки сводились к переменному количеству конъюгата, при этом конъюгат находился в основном в агрегированной форме.
[00047] Неожиданно авторам настоящего изобретения удалось получить мономерные формы конъюгата посредством перемешивания первого элюата, полученного на стадии a), и буфера для подбора непосредственно на указанной хроматографической колонке или смоле, более конкретно, непосредственно в смесительной камере указанной хроматографической колонки или смоле.
[00048] Стадию элюирования проводят в градиенте с применением солевого раствора буфера, от 2 до 0 M сульфата аммония, предпочтительно от 1,5 до 0 M сульфата аммония.
[00049] Способ по настоящему изобретению может предусматривать одну или несколько дополнительных стадий.
[00050] В качестве примера, способ по настоящему изобретению может предусматривать стадию осуществления эксклюзионной хроматографии (SEC) в отношении второго элюата с получением третьего элюата.
[00051] Указанная стадия эксклюзионной хроматографии (SEC) может быть осуществлена с применением SEC колонки, такой как Superdex 200 или Superdex 75.
[00052] В другом примере, способ по настоящему изобретению может также предусматривать стадию осуществления другого типа хроматографии - анионообменной хроматографии (AEX) в отношении второго элюата с получением третьего элюата.
[00053] Такая стадия анионообменной хроматографии может быть осуществлена как описано выше.
[00054] В еще одном предпочтительном варианте осуществления способ по настоящему изобретению дополнительно включает стадию применения полученного конъюгата для получения лекарственного препарата.
[00055] Термин «конъюгат» применяется в его общем значении в данной области и относится к ковалентному или нековалентному комплексу, предпочтительно к ковалентному комплексу и наиболее предпочтительно к слитому белку.
[00056] Термин «интерлейкин 15» в его общем значении в данной области относится к цитокину со структурным сходством с IL-2 (Grabstein et al., Science, vol.264(5161), p:965-968, 1994). Этот цитокин также известен как IL-15, IL15 или MGC9721. Этот цитокин и IL-2 обладают многими общими видами биологической активности и, как было обнаружено, связываются с одинаковыми субъединицами рецептора гематопоэтина. Таким образом, они могут конкурировать за один и тот же рецептор, отрицательно регулируя активность друг друга. Было установлено, что IL-15 регулирует активацию и пролиферацию T-клеток и естественных клеток-киллеров и что число клеток памяти CD8+, как показано, контролируется балансом между этим цитокином и IL2. Активность IL-15 можно измерить с помощью определения его индукции пролиферации на линии клеток kit225 (HORI et al., Blood, vol.70(4), p:1069-72, 1987), как раскрыто в примерах.
[00057] Упомянутый IL-15 или его производные имеют по меньшей мере 10% активности интерлейкина-15 человека в отношении индукции пролиферации линии клеток kit225, предпочтительно по меньшей мере 25% и более предпочтительно по меньшей мере 50%.
[00058] Упомянутый интерлейкин 15 представляет собой интерлейкин 15 млекопитающих, предпочтительно интерлейкин 15 приматов и более предпочтительно интерлейкин 15 человека.
[00059] Интерлейкин 15 млекопитающих может быть легко идентифицирован специалистом в данной области. В качестве примера можно привести интерлейкин 15 Sus scrofa (номер доступа ABF82250), Rattus norvegicus (номер доступа NP_037261), Mus masculus (номер доступа NP_032383), Bos Taurus (номер доступа NP_776515), Oryctolagus cuniculus (номер доступа NP_001075685), Ovies aries (номер доступа NP_001009734), Felis catus (номер доступа NP_001009207), Macaca fascicularis (номер доступа BAA19149), Homo sapiens (номер доступа NP_000576), Macaca Mulatta (номер доступа NP_001038196), Cavia porcellus (номер доступа NP_001166300) или Chlorocebus sabaeus (номер доступа ACI289).
[00060] Используемый в данном документе термин «интерлейкин 15 млекопитающих» относится к консенсусной последовательности SEQ ID n 1.
[00061] Интерлейкин 15 приматов может быть легко идентифицирован специалистом в данной области. В качестве примера можно привести интерлейкин 15 Sus scrofa (номер доступа ABF82250), Oryctolagus cuniculus (номер доступа NP_001075685), Macaca fascicularis (номер доступа BAA19149), Homo sapiens (номер доступа NP_000576), Macaca Mulatta (номер доступа NP_001038196) или Chlorocebus sabaeus (номер доступа ACI289).
[00062] Используемый в данном документе термин «интерлейкин 15 приматов» относится к консенсусной последовательности SEQ ID n 2.
[00063] Интерлейкин 15 человека может быть легко идентифицирован специалистом и относится к аминокислотной последовательности SEQ ID n 3.
[00064] Используемый в данном документе термин «производные интерлейкина 15» относится к аминокислотной последовательности, имеющей процент идентичности по меньшей мере 92,5% (т.е. соответствующий приблизительно 10 аминокислотным заменам) по отношению к аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID n : 1, SEQ ID n 2 и SEQ ID n 3, предпочтительно по меньшей мере 96% (т.е. соответствующий приблизительно 5 аминокислотным заменам) и более предпочтительно по меньшей мере 98,5% (т.е. соответствующий приблизительно 2 аминокислотным заменам) или по меньшей мере 99% (т.е. соответствующий приблизительно 1 аминокислотной замене). Такие производные могут быть легко идентифицированы специалистом в данной области, исходя из его личных знаний и идеи настоящей заявки на патент. В качестве примера таких производных можно привести таковые, описанные в международной заявке на патент PCT WO 2009/135031. Также будет понятно, что встречающиеся в природе аминокислоты могут быть замещены химически модифицированными аминокислотами. Обычно такие химически модифицированные аминокислоты повышают время полужизни полипептида.
[00065] Как используется в данном документе, «процент идентичности» между двумя аминокислотными последовательностями означает процент идентичных аминокислот между двумя последовательностями, подлежащими сравнению, полученный с наилучшим выравниванием упомянутых последовательностей, при этом этот процент является чисто статистическим и различия между этими двумя последовательностями случайно распределяются в аминокислотных последовательностях. Как используется в данном документе, «наилучшее выравнивание» или «оптимальное выравнивание» означает выравнивание, для которого определенный процент идентичности (см. ниже) является наивысшим. Сравнение последовательностей между двумя аминокислотными последовательностями обычно осуществляют с помощью сравнения этих последовательностей, которые ранее были выравнены в соответствии с наилучшим выравниванием; это сравнение осуществляют на сегментах сравнения для того, чтобы идентифицировать и сравнить локальные участки сходства. Наилучшее выравнивание последовательностей, подлежащих сравнению, можно осуществить, помимо ручного способа, с помощью алгоритма глобальной гомологии, разработанного Smith и Waterman (Ad. App. Math., vol.2, p:482, 1981), с помощью алгоритма локальной гомологии, разработанного Neddleman и Wunsch (J. Mol. Biol., vol.48, p:443, 1970), с помощью метода подобия, разработанного Pearson и Lipman (Proc. Natl. Acd. Sci. USA, vol.85, p:2444, 1988), с помощью компьютерных программ, использующих такие алгоритмы (GAP, BESTFIT, BLAST P, BLAST N, FASTA, TFASTA в пакете программного обеспечения Wisconsin Genetics, Genetics Computer Group, 575 Science Dr., Мадисон, Висконсин, США), с помощью алгоритмов множественного выравнивания MUSCLE (Edgar, Robert C., Nucleic Acids Research, vol. 32, p:1792, 2004). Чтобы получить наилучшее локальное выравнивание предпочтительно можно использовать программное обеспечение BLAST с матрицей BLOSUM 62. Процент идентичности между двумя последовательностями аминокислот определяют путем сравнения этих двух оптимально выравненных последовательностей, при этом для того, чтобы получить оптимальное выравнивание между этими двумя последовательностями, аминокислотные последовательности могут охватывать добавления или делеции в отношении эталонной последовательности. Процент идентичности рассчитывают с помощью определения числа идентичных положений между этими двумя последовательностями и деления этого числа на общее число сравниваемых положений, а затем умножения полученного результата на 100 для того, чтобы получить процент идентичности между этими двумя последовательностями.
[00066] Предпочтительно производными интерлейкина 15 являются агонист или суперагонист IL-15. Специалист в данной области может легко идентифицировать агонист или суперагонист IL-15. В качестве примера агониста или суперагониста IL-15 можно привести таковые, раскрытые в международной заявке на патент WO 2005/085282 или в ZHU et al. (J. Immunol., vol.183 (6), p:3598-607, 2009).
[00067] Еще более предпочтительно упомянутый агонист или суперагонист IL-15 выбирают в группе, включающей/состоящей из L45D, L45E, S51D, L52D, N72D, N72E, N72A, N72S, N72Y и N72P (в отношении последовательности IL-15 человека, SEQ ID n 3).
[00068] Как используется в данном документе, выражение «домен sushi IL-15Rα» имеет свое общее значение в данной области и относится к домену, который начинается с первого остатка цистеина (C1) после сигнального пептида IL-15Rα и заканчивается четвертым остатком цистеина (C4) после упомянутого сигнального пептида. Упомянутый домен sushi, соответствующий части внеклеточной области IL-15Rα, необходим для его связывания с IL-15 (WEI et al., J. Immunol., vol.167(1), p:277-282, 2001).
[00069] Упомянутый домен sushi IL-15Rα или его производные характеризуется по меньшей мере 10% связывающей активностью домена sushi IL-15Rα человека с интерлейкином-15 человека, предпочтительно по меньшей мере 25% и более предпочтительно по меньшей мере 50%. Упомянутая связывающая активность может быть легко определена с помощью способа, раскрытого в WEI et al. (упомянутого выше, 2001).
[00070] Упомянутый домен sushi IL-15Rα представляет собой домен sushi IL-15Rα млекопитающих, предпочтительно домен sushi IL-15Rα приматов и более предпочтительно домен sushi IL-15Rα человека.
[00071] Домен sushi IL-15Rα млекопитающих может быть легко идентифицирован специалистом в данной области. В качестве примера можно привести домен sushi IL-15Rα Rattus norvegicus (номер доступа XP_002728555), Mus masculus (номер доступа EDL08026), Bos Taurus (номер доступа XP_002692113), Oryctolagus cuniculus (номер доступа XP_002723298), Macaca fascicularis (номер доступа ACI42785), Macaca nemestrina (номер доступа ACI42783), Homo sapiens (номер доступа CAI41081), Macaca Mulatta (номер доступа NP_001166315), Pongo abelii (номер доступа XP_002820541), Cercocebus torquatus (номер доступа ACI42784), Callithrix jacchus (номер доступа XP_002750073) или Cavia porcellus (номер доступа NP_001166314).
[00072] Используемый в данном документе термин «домен sushi IL-15Rα млекопитающих» относится к консенсусной последовательности SEQ ID n°4.
[00073] Предпочтительно полипептид, содержащий аминокислотную последовательность домена sushi IL-15Rα млекопитающих, относится к консенсусной последовательности SEQ ID n°5.
[00074] Домен sushi IL-15Rα приматов может быть легко идентифицирован специалистом в данной области. В качестве примера можно привести домены sushi IL-15Rα Oryctolagus cuniculus, Macaca fascicularis, Macaca nemestrina, Homo sapiens, Macaca Mulatta, Pongo abelii, Cercocebus torquatus или Callithrix jacchus.
[00075] Используемый в данном документе термин «домен sushi IL-15Rα приматов» относится к консенсусной последовательности SEQ ID n 6.
[00076] Предпочтительно полипептид, содержащий аминокислотную последовательность домена sushi IL-15Rα приматов, относится к консенсусной последовательности SEQ ID n 7.
[00077] Домен sushi IL-15Rα человека может быть легко идентифицирован специалистом и относится к аминокислотной последовательности SEQ ID n 8.
[00078] Предпочтительно полипептид, содержащий аминокислотную последовательность домена sushi IL-15Rα человека, относится к SEQ ID n 9.
[00079] Используемый в данном документе термин «производные домена sushi IL-15Rα» относится к аминокислотной последовательности, имеющей процент идентичности по меньшей мере 92% (т.е. соответствующий приблизительно 5 аминокислотным заменам) в отношении аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID n : 4, SEQ ID n 5, SEQ ID n 6, SEQ ID n : 7, SEQ ID n 8 и SEQ ID n 9, предпочтительно по меньшей мере 96 % (т.е. соответствующий приблизительно 2 аминокислотным заменам) и более предпочтительно по меньшей мере 98% (т.е. соответствующий приблизительно 1 аминокислотной замене). Такие производные содержат четыре остатка цистеина домена sushi L-15Rα и могут быть легко идентифицированы специалистом в данной области исходя из его/ее общих знаний и идеи настоящей заявки на патент. Также будет понятно, что встречающиеся в природе аминокислоты могут быть замещены химически модифицированными аминокислотами. Обычно такие химически модифицированные аминокислоты способны повышать время полужизни полипептида.
[00080] В соответствии с предпочтительным вариантом осуществления конъюгат содержит (ii) полипептид, содержащий аминокислотную последовательность домена sushi и шарнирного домена IL-15Rα или его производных.
[00081] Шарнирный домен IL-15Rα определяют как аминокислотную последовательность, которая начинается с первого аминокислотного остатка после домена sushi и которая заканчивается последним аминокислотным остатком перед первым потенциальным сайтом гликозилирования. В IL-15Rα человека аминокислотная последовательность шарнирного участка состоит из четырнадцати аминокислот, которые расположены после домена sushi этого IL-15R альфа, в C-концевом положении по отношению к упомянутому домену sushi, т.е. упомянутый шарнирный участок IL-15R альфа начинается с первой аминокислоты после упомянутого (C4) остатка цистеина и заканчивается четырнадцатой аминокислотой (считая в стандартной ориентации «от N-конца до C-конца»).
[00082] Упомянутый домен sushi и шарнирный домен IL-15Rα представляют собой домен sushi и шарнирный домен IL-15Rα млекопитающих, предпочтительно домен sushi и шарнирный домен IL-15Rα приматов и более предпочтительно домен sushi и шарнирный домен IL-15Rα человека.
[00083] Аминокислотная последовательность домена sushi и шарнирного домена IL-15Rα млекопитающих может быть легко идентифицирована специалистом в данной области. Используемый в данном документе термин «домен sushi и шарнирный домен IL-15Rα млекопитающих» относится к консенсусной последовательности SEQ ID n 10.
[00084] Аминокислотная последовательность домена sushi и шарнирного домена IL-15Rα приматов может быть легко идентифицирована специалистом в данной области. Используемый в данном документе термин «домен sushi и шарнирный домен IL-15Rα приматов» относится к консенсусной последовательности SEQ ID n 11.
[00085] Аминокислотная последовательность домена sushi и шарнирного домена IL-15Rα человека может быть легко идентифицирована специалистом в данной области. Используемый в данном документе термин «домен sushi и шарнирный домен IL-15Rα человека» относится к консенсусной последовательности SEQ ID n 12.
[00086] Используемый в данном документе термин «производные домена sushi и шарнирного домена IL-15Rα» относится к аминокислотной последовательности, имеющей процент идентичности по меньшей мере 93% (т.е. соответствующий приблизительно 5 аминокислотным заменам) в отношении аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID n : 10, SEQ ID n 11 и SEQ ID n 12, предпочтительно по меньшей мере 97% (т.е. соответствующий приблизительно 2 аминокислотным заменам) и более предпочтительно по меньшей мере 98% (т.е. соответствующий приблизительно 1 аминокислотной замене). Такие производные содержат четыре остатка цистеина домена sushi L-15Rα и могут быть легко идентифицированы специалистом в данной области, исходя из его общих знаний и идеи настоящей заявки на патент. Также будет понятно, что встречающиеся в природе аминокислоты могут быть замещены химически модифицированными аминокислотами. Обычно такие химически модифицированные аминокислоты способны повышать время полужизни полипептида.
[00087] Оба полипептида a) и b) конъюгата могут быть связаны нековалентной связью, такой как в комплексе, раскрытом в патенте US 8124084 B2. Упомянутый конъюгат или комплекс может быть легко получен путем обеспечения подходящего количества полипептида a), обеспечения подходящего количества полипептида b), смешивания обоих полипептидов при подходящем pH и ионных условиях в течение времени, достаточного для получения комплекса (т.е. конъюгата), и необязательно концентрирования и очистки упомянутого комплекса. Полипептиды комплекса (т.е. конъюгата) могут быть образованы, например, с помощью синтезатора пептидов в соответствии со стандартными способами, с помощью экспрессии каждого полипептида отдельно в клетке или клеточном экстракте, затем выделения и очистки полипептида. Необязательно терапевтический полипептидный комплекс в соответствии с настоящим изобретением может быть получен с помощью экспрессии обоих полипептидов i) и ii) в одной и той же клетке или клеточном экстракте, затем выделения и очистки комплексов, например, с помощью хроматографических методик, таких как аффинная хроматография с антителами к части лимфокина, части рецептора лимфокина или к комплексу.
[00088] Оба полипептида a) и b) конъюгата могут быть также ковалентно связаны с помощью бифункциональных белок-связывающих средств или в слитом белке.
[00089] Полипептиды a) и b) конъюгата могут быть гликозилированными или негликозилированными. К тому же, авторы настоящего изобретения установили, что, и гликозилированный, и негликозилированный RLI проявляют одинаковую специфическую активность in vitro. В настоящее время полипептиды a) и b) конъюгата являются предпочтительно гликозилированными.
[00090] Бифункциональные белок-связывающие средства хорошо известны специалисту в данной области, также как и способы их использования, и включают, в качестве примеров, N-сукцинимидил(2-пиридилдитио)пропионат (SPDP), сукцинимидил(N-малеимидометил)циклогексан-1-карбоксилат, иминотиолан (IT), бифункциональные производные имидоэфиров (такие как диметиладипимидат HCL), активные сложные эфиры (такие как дисукцинимидил суберат), альдегиды (такие как глутаральдегид), бис-азидосоединения (такие как бис(п-азидобензоил)гександиамин), производные бис-диазония (такие как бис-(п-диазонийбензоил)-этилендиамин), диизоцианаты (такие как толуол 2,6-диизоцианат) и бис-активные соединения фтора (такие как l,5-дифтор-2,4-динитробензол).
[00091] Термин «слитый белок» относится к белку, полученному путем объединения двух или более генов, которые изначально кодировали отдельные белки. Он также известен как химерный белок. Трансляция этого слитого гена приводит к образованию одного полипептида с функциональными свойствами, полученными от каждого из исходных белков. Рекомбинантные слитые белки получают искусственным путем с помощью технологии рекомбинантных ДНК для использования в биологических исследованиях или терапии. Рекомбинантный слитый белок представляет собой белок, полученный в процессе генетической инженерии из слитого гена. Этот процесс обычно включает удаление стоп-кодона из последовательности кДНК, кодирующей первый белок, затем прибавление последовательности кДНК второго белка в рамке путем опосредованной лигированием ПЦР или ПЦР с перекрывающимися праймерами. Эта последовательность ДНК будет затем экспрессироваться клеткой в виде одного белка. Белок может быть сконструирован генетически таким образом, чтобы включать полную последовательность обоих исходных белков или только часть каждого.
[00092] В предпочтительном варианте осуществления конъюгат является слитым белком.
[00093] Аминокислотная последовательность интерлейкина 15 или его производных может располагаться в C-концевом или в N-концевом положении по отношению к аминокислотной последовательности домена sushi IL-15Rα или его производных. Предпочтительно аминокислотная последовательность интерлейкина 15 или его производных расположена в C-концевом положении по отношению к аминокислотной последовательности домена sushi IL-15Rα или его производных.
[00094] Аминокислотная последовательность интерлейкина 15 или его производных и аминокислотная последовательность домена sushi IL-15Rα или его производных могут быть отделены «линкерной» аминокислотной последовательностью. Упомянутая «линкерная» аминокислотная последовательность может быть равной длине, достаточной для обеспечения того, чтобы слитый белок формировал надлежащие вторичные и третичные структуры.
[00095] Длина линкерной аминокислотной последовательности может варьировать без значительного влияния на биологическую активность слитого белка. Обычно линкерная аминокислотная последовательность содержит по меньшей мере одну, но менее 30 аминокислот, например, линкер из 5-30 аминокислот, предпочтительно из 10-30 аминокислот, более предпочтительно из 15-30 аминокислот, еще более предпочтительно из 15-25 аминокислот, наиболее предпочтительно из 18-22 аминокислот.
[00096] Предпочтительными линкерными аминокислотными последовательностями являются таковые, которые способствуют тому, что конъюгат принимает надлежащую конформацию (т.е. конформацию, способствующую надлежащей активности проведения сигнала по сигнальному пути IL-15Rбета/гамма).
[00097] Наиболее подходящие линкерные аминокислотные последовательности (1) будут принимать гибкую растянутую конформацию, (2) не будут склонны к образованию упорядоченной вторичной структуры, которая могла бы взаимодействовать с функциональными доменами слитых белков, и (3) будут иметь минимальную гидрофобную характеристику или характеристику заряда, которая способствовала бы взаимодействию с функциональными доменами белка.
[00098] Предпочтительно линкерная аминокислотная последовательность содержит близкие к нейтральным аминокислоты, выбранные из группы, включающей Gly (G), Asn (N), Ser (S), Thr (T), Ala (A), Leu (L) и Gln (Q), наиболее предпочтительно из группы, включающей Gly (G), Asn (N) и Ser (S).
[00099] Примеры линкерных последовательностей описаны в патентных документах США № 5073627 и № 5108910.
[000100] Иллюстративные гибкие линкеры, которые являются, в частности, более подходящими для настоящего изобретения, включают таковые, кодируемые последовательностями SEQ ID n 13 (SGGSGGGGSGGGSGGGGSLQ), SEQ ID n 14 (SGGSGGGGSGGGSGGGGSGG) или SEQ ID n 15 (SGGGSGGGGSGGGGSGGGSLQ).
[000101] Еще более предпочтительно, конъюгат представляет собой слитый белок с последовательностью SEQ ID n 16 или SEQ ID n 17.
[000102] Во втором аспекте настоящее изобретение относится к фармацевтической композиции, содержащей упомянутый мономерный конъюгат, впоследствии связанный с фармацевтически приемлемым носителем.
[000103] Выражение «фармацевтически приемлемый» относится к молекулярным частицам и композициям, которые являются физиологически переносимыми и обычно не вызывают аллергических или подобных нежелательных реакций, таких как расстройство желудка, головокружение и т.п. при введении человеку. Предпочтительно используемое в данном документе выражение «фармацевтически приемлемый» означает разрешенный органом регулирования федерального правительства или правительства штата или указанный в Фармакопее США или другой общепризнанной фармакопее для применения у животных, и, в частности, у человека.
[000104] Термин «носитель» относится к растворителю, вспомогательному средству, вспомогательному веществу или переносчику, с которыми соединение вводят. Такими фармацевтическими носителями могут быть стерильные жидкости, такие как вода и масла, в том числе таковые нефтяного, животного, растительного или синтетического происхождения, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п.
[000105] Путь введения комбинации по настоящему изобретению представляет собой предпочтительно парентеральный путь введения; в контексте настоящего изобретения термин «парентеральный» подразумевает внутривенное, внутримышечное, подкожное, ректальное, вагинальное или внутрибрюшинное введение. Таким образом, фармацевтическая композиция содержит переносчики, которые являются фармацевтически приемлемыми для состава, предназначенного для инъецирования. Они могут быть, в частности, изотоническими, стерильными, физиологическими растворами (мононатрийфосфат или динатрийфосфат, хлорид натрия, калия, кальция или магния и т.п. или смеси таких солей), или сухими, особенно лиофилизованными композициями, которые при добавлении, в зависимости от случая, стерильной воды или физиологического солевого раствора, обеспечивают состав инъецируемых растворов. Подходящие фармацевтические носители описаны в «Remington's Pharmaceutical Sciences» автора E.W. Martin.
[000106] Среди указанных, внутривенный путь введения является наиболее предпочтительным.
[000107] Конъюгат можно растворить в буфере или воде или включать в эмульсии, микроэмульсии, гидрогели (например, гидрогели на основе триблочных сополимеров PLGA-PEG-PLGA), в микросферы, в наносферы, в микрочастицы, в наночастицы (например, микрочастицы сополимера молочной и гликолевой кислоты (например, полимолочной кислоты (PLA); сополимера лактида и гликолевой кислоты (PLGA)); полиглутаматные микросферы, наносферы, микрочастицы или наночастицы), в липосомы или другие галеновые составы. Во всех случаях состав должен быть стерильным и жидким в той степени, которая обеспечивает приемлемую возможность введения с помощью шприца. Он должен быть стабильным в условиях производства и хранения и должен быть защищен от загрязняющего действия микроорганизмов, таких как бактерии и грибы.
[000108] Также могут быть получены дисперсии в глицерине, жидких полиэтиленгликолях, их смесях и в маслах. При обычных условиях хранения и применения эти препараты содержат консервант для предупреждения роста микроорганизмов.
[000109] Конъюгат может быть составлен в композицию в нейтральной форме или форме соли. Фармацевтически приемлемые соли включают соли присоединения кислоты (полученные с помощью свободных аминогрупп белка), которые образуются с участием неорганических кислот, таких как, например, соляная или фосфорная кислоты, или таких органических кислот, как уксусная, щавелевая, винная, миндальная и т.п. Соли, образованные с помощью свободных карбоксильных групп, также могут быть получены из неорганических оснований, таких как, например, гидроксиды натрия, калия, аммония, кальция или железа, и таких органических оснований, как изопропиламин, триметиламин, гистидин, прокаин и т.п.
[000110] Носитель также может быть раствором или дисперсионной средой, содержащей, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и т.п.), их подходящие смеси и растительные масла. Конъюгаты по настоящему изобретению также могут быть модифицированы, например, посредством пегилирования, с тем, чтобы повысить их биодоступность.
[000111] Подходящая текучесть может поддерживаться, например, за счет использования покрытия, такого как лецитин, с помощью поддержания требуемого размера частиц в случае дисперсии и с использованием поверхностно-активных веществ. Предупреждение действия микроорганизмов может осуществляться с помощью различных антибактериальных и противогрибковых средств, например, парабенов, хлорбутанола, фенола, сорбиновой кислоты, тимеросала и т.п. Во многих случаях предпочтительным будет включение изотонических средств, например, сахара или хлорида натрия.
[000112] Пролонгированное всасывание инъецируемых композиций может осуществляться с помощью использования в композициях средств, задерживающих всасывание, например, моностеарата алюминия, желатина, полиолов, повышающих период полужизни ковалентных и нековалентных составов.
[000113] Существуют многочисленные причины нестабильности или разрушения пептидов, в том числе гидролиз и денатурация. Гидрофобное взаимодействие может вызывать скопление молекул вместе (т.е. агрегацию). Можно добавлять стабилизаторы, чтобы уменьшить или предупредить такие проблемы.
[000114] Стабилизаторы включают циклодекстрин и его производные (см. патентный документ США № 5730969). Также можно добавлять подходящие консерванты, такие как сахароза, маннит, сорбит, трегалоза, декстран и глицерин, чтобы стабилизировать конечный состав. К составу можно добавлять стабилизатор, выбранный из ионных и неионных поверхностно-активных веществ, D-глюкозы, D-галактозы, D-ксилозы, D-галактуроновой кислоты, трегалозы, декстранов, гидроксиэтиловых крахмалов и их смесей. Добавление соли щелочных металлов или хлорида магния может стабилизировать пептид. Пептид можно также стабилизировать путем его взаимодействия с сахаридом, выбранным из группы, включающей декстран, хондроитинсерную кислоту, крахмал, гликоген, декстрин и соли альгиновой кислоты. Другие сахара, которые могут быть добавлены, включают моносахариды, дисахариды, сахарные спирты и их смеси (например, глюкозу, маннозу, галактозу, фруктозу, сахарозу, мальтозу, лактозу, маннит, ксилит). Полиолы могут стабилизировать пептид, а также являются смешивающимися с водой или водорастворимыми. Подходящими полиолами могут быть полигидроксиспирты, моносахариды и дисахариды, в том числе маннит, глицерин, этиленгликоль, пропиленгликоль, триметилгликоль, винилпирролидон, глюкоза, фруктоза, арабиноза, манноза, мальтоза, сахароза и их полимеры. Различные вспомогательные вещества также могут стабилизировать пептиды, в том числе, сывороточный альбумин, аминокислоты, гепарин, жирные кислоты и фосфолипиды, поверхностно-активные вещества, металлы, полиолы, восстанавливающие средства, металлохелатирующие средства, поливинилпирролидон, гидролизованный желатин и сульфат аммония.
[000115] В третьем аспекте настоящее изобретение относится к применению указанной фармацевтической композиции для лечения ракового заболевания, инфекционного заболевания и/или иммунодефицитного состояния у субъекта.
[000116] Используемый в данном документе термин «субъект» означает млекопитающего, такого как грызун, представитель кошачьих, представитель псовых или примат и наиболее предпочтительно человек.
[000117] В контексте настоящего изобретения термин «лечение», используемый в данном документе, означает купирование, ослабление, ингибирование прогрессирования или предупреждение нарушения или состояния, к которому такой термин применяется, или одного или нескольких симптомов такого нарушения или состояния.
[000118] Термин «лечение рака», используемый в данном документе, означает ингибирование роста раковых клеток. Предпочтительно такое лечение также приводит к регрессии опухолевого роста, т.е. снижению размера измеряемой опухоли. Наиболее предпочтительно такое лечение приводит к полной регрессии опухоли.
[000119] Термин «лечение инфекции», используемый в данном документе, означает ингибирование репликации/пролиферации микроорганизмов.
[000120] Термин «лечение иммунодефицитного состояния», используемый в данном документе, означает индукцию NK-клеток и/или T-клеток.
[000121] «Эффективное количество» конъюгата представляет собой количество, которое является достаточным для индукции регрессии роста опухоли или репликации микроорганизмов. Дозы, используемые для введения, можно адаптировать в виде функции различных параметров, в частности, функции используемого режима введения, сопутствующей патологии или альтернативно желательной продолжительности лечения. Естественно, что форма фармацевтической композиции, путь введения, доза и режим, разумеется, зависят от состояния, подлежащего лечению, тяжести заболевания, возраста, веса и пола субъекта и т.д. Диапазоны эффективных доз, представленные ниже, не предназначены для ограничения настоящего изобретения и представляют предпочтительные диапазоны доз. Однако, предпочтительная доза может быть адаптирована к отдельному субъекту, как понимается и определяется специалистом в данной области, без излишнего экспериментирования.
[000122] Далее настоящее изобретение описано более подробно со ссылкой на аминокислотные последовательности, последовательности нуклеиновых кислот и примеры. Однако подробности примеров не предназначены для ограничения настоящего изобретения. Наоборот, настоящее изобретение относится к любому варианту осуществления, который предусматривает подробности, которые не упоминаются явным образом в примерах в данном документе, однако, которые специалист в данной области находит без излишних усилий.
ПРИМЕРЫ
[000123] 1) Анализ профиля продукции RLI
[000124] Нуклеотидную последовательность, кодирующую RLI1 и RLI2 (SEQ ID n 16 и SEQ ID n 17) клонировали в плазмидах pcDNA3.1 с помощью GENEART. Линейный PEI из 40 кДа получали от Polyscience. 1 мг/мл маточного раствора получали растворением PEI в воде с нагреванием, нейтрализацией NaOH и стерилизацией с помощью фильтрации через фильтр с размером пор 0,22 мкм. Маточный раствор разделяли на аликвоты и хранили при -20°C. Плазмидную ДНК для трансфекций очищали с помощью наборов для очистки плазмид в соответствии с протоколом производителя (Macherey-Nagel) и стерилизовали с помощью фильтрации через фильтр с размером пор 0,22 мкм.
[000125] Поддерживаемые в стандартных условиях клетки CHO-S (Invitrogen) высевали с плотностью 1×106 клеток/мл в среду PowerCHO2 (Lonza) и культивировали в течение ночи при 37°C во встряхивателе-инкубаторе (100 об./мин.) с 5% CO2. Для трансфекции клетки затем разбавляли в среде CD-CHO (Invitrogen) до 2×106 клеток/мл. Трансфекционные комплексы получали в 10% объема культуры с использованием 150 мМ NaCl. ДНК экспрессионных конструкций (2,5 мг/л объема культуры) смешивали с PEI, разбавленным в NaCl (10 мг/л конечного объема культуры), и инкубировали в течение 10 минут при комнатной температуре перед добавлением в культуру. Клетки культивировали во встряхивателе-инкубаторе (130 об./мин.) при 37°C в течение 5 часов перед удвоением объема культуры с использованием среды PowerCHO2. Супернатанты собирали через 5 дней после трансфекции.
[000126] Собранный супернатант центрифугировали при 3000 об./мин. в течение 20 минут при 4°C, уравновешивали при pH 7,8 с помощью NaOH и фильтровали через фильтр с размером пор 0,22 мкм до анализа. Профиль экспрессии RLI анализировали с применением SUPERDEX 200 5/150 GL в соответствии с инструкцией производителя. Для этого анализа использовали разбавленные (0,15мг/мл) и неразбавленные образцы. Использовали скорость потока 0,2 мл/мин и подвижный буфер PBS. Элюирование белков контролировали по абсорбционной способности при 215 нм.
[000127] Результаты различных очисток показаны в таблице I и на фигуре 1.
Таблица I
[000128] Результаты показывают наличие двух отличительных пиков на хроматограмме. Первый пик соответствует агрегатам, размер которых больше, чем 2000 кДа. Второй пик соответствует мономерной форме RLI. Также этот второй пик иногда содержит плечо (обозначенное стрелкой), которое может представлять димерную форму RLI.
[000129] Таким образом, продукция RLI частично содержит агрегаты. Такой вывод не удивителен, поскольку уже известно, что сам по себе IL15 характеризуется агрегацией на низких уровнях в культуральном супернатанте. На самом деле, такая агрегация представляет собой проблему, поскольку полученная композиция не может быть использована как фармацевтическая композиция.
[000130] Согласно литературным данным, причин для агрегации может быть несколько. Такая агрегация может происходить, начиная с процесса культивирования и до конечной процедуры заполнения. Причиной этой агрегации могут быть компоненты среды (белки клетки-хозяина, концентрация RLI или растворенный кислород), способ очистки (техника очистки (HIC, AEX, Афинная …), условия элюирования (pH, ионная сила, концентрация белка …), способ ультрафильтрации/диафильтрации (напряжение сдвига, поверхностная концентрация) или состав (буфер (pH, ионная сила, вспомогательное средство …). В связи с такой многопараметрической задачей, идентификация причины агрегации в ходе целостного процесса представляет собой сложную работу, результат которой не всегда является успешным.
[000131] 2) Анализ фракционирования
[000132] Для того, чтобы определить хроматографическое поведение очищенных компонентов и анализировать содержание каждого пика элюирования, образец предварительно очищенного белка анализировали с использованием SUPERDEX 75 10/300 GL в соответствии с инструкцией изготовителя. Для этого анализа использовали 50 мкл образца. Использовали скорость потока 1мл/мин и подвижный буфер PBS. Элюирование белков контролировали по абсорбционной способности при 215 нм.
[000133] Хроматограмма SEC (Size Exclusion Chromatography (эксклюзионная хроматография)) показана на фигуре 2, вестерн-блоттинг анализ нескольких элюированных фракций показан на фигуре 3, и результаты такой очистки приведены в таблице II.
Таблица II

[000134] Полученные результаты подтверждают существование первого пика, соответствующего эксклюзионному пределу колонки (Фигура 2). Этот пик включает растворимые агрегаты (> 110 кДа) белка RLI, которые включают гликозилированные и негликозилированные белки RLI (Фигура 3). Второй пик соответствует димеру RLI, а третий соответствует глобулярному белку размером 28,5 кДа, соответствующему мономерной форме RLI (Фигура 2). Капиллярный электрофорез показал, что этот третий пик включает гликозилированные и негликозилированные формы, но с элюированием с небольшим сдвигом (Фигура 3). В качестве контроля использовали белок, очищенный из Pichia pastoris . Как и предполагалось, гликозилированная форма элюировалась до негликозилированной.
[000135] И, наконец, распределение видов согласуется с предыдущим анализом с 49% олигомеров и/или агрегатов и 51% мономеров.
[000136] Было замечено, что температура хранения, т.е. 4°С или -80°C, не влияет на состояние олигомеризации RLI. Кроме того, данные результаты показали, что RLI очень стабилен при хранении при 4°C и также после 6 циклов замораживания/размораживания при -80°C.
[000137] Для того, чтобы лучше описать состояние агрегации RLI продуктов, применяют SEC-MALLS (эксклюзионная хроматография в сочетании с рассеиванием лазерного излучения с кратными углами). Этот способ позволяет определить распределение по размеру различных мультимерных видов, содержащихся в образце белка. С помощью этого способа, различные виды сначала отделяли и разбавляли с помощью SEC, а затем анализировали с помощью MALLS.
[000138] Для этого анализа использовали образцы белка весом приблизительно 35 мкг. Скорость потока составляла 0,35 мл/мин при 20°C с SEC буфером (4,3 мM Na2HPO4, 1,4 мM KH2PO4, 2,7 мM KCl, 137 мM NaCl) на SHODEX (kW402.5-4F) в соответствии с инструкцией изготовителя. Систему хроматографии INFINITY 1260 применяли в качестве детектора HPLC, DAW-HELEOS 8+ (WYATT TECHNOLOGIES) применяли в качестве детектора MALLS и OPTILAB-rEX.
[000139] На фигуре 4 показан пример SEC-MALLS хроматограммы для RLI продукта (для рассеивания излучения).
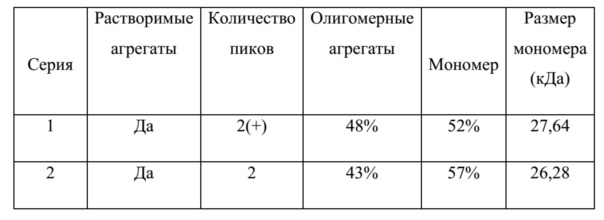
[000140] В таблице III описывают распределение различных белковых пиков для двух RLI серий при комнатной температуре и следующие три часа инкубации.
Таблица III

[000141] Результаты указывают на существование шести пиков белков с несколькими незначительными пиками, соответствующих различным формам RLI в большинстве образцов. В данном случае, эти пики не проявляют существенного развития в распределении после 3 часов инкубации при комнатной температуре.
[000142] Эти результаты подтверждают существование мультимерных форм в связи с мономерной.
[000143] 3) Первая стадия очистки
[000144] Первая стадия очистки была разработана для продукции RLI в Pichia pastoris. На первой стадии осветления различные супернатанты, полученные в ходе продукции RLI в клетках CHO фильтровали при помощи мембраны толщиной 0,22 мкм (целлюлозная). Данные супернатанты подвергали диафильтрации с помощью Tris HCl pH 7,5. Далее сульфат аммония (AS = (NH4)2SO4) растворяли в диафильтрованных супернатантах, с тем, чтобы получить окончательную концентрацию AS 1,5 М, соответствующую буферу для связывания. Колонки для хроматографии гидрофобного взаимодействия (Phenyl Sepharose FF) подвергали отбору с полученными буферами для связывания.
[000145] Далее осуществляли элюирование в соответствии с инструкцией производителя.
[000146] По сравнению с продукцией из Pichia pastoris, эта первая стадия показывает низкие результаты выхода и плохую воспроизводимость результатов.
[000147] В связи с некорректностью эксперимента, для первого этапа использовали анионнообменную хроматографию (AEX). Неожиданно авторы изобретения наблюдали, что эта специфическая хроматография позволяет получить очень высокий выход. Этого достигли в результате дальнейших экспериментов, которые давали очень высокий выход и наблюдалась очень высокая воспроизводимость.
[000148] Сравнительные эксперименты между DEAE-Sepharose и Q-Sepharose показали, что наилучший выход получается с помощью Q Sepharose, и, что оптимальный буфер для подбора на Q- или DEAE-Sepharose представлял собой 20 мM Tris HCl, pH 7,5, 1 M NaCl. Хотя инструкция производителя предполагает применение буфера для подбора, pH которого по меньшей мере на одну единицу ниже, чем pH белка для очистки, результаты неожиданно показали, что наилучший подбор наблюдается при pH равном или выше, чем 7,5 (Tris HCl буфер), который примерно на две единицы выше, чем pH белка RLI. В данном случае, низкий уровень pH приводит к скудным результатам подбора и, таким образом, к низкому выходу и воспроизводимости при очистке белков RLI.
[000149] Кроме того, предполагают, что ДНК клеток HO связывается с RLI, и элюат, полученный после первой стадии очистки, загрязнен этими ДНК.
[000150] 4) Вторая стадия очистки
[000151] Таким образом, чтобы получить свободную от нуклеиновой кислоты и эндотоксина композицию, авторы настоящего изобретения инициировали второй цикл очистки.
[000152] Наилучшие результаты получали с помощью колонок хроматографии гидрофобного взаимодействия (Phenyl Sepharose Butyl Sepharose, Octyl Sepharose) с 20 мM Tris HCl pH 7,5 - 2 M сульфата аммония (AS = (NH4)2SO4).
[000153] В данном случае, и что касается экспериментов с первой стадией очистки, эти эксперименты давали возможность получать белок RLI с очень низким выходом и воспроизводимостью.
[000154] Неожиданно авторы настоящего изобретения обнаружили, что смесь, т.е. смесь образца с сульфатом аммония, более быстро загружаемая после получения, дает лучшие результаты выхода и воспроизводимости. Предположительно, интервал стабильности соли белка зависит от множества параметров, в том числе температуры, оказывающих воздействие на процесс очистки. Следовательно, авторы настоящего изобретения для стадии подбора смешивают сульфат аммония - т.е. от 0,75 M-и первичный элюат непосредственно на колонках хроматографии гидрофобного взаимодействия.
[000155] После стадий отмывки и элюирования с применением градиента между буферным раствором A2 (20 мM Tris HCl, pH 7,5) и раствором буфера B2 (20 мM Tris HCl, 2 M сульфата аммония, pH 7,5), получали белок RLI с очень высоким выходом и воспроизводимостью при 37,5% градиента. Гликозилированная форма элюировалась слегка позже, чем негликозилированная форма, и окно элюирования гликозилированной формы частично перекрывается. Наконец, образец концентрировали от 0,5 до 1 мг/л на ультрафильтрационной кассете с MWCO (номинальное отсечение по молекулярной массе) 5 кДа, и подвергали диафильтрации против буфера PBS.
[000156] И, наконец, результаты, полученные с помощью способа очистки, разработанного авторами настоящего изобретения, показали, что белок RLI получаются с чистотой более 98%, без определяемого уровня эндотоксина, белков теплового шока или остаточной ДНК. Более того, анализ полученной композиции показал, что более 90% белка RLI находится в мономерной форме, удовлетворяющей его применению в фармацевтической композиции.
[000157] 5) Пролиферативная активность полученной фармацевтической композиции
[000158] Для того, чтобы оценить пролиферативную активность интерлейкина-15 очищенных белков, измеряли пролиферативные ответы клеток Kit 225 и 32Dβ на ICK указанных белков по включению тимидина[3H].
[000159] Клетки поддерживали в среде для культивирования в течение 3 дней, дважды промывали и истощали в среде без цитокина в течение 24 часов или 4 часов для набора 225 и 32Dβ, соответственно. Затем их высевали в многолуночные планшеты при 104 клеток/лунку в 100 мкл и культивировали в течение 48 часов в среде с добавлением возрастающей концентрации нескольких образцов RLI CHO. В качестве контроля использовали человеческий rIL-15 и RLI из бакуловируса и из Pichia pastoris .
[000160] Клетки сенсибилизировали в течение 16 ч. с использованием 0,5 мкКи/лунку [3H] тимидина, собирали на фильтры из стекловолокна и измеряли связанную с клетками радиоактивность.
[000161] На фигурах 5 и 6 показано включение тимидина [3H] клетками Kit 225 и 32Dβ соответственно, культивируемых с возрастанием концентраций rIL-15, RLI из бакуловируса, RLI из Pichia pastoris и RLI, очищенных из некоторой продукции CHO.
[000162] Результаты показывают, что биологическая активность белка RLI, очищенного с помощью способа по настоящему изобретению сравнима с таковой у частично очищенных белков RLI. Следовательно, способ очистки по настоящему изобретению не влияет на биологическую активность RLI.
[000163] 6) Биоактивность полученной фармацевтической композиции в мышиной модели in vivo
[000164] Мышам C57BL/6, полученным из Harlan Laboratories, в день 0 и в день 1 в качестве отрицательного контроля внутрибрюшинно (i.p) вводили 100 мкл PBS, RLI из бакуловируса (2 мкг/мышь), RLI из Pichia pastoris (2 мкг/мышь) и RLI, очищенный из продукции CHO (2 мкг/мышь). В каждой группе использовали 5 мышей.
[000165] На 4 день мышей умерщвляли посредством цервикальной дислокации и селезенки удаляли. Селезенку диссоциировали в суспензию отдельных клеток на 100 мкм-клеточном фильтре, за которым находился шприц. Затем клетки крови лизировали с помощью раствора ACK (Ammonium-Chloride-Potassium (аммоний-хлорид-калия). Спленоциты промывали дважды в полной среде и жизнеспособные клетки подсчитывали с помощью сетки для подсчета Kova. Для отбора жизнеспособных клеток два миллиона спленоцитов окрашивали следующими антителами: к CD3, CD4, CD8, NKp46 и LIVE/DEAD® Fixable Aqua. Далее спленоциты пермеабилизировали в соответствии с инструкцией производителя (буферы для пермеабилизации eBioscience FoxP3) и окрашивали с помощью антител к FoxP3 и Ki67. Изотип Ki67 использовали для определения положительных клеток. Окрашенные клетки сразу перемещали на проточный цитометр FACSCanto II и анализы выполняли при помощи программного обеспечения FlowJo (Tree Star). NK клетки представляют собой CD3 негативные NKp46 положительные клетки.
[000166] На фигуре 7 представлена доля пролиферирующих NK клеток, CD8+ T клеток, Foxp3+ CD4+ T клеток и Foxp3- CD4+ T клеток.
[000167] На фигуре 7 показано соотношение NK клеток и абсолютного количества NK клеток для каждой группы.
[000168] На фигуре 7 также показан процент пролиферирующих NK клеток по сравнению с общим числом NK клеток и абсолютным числом пролиферирущих клеток NK.
[000169] Результаты показывают, что RLI, продуцируемый в Pichia pastoris проявляет низкий уровень активности in vivo по сравнению с RLI, продуцируемым в бакуловирусе. Удовлетворительно, что RLI, продуцируемый в CHO и очищенный с помощью способа по настоящему изобретению проявляет очень хорошую активность in vivo в отношении NK клеток.
Реферат
Группа изобретений относится к улучшенному способу биохимического извлечения конъюгата на основе IL-15/IL-15Rα в мономерной форме и фармацевтической композиции, включающей эффективное количество композиции, содержащей мономерные конъюгаты IL-15/IL-15Rα. Способ предусматривает очистку осветленного супернатанта из культуральной средытрансформированной клетки-хозяина, экспрессирующей конъюгат, имеющий аминокислотную последовательность SEQ ID NO:16 или SEQ ID NO:17. Очистку проводят посредством анионообменной хроматографии (AEX) при pH, равном или выше чем 7,0, предпочтительно равном или выше чем 7,5. Далее полученный элюат очищают хроматографией гидрофобного взаимодействия (HIC), проводимой в буферном растворе, содержащем 0,75 М - 2,5 М сульфата аммония, предпочтительно 1 М - 2 М сульфата аммония. Элюируют конъюгаты в градиенте от 2 М до 0 M, предпочтительно от 1,5 до 0 M сульфата аммония. Полученная композиция содержит по меньшей мере 80% конъюгатов в мономерной форме, удовлетворяющей их применению в фармацевтической композиции для лечения ракового заболевания у субъекта. Изобретения позволяют получать конъюгат с высоким выходом и воспроизводимостью, с чистотой более 98%, без определяемого уровня эндотоксина, белков теплового шока или остаточной ДНК. 2 н. и 6 з.п. ф-лы, 7 ил., 3 табл.
Формула
Документы, цитированные в отчёте о поиске
Композиции и способы достижения иммунной супрессии
Модуляция il-2- и il-15-опосредованных т-клеточных ответов

Комментарии