Химерные аналоги соматостатина-дофамина - RU2277539C2
Код документа: RU2277539C2
Описание
Предпосылки изобретения
Настоящее изобретение относится к химерным аналогам соматостатина-дофамина.
Дофамин представляет собой катехоламиновый нейротрансмиттер, который вовлечен в патогенез болезни Паркинсона и шизофрении. Graybiel, et al., Adv. Neurol. 53, 17-29 (1990); Goldstein, et al., FASEB J. 6, 2413-2421 (1992); Olanow, et al., Annu. Rev. Neurosci. 22, 123-144 (1999). Egan, et al., Curr. Opin. Neurobiol. 7, 701-707 (1997). Дофамин и родственные молекулы, как было показано, ингибируют рост некоторых типов злокачественных опухолей у мышей, и данная активность различным образом объясняется ингибированием пролиферации опухолевых клеток, стимуляцией противоопухолевого иммунитета или действием на метаболизм меланина в злокачественных меланомах. Wick, M.M., J. Invest. Dermatol. 71, 163-164 (1978); Wick, M.M., J. Natl. Cancer Inst. 63, 1465-1467 (1979); Wick, M.M., Cancer Treat Rep. 63, 991-997 (1979); Wick, M.M., Cancer Res. 40, 1414-1418 (1980); Wick, M.M., Cancer Treat Rep. 65, 861-867 (1981); Wick, M.M. & Mui, J. Natl. Cancer Inst 66, 351-354 (1981); Dasgupta, et al., J. Cancer Res. Clin. Oncol. 113, 363-368 (1987); Basu, et al., Endocrine 12, 237-241 (2000); Basu, et al., J. Neuroimmunol. 102, 113-124 (2000). Последние исследования продемонстрировали наличие D2-дофаминовых рецепторов на эндотелиальных клетках. Ricci, et al., J. Auton. Pharmacol, 14, 61-68 (1994); Bacic, et al., J. Neurochem. 57, 1774-1780 (1991). Недавно появилось сообщение о том, что дофамин сильно и избирательно ингибирует при нетоксичных уровнях активность по повышению проницаемости сосудов и ангиогенную активность VPF/VEGF. Basu et al., Nat. Med. 7 (5), 569-574 (2001).
Показано, что соматостатин (SS), тетрадекапептид, открытый Brazeau et al., оказывает мощное ингибирующее действие на различные секреторные процессы в тканях, таких как гипофиз, поджелудочная железа и желудочно-кишечный тракт. SS также действует как нейромодулятор в центральной нервной системе. Данные биологические эффекты SS, все ингибирующие по природе, осуществляются через серию связанных с G-белком рецепторов, пять различных подтипов которых охарактеризованы (SSTR1-SSTR5) (Reubi JC, et al., Cancer Res 47: 551-558, Reisine T, et al., Endocrine Review 16: 427-442, Lamberts SW, et al., Endocr Rev 12: 450-482, 4 Patel YC, 1999 Front Neuroendocrinology 20: 157-198). Данные пять подтипов имеют сходные аффинности в отношении эндогенных лигандов SS, но имеют разное распределение в различных тканях. Соматостатин связывается с пятью различными подтипами рецептора (SSTR) с относительно высокой и равной аффинностью для каждого подтипа.
Имеется подтверждение того, что SS регулирует пролиферацию клеток путем торможения клеточного роста через подтипы SSTR1, 2, 4 и 5 (Buscail L, et al., 1995 Proc Natl Acad Sci USA 92: 1580-1584; Buscail L, et al., 1994 Proc Natl Acad Sci USA 91: 2315-2319; Florio T, et al., 1999 Mol Endocrinol 13: 24-37; Sharma K, et al., 1999 Mol Endocrinol 13: 82-90) или путем индукции апоптоза через подтип SSTR3 (Sharma K, et al., 1996 Mol Endocrinol 10: 1688-1696). SS и различные его аналоги, как было показано, ингибируют пролиферацию нормальных клеток и клеток неоплазии in vitro и vivo (Lamberts SW, et al., Endocr Rev 12: 450-482) через специфические рецепторы SS (SSTR) (Patel YC, 1999 Front Neuroendocrinology 20: 157-198) и возможно путем различных послерецепторных действий (Weckbecker G, et al., Pharmacol Ther 60: 245-264; Bell GI, Reisine T 1993 Trends Neurosci 16: 34-38; Patel YC, et al., Biochem Biophys Res Commun 198: 605-612; Law SF, et al., Cell Signal 7: 1-8). Кроме того, имеется подтверждение, что различные подтипы SSTR экспрессируются в нормальных и неопластических тканях человека (9), обеспечивая различную тканевую аффинность для разных аналогов SS и различный клинический ответ на их терапевтическое действие.
Связывание с различными видами подтипов рецепторов соматостатина ассоциировано с лечением различных состояний и/или заболеваний. («SSTR2») (Raynor, et al., Molecular Pharmacol. 43: 838 (1993); Lloyd, et al., Am. J. Physiol. 268:G102 (1995)), в то время как ингибирование инсулина приписывается рецептору соматостатина 5 типа («SSTR5») (Coy, et al. 197: 366-371 (1993)). Активация типов 2 и 5 ассоциирована с подавлением гормона роста, и, более конкретно, секретирующих GH аденом (акромегалия) и секретирующих TSH тиреотропный гормон аденом. Активация типа 2, но не типа 5, ассоциирована с лечением секретирующих пролактин аденом. Другие показания, связанные с активацией подтипов рецепторов соматостатина, включают ингибирование инсулина и/или глюкагона для лечения сахарного диабета, ангиопатии, пролиферативной ретинопатии, феномена «утренней зари» и нефропатии; ингибирование секреции кислоты в желудке и, более конкретно, пептических язв, кишечного или панкреатического свища, синдрома раздраженной толстой кишки, демпинг-синдрома, синдрома водянистой диареи, связанной со СПИД диареи, индуцированной химиотерапией диареи, острого или хронического панкреатита и опухолей, секретирующих желудочно-кишечные гормоны; лечение злокачественной опухоли, такой как гепатома; ингибирование ангиогенеза; лечение воспалительных нарушений, таких как артрит; ретинопатию; хроническое отторжение аллотрансплантата; ангиопластику; предотвращение кровотечения из сосудов трансплантата и гастроинтестинального кровотечения. Предпочтительно иметь в распоряжении аналог, селективный для конкретного подтипа или подтипов соматостатинового рецептора, ответственных за требуемую биологическую реакцию, таким образом, снижая взаимодействие с другими подтипами рецептора, которое может привести к нежелательным побочным эффектам.
Соматостатин (SS) и его рецепторы (SSTR1-SSTR5) экспрессируются в нормальных парафолликулярных С-клетках человека и медуллярной карциноме щитовидной железы (MTC). MTC представляет собой опухоль, происходящую из парафолликулярных C-клеток щитовидной железы, которая продуцирует кальцитонин (CT), соматостатин, а также несколько других пептидов (Moreau JP, et al., Metabolism 45 (8 Suppl 1): 24-26). Недавно Mato et al. показали, что SS и SSTR экспрессированы в MTC человека (Mato E, et al., J Clin Endocrinol Metab 83: 2417-2420). Было документировано, что SS и его аналоги индуцируют снижение в плазме уровней CT и симптоматическое улучшение у пациентов с MTC. Однако до сих пор антипролиферативная активность аналогов SS в отношении опухолевых клеток не была ясно продемонстрирована (Mahler C, et al., Clin Endocrinol 33: 261-9; Lupoli G, et al., Cancer 78: 1114-8; Smid WM, et al., Neth J Med 40: 240-243). Таким образом, разработка и оценка аналогов подтипы SSTR, селективных в отношении роста клеток MTC предоставляет подходящий способ для клинического применения. До сих пор не приводились данные, касающиеся участия в регуляции роста клеток МТС конкретных подтипов SSTR.
Сущность изобретения
Настоящее изобретение относится к открытию серии химерных аналогов соматостатина-дофамина, которые сохраняют in vivo как соматостатиновую, так и дофаминовую активность, включая некоторые из них, которые проявляют повышенную биологическую активность по сравнению с отдельными нативными аналогами соматостатина и дофамина, и к их терапевтическим применениям.
В одном из аспектов изобретение относится к химерному соединению дофамина-соматостатина формулы (I),

где:
Х представляет собой H, Cl, Br, I, F, -CN или C1-5алкил;
R1 представляет собой H, C1-4алкил, аллил, алкенил или -CN;
R2 и R3 оба независимо представляют собой H или отсутствуют, причем если R2 и R3 отсутствуют, между атомами углерода, к которым они присоединены, присутствует двойная связь;
R4 представляет собой H или -CH3;
Y представляет собой -O-, -C(O)-, -S-, -S-(CH2)s-C(O)-, -S(O)-, -S(O)2-, -SC(O)-, -OC(O)-, -N(R5)-C(O)- или -N(R6)-;
R5, R6, R7 и R8 каждый независимо представляет собой H или C1-5алкил;
R6 представляет собой H или C1-5алкил;
m представляет собой 0 или 1;
n представляет собой 0-10;
L представляет собой -(CH2)p-C(O)-, когда Y представляет собой -S-, -S(O)-, -S(O)2-, -O- или -N(R6)-;
L представляет собой -C(O)-(CR7R8)q-C(O)-, когда Y представляет собой -N(R6)-, -O- или -S-;
L представляет собой -(Doc)t-, когда Y представляет собой -C(O)-, SC(O)-, -OC(O)-, -S-(CH2)s-C(O)- или -N(R5)-C(O)-;
p представляет собой 1-10;
q представляет собой 2-4;
s представляет собой 1-10;
t представляет собой 1-10; и
Z представляет собой аналог соматостатина,
или его фармацевтически приемлемой соли.
В другом аспекте изобретение относится к химерному соединению дофамина-соматостатина формулы (II),

где:
X представляет собой H, Cl, Br, I, F, -CN или C1-5алкил;
R1 представляет собой C1-4алкил, H, аллил, алкенил или -CN;
R2 и R3 оба независимо представляют собой H или отсутствуют, причем если R2 и R3 отсутствуют, между атомами углерода, к которым они присоединены, присутствует двойная связь;
R4 представляет собой H или -CH3;
R5 представляет собой C1-5алкильную группу или группу формулы -(CH2)rN(CH3)q;
Y представляет собой -O-, -C(O)-, -S-, -SC(O)-, -OC(O)-, -N(R6)-C(O)-, -N(R7)- или -N(R8)-(CH2)s-C(O)-;
R6, R7, R8, R9 и R10 каждый независимо представляет собой H или C1-5алкил;
L представляет собой -(CH2)p-C(O)-, когда Y представляет собой -S-, -O- или -N(R7)-;
L представляет собой -C(O)-(CR9R10)q-C(O)-, когда Y представляет собой -N(R7)-, -O- или -S-;
L представляет собой -(Doc)t-, где Y представляет собой -C(O)-, SC(O)-, -OC(O)-, -N(R8)-(CH2)s-C(O)- или -N(R6)-C(O)-;
m представляет собой 0 или 1;
n представляет собой 2-10;
r представляет собой 1-8;
q представляет собой 2-4;
p представляет собой 1-10;
s представляет собой 1-10;
t представляет собой 1-10; и
Z представляет собой аналог соматостатина,
или его фармацевтически приемлемой соли.
В одном из осуществлений изобретение относится к соединению формулы:




Caeg=N-(2-аминоэтил)-N-(2-цитозинил-1-оксоэтил)глицин






























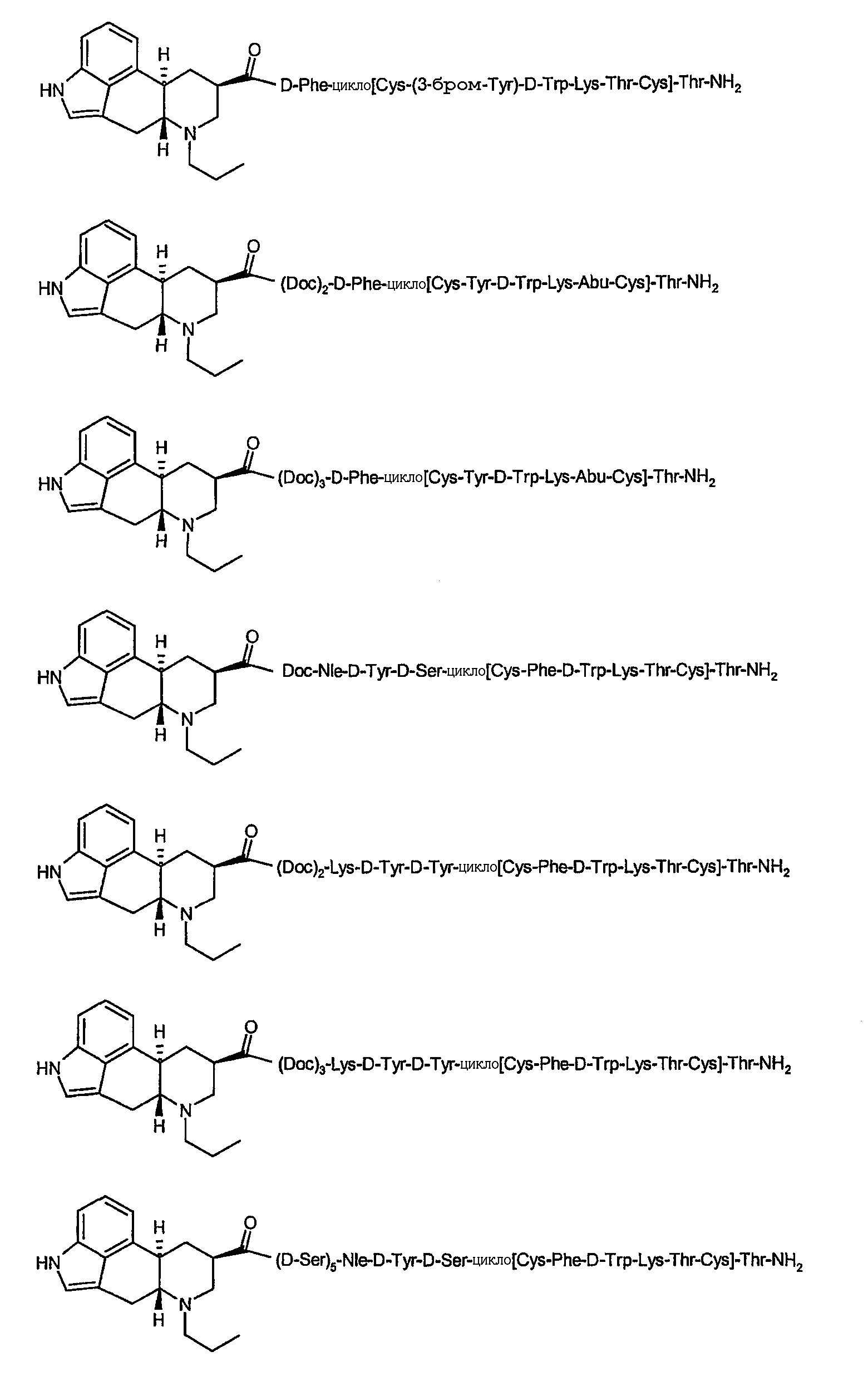
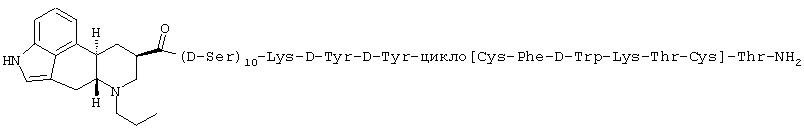






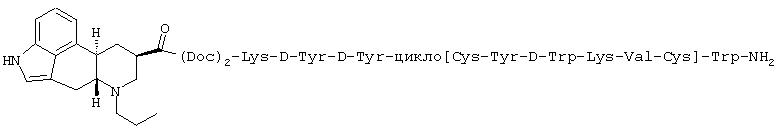





























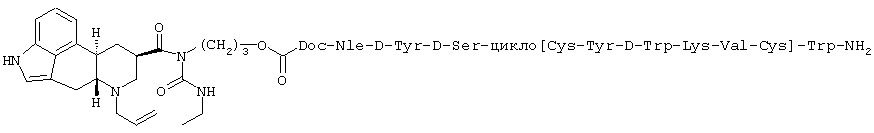


























AEPA=4-(2-аминоэтил)-1-карбоксиметилпиперазин






или к его фармацевтически приемлемой соли.
В другом осуществлении изобретение относится к соединению формулы:




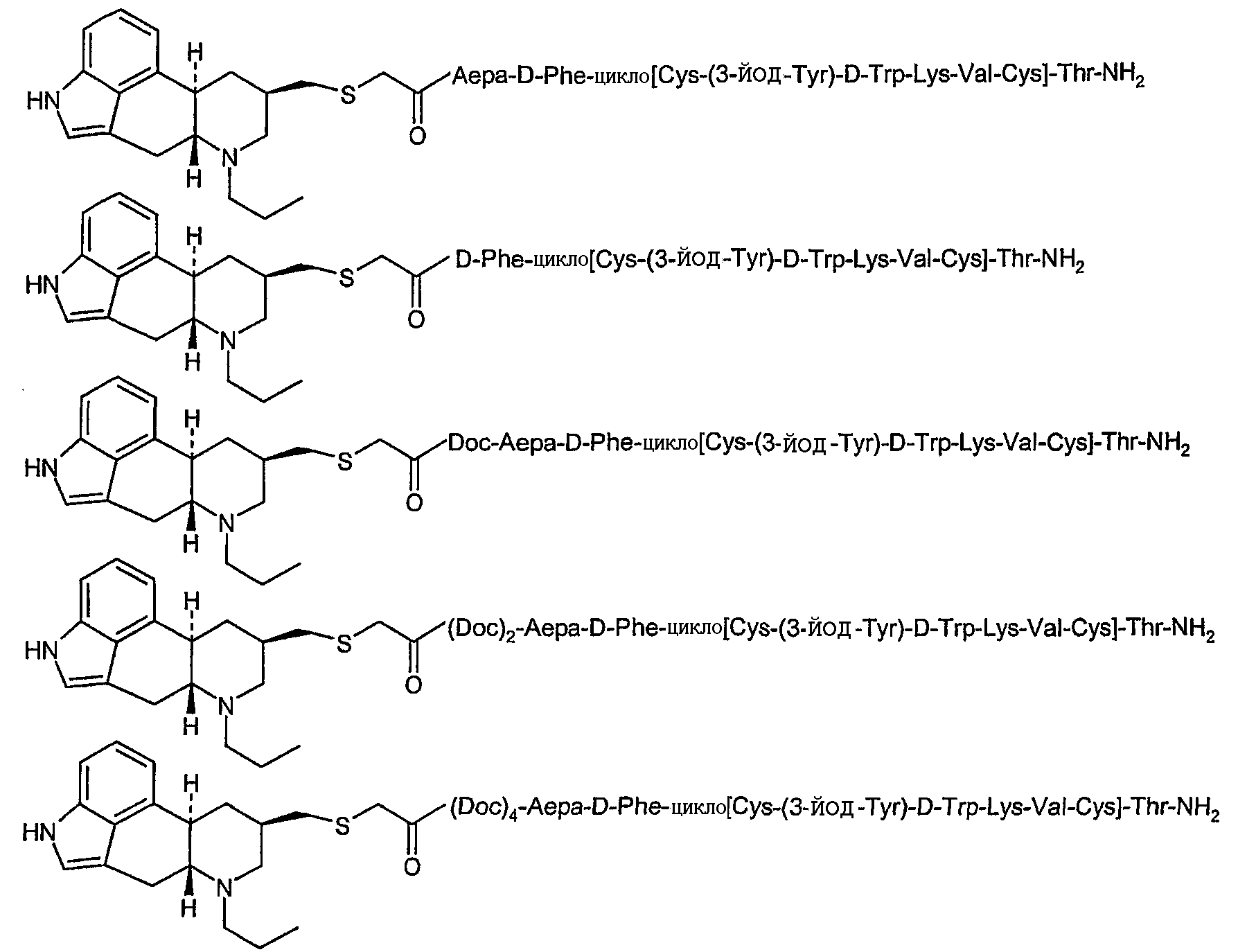












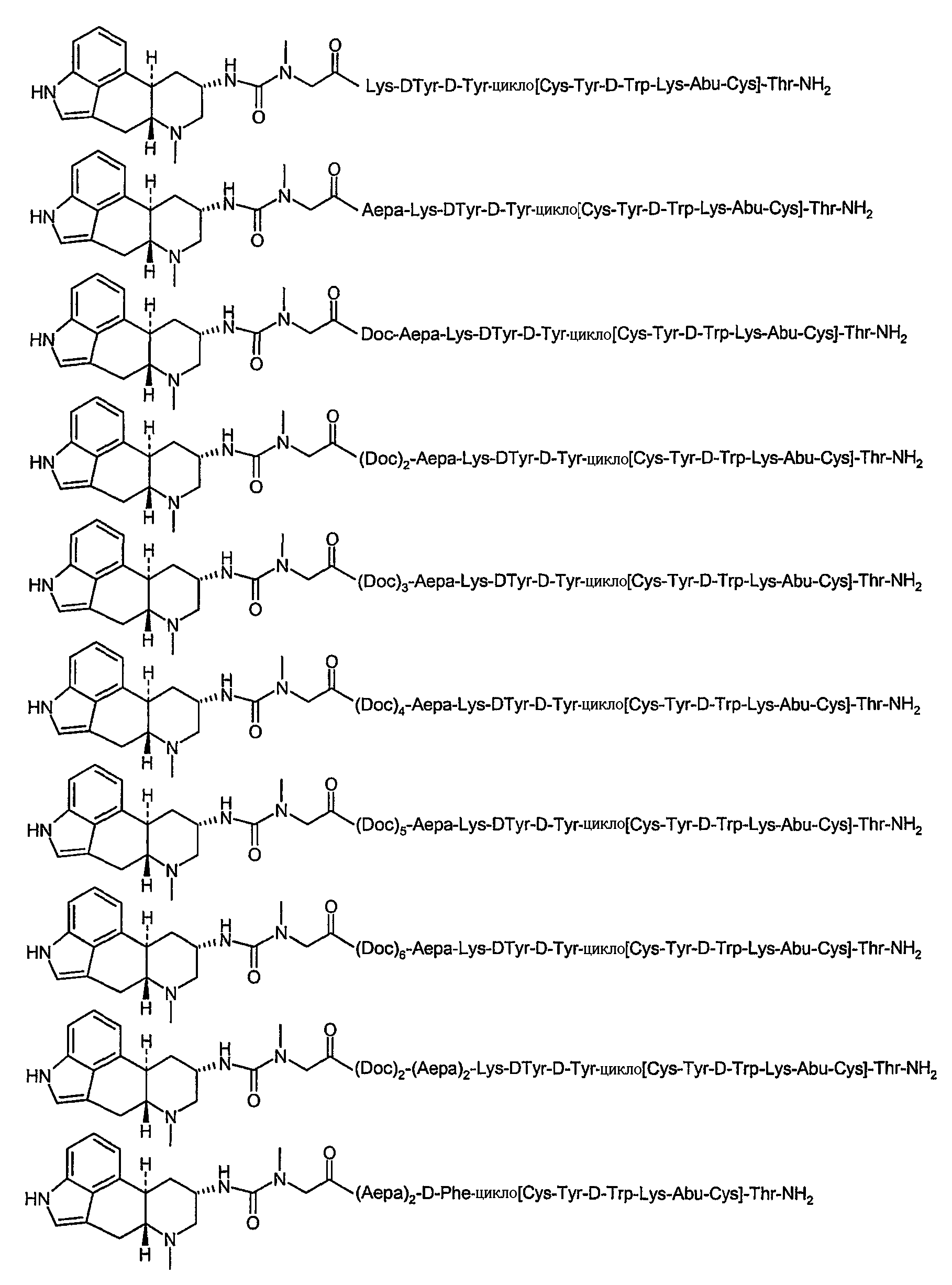





или к его фармацевтически приемлемой соли.
В одном из аспекте изобретение относится к способу индукции эффекта агониста дофаминового рецептора у нуждающегося в этом субъекта, где указанный способ включает введение указанному субъекту эффективного количества соединения формулы (I) или формулы (II), или его фармацевтически приемлемой соли. В предпочтительном осуществлении данного аспекта соединение выбирают из конкретно описываемых соединений.
В другом аспекте изобретение относится к способу индукции эффекта агониста соматостатинового рецептора у нуждающегося в этом субъекта, где указанный способ включает введение указанному субъекту эффективного количества соединения формулы (I) или формулы (II), или его фармацевтически приемлемой соли. В предпочтительном осуществлении данного аспекта соединение выбирают из конкретно описываемых соединений.
В другом аспекте изобретение относится к способу одновременной индукции эффекта агониста дофаминового рецептора и эффекта агониста соматостатинового рецептора у нуждающегося в этом субъекта, где указанный способ включает введение указанному субъекту эффективного количества соединения формулы (I) или формулы (II), или его фармацевтически приемлемой соли. В предпочтительном осуществлении данного аспекта соединение выбирают из конкретно описываемых соединений.
В другом аспекте изобретение относится к фармацевтической композиции, содержащей эффективное количество соединения формулы (I) или формулы (II), или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель. В предпочтительном осуществлении данного аспекта соединение выбирают из конкретно описываемых соединений.
В другом аспекте изобретение относится к способу лечения у субъекта заболевания или состояния, причем указанный способ включает введение указанному субъекту терапевтически эффективного количества соединения формулы (I) или формулы (II), или его фармацевтически приемлемой соли, где указанное заболевание выбрано из перечня, состоящего из рака легких, глиомы, анорексии, гипотиреоза, гиперальдостеронизма, пролиферации H. pylori, акромегалии, рестеноза, болезни Крона, системного склероза, внешних и внутренних панкреатических псевдоцист и асцитов, випомы, гиперплазии островковых клеток поджелудочной железы, гиперинсулинизма, гастриномы, синдрома Золлингера-Эллисона, диарреи, связанной со СПИД диарреи, связанной с химиотерапией диарреи, склеродермы, синдрома раздраженной толстой кишки, панкреатита, обструкции тонкого кишечника, желудочно-пищеводного рефлюкса, дуоденогастрального рефлюкса, синдрома Кушинга, гонадотропиномы, гиперпаратиреоидизма, базедовой болезни, диабетической невропатии, болезни Педжета, поликистоза яичника, рака щитовидной железы, гепатомы, лейкоза, менингиомы, кахексии при злокачественной опухоли, ортостатической гипотензии, послеобеденной гипотензии, острого тревожного состояния с реакцией паники, секретирующих GH аденом, акромегалии, секретирующих TSH аденом, секретирующих пролактин аденом, инсулиномы, глюкагономы, сахарного диабета, гиперлипидемии, нечувствительности к инсулину, синдрома Тернера, ангиопатии, пролиферативной ретинопатии, феномена «восходящего солнца», нефропатии, гиперсекреции кислоты желудка, пептических язв, кишечного свища, панкреатического свища, демпинг-синдрома, синдром водянистой диареи, панкреатита, секретирующий гастроинтестинальные гормоны опухоли, ангиогенеза, артрита, отторжения аллотрансплантата, кровотечения из сосудов трансплантата, портальной гипертезии, желудочно-кишечного кровотечения, ожирения и передозировки опиоидов. В предпочтительном осуществлении данного аспекта соединение выбирают из конкретно описанных здесь соединений. В более предпочтительном осуществлении данного аспекта изобретения указанное заболевание или состояние представляет собой акромегалию.
В особенно предпочтительном осуществлении каждого из следующих способов соединение выбирают из списка соединений, состоящего из соединений от соединения A до соединения K, или из списка соединений, состоящего из соединений от примера L до примера V, как описано ниже в разделе под заголовком «Синтез химерных соединений соматостатина-дофамина».В другом аспекте изобретение относится к агонисту дофамина формулы (I) или формулы (II), приведенных выше, где аналог соматостатина «z» заменен группой, включающей -H, -OH, (C1-C6)алкокси, арилалкокси, (например, бензилом, замещенным бензилом и подобным), -NH2, -NR9R10, где R9 и R10 определены в формуле (II). В предпочтительном осуществлении данного аспекта указанный агонист дофамина выбирают из компонентов дофаминовой группы описываемых химерных соединений дофамина-соматостатина или их фармацевтически приемлемой соли. В наиболее предпочтительном осуществлении данного аспекта указанный агонист дофамина представляет собой:

или их фармацевтически приемлемую соль.
Подробное описание изобретения
Предполагается, что специалист в данной области может, основываясь на приведенном описании, применять настоящее изобретение в полнейшей степени. Поэтому подразумевается, что следующие конкретные осуществления являются сугубо иллюстративными и никоим образом не ограничивают остальной части изобретения.
Кроме иначе определенных случаев, все используемые в данном описании технические и научные термины имеют то же самое значение, которое обычно подразумевается обычным специалистом в данной области, к которой относится данное изобретение. Кроме того, все публикации, патентные заявки, патенты и другие, приведенные в данном описании источники информации, включены в данное описание во всей своей полноте посредством ссылки.
Выделены различные рецепторы соматостатина (SSTR), например, SSTR-1, SSTR-2, SSTR-3, SSTR-4 и SSTR-5. Таким образом, агонист соматостатина может быть агонистом SSTR-1, агонистом SSTR-2, агонистом SSTR-3, агонистом SSTR-4 или агонистом SSTR-5, и при этом относиться к одному или нескольким из указанных типов. Это означает, что, например, агонист рецептора соматостатина типа 2 (т.е. агонист SSTR-2) представляет собой соединение, которое имеет высокую аффинность связывания (например, Ki менее 100 нМ, или предпочтительно менее 10 нм, или более предпочтительно менее 1 нМ) с SSTR-2 (что, например, определено посредством анализа связывания рецептора, описанного ниже). Под селективным агонистом соматостатинового рецептора типа 2, например, подразумевается агонист соматостатинового рецептора типа 2, который обладает более высокой аффинностью связывания (например, более низкой Ki) с SSTR-2, чем с любым другим соматостатиновым рецептором.
В одном из осуществлений агонист SSTR-2 также представляет собой селективный агонист SSTR-2. Примеры агонистов SSTR-2, которые могут использоваться для осуществления настоящего изобретения на практике, включают в качестве неограничивающих примеров:
D-Nal-цикло[Cys-Tyr-D-Trp-Lys-Val-Cys]-Thr-NH2;
цикло[Tic-Tyr-D-Trp-Lys-Abu-Phe];
4-(2-гидроксиэтил)-1-пиперазинилацетил-D-Phe-цикло(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и
4-(2-гидроксиэтил)-1-пиперазин-2-этансульфонил-D-Phe-цикло(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2.
Дальнейшими примерами агонистов соматостатина являются те, что охватываются формулами, или те, что конкретно цитированы в приведенных ниже публикациях, каждая из которых включена в данное описание во всей своей полноте в качестве ссылки.
Заявка на выдачу Европейского патента №P5 164 EU (автор изобретения: G. Keri);
Van Binst, G. et al. Peptide Research 5: 8 (1992);
Horvath, A. et al. Abstract, "Conformations of Somatostatin Analogs Having Antitumor Activity", 22nd European peptide Symposium, September 13-19, 1992, Interlaken, Switzerland;
Заявка PCT №WO 91/09056 (1991);
Заявка на выдачу Европейского патента №0 363 589 A2 (1990);
Патент США №4904642 (1990);
Патент США №4871717 (1989);
Патент США №4853371 (1989);
Патент США №4725577 (1988);
Патент США №4684620 (1987);
Патент США №4650787 (1987);
Патент США №4603120 (1986);
Патент США №4585755 (1986);
Заявка на выдачу Европейского патента №0 203 031 A2 (1986);
Патент США №4522813 (1985);
Патент США №4486415 (1984);
Патент США №4485101 (1984);
Патент США №4435385 (1984);
Патент США №4395403 (1983);
Патент США №4369179 (1983);
Патент США №4360516 (1982);
Патент США №4358439 (1982);
Патент США №4328214 (1982);
Патент США №4316890 (1982);
Патент США №4310518 (1982);
Патент США №4291022 (1981);
Патент США №4238481 (1980);
Патент США №4235886 (1980);
Патент США №4224199 (1980);
Патент США №4211693 (1980);
Патент США №4190648 (1980);
Патент США №4146612 (1979);
Патент США №4133782 (1979);
Патент США №5506339 (1996);
Патент США №4261885 (1981);
Патент США №4728638 (1988);
Патент США №4282143 (1981);
Патент США №4215039 (1980);
Патент США №4209426 (1980);
Патент США №4190575 (1980);
Европейский патент №0 389 180 (1990);
Заявка на выдачу Европейского патента №0 505 680 (1982);
Заявка на выдачу Европейского патента №0 083 305 (1982);
Заявка на выдачу Европейского патента №0 030 920 (1980);
Заявка PCT №WO 88/05052 (1988);
Заявка PCT №WO 90/12811 (1990);
Заявка PCT №WO 97/01579 (1997);
Заявка PCT №WO 91/18016 (1991);
Заявка на выдачу патента Великобритании №GB 2095261 (1981); и
Заявка на выдачу патента Франции №FR 2522655 (1983).
Необходимо отметить, что для всех описываемых агонистов соматостатина каждый аминокислотный остаток представляет собой структуру -NH-C(R)H-CO-, в которой R представляет собой боковую цепь (например, CH3 для Ala). Линии между аминокислотными остатками представляют собой пептидные связи, которые соединяют аминокислоты. Также, в случае, где аминокислотный остаток оптически активен, он находится в конфигурации L-формы, которая подразумевается, если D-форма специально не обозначена. Для простоты дисульфидные связи (например, дисульфидный мостик), существующие между двумя свободными тиолами остатков Cys не показаны. Обозначения обычных аминокислот приводятся согласно рекомендациям IUPAC-IUB.
Синтез агонистов соматостатина
Способы синтеза пептидных агонистов соматостатина хорошо описаны в литературе и находятся в компетенции обычного специалиста в данной области. Например, пептиды синтезируют на амидной MBHA-смоле Rink (смола 4-(2',4'-диметоксифенил-Fmoc-аминометил)феноксиацетамидонорлейцил-MBHA) с использованием стандартного протокола твердофазного синтеза Fmoc-химии. Комплекс пептид-смола со свободной функциональной аминогруппой на N-конце затем обрабатывают соответствующим соединением, содержащим дофаминовую группу. Конечный продукт отщепляют от смолы смесью TFA/вода/триизопропилсилан (TIS).
Например, синтез H-D-Phe-Phe-Phe-D-Trp-Lys-Thr-Phe-Thr-NH2 может быть осуществлен, следуя методике, указанной в примере I заявки на выдачу Европейского патента 0 395 417 A1. Синтез агонистов соматостатина с замещенным N-концом, например, может быть осуществлен, следуя методике, указанной в публикации заявки PCT №WO 88/02756, публикации заявки PCT №WO 94/04752, и/или в заявке на выдачу Европейского патента 0 329 295.
Пептиды могут быть и были циклизованы с использованием раствора йода в смеси MeOH/вода и очищены на C18 препаративной ВЭЖХ с обращенной фазой с использованием буферов ацетонитрил-0,1% TFA/вода-0,1% TFA. Гомогенность оценивали аналитической ВЭЖХ и масс-спектрометрии, и определили, что она составляла >95% для каждого пептида.
Некоторые редкие аминокислоты приобретали у следующих торговых компаний:
Fmoc-Doc-OH и Fmoc-AEPA приобретали у Chem-Impex International, Inc. (Wood Dale, Иллинойс, США). Fmoc-Caeg(Bhoc)-OH приобретали у PerSeptive Biosystems (Framingham, Массачусетс, США). Bhoc обозначает бензгидрилоксикарбонил.
Синтез агонистов дофамина
Способы синтеза многих агонистов дофамина также хорошо описаны в литературе и находятся в компетенции обычного специалиста в данной области. Дальнейшие методики синтеза представлены следующими схемами реакций и примерами.
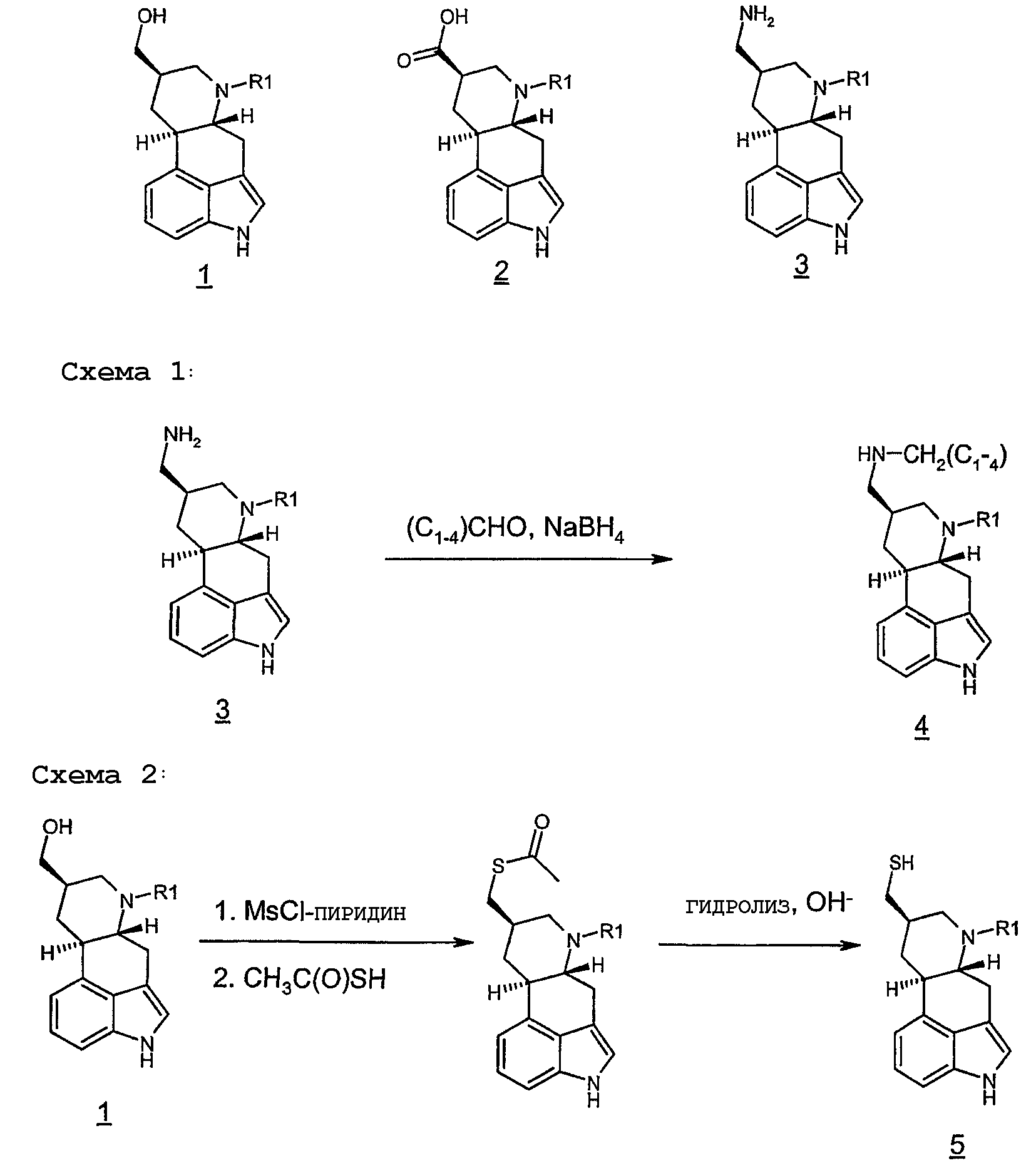














Синтез химерных соединений соматостатина-дофамина
Химерные соединения соматостатина могут быть синтезированы по следующим схемам реакций и примерам. Исходный продукт и промежуточные продукты соединений (I), (II) и (III), отображенные на схеме I, II и III, соответственно, коммерчески доступны или их получают по литературным источникам; Pharmazie 39, 537 (1984); Collect Czech. Chem. Commun. 33, 577 (1966); Helv. Chim. Acta 32, 1947, (1949); патент США 5097031; патент США 3901894; EP 0003667; патент США 4526892. Синтез пептидов находится в компетенции специалиста в данной области и, в любом случае, легко доступен из литературы. См., например, Stewart et al., Solid Phase Synthesis, Pierce Chemical, 2nd Ed. 1984; G.A. Grant; Synthetic peptide. WH., Freenand Co., New York, 1992; M. Bodenszky, A. Bodanszky, The Practice of Peptide Synthesis. Spring Venlag. N. Y. 1984.
Получение соединения A:

Соединение 8 (3 экв.) смешивают с H-(Doc)3 -D-Phe-Cys(Acm)-Tyr(tBu)-D-Trp(Boc)-Lys(Boc)-Abu-Cys(Acm)-Thr(tBu)-амидной MBHA-смолой Rink (1 экв.), HBTU (2,9 экв.), HOBt (3,0 экв.) и DIEA (6 экв.) в DMF. Смесь встряхивают при комнатной температуре в течение 4 часов. Смолу промывают DMF и DCM и сушат при пониженном давлении досуха. Сухую смолу обрабатывают смесью TFA/TIS/вода (92/5/3, об./об.) в течение 1 ч при комнатной температуре. Раствор фильтруют и концентрируют. К концентрированному раствору добавляют холодный простой эфир. Осадок собирают и растворяют в системе растворителей вода-метанол. К раствору добавляют раствор йода в метаноле до появления бурой окраски. Затем раствор выдерживают при комнатной температуре в течение 1 часа. К раствору добавляют водный раствор Na2S2О3 до исчезновения бурой окраски. Полученный в результате раствор очищают с использованием C18 препаративной ВЭЖХ с обращенной фазой, элюируя линейным градиентом смеси буфер A (1% TFA в воде)/буфер B (1% TFA в CH3CN). Фракции проверяют аналитической ВЭЖХ. Фракции, содержащие чистое требуемое соединение, объединяют и лиофилизируют досуха. Молекулярную массу соединения измеряют, используя MS, сопряженной с источником электроспрея.
Получение соединения B:
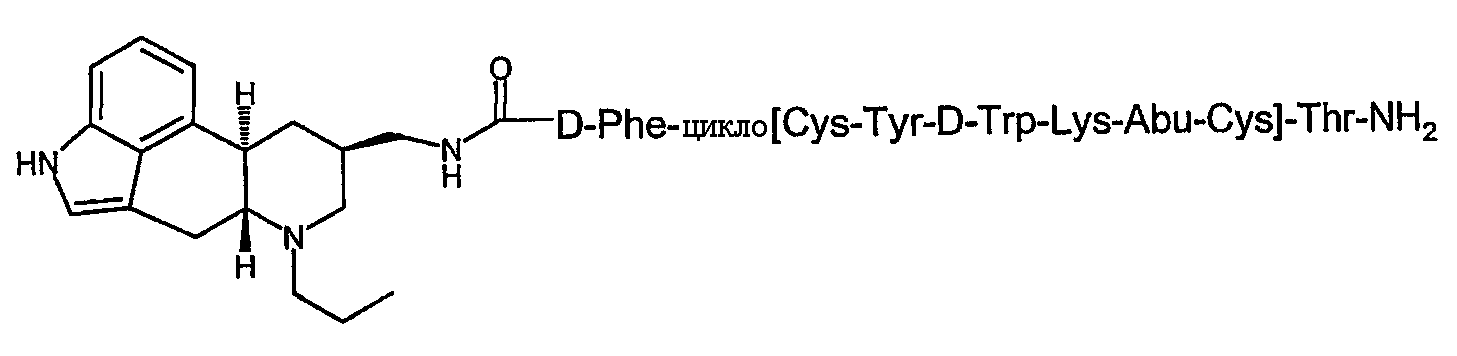
Соединение 12, где R1 представляет собой н-пропил, (1,5 экв.) смешивают с H-D-Phe-Cys(Acm)-Tyr(tBu)-D-Trp(Boc)-Lys(Boc)-Abu-Cys(Acm)-Thr(tBu)-амидной MBHA-смолой Rink (1 экв.) и DIEA (2 экв.) в DMF. Смесь встряхивают при комнатной температуре в течение 5 часов. Смолу промывают DMF и DCM и сушат при пониженном давлении досуха. Сухую смолу обрабатывают смесью TFA/TIS/вода (92/5/3, об./об.) в течение 1 ч при комнатной температуре. Раствор фильтруют и концентрируют. К концентрированному раствору добавляют холодный простой эфир. Осадок собирают и растворяют в системе растворителей вода-метанол. К раствору добавляют раствор йода в метаноле до появления бурой окраски. Затем раствор выдерживают при комнатной температуре в течение 1 часа. К раствору добавляют водный раствор Na2S2О3 до исчезновения бурой окраски. Полученный в результате раствор очищают с использованием C18 препаративной ВЭЖХ с обращенной фазой, элюируя линейным градиентом смеси буфер A (1% TFA в воде)/буфер B (1% TFA в CH3CN). Фракции проверяют аналитической ВЭЖХ. Фракции, содержащие чистое требуемое соединение, объединяют и лиофилизируют досуха. Молекулярную массу соединения измеряют, используя MS, сопряженной с источником электроспрея.
Получение соединения C:

Соединение 11, где R1 представляет собой н-пропил, (1,5 экв.) смешивают с H-AEPA-D-Phe-Cys(Acm)-Tyr(tBu)-D-Trp(Boc)-Lys(Boc)-Abu-Cys(Acm)-Thr(tBu)-амидной MBHA-смолой Rink (1 экв.) и DIEA (2 экв.) в DMF. Смесь встряхивают при комнатной температуре в течение 5 часов. Смолу промывают DMF и DCM и сушат при пониженном давлении досуха. Сухую смолу обрабатывают смесью TFA/TIS/вода (92/5/3, об./об.) в течение 1 ч при комнатной температуре. Раствор фильтруют и концентрируют. К концентрированному раствору добавляют холодный простой эфир. Осадок собирают и растворяют в системе растворителей вода-метанол. К раствору добавляют раствор йода в метаноле до появления бурой окраски. Затем раствор выдерживают при комнатной температуре в течение 1 часа. К раствору добавляют водный раствор Na2S2О3 до исчезновения бурой окраски. Полученный в результате раствор очищают с использованием C18 препаративной ВЭЖХ с обращенной фазой, элюируя линейным градиентом смеси буфер A (1% TFA в воде)/буфер B (1% TFA в CH3CN). Фракции проверяют аналитической ВЭЖХ. Фракции, содержащие чистое требуемое соединение, объединяют и лиофилизируют досуха. Молекулярную массу соединения измеряют, используя MS, сопряженной с источником электроспрея.
Получение соединения D:

Соединение 25 (3 экв.) смешивают с H-Doc-D-Phe-Cys(Acm)-Tyr(tBu)-D-Trp(Boc)-Lys(Boc)-Abu-Cys(Acm)-Thr(tBu)-амидной MBHA-смолой Rink (1 экв.), HBTU (2,9 экв.), HOBt (3,0 экв.) и DIEA (6 экв.) в DMF. Смесь встряхивают при комнатной температуре в течение 4 часов. Смолу промывают DMF и DCM и сушат при пониженном давлении досуха. Сухую смолу обрабатывают смесью TFA/TIS/вода (92/5/3, об./об.) в течение 1 ч при комнатной температуре. Раствор фильтруют и концентрируют. К нему добавляют холодный простой эфир, осадок собирают и растворяют в системе растворителей вода-метанол. К раствору добавляют раствор йода в метаноле до появления бурой окраски. Затем раствор выдерживают при комнатной температуре в течение 1 часа. К раствору добавляют водный раствор Na2S2О3 до исчезновения бурой окраски. Полученный в результате раствор очищают с использованием C18 препаративной ВЭЖХ с обращенной фазой, элюируя линейным градиентом смеси буфер A (1% TFA в воде)/буфер B (1% TFA в CH3CN). Фракции проверяют аналитической ВЭЖХ. Фракции, содержащие чистое требуемое соединение, объединяют и лиофилизируют досуха. Молекулярную массу соединения измеряют, используя MS, сопряженной с источником электроспрея.
Получение соединения Е:

Соединение 26 (3 экв.) смешивают с H-(D-Ser(tBu))5-Lys(Boc)-D-Tyr(tBu)-D-Tyr(tBu)-Cys(Acm)-Tyr(tBu)-D-Trp(Boc)-Lys(Boc)-Val-Cys(Acm)-Trp(Boc)-амидной MBHA-смолой Rink (1 экв.), HBTU (2,9 экв.), HOBt (3,0 экв.) и DIEA (6 экв.) в DMF. Смесь встряхивают при комнатной температуре в течение 4 часов. Смолу промывают DMF и DCM и сушат при пониженном давлении досуха. Сухую смолу обрабатывают смесью TFA/TIS/вода (92/5/3, об./об.) в течение 1 ч при комнатной температуре. Раствор фильтруют и концентрируют. К концентрированному раствору добавляют холодный простой эфир. Осадок собирают и растворяют в системе растворителей вода-метанол. К раствору добавляют раствор йода в метаноле до появления бурой окраски. Затем раствор выдерживают при комнатной температуре в течение 1 часа. К раствору добавляют водный раствор Na2S2О3 до исчезновения бурой окраски. Полученный в результате раствор очищают с использованием C18 препаративной ВЭЖХ с обращенной фазой, элюируя линейным градиентом буфер A (1% TFA в воде)/буфер B (1% TFA в CH3CN). Фракции проверяют аналитической ВЭЖХ. Фракции, содержащие чистое требуемое соединение, объединяют и лиофилизируют досуха. Молекулярную массу соединения измеряют, используя MS, сопряженной с источником электроспрея.
Получение соединения F:
Этил [6-метил-8β-эрголинилметил]тиоацетат
К раствору дигидролизергола (240 мг) в 10 мл пиридина добавляли 250 мкл метансульфонилхлорида. После перемешивания при комнатной температуре в течение 2 часов, реакционную смесь выливали в 100 мл воды, экстрагировали хлороформом (2×20 мл). Органический слой промывали водой, затем сушили над MgSO4 и удаляли растворитель в вакууме досуха с получением 140 мг бледно-коричневого твердого вещества. Дальнейшей экстракцией из водного раствора после подщелачивания NaHCO3 получали дополнительные 100 мг продукта. Общий выход 240 мг. Масс-спектрометрия (электроспрей) 335,2.
К раствору полученного выше D-6-метил-8β-мезилоксиметилэрголина (140 нг) в 3 мл диметилформамида добавляли порошкообразный K2CO3 (150 мг) с последующим добавлением 150 мкл этил-2-меркаптоацетата, и смесь нагревали при 40°C в течение 2 часов в атмосфере азота. Растворитель удаляли в вакууме досуха и остаток распределяли между хлороформом и водой. Затем органический слой сушили (MgSO4), и после упаривания растворителя остаток подвергали препаративной тонкослойной хроматографии на силикагеле с использованием смеси хлороформ/метанол (9:1) в качестве растворителей для разделения. Соответствующую часть отделяли, экстрагировали смесью хлороформ-метанол и удаляли растворитель в вакууме досуха. Получали бледно-коричневое твердое вещество, 100 мг. Масс-спектрометрия (электроспрей) 359,2.
Получение соединения G:
6-Метил-8β -эрголинилметилтиоацетил-D-Phe-цикло(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
К раствору 6-метил-8β-эрголинилметилтиоуксусной кислоты (Схема I, соединение 7) (50 мг) и D-Phe-цикло(Cys-Tyr(OBT)-D-Trp-Lys(BOC)-Abu-Cys)-Thr-NH2 (100 мг), полученных путем твердофазного синтеза с использованием Fmoc-химии, в 10 мл диметилформамида добавляли 200 мг EDC (1-[3-(диметиламино)пропил]-3-этилкарбодиимид-HCl), 100 мг HOAT (1-гидрокси-7-азабензотриазол) с последующим добавлением 200 мкл диизопропилэтиламина и смесь перемешивали в течение ночи при комнатной температуре. Летучие вещества удаляли в вакууме досуха. Остаток распределяли между хлороформом, метанолом и насыщенным раствором соли. Органический слой промывали водным NaHCO3, сушили в течение ночи над MgSO4. После упаривания растворителя остаток подвергали препаративной тонкослойной хроматографии с использованием смеси хлороформ-метанол (85:15) в качестве растворителей для разделения. Соответствующую часть выделяли, экстрагировали смесью хлороформ/метанол и удаляли растворители в вакууме с получением 40 мг защищенного продукта. Масс-спектрометрия (электроспрей) 1500, 7.
Защищенный продукт затем обрабатывали 30%-ной трифторуксусной кислотой в дихлорметане (10 мл), содержащей несколько капель триизопропилсилана, в течение 30 минут. Летучие вещества удаляли в вакууме досуха. Остаток очищали с использованием колонки ВЭЖХ Vydac C18 и смеси CH3CN/0,1% водная TFA, с получением в результате 17 мг белого твердого вещества. Масс-спектрометрия (электроспрей) 1344,8, 673,2.
Получение соединения H:
Этил (6-н-пропил-8β-эрголинил)метилтиоацетат
Данное соединение получали так же, как соединение F, исходя из D-н-пропил-8β-гидроксиметилэрголина, который получали согласно EP 000667. Бледно-желтое твердое вещество. Масс-спектрометрия (электроспрей) 387,2.
Получение соединения I:
6-н-пропил-8β-эрголинилметилтиоацетил-D-Phe-цикло(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
Данное соединение получали так же, как соединение G, исходя из 6-н-пропил-8β-эрголинил)метилтиоуксусной кислоты (схема I, соединение 6, где R1=пропил и s=1) и D-Phe-цикло(Cys-Tyr(OBT)-D-Trp-Lys(BOC)-Abu-Cys)-Thr-NH2. Белое твердое вещество. Масс-спектрометрия (электроспрей) 1372,5, 687,3.
Получение соединения J:
6-D-метил-8β -эрголинилметилтиоаминосукциноил-D-Phe-цикло(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
Данное соединение получали так же, как соединение G, исходя из 6-метил-8β -сукциноиламинометилэрголин и D-Phe-цикло(Cys-Tyr(OBT)-D-Trp-Lys(BOC)-Abu-Cys)-Thr-NH2. Белое твердое вещество. Масс-спектрометрия (электроспрей) 1344,8, 673,2.
Получение соединения K:
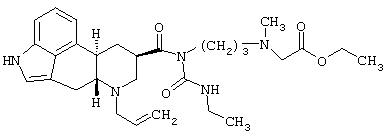
6-аллил-8β-(1-этил-(3-N-метил-3-карбонилметил)аминопропилуреидокарбонилэрголин-D-Phe-цикло(Cys-Thy-D-Trp-Lys-Abu-Cys)-Thr-NH2, то есть соединение следующей структуры:

A. 1-[[6-аллилэрголин-8-ил]карбонил]-1-[3-(N-(этоксикарбонил)метил-N-метил)аминопропил]-3-этилмочевина, т.е. соединение следующей структуры:

(1) 3,3-BOC,N-метилпропандиамин
К раствору 3-N-метилпропандиамина (1,8 г) в дихлорметане (30 мл) добавляли безводный MgSO4 (5,5 г) с последующим добавлением бензальдегида (2,3 г) и смесь перемешивали при комнатной температуре в течение ночи. После фильтрования фильтрат обрабатывали (BOC)2 (4,3 г) и DMAP (0,35 г) и перемешивали примерно в течение 1 часа. Затем смесь промывали 5%-ной водной лимонной кислотой, затем - 5%-ным NaHCO3 и затем сушили над MgSO4.
После упаривания растворителя остаток растворяли в этаноле (50 мл). Добавляли Pd(OH)2 (600 мг), уксусную кислоту (1 мл) и циклогексен (3 мл) и проводили гидрирование в течение ночи. Смесь фильтровали через слой целлита и фильтрат упаривали в вакууме досуха с получением 3,3-BOC,N-метилпропандиамина в виде бесцветной жидкости. 2,3 г. Масс-спектрометрия (электроспрей)=189, 1.
(2) 6-аллил-8β-(3,3-BOC,N-метиламинопропилкарбамоил)эрголин
К раствору 6-аллилдигидролизергиновой кислоты (150 мг), полученному по методике, раскрытой в EP 0 003667, и 3,3-BOC,N-метилпропандиамина (150 мг) в DMF (5 мл) добавляли диизопропилэтиламин (175 мкл) с последующим добавлением диэтилцианофосфоната (150 мкл) и перемешивали смесь при комнатной температуре в течение ночи. Летучие вещества удаляли в вакууме досуха. Остаток распределяли между CHCl3 и водой. Затем органический слой промывали водным NaHCO3 и сушили над MgSO4. Растворитель удаляли в вакууме с получением 6-аллил-8β-(3,3-BOC,N-метиламинопропилкарбамоил)эрголина.
(3) 6-аллил-8β -(3-N-метиламинопропилкарбамоил)эрголин, соль TFA
6-аллил-8β-(3,3-BOC,N-метиламинопропилкарбамоил)эрголин с предыдущей стадии обрабатывали 30% TFA в дихлорметане в течение 30 минут и удаляли летучие вещества в вакууме досуха с выходом 250 мг 6-аллил-8β-(3-N-метиламинопропилкарбамоил)эрголина, соли TFA. Масс-спектрометрия (электроспрей)=367,2.
(4) 6-аллил-8β-(3-N-метил-3-карбэтоксиметил)аминопропилкарбамоилэрголин
К раствору соли TFA 6-аллил-8β-(3-N-метиламинопропилкарбамоил)эрголина (250 мг) и K2CO3 (140 мг) в DMF (5 мл) добавляли этилбромацетат (70 мкл) и смесь перемешивали при комнатной температуре в течение ночи. После упаривания растворителя остаток распределяли между хлороформом и водой. Органический слой сушили с использованием MgSO4 и затем растворитель удаляли в вакууме с получением неочищенного 6-аллил-8β -(3-N-метил-3-карбэтоксиметил)аминопропилкарбамоилэрголина (240 мг). Масс-спектрометрия (электроспрей)=453,2.
(5) 6-аллил-8β -(1-этил-(3-N-метил-3-карбэтоксиметил)аминопропилуреидокарбонилэрголин
6-аллил-8β-(3-N-метил-3-карбэтоксиметил)аминопропилкарбамоилэрголин с предыдущей стадии растворяли в толуоле (10 мл) и добавляли этилизоцианат (3 мл). Смесь кипятили с обратным холодильником в атмосфере азота в течение 3 суток и после упаривания летучих веществ остаток подвергали препаративной хроматографии на силикагеле с использованием смеси хлороформ/метанол (19→1) в качестве проявляющих растворителей. Соответствующую часть экстрагировали смесью хлороформ/метанол и растворители удаляли в вакууме с получением 6-аллил-8β-(1-этил-(3-N-метил-3-карбэтоксиметил)аминопропилуреидокарбонилэрголина в виде бледно-желтого вязкого вещества (30 мг). Масс-спектрометрия (электроспрей) = 524,3.
B. 6-аллил-8β-(1-этил-(3-N-метил-3-карбоксиметил)аминопропилуреидокарбонилэрголин, т.е. соединение следующей структуры:
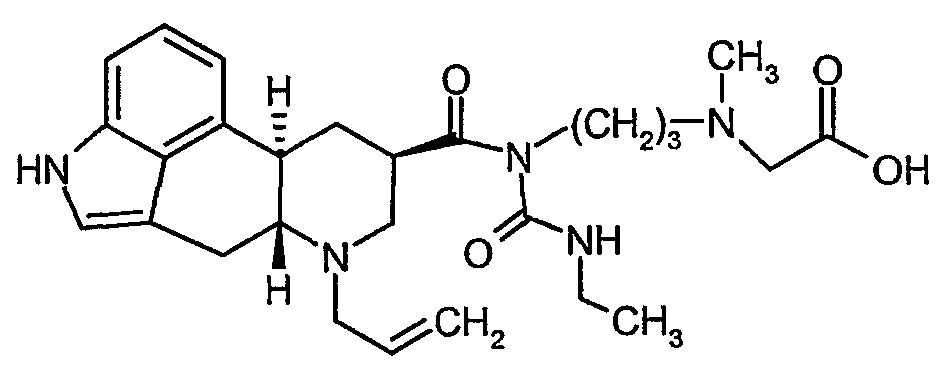
К смеси 6-аллил-8β-(1-этил-(3-N-метил-3-карбэтоксиметил)аминопропилуреидокарбонилэрголина (520 мг) в 10 мл ацетона добавляли 15 мл 0,2 M фосфатного буфера (pH=примерно 7) и 0,6 мл ChiroCLEC-BL (Altus Biologics, Cambridge, Массачусетс). Смесь инкубировали на вращающемся шейкере примерно при 40°C в течение ночи. Смесь подкисляли 5%-ной водной лимонной кислотой и экстрагировали смесью CHCl3-метанол. Органический экстракт сушили и растворители удаляли в вакууме с получением 6-аллил-8β-(1-этил-(3-N-метил-3-карбоксиметил)аминопропилуреидокарбонилэрголина.
C. 6-аллил-8β -(1-этил-(3-N-метил-3-карбонилметил)аминопропилуреидокарбонилэрголин-D-Phe-цикло(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, т.е. соединение K
К раствору 6-аллил-8β -(1-этил-(3-N-метил-3-карбоксиметил)аминопропилуреидокарбонилэрголина (50 мг) и D-Phe-цикло(Cys-Tyr-D-Trp-Lys(FMOC)-Abu-Cys)-Thr-NH2 (100 мг, получен путем твердофазного синтеза) в 10 мл диметилформамида добавляли 200 мг EDC (1-[3-(диметиламино)пропил]-3-этилкарбодиимид-HCl), 100 мг HOAT (1-гидрокси-7-азабензотриазол) с последующим добавлением 200 мкл диизопропилэтиламина и смесь перемешивали при комнатной температуре в течение ночи. Летучие вещества удаляли в вакууме досуха. Остаток распределяли между хлороформом, метанолом и насыщенным раствором соли. Органический слой промывали водным NaHCO3 и затем сушили над MgSO4. После испарения растворителя защищенный продукт затем обрабатывали 5% пиперидином в DMF (10 мл) в течение 30 минут. Летучие вещества удаляли в вакууме до малого объема (около 2 мл). Продукт очищали с использованием ВЭЖХ VYDAC C18 и смеси CH3CN/0,1% водная TFA с получением очищенного продукта со снятыми защитными группами.
Пример L

A. H-Aepa-Lys(Boc)-DTyr(tBu)-DTyr(tBu)-Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Abu-Cys(Trt)-Thr(tBu)-амидная MBHA-смола Rink
Комплекс защищенный пептид-смола синтезировали автоматически на пептидном синтезаторе Applied Biosystems (Foster City, Калифорния), модель 433A, применяя химию флуоренилметилоксикарбонила (Fmoc). Использовали амидную MBHA-смолу Rink (Novabiochem, San Diego, Калифорния) с замещением 0,72 ммоль/г. Fmoc-аминокислоты (AnaSpec, San Jose, Калифорния) использовали со следующими защитами боковых цепей: Fmoc-Thr(tBu)-OH, Fmoc-Cys(Trt)-OH, Fmoc-Lys(Boc)-OH, Fmoc-DTrp(Boc)-OH, Fmoc-Tyr(tBu)-OH, Fmoc-DTyr(tBu)-OH, Fmoc-Phe-OH, Fmoc-Cys(Trt)-OH, Fmoc-Thr(tBu)-OH и Fmoc-Abu-OH. Fmoc-Aepa-OH приобретали от Chem-Impex International, Inc. (Wood Dale, Иллинойс). Синтез проводили в масштабе 0,25 ммоль. Fmoc-группы удаляли обработкой 20% пиперидином в N-метилпирролидоне (NMP) в течение 30 мин. На каждой стадии присоединения Fmoc-аминокислоту (4 экв, 1 ммоль) вначале преактивировали в 2 мл раствора 0,45 M гексафторфосфат 2-(1H-бензотриазол-1-ил)-1,1,2,3-тетраметилурония/1-гидроксибензотриазол (HBTU/HOBT) в N,N-диметилформамиде (DMF). Данный активированный сложный эфир аминокислоты, 1 мл диизопропилэтиламина (DIEA) и 1 мл NMP добавляли к смоле. Пептидный синтезатор ABI 433A программировали для проведения следующего реакционного цикла: (1) промывка NMP, (2) удаление защитной группы Fmoc 20%-ным пиперидином в NMP в течение 30 мин, (3) промывка NMP, (4) присоединение преактивированной Fmoc-аминокислоты в течение 1 ч. Присоединение к смоле проводили последовательно согласно указанной последовательности. После объединения пептидной цепи, Fmoc удаляли и промывали полностью, используя DMF и дихлорметан (DCM).
MBHA=4-метилбензилгидриламин
Aepa=

B. Полученную в результате H-Aepa-Lys(Boc)-DTyr(tBu)-DTyr(tBu)-Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Abu-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink (0,188 ммоль) смешивали с соединением 7 (92 мг, 0,28 ммоль, 1,5 экв.), [гексафторфосфатом 7-азабензотриазол-1-илокситрис(пирролидино)фосфония] (PyAOP) (146 мг, 0,28 ммоль, 1,5 экв.) и 1-гидрокси-7-азабензотриазолом (HOAT) (38 мг, 0,28 ммоль, 1,5 экв.) в 5 мл DCM. Смесь встряхивали в течение ночи. Смолу сушили и промывали последовательно DMF, метанолом и DCM. После сушки на воздухе смолу обрабатывали смесью TFA, H2О и триизопропилсилана (TIS) (9,5 мл/0,85 мл/0,8 мл) в течение 2 ч. Смолу отфильтровывали и выливали фильтрат в 50 мл холодного эфира. Осадок собирали после центрифугирования. Неочищенный продукт растворяли в 100 мл 5% водного раствора AcOH, к которому по каплям добавляли раствор йода в метаноле до установления желтой окраски. Реакционный раствор перемешивали в течение дополнительного 1 ч. 10%-ный водный раствор Na2S2 О3 добавляли для гашения избытка йода. Неочищенный продукт в растворе очищали на препаративной системе ВЭЖХ с колонкой (4×43 см) C18 DYNAMAX-100 A° (Varian, Walnut Creek, Калифорния). Колонку элюировали линейным градиентом от 80% A и 20% B до 55% A и 45% B за 50 мин, где A представлял собой 0,1% TFA в воде и B представлял собой 0,1% TFA в ацетонитриле. Фракции проверяли аналитической ВЭЖХ. Те, что содержали чистый продукт, объединяли и лиофилизировали досуха. Выход: 40%. Чистота составляла 96,8% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1820,8 (согласно рассчитанной молекулярной массе, равной 1821,3).
Пример M

Соединение примера M синтезировали, в сущности, по методике, описанной для соединения примера L, с использованием H-Lys(Boc)-DTyr(tBu)-DTyr(tBu)-Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Abu-Cys(Trt)-Thr(tBu)-амидной MBHA-смолы Rink. Чистота конечного продукта составляла 97,9% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1652,1 (согласно рассчитанной молекулярной массе, равной 1652,03).
Пример N

Соединение примера N синтезировали, в сущности, по методике, описанной для соединения примера L, используя H-Doc-Lys(Boc)-DTyr(tBu)-DTyr(tBu)-Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Abu-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink. Чистота конечного продукта составляла 99,2% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1797,1 (согласно рассчитанной молекулярной массе, равной 1797,19).
Fmoc-Doc-OH приобретали от Chem-Impex International, Inc. (Wood Dale, Иллинойс).
Doc=

Пример О

Соединение примера O синтезировали, в сущности, по методике, описанной для соединения примера L, используя (6-N-пропил-8β-эрголинил)метилтиоуксусную кислоту и H-Lys(Boc)-DTyr(tBu)-DTyr(tBu)-Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Abu-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink. Чистота конечного продукта составляла 97,4% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1680,6 (согласно рассчитанной молекулярной массе, равной 1680,1).
Пример P

Соединение примера P синтезировали, в сущности, по методике, описанной для соединения примера L, используя (6-N-пропил-8β-эрголинил)метилтиоуксусную кислоту и H-Aepa-Aepa-DPhe-Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Abu-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink. Чистота конечного продукта составляла 99,9% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1710,7 (согласно рассчитанной молекулярной массе, равной 1711,2).
Пример Q

Соединение примера Q синтезировали, в сущности, по методике, описанной для соединения примера L, используя (6-N-пропил-8β-эрголинил)метилтиоуксусную кислоту и H-Aepa-Aepa-DPhe-Cys(Trt)-(3-йод)Tyr-DTrp(Boc)-Lys(Boc)-Val-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink. Чистота конечного продукта составляла 99% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1851,1 (согласно рассчитанной молекулярной массе, равной 1851,1).
Fmoc-(3-йод)Tyr-OH приобретали от Advanced ChemTech (Louisville, Кентукки).
(3-йод)Tyr=

Пример R

Соединение примера R синтезировали, в сущности, по методике, описанной для соединения примера L, используя H-Aepa-DPhe-Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Abu-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink. Чистота конечного продукта составляла 98,3% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1513,8 (согласно рассчитанной молекулярной массе, равной 1513,9).
Пример S

Соединение примера S синтезировали, в сущности, по методике, описанной для соединения примера L, используя H-Aepa-Aepa-DPhe-Cys(Trt)-(3-йод)Tyr-DTrp(Boc)-Lys(Boc)-Val-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink. Чистота конечного продукта составляла 85,7% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1822,9 (согласно рассчитанной молекулярной массе, равной 1823,06).
Пример Т

Соединение примера Т синтезировали, в сущности, по методике, описанной для соединения примера L, используя H-Doc-DPhe-Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Abu-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink. Чистота конечного продукта составляла 98,9% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1489,6 (согласно рассчитанной молекулярной массе, равной 1489,84).
Пример U

Соединение примера U синтезировали, в сущности, по методике, описанной для соединения примера L, используя H-Doc-DPhe-Cys(Trt)-(3-йод)Tyr-DTrp(Boc)-Lys(Boc)-Val-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink. MS (электроспрей): 1629,8 (согласно рассчитанной молекулярной массе, равной 1629,7).
Пример V

Указанное в заголовке соединение синтезировали, в сущности, по методике, описанной для соединения примера L, используя H-Doc-Doc-DPhe-Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Abu-Cys(Trt)-Thr(tBu)-амидную MBHA-смолу Rink. Чистота конечного продукта составляла 99% на основе анализа с использованием аналитической ВЭЖХ. MS (электроспрей): 1635,0 (согласно рассчитанной молекулярной массе, равной 1633).
Некоторые из соединений настоящего изобретения могут содержать, по крайней мере, один асимметричный центр. Дополнительные асимметричные центры могут присутствовать в молекуле в зависимости от природы различных заместителей в молекуле. Каждый такой асимметричный центр будет приводить к образованию двух оптических изомеров, и подразумевается, что все такие оптические изомеры, в виде отдельных, чистых или частично очищенных оптических изомеров, рацемических смесей или их диастереомерных смесей, включены в объем настоящего изобретения.
Соединения по настоящему изобретению, в общем, могут быть выделены в виде их фармацевтически приемлемых аддитивных солей кислот, таких как соли, полученные с использованием неорганических и органических кислот. Примерами таких кислот являются хлористо-водородная, азотная, серная, фосфорная, муравьиная, уксусная, трифторуксусная, пропионовая, малеиновая, янтарная, D-винная, L-винная, малоновая, метансульфоновая и подобные. Кроме того, некоторые соединения, содержащие кислотную группу, такую как карбоксигруппа, могут быть выделены в виде их неорганических солей, в которых противоион может быть выбран из натрия, калия, лития, кальция, магния и подобного, а также из неорганических оснований.
Фармацевтически приемлемые соли могут быть образованы путем взятия примерно 1 эквивалента соединения по изобретению (например, соединения C, ниже) и его контактирования примерно с 1 эквивалентом или более подходящей соответствующей кислоты, соль которой требуется. Получение и выделение полученной в результате соли хорошо известны обычному специалисту в данной области.
Соединения по изобретению могут вводиться пероральным, парентеральным (например, путем внутримышечной, внутрибрюшинной, внутривенной или подкожной инъекции, или имплантации), назальным, вагинальным, ректальным, сублингвальным или местным путем введения и могут быть составлены в дозированной форме с фармацевтически приемлемыми носителями, подходящими для каждого пути введения. Соответственно, настоящее изобретение включает в свой объем фармацевтические композиции, содержащие в качестве активного ингредиента, по крайней мере, одно соединение по изобретению в ассоциации с фармацевтически приемлемым носителем.
Твердые дозированные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых дозированных формах активное соединение смешано, по крайней мере, с одним инертным фармацевтически приемлемым носителем, таким как сахароза, лактоза или крахмал. Такие дозированные формы также могут включать в качестве обычной практики дополнительные вещества, отличные от таких инертных разбавителей, например, лубриканты, такие как стеарат магния. В случае капсул, таблеток и пилюль дозированные формы могут также включать буферные средства. Таблетки и пилюли, кроме того, могут быть получены с энтеросолюбильными покрытиями.
Жидкие дозированные формы для перорального введения включают фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы, эликсиры, содержащие инертные разбавители, обычно используемые в данной области, такие как вода. Кроме данных инертных разбавителей, композиции также могут включать адъюванты, такие как увлажняющие средства, эмульгирующие и суспендирующие средства, и подсластители, вкусовые добавки и отдушки.
Препараты данного изобретения для парентерального введения включают стерильные водные и неводные растворы, суспензии или эмульсии. Примерами неводных растворителей или разбавителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и кукурузное масло, желатин и инъецируемые органические сложные эфиры, такие как этилолеат. Такие дозированные формы могут также содержать адъюванты, такие как консерванты, увлажняющие средства, эмульгирующие и диспергирующие средства. Их можно стерилизовать, например, путем фильтрации через задерживающий бактерии фильтр, путем введения в композиции стерилизующих средств, путем облучения композиций или путем нагревания композиций. Также они могут производиться в виде стерильных твердых композиций, которые могут быть растворены в стерильной воде или в некоторых других стерильных средах для инъекции непосредственно перед применением.
Композиции для ректального или вагинального введения предпочтительно представляют собой суппозитории, которые могут содержать, в дополнение к активному веществу, эксципиенты, такие как масло коки или воск для суппозиториев.
Композиции для назального или сублингвального применения также получают со стандартными эксципиентами, хорошо известными в данной области.
В общем, эффективная дозировка активного ингредиента в композициях по настоящему изобретению может варьироваться; однако необходимо, чтобы количество активного ингредиента было таким, что получается подходящая дозированная форма. Выбранная дозировка зависит от требуемого терапевтического эффекта, от пути введения и от длительности лечения, причем все это лежит в сфере знаний обычного специалиста в данной области. В общем, людям и другим животным, например млекопитающим, вводят уровни дозировки, составляющие от 0,0001 до 100 мг/кг массы тела.
Предпочтительный интервал дозировки составляет от 0,01 до 10,0 мг/кг массы тела ежесуточно, которую можно вводить единой дозой или разделять на множественные дозы.
Анализ специфичности и селективности соматостатиновых рецепторов
Специфичность и селективность аналогов соматостатина, которые применялись для синтеза химерных соединений соматостатина-дофамина, определяли путем анализа связывания радиоактивного лиганда на клетках CHO-K1, стабильно трансфицированных каждым из подтипов SSTR, следующим образом.
Полные кодирующие последовательности геномных фрагментов генов SSTR 1, 2, 3 и 4 и клон кДНК SSTR 5 субклонировали в экспрессирующий вектор млекопитающих pCMV (Life Technologies, Милан, Италия). Клонируемые клеточные линии, стабильно экспрессирующие SSTR 1-5, получали путем трансфекции клеток CHO-K1 (ATCC, Manassas, Виргиния, США) с использованием способа совместного осаждения с фосфатом кальция (Davis L, et al., 1994 In: Basic methods in Molecular Biology, 2nd edition, Appleton & Lange, Norwalk, CT, USA: 611-646). Плазмиду pRSV-neo (ATCC) включали в качестве селективного маркера. Клонируемые клеточные линии отбирали в среде RPMI 1640, содержащей 0,5 мг/мл G418 (Life Technologies, Милан, Италия), клонировали кольцевым способом и размножали культивированием.
Мембраны для анализов связывания рецепторов in vitro получали путем гомогенизации клеток CHO-K1, экспрессирующих подтипы SSTR, в ледяном 50 мМ Tris-HCl и центрифугирования дважды при 39000 g (10 мин) с ресуспендированием между центрифугированиями в свежем буфере. Конечный осадок ресуспендировали в 10 мМ Tris-HCl для анализа. Для анализа SSTR 1, 3, 4 и 5 аликвоты мембранных препаратов инкубировали 90 мин при 25°C с 0,05 нМ [125I-Tyr11]SS-14 в 50 мМ HEPES (pH 7,4), содержащем 10 мг/мл BSA, 5 мМ MgCl2, 200 KIU/мл Trasylol, 0,02 мг/мл бацитрацина и 0,02 мг/мл фенилметилсульфонилфторида. Конечный объем среды анализа составлял 0,3 мл. Для анализа SSTR 2 в качестве радиоактивного лиганда применяли 0,05 нМ [125I]MK-678, и время инкубации составляло 90 мин при 25°C. Инкубации заканчивали быстрой фильтрацией через фильтры GF/C (предварительно вымоченные в 0,3% полиэтиленимине) с использованием коллектора для фильтрации Brandel. Затем каждую пробирку и фильтр промывали три раза 5 мл аликвотами ледяного буфера. Специфическое связывание определяли как общий связанный радиоактивный лиганд минус тот, что связывался в присутствии 1000 нМ SS-14 для SSTR 1, 3, 4 и 5, или 1000 нМ MK-678 для SSTR2.
Анализ специфичности и селективности дофаминовых рецепторов
Специфичность и селективность дофаминового рецептора-2 в отношении аналогов дофамина, применяемых для синтеза химерных соединений соматостатина-дофамина, может быть определена путем анализа связывания радиоактивного лиганда следующим образом.
Неочищенные мембраны получали путем гомогенизации замороженного полосатого тела крысы (Zivic Laboratories, Питтсбург, Пенсильвания) в 20 мл ледяного 50 мМ Tris-HCl с помощью Brinkman Poltron (установка в положение 6, 15 с). Буфер добавляли для получения конечного объема 40 мл и гомогенат центрифугировали в роторе Sorval SS-34 при 39000 g в течение 10 мин при 0-4°C. Полученную в результате надосадочную жидкость декантировали и отбрасывали. Осадок повторно гомогенизировали в ледяном буфере, предварительно инкубировали при 37°C в течение 10 мин, разбавляли и центрифугировали, как ранее. Конечный осадок ресуспендировали в буфере и держали на льду во время анализа связывания рецептора.
Для анализа аликвоты промытых мембранных препаратов и тестируемых соединений инкубировали в течение 15 мин (37°С) с 0,25 нМ [3HI] спиперона (16,5 Ки/ммоль, New England Nuclear, Boston, Массачусетс) в 50 мМ Tris-HCl, 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2, 1 мМ MgCl2. Конечный объем среды анализа составлял 1,0 мл. Инкубации заканчивали быстрой фильтрацией через фильтры GF/C с использованием коллектора для фильтрации Brandel. Затем каждую пробирку и фильтр промывали три раза 5 мл аликвотами ледяного буфера. Специфическое связывание определяли как общий связанный радиоактивный лиганд минус тот, что связывался в присутствии 1000 нМ (+) бутакламола.
Результаты анализа специфичности и селективности соматостатиновых рецепторов/анализа специфичности и селективности дофаминовых рецепторов для ряда соединений изобретения

Пример # 1

Пример # 2

Пример # 3
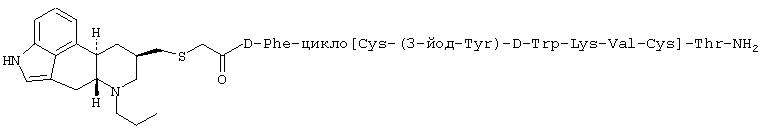
Пример # 4

Пример # 5
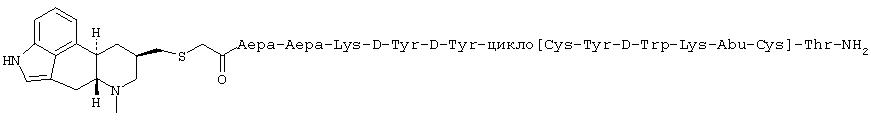
Пример # 6

Пример # 7

Соединение G

Соединение I

Соединение L

Соединение М
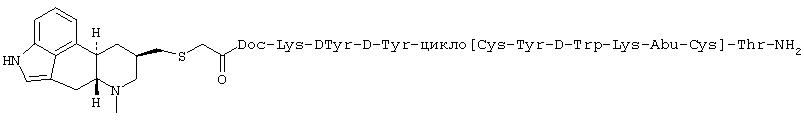
Соединение N

Соединение О

Соединение Р

Соединение Q

Соединение R

Соединение S

Соединение Т

Соединение U

Соединение V
Другие осуществления
Следует понимать, что, хотя изобретение описано в связи с его подробным описанием, предшествующее описание предназначено для иллюстрации и не ограничивает объем изобретения, который определяется объемом прилагаемой формулы изобретения. Другие аспекты, преимущества и модификации находятся в пределах данной формулы изобретения. Кроме того, все приведенные в данном описании публикации включены в данное описание во всей своей полноте посредством ссылки.
Реферат
Описана серия химерных аналогов соматостатина-дофамина, которые сохраняют in vivo активность и соматостатина, и дофамина. Примером является 6-н-пропил-8β -эрголинилметилтиоацетил-D-Phe-цикло(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2. 11 н. и 5 з.п. ф-лы.
Формула






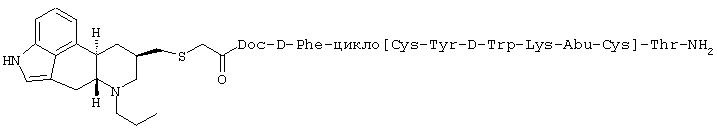








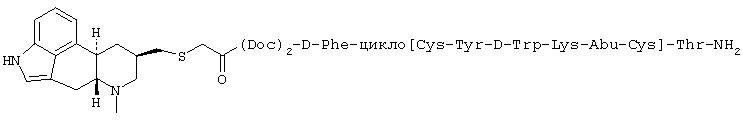

















Комментарии