Агонисты протеинтирозинфосфатазы-1, содержащей домен гомологии-2 src, и способы лечения с применением указанных агонистов - RU2584986C2
Код документа: RU2584986C2
Чертежи





















Описание
ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к новым соединениям, обладающим агонистической активностью в отношении протеинтирозинфосфатазы-1, содержащей домен гомологии-2 Src, (SHP-1), и способам лечения с применением указанных соединений.
УРОВЕНЬ ТЕХНИКИ
[0002] SHP-1, представляющая собой протеинтирозинфосфатазу с двумя доменами гомологии-2 (SH2) Src, является регулятором различных внутриклеточных сигнальных молекул, таких как сигнальный трансдуктор и активатор транскрипции 3 (STAT3), KIT, CD22, CD5, CD72, SHPS-1, TIMP (металлопротеиназы), CDK2, р27, SRC, ZAP70, IL-10, NF-κВ, Lck, 3ВР2, Lyn и циклин D1.
[0003] STAT3 представляет собой фактор транскрипции, который регулирует рост и выживаемость клеток посредством модуляции экспрессии генов-мишеней. Указанный фактор транскрипции выступает в качестве онкогена, который является конститутивно активным при многих злокачественных новообразованиях, включая рак печени, легких, головы и шеи, предстательной железы и молочной железы, а также миелому и лейкоз. Основным регулятором активности STAT3 является SHP-1. Что касается механизма действия, SHP-1 проявляет протеинфосфатазную активность, которая снижает уровень фосфо-STAT3 (P-STAT) и, как следствие, блокирует димеризацию P-STAT3. Вследствие этого значительно снижается экспрессия генов-мишеней, таких как циклин D1 и сурвивин, транскрибируемых STAT3. Кроме того, исследования белка SHP-1 и мРНК SHP-1 показали, что в большинстве клеток злокачественных новообразований уровень экспрессии SHP-1 был низким, и генетическое повышение уровня SHP-1 в клетках злокачественных новообразований приводило к подавлению роста клеток, что позволяет предположить, что ген SHP-1 действует как супрессор опухолей. С точки зрения поиска новых лекарственных средств, разработка синтетического лекарственного средства, которое может понижать уровень Р-STAT3 и повышать уровень SHP-1, представляет собой перспективное направление терапии злокачественных новообразований. Также SHP-1 играет важную роль в ремоделировании костной ткани, процессе формирования костной ткани с помощью остеобластов и резорбции костной ткани с помощью остеокластов. Утрата функции SHP-1 приводит к образованию остеокластов и в конечном итоге вызывает остеопороз. Таким образом, повышение активности SHP-1 может представлять собой предписание для пациента, страдающего остеопорозом. Кроме того, повышение SHP-1 оказывает положительное действие на макрофагов у пациентов, страдающих рассеянным склерозом.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0004] Настоящее изобретение основано на неожиданном обнаружении того факта, что разработанные в настоящем изобретении соединения выступают в качестве агонистов SHP-1 и обладают способностью снижать P-STAT3, а также подходят для лечения некоторых заболеваний, таких как онкологические заболевания. При этом соединения согласно настоящему изобретению не блокируют активность киназ, таких как Raf-1 и VEGFR2.
[0005] В частности, в одном из аспектов настоящего изобретения предложено соединение формулы I
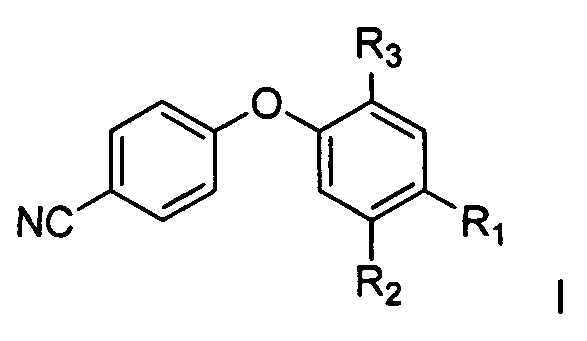
где R1, R2, и R3 независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил, -(C)mNHC(X)NH(C)nRa-, -(C)pNHC(X)Rb-, -(C)qNHS(O)2Rc, -(C)r(X)NHRd- или -(C)sNH(C)tRe,
где Ra, Rb, Rc, Rd и Re независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил;
X представляет собой О или S; а
m, n, p, q, r, s, t составляют 0, 1 или 2.
[0006] В другом аспекте настоящего изобретения предложено соединение формулы II, включая соединение формулы II(а), соединение формулы II(b) или соединение формулы II(с),


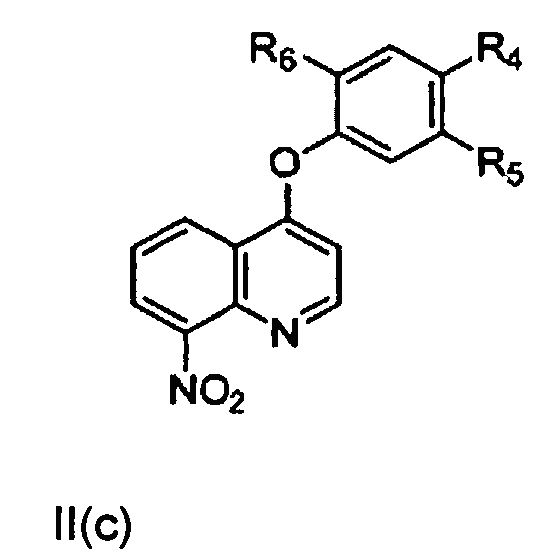
где R4, R5 и R6 независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил, -(C)mNHC(X)NH(C)nRa-, -(C)pNHC(X)Rb-, -(C)qNHS(O)2Rc, -(C)r(X)NHRd- или -(C)sNH(C)tRe;
где Ra, Rb, Rc, Rd и Re независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил;
X представляет собой О или S; а
m, n, p, q, r, s, t составляют 0, 1 или 2.
[0007] В еще одном аспекте настоящего изобретения предложено соединение формулы III

где R7 представляет собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил, -(C)mNHC(X)NH(C)nRa-, -(C)pNHC(X)Rb-, -(C)qNHS(O)2Rc, -(C)r(X)NHRd- или -(C)sNH(C)tRe;
где Ra, Rb, Rc, Rd и Re независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил;
X представляет собой О или S; а
m, n, p, q, r, s, t составляют 0,1 или 2.
[0008] В настоящем изобретении также предложена фармацевтическая композиция, содержащая одно или более вышеописанных соединений. Фармацевтическая композиция согласно настоящему изобретению может быть применена для повышения уровня экспрессии или биологической активности SHP-1 в клетке или лечения заболевания или патологического состояния, характеризующегося пониженным уровнем экспрессии или пониженной биологической активностью протеинтирозинфосфатазы-1, содержащей домен гомологии-2 Src, которое включает, но не ограничивается указанными, злокачественное новообразование (например, гепатоцеллюлярную карциному, лейкоз, рак легкого, рак молочной железы, рак почки, рак щитовидной железы, рак головы и рак шеи), склероз и остеопороз. Также в объем настоящего изобретения входит применение любого из вышеописанных соединений для повышения уровня экспрессии или биологической активности SHP-1 в клетке или лечения заболевания или патологического состояния, характеризующегося пониженным уровнем экспрессии или пониженной биологической активностью SHP-1, описанного в настоящей заявке, и для производства лекарственного средства для лечения указанного заболевания или патологического состояния.
[0009] Также в настоящем изобретении предложен способ повышения уровня экспрессии или биологической активности SHP-1 в клетке, включающий приведение указанной клетки в контакт с эффективным количеством соединения или фармацевтической композиции, описанной в настоящей заявке.
[0010] Также в настоящем изобретении предложен способ лечения заболевания или патологического состояния, характеризующегося пониженным уровнем экспрессии или пониженной биологической активностью SHP-1, у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества соединения или фармацевтической композиции, описанной в настоящей заявке.
[0011] Различные варианты реализации настоящего изобретения подробно описаны ниже. Другие особенности настоящего изобретения будут в явном виде представлены с помощью следующих подробных описаний и чертежей различных вариантов реализации и формулы изобретения.
[0012] Предполагается, что средний специалист в области техники, к которой принадлежит настоящее изобретение, может применять настоящее изобретение в самом полном объеме на основании описаний, приведенных в настоящей заявке, без необходимости в дополнительной иллюстрации. Таким образом, следует понимать, что следующие описания приведены с целью иллюстрации, а не ограничения объема настоящего изобретения каким бы то ни было образом.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0013] С целью иллюстрации настоящего изобретения на чертежах представлены варианты реализации, которые в настоящее время являются предпочтительными. Однако следует понимать, что настоящее изобретение не ограничено представленными предпочтительными вариантами реализации.
[0014] На чертежах:
[0015] На Фиг. 1 представлена химическая структура сорафениба и соединения SC-1.
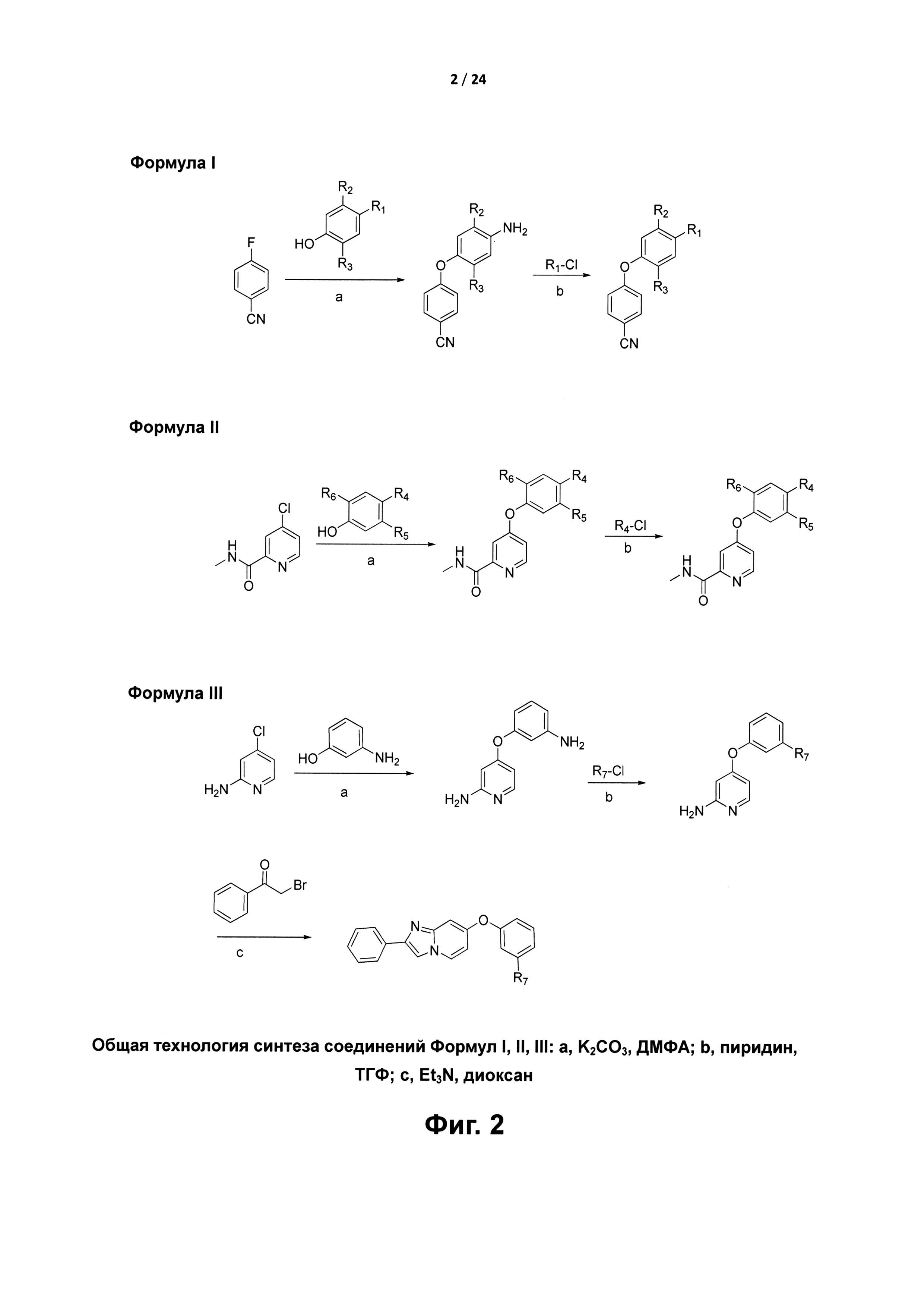
[0016] На Фиг. 2 представлена общая технология синтеза соединений формул I, II и III согласно настоящему изобретению.
[0017] На Фиг. 3 представлена активность Raf-1 в клетках, обработанных сорафенибом и соединением 1 соответственно. Клетки Huh-7 подвергали воздействию сорафениба или соединения 1 в концентрации 10 мкМ в течение 24 часов и клеточные лизаты подвергали анализу для определения активности raf-1. Столбики отражают среднее значение; планки погрешностей отражают SD (n=3). *Р<0,05.
[0018] На Фиг. 4 представлены результаты твердофазного ИФА, касающиеся ингибирующего воздействия соединений 1-25 на IL-6 стимулированный P-STAT в клетках PLC5 после 24 ч обработки по сравнению с сорафенибом, при этом концентрация каждого из соединений составляла 10 мкМ. Столбики отражают среднее значение, планки погрешностей отражают SD (N=3).
[0019] На Фиг. 5 представлены результаты вестерн-блоттинга, касающиеся воздействия соединений 1 и 12, каждое из которых находилось в концентрациях 5 мкМ и 10 мкМ, на фосфорилирование P-STAT3, STAT3, циклина D и сурвивина в клетках PLC5 в ФБС-содержащей среде после 24 ч обработки.
[0020] На Фиг. 6 представлены (А) результаты твердофазного ИФА, касающиеся гибели клеток, индуцированной соединениями 1 и 12 в концентрациях 5 и 10 мкМ, после 24 ч обработки клеток PLC5, и (В) результаты проточно-цитометрического анализа гибели клеток, индуцированной соединениями 1 и 12 в концентрациях 5 и 10 мкМ, после 24 ч обработки клеток PLC5.
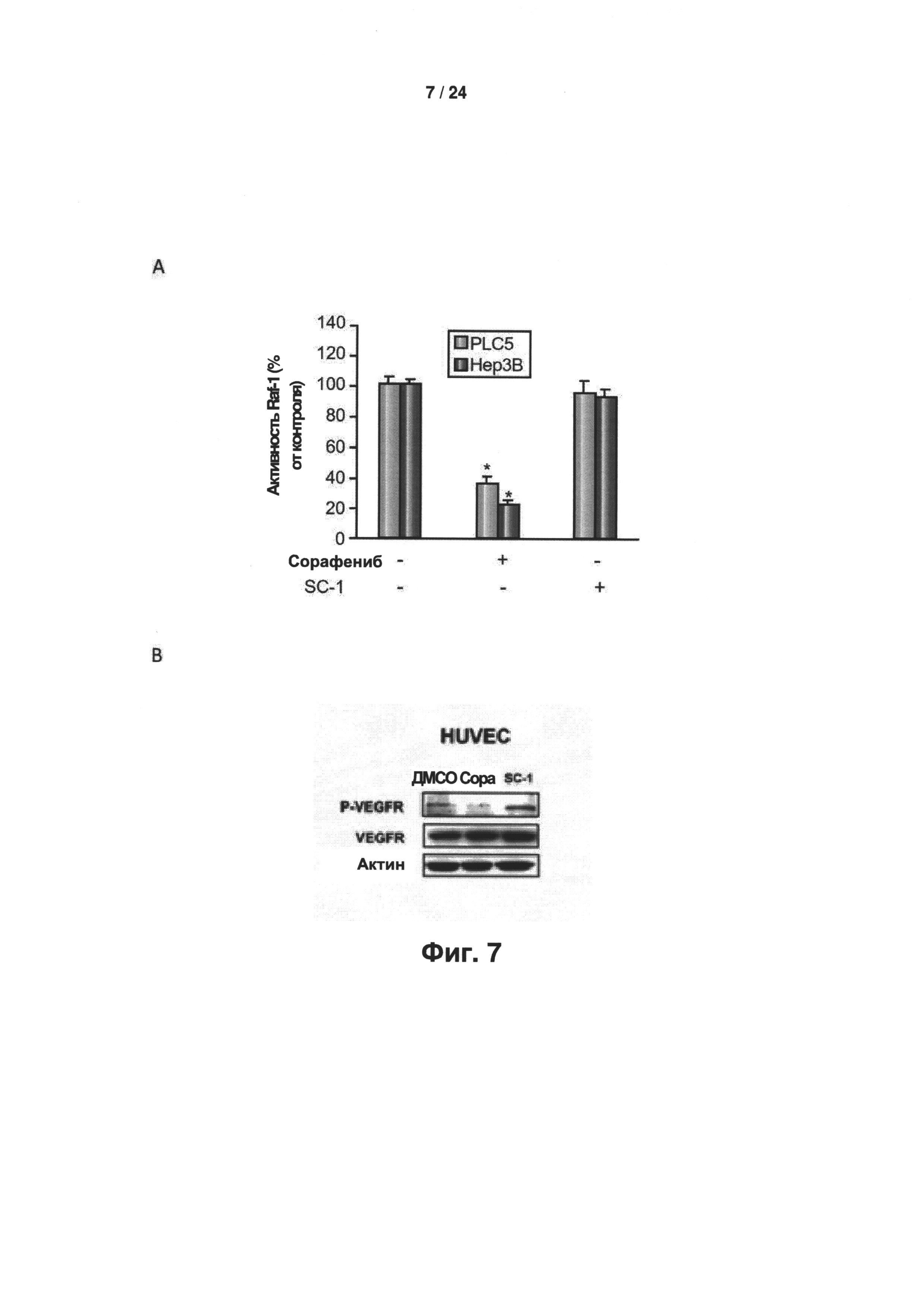
[0021] На Фиг. 7 представлены (А) воздействие сорафениба и SC-1 на фосфо-VEGFR2 в клетках HUVEC, причем указанные клетки подвергали воздействию сорафениба или SC-1 в концентрации 10 мкМ в течение 24 ч; (В) влияние сорафениба и SC-1 на активность Raf-1, причем клетки подвергали воздействию сорафениба или SC-1 в концентрации 10 мкМ в течение 24 ч. Точки отражают среднее значение, планки погрешностей отражают SD (n=6).
[0022] На Фиг. 8 представлены влияние сорафениба и SC-1 на жизнеспособность клеток в четырех линиях клеток ГЦК при повышении дозы, причем клетки подвергали воздействию сорафениба или SC-1 в указанных дозах в течение 72 ч, и жизнеспособность клеток оценивали посредством МТТ-анализа (А); и влияние сорафениба и SC-1 на апоптоз в четырех линиях клеток ГЦК при повышении дозы, причем клетки подвергали воздействию сорафениба или SC-1 в указанных дозах в течение 24 ч, и клеточные лизаты анализировали посредством проточной цитометрии (В) или твердофазного ИФА гибели клеток (С). Точки отражают среднее значение, планки погрешностей отражают SD (n=6).
[0023] На Фиг. 9 представлены (А) воздействие сорафениба или SC-1 на STAT3-зависимые белки, причем клетки обрабатывали сорафенибом или SC-1 в концентрации 10 мкМ в течение 24 ч; (В) воздействие сорафениба или SC-1 на фосфо-STAT3 в клетках PLC5 при повышении дозы, причем клетки обрабатывали лекарственными средствами в указанных концентрациях в течение 24 ч; (С) влияние сорафениба и SC-1 на активность STAT3 (левая, твердофазный ИФА фосфо-STAT3; правая, люциферазный репортерный анализ STAT3), причем клетки обрабатывали сорафенибом или SC-1 в концентрации 10 мкМ в течение 24 ч, и измеряли фосфо-STAT3 методом твердофазного ИФА или активность люциферазы; (D) защитное воздействие STAT3 на апоптоз, индуцированный сорафенибом в клетках PLC5, причем клетки (дикого типа или с эктопической экспрессией STAT3) подвергали воздействию сорафениба или SC-1 в концентрации 10 мкМ в течение 24 ч, и апоптотические клетки анализировали посредством проточной цитометрии. Столбики отражают среднее значение, планки погрешностей отражают SD (n=3). *Р<0,05.
[0024] На Фиг. 10 показано, что ингибирование SHP-1 аннулирует воздействие сорафениба и SC-1 на фосфо-STAT3 и апоптоз. На Фиг. 10А слева представлено воздействие ванадата, представляющего собой неспецифический ингибитор фосфатаз. На Фиг. 10А справа представлено воздействие специфического ингибитора SHP-1. Столбики отражают среднее значение; планки погрешностей отражают SD (n=3). *Р<0,05. На Фиг. 10В слева показано, что выключение SHP-1 посредством миРНК снижает воздействие сорафениба или SC-1 на p-STAT3 в клетках ГЦК. Клетки PLC5 трансфицировали контрольной миРНК или миРНК SHP-1 в течение 24 ч, затем обрабатывали сорафенибом или SC-1 в течение еще 24 ч. На средней диаграмме представлена активность SHP-1 в клетках PLC5. Столбики отражают среднее значение; планки погрешностей отражают SD (n=3). *Р<0,05. На Фиг. 10В справа представлено влияние сорафениба или SC-1 на белковые взаимодействия между SHP-1 и STAT3. Клетки PLC5 обрабатывали сорафенибом или SC-1 в концентрации 10 мкМ в течение 24 часов. На Фиг. 10С показано, что нокдаун SHP-2 не оказывает влияния на воздействие сорафениба или SC-1 на p-STAT3 и апоптоз. На Фиг. 10D показано, что нокдаун РТР-1 В не оказывает влияния на воздействие сорафениба на p-STAT3 и апоптоз. Клетки PLC5 трансфицировали контрольной миРНК или миРНК SHP-2 или миРНК РТР-1В в течение 24 ч, затем обрабатывали сорафенибом или SC-1 в концентрации 10 мкМ в течение 24 ч.
[0025] На Фиг. 11 показано, что SC-1 обеспечивает даун-регуляцию p-STAT3 и индуцирует апоптоз в клетках HUVEC. На Фиг. 11А представлено воздействие сорафениба или SC-1 на p-STAT3 (слева) и апоптоз (справа) в клетках HUVEC. Клетки подвергали воздействию сорафениба или SC-1 в концентрации 10 мкМ в течение 24 ч. Апоптотические клетки анализировали посредством проточной цитометрии (sub-G1). На Фиг. 11В представлено влияние SC-1 на сенсибилизацию к TRAIL в ГЦК. Клетки PLC5 обрабатывали SC-1 (10 мкМ) и/или TRAIL (100 нг/мл) в течение 24 ч. На Фиг. 11С показано, что выключение Raf-1 не оказывает влияния на воздействие указанных лекарственных средств на p-STAT3. Клетки PLC5 трансфицировали контрольной миРНК или миРНК Raf-1 в течение 24 ч, затем обрабатывали сорафенибом или SC-1 в концентрации 10 мкМ в течение 24 ч. На Фиг. 11D представлено влияние сорафениба и SC-1 на активность JAK2. Клетки PLC5 подвергали воздействию сорафениба или SC-1 в концентрации 10 мкМ в течение 24 ч. Точки отражают среднее значение; планки погрешностей отражают SD (n=6). На Фиг. 11Е представлено воздействие сорафениба и SC-1 на SOCS-1 и SOCS-3. Клетки Sk-Hep1 предварительно обрабатывали IL-6 в течение 24 ч, затем обрабатывали сорафенибом или SC-1 в указанных дозах в течение еще 24 ч в присутствии IL-6. На Фиг. 11F представлено влияние STAT-C на апоптоз, индуцированный SC-1 в клетках PLC5. Клетки (дикого типа или с эктопической экспрессией STAT3-C) подвергали воздействию сорафениба или SC-1 в концентрации 10 мкМ в течение 24 ч. На Фиг. 11G представлено воздействие сорафениба и SC-1 на SHP-1. Столбики отражают среднее значение; планки погрешностей отражают SD (n=3). *Р<0,05.
[0026] На Фиг. 12 представлено in vivo воздействие сорафениба и SC-1 на «голых» мышей с ксенотрансплантатными клетками Huh-7. На Фиг. 12А показано, что сорафениб демонстрирует противоопухолевое воздействие на опухоли Huh-7. На графике слева точки отражают среднее значение (n=6); планки погрешностей отражают SE. *, P<0,05; **, P<0,01. На Фиг. 12A справа сверху представлен вестерн-блоттинг p-STAT3 и STAT3 в опухолях Huh-7. На Фиг. 12А справа снизу представлена активность SHP-1 в опухолях Huh-7. На Фиг. 12В показано, что SC-1 демонстрирует значительное противоопухолевое воздействие на опухоли Huh-7. На графике слева точки отражают среднее значение (n=6); планки погрешностей отражают SE. На Фиг. 12В справа сверху представлен вестерн-блоттинг p-STAT3 и STAT3 в опухолях Huh-7. На Фиг. 12В справа снизу представлена активность SHP-1 в опухолях Huh-7.
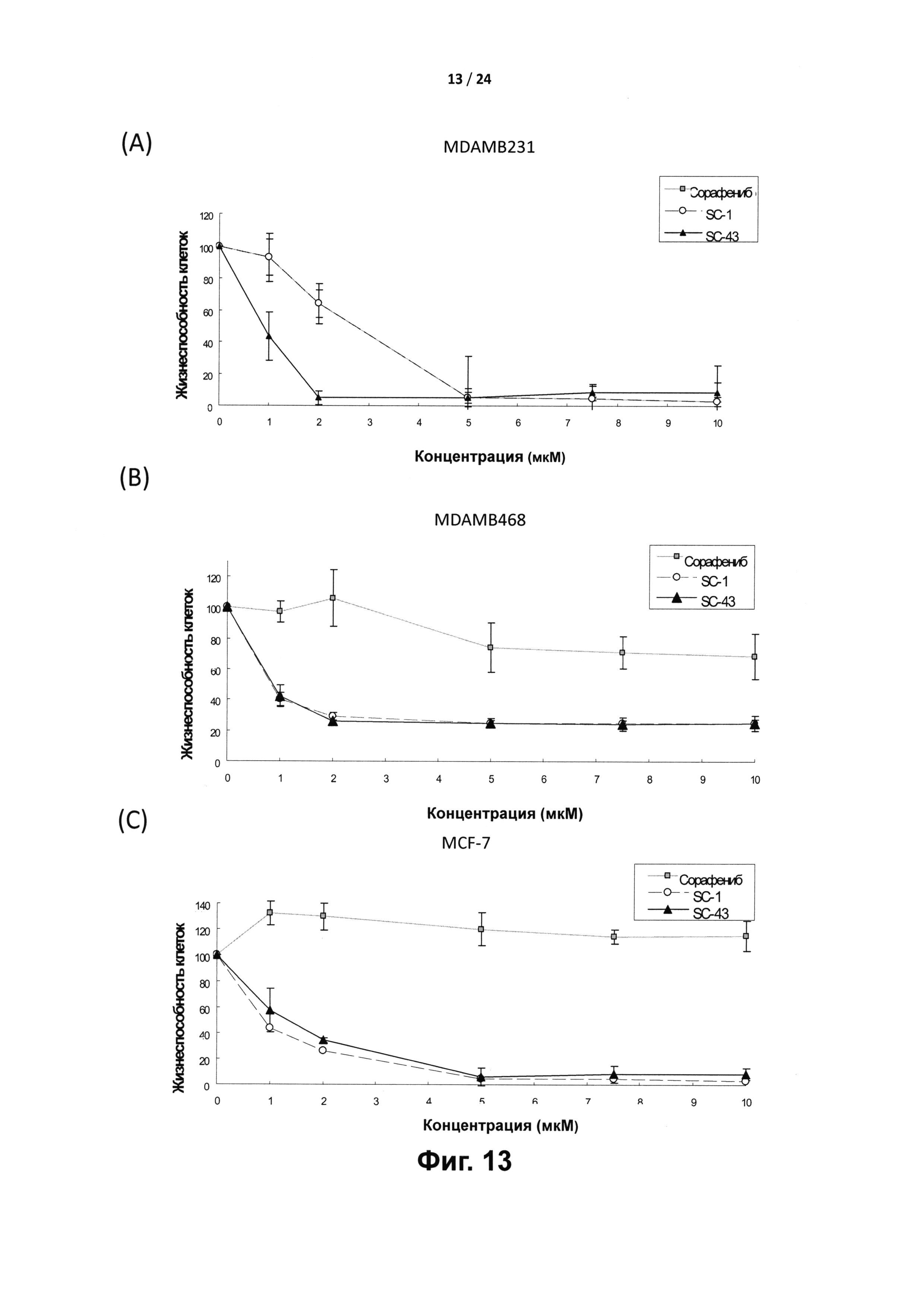
[0027] На Фиг. 13 представлен антипролиферативный эффект SC-1 и SC-43 в линиях клеток различных злокачественных новообразований, включая линии клеток рака молочной железы (A) MDAMB231, (В) MDAMB468 и (С) MCF-7 и линии клеток лейкоза (D) HL-60, (Е) KG-1 и (F) ML-1.
[0028] На Фиг. 14 показано, что производные сорафениба индуцируют значительный апоптоз в степени, зависящей от дозы, где (А), (В), (С), (D) и (Е) относятся к SC-43 в случае PLC5, HepG2, Hep3B, НА59Т и SK-Hep1 клеток соответственно; a (F), (G), (Н), (I) и (J) относятся к SC-40 в случае PLC5, HepG2, Hep3B, НА59Т и SK-Hep1 клеток соответственно. Точки отражают среднее значение; планки погрешностей отражают SD (n=6).
[0029] На Фиг. 15 показано, что SC-43 подвергает даун-регуляции фосфо-STAT3-зависимый сигнальный путь в клетках ГЦК, включая клетки PLC5, HepG2, Hep3B, НА59Т и SK-Hep1.
[0030] На Фиг. 16 показано, что SC-40 подвергает даун-регуляции фосфо-STAT3-зависимый сигнальный путь в клетках ГЦК, включая клетки PLC5, HepG2, Hep3B, НА59Т и SK-Hep1.
[0031] На Фиг. 17 показано, что SC-43 демонстрирует лучшее ингибирование p-STAT3-зависимого сигнального пути в клетках ГЦК, а именно (A) PLC5 и (В) Hep3B, чем сорафениб.
[0032] На Фиг. 18 показано, что как SC-43, так и SC-40 индуцируют сильное ингибирование активности p-STAT3, причем (А) и (В) относятся к твердофазному ИФА p-STAT3 для SC-43 и SC-40 соответственно, а (С) и (D) относятся к репортерному анализу STAT3 для SC-43 и SC-40 соответственно.
[0033] На Фиг. 19 показано, что SC производные, повышают фосфатазную активность SHP-1 in vitro, (A) SC-43, (В) SC-40 и (С) SC-49.
[0034] На Фиг. 20 показано, что SC производные, повышают фосфатазную активность SHP-1 in vitro, (A) SC-43 и (В) SC-40.
[0035] На Фиг. 21 представлены (А) противоопухолевое воздействие SC-40 на клетки опухолей PLC5; (В) вестерн-блоттинг p-STAT3 и STAT3 в клетках опухолей PLC5; (С) масса тела животных; (D) масса опухолей и (Е) активность SHP-1 в клетках опухолей PLC5. Точки отражают среднее значение (n=6); планки погрешностей отражают SE.
[0036] На Фиг. 22 показано, что SC-43 обнаруживает противоопухолевый эффект в условиях in vitro и in vivo, а именно представлены (А) цитотоксичность SC-43 в клетках ГЦК, (В) противоопухолевое воздействие SC-43 на мышей, являющихся носителями ГЦК, (С) активность SHP-1, индуцированная SC-43, и (D) вестерн-блоттинг p-STAT3 и STAT3 в клетках ГЦК, обработанных SC-43 (10 мкМ и 20 мкМ).
[0037] На Фиг. 23 представлены (А) изображение мышей, подвергнутых лечению, полученное посредством системы неинвазивной визуализации in vivo imaging system, (В) масса тела указанных мышей и (С) графики выживаемости мышей контрольной группы и мышей, подвергнутых лечению.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0038] Если не указано иное, все технические и научные термины в настоящей заявке имеют значения, обычно подразумеваемые специалистом в области техники, к которой принадлежит настоящее изобретение. Все публикации, упомянутые в настоящей заявке, включены в настоящее описание посредством ссылок для раскрытия и описания способов и/или материалов, в связи с которыми цитируются указанные публикации.
[0039] В настоящей заявке формы единственного числа включают ссылки на формы множественного числа кроме случаев, когда из контекста явно следует иное. Таким образом, например, упоминание «образца» включает множество таких образцов и их эквивалентов, известных специалистам в данной области.
[0040] Сорафениб (BAY43-9006, Нексавар) клинически применяют для лечения почечно-клеточной карциномы и гепатоцеллюлярной карциномы (ГЦК). Указанное средство известно как мультикиназный ингибитор, который подавляет активность Raf-1 и других тирозинкиназ, таких как VEGFR2, VEGFR3, Flt-3, PDGFR и FGFR-1.
[0041] В настоящем изобретении авторы изучали взаимосвязь между структурой сорафениба и его биоактивностью и модифицировали структуру сорафениба. Исходя из этого, авторы настоящего изобретения разработали ряд производных сорафениба, не обладающих способностью блокировать активность киназы, и неожиданно обнаружили, что указанные соединения демонстрируют хороший терапевтический эффект при некоторых заболеваниях, таких как онкологические заболевания, по меньшей мере сравнимый с эффектом сорафениба. Согласно настоящему изобретению недавно разработанные соединения согласно настоящему изобретению действуют как агонисты SHP-1 и подходят для лечения заболевания или патологического состояния, характеризующегося пониженным уровнем экспрессии или пониженной биологической активностью SHP-1, такого как злокачественное новообразование (например, гепатоцеллюлярная карцинома, лейкоз, рак легкого, рак молочной железы, рак почки, рак щитовидной железы, рак головы и шеи), склероз и остеопороз. Соединения согласно настоящему изобретению также обеспечивают новый вариант терапии для пациентов с устойчивостью к ингибиторам киназы. Указанные опухоли вызывают мутацию киназы после лечения в конститутивно активную фосфорилированную форму даже в присутствии ингибитора киназы. Таким образом, повышающая регуляция супрессора опухолей, в частности SHP-1, для подавления активных мутантных форм киназ является перспективным направлением для пациентов, устойчивых к химиотерапии. Другими словами, соединения согласно настоящему изобретению, действующие по новому таргетному механизму (киназанезависимому), обеспечивают альтернативные варианты терапии, которые могут быть полезными в лечении онкологических заболеваний при наличии устойчивости к традиционной терапии.
[0042] В одном из аспектов настоящего изобретения предложено соединение формулы I

[0043]
где R1, R2, и R3 независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил, -(C)mNHC(X)NH(C)nRa-, -(C)pNHC(X)Rb-, -(C)qNHS(O)2Rc, -(C)r(X)NHRd- или -(C)sNH(C)tRe;
где Ra, Rb, Rc, Rd и Re независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил;
X представляет собой О или S; а
m, n, p, q, r, s, t составляют 0, 1 или 2.
[0044] В одном из вариантов реализации настоящего изобретения соединение формулы I включает те соединения, в которых R1, R2 и R3 независимо представляют собой водород, необязательно замещенный низший алкил, -(C)mNHC(X)NH(C)nRa-, -(C)pNHC(X)Rb-, -(C)qNHS(O)2Rc или -(C)sNH(C)tRe.
[0045] В другом варианте реализации настоящего изобретения соединение формулы I включает те соединения, в которых Ra, Rb, Rc, Rd и Re независимо представляют собой фенил или нафтил, необязательно замещенный 1-3 группами, выбранными из группы, состоящей из галогена, необязательно замещенного низшего алкила (такого как галогензамещенный низший алкил, например трифторметил), необязательно замещенного алкоксила (например, такого как галогензамещенный низший алкоксил, например трифторметил) и необязательно замещенного арилокси (например, цианозамещенного фенокси).
[0046] В некоторых примерах соединение формулы I представляет собой одно из соединений SC-1, SC-48, SC-49, SC-54, SC-55, SC-56, SC-58, SC-43, SC-44, SC-45, SC-50, SC-51, SC-52, SC-59, SC-60 и SC-40, перечисленных в таблице 1.
[0047]


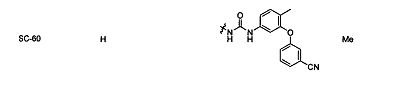
[0048] В другом аспекте настоящего изобретения предложено соединение формулы II, включая соединение формулы II(а), соединение формулы II(b) или соединение формулы II(с)



[0049] где R4, R5 и R6 независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил, -(C)mNHC(X)NH(C)nRa-, -(C)pNHC(X)Rb-, -(C)qNHS(O)2Rc, -(C)r(X)NHRd- или -(C)sNH(C)tRe;
где Ra, Rb, Rc, Rd и Re независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил;
X представляет собой О или S; а
m, n, p, q, r, s, t составляют 0, 1 или 2.
[0050] В одном из вариантов реализации настоящего изобретения соединение формулы II включает те соединения, в которых R4, R5 и R6 независимо представляют собой водород, необязательно замещенный низший алкил, -(C)mNHC(X)NH(C)nRa-, -(C)pNHC(X)Rb-, -(C)qNHS(O)2Rc или -(C)sNH(C)tRe.
[0051] В другом варианте реализации настоящего изобретения соединение формулы II включает те соединения, в которых Ra, Rb, Rc, Rd и Re независимо представляют собой фенил или нафтил, необязательно замещенный 1-3 группами, выбранными из группы, состоящей из галогена, необязательно замещенного низшего алкила (такого как галогензамещенный низший алкил, например трифторметил), необязательно замещенного алкоксила (например, такого как галогензамещенный низший алкоксил, например трифторметил) и необязательно замещенного арилокси (например, цианозамещенного фенокси).
[0052] В некоторых примерах соединение формулы II представляет собой одно из соединений SC-31, SC-32, SC-33, SC-34 и SC-35, перечисленных в Таблице 2.
[053]

[0054] В другом аспекте настоящего изобретения предложено соединение формулы III

где R7 представляет собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил, -(C)mNHC(X)NH(C)nRa-, -(C)pNHC(X)Rb-, -(C)qNHS(O)2Rc, -(C)r(X)NHRd- или -(C)sNH(C)tRe;
где Ra, Rb, Rc, Rd и Re независимо представляют собой водород, галоген, гидроксил, необязательно замещенный алкоксил, необязательно замещенный тиоалкокси, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил;
X представляет собой О или S; и
m, n, p, q, r, s, t составляют 0, 1 или 2.
[0055] В одном из вариантов реализации настоящего изобретения соединение формулы III включает те соединения, в которых R7 независимо представляет собой водород, необязательно замещенный низший алкил, -(C)mNHC(X)NH(C)nRa-, (C)pNHC(X)Rb-, -(C)qNHS(O)2Rc или -(C)sNH(C)tRe.
[0056] В другом варианте реализации настоящего изобретения соединение формулы III включает те соединения, в которых Ra, Rb, Rc, Rd и Re независимо представляют собой фенил или нафтил, необязательно замещенный 1-3 группами, выбранными из группы, состоящей из галогена, необязательно замещенного низшего алкила (такого как галогензамещенный низший алкил, например трифторметил), необязательно замещенного алкоксила (например, такого как галогензамещенный низший алкоксил, например трифторметил) и необязательно замещенного арилокси (например, цианозамещенного фенокси).
[0057] В некоторых примерах соединение формулы III представляет собой одно из соединений SC-36, SC-37 и SC-38, перечисленных в Таблице 3.
[0058]

[0059] Термин «гало» или «галоген» отдельно или в комбинации означает любой из галогенов, такой как фтор (F), хлор (Cl), бром (Br) или йод (I).
[0060] Термин «гидроксил» означает группу -ОН.
[0061] Термины «тио» и «меркапто» используются взаимозаменяемо и означают группу -SH.
[0062] Термин «алкил» отдельно или в комбинации означает радикал, представляющий собой производное алкана, содержащий, если не указано иное, 1-20 атомов углерода (С1-С20), предпочтительно 1-15 атомов углерода (С1-С15), более предпочтительно 1-10 атомов углерода (C1-С10). Указанный радикал представляет собой алкильные группы с прямой цепью, разветвленные алкильные группы или циклоалкильные группы, предпочтительно неразветвленные или разветвленные алкильные группы, содержащие 1-15, более предпочтительно 1-8, еще более предпочтительно 1-6, еще более предпочтительно 1-4 и наиболее предпочтительно 1-2 атома углерода, такие как метил, этил, пропил, изопропил, бутил, трет-бутил и т.п. Термин «низший алкил» в настоящей заявке используется для описания алкильных групп с прямой цепью, описанных выше. Предпочтительно циклоалкильные группы представляют собой моноциклические, бициклические или трициклические кольцевые системы из 3-8, более предпочтительно 3-6, атомов в одном кольце, такие как циклопропил, циклопентил, циклогексил, адамантил и т.п. Алкил также включает алкильную группу с прямой цепью или разветвленную алкильную группу, которая содержит циклоалкильный фрагмент или прерывается им. Алкильную группу с прямой или разветвленной цепью присоединяют по любому доступному положению с получением стабильного соединения. Примеры указанных алкилов включают, но не ограничиваются указанными, 4-(изопропил)циклогексилен или 2-метилциклопропилпентил. Замещенный 1-3 группами или заместителями, представляющими собой галоген, гидроксил, алкокси, алкилтио, алкилсульфинил, алкилсульфонил, ацилокси, арилокси, гетероарилокси, амин, необязательно моно- или дизамещенный алкильными, арильными или гетероарильными группами, амидино, мочевину, необязательно замещенную алкильными, арильными, гетероарильными или гетероциклильными группами, аминосульфинил, необязательно N-моно- или N,N-дизамещенный алкильными, арильными или гетероарильными группами, алкилсульфониламино, арилсульфониламино, гетероарилсульфониламино, алкилкарбониламино, арилкарбониламино, гетероарилкарбониламино или иные подобные заместители.
[0063] Термин «алкенил» отдельно или в комбинации означает неразветвленный, разветвленный или циклический углеводород, содержащий 2-20, предпочтительно 2-17, более предпочтительно 2-10, еще более предпочтительно 2-8, наиболее предпочтительно 2-4 атома углерода, и по меньшей мере одну, предпочтительно 1-3, более предпочтительно 1-2, наиболее предпочтительно одну двойную связь углерод-углерод. В случае циклоалкенильной группы сопряжение более чем одной двойной связи углерод-углерод отличается от сопряжения, придающего кольцу ароматичность. Двойные связи углерод-углерод могут содержаться или в циклоалкильном фрагменте, за исключением циклопропила, или во фрагменте, представляющем собой прямую или разветвленную цепь. Примеры алкенильных групп включают этенил, пропенил, изопропенил, бутенил, циклогексенил, циклогексенилалкил и т.п. Замещенный алкенил представляет собой алкенильные группы с прямой цепью, разветвленные алкенильные группы или циклоалкенильные группы, определенные ранее, независимо замещенные 1-3 группами или заместителями, представляющими собой галоген, гидроксил, арилокси, алкилтио, алкилсульфинил, алкилсульфонил, независимо замещенный алкильными, арильными или гетероарильными группами, амидино, мочевину, необязательно замещенную алкильными, арильными, гетероарильными или гетероциклильными группами, аминосульфонил, необязательно N-моно- или N.N-дизамещенный алкильными, арильными или гетероарильными группами, алкилсульфониламино, алкилкарбониламино, арилкарбониламино, арилоксикарбонил, гетероарилоксикарбонил или иные подобные заместители, присоединенные по любому доступному положению с получением стабильного соединения.
[0064] Термин «алкинил» отдельно или в комбинации означает неразветвленный, разветвленный или циклический углеводород, содержащий 2-20, предпочтительно 2-17, более предпочтительно 2-10, еще более предпочтительно 2-8, наиболее предпочтительно 2-4 атома углерода, и по меньшей мере одну, предпочтительно 1-3, более предпочтительно 1-2, наиболее предпочтительно одну тройную связь углерод-углерод. Примеры алкинильных групп включают этинил, пропинил, изопропинил, бутинил и т.п. Замещенный алкинил представляет собой алкинильные группы с прямой цепью, разветвленные алкинильные группы, определенные ранее, независимо замещенные 1-3 группами или заместителями, представляющими собой галоген, гидроксил, арилокси, алкилтио, алкилсульфинил, алкилсульфонил, независимо замещенный алкильными, арильными или гетероарильными группами, амидино, мочевину, необязательно замещенную алкильными, арильными, гетероарильными или гетероциклильными группами, аминосульфонил, необязательно N-моно- или N,N-дизамещенный алкильными, арильными или гетероарильными группами, алкилсульфониламино, алкилкарбониламино, арилкарбониламино, арилоксикарбонил, гетероарилоксикарбонил или иные подобные заместители, присоединенные по любому доступному положению с получением стабильного соединения.
[0065] Термин «алкилалкенил» означает группу -R-CR′=CR″R′′′, где R представляет собой низший алкил или замещенный низший алкил, R′, R″, R′′′ независимо могут представлять собой водород, галоген, низший алкил, замещенный низший алкил, ацил, арил, замещенный арил, гетарил или замещенный гетарил, определенный ниже.
[0066] Термин «алкилалкинил» означает группу -R-CCR′, где R представляет собой низший алкил или замещенный низший алкил, R′ представляет собой водород, галоген, низший алкил, замещенный низший алкил, ацил, арил, замещенный арил, гетарил или замещенный гетарил, определенный ниже.
[0067] Термин «алкокси» означает группу -OR, где R представляет собой низший алкил, замещенный низший алкил, ацил, арил, замещенный арил, аралкил, замещенный аралкил, гетероалкил, гетероарилалкил, циклоалкил, замещенный циклоалкил, циклогетероалкил или замещенный циклогетероалкил, определенный в настоящей заявке.
[0068] Термин «алкилтио» или «тиоалкокси» означает группу -SR, S(O)n=1-2-R, где R представляет собой низший алкил, замещенный низший алкил, ацил, арил, замещенный арил, аралкил или замещенный аралкил, определенный в настоящей заявке.
[0069] Термин «ацил» означает группы -C(O)R, где R представляет собой водород, низший алкил, замещенный низший алкил, арил, замещенный арил и т.п., определенные в настоящей заявке.
[0070] Термин «арилокси» означает группы -OAr, где Ar представляет собой арильную, замещенную арильную, гетероарильную или замещенную гетероарильную группу, определенную в настоящей заявке.
[0071] Термин «амидо» означает группу -C(O)NRR′, где R и R′ независимо могут представлять собой водород, низший алкил, замещенный низший алкил, арил, замещенный арил и т.п., определенные в настоящей заявке.
[0072] Термин «карбоксил» означает группу -C(O)OR, где R представляет собой водород, низший алкил, замещенный низший алкил, арил, замещенный арил и т.п., определенные в настоящей заявке.
[0073] Термин «арил» отдельно или в комбинации означает фенил или нафтил, необязательно карбоциклически конденсированный с циклоалкилом, который содержит предпочтительно 5-7, более предпочтительно 5-6 атомов в кольце, и/или необязательно замещенный 1-3 группами или заместителями, представляющими собой галоген, гидроксил, арилокси, алкилтио, алкилсульфинил, алкилсульфонил, независимо замещенный алкильными, арильными или гетероарильными группами, амидино, мочевину, необязательно замещенную алкильными, арильными, гетероарильными или гетероциклильными группами, аминосульфонил необязательно N-моно- или N,N-дизамещенный алкильными, арильными или гетероарильными группами, алкилсульфониламино, алкилкарбониламино, арилкарбониламино, арилоксикарбонил, гетероарилоксикарбонил или иные подобные заместители.
[0074] Термин «гетероцикл» означает насыщенную, ненасыщенную или ароматическую карбоциклическую группу, содержащую единственное кольцо (например, морфолино, пиридил или фурил) или несколько конденсированных колец (например, нафтиридил, хиноксалил, хинолинил, индолизинил или бензо[b]тиенил) и содержащую по меньшей мере один гетероатом, такой как N, О или S, в кольце, которое необязательно может быть незамещенным или замещенным, например, галогеном, низшим алкилом, низшим алкокси, алкилтиоацетиленом, амино, амидо, карбоксилом, гидроксилом, арилом, арилокси, гетероциклом, гетарилом, замещенным гетарилом, нитро, циано, тиолом, сульфамино и т.п.
[0075] Термин «гетероарил» отдельно или в комбинациях означает моноциклическую ароматическую кольцевую структуру, содержащую 5 или 6 атомов в кольце, или бициклическую ароматическую группу из 8-10 атомов, содержащую один или более гетероатомов, предпочтительно 1-4, более предпочтительно 1-3, еще более предпочтительно 1-2 гетероатома, независимо выбранных из группы, состоящей из О, S и N, и необязательно замещенную 1-3 группами или заместителями, представляющими собой галоген, гидроксил, алкокси, алкилтио, алкилсульфинил, алкилсульфонил, ацилокси, арилокси, гетероарилокси, амин, необязательно моно- или дизамещенный алкильными, арильными или гетероарильными группами, амидино, мочевину, необязательно замещенную алкильными, арильными, гетероарильными или гетероциклильными группами, аминосульфинил, необязательно N-моно- или N,N-дизамещенный алкильными, арильными или гетероарильными группами, алкилсульфониламино, арилсульфониламино, гетероарилсульфониламино, алкилкарбониламино, арилкарбониламино, гетероарилкарбониламино или иные подобные заместители. Также подразумевается, что гетероарил включает окисленный S или N, такой как сульфинил, сульфонил и N-оксид третичного азота в кольце. Атом углерода или азота представляет собой место присоединения гетероарильной кольцевой структуры, так что стабильное ароматическое кольцо сохраняется. Примерами гетероарильных групп являются пиридинил, пиридазинил, пиразинил, хиназолинил, пуринил, индонил, хинолинил, пиримидинил, пирролил, оксазолил, тиазолил, тиенил, изоксазолил, оксатиадиазолил, изотиазолил, тетразолил, имидазолил, триазинил, фуранил, бензофурил, индолил и т.п. Замещенный гетероарил содержит заместитель, присоединенный к доступному углероду или азоту с получением стабильного соединения.
[0076] Термин «гетероциклил» отдельно или в комбинации означает неароматическую циклоалкильную группу, содержащую от 5 до 10 атомов, в которой от 1 до 3 атомов углерода в кольце заменены гетероатомами О, S, N, и которая необязательно является бензоконденсированной или конденсированной с гетероарилом, содержащим 5-6 атомов в кольце, и/или необязательно является замещенной, как в случае циклоалкила. Также подразумевается, что гетероциклил включает окисленный S или N, такой как сульфинил, сульфонил и N-оксид третичного азота в кольце. Местом присоединения является атом углерода или азота. Примерами гетероциклильной группы являются тетрагидрофуранил, дигидропиридинил, пиперидинил, пирролидинил, пиперазинил, дигидробензофурил, дигидроиндолил и т.п. Замещенный гетероциклил содержит заместитель, представляющий собой азот, присоединенный к доступному углероду или азоту с получением стабильного соединения.
[0077] Термин «замещенный гетероарил» означает гетероцикл, необязательно моно- или полизамещенный одной или более функциональными группами, например галогеном, низшим алкилом, низшим алкокси, алкилтиоацетиленом, амино, амидо, карбоксилом, гидроксилом, арилом, арилокси, гетероциклом, замещенным гетероциклом, гетарилом, замещенным гетарилом, нитро, циано, тиолом, сульфамидо и т.п.
[0078] Термин «аралкил» означает группу -R-Ar, где Ar представляет собой арильную группу, a R представляет собой низшую алкильную или замещенную низшую алкильную группу. Арильные группы необязательно могут быть незамещенными или замещенными, например, галогеном, низшим алкилом, низшим алкокси, алкилтиоацетиленом, амино, амидо, карбоксилом, гидроксилом, арилом, арилокси, гетероциклом, замещенным гетероциклом, гетарилом, замещенным гетарилом, нитро, циано, тиолом, сульфамидо и т.п.
[0079] Термин «гетероалкил» означает группу -R-Het, где Het представляет собой гетероциклическую группу, a R представляет собой низшую алкильную группу. Гетероалкильные группы необязательно могут быть незамещенными или замещенными галогеном, низшим алкилом, низшим алкокси, алкилтиоацетиленом, амино, амидо, карбоксилом, гидроксилом, арилом, арилокси, гетероциклом, замещенным гетероциклом, гетарилом, замещенным гетарилом, нитро, циано, тиолом, сульфамидо и т.п.
[0080] Термин «гетероарилалкил» означает группу -R-HetAr, где HetAr представляет собой гетероарильную группу, a R представляет собой низшую алкильную группу. Гетероарилалкильные группы необязательно могут быть незамещенными или замещенными галогеном, низшим алкилом, низшим алкокси, алкилтиоацетиленом, амино, амидо, карбоксилом, гидроксилом, арилом, арилокси, гетероциклом, замещенным гетероциклом, гетарилом, замещенным гетарилом, нитро, циано, тиолом, сульфамидо и т.п.
[0081] Термин «циклоалкил» означает двухвалентную циклическую или полициклическую алкильную группу, содержащую от 3 до 15 атомов углерода.
[0082] Термин «замещенный циклоалкил» означает циклоалкильную группу, содержащую один или более заместителей, например галоген, низший алкил, низший алкокси, алкилтиоацетилен, амино, амидо, карбоксил, гидроксил, арил, арилокси, гетероцикл, замещенный гетероцикл, гетарил, замещенный гетарил, нитро, циано, тиол, сульфамидо и т.п.
[0083] Термин «циклогетероалкил» означает циклоалкильную группу, в которой один или более атомов углерода в кольце заменены гетероатомом (например, N, О, S или Р).
[0084] Термин «замещенный циклогетероалкил» означает циклогетероалкильную группу, определенную в настоящей заявке, которая содержит один или более заместителей, таких как галоген, низший алкил, низший алкокси, алкилтиоацетилен, амино, амидо, карбоксил, гидроксил, арил, арилокси, гетероцикл, замещенный гетероцикл, гетарил, замещенный гетарил, нитро, циано, тиол, сульфамидо и т.п.
[0085] Термин «алкилциклоалкил» означает группу -R′-циклоалкил, где циклоалкил представляет собой циклоалкильную группу, a R′ представляет собой низший алкил или замещенный низший алкил. Циклоалкильные группы необязательно могут быть незамещенными или замещенными, например, галогеном, низшим алкилом, низшим алкокси, алкилтиоацетиленом, амино, амидо, карбоксилом, гидроксилом, арилом, арилокси, гетероциклом, замещенным гетероциклом, гетарилом, замещенным гетарилом, нитро, циано, тиолом, сульфамидо и т.п.
[0086] Термин «алкилциклогетероалкил» означает группу -R′-циклогетероалкил, где R′ представляет собой низший алкил или замещенный низший алкил. Циклогетероалкильные группы необязательно могут быть незамещенными или замещенными, например, галогеном, низшим алкилом, низшим алкокси, алкилтиоацетиленом, амино, амидо, карбоксилом, гидроксилом, арилом, арилокси, гетероциклом, замещенным гетероциклом, гетарилом, замещенным гетарилом, нитро, циано, тиолом, сульфамидо и т.п.
[0087] Соединения согласно настоящему изобретению могут быть получены посредством традиционной химической технологии, такой как технологии, описанные в «Advanced organic chemistry», написанной Francis Carey и Richard Sundberg, и обзорном журнале «Account of Chemical research».
[0088] В частности, технология, представленная на общей схеме ниже, является примером синтеза некоторых соединений согласно настоящему изобретению.
Формула I

Формула II

Формула III

Общая технология синтеза соединений Формул I, II, III: а, K2CO3, ДМФА; b, пиридин, ТГФ; с, Et3N, диоксан
Синтезированные таким образом соединения согласно настоящему изобретению могут быть подвергнуты дополнительной очистке посредством хроматографии, или кристаллизации, или любого другого подходящего способа, известного в данной области техники.
[0089] Также в настоящем изобретении предложена фармацевтическая композиция, содержащая одно или более вышеописанных соединений и фармацевтически приемлемый носитель. Фармацевтическая композиция согласно настоящему изобретению может быть применена для повышения уровня экспрессии или биологической активности SHP-1 в клетке или лечения заболевания или патологического состояния, характеризующегося пониженным уровнем экспрессии или пониженной биологической активностью SHP-1. Также в объем настоящего изобретения входит применение любого из вышеописанных соединений для повышения уровня экспрессии или биологической активности SHP-1 в клетке или лечения заболевания или патологического состояния, характеризующегося пониженным уровнем экспрессии или пониженной биологической активностью SHP-1, описанной в настоящей заявке, и для производства лекарственного средства для лечения указанного заболевания или патологического состояния.
[0090] Также в настоящем изобретении предложен способ повышения уровня экспрессии или биологической активности SHP-1 в клетке, включающий приведение указанной клетки в контакт с эффективным количеством соединения или фармацевтической композиции, описанных в настоящей заявке. Также предложен способ лечения заболевания или патологического состояния, характеризующегося пониженным уровнем экспрессии или пониженной биологической активностью SHP-1, у субъекта, нуждающегося в таком лечении, включающий введение указанному субъекту эффективного количества соединения или фармацевтической композиции, описанных в настоящей заявке.
[0091] Термин «лечение» включает профилактику конкретного нарушения или патологического состояния или ослабление симптомов, обусловленных конкретным нарушением или патологическим состоянием, и/или предотвращение или устранение указанных симптомов.
[0092] Соединения согласно настоящему изобретению могут быть применены для лечения заболеваний или патологических состояний, характеризующихся пониженным уровнем экспрессии или пониженной биологической активностью SHP-1. Соединение согласно настоящему изобретению может быть введено пациенту, представляющему собой человека, в виде самостоятельного лекарственного средства или в составе фармацевтических композиций, в которых указанное соединение смешано с подходящими носителями или наполнителями в дозах, достаточных для лечения или улучшения различных патологических состояний, характеризующихся пониженным уровнем экспрессии или пониженной биологической активностью SHP-1. Повышенный или пониженный уровень экспрессии или повышенную или пониженную биологическую активность фактора (например, SHP-1) можно легко обнаружить посредством продукта гена фактора, такого как белок или РНК, в образце, взятом у субъекта, (например, образце крови или образце ткани, взятой посредством биопсии), и анализа указанного образца in vitro для определения уровня РНК, структуры и/или активности экспрессированных белков и т.п.с применением способов детектирования, известных в данной области техники, таких как твердофазный иммуноферментный анализ (ИФА), вестерн-блоттинг и нозерн-блоттинг. Конкретные примеры заболеваний или патологических состояний, характеризующихся пониженным уровнем экспрессии или пониженной биологической активностью SHP-1, согласно настоящему изобретению включают, но не ограничиваются ими, злокачественное новообразование (например, гепатоцеллюлярную карциному, лейкоз, рак легкого, рак молочной железы, рак почки) и остеопороз.
[0093] «Субъект» представляет собой, в частности, млекопитающее, такое как человек, но может также представлять собой домашних животных (например, собак, кошек и т.п.), сельскохозяйственных животных (например, коров, овец, свиней, лошадей и т.п.) или лабораторных животных (например, крыс, мышей, морских свинок и т.п.), нуждающихся в лечении, описанном в настоящей заявке.
[0094] В настоящей заявке «эффективное количество» означает количество активного агента, необходимое для придания терапевтического эффекта при воздействии на субъекта отдельно или в комбинации с одним или более другими активными агентами. Как понятно специалистам в данной области техники, эффективные количества варьируются в зависимости от способа введения, примененного наполнителя и совместного применения с другими активными агентами.
[0095] Подходящие способы введения могут включать, например, пероральное, ректальное, трансмукозальное или интестинальное введение; парентеральное поступление, включая внутримышечные, подкожные, внутримозговые инъекции, а также интратекальные, прямые интравентрикулярные, внутривенные, внутрибрюшинные, интраназальные или внутриглазные инъекции, и необязательно введение в составе пролонгированного действия или замедленного высвобождения.
[0096] Фармацевтические композиции согласно настоящему изобретению могут быть получены способом, известным в данной области техники, например посредством традиционных способов смешивания, растворения, эмульгирования, инкапсулирования, включения или лиофилизации. Таким образом, фармацевтические композиции для применения согласно настоящему изобретению могут быть приготовлены традиционным способом с применением одного или более физиологически приемлемых носителей, включающих наполнители и/или вспомогательные вещества, которые способствуют переработке активных соединений в препараты, которые могут быть применены фармацевтически. В настоящей заявке «приемлемый» означает, что носитель должен быть совместим с активным ингредиентом композиции (и предпочтительно способен стабилизировать активный ингредиент) и безвреден для субъекта, подвергаемого лечению. Точный состав зависит от выбранного способа введения.
[0097] В частности, в случае инъекции соединения согласно настоящему изобретению могут быть приготовлены, например, в физиологически совместимых буферных растворах, таких как раствор Ханка, раствор Рингера или физиологический буферный раствор. В случае перорального введения соединения согласно настоящему изобретению могут быть приготовлены посредством объединения активных соединений с фармацевтически приемлемыми носителями, известными в данной области, такими как лактоза, сахароза, маннит, сорбит, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакант, метилцеллюлоза, гидроксипропил метил целлюлоза, натрий-карбоксиметилцеллюлоза и/или поливинилпирролидон (ПВП), чтобы обеспечить возможность приготовления соединений согласно настоящему изобретению в форме таблеток, пилюль, драже, капсул, жидких составов, гелей, сиропов, паст, суспензий и т.п. В случае введения посредством ингаляции соединения согласно настоящему изобретению могут быть приготовлены в форме аэрозольного спрея, распыляемого из упаковок, в которых создано повышенное давление, или ингалятора, с применением подходящего пропеллента, например дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа.
[0098] Без дальнейших уточнений подразумевается, что вышеуказанное описание в достаточной мере включено в настоящее изобретение. Исходя из этого, следующий конкретный пример следует рассматривать только в качестве иллюстративного и не ограничивающего остальное описание каким бы то ни было образом. Все публикации, включая патенты, цитируемые в настоящей заявке, полностью включены в настоящее описание посредством ссылок.
[0099] Пример 1: Химический синтез
[00100] 1.1 Материалы
[00101] Спектры протонного ядерного магнитного резонанса (1Н-ЯМР) регистрировали на приборах Bruker DPX300 (400 МГц). Химические сдвиги представлены в виде значений δ (м.д.) в сторону слабого поля по сравнению с дейтерированным хлороформом в качестве внутреннего эталона указанного органического раствора. Мультиплетность пиков обозначена следующим образом: с, синглет; д, дублет; т, триплет; кв, квартет; дд, дублет дублетов; ддд, дублет дублета дублетов; дт, дублет триплетов; ушир. с, уширенный синглет; м, мультиплет. Константы спин-спинового взаимодействия (значения J) приведены в герцах (Гц). Степень протекания реакции определяли с применением пластины для тонкослойного хроматографического (ТСХ) анализа на силикагеле 60 F254 (Merck). Хроматографическую очистку проводили на колонке, заполненной щелочным силикагелем 60 (0,063-0,200 мм или 0,040-0,063 мм, Merck). Коммерчески доступные реагенты и растворители применяли без дополнительной очистки. В настоящей заявке применены следующие аббревиатуры: CDCl3 обозначает дейтерированный хлороформ; ДМСО-d6 обозначает диметилсульфоксид-d6; EtOAc обозначает этилацетат; ДМФА обозначает N,N-диметилформамид; MeOH обозначает метанол; ТГФ обозначает тетрагидрофуран; EtOH обозначает этанол; ДМСО обозначает диметилсульфоксид; NMP обозначает N-метилпирролидон. Масс-спектры высокого разрешения регистрировали на масс-спектрометре FINNIGAN MAT 95S.
[00102] 1.2 Способы
[00103] Структурное конструирование соединений согласно настоящему изобретению описано ниже. Сначала для изучения взаимосвязи между подавлением киназы Raf и даун-регуляцией P-STAT3 посредством сорафениба, авторы настоящего изобретения применяли химический способ уменьшения взаимодействия между амидной группой сорафениба и Raf посредством водородной связи, заключавшийся в замене амидогруппы на фенилцианогруппу (соединение 1, Фиг. 1). Авторы настоящего изобретения также производили модификацию SC-1 с применением функциональных групп, которые имеют различный размер, являются донорами водорода, акцепторами водорода, обладают гидрофобной и гидрофильной способностью, с получением серии соединений SC-48, SC-49, SC-54, SC-55, SC-56, SC-58, SC-43, SC-44, SC-45, SC-50, SC-51, SC-52, SC-59, SC-60 и SC-40. Кроме того, авторы настоящего изобретения заменяли мочевинную функциональную группу в главной цепи сорафениба на различные амиды и сульфонамиды с получением соединений 2-11. Далее авторы настоящего изобретения заменяли пиридиновое кольцо на хинолин и применяли его в качестве основы для проведения структурной модификации с получением серии соединений 12-19 и 20-25. Указанные производные SC-1 синтезировали согласно общей технологии, описанной выше в формуле II Фиг. 2. Более того, авторы настоящего изобретения увеличивали длину соединения посредством добавления одного фенильного кольца для изучения зависимости активности от структуры соединений 36-38 с применением другой функциональной группы.
[00104] 1.2.1 Технологии синтеза соединения 1 (формула I)
[00105] К 50 мл раствора трифосгена в ТГФ (0,30 г, 1,0 ммоль) добавляли 4-хлор-3-(трифторметил)анилин (0,21 г, 1,1 ммоль) и 2 эквивалента триэтиламина. Смесь нагревали до 50°C в течение 30 мин. После возвращения температуры на уровень комнатной температуры к смеси добавляли 10 мл раствора 4-(4-аминофенокси)бензонитрила в ТГФ и нагревали до 50°C в течение еще 30 мин. Смесь выпаривали, разбавляли водой и подвергали экстракции EtOAc. Экстракт промывали рассолом, сушили над безводным сульфатом магния и концентрировали при пониженном давлении с получением соединения 1 (0,34 г, 80%).
[00106] 1.2.1.1
[00107] 1-(4-хлор-3-(трифторметил)фенил)-3-(4-(4-цианофенокси)фенил)мочевина (1)

[00108]1Н ЯМР (400 МГц, CDCl3): δ 9,17 (с, 1Н), 8,94 (с, 1Н), 8,10 (с, 1Н), 7,81 (д, 2Н, J=6,8), 7,63-7,59 (м, 2Н), 7,54 (д, 2Н, J=7,2 Гц), 7,10 (д, 2Н, J=6,8 Гц), 7,05 (д, 2Н, J=7,2 Гц);13С ЯМР (100 МГц, метанол-d4): δ 163,7, 163,6, 154,8, 151.4, 151,2, 140,1, 137,7, 137,4, 135,3, 132,9, 129,7, 129,4, 129,1, 128,8, 128,3, 125,6, 125,5, 125,4, 124,2, 122,9, 122,4, 122,3, 122,1, 120,2, 119,7, 118,8, 118,7, 118,6, 118,6, 106,5, 106,4; МСВР, вычисленное значение для C21H13ClF3N3O2 (М+Н): 431,0648; полученное значение: 431,0656.
[00109] 1.2.1.2
[00110] 1-(3-(4-цианофенокси)фенил)-3-(4-хлор-3-(трифторметил)фенил)мочевина (43)

[00111]1Н ЯМР (400 МГц, ДМСО): δ 9,17 (с, 1Н), 9,03 (с, 1Н), 8,04 (д, J=2,4 Гц, 1Н), 7,83 (д, J=8,8 Гц, 2Н), 7,64-7,55 (м, 2Н), 7,41-7,32 (м, 2Н), 7,23 (д, J=7,2 Гц, 1Н), 7,11 (д, J=8,0 Гц, 2Н), 6,75 (дд, J=8,0 Гц, 2,4 Гц, 1Н); МСВР, вычисленное значение для C21H12N3O2F3Cl [М-Н]-: 430,0570; полученное значение: 430,0576.
[00112] 1.2.1.3
[00113] 4-(3-(3-(трифторметил)бензолсульфониламино)фенокси)бензонитрил (44)
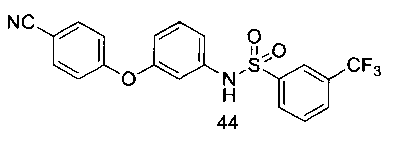
[00114]1Н ЯМР (400 МГц, CDCl3): δ 8,00 (с, 1Н), 7,96 (д, J=8,0 Гц, 1Н), 7,81 (д, J=8,0 Гц, 1Н), 7,65-7,54 (м, 3Н), 7,26 (т, J=8,0 Гц, 1Н), 7,08 (с, 1Н), 7,05-6,97 (м, 1Н), 6,94-6,86 (м, 3Н), 6,84 (т, J=2,0 Гц, 1Н), 6,81 (дд, J=8,4 Гц, 2,0 Гц, 1Н); МСВР, вычисленное значение для C20H12N2O3F3S [М-Н]-: 417,0521; полученное значение: 417,0518.
[00115] 1.2.1.4
[00116] 4-(3-(3-(трифторметокси)бензиламино)фенокси)бензонитрил (45)

[00117]1Н ЯМР (400 МГц, CDCl3): δ 7,61 (д, J=8,8 Гц, 2Н), 7,43 (т, J=8,0 Гц, 1Н), 7,33 (д, J=8,4 Гц, 1Н), 7,29-7,16 (м, 3Н), 7,04 (д, J=8,8 Гц, 2Н), 6,55 (дд, J=8,0 Гц, 2,4 Гц, 1Н), 6,46 (дд, J=8,0 Гц, 2,0 Гц, 1Н), 6,34 (т, J=2,4 Гц, 1Н), 4,41 (с, 2Н); МСВР, вычисленное значение для C21H16N2O2F3 [М+Н]+: 385,1164; полученное значение: 385,1157.
[00118] 1.2.1.5
[00119] 1-(4-(4-цианофенокси)фенил)-3-(3,4-диметоксибензил)мочевина (48)

[00120]1Н ЯМР (400 МГц, CDCl3): δ 7,56 (д, J=6,8 Гц, 2Н), 7,34 (д, J=8,8 Гц, 2Н), 6,98-6,94 (м, 4Н), 6,88-6,75 (м, 4Н), 6,56 (ушир. с, 1Н), 4,36 (с, 2Н), 3,84 (с, 6Н); МСВР, вычисленное значение для C23H20N3O4 [М-Н]-: 402,1454; полученное значение: 402,1462.
[00121] 1.2.1.6
[00122] 1-(4-хлор-3-(трифторметил)фенил)-3-(4-(4-цианофенокси)бензил)мочевина (49)

[00123]1Н ЯМР (400 МГц, CDCl3): δ 7,76 (с, 1Н), 7,51-7,39 (м, 3Н), 7,29 (дд, J=8,8 Гц, 2,4 Гц, 1Н), 7,13 (д, J=8,4 Гц, 3Н), 6,83 (дд, J=8,8 Гц, 4,8 Гц, 4Н), 5,93 (т, J=6,0 Гц, 1Н), 4,24 (д, J=6,0 Гц, 2Н); МСВР, вычисленное значение для C22H14N3O2F3Cl [М-Н]-: 444,0727; полученное значение: 444,0732.
[00124] 1.2.1.7
[00125] 1-(3-(4-цианофенокси)фенил)-3-(3-фторфенил)мочевина (50)

[00126]1Н ЯМР (400 МГц, MeOD): δ 7,66 (д, J=9,2 Гц, 2Н), 7,60 (с, 1Н), 7,41-7,34 (м, 2Н), 7,22 (кв, J=8,0 Гц, 1Н), 7,18 (дд, J=8,0 Гц, 2,0 Гц, 1Н), 7,10-7,02 (м, 3Н), 6,71 (дд, J=8,8 Гц, 2,4 Гц, 2Н); МСВР, вычисленное значение для C20H13N3O2 [М-Н]-: 346,0992; полученное значение: 346,0999.
[00127] 1.2.1.8
[00128] N-(3-(4-цианофенокси)фенил)бензамид (51)

[00129]1Н ЯМР (400 МГц, CDCl3): δ 8,82 (с, 1Н), 7,75 (д, J=7,6 Гц, 2Н), 7,53 (с, 1Н), 7,46-7,35 (м, 4Н), 7,28 (т, J=8,0 Гц, 2Н), 7,22 (т, J=8,0 Гц, 1Н), 6,90 (д, J=8,8 Гц, 2Н), 6,72 (дд, J=8,0 Гц, 2,0 Гц, 1Н); МСВР, вычисленное значение для C20H13N2O2 [М-Н]-: 313,0977; полученное значение: 313,0971.
[00130] 1.2.1.9
[00131] N-(3-(4-цианофенокси)фенил)бензолсульфонамид (52)

[00132]1Н ЯМР (400 МГц, CDCl3): δ 7,79 (д, J=8,4 Гц, 2Н), 7,53 (т, J=4,4 Гц, 3Н), 7,42 (т, J=8,0 Гц, 2Н), 7,20 (т, J=8,0 Гц, 1Н), 6,93 (дд, J=8,0 Гц, 2,0 Гц, 1Н), 6,86-6,83 (м, 3Н), 6,73 (дд, J=8,0 Гц, 2,0 Гц, 1Н); МСВР, вычисленное значение для C19H13N2O3S [М-Н]-: 349,0647; полученное значение: 2349,0643.
[00133] 1.2.1.10
[00134] 1-(4-(4-цианофенокси)бензил)-3-(3,4-диметоксибензил)мочевина (54)

[00135]1Н ЯМР (400 МГц, ДМСО): δ 7,81 (д, J=9,2 Гц, 2Н), 7,33 (д, J=8,4 Гц, 2Н), 7,06 (дд, J=15,6 Гц, 9,2 Гц, 4Н), 6,86 (д, J=9,2 Гц, 2Н), 6,76 (дд, J=8,0 Гц, 2,0 Гц, 1Н), 6,45 (т, J=6,0 Гц, 1Н), 6,38 (т, J=6,0 Гц, 1Н), 4,23 (д, J=5,2 Гц, 2Н), 4,14 (д, J=5,2 Гц, 2Н), 3,69 (с, 6Н); МСВР, вычисленное значение для C24H24N3O4 [М+Н]+: 418,1767; полученное значение: 418,1773.
[00136] 1.2.1.11
[00137] 1-(4-(4-цианофенокси)бензил)-3-(3-(трифторметокси)бензил)мочевина (55)

[00138]1Н ЯМР (400 МГц, CDCl3): δ 7,49 (д, J=9,2 Гц, 2Н), 7,17 (т, J=8,0 Гц, 1Н), 7,10 (д, J=8,4 Гц, 2Н), 7,00-6,92 (м, 3Н), 6,88 (д, J=9,2 Гц, 2Н), 6,84 (д, J=8,4 Гц, 2Н), 6,17-6,05 (м, 2Н), 4,10 (м, 4Н); МСВР, вычисленное значение для C23H19N3F3 [М+Н]+: 442,1379; полученное значение: 442,1381.
[00139] 1.2.1.12
[00140] (R)-1-(4-(4-цианофенокси)фенил)-3-(1-(нафталин-1-ил)этил)мочевина (56)

[00141]1Н ЯМР (400 МГц, MeOD): δ 8,17 (д, J=8,0 Гц, 1Н), 7,87 (д, J=8,0 Гц, 1Н), 7,78 (д, J=8,0 Гц, 1Н), 7,65 (д, J=8,8 Гц, 2Н), 7,58 (д, J=7,2 Гц, 1Н), 7,53 (д, J=7,2 Гц, 1Н), 7,50-7,45 (м, 2Н), 7,41 (д, J=8,8 Гц, 2Н), 6,99 (т, J=9,2 Гц, 4Н), 5,74 (д, J=6,8 Гц, 1Н), 1,63 (д, J=6,8 Гц, 3Н); МСВР, вычисленное значение для C26H20N3O2 [М-Н]-: 406,1556; полученное значение: 406,1563.
[00142] 1.2.1.13
[00143] 1-(4-хлор-3-(трифторметил)бензил)-3-(4-(4-цианофенокси)фенил)мочевина (58)

[00144]1Н ЯМР (400 МГц, MeOD): δ 7,74 (ушир. с, 1Н), 7,66 (д, J=9,2 Гц, 2Н), 7,56 (д, J=2,0 Гц, 2Н), 7,44 (д, J=9,2 Гц, 2Н), 7,05-6,98 (м, 4Н), 4,43 (с, 2Н); МСВР, вычисленное значение для C22H14N3O2F3Cl [М-Н]-: 444,0727; полученное значение: 444,0736.
[00145] 1.2.1.14
[00146] 1-(4-хлор-3-(трифторметил)фенил)-3-(3-(4-цианофенокси)-4-метилфенил)мочевина (59)
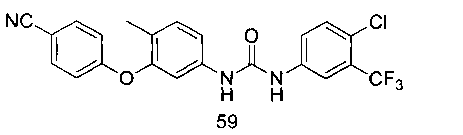
[00147]1Н ЯМР (400 МГц, MeOD): δ 7,87 (д, J=2,8 Гц, 1Н), 7,60 (д, J=9,2 Гц, 2Н), 7,54 (дд, J=8,4 Гц, 2,4 Гц, 1Н), 7,39 (д, J=8,8 Гц, 1Н), 7,25 (д, J=2,4 Гц, 1Н), 7,18 (д, J=8,0 Гц, 1Н), 7,12 (дд, J=8,0 Гц, 2,4 Гц, 1Н), 6,93 (д, J=9,6 Гц, 2Н), 2,02 (с, 3Н); МСВР, вычисленное значение для C22H14N3O2F3Cl [М-Н]-: 444,0727; полученное значение: 444,0725.
[00148] 1.2.1.15
[00149] 1,3-бис(3-(4-цианофенокси)-4-метилфенил)мочевина (60)

[00150]1Н ЯМР (400 МГц, ДМСО): δ 8,77 (с, 2Н), 7,80 (д, J=8,0 Гц, 4Н), 7,29 (с, 2Н), 7,24 (д, J=8,0 Гц, 2Н), 7,13 (д, J=8,4 Гц, 2Н), 6,98 (д, J=8,4 Гц, 4Н), 2,02 (с, 6Н); МСВР, вычисленное значение для C29H21N4O3 [М-Н]-: 473,1614; полученное значение: 473,1619.
[00151] 1.2.2 Общие технологии синтеза соединений 2-25
[00152] Производные анилина (1 ммоль) и каталитическое количество пиридина помещали в безводный ТГФ (10 мл) в 25 мл двугорлой круглодонной колбе при комнатной температуре. К смеси добавляли соединения, представляющие собой ацилхлориды или сульфонил хлориды, и перемешивали в течение 2 ч при комнатной температуре. Растворитель удаляли под вакуумом и неочищенный остаток очищали посредством хроматографии на колонке, заполненной силикагелем, с применением EtOAc/гексана в качестве элюента (от 1/10 до 1/2). Указанная технология приводила к получению желаемого продукта взаимодействия в виде белого твердого вещества с выходом от 70% до 95%.
[00153] 1.2.2.1
[00154] N-метил-4-(4-(фенилсульфонамидо)фенокси)пиколинамид (2)

[00155]1Н ЯМР (400 МГц, CDCl3): δ 8,36 (д, 1Н, J=5,6 Гц), 8,01 (ушир. с, 1Н), 7,76 (д, 2Н, J=7,6 Гц), 7,59 (с, 1Н), 7,54 (т, 1Н, J=8,0 Гц), 7,46 (т, 2Н, J=8,0 Гц), 7,12 (д, 2Н, J=8,8 Гц), 6,94 (д, 2Н, J=8,8 Гц), 6,92-6,90 (м, 1Н), 3,00 (д, 3Н, J=5,2 Гц);13С ЯМР (100 МГц, CDCl3): δ 166,0, 164,6, 152,1, 151,0, 149,7, 138,9, 134,2, 133,0, 129,0, 127,1, 123,9, 121,6, 114,3, 109,9, 26,1; МСВР, вычисленное значение для C19H17N3O4S (М+Н): 383,0940; полученное значение: 383,0941.
[00156] 1.2.2.2
[00157] N-метил-4-(4-(4-нитрофенилсульфонамидо)фенокси)пиколинамид (3)

[00158]1Н ЯМР (400 МГц, CDCl3): δ 8,39 (д, 1Н, J=5,6 Гц), 8,30 (д, 2Н, J=8,8 Гц), 8,07 (ушир. с, 1Н), 7,93 (д, 2Н, J=8,8 Гц), 7,49 (с, 1Н), 7,17 (д, 2Н, J=8,8 Гц), 7,01-6,98 (м, 3Н), 3,00 (д, ЗН, J=5,2 Гц); МСВР, вычисленное значение для C19H16N4O6S (М+Н): 428,0791; полученное значение: 428,0798.
[00159] 1.2.2.3
[00160] 4-(4-(4-фторфенилсульфонамидо)фенокси)-N-метилпиколинамид (4)

[00161]1Н ЯМР (400 МГц, CDCl3): δ 8,37 (д, 1Н, J=5,6 Гц), 8,00 (ушир. с, 1Н), 7,77-7,43 (м, 2Н), 7,57 (с, 1Н), 7,17-7,09 (м, 4Н), 6,99-6,93 (м, 4Н), 3,00 (д, 3Н, J=4,8 Гц); ЯМР (100 МГц, CDCl3): δ 166,5, 165,9, 164,6, 163,9, 152,1, 151,2, 149,7, 135,0, 134,0, 130,0, 129,9, 124,1, 121,7, 116,4, 116,2, 114,5, 109,8, 26,19; МСВР, вычисленное значение для C19H16FN3O4S (М+Н): 401,0846; полученное значение: 401,0849.
[00162] 1.2.2.4
[00163] 4-(4-(4-трет-бутилфенилсульфонамидо)фенокси)-N-метилпиколинамид (5)

[00164]1Н ЯМР (400 МГц, CDCl3): δ 8,33 (д, 1Н, J=6,0 Гц), 8,21 (ушир. с, 1Н), 7,79 (ушир. с, 1Н), 7,69 (д, 2Н, J=6,8 Гц), 7,62 (с, 1Н), 7,44 (д, 2Н, J=6,8 Гц), 7,15 (д, 2Н, J=6,8 Гц), 6,91 (с, 2Н, J=6,8 Гц), 6,88-6,86 (м, 1Н), 2,98 (д, 3Н, J=5,2 Гц);13С ЯМР (100 МГц, CDCl3): δ 166,0, 164,6, 156,8, 152,2, 150,8, 149,7, 136,1, 134,4, 127,0, 126,1, 123,6, 121,6, 114,1, 110,1, 35,1, 30,1, 26,1; МСВР, вычисленное значение для C23H25N3O4S (М+Н): 439,1566; полученное значение: 439,1564.
[00165] 1.2.2.5
[00166] N-метил-4-(4-(нафталин-2-сульфонамидо)фенокси)пиколинамид (6)

[00167]1Н ЯМР (400 МГц, CDCl3): δ 8,34 (с, 1Н), 8,30 (д, 1Н, J=5,2 Гц), 8,05-8,02 (м, 1Н), 7,89-7,83 (м, 4Н), 7,74 (дд, 1Н, J=8,4, 1,6 Гц), 7,60-7,52 (м, 3Н), 7,16 (д, 2Н, J=8,8 Гц), 6,88 (д, 2Н, J=8,8 Гц), 6,84-6,82 (м, 1Н);13С ЯМР (100 МГц, CDCl3): 165,9, 164,6, 152,1, 151,0, 149,7, 135,9, 134,9, 134,2, 132,0, 129,4, 129,3, 128,9, 128,7, 127,9, 127,5, 123,9, 122,2, 121,6, 114,2, 110,1, 26,2; МСВР, вычисленное значение для C23H19N3O4S (М+Н): 433,1096; полученное значение: 433,1079.
[00168] 1.2.2.6 4-(4-(2-бром-4-(трифторметил)фенилсульфонамидо)фенокси)-7-метилпиколинамид (7)

[00169]1Н ЯМР (400 МГц, CDCl3): δ 8,35 (д, 1Н, J=5,6 Гц), 8,15 (д, 1Н, J=8,0 Гц), 7,79 (ушир. с, 1Н), 7,96 (с, 1Н), 7,67 (д, 2Н, J=8,0 Гц), 7,57 (с, 1Н), 7,18 (д, 2Н, J=9,2 Гц), 6,95 (д, 2Н, J=9,2 Гц), 6,90-6,88 (м, 1Н), 2,98 (д, 3Н, J=5,2 Гц);13С ЯМР (100 МГц, CDCl3): δ 165,7, 164,5, 152,2, 151,6, 149,8, 141,5, 136,1, 135,8, 135,5, 135,2, 132,7, 132,2 (м), 124,9 (м), 124,1, 123,5, 121,7, 120,8, 120,4, 114,5, 110,0, 26,1; МСВР, вычисленное значение для C20H15BrF3N3O4S (М+Н): 528,9919; полученное значение: 528,9917.
[00170] 1.2.2.7
[00171] N-метил-4-(4-(2-нитрофенилсульфонамидо)фенокси)пиколинамид (8)

[00172]1Н ЯМР (400 МГц, CDCl3): δ 8,37 (д, 1Н, J=6,0 Гц), 7,98 (ушир. с, 1Н), 7,86-7,83 (м, 2Н), 7,72-7,68 (м, 2Н), 7,55 (с, 1Н), 7,24 (д, 2Н, J=8,8 Гц), 6,98 (д, 2Н, J=8,8 Гц), 6,94-6,92 (м, 1Н), 2,98 (д, 3Н, J=4,8 Гц); МСВР, вычисленное значение для C19H16N4O6S (М+Н): 428,0791; полученное значение: 428,0796.
[00173] 1.2.2.8
[00174] 4-(4-(3,5-бис(трифторметил)бензамидо)фенокси)-N-метилпиколинамид (9)

[00175]1Н ЯМР (400 МГц, CDCl3): δ 9,92 (с, 1Н), 8,40 (с, 1Н), 8,33 (д, 1Н, J=5,6 Гц), 8,10 (кв, 1Н, J=5,2 Гц), 7,90 (с, 1Н), 7,71 (д, 2Н, J=8,8 Гц), 7,40 (д, 1Н, J=2,8 Гц), 6,99-6,97 (м, 1Н), 6,93 (д, 2Н, J=8,8 Гц), 2,91 (д, 3Н, J=4,8 Гц);13С ЯМР (100 МГц, метанол-d4): δ 167,8, 166,8, 165,1, 153,4, 151,8, 151,6, 138,6, 137,6, 133,6, 133,3, 133,0, 132.6, 129,4 (д), 126,2 (м), 126,0, 124,2, 123,2, 122,4, 115,2, 110,7, 26,4; МСВР, вычисленное значение для C22H15F6N3O3 (М+Н): 483,1018; полученное значение: 483,1017.
[00176] 1.2.2.9
[00177] 4-(4-(5-фтор-2-(трифторметил)бензамидо)фенокси)-N-метилпиколинамид (10)

[00178]1Н ЯМР (400 МГц, CDCl3): δ 8,66 (д, 1Н, J=12,4 Гц), 8,31-8,26 (м, 2Н), 7,93 (с, 1Н), 7,70-7,65 (м, 3Н), 7,56 (т, 1Н, J=2,4 Гц), 7,24-7,19 (м, 1Н), 7,02 (д, 2Н, J=6,4 Гц), 6,89-6,87 (м, 1Н), 2,90 (д, 3Н, J=3,2 Гц);13С ЯМР (100 МГц, метанол-d4): δ 166,2, 164,5, 162,9, 160,4, 160,0, 159,9, 152,2, 150,4, 149,7, 135,0, 130,6 (м), 129,8 (м), 128,3, 128,1, 127,7, 127,4, 124,5, 122,5, 122,4, 122,3, 121,8, 121,5, 117,2, 117,0, 114,1, 110,1, 26,1; МСВР, вычисленное значение для C21H15F4N3O3 (М+Н): 433,1050; полученное значение: 433,0152.
[00179] 1.2.2.10
[00180] N-метил-4-(4-(4-(трифторметил)бензамидо)фенокси)пиколинамид (11)

[00181]1Н ЯМР (400 МГц, CDCl3): δ 9,45 (с, 1Н), 8,31 (д, 1Н, J=5,6 Гц), 8,15 (С, 1Н), 8,08 (д, 2Н, J=8,0 Гц), 7,71-7,65 (м, 3Н), 7,50 (д, 1Н, J=2,4 Гц), 7,47 (т, 1Н, J=8,0 Гц), 6,96-6,91 (м, 3Н), 2,92 (д, 3Н, J=5,2 Гц);13С ЯМР (100 МГц, CDCl3): δ 166,4, 164,8, 164.7, 151,8, 149,9, 149,8, 138,8, 135,5, 131,4, 131,1, 130,8, 130,7, 130,5, 129,1, 128,1, 125,0, 124,3 (м), 122,6, 122,3, 121,2, 114,4, 109,5, 26,1; МСВР, вычисленное значение для C21H16F3N3O3 (М+Н): 415,1144; полученное значение: 415,1146.
[00182] 1.2.2.11
[00183] 2-нитро-N-(4-(хинолин-4-илокси)фенил)-4-(трифторметил)бензолсульфонамид (12)

[00184]1Н ЯМР (400 МГц, CDCl3): δ 8,71 (д, 1Н, J=5,2 Гц), 8,28 (д, 1Н, J=8,4 Гц), 8,12 (д, 1Н, J=8,4 Гц), 8,10 (с, 1Н), 8,05 (д, 1Н, J=8,4 Гц), 7,89 (д, 1Н, J=8,4 Гц), 7,80-7,76 (м, 1Н), 7,61-7,57 (м, 1Н), 7,31 (д, 2Н, J=8,8 Гц), 7,13 (д, 1Н, J=8,8 Гц), 6,53 (д, 1Н, J=5,2 Гц); МСВР, вычисленное значение для C22H14F3N3O5S (М+Н): 489,0606; полученное значение: 489,0610.
[00185] 1.2.2.12
[00186] 2-нитро-N-(4-(8-нитрохинолин-4-илокси)фенил)-4-(трифторметил)бензолсульфонамид (13)

[00187]1Н ЯМР (400 МГц, CDCl3): δ 38,78 (д, 1Н, J=5,2 Гц), 8,51 (д, 1Н, J=8,8 Гц), 8,19 (с, 1Н), 8,12-8,02 (м, 3Н), 7,89 (т, 1Н, J=9,6 Гц), 7,62 (т, 1Н, J=8,4 Гц), 7,34 (д, 2Н, J=9,6 Гц), 7,15 (д, 2Н, J=9,6 Гц), 6,91 (д, 1Н, J=6,8 Гц), 6,59 (д, 1Н, J=5,2 Гц), 6,55 (д, 1Н, J=6,8 Гц); МСВР, вычисленное значение для C22H13F3N4O7S (М+Н): 534,0457; полученное значение: 534,0423.
[00188] 1.2.2.13
[00189] 2-бром-N-(4-(хинолин-4-илокси)фенил)-4-(трифторметил)бензолсульфонамид (14)
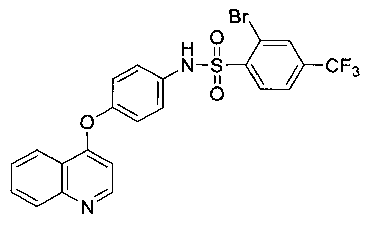
[00190]1Н ЯМР (400 МГц, CDCl3): δ 8,65 (д, 1Н, J=5,2 Гц), 8,25 (д, 1Н, J=8,4 Гц), 8,18 (д, 1Н, J=8,4 Гц), 8,07 (д, 1Н, J=8,4 Гц), 7,98 (с, 1Н), 7,73 (т, 1Н, J=7,6 Гц), 7,67 (д, 1Н, J=8,4 Гц), 7,54 (т, 1Н, J=7,6 Гц), 7,24 (д, 2Н, J=8,8 Гц), 7,05 (д, 2Н, J=8,8 Гц), 6,43 (д, 1Н, J=5,2 Гц);13С ЯМР (100 МГц, CDCl3): δ 161,3, 152,6, 150,9, 149,7, 141,4, 135,9, 135,6, 135,3, 132,7, 132,4, 132,2 (м), 130,3, 129,1, 126,3, 124,9 (м), 124,4, 123,5, 122,1, 122,0, 121,9, 121,6, 121,3, 120,8, 120,4, 116,3, 104,4; МСВР, вычисленное значение для C22H14BrF3N2O3S (М+Н): 521,9861; полученное значение: 521,9858.
[00191] 1.2.2.14
[00192] 2-бром-N-(4-(8-нитрохинолин-4-илокси)фенил)-4-(трифторметил)бензолсульфонамид (15)
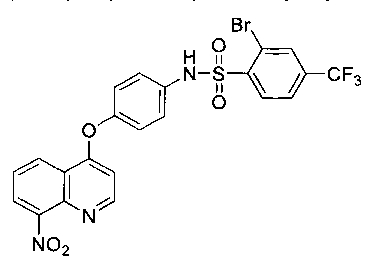
[00193]1Н ЯМР (400 МГц, CDCl3): δ 8,76 (д, 1Н, J=5,2 Гц), 8,49 (д, 1Н, J=8,4 Гц), 8,18 (д, 1Н, J=8,4 Гц), 8,04 (д, 1Н, J=7,6 Гц), 7,99 (с, 1Н), 7,68 (д, 1Н, J=8,4 Гц), 7,60 (т, 1Н, J=8,4 Гц), 7,25 (д, 2Н, J=8,4 Гц), 7,07 (д, 2Н, J=8,4 Гц), 6,53 (д, 1Н, J=5,2 Гц); МСВР, вычисленное значение для C22H13BrF3N3O5S (М+Н): 566,9711; полученное значение: 566,9706.
[00194] 1.2.2.15 N-(4-(хинолин-4-илокси)фенил)-3,5-бис(трифторметил)бензамид (16)

[00195]1Н ЯМР (400 МГц, CDCl3): δ 10,02 (с, 1Н), 8,59 (д, 1Н, J=5,6 Гц), 8,37 (с, 2Н), 8,34 (д, 1Н, J=8,4 Гц), 7,99 (д, 1Н, J=8,4 Гц), 7,92 (с, 1Н), 7,80 (д, 2Н, J=9,2 Гц), 7,70 (т, 1Н, J=7,6 Гц), 6,56 (т, 1Н, J=7,6 Гц), 7,14 (д, 2Н, J=9,2 Гц), 6,52 (д, 1Н, J=5,2 Гц);13С ЯМР (100 МГц, ДМСО-d6): δ 162,6, 161,0, 151,5, 150,0, 149,2, 137,0, 136,1, 131,0, 130,7, 130,4, 130,3, 130,0, 128,8, 128,5 (м), 126,4, 125,2 (м), 124,5, 122,5, 121,7, 121,5, 121,3, 120,6, 104,3; МСВР, вычисленное значение для C24H14F6N2O2 (М+Н): 476,0959; полученное значение: 476,0958.
[00196] 1.2.2.16
[00197] N-(4-(8-нитрохинолин-4-илокси)фенил)-3,5-бис(трифторметил)бензамид (17)

[00198]1Н ЯМР (400 МГц, CDCl3): δ 9,05 (с, 1Н), 8,69 (д, 1Н, J=5,0 Гц), 8,59 (д, 1Н, J=5,0 Гц), 8,35 (с, 2Н), 8,06 (д, 1Н, J=7,8 Гц), 7,97 (с, 1Н), 7,80 (д, 2Н, J=9,0 Гц), 7,63 (т, 1Н, J=8,6 Гц), 7,16 (д, 2Н, J=9,0 Гц), 6,62 (д, 1Н, J=5,0 Гц); МСВР, вычисленное значение для C24H13F6N3O4 (М+Н): 521,0810; полученное значение: 521,0814.
[00199] 1.2.2.17 2-фтор-N-(4-(хинолин-4-илокси)фенил)-5-(трифторметил)бензамид (18)

[00200]1Н ЯМР (400 МГц, CDCl3): δ 8,83 (д, 1Н, J=12,8 Гц), 8,68 (д, 1Н, J=5,2 Гц), 8,39-8,30 (м, 2Н), 8,11 (д, 1Н, J=8,4 Гц), 7,79-7,67 (м, 4Н), 7,58 (т, 1Н, J=8,0 Гц), 7,27-7,22 (м, 1Н), 7,18(д, 2Н, J=9,2 Гц), 6,56 (д, 1Н, J=5,2 Гц);13С ЯМР (100 МГц, метанол-d4): δ 164,4, 164,2, 163,8, 161,7, 151,9, 151,8, 149,7, 137,5, 132,1 (м), 131,2 (м), 128,9 (м), 128,3, 128,1, 127,9, 126,5, 126,3, 123,7, 123,6, 123,0, 122,7, 122,6, 119,1, 119,8, 118,7, 118,5, 105,2; МСВР, вычисленное значение для C23H14F4N2O2 (М+Н): 426,0991; полученное значение: 426,0991.
[00201] 1.2.2.18
[00202] 2-фтор-N-(4-(8-нитрохинолин-4-илокси)фенил)-5-(трифторметил)бензамид (19)

[00203]1Н ЯМР (400 МГц, CDCl3): δ 8,81 (д, 1Н, J=5,2 Гц), 8,59 (д, 1Н, J=8,8 Гц), 8,53-8,47 (м, 2Н), 8,06 (д, 1Н, J=7,6 Гц), 7,83-7,77 (м, ЗН), 7,64 (т, 1Н, J=7,6 Гц), 7,37-7,32 (м, 1Н), 7,23-7,20 (м, 2Н), 6,68 (д, 1Н, J=5,2 Гц); МСВР, вычисленное значение для C23H13F4N3O4 (M+H): 471,0842; полученное значение: 471,0850.
[00204] 1.2.2.19
[00205] N-(3-метил-4-(8-нитрохинолин-4-илокси)фенил)-3,5-бис(трифторметил)бензамид (20)

[00206]1Н ЯМР (400 МГц, CDCl3): δ 9,86 (с, 1Н), 8,45 (д, 1Н, J=5,2 Гц), 8,38 (с, 2Н), 8,31 (д, 1Н, J=8,4 Гц), 7,92 (с, 1Н), 7,89 (д, 1Н, J=8,4 Гц), 7,69-7,63 (м, 2Н), 7,53 (т, 1Н, J=7,6 Гц), 7,33 (с, 1Н), 7,28 (д, 1Н, J=8,4 Гц), 6,33 (д, 1Н, J=5,2 Гц); МСВР, вычисленное значение для C25H15F6N3O4 (М+Н): 535,0967; полученное значение: 535,0956.
[00207] 1.2.2.20
[00208] N-(4-(8-аминохинолин-4-илокси)-3-метилфенил)-3,5-бис(трифторметил)бензамид (21)
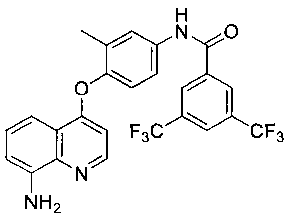
[00209]1Н ЯМР (400 МГц, CDCl3): δ 8,49 (д, 1Н, J=2,0 Гц), 8,27 (с, 1Н), 8,02 (с, 1Н), 7,94 (с, 1Н), 7,65 (д, 1Н, J=8,0 Гц), 7,48-7,45 (м, 2Н), 7,37-7,32 (м, 2Н), 6,96 (д, 1Н, J=7,6 Гц), 4,95 (с, 2Н), 2,16 (с, 3Н); МСВР, вычисленное значение для C25H17F6N3O2 (М+Н): 505,1225; полученное значение:
505,1216. [00210] 1.2.2.21
[00211] N-(4-(8-ацетамидохинолин-4-илокси)-3-метилфенил)-3,5-бис(трифторметил)бензамид (22)

[00212]1Н ЯМР (400 МГц, CDCl3): δ 9,77 (с, 1Н), 9,36 (с, 1Н), 8,65 (д, 1Н, J=7,2 Гц), 8,46 (с, 2Н), 8,44 (д, 1Н, J=5,2 Гц), 7,97 (с, 1Н), 7,87 (д, 1Н, J=8,4 Гц), 7,72 (д, 1Н, J=8,4 Гц), 7,50 (д, 1Н, J=2,0 Гц), 7,37 (т, 1Н, J=8,0 Гц), 7,28 (д, 1Н, J=8,4 Гц), 6,41 (д, 1Н, J=5,2 Гц), 2,26 (с, 3Н), 2,10 (с, 3Н);13С ЯМР (100 МГц, CDCl3): δ 169,2, 163,0, 161,2, 152.0, 148,8, 139,5, 137,2, 136,7, 133,8, 132,6, 132,3, 132,2, 132,0, 131,6, 127,8, 127,1, 126,3, 125,2 (м), 124,2, 121,5, 120,4, 118,8, 118,3, 116,7, 115,7, 113,8, 25,0, 15,4; МСВР, вычисленное значение для C27H19F6N3O3 (М+Н): 547,1331; полученное значение: 547,1325.
[00213] 1.2.2.22
[00214] N-(3-(8-нитрохинопин-4-илокси)фенил)-3,5-бис(трифторметил)бензамид (23)
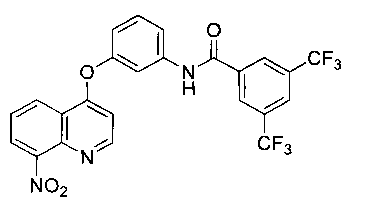
[00215]1Н ЯМР (400 МГц, CDCl3): δ 8,78 (д, 1Н, J=5,6 Гц), 8,58 (д, 1Н, J=8,4 Гц), 8,52 (с, 1Н), 8,31 (с, 2Н), 8,22 (с, 1Н), 8,08-8,04 (м, 2Н), 7,71 (с, 1Н), 7,64 (т, 1Н, J=8,0 Гц), 7,53-7,49 (м, 2Н), 7,03 (д, 1Н, J=7,2 Гц), 6,71 (д, 1Н, J=4,8 Гц); МСВР, вычисленное значение для C24H13FeN3O4 (М+Н): 521,0810; полученное значение: 521,0821.
[00216] 1.2.2.23
[00217] N-(3-(8-аминохинолин-4-илокси)фенил)-3,5-бис(трифторметил)бензамид (24)

[00218]1Н ЯМР (400 МГц, CDCl3): δ 8,55 (д, 1Н, J=4,8 Гц), 8,29 (с, 2Н), 8,05 (с, 1Н), 7,90 (с, 1Н), 7,60 (д, 1Н, J=8,4 Гц), 7,55 (с, 1Н), 7,70-7,43 (м, 2Н), 7,34 (т, 1Н, J=8,0 Гц), 7,01 (д, 1Н, J=8,0 Гц), 6,96 (д, 1Н, J=7,9 Гц), 6,63 (д, 1H,J=4,8 Гц);13С ЯМР (100 МГц, CDCl3): δ 163,1, 161,3, 155,3, 147,9, 143,6, 139,9, 138,8, 136,5, 132,7, 132,4, 132,1, 131,7, 130,6, 127,5 (д), 127,0, 126,8, 125,3 (м), 124,1, 122,0, 118,7, 117,4, 117,2, 113,1, 111.1, 110,0, 105,4; МСВР, вычисленное значение для C24H15F6N3O2 (М+Н): 491,1068; полученное значение: 491,1068.
[00219] 1.2.2.24
[00220] N-(3-(8-ацетамидохинолин-4-илокси)фенил)-3,5-бис(трифторметил)бензамид (25)

[00221]1Н ЯМР (400 МГц, CDCl3): δ 9,77 (с, 1Н), 8,74 (д, 1Н, J=7,6 Гц), 8,54 (д, 1Н, J=5,2 Гц), 8,48 (с, 1Н), 8,39 (с, 2Н), 8,04 (с, 1Н), 7,87 (д, 1Н, J=8,4 Гц), 7,67-7,60 (м, 2Н), 7,50-7,43 (м, 2Н), 7,37 (т, 1Н, J=8,0 Гц), 7,00 (д, 1Н, J=8,4 Гц), 6,65 (д, 1Н, J=5,2 Гц), 2,30 (с, 3Н);13С ЯМР (100 МГц, CDCl3): δ 0169,3, 163,1, 161,7, 154,6, 148,7, 139,6, 136,6, 133,8, 132,7, 132,4, 132,1, 131,7, 130,8, 127,8 (д), 126,9, 126,5, 125,3 (м), 124,2, 121,5, 120,8, 117,7, 117,3, 116,8, 115,7, 113,2, 104,9, 25,0; МСВР, вычисленное значение для C26H17F6N3O3 (М+Н): 533,1174; полученное значение: 533,1167.
[00222] 1.2.2.25
[00223] N-(3-(трифторметил)бензолсульфонил)-3-(3-амино-4-нитрофенокси)бензоламин (SC-40)

1Н ЯМР (400 МГц, CDCl3): δ 8,06 (д, J=9,6 Гц, 1Н), 8,00 (с, 1Н), 7,96 (д, J=8,0 Гц, 1Н), 7,81 (д, J=8,0 Гц, 1Н), 7,61 (т, J=8,0 Гц, 1Н), 7,27 (т, J=8,0 Гц, 1Н), 6,91-6,80 (м, 3Н), 6,19 (дд, J=9,6 Гц, 2,4 Гц, 1Н), 6,14 (д, J=2,4 Гц, 1Н), 6,10 (ушир. с, 2Н);13С ЯМР (100 МГц, CDCl3): δ 163,1, 155,5, 146,7, 140,0, 137,6, 132,0, 131,6, 130,9, 130,3, 130,0, 129,9 (м), 128,8, 128,0, 124,4, 124,3, 124,2, 124,2, 124,0, 121,6, 117,8, 117,6, 113,6, 107,6, 104,3; ЖХ-МС (ИЭР): M/Z 452 [М-Н]-; МСВР, вычисленное значение для C19H13N3O5F3S [М-Н]-: 452,0528; полученное значение: 452,0529.
[00224] 1.2.3 Соединения 36-38
[00225] 1.2.3.1
[00226] 3-(2-фенилимидазо[1,2-а]пиридин-7-илокси)-N-(3-(трифторметокси)бензил)6ензоламин (36)

[00227]1Н ЯМР (400 МГц, CDCl3): δ 7,96 (д, J=8,0 Гц, 1Н), 7,89 (д, J=8,0 Гц, 2Н), 7,71 (с, 1Н), 7,40 (т, J=7,2 Гц, 2Н), 7,35-7,24 (м, ЗН), 7,18 (с, 1Н), 7,14 (т, J=8,0 Гц, 1Н), 7,09 (д, J=7,6 Гц, 1Н), 6,98 (д, J=2,4 Гц, 1Н), 6,60 (дд, J=7,2 Гц, 2,4 Гц, 1Н), 6,46-6,40 (м, 2Н), 6,32 (т, J=2,4 Гц, 1Н), 4,31 (с, 1Н), 4,20 (с, 1Н); МСВР, вычисленное значение для C27H21N3O2F3 [М+Н]+: 476,1586; полученное значение: 476,1592.
[00228] 1.2.3.2
[00229] N-(3-(2-фенилимидазо[1,2-а]пиридин-7-илокси)фенил)-3-(трифторметил)бензолсульфонамид (37)

[00230]1Н ЯМР (400 МГц, CDCl3): δ 8,03 (д, J=6,8 Гц, 2Н), 7,92 (д, J=8,0 Гц, 1Н), 7,87 (д, J=6,8 Гц, 2Н), 7,76 (д, J=6,0 Гц, 2Н), 7,60 (т, J=7,6 Гц, 1Н), 7,39 (т, J=8,0 Гц, 2Н), 7,30 (т, J=6,4 Гц, 1Н), 7,21 (д, J=8,8 Гц, 1Н), 6,96-6,90 (м, 2Н), 6,83 (дд, J=13,6 Гц, 2,4 Гц, 1Н), 6,82 (т, J=2,0 Гц, 2Н), 6,60 (дд, J=7,2 Гц, 2,4 Гц, 1Н); МСВР, вычисленное значение для C26H19N3O3F3S [М+Н]+: 510,1099; полученное значение: 510,1100.
[00231] 1.2.3.3
[00232] N-(3-(2-фенилимидазо[1,2-а]пиридин-7-илокси)фенил)бензолсульфонамид (38)
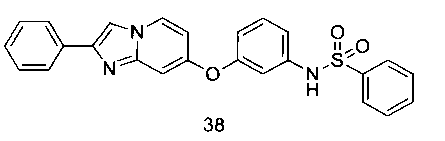
[00233]1Н ЯМР (400 МГц, ДМСО): δ 8,52 (д, J=7,2 Гц, 1Н), 8,33 (с, 1Н), 7,93 (д, J=7,2 Гц, 2Н), 7,76-7,70 (м, 2Н), 7,66-7,54 (м, 3Н), 7,43 (т, J=7,6 Гц, 2Н), 7,33-7,26 (м, 2Н), 6,92 (д, J=7,6 Гц, 1Н), 6,84-6,76 (м, 3Н), 6,64 (дд, J=7,6 Гц, 2,4 Гц, 1Н); МСВР, вычисленное значение для C25H20N3O3S [М+Н]+: 442,1225; полученное значение: 442,1216.
[00234] Пример 2: Биологический анализ
[00235] 2.1 Материалы и способы
[00236] 2.1.1 Реагенты и антитела
[00237] Сорафениб (Нексавар®) был любезно предоставлен Bayer Pharmaceuticals (Уэст-Хейвен, СТ). Ванадат натрия и ингибитор SHP-1 были приобретены у Cayman Chemical (Энн-Арбор, MI). Антитела для иммуноблоттинга, такие как антитела к Raf-1, циклину D1 и PARP, были приобретены у Santa Cruz Biotechnology (Сан-Диего, СА). Другие антитела, такие как антитела к pVEGFR2 (Y1175), VEGFR2, сурвивину, фосфо-STAT3 (Tyr705) и STAT3, были предоставлены Cell Signaling (Данверс, MA).
[00238] 2.1.2 Клеточная культура
[00239] Линию клеток ГКК Huh-7 получали из Банка ресурсов для исследований в области медицинских наук (Health Science Research Resources Bank) (Осака, Япония; JCRB0403). Линии клеток PLC/PRF/5 (PLC5), Sk-Hep-1 и Hep3B получали из Американской коллекции типовых культур (Манассас, VA). Клетки выдерживали в DMEM с добавлением 10% ЭТС, 100 единиц/мл пенициллина G, 100 мкг/мл стрептомицина сульфата и 25 мкг/мл амфотерицина В во влажной камере при 37°C в атмосфере, содержащей 5% CO2 в воздухе. Для анализов, описанных ниже, также обеспечивали наличие других линий клеток, включая клетки рака молочной железы, например MDAMB231, MDAMB468, MCF-7, и клетки лейкоза, например HL-60, KG-1 и ML-1.
[00240] 2.1.3 Детектирование гибели клеток посредством твердофазного ИФА
[00241] Влияние соединений согласно настоящему изобретению на жизнеспособность клеток оценивали посредством твердофазного ИФА гибели клеток (Roche Applied Science, Мангейм, Германия). Клетки обрабатывали испытываемым соединением, например в концентрации 5 и 10 мкМ в течение 24 ч. Клетки собирали и применяли согласно стандартному протоколу, предоставленному производителем.
[00242] 2.1.4 Анализ апоптоза
[00243] Апоптотические клетки измеряли посредством проточной цитометрии (sub-G1). После обработки различными соединениями клетки трипсинизировали, собирали посредством центрифугирования и ресуспендировали в ФСБ. После центрифугирования клетки промывали в ФСБ и ресуспендировали в окрашивающем растворе йодида калия (PI). Образцы инкубировали в темноте в течение 30 мин при 37°C, а затем анализировали с применением проточного цитометра EPICS Profile II (Coulter Corp., Хайалиа, FL). Все эксперименты проводили посредством трех параллельных испытаний.
[00244] 2.1.5 Уровень фосфо-STAT3
[00245] Для детектирования фосфо-STAT3 применяли набор PathScan Фосфо-Stat3 (Tyr705) Sandwich ELISA Kit (Cell Signaling, Данверс, MA). Клетки предварительно обрабатывали 1 нг/мл IL-6, а затем подвергали воздействию различных соединений в концентрации 10 мкМ в течение 24 ч. После инкубации с клеточными лизатами как нефосфорилированные, так и фосфо-STAT3 белки были захвачены посредством создания покрытия из антител. Экспрессию фосфо-STAT3 измеряли по поглощению при длине волны 450 нм.
[00246] 2.1.6 Вестерн-блот
[00247] Клетки обрабатывали различными соединениями в концентрации 5 и 10 мкМ в течение 24 ч. Клеточные лизаты анализировали посредством вестерн-блота.
[00248] 2.1.7 Нокдаун гена с применением миРНК
[00249] Весь пул миРНК smart-pool, включая контрольную миРНК (D-001810-10), Raf-1, SHP-1, SHP-2 и РТР-1 В, были приобретены у Dharmacon Inc. (Чикаго, IL). Технология была описана ранее (Chen KF и др. J Biol Chem 2009; 284:11121-11133).
[00250] 2.1.8 PLC5 с эктопической экспрессией STAT3
[00251] кДНК STAT3 (KIAA1524) и STAT3-C были приобретены у Addgene plasmid repository (http://www.addgene.org/). Вкратце, после трансфекции клетки инкубировали в присутствии G418 (0,78 мг/мл). После 8 недель селекции выжившие колонии, то есть колонии, образованные стабильно трансфицированными клетками, отбирали и по отдельности подвергали амплификации.
[00252] 2.1.9 Активность фосфатазы и киназы
[00253] Для анализа активности SHP-1 применяли набор RediPlate 96 EnzChek® Tyrosine Phosphatase Анализ Kit (R-22067) (Molecular Probes, Карлсбад, CA). Для исследования активности киназы Raf-1 применяли набор Raf-1 Kinase Cascade Анализ Kit (Upstate-Millipore, Биллерика, MA). Набор для анализа активности киназы JAK2 был приобретен у Reaction Biology Corp. (Малверн, PA).
[00254] 2.1.10 Репортерный анализ STAT3
[00255] Клетки высевали в 96-луночный планшет и предварительно обрабатывали IL-6 в дозе 10 нг/мкл в течение 30 мин. Набор для репотерного анализа STAT3 был приобретен у SABiosciences (Фредерик, MD).
[00256] 2.1.11 Рост ксенотрансплантатной опухоли
[00257] Самцы бестимусных «голых» мышей NCr (возрастом 5-7 недель) были получены из Национального центра лабораторных животных (National Laboratory Animal Center) (Тайбэй, Тайвань). Все процедуры экспериментов с применением указанных мышей осуществляли согласно протоколам, одобренным Национальным университетом Тайваня. Когда опухоли Huh-7 достигали 100-200 мм3, мыши получали сорафениба тозилат (10 мг/кг) п/о (перорально) один раз в сутки или SC-1 (10 мг/кг) п/о (перорально) один раз в сутки. Мыши контрольной группы получали плацебо (Chen KF et al. Cancer Res. 2008; 68:6698-6707).
[00258] 2.1.12 Статистический анализ
[00259] Сравнения средних значений осуществляли с применением критерия Стьюдента для независимых выборок в SPSS для Windows 11.5 (SPSS, Inc., Чикаго, IL) (Chen KF и др. Cancer Res 2008; 68:6698-6707).
[00260] 2.2 Результаты
[00261] 2.2.1 Соединение 1 не влияет на активность киназы Raf
[00262] Как описано выше, авторы настоящего изобретения синтезировали производное сорафениба, не обладающее способностью отдавать водород, посредством замены пиридинового кольца и амидной функциональной группы на фенилцианид. Затем авторы настоящего изобретения испытывали соединение 1 на способность ингибировать активность киназы Raf в клетках PLC5 по сравнению с аналогичной способностью сорафениба. Как представлено на Фиг. 3, сорафениб в концентрации 5 мкМ обладал способностью ингибировать 50% активности киназы Raf-1 необработанных клеток в клетках PLC5, однако клетки, обработанные соединением 1, демонстрировали такую же активность Raf-1, как и клетки, обработанные контрольным соединением, представлявшим собой плацебо. Потеря способности ингибировать Raf-1 предположительно может объясняться потерей способности образовывать водородную связь в результате замены пиридинового кольца и амидной функциональной группы на фенилцианид.
[00263] 2.2.2. Зависимость активности, проявлявшейся в гибели клеток, от структуры при замене мочевинной группы и пиридинового кольца
[00264] Как описано выше, авторы настоящего изобретения заменяли мочевинную группировку сорафениба на различные амиды и сульфонамиды с получением соединений 2-11. Указанные соединения анализировали посредством МТТ-анализа на ингибирование роста клеток PLC5. Результаты представлены в Таблице 4.
[00265]


[00266] Результаты показывают, что ни одно из указанных производных, относящихся к электронодонорной или электроноакцепторной группе, не оказывало большего токсического действия на клетки, чем сорафениб и соединение 1.
[00267] На следующем этапе авторы настоящего изобретения заменяли пиридин на хинолиновое кольцо и амидный мостик с получением соединений 12-25. Указанные соединения также анализировали посредством МТТ-анализа на ингибирование роста клеток PLC5. Результаты представлены в Таблице 5.
[00268]

[00269]

[00270]

[00271] Амидный мостик имел конформацию, отличную от конформации сульфонильного мостика, при этом соединения, содержащие амидный мостик, обнаруживали большую активность, чем соединения, содержащие сульфонильный мостик. Например, соединение 16 оказывало лучшее токсическое действие на клетки, чем соединение 12. Соединение 25 оказывало цитотоксическое действие, сравнимое с действием сорафениба и соединения 1. Авторы настоящего изобретения пришли к выводу, что соединения, содержащие мочевинный и амидный мостики, проявляли наиболее мощное токсическое действие на клетки PLC5.
[00272] 2.2.3. Механистическая валидация механизма действия производных сорафениба
[00273] Для проверки дефосфорилирования STAT3 производными сорафениба авторы настоящего изобретения оценивали уровень P-STAT3 в клетках PLC5, подвергнутых воздействию каждого соединения в концентрации 10 мкМ в течение 24 ч, посредством твердофазного ИФА. Как показано на Фиг. 4, соединения, содержащие сульфонильный мостик, не вызывали заметного изменения уровня P-STAT3, однако соединение 1 и некоторые соединения, содержащие амидный мостик, демонстрировали высокую степень дефосфорилирования STAT3. Пониженный уровень P-STAT3, вызванный указанными производными, коррелировал с токсическим действием на клетки. Другими словами, указанные производные вызывали гибель клеток частично посредством ингибирования STAT3.
[00274] Кроме того, авторы настоящего изобретения подвергали испытанию нисходящий сигнальный путь после ингибирования P-STAT3. Уровень экспрессии генов циклина D1 и сурвивина, представляющих собой гены-мишени нисходящего пути STAT3, оценивали с применением соединений 1 и 12. Как показано на Фиг. 5, соединение 1, обладающее ингибирующей активностью по отношению к STAT3, было способно понизить уровень циклина D1 и сурвивина, однако соединение 12 не оказывало влияния на оба белка. Далее были проведены фрагментация ДНК и проточный цитометрический анализ клеток PLC5, обработанных соединением 1, и результаты показывают, что гибель клеток была связана с ингибированием STAT3 и дополнительно индуцирована апоптотическим сигналом (Фиг. 6).
[00275] Предположение авторов настоящего изобретения о том, что ингибирование сорафенибом Raf и STAT3 может происходить при участии различных структурных фрагментов, было подтверждено посредством соединения 1, которое, не влияя на активность Raf, демонстрировало тот же уровень даун-регуляции P-STAT3, что и сорафениб. Авторы настоящего изобретения полагают, что цианидная группа соединения 1 ослабляет его взаимодействие с Raf. Последовательные преобразования сорафениба посредством замены мостика и пиридинового кольца на амид и хинолин (соединения 1, 16 и 25 соответственно) приводили к снижению активности при подавлении STAT3.
[00276] 2.2.4 SC-1, представляющее собой производное сорафениба, при отсутствии ингибирующего действия на Raf-1 демонстрировало летальный эффект по отношению к линиям клеток ГЦК, аналогичный эффекту сорафениба
[00277] В ходе указанного эксперимента авторы настоящего изобретения снова исследовали влияние сорафениба и SC-1 на активность Raf-1. Raf-1, иммунопреципитированную из экстрактов клеток PLC5 или Hep3B, инкубировали с рекомбинантным белком МЕК и анализировали содержание фосфо-МЕК в клетках, обработанных сорафенибом или SC-1. Авторы настоящего изобретения отмечали 20-40% снижение киназной активности Raf-1 в присутствии сорафениба, однако соединение SC-1 не ингибировало активность Raf-1, что свидетельствует о том, что SC-1 не является ингибитором Raf-1 (Фиг. 7А). Кроме того, авторы настоящего изобретения анализировали фосфорилирование VEGFR2, представляющего собой основную мишень сорафениба в ходе лечения рака. В клетках PLC5, обработанных сорафенибом, экспрессия p-VEGFR2 (Tyr1175) снижалась, тогда как соединение SC-1 не оказывало значительного эффекта (Фиг. 7В). Указанные данные позволяют предположить, что SC-1, полученное из сорафениба, не оказывает ингибирующего воздействия на киназу.
[00278] На следующем этапе авторы настоящего изобретения исследовали антипролиферативный эффект сорафениба и SC-1. Как SC-1, так и сорафениб понижали жизнеспособность различных клеток ГЦК, включая PLC5, SK-Hep1, Huh7 и Hep3B, в степени, зависящей от дозы (Фиг. 8А). Кроме того, клетки ГЦК, обработанные SC-1 или сорафенибом, демонстрировали значительное повышение численности в фазе sub-G1 после 24 ч воздействия (Фиг. 8В). Оба лекарственных средства индуцировали апоптотическую гибель значительного количества клеток, детектируемую посредством индукции фрагментации ДНК в клетках ГЦК, обработанных SC-1 или сорафенибом (Фиг. 8С). Указанные данные свидетельствуют о том, что SC-1 оказывает значительное влияние на апоптоз и является столь же активным в ингибировании роста клеток ГЦК, как и сорафениб, даже несмотря на то, что SC-1 не обладает способностью блокировать активность киназы, что приводит к выводу, что механизм, по которому сорафениб индуцирует апоптоз в ГЦК, может быть не связан с ингибированием активности киназы.
[00279] 2.2.5 STAT3 является жизненно важным при сенсибилизирующем эффекте сорафениба и SC-1 в линиях клеток ГЦК
[00280] Чтобы проверить, зависит ли даун-регуляция p-STAT3 от ингибирования киназы сорафенибом, авторы настоящего изобретения дополнительно анализировали STAT3-зависимый сигнальный путь в клетках ГЦК, обработанных SC-1. Учитывая тот факт, что STAT3 подвергался даун-регуляции сорафенибом, что приводило к индукции гибели клеток, исследовали молекулы, связанные с апоптозом, включая Мсl-1, циклин D1 и сурвивин. Авторы настоящего изобретения обнаружили, что подавление p-STAT3 играет роль в опосредовании SC-1-индуцированной или сорафениб-индуцированной гибели клеток. Соединение SC-1 снижало экспрессию STAT3-зависимых белков в клетках ГЦК. Фосфорилирование STAT3 по тирозину 705 имеет решающее значение для трансактивации STAT3. Соединение SC-1, как и сорафениб, подвергало даун-регуляции p-STAT3 по остатку Y705 и подавляло Mcl-1 и циклин D1 во всех испытываемых линиях клеток ГЦК, включая PLC5, Huh7 и Sk-Hep1 (Фиг. 9А). Примечательно, что весь белок STAT3 не подвергался действию сорафениба и SC-1 (Фиг. 9А). Более того, SC-1 и сорафениб подвергали даун-регуляции p-STAT3 в степени, зависящей от дозы и времени (Фиг. 9В). Указанные данные дополнительно указывают на то, что сорафениб ингибировал STAT3 по киназа-независимому механизму.
[00281] Авторы настоящего изобретения также анализировали состояние активации p-STAT3 посредством твердофазного ИФА STAT3. В течение двадцати четырех часов перед воздействием сорафениба или SC-1 клетки Sk-Hep1 предварительно обрабатывали рекомбинантным IL-6 для имитации высокого уровня экспрессии STAT3, а затем обрабатывали SC-1 или сорафенибом в течение еще 24 часов в присутствии IL-6. Экстракты клеток, обработанных SC-1 или сорафенибом, инкубировали с антителом против фосфорилированного STAT3 по Y705. Результаты твердофазного ИФА показали, что сорафениб, как и SC-1, значительно понижал активность p-STAT3 (Фиг. 9С, слева). Для оценки транскрипционной активности связывающий участок STAT3 клонировали в репортер Luc. Авторы настоящего изобретения обнаружили, что транскрипционная активность STAT3 значительно снижалась в присутствии сорафениба или SC-1 (Фиг. 9С, справа). Активность люциферазы светляков оценивали и подвергали нормализации посредством люциферазы Renilla. Указанные результаты показали, что как сорафениб, так и SC-1 сильно понижали уровень фосфорилирования STAT3 путем подавления транскрипции. Затем авторы настоящего изобретения создавали стабильный клон клеток ГЦК со сверхэкспрессированным STAT3 для проверки воздействия сорафениба на ГЦК. Как показано на Фигуре 9D, как сорафениб-индуцированный, так и SC-1-индуцированный апоптоз прекращался в клетках ГЦК со сверхэкспрессированным STAT3, о чем свидетельствует анализ sub-G1, что указывает на то, что STAT3 является основным медиатором сорафениб- и SC-1-индуцированного апоптоза.
[00282] 2.2.6 Фосфатаза SHP-1 играет роль в воздействии сорафениба и SC-1 на фосфо-STAT3 и апоптоз
[00283] Для дальнейшего изучения того, каким образом сорафениб ингибирует STAT3 в ГЦК, авторы настоящего изобретения исследовали несколько протеинфосфатаз, которые могли быть вовлечены в регуляцию p-STAT3. Результаты, полученные авторами настоящего изобретения, показали, что ванадат натрия, представляющий собой общий ингибитор фосфатаз, снижал апоптоз и повышал уровень p-STAT3 (Фиг. 10А, слева). Указанные данные свидетельствуют о том, что сорафениб и SC-1 могут воздействовать на p-STAT3 посредством таргетинга STAT3-зависимых протеинфосфатаз. Кроме того, авторы настоящего изобретения обнаружили, что фосфатаза-специфический ингибитор SHP-1 прекращал сорафениб-индуцированную гибель клеток и ингибирование p-STAT3 (Фиг. 10А, справа). Для дальнейшего установления роли SHP-1 в SC-1- и сорафениб-индуцированном ингибировании p-STAT3 авторы настоящего изобретения применяли миРНК, специфичную к SHP-1, для исследования воздействия сорафениба и SC-1. Авторы настоящего изобретения обнаружили, что выключение SHP-1 прекращало сорафениб- или SC-1-индуцированный апоптоз и ингибирование p-STAT3 (Фиг. 10В, слева). Кроме того, как сорафениб, так и SC-1 повышали активность SHP-1 до 3-кратной по сравнению с контрольными клетками (Р<0,05) (Фиг. 10 В, средняя диаграмма). Клетки PLC5, обработанные сорафенибом или SC-1, иммунопреципитировали антителом, специфичным к SHP-1, а затем SHP-1-содержащий комплекс подвергали анализу фосфогруппы, основанному на флуоресценции. Примечательно, что ни сорафениб, ни SC-1 не влияли на взаимодействие STAT3 и SHP-1, о чем свидетельствует иммунопреципитация SHP-1 (Фиг. 10В, справа). Указанные данные свидетельствуют о том, что сорафениб индуцировал гибель клеток путем SHP-1-зависимой инактивации STAT3.
[00284] В известных из уровня техники источников описано, что кроме SHP-1 p-STAT3 регулируют другие фосфатазы, такие как SHP-2 и РТР-1 В. Как показано на Фиг. 10С, воздействие сорафениба на апоптоз и p-STAT3 не прекращалось посредством выключения SHP-2 или РТР-1В, что свидетельствует о том, что ни SHP-2, ни РТР-1В не играли роли в опосредовании воздействия сорафениба или SC-1 на p-STAT3.
[00285] 2.2.7 SC-1 подвергает даун-регуляции p-STAT3 в клетках HUVEC и индуцирует апоптоз указанных клеток
[00286] Для выяснения того, какое воздействие оказывает сорафениб на p-VEGFR2, представляющий собой основную мишень сорафениба в ходе лечения рака, авторы настоящего изобретения исследовали действие сорафениба и SC-1 в клетках HUVEC. Как показано на Фиг. 11А слева как сорафениб, так и SC-1 подвергали даун-регуляции p-STAT3 в клетках HUVEC и индуцировали апоптотическую гибель значительного количества клеток ГЦК (Р<0,05). Примечательно, что сорафениб, но не SC-1, подвергал даун-регуляции фосфорилирование VEGFR в клетках HUVEC (Фиг. 7А, средняя). Указанные результаты показывают, что ни Raf-1, ни VEGFR не опосредуют воздействие сорафениба на апоптоз и p-STAT3.
[00287] Предварительное изучение также свидетельствует о том, что Mcl-1 имеет решающее значение в опосредовании воздействия сорафениба на сенсибилизацию к TRAIL. Интересно, что данные, полученные авторами настоящего изобретения, показали, что SC-1 также демонстрировало аналогичное усиление TRAIL-индуцированного апоптоза в ГЦК посредством даун-регуляции p-STAT3 (Фиг. 11B). Для дальнейшего исследования того, связано ли ингибирование p-STAT3 сорафенибом с Raf-1, авторы настоящего изобретения осуществляли нокдаун Raf-1 посредством применения малой интерферирующей РНК. Выключение Raf-1 не оказывало влияния на воздействие сорафениба или SC-1 на p-STAT3 (Фиг. 11С), что свидетельствует о том, что Raf-1 не опосредует воздействие сорафениба на p-STAT3. Примечательно, что ни сорафениб, ни SC-1 не изменяли активность киназы JAK2 (Фиг. 11D), что свидетельствует о том, что JAK2 не опосредует воздействия обоих соединений на p-STAT3. Кроме того, данные, полученные авторами настоящего изобретения, показали, что сорафениб и SC-1 не оказывали влияния на уровни белков SOCS-1 и SOCS-3 (Фиг. 11Е). Интересно, что клетки ГЦК с конститутивно активным STAT-3 (STAT3-C) не были полностью устойчивы к SC-1 (Фиг. 11F). Так как соединение SC-1 повышало активность SHP-1 (Фиг. 11В, средняя), данные, полученные авторами настоящего изобретения, свидетельствуют о том, что помимо STAT-3 другие SHP-1-зависимые молекулы также могут играть роль в опосредовании воздействия SC-1. Для исследования того, является ли SHP-1 непосредственной мишенью сорафениба или SC-1, клетки PLC5 иммунопреципитировали антителом к SHP-1, а затем инкубировали с сорафенибом или SC-1 в течение 6 часов. Как показано на Фиг. 11Г, сорафениб и SC-1 повышают активность SHP-1 в указанных лизатах, что свидетельствует о том, что сорафениб и SC-1 воздействуют непосредственно на SHP-1.
[00288] 2.2.8 Терапевтическая оценка воздействия SC-1 и сорафениба на мышей, являющихся носителями Huh7
[00289] Для проверки терапевтического эффекта SC-1 авторы настоящего изобретения также применяли SC-1 по отношению к ксенотрансплантатной ГЦК для оценки ценности указанного соединения in vivo. Сначала мыши, являвшиеся носителями Huh7, ежесуточно получали лечение, заключавшееся в пероральном введении плацебо или сорафениба в дозе 10 мг/кг/сутки. Лечение сорафенибом значительно ингибировало рост ксенотрансплантатных опухолей Huh7, и животные, подвергнутые лечению сорафенибом, имели опухоли размером менее половины размера опухолей мышей контрольной группы (Фиг. 12Д слева). У всех мышей не было заметной разницы в массе тела или заметных отличий в токсическом действии (данные не показаны). Кроме того, экстракты клеток опухолей мышей, подвергнутых лечению плацебо и сорафенибом, подвергали иммуноблоттингу для выявления p-STAT3. В опухоли, обработанной сорафенибом, p-STAT3 подвергался даун-регуляции (Фиг. 12A справа). p-STAT3/STAT3 обнаруживали в гомогенатах трех репрезентативных опухолей Huh7. Кроме того, авторы настоящего изобретения исследовали активность SHP-1 в ксенотрансплантатной опухоли Huh7, обработанной сорафенибом. Опухоль, обработанная сорафенибом, демонстрировала значительную индукцию активности SHP-1 in vivo (Фиг. 12A справа). В совокупности указанные результаты подтвердили, что сорафениб может повышать активность SHP-1 для подавления p-STAT3, вовлеченного в ингибирование опухоли, в ксенотрансплантатной модели ГЦК.
[00290] Кроме того, лечение с применением SC-1 производило сильный ингибирующий эффект (Р<0,05), и размер опухолей в указанной группе составлял только 25% от размера опухолей мышей, подвергнутых лечению плацебо, по завершении лечения (Фиг. 12В, слева). Также на образцах опухолей, взятых из животных, подвергнутых лечению SC-1, проводили анализ методом иммуноблота для выявления p-STAT3 и анализ активности SHP-1. Интересно, что SC-1 индуцировало значительное повышение активности SHP-1 и подвергало даун-регуляции p-STAT3 (Фиг. 12В, справа). Указанные данные свидетельствуют о том, что соединение SC-1, являющееся агонистом SHP-1 и ингибитором STAT3, обнаруживает терапевтический эффект при ингибировании роста опухоли.
[00291] 2.2.9 Ингибирование роста клеток злокачественных новообразований
[00292] Авторы настоящего изобретения также исследовали воздействие SC-1 и SC-43 в линиях клеток других злокачественных новообразований, включая линии клеток рака молочной железы, например MDAMB231, MDAMB468, MCF-7, и линии клеток лейкоза, например HL-60, KG-1 и ML-1. Результаты представлены на Фиг. 13. Указанные данные показывают, что соединения согласно настоящему изобретению являются эффективными при ингибировании роста клеток злокачественных новообразований
[00293] 2.2.10 Противораковый эффект в клетках ГЦК
[00294] Клетки ГЦК обрабатывали производными сорафениба (SC-43 или SC-40) в указанной дозе в течение 24 ч. Собранные клетки фиксировали в 75% этаноле и окрашивали 20 мкг/мл пропидий йодида (PI). Анализ sub-G1 осуществляли посредством проточной цитометрии. На Фиг. 14 показано, что SC-43 и SC-40, представляющие собой производные сорафениба, демонстрируют значительный противораковый эффект в клетках ГЦК; (А), (В), (С), (D) и (Е) относятся к SC-43 в случае PLC5, HepG2, Hep3B, НА59Т и SK-Hep1 клеток соответственно, a (F), (G), (Н), (I) и (J) относятся к SC-40 в случае PLC5, HepG2, Hep3B, НА59Т и SK-Hep1 клеток соответственно. Точки отражают среднее значение; планки погрешностей отражают SD (n=6).
[00295] 2.2.11 Воздействие сорафениба или SC-43 на STAT3-зависимые белки
[00296] Клетки ГЦК, обработанные SC-43 (10 мкМ в течение 24 ч), собирали с применением лизирующего буфера RIPA. Антитела для иммуноблоттинга, такие как антитела к циклину D1, приобретали у Santa Cruz Biotechnology. Другие антитела, такие как антитела к сурвивину, cpoccpo-STAT3 (Tyr705), STAT3, Mcl-1, SOCS1 и SOCS3, были предоставлены Cell Signaling. На Фиг. 15 показано, что SC-43 подвергает даун-регуляции фосфо-STAT3-зависимый сигнальный путь в ГЦК.
[00297] 2.2.12 Воздействие сорафениба или SC-40 на STAT3-зависимые белки
[00298] Клетки ГЦК, обработанные SC-40 (10 мкМ в течение 24 ч), собирали с применением лизирующего буфера RIPA. Антитела для иммуноблоттинга, такие как антитела к циклину D1, приобретали у Santa Cruz Biotechnology. Другие антитела, такие как антитела к сурвивину, фосфо-STAT3 (Tyr705), STAT3, Mcl-1, SOCS1 и SOCS3, были предоставлены Cell Signaling. На Фиг. 16 показано, что SC-40 подвергает даун-регуляции фосфо-STAT3-зависимый сигнальный путь в ГЦК.
[00299] 2.2.13 Воздействие сорафениба или SC-43 на STAT3-зависимые белки
[00300] Клетки ГЦК, обработанные SC-43 (10 мкМ в течение 24 ч), собирали с применением лизирующего буфера RIPA. Антитела для иммуноблоттинга, такие как антитела к циклину D1, приобретали у Santa Cruz Biotechnology. Другие антитела, такие как антитела к сурвивину, фосфо-STAT3 (Tyr705), STAT3 и Mcl-1, были предоставлены Cell Signaling. На Фиг. 17 показано, что SC-43 демонстрирует лучшее ингибирование p-STAT3-зависимого сигнального пути в ГЦК, а именно в PLC5 (А) и Hep3B (В), чем сорафениб. SC-43 демонстрирует значительное ингибирование p-STAT3-зависимых белков при введении в более низкой дозе, чем сорафениб.
[00301] 2.2.14 Влияние SC-43 и SC-40 на активность STAT3
[00302] Активность p-STAT3: клетки PLC5, обработанные производными SC, собирали в буфере RIPA и анализировали p-STAT3 с применением набора для твердофазного ИФА. Протокол анализа предоставлен производителем.
[00303] Репортерный анализ STAT3: клетки PLC5 высевали в 96-луночный планшет. Клетки предварительно трансфицировали с применением репортерной конструкции STAT3 в течение 24 ч и обрабатывали указанными производными в течение еще 24 ч. STAT3 Reporter Kit приобретали у SABiosciences.
[00304] Клетки обрабатывали SC-43 или SC-40 в концентрации 10 мкМ в течение 24 ч и измеряли фосфо-STATS посредством твердофазного ИФА или активность люциферазы. На Фиг. 18 показано, что как SC-43, так и SC-40 индуцируют сильное ингибирование активности p-STAT3, (А) и (В) относятся к твердофазному ИФА p-STAT3 для SC-43 и SC-40 соответственно, а (С) и (D) относятся к репортерному анализу STAT3 для SC-43 и SC-40 соответственно.
[00305] 2.2.15 Влияние SC-43/40 на фосфатазную активность
[00306] Белковый экстракт PLC5 инкубировали с антителом анти-SHP-1 в буфере для иммунопреципитации в течение ночи. Protein G Sepharose 4 Fast Flow (GE Healthcare Bio-Science) добавляли к каждому образцу с последующей инкубацией в течение 3 часов при 4°C при вращении. Указанный SHP-1-содержащий белковый экстракт далее инкубировали с SC соединениями (в концентрации 10 или 100 нмоль/л) в течение 30 мин при 4°C. Для анализа активности SHP-1 применяли набор RediPlate 96 EnzChek Tyrosine Phosphatase Анализ Kit (R-22067) (Molecular Probes). На Фиг. 19 показано, что производные SC, а именно SC-43 (A), SC-40 (В) и SC-49 (С), повышают фосфатазную активность SHP-1 in vitro.
[00307] 2.2.16 Влияние производных SC на фосфатазную активность рекомбинантной SHP-1
[00308] Для анализа активности SHP-1 применяли набор RediPlate 96 EnzChek Tyrosine Phosphatase Анализ Kit (R-22067) (Molecular Probes). Рекомбинантный белок SHP-1 (25 нг) инкубировали с SC-43 или SC-40 в указанной дозе в течение 30 минут, а затем анализировали фосфатазную активность SHP-1. На Фиг. 20 показано, что производные SC, а именно SC-43 (А) и SC-40 (В), повышают фосфатазную активность SHP-1 in vitro.
[00309] 2.2.17 In vivo воздействие SC-40 на PLCS-содержащий ксенотрансплантат
[00310] Самцов бестимусных «голых» мышей NCr (возрастом 5-7 недель) получали из Национального центра лабораторных животных (National Laboratory Animal Center) (Тайбэй, Тайвань). Все процедуры экспериментов с применением указанных мышей производили согласно протоколам, одобренным Институциональным комитетом по содержанию и использованию животных (Institutional Laboratory Animal Care and Use Committee) Национального университета Тайваня. Посредством инъекции в верхнюю боковую часть тела каждой мыши п/к инокулировали 1×106 клеток PLC5, суспендированных в 0,1 мл бессывороточной среды, содержащей 50% Matrigel (BD Biosciences). Когда опухоли достигали от 100 до 200 мм3, мыши принимали SC-40 тозилат (10 или 20 мг/кг) перорально один раз в сутки. Опухоли еженедельно измеряли с применением калиперов, и объемы указанных опухолей вычисляли с применением следующей стандартной формулы: ширина × длина × высота × 0,52.
[00311] На Фиг. 21 представлены (А) противоопухолевое воздействие SC-40 на клетки опухолей PLC5; точки отражают среднее значение (n=6); планки погрешностей отражают SE; (В) вестерн-блот анализ p-STAT3 и STAT3 в клетках опухолей PLC5; (С) масса тела животных; (D) масса опухолей и (Е) активность SHP-1 в клетках опухолей PLC5. Результаты показывают, что SC-40 оказывает значительное противоопухолевое воздействие на клетки опухолей PLC5, однако не влияет на массу тела животных. Между мышами контрольной группы и мышами, подвергнутыми лечению SC-40, не было значительной разницы в массе тела.
[00312] 2.2.18 Противоопухолевый эффект SC-43
[00313] В указанном примере авторы настоящего изобретения показывают, что SC-43 обнаруживает противоопухолевый эффект in vitro и in vivo. SC-43 демонстрирует значительную цитотоксичность в клетках ГЦК (IC50 составляет примерно 0,5 мкМ). Кроме того, SC-43 вызывает значительное ингибирование роста опухолей у мышей, являющихся носителями ГЦК. SHP-1/STAT3-зависимый сигнальный путь выступает в качестве важной цели противоопухолевого воздействия SC-43. См. Фиг. 22, на которой представлены (А) цитотоксичность SC-43 в клетках ГЦК, (В) противоопухолевое воздействие SC-43 на мышей, являющихся носителями ГЦК, (С) активность SHP-1, индуцированная SC-43, и (D) вестерн-блот анализ p-STAT3 и STAT3 в клетках ГЦК, обработанных SC-43 (10 мкМ и 20 мкМ).
[00314] 2.2.19 In vivo воздействие SC-43 на PLC5/luc ортотопической модели
[00315] Самцов бестимусных «голых» мышей NCr (возрастом 5-7 недель) получали из Национального центра лабораторных животных (National Laboratory Animal Center) (Тайбэй, Тайвань). Все процедуры экспериментов с применением указанных мышей производили согласно протоколам, одобренным Институциональным комитетом по содержанию и использованию животных (Institutional Laboratory Animal Care and Use Committee) Национального университета Тайваня. Посредством инъекции в верхнюю боковую часть тела каждой мыши инокулировали в печень 1×104 клеток PLC5/luc, суспендированных в 0,1 мл бессывороточной среды, содержащей 50% Matrigel (BD Biosciences). После образования опухолей мыши принимали сорафениб или SC-43 тозилат (10 мг/кг) перорально один раз в сутки. Мониторинг роста опухолей осуществляли посредством системы неинвазивной визуализации in vivo imaging system (IVIS) два раза в неделю.
[00316] SC-40 демонстрирует значительное противоопухолевое воздействие на мышей, являющихся носителями ортотопических опухолей, состоящих из клеток PLC5. Мониторинг роста опухолей осуществляли в указанный период времени посредством системы визуализации MS. Производили лечение мышей с применением плацебо, сорафениба (10 мг/кг) или SC-43 (10 мг/кг). На Фиг. 23 представлены (А) изображения мышей, подвергнутых лечению, (В) масса тела указанных мышей и (С) графики выживаемости мышей контрольной группы и мышей, подвергнутых лечению. Результаты показывают, что SC-40 демонстрирует значительное противоопухолевое воздействие на мышей, являющихся носителями ортотопических опухолей, состоящих из клеток PLC5. Между мышами контрольной группы и мышами, подвергнутыми лечению SC-43, не было значительной разницы в массе тела.
Реферат
Изобретение относится к новым соединениям формулы I, которые обладают агонистической активностью в отношении протеинтирозинфосфатазы-1, содержащей домен гомологии-2 Src (SHP-1). В формуле I Rи Rнезависимо представляют собой водород, и Rпредставляет собой,,,,илиRнезависимо представляет собой водород, Rпредставляет собой метил, и Rпредставляет собойилиили Rи Rнезависимо представляют собой водород, и Rпредставляет собой. Изобретение относится также к фармацевтическим композициям, содержащим указанное соединение, к способу повышения экспрессии в клетке протеинтирозинфосфатазы-1, содержащей домен гомологии-2 Src (SHP-1), способу лечения заболевания или патологического состояния, характеризующегося пониженной экспрессией SHP-1, и к применению указанного соединения для получения лекарственного средства для лечения заболевания или патологического состояния, характеризующегося пониженной экспрессией SHP-1. 7 н. и 4 з.п. ф-лы, 6 табл., 23 ил., 2 пр.
Формула

где R1 и R3 независимо представляют собой водород, и
R2 представляет собой






где R1 независимо представляет собой водород, R3 представляет собой метил, и R2 представляет собой

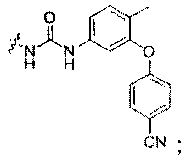
где R2 и R3 независимо представляют собой водород, и R1 представляет собой


Комментарии