Варианты плазминогена и плазмина - RU2604810C2
Код документа: RU2604810C2
Чертежи











































































Описание
Область изобретения
Настоящее изобретение относится к вариантам плазминогена и плазмина, содержащим одну или несколько точечных мутаций в каталитическом домене, которые снижают или предотвращают аутокаталитическую потерю протеазной активности плазмина. Также раскрыты композиции, применения и способы применения указанных вариантов плазминогена и плазмина.
Предпосылки изобретения
Активация зимогена плазминогена приводит к образованию фибринолитически/тромболитически активной сериновой протеиназы - плазмина. Активация эндогенного плазминогена может быть запущена или усилена введением активатора плазминогена, такого как урокиназа, стрептокиназа, стафилокиназа или tPA или любого их варианта. При активации белок плазминоген протеолитически расщепляется до тяжелой цепи, содержащей 5 доменов типа “двойная петля”, и легкой цепи, содержащей каталитический домен. Обе цепи скрепляются вместе посредством 2 дисульфидных связей. После активации в результате аутолитического расщепления удаляется N-концевой сегмент из тяжелой цепи (78 аминокислот плазмина человека; 77 аминокислот бычьего плазмина), и тяжелая цепь бычьего плазмина может быть дополнительно аутокаталитически расщеплена между доменами типа “двойная петля” 3 и 4, таким образом давая в результате бычий мидиплазмин (Christensen et al. 1995, Biochem J 305, 97-102). Активация плазминогена до плазмина, запущенная с помощью расщепления R561-V562 пептидной связи в плазминогене человека, вызывает большое конформационное изменение в легкой цепи, где указанное изменение приводит к стимуляции, или активации, каталитической триады внутри указанной легкой цепи. Бактериальные активаторы плазминогена, такие как стрептокиназа и стафилокиназа, формируют комплекс с плазминогеном, и без расщепления пептидной связи R561-V562 плазминогена каталитический сайт плазминогена активируется посредством конформационных изменений при образовании комплекса активатор-плазминоген (механизмы активации плазминогена подытожены, например, в разделе Введение Terzyan et al. 2004; Proteins 56: 277-284).
Поскольку активаторы плазминогена действуют как непрямые тромболитические средства, то альтернативно было предложено применение плазмина самого по себе в качестве непосредственного фибринолитического/тромболитического средства. Такое непосредственное применение, однако, затрудняется из-за того факта, что плазмин, подобно многим протеазам, подвергается аутокаталитическому протеолитическому распаду, который подчиняется кинетике второго порядка в отношении ингибирования продукта (Jespersen et al. 1986, Thrombosis Research 41, 395-404).
В начале 1960-х было установлено, что плазмин может быть стабилизирован в кислом pH или, альтернативно, в нейтральном pH при условии присутствия такой аминокислоты, как лизин. Тем не менее, сообщалось, что имело место аутолитическое расщепление после Lys104, Arg189 и Lys622 (нумерация относительно Lys-плазмина) даже если плазмин хранили при pH 3,8 (WO 01/36608). При хранении плазмина при еще более низком pH, равном 2,2, не-аутолитическое кислотное расщепление происходит между Asp-Pro (D-P) в положениях Asp62, Asp154 и Asp346 (WO 01/36608). Это иллюстрирует, что pH может быть понижен до точки, где больше не возникает очевидный аутокаталитический распад, но в которой фактором дестабилизации становится кислотный гидролиз. Отсутствует информация в WO 01/36608 в отношении того, что пептидные связи в плазмине являются чувствительными к (аутокаталитическому) гидролизу при нейтральном pH. Известные стабилизаторы плазмина включают глицерин, достаточно высокую ионную силу, фибриноген и ε-аминокапроновую кислоту (EACA), как раскрывается Jespersen et al. (1986, Thromb Res 41, 395-404). Лизин и лизиновые производные (такие как EACA и транексамовая кислота) и p-аминометилбензойная кислота (PAMBA) являются некоторыми дополнительными известными стабилизаторами (Uehsima et al. 1996, Clin Chim Acta 245, 7-18; Verstraete 1985, Drugs 29, 236-261). В патенте США №4462980 сообщалось об образовании плазминовых агрегатов, которые вносили свой вклад в распад плазмина, несмотря на хранение в кислотных условиях. Решение этой проблемы было представлено в патенте США №4462980 посредством добавления полигидроксидного соединения. Другие способы стабилизации плазмина включают добавление олигопептидных соединений (например, патент США №5879923). Альтернативно, каталитический сайт плазмина может быть обратимо блокирован посредством дериватизации, например, ацилирования (европейский патент № EP 0009879). В качестве способа стабилизации фермента также было предложено пегилирование плазмина (WO 93/15189).
Описан ряд вариантов плазмина, отличных от процессированных форм плазмина, и он включает химерный микроплазмин (WO 2004/045558) и варианты с точечной мутацией в сайте расщепления двух цепей (патент США №5087572) или в аминокислоте каталитической триады (Mhashilkar et al. 1993, Proc Natl Acad Sci USA 90, 5374-5377; Wang et al., 2001, J Mol Biol 295, 903-914). Wang et al. (1995, Protein Science 4, 1758-1767 and 1768-1779) сообщали о широком ряде мутантов микроплазминогена по аминокислотным положениям 545, 548, 550, 555, 556, 558, 560-564, 585, 740 и 788. Двойной мутант, где серин в аминокислотных положениях 558 и 566 были заменены на цистеины, описан Linde et al. (1998, Eur J Biochem 251, 472-479). Takeda-Shitaka et al. (1999, Chem Pharm Bull 47, 322-328) приводят вариант плазмина с уменьшенной активностью, где изменение включает замену аланина в аминокислотном положении 601 на треонин. Все приведенные выше аминокислотные положения считают относительно Glu-плазминогена, начиная с Glu в аминокислотном положении 1. Нерасщепляемый вариант плазминогена (расщепление между тяжелой и легкой цепью нарушено) описан в WO 91/08297. Dawson et al. (1994, Biochemistry 33, 12042-12047) описывают уменьшенную аффинность в отношении стрептокиназы у варианта Glu-плазминогена с Glu вместо Arg в положении 719 (R719E). Jespers et al. (1998, Biochemistry 37, 6380-6386) получили при сканировании по Ala ряд полученных с помощью фагового дисплея моносайтовых мутантов микроплазминогена H569A, R610A, K615A, D660A, Y672A, R712A, R719A, T782A, R789A, и обнаружили, что аргинин в положении 719 является ключевым для взаимодействия со стафилокиназой; мутант D660A не был дополнительно охарактеризован из-за очень низкой экспрессии; только мутант R719A был дополнительно получен в растворимой форме. Ни у одного из мутантов не наблюдали существенного изменения протеолитической активности (субстрат S-2403). Jespers et al. (1998) также включили в свой анализ мутанта с активным сайтом S741A; кристаллическая структура этого мутанта раскрыта в Wang et al. (2000, J Mol Biol 295, 903-914). В дальнейших попытках обнаружить сайты взаимодействия стрептокиназа/плазминоген, Terzyan et al. (2004, Proteins 56, 277-284) сообщали о ряде мутантов микроплазминогена (K698M, D740N, S741A) в уже мутированном окружении (R561A), причем последний подавлял протеолитическую активацию плазминогена и, таким образом, подавлял образование активного микроплазмина (что будет затруднять изучение механизма контакта-активации комплекса стрептокиназа-микроплазминоген). Terzyan et al. (2004) дополнительно упоминают “произвольного” тройного мутанта R561A/H569Y/K698M, очевидно функционально не отличающегося от двойного мутанта R561A/K698M. Wang et al. (2000, Eur J Biochem 267, 3994-4001) при изучении взаимодействия стрептокиназы/плазмина (плазминогена) получили набор мутантов микроплазминогена (аминокислоты 530-791 Glu-плазминогена) в Cys536Ala и Cys541Ser окружении. Эти мутанты включают мутацию R561A, которая описана выше (Terzyan et al. (2004)), а также двойные мутации R561A/K698G, R561A/K698A и R561A/K698Q. В такое же C536A/C541S окружение также были введены отдельные мутации K698G и K698A, из которых K698G не была в дальнейшем охарактеризована из-за трудностей с очисткой. Описанные выше исследования были направлены на достижение лучшего понимания характеристик молекулы плазминогена/плазмина и не сообщали о какой-либо клинической пользе, или благоприятном эффекте, или предполагаемых клинических преимуществах мутантов плазминогена/плазмина. Peisach et al. (1999, Biochemistry 38, 11180-11188) добились успеха в определении кристаллической структуры микроплазминогена, содержащего мутации M585Q, V673M и M788L.
Nguyen и Chrambach (1981, Preparative Biochem 11, 159-172) сообщили о присутствии “минорного и неидентифицированного белкового компонента” размером 10,0 кДа, исходя из результатов SDS-PAGE в восстанавливающих условиях сырого коммерческого препарата активируемого урокиназой плазмина (Homolysin). Отличия в аутолизе плазмина человека в зависимости от pH были описаны детально Shi и Wu (1988, Thrombosis Research 51, 355-364). Ohyama et al. (2004, Eur J Biochem 271, 809-820) предложили применение нелизиновых аналоговых модуляторов плазминогена при лечении рака благодаря усилению аутопротеолиза плазмина такими соединениями, которые приводят к усиленному образованию ангиостатинов (в присутствии активатора плазминогена - урокиназы). В таблице 3 в Ohyama et al. (2004) приведены по меньшей мере 15 сайтов расщепления в плазмине, подвергнутом действию усиливающих аутопротеолиз соединений. При обсуждении результатов их наблюдений в свете ранее проведенных исследований можно предположить, что усиливающие аутопротеолиз соединения являются более или менее избирательно усиливающими протеолиз B/легкой цепи, поскольку при отсутствии усиливающих аутопротеолиз соединений был обнаружен минимальный распад как A/тяжелой, так и B/легкой цепи.
Ясно, что ни один из описанных выше способов/вариантов не решал проблему получения плазмина, стабилизированного на молекулярном уровне. Получение варианта плазмина (или соответствующего варианта плазминогена, из которого может быть получен плазмин) с каталитическим доменом, по сути являющимся устойчивым к аутокаталитическому распаду, будет значительным шагом вперед по направлению к эффективному и безопасному длительному хранению, а также по направлению к эффективному и безопасному терапевтическому применению плазмина, например при тромболитической терапии или при индукции заднего отслоения стекловидного тела или разжижения стекловидного тела глаза.
Краткое описание изобретения
Настоящее изобретение относится к выделенным вариантам плазминогена или вариантам плазмина, получаемым из них, или к выделенным вариантам плазмина, или протеолитически активным или обратимо неактивным производным любого из указанных вариантов плазминов, где указанные варианты содержат сайт активации и каталитический домен, отличающийся тем, что указанный каталитический домен содержит мутацию одной или нескольких аминокислот в положениях 1-4 каталитического домена плазмина человека или в положениях, соответствующих таковым в каталитическом домене плазмина, отличном от плазмина человека, где указанный каталитический домен плазмина человека начинается с аминокислоты валин в положении 1, которая является той же аминокислотой валин, которая находится в положении 562 Glu-плазминогена человека. Более конкретно, если указанный каталитический домен мутирован в положении 1, то (i) аминокислота в положении -1 по отношению к каталитическому домену плазмина представляет собой аргинин, лизин или другую аминокислоту, которая поддерживает функциональность сайта активации, (ii) аминокислота в положении 24 каталитического домена плазмина человека, или в соответствующем положении каталитического домена плазмина, отличного от плазмина человека, представляет собой метионин, и (iii) аминокислота в положении 1 мутирована в аминокислоту, отличную от глицина или пролина. Альтернативно, если указанный каталитический домен мутирован в положениях 1 и 2, то аминокислота в положении 24 каталитического домена плазмина человека или в соответствующем положении каталитического домена плазмина, отличного от плазмина человека, представляет собой метионин.
Мутация или мутации в вариантах плазминогена, вариантах плазмина или производных плазмина согласно настоящему изобретению уменьшают степень аутопротеолитического распада указанного варианта плазмина по сравнению со степенью аутопротеолитического распада плазмина дикого типа, которая, например, определена с помощью хромогенного анализа или анализа биологической активности к субстрату.
Вариантами плазминогена, вариантами плазмина или производными плазмина согласно настоящему изобретению могут быть следующие: Glu-плазминоген или Glu-плазмин, Lys-плазминоген или Lys-плазмин, мидиплазминоген или мидиплазмин, миниплазминоген или миниплазмин, микроплазминоген или микроплазмин, дельтаплазминоген или дельтаплазмин.
Варианты плазминогена, варианты плазмина или производные плазмина согласно настоящему изобретению представляют особый интерес для применения в качестве лекарственного препарата и необязательно могут быть включены и/или объединены в композиции, дополнительно содержащей по меньшей мере фармацевтически приемлемый разбавитель, носитель или вспомогательное средство. Такие композиции могут дополнительно содержать одно или несколько из антикоагулянта, тромболитического средства, противовоспалительного средства, противовирусного средства, антибактериального средства, противогрибкового средства, антиангиогенного средства, антимитотического средства, антигистамина или анестетика.
Настоящее изобретение дополнительно относится к способам скрининга в отношении аутопротеолитически стабильных вариантов плазмина, причем указанные способы включают:
(i) получение варианта плазмина согласно настоящему изобретению и получение плазмина дикого типа,
(ii) сравнение аутопротеолитической стабильности вариантного плазмина и плазмина дикого типа, полученных на этапе (i), и
(iii) отбор по результатам этапа (ii) варианта, который сохраняет протеолитическую активность, и у которого аутопротеолитическая стабильность повышена по сравнению с аутопротеолитической стабильностью плазмина дикого типа.
Настоящее изобретение дополнительно относится к способам получения варианта плазминогена согласно настоящему изобретению, при этом указанные способы включают следующие этапы:
(i) введение нуклеиновой кислоты, кодирующей плазминоген согласно настоящему изобретению, в подходящую клетку-хозяина, способную экспрессировать указанный плазминоген;
(ii) выращивание клетки-хозяина, полученной на этапе (i), в условиях и в течение времени, достаточных для экспрессии указанного плазминогена в указанной клетке-хозяине; и
(iii) сбор плазминогена, экспрессированного на этапе (ii).
Настоящее изобретение дополнительно относится к способам получения варианта плазмина согласно настоящему изобретению, при этом указанные способы включают следующие этапы:
(i) введение нуклеиновой кислоты, кодирующей плазминоген согласно настоящему изобретению, в подходящую клетку-хозяина, способную экспрессировать указанный плазминоген;
(ii) выращивание клетки-хозяина, полученной на этапе (i), в условиях и в течение времени, достаточных для экспрессии указанного плазминогена в указанной клетке-хозяине;
(iii) сбор плазминогена, экспрессированного на этапе (ii).
(iv) активация плазминогена из этапа (iii) до плазмина.
Настоящее изобретение также относится к выделенным последовательностям нуклеиновых кислот, кодирующим вариант плазминогена или вариант плазмина согласно настоящему изобретению, а также к рекомбинантному вектору, содержащему такую нуклеиновую кислоту. Клетки-хозяева, трансформированные вышеуказанной нуклеиновой кислотой или вектором, аналогично являются частью настоящего изобретения.
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ НА ФИГУРАХ
ФИГУРА 1. Аминокислотная последовательность с двойной нумерацией аминокислотных положений Glu-плазминогена дикого типа человека (1-791) и каталитического домена плазмина (1-230, аминокислотная последовательность и нумерация выделены жирным шрифтом). Микроплазминоген, используемый для демонстрации настоящего изобретения, начинается в положении аминокислоты 543 (нумерация относительно Glu-плазминогена). Домены типа “двойная петля” (полученные из информации, включенной в GenBank по номером доступа AAA36451) заключены в рамки и их аминокислотные последовательности напечатаны с заменой букв нормального шрифта на курсив. Аминокислоты каталитической триады обведены кружком.
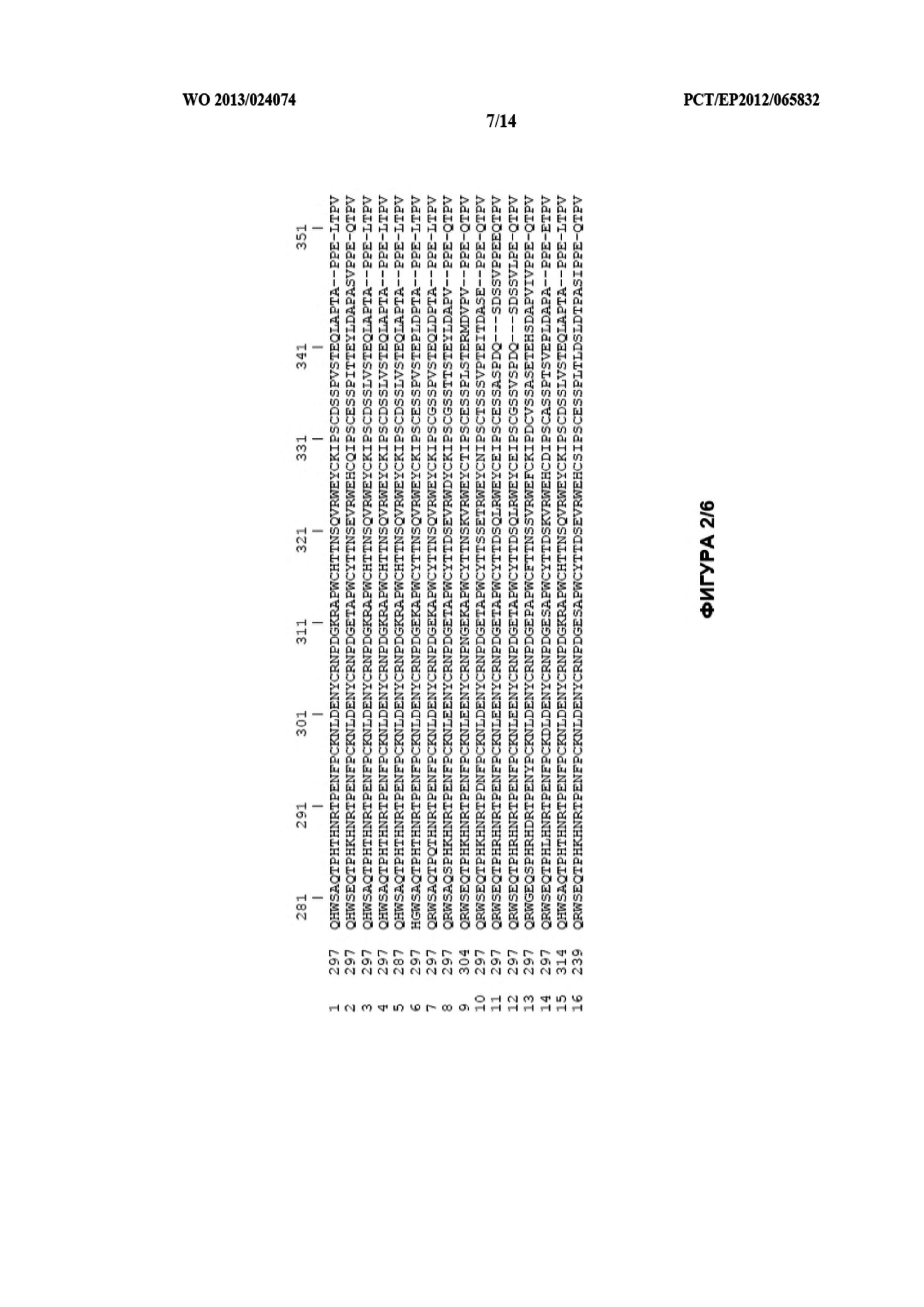
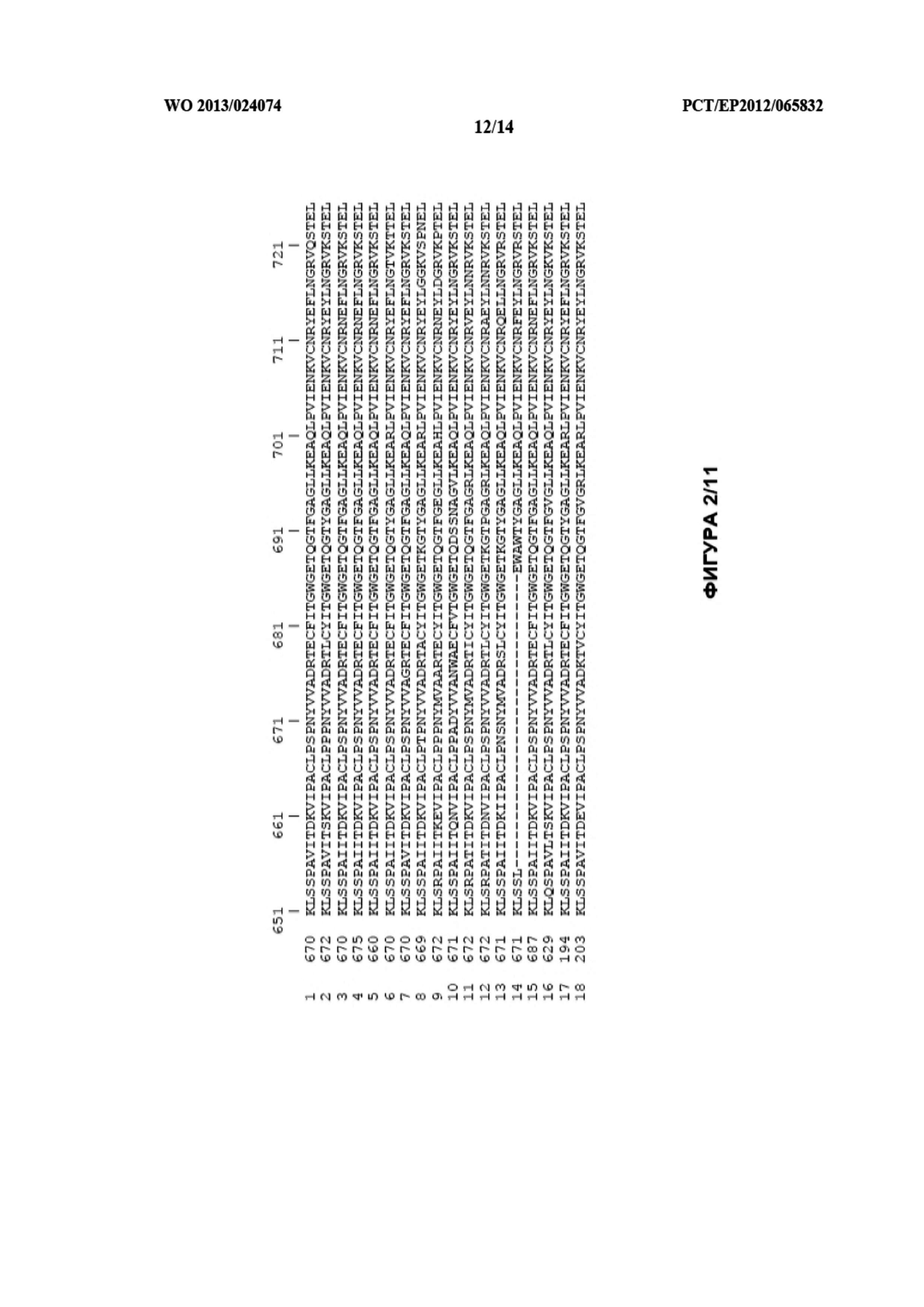
ФИГУРА 2. Выравнивание аминокислотной последовательности белков плазминогена млекопитающих, полученных из GenBank. Выравнивание последовательностей проводили с помощью программного обеспечения COBALT (Constraint-based Multiple Alignment Tool; Papadopoulos & Agarwala, Bioinformatics 23:1073-79, 2007 доступного с сайта Национального центра биотехнологической информации (NCBI), с установками по умолчанию. ▼: обозначение начала Glu-плазминогена. Аминокислотная нумерация дана по отношению к плазминогену человека.
ФИГУРА 3. Изображение (x 10) заднего отслоения стекловидного тела, индуцированного через 5 дней после инъекции 30 нг варианта микроплазмина Val1Ile.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение основано на результатах исследований влияния точечных мутаций в молекуле плазмина и, более конкретно, в каталитическом домене молекулы плазмина на аутопротеолиз. Пептидные связи, подверженные расщеплению плазмином, расположены на C-конце лизина или аргинина (Weinstein and Doolittle, 1972, Biochim Biophys Acta 258, 577-590). Приблизительно 10% (22 из 230) аминокислот каталитического домена плазмина (начиная с аминокислотного положения 562, валин, в Glu-плазминогене человека) представляют собой лизины или аргинины. Теоретически, все пептидные связи, С-концевые для этих лизинов и аргининов, независимо от структуры аминокислоты, С-концевой по отношению к указанному лизину или аргинину, в одной молекуле плазмина могут протеолитически расщепляться другой молекулой плазмина. Кроме того, теоретически, мутация любого одного или нескольких из этих лизинов или аргининов в аминокислоту, не являющуюся ни лизином, ни аргинином, может сделать молекулу плазмина более устойчивой к аутопротеолитическому распаду. Было доказано, что данная теория верна, как описано в международной патентной заявке № WO 2011/004011. Основанием для настоящего изобретения является неожиданное наблюдение, что мутация аминокислоты дикого типа, расположенной на N-конце каталитического домена, т.е. аминокислота в положениях 1-4 каталитического домена, в аминокислоту, отличную от аминокислоты дикого типа, значительно повышает устойчивость полученного мутантного плазмина к аутопротеолитическому распаду в сочетании с сохранением протеолитической способности мутантным плазмином.
Настоящее изобретение относится к выделенным вариантам плазминогена или вариантам плазмина, получаемым из них, или к выделенным вариантам плазмина, или протеолитически активным или обратимо неактивным производным любого из указанных вариантов плазминов, где указанные варианты содержат сайт активации и каталитический домен, отличающийся тем, что указанный каталитический домен содержит мутацию одной или нескольких аминокислот в положениях 1-4 каталитического домена плазмина человека или в положениях, соответствующих таковым в каталитическом домене плазмина, отличном от плазмина человека, где указанный каталитический домен плазмина человека начинается с аминокислоты валин в положении 1, которая является той же аминокислотой валин, которая находится в положении 562 Glu-плазминогена человека. Более конкретно, если указанный каталитический домен мутирован в положении 1, то (i) аминокислота в положении -1 по отношению к каталитическому домену плазмина представляет собой аргинин, лизин или другую аминокислоту, которая поддерживает функциональность сайта активации, (ii) аминокислота в положении 24 каталитического домена плазмина человека, или в соответствующем положении каталитического домена плазмина, отличного от плазмина человека, представляет собой метионин, и (iii) аминокислота в положении 1 мутирована в аминокислоту, отличную от глицина или пролина. Альтернативно, если указанный каталитический домен мутирован в положениях 1 и 2, то аминокислота в положении 24 каталитического домена плазмина человека или в соответствующем положении каталитического домена плазмина, отличного от плазмина человека, представляет собой метионин. В частности, вышеуказанный вариант плазминогена, вариант плазмина или производное плазмина содержат мутацию аминокислоты валин в положении 1 каталитического домена в изолейцин.
Мутация или мутации в вариантах плазминогена, вариантах плазмина или производных плазмина согласно настоящему изобретению уменьшают степень аутопротеолитического распада указанного варианта плазмина по сравнению со степенью аутопротеолитического распада плазмина дикого типа, которая, например, определена с помощью хромогенного анализа или анализа биологической активности к субстрату.
Мутации, отличные от описанной или описанных выше, могут также присутствовать в каталитическом домене плазмина, как проиллюстрировано в разделе Примеры.
Вариантами плазминогена, вариантами плазмина или производными плазмина согласно настоящему изобретению могут быть следующие: Glu-плазминоген или Glu-плазмин, Lys-плазминоген или Lys-плазмин, мидиплазминоген или мидиплазмин, миниплазминоген или миниплазмин, микроплазминоген или микроплазмин, дельтаплазминоген или дельтаплазмин.
Мутацию аминокислоты в заданном положении в "аминокислоту, отличную от аминокислоты дикого типа" или в "аминокислоту, отличную от природной аминокислоты" рассматривают как изменение аминокислоты в указанном заданном положении плазминогена или плазмина дикого типа в любую аминокислоту, отличную от природной аминокислоты или аминокислоты дикого типа, в таком указанном заданном положении такого указанного плазминогена или плазмина дикого типа. Некоторые аспекты, касающиеся выбора мутаций, приведены далее.
Специалист в данной области сможет легко решить, в какую другую аминокислоту можно мутировать аминокислоту дикого типа. Такое решение может, но не обязательно должно, следовать критериям, таким как размер аминокислоты, заряд аминокислоты, полярность аминокислоты и/или индекс гидрофобности аминокислоты (смотри Таблицу 1). Более того, наличие кристаллической структуры плазминогена и микроплазмина (MMDB ID: 12717; PDB ID: 1DDJ; Wang et al., 2001, J Mol Biol 295, 903-914) значительно помогает определению мутантных аминокислот так, чтобы полученная мутантная молекула плазмина или плазминогена сохраняла протеолитическую активность. Кроме того, можно ожидать, что мутация аминокислоты дикого типа в заданном положении [P+/-n] и необязательно дополнительно в одном или нескольких из заданных положений P, P′, P′′ и т. д. в любую из аминокислот данной группы будет давать похожие результаты. На основе Таблицы 1, указанные данные группы могут быть обозначены следующим образом:
- гидрофобные алифатические аминокислоты: Met, Ile, Leu и Val
- гидрофобные ароматические аминокислоты: Phe
- гидрофильные кислые аминокислоты: Asp, Glu, Asn и Gln
- гидрофильные основные аминокислоты: Arg, Lys и His
- умеренно гидрофобные алифатические аминокислоты: Gly, Ala, Ser, Thr, Cys, Pro
- умеренно гидрофобные ароматические аминокислоты: Tyr и Trp.
Из них, и с целью мутации, Cys и Pro могут быть менее предпочтительными аминокислотами-заменителями аминокислот дикого типа плазмина или плазминогена из-за создания возможной свободной тиольной группы с помощью Cys или из-за более обширного нарушения белковой структуры с помощью Pro. Другие аминокислотные замены включают мутацию аминокислоты дикого типа в положении [P+/-n] и необязательно дополнительно в одном или нескольких положениях P, P', P” и т.д. каталитического домена плазмина (плазминогена) в неприродную или неканоническую аминокислоту или в аналоги аминокислот, такие как норлейцин, норвалин, орнитин или цитруллин (для более обширного списка, смотри, например, Hendrickson et al. 2004, Annu Rev Biochem 73, 147-176).
Таблица 1. Характеристики аминокислот.
Определение аминокислоты в последовательности плазмина (плазминогена), отличного от плазмина (плазминогена) человека, которая “соответствует” (т. е. определение “соответствующей” аминокислоты) аминокислоте в плазмине (плазминогене) человека, в первую очередь подразумевает выравнивание обеих аминокислотных последовательностей. Такое выравнивание может требовать некоторой оптимизации, такой как введение минорных гэпов в одну или обе выравниваемые последовательности, для получения наивысшей идентичности и гомологии. Во-вторых, аминокислота в плазмине (плазминогене), отличном от плазмина (плазминогена) человека, выравнивающаяся с аминокислотой в плазмине (плазминогене) человека, определяется и называется в данном документе как “соответствующая” аминокислота. На фигуре 2 в данном документе изображено такое выравнивание общедоступных последовательностей белка плазминогена млекопитающих и выделены аминокислоты, представляющие особый интерес для настоящего изобретения, в последовательности плазминогена человека (строка 1) вместе с соответствующими аминокислотами в последовательностях плазминогена, отличного от плазминогена человека (строки 2-18). Представляющими особый интерес аминокислотами Р, Р′ и т. д. являются Lys в положении 698 (положение 137 в каталитическом домене, смотри Фигуру 1), Lys в положении 708 (положение 147 в каталитическом домене, смотри Фигуру 1) и Arg в положении 719 (положение 158 в каталитическом домене, смотри Фигуру 1).
“Плазмин”, также известный как фибринолизин или лизофибрин, представляет собой протеазу серинового типа, которая является результатом активации зимогена плазминогена. Активация является результатом протеолитического расщепления между аминокислотами 561 и 562 (нумерация относительно Glu-плазминогена человека). Плазмин несет тяжелую цепь, содержащую 5 доменов типа “двойная петля”, и легкую цепь, содержащую каталитический домен. Плазминоген может быть получен из плазмы крови, например, посредством аффинной к лизину хроматографии (Deutsch and Mertz, 1970, Science 170, 1095-1096). Процессинг молекулы плазмина (снаружи и/или внутри каталитического домена плазмина) возможен при условии, что каталитический домен остается функциональным, такой процессинг, таким образом, приводит к образованию “протеолитически активного производного” плазмина. В связи с этим, один или несколько из 5 доменов типа “двойная петля” могут быть удалены полностью или частично. Процессированные плазмины, в которых не достает одного или нескольких доменов типа “двойная петля” и/или не достает частей одного или нескольких доменов типа “двойная петля”, следовательно, рассматриваются согласно настоящему изобретению как примеры протеолитически активных производных плазмина. Примеры процессированных вариантов плазмина включают, но без ограничений, следующее: “мидиплазмин”, “миниплазмин”, “микроплазмин” и “дельта-плазмин”. Мидиплазмин, в основном, не содержит домены типа “двойная петля” 1-3 (например, Christensen et al., 1995, Biochem J 305, 97-102). Миниплазмин изначально получали путем ограниченного расщепления плазмина эластазой, и он, в основном, не содержит домены типа “двойная петля” 1-4 (например, Christensen et al., 1979, Biochim Biophys Acta 567, 472-481; Powell and Castellino, 1980, J Biol Chem 255, 5329). Миниплазмин был впоследствии получен рекомбинантно (WO 2002/050290). Микроплазмин изначально был получен путем инкубации плазмина при повышенном pH, и он, в основном, не содержит все домены типа “двойная петля” (например, WO 89/01336). Тогда как микроплазмин, полученный в результате инкубации плазмина при повышенном pH, содержит 30-31 карбокси-концевых аминокислот тяжелой цепи, рекомбинантно полученный вариант микроплазмина содержит 19 карбокси-концевых аминокислот тяжелой цепи (WO 2002/050290). Это иллюстрирует допустимую молекулярную изменчивость в данном семействе плазминов, таком как семейство микроплазминов (например, множество видов образуют семейство микроплазминов). Дельта-плазмин представляет собой рекомбинантную версию плазмина, в котором домен типа “двойная петля” 1 связан непосредственно с каталитическим доменом (WO 2005/105990). Вышеописанные процессированные варианты плазмина получают путем активации “мидиплазминогена”, “миниплазминогена”, “микроплазминогена” и “дельтаплазминогена”, соответственно. Для того чтобы быть активируемым, процессированный плазминоген должен содержать минимальное количество аминокислот линкера между доменом типа “двойная петля” (таким как домен типа “двойная петля” 5 у миниплазмина) и каталитическим доменом или С-концом каталитического домена в случае плазмина с удаленным в результате процессинга доменом типа “двойная петля” (смотри, например, Wang et al., 1995, Protein Science 4, 1758-1767). В контексте настоящего изобретения может быть необходимо, чтобы плазминоген содержал “интактный сайт активации”, который предполагает, что по меньшей мере аминокислоты 561 и 562 (относительно Glu-плазминогена человека; или соответствующие аминокислоты в плазминогене, отличном от плазминогена человека) являются такими, чтобы могла проходить активация/превращение плазминогена в плазмин, хотя возможно с различной кинетикой, как это происходит в плазмине дикого типа. В качестве альтернативы плазмину или его активному процессированному варианту в контексте настоящего изобретения можно использовать активируемый плазминоген или его процессированный вариант (смотри, например, EP 0480906; US 5304383; EP 0631786; US 5520912; US 5597800; US 5776452). “Плазминоген” относится к любой форме плазминогена, например, Glu-плазминогену или Lys-плазминогену (начинающихся с Arg в положении 68 или Lys в положениях 77 или 78). При использовании активируемого плазминогена или его активируемого процессированного варианта, активация до плазмина может быть отсрочена и будет, как правило, происходить после его контакта с органом, тканью или жидкостью организма, т.е. после введения субъекту. В еще одной альтернативе плазмином или его активным процессированным вариантом в контексте настоящего изобретения можно заменить активируемый плазминоген или его активируемый процессированный вариант совместно с активатором плазминогена (таким как тканевой активатор плазминогена (tPA), урокиназа, стрептокиназа или стафилокиназа или любой их вариант; смотри, например, US 6733750, US 6585972, US 6899877, WO 03/33019). В еще дополнительной альтернативе в контексте настоящего изобретения можно использовать смесь любого из следующего: (i) плазмин или его производное (ii) активируемый плазминоген или его активируемое производное, и, необязательно, (iii) активатор плазминогена (смотри, например, US 2004/0081643). Для того чтобы обеспечить стабильность плазмина (или плазминогена), его будут, как правило, хранить при пониженных температурах (например,+4 градуса Цельсия или -20 градусов Цельсия). Композицией для хранения может быть стабилизирующая композиция, такая как композиция с низким рН (pH 4 или ниже; полученная, например, с помощью 1 мМ - 250 мМ кислоты, такой как лимонная кислота, смотри, например, Castellino & Sodetz, 1976, Methods Enzymol 45, 273-286; WO 01/36608; WO 01/36609; WO 01/36611) или композиция с высоким содержанием глицерина (30-50% объемного содержания, например, Castellino & Sodetz, 1976, Methods Enzymol 45, 273-286), альтернативно в или совместно с одной или несколькими дополнительными композициями стабилизаторов, содержащими, например, аминокислоту (например, лизин или его аналог, такой как EACA или транексамовая кислота), сахар (например, маннит) или любой стабилизатор, который известен в данной области техники (например, дипептиды, WO 97/01631). В семейство “плазминов” дополнительно включено любое его активное производное (или активный процессированный вариант плазмина) или сходное производное активируемого плазминогена (или его активируемого процессированного варианта). Такие производные включают, например, меченый плазмин или плазминоген (или их процессированные варианты), такой как Tc99-меченный плазмин (Deacon et al., 1980, Br J Radiol 53, 673-677) или пегилированный или ацилированный плазмин или плазминоген (или их процессированные варианты; EP 9879, WO 93/15189). Также можно использовать любую другую метку (радиоактивную, флюоресцентную и т.п.) для получения производного плазмина или плазминогена. Указанные производные дополнительно включают гибридные или химерные молекулы плазмина или плазминогена, содержащие, например, процессированный плазмин или плазминоген согласно настоящему изобретению, слитый, например, с фибрин-связывающей молекулой (такой как “двойная петля” 2 tPA, аполипопротеиновая “двойная петля”, пальцеобразный домен tPA или фибронектина или Fab домен фибрин-связывающего антитела).
Сравнение аутопротеолитической устойчивости (т.е. стабильности) плазмина дикого типа и вариантов плазмина или производных плазмина согласно настоящему изобретению может быть проведено сходным образом, как для сравнения протеолитической активности, например, при хромогенном анализе активности или анализе биологического субстрата на основе, например, фибрина, фибриногена фибронектина, желатина, ламинина или коллагена.
Для того чтобы определить аутопротеолитическую устойчивость, может быть определена константа скорости аутолиза. Предусматривается, что варианты плазмина согласно настоящему изобретению, включая плазмины, полученные из вариантов плазминогена согласно настоящему изобретению, или любое из производных плазмина согласно настоящему изобретению могут характеризоваться константой скорости аутолиза, которая является по меньшей мере на 5% или по меньшей мере на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 75%, 80%, 90%, 95%, 99% или 99,5% ниже константы скорости аутолиза плазмина дикого типа, или, альтернативно, константой скорости аутолиза, которая составляет не более 95% или не более 0,5%, 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 75%, 80% или 90% константы скорости аутолиза плазмина дикого типа. Для того чтобы определить указанный процент, расчет может быть произведен на основе абсолютных значений константы скорости аутолиза. Например, для микроплазмина дикого типа была определена константа скорости аутолиза 123 M-1с-1, в то время как для варианта микроплазмина V1I была определена константа скорости аутолиза 33 M-1с-1 (см. Примеры). Константа скорости аутолиза варианта V1I, следовательно, составляет 26,8% константы скорости аутолиза микроплазмина дикого типа.
Дополнительно, любой из вариантов плазмина согласно настоящему изобретению, включая плазмины, полученные из вариантов плазминогена согласно настоящему изобретению, или производные любого из указанных плазминов могут сохранять протеолитическую активность, отличную (выше или ниже) от протеолитической активности плазмина дикого типа, такой, которая определена с помощью, например, анализа хромогенной активности или анализа биологического субстрата на основе, например, фибрина, фибриногена, фибронектина, желатина, ламинина или коллагена.
Протеолитические активности вариантов плазмина согласно настоящему изобретению, включая плазмины, полученные из вариантов плазминогена согласно настоящему изобретению, или любое из производных плазмина согласно настоящему изобретению можно сравнить с протеолитической активностью плазмина дикого типа посредством каталитической константы kкат, которая является мерой числа молекул субстрата, которые каждый сайт фермента превращает в продукт за единицу времени. Таким образом, любой из вариантов плазмина согласно настоящему изобретению, включая плазмины, полученные из вариантов плазминогена согласно настоящему изобретению, или любое из производных плазмина согласно настоящему изобретению может характеризоваться значением kкат, которое находится в диапазоне от +100% до -90% или от +50% до -50% значения kкат плазмина дикого типа, т. е. характеризоваться значением kкат в диапазоне от 10% до 200% или от 50% до 150% значения kкат плазмина дикого типа. Для определения указанного процента производят расчет на основании абсолютных значений kкат. Например, микроплазмин дикого типа имеет kкат 46 с-1, тогда как вариант микроплазмина K137M имеет kкат 36 с-1 (смотри Пример 4/Таблицу 3 WO 2011/004011). Значение kкат варианта K137M, следовательно, составляет 78,3% kкат микроплазмина дикого типа.
Другой способ сравнения протеолитической активности вариантов плазмина согласно настоящему изобретению, включая плазмины, полученные из вариантов плазминогена согласно настоящему изобретению, или любых из производных плазмина согласно настоящему изобретению с протеолитической активностью плазмина дикого типа включает сравнение kкат/Kм. Несмотря на то, что могут быть предпочтительны более высокие, сравнимые или более низкие значения kкат/Kм, до 1000-раз или до 500-раз более низкое kкат/Kм вариантов плазмина согласно настоящему изобретению, включая плазмины, полученные из вариантов плазминогена согласно настоящему изобретению, или любого из производных плазмина согласно настоящему изобретению по сравнению с kкат/Kм плазмина дикого типа все еще может быть приемлемым (смотри далее). В качестве примера, определили, что kкат/Kм варианта микроплазмина V1I составляло 1×106, тогда как определили, что kкат/Kм плазмина дикого типа составляло 6,9×105 (см. Примеры), т.е. значение kкат/Kм микроплазмина V1I в 1,45 раза выше значения kкат/Kм микроплазмина дикого типа.
Альтернативно, любой из вариантов плазмина согласно настоящему изобретению, включая плазмины, полученные из вариантов плазминогена согласно настоящему изобретению, или любое из производных плазмина согласно настоящему изобретению можно сравнить с плазмином дикого типа путем объединения данных по константе скорости аутолитической реакции и данных по kкат/Kм. Например, вариант плазмина с константой скорости аутолитической реакции, которая в 20 раз ниже по сравнению с плазмином дикого типа, и с kкат/Kм, которое в 10 раз ниже по сравнению с плазмином дикого типа, будет в 2 раза лучше, чем плазмин дикого типа. Разумеется, в зависимости от конечного применения, очень стабильный плазмин (т.е. нет или почти нет аутопротеолитического распада) с низкой протеолитической активностью может быть очень желательным, например, в случаях, где низкая, но пролонгированная активность плазмина, желательна или даже необходима для достижения предполагаемого клинического эффекта. Такие высокостабильные варианты плазмина с низкой протеолитической активностью будут, по сути, фактически равными составам с замедленным высвобождением без действительной необходимости фактического применения носителя или вспомогательного средства для замедленного высвобождения.
Еще одна альтернатива сравнению любого из вариантов плазмина согласно настоящему изобретению, включая плазмины, полученные из вариантов плазминогена согласно настоящему изобретению, или любого из производных плазмина согласно настоящему изобретению может заключаться в сравнении с плазмином дикого типа путем объединения данных по константе скорости аутолитической реакции и данных по kкат.
Дополнительно, любой из вариантов плазмина согласно настоящему изобретению, включая плазмины, полученные из вариантов плазминогена согласно настоящему изобретению, или любое из производных плазмина согласно настоящему изобретению может характеризоваться любой комбинацией определенных выше константы скорости аутолиза, каталитической константы kкат и/или kкат/Kм.
Разумеется, для любых сравнительных измерений, таких, которые описаны выше, необходимо сравнивать варианты плазмина с наиболее близким к ним плазмином дикого типа, например, сравнивать вариант микроплазмина с микроплазмином дикого типа или вариант миниплазмина с миниплазмином дикого типа. Кроме того ясно, что для любого измерения активности, обратимо инактивированное производное варианта плазмина согласно настоящему изобретению следует сначала активировать путем устранения причины обратимой инактивации (например, ацилирование или неоптимальный pH).
Любой из вариантов плазминогена согласно настоящему изобретению или плазминов, полученных из них, вариантов плазмина согласно настоящему изобретению может быть следующим: Glu-плазминоген или Glu-плазмин, Lys-плазминоген или Lys-плазмин, мидиплазминоген или мидиплазмин, миниплазминоген или миниплазмин, микроплазминоген или микроплазмин, дельтаплазминоген или дельтаплазмин.
Существует много анализов для определения того, является или нет вид плазмина протеолитически активным. Простые и прямые анализы основаны на расщеплении хромогенного субстрата плазмином, присутствующим в образце; хромогенные субстраты включают S-2403 (Glu-Phe-Lys-pNA) и S-2251 (Val-Leu-Lys-pNA), которые высвобождают p-нитроанилин (pNA) при протеолитическом расщеплении. Количество образованного pNA может быть измерено с помощью поглощения света при 405 нм. Альтернативным анализом для определения активности плазмина является потенциометрический анализ. Колориметрические (с использованием хромогенного субстрата) и потенциометрические анализы описаны, например, в работе Castellino и Sodetz (1976, Methods Enzymol 45, 273-286). Следующим альтернативным анализом для определения активности плазмина является казеинолитический анализ (например, Robbins & Summaria, 1970, Methods Enzymol 19, 184-199; Ruyssen & Lauwers, 1978, Chapter IX - Plasmin, In “Pharmaceutical Enzymes”, Story-Scientia, Gent, Belgium, pp. 123-131). Еще одним альтернативным анализом для определения активности плазмина является фибринолитический анализ (например, Astrup & Mullertz, 1952, Arch Biochem Biophys 40, 346-351). Можно легко разработать дополнительные анализы активности с применением других белковых субстратов. Ясно, что такие анализы также могут использоваться для отслеживания исчезновения протеолитической активности плазмина с течением времени вследствие аутопротеолитического распада фермента. В качестве альтернативы для оценки стабильности варианта плазмина или любого его активного процессированного варианта или их производного в соответствии с настоящим изобретением, можно инкубировать указанный вариант плазмина в присутствии плазмина дикого типа и можно отследить устойчивость варианта плазмина к расщеплению плазмином дикого типа.
Применение плазмина при удалении некротических элементов или инородных остатков из повреждений, ран, изъязвляющихся ран (таких как изъязвляющиеся зашитые раны) и т.д. было описано, например, в патенте США №3208908. Аналогично, местное применение плазмин-содержащих терапевтических препаратов для лечения ожогов было раскрыто, например, в патенте США №4122158. Обработка раны относится к удалению мертвой, поврежденной и/или инфицированной ткани для улучшения или повышения заживление оставшейся здоровой ткани. Такое удаление может быть достигнуто с помощью хирургических, механических или химических средств или посредством определенных видов живых личинок, которые избирательно поедают некротическую ткань (терапия личинками). Обработка раны может также быть проведена с использованием ферментов или может быть выполнена с помощью ферментов, этот процесс называется ферментное очищение раны. Обработка раны является важным аспектом в процессе заживления ожогов и других серьезных ран, и ее также используют при лечении некоторых типов укусов змей. Применение плазмина (или любого его варианта или производного или, соответственно, альтернативы, как описано выше) при ферментном очищении раны (отдельно или в комбинации с другими типами обработки раны) является особенно пригодным при стимулировании или облегчении заживления раны и в качестве вспомогательного средства в хирургических процедурах, таких как пересадка кожи.
Более общеизвестное применение плазмина (или любого его варианта или производного или, соответственно, альтернативы, которые описаны выше) относится, в общих выражениях, к лечению патологического (патологических) отложения (отложений) фибрина. Отложения фибрина могут быть результатом широкого разнообразия патологических ситуаций в организме. Например, содержащие фибрин кровяные сгустки могут формироваться в сосудах ткани, приводя к закупорке или тромбозу глубокой вены, коронарной артерии, мозговой артерии или ретинальной вены. Небольшие скопления фибрина предшествуют и могут обуславливать предвестник угрожающего катастрофического тромбоза. Примеры включают нестабильную стенокардию, которая рассматривается как предвестник угрожающего коронарного тромбоза и транзиторных ишемических атак, которые могут предшествовать инсультам. Фибрин, кроме того, часто откладывается в ткани в связи с воспалением, связанным со многими патологическими процессами, включая инфекцию, аутоиммунное заболевание и рак. Другая ситуация, при которой откладывается фибрин - это вокруг абсцессов, вызванных инфицированием микроорганизмами. Фибриновые отложения, кроме того, часто обнаруживаются связанными с определенными солидными опухолями. Фибриновое отложение может также происходить во время заживления любого типа раны, включая полученные в результате хирургического вмешательства, в том числе, например, трабекулэктомию. Еще одна ситуация отложения фибрина - это накопление фибрина в ретинальной вене, которое может привести к дегенерации сетчатки, нарушенному зрению или даже потере зрения. Выражение "патологическое отложение фибрина" дополнительно включает такие отложения, как сформированные или присутствующие в или на кончике катетера, катетерного устройства или другого имплантата, такого как протезные сосуды и трансплантаты синтетического, человеческого или животного происхождения и эффективно блокируемые закупоркой, содержащей фибрин. Выражение "катетерное устройство" относится к любому катетеру или трубко-подобному устройству, которое может проникать в организм, включая артериальные катетеры, кардиальные катетеры, центральные венозные катетеры, внутривенные катетеры, периферически вводимые центральные катетеры, пульмонарные артериальные катетеры, туннельные центральные венозные катетеры и артериально-венозные шунты.
Среди различных факторов, вовлеченных в процесс тромбоза, т.е. образование тромба или гемостатической пробки, имеют место следующие: (1) повреждение выстилки эндотелиальных клеток пораженного кровеносного сосуда, (2) повышение свертывающих свойств крови и (3) застой крови в пораженном кровеносном сосуде. Тромбоз может начинаться как очень маленький комочек, прикрепленный к поврежденной части выстилки кровеносного сосуда. Его присутствие стимулирует дальнейшее протекание тромбоза и вызывает замедление потока крови путем уменьшения внутреннего диаметра сосуда. Дальнейший рост изначально небольшого тромба часто ведет к полной или почти полной закупорке пораженного кровеносного сосуда. Если тромбоз имеет место в одной из артерий, то ткани, которые снабжаются этой артерией, могут быть лишены кислорода и питательных веществ, что приведет к повреждению или смерти ткани (гангрене). Тяжесть повреждения зависит от положения и размера тромбоза, скорости, с которой он растет, и того, имеет ли пораженная область только одну артерию или снабжена коллатеральными кровеносными сосудами. Если затронут сосуд к жизненному органу, например, сердцу или мозгу, то индивидуум может получить тяжелые увечья или умереть. Иногда тромб может содержать инфекционные организмы, такие как бактерии, может иметь место и септический тромбоз с образованием гноя и инфицированием окружающих тканей.
Дополнительные применения плазмина (или любого его варианта или производного или, соответственно, альтернативы, которые описаны выше) включают снижение уровня циркулирующего фибриногена (например, WO 93/07893) и его применение как ингибитора α2-антиплазмина (который, как сообщалось, снижает размер церебрального инфаркта после ишемического инсульта; WO 00/18436).
Еще одно применение плазмина (или любого его варианта, или производного, или, соответственно, альтернативы, как описано выше) связано с индукцией заднего отслоения стекловидного тела (PVD) и/или разжижения стекловидного тела глаза в качестве альтернативы механической витрэктомии или в качестве вспомогательного средства для механической витрэктомии (WO 2004/052228, US 6733750, US 6585972, US 6899877, WO 03/33019, WO 2006/122249, WO 2007/047874, US 5304118, US 2006/0024349, US 2003/0147877). Витрэктомия и/или разжижение стекловидного тела оказывает благоприятный эффект при ряде состояний глаза, таких как плавающие помутнения стекловидного тела (подвижные инородные остатки/отложения стекловидного тела внутри жидкости стекловидного тела с нормальной прозрачностью, которые могут нарушать зрение), отслоение сетчатки (ведущее к слепоте состояние, которое может быть вызвано витреальной тракцией), макулярная складчатость (рубцовая ткань на желтом пятне; желтое пятно необходимо для острого центрального зрения; макулярная складчатость также известна как эпи- или преретинальная мембрана, целлофановая макулопатия, складка сетчатки, ретинопатия с образованием поверхностных складок, премакулярный фиброз или заболевание внутренней ограничивающей мембраны), диабетическая ретинопатия (пролиферативная или непролиферативная), которая может приводить к кровоизлиянию в стекловидное тело и/или образованию фиброзной рубцовой ткани на сетчатке (которая может вызывать отслоение сетчатки), макулярные отверстия (макулярное отверстие, приводящее к образованию слепого пятна и вызванное витреальной тракцией, травмой или травматичным событием), кровоизлияние в стекловидное тело (вызванное диабетической ретинопатией, травмами, отслоением сетчатки или разрывами сетчатки, субарахноидальными кровоизлияниями (синдром Терсона) или закупоренными сосудами), субгиалоидная гемморагия (кровоизлияние под гиалоидной мембраной, покрывающей стекловидное тело), макулярная эдема (скопление жидкости и белка на желтом пятне глаза или под ним) и дегенерация желтого пятна (начинающееся с образования друзы; встречается в сухой и мокрой форме; при корреляции с возрастом вызывала возрастную макулярную дегенерацию). Другие применения плазмина для глаз включают поддержание или восстановление фильтрационной подушки после трабекулоэктомической операции (проведенной для снижения внутриглазного давления), смотри, например, WO 2009/073457.
Другое дополнительное применение плазмина (или любого его варианта, или производного, или, соответственно, альтернативы, которые описаны выше) принадлежит к диагностике, более конкретно, подходящим образом меченный (например, Tc99-меченный, смотри выше) плазмин (или любой его вариант, или производное, или, соответственно, альтернатива, как описано выше) можно применять для обнаружения патологических отложений фибрина. При применении процессированного плазмина или варианта плазминогена согласно настоящему изобретению в таких диагностиках следует проявлять осторожность, так как указанный вариант все еще содержит фибрин-связывающий сайт (вне зависимости от того, происходит он из плазмина самого по себе, или добавлен, например, к каталитическому домену плазмина путем создания гибридной молекулы).
Плазмин, или любой его вариант или производное, или, соответственно, альтернатива согласно настоящему изобретению могут храниться в фармацевтически приемлемом носителе, разбавителе или вспомогательном средстве. Такой носитель, разбавитель или вспомогательное средство может состоять из или содержать кислый буфер с низким рН, такой как 1-100 мМ ацетат или цитрат. Если он кислый, то фармацевтически приемлемый носитель, разбавитель или вспомогательное средство может иметь pH 2,5-5,0, такой как pH 2,5-4,0, или такой как pH 3,0-3,5, или такой как pH 3,1. Пригодные кислые соединения включают уксусную кислоту, лимонную кислоту, соляную кислоту, молочную кислоту, яблочную кислоту, винную кислоту или бензойную кислоту. Можно использовать муравьиную кислоту, но следует проявлять осторожность, так как это соединение не индуцирует протеолитическое расщепление на C-конце Asp-остатков. Фармацевтически приемлемый носитель, разбавитель или вспомогательное средство, если оно либо кислое, либо нейтральное, либо основное, может содержать одну или несколько аминокислот, таких как серин, треонин, метионин, глутамин, глицин, изолейцин, валин, аланин, аспарагиновая кислота, лизин, гистидин или любые их производные или аналоги. Фармацевтически приемлемый носитель, разбавитель или вспомогательное средство может включать углевод, такой как моносахарид, дисахарид, полисахарид или многоатомный спирт. Примеры включают сахара, такие как сахароза, глюкоза, фруктоза, лактоза, трегалоза, мальтоза и манноза, сахарные спирты, такие как сорбит и маннит, и полисахариды, такие как декстрины, декстраны, гликоген, крахмалы и целлюлозы. Фармацевтически приемлемый носитель, разбавитель или вспомогательное средство может включать соединения, такие как глицерин, ниацинамид, глюкозамин, тиамин, цитруллин, неорганические соли (такие как хлорид натрия, хлорид калия, хлорид магния, хлорид кальция), бензиловый спирт или бензойную кислоту. Фармацевтически приемлемый носитель, разбавители или вспомогательное средство может включать такие соединения, как ε-аминокапроновая кислота (EACA) и/или транексамовая кислота (смотри также выше и раздел Предпосылки изобретения). Некоторые из этих соединений могут быть использованы как стабилизатор плазмина, или любого его варианта или производного, или, соответственно, альтернативы, которые описаны выше.
В свете описанного выше, другой аспект настоящего изобретения относится к выделенному плазминогену, плазмину, или любому их варианту или производному, или, соответственно, альтернативе согласно настоящему изобретению, или комбинации любых из них для применения в качестве лекарственного препарата.
Дополнительный аспект настоящего изобретения относится к композициям, содержащим выделенный плазминоген, плазмин, или любой их вариант или производное, или, соответственно, альтернативы согласно настоящему изобретению, или комбинацию любых из них, и по меньшей мере одно из фармацевтически приемлемого разбавителя, носителя или вспомогательного средства. В дополнительном варианте осуществления указанная композиция может дополнительно содержать по меньшей мере одно из следующего: антикоагулянт, дополнительное тромболитическое средство, противовоспалительное средство, противовирусное средство, антибактериальное средство, противогрибковое средство, антиангиогенное средство, антимитотическое средство, антигистамин или анестетик.
В варианте осуществления к описанным выше двум аспектам настоящего изобретения выделенный плазминоген, плазмин, или любой их вариант, или производное, или, соответственно, альтернативу согласно настоящему изобретению, или комбинацию любых из них, или композицию согласно настоящему изобретению можно применять в любой клинически важной установке, такой как для лечения патологического отложения фибрина, для индуцирования заднего отслоения стекловидного тела глаза, для индуцирования разжижения стекловидного тела глаза, как вспомогательное и облегчающее вещество витрэктомии глаза, для индуцирования заднего отслоения стекловидного тела, для расщепления витреомакулярной адгезии, для закрытия макулярных отверстий, для ферментного очищения раны, для снижения циркулирующего фибриногена, для снижения уровней α2-антиплазмина или совместно с трабекулэктомией.
В другом варианте осуществления к описанным выше двум аспектам настоящего изобретения выделенный плазминоген, плазмин, или любой их вариант или производное, или, соответственно, альтернативу согласно настоящему изобретению, или комбинацию любых из них, или композицию согласно настоящему изобретению можно применять для профилактических целей или в способах профилактического лечения. Профилактические применения включают снижение риска развития патологического отложения фибрина у млекопитающего с повышенным риском его развития (такого как страдающее ожирением млекопитающее, млекопитающее, которое не делает достаточных физических упражнений или млекопитающее, которому предписано серьезное хирургическое вмешательство или операция). Другие профилактические применения включают индукцию заднего отслоения стекловидного тела и/или разжижения стекловидного тела в явно здоровом глазу млекопитающего, у которого другой глаз, как показывает(показывала) диагностика, нуждается в индукции заднего отслоения стекловидного тела и/или разжижения стекловидного тела.
Альтернативно, настоящее изобретение относится к способам лечения, растворения, разрыхления, размягчения, лизирования, индукции или активации лизиса патологического отложения фибрина у субъекта, при этом указанные способы включают осуществление контакта указанного отложения фибрина с эффективным количеством выделенного плазминогена, плазмина, или любого их варианта или производного, или, соответственно, альтернативы согласно настоящему изобретению, или комбинации любых из них, при этом указанное осуществление контакта приводит к лечению, растворению, разрыхлению, размягчению, лизису или индукции или активации лизиса указанного патологического отложения фибрина.
Настоящее изобретение дополнительно относится к способам индукции заднего отслоения стекловидного тела глаза и/или индуцирования разжижения стекловидного тела глаза, или облегчения хирургической витрэктомии глаза у субъекта, при этом указанные способы включают осуществление контакта глаза указанного субъекта, нуждающегося в таком лечении, с эффективным количеством выделенного плазминогена, плазмина, или любого их варианта или производного, или, соответственно, альтернативы согласно настоящему изобретению, или комбинации любых из них, при этом указанное осуществление контакта приводит к индукции указанного заднего отслоения стекловидного тела и/или указанного разжижения стекловидного тела или к облегчению указанной хирургической витрэктомии.
Настоящее изобретение также относится к способам ферментного очищения раны поврежденной ткани субъекта, при этом указанный способ включает осуществление контакта указанной поврежденной ткани с эффективным количеством выделенного плазминогена, плазмина, или любого их варианта или производного, или, соответственно, альтернативы согласно настоящему изобретению, или комбинации любых из них, при этом указанное осуществление контакта приводит к указанному ферментному очищению раны указанной поврежденной ткани.
Другие способы в соответствии с настоящим изобретением представляют собой лечение или предупреждение любого другого клинически соответствующего симптома, включая способы снижения циркулирующего фибриногена или снижения уровней α2-антиплазмина у субъекта, при этом указанные способы включают контактирование субъекта, нуждающегося в таком лечении, с эффективным количеством выделенного плазминогена, плазмина, или любого их варианта или производного или, соответственно, альтернативы согласно настоящему изобретению, или комбинации любых из них, при этом указанное осуществление контакта приводит к указанному снижению циркулирующего фибриногена или указанных уровней α2-антиплазмина.
В основном, лекарственный препарат или композиция в соответствии с настоящим изобретением, содержащая плазмин (или любой его вариант или производное, или, соответственно, альтернативу) согласно настоящему изобретению, в зависимости от их конечного применения и способа введения, могут содержать один или несколько дополнительных активных ингредиентов, таких как антикоагулянт, дополнительное тромболитическое средство, противовоспалительное средство, противовирусное средство, антибактериальное средство, противогрибковое средство, антиангиогенное средство, антимитотическое средство, антигистамин или анестетик.
“Антикоагулянты” включают гирудины, гепарины, кумарины, низкомолекулярный гепарин, ингибиторы тромбина, ингибиторы тромбоцитов, ингибиторы агрегации тромбоцитов, ингибиторы фактора коагуляции, антитела к фибрину и ингибиторы фактора VIII (такие как описываемые в WO 01/04269 и WO 2005/016455).
“Тромболитические средства” включают плазмин дикого типа, плазминоген дикого типа, урокиназу, стрептокиназу, активатор плазминогена тканевого типа (tPA или альтеплаза), активатор плазминогена урокиназного типа (uPA) и стафилокиназу или любой вариант или производное любого из них, например, APSAC (анизоилированный активаторный комплекс стрептокиназы и плазминогена), ретеплаза, тенектеплаза, scuPA (одноцепочечный uPA) или комбинацию любых из них.
“Противовоспалительные средства” включают стероиды (например, преднизолон, метилпреднизолон, кортизон, гидрокортизон, преднизон, триамцинолон, дексаметазон) и нестероидные противовоспалительное средства (NSAID, например, ацетаминофрен, ибупрофен, аспирин).
“Противовирусные средства” включают трифлуридин, видарабин, ацикловир, валацикловир, фамцикловир и доксуридин.
“Антибактериальные средства” или антибиотики включают ампициллин, пенициллин, тетрациклин, окситетрациклин, фрамицетин, гатифлоксацин, гентамицин, тобрамицин, бацитрацин, неомицин и полимиксин.
“Антимикотические/фунгистатические/противогрибковые средства” включают флюконазол, амфотерицин, клотримазол, эконазол, итраконазол, миконазол, 5-фторцитозин, кетоконазол и натамицин.
“Антиангиогенные средства” включают антитела (или их фрагменты), такие как антитела к VEGF (фактор роста эндотелия сосудов) или к PlGF (плацентарный фактор роста), и средства, такие как макуген (пегаптаниб натрия), триптофанил-тРНК-синтаза (TrpRS), анекортав ацетат, пролекарство комбрестатин A4, AdPEDF (аденовектор, способный экспрессировать полученный из пигментного эпителия фактор), VEGF-ловушка, ингибитор VEGF рецептора-2, ингибиторы VEGF, PlGF или TGF-β, сиролимус (рапамицин) и эндостатин.
“Антимитотические средства” включают митомицин C и 5-фторурацил.
“Антигистаминное средство” включает кетитофена фумарат и фенирамина малеат.
“Анестетики” включают бензокаин, бутамбен, дибукаин, лидокаин, оксибупрокаин, прамоксин, пропаракаин, проксиметакаин, тетракаин и аметокаин.
“Осуществление контакта”, при использовании в данном документе, означает любой способ введения, который приводит к взаимодействию между композицией, такой как лекарственный препарат, и тканью, жидкостью организма, органом, организмом и т.д., с которым указанная композиция контактирует. Взаимодействие между композицией и тканью, жидкостью организма, органом, организмом и т.д. может происходить, начинаясь немедленно или почти немедленно с введением композиции, может происходить в течение длительного периода времени (начинаясь немедленно или почти немедленно с введением композиции), или может быть отсроченным по отношению ко времени введения композиции.
По отношению к такому отложению фибрина можно использовать любой способ осуществления контакта патологического отложения фибрина, который обеспечивает (или немедленно, отсрочено или в течение длительного периода времени) эффективное количество плазмина (или любого его варианта или производного или, соответственно, альтернативы). Если такое отложение фибрина связано со сгустком крови, то плазмин (или любой его вариант или производное, или, соответственно, альтернатива) может быть доставлен внутриартериально, внутривенно или местно (на малое расстояние от сгустка или даже в сгусток) посредством инъекции и/или инфузии, и/или катетера.
При применении плазмина (или любого его варианта или производного, или, соответственно, альтернативы) в ферментной обработке раны он может быть включен в гелеподобную композицию, которую можно применять местно, или можно применять в жидкой форме.
Может быть использован любой способ осуществления контакта стекловидного тела глаза и/или водянистой влаги, который обеспечивает (или немедленно, отсрочено или в течение длительного периода времени) эффективное количество плазмина (или любого его варианта или производного, или, соответственно, альтернативы) в стекловидном теле и/или водянистой влаге. Один способ осуществления контакта стекловидного тела и/или водянистой влаги предусматривает одну или несколько внутриглазных инъекций непосредственно в стекловидное тело и/или водянистую влагу. Альтернативно, указанное осуществление контакта может включать субконъюктивальные, внутримышечные или внутривенные инъекции. Дополнительный альтернативный способ осуществления контакта включает размещение интравитреального имплантируемого устройства, такого как OCUSERT® (Alza Corp., Пало-Альто, Калифорния) или VITRASERT® (Bausch & Lomb Inc., Рочестер, Нью-Йорк). Осуществление контакта стекловидного тела и/или водянистой влаги с эффективным количеством плазмина (или любого его варианта или производного, или, соответственно, альтернативы) может происходить непрерывным способом с применением состава пролонгированного, замедленного высвобождения или любого подходящего для этого имплантируемого устройства.
Выражение “эффективное количество” относится к режиму дозирования лекарственного препарата согласно настоящему изобретению, в частности, активного ингредиента лекарственного препарата согласно настоящему изобретению, т.е. плазмина или его активного процессированного варианта (или, следовательно, любой альтернативы, как описано выше). Эффективное количество будет, как правило, зависеть от и нуждаться в регулировании относительно способа осуществления контакта или введения и состояния, которое подлежит лечению. Эффективное количество лекарственного препарата, более конкретно, его активного ингредиента, представляет собой количество, необходимое для получения необходимого клинического результата или терапевтического или профилактического эффекта, не вызывая значительных или нежелательных токсических эффектов. Для получения или поддержания эффективного количества лекарственный препарат может быть введен в виде однократной дозы или во множественных дозах. Эффективное количество может дополнительно варьировать в зависимости от тяжести состояния, подлежащего лечению, или предполагаемой тяжести состояния, подлежащего предупреждению; оно может зависеть от общего состояния здоровья и физического состояния пациента, и обычно будет необходима оценка лечащего врача или терапевта для установления того, каким является эффективное количество. Эффективное количество дополнительно может быть получено путем комбинирования различных типов введения. Лекарственный препарат может быть введен в виде раствора (жидкого или полужидкого, например, гелеподобного или в дисперсии или суспензии, коллоидного, в эмульсии, суспензии наночастиц) или в виде твердой формы (например, таблетка, минитаблетка, капсулы с твердой или мягкой оболочкой).
В целях тромболиза, дозировка плазмина и длительность терапии плазмином будет, как правило, зависеть от размера и расположения кровяного сгустка, а также от размера, веса и возраста пациента. Если сгусток является венозным, то лечение плазмином может продолжаться несколько дней, тогда как если сгусток является артериальным, то могут быть необходимы лишь часы терапии плазмином. Инфаркт миокарда можно лечить коротким лечением однократными дозами, тогда как состояния, такие как тромбофлебит и эмболия сосудов легких, могут требовать более длительного лечения многократными дозами. Пролонгированная непрерывная и/или периодическая тромболитическая терапия плазмином может быть применена для лечения коронарной окклюзии или в случае профилактической терапии для снижения риска образования сгустка у субъектов, у которых известно наличие повышенного риска развития образования сгустка. Дополнительный фактор, влияющий на дозировку плазмина, включает уровни циркулирующих в крови ингибиторов плазмина, таких как α2-антиплазмин и/или α2-макроглобулин, начальный уровень которых, при этом, зависит от пациента. Для достижения эффективной тромболитической терапии может быть целесообразно откорректировать дозировку плазмина так, чтобы оставалось не более 15% общего циркулирующего α2-антиплазмина. С целью индуцирования тромболиза контактный способ доставки плазмина или любого его варианта, или производного или, соответственно, альтернативы близко к тромбу может быть выгодным, поскольку воздействие сывороточных ингибиторов снижается. Такой контактный способ, как правило, включает доставку посредством катетерного устройства. Для применения в тромболизе типичные дозировки плазмина находятся в диапазоне от 500 микрограмм/кг веса тела до 10 миллиграмм/кг веса тела, вводимые как одноразовая ударная доза вещества или разделенные на 1 начальную инъекцию с последующей 1 или несколькими повторными инъекциями ударной дозы вещества. Плазмин, альтернативно, можно вводить в течение длительного периода времени, например, путем инфузии или с помощью микронасоса для доставки лекарственного средства. Дозировки плазмина для продолжительного введения могут находиться в диапазоне от 1 до 10 мг/кг/час.
Типичная дозировка плазмина для индукции задней отслойки стекловидного тела, разжижения стекловидного тела, очищения от крови в стекловидном теле или кровоизлияний или очищения от токсичных материалов или посторонних веществ из полости стекловидного тела может быть в диапазоне от приблизительно 0,1 микрограмм до приблизительно 250 микрограмм на глаз на дозу, которая может быть доставлена в объеме разбавителя или носителя от приблизительно 50 микролитров до приблизительно 300 микролитров на глаз на дозу. Разбавитель или носитель могут быть, например, стерильным сбалансированным солевым раствором (BSS или BSS Plus), физиологическим солевым раствором или раствором, содержащим 1-10 мМ лимонную кислоту. В одном варианте осуществления плазмин доставляют к глазу в дозе 125 микрограмм, содержащихся в 0,1 мл разбавителя или носителя. В случае запланированной хирургической витрэктомии указанный плазмин может быть доставлен к глазу за 15-300 минут или 15-120 минут до витрэктомии. В альтернативном случае целью введения плазмина в глаз является попытка избежать хирургической витрэктомии или облегчить последующую хирургическую витрэктомию в случае, если сама по себе обработка плазмином не будет способна осуществить полное заднее отслоение стекловидного тела. Если плазминоген используется как альтернативный источник плазмина (смотри определение “плазмин”), на каждый глаз может быть введено до 250 микрограмм плазминогена, и указанный плазминоген может сопровождаться до 2000 IU урокиназы или стрептокиназы в качестве активатора плазминогена или до 25 микрограмм tPA. При использовании в глазу введение плазмина или плазминогена может дополнительно сопровождаться введением газообразного вспомогательного средства, такого как воздух, расширяющийся газ, или сжижаемый газ, или их смеси, при условии, что он является нетоксичным для глаза. Другие подходящие газообразные материалы включают SF6 (гексафторид серы) и перфторуглероды, такие как C2F6 (гексафторэтан), C3Fs (октафторпропан), C4Fs (октафторциклобутан), кислород, азот, диоксид углерода, аргон и другие инертные газы. Объем газообразного материала, который вводят в глаз, может изменяться в зависимости от газообразного материала, пациента и желаемого результата. Например, объем воздуха, который вводят в заднюю камеру, может находиться в диапазоне от приблизительно 0,5 мл до приблизительно 0,9 мл. Другие газообразные материалы, такие как SF6 и газы-перфторуглероды, могут находиться в диапазоне от приблизительно 0,3 мл до 0,5 мл. Предпочтительно, газообразный материал вводят в заднюю камеру глаза в количестве, достаточном для сжатия стекловидного тела напротив задней гиалоидной мембраны и образования полости в стекловидном теле без повреждения глаза. В предпочтительных вариантах осуществления газообразное вспомогательное средство вводят в стекловидное тело с образованием полости, которая заполняет от приблизительно 40% до приблизительно 60% внутреннего объема внутриглазной полости.
Перечисленные выше дозировки являются показательными значениями, не подразумевающими, что они являются каким-либо образом ограничивающими. Указанные дозировки, кроме того, относятся к плазмину или плазминогену дикого типа или любому их активному или активируемому процессированному варианту. При применении плазмина с повышенной стабильностью согласно настоящему изобретению (или любого его варианта, или производного, или, соответственно, альтернативы), и в зависимости от конечной стабильности и остаточной активности плазмина согласно настоящему изобретению, для получения такого же или лучшего суммарного клинического эффекта, чем получаемый с плазмином дикого типа, дозировки могут быть сходными, более высокими или более низкими. Дозировка плазмина согласно настоящему изобретению может также зависеть от скорости ингибирования эндогенными ингибиторами, такими как α2-антиплазмин.
Настоящее изобретение дополнительно относится к способам скрининга в отношении аутопротеолитически стабильных вариантов плазмина, причем указанные способы включают:
(i) получение варианта плазмина согласно настоящему изобретению и получение плазмина дикого типа,
(ii) сравнение аутопротеолитической стабильности вариантного плазмина и плазмина дикого типа, полученных на этапе (i), и
(iii) отбор по результатам этапа (ii) варианта, который сохраняет протеолитическую активность, и у которого аутопротеолитическая стабильность повышена по сравнению с аутопротеолитической стабильностью плазмина дикого типа.
Описанные выше способы скрининга могут дополнительно включать этап, где определяют протеолитическую активность аутопротеолитически стабильного варианта плазмина.
Многие продукты, включая медикаменты (здесь понимаемые, в частности, как готовый к употреблению активный ингредиент, т.е. в конечном составе для введения пациенту) и бестарно хранящиеся активные ингредиенты медикаментов, обычно хранят в течение значительного срока перед применением. Представляет интерес как можно более длительное увеличение срока хранения продуктов. Под сроком хранения понимают время, в течение которого продукт можно безопасно использовать и в течение которого продукт сохраняет свою эффективную применимость, т.е. свою активность в случае медикамента и/или его активного ингредиента. Как правило, срок хранения указан на продукте или его упаковке. По истечении срока хранения безопасная и эффективная применимость продукта больше не гарантируется. Дополнительным важным аспектом в хранении продуктов является температура хранения, при которой может быть достигнут необходимый срок хранения. Например, срок хранения продукта, хранящегося при +4°C или средней температуре холодильника, может составлять до 12 месяцев, тогда как срок хранения того же продукта, хранящегося при -20°C или средней температуре морозильной камеры, может составлять до 36 месяцев. Логично, однако, что поддержание холодовой цепи при температурах замораживания, например, -20°C, является более сложным, трудным и дорогим, чем поддержание холодовой цепи при +4°C. Таким образом, еще быть может привлекательным получение более короткого, но достаточно длительного срока хранения в сочетании с возможностью хранения продукта при +4°C. Настоящее изобретение предлагает решение для продления, увеличения или повышения срока хранения или стабильности при длительном хранении плазмина, или любого его активного фрагмента, или производного, или композиции, содержащей плазмин или любое его активное производное. Решение заключается в предоставлении вариантов плазмина, которые описаны в данном документе, где указанные варианты имеют увеличенную стабильность, которая, в сущности, повышает, увеличивает или продлевает их срок хранения.
Настоящее изобретение аналогично относится к способам повышения стабильности при длительном хранении содержащей плазмин композиции, причем указанные способы включают этап определения аутопротеолитически стабильного варианта плазмина, способного храниться в течение длительного периода времени без существенной потери протеолитической активности. Для определения долговременной стабильности отбирают аликвоту препарата плазмина согласно настоящему изобретению и многократно проводят измерения активности во время предусмотренного срока хранения. Если предусмотренный срок хранения составляет, например, 24 месяца, то измерения активности можно проводить, например, ежемесячно. Допустимая потеря протеолитической активности в конце предусмотренного срока хранения будет в большей степени зависеть от предусмотренного клинического применения, но, как правило, может быть не более, например, 10%-15%.
Настоящее изобретение дополнительно относится к способам получения варианта плазминогена согласно настоящему изобретению, при этом указанные способы включают этапы следующие этапы:
(i) введение нуклеиновой кислоты, кодирующей плазминоген согласно настоящему изобретению, в подходящую клетку-хозяина, способную экспрессировать указанный плазминоген;
(ii) выращивание клетки-хозяина, полученной на этапе (i), в условиях и в течение времени, достаточных для экспрессии указанного плазминогена в указанной клетке-хозяине; и
(iii) сбор плазминогена, экспрессированного на этапе (ii).
Настоящее изобретение дополнительно относится к способам получения варианта плазмина согласно настоящему изобретению, при этом указанные способы включают следующие этапы:
(i) введения нуклеиновой кислоты, кодирующей плазминоген согласно настоящему изобретению, в подходящую клетку-хозяина, способную экспрессировать указанный плазминоген;
(ii) выращивание клетки-хозяина, полученной на этапе (i), в условиях и в течение времени, достаточных для экспрессии указанного плазминогена в указанной клетке-хозяине;
(iii) сбор плазминогена, экспрессированного на этапе (ii).
(iv) активация плазминогена из этапа (iii) до плазмина.
Подходящие клетки-хозяева и способы экспрессии и получения раскрыты, например, в WO 90/13640 (клетки насекомых), WO 2002/050290 и WO 03/066842 (дрожжевые клетки), WO 2008/054592 (бактериальные клетки/процесс рефолдинга) и WO 2005/078109 (трансгенные растения ряски или клетки трансгенного растения).
Настоящее изобретение также относится к выделенной(ым) последовательности(ям) нуклеиновой кислоты, кодирующей(им) вариант плазминогена или вариант плазмина согласно настоящему изобретению. Настоящее изобретение также относится к рекомбинантному(ым) вектору(ам), содержащему(им) такую нуклеиновую кислоту. Настоящее изобретение также относится к клетке-хозяину (клеткам-хозяевам), трансформированной(ым) такой нуклеиновой кислотой или таким рекомбинантным вектором.
ПРИМЕРЫ
ПРИМЕР 1 Построение и экспрессия вариантов плазминогена и активация до плазмина
Вектор экспрессии
Вектор секреции pPICZαA, приобретенный у Invitrogene Corporation (Карлсбад, Калифорния), использовали для прямой экспрессии и секреции рекомбинантного микроплазминогена человека в Pichia pastoris.
Этот вектор содержал сигнал секреции препропептида α-фактора Saccharomyces cerevisiae. Последовательность распознавания XhoI присутствовала на COOH-конце сигнала секреции α-фактора непосредственно перед сайтом Lys-Arg, который расщепляется Kex2 с удалением сигнала секреции из зрелого белка. Этот сайт рестрикции XhoI можно применять для клонирования представляющего интерес гена наравне с сайтом расщепления Kex2 путем синтеза гена с сайтами распознавания XhoI и Kex2 на его 5′ конце. Представляющий интерес рекомбинантный ген будет затем экспрессироваться с нативным NH2-концом. Сконструированный непосредственно ниже сигнала секреции α-фактора в pPICZαA вектор являлся сайтом множественного клонирования с сайтами распознавания для ферментов рестрикции EcoRI, SfiI, KpnI, SacII и XbaI для облегчения клонирования гетерологичных генов.
Синтез генов
Для увеличения экспрессии микроплазминогена человека в Pichia pastoris гены, кодирующие микроплазминоген человека и его варианты, синтезировали de novo, принимая во внимание предпочтительную частоту использования кодонов Pichia pastoris.
Для конструирования кодон-оптимизированной последовательности гена аминокислотную последовательность микроплазминогена человека (SEQ ID NO:19) вносили в программу Gene Designer, которая разработана DNA2.0 (Менло-Парк, Калифорния) и находится в свободном доступе в интернете. Эту последовательность обратно считывали в последовательность ДНК с использованием предоставленной с программой таблицы частоты использования кодонов Pichia pastoris. Нуклеотидную последовательность затем проверяли вручную и доводили до лучшего соответствия частоты использования кодонов Escherichia coli (SEQ ID NO:20). Кроме того, по возможности удаляли палиндромные последовательности из 6 пар оснований и нуклеотидные повторы. На 5′ конце добавляли сайт рестрикции XhoI и сайт расщепления Kex2 и на 3′ конце добавляли сайт рестрикции XbaI.
Мутации вводили путем сайт-направленного мутагенеза с применением набора для сайт-направленного мутагенеза QuikChange II от Agilent (Ла-Хойя, Калифорния) в последовательность микроплазминогена дикого типа или последовательность вариантного микроплазминогена, в которой уже была(и) заменена(ы) конкретная(ые) другая(ие) аминокислота(ы). Штамм E.coli TOP10 (Invitrogen) трансформировали смесью для сайт-направленного мутагенеза и отбирали устойчивые к ампициллину клоны. Определение последовательностей полученных плазмидных клонов подтверждало точный мутагенез целевой кодирующей области микроплазминогена, а также отсутствие нежелательных мутаций в кодирующей области.
Для сайт-направленного мутагенеза применяли следующие праймеры:
Мутация Val1Ile
GAAGTGTCCAGGTCGTATTGTCGGTGGCTGTGTGGCTC (смысловой; SEQ ID NO:21) и
GAGCCACACAGCCACCGACAATACGACCTGGACACTTC (антисмысловой; SEQ ID NO:22)
В первом варианте валин в положении 1 замещен изолейцином. Val1 кодируется кодоном GTT в положениях 58-60. Нуклеотиды GTT (положения 58-60) меняли на ATT с заменой Val1 на Ile в белке микроплазминогена (нуклеотидная последовательность приведена в SEQ ID NO:23, а расшифрованная аминокислотная последовательность в SEQ ID NO:24).
Экспрессия вариантов микроплазминогена и активация до плазмина
Варианты микроплазминогена и активированные варианты микроплазмина получали, по сути, следуя процедуре, которая описана в Примере 2 WO 02/50290.
Перед активацией мутанты микроплазминогена очищали с помощью иммуноаффинности непосредственно из супернатантов Pichia pastoris. Мышиное антитело к микроплазмину человека (индуцируемое у мышей Balb/c при использовании микроплазмина как антигена; продуцируемое клеточной линией гибридомы 5D10A4, доступное от ThromboGenics N.V.) связывали на сефарозных бусинах согласно протоколу №71500015 AD от GE Healthcare. Согласно этому протоколу 7,5 мл смолы для иммуноаффинной хроматографии получали из 45 мг антитела и упаковывали в колонку XK 16/20. На аффинную колонку 5D10A4 непосредственно нагружали 200-400 мл неочищенного супернатанта (отфильтрованного через фильтр 0,2 мкм из культуры Pichia/pH 6,0). После этапа промывки (100 мМ KH2PO4, 0,5M NaCl, pH 6,2, 10 объемов колонки) вариант микроплазминогена элюировали с 0,2M глицин-HCl, pH буфера 3,0.
Элюат (фракции 4-6) нейтрализовывали и подвергали диализу против 25 мМ натрий-фосфатного буфера, pH 7,2.
Аминокислотные последовательности и нуклеотидные последовательности описанных выше видов микроплазминогена дикого типа и вариантного микроплазминогена приведены ниже.
SEQ ID NO:19 - Аминокислотная последовательность человеческого микроплазминогена дикого типа
apsfdcgkpqvepkkcpgrvvggcvahphswpwqvslrtrfgmhfcggtlispewvltaahcleksprpssykvilgahqevnlephvqeievsrlfleptrkdiallklsspavitdkvipaclpspnyvvadrtecfitgwgetqgtfgagllkeaqlpvienkvcnryeflngrvqstelcaghlaggtdscqgdsggplvcfekdkyilqgvtswglgcarpnkpgvyvrvsrfvtwiegvmrnn
SEQ ID NO:20 - Искусственная последовательность нуклеиновой кислоты с оптимизированной частотой использования кодона для экспрессии в Pichia. Последовательность нуклеиновой кислоты кодирует аминокислотную последовательность человеческого микроплазминогена дикого типа SEQ ID NO:19
GCACCTTCATTCGACTGTGGTAAGCCTCAGGTCGAACCTAAGAAGTGTCCAGGTCGTGTTGTCGGTGGCTGTGTGGCTCATCCTCATTCTTGGCCTTGGCAAGTGTCTCTTAGAACTAGATTTGGTATGCACTTCTGTGGTGGCACCTTGATCTCACCTGAATGGGTCTTAACCGCAGCTCATTGTCTGGAGAAGTCACCACGTCCATCTTCATACAAGGTCATCCTTGGCGCACATCAGGAAGTCAATCTTGAGCCTCATGTTCAGGAGATCGAAGTCTCTCGTTTGTTCTTGGAACCAACTCGTAAAGACATTGCTCTTCTGAAGCTGTCATCTCCTGCCGTGATTACCGACAAGGTAATTCCTGCCTGCTTGCCTAGTCCTAATTACGTCGTTGCCGACCGTACCGAATGCTTCATTACTGGTTGGGGTGAGACTCAAGGTACGTTCGGTGCTGGTCTGTTGAAAGAAGCACAATTACCTGTGATTGAGAACAAGGTTTGTAACAGATACGAGTTCCTGAATGGTCGTGTTCAGTCCACTGAGTTGTGTGCAGGTCACCTTGCAGGTGGTACTGATAGTTGTCAAGGTGATTCTGGTGGACCACTGGTGTGCTTCGAGAAGGATAAGTACATCTTACAAGGTGTTACGTCTTGGGGTCTTGGATGTGCTCGTCCTAACAAGCCAGGTGTCTACGTCAGAGTCTCCAGATTCGTAACTTGGATCGAAGGTGTCATGCGTAACAACTAA
SEQ ID NO:23 - Вариант микроплазминогена с заменой Val1Ile (мутантный кодон показан жирным курсивом)
GCACCTTCATTCGACTGTGGTAAGCCTCAGGTCGAACCTAAGAAGTGTCCAGGTCGTATTGTCGGTGGCTGTGTGGCTCATCCTCATTCTTGGCCTTGGCAAGTGTCTCTTAGAACTAGATTTGGTATGCACTTCTGTGGTGGCACCTTGATCTCACCTGAATGGGTCTTAACCGCAGCTCATTGTCTGGAGAAGTCACCACGTCCATCTTCATACAAGGTCATCCTTGGCGCACATCAGGAAGTCAATCTTGAGCCTCATGTTCAGGAGATCGAAGTCTCTCGTTTGTTCTTGGAACCAACTCGTAAAGACATTGCTCTTCTGAAGCTGTCATCTCCTGCCGTGATTACCGACAAGGTAATTCCTGCCTGCTTGCCTAGTCCTAATTACGTCGTTGCCGACCGTACCGAATGCTTCATTACTGGTTGGGGTGAGACTCAAGGTACGTTCGGTGCTGGTCTGTTGAAAGAAGCACAATTACCTGTGATTGAGAACAAGGTTTGTAACAGATACGAGTTCCTGAATGGTCGTGTTCAGTCCACTGAGTTGTGTGCAGGTCACCTTGCAGGTGGTACTGATAGTTGTCAAGGTGATTCTGGTGGACCACTGGTGTGCTTCGAGAAGGATAAGTACATCTTACAAGGTGTTACGTCTTGGGGTCTTGGATGTGCTCGTCCTAACAAGCCAGGTGTCTACGTCAGAGTCTCCAGATTCGTAACTTGGATCGAAGGTGTCATGCGTAACAACTAA
SEQ ID NO:24 - Расшифрованная аминокислотная последовательность SEQ ID NO:23 (введенная мутация по аминокислоте указана жирным шрифтом/курсивом и подчеркнута)
APSFDCGKPQVEPKKCPGRIVGGCVAHPHSWPWQVSLRTRFGMHFCGGTLISPEWVLTAAHCLEKSPRPSSYKVILGAHQEVNLEPHVQEIEVSRLFLEPTRKDIALLKLSSPAVITDKVIPACLPSPNYVVADRTECFITGWGETQGTFGAGLLKEAQLPVIENKVCNRYEFLNGRVQSTELCAGHLAGGTDSCQGDSGGPLVCFEKDKYILQGVTSWGLGCARPNKPGVYVRVSRFVTWIEGVMRNN
Результаты:
Значения kкат и Kм, полученные для различных мутантов микроплазмина, приведены в Таблице 1 ниже.
Таблица 1.
ПРИМЕР 2 Терапевтическая эффективность вариантов плазмина в моделях in vitro или in vivo
2.1 Эффект вариантов плазмина на размер церебрального инфаркта
Эффективность вариантов плазмина настоящего изобретения при снижении размера церебрального инфаркта может быть продемонстрирована в мышиной модели церебрального инфаркта, как, например, описанной в Примере 2 WO 00/18436 или согласно Welsh et al. (1987, J Neurochem 49, 846-851). Благоприятный эффект плазмина дикого типа на размер церебрального инфаркта был продемонстрирован в Примере 5 WO 00/18436. Аналогичный эксперимент проводили с любым из вариантов плазмина в соответствии с настоящим изобретением и благоприятный эффект этих вариантов плазмина измеряли и сравнивали с благоприятным эффектом плазмина дикого типа.
2.2 Тромболитическая активность вариантов плазмина in vivo
Для демонстрации in vivo тромболитической активности вариантов плазмина настоящего изобретения может быть использована кроличья модель тромболиза с экстракорпоральной петлей (Пример 6 WO 02/50290; Hotchkiss et al., 1987, Thromb Haemost 58, 107 - Abstract 377), модель тромбоза, индуцированного медной спиралью в огибающей ветви коронарной артерии собаки (Пример 8 WO 02/50290; Bergmann et al., 1983, Science 220, 1181-1183) или модель тромбоза яремной вены кролика (Collen et al., 1983, J Clin Invest 71, 368-376). С помощью этих моделей демонстрировали благоприятный эффект плазмина дикого типа на тромболиз, как описано в Примерах 7 и 9 WO 00/18436 и Collen et al. (1983). Сходные эксперименты проводили с любым из вариантов плазмина в соответствии с настоящим изобретением и благоприятный эффект этих вариантов плазмина измеряли и сравнивали с благоприятным эффектом плазмина дикого типа.
2.3 Тромболитическая активность вариантов плазмина in vitro
Модель закупорки периферической артерии (P AO) in vitro описана в Примере 6 WO 01/36609, и в данной модели демонстрировали тромболитическую эффективность плазмина дикого типа. Сходный эксперимент проводили с любым из вариантов плазмина в соответствии с настоящим изобретением и благоприятный эффект этих вариантов плазмина на тромболиз закупорок периферических артерий измеряли и сравнивали с благоприятным эффектом плазмина дикого типа.
2.4 Разжижение стекловидного тела глаза и заднее отслоение стекловидного тела, индуцированные вариантами плазмина
В Примере 5 WO 2004/052228 раскрыт анализ для определения эффективности, а также эффективность микроплазмина в разжижении стекловидного тела в глазах свиньи после смерти. В Примере 6 WO 2004/052228 раскрыт анализ для определения эффективности, а также эффективность микроплазмина в индукции заднего отслоения стекловидного тела (PVD) в глазах человека после смерти. Индукцию разжижения стекловидного тела и PVD с помощью вариантов плазмина в соответствии с настоящим изобретением демонстрировали в сходных посмертных моделях.
2.5 PVD in vivo, индуцированное вариантами плазмина
В Примере 7 WO 2004/052228 раскрыт анализ для определения эффективности, а также эффективность микроплазмина в индукции PVD в кошачьей модели in vivo. Индукцию PVD вариантами плазмина настоящего изобретения демонстрировали в сходной модели in vivo.
Интравитреальная инъекция варианта плазмина Val1Ile (V1I)
Эффект варианта микроплазмина V1I на заднее отслоение стекловидного тела (PVD) исследовали после интравитреальной инъекции. Кратко, взрослых мышей C57BL/6 наркотизировали с применением нембутала (0,6 мг/кг веса тела). Интравитреальные инъекции осуществляли с применением набора для внутриглазных инъекций, 10 мкл шприца со скошенной иглой 35G, а также устройства для инъекций с микронасосом. Каждую инъекцию одного мкл носителя, содержащего либо микроплазмин дикого типа, либо вариант микроплазмина V1I в различных концентрациях, осуществляли под препаровальной лупой при нажатии педального переключателя. Кончик иглы пропускали позади склеры к лимбу и располагали так, чтобы избежать прикосновения к хрусталикам. Нажатие педального переключателя вызывало впрыскивание инъецируемого продукта в полость среднего отдела стекловидного тела.
Через пять после инъекции мышей умерщвляли и их глаза фиксировали в 1% параформальдегиде. Глаза погружали в парафиновый воск с последующим изготовлением срезов и окрашивали срезы с помощью фуксинсернистой кислоты-реактива Шиффа (PAS). Для оценки индукции PVD проводили морфологический анализ по всему срезу глаза с применением световой микроскопии.
Влияние интравитреальной инъекции микроплазмина и V1I
Иллюстративное изображение, полученное с помощью световой микроскопии, глаз с инъекцией V1I через 5 дней после инъекций показано на фигуре 3. Окрашенные с помощью PAS срезы глазных яблок демонстрировали отслоение стекловидного тела от поверхности сетчатки после инъекции V1I. Инъецированные микроплазмином животные демонстрировали~20% индукцию PVD по сравнению с~50% индукцией PVD после инъекции V1I (таблица 2). Данное очевидное 2-3-кратное повышение индукции PVD наблюдали при всех тестируемых концентрациях.
Таблица 2. Индукция PVD с помощью V1I и микроплазмина дикого типа в глазах мышей.
Реферат
Изобретение относится к области биотехнологии и может быть использовано для получения вариантов плазминогена и плазмина. Получают вариант плазминогена, содержащий сайт активации и каталитический домен, в котором каталитический домен содержит замену валина на изолейцин в положении 1 каталитического домена плазмина человека или в положении, соответствующем таковому в каталитическом домене плазмина, отличном от плазмина человека, где указанный каталитический домен плазмина человека начинается с аминокислоты валин в положении 1, которая является той же аминокислотой валин, которая находится в положении 562 Glu-плазминогена человека с SEQ ID NO: 1. Изобретение позволяет получить аутопротеолитически стабильный вариант плазмина. 11 н. и 8 з.п. ф-лы, 14 ил., 3 табл., 2 пр.
Формула
(i) введение нуклеиновой кислоты, кодирующей плазминоген по любому из пп. 1 или 2, в подходящую клетку-хозяина, способную экспрессировать указанный плазминоген,
(ii) выращивание клетки-хозяина, полученной на этапе (i), в условиях и в течение времени, достаточных для экспрессии указанного плазминогена в указанной клетке-хозяине, и
(iii) сбор плазминогена, экспрессированного на этапе (ii).
(i) введение нуклеиновой кислоты, кодирующей плазминоген по любому из пп. 1 или 2, в подходящую клетку-хозяина, способную экспрессировать указанный плазминоген,
(ii) выращивание клетки-хозяина, полученной на этапе (i), в условиях и в течение времени, достаточных для экспрессии указанного плазминогена в указанной клетке-хозяине,
(iii) сбор плазминогена, экспрессированного на этапе (ii),
(iv) активация плазминогена из этапа (iii) до плазмина.
Документы, цитированные в отчёте о поиске
Экспрессия плазминогена и микроплазминогена в ряске

Комментарии