Композиции и способы с участием нуклеиновых кислот, нацеленных на нуклеиновые кислоты - RU2662932C2
Код документа: RU2662932C2
Чертежи








































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































Описание
С ПЕРЕКРЕСТНЫМИ ССЫЛКАМИ НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет по предварительной заявке на патент США №61/818386, поданной 1 мая 2013 г. [№ в патентном реестре: 44287-710.101], предварительной заявке на патент США №61/902723, поданной 11 ноября 2013 г. [№ в патентном реестре: 44287-710.103], предварительной заявке на патент США №61/818382, поданной 1 мая 2013 г. [№ в патентном реестре: 44287-712.101], предварительной заявке на патент США №61/859,661, поданной 29 июля 2013 г. [№ в патентном реестре: 44287-712.102], предварительной заявке на патент США №61/858767, поданной 26 июля 2013 г. [№ в патентном реестре: 44287-713.102], предварительной заявке на патент США №61/822002, поданной 10 мая 2013 г. [№ в патентном реестре: 44287-717.101], предварительной заявке на патент США №61/832690, поданной 7 июня 2013 г. [№ в патентном реестре: 44287-719.101], предварительной заявке на патент США №61/906211, поданной 19 ноября 2013 г. [№ в патентном реестре: 44287-719.102], предварительной заявке на патент США №61/900311, поданной 5 ноября 2013 г. [№ в патентном реестре: 44287-719.103], предварительной заявке на патент США №61/845714, поданной 12 июля 2013 г. [№ в патентном реестре: 44287-721.101], предварительной заявке на патент США №61/883804, поданной 27 сентября 2013 г. [№ в патентном реестре: 44287-721.102], предварительной заявке на патент США №61/781598, поданной 14 марта 2013 г. [№ в патентном реестре: 44287-722.101], предварительной заявке на патент США №61/899712, поданной 4 ноября 2013 г. [№ в патентном реестре: 44287-727.101], предварительной заявке на патент США №61/865743, поданной 14 августа 2013 г. [№ в патентном реестре: 44287-733.101], предварительной заявке на патент США №61/907777, поданной 22 ноября 2013 г. [№ в патентном реестре: 44287-734.101], предварительной заявке на патент США №61/903,232, поданной 12 ноября 2013 г. [№ в патентном реестре: 44287-751.101], предварительной заявке на патент США №61/906335, поданной 19 ноября 2013 г. [№ в патентном реестре: 44287-752.101], предварительной заявке на патент США №61/907216, поданной 21 ноября 2013 г. [№ в патентном реестре: 44287-753.101], содержание которых полностью включено в настоящий документ посредством ссылки
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящий документ включает перечень последовательностей, представленный в электронном виде в формате ASCII и полностью включенный в настоящий документ посредством ссылки. Указанный файл в формате ASCII, созданный 10 марта 2014 г., имеет название «44287-722-601_SeqList», и его размер составляет 7828964 бита.
ОБЛАСТЬ ТЕХНИКИ
[0003] Геномная инженерия может относиться к изменению генома путем удаления, вставки, мутации или замены конкретных последовательностей нуклеиновых кислот. Указанное изменение может быть геноспецифическим или происходить в специфической локализации. В геномной инженерии могут использоваться нуклеазы для расщепления нуклеиновой кислоты, с созданием таким образом сайта для изменения. Также включено конструирование негеномной нуклеиновой кислоты. Белок, содержащий нуклеазный домен, может связывать и расщеплять целевую нуклеиновую кислоту за счет формирования комплекса с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту. В одном примере при указанном расщеплении могут происходить двуцепочечные разрывы в указанной целевой нуклеиновой кислоте. Репарация нуклеиновой кислоты может происходить, например, за счет эндогенного механизма негомологичного соединения концов (NHEJ). В дополнительном примере может встраиваться часть нуклеиновой кислоты. Модификации нуклеиновых кислот, которые нацелены на нуклеиновые кислоты, и сайт-специфических полипептидов могут обеспечивать введение новых функций, подходящих для применения в геномной инженерии.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0004] Согласно одному аспекту в описании предложена сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержащая: мутацию в Р-домене указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанный Р-домен начинается в направлении 3' от последнего спаренного нуклеотида дуплекса между повтором CRISPR и последовательностью tracrRNA (транс-активирующей CRISPR-PHK) указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, дополнительно содержит линкерную последовательность. Согласно некоторым вариантам реализации указанная линкерная последовательность соединяет повтор CRISPR и последовательность tracrRNA. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту представляет собой выделенную сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой рекомбинантную сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, способна гибридизоваться с целевой нуклеиновой кислотой. Согласно некоторым вариантам реализации указанный Р-домен содержит 2 смежных нуклеотида. Согласно некоторым вариантам реализации указанный Р-домен содержит 3 смежных нуклеотида. Согласно некоторым вариантам реализации указанный Р-домен содержит 4 смежных нуклеотида. Согласно некоторым вариантам реализации указанный Р-домен содержит 5 смежных нуклеотидов. Согласно некоторым вариантам реализации указанный Р-домен содержит 6 или большее количество смежных нуклеотидов. Согласно некоторым вариантам реализации указанный Р-домен начинается через 1 нуклеотид в направлении 3' от последнего спаренного нуклеотида дуплекса. Согласно некоторым вариантам реализации указанный Р-домен начинается через 2 нуклеотида в направлении 3' от последнего спаренного нуклеотида дуплекса. Согласно некоторым вариантам реализации указанный Р-домен начинается через 3 нуклеотида в направлении 3' от последнего спаренного нуклеотида дуплекса. Согласно некоторым вариантам реализации указанный Р-домен начинается через 4 нуклеотида в направлении 3' от последнего спаренного нуклеотида дуплекса. Согласно некоторым вариантам реализации указанный Р-домен начинается через 5 нуклеотидов в направлении 3' от последнего спаренного нуклеотида дуплекса. Согласно некоторым вариантам реализации указанный Р-домен начинается через 6 или большее количество нуклеотидов в направлении 3' от последнего спаренного нуклеотида дуплекса. Согласно некоторым вариантам реализации указанная мутация включает одну или большее количество мутаций. Согласно некоторым вариантам реализации указанная одна или большее количество мутаций являются смежными. Согласно некоторым вариантам реализации указанная одна или большее количество мутаций отделены друг от друга. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, способность гибридизоваться с другим примыкающим к протоспейсеру мотивом (РАМ). Согласно некоторым вариантам реализации указанный другой примыкающий к протоспейсеру мотив содержит по меньшей мере 4 нуклеотида. Согласно некоторым вариантам реализации указанный другой примыкающий к протоспейсеру мотив содержит по меньшей мере 5 нуклеотидов. Согласно некоторым вариантам реализации указанный другой примыкающий к протоспейсеру мотив содержит по меньшей мере 6 нуклеотидов. Согласно некоторым вариантам реализации указанный другой примыкающий к протоспейсеру мотив содержит по меньшей мере 7 или большее количество нуклеотидов. Согласно некоторым вариантам реализации указанный другой примыкающий к протоспейсеру мотив содержит две несмежных области. Согласно некоторым вариантам реализации указанный другой примыкающий к протоспейсеру мотив содержит три несмежных области. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, связываться с целевой нуклеиновой кислотой с меньшей константой диссоциации относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, связываться с целевой нуклеиновой кислотой с большей специфичностью относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы уменьшать связывание сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, с неспецифической последовательностью в целевой нуклеиновой кислоте относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, дополнительно содержит две шпильки, причем одна из двух шпилек содержит дуплекс между полинуклеотидом, содержащим последовательность, по меньшей мере на 50% идентичную последовательности CRISPR РНК на протяжении 6 последовательных нуклеотидов, и полинуклеотидом, содержащим последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов; причем одна из двух шпилек расположена в направлении 3' от первой шпильки, а вторая шпилька содержит сконструированный Р-домен. Согласно некоторым вариантам реализации указанная вторая шпилька способна дедуплицироваться, когда указанную нуклеиновую кислоту приводят в контакт с целевой нуклеиновой кислотой. Согласно некоторым вариантам реализации указанный Р-домен способна гибридизоваться с первым полинуклеотидом, при этом указанный первый полинуклеотид содержит область сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, гибридизации с вторым полинуклеотидом, при этом указанный второй полинуклеотид содержит целевую нуклеиновую кислоту, и специфической гибридизации с первым или вторым полинуклеотидом. Согласно некоторым вариантам реализации указанный первый полинуклеотид содержит последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанный первый полинуклеотид расположен в направлении 3' от дуплекса между полинуклеотидом, содержащим последовательность, по меньшей мере на 50% идентичную последовательности повтора CRISPR на протяжении 6 последовательных нуклеотидов, и полинуклеотидом, содержащим последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанный второй полинуклеотид содержит примыкающий к протоспейсеру мотив. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, способна связываться с сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанная мутация включает вставку одного или большего количества нуклеотидов в Р-домен. Согласно некоторым вариантам реализации указанная мутация включает удаление одного или большего количества нуклеотидов из Р-домена. Согласно некоторым вариантам реализации указанная мутация включает мутацию одного или большего количества нуклеотидов. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать гибридизацию нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, с другим примыкающим к протоспейсеру мотивом. Согласно некоторым вариантам реализации указанный другой примыкающий к протоспейсеру мотив включает примыкающий к протоспейсеру мотив, выбранный из группы, состоящей из: 5'-NGGNG-3', 5'-NNAAAAW-3', 5'-NNNNGATT-3', 5'-GNNNCNNA-3', и 5'-NNNACA-3' или любой их комбинации. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать связывание сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, с меньшей константой диссоциации относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать связывание сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, с большей специфичностью относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы уменьшать связывание сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту с неспецифической последовательностью в целевой нуклеиновой кислоте относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту.
[0005] Согласно одному аспекту в описании предложен способ модификации целевой нуклеиновой кислоты, включающий приведение целевой нуклеиновой кислоты в контакт со сконструированной нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, содержащей: мутацию в Р-домене указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, и модификацию целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный способ дополнительно включает встраивание донорного полинуклеотида в целевую нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная модификация включает расщепление целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная модификация включает модификацию транскрипции целевой нуклеиновой кислоты.
[0006] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую мутацию в Р-домене указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту.
[0007] Согласно одному аспекту в описании предложен набор, содержащий: сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую: мутацию в Р-домене указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит сайт-специфический полипептид. Согласно некоторым вариантам реализации указанный набор дополнительно содержит донорный полинуклеотид. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0008] Согласно одному аспекту в описании предложена сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержащая мутацию в области петли нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная петля расположен в дуплексе между повтором CRISPR и последовательностью tracrRNA указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, дополнительно содержит линкерную последовательность. Согласно некоторым вариантам реализации указанная линкерная последовательность соединяет повтор CRISPR и последовательность tracrRNA. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой выделенную сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой рекомбинантную сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере 1 неспаренный нуклеотид на повторе CRISPR и 1 неспаренный нуклеотид на последовательности tracrRNA. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере 1 неспаренный нуклеотид на повторе CRISPR и по меньшей мере 2 неспаренных нуклеотида на последовательности tracrRNA. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере 1 неспаренный нуклеотид на повторе CRISPR и по меньшей мере 3 неспаренных нуклеотида на последовательности tracrRNA. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере 1 неспаренный нуклеотид на повторе CRISPR и по меньшей мере 4 неспаренных нуклеотида на последовательности tracrRNA. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере один 1 неспаренный нуклеотид на повторе CRISPR и по меньшей мере 5 неспаренных нуклеотидов на последовательности tracrRNA. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере 2 неспаренных нуклеотида на повторе CRISPR и 1 неспаренный нуклеотид на последовательности tracrRNA. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на повторе CRISPR, и по меньшей мере 2 неспаренных нуклеотида на последовательности tracrRNA. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере 4 неспаренных нуклеотида на повторе CRISPR и по меньшей мере 3 неспаренных нуклеотида на последовательности tracrRNA. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере 5 неспаренных нуклеотидов на повторе CRISPR и по меньшей мере 4 неспаренных нуклеотида на последовательности tracrRNA. Согласно некоторым вариантам реализации указанная петля содержит по меньшей мере один нуклеотид на повторе CRISPR, способный формировать неоднозначную пару по меньшей мере с одним нуклеотидом последовательности tracrRNA. Согласно некоторым вариантам реализации указанная мутация содержит одну или большее количество мутаций. Согласно некоторым вариантам реализации указанная одна или большее количество мутаций являются смежными. Согласно некоторым вариантам реализации указанная одна или большее количество мутаций отделены друг от друга. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, связываться с другим сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанный другой сайт-специфический полипептид представляет собой гомолог Cas9. Согласно некоторым вариантам реализации указанный другой сайт-специфический полипептид представляет собой мутантный вариант Cas9. Согласно некоторым вариантам реализации последовательность аминокислот указанного другого сайт-специфического полипептида на 10% идентична последовательности аминокислот Cas9 в нуклеазном домене, выбранном из группы, состоящей из: нуклеазного домена RuvC, нуклеазного домена HNH или любой их комбинации. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, гибридизоваться с другим примыкающим к протоспейсеру мотивом. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, связываться с сайт-специфическим полипептидом с меньшей константой диссоциации относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы обеспечивать сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, связываться с сайт-специфическим полипептидом с большей специфичностью относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы позволять сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, направлять сайт-специфический полипептид для расщепления целевой нуклеиновой кислоты с большей специфичностью относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы уменьшать связывание сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту с неспецифической последовательностью в целевой нуклеиновой кислоте относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, способна гибридизоваться с целевой нуклеиновой кислотой. Согласно некоторым вариантам реализации указанная мутация содержит вставку из одного или большего количества нуклеотидов в петле. Согласно некоторым вариантам реализации указанная мутация включает удаление одного или большего количества нуклеотидов из петли. Согласно некоторым вариантам реализации указанная мутация включает мутацию одного или большего количества нуклеотидов. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы позволять сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, гибридизоваться с другим примыкающим к протоспейсеру мотивом относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы позволять сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, связываться с сайт-специфическим полипептидом с меньшей константой диссоциации относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы позволять сконструированной нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, связываться с сайт-специфическим полипептидом с большей специфичностью относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная мутация осуществлена таким образом, чтобы уменьшать связывание сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту с неспецифической последовательностью в целевой нуклеиновой кислоте относительно несконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту.
[0009] Согласно одному аспекту в описании предложен способ модификации целевой нуклеиновой кислоты, включающий приведение целевой нуклеиновой кислоты в контакт со сконструированной нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, содержащей мутацию в области петли нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; и модификацию целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный способ дополнительно включает встраивание донорного полинуклеотида в целевую нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная модификация включает расщепление целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная модификация включает модификацию транскрипции целевой нуклеиновой кислоты.
[0010] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую: мутацию в области петли нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; и модификацию целевой нуклеиновой кислоты.
[0011] Согласно одному аспекту в описании предложен набор, содержащий: сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую: мутацию в области петли нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; модификацию целевой нуклеиновой кислоты; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит сайт-специфический полипептид. Согласно некоторым вариантам реализации указанный набор дополнительно содержит донорный полинуклеотид. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0012] Согласно одному аспекту в описании предложен способ получения меченой донорным полинуклеотидом клетки, включающий: расщепление целевой нуклеиновой кислоты в клетке с применением комплекса, содержащего сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, встраивание донорного полинуклеотида в расщепленную целевую нуклеиновую кислоту, размножение клетки, несущей указанный донорный полинуклеотид, и определение происхождения указанной донорным полинуклеотидом клетки. Согласно некоторым вариантам реализации указанный способ реализуют in vivo. Согласно некоторым вариантам реализации указанный способ реализуют in vitro. Согласно некоторым вариантам реализации указанный способ реализуют in situ. Согласно некоторым вариантам реализации указанное размножение обеспечивает получение популяции клеток. Согласно некоторым вариантам реализации указанное размножение обеспечивает получение клеточной линии. Согласно некоторым вариантам реализации указанный способ дополнительно включает определение последовательности нуклеиновой кислоты в клетке. Согласно некоторым вариантам реализации указанная последовательность нуклеиновой кислоты определяет происхождение указанной клетки. Согласно некоторым вариантам реализации указанное определение включает определение генотипа указанной клетки. Согласно некоторым вариантам реализации указанное размножение включает дифференцировку указанной клетки. Согласно некоторым вариантам реализации указанное размножение включает де-дифференцировку указанной клетки. Согласно некоторым вариантам реализации указанное размножение включает дифференцировку указанной клетки и затем де-дифференцировку указанной клетки. Согласно некоторым вариантам реализации указанное размножение включает пересев указанной клетки. Согласно некоторым вариантам реализации указанное размножение включает индуцирование деления указанной клетки. Согласно некоторым вариантам реализации указанное размножение включает индуцирование вхождения указанной клетки в клеточный цикл. Согласно некоторым вариантам реализации указанное размножение включает формирование метастазов указанной клеткой. Согласно некоторым вариантам реализации указанное размножение включает дифференцировку плюрипотентной клетки в дифференцированную клетку. Согласно некоторым вариантам реализации указанная клетка представляет собой дифференцированную клетку. Согласно некоторым вариантам реализации указанная клетка представляет собой де-дифференцированную клетку. Согласно некоторым вариантам реализации указанная клетка представляет собой стволовую клетку. Согласно некоторым вариантам реализации указанная клетка представляет собой плюрипотентную стволовую клетку. Согласно некоторым вариантам реализации указанная клетка представляет собой клетку эукариотической клеточной линии. Согласно некоторым вариантам реализации указанная клетка представляет собой клетку первичной клеточной линии. Согласно некоторым вариантам реализации указанная клетка представляет собой клетку полученной от пациента клеточной линии. Согласно некоторым вариантам реализации указанный способ дополнительно включает трансплантацию указанной клетки в организм. Согласно некоторым вариантам реализации указанный организм представляет собой человека. Согласно некоторым вариантам реализации указанный организм представляет собой млекопитающее. Согласно некоторым вариантам реализации указанный организм выбрана из группы, состоящей из: человека, собаки, крысы, мыши, курицы, рыбы, кошки, растения и примата. Согласно некоторым вариантам реализации указанный способ дополнительно включает выбор клетки. Согласно некоторым вариантам реализации указанный донорный полинуклеотид встраивают в целевую нуклеиновую кислоту, экспрессируемую в одном состоянии клетки. Согласно некоторым вариантам реализации указанный донорный полинуклеотид встраивают в целевую нуклеиновую кислоту, экспрессируемую в совокупности клеточных типов. Согласно некоторым вариантам реализации указанный донорный полинуклеотид встраивают в целевую нуклеиновую кислоту, экспрессирующуюся в плюрипотентном состоянии. Согласно некоторым вариантам реализации указанный донорный полинуклеотид встраивают в целевую нуклеиновую кислоту, экспрессируемую в дифференцированном состоянии.
[0013] Согласно одному аспекту в описании предложен способ получения клеточной линии клонального происхождения, включающий: введение в клетку комплекса, содержащего: сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, приведение в контакт указанного комплекса с целевой нуклеиновой кислотой, расщепление целевой нуклеиновой кислоты, при этом указанное расщепление осуществляется указанным комплексом, с получением таким образом расщепленной целевой нуклеиновой кислоты, встраивание донорного полинуклеотида в расщепленную целевую нуклеиновую кислоту, размножение указанной клетки, при этом указанное размножение обеспечивает получение клеточной линии клепального происхождения. Согласно некоторым вариантам реализации указанная клетка выбрана из группы, состоящей из: клетки HeLa, клетки яичника китайского хомячка, клетки 293-Т, феохромоцитомы, фибробласта нейробластомы, рабдомиосаркомы, клетки ганглия заднего корешка, клетки NSO, CV-I (ATCC CCL 70), COS-I (ATCC CRL 1650), COS-7 (АТСС CRL 1651), СНО-K1 (ATCC CCL 61), 3Т3 (ATCC CCL 92), NIH/3T3 (ATCC CRL 1658), HeLa (ATCC CCL 2), С 1271 (ATCC CRL 1616), BS-C-I (ATCC CCL 26), MRC-5 (ATCC CCL 171), L-клетки, HEK-293 (ATCC CRL1 573) и PC 12 (ATCC CRL-1721), HEK293T (ATCC CRL-11268), RBL (ATCC CRL-1378), SH-SY5Y (ATCC CRL-2266), MDCK (ATCC CCL-34), SJ-RH30 (ATCC CRL-2061), HepG2 (ATCC HB-8065), ND7/23 (ECACC 92090903), СНО (ECACC 85050302), Vera (ATCC CCL 81), Caco-2 (ATCC HTB 37), K562 (ATCC CCL 243), Jurkat (ATCC TIB-152),

[0014] Согласно одному аспекту в описании предложен способ мультиплексного анализа клеточного типа, включающий: расщепление по меньшей мере одной целевой нуклеиновой кислоты в двух или большем количестве клеток с применением комплекса, содержащего сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, для получения двух расщепленных целевых нуклеиновых кислот, встраивание разных донорных полинуклеотидов в каждую из расщепленных целевых нуклеиновых кислот и анализ указанных двух или большего количества клеток. Согласно некоторым вариантам реализации указанный анализ включает одновременный анализ двух или большего количества клеток. Согласно некоторым вариантам реализации указанный анализ включает определение последовательности целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный анализ включает сравнение указанных двух или большего количества клеток. Согласно некоторым вариантам реализации указанный анализ включает определение генотипа указанных двух или большего количества клеток. Согласно некоторым вариантам реализации указанная клетка представляет собой дифференцированную клетку. Согласно некоторым вариантам реализации указанная клетка представляет собой де-дифференцированную клетку. Согласно некоторым вариантам реализации указанная клетка представляет собой стволовую клетку. Согласно некоторым вариантам реализации указанная клетка представляет собой плюрипотентную стволовую клетку. Согласно некоторым вариантам реализации указанная клетка представляет собой клетку эукариотической клеточной линии. Согласно некоторым вариантам реализации указанная клетка представляет собой клетку первичной клеточной линии. Согласно некоторым вариантам реализации указанная клетка представляет собой клетку полученной от пациента клеточной линии. Согласно некоторым вариантам реализации совокупность донорных полинуклеотидов встраивают в совокупность расщепленных целевых нуклеиновых кислот в клетке.
[0015] Согласно одному аспекту в описании предложена композиция, содержащая: сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую 3'-гибридизующееся удлинение и донорный полинуклеотид, при этом указанный донорный полинуклеотид гибридизуется с указанным 3'-гибридизующимся удлинением. Согласно некоторым вариантам реализации указанное 3'-гибридизующееся удлинение способно гибридизоваться по меньшей мере с 5 нуклеотидами, расположенными в направлении 3' от донорного полинуклеотида. Согласно некоторым вариантам реализации указанное 3'-гибридизующееся удлинение способно гибридизоваться по меньшей мере с 5 нуклеотидами расположенными в направлении 5' от донорного полинуклеотида. Согласно некоторым вариантам реализации указанное 3'-гибридизующееся удлинение способно гибридизоваться по меньшей мере с 5 смежными нуклеотидами в донорном полинуклеотиде. Согласно некоторым вариантам реализации указанное 3'-гибридизующееся удлинение способно гибридизоваться со всей последовательностью донорного полинуклеотида. Согласно некоторым вариантам реализации указанное 3'-гибридизующееся удлинение содержит матрицу обратной транскрипции. Согласно некоторым вариантам реализации указанная матрица обратной транскрипции выполнен с возможностью обратного транскрибирования обратной транскриптазой. Согласно некоторым вариантам реализации указанная композиция дополнительно содержит обратно-транскрибируемый ДНК-полинуклеотид. Согласно некоторым вариантам реализации указанный обратно-транскрибируемый ДНК-полинуклеотид способен гибридизоваться с матрицей обратной транскрипции. Согласно некоторым вариантам реализации указанный донорный полинуклеотид представляет собой ДНК. Согласно некоторым вариантам реализации указанное 3'-гибридизующееся удлинение представляет собой РНК. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой выделенную сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная сконструированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой рекомбинантную сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту.
[0016] Согласно одному аспекту в описании предложен способ введения донорного полинуклеотида в целевую нуклеиновую кислоту, включающий: приведение целевой нуклеиновой кислоты в контакт с композицией, содержащей: сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую 3'-гибридизующееся удлинение, и донорный полинуклеотид, при этом указанный допорный полинуклеотид гибридизуется с указанным 3'-гибридизующимся удлинением. Согласно некоторым вариантам реализации указанный способ дополнительно включает расщепление целевой нуклеиновой кислоты с получением расщепленной целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанное расщепление осуществляется сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанный способ дополнительно включает встраивание донорного полинуклеотида в расщепленную целевую нуклеиновую кислоту.
[0017] Согласно одному аспекту в описании предложена композиция, содержащая: эффекторный белок и нуклеиновую кислоту, при этом последовательность указанной нуклеиновой кислоты по меньшей мере на 50% идентична последовательности crRNA на протяжении 6 последовательных нуклеотидов, по меньшей мере на 50% идентична последовательности tracrRNA на протяжении 6 последовательных нуклеотидов; и ненативную последовательность, при этом указанная нуклеиновая кислота способна связываться с указанным эффекторным белком. Согласно некоторым вариантам реализации указанная композиция дополнительно содержит полипептид, последовательность аминокислот которого по меньшей мере на 10% идентична последовательности нуклеазного домена Cas9, при этом указанная нуклеиновая кислота связывается с указанным полипептидом. Согласно некоторым вариантам реализации последовательность аминокислот нуклеазного домена указанного полипептида по меньшей мере на 60% идентична последовательности нуклеазного домена Cas9. Согласно некоторым вариантам реализации указанный полипептид представляет собой Cas9. Согласно некоторым вариантам реализации указанная нуклеиновая кислота дополнительно содержит линкерную последовательность, при этом указанная линкерная последовательность соединяет последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная ненативная последовательность расположена в положении нуклеиновой кислоты, выбранном из группы, состоящей из: 5'-конца, 3'-конца или любой их комбинации. Согласно некоторым вариантам реализации указанная нуклеиновая кислота содержит две молекулы нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная нуклеиновая кислота содержит одну непрерывную молекулу нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная ненативная последовательность включает последовательность, связывающую связывающий CRISPR РНК белок. Согласно некоторым вариантам реализации указанная ненативная последовательность содержит связывающую последовательность, выбранную из группы, состоящей из: Cas5 РНК-связывающей последовательности, Cas6 РНК-связывающей последовательности, Csy4 РНК-связывающей последовательности или любой их комбинации. Согласно некоторым вариантам реализации указанный эффекторный белок содержит CRISPR РНК-связывающий белок. Согласно некоторым вариантам реализации последовательность аминокислот указанного эффекторного белка по меньшей мере на 15% идентична последовательности белка, выбранного из группы, состоящей из: Cas5, Cas6 и Csy4, или любой их комбинации. Согласно некоторым вариантам реализации РНК-последовательность аминокислот связывающего домена эффекторного белка по меньшей мере на 15% идентична последовательности РНК-связывающего домена белка, выбранного из группы, состоящей из: Cas5, Cas6 и Csy4, или любой их комбинации. Согласно некоторым вариантам реализации указанный эффекторный белок выбран из группы, состоящей из: Cas5, Cas6 и Csy4, или любой их комбинации. Согласно некоторым вариантам реализации указанный эффекторный белок дополнительно содержит одну или большее количество ненативных последовательностей. Согласно некоторым вариантам реализации указанная ненативная последовательность придает эффекторному белку ферментативную активность. Согласно некоторым вариантам реализации указанная ферментативная активность выбрана из группы, состоящей из: метилтрансферазной активности, деметилазной активности, ацетилирующей активности, деацетилирующей активности, убиквитинирующей активности, деубиквитинирующей активности, деаминирующей активности, дисмутазной активности, алкилирующей активности, депуринизирующей активности, окислительной активности, направленной на образование пиримидиновых димеров активности, транспозазной активности, рекомбиназной активности, полимеразной активности, лигазной активности, геликазной активности, фотолиазной активности или гликозилазной активности, ацилтрансферазной активности, деацетилазной активности, киназной активности, фосфатазной активности, убиквитинлигазной активности, деубиквитинирующей активности, аденилирующей активности, деаденилирующей активности, сумоилирующей активности, десумоилирующей активности, рибозилирующей активности, дерибозилирующей активности, миристоилирующей активности, ремоделирующей активности, протеазной активности, оксидоредуктазной активности, трансферазной активности, гидролазной активности, лиазной активности, изомеразной активности, синтазной активности, синтетазной активности, и демиристоилирующей активности или любой их комбинации. Согласно некоторым вариантам реализации указанная нуклеиновая кислота представляет собой РНК. Согласно некоторым вариантам реализации указанный эффекторный белок содержит гибридный белок, содержащий РНК-связывающий белок и ДНК-связывающий белок. Согласно некоторым вариантам реализации указанная композиция дополнительно содержит донорный полинуклеотид. Согласно некоторым вариантам реализации указанный донорный полинуклеотид прямо связывается с указанным ДНК-связывающим белком, и при этом указанный РНК-связывающий белок связывается с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации 5'-конец донорного полинуклеотида связывается с ДНК-связывающим белком. Согласно некоторым вариантам реализации 3'-конец донорного полинуклеотида связывается с ДНК-связывающим белком. Согласно некоторым вариантам реализации по меньшей мере 5 нуклеотидов донорного полинуклеотида связываются с ДНК-связывающим белком. Согласно некоторым вариантам реализации указанная нуклеиновая кислота представляет собой выделенную нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная нуклеиновая кислота представляет собой рекомбинантную нуклеиновую кислоту.
[0018] Согласно одному аспекту в описании предложен способ введения донорного полинуклеотида в целевую нуклеиновую кислоту, включающий: приведение целевой нуклеиновой кислоты в контакт с комплексом, содержащим сайт-специфический полипептид и композицию, включающую: эффекторный белок и нуклеиновую кислоту, при этом последовательность указанной нуклеиновой кислоты по меньшей мере на 50% идентична последовательности crRNA на протяжении 6 последовательных нуклеотидов, по меньшей мере на 50% идентична последовательности tracrRNA на протяжении 6 последовательных нуклеотидов; и ненативную последовательность, при этом указанная нуклеиновая кислота способна связываться с указанным эффекторным белком. Согласно некоторым вариантам реализации указанный способ дополнительно включает расщепление целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанное расщепление осуществляется сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанный способ дополнительно включает встраивание донорного полинуклеотида в целевую нуклеиновую кислоту.
[0019] Согласно одному аспекту в описании предложен способ модуляции целевой нуклеиновой кислоты, включающий: приведение целевой нуклеиновой кислоты в контакт с одним или большим количеством комплексов, причем каждый комплекс содержит сайт-специфический полипептид и композицию, включающую: эффекторный белок и нуклеиновую кислоту, при этом последовательность указанной нуклеиновой кислоты по меньшей мере на 50% идентична последовательности crRNA на протяжении 6 последовательных нуклеотидов, по меньшей мере на 50% идентична последовательности tracrRNA на протяжении 6 последовательных нуклеотидов; и ненативную последовательность, при этом указанная нуклеиновая кислота способна связываться с указанным эффекторным белком и модулировать целевую нуклеиновую кислоту. Согласно некоторым вариантам реализации последовательность аминокислот указанного сайт-специфического полипептида по меньшей мере на 10% идентична последовательности нуклеазного домена Cas9. Согласно некоторым вариантам реализации указанная модуляция осуществляется эффекторным белком. Согласно некоторым вариантам реализации указанная модуляция включает активность, выбранную из группы, состоящей из: метилтрансферазной активности, деметилазной активности, ацетилирующей активности, деацетилирующей активности, убиквитинирующей активности, деубиквитинирующей активности, деаминирующей активности, дисмутазной активности, алкилирующей активности, депуринизирующей активности, окислительной активности, направленной на образование пиримидиновых димеров активности, транспозазной активности, рекомбиназной активности, полимеразной активности, лигазной активности, геликазной активности, фотолиазной активности или гликозилазной активности, ацилтрансферазной активности, деацетилазной активности, киназной активности, фосфатазной активности, убиквитин- лигазной активности, деубиквитинирующей активности, аденилирующей активности, деаденилирующей активности, сумоилирующей активности, десумоилирующей активности, рибозилирующей активности, дерибозилирующей активности, миристоилирующей активности, ремоделирующей активности, протеазной активности, оксидоредуктазной активности, трансферазной активности, гидролазной активности, лиазной активности, изомеразной активности, синтазной активности, синтетазной активности, и демиристоилирующей активности или любой их комбинации. Согласно некоторым вариантам реализации указанный эффекторный белок содержит один или большее количество эффекторных белков.
[0020] Согласно одному аспекту в описании предложен способ детекции того, расположены ли два комплекса поблизости друг от друга, включающий: приведение в контакт первой нуклеиновой кислоты с первым комплексом, при этом указанный первый комплекс содержит первый сайт-специфический полипептид, первую модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и первый эффекторный белок, при этом указанный эффекторный белок выполнен с возможностью связывания с модифицированной нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, и при этом указанный первый эффекторный белок содержит ненативную последовательность, которая содержит первый фрагмент комбинированной системы; и приведение второй целевой нуклеиновой кислоты в контакт с вторым комплексом, при этом указанный второй комплекс содержит второй сайт-специфический полипептид, вторую модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и второй эффекторный белок, при этом указанный эффекторный белок выполнен с возможностью связывания с модифицированной нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, и при этом указанный второй эффекторный белок содержит ненативную последовательность, которая содержит второй фрагмент комбинированной системы. Согласно некоторым вариантам реализации указанная первая целевая нуклеиновая кислота и указанная вторая целевая нуклеиновая кислота входят в один полинуклеотидный полимер. Согласно некоторым вариантам реализации указанная комбинированная система содержит два или большее количество белковых фрагментов, которые по отдельности не являются активными, но их объединение в комплекс приводит к образованию активного белкового комплекса. Согласно некоторым вариантам реализации указанный способ дополнительно включает детекцию взаимодействия между первым фрагментом и вторым фрагментом. Согласно некоторым вариантам реализации детекция указывает на то, что первый и второй комплексы находятся поблизости друг от друга. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид получен таким образом, что он не способен расщеплять целевую нуклеиновую кислоту. Согласно некоторым вариантам реализации детекция включает определение того, произошло ли явление генетической мобильности. Согласно некоторым вариантам реализации указанный явление генетической мобильности включает транслокацию. Согласно некоторым вариантам реализации до явления генетической мобильности указанные два фрагмента комбинированной системы не взаимодействуют. Согласно некоторым вариантам реализации после явления генетической мобильности указанные два фрагмента комбинированной системы взаимодействуют. Согласно некоторым вариантам реализации указанный явление генетической мобильности представляет собой транслокацию между генами BCR и Abl. Согласно некоторым вариантам реализации указанное взаимодействие активирует указанную комбинированную систему. Согласно некоторым вариантам реализации указанное взаимодействие указывает на то, что целевые нуклеиновые кислоты, связанные указанными комплексами, расположены близко друг к другу. Согласно некоторым вариантам реализации указанная комбинированная система выбрана из группы, состоящей из: комбинированной GFP-системы, комбинированной убиквитиновой системы, комбинированной системы транскрипционных факторов и комбинированной системы с аффинной меткой, или любой их комбинации. Согласно некоторым вариантам реализации указанная комбинированная система включает комбинированную GFP-систему. Согласно некоторым вариантам реализации при детекции определяют генотип. Согласно некоторым вариантам реализации указанный способ дополнительно включает: определение курса лечения заболевания на основании указанного генотипа. Согласно некоторым вариантам реализации указанный способ дополнительно включает лечение указанного заболевания. Согласно некоторым вариантам реализации указанное лечение включает введение лекарственного средства. Согласно некоторым вариантам реализации указанное лечение включает введение комплекса, содержащего нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и сайт-специфический полипептид, при этом указанный комплекс может модифицировать генетический элемент, вовлеченный в указанное заболевание. Согласно некоторым вариантам реализации указанная модификация выбрана из группы, состоящей из: добавления последовательности нуклеиновой кислоты в генетический элемент, замены последовательности нуклеиновой кислоты в генетическом элементе и удаление последовательности нуклеиновой кислоты из генетического элемента, или любой их комбинации. Согласно некоторым вариантам реализации указанный способ дополнительно включает: передачу информации о генотипе от осуществляющего уход лица пациенту. Согласно некоторым вариантам реализации указанная передача информации включает передачу информации из запоминающего устройства на удаленный компьютер. Согласно некоторым вариантам реализации при детекции осуществляют диагностику заболевания. Согласно некоторым вариантам реализации указанный способ дополнительно включает: передачу информации о диагнозе от осуществляющего уход лица пациенту. Согласно некоторым вариантам реализации детекция указывает на присутствие однонуклеотидного полиморфизма (SNP). Согласно некоторым вариантам реализации указанный способ дополнительно включает: передачу информации о наступлении явления генетической мобильности от осуществляющего уход лица пациенту. Согласно некоторым вариантам реализации указанная передачу информации включает передачу информации с запоминающего устройства на удаленный компьютер. Согласно некоторым вариантам реализации последовательность аминокислот указанного сайт-специфического полипептида по меньшей мере на 20% идентична последовательности Cas9. Согласно некоторым вариантам реализации последовательность аминокислот указанного сайт-специфического полипептида по меньшей мере на 60% идентична последовательности Cas9. Согласно некоторым вариантам реализации последовательность аминокислот в нуклеазном домене указанного сайт-специфического полипептида по меньшей мере на 60% идентична последовательности нуклеазного домена Cas9. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид представляет собой Cas9. Согласно некоторым вариантам реализации указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность. Согласно некоторым вариантам реализации указанная ненативная последовательность расположена в положении модифицированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, выбранном из группы, состоящей из: 5'-конца, 3'-конца или любой их комбинации. Согласно некоторым вариантам реализации указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит две молекулы нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная нуклеиновая кислота содержит одну непрерывную молекулу нуклеиновой кислоты, содержащую первый фрагмент, последовательность которого по меньшей мере на 50% идентична последовательности повтора CRISPR на протяжении 6 последовательных нуклеотидов, и второй фрагмент, последовательность которого по меньшей мере на 50% идентична последовательности tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанный первый фрагмент и указанный второй фрагмент соединены линкером. Согласно некоторым вариантам реализации указанная ненативная последовательность содержит последовательность, связывающую связывающий CRISPR РНК белок. Согласно некоторым вариантам реализации указанная ненативная последовательность содержит связывающую последовательность, выбранную из группы, состоящей из: Cas5 РНК-связывающей последовательности, Cas6 РНК-связывающей последовательности и Csy4 РНК-связывающей последовательности, или любой их комбинации. Согласно некоторым вариантам реализации указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, способна связываться с эффекторным белком. Согласно некоторым вариантам реализации указанный эффекторный белок представляет собой CRISPR РНК-связывающий белок. Согласно некоторым вариантам реализации последовательность аминокислот указанного эффекторного белка по меньшей мере на 15% идентична последовательности белка, выбранного из группы, состоящей из: Cas5, Cas6 и Csy4, или любой их комбинации. Согласно некоторым вариантам реализации последовательность аминокислот РНК-связывающего домена эффекторного белка по меньшей мере на 15% идентична последовательности РНК-связывающего домена белка, выбранного из группы, состоящей из: Cas5, Cas6 и Csy4, или любой их комбинации. Согласно некоторым вариантам реализации указанный эффекторный белок выбран из группы, состоящей из: Cas5, Cas6 и Csy4, или любой их комбинации. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой РНК. Согласно некоторым вариантам реализации указанный целевая нуклеиновая кислота представляет собой ДНК. Согласно некоторым вариантам реализации указанное взаимодействие включает образование аффинной метки. Согласно некоторым вариантам реализации детекция включает захват указанной аффинной метки. Согласно некоторым вариантам реализации указанный способ дополнительно включает секвенирование нуклеиновой кислоты, связанной с первым и вторым комплексами. Согласно некоторым вариантам реализации указанный способ дополнительно включает фрагментацию указанной нуклеиновой кислоты перед захватом. Согласно некоторым вариантам реализации при указанном взаимодействии образуется активированная система. Согласно некоторым вариантам реализации указанный способ дополнительно включает изменение транскрипции первой целевой нуклеиновой кислоты или второй целевой нуклеиновой кислоты, при этом указанное изменение осуществляется указанной активированной системой. Согласно некоторым вариантам реализации указанная вторая целевая нуклеиновая кислота не присоединена к первой целевой нуклеиновой кислоте. Согласно некоторым вариантам реализации указанное изменение транскрипции второй целевой нуклеиновой кислоты осуществляется in trans. Согласно некоторым вариантам реализации указанный изменение транскрипции первой целевой нуклеиновой кислоты осуществляется in cis. Согласно некоторым вариантам реализации указанный первая или вторая целевая нуклеиновая кислота выбрана из группы, состоящей из: эндогенной нуклеиновой кислоты и экзогенной нуклеиновой кислоты, или любой их комбинации. Согласно некоторым вариантам реализации указанное изменение включает увеличение транскрипции первой или второй целевых нуклеиновых кислот. Согласно некоторым вариантам реализации указанный первая или вторая целевая нуклеиновая кислота содержит полинуклеотид, кодирующий один или большее количество генов, вызывающих клеточную смерть. Согласно некоторым вариантам реализации указанная первая или вторая целевая нуклеиновая кислота содержит полинуклеотид, кодирующий индуцирующий лизис клеток пептид. Согласно некоторым вариантам реализации указанный первая или вторая целевая нуклеиновая кислота содержит полинуклеотид, кодирующий осуществляющий рекрутинг иммунных клеток антиген. Согласно некоторым вариантам реализации указанная первая или вторая целевая нуклеиновая кислота содержит полинуклеотид, кодирующий один или большее количество генов, вовлеченных в апоптоз. Согласно некоторым вариантам реализации указанный(ые) один или большее количество генов, вовлеченных в апоптоз, содержит каспазы. Согласно некоторым вариантам реализации указанный(ые) один или большее количество генов, вовлеченных в апоптоз, включает(ют) цитокины. Согласно некоторым вариантам реализации указанный(е) один или большее количество генов, вовлеченных в апоптоз, выбраны из группы, состоящей из: фактора некроза опухоли (ФНО), рецептора ФНО 1 (рФНО-1), рецептора ФНО 2 (рФНО-2), рецептора Fas, FasL, каспаза-8, каспазы-10, каспазы-3, каспазы-9, каспазы-3, каспазы-6, каспазы-7, Bcl-2 и апоптоз-индуцирующего фактора (АИФ), или любой их комбинации. Согласно некоторым вариантам реализации указанная(ые) первая или вторая целевая нуклеиновая кислота содержит полинуклеотид, кодирующий один или большее количество нуклеиновых кислот, которые нацелены на нуклеиновые кислоты. Согласно некоторым вариантам реализации указанная(ые) одна или большее количество нуклеиновых кислот, которые нацелены на нуклеиновые кислоты, нацелены на совокупность целевых нуклеиновых кислот. Согласно некоторым вариантам реализации детекция включает получение генетических данных. Согласно некоторым вариантам реализации указанный способ дополнительно включает передачу информации о генетических данных с запоминающего устройства на удаленный компьютер. Согласно некоторым вариантам реализации генетические данные указывают на генотип. Согласно некоторым вариантам реализации генетические данные указывают на наступление явления генетической мобильности. Согласно некоторым вариантам реализации генетические данные указывают на пространственную локализацию генов.
[0021] Согласно одному аспекту в описании предложен набор, содержащий: сайт-специфический полипептид, модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность, эффекторный белок, который выполнен с возможностью связывания с ненативной последовательностью; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0022] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность. Согласно некоторым вариантам реализации указанная полинуклеотидная последовательность функционально связана а с промотором. Согласно некоторым вариантам реализации указанный промотор представляет собой индуцируемый промотор.
[0023] Согласно одному аспекту в описании предложен вектор, содержащий: полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит последовательность, обеспечивающую возможность связывания с эффекторным белком, и сайт-специфический полипептид. Согласно некоторым вариантам реализации указанная полинуклеотидная последовательность функционально связана с промотором. Согласно некоторым вариантам реализации указанный промотор представляет собой индуцируемый промотор.
[0024] Согласно одному аспекту в описании предложен вектор, содержащий: полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность, сайт-специфический полипептид и эффекторный белок. Согласно некоторым вариантам реализации указанная полинуклеотидная последовательность функционально связана с промотором. Согласно некоторым вариантам реализации указанный промотор представляет собой индуцируемый промотор.
[0025] Согласно одному аспекту в описании предложена генетически модифицированная клетка, содержащая композицию, содержащую: эффекторный белок и нуклеиновую кислоту, при этом последовательность указанной нуклеиновой кислоты по меньшей мере на 50% идентична последовательности crRNA на протяжении 6 последовательных нуклеотидов, по меньшей мере на 50% идентична последовательности tracrRNA на протяжении 6 последовательных нуклеотидов; и ненативную последовательность, при этом указанная нуклеиновая кислота способна связываться с указанным эффекторным белком.
[0026] Согласно одному аспекту в описании предложена генетически модифицированная клетка, содержащая вектор, содержащий полинуклеотидную последовательность, кодирующую модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность.
[0027] Согласно одному аспекту в описании предложена генетически модифицированная клетка, содержащая вектор, включающий: полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит последовательность, подходящую для связывания с эффекторным белком, и сайт-специфический полипептид.
[0028] Согласно одному аспекту в описании предложена генетически модифицированная клетка, содержащая вектор, включающий: полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность, сайт-специфический полипептид и эффекторный белок.
[0029] Согласно одному аспекту в описании предложен набор, содержащий: вектор, содержащий полинуклеотидную последовательность, кодирующую модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0030] Согласно одному аспекту в описании предложен набор, содержащий: вектор, включающий: полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит последовательность, подходящую для связывания с эффекторным белком, и сайт-специфический полипептид; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0031] Согласно одному аспекту в описании предложен набор, содержащий: вектор, включающий: полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность, сайт-специфический полипептид и эффекторный белок; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0032] Согласно одному аспекту в описании предложена композиция, содержащая: агент для мультиплексного генетического нацеливания, при этом указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, и при этом указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, при этом указанный модуль нуклеиновой кислоты способен гибридизоваться с целевой нуклеиновой кислотой. Согласно некоторым вариантам реализации указанный модуль нуклеиновой кислоты содержит первую последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и вторую последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная композиция дополнительно содержит линкерную последовательность, которая соединяет указанные первую и вторую последовательности. Согласно некоторым вариантам реализации указанный один или большее количество модулей нуклеиновых кислот гибридизует(ют)ся с одной или большим количеством целевых нуклеиновых кислот. Согласно некоторым вариантам реализации указанный один или большее количество модулей нуклеиновых кислот отличает(ют)ся по меньшей мере одним нуклеотидом в спейсерной области указанного одного или большего количества модулей нуклеиновых кислот. Согласно некоторым вариантам реализации указанный один или большее количество модулей нуклеиновых кислот представляет собой РНК. Согласно некоторым вариантам реализации указанный агент для мультиплексного генетического нацеливания представляет собой РНК. Согласно некоторым вариантам реализации указанная ненативная последовательность включает рибозим. Согласно некоторым вариантам реализации указанная ненативная последовательность включает последовательность связывания эндорибонуклеазы. Согласно некоторым вариантам реализации указанная последовательность связывания эндорибонуклеазы расположена на 5'-конце модуля нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная последовательность связывания эндорибонуклеазы расположена на 3'-конце модуля нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная последовательность связывания эндорибонуклеазы выполнена с возможностью связывания с эндорибонуклеазой CRISPR. Согласно некоторым вариантам реализации указанная последовательность связывания эндорибонуклеазы выполнена с возможностью связывания с эндорибонуклеазой, содержащей домен RAMP. Согласно некоторым вариантам реализации указанная последовательность связывания эндорибонуклеазы выполнена с возможностью связывания с эндорибонуклеазой, выбранной из группы, состоящей из: эндорибонуклеазы из суперсемейства Cas5 и эндорибонуклеазы из суперсемейства Cas6, или любой их комбинации. Согласно некоторым вариантам реализации указанная последовательность связывания эндорибонуклеазы выполнена с возможностью связывания с эндорибонуклеазой, содержащей последовательность аминокислот, по меньшей мере на 15% идентичную последовательности белка, выбранного из группы, состоящей из: Csy4, Cas5 и Cas6. Согласно некоторым вариантам реализации указанная последовательность связывания эндорибонуклеазы выполнена с возможностью связывания с эндорибонуклеазой, содержащей последовательность аминокислот, по меньшей мере на 15% идентичную последовательности нуклеазного домена белка, выбранного из группы, состоящей из: Csy4, Cas5 и Cas6. Согласно некоторым вариантам реализации указанная последовательность связывания эндорибонуклеазы содержит шпильку. Согласно некоторым вариантам реализации указанная шпилька содержит по меньшей мере 4 последовательных нуклеотида в структуре типа «петля-на-стебле». Согласно некоторым вариантам реализации указанная последовательность связывания эндорибонуклеазы по меньшей мере на 60% идентична последовательности, выбранной из группы, состоящей из:

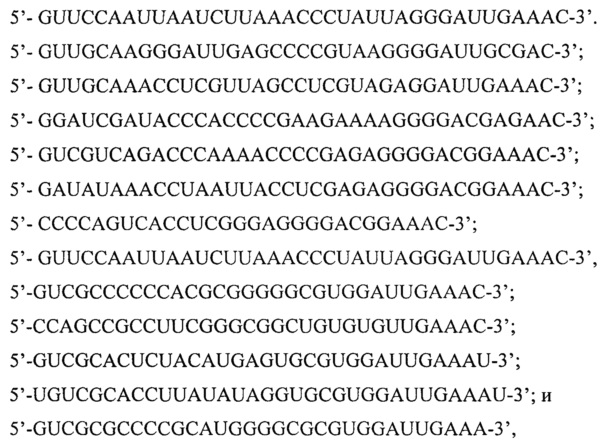
или любой их комбинации. Согласно некоторым вариантам реализации указанный один или большее количество модулей нуклеиновых кислот подходит(ят) для связывания разными эндорибонуклеазами. Согласно некоторым вариантам реализации указанный агент для мультиплексного генетического нацеливания представляет собой выделенный агент для мультиплексного генетического нацеливания. Согласно некоторым вариантам реализации указанный агент для мультиплексного генетического нацеливания представляет собой рекомбинантный агент для мультиплексного генетического нацеливания.
[0033] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую агент для мультиплексного генетического нацеливания, при этом указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, и при этом указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, и при этом указанный модуль нуклеиновой кислоты выполнен с возможностью гибридизации с целевой нуклеиновой кислотой. Согласно некоторым вариантам реализации указанная полинуклеотидная последовательность функционально связана с промотором. Согласно некоторым вариантам реализации указанный промотор представляет собой индуцируемый промотор.
[0034] Согласно одному аспекту в описании предложена генетически модифицированная клетка, содержащая агент для мультиплексного генетического нацеливания, при этом указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, и при этом указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, и при этом указанный модуль нуклеиновой кислоты способна гибридизоваться с целевой нуклеиновой кислотой.
[0035] Согласно одному аспекту в описании предложена генетически модифицированная клетка, содержащая вектор, содержащий полинуклеотидную последовательность, кодирующую агент для мультиплексного генетического нацеливания, при этом указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, и указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, и при этом указанный модуль нуклеиновой кислоты способна гибридизоваться с целевой нуклеиновой кислотой.
[0036] Согласно одному аспекту в описании предложен набор, содержащий агент для мультиплексного генетического нацеливания, при этом указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, и при этом указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, и при этом указанный модуль нуклеиновой кислоты способна гибридизоваться с целевой нуклеиновой кислотой; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0037] Согласно одному аспекту в описании предложен набор, содержащий: вектор, содержащий полинуклеотидную последовательность, кодирующую агент для мультиплексного генетического нацеливания, при этом указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, и при этом указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, и при этом указанный модуль нуклеиновой кислоты способна гибридизоваться с целевой нуклеиновой кислотой; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0038] Согласно одному аспекту в описании предложен способ получения нуклеиновой кислоты, отличающийся тем, что указанная нуклеиновая кислота связывается с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, и гибридизуется с целевой нуклеиновой кислотой, включающий: введение агента для мультиплексного генетического нацеливания, при этом указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, и при этом указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, при этом указанный модуль нуклеиновой кислоты способна гибридизоваться с целевой нуклеиновой кислотой, в клетку-хозяина, процессинг указанного агента для мультиплексного генетического нацеливания на один или большее количество модулей нуклеиновых кислот, и приведение в контакт процессированного одного или большего количества модулей нуклеиновых кислот с одной или большим количеством целевых нуклеиновых кислот в клетке. Согласно некоторым вариантам реализации указанный способ дополнительно включает расщепление целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный способ дополнительно включает модификацию целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная модификация включает изменение транскрипции целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная модификация включает встраивание донорного полинуклеотида в целевую нуклеиновую кислоту.
[0039] Согласно одному аспекту в описании предложен модифицированный сайт-специфический полипептид, содержащий: первый нуклеазный домен, второй нуклеазный домен и встроенный нуклеазный домен. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид содержит последовательность, по меньшей мере на 15% идентичную последовательности нуклеазного домена Cas9. Согласно некоторым вариантам реализации указанный первый нуклеазный домен включает нуклеазный домен, выбранный из группы, состоящей из: домена HNH и домена RuvC, или любой их комбинации. Согласно некоторым вариантам реализации указанный второй нуклеазный домен включает нуклеазный домен, выбранный из группы, состоящей из: домена HNH и домена RuvC, или любой их комбинации. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен включает домен HNH. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен включает домен RuvC. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен расположен в направлении N-конца от первого нуклеазного домена. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен расположен в направлении N-конца от второго нуклеазного домена. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен расположен в направлении С-конца от первого нуклеазного домена. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен расположен в направлении С-конца от второго нуклеазного домена. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен находится в тандеме с первым нуклеазным доменом. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен находится в тандеме с вторым нуклеазным доменом. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен выполнен с возможностью расщепления целевой нуклеиновой кислоты в сайте, отличном от сайта расщепления первым или вторым нуклеазным доменом. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен выполнен с возможностью расщепления РНК в гибриде ДНК/РНК. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен выполнен с возможностью расщепления ДНК в гибриде ДНК/РНК. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен выполнен с возможностью увеличения специфичности связывания модифицированного сайт-специфического полипептида с целевой нуклеиновой кислотой. Согласно некоторым вариантам реализации указанный встроенный нуклеазный домен выполнен с возможностью увеличения силы связывания модифицированного сайт-специфического полипептида с целевой нуклеиновой кислотой.
[0040] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую модифицированный сайт-специфический полипептид, содержащий: первый нуклеазный домен, второй нуклеазный домен и встроенный нуклеазный домен.
[0041] Согласно одному аспекту в описании предложен набор, содержащий: модифицированный сайт-специфический полипептид, содержащий: первый нуклеазный домен, второй нуклеазный домен и встроенный нуклеазный домен; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0042] Согласно одному аспекту в описании предложена композиция, содержащая: модифицированный сайт-специфический полипептид, при этом указанный полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на второй примыкающий к протоспейсеру мотив. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид модифицирован путем модификации, выбранной из группы, состоящей из: добавления аминокислоты, замещения аминокислоты, замены аминокислоты и удаления аминокислоты, или любой их комбинации. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид содержит ненативную последовательность. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью нацеливания на второй примыкающий к протоспейсеру мотив с большей специфичностью по сравнению с сайт-специфическим полипептидом дикого типа. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью нацеливания на второй примыкающий к протоспейсеру мотив с меньшей константой диссоциации по сравнению с сайт-специфическим полипептидом дикого типа. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью нацеливания на второй примыкающий к протоспейсеру мотив с более высокой константой диссоциации по сравнению с сайт-специфическим полипептидом дикого типа. Согласно некоторым вариантам реализации указанный второй примыкающий к протоспейсеру мотив включает примыкающий к протоспейсеру мотив, выбранный из группы, состоящей из: 5'-NGGNG-3', 5'-NNAAAAW-3', 5'-NNNNGATT-3', 5'-GNNNCNNA-3' и 5'-NNNACA-3', или любой их комбинации.
[0043] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую модифицированный сайт-специфический полипептид, при этом указанный полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на второй примыкающий к протоспейсеру мотив.
[0044] Согласно одному аспекту в описании предложен набор, содержащий: модифицированный сайт-специфический полипептид, при этом указанный полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на второй примыкающий к протоспейсеру мотив; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0045] Согласно одному аспекту в описании предложена композиция, содержащая: модифицированный сайт-специфический полипептид, при этом указанный полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид модифицирован путем модификации, выбранной из группы, состоящей из: добавления аминокислоты, замещения аминокислоты, замены аминокислоты и удаления аминокислоты, или любой их комбинации. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид содержит ненативную последовательность. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью нацеливания на вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, с большей специфичностью по сравнению с сайт-специфическим полипептидом дикого типа. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью нацеливания на вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, с меньшей константой диссоциации по сравнению с сайт-специфическим полипептидом дикого типа. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью нацеливания на вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, с более высокой константой диссоциации по сравнению с сайт-специфическим полипептидом дикого типа. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид нацелен на фрагмент tracrRNA второй нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту.
[0046] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую модифицированный сайт-специфический полипептид, при этом указанный полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту.
[0047] Согласно одному аспекту в описании предложен набор, содержащий: модифицированный сайт-специфический полипептид, при этом указанный полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту; и буфер. Согласно некоторым, вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0048] Согласно одному аспекту в описании предложена композиция, содержащая: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в спиральном мостике. Согласно некоторым вариантам реализации указанная композиция выполнена с возможностью расщепления целевой нуклеиновой кислоты.
[0049] Согласно одному аспекту в описании предложена композиция, содержащая: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в высокоосновном участке. Согласно некоторым вариантам реализации указанная композиция выполнена с возможностью расщепления целевой нуклеиновой кислоты.
[0050] Согласно одному аспекту в описании предложена композиция, содержащая: модифицированный сайт-специфический полипептид, содержащий модификацию относительно SEQ ID: 8 в полимераза-подобном домене. Согласно некоторым вариантам реализации указанная композиция выполнена с возможностью расщепления целевой нуклеиновой кислоты.
[0051] Согласно одному аспекту в описании предложена композиция, содержащая: модифицированный сайт-специфический полипептид, содержащий модификацию относительно SEQ ID: 8 в спиральном мостике, высокоосновном участке, нуклеазном домене и полимеразном домене, или любую их комбинацию.
[0052] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую модифицированный сайт-специфический полипептид, содержащий модификацию относительно SEQ ID: 8 в спиральном мостике, высокоосновном участке, нуклеазном домене и полимеразном домене, или любой их комбинации.
[0053] Согласно одному аспекту в описании предложен набор, содержащий: модифицированный сайт-специфический полипептид, содержащий модификацию относительно SEQ ID: 8 в спиральном мостике, высокоосновном участке, нуклеазном домене и полимеразном домене, или любую их комбинацию; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению. Согласно некоторым вариантам реализации указанный набор дополнительно содержит нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту.
[0054] Согласно одному аспекту в описании предложена генетически модифицированная клетка, содержащая модифицированный сайт-специфический полипептид, содержащий модификацию относительно SEQ ID: 8 в спиральном мостике, высокоосновном участке, нуклеазном домене и полимеразном домене, или любую их комбинацию.
[0055] Согласно одному аспекту в описании предложен способ для применения в геномной инженерии, включающий: приведение целевой нуклеиновой кислоты в контакт с комплексом, при этом указанный комплекс содержит модифицированный сайт-специфический полипептид, содержащий модификацию в спиральном мостике, высокоосновном участке, нуклеазном домене и полимеразном домене относительно SEQ ID: 8, или любой их комбинации, и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту; и модификацию целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанное приведение в контакт включает приведение указанного комплекса в контакт с примыкающим к протоспейсеру мотивом в указанной целевой нуклеиновой кислоте. Согласно некоторым вариантам реализации указанное приведение в контакт включает приведение указанного комплекса в контакт с более длинной последовательностью целевой нуклеиновой кислоты по сравнению с немодифицированным сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанная модификация включает расщепление целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный целевая нуклеиновая кислота содержит РНК. Согласно некоторым вариантам реализации указанный целевая нуклеиновая кислота содержит ДНК. Согласно некоторым вариантам реализации указанная модификация включает расщепление цепи РНК гибридизированных РНК и ДНК. Согласно некоторым вариантам реализации указанная модификация включает расщепление цепи ДНК гибридизированных РНК и ДНК. Согласно некоторым вариантам реализации указанная модификация включает встраивание в целевую нуклеиновую кислоту донорного полинуклеотида, фрагмента донорного полинуклеотида, копии донорного полинуклеотида или фрагмента копии донорного полинуклеотида, или любой их комбинации. Согласно некоторым вариантам реализации указанная модификация включает модификацию транскрипционной активности целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная модификация включает удаление одного или большего количества нуклеотидов целевой нуклеиновой кислоты.
[0056] Согласно одному аспекту в описании предложена композиция, содержащая: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модифицированный нуклеазный домен. Согласно некоторым вариантам реализации указанная композиция выполнена с возможностью расщепления целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный модифицированный нуклеазный домен включает нуклеазный домен RuvC. Согласно некоторым вариантам реализации указанный модифицированный нуклеазный домен включает нуклеазный домен HNH. Согласно некоторым вариантам реализации указанный модифицированный нуклеазный домен включает удвоенный нуклеазный домен HNH. Согласно некоторым вариантам реализации указанный модифицированный нуклеазный домен выполнен с возможностью повышения специфичности последовательности аминокислот в отношении целевой нуклеиновой кислоты по сравнению с немодифицированным сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанный модифицированный нуклеазный домен выполнен с возможностью повышения специфичности последовательности аминокислот в отношении нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, по сравнению с немодифицированным сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанный модифицированный нуклеазный домен содержит модификацию, выбранную из группы, состоящей из: добавления аминокислоты, замещения аминокислоты, замены аминокислоты и удаления аминокислоты, или любой их комбинации. Согласно некоторым вариантам реализации указанный модифицированный нуклеазный домен содержит встроенную ненативную последовательность. Согласно некоторым вариантам реализации указанная ненативная последовательность обеспечивает ферментативную активность модифицированного сайт-специфического полипептида. Согласно некоторым вариантам реализации указанная ферментативная активность выбрана из группы, состоящей из: нуклеазной активности, метилазной активности, ацетилазной активности, деметилазной активности, деаминирующей активности, дисмутазной активности, алкилирующей активности, депуринизирующей активности, окислительной активности, направленной на образование пиримидиновых димеров активности, интегразной активности, транспозазной активности, рекомбиназной активности, полимеразной активности, лигазной активности, геликазной активности, фотолиазной активности или гликозилазной активности, ацилтрансферазной активности, деацетилазной активности, киназной активности, фосфатазной активности, убиквитин-лигазной активности, деубиквитинирующей активности, аденилирующей активности, деаденилирующей активности, сумоилирующей активности, десумоилирующей активности, рибозилирующей активности, дерибозилирующей активности, миристоилирующей активности, ремоделирующей активности, протеазной активности, оксидоредуктазной активности, трансферазной активности, гидролазной активности, лиазной активности, изомеразной активности, синтазной активности, синтетазной активности, и демиристоилирующей активности, или любой их комбинации. Согласно некоторым вариантам реализации указанная ферментативная активность способна модулировать транскрипцию целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный модифицированный нуклеазный домен выполнен с возможностью связывания последовательности аминокислот с последовательностью примыкающего к протоспейсеру мотива, отличной от последовательности примыкающего к протоспейсеру мотива, с которым способен связываться немодифицированный сайт-специфический полипептид. Согласно некоторым вариантам реализации указанный модифицированный нуклеазный домен выполнен с возможностью связывания последовательности аминокислот с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, которая отличается от нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, с которой способен связываться немодифицированный сайт-специфический полипептид. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью связывания с более длинной последовательностью целевой нуклеиновой кислоты, чем немодифицированный сайт-специфический полипептид. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью расщепления двуцепочечной ДНК. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью расщепления цепи РНК гибридизированных РНК и ДНК. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид выполнен с возможностью расщепления цепи ДНК гибридизированных РНК и ДНК. Согласно некоторым вариантам реализации указанная композиция дополнительно содержит модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модификация сайт-специфического полипептида осуществлена таким образом, чтобы обеспечивать возможностью связывания сайт-специфического полипептида с модифицированной нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, и указанный модифицированный сайт-специфический полипептид содержат компенсационные мутации.
[0057] Согласно одному аспекту в описании предложен способ обогащения целевой нуклеиновой кислоты для секвенирования, включающий: приведение целевой нуклеиновой кислоты в контакт с комплексом, содержащим нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту и сайт-специфический полипептид, обогащение целевой нуклеиновой кислоты с применением указанного комплекса и определение последовательности целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный способ не включает этап амплификации. Согласно некоторым вариантам реализации указанный способ дополнительно включает анализ последовательности целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный способ дополнительно включает фрагментацию целевой нуклеиновой кислоты перед обогащением. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит РНК. Согласно некоторым вариантам реализации указанного способа нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит две молекулы РНК. Согласно некоторым вариантам реализации указанного способа фрагменты каждой из двух молекул РНК гибридизуются друг с другом. Согласно некоторым вариантам реализации указанного способа одна из двух молекул РНК содержит последовательность повтора CRISPR. Согласно некоторым вариантам реализации указанная последовательность повтора CRISPR гомологична crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная последовательность повтора CRISPR по меньшей мере на 60% идентична последовательности crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации одна из двух молекул РНК содержит последовательность tracrRNA. Согласно некоторым вариантам реализации указанная последовательность tracRNA гомологична tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная последовательность tracRNA по меньшей мере на 60% идентична последовательности tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой двойную направляющую нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит одну непрерывную молекулу РНК, при этом указанная непрерывная молекула РНК дополнительно содержит два домена и линкер. Согласно некоторым вариантам реализации фрагмент каждого из указанных двух доменов указанной непрерывной молекулы РНК гибридизуются друг с другом. Согласно некоторым вариантам реализации указанная непрерывная молекула РНК содержит последовательность повтора CRISPR. Согласно некоторым вариантам реализации указанная последовательность повтора CRISPR гомологична crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная последовательность повтора CRISPR по меньшей мере на 60% идентична последовательности crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная непрерывная молекула РНК содержит последовательность tracrRNA. Согласно некоторым вариантам реализации указанная последовательность tracRNA гомологична tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная последовательность tracRNA по меньшей мере на 60% идентична последовательности tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой одиночную направляющую нуклеиновую кислоту. Согласно некоторым вариантам реализации указанное приведение в контакт включает гибридизацию фрагмента указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, с фрагментом целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, гибридизуется с целевой нуклеиновой кислотой на протяжении области, содержащей 6-20 нуклеотидов. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид содержит Cas9. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид по меньшей мере на 20% гомологичен нуклеазному домену Cas9. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид по меньшей мере на 60% гомологичен Cas9. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид содержит сконструированный нуклеазный домен, при этом указанный нуклеазный домен обладает пониженной нуклеазной активностью по сравнению с сайт-специфическим полипептидом, который содержит несконструированный нуклеазный домен. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид вводит одноцепочечный разрыв в указанную целевую нуклеиновую кислоту. Согласно некоторым вариантам реализации указанный сконструированный нуклеазный домен содержит мутацию консервативной аспарагиновой кислоты. Согласно некоторым вариантам реализации указанный сконструированный нуклеазный домен содержит мутацию D10A. Согласно некоторым вариантам реализации указанный сконструированный нуклеазный домен содержит мутацию консервативного гистидина. Согласно некоторым вариантам реализации указанный сконструированный нуклеазный домен содержит мутацию Н840А. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид содержит аффинную метку. Согласно некоторым вариантам реализации указанная аффинная метка расположена на N-конце сайт-специфического полипептида, С-конце сайт-специфического полипептида, поверхностно-доступной области или любой их комбинации. Согласно некоторым вариантам реализации указанная аффинная метка выбрана из группы, включающей: биотин, FLAG, His6x, His9x и флуоресцентный белок, или любую их комбинацию. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит нуклеиново-кислотную аффинную метку. Согласно некоторым вариантам реализации указанная нуклеиново-кислотная аффинная метка расположена на 5'-конце указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, 3'-конце указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, на поверхностно-доступной области, или любой их комбинации. Согласно некоторым вариантам реализации указанная нуклеиново-кислотная аффинная метка выбрана из группы, содержащей малую молекулу, флуоресцентную метку, радиоактивную метку или любую их комбинацию. Согласно некоторым вариантам реализации указанная нуклеиново-кислотная аффинная метка содержит последовательность, подходящую для связывания Csy4, Cas5, Cas6 или любой их комбинацией. Согласно некоторым вариантам реализации указанная нуклеиново-кислотная аффинная метка на 50% идентична последовательности
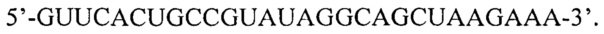
[0058] Согласно одному аспекту в описании предложен способ вырезания нуклеиновой кислоты, включающий: приведение целевой нуклеиновой кислоты в контакт с двумя или большим количеством комплексов, при этом каждый комплекс содержит сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту; и расщепление целевой нуклеиновой кислоты, при этом указанное расщепление обеспечивает получение вырезанной целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанное расщепление осуществляется нуклеазным доменом сайт-специфического полипептида. Согласно некоторым вариантам реализации указанный способ не включает амплификацию. Согласно некоторым вариантам реализации указанный способ дополнительно включает обогащение вырезанной целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный способ дополнительно включает секвенирование вырезанной целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой РНК. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит две молекулы РНК. Согласно некоторым вариантам реализации фрагмент каждой из указанных двух молекул РНК гибридизуются друг с другом. Согласно некоторым вариантам реализации одна из двух молекул РНК содержит последовательность повтора CRISPR. Согласно некоторым вариантам реализации указанная последовательность повтора CRISPR содержит последовательность, гомологичную crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная последовательность повтора CRISPR содержит последовательность, по меньшей мере на 60% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации одна из двух молекул РНК содержит последовательность tracrRNA. Согласно некоторым вариантам реализации указанная последовательность tracRNA гомологична crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная последовательность tracRNA по меньшей мере на 60% идентична последовательности crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой двойную направляющую нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит одну непрерывную молекулу РНК, при этом указанная непрерывная молекула РНК дополнительно содержит два домена и линкер. Согласно некоторым вариантам реализации фрагменты каждого из указанных двух доменов указанной непрерывной молекулы РНК гибридизуются друг с другом. Согласно некоторым вариантам реализации указанная непрерывная молекула РНК содержит последовательность повтора CRISPR. Согласно некоторым вариантам реализации указанная последовательность повтора CRISPR гомологична crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная последовательность повтора CRISPR по меньшей мере на 60% идентична последовательности crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная непрерывная молекула РНК содержит последовательность tracrRNA. Согласно некоторым вариантам реализации указанная последовательность tracRNA гомологична crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная последовательность tracRNA по меньшей мере на 60% идентична последовательности crRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, представляет собой одиночную направляющую нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, гибридизуется с целевой нуклеиновой кислотой. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, гибридизуется с целевой нуклеиновой кислотой на протяжении некоторой области, при этом указанная область содержит по меньшей мере 6 нуклеотидов и максимум 20 нуклеотидов. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид представляет собой Cas9. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид содержит полипептид, по меньшей мере на 20% гомологичный нуклеазному домену Cas9. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид содержит полипептид, по меньшей мере на 60% гомологичный Cas9. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид содержит аффинную метку. Согласно некоторым вариантам реализации указанная аффинная метка расположена на N-конце сайт-специфического полипептида, С-конце сайт-специфического полипептида, поверхностно-доступной области, или любой их комбинации. Согласно некоторым вариантам реализации указанная аффинная метка выбрана из группы, включающей: биотин, FLAG, His6x, His9x и флуоресцентный белок, или любую их комбинацию. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит нуклеиново-кислотную аффинную метку. Согласно некоторым вариантам реализации указанная нуклеиново-кислотная аффинная метка расположена на 5'-конце указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, 3'-конце указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, поверхностно-доступной области или любой их комбинации. Согласно некоторым вариантам реализации указанная нуклеиново-кислотная аффинная метка выбрана из группы, включающей малую молекулу, флуоресцентную метку, радиоактивную метку или любую их комбинацию. Согласно некоторым вариантам реализации указанная нуклеиново-кислотная аффинная метка представляет собой последовательность, способную связываться с Csy4, Cas5, Cas6 или любой их комбинацией. Согласно некоторым вариантам реализации указанная нуклеиново-кислотная аффинная метка на 50% идентична последовательности

[0059] Согласно одному аспекту в описании предложен способ получения библиотеки целевых нуклеиновых кислот, включающий: приведение совокупности целевых нуклеиновых кислот в контакт с комплексом, содержащим сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, расщепление указанной совокупности целевых нуклеиновых кислот и очищение указанной совокупности целевых нуклеиновых кислот для получения библиотеки целевых нуклеиновых кислот. Согласно некоторым вариантам реализации указанный способ дополнительно включает скрининг указанной библиотеки целевых нуклеиновых кислот.
[0060] Согласно одному аспекту в описании предложена композиция, содержащая: первый комплекс, содержащий: первый сайт-специфический полипептид и первую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, второй комплекс, включающий: второй сайт-специфический полипептид и вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанные первая и вторая нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, различаются. Согласно некоторым вариантам реализации указанная композиция дополнительно содержит целевую нуклеиновую кислоту, связываемую указанным первым или указанным вторым комплексом. Согласно некоторым вариантам реализации указанный первый сайт-специфический полипептид и указанный второй сайт-специфический полипептид идентичны. Согласно некоторым вариантам реализации указанный первый сайт-специфический полипептид и указанный второй сайт-специфический полипептид различаются.
[0061] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую: два или большее количество нуклеиновых кислот, которые нацелены на нуклеиновые кислоты, отличающихся по меньшей мере одним нуклеотидом, и сайт-специфический полипептид.
[0062] Согласно одному аспекту в описании предложена генетически модифицированная клетка-хозяин, содержащая: вектор, содержащий полинуклеотидную последовательность, кодирующую: два или большее количество нуклеиновых кислот, которые нацелены на нуклеиновые кислоты, отличающихся по меньшей мере одним нуклеотидом, и сайт-специфический полипептид.
[0063] Согласно одному аспекту в настоящем изобретении предложен набор, включающий: вектор, содержащий полинуклеотидную последовательность, кодирующую: две или большее количество нуклеиновых кислот, которые нацелены на нуклеиновые кислоты, отличающихся по меньшей мере одним нуклеотидом, сайт-специфический полипептид; и подходящий буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит: агент захвата, твердую подложку, адаптеры для секвенирования и положительный контроль, или любую их комбинацию. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0064] Согласно одному аспекту в описании предложен набор, содержащий: сайт-специфический полипептид, обладающий пониженной ферментативной активностью относительно сайт-специфического полипептида дикого типа, нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и агент захвата. Согласно некоторым вариантам реализации указанный набор дополнительно содержит: инструкции по применению. Согласно некоторым вариантам реализации указанный набор дополнительно содержит буфер, выбранный из группы, включающей: отмывочный буфер, стабилизирующий буфер, восстанавливающий буфер или разбавляющий буфер.
[0065] Согласно одному аспекту в описании предложен способ расщепления целевой нуклеиновой кислоты с применением двух или большего количества никаз, включающий: приведение целевой нуклеиновой кислоты в контакт с первым комплексом и вторым комплексом, при этом указанный первый комплекс содержит первую никазу и первую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанный второй комплекс содержит вторую никазу и вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, причем указанная целевая нуклеиновая кислота содержит первый примыкающий к протоспейсеру мотив на первой цепи и второй примыкающий к протоспейсеру мотив на второй цепи, при этом указанная первая нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, способна гибридизоваться с первым примыкающим к протоспейсеру мотивом, и при этом указанная вторая нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, способна гибридизоваться со вторым примыкающим к протоспейсеру мотивом и никирования первой и второй цепей целевой нуклеиновой кислоты, при этом при указанном никировании образуется расщепленная целевая нуклеиновая кислота. Согласно некоторым вариантам реализации указанные первая и вторая никазы идентичны. Согласно некоторым вариантам реализации указанные первая и вторая никазы различаются. Согласно некоторым вариантам реализации указанные первая и вторая нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, различаются. Согласно некоторым вариантам реализации между первым примыкающим к протоспейсеру мотивом и вторым примыкающим к протоспейсеру мотивом располагается менее 125 нуклеотидов. Согласно некоторым вариантам реализации указанные первый и второй примыкающие к протоспейсеру мотивы состоят из последовательности NGG, где N представляет собой любой нуклеотид. Согласно некоторым вариантам реализации указанная первая или вторая никаза содержит по меньшей мере один по существу неактивный нуклеазный домен. Согласно некоторым вариантам реализации указанная первая или вторая никаза содержит мутацию консервативной аспарагиновой кислоты. Согласно некоторым вариантам реализации указанная мутация представляет собой мутацию D10A. Согласно некоторым вариантам реализации указанная первая или вторая никаза содержит мутацию консервативного гистидина. Согласно некоторым вариантам реализации указанная мутация представляет собой мутацию Н840А. Согласно некоторым вариантам реализации между указанными первым и вторым примыкающими к протоспейсеру мотивами располагается менее 15 нуклеотидов. Согласно некоторым вариантам реализации между указанными первым и вторым примыкающими к протоспейсеру мотивами располагается менее 10 нуклеотидов. Согласно некоторым вариантам реализации между указанными первым и вторым примыкающими к протоспейсеру мотивами располагается менее 5 нуклеотидов. Согласно некоторым вариантам реализации указанные первый и второй примыкающие к протоспейсеру мотивы являются смежными. Согласно некоторым вариантам реализации указанное никирование включает никирование первой никазой первой цепи и никирование второй никазой второй цепи. Согласно некоторым вариантам реализации при указанном никировании образуется «липкий конец». Согласно некоторым вариантам реализации при указанном никировании образуется «тупой конец». Согласно некоторым вариантам реализации указанный способ дополнительно включает встраивание донорного полинуклеотида в расщепленную целевую нуклеиновую кислоту.
[0066] Согласно одному аспекту в описании предложена композиция, содержащая: совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула нуклеиновой кислоты из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна молекула из указанной совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид, и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты. Согласно некоторым вариантам реализации один или большее количество белков из совокупности белков, связывающих нуклеиновые кислоты, содержит(ат) ненативную последовательность. Согласно некоторым вариантам реализации указанная ненативная последовательность расположена в положении, выбранном из группы, состоящей из: N-конца, С-конца, поверхностно-доступной области или любой их комбинации. Согласно некоторым вариантам реализации указанная ненативная последовательность кодирует сигнал ядерной локализации. Согласно некоторым вариантам реализации белки указанной совокупности белков, связывающих нуклеиновые кислоты, разделены линкером. Согласно некоторым вариантам реализации некоторые белки совокупности белков, связывающих нуклеиновые кислоты, представляют собой один и тот же белок, связывающий нуклеиновые кислоты. Согласно некоторым вариантам реализации все белки из совокупности белков, связывающих нуклеиновые кислоты, представляют собой один и тот же белок, связывающий нуклеиновые кислоты. Согласно некоторым вариантам реализации указанная совокупность белков, связывающих нуклеиновые кислоты, представляют собой разные белки, связывающие нуклеиновые кислоты. Согласно некоторым вариантам реализации указанная совокупность белков, связывающих нуклеиновые кислоты, содержит РНК-связывающие белки. Согласно некоторым вариантам реализации указанные РНК-связывающие белки выбраны из группы, состоящей из: эндорибонуклеазы системы регулярно расположенных группами коротких палиндромных повторов I типа, эндорибонуклеазы системы регулярно расположенных группами коротких палиндромных повторов типа II или эндорибонуклеазы системы регулярно расположенных группами коротких палиндромных повторов типа III, или любой их комбинации. Согласно некоторым вариантам реализации указанные РНК-связывающие белки выбраны из группы, состоящей из: Cas5, Cas6 и Csy4, или любой их комбинации. Согласно некоторым вариантам реализации указанная совокупность белков, связывающих нуклеиновые кислоты, содержит ДНК-связывающие белки. Согласно некоторым вариантам реализации сайт связывания связывающего нуклеиновые кислоты белка выполнен с возможностью того, чтобы связывать связывающий нуклеиновые кислоты белок, выбранный из группы, состоящей из: белка, связывающего нуклеиновые кислоты системы регулярно расположенных группами коротких палиндромных повторов типа I, типа II и типа III, или любой их комбинации. Согласно некоторым вариантам реализации указанный сайт связывания связывающего нуклеиновые кислоты белка выполнен с возможностью того, чтобы связывать связывающий нуклеиновые кислоты белок, выбранный из группы, состоящей из: Cas6, Cas5 и Csy4, или любой их комбинации. Согласно некоторым вариантам реализации некоторые белки совокупности молекул нуклеиновых кислот содержат один и тот же сайт связывания белка, связывающего нуклеиновые кислоты. Согласно некоторым вариантам реализации молекулы указанной совокупности молекул нуклеиновых кислот содержат один и тот же сайт связывания белка, связывающего нуклеиновые кислоты. Согласно некоторым вариантам реализации никакие молекулы из совокупности молекул нуклеиновых кислот не содержат одинаковых сайтов связывания белка, связывающего нуклеиновые кислоты. Согласно некоторым вариантам реализации последовательность указанного сайт-специфического полипептида по меньшей мере на 20% идентична нуклеазному домену Cas9. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид представляет собой Cas9. Согласно некоторым вариантам реализации по меньшей мере одна из указанных молекул нуклеиновых кислот кодирует эндорибонуклеазу регулярно расположенных группами коротких палиндромных повторов. Согласно некоторым вариантам реализации последовательность указанной эндорибонуклеазы регулярно расположенных группами коротких палиндромных повторов по меньшей мере на 20% сходна с Csy4. Согласно некоторым вариантам реализации последовательность указанной эндорибонуклеазы регулярно расположенных группами коротких палиндромных повторов по меньшей мере на 60% сходна с Csy4. Согласно некоторым вариантам реализации указанная эндорибонуклеаза регулярно расположенных группами коротких палиндромных повторов представляет собой Csy4. Согласно некоторым вариантам реализации указанная совокупность белков, связывающих нуклеиновые кислоты, обладает пониженной ферментативной активностью. Согласно некоторым вариантам реализации белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с сайтом связывания белка, связывающего нуклеиновые кислоты, не способны расщеплять указанный сайт связывания белка, связывающего нуклеиновые кислоты. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит две молекулы РНК. Согласно некоторым вариантам реализации фрагменты каждой из указанных двух молекул РНК гибридизуются друг с другом. Согласно некоторым вариантам реализации первая молекула из указанных двух молекул РНК содержит последовательность, по меньшей мере на 60% идентичную последовательности РНК регулярно расположенных группами коротких палиндромных повторов на протяжении 8 последовательных нуклеотидов, при этом вторая молекула из указанных двух молекул РНК содержит последовательность, по меньшей мере на 60% идентичную последовательность транс-активирующей РНК регулярно расположенных группами коротких палиндромных повторов на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит одну непрерывную молекулу РНК, при этом указанная непрерывная молекула РНК дополнительно содержит два домена и линкер. Согласно некоторым вариантам реализации фрагменты указанных двух доменов указанной непрерывной молекулы РНК гибридизуются друг с другом. Согласно некоторым вариантам реализации первый фрагмент указанной непрерывной молекулы РНК содержит последовательность, по меньшей мере на 60% идентичную последовательности РНК регулярно расположенных группами коротких палиндромных повторов на протяжении 8 последовательных нуклеотидов, и второй фрагмент указанной непрерывной молекулы РНК содержит последовательность, по меньшей мере на 60% идентичную последовательности транс-активирующей РНК регулярно расположенных группами коротких палиндромных повторов на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, способна гибридизоваться с целевой нуклеиновой кислотой на протяжении 6-20 нуклеотидов. Согласно некоторым вариантам реализации указанная композиция выполнена с возможностью доставки в клетку. Согласно некоторым вариантам реализации указанная композиция выполнена с возможностью доставки равных количеств молекул из совокупности молекул нуклеиновых кислот в клетку. Согласно некоторым вариантам реализации указанная композиция дополнительно содержит молекулу донорного полинуклеотида, при этом указанная молекула донорного полинуклеотида содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом указанный сайт связывания связывается связывающим нуклеиновые кислоты белком гибридного полипептида.
[0067] Согласно одному аспекту в описании предложен способ доставки нуклеиновых кислот во внутриклеточную локализацию в клетке, включающий: введение в клетку композиции, содержащей: совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула нуклеиновой кислоты из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна молекула из совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид, и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты, с обеспечением стехиометрической доставки композиции во внутриклеточную локализацию, образуя структурную единицу, содержащую сайт-специфический полипептид, транслированный с молекулы нуклеиновой кислоты, кодирующей сайт-специфический полипептид, и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и расщепление целевой нуклеиновой кислоты, при этом указанный сайт-специфический полипептид структурной единицы расщепляет целевую нуклеиновую кислоту. Согласно некоторым вариантам реализации белки указанной совокупности белков, связывающих нуклеиновые кислоты, связываются с когнатным сайтом связывания белка, связывающего нуклеиновые кислоты. Согласно некоторым вариантам реализации эндорибонуклеаза расщепляет один из одного или большего количества сайтов связывания белков, связывающих нуклеиновые кислоты. Согласно некоторым вариантам реализации эндорибонуклеаза расщепляет сайты связывания белков, связывающих нуклеиновые кислоты, нуклеиновой кислоты, кодирующей нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, с высвобождением таким образом указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная внутриклеточная локализация выбрана из группы, состоящей из: нуклеазы, ЭР, аппарата Гольджи, митохондрии, клеточной стенки, лизосомы и ядра. Согласно некоторым вариантам реализации указанная внутриклеточная локализация представлена ядром.
[0068] Согласно одному аспекту в описании предложен вектор, содержащий: полинуклеотидную последовательность, кодирующую композицию, содержащую: совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула нуклеиновой кислоты из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна молекула из совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид; и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты, с обеспечением стехиометрической доставки композиции во внутриклеточную локализацию. Согласно некоторым вариантам реализации указанный вектор дополнительно содержит полинуклеотид, кодирующий промотор. Согласно некоторым вариантам реализации указанный промотор функционально связан с полинуклеотидом. Согласно некоторым вариантам реализации указанный промотор представляет собой индуцируемый промотор.
[0069] Согласно одному аспекту в описании предложен генетически модифицированный организм, содержащий вектор, включающий: полинуклеотидную последовательность, кодирующую совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула нуклеиновой кислоты из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна молекула из совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид, и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты, с обеспечением стехиометрической доставки композиции во внутриклеточную локализацию.
[0070] Согласно одному аспекту в описании предложен генетически модифицированный организм, содержащий: композицию, содержащую: совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула нуклеиновой кислоты из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна молекула из совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид; и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты.
[0071] Согласно одному аспекту в описании предложен набор, содержащий: композицию, содержащую: совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула нуклеиновой кислоты из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна молекула из совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид, и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты; и буфер.
[0072] Согласно одному аспекту в описании предложен набор, содержащий: вектор, включающий: полинуклеотидную последовательность, кодирующую совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула нуклеиновой кислоты из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна молекула из совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид; и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты, с обеспечением стехиометрической доставки композиции во внутриклеточную локализацию; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению. Согласно некоторым вариантам реализации указанный буфер выбран из группы, включающей: разбавляющий буфер, восстанавливающий буфер и стабилизирующий буфер, или любую их комбинацию.
[0073] Согласно одному аспекту в описании предложен донорный полинуклеотид, содержащий: представляющий интерес генетический элемент и репортерный элемент, при этом указанный репортерный элемент содержит полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и одну или большее количество нуклеиновых кислот, при этом указанная одна или большее количество нуклеиновых кислот содержит последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов. Согласно некоторым вариантам реализации указанный представляющий интерес генетический элемент содержит ген. Согласно некоторым вариантам реализации указанный представляющий интерес генетический элемент содержит некодирующую нуклеиновую кислоту, выбранную из группы, состоящей из: микроРНК, миРНК и длинной некодирующей РНК, или любой их комбинации. Согласно некоторым вариантам реализации указанный представляющий интерес генетический элемент содержит некодирующий ген. Согласно некоторым вариантам реализации указанный представляющий интерес генетический элемент содержит некодирующую нуклеиновую кислоту, выбранную из группы, состоящей из: микроРНК, миРНК и длинной некодирующей РНК, или любой их комбинации. Согласно некоторым вариантам реализации указанный репортерный элемент содержит ген, выбранный из группы, состоящей из: гена, кодирующего флуоресцентный белок, гена, кодирующего хемилюминесцентный белок и гена устойчивости к антибиотикам, или любой их комбинации. Согласно некоторым вариантам реализации указанный репортерный элемент содержит ген, кодирующий флуоресцентный белок. Согласно некоторым вариантам реализации указанный флуоресцентный белок содержит зеленый флуоресцентный белок. Согласно некоторым вариантам реализации указанный репортерный элемент функционально связан с промотором. Согласно некоторым вариантам реализации указанный промотор включает индуцируемый промотор. Согласно некоторым вариантам реализации указанный промотор включает тканеспецифический промотор. Согласно некоторым вариантам реализации последовательность аминокислот указанного сайт-специфического полипептида по меньшей мере на 15% идентична последовательности нуклеазного домена Cas9. Согласно некоторым вариантам реализации последовательность аминокислот указанного сайт-специфического полипептида по меньшей мере на 95% идентична последовательности Cas9 на протяжении 10 аминокислот. Согласно некоторым вариантам реализации указанный нуклеазный домен выбран из группы, состоящей из: домена HNH, HNH-подобного домена, домена RuvC и RuvC-подобного домена, или любой их комбинации.
[0074] Согласно одному аспекту в описании предложен экспрессионный вектор, содержащий полинуклеотидную последовательность, кодирующую представляющий интерес генетический элемент; и репортерный элемент, при этом указанный репортерный элемент содержит полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и одну или большее количество нуклеиновых кислот, при этом указанная одна или большее количество нуклеиновых кислот содержит последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов.
[0075] Согласно одному аспекту в описании предложена генетически модифицированная клетка, содержащая донорный полинуклеотид, содержащий: представляющий интерес генетический элемент; и репортерный элемент, при этом указанный репортерный элемент содержит полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и одну или большее количество нуклеиновых кислот, при этом указанная одна или большее количество нуклеиновых кислот содержит последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов.
[0076] Согласно одному аспекту в описании предложен набор, содержащий: донорный полинуклеотид, содержащий: представляющий интерес генетический элемент; и репортерный элемент, при этом указанный репортерный элемент содержит полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и одну или большее количество нуклеиновых кислот, при этом указанная одна или большее количество нуклеиновых кислот содержит последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит: полипептид, последовательность аминокислот которого по меньшей мере на 10% идентичная последовательности аминокислот Cas9; и нуклеиновая кислота, при этом указанная нуклеиновая кислота связывается с указанным полипептидом и гибридизуется с целевой нуклеиновой кислотой. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению. Согласно некоторым вариантам реализации указанный набор дополнительно содержит полинуклеотид, кодирующий полинуклеотид, при этом последовательность аминокислот указанного полипептида по меньшей мере на 15% идентична Cas9. Согласно некоторым вариантам реализации указанный набор дополнительно содержит полинуклеотид, кодирующий нуклеиновую кислоту, при этом указанная нуклеиновая кислота содержит последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов.
[0077] Согласно одному аспекту в описании предложен способ выбора клетки с применением репортерного элемента и удалением репортерного элемента из клетки, включающий: приведение целевой нуклеиновой кислоты в контакт с комплексом, содержащим сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту; расщепление целевой нуклеиновой кислоты сайт-специфическим полипептидом для получения расщепленной целевой нуклеиновой кислоты; встраивание донорного полинуклеотида, содержащего генетический элемент, представляющий интерес; и репортерного элемента, при этом указанный репортерный элемент содержит полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и одну или большее количество нуклеиновых кислот, при этом указанная одна или большее количество нуклеиновых кислот содержит последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов расщепленную целевую нуклеиновую кислоту; и выбор клетки на основании донорного полинуклеотида для получения выбранной клетки. Согласно некоторым вариантам реализации выбор включает выбор клетки от субъекта, получающего лечение заболевания. Согласно некоторым вариантам реализации выбор включает выбор клетки от субъекта, у которого диагностируют заболевание. Согласно некоторым вариантам реализации после выбора клетка содержит указанный донорный полинуклеотид. Согласно некоторым вариантам реализации указанный способ дополнительно включает вырезание всех репортерных элементов, некоторых репортерных элементов или ни одного из репортерных элементов, с получением таким образом второй выбранной клетки. Согласно некоторым вариантам реализации вырезание включает приведение 5'-конца репортерного элемента в контакт с комплексом, содержащим сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанный комплекс расщепляет указанный 5'-конец. Согласно некоторым вариантам реализации вырезание включает приведение 3'-конца репортерного элемента в контакт с комплексом, содержащим сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанный комплекс расщепляет указанный 3'-конец. Согласно некоторым вариантам реализации вырезание включает приведение в контакт 5'-и 3'-концов репортерного элемента с одним или большим количеством комплексов, содержащих сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанный комплекс расщепляет указанные 5'- и 3'-конец. Согласно некоторым вариантам реализации указанный способ дополнительно включает скрининг указанной второй выбранной клетки. Согласно некоторым вариантам реализации скрининг включает наблюдение отсутствия всех или некоторых репортерных элементов.
[0078] Согласно одному аспекту в описании предложена композиция, содержащая: нуклеиновую кислоту, содержащую: спейсер, причем длина указанного спейсера составляет 12-30 нуклеотидов, включительно, при этом указанный спейсер способен гибридизоваться с последовательностью, расположенной в направлении 5' от РАМ; первый дуплекс, при этом указанный первый дуплекс расположен в направлении 3' от указанного спейсера; петлю, при этом указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на первой цепи первого дуплекса и по меньшей мере 1 неспаренный нуклеотид на второй цепи первого дуплекса; линкер, при этом указанный линкер соединяет первую цепь и вторую цепь дуплекса и его длина составляет по меньшей мере 3 нуклеотида; Р-домен; и второй дуплекс, при этом указанный второй дуплекс расположен в направлении 3' от Р-домена и выполнен с возможностью связывания с сайт-специфическим полипептидом. Согласно некоторым вариантам реализации длина последовательности, расположенной в направлении 5' от РАМ, составляет по меньшей мере 18 нуклеотидов. Согласно некоторым вариантам реализации последовательность, расположенная в направлении 5' от РАМ, примыкает к РАМ. Согласно некоторым вариантам реализации указанный РАМ включает 5'-NGG-3'. Согласно некоторым вариантам реализации указанный первый дуплекс примыкает к спейсеру. Согласно некоторым вариантам реализации указанный Р-домен начинается через 1-5 нуклеотидов в направлении 3' от дуплекса, содержит по меньшей мере 4 нуклеотида и способна гибридизоваться с последовательностью, выбранной из группы, состоящей из: последовательности примыкающего к протоспейсеру мотива 5'-NGG-3', последовательности, по меньшей мере на 50% идентичной последовательности аминокислот 1096-1225 Cas9 S. pyogenes, или любой их комбинации. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид содержит последовательность, по меньшей мере на 15% идентичную последовательности нуклеазного домена Cas9 S. pyogenes. Согласно некоторым вариантам реализации указанная нуклеиновая кислота представляет собой РНК. Согласно некоторым вариантам реализации указанная нуклеиновая кислота представляет собой А-форму РНК. Согласно некоторым вариантам реализации длина указанного первого дуплекса составляет по меньшей мере 6 нуклеотидов. Согласно некоторым вариантам реализации 3 неспаренных нуклеотида петли включают 5'-AAG-3'. Согласно некоторым вариантам реализации к 3 неспаренным нуклеотидам примыкает нуклеотид, образующий неоднозначную пару с нуклеотидом на второй цепи первого дуплекса. Согласно некоторым вариантам реализации указанный полипептид связывается с областью нуклеиновой кислоты, выбранной из группы, состоящей из: первого дуплекса, второго дуплекса и Р-домена, или любой их комбинации.
[0079] Согласно одному аспекту в описании предложен способ модификации целевой нуклеиновой кислоты, включающий: приведение целевой нуклеиновой кислоты в контакт с композицией, содержащей: нуклеиновую кислоту, содержащую: спейсер, причем длина указанного спейсера составляет 12-30 нуклеотидов включительно, при этом указанный спейсер способен гибридизоваться с последовательностью, расположенной в направлении 5' от РАМ; первый дуплекс, при этом указанный первый дуплекс расположен в направлении 3' от указанного спейсера; петлю, при этом указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на первой цепи первого дуплекса и по меньшей мере 1 неспаренный нуклеотид на второй цепи первого дуплекса; линкер, при этом указанный линкер соединяет первую цепь и вторую цепь указанного дуплекса и его длина составляет по меньшей мере 3 нуклеотида; Р-домен; и второй дуплекс, при этом указанный второй дуплекс расположен в направлении 3' от указанного Р-домена и выполнен с возможностью связывания с сайт-специфическим полипептидом; и модификацию целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный способ дополнительно включает приведение в контакт с сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанное приведение в контакт включает приведение спейсера в контакт с целевой нуклеиновой кислотой. Согласно некоторым вариантам реализации указанная модификация включает расщепление целевой нуклеиновой кислоты с получением расщепленной целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанное расщепление осуществляется сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанный способ дополнительно включает встраивание донорного полинуклеотида в расщепленную целевую нуклеиновую кислоту. Согласно некоторым вариантам реализации указанная модификация включает модификацию транскрипции целевой нуклеиновой кислоты.
[0080] Согласно одному аспекту в описании предложен вектор, содержащий полинуклеотидную последовательность, кодирующую нуклеиновую кислоту, содержащую: спейсер, причем длина указанного спейсера составляет 12-30 нуклеотидов включительно, при этом указанный спейсер способен гибридизоваться с последовательностью, расположенной в направлении 5' от РАМ; первый дуплекс, при этом указанный первый дуплекс расположен в направлении 3' от указанного спейсера; петлю, при этом указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на первой цепи первого дуплекса и по меньшей мере 1 неспаренный нуклеотид на второй цепи первого дуплекса; линкер, при этом указанный линкер соединяет первую цепь и вторую цепь указанного дуплекса и его длина составляет по меньшей мере 3 нуклеотидов; Р-домен; и второй дуплекс, при этом указанный второй дуплекс расположен в направлении 3' от указанного Р-домена и выполнен с возможностью связывания с сайт-специфическим полипептидом.
[0081] Согласно одному аспекту в описании предложен набор, содержащий: композицию, содержащую: нуклеиновую кислоту, содержащую: спейсер, причем длина указанного спейсера составляет 12-30 нуклеотидов, включительно, при этом указанный спейсер способен гибридизоваться с последовательностью, расположенной в направлении 5' от РАМ; первый дуплекс, при этом указанный первый дуплекс расположен в направлении 3' от указанного спейсера; петлю, при этом указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на первой цепи первого дуплекса и по меньшей мере 1 неспаренный нуклеотид на второй цепи первого дуплекса; линкер, при этом указанный линкер соединяет первую цепь и вторую цепь указанного дуплекса и его длина составляет по меньшей мере 3 нуклеотидов; Р-домен; и второй дуплекс, при этом указанный второй дуплекс расположен в направлении 3' от указанного Р-домена и выполнен с возможностью связывания с сайт-специфическим полипептидом; и буфер. Согласно некоторым вариантам реализации указанный набор дополнительно содержит сайт-специфический полипептид. Согласно некоторым вариантам реализации указанный набор дополнительно содержит донорный полинуклеотид. Согласно некоторым вариантам реализации указанный набор дополнительно содержит инструкции по применению.
[0082] Согласно одному аспекту в описании предложен способ получения сконструированной синтетическим путем нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, включающий: конструирование композиции, содержащей: нуклеиновую кислоту, содержащую: спейсер, причем длина указанного спейсера составляет 12-30 нуклеотидов, включительно, при этом указанный спейсер способен гибридизоваться с последовательностью, расположенной в направлении 5' от РАМ; первый дуплекс, при этом указанный первый дуплекс расположен в направлении 3' от указанного спейсера; петлю, при этом указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на первой цепи первого дуплекса и по меньшей мере 1 неспаренный нуклеотид на второй цепи первого дуплекса; линкер, при этом указанный линкер соединяет первую цепь и вторую цепь указанного дуплекса и его длина составляет по меньшей мере 3 нуклеотидов; Р-домен; и второй дуплекс, при этом указанный второй дуплекс расположен в направлении 3' от указанного Р-домена и выполнен с возможностью связывания с сайт-специфическим полипептидом.
[0083] Согласно одному аспекту в описании предложена фармацевтическая композиция, содержащая сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, выбранную из группы, состоящей из: сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, содержащей: мутацию в Р-домене указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, содержащей: мутацию в области петли нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту
[0084] Согласно одному аспекту в описании предложена фармацевтическая композиция, включающая композицию, выбранную из группы, состоящей из: композиции, содержащей: сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую 3'-гибридизующееся удлинение, и донорный полинуклеотид, отличающийся тем, что донорный полинуклеотид гибридизуется с указанным 3'-гибридизующимся удлинением; композиции, содержащей: эффекторный белок и нуклеиновую кислоту, при это указанная нуклеиновая кислота содержит: последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов, и ненативную последовательность, при этом нуклеиновая кислота способна связываться с указанным эффекторным белком; композиции, содержащей: агент для мультиплексного генетического нацеливания, отличающийся тем, что указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность и выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, при этом указанный модуль нуклеиновой кислоты способна гибридизоваться с целевой нуклеиновой кислотой; композиции, содержащей: модифицированный сайт-специфический полипептид, отличающийся тем, что указанный полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на второй примыкающий к протоспейсеру мотив; композиции, содержащей: модифицированный сайт-специфический полипептид, отличающийся тем, что полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту; композиции, содержащей: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в спиральном мостике; композиции, содержащей: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в высокоосновном участке; композиции, содержащей: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в полимераза-подобном домене; композиции, содержащей: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в спиральном мостике, высокоосновном участке, нуклеазном домене и полимеразном домене, или любую их комбинацию; композиции, содержащей: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модифицированный нуклеазный домен; композиции, содержащей: первый комплекс, включающий: первый сайт-специфический полипептид и первую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, второй комплекс, включающий: второй сайт-специфический полипептид и вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, причем указанные первая и вторая нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, различаются; композиции, содержащей: совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна из молекул указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна из молекул указанной совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид, и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность указанных белков, связывающих нуклеиновые кислоты, причем белки указанной совокупности белков, связывающие нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты; и композиции, содержащей: нуклеиновую кислоту, содержащую: спейсер, длина которого составляет 12-30 нуклеотидов включительно, и который способна гибридизоваться с последовательностью, расположенной в направлении 5' от РАМ, первый дуплекс, отличающийся тем, что указанный первый дуплекс расположен в направлении 3' от указанного спейсера, петлю, отличающуюся тем, что указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на первой цепи указанного первого дуплекса и по меньшей мере 1 неспаренный нуклеотид на второй цепи указанного первого дуплекса, линкер, отличающийся тем, что указанный линкер соединяет указанную первую цепь и указанную вторую цепь указанного дуплекса, и его длина составляет по меньшей мере 3 нуклеотида, Р-домен и второй дуплекс, отличающийся тем, что указанный второй дуплекс расположен в направлении 3' от указанного Р-домена и выполнен с возможностью связывания с сайт-специфическим полипептидом; или любую их комбинацию.
[0085] Согласно одному аспекту в описании предложена фармацевтическая композиция, содержащая модифицированный сайт-специфический полипептид, содержащий: первый нуклеазный домен, второй нуклеазный домен и встроенный нуклеазный домен.
[0086] Согласно одному аспекту в описании предложена фармацевтическая композиция, содержащая донорный полинуклеотид, содержащий: представляющий интерес генетический элемент и репортерный элемент, отличающийся тем, что указанный репортерный элемент содержит полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и одну или большее количество нуклеиновых кислот, при этом указанные одна или большее количество нуклеиновых кислот содержат последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов.
[0087] Согласно одному аспекту в описании предложена фармацевтическая композиция, содержащая вектор, выбранный из группы, состоящей из: вектора, содержащего полинуклеотидную последовательность, кодирующую сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую: мутацию в Р-домене указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; вектора, содержащего полинуклеотидную последовательность, кодирующую сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую: мутацию в области петли нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; и модификацию целевой нуклеиновой кислоты; вектора, содержащего полинуклеотидную последовательность, кодирующую модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность; вектора, содержащего: полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит последовательность, подходящую для связывания с эффекторным белком, и сайт-специфический полипептид; вектора, содержащего полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность, сайт-специфический полипептид и эффекторный белок; вектора, содержащего полинуклеотидную последовательность, кодирующую агент для мультиплексного генетического нацеливания, при этом указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, и при этом указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, и при этом указанный модуль нуклеиновой кислоты способен гибридизоваться с целевой нуклеиновой кислотой; вектора, содержащего полинуклеотидную последовательность, кодирующую модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в спиральном мостике, высокоосновном участке, нуклеазном домене и полимеразном домене, или любую их комбинацию; вектора, содержащего полинуклеотидную последовательность, кодирующую: две или большее количество нуклеиновых кислот, которые нацелены на нуклеиновые кислоты, отличающихся по меньшей мере одним нуклеотидом; и сайт-специфический полипептид; вектора, содержащего полинуклеотидную последовательность, кодирующую композицию, содержащую: совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула нуклеиновой кислоты из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна молекула из совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид; и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты, с обеспечением стехиометрической доставки композиции во внутриклеточную локализацию; экспрессионного вектора, содержащего полинуклеотидную последовательность, кодирующую представляющий интерес генетический элемент; и репортерный элемент, при этом указанный репортерный элемент содержит полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и одну или большее количество нуклеиновых кислот, при этом указанная одна или большее количество нуклеиновых кислот содержит последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов; и вектора, содержащего полинуклеотидную последовательность, кодирующую нуклеиновую кислоту, содержащую: спейсер, причем длина указанного спейсера составляет 12-30 нуклеотидов включительно, при этом указанный спейсер способен гибридизоваться с последовательностью, расположенной в направлении 5' от РАМ; первый дуплекс, при этом указанный первый дуплекс расположен в направлении 3' от указанного спейсера; петлю, при этом указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на первой цепи первого дуплекса и по меньшей мере 1 неспаренный нуклеотид на второй цепи первого дуплекса; линкер, при этом указанный линкер соединяет первую цепь и вторую цепь указанного дуплекса и его длина составляет по меньшей мере 3 нуклеотидов; Р-домен; и второй дуплекс, при этом указанный второй дуплекс расположен в направлении 3' от указанного Р-домена и способна связываться с сайт-специфическим полипептидом; или любую их комбинацию.
[0088] Согласно одному аспекту в описании предложен способ лечения заболевания, включающий введение субъекту: сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, содержащей: мутацию в Р-домене указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, содержащей: мутацию в области петли нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; композиции, содержащей: сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую 3'-гибридизующееся удлинение и донорный полинуклеотид, причем указанный донорный полинуклеотид гибридизуется с указанным 3'-гибридизующимся удлинением; композиции, содержащей: эффекторный белок и нуклеиновую кислоту, причем указанная нуклеиновая кислота содержит: последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов, и ненативную последовательность, отличающуюся тем, что указанная нуклеиновая кислота способна связываться с указанным эффекторным белком; композиции, содержащей: агент для мультиплексного генетического нацеливания, отличающийся тем, что указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, при этом указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, и при этом указанный модуль нуклеиновой кислоты способна гибридизоваться с целевой нуклеиновой кислотой; композиции, содержащей: модифицированный сайт-специфический полипептид, отличающийся тем, что указанный полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на второй примыкающий к протоспейсеру мотив; композиции, содержащей: модифицированный сайт-специфический полипептид, отличающийся тем, что указанный полипептид модифицирован относительно сайт-специфического полипептида дикого типа таким образом, что он выполнен с возможностью нацеливания на вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту; композиции, содержащей: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в спиральном мостике; композиции, содержащей: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в высокоосновном участке; композиции, содержащей: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в полимераза-подобном домене; композиции, содержащей: модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в спиральном мостике, высокоосновном участке, нуклеазном домене и полимеразном домене, или любую их комбинацию; композиции, содержащей: модифицированный сайт-специфический полипептид, содержащий модифицированный относительно SEQ ID: 8нуклеазный домен; композиции, содержащей: первый комплекс, включающий: первый сайт-специфический полипептид и первую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, второй комплекс, включающий: второй сайт-специфический полипептид и вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при это указанные первая и вторая нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, различаются; композиции, содержащей: совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту и одна молекула из указанной совокупность молекул нуклеиновых кислот кодирует сайт-специфический полипептид, и гибридный полипептид, отличающийся тем, что указанный гибридный полипептид содержит совокупность указанных белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты; композиции, содержащей: нуклеиновую кислоту, содержащую: спейсер, длина которого составляет 12-30 нуклеотидов включительно, при этом указанный спейсер способен гибридизоваться с последовательностью, расположенной в направлении 5' от РАМ, первый дуплекс, отличающийся тем, что указанный первый дуплекс расположен в направлении 3' от указанного спейсера, петлю, отличающуюся тем, что указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на первой цепи указанного первого дуплекса и по меньшей мере 1 неспаренный нуклеотид на второй цепи указанного первого дуплекса, линкер, отличающийся тем, что указанный линкер соединяет указанную первую цепь и указанная вторая цепь указанного дуплекса, и его длина составляет по меньшей мере 3 нуклеотидов, Р-домен и второй дуплекс, отличающийся тем, что указанный второй дуплекс расположен в направлении 3' от указанного Р-домена и выполнен с возможностью связывания с сайт-специфическим полипептидом; модифицированный сайт-специфический полипептид, содержащий: первый нуклеазный домен, второй нуклеазный домен и встроенный нуклеазный домен; донорный полинуклеотид, содержащий: представляющий интерес генетический элемент и репортерный элемент, отличающийся тем, что указанный репортерный элемент содержит полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и одну или большее количество нуклеиновых кислот, при этом указанные одна или большее количество нуклеиновых кислот содержат последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов; вектора, содержащего полинуклеотидную последовательность, кодирующую сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую: мутацию в Р-домене указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; вектора, содержащего полинуклеотидную последовательность, кодирующего сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую: мутацию в области петли нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту; и модификацию целевой нуклеиновой кислоты; вектора, содержащего полинуклеотидную последовательность, кодирующую модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность; вектора, содержащего: полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит последовательность, подходящую для связывания с эффекторным белком, и а сайт-специфический полипептид; вектора, содержащего полинуклеотидную последовательность, кодирующую: модифицированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанная модифицированная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит ненативную последовательность, сайт-специфический полипептид и эффекторный белок; вектора, содержащего полинуклеотидную последовательность, кодирующую агент для мультиплексного генетического нацеливания, при этом указанный агент для мультиплексного генетического нацеливания содержит один или большее количество модулей нуклеиновых кислот, при этом указанный модуль нуклеиновой кислоты содержит ненативную последовательность, и при этом указанный модуль нуклеиновой кислоты выполнен с возможностью связывания с полипептидом, содержащим последовательность аминокислот, по меньшей мере на 10% идентичную последовательности нуклеазного домена Cas9, и при этом указанный модуль нуклеиновой кислоты способен гибридизоваться с целевой нуклеиновой кислотой; вектора, содержащего полинуклеотидную последовательность, кодирующую модифицированный относительно SEQ ID: 8 сайт-специфический полипептид, содержащий модификацию в спиральном мостике, высокоосновном участке, нуклеазном домене и полимеразном домене, или любую их комбинацию; вектора, содержащего полинуклеотидную последовательность, кодирующую: два или большее количество нуклеиновых кислот, которые нацелены на нуклеиновые кислоты, отличающихся по меньшей мере одним нуклеотидом; и сайт-специфический полипептид; вектора, содержащего полинуклеотидную последовательность, кодирующую композицию, содержащую: совокупность молекул нуклеиновых кислот, где каждая молекула нуклеиновой кислоты содержит сайт связывания белка, связывающего нуклеиновые кислоты, при этом по меньшей мере одна молекула нуклеиновой кислоты из указанной совокупности молекул нуклеиновых кислот кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна молекула из совокупности молекул нуклеиновых кислот кодирует сайт-специфический полипептид; и гибридный полипептид, при этом указанный гибридный полипептид содержит совокупность белков, связывающих нуклеиновые кислоты, при этом белки указанной совокупности белков, связывающих нуклеиновые кислоты, подходят для связывания с соответствующим им когнатным сайтом связывания белков, связывающих нуклеиновые кислоты, с обеспечением стехиометрической доставки композиции во внутриклеточную локализацию; экспрессионный вектор, содержащий полинуклеотидную последовательность, кодирующую представляющий интерес генетический элемент; и репортерный элемент, при этом указанный репортерный элемент содержит полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и одну или большее количество нуклеиновых кислот, при этом указанная одна или большее количество нуклеиновых кислот содержит последовательность, по меньшей мере на 50% идентичную последовательности crRNA на протяжении 6 последовательных нуклеотидов, и последовательность, по меньшей мере на 50% идентичную последовательности tracrRNA на протяжении 6 последовательных нуклеотидов; и вектор, содержащий полинуклеотидную последовательность, кодирующую нуклеиновую кислоту, содержащую: спейсер, причем длина указанного спейсера составляет 12-30 нуклеотидов включительно, при этом указанный спейсер способен гибридизоваться с последовательностью, расположенной в направлении 5' от РАМ; первый дуплекс, при этом указанный первый дуплекс расположен в направлении 3' от указанного спейсера; петлю, при этом указанная петля содержит по меньшей мере 3 неспаренных нуклеотида на первой цепи первого дуплекса и по меньшей мере 1 неспаренный нуклеотид на второй цепи первого дуплекса; линкер, при этом указанный линкер соединяет первую цепь и вторую цепь указанного дуплекса и его длина составляет по меньшей мере 3 нуклеотидов; Р-домен; и второй дуплекс, при этом указанный второй дуплекс расположен в направлении 3' от указанного Р-домена и выполнен с возможностью связывания с сайт-специфическим полипептидом; или любую их комбинацию. Согласно некоторым вариантам реализации указанное введение включает введение путем вирусной доставки. Согласно некоторым вариантам реализации указанное введение включает введение путем электропорации. Согласно некоторым вариантам реализации указанное введение включает введение с применением наночастиц. Согласно некоторым вариантам реализации указанное введение включает введение путем липосомальной доставки. Согласно некоторым вариантам реализации указанное введение включает введение с применением способа, выбранного из группы, состоящей из: внутривенного, подкожного, внутримышечного, перорального, ректального, аэрозольного, патентерального, офтальмологического, пульмонального, чрескожного, вагинального, отикального, назального и местного введения, или любой их комбинации. Согласно некоторым вариантам реализации предложенные в настоящем изобретении способы реализуют в клетке, выбранной из группы, состоящей из: растительной клетки, клетки микроорганизма и грибной клетки, или любой их комбинации.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛОК
[0089] Все публикации, патенты и патентные заявки, упоминаемые в настоящем описании, включены в него посредством ссылки в том же объеме, как если бы каждая индивидуальная публикация, патент или патентная заявка был(а) конкретным образом индивидуально включен(а) посредством ссылки.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0090] Новые признаки предложенного изобретения конкретным образом представлены в прилагаемой формуле изобретения. Лучшее понимание признаков и преимуществ настоящего изобретения может быть достигнуто при обращении к приведенному ниже подробному описанию, проиллюстрированному конкретными примерами вариантов реализации, в которых применяются принципы настоящего изобретения, и следующим сопроводительным чертежам:
[0091] На Фиг. 1А показан пример варианта реализации одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту предложенного в настоящем изобретении.
[0092] На Фиг. 1В показан пример варианта реализации одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, предложенного в настоящем изобретении.
[0093] На Фиг. 2 показан пример варианта реализации двойной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, предложенного в настоящем изобретении.
[0094] На Фиг. 3 показан пример варианта реализации способа обогащения последовательностей предложенного в настоящем изобретении с применением расщепления целевой нуклеиновой кислоты.
[0095] На Фиг. 4 показан пример варианта реализации предложенного в настоящем изобретении способа обогащения последовательностей с применением обогащения целевой нуклеиновой кислоты.
[0096] На Фиг. 5 показан пример варианта реализации предложенного в настоящем изобретении способа определения нецелевых сайтов связывания сайт-специфического полипептида с применением очищения сайт-специфического полипептида.
[0097] На Фиг. 6 показан пример варианта реализации предложенного в настоящем изобретении способа определения нецелевых сайтов связывания сайт-специфического полипептида с применением очищения нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту.
[0098] На Фиг. 7 представлен пример варианта реализации метода секвенирования на основе матриц с применением сайт-специфического полипептида, предложенного в настоящем изобретении.
[0099] На Фиг. 8 представлен пример варианта реализации метода секвенирования на основе матриц с применением сайт-специфического полипептида, предложенного в настоящем изобретении, с секвенированием расщепленных продуктов.
[00100] На Фиг. 9 представлен пример варианта реализации способа на основе секвенирования нового поколения с применением сайт-специфического полипептида, предложенного в настоящем изобретении.
[00101] На Фиг. 10 представлен пример меченой одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту.
[00102] На Фиг. 11 представлен пример меченой двойной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту.
[00103] На Фиг. 12 представлен пример варианта реализации способа применения меченой нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту с комбинированной системой (например, комбинированной флуоресцентной системой).
[00104] На Фиг. 13 представлены некоторые примеры данных относительно эффекта 5'-меченой нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, на расщепление целевой нуклеиновой кислоты.
[00105] На Фиг. 14 представлен пример 5'-меченой нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, содержащей линкерную последовательность метки между нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, и меткой.
[00106] На Фиг. 15 представлен пример варианта реализации способа мультиплексного расщепления целевых нуклеиновых кислот.
[00107] На Фиг. 16 представлен пример варианта реализации способа стехиометрической доставки рибонуклеиновых кислот.
[00108] На Фиг. 17 представлен пример варианта реализации способа стехиометрической доставки нуклеиновых кислот.
[00109] На Фиг. 18 представлен пример варианта реализации эффективного встраивания репортерного элемента в целевую нуклеиновую кислоту с применением сайт-специфического полипептида, предложенного в настоящем изобретении.
[00110] На Фиг. 19 представлен пример варианта реализации способа удаления репортерного элемента из целевой нуклеиновой кислоты.
[00111] На Фиг. 20 показаны комплементарные фрагменты последовательностей нуклеиновых кислот пре-CRISPR и последовательностей нуклеиновых кислот tracr из Streptococcus pyogenes SF370.
[00112] На Фиг. 21 представлен пример вторичной структуры синтетической одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту.
[00113] На Фиг. 22А и В представлен пример вариантов остова одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Нуклеотиды внутри прямоугольников соответствуют нуклеотидам, которые были изменены относительно последовательностей CRISPR, отмеченных как последовательность FL-tracr-crRNA.
[00114] На Фиг. 23А-С представлен пример данных анализа расщепления in vitro. Результаты показывают, что расщепление сайт-специфическим полипептидом может поддерживаться более чем одной синтетической последовательностью остова нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту (например, Cas9).
[00115] На Фиг. 24 представлен пример синтетических последовательностей одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, с вариациями в комплементарной области/дуплексе. Нуклеотиды внутри прямоугольников соответствуют нуклеотидам, которые были изменены относительно последовательностей CRISPR, отмеченных как последовательность FL-tracr-crRNA.
[00116] На Фиг. 25 представлены примеры вариантов структуры одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, в области, расположенной 3' от комплементарной области/дуплекса. Нуклеотиды внутри прямоугольников соответствуют нуклеотидам, которые были изменены относительно встречающегося в природе спаривания последовательностей нуклеиновых кислот S. pyogenes SF370 CRISPR и tracr.
[00117] На Фиг. 26А-В представлены примеры вариантов структуры одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, в области, расположенной 3' от комплементарной области/дуплекса. Нуклеотиды внутри прямоугольников соответствуют нуклеотидам, которые были изменены относительно встречающегося в природе спаривания последовательностей нуклеиновых кислот S. pyogenes SF370 CRISPR и tracr.
[00118] На Фиг. 27А-В представлен пример варианта структур нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, содержащего дополнительные шпилечные последовательности, полученные из повтора CRISPR Pseudomonas aeruginosa (PA14). Последовательности внутри прямоугольников могут связываться с рибонуклеазой Csy4 из PA14.
[00119] На Фиг. 28 представлен пример данных, полученных в анализе расщепления in vitro, показывающих, что расщеплению Cas9 способствуют несколько синтетических последовательностей остова нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Верхние и нижние снимки геля соответствуют двум независимым повторностям анализа.
[00120] На Фиг. 29 представлен пример данных, полученных в анализе расщепления in vitro показывающих, что расщеплению Cas9 способствуют несколько синтетических последовательностей остова нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Верхние и нижние снимки геля соответствуют двум независимым повторностям анализа.
[00121] На Фиг. 30 представлены примеры предложенных в настоящем изобретении способов доставки донорного полинуклеотида к сайту модификации в целевой нуклеиновой кислоте.
[00122] На Фиг. 31 показана система хранения и распространения информации в электронном виде.
[00123] На Фиг. 32 показан пример варианта реализации двух никаз, обеспечивающих образование «тупого конца» в целевой нуклеиновой кислоте. Сайт-специфические модифицирующие полипептиды, образующие комплекс с нуклеиновыми кислотами, которые нацелены на нуклеиновые кислоты, не показаны.
[00124] На Фиг. 33 показан пример варианта реализации ступенчатого разрыва целевой нуклеиновой кислоты с применением двух никаз и получением липких концов. Сайт-специфические модифицирующие полипептиды, образующие комплекс с нуклеиновыми кислотами, которые нацелены на нуклеиновые кислоты, не показаны.
[00125] На Фиг. 34 показан пример варианта реализации ступенчатого разрыва целевой нуклеиновой кислоты с применением двух никаз и получением липких концов среднего размера. Сайт-специфические модифицирующие полипептиды, образующие комплекс с нуклеиновыми кислотами, которые нацелены на нуклеиновые кислоты, не показаны.
[00126] На Фиг. 35 показано выравнивание последовательностей ортологов Cas9. Аминокислоты с символом «X» под ними могут считаться одинаковыми. Аминокислоты с символом «Y» под ними могут считаться высококонсервативными или идентичными во всех последовательностях. Остатки аминокислот без «X» или «Y» могут не быть консервативными.
[00127] На Фиг. 36 показана функциональность вариантов нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, в отношении расщепления целевой нуклеиновой кислоты. Протестированные варианты на Фиг. 36 соответствуют вариантам, представленным на Фиг. 22, Фиг. 24 и Фиг. 25.
[00128] На Фиг. 37A-D представлены анализы расщепления in vitro с применением вариантов нуклеиновых кислот, которые нацелены на нуклеиновые кислоты.
[00129] На Фиг. 38 приведены примеры последовательностей аминокислот Csy4 P. aeruginosa дикого типа
[00130] На Фиг. 39 приведены примеры последовательностей аминокислот ферментативно неактивной эндорибонуклеазы (например, Csy4).
[00131] На Фиг. 40 приведены примеры последовательностей аминокислот Csy4 из Р. aeruginosa.
[00132] На Фиг. 41A-J приведены примеры последовательностей аминокислот Cas6.
[00133] На Фиг. 42А-С приведены примеры последовательностей аминокислот Cas6.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0134] Определения
[0135] В настоящей заявке термин «аффинная метка» может относиться к пептидной аффинной метке или нуклеиновой аффинной метке. Аффинная метка, как правило, относится к белку или последовательности нуклеиновой кислоты, которая может быть связана с молекулой (например, связана ковалентной связью с малой молекулой, белком). Аффинная метка может представлять собой ненативную последовательность. Пептидная аффинная метка может содержать пептид. Пептидная аффинная метка может представлять собой метку, которая может быть частью комбинированной системы (например, два неактивных пептидных фрагмента могут объединиться в процессе трансляции с образованием активной аффинной метки). Нуклеиновая аффинная метка может содержать нуклеиновую кислоту. Нуклеиновая аффинная метка может представлять собой последовательность, которая способна селективно связываться с известной последовательностью нуклеиновой кислоты (например, посредством гибридизации). Нуклеиновая аффинная метка может представлять собой последовательность, которая способна селективно связываться с белком. Аффинная метка может быть гибридизована с нативным белком. Аффинная метка может быть гибридизована с нуклеотидной последовательностью. В некоторых случаях одна, две или более аффинных меток могут быть гибридизованы с нативным белком или нуклеотидной последовательностью. Аффинная метка может быть введена в нуклеиновую кислоту, направленную против нуклеиновой кислоты, с использованием методов транскрипции в условиях in vitro или in vivo. Нуклеиновые аффинные метки могут включать, например, химическую метку, последовательность, связывающую РНК-связывающий белок, последовательность, связывающую ДНК-связывающий белок, последовательность, которая может быть гибридизована с аффинномеченым полинуклеотидом, синтетический РНК-аптамер или синтетический ДНК-аптамер. Примеры химических нуклеиновых аффинных меток могут включать, но не ограничиваются ими, рибонуклеотрифосфаты, содержащие биотин, флуоресцентные красители и дигоксигенин. Примеры белоксвязывающих нуклеиновых аффинных меток могут включать, но не ограничиваются ими, MS2-связывающую последовательность, U1A-связывающую последовательность, белковую последовательность, связывающую структуру типа «стебель-петля», последовательность boxB, последовательность eIF4A или любую последовательность, которая распознается РНК-связывающим белком. Примеры олигонуклеотидов, содержащих нуклеиновую аффинную метку, могут включать, но не ограничиваются ими, биотинилированные олигонуклеотиды, 2,4-динитрофенил-содержащие олигонуклеотиды, меченые флуоресцеином олигонуклеотиды и олигонуклеотиды, конъюгированные с первичными аминами.
[0136] Нуклеиновая аффинная метка может представлять собой РНК-аптамер. Аптамеры могут включать, аптамеры, которые связываются с теофиллином, стрептавидином, декстраном В512, аденозином, гуанозином, гуанином/ксантином, 7-метил-ГТФ, аминокислотные аптамеры, такие как аптамеры, которые связываются с аргинином, цитруллином, валином, триптофаном, цианкобаламином, N-метилмезопорфирином IX, флавином, НАД, и антибиотические аптамеры, такие как аптамеры, которые связываются с тобрамицином, неомицином, ливидомицином, канамицином, стрептомицином, виомицином и хлорамфениколом.
[0137] Нуклеиновая аффинная метка может содержать последовательность РНК, которая может быть связана с сайт-направленным полипептидом. Сайт-направленный полипептид может быть условно ферментативно неактивным. Последовательность РНК может содержать последовательность, которая может быть связана с членом систем CRISPR типа I, типа II и/или типа III. Последовательность РНК может быть связана с членом семейства загадочных белков, ассоциированных с повторами (RAMP). Последовательность РНК может быть связана с членом семейства белков Cas6 (например, Csy4, Cas6). Последовательность РНК может быть связана с членом семейства белков Cas5 (например, Cas5). Например, Csy4 может с высокой аффинностью связываться со специфичной последовательностью-шпилькой РНК (Kd ~ 50 пМ) и может расщеплять РНК в участке, расположенном в направлении 3'-конца относительно шпильки. Член семейства белков Cas5 или Cas6 может связываться с последовательностью РНК, которая по меньшей мере приблизительно или не более чем приблизительно на 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95% или 100% идентична и/или гомологична следующим нуклеотидным последовательностям:


[0138] Нуклеиновая аффинная метка может содержать последовательность ДНК, которая может быть связана с сайт-направленным полипептидом. Сайт-направленный полипептид может быть условно ферментативно неактивным. Последовательность ДНК может содержать последовательность, которая может быть связана с членом системы CRISPR типа I, типа II и/или типа III. Последовательность ДНК может быть связана с белком Argonaut. Последовательность ДНК может быть связана с белком, содержащим домен «цинковый палец», домен TALE или любой другой ДНК-связывающий домен.
[0139] Нуклеиновая аффинная метка может содержать последовательность рибозима. Подходящие рибозимы могут включать пептидилтрансферазу в V-домене 23 S рРНК, РНКазу Р, интроны группы I, интроны группы II, GIR1-копирующий рибозим, лидзим, рибозимы шпильки, рибозимы типа hammerhead, рибозимы HDV, рибозимы СРЕВ3, рибозимы VS, рибозим glmS, рибозим СоТС и синтетические рибозимы.
[0140] Пептидные аффинные метки могут включать те, которые можно использовать для отслеживания или очистки (например, флуоресцентный белок, зеленый флуоресцентный белок (GFP), YFP, RFP, CFP, mCherry, tdTomato, полигистидиновую метку (например, метку 6×His), гемагглютининовую метку (НА), метку FLAG, метку Мус, метку GST, метку MBP, хитин-связывающую белковую метку, метку на основе кальмодулина, метку V5, стрептавидин-связывающую метку и т.п.).
[0141] Оба типа меток, нуклеиновые и пептидные аффинные метки, могут содержать низкомолекулярные метки, такие как биотин, или дигитоксин, флуоресцентные метки, такие как, например, флуоресцеин, родамин, красители Alexa Fluor, краситель Cyanine3, краситель Cyanine5.
[0142] Нуклеиновые аффинные метки могут быть расположены на 5'-конце нуклеиновой кислоты (например, нуклеиновой кислоты, направленной против нуклеиновой кислоты). Нуклеиновые аффинные метки могут быть расположены на 3'-конце нуклеиновой кислоты. Нуклеиновые аффинные метки могут быть расположены на 5'- и 3'-конце нуклеиновой кислоты. Нуклеиновые аффинные метки могут быть расположены в пределах последовательности нуклеиновой кислоты. Пептидные аффинные метки могут быть расположены на N-конце полипептидной последовательности. Пептидные аффинные метки могут быть расположены на С-конце полипептидной последовательности. Пептидные аффинные метки могут быть расположены на N-конце и С-конце полипептидной последовательности. Многие аффинные метки могут быть гибридизованы с нуклеиновой кислотой и/или полипептидной последовательностью.
[0143] В настоящей заявке термин «захватывающий агент» в целом может относиться к агенту, который обеспечивает очистку полипептида и/или нуклеиновой кислоты. Захватывающий агент может представлять собой биологически активную молекулу или материал (например, любое биологическое вещество, обнаруженное в природе, или синтетическое вещество, и включает, но не ограничивается ими, клетки, вирусы, субклеточные частицы, белки, включая более конкретно антитела, иммуноглобулины, антигены, липопротеины, гликопротеины, пептиды, полипептиды, белковые комплексы, (стрепт)авидин-биотиновые комплексы, лиганды, рецепторы или малые молекулы, аптамеры, нуклеиновые кислоты, ДНК, РНК, пептидные нуклеиновые кислоты, олигосахариды, полисахариды, липополисахариды, клеточные метаболиты, гаптены, фармакологически активные вещества, алкалоиды, стероиды, витамины, аминокислоты и сахара). Согласно некоторым вариантам реализации настоящего изобретения захватывающий агент может содержать аффинную метку. Согласно некоторым вариантам реализации настоящего изобретения захватывающий агент может преимущественно связываться с полипептидом-мишенью или нуклеиновой кислотой, представляющей интерес. Захватывающие агенты могут свободно диффундировать в смеси. Захватывающие агенты могут быть связаны с частицей (например, гранулой, микрогранулой, наночастицей). Захватывающие агенты могут быть связаны с твердой или полутвердой поверхностью. В некоторых случаях захватывающие агенты необратимо связываются с мишенью. В других случаях захватывающие агенты обратимо связываются с мишенью (например, если мишень может быть подвергнута элюированию, или с помощью химических веществ, таких как имидазол).
[0144] В настоящей заявке термин «Cas5» в целом может относиться к полипептиду, последовательность которого по меньшей мере приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичного полипептида Cas5 дикого типа (например, Cas5 из D. vulgaris и/или любой последовательности, показанной на Фиг. 42). В целом, Cas5 может относиться к полипептиду, последовательность которого не более чем приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичного полипептида Cas5 дикого типа (например, Cas5 из D. vulgaris). Cas5 может относиться к форме белка дикого типа или модифицированной форме белка Cas5, которая может содержать аминокислотную замену, такую как делеция, вставка или замена, вариант, мутацию, гибридную последовательность, химерную последовательность или любую их комбинацию.
[0145] В настоящей заявке термин «Cas6» в целом может относиться к полипептиду, последовательность которого по меньшей мере приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичного полипептида Cas6 дикого типа (например, Cas6 из Т. thermophilus и/или последовательностям, показанным на Фиг. 41). В целом Cas6 может относиться к полипептиду, последовательность которого не более чем приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичного полипептида Cas6 дикого типа (например, Cas6 из Т. thermophilus). Cas6 может относиться к форме белка дикого типа или модифицированной форме белка Cas6, которая может содержать аминокислотную замену, такую как делеция, вставка или замена, вариант, мутацию, гибридную последовательность, химерную последовательность или любую их комбинацию.
[0146] В настоящей заявке термин «Cas9» в целом может относиться к полипептиду, последовательность которого по меньшей мере приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичного полипептида Cas9 дикого типа (например, Cas9 из S. pyogenes (SEQ ID NO: 8, SEQ ID NO: 1-256, SEQ ID NO: 795-1346). Cas9 может относиться к полипептиду, последовательность которого не более чем приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичного полипептида Cas9 дикого типа (например, Cas9 из S. pyogenes). Cas9 может относиться к форме белка дикого типа или модифицированной форме белка Cas9, которая может содержать аминокислотную замену, такую как делеция, вставка или замена, вариант, мутацию, гибридную последовательность, химерную последовательность или любую их комбинацию.
[0147] В настоящей заявке термин «клетка» в целом может относиться к биологической клетке. Клетка может представлять собой основную структурную, функциональную и/или биологическую единицу живого организма. Клетка может происходить от любого организма, имеющего одну или более клеток. Некоторые неограничивающие примеры включают: прокариотическую клетку, эукариотическую клетку, бактериальную клетку, клетку архей, клетку одноклеточного эукариотического организма, клетку простейших, клетку из растения (например, клетки из сельскохозяйственных культур, фруктов, овощей, зерна, соевых бобов, кукурузы, маиса, пшеницы, семян, томатов, риса, маниоки, сахарного тростника, тыквы, сена, картофеля, хлопчатника, конопли, табака, цветущих растений, хвойных, голосеменных, папоротников, плаунов, роголистников, печеночников, мхов), клетку водорослей (например, Botryococcus braunii, Chlamydomonas reinhardtii, Nannochloropsis gaditana, Chlorella pyrenoidosa, Sargassum patens C. agardh и т.п.), клетку морских водорослей (например, ламинарии), грибковую клетку (например, дрожжевую клетку, клетку из гриба), животную клетку, клетку из беспозвоночного животного (например, плодовой мухи, гидроидного, иглокожего, нематоды и т.д.), клетку из позвоночного животного (например, рыбы, амфибии, рептилии, птицы, млекопитающего), клетку из млекопитающего (например, свиньи, коровы, козы, овцы, грызуна, крысы, мыши, примата, не относящегося к человеку, человека и т.д.) и т.д. В некоторых случаях клетка может происходить не из природного организма (например, клетка может быть получена синтетическими способами, такая клетка в некоторых случаях называется искусственной).
[0148] Клетка может находиться в условиях in vitro. Клетка может находиться в условиях in vivo. Клетка может представлять собой выделенную клетку. Клетка может представлять собой клетку внутри организма. Клетка может представлять собой организм. Клетка может представлять собой клетку в клеточной культуре. Клетка может представлять собой клетку из популяции клеток. Клетка может представлять собой прокариотическую клетку или может быть получена из прокариотической клетки. Клетка может представлять собой бактериальную клетку или может быть получена из бактериальной клетки. Клетка может представлять собой клетку архей или может быть получена из клетки архей. Клетка может представлять собой эукариотическую клетку или может быть получена из эукариотической клетки. Клетка может представлять собой растительную клетку или может быть получена из клетки растения. Клетка может представлять собой клетку животного или может быть получена из клетки животного. Клетка может представлять собой клетку беспозвоночного или может быть получена из клетки беспозвоночного. Клетка может представлять собой клетку позвоночного или может быть получена из клетки позвоночного. Клетка может представлять собой клетку млекопитающего или может быть получена из клетки млекопитающего. Клетка может представлять собой клетку грызуна или может быть получена из клетки грызуна. Клетка может представлять собой клетку человека или может быть получена из клетки человека. Клетка может представлять собой микробиальную клетку или может быть получена из микробиальной клетки. Клетка может представлять собой грибковую клетку или может быть получена из грибковой клетки.
[0149] Клетка может представлять собой стволовую клетку или клетку-предшественника. Клетки могут включать стволовые клетки (например, стволовые клетки взрослых, эмбриональные стволовые клетки, индуцированные плюрипотентные клетки) и клетки-предшественники (например, клетки-предшественники кардиомиоцитов, нейрональные клетки-предшественники и т.д.). Клетки могут включать стволовые клетки и клетки-предшественники млекопитающих, включая стволовые клетки грызунов, клетки-предшественники грызунов, стволовые клетки человека, клетки-предшественники человека и т.д. Клональные клетки могут включать потомство клетки. Клетка может содержать нуклеиновую кислоту-мишень. Клетка может находиться в живом организме. Клетка может представлять собой генетически модифицированную клетку. Клетка может представлять собой клетку-хозяина.
[0150] Клетка может представлять собой тотипотентную стволовую клетку, однако, в некоторых вариантах реализации настоящего изобретения, термин «клетка» может быть использован, но при этом может не относиться к тотипотентной стволовой клетке. Клетка может представлять собой растительную клетку, однако, в некоторых вариантах реализации настоящего изобретения, термин «клетка» может быть использован, но при этом может не относиться к растительной клетке. Клетка может представлять собой плюрипотентную клетку. Например, клетка может представлять собой плюрипотентную кроветворную клетку, которая может дифференцироваться в другие клетки в линии кроветворных клеток, но при этом может быть неспособна дифференцироваться в любую другую некроветворную клетку. Клетка может быть способна развиваться в целый организм. Клетка может быть способна развиваться в целый организм или может не обладать такой способностью. Клетка может представлять собой целый организм.
[0151] Клетка может представлять собой первичную клетку. Например, культуры первичных клеток могут быть перепассированы 0 раз, 1 раз, 2 раза, 4 раза, 5 раз, 10 раз, 15 раз или более. Клетки могут представлять собой одноклеточные организмы. Клетки могут быть выращены в культуре.
[0152] Клетка может представлять собой больную клетку. Больная клетка может иметь измененные метаболические и/или морфологические признаки, и измененный профиль экспрессии генов. Больная клетка может представлять собой раковую клетку, диабетическую клетку и апоптотическую клетку. Больная клетка может представлять собой клетку, полученную от больного субъекта. Типичные заболевания могут включать заболевания крови, рак, нарушения обмена веществ, заболевания глаз, заболевания органов, заболевания опорно-двигательного аппарата, заболевания сердца и тому подобное.
[0153] В том случае, если клетки представляют собой первичные клетки, они могут быть собраны у индивидуума с помощью любого способа. Например, лейкоциты могут быть собраны с помощью афереза, лейкоцитофореза, разделения в градиенте плотности и т.д. Клетки из таких тканей как кожа, мышцы, костный мозг, селезенка, печень, поджелудочная железа, легкие, кишечник, желудок и т.д. могут быть собраны с помощью биопсии. Соответствующий раствор может быть использован для получения дисперсии или суспензии собранных клеток. Такой раствор в целом может представлять собой сбалансированный солевой раствор (например, физиологический раствор, забуференный фосфатом физиологический раствор (ФСБ), сбалансированный солевой раствор Хенкса и т.д.), подходящим образом дополненный фетальной телячьей сывороткой или другими природными факторами, в комбинации с приемлемым буфером в низкой концентрации. Буферы могут включать HEPES, фосфатные буферы, лактатные буферы и т.д. Клетки могут быть использованы немедленно, либо они могут быть сохранены (например, путем замораживания). Замороженные клетки могут быть подвергнуты оттаиванию и могут быть пригодны для повторного использования. Клетки могут быть заморожены в ДМСО, сыворотке, буферной среде (например, 10% ДМСО, 50% сыворотки, 40% забуференной среды), и/или в некоторых других распространенных растворах, используемых для сохранения клеток при низких температурах.
[0154] В настоящей заявке термин «условно ферментативно неактивный сайт-направленный полипептид» в целом может относиться к полипептиду, который может специфично связываться с конкретной последовательностью нуклеиновой кислоты в полинуклеотиде, однако не может расщеплять полинуклеотид-мишень, за исключением одного или более условий, которые обеспечивают активность ферментативного домена. Условно ферментативно неактивный сайт-направленный полипептид может содержать ферментативно неактивный домен, который может быть условно активирован. Условно ферментативно неактивный сайт-направленный полипептид может быть условно активирован в присутствии имидазола. Условно ферментативно неактивный сайт-направленный полипептид может содержать мутированный активный сайт, который не способен связаться со своим когнатным лигандом, что обеспечивает ферментативно неактивный сайт-направленный полипептид. Мутированный активный сайт может быть сконструирован для связывания с аналогами лиганда, так, что аналог лиганда может связываться с мутированным активным сайтом и реакционноспособным сайт-направленным полипептидом. Например, АТФ-связывающие белки могут содержать мутированный активный сайт, способный ингибировать активность белка, который сконструирован для специфичного связывания с аналогами АТФ. Связывание аналога АТФ, но не АТФ, может повторно активировать белок. Условно ферментативно неактивный сайт-направленный полипептид может содержать одну или более ненативных последовательностей (например, гибридную последовательность, аффинную метку).
[0155] В настоящей заявке термин «crPHK» может в целом относиться к нуклеиновой кислоте, последовательность которой по меньшей мере приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичной crPHK дикого типа (например, crPHK из S. pyogenes (например, SEQ ID NO: 569, SEQ ID NO: 563-679). crPHK в целом может относиться к нуклеиновой кислоте, последовательность которой не более чем приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичной crPHK дикого типа (например, crPHK из S. pyogenes). crPHK может относиться к модифицированной форме crPHK, которая может содержать замену нуклеотида, такую как делеция, вставка или замена, вариант, мутацию или химерную последовательность. crPHK может представлять собой нуклеиновую кислоту, последовательность которой по меньшей мере приблизительно на 60% идентична последовательности типичной crPHK дикого типа (например, crPHK из S. pyogenes) в участке, содержащем по меньшей мере 6 последовательных нуклеотидов. Например, последовательность crPHK может быть по меньшей мере приблизительно на 60% идентична, по меньшей мере приблизительно на 65% идентична, по меньшей мере приблизительно на 70% идентична, по меньшей мере приблизительно на 75% идентична, по меньшей мере приблизительно на 80% идентична, по меньшей мере приблизительно на 85% идентична, по меньшей мере приблизительно на 90% идентична, по меньшей мере приблизительно на 95% идентична, по меньшей мере приблизительно на 98% идентична, по меньшей мере приблизительно на 99% идентична или на 100% идентична последовательности типичной crPHK дикого типа (например, crPHK из S. pyogenes) в участке, содержащем по меньшей мере 6 последовательных нуклеотидов.
[0156] В настоящей заявке термин «повтор CRISPR» или «последовательность повтора CRISPR» может относиться к минимальной последовательности повтора CRISPR.
[0157] В настоящей заявке термин «Csy4» в целом может относиться к полипептиду, последовательность которого не более чем приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичного полипептида Csy4 дикого типа (например, Csy4 из Р. aeruginosa, см. Фигуру 40). Csy4 в целом может относиться к полипептиду, последовательность которого по меньшей мере приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична последовательности типичного полипептида Csy4 дикого типа (например, Csy4 из Р. aeruginosa). Csy4 может относиться к форме белка дикого типа или модифицированной форме белка Csy4, которая может содержать аминокислотную замену, такую как делеция, вставка, замена, вариант, мутацию, гибридную последовательность, химерную последовательность или любую их комбинацию.
[0158] В настоящей заявке термин «эндорибонуклеаза» в целом может относиться к полипептиду, который может расщеплять РНК. Согласно некоторым вариантам реализации настоящего изобретения эндорибонуклеаза может представлять собой сайт-направленный полипептид. Эндорибонуклеаза может быть членом системы CRISPR (например, типа I, типа II, типа III). Эндорибонуклеаза может относиться к надсемейству загадочных белков, ассоциированных с повторами (RAMP) (например, к семействам Cas6, Cas6, Cas5). Эндорибонуклеазы также могут включать членов семейства РНКазы А, РНКазы Н, РНКазы I, РНКазы III (например, Drosha, Dicer, РНКазу N), РНКазу L, РНКазу Р, РНКазу PhyM, РНКазу Т1, РНКазу Т2, РНКазу U2, РНКазу VI, РНКазу V. Эндорибонуклеаза может относиться к условно ферментативно неактивной эндорибонуклеазе. Эндорибонуклеаза может относиться к каталитически неактивной эндорибонуклеазе.
[0159] В настоящей заявке термин «донорный полинуклеотид» может относиться к нуклеиновой кислоте, которая может быть встроена в участок нуклеиновой последовательности путем геномной инженерии или конструирования нуклеиновой кислоты-мишени.
[0160] В настоящей заявке термин «фиксатор» или «сшивающий агент» в целом может относиться к агенту, который может фиксировать или сшивать клетки. Фиксированные или сшитые клетки могут стабилизировать комплексы белок-нуклеиновая кислота в клетке. Подходящие фиксаторы и сшивающие агенты могут включать формальдегид, глутаровый альдегид, фиксаторы на основе этанола, фиксаторы на основе метанола, ацетон, уксусную кислоту, тетраоксид осмия, бихромат калия, хромовую кислоту, перманганат калия, производные ртути, пикраты, формалин, параформальдегид, аминореактивные сшивающие агенты на основе NHS-эфира, такие как бис[сульфосукцинимидил]суберат (BS3), 3,3'-дитиобис-[сульфосукцинимидилпропионат] (DTSSP), этиленгликоль-бис-[сульфосукцинимидилсукцинат] (сульфо-EGS), дисукцинимидилглутарат (DSG), дитиобис-[сукцинимидилпропионат] (DSP), дисукцинимидилсуберат (DSS), этиленгликоль-бис-[сукцинимидилсукцинат] (EGS), сшивающие агенты на основе NHS-эфира/диазирина, такие как NHS-диазирин, NHS-LC-диазирин, NHS-SS-диазирин, сульфо-NHS-диазирин, сульфо-NHS-LC-диазирин и сульфо-NHS-SS-диазирин.
[0161] В настоящей заявке термин «гибридный» может относиться к белку и/или нуклеиновой кислоте, содержащей одну или более ненативных последовательностей (например, фрагментов). Гибридная последовательность может содержать одну или более идентичных ненативных последовательностей. Гибридная последовательность может содержать одну или более различных ненативных последовательностей. Гибридная последовательность может представлять собой химеру. Гибридная последовательность может содержать нуклеиновую аффинную метку. Гибридная последовательность может содержать штрихкод. Гибридная последовательность может содержать пептидную аффинную метку. Гибридная последовательность может обеспечить субклеточную локализацию сайт-направленного полипептида (например, сигнал ядерной локализации (NLS) для направления в ядро, сигнал митохондриальной локализации для направления в митохондрии, сигнал хлоропластной локализации для направления в хлоропласты, сигнал удержания в эндоплазматическом ретикулуме (ЭР) и т.п.). Гибридная последовательность может обеспечить ненативную последовательность (например, аффинную метку), которую можно использовать для отслеживания или очистки. Гибридная последовательность может представлять собой малую молекулу, такую как биотин или краситель, такой как красители Alexa Fluor, краситель Cyanine3, краситель Cyanine5. Гибридная последовательность может обеспечить повышенную или пониженную стабильность.
[0162] Согласно некоторым вариантам реализации настоящего изобретения гибридная последовательность может содержать детектируемую метку, включая фрагмент, который может обеспечить детектируемый сигнал. Подходящие детектируемые метки и/или фрагменты, которые могут обеспечить детектируемый сигнал, могут включать, но не ограничиваются ими, фермент, радиоизотоп, одного из членов специфичной связывающейся пары; флуорофор; флуоресцентный белок; квантовую точку; и тому подобное.
[0163] Гибридная последовательность может содержать одного из членов FRET-пары. Подходящие для использования FRET-пары (донор/акцептор) могут включать, но не ограничиваются ими, EDANS/флуоресцеин, IAEDANS/флуоресцеин, флуоресцеин/тетраметилродамин, флуоресцеин/Су5, IEDANS/DABCYL, флуоресцеин/QSY-7, флуоресцеин/LC Red 640, флуоресцеин/Су5.5 и флуоресцеин/LC Red 705.
[0164] Такая пара донор/акцептор как флуорофор/квантовая точка может быть использована в качестве гибрида. Подходящие флуорофоры («флуоресцентные метки») могут включать любую молекулу, которая поддается детектированию благодаря своим исходным флуоресцентным свойствам, которые могут включать флуоресценцию, детектируемую при возбуждении. Подходящие флуоресцентные метки могут включать, но не ограничиваются ими, флуоресцеин, родамин, тетраметилродамин, эозин, эритрозин, кумарин, метилкумарины, пирен, малахитовый зеленый, стильбен, люцифер желтый, Cascade Blue™, техасский красный, IAEDANS, EDANS, BODIPY FL, LC Red 640, Су5, Су 5.5, LC Red 705 и орегоновый зеленый.
[0165] Гибридная последовательность может содержать фермент. Подходящие ферменты могут включать, но не ограничиваются ими, пероксидазу хрена, люциферазу, бета-галактозидазу и тому подобное.
[0166] Гибридная последовательность может содержать флуоресцентный белок. Подходящие флуоресцентные белки могут включать, но не ограничиваются ими, зеленый флуоресцентный белок (GFP), (например, GFP из Aequoria victoria, флуоресцентные белки из Anguilla japonica или их мутированные варианты или производные), красный флуоресцентный белок, желтый флуоресцентный белок, любой из множества флуоресцентных и окрашенных белков.
[0167] Гибридная последовательность может содержать наночастицу. Подходящие наночастицы могут включать флуоресцентные наночастицы или люминесцентные и магнитные наночастицы. Можно детектировать любое оптическое или магнитное свойство или характеристику наночастиц(ы).
[0168] Гибридная последовательность может содержать квантовые точки (КТ). КТ могут быть модифицированы для придания им способности к растворению в воде путем нанесения покрытий, содержащих различные материалы. Например, КТ можно солюбилизировать при помощи амфифильных полимеров. Типичные полимеры, которые были использованы, включают низкомолекулярную полиакриловую кислоту, модифицированную октиламином, фосфолипиды, модифицированные полиэтиленгликолем (ПЭГ), полиангидриды, блок-сополимеры и т.п. КТ могут быть конъюгированы с полипептидом с помощью любой из нескольких различных функциональных групп или сшивающих агентов, которые могут быть прямо или косвенно связаны с покрывающим слоем. КТ с широким разнообразием спектров поглощения и испускания коммерчески доступны, например, от Quantum Dot Corp. (Hayward Calif.; в настоящее время принадлежит Invitrogen) или от Evident Technologies (Troy, N.Y.). Например, доступны КТ с пиком испускания при длине волны приблизительно 525, 535, 545, 565, 585, 605, 655, 705 и 800 нм. Таким образом, КТ могут иметь ряд различных расцветок в видимой части спектра и в некоторых случаях даже за его пределами.
[0169] Подходящие радиоизотопы могут включать, но не ограничиваются ими,14С,3Н,32P,33Р,35S и125I.
[0170] В настоящей заявке термин «генетически модифицированная клетка» в целом может относиться к клетке, которая была генетически модифицирована. Некоторые неограничивающие примеры генетических модификаций могут включать: вставки, делеции, инверсии, транслокации, гибридизацию генов или изменения одного или более нуклеотидов. Генетически модифицированная клетка может содержать нуклеиновую кислоту-мишень с введенным разрывом двойной цепи (например, разрыв ДНК). Генетически модифицированная клетка может содержать экзогенно введенную нуклеиновую кислоту (например, вектор). Генетически модифицированная клетка может содержать экзогенно введенный полипептид согласно настоящему изобретению и/или нуклеиновую кислоту согласно настоящему изобретению. Генетически модифицированная клетка может содержать донорный полинуклеотид. Генетически модифицированная клетка может содержать экзогенную нуклеиновую кислоту, введенную в геном указанной генетически модифицированной клетки. Генетически модифицированная клетка может содержать делецию ДНК. Генетически модифицированная клетка также может относиться к клетке с модифицированной митохондриальной ДНК или ДНК хлоропластов.
[0171] В настоящей заявке термин «геномная инженерия» может относиться к способу модификации нуклеиновой кислоты-мишени. Геномная инженерия может относиться к введению ненативной нуклеиновой кислоты в нативную нуклеиновую кислоту. Геномная инженерия может относиться к направлению сайт-направленного полипептида и нуклеиновой кислоты, направленной против нуклеиновой кислоты, к нуклеиновой кислоте-мишени, без встраивания или удаления оснований в последовательности нуклеиновой кислоты-мишени. Геномная инженерия может относиться к расщеплению нуклеиновой кислоты-мишени и повторному соединению нуклеиновой кислоты-мишени без встраивания экзогенной последовательности в нуклеиновую кислоту-мишень или введения делеции в последовательность нуклеиновой кислоты-мишени. Нативная нуклеиновая кислота может содержать ген. Ненативная нуклеиновая кислота может содержать донорный полинуклеотид. В соответствии со способами согласно настоящему изобретению сайт-направленный полипептид (например, Cas9) может вводить двухцепочечные разрывы в нуклеиновую кислоту (например, геномную ДНК). Двухцепочечный разрыв может стимулировать эндогенные пути репарации ДНК клетки (например, гомологичную рекомбинацию (HR) и/или негомологичное соединение концов (NHEJ), или A-NHEJ (альтернативное негомологичное соединение концов)). Мутации, делеции, изменения и встраивания чужеродной, экзогенной и/или альтернативной нуклеиновой кислоты могут быть введены в сайт разрыва двухцепочечной ДНК.
[0172] В настоящей заявке термин «выделенный» может относиться к нуклеиновой кислоте или полипептиду, который, в результате манипуляций человека, существует отдельно от своей естественной среды, и, следовательно, не является природным. Выделенный может означать по существу чистый. Выделенная нуклеиновая кислота или полипептид могут существовать в очищенной форме и/или могут существовать в неестественной среде, например, такой как трансгенная клетка.
[0173] В настоящей заявке термин «ненативный» может относиться к нуклеиновой кислоте или полипептидпой последовательности, которая не обнаружена в нативной нуклеиновой кислоте или белке. Ненативный может относиться к аффинным меткам. Ненативный может относиться к гибридной последовательности. Ненативный может относиться к природной нуклеотидной последовательности или полипептидной последовательности, которые содержат мутации, вставки и/или делеции. Ненативная последовательность может иметь и/или кодировать вид активности (например, ферментативную активность, метилтрансферазную активность, ацетилтрансферазную активность, киназную активность, убиквитиназную активность и т.д.), которую также может проявлять нуклеиновая последовательность и/или полипептидная последовательность, с которой гибридизована ненативная последовательность. Ненативная последовательность нуклеиновой кислоты или полипептида может быть связана с природной последовательностью нуклеиновой кислоты или полипептида (или их вариантом) с помощью модификации генома, чтобы получить химерную последовательность нуклеиновой кислоты и/или полипептида, кодирующую химерную нуклеиновую кислоту и/или полипептид. Ненативная последовательность может относиться к удлиненной последовательности, которая способна гибридизоваться с 3'-концом.
[0174] В настоящей заявке термин «нуклеиновая кислота» в целом может относиться к полинуклеотидной последовательности или ее фрагменту. Нуклеиновая кислота может содержать нуклеотиды. Нуклеиновая кислота может быть эндогенной или экзогенной по отношению к клетке. Нуклеиновая кислота может существовать в бесклеточной среде. Нуклеиновая кислота может представлять собой ген или его фрагмент. Нуклеиновая кислота может представлять собой ДНК. Нуклеиновая кислота может представлять собой РНК. Нуклеиновая кислота может содержать один или более аналогов (например, измененный нуклеотидный остов, сахар или нуклеиновое основание). Некоторые неограничивающие примеры аналогов включают: 5-бромурацил, пептидную нуклеиновую кислоту, чужеродную нуклеиновую кислоту, морфолины, закрытые нуклеиновые кислоты, гликоль-содержащие нуклеиновые кислоты, треоза-содержащие нуклеиновые кислоты, дидезоксинуклеотиды, кордицепин, 7-деаза-ГТФ, флуорофоры (например родамин или флуоресцеин, связанный с сахаром), тиол-содержащие нуклеотиды, связанные с биотином нуклеотиды, флуоресцентные аналоги оснований, островки CpG, метил-7-гуанозин, метилированные нуклеотиды, инозин, тиоуридин, псевдоуридин, дигидроксиуридин, квеуозин и виозин.
[0175] В настоящей заявке термин «образец нуклеиновой кислоты» в целом может относиться к образцу, полученному из биологического организма. Образец нуклеиновой кислоты может содержать нуклеиновую кислоту. Нуклеиновая кислота из образца нуклеиновой кислоты может быть очищена и/или обогащена. Образец нуклеиновой кислоты может проявить исходные характеристики целой нуклеиновой кислоты. Образцы нуклеиновых кислот могут быть получены из различных источников. Образцы нуклеиновых кислот могут быть получены от одного или более индивидуумов. Один или более образцов нуклеиновых кислот могут быть получены от одного и того же индивидуума. Один неограничивающий пример может включать один образец, полученный из крови индивидуума, и второй образец, полученный из биопсии опухоли индивидуума. Примеры источников образцов нуклеиновых кислот могут включать, но не ограничиваются ими, кровь, сыворотку, плазму, назальный тампон или смыв носоглотки, слюну, мочу, желудочный сок, спинальную жидкость, слезы, стул, слизь, пот, ушную серу, масло, секрет желез, спинномозговую жидкость, ткань, сперму, влагалищные выделения, интерстициальные жидкости, включая интерстициальные жидкости, полученные из опухолевой ткани, глазные жидкости, спинальную жидкость, мазок из горла, защечный тампон, пробу выдыхаемого воздуха, волосы, ногти, кожу, биопсию, плацентарную жидкость, амниотическую жидкость, пуповинную кровь, эфирные жидкости, полостные жидкости, мокроту, гной, микробиоту, меконий, грудное молоко, буккальные образцы, смыв носоглотки, другие выделения или любую их комбинацию. Образцы нуклеиновых кислот могут быть получены из тканей. Примеры образцов тканей могут включать, но не ограничиваются ими, соединительную ткань, мышечную ткань, нервную ткань, эпителиальную ткань, хрящ, образец рака или опухоли, костный мозг или кости. Образец нуклеиновой кислоты может быть получен от человека или животного. Образец нуклеиновой кислоты может быть получен от млекопитающего, позвоночного, такого как мыши, обезьяны, люди, сельскохозяйственные животные, спортивные животные или домашние животные. Образец нуклеиновой кислоты может быть собран от живого или мертвого субъекта. Образец нуклеиновой кислоты может быть собран в свежей форме от субъекта или мог быть подвергнут некоторой форме предварительной обработки, хранению или транспортировке.
[0176] Образец нуклеиновой кислоты может содержать нуклеиновую кислоту-мишень. Образец нуклеиновой кислоты может быть получен из клеточного лизата. Клеточный лизат может быть получен из клетки.
[0177] В настоящей заявке термин «нуклеиновая кислота, направленная против нуклеиновой кислоты» может относиться к нуклеиновой кислоте, которая может гибридизоваться с другой нуклеиновой кислотой. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может представлять собой РНК. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может представлять собой ДНК. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть запрограммирована на сайт-специфичное связывание с последовательностью нуклеиновой кислоты. Нуклеиновая кислота, на которую воздействуют, или нуклеиновая кислота-мишень может содержать нуклеотиды. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать нуклеотиды. Часть нуклеиновой кислоты-мишени может быть комплементарна части нуклеиновой кислоты, направленной против нуклеиновой кислоты. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать одну полинуклеотидную цепь и может быть названа «одиночная направляющая нуклеиновая кислота» (т.е. «одиночная направляющая нуклеиновая кислота, направленная против нуклеиновой кислоты»). Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать две полинуклеотидные цепи и может быть названа «двойная направляющая нуклеиновая кислота» (т.е. «двойная направляющая нуклеиновая кислота, направленная против нуклеиновой кислоты»). Если не указано иное, термин «нуклеиновая кислота, направленная против нуклеиновой кислоты» может быть сборным, относясь к обоим типам: одиночным направляющим нуклеиновым кислотам и двойным направляющим нуклеиновым кислотам.
[0178] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать сегмент, который может быть назван «сегмент, направленный против нуклеиновой кислоты» или «последовательность, направленная против нуклеиновой кислоты». Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать сегмент, который может быть назван «белоксвязывающий сегмент» или «белоксвязывающая последовательность».
[0179] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать одну или более модификаций (например, модификацию основания, модификацию остова), чтобы обеспечить нуклеиновую кислоту с новой или улучшенной характеристикой (например, улучшенной стабильностью). Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать нуклеиновую аффинную метку. Нуклеозид может представлять собой комбинацию основания и сахара. Часть нуклеозида, представленная основанием, может быть гетероциклическим основанием. Два наиболее распространенных класса таких гетероциклических оснований представляют собой пурины и пиримидины. Нуклеотиды могут представлять собой нуклеозиды, которые дополнительно включают фосфатную группу, ковалентно связанную с частью нуклеозида, представленной остатком сахара. В тех нуклеозидах, которые содержат пентафуранозильный сахар, фосфатная группа может быть связана с 2', 3' или 5'-гидроксильным фрагментом сахара. При образовании нуклеиновых кислот, направленных против нуклеиновой кислоты, фосфатные группы могут ковалентного связывать смежные нуклеозиды для образования линейного полимерного соединения. В свою очередь, соответствующие концы такого линейного полимерного соединения могут быть дополнительно соединены с образованием циклического соединения; однако линейные соединения в целом являются подходящими. Помимо этого нуклеотидные основания такого линейного соединения могут быть исходно комплементарны, и, следовательно, могут сворачиваться с образованием полностью или частично двухцепочечного соединения. В последовательностях нуклеиновых кислот, направленных против нуклеиновой кислоты, фосфатные группы обычно могут быть названы группами, образующими межнуклеозидный остов нуклеиновой кислоты, направленной против нуклеиновой кислоты. Связь или остов нуклеиновых кислот, направленных против нуклеиновой кислоты, может представлять собой фосфодиэфирную связь в направлении 3'-5'.
[0180] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать модифицированный остов и/или модифицированные межнуклеозидные связи. Модифицированные остовы могут включать те, которые сохраняют атом фосфора в остове, и те, которые не содержат атома фосфора в остове.
[0181] Подходящие модифицированные остовы нуклеиновых кислот, направленных против нуклеиновой кислоты, содержащие атом фосфора в своем составе, могут включать, например, фосфотиоаты, хиральные фосфотиоаты, фосфодитиоаты, фосфотриэфиры, аминоалкилфосфотриэфиры, метил- и другие алкильные фосфонаты, такие как 3'-алкиленфосфонат, 5'-алкиленфосфонат, хиральные фосфонаты, фосфинаты, фосфоамидаты, включая 3'-аминофосфоамидат и аминоалкилфосфоамидаты, фосфодиамидаты, тионфосфоамидаты, тионалкилфосфонаты, тионалкилфосфотриэфиры, селенофосфаты и борфосфаты, имеющие нормальные 3'-5' связи, 2'-5' связанные аналоги, и те, которые имеют инвертированную полярность, при которой одна или более межнуклеотидных связей представляют собой 3'-3', 5'-5 или 2'-2' связи. Подходящие нуклеиновые кислоты, направленные против нуклеиновой кислоты, имеющие инвертированную полярность, могут содержать одну 3'-3'-связь в положении 3'-концевой межнуклеотидной связи (т.е. одиночный инвертированный нуклеозидный остаток, в котором отсутствует нуклеиновое основание либо вместо него присутствует гидроксильная группа). В область настоящего изобретения также могут быть включены различные соли (например, хлорид калия или хлорид натрия), смешанные соли, а также формы, представленные свободной кислотой.
[0182] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать одну или более фосфотиоатных и/или гетероатомных межнуклеозидных связей, в частности-СН2-NH-О-СН2-, -СН2-N(СН3)-O-СН2- (т.е. метилен (метилимино) или MMI остов), -СН2-O-Н(СН3)-СН2-, -CH2-N(CH3)- N(CH3)-CH2- и -O-N(CH3)-CH2-CH2- (в котором нативная фосфодиэфирная межнуклеотидная связь представлена -O-Р(=O)(ОН)-O-СН2-).
[0183] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать в остове морфолиновые структуры. Например, нуклеиновая кислота может содержать 6-членное морфолиновое кольцо вместо рибозного кольца. В некоторых из таких вариантов реализации фосфодиамидат или другая нефосфодиэфирная межнуклеозидная связь может замещать фосфодиэфирную связь.
[0184] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать полинуклеотидные остовы, которые образованы короткоцепочечными алкильными или циклоалкильными межнуклеозидными связями, либо смешанными межнуклеозидными связями между гетероатомом и алкилом или циклоалкилом, либо одной или более короткоцепочечными гетероатомными или гетероциклическими межнуклеозидными связями. Такие нуклеиновые кислоты могут включать те, которые имеют морфолино связи (частично образованные сахарной частью нуклеозида); силоксановые остовы; сульфидные, сульфоксидные и сульфоновые остовы; формацетильные и тиоформацетильные остовы; метиленформацетильные и тиоформацетильные остовы; рибоацетильные остовы; алкен-содержащие остовы; сульфаматные остовы; метилениминовые и метиленгидразиновые остовы; сульфонатные и сульфонамидные остовы; амидные остовы; и другие типы остовов, имеющих смешанные N, О, S и СН2 составные части.
[0185] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать нуклеиновую кислоту-миметик. Термин «миметик» может включать полинуклеотиды, в которых только фуранозное кольцо или фуранозное кольцо и межнуклеотидная связь замещены нефуранозной группой, замена только фуранозного кольца также может упоминаться как сахар-суррогат. Фрагмент гетероциклического основания или фрагмент модифицированного гетероциклического основания может быть сохранен для гибридизации с соответствующей нуклеиновой кислотой-мишенью. Одна такая нуклеиновая кислота может представлять собой пептидную нуклеиновую кислоту (PNA). В PNA сахарный остов полинуклеотида может быть замещен амид-содержащим остовом, в частности аминоэтилглициновым остовом. Нуклеотиды могут быть сохранены и связаны, непосредственно или косвенно, с атомами азота азагрупп амидной части остова. Остов в соединениях PNA может содержать два или более связанных аминоэтилглициновых блока, которые обеспечивают пептидной нуклеиновой кислоте амид-содержащий остов. Фрагменты гетероциклических оснований могут быть связаны, непосредственно или косвенно, с атомами азота азагрупп амидной части остова.
[0186] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать связанные морфолиновые блоки (т.е. представляет собой морфолинонуклеиновую кислоту), которые содержат гетероциклические основания, прикрепленные к морфолиновому кольцу. Связывающие группы могут связывать мономерные морфолиновые блоки в морфолинонуклеиновой кислоте. Неионные морфолиновые олигомерные соединения могут иметь меньше нежелательных взаимодействий с клеточными белками. Морфолиновые полинуклеотиды могут быть неионными миметиками нуклеиновых кислот, направленных против нуклеиновой кислоты. Многие соединения из класса морфолиновых олигонуклеотидов могут быть соединены с использованием различных связывающих групп. Другой класс полинуклеотидных миметиков может упоминаться как циклогексенилнуклеиновые кислоты (CeNA). Фуранозное кольцо, обычно присутствующее в молекуле нуклеиновой кислоты, может быть замещено циклогексенильным кольцом. DMT-защищенные фосфоамидитные мономеры CeNA могут быть получены и использованы для синтеза олигомерных соединений с помощью фосфоамидитного метода. Встраивание мономеров CeNA в цепь нуклеиновой кислоты может увеличить стабильность гибрида ДНК/РНК. CeNA олигоаденилаты могут образовывать комплексы с комплементарными основаниями нуклеиновой кислоты, устойчивость которых аналогична таковой для нативных комплексов. Другая модификация может включать закрытые нуклеиновые кислоты (LNA), в которых 2'-гидроксильная группа связана с 4' атомом углерода сахарного кольца, что приводит к замыканию 2'-С, 4'-С-оксиметиленовой связи с образованием бициклического фрагмента сахара. Связь может представлять собой метилен (-СН2-), группу которая связывает 2' атом кислорода и 4' атом углерода, где n равно 1 или 2. LNA и аналоги LNA могут иметь очень высокую термическую устойчивость дуплексов с комплементарной нуклеиновой кислотой (Tm = от +3 до +10°С), устойчивость по отношению к расщеплению 3'-экзонуклеазами и хорошие показатели растворимости.
[0187] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать один или более замещенных сахарных фрагментов. Подходящие полинуклеотиды могут содержать группу, замещающую сахар, выбранную из: ОН, F, O-, S-, или N-алкил; O-, S-, или N-алкенил; O-, S- или N-алкинил; или О-алкил-O-алкил, где алкил, алкенил и алкинил могут представлять собой замещенный или незамещенный C1-С10-алкил или С2-С10-алкенил и алкинил. Особенно подходящими являются O((СН2)nO)mCH3, O(СН2)nOCH3, O(CH2)nNH2, O(СН2)nCH3, O(CH2)nONH2 и O(CH2)nON((CH2)nCH3)2, где n и m составляют от 1 до приблизительно 10. Группа, замещающая сахар, может быть выбрана из: C1-С10-низшего алкила, замещенного низшего алкила, алкенила, алкинила, алкарила, аралкила, O-алкарила или O-аралкила, SH, SCH3, OCN, Cl, Br, CN, CF3, OCF3, SOCH3, SO2CH3, ONO2, NO2, N3, NH2, гетероциклоалкила, гетероциклоалкарила, аминоалкиламино, полиалкиламино, замещенного силила, РНК-расщепляющей группы, репортерной группы, интеркалирующей группы, группы для улучшения фармакокинетических свойств нуклеиновой кислоты, направленной против нуклеиновой кислоты, или группы для улучшения фармакодинамических свойств нуклеиновой кислоты, направленной против нуклеиновой кислоты, и других заместителей, имеющих аналогичные свойства. Подходящая модификация может включать 2'-метоксиэтоксигруппу (2'-O-СН2 CH2OCH3, также известную как 2'-O-(2-метоксиэтил) или 2'-МОЕ, т.е. алкоксиалкоксигруппу). Другая подходящая модификация может включать 2'-диэтиламинооксиэтоксигруппу (т.е., группу O(СН2)2ON(СН3)2, также известную как 2'-DMAOE) и 2'-диметиламиноэтоксиэтоксигруппу (также известную как 2'-O-диметиламиноэтоксиэтил или 2'-DMAEOE), т.е. 2'-O-СН2-O-СН2-N(СН3)2.
[0188] Другие подходящие группы, замещающие сахара, могут включать метокси (-O-СН3), аминопропокси (-OCH2CH2CH2NH2), аллил (-СН2-СН=СН2), -O-аллил (-О-CH2-СН=СН2) и фтор (F). Группы, замещающие 2'-сахара, могут присутствовать в арабино (вверх) положении или рибо (вниз) положении. Подходящая 2'-арабино модификация представляет собой 2'-F. Аналогичные модификации могут быть сделаны в других положениях на олигомерном соединении, в частности, 3'-положении сахара на 3'-концевом нуклеозиде или в 2'-5'-связанных нуклеотидах и в 5'-положении 5'-концевого нуклеотида. Олигомерные соединения также могут содержать миметики сахара, такие как фрагменты циклобутила вместо пентофуранозильного фрагмента сахара.
[0189] Нуклеиновая кислота, направленная против нуклеиновой кислоты, также может содержать модификации и замены нуклеинового основания (часто называемого просто «основание»). В настоящей заявке термин «немодифицированные» или «природные» нуклеиновые основания могут включать пуриновые основания (например, аденин (А) и гуанин (G)), и пиримидиновые основания (например, тимин (Т), цитозин (С) и урацил (U)). Модифицированные нуклеиновые основания могут включать другие синтетические и природные нуклеиновые основания, такие как 5-метилцитозин (5-Ме-С), 5-гидроксиметилцитозин, ксантин, гипоксантин, 2-аминоаденин, 6-метил- и другие алкильные производные аденина и гуанина, 2-пропил- и другие алкильные производные аденина и гуанина, 2-тиоурацил, 2-тиотимин и 2-тиоцитозин, 5-галоурацил и цитозин, 5-пропинил- (-С=С-СН3) урацил и цитозин и другие алкинильные производные пиримидиновых оснований, 6-азоурацил, цитозин и тимин, 5-урацил (псевдоурацил), 4-тиоурацил, 8-галоген, 8-амино, 8-тиол, 8-тиоалкил, 8-гидрокси и другие 8-замещенные аденины и гуанины, 5-гало, в частности, 5-бром, 5-трифторметил и другие 5-замещенные урацилы и цитозины, 7-метилгуанин, 7-метиладенин, 2-F-аденин, 2-аминоаденин, 8-азагуанин и 8-азааденин, 7-деазагуанин и 7-деазааденин, и 3-деазагуанин и 3-деазааденин. Модифицированные нуклеиновые основания могут включать трициклические пиримидины, такие как феноксазинцитидин (1Н-пиримидо(5,4-b) (1,4) бензоксазин-2(3Н)-он), фенотиазинцитидин (1Н-пиримидин(5,4-b) (1,4)бензотиазин-2(3Н)-он), G-клэмпы, такие как замещенный феноксазинцитидин (например 9-(2-аминоэтокси)-Н-пиримидин(5,4-(b)(1,4)бензоксазин-2(3Н)-он), карбазолцитидин (2Н-пиримидин(4,5-b) индол-2-он), пиридоиндолцитидин (Н-пиридо(3',2':4,5)пирроло(2,3-d)пиримидин-2-он).
[0190] Фрагменты гетероциклических оснований могут включать те, в которых пуриновое или пиримидиновое основание замещено другими гетероциклами, например, 7-деазааденином, 7-деазагуанозином, 2-аминопиридином и 2-пиридоном. Нуклеиновые основания можно применять для увеличения аффинности связывания полинуклеотидного соединения. Они могут включать 5-замещенные пиримидины, 6-азапиримидины и N-2, N-6 и O-6 замещенные пурины, включая 2-аминопропиладенин, 5-пропинилурацил и 5-пропилцитозин. Замены 5-метилцитозином могут увеличить стабильность дуплекса нуклеиновой кислоты на 0,6-1,2°С и могут представлять собой подходящие замены нуклеиновых оснований (например, в комбинации с 2'-O-метоксиэтильными модификациями сахара).
[0191] Модификация нуклеиновой кислоты, направленной против нуклеиновой кислоты, может включать химическое связывание с нуклеиновой кислотой, направленной против нуклеиновой кислоты, одного или более фрагментов или конъюгатов, которые могут повысить активность, клеточное распределение или поглощение клетками указанной нуклеиновой кислоты, направленной против нуклеиновой кислоты. Эти фрагменты или конъюгаты могут включать группы конъюгатов, ковалентно связанные с функциональными группами, такими как первичные или вторичные гидроксильные группы. Группы конъюгатов могут включать, но не ограничиваются ими, интеркалирующие группы, репортерные молекулы, полиамины, полиамиды, полиэтиленгликоли, простые полиэфиры, группы, которые улучшают фармакодинамические свойства олигомеров, и группы, которые улучшают фармакокинетические свойства олигомеров. Группы конъюгатов могут включать, но не ограничиваются ими, холестерины, липиды, фосфолипиды, биотин, феназин, фолат, фенантридин, антрахинон, акридин, флуоресцеины, родамин, кумарины и красители. Группы, которые улучшают фармакодинамические свойства, включают группы, которые улучшают поглощение, повышают устойчивость к расщеплению и/или усиливают специфичную в отношении последовательности гибридизацию с нуклеиновой кислотой-мишенью. Группы, которые могут улучшить фармакокинетические свойства, включают группы, которые улучшают поглощение, распределение, метаболизм или выведение нуклеиновой кислоты. Фрагменты конъюгатов могут включать, но не ограничиваются ими, липидные фрагменты, такие как фрагмент холестерина, тиоэфир холевой кислоты (например, гексил-S-тритилтиол), тиохолестерин, алифатическую цепь (например, остатки додекандиола или ундецила), фосфолипид (например, дигексадецил-рац-глицерин или триэтиламмоний 1,2-ди-О-гексадецил-рац-глицеро-3-Н-фосфонат), цепь полиамина или полиэтиленгликоля, или адамантан уксусную кислоту, пальмитиловый фрагмент, или фрагмент октадециламина или гексиламинокарбонилоксихолестерина.
[0192] Модификация может включать «домен белковой трансдукции» или PTD (т.е. пептид, обеспечивающий проникновение в клетку (СРР)). PTD может относиться к полипептиду, полинуклеотиду, углеводу или органическому или неорганическому соединению, которое облегчает пересечение липидного бислоя, мицеллы, клеточной мембраны, мембраны органеллы или мембраны везикулы. PTD может быть прикреплен к другой молекуле, которая может варьироваться от небольшой полярной молекулы до крупной макромолекулы и/или наночастицы, и может облегчить пересечение мембраны молекулой, например, перемещение из внеклеточного пространства во внутриклеточное пространство, или из цитозоля внутрь органеллы. PTD может быть ковалентно связан с аминоконцом полипептида. PTD может быть ковалентно связан с карбоксильным концом полипептида. PTD может быть ковалентно связан с нуклеиновой кислотой. Типичные PTD могут включать, но не ограничиваются ими, минимальный пептид домена трансдукции белка; полиаргининовую последовательность, содержащую несколько остатков аргинина, достаточных для непосредственного ввода в клетку (например, 3, 4, 5, 6, 7, 8, 9, 10 или 10-50 остатков аргинина), домен VP22, домен трансдукции белка локуса Antennapedia Drosophila, усеченный пептид кальцитонина человека, полилизин и транспортин, гомополимер аргинина, содержащий от 3 остатков аргинина до 50 остатков аргинина. PTD может быть активирован под действием СРР (АСРР). АСРР может содержать поликатионный СРР (например, arg9 или «R9»), соединенный посредством расщепляемого линкера к соответствующим полианионом (например, Glu9 или «Е9»), который может уменьшить суммарный заряд практически до нуля, и тем самым ингибирует адгезию и поглощение клетками. Полианион может высвобождаться при расщеплении линкера, локально снимая маскировку с полиаргинина и его природной адгезивности, тем самым «активируя» прохождение АСРР через мембрану.
[0193] «Нуклеотид» в целом может относиться к комбинации основание-сахар-фосфат. Нуклеотид может содержать синтетический нуклеотид. Нуклеотид может содержать синтетический аналог нуклеотида. Нуклеотиды могут представлять собой мономерные блоки последовательности нуклеиновой кислоты (например, дезоксирибонуклеиновой кислоты (ДНК) и рибонуклеиновой кислоты (РНК)). Термин нуклеотид может включать рибонуклеозидтрифосфаты, аденозинтрифосфат (АТФ), уридинтрифосфат (УТФ), цитозинтрифосфат (ЦТФ), гуанозицтрифосфат (ГТФ), и дезоксирибонуклеозидтрифосфаты, такие как дАТФ, дЦТФ, дИТФ, дУТФ, дГТФ, дТТФ, или их производные. Такие производные могут включать, например, [αS]дАТФ; 7-деаза-дГТФ и 7-деаза-дАТФ, и производные нуклеотидов, которые придают содержащей их молекуле нуклеиновой кислоты устойчивость к действию нуклеаз. В настоящей заявке термин нуклеотид может относиться к дидезоксирибонуклеозидтрифосфатам (ддНТФ) и их производным. Типичные примеры дидезоксирибонуклеозидтрифосфатов могут включать, но не ограничиваются ими, ддАТФ, ддЦТФ, ддГТФ, ддИТФ и ддТТФ. Нуклеотид может быть немеченым или помечен детектируемой меткой с помощью известных методов. Введение метки также может быть проведено с использованием квантовых точек. Детектируемые метки могут включать, например, радиоактивные изотопы, флуоресцентные метки, хемилюминесцентные метки, биолюминесцентные метки и ферментные метки. Флуоресцентные метки нуклеотидов могут включать, но не ограничивается ими, флуоресцеин, 5-карбоксифлуоресцеин (FAM), 2'7'-диметокси-4'5-дихлор-6-карбокеифлуоресцеин (JOE), родамин, 6-карбоксиродамин (R6G), N,N,N',N'-тетраметил-6-карбоксиродамин (TAMRA), 6-карбокси-Х-родамин (ROX), 4-(4'-диметиламинофенилазо)бензойную кислоту (DABCYL), каскад синий, орегоновый зеленый, техасский красный, цианин и 5-(2'-аминоэтил)аминонафталин-1-сульфоновую кислоту (EDANS). Конкретные примеры флуоресцентномеченых нуклеотидов могут включать [R6G]дУТФ, [TAMRA]дУТФ, [R110]дЦТФ [R6G]дЦТФ [TAMRA]дЦТФ [JOE]ддАТФ, [R6G]ддАТФ, [FAM]ддЦТФ, [R110]ддЦТФ, [TAMRA]ддГТФ, [ROX]ддТТФ, [dR6G]ддАТФ, [dR110]ддЦТФ, [dTAMRA]ддГТФ и [dROX]ддТТФ, которые доступны от Perkin Elmer, Фостер-Сити, Калифорния, США. FluoroLink дезоксинуклеотиды, FluoroLink Су3-дЦТФ, FluoroLink Су5-дЦТФ, FluoroLink Fluor X-дЦТФ, FluoroLink Су3-дУТФ и FluoroLink Су5-дУТФ, которые доступны от Amersham, Arlington Heights, Иллинойс, США; флуоресцеин-15-дАТФ, флуоресцеин-12-дУТФ, тетраметилродамин-6-дУТФ, IR770-9-дАТФ, флуоресцеин-12-ддУТФ, флуоресцеин-12-УТФ и флуоресцеин-15-2'-дАТФ, которые доступны от Boehringer Mannheim, Индианаполис, Индиана, США; и меченые хромосомные нуклеотиды, BODIPY-FL-14-УТФ, BODIPY-FL-4-УТФ, BODIPY-TMR-14-УТФ, BODIPY-TMR-14-дУТФ, BODIPY-TR-14-УТФ, BODIPY-TR-14-дУТФ, каскад синий-7-УТФ, каскад синий-7-дУТФ, флуоресцеин-12-УТФ, флуоресцеин-12-дУТФ, орегоновый зеленый 488-5-дУТФ, родамин зеленый-5-УТФ, родамин зеленый-5-дУТФ, тетраметилродамин-6-УТФ, тетраметилродамин-6-дУТФ, техасский красный-5-УТФ, техасский красный-5-дУТФ и техасский красный -12-дУТФ, которые доступны от Molecular Probes, Юджин, Орегон, США. Нуклеотиды также могут быть помечены или маркированы путем химической модификации. Химически модифицированный одиночный нуклеотид может представлять собой биотин-дНТФ. Некоторые неограничивающие примеры биотинилированных дНТФ могут включать, биотин-дАТФ (например, био-N6-ддАТФ, биотин-14-дАТФ), биотин-дЦТФ (например, биотин-11-дЦТФ, биотин-14-дЦТФ) и биотин-дУТФ (например, биотин-11-дУТФ, биотин-16-дУТФ, биотин-20-дУТФ).
[0194] В настоящей заявке термин «Р-домен» может относиться к области в нуклеиновой кислоте, направленной против нуклеиновой кислоты. Р-домен может взаимодействовать с мотивом, прилегающим к протоспейсеру (РАМ), сайт-направленным полипептидом и/или нуклеиновой кислотой, направленной против нуклеиновой кислоты. Р-домен может взаимодействовать непосредственно или косвенно с мотивом, прилегающим к протоспейсеру (РАМ), сайт-направленным полипептидом и/или нуклеиновой кислотой, направленной против нуклеиновой кислоты. В настоящей заявке термины «область, взаимодействующая с РАМ» «область, направленная против области, прилегающей к повтору» и «Р-домен» могут быть использованы взаимозаменяемо.
[0195] В настоящей заявке термин «очищенный» может относиться к молекуле (например, сайт-направленному полипептиду, нуклеиновой кислоте, направленной против нуклеиновой кислоты), которая составляет по меньшей мере 50, 60, 70, 80, 90, 95, 96, 97, 98, 99 или 100% композиции. Например, образец, который содержит 10% сайт-направленного полипептида, но после этапа очистки содержит 60% сайт-направленного полипептида, затем может быть назван очищенным. Очищенный образец может относиться к обогащенному образцу, или образцу, который обрабатывали с помощью методов для удаления частиц, отличных от частиц, представляющих интерес.
[0196] В настоящей заявке термин «агент повторной активации» в целом может относиться к любому агенту, который может конвертировать ферментативно неактивный полипептид в ферментативно активный полипептид. Агент повторной активации может представлять собой имидазол. Агент повторной активации может представлять собой аналог лиганда.
[0197] В настоящей заявке термин «рекомбинантный» может относиться к последовательности, полученной из источника, который является чужеродным по отношению к конкретному хозяину (например, клетке), или, если последовательность получена из того же самого источника, она является модифицированной относительно своей исходной формы. Рекомбинантная нуклеиновая кислота в клетке может включать нуклеиновую кислоту, которая является эндогенной для конкретной клетки, но была модифицирована с помощью, например, метода сайт-направленного мутагенеза. Термин может включать неприродные множественные копии природной последовательности ДНК. Таким образом, термин может относиться к нуклеиновой кислоте, которая является чужеродной или гетерологичной для клетки, или является гомологичной для клетки, однако присутствует в клетке в таком положении или форме, в которой нуклеиновая кислота обычно не встречается. Аналогичным образом, при использовании данного термина в отношении полипептидной или аминокислотной последовательности, экзогенный полипептид или аминокислотная последовательность может представлять собой полипептид или аминокислотную последовательность, которая происходит из источника, являющегося чужеродным по отношению к конкретной клетке или, если последовательность получена из того же самого источника, она модифицирована относительно своей исходной формы.
[0198] В настоящей заявке термин «сайт-направленные полипептиды» в целом может относиться к нуклеазам, сайт-направленным нуклеазам, эндорибонуклеазам, условно ферментативно неактивным эндорибонуклеазам, белкам Argonaut и белкам, связывающим нуклеиновые кислоты. Сайт-направленный полипептид или белок может включать нуклеазы, такие как эндонуклеазы с эффектом «хоуминга», например, нуклеазы семейств PI-TliII, H-DreI, I-DmoI и I-CreI, I-SceI, LAGLIDADG, мегануклеазы, нуклеазы семейства GIY-YIG, нуклеазы семейства His-Cys-бокса, Vsr-подобные нуклеазы, эндорибонуклеазы, экзорибонуклеазы, эндонуклеазы и экзонуклеазы. Сайт-направленный полипептид может относиться к члену семейства генов Cas системы CRISPR/Cas типа I, типа II, типа III, и/или типа U. Сайт-направленный полипептид может относиться к члену надсемейства загадочных белков, ассоциированных с повторами (RAMP) (например, подсемейств Cas5, Cas6). Сайт-направленный полипептид может относиться к белку Argonaut.
[0199] Сайт-направленный полипептид может представлять собой любой тип белка. Сайт-направленный полипептид может относиться к нуклеазе. Сайт-направленный полипептид может относиться к эндорибонуклеазе. Сайт-направленный полипептид может относиться к любой модифицированной (например, укороченной, мутированной, удлиненной) полипептидной последовательности или гомологу сайт-направленного полипептида. Сайт-направленный полипептид может быть подвергнут оптимизации кодонов. Сайт-направленный полипептид может представлять собой гомолог сайт-направленного полипептида, подвергнутый оптимизации кодонов. Сайт-направленный полипептид может быть ферментативно неактивным, частично активным, конститутивно активным, полностью активным, активироваться при индукции и/или обладать другими видами активности (например, большим количеством видов активности, чем характерно для гомолога белка или полипептида дикого типа). Сайт-направленный полипептид может представлять собой Cas9, Сайт-направленный полипептид может представлять собой Csy4. Сайт-направленный полипептид может представлять собой Cas5 или члена семейства Cas5. Сайт-направленный полипептид может представлять собой Cas6 или члена семейства Cas6.
[0200] В некоторых случаях сайт-направленный полипептид (например, вариант, мутированный вариант, ферментативно неактивный и/или условно ферментативно неактивный сайт-направленный полипептид) может быть направлен против нуклеиновой кислоты. Сайт-направленный полипептид (например, вариант, мутированный вариант, ферментативно неактивная и/или условно ферментативно неактивная эндорибонуклеаза) может быть направлен против РНК. Эндорибонуклеазы, которые могут быть направлены против РНК, могут включать представителей других подсемейств CRISPR, таких как Cas6 и Cas5.
[0201] В настоящей заявке термин «специфичный» может относиться к взаимодействию двух молекул, при котором одна из молекул с помощью, например, химических или физических средств специфично связывается со второй молекулой. Типичные специфичные взаимодействия, приводящие к связыванию, могут относиться к связыванию антиген-антитело, связыванию авидин-биотин, связыванию углеводов и пектинов, связыванию комплементарных последовательностей нуклеиновых кислот (например, гибридизации), связыванию комплементарных пептидных последовательностей, включая те, которые образованы с помощью рекомбинантных методов, связыванию эффекторных и рецепторных молекул, связыванию кофакторов ферментов и ферментов, связыванию ингибиторов ферментов и ферментов и т.п. Термин «неспецифичный» может относиться к взаимодействию между двумя молекулами, которое не является специфичным.
[0202] В настоящей заявке термин «твердая подложка» в целом может относиться к любому нерастворимому или частично растворимому материалу. Твердая подложка может относиться к индикаторной полоске, многолуночной чашке и т.п. Твердая подложка может включать различные вещества (например, стекло, полистирол, поливинилхлорид, полипропилен, полиэтилен, поликарбонат, декстран, нейлон, амилозу, природные и модифицированные целлюлозы, полиакриламиды, агарозы и магнетит) и может быть обеспечена в различных формах, включая гранулы агарозы, гранулы полистирола, гранулы латекса, магнитные гранулы, коллоидные металлические частицы, стеклянные и/или кремниевые чипы и поверхности, полоски из нитроцеллюлозы, нейлоновые мембраны, листы, лунки реакционных планшетов (например, многолуночные планшеты), пластиковые пробирки и т.д. Твердая подложка может представлять собой твердую или полутвердую подложку, гранулу или поверхность. Подложка может быть подвижной в растворе или может быть неподвижной. Твердая подложка может быть использована для захвата полипептида. Твердая подложка может содержать захватывающий агент.
[0203] В настоящей заявке термин «нуклеиновая кислота-мишень» в целом может относиться к нуклеиновой кислоте, которая будет использована в соответствии со способами согласно настоящему изобретению. Нуклеиновая кислота-мишень может относиться к хромосомной последовательности или внехромосомной последовательности (например, эписомальной последовательности, небольшой кольцевой последовательности, митохондриальной последовательности, последовательности в хлоропластах и т.д.). Нуклеиновая кислота-мишень может представлять собой ДНК. Нуклеиновая кислота-мишень может представлять собой РНК. В настоящей заявке термин «нуклеиновая кислота-мишень» может быть использован взаимозаменяемо с терминами «полинуклеотид», «нуклеотидная последовательность» и/или «полинуклеотид-мишень». Нуклеиновая кислота-мишень может представлять собой последовательность нуклеиновой кислоты, которая может быть неродственной по отношению к любой другой последовательности в образце нуклеиновой кислоты на основании замены одного нуклеотида. Нуклеиновая кислота-мишень может представлять собой последовательность нуклеиновой кислоты, которая может быть неродственной по отношению к любой другой последовательности в образце нуклеиновой кислоты на основании замены 2, 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидов. Согласно некоторым вариантам реализации настоящего изобретения замена может происходить в пределах последовательности из 5, 10, 15, 20, 25, 30 или 35 нуклеотидов на 5'-конце нуклеиновой кислоты-мишени. Согласно некоторым вариантам реализации настоящего изобретения замена может происходить в пределах последовательности из 5, 10, 15, 20, 25, 30, 35 нуклеотидов на 3'-конце нуклеиновой кислоты-мишени.
[0204] В настоящей заявке термин «tracrPHK» в целом может относиться к нуклеиновой кислоте, последовательность которой по меньшей мере приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична типичной последовательности tracrPHK дикого типа (например, tracrPHK из S. pyogenes (SEQ ID NO: 433), SEQ ID NO: 431-562). TracrPHK может относиться к нуклеиновой кислоте, последовательность которой не более чем приблизительно на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% идентична и/или гомологична типичной последовательности tracrPHK дикого типа (например, tracrPHK из S. pyogenes). TracrPHK может относиться к модифицированной форме tracrPHK, которая может содержать изменение нуклеотидной последовательности, такое как делеция, вставка или замена, вариант, мутация или химера. TracrPHK может относиться к нуклеиновой кислоте, последовательность которой может быть по меньшей мере приблизительно на 60% идентична последовательности типичной tracrPHK дикого типа (например, tracrPHK из S. pyogenes) в участке, содержащем по меньшей мере 6 последовательных нуклеотидов. Например, последовательность tracrPHK может быть по меньшей мере приблизительно на 60% идентична, по меньшей мере приблизительно на 65% идентична, по меньшей мере приблизительно на 70% идентична, по меньшей мере приблизительно на 75% идентична, по меньшей мере приблизительно на 80% идентична, по меньшей мере приблизительно на 85% идентична, по меньшей мере приблизительно на 90% идентична, по меньшей мере приблизительно на 95% идентична, по меньшей мере приблизительно на 98% идентична, по меньшей мере приблизительно на 99% идентична или на 100% идентична последовательности типичной tracrPHK дикого типа (например, tracrPHK из S. pyogenes) в участке, содержащем по меньшей мере 6 последовательных нуклеотидов. TracrPHK может относиться к средней последовательности tracrPHK. TracrPHK может относиться к минимальной последовательности tracrPHK.
[0205] Системы CRISPR
[0206] CRISPR (короткие палиндромные повторы, регулярно расположенные группами) представляет собой геномный локус, обнаруженный в геномах многих прокариот (например, бактерий и архей). У прокариот локусы CRISPR могут обеспечить устойчивость к инвазиям чужеродных организмов (например, вирусов, фагов). Таким образом, как полагают, система CRISPR функционирует в качестве разновидности иммунной системы, обеспечивающей защиту прокариот от вторжения чужеродных организмов. Выявлено три этапа функционирования локуса CRISPR: встраивание новых последовательностей в локус, биогенез РНК CRISPR (crPHK) и подавление нуклеиновой кислоты вторгающегося чужеродного организма. Существует четыре типа систем CRISPR (например, тип I, тип II, тип III, тип U).
[0207] Локус CRISPR может включать ряд коротких повторяющихся последовательностей, называемых «повторами». Повторы могут образовывать шпилечные структуры и/или могут представлять собой неструктурированные одноцепочечные последовательности. Повторы могут находиться в кластерах. Последовательности повторов часто могут различаться между видами. Повторы могут перемежаться уникальными участками, которые называются «спейсеры», в результате чего архитектура локуса имеет вид повтор-спейсер-повтор. Спейсеры могут быть идентичны или имеют высокую степень гомологии с известными последовательностями вторгающегося чужеродного организма. Блок спейсер-повтор может кодировать crisprRNA (crPHK). CrPHK может относиться к зрелой форме блока спейсер-повтор. CrPHK может содержать «затравочную» последовательность, которая может участвовать в направлении на нуклеиновую кислоту-мишень (например, возможно, в качестве механизма наблюдения за чужеродной нуклеиновой кислотой). Затравочная последовательность может быть расположена на 5' или 3'-конце crPHK.
[0208] Локус CRISPR может содержать полинуклеотидные последовательности, кодирующие сцепленные с CRISPR гены (Cas). Гены Cas могут быть вовлечены в биогенез и/или этапы интерференции, которая является функцией crPHK. Последовательности генов Cas (например, первичная последовательность) могут очень сильно различаться между видами и гомологами. Например, гомологи Cas1 могут иметь менее чем 10% идентичность первичной последовательности между гомологами. Некоторые гены Cas могут содержать гомологичные вторичные и/или третичные структуры. Например, несмотря на очень сильное различие последовательностей, многие члены семейства Cas6 белков CRISPR содержат N-концевую ферредоксин-подобную складку. Гены Cas могут быть названы в соответствии с организмом, из которого они получены. Например, гены Cas из Staphylococcus epidermidis могут упоминаться как Csm-тип, гены Cas из Streptococcus thermophilus могут упоминаться как Csn-тип, и гены Cas из Pyrococcus furiosus могут упоминаться как Cmr-тип.
[0209] Встраивание
[0210] Этап встраивания системы CRISPR может относиться к способности локуса CRISPR встраивать новые спейсеры в массив crPHK при инфицировании чужеродным возбудителем. Поглощение спейсеров чужеродных возбудителей может способствовать развитию иммунитета к последующим атакам этого же чужеродного возбудителя. Встраивание может происходить в лидерном конце локуса CRISPR. Белки Cas (например, Cas1 и Cas2) могут быть вовлечены в процесс встраивания новых спейсерных последовательностей. Для некоторых типов систем CRISPR (например, типа I-III) встраивание может осуществляться аналогичным способом.
[0211] Биогенез
[0212] Зрелые crPHK могут быть получены в результате расщепления более длинного транскрипта полицистронного локуса CRISPR (т.е. пре-crPHK массив). Массив пре-crPHK может содержать множество crPHK. Повторы в массиве пре-crPHK могут распознаваться белками Cas. Белки Cas могут связываться с повторами и отщеплять повторы. Этот процесс может приводить к высвобождению множества crPHK. CrPHK могут быть подвергнуты дальнейшим воздействиям для получения зрелой формы crPHK, например, укорочению (например, под действием экзонуклеазы). CrPHK может содержать все, некоторые или ни одной из последовательностей повторов CRISPR.
[0213] Интерференция
[0214] Интерференция может относиться к этапу работы системы CRISPR, функция которой заключается в борьбе с инфекцией чужеродным возбудителем. Интерференция с помощью системы CRISPR может осуществляться в соответствии с аналогичным механизмом для РНК-интерференции (RNAi (например, при которой происходит направленное воздействие на РНК-мишень (например, гибридизация) малых интерферирующих РНК (миРНК)), что вызывает деградацию и/или дестабилизацию РНК-мишени. Системы CRISPR могут интерферировать с нуклеиновой кислотой-мишенью путем соединения транскриптов crPHK и генов Cas с образованием рибонуклеопротеинов CRISPR (crRNP). crPHK из crRNP могут направлять crRNP к нуклеиновой кислоте чужеродного возбудителя (например, за счет распознавания нуклеиновой кислоты чужеродного возбудителя путем гибридизации). Блоки, содержащие нуклеиновую кислоту чужеродного возбудителя, гибридизованную с crPHK, могут расщепляться белками Cas. Интерференция с нуклеиновой кислотой-мишенью может потребовать присутствия в нуклеиновой кислоте-мишени мотива, прилегающего к протоспейсеру (РАМ).
[0215] Типы систем CRISPR
[0216] Существуют четыре типа систем CRISPR: тип I, тип II, тип III и тип U. В организме может быть обнаружено более одной системы CRISPR. Системы CRISPR могут дополнять друг друга, и/или могут временно активировать транс-действующие функциональные блоки, чтобы облегчить процессинг локуса CRISPR.
[0217] Системы CRISPR типа I
[0218] Биогенез crPHK в системах CRISPR типа I может включать расщепление повторов в массиве пре-crPHK под действием эндорибонуклеазы, что может привести к образованию множества crPHK. CrPHK систем типа I могут не подвергаться укорочению. CrPHK могут отщепляться из массива пре-crPHK с помощью полибелкового комплекса, называемого Cascade (расшифровываемого как CRISPR-сцепленный комплекс для антивирусной защиты). Cascade может включать субъединицы белков (например, CasA-CasE). Некоторые из субъединиц могут быть членами надсемейства загадочных белков, ассоциированных с повторами (RAMP) (например, семейств Cas5 и Cas6). Комплекс Cascade-crPHK (т.е. комплекс интерференции) может распознавать нуклеиновую кислоту-мишень посредством гибридизации crPHK с нуклеиновой кислотой-мишенью. Комплекс интерференции Cascade может привлекать хеликазу/нуклеазу Cas3, которая функционирует в качестве транс-действующего элемента и облегчает расщепление нуклеиновой кислоты-мишени. Нуклеаза Cas3 может расщеплять нуклеиновую кислоту-мишень (например, с помощью гистидин-аспартатной субъединицы (HD), придающей нуклеазную активность). Нуклеиновая кислота-мишень в системе CRISPR типа I может содержать РАМ. Нуклеиновая кислота-мишень в системе CRISPR типа I может представлять собой ДНК.
[0219] Системы I типа могут дополнительно подразделяться в зависимости от видового происхождения. Системы типа I могут включать: типы IA (Aeropyrum pernix или CASS5); IB (Thermotoga neapolitana-Haloarcuda marismortui или CASS7); 1C (Desulfovibrio vulgaris или CASS1); ID; IE (Escherichia coli или CASS2); и IF (Yersinia pestis или CASS3) надсемейства.
[0220] Системы CRISPR типа II
[0221] Биогенез crPHK в системе CRISPR типа II может включать транс-активирующие РНК CRISPR (tracrPHK). TracrPHK может быть модифицирована эндогенной РНКазой III. TracrPHK комплекса может гибридизоваться с повтором crPHK в массиве пре-crPHK. Эндогенная РНКаза II может быть привлечена для расщепления пре-crPHK. Расщепленная crPHK может быть укорочена под действием экзорибонуклеазы для получения зрелой формы crPHK (например, укорочение с 5'-конца). TracrPHK может оставаться гибридизованной с crPHK. TracrPHK и crPHK могут связываться с сайт-направленным полипептидом (например, Cas9). CrPHK в составе комплекса crPHK-tracrPHK-Cas9 может направлять комплекс к нуклеиновой кислоте-мишени, с которой гибридизуется crPHK. Гибридизация crPHK с нуклеиновой кислотой-мишенью может активировать Cas9 для расщепления нуклеиновой кислоты-мишени. Нуклеиновая кислота-мишень в системе CRISPR типа II может содержать РАМ. Согласно некоторым вариантам реализации настоящего изобретения РАМ играет важную роль в облегчении связывания сайт-направленного полипептида (например, Cas9) с нуклеиновой кислотой-мишенью. Системы типа II могут дополнительно подразделяться на II-A (Nmeni или CasS4) и II-B (Nmeni или CasS4).
[0222] Системы CRISPR типа III
[0223] Биогенез crPHK в системах CRISPR типа III может включать этап расщепления повторов в массиве пре-crPHK под действием эндорибонуклеазы с образованием множества crPHK. Повторы в системы CRISPR типа III могут представлять собой неструктурированные одноцепочечные области. Повторы могут распознаваться и расщепляться под действием члена RAMP-надсемейства эндорибонуклеаз (например, Cas6). CrPHK систем типа III (например, типа III-B) могут быть укорочены (например, укорочены с 3'-конца). Системы типа III могут содержать белок, сходный с полимеразой, (например, Cas10). Cas10 может содержать домен, гомологичный palm-домену («домен-ладонь»).
[0224] Системы типа III могут расщеплять пре-crPHK с помощью комплекса, содержащего множество белков членов RAMP-надсемейства, и одного или более белков, сходных с полимеразами CRISPR. Системы типа III могут подразделяться на подтипы III-А и III-B. Мишенью интерферирующего комплекса системы типа III-A (т.е., комплекса Csm) может быть нуклеиновая кислота плазмиды. Расщепление нуклеиновой кислоты плазмиды может произойти под действием HD-нуклеазного домена белка, сходного с полимеразой, в составе комплекса. Мишенью интерферирующего комплекса системы типа III-B (т.е., комплекса Cmr) может быть РНК.
[0225] Системы CRISPR типа U
[0226] Системы CRISPR типа U могут не содержать генов, характерных для систем типа CRISPR I-III (например, Cas3, Cas9, Cas6, Cas1, Cas2). Примеры генов Cas системы CRISPR типа U могут включать, но не ограничиваются ими, Csf1, Csf2, Csf3, Csf4. Гены Cas типа U могут иметь низкую степень гомологии с генами Cas типа I-III. Например, Csf3 может существенно отличаться, но при этом быть функционально аналогичным членам семейства Cas5. Система типа U может обладать дополняющей транс-активностью в отношении систем типа I-III. В некоторых случаях системы типа U могут не принимать участия в расщеплении массивов пре-РНК CRISPR. Системы типа U могут представлять собой альтернативную систему защиты от чужеродных возбудителей.
[0227] Надсемейство RAMP
[0228] Загадочные белки, ассоциированные с повторами (белки RAMP), характеризуются наличием складки белковой последовательности, включающей мотив βαββαβ [бета-альфа-бета-бета-альфа-бета], бета-нитей (β) и альфа-спиралей (α). Белок RAMP может содержать мотив распознавания РНК (RRM) (который может содержать ферредоксин или ферредоксин-подобную складку). Белки RAMP могут содержать N-концевой RRM. С-концевой домен белков RAMP может быть различным, но также может включать RRM. Члены семейства RAMP могут распознавать структурированную и/или неструктурированную нуклеиновую кислоту. Члены семейства RAMP могут распознавать одноцепочечную и/или двухцепочечную нуклеиновую кислоту. Белки RAMP могут быть вовлечены в этапы биогенеза и/или интерференции с участием систем CRISPR типа I и типа III. Члены надсемейства RAMP могут включать членов семейств Cas7, Cas6 и Cas5. Члены надсемейства RAMP могут представлять собой эндорибонуклеазы.
[0229] Домены RRM в надсемействе RAMP могут чрезвычайно отличаться друг от друга. Домены RRM могут обладать по меньшей мере приблизительно 5%, по меньшей мере приблизительно 10%, по меньшей мере приблизительно 15%, по меньшей мере приблизительно 20%, по меньшей мере приблизительно 25%, по меньшей мере приблизительно 30%, по меньшей мере приблизительно 35%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 45%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 55%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95% или 100% гомологией последовательности или структуры при сравнении с таковыми для типичного домена RRM дикого типа (например, домен RRM из Cas7). Домены RRM могут обладать не более чем приблизительно 5%, не более чем приблизительно 10%, не более чем приблизительно 15%, не более чем приблизительно 20%, не более чем приблизительно 25%, не более чем приблизительно 30%, не более чем приблизительно 35%, не более чем приблизительно 40%, не более чем приблизительно 45%, не более чем приблизительно 50%, не более чем приблизительно 55%, не более чем приблизительно 60%, не более чем приблизительно 65%, не более чем приблизительно 70%, не более чем приблизительно 75%, не более чем приблизительно 80%, не более чем приблизительно 85%, не более чем приблизительно 90%, не более чем приблизительно 95% или 100% гомологией последовательности или структуры при сравнении с таковыми для типичного домена RRM дикого типа (например, домен RRM из Cas7).
[0230] Семейство Cas7
[0231] Члены семейства Cas7 могут представлять собой подкласс белков семейства RAMP. Белки семейства Cas7 могут быть отнесены к категории систем CRISPR типа I. Члены семейства Cas7 могут не содержать богатой глицином петли, которая является типичной для многих членов семейства RAMP. Члены семейства Cas7 могут содержать один домен RRM. Члены семейства Cas7 могут включать, но не ограничиваются ими, Cas7 (COG1857), Cas7 (COG3649), Cas7 (СТ1975), Csy3, Csm3, Cmr6, Csm5, Cmr4, CMR1, Csf2 и Csc2.
[0232] Семейство Cas6
[0233] Семейство Cas6 может представлять собой подсемейство RAMP. Члены семейства Cas6 могут содержать два домена, сходных с мотивом распознавания РНК (RRM). Член семейства Cas6 (например, Cas6f) может содержать N-концевой домен RRM и другой С-концевой домен, последовательность или структура которого могут иметь низкую степень гомологии при сравнении с таковыми для домена RRM. Члены семейства Cas6 могут содержать каталитический гистидин, который может быть вовлечен в эндорибонуклеазную активность. Аналогичный мотив может быть обнаружен у членов RAMP-подсемейств Cas5 и Cas7. Члены семейства Cas6 могут включать, но не ограничиваются ими, Cas6, Cas6e, Cas6f (например, Csy4).
[0234] Семейство Cas5
[0235] Семейство Cas5 может представлять собой подсемейство RAMP. Семейство Cas5 можно разделить на две подгруппы: первую подгруппу, содержащую два домена RRM, и вторую подгруппу, содержащую один домен RRM. Члены семейства Cas5 могут включать, но не ограничиваются ими, Csm4, Csx10, Cmr3, Cas5, Cas5 (ВН0337), Csy2, Csc1l, Csf3.
[0236] Гены Cas
[0237] Типичные гены Cas системы CRISPR могут включать Cas1, Cas2, Cas3' (Cas3-штрих), Cas3'' (Саз3-двойной штрих), Cas4, Cas5, Cas6, Cas6e (ранее назывался CasE, Cse3), Cas6f (т.е., Csy4), Cas7, Cas8a1, Cas8a2, Cas8b, Cas8c, Cas9, Cas10, Cas10d, Csy1, Csy2, Csy3, Cse1, Cse2, Csc1, Csc2, Csa5, Csn2, Csm2, Csm3, Csm4, Csm5, Csm6, Cmr1, Cmr3, Cmr4, Cmr5, Cmr6, Csb1, Csb2, Csb3, Csx17, Csx14, Csx10, Csx16, CsaX, Csx3, Csx1, Csx15, Csf1, Csf2, Csf3, Csf4. В таблице 1 приведена типичная классификация генов Cas CRISPR в соответствии с типом системы CRISPR.
[0238] Номенклатура генов Cas системы CRISPR была существенно пересмотрена ввиду открытия новых генов Cas. Применительно к настоящей заявке названия генов Cas, используемые в данном описании, основаны на номенклатуре, изложенной в Makarova et al. Evolution and classification of the CRISPR-Cas systems. Nature Reviews Microbiology. 2011 June; 9(6): 467-477. Doi:10.1038/nrmicro2577.

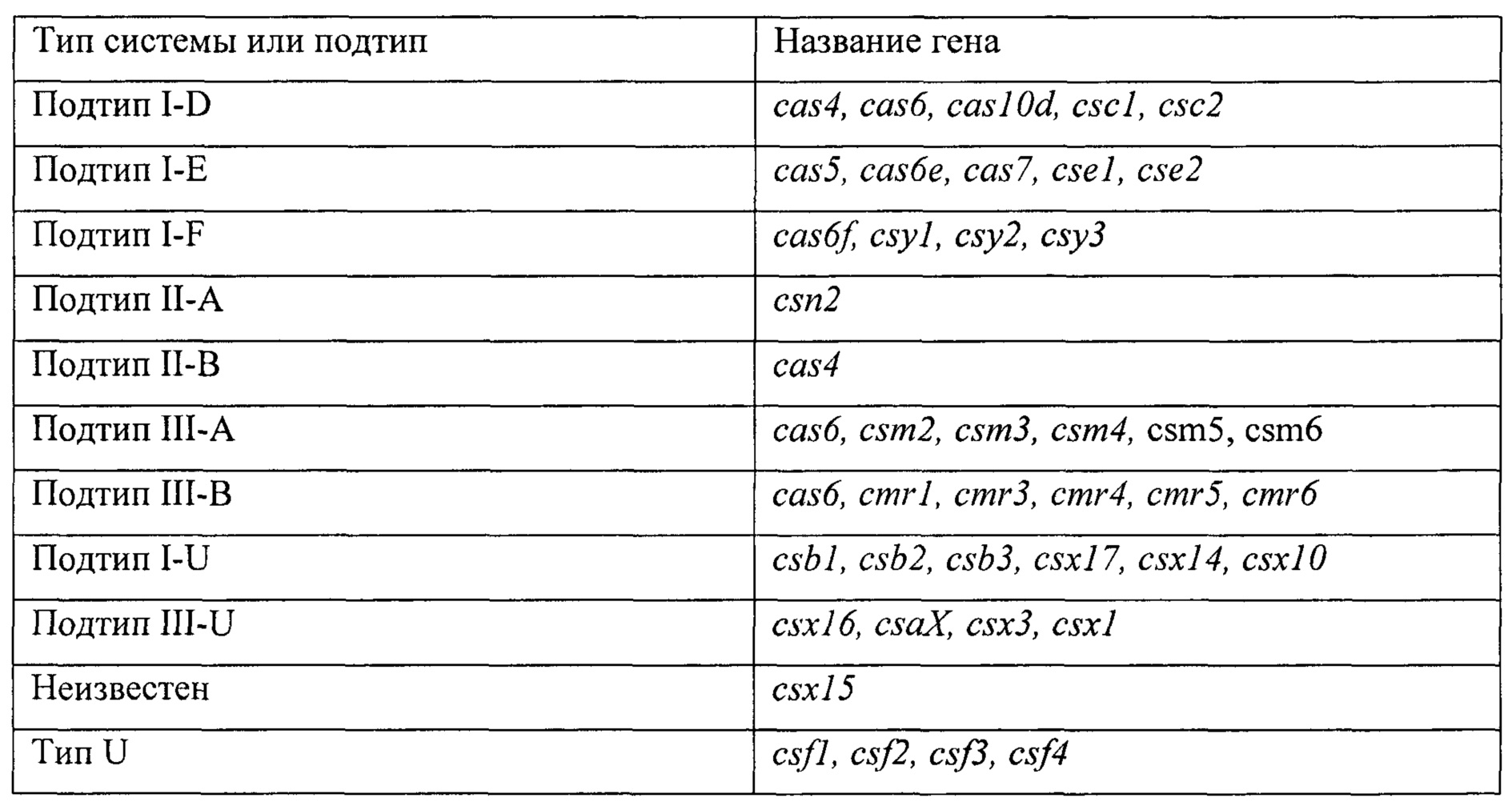
[0239] Сайт-направленные полипептиды
[0240] Сайт-направленный полипептид может представлять собой полипептид, который способен связываться с нуклеиновой кислотой-мишенью. Сайт-направленный полипептид может представлять собой нуклеазу.
[0241] Сайт-направленный полипептид может содержать домен, связывающий нуклеиновую кислоту. Домен, связывающий нуклеиновую кислоту, может содержать область, которая вступает в контакт с нуклеиновой кислотой. Домен, связывающий нуклеиновую кислоту, может содержать нуклеиновую кислоту. Домен, связывающий нуклеиновую кислоту, может содержать белковый материал. Домен, связывающий нуклеиновую кислоту, может содержать нуклеиновую кислоту и белковый материал. Домен, связывающий нуклеиновую кислоту, может содержать РНК. Домен, связывающий нуклеиновую кислоту, может представлять собой одиночный домен. Примеры доменов, связывающих нуклеиновую кислоту, могут включать, но не ограничиваются ими, домен спираль-поворот-спираль, домен цинкового пальца, домен лейциновой молнии (bZIP), домен крылатая спираль, домен крылатая спираль-поворот-спираль, домен спираль-поворот-спираль, домен HMG-бокс, домен Wor3, домен иммуноглобулина, домен В3, домен TALE, домен, содержащий мотив распознавания РНК, домен, содержащий мотив связывания двухцепочечной РНК, домен связывания двухцепочечной нуклеиновой кислоты, домены связывания одноцепочечной нуклеиновой кислоты, домен KН, домен PUF, домен RGG-бокс, домен DEAD/DEAH-бокс, домен PAZ, домен Piwi и домен холодового шока.
[0242] Домен, связывающий нуклеиновую кислоту, может представлять собой домен белка Argonaute. Белок Argonaute может представлять собой эукариотический Argonaute или прокариотический Argonaute. Белок Argonaute может связываться с РНК, ДНК или с обоими, РНК и ДНК. Белок Argonaute может расщеплять РНК или ДНК, или РНК и ДНК. В некоторых случаях белок Argonaute связывается с ДНК и расщепляет ДНК-мишень.
[0243] В некоторых случаях два или более доменов, связывающих нуклеиновую кислоту, могут быть соединены вместе. Соединение нескольких доменов, связывающих нуклеиновую кислоту, может обеспечить повышенную специфичность в отношении полинуклеотидной последовательности. Два или более доменов, связывающих нуклеиновую кислоту, могут быть соединены с помощью одного или более линкеров. Линкер может представлять собой гибкий линкер. Линкеры могут содержать 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40 или более аминокислот в длину. Линкеры могут содержать по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% глицина. Линкеры могут содержать не более чем 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% глицина. Линкеры могут содержать по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% серина. Линкеры могут содержать не более чем 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% серина.
[0244] Домены, связывающие нуклеиновую кислоту, могут связываться с последовательностями нуклеиновых кислот. Домены, связывающие нуклеиновую кислоту, могут связываться с нуклеиновыми кислотами путем гибридизации. Домены, связывающие нуклеиновую кислоту, могут быть сконструированы (например, сконструированы для придания им способности гибридизоваться с последовательностью в геноме). Домен, связывающий нуклеиновую кислоту, может быть сконструирован с помощью методов молекулярного клонирования (например, направленной эволюции, сайт-специфичного мутагенеза и рационального мутагенеза).
[0245] Сайт-направленный полипептид может содержать домен, расщепляющий нуклеиновую кислоту. Домен, расщепляющий нуклеиновую кислоту, может представлять собой домен, расщепляющий нуклеиновую кислоту, из любого белка, расщепляющего нуклеиновую кислоту. Домен, расщепляющий нуклеиновую кислоту, может быть получен из нуклеазы. Подходящие домены, расщепляющие нуклеиновую кислоту, включают домен, расщепляющий нуклеиновую кислоту, из эндонуклеаз (например, эндонуклеазы АР, эндонуклеазы RecBCD, эндонуклеазы Т7, эндонуклеазы Т4 IV, эндонуклеазы Bal 31, эндонуклеазы I (эндо I), нуклеазы микрококков, эндонуклеазы II (эндо VI, экзо-III)), экзонуклеаз, нуклеаз рестрикции, эндорибонуклеаз, экзорибонуклеаз, РНКаз (например, РНКазы I, II или III). В некоторых случаях домен, расщепляющий нуклеиновую кислоту, может быть получен из эндонуклеазы FokI. Сайт-направленный полипептид может содержать множество доменов, расщепляющих нуклеиновую кислоту. Домены, расщепляющие нуклеиновую кислоту, могут быть соединены. Два или более доменов, расщепляющих нуклеиновую кислоту, могут быть связаны посредством линкера. Согласно некоторым вариантам реализации настоящего изобретения линкер может представлять собой гибкий линкер. Линкеры могут содержать 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40 или более аминокислот в длину. Согласно некоторым вариантам реализации настоящего изобретения сайт-направленный полипептид может содержать множество доменов, расщепляющих нуклеиновую кислоту.
[0246] Сайт-направленный полипептид (например, Cas9, Argonaute) может содержать два или более нуклеазных доменов. Cas9 может содержать домен HNH или HNH-подобный нуклеазный домен и/или домен RuvC или RuvC-подобный нуклеазный домен. HNH или HNH-подобный домены могут содержать McrA-подобную складку. HNH или HNH-подобный домены могут состоять из двух антипараллельных бета-цепей и альфа-спирали. HNH или HNH-подобный домены могут содержать сайт связывания металла (например, сайт связывания двухвалентного катиона). HNH или HNH-подобный домены могут расщеплять одну цепь нуклеиновой кислоты-мишени (например, комплементарную цепь цепи-мишени crPHK). Белки, которые содержат HNH или HNH-подобный домен, могут включать эндонуклеазы, клицины, эндонуклеазы рестрикции, транспозазы и факторы, упаковывающие ДНК.
[0247] RuvC или RuvC-подобные домены могут содержать RNaseH или RNaseH-подобную складку. RuvC/RNaseH домены могут быть вовлечены в различные функции, связанные с нуклеиновыми кислотами, включая воздействие на РНК и ДНК. Домен RNaseH может содержать 5 β-цепей, окруженных множеством альфа-спиралей. RuvC/RNaseH домен или RuvC/RNaseH-подобный домен могут содержать сайт связывания металлов (например, сайт связывания двухвалентного катиона). RuvC/RNaseH домен или RuvC/RNaseH-подобный домен могут расщеплять одну цепь нуклеиновой кислоты-мишени (например, некомплементарную цепь цепи-мишени crPHK). Белки, которые содержат RuvC, RuvC-подобный или RNaseH-подобный домен, могут включать RNaseH, RuvC, транспозазы ДНК, ретровирусные интегразы и белки Argonaute.
[0248] Сайт-направленный полипептид может представлять собой эндорибонуклеазу. Сайт-направленный полипептид может представлять собой ферментативно неактивный сайт-направленный полипептид. Сайт-направленный полипептид может представлять собой условно ферментативно неактивный сайт-направленный полипептид. Сайт-направленный полипептид может вводить двухцепочечные разрывы или одноцепочечные разрывы в нуклеиновую кислоту (например, геномную ДНК). Двухцепочечный разрыв может стимулировать эндогенные пути репарации ДНК в клетке (например, гомологичную рекомбинацию и негомологичное соединение концов (NHEJ) или альтернативное негомологичное соединение концов (A-NHEJ)). NHEJ может восстановить расщепленную нуклеиновую кислоту-мишень без использования гомологичной матрицы. Такое восстановление может привести к делециям в последовательности нуклеиновой кислоты-мишени. Гомологичная рекомбинация (HR) может происходить с использованием гомологичной матрицы. Гомологичная матрица может содержать последовательности, которые гомологичны последовательностям, фланкирующим сайт расщепления нуклеиновой кислоты-мишени. После расщепления нуклеиновой кислоты-мишени под действием сайт-направленного полипептида, сайт расщепления может быть разрушен (например, сайт может быть недоступным для другого раунда расщепления с участием исходной нуклеиновой кислоты, направленной против нуклеиновой кислоты, и сайт-направленного полипептида).
[0249] В некоторых случаях Гомологичная рекомбинация может приводить к вставке экзогенной полинуклеотидной последовательности в сайт расщепления нуклеиновой кислоты-мишени. Экзогенная полинуклеотидная последовательность может быть названа донорным полинуклеотидом. В некоторых способах согласно настоящему изобретению донорный полинуклеотид, часть донорного полинуклеотида, копия донорного полинуклеотида или часть копии донорного полинуклеотида может быть вставлена в сайт расщепления нуклеиновой кислоты-мишени. Донорный полинуклеотид может представлять собой экзогенную полинуклеотидную последовательность. Донорный полинуклеотид может представлять собой последовательность, которая отсутствует в природных условиях в сайте расщепления нуклеиновой кислоты-мишени. Вектор может содержать донорный полинуклеотид. Модификации ДНК-мишени за счет NHEJ и/или HR могут привести, например, к мутациям, делециям, изменениям, встраиванию, коррекции гена, замене гена, введению метки в ген, вставке трансгена, удалению нуклеотида, разрушению гена и/или мутации гена. Процесс встраивания ненативной нуклеиновой кислоты в геномную ДНК может быть назван геномной инженерией.
[0250] В некоторых случаях сайт-направленный полипептид может содержать аминокислотную последовательность, которая не более чем на 10%, не более чем на 15%, не более чем на 20%, не более чем на 30%, не более чем на 40%, не более чем на 50%, не более чем на 60%, не более чем на 70%, не более чем на 75%, не более чем на 80%, не более чем на 85%, не более чем на 90%, не более чем на 95%, не более чем на 99% или на 100% идентична аминокислотной последовательности типичного сайт-направленного полипептида дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8).
[0251] В некоторых случаях сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 99% или на 100% идентична аминокислотной последовательности типичного сайт-направленного полипептида дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8).
[0252] В некоторых случаях сайт-направленный полипептид может содержать аминокислотную последовательность, которая не более чем на 10%, не более чем на 15%, не более чем на 20%, не более чем на 30%, не более чем на 40%, не более чем на 50%, не более чем на 60%, не более чем на 70%, не более чем на 75%, не более чем на 80%, не более чем на 85%, не более чем на 90%, не более чем на 95%, не более чем на 99% или на 100% идентична аминокислотной последовательности нуклеазного домена типичного сайт-направленного полипептида дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8).
[0253] Сайт-направленный полипептид может быть по меньшей мере на 70, 75, 80, 85, 90, 95, 97, 99 или 100% идентичен сайт-направленному полипептиду дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8) в участке, содержащем 10 последовательных аминокислот в длину. Сайт-направленный полипептид может быть не более чем на 70, 75, 80, 85, 90, 95, 97, 99 или 100% идентичен сайт-направленному полипептиду дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8) в участке, содержащем 10 последовательных аминокислот в длину. Сайт-направленный полипептид может быть по меньшей мере на 70, 75, 80, 85, 90, 95, 97, 99 или 100% идентичен сайт-направленному полипептиду дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8) в участке, содержащем 10 последовательных аминокислот в длину, в HNH нуклеазном домене сайт-направленного полипептида. Сайт-направленный полипептид может быть не более чем на 70, 75, 80, 85, 90, 95, 97, 99 или 100% идентичен сайт-направленному полипептиду дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8) в участке, содержащем 10 последовательных аминокислот в длину, в HNH нуклеазном домене сайт-направленного полипептида. Сайт-направленный полипептид может быть по меньшей мере на 70, 75, 80, 85, 90, 95, 97, 99 или 100% идентичен сайт-направленному полипептиду дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8) в участке, содержащем 10 последовательных аминокислот в длину, в RuvC нуклеазном домене сайт-направленного полипептида. Сайт-направленный полипептид может быть не более чем на 70, 75, 80, 85, 90, 95, 97, 99 или 100% идентичен сайт-направленному полипептиду дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8) в участке, содержащем 10 последовательных аминокислот в длину, в RuvC нуклеазном домене сайт-направленного полипептида.
[0254] В некоторых случаях сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 99% или 100% идентична аминокислотной последовательности нуклеазного домена типичного сайт-направленного полипептида дикого типа (например, Cas9 из S. pyogenes).
[0255] Сайт-направленный полипептид может содержать модифицированный вариант типичного сайт-направленного полипептида дикого типа. Модифицированный вариант типичного сайт-направленного полипептида дикого типа может содержать замену аминокислоты (например, делецию, вставку или замену), которая снижает активность сайт-направленного полипептида, направленную на расщепление нуклеиновой кислоты. Например, активность модифицированного варианта типичного сайт-направленного полипептида дикого типа может составлять менее чем 90%, менее чем 80%, менее чем 70%, менее чем 60%, менее чем 50%, менее чем 40%, менее чем 30%, менее чем 20%, менее чем 10%, менее чем 5% или менее 1% от активности, направленной на расщепление нуклеиновой кислоты, типичного сайт-направленного полипептида дикого типа (например, Cas9 из S. pyogenes). Модифицированный вариант сайт-направленного полипептида может не иметь существенной активности, направленной на расщепление нуклеиновой кислоты. В том случае, если сайт-направленный полипептид представляет собой модифицированный вариант, который не имеет существенной активности, направленной на расщепление нуклеиновой кислоты, он может называться «ферментативно неактивным».
[0256] Активность модифицированного варианта типичного сайт-направленного полипептида дикого типа может составлять более чем 90%, более чем 80%, более чем 70%, более чем 60%, более чем 50%, более чем 40%, более чем 30%, более чем 20%, более чем 10%, более чем 5% или более чем 1% от активности, направленной на расщепление нуклеиновой кислоты, типичного сайт-направленного полипептида дикого типа (например, Cas9 из S. pyogenes).
[0257] Модифицированный вариант сайт-направленного полипептида может содержать мутацию. Модифицированный вариант сайт-направленного полипептида может содержать мутацию, которая придает ему способность индуцировать одноцепочечные разрывы (ssb) на нуклеиновой кислоте-мишени (например, путем разрезания только одного из сахарофосфатных остовов нуклеиновой кислоты-мишени). В результате мутации активность может составлять менее чем 90%, менее чем 80%, менее чем 70%, менее чем 60%, менее чем 50%, менее чем 40%, менее чем 30%, менее чем 20%, менее чем 10%, менее чем 5% или менее чем 1% от активности, направленной на расщепление нуклеиновой кислоты, в одном или более из множества доменов, расщепляющих нуклеиновую кислоту, сайт-направленного полипептида дикого типа (например, Cas9 из S. pyogenes). Мутация может привести к сохранению способности одного или более из множества доменов, расщепляющих нуклеиновую кислоту, расщеплять комплементарную цепь нуклеиновой кислоты-мишени, но к снижению способности расщеплять некомплементарную цепь нуклеиновой кислоты-мишени. Мутация может привести к сохранению способности одного или более из множества доменов, расщепляющих нуклеиновую кислоту, расщеплять некомплементарную цепь нуклеиновой кислоты-мишени, но к снижению способности расщеплять комплементарную цепь нуклеиновой кислоты-мишени. Например, остатки в типичном полипептиде Cas9 дикого типа из S. pyogenes, такие как Asp10, His840, Asn854 и Asn856, могут быть мутированы для инактивации одного или более из множества доменов, расщепляющих нуклеиновую кислоту (например, нуклеазных доменов). Остатки для проведения мутагенеза могут соответствовать остаткам Asp10, His840, Asn854 и Asn856 в типичном полипептиде Cas9 дикого типа из S. pyogenes (например, остатки, определенные по результатам выравнивания последовательностей и/или структур). Неограничивающие примеры включают мутации D10A, Н840А, N854A или N856A. Специалисты в данной области техники поймут, что подходящими являются мутации, за исключением замен аминокислот аланином.
[0258] Мутацию D10A можно комбинировать с одной или более из мутаций Н840А, N854A или N856A для получения сайт-направленного полипептида, по существу не обладающего ДНК-расщепляющей активностью. Мутацию Н840А можно комбинировать с одной или более из мутаций D10A, N854A или N856A для получения сайт-направленного полипептида, по существу не обладающего ДНК-расщепляющей активностью. Мутацию N854A можно комбинировать с одной или более из мутаций Н840А, D10A или N856A для получения сайт-направленного полипептида, по существу не обладающего ДНК-расщепляющей активностью. Мутацию N856A можно комбинировать с одной или более из мутаций Н840А, N854A или D10A для получения сайт-направленного полипептида, по существу не обладающего ДНК-расщепляющей активностью. Сайт-направленные полипептиды, которые содержат один по существу неактивный нуклеазный домен, могут называться никазами.
[0259] Мутации согласно настоящему изобретению могут быть получены методом сайт-направленного мутагенеза. Мутации могут включать замены, добавления и делеции, или любую их комбинацию. В некоторых случаях мутация превращает мутированную аминокислоту в аланин. В некоторых случаях мутация превращает мутированную аминокислоту в другую аминокислоту (например, глицин, серин, треонин, цистеин, валин, лейцин, изолейцин, метионин, пролин, фенилаланин, тирозин, триптофан, аспарагиновую кислоту, глутаминовую кислоту, аспарагин, глутамин, гистидин, лизин или аргинин). Мутация может превращать мутированную аминокислоту в неприродную аминокислоту (например, селенометионин). Мутация может превращать мутированную аминокислоту в миметики аминокислот (например, фосфомиметики). Мутация может представлять собой консервативную мутацию. Например, мутация может превращать мутированную аминокислоту в аминокислоты, размер, форма, заряд, полярность, конформация и/или ротамеры которых аналогичны таковым для мутированных аминокислот (например, мутация цистеин/серин, мутация лизин/аспарагин, мутация гистидин/фенилаланин).
[0260] В некоторых случаях сайт-направленный полипептид (например, вариант, мутированный вариант, ферментативно неактивный и/или условно ферментативно неактивный сайт-направленный полипептид) может быть направлен против нуклеиновой кислоты. Сайт-направленный полипептид (например, вариант, мутированный вариант, ферментативно неактивная и/или условно ферментативно неактивная эндорибонуклеаза) может быть направлен против РНК. Сайт-направленные полипептиды, которые могут быть направлены против РНК, могут включать членов других подсемейств CRISPR, таких как Cas6 и Cas5.
[0261] Сайт-направленный полипептид может содержать одну или более ненативных последовательностей (например, гибридную последовательность).
[0262] Сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из бактерии (например, S. pyogenes), домен, связывающий нуклеиновую кислоту, и два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC).
[0263] Сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из бактерии (например, S. pyogenes), и два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC).
[0264] Сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из бактерии (например, S. pyogenes), и два домена, расщепляющих нуклеиновую кислоту, причем последовательность одного или обоих доменов, расщепляющих нуклеиновую кислоту, по меньшей мере на 50% идентична аминокислотной последовательности нуклеазного домена Cas9 из бактерии (например, S. pyogenes).
[0265] Сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из бактерии (например, S. pyogenes), два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и линкер, соединяющий сайт-направленный полипептид с ненативной последовательностью.
[0266] Сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из бактерии (например, S. pyogenes), два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем Сайт-направленный полипептид содержит мутацию в одном или обоих из доменов, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%.
[0267] Сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из бактерии (например, S. pyogenes), и два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем один из нуклеазных доменов содержит мутацию аспарагиновой кислоты 10, и/или один из нуклеазных доменов содержит мутацию гистидина 840, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%.
[0268] Эндорибонуклеазы
[0269] Согласно некоторым вариантам реализации настоящего изобретения сайт-направленный полипептид может представлять собой эндорибонуклеазу.
[0270] В некоторых случаях эндорибонуклеаза может содержать аминокислотную последовательность, которая не более чем приблизительно на 20%, не более чем приблизительно на 30%, не более чем приблизительно на 40%, не более чем приблизительно на 50%, не более чем приблизительно на 60%, не более чем приблизительно на 70%, не более чем приблизительно на 75%, не более чем приблизительно на 80%, не более чем приблизительно на 85%, не более чем приблизительно на 90%, не более чем приблизительно на 95%, не более чем приблизительно на 99% или на 100% идентична и/или гомологична аминокислотной последовательности стандартной Эндорибонуклеазы дикого типа. Эндорибонуклеаза может содержать аминокислотную последовательность, которая по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 30%, по меньшей мере приблизительно на 40%, по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 60%, по меньшей мере приблизительно на 70%, по меньшей мере приблизительно на 75% по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 99% или 100% идентична и/или гомологична аминокислотной последовательности стандартной Эндорибонуклеазы дикого типа (например, Csy4 из Р. aeruginosa). Стандартная эндорибонуклеаза может быть членом семейства Cas6 (например, Csy4, Cas6). Стандартная эндорибонуклеаза может быть членом семейства Cas5 (например, Cas5 из D. vulgaris). Стандартная эндорибонуклеаза может быть членом семейства CRISPR типа I (например, Cas3). Стандартная эндорибонуклеаза может быть членом семейства CRISPR типа II. Стандартная эндорибонуклеаза может быть членом семейства CRISPR типа III (например, Cas6). Стандартная эндорибонуклеаза может быть членом надсемейства загадочных белков, ассоциированных с повторами (RAMP) (например, Cas7).
[0271] Эндорибонуклеаза может содержать модификации аминокислот (например, замены, делеции, добавления и т.д.). Эндорибонуклеаза может содержать одну или более ненативных последовательностей (например, гибридную последовательность, аффинную метку). Модификации аминокислот могут по существу не изменять активность Эндорибонуклеазы. Эндорибонуклеаза, содержащая модификации аминокислот и/или гибридные последовательности, может сохранить по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 97% или 100% активности, относительно таковой для эндорибонуклеазы дикого типа.
[0272] Модификация может привести к изменению ферментативной активности эндорибонуклеазы. Величина активности в результате модификации может составить менее чем 90%, менее чем 80%, менее чем 70%, менее чем 60%, менее чем 50%, менее чем 40%, менее чем 30%, менее чем 20%, менее чем 10%, менее чем 5% или менее 1% от исходной величины активности эндорибонуклеазы. В некоторых случаях модификация эндорибонуклеазы происходит в нуклеазном домене. В результате таких модификаций способность расщеплять нуклеиновую кислоту может составлять менее чем 90%, менее чем 80%, менее чем 70%, менее чем 60%, менее чем 50%, менее чем 40%, менее чем 30%, менее чем 20%, менее чем 10%, менее чем 5% или менее чем 1% от способности расщеплять нуклеиновую кислоту одного или более из множества доменов, расщепляющих нуклеиновую кислоту, эндорибонуклеазы дикого типа.
[0273] Условно ферментативно неактивные эндорибонуклеазы
[0274] Согласно некоторым вариантам реализации настоящего изобретения эндорибонуклеазы могут быть условно ферментативно неактивным. Условно ферментативно неактивная эндорибонуклеаза может связываться с полинуклеотидой последовательностью специфичным образом. Условно ферментативно неактивная эндорибонуклеаза может связываться с полинуклеотидой последовательностью специфичным образом, но не может расщеплять полирибонуклеотид-мишень.
[0275] В некоторых случаях условно ферментативно неактивная эндорибонуклеаза может содержать аминокислотную последовательность, которая не более чем приблизительно на 20%, не более чем приблизительно на 30%, не более чем приблизительно на 40%, не более чем приблизительно на 50%, не более чем приблизительно на 60%, не более чем приблизительно на 70%, не более чем приблизительно на 75%, не более чем приблизительно на 80%, не более чем приблизительно на 85%, не более чем приблизительно на 90%, не более чем приблизительно на 95%, не более чем приблизительно на 99% или 100% идентична и/или гомологична аминокислотной последовательности стандартной условно ферментативно активной эндорибонуклеазы (например, Csy4 из Р. aeruginosa). В некоторых случаях условно ферментативно неактивная эндорибонуклеаза может содержать аминокислотную последовательность, которая по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 30%, по меньшей мере приблизительно на 40%, по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 60%, по меньшей мере приблизительно на 70%, по меньшей мере приблизительно на 75%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 99% или 100% идентична и/или гомологична аминокислотной последовательности стандартной условно ферментативно активной эндорибонуклеазы (например, Csy4 из Р. aeruginosa).
[0276] Условно ферментативно неактивная эндорибонуклеаза может содержать модифицированный вариант эндорибонуклеазы. Модифицированный вариант эндорибонуклеазы может содержать замену аминокислоты (например, делецию, вставку или замену), которая снижает активность эндорибонуклеазы, направленную на расщепление нуклеиновой кислоты. Например, величина активности модифицированного варианта условно ферментативно неактивной эндорибонуклеазы может составлять менее чем 90%, менее чем 80%, менее чем 70%, менее чем 60%, менее 50%, менее 40%, менее 30%, менее чем 20%, менее чем 10%, менее чем 5% или менее 1% от величины активности, направленной на расщепление нуклеиновой кислоты, стандартной условно ферментативно неактивной эндорибонуклеазы (например, дикого типа) (например, Csy4 из Р. aeruginosa). Модифицированный вариант условно ферментативно неактивной эндорибонуклеазы может не иметь значительной активности, направленной на расщепление нуклеиновой кислоты. В том случае, если условно ферментативно неактивная эндорибонуклеаза представляет собой модифицированный вариант, который не имеет значительной активности, направленной на расщепление нуклеиновой кислоты, такой вариант может называться «ферментативно неактивным».
[0277] Модифицированный вариант условно ферментативно неактивной эндорибонуклеазы может содержать мутацию, которая может привести к снижению активности, направленной на расщепление нуклеиновой кислоты (т.е. так, что условно ферментативно неактивная эндорибонуклеаза может быть ферментативно неактивной в одном или более доменов, расщепляющих нуклеиновую кислоту). В результате мутации величина активности, направленной на расщепление нуклеиновой кислоты, может составлять менее чем 90%, менее чем 80%, менее чем 70%, менее чем 60%, менее чем 50%, менее чем 40%, менее чем 30%, менее чем 20%, менее чем 10%, менее чем 5% или менее чем 1% от величины активности, направленной на расщепление нуклеиновой кислоты, одного или более из множества доменов, расщепляющих нуклеиновую кислоту, эндорибонуклеазы дикого типа (например, Csy4 из Р. aeruginosa). Мутация может произойти в нуклеазном домене эндорибонуклеазы. Мутация может произойти в ферредоксин-подобной складке. Мутация может представлять собой мутацию консервативной ароматической аминокислоты. Мутация может представлять собой мутацию каталитической аминокислоты. Мутация может представлять собой мутацию гистидина. Например, мутация может представлять собой мутацию Н29А в Csy4 (например, Csy4 из Р. aeruginosa) или любого остатка, соответствующего Н29А, согласно результатам выравнивания последовательностей и/или структур. Другие остатки могут быть мутированы для достижения аналогичного эффекта (т.е. для инактивации одного или более из множества нуклеазных доменов).
[0278] Мутации согласно настоящему изобретению могут быть получены методом сайт-направленного мутагенеза. Мутации могут включать замены, добавления и делеции, или любую их комбинацию. В некоторых случаях мутация превращает мутированную аминокислоту в аланин. В некоторых случаях мутация превращает мутированную аминокислоту в другую аминокислоту (например, глицин, серин, треонин, цистеин, валин, лейцин, изолейцин, метионин, пролип, фенилаланин, тирозин, триптофан, аспарагиновую кислоту, глутаминовую кислоту, аспарагин, глутамин, гистидин, лизин или аргинин). Мутация может превращать мутированную аминокислоту в неприродную аминокислоту (например, селенометионин). Мутация может превращать мутированную аминокислоту в миметики аминокислот (например, фосфомиметики). Мутация может представлять собой консервативную мутацию. Например, мутация может превращать мутированную аминокислоту в аминокислоты, размер, форма, заряд, полярность, конформация и/или ротамеры которых аналогичны таковым для мутированных аминокислот (например, мутация цистеин/серин, мутация лизин/аспарагин, мутация гистидин/фенилаланин).
[0279] Условно ферментативно неактивная эндорибонуклеаза может быть ферментативно неактивной в отсутствие повторной активации агентом (например, имидазолом). Агент для повторной активации может представлять собой агент, который имитирует остаток гистидина (например, может иметь имидазольное кольцо). Условно ферментативно неактивная эндорибонуклеаза может быть повторно активирована при контакте с агентом для повторной активации. Агент для повторной активации может содержать имидазол. Например, условно ферментативно неактивная эндорибонуклеаза может быть подвергнута ферментативной активации путем приведения условно ферментативно неактивной эндорибонуклеазы в контакт с имидазолом в концентрации от приблизительно 100 мМ до приблизительно 500 мМ. Концентрация имидазола может составлять приблизительно 100 мМ, приблизительно 150 мМ, приблизительно 200 мМ, приблизительно 250 мМ, приблизительно 300 мМ, приблизительно 350 мМ, приблизительно 400 мМ, приблизительно 450 мМ, приблизительно 500 мМ, приблизительно 550 мМ или приблизительно 600 мМ. Присутствие имидазола (например, в диапазоне концентраций от приблизительно 100 мМ до приблизительно 500 мМ) может повторно активировать условно ферментативно неактивную эндорибонуклеазу так, что условно ферментативно неактивная эндорибонуклеаза становится ферментативно активной, например, величина активности условно ферментативно неактивной эндорибонуклеазы составляет по меньшей мере приблизительно 50%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95% или более чем 95% от величины активности, направленной на расщепление нуклеиновой кислоты, стандартной условно ферментативно неактивной эндорибонуклеазы (например, Csy4 из Р. aeruginosa, содержащей мутацию Н29А).
[0280] Условно ферментативно неактивная эндорибонуклеаза может быть по меньшей мере на 20% идентична аминокислотной последовательности Csy4 из Р. aeruginosa, содержащей мутацию гистидина 29, при этом указанная мутация приводит по меньшей мере к 50% уменьшению нуклеазной активности эндорибонуклеазы, и по меньшей мере 50% потерянной нуклеазной активности может быть восстановлено путем инкубации эндорибонуклеазы в присутствии по меньшей мере 100 мМ имидазола.
[0281] Оптимизация кодонов
[0282] Полинуклеотид, кодирующий сайт-направленный полипептид и/или эндорибонуклеазу, может быть подвергнут оптимизации кодонов. Этот тип оптимизации может повлечь за собой мутацию ДНК чужеродного происхождения (например, рекомбинантной), чтобы имитировать кодоны, которые являются предпочтительными у предполагаемого организма-хозяина или клетки-хозяина при кодировании аналогичного белка. Следовательно, кодоны могут быть изменены, но кодируемый белок остается неизменным. Например, если предполагаемая клетка-мишень представляла собой клетку человека, то для получения подходящего сайт-направленного полипептида мог быть использован полинуклеотид Cas9 человека, подвергнутый оптимизации кодонов. В соответствии с другим неограничивающим примером, если предполагаемая клетка-хозяин представляла собой клетку мыши, то кодирующий Cas9 полинуклеотид мыши, подвергнутый оптимизации кодонов, мог представлять собой подходящий сайт-направленный полипептид. Полинуклеотид, кодирующий сайт-направленный полипептид, может быть подвергнут оптимизации кодонов для многих клеток-хозяев, представляющих интерес. Клетка-хозяин может представлять собой клетку из любого организма (например, бактериальную клетку, клетку архей, клетку одноклеточного эукариотического организма, растительную клетку, клетку водорослей, например, Botryococcus braunii, Chlamydomonas reinhardtii, Nannochloropsis gaditana, Chlorella pyrenoidosa, Sargassum patens C. agardh и т.п., грибковую клетку (например, клетку дрожжей), клетку животного, клетку беспозвоночного животного (например, плодовой мухи, гидроидного, иглокожего, нематоды и т.д.), клетку позвоночного животного (например, рыбы, амфибии, рептилии, птицы, млекопитающего), клетку млекопитающего (например, свиньи, коровы, козы, овцы, грызуна, крысы, мыши, примата, не относящегося к человеку, человека и т.д.), и т.д. Оптимизация кодонов может не требоваться. В некоторых случаях оптимизация кодонов может быть предпочтительной.
[0283] Нуклеиновая кислота, направленная против нуклеиновой кислоты
[0284] В настоящем изобретении предложена нуклеиновая кислота, направленная против нуклеиновой кислоты, которая может направлять активность ассоциированного полипептида (например, сайт-направленного полипептида) на специфичную последовательность-мишень в нуклеиновой кислоте-мишени. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать нуклеотиды. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может представлять собой РНК. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать одиночную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты. Типичная одиночная направляющая нуклеиновая кислота показана на Фиг. 1А. Удлиненная последовательность спейсера 105 и удлиненная последовательность tracrPHK 135 могут содержать элементы, придающие дополнительную функциональность (например, стабильность) нуклеиновой кислоте, направленной против нуклеиновой кислоты. В некоторых вариантах удлиненная последовательность спейсера 105 и удлиненная последовательность tracrPHK 135 являются необязательными. Последовательность спейсера 110 может содержать последовательность, которая способна гибридизоваться с последовательностью нуклеиновой кислоты-мишени. Последовательность спейсера 110 может представлять собой вариабельную часть нуклеиновой кислоты, направленной против нуклеиновой кислоты. Последовательность спейсера 110 может быть сконструирована для гибридизации с последовательностью нуклеиновой кислоты-мишени. Повтор CRISPR 115 (называемый в этом примерном варианте реализации минимальным повтором CRISPR) может содержать нуклеотиды, которые способны гибридизоваться с последовательностью tracrPHK 125 (называемой в этом примерном варианте реализации минимальной последовательностью tracrPHK). Минимальный повтор CRISPR 115 и минимальная последовательность tracrPHK 125 могут взаимодействовать, взаимодействующие молекулы содержат комплементарно спаренную, двухцепочечную структуру. Вместе минимальный повтор CRISPR 115 и минимальная последовательность tracrPHK 125 могут облегчить связывание с сайт-направленным полипептидом. Минимальный повтор CRISPR 115 и минимальная последовательность tracrPHK 125 могут быть соединены посредством одноцепочечного направляющего линкера 120 с образованием структуры шпильки. 3'-Концевая последовательность tracrPHK 130 может содержать последовательность распознавания мотива, прилегающего к протоспейсеру. 3'-Концевая последовательность tracrPHK 130 может быть идентична или гомологична части последовательности tracrPHK. Согласно некоторым вариантам реализации настоящего изобретения 3'-концевая последовательность tracrPHK 130 может содержать одну или более шпилек.
[0285] Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать одиночную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, как показано на Фиг. 1В. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать последовательность спейсера 140. Последовательность спейсера 140 может содержать последовательность, которая способна гибридизоваться с последовательностью нуклеиновой кислоты-мишени. Последовательность спейсера 140 может представлять собой вариабельную часть нуклеиновой кислоты, направленной против нуклеиновой кислоты. Последовательность спейсера 140 может представлять собой 5'-конец первого дуплекса 145. Первый дуплекс 145 содержит область гибридизации между минимальным повтором CRISPR 146 и минимальной последовательностью tracrPHK 147. Первый дуплекс 145 может быть прерван выпячиванием 150. Выпячивание 150 может содержать неспаренные нуклеотиды. Выпячивание 150 может способствовать привлечению сайт-направленного полипептида к нуклеиновой кислоте, направленной против нуклеиновой кислоты. После выпячивания 150 может быть расположен первый стебель 155. Первый стебель 155 содержит линкерную последовательность, связывающую минимальный повтор CRISPR 146 и минимальную последовательность tracrPHK 147. Последний спаренный нуклеотид на 3'-конце первого дуплекса 145 может быть соединен со второй линкерной последовательностью 160. Второй линкер 160 может содержать Р-домен. Второй линкер 160 может соединять первый дуплекс 145 с mid-tracrPHK 165. Mid-tracrPHK 165 может, согласно некоторым вариантам реализации настоящего изобретения, содержать одну или более шпилек. Например, mid-tracrPHK 165 может содержать второй стебель 170 и третий стебель 175.
[0286] Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать двойную направляющую нуклеиновую кислоту. На Фиг. 2 показана типичная структура двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты. Аналогично структуре одиночной направляющей нуклеиновой кислоты, показанной на Фиг. 1, структура двойной направляющей нуклеиновой кислоты может содержать удлиненную последовательность спейсера 205, спейсер 210, минимальный повтор CRISPR 215, минимальную последовательность tracrPHK 230, 3'-концевую последовательность tracrPHK 235 и удлиненную последовательность tracrPHK 240. Однако двойная направляющая нуклеиновая кислота, направленная против нуклеиновой кислоты, может не содержать одиночного направляющего линкера 120. Вместо этого минимальная последовательность повтора CRISPR 215 может содержать 3'-концевую последовательность повтора CRISPR 220, которая может быть идентична или гомологична части повтора CRISPR. Аналогичным образом, минимальная последовательность tracrPHK 230 может содержать 5'-концевую последовательность tracrPHK 225, которая может быть идентична или гомологична части tracrPHK. Двойные направляющие РНК могут гибридизоваться друг с другом посредством минимального повтора CRISPR 215 и минимальной последовательности tracrPHK 230.
[0287] Согласно некоторым вариантам реализации настоящего изобретения первый сегмент (т.е. сегмент, направляющий на нуклеиновую кислоту) может содержать удлиненную последовательность спейсера (например, 105/205) и спейсер (например, 110/210). Нуклеиновая кислота, направленная против нуклеиновой кислоты, может направлять связанный полипептид к специфичной нуклеотидной последовательности в пределах нуклеиновой кислоты-мишени с помощью вышеуказанного сегмента, направляющего на нуклеиновую кислоту.
[0288] Согласно некоторым вариантам реализации настоящего изобретения второй сегмент (т.е. белоксвязывающий сегмент) может содержать минимальный повтор CRISPR (например, 115/215), минимальную последовательность tracrPHK (например, 125/230), 3'-концевую последовательность tracrPHK (например, 130/235), и/или удлиненную последовательность tracrPHK (например, 135/240). Белоксвязывающий сегмент нуклеиновой кислоты, направленной против нуклеиновой кислоты, может взаимодействовать с сайт-направленным полипептидом. Белоксвязывающий сегмент нуклеиновой кислоты, направленной против нуклеиновой кислоты, может содержать два участка нуклеотидов, которые могут гибридизоваться друг с другом. Нуклеотиды в белоксвязывающем сегменте могут гибридизоваться с образованием двухцепочечного дуплекса нуклеиновой кислоты. Двухцепочечный дуплекс нуклеиновой кислоты может представлять собой РНК. Двухцепочечный дуплекс нуклеиновой кислоты может представлять собой ДНК.
[0289] В некоторых случаях нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать, в направлении от 5'-конца к 3'-концу, удлиненную последовательность спейсера, спейсер, минимальный повтор CRISPR, одиночный направляющий линкер, минимальную последовательность tracrPHK, 3'-концевую последовательность tracrPHK и удлиненную последовательность tracrPHK. В некоторых случаях нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать удлиненную последовательность tracrPHK, 3'-концевую последовательность tracrPHK, минимальную последовательность tracrPHK, одиночный направляющий линкер, минимальный повтор CRISPR, спейсер и удлиненную последовательность спейсера, расположенные в любом порядке.
[0290] Нуклеиновая кислота, направленная против нуклеиновой кислоты, и сайт-направленный полипептид могут образовать комплекс. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может обеспечить комплексу специфичность в отношении мишени за счет содержания нуклеотидной последовательности, которая может гибридизоваться с последовательностью нуклеиновой кислоты-мишени. Другими словами, сайт-направленный полипептид может быть направлен к последовательности нуклеиновой кислоты благодаря его ассоциации по меньшей мере с белоксвязывающим сегментом нуклеиновой кислоты, направленной против нуклеиновой кислоты. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может направлять активность белка Cas9. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может направлять активность ферментативно неактивного белка Cas9.
[0291] Способы в соответствии с настоящим изобретением могут обеспечить генетически модифицированную клетку. Генетически модифицированная клетка может содержать экзогенную нуклеиновую кислоту, направленную против нуклеиновой кислоты, и/или экзогенную нуклеиновую кислоту, содержащую нуклеотидную последовательность, кодирующую нуклеиновую кислоту, направленную против нуклеиновой кислоты.
[0292] Удлиненная последовательность спейсера
[0293] Удлиненная последовательность спейсера может обеспечить стабильность и/или обеспечить место для модификаций нуклеиновой кислоты, направленной против нуклеиновой кислоты. Удлиненная последовательность спейсера может содержать от приблизительно 1 нуклеотида до приблизительно 400 нуклеотидов в длину. Удлиненная последовательность спейсера может содержать более 1, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320, 340, 360, 380, 400, 1000, 2000, 3000, 4000, 5000, 6000 или 7000, или более нуклеотидов в длину. Удлиненная последовательность спейсера может содержать менее 1, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320, 340, 360, 380, 400, 1000, 2000, 3000, 4000, 5000, 6000, 7000 или более нуклеотидов в длину. Удлиненная последовательность спейсера может содержать менее 10 нуклеотидов в длину. Удлиненная последовательность спейсера может содержать от 10 до 30 нуклеотидов в длину. Удлиненная последовательность спейсера может содержать от 30 до 70 нуклеотидов в длину.
[0294] Удлиненная последовательность спейсера может содержать фрагмент (например, последовательность для контроля стабильности, последовательность связывания эндорибонуклеазы, рибозим). Фрагмент может влиять на стабильность РНК, направленной против нуклеиновой кислоты. Фрагмент, может представлять собой сегмент терминатора транскрипции (т.е. последовательность терминации транскрипции). Фрагмент нуклеиновой кислоты, направленной против нуклеиновой кислоты, может иметь общую длину от приблизительно 10 нуклеотидов до приблизительно 100 нуклеотидов, от приблизительно 10 нуклеотидов (нт.) до приблизительно 20 нт., от приблизительно 20 нт. до приблизительно 30 нт., от приблизительно 30 нт. до приблизительно 40 нт., от приблизительно 40 нт. до приблизительно 50 нт., от приблизительно 50 нт. до приблизительно 60 нт., от приблизительно 60 нт. до приблизительно 70 нт., от приблизительно 70 нт. до приблизительно 80 нт., от приблизительно 80 нт. до приблизительно 90 нт., или от приблизительно 90 нт. до приблизительно 100 нт., от приблизительно 15 нуклеотидов (нт.) до приблизительно 80 нт., от приблизительно 15 нт. до приблизительно 50 нт., от приблизительно 15 нт. до приблизительно 40 нт., от приблизительно 15 нт. до приблизительно 30 нт., или от приблизительно 15 нт. до приблизительно 25 нт. Фрагмент может представлять собой фрагмент, который может функционировать в эукариотической клетке. В некоторых случаях фрагмент может представлять собой фрагмент, который может функционировать в прокариотической клетке. Фрагмент может представлять собой фрагмент, который может функционировать как в эукариотической клетке, так и прокариотической клетке.
[0295] Неограничивающие примеры подходящих фрагментов могут включать: 5'-кэп (например, 7-метилгуанилатный кэп (m7 G)), последовательность рибопереключателя (например, чтобы обеспечить регулируемую стабильность и/или регулируемую доступность для белков и белковых комплексов), последовательность, которая образует дуплекс дцРНК (т.е. шпильку), последовательность, которая направляет РНК к месту внутриклеточной локализации (например, в ядро, митохондрии, хлоропласты и т.п.), модификация или последовательность, которая обеспечивает отслеживание (например, непосредственная конъюгация с флуоресцентной молекулой, конъюгация с фрагментом, который облегчает флуоресцентное детектирование, последовательность, которая обеспечивает флуоресцентное детектирование и т.д.), модификация или последовательность, которая обеспечивает сайт связывания для белков (например, белков, которые действуют на ДНК, включая активаторы транскрипции, репрессоры транскрипции, ДНК-метилтрансферазы, ДНК-деметилазы, гистонацетилтрансферазы, гистондеацетилазы и т.п.), модификация или последовательность, которая обеспечивает повышенную, пониженную и/или контролируемую стабильность, или любую их комбинацию. Удлиненная последовательность спейсера может содержать сайт связывания праймера, молекулярный индекс (например, последовательность штрихкода). Удлиненная последовательность спейсера может содержать нуклеиновую аффинную метку.
[0296] Спейсер
[0297] Сегмент, направленный против нуклеиновой кислоты, в нуклеиновой кислоте, направленной против нуклеиновой кислоты, может содержать нуклеотидную последовательность (например, спейсер), которая способна гибридизоваться с последовательностью в нуклеиновой кислоте-мишени. Спейсер нуклеиновой кислоты, направленной против нуклеиновой кислоты, может специфично взаимодействовать с последовательностью нуклеиновой кислоты-мишени посредством гибридизации (т.е. спаривания оснований). Таким образом, нуклеотидная последовательность спейсера может изменяться и может определять местоположение в нуклеиновой кислоте-мишени, в котором может взаимодействовать нуклеиновая кислота, направленная против нуклеиновой кислоты, и нуклеиновая кислота-мишень.
[0298] Последовательность спейсера может гибридизоваться с нуклеиновой кислотой-мишенью, которая расположена в направлении 5'-конца относительно мотива, прилегающего к протоспейсеру (РАМ). Различные организмы могут содержать различные последовательности РАМ. Например, в S. pyogenes РАМ может представлять собой последовательность в нуклеиновой кислоте-мишени, которая содержит последовательность 5'-XRR-3', где R может представлять собой А или G, где Х обозначает любой нуклеотид и Х расположен в направлении 3'-конца непосредственно за последовательностью нуклеиновой кислоты-мишени, которая служит мишенью для последовательности спейсера.
[0299] Последовательность нуклеиновой кислоты-мишени может содержать 20 нуклеотидов. Последовательность нуклеиновой кислоты-мишени может содержать менее 20 нуклеотидов. Последовательность нуклеиновой кислоты-мишени может содержать по меньшей мере 5, 10, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30 или более нуклеотидов. Последовательность нуклеиновой кислоты-мишени может содержать не более чем 5, 10, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30 или более нуклеотидов. Последовательность нуклеиновой кислоты-мишени может содержать 20 оснований, расположенных в направлении 5'-конца поблизости от первого нуклеотида РАМ. Например, в последовательности, содержащей
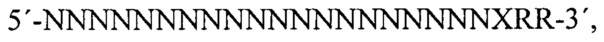
[0300] Последовательность спейсера, направленная против нуклеиновой кислоты, которая может гибридизоваться с нуклеиновой кислотой-мишенью, может содержать в длину по меньшей мере приблизительно 6 нт. Например, последовательность спейсера, которая может гибридизоваться с нуклеиновой кислотой-мишенью, может содержать в длину по меньшей мере приблизительно 6 нт., по меньшей мере приблизительно 10 нт., по меньшей мере приблизительно 15 нт., по меньшей мере приблизительно 18 нт., по меньшей мере приблизительно 19 нт., по меньшей мере приблизительно 20 нт., по меньшей мере приблизительно 25 нт., по меньшей мере приблизительно 30 нт., по меньшей мере приблизительно 35 нт. или по меньшей мере приблизительно 40 нт., от приблизительно 6 нт. до приблизительно 80 нт., от приблизительно 6 нт. до приблизительно 50 нт., от приблизительно 6 нт. до приблизительно 45 нт., от приблизительно 6 нт. до приблизительно 40 нт., от приблизительно 6 нт. до приблизительно 35 нт., от приблизительно 6 нт. до приблизительно 30 нт., от приблизительно 6 нт. до приблизительно 25 нт., от приблизительно 6 нт. до приблизительно 20 нт., от приблизительно 6 нт. до приблизительно 19 нт., от приблизительно 10 нт. до приблизительно 50 нт., от приблизительно 10 нт. до приблизительно 45 нт., от приблизительно 10 нт. до приблизительно 40 нт., от приблизительно 10 нт. до приблизительно 35 нт., от приблизительно 10 нт. до приблизительно 30 нт., от приблизительно 10 нт. до приблизительно 25 нт., от приблизительно 10 нт. до приблизительно 20 нт., от приблизительно 10 нт. до приблизительно 19 нт., от приблизительно 19 нт. до приблизительно 25 нт., от приблизительно 19 нт. до приблизительно 30 нт., от приблизительно 19 нт. до приблизительно 35 нт., от приблизительно 19 нт. до приблизительно 40 нт., от приблизительно 19 нт. до приблизительно 45 нт., от приблизительно 19 нт. до приблизительно 50 нт., от приблизительно 19 нт. до приблизительно 60 нт., от приблизительно 20 нт. до приблизительно 25 нт., от приблизительно 20 нт. до приблизительно 30 нт., от приблизительно 20 нт. до приблизительно 35 нт., от приблизительно 20 нт. до приблизительно 40 нт., от приблизительно 20 нт. до приблизительно 45 нт., от приблизительно 20 нт. до приблизительно 50 нт., или от приблизительно 20 нт. до приблизительно 60 нт. В некоторых случаях последовательность спейсера, которая может гибридизоваться с нуклеиновой кислотой-мишенью, может содержать 20 нуклеотидов в длину. Спейсер, который может гибридизоваться с нуклеиновой кислотой-мишенью, может содержать 19 нуклеотидов в длину.
[0301] Процент комплементарности между последовательностью спейсера и последовательностью нуклеиновой кислоты-мишени может составлять по меньшей мере приблизительно 30%, по меньшей мере приблизительно 40%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или 100%. Процент комплементарности между последовательностью спейсера и последовательностью нуклеиновой кислоты-мишени может составлять не более чем приблизительно 30%, не более чем приблизительно 40%, не более чем приблизительно 50%, не более чем приблизительно 60%, не более чем приблизительно 65%, не более чем приблизительно 70%, не более чем приблизительно 75%, не более чем приблизительно 80%, не более чем приблизительно 85%, не более чем приблизительно 90%, не более чем приблизительно 95%, не более чем приблизительно 97%, не более чем приблизительно 98%, не более чем приблизительно 99% или 100%. В некоторых случаях процент комплементарности между последовательностью спейсера и последовательностью нуклеиновой кислоты-мишени может составлять 100% в участке, содержащем шесть последовательных 5'-концевых нуклеотидов последовательности-мишени комплементарной цепи нуклеиновой кислоты-мишени. В некоторых случаях процент комплементарности между последовательностью спейсера и последовательностью нуклеиновой кислоты-мишени может составлять по меньшей мере 60% в участке, содержащем приблизительно 20 последовательных нуклеотидов. В некоторых случаях процент комплементарности между последовательностью спейсера и последовательностью нуклеиновой кислоты-мишени может составлять 100% в участке, содержащем четырнадцать последовательных 5'-концевых нуклеотидов последовательности-мишени комплементарной цепи нуклеиновой кислоты-мишени, и менее 0% в остальной части. В этом случае полагают, что последовательность спейсера может содержать 14 нуклеотидов в длину. В некоторых случаях процент комплементарности между последовательностью спейсера и последовательностью нуклеиновой кислоты-мишени может составлять 100% в участке, содержащем шесть последовательных 5'-концевых нуклеотидов последовательности-мишени комплементарной цепи нуклеиновой кислоты-мишени, и менее 0% в остальной части. В этом случае полагают, что последовательность спейсера содержит 6 нуклеотидов в длину. Нуклеиновая кислота-мишень может быть более чем приблизительно на 50%, 60%, 70%, 80%, 90% или 100% комплементарна затравочной области crPHK. Нуклеиновая кислота-мишень может быть менее чем приблизительно на 50%, 60%, 70%, 80%, 90% или 100% комплементарна затравочной области crPHK.
[0302] Спейсерный сегмент нуклеиновой кислоты, направленной против нуклеиновой кислоты, может быть модифицирован (например, с помощью модификации генома) для гибридизации с любой желаемой последовательностью в нуклеиновой кислоте-мишени. Например, спейсер может быть сконструирован (например, модифицирован, запрограммирован) для гибридизации с последовательностью в нуклеиновой кислоте-мишени, которая вовлечена в патофизиологию рака, размножение клеток, репликацию ДНК, репарацию ДНК, гены HLA, белки клеточной поверхности, Т-клеточные рецепторы, надсемейство генов иммуноглобулинов, гены-супрессоры опухолей, гены микроРНК, гены длинных некодирующих РНК, факторы транскрипции, глобины, вирусные белки, митохондриальные гены и тому подобное.
[0303] Последовательность спейсера может быть идентифицирована с помощью компьютерной программы (например, машиночитаемый код). Компьютерная программа может использовать переменные, такие как предсказанная температура плавления, образование вторичной структуры, предсказанная температура отжига, идентичность последовательности, положение в геноме, доступность хроматина,% пар GC, частота возникновения в геноме, статус метилирования, наличие полиморфизмов и тому подобное.
[0304] Минимальная последовательность повтора CRISPR
[0305] Минимальная последовательность повтора CRISPR может представлять собой последовательность, которая по меньшей мере приблизительно на 30%, 40%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% идентична и/или гомологична стандартной последовательности повтора CRISPR (например, crPHK из S. pyogenes). Минимальная последовательность повтора CRISPR может представлять собой последовательность, которая не более чем приблизительно на 30%, 40%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% идентична и/или гомологична стандартной последовательности повтора CRISPR (например, crPHK из S. pyogenes). Минимальный повтор CRISPR может содержать нуклеотиды, которые могут гибридизоваться с минимальной последовательностью tracrPHK. Минимальный повтор CRISPR и минимальная последовательность tracrPHK могут образовать комплементарно спаренную, двухцепочечную структуру. Вместе минимальный повтор CRISPR и минимальная последовательность tracrPHK могут облегчить связывание с сайт-направленным полипептидом. Часть минимальной последовательности повтора CRISPR может гибридизоваться с минимальной последовательностью tracrPHK. Часть минимальной последовательности повтора CRISPR может быть по меньшей мере приблизительно на 30%, 40%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% комплементарна минимальной последовательности tracrPHK. Часть минимальной последовательности повтора CRISPR может быть не более чем приблизительно на 30%, 40%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% комплементарна минимальной последовательности tracrPHK.
[0306] Минимальная последовательность повтора CRISPR может содержать от приблизительно 6 нуклеотидов до приблизительно 100 нуклеотидов в длину. Например, минимальная последовательность повтора CRISPR может содержать в длину от приблизительно 6 нуклеотидов (нт.) до приблизительно 50 нт., от приблизительно 6 нт. до приблизительно 40 нт., от приблизительно 6 нт. до приблизительно 30 нт., от приблизительно 6 нт. до приблизительно 25 нт., от приблизительно 6 нт. до приблизительно 20 нт., от приблизительно 6 нт. до приблизительно 15 нт., от приблизительно 8 нт. до приблизительно 40 нт., от приблизительно 8 нт. до приблизительно 30 нт., от приблизительно 8 нт. до приблизительно 25 нт., от приблизительно 8 нт. до приблизительно 20 нт. или от приблизительно 8 нт. до приблизительно 15 нт., от приблизительно 15 нт. до приблизительно 100 нт., от приблизительно 15 нт. до приблизительно 80 нт., от приблизительно 15 нт. до приблизительно 50 нт., от приблизительно 15 нт. до приблизительно 40 нт., от приблизительно 15 нт. до приблизительно 30 нт., или от приблизительно 15 нт. до приблизительно 25 нт. Согласно некоторым вариантам реализации настоящего изобретения минимальная последовательность повтора CRISPR содержит приблизительно 12 нуклеотидов в длину.
[0307] Минимальная последовательность повтора CRISPR может быть по меньшей мере приблизительно на 60% идентична стандартной минимальной последовательности повтора CRISPR (например, crPHK дикого типа из S. pyogenes) в участке, содержащем по меньшей мере 6, 7 или 8 последовательных нуклеотидов. Минимальная последовательность повтора CRISPR может быть по меньшей мере приблизительно на 60% идентична стандартной минимальной последовательности повтора CRISPR (например, crPHK дикого типа из S. pyogenes) в участке, содержащем по меньшей мере 6, 7 или 8 последовательных нуклеотидов. Например, минимальная последовательность повтора CRISPR может быть по меньшей мере приблизительно на 65% идентична, по меньшей мере приблизительно на 70% идентична, по меньшей мере приблизительно на 75% идентична, по меньшей мере приблизительно на 80% идентична, по меньшей мере приблизительно на 85% идентична, по меньшей мере приблизительно на 90% идентична, по меньшей мере приблизительно на 95% идентична, по меньшей мере приблизительно на 98% идентична, по меньшей мере приблизительно на 99% идентична или на 100% идентична стандартной минимальной последовательности повтора CRISPR в участке, содержащем по меньшей мере 6, 7 или 8 последовательных нуклеотидов.
[0308] Минимальная последовательность tracrPHK
[0309] Минимальная последовательность tracrPHK может представлять собой последовательность, которая по меньшей мере приблизительно на 30%, 40%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, или 100% идентична и/или гомологична стандартной последовательности tracrPHK (например, tracrPHK дикого типа из S. pyogenes). Минимальная последовательность tracrPHK может представлять собой последовательность, которая не более чем приблизительно на 30%, 40%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% идентична и/или гомологична стандартной последовательности tracrPHK (например, tracrPHK дикого типа из S. pyogenes). Минимальная последовательность tracrPHK может содержать нуклеотиды, которые могут гибридизоваться с минимальной последовательностью повтора CRISPR. Минимальная последовательность tracrPHK и минимальная последовательность повтора CRISPR могут образовать комплементарно спаренную, двухцепочечную структуру. Вместе минимальная последовательность tracrPHK и минимальная последовательность повтора CRISPR могут облегчить связывание с сайт-направленным полипептидом. Часть минимальной последовательности tracrPHK может гибридизоваться с минимальной последовательностью повтора CRISPR. Часть минимальной последовательности tracrPHK может быть на 30%, 40%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100%, комплементарна минимальной последовательности повтора CRISPR.
[0310] Минимальная последовательность tracrPHK может содержать от приблизительно 6 нуклеотидов до приблизительно 100 нуклеотидов в длину. Например, минимальная последовательность tracrPHK может содержать в длину от приблизительно 6 нуклеотидов (нт.) до приблизительно 50 нт., от приблизительно 6 нт. до приблизительно 40 нт., от приблизительно 6 нт. до приблизительно 30 нт., от приблизительно 6 нт. до приблизительно 25 нт., от приблизительно 6 нт. до приблизительно 20 нт., от приблизительно 6 нт. до приблизительно 15 нт., от приблизительно 8 нт. до приблизительно 40 нт., от приблизительно 8 нт. до приблизительно 30 нт., от приблизительно 8 нт. до приблизительно 25 нт., от приблизительно 8 нт. до приблизительно 20 нт. или от приблизительно 8 нт. до приблизительно 15 нт., от приблизительно 15 нт. до приблизительно 100 нт., от приблизительно 15 нт. до приблизительно 80 нт., от приблизительно 15 нт. до приблизительно 50 нт., от приблизительно 15 нт. до приблизительно 40 нт., от приблизительно 15 нт. до приблизительно 30 нт., или от приблизительно 15 нт. до приблизительно 25 нт. Согласно некоторым вариантам реализации настоящего изобретения минимальная последовательность tracrPHK содержит приблизительно 14 нуклеотидов в длину.
[0311] Минимальная последовательность tracrPHK может быть по меньшей мере приблизительно на 60% идентична стандартной минимальной последовательности tracrPHK (например, tracrPHK дикого типа из S. pyogenes) в участке, содержащем по меньшей мере 6, 7 или 8 последовательных нуклеотидов. Минимальная последовательность tracrPHK может быть по меньшей мере приблизительно на 60% идентична стандартной минимальной последовательности tracrPHK (например, tracrPHK дикого типа из S. pyogenes) в участке, содержащем по меньшей мере 6, 7 или 8 последовательных нуклеотидов. Например, минимальная последовательность tracrPHK может быть по меньшей мере приблизительно на 65% идентична, по меньшей мере приблизительно на 70% идентична, по меньшей мере приблизительно на 75% идентична, по меньшей мере приблизительно на 80% идентична, по меньшей мере приблизительно на 85% идентична, по меньшей мере приблизительно на 90% идентична, по меньшей мере приблизительно на 95% идентична, по меньшей мере приблизительно на 98% идентична, по меньшей мере приблизительно на 99% идентична или на 100% идентична стандартной минимальной последовательности tracrPHK в участке, содержащем по меньшей мере 6, 7 или 8 последовательных нуклеотидов.
[0312] Дуплекс (т.е. первый дуплекс на Фиг. 1В) между минимальной РНК CRISPR и минимальной tracrPHK может содержать двойную спираль. Первое основание первой цепи дуплекса (например, минимальной последовательности повтора CRISPR на Фиг. 1В) может представлять собой гуанин. Первое основание первой цепи дуплекса (например, минимальной последовательности повтора CRISPR на Фиг. 1В) может представлять собой аденин. Дуплекс (т.е. первый дуплекс на Фиг. 1В) между минимальной РНК CRISPR и минимальной tracrPHK может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов. Дуплекс (т.е. первый дуплекс на Фиг. 1В) между минимальной РНК CRISPR и минимальной tracrPHK может содержать не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов.
[0313] Дуплекс может содержать несоответствия. Дуплекс может содержать по меньшей мере приблизительно 1, 2, 3, 4 или 5 или более несоответствий. Дуплекс может содержать не более чем приблизительно 1, 2, 3, 4 или 5 или более несоответствий. В некоторых случаях дуплекс содержит не более 2 несоответствий.
[0314] Выпячивание
[0315] Выпячивание может относиться к неспаренной области нуклеотидов в дуплексе, состоящем из минимальной последовательности повтора CRISPR и минимальной последовательности tracrPHK. Выпячивание может играть важную роль в связывании с сайт-направленным полипептидом. Выпячивание может содержать, с одной стороны дуплекса, неспаренный участок 5'-XXXY-3', где Х обозначает любой пурин и Y может представлять собой нуклеотид, который может неканонически спариваться с нуклеотидом на противоположной цепи, и неспаренную нуклеотидную область на другой стороне дуплекса.
[0316] Например, выпячивание может содержать неспаренный пурин (например, аденин) на цепи минимальной последовательности повтора CRISPR указанного выпячивания. Согласно некоторым вариантам реализации настоящего изобретения выпячивание может содержать неспаренный участок 5'-AAGY-3' на цепи минимальной последовательности tracrPHK указанного выпячивания, где Y может представлять собой нуклеотид, который может неканонически спариваться с нуклеотидом на цепи минимального повтора CRISPR.
[0317] Выпячиванием на первой стороне дуплекса (например, на стороне минимального повтора CRISPR) может содержать по меньшей мере 1, 2, 3, 4 или 5, или более неспаренных нуклеотидов. Выпячивание на первой стороне дуплекса (например, на стороне минимального повтора CRISPR) может содержать не более чем 1, 2, 3, 4 или 5, или более неспаренных нуклеотидов. Выпячивание на первой стороне дуплекса (например, на стороне минимального повтора CRISPR) может содержать 1 неспаренный нуклеотид.
[0318] Выпячивание на второй стороне дуплекса (например, на стороне минимальной последовательности tracrPHK дуплекса) может содержать по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более неспаренных нуклеотидов. Выпячивание на второй стороне дуплекса (например, на стороне минимальной последовательности tracrPHK дуплекса) может содержать не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более неспаренных нуклеотидов. Выпячивание на второй стороне дуплекса (например, на стороне минимальной последовательности tracrPHK дуплекса) может содержать 4 неспаренных нуклеотида.
[0319] Области, содержащие различное число неспаренных нуклеотидов на каждой цепи дуплекса, могут быть спарены друг с другом. Например, выпячивание может содержать 5 неспаренных нуклеотидов из первой цепи и 1 неспаренный нуклеотид из второй цепи. Выпячивание может содержать 4 неспаренных нуклеотида из первой цепи и 1 неспаренный нуклеотид из второй цепи. Выпячивание может содержать 3 неспаренных нуклеотида из первой цепи и 1 неспаренный нуклеотид из второй цепи. Выпячивание может содержать 2 неспаренных нуклеотида из первой цепи и 1 неспаренный нуклеотид из второй цепи. Выпячивание может содержать 1 неспаренный нуклеотид из первой цепи и 1 неспаренный нуклеотид из второй цепи. Выпячивание может содержать I неспаренный нуклеотид из первой цепи и 2 неспаренных нуклеотида из второй цепи. Выпячивание может содержать 1 неспаренный нуклеотид из первой цепи и 3 неспаренных нуклеотида из второй цепи. Выпячивание может содержать 1 неспаренный нуклеотид из первой цепи и 4 неспаренных нуклеотида из второй цепи. Выпячивание может содержать 1 неспаренный нуклеотид из первой цепи и 5 неспаренных нуклеотидов из второй цепи.
[0320] В некоторых случаях выпячивание может содержать по меньшей мере одно неканоническое спаривание, В некоторых случаях выпячивание может содержать не более одного неканонического спаривания. Последовательность выпячивания может содержать по меньшей мере один пуриновый нуклеотид. Последовательность выпячивания может содержать по меньшей мере 3 пуриновых нуклеотида. Последовательность выпячивания может содержать по меньшей мере 5 пуриновых нуклеотидов. Последовательность выпячивания может содержать по меньшей мере один гуаниновый нуклеотид. Последовательность выпячивания может содержать по меньшей мере один адениновый нуклеотид.
[0321] Р-домен (Р-ДОМЕН)
[0322] Р-домен может относиться к области нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может распознавать мотив, прилегающий к протоспейсеру (РАМ), в нуклеиновой кислоте-мишени. Р-домен может гибридизоваться с РАМ в нуклеиновой кислоте-мишени. Таким образом, Р-домен может содержать последовательность, которая комплементарна РАМ. Р-домен может быть расположен в направлении 3'-конца относительно минимальной последовательности tracrPHK. Р-домен может быть расположен в пределах 3'-концевой последовательности tracrPHK (то есть, последовательности mid-tracrPHK).
[0323] Р-домен начинается на расстоянии по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15 или 20, или более нуклеотидов в направлении 3'-конца от последнего спаренного нуклеотида в минимальной последовательности повтора CRISPR и минимальной последовательности tracrPHK дуплекса. Р-домен может начинаться на расстоянии не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов в направлении 3'-конца от последнего спаренного нуклеотида в минимальной последовательности повтора CRISPR и минимальной последовательности tracrPHK дуплекса.
[0324] Р-домен может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15 или 20, или более последовательных нуклеотидов. Р-домен может содержать не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15 или 20, или более последовательных нуклеотидов.
[0325] В некоторых случаях Р-домен может содержать СС динуклеотид (например, два последовательных цитозиновых нуклеотида). СС динуклеотид может взаимодействовать с GG динуклеотидом РАМ, при этом РАМ содержит последовательность 5'-XGG-3'.
[0326] Р-домен может представлять собой нуклеотидную последовательность, расположенную в 3'-концевой последовательности tracrPHK (т.е. последовательности mid-tracrPHK). Р-домен может содержать дуплексные нуклеотиды (например, нуклеотиды в шпильке, гибридизованные друг с другом). Например, Р-домен может содержать СС динуклеотид, который гибридизуется с GG динуклеотидом в дуплексе шпильки 3'-концевой последовательности tracrPHK (т.е., последовательности mid-tracrPHK). Активность Р-домена (например, способность нуклеиновой кислоты, направленной против нуклеиновой кислоты, направлено действовать на нуклеиновую кислоту-мишень) может регулироваться состоянием гибридизации Р-домена. Например, если Р-домены гибридизованы, то нуклеиновая кислота, направленная против нуклеиновой кислоты, может не распознать свою мишень. Если Р-домены не гибридизованы, то нуклеиновая кислота, направленная против нуклеиновой кислоты, может распознать свою мишень.
[0327] Р-домен может взаимодействовать с областью, взаимодействующей с Р-доменом, в сайт-направленном полипептиде. Р-домен может взаимодействовать с основным участком, богатым остатками аргинина, в сайт-направленном полипептиде. Области, взаимодействующие с Р-доменом, могут взаимодействовать с последовательностью РАМ. Р-домен может содержать структуру «стебель-петля». Р-домен может содержать выпячивание.
[0328] 3'-Концевая последовательность tracrPHK
[0329] 3'-Концевая последовательность tracrPHK может представлять собой последовательность, которая по меньшей мере приблизительно на 30%, 40%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% идентична и/или гомологична стандартной последовательности tracrPHK (например, tracrPHK из S. pyogenes). 3'-концевая последовательность tracrPHK может представлять собой последовательность, которая не более чем приблизительно на 30%, 40%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% идентична и/или гомологична стандартной последовательности tracrPHK (например, tracrPHK из S. pyogenes).
[0330] 3'-Концевая последовательность tracrPHK может содержать от приблизительно 6 нуклеотидов до приблизительно 100 нуклеотидов в длину. Например, 3'-концевая последовательность tracrPHK может содержать в длину от приблизительно 6 нуклеотидов (нт.) до приблизительно 50 нт., от приблизительно 6 нт. до приблизительно 40 нт., от приблизительно 6 нт. до приблизительно 30 нт., от приблизительно 6 нт. до приблизительно 25 нт., от приблизительно 6 нт. до приблизительно 20 нт., от приблизительно 6 нт. до приблизительно 15 нт., от приблизительно 8 нт. до приблизительно 40 нт., от приблизительно 8 нт. до приблизительно 30 нт., от приблизительно 8 нт. до приблизительно 25 нт., от приблизительно 8 нт. до приблизительно 20 нт. или от приблизительно 8 нт. до приблизительно 15 нт., от приблизительно 15 нт. до приблизительно 100 нт., от приблизительно 15 нт. до приблизительно 80 нт., от приблизительно 15 нт. до приблизительно 50 нт., от приблизительно 15 нт. до приблизительно 40 нт., от приблизительно 15 нт. до приблизительно 30 нт., или от приблизительно 15 нт. до приблизительно 25 нт. Согласно некоторым вариантам реализации настоящего изобретения 3'-концевая последовательность tracrPHK содержит приблизительно 14 нуклеотидов в длину.
[0331] 3'-Концевая последовательность tracrPHK может быть по меньшей мере приблизительно на 60% идентична стандартной 3'-концевой последовательности tracrPHK (например, 3'-концевой последовательности tracrPHK дикого типа из S. pyogenes) в участке, содержащем по меньшей мере 6, 7 или 8 последовательных нуклеотидов. Например, 3'-концевая последовательность tracrPHK может быть по меньшей мере приблизительно на 60% идентична, по меньшей мере приблизительно на 65% идентична, по меньшей мере приблизительно на 70% идентична, по меньшей мере приблизительно на 75% идентична, по меньшей мере приблизительно на 80% идентична, по меньшей мере приблизительно на 85% идентична, по меньшей мере приблизительно на 90% идентична, по меньшей мере приблизительно на 95% идентична, по меньшей мере приблизительно на 98% идентична, по меньшей мере приблизительно на 99% идентична или на 100% идентична стандартной 3'-концевой последовательности tracrPHK (например, 3'-концевой последовательности tracrPHK дикого типа из S. pyogenes) в участке, содержащем по меньшей мере 6, 7 или 8 последовательных нуклеотидов.
[0332] 3'-Концевая последовательность tracrPHK может содержать более одной дуплексной области (например, шпильку, гибридизованную область). 3'-Концевая последовательность tracrPHK может содержать две дуплексные области.
[0333] 3'-Концевая последовательность tracrPHK также может называться mid-tracrPHK (см. Фигуру 1В). Последовательность mid-tracrPHK может содержать структуру стебель-петля. Другими словами, последовательность mid-tracrPHK может содержать шпильку, которая отличается от второго или третьего стеблей, как показано на Фиг. 1В. Структура стебель-петля в mid-tracrPHK (т.е. 3' tracrPHK) может содержать по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15 или 20, или более нуклеотидов. Структура стебель-петля в mid-tracrPHK (т.е. 3' tracrPHK) может содержать не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов. Структура стебель-петля может содержать функциональный фрагмент. Например, структура стебель-петля может содержать аптамер, рибозим, шпильку, взаимодействующую с белком, массив CRISPR, интрон и экзон. Структура стебель-петля может содержать по меньшей мере приблизительно 1, 2, 3, 4 или 5, или более функциональных фрагментов. Структура стебель-петля может содержать не более чем приблизительно 1, 2, 3, 4 или 5, или более функциональных фрагментов.
[0334] Шпилька в последовательности mid-tracrPHK может содержать Р-домен. Р-домен может содержать двухцепочечную область в шпильке.
[0335] Удлиненная последовательность tracrPHK
[0336] Удлиненная последовательность tracrPHK может обеспечить стабильность и/или положение для модификаций нуклеиновой кислоты, направленной против нуклеиновой кислоты. Удлиненная последовательность tracrPHK может содержать от приблизительно 1 нуклеотида до приблизительно 400 нуклеотидов в длину. Удлиненная последовательность tracrPHK может содержать в длину более 1, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320, 340, 360, 380, 400 или более нуклеотидов. Удлиненная последовательность tracrPHK может содержать в длину от приблизительно 20 до приблизительно 5000 или более нуклеотидов. Удлиненная последовательность tracrPHK может содержать в длину более 1000 нуклеотидов. Удлиненная последовательность tracrPHK может содержать в длину менее 1, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320, 340, 360, 380, 400 нуклеотидов. Удлиненная последовательность tracrPHK может содержать менее 1000 нуклеотидов в длину. Удлиненная последовательность tracrPHK может содержать менее 10 нуклеотидов в длину. Удлиненная последовательность tracrPHK может содержать от 10 до 30 нуклеотидов в длину. Удлиненная последовательность tracrPHK может содержать от 30 до 70 нуклеотидов в длину.
[0337] Удлиненная последовательность tracrPHK может содержать фрагмент (например, последовательность для контроля стабильности, рибозим, последовательность, связывающую эндорибонуклеазу). Фрагмент может влиять на стабильность РНК, направленной против нуклеиновой кислоты. Фрагмент может представлять собой сегмент терминатора транскрипции (т.е. последовательность терминации транскрипции). Фрагмент нуклеиновой кислоты, направленной против нуклеиновой кислоты, может иметь общую длину от приблизительно 10 нуклеотидов до приблизительно 100 нуклеотидов, от приблизительно 10 нуклеотидов (нт.) до приблизительно 20 нт., от приблизительно 20 нт. до приблизительно 30 нт., от приблизительно 30 нт. до приблизительно 40 нт., от приблизительно 40 нт. до приблизительно 50 нт., от приблизительно 50 нт. до приблизительно 60 нт., от приблизительно 60 нт. до приблизительно 70 нт., от приблизительно 70 нт. до приблизительно 80 нт., от приблизительно 80 нт. до приблизительно 90 нт., или от приблизительно 90 нт. до приблизительно 100 нт., от приблизительно 15 нуклеотидов (нт.) до приблизительно 80 нт., от приблизительно 15 нт. до приблизительно 50 нт., от приблизительно 15 нт. до приблизительно 40 нт., от приблизительно 15 нт. до приблизительно 30 нт., или от приблизительно 15 нт. до приблизительно 25 нт. Фрагмент может представлять собой тот, который может функционировать в эукариотической клетке. В некоторых случаях фрагмент может представлять собой тот, который может функционировать в прокариотической клетке. Фрагмент может представлять собой тот, который может функционировать как в эукариотической клетке, так и в прокариотической клетке.
[0338] Неограничивающие примеры подходящих фрагментов удлиненной последовательности tracrPHK включают: 3'полиаденилированный конец, последовательность рибопереключателя (например, для обеспечения регулируемой стабильности и/или регулируемой доступности для белков и белковых комплексов), последовательность, которая образует дуплекс дцРНК (т.е. шпильку), последовательность, которая направляет РНК в место внутриклеточной локализации (например, в ядро, митохондрии, хлоропласты и т.п.), модификация или последовательность, которая обеспечивает отслеживание (например, прямая конъюгация с флуоресцентной молекулой, конъюгация с фрагментом, который облегчает флуоресцентное детектирование, последовательность, которая обеспечивает флуоресцентное детектирование и т.д.), модификация или последовательность, которая обеспечивает сайт связывания белков (например, белки, которые действуют на ДНК, включая активаторы транскрипции, репрессоры транскрипции, метилтрансферазы ДНК, деметилазы ДНК, гистонацетилтрансферазы, гистондеацетилазы и т.п.), модификация или последовательность, которая обеспечивает повышенную, пониженную, и/или контролируемую стабильность, или любую их комбинацию. Удлиненная последовательность tracrPHK может содержать сайт связывания праймера, молекулярный индекс (например, последовательность штрихкода). Согласно некоторым вариантам реализации настоящего изобретения удлиненная последовательность tracrPHK может содержать одну или более аффинных меток.
[0339] Одиночная направляющая нуклеиновая кислота
[0340] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может представлять собой одиночную направляющую нуклеиновую кислоту. Одиночная направляющая нуклеиновая кислота может представлять собой РНК. Одиночная направляющая нуклеиновая кислота может содержать линкер (т.е. элемент 120 из Фигуры 1А) между минимальной последовательностью повтора CRISPR и минимальной последовательностью tracrPHK, который может быть назван одиночной направляющей линкерной последовательностью.
[0341] Одиночная направляющая линкерная последовательность из одиночной направляющей нуклеиновой кислоты может содержать от приблизительно 3 нуклеотидов до приблизительно 100 нуклеотидов в длину. Например, линкер может содержать в длину от приблизительно 3 нуклеотидов (нт.) до приблизительно 90 нт., от приблизительно 3 нт. до приблизительно 80 нт., от приблизительно 3 нт. до приблизительно 70 нт., от приблизительно 3 нт. до приблизительно 60 нт., от приблизительно 3 нт. до приблизительно 50 нт., от приблизительно 3 нт. до приблизительно 40 нт., от приблизительно 3 нт. до приблизительно 30 нт., от приблизительно 3 нт. до приблизительно 20 нт., или от приблизительно 3 нт. до приблизительно 10 нт. Например, линкер может содержать в длину от приблизительно 3 нт. до приблизительно 5 нт., от приблизительно 5 нт. до приблизительно 10 нт., от приблизительно 10 нт. до приблизительно 15 нт., от приблизительно 15 нт. до приблизительно 20 нт., от приблизительно 20 нт. до приблизительно 25 нт., от приблизительно 25 нт. до приблизительно 30 нт., от приблизительно 30 нт. до приблизительно 35 нт., от приблизительно 35 нт. до приблизительно 40 нт., от приблизительно 40 нт. до приблизительно 50 нт., от приблизительно 50 нт. до приблизительно 60 нт., от приблизительно 60 нт. до приблизительно 70 нт., от приблизительно 70 нт. до приблизительно 80 нт., от приблизительно 80 нт. до приблизительно 90 нт., или от приблизительно 90 нт. до приблизительно 100 нт. Согласно некоторым вариантам реализации настоящего изобретения линкер из одиночной направляющей нуклеиновой кислоты содержит от 4 до 40 нуклеотидов. Линкер может содержать по меньшей мере приблизительно 100, 500, 1000, 1500, 2000, 2500, 3000, 3500, 4000, 4500, 5000, 5500, 6000, 6500 или 7000, или более нуклеотидов в длину. Линкер может содержать не более чем приблизительно 100, 500, 1000, 1500, 2000, 2500, 3000, 3500, 4000, 4500, 5000, 5500, 6000, 6500 или 7000, или более нуклеотидов в длину.
[0342] Последовательность линкера может содержать функциональный фрагмент. Например, последовательность линкера может содержать аптамер, рибозим, шпильку, взаимодействующую с белком, массив CRISPR, интрон и экзон. Последовательность линкера может содержать по меньшей мере приблизительно 1, 2, 3, 4 или 5, или более функциональных фрагментов. Последовательность линкера может содержать не более чем приблизительно 1, 2, 3, 4 или 5, или более функциональных фрагментов.
[0343] Согласно некоторым вариантам реализации настоящего изобретения одиночный направляющий линкер может соединять 3'-конец минимального повтора CRISPR и 5'-конец минимальной последовательности tracrPHK. Согласно другому подходу, одиночный направляющий линкер может соединять 3'-конец последовательности tracrPHK и 5'-конец минимального повтора CRISPR. Иными словами, одиночная направляющая нуклеиновая кислота может содержать 5'-концевой ДНК-связывающий сегмент, соединенный с 3'-концевым белоксвязывающим сегментом. Одиночная направляющая нуклеиновая кислота может содержать 5'-концевой белоксвязывающий сегмент, соединенный с 5'-концевым ДНК-связывающим сегментом.
[0344] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать удлиненную последовательность спейсера, состоящую из 10-5000 нуклеотидов в длину; последовательность спейсера, состоящую из 12-30 нуклеотидов в длину, при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который связывает минимальный повтор CRISPR с минимальной последовательностью tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть названа одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0345] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, которая по меньшей мере на 50% комплементарна нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимальной последовательности повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который связывает минимальный повтор CRISPR и минимальную последовательность tracrPHK и имеет от 3 до 5000 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит от 1 до 10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0346] Двойная направляющая нуклеиновая кислота
[0347] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может представлять собой двойную направляющую нуклеиновую кислоту. Двойная направляющая нуклеиновая кислота может представлять собой РНК. Двойная направляющая нуклеиновая кислота может содержать две отдельные молекулы нуклеиновых кислот (т.е. полинуклеотидов). Каждая из двух молекул нуклеиновых кислот указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, может содержать участок нуклеотидов, которые могут гибридизоваться друг с другом так, что комплементарные нуклеотиды двух молекул нуклеиновых кислот гибридизуются с образованием двухцепочечного дуплекса белоксвязывающего сегмента. Если не указано иное, термин «нуклеиновая кислота, направленная против нуклеиновой кислоты» может быть всеобъемлющим и относиться к обоим типам: одиночной молекуле нуклеиновой кислоты, направленной против нуклеиновой кислоты, и двойной молекуле нуклеиновой кислоты, направленной против нуклеиновой кислоты.
[0348] Двойная направляющая нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, которая по меньшей мере на 50% комплементарна последовательности нуклеиновой кислоты-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, содержащую минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0349] В некоторых случаях двойная направляющая нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид выпячивания расположен в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-коцевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и расположен в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0350] Комплекс нуклеиновой кислоты, направленной против нуклеиновой кислоты, и сайт-направленного полипептида
[0351] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может взаимодействовать с сайт-направленным полипептидом (например, нуклеазы, направленные против нуклеиновой кислоты, Cas9) с образованием комплекса. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может направлять сайт-направленный полипептид к нуклеиновой кислоте-мишени.
[0352] Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть сконструирована так, что комплекс (например, содержащий сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты) может связываться за пределами сайта расщепления сайт-направленного полипептида. В этом случае нуклеиновая кислота-мишень может не взаимодействовать с комплексом, и нуклеиновая кислота-мишень может быть вырезана (например, высвобождена из комплекса).
[0353] Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть сконструирована так, что комплекс может связываться внутри сайта расщепления сайт-направленного полипептида. В этом случае нуклеиновая кислота-мишень может взаимодействовать с комплексом, и нуклеиновая кислота-мишень может быть связана (например, связана с комплексом).
[0354] В некоторых случаях комплекс может содержать сайт-направленный полипептид, содержащий аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту (т.е., домен HNH и домен RuvC); и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и содержит дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0355] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту (т.е., домен HNH и домен RuvC); и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, 5. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0356] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC); и нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0357] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту (т.е., домен HNH и домен RuvC); и нуклеиновую кислоту, направленную против нуклеиновой кислоты, которая может содержать удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и расположен в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и линкер, соединяющий сайт-направленный полипептид с ненативной последовательностью; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0358] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и линкер, соединяющий сайт-направленный полипептид с ненативной последовательностью; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0359] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и линкер, соединяющий сайт-направленный полипептид с ненативной последовательностью; и нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3' -концевая tracrPHK содержит от 10 до 20 нуклеотидов и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0360] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и линкер, соединяющий сайт-направленный полипептид с ненативной последовательностью; и нуклеиновую кислоту, направленную против нуклеиновой кислоты, которая может содержать удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0361] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), при этом сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0362] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1 -10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0363] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0364] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и нуклеиновую кислоту, направленную против нуклеиновой кислоты, которая может содержать удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0365] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину, и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0366] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину, и включает дуплексную область; Р-домен, который начинается на расстоянии 1 -5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0367] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов, и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0368] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и нуклеиновую кислоту, направленную против нуклеиновой кислоты, которая может содержать удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0369] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая уменьшает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0370] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту, при этом один или оба домена, расщепляющих нуклеиновую кислоту, по меньшей мере на 50% идентичны аминокислотной последовательности нуклеазного домена Cas9 из S. pyogenes; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишеии; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0371] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту, причем один или оба домена, расщепляющих нуклеиновую кислоту, по меньшей мере на 50% идентичны аминокислотной последовательности нуклеазного домена Cas9 из S. pyogenes; и нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в ' длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0372] В некоторых случаях комплекс может содержать сайт-направленный полипептид, аминокислотная последовательность которого по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту, причем один или оба домена, расщепляющих нуклеиновую кислоту, по меньшей мере на 50% идентичны аминокислотной последовательности нуклеазного домена Cas9 из S. pyogenes; и нуклеиновую кислоту, направленную против нуклеиновой кислоты, которая может содержать удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0373] Любая нуклеиновая кислота, направленная против нуклеиновой кислоты, согласно настоящему изобретению, сайт-направленный полипептид согласно настоящему изобретению, эффекторный белок, мультиплексный генетический нацеливающий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любая нуклеиновая кислота или белковая молекула, необходимая для осуществления способов согласно настоящему изобретению, могут быть рекомбинантными, очищенными и/или выделенными.
[0374] Нуклеиновые кислоты, кодирующие нуклеиновую кислоту, направленную против нуклеиновой кислоты, и/или сайт-направленный полипептид
[0375] В настоящем изобретении предложена нуклеиновая кислота, содержащая нуклеотидную последовательность, кодирующую нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению, сайт-направленный полипептид согласно настоящему изобретению, эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению. Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота, которая кодирует нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению, сайт-направленный полипептид согласно настоящему изобретению, эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению, может представлять собой вектор (например, рекомбинантный вектор экспрессии).
[0376] Согласно некоторым вариантам реализации настоящего изобретения рекомбинантный вектор экспрессии может представлять собой вирусную конструкцию (например, рекомбинантную конструкцию на основе аденоассоциированного вируса), рекомбинантную аденовирусную конструкцию, рекомбинантную лентивирусную конструкцию, рекомбинантную ретровирусную конструкцию и т.д.
[0377] Подходящие векторы экспрессии могут включать, но не ограничиваются ими, вирусные векторы (например, вирусные векторы на основе вируса коровьей оспы, вируса полиомиелита, аденовируса, аденоассоциированного вируса, вируса SV40, вируса простого герпеса, вируса иммунодефицита человека), ретровирусный вектор (например, вирус мышиного лейкоза, вирус некроза селезенки, и векторы, полученные из ретровирусов, таких как вирус саркомы Рауса, вирус саркомы Харви, вирус птичьего лейкоза, лентивирус, вирус иммунодефицита человека, вирус миелопролиферативной саркомы и вирус опухоли молочной железы), векторы растений (например, вектор на основе Т-ДНК) и т.п. Следующие векторы могут быть предусмотрены в качестве примера для эукариотических клеток-хозяев: pXT1, pSG5, pSVK3, pBPV, pMSG и pSVLSV40 (Pharmacia). Другие векторы могут быть использованы при условии, что они совместимы с клеткой-хозяином.
[0378] В некоторых случаях вектор может представлять собой линеаризованный вектор. Линеаризованный вектор может содержать сайт-направленный полипептид и/или нуклеиновую кислоту, направленную против нуклеиновой кислоты. Линеаризованный вектор не является кольцевой плазмидой. Линеаризованный вектор может содержать двухцепочечный разрыв. Линеаризованный вектор может содержать последовательность, кодирующую флуоресцентный белок (например, оранжевый флуоресцентный белок (OFP)). Линеаризованный вектор может содержать последовательность, кодирующую антиген (например, CD4). Линеаризованный вектор можно линеаризовать (например, разрезать) в области вектора, кодирующей части нуклеиновой кислоты, направленной против нуклеиновой кислоты. Например, линеаризованный вектор можно линеаризовать (например, разрезать) в области нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая расположена в направлении 5'-конца относительно части' crPHK нуклеиновой кислоты, направленной против нуклеиновой кислоты. Линеаризованный вектор можно линеаризовать (например, разрезать) в области нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая расположена в направлении 3'-конца относительно удлиненной последовательности спейсера нуклеиновой кислоты, направленной против нуклеиновой кислоты. Линеаризованный вектор можно линеаризовать (например, разрезать) в области нуклеиновой кислоты, направленной против нуклеиновой кислоты, кодирующей последовательность crPHK нуклеиновой кислоты, направленной против нуклеиновой кислоты. В некоторых случаях линеаризованный вектор или замкнутый сверхскрученный вектор содержит последовательность, кодирующую сайт-направленный полипептид (например, Cas9), промотор, инициирующий экспрессию последовательности, кодирующей сайт-направленный полипептид (например, промотор цитомегаловируса), последовательность, кодирующую линкер (например, 2А), последовательность, кодирующую маркер (например, CD4 или OFP), последовательность, кодирующую часть нуклеиновой кислоты, направленной против нуклеиновой кислоты, промотор, инициирующий экспрессию последовательности, кодирующей часть нуклеиновой кислоты, направленной против нуклеиновой кислоты, и последовательность, кодирующую селективный маркер (например, ампициллин), или любую их комбинацию.
[0379] Вектор может содержать элемент, регулирующий транскрипцию и/или трансляцию. В зависимости от типа используемой системы хозяин/вектор любой из ряда элементов, регулирующих транскрипцию и/или трансляцию, включая конститутивные и индуцируемые промоторы, энхансеры транскрипции, терминаторы транскрипции и т.д., может быть использован в составе вектора экспрессии.
[0380] Согласно некоторым вариантам реализации настоящего изобретения нуклеотидная последовательность, которая кодирует нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению, сайт-направленный полипептид согласно настоящему изобретению, эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению, может быть функционально связана с регуляторным элементом (например, элементом, регулирующим транскрипцию), таким как промотор. Элемент, регулирующий транскрипцию, может быть функциональным в эукариотической клетке (например, клетке млекопитающего), в прокариотической клетке (например, бактериальной клетке или клетке архей). Согласно некоторым вариантам реализации настоящего изобретения нуклеотидная последовательность, которая кодирует нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению, сайт-направленный полипептид согласно настоящему изобретению, эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению, может быть функционально связана с несколькими регуляторными элементами. Функциональная связь с несколькими регуляторными элементами может обеспечить экспрессию нуклеотидной последовательности, которая кодирует нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению, сайт-направленный полипептид согласно настоящему изобретению, эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению в прокариотических и эукариотических клетках.
[0381] Неограничивающие примеры подходящих эукариотических промоторов (т.е. промоторов, которые функциональны в эукариотических клетках) могут включать промоторы ранних и поздник генов цитомегаловируса (ЦМВ), промотор тимидинкиназы вируса простого герпеса (ВПГ), промоторы ранних и поздних генов SV40, промотор длинных концевых повторов (LTR) ретровируса, промотор фактора элонгации 1 человека (EF1), гибридную конструкцию, содержащую энхансер цитомегаловируса (ЦМВ), гибридизованный с куриным промотором бета-актина (CAG), промотор вируса стволовых клеток мыши (MSCV), промотор локуса фосфоглицераткиназы-1 (PGK.) и промотор металлотионеина-1 мыши. Промотор может представлять собой промотор грибка. Промотор может представлять собой промотор растений. Существует база данных промоторов растений (например, PlantProm). Вектор экспрессии также может содержать сайт связывания рибосом для инициации трансляции и терминатор транскрипции. Вектор экспрессии также может содержать соответствующие последовательности для усиления экспрессии. Вектор экспрессии также может содержать нуклеотидные последовательности, кодирующие ненативные метки (например, метку 6×His, гемагглютининовую метку, зеленый флуоресцентный белок и т.д.), которые гибридизованы с сайт-направленным полипептидом с образованием гибридного белка.
[0382] Согласно некоторым вариантам реализации настоящего изобретения нуклеотидная последовательность или последовательности, которые кодируют нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению, сайт-направленный полипептид согласно настоящему изобретению, эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению, могут быть функционально связаны с индуцируемым промотором (например, промотором белков теплового шока, тетрациклин-регулируемым промотором, стероид-регулируемым промотором, металл-регулируемым промотором, промотором, регулируемым рецептором эстрогенов, и т.д.). Согласно некоторым вариантам реализации настоящего изобретения нуклеотидная последовательность, которая кодирует нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению, сайт-направленный полипептид согласно настоящему изобретению, эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению, может быть функционально связана с конститутивным промотором (например, промотором цитомегаловируса, промотором UBC). Согласно некоторым вариантам реализации настоящего изобретения нуклеотидная последовательность может быть функционально связана с пространственно ограниченным и/или ограниченным по времени промотором (например, тканеспецифичным промотором, промотором, специфичным в отношении определенного типа клеток, и т.д.).
[0383] Нуклеотидная последовательность или последовательности, которые кодируют нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению, сайт-направленный полипептид согласно настоящему изобретению, эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению, могут быть упакованы внутрь или находиться на поверхности биологических компартментов для доставки к клеткам. Биологические компартменты могут включать, но не ограничиваются ими, вирусы (лентивирус, аденовирус), наносферы, липосомы, квантовые точки, наночастицы, частицы полиэтилеигликоля, гидрогели и мицеллы.
[0384] Введение комплексов, полипептидов и нуклеиновых кислот согласно настоящему изобретению в клетки может происходить с помощью инфекции вирусом или бактериофагом, трансфекции, конъюгации, слияния протопластов, электропорации, липофекции, осаждения фосфатом кальция, полиэтиленимин (ПЭИ)-опосредованной трансфекции, опосредованной DEAE-декстраном трансфекции, опосредованной липосомами трансфекции, технологии бомбардировки частицами, осаждения фосфатом кальция, прямой микроинъекции, опосредованной наночастицами доставки нуклеиновой кислоты и т.п.
[0385] Трансгенные клетки и организмы
[0386] В настоящем изобретении предложены трансгенные клетки и организмы. Нуклеиновая кислота генетически модифицированной клетки-хозяина и/или трансгенного организма может быть мишенью для геномной инженерии.
[0387] Примеры клеток, которые можно использовать для получения трансгенных клеток в соответствии со способами согласно настоящему изобретению, могут включать, но не ограничиваются ими, клетку HeLa, клетку яичника китайского хомячка, клетку 293-Т, феохромоцитому, фибробласт нейробластомы, рабдомиосаркому, ганглионарную клетку задних корешков, клетку NSO, клетку культуры табака BY-2, CV-I (ATCC CCL 70), COS-I (АТСС CRL 1650), COS-7 (ATCC CRL 1651), CHO-K1 (ATCC CCL 61), 3T3(ATCC CCL 92), NIH/3T3 (ATCC CRL 1658), HeLa (ATCC CCL 2), С 1271 (ATCC CRL 1616), BS-C-I (ATCC CCL 26), MRC-5 (ATCC CCL 171), L-клетки, HEK-293 (ATCC CRL1 573) и PC 12 (ATCC CRL- 1721), HEK293T (ATCC CRL-11268), RBL (ATCC CRL-1378), SH-SY5Y (ATCC CRL-2266), MDCK (ATCC CCL-34), SJ-RH30 (ATCC CRL-2061), HepG2 (ATCC HB-8065), ND7/23 (ECACC 92090903), CHO (ECACC 85050302), Vera (ATCC CCL 81). Caco-2 (ATCC HTB 37), K562 (ATCC CCL 243), Jurkat (ATCC TIB- 152),

[0388] Организмы, которые могут быть трансгенными, включают бактерии, архей, одноклеточных эукариот, растения, водоросли, грибки (например, дрожжи), беспозвоночных (например, дрозофилу, гидроидного, иглокожего, нематоду и т.д.), позвоночных (например, рыбу, амфибию, рептилию, птицу, млекопитающего), млекопитающих (например, свинью, корову, козу, овцу, грызуна, крысу, мышь, примата, не относящегося к человеку, человека и т.д.) и т.д.
[0389] Трансгенные организмы могут содержать генетически модифицированные клетки. Трансгенные организмы и/или генетически модифицированные клетки могут включать организмы и/или клетки, которые были генетически модифицированы экзогенной нуклеиновой кислотой, содержащей нуклеотидную последовательность, которая кодирует нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению, эффекторный белок и/или сайт-направленный полипептид, или любую их комбинацию.
[0390] Генетически модифицированная клетка может содержать экзогенный сайт-направленный полипептид и/или экзогенную нуклеиновую кислоту, содержащую нуклеотидную последовательность, которая кодирует сайт-направленный полипептид. Экспрессия сайт-направленного полипептида в клетке может осуществляться в течение 0,1, 0,2, 0,5, 1, 2, 3, 4, 5, 6 или более дней. Клетки, в которые был введен сайт-направленный полипептид, можно выращивать в течение 0,1, 0,2, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или даже более дней перед выделением клеток из культуры клеток и/или организма-хозяина.
[0391] Субъекты
[0392] В настоящем изобретении предложено применение способов согласно настоящему изобретению у субъекта. Субъект может представлять собой человека. Субъект может представлять собой млекопитающее (например крысу, мышь, корову, собаку, свинью, овцу, лошадь). Субъект может представлять собой позвоночное или беспозвоночное животное. Субъект может представлять собой лабораторное животное. Субъект может представлять собой пациента. Субъект может страдать от заболевания. Субъект может проявлять симптомы заболевания. Субъект может не проявлять симптомы заболевания, но при этом иметь заболевание. Субъект может находиться под медицинским наблюдением лица, осуществляющего уход (например, госпитализированный субъект, получающий лечение по назначению врача). Субъект может представлять собой растение или сельскохозяйственную культуру.
[0393] Наборы
[0394] В настоящем изобретении предложены наборы для осуществления способов согласно настоящему изобретению. Набор может содержать одно или более из перечисленных: нуклеиновая кислота, направленная против нуклеиновой кислоты, согласно настоящему изобретению, полинуклеотид, кодирующий нуклеиновую кислоту, направленную против нуклеиновой кислоты, сайт-направленный полипептид согласно настоящему изобретению, полинуклеотид, кодирующий сайт-направленный полипептид, эффекторный белок, полинуклеотид, кодирующий эффекторпый белок, мультиплексный генетический направляющий агент, полинуклеотид, кодирующий мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, полинуклеотид, кодирующий тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению, или любую их комбинацию.
[0395] Нуклеиновая кислота, направленная против нуклеиновой кислоты, согласно настоящему изобретению, полинуклеотид, кодирующий нуклеиновую кислоту, направленную против нуклеиновой кислоты, сайт-направленный полипептид согласно настоящему изобретению, полинуклеотид, кодирующий сайт-направленный полипептид, эффекторный белок, полинуклеотид, кодирующий эффекторный белок, мультиплексный генетический направляющий агент, полинуклеотид, кодирующий мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, полинуклеотид, кодирующий тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любая нуклеиновая кислота или белковая молекула, необходимая для осуществления способов согласно настоящему изобретению, подробно описаны выше.
[0396] Набор может содержать: (1) вектор, содержащий нуклеотидную последовательность, кодирующую нуклеиновую кислоту, направленную против нуклеиновой кислоты, и (2) вектор, содержащий нуклеотидную последовательность, кодирующую сайт-направленный полипептид, и (2) реагент для восстановления и/или разбавления векторов.
[0397] Набор может содержать: (1) вектор, содержащий (i) нуклеотидную последовательность, кодирующую нуклеиновую кислоту, направленную против нуклеиновой кислоты, и (ii) нуклеотидную последовательность, кодирующую сайт-направленный полипептид, и (2) реагент для восстановления и/или разбавления вектора.
[0398] Набор может содержать: (1) вектор, содержащий нуклеотидную последовательность, кодирующую нуклеиновую кислоту, направленную против нуклеиновой кислоты, (2) вектор, содержащий нуклеотидную последовательность, кодирующую сайт-направленный полипептид, (3) вектор, содержащий нуклеотидную последовательность, кодирующую эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению, и (4) реагент для восстановления и/или разбавления векторов.
[0399] Набор может содержать: (1) вектор, содержащий (i) нуклеотидную последовательность, кодирующую нуклеиновую кислоту, направленную против нуклеиновой кислоты, (ii) нуклеотидную последовательность, кодирующую сайт-направленный полипептид, (2) вектор, содержащий нуклеотидную последовательность, кодирующую эффекторный белок, мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любую нуклеиновую кислоту или белковую молекулу, необходимую для осуществления способов согласно настоящему изобретению, и (3) реагент для восстановления и/или разбавления рекомбинантных векторов экспрессии.
[0400] В некоторых случаях набор может содержать сайт-направленный. полипептид (и/или нуклеиновую кислоту, кодирующую указанный пептид), причем сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC); и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0401] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC); и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом; прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0402] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC); и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0403] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид может содержать аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC); и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), которая может содержать удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0404] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и линкер, соединяющий сайт-направленный полипептид с ненативной последовательностью; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0405] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и линкер, соединяющий сайт-направленный полипептид с ненативной последовательностью; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0406] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и линкер, соединяющий сайт-направленный полипептид с ненативной последовательностью; и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую удлиненную последовательность спей сера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0407] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и линкер, соединяющий сайт-направленный полипептид с ненативной последовательностью; и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0408] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0409] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0410] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0411] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0412] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3' -концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0413] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S: pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1 -5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0414] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0415] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается па расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0416] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), причем сайт-направленный полипептид содержит мутацию в одном или обоих доменах, расщепляющих нуклеиновую кислоту, которая снижает расщепляющую активность нуклеазных доменов по меньшей мере на 50%; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; и минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0417] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту, причем один или оба из доменов, расщепляющих нуклеиновую кислоту, содержат аминокислотную последовательность, которая по меньшей мере на 50% идентична аминокислотной последовательности нуклеазного домена Cas9 из S. pyogenes; и двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую: 1) первую молекулу нуклеиновой кислоты, содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 3 неспаренных нуклеотида в выпячивании; и 2) вторую молекулу нуклеиновой кислоты указанной двойной направляющей нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может содержать минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину и по меньшей мере 1 неспаренный нуклеотид в выпячивании, причем 1 неспаренный нуклеотид в выпячивании находится в том же выпячивании, что и 3 неспаренных нуклеотида минимального повтора CRISPR; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0418] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту, причем один или оба из доменов, расщепляющих нуклеиновую кислоту, содержат аминокислотную последовательность, которая по меньшей мере на 50% идентична аминокислотной последовательности нуклеазного домена Cas9 из S. pyogenes, и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину; минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6, 7 или 8 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов и включает дуплексную область; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию. Такая нуклеиновая кислота, направленная против нуклеиновой кислоты, может называться одиночной направляющей нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0419] В некоторых случаях набор может содержать сайт-направленный полипептид (и/или нуклеиновую кислоту, кодирующую указанный полипептид), причем сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, и два домена, расщепляющих нуклеиновую кислоту, причем один или оба из доменов, расщепляющих нуклеиновую кислоту, содержат аминокислотную последовательность, которая по меньшей мере на 50% идентична аминокислотной последовательности нуклеазного домена Cas9 из S. pyogenes; и нуклеиновую кислоту, направленную против нуклеиновой кислоты (и/или нуклеиновую кислоту, кодирующую указанную кислоту), содержащую удлиненную последовательность спейсера, содержащую от 10 до 5000 нуклеотидов в длину; последовательность спейсера, содержащую от 12 до 30 нуклеотидов в длину, и при этом спейсер по меньшей мере на 50% комплементарен нуклеиновой кислоте-мишени; дуплекс, содержащий: 1) минимальный повтор CRISPR, который по меньшей мере на 60% идентичен crPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальный повтор CRISPR содержит от 5 до 30 нуклеотидов в длину, 2) минимальную последовательность tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из бактерии (например, S. pyogenes) в участке, содержащем 6 последовательных нуклеотидов, и при этом минимальная последовательность tracrPHK содержит от 5 до 30 нуклеотидов в длину, и 3) выпячивание, которое содержит по меньшей мере 3 неспаренных нуклеотида на цепи минимального повтора CRISPR в дуплексе и по меньшей мере 1 неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе; последовательность линкера, который соединяет минимальный повтор CRISPR и минимальную последовательность tracrPHK и содержит в длину от 3 до 5000 нуклеотидов; 3'-концевую tracrPHK, которая по меньшей мере на 60% идентична tracrPHK из прокариотического организма (например, S. pyogenes) или фага в участке, содержащем 6 последовательных нуклеотидов, и при этом 3'-концевая tracrPHK содержит от 10 до 20 нуклеотидов в длину и включает дуплексную область; Р-домен, который начинается на расстоянии 1-5 нуклеотидов после дуплекса, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK, содержит 1-10 нуклеотидов, содержит последовательность, которая может гибридизоваться с мотивом, прилегающим к протоспейсеру, в нуклеиновой кислоте-мишени, может образовывать шпильку, и находится в области 3'-концевой tracrPHK; и/или удлиненную последовательность tracrPHK, содержащую от 10 до 5000 нуклеотидов в длину, или любую их комбинацию.
[0420] Согласно некоторым вариантам реализации любого из указанных выше наборов, набор может содержать одиночную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты. Согласно некоторым вариантам реализации любого из указанных выше наборов, набор может содержать двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты. Согласно некоторым вариантам реализации любого из указанных выше наборов, набор может содержать две или более двойных направляющих или одиночных направляющих нуклеиновых кислот, направленных против нуклеиновой кислоты. Согласно некоторым вариантам реализации настоящего изобретения вектор может кодировать нуклеиновую кислоту, направленную против нуклеиновой кислоты.
[0421] Согласно некоторым вариантам реализации любого из указанных выше наборов, набор может дополнительно содержать донорный полинуклеотид или полинуклеотидную последовательность, кодирующую донорный полинуклеотид, для осуществления желаемой генетической модификации. Компоненты набора могут находиться в отдельных контейнерах; или могут быть объединены в одном контейнере.
[0422] Набор, описанный выше, дополнительно содержит один или более дополнительных реагентов, которые могут быть выбраны из: буфера, буфера для введения в клетку полипептида или полинуклеотида, присутствующего в наборе, буфера для промывки, контрольного реагента, контрольного вектора, контрольного полинуклеотида РНК, реагента для получения полипептида из ДНК в условиях in vitro, адаптеров для секвенирования и т.п. Буфер может представлять собой буфер для стабилизации, буфер для восстановления или буфер для разбавления.
[0423] В некоторых случаях набор может содержать один или более дополнительных реагентов, специфичных для растений и/или грибов. Один или более дополнительных реагентов, специфичных для растений и/или грибов, могут включать, например, почву, питательные вещества, растения, семена, споры, Agrobacterium, вектор Т-ДНК и вектор pBINAR.
[0424] В дополнение к упомянутым выше компонентам набор может дополнительно содержать инструкции по использованию компонентов набора для осуществления способов согласно настоящему изобретению. Инструкции для осуществления способов согласно настоящему изобретению, как правило, записаны на соответствующем носителе записи. Например, инструкции могут быть напечатаны на подложке, такой как бумага или пластик, и т.д. Инструкции могут присутствовать в наборах в виде листка-вкладыша, в виде этикетки контейнера указанного набора или его компонентов (т.е. связаны с упаковкой или дополнительной упаковкой) и т.д. Инструкции могут присутствовать в виде электронного файла, содержащего данные для хранения, который представлен на соответствующем машиночитаемом носителе информации, например, CD-ROM, дискете, флеш-накопителе и т.д. В некоторых случаях в наборе отсутствуют действующие инструкции, но могут быть обеспечены средства для получения инструкций из удаленного источника (например, через Интернет). Примером такого варианта реализации является набор, который включает веб-адрес страницы, на которой можно просмотреть и/или загрузить инструкции. Как и в случае инструкций, такое средство для получения инструкций может быть записано на подходящем носителе.
[0425] Согласно некоторым вариантам реализации настоящего изобретения набор может содержать линеаризованный вектор. Линеаризованный вектор может содержать плазмиду, содержащую сайт-направленный полипептид и/или нуклеиновую кислоту, направленную против нуклеиновой кислоты, которая линеаризована (например, не является кольцевой). Линеаризованный вектор может храниться в буфере, содержащем 10 мМ Трис-HCl, рН=8,0 и 1 мМ ЭДТА, рН=8,0. Набор может содержать приблизительно 20 мкл линеаризованного вектора, несущего нуклеазу CRISPR. Согласно некоторым вариантам реализации настоящего изобретения набор может содержать один или более кольцевых векторов.
[0426] Согласно некоторым вариантам реализации настоящего изобретения набор может содержать буфер для ренатурирования олигонуклеотидов. Буфер для ренатурирования олигонуклеотидов может представлять собой буфер, используемый для ренатурирования олигонуклеотидов ДНК друг с другом для получения двухцепочечной ДНК, которая кодирует нуклеиновую кислоту, направленную против нуклеиновой кислоты. Буфер для ренатурирования олигонуклеотидов может быть концентрированным по меньшей мере приблизительно в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более раз по сравнению с используемой концентрацией. Буфер для ренатурирования олигонуклеотидов может быть в 10 раз более концентрированным по сравнению с используемой концентрацией. Буфер для отжига олигонуклеотидов может содержать 100 мМ Трис-HCl, рН=8,0, 10 мМ ЭДТА, рН=8,0 и 1 М NaCl. Набор может содержать 250 мкл буфера для ренатурирования олигонуклеотидов.
[0427] Набор может содержать воду, не содержащую ДНКаз. Набор может содержать воду, не содержащую РНКаз. Набор может содержать по меньшей мере 1,5 мл воды, не содержащей РНКазы и/или ДНКазы.
[0428] Набор может содержать буфер для лигирования. Буфер для лигирования можно использовать для лигирования олигонуклеотидов в линеаризованный вектор, несущий нуклеазу CRISPR. Буфер для лигирования может быть концентрированным по меньшей мере приблизительно в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более раз по сравнению с используемой концентрацией. Буфер для лигирования может быть в 5 раз более концентрированным по сравнению с используемой концентрацией. 5-кратный буфер для лигирования может содержать 250 мМ Трис-HCl, рН=7,6, 50 мМ MgCl2, 5 мМ АТФ, 5 мМ ДТТ и 25% (масс./об.) полиэтиленгликоля-8000. Набор может содержать приблизительно 80 мкл буфера для лигирования.
[0429] Набор может содержать ДНК-лигазу. ДНК-лигазу можно использовать для лигирования олигонуклеотидов в линеаризованный вектор, несущий нуклеазу CRISPR. ДНК-лигаза может содержать 10 мМ Трис-HCl, рН=7,5, 50 мМ KCl, 1 мМ ДТТ и 50% (об./об.) глицерина. Набор может содержать 20 мкл ДНК-лигазы.
[0430] Набор может содержать праймер для секвенирования. Праймер для секвенирования можно использовать для секвенирования вектора, после того как олигонуклеотиды были лигированы в линеаризованный вектор. Праймер для секвенирования может быть разведен в Трис-ЭДТА, рН=8,0. Набор может содержать 20 мкл праймера для секвенирования.
[0431] Набор может содержать контрольный олигонуклеотид. Контрольный олигонуклеотид может представлять собой олигонуклеотид, который будет лигирован в линеаризованный вектор, но не кодирует нуклеиновую кислоту, направленную против нуклеиновой кислоты. Контрольный олигонуклеотид может быть разбавлен до 1-кратной концентрации в буфере для ренатурирования олигонуклеотидов. Набор может содержать 10 мкл контрольного олигонуклеотида.
[0432] В некоторых случаях набор может содержать линеаризованный вектор, содержащий сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты, буфер для ренатурирования олигонуклеотидов, воду, не содержащую ДНКазы/РНКазы, буфер для лигирования, фермент лигазу, праймер для секвенирования и контрольный олигонуклеотид, или любую их комбинацию.
[0433] Фармацевтические композиции
[0434] Молекулы, такие как нуклеиновая кислота, направленная против нуклеиновой кислоты, согласно настоящему изобретению, описанная в настоящей заявке, полинуклеотид, кодирующий нуклеиновую кислоту, направленную против нуклеиновой кислоты, сайт-направленный полипептид согласно настоящему изобретению, полинуклеотид, кодирующий сайт-направленный полипептид, эффекторный белок, полинуклеотид, кодирующий эффекторный белок, мультиплексный генетический направляющий агент, полинуклеотид, кодирующий мультиплексный генетический направляющий агент, донорный полинуклеотид, тандемный гибридный белок, полинуклеотид, кодирующий тандемный гибридный белок, репортерный элемент, генетический элемент, представляющий интерес, компонент комбинированной системы и/или любая нуклеиновая кислота или белковая молекула, необходимая для осуществления способов согласно настоящему изобретению, могут быть изготовлены в виде фармацевтической композиции.
[0435] Фармацевтическая композиция может содержать комбинацию любых молекул, описанных в настоящей заявке, с другими химическими компонентами, такими как носители, стабилизаторы, разбавители, диспергирующие агенты, суспендирующие агенты, загустители и/или вспомогательные вещества. Фармацевтическая композиция может облегчить введение молекулы в организм. Фармацевтические композиции можно вводить в терапевтически эффективных количествах в виде различных форм и с помощью различных путей введения, включая, например, внутривенный, подкожный, внутримышечный, оральный, ректальный, аэрозольный, парентеральный, глазной, легочной, трансдермальный, вагинальный, ушной, назальный и местный путь введения.
[0436] Фармацевтическую композицию можно вводить местным или системным способом, например, с помощью инъекции молекулы непосредственно в орган, необязательно в виде лекарственных форм с пролонгированным или замедленным высвобождением. Фармацевтические композиции могут быть обеспечены в виде лекарственных форм с быстрым высвобождением, в виде лекарственных форм с продленным высвобождением или в виде лекарственных форм с промежуточным высвобождением. Лекарственная форма с быстрым высвобождением может обеспечить немедленное высвобождение. Лекарственная форма с продленным высвобождением может обеспечить контролируемое высвобождение или отсроченное замедленное высвобождение.
[0437] Фармацевтические композиции для перорального введения могут быть легко изготовлены путем комбинирования молекулы с фармацевтически приемлемыми носителями или вспомогательными веществами. Такие носители могут быть использованы для изготовления таблеток, порошков, пилюль, драже, капсул, жидкостей, гелей, сиропов, эликсиров, взвесей, суспензий и т.п. для перорального приема субъектом.
[0438] Фармацевтические препараты для перорального введения могут быть получены путем смешивания одного или более твердых вспомогательных веществ с одной или более из молекул, описанных в настоящей заявке, возможно, с последующим измельчением полученной смеси и обработкой смеси гранул после добавления подходящих вспомогательных веществ, в случае необходимости, для получения гранульных заготовок таблеток или драже. Гранульные заготовки могут быть обеспечены с подходящими покрытиями. В качестве покрытий можно использовать концентрированные растворы сахара, которые могут содержать вспомогательное вещество, такое как гуммиарабик, тальк, поливинилпирролидон, карбопол в виде геля, полиэтиленгликоль и/или диоксид титана, лаковые растворы и подходящие органические растворители или смеси растворителей. Красители или пигменты могут быть добавлены к покрытиям для таблеток или драже, например, для идентификации или характеристики различных комбинаций доз активного соединения.
[0439] Фармацевтические препараты, которые могут быть использованы перорально, могут включать твердые капсулы, изготовленные из желатина, а также мягкие герметичные капсулы, изготовленные из желатина и пластификатора, такого как глицерин или сорбит. Согласно некоторым вариантам реализации настоящего изобретения капсула содержит твердую желатиновую капсулу, содержащую один или более видов желатина фармацевтического качества, полученных от крупного рогатого скота и из растений. Желатин может быть подвергнут щелочной обработке. Твердые капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, связующими веществами, такими как крахмалы, и/или смазывающими веществами, такими как тальк или стеарат магния, и стабилизаторами. В мягких капсулах молекула может быть растворена или суспендирована в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкие полиэтиленгликоли. В смесь могут быть добавлены стабилизаторы. Все препараты для перорального введения обеспечены в дозах, подходящих для такого пути введения.
[0440] Композиции, предназначенные для буккального или сублингвального введения, могут представлять собой таблетки, пастилки или гели.
[0441] Композиции для парентеральных инъекций могут быть изготовлены для введения с помощью болюсной инъекции или непрерывной инфузии. Фармацевтические композиции могут быть обеспечены в форме, подходящей для парентерального введения, в виде стерильной суспензии, раствора или эмульсии в масляных или водных носителях, и могут содержать дополнительные агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Фармацевтические композиции для парентерального введения могут содержать водные растворы активных соединений в водорастворимой форме.
[0442] Суспензии молекул могут быть изготовлены в виде масляных суспензий для инъекций. Подходящие липофильные растворители или носители включают жирные масла, такие как кунжутное масло, или синтетические сложные эфиры жирных кислот, такие как этилолеат или триглицериды, или липосомы. Водные суспензии для инъекций могут содержать вещества, которые увеличивают вязкость суспензии, такие как натрий карбоксиметилцеллюлоза, сорбит или декстран. Суспензия также может содержать подходящие стабилизаторы или агенты, которые повышают растворимость молекул, чтобы обеспечить получение высококонцентрированных растворов. Согласно другому подходу, активный ингредиент может быть в форме порошка для восстановления перед применением с использованием подходящего носителя, например, стерильной апирогенной воды.
[0443] Активные соединения могут быть введены местно и могут быть изготовлены в виде различных композиций для местного введения, таких как растворы, суспензии, лосьоны, гели, пасты, лечебные палочки, бальзамы, кремы и мази. Такие фармацевтические композиции могут содержать солюбилизаторы, стабилизаторы, увеличивающие тоничность агенты, буферы и консерванты.
[0444] Композиции, подходящие для трансдермального введения молекул, могут содержать устройства для трансдермальной доставки и пластыри для трансдермальной доставки, и могут представлять собой липофильные эмульсии или забуференные водные растворы, могут быть растворены и/или диспергированы в полимере или клеящем веществе. Такие пластыри могут быть изготовлены для непрерывного, прерывистого или другого вида доставки молекул. Трансдермальную доставку можно осуществлять с помощью пластырей для ионофореза и т.п. Помимо этого трансдермальные пластыри могут обеспечить контролируемую доставку. Скорость всасывания можно замедлить с помощью мембран, регулирующих скорость всасывания, или путем иммобилизации соединения на полимерном матриксе или геле. С другой стороны, усилители всасывания могут быть использованы для того чтобы увеличить скорость всасывания. Усилитель всасывания или носитель может содержать рассасывающиеся фармацевтически приемлемые растворители, способствующие проникновению через кожу. Например, устройства для трансдермального введения могут быть в форме бинта, содержащего наружный элемент, резервуар, содержащий соединения и носители, и барьер, контролирующий скорость всасывания, для доставки соединений к коже субъекта с контролируемой и заранее определенной скоростью в течение продолжительного периода времени, и клеящие вещества для закрепления устройства на коже.
[0445] Для введения путем ингаляции молекула может быть обеспечена в форме аэрозоля, взвешенной суспензии или порошка. Фармацевтические композиции могут быть доставлены в форме аэрозольного спрея из упаковок под давлением или небулайзера с использованием подходящего пропеллента, например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, двуокиси углерода или другого подходящего газа. В случае использования аэрозоля под давлением стандартная доза может быть определена с помощью клапана для доставки дозированного количества. Могут быть изготовлены капсулы и картриджи, например, из желатина, для использования в ингаляторе или инсуффляторе, содержащие порошкообразную смесь соединения и подходящую порошковую основу, такую как лактоза или крахмал.
[0446] Молекулы также могут быть изготовлены в виде композиций для ректального введения, таких как клизмы, ректальные гели, ректальные пены, ректальные аэрозоли, суппозитории, желеобразные суппозитории или удерживающие клизмы, содержащие обычные основы для суппозиториев, такие как масло какао или другие глицериды, а также синтетические полимеры, такие как поливинилпирролидон и ПЭГ. В случае использования композиций в форме суппозиториев применяют воск с низкой температурой плавления, такой как смесь глицеридов жирных кислот или масло какао.
[0447] При осуществлении способов согласно настоящему изобретению терапевтически эффективные количества соединений, описанных в настоящей заявке, могут быть введены в форме фармацевтических композиций субъекту, имеющему заболевание или состояние, подлежащее лечению. Терапевтически эффективное количество может широко варьироваться в зависимости от степени тяжести заболевания, возраста и относительного состояния здоровья субъекта, эффективности используемых соединений и других факторов. Соединения могут быть использованы по отдельности или в комбинации с одним или более терапевтическими агентами в качестве компонентов смесей.
[0448] Фармацевтические композиции могут быть изготовлены с использованием одного или более физиологически приемлемых носителей, включая вспомогательные вещества и вспомогательные ингредиенты, которые облегчают обработку молекулы при производстве препаратов, которые могут быть использованы в фармацевтических целях. Композиция может быть модифицирована в зависимости от выбранного пути введения. Фармацевтические композиции, содержащие молекулу, описанную в настоящей заявке, могут быть изготовлены, например, путем смешивания, растворения, гранулирования, изготовления драже, растирания в порошок, эмульгирования, инкапсулирования, захватывания или сжатия.
[0449] Фармацевтические композиции могут содержать по меньшей мере один фармацевтически приемлемый носитель, разбавитель или вспомогательное вещество и молекулу, описанную в настоящей заявке, в виде свободного основания или фармацевтически приемлемой соли. Способы и фармацевтические композиции, описанные в настоящей заявке, включают использование кристаллических форм (также известных как полиморфы), и активных метаболитов указанных соединений, имеющих тот же тип активности.
[0450] Способы получения композиций, содержащих соединения, описанные в настоящей заявке, могут включать смешивание молекулы с одним или более инертными, фармацевтически приемлемыми вспомогательными веществами или носителями, с образованием твердой, полутвердой или жидкой композиции. Твердые композиции могут включать, например, порошки, таблетки, диспергируемые гранулы, капсулы, облатки и суппозитории. Жидкие композиции могут включать, например, растворы, в которых растворено соединение, эмульсии, содержащие соединение, или раствор, содержащий липосомы, мицеллы, или наночастицы, содержащие соединение, описанное в настоящей заявке. Полутвердые композиции могут включать, например, гели, суспензии и кремы. Композиции могут быть обеспечены в виде жидких растворов или суспензий, твердых форм, подходящих для растворения или суспендирования в жидкости перед применением, либо в виде эмульсий. Такие композиции также могут содержать небольшие количества нетоксичных вспомогательных веществ, таких как смачивающие или эмульгирующие агенты, рН-забуферивающие агенты и другие фармацевтически приемлемые добавки.
[0451] Неограничивающие примеры лекарственных форм могут включать корм, пищевой продукт, гранулу, пастилку и жидкость, эликсир, аэрозоль, форму для ингаляции, спрей, порошок, таблетку, пилюлю, капсулу, гель, гелевую таблетку, наносуспензию, наночастицу, микрогель, суппозиторные пастилки, водные или масляные суспензии, мазь, пластырь, лосьон, средство для ухода за зубами, эмульсию, кремы, капли, диспергируемые порошки или гранулы, эмульсии в твердых или мягких гелевых капсулах, сиропы, фитоцевтики и нутрицевтики, или любую их комбинацию.
[0452] Неограничивающие примеры фармацевтически приемлемых вспомогательных веществ могут включать гранулирующие агенты, связующие агенты, смазывающие агенты, разрыхлители, подсластители, вещества, обеспечивающие скольжение, антиадгезивы, антистатики, поверхностно-активные вещества, антиоксиданты, камеди, покрывающие агенты, красители, ароматизирующие агенты, покрывающие агенты, пластификаторы, консерванты, суспендирующие агенты, эмульгирующие агенты, целлюлозные материалы растительного происхождения и агенты для сфероидизации, или любую их комбинацию.
[0453] Композиция может представлять собой, например, лекарственную форму с немедленным высвобождением или лекарственную форму с контролируемым высвобождением. Композиция с немедленным высвобождением может быть изготовлена, чтобы обеспечить быстрое начало действия молекулы. Неограничивающие примеры композиций с немедленным высвобождением могут включать легкорастворимые композиции. Композиция с контролируемым высвобождением может представлять собой фармацевтическую композицию, которая была адаптирована так, что скорости высвобождения лекарственных препаратов и профили высвобождения лекарственных препаратов могут быть сопоставлены с физиологическими, временными и терапевтическими требованиями или, согласно другому варианту, была приготовлена так, чтобы осуществлять высвобождение лекарственного препарата с заранее установленной скоростью. Неограничивающие примеры композиций с контролируемым высвобождением могут включать гранулы, гранулы с отсроченным высвобождением, гидрогели (например, синтетического или природного происхождения), другие гелеобразующие агенты (например, гелеобразующие пищевые волокна), композиции на основе матрикса (например, композиции, содержащие полимерный материал, в котором диспергирован по меньшей мере один активный ингредиент), гранулы внутри матрикса, полимерные смеси, гранулированные массы и тому подобное.
[0454] Композиция с контролируемым высвобождением может представлять собой форму с отсроченным высвобождением. Форма с отсроченным высвобождением может быть изготовлена, чтобы отсрочить действие молекулы в течение длительного периода времени. Форма с отсроченным высвобождением может быть изготовлена, чтобы отсрочить высвобождение эффективной дозы одной или более молекул, например, в течение приблизительно 4, приблизительно 8, приблизительно 12, приблизительно 16 или приблизительно 24 часов.
[0455] Композиция с контролируемым высвобождением может представлять собой форму с замедленным высвобождением. Форма с замедленным высвобождением может быть изготовлена, чтобы замедлить, например, действие молекулы в течение длительного периода времени. Форма с замедленным высвобождением может быть изготовлена, чтобы обеспечить эффективную дозу любой молекулы, описанной в настоящей заявке (например, обеспечить физиологически эффективный профиль в крови), в течение приблизительно 4, приблизительно 8, приблизительно 12, приблизительно 16 или приблизительно 24 часов.
[0456] Способы введения и способы лечения.
[0457] Фармацевтические композиции, содержащие молекулы, описанные в настоящей заявке, могут быть введены для осуществления профилактических и/или терапевтических способов лечения. При терапевтическом применении композиции могут быть введены субъекту, уже страдающему от заболевания или состояния, в количестве, достаточном для лечения или по меньшей мере частичного купирования симптомов заболевания или состояния, или для лечения, заживления, улучшения или облегчения состояния. Количества, эффективные для такого способа применения, могут варьироваться в зависимости от степени тяжести и течения заболевания или состояния, предшествующей терапии, состояния здоровья субъекта, массы тела и ответа на лекарственные препараты, а также решения лечащего врача.
[0458] Несколько терапевтических агентов можно вводить в любом порядке или одновременно. При одновременном введении несколько терапевтических агентов могут быть обеспечены в виде единичной дозированной лекарственной формы или в виде множественных дозированных лекарственных форм, например, в виде нескольких отдельных пилюль. Молекулы могут быть упакованы вместе или по отдельности, в одной упаковке или в виде множества упаковок. Один или все из терапевтических агентов могут быть введены в виде многократных доз. В случае неодновременного введения интервал времени между несколькими дозами может изменяться вплоть до приблизительно месяца.
[0459] Молекулы, описанные в настоящей заявке, могут быть введены перед, во время или после возникновения заболевания или состояния, и время введения композиции, содержащей соединение, может изменяться. Например, фармацевтические композиции можно использовать в профилактических целях и можно непрерывно вводить субъектам, которые склоны к развитию состояний или заболеваний, чтобы предотвратить возникновение заболевания или состояния. Молекулы и фармацевтические композиции могут быть введены субъекту во время или как можно скорее после появления симптомов. Введение молекул может быть начато в течение первых 48 часов после появления симптомов, в течение первых 24 часов после появления симптомов, в течение первых 6 часов после появления симптомов, или в течение 3 часов после появления симптомов. Начальное введение можно осуществлять любым удобным путем, например, любым путем, описанным в настоящей заявке, с использованием любой композиции, описанной в настоящей заявке. Молекула может быть введена как можно скорее, когда это будет удобно, после обнаруженного или подозреваемого начала заболевания или состояния, и в течение периода времени, необходимого для лечения заболевания, такого как, например, от приблизительно 1 месяца до приблизительно 3 месяцев. Продолжительность лечения может варьироваться для каждого субъекта.
[0460] Молекула может быть упакована в биологический компартмент. Биологический компартмент, содержащий молекулу, можно вводить субъекту. Биологические компартменты могут включать, но не ограничиваются ими, вирусы (лентивирус, аденовирус), наносферы, липосомы, квантовые точки, наночастицы, микрочастицы, нанокапсулы, везикулы, частицы полиэтиленгликоля, гидрогели и мицеллы.
[0461] Например, биологический компартмент может содержать липосому. Липосома может представлять собой самособирающуюся структуру, содержащую один или более двойных липидных слоев, каждый из которых может состоять из двух монослоев, содержащих противоположно ориентированные амфипатические липидные молекулы. Амфипатические липиды могут содержать полярную (гидрофильную) головную группу, которая ковалентно связана с одной или двумя, или более неполярными (гидрофобными) ацильными или алкильными цепями. Энергетически невыгодные контакты между гидрофобными ацильными цепями и окружающей водной средой индуцируют самопроизвольную перестройку амфипатических липидных молекул так, что полярные головные группы могут быть ориентированы по направлению к поверхности бислоя и ацильные цепи ориентированы по направлению к внутренней части бислоя, что обеспечивает эффективное экранирование ацильных цепей от контакта с водной средой.
[0462] Примеры предпочтительных амфипатических соединений, используемых в липосомах, могут включать фосфоглицериды и сфинголипиды, типичные примеры которых включают фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозитол, фосфатидную кислоту, фосфатидилглицерол, пальмитоилолеоил фосфатидилхолин, лизофосфатидилхолин, лизофосфатидилэтаноламин, димиристоилфосфатидилхолин (ДМФХ), дипальмитоилфосфатидилхолин (ДПФХ), диолеофосфатидилхолин, дистеароилфосфатидилхолин (ДСФХ), дилинолеоилфосфатидилхолин и яичный сфингомиелин, или любую их комбинацию.
[0463] Биологический компартмент может содержать наночастицу. Наночастица может иметь в диаметре от приблизительно 40 нм до приблизительно 1,5 микрон, от приблизительно 50 нм до приблизительно 1,2 микрон, от приблизительно 60 нм до приблизительно 1 микрона, от приблизительно 70 нм до приблизительно 800 нм, от приблизительно 80 нм до приблизительно 600 нм, от приблизительно 90 нм до приблизительно 400 нм, от 100 нм до приблизительно 200 нм.
[0464] В некоторых случаях при увеличении размера наночастицы скорость высвобождения может быть замедлена или снижена, и при уменьшении размера наночастицы скорость высвобождения может быть увеличена.
[0465] Количество альбумина в наночастицах может варьироваться от приблизительно 5% до приблизительно 85% альбумина (об./об.), от приблизительно 10% до приблизительно 80%, от приблизительно 15% до приблизительно 80%, от приблизительно 20% до приблизительно 70% альбумина (об./об.), от приблизительно 25% до приблизительно 60%, от приблизительно 30% до приблизительно 50%, или от приблизительно 35% до приблизительно 40%. Фармацевтическая композиция может содержать вплоть до 30, 40, 50, 60, 70 или 80% или более наночастиц. В некоторых случаях молекулы нуклеиновой кислоты согласно настоящему изобретению могут быть связаны с поверхностью наночастицы.
[0466] Биологический компартмент может содержать вирус. Вирус может представлять собой систему доставки для фармацевтических композиций согласно настоящему изобретению. Типичные вирусы включают лентивирус, ретровирус, аденовирус, вирус простого герпеса I или II, парвовирус, вирус ретикулоэндотелиоза и аденоассоциированный вирус (AAV). Фармацевтические композиции согласно настоящему изобретению могут быть доставлены в клетку с помощью вируса. Вирус может инфицировать и трансдуцировать клетку в условиях in vivo, ex vivo или in vitro. При доставке в условиях ex vivo или in vitro трансдуцированные клетки можно вводить субъекту, нуждающемуся в терапии.
[0467] Фармацевтические композиции могут быть упакованы в вирусные системы доставки. Например, композиции могут быть упакованы в вирионы с помощью системы упаковки, не содержащей вируса-помощника HSV-1.
[0468] Вирусные системы доставки (например, вирусы, содержащие фармацевтические композиции согласно настоящему изобретению) могут быть введены в клетку, ткань или орган субъекта, нуждающегося в таком лечении, путем прямой инъекции, стереотаксической инъекции, интрацеребровентрикулярно, с помощью инфузионных мининасосов, с помощью конвекции, катетеров, внутривенной, парентеральной, внутрибрюшинной и/или подкожной инъекции. В некоторых случаях клетки могут быть трансдуцированы в условиях in vitro и ex vivo с использованием вирусных систем доставки. Трансдуцированные клетки можно вводить субъекту, имеющему заболевание. Например, стволовую клетку можно трансдуцировать с использованием вирусной системы доставки, содержащей фармацевтическую композицию, и такая стволовая клетка может быть имплантирована пациенту для лечения заболевания. В некоторых случаях доза трансдуцированных клеток, введенных субъекту, может составлять приблизительно 1×105 клеток/кг, приблизительно 5×105 клеток/кг, приблизительно 1×106 клеток/кг, приблизительно 2×106 клеток/кг, приблизительно 3×106 клеток/кг, приблизительно 4×106 клеток/кг, приблизительно 5×106 клеток/кг, приблизительно 6×106 клеток/кг, приблизительно 7×106 клеток/кг, приблизительно 8×106 клеток/кг, приблизительно 9×106 клеток/кг, приблизительно 1×107 клеток/кг, приблизительно 5×107 клеток/кг, приблизительно 1×108 клеток/кг или более в виде однократной дозы.
[0469] Фармацевтические композиции в биологических компартментах можно использовать для лечения воспалительных заболеваний, таких как артрит, разные виды рака, такие как, например, рак костей, рак молочной железы, рак кожи, рак простаты, рак печени, рак легких, рак горла и рак почек, бактериальных инфекций, для лечения повреждения нервов, заболеваний легких, печени и почек, лечения глаз, лечения травм спинного мозга, заболевания сердца, артериального заболевания.
[0470] Введение биологических компартментов в клетки может происходить с помощью инфекции вирусом или бактериофагом, трансфекции, конъюгации, слияния протопластов, электропорации, липофекции, осаждения фосфатом кальция, полиэтиленимин (ПЭИ)-опосредованной трансфекции, опосредованной DEAE-декстраном трансфекции, опосредованной липосомами трансфекции, технологии бомбардировки частицами, осаждения фосфатом кальция, прямой микроинъекции, опосредованной наночастицами доставки нуклеиновой кислоты и т.п.
[0471] Дозировка
[0472] Фармацевтические композиции, описанные в настоящей заявке, могут быть обеспечены в виде стандартных лекарственных форм, подходящих для однократного введения точных доз. В стандартной лекарственной форме композиция может быть разделена на стандартные дозы, содержащие соответствующие количества одного или более соединений. Стандартная лекарственная форма может быть представлена в форме упаковки, содержащей отдельные порции композиции. Неограничивающие примеры могут включать упакованные таблетки или капсулы и порошки во флаконах или ампулах. Водная суспензия композиции может быть упакована в однодозные контейнеры, не пригодные для повторной герметизации. Многодозные контейнеры, пригодные для повторной герметизации, могут быть использованы, например, в комбинации с консервантом. Композиции для парентерального введения могут быть представлены в виде стандартной лекарственной формы, например, в ампулах, или в многодозных контейнерах с добавлением консерванта.
[0473] Молекула, описанная в настоящей заявке, может присутствовать в композиции в количестве, которое находится в пределах от приблизительно 1 мг до приблизительно 2000 мг; от приблизительно 5 мг до приблизительно 1000 мг, от приблизительно 10 мг до приблизительно 25 мг или до 500 мг, от приблизительно 50 мг до приблизительно 250 мг, от приблизительно 100 мг до приблизительно 200 мг, от приблизительно 1 мг до приблизительно 50 мг, от приблизительно 50 мг до приблизительно 100 мг, от приблизительно 100 мг до приблизительно 150 мг, от приблизительно 150 мг до приблизительно 200 мг, от приблизительно 200 мг до приблизительно 250 мг, от приблизительно 250 мг до приблизительно 300 мг, от приблизительно 300 мг до приблизительно 350 мг, от приблизительно 350 мг до приблизительно 400 мг, от приблизительно 400 мг до приблизительно 450 мг, от приблизительно 450 мг до приблизительно 500 мг, от приблизительно 500 мг до приблизительно 550 мг, от приблизительно 550 мг до приблизительно 600 мг, от приблизительно 600 мг до приблизительно 650 мг, от приблизительно 650 мг до приблизительно 700 мг, от приблизительно 700 мг до приблизительно 750 мг, от приблизительно 750 мг до приблизительно 800 мг, от приблизительно 800 мг до приблизительно 850 мг, от приблизительно 850 мг до приблизительно 900 мг, от приблизительно 900 мг до приблизительно 950 мг, или от приблизительно 950 мг до приблизительно 1000 мг.
[0474] Молекула, описанная в настоящей заявке, может присутствовать в композиции в количестве, составляющем приблизительно 1 мг, приблизительно 2 мг, приблизительно 3 мг, приблизительно 4 мг, приблизительно 5 мг, приблизительно 10 мг, приблизительно 15 мг, приблизительно 20 мг, приблизительно 25 мг, приблизительно 30 мг, приблизительно 35 мг, приблизительно 40 мг, приблизительно 45 мг, приблизительно 50 мг, приблизительно 55 мг, приблизительно 60 мг, приблизительно 65 мг, приблизительно 70 мг, приблизительно 75 мг, приблизительно 80 мг, приблизительно 85 мг, приблизительно 90 мг, приблизительно 95 мг, приблизительно 100 мг, приблизительно 125 мг, приблизительно 150 мг, приблизительно 175 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг, приблизительно 500 мг, приблизительно 550 мг, приблизительно 600 мг, приблизительно 650 мг, приблизительно 700 мг, приблизительно 750 мг, приблизительно 800 мг, приблизительно 850 мг, приблизительно 900 мг, приблизительно 950 мг, приблизительно 1000 мг, приблизительно 1050 мг, приблизительно 1100 мг, приблизительно 1150 мг, приблизительно 1200 мг, приблизительно 1250 мг, приблизительно 1300 мг, приблизительно 1350 мг, приблизительно 1400 мг, приблизительно 1450 мг, приблизительно 1500 мг, приблизительно 1550 мг, приблизительно 1600 мг, приблизительно 1650 мг, приблизительно 1700 мг, приблизительно 1750 мг, приблизительно 1800 мг, приблизительно 1850 мг, приблизительно 1900 мг, приблизительно 1950 мг или приблизительно 2000 мг.
[0475] Молекула (например, сайт-направленный полипептид, нуклеиновая кислота, направленная против нуклеиновой кислоты, и/или комплекс сайт-направленного полипептида и нуклеиновой кислоты, направленной против нуклеиновой кислоты), описанная в настоящей заявке, может присутствовать в композиции, которая обеспечивает по меньшей мере 0,1, 0,5, 1, 1,5, 2, 2,5 3, 3,5, 4, 4,5, 5, 5,5, 6, 6,5, 10 или более единиц активности/мг молекулы. Согласно некоторым вариантам реализации настоящего изобретения общее количество единиц активности молекулы, которые доставлены субъекту, составляет по меньшей мере 25000, 30000, 35000, 40000, 45000, 50000, 60000, 70000, 80000, 90000, 110000, 120000, 130000, 140000, 150000, 160000, 170000, 180000, 190000, 200000, 210000, 220000, 230000 или 250000, или более единиц. Согласно некоторым вариантам реализации настоящего изобретения общее количество единиц активности молекулы, которые доставлены субъекту, составляет не более чем 25000, 30000, 35000, 40000, 45000, 50000, 60000, 70000, 80000, 90000, 110000, 120000, 130000, 140000, 150000, 160000, 170000, 180000, 190000, 200000, 210000, 220000, 230000 или 250000, или более единиц.
[0476] Согласно некоторым вариантам реализации настоящего изобретения субъекту доставляют по меньшей мере приблизительно 10000 единиц активности, нормированных на 50 кг массы тела. Согласно некоторым вариантам реализации настоящего изобретения субъекту доставляют по меньшей мере приблизительно 10000, 15000, 25000, 30000, 35000, 40000, 45000, 50000, 60000, 70000, 80000, 90000, 110000, 120000, 130000, 140000, 150000, 160000, 170000, 180000, 190000, 200000, 210000, 220000, 230000, 250000 или более единиц активности молекулы, нормированных на 50 кг массы тела. Согласно некоторым вариантам реализации настоящего изобретения терапевтически эффективная доза содержит по меньшей мере 5×105, 1×106, 2×106, 3×106, 4×106, 5×106, 6×106, 7×106, 8×106, 9×106, 1×107, 1,1×107, 1,2×107, 1,5×107, 1,6×107, 1,7×107, 1,8×107, 1,9×107, 2×107, 2,1×107, или 3×107, или более единиц активности молекулы. Согласно некоторым вариантам реализации настоящего изобретения терапевтически эффективная доза составляет не более чем 5×105, 1×106, 2×106, 3×106, 4×106, 5×106, 6×106, 7×106, 8×106, 9×106, 1×107, 1,1×107, 1,2×107, 1,5×107, 1,6×107, 1,7×107, 1,8×107, 1,9×107, 2×107, 2,1×107 или 3×107 или более единиц активности молекулы.
[0477] Согласно некоторым вариантам реализации настоящего изобретения терапевтически эффективная доза составляет по меньшей мере приблизительно 10000, 15000, 20000, 22000, 24000, 25000, 30000, 40000, 50000, 60000, 70000, 80000, 90000, 100000, 125000, 150000, 200000 или 500000 единиц/кг массы тела. Согласно некоторым вариантам реализации настоящего изобретения терапевтически эффективная доза составляет не более чем приблизительно 10000, 15000, 20000, 22000, 24000, 25000, 30000, 40000, 50000, 60000, 70000, 80000, 90000, 100000, 125000, 150000, 200000 или 500000 единиц/кг массы тела.
[0478] Согласно некоторым вариантам реализации настоящего изобретения активность молекулы, доставленной субъекту, составляет по меньшей мере 10000, 11000, 12000, 13000, 14000, 20000, 21000, 22000, 23000, 24000, 25000, 26000, 27000, 28000, 30000, 32000, 34000, 35000, 36000, 37000, 40000, 45000 или 50000, или более ед./мг молекулы. Согласно некоторым вариантам реализации настоящего изобретения активность молекулы, доставленной пациенту, составляет не более чем 10000, 11000, 12000, 13000, 14000, 20000, 21000, 22000, 23000, 24000, 25000, 26000, 27000, 28000, 30000, 32000, 34000, 35000, 36000, 37000, 40000, 45000 или 50000, или более ед./мг молекулы.
[0479] Измерения фармакокинетических и фармакодинамических параметров
[0480] Фармакокинетические и фармакодинамические данные могут быть получены с помощью различных экспериментальных методик. Соответствующие компоненты фармакокинетического и фармакодинамического профиля, описывающие конкретную композицию, могут изменяться из-за различий в метаболизме лекарственного препарата у субъектов-людей. Фармакокинетические и фармакодинамические профили могут быть основаны на определении средних параметров группы субъектов. Группа субъектов включает любое обоснованное количество субъектов, подходящих для определения репрезентативного среднего значения, например, 5 субъектов, 10 субъектов, 15 субъектов, 20 субъектов, 25 субъектов, 30 субъектов, 35 субъектов или более. Среднее значение может быть определено путем расчета усредненной величины для измерений всех субъектов для каждого оцениваемого параметра. Дозу можно модулировать, чтобы достичь желаемого фармакокинетического или фармакодинамического профиля, такого как желаемый или эффективный профиль в крови, описанный в настоящей заявке.
[0481] Фармакокинетические параметры могут представлять собой любые параметры, подходящие для описания молекулы. Например, величина Cmax может составлять, например, не менее чем приблизительно 25 нг/мл; не менее чем приблизительно 50 нг/мл; не менее чем приблизительно 75 нг/мл; не менее чем приблизительно 100 нг/мл; не менее чем приблизительно 200 нг/мл; не менее чем приблизительно 300 нг/мл; не менее чем приблизительно 400 нг/мл; не менее чем приблизительно 500 нг/мл; не менее чем приблизительно 600 нг/мл; не менее чем приблизительно 700 нг/мл; не менее чем приблизительно 800 нг/мл; не менее чем приблизительно 900 нг/мл; не менее чем приблизительно 1000 нг/мл; не менее чем приблизительно 1250 нг/мл; не менее чем приблизительно 1500 нг/мл; не менее чем приблизительно 1750 нг/мл; не менее чем приблизительно 2000 нг/мл; или любое другое значение Cmax, подходящее для описания фармакокинетического профиля молекулы, описанной в настоящей заявке.
[0482] Величина Tmax молекулы, описанной в настоящей заявке, может составлять, например, не более чем приблизительно 0,5 часа, не более чем приблизительно 1 час, не более чем приблизительно 1,5 часа, не более чем приблизительно 2 часа, не более чем приблизительно 2,5 часа, не более чем приблизительно 3 часа, не более чем приблизительно 3,5 часа, не более чем приблизительно 4 часа, не более чем приблизительно 4,5 часа, не более чем приблизительно 5 часов, или любое другое значение Tmax, подходящее для описания фармакокинетического профиля молекулы, описанной в настоящей заявке.
[0483] Величина AUC(0-∞) молекулы, описанной в настоящей заявке, может составлять, например, не менее чем приблизительно 50 нг⋅ч/мл, не менее чем приблизительно 100 нг⋅ч/мл, не менее чем приблизительно 150 нг⋅ч/мл, не менее чем приблизительно 200 нг⋅ч/мл, не менее чем приблизительно 250 нг⋅ч/мл, не менее чем приблизительно 300 нг⋅ч/мл, не менее чем приблизительно 350 нг⋅ч/мл, не менее чем приблизительно 400 нг⋅ч/мл, не менее чем приблизительно 450 нг⋅ч/мл, не менее чем приблизительно 500 нг⋅ч/мл, не менее чем приблизительно 600 нг⋅ч/мл, не менее чем приблизительно 700 нг⋅ч/мл, не менее чем приблизительно 800 нг⋅ч/мл, не менее чем приблизительно 900 нг⋅ч/мл, не менее чем приблизительно 1000 нг⋅ч/мл, не менее чем приблизительно 1250 нг⋅ч/мл, не менее чем приблизительно 1500 нг⋅ч/мл, не менее чем приблизительно 1750 нг⋅ч/мл, не менее чем приблизительно 2000 нг⋅ч/мл, не менее чем приблизительно 2500 нг⋅ч/мл, не менее чем приблизительно 3000 нг⋅ч/мл, не менее чем приблизительно 3500 нг⋅ч/мл, не менее чем приблизительно 4000 нг⋅ч/мл, не менее чем приблизительно 5000 нг⋅ч/мл, не менее чем приблизительно 6000 нг⋅ч/мл, не менее чем приблизительно 7000 нг⋅ч/мл, не менее чем приблизительно 8000 нг⋅ч/мл, не менее чем приблизительно 9000 нг⋅ч/мл, не менее чем приблизительно 10000 нг⋅ч/мл, или любое другое значение AUC(0-∞), подходящее для описания фармакокинетического профиля молекулы, описанной в настоящей заявке.
[0484] Концентрация в плазме крови молекулы, описанной в настоящей заявке, приблизительно через один час после введения может составлять, например, не менее чем приблизительно 25 нг/мл, не менее чем приблизительно 50 нг/мл, не менее чем приблизительно 75 нг/мл, не менее чем приблизительно 100 нг/мл, не менее чем приблизительно 150 нг/мл, не менее чем приблизительно 200 нг/мл, не менее чем приблизительно 300 нг/мл, не менее чем приблизительно 400 нг/мл, не менее чем приблизительно 500 нг/мл, не менее чем приблизительно 600 нг/мл, не менее чем приблизительно 700 нг/мл, не менее чем приблизительно 800 нг/мл, не менее чем приблизительно 900 нг/мл, не менее чем приблизительно 1000 нг/мл, не менее чем приблизительно 1200 нг/мл, или любую другую концентрацию в плазме крови молекулы, описанной в настоящей заявке.
[0485] Фармакодинамические параметры могут представлять собой любые параметры, подходящие для описания фармацевтических композиций согласно настоящему изобретению. Например, фармакодинамический профиль может демонстрировать снижение факторов, связанных с воспалением, через, например, приблизительно 2 часа, приблизительно 4 часа, приблизительно 8 часов, приблизительно 12 часов или приблизительно 24 часа.
[0486] Фармацевтически приемлемые соли
[0487] В настоящем изобретении предложено применение фармацевтически приемлемых солей любой молекулы, описанной в настоящей заявке. Фармацевтически приемлемые соли могут включать, например, соли присоединения кислоты и соли присоединения основания. Кислота, которую добавляют к соединению для образования соли присоединения кислоты, может представлять собой органическую кислоту или неорганическую кислоту. Основание, которое добавляют к соединению для образования соли присоединения основания, может представлять собой органическое основание или неорганическое основание. Согласно некоторым вариантам реализации настоящего изобретения фармацевтически приемлемой солью является соль металла. Согласно некоторым вариантам реализации настоящего изобретения фармацевтически приемлемой солью является соль аммония.
[0488] Соли металлов могут образоваться в результате добавления неорганического основания к соединению согласно настоящему изобретению. Неорганическое основание состоит из катиона металла, спаренного с основным противоионом, таким как, например, гидроксид, карбонат, бикарбонат или фосфат. Металл может представлять собой щелочной металл, щелочноземельный металл, переходный металл или металл основной группы. Согласно некоторым вариантам реализации настоящего изобретения металл представляет собой литий, натрий, калий, цезий, церий, магний, марганец, железо, кальций, стронций, кобальт, титан, алюминий, медь, кадмий или цинк.
[0489] Согласно некоторым вариантам реализации настоящего изобретения соль металла представляет собой соль лития, соль натрия, соль калия, соль цезия, соль церия, соль магния, соли марганца, соль железа, соль кальция, соль стронция, соль кобальта, соль титана, соль алюминия, соль меди, соль кадмия или соль цинка, или любую их комбинацию.
[0490] Соли аммония могут образоваться при добавлении аммиака или органического амина к соединению согласно настоящему изобретению. Согласно некоторым вариантам реализации настоящего изобретения органический амин представляет собой триэтиламин, диизопропиламин, этаноламин, диэтаноламин, триэтаноламин, морфолин, N-метилморфолин, пиперидин, N-метилпиперидин, N-этилпиперидин, дибензиламин, пиперазин, пиридин, пирразол, пипирразол, имидазол, пиразин, или пипиразин, или любую их комбинацию.
[0491] Согласно некоторым вариантам реализации настоящего изобретения соль аммония представляет собой соль триэтиламина, соль диизопропиламина, соль этаноламина, соль диэтаноламина, соль триэтаноламина, соль морфолина, соль N-метилморфолина, соль пиперидина, соль N-метилпиперидина, соль N-этилпиперидина, соль дибензиламина, соль пиперазина, соль пиридина, соль пирразола, соль пипирразола, соль имидазола, соль пиразина или соль пиперазина, или любую их комбинацию.
[0492] Соли присоединения кислоты могут образоваться в результате добавления кислоты к молекуле согласно настоящему изобретению. Согласно некоторым вариантам реализации настоящего изобретения кислота представляет собой органическую кислоту. Согласно некоторым вариантам реализации настоящего изобретения кислота представляет собой неорганическую кислоту. Согласно некоторым вариантам реализации настоящего изобретения кислота представляет собой хлористоводородную кислоту, бромистоводородную кислоту, иодистоводородную кислоту, азотную кислоту, азотистую кислоту, серную кислоту, сернистую кислоту, фосфорную кислоту, изоникотиновую кислоту, молочную кислоту, салициловую кислоту, винную кислоту, аскорбиновую кислоту, гентизиновую кислоту, глюконовую кислоту, глюкуроновую кислоту, сахаристую кислоту, муравьиную кислоту, бензойную кислоту, глутаминовую кислоту, пантотеновую кислоту, уксусную кислоту, пропионовую кислоту, масляную кислоту, фумаровую кислоту, янтарную кислоту, метансульфоновую кислоту, этансульфоновую кислоту, бензолсульфоновую кислоту, п-толуолсульфоновую кислоту, лимонную кислоту, щавелевую кислоту или малеиновую кислоту, или любую их комбинацию.
[0493] Согласно некоторым вариантам реализации настоящего изобретения соль представляет собой гидрохлоридную соль, гидробромидную соль, гидроиодидную соль, нитратную соль, нитритную соль, сульфатную соль, сульфитную соль, фосфатную соль, изоникотинатную соль, лактатную соль, салицилатную соль, тартратную соль, аскорбатную соль, гентизинатную соль, глюконатную соль, глюкуронатную соль, сахаристую соль, формиатную соль, бензоатную соль, глутаматную соль, пантотенатную соль, ацетатную соль, пропионатную соль, бутиратную соль, фумаратную соль, сукцинатную соль, метансульфонатную соль, этансульфонатную соль, бензолсульфонатную соль, п-толуолсульфонатную соль, цитратную соль, оксалатную соль или малеатную соль, или любую их комбинацию.
[0494] Сконструированные сайт-направленные полипептиды
[0495] Общий обзор
[0496] В настоящем изобретении предложены способы, композиции, системы и/или наборы для модификации сайт-направленных полипептидов (например, Cas9, Csy4, Cas5, Cas6, Argonaute, и т.д.) и/или родственных ферментов. Модификации могут включать любую ковалентную или нековалентную модификацию сайт-направленных полипептидов. В некоторых случаях такие модификации могут включать химические модификации одной или более областей сайт-направленного полипептида. В некоторых случаях модификации могут включать консервативные или неконсервативные замены аминокислот в сайт-направленном полипептиде. В некоторых случаях модификации могут включать добавление, делецию или замену любой части сайт-направленного полипептида аминокислотами, пептидами или доменами, которые не обнаружены в нативном сайт-направленном полипептиде. В некоторых случаях один или более ненативных доменов могут быть добавлены, удалены или замещены в сайт-направленном полипептиде. В некоторых случаях сайт-направленный полипептид может существовать в виде гибридного белка.
[0497] В некоторых случаях настоящее изобретение обеспечивает способ конструирования сайт-направленного полипептида для распознавания желаемой последовательности нуклеиновой кислоты-мишени с желаемой ферментативно специфичностью и/или активностью. Модификации сайт-направленного полипептида можно осуществлять с помощью методов конструирования белков. Методы конструирования белков могут включать гибридизацию функциональных доменов с указанным сконструированным сайт-направленным полипептидом, которую можно использовать для модификации функционального состояния всего сайт-направленного полипептида или реальной последовательности нуклеиновой кислоты-мишени эндогенного клеточного локуса. Сайт-направленный полипептид согласно настоящему изобретению можно использовать для регулирования экспрессии эндогенного гена посредством как активации, так и репрессии транскрипции эндогенного гена.
[0498] Гибридный сайт-направленный полипептид также может быть связан с другими регуляторными или функциональными доменами, например, нуклеазами, транспозазами или метилазами, для модификации эндогенных хромосомных последовательностей. В некоторых случаях сайт-направленный полипептид может быть связан с по меньшей мере одним или более регуляторными доменами, описанными в настоящей заявке. Неограничивающие примеры регуляторных или функциональных доменов включают домены репрессора или активатора фактора транскрипции, такие как KRAB и VP16, домены корепрессора и коактиватора, ДНК-метилтрансферазы, гистонацетилтрансферазы, гистондеацетилазы и домены расщепления ДНК, такие как домен расщепления из эндонуклеазы FokI.
[0499] В некоторых случаях один или более специфичных доменов, областей или структурных элементов сайт-направленного полипептида могут быть модифицированы вместе. Модификации сайт-направленного полипептида могут произойти, но не ограничиваются ими, в элементах сайт-направленного полипептида, таких как области, которые распознают или связываются с мотивом, прилегающим к протоспейсеру (РАМ), и/или области, которые распознают или связываются с нуклеиновой кислотой, направленной против нуклеиновой кислоты. Такие элементы, способные к связыванию или распознаванию, могут включать консервативную F-спираль, сильноосновную область, N-концевую область, С-концевую область, мотивы RuvC (например, RuvC и/или RuvC-подобные нуклеазые домены) и один или более нуклеазных доменов, таких как HNH и/или HNH-подобные домены. Модификации могут быть сделаны в дополнительных доменах, структурных элементах, последовательности или аминокислотных остатках в пределах сайт-направленного полипептида.
[0500] Модификации одной или более областей сайт-направленного полипептида могут быть осуществлены, чтобы изменить различные свойства сайт-направленного полипептида. В некоторых случаях модификации могут изменить способность распознавать и связываться с определенными последовательностями нуклеиновых кислот-мишеней. Такие изменения могут включать, но не ограничивается ими, увеличение аффинности связывания и/или специфичности в отношении некоторых последовательностей или предпочтительное направленное действие на определенные последовательности нуклеиновых кислот-мишеней/распознающие элементы. В некоторых случаях модификации можно использовать для изменения нативной нуклеазной функции. В некоторых случаях модификации сайт-направленного полипептида способны изменить специфичность в отношении РАМ, специфичность tracrPHK, специфичность crPHK или специфичность в отношении дополнительных элементов нуклеиновых кислот, таких как нуклеиновая кислота, направленная против нуклеиновой кислоты.
[0501] В настоящей заявке также описаны композиции и способы, включающие гибридные белки, содержащие сайт-направленный полипептид (например, Cas9), и один или более доменов или областей, сконструированных для изменения генома (например, расщепление генов; изменение генов, например, путем расщепления с последующей вставкой (физическая вставка или вставка с помощью гомологичной репарации) экзогенной последовательности и/или расщепление с последующей NHEJ; частичная или полная инактивация одного или более генов, создание аллелей с измененными функциональными состояниями эндогенных генов, вставка регуляторных элементов; и т.д.), и изменения генома, которые осуществляют в зародышевой линии. В настоящем изобретении также предложены способы получения и применения указанных композиций (т.е. реагентов), например, для корректировки (изменения) одного или более генов в клетке-мишени. Следовательно, способы и композиции, описанные в настоящей заявке, обеспечивают высокоэффективные способы целевого изменения гена (например, вставки) и/или блокирования (частичного или полного) одного или более генов и/или рандомизированного мутагенеза последовательности любого аллеля-мишени, и, следовательно, обеспечивают получение животных моделей заболеваний человека. Специалист в данной области техники поймет, что, несмотря на то, что термины «геномная инженерия» или «изменение генома» часто используются для описания способов, предложенных в настоящей заявке, способы и композиции, описанные в настоящей заявке, также можно использовать для изменения любой нуклеиновой кислоты-мишени, которая по существу может не относиться к геному клетки (например, могут быть использованы на синтетической нуклеиновой кислоте, плазмиде, векторе, вирусной нуклеиновой кислоте, рекомбинантной нуклеиновой кислоте и т.д.).
[0502] Способы и композиции, описанные в настоящей заявке, обеспечивают новые виды терапевтического применения (например, профилактика и/или лечение: генетических заболеваний, рака, грибковых, бактериальных, протозойных и вирусных инфекций, ишемии, сосудистого заболевания, артрита, иммунологических нарушений и т.д.), новые методы диагностики (например, прогнозирование и/или диагностика состояния), а также обеспечивают научно-исследовательские инструменты (например, наборы, количественные методы для функционального исследования генома и способы получения сконструированных клеточных линий и моделей животных для исследований и скрининга лекарственных препаратов) и средства для разработки растений с измененными фенотипами, включая, но не ограничиваясь ими, повышенную устойчивость к заболеваниям, и изменение характеристик созревания фруктов, композиции сахаров и масел, урожайности и цвета. Способы и композиции, описанные в настоящей заявке, обеспечивают новые эпигенетические исследования.
[0503] Модификации и конструирование белков
[0504] Изменения аминокислот
[0505] Сайт-направленные полипептиды, описанные в настоящей заявке, могут быть модифицированы. Модификация может включать модификации аминокислотных остатков в сайт-направленном полипептиде. Модификации могут изменить первичную аминокислотную последовательность и/или вторичную, третичную и четвертичную структуру аминокислотной последовательности. В некоторых случаях некоторые аминокислотные последовательности сайт-направленного полипептида согласно настоящему изобретению можно изменять без существенного влияния на структуру или функцию белка. Тип мутации может совершенно не иметь значения, если изменение происходит в некоторых областях (например, некритических) белка. В некоторых случаях, в зависимости от расположения замены, мутация может не оказывать существенного влияния на биологические свойства полученного варианта. Например, свойства и функции вариантов Cas9 могут быть аналогичны таковым для Cas9 дикого типа. В некоторых случаях мутация может критически влиять на структуру и/или функцию сайт-направленного полипептида.
[0506] Положение, в котором может быть проведена модификация сайт-направленного полипептида (например, варианта Cas9), может быть определено с использованием выравнивания последовательностей и/или структур. Выравнивание последовательностей может обеспечить идентификацию сходных или различных областей полипептида (например, консервативных, неконсервативных, гидрофобных, гидрофильных и т.д.). В некоторых случаях для модификации подходит область в последовательности, представляющей интерес, которая сходна с другими последовательностями. В некоторых случаях для модификации подходит область в последовательности, представляющей интерес, которая отлична от других последовательностей. Например, выравнивание последовательностей может быть выполнено с помощью поиска в базе данных, попарного выравнивания, множественного выравнивания, геномного анализа, поиска мотивов, сравнительной оценки и/или с использованием программы, такой как BLAST, CS-BLAST, HHPRED, psi-BLAST, LALIGN, PyMOL и SEQALN. Структурное выравнивание может быть выполнено с помощью таких программ как Dali, PHYRE, Chimera, COOT&O и PyMOL. Выравнивание может быть выполнено путем поиска в базе данных, попарного выравнивания, множественного выравнивания, геномного анализа, поиска мотивов или сравнительной оценки, или любой их комбинации.
[0507] Сайт-направленный полипептид может быть модифицирован для увеличения специфичности связывания с нуклеиновой кислотой, направленной против нуклеиновой кислоты, и/или с нуклеиновой кислотой-мишенью. Сайт-направленный полипептид может быть модифицирован для увеличения связывания с конкретными областями нуклеиновой кислоты, направленной против нуклеиновой кислоты (например, удлиненной последовательностью спейсера, спейсером, минимальным повтором CRISPR, минимальной последовательностью tracrPHK, последовательностью 3'-tracrPHK, удлиненной последовательностью tracrPHK) и/или нуклеиновой кислотой-мишенью.
[0508] В некоторых случаях модификация может включать консервативную модификацию. Консервативная замена аминокислоты может включать замену одной из семейства аминокислот, которые родственны по своим боковым цепям (например, цистеин/серин).
[0509] В некоторых случаях замены аминокислот в белке Cas9 согласно настоящему изобретению представляют собой неконсервативные замены аминокислот (т.е. замены несходных заряженных или незаряженных аминокислот). Неконсервативная замена аминокислоты может включать замену одной из семейства аминокислот, которые могут быть неродственными по своим боковым цепям, или замену, которая изменяет биологическую активность сайт-направленного полипептида.
[0510] Мутация аминокислот также может изменить селективность связывания с нуклеиновой кислотой-мишенью. Мутация может привести к изменению, которое может включать изменение константы диссоциации (Kd) для связывания мутированного сайт-направленного полипептида с нуклеиновой кислотой-мишенью. Величина Kd для связывания мутированного сайт-направленного полипептида с нуклеиновой кислотой-мишенью может увеличиться или уменьшиться более чем в 1000 раз, более чем в 500 раз, более чем в 100 раз, более чем в 50 раз, более чем в 25 раз, более чем в 10 раз, более чем в 5 раз, более чем в 4 раза, более чем в 3 раза, более чем в 2 раза по сравнению с величиной Kd для связывания немутированного сайт-направленного полипептида с нуклеиновой кислотой-мишенью. Величина Kd для связывания мутированного сайт-направленного полипептида с нуклеиновой кислотой-мишенью может увеличиться или уменьшиться менее чем в 1000 раз, менее чем в 500 раз, менее чем в 100 раз, менее чем в 50 раз, менее чем в 25 раз, менее чем в 10 раз, менее чем в 5 раз, менее чем в 4 раза, менее чем в 3 раза, менее чем в 2 раза по сравнению с величиной Kd для связывания немутированного сайт-направленного полипептида с нуклеиновой кислотой-мишенью.
[0511] Мутация может привести к изменению, которое может включать изменение величины Kd для связывания мутированного сайт-направленного полипептида с мотивом РАМ. Величина Kd для связывания мутированного сайт-направленного полипептида с мотивом РАМ может увеличиться или уменьшиться более чем в 1000 раз, более чем в 500 раз, более чем в 100 раз, более чем в 50 раз, более чем в 25 раз, более чем в 10 раз, более чем в 5 раз, более чем в 4 раза, более чем в 3 раза, более чем в 2 раза по сравнению с величиной Kd для связывания немутированного сайт-направленного полипептида с мотивом РАМ. Величина Kd для связывания мутированного сайт-направленного полипептида с мотивом РАМ может увеличиться или уменьшиться менее чем в 1000 раз, менее чем в 500 раз, менее чем в 100 раз, менее чем в 50 раз, менее чем в 25 раз, менее чем в 10 раз, менее чем в 5 раз, менее чем в 4 раза, менее чем в 3 раза, менее чем в 2 раза по сравнению с величиной Kd для связывания немутированного сайт-направленного полипептида с мотивом РАМ.
[0512] Мутация может привести к изменению, которое может включать изменение величины Kd для связывания мутированного сайт-направленного полипептида с нуклеиновой кислотой, направленной против нуклеиновой кислоты. Величина Kd для связывания мутированного сайт-направленного полипептида с нуклеиновой кислотой, направленной против нуклеиновой кислоты, может увеличиться или уменьшиться более чем в 1000 раз, более чем в 500 раз, более чем в 100 раз, более чем в 50 раз, более чем в 25 раз, более чем в 10 раз, более чем в 5 раз, более чем в 4 раза, более чем в 3 раза, более чем в 2 раза по сравнению с величиной Kd для связывания немутированного сайт-направленного полипептида с нуклеиновой кислотой, направленной против нуклеиновой кислоты. Величина Kd для связывания мутированного сайт-направленного полипептида с нуклеиновой кислотой, направленной против нуклеиновой кислоты, может увеличиться или уменьшиться менее чем в 1000 раз, менее чем в 500 раз, менее чем в 100 раз, менее чем в 50 раз, менее чем в 25 раз, менее чем в 10 раз, менее чем в 5 раз, менее чем в 4 раза, менее чем в 3 раза, менее чем в 2 раза по сравнению с величиной Kd для связывания немутированного сайт-направленного полипептида с нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0513] Мутация сайт-направленного полипептида также может изменить кинетику ферментативного действия сайт-направленного полипептида. Мутация может привести к изменению величины Km мутированного сайт-направленного полипептида. Величина Km мутированного сайт-направленного полипептида может увеличиться или уменьшиться более чем в 1000 раз, более чем в 500 раз, более чем в 100 раз, более чем в 50 раз, более чем в 25 раз, более чем в 10 раз, более чем в 5 раз, более чем в 4 раза, более чем в 3 раза, более чем в 2 раза по сравнению с величиной Km немутированного сайт-направленного полипептида. Величина Km мутированного сайт-направленного полипептида может увеличиться или уменьшиться менее чем в 1000 раз, менее чем в 500 раз, менее чем в 100 раз, менее чем в 50 раз, менее чем в 25 раз, менее чем в 10 раз, менее чем в 5 раз, менее чем в 4 раза, менее чем в 3 раза, менее чем в 2 раза по сравнению с величиной Km немутированного сайт-направленного полипептида.
[0514] Мутация сайт-направленного полипептида может привести к изменению, которое может включать изменение метаболизма сайт-направленного полипептида. Скорость метаболизма мутированного сайт-направленного полипептида может увеличиться или уменьшиться более чем в 1000 раз, более чем в 500 раз, более чем в 100 раз, более чем в 50 раз, более чем в 25 раз, более чем в 10 раз, более чем в 5 раз, более чем в 4 раза, более чем в 3 раза, более чем в 2 раза по сравнению со скоростью метаболизма немутированного сайт-направленного полипептида. Скорость метаболизма мутированного сайт-направленного полипептида может увеличиться или уменьшиться менее чем в 1000 раз, менее чем в 500 раз, менее чем в 100 раз, менее чем в 50 раз, менее чем в 25 раз, менее чем в 10 раз, менее чем в 5 раз, менее чем в 4 раза, менее чем в 3 раза, менее чем в 2 раза по сравнению со скоростью метаболизма немутированного сайт-направленного полипептида.
[0515] Мутация может привести к изменению, которое может включать изменение величины ΔG ферментативного действия сайт-направленного полипептида. Величина ΔG мутированного сайт-направленного полипептида может увеличиться или уменьшиться более чем в 1000 раз, более чем в 500 раз, более чем в 100 раз, более чем в 50 раз, более чем в 25 раз, более чем в 10 раз, более чем в 5 раз, более чем в 4 раза, более чем в 3 раза, более чем в 2 раза по сравнению с величиной ΔG немутированного сайт-направленного полипептида. Величина ΔG мутированного сайт-направленного полипептида может увеличиться или уменьшиться менее чем в 1000 раз, менее чем в 500 раз, менее чем в 100 раз, менее чем в 50 раз, менее чем в 25 раз, менее чем в 10 раз, менее чем в 5 раз, менее чем в 4 раза, менее чем в 3 раза, менее чем в 2 раза по сравнению с величиной ΔG немутированного сайт-направленного полипептида.
[0516] Мутация может привести к изменению, которое включает изменение величины Vmax ферментативного действия сайт-направленного полипептида. Величина Vmax мутированного сайт-направленного полипептида может увеличиться или уменьшиться более чем в 1000 раз, более чем в 500 раз, более чем в 100 раз, более чем в 50 раз, более чем в 25 раз, более чем в 10 раз, более чем в 5 раз, более чем в 4 раза, более чем в 3 раза, более чем в 2 раза по сравнению с величиной Vmax немутированного сайт-направленного полипептида. Величина Vmax мутированного сайт-направленного полипептида может увеличиться или уменьшиться менее чем в 1000 раз, менее чем в 500 раз, менее чем в 100 раз, менее чем в 50 раз, менее чем в 25 раз, менее чем в 10 раз, менее чем в 5 раз, менее чем в 4 раза, менее чем в 3 раза, менее чем в 2 раза по сравнению с величиной Vmax немутированного сайт-направленного полипептида.
[0517] Мутация может привести к изменению, которое может включать изменение любого кинетического параметра сайт-направленного полипептида. Мутация может привести к изменению любого термодинамического параметра сайт-направленного полипептида. Мутация может привести к изменению поверхностного заряда, площади неэкспонируемой поверхности, и/или кинетики складывания сайт-направленного полипептида и/или ферментативного действия сайт-направленного полипептида.
[0518] Аминокислоты в сайт-направленном полипептиде согласно настоящему изобретению, которые имеют критическое значение для его функции, могут быть определены с помощью таких методов как сайт-направленный мутагенез, аланин-сканирующий мутагенез, анализ структуры белка, ядерный магнитный резонанс, фотоаффинное мечение и электронная томография, высокопроизводительный скрининг, ИФА, биохимические количественные исследования, количественные исследования связывания, количественные исследования с использованием расщепления (например, количественное исследование с использованием нуклеазы Surveyor), количественные исследования с использованием репортера и т.п.
[0519] Другие изменения аминокислот также могут включать аминокислоты с гликозилированными формами, агрегированные конъюгаты с другими молекулами и ковалентные конъюгаты с неродственными химическими фрагментами (например, пегилированные молекулы). Ковалентные варианты могут быть получены путем присоединения функциональных фрагментов к группам, которые присутствуют в аминокислотной цепи или в N- или С-концевом остатке. В некоторых случаях мутированные сайт-направленные полипептиды также могут включать аллельные варианты и видоспецифичные варианты.
[0520] Могут быть сконструированы укорочения областей, которые не влияют на функциональную активность белков Cas9. Могут быть сконструированы укорочения областей, которые влияют на функциональную активность белков Cas9. Область может быть укорочена менее чем на 5, менее чем на 10, менее чем на 15, менее чем на 20, менее чем на 25, менее чем на 30, менее чем на 35, менее чем на 40, менее чем на 45, менее чем на 50, менее чем на 60, менее чем на 70, менее чем на 80, менее чем на 90, менее чем на 100 или более аминокислот. Область может быть укорочена более чем на 5, более чем на 10, более чем на 15, более чем на 20, более чем на 25, более чем на 30, более чем на 35, более чем на 40, более чем на 45, более чем на 50, более чем на 60, более чем на 70, более чем на 80, более чем на 90, более чем на 100 или более аминокислот. Укороченная область может составлять приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% сайт-направленного полипептида.
[0521] Могут быть сконструированы делеции областей, которые не влияют на функциональную активность белков Cas9. Могут быть сконструированы делеции областей, которые влияют на функциональную активность белков Cas9. Делеция может включать делецию менее чем 5, менее чем 10, менее чем 15, менее чем 20, менее чем 25, менее чем 30, менее чем 35, менее чем 40, менее чем 45, менее чем 50, менее чем 60, менее чем 70, менее чем 80, менее чем 90, менее чем 100 или более аминокислот. Делеция может включать делецию более чем 5, более чем 10, более чем 15, более чем 20, более чем 25, более чем 30, более чем 35, более чем 40, более чем 45, более чем 50, более чем 60, более чем 70, более чем 80, более чем 90, более чем 100 или более аминокислот. Делеция может включать делецию приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% сайт-направленного полипептида. Делеция может происходить в N-конце, С-конце или в любой области полипептидной цепи.
[0522] Способы скрининга
[0523] В настоящем изобретении предложены способы конструирования сайт-направленного полипептида. Для конструирования сайт-направленного полипептида можно использовать способы скрининга. Например, скрининг может быть проведен, чтобы определить влияние мутаций в области сайт-направленного полипептида. Например, скрининг может быть проведен, чтобы испытать влияние модификаций сильноосновного участка на аффинность в отношении структуры РНК (например, структуры нуклеиновой кислоты, направленной против нуклеиновой кислоты) или способность к расщеплению (например, расщеплению нуклеиновой кислоты-мишени). Примеры способов скрининга могут включать, но не ограничиваются ими, методы сортировка клеток, дисплей мРНК, фаговый дисплей и направленную эволюцию.
[0524] Гибридные последовательности
[0525] В некоторых случаях сайт-направленный полипептид модифицирован так, что он содержит ненативную последовательность (т.е. полипептид имеет модификацию, которая приводит к его изменению относительно аллеля или последовательности, из которой он был получен) (например, полипептид может быть назван гибридной последовательностью). Ненативная последовательность также может содержать один или более дополнительных белков, белковых доменов, поддоменов или полипептидов. Например, Cas9 может быть гибридизован с любыми подходящими дополнительными ненативными белками и/или доменами, связывающими нуклеиновую кислоту, включая, но не ограничиваясь ими, домены факторов транскрипции, нуклеазные домены, домены, полимеризующие нуклеиновые кислоты. Ненативная последовательность может содержать последовательность Cas9 и/или гомолога Cas9.
[0526] Ненативная последовательность может придать гибридному белку новые функции. Эти функции могут включать, например, расщепление ДНК, метилирование ДНК, повреждение ДНК, репарацию ДНК, модификацию полипептида-мишени, связанного с ДНК-мишенью (например, гистона, ДНК-связывающего белка и т.д.), что приводит, например, к метилированию гистонов, ацетилированию гистонов, убиквитинированию гистонов и т.п. Другие функции, которые придает гибридный белок, могут включать метилтрансферазную активность, деметилазную активность, дезаминазную активность, дисмутазную активность, алкилирующую активность, депуринизирующую активность, оксидазную активность, активность в отношении образования димеров пиримидина, интегразную активность, транспозазную активность, рекомбиназную активность, полимеразную активность, лигазную активность, геликазную активность, фотолиазную активность, гликозилазную активность, ацетилтрансферазную активность, деацетилазную активность, киназную активность, фосфатазную активность, убиквитинлигазную активность, деубиквитиназную активность, аденилирующую активность, деаденилирующую активность, активность в отношении присоединения SUMO, активность в отношении удаления SUMO, рибозилирующую активность, дерибозилирующую активность, миристоилирующую активность, ремоделирующую активность, протеазную активность, оксидоредуктазную активность, трансферазную активность, гидролазную активность, лиазную активность, изомеразную активность, синтазную активность, синтетазную активность и демиристоилирующую активность, или любую их комбинацию.
[0527] Модификации F-спирали
[0528] В некоторых случаях область F-спирали Cas9 может быть модифицирована (например, чтобы изменить специфичность РАМ). В некоторых случаях F-спираль может быть гомологична F-спирали, выявленной в белке Cas9 из S. pyogenes (остатки 551-566). В некоторых случаях F-спираль может быть по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологична остаткам 551-556 F-спирали Cas9 из S. pyogenes. В некоторых случаях F-спираль может быть не более чем на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологична остаткам 551-556 F-спирали Cas9 из S. pyogenes.
[0529] В некоторых случаях модификации F-спирали могут включать, но не ограничивается ими, модификации отдельных аминокислот, описанные в настоящей заявке. В некоторых случаях модификации F-спирали могут включать, но не ограничиваются ими, вставки, делеции или замены отдельных аминокислот, или полипептидов, например, таких как другие элементы белка (например, домены, структурные мотивы, белки).
[0530] Модификации могут включать модификации по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот F-спирали. Модификации могут включать модификации не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот F-спирали. Модификации также могут включать по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% F-спирали. Модификации также могут включать не более чем 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% F-спирали.
[0531] В некоторых случаях модификации последовательностей F-спирали сайт-направленного полипептида могут включать конкретные структурные мотивы полипептида, включая, но не ограничиваясь ими, альфа-спираль, бета-цепь, бета-лист, 310-спираль, пи-спираль, мотив полипролина I, мотив полипролина II, мотив полипролина III, бета-поворот, альфа спираль-поворот-альфа спираль или перегибы спирали или шарниры. Например, замены в F-спирали сайт-направленного полипептида могут включать замену или добавление одного или более остатков аминокислоты пролина. Введение остатков пролина может создавать перегибы F-спирали, которые могут изменить специфичность связывания F-спирали в отношении РАМ. В другом примере, замена или добавление может включать один или более остатков аминокислоты глицина. Вставка или замещение остатками глицина может придать повышенную гибкость F-спирали, или «шарнирам», которые также могут изменять специфичность связывания F-спирали в отношении РАМ. Изменение специфичности связывания может повлиять на ферментативную активность белка Cas9 или может не оказывать на нее влияния.
[0532] В некоторых случаях модификации последовательностей F-спирали сайт-направленного полипептида могут включать делецию по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% F-спирали. В некоторых случаях модификации последовательностей F-спирали сайт-направленного полипептида могут включать делению не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% F-спирали.
[0533] В некоторых случаях модификации последовательностей F-спирали сайт-направленного полипептида могут включать добавление или замену по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичной F-спирали сайт-направленного полипептида. В некоторых случаях модификации последовательностей F-спирали сайт-направленного полипептида могут включать добавление или замену не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичной F-спирали сайт-направленного полипептида.
[0534] Например, ненативные F-спирали Cas9 могут быть получены из любого подходящего организма. В некоторых случаях белок Cas9 и F-спираль могут быть получены из прокариотического организма, включая, но не ограничиваясь ими, архей, бактерии, простейших (например, Е. coli, S. pyogenes, S. thermophilus, P. furiosus и т.д.).
[0535] Например, F-спираль фермента Cas9 из S. pyogenes может быть замещена или содержать в качестве компонента F-спираль или ее фрагмент, полученный из другого фермента Cas9 из другого вида.
[0536] В некоторых случаях сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и модифицированную F-спираль.
[0537] Модификации сильноосновного участка
[0538] Дополнительные области в белке Cas9 также могут влиять на связывание и специфичность в отношении РАМ. В некоторых случаях сильноосновный участок или область, включающая остатки основных аминокислот, смежных с сайтом связывания РАМ, также может быть модифицирована, чтобы изменить специфичность в отношении РАМ. В некоторых случаях сильноосновный участок или область может быть гомологична сильноосновному участку, выявленному в Cas9 из S. pyogenes, который расположен в N-концевой области, или аминокислотным остаткам 1-270 Cas9 из S. pyogenes. В некоторых случаях сильноосновный участок может быть по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичен сильноосновному участку Cas9 из S. pyogenes. В некоторых случаях сильноосновный участок может быть не более чем на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичен сильноосновному участку Cas9 из S. pyogenes.
[0539] В некоторых случаях модификации сильноосновного участка могут включать, но не ограничиваются ими, модификации отдельных аминокислот, описанные в настоящей заявке. В некоторых случаях модификация сильноосновного участка может включать, но не ограничивается ими, вставки, делеции или замены отдельных аминокислот, полипептидов, например, других элементов белка (например, доменов, структурных мотивов, белков).
[0540] Модификации могут включать модификации по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50 или более аминокислот сильноосновного участка. Модификации могут включать модификации не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 21, 42, 43, 44, 45, 46, 47, 48, 49, 50 или более аминокислот сильноосновного участка. Модификации также могут включать по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%. 85%, 90%, 95%, 98%, 99% или 100% сильноосновного участка. Модификации также могут включать не более чем 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% сильноосновного участка.
[0541] В некоторых случаях модификации последовательности сильноосновного участка сайт-направленного полипептида могут включать конкретные полипептидные структурные мотивы, включая, но не ограничиваясь ими, альфа-спираль, бета-цепь, бета-лист, 310-спираль, пи-спираль, мотив полипролина I, мотив полипролина II, мотив полипролина III, бета-поворот, альфа спираль-поворот-альфа спираль, или перегибы спирали или шарниры.
[0542] Замены в сильноосновном участке сайт-направленного полипептида могут включать замену или добавление одного или более остатков кислых аминокислот. Вставка остатков кислых аминокислот может снизить общий основный заряд этой области сайт-направленного полипептида и может изменить специфичность связывания сильноосновного участка в отношении РАМ. В другом примере замена или добавление могут включать один или более остатков основных аминокислот. Вставка или замещение остатками основных аминокислот может увеличить площадь заряда или ионную силу взаимодействия между полипептидом и нуклеиновой кислотой, а также может изменить специфичность связывания сильноосновного участка в отношении РАМ. Изменение специфичности связывания может повлиять па ферментативную активность сайт-направленного полипептида или может не оказывать на нее влияния.
[0543] В некоторых случаях модификации последовательностей сильноосновного участка сайт-направленного полипептида могут включать делецию по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% сильноосновного участка. В некоторых случаях модификации последовательностей сильноосновного участка сайт-направленного полипептида могут включать делецию не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%. 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% сильноосновного участка.
[0544] В некоторых случаях модификации последовательностей сильноосновного участка сайт-направленного полипептида могут включать добавление или замену по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичного сильноосновного участка Cas9. В некоторых случаях модификации последовательностей сильноосновного участка сайт-направленного полипептида могут включать добавление или замену не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичного сильноосновного участка Cas9.
[0545] Гомологичные последовательности сильноосновного участка Cas9 могут быть получены из любого подходящего организма. В некоторых случаях белок Cas9 может быть получен из прокариотических организмов, таких как археи, бактерии, простейшие, (например, Е. coli, S. pyogenes, S. thermophilus, P. furiosus и т.д.). Например, сильноосновный участок фермента Cas9 из S. pyogenes может быть замещен или содержать в качестве компонента сильноосновный участок, или его фрагмент, полученный из Cas9 другого вида.
[0546] В некоторых случаях сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и модифицированный сильноосновный участок.
[0547] Модификации домена HNH
[0548] В некоторых случаях домен HNH в сайт-направленном полипептиде может быть модифицирован, чтобы изменить специфичность в отношении РАМ. В некоторых случаях домен HNH может быть гомологичен домену HNH, выявленному в С-концевом домене белка Cas9 из S. pyogenes (остатки 860-1100). В некоторых случаях домен HNH может быть по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичен остаткам 551-556 домена HNH Cas9 из S. pyogenes. В некоторых случаях домен HNH может быть не более чем на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичен остаткам 860-1100 домена HNH Cas9 из S. pyogenes.
[0549] В некоторых случаях модификации домена HNH могут включать, но не ограничиваются ими, модификации отдельных аминокислот, описанные в настоящей заявке. В некоторых случаях модификации домена HNH могут включать, но не ограничиваются ими, вставки, делеции или замены отдельных аминокислот, или полипептидов, например, других элементов белка (например, доменов, структурных мотивов, белков).
[0550] Модификации могут включать модификации по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот домена HNH. Модификации могут включать модификации не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот домена HNH. Модификации также могут включать по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% домена HNH. Модификации также могут включать не более чем 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% домена HNH.
[0551] В некоторых случаях модификации последовательностей домена HNH сайт-направленного полипептида могут включать конкретные структурные мотивы полипептида, включая, но не ограничиваясь ими, альфа-спираль, бета-цепь, бета-лист, 310-спираль, пи-спираль, мотив полипролина I, мотив полипролина II, мотив полипролина III, бета-поворот, альфа спираль-поворот-альфа спираль, или перегибы спирали или шарниры.
[0552] Замены в домене HNH сайт-направленного полипептида могут включать замену или добавление одного или более аминокислотных остатков. В некоторых случаях домен HNH может быть замещен или гибридизован с другими подходящими доменами, связывающими нуклеиновую кислоту. Домен, связывающий нуклеиновую кислоту, может содержать РНК. Такой домен может представлять собой одиночный домен, связывающий нуклеиновую кислоту. Примеры доменов, связывающих нуклеиновую кислоту, могут включать, но не ограничиваются ими, домен спираль-поворот-спираль, домен цинкового пальца, домен лейциновой молнии (bZIP), домен «крылатая спираль», домен «крылатая спираль»-поворот-спираль, домен спираль-петля-спираль, домен HMG-бокс, домен Wor3, домен иммуноглобулина, домен В3, домен TALE, домен цинкового пальца, домен мотива распознавания РНК, домен мотива связывания двухцепочечной РНК, домен связывания двухцепочечной нуклеиновой кислоты, домены связывания одноцепочечной нуклеиновой кислоты, домен KH, домен PUF, домен RGG-бокс, домен DEAD/DEAH-бокс, домен PAZ, домен Piwi и домен холодового шока, домен RNAseH, домен HNH, RuvC-подобный домен, домен RAMP, домен Cas5 и домен Cas6.
[0553] В некоторых случаях модификации последовательностей доменов HNH сайт-направленного полипептида могут включать делецию по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% домена HNH. В некоторых случаях модификации последовательностей доменов HNH сайт-направленного полипептида могут включать делецию не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% домена HNH.
[0554] В некоторых случаях модификации последовательностей доменов HNH сайт-направленного полипептида могут включать добавление или замену по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичного домена HNH Cas9. В некоторых случаях модификации последовательностей доменов HNH сайт-направленного полипептида могут включать добавление или замену не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичного домена HNH Cas9.
[0555] Гомологичные домены HNH Cas9 могут быть получены из любого подходящего организма. В некоторых случаях белок Cas9 может быть получен из прокариотических организмов, таких как археи, бактерии, простейшие (например, Е. coli, S. pyogenes, S. thermophilus, P. furiosus и т.д.). Например, домен HNH фермента Cas9 из S. pyogenes может быть замещен или содержать в качестве компонента домен HNH, или его фрагмент, полученный из фермента Cas9 другого вида. В некоторых случаях по меньшей мере один гомологичный домен HNH из Cas9 может быть вставлен в домен HNH. В некоторых случаях по меньшей мере один гомологичный домен HNH из Cas9 может образовать массив доменов HNH, содержащий по меньшей мере два домена HNH. В некоторых случаях массив доменов HNH может содержать по меньшей мере один домен HNH из Cas9 и по меньшей мере один второй домен HNH.
[0556] В некоторых случаях модификация домена HNH или HNH-подобного домена может включать вставку аналогичного или сходного домена HNH или HNH-подобного домена в тандеме (например, рядом) с доменом HNH из Cas9. HNH или HNH-подобный домен может быть вставлен в N-концевой и/или С-концевой домен HNH в Cas9. Введение одного или более HNH или HNH-подобных доменов в Cas9 можно использовать для расширения специфичности в нуклеиновой кислоте-мишени. Введение одного или более HNH или HNH-подобных доменов в Cas9 можно использовать для дублирования специфичности в нуклеиновой кислоте-мишени. Например, вставка одного или более HNH или HNH-подобных доменов может изменить структур Cas9 так, чтобы он распознавал более длинный участок нуклеиновой кислоты-мишени, распознавал другой гибрид РНК-ДНК, и/или распознавал нуклеиновую кислоту-мишень с более высокой аффинностью связывания.
[0557] В некоторых случаях сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и модифицированный домен HNH.
[0558] Модификации домена RuvC или RuvC-подобного домена
[0559] В некоторых случаях домен RuvC или RuvC-подобный домен в сайт-направленном полипептиде могут быть модифицированы, чтобы изменить специфичность в отношении РАМ. В некоторых случаях домен RuvC или RuvC-подобный домен могут быть гомологичны домену RuvC или RuvC-подобному домену, выявленному в белке Cas9 из S. pyogenes (остатки 1-270). В некоторых случаях RuvC или RuvC-подобный домен может быть по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичен остаткам 551-556 домена RuvC или RuvC-подобного домена Cas9 из S. pyogenes. В некоторых случаях RuvC или RuvC-подобный домен может быть не более чем на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичен остаткам 1-270 домена RuvC или RuvC-подобного домена Cas9 из S. pyogenes.
[0560] В некоторых случаях модификации домена RuvC или RuvC-подобного домена могут включать, но не ограничиваются ими, модификации отдельных аминокислот, описанные в настоящей заявке. В некоторых случаях модификация домена RuvC или RuvC-подобного домена может включать, но не ограничивается ими, вставки, делеции или замену отдельных аминокислот, или полипептидов, например, других элементов белка (например, доменов, структурных мотивов, белков).
[0561] Модификации могут включать модификации по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот домена RuvC или RuvC-подобного домена. Модификации могут включать модификации не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот домена RuvC или RuvC-подобного домена. Модификации также могут включать по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%. 95%, 98%, 99% или 100% домена RuvC или RuvC-подобного домена. Модификации также могут включать не более чем 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% домена RuvC или RuvC-подобного домена.
[0562] В некоторых случаях модификации последовательностей домена RuvC или RuvC-подобного домена сайт-направленного полипептида могут включать конкретные структурные мотивы полипептида, включая, по не ограничиваясь ими, альфа-спираль, бета-цепь, бета-лист, 310-спираль, пи-спираль, мотив полипролина I, мотив полипролина II, мотив полипролина III, бета-поворот, альфа спираль-поворот-альфа спираль, или перегибы спирали или шарниры.
[0563] Замены в домене RuvC или RuvC-подобном домене сайт-направленного полипептида могут включать замену или добавление одного или более аминокислотных остатков. В некоторых случаях домен RuvC или RuvC-подобный домен может быть замещен или гибридизован с другими подходящими доменами, связывающими нуклеиновую кислоту. Домен, связывающий нуклеиновую кислоту, может содержать РНК. Такой домен может представлять собой одиночный домен, связывающий нуклеиновую кислоту. Примеры доменов, связывающих нуклеиновую кислоту, могут включать, но не ограничиваются ими, домен спираль-поворот-спираль, домен цинкового пальца, домен лейциновой молнии (bZIP), домен «крылатая спираль», домен «крылатая спираль»-поворот-спираль, домен спираль-петля-спираль, домен HMG-бокс, домен Wor3, домен иммуноглобулина, домен В3, домен TALE, домен цинкового пальца, домен мотива распознавания РНК, домен мотива связывания двухцепочечной РНК, домен связывания двухцепочечной нуклеиновой кислоты, домены связывания одноцепочечной нуклеиновой кислоты, домен KH, домен PUF, домен RGG-бокс, домен DEAD/DEAH-бокс, домен PAZ, домен Piwi и домен холодового шока, домен RNAseH, домен HNH, RuvC-подобный домен, домен RAMP, домен Cas5 и домен Cas6.
[0564] В некоторых случаях модификации последовательностей домена RuvC или RuvC-подобного домена сайт-направленного полипептида могут включать делецию по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% домена RuvC или RuvC-подобного домена. В некоторых случаях модификации последовательностей домена RuvC или RuvC-подобного домена сайт-направленного полипептида могут включать делецию не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%. 85%, 90%, 95%, 98%, 99% или 100% домена RuvC или RuvC-подобного домена.
[0565] В некоторых случаях модификации последовательностей домена RuvC или RuvC-подобного домена сайт-направленного полипептида могут включать добавление или замену по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%. 60%, 65%, 70%, 75%. 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичного домена RuvC или RuvC-подобного домена Cas9. В некоторых случаях модификации последовательностей домена RuvC или RuvC-подобного домена сайт-направленного полипептида могут включать добавление или замену не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичного домена RuvC или RuvC-подобного домена Cas9.
[0566] Гомологичные домены RuvC или RuvC-подобные домены Cas9 могут быть получены из любого подходящего организма. В некоторых случаях белок Cas9 может быть получен из прокариотических организмов, таких как археи, бактерии, простейшие, (например, Е. coli, S. pyogenes, S. thermophilus, P. furiosus и т.д.). Например, домен RuvC или RuvC-подобный домен фермента Cas9 из S. pyogenes может быть замещен или содержать в качестве компонента домен RuvC или RuvC-подобный домен, или его фрагмент, полученный из другого фермента Cas9, например, из фермента Cas9 другого вида.
[0567] В некоторых случаях модификация домена RuvC или RuvC-подобного домена может содержать вставку идентичного или сходного домена RuvC или RuvC-подобного домена в тандеме (например, рядом) с доменом RuvC или RuvC-подобным доменом Cas9. Домен RuvC или RuvC-подобный домен может быть вставлен в N-концевой и/или С-концевой домен RuvC или RuvC-подобный домен в Cas9. Вставку одного или более доменов RuvC или RuvC-подобных доменов в Cas9 можно использовать для расширения специфичности в нуклеиновой кислоте-мишени. Вставку одного или более доменов RuvC или RuvC-подобных доменов в Cas9 можно использовать для дублирования специфичности в нуклеиновой кислоте-мишени. Например, вставка одного или более доменов RuvC или RuvC-подобных доменов может изменить структуру Cas9 так, чтобы распознавать более длинный участок нуклеиновой кислоты-мишени, распознавать другой гибрид РНК-ДНК, и/или распознавать нуклеиновую кислоту-мишень с более высокой аффинностью связывания.
[0568] В некоторых случаях сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и модифицированный домен RuvC.
[0569] Модификации доменов Cas9, содержащих области, гомологичные РНК-полимеразе
[0570] В некоторых случаях сайт-направленный полипептид может быть гомологичен РНК-полимеразе. Оба белка могут иметь сходные, функционально гомологичные домены, которые вовлечены в катализ связывания и манипуляции с нуклеиновыми кислотами. Например, РНК-полимераза может содержать области полипептидной последовательности, которая участвует в связывании дуплексов РНК-ДНК. В некоторых случаях эти области могут облегчить плавление дуплекса.
[0571] В некоторых случаях сайт-направленный полипептид также может содержать определенные области, которые влияют на специфичность связывания фермента с нуклеиновыми кислотами. В некоторых случаях последовательности или функции этих областей могут быть гомологичны таковым для доменов или областей, которые обнаруживаются в РНК-полимеразе. В некоторых случаях основная область N-конца сайт-направленного полипептида может связываться с tracrPHK и crPHK или одиночной РНК (sgRNA). Такая область может соответствовать области с 50 по 100 остаток в S. pyogenes.
[0572] В целом, настоящее изобретение обеспечивает любую подходящую модификацию указанной области или соседних областей. В некоторых случаях область связывания tracrPHK/crPHK (например, область связывания нуклеиновой кислоты, направленной против нуклеиновой кислоты) в сайт-направленном полипептиде может быть модифицирована, чтобы изменить специфичность в отношении нуклеиновой кислоты. В некоторых случаях область связывания tracrPHK/crPHK может быть гомологична области связывания tracrPHK/crPHK, выявленной в белке Cas9 из S. pyogenes (остатки 50-100). В некоторых случаях область связывания tracrPHK/crPHK может быть по меньшей мере на 5%, 10%, 15%. 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологична остаткам 50-100 области связывания tracrPHK/crPHK Cas9 из S. pyogenes. В некоторых случаях область связывания tracrPHK/crPHK может быть не более чем на 5%, 10%, 15%, 20%, 25%. 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологична остаткам 50-100 области связывания tracrPHK/crPHK Cas9 из S. pyogenes.
[0573] В некоторых случаях модификации области связывания tracrPHK/crPHK могут включать, но не ограничиваются ими, модификации отдельных аминокислот, описанные в настоящей заявке. В некоторых случаях модификация области связывания tracrPHK/crPHK может включать, но не ограничивается ими, вставки, делеции или замены отдельных аминокислот, или полипептидов, например, других элементов белка (например, доменов, структурных мотивов, белков).
[0574] Модификации могут включать модификации по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот в области связывания tracrPHK/crPHK. Модификации могут включать модификации не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот в области связывания tracrPHK/crPHK. Модификации также могут включать по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% области связывания tracrPHK/crPHK. Модификации также могут включать не более чем 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% области связывания tracrPHK/crPHK.
[0575] В некоторых случаях модификации последовательностей областей связывания tracrPHK/crPHK сайт-направленного полипептида могут включать конкретные структурные мотивы полипептида, включая, но не ограничиваясь ими, альфа-спираль, бета-цепь, бета-лист, 310-спираль, пи-спираль, мотив полипролина I, мотив полипролина II, мотив полипролина III, бета-поворот, альфа спираль-поворот-альфа спираль, или перегибы спирали или шарниры.
[0576] Например, замены в области связывания tracrPHK/crPHK сайт-направленного полипептида могут включать замену или добавление одного или более белков или их фрагментов. Например, область связывания tracrPHK/crPHK может быть замещена РНК-связывающим доменом из любого известного РНК-связывающего члена системы CRISPR типа I, типа II или типа III. Область связывания tracrPHK/crPHK может быть замещена РНК-связывающим доменом из любого известного РНК-связывающего члена надсемейства RAMP. Область связывания tracrPHK/crPHK может быть замещена РНК-связывающим доменом из любого известного РНК-связывающего члена семейства Cas7, Cas6, Cas5. В одном примере необходимая tracrPHK может быть замещена необходимой последовательностью 5'-шпильки, содержащей спейсерную последовательность, которая расположена после участка шпильки, для распознавания ДНК.
[0577] В некоторых случаях модификации последовательностей областей связывания tracrPHK/crPHK сайт-направленного полипептида могут включать делецию по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% области связывания tracrPHK/crPHK. В некоторых случаях модификации последовательностей областей связывания tracrPHK/crPHK сайт-направленного полипептида могут включать делецию не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% области связывания tracrPHK/crPHK.
[0578] В некоторых случаях модификации последовательностей областей связывания tracrPHK/crPHK сайт-направленного полипептида могут включать добавление или замену по меньшей мере 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичной области связывания tracrPHK/crPHK из Cas9. В некоторых случаях модификации последовательностей областей связывания tracrPHK/crPHK сайт-направленного полипептида могут включать добавление или замену не более чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 3й5%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 99% или 100% гомологичной области связывания tracrPHK/crPHK из Cas9.
[0579] Гомологичные области связывания tracrPHK/crPHK сайт-направленного полипептида могут быть получены из любого подходящего организма. В некоторых случаях область связывания tracrPHK/crPHK может быть получена из прокариотического организма, включая, но не ограничиваясь ими, архей, бактерии, простейших (например, Е. coli, S. pyogenes, S. thermophilus, P. furiosus и т.д.). Например, область связывания tracrPHK/crPHK фермента Cas9 из S. pyogenes может быть замещена или содержать в качестве компонента область связывания tracrPHK/crPHK, или ее фрагмент, полученную из другого Cas9, такого как Cas9 из другого вида.
[0580] В некоторых случаях сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и модифицированный полимераза-подобный домен.
[0581] Модификации для изменения специфичности в отношении РАМ
[0582] В некоторых случаях сайт-направленный полипептид может распознавать мотив, прилегающий к протоспейсеру (РАМ). РАМ может представлять собой любую последовательность в нуклеиновой кислоте-мишени, которая может быть распознана сайт-направленным полипептидом и расположена в направлении 3'-конца непосредственно за последовательностью нуклеиновой кислоты-мишени, которая является мишенью спейсера нуклеиновой кислоты, направленной против нуклеиновой кислоты. Например, РАМ может содержать 5'-NGG-3' или 5'-NGGNG-3', 5'-NNAAAAW-3', 5'-NNNNGATT-3', 5'-GNNNCNNA-3', 5'-NNNACA-3', где N представляет собой любой нуклеотид и N расположен в направлении 3'-конца непосредственно за последовательностью нуклеиновой кислоты-мишени, которая является мишенью последовательности спейсера.
[0583] Сайт-направленный полипептид может быть модифицирован для изменения специфичности в отношении РАМ. Например, сайт-направленный полипептид может быть модифицирован так, что перед проведением модификации полипептид распознает первый мотив, прилегающий к протоспейсеру, и после модификации сайт-направленный полипептид распознает второй мотив, прилегающий к протоспейсеру. В некоторых случаях измененная специфичность в отношении РАМ может включать изменение специфичности связывания (например, увеличение связывания, уменьшение связывания), и/или изменение константы связывания (например, увеличение Kd, уменьшение Kd).
[0584] Сайт-направленный полипептид может быть модифицирован так, что сайт-направленный полипептид может распознать новый тип РАМ, отличный от типа, который распознает сайт-направленный полипептид дикого типа. Например, сайт-направленный полипептид, который распознает 5'-NGG-3' РАМ, может быть модифицирован так, что он может распознавать 5'-NGGNG-3', 5'-NNAAAAW-3', 5'-NNNNGATT-3', 5'-GNNNCNNA-3' или 5 '-NNNACA-3' РАМ.
[0585] Любая область сайт-направленного полипептида может быть сконструирована (например, F-спираль, домен HNH и/или HNH-подобный домен, домен RuvC и/или RuvC-подобный домен, сильноосновный участок), чтобы изменить специфичность в отношении РАМ в соответствии со способами согласно настоящему изобретению.
[0586] Области, соответствующие остаткам 445-507, 446-497, 1096-1225, 1105-1138 сайт-направленного полипептида дикого типа (например, Cas9 из S. pyogenes, SEQ ID NO: 8), могут быть сконструированы, чтобы изменить характеристики распознавания РАМ. Конструирование таких областей могут включать введение мутаций, замену соответствующими областями из других ортологов Cas9, делеции, вставки и т.д. Области, соответствующие остаткам 718-757, 22-49, 65-95, 445-507, 446-497, 1096-1225, 1105-1138, могут быть сконструированы, чтобы изменить характеристики распознавания нуклеиновой кислоты, направленной против нуклеиновой кислоты. Области, соответствующие остаткам 445-507 и 1105-1138, могут быть сконструированы, чтобы изменить характеристики распознавания Р-домена.
[0587] В некоторых случаях сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и модификацию, причем перед введением модификации сайт-направленный полипептид приспособлен для связывания первого РАМ, тогда как после введения модификации сайт-направленный полипептид приспособлен для связывания с другим РАМ.
[0588] Модификации для изменения специфичности нуклеиновой кислоты, направленной против нуклеиновой кислоты
[0589] В некоторых случаях сайт-направленный полипептид может распознавать нуклеиновую кислоту, направленную против нуклеиновой кислоты. Сайт-направленный полипептид может быть модифицирован для изменения специфичности в отношении нуклеиновой кислоты, направленной против нуклеиновой кислоты. Например, сайт-направленный полипептид может быть модифицирован так, что перед проведением модификации полипептид распознавал первую нуклеиновую кислоту, направленную против нуклеиновой кислоты, и после проведения модификации сайт-направленный полипептид распознавал вторую нуклеиновую кислоту, направленную против нуклеиновой кислоты. В некоторых случаях измененная специфичность в отношении нуклеиновой кислоты, направленной против нуклеиновой кислоты, может включать изменение специфичности связывания (например, увеличение связывания, уменьшение связывания), и/или изменение константы связывания (например, увеличение Kd, уменьшение Kd).
[0590] Сайт-направленный полипептид может быть модифицирован так, что сайт-направленный полипептид может распознавать новый тип нуклеиновой кислоты, направленной против нуклеиновой кислоты, отличной от типа, который распознает сайт-направленный полипептид дикого типа. Любая область сайт-направленного полипептида может быть сконструирована (например, F-спираль, домен HNH и/или HNH-подобный домен, домен RuvC и/или RuvC-подобный домен, сильноосновный участок), чтобы изменить специфичность в отношении РАМ в соответствии со способами согласно настоящему изобретению.
[0591] В некоторых случаях сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и модификацию, причем перед введением модификации сайт-направленный полипептид приспособлен для связывания с первой нуклеиновой кислотой, направленной против нуклеиновой кислоты, и после введения модификации сайт-направленный полипептид приспособлен для связывания с другой нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0592] Модификации для изменения критериев гибридизации
[0593] Вставки
[0594] Сайт-направленный полипептид может быть модифицирован, чтобы увеличить специфичность связывания с нуклеиновой кислотой-мишенью. В сайт-направленный полипептид может быть вставлена последовательность. В некоторых случаях в сайт-направленный полипептид может быть вставлен домен HNH и/или HNH-подобный домен. Ненативная последовательность (например, домен HNH и/или HNH-подобный домен) может быть получена из любого вида. Вставка может происходить в любом положении сайт-направленного полипептида. Вставка может произойти в тандеме (например, рядом) с нативным доменом HNH и/или HNH-подобным доменом сайт-направленного полипептида. Вставленный домен HNH и/или HNH-подобный домен может содержать мутацию. Вставленный домен HNH и/или HNH-подобный домен может содержать мутацию, которая снижает нуклеазную активность домена. В некоторых случаях в сайт-направленный полипептид может быть вставлен домен RuvC и/или RuvC-подобный домен. Вставка может происходить в любом положении сайт-направленного полипептида. Вставка может произойти в тандеме (например, рядом) с нативным доменом RuvC и/или RuvC-подобным доменом сайт-направленного полипептида. Вставленный домен RuvC и/или RuvC-подобный домен может содержать мутацию. Вставленный домен RuvC и/или RuvC-подобный домен может содержать мутацию, которая снижает нуклеазную активность домена.
[0595] Сайт-направленный полипептид может быть модифицирован, чтобы увеличить специфичность связывания с нуклеиновой кислотой, направленной против нуклеиновой кислоты. В сайт-направленный полипептид может быть вставлена последовательность. В сайт-направленный полипептид может быть вставлен домен HNH и/или HNH-подобный домен. Ненативная последовательность (например, домен HNH и/или HNH-подобный домен) может быть получена из любого вида. Вставка может происходить в любом положении сайт-направленного полипептида. Вставка может произойти в тандеме (например, рядом) с нативным доменом HNH и/или HNH-подобным доменом сайт-направленного полипептида. Вставленный домен HNH и/или HNH-подобный домен может содержать мутацию. Вставленный домен HNH и/или HNH-подобный домен может содержать мутацию, которая снижает нуклеазную активность домена. В сайт-направленный полипептид может быть вставлен домен RuvC и/или RuvC-подобный домен. Вставка может происходить в любом положении сайт-направленного полипептида. Вставка может произойти в тандеме (например, рядом) с нативным доменом RuvC и/или RuvC-подобным доменом сайт-направленного полипептида. Вставленный домен RuvC и/или RuvC-подобный домен может содержать мутацию, которая снижает нуклеазную активность области.
[0596] Сайт-направленный полипептид может быть сконструирован для включения полипептидного домена, который может связываться с гибридами РНК-ДНК (например, домен РНКазы, домен цинкового пальца). Например, сайт-направленный полипептид может быть сконструирован, чтобы содержать домен RNaseH. Вставленный домен RNaseH может содержать мутацию. Вставленный домен RNaseH может содержать мутацию, которая снижает нуклеазную активность области.
[0597] Сайт-направленный полипептид может быть сконструирован, чтобы содержать полипептидный домен, который может связываться с двухцепочечной ДНК (например, домены, содержащие мотивы спираль-поворот-спираль, домены, содержащие мотивы лейциновой молнии, домены, содержащие мотивы спираль-петля-спираль, домены, содержащие мотивы цинкового пальца). Например, сайт-направленный полипептид может быть сконструирован, чтобы содержать мотив спираль-поворот-спираль. Неограничивающие примеры мотивов спираль-поворот-спираль включают мотивы из dnaB, TetR, MuB, P2R, CysB, BirA, репрессора бактериофага лямбда. Engrailed, Myb, LuxR, MarR, ETS, ZNF10a, Kox-1. Мотив спираль-петля-спираль может быть диспиральным, триспиральным, тетраспиральным, иметь структуру крылатая спираль-поворот-спираль или другую модифицированную структуру крылатая спираль-поворот-спираль. Вставленный домен может содержать мутацию. Вставленный домен может содержать мутацию, которая снижает нуклеазную активность области.
[0598] Компенсационные мутации
[0599] Сайт-направленный полипептид может содержать мутацию и/или может быть сконструирован так, что он может преимущественно связываться с мутированной и/или сконструированной нуклеиновой кислотой, направленной против нуклеиновой кислоты. Такая мутация пары сайт-направленного полипептида и нуклеиновой кислоты, направленной против нуклеиновой кислоты, может называться компенсационной мутацией. Например, сайт-направленный полипептид может быть модифицирован так, что его нуклеазный домен (например, домен HNH и/или HNH-подобный домен, домен RuvC и/или RuvC-подобный домен) замещен доменом связывания нуклеиновой кислоты (например, доменом связывания нуклеиновой кислоты из Csy4, Cas5, Cas6). Сайт-направленный полипептид может быть сконструирован так, что домен связывания нуклеиновой кислоты (например, домен связывания нуклеиновой кислоты из Csy4, Cas5, Cas6) вставлен в сайт-направленный полипептид. Полученный сайт-направленный полипептид может связываться с нуклеиновой кислотой, направленной против нуклеиновой кислоты, которая мутировала и/или сконструирована так, чтобы содержать сайт связывания для домена, связывающего нуклеиновую кислоту (например, сайт связывания для домена, связывающего нуклеиновую кислоту, из Csy4, Cas5, Cas6). Нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть мутирована и/или сконструирована так, чтобы содержать сайт связывания домена, связывающего нуклеиновую кислоту, в минимальной последовательности tracrPHK. Нуклеиновая кислота, направленная против нуклеиновой кислоты. Может быть мутирована и/или сконструирована так, чтобы содержать сайт связывания домена, связывающего нуклеиновую кислоту, в последовательности 3'tracrPHK. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть мутирована и/или сконструирована так, чтобы содержать сайт связывания домена, связывающего нуклеиновую кислоту, в удлиненной последовательности tracrPHK.
[0600] В некоторых случаях сайт-направленный полипептид содержит аминокислотную последовательность, которая по меньшей мере на 15% идентична аминокислотной последовательности Cas9 из S. pyogenes, два домена, расщепляющих нуклеиновую кислоту (т.е. домен HNH и домен RuvC), и компенсационную мутацию, причем сайт-направленный полипептид способен связываться со сконструированной нуклеиновой кислотой, направленной против нуклеиновой кислоты, но не с немодифицированной нуклеиновой кислотой, направленной против нуклеиновой кислоты.
[0601] Способы получения липких концов и разрезов с тупыми концами
[0602] В некоторых случаях одна или более никаз (т.е. сайт-направленных полипептидов, содержащих один по существу неактивный нуклеазный домен) могут быть использованы для получения целевых двухцепочечных разрезов нуклеиновой кислоты-мишени. Каждая никаза из одной или более никаз может воздействовать на одну цепь двухцепочечной нуклеиновой кислоты-мишени. В некоторых случаях две никазы могут быть использованы для получения целевого двухцепочечного разреза.
[0603] Две никазы могут разрезать нуклеиновую кислоту-мишень с получением разреза с тупыми концами (при этом участки разреза нуклеиновой кислоты-мишени расположены в аналогичном положении на каждой нити). Две никазы могут разрезать нуклеиновую кислоту-мишень в разных положениях в пределах каждой цепи, оставляя несколько одноцепочечных нуклеотидов, с образованием тем самым липкого конца.
[0604] Расщепление нуклеиновой кислоты-мишени под действием двух модифицированных сайт-направленных полипептидов, имеющих никазную активность, можно использовать для внесения делеций или вставок материала нуклеиновой кислоты из нуклеиновой кислоты-мишени путем расщепления нуклеиновой кислоты-мишени, и обеспечивая клетке возможность восстановить последовательность в отсутствие экзогенных донорных полинуклеотидов. В некоторых случаях способы согласно настоящему изобретению можно применять для блокирования гена. Если нуклеиновую кислоту, направленную против нуклеиновой кислоты, и два модифицированных сайт-направленных полипептида, имеющих никазную активность, вводят совместно в клетку в комбинации с донорной полинуклеотидной последовательностью, которая включает по меньшей мере один сегмент, который гомологичен нуклеиновой кислоте-мишени, новый материал нуклеиновой кислоты может быть вставлен/скопирован в указанный сайт. Такие способы можно применять для добавления, т.е. вставки или замены, материала нуклеиновой кислоты к нуклеиновой кислоте-мишени (например, «внесение» нуклеиновой кислоты, которая кодирует белок, миРНК, микроРНК и т.д.), для добавления метки (например, 6×His, флуоресцентного белка (например, зеленого флуоресцентного белка; желтого флуоресцентного белка и т.д.), гемагглютинина (НА), FLAG-метки и т.д.), для добавления регуляторной последовательности к гену (например, промотора, сигнала полиаденилирования, последовательности внутренней посадки рибосомы (IRES), пептида 2А, старт-кодона, стоп-кодона, сплайс-сигнала, сигнала локализации, и т.д.), для модификации последовательности нуклеиновой кислоты (например, введения мутации) и т.п.
[0605] На Фиг. 32 показан способ получения тупых концов с помощью никаз. Дуплекс нуклеиновой кислоты-мишени 3210 может содержать множество последовательностей РАМ 3215 (помещены в рамку), при этом один РАМ расположен на одной цепи нуклеиновой кислоты-мишени 3210, и один РАМ расположен на другой цепи нуклеиновой кислоты-мишени 3210. Нуклеиновая кислота, направленная против нуклеиновой кислоты, 3205 в составе комплекса с никазой (никаза не показана) может гибридизоваться с последовательностью спейсера, примыкающей к РАМ, 3215 на каждой цепи нуклеиновой кислоты-мишени 3210. Никаза может расщеплять одну цепь нуклеиновой кислоты-мишени 3210. Расщепление указано треугольниками. Если последовательности РАМ расположены в пространстве надлежащим образом, то никазы могут разрезать нуклеиновую кислоту-мишень по существу в аналогичном положении на каждой цепи с образованием тупого конца. Последовательности РАМ могут быть разделены по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40 или 50, или более нуклеотидами. Последовательности РАМ могут быть разделены не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40 или 50, или более нуклеотидами. В некоторых случаях РАМ разделены 6 нуклеотидами (т.е. между каждым РАМ находится 6 нуклеотидов). В некоторых случаях нуклеиновая кислота, направленная против нуклеиновой кислоты, отщепляет приблизительно 3 нуклеотида в направлении 5'-конца относительно РАМ.
[0606] Согласно некоторым вариантам реализации настоящего изобретения две или более никаз можно применять для получения липких концов. На Фиг. 33 показано, как две никазы, направленные на перекрывающиеся области на нуклеиновой кислоте-мишени, могут создать смещенный двухцепочечный разрыв с образованием липких концов. Дуплекс нуклеиновой кислоты-мишени 3310 может содержать множество последовательностей РАМ 3315 (приведены в рамке). Нуклеиновая кислота, направленная против нуклеиновой кислоты, 3305 в составе комплекса с никазой (никаза не показана) может гибридизоваться с последовательностью спейсера, примыкающей к РАМ, 3315 на каждой цепи нуклеиновой кислоты-мишени 3310. Никаза может расщеплять одну цепь нуклеиновой кислоты-мишени 3310. Расщепление показано треугольниками. Если последовательности РАМ расположены в пространстве надлежащим образом, то никазы могут разрезать нуклеиновую кислоту-мишень в смещенных относительно друг друга положениях с образованием липкого конца. Последовательности РАМ могут быть разделены по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. Последовательности РАМ могут быть разделены не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. Расстояние между последовательностями РАМ может быть связано с длиной образованных липких концов. Например, чем дальше друг от друга расположены последовательности РАМ, тем длиннее будет липкий конец.
[0607] Способ получения липких концов с помощью двух или более никаз может включать последовательности РАМ, которые являются по существу смежными (но расположены на противоположных цепях). В некоторых случаях последовательности РАМ разделены по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. В некоторых случаях последовательности РАМ разделены не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. В некоторых случаях последовательности РАМ разделены одним нуклеотидом. В некоторых случаях последовательности РАМ не разделены нуклеотидами.
[0608] Способы обогащения и секвенирования нуклеиновых кислот-мишеней
[0609] Общий обзор
[0610] Секвенирование можно использовать для диагностики заболевания путем выявления мутаций и/или других вариантов последовательности (например, полиморфизмов). Способы согласно настоящему изобретению предусматривают способы, наборы и композиции для обогащения последовательности нуклеиновой кислоты-мишени без использования методик амплификации. Нуклеиновая кислота-мишень может быть обогащена с использованием сайт-направленного полипептида и нуклеиновой кислоты, направленной против нуклеиновой кислоты.
[0611] На Фиг. 3 показан примерный вариант реализации способов согласно настоящему изобретению. Сайт-направленный полипептид 305 может связываться с нуклеиновой кислотой, направленной против нуклеиновой кислоты 310, с образованием тем самым комплекса 306. Нуклеиновая кислота, направленная против нуклеиновой кислоты, 310 может содержать нуклеиновую аффинную метку 311. Сайт-направленный полипептид 305 может включать нуклеазный домен. Сайт-направленный полипептид 305 может быть ферментативно активным. Сайт-направленный полипептид 305 может содержать аффинную метку 315. Нуклеиновая кислота, направленная против нуклеиновой кислоты, 310 может гибридизоваться с нуклеиновой кислотой-мишенью 320. Согласно некоторым вариантам реализации настоящего изобретения множество комплексов 306 могут гибридизоваться с множеством положений в нуклеиновой кислоте-мишени 320. На этапе расщепления 325 нуклеазный домен сайт-направленного полипептида 305 может расщеплять или разрезать 330 нуклеиновую кислоту-мишень 320. Вырезанная нуклеиновая кислота-мишень 340 может быть очищена на этапе очистки 335. Адаптеры 345 могут быть лигированы в вырезанную нуклеиновую кислоту-мишень. Адаптеры могут облегчать секвенирование вырезанной нуклеиновой кислоты-мишени.
[0612] На Фиг. 4 показан примерный вариант реализации способов согласно настоящему изобретению. Сайт-направленный полипептид 405 может взаимодействовать с нуклеиновой кислотой, направленной против нуклеиновой кислоты 410, с образованием тем самым комплекса 406. Сайт-направленный полипептид может содержать 405 нуклеазный домен. Согласно некоторым вариантам реализации настоящего изобретения нуклеазный домен сайт-направленного полипептида 405 может быть ферментативно неактивным. Сайт-направленный полипептид 405 может содержать аффинную метку 415. Нуклеиновая кислота, направленная против нуклеиновой кислоты, 410 может гибридизоваться с нуклеиновой кислотой-мишенью 420. Нуклеиновая кислота, направленная против нуклеиновой кислоты, 410 может содержать нуклеиновую аффинную метку 411. Аффинная метка 411 нуклеиновой кислоты, направленной против нуклеиновой кислоты, может содержать структуру шпильки. Множество комплексов 406 могут гибридизоваться с множеством положений в нуклеиновой кислоте-мишени 420. На этапе фрагментации 225 нуклеиновая кислота-мишень 420 может быть подвергнута фрагментации с образованием фрагмента нуклеиновой кислоты-мишени 445 (также называемого в настоящей заявке «нуклеиновая кислота-мишень»). Сайт-направленный полипептид 405 может быть очищен с помощью захватывающего агента 440, который может связываться с аффинной меткой 415 сайт-направленного полипептида 405. Фрагментированная нуклеиновая кислота-мишень 445 может быть элюирована из комплекса 406 на этапе очистки 450. На этом же этапе, или, необязательно, на другом этапе, адаптеры 455 могут быть лигированы в нуклеиновую кислоту-мишень. Адаптеры могут облегчать секвенирование нуклеиновой кислоты-мишени.
[0613] Комплекс нуклеиновой кислоты, направленной против нуклеиновой кислоты, и сайт-направленного полипептида
[0614] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может взаимодействовать с сайт-направленным полипептидом (например, нуклеазой, направляемой нуклеиновой кислотой, например, Cas9) с образованием комплекса. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может направлять сайт-направленный полипептид к нуклеиновой кислоте-мишени.
[0615] Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть сконструирована так, что комплекс (например, содержащий сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты) может связываться за пределами сайта расщепления сайт-направленного полипептида. В этом случае нуклеиновая кислота-мишень может не взаимодействовать с комплексом, и нуклеиновая кислота-мишень может быть вырезана (например, высвобождена из комплекса).
[0616] Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть сконструирована так, что комплекс может связываться внутри сайта расщепления сайт-направленного полипептида. В этом случае нуклеиновая кислота-мишень может взаимодействовать с комплексом, и нуклеиновая кислота-мишень может быть связана (например, связана с комплексом).
[0617] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть сконструирована так, что комплекс (например, содержащий сайт-направленный полипептид и/или нуклеиновую кислоту, направленную против нуклеиновой кислоты) может гибридизоваться с множеством положений в образце нуклеиновой кислоты.
[0618] Множество комплексов могут вступать в контакт с образцом нуклеиновой кислоты. Множество комплексов могут содержать нуклеиновые кислоты, направленные против нуклеиновой кислоты, которые сконструированы для придания им способности гибридизоваться с одной и той же последовательностью. Множество комплексов могут содержать нуклеиновые кислоты, направленные против нуклеиновой кислоты, которые сконструированы для придания им способности гибридизоваться с различными последовательностями.
[0619] Последовательности могут быть расположены в различных положениях в пределах нуклеиновой кислоты-мишени. Положения могут содержать аналогичные или сходные последовательности нуклеиновой кислоты-мишени. Положения могут содержать различные последовательности нуклеиновой кислоты-мишени. Положения могут быть на определенном расстоянии друг от друга. Положения могут находиться на расстоянии менее чем 10 тысяч пар нуклеотидов (т.п.н.) друг от друга, менее чем 8 т.п.н. друг от друга, менее чем 6 т.п.н. друг от друга, менее чем 4 т.п.н. друг от друга, менее чем 2 т.п.н. друг от друга, менее чем 1 т.п.н. друг от друга, менее чем 900 нуклеотидов друг от друга, менее чем 800 нуклеотидов друг от друга, менее чем 700 нуклеотидов друг от друга, менее чем 600 нуклеотидов друг от друга, менее чем 500 нуклеотидов друг от друга, менее чем 400 нуклеотидов друг от друга, менее чем 300 нуклеотидов друг от друга, менее чем 200 нуклеотидов друг от друга, менее чем 100 нуклеотидов друг от друга.
[0620] Комплексы могут расщеплять нуклеиновую кислоту-мишень с образованием вырезанной нуклеиновой кислоты-мишени, длина которой может составлять менее чем 10 тысяч пар нуклеотидов (т.п.н.), менее чем 8 т.п.н., менее чем 6 т.п.н., менее чем 4 т.п.н., менее чем 2 т.п.н., менее чем 1 т.п.н., менее чем 900 нуклеотидов, менее чем 800 нуклеотидов, менее чем 700 нуклеотидов, менее чем 600 нуклеотидов, менее чем 500 нуклеотидов, менее чем 400 нуклеотидов, менее чем 300 нуклеотидов, менее чем 200 нуклеотидов, менее чем 100 нуклеотидов.
[0621] Комплексы могут быть связаны с фрагментированной нуклеиновой кислотой-мишенью, длина которой может составлять менее чем 10 тысяч пар нуклеотидов (т.п.н.), менее чем 8 т.п.н., менее чем 6 т.п.н., менее чем 4 т.п.н., менее чем 2 т.п.н., менее чем 1 т.п.н., менее чем 900 нуклеотидов, менее чем 800 нуклеотидов, менее чем 700 нуклеотидов, менее чем 600 нуклеотидов, менее чем 500 нуклеотидов, менее чем 400 нуклеотидов, менее чем 300 нуклеотидов, менее чем 200 нуклеотидов, менее чем 100 нуклеотидов.
[0622] Способы детектирования нецелевых сайтов связывания сайт-направленных полипептидов
[0623] Общий обзор
[0624] В настоящем изобретении описаны способы, композиции, системы и/или наборы для определения нецелевых сайтов связывания сайт-направленных полипептидов. Согласно некоторым вариантам реализации настоящего изобретения сайт-направленный полипептид может содержать нуклеиновую кислоту, направленную против нуклеиновой кислоты, с образованием тем самым комплекса. Комплекс может быть приведен в контакт с нуклеиновой кислотой-мишенью. Нуклеиновая кислота-мишень может быть связана с захватывающими агентами, которые могут связываться с аффинными метками комплекса. Идентичность нуклеиновой кислоты-мишени можно определить путем секвенирования. Секвенирование (например, высокопроизводительное секвенирование, например, Illumina, Ion Torrent) также может выявить частоту нецелевых сайтов связывания сайт-направленного полипептида и/или комплекса путем подсчета количества случаев регистрации конкретного сайта связывания. Способы, композиции, системы и/или наборы согласно настоящему изобретению могут способствовать разработке более точно и специфично нацеленных сайт-направленных полипептидов.
[0625] На ФИГ. 5 показан примерный вариант реализации способов согласно настоящему изобретению. Сайт-направленный полипептид 505 может содержать аффинную метку 510. Сайт-направленный полипептид может содержать домен связывания нуклеиновой кислоты 515. Домен связывания нуклеиновой кислоты 515 может представлять собой нуклеиновую кислоту. Согласно некоторым вариантам реализации настоящего изобретения домен связывания нуклеиновой кислоты 515 и сайт-направленный полипептид 505 образуют комплекс 531. Комплекс 531 может быть приведен в контакт 525 с нуклеиновой кислотой-мишенью 530. В предпочтительном варианте реализации нуклеиновая кислота-мишень 530 представляет собой ДНК (например, геномную ДНК или гДНК). Комплекс может быть подвергнут аффинной очистке 535 с использованием захватывающего агента 540. Захватывающий агент 540 может связываться с аффинной меткой 510 сайт-направленного полипептида 505. Захватывающий агент 540 может содержать вторую аффинную метку 545. Захватывающий агент 540 может быть подвергнут аффинной очистке 550 путем связывания с твердой подложкой 555. Согласно некоторым вариантам реализации настоящего изобретения твердая подложка 555 представляет собой гранулу, покрытую аффинным реагентом, который может связываться с аффинной меткой 545 захватывающего агента. При необходимости твердая подложка 555 может связываться с аффинной меткой 510 сайт-направленного полипептида 505 для облегчения процесса очистки. Согласно некоторым вариантам реализации настоящего изобретения может быть проведен один или более этапов очистки. Каждый этап может включать приведение твердой подложки 555 в контакт с аффинными метками сайт-направленного полипептида 510 и/или захватывающего агента 545. Комплекс после аффинной очистки может быть подвергнут элюированию из нуклеиновой кислоты-мишени 530. Нуклеиновая кислота-мишень может быть впоследствии получена для дальнейшей обработки. Обработка может включать последующие способы исследования, например, секвенирование.
[0626] На Фиг. 6 показан примерный вариант реализации способов согласно настоящему изобретению. Сайт-направленный полипептид 605 может содержать аффинную метку 610. Сайт-направленный полипептид 605 может содержать домен связывания нуклеиновой кислоты 615. Домен связывания нуклеиновой кислоты 615 может представлять собой нуклеиновую кислоту. Согласно некоторым вариантам реализации настоящего изобретения домен связывания нуклеиновой кислоты 615 может содержать аффинную метку 620. В некоторых вариантах домен связывания нуклеиновой кислоты 615 и сайт-специфичный полипептид 605 могут образовать комплекс 631. Комплекс 631 может вступать в контакт 625 с нуклеиновой кислотой-мишенью 630. В предпочтительном варианте реализации нуклеиновая кислота-мишень 630 представляет собой ДНК. Комплекс 631 может быть подвергнут аффинной очистке 635 с использованием захватывающего агента 640. Захватывающий агент 640 может представлять собой условно ферментативно неактивный сайт-направленный полипептид. Захватывающий агент 640 может представлять собой условно ферментативно неактивный вариант Csy4. Захватывающий агент 640 может связываться с аффинной меткой 620. Захватывающий агент 640 может содержать аффинную метку 645. Захватывающий агент 640 может быть подвергнут аффинной очистке 650 путем связывания с твердой подложкой 655. Согласно некоторым вариантам реализации настоящего изобретения твердая подложка представляет собой гранулу, покрытую аффинным реагентом, который может связываться с аффинной меткой 645 захватывающего агента 640. При необходимости, твердая подложка 655 может связываться с аффинной меткой 610 сайт-направленного полипептида 605 для облегчения очистки. Согласно некоторым вариантам реализации настоящего изобретения может быть проведено два этапа очистки, каждый их которых включает приведение твердой подложки 655 в контакт с аффинными метками сайт-направленного полипептида 610 и/или захватывающего агента 640. Расщепление аффинной метки 620 может облегчить элюирование 660 нуклеиновой кислоты-мишени 630 от твердой подложки 655. Нуклеиновая кислота-мишень 630 затем может быть подготовлена для последующих дополнительных исследований, таких как секвенирование.
[0627] Способы
[0628] В настоящем изобретении предложены способы иммунопреципитации и секвенирования с использованием нуклеазы (NIP-Seq). Согласно некоторым вариантам реализации настоящего изобретения способ может включать а) приведение образца нуклеиновой кислоты в контакт с комплексом, содержащим ферментативно неактивный сайт-направленный полипептид, сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты. Комплекс может гибридизоваться с нуклеиновой кислотой-мишенью. Комплекс может быть связан с захватывающим агентом, и нуклеиновая кислота-мишень, связанная с комплексом, может быть подвергнута секвенированию. Согласно некоторым вариантам реализации настоящего изобретения способ может дополнительно включать определение идентичности нецелевого сайта связывания. Способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке.
[0629] Указанные способы можно осуществлять за пределами клетки. Например, образец может содержать очищенную геномную ДНК, клеточный лизат, гомогенизированную ткань, плазму и тому подобное. Указанные способы можно осуществлять в клетках.
[0630] Комплексы сайт-направленного полипептида и нуклеиновой кислоты-мишени могут быть фиксированы или сшиты с образованием комплексов. Клетки могут быть сшиты перед лизированием. Фиксированные или сшитые клетки могут стабилизировать комплексы белок-ДНК в клетке. Подходящие фиксаторы и сшивающие агенты могут включать формальдегид, глутаровый альдегид, фиксаторы на основе этанола, фиксаторы на основе метанола, ацетон, уксусную кислоту, тетраоксид осмия, бихромат калия, хромовую кислоту, перманганат калия, производные ртути, пикраты, формалин, параформальдегид, аминореактивные сшивающие агенты на основе NHS-эфира, такие как бис[сульфосукцинимидил]суберат (BS3), 3,3'-дитиобис-[сульфосукцинимидилпропионат] (DTSSP), этиленгликоль-бис-[сульфосукцинимидилсукцинат] (сульфо-EGS), дисукцинимидилглутарат (DSG), дитиобис-[сукцинимидилпропионат] (DSP), дисукцинимидилсуберат (DSS), этиленгликоль-бис-[сукцинимидилсукцинат] (EGS), сшивающие агенты на основе NHS-эфира/диазирина, такие как NHS-диазирин, NHS-LC-диазирин, NHS-SS-диазирин, сульфо-MHS-диазирин, сульфо-MHS-LC-диазирин и сульфо-NHS-SS-диазирин.
[0631] Нуклеиновая кислота (например, геномная ДНК) может быть обработана, чтобы фрагментировать ДНК перед проведением аффинной очистки. Фрагментация может быть выполнена с помощью физических, механических или ферментативных способов. Физическая фрагментация может включать воздействие тепла и ультрафиолетового (УФ) света на полинуклеотид-мишень. Механическое разрушение можно использовать для механического разрезания полинуклеотида-мишени на фрагменты нужного диапазона. Механический сдвиг можно осуществлять с помощью ряда способов, известных в данной области техники, включая повторяющееся пипетирование полинуклеотида-мишени, воздействие ультразвука и распыление. Полинуклеотиды-мишени также можно фрагментировать с помощью ферментативных методов. В некоторых случаях ферментативное расщепление можно осуществлять с использованием ферментов, таких как рестрикционные ферменты. Рестрикционные ферменты можно использовать для выполнения специфичной или неспецифичной фрагментации полинуклеотидов-мишеней. Для осуществления указанных методов можно применять один или более типов рестрикционных ферментов, как правило, описанных как в ферменты типа I, ферменты типа II, и/или ферменты типа III. Ферменты типа II и типа III, как правило, коммерчески доступны и хорошо известны в данной области техники. Ферменты типа II и типа III распознают специфичные нуклеотидные последовательности в двухцепочечной полинуклеотидной последовательности («последовательности распознавания» или «сайты распознавания»). После связывания и распознавания этих последовательностей ферменты типа II и типа III расщепляют полинуклеотидную последовательность. В некоторых случаях расщепление приводит к образованию полинуклеотидного фрагмента, содержащего часть выступающей одноцепочечной ДНК, называемой «липким концом». В других случаях расщепление не приведет к образованию выступающего фрагмента, создавая «тупой конец». Способы могут включать использование рестрикционных ферментов, которые создают липкие концы или тупые концы. Фрагменты нуклеиновых кислот также можно получать с помощью методов амплификации (например, полимеразной цепной реакции, полимеразной цепной реакции длинных фрагментов, линейной полимеразной цепной реакции и т.п.).
[0632] После фрагментирования комплексы, содержащие сайт-направленный полипептид, могут быть очищены путем инкубации с твердой подложкой. Например, если сайт-направленный полипептид содержит биотиновую метку, то твердая подложка может быть покрыта авидином или стрептавидином для связывания с биотиновой меткой.
[0633] Согласно некоторым вариантам реализации настоящего изобретения после фрагментирования комплексы, содержащие сайт-направленный полипептид, нуклеиновую кислоту-мишень и/или нуклеиновую кислоту, направленную против нуклеиновой кислоты, очищают путем инкубации с захватывающим агентом. Захватывающий агент может относиться к любому агенту, который может связываться с аффинной меткой, гибридизованной с сайт-направленным полипептидом. Типичные захватывающие агенты могут включать биотин, стрептавидин и антитела. Например, если аффинная метка, гибридизованная с сайт-направленным полипептидом, представляет собой метку FLAG, то захватывающий агент будет представлять собой антитело к метке FLAG. Согласно некоторым вариантам реализации настоящего изобретения захватывающий агент может содержать аффинную метку (например, биотин, стрептавидин).
[0634] В некоторых случаях захватывающий агент представляет собой ферментативно неактивную эндорибонуклеазу. Например, захватывающий агент может представлять собой ферментативно неактивный сайт-направленный полипептид, ферментативно неактивный Csy4, Cas5 или Cas6.
[0635] Захватывающий агент может быть очищен с использованием твердой подложки. Например, если захватывающий агент представляет собой биотиновую метку, то гранула может быть покрыта авидином или стрептавидином, чтобы связать биотинилированный захватывающий агент.
[0636] Согласно некоторым вариантам реализации указанного способа может быть выполнено два или более раундов очистки. Может быть выполнено по меньшей мере 1, 2, 3, 4, 5, 6, 7 или более раундов очистки. Может быть выполнено не более чем 1, 2, 3, 4, 5, 6, 7 или более раундов очистки. Первый раунд очистки может включать очистку с использованием твердой подложки, которая может связываться с аффинной меткой захватывающего агента, и второй раунд очистки может включать очистку с использованием твердой подложки, которая может связываться с аффинной меткой сайт-направленного полипептида. Первый раунд очистки может включать очистку с использованием твердой подложки, которая может связываться с аффинной меткой сайт-направленного полипептида, и второй раунд очистки может включать очистку с использованием твердой подложки, которая будет связываться с аффинной меткой захватывающего агента. Указанный способ можно применять для оптимизации специфичности связывания сайт-направленного полипептида путем осуществления указанного способа более одного раза.
[0637] Захваченный комплекс может содержать сайт-направленный полипептид и нуклеиновую кислоту-мишень. Нуклеиновая кислота-мишень может быть элюирована из сайт-направленного полипсптидного комплекса с помощью таких методов как промывание растворами с высоким содержанием соли, осаждение этанолом, кипячение и очистка на геле.
[0638] Элюированная ДНК может быть подготовлена для секвенирования (например, гидродинамическая фрагментация, дотирование адаптеров). Подготовка к секвенированию может включать создание библиотек для секвенирования элюированной нуклеиновой кислоты-мишени. С помощью секвенирования можно определить идентичность и частоту нецелевых сайтов связывания сайт-направленных полипептидов. Определение последовательности также может быть выполнено с использованием методов, позволяющих определить множество (как правило, от тысячи до миллионов) последовательностей нуклеиновых кислот по существу одновременно, в которых множество последовательностей считываются предпочтительно одновременно с помощью последовательного процесса с высокой пропускной способностью. Такие методы включают, но не ограничиваются ими, пиросеквенирование (например, метод, запущенный в серийное производство 454 Life Sciences, Inc., Бранфорд, Коннектикут, США); секвенирование путем лигирования (например, технология SOLiD™, запущенная в серийное производство Life Technology, Inc., Карлсбад, Калифорния, США); секвенирование путем синтеза с использованием модифицированных нуклеотидов (например, запущенные в серийное производство технологии TruSeq™ и HiSeq™ от Illumina, Inc., Сан-Диего, Калифорния, HeliScope™ от Helicos Biosciences Corporation, Кембридж, Массачусетс, и PacBio RS от Pacific Biosciences of California, Inc., Менло-Парк, Калифорния), секвенирование с помощью технологии детектирования ионов (Ion Torrent, Inc., Южный Сан-Франциско, Калифорния); секвенирование наношариков ДНК (Complete Genomics, Inc., Маунтин-Вью, Калифорния США); технологии секвенирования на основе нанопористых материалов (например, разработанные Oxford Nanopore Technologies, LTD, Оксфорд, Великобритания), и другие известные методы высокоэффективного распараллеленного секвенирования.
[0639] Согласно некоторым вариантам реализации настоящего изобретения способ дополнительно включает сбор данных и хранение данных. Данные могут быть представлены в пригодной для ввода в компьютер форме и могут быть сохранены и/или собраны на компьютерном сервере (например. Фигура 31 и пример 27).
[0640] Способы детектирования вариантов последовательностей в нуклеиновых кислотах
[0641] Общий обзор
[0642] В некоторых вариантах реализации настоящего изобретения способы согласно настоящему изобретению предусматривают детектирование вариантов последовательности в нуклеиновых кислотах. Способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке. Как изображено на ФИГ. 7, образец нуклеиновой кислоты 705 может быть лигирован 720 с меткой нуклеиновой кислоты 710. Метка нуклеиновой кислоты может представлять собой одиночную направляющую РНК. Метка нуклеиновой кислоты может содержать crPHK. Метка нуклеиновой кислоты может содержать детектируемую метку 715. В совокупности, образец нуклеиновой кислоты 705, лигированный с меткой нуклеиновой кислоты 710, может быть назван меченым испытываемым образцом 721. Меченый испытываемый образец 721 может быть приведен в контакт 725 с массивом 740, содержащим иммобилизованные олигонуклеотиды 735. Иммобилизованные олигонуклеотиды 735 могут быть названы библиотекой нуклеиновых кислот. Олигонуклеотиды 735 могут представлять собой двухцепочечную ДНК. Олигонуклеотиды 735 могут содержать детектируемую метку 730. Отдельные члены меченого испытываемого образца 721 могут гибридизоваться 745 с олигонуклеотидами 735, в отношении которых они обладают достаточной степенью комплементарности, чтобы облегчить гибридизацию. Степень гибридизации можно количественно оценить путем сравнения интенсивностей двух детектируемых меток 715 и 730. Например, гибридизованные олигонуклеотиды могут отображать две детектируемые метки. Негибридизированные олигонуклеотиды могут отображать одну детектируемую метку 730. Гибридизованный образец может быть приведен в контакт с сайт-направленным полипептидом 750. Сайт-направленный полипептид может расщеплять 755 олигонуклеотиды 735 в массиве 740, которые гибридизовались с членами меченого испытываемого образца 721. Расщепление под действием сайт-направленного полипептида может обеспечить удаление гибридизованных членов меченого испытываемого образца 721. После расщепления под действием сайт-направленного полипептида 750, на массиве останутся только детектируемые метки негибридизованных олигонуклеотидов 760. Оставшаяся детектируемая метка 760 может быть определена количественно. Количественное определение оставшихся детектируемых меток 760 будет зависеть от того, какие последовательности были представлены в образце нуклеиновой кислоты 705, и какие последовательности отсутствовали. Олигонуклеотиды, которые не отображают оставшуюся детектируемую метку 760, соответствуют последовательностям, которые были представлены в образце нуклеиновой кислоты 705. Олигонуклеотиды, которые отображают оставшуюся детектируемую метку 760, соответствуют последовательностям, которые не были представлены в образце нуклеиновой кислоты 705.
[0643] Согласно некоторым вариантам реализации настоящего изобретения образец нуклеиновой кислоты 805 может быть лигирован 820 с меткой нуклеиновой кислоты 810. Метка нуклеиновой кислоты может представлять собой одиночную направляющую РНК. Метка нуклеиновой кислоты может содержать crPHK. Метка нуклеиновой кислоты может содержать детектируемую метку 815. В совокупности, образец нуклеиновой кислоты, дотированный с меткой нуклеиновой кислоты, может быть назван меченым испытываемым образцом 821. Меченый испытываемый образец 821 может быть приведен в контакт 825 с массивом 840, содержащим иммобилизованные Олигонуклеотиды 835. Иммобилизованные Олигонуклеотиды могут быть названы библиотекой нуклеиновых кислот. Олигонуклеотиды 835 могут представлять собой двухцепочечную ДНК. Отдельные члены меченого испытываемого образца 821 могут гибридизоваться 845 с олигонуклеотидами 835, в отношении которых они обладают достаточной степенью комплементарности, чтобы облегчить гибридизацию. Гибридизованный образец может вступать в контакт с сайт-направленным полипептидом 850. Сайт-направленный полипептид может расщеплять 855 Олигонуклеотиды 835 в массиве 840, которые гибридизовались с членами меченого испытываемого образца 821. Расщепление под действием сайт-направленного полипептида 850 может обеспечить удаление гибридизованных членов меченого испытываемого образца 821. Расщепление под действием сайт-направленного полипептида 850 может обеспечить отщепление и отделение 860 части иммобилизованных олигонуклеотидов от массива. Отделенные отщепленные Олигонуклеотиды 860 можно лигировать 865 с соответствующими адаптерами 870 для секвенирования. С помощью секвенирования отщепленных олигонуклеотидов 860 можно определить последовательности, представленные в образце нуклеиновой кислоты 805.
[0644] Согласно некоторым вариантам реализации настоящего изобретения библиотека нуклеиновых кислот может быть создана для секвенирования с использованием коммерчески доступных высокопроизводительных платформ для секвенирования. Библиотека может содержать нуклеиновые кислоты, которые могут содержать одну или более меток для секвенирования 930 и последовательность-мишень 945. Последовательность-мишень 945 может представлять собой последовательность, которая присутствует в образце нуклеиновой кислоты 905. Последовательность-мишень 945 может содержать последовательность мотива, прилегающего к протоспейсеру (РАМ). При необходимости, нуклеиновые кислоты в библиотеке нуклеиновых кислот могут содержать одну или более полинуклеотидных последовательностей для идентификации 935, и одну или более удлиненных последовательностей 940. В этом варианте реализации образец нуклеиновой кислоты 905 может быть лигирован 920 с меткой нуклеиновой кислоты 910. Метка нуклеиновой кислоты может представлять собой одиночную направляющую РНК. Метка нуклеиновой кислоты может содержать crPHK. Необязательно, метка нуклеиновой кислоты может содержать аффинную метку 915. В совокупности, образец нуклеиновой кислоты, лигированный с меткой нуклеиновой кислоты, может быть назван меченым испытываемым образцом 921. Меченый испытываемый образец 921 может быть приведен в контакт 925 с библиотекой нуклеиновых кислот. Меченый испытываемый образец 921 может гибридизоваться с нуклеиновой кислотой в библиотеке нуклеиновых кислот, образуя комплекс 946. Гибридизованный меченый испытываемый образец и библиотека нуклеиновых кислот могут быть приведены в контакт с сайт-направленным полипептидом 950. Сайт-направленный полипептид 950 может отщеплять гибридизованных членов библиотеки нуклеиновых кислот. Отщепленные члены библиотеки нуклеиновых кислот 965 могут быть отделены от нерасщепленных членов. Нерасщепленные члены могут быть подвергнуты секвенированию. С помощью секвенирования можно определить, какие последовательности были представлены в образце нуклеиновой кислоты 905. Например, последовательности нерасщепленных членов могут соответствовать последовательностям, которые не были представлены в образце нуклеиновой кислоты 905. Эти последовательности могут быть отделены от известных последовательностей в библиотеке нуклеиновых кислот. Полученные последовательности могут представлять собой последовательности расщепленных членов 965 библиотеки нуклеиновых кислот, которые могут соответствовать последовательностям, которые были представлены в образце нуклеиновой кислоты 905.
[0645] Сайт-направленный полипептид 950 может содержать аффинную метку 955. Необязательно, сайт-направленный полипептид 950 может представлять собой ферментативно неактивный вариант сайт-направленного полипептида. Согласно некоторым вариантам реализации настоящего изобретения ферментативно неактивный сайт-направленный полипептид может быть приведен в контакт с гибридизованной библиотекой нуклеиновых кислот (например, комплекс 946). Сайт-направленный полипептид может связываться с гибридизованными членами библиотеки нуклеиновых кислот, но не может отщеплять их. Сайт-направленный полипептид может быть подвергнут аффинной очистке 970 с использованием захватывающего агента 975, который может связываться с аффинной меткой 955. Необязательно, комплекс 946 может быть подвергнут аффинной очистке с использованием захватывающего агента, который может связываться с аффинной меткой 915. Члены библиотеки нуклеиновых кислот, подвергнутые аффинной очистке, могут быть подвергнуты секвенированию. В этом варианте реализации секвенированные члены библиотеки нуклеиновых кислот могут соответствовать последовательностям, которые представлены в образце нуклеиновой кислоты 905.
[0646] Секвенирование
[0647] Способы детектирования вариантов последовательности могут включать секвенирование вариантов. Определение последовательности может быть выполнено с использованием методов, позволяющих определять множество (как правило, от тысяч до миллионов) последовательностей нуклеиновых кислот по существу одновременно, в которых множество последовательностей считываются предпочтительно одновременно с помощью последовательного процесса с высокой пропускной способностью. Такие методы могут включать, но не ограничиваются ими, пиросеквенирование (например, метод, запущенный в серийное производство 454 Life Sciences, Inc., Бранфорд, Коннектикут, США); секвенирование путем лигирования (например, технология SOLiD™, запущенная в серийное производство Life Technology, Inc., Карлсбад, Калифорния, США); секвенирование путем синтеза с использованием модифицированных нуклеотидов (например, запущенные в серийное производство технологии TruSeq™ и HiSeq™ от Illumina, Inc., Сан-Диего, Калифорния, HeliScope™ от Helicos Biosciences Corporation, Кембридж, Массачусетс, и PacBio RS от Pacific Biosciences of California, Inc., Менло-Парк, Калифорния), секвенирование с помощью технологии детектирования ионов (Ion Torrent, Inc., Южный Сан-Франциско, Калифорния); секвенирование наношариков ДНК (Complete Genomics, Inc., Маунтин-Вью, Калифорния США); технологии секвенирования на основе нанопористых материалов (например, разработанные Oxford Nanopore Technologies, LTD, Оксфорд, Великобритания), капиллярное секвенирование (например, технология MegaBACE, запущенная в серийное производство Molecular Dynamics), электронное секвенирование, секвенирование одной молекулы (например, технология SMRT™, запущенная в серийное производство Pacific Biosciences, Менло-Парк, Калифорния), капельное микроструйное секвенирование, секвенирование с помощью гибридизации (например, технологии, коммерчески доступные от Affymetrix Inc, Санта-Клара, Калифорния), секвенирование с использованием бисульфата, и другие известные методы высокоэффективного распараллеленного секвенирования.
[0648] ПЦР в реальном времени
[0649] Способы детектирования вариантов последовательности могут включать детектирование вариантов с использованием метода ПЦР в реальном времени. Определение последовательности может быть выполнено с использованием полимеразной цепной реакции в режиме реального времени (ПЦР-РВ, также называемой количественной ПЦР (qPCR)) для количественного детектирования поддающейся амплификации нуклеиновой кислоты, присутствующей в образце. кПЦР представляет собой методику, основанную на полимеразной цепной реакции, которая может быть использована для амплификации и одновременного количественного определения нуклеиновой кислоты-мишени. кПЦР может обеспечивать как детектирование, так и количественное определение специфичной последовательности в образце нуклеиновой кислоты-мишени. Этот способ может следовать общему принципу полимеразной цепной реакции, с дополнительной возможностью количественного определения амплифицированной нуклеиновой кислоты-мишени, поскольку она накапливается в ходе реакции в режиме реального времени после каждого цикла амплификации. Два способа количественного определения могут включать: (1) использование флуоресцентных красителей, которые встраиваются между нуклеотидами двухцепочечной нуклеиновой кислоты-мишени, и (2) использование модифицированных зондов на основе олигонуклеотидов ДНК, которые флуоресцируют при гибридизации с комплементарной нуклеиновой кислотой-мишенью. В соответствии с первым способом краситель, связывающийся с нуклеиновой кислотой-мишенью, может связываться со всей двухцепочечной (дц) нуклеиновой кислотой при ПЦР, что приводит к испусканию красителем флуоресцентного сигнала. Увеличение количества продукта нуклеиновой кислоты в процессе ПЦР, следовательно, может привести к увеличению интенсивности флуоресценции и может быть измерено в каждом цикле, обеспечивая тем самым количественное определение концентраций нуклеиновых кислот. Реакционная смесь может быть приготовлена аналогично стандартной реакционной смеси для ПЦР с добавлением флуоресцентного красителя (дц) нуклеиновых кислот. Реакция может быть запущена в амплификаторе, и после каждого цикла интенсивность флуоресценции может быть измерена с помощью детектора; краситель может флуоресцировать только при связывании с (дц) нуклеиновой кислотой (т.е. продуктом ПЦР). При нормировании с учетом стандартного разбавления, концентрация (дц) нуклеиновой кислоты может быть определена при выполнении ПЦР. Полученные величины не могут иметь абсолютных единиц, связанных с ними. Сравнение интенсивности сигнала в измеренном образце ДНК/РНК с интенсивностью для стандартного разбавления может дать фракцию или отношение интенсивности сигнала образца к интенсивности сигнала стандарта, что позволяет провести относительные сравнения между различными тканями или экспериментальными условиями. Для обеспечения точности при количественном определении, уровень экспрессии гена-мишени может быть нормирован к уровню стабильно экспрессированного гена. Такое нормирование может обеспечить коррекцию для учета возможных различий в количестве нуклеиновой кислоты или качестве различных образцов. В соответствии со вторым способом РНК- или ДНК-зонд, специфичный в отношении последовательности, можно использовать для количественного определения только нуклеиновой кислоты, содержащей последовательность зонда; следовательно, использование репортерного зонда может увеличить специфичность, и может обеспечить количественное определение даже в присутствии незначительной амплификации неспецифической нуклеиновой кислоты. Такой способ может обеспечить мультиплексирование (т.е. количественное определение нескольких генов в одной и той же реакции с использованием специфичных зондов с метками разного цвета), при условии, что все гены амплифицированы с одинаковой эффективностью. Этот способ можно осуществлять с использованием зонда на основе нуклеиновой кислоты с флуоресцентным репортером (например, 6-карбоксифлуоресцеином) на одном конце и гасителем флуоресценции (например, 6-карбокситетраметилродамином) на противоположном конце зонда. Близость репортера к гасителю может предотвратить детектирование его флуоресценции. Распад зонда в результате 5'-3'-экзонуклеазной активности полимеразы (например, Taq-полимеразы) может нарушить близость репортера и гасителя, и, следовательно, может обеспечить испускание детектируемой флуоресценции без тушения. Увеличение количества продукта, который является мишенью репортерного зонда в каждом цикле ПЦР, может привести к пропорциональному увеличению интенсивности флуоресценции за счет распада зонда и высвобождения репортера.
[0650] Реакционную смесь можно приготовить аналогично стандартной реакционной смеси для ПЦР с добавлением репортерного зонда. После начала реакции, на этапе отжига ПЦР, зонд и праймеры могут ренатурировать с нуклеиновой кислотой-мишенью. Полимеризация новой цепи ДНК может быть инициирована, начиная от последовательностей праймеров, и как только полимераза достигает зонда, ее 5'-3'-экзонуклеазная активность может разрушить зонд, что приводит к физическому отделению флуоресцентного репортера от гасителя с последующим увеличением интенсивности флуоресценции. Флуоресценцию можно детектировать и измерять в амплификаторе для ПЦР в реальном времени, и геометрическое увеличение интенсивности флуоресценции, которое может соответствовать экспоненциальному увеличению количества продукта, используется для определения порогового цикла в каждой реакции. Относительные концентрации ДНК, присутствующей во время экспоненциальной фазы реакции, могут быть определены путем построения зависимости интенсивности флуоресценции от количества циклов на логарифмической шкале (экспоненциально увеличивающееся количество может дать прямую линию). Может быть определен порог для детектирования интенсивности флуоресценции, которая превышает неспецифический сигнал. Цикл, в котором интенсивность флуоресценции образца превышает порог, может быть назван пороговым циклом, Ct. Поскольку количество ДНК может удваиваться в каждом цикле во время экспоненциальной фазы, то можно вычислить относительные количества ДНК (например, образец с Ct на 3 цикла раньше, чем у другого образца, имеет 23=8 раз больше матрицы). Количества нуклеиновой кислоты (например, РНК или ДНК) можно определить путем сравнения результатов со стандартной кривой, полученной с помощью ПЦР в реальном времени для серийных разведении (например, неразбавленный образец, 1:4, 1:16, 1:64) известного количества нуклеиновой кислоты. Реакция кПЦР может включать подход на основе применения двойного флуорофора, который использует резонансный перенос энергии флуоресценции (FRET), (например, зонды для гибридизации LightCycler, где два олигонуклеотидных зонда могут гибридизоваться с ампликоном). Олигонуклеотиды могут быть сконструированы для гибридизации в ориентации голова-к-хвосту с флуорофорами, разделенными расстоянием, которое совместимо с эффективным переносом энергии. Другие примеры меченых олигонуклеотидов, которые структурированы так, чтобы испускать сигнал при связывании с нуклеиновой кислотой или при встраивании в продукт удлинения, включают: зонды Scorpions, праймеры Sunrise (или AMPLIFLOUR), и праймеры LUX и зонды MOLECULAR BEACONS. Для проведения реакции методом кПЦР можно использовать флуоресцентную методологию Taqman и устройство, способное измерять флуоресценцию в режиме реального времени (например, детектор последовательностей ABI Prism 7700). Реакция Taqman может протекать с использованием зонда для гибридизации, меченного двумя различными флуоресцентными красителями. Один краситель может представлять собой репортерный краситель (6-карбоксифлуоресцеин), другой краситель может представлять собой гаситель (6-карбокситетраметилродамин). Если зонд является интактным, то может происходить перенос энергии флуоресценции, и флуоресценция, испускаемая репортерным красителем, может поглощаться гасящим красителем. Во время фазы элонгации цикла ПЦР флуоресцентный зонд для гибридизации может быть расщеплен в результате 5'-3' нуклеолитической активности ДНК-полимеразы. При расщеплении зонда энергия флуоресценции, испускаемая репортерным красителем, больше не может эффективно передаваться гасящему красителю, что приводит к увеличению интенсивности флуоресценции репортерного красителя в характерной для него части спектра. Любой способ количественного определения нуклеиновой кислоты, включая способы в режиме реального времени или способы одноточечного детектирования, можно использовать для определения количества нуклеиновой кислоты в образце. Детектирование может быть выполнено с использованием нескольких различных методик (например, окрашивание, гибридизация с меченым зондом; введение биотинилированных праймеров с последующим детектированием конъюгата авидин-фермент; включение32Р-меченых дезоксинуклеотидтрифосфатов, таких как дЦТФ или дАТФ, в амплифицированный сегмент. Количественное определение может включать стадию амплификации или может не включать ее. Количественное определение не может быть экспериментальным.
[0651] Микрочип
[0652] Способы детектирования вариантов последовательности могут включать секвенирование и/или детектирование вариантов с использованием микрочипа. Микрочипы можно использовать для определения уровня экспрессии множества генов в образце нуклеиновой кислоты. Микрочипы можно использовать для определения идентичности последовательности из множества последовательностей в образце нуклеиновой кислоты.
[0653] Микрочип может содержать субстрат. Субстраты могут включать, но не ограничиваются ими, стекло и модифицированные или функционализированные виды стекла, пластмассы (включая акрилы, полистирол и сополимеры стирола и других материалов, полипропилен, полиэтилен, полибутилен, полиуретаны, Тефлон™ и т.п.), полисахариды, нейлон или нитроцеллюлозу, смолы, диоксид кремния или материалы на основе диоксида кремния, включая кремний и модифицированный кремний, углерод, металлы, неорганические стекла и пластмассы.
[0654] Микрочипы могут содержать множество полинуклеотидных зондов. Микрочип может содержать приблизительно 1, 10, 100, 1000, 5000, 10000, 20000, 30000, 40000, 50000, 60000, 70000, 80000, 90000, 100000, 110000, 120000 или более зондов.
[0655] Зонды могут содержать по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140 или более нуклеотидов в длину.
[0656] Согласно некоторым вариантам реализации настоящего изобретения зонды могут содержать информацию о последовательности для конкретного набора генов и/или видов. Зонд может быть комплементарен последовательности нуклеиновой кислоты, кодирующей белок хозяина. Зонд может быть комплементарен некодирующей последовательности нуклеиновой кислоты. Зонд может быть комплементарен последовательности ДНК. Зонд может быть комплементарен последовательности РНК.
[0657] Зонды могут быть иммобилизованы на микрочипе. Иммобилизация полинуклеотидов на твердом субстрате может быть достигнута путем прямого синтеза (например, фотолитографического синтеза) полинуклеотидов на твердом субстрате или путем иммобилизации (локального нанесения) ранее синтезированных полинуклеотидов на заранее определенные области твердого субстрата. Полинуклеотиды могут быть иммобилизованы на субстрате микрочипа путем активации поверхности твердого субстрата с использованием нуклеофильной функциональной группы (например, аминогруппы), связывания биологических молекул (например, полинуклеотидов), активированных с использованием соответствующей уходящей группы, с поверхностно-активированным твердым субстратом, и с последующим удалением не вступивших в реакцию реагентов. Зонды могут быть иммобилизованы на грануле, которая дополнительно конъюгирована посредством ковалентной или ионной связи с твердым субстратом. Зонды могут быть иммобилизованы на субстрате с использованием специфичной пленки, имеющей низкую проводимость и низкую температуру плавления, в частности, золотой пленки. Обработка электромагнитным излучением может расплавить и может удалить пленку в сайте столкновения. Пленка может находиться в контакте с коллоидной дисперсией и при плавлении может создавать конвективный поток в реакционном участке, что приводит к присоединению нерастворимой частицы в дисперсии к конкретному расплавленному участку.
[0658] С помощью микрочипа можно исследовать образец нуклеиновой кислоты, содержащий нуклеиновую кислоту неизвестной идентичности (например, испытываемый образец), путем сравнения образца нуклеиновой кислоты неизвестной идентичности с эталонным образцом. Образец нуклеиновой кислоты может быть получен из ДНК (например, выделенной ДНК, геномной ДНК, внехромосомной ДНК). Образец нуклеиновой кислоты может быть получен из РНК. РНК может быть подвергнута обратной транскрипции с образованием ДНК, используя геноспецифичный праймер или универсальный праймер. ДНК, полученная в результате обратной транскрипции (например, кДНК), может быть обработана РНКазой или основанием (например, NaOH) для гидролиза РНК. Молекула кДНК может быть помечена красителем (например, Су3, Су5) посредством реакций с участием N-гидроксисукцинимида или аналогичных реагентов для введения меток. Подходящие флуоресцентные красители могут включать различные коммерческие красители и производные красителей, такие как те, которые обозначены Alexa, флуоресцеин, родамин, FAM, TAMRA, Joe, ROX, техасский красный, BODIPY, FITC, орегоновый зеленый, Lissamine и другие. Эталонный образец и испытываемый образец могут быть помечены различными красителями.
[0659] Испытываемый образец и эталонный образец могут быть нанесены на микрочип так, чтобы взаимодействовать с несколькими точками одновременно. Испытываемый образец и эталонный образец могут быть нанесены на микрочип в условиях подходящих для гибридизации, которые могут обеспечить связывание нуклеиновых кислот в образце нуклеиновой кислоты с комплементарным зондом на микрочипе. Различные стадии реакции могут быть выполнены с использованием связанных молекул на микрочипе, включая стадии промывки связанных молекул реагентов. Прогресс или результат реакции можно контролировать для каждого пятна (например, зонда) на микрочипе, чтобы охарактеризовать образец нуклеиновой кислоты, иммобилизованной на чипе. Исследование с использованием микрочипа, как правило, может потребовать инкубационного периода, который может варьироваться от нескольких минут до нескольких часов. Продолжительность инкубационного периода может зависеть от конкретного способа количественного исследования и может быть определена с помощью различных факторов, таких как тип реагента, степень перемешивания, объем пробы, количество копий мишени и плотность чипа. Во время инкубационного периода нуклеиновые кислоты в образце нуклеиновой кислоты могут находиться в тесном контакте с зондами микрочипа.
[0660] Детектирование можно осуществлять с использованием конфокального сканирующего микроскопа, оснащенного лазерными источниками возбуждения и ФЭУ для детектирования, например, ScanArray 3000, доступного от GSI Lumonics (Биллерика, Массачусетс, США). Конфокальные и неконфокальные системы детектирования флуоресценции могут быть использованы для реализации указанного способа, такие как те, которые доступны от Axon Instruments (Фостер Сити, Калифорния), Genetic MicroSystems (Санта-Клара, Калифорния), Molecular Dynamics (Саннивейл, Калифорния) и Virtek (Вобурн, Массачусетс). Альтернативные системы детектирования могут включать сканирующие системы, в которых применяются газовые, диодные и твердотельные лазеры, а также те, в которых применяются различные другие типы источников света, такие как ксеноновые и галогеновые лампы. В дополнение к фотоэлектронным умножителям, детекторы могут включать камеры, в которых применяются приборы с зарядовой связью (ПЗС-матрицы) и чипы на основе комплементарных структур «металл-оксид-полупроводник» (CMOS).
[0661] Для каждого зонда можно сравнить отношение интенсивностей свечения двух красителей из испытываемого образца и эталонного образца. Интенсивность сигнала, детектированного в конкретном пятне микрочипа, может быть прямо пропорциональна степени гибридизации нуклеиновой кислоты в образце с зондом в конкретном пятне (например, пятно содержит зонд). Исследование интенсивностей флуоресценции гибридизованных микрочипов может включать сегментацию пятна, определение неспецифического сигнала (и, возможно, вычитание), устранение нецелевых пятен, с последующим нормированием для корректировки любого оставшегося шума. Методики нормирования могут включать общее нормирование всех пятен или подгруппы пятен, таких как конститутивные гены, пре-лог сдвиг для достижения наилучшего соответствия начальных значений, или, в случае двухканальной (или более) гибридизации, нахождение наилучшего соответствия, которое помогает получить графическую зависимость М от А, которая центрирована относительно М=0, и/или которая помогает получить графическую зависимость log(Red) от log(Green), которая центрирована относительно диагонали с наименьшим рассеянием. График зависимости М от А также можно называть графиком зависимости R от I, где R представляет собой соотношение, такое как R = log2(Red/Green), и I представляет собой интенсивность, например, I = log VRed * Green. Масштабирование, сдвиг, нахождение наилучшего соответствия по всем диаграммам разброса данных и т.д., можно использовать в качестве методик нормирования наборов данных, полученных с помощью микрочипов, а также для получения наилучшей математической модели для последующего исследования. Большинство из этих методик нормирования основывается на ряде основополагающих гипотез (например, «большинство генов в рамках исследования не сильно различаются»).
[0662] Меченые нуклеиновые кислоты и способы их применения
[0663] Общий обзор
[0664] В настоящем изобретении предложены наборы, способы и композиции для меченых нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке. На ФИГ. 10 показан примерный вариант реализации нуклеиновой кислоты, направленной против нуклеиновой кислоты, 1005 согласно настоящему изобретению. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать одну или более ненативных последовательностей (например, меток) 1010/1015. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать ненативную последовательность 1010/1015 на 3'-конце, 5'-конце, или на обоих 3'-конце и 5'-конце нуклеиновой кислоты, направленной против нуклеиновой кислоты.
[0665] В некоторых случаях нуклеиновая кислота, направленная против нуклеиновой кислоты, может представлять собой нуклеиновую кислоту, направленную против нуклеиновой кислоты, описанную в настоящей заявке, и содержит одну или более ненативных последовательностей, например, на 3'-конце, 5'-конце или на обоих 3'-конце и 5' конце нуклеиновой кислоты, направленной против нуклеиновой кислоты.
[0666] В некоторых случаях нуклеиновая кислота, направленная против нуклеиновой кислоты, представляет собой двойную направляющую нуклеиновую кислоту, направленную против нуклеиновой кислоты, описанную в настоящей заявке, и как показано на Фиг. 11. Двойная направляющая нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать две молекулы нуклеиновой кислоты 1105/1110. Двойная направляющая нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать множество ненативных последовательностей 1115/1120/1125/1130. Ненативная последовательность может быть расположена на 3'-конце, 5'-конце или обоих 3'- и 5'-концах каждой молекулы нуклеиновой кислоты, направленной против нуклеиновой кислоты. Например, ненативная последовательность может быть расположена на 3'-конце, 5'-конце или обоих 3'- и 5'-концах первой молекулы нуклеиновой кислоты 1105. Ненативная последовательность может быть расположена на 3'-конце, 5'-конце или обоих 3'- и 5'-концах второй молекулы 1110. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать одну или более ненативных последовательностей в любой из конфигураций, перечисленных на Фиг. 11.
[0667] В настоящем изобретении предложены способы применения меченых нуклеиновых кислот, направленных против нуклеиновой кислоты. Способ может быть выполнен с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке. В некоторых случаях множество меченых нуклеиновых кислот, направленных против нуклеиновой кислоты, может быть приведено в контакт с множеством нуклеиновых кислот-мишеней. На Фиг. 12 показан примерный способ применения меченых нуклеиновых кислот, направленных против нуклеиновой кислоты. Меченая нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать спейсер 1210, который может гибридизоваться с нуклеиновой кислотой-мишенью 1205. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать ненативную последовательность (например, метку) 1220. Ненативная последовательность 1220 может представлять собой последовательность связывания РНК-связывающего белка. В некоторых случаях ненативная последовательность 1220 может представлять собой последовательность связывания РНК-связывающего белка CRISPR. Ненативная последовательность 1220 может быть связана с РНК-связывающим белком 1215. РНК-связывающий белок 1215 может содержать ненативную последовательность 1225 (например, гибридную последовательность, т.е. РНК-связывающий белок 1215 может представлять собой гибридный полипептид). Ненативная последовательность (например, гибридная последовательность) 1225 может изменять транскрипцию нуклеиновой кислоты-мишени и/или экзогенной нуклеиновой кислоты. Ненативная последовательность (например, гибридная последовательность) 1225 может содержать первую часть комбинированной системы.
[0668] Согласно некоторым вариантам реализации настоящего изобретения вторая нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая второй спейсер 1240, который может гибридизоваться со второй нуклеиновой кислотой-мишенью 1245, может содержать вторую ненативную последовательность (например, метку) 1250. Вторая ненативная последовательность (например, метка) 1250 может представлять собой последовательность связывания РНК-связывающего белка. Вторая ненативная последовательность (например, метка) 1250 может представлять собой последовательность связывания РНК-связывающего белка CRISPR. Вторая ненативная последовательность 1250 может быть связана с РНК-связывающим белком 1235. РНК-связывающий белок может содержать ненативную последовательность 1230 (например, гибридную последовательность, т.е. РНК-связывающий белок 1235 может представлять собой гибридную последовательность). Ненативная последовательность 1230 (например, гибридная последовательность) может представлять собой вторую часть комбинированной системы.
[0669] В некоторых случаях первая часть комбинированной системы 1225 и вторая часть комбинированной системы 1230 могут быть расположены близко друг к другу так, что первая часть комбинированной системы 1225 и вторая часть комбинированной системы 1230 взаимодействуют 1255 с образованием активной комбинированной системы 1260. Активная комбинированная система 1260 может называться цельной системой, причем первая часть и вторая часть образуют целую комбинированную систему. Активация комбинированной системы может указывать на то, что две нуклеиновые кислоты-мишени 1205/1245 расположены близко друг к другу в пространстве.
[0670] Способы
[0671] В настоящем изобретении предложены способы, обеспечивающие приведение нуклеиновой кислоты-мишени в контакт с комплексом, содержащим сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты, и введение одного или более эффекторных белков, причем один или более эффекторных белков содержат ненативную последовательность и могут связываться с модифицированной нуклеиновой кислотой, направленной против нуклеиновой кислоты. Эффекторный белок может относиться к любому белку с функциональным действием. Например, Эффекторный белок может иметь ферментативную активность, может ремоделировать биологические молекулы (например, складывающие шапероны), может представлять собой поддерживающий белок, и/или связывать малую молекулу или метаболит. Эффекторный белок может модифицировать нуклеиновую кислоту-мишень (например, осуществлять расщепление, ферментативную модификацию, транскрипционную модификацию). Способы согласно настоящему изобретению предусматривают применение композиций согласно настоящему изобретению в качестве биосенсоров. Например, комплексы (например, содержащие модифицированную нуклеиновую кислоту, направленную против нуклеиновой кислоты, сайт-направленный полипептид и/или Эффекторный белок) можно применять для контроля событий, относящихся к перемещению генетических элементов, детектирования близости расположения последовательностей относительно друг друга в трехмерном пространстве, и условного изменения транскрипции.
[0672] События, относящиеся к перемещению генетических элементов
[0673] В настоящем изобретении предложены способы определения событий, относящихся к перемещению генетических элементов. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке. События, относящиеся к перемещению генетических элементов, включают, например, транслокацию, рекомбинацию, встраивание, транспозицию, событие горизонтального переноса генов, трансформацию, трансдукцию, конъюгацию, событие генной конверсии, дублирование, транслокацию, инверсию, делецию, замещение или любую их комбинацию.
[0674] Событие, относящееся к перемещению генетических элементов, может включать рекомбинацию между генами. Рекомбинация может привести к образованию вредных генных продуктов (например, рекомбинация BCR-ABL, которая может способствовать развитию рака молочной железы). Рекомбинация может включать, например, гомологичную рекомбинацию, негомологичную рекомбинацию (например, негомологичное соединение концов) и рекомбинацию V(D)J. Рекомбинация может относиться к перекресту хромосом. Рекомбинация может произойти во время профазы I мейоза (например, синапсиса). Рекомбинация может включать двухцепочечный разрыв нуклеиновых цепей ДНК, с последующим образованием структуры Холлидея под действием рекомбиназ, которые могут катализировать перестановку цепей ДНК.
[0675] События, относящиеся к перемещению генетических элементов, могут привести к заболеванию. Например, в результате события, относящегося к перемещению генетических элементов, может развиться хронический миелолейкоз. Транслокация между хромосомой 9 и 22 может привести к образованию гибридного гена BCR-ABL1, который может привести к удлинению одной хромосомы (например, 9), и укорочению другой хромосомы (например, 22, т.е. к образованию филадельфийской хромосомы). Транслокация BCR-ABL1 может привести к образованию гибридного белка BCR-ABL, который может взаимодействовать с рецепторами (например, рецептором интерлейкина-3) для усиления деления клеток, что приводит к хроническому миелолейкозу (ХМЛ). Другие неограничивающие примеры событий, относящихся к перемещению генетических элементов, включают BRD3-NUT, BRD4-NUT, KIAA1549-BRAF, FIG/GOPC-ROS1, ETV6-NTRK3, BCAS4-BCAS3, TBL1XR1-RGS17, ODZ4-NRG1, MALAT1-TFEB, APSCR1-TFE3, PRCC-TFE3, CLTC-TFE3, NONO-TFE3, SFPQ-TFE3, ETV6-NRTK3, EML4-ALK, EWSR1-ATF1, MN1-ETV6, CTNNB1-PLAG1, LIFR-PLAG1, TCEA1-PLAG1, FGFr1-PLAG1, CHCHD7-PLAG1, HMGA2-FHIT, HMGA-NFIB, CRTC1-MAM12, CRCT3-MAML2, EWSR1-POUF5F1, TMPRSS1-ERG, TMPRSS2-ETV4, TMPRSS2-ETV5, HNRNPA2B1-ETV1, HERV-K-ETV1, C150RF21-ETV1, SLC45A3-ETV1, SLC45A3-ETV5, SLC45A3-ELK4, KLK2-ETV4, CANT1-ETV4, RET-PTC1/CCDC6, RET-PTC2/PRKAR1A, RET-PTC3,4/NCOA4, RET-PTC5/GOLGA5, RET-PTC6/TRIM24, RET-PTC7/TRIM33, RET-PTC8/KTN1, RET-PTC9/RFG9, RET-PTCM1, TFG-NTRK1, TPM3-NRTK1, TPR-NRTK1, RET-D10S170, ELKS-RET, HOOKS3-RET, RFP-RET, AKAP9-BRAF и PAX8-PPARG.
[0676] Заболевания, которые могут быть вызваны событиями, относящимися к перемещению генетических элементов, могут включать заболевание Шарко-Мари-Тута типа 1А (СМТ1А), ювенильный нефронофтиз (NPH), сцепленный с Х-хромосомой ихтиоз, семейный дефицит гормона роста типа 1А, плече-лопаточно-лицевую форму мышечной дистрофии (ЛЛПД), α-талассемию, гемофилию А, синдром Хантера (т.е. мукополисахаридоз II), мышечную дистрофию Эмери-Дрейфуса, гемоглобин Лепора, дефицит стероид-21-гидроксилазы, подавляемый глюкокортикоидами гиперальдостеронизм (GSH), дальтонизм (например, дихроматическое зрение), аутосомно-рецессивную спинальную мышечную атрофию (SMA), рак, Т-клеточный острый лимфобластный лейкоз (Т-ОЛЛ), агрессивную срединную карциному, астроцитому, секреторную карциному молочной железы, рак молочной железы, карциному почек, аденомиосаркому, аденокарциному легких, меланому, менингиому, полиморфную аденому, мукоэпидермоидный рак, рак предстательной железы, рак щитовидной железы и острый промиелоцитарный лейкоз.
[0677] Способы согласно настоящему изобретению предусматривают определение событий, относящихся к перемещению генетических элементов, и включают приведение нуклеиновой кислоты-мишени в контакт с двумя комплексами, причем каждый комплекс содержит сайт-направленный полипептид и модифицированную нуклеиновую кислоту, направленную против нуклеиновой кислоты, и введение двух или более эффекторных белков, причем два или более эффекторных белков могут связываться с модифицированными нуклеиновыми кислотами, направленными против нуклеиновой кислоты, при этом один из двух или более эффекторных белков содержит ненативную последовательность, которая представляет собой первую часть комбинированной системы, и один из двух или более эффекторных белков содержит ненативную последовательность, которая представляет собой вторую часть комбинированной системы. Комбинированная система может относиться к белковому комплексу, состоящему из двух или более фрагментов белка, которые по отдельности не являются флуоресцентными, но, при объединении в комплекс, образуют функциональный (то есть флуоресцирующий) флуоресцентный белковый комплекс. Отдельные белковые фрагменты комбинированной системы (например, комбинированный флуоресцентный белок) могут называться «дополняющие фрагменты» или «комплементарные фрагменты». Дополняющие фрагменты, которые могут спонтанно собираться в функциональный флуоресцентный белковый комплекс, известны как самодополняющие фрагменты, самособирающиеся фрагменты или спонтанно связывающиеся дополняющие фрагменты. Например, комбинированная система может содержать GFP. В комбинированной системе, содержащей GFP, дополняющие фрагменты получены из трехмерной структуры GFP, которая включает одиннадцать анти-параллельных внешних бета-цепей и одну внутреннюю альфа-цепь. Первый фрагмент может содержать одну из одиннадцати бета-цепей молекулы GFP (например, GFP S11), и второй фрагмент может содержать оставшиеся цепи (например, GFP S1-10).
[0678] Перед событием перемещения генетических элементов последовательность нуклеиновой кислоты-мишени, которая является мишенью одного комплекса, может находиться на значительном удалении от последовательности нуклеиновой кислоты-мишени, которая является мишенью другой последовательности. Расстояние между последовательностями двух нуклеиновых кислот-мишеней может составлять по меньшей мере приблизительно 0,1, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более тысяч пар оснований. Расстояние между последовательностями двух нуклеиновых кислот-мишеней может составлять не более чем приблизительно 0,1, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более тысяч пар оснований. Последовательности двух нуклеиновых кислот-мишеней могут быть расположены на разных хромосомах. Последовательности двух нуклеиновых кислот-мишеней могут быть расположены на одной и той же хромосоме.
[0679] Перед событием перемещения генетических элементов эффекторные белки, которые представляют собой части комбинированной системы, могут быть неспособны взаимодействовать друг с другом (например, комбинированная система может быть неактивной). После события перемещения генетических элементов последовательность нуклеиновой кислоты-мишени, которая является мишенью для одного комплекса, может быть расположена поблизости от последовательности нуклеиновой кислоты-мишени, которая является мишенью другого комплекса. После события перемещения генетических элементов эффекторные белки, которые представляют собой фрагменты комбинированной системы, приобретают способность взаимодействовать друг с другом, активируя тем самым комбинированную систему.
[0680] Активированная комбинированная система может указывать на то, что произошло перемещение генетических элементов. Например, если активированная комбинированная система представляет собой комбинированную систему на основе флуоресцентного белка, то перед событием перемещения генетических элементов флуоресценция может не детектироваться в образце. В некоторых случаях интенсивность флуоресценции неактивной комбинированной системы (например, фоновые уровни) может быть в 0,01, 0,05, 0,1, 0,5, 1, 1,5, 2, 2,5, 3, 3,5 или более раз ниже, чем интенсивность флуоресценции в контрольном образце (например, в клетке), который не содержит комбинированной системы. В некоторых случаях интенсивность флуоресценции неактивной комбинированной системы (например, фоновый уровень) может быть в 0,01, 0,05, 0,1, 0,5, 1, 1,5, 2, 2,5, 3, 3,5 или более раз выше, чем интенсивность флуоресценции в контрольном образце (например, в клетке), который не содержит комбинированной системы.
[0681] После перемещения генетических элементов, две разделенные части могут объединиться с образованием активного флуоресцентного белка, и в образце может детектироваться флуоресценция. Активная комбинированная система может привести к увеличению интенсивности флуоресценции по меньшей мере приблизительно в 0,1, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более раз. Активная комбинированная система может привести к увеличению интенсивности флуоресценции более чем приблизительно в 0,1, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более раз.
[0682] Детектирование перемещения генетических элементов можно использовать для определения генотипа субъекта (например, пациента). Генотип может указывать на риск развития заболевания. Детектирование перемещения генетических элементов можно использовать для постановки диагноза субъекта. Генетическая и диагностическая информация, полученная в результате осуществления способов, описанных в настоящей заявке, может быть передана субъекту. Генетическая и диагностическая информация, полученная в результате осуществления способов, описанных в настоящей заявке, может быть использована для разработки плана лечения для конкретного субъекта. Например, если данные, полученные при осуществлении способов согласно настоящему изобретению, показывают, что пациент имеет генотип, который придает ему устойчивость к конкретной терапевтической схеме, то для указанного субъекта может быть разработан новый план лечения.
[0683] Изменение транскрипции
[0684] Способы согласно настоящему изобретению могут предусматривать изменение транскрипции нуклеиновой кислоты. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке. Указанный способ предусматривает приведение нуклеиновой кислоты-мишени в контакт с двумя комплексами, причем каждый комплекс содержит сайт-направленный полипептид и модифицированную нуклеиновую кислоту, направленную против нуклеиновой кислоты, и введение двух или более эффекторных белков, причем два или более эффекторных белков могут связываться с модифицированной нуклеиновой кислотой, направленной против нуклеиновой кислоты, при этом один из двух или более эффекторных белков содержит ненативную последовательность, которая является первой частью комбинированной системы факторов транскрипции, и один из двух или более эффекторных белков содержит ненативную последовательность, которая является второй частью комбинированной системы факторов транскрипции, причем взаимодействие между первой частью и второй частью комбинированной системы приводит к образованию фактора транскрипции, который изменяет транскрипцию нуклеиновой кислоты.
[0685] Фактор транскрипции может изменить уровни транскрипции нуклеиновой кислоты и/или нуклеиновой кислоты-мишени. Измененная транскрипция может включать повышенные уровни транскрипции и/или пониженные уровни транскрипции. Фактор транскрипции может повысить или понизить уровни транскрипции более чем в 2 раза, 3 раза, 5 раз, 10 раз, 50 раз, 100 раз, 1000 раз или более относительно неизмененных уровней транскрипции. Фактор транскрипции может повысить или понизить уровни транскрипции менее чем в 2 раза, 3 раза, 5 раз, 10 раз, 50 раз, 100 раз, 1000 раз или более относительно неизмененных уровней транскрипции.
[0686] Фактор транскрипции может изменить транскрипцию нуклеиновой кислоты-мишени и/или экзогенной нуклеиновой кислоты. Нуклеиновая кислота-мишень может представлять собой нуклеиновую кислоту, которая взаимодействует с комплексом, содержащим сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты. Экзогенная нуклеиновая кислота может содержать донорный полинуклеотид, плазмиду и/или нуклеиновую кислоту-мишень.
[0687] Экзогенная нуклеиновая кислота может содержать кодирующие полинуклеотид гены, которые вовлечены в апоптоз. Подходящие гены, вовлеченные в апоптоз, могут включать фактор некроза опухоли (TNF), TNF-R1, TNF-R2, связанный с TNF-рецептором протеин домена смерти (TRADD), Fas-рецептор и Fas-лиганд, каспазы (например, каспазу-3, каспазу-8, каспазу-10), Apaf-1, FADD и индуцирующий апоптоз фактор (AIF). Экзогенная нуклеиновая кислота может содержать кодирующие полинуклеотид гены, которые приводят к лизису клеток. Подходящие гены могут включать белок смерти аденовируса (ADP), дефенсины, лизирующие мембрану пептиды, полученные из c-FLIP, прокаспазы, проникающие в клетки пептиды, например, HIV ТАТ. Экзогенная нуклеиновая кислота может содержать полинуклеотид, кодирующий антиген, который может привести к привлечению иммунных клеток к месту локализации клеток (например, пептиды класса ГКГС). Экзогенная нуклеиновая кислота может содержать полинуклеотид, кодирующий нуклеиновую кислоту, направленную против нуклеиновой кислоты, мишенью которой являются многократно повторяющиеся в геноме последовательности (например, микроспутники, тандемные повторы), что приводит к крупномасштабной фрагментации генома и гибели клеток.
[0688] Модификация нуклеиновой кислоты-мишени
[0689] В настоящем изобретении предложены способы модификации нуклеиновой кислоты-мишени с использованием нуклеиновой кислоты, направленной против нуклеиновой кислоты, согласно настоящему изобретению. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке. Например, нуклеиновая кислота-мишень может быть приведена в контакт с комплексом, содержащим сайт-направленный полипептид, нуклеиновую кислоту, направленную против нуклеиновой кислоты, и один или более эффекторных белков, при этом один или более эффекторных белков содержат ненативную последовательность и могут связываться с модифицированной нуклеиновой кислотой, направленной против нуклеиновой кислоты. Ненативная последовательность может обеспечить ферментативную активность и/или транскрипционную активность эффекторному белку, для придания ему способности модифицировать нуклеиновую кислоту-мишень. Например, если эффекторный белок содержит ненативную последовательность, соответствующую метилтрансферазе, то метилтрансфераза может быть способна метилировать нуклеиновую кислоту-мишень. Модификация нуклеиновой кислоты-мишени может произойти на расстоянии по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или более нуклеотидов от 5'-конца или 3'-конца нуклеиновой кислоты-мишени. Модификация нуклеиновой кислоты-мишени может произойти на расстоянии не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или более нуклеотидов от 5'-конца или 3'-конца нуклеиновой кислоты-мишени. Модификация может произойти на отдельной нуклеиновой кислоте, которая не содержит нуклеиновую кислоту-мишень (например, на другой хромосоме).
[0690] Типичные модификации могут включать метилирование, ацетилирование, деметилирование, деацетилирование, убиквитинирование, деубиквитинирование, дезаминирование, алкилирование, депуринизацию, окисление, образование димера пиримидина, транспозицию, рекомбинацию, удлинение цепи, лигирование, гликозилирование, фосфорилирование, дефосфорилирование, аденилирование, деаденилирование, присоединение SUMO, удаление SUMO, рибозилирование, дерибозилирование, миристоилирование, ремоделирование, расщепление, окисление-восстановление, гидроксилирование и изомеризацию.
[0691] Определение генотипа и лечение
[0692] В настоящем изобретении предложены способы лечения заболевания с помощью нуклеиновой кислоты, направленной против нуклеиновой кислоты, согласно настоящему изобретению. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленного полипептида и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке. Например, с помощью комбинированной системы, описанной в настоящей заявке, можно выявить присутствие двух или более нуклеиновых кислот-мишеней поблизости друг от друга в пространстве (например, при перемещении генетических элементов, в структуре хроматина, или на линейной нуклеиновой кислоте), что может указывать на характерный генотип (например, у субъекта). Генотип может относиться к наличию или отсутствию определенной последовательности нуклеиновой кислоты, нуклеотидного полиморфизма (т.е. полиморфизма единичного нуклеотида или полиморфизма нескольких нуклеотидов), аллельного варианта, или любого другого признака, характерного для последовательности нуклеиновой кислоты. Генотип может указывать на то, страдает ли пациент от заболевания и/или он предрасположен к заболеванию.
[0693] Определение генотипа может включать, например, определение присутствия у субъекта мутантной последовательности (например, последовательности нуклеиновой кислоты, содержащей мутацию). В некоторых случаях первая нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая соответствующие компоненты, описанные в настоящей заявке, которые составляют первую часть комбинированной системы, может быть сконструирована так, что ее мишенью является область вблизи предсказанной мутированной последовательности. В некоторых случаях вторая нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая соответствующие компоненты, описанные в настоящей заявке, которые составляют вторую часть комбинированной системы, может быть сконструирована так, что ее мишенью является область, содержащая предсказанную мутированную последовательность. Если мутированная последовательность действительно существует, то вторая нуклеиновая кислота, направленная против нуклеиновой кислоты, может связываться с ней, и две части комбинированной системы могут взаимодействовать. Взаимодействие может генерировать сигнал, который указывает на наличие мутированной последовательности.
[0694] Генотип может быть идентифицирован с помощью биомаркера. Биомаркер может указывать на какой-либо физиологический процесс. Биомаркер может служить индикатором эффективности лечения (например, медикаментозного лечения). Биомаркер может представлять собой нуклеиновую кислоту, полипептид, аналит, растворенное вещество, малую молекулу, ион, атом, модификацию в нуклеиновой кислоте и/или полипептиде, и/или продукт деградации. Биомаркер может относиться к относительному уровню экспрессии нуклеиновой кислоты и/или полипептида.
[0695] Схема лечения, специфичная в отношении субъекта, может быть установлена на основании определения генотипа субъекта с использованием способов согласно настоящему изобретению. Например, если субъект имеет определенный генотип, который, как известно, не отвечает на конкретную терапию, то субъект может получать лечение с использованием другого вида терапии. В соответствии с результатами определения генотипа субъект может быть отобран или исключен из популяции для участия в клинических исследованиях.
[0696] Результаты определения генотипа могут быть переданы субъекту лицом, осуществляющим уход (например, от врача пациенту, или от лица, осуществляющего анализ генотипа, клиенту). Предоставление информации может произойти в личной форме (например, в кабинете врача), по телефону, в письменной форме, или в электронном виде. Предоставление информации может дополнительно увеличить осведомленность субъекта касательно схемы лечения, специфичной в отношении субъекта, которая была определена на основании данных о генотипе субъекта.
[0697] Указанный способ можно осуществлять у субъекта более одного раза (например, многократно). Например, может быть определен генотип субъекта, затем субъекту может быть назначен курс лечения, после этого генотип субъекта может быть определен повторно. Два генотипа могут быть сопоставлены, чтобы определить эффективность курса лечения. Схема лечения может быть изменена на основании результатов сравнения генотипов.
[0698] Расположение последовательностей в трехмерном пространстве
[0699] В некоторых случаях в настоящем изобретении предложен способ определения расположения последовательностей в трехмерном пространстве в клетке. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке. Определение трехмерной организации хроматина и нуклеиновой кислоты может иметь большое значение для понимания процессов регуляции генов, таких как активация транскрипции и/или репрессия генов. В некоторых случаях способ включает приведение нуклеиновой кислоты-мишени в контакт с двумя комплексами, причем каждый комплекс связывается со своей когнатной нуклеиновой кислотой-мишенью. Комплексы могут содержать сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты, согласно настоящему изобретению. Может быть введено два или более эффекторных белков, при этом каждый из двух или более эффекторных белков связывается с комплексом. Эффекторные белки могут быть сходны с комбинированной системой, описанной выше, причем каждый эффекторный белок может содержать неактивный фрагмент целого полипептида. Если эффекторные белки расположены в пространстве далеко друг от друга, то такие эффекторные белки являются неактивными (например, сигнал не детектируется). Если эффекторные белки расположены в пространстве достаточно близко для того чтобы взаимодействовать, то они могут образовать детектируемый активный полипептид.
[0700] Эффекторные белки могут быть частью системы комбинированной аффинной метки. В системе комбинированной аффинной метки два неактивных полипептидных фрагмента системы могут соответствовать двум неактивным фрагментам аффинной метки. Когда два фрагмента связываются вместе, то восстанавливается целая аффинная метка, так, что аффинная метка может поддаваться детектированию с помощью связывающего агента. Связывающий агент может относиться к молекуле, которая может связывать и обеспечивать очистку аффинной метки. Примеры связывающих агентов могут включать антитела, конъюгированные с антителами гранулы и конъюгированные с малыми молекулами гранулы.
[0701] Внедрение комплексов и полипептидов согласно настоящему изобретению может происходить путем инфекции вирусом или бактериофагом, трансфекции, конъюгации, слияния протопластов, электропорации, липофекции, осаждения фосфатом кальция, полиэтиленимин (ПЭИ)-опосредованной трансфекции, опосредованной DEAE-декстраном трансфекции, опосредованной липосомами трансфекции, технологии бомбардировки частицами, осаждения фосфатом кальция, прямой микроинъекции, опосредованной наночастицами доставки нуклеиновой кислоты и тому подобного.
[0702] Клетки можно культивировать с комплексами в течение по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более дней. Клетки можно культивировать с комплексами в течение не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более дней. После соответствующего периода времени (например, периода времени, достаточного для связывания комплексов с нуклеиновой кислотой-мишенью) клетки можно лизировать.
[0703] Клетки могут быть сшиты перед лизированием. Фиксированные или сшитые клетки могут стабилизировать комплексы белок-ДНК в клетке. Подходящие фиксаторы и сшивающие агенты могут включать формальдегид, глутаровый альдегид, фиксаторы на основе этанола, фиксаторы на основе метанола, ацетон, уксусную кислоту, тетраоксид осмия, бихромат калия, хромовую кислоту, перманганат калия, производные ртути, пикраты, формалин, параформальдегид, аминореактивные сшивающие агенты на основе NHS-эфира, такие как бис[сульфосукцинимидил]суберат (BS3), 3,3'-дитиобис-[сульфосукцинимидилпропионат] (DTSSP), этиленгликоль-бис-[сульфосукцинимидилсукцинат] (сульфо-EGS), дисукцинимидилглутарат (DSG), дитиобис-[сукцинимидилпропионат] (DSP), дисукцинимидилсуберат (DSS), этиленгликоль-бис-[сукцинимидилсукцинат] (EGS), сшивающие агенты на основе NHS-эфира/диазирина, такие как NHS-диазирин, NHS-LC-диазирин, NHS-SS-диазирин, сульфо-NHS-диазирин, сульфо-NHS-LC-диазирин и сульфо-NHS-SS-диазирин.
[0704] Лизированные клетки могут быть приведены в контакт со связывающим агентом (например, антителом), который направлен на связывание с аффинной меткой. Взаимодействие может произойти в пробирке. Взаимодействие может произойти в хроматографической установке (например, на колонке для аффинной хроматографии). Взаимодействие со связывающим агентом может происходить по меньшей мере 1 минуту, 5 минут, 10 минут, 15 минут, 20 минут, 25 минут, 30 минут, 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 15 часов, 20 часов, 25 часов, 30 часов, 35 часов, 40 часов, 45 часов или более. Взаимодействие со связывающим агентом может происходить не более чем 1 минуту, 5 минут, 10 минут, 15 минут, 20 минут, 25 минут, 30 минут, 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 15 часов, 20 часов, 25 часов, 30 часов, 35 часов, 40 часов, 45 часов или более. В некоторых случаях взаимодействие со связывающим агентом происходит перед лизисом клеток.
[0705] Комплексы могут быть очищены с использованием связывающего агента. Очищенные комплексы могут быть подвергнуты методикам очистки нуклеиновых кислот, чтобы отделить нуклеиновую кислоту-мишень от комплексов. Методики очистки нуклеиновых кислот могут включать разделение на микроцентрифужной колонке, осаждение и электрофорез.
[0706] Нуклеиновая кислота (например, нуклеиновая кислота, содержащая нуклеиновую кислоту-мишень) может быть подвергнута методикам секвенирования. Нуклеиновая кислота может быть подготовлена для секвенирования путем лидирования одного или нескольких адаптеров. Секвенированные нуклеиновые кислоты могут быть исследованы, чтобы определить полиморфизмы, диагностировать заболевание, определить курс лечения заболевания, и/или определить трехмерную структуру генома.
[0707] Меченые нуклеиновые кислоты, направленные против нуклеиновой кислоты, содержащие линкеры
[0708] В настоящем изобретении предложены композиции, способы получения и применения меченых нуклеиновых кислот, направленных против нуклеиновой кислоты. На Фиг. 13А показана типичная немеченая нуклеиновая кислота, направленная против нуклеиновой кислоты. Немеченая нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать протоспейсер (PS), минимальный повтор CRISPR (MCR), одиночный направляющий линкер (SGC), минимальную последовательность tracrPHK (MtS), последовательность 3'tracrPHK (3TS) и удлиненную последовательность tracrPHK (ТЕ). Меченая нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая линкер, может относиться к любой из нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке, и содержать линкер на 5'-конце, 3'-конце, или обоих 5'- и 3'-концах нуклеиновой кислоты, направленной против нуклеиновой кислоты.
[0709] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать ненативную последовательность, как показано на Фиг. 13В. Ненативная последовательность может быть названа меткой. Метка может быть гибридизована с 5'-концом, 3'-концом или обоими 5'- и 3'-концами нуклеиновой кислоты, направленной против нуклеиновой кислоты. Ненативная последовательность может содержать связывающую последовательность для РНК-связывающего белка. РНК-связывающий белок может представлять собой Csy4. Ненативная последовательность может быть гибридизована с последовательностью протоспейсера нуклеиновой кислоты, направленной против нуклеиновой кислоты.
[0710] Гибридизованная ненативная последовательность может быть отделена от нуклеиновой кислоты, направленной против нуклеиновой кислоты, с помощью линкера. На Фиг. 14 показан типичный линкер (например, метка-линкер), отделяющий ненативную последовательность (например, шпильку Csy4) от протоспейсера нуклеиновой кислоты, направленной против нуклеиновой кислоты. Последовательность линкера может быть комплементарна нуклеиновой кислоте-мишени. Последовательность линкера может содержать по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более несоответствий с нуклеиновой кислотой-мишенью. Последовательность линкера может содержать не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более несоответствий с нуклеиновой кислотой-мишенью. В некоторых случаях, чем меньше количество несоответствий между линкером и нуклеиновой кислотой, тем выше эффективность расщепления комплекса Cas9: нуклеиновая кислота, направленная против нуклеиновой кислоты.
[0711] Последовательность линкера может содержать по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60 или более нуклеотидов в длину. Последовательность линкера может содержать не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13,14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60 или более нуклеотидов в длину.
[0712] Мультиплексные генетические направляющие агенты
[0713] Общий обзор
[0714] В настоящем изобретении предложены способы, композиции, системы и/или наборы для мультиплексной геномной инженерии. Согласно некоторым вариантам реализации настоящего изобретения сайт-направленный полипептид может содержать нуклеиновую кислоту, направленную против нуклеиновой кислоты, с образованием тем самым комплекса. Комплекс может быть приведен в контакт с нуклеиновой кислотой-мишенью. Нуклеиновая кислота-мишень может быть расщеплена и/или модифицирована под действием комплекса. Способы, композиции, системы и/или наборы согласно настоящему изобретению можно применять для быстрой, эффективной и/или одновременной модификации нескольких нуклеиновых кислот-мишеней. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленного полипептида и нуклеиновых кислот, направленных против нуклеиновой кислоты, как описано в настоящей заявке.
[0715] На Фиг. 15 показан примерный вариант осуществления способов согласно настоящему изобретению. Нуклеиновая кислота (например, нуклеиновая кислота, направленная против нуклеиновой кислоты) 1505 может быть гибридизована с ненативной последовательностью (например, фрагментом, последовательностью связывания эндорибонуклеазы, рибозимом) 1510 с образованием модуля нуклеиновой кислоты 1512. Модуль нуклеиновой кислоты 1512 (например, содержащий нуклеиновую кислоту, гибридизованную с ненативной последовательностью) может быть конъюгирован в тандеме, с образованием тем самым мультиплексного генетического направляющего агента (например, полимодуля, например, массива) 1511. Мультиплексный генетический направляющий агент 1511 может содержать РНК. Мультиплексный генетический направляющий агент может вступать в контакт 1515 с одной или более эндорибонуклеазами 1520. Эндорибонуклеазы могут связываться с ненативной последовательностью 1510. Связанная эндорибонуклеаза может расщеплять модуль нуклеиновой кислоты 1512 мультиплексного генетического направляющего агента 1511 в заданном положении, которое определяется ненативной последовательностью 1510. Расщепление 1525 (например, высвобождение) может воздействовать на отдельные модули нуклеиновых кислот 1512. В некоторых вариантах расщепленные модули нуклеиновых кислот 1512 могут включать все, некоторые, или ни одной, из ненативных последовательностей 1510. Расщепленные модули нуклеиновых кислот 1512 могут быть связаны с помощью сайт-направленного полипептида 1530, с образованием тем самым комплекса 1531. Комплекс 1531 может быть направлен 1535 к нуклеиновой кислоте-мишени 1540. Нуклеиновая кислота-мишень 1540 может быть расщеплена и/или модифицирована под действием комплекса 1531.
[0716] Мультиплексные генетические направляющие агенты
[0717] Мультиплексный генетический направляющий агент можно использовать для модификации нескольких нуклеиновых кислот-мишеней в одно и то же время, и/или в стехиометрических количествах. Мультиплексный генетический направляющий агент может представлять собой любую нуклеиновую кислоту, направленную против нуклеиновой кислоты, как описано в настоящей заявке, в тандеме. Мультиплексный генетический направляющий агент может относиться к непрерывной молекуле нуклеиновой кислоты, содержащей один или более модулей нуклеиновых кислот. Модуль нуклеиновой кислоты может содержать нуклеиновую кислоту и ненативную последовательность (например, фрагмент, последовательность связывания эндорибонуклеазы, рибозим). Нуклеиновая кислота может представлять собой некодирующую РНК, такую как микроРНК (миРНК), малую интерферирующую РНК (миРНК), длинную некодирующую РНК (lncRNA или lincRNA), эндогенную миРНК (эндо-миРНК), piwi-взаимодействующую РНК (piPHK), транс-действующую малую интерферирующую РНК (tasiPHK), сцепленную с повторами малую интерферирующую РНК (rasiPHK), малую ядрышковую РНК (snoPHK), малую ядерную РНК (мяРНК), транспортную РНК (тРНК) и рибосомальную РНК (рРНК), или любую их комбинацию. Нуклеиновая кислота может представлять собой кодирующую РНК (например, мРНК). Нуклеиновая кислота может представлять собой любой тип РНК. Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота может представлять собой нуклеиновую кислоту, направленную против нуклеиновой кислоты.
[0718] Ненативная последовательность может быть расположена на 3'-конце модуля нуклеиновой кислоты. Ненативная последовательность может быть расположена на 5'-конце модуля нуклеиновой кислоты. Ненативная последовательность может быть расположена на обоих 3'- и 5'-концах модуля нуклеиновой кислоты. Ненативная последовательность может содержать последовательность, которая может связываться с эндорибонуклеазой (например, последовательность связывания эндорибонуклеазы). Ненативная последовательность может представлять собой последовательность, которая специфично распознается эндорибонуклеазой (например, РНКаза Т1 расщепляет неспаренные G-основания, РНКаза Т2 расщепляет 3'-конец по А-основаниям, РНКаза U2 расщепляет 3'-конец по неспаренным А-основаниям). Ненативная последовательность может представлять собой последовательность, которая структурно распознается эндорибонуклеазой (например, структура шпильки, одноцепочечные-двухцепочечные соединения, например, Drosha распознает одноцепочечное-двухцепочечное соединение внутри шпильки). Ненативная последовательность может содержать последовательность, которая может связываться с эндорибонуклеазой системы CRISPR (например, белком Csy4, Cas5 и/или Cas6). Ненативная последовательность может содержать нуклеотидную последовательность, которая по меньшей мере или не более чем приблизительно на 40%, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 98%, 99% или 100% идентична и/или гомологична одной из следующих нуклеотидных последовательностей:

[0719] Согласно некоторым вариантам реализации настоящего изобретения, в том случае, если ненативная последовательность содержит последовательность связывания эндорибонуклеазы, модули нуклеиновых кислот могут быть связаны с помощью той же эндорибонуклеазы. Модули нуклеиновых кислот могут не содержать одинаковую последовательность связывания эндорибонуклеазы. Модули нуклеиновых кислот могут содержать различные последовательности связывания эндорибонуклеазы. Различные последовательности связывания эндорибонуклеазы могут быть связаны с одной и той же эндорибонуклеазой. Согласно некоторым вариантам реализации настоящего изобретения модули нуклеиновых кислот могут быть связаны с различными эндорибонуклеазами.
[0720] Фрагмент может содержать рибозим. Рибозим может расщеплять сам себя, высвобождая тем самым каждый модуль мультиплексного генетического направляющего агента. Подходящие рибозимы могут включать пептидилтрансферазу в V-домене 23 S рРНК, РНКазу Р, интроны группы I, интроны группы II, GIR1-кэпирующий рибозим, лидзим, рибозимы шпильки, рибозимы типа hammerhead, рибозимы HDV, рибозимы СРЕВ3, рибозимы VS, рибозим glmS, рибозим СоТС и синтетические рибозимы.
[0721] Нуклеиновые кислоты модулей нуклеиновых кислот из мультиплексного генетического направляющего агента могут быть одинаковыми. Модули нуклеиновых кислот могут различаться по 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50 или более нуклеотидам. Например, различные модули нуклеиновых кислот могут различаться в спейсерной области модуля нуклеиновой кислоты, направляя тем самым модуль нуклеиновой кислоты на другую нуклеиновую кислоту-мишень. В некоторых случаях различные модули нуклеиновых кислот могут различаться в спейсерной области модуля нуклеиновой кислоты, но при этом могут быть направлены против одной и той же нуклеиновой кислоты-мишени. Модули нуклеиновых кислот могут быть направлены против одной и той же нуклеиновой кислоты-мишени. Модули нуклеиновых кислот могут быть направлены против одной или более нуклеиновых кислот-мишеней.
[0722] Модуль нуклеиновой кислоты может содержать регуляторную последовательность, которая может обеспечивать надлежащую трансляцию или амплификацию модуля нуклеиновой кислоты. Например, модуль нуклеиновой кислоты может содержать промотор, ТАТА-бокс, энхансерный элемент, элемент терминации транскрипции, сайт связывания рибосомы, 3'-нетранслируемую область, 5'-нетранслируемую область, последовательность 5'-кэпа, последовательность 3'-полиаденилирования, элемент стабильности РНК и тому подобное.
[0723] Способы
[0724] В настоящем изобретении предложены способы одновременной модификации нескольких нуклеиновых кислот-мишеней за счет использования мультиплексного генетического направляющего агента. Сайт-направленный полипептид, эндорибонуклеаза и мультиплексный генетический направляющий агент могут быть введены в клетку-хозяина. Вектор согласно настоящему изобретению (например, содержащий мультиплексный генетический направляющий агент, эндорибонуклеазу и/или сайт-направленный полипептид) может быть введен в клетку-хозяина. В некоторых случаях в клетки может быть введено более одной эндорибонуклеазы и/или мультиплексного генетического направляющего агента. Если мультиплексный генетический направляющий агент содержит различные типы фрагментов, причем фрагменты представляют собой различные последовательности связывания эндорибонуклеазы, то одна или более эндорибонуклеаз, соответствующих типам связывающих последовательностей, которые присутствуют в мультиплексном генетическом направляющем агенте, могут быть введены в клетки.
[0725] Введение может происходить с помощью любых способов введения нуклеиновой кислоты в клетку, таких инфекция вирусом или бактериофагом, трансфекция, конъюгация, слияние протопластов, липофекция, электропорация, осаждение фосфатом кальция, полиэтиленимин (ПЭИ)-опосредованная трансфекция, опосредованная DEAE-декстраном трансфекция, опосредованная липосомами трансфекция, технология бомбардировки частицами, осаждение фосфатом кальция, прямая микроинъекция, опосредованная наночастицами доставка нуклеиновой кислоты и т.п. Вектор может быть временно экспрессирован в клетке-хозяине. Вектор может быть стабильно экспрессирован в клетке-хозяине (например, стабильно интегрирован в геном клетки-хозяина).
[0726] В тех случаях, когда фрагмент содержит последовательность связывания эндорибонуклеазы, эндорибонуклеаза может быть экспрессирована и может связываться с сайтом связывания эндорибонуклеазы на мультиплексном генетическом направляющем агенте. Эндорибонуклеаза может расщеплять мультиплексный генетический направляющий агент на отдельные модули нуклеиновых кислот.
[0727] В тех случаях, когда фрагмент содержит рибозим, экспрессия эндорибонуклеазы в клетке-хозяине может не потребоваться. Рибозим может расщеплять сам себя, что приводит к расщеплению мультиплексного генетического направляющего агента на отдельные модули нуклеиновых кислот.
[0728] Отдельные (например, отщепленные) модули нуклеиновых кислот могут содержать полный фрагмент, часть фрагмента или не содержать его (например, последовательность связывания эндорибонуклеазы). Например, высвобожденный (например, отщепленный) модуль нуклеиновой кислоты может быть подвергнут укорочению и/или деградации под действием экзонуклеаз, что может привести к удалению 5'- и/или 3'-конца модуля нуклеиновой кислоты. В таких случаях укорочение и/или деградация под действием экзонуклеаз может привести к удалению всего или части фрагмента, или не влиять на него (например, последовательность связывания эндорибонуклеазы).
[0729] Высвобожденный (например, отщепленный) модуль нуклеиновой кислоты может связываться с сайт-направленным полипептидом, с образованием тем самым комплекса. Комплекс может быть направлен к нуклеиновой кислоте-мишени с помощью нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая может специфично гибридизоваться с последовательностью нуклеиновой кислоты-мишени. После гибридизации сайт-направленный полипептид, входящий в состав комплекса, может модифицировать нуклеиновую кислоту-мишень (например, расщеплять нуклеиновую кислоту-мишень). В некоторых случаях модификация включает введение двухцепочечного разрыва в нуклеиновую кислоту-мишень. В некоторых случаях модификация включает введение одноцепочечного разрыва в нуклеиновую кислоту-мишень.
[0730] Согласно некоторым вариантам реализации настоящего изобретения в клетку вводят один или более донорных полинуклеотидов и/или векторов, кодирующих такие полинуклеотиды. Один или более донорных полинуклеотидов могут быть встроены в модифицированные (например, расщепленные) нуклеиновые кислоты-мишени, что приводит к вставке. Аналогичный донорный полинуклеотид может быть встроен в нескольких сайтах расщепления нуклеиновых кислот-мишеней. Один или более донорных полинуклеотидов могут быть встроены в один или более сайтов расщепления нуклеиновых кислот-мишеней. Такое встраивание может быть названо мультиплексной геномной инженерией. В некоторых случаях в клетки не водят донорный полинуклеотид и/или вектор, кодирующий указанный полинуклеотид. В этих случаях модифицированная нуклеиновая кислота-мишень может содержать делеции.
[0731] Стехиометрическая доставка нуклеиновых кислот
[0732] Общий обзор
[0733] В настоящем изобретении предложены композиции, способы и наборы для стехиометрической доставки нуклеиновой кислоты в клетку и/или внутриклеточное положение. Стехиометрическая доставка может быть опосредована комплексом. На Фиг. 16 показан типичный комплекс для стехиометрической доставки множества нуклеиновых кислот в клетку и/или внутриклеточное положение. Комплекс может содержать множество нуклеиновых кислот 1605. Каждая нуклеиновая кислота может содержать сайт связывания белка, связывающего нуклеиновую кислоту 1610. Сайты связывания белка, связывающего нуклеиновую кислоту, 1610 могут иметь идентичные последовательности для всех сайтов, могут иметь различные последовательности, или некоторые из них могут иметь идентичные последовательности, и некоторые могут иметь различные последовательности. Согласно некоторым вариантам реализации настоящего изобретения сайты связывания белка, связывающего нуклеиновую кислоту, могут связываться с членом семейства Cas6, Cas5 или Csy4. Комплекс может содержать тандемный гибридный полипептид 1630. Тандемный гибридный полипептид может содержать белки, связывающие нуклеиновую кислоту 1625, гибридизованные вместе в тандеме. Белки, связывающие нуклеиновую кислоту, могут быть разделены с помощью линкера 1620. Белки, связывающие нуклеиновую кислоту, 1625 могут представлять собой один и тот же белок, могут представлять собой различные белки, или некоторые из них могут представлять собой идентичные белки, и некоторые из них могут представлять собой различные белки. Белки, связывающие нуклеиновую кислоту, 1625 могут представлять собой белки Csy4. Белки, связывающие нуклеиновую кислоту, 1625 могут связываться с сайтом связывания белка, связывающего нуклеиновую кислоту, 1610 на нуклеиновой кислоте 1605. Тандемный гибридный полипептид 1630 может содержать ненативную последовательность 1615. В некоторых случаях ненативная последовательность является последовательностью внутриклеточной (например, ядерной) локализации. Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота 1605 может кодировать ненативную последовательность (например, последовательность внутриклеточной (например, ядерной) локализации). Комплекс может быть введен 1635 в клетки, при этом одна или более из нуклеиновых кислот 1605 могут транслироваться с образованием полипептидов 1640. Транслированный полипептид 1640 может связываться и расщеплять сайт связывания белков, связывающих нуклеиновую кислоту, 1610 на нуклеиновой кислоте 1605. Расщепление 1645 может высвобождать нуклеиновую кислоту 1650, которая может представлять собой нуклеиновую кислоту, направленную против нуклеиновой кислоты. Высвобожденная нуклеиновая кислота 1650 может связываться с транслированным полипептидом 1645 (например, сайт-направленным полипептидом), образуя тем самым единый блок. Транслированный полипептид 1645 может содержать сигнал ядерной локализации. Блок может перемещаться в ядро, в котором блок может быть направлен к нуклеиновой кислоте-мишени, которая способна гибридизоваться со спейсером высвобожденной нуклеиновой кислоты 1650. Блок может быть гибридизован с нуклеиновой кислотой-мишенью. Сайт-направленный полипептид, входящий в состав блока, может расщеплять нуклеиновую кислоту-мишень. Расщепление нуклеиновой кислоты-мишени может называться геномной инженерией. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, как описано в настоящей заявке.
[0734] Согласно некоторым вариантам реализации настоящего изобретения множество нуклеиновых кислот, направленных против нуклеиновой кислоты, могут быть стехиометрически доставлены в клетки и/или к месту внутриклеточной локализации. На ФИГ. 17 показан типичный комплекс для стехиометрической доставки множества нуклеиновых кислот. Комплекс может содержать множество нуклеиновых кислот 1705. Каждая нуклеиновая кислота может содержать множество сайтов связывания белков, связывающих нуклеиновую кислоту 1710/1711. Сайты связывания белков, связывающих нуклеиновую кислоту, 1710/1711 все могут иметь идентичные последовательности, все могут иметь различные последовательности, или некоторые из них могут иметь идентичные последовательности, и некоторые из них могут иметь различные последовательности. Согласно некоторым вариантам реализации настоящего изобретения сайты связывания белков, связывающих нуклеиновую кислоту, 1710/1711 могут связываться с членом семейства Cas6, Cas5 или Csy4. Комплекс может содержать тандемный гибридный полипептид 1730. Тандемный гибридный полипептид может содержать белки, связывающие нуклеиновую кислоту, 1725 гибридизованные вместе в тандеме. Белки, связывающие нуклеиновую кислоту, могут быть разделены с помощью линкера 1720. Белки, связывающие нуклеиновую кислоту, 1725 могут представлять собой идентичные белки, могут представлять собой различные белки, или некоторые из них могут представлять собой идентичные белки, и некоторые из них могут представлять собой различные белки. РНК-связывающие белки 1725 могут представлять собой комбинацию полипептидов Csy4, Cas5 и Cas6. Белки, связывающие нуклеиновую кислоту, 1725 могут связываться с сайтом связывания белка, связывающего нуклеиновую кислоту, 1710 на нуклеиновой кислоте 1705. Тандемный гибридный полипептид 1730 может содержать ненативную последовательность 1715. В некоторых случаях ненативная последовательность представляет собой последовательность внутриклеточной (например, ядерной) локализации. Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота 1705 может кодировать ненативную последовательность (например, последовательность внутриклеточной (например, ядерной) локализации). Комплекс может быть введен 1735 в клетки, в которых одна или более из нуклеиновых кислот могут транслироваться в полипептиды 1740/1750. Транслированный полипептид 1740 может связываться и расщеплять сайт связывания белков, связывающих нуклеиновую кислоту, 1711 на нуклеиновой кислоте 1705. Расщепление 1745 может высвобождать нуклеиновую кислоту 1755, которая может представлять собой нуклеиновую кислоту, направленную против нуклеиновой кислоты, и/или донорный полинуклеотид. Высвобожденная нуклеиновая кислота 1755 может связываться с транслированным полипептидом 1750 (например, сайт-направленным полипептидом), с образованием тем самым единого блока. В некоторых случаях транслированный полипептид 1750 включает сигнал ядерной локализации. Блок может перемещаться в ядро, в котором блок может быть направлен к нуклеиновой кислоте-мишени, которая способна гибридизоваться со спейсером высвобожденной РНК 1755. Блок может гибридизоваться с нуклеиновой кислотой-мишенью. Сайт-направленный полипептид, входящий в состав блока, может расщеплять нуклеиновую кислоту-мишень.
[0735] Способы
[0736] В настоящем изобретении предложены способы стехиометрической доставки нуклеиновых кислот в клетку (например, доставляемые в стехиометрическом соотношении нуклеиновые кислоты). Способ может включать связывание тандемного гибридного полипептида с множеством доставляемых в стехиометрическом соотношении нуклеиновых кислот, с образованием тем самым комплекса. Комплекс может содержать стехиометрические количества нуклеиновых кислот (например, комплекс может содержать множество нуклеиновых кислот в заданном соотношении и/или количестве). 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более нуклеиновых кислот могут быть доставлены в стехиометрическом соотношении. В некоторых случаях 3 стехиометрически доставляемые нуклеиновые кислоты могут быть доставлены в стехиометрическом соотношении. В некоторых случаях 4 стехиометрически доставляемые нуклеиновые кислоты могут быть доставлены в стехиометрическом соотношении.
[0737] Нуклеиновая кислота, доставляемая в стехиометрическом соотношении, может кодировать полипептид или некодирующую РНК. Полипептид может представлять собой полипептид системы CRISPR (например, сайт-направленный полипептид, эндорибонуклеазу). Нуклеиновая кислота, доставляемая в стехиометрическом соотношении, может кодировать более одного полипептида. Нуклеиновая кислота, доставляемая в стехиометрическом соотношении, может содержать множество нуклеиновых кислот, доставляемых в стехиометрическом соотношении (например, в массиве). Нуклеиновая кислота, доставляемая в стехиометрическом соотношении, может кодировать некодирующую РНК. Примеры некодирующих РНК могут включать микроРНК (миРНК), малую интерферирующую РНК (миРНК), длинную некодирующую РНК (lncPHK или lincPHK), эндогенную миРНК (эндо-миРНК), piwi-взаимодействующую РНК (пиРНК), транс-действующую малую интерферирующую РНК (tasiPHK), сцепленную с повторами малую интерферирующую РНК (rasiPHK), малую ядрыщковую РНК (snoPHK), малую ядерную РНК (мяРНК), транспортную РНК (тРНК) и рибосомальную РНК (рРНК). Нуклеиновая кислота, доставляемая в стехиометрическом соотношении, может представлять собой РНК.
[0738] Нуклеиновая кислота, доставляемая в стехиометрическом соотношении, может кодировать ненативную последовательность. В некоторых случаях нуклеиновая кислота, доставляемая в стехиометрическом соотношении, кодирует ненативную последовательность, так, что при трансляции полипептида из стехиометрически доставляемой нуклеиновой кислоты, кодирующей полипептид, указанный полипептид гибридизуется с ненативной последовательностью (например, с образованием гибридного белка). Ненативная последовательность может представлять собой пептидную аффинную метку. Ненативная последовательность (например, пептидная аффинная метка) может быть расположена на N-конце полипептида, С-конце полипептида, или в любом положении в пределах полипептида (например, поверхностная доступная петля). Согласно некоторым вариантам реализации настоящего изобретения ненативная последовательность представляет собой сигнал ядерной локализации (NLS). NLS может представлять собой однокомпонентную и двухкомпонентную последовательность. NSL может быть распознан молекулярным импортирующим аппаратом ядра (например, импортинами). NLS может представлять собой небольшой пептид (например, PKK.KRKV большого t-антигена SV40). NLS может представлять собой полипептидный домен (например, кислый домен М9 hnRNP A1).
[0739] Ненативная последовательность может представлять собой нуклеиновую аффинную метку (например, сигнал локализации нуклеиновой кислоты). Например, нуклеиновая кислота, доставляемая в стехиометрическом соотношении, кодирующая ДНК (например, донорный полинуклеотид), может содержать сигнал локализации нуклеиновой кислоты, который может локализовать ДНК в ядре. Такие сигналы локализации нуклеиновых кислот могут включать, например, последовательности пептид-нуклеиновая кислота (PNA).
[0740] Нуклеиновая кислота, доставляемая в стехиометрическом соотношении, может содержать регуляторные последовательности, которые могут обеспечивать надлежащую трансляцию или амплификацию нуклеиновой кислоты. Например, нуклеиновая кислота может содержать промотор, ТАТА-бокс, эпхансерный элемент, элемент терминации транскрипции, элемент стабильности ДНК, сайт связывания рибосом, 3'-нетранслируемую область, 5'-нетранслируемую область, последовательность 5'-кэпа, последовательность 3'-полиаденилирования, элемент стабильности РНК и тому подобное.
[0741] Нуклеиновая кислота может содержать сайт связывания белка, связывающего нуклеиновую кислоту. Сайт связывания белка, связывающего нуклеиновую кислоту, может быть связан с белком, связывающим нуклеиновую кислоту. Сайт связывания белка, связывающего нуклеиновую кислоту, может быть связан с полипептидом CRISPR (например, сайт-направленным полипептидом, эндорибонуклеазой). Сайт связывания белка, связывающего нуклеиновую кислоту, может быть связан с полипептидом семейства Cas5 или Cas6. Сайт связывания белка, связывающего нуклеиновую кислоту, может быть связан с полипептидом Csy4, Cas5 или Cas6. Некоторые примеры сайтов связывания белка, связывающего нуклеиновую кислоту, могут включать, например, последовательности, которые могут быть связаны с РНК-связывающими белками, такими как MS2-связывающая последовательность, U1A-связывающая последовательность, последовательность ВохВ, последовательность eIF4A, шпильки, последовательности, которые могут быть связаны с доменами РНК-распознающих мотивов (RRM) (например, U1A), последовательности, которые могут быть связаны с доменами, связывающими двухцепочечные РНК (dsRBD) (например, Staufen), последовательности, которые могут быть связаны с доменами PAZ (например, PAZ, Argonaute), последовательности, которые могут быть связаны с доменами PIWI (например, PIWI, MILI, MIWI, Argonaute) и тому подобное. Некоторые примеры сайтов связывания белка, связывающего нуклеиновую кислоту, могут включать, например, последовательности, которые могут быть связаны с ДНК-связывающими белками, такими как цинковые пальцы, домен спираль-поворот-спираль, домен цинкового пальца, домен лейциновой молнии (bZIP), домен крылатой спирали, домен крылатая спираль-поворот-спираль, домен спираль-петля-спираль, домен HMG-box, домен Wor3, домен иммуноглобулина, домен В3, домен TALE и тому подобное.
[0742] Нуклеиновая кислота может содержать один или более сайтов связывания белка, связывающего нуклеиновую кислоту. Нуклеиновая кислота может включать 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более сайтов связывания белка, связывающего нуклеиновую кислоту. Один или более сайтов связывания белка, связывающего нуклеиновую кислоту, могут быть идентичными. Один или более сайтов связывания белка, связывающего нуклеиновую кислоту, могут быть различными. Например, нуклеиновая кислота может содержать сайт связывания Csy4 и сайт связывания MS2. Один или более сайтов связывания белка, связывающего нуклеиновую кислоту, могут быть разделены 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 250, 300, 350, 400, 450, 500 или более нуклеотидами. Согласно некоторым вариантам реализации настоящего изобретения 3'-концевой сайт связывания белка, связывающего нуклеиновую кислоту, может быть связан с тандемным гибридным полипептидом согласно настоящему изобретению.
[0743] Тандемный гибридный полипептид
[0744] В некоторых вариантах реализации настоящего изобретения способ согласно настоящему изобретению обеспечивает связывание множества нуклеиновых кислот с тандемным гибридным полипептидом. Тандемный гибридный полипептид может содержать множество белков, связывающих нуклеиновую кислоту, гибридизованных вместе с образованием одной полипептидной цепи. Тандемный гибридный полипептид может содержать 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более белков, связывающих нуклеиновую кислоту. Белки, связывающие нуклеиновую кислоту, входящие в состав тандемного гибридного полипептида, могут связываться с сайтами связывания белка, связывающего нуклеиновую кислоту, нуклеиновых кислот настоящего согласно настоящему изобретению. Примеры белков, связывающих нуклеиновую кислоту, могут включать белки, связывающие MS2, U1A, последовательность ВохВ (например, цинковые пальцы), eIF4A, Staufen, PAZ, Argonaute, Piwi, MILI, MIWI, цинковые пальцы, домен спираль-поворот-спираль, домен цинкового пальца, домен лейциновой молнии (bZIP), домен крылатая спираль, домен крылатая спираль-поворот-спираль, домен спираль-петля-спираль, домен HMG-бокс, домен Wor3, домен иммуноглобулина, домен В3, домен TALE, и тому подобное. Согласно некоторым вариантам реализации настоящего изобретения белок, связывающий нуклеиновую кислоту, представляет собой РНК-связывающий белок. РНК-связывающий белок может быть членом системы CRISPR. Согласно некоторым вариантам реализации настоящего изобретения РНК-связывающий белок может быть членом семейства белков Cas5 или Cas6. Согласно некоторым вариантам реализации настоящего изобретения РНК-связывающий белок может представлять собой Csy4, Cas5, Cas6 или любую их комбинацию. Согласно некоторым вариантам реализации настоящего изобретения белок, связывающий нуклеиновую кислоту, представляет собой ДНК-связывающий белок (например, цинковый палец).
[0745] В некоторых случаях белки, связывающие нуклеиновую кислоту, разделены с помощью линкера. Линкер может содержать приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или более аминокислот.
[0746] Тандемный гибридный полипептид может содержать ненативную последовательность (например, пептидную аффинную метку). Ненативная последовательность может содержать сигнал ядерной локализации (NLS), который может направить тандемный гибридный полипептид к месту внутриклеточной локализации (например, в ядро).
[0747] Каждый белок, связывающий нуклеиновую кислоту, в тандемном гибридном полипептиде может содержать свою собственную ненативную последовательность. Ненативная последовательность каждого белка, связывающего нуклеиновую кислоту, может быть идентична другим ненативным последовательностям. Ненативная последовательность каждого белка, связывающего нуклеиновую кислоту, может отличаться от других ненативных последовательностей. Ненативные последовательности некоторых белков, связывающих нуклеиновую кислоту, тандемного гибридного полипептида могут представлять собой идентичные последовательности, и ненативные последовательности некоторых белков, связывающих нуклеиновую кислоту, тандемного гибридного полипептида могут быть различными.
[0748] В некоторых случаях способы согласно настоящему изобретению могут обеспечить образование комплекса, содержащего тандемный гибридный полипептид и множество нуклеиновых кислот согласно настоящему изобретению. Образование комплекса может включать связывание белков, связывающих нуклеиновые кислоты, которые входят в состав тандемного гибридного полипептида, со своими когнатными последовательностями для связывания белков, связывающих нуклеиновую кислоту, согласно настоящему изобретению. Например, стехиометрически доставляемая нуклеиновая кислота, содержащая сайт связывания Csy4, может связываться с субъединицей белка Csy4 в тандемном гибридном белке. Комплекс может быть образован за пределами клетки (например, в условиях in vitro). Комплекс может быть образован в клетках (например, в условиях in vivo). Если комплекс образуется в условиях in vitro, то он может быть введен в клетку, например, путем трансфекции, трансформации, вирусной трансдукции, электропорации, инъекции и т.п.
[0749] Способы согласно настоящему изобретению предусматривают терапевтическую доставку нескольких нуклеиновых кислот в условиях in vivo, in vitro, ex vivo. Доставленные нуклеиновые кислоты могут быть использованы для лечения заболевания. Например, доставленные нуклеиновые кислоты могут быть использованы в генной терапии и/или могут встраиваться в геном клетки, обеспечивая тем самым терапевтический результат. Терапевтический результат может относиться к увеличению или уменьшению уровней белка, нуклеиновой кислоты или любой биологической молекулы, связанной с заболеванием, например, продукта деградации, малой молекулы, и/или иона. Например, терапевтический результат может включать увеличение уровня противовоспалительного гена, или уменьшение уровня белка в пути передачи сигналов, связанного с заболеванием. Терапевтический результат может относиться к физиологическому действию. Физиологическое действие может включать, морфологические изменения, метаболические изменения и/или структурные изменения в клетке. Терапевтический результат может относиться к изменениям в модификациях белка и/или нуклеиновой кислоты, таким как гликозилирование, ацетилирование, метилирование, деметилирование, депуринизация, убиквитинилирование и т.п.
[0750] Терапевтический результат может быть измерен путем оценки изменений в генетической структуре клетки, уровней представляющих интерес биомолекул в клетке, и/или физиологических изменений в клетке. Измерения могут быть выполнены с использованием методов молекулярной биологии, таких как спектроскопия, спектрометрия, секвенирование, ИФА, микроскопия и/или рентгеноструктурная кристаллография. Измерения могут быть выполнены с использованием животных моделей, таких как мыши, крысы, собаки и приматы. Например, генетически модифицированные клетки согласно настоящему изобретению могут быть введены в организм мышей, с последующей оценкой биологических и физиологических изменений, таких как, например, способность к метастазированию и/или дифференциации.
[0751] Спейсеры для лечения заболеваний крови
[0752] В настоящем изобретении предложены композиции, способы и наборы для генетического конструирования кроветворных стволовых клеток (КСК).
[0753] Композиции
[0754] КСК может содержать сайт-направленный полипептид (например, Cas9).
[0755] КСК может содержать нуклеиновую кислоту, направленную против нуклеиновой кислоты. Нуклеиновая кислота, направленная против нуклеиновой кислоты, согласно настоящему изобретению может быть направлена против гена, вовлеченного в патофизиологию генетического заболевания. В таблице 1 перечислены типичные гены, которые вовлечены в патофизиологию заболеваний. Гены, перечисленные в таблице 1, могут представлять собой гены, которые могут быть мишенью нуклеиновой кислоты, направленной против нуклеиновой кислоты. Нуклеиновая кислота, направленная против нуклеиновой кислоты, согласно настоящему изобретению может содержать спейсер, который может быть направлен против генов, перечисленных в таблице 1.
[0756] В таблице 2 приведены типичные спейсеры нуклеиновых кислот, направленных против нуклеиновой кислоты, согласно настоящему изобретению. Каждый спейсер, из перечисленных в таблице 2, может представлять собой спейсер, который может быть вставлен в нуклеиновую кислоту, направленную против нуклеиновой кислоты. Типичные спейсеры приведены в соответствии с названием расстройства и геном, вовлеченным в расстройство, которое является мишенью указанного спейсера.


[0757] Способы
[0758] В настоящем изобретении предложены способы введения нуклеиновой кислоты, направленной против нуклеиновой кислоты, и сайт-направленного полипептида в КСК. Согласно некоторым вариантам реализации настоящего изобретения КСК извлекают из пациента перед введением. Извлеченная КСК может быть очищена (например, путем афереза). Сайт-направленный полипептид и/или нуклеиновая кислота, направленная против нуклеиновой кислоты, могут быть введены в КСК, которая была очищена. Сайт-направленный полипептид и/или нуклеиновая кислота, направленная против нуклеиновой кислоты, могут быть введены в КСК, которая не была очищена. Введение в КСК может происходить в условиях in vitro (например, вне организма пациента, извлеченная клетка). В некоторых случаях введение в КСК происходит в условиях in vivo (например, в организме пациента, неизвлеченная клетка).
[0759] Введение сайт-направленного полипептида и/или нуклеиновой кислоты, направленной против нуклеиновой кислоты, согласно настоящему изобретению может происходить, например, путем вирусной трансдукции, трансфекции, электропорации, оптический трансфекции и/или химической трансфекции.
[0760] После введения в КСК нуклеиновая кислота, направленная против нуклеиновой кислоты, согласно настоящему изобретению и сайт-направленный полипептид могут образовать комплекс. Комплекс может быть направлен на нуклеиновую кислоту-мишень (например, гены, перечисленные в таблице 3) с помощью нуклеиновой кислоты, направленной против нуклеиновой кислоты. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может гибридизоваться с нуклеиновой кислотой-мишенью. Сайт-направленный полипептид может модифицировать нуклеиновую кислоту-мишень (например, путем расщепления нуклеиновой кислоты-мишени).
[0761] В некоторых случаях модифицированная нуклеиновая кислота-мишень содержит делецию. В некоторых случаях модифицированная нуклеиновая кислота-мишень содержит вставку донорного полинуклеотида. Донорный полинуклеотид, часть донорного полинуклеотида, копия донорного полинуклеотида или части копии донорного полинуклеотида могут быть вставлены в нуклеиновую кислоту-мишень. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, как описано в настоящей заявке.


[0762] Вычислительные способы
[0763] В настоящем изобретении предложены вычислительные способы выявления спейсеров для нуклеиновых кислот, направленных против нуклеиновой кислоты. Вычислительный способ может включать сканирование последовательности нуклеиновой кислоты генома для выявления мотива, прилегающего к протоспейсеру. После обнаружения мотива, прилегающего к протоспейсеру, программа может автоматически рассчитать от 10 до 30 нуклеотидов, расположенных в направлении 5'-конца относительно мотива, прилегающего к протоспейсеру. Последовательность из 10-30 нуклеотидов, расположенных в направлении 5'-конца относительно мотива, прилегающего к протоспейсеру, может составлять предполагаемую последовательность спейсера. Другими словами, последовательность из 10-30 нуклеотидов, расположенных в направлении 5'-конца относительно мотива, прилегающего к протоспейсеру, в геноме может соответствовать нуклеиновой кислоте-мишени, и последовательность, комплементарная нуклеиновой кислоте-мишени, может быть названа спейсером.
[0764] Программа может проверить каждую итерацию последовательности предполагаемой спейсерной последовательности, чтобы установить, насколько эффективной будет последовательность в качестве спейсера в составе нуклеиновой кислоты, направленной против нуклеиновой кислоты. Например, программа может брать каждую итерацию предполагаемой спейсерной последовательности и выполнить in silico прогнозирование вторичной структуры для данной последовательности. Прогнозирование вторичной структуры может включать добавление предполагаемой спейсерной последовательности к остову нуклеиновой кислоты, направленной против нуклеиновой кислоты (например, нуклеиновая кислота, направленная против нуклеиновой кислоты, без спейсера). С помощью прогнозирования вторичной структуры можно провести оценку прогноза вторичной структуры пристыкованной предполагаемой спейсерной последовательности в остове нуклеиновой кислоты, направленной против нуклеиновой кислоты. Исследование предполагаемой вторичной структуры может включать, например, прогнозирование нуклеотидов, которые способны образовывать дуплексы, шпильки, и тех, которые являются неструктурированными нуклеотидами и/или неспаренными нуклеотидами.
[0765] Вычислительный способ может включать применение теста на сворачивание для каждой предполагаемой спейсерной последовательности, которая была подвергнута исследованию прогнозируемой вторичной структуры. Тест на сворачивание может включать исследование в условиях in silico сворачивания нуклеиновой кислоты, направленной против нуклеиновой кислоты, содержащей предполагаемую спейсерную последовательность. Нуклеиновая кислота, направленная против нуклеиновой кислоты, и предполагаемая последовательность спейсера могут как соответствовать, так и не соответствовать критериям теста на сворачивание.
[0766] Чтобы удовлетворять критериям теста на сворачивание, вторичная структура остова нуклеиновой кислоты, направленной против нуклеиновой кислоты, должна сохраниться, менее 5, 4, 3, 2 или 1 нуклеотида в спейсере должны быть гибридизованы с нуклеотидами за пределами спейсера, и другая вторичная структура в спейсере должна находиться в пределах спейсера.
[0767] Выбор легко встраиваемого репортера
[0768] Общий обзор
[0769] В настоящем изобретении предложены способы, композиции, системы и наборы для генетической модификации клеток и отбора таких генетически модифицированных клеток путем беспрепятственного встраивания, детектирования и удаления репортерного элемента. Согласно некоторым вариантам реализации настоящего изобретения донорный полинуклеотид может содержать нуклеиновую кислоту, которая будет введена в геном клетки (называемую в настоящей заявке «генетический элемент, представляющий интерес»), а также последовательность нуклеиновой кислоты, кодирующей репортерный элемент (например, GFP), сайт-направленный полипептид и две нуклеиновые кислоты, направленные против нуклеиновой кислоты. Любой из сайт-направленного полипептида, нуклеиновой кислоты, направленной против нуклеиновой кислоты, и/или все три элемента можно контролировать с помощью индуцируемого промотора. Сайт-направленный полипептид и нуклеиновая кислота, направленная против нуклеиновой кислоты, могут образовывать комплекс, который может направленно воздействовать на сайт в геноме клетки путем гибридизации нуклеиновой кислоты, направленной против нуклеиновой кислоты, с нуклеиновой кислотой-мишенью в геноме. Сайт-направленный полипептид комплекса может расщеплять нуклеиновую кислоту-мишень. Донорный полинуклеотид может быть вставлен в расщепленную нуклеиновую кислоту-мишень. После введения двухцепочечного разрыва (или одноцепочечного разрыва) в сайт-мишень в присутствии донорного полинуклеотида, популяция клеток-реципиентов может быть подвергнута скринингу для определения присутствия репортерной молекулы в качестве посредника, указывающего на присутствие генетического элемента, представляющего интерес. После выделения клеток, содержащих репортерную молекулу, репортерный элемент может быть вырезан путем индукции экспрессии сайт-направленного полипептида и/или нуклеиновой кислоты, направленной против нуклеиновой кислоты. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может действовать на 5'- и 3'-концы репортерного элемента и может привести к вырезанию репортерного элемента. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, как описано в настоящей заявке.
[0770] На Фиг. 18 показан примерный вариант осуществления способов согласно настоящему изобретению. Нуклеиновая кислота может содержать множество генетических элементов 1805/1810. Генетические элементы 1805 и 1810 могут представлять собой, например, гены, некодирующие нуклеиновые кислоты, интроны, экзоны, ДНК и/или РНК. Генетические элементы 1805 и 1810 могут быть частью одного и того же гена. Между генетическими элементами может присутствовать нуклеиновая кислота-мишень 1806, пригодная для генетического конструирования. Сайт-направленный полипептид и нуклеиновая кислота, направленная против нуклеиновой кислоты, согласно настоящему изобретению могут образовать комплекс, который может быть направлен против 1815 нуклеиновой кислоты-мишени 1806. Сайт-направленный полипептид комплекса может расщеплять 1820 нуклеиновую кислоту-мишень 1806. Донорный полинуклеотид может быть вставлен 1825 в расщепленную нуклеиновую кислоту-мишень 1806. Донорный полинуклеотид может содержать генетический элемент, представляющий интерес, 1830. Генетический элемент, представляющий интерес, 1830 может представлять собой ген. Донорный полинуклеотид также может содержать репортерный элемент 1835. Донорный полинуклеотид также может содержать полинуклеотидную последовательность, кодирующую сайт-направленный полипептид и одну или более нуклеиновых кислот, направленных против нуклеиновой кислоты. В некоторых случаях полинуклеотид, кодирующий сайт-направленный полипептид и одну или более нуклеиновых кислот, направленных против нуклеиновой кислоты, кодирует две нуклеиновые кислоты, направленные против нуклеиновой кислоты. Последовательность полинуклеотида, кодирующая сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты, может быть функционально связана с индуцируемым промотором. Вставка донорного полинуклеотида в нуклеиновую кислоту-мишень 1806 может привести к экспрессии репортерного элемента 1835. Репортерный элемент 1835 может быть использован в качестве инструмента для отбора клеток, которые содержат донорный полинуклеотид.
[0771] На Фиг. 19 показан примерный вариант способа удаления репортерного элемента 1915 из нуклеиновой кислоты-мишени. Нуклеиновая кислота-мишень может содержать множество генетических элементов 1905/1920. Репортерный элемент 1915 может быть гибридизован с генетическим элементом, представляющим интерес 1910. Экспрессия гена-репортера 1915 может быть индуцирована, что может привести к получению сайт-направленного полипептида и одной или более нуклеиновых кислот, направленных против нуклеиновой кислоты. Сайт-направленный полипептид может образовывать комплексы с нуклеиновыми кислотами, направленными против нуклеиновой кислоты. Комплексы могут быть направлены на репортерный элемент 1915 с помощью нуклеиновой кислоты, направленной против нуклеиновой кислоты, в комплексе. Одна из двух нуклеиновых кислот, направленных против нуклеиновой кислоты, может направлено действовать 1925 на 5'-конец репортерного элемента 1915. Одна из двух нуклеиновых кислот, направленных против нуклеиновой кислоты, может направлено действовать 1930 на 3'-конец репортерного элемента 1915. Концы-мишени репортерного элемента 1915 могут быть расщеплены под действием сайт-направленного полипептида, входящего в состав комплекса, что приводит к вырезанию 1935 репортерного элемента 1915. Нуклеиновая кислота-мишень может содержать часть донорного полинуклеотида, которая является генетическим элементом, представляющим интерес 1910. Нуклеиновые кислоты, направленные против нуклеиновой кислоты, могут быть сконструированы так, что донорный полинуклеотид вырезается (включая генетический элемент, представляющий интерес).
[0772] Способы
[0773] В настоящем изобретении предложены способы отбора клеток с использованием репортерного элемента и удаления репортерного элемента. В клетку может быть введен сайт-направленный полипептид, эндорибонуклеаза, нуклеиновая кислота, направленная против нуклеиновой кислоты, донорный полинуклеотид и/или нуклеиновая кислота, направленная против нуклеиновой кислоты. Донорный полинуклеотид может содержать один или более генетических элементов, представляющих интерес. Донорный полинуклеотид может содержать один или более репортерных элементов. Донорный полинуклеотид содержит один или более генетических элементов, представляющих интерес, и один или более репортерных элементов. В клетку может быть введено более одного сайт-направленного полипептида, эндорибонуклеазы, донорного полинуклеотида и/или нуклеиновой кислоты, направленной против нуклеиновой кислоты. В некоторых случаях клетка уже экспрессирует сайт-направленный полипептид и/или нуклеиновую кислоту, направленную против нуклеиновой кислоты. В некоторых случаях сайт-направленный полипептид и/или нуклеиновая кислота, направленная против нуклеиновой кислоты, кодируются на плазмиде. В некоторых случаях сайт-направленный полипептид и/или нуклеиновая кислота, направленная против нуклеиновой кислоты, кодируются более чем на одной плазмиде. В некоторых случаях в клетку водят более одного сайт-направленного полипептида или нуклеиновой кислоты, кодирующей сайт-направленный полипептид. В некоторых случаях клетка представляет собой клеточный лизат.
[0774] Введение может происходить с помощью любого способа введения нуклеиновой кислоты в клетку, такого как инфекция вирусом или бактериофагом, трансфекция, конъюгация, слияние протопластов, электропорация, липофекция, осаждение фосфатом кальция, полиэтиленимин (ПЭИ)-опосредованная трансфекция, опосредованная DEAE-декстраном трансфекция, опосредованная липосомами трансфекция, технология бомбардировки частицами, осаждение фосфатом кальция, прямая микроинъекция, опосредованная наночастицами доставка нуклеиновой кислоты и т.п. Вектор может быть временно экспрессирован в клетке-хозяине. Вектор может быть стабильно экспрессирован в клетке-хозяине (например, стабильно встроен в геном клетки-хозяина).
[0775] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может связываться с нуклеиновой кислотой, которая характеризуется определенной последовательностью-мишенью и/или любой последовательностью, гомологичной определенной последовательности. Последовательность-мишень может представлять собой часть или полную последовательность гена, 5'-конец гена, 3'-конец гена, регуляторный элемент (например, промотор, энхансер), псевдоген, некодирующую ДНК, микроспутник, интрон, экзон, хромосомную ДНК, митохондриальную ДНК, смысловую ДНК, антисмысловую ДНК, нуклеотидную ДНК, ДНК хлоропластов или РНК, наряду с другими молекулами нуклеиновых кислот.
[0776] Сайт-направленный полипептид может расщеплять нуклеиновую кислоту-мишень, связанную с нуклеиновой кислотой, направленной против нуклеиновой кислоты. Сайт-направленный полипептид может не расщеплять нуклеиновую кислоту-мишень. В некоторых случаях эндорибонуклеаза расщепляет нуклеиновую кислоту-мишень. Эндорибонуклеаза может кодироваться вектором. Эндорибонуклеаза может кодироваться донорным полинуклеотидом. Эндорибонуклеаза может присутствовать в клетке. Экспрессия эндорибонуклеазы и/или сайт-направленного полипептида может быть индуцирована условным промотором. Донорный полинуклеотид может быть встроен в нуклеиновую кислоту-мишень в том сайте, где он был расщеплен.
[0777] Вырезание
[0778] Способы, описанные в настоящей заявке, могут дополнительно включать вырезание всего или части репортерного элемента, или могут не влиять на него. Первая нуклеиновая кислота, направленная против нуклеиновой кислоты, репортерного элемента может направлено действовать на 5'-конец репортерного элемента. Вторая нуклеиновая кислота, направленная против нуклеиновой кислоты, репортерного элемента может направлено действовать на 3'-конец репортерного элемента. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может направленно действовать как на 5'-конец, так и на 3'-конец репортерного элемента. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может направлено действовать на две последовательности в репортерном элементе и/или донорном полинуклеотиде. Два последовательности-мишени могут быть по меньшей мере приблизительно на 70, 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100% идентичны. Два последовательности-мишени могут быть не более чем приблизительно на 70, 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100% идентичны. Если нуклеиновые кислоты, направленные против нуклеиновой кислоты, репортерного элемента экспрессированы, то они могут образовывать комплекс с сайт-направленным полипептидом и направлено действовать на 5'- и 3' -концы репортерного элемента путем гибридизации с комплементарной областью на 5'- и 3'-концах репортерного элемента. Гибридизация комплекса с репортерным элементом может привести к отщеплению всего или части репортерного элемента, или не влиять на него. Расщепленная нуклеиновая кислота может повторно соединиться, например, путем негомологичного соединения концов. Повторно соединенная нуклеиновая кислота не может вводить делецию или вставку. Повторно соединенная нуклеиновая кислота может вводить делецию или вставку. Расщепленная нуклеиновая кислота может быть повторно соединена, например, путем гомологичной рекомбинации. Гомологичная рекомбинация может быть использована для повторного соединения расщепленной нуклеиновой кислоты-мишени, когда сайты нуклеиновой кислоты-мишени являются по существу идентичными.
[0779] Скрининг
[0780] Способы, раскрытые в настоящей заявке, могут дополнительно включать вырезание репортерного элемента из выбранной клетки, с образованием тем самым второй клетки; и скрининг второй клетки. Скрининг может быть проведен для того чтобы выявить отсутствие всего или части репортерного элемента. Скрининг может включать сортировку флуоресцентно-активированных клеток (FACS), при которой клетки, экспрессирующие флуоресцентный белок, кодируемый репортерным элементом, отделяют от клеток, которые не экспрессируют флуоресцентный белок. Клетки могут быть приведены в контакт с флуоресцентным белком, флуоресцентным зондом или антителами, конъюгированными с флуорохромом, которые связываются с белками, кодируемыми репортерным элементом или генетическим элементом, и затем отобраны с помощью метода FACS. Флуорохромы могут включать, но не ограничивается ими, Cascade Blue, Pacific Blue, Pacific Orange, Lucifer yellow, NBD, R-фикоэритрин (PE), конъюгаты РЕ-Су5, конъюгаты РЕ-Су7, Red 613, PerCP, TruRed, FluorX, флуоресцеин, BODIPY-FL, TRITC, Texas Red, аллофикоцианин, конъюгаты АРС-Су7 (PharRed), различные красители Alexa Fluor, Cy2, Су3, Су3 В, Су3.5, Су5, Су5.5, Су7, различные красители DyLights, Y66H, Y66F, EBFP, EBFP2, Azurite, GFPuv, T-Sapphire, TagBFP, Cerulean, mCFP, ECFP, CyPet, Y66W, dKeima-Red, mKeima-Red, TagCFP, AmCyan1, mTFP1, S65A, Midoriishi-Cyan, GFP, Turbo GFP, TagGFP, TagGFP2, AcGFP1, S65L, Emerald, S65T, S65C, EGFP, Azami-Green, ZaGreen1, Dronpa-Green, TagYFP, EYFP, Topaz, Venus, mCitirine, YPet, Turbo YFP, PhiYFP, PhiYFPm, ZaYellow1, mBanana, Kusabira-Orange, mOrange, mOrane2, mKO, TurboRFP, tdTomato, DsRed-Express2, TagRFP, мономер DsRed, DsRed2, mStrawberry, Turbo FP602, AsRed2, mRFP1, J-Red, mCherry, HcRed1, mKate2, Katushka, mKate, TurboFP635, mPlum, mRaspberry, mNeptune, E2-Crimson.
[0781] Клетки могут быть приведены в контакт с антителами, которые связываются с пептидными аффинными метками, кодируемыми репортерным элементом или генетическим элементом, и затем могут быть отобраны с помощью иммуномагнитных гранул, которые распознают антитела. Скрининг может включать окрашивание клеток путем добавления Х-гал, если репортерный элемент или генетический элемент кодирует бета-галактозидазу. Скрининг может включать ручную сортировку (например, разбавление клеточной суспензии) и микроскопию (например, флуоресцентную микроскопию). Скрининг может включать высокопроизводительный скрининг.
[0782] Репортерные элементы могут кодировать гены лекарственной устойчивости, обеспечивая тем самым селекцию клеток, содержащих репортерный элемент, путем добавления лекарственных препаратов, лекарственных препаратов, вызывающих гибель клеток, которые не экспрессируют репортерный элемент. Такие лекарственные препараты могут включать, но не ограничиваются ими, эритромицин, клиндамицин, хлорамфеникол, гентамицин, канамицин, стрептомицин, тетрациклин, комбинацию хинупристина и дальфопристина, энрофлоксацин, ванкомицин, оксациллин, пенициллин, сульфаниламид сульфизоксазол, триметоприм, метионина сульфоксимин, метотрексат, пуромицин, бластицидин, гистидинол, гигромицин, зеоцин, блеомицин и неомицин.
[0783] Библиотеки
[0784] В настоящем изобретении предложены библиотеки векторов экспрессии, содержащих донорные полинуклеотиды. Согласно некоторым вариантам реализации настоящего изобретения библиотека может содержать векторы экспрессии, содержащие полинуклеотидные последовательности, кодирующие различные генетические элементы, представляющие интерес, но идентичные репортерные элементы. Согласно некоторым вариантам реализации настоящего изобретения библиотека может содержать векторы экспрессии, содержащие полинуклеотидные последовательности, кодирующие различные генетические элементы, представляющие интерес, и различные репортерные элементы. Репортерные элементы могут различаться по своим последовательностям, направленным против нуклеиновых кислот (crPHK и tracrPHK). Репортерные элементы могут различаться по своим репортерным генам (например, гены, кодирующие флуоресцентные белки). В настоящем изобретении предложены способы применения библиотеки для получения множества генетически модифицированных клеток. В настоящем изобретении предложены способы применения библиотеки для высокопроизводительного генетического скрининга. Такие библиотеки могут обеспечить исследование большого числа отдельных генов для выявления функции гена. Библиотеки могут содержать от приблизительно 10 отдельных членов до приблизительно 1012 отдельных членов; например, библиотека может содержать от приблизительно 10 отдельных членов до приблизительно 102 отдельных членов, от приблизительно 102 отдельных членов до приблизительно 103 отдельных членов, от приблизительно 103 отдельных членов до приблизительно 105 отдельных членов, от приблизительно 105 отдельных членов до приблизительно 107 отдельных членов, от приблизительно 107 отдельных членов до приблизительно 109 отдельных членов, или от приблизительно 109 отдельных членов до приблизительно 1012 отдельных членов.
[0785] Модификация клеток (Трансфекция/инфекция)
[0786] Способы согласно настоящему изобретению обеспечивают отбор клеток, содержащих донорный полинуклеотид. Согласно некоторым вариантам реализации настоящего изобретения способ может включать приведение нуклеиновой кислоты-мишени в контакт с клеткой либо введение в клетку (или популяцию клеток) одной или более нуклеиновых кислот, содержащих нуклеотидные последовательности, кодирующие нуклеиновую кислоту, направленную против нуклеиновой кислоты, сайт-направленный полипептид и/или донорный полинуклеотид согласно настоящему изобретению. Способы введения нуклеиновой кислоты в клетку могут включать инфекцию вирусом или бактериофагом, трансфекцию, конъюгацию, слияние протопластов, электропорацию, липофекцию, осаждение фосфатом кальция полиэтиленимин (ПЭИ)-опосредованную трансфекцию, опосредованную DEAE-декстраном трансфекцию, опосредованную липосомами трансфекцию, технологию бомбардировки частицами, осаждение фосфатом кальция, прямую микроинъекцию, опосредованную наночастицами доставку нуклеиновой кислоты и тому подобное. Согласно некоторым вариантам реализации настоящего изобретения приведение нуклеиновой кислоты-мишени в контакт с клеткой либо введение в клетку (или популяцию клеток) одной или более нуклеиновых кислот не может включать инфицирование вирусом. Согласно некоторым вариантам реализации настоящего изобретения приведение нуклеиновой кислоты-мишени в контакт с клеткой либо введение в клетку (или популяцию клеток) одной или более нуклеиновых кислот не может включать инфицирование бактериофагом. Согласно некоторым вариантам реализации настоящего изобретения приведение нуклеиновой кислоты-мишени в контакт с клеткой либо введение в клетку (или популяцию клеток) одной или более нуклеиновых кислот не может включать трансфекцию.
[0787] Сконструированные нуклеиновые кислоты, направленные против нуклеиновой кислоты
[0788] Сконструированные Р-домены
[0789] Нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть сконструирована (например, содержит модификации). Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, может относиться к любой из сконструированных нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке. Например, сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать минимальный повтор CRISPR, минимальную последовательность tracrPHK и 3'-концевую tracrPHK. Р-домен нуклеиновой кислоты, направленной против нуклеиновой кислоты, может взаимодействовать с областью сайт-направленного полипептида. Р-домен может взаимодействовать с множеством областей сайт-направленного полипептида. Р-домен может взаимодействовать с множеством областей сайт-направленного полипептида, при этом по меньшей мере одна из областей взаимодействует с РАМ в мотиве, прилегающем к протоспейсеру. Примеры таких областей могут включать аминокислоты 1096-1225 и 1105-1138 в Cas9 из S. pyogenes.
[0790] Модификация может быть введена в Р-домен. Р-домен может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25 или 30, или более смежных нуклеотидов. Р-домен может содержать не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25 или 30, или более смежных нуклеотидов. Р-домен может начинаться с первого нуклеотида, расположенного в направлении 3'-конца, относительно последнего спаренного нуклеотида в дуплексе, содержащем минимальный повтор CRISPR и минимальную последовательность tracrPHK. Р-домен может начинаться на расстоянии по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25 или 30, или более нуклеотидов, расположенных в направлении 3'-конца относительно последнего спаренного нуклеотида в дуплексе, содержащем минимальный повтор CRISPR и минимальную последовательность tracrPHK. Р-домен может начинаться на расстоянии не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25 или 30, или более нуклеотидов, расположенных в направлении 3'-конца относительно последнего спаренного нуклеотида в дуплексе, содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK.
[0791] Сконструированный Р-домен может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более мутаций. Сконструированный Р-домен может содержать не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более мутаций. Мутации могут быть смежными (например, последовательными). Мутации могут быть отделены друг от друга. Мутации могут быть разделены по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. Мутации могут быть разделены по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. Мутации в нуклеиновой кислоте, направленной против нуклеиновой кислоты, могут включать вставки, делеции и замены нуклеотидов в нуклеиновой кислоте, направленной против нуклеиновой кислоты.
[0792] В некоторых случаях сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, не более чем приблизительно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30% или более идентична и/или гомологична последовательности нуклеиновой кислоты, направленной против нуклеиновой кислоты, дикого типа. В некоторых случаях сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, по меньшей мере приблизительно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30% или более идентична и/или гомологична последовательности нуклеиновой кислоты, направленной против нуклеиновой кислоты, дикого типа,
[0793] В некоторых случаях часть нуклеиновой кислоты CRISPR в сконструированной нуклеиновой кислоте, направленной против нуклеиновой кислоты, не более чем приблизительно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30% или более идентична и/или гомологична последовательности нуклеиновой кислоты CRISPR дикого типа. В некоторых случаях часть нуклеиновой кислоты CRISPR в сконструированной нуклеиновой кислоте, направленной против нуклеиновой кислоты, по меньшей мере приблизительно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30% или более идентична и/или гомологична последовательности нуклеиновой кислоты CRISPR дикого типа.
[0794] Часть нуклеиновой кислоты tracrPHK сконструированной нуклеиновой кислоты, направленной против нуклеиновой кислоты, может быть не более чем приблизительно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30% или более идентична и/или гомологична последовательности нуклеиновой кислоты tracrPHK дикого типа. Часть нуклеиновой кислоты tracrPHK сконструированной нуклеиновой кислоты, направленной против нуклеиновой кислоты, может быть по меньшей мере приблизительно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30% или более идентична и/или гомологична последовательности нуклеиновой кислоты tracrPHK дикого типа.
[0795] Модификации Р-домена могут обеспечивать формирование новой структуры сконструированной нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая приобретает способность к гибридизации с новой последовательностью РАМ в нуклеиновой кислоте-мишени. Модификация Р-домена может быть комплементарна РАМ в нуклеиновой кислоте-мишени. Модификация Р-домена может содержать последовательность, обратно комплементарную РАМ в нуклеиновой кислоте-мишени. Новый РАМ может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов. Новый РАМ может содержать не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов. Модификации Р-домена могут произойти во взаимодействии с модификациями области сайт-направленного полипептида, связывающей Р-домен либо РАМ. Такие модификации могут быть компенсаторными, при этом модифицированный Р-домен подвергается специфичной модификации для связывания с модифицированным сайт-направленным полипептидом, причем модификация придает сайт-направленному полипептиду способность связываться со сконструированным Р-доменом с большей специфичностью.
[0796] Сконструированный Р-домен может быть сконструирован для связывания с новым РАМ (например, сконструированный Р-домен может гибридизоваться с новым РАМ). Новый РАМ (например, другой РАМ) может быть бимодальным (т.е. бимодальный РАМ может содержать две отдельные области РАМ). Две отдельные области бимодального РАМ могут быть разделены по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. Две отдельные области бимодального РАМ могут быть разделены не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами.
[0797] Сконструированный Р-домен может быть сконструирован для связывания с новым РАМ (например, другим РАМ), при этом новый РАМ является тримодальным. Тримодальный РАМ может содержать три отдельные области в последовательности РАМ (например, три отдельные области, которые могут быть использованы для нацеливания нуклеиновой кислоты, направленной против нуклеиновой кислоты, на нуклеиновую кислоту-мишень). Три отдельные области тримодального РАМ могут быть разделены по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. Три отдельные области тримодального РАМ могут быть разделены не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами.
[0798] Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать по меньшей мере две шпильки. Первая шпилька может содержать дуплекс между минимальным повтором CRISPR и минимальной последовательностью tracrPHK. Вторая шпилька может быть расположена в направлении 3'-конца относительно первой шпильки. Вторая шпилька может начинаться по меньшей мере с 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов, расположенных в направлении 3'-конца после последнего спаренного нуклеотида первого дуплекса. Вторая шпилька может начинаться не более чем с 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов, расположенных в направлении 3'-конца после последнего спаренного нуклеотида первого дуплекса. Вторая шпилька может содержать модифицированный Р-домен.
[0799] Сконструированный Р-домен второй шпильки может быть расположен на одной стороне шпильки дуплекса. Сконструированный Р-домен второй шпильки может быть расположен на обеих сторонах шпильки дуплекса. Сконструированный Р-домен второй шпильки может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 10 или 20% нуклеотидов во второй шпильке. Сконструированный Р-домен второй шпильки может содержать не более чем приблизительно 1, 2, 3, 4, 5, 10 или 20% нуклеотидов во второй шпильке.
[0800] Вторая шпилька может содержать tracrPHK (например, mid-tracrPHK или 3'tracrPHK нуклеиновой кислоты, направленной против нуклеиновой кислоты). Вторая шпилька может быть по меньшей мере приблизительно на 1, 5, 10, 15, 20, 25, 30, 35, 40, 45 или 50%, или более идентична tracrPHK. Вторая шпилька может быть не более чем приблизительно на 1, 5, 10, 15, 20, 25, 30, 35, 40, 45 или 50%, или более идентична tracrPHK.
[0801] Структура второй шпильки, содержащей сконструированный Р-домен, может быть изменена для устранения дуплекса (например, расплавлена, раскручена). Вторая шпилька может потерять дуплексную структуру при взаимодействии с нуклеиновой кислотой-мишенью. Вторая шпилька может потерять дуплексную структуру при взаимодействии с мотивом, прилегающим к протоспейсеру, нуклеиновой кислоты-мишени.
[0802] В некоторых случаях структура сконструированного Р-домена может быть изменена для придания ему способности гибридизоваться с областью в нуклеиновой кислоте, направленной против нуклеиновой кислоты (например, в аналогичной нуклеиновой кислоте, направленной против нуклеиновой кислоты, содержащей сконструированный Р-домен), и структура сконструированного Р-домена может быть изменена для придания ему способности гибридизоваться с нуклеиновой кислотой-мишенью. Другими словами, сконструированный Р-домен может содержать переключаемую последовательность, в которой, в некоторых случаях, Р-домен гибридизован с нуклеиновой кислотой, направленной против нуклеиновой кислоты, с образование шпильки, и в некоторых случаях Р-домен гибридизован с РАМ в нуклеиновой кислоте-мишени.
[0803] Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированный Р-домен, может быть сконструирована для придания ей способности связываться с РАМ с более низкой величиной константы диссоциации, по сравнению с таковой для нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержит сконструированного Р-домена (например, нуклеиновой кислотой, направленной против нуклеиновой кислоты, дикого типа). Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая модифицированный Р-домен, может быть сконструирована для придания ей способности связываться с РАМ с величиной константы диссоциации, которая по меньшей мере приблизительно на 10, 50, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550 или 600%, или более ниже или выше величины константы диссоциации для нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержит сконструированного Р-домена.
[0804] Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированный Р-домен, может быть сконструирована для придания ей способности связываться с РАМ с величиной константы диссоциации, которая не более чем приблизительно на 10, 50, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550 или 600%, или более ниже или выше величины константы диссоциации для нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержит сконструированного Р-домена. Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированный Р-домен, может быть сконструирована для придания ей способности связываться с РАМ с величиной константы диссоциации, которая по меньшей мере приблизительно в 1 раз, 2 раза, 3 раза, 4 раза, 5 раз, 10 раз, 20 раз, 30 раз, 40 раз или 50 раз, или более ниже или выше величины константы диссоциации для нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержит сконструированного Р-домена. Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированный Р-домен, может быть сконструирована для придания ей способности связываться с РАМ с величиной константы диссоциации, которая не более чем приблизительно в 1 раз, 2 раза, 3 раза, 4 раза, 5 раз, 10 раз, 20 раз, 30 раз, 40 раз или 50 раз, или более ниже или выше величины константы диссоциации для нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержит сконструированного Р-домена.
[0805] Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированный Р-домен, может быть сконструирована для придания ей способности связываться с РАМ с большей специфичностью, чем нуклеиновая кислота, направленная против нуклеиновой кислоты, которая не содержит сконструированного Р-домена (например, нуклеиновая кислота, направленная против нуклеиновой кислоты, дикого типа). Большая специфичность может относиться к снижению неспецифического связывания (например, связывания нуклеиновой кислоты, направленной против нуклеиновой кислоты, с некорректным РАМ или РАМ-подобной последовательностью). Например, сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированный Р-домен, может быть сконструирована для снижения неспецифического связывания по меньшей мере приблизительно на 10, 50, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550 или 600%, или более по сравнению с нуклеиновой кислотой, направленной против нуклеиновой кислоты, которая не содержит сконструированного Р-домена. Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированный Р-домен, может быть сконструирована для снижения неспецифического связывания не более чем приблизительно на 10, 50, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550 или 600%, или более, по сравнению с нуклеиновой кислотой, направленной против нуклеиновой кислоты, которая не содержит сконструированного Р-домена. Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированный Р-домен, может быть сконструирована для снижения неспецифического связывания по меньшей мере приблизительно в 1 раз, 2 раза, 3 раза, 4 раза, 5 раз, 10 раз, 20 раз, 30 раз, 40 раз или 50 раз, или более, по сравнению с нуклеиновой кислотой, направленной против нуклеиновой кислоты, которая не содержит сконструированного Р-домена. Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированный Р-домен, может быть сконструирована для снижения неспецифического связывания не более чем приблизительно в 1 раз, 2 раза, 3 раза, 4 раза, 5 раз, 10 раз, 20 раз, 30 раз, 40 раз или 50 раз, или более, по сравнению с нуклеиновой кислотой, направленной против нуклеиновой кислоты, которая не содержит сконструированного Р-домена.
[0806] Сконструированные выпячивания
[0807] Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть сконструирована так, что модификация может быть введена в область выпячивания нуклеиновой кислоты, направленной против нуклеиновой кислоты. Выпячивание является характерной структурой нуклеиновой кислоты, которая содержит неспаренные нуклеотиды. Выпячивание может содержать неспаренные нуклеотиды на каждой цепи дуплекса, который содержит такое выпячивание. Другими словами, выпячивание может содержать неспаренный нуклеотид на цепи минимального повтора CRISPR в дуплексе и неспаренный нуклеотид на цепи минимальной последовательности tracrPHK в дуплексе.
[0808] Выпячивание может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более неспаренных нуклеотидов на первой цепи дуплекса в нуклеиновой кислоте, направленной против нуклеиновой кислоты (т.е. на цепи минимального повтора CRISPR в дуплексе, содержащем минимальный повтор CRISPR и минимальную последовательность tracrPHK). Выпячивание может содержать не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более неспаренных нуклеотидов на первой цепи дуплекса в нуклеиновой кислоте, направленной против нуклеиновой кислоты (т.е. на цепи минимального повтора CRISPR в дуплексе, содержащем минимальный повтор CRISPR и минимальную последовательность tracrPHK). Выпячивание может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более неспаренных нуклеотидов на второй цепи дуплекса в нуклеиновой кислоте, направленной против нуклеиновой кислоты (т.е. на цепи минимальной последовательности tracrPHK в дуплексе, содержащем минимальный повтор CRISPR и минимальную последовательность tracrPHK). Выпячивание может содержать не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более неспаренных нуклеотидов на второй цепи дуплекса в нуклеиновой кислоте, направленной против нуклеиновой кислоты (т.е. на цепи минимальной последовательности tracrPHK в дуплексе, содержащем минимальный повтор CRISPR и минимальную последовательность tracrPHK). Выпячивание может содержать один неспаренный нуклеотид на минимальной последовательности РНК CRISPR и 3 неспаренных нуклеотида на цепи минимальной последовательности tracrPHK.
[0809] Нуклеотиды, прилегающие к неспаренному нуклеотиду, могут представлять собой нуклеотид, который участвует в неканоническом спаривании оснований. Неканоническое спаривание оснований может включать взаимодействия гуанин-урацил, гипоксантин-урацил, гипоксантин-аденин и гипоксантин-цитозин. По меньшей мере 1, 2, 3, 4 или 5, или более нуклеотидов, прилегающих к неспаренному нуклеотиду, могут участвовать в неканоническом спаривании оснований. Не более чем 1, 2, 3, 4 или 5, или более нуклеотидов, прилегающих к неспаренному нуклеотиду, могут участвовать в неканоническом спаривании оснований.
[0810] Сконструированное выпячивание может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более мутаций. Сконструированное выпячивание может содержать не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более мутаций. Мутации могут быть смежными друг с другом (например, последовательными). Мутации могут быть отделены друг от друга. Мутации могут быть разделены по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. Мутации могут быть разделены по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами. Мутации нуклеиновой кислоты, направленной против нуклеиновой кислоты, могут содержать вставки, делеции и замены нуклеотидов в нуклеиновой кислоте, направленной против нуклеиновой кислоты.
[0811] Последовательность выпячивания сконструированной нуклеиновой кислоты, направленной против нуклеиновой кислоты, может быть не более чем приблизительно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30% или более идентична и/или гомологична последовательности нуклеиновой кислоты, направленной против нуклеиновой кислоты, дикого типа. Последовательность выпячивания сконструированной нуклеиновой кислоты, направленной против нуклеиновой кислоты, может быть по меньшей мере приблизительно на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30% или более идентична и/или гомологична последовательности нуклеиновой кислоты, направленной против нуклеиновой кислоты, дикого типа.
[0812] Одна цепь выпячивания может быть мутированной, тогда как другая цепь выпячивания может быть немутированной. Другими словами, в некоторых случаях, последовательность выпячивания на цепи минимального повтора РНК CRISPR аналогична последовательности нуклеиновой кислоты, направленной против нуклеиновой кислоты, дикого типа, и последовательность выпячивания на минимальной последовательности tracrPHK является мутированной. Другими словами, последовательность выпячивания на цепи минимального повтора РНК CRISPR является мутированной, и последовательность выпячивания на цепи минимальной последовательности tracrPHK аналогична последовательности нуклеиновой кислоты, направленной против нуклеиновой кислоты, дикого типа.
[0813] Модификации в выпячивании могут обеспечивать формирование новой структуры сконструированной нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая приобретает способность связываться с новым сайт-направленным полипептидом. Аминокислотная последовательность нового сайт-направленного полипептида может быть по меньшей мере приблизительно на 5, 10, 15, 20, 25, 30, 35, 40, 45 или 50%, или более идентична аминокислотной последовательности сайт-направленного полипептида дикого типа. Аминокислотная последовательность нового сайт-направленного полипептида может быть не более чем приблизительно на 5, 10, 15, 20, 25, 30, 35, 40, 45 или 50%, или более идентична аминокислотной последовательности сайт-направленного полипептида дикого типа. Новый сайт-направленный полипептид может представлять собой гомолог Cas9. Новый сайт-направленный полипептид может представлять собой ортолог Cas9. Новый сайт-направленный полипептид может представлять собой химерный белок двух различных сайт-направленных полипептидов. Новый сайт-направленный полипептид может содержать мутацию, описанную в настоящей заявке.
[0814] Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированное выпячивание, может быть сконструирована для придания ей способности связываться с сайт-направленным полипептидом с величиной константы диссоциации, которая ниже или выше величины константы диссоциации нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержат сконструированного выпячивания (например, нуклеиновой кислоты, направленной против нуклеиновой кислоты, дикого типа). Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированное выпячивание, может быть сконструирована для придания ей способности связываться с сайт-направленным полипептидом с величиной константы диссоциации, которая по меньшей мере приблизительно на 10, 50, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550 или 600%, или более ниже или выше величины константы диссоциации для нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержит сконструированного выпячивания. Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированное выпячивание, может быть сконструирована для придания ей способности связываться с сайт-направленным полипептидом с величиной константы диссоциации, которая не более чем приблизительно на 10, 50, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550 или 600%, или более ниже или выше величины константы диссоциации для нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержит сконструированного выпячивания. Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированное выпячивание, может быть сконструирована для придания ей способности связываться с сайт-направленным полипептидом с величиной константы диссоциации, которая по меньшей мере приблизительно в 1 раз, 2 раза, 3 раза, 4 раза, 5 раз, 10 раз, 20 раз, 30 раз, 40 раз или 50 раз, или более ниже или выше величины константы диссоциации для нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержит сконструированного выпячивания. Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, содержащая сконструированное выпячивание, может быть сконструирована для придания ей способности связываться с сайт-направленным полипептидом с величиной константы диссоциации, которая не более чем приблизительно в 1 раз, 2 раза, 3 раза, 4 раза, 5 раз, 10 раз, 20 раз, 30 раз, 40 раз или 50 раз, или более ниже или выше величины константы диссоциации для нуклеиновой кислоты, направленной против нуклеиновой кислоты, которая не содержит сконструированного выпячивания.
[0815] Способы
[0816] В настоящем изобретении предложены способы конструирования нуклеиновых кислот, направленных против нуклеиновой кислоты. Способы могут включать модифицирование нуклеиновой кислоты, направленной против нуклеиновой кислоты. Модифицирование может включать вставки, делеции, замены и мутации нуклеотидов в нуклеиновой кислоте, направленной против нуклеиновой кислоты. Модифицирование может изменять нуклеиновую кислоту, направленную против нуклеиновой кислоты, так, что указанная нуклеиновая кислота, направленная против нуклеиновой кислоты, приобретает способность связываться с новым мотивом, прилегающим к протоспейсеру, и/или новым сайт-направленным полипептидом, по сравнению с нуклеиновой кислотой, направленной против нуклеиновой кислоты, дикого типа. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке.
[0817] Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть использована для расщепления нуклеиновой кислоты-мишени. Сконструированная нуклеиновая кислота, направленная против нуклеиновой кислоты, может быть введена в клетки совместно с сайт-направленным полипептидом, с образованием тем самым комплекса. Комплекс может гибридизоваться с нуклеиновой кислотой-мишенью, содержащей мотив, прилегающий к протоспейсеру. Сайт-направленный полипептид, входящий в состав комплекса, может расщеплять нуклеиновую кислоту-мишень.
[0818] Комплементарные части последовательностей нуклеиновой кислоты пре-РНК CRISPR и нуклеиновой кислоты tracrPHK из Streptococcus pyogenes SF370 показаны на Фиг. 20.
[0819] На Фиг. 21 показана типичная структура дуплекса (например, шпильки), содержащего минимальный повтор CRISPR и минимальную последовательность tracrPHK и часть последовательности 3'-концевой tracrPHK. Дуплекс содержит область выпячивания.
[0820] В таблице 4.1 приведены последовательности ДНК-матриц, использованных для синтеза одиночных направляющих нуклеиновых кислот, направленных против нуклеиновой кислоты, согласно настоящему изобретению.





[0821] В таблице 4.2 приведены последовательности РНК для ДНК-матриц, приведенных в таблице 1.
[0822] Таблица 4.2. Последовательности РНК одиночных направляющих нуклеиновых кислот, направленных против нуклеиновой кислоты, согласно настоящему изобретению





[0823] В таблице 5 указаны величины активности и цель создания дополнительных вариантов нуклеиновых кислот, направленных против нуклеиновой кислоты; + относится к активному варианту; - относится к неактивному варианту. Экспериментальные данные, полученные при использовании этих вариантов, приведены на Фиг. 37.

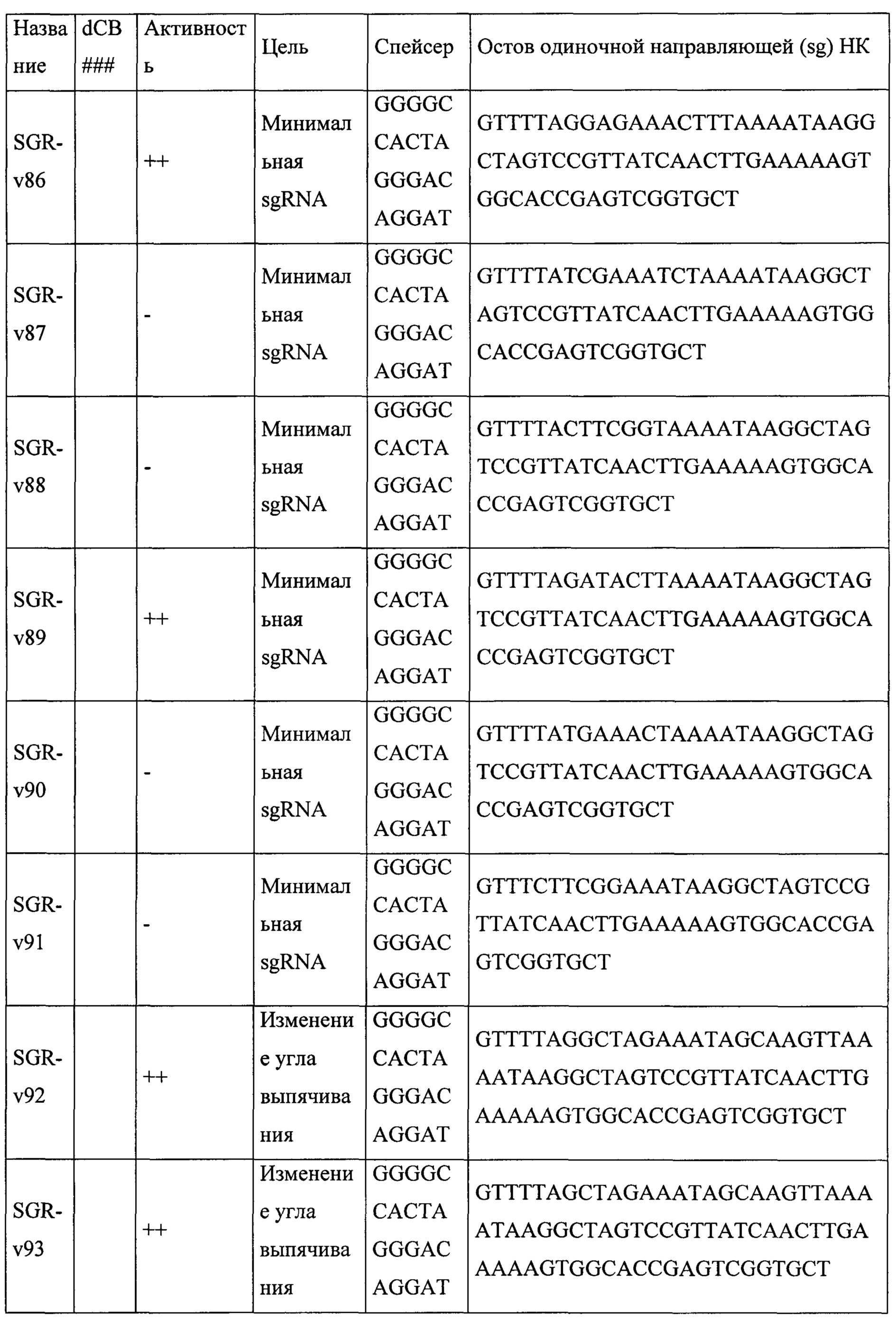






[0824] Способы получения меченых клеточных линий с использованием нуклеиновой кислоты, направленной против нуклеиновой кислоты
[0825] Способы согласно настоящему изобретению предусматривают введение метки в клетку с использованием донорного полинуклеотида, при этом донорный полинуклеотид может удваиваться при делении и/или сохраняться при дифференциации, и указанный донорный полинуклеотид может быть передан в каждую дочернюю клетку при делении клеток. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке.
[0826] Меченая клетка может быть получена путем приведения клетки в контакт с донорным полинуклеотидом и комплексом, содержащим сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты. Донорный полинуклеотид может быть встроен в расщепленную нуклеиновую кислоту-мишень, с образованием тем самым меченой клетки. Меченую клетку можно размножать, например, с помощью способов, подходящих для клеточной линии, либо для получения размноженной популяции клеток.
[0827] Донорный полинуклеотид может быть введен в сайт разрезания с использованием донорной кассеты для гомологичной рекомбинации, которая содержит концы, гомологичные последовательностям, расположенным по обе стороны от двухцепочечного разрыва. Донорный полинуклеотид может содержать дополнительную последовательность между двумя концами. Дополнительная последовательность может представлять собой последовательность нуклеиновой кислоты. Дополнительная последовательность может кодировать ген. Дополнительная последовательность может кодировать некодирующий элемент нуклеиновой кислоты.
[0828] Донорный полинуклеотид (например, дополнительная последовательность донорного полинуклеотида между двумя гомологичными концами) может содержать маркер. Маркер может содержать маркер для визуализации (например, флуоресцентный маркер, такой как GFP). Маркер может содержать случайную полинуклеотидную последовательность (например, такую как случайная гексамерная последовательность). Маркер может представлять собой последовательность штрихкода.
[0829] NHEJ может ввести уникальную характерную последовательность в каждый сайт разреза. Механизм репарации может привести к введению вставок (например, вставки донорного полинуклеотида), делеций или мутаций в сайт разреза. Клетка, которая подвергается NHEJ для репарации двухцепочечного разрыва, может содержать уникальную последовательность после завершения репарации (например, уникальная последовательность может быть вставлена в двухцепочечный разрыв). Если в клетке разрезанию подвергается более одного сайта, то комплекс репарации может ввести донорный полинуклеотид в каждый сайт, придав тем самым разнообразие последовательностей этой клетке. Восстановленный сайт может обеспечить уникальную последовательность штрихкода в клетке, которая может быть сохранена во время деления клеток и передана всем потомкам модифицированной клетки. Донорный полинуклеотид может быть вставлен по меньшей мере приблизительно в 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более сайтов (например, в расщепленных нуклеиновых кислотах-мишенях). Донорный полинуклеотид может быть вставлен не более чем приблизительно в 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более сайтов (например, в расщепленных нуклеиновых кислотах-мишенях).
[0830] Гомологичную рекомбинацию (HR) можно использовать для введения последовательности штрихкода в клетку и/или клеточную популяцию (например, в клетку человека, клетку млекопитающего, клетку дрожжей, грибков, простейших, архей). Библиотека донорных плазмид (например, содержащих донорный полинуклеотид) может быть получена с использованием рандомизированных последовательностей в донорной кассете. Библиотека может быть получена из олигонуклеотидов, части двухцепочечной ДНК, плазмиды и/или миникольца.
[0831] Последовательности донорных полинуклеотидов могут быть введены в геномы отдельных клеток для отслеживания клеточной линии. Сайты введения могут быть выбраны для внесения модификаций в молчащие или «безопасные» области генома, удаленные от генов и регуляторных элементов, чтобы свести к минимуму возможное вредное воздействие на функции клеток. Сайты, расположенные в пределах функциональных генетических элементов, также могут быть использованы для отслеживания судьбы клеток.
[0832] Например, донорные полинуклеотиды могут быть введены в стволовую клетку и/или популяции стволовых клеток. Способы согласно настоящему изобретению можно применять для отслеживания развития клеточной линии в животных моделях. Например, судьбу клеток и/или дифференцировку в процессе кроветворения можно отслеживать с помощью способов согласно настоящему изобретению. Способы согласно настоящему изобретению можно применять для терапии на основании конструирования клеток для терапевтического применения. Например, клетка может быть помечена с использованием донорного полинуклеотида, кодирующего терапевтический белок. Клетка может быть размножена. Размноженная клетка может быть введена пациенту. В качестве другого примера, дифференцированная клетка может быть выделена от субъекта. Дифференцированная клетка может быть помечена двумя маркерами: первый маркер экспрессируется при дифференцировке клетки, и второй маркер экспрессируется при потере клеткой дифференцировки. Выявление маркеров можно использовать при определении событий дифференцировки. В другом примере, дифференцированная клетка может быть получена от субъекта. Дифференцированная клетка может быть дедифференцирована в плюрипотентную клетку. Плюрипотентная клетка может быть помечена донорным полинуклеотидом, кодирующим терапевтический белок. Клетка может повторно дифференцироваться в новый тип клеток, во время экспрессии терапевтического белка, создавая тем самым терапевтическую клетку, специфичную для пациента. Меченые клетки могут делиться и дифференцироваться, и модификация(и) их генома может быть передана каждой дочерней клетке при делении клеток.
[0833] В некоторых случаях две клетки могут быть помечены двумя различными маркерами донорных полинуклеотидов. Две клетки могут быть объединены. Комбинированную смесь можно одновременно исследовать количественно. Донорные полинуклеотиды могут обеспечить мультиплексное исследование двух клеток, поскольку донорный полинуклеотид можно использовать, чтобы различить две клетки.
[0834] Клеточная популяция может быть выбрана для введения двухцепочечных разрывов или получения уникальных клеточных характеристик. Клетки могут быть очищены или отобраны. Например, популяция кроветворных стволовых клеток (CD45+) может быть отобрана с помощью метода FACS или очистки с использованием магнитных гранул. Костный мозг можно обрабатывать в условиях ex vivo с использованием нуклеазы. Клетки могут быть подвергнуты направленному воздействию в условиях in vivo с использованием вирусов с определенным тропизмом. Клетки могут быть выбраны с помощью сконструированных вирусов, направленных против клеток-мишеней, несущих определенный рецептор.
[0835] Меченые клетки можно исследовать с помощью высокопроизводительного секвенирования на популяционном уровне или на уровне одиночной клетки. На популяционном уровне совокупность клеток может быть лизирована. Геномная ДНК может быть экстрагирована. ПЦР-праймеры могут быть сконструированы для амплификации геномной области, которая была модифицирована нуклеазой. Последовательности могут быть обогащены посредством гибридизации. Библиотека последовательностей может быть получена из геномной ДНК и обогащена. Область, представляющая интерес, может быть обогащена, и может быть получена библиотека последовательностей. Библиотека последовательностей может быть получена одновременно во время обогащения с использованием праймеров, содержащих соответствующие метки последовательности, которые будут использованы при осуществлении методик секвенирования нуклеиновых кислот. Если двухцепочечный разрыв сделан в области, которая может быть транскрибирована, то для получения библиотек последовательностей может быть использована РНК.
[0836] После получения данных о последовательности нуклеиновой кислоты, последовательности можно исследовать для определения клональной структуры. Такое определение можно осуществлять путем сбора общих последовательностей вместе и подсчета количества таких последовательностей.
[0837] Клетки могут быть подвергнуты дополнительным этапам отбора путем сортировки клеток на основании присутствия поверхностных клеточных маркеров, используя методы проточной цитометрии или аффинной очистки. Поверхностные клеточные маркеры можно использовать для определения состояния клеток, и судьба модифицированных клеточных популяций может быть определена путем сравнения состояний клеток с клональной структурой.
[0838] Клетки могут быть выделены при проведении исследований на уровне одиночной клетки. ПЦР-продукты могут быть получены из каждой отдельной клетки. Выделение продуктов может быть достигнуто в микролунках чипов, микрожидкостных устройствах, и/или эмульсиях. Если в отдельной клетке осуществляют более одной геномной модификации, то ПЦР-продукты могут быть соединены вместе, физическим или химическим способом, чтобы обеспечить их взаимосвязь с исходной клеткой.
[0839] Способы количественной оценки событий редактирования генома
[0840] У РНК-зависимых нуклеаз, таких как Cas9, способность распознавать нуклеиновые кислоты и нуклеазная активность могут быть связаны между собой. В некоторых случаях способность распознавать нуклеиновые кислоты и нуклеазная активность могут быть не связаны между собой. Сайты действия нуклеазы могут быть расположены в пределах специфичной последовательности, распознаваемой нуклеазой.
[0841] Негомологичное соединение концов может представлять собой несовершенный процесс восстановления, который может привести к вставке нескольких оснований в сайт двухцепочечного разрыва. NHEJ может привести к введению вставок, делеций и/или мутаций в сайт разреза. NHEJ может значительно нарушить исходную последовательность. Нарушение нативной последовательности, как следствие работы механизмов репарации, можно использовать для оценки эффективности подходов редактирования генома.
[0842] Гомологичная рекомбинация может обеспечить более полное восстановление разрыва нуклеиновой кислоты-мишени путем обмена нуклеотидных последовательностей между аналогичными или идентичными молекулами нуклеиновой кислоты. Дополнительная последовательность может быть введена в нуклеиновую кислоту-мишень в сайте разреза путем использования донорной кассеты (например, донорного полинуклеотида), которая содержит концы, гомологичные последовательностям, расположенным по обеим сторонам от двухцепочечного разрыва, и дополнительную последовательность между двумя концами.
[0843] В настоящем изобретении описан подход к оценке активности в отношении введения двухцепочечных разрывов и NHEJ-опосредованных вставок/удалений, которые вводят нуклеазы, зависящие от нуклеиновой кислоты, такие как Cas9. Указанный способ основан на том факте, что сайты в нуклеиновой кислоте-мишени, которые распознаются Cas9 в течение начальной фазы распознавания нуклеазой, и активность, направленная на расщепление нуклеиновой кислоты, могут быть нарушены во время процесса NHEJ путем введения либо вставки, либо делеций.
[0844] В некоторых случаях способ обеспечивает конструирование нуклеиновой кислоты, направленной против нуклеиновой кислоты, для направленного действия на сайт, представляющий интерес, в нуклеиновой кислоте-мишени (например, в геноме). Нуклеиновая кислота-матрица, кодирующая нуклеиновую кислоту, направленную против нуклеиновой кислоты, может быть сконструирована с включением промоторной последовательности, присоединенной к 5'-концу нуклеиновой кислоты, направленной против нуклеиновой кислоты, чтобы обеспечить синтез нуклеиновой кислоты, направленной против нуклеиновой кислоты, в условиях in vitro.
[0845] Праймеры могут быть сконструированы в положениях, которые фланкируют сайт расщепления. Сайт расщепления (и/или области нуклеиновых кислот вокруг сайта расщепления) может быть амплифицирован (например, из геномной нуклеиновой кислоты) с образованием продукта (например, амплифицированного продукта ПЦР). Продукт (например, амплифицированный продукт ПЦР) может содержать по меньшей мере приблизительно 100, 200, 300,400, 500, 600, 700, 800, 900, 1000, 1100, 1200 или более оснований в длину. Продукт (например, амплифицированный продукт ПЦР) может содержать не более чем приблизительно 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 1100, 1200 или более оснований в длину. Продукт (например, амплифицированный продукт ПЦР) может содержать приблизительно 200-600 пар оснований в длину.
[0846] Продукты могут быть очищены. Продукты можно инкубировать с РНК-зависимой нуклеазой (например, Cas9) и нуклеиновой кислотой, направленной против нуклеиновой кислоты. Те молекулы, которые были амплифицированы из геномной нуклеиновой кислоты, которая не подвергалась модификации путем NHEJ, могут содержать правильную последовательность, которая может быть распознана и расщеплена Cas9. Молекулы, которые были амплифицированы из геномной нуклеиновой кислоты, которая была модифицирована путем NHEJ, могут не содержать сайты, которые могут быть распознаны и/или расщеплены Cas9.
[0847] Расщепленные продукты затем можно исследовать с помощью таких способов как гель-электрофорез, капиллярный электрофорез, высокопроизводительное секвенирование и/или количественная ПЦР (например, кПЦР). При использовании гель-электрофореза гель можно исследовать с помощью методов визуализации. После получения изображений геля, долю клеток, модифицированных путем NHEJ, можно оценить с помощью измерения интенсивности полос, соответствующих расщепленным продуктам, с последующим сопоставлением с интенсивностью полос, соответствующих нерасщепленным продуктам.
[0848] Способы доставки донорного полинуклеотида к двухцепочечному разрыву для вставки в двухцепочечный разрыв
[0849] В настоящем изобретении описаны способы доставки донорного полинуклеотида рядом с сайт-направленным разрывом нуклеиновой кислоты-мишени, чтобы облегчить вставку (например, путем гомологичной рекомбинации) донорного полинуклеотида в сайт двухцепочечного разрыва. Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке.
[0850] В некоторых случаях способы согласно настоящему изобретению обеспечивают доставку донорного полинуклеотида рядом с сайтом двухцепочечного разрыва в нуклеиновой кислоте-мишени путем связывания его с нуклеазой, которая образует двухцепочечный разрыв (например, Cas9).
[0851] Комплекс, содержащий сайт-направленный полипептид, нуклеиновую кислоту, направленную против нуклеиновой кислоты, и донорный полинуклеотид, может быть доставлен к нуклеиновой кислоте-мишени. На Фиг. 30 показаны типичные способы доставки донорного полинуклеотида рядом с сайтом двухцепочечного разрыва в нуклеиновой кислоте-мишени. Например, нуклеиновая кислота, направленная против нуклеиновой кислоты, может содержать 3'-гибридизующуюся удлиненную последовательность, которая может представлять собой часть удлиненной последовательности tracrPHK (показана светлой пунктирной линией, прикрепленной к нуклеиновой кислоте, направленной против нуклеиновой кислоты). 3'-Гибридизующаяся удлиненная последовательность может представлять собой ненативную последовательность. На Фиг. 30А показано, что удлиненная последовательность tracrPHK на 3'-конце нуклеиновой кислоты, направленной против нуклеиновой кислоты, может содержать последовательность, которая может гибридизоваться с концом донорного полинуклеотида (например, 3'-концом) (донорный полинуклеотид показан более жирной пунктирной линией). 3'-Гибридизующаяся удлиненная последовательность может содержать по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов в длину. 3'-Гибридизующаяся удлиненная последовательность может содержать не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидов в длину. 3'-Гибридизующаяся последовательность может гибридизоваться с по меньшей мере приблизительно 1, 2, 3, 4, 5, 5, 6, 7, 8, 9 или 10, или более нуклеотидами донорного полинуклеотида. 3'-Гибридизующаяся последовательность может гибридизоваться с не более чем приблизительно 1, 2, 3, 4, 5, 5, 6, 7, 8, 9 или 10, или более нуклеотидами донорного полинуклеотида. 3'-Гибридизующаяся последовательность может гибридизоваться с донорным полинуклеотидом с образованием по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более несоответствий. 3'-Гибридизующаяся последовательность может гибридизоваться с донорным полинуклеотидом с образованием не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более несоответствий.
[0852] 3'-Гибридизующаяся удлиненная последовательность может гибридизоваться с 3'-концом донорного полинуклеотида. 3'-Гибридизующаяся удлиненная последовательность может гибридизоваться с по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более 3'-концевыми нуклеотидами донорного полинуклеотида. 3'-Гибридизующаяся удлиненная последовательность может гибридизоваться с не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более 3'-концевыми нуклеотидами донорного полинуклеотида.
[0853] Как показано на Фиг. 30В, удлиненная последовательность нуклеиновой кислоты tracr на 3'-конце нуклеиновой кислоты, направленной против нуклеиновой кислоты, может содержать последовательность, которая может гибридизоваться с 5'-концом донорной ДНК. 3'-Гибридизующаяся удлиненная последовательность может гибридизоваться с по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более 5'-концевыми нуклеотидами донорного полинуклеотида. 3'-Гибридизующаяся удлиненная последовательность может гибридизоваться с не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более 5 '-концевыми нуклеотидами донорного полинуклеотида.
[0854] Удлиненная последовательность нуклеиновой кислоты tracr на 3'-конце нуклеиновой кислоты, направленной против нуклеиновой кислоты, может содержать последовательность, которая может гибридизоваться с областью между 3'-концом и 5'-концом донорного полинуклеотида, как показано на Фиг. 30С. 3'-Гибридизующаяся удлиненная последовательность может гибридизоваться с по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами между 3'-концом и 5'-концом донорного полинуклеотида. 3'-Гибридизующаяся удлиненная последовательность может гибридизоваться с не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более нуклеотидами между 3'-концом и 5'-концом донорного полинуклеотида.
[0855] Удлиненная последовательность нуклеиновой кислоты tracr на 3'-конце нуклеиновой кислоты, направленной против нуклеиновой кислоты, может содержать последовательность, которая может гибридизоваться по всей длине донорного полинуклеотида, как показано на Фиг. 30D. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может гибридизоваться с по меньшей мере приблизительно 20, 30, 40, 50, 60, 70, 80, 90 или 100% донорного полинуклеотида. Нуклеиновая кислота, направленная против нуклеиновой кислоты, может гибридизоваться с не более чем приблизительно 20, 30, 40, 50, 60, 70, 80, 90 или 100% донорного полинуклеотида. 3'-Гибридизующаяся удлиненная последовательность может гибридизоваться по всей длине донорного полинуклеотида с образованием по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более несоответствий. 3'-Гибридизующаяся удлиненная последовательность может гибридизоваться по всей длине донорного полинуклеотида с образованием не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, или более несоответствий.
[0856] Удлиненная последовательность нуклеиновой кислоты tracr на 3'-конце нуклеиновой кислоты, направленной против нуклеиновой кислоты (например, 3'-гибридизующаяся удлиненная последовательность), может содержать последовательность, которую можно использовать в качестве матрицы и которую можно конвертировать, например, с помощью обратной транскриптазы, для получения гибридной нуклеиновой кислоты (например, полученная нуклеиновая кислота представляет собой гибрид РНК-ДНК, в котором новая транскрибированная нуклеиновая кислота может представлять собой ДНК), как показано на Фиг. 30Е. Примерные обратные транскриптазы включают Superscript, ThermoScript, обратную транскриптазу ВИЧ и обратную транскриптазу MMLV. Обратная транскриптаза может удлинить последовательность донорного полинуклеотида с матрицы 3'-гибридизующейся удлиненной последовательности.
[0857] Удлиненная последовательность нуклеиновой кислоты tracr на 3'-конце нуклеиновой кислоты, направленной против нуклеиновой кислоты, может содержать последовательность нуклеиновой кислоты, которая может связываться с РНК-связывающим белком (RBP). РНК-связывающий белок может быть гибридизован с ДНК-связывающим белком (DBP), как показано на Фиг. 30F. ДНК-связывающий белок может связываться с донорным полинуклеотидом.
[0858] Последовательности, используемые для доставки донорного полинуклеотида рядом с двухцепочечным разрывом, могут быть присоединены к 5'-концу нуклеиновой кислоты, направленной против нуклеиновой кислоты (например, к удлиненной последовательности спейсера). Последовательности, используемые для доставки донорного полинуклеотида рядом с двухцепочечным разрывом, могут быть присоединены как к 5'-концу, так и 3'-концу нуклеиновой кислоты, направленной против нуклеиновой кислоты.
[0859] Нуклеаза, используемая в соответствии со способами согласно настоящему изобретению (например, Cas9), может обладать никазной активностью, при наличии которой нуклеаза может вводить одноцепочечные разрывы в нуклеиновую кислоту-мишень. Пары нуклеаз с никазной активностью могут быть направлены в области, которые расположены поблизости друг от друга. Первая нуклеаза может связываться с первой нуклеиновой кислотой, направленной против нуклеиновой кислоты, которая может взаимодействовать с первым донорным полинуклеотидом. Вторая нуклеаза может связываться со второй нуклеиновой кислотой, направленной против нуклеиновой кислоты, которая может взаимодействовать со вторым донорным полинуклеотидом. Первый и второй донорные полинуклеотиды могут быть модифицированы для придания им способности гибридизоваться друг с другом, чтобы получить двухцепочечный донорный полинуклеотид. Два отдельных донорных полинуклеотида могут быть доставлены в сайт-мишень нуклеазы.
[0860] Согласно некоторым вариантам реализации настоящего изобретения донорный полинуклеотид может быть одноцепочечным. Согласно некоторым вариантам реализации настоящего изобретения донорный полинуклеотид может быть двухцепочечным. Согласно некоторым вариантам реализации настоящего изобретения донорная ДНК может представлять собой миникольцо. Согласно некоторым вариантам реализации настоящего изобретения донорный полинуклеотид может представлять собой плазмиду. Согласно некоторым вариантам реализации настоящего изобретения плазмида может быть суперспирализована. Согласно некоторым вариантам реализации настоящего изобретения донорный полинуклеотид может быть метилированным. Согласно некоторым вариантам реализации настоящего изобретения донорный полинуклеотид может быть неметилированным. Донорный полинуклеотид может содержать модификацию. Модификации могут включать те, которые описаны в настоящей заявке, включая, но не ограничиваясь ими, биотинилирование, химический конъюгат и синтетические нуклеотиды.
[0861] Способы клонирования и экспрессии вектора, содержащего сайт-направленный полипептид и нуклеиновую кислоту, направленную против нуклеиновой кислоты
[0862] В настоящем изобретении предложены способы клонирования сконструированной нуклеиновой кислоты, направленной против нуклеиновой кислоты, в вектор (например, линеаризованный вектор). Указанный способ можно осуществлять с помощью любого из сайт-направленных полипептидов, нуклеиновых кислот, направленных против нуклеиновой кислоты, и комплексов сайт-направленных полипептидов и нуклеиновых кислот, направленных против нуклеиновой кислоты, описанных в настоящей заявке.
[0863] Пользователь (например, ученый) может сконструировать одноцепочечные олигонуклеотиды ДНК. Одноцепочечные олигонуклеотиды ДНК могут, при гибридизации друг с другом, кодировать последовательность спейсера для направленного действия на нуклеиновую кислоту-мишень. Одноцепочечные олигонуклеотиды ДНК могут содержать по меньшей мере приблизительно 5, 10, 15, 20, 25, 30 или более нуклеотидов в длину. Одноцепочечные олигонуклеотиды ДНК могут содержать не более чем приблизительно 5, 10, 15, 20, 25, 30 или более нуклеотидов в длину. Одноцепочечные олигонуклеотиды ДНК могут содержать 19-20 нуклеотидов в длину.
[0864] Одноцепочечный олигонуклеотид ДНК может быть сконструирован так, что он может гибридизоваться с нуклеиновой кислотой-мишенью (например, с последовательностью, примыкающей к мотиву, прилегающему к протоспейсеру, например, с 3'-концом или 5'-концом мотива, прилегающего к протоспейсеру). Олигонуклеотид ДНК может кодировать последовательность, соответствующую смысловой или антисмысловой цепи последовательности нуклеиновой кислоты-мишени. [0865] Одноцепочечный олигонуклеотид может содержать первую часть, которая может гибридизоваться и/или является комплементарной нуклеиновой кислоте-мишени. Одноцепочечный олигонуклеотид может содержать первую часть, которая может гибридизоваться и/или является комплементарной другому одноцепочечному олигонуклеотиду. Одноцепочечный олигонуклеотид может содержать вторую часть, которая может гибридизоваться с последовательностью в линеаризованном векторе. Другими словами, пара одноцепочечных олигонуклеотидов может содержать первую часть, которая обеспечивает их гибридизацию друг с другом, и вторую часть, которая содержит одноцепочечные выступающие концы, причем выступающие концы могут гибридизоваться с липкими концами в линеаризованном векторе. В некоторых случаях выступающий конец содержит 5'-GTTTT-3'. В некоторых случаях выступающий конец содержит 5'-CGGTG-3'
[0866] Одноцепочечные нуклеотиды ДНК можно ренатурировать друг с другом, чтобы получить двухцепочечный олигонуклеотид. Одноцепочечные нуклеотиды ДНК можно ренатурировать друг с другом в буфере для ренатурации олигонуклеотидов (например, содержащем Трис-HCl, ЭДТА и NaCl). Двухцепочечный олигонуклеотид может быть разбавлен до рабочей концентрации (например, концентрации, подходящей для лигирования в линеаризованную плазмиду). Разбавленный двухцепочечный олигонуклеотид может быть лигирован в линеаризованный вектор. Лигирование может быть выполнено в буфере для лигирования (например, содержащем Трис-HCl, MgCl2, АТФ) и с использованием лигазы (например, ДНК-лигазы Т4). Двухцепочечный олигонуклеотид может быть лигирован в линеаризованный вектор в области в пределах последовательности, кодирующей нуклеиновую кислоту, направленную против нуклеиновой кислоты. Другими словами, линеаризованный вектор можно линеаризовать в точке в пределах области, кодирующей нуклеиновую кислоту, направленную против нуклеиновой кислоты, в которой линеаризация позволяет получить липкие концы, которые комплементарны липким концам двухцепочечного олигонуклеотида. При лигировании двухцепочечного олигонуклеотида в вектор, он может обеспечить последовательность, кодирующую сконструированную нуклеиновую кислоту, направленную против нуклеиновой кислоты, содержащую последовательность спейсера, соответствующую двухцепочечной олигонуклеотидной последовательности.
[0867] Лигированный вектор может быть трансформирован в химически компетентные клетки (например, DH5-альфа, Тор 10), отобранные для экспрессии корректно лигированного вектора (например, путем скрининга на средах с антибиотиком). Отобранные трансформанты могут быть исследованы, чтобы определить у них наличие вставки с помощью секвенирования. Секвенирование может быть выполнено с использованием праймера для секвенирования, который может гибридизоваться с частью вектора.
[0868] Корректно лигированный вектор может быть получен (например, с помощью крупномасштабного выделения ДНК, максипрепарат) и очищен. Вектор, содержащий сайт-направленный полипептид, нуклеиновую кислоту, направленную против нуклеиновой кислоты, которая содержит двухцепочечные олигонуклеотиды ДНК, может быть введен (например, трансфецирован) в клеточную линию по выбору (например, линию клеток млекопитающего).
[0869] Несмотря на то, что в настоящей заявке были приведены и описаны предпочтительные варианты реализации настоящего изобретения, специалисты в данной области техники поймут, что такие варианты приведены исключительно в качестве примера. Для специалистов в данной области техники будут очевидны многочисленные вариации, изменения и замены, не отступающие от сущности настоящего изобретения. Следует понимать, что различные альтернативные варианты реализации настоящего изобретения, описанного в настоящей заявке, могут быть использованы при практической реализации настоящего изобретения. Предполагается, что нижеследующая формула изобретения определяет объем настоящего изобретения, и тем самым включает способы и структуры, и их эквиваленты, находящиеся в пределах объема формулы настоящего изобретения.
[00870] Примеры
[00871] ПРИМЕР 1: МОДИФИКАЦИЯ САЙТ-СПЕЦИФИЧЕСКОГО ПОЛИПЕПТИДА ДЛЯ ИЗМЕНЕНИЯ СПЕЦИФИЧНОСТИ РАМ
[00872] Согласно некоторым вариантам реализации в описании предложен модифицированный сайт-специфический полипептид, который модифицирован для изменения специфичности РАМ. Нуклеиновую кислоту, кодирующую модифицированный сайт-специфический полипептид, вводят в клетки путем трансфекции. Указанный модифицированный сайт-специфический полипептид содержит встроенный нуклеазный домен HNH или RuvC. Указанный модифицированный сайт-специфический полипептид содержит модифицированный высокоосновной участок. Нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, которая содержит спейсер, способный гибридизоваться с целевой нуклеиновой кислотой также вводят в клетки путем трансфекции. Указанный модифицированный сайт-специфический полипептид и указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, образуют комплекс. Нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, направляет указанный комплекс на целевую нуклеиновую кислоту. После гибридизации с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, указанная целевая нуклеиновая кислота расщепляется нуклеазными доменами сайт-специфического полипептида. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид связывается с целевой нуклеиновой кислотой с более низкой Kd.
[00873] Согласно некоторым вариантам реализации донорный полинуклеотид также вводят в клетки. В некоторых случаях донорный полинуклеотид, фрагмент донорного полинуклеотида, копию донорного полинуклеотида или фрагмент копии донорного полинуклеотида встраивают в расщепленную целевую нуклеиновую кислоту.
[00874] ПРИМЕР 2: МОДИФИКАЦИЯ САЙТ-СПЕЦИФИЧЕСКОГО ПОЛИПЕПТИДА ДЛЯ ИЗМЕНЕНИЯ СПЕЦИФИЧНОСТИ ЦЕЛЕВОЙ НУКЛЕИНОВОЙ КИСЛОТЫ
[00875] Согласно некоторым вариантам реализации в описании предложен модифицированный сайт-специфический полипептид, модифицированный для изменения специфичности целевой нуклеиновой кислоты. Модифицированный сайт-специфический полипептид вводят в клетки. Указанный модифицированный сайт-специфический полипептид содержит модификацию в высокоосновном участке и/или HNH-подобном домене. Нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, которая содержит спейсер, способный гибридизоваться с целевой нуклеиновой кислотой, также вводят в клетки. Указанный модифицированный сайт-специфический полипептид и указанная нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, образуют комплекс. Нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, направляет указанный комплекс на целевую нуклеиновую кислоту. После гибридизации с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, указанная целевая нуклеиновая кислота расщепляется сайт-специфическим полипептидом. Согласно некоторым вариантам реализации указанный модифицированный сайт-специфический полипептид связывается с целевой нуклеиновой кислотой с более низкой Kd.
[00876] Согласно некоторым вариантам реализации донорный полинуклеотид также вводят в клетки. В некоторых случаях донорный полинуклеотид, фрагмент донорного полинуклеотида, копию донорного полинуклеотида или фрагмент копии донорного полинуклеотида встраивают в расщепленную целевую нуклеиновую кислоту.
[00877] ПРИМЕР 3: РЕКОМБИНАНТНАЯ ЭКСПРЕССИЯ САЙТ-СПЕЦИФИЧЕСКОГО ПОЛИПЕПТИДА
[00878] Может быть собрана рекомбинантная последовательность ДНК, кодирующая модифицированный сайт-специфический полипептид и обеспечивающая экспрессию модифицированного сайт-специфического полипептида в организме-хозяине. Указанная рекомбинантная последовательность ДНК содержит промоторную последовательность, и может дополнительно содержать аффинную метку для очищения, или эпитопную метку. В неограничивающем примере плазмида содержит рекомбинантную последовательность ДНК для экспрессирования модифицированного сайт-специфического полипептида.
[00879] Получение рекомбинантного белка.
[00880] Плазмиду, кодирующую сайт-специфический модифицированный полипептид, вводят в бактериальные клетки (например, Е coli). Указанный полипептид экспрессируют в бактериальных клетках, а затем очищают от клеточного лизата с применением хроматографических способов. Активность модифицированного сайт-специфического полипептида измеряют с применением способов анализа, разработанных для определения специфичности модифицированного полипептида, последовательности РАМ, профиля специфичности сайт-специфического полипептида и предпочтительных нуклеиновых кислот (например, ДНК или РНК, или модифицированные нуклеиновые кислоты) для указанного полипептида.
[00881] Разрабатывают программное обеспечение для выбора сайтов, которые могут быть вырезаны с применением модифицированного сайт-специфического полипептида. Конструируют направляющие последовательности РНК для нацеливания активности сайт-специфического полипептида. После создания сайт-специфического полипептида его используют для расщепления нуклеиновых кислот.
[00882] Введение модифицированного сайт-специфического полипептида в клетки
[00883] Модифицированный пептид вводят в клетки в сайты целевой нуклеиновой кислоты. Полипептид, сохраняющий нуклеазную активность, используют для введения одноцепочечных или двуцепочечных разрывов ДНК в целевую ДНК. Полипептид, обладающий ДНК-связывающей, но не ДНК-расщепляющей активностью, используют для связывания двуцепочечной ДНК в клетке. Это может применяться для воздействия на активацию или подавление транскрипции.
[00884] ПРИМЕР 4: ВЫБОР САЙТОВ ДЛЯ МОДИФИКАЦИИ В ПОСЛЕДОВАТЕЛЬНОСТЯХ CAS9
[00885] Как было описано выше, системы типа II CRISPR, содержащие ортологи Cas9, могут быть разделены на три группы (тип II-A, тип II-B и тип II-C) на основании анализа локусов CRISPR-Cas. Ортологи Cas9 в указанных группах в общих чертах можно разделить на две клады, содержащие более короткие (тип Cas9/Csn1) и более длинные последовательности (тип Cas9/Csx12). Помимо указанных больших групп, могут присутствовать два дополнительных семейства гомологов, которые содержат домены HNH и RuvC, топологически расположенные аналогично Cas9, но значимо отличающиеся длиной и последовательностью вставок между консервативными элементами последовательностей. Для определения областей полипептида для модификации используют предсказание вторичной структуры и выравнивание последовательностей. Области, расположенные между элементами вторичной структуры элементы или между областями высококонсервативных последовательностей, выбирают в качестве кандидатов для встраивания или удаления. Области, обладающие сходством с доменами известной структуры, анализируют для идентификации конкретных областей для встраивания или удаления последовательностей.
[00886] На Фиг. 35 показано выравнивание последовательностей TIGR0185 с использованием CDD для небольшого числа различных ортологов Cas9. Аминокислоты с символом «X» под ними считаются одинаковыми. Аминокислоты с символом «Y» под ними могут считаться высококонсервативными или идентичными во всех последовательностях. Остатки аминокислот без символов «X» или «Y» не являются консервативными. Указанное выравнивание не включает С-концевую область (приблизительно соответствующую остаткам аминокислот 1100-1350) более длинных ортологов Cas9. Последовательности, представленные на Фиг. 35, приведены в таблице 6.

[00888] Локализации для встраивания новых функциональных доменов, областей для встраивания альтернативных последовательностей, или для удаления или уменьшения размера области, модифицирующего активность Cas9, могут включать, не ограничиваясь перечисленными, области, отмеченные в таблице 7. Нумерация основана на последовательности аминокислот Cas9 из Streptococcus pyogenes M1 GAS.

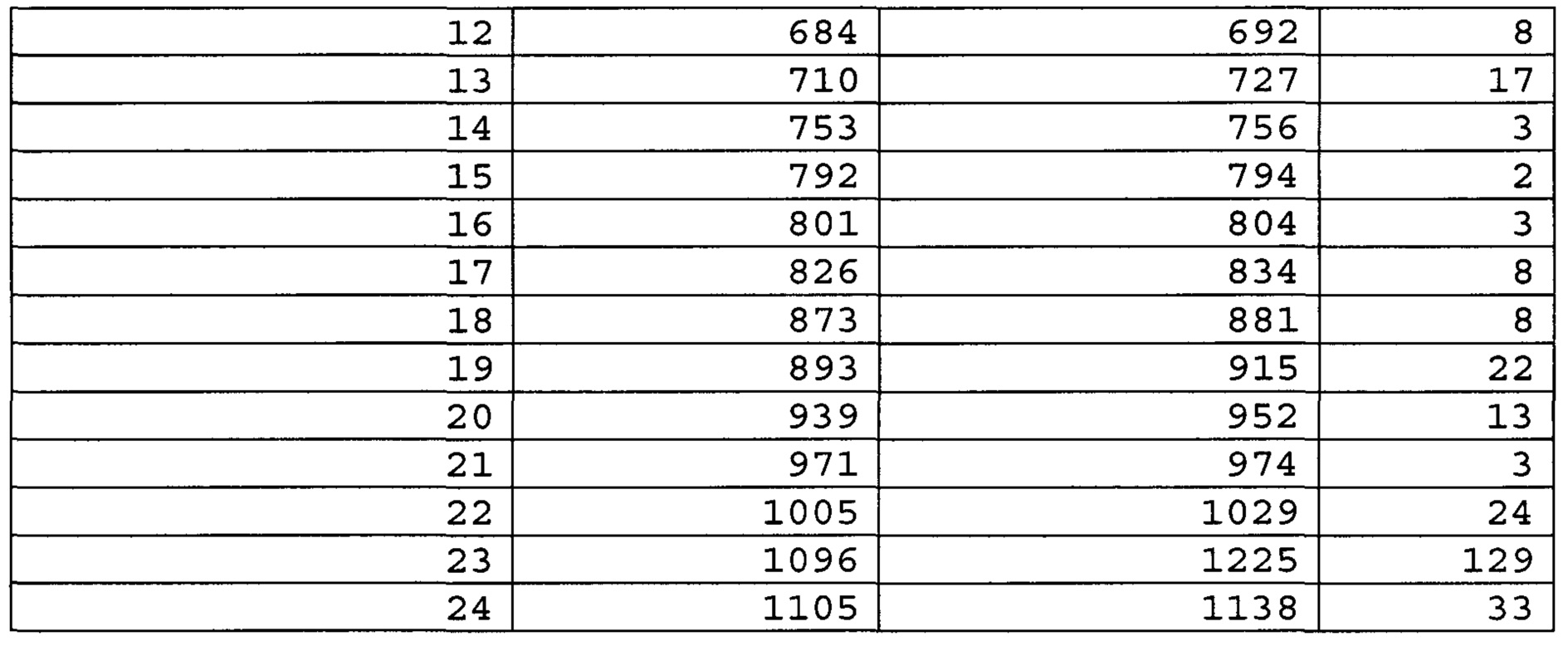
[00890] После идентификации потенциальной области для встраивания в белок новой полипептидной последовательности или удаления области указанного белка последовательность ДНК, кодирующую указанный белок, модифицируют с включением указанной модификации.
[00891] ПРИМЕР 5: ОБОГАЩЕНИЕ ПОСЛЕДОВАТЕЛЬНОСТЕЙ СВЯЗАННОЙ С САЙТ-СПЕЦИФИЧЕСКИМ ПОЛИПЕПТИДОМ ЦЕЛЕВОЙ НУКЛЕИНОВОЙ КИСЛОТЫ
[00892] В описании предложены способы обогащения последовательностей без амплификации с применением сайт-специфических полипептидов.
[00893] Согласно некоторым вариантам реализации указанный способ включает а) приведение целевой нуклеиновой кислоты в контакт с комплексом, содержащим нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и сайт-специфический полипептид, b) расщепление целевой нуклеиновой кислоты с) очищение указанной целевой нуклеиновой кислоты и d) секвенирование указанной целевой нуклеиновой кислоты, при этом целевая нуклеиновая кислота обогащена.
[00894] Согласно некоторым вариантам реализации указанный сайт-специфический полипептид ферментативно неактивен. Применение ферментативно неактивного сайт-специфического полипептида способствует связыванию целевой нуклеиновой кислоты с комплексом сайт-специфического полипептида. Согласно некоторым вариантам реализации указанный сайт-специфический полипептид ферментативно активен.
[00895] Согласно некоторым вариантам реализации обогащение последовательностей проводится вне клеток (например, в бесклеточном образце). Например, образец содержит очищенную геномную ДНК. Согласно некоторым вариантам реализации обогащение последовательностей проводится в клеточном образце (например, в клетках, клеточном лизате).
[00896] В некоторых случаях комплексы сайт-специфический полипептид-целевая нуклеиновая кислота связывают или перекрестно связывают для получения комплексов. В том случае, если указанный способ применяют для клеток, клетки лизируют. Выбирают условия лизиса, подходящие для сохранения интакных комплексов белков/ДНК.
[00897] Образец нуклеиновой кислоты обрабатывают для фрагментирования целевой нуклеиновой кислоты до аффинной очистки. Фрагментация может осуществляться с применением физических, механических или ферментативных способов. Физическая фрагментация включает термообработку целевого полинуклеотида или обработку целевого полинуклеотида ультрафиолетовым излучением (УФ). Механическое разрушение используют для механического расщепления целевого полинуклеотида на фрагменты в требуемом диапазоне. Механическое расщепление может проводиться с применением ряда способов, в том числе многократного пипетирования целевого полинуклеотида, воздействия ультразвуком и распыления. Целевые нуклеиновые кислоты также фрагментируют с применением ферментных методов. В некоторых случаях ферментативное расщепление проводится с применением ферментов, например, с применением рестрикционных ферментов. Рестрикционные ферменты используют для осуществления специфической или неспецифической фрагментации целевых полинуклеотидов. В указанных способах применяется один или большее количество типов рестрикционных ферментов, обычно описываемых как ферменты типа I, ферменты типа II и/или ферменты типа III. Ферменты типа II и типа III распознают конкретные последовательности нуклеотидов внутри двуцепочечной полинуклеотидной последовательности («последовательность распознавания», или «сайт распознавания»). После связывания и распознавания указанных последовательностей ферменты типа II и типа III расщепляют полинуклеотидную последовательность. В некоторых случаях расщепление приводит к образованию полинуклеотидного фрагмента с выступающим участком одноцепочечной нуклеиновой кислоты, называемым «липким концом». В других случаях расщепление не приводит к образованию фрагмента с выступающим участком, и формируется «тупой конец». В указанных способах могут использоваться рестрикционные ферменты, обеспечивающие получение липких концов или тупых концов.
[00898] После фрагментации указанные комплексы, содержащие сайт-специфический полипептид, очищают путем инкубирования на твердой подложке. Например, в том случае, если сайт-специфический полипептид содержит биотиновую метку, твердую подложку покрывают авидином или стрептавидином для связывания с биотиновой меткой.
[00899] Согласно альтернативному варианту реализации после фрагментации указанные комплексы, содержащие сайт-специфический полипептид, целевую нуклеиновую кислоту и/или нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, очищают путем инкубирования с агентом захвата. Указанный агент захвата связывается с аффинной меткой, соединенной с указанным сайт-специфическим полипептидом. Указанный агент захвата включает антитело. Например, в том случае, если аффинная метка, соединенная с сайт-специфическим полипептидом, представляет собой метку FLAG, указанный агент захвата представляет собой антитело против метки FLAG.
[00900] Согласно некоторым вариантам реализации указанный агент захвата очищают на твердой подложке. Например, в том случае, если агент захвата содержит биотиновую метку, твердую подложку покрывают авидином или стрептавидином для связывания биотинилированного агента захвата.
[00901] Согласно некоторым вариантам реализации нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит аффинную метку. Указанная аффинная метка содержит последовательность, способную связываться с эндорибонуклеазой. В некоторых случаях указанная аффинная метка содержит последовательность, способная связываться с условно ферментативно неактивной эндорибонуклеазой. Указанная условно ферментативно неактивная эндорибонуклеаза связывает, но не расщепляет указанную аффинную метку.
[00902] Согласно некоторым вариантам реализации эндорибонуклеаза и/или условно ферментативно неактивная эндорибонуклеаза содержит аффинную метку.
[00903] Указанную условно ферментативно неактивную эндорибонуклеазу очищают на твердой подложке. Указанная твердая подложка связывается с аффинной меткой условно ферментативно неактивной эндорибонуклеазы. Например, в том случае, если условно ферментативно неактивная эндорибонуклеаза содержит биотиновую метку, твердую подложку покрывают авидином или стрептавидином для связывания биотинилированного агента захвата.
[00904] Согласно некоторым вариантам реализации указанную условно ферментативно неактивную эндорибонуклеазу иммобилизуют на любой из разнообразных нерастворимых подложек.
[00905] Согласно некоторым вариантам реализации предложенного способа проводят два раунда очищения. В некоторых случаях первый раунд включает очищение на твердой подложке, которая связывается с аффинной меткой агента захвата, а второй раунд включает очищение на твердой подложке, которая связывается с аффинной меткой сайт-специфического полипептида. В некоторых случаях первый раунд включает очищение на твердой подложке, которая связывается с аффинной меткой сайт-специфического полипептида, а второй раунд включает очищение на твердой подложке, которая связывается с аффинной меткой агента захвата.
[00906] Согласно некоторым вариантам реализации способы предложенного в настоящем изобретении применяют для мультиплексного обогащения последовательностей. Согласно указанному варианту реализации в контакт с образцом нуклеиновой кислоты может приводиться совокупность нуклеиновых кислот, которые нацелены на нуклеиновые кислоты, при этом каждая нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, указанной совокупности сконструирована для нацеливания на отличную целевую нуклеиновую кислоту (например, последовательность в геноме) в образце нуклеиновой кислоты.
[00907] Захваченные комплексы содержат целевую нуклеиновую кислоту. Указанную целевую нуклеиновую кислоту элюируют из комплекса с сайт-специфическим полипептидом с применением стандартных способов, в том числе промывки высокосолевым раствором, осаждения этанолом, кипячением, очищением на геле и т.п.
[00908] Элюированную ДНК подготавливают для анализа секвенированием лигированием одного или большего количества адаптеров.
[00909] Библиотеки секвенирования секвенируют согласно описанию в настоящем документе. Секвенированную библиотеку анализируют для идентификации полиморфизмов, диагностики заболевания, определения курса лечения заболевания и/или получения библиотек антител.
[00910] ПРИМЕР 6: ОБОГАЩЕНИЕ ПОСЛЕДОВАТЕЛЬНОСТЕЙ ЦЕЛЕВОЙ НУКЛЕИНОВОЙ КИСЛОТЫ, НЕ СВЯЗАННОЙ С КОМПЛЕКСОМ, СОДЕРЖАЩИМ САЙТ-СПЕЦИФИЧЕСКИЙ ПОЛИПЕПТИД
[00911] Согласно некоторым вариантам реализации проводят обогащение последовательностей с применением ферментативно активного сайт-специфического полипептида. В некоторых случаях указанный сайт-специфический полипептид ферментативно активен. В указанном случае целевая нуклеиновая кислота не связывается с сайт-специфическим полипептидом, а вырезается.
[00912] Идентифицируют целевую нуклеиновую кислоту, и конструируют нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, для направления сайт-специфического полипептида к последовательностям, фланкирующим указанную целевую нуклеиновую кислоту. Образец инкубируют с комплексом, содержащим сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и сайт-специфический полипептид, таким образом, что сайт-специфический полипептид расщепляет ДНК на обоих концах целевой нуклеиновой кислоты. После расщепления целевой нуклеиновой кислоты указанная целевая нуклеиновая кислота отщепляется от исходной нуклеиновой кислоты. Расщепленную целевую нуклеиновую кислоту очищают (например, путем гель-электрофореза, селективного элюирования с гранул по размеру, или применения других карбоксилат-дериватизированных гранул, или осаждением с использованием подходящих концентраций соли и ПЭГ для преимущественного осаждения ДНК большего или меньшего размера).
[00913] Согласно некоторым вариантам реализации обогащение последовательностей проводится вне клеток (например, в бесклеточном образце). Например, образец содержит очищенную геномную ДНК. Согласно некоторым вариантам реализации обогащение последовательностей проводится в клеточном образце (например, в клетках, клеточном лизате).
[00914] В том случае, если указанный способ применяют для клеток, клетки лизируют. Выбирают условия лизиса, подходящие для сохранения интакных комплексов белков/ДНК.
[00915] Согласно некоторым вариантам реализации целевая нуклеиновая кислота для секвенирования не связывается с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, и/или сайт-специфическим полипептидом. Согласно указанному варианту реализации нуклеиновую кислоту, связанную с сайт-специфическим полипептидом и/или нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, очищают. Очищение сайт-специфического полипептида проводят согласно приведенному выше в настоящем документе описанию. Вкратце, комплексы, содержащие сайт-специфический полипептид, очищают путем инкубирования на твердой подложке. Например, в том случае, если сайт-специфический полипептид содержит биотиновую метку, твердую подложку покрывают авидином или стрептавидином для связывания с биотиновой меткой.
[00916] Согласно альтернативному варианту реализации после фрагментации указанные комплексы, содержащие сайт-специфический полипептид, нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и нецелевую нуклеиновую кислоту очищают путем инкубирования с агентом захвата. Указанный агент захвата связывается с аффинной меткой, соединенной с указанным сайт-специфическим полипептидом. Указанный агент захвата включает антитело. Например, в том случае, если аффинная метка, соединенная с сайт-специфическим полипептидом, представляет собой метку FLAG, указанный агент захвата представляет собой антитело против метки FLAG.
[00917] Агент захвата очищают на твердой подложке. Например, в том случае, если указанный агент захвата содержит биотиновую метку, твердую подложку покрывают авидином или стрептавидином для связывания биотинилированного агента захвата.
[00918] Согласно некоторым вариантам реализации предложенные в настоящем изобретении способы используют для мультиплексного обогащения последовательностей. Согласно указанному варианту реализации в клетку может вводиться совокупность нуклеиновых кислот, которые нацелены на нуклеиновые кислоты, при этом каждая нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, указанной совокупности сконструирована для нацеливания на отличную целевую нуклеиновую кислоту (например, последовательность в геноме).
[00919] Захваченный комплекс не содержит целевой нуклеиновой кислоты.
[00920] Целевая нуклеиновая кислота включает нуклеиновую кислоту, не связанную с указанными комплексами, содержащими сайт-специфический полипептид. Целевая нуклеиновая кислота может быть собрана с применением стандартных методов очищения нуклеиновых кислот (например, с применением коммерчески доступного набора для очистки продуктов ПЦР, агарозного геля).
[00921] Собранную целевую нуклеиновую кислоту подготавливают для анализа секвенированием (например, глубоким секвенированием), лигируя один или большее количество адаптеров согласно описанию в настоящем документе.
[00922] Секвенированную целевую нуклеиновую кислоту анализируют для идентификации полиморфизмов, диагностики заболевания, определения курса лечения заболевания и/или получения библиотек антител.
[00923] ПРИМЕР 7: СЕКВЕНИРОВАНИЕ
[00924] Элюированные целевые нуклеиновые кислоты подготавливают для анализа секвенированием. Подготовка для анализа секвенированием включает получение библиотек секвенирования элюированной целевой нуклеиновой кислоты. Анализ секвенированием позволяет идентифицировать нецелевые сайты связывания и определить их частоту в сайт-специфических полипептидах.
[00925] Определение последовательностей проводится с применением способов, определяющих множество (как правило, от тысяч до миллиардов) последовательностей нуклеиновых кислот по существу параллельно, при этом указанное множество считывают предпочтительно параллельно с применением последовательного процесса с высокой пропускной способностью. Такие способы может включать, не ограничиваясь перечисленными, пиросеквенирование (например, коммерциализированное 454 Life Sciences, Inc., Брэнфорд, Коннектикут); секвенирование лигированием (например, коммерциализированное в виде технологии SOLiD™, Life Technology, Inc., Карлсбад, Калифорния); секвенирование синтезом с применением модифицированных нуклеотидов (например, коммерциализированное в виде технологий TruSeq™ и HiSeq™ от Illumina, Inc., Сан-Диего, Калифорния, HeliScope™ от Helicos Biosciences Corporation, Кембридж, Массачусетс, и PacBio RS от Pacific Biosciences of California, Inc., Менло-Парк, Калифорния), секвенирование с применением технологий детекции ионов (Ion Torrent, Inc., Южный Сан-Франциско, Калифорния); секвенирование «наношариков» с ДНК (Complete Genomics, Inc., Маунтин-Вью, Калифорния); технологии секвенирования на основе нанопор (например, разрабатываемых Oxford Nanopore Technologies, LTD, Оксфорд, Великобритания), капиллярное секвенирование (например, коммерциализированное в MegaBACE от Molecular Dynamics), электронное секвенирование, одномолекулярное секвенирование (например, коммерциализированное в виде технологии SMRT™ от Pacific Biosciences, Менло-Парк, Калифорния), капельное микрофлюидное секвенирование, секвенирование гибридизацией (например, коммерциализированное Affymetrix, Санта-Клара, Калифорния), бисульфитное секвенирование и другие известные способы высокопараллельного секвенирования.
[00926] Согласно некоторым вариантам реализации секвенирование проводится путем анализа на микрочипах.
[00927] ПРИМЕР 8: ПОЛУЧЕНИЕ БИБЛИОТЕК АНТИТЕЛ
[00928] Раскрытые в настоящем документе способы используют для получения библиотеки белков (например, библиотек антител). Библиотеки белков подходят для получения экспрессионных библиотек, используемых для скрининга белков (например, антител) для применения в терапевтиках, реагентах и/или при диагностике. Библиотеки белков подходят также для синтеза и/или клонирования дополнительных антител.
[00929] Библиотеки белков получают путем конструирования нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, гибридизующейся с целевыми последовательностями нуклеиновых кислот, кодирующих иммуноглобулины. Указанные комплексы, содержащие сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, очищают с применением описанных в настоящем документе способов. Согласно некоторым вариантам реализации нуклеиновая кислота, гибридизующаяся с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, представляет собой целевую нуклеиновую кислоту, которую элюируют и секвенируют с применением способов, описанных в настоящем документе. Согласно некоторым вариантам реализации нуклеиновая кислота, гибридизующаяся с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, не представляет собой целевую нуклеиновую кислоту. Целевая нуклеиновая кислота представляет собой нуклеиновую кислоту, вырезаемую между сайтами расщепления совокупности комплексов (например, комплексов, содержащих сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту). Указанную вырезанную целевую нуклеиновую кислоту очищают и секвенируют с применением способов, описанных в настоящем документе.
[00930] ПРИМЕР 9: ГЕНОТИПИРОВАНИЕ
[00931] Раскрытые в настоящем документе способы используют для проведения типирования человеческого лейкоцитарного антигена (HLA). Гены HLA являются одними из самых полиморфных генов в организме человека. Понимание генотипов указанных областей имеет важное значение для обеспечения хорошей совместимости трансплантатов тканей и органов.
[00932] Для проведения типирования HLA сконструируют нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, для гибридизации с последовательностями целевой нуклеиновой кислоты в генах HLA. Комплексы, содержащие сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, очищают с применением способов, описанных в настоящем документе. Согласно некоторым вариантам реализации нуклеиновая кислота, гибридизующаяся с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, представляет собой целевую нуклеиновую кислоту, которую элюируют и секвенируют с применением способов, описанных в настоящем документе. Согласно некоторым вариантам реализации нуклеиновая кислота, гибридизующаяся с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, не представляет собой целевую нуклеиновую кислоту. Целевая нуклеиновая кислота представляет собой нуклеиновую кислоту, вырезаемую между сайтами расщепления совокупности комплексов (например, комплексов, содержащих сайт-специфический полипептид и нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту). Указанную вырезанную целевую нуклеиновую кислоту очищают и секвенируют с применением способов, описанных в настоящем документе.
[00933] ПРИМЕР 10: ИММУНОПРЕЦИПИТАЦИЯ САЙТ-СПЕЦИФИЧЕСКОГО ПОЛИПЕПТИДА
[00934] В описании предложены способы нуклеазной иммунопреципитации и секвенирования (NIP-Seq). Согласно некоторым вариантам реализации указанный способ включает а) приведение образца нуклеиновой кислоты в контакт с ферментативно неактивным сайт-специфическим полипептидом, при этом указанный ферментативно неактивный сайт-специфический полипептид связывает целевую нуклеиновую кислоту с образованием таким образом комплекса, b) захват указанного комплекса агентом захвата и с) секвенирование целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный способ дополнительно включает d) идентификацию нецелевого сайта связывания.
[00935] Согласно некоторым вариантам реализации предложенные в настоящем изобретении способы реализуют вне клеток. Например, образец содержит очищенную геномную ДНК.
[00936] Комплексы сайт-специфического полипептида с целевой нуклеиновой кислотой связывают или перекрестно связывают для получения комплексов.
[00937] Нуклеиновую кислоту (например, геномную ДНК) обрабатывают для фрагментирования ДНК до аффинной очистки. Фрагментация может осуществляться с применением физических, механических или ферментативных способов. Физическая фрагментация может включать термообработку целевого полинуклеотида или обработку ультрафиолетовым излучением (УФ). Механическое разрушение могут применяться для механического расщепления целевого полинуклеотида на фрагменты в требуемом диапазоне. Механическое расщепление может проводиться с применением ряда способов, известных в данной области техники, в том числе многократного пипетирования целевого полинуклеотида, воздействия ультразвуком и распыления. Целевые полинуклеотиды могут быть также фрагментированы с применением ферментных методов. В некоторых случаях ферментативное расщепление может осуществляться с применением ферментов, например, с применением рестрикционных ферментов. Рестрикционные ферменты могут применяться для осуществления специфической или неспецифической фрагментации целевых полинуклеотидов. В указанных способах может применяться один или большее количество типов рестрикционных ферментов, обычно описываемых как ферменты типа I, ферменты типа II и/или ферменты типа III. Ферменты типа II и типа III, как правило, коммерчески доступны и хорошо известны в данной области техники. Ферменты типа II и типа III распознают конкретные последовательности нуклеотидов внутри двуцепочечной полинуклеотидной последовательности («последовательность распознавания», или «сайт распознавания»). После связывания и распознавания указанных последовательностей ферменты типа II и типа III расщепляют полинуклеотидную последовательность. В некоторых случаях расщепление приводит к образованию полинуклеотидного фрагмента с выступающим участком одноцепочечной ДНК, называемым «липким концом». В других случаях расщепление не приводит к образованию фрагмента с выступающим участком, и формируется «тупой конец». В указанных способах могут использоваться рестрикционные ферменты, обеспечивающие получение липких концов или тупых концов.
[00938] После фрагментации комплексы, содержащие сайт-специфический полипептид, очищают путем инкубирования на твердой подложке. Например, в том случае, если сайт-специфический полипептид содержит биотиновую метку, твердую подложку покрывают авидином или стрептавидином для связывания с биотиновой меткой.
[00939] Согласно альтернативному варианту реализации после фрагментации комплексы, содержащие сайт-специфический полипептид, целевую нуклеиновую кислоту и/или нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, очищают путем инкубирования с агентом захвата. Указанный агент захвата связывается с аффинной меткой, соединенной с сайт-специфическим полипептидом. Указанный агент захвата включает антитело. Например, в том случае, если аффинная метка, соединенная с сайт-специфическим полипептидом, представляет собой метку FLAG, агент захвата представляет собой антитело против метки FLAG.
[00940] Агент захвата очищают на твердой подложке. Например, в том случае, если указанный агент захвата содержит биотиновую метку, гранулу покрывают авидином или стрептавидином для связывания биотинилированного агента захвата.
[00941] Согласно некоторым вариантам реализации предложенного способа проводится два или большее количество раундов очищения. Первый раунд включает очищение на твердой подложке, способной связываться с аффинной меткой агента захвата, а второй раунд включает очищение на твердой подложке, способной связываться с аффинной меткой сайт-специфического полипептида. Первый раунд включает очищение на твердой подложке, которая связывается с аффинной меткой сайт-специфического полипептида, а второй раунд включает очищение на твердой подложке, которая связывается с аффинной меткой агента захвата.
[00942] Согласно некоторым вариантам реализации указанный способ используют для оптимизации специфичности связывания сайт-специфического полипептида, реализуя указанный способ более одного раза.
[00943] Захваченный комплекс содержит сайт-специфический полипептид и целевую нуклеиновую кислоту. Указанную целевую нуклеиновую кислоту элюируют из комплекса с сайт-специфическим полипептидом с применением стандартных способов, в том числе промывки высокосолевым раствором, осаждения этанолом, кипячением, очищением на геле и т.п.
[00944] Элюированную ДНК подготавливают для анализа секвенированием с применением стандартных способов. Указанные библиотеки секвенирования секвенируют и анализируют для идентификации последовательности и частоты сайтов связывания нуклеаз.
[00945] Согласно некоторым вариантам реализации указанный способ реализуется многократно. Согласно некоторым вариантам реализации указанный способ дополнительно включает сбор данных и хранение данных. Указанные данные могут собираться и храниться на компьютерном сервере.
[00946] ПРИМЕР 11: ИММУНОПРЕЦИПИТАЦИЯ САЙТ-СПЕЦИФИЧЕСКОГО ПОЛИПЕПТИДА IN VIVO
[00947] Согласно некоторым вариантам реализации указанный способ включает: а) введение ферментативно неактивного сайт-специфического полипептида в клетку, при этом указанный ферментативно неактивный сайт-специфический полипептид связывает целевую нуклеиновую кислоту с образованием таким образом комплекса, b) захват указанного комплекса агентом захвата и с) секвенирование указанной целевой нуклеиновой кислоты. Согласно некоторым вариантам реализации указанный способ дополнительно включает d) идентификацию нецелевого сайта связывания.
[00948] В некоторых случаях указанный сайт-специфический полипептид содержит аффинную метку. Полипептиды, содержащие аффинную метку, были описаны в настоящей документе.
[00949] Клетки связывают или перекрестие связывают. Связанные и/или перекрестно связанные клетки лизируют. Выбирают условия лизиса, подходящие для сохранения интакных комплексов белков/ДНК. Лизат обрабатывают для фрагментирования ДНК до аффинной очистки. Подходящие техники фрагментации описаны в настоящем документе.
[00950] После фрагментации указанные комплексы, содержащие сайт-специфический полипептид, целевую нуклеиновую кислоту и/или нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, очищают от лизата путем инкубирования на твердой подложке. Например, в том случае, если сайт-специфический полипептид содержит биотиновую метку, твердую подложку покрывают авидином или стрептавидином для связывания с биотиновой меткой.
[00951] Согласно альтернативному варианту реализации после фрагментации указанные комплексы, содержащие сайт-специфический полипептид, очищают от лизата путем инкубирования с агентом захвата. Указанный агент захвата связывается с аффинной меткой, соединенной с указанным сайт-специфическим полипептидом. Указанный агент захвата включает антитело. Например, в том случае, если аффинная метка, соединенная с сайт-специфическим полипептидом, представляет собой метку FLAG, указанный агент захвата представляет собой антитело к метке FLAG.
[00952] Согласно некоторым вариантам реализации указанный агент захвата содержит аффинную метку. Указанный агент захвата очищают на твердой подложке. Указанная твердая подложка связывается с аффинной меткой агента захвата. Например, в том случае, если агент захвата содержит биотиновую метку, гранулу покрывают авидином или стрептавидином для связывания биотинилированного агента захвата.
[00953] Согласно некоторым вариантам реализации предложенного способа проводится два раунда очищения. В некоторых случаях первый раунд включает очищение на твердой подложке, которая связывается с аффинной меткой агента захвата, а второй раунд включает очищение на твердой подложке, которая связывается с аффинной меткой сайт-специфического полипептида. В некоторых случаях первый раунд включает очищение на твердой подложке, которая связывается с аффинной меткой сайт-специфического полипептида, а второй раунд включает очищение на твердой подложке, которая связывается с аффинной меткой агента захвата.
[00954] Согласно некоторым вариантам реализации указанный способ используют для оптимизации специфичности связывания сайт-специфического полипептида, реализуя указанный способ более одного раза.
[00955] Захваченный комплекс содержит сайт-специфический полипептид и целевую нуклеиновую кислоту. Указанную целевую нуклеиновую кислоту элюируют из комплекса с сайт-специфическим полипептидом с применением стандартных способов, в том числе промывки высокосолевым раствором, осаждения этанолом, кипячением, очищением на геле и т.п.
[00956] Элюированную ДНК подготавливают для анализа секвенированием. Из элюированной целевой нуклеиновой кислоты получают библиотеки секвенирования. Указанные библиотеки секвенирования секвенируют и анализируют для идентификации последовательности и частоты сайтов связывания нуклеаз.
[00957] ПРИМЕР 12: ИММУНОПРЕЦИПИТАЦИЯ С ФЕРМЕНТАТИВНО НЕАКТИВНЫМ ЭНДОРИБОНУКЛЕАЗНЫМ АГЕНТОМ ЗАХВАТА
[00958] Способ идентификации нецелевого сайта связывания нуклеазы включает: а) приведение образца нуклеиновой кислоты в контакт с ферментативно неактивным сайт-специфическим полипептидом и нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, при этом указанный ферментативно неактивный сайт-специфический полипептид и нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, связывают целевую нуклеиновую кислоту, с образованием таким образом комплекса, b) захват указанного комплекса агентом захвата, при этом указанный агент захвата содержит условно ферментативно неактивный сайт-специфический полипептид, с) секвенирование целевой нуклеиновой кислоты и d) идентификацию нецелевого сайта связывания. Указанный способ подходит для применения на бесклеточном образце нуклеиновой кислоты и/или образце нуклеиновой кислоты, происходящем из клетки.
[00959] Комплексы сайт-специфического полипептида и целевой нуклеиновой кислоты связывают или перекрестно связывают для получения комплексов.
[00960] В том случае, если образец нуклеиновой кислоты происходит из клеток, указанные связанные и/или перекрестно связанные комплексы лизируют. Условия лизиса могут быть выбраны таким образом, чтобы обеспечить сохранение интактных комплексов белков/ДНК. Лизат обрабатывают для фрагментирования ДНК до аффинной очистки. В том случае, если образец нуклеиновой кислоты происходит из бесклеточного образца, обрабатывают бесклеточную нуклеиновую кислоту для фрагментирования ДНК. Подходящие техники фрагментации описаны в настоящем документе.
[00961] Согласно некоторым вариантам реализации нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, содержит аффинную метку. Указанная аффинная метка содержит последовательность, способную связываться с условно ферментативно неактивным сайт-специфическим полипептидом. В некоторых случаях указанная аффинная метка содержит последовательность, способная связываться с условно ферментативно неактивной эндорибонуклеазой. В некоторых случаях указанная аффинная метка содержит последовательность, способную связываться с условно ферментативно неактивным белком Csy4. Указанный условно ферментативно неактивный сайт-специфический полипептид связывает, но не расщепляет указанную аффинную метку. Указанная аффинная метка содержит нуклеотидную последовательность 5'-GUUCACUGCCGUAUAGGCAGCUAAGAAA-3'. Указанную аффинную метку вводят в нуклеиновую кислоту с применением стандартных рекомбинантных способов.
[00962] После фрагментации указанные комплексы, содержащие сайт-специфический полипептид, целевую нуклеиновую кислоту и/или нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, очищают путем инкубирования с условно ферментативно неактивным сайт-специфическим полипептидом (например, вариантом Csy4).
[00963] Согласно некоторым вариантам реализации указанный условно ферментативно неактивный сайт-специфический полипептид содержит аффинную метку.
[00964] Указанный условно ферментативно неактивный сайт-специфический полипептид очищают на твердой подложке. Твердая подложка связывается с аффинной меткой указанного условно ферментативно неактивного сайт-специфического полипептида. Например, в том случае, если условно ферментативно неактивный сайт-специфический полипептид содержит биотиновую метку, гранулу покрывают авидином или стрептавидином для связывания биотинилированного агента захвата.
[00965] Согласно некоторым вариантам реализации указанный ферментативно неактивный сайт-специфический полипептид иммобилизуют на любой из разнообразных нерастворимых подложек.
[00966] Согласно некоторым вариантам реализации предложенного способа проводят два раунда очищения. В некоторых случаях первый раунд включает очищение на твердой подложке, которая связывается с аффинной меткой указанного условно ферментативно неактивного сайт-специфического полипептида (например, варианта Csy4), а второй раунд включает очищение на твердой подложке, которая связывается с аффинной меткой сайт-специфического полипептида. В некоторых случаях первый раунд включает очищение на твердой подложке, которая связывается с аффинной меткой сайт-специфического полипептида, а второй раунд включает очищение на твердой подложке, которая связывается с аффинной меткой указанного ферментативно неактивного сайт-специфического полипептида (например, варианта Csy4).
[00967] Согласно некоторым вариантам реализации указанный способ используют для оптимизации специфичности связывания сайт-специфического полипептида, реализуя указанный способ более одного раза.
[00968] Захваченный комплекс содержит сайт-специфический полипептид и целевую нуклеиновую кислоту. Указанную целевую нуклеиновую кислоту элюируют из комплекса с сайт-специфическим полипептидом с применением стандартных способов, в том числе промывки высокосолевым раствором, осаждения этанолом, кипячением, очищением на геле и т.п.
[00969] Элюированную ДНК подготавливают для анализа секвенированием. Библиотеки секвенирования секвенируют и анализируют для идентификации последовательности и частоты сайтов связывания нуклеаз.
[00970] ПРИМЕР 13: СЕКВЕНИРОВАНИЕ
[00971] Элюированные целевые нуклеиновые кислоты подготавливают для анализа секвенированием. Подготовка для анализа секвенированием включает получение библиотек секвенирования элюированной целевой нуклеиновой кислоты. Анализ секвенированием позволяет идентифицировать нецелевые сайты связывания и определить их частоту в сайт-специфических полипептидах.
[00972] Определение последовательностей также проводится с применением способов для определения множества (как правило, от тысяч до миллиардов) последовательностей нуклеиновых кислот по существу параллельно, при этом указанное множество последовательностей считываются предпочтительно параллельно с использованием последовательного процесса с высокой пропускной способностью. Такие способы включают, не ограничиваясь перечисленными, пиросеквенирование (например, коммерциализированное 454 Life Sciences, Inc., Брэнфорд, Коннектикут); секвенирование лигированием (например, коммерциализированное в виде технологии SOLiD™, Life Technology, Inc., Карлсбад, Калифорния); секвенирование синтезом с применением модифицированных нуклеотидов (например, коммерциализированное в виде технологий TruSeq™ и HiSeq™ от Illumina, Inc., Сан-Диего, Калифорния, HeliScope™ от Helicos Biosciences Corporation, Кембридж, Массачусетс, и PacBio RS от Pacific Biosciences of California, Inc., Менло-Парк, Калифорния), секвенирование с применением технологий детекции ионов (Ion Torrent, Inc., Южный Сан-Франциско, Калифорния); секвенирование «наношариков» с ДНК (Complete Genomics, Inc., Маунтин-Вью, Калифорния); технологий секвенирования на основе нанопор (например, разрабатываемых Oxford Nanopore Technologies, LTD, Оксфорд, Великобритания) и других известных способов высокопараллельного секвенирования.
[00973] ПРИМЕР 14: Модификация целевой нуклеиновой кислоты эффекторным белком
[00974] В клетку вводят вектор, содержащий сайт-специфический полипептид, нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и/или эффекторный белок. Внутри клетки образуется комплекс, содержащий элементы, кодируемые вектором. Нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, модифицируют связывающей белок Csy4 последовательностью. Эффекторный белок, Csy4, связывается с указанной модифицированной нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту. Csy4 содержит ненативную последовательность (например, гибридную), модифицирующую целевую нуклеиновую кислоту. Указанная ненативная последовательность представляет собой последовательность, которая модифицирует транскрипцию целевой нуклеиновой кислоты. Указанная ненативная последовательность представляет собой транскрипционный фактор. Указанный транскрипционный фактор повышает уровень транскрипции целевой нуклеиновой кислоты. В некоторых случаях указанная ненативная последовательность представляет собой метилазу. Метилаза обуславливает увеличение метилирования целевой нуклеиновой кислоты. В некоторых случаях указанная ненативная последовательность представляет собой деметилаза. Деметилаза обуславливает уменьшение метилирования целевой нуклеиновой кислоты. В некоторых случаях указанная ненативная последовательность представляет собой пептид, осуществляющий рекрутинг Rad51. Пептид, осуществляющий рекрутинг Rad51, увеличивает уровень гомологичной рекомбинации в целевом сайте. В некоторых случаях указанная ненативная последовательность представляет собой пептид, осуществляющий рекрутинг BCRA-2. Пептид, осуществляющий рекрутинг BRCA-2, увеличивает уровень гомологичной рекомбинации в целевом сайте.
[00975] ПРИМЕР 15: Применение сайт-специфического полипептида в качестве биосенсора явления генетической мобильности
[00976] Вектор(ы), содержащий(ие) сайт-специфический полипептид, нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и/или Эффекторный белок вводят в клетку. Сайт-специфический полипептид и эффекторные белки соединяют с последовательностями клеточной локализации (например, сигналом ядерной локализации). Внутри клетки образуется комплекс, содержащий элементы, кодируемые указанным(и) вектором(ами). В некоторых случаях в клетку вводят два вектора. Указанный(ые) вектор(ы) кодирует(ют) первый Эффекторный белок (Csy4), который содержит первый неактивный фрагмент разделенного зеленого флуоресцентного белка (GFP) и связывается с первой нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, и второй Эффекторный белок (Csy4, Cas5 или Cas6), который содержит второй неактивный фрагмент разделенного GFP и связывается с второй нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту. Первая нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, модифицирована связывающей первый белок Csy4, Cas5 или Cas6 последовательностью, которая может быть связана первым белком Csy4, Cas5 или Cas6. Вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, модифицируют второй связывающей белок Csy4, Cas5 или Cas6 последовательностью, которая может быть связана вторым белком Csy4, Cas5 или Cas6. Согласно некоторым вариантам реализации указанный первый белок Csy4, Cas5 или Cas6 взаимодействует со связывающей первый белок Csy4, Cas5 или Cas6 последовательностью, и указанный второй белок Csy4, Cas5 или Cas6 взаимодействует с второй связывающей белок Csy4, Cas5 или Cas6 последовательностью. Когда указанные первая и вторая нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, направляют сайт-специфический полипептид для связывания с двумя последовательностями, располагающимися поблизости, первый эффекторный белок и второй эффекторный белок приводят первый неактивный фрагмент разделенного GFP в контакт с вторым неактивным фрагментом разделенного GFP с получением активного GFP. Нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, указанного комплекса сконструированы таким образом, что одна нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, направляет указанный комплекс, например, в область внутри или возле гена Bcr, а другая нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, направляет указанный комплекс, например, в область внутри или возле гена Abl. В том случае, если транслокация не произошла, ген Bcr находится на хромосоме 22, а ген Abl находится на хромосоме 9, и последовательности целевой нуклеиновой кислоты располагаются достаточно далеко друг от друга, так что два неактивных фрагмента комбинированной GFP-системы неспособны взаимодействовать; таким образом, сигнал не формируется. В том случае, если транслокация произошла, ген Bcr и ген Abl транслоцируются таким образом, что указанные гены сближаются. В этом случае последовательности целевой нуклеиновой кислоты находятся достаточно близко друг к другу, чтобы указанные два неактивных фрагмента комбинированной GFP-системы сближались с формированием активного GFP. GFP-сигнал может быть детектирован с помощью флуориметра. Указанный сигнал указывает на конкретный генотип, образовавшийся в результате явления генетической мобильности.
[00977] ПРИМЕР 16: Применение сайт-специфического полипептида в качестве биосенсора генетической мутации
[00978] Система, описанная в примере 2, может также использоваться для детекции присутствия конкретной мутации в клетке. В указанном примере выбирают первую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, для нацеливания сайт-специфического полинуклеотида на нативную последовательность, расположенную возле сайта мутации. Вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, выбирают таким образом, чтобы она распознавала мутантную последовательность (например, мутантную последовательность, идентифицируемую путем секвенирования ДНК). Указанную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, выбирают таким образом, чтобы указанная мутантная последовательность располагалась в пределах первых 12 нуклеиновых кислот непосредственно 5' от последовательности РАМ в указанном сайте. В этом случае последовательности целевой нуклеиновой кислоты находятся достаточно близко друг к другу, чтобы указанные два неактивных фрагмента комбинированной GFP-системы сближались с формированием активного GFP. GFP-сигнал может быть детектирован с помощью флуориметра. Этот сигнал указывает на конкретный генотип.
[00979] ПРИМЕР 17: Применение сайт-специфического полипептида в качестве терапевтического средства при заболеваниях, включающих явление генетической мобильности
[00980] В клетку также вводят вектор(ы), содержащий(ие) сайт-специфический полипептид, нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и/или эффекторный белок, нуклеиновую кислоту, содержащую индуцирующий лизис клеток пептид (например, аденовирусный белок смерти), функционально связанную с первым промотором. Внутри клетки образуется комплекс, содержащий элементы, кодируемые указанным(и) вектором(ами). В некоторых случаях в клетку вводят два вектора. Указанный(ые) вектор(ы) кодирует(ют) первый эффекторный белок (содержащий первую последовательность белка Csy4, Cas5 или Cas6), который связывается с первой нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, и содержит активирующий домен для первого транскрипционного фактора, который связывается с первым промотором, и второй эффекторный белок (содержащий вторую последовательность Csy4, Cas5 или Cas6), который связывается с второй нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, и содержит ДНК-связывающий домен для первого транскрипционного фактора. Первая нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, модифицирована первой связывающей белок Csy4, Cas5 или Cas6 последовательностью, которая может быть связана первой последовательностью белка Csy4, Cas5 или Cas6. Вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, модифицируют второй связывающей белок Csy4, Cas5 или Cas6 последовательностью, которая может быть связана вторым белком Csy4, Cas5 или Cas6. Согласно некоторым вариантам реализации указанный первый белок Csy4, Cas5 или Cas6 взаимодействует преимущественно с первой связывающей белок Csy4, Cas5 или Cas6 последовательностью, а указанный второй белок Csy4, Cas5 или Cas6 взаимодействует преимущественно с второй связывающей белок Csy4, Cas5 или Cas6 последовательностью. В том случае, когда пораженная заболеванием клетка содержит геном, включающий явление генетической мобильности, если указанные первая и вторая нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, направляют сайт-специфический полипептид для связывания с двумя последовательностями, которые находятся поблизости, первый эффекторный белок и второй эффекторный белок приводят указанные активирующий домен и указанный ДНК-связывающий домен первого транскрипционного фактора в непосредственную близость. Указанный ДНК-связывающий домен первого транскрипционного фактора может связываться с первым промотором, функционально связанным с индуцирующим лизис клеток пептидом, и проксимальный активирующий домен индуцирует транскрипцию РНК, кодирующей индуцирующий лизис клеток пептид. В клетке, не пораженной заболеванием, не включающей явление генетической мобильности, ДНК-связывающий домен и активирующие домены первого транскрипционного фактора не будут приведены в непосредственную близость, и не будет происходить транскрипция индуцирующего лизис клеток пептида.
[00981] Нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, указанного комплекса сконструированы таким образом, что одна нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, направляет указанный комплекс, например, в область внутри или возле гена Bcr, а другая нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, направляет указанный комплекс, например, в область внутри или возле гена Abl. В клетке, не пораженной заболеванием, транслокация не произошла, ген Bcr находится на хромосоме 22, а ген Abl находится на хромосоме 9, и последовательности целевой нуклеиновой кислоты располагаются достаточно далеко друг от друга, так что два неактивных фрагмента системы транскрипционных факторов не способны взаимодействовать и не могут индуцировать транскрипцию индуцирующего лизис клеток пептида. В пораженной заболеванием клетке, где произошла транслокация, ген Bcr и ген Abl транслоцируются таким образом, что указанные гены сближаются. В этом случае последовательности целевой нуклеиновой кислоты находятся достаточно близко друг к другу, чтобы указанные два неактивных фрагмента системы транскрипционных факторов сближаются, индуцируя транскрипцию индуцирующего гибель указанной клетки пептида. Лизис клетки зависит от конкретного генотипа, сформировавшегося в результате явления генетической мобильности.
[00982] ПРИМЕР 18: Применение сайт-специфического полипептида в качестве терапевтического средства при заболеваниях, включающих генетическую мутацию
[00983] Система, описанная в примере 4, может также использоваться для детекции присутствия конкретной мутации в клетке. В указанном примере выбирают первую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, для нацеливания сайт-специфического полинуклеотида на нативную последовательность, расположенную возле сайта мутации. Вторую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, выбирают таким образом, чтобы она распознавала мутантную последовательность (например, мутантную последовательность, идентифицируемую путем секвенирования ДНК). Указанную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, выбирают таким образом, чтобы указанная мутантная последовательность располагалась в пределах первых 12 нуклеиновых кислот непосредственно 5' от последовательности РАМ в указанном сайте. В этом случае последовательности целевой нуклеиновой кислоты находятся достаточно близко друг к другу, чтобы указанные два неактивных фрагмента транскрипционного фактора сближались, обеспечивая транскрипцию индуцирующего лизис клеток пептида.
[00984] ПРИМЕР 19: Рекрутинг иммунной системы для воздействия на пораженную заболеванием ткань, включающую явление генетической мобильности или генетическую мутацию.
[00985] Система, описанная в примере 4 и/или 5, может также использоваться для направления транскрипции комбинированной системой транскрипционных факторов, приводящего к презентации антигена на клеточной поверхности. В некоторых случаях указанный антиген представляет собой пептид, презентируемый молекулами ГКГС II класса. В некоторых случаях указанный антиген представляет собой белок клеточной поверхности, осуществляющий рекрутинг эффекторных клеток иммунной системы в указанный сайт.
[00986] ПРИМЕР 20: Детекция пространственного положения нуклеиновых кислот
[00987] Вектор(ы), содержащий(ие) сайт-специфический полипептид, нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и/или эффекторный белок, вводят в клетку. Внутри клетки образуется комплекс, содержащий элементы, кодируемые указанным(и) вектором(ами). В клетку вводят два вектора. Один вектор кодирует эффекторный белок (Csy4), который содержит первый неактивный фрагмент комбинированной системы с аффинной меткой. Второй вектор кодирует эффекторный белок (Csy4, Cas5 или Cas6), который содержит второй неактивный фрагмент комбинированной аффинной метки. Нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, указанных комплексов модифицирована связывающей белок Csy4, Cas5 или Cas6 последовательностью. Эффекторные белки связываются с указанной модифицированной нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту. Нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, сконструированы таким образом, чтобы направлять указанные комплексы в представляющие интерес области пространственной структуры нуклеиновой кислоты (например, хроматина). В том случае, если целевые последовательности не расположены близко друг от друга в пространстве, два неактивных фрагмента комбинированной аффинной метки неспособны взаимодействовать. В том случае, если целевые последовательности расположены близко друг от друга в пространстве, указанные два неактивных фрагмента комбинированной аффинной метки могут сближаться с формированием полной аффинной метки.
[00988] Клетки лизируют и клеточный лизат инкубируют с антителом, которое связывается с указанной аффинной меткой. Антитело очищают, с очищением таким образом аффинной метки и нуклеиновой кислоты, с которыми связаны указанные комплексы. Очищенную нуклеиновую кислоту отделяют от указанных комплексов с применением отмывки высокосолевым раствором. Отделенную очищенную нуклеиновую кислоту подготавливают для анализа секвенированием и секвенируют. Результаты секвенирования показывают области хроматина, расположенные близко в пространстве. Результаты секвенирования могут быть использованы для лучшего понимания генной экспрессии и лечения заболевания.
[00989] ПРИМЕР 21: МУЛЬТИПЛЕКСНАЯ ГЕНОМНАЯ ИНЖЕНЕРИЯ
[00990] В клетку вводят вектор, содержащий агент для мультиплексного генетического нацеливания, содержащий модули нуклеиновых кислот, которые содержат нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и последовательность связывания эндорибонуклеазы. Согласно некоторым вариантам реализации указанная клетка уже содержит сайт-специфический полипептид и эндорибонуклеазу. В некоторых случаях указанную клетку приводят в контакт с вектором, содержащим полинуклеотидную последовательность, кодирующую сайт-специфический полипептид, и вектором, содержащим полинуклеотидную последовательность, кодирующую эндорибонуклеазу. В некоторых случаях указанную клетку приводят в контакт с вектором, содержащим полинуклеотидную последовательность, кодирующую и сайт-специфический полипептид и эндорибонуклеазу. Согласно некоторым вариантам реализации указанный вектор содержит полинуклеотидную последовательность, кодирующую один или большее количество эндорибонуклеаз. Согласно некоторым вариантам реализации указанный вектор содержит полинуклеотидную последовательность, кодирующую агент для мультиплексного генетического нацеливания, сайт-специфический полипептид и одну или большее количество эндорибонуклеаз. Матрицу транскрибируют в РНК. Указанная одна или большее количество эндорибонуклеаз связываются с одной или большим количеством последовательностей связывания эндорибонуклеазы в указанном агенте для мультиплексного генетического нацеливания. Указанная одна или большее количество эндорибонуклеаз расщепляют указанную одну или большее количество последовательностей связывания эндорибонуклеазы в агенте для мультиплексного генетического нацеливания, таким образом высвобождая индивидуальные модули нуклеиновых кислот. Согласно некоторым вариантам реализации указанные модули нуклеиновых кислот содержат все или некоторые последовательности связывания эндорибонуклеазы, или не содержат последовательностей связывания эндорибонуклеазы.
[00991] Высвобожденные модули нуклеиновых кислот связываются с сайт-специфическими полипептидами с образованием таким образом комплексов. Указанные комплексы нацеливают на один или большее количество целевых нуклеиновых кислот. Указанные один или большее количество модулей нуклеиновых кислот гибридизуются с одной или большим количеством целевых нуклеиновых кислот. Указанные один или большее количество сайт-специфических полипептидов расщепляют указанную одну или большее количество целевых нуклеиновых кислот в сайте расщепления, определяемом модулем нуклеиновой кислоты, что приводит к получению одной или большего количества модифицированных целевых нуклеиновых кислот.
[00992] Согласно некоторым вариантам реализации в клетку вводят один или большее количество донорных полинуклеотидов и/или кодирующих их векторов. Один или большее количество донорных полинуклеотидов встраивают в одну или большее количество расщепленных целевых нуклеиновых кислот, что приводит к получению одной или большего количества модифицированных целевых нуклеиновых кислот (например, путем добавления). В некоторых случаях один и тот же донорный полинуклеотид встраивают в несколько сайтов расщепления. В некоторых случаях один или большее количество донорных полинуклеотидов встраивают в несколько сайтов расщепления. В некоторых случаях в клетки не вводят донорный полинуклеотид и/или кодирующий его вектор. В указанных случаях модифицированная целевая нуклеиновая кислота может включать удаление.
[00993] ПРИМЕР 22: СПОСОБ СТЕХИОМЕТРИЧЕСКОЙ ДОСТАВКИ РНК В КЛЕТКУ
[00994] Согласно некоторым вариантам реализации в описании предложен способ стехиометрической доставки нуклеиновых кислот в ядро клетки. Согласно некоторым вариантам реализации используют три подходящих для стехиометрической доставки нуклеиновых кислоты: одна из них кодирует Cas9, одна кодирует нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и одна кодирует Csy4. Каждая из указанных трех нуклеиновых кислот содержит сайт связывания Csy4.
[00995] Согласно некоторым вариантам реализации указанный способ обеспечивает получения тандемного гибридного полипептида. Указанный гибридный полипептид содержит три полипептида Csy4. Указанные три полипептида Csy4 разделены линкером. Указанные три полипептида Csy4 связываются с сайтами связывания Csy4 на каждой из трех молекул нуклеиновых кислот с образованием таким образом комплекса.
[00996] Согласно некоторым вариантам реализации указанный комплекс образуется вне клетки и вводится в клетку. Указанный комплекс получают, смешивая указанные три подходящих для стехиометрической доставки нуклеиновых кислоты и гибридного белка, и оставляя для реакции связывания между тандемным гибридным полипептидом и тремя сайтами связывания Csy4. Указанный комплекс вводят путем инъекции, электропорации, трансфекции, трансформации, вирусной трансдукции и т.п. Внутри клетки некоторые из нуклеиновых кислот указанного комплекса транслируются. Согласно некоторым вариантам реализации полученные продукты трансляции представляют собой Csy4 и NLS-Cas9 (например, Cas9, содержащий NLS. Указанная NLS не обязательно располагается на N-конце). Указанный Csy4 расщепляет сайт связывания Csy4 на нуклеиновой кислоте, кодирующей нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, с высвобождением таким образом указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту из тандемного гибридного полипептида. NLS-Cas9 связывается высвобожденной нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, с образованием таким образом структурной единицы. Указанная структурная единица перемещается в ядро. Внутри ядра указанная структурная единица направляется к целевой нуклеиновой кислоте, которая гибридизуется со спейсером нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Cas9 указанной структурной единицы расщепляет целевую нуклеиновую кислоту. Указанное расщепление целевой нуклеиновой кислоты Cas9 называют «геномной инженерией».
[00997] Согласно некоторым вариантам реализации указанный комплекс образуется внутри клетки. Вектор, кодирующий указанные три подходящие для стехиометрической доставки нуклеиновые кислоты, вводят в указанную клетку. Три разных вектора, каждый из которых кодирует одну из трех подходящих для стехиометрической доставки нуклеиновых кислот, вводят в клетку. В клетку вводят два вектора, при этом один из указанных двух векторов кодирует две подходящие для стехиометрической доставки нуклеиновые кислоты, и один из двух векторов кодирует одну подходящую для стехиометрической доставки нуклеиновую кислоту. Любой из указанных векторов может кодировать тандемный гибридный полипептид.
[00998] Внутри клетки вектор, кодирующий рибонуклеиновую кислоту, или полипептид, транскрибируется в РНК. Образуется комплекс, содержащий три нуклеиновые кислоты и тандемный гибридный полипептид, в результате чего каждый из Csy4-связывающих белков связывается с сайтом связывания Csy4 на каждой из трех нуклеиновых кислот; Нуклеиновые кислоты указанного комплекса транслируются. Согласно некоторым вариантам реализации полученные продукты трансляции представляют собой Csy4 и NLS-Cas9 (например, Cas9, содержащий NLS. Указанная NLS не обязательно находится на N-конце). Csy4 расщепляет сайт связывания Csy4 на нуклеиновой кислоте, кодирующей нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, с высвобождением таким образом указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, из тандемного гибридного полипептида. NLS-Cas9 связывает высвобожденную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, с образованием таким образом структурной единицы. Указанная структурная единица перемещается в ядро. Внутри ядра указанная структурная единица направляется к целевой нуклеиновой кислоте, которая гибридизуется со спейсером нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Cas9 указанной структурной единицы расщепляет целевую нуклеиновую кислоту.
[00999] ПРИМЕР 23: СПОСОБ СТЕХИОМЕТРИЧЕСКОЙ ДОСТАВКИ СОВОКУПНОСТИ НУКЛЕИНОВЫХ КИСЛОТ, КОТОРЫЕ НАЦЕЛЕНЫ НА НУКЛЕИНОВЫЕ КИСЛОТЫ, В КЛЕТКУ
[001000] Согласно некоторым вариантам реализации в описании предложен способ стехиометрической доставки совокупности нуклеиновых кислот в клетку, отличающийся тем, что некоторые из указанной совокупности нуклеиновых кислот представляют собой нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты. Согласно некоторым вариантам реализации указанная совокупность нуклеиновых кислот содержит четыре нуклеиновые кислоты, одна из которых кодирует Cas9, две кодируют нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, и одна кодирует Csy4.
[001001] Указанные нуклеиновые кислоты содержат два или большее количество сайтов связывания белков, связывающих нуклеиновые кислоты. В некоторых случаях первый сайт связывания белка, связывающего нуклеиновые кислоты (например, расположенный ближе к 5'-концу сайт), включает сайт связывания Csy4. В некоторых случаях второй сайт связывания белка, связывающего нуклеиновые кислоты (например, расположенный ближе к 3'-концу сайт), включает другой сайт связывания белка, связывающего нуклеиновые кислоты (например, сайт связывания MS2). В некоторых случаях вторые сайты связывания связывающего нуклеиновые кислоты белка каждой из подходящих для стехиометрической доставки нуклеиновых кислот отличаются. Например, второй сайт связывания белка, связывающего нуклеиновые кислоты, может представлять собой сайт, который связывает один из полипептидов CRISPR (например, Cas5, Cas6) В некоторых случаях кодирующая Cas9 нуклеиновая кислота также содержит сигнал ядерной локализации (NLS).
[001002] Согласно некоторым вариантам реализации указанный тандемный гибридный полипептид содержит три белка, связывающих нуклеиновые кислоты. Указанные три белка, связывающие нуклеиновые кислоты, представлены Csy4, Cas5, Cas6. Указанный тандемный гибридный полипептид содержит сигнал ядерной локализации. Указанный тандемный гибридный полипептиды содержит более чем одну копию белка, связывающего нуклеиновые кислоты (например, 2 копии Csy4, одну копию Cas5, одну копию Cas6).
[001003] Согласно некоторым вариантам реализации комплекс, содержащий тандемный гибридный белок и четыре нуклеиновые кислоты, образуется вне клетки. Указанный комплекс получают, смешивая указанные четыре нуклеиновые кислоты и указанный тандемный гибридный белок и оставляя для реакции, обеспечивающей связывание между указанным тандемным гибридным полипептидом и четырьмя сайтами связывания белков, связывающих нуклеиновые кислоты. Указанный комплекс вводят в клетку. Введение осуществляют с применением чего-либо из трансформации, трансфекции, вирусной трансдукции, микроинъекции или электропорации, или любой техники, позволяющей вводить биомолекулы через клеточную мембрану. Указанный комплекс образуется внутри клетки (например, после введение векторов, содержащих последовательности нуклеиновых кислот, кодирующих нуклеиновые кислоты и тандемный гибридный белок).
[001004] Внутри клетки нуклеиновые кислоты, кодирующие Csy4 и Cas9, транслируются, что приводит к образованию Csy4 и NLS-Cas9 (например, Cas9, содержащего NLS. Указанная NLS не обязательно располагается на N-конце). Csy4 расщепляет сайт связывания Csy4 на нуклеиновых кислотах, кодирующих нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, с высвобождением их таким образом из тандемного гибридного полипептида.
[001005] NLS-Cas9 связывается с высвобожденными нуклеиновыми кислотами, которые нацелены на нуклеиновые кислоты, с образованием таким образом совокупности структурных единиц. Указанные структурные единицы транслоцируются в ядро. Внутри ядра указанные структурные единицы направляются к целевой нуклеиновой кислоте, которая гибридизуется со спейсером нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, структурной единицы. Cas9 указанной структурной единицы расщепляет целевую нуклеиновую кислоту.
[001006] ПРИМЕР 24: СПОСОБ СТЕХИОМЕТРИЧЕСКОЙ ДОСТАВКИ РНК И ДОНОРНОГО ПОЛИНУКЛЕОТИДА
[001007] В описании предложен способ стехиометрической доставки РНК-компонентов, подходящих для применения в геномной инженерии. Указанный способ может дополнительно включать доставку донорного полинуклеотида, который может быть встроен в сайт геномной инженерии.
[001008] В описании предложен способ стехиометрической доставки совокупности РНК и донорного полинуклеотида в клетку. Согласно некоторым вариантам реализации указанная совокупность РНК включает три РНК и одну ДНК. В некоторых случаях указанные три РНК представлены: одной кодирующей Cas9, одной кодирующей Csy4 и одной кодирующей нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту. Указанная ДНК представляет собой ДНК, кодирующую донорный полинуклеотид.
[001009] В некоторых случаях указанные RNA содержат совокупность сайтов связывания белков, связывающих нуклеиновые кислоты (например, два сайта связывания белков, связывающих нуклеиновые кислоты). Первый сайт связывания белка, связывающего нуклеиновые кислоты (например, расположенный ближе к 5'-концу сайт) содержит сайт связывания Csy4. Второй сайт связывания белка, связывающего нуклеиновые кислоты (например, расположенный ближе к 3'-концу сайт) содержит другой сайт связывания белка, связывающего нуклеиновые кислоты). Второй сайт связывания белка, связывающего нуклеиновые кислоты в каждой из нуклеиновых кислот предложенного в настоящем изобретении отличается. Например, второй сайт связывания белка, связывающего нуклеиновые кислоты, связывает полипептид CRISPR (например, Cas5, Cas6) и/или ДНК-связывающий белок (например, белок типа «цинковые пальцы»), Нуклеиновые кислоты согласно предложенному способу также содержат последовательность, кодирующую сигнал ядерной локализации (например, РНК, кодирующую Cas9, и ДНК, кодирующую донорный полинуклеотид).
[001010] Согласно некоторым вариантам реализации указанный тандемный гибридный полипептид содержит четыре белка, связывающих нуклеиновые кислоты (например, РНК-связывающие белки и ДНК-связывающие белки). В некоторых случаях три белка, связывающие нуклеиновые кислоты, представляют собой Csy4, Cas5, Cas6, а четвертый белок, связывающий нуклеиновые кислоты, представляет собой ДНК-связывающий белок (например, белок типа «цинковые пальцы»). В некоторых случаях указанный тандемный гибридный полипептид содержит сигнал ядерной локализации.
[001011] Согласно некоторым вариантам реализации комплекс, содержащий тандемный гибридный белок и нуклеиновые кислоты (например, три РНК и одну ДНК) образуется вне клетки. Указанный комплекс получают, смешивая нуклеиновые кислоты (например, три РНК и одну ДНК) и указанный тандемный гибридный белок и оставляя для реакции, обеспечивающей связывание между указанным тандемным гибридным полипептидом и четырьмя сайтами связывания РНК-связывающих белков. Указанный комплекс может быть введен в клетку. Указанный комплекс образуется внутри клетки (например, после введения векторов, содержащих последовательности нуклеиновых кислот, кодирующие нуклеиновые кислоты и тандемный гибридный белок).
[001012] Внутри клетки РНК, кодирующие Csy4 и Cas9, транслируются, что приводит к образованию Csy4 и NLS-Cas9 (например, Cas9, содержащего NLS. Указанная NLS не обязательно располагается на N-конце, как было отмечено в настоящем документе). Csy4 может расщеплять сайт связывания Csy4 на РНК, кодирующих нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и ДНК, с высвобождением таким образом их из указанного тандемного гибридного полипептида. В некоторых случаях высвобожденный донорный полинуклеотид перемещается в ядро с помощью своего сигнала ядерной локализации.
[001013] NLS-Cas9 связывает высвобожденную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, с образованием таким образом структурной единицы. Указанная структурная единица перемещается в ядро. Внутри ядра указанная структурная единица направляется к целевой нуклеиновой кислоте, которая гибридизуется со спейсером нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, указанной структурной единицы. Cas9 указанной структурной единицы расщепляет целевую нуклеиновую кислоту. Донорный полинуклеотид, фрагмент донорного полинуклеотида, копия донорного полинуклеотида или фрагмент копии донорного полинуклеотида может быть встроен(а) в расщепленную целевую нуклеиновую кислоту.
[001014] ПРИМЕР 25: Эффективный отбор генетически модифицированных клеток
[001015] Совокупность клеток приводят в контакт с вектором, содержащим последовательности, кодирующие полинуклеотид, гомологичный Cas9, нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и донорный полинуклеотид. В некоторых случаях одна или большее количество последовательностей, кодирующих полипептид, гомологичный Cas9, нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, и донорный полинуклеотид расположены на разных векторах. Клетки трансфицируют указанным вектором. В некоторых случаях указанные клетки инфицируют вирусом, несущим указанный вектор. В некоторых случаях указанная клетка уже содержит белок, гомологичный Cas9, и вектор не кодирует указанный полипептид. В некоторых случаях указанная клетка уже содержит систему CRISPR (например, белки Cas, crRNA и tracrRNA) и вектор кодирует только донорный полинуклеотид. Указанный донорный полинуклеотид содержит последовательности, кодирующие представляющий интерес генетический элемент и репортерный элемент. Указанный репортерный элемент содержит последовательности нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, белок, гомологичный Cas 9 и флуоресцентный белок. Нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, направляет Cas9 к целевой нуклеиновой кислоте (например, сайту в геноме клетки-хозяина), что приводит к двуцепочечному разрыву ДНК целевой нуклеиновой кислоты и встраиванию донорного полинуклеотида. Встраивание донорного полинуклеотида отслеживают путем скрининга репортера. В некоторых случаях скрининг включает сортировку клеток с активированной флуоресценцией. Скрининг включает несколько способов селекции. Cas9 и/или нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, находятся под контролем индуцируемого промотора. После выбора популяции клеток, которые содержат репортерный сигнал, указанный репортерный элемент удаляют путем активации указанного индуцируемого промотора, который транскрибирует нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, и сайт-специфический полипептид донорного полинуклеотида. Транскрибированные нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, и транскрибированный сайт-специфический полипептид могут образовывать комплексы. Один комплекс может быть нацелен на 3'-конец репортерного элемента донорного полинуклеотида. Один комплекс может быть нацелен на 5'-конец репортерного элемента донорного полинуклеотида. 3'- и 5'-концы репортерного элемента могут расщепляться. Расщепленная целевая нуклеиновая кислота может быть восстановлена за счет клеточных механизмов, с образованием таким образом последовательности нуклеиновой кислоты внутри рамки считывания, кодирующей ту же последовательность нуклеиновых кислот, что и до встраивания донорного полинуклеотида. Таким образом репортерный элемент эффективно встраивается и удаляется из клеток.
[001016] ПРИМЕР 26: Способ расщепления Cas9 с применением сконструированных нуклеиновых кислот, которые нацелены на нуклеиновые кислоты,
[001017] Реагенты
[001018] Плазмиду рСВ002, содержащий целевую последовательность ДНК temp3, расщепляли 1 ед. AscI на 1 мкг ДНК для линеаризации вектора. Реакцию останавливали путем инкубирования реакционной смеси при 80°С в течение 20 мин. Затем реакционную смесь очищали с применением набора для очищения продуктов ПЦР от Qiagen.
[001019] Одиночную направляющую нуклеиновую кислоту получали с помощью набора для высокоэффективного синтеза РНК Т7 (кат. №: E2040S), с применением половины объема реагентов, рекомендованного производителями для РНК длиной >300 нуклеотидов. Как правило, использовали 200-350 нг матрицы в реакционном объеме 20 мкл, который инкубировали в течение 16 часов. Образцы обрабатывали ДНКазой, очищали с применением набора для очищения РНК Thermo GeneJet (кат. №: K0732) и элюировали в 20 мкл. Типичный выход варьирует от 1,4 до 2 мкг/мкл.
[001020] В начале подготовки анализа расщепления все онРНК разводили до концентрации 3500 нМ и подвергали тепловому шоку при 80°С в течение 15 минут. Образцы извлекали из нагревательного элемента и оставляли для охлаждения до комнатной температуры. Аликвота объемом 4 мкл одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, может быть проведена через агарозный гель для подтверждения целостности РНК.
[001021] Аликвоты Cas9 в концентрации 2-2,5 мг/мл извлекали из морозильной камеры и максимально быстро размораживали, после чего разводили в 1× расщепляющий буфер до подходящей базовой концентрации.
[001022] Анализ расщепления
[001023] Аликвоты основной смеси из воды, 5× расщепляющего буфера (100 мМ HEPES, 500 мМ KCl, 25 мМ MgCl2, 5 мМ ДТТ и 25% глицерин, рН 7,4) и Cas9 в концентрации до 250 нМ помещали в тонкостенные пробирки для ПЦР. онРНК добавляли в подходящие пробирки в конечной концентрации 250 нМ.
[001024] Реакционную смесь инкубировали при 37°С в течение 10 минут, добавляли 10 нМ линеаризованную плазмиду и реакции (конечный реакционный объем 20 мкл) инкубировали при 37°С на протяжении часа. Реакцию останавливали нагреванием до 60С в течение 20 минут. Аликвоты объемом 10 мкл смешивали с 2 мкл 6× загрузочного красителя для ДНК и анализировали посредством электрофореза на 1,5% агарозном геле, окрашенном красителем SYBR safe. Появление фрагментов размером ~2800 п.о. и ~1300 п.о. указывало на опосредованное Cas9 расщепление. Результаты указанных экспериментов представлены на Фиг. 6, 10 и 11. Все сконструированные и представленные на Фиг. 5 синтетические направляющие последовательности РНК поддерживали расщепление онРНК, кроме SGRv8, в котором вся комплементарная область была инвертирована. Указанные результаты показывают, что разные области онРНК могут подвергаться перестройке и тем не менее сохранять функцию.
[001025] Сконструированные нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, тестировали в описанном выше анализе. На Фиг. 22А и 22В представлен дизайн начального набора вариантов дуплекса во вариантах остова одиночной направляющей нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, использованных для тестирования нацеливающей и расщепляющей активности.
[001026] На Фиг. 25 представлен второй набор вариантов дуплекса с менее выраженными модификациями в дуплексе. V28 содержит вставку размером 2 основания в направлении 3'от комплементарной области; V29 содержит удаление размером 3 основания в направлении 3' 3'от комплементарной области.
[001027] На Фиг. 26А и 26В показаны варианты tracr, которые содержат мутации во фрагменте tracrRNA нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту (т.е. минимальная последовательность tracrRNA и последовательность 3'-tracrRNA). V38-V41 содержат соединения между комплементарной областью/дуплексом и 3'-концами последовательностей нуклеиновых кислот tracr из М. mobile 163K (v38), S. thermophilus LMD-9 (V39), С. jejuni (V40) и N. meningitides.
[001028] На Фиг. 27А и 27В изображены варианты, содержащие модификаций, обеспечивающие возможность связывания Csy4 с нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту. Дополнительные шпилечные последовательности получены из повтора CRISPR Pseudomonas aeruginosa PA14.
[001029] На Фиг. 23А-С представлены данные анализа расщепления in vitro, демонстрирующие активность вариантов нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, в отношении расщепления Cas9. Вариант SGRv8 не был способен поддерживать расщепление целевой нуклеиновой кислоты (на Фиг. 23В дорожка 9).
[001030] На Фиг. 28 и Фиг. 29 представлены две независимые повторности анализа расщепления Cas9, в котором тестировались варианты, изображенные на Фиг. 24-27.
[001031] Дополнительно были получены и протестированы в таком же анализе сконструированные нуклеиновые кислоты, которые нацелены на нуклеиновые кислоты, перечисленные в таблице 2. Результаты данного анализа представлены на Фиг. 37 и приведены в колонке «Активность» в таблице 5.
[001032] Результаты указанных экспериментов указывают на важность областей петли и Р-домена для обеспечения расщепления целевой нуклеиновой кислоты. Функциональность вариантов 42-45 показывает, что добавление связывающей Csy4 последовательности к нуклеиновой кислоте, которая нацелена на нуклеиновую кислоту, не нарушает расщепление целевой нуклеиновой кислоты.
[001033] ПРИМЕР 27: СИСТЕМЫ ДЛЯ АНАЛИЗА СЕКВЕНИРОВАНИЕМ
[001034] На Фиг. 30 изображена система, предназначенная для реализации предложенных в настоящем изобретении способов. Указанная система может включать компьютерный сервер («сервер»), запрограммированный для реализации описанных в настоящем документе способов. На Фиг. 30 изображена система 3000, выполненная таким образом, чтобы обеспечивать пользователю возможность детекции, анализа и обмена информацией о результатах секвенирования, например, обогащенных мишенями нуклеаз нуклеиновых кислот, секвенированных целевых нуклеиновых кислот, данных, касающихся предложенных в настоящем изобретении способов, диагностики заболевания, генотипирования пациента, принятия решения о конкретном лечении для пациента или любой их комбинации. Система 3000 включает центральный компьютерный сервер 3001, запрограммированный для реализации примеров описанных в настоящем документе способов. Сервер 3001 включает центральный процессор (CPU, также «процессор») 3005, который может представлять собой одноядерный процессор, многоядерный процессор или совокупность процессоров для параллельной обработки. Сервер 3001 также включает память 3010 (например, запоминающее устройство с произвольным доступом, постоянное запоминающее устройство, флеш-память); электронное устройство хранения данных 3015 (например, жесткий диск); интерфейс передачи данных 3020 (например, сетевой адаптер) для обмена информацией с одной или большим количеством других систем; и периферийные устройства 3025, которые могут включать буферная память, другой тип памяти, устройство хранения данных и/или электронные адаптеры дисплея. Память 3010, устройство хранения данных 3015, интерфейс 3020 и периферийные устройства 3025 сообщаются с процессором 3005 посредством коммуникационной шины (сплошная линия), такой как материнская плата. Устройство хранения 3015 может представлять собой устройство хранения для хранения данных. Сервер 3001 функционально связан с компьютерной сетью («сеть») 3030 с помощью интерфейса передачи данных 3020. Сеть 3030 может представлять собой сеть Интернет, Интранет и/или Экстранет, сеть Интранет и/или Экстранет, обменивающуюся данными с сетью Интернет, телекоммуникационная сеть или сеть данных. Сеть 3030 в некоторых случаях с помощью сервера 3001 может обеспечивать пиринговую сеть, которая может позволять устройствам, соединенным с сервером 3001, функционировать в качестве клиента или сервера. Микроскоп и микроманипулятор могут представлять собой периферийные устройства 3025 или удаленные компьютерные системы 3040.
[001035] В устройстве хранения данных 3015 могут храниться файлы, например, результаты секвенирования, сайты связывания мишеней, персональные генетические данные, генотипы, изображения, анализ изображений и/или результаты секвенирования, или любой аспект данных, связанных с настоящим исследованием.
[001036] Сервер может сообщаться с одной или большим количеством удаленных компьютерных систем через сеть 3030. Указанные одна или большее количество удаленных компьютерных систем могут представлять собой, например, персональные компьютеры, портативные компьютеры, планшеты, телефоны, смартфоны или КПК.
[001037] В некоторых ситуациях система 3000 включает единственный сервер 3001. В других ситуациях система включает несколько северов, сообщающихся друг с другом через сеть Интранет, Экстранет или Интернет.
[001038] Сервер 3001 может подходить для хранения результатов секвенирования, сайтов связывания мишеней, персональных генетических данных и/или другой потенциально релевантной информации. Такая информация может храниться на устройстве хранения данных 3015 или сервере 3001, и такие данные могут передаваться через сеть.
[001039] Способы согласно описанию в настоящем документе могут быть реализованы посредством машиноисполняемого (или исполняемого компьютерным процессором) кода (или программного обеспечения), хранящегося в электронном ЗУ, расположенном на сервере 3001, например, в памяти 3010 или электронном устройство хранения данных 3015. Во время использования код может выполняться процессором 3005. В некоторых случаях код может считываться из указанного устройства хранения данных 3015 и храниться в памяти 3010 для быстрого доступа к нему процессора 3005. В некоторых ситуациях электронное устройство хранения данных 3015 может быть исключена, и машиноисполняемые инструкции хранятся в памяти 3010. Как вариант, код может выполняться во второй компьютерной системе 3040.
[001040] Аспекты предложенных в настоящем документе систем и способов, таких как сервер 3001, могут быть реализованы в программной среде. Различные аспекты указанной технологии могут считаться «продуктами» или «изделиями», как правило, в форме машиноисполняемого (или исполняемого процессором) кода и/или связанных данных, переносимых или реализованных в виде типа машиночитаемого носителя. Машиноисполняемый код может храниться на электронном устройстве хранения данных, например, в памяти (такой как постоянное запоминающее устройство, запоминающее устройство с произвольным доступом, флеш-память) или жесткий диск. Среда для «хранения» может включать все или любые из материальных устройств памяти компьютеров, процессоров или т.п., или связанных с ними модулей, например, различные виды полупроводниковой памяти, запоминающие устройства на ленте, запоминающие устройства на диске и т.п., способные обеспечивать энергонезависимое хранение в любой момент времени для разработки программного обеспечения. Программное обеспечение полностью или его фрагменты могут периодически сообщаться через Интернет или различные другие телекоммуникационные сети. Такое сообщение, например, может позволять загрузку программного обеспечения с одного компьютера или процессор на другой, например, с административного сервера или центрального компьютера на компьютерную платформу сервера приложения. Таким образом, другой тип среды, способный переносить элементы программного обеспечения, включает оптические, электрические и электромагнитные волны, например, используемые в различных физических интерфейсах для передачи между локальными устройствами, через проводные и наземные сети и разнообразные воздушные каналы связи. Физические элементы, передающие такие волны, такие как проводные или беспроводные аналоги, оптические каналы связи или т.п., также могут рассматриваться в качестве среды, несущей программное обеспечение. В настоящем документе, при отсутствии ограничения энергонезависимым материальным носителем для «хранения», такие термины, как «машиночитаемая среда/носитель», относятся к любому носителю, участвующему в обеспечении инструкций для выполнения процессору.
[001041] Соответственно, машиночитаемая среда, например, исполняемый компьютером код, может принимать различные формы, включая, но не ограничиваясь перечисленными, материальный носитель для хранения данных, несущую волну или физическую среду для передачи данных. Энергонезависимое запоминающее устройство может включать, например, оптические или магнитные диски, например, любые запоминающие устройства на любом(ых) компьютере(ах) или т.п., которые могут применяться для реализации системы. Материальная среда для передачи данных может включать: коаксиальные кабели, медные провода и оптоволокно (в том числе провода, включающие шину в компьютерной системе). Волновая среда для передачи данных может принимать форму электрических или электромагнитных сигналов, или акустических или световых волн, например, генерируемых при передаче данных на частоте радиосвязи (РЧ) и в инфракрасном диапазоне (ИК). Распространенные формы машиночитаемых носителей, соответственно, включают, например: дискету, гибкий диск, жесткий диск, магнитную ленту, любой другой магнитный носитель, CD-ROM, DVD, DVD-ROM, любой другой оптический носитель, перфокарты, бумажная перфолента, любой другой физический носитель информации с паттернами отверстий, ОЗУ, ПЗУ, ППЗУ и ЭППЗУ, флэш-ЭППЗУ, любой(ая) другой(ая) микросхема памяти или картридж памяти, несущая волна для передачи данных или инструкций, кабели или каналы, передающие такую несущую волну, или любой другой носитель, с которого компьютер может считывать программный код и/или данные. Многие из указанных форм машиночитаемых носителей могут участвовать в передаче одной или большего количества последовательностей одной или большего количества инструкций для выполнения процессору.
[001042] ПРИМЕР 28: СЕКВЕНИРОВАНИЕ НА МАТРИЦАХ С ПРИМЕНЕНИЕМ САЙТ-СПЕЦИФИЧЕСКОГО ПОЛИПЕПТИДА
[001043] Образец нуклеиновой кислоты лигируют с нуклеиновокислотной меткой, содержащей одиночную направляющую РНК (онРНК) и детектируемую метку. В совокупности образец нуклеиновой кислоты, лигированный с нуклеиновокислотной меткой, называют «меченым экспериментальным образцом». Меченый экспериментальный образец приводят в контакт с микрочипом, содержащим иммобилизованные олигонуклеотиды. Указанные иммобилизованные олигонуклеотиды представляют собой библиотеку двуцепочечных нуклеиновых кислот. Указанные олигонуклеотиды содержат детектируемую метку (например, флуоресцентную метку). Индивидуальные элементы меченого экспериментального образца гибридизуются с олигонуклеотидами, комплементарными им в достаточной степени для того, чтобы это способствовало гибридизации. Величина гибридизации может быть количественно определена путем сравнения интенсивности указанных двух детектируемых меток из библиотеки образцов и иммобилизованных олигонуклеотидов. Например, в гибридизовавшихся олигонуклеотидах могут наблюдаться две детектируемых метки (из библиотеки образцов и из олигонуклеотида). В негибридизовавшихся олигонуклеотидах может наблюдаться одна детектируемая метка (из указанного олигонуклеотида). Гибридизованные зонды приводят в контакт с Cas9. Cas9 расщепляет на микрочипе олигонуклеотиды, гибридизовавшиеся с элементами меченого экспериментального образца. Расщепление сайт-специфическим полипептидом позволяет удалить гибридизованные элементы меченого экспериментального образца. После расщепления сайт-специфическим полипептидом на микрочипе остаются только негибридизованные олигонуклеотидные детектируемые метки. Оставшуюся детектируемую метку количественно определяют. Количественное определение оставшихся детектируемых меток коррелирует с тем, какие последовательности были представлены в образце нуклеиновой кислоты, а какие нет (например, путем позиционного картирования). Олигонуклеотиды, в которых не обнаруживается сохранившаяся детектируемая метка, соответствуют последовательностям, которые были представлены в образце нуклеиновой кислоты. Олигонуклеотиды, в которых обнаруживается сохранившаяся детектируемая метка, соответствуют последовательностям, которые не были представлены в образце нуклеиновой кислоты.
[001044] ПРИМЕР 29: РАСЩЕПЛЕНИЕ ЦЕЛЕВОЙ НУКЛЕИНОВОЙ КИСЛОТЫ С ПОМОЩЬЮ МЕЧЕНОЙ НУКЛЕИНОВОЙ КИСЛОТЫ, КОТОРАЯ НАЦЕЛЕНА НА НУКЛЕИНОВУЮ КИСЛОТУ
[001045] В данном примере описаны результаты расщепления целевой нуклеиновой кислоты нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, содержащей связывающую последовательность Csy4 на 5'-конце указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Cas9 инкубировали с направляющей РНК или без направляющей РНК, нацеленной на один сайт в линейной двуцепочечной последовательности ДНК. Через 1 час продукты расщепления разделяли и визуализировали на агарозном геле. На Фиг. 13D показано, что расщепление Cas9, опосредованное меченой нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, (дорожка 3) было менее эффективным, чем расщепление Cas9, опосредованное немеченой нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, (дорожка 1). Через 1 час ~100% мишени расщепляется Cas9, направляемой нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, при этом за то же время Cas9, направляемый меченой нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, расщеплял только незначительную долю мишени. Указанные эксперименты показывают, что локализация ненативной последовательности может использоваться для настройки эффективности расщепления комплексом Cas9: нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. Например, на Фиг. 27 и Фиг. 29 показана функциональность добавления связывающей Csy4 последовательности в различные локализации нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, сохраняющей активность.
[001046] ПРИМЕР 30: ГЕНОМНАЯ ИНЖЕНЕРИЯ ГЕНОВ ПРИ НАРУШЕНИЯХ СИСТЕМЫ КРОВИ
[001047] Нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, содержащую спейсерную последовательность, описанную в Таблице 2, вводят в клетку с сайт-специфическим полипептидом, с образованием таким образом комплекса. Указанный комплекс нацелен на вовлеченный в нарушение системы крови ген, существенно комплементарный указанной спейсерной последовательности нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту. После того как нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, гибридизовалась с целевой нуклеиновой кислотой, сайт-специфический полипептид расщепляет целевую нуклеиновую кислоту. Может быть получена расщепленная целевая нуклеиновая кислота с донорным полинуклеотидом.
[001048] ПРИМЕР 31: ПРОТОКОЛ ДЛЯ ОПРЕДЕЛЕНИЯ РАСЩЕПЛЕНИЯ И МОДИФИКАЦИИ ЦЕЛЕВОЙ НУКЛЕИНОВОЙ КИСЛОТЫ
[001049] Указанный протокол может применяться для определения того, была ли целевая нуклеиновая кислота расщеплена, или была ли целевая нуклеиновая кислота модифицирована, например, посредством вставки или удаления. Праймеры, окружающие целевой сайт, используют для ПЦР-амплификации, в реакционном объеме 25 мкл, продукта размером 500-600 нуклеотидов из гДНК. Праймеры содержат по меньшей мере 100 нуклеотидов с каждой стороны расщепляемого сайта. Размер полученных в результате анализа расщепления продуктов составляет приблизительно или более чем 100 нуклеотидов.
[001050] Приблизительно 5 мкл ПЦР-продукта проводят через агарозный гель для подтверждения чистоты амплификации. Для оставшегося ПЦР-продукта используют следующий протокол плавления и ренатурации:


[001051] Получают основную смесь Т7Е1 из воды, буфера NEB2 и фермента Т7Е1. Получают нужное количество путем умножения на число реакций, плюс дополнительное количество. В таблице 8 показаны компоненты основной смеси Т7Е1.

[001052] К каждой реакции в стрип-пробирке с крышкой объемом 200 мкл добавляют следующие реагенты: основная смесь Т7Е1 (10 мкл) и GWH-образец (10 мкл). Реакцию инкубируют при 37°С в течение 25 минут.
[001053] В образец добавляют загрузочный буфер и целиком проводят через 3% гель при 120 В в течение 20 минут. Гель может работать дольше в том случае, если требуется большее разрешение. Гель визуализируют и сохраняют изображения.
[001054] Проводят количественный анализ изображения для определения величины расщепления целевой нуклеиновой кислоты.
[001055] ПРИМЕР 31: ТЕСТИРОВАНИЕ ВАРИАНТОВ НУКЛЕИНОВОЙ КИСЛОТЫ, КОТОРАЯ НАЦЕЛЕНА НА НУКЛЕИНОВУЮ КИСЛОТУ, В КЛЕТКАХ
[001056] Указанный пример отражает тестирование в анализе на клетках вариантов нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, представленных на Фиг. 22, 24 и 25 и в примере 26, для определения того, соответствует ли функциональности in vivo функциональность in vitro, определенная в примере 26. Клетки НЕК293 культивировали до 60-70% конфлюэнтности в чашках размером 10 см. Клетки извлекали трипсинизацией, подсчитывали с применением гемоцитометра, после чего разделяли на аликвоты по 7×104 клеток для каждой лунки для трансфекции. Для каждой лунки смешивали 250 нг плазмиды рСВ045, экспрессирующей кодон-оптимизированный Cas9 млекопитающих, с 30 нг направляющей РНК, 40 нг ДНК с copGFP (зеленый флуоресцентный белок Pontellina plumata) и 0,5 мкл Липофектамина 2000 в конечном объеме 50 мкл DMEM. ДНК и липид инкубировали в течение 15 минут перед трансфекцией. Трансфекцию проводили при высевании путем добавления смеси липид : ДНК к 450 мкл DMEM + 10% фетальной бычьей сыворотки, содержащим 7×104 клеток. Смесь состава для трансфекции и клеток добавляли в 96-луночные тканевые культуральные планшеты, покрытые коллагеном из хвоста крыс I типа. Клетки инкубировали при 37°С в термостате при 5% CO2 в течение 40 часов.
[001057] Из всех лунок удаляли среду и клетки лизировали с применением раствора Quickextract (Epicentre) в соответствии с инструкциями производителя. Собранную при лизировании QuickExtract ДНК разбавляли в пропорции 1:10 и использовали в качестве матрицы в ПЦР-реакциях для анализов Т7Е1 согласно описанию в примере 30.
[001058] На Фиг. 36 показано, что все варианты, кроме v8 и v9, были способы расщеплять целевую нуклеиновую кислоту. Вариант v8 нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, также был по существу неактивен в анализах in vitro, как видно на Фиг. 23В. Вариант нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, v9 проявлял очень слабовыраженную активность в анализе in vitro, представленном на Фиг. 23В.
[001059] ПРИМЕР 32: ОПРЕДЕЛЕНИЕ СУДЬБЫ КЛЕТОК С ИСПОЛЬЗОВАНИЕМ МЕЧЕНОЙ КЛЕТКИ
[001060] В указанном примере описан способ отслеживания развития клетки клеточного пути. Гемопоэтическую стволовую клетку (например, гемоцитобласт) приводят в контакт с сайт-специфическим полипептидом, нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту, и донорным полинуклеотидом. Сайт-специфический полипептид и нуклеиновая кислота, которая нацелена на нуклеиновую кислоту, образуют комплекс и направляются в область гемопоэтического генома для осуществления расщепления. После расщепления в расщепленный сайт в геноме гемопоэтической клетки встраивают донорный полинуклеотид. Индуцируют дифференцировку гемопоэтической стволовой клетки с прохождением нормальных процессов дифференцировки. На разных стадиях дифференцировки может быть проведен анализ на присутствие донорного полинуклеотида в образце, содержащем дифференцированные гемопоэтические клетки. Таким образом, может отслеживаться процесс дифференцировки клетки.
[001061] ПРИМЕР 33: КЛОНИРОВАНИЕ ДВУЦЕПОЧЕЧНОГО ОЛИГОНУКЛЕОТИДА, КОДИРУЮЩЕГО НУКЛЕИНОВУЮ КИСЛОТУ, КОТОРАЯ НАЦЕЛЕНА НА НУКЛЕИНОВУЮ КИСЛОТУ, В ЛИНЕАРИЗОВАННЫЙ ВЕКТОР
[001062] В указанном примере описан способ получения двуцепочечного олигонуклеотида, кодирующего фрагмент нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, (например, спейсер) и его встраивания в линеаризованный вектор. Линеаризованный вектор или замкнутый суперспиральный вектор содержит последовательность, кодирующую сайт-специфический полипептид (например, Cas9), промотор, управляющий экспрессией последовательности, кодирующей сайт-специфический полипептид (например, ЦМВ-промотор), последовательность, кодирующая линкер (например, 2А), последовательность, кодирующая маркер (например, CD4 или OFP), последовательность, кодирующая фрагмент нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, промотор, управляющий экспрессией последовательности, кодирующей фрагмент указанной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, и последовательность, кодирующая селективный маркер (например, ампициллин), или любую их комбинацию.
[001063] Равные количества двух одноцепочечных олигонуклеотидов ренатурируют совместно (например, 50 мкМ). Указанные два одноцепочечных олигонуклеотида могут гибридизоваться друг с другом. По меньшей мере один из двух одноцепочечных олигонуклеотидов комплементарен целевой нуклеиновой кислоте (например, в области длиной 10-30 нуклеотидов, смежной с примыкающим к протоспейсеру мотивом в мишени). По меньшей мере один из двух одноцепочечных нуклеотидов содержит 3' выступающую последовательность, содержащую последовательность 5'-GTTT-3'. По меньшей мере один из двух одноцепочечных олигонуклеотидов содержит 3' выступающую последовательность, содержащую последовательность 5'-CGGTG-3'. В некоторых случаях один из двух одноцепочечных олигонуклеотидов содержит выступающую последовательность 5'-GTTT-3', а другой содержит последовательность 5'-CGGTG-3'. Ренатурацию осуществляют в ренатурирующем буфере, содержащем по меньшей мере 10 мМ Tris-HCl, рН 8,0, 1 мМ EDTA, рН 8,0, и 100 мМ NaCl. Ренатурацию осуществляют путем нагревания смеси олигонуклеотидов при 95°С в течение 3-5 минут, извлечения смеси олигонуклеотидов из нагревателя и охлаждения смеси до комнатной температуры в течение 5-10 минут. Смесь двуцепочечных олигонуклеотидов аккуратно центрифугируют. После ренатурации смесь может храниться при 4°С или -20°С. Указанную смесь, содержащую уже двуцепочечные олигонуклеотиды, разводят для получения двух базовых растворов с концентрациями 500 нМ и 5 нМ. Указанные базовые растворы получают путем разведения смеси олигонуклеотидов в воде.
[001064] Двуцепочечный олигонуклеотид (дц-олинонуклеотид) лигируют в линеаризованный вектор. Указанный линеаризованный вектор содержит последовательность, кодирующую сайт-специфический полипептид (например, Cas9), маркерный белок (например, оранжевый флуоресцентный белок), и/или последовательность, кодирующую нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, при этом указанный линеаризованный вектор линеаризован в области последовательности, кодирующей указанную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, таким образом, что образующиеся липкие концы соответствуют выступающим концам указанного дц-олинонуклеотида. Реакция лигирования может включать 1× лигирующий буфер (например, 50 мМ Tris-HCl, рН 7,6, 5 мМ MgCl2, 1 мМ АТФ, 1 мМ ДТТ и/или 5% ПЭГ 8000), 30 нг линеаризованного вектора, 5 нМ дц-олинонуклеотид и ДНК-лигазу (например, 4 мкл 5× лигирующего буфера, 2 мкл линеаризованного вектора в концентрации 15 нг/мкл, 2 мкл 5 нМ дц-олинонуклеотида, 11 мкл воды, 1 мкл Т4 ДНК-лигазы). Реакционную смесь перемешивают. Реакционную смесь инкубируют при комнатной температуре в течение 10 минут - 2 часов. Реакционную смесь помещают на лед и проводят трансформацию с получением компетентных клеток.
[001065] Трансформация в компетентные клетки включает трансформацию в химически компетентные клетки ТОР10 Е. coli. Компетентные клетки размораживают на льду. 3 мкл реакционной смеси добавляют в компетентные клетки и аккуратно перемешивают. Клетки инкубируют на льду в течение 10-30 минут. Клетки подвергают тепловому шоку в течение 30 секунд при 42С. Клетки переносят на лед на 2 минуты. В клетки добавляют 250 мкл среды (SOC или LB). Клетки перемешивают встряхиванием на 200 об/мин в течение 1 часа при 37°С. Затем клетки распределяют в чашке с агаром, содержащим 100 мкл/мл ампициллина, и оставляют на ночь при 37°С.
[001066] Указанные трансформанты анализируют. Например, трансформанты анализируют для идентификации дц-олинонуклеотида, лигированного в вектор, и/или для подтверждения того, что лигирование не является ложноположительным. Для анализа трансформантов собирают колонии и культивируют в течение ночи на среде LB, содержащей 100 мкл/мл ампициллина, при 37°С. Выделяют плазмиду, содержащую сайт-специфический полипептид и дц-олинонуклеотид (например, с применением набора Miniprep). Реакцию секвенирования проводят на выделенной плазмиде. Для реакции секвенирования используют праймер для секвенирования, сконструированный с возможностью секвенирования дц-олинонуклеотида (например, праймер для секвенирования представляет собой праймер для секвенирования U6, который связывается с промотором U6, расположенным в направлении 5' непосредственно за последовательностью, кодирующей дц-олинонуклеотид.
[001067] После идентификации нужной вставки дц-олинонуклеотида плазмида может храниться при -20°С или в базовом банке в глицерине при -80°С. Для получения базового банка в глицерине исходную колонию, содержащую нужную плазмиду, высевают методом штриха на чашку с агаром, содержащую 100 мкл/мл ампициллина, и инкубируют в течение ночи при 37°С. Выделяют одиночную колонию, выросшую на LB, содержащей 100 мкл/мл ампициллина, до вхождения культуры в стационарную фазу. Культуру смешивают с глицерином и мгновенно замораживают в жидком азоте (например, 0,85 мл культуры смешивают с 0,15 мл глицерина).
[001068] Очищенную плазмиду, содержащую нужный дц-олинонуклеотид, встраивают в клеточную линию (например, линию клеток млекопитающих, HeLa) путем трансфекции. Для трансфекции плазмиды ее очищают до высоких концентраций с применением например, набора Maxi Prep. Плазмидой с применением буфера на основе липидов (например, Липофектамин а2000) трансфицируют клетки, которые высевают при 70% конфлюэнтности. Клетки трансфицируют 3 мкг вектора.
[001069] ПРИМЕР 34: ДОСТАВКА СКОНСТРУИРОВАННОЙ НУКЛЕИНОВОЙ КИСЛОТЫ, КОТОРАЯ НАЦЕЛЕНА НА НУКЛЕИНОВУЮ КИСЛОТУ, НА ОСНОВЕ НАНОЧАСТИЦ
[001070] Получают наночастицу, в которой инкапсулирована нуклеиновая кислота, кодирующая сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту и сайт-специфический полипептид. Наночастицы получают, смешивая ДОФЭ, холестерин (Chol), ДСФЭ-ПЭГ и C16 мПЭГ-керамид в молярном соотношении 18:60:20:1:1 в 10 мл 90% этанола (всего 30 мкмоль липидов). Нуклеиновую кислоту растворяют в 10 мл 20 мМ Tris-буфера (рН 7,4-7,6). После нагревания до 37°С указанные два раствора смешивают с помощью двойного шприцевого насоса, после чего смешанный раствор разбавляют 20 мл 20 мМ Tris-буфера (300 мМ NaCl, рН 7,4-7,6). Смесь инкубируют при 37°С в течение 30 минут и диализируют в 10 мМ ФСБ-буфере (138 мМ NaCI, 2,7 мМ KCl, рН 7,4). Получают стабильные частицы после удаления этанола из смеси путем диализа. Раствор наночастиц концентрируют центрифугированием при 3000 об/мин и температуре 4°С. Через определенное время собирают концентрированную суспензию и стерилизуют фильтрацией через шприцевый фильтр с размером пор 0,22 мкм (Millex-GV, Millipore, США). Получают гомогенную суспензию наночастиц, содержащих нуклеиновую кислоту, кодирующую сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и сайт-специфический полипептид.
[001071] Указанные наночастицы приводят в контакт с клеткой. Наночастица проникает в клетку. Внутри клетки указанная наночастица высвобождает нуклеиновую кислоту, кодирующую сконструированную нуклеиновую кислоту, которая нацелена на нуклеиновую кислоту, и сайт-специфический полипептид. Нуклеиновую кислоту транскрибируют и/или транслируют для получения сконструированной нуклеиновой кислоты, которая нацелена на нуклеиновую кислоту, которая связывается с сайт-специфическим полипептидом с образованием таким образом комплекса. Указанный комплекс нацелен на целевую нуклеиновую кислоту, которая гибридизуется со сконструированной нуклеиновой кислотой, которая нацелена на нуклеиновую кислоту. Указанный комплекс расщепляет указанную целевую нуклеиновую кислоту.
[001072] В некоторых случаях указанная наночастица дополнительно содержит нуклеиновую кислоту, кодирующую донорный полинуклеотид. В тех случаях, когда целевая нуклеиновая кислота расщепляется сайт-специфическим полипептидом, донорный полинуклеотид встраивают в сайт расщепленной целевой нуклеиновой кислоты.
Реферат
Изобретение относится к области биохимии и генной инженерии, в частности к сконструированной одиночной направляющей нуклеиновой кислоте. Указанная нуклеиновая кислота нацелена на нуклеиновую кислоту и способна образовывать комплекс с белком Cas9 CRISPR II типа. Настоящая нуклеиновая кислота содержит последовательность спейсера, дуплекс, линкерную последовательность и последовательность tracr и отличается тем, что не содержит область первого стебля. Изобретение также относится к композиции и к набору, которые содержат указанную нуклеиновую кислоту. Настоящее изобретение позволяет получать сконструированную одиночную направляющую нуклеиновую кислоту, нацеленную на нуклеиновую кислоту и способную образовывать комплекс с белком Cas9 CRISPR II типа. 3 н. и 15 з.п. ф-лы, 42 ил., 8 табл., 34 пр.
Формула
Документы, цитированные в отчёте о поиске
Ген, придающий устойчивость к phytophthora infestans (фитофторозу) в семействе solanaceae

Комментарии