Дифференцирование эмбриональных стволовых клеток человека - RU2587634C2
Код документа: RU2587634C2
Чертежи




Описание
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка истребует приоритет по предварительной заявке на патент США с серийным номером 61/333831, поданной 12 мая 2010 г., которая полностью включена в настоящий документ путем ссылки для любых целей.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение представляет способы стимулирования дифференцирования плюрипотентных стволовых клеток в инсулин-продуцирующие клетки. В частности, настоящее изобретение представляет способ получения популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 50% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Последние достижения в области заместительной клеточной терапии для лечения сахарного диабета 1 типа и нехватка доступных для трансплантации островков Лангерганса стимулировали интерес к разработке источников инсулин-продуцирующих клеток, или β-клеток, подходящих для трансплантации. Одним из подходов является формирование функциональных β-клеток из плюрипотентных стволовых клеток, таких как, например, эмбриональные стволовые клетки.
При эмбриональном развитии позвоночных плюрипотентные клетки дают начало группе клеток, содержащих три зародышевых листка (эктодерму, мезодерму и энтодерму) в ходе процесса, именуемого гаструляцией. Такие ткани, как, например, щитовидная железа, тимус, поджелудочная железа, кишечник и печень, будут развиваться из энтодермы через промежуточную стадию. Промежуточной стадией в данном процессе является образование дефинитивной энтодермы. Клетки дефинитивной энтодермы экспрессируют ряд маркеров, таких как HNF3 бета, GATA4, MIXL1, CXCR4 и SOX 17.
Формирование поджелудочной железы происходит при дифференцировании дефинитивной энтодермы в панкреатическую энтодерму. Клетки панкреатической энтодермы экспрессируют ген панкреатическо-дуоденального гомеобокса, PDX1. При отсутствии PDX1 развитие поджелудочной железы не происходит дальше формирования вентрального и дорзального зачатков. Таким образом, экспрессия PDX1 характеризует критическую стадию органогенеза поджелудочной железы. Зрелая поджелудочная железа содержит, помимо других типов клеток, экзокринную ткань и эндокринную ткань. Экзокринная и эндокринная ткани образуются при дифференцировании панкреатической энтодермы.
По имеющимся данным, клетки, обладающие свойствами островковых клеток, были получены из эмбриональных клеток мыши. Например, в работе Lumelsky et al. (Science 292:1389, 2001) сообщается о дифференцировании мышиных эмбриональных стволовых клеток в инсулин-секретирующие структуры, аналогичные островкам поджелудочной железы. В работе Soria et al. (Diabetes 49:157, 2000) сообщается, что полученные из мышиных эмбриональных стволовых клеток инсулин-секретирующие клетки нормализуют гликемию у мышей с диабетом, вызванным стрептозотоцином.
В одном примере в работе Hori et al. (PNAS 99: 16105, 2002) раскрывается, что обработка мышиных эмбриональных стволовых клеток ингибиторами фосфоинозитид-3-киназы (LY294002) приводила к получению клеток, подобных β-клеткам.
В другом примере в работе Blyszczuk et al. (PNAS 100:998, 2003) сообщается о получении инсулин-продуцирующих клеток из мышиных эмбриональных стволовых клеток с конститутивной экспрессией Pax4.
В работе Micallef et al. сообщается, что ретиноевая кислота может регулировать способность эмбриональных стволовых клеток формировать PDX1-положительную панкреатическую энтодерму. Ретиноевая кислота с наибольшей эффективностью индуцирует экспрессию Pdx1 при добавлении в культуры на 4 день дифференцирования эмбриональной стволовой клетки в течение периода, соответствующего концу гаструляции эмбриона (Diabetes 54:301, 2005).
В работе Miyazaki et al. сообщается о линии мышиных эмбриональных стволовых клеток со сверхэкспрессией PDX1. Результаты авторов показывают, что экспрессия экзогенного PDX1 явно повышает экспрессию генов инсулина, соматостатина, глюкокиназы, нейрогенина 3, p48, Pax6 и HNF6 в образующихся дифференцированных клетках (Diabetes 53: 1030, 2004).
В работе Skoudy et al. сообщается, что активин A (входящий в суперсемейство TGF-β) повышает экспрессию экзокринных панкреатических генов (p48 и амилаза) и эндокринных генов (PDX1, инсулин и глюкагон) в эмбриональных стволовых клетках мыши. Максимальный эффект наблюдали при использовании активина A в концентрации 1 нМ. Авторы также отмечали, что уровень экспрессии инсулина и PDX1 mRNA не зависел от наличия ретиноевой кислоты. Однако обработка с использованием 3 нМ FGF7 привела к повышению уровня транскрипта для PDX1 (Biochem. J. 379: 749, 2004).
В работе Shiraki et al. изучены эффекты факторов роста, специфически ускоряющих дифференцирование эмбриональных стволовых клеток в PDX1-положительные клетки. Авторы отмечали, что TGF-β2 приводил к воспроизводимому увеличению доли PDX1-положительных клеток (Genes Cells, июнь 2005 г.; 10(6): 503-16).
В работе Gordon et al. продемонстрирована индукция образования брахиурических [положительных]/HNF3 бета [положительных] энтодермальных клеток из эмбриональных стволовых клеток мыши в отсутствие сыворотки и в присутствии активина в сочетании с ингибитором сигнального каскада Wnt (патент США № 2006/0003446A1).
В работе Gordon et al. (PNAS, т. 103, стр. 16806, 2006) говорится: «Для образования передней первичной полоски требовались одновременно сигнальные каскады Wnt и TGF-бета/Nodal/активин».
Однако модель развития эмбриональных стволовых клеток на мышах не может в точности имитировать программу развития у высших млекопитающих, например у человека.
В работе Thomson et al. выделяли эмбриональные стволовые клетки из бластоцист человека (Science 282:114, 1998). Параллельно, Gearhart и соавторы получили клеточные линии эмбриональных зародышевых клеток человека (hEG) из ткани половых желез эмбриона (Shamblott et al., Proc. Natl. Acad. Sci. USA 95:13726, 1998). В отличие от эмбриональных стволовых клеток мыши, воспрепятствовать дифференцированию которых можно путем простого культивирования с фактором торможения лейкемии (LIF), эмбриональные стволовые клетки человека необходимо культивировать в крайне специфических условиях (патент США № 6200806; международные заявки на патент №№ 99/20741, 01/51616).
В работе D'Amour et al. описывается производство обогащенных культур дефинитивной энтодермы, производной от эмбриональных стволовых клеток человека, в присутствии высокой концентрации активина и низкой концентрации сыворотки (Nature Biotechnology 2005). Трансплантация этих клеток под почечную капсулу мышей привела к их дифференцированию в более зрелые клетки, обладающие характерными особенностями некоторых энтодермальных органов. Клетки дефинитивной энтодермы, производные от эмбриональных стволовых клеток человека, можно далее дифференцировать в PDX1-положительные клетки после добавления FGF-10 (патент США № 2005/0266554A1).
В работе D'Amour et al. (Nature Biotechnology - 24, 1392-1401 (2006)) говорится: «Мы разработали способ дифференцирования, преобразующий эмбриональные стволовые клетки человека (hES) в эндокринные клетки, способные синтезировать гормоны поджелудочной железы: инсулин, глюкагон, соматостатин, панкреатический полипептид и грелин. Данный способ имитирует органогенез поджелудочной железы in vivo, проводя клетки через стадии, напоминающие образование дефинитивной энтодермы, энтодермы кишечной трубки, панкреатической энтодермы и превращение предшественников эндокринных клеток в клетки, экспрессирующие эндокринные гормоны».
В другом примере в работе Fisk et al. сообщается о системе для производства островковых клеток поджелудочной железы из эмбриональных стволовых клеток человека (патент США № 2006/0040387A1). В данном случае процесс дифференцирования был разделен на три стадии. Сначала эмбриональные стволовые клетки человека были дифференцированы до энтодермы с помощью комбинации бутирата натрия и активина А. Далее клетки культивировали с антагонистами TGF-β, такими как Ноггин, в комбинации с EGF или бетацеллюлином с получением PDX1-положительных клеток. Окончательное дифференцирование индуцировали никотинамидом.
В одном примере в работе Benvenistry et al. сообщается: «Мы делаем вывод, что сверхэкспрессия PDX1 повышала экспрессию панкреатических обогащенных генов, а для индукции экспрессии инсулина могут требоваться дополнительные сигналы, присутствующие только in vivo» (Benvenistry et al., Stem Cells 2006; 24:1923-1930).
В другом примере в работе Grapin-Botton et al. сообщается: «Ранняя активация Ngn3 почти во всех случаях индуцировала глюкагон-положительные клетки, уменьшая при этом количество клеток-предшественников поджелудочной железы. Как и в случае E11.5, предшественники PDX-1 могут дифференцироваться в инсулин-[положительные] и PP-[положительные] клетки» (Johansson KA et al., Developmental Cell 12, 457-465, март 2007 г.).
Например, в работе Diez et al. сообщается: «После 9 и 10 недель большинство глюкагон-положительных клеток одновременно экспрессировали инсулин, хотя на этих стадиях явно обнаруживались и отдельные клетки, экспрессирующие только инсулин. Клетки, одновременно экспрессирующие инсулин и глюкагон, наблюдали в течение всего периода исследования (от 9 до 21 недели), но они представляли лишь небольшую часть от общего количества экспрессирующих инсулин и глюкагон клеток» (J Histochem Cytochem., сентябрь 2009 г.; 57(9):811-24, 13 апреля 2009 г.).
В одном примере в работе Chen et al. сообщается: «(-)-индолактам V [(ILV)] активирует сигнальный каскад протеинкиназы С и задает поджелудочную спецификацию эмбриональных стволовых клеток человека, которые уже были определены для дифференцирования в линии энтодермы...ILV и ретиноевая кислота воздействуют через связанный механизм...ILV демонстрирует более сильную индукцию экспрессирующих PDX-1 клеток (большую процентную долю экспрессирующих PDX-1 клеток), чем ретиноевая кислота» (Nature Chemical Biology 5, 195-196 (апрель 2009 г.) doi:10.1038/nchembio0409-195).
В работе Lyttle et al. сообщается: «NKX6-1 со-локализованы только с инсулиновыми клетками, что указывает на то, что NKX6-1 участвует только в развитии бета-клеток человека» (Diabetologia, июль 2008 г.: 51(7):1169-80, 2008).
Таким образом, сохраняется значительная потребность в разработке лабораторных способов создания функциональной экспрессирующей инсулин клетки, более близкой к β-клетке. Настоящее изобретение представляет альтернативный подход к повышению эффективности дифференцирования эмбриональных стволовых клеток человека в экспрессирующие инсулин клетки путем генерирования популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 50% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1.
КРАТКОЕ ОПИСАНИЕ
В одном варианте осуществления настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 50% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1.
В одном варианте осуществления настоящее изобретение представляет способ дифференцирования популяции плюрипотентных стволовых клеток в популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, содержащий следующие стадии:
а. культивирование популяции плюрипотентных стволовых клеток;
b. дифференцирование популяции плюрипотентных стволовых клеток в популяцию клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы; и
c. дифференцирование популяции клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы, в популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, посредством обработки популяции клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы, средой, в которую добавлен активатор протеинкиназы С.
В одном варианте осуществления более 50% клеток в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, которые получены способами, составляющими предмет настоящего изобретения, одновременно экспрессируют PDX-1 и NKX6.1.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фигурах 1A и 1B приведены данные по экспрессии PDX1, NKX6.1 и ISL-1 на стадии 4, день 4, протокола дифференцирования, приведенного в примере 1. На фиг. 1A приведены данные по экспрессии PDX1 и NKX6.1. На фиг. 1B приведены данные по экспрессии NKX6.1 и ISL-1.
На фигурах 2A и 2B показан эффект обработки активатором протеинкиназы С (PKC) на долю клеток, экспрессирующих PDX1, NKX6.1 и CDX2, анализируемый с помощью анализатора IN Cell Analyzer 1000 (фиг. 2A), а также сравнение различных активаторов PKC и эффектов их воздействия на долю клеток, экспрессирующих PDX1 и NKX6.1, по данным, полученным на анализаторе IN Cell Analyzer (фиг. 2B).
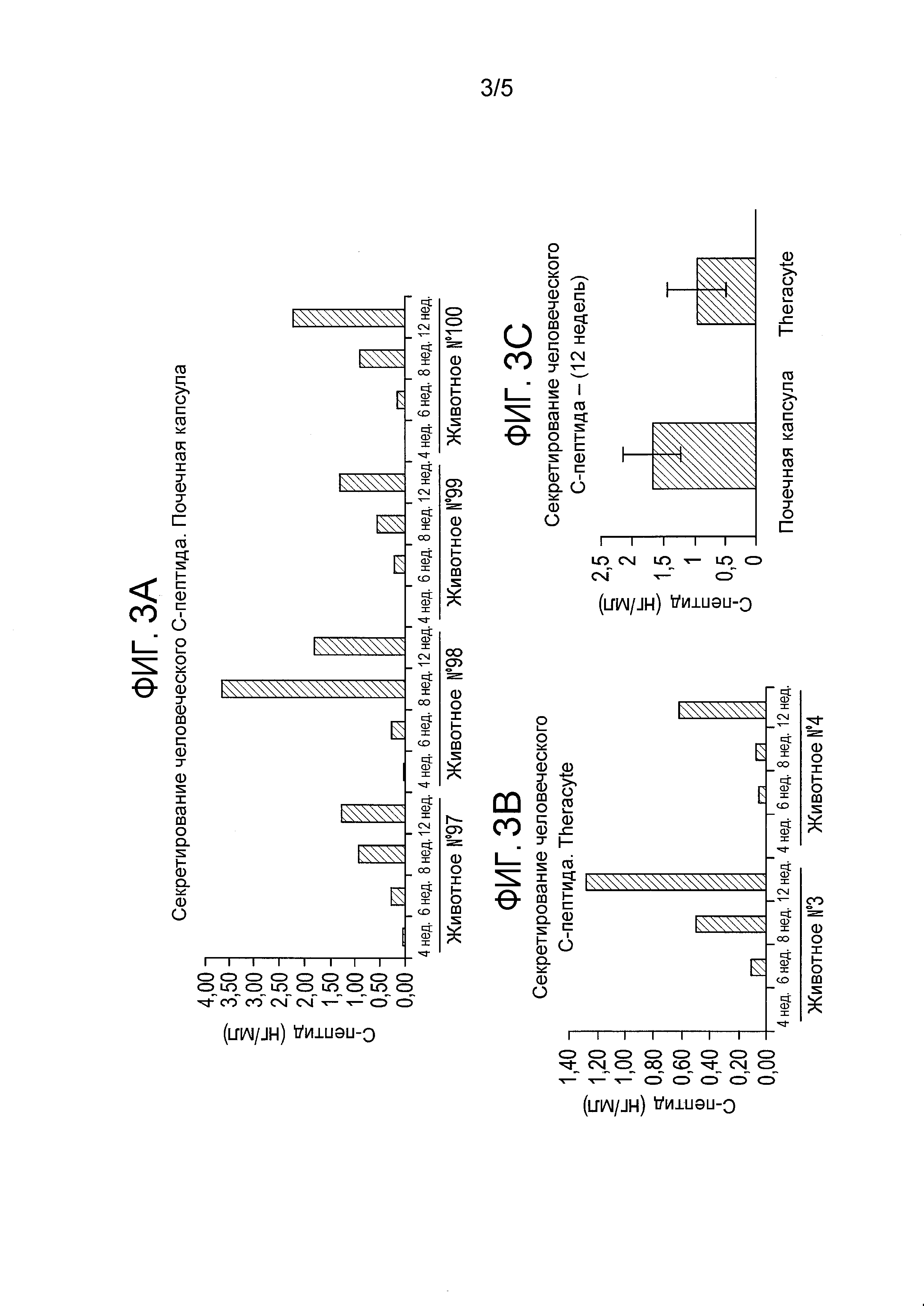
На фигурах 3A, 3B и 3C приведены уровни циркулирующего C-пептида у мышей линии SCID с врожденным отсутствием клеток-киллеров, которым вводили клетки, составляющие предмет настоящего изобретения, под почечную капсулу (фиг. 3A) и через имплантированное под кожу устройство Theracyte (фиг. 3B). Уровни C-пептида регистрировали в указанные моменты времени. На фиг. 3C показано сравнение уровней С-пептида, наблюдаемых в группе, получавшей клетки под почечную капсулу, и группе, получавшей клетки через подкожное устройство Theracyte, через 12 недель после трансплантации.
На фигурах 4A, 4B, 4C и 4D показан эффект обработки активатором PKC на экспрессию PDX1, NKX6.1, NGN3 и PTF1 альфа в клетках, обработанных в соответствии со способами, описанными в примере 3.
На фигурах 5A, 5B, 5C и 5D показан эффект FGF7 на экспрессию NKX6.1, PDX1, PTF1 альфа и CDX2 в клетках, обработанных в соответствии со способами, описанными в примере 4.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Для ясности описания, а не для ограничения изобретения, подробное описание настоящего изобретения разделено на следующие подразделы, описывающие или иллюстрирующие определенные особенности, варианты осуществления или области применения настоящего изобретения.
Определения
Стволовые клетки представляют собой недифференцированные клетки, определяемые по их способности на уровне единичной клетки как самообновляться, так и дифференцировать с образованием клеток-потомков, таких как самообновляющиеся клетки-предшественники, необновляющиеся клетки-предшественники и окончательно дифференцированные клетки. Стволовые клетки также характеризуются способностью дифференцироваться in vitro в функциональные клетки различных клеточных линий дифференцирования из множества зародышевых листков (энтодермы, мезодермы и эктодермы), а также после трансплантации давать начало тканям, происходящим от множества зародышевых листков, и по существу способствовать формированию большинства, если не всех, тканей после инъекции в бластоцисты.
Стволовые клетки классифицируют по потенциалу развития следующим образом: (1) тотипотентные, способные преобразоваться в любой из эмбриональных и внеэмбриональных типов клеток; (2) плюрипотентные, способные преобразоваться во все типы эмбриональных клеток; (3) мультипотентные, способные преобразоваться во множество клеточных линий, но в рамках одной ткани, органа или физиологической системы (например, гемопоэтические стволовые клетки (ГСК) могут порождать ГСК (самообновление), олигопотентные ограниченные клетки-предшественники крови и все типы клеток и элементы (например, тромбоциты), являющиеся стандартными составляющими крови); (4) олигопотентные, способные преобразоваться в более ограниченное подмножество клеточных линий, чем мультипотентные стволовые клетки; и (5) унипотентные, способные преобразоваться в единственную клеточную линию (например, сперматогенные стволовые клетки).
Дифференцирование представляет собой процесс, при помощи которого неспециализированная («некоммитированная») или менее специализированная клетка приобретает свойства специализированной клетки, например, нервной или мышечной клетки. Дифференцированная клетка или клетка с индуцированным дифференцированием представляет собой клетку, занявшую более специализированное («коммитированное») положение в линии дифференцирования клетки. Термин «коммитированная» применительно к процессу дифференцирования обозначает клетку, дошедшую в ходе процесса дифференцирования до стадии, от которой в нормальных условиях она продолжит дифференцироваться до определенного типа клеток или множества типов клеток и не сможет в нормальных условиях дифференцироваться в иной тип клеток или вернуться обратно к менее дифференцированному типу. Дедифференцированием называется процесс, в ходе которого клетка возвращается к менее специализированному (или коммитированному) положению в линии дифференцирования. Используемый в настоящей заявке термин «линия дифференцирования клетки» определяет наследственность клетки, то есть определяет, из какой клетки произошла данная клетка и каким клеткам она может дать начало. В линии дифференцирования клетка помещается в наследственную схему развития и дифференцирования. Маркером, специфичным для линии дифференцирования, называется характерная особенность, специфически ассоциированная с фенотипом клеток конкретной линии дифференцирования, которую можно использовать для оценки дифференцирования некоммитированной клетки данную линию дифференцирования.
Используемые в настоящей заявке термины «клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы», «клетки стадии 1» или «стадия 1», относятся к клеткам, экспрессирующим по меньшей мере один из следующих маркеров: SOX17, GATA4, HNF3 бета, GSC, CER1, Nodal, FGF8, Brachyury, Mix-подобный гомеобоксный белок, FGF4 CD48, эомезодермин (EOMES), DKK4, FGF17, GATA6, CXCR4, C-Kit, CD99 или OTX2. Клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, включают в себя клетки-предшественники клеток первичной полоски, клетки первичной полоски, клетки мезоэнтодермы и клетки дефинитивной энтодермы.
Термин «клетки, экспрессирующие маркеры, характерные для линии панкреатической энтодермы» в настоящем документе обозначает клетки, экспрессирующие по меньшей мере один из следующих маркеров: PDX1, NKX6.1, HNF1 бета, PTF1 альфа, HNF6, HNF4 альфа, SOX9, HB9 или PROX1. Клетки, экспрессирующие маркеры, характерные для линии панкреатической энтодермы, включают в себя клетки панкреатической энтодермы, клетки первичной кишечной трубки и поздние клетки передней кишки.
Используемый в настоящей заявке термин «дефинитивная энтодерма» относится к клеткам, обладающим характерными особенностями клеток, происходящих в ходе гаструляции от эпибласта, и формирующим желудочно-кишечный тракт и его производные. Клетки дефинитивной энтодермы экспрессируют следующие маркеры: HNF3 бета, GATA4, SOX17, Cerberus, OTX2, goosecoid, C-Kit, CD99 и MIXL1.
Используемый в настоящей заявке термин «маркеры» означает молекулы нуклеиновых кислот или полипептидов с дифференциальной экспрессией в интересующих клетках. В данном контексте под дифференциальной экспрессией подразумевается повышение уровня экспрессии для положительного маркера и понижение уровня экспрессии для отрицательного маркера. Поддающийся обнаружению уровень маркерной нуклеиновой кислоты или полипептида в интересующих клетках оказывается значительно выше или ниже по сравнению с другими клетками, что позволяет выявлять интересующую клетку и отличать ее от других клеток с помощью любого из множества известных в данной области способов.
Используемые в настоящей заявке термины «панкреатическая эндокринная клетка», или «клетка, экспрессирующая гормон поджелудочной железы», или «клетка, экспрессирующая маркеры, характерные для линии панкреатических эндокринных клеток», относятся к клетке, способной экспрессировать по меньшей мере один из следующих гормонов: инсулин, глюкагон, соматостатин и панкреатический полипептид.
Выделение, размножение и культивирование плюрипотентных стволовых клеток
Характеристика плюрипотентных стволовых клеток
Плюрипотентные стволовые клетки могут экспрессировать один или более стадиеспецифических эмбриональных антигенов (SSEA) 3 и 4, а также маркеры, определяемые антителами, обозначаемыми как Tra-1-60 и Tra-1-81 (Thomson et al., Science 282:1145, 1998 г.). Дифференцирование плюрипотентных стволовых клеток in vitro приводит к потере экспрессии SSEA-4, Tra 1-60 и Tra 1-81 (при наличии) и к повышению экспрессии SSEA-1. В недифференцированных плюрипотентных стволовых клетках, как правило, активна щелочная фосфатаза, которую можно обнаружить путем фиксации клеток с помощью 4% параформальдегида, с последующим обнаружением с помощью Vector Red, применяемого в качестве субстрата, в соответствии с инструкциями производителя (Vector Laboratories, г. Берлингейм, штат Калифорния). Недифференцированные плюрипотентные стволовые клетки также, как правило, экспрессируют OCT4 и TERT, определяемые с помощью ОТ-ПЦР.
Другим желательным фенотипическим свойством выращенных плюрипотентных стволовых клеток является потенциал дифференцирования в клетки всех трех зародышевых листков: в энтодермальные, мезодермальные и эктодермальные ткани. Плюрипотентность плюрипотентных стволовых клеток может быть подтверждена, например, путем инъекции клеток мышам с тяжелым комбинированным иммунодефицитом (SCID), фиксирования образующихся тератом с помощью 4% параформальдегида и их гистологического исследования для получения доказательств наличия клеточных типов, происходящих от трех зародышевых листков. В альтернативном варианте осуществления плюрипотентность можно определить по образованию эмбриоидных тел и их анализа на предмет присутствия маркеров, которые ассоциируются с тремя зародышевыми листками.
Выращенные линии плюрипотентных стволовых клеток могут быть кариотипированы с применением стандартного способа окрашивания с использованием красителя Гимза и сравнения с опубликованными кариотипами соответствующих видов приматов. Желательно получить клетки, имеющие «нормальный кариотип», то есть эуплоидные клетки, в которых все человеческие хромосомы присутствуют и не имеют видимых изменений.
Источники плюрипотентных стволовых клеток
К типам плюрипотентных стволовых клеток, которые можно использовать, относятся устойчивые линии плюрипотентных клеток, получаемые из ткани, формируемой после вынашивания плода, в том числе из преэмбриональной ткани (такой как бластоциста), эмбриональной ткани или ткани плода, взятой в любой момент в период вынашивания, как правило, но не обязательно, до срока приблизительно 10-12 недель беременности. Неограничивающими примерами являются устойчивые линии эмбриональных стволовых клеток человека или эмбриональных зародышевых клеток человека, например, линии эмбриональных стволовых клеток человека H1, H7 и H9 (WiCell). Также возможно использование описываемых в настоящей заявке композиций во время первоначального установления или стабилизации таких клеток. В этом случае исходными клетками являются первичные плюрипотентные клетки, взятые напрямую из тканей-источников. Целям настоящего изобретения также соответствуют клетки, взятые из популяции плюрипотентных стволовых клеток, уже культивированных в отсутствие питающих клеток. Целям настоящего изобретения также соответствуют линии мутантных эмбриональных стволовых клеток человека, такие как BG01v (BresaGen, г. Афины, штат Джорджия).
В одном варианте осуществления эмбриональные стволовые клетки человека готовят, как описано в работе Thomson et al. (патент США № 5843780; Science 282:1145, 1998; Curr. Top. Dev. Biol. 38:133 ff., 1998; Proc. Natl. Acad. Sci. U.S.A. 92:7844, 1995).
Культивирование плюрипотентных стволовых клеток
В одном варианте осуществления плюрипотентные стволовые клетки культивируют на слое питающих клеток, которые поддерживают плюрипотентные стволовые клетки в различных отношениях. В альтернативном варианте осуществления плюрипотентные стволовые клетки культивируют в культуральной системе, по существу не содержащей питающих клеток, но, тем не менее, поддерживающей пролиферацию плюрипотентных стволовых клеток и не допускающей существенного дифференцирования. Рост плюрипотентных стволовых клеток в не содержащей питающих клеток культуральной системе без дифференцирования поддерживается путем использования среды, кондиционированной предварительным культивированием клеток иного типа. В альтернативном варианте осуществления рост плюрипотентных стволовых клеток в не содержащей питающих клеток культуральной системе без дифференцирования поддерживается путем использования среды с химически определенным составом.
В одном варианте осуществления плюрипотентные стволовые клетки можно культивировать на слое питающих клеток фибробластов эмбриона мыши в соответствии со способами, изложенными в работе Reubinoff et al. (Nature Biotechnology 18: 399-404 (2000)). В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать на слое питающих клеток фибробластов эмбриона мыши в соответствии со способами, изложенными в работе Thompson et al. (Science 6, ноябрь 1998 г.: т. 282, № 5391, стр. 1145-1147). В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать на любом из слоев питающих клеток, раскрытых в работе Richards et al, (Stem Cells 21: 546-556, 2003).
В одном варианте осуществления плюрипотентные стволовые клетки можно культивировать на слое питающих клеток человека в соответствии со способами, изложенными в работе Wang et al. (Stem Cells 23: 1221-1227, 2005). В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать на слое питающих клеток человека, раскрытых в работе Stojkovic et al. (Stem Cells 2005 23: 306-314, 2005). В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать на слое питающих клеток человека, раскрытых в работе Miyamoto et al. (Stem Cells 22: 433-440, 2004). В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать на слое питающих клеток человека, раскрытых в работе Amit et al. (Biol. Reprod 68: 2150-2156, 2003). В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать на слое питающих клеток человека, раскрытых в работе Inzunza et al. (Stem Cells 23: 544-549, 2005).
В одном варианте осуществления плюрипотентные стволовые клетки можно культивировать в культуральной среде, полученной в соответствии со способами, представленными в патенте США № 20020072117. В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в культуральной среде, полученной в соответствии со способами, представленными в патенте США № 6642048. В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в культуральной среде, полученной в соответствии со способами, представленными в международном патенте WO2005014799. В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в культуральной среде, полученной в соответствии со способами, представленными в работе Xu et al. (Stem Cells 22: 972-980, 2004). В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в культуральной среде, полученной в соответствии со способами, представленными в патенте США № 20070010011. В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в культуральной среде, полученной в соответствии со способами, представленными в патенте США № 20050233446. В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в культуральной среде, полученной в соответствии со способами, представленными в патенте США № 6800480. В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в культуральной среде, полученной в соответствии со способами, представленными в международном патенте WO2005065354.
В одном варианте осуществления плюрипотентные стволовые клетки можно культивировать в соответствии со способами, представленными в работе Cheon et al. (BioReprod DOI:10.1095/biolreprod. 105.046870, 19 октября 2005 г.). В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в соответствии со способами, представленными в работе Levenstein et al. (Stem Cells 24: 568-574, 2006). В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в соответствии со способами, представленными в патенте США № 20050148070. В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в соответствии со способами, представленными в патенте США № 20050244962. В альтернативном варианте осуществления плюрипотентные стволовые клетки можно культивировать в соответствии со способами, представленными в международной заявке на патент № WO2005086845.
Плюрипотентные стволовые клетки могут быть высеяны на соответствующий культуральный субстрат. В одном варианте осуществления соответствующим культуральным субстратом является компонент внеклеточного матрикса, такой как, например, полученный из базальной мембраны или тот, который может участвовать в лиганд-рецепторном взаимодействии с участием молекулы адгезивного слоя. В одном варианте осуществления соответствующим культуральным субстратом является MATRIGEL® (Becton Dickenson). MATRIGEL® представляет собой растворимый препарат из клеток опухоли Энгельбрета-Холма-Суорма, который при комнатной температуре превращается в гель и образует восстановленную базальную мембрану.
В качестве альтернативы можно использовать другие компоненты внеклеточного матрикса и смеси компонентов. В зависимости от типа пролиферирующих клеток, последние могут включать в себя ламинин, фибронектин, протеогликан, энтактин, гепарансульфат и т.п., по отдельности или в различных комбинациях.
Плюрипотентные стволовые клетки могут быть высеяны на субстрат с соответствующим распределением по поверхности и в присутствии среды, поддерживающей выживаемость, размножение и сохранение требуемых характеристик клеток. Все эти характеристики улучшаются при тщательном подходе к распределению клеток при посеве и могут быть определены специалистом в данной области.
Соответствующая культуральная среда может быть изготовлена, например, из следующих компонентов: модифицированная по способу Дульбекко среда Игла (DMEM), Gibco № 11965-092, нокаутная модифицированная по способу Дульбекко среда Игла (KO DMEM), Gibco № 10829-018, основная среда Хэма F12/50% DMEM, 200 мМ L-глутамина, Gibco № 15039-027; раствор неосновных аминокислот, Gibco 11140-050; β-меркаптоэтанол, Sigma № M7522; рекомбинантный основной фактор роста фибробластов человека (bFGF), Gibco № 13256-029.
Формирование клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, из плюрипотентных стволовых клеток
В одном варианте осуществления настоящее изобретение представляет способ получения популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы из плюрипотентных стволовых клеток, содержащий следующие стадии:
а. культивирование популяции плюрипотентных стволовых клеток;
b. дифференцирование популяции плюрипотентных стволовых клеток в популяцию клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы; и
c. дифференцирование популяции клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы, в популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, посредством обработки популяции клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы, средой, в которую добавлен активатор протеинкиназы С.
В одном аспекте настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 50% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1. В альтернативном варианте осуществления настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 60% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1. В альтернативном варианте осуществления настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 70% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1. В альтернативном варианте осуществления настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 80% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1. В альтернативном варианте осуществления настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 90% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1.
В одном аспекте настоящего изобретения популяция клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, можно дополнительно обрабатывать для получения популяции клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток.
Эффективность дифференцирования может быть определена путем обработки популяции клеток агентом (например, антителом), специфически распознающим белковый маркер, экспрессированный клетками, экспрессирующими маркеры, характерные для желательного вида клеток.
Способы оценки экспрессии маркеров белков и нуклеиновых кислот в культивированных или выделенных клетках являются стандартными для данной области. К подобным способам относятся количественная полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР), Нозерн-блоттинг, гибридизация in situ (см., например, Current Protocols in Molecular Biology (под ред. Ausubel et al., 2001, доп.)), а также способы иммунологического анализа, такие как иммуногистохимический анализ среза материала, Вестерн-блоттинг, а для маркеров, доступных в интактных клетках, - способ проточной цитометрии (FACS) (см., например, Harlow and Lane, Using Antibodies: A Laboratory Manual, New York: Cold Spring Harbor Laboratory Press (1998)).
Характеристики плюрипотентных стволовых клеток хорошо известны специалистам в данной области, и продолжается выявление дополнительных характеристик плюрипотентных стволовых клеток. К маркерам плюрипотентных стволовых клеток относится, например, экспрессия одного или более из следующих маркеров: ABCG2, CRIPTO, FOXD3, CONNEXIN43, CONNEXIN45, OCT4, SOX2, NANOG, hTERT, UTF1, ZFP42, SSEA-3, SSEA-4, Tra 1-60, Tra 1-81.
После обработки плюрипотентных стволовых клеток с применением способов, составляющих предмет настоящего изобретения, дифференцированные клетки могут быть очищены путем воздействия на популяцию клеток агентом (например, антителом), специфически распознающим белковый маркер, например, CXCR4, экспрессируемый клетками, экспрессирующими маркеры, характерные для линии дефинитивной энтодермы.
К плюрипотентным стволовым клеткам, допустимым для использования в целях настоящего изобретения, относятся, например, эмбриональные стволовые клетки человека линии H9 (код NIH: WA09), эмбриональные стволовые клетки человека линии H1 (код NIH: WA01), эмбриональные стволовые клетки человека линии H7 (код NIH: WA07) и эмбриональные стволовые клетки человека линии SA002 (Cellartis, Швеция). Также целям настоящего изобретения соответствуют клетки, экспрессирующие по меньшей мере один из следующих маркеров, характерных для плюрипотентных клеток: ABCG2, CRIPTO, CD9, FOXD3, CONNEXIN43, CONNEXIN45, OCT4, SOX2, NANOG, hTERT, UTF1, ZFP42, SSEA-3, SSEA-4, Tra 1-60 и Tra 1-81.
Маркеры, характерные для линии дефинитивной энтодермы, выбраны из группы, состоящей из SOX17, GATA4, HNF3 бета, GSC, CER1, Nodal, FGF8, Brachyury, Mix-подобного гомеобоксного белка, FGF4, CD48, эомезодермина (EOMES), DKK4, FGF17, GATA6, CXCR4, C-Kit, CD99 и OTX2. Целям настоящего изобретения соответствует клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии дефинитивной энтодермы. В одном аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии дефинитивной энтодермы, представляет собой клетку-предшественник первичной полоски. В другом аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии дефинитивной энтодермы, представляет собой мезэнтодермальную клетку. В другом аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии дефинитивной энтодермы, представляет собой клетку дефинитивной энтодермы.
Маркеры, характерные для линии панкреатической энтодермы, выбраны из группы, состоящей из PDX1, NKX6.1, HNF1 бета, PTF1 альфа, HNF6, HNF4 альфа, SOX9, HB9 и PROX1. Целям настоящего изобретения соответствует клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии панкреатической энтодермы. В одном аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии панкреатической энтодермы, представляет собой клетку панкреатической энтодермы.
Маркеры, характерные для линии панкреатических эндокринных клеток, выбраны из группы, состоящей из NGN3, NEUROD, NKX2.2, PDX1, NKX6.1, PAX4 и PAX6. В одном варианте осуществления панкреатическая эндокринная клетка способна к экспрессии по меньшей мере одного из следующих гормонов: инсулина, глюкагона, соматостатина и панкреатического полипептида. Целям настоящего изобретения соответствует клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии панкреатических эндокринных клеток. В одном аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии панкреатических эндокринных клеток, представляет собой панкреатическую эндокринную клетку. Панкреатическая эндокринная клетка может представлять собой панкреатическую клетку, экспрессирующую гормоны. В альтернативном варианте осуществления панкреатическая эндокринная клетка может представлять собой панкреатическую клетку, секретирующую гормоны.
В одном аспекте настоящего изобретения панкреатическая эндокринная клетка представляет собой клетку, экспрессирующую маркеры, характерные для линии дифференцирования β-клеток. Клетка, экспрессирующая маркеры, характерные для линии дифференцирования β-клеток, экспрессирует PDX1 и по меньшей мере один из следующих транскрипционных факторов: NGN3, NKX2.2, NKX6.1, NEUROD, ISL1, HNF3 бета, MAFA, PAX4 и PAX6. В одном аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии дифференцирования β-клеток, представляет собой β-клетку.
Дифференцирование плюрипотентных стволовых клеток в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы.
Образование клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы, может быть выявлено путем проверки на наличие маркеров до и после выполнения конкретного протокола. Плюрипотентные стволовые клетки, как правило, не экспрессируют такие маркеры. Таким образом, дифференцирование плюрипотентных клеток определяется по началу экспрессии таких маркеров.
Плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, с использованием любого известного специалистам способа или с использованием любого способа, предложенного в настоящем изобретении.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, способами, описанными в работе D'Amour et al., Nature Biotechnology 23, 1534-1541 (2005).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, способами, описанными в работе Shinozaki et al., Development 131, 1651-1662 (2004).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, способами, описанными в работе McLean et al., Stem Cells 25, 29-38 (2007).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, способами, описанными в работе D'Amour et al., Nature Biotechnology 24, 1392-1401 (2006).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 11/736908.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 11/779311.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 60/990529.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 61/076889.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 61/076900.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 61/076908.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии дефинитивной энтодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 61/076915.
Дифференцирование клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы, в клетки, экспрессирующие маркеры, характерные для линии панкреатической энтодермы
В одном варианте осуществления настоящее изобретение представляет способ получения популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы из плюрипотентных стволовых клеток, содержащий следующие стадии:
а. культивирование популяции плюрипотентных стволовых клеток;
b. дифференцирование популяции плюрипотентных стволовых клеток в популяцию клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы; и
c. дифференцирование популяции клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы, в популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, посредством обработки популяции клеток, экспрессирующих маркеры, характерные для линии дефинитивной энтодермы, средой, в которую добавлен активатор протеинкиназы С.
В одном аспекте настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 50% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1. В альтернативном варианте осуществления настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 60% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1. В альтернативном варианте осуществления настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 70% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1. В альтернативном варианте осуществления настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 80% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1. В альтернативном варианте осуществления настоящее изобретение представляет популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, причем более 90% клеток в популяции одновременно экспрессируют PDX-1 и NKX6.1.
В одном варианте осуществления активатор протеинкиназы С выбран из группы, состоящей из (2S, 5S)-(E, E)-8-(5-(4-(трифторметил)фенил)-2,4-пентадиемоиламино)бензолактама, индолактама V (ILV), форбол-12-миристат-13-ацетата (PMA) и форбол-12,13-дибутирата (PDBu). В одном варианте осуществления активатор протеинкиназы С представляет собой (2S, 5S)-(E, E)-8-(5-(4-(трифторметил)фенил)-2,4-пентадиемоиламино)бензолактам. (2S, 5S)-(E, E)-8-(5-(4-(Трифторметил)фенил)-2,4-пентадиемоиламино)бензолактам можно использовать в концентрации от приблизительно 20 нМ до приблизительно 500 нМ. (2S, 5S)-(E, E)-8-(5-(4-(Трифторметил)фенил)-2,4-пентадиемоиламино)бензолактам в настоящем документе называется «TPB».
В одном варианте осуществления в среду, в которую добавлен активатор протеинкиназы С, дополнительно добавлен по меньшей мере один фактор, выбранный из группы, состоящей из фактора, способного ингибировать BMP, ингибитора сигнального каскада рецепторов TGFβ, а также фактора роста фибробластов.
В одном варианте осуществления фактор, способный ингибировать BMP, представляет собой Ноггин. Ноггин можно использовать в концентрации от приблизительно 50 нг/мл до приблизительно 500 нг/мл. В одном варианте осуществления Ноггин используют в концентрации 100 нг/мл.
В одном варианте осуществления ингибитор сигнального каскада рецептора TGFβ представляет собой ингибитор ALK5. В одном варианте осуществления ингибитор ALK5 представляет собой ингибитор ALK5 II. Ингибитор ALK5 II можно использовать в концентрации от приблизительно 0,1 мкМ до приблизительно 10 мкМ. В одном варианте осуществления ингибитор ALK5 II используют в концентрации 1 мкМ.
В одном варианте осуществления фактор роста фибробластов представляет собой FGF7. В альтернативном варианте осуществления фактор роста фибробласта представляет собой FGF10.
В одном варианте осуществления фактор роста фибробластов можно использовать в концентрации от приблизительно 50 пг/мл до приблизительно 50 мкг/мл. В одном варианте осуществления фактор роста фибробластов используют в концентрации 50 нг/мл.
Дифференцирование клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток
В одном варианте осуществления популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, дополнительно дифференцируются в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток, с использования любого способа, известного специалистам в данной области.
Например, популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, могут быть дополнительно дифференцированы в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, в соответствии со способами, представленными в работе D' Amour et al., Nature Biotechnology, 2006.
Например, популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, могут быть дополнительно дифференцированы в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, в соответствии со способами, представленными в работе D' Amour et al., Nature Biotechnology, 2006.
Например, популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, могут быть дополнительно дифференцированы в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, в соответствии со способами, представленными в заявке на патент США № 11/736908.
Например, популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, могут быть дополнительно дифференцированы в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, в соответствии со способами, представленными в заявке на патент США № 11/779311.
Например, популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, могут быть дополнительно дифференцированы в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, в соответствии со способами, представленными в заявке на патент США № 60/953178.
Например, популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, могут быть дополнительно дифференцированы в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, в соответствии со способами, представленными в заявке на патент США № 60/990529.
Например, популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, могут быть дополнительно дифференцированы в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, в соответствии со способами, представленными в заявке на патент США № 61/289671.
Настоящее изобретение далее без ограничений иллюстрируется следующими примерами.
ПРИМЕРЫ
Пример 1
Формирование популяции клеток, составляющих предмет настоящего изобретения
Клетки линии эмбриональных стволовых клеток человека H1 культивировали в покрытых MATRIGEL® (разведение 1:30) (BD Biosciences; № по кат. 356231) чашках со средой RPMI (Invitrogen, № по кат. 22400) + 0,2% FBS + 100 нг/мл активина A (PeproTech; № по кат. 120-14) + 20 нг/мл WNT-3a (R&D Systems; № по кат. 1324-WN/CF) в течение одного дня, с последующей обработкой средой RPMI, дополненной 0,5% FBS + 100 нг/мл активина A в течение еще двух дней (стадия 1), затем
а. DMEM/F12 + 2% FBS + 50 нг/мл FGF7 в течение трех дней (стадия 2), затем
b. DMEM с высоким содержанием глюкозы + 1% B27 + 0,25 мкМ циклопамин-KAAD + 2 мкМ ретиноевой кислоты (RA) + 100 нг/мл Ноггина в течение четырех дней (стадия 3), затем либо
c. обработка 1: DMEM с высоким содержанием глюкозы + 1% B27 в течение четырех дней (стадия 4 - основная среда - BM), либо
d. обработка 2: DMEM с высоким содержанием глюкозы + 1% B27 + 100 нг/мл Ноггина + 1 мкМ ингибитора ALK5 II в течение четырех дней (стадия 4), либо
e. обработка 3: DMEM с высоким содержанием глюкозы + 1% B27 + 100 нг/мл Ноггина + 1 мкМ ингибитора ALK5 II + 20 нм форбол-12,13-дибутирата (PDBu) (Calbiochem, № по кат. 524390) в течение четырех дней (стадия 4).
Образцы культур отбирали в дублях на стадии 4, день 4, и получали их изображения с помощью анализатора IN Cell Analyzer 1000 (GE Healthcare). Для компенсации возможных потерь клеток в ходе процедур анализа и последующего окрашивания для каждой лунки снимали по 100 проекций. Для каждой лунки с использованием программного обеспечения IN Cell Developer Toolbox 1.7 (GE Healthcare) измеряли общее количество клеток, общее количество клеток, экспрессирующих PDX1, общее количество клеток, экспрессирующих NKX6.1, и общее количество клеток, экспрессирующих CDX-2. Для каждой повторной совокупности данных рассчитали средние значения и стандартные отклонения. Общие количества клеток, экспрессирующих PDX 1, NKX6.1 и CDX-2, приведены в процентах от общей популяции клеток.
Как показано на фиг. 2A, во всех экспериментальных популяциях в конце стадии 4, день 4, приблизительно 92%±4% клеток в популяции экспрессировали PDX 1. При этом обработка PDBu (активатор протеинкиназы C) вызвала значительное увеличение доли клеток, экспрессирующих NKX6.1, в популяции, экспрессирующей PDX1 (фиг. 2A), по сравнению с популяциями клеток, обработанных либо основной средой (обработка 1), либо ингибитором ALK5 II в присутствии Ноггина (обработка 2). В группе, обработанной PDBu, 88%±4,2% от всей популяции экспрессировали NKX6.1, тогда как при обработке 2 NKX6.1 экспрессировали 62%±8% клеток, а при обработке 1 NKX6.1 экспрессировали 46,7%±0,2% клеток. Большинство экспрессирующих NKX6.1 клеток на стадии 4 также экспрессировали PDX1. Эти наблюдения подтверждаются наложением изображений экспрессии PDX1 и NKX6.1, полученных для конкретной популяции клеток (фиг. 1A). Приведенные данные показывают, что обработка клеток средой с добавлением активатора протеинкиназы С увеличила процент клеток, одновременно экспрессирующих PDX1 и NKX6.1, в популяции клеток, которые экспрессируют маркеры, характерные для линии панкреатической энтодермы.
В популяции клеток, прошедших обработку 1, 10% клеток экспрессировали CDX2 (маркер ткани кишечника) (фиг. 2A). В популяциях клеток, прошедших обработку 2 или 3, CDX2 экспрессировали менее 5% клеток. Во всех случаях большинство клеток, экспрессировавших CDX2, не экспрессировали одновременно PDX1 и NKX6.1.
Параллельные популяции клеток стадии 3 также обрабатывали следующими активаторами протеинкиназы С: форбол-12-миристат-13-ацетат (PMA) с концентрацией 20 нМ (Calbiochem № 524400) или [(2S, 5S)-(E, E)-8-(5-(4-(трифторметил)фенил)-2,4-пентадиеноиламино)бензолактам] (TPB) с концентрацией 50 нМ (Calbiochem № 565740), которые были использованы вместо PDBu при указанной выше обработке 3. В конце стадии 4, день 4, 91% клеток в популяции, обрабатываемой PMA, и 90% клеток в популяции, обрабатываемой TPB, экспрессировали NKX6.1. Для общего количества клеток, экспрессировавших PDX1, при всех вариантах обработки значительных различий не наблюдали. См. фиг. 2B.
Приведенный пример показывает, что активаторы протеинкиназы C можно использовать при сравнительно низких концентрациях, чтобы стимулировать повышение экспрессии NKX6.1 и увеличить процент клеток, одновременно экспрессирующих PDX1 и NKX6.1, в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы.
Пример 2
Имплантация клеток, составляющих предмет настоящего изобретения, мышам с врожденным отсутствием естественных клеток-киллеров с тяжелым комбинированным иммунодефицитом (SCID-Bg)
Клетки линии эмбриональных стволовых клеток человека H1 культивировали в покрытых MATRIGEL® (разведение 1:30) чашках со средой RPMI + 0,2% FBS + 100 нг/мл активина A + 20 нг/мл WNT-3a в течение одного дня с последующей обработкой средой RPMI + 0,5% FBS + 100 нг/мл активина A в течение еще двух дней (стадия 1), затем
а. DMEM/F12 + 2% FBS + 50 нг/мл FGF7 в течение трех дней (стадия 2), затем
b. DMEM с высоким содержанием глюкозы + 1% B27 + 0,25 мкМ циклопамин-KAAD + 2 мкМ ретиноевой кислоты (RA) + 100 нг/мл Ноггина в течение четырех дней (стадия 3), затем
c. DMEM с высоким содержанием глюкозы + 1% B27 + 100 нг/мл Ноггина + 1 мкМ ингибитора ALK5 II + 50 нМ TPB в течение четырех дней (стадия 4).
Мышей линии SCID-Bg (С.B-Igh-1b/GbmsTac-Prkdcscid-Lystbg N7) возрастом от пяти до шести недель приобрели в компании Taconic Farms. Мышей содержали в клетках-микроизоляторах со свободным доступом к стерилизованной пище и воде. В ходе подготовки к хирургической операции мыши были помечены нанесенной на ухо идентификационной меткой, у них была измерена масса тела, а также содержание глюкозы в крови с помощью ручного глюкометра (LifeScan, One Touch).
Мышей анестезировали смесью изофлурана и кислорода и на операционном поле выстригли шерсть малыми ножницами для животных. Перед операцией мышам подкожно ввели 0,1 мг/кг Buprenex. Операционное поле подготовили последовательным промыванием 70% раствором изопропилового спирта и 10% повидон-йодидом.
Находящиеся в конце четвертой стадии клетки механически собирали стеклянной пипеткой на 1 мл и далее переносили на не допускающие прикрепления планшеты и культивировали в течение ночи. В ходе предоперационной подготовки мышей клетки отцентрифугировали в 1,5 мл микроцентрифужной пробирке, большую часть супернатанта удалили, оставив количество среды, достаточное лишь для отбора осажденных клеток. Клетки отобрали с помощью пипетки с объемным вытеснением Rainin Pos-D, после чего пипетку перевернули, чтобы клетки могли осесть под собственным весом. Излишки среды вытеснили, оставив компактный препарат клеток для трансплантации.
При трансплантации для проникновения в почечную капсулу использовали катетер для внутривенных введений 24G × 1,9 см (3/4 дюйма), после чего иглу извлекли. Затем катетер продвинули под почечной капсулой к дистальному краю почки. Наконечник пипетки Pos-D плотно вставили во втулку катетера и ввели 5 миллионов клеток через катетер под почечную капсулу, к дистальному краю почки. Почечную капсулу загерметизировали, используя низкотемпературное прижигание, после чего почку вернули в первоначальное анатомическое положение. Одновременно агрегаты по 5 миллионов клеток загрузили в устройство для имплантации на 50 мкл при помощи наконечника пипетки Post-D. Устройства на 50 мкл приобрели в компании TheraCyte, Inc (г. Ирвайн, штат Калифорния). Устройство после загрузки клеток герметизировали медицинским клейким силиконом типа А (Dow Corning, № по каталогу 129109) и имплантировали под кожу мышам линии SICD-Bg (животные №№ 3 и 4). Мышцы сшили непрерывным швом с помощью викриловой нити 5-0, а кожу стянули скобами для ран. После операции мышам подкожно ввели 1,0 мг/кг Metacam. Мышей вывели из наркоза и дали им возможность полностью восстановиться.
После трансплантации мышей взвешивали раз в неделю и дважды в неделю брали анализ крови для определения уровня глюкозы. На разных сроках после трансплантации мышам интраперитонеально ввели 3 г/кг глюкозы. Через 60 минут после введения глюкозы через ретроорбитальный синус отобрали кровь, поместив ее в микроцентрифужные пробирки, содержащие небольшое количество гепарина. Кровь центрифугировали, плазму собирали во вторую микроцентрифужную пробирку, замораживали на сухом льду и хранили при -80°C до проведения анализа на С-пептид человека. Уровни человеческого С-пептида измеряли с помощью комплекта Mercodia/ALPCO Diagnotics Ultrasensitive C-peptide ELISA (№ по каталогу 80-CPTHU-E01, Alpco Diagnostics, г. Нью-Гемпшир) в соответствии с инструкциями производителя.
С-пептид человека обнаруживали в сыворотке крови животных и в группе почечной капсулы, и в группе с имплантированным устройством Theracyte, уже через 4-6 недель после трансплантации, и его концентрация нарастала во времени (фиг. 3A и 3B). По истечении трех месяцев в ответ на введение глюкозы регистрировались значительное количество циркулирующего С-пептида человека как у 100% животных с почечной капсулой, так и в группе с имплантированным устройством Theracyte. Через три месяца уровень стимулированного глюкозой С-пептида человека в сыворотке в группе почечной капсулы составил 1,7±0,5 нг/мл (n=4), а концентрация человеческого С-пептида у мышей с имплантированным устройством Theracyte составила 1±0,5 нг/мл (n=2) (фиг. 3C).
Данный пример показывает, что популяция клеток, одновременно экспрессирующих PDX1 и NKX6.1, которую получили под действием активаторов протеинкиназы С, способна к дальнейшему дифференцированию в инсулин-секретирующие клетки in vivo. Способность к дальнейшему дифференцированию в инсулин-секретирующие клетки не зависит от локального окружения. Авторы показали, что клетки, одновременно экспрессирующие PDX1 и NKX6.1, способны к дальнейшему дифференцированию в инсулин-секретирующие клетки как в почечной капсуле, так и в иммуннопротекторном устройстве при его подкожной имплантации.
Пример 3
Альтернативный способ формирования популяции клеток, составляющих предмет настоящего изобретения
Клетки линии эмбриональных стволовых клеток человека H1 культивировали в покрытых MATRIGEL® (разведение 1:30) (BD Biosciences; № по кат. 356231) чашках со средой RPMI (Invitrogen, № по кат. 22400) + 0,2% FBS + 100 нг/мл активина A (PeproTech; № по кат. 120-14) + 20 нг/мл WNT-3a (R&D Systems; № по кат. 1324-WN/CF) в течение одного дня с последующей обработкой средой RPMI, дополненной 0,5% FBS + 100 нг/мл активина A в течение еще двух дней (стадия 1), затем
а. DMEM/F12 + 2% FBS + 50 нг/мл FGF7 в течение трех дней (стадия 2), затем
b. DMEM с высоким содержанием глюкозы + 1% B27 + 0,25 мкМ циклопамин-KAAD + 2 мкМ ретиноевой кислоты (RA) + 100 нг/мл Ноггина в течение четырех дней (стадия 3), затем либо
c. обработка 4: DMEM с высоким содержанием глюкозы + 1% B27 + 20 нМ PDBu + 100 нг/мл Ноггина в течение четырех дней (стадия 4), или
d. обработка 5: DMEM с высоким содержанием глюкозы + 1% B27 + 100 нг/мл Ноггина + 1 мкМ ингибитора ALK5 II + 20 нМ PDBu в течение четырех дней (стадия 4), или
e. обработка 6: DMEM с высоким содержанием глюкозы + 1% B27 + 50 нг/мл FGF10 + 20 нМ PDBu в течение четырех дней (стадия 4).
Исследовали воздействие дополнительных факторов на опосредованное активатором протеинкиназы С увеличение процента клеток, одновременно экспрессирующих PDX1 и NKX6.1. Образцы культур отбирали в дублях на стадии 4, день 4, и анализ изображений проводили, как описано в примере 1 выше. Также регистрировали экспрессию ISL1 и NEUROD1.
В данном исследовании большинство клеток из популяции, экспрессирующей маркеры, характерные для линии панкреатической энтодермы, демонстрировали положительную экспрессию PDX 1. Большинство клеток, экспрессирующих PDX1, также одновременно демонстрировали положительную экспрессию NKX6.1. Как показано в таблице 1, добавление одного только активатора PKC способствовало появлению клеток, экспрессирующих NKX6.1, в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы (обработка 4). На день 4 стадии 4 93% всей популяции были положительны по NKX6.1, и почти все клетки, экспрессирующие NKX6.1, демонстрировали положительную экспрессию PDX1.
Добавление ингибитора ALK5 II к среде, содержащей активатор протеинкиназы C (обработка 5), не оказывало никакого воздействия на наблюдаемое увеличение экспрессии NKX6.1. 57,1% клеток популяции экспрессировали NEUROD1, и 52,4% клеток популяции экспрессировали ISL1, что указывает на увеличение доли эндокринных клеток-предшественников в популяции после такой обработки. См. таблицу 1.
ПЦР-анализ взятых в этом примере образцов показал, что экспрессия PDX 1, NKX6.1 и PTF1 альфа возрастала в популяции клеток, прошедших обработку 4, по сравнению с клетками, прошедшими обработку 5. См. фиг. 4A-4D. С другой стороны, в клетках, получавших ингибитор ALK5 II и PDBu (обработка 5), наблюдали значительное увеличение экспрессии NGN3. См. фиг. 4A-4D.
Также исследовали эффект добавления FGF10 к среде, содержащей активатор протеинкиназы С (обработка 6). Добавление FGF10 в концентрации 50 нг/мл в сочетании с PDBu (обработка 6) привело к формированию популяции клеток, экспрессирующих маркер, характерный для линии панкреатической энтодермы, где 90% клеток в популяции экспрессируют NKX6.1, однако многие из экспрессирующих NKX6.1 клеток также демонстрировали положительную экспрессию CDX2. См. таблицу 1. Уровень мРНК для PDX1, NKX6.1 и PTF1 альфа не возрастал по сравнению с уровнем, наблюдаемым для клеток, обработанных PDBu и Ноггином. См. фиг. 4A-4D.
Данный пример показывает, что активатор протеинкиназы С в относительно низкой концентрации (примерно 20 нМ) в сочетании с ингибитором BMP можно использовать для формирования популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, при этом более 90% клеток одновременно экспрессируют PDX1 и NKX6.1.
Пример 4
Альтернативный способ формирования популяции клеток, составляющих предмет настоящего изобретения
Клетки линии эмбриональных стволовых клеток человека H1 культивировали в покрытых MATRIGEL® (разведение 1:30) (BD Biosciences; № по кат. 356231) чашках со средой RPMI (Invitrogen, № по кат. 22400) + 0,2% FBS + 100 нг/мл активина A (PeproTech; № по кат. 120-14) + 20 нг/мл WNT-3a (R&D Systems; № по кат. 1324-WN/CF) в течение одного дня с последующей обработкой средой RPMI, дополненной 0,5% FBS + 100 нг/мл активина A в течение еще двух дней (стадия 1), затем
а. DMEM/F12 + 2% FBS + 50 нг/мл FGF7 в течение трех дней (стадия 2), затем либо
b. обработка 7 (T7): DMEM с высоким содержанием глюкозы + 1% B27 + 0,25 мкМ циклопамин-KAAD + 2 мкМ ретиноевой кислоты (RA) + 100 нг/мл Ноггина в течение четырех дней (стадия 3), либо
c. обработка 8 (T8): DMEM с высоким содержанием глюкозы + 1% B27 + 0,25 мкМ циклопамин-KAAD + 2 мкМ ретиноевой кислоты (RA) + 100 нг/мл Ноггина + 50 нг/мл FGF7 в течение четырех дней (стадия 3), затем либо
d. обработка 9 (T9): DMEM с высоким содержанием глюкозы + 1% B27 + 100 нг/мл Ноггина + 1 мкМ ингибитора ALK5 II + 20 нМ PDBu в течение четырех дней (стадия 4), или
e. обработка 10 (T10): DMEM с высоким содержанием глюкозы + 1% B27 + 50 нг/мл FGF10 + 20 нМ PDBu в течение четырех дней (стадия 4), или
f. обработка 11 (T11): DMEM с высоким содержанием глюкозы + 1% B27 + 20 нМ PDBu + 100 нг/мл Ноггина в течение четырех дней (стадия 4).
Образцы культур отбирали в дублях на стадии 4, день 4, и получали их изображения с помощью анализатора IN Cell Analyzer 1000 (GE Healthcare). Для компенсации возможных потерь клеток в ходе процедур анализа и последующего окрашивания для каждой лунки снимали по 100 проекций. Для каждой лунки с использованием программного обеспечения IN Cell Developer Toolbox 1.7 (GE Healthcare) измеряли общее количество клеток, общее количество клеток, экспрессирующих PDX1, общее количество клеток, экспрессирующих NKX6.1, и общее количество клеток, экспрессирующих CDX2. Для каждой повторной совокупности данных рассчитали средние значения и стандартные отклонения. Общие количества клеток, экспрессирующих PDX 1, NKX6.1 и CDX-2, приведены в процентах от общей популяции клеток.
В популяциях клеток, обработанных T7 с последующим добавлением среды T9, приблизительно 80% клеток в популяции экспрессировали NKX6.1. См. таблицу 2. В популяциях клеток, обработанных T7 с последующим добавлением среды T10, приблизительно 90% клеток экспрессировали NKX6.1, при этом в данном варианте обработки отмечали больше клеток, экспрессирующих CDX2. См. таблицу 2. Обработка популяций клеток T7 с последующей обработкой средой T11 приводила к популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, где 93% клеток в популяции экспрессировали NKX6.1. Большинство клеток популяций, экспрессирующих NKX6.1, также экспрессировали PDX1.
Культуры, обработанные T8 с последующей обработкой средой T9, формировали популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, где 56,7% клеток популяции экспрессировали NKX6.1. См. таблицу 2. Культуры, обработанные T8 с последующей обработкой средой T10, формировали популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, где 63,5% клеток популяции экспрессировали NKX6.1, после обработки отмечалось возрастание числа клеток, экспрессирующих CDX2. См. таблицу 2. Культуры, обработанные T8 с последующей обработкой средой Т11, формировали популяцию клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, где 74% клеток популяции экспрессировали NKX6.1. См. таблицу 2. Большинство экспрессирующих NKX6.1 клеток также экспрессировали PDX 1.
ПЦР-анализ также подтвердил результаты, полученные на анализаторе IN Cell, в том что обработка ретиноевой кислотой, циклопамином и Ноггином на стадии 3 с последующим добавлением активатора PKC на стадии 4 на день 4 стадии 4 приводила к повышению уровней мРНК для NKX6.1 и PTF1 альфа (фиг. 5A-5D).
Все цитируемые в настоящем документе публикации полностью включены в настоящий документ путем ссылки. Хотя различные аспекты настоящего изобретения проиллюстрированы выше путем ссылки на примеры и предпочтительные варианты осуществления, подразумевается, что сущность настоящего изобретения ограничивается не указанным выше описанием, а следующими пунктами формулы изобретения, составленными в соответствии с принципами патентного законодательства.
Реферат
Изобретение относится к клеточным технологиям. Описана клеточная популяция клеток человека, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, где указанная изолированная популяция клеток человека получена путем культивирования линии эмбриональных стволовых клеток человека, выбранной из группы, включающей H1 (код NIH: WA01), Н7 (код NIH: WA07) и Н9 (код NIH: WA09) (WiCell Research Institute (WiCell)) в среде, дополненной активатором протеинкиназы С, причем более 60% клеток в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, одновременно экспрессируют PDX1 и NKX6.1, и где клетки в популяции клеток, экспрессирующих маркеры, характерные для линии панкреатической энтодермы, экспрессируют CDX2. Изобретение расширяет арсенал клеточных линий человека. 1 н. и 5 з.п. ф-лы, 5 ил., 2 табл., 4 пр.

Комментарии