Материалы и способы, связанные с линкерами для применения в конъюгатах лекарственного средства и белка - RU2737553C2
Код документа: RU2737553C2
Чертежи




































Описание
Настоящее изобретение относится к конъюгатам лекарственного средства и белка и способам их получения. Более конкретно, настоящее изобретение относится к предоставлению белка, линкера и лекарственного средства, например цитотоксина, для получения конъюгата лекарственного средства и белка. Дополнительно настоящее изобретение предоставляет улучшенный линкер для применения в конъюгатах лекарственного средства и белка и способы введения указанного линкера в указанные конъюгаты лекарственного средства и белка. Более конкретно, конъюгат лекарственного средства и белка может представлять собой конъюгат лекарственного средства и антитела (ADC) и конъюгат лекарственного средства и альбумина или линкера.
Известно, что конъюгаты лекарственного средства и белка, в частности, конъюгаты лекарственного средства и антитела, обеспечивают направленную доставку высокоактивных лекарственных средств в конкретную ткань для лечения. Более конкретно, ADC, которые, как правило, состоят из антитела, связанного посредством химического линкера с лабильными связями с биологически активным цитотоксическим или лекарственным объектом, как известно, применяют в противораковой терапии. Направленная доставка, обеспеченная данными конъюгатами лекарственного средства и белка, является результатом способности антитела и тому подобного тонко различать здоровую и больную ткань, обеспечивая таким образом безопасную доставку высокоактивного лекарственного средства.
Как таковые данные антитела, в частности моноклональные антитела (mAb), являются пригодными в направленных исследовательских, терапевтических, диагностических и других способах биотехнологического применения. Более конкретно, mAb являются пригодными в области направленных видов лечения и лекарственных препаратов. mAb можно использовать посредством включения в лечение с помощью конъюгата лекарственного средства и антитела (ADC). Как обсуждалось выше, ADC представляют собой тип биоактивного лекарственного препарата, имеющий, как ожидается, особую пользу в лечении видов рака, наряду с другими вещами, и представляют собой относительно новую методику. В целом, ADC (например) для лечения рака будет включать в себя mAb, связанное с цитотоксическим объектом или лекарственным средством, которое может обеспечивать уничтожающее клетки действие. Соединение между mAb и цитотоксическим материалом (цитотоксином) в целом будет предоставлено посредством молекулы химически стабильного линкера. В данной области техники известны два типа линкерных систем ADC: расщепляемый и нерасщепляемый. Для расщепляемых линкерных систем ADC существует механизм высвобождения, который является предпочтительно энзиматически управляемым, хотя известны альтернативные расщепляемые системы, которые являются химически лабильными, как подробно описано в Methods in Molecular Biology, Volume 1045, 2013, опубликованной Humana Press. В нерасщепляемых линкерных системах ADC путь высвобождения объясняется деградацией mAb клеточным механизмом при использовании ADC.
Одобрение рынка ADС Adcetris® (Seattle Genetics/Takeda Group) и Kadcyla® (Genentech/Roche) в Европе и США проложило путь для расширенного исследования в данный класс ADC биотерапевтических препаратов.
Adcetris®, продемонстрированный ниже (также известный как брентуксимаб ведотин), направлен на белок CD30, который экспрессируется при классической ходжкинской лимфоме (HL) и системной анапластической крупноклеточной лимфоме (sALCL). Брентуксимаб ведотин состоит из химерного моноклонального антитела брентуксимаба (cAC10, которое выделяет мембранноклеточный белок CD30), связанного с расщепляемым катепсином линкером (валин-цитруллином), пара-аминобензилкарбаматным спейсером и антимитотическим агентом монометил ауристатином E (MMAE).

Kadcyla®, продемонстрированный ниже, представляет собой трастузумаб эмтанзин, ADC, состоящий из моноклонального антитела трастузумаба (Трастузумаб), связанного с цитотоксическим агентом мертанзином (DM1). Сам по себе трастузумаб останавливает рост раковых клеток посредством связывания с рецептором HER2/neu, тогда как мертанзин входит в клетку и предотвращает деление клетки посредством связывания с тубулином; в итоге данное связывающее действие будет приводить к апоптозу клеток. Как правило, конъюгат сокращенно обозначают как T-DM1. Каждая молекула трастузумаба эмтанзина состоит из единственной молекулы трастузумаба, связанной с несколькими молекулами мертанзина, цитотоксическим майтанзиноидом, содержащим сульфгидрильную группу, посредством реагента, образующего поперечные связи, известного как SMCC. SMCC представляет собой сукцинимидил транс-4-(малеимидилметил) циклогексан-1-карбоксилат, бифункциональный перекрестносшивающий агент, который содержит две реакционноспособные функциональные группы, сукцинимидный сложный эфир и малеимид. Сукцинимидная группа SMCC взаимодействует со свободной аминогруппой остатка лизина в молекуле трастузумаба, а активный малеимид SMCC связывается со свободной сульфгидрильной группой мертанзина, образуя ковалентную связь между антителом и мертанзином.

Несмотря на то, что ADC являются хорошо известными в области изобретения, другие конъюгаты лекарственного средства и белка, содержащие глобулярный белок со способностью обеспечивать направленную доставку лекарственного объекта, не являются хорошо известными. Например, альбумин может являться подходящей альтернативой антителам в данных конъюгатах лекарственного средства и белка.
Альбумин состоит из трех структурно гомологичных, в основном спиральных доменов (I, II и III), каждый из которых состоит из двух субдоменов, A и B. Подобно альбуминам других млекопитающих, человеческий альбумин содержит 17 дисульфидных мостиков и свободный тиол Cys34, который предоставляет наибольшую фракцию свободного тиола в сыворотке крови.
Альбумин представляет собой основной белок, ответственный за коллоидно-осмотическое давление крови и такие функции, как несущая среда для длинноцепочных жирных кислот, билирубина, ионов металлов, таких как медь (II) и никель (II), кальций и цинк. Альбумин имеет приблизительный период полужизни в сыворотке, составляющий 20 дней, объясняемый размером белка (прибл. 67 кДа), а также следствием рециркуляции через неонатальные Fc-рецепторы (FcRn). FcRn возвращает альбумин, а также антитела (более конкретно, IgG), зависимым от pH неконкурентным образом, защищая и то и другое от деградации белка в лизосоме. Циркулирующий альбумин интернализируется эндотелиальными клетками, где он связывается с FcRn в кислой среде ранней эндосомы (pH 6). Это обеспечивает возможность возврата альбумина на поверхность клетки и выделения обратно в кровь (физиологический pH). Альбумин может быть ковалентно конъюгирован с цитотоксическим средством или в качестве альтернативы слит с лекарством на белковой основе с целью повышения биодоступности и улучшения фармакокинетики лекарственного средства.
Солидные опухоли имеют проницаемую сосудистую сеть, а также плохой лимфоотток, которые приводят к накоплению и задержке макромолекул (>40 кДа) в интерстициальной жидкости опухоли. Исследования продемонстрировали задержку альбумина в различных злокачественных солидных опухолях. Также существуют новые свидетельства о специфическом связывании альбумина различными рецепторами, некоторые из которых, как было показано, высоко экспрессируются на злокачественных клетках. Подобным образом альбумин, как известно, накапливается в воспаленных суставах больных ревматоидным артритом вследствие повышенной проницаемости гематоартикулярного барьера. Известным применением альбумина в доставке лекарственного средства является выделение печени в качестве мишени с применением конъюгатов альбумина, содержащих остатки галактозы, которые поступают в гепатоциты после взаимодействия с асиалогликопротеиновым рецептором (ASGP-R), присутствующем в больших количествах и высокоаффинным только на данных клетках.
Соответственно, данные свойства выделения мишени, а также его доступность, биоразлагаемость, отсутствие токсичности и иммуногенности наравне с его весьма долгим периодом полувыведения делают альбумин подходящим кандидатом для доставки лекарственного средства. Как таковой, альбумин представляет собой подходящую альтернативу антителам в конъюгатных системах лекарственного средства и белка.
Успешная доставка лекарственного средства или цитотоксического объекта в ткань-мишень зависит от способности линкера связываться с белком и лекарственным средством и оставаться связанным до тех пор, пока конъюгат лекарственного средства и белка не достигнет ткани-мишени. Соответственно, существует потребность в предоставлении альтернативных и/или улучшенных линкеров для применения в данных конъюгатах лекарственного средства и белка, которые обеспечивают успешную доставку.
Дополнительно, существует потребность в предоставлении новых и/или улучшенных конъюгатов лекарственного средства и белка, таких как конъюгаты, включающие в себя альбумин, для безопасной и эффективной доставки цитотоксических средств или терапевтических пептидов или полипептидов.
В одном варианте осуществления существует потребность в предоставлении альтернативных и улучшенных ADC, которые могут эффективно обеспечивать апоптотические свойства клеток. Более конкретно, существует потребность в предоставлении улучшенных линкерных молекул ADC для обеспечения избирательной и эффективной конъюгации во время получения указанных ADC и предоставления эффективного объекта цитотоксина при применении.
Соответственно, в первом аспекте настоящего изобретения предоставлен конъюгат лекарственного средства и белка, включающий в себя глобулярный белок, линкер и лекарственное средство. Более конкретно, настоящее изобретение предоставляет конъюгат лекарственного средства и белка, включающий в себя линкер, способный обеспечивать сайт-специфическую конъюгацию посредством группы лизина или цистеина, имеющейся в белке, предпочтительно азотсодержащее гетероциклическое ароматическое кольцо, включающее в себя винильный заместитель.
Настоящее изобретение предоставляет линкер для применения в конъюгатах лекарственного средства и белка, полезный для связывания белков и лекарственных средств, например, антител и цитотоксинов, для предоставления молекул ADC. Линкер обеспечивает улучшенный направленный объект лекарственного средства. Дополнительно или в качестве альтернативы, линкер обеспечивает конъюгат лекарственного средства и белка с повышенной стабильностью по сравнению с известными в настоящее время линкерными молекулами для применения в ADC, таким образом предоставляя конъюгаты лекарственного средства и белка с улучшенными свойствами безопасности и, следовательно, улучшенными профилями толерантности. Более конкретно, применение раскрытой в настоящем изобретении линкерной молекулы в ADC обеспечивает повышенную активность ADC при применении, по сравнению и выше, чем у эквивалентного неконъюгированного антитела.
В контексте настоящего изобретения термин «глобулярный белок» следует истолковывать как охват любого белка, который обладает свойствами выделения мишени и, таким образом, обладает способностями доставлять лекарственный объект в конкретную ткань-мишень. Соответственно, «глобулярные белки» включают антитела и их фрагменты, альбумин и трансферрин, а также любые другие альтернативные компоненты, известные для применения в конъюгатах лекарственных средств.
«Лекарственным средством» обозначают любое химическое вещество, которое обладает известным биологическим действием на людей или животных. В частности, лекарственное средство может представлять собой фармацевтическое лекарственное средство, которое применяют при лечении, терапии, предотвращении или диагностике заболевания или улучшения иным способом физического или психического благополучия. Следует иметь в виду, что лекарственное средство может представлять собой известное лекарственное средство, которое получило необходимое регистрационное удостоверение лекарственного средства, или новое лекарственное средство, которое до сих пор не прошло тестирование или не получило регистрационное удостоверение лекарственного средства.
В одном варианте осуществления настоящего изобретения предоставлен конъюгат лекарственного средства и антитела, включающий в себя антитело, линкер и цитотоксин.
Предпочтительно антитело представляет собой антитело или его фрагмент, и более предпочтительно моноклональное антитело (mAb). mAb может быть выбрано из любого известного mAb. Единственным ограничением при выборе mAb для применения в настоящем изобретении является то, что оно должно иметь цистеиновый или лизиновый остаток, присутствующий, чтобы дать возможность произойти реакции конъюгации. Особенно предпочтительно, чтобы mAb содержало цистеиновый остаток, поскольку некоторые особенно предпочтительные варианты осуществления линкера настоящего изобретения демонстрируют повышенную избирательность по отношению к тиольной группе, присутствующей в цистеиновом остатке. Однако, в случае, когда идентифицировано mAb, которое обычно не содержит предпочтительный цистеиновый остаток, квалифицированному специалисту в данной области известны способы введения цистеина в mAb.
В соответствии с альтернативным вариантом осуществления настоящего изобретения (как дополнительно подробно описано ниже), антитело может быть замещено на альбумин.
Все предпочтительные варианты осуществления, рассмотренные ниже, которые могут или не могут быть описаны в отношении ADC, содержащих антитело, или конъюгатов альбумина и лекарственного средства, можно в равной степени считать предпочтительными вариантами осуществления для конъюгата лекарственного средства и белка, а также вариант осуществления ADC и вариант осуществления конъюгата альбумина и лекарственного средства. Более конкретно, описание ниже лекарственного средства и линкера следует считать равно применимым к различным вариантам осуществления конъюгатов лекарственного средства и белка.
Лекарственное средство может представлять собой цитотоксический объект или терапевтический пептид или полипептид. Конкретно, когда белок представляет собой антитело или его фрагмент, а конъюгат лекарственного средства и белка представляет собой ADC, лекарственное средство представляет собой предпочтительно цитотоксин. В качестве альтернативы, если белок представляет собой альбумин, лекарственное средство может представлять собой цитотоксин или терапевтический пептид или полипептид.
Предпочтительно цитотоксин представляет собой биологически активный цитотоксический материал. Наиболее предпочтительно цитотоксин представляет собой противораковое лекарственное средство. Цитотоксин может быть выбран из группы, включающей в себя ауристатины, майтансины, калихимицин, антрациклин и пирролобензодиазепины. Более конкретно, цитотоксин может представлять собой монометил ауристатин E (MMAE), доксорубицин или мертанзин (DM1). Для квалифицированного специалиста в данной области должно быть очевидно, что MMAE также известен как (S)-N-((3R,4S,5S)-1-((S)-2-((1R,2R)-3-(((1S,2R)-1-гидрокси-1-фенилпропан-2-ил)амино)-1-метокси-2-метил-3-оксопропил)пирролидин-1-ил)-3-метокси-5-метил-1-оксогептан-4-ил)-N,3-диметил-2-((S)-3-метил-2-(метиламино)бутанамидо)бутанамид.
Однако, дополнительно или в качестве альтернативы, цитотоксин также может быть выбран из других известных цитотоксинов, включая субъединицы рицина и другие цитотоксические материалы пепидной природы, хотя данные материалы менее часто используют в данной области техники.
Если лекарственное средство представляет собой терапевтический пептид или полипептид, пептид или полипептид может представлять собой любой пептид или полипептид, который обладает терапевтическими свойствами, например антиноцицептивной, противодиабетической, противоопухолевой или противовирусной активностью.
Дополнительно или в качестве альтернативы, лекарственное средство предпочтительно включает в себя аминогруппу, тиольную группу или группу карбоновых кислот, поскольку данные типы групп предоставляют идеальные сайты для конъюгации лекарственного средства с линкером настоящего изобретения.
Предпочтительно линкер (также называемый в данной заявке линкерной молекулой или линкерной группой) обеспечивает сайт-специфическую конъюгацию посредством группы лизина или цистеина, присутствующей на белке, таком как антитело.
Более предпочтительно линкер настоящего изобретения включает в себя азотсодержащее гетероциклическое ароматическое кольцо, включающее в себя винильный заместитель.
В самых общих чертах можно считать, что линкер состоит из трех частей; винильной группы, азотсодержащего гетероциклического ароматического кольца и линкерной ножки. Линкерная ножка может изменяться, чтобы приводить к различным терминальным группам для предоставления реакционно-активных участков для лекарственного средства либо для белка, например, антитела ADC, чтобы связываться с линкером.
Предпочтительно, азотсодержащее гетероциклическое ароматическое кольцо представляет собой пиридиновое, пиримидиновое, имидазольное или азиридиновое кольцо. Более предпочтительно, азотсодержащее гетероциклическое ароматическое кольцо представляет собой пиридиновое кольцо или пиримидиновое кольцо, а наиболее предпочтительно, оно представляет собой пиридиновое кольцо. При использовании пиридинового или пиримидинового колец предпочтительно винильная группа находится во 2 позиции или 4 позиции по отношению к гетероатому азота. 4-винилпиридины являются особенно предпочтительными, поскольку они, как было обнаружено, обеспечивают коммерчески приемлемые скорости реакции в определенных обстоятельствах, как дополнительно рассмотрено ниже.
Примеры предпочтительных линкеров в соответствии с настоящим изобретением включают:
В примерах, продемонстрированных выше, 4-винилпиридиновые структуры являются особенно предпочтительными, а структура, показанная как [13], является наиболее предпочтительной. 4-винилпиридиновые структуры являются предпочтительными, поскольку при определенных условиях они демонстрируют повышенную реактивность сравнению и выше, чем у эквивалентных 2-винилпиридиновых структур.
Как будет очевидно для квалифицированного специалиста в данной области, каждая из структур, представленных в качестве примера выше, в основном предоставлена с концевой карбоксильной группой на линкерной ножке. Однако данные структуры могут быть предпочтительно предоставлены в замещенной форме, так чтобы предпочтительная винилпиридиновая структура включала в себя предпочтительную группу поли(алкиленгликоля), наиболее предпочтительно молекулу PEG. Было обнаружено, что присутствие группы ПЭГ на молекуле линкерной ножки является наиболее предпочтительным, поскольку она улучшает реакционную эффективность при стремлении получить требуемое соотношение лекарственного средства и белка в способах получения конъюгата лекарственного средства и белка.
Данные предпочтительные линкерные молекулы включают следующие примеры:


PL15

двойная асимметрично включенная PL13

двойная симметрично включенная PL-13
В предпочтительном варианте осуществления настоящего изобретения линкер включает в себя молекулу, имеющую общую формулу:

в которой:
- X и Y независимо выбирают из CH или N.
- R1 выбирают из:
(CH2)n-C(O)-R, или
(CH2)m-Z-R, или,
(CH2)m-Z-C(O)-R, или,
(CH2)n-C(O)- Z-R, или,
(CH2)m-Z- (CH2)n-C(O)- R, или,
(CH2)m-Z- (CH2)n-C(O)- Z-R, или,
(CH2)m-Z-C(O)- (CH2)n-Z- (CH2)n-C(O)- Z-R, или
(CH2)n-CH(CO2R)2, или
(CH2)m-Z- (CH2)2CH(CO2R)2, или
(CH2)n-Z1.
- R2 и/или R3 может быть выбран из такой же группы молекул, что и R1. Однако R2 и/или R3 предпочтительно выбирают из водорода или электроноакцепторной группы, такой как галоген (F, Cl или Br), -NO2, -CO2H, -CO2R4, COR4, -CHO, -CN, -CF3, -SO2NR4R5, где R4 и R5 независимо выбирают из водорода или C1-10 алкила; или,
- R2 и/или R3 может быть выбран из водорода, алкила или фенила, особенно предпочтительным является, когда линкерная молекула включает в себя пиридиновое кольцо, поскольку альтернативные электроноакцепторные группы могут обладать отрицательным действием на реактивность линкера; или
- R2 и R3 вместе образуют заместитель слитого (гетеро)ароматического кольца, который может включать, но без ограничения, индол, индазол, бензимидазол, хинолин, изохинолин, азиридин или пурин.
Предпочтительно, чтобы R2 и/или R3 был выбран из алкильной группы, метильной группы (CH3) или терт-бутила ((CH3)3C). Наличие алкильной группы на линкерной молекуле является предпочтительным, поскольку наличие данной группы повышает основность азота, присутствующего в структуре кольца и приводит к линкерной структуре, имеющей повышенную реактивность по сравнению и выше, чем у эквивалентных линкерных молекул.
Если R2 и/или R3 выбирают из электроноакцепторной группы, предпочтительным является CF3. Присутствие CF3 повышает реактивность винильной группы, присутствующей в линкерной молекуле, и он является стабильным при физиологических условиях.
В качестве альтернативы следует иметь в виду, что в некоторых вариантах осуществления является возможным использование более расширенной слитой гетероциклической ароматической кольцевой системы, такой как индол, индазол, бензимидазол, хинолин, изохинолин, азирадин или пурин.
В формулах, приведенных выше,
- Z может быть независимо выбирают из NH, O или S,
- Z1 представляет собой группу N3 или группу OH
- n может представлять собой любое целое число от 0 до 10. В некоторых предпочтительных вариантах осуществления n представляет собой значение от 0 до 5.
- m может представлять собой любое целое число от 0 до 10. Предпочтительно m составляет от 0 до 5, и наиболее предпочтительно m составляет от 0 до 3, как показано в примерах, приведенных выше. Дополнительно или в качестве альтернативы, в линкерных молекулах, где группа Z после группы (CH2)m представляет собой группу O, а R1 (и R2 и/или R3, когда они выбирают из одной и той же группы молекул) находится во 2 или 6 позиции на кольцевой структуре, тогда m составляет предпочтительно по меньшей мере 3, поскольку группа O должна располагаться на расстоянии от азота кольцевой структуры. Это происходит вследствие уменьшения действия, которое группа кислорода, как было обнаружено, оказывает на реактивность структур линкерных молекул. Данное действие не ощущается, когда группа кислорода отстоит дальше от кольцевой структуры. Эта ситуация находит свое отражение в структурах, приведенных выше в качестве примера.
- R может представлять собой группу водорода (H), гидроксида (OH), амина или поли-(алкиленгликоля). Предпочтительно R представляет собой поли-(алкиленгликоль), и наиболее предпочтительно он представляет собой PEG. Как будет очевидно для квалифицированного специалиста в данной области, если группа R представляет собой PEG, то за ним предпочтительно следует группа Z в виде NH благодаря продукту реакции добавления PEG. Данная опция подробно описана в общих формулах R1, приведенных выше. В целом, молекула поли-(алкиленгликоля) напрямую ковалентно связана с группами R1 и/или R2, как показано в формуле выше. Группы линкерных ножек могут иметь различную длину, чтобы сохранять молекулу поли-(алкиленгликоля) ближе или дальше от белка, например, антитела.
Предпочтительно лекарственное средство, например, цитотоксическое, связано с линкерной группой R1. В случаях, когда R2 и/или R3 выбирают из той же группы молекул, что и R1, как описано выше, то возможно, что данные группы также будут связаны с лекарственными средствами, такими как цитотоксины, чтобы предоставить конъюгат лекарственного средства и белка, такой как ADC, с множественными лекарственными средствами, присутствующими в их структурах. Некоторые варианты осуществления данного типа можно рассматривать, как симметричную загрузку лекарственного средства в конъюгате лекарственного средства и белка.
Дополнительно или в качестве альтернативы, если R1 и необязательно R2 и/или R3 выбирают из (CH2)n-CH(CO2R)2, или (CH2)m-Z- (CH2)2CH(CO2R)2, т.е. когда линкерная ножка разветвлена, то возможно, что лекарственные средства связаны с каждой концевой группой линкерной ножки. Как таковые, множественные лекарственные средства присутствуют в конъюгате лекарственного средства и белка и могут быть описаны, как aсимметричная загрузка лекарственного средства.
Предпочтительно азотсодержащее гетероциклическое ароматическое кольцо представляет собой замещенное пиридиновое кольцо (X и Y оба представляют собой CH) или замещенное пиримидиновое кольцо (один из X и Y представляет собой CH, а другой представляет собой N). Наиболее предпочтительно азотсодержащее гетероциклическое ароматическое кольцо представляет собой пиридиновое кольцо.
В одном особенно предпочтительном варианте осуществления R1 представляет собой либо:
(CH2)n-C(O)- R, или,
(CH2)n-C(O)- Z-R, или,
(CH2)m-Z- (CH2)n-C(O)- R, или
(CH2)m-Z- (CH2)n-C(O)- Z-R.
В дополнительном варианте осуществления настоящего изобретения может быть желательным включить в описанную выше линкерную молекулу линкер-удлинитель. Данный линкер-удлинитель может быть необходим для изменения растворимости или иммуногенных свойств функционализирующей группы. Более конкретно, данный линкер-удлинитель будет пригоден в системе расщепляемого линкера ADC, которая более подробно будет описана ниже. Пригодные линкеры-удлинители для использования в настоящем изобретении будут очевидны для квалифицированного специалиста в данной области, а особенно предпочтительные линкеры-удлинители описаны в Патенте США номер 7659241 и Патенте США номер 5609105. Наиболее предпочтительно линкер-удлинитель представляет собой ферментативно расщепляемый линкер-удлинитель, который включает в себя совокупность аминокислот, которая может быть расщеплена внутриклеточной протеазой.
В дополнительном варианте осуществления настоящего изобретения может быть необходимо предоставить линкер в модифицированной форме, так чтобы он включал в себя группу сложного эфира для облегчения связывания линкера с белком конъюгата лекарственного средства и белка. Данный аспект будет дополнительно описан ниже.
Предпочтительные линкеры в соответствии с настоящим изобретением могут быть представлены с помощью следующих формул


в которых:
R1 выбирают из:
(CH2)n-C(O)-R, или
(CH2)m-Z-R, или
(CH2)m-Z-C(O)-R, или
(CH2)n-C(O)- Z-R, или
(CH2)m-Z- (CH2)n-C(O)- R, или
(CH2)m-Z- (CH2)n-C(O)- Z-R, или
(CH2)m-Z-C(O)- (CH2)n-Z- (CH2)n-C(O)- Z-R, или
(CH2)n-CH(CO2R)2, или
(CH2)m-Z- (CH2)2CH(CO2R)2, или
(CH2)n-Z1
- R2 может быть выбран из такой же группы молекул, что и R1. Однако предпочтительно R2 выбирают из водорода или электроноакцепторной группы, такой как галоген (F, Cl или Br), -NO2, -CO2H, -CO2R4, COR4, -CHO, -CN, -CF3, -SO2NR4R5, где R4 и R5 независимо выбирают из водорода или C1-10 алкила; или,
- R2 может быть выбран из водорода, алкила или фенила, это является особенно предпочтительным, поскольку альтернативные электроноакцепторные группы могут обладать отрицательным действием на реактивность линкера.
Предпочтительно, чтобы R2 был выбран из алкильной группы, метильной группы (CH3) или терт-бутила ((CH3)3C). Присутствие алкильной группы в линкерной молекуле является предпочтительным, поскольку присутствие данной группы повышает основность азота, присутствующего в кольцевой структуре и приводит к линкерной структуре, обладающей повышенной реактивностью по сравнению и выше, чем у эквивалентных линкерных молекул.
Если R2 выбирают из электроноакцепторной группы, CF3 является предпочтительным. Присутствие CF3 повышает реактивность винильной группы, присутствующей в линкерной молекуле, и является стабильным при физиологических условиях.
В формулах, приведенных выше,
- Z может быть независимо выбран из NH, O или S,
- Z1 независимо выбирают из N3 или OH,
- n может представлять собой любое целое число от 0 до 10. В некоторых предпочтительных вариантах осуществления n представляет собой значение от 0 до 5,
- m может представлять собой любое целое число от 0 до 10. Предпочтительно m составляет от 0 до 5, и наиболее предпочтительно m составляет от 0 до 3, как показано в примерах, приведенных выше. Дополнительно или в качестве альтернативы, в линкерных молекулах формулы (III), если группа Z после группы (CH2)m представляет собой группу O, то m предпочтительно составляет по меньшей мере 3, поскольку группа О должна располагаться на расстоянии от азота кольцевой структуры. Это происходит вследствие уменьшения воздействия, которое группа кислорода, как было обнаружено, оказывает на реактивность структур линкерных молекул. Данное воздействие не ощущается, когда группа кислорода отстоит дальше от кольцевой структуры. Эта ситуация находит свое отражение в структурах, приведенных выше в качестве примера.
- R может представлять собой группу водорода (H), гидроксида (OH), амина или поли-(алкиленгликоля). Предпочтительно R представляет собой поли-(алкиленгликоль), и наиболее предпочтительно он представляет собой ПЭГ. Как будет очевидно для квалифицированного специалиста в данной области, если группа R представляет собой ПЭГ, то за ним предпочтительно следует группа Z в виде NH благодаря продукту реакции добавления ПЭГ. Данная опция подробно описана в общих формулах R1, приведенных выше. В целом, молекула поли-(алкиленгликоля) напрямую ковалентно связана с группами R1 и/или R2, как показано в формуле выше. Группа линкерных ножек может иметь различную длину, чтобы сохранять молекулу поли-(алкиленгликоля) ближе или дальше от белка, например, антитела.
Предпочтительно лекарственное средство, например цитотоксическое, связано с линкерной группой R1. В случаях, когда R2 и/или R3 выбирают из той же группы молекул, что и R1, как описано выше, то возможно, что данные группы также будут связаны с лекарственными средствами, такими как цитотоксины, чтобы предоставить конъюгат лекарственного средства и белка, такой как ADC, с множественными лекарственными средствами, присутствующими в их структурах. Некоторые варианты осуществления данного типа можно рассматривать как симметричную загрузку лекарственного средства в конъюгате лекарственного средства и белка.
Дополнительно или в качестве альтернативы, если R1 и необязательно R2 и/или R3 выбирают из (CH2)n-CH(CO2R)2, или (CH2)m-Z- (CH2)2CH(CO2R)2, т.е. когда линкерная ножка является разветвленной, то возможно, что лекарственные средства связаны с каждой концевой группой линкерной ножки. Как таковые, множественные лекарственные средства присутствуют в конъюгате лекарственного средства и белка и могут быть описаны как aсимметричная загрузка лекарственного средства.
В одном варианте осуществления настоящего изобретения линкер представлен формулой (III).
Дополнительно или в качестве альтернативы, если присутствует группа поли-(алкиленгликоля), основная структура поли-(алкиленгликоля) может быть предоставлена с одной или более реакционноспособными функциональными группами, такими как гидрокси, амино, карбоновых кислот, галоидалкильная, азидная, сукцинимидильная или тиольная группы, чтобы облегчить реакцию молекулы поли-(алкиленгликоля) с лекарственным средством или белком. Особенно предпочтительные молекулы поли-(алкиленгликоля) включают молекулы, замещенные в одной или более гидроксильных позициях химической группой, такой как алкильная группа, имеющая между одним и четырех атомов углерода. Наиболее предпочтительные молекулы поли-(алкиленгликоля) для применения в соответствии с настоящим изобретением представляют собой молекулы полиэтиленгликоля («ПЭГ»), как указано выше, хотя квалифицированный специалист в данной области способен применять методики, раскрытые в данном документе, в совокупности с другими молекулами поли-(алкиленгликоля), такими как полипропиленгликоль или сополимеры полиэтилен-полипропиленгликоля. Молекулы поли-(алкиленгликоля), включающие ПЭГ, как правило, имеют молекулярную массу между около 200 Да и около 80 кДа. Предпочтительные молекулы поли-(алкиленгликоля) имеют молекулярную массу между около 200 Да и 1 кДа. Молекулы поли-(алкиленгликоля), которые можно применять в соответствии с настоящим изобретением, являются хорошо известными в области изобретения и доступны для всеобщего ознакомления, например из коммерчески доступных источников, таких как Sigma Aldrich.
В дополнительном аспекте настоящего изобретения предоставлены нерасщепляемые и/или расщепляемые линкерные системы конъюгата лекарственного средства и белка (напр., ADC).
Может быть представлена нерасщепляемая линкерная система конъюгата лекарственного средства и белка (напр., ADC), которая включает в себя белок (напр., антитело), линкер и лекарственное средство (напр., цитотоксин). В одной системе данного типа конъюгация аминогруппы на антителе достигается через активированный сложный эфир, присутствующий на линкере, который затем, в свою очередь, связывается с цитотоксином посредством винильной группы. В данной нерасщепляемой системе антитело предпочтительно представляет собой mAb. Дополнительно, линкер предпочтительно включает в себя молекулу поли-(алкиленгликоля), наиболее предпочтительно молекулу полиэтиленгликоля (ПЭГ), а цитотоксин содержит тиол. Следует иметь в виду, что в описанной выше системе антитело предоставлено в качестве примера белка и может быть замещено на альбумин, а цитотоксин предоставлен в качестве примера лекарственного средства и может быть замещен на терапевтический пептид или полипептид.
В альтернативной системе данного типа конъюгация тиольной группы на антителе достигается посредством винильной линкерной группы, который в свою очередь связывается с лекарственным средством посредством группы поли-(алкиленгликоля), присутствующей на линкерной ножке.
В альтернативном варианте осуществления предоставлена расщепляемая линкерная система конъюгата лекарственного средства и белка (напр., ADC), которая включает в себя белок (напр., антитело), линкер, линкер-удлинитель и лекарственное средство (напр., цитотоксин).
В линкерной системе расщепляемого ADC винильный заместитель линкерной молекулы особенно пригоден для вступления в реакцию с одной или более тиольными группами, которые естественным образом присутствуют или были введены в антитело (например, за счет использования тиольной группы одного или более остатков цистеина, присутствующих на антителе). Затем боковое плечо линкера соединяется с линкером-удлинителем, предпочтительно посредством молекулы поли-(алкиленгликоля); в данном варианте осуществления линкер-удлинитель обеспечивает функцию «расщепления» ADC. Затем цитотоксин связывается с линкером посредством линкера-удлинителя. Предпочтительно, антитело представляет собой mAb. Более предпочтительно, линкер включает в себя молекулу поли-(алкиленгликоля), наиболее предпочтительно молекулу полиэтиленгликоля (ПЭГ). Предпочтительно, чтобы линкер-удлинитель был ферментативно расщепляемым, как дополнительно подробно описано выше. Следует иметь в виду, что в описанной выше системе антитело предоставлено в качестве примера белка и может быть замещено на альбумин, а цитотоксин предоставлен в качестве примера лекарственного средства и может быть замещен на терапевтический пептид или полипептид.
Должно быть понятно, что в настоящей заявке термин «расщепляемый» используется, чтобы охватить конъюгаты лекарственного средства и белка (напр., ADC), которые являются способными к самоуничтожению, или ими можно манипулировать для высвобождения их лекарственного средства (напр., цитотоксического) объекта. Применение термина предназначено для разграничения данных конъюгатов лекарственного средства и белка (напр, ADC) и тех «нерасщепляемых» конъюгатов лекарственного средства и белка (напр, ADC), которые, что понятно, высвобождают свой лекарственный (напр., цитотоксический) объект, если только находятся в клетке-мишени.
Должно быть понятно, что предпочтительные свойства белка (напр., антитела), линкера и лекарственного средства (напр., цитотоксина) для использования в данном аспекте изобретения, как описано выше, связаны с первым аспектом. Более конкретно, описание линкерной молекулы и ее предпочтительных свойств являются особенно подходящими для применения в указанных расщепляемых и нерасщепляемых системах.
Хотя является предпочтительным, чтобы белок (напр., антитело), используемый в настоящем изобретении, включал по меньшей мере одну или более тиолсодержащую группу цистеина, также предполагается, что белок (напр., антитело) может содержать одну или более группу лизина. Когда дело обстоит именно так, предполагается, что квалифицированный специалист может предпочесть присоединить к линкеру настоящего изобретения группу лизина в качестве альтернативы группе цистеина. В данной ситуации является предпочтительным модифицировать линкерную молекулу так, чтобы она представляла собой сложноэфирную форму линкера. В данном варианте осуществления группа сложного эфира модифицированного линкера способна связываться с лизином, присутствующем на белке (напр., антителе) посредством линкерной ножки. В данном варианте осуществления белок (напр., антитело) будет связан посредством группы лизина с модифицированным линкером сложного эфира, и в свою очередь он будет связан с лекарственным средством (напр., цитотоксином) посредством винильной группы. Данный модифицированный линкер может включать молекулу поли-(алкиленгликоля), наиболее предпочтительно молекулу полиэтиленгликоля (ПЭГ).
В третьем аспекте настоящего изобретения предоставлен способ получения конъюгата лекарственного средства и белка, который включает контакт белка с линкером, способным обеспечивать сайт-специфическую конъюгацию посредством группы лизина или цистеина, присутствующей на белке, предпочтительно включающем в себя азотсодержащее ароматическое гетероциклическое кольцо, включающее в себя винильный заместитель, при этом линкер связан с лекарственным средством. В альтернативном аспекте предоставлен способ получения конъюгата лекарственного средства и белка, который включает контакт белка с линкером, способным предоставить сайт-специфическую конъюгацию посредством группы лизина или цистеина, присутствующей на белке, предпочтительно включающем в себя азотсодержащее ароматическое гетероциклическое кольцо, включающее в себя винильный заместитель, и впоследствии связывая линкер с лекарственным средством.
Предпочтительно способ включает контакт белка (напр., антитела), имеющего по меньшей мере одну реакционноспособную тиольную группу с линкером, который включает в себя функционализирующий реагент, включающий в себя азотсодержащее гетероциклическое ароматическое кольцо, имеющее винильный заместитель, способный взаимодействовать по меньшей мере с одной тиольной группой белка (напр., антитела), при этом функционализирующий реагент линкера ковалентно связывается с молекулой поли-(алкиленгликоля), так что винильный заместитель функционализирующего реагента линкера взаимодействует с тиольной группой белка (напр., антитела), тем самым ковалентно связывая линкерную молекулу поли-(алкиленгликоля) с белком (напр., антителом).
В дополнение, способы настоящего изобретения могут включать один или более этапов в дополнение к этапу взаимодействия функционализирующего реагента и белка (напр., антитела), чтобы связывать их вместе. В качестве примера, способы могут включать первоначальный этап взаимодействия предшественника функционализирующего реагента, включающего в себя азотсодержащее гетероциклическое ароматическое кольцо, имеющее винильный заместитель с молекулой поли-(алкиленгликоля) для получения функционализирующего реагента.
В вариантах осуществления настоящего изобретения, в которых белок (напр., антитело) не содержит подходящую тиольную группу, или не содержит подходящую тиольную группу в желаемой позиции в своей полипептидной цепи, настоящее изобретение может включать первоначальный этап модифицирования белка (напр., антитела), напр., посредством химической реакции или сайтнаправленного мутагенеза, для получения вариантного полипептида, имеющего тиольную группу в одной или более желаемых позициях полипептида. Предпочтительно, это сделано посредством замещения одной или более аминокислот в полипептидной цепи белка (напр., антитела) цистеиновым остатком.
Предпочтительно, реакционноспособная тиольная группа, присутствует ли она естественным образом в белке (напр., антителе) или была введена, представляет собой часть цистеинового аминокислотного остатка.
Дополнительно или в качестве альтернативы, настоящее изобретение предоставляет альбумин в комбинации с линкером, при этом линкер, как описано выше, имеет отношение к первому варианту осуществления настоящего изобретения.
Следует иметь в виду, что альбумин, предназначенный для применения в настоящем изобретении, представляет собой сывороточный альбумин, который представляет собой белок плазмы крови, продуцируемый в печени. Предпочтительно альбумин представляет собой человеческий альбумин.
Предпочтительно линкер включает в себя молекулу поли-(алкиленгликоля), наиболее предпочтительно молекулу полиэтиленгликоля (ПЭГ).
Дополнительно или в качестве альтернативы, настоящее изобретение предоставляет конъюгат лекарственного средства и белка, включающий в себя альбумин, линкер и лекарственное средство (напр., цитотоксин), при этом линкер и лекарственное средство (напр., цитотоксин), как описано выше, имеют отношение к конъюгату лекарственного средства и белка и/или ADC изобретения. В частности, предпочтительно, чтобы линкер включал в себя молекулу поли-(алкиленгликоля), наиболее предпочтительно молекулу полиэтиленгликоля (ПЭГ), которая связана с лекарственным средством (напр., цитотоксином).
Настоящее изобретение также предоставляет конъюгат лекарственного средства и белка, включающий в себя альбумин, линкер и терапевтический пептид или полипептид. Линкер и терапевтический пептид или полипептид являются такими, как описано выше, и является предпочтительным, чтобы линкер включал в себя молекулу поли-(алкиленгликоля), наиболее предпочтительно молекулу полиэтиленгликоля (ПЭГ), которая связана с терапевтическим пептидом или полипептидом.
Дополнительно или в качестве альтернативы, как описано выше, основная структура поли-(алкиленгликоля) может быть снабжена одной или более реакционноспособными функциональными группами, такими как гидрокси, амино, карбоновых кислот, галоидалкильная, азидная, сукцинимидильная или тиольная группы, чтобы облегчить реакцию молекулы поли-(алкиленгликоля) с лекарственным средством, напр., цитотоксическим или терапевтическим пептидом или полипептидом.
Дополнительно, поли-(алкиленгликолевая) линкерная структура также может взаимодействовать со вторым линкером посредством линкерной ножки для предоставления гомобифункционального линкера, так что винильная группа одного линкера может взаимодействовать с тиольной группой лекарственного средства, напр., цитотоксическим или терапевтическим пептидом или полипептидом, а винильная группа другого линкера может быть конъюгирована с тиольной группой белка, например альбумина. В данном варианте осуществления конъюгат лекарственного средства и белка, напр., конъюгат альбумина и лекарственного средства, будет включать две линкерные молекулы, которые будут способствовать присоединению альбумина к тиолсодержащим цитотоксинам, терапевтическим пептидам или терапевтическим полипептидам.
В дополнительном варианте осуществления настоящего изобретения предоставлен способ, который включает контакт альбумина с линкером, который содержит функционализирующий реагент, включающий в себя азотсодержащее гетероциклическое ароматическое кольцо, имеющее винильный заместитель, способный взаимодействовать со свободной тиольной группой альбумина, при этом функционализирующий реагент линкера ковалентно связывается с молекулой поли-(алкиленгликоля), так что винильный заместитель функционализирующего реагента линкера взаимодействует с тиольной группой альбумина, тем самым ковалентно связывая линкерную молекулу поли-(алкиленгликоля) с альбумином.
Данный дополнительный способ может включать первоначальный этап модифицирования альбумина, напр., посредством химической реакции или сайтнаправленного мутагенеза, для получения варианта, имеющего тиольную группу в одной или более желаемых позиций полипептида, напр., для введения гидрофильного остатка цистеина. Предпочтительно, это сделано посредством замещения одной или более аминокислот в полипептидной цепи альбумина цистеиновым остатком.
В дополнительном аспекте настоящее изобретение предоставляет конъюгат лекарственного средства и белка, как определено выше, для применения в терапии.
В одном варианте осуществления предоставлен ADC, как определено выше, для применения в терапии. Предпочтительно ADC предназначен для применения в противораковой терапии.
В дополнительном варианте осуществления настоящее изобретение предоставляет конъюгат лекарственного средства и альбумина, как определено выше, для применения в терапии. Предпочтительно конъюгат лекарственного средства и альбумина предназначен для применения в противораковой, антиноцицептивной, противодиабетической, противоопухолевой или противовирусной терапии.
Далее варианты осуществления настоящего изобретения будут описаны путем примера, а не ограничения, со ссылкой на прилагаемые чертежи.
Краткое описание чертежей
Фигура 1. Относительные скорости реакции, например, линкеров, в соответствии с настоящим изобретением, и глутатиона.
Фигура 2. Анализ с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии реакционной способности свободной кислоты PL13 с N-ацетилцистеином (NAC) спустя 24 часа при трех различных рН (7,0, 7,5 и 8,0).
Фигура 3. Данные масс-спектрометрии для демонстрации образования аддукта PL-13-NAC при pH 7,0.
Фигура 4. Данные масс-спектрометрии для демонстрации образования аддукта PL-13-NAC при pH 8,0.
Фигура 5. Анализ с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии реакционной способности свободной кислоты PL13 с NAC при pH 8,0.
Фигура 6. Анализ с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии реакционной способности свободной кислоты PL13 со смесью аминокислот (Tyr/Lys/His/NAC) при рН 7,0.
Фигура 7. Данные масс-спектрометрии для демонстрации образования PL13-NAC при реакционной способности со смесью аминокислот при рН 7,0.
Фигура 8. Анализ с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии реакционной способности свободной кислоты PL13 с 10 эквивалентами лизина при рН 7,0.
Фигура 9. Анализ с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии реакционной способности свободной кислоты PL13 с 10 эквивалентами аспарагиновой кислоты.
Фигура 10. Структура PL13-val-cit-4-аминобензоил-MMAE.
Фигура 11. Масс-спектрометрический анализ PL13-val-cit-4-аминобензоил-MMAE.
Фигура 12. Профили ХГВ и спектрографии в УФ и видимой части спектра трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE после 1 часа реакции.
Фигура 13. профили ХГВ и спектрографии в УФ и видимой части спектра конъюгата трастузумаб-PL13-val-cit-4-аминобензоил-MMAE через 1, 8 и 16 часов инкубации с молярным избытком лекарственного средства-линкера по отношению к тиолу, составляющим 1,25.
Фигура 14. профиль ХГВ конъюгата трастузумаб-PL13-val-cit-4-аминобензоил-MMAE через 16 часов инкубации с молярным избытком лекарственного средства-линкера по отношению к тиолу, составляющим 5.
Фигура 15. Профиль ХГВ трастузумаб-PL13-val-cit-4-аминобензоил-MMAE, полученный посредством конъюгации молярного избытка PL13-val-cit-4-аминобензоил-MMAE, составляющего 10, спустя 16 часов инкубации.
Фигура 16. PLRP профиль трастузумаб-PL13-val-cit-4-аминобензоил-MMAE, конъюгированного при молярном избытке PL13-val-cit-4-аминобензоил-MMAE, составляющем, 10 спустя 16 часов инкубации.
Фигура 17. PLRP профиль дважды обессоленного трастузумаб-PL13-val-cit-4-аминобензоил-MMAE.
Фигура 18. Анализ с помощью гидрофобной интерактивной хроматографии конъюгата трастузумаб-PL13-val-cit-4-аминобензоил-MMAE в присутствии NAC через 0, 24 и 48 часов.
Фигура 19. PLRP профиль конъюгата трастузумаб-PL13-val-cit-4-аминобензоил-MMAE в присутствии NAC через 0, 24 и 48 часов.
Фигура 20. Анализ с помощью гидрофобной интерактивной хроматографии конъюгата трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE в присутствии NAC через 0, 24 и 48 часов.
Фигура 21. Анализ конъюгатов трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE (A) и трастузумаб-PL13-val-cit-4-аминобензоил-MMAE (B) посредством эксклюзионной хроматографии.
Фигура 22. Анализ с помощью ДСН-ПААГ-электрофореза в невосстанавливающих условиях трастузумаб-PL13-val-cit-4-аминобензоил-MMAE и трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE.
Фигура 23. Линкерная структура PL13-NH-ПЭГ4-OSu.
Фигура 24. Анализ посредством масс-спектрометрии и ионизации электрораспылением промежуточного линкера PL13-NH-ПЭГ4-COOH.
Фигура 25. Анализ перекрестного сшивания трастузумаба посредством линкера SMCC или PL13-NH-ПЭГ4-OSu посредством ДСН-ПААГ-электрофорез в восстанавливающих условиях.
Фигура 26. Линкерная структура PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE.
Фигура 27. Профиль ХГВ трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE (A) и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE (B).
Фигура 28. PLRP профиль трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE (A) и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE (B).
Фигура 29. Расчет DAR для трастузумаб-PL13-NH-ПЭГ4-val-cit-MMAE и трастузумаб-mal-val-cit-MMAE, основанный на профиле элюции PLRP Фигуры 28.
Фигура 30. Анализ с помощью эксклюзионной хроматографии трастузумаб-mal-val-cit-MMAE (A) и трастузумаб-PL13-NH-ПЭГ4-val-cit-MMAE (B).
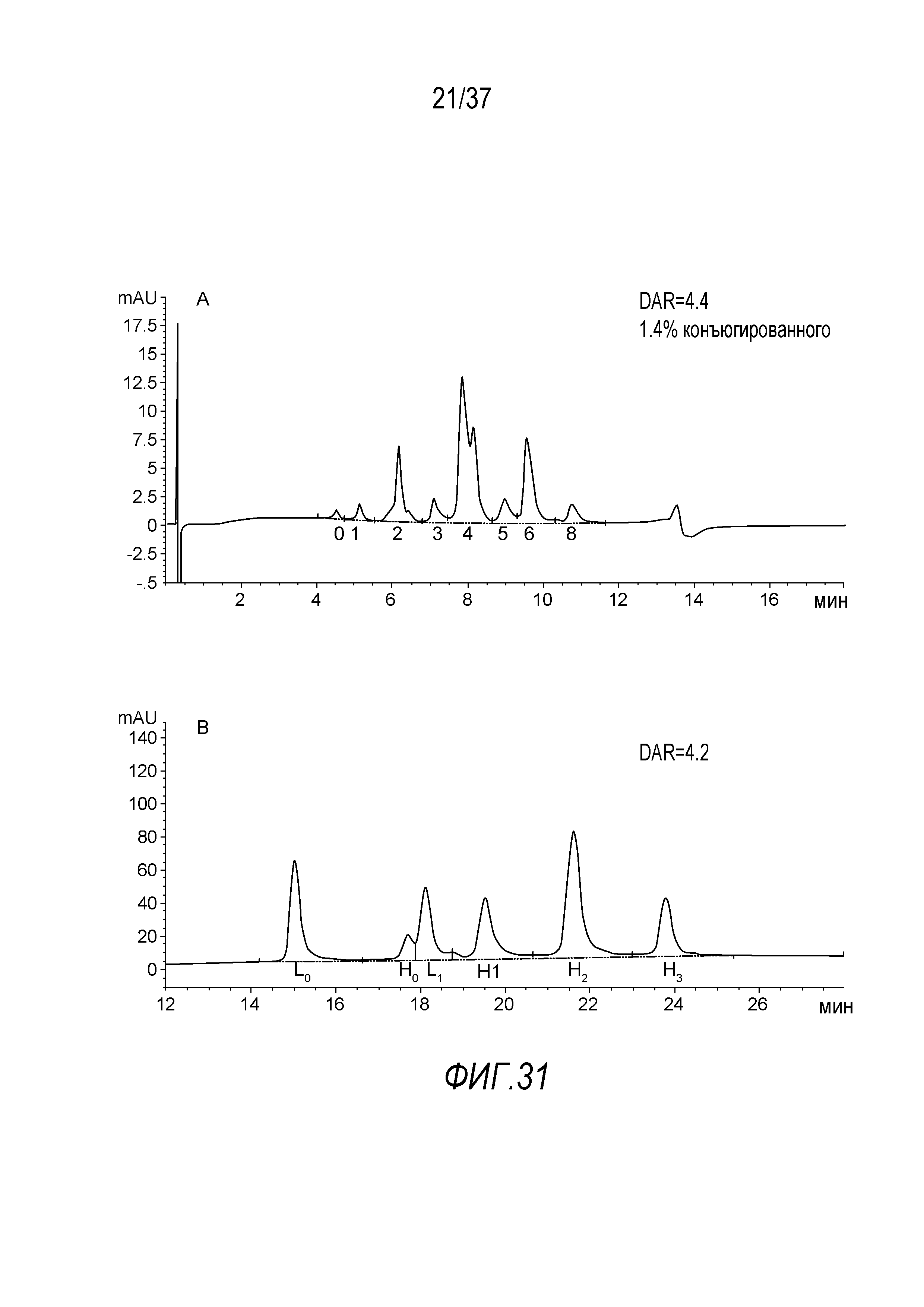
Фигура 31. Репрезентативные профили ХГВ (A) и PLRP (B) трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE, достигнутые после оптимизации процесса в масштабе 1 мг.
Фигура 32. ХГВ профили трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE (A) и трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE (B), достигнутые в масштабе 150 мг.
Фигура 33. Профили эксклюзионной хроматографии трастузумаб-PL13-NH-ПЭГ4-val-cit-аминобензоил-MMAE (A) и трастузумаб-малеимид-val-cit-аминобензоил-MMAE (B), достигнутые в масштабе 150 мг.
Фигура 34. Профиль ХГВ тиомаб-PL13-NH-ПЭГ4-val-cit-MMAE при рН 7,0 (сплошная линия) и pH 7,5 (пунктирная линия).
Фигура 35. PLRP профиль для демонстрации высвобождения лекарственного средства для трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE.
Фигура 36. PLRP профиль для демонстрации высвобождения лекарственного средства для трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE с DAR, составляющим 3,8.
Фигура 37. Стабильность ADC in vitro: трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE, Mal-ADC (A) по сравнению с трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE, PL13-ADC (B)
Фигура 38. Стабильность ADC in vivo: PL13-ADC по сравнению с Mal-ADC
Фигура 39. Данные о гибели клеток для клеточной линии SKBR3 (A), клеточной линии BT474 (B) и клеточной линии JIMT-1 (C).
Фигура 40. Данные мультидозового ксенотрансплантата для демонстрации токсичности ADC.
Фигура 41. Данные мультидозового ксенотрансплантата для демонстрации действия ADC на опухолевый рост.
Фигура 42. Гистопатологические данные зрелости опухоли
Фигура 43. Сравнительные данные для конъюгации 20 КДа PEG-PL12 и PEG-PL13 против 20 КДа PEG-малеимида с восстановленным альбумином при рН 7,4.
Фигура 44. Оптимизация конъюгации PL11 (A), PL12 (B) и PL13 (C) с альбумином.
Фигура 45. Анализ конъюгации PL11 (A), PL12 (B) и PL13 (C) с альбумином посредством масс-спектрометрии с ионизацией электрораспылением.
Фигура 46. Стабильность конъюгата альбумин-PL-12 в присутствии 1 мМ GSH, продемонстрированная посредством масс-спектрометрии с ионизацией электрораспылением.
Фигура 47. Линкерная структура PL13-NH-ПЭГ4-val-cit-4-аминобензоил-доксорубицина.
Фигура 48. Сравнительные данные для конъюгации линкера PL13-NH-ПЭГ4-val-cit-4-аминобензоил-доксорубицина с альбумином, тиоальбумином (однонаправленным мутантом) и тиоальбумином (двунаправленным мутантом).
Фигура 49. Анализ посредством ДСН-ПААГ-электрофореза в невосстанавливающих условиях конъюгатов альбумин-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-доксорубицин. (1) тиоальбумин-двунаправленный мутант-DOX; (2) тиоальбумин-однонаправленный мутант-DOX; (3) Альбумин-DOX; (M)-белковый маркер.
Фигура 50. Анализ с помощью эксклюзионной хроматографии конъюгатов альбумин-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-доксорубицин: Альбумин (A) и конъюгат альбумин-DOX (B); тиоальбумин (однонаправленный мутант) (C) и тиоальбумин-DOX (однонаправленный мутант) (D); тиоальбумин (двунаправленный мутант) (E) и тиоальбумин-DOX (двунаправленный мутант) (F).
Способы настоящего изобретения способны предоставить конъюгаты лекарственного средства и белка, такие как ADC, или конъюгаты лекарственного средства и альбумина в соответствии с настоящим изобретением, которые содержат антитело или альбумин, связанный с линкером, который, в свою очередь, связан с лекарственным средством, таким как цитотоксин или терапевтический пептид или полипептид.
В настоящем изобретении ссылки на антитела включают иммуноглобулины, натуральные либо полученные синтетически частично или целиком. Термин также охватывает любой полипептид или белок, включающий в себя антигенсвязывающий домен. Также предусматриваются фрагменты антител, которые содержат антигенсвязывающие домены, содержащие фрагменты Fab, scFv, Fv, dAb, Fd, диатела, триотела или нанотела. Можно взять моноклональные и другие антитела и использовать методики технологии рекомбинантной ДНК для получения других антител или химерных молекул, которые сохраняют специфичность оригинального антитела. Подобные методики могут включать введение ДНК, кодирующей вариабельную область иммуноглобулина или определяющие комплементарность области (CDR) антитела, в константные области или константные области плюс каркасные области другого иммуноглобулина. См., например, EP 0 184 187 A, GB 2188638 A или EP 0 239 400 A. Антитела могут быть модифицированы множеством способов, и термин необходимо истолковывать, как охват любого специфически связывающего элемента или вещества, имеющего антигенсвязывающий домен антитела с требуемой специфичностью. Таким образом, данный термин охватывает фрагменты антител и производные, включая любой полипептид, содержащий связывающий домен иммуноглобулина, натуральный ли или синтетический целиком или частично. Вследствие этого, включены химерные молекулы, включающие в себя связывающий домен иммуноглобулина или эквивалент, слитые с другим полипептидом. Клонирование и экспрессия химерных антител описаны в EP 0 120 694 A и EP 0 125 023 A.
В предшествующей области техники было показано, что фрагменты целого антитела могут выполнять функцию связывания антигенов. Примерами связывающих фрагментов являются (i) Fab-фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) Fd-фрагмент, состоящий из доменов VH и CH1; (iii) Fv-фрагмент, состоящий из доменов VL и VH единственного антитела; (iv) dAb-фрагмент (Ward, E.S. et al., Nature 341, 544-546 (1989)), который состоит из домена VH; (v) выделенные CDR области; (vi) F(ab')2-фрагменты, бивалентный фрагмент, включающий в себя два связанных Fab-фрагмента (vii) молекулы с одноцепочечным Fv (scFv), в которых VH-домен и VL-домен связаны пептидным линкером, который обеспечивает возможность ассоциирования двух доменов с образованием антигенсвязывающего участка (Bird et al, Science, 242; 423-426, 1988; Huston et al, PNAS USA, 85: 5879-5883, 1988); (viii) биспецифические одноцепочечные Fv-димеры (PCT/US92/09965) и (ix) «диатела», мультивалентные или мультиспецифические фрагменты, полученные за счет слияния генов (WO 94/13804; Holliger et al, P.N.A.S. USA, 90: 6444-6448, 1993). Fv, scFv или диабоди молекулы могут быть стабилизированы за счет включения дисульфидных мостиков, связывающих VH- и VL-домены (Reiter et al, Nature Biotech, 14: 1239-1245, 1996). Также могут быть получены миниантитела, включающие в себя scFv, объединенные с CH3 доменом (Hu et al, Cancer Res., 56: 3055-3061, 1996). Соответственно, настоящее изобретение предусматривает подобные связывающие фрагменты.
В предпочтительных вариантах осуществления в способах, раскрытых в данном документе, используются реагенты и условия, которые хорошо адаптированы для связывания белка, такого как антитело, посредством линкера с лекарственным средством, таким как цитотоксин. Конкретно, условия реакции, которые используются в представленном способе, помогают избегать проблем, которые стремятся возникать при использовании реагентов предшествующего уровня техники, таких как малеимид, которые имеют тенденцию получения смеси различных продуктов с диапазоном различных свойств. Более конкретно, как можно видеть из экспериментальных данных ниже, способы получения конъюгатов лекарственного средства и белка, таких как ADC, которые используют линкеры в соответствии с настоящим изобретением, избегают проблем, связанных с поперечным сшиванием малеимида.
Как указано выше, интересующий белок (напр., антитело) для композиции конъюгата лекарственного средства и белка (напр., ADC) может быть связан с линкером с использованием существующих тиольных групп или за счет введения тиольных групп на начальном этапе способа, например, за счет взаимодействия одной или более функциональных групп белка (напр., антитела) для получения тиольной группы, или за счет введения в белок (напр., антитело) тиольной группы или ее предшественника. В качестве примера, он может включать этап введения в белок (в примере антитело) цистеинового остатка на участке, где требуется связать линкер с белком (напр., антителом). Это может быть полезно в ситуациях, когда в первоначальном полипептиде/белке или полипептиде/белке дикого типа не имеется удобного цистеинового остатка для реакции в соответствии с настоящим изобретением. В целях удобства это может достигаться с использованием сайтнаправленного мутагенеза белка, такого как полипептид антитела, применение которого вполне устоялось в данной области.
В качестве альтернативы или дополнительно, может потребоваться начальная стадия восстановления, когда белком является альбумин промышленного класса, так как большая часть имеющихся цистеиновых тиолов заблокированы, как рассмотрено с дополнительными подробностями ниже.
Экспериментальные Данные и Обсуждение
Следующие экспериментальные данные были получены главным образом с использованием линкерных молекул, идентифицируемых и упоминаемых в данном документе, как PL13, в форме свободной кислоты или в NH-пегилированной форме, как продемонстрировано ниже.
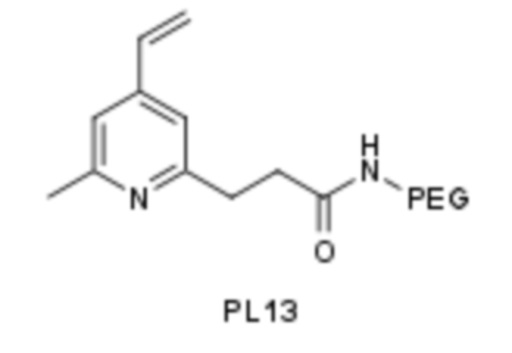
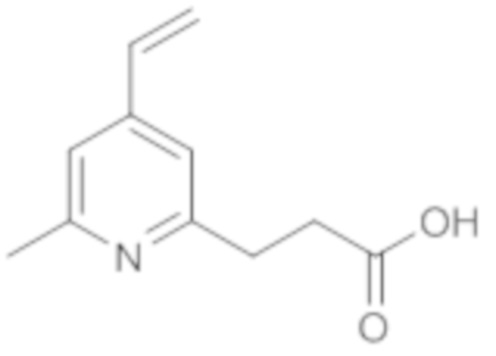
1. Демонстрация реакционной способности линкера PL11, PL12 и PL13 с глутатионом.
Глутатион содержит тиольную группу, которая является легкодоступной для конъюгации и может предоставлять хорошую модель для белков для оценки пригодности линкеров для применения в настоящем изобретении для практической ценности в конъюгатах лекарственного средства и белка, таких как ADC. Фигура 1 показывает три примера линкерной группы в соответствии с настоящим изобретением и демонстрирует их способности конъюгировать с тиольными группами, присутствующими в глутатионе. Примерами на фигуре 1 являются PL11, PL12 и PL13, а их структуры продемонстрированы ниже.

2. Определение избирательности свободной кислоты PL13
Данные, приведенные ниже, демонстрируют, что линкеры в соответствии с настоящим изобретением показывают специфичность к цистеиновым группам. Свободная кислота PL13 идентифицирована как:

Реакционная способность свободной кислоты PL13 с N-ацетилцистеином при рН 7,0, 7,5 и 8,0
Проводили реакцию свободной кислоты PL13 с 2 молярными эквивалентами N-ацетилцистеина (NAC) при трех отдельных pH: 7,0, 7,5 и 8,0. Реакции проводили в забуференном метанолом/фосфатом солевом (PBS) растворе (соотношение, составляющее 9:1), забуференном до надлежащего pH при комнатной температуре (RT). Анализ с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии с градиентом от 1% до 50% B (ацетонитрил с 0,1% TFA) в течение 15 минут, и выполняли детектирование при 254 нм для мониторинга добавления свободного тиола к винильной группе PL13 с течением времени.
Способ:
210 мкл 2,61 мМ свободной кислоты PL13 в метаноле смешали с 22 мкл 50 мМ NAC в буфере для придания итоговой концентрации, составляющей 2,37 мМ свободной кислоты PL13 и 4,74 мМ NAC.
Результаты:
Аддукт PL13-NAC элюировали с задержкой времени, равной 5,1 минуты, при всех pH спустя 24 часа (см. фигуру 2). Количество продукта (Аддукт PL13-NAC) было аналогичным при рН 7,0 и 8,0. Реакционная способность свободной кислоты PL13 при рН 7,5 была более медленной. В дополнение, идентифицированный пик элюировали через 4 минуты.
Анализ масс-спектрометрии с ионизацией электрораспылением подтвердил присутствие аддукта PL13-NAC при всех проанализированных pH. Данные следов в масс-спектре включены настоящим, чтобы показать данный анализ, который выполняли при рН 7,0 (Фигура 3.), и pH 8,0 (Фигура 4).
Реакционная способность свободной кислоты PL13 с N-ацетилцистеином при рН 8,0
Проводили реакцию свободной кислоты PL13 с 2 молярными эквивалентами NAC в растворе метанола/PBS (9:1), pH 8,0. Прохождение реакции отслеживали посредством обращенно-фазовой высокоэффективной жидкостной хроматографии с использованием градиента от 1% до 50% B на протяжении 15 минут с детектированием при 254 нм. Образцы проанализировали при 0, 1, 4 и 72 часах инкубации при комнатной температуре (см. фигуру 5).
Способ:
100 мкл 2,61 мМ свободной кислоты PL13 в метаноле смешали с 11 мкл 50 мМ NAC в буфере при рН 8,0 для придания итоговой концентрации, составляющей 2,35 мМ свободной кислоты PL13 и 5 мМ NAC.
Результаты:
Добавление свободной кислоты PL13 к NAC является медленным в течение первых 4 часов. После 72 часов инкубации ~70% свободной кислоты PL13 было преобразовано в продукт (Аддукт PL13-NAC) при рН 8,0.
Реакционная способность свободной кислоты PL13 с 10 эквивалентами тирозина, гистидина, лизина и N-ацетилцистеина при рН 7,0
Свободную кислоту PL13 индуцировали 10 эквивалентами каждой аминокислоты (тирозина (Tyr), гистидина (His), лизина (Lys) и N-ацетилцистеина (NAC)) при рН 7,0. Реакцию анализировали посредством обращенно-фазовой высокоэффективной жидкостной хроматографии с использованием градиента от 1 до 50% B на протяжении 15 минут с установкой детектирования при 254 нм.
Способ:
50 мкл 2,61 мМ PL13 в метаноле смешали с 260 мкл 20 мМ Tyr/His/Lys и NAC в буфере для придания итоговой концентрации, составляющей 0,42 мМ PL13 и 4,2 мМ каждого из Tyr, His, Lys и NAC.
Результаты:
Свободная кислота PL13 избирательно реагировала с NAC в присутствии Tyr, His и Lys при рН 7,0 (см. фигуру 6). Фигура 7 показывает данные масс-спектрометрии для демонстрации, что образовался только аддукт PL13 NAC.
Реакция присоединения между PL13 и NAC значительно усилилась при молярном избытке аминокислоты, составляющем 10. Преобразование свободной кислоты PL13 в желаемый аддукт PL13-NAC завершается на 90% после 4 часов при комнатной температуре (RT) и полностью завершается < чем за 18 часов.
Полученные результаты демонстрируют избирательность формы свободной кислоты линкерной молекулы в соответствии с настоящим изобретением для реакционной способности цистеина за счет винильной группы линкерной молекулы.
Анализ с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии реакционной способности свободной кислоты PL13 с лизином.
Свободную кислоту PL13 индуцировали 10 эквивалентами Lys в PBS буфере, pH 7,4 при комнатной температуре. Реакцию анализировали посредством обращенно-фазовой высокоэффективной жидкостной хроматографии с использованием градиента от 12 до 50% ацетонитрила в воде в течение 30 минут с установкой детектирования при 270 нм.
Способ:
10 мкл 4 мМ PL13 в метаноле смешали с 50 мкл раствора 8 мМ Lys и 40 мкл PBS буфера pH 7,4 для придания итоговой концентрации, составляющей 0,4 мМ PL13 и 4,0 мМ Lys. Реакцию анализировали посредством обращенно-фазовой высокоэффективной жидкостной хроматографии с использованием градиента от 12 до 50% ацетонитрила в воде в течение 30 минут с установкой детектирования при 270 нм.
Результаты:
Свободная кислота PL13 не вступала в реакцию с Lys при рН 7,4, так как в анализе с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии не наблюдалось никакого пика, соответствующего аддукту PL13-Lys (см. фигуру 8).
Полученные результаты демонстрируют, что за счет инкубирования свободной кислоты PL13 с Lys аддукт не образуется. Эти данные подтверждают избирательность цистеиновой группы формы свободной кислоты линкеров настоящего изобретения. Следует принимать во внимание, что малеимид не демонстрирует подобной специфичности цистеина, и в связи с этим линкеры настоящего изобретения в этом отношении обеспечивают преимущество.
Несмотря на то, что данные выше показывают специфичность цистеина, демонстрируемую линкерами настоящего изобретения, легко понять, что в качестве альтернативы специфичность лизина может достигаться, если линкер модифицировать способами, хорошо известными в области изобретения.
Реакционная способность свободной кислоты PL13 с аспарагиновой кислотой
Свободную кислоту PL13 обработали 10 эквивалентами аспарагиновой кислоты (Asp) при рН 7,0 и при комнатной температуре. Анализ выполняли посредством обращенно-фазовой высокоэффективной жидкостной хроматографии с градиентом от 1% до 50% B на протяжении 15 минут с детектирование при 254 нм.
Способ:
50 мкл 2,61 мМ свободной кислоты PL13 в метаноле смешали с 280 мкл 50 мМ Asp в буфере для придания итоговой концентрации, составляющей 0,42 мМ свободной кислоты PL13 и 4,2 мМ Asp.
Результаты:
Свободная кислота PL13 является стабильной в присутствии Asp при рН 7,0 в течение 18 часов при комнатной температуре (см. фигуру 9).
Спектр МС подтверждает, что аддукт не образуется за счет инкубирования свободной кислоты PL13 с Asp (данные не показаны). Кроме того, эти данные подтверждают избирательность цистеиновой группы линкеров настоящего изобретения. Следует принимать во внимание, что малеимид не демонстрирует подобной специфичности цистеина, и в связи с этим линкеры настоящего изобретения проявляют свое преимущество над ним.
3. Синтез линкера PL13-Val-Cit-4-аминобензоил-MMAE и цитотоксического лекарственного средства
PL13-val-cit-4-аминобензоил-MMAE синтезировали с помощью фрагментного подхода, который должен быть хорошо знаком квалифицированному специалисту в данной области.
Способ:
Свободную кислоту PL13 соединили со свободным аминоконцом H-val-cit-4-аминобензоил-MMAE, иллюстративным цитотоксином, методом образования активного сложного эфира с гидроксибензотриазолом.
Результаты:
Синтезировали 3,1 мг PL13-val-cit-4-аминобензоил-MMAE (см. фигуру 10). Материал солюбилизировали в диметил-ацетамиде (DMA) для предоставления раствора линкера лекарственного средства в концентрации, равной 50 мМ.
Обращенно-фазовая высокоэффективная жидкостная хроматография подтвердила чистоту линкера PL13-val-cit-4-аминобензоил-MMAE (данные не показаны).
Анализ с помощью масс-спектрометрии с ионизацией электрораспылением подтвердил идентичность линкера цитотоксического лекарственного средства (ожидаемая молекулярная масса составляет 1296,67 Да, экспериментальный результат дал молекулярную массу, равную 1296,5 Да) (см. фигуру 11).
4. Образование трастузумаб-PL13-Val-Cit-4-аминобензоил-MMAE и трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE
Получили 20 мг конъюгата трастузумаб-PL13-val-cit-4-аминобензоил-MMAE, иллюстративного ADC настоящего изобретения и 20 мг конъюгата трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE, ADC, содержащего известный малеимидовый линкер.
Конъюгация PL13-val-cit-4-аминобензоил-MMAE и малеимид-val-cit-4-аминобензоил-MMAE с трастузумабом
Способ:
Трастузумаб восстановили, чтобы обеспечить возможность конъюгации 3-4 лекарственных средств на молекулу трастузумаба. Не предоставлен подробный способ восстановления трастузумаба, как это должно быть хорошо известно квалифицированному специалисту в данной области.
Малеимид-val-cit-4-аминобензоил-MMAE конъюгировали с трастузумабом с молярным избытком над свободным тиолом, составляющем 1,25, при рН 7,0. Реакцию проводили в течение 1 часа при комнатной температуре. Реакцию конъюгации останавливали за счет избытка NAC. Анализ конъюгата трастузумаба осуществляли с помощью хроматографии гидрофобного взаимодействия (ХГВ) с использованием колонки бутил-непористая смола (4,6×3,5, 2,5 мкм) Tosoh и с помощью спектроскопии в УФ и видимой части спектра. MMAE имеет характерное поглощение ультрафиолетовых лучей при 248 нм (ε248= 1500 M-1 см, ε280= 15900 M-1 см).
PL13-val-cit-4-аминобензоил-MMAE соединили с трастузумабом с молярным избытком, составляющим 1,25, 2,5, 5 и 10 над свободным тиолом. Реакции проводили в течение 16 часов при рН 7,0. Реакции конъюгации анализировали как с помощью ХГВ (разделение в колонке бутил-непористая смола Tosoh), так и хроматографии PLRP (разделение в колонке PLRP 2,1 мм x 5 см, 5 мкм). Конъюгаты трастузумаба исследовали с помощью спектроскопии в УФ и видимой части спектра. Как линкер MMAE и цитотоксического лекарственного средства, так и PL13 участвуют в поглощении ультрафиолетовых лучей при 248 нм.
Результаты:
Реакцию малеимид-val-cit-4-аминобензоил-MMAE с трастузумабом завершили в пределах 1 часа с использованием соотношения лекарственного средства и свободного тиола, составляющего 1,25 (см. фигуру 12). Цифры на фигуре 12 обозначают количество лекарственного средства, конъюгированного с полноразмерным антителом. На входе представлен профиль спектроскопии в УФ и видимой части спектра, который отображает увеличение поглощения при 248 нм благодаря конъюгации малеимид-val-cit-4-аминобензоил-MMAE с трастузумабом. Получили 10 мг конъюгата трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE (соотношение лекарственного средства и антитела (DAR) 2,2) и отложили для исследований in vitro, которые обсуждаются дополнительно ниже.
Скорость и эффективность реакции PL13-val-cit-4-аминобензоил-MMAE значительно ниже, чем малеимид-val-cit-4-аминобензоил-MMAE благодаря низкой растворимости линкера (см. фигуру 13). Конъюгацию проводили с молярным избытком лекарственного средства-линкера по сравнению с тиолом, составляющим 1,25. На входе представлен профиль спектроскопии в УФ и видимой части спектра, который изображает увеличение поглощения при 248 нм благодаря соединению PL13-val-cit-4-аминобензоил-MMAE с трастузумабом в пределах 16 часов. Наблюдалось медленное увеличение скорости конъюгации PL13-val-cit-4-аминобензоил-MMAE с трастузумабом за счет применения молярного избытка лекарственного средства-линкера по сравнению с тиолом, составляющим 5 (см. фигуру 14). На фигуре 14 цифры обозначают количество лекарственного средства, конъюгированного с полноразмерным антителом. DL обозначает неконъюгированное лекарственное средство.
Конъюгация PL13-val-cit-4-аминобензоил-MMAE с трастузумабом при молярном избытке, составляющем 10, и в присутствии 50% пропиленгликоля привела к 90% выходу в пределах 4 часов (см. фигуру 15 и Фигуру 16). На фигуре 15 цифры обозначают количество лекарственного средства, конъюгированного с полноразмерным антителом. DL обозначает неконъюгированное лекарственное средство. На фигуре 16 цифры обозначают количество лекарственного средства, конъюгированного с антителом с легкой (L) или тяжелой (H) цепью. Получили 7,2 мг конъюгата трастузумаб-PL13-val-cit-4-аминобензоил-MMAE (DAR 3,03) и отложили для исследовании in vitro, которые обсуждаются дополнительно ниже.
Определение Соотношение Лекарственного Средства и Антитела (DAR) для трастузумаб-PL13-val-cit-4-аминобензоил-MMAE и трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE.
ХГВ и PLRP хроматографию часто применяют, чтобы охарактеризовать среднее распределение лекарственного объекта и лекарственного объекта для связанных с цистеином ADC. Определение среднего распределения лекарственного объекта и лекарственного объекта является важнейшим свойством, так как оно влияет на активность и фармакокинетику ADC.
Результаты:
Определение с помощью ХГВ характеристик трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE привело к расчету DAR, равному 2,2, с 1,8% неконъюгированного трастузумаба (см. фигуру 12). Расчет DAR из профиля ХГВ определяют с помощью хорошо известных способов в данной области, как обсуждается ниже в связи с фигурой 27.
Результатом анализа с помощью ХГВ трастузумаб-PL13-val-cit-4-аминобензоил-MMAE были пики, которые не являются достаточно хорошо различимыми для подтверждения определения DAR (см. фигуру 15). Однако эти данные включены в данный документ для полноты. ХГВ использовали для расчета количества трастузумаба с рассчитанным DAR 0, составляющим ~8,4%.
Отделение восстановленного дитиотреитолом (DTT) трастузумаб-PL13-val-cit-4-аминобензоил-MMAE посредством PLRP колонки давало хорошо различимые пики (Фигура 16), соответствующие неконъюгированным или конъюгированным с лекарственным средством легкой и тяжелой цепям антитела. Для трастузумаб-PL13-val-cit-4-аминобензоил-MMAE рассчитали DAR, равное 3,0, (см. фигуру 17). Таблица на фигуре 17 показывает расчет DAR для трастузумаб-PL13-val-cit-4-аминобензоил-MMAE на основании процента площади неконъюгированных и содержащих лекарственное средство легкой и тяжелой цепей.
5. Исследования стабильности трастузумаб-PL13-Val-Cit-4-аминобензоил-MMAE и трастузумаб-малеимид-Val-Cit-4-аминобензоил-MMAE
Стабильность лекарственного средства-линкера для конъюгатов трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE и трастузумаб-PL13-val-cit-4-аминобензоил-MMAE оценивали в присутствии NAC в PBS буфере.
Способ:
Каждый ADC (в концентрации, составляющей 1-2 мг/мл), инкубировали с 1 мМ NAC в PBS буфере в течение 24 часов при 37°C.
Результаты:
На конъюгат трастузумаб-PL13-val-cit-4-аминобензоил-MMAE не оказывало влияние присутствие NAC в буфере (см. фигуры 18 и 19). Трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE показал сниженную стабильность в присутствии NAC (см. фигуру 20). На фигуре 18 цифры обозначают количество лекарственного средства, конъюгированного с полноразмерным антителом. DL обозначает неконъюгированное лекарственное средство.
Фигура 19 в частности демонстрирует отсутствие изменения профиля для содержащего PL13 ADC, обусловленного стимуляцией свободным тиолом, показывающее стабильность конструкции.
6. Анализ с помощью ДСН-ПААГ-электрофореза и эксклюзионной хроматографии трастузумаб-PL13-Val-Cit-4-аминобензоил-MMAE и трастузумаб-малеимид-Val-Cit-4-аминобензоил-MMAE
Трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE и трастузумаб-PL13-val-cit-4-аминобензоил-MMAE оценивали посредством эксклюзионной хроматографии и ДСН-ПААГ-электрофореза в невосстанавливающих условиях.
Результаты:
Трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE присутствует в виде 99,5% мономера (см. фигуру 21 (A)). Трастузумаб-PL13-val-cit-4-аминобензоил-MMAE присутствует в виде 93,5% мономера (см. фигуру 21 (B)).
Анализ с помощью ДСН-ПААГ-электрофореза в невосстанавливающих условиях показал наличие множества полос как в образцах трастузумаб-PL13-val-cit-4-аминобензоил-MMAE, так и в образцах трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE благодаря разрыву дисульфидных связей между цепями антитела в процессе алкилирования цистеиновых остатков с фрагментами линкера-лекарственного средства (см. фигуру 22). На фигуре 22 дорожка 1 отображает анализ 5 мкл образца трастузумаб-PL13-val-cit-4-аминобензоил-MMAE, нанесенного на гель в концентрации, равной 1,8 мг/мл, а дорожка 2 отображает анализ 5 мкл образца трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE, нанесенного на гель в концентрации, равной 5 мг/мл. Благодаря сильным нековалентным взаимодействиям между тяжелой и легкой цепями по-прежнему поддерживается целостность полноразмерного антитела, которая была подтверждена анализом с помощью эксклюзионной хроматографии.
7. Синтез Гетеробифункционального Линкера PL13-NH-ПЭГ4-OSu
Для предоставления PL13-NH-ПЭГ4-OSu в участок линкерной ножки линкерной молекулы ввели гидрофильный ПЭГ (ПЭГ-4), чтобы улучшить растворимость линкера по сравнению с примером, приведенным в разделе 1 выше (см. фигуру 23).
Способ:
Свободную кислоту PL13 (которая описана выше) соединили с 1-Амино-3, 6, 9, 12-тетраоксапентадекан-15-оевой кислотой. Активацию карбоксильной группы в требуемый сложный эфир сукцинимидила провели с использованием N,N-дициклогексилкарбодиимида (DCC) 2,5 эквивалентов /гидроксисукцинимида, соединенного с безводным дихлорметаном (DCM). Не вступивший в реакцию DCC и побочный продукт диисопропилмочевину удаляли посредством фильтрации из холодного DCM.
Результаты:
Масс-спектрометрия с ионизацией электрораспылением PL13-NH-ПЭГ4-COOH (см. фигуру 24) подтвердила идентичность линкера.
Сравнение перекрестной реактивности PL13-NH-ПЭГ4-OSu и линкеров SMCC
Степень поперечного связывания трастузумаба посредством сукцинимидил-транс-4-(малеимидилметил)циклогексан-1-карбоксилата (SMCC), известного линкера и PL13-NH-ПЭГ4-OSu оценивали посредством ДСН-ПААГ-электрофореза в восстанавливающих условиях.
Способ:
Трастузумаб в итоговой концентрации, составляющей 2 мг/мл, инкубировали с избытком SMCC или PL13-NH-ПЭГ4-OSu, составляющим 10. Образцы инкубировали при комнатной температуре.
Результаты:
Исходя из ДСН-ПААГ-электрофореза очевидно, что PL13-NH-ПЭГ4-OSu демонстрирует полосы меньшей молекулярной массы, чем линкер SMCC (см. фигуру 25, дорожки 5-9). На ДСН-ПААГ-электрофорезе PL13-NH-ПЭГ4-OSu имеется несколько полос более высокой молекулярной массы, но в некоторой степени они также присутствуют на первоначальной дорожке трастузумаба (см. фигуру 25, дорожка 5).
В противоположность линкерам настоящего изобретения, линкер SMCC индуцирует поперечное связывание трастузумаба благодаря неспицифической реакционной способности малеимидной группы особенно по отношению к аминовым боковым цепям лизиновых остатков.
8. Синтез PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE
Для дополнительного улучшения растворимости синтезированного ранее линкера цитотоксического лекарственного средства PL13-val-cit-4-аминобензоил-MMAE в молекулу ввели короткое гидрофильное ПЭГ звено (см. фигуру 26). ПЭГ звено также вводит «спейсер» в линкерную ножку ADC, увеличивая отделение цитотоксического объекта MMAE и места прикрепления антитела посредством PL13 приблизительно на 39 атомов (против 22 атомов ранее в PL13-vcMMAE). Полагают, что данный «спейсер» должен увеличить гибкость вращения звена PL13, которая может влиять на кинетику присоединения по Михаэлю к свободному тиолу.
Способ:
Очистили 40 мг неочищенного Fmoc-val-cit-4-аминобензоил-MMAE. Затем посредством аминолизиса удалили группу N-Fmoc, и для предоставления 24 мг материала очистили функционализированное амином цитотоксическое соединение. Его использовали для присоединения PL13-NH-ПЭГ4-COOH посредством стандартного химического образования активного сложного эфира с гидроксибензотриазолом.
Результаты:
Синтезировали PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE. Данная молекула отображает пример расщепляемой системы ADC в соответствии с настоящим изобретением.
9. Конъюгация PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE и Малеимид-val-cit-4-аминобензоил-MMAE с трастузумабом.
Способ:
Трастузумаб восстановили с 2,4-кратным избытком трис(2-карбоксиэтил)фосфина (TCEP) в течение 1 часа при комнатной температуре в присутствии этилендиаминтетрауксусной кислоты (ЭДТА). Антитело повторно помещали в виде буфера в PBS. Трастузумаб в концентрации, равной 20 мг/мл, конъюгировали с 20-кратным избытком PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE в присутствии 5% о/о DMA при комнатной температуре в течение 16 часов. Дополнительно линкер малеимид-val-cit-4-аминобензоил-MMAE присоединяли к трастузумабу (20 мг/мл) с молярным избытком, составляющим 6, при комнатной температуре в течение 1 часа. Полученный ADC анализировали с помощью ХГВ, PLRP и эксклюзионной хроматографии.
Результаты:
Результатом характеристики с помощью ХГВ трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE был расчет DAR, равного 4,29 (см. фигуру 27 A).
Результатом характеристики с помощью ХГВ трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE был расчет DAR, равного 3,15 (см. фигуру 27 B).
На Фигурах 27A и 27B цифры обозначают количество лекарственного средства, конъюгированного с полноразмерным антителом. Таблица отображает относительную процентную долю площади каждого пика из профиля элюции ХГВ. Среднее DAR рассчитывают посредством умножения процентной доли площади пика на соответствующий лекарственный объект для получения взвешенной площади пика. Взвешенные площади пиков суммируют и делят на 100 для придания итогового значения DAR.
Анализ DAR восстановленного DTT трастузумаб-малеимид-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE с помощью PLRP подтвердил, что средний лекарственный объект составляет 4,3 (см. фигуру 28A и Фигуру 29).
Анализ восстановленного DTT трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE с помощью PLRP подтвердил, что средний лекарственный объект составляет 3,8 (см. фигуру 28B и Фигуру 29).
На Фигурах 28A и 28B цифры обозначают количество лекарственного средства, конъюгированного с легкой (L) или тяжелой (H) цепью антитела.
Анализ как трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE (HER-MAL-MMEA), так и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE (HER-PL-13-MMEA) при эксклюзионной хроматографии показал, что оба образца представлены в виде мономерных разновидностей (см. фигуру 30A и B). Таблица под Фигурами 30A и 30B показывает расчет разновидностей с высокой молекулярной массой (HMW), мономерных разновидностей и разновидностей с низкой молекулярной массой (LMW).
10. Оптимизированные условия для конъюгации PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE
Способ:
Трастузумаб (23,5 мг/мл) восстанавливали 2,4 эквивалентами TCEP в течение 2 часов при комнатной температуре для получения среднего значения 4,5 свободных тиолов. Восстановленный трастузумаб конъюгировали с 20-кратным избытком PL13-NH-ПЭГ4-val-cit-MMAE в присутствии 10% о/о DMA при 30°C в течение 18 часов. Конъюгат анализировали с помощью ХГВ и PLRP хроматографии (см. фигуру 31 A и B).
Результаты:
Данные ХГВ и PLRP показывают существенное улучшение эффективности конъюгации. Более высокий уровень эффективности конъюгации также приводил к значительному уменьшению уровня «добавочных» видов DAR и к уменьшению уровня неконъюгированных антител.
11. Конъюгация трастузумаб-PL13-NH-ПЭГ4-val-cit-аминобензоил-MMAE (A) и трастузумаб-малеимид-val-cit-аминобензоил-MMAE (B) в масштабе 150 мг, демонстрирующая масштабируемость процесса
Способ:
Трастузумаб (24,53 мг/мл) восстанавливали 2,1 эквивалентами TCEP в течение 2 часов при комнатной температуре. Восстановленный трастузумаб конъюгировали с 20-кратным избытком PL13-NH-ПЭГ4-val-cit-MMAE в присутствии 10% о/о DMA при 30°C в течение 18 часов.
Трастузумаб в концентрации, составляющей 25,68 мг/мл, восстанавливали 1,95 эквивалентами TCEP в течение 2 часов при комнатной температуре. Восстановленный трастузумаб конъюгировали с 6-кратным избытком малеимид-val-cit-MMAE в присутствии 10% о/о DMA при комнатной температуре в течение 1 часа.
Конъюгаты проанализировали с помощью ХГВ и эксклюзионной хроматографии (см. фигуры 32 и 33).
Результаты:
Профили ХГВ показали аналогичную эффективность конъюгации для трастузумаб-PL13-NH-ПЭГ4-val-cit-аминобензоил-MMAE (Фигура 32A) и трастузумаб-малеимид-val-cit-аминобензоил-MMAE (Фигура 32B). Эксклюзионная хроматография (Фигуры 33A и 33B) подтвердила, что оба конъюгата представляют собой мономеры с наличием только небольшого количества разновидностей высокой молекулярной массы (1,4-2,4%). это демонстрирует масштабируемость процесса конъюгации, разрабатываемого с использованием линкеров настоящего изобретения.
12. Конъюгация PL13-NH-ПЭГ4-val-cit-аминобензоил-MMAE с Thiomab, демонстрирующая успешную конъюгацию со сконструированным трастузумабом (Thiomab)
Способ:
Трастузумаб с цистеиновой мутацией (V205C), введенный в легкую цепь антитела, конъюгировал в концентрации, равной 10 мг/мл, с 40-кратным избытком PL13-NH-ПЭГ4-val-cit-MMAE в присутствии 10% DMA в буфере pH 7,4. Реакции конъюгации проводили при 35°C в течение 48 часов.
Результаты:
Профиль ХГВ трастузумаба (V2015C)-PL13-NH-ПЭГ4-val-cit-MMAE демонстрирует, что PL13 может быть успешно конъюгирована с антителами со сконструированными остатками Cys при обоих pH (Фигура 34). Похоже, что на скорость и степень реакции конъюгации влияет микроокружение тиола.
13. Практическая ценность ADC в соответствии с настоящим изобретением в виде ADC.
Продукты конъюгации ADC, которые описаны выше в разделе 8, дополнительно подвергали тестированию in vivo и in vitro для демонстрации их практической ценности в качестве коммерческих ADC.
Стабильность in vitro трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE в присутствии NAC
Способ:
Стабильность лекарственного средства-линкера для конъюгатов трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE оценивали в присутствии NAC в буфере PBS.
Результаты:
На конъюгат трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE не оказывало влияние присутствие NAC в буфере (Фигура 36). Трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE показал сниженную стабильность в присутствии NAC (см. фигуру 35). Фигура 36, в частности, демонстрирует отсутствие изменения профиля для содержащего PL13 ADC, обусловленного стимуляцией свободным тиолом, показывающее стабильность конструкции.
Стабильность in vitro трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE в плазме мышей.
Стабильность сыворотки in vitro ADC трастузумаб-PL13-NH-ПЭГ4-val-cit-аминобензоил-MMAE и трастузумаб-малеимид-val-cit-аминобензоил-MMAE сравнивали в плазме мышей.
Способ:
Трастузумаб-PL13-NH-ПЭГ4-val-cit-аминобензоил-MMAE и трастузумаб-малеимид-val-cit-аминобензоил-MMAE по отдельности добавляли в фильтрованную плазму голых бестимусных мышей до концентрации, составляющей 0,2 мг/мл. Растворы перемешивали, и в трех экземплярах брали аликвоты, равные 50 мкл, и быстро замороженные в жидком азоте (временная точка - 0 ч). Растворы плазмы ADC инкубировали при 37°C в течение 7 дней. Аликвоты, равные 50 мкл, отбирали в трех экземплярах для каждой временной точке: 1, 2, 3, 4, 5, 6 и 7 день, и хранили при -80°C до анализа.
Результаты:
Стабильность ADC отслеживали с помощью анализа жидкостной хроматографии с ионизацией электрораспылением/масс-спектрометрического анализа. Перед масс-спектрометрическим анализом образцы плазмы предварительно очищали и обрабатывали трипсином/бромцианом. Четыре неконъюгированных пептида (два из тяжелой цепи и два из легкой цепи) и два конъюгированных пептида (один из тяжелой цепи и один из легкой цепи) отбирали для мониторинга стабильности ADC. Усредненные данные по неконъюгированным пептидам соответствуют стабильности компонента антитела в плазме мышей (общие антитела), а данные по конъюгированным пептидам показывают стабильность ADC конъюгата (конъюгированный пептид из легкой цепи, конъюгированный пептид из тяжелой цепи).
Эти данные in vitro показали, что трастузумаб-малеимид-val-cit-аминобензоил-MMAE претерпевает высвобождение лекарственного средства как в легкой цепи, так и в тяжелой цепи, тогда как компонент антитела является стабильным (Фигура 37A). Потеря лекарственного средства из пептида тяжелой цепи была более быстрой по сравнению с пептидом легкой цепи, показывая, что на скорость потери лекарственного средства влияет участок конъюгации.
Конъюгат трастузумаб-PL13-NH-ПЭГ4-val-cit-аминобензоил-MMAE удерживал лекарственное средство MMAE на протяжении всего 7-дневного периода инкубирования, показывая, что PL13 придает стабильность обоим участкам конъюгации (Фигура 37B). Наблюдаемая изменчивость обоих конъюгатов обусловлена эффективностью извлечения образцов для способа масс-спектрометрии с ионизацией электрораспылением, применяемого для анализа образцов.
Стабильность in vivo трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE у мышей
Способ:
Стабильность in vivo оценивали у мышей, которым инъецировали 5 мг/кг конъюгатов трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE. Перед анализом жидкостной хроматографии с масс-спектрометрией образцы плазмы предварительно очищали и обрабатывали трипсином/бромцианом. Для мониторинга стабильности ADC отбирали два конъюгированных пептида (один из тяжелой цепи и один из легкой цепи).
Результаты:
Стабильность конъюгированных пептидов является результатом двух явлений: 1) катаболической деградации ADC и 2) потери лекарственного средства вследствие нестабильности линкера. Конъюгированные пептиды, происходящие из трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE, показывают более хорошую стабильность в 1 день в плазме мышей, чем пептиды, происходящие из трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE. Наблюдаемое различие, вероятно, является следствием более быстрой потери лекарственного средства из конъюгированных пептидов, происходящих из трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE, чем из трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE, что согласуется с данными плазмы мышей in vitro, показывающими быстрое высвобождение лекарственного средства для трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE в пределах первых четырех дней инкубации (Фигура 38); приблизительно 70% лекарственного средства, связанного с легкой цепью, и 90% лекарственного средства на тяжелой цепи терялось в пределах первых двух дней. В отличие от этого, трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE удерживает больше лекарственного средства благодаря стабильности линкера в течение более долгого периода времени.
Стабильность in vitro трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE в различных клеточных линиях
На Фигурах 39A-39C SKBR3, BT747 и JIMT-1 показаны данные гибели клеток для ADC, описанных выше. В данном тесте отобрали клеточные линии SKBR3, BT747 и JIMT-1, так как известно, что они экспрессируют рецептор Her2. Дополнительно известно, что клеточная линия JIMT-1 является устойчивой к трастузумабу. На фигурах 39A-39C «ADC mal» относится к трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE, а «ADC-PL13» относится к трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE. Относительная активность in vitro протестированных конъюгатов против трех клеточных линий показывает, что данные для трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE сопоставимы с трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE. Соответственно, эти данные показывают, что ADC настоящего изобретения является активным, и поэтому присутствие PL13 не оказывает отрицательного действия на уничтожение клеток.
Стабильность in vivo трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE у мышей, имеющих опухоли из клеток рака молочной железы
На Фигурах 40, 41 и 42 показаны данные о ксенотрансплантате, связанном с воздействием ADC на мышей, имеющих опухоли из клеток рака молочной железы. Использовали клеточную линию рака молочной железы BT474 (экспрессор Her2 с высокой восприимчивостью к трастузумабу).
Для измерения токсичности ADC in vivo используют массу мышей (как показано на фигуре 40). Из полученных данных можно видеть, что трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE (ADC-mal) (Фигура 40A) и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE (ADC-PL13) (Фигура 40B) оказывают незначительное воздействие на массу мышей в течение периода лечения. Это является показателем, что ADC настоящего изобретения обладают пригодными уровнями токсичности для коммерческого использования.
Фигура 41 показывает эффективность протестированных ADC в трех дозах (0,1, 5 и 10 мг/кг) при опухолевом росте в течение 21-дневного периода лечения. Рост опухоли определяли посредством изменений объемов опухоли. По сравнению с группой, не получавшей лечение, мыши, получающие лечение обоими соединениями с 0,1 мг/кг, испытывали задержку роста опухоли. В отличие от этого, все животные, получавшие дозы трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE (ADC-mal) и трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE (ADC-PL13) с 5 и 10 мг/кг, показали полные ответы на протяжении периода лечения.
Фигура 42 показывает эффективность протестированных ADC в трех дозах (0,1, 5 и 10 мг/кг) при гистологическом фенотипе зрелости опухоли в течение 10-дневного периода лечения. Ткани опухоли исследовали микроскопически после окрашивания гематоксилином и эозином и классифицировали следующим образом:
0: отсутствие массы ксенотрансплантата; случайно выделенные опухолевые клетки в подкожном слое или жировой ткани
1: небольшая фрагментированная масса; неполная последовательность развития эпителия
2: ксенотрансплантат, демонстрирующий значительную потерю клеток
3: зональная потеря клеток с областями зрелой опухоли
4: интактная масса ксенотрансплантата, демонстрирующая полную последовательность развития эпителия и связанную патологию
Не наблюдалось уменьшения зрелости опухоли либо для трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE (ADC-PL13), либо для трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE (ADC-mal), вводимых дозами по 0,1 мг/кг, при этом между двумя ADC не наблюдалось значительных различий. Однако трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE, вводимый дозами по 5 и 10 мг/кг, показал значительно уменьшенную зрелость опухоли, начиная с 3 дня (степень злокачественности 3 и степень злокачественности 3/2, соответственно). Данный эффект был более выражен на 10 день (степень злокачественности 1 для 5 мг/кг и степень злокачественности 1/0 для 10 мг/кг) с несколькими образцами, показывающими отсутствие опухолевой массы. Трастузумаб-малеимид-val-cit-4-аминобензоил-MMAE, вводимый дозами 5 и 10 мг/кг уменьшал зрелость опухоли (степень злокачественности 4/3 и степень злокачественности 4/3/2, соответственно), начиная с 3 дня, но эффект был менее выраженным по сравнению с животными, которым вводили соответствующие дозы трастузумаб-PL13-NH-ПЭГ4-val-cit-4-аминобензоил-MMAE на 3 день. Более того, отмечали значительно более высокую гетерогенность опухоли для ADC-mal, чем наблюдаемую для ADC-PL13 для доз 5 и 10 мг/кг на 10 день.
14. Демонстрация реакционной способности линкера PL11-PEG20КДа, PL12-PEG20КДа и PL13-PEG20КДа с альбумином
Как указано выше, основная часть цистеинтиолов, присутствующих в альбумине промышленного класса являются заблокированными, и поэтому перед конъюгацией с линкерной молекулы необходима стадия восстановления.
Способ:
Альбумин (221 мкМ) восстанавливали дитиотреитолом (DTT) (1 мМ) в забуференном фосфатом солевом растворе (PBS), pH 7,0, содержащем этилендиаминтетрауксусную кислоту (ЭДТА) (1 мМ) в течение 1 часа при комнатной температуре (RT) с последующим обессоливанием на колонке Nap-5 и количественным определением посредством УФ-измерения. Конъюгацию 20 КДа PEG-PL-12 (молярный избыток, составляющий 10) или 20 КДа PEG-PL-13 (молярный избыток, составляющий 10) с восстановленным альбумином (20 мкМ) проводили в PBS, pH 7,4, с 1 мМ ЭДТА в течение 1 дня при комнатной температуре. Аналогичным образом конъюгацию 20 КДа PEG-малеимида (молярный избыток, составляющий 1,1) с восстановленным альбумином (20 мкМ) проводили с PBS, pH 7,4, содержащем 1 мМ ЭДТА, в течение 1 дня при комнатной температуре. Реакции анализировали с помощью ДСН-ПААГ-электрофореза, и количественное определение выполняли посредством анализа плотности полосы белка с помощью ДСН-ПААГ-электрофореза с использованием программного обеспечения ImageLab (Biorad).
Результаты:
Спустя 1 день наблюдали только умеренные показатели конъюгации с восстановленным альбумином промышленного класса. Конъюгация PL13 проходила с сопоставимым с контролем малеимидом показателем, тогда как PL12 дал немного более низкий показатель на протяжении такого же временного периода. Это показано на фигуре 43.
15. Оптимизация конъюгации PL11, PL12 и PL13 с альбумином
Конъюгацию линкера с альбумином определяли при рН 5,5 для PL-11 и при рН 5,5, 6,5, 7,5, 8,0 и 8,5 для PL-12 и PL -13.
Способ:
Конъюгацию PL-11 (молярный избыток, составляющий 10) с альбумином (50 мкМ) проводили в 50 мМ ацетата натрия, pH 5,5, в течение 24 часов при 37°C. Конъюгацию PL-12 и PL-13 (молярный избыток, составляющий 10) с альбумином (50 мкМ) проводили в следующих буферах: 50 мМ ацетата натрия, pH 5,5; PBS 1 мМ ЭДТА, pH 6,5; PBS 1 мМ ЭДТА, pH 7,5; 100 мМ фосфат; 1 мМ ЭДТА, pH 8,0; и 100 мМ карбоната натрия, 1 мМ ЭДТА, pH 8,5; в течение 24 часов при 37°C.
После завершения все образцы альбумина обессоливали на колонке Nap-5 в буфер PBS (pH 7,4). Эффективность конъюгации количественно определяли посредством анализа Эллмана. Анализ Эллмана выявляет и количественно определяет свободные цистеиновые остатки посредством взаимодействия 5,5'-дитио-бис-(2-нитробензойной кислоты) со свободными тиольными группами. Конъюгация линкерных молекул со свободной тиольной группой 34Cys в альбумине блокирует выявление данных групп посредством реагента Эллмана по сравнению с контролем неконъюгированным альбумином. Уменьшение концентрации определяемых свободных тиолов использовали для подсчета количества линкерных молекул, конъюгированных с альбумином.
Результаты:
Конъюгация PL-11 с альбумином при рН 5,5 проходила с показателем 82%. Определили, что оптимальный pH для конъюгации PL-12 (91%) и PL-13 (94%) составляет 7,5. Данные результаты показаны на фигуре 44.
16. Демонстрация стабильности конъюгата линкер-альбумин посредством масс-спектрометрии с ионизацией электрораспылением
В дополнение, конъюгаты альбумин-PL11, альбумин-PL12 и альбумин-PL13 проанализировали посредством масс-спектрометрии с ионизацией электрораспылением.
Способ:
Конъюгацию PL-11 (молярный избыток, составляющий 20) с альбумином (50 мкМ) проводили в PBS, содержащем ЭДТА (1 мМ) при рН 6,5 в течение 24 часов при 37°C. Конъюгацию PL-12 и PL-13 (молярный избыток, составляющий 10) с альбумином (50 мкМ) проводили в PBS, содержащем ЭДТА (1 мМ) при рН 7,5 в течение 24 часов при 37°C. Конъюгаты альбумин-линкер проанализировали посредством масс-спектрометрии с ионизацией электрораспылением.
Результаты:
Фигура 45 показывает результаты масс-спектрометрии с ионизацией электрораспылением, полученные для конъюгации альбумин-PL-11 (A), конъюгации альбумин-PL-12 (B) и конъюгации альбумин-PL-13 (C).
На основании интенсивности масс-спектрометрического сигнала были выявлены и количественно определены следующие разновидности альбумина (необходимо отметить, что MW означает молекулярную массу):
Альбумин-PL11
Неконъюгированный альбумин - 6%
Ожидаемая MW неконъюгированного альбумина-66440 (определенная MW=66445 Да)
Конъюгат альбумин-PL11-90%
Ожидаемая MW альбумин-PL11-66649 Да (определенная MW=66650 Да)
Альбумин, конъюгированный с двумя PL11 ~ 4%
Ожидаемая MW альбумин-2-PL11-66858 Да (определенная MW=66858 Да)
Альбумин-PL12
Неконъюгированный Альбумин - 1%
Ожидаемая MW неконъюгированного альбумина - 66440 Да (определенная MW=66441 Да)
Альбумин-PL12-92%
Ожидаемая MW альбумин-PL12-66663 Да (Определенная MW=66664 Да)
Альбумин, конъюгированный с двумя PL12-7%
Ожидаемая MW альбумин-2-PL12-66886 Да (Определенная MW=66886 Да)
Альбумин-PL13
Неконъюгированный Альбумин - 5%
Ожидаемая MW неконъюгированного альбумина - 66440 Да (Определенная MW=66441 Да)
Альбумин-PL13-94%
Ожидаемая MW альбумин-PL13-66631 Да (Определенная MW=66632 Да)
Альбумин, конъюгированный с двумя PL13-1%
Ожидаемая MW альбумин-2-PL13-66822 Да (Определенная MW=66822 Да)
Конкретно, со ссылкой на фигуру 45, пики (4501), (4504) и (4507) соответствуют не вступившему в реакцию и окисленному альбумину, пики (4502), (4505) и (4508) соответствуют одиночному конъюгату альбумина, а пики (4503), (4506) и (4509) соответствуют двойному конъюгату альбумина.
17. Демонстрация стабильности конъюгатов альбумин-линкер в глутатионе
Стабильность конъюгатов альбумин-линкерная молекула определяли в присутствии избытка глутатиона и проанализировали посредством масс-спектрометрии с ионизацией электрораспылением в течение периода, составившего 7 дней.
Способ:
Образцы конъюгата альбумин-PL-12 (0,5 мг/мл) инкубировали с восстановленным глутатионом (1 мМ) в PBS (pH 7,4) при 37°C в течение 7 дней. Образцы анализировали с помощью масс-спектрометрии с ионизацией электрораспылением.
Результаты:
Фигура 46 показывает полученные результаты для конъюгата альбумин-PL-12 в качестве репрезентативного примера. Аналогичную тенденцию наблюдали для конъюгатов альбумин-PL-11 и альбумин-PL-13.
Фигура 46 показывает результаты масс-спектрометрии с ионизацией электрораспылением на 0, 1, 4 и 7 день. На фигуре 46 пики (4601), (4603), (4605) и (4608) соответствуют альбумину, пики (4602), (4604), (4606) и (4609) соответствуют конъюгату альбумин-PL12, а пики (4607) и (4610) соответствуют GSH-альбумин. Соответственно, показано, что:
- основной присутствующей разновидностью является конъюгат альбумин-PL12 (MW=~66664 Да)
- после инкубации с 1 мМ глутатиона имеется крайне медленное увеличение сигнала альбумин-GSH (~8%, MW=66752 Да), начинающееся с 4 дня инкубации с глутатионом и достигающее ~13% на 7-ой день инкубации.
Можно заключить, что конъюгаты альбумин-линкер настоящего изобретения демонстрируют удовлетворительную стабильность в конкурентной среде.
18. Производство конъюгатов альбумин-доксорубицин с использованием линкеров в соответствии с настоящим изобретением
Способ:
Альбумин, тиоальбумин (простой цистеиновый мутант) и тиоальбумин (двойной цистеиновый мутант) конъюгировали с 14, 20 и 30-кратным избытком линкера PL13-NH-ПЭГ4-val-cit-4-аминобензоил-доксорубицин (Фигура 47), соответственно. Реакции проводили в 147 мМ фосфата натрия, pH 7,5, в присутствии 10% о/о DMA и 0,6 мМ ЭДТА при 37°C в течение 2 дней в темноте. После данного времени реакции обессоливали на колонках PD-10, уравновешенных в буфере PBS, pH 7,4.
Эффективность конъюгации определяли посредством спектроскопии в УФ и видимой части спектра с использованием коэффициента поглощения и экстинкции доксорубицина при 495 нм (ɛ=8030 M-1, см-1) и коэффициента поглощения и экстинкции альбумина при 280 (ɛ=34445 M-1, см-1) с поправкой для поглощения доксорубицина при 280 нм в соответствии с уравнением:
Степень агрегации конъюгата альбумин-доксорубицин определяли анализом с помощью ДСН-ПААГ-электрофореза в невосстанавливающих условиях и эксклюзионной хроматографии.
10 мкл каждого конъюгата альбумин-доксорубицин в загрузочном буфере для ДСН-ПААГ-электрофореза загрузили на NuPAGE 4-12% Бис-Трис гель и подвергали воздействию в течение 45 минут при 200 В. Свойство нативной флуоресценции доксорубицина использовали для визуализации конъюгатов альбумин-доксорубицин перед окрашиванием геля красителем Кумасси для разновидностей белка.
5 мкл каждого конъюгата загрузили в колонку HPLC для эксклюзионной хроматографии, уравновешенной 150 мМ натрий-фосфатного буфера при рН 7,0 и элюировали при скоростью потока, составляющей 1 мл/мин с детектированием при 280 нм.
Результаты:
Конъюгация доксорубицина с альбумином дикого типа и мутантами альбумина привела к показателям, составившим 55% для альбумина, 32% для тиоальбумин-однонаправленный мутант и 14% для тиоальбумин-двунаправленный мутант (см. фигуру 48).
Анализ посредством ДСН-ПААГ-электрофореза показал присутствие небольшого количества высокомолекулярных разновидностей (HMWS) во всех образцах альбумин-доксорубицин (см. фигуру 49). Эти данные согласовываются с данными, наблюдаемыми при анализе с помощью эксклюзионной хроматографии (см. фигуру 50). В дополнение, анализ с помощью ДСН-ПААГ-электрофореза подтвердил конъюгацию доксорубицина с альбумином, наблюдаемую посредством спектроскопии в УФ и видимой части спектра (см. фигуру 49, флуоресценция DOX)
Наряду с контролем неконъюгированным альбумином и неконъюгированным тиоальбумином посредством анализа эксклюзионной хроматографии проанализировали конъюгаты альбумин-доксорубицин и тиоальбумин-доксорубицин. Анализ конъюгатов доксорубицина показал, что содержание мономеров составило приблизительно 97,6% для альбумин-DOX, 86,8% для альбумин-DOX (однонаправленного мутанта) и 88,2% для альбумин-DOX (двунаправленного мутанта) (см. фигуру 50 B, D и F). Контроль неконъюгированным альбумином и тиоальбумином (см. фигуры 50 A, C и E) показал аналогичное содержание мономеров и высокомолекулярных разновидностей конъюгированного доксорубицина. В частности, Фигура 50 показывает пики на (5001), (5003), (5005), (5007), (5009) и (5011), соответствующие наличию HMWS, и пики на (5002), (5004), (5006), (5008), (5010) и (5012), соответствующие содержанию мономеров.
Оба мутанта тиоальбумина демонстрируют более выраженную тенденцию к агрегации, чем альбумин дикого типа: 13,2-14,5% для тиоальбумина (однонаправленного мутанта) и 11,8-16,6% для тиоальбумина (двунаправленного мутанта), по сравнению с 2,4-2,6% для нативного альбумина. Анализ данных образцов подтвердил, что конъюгация доксорубицина посредством PL13-ПЭГ4-val-cit-4-аминобензоила является хорошо переносимой и не вызывает дополнительную агрегацию (см. фигуру 50 A, C и F).
Соответственно, было показано, что конъюгаты лекарственного средства и белка настоящего изобретения предоставляют пригодные альтернативы известным конъюгатам лекарственного средства и белка. Кроме того, линкер, заключенный в конъюгаты лекарственного средства и белка настоящего изобретения, делает возможным безопасную и эффективную доставку лекарственного средства посредством успешного связывания лекарственного средства с белком и сохранение лекарственного средства до тех пор, пока не достигнет ткань-мишень.
Реферат
Группа изобретений относится к биотехнологии и медицине, в частности к конъюгатам лекарственного средства и белка и способам их получения. Конъюгат лекарственного средства и белка для доставки лекарственного средства получен путем взаимодействия глобулярного белка, линкера и лекарственного средства, где линкер включает азотсодержащее гетероциклическое ароматическое кольцо, включающее винильный заместитель формулы(III). Способы получения конъюгата лекарственного средства и белка включают контакт белка с линкером, связанным с лекарственным средством, либо контакт белка с линкером и последующий контакт линкера с лекарственным средством. Изобретение обеспечивает избирательную и эффективную конъюгацию, а также приводит к значительному уменьшению уровня «добавочных» видов DAR и к уменьшению уровня неконъюгированных глобулярных белков. Конъюгат удерживает больше лекарственного средства благодаря стабильности линкера в течение более долгого периода времени. 3 н. и 11 з.п. ф-лы, 50 ил., 18 пр.
Формула



Документы, цитированные в отчёте о поиске
Способ лечения опухоли у субъекта
Анти-cd79b антитела и иммуноконъюгаты и способы их применения


















Комментарии