Фторированные 4-фурфурил-3,4-дигидро-2н-бензо[1,4]тиазин-1,1-диоксиды, обладающие высокой аритмической активностью - RU2626239C1
Код документа: RU2626239C1
Описание
Изобретение относится к области медицинской химии и фармакологии, а именно к биологически активным соединениям, обладающим антиаритмическим действием.
Известны антиаритмические препараты, представлены 4 классами по фармакологическому действию - это блокаторы натриевых каналов (хинидин, лидокаин, мексилетин, прокаинамид), бета-адреноблокаторами (небиволол, метопролол), блокаторами кальциевых каналов (верапамил, дилтиазем, бепридил) и другие [1]. К побочным эффектам этих препаратов, возникающим при их длительном использовании, относят снижение сократимости миокарда, замедление пульса, развитие атриовентрикулярной блокады, аритмии. Эти медикаменты влияют и на нервную систему: они способны вызывать головокружение, сонливость, ухудшение памяти и депрессию. Кроме того, они изменяют нервно-мышечную проводимость, являясь причиной слабости, утомляемости, снижения силы мышц. Иногда после приема бета-блокаторов отмечаются кожные реакции (сыпь, зуд, алопеция) и изменения со стороны крови (агранулоцитоз, тромбоцитопения). Прием этих средств у некоторых мужчин приводит к развитию эректильной дисфункции. Именно поэтому кардиологи раз в полгода проводят смену схемы лечения аритмий и замену препарата.
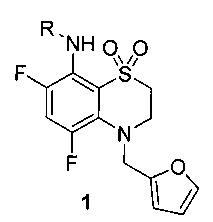
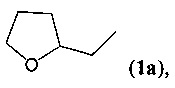
Задача, на решение которой направлено изобретение, заключается в поиске новых эффективных низкотоксичных лекарственных средств, обладающих антиаритмической активностью. Поставленная задача решается путем использования в качестве антиаритмических средств фторированных 4-фурфурил-3,4-дигидро-2-бензо[1,4]тиазин-1,1-диоксидов общей формулы 1, где R может быть метальной, циклопентильной или тетрагидрофурфурильной группой.

Соединения общей формулы 1 ранее не были описаны в литературе. Нами показано, что они могут быть получены по общей схеме, включающей в себя две стадии. На первой стадии проводят синтез 4-фурфурил-5,7,8-трифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида (3) путем взаимодействия (2-хлорэтилсульфонил)-2,3,5,6-тетрафторбензола (2) с небольшим избытком фурфуриламина в присутствии Et3N в спирте, ацетоне или ацетонитриле. Способ получения исходного соединения 2 был описан одним из соавторов в работе: В.В. Литвак, А.С. Кондратьев, В.Д. Штейнгарц. Журн, орган, химии, 2009, 45, 1648.
На второй стадии полученное трифторпроизводное 3 обрабатывали при нагревании избытком соответствующего амина RNH2 в ДМСО при 90-120°С и получали целевые препараты 1 с выходами 81-83%.

Биологическая активность соединений 1а-с была изучена путем определения острой токсичности и антиаритмического эффекта.
Острую токсичность определяли на белых беспородных мышах массой 18-22 г при пероральном введении в дозах от 50 мг/кг до 1000 мг/кг. Параметры острой токсичности рассчитывали по методу Кербера. LD50 для соединений 1а-с составила более 1000 мг/кг.
Исследование антиаритмической активности 8-тетрагидрофурфуриламино - (1а), 8-метиламино - (1b) и 8-циклопентиламино-4-фурфурил-5,7-дифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида (1с) проводили на наркотизированных половозрелых самцах крыс линии Вистар массой 180-220 г в группах по 10 животных. Аритмию вызывали путем однократного введения в бедренную вену 10% раствора CaCl2 в дозе 250 мг/кг или адреналина гидрохлорида в дозе 0.3 мг/кг, являющихся летальными для крыс в 100% случаях. В качестве эталона сравнения использовали раствор метопролола, вводимый внутривенно в дозах 3 и 0,15 мг/кг.
Обнаружено, что введение препарата 1а в дозе 0.5 мг/кг в виде раствора полностью предотвращает развитие хлоридкальцевой аритмии и восстанавливает показатели ЭКГ до нормы у 50% крыс, которым был введен адреналин. Снижение дозы препарата до 0.05 мг/кг приводит к увеличению эффективности на адреналиновой аритмии (90%) и к отсутствию таковой на хлоридкальциевой аритмии. Увеличение дозы до 5.0 мг/кг определяет его ЕД50 на обеих моделях.
Введение исследуемого препарата 1b в дозе 5 мг/кг блокирует развитие адреналиновой аритмии у 50% исследуемых животных и развитие хлоридкальциевой аритмии у 40%. Снижение дозы до 0.5 мг/кг и 0.05 мг/кг увеличивает эффективность на адреналиновой аритмии и приводит к отсутствию эффекта на хлоридкальциевой. Препарат 1с не показал активности на хлоридкальциевой аритмии, но полностью купировал адреналовую аритмию в дозе 5.0 и 0.5 мг/кг. Данные по изучению антиаритмических препаратов 1а-с представлены в Таблице 1.
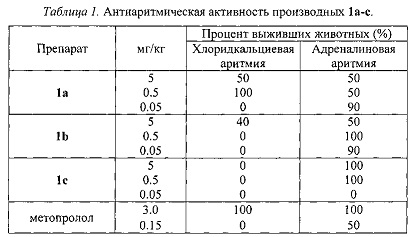
Из таблицы 1 видно, что препараты 1а и 1b в дозах в более чем в три раза ниже дозы метопролола имеет более выраженный антиаритмический эффект, чем препарат сравнения. Обобщая проведенные исследования, можно заключить, что новые соединения - производные фторированных 4-(2-фурилметил)-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксидов общей формулы 1 в дозах 0.05, 0.5 и 5 мг/кг обладают высокой антиаритмической активностью на моделях хлоридкальцевой (1а) и адреналиновой аритмии. Соединения проявляют дозозависимый эффект на обеих моделях.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение 4-фурфурил-5,7,8-трифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида (3).
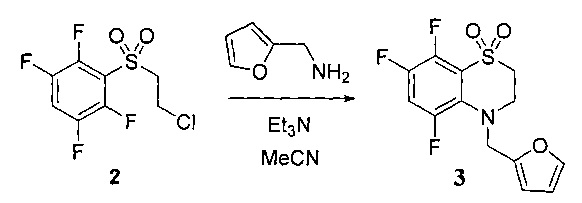
Смесь 0.92 г (0.0033 моль) (2-хлорэтилсульфонил)-2,3,5,6-тетрафторбензола (2), 0.485 г (0.005 моль) 2-фурфуриламина и 0.833 г (0.0083 моль) триэтиламина в 20 мл ацетонитрила выдерживали 72 ч при комнатной температуре. Смесь упарили, сухой остаток промыли 50 мл воды, отфильтровали, перекристаллизовали из водного пропанола-2 и сушили на воздухе. Выход 4-фурфурил-5,7,8-трифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида составил 0.869 г (82%). Т.пл. 106-107°C. Спектр ЯМР1Н (CDCl3), δ, м.д.: 3.19 м (2Н), 3.86 м (2Н), 4.46 с (2Н), 6.25 д (1H J=3.2 Гц), 6.32 д.д. (1Н, J=3.2, 1.9 Гц), 7.08 д.д.д. (1Н, J=12.1, 9.5, 7.3 Гц), 7.36 д.д. (1Н, J=1.7, 0.5 Гц). Спектр ЯМР19F δ, м.д.: 20.2 д.д. (I1F, J=22.5, 9.5 Гц), 21.6 д.д.д. (1F, J=22.5, 13.6, 7.2 Гц), 42.2 т (1F, J=12.8 Гц). Найдено: m/z 317.0335 [М]+ C13H10F3NO3S. Вычислено: М 317.0328.
Пример 2. Получение 4-фурфурил-8-тетрагидрофурфуриламино-5,7-дифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида (1а).
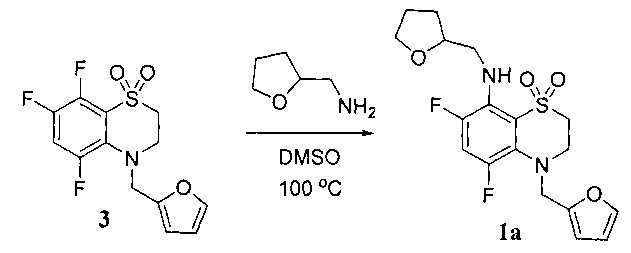
Смесь 1 г (0.00315 моль) 4-фурфурил-5,7,8-трифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида (3) и 0.954 г (0.00945 моль) тетрагидрофурфуриламина в 3 мл ДМСО выдерживали 48 ч при 100°C. Смесь разбавляли 30 мл воды, выпавший осадок отфильтровывали, перекристаллизовали из водного пропанола-2 и сушили на воздухе. Выход 1.048 г (83%). Т.пл. 102-103°C. Спектр ЯМР1Н (CDCl3), δ, м.д.: 1.71 м (1Н), 1.83-2.05 (3Н), 3.19 м (2Н), 3.34-3.47 (2Н), 3.72-3.83 (3Н), 3.89 м (1Н), 4.10 м. (1Н), 4.36 с (2Н), 5.25 уш.с (1Н), 6.23 д (1H, J=3.2 Гц), 6.32 д.д. (1Н, J=3.2, 1.9 Гц), 6.90 т. (1Н, J=12.1 Гц), 7.37 д.д. (1Н, J=1.7, 0.8 Гц). Спектр ЯМР19F δ, м.д.: 32.0 д (1F, J=12.1 Гц), 33.0 д (1F, J=12.0 Гц). Найдено: m/z 398.1114 [М]+ C18H20F2N2O4S Вычислено: М 398.1106.
Пример 3. Получение 8-метиламино-4-фурфурил-5,7-дифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида (1b).

Смесь 1 г (0.00315 моль) 4-фурфурил-5,7,8-трифтор-3,4-дигидро-2Я-бензо[1,4]тиазин-1,1-диоксида (3) и 1.17 г (0.0126 моль) метиламина (35% водн.) в 3 мл ДМСО выдерживали 48 ч при 100°C. Смесь разбавляли 30 мл воды, выпавший осадок отфильтровывали, перекристаллизовали из водной уксусной кислоты, сушили сперва на воздухе, затем в вакууме. Выход 0.840 г (81%). Т.пл. 87-88°C. Спектр ЯМР1Н (CDCl3), δ, м.д.: 3.01 д (3Н, J=4.1 Гц), 3.18 м (2Н), 3.78 м (2Н), 4.36 с (2Н), 4.92 уш.с (1Н), 6.23 д (1Н, J=3.1 Гц), 6.32 д.д. (1Н, J=3.1, 1.9 Гц), 6.90 т. (1H, J=12.2 Гц), 7.37 д.д. (1Н, J=1.7, 0.7 Гц). Спектр ЯМР19F δ, м.д.: 31.1 м (1F), 32.9 д (1F, J=12.0 Гц). Найдено: m/z 328.0689 [M]+ C14H14F2N2O3S. Вычислено: М 328.0688.
Пример 4. Получение 4-фурфурил-8-циклопентиламино-5,7-дифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида (1с).
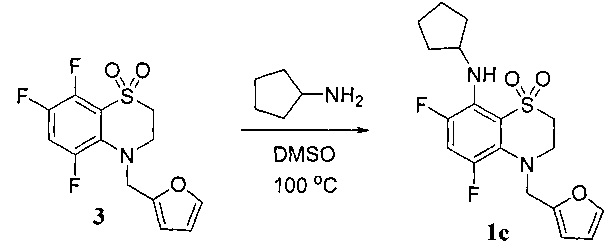
Смесь 1 г (0.00315 моль) 4-фурфурил-5,7,8-трифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида (3) и 0.665 г (0.00783 моль) циклопентиламина в 3 мл ДМСО выдерживали 2 суток при 100°C. Смесь разбавляли 30 мл воды, выпавший осадок отфильтровывали, перекристаллизовали из водной уксусной кислоты, сушили на воздухе, затем в вакууме. Выход 0.995 г (83%). Т.пл. 88-89°C. Спектр ЯМР1Н (CDCl3), δ, м.д.: 1.46-1.64 (4Н), 1.66-1.80 (2Н), 1.81-1.95 (2Н), 3.17 м (2Н), 3.77 м (2Н), 4.08 м. (1Н), 4.34 с (2Н), 5.01 уш.с (1Н), 6.23 д (1H, J=3.2 Гц), 6.31 д.д. (1Н, J=3.2, 1.9 Гц), 6.89 т. (1H, J=12.1 Гц), 7.36 д.д. (1H, J=1.9, 0.8 Гц). Спектр ЯМР19F δ, м.д.: 32.2 д (1F, J=12.1 Гц), 33.1 д.д. (1F, J=12.0, 2.7 Гц). Найдено: m/z 382.1156 [М]+ C18H20F2N2O3S. Вычислено: М 382.1157.
Пример 5. Исследование антиаритмической активности 8-тетрагидрофурфуриламино - (1а), 8-метиламино (1b) и 8-циклопентиламино-4-фурфурил-5,7-дифтор-3,4-дигидро-2H-бензо[1,4]тиазин-1,1-диоксида (1с). Опыты проводили на наркотизированных (тиопентал натрия в дозе 30 мг/кг внутрибрюшинно) половозрелых самцах крыс линии Вистар массой 180-220 г. Животные были получены из вивария ИЦиГ СО РАН, все манипуляции проводили в соответствии с правилами и принципами гуманного обращения с животными. Опыты проводились в одно и то же время с 900 до 1200. Для выполнения исследований животных разделяли на группы по 10 особей в каждой.
Препараты вводили внутривенно в дозах 5 мг/кг, 0.5 мг/кг и 0.05 мг/кг. Аритмию вызывали путем однократного введения в бедренную вену 10% раствора CaCl2 в дозе 250 мг/кг или адреналина гидрохлорида (АГ) в дозе 0.3 мг/кг. Данные дозы CaCl2 и АГ являются летальными для крыс в 100% случаях. Запись ЭКГ производилась в течение 10 мин. ЭКГ регистрировали во втором стандартном отведении на приборе фирмы «LabLinc V» model v75-ll. Оценивали длительность интервалов RR, PQ, QRS, QT, зубца Р; амплитуду зубцов Р, Т, R. Обработка данных велась программой "Statistica 6.0", используя параметрический анализ Стьюдента. В качестве отклонения от среднего значения использовалась средняя статистическая ошибка.
Результаты приведены в таблице 1.
Установлено, что соединения 1а-с обладают высокой антиаритмической активностью в тестах хлоридкальциевой (1а) и адреналиновой аритмии (1а-с).
Источник информации
1. Машковский М.Д. Лекарственные средства. Т. 1. М.: Новая волна. 2012.
Реферат
Изобретение относится к новым фторированным 4-фурил-3,4-дигидро-2Н-бензо[1,4]тиазин-1,1-диоксидам общей формулы 1. Технический результат: получены новые соединения формулы 1, обладающие высокой антиаритмической активностью. 1 табл., 5 пр.
Формула


Документы, цитированные в отчёте о поиске
Гетероциклические противовирусные соединения

Комментарии