Конъюгаты белок-полимер-лекарственное средство - RU2617402C2
Код документа: RU2617402C2
Чертежи






Описание
РОДСТВЕННЫЕ ЗАЯВКИ
Эта заявка включает в себя путем ссылок содержание указанных далее заявок на патент США и, на основании Кодекса законов США 35 USC § 119(e), испрашивает приоритет заявки на патент США № 61/495771, зарегистрированной 10 июня 2011 года; заявки на патент США № 61/501000, зарегистрированной 24 июня 2011 года; заявки на патент США № 61/513234, зарегистрированной 29 июля 2011 года; заявки на патент США № 61/566935, зарегистрированной 5 декабря 2011 года; заявки на патент США № 61/605618, зарегистрированной 1 марта 2012 года; и заявки на патент США № 61/618499, зарегистрированной 30 марта 2012 года. Содержание этих заявок приводится в описании настоящего изобретения путем ссылок на них.
УРОВЕНЬ ТЕХНИКИ
Обычно, лекарственные препараты состоят из синтетических малых молекул, которые вводят перорально (в виде твердых пилюль или жидкостей) или в виде инъекций. За последние тридцать лет, лекарственные формы (то есть, композиции, которые позволяют регулировать направление и/или скорость доставки лекарственного средства и обеспечивают доставку лекарственного средства в заданное место) становятся все более распространенными и все более сложными. Тем не менее, многие вопросы и проблемы, касающиеся разработки новых методов лечения, а также механизмов, с помощью которых они могут быть реализованы, остаются нерешенными. Например, многие лекарственные препараты проявляют ограниченные или же пониженные активности и терапевтические эффекты в силу того, что они обычно либо подвергаются частичному разложению до того, как достигают требуемого органа или области в организме, либо накапливаются в тканях, не являющихся объектом лечения, либо в силу и той и другой причины.
Поэтому, одной задачей в области систем доставки лекарственных средств является доставка лекарственных препаратов в неизменном виде в конкретно заданные области организма с помощью системы, которая может стабилизировать лекарственное средство и регулировать in vivo перенос лекарственного средства, используя либо физиологические, либо химические механизмы, либо и те и другие.
В качестве лекарственных средств с направленной доставкой были разработаны конъюгаты антитело-лекарственное средство. Антитела против антигенов поверхности различных раковых клеток были конъюгированы с различными цитотоксическими средствами, которые ингибируют различные важные клеточные мишени, такие как микротрубочки (мейтанзиноиды, ауристатины, таксаны: патенты США № 5208020; 5416064; 6333410; 6441163; 6340701; 6372738; 6436931; 6596757 и 7276497); ДНК (калихимицин, доксорубицин, аналоги CC-1065; патенты США № 5475092; 5585499; 5846545; 6534660; 6756397 и 6630579). Конъюгаты антител с некоторыми из этих цитотоксических средств в настоящее время активно исследуются в клинике в качестве противораковой терапии (Ricart, A. D., and Tolcher, A. W., 2007, Nature Clinical Practice, 4, 245-255; Krop et al., 2010, J. Clin. Oncol, 28, 2698-2704). Однако существующие конъюгаты антитело-лекарственное средство характеризуются рядом недостатков. Основным недостатком является их неспособность обеспечивать достаточную концентрацию лекарственного средства в требуемом месте вследствие ограниченного числа целевых антигенов и относительно умеренной цитотоксичности противораковых лекарственных средств, таких как метотрексат, даунорубицин, мейтанзиноиды, таксаны и винкристин. Одним подходом для достижения значительной цитотоксичности является связывание большого числа молекул лекарственного средства, либо непосредственно, либо косвенно, с антителом. Однако такие сильно модифицированные антитела часто характеризуются неудовлетворительным связыванием с антигеном-мишенью и быстрым in vivo выведением из кровотока. Поэтому, для того чтобы лекарственное средство проявляло максимальную цитотоксичность, существует необходимость в создании возможности обеспечения достаточной концентрации лекарственного средства в требуемом месте.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к конъюгату белок-полимер-лекарственное средство, который является биоразлагаемым, биосовместимым и характеризуется высокой концентрацией лекарственного средства, а также сильным связыванием с антигеном-мишенью. Настоящее изобретение также относится к полимерной каркасной структуре, применяемой для образования конъюгата с распознающей молекулой на основе белка (PBRM) с получением конъюгата белок-полимер-лекарственное средство.
В одном аспекте, изобретение предлагает полимерную каркасную структуру, применяемую для образования конъюгата с PBRM. Каркасная структура включает полимерный носитель, один или более -LD-D, соединенных с полимерным носителем, и одно или более LP, соединенных с полимерным носителем, которые используют для присоединения PBRM к полимерному носителю, где:
в каждом случае присутствия, D представляет собой независимо терапевтическое средство, имеющее молекулярную массу ≤5 кДа;
полимерный носитель представляет собой полиацеталь или поликеталь,
LD представляет собой связующее звено, имеющее структуру:


LD1 представляет собой карбонилсодержащий фрагмент;
LP представляет собой связующее звено, отличающееся от LD и имеющее структуру: -RL2-C(=O)-LP1, где RL2 соединен с атомом кислорода полимерного носителя, и LP1 используется для прямого или непрямого присоединения к PBRM;
каждый из RL1 и RL2 независимо отсутствует, представляет собой алкил, гетероалкил, циклоалкил или гетероциклоалкил; и
LP1 представляет собой фрагмент, содержащий функциональную группу, которая способна образовывать ковалентную связь с функциональной группой, содержащейся в PBRM.
Полимерная каркасная структура может включать один или более из характерных признаков.
LP представляет собой связующее звено, имеющее структуру
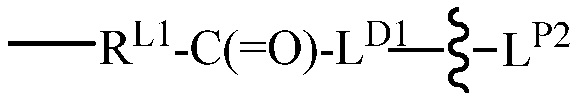

Функциональную группу LP1 или LP2 выбирают из -SRP, -S-S-LG, малеимидо и галогена, где LG представляет собой уходящую группу, и RP представляет собой H или защитную группу для серосодержащей группы.
LD1 включает -X-(CH2)v-C(=O)-, где X непосредственно присоединен к карбонильной группе RL1-C(=O), где X представляет собой CH2, O или NH, и v представляет собой целое число от 1 до 6.
LP1 или LP2 содержит биоразлагаемую химическую связь.
Каждый из RL1 и RL2 отсутствует.
Полимерный носитель каркасной структуры изобретения представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу (MW) немодифицированного PHF) в диапазоне от приблизительно 2 кДа до приблизительно 300 кДа.
Для конъюгирования PBRM, имеющей молекулярную массу 40 кДа или более (например, 80 кДа или более), полимерный носитель каркасной структуры изобретения представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу (MW) немодифицированного PHF) в диапазоне от приблизительно 2 кДа до приблизительно 40 кДа (например, приблизительно 6-20 кДа или приблизительно 8-15 кДа).
Для конъюгирования PBRM, имеющей молекулярную массу 200 кДа или менее (например, 80 кДа или менее), полимерный носитель каркасной структуры изобретения представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу (MW) немодифицированного PHF) в диапазоне от приблизительно 20 кДа до приблизительно 300 кДа (например, приблизительно 40-150 кДа или приблизительно 50-100 кДа).
Каркасная структура имеет формулу (Ia):

где:
m представляет собой целое число от 1 до приблизительно 2200,
m1 представляет собой целое число от 1 до приблизительно 660,
m2 представляет собой целое число от 1 до приблизительно 300,
m3 представляет собой целое число от 1 до приблизительно 110, и
сумма m, m1, m2 и m3 составляет от приблизительно 15 до приблизительно 2200.
Когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от приблизительно 2 кДа до приблизительно 40 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 15 до приблизительно 300), m2 представляет собой целое число от 1 до приблизительно 40, m3 представляет собой целое число от 1 до приблизительно 18, и/или m1 представляет собой целое число от 1 до приблизительно 140 (например, m1 составляет приблизительно 1-90).
Когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от приблизительно 6 кДа до приблизительно 20 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 45 до приблизительно 150), m2 представляет собой целое число от 2 до приблизительно 20, m3 представляет собой целое число от 1 до приблизительно 9, и/или m1 представляет собой целое число от 1 до приблизительно 75 (например, m1 составляет приблизительно 4-45).
Когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от приблизительно 8 кДа до приблизительно 15 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 60 до приблизительно 110), m2 представляет собой целое число от 2 до приблизительно 15, m3 представляет собой целое число от 1 до приблизительно 7 и/или m1 представляет собой целое число от 1 до приблизительно 55 (например, m1 составляет приблизительно 4-30).
Когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от 20 кДа до 300 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 150 до приблизительно 2200), m2 представляет собой целое число от 3 до приблизительно 300, m3 представляет собой целое число от 1 до приблизительно 110 и/или m1 представляет собой целое число от 1 до приблизительно 660 (например, m1 составляет приблизительно 10-250).
Когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от 40 кДа до 150 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 300 до приблизительно 1100), m2 представляет собой целое число от 4 до приблизительно 150, m3 представляет собой целое число от 1 до приблизительно 75 и/или m1 представляет собой целое число от 1 до приблизительно 330 (например, m1 составляет приблизительно 15-100).
Когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от приблизительно 50 кДа до приблизительно 100 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 370 до приблизительно 740), m2 представляет собой целое число от 5 до приблизительно 100, m3 представляет собой целое число от 1 до приблизительно 40 и/или m1 представляет собой целое число от 1 до приблизительно 220 (например, m1 составляет приблизительно 15-80).
Каркасная структура дополнительно включает PBRM, соединенную с полимерным носителем через LP.
Одна или более PBRM присоединены к одному несущему лекарственное средство полимерному носителю.
Каркасная структура (например, конъюгат PBRM-полимер-лекарственное средство) имеет формулу (Ib):

где:

в каждом случае присутствия, PBRM независимо имеет молекулярную массу менее чем 200 кДа,
m представляет собой целое число от 1 до приблизительно 2200,
m1 представляет собой целое число от 1 до приблизительно 660,
m2 представляет собой целое число от 3 до приблизительно 300,
m3 представляет собой целое число от 0 до приблизительно 110,
m4 представляет собой целое число от 1 до приблизительно 60; и
сумма m, m1, m2, m3 и m4 составляет от приблизительно 150 до приблизительно 2200.
В формуле (Ib), m1 представляет собой целое число от приблизительно 10 до приблизительно 660 (например, приблизительно 10-250).
Когда PHF в формуле (Ib) имеет молекулярную массу в диапазоне от 40 кДа до 150 кДа (то есть, сумма m, m1, m2, m3 и m4 составляет от приблизительно 300 до приблизительно 1100), m2 представляет собой целое число от 4 до приблизительно 150, m3 представляет собой целое число от 1 до приблизительно 75, m4 представляет собой целое число от 1 до приблизительно 30 и/или m1 представляет собой целое число от 1 до приблизительно 330 (например, m1 составляет приблизительно 10-330 или приблизительно 15-100).
Когда PHF в формуле (Ib) имеет молекулярную массу в диапазоне от приблизительно 50 кДа до приблизительно 100 кДа (то есть, сумма m, m1, m2, m3 и m4 составляет от приблизительно 370 до приблизительно 740), m2 представляет собой целое число от 5 до приблизительно 100, m3 представляет собой целое число от 1 до приблизительно 40, m4 представляет собой целое число от 1 до приблизительно 20 и/или m1 представляет собой целое число от 1 до приблизительно 220 (например, m1 составляет приблизительно 15-80).
В качестве варианта или дополнительно, один или более несущих лекарственное средство полимерных носителей соединены с одной PBRM. Каркасная структура (например, конъюгат PBRM-полимер-лекарственное средство) включает PBRM с молекулярной массой более чем 40 кДа и один или более D-несущих полимерных носителей, соединенных с PBRM, где каждый из D-несущих полимерных носителей независимо имеет формулу (Ic):

где:
терминальное

m представляет собой целое число от 1 до 300,
m1 представляет собой целое число от 1 до 140,
m2 представляет собой целое число от 1 до 40,
m3 представляет собой целое число от 0 до 18,
m4 представляет собой целое число от 1 до 10; и
сумма m, m1, m2, m3 и m4 составляет от 15 до 300; при условии, что суммарное число LP2,присоединенных к PBRM, составляет 10 или менее.
В формуле (Ic), m1 представляет собой целое число от 1 до приблизительно 120 (например, приблизительно 1-90) и/или m3 представляет собой целое число от 1 до приблизительно 10 (например, приблизительно 1-8).
Когда PHF в формуле (Ic) имеет молекулярную массу от приблизительно 6 кДа до приблизительно 20 кДа (то есть, сумма m, m1, m2, m3 и m4 составляет от приблизительно 45 до приблизительно 150), m2 представляет собой целое число от 2 до приблизительно 20, m3 представляет собой целое число от 1 до приблизительно 9, и/или m1 представляет собой целое число от 1 до приблизительно 75 (например, m1 составляет приблизительно 4-45).
Когда PHF в формуле (Ic) имеет молекулярную массу от приблизительно 8 кДа до приблизительно 15 кДа (то есть, сумма m, m1, m2, m3 и m4 составляет от приблизительно 60 до приблизительно 110), m2 представляет собой целое число от 2 до приблизительно 15, m3 представляет собой целое число от 1 до приблизительно 7, и/или m1 представляет собой целое число от 1 до приблизительно 55 (например, m1 составляет приблизительно 4-30).
В каждом случае присутствия, D независимо выбирают из алкалоидов барвинка, ауристатинов, тубулизинов, дуокармицинов, ингибиторов киназы, ингибиторов MEK, ингибиторов KSP и их аналогов.
LD представляет собой -RL1-C(=O)-XD-MD1-YD-MD2-ZD-MD3-QD-MD4-, где MD4 непосредственно присоединен к D, где
XD представляет собой -O-, -S-, -N(R1)- или отсутствует, где R1 представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент, -C(=O)R1B, -C(=O)OR1B или -SO2R1B, или -N(R1)- представляет собой гетероциклоалкильный фрагмент, где R1B представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент;
каждый из YD, ZD и QD независимо отсутствует или представляет собой фрагмент биоразлагаемого связующего звена, выбранный из группы, состоящей из -S-S- , -C(=O)O-, -C(=O)NR2-, -OC(=O)-, -NR2C(=O)—, —OC(=O)O-, -OC(=O)NR2-, -NR2C(=O)O-, -NR2C(=O)NR3-, -C(OR2)O-, -C(OR2)S-, -C(OR2)NR3-, -C(SR2)O-, -C(SR2)S-, -C(SR2)NR3-, -C(NR2R3)O-, -C(NR2R3)S-, -C(NR2R3)NR4-, -C(=O)S-, -SC(=O)-, -SC(=O)S-, -OC(=O)S-, -SC(=O)O-, -C(=S)S-, -SC(=S)-, -OC(=S)-, -C(=S)O-, -SC(=S)O-, -OC(=S)S-, -OC(=S)O-, -SC(=S)S-, -C(=NR2)O-, -C(=NR2)S-, -C(=NR2)NR3-, -OC(=NR2)-, -SC(=NR2)-, -NR3C(=NR2)-, -NR2SO2-, -NR2NR3-, -C(=O)NR2NR3-, -NR2NR3C(=O)-, -OC(=O)NR2NR3-, -NR2NR3C(=O)O-, -C(=S)NR2NR3-, -NR2NR3C(=S)-, -C(=NR4)NR2NR3-, -NR2NR3C(=NR4)-, -O(N=CR3-, -(CR3=N)O-, -C(=O)NR2-(N=CR3)-, -(CR3=N)-NR2C(=O)-, -SO3-, -NR2SO2NR3-, -SO2NR2- и полиамида, где в каждом случае присутствия, R2, R3 и R4 независимо представляют собой водород или алифатический, гетероалифатический, карбоциклический или гетероциклический фрагмент, или в каждом случае присутствия, -NR2- или -NR2NR3- представляют собой гетероциклоалкильный фрагмент; и
каждый из MD1, MD2, MD3 и MD4 независимо отсутствует или представляет собой фрагмент бионеразлагаемого связующего звена, выбранный из группы, состоящей из алкильного, алкенильного, алкинильного, гетероалкильного, гетероалкенильного, гетероалкинильного, карбоциклического фрагмента, гетероциклического фрагмента и их комбинации, и каждый из MD1, MD2 и MD3 необязательно содержит один или более -(C=O)-, но не содержит любой указанный фрагмент биоразлагаемого связующего звена;
при условии, что для каждого LD1 по меньшей мере один из XD, YD, ZD и QD не отсутствует.
Каждое


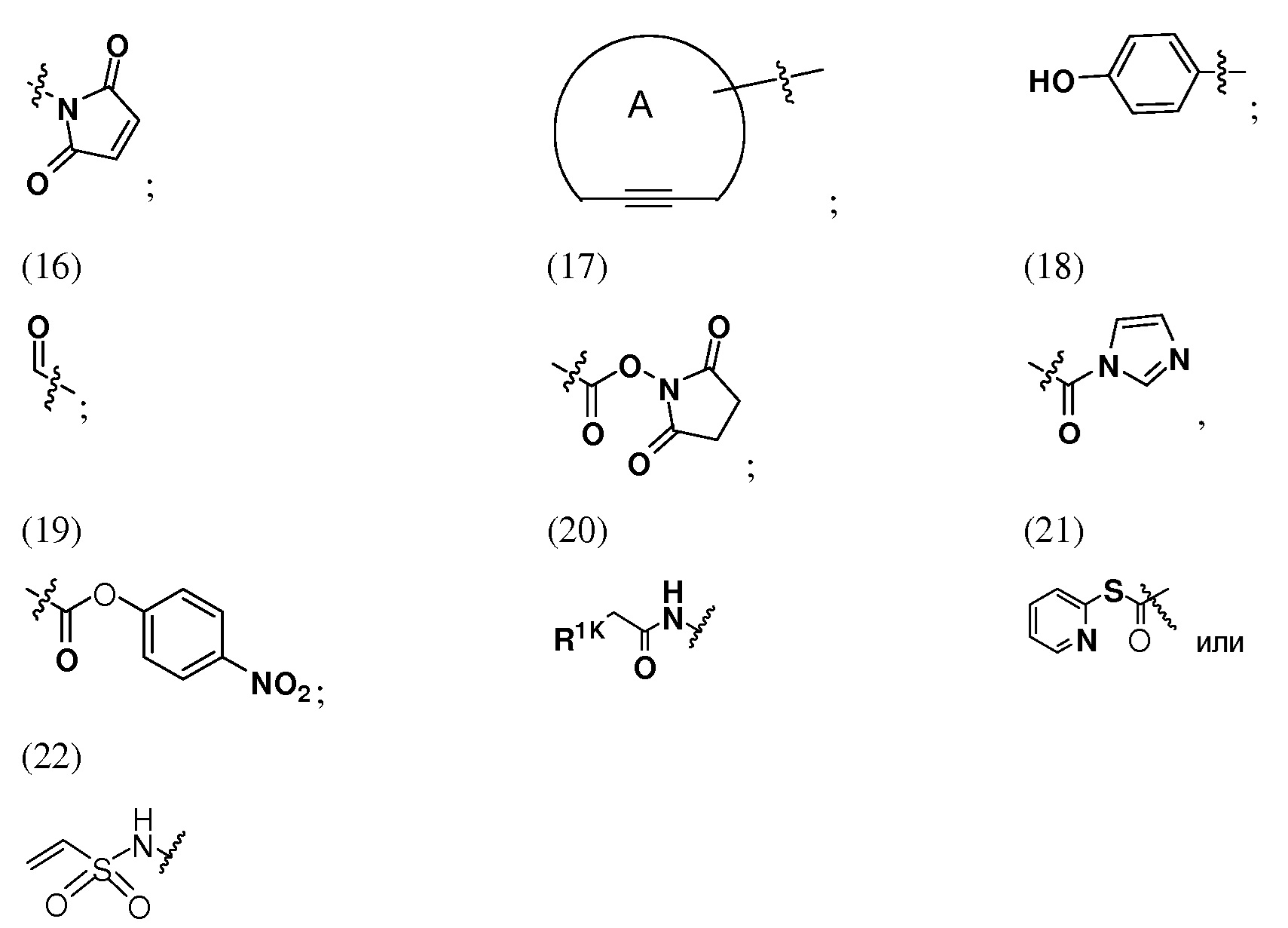
где R1K представляет собой уходящую группу (например, галогенид или RC(O)O-, где R представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент), R1A представляет собой защитную группу для серосодержащей группы, и кольцо A представляет собой циклоалкил или гетероциклоалкил, и R1J представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент.
Каждый R1A независимо представляет собой



Каждое

XP представляет собой -O-, -S-, -N(R1)- или отсутствует, где R1 представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент, -C(=O)R1B, -C(=O)OR1B или -SO2R1B, или -N(R1)- представляет собой гетероциклоалкильный фрагмент, где R1B представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент;
каждый из YP, ZP и QP независимо отсутствует или представляет собой фрагмент биоразлагаемого связующего звена, выбранный из группы, состоящей из -S-S-, -C(=O)O-, -C(=O)NR2-, -OC(=O)-, -NR2C(=O)-, -OC(=O)O-, -OC(=O)NR2-, -NR2C(=O)O-, -NR2C(=O)NR3-, -C(OR2)O-, -C(OR2)S-, -C(OR2)NR3-, -C(SR2)O-, -C(SR2)S-, -C(SR2)NR3-, -C(NR2R3)O-, -C(NR2R3)S-, -C(NR2R3)NR4-, -C(=O)S-, -SC(=O)-, -SC(=O)S-, -OC(=O)S-, -SC(=O)O-, -C(=S)S-, -SC(=S)-, -OC(=S)-, -C(=S)O-, -SC(=S)O-, -OC(=S)S-, -OC(=S)O-, -SC(=S)S-, -C(=NR2)O-, -C(=NR2)S-, -C(=NR2)NR3-, -OC(=NR2)-, -SC(=NR2)-, -NR3C(=NR2)-, -NR2SO2-, -NR2NR3-, -C(=O)NR2NR3-, -NR2NR3C(=O)-, -OC(=O)NR2NR3-, -NR2NR3C(=O)O-, -C(=S)NR2NR3-, -NR2NR3C(=S)-, -C(=NR4)NR2NR3-, -NR2NR3C(=NR4)-, -O(N=CR3)-, -(CR3=N)O-, -C(=O)NR2-(N=CR3)-, -(CR3=N)-NR2C(=O)-, -SO3-, -NR2SO2NR3-, -SO2NR2- и полиамида, где в каждом случае присутствия, R2, R3 и R4 независимо представляют собой водород или алифатический, гетероалифатический, карбоциклический или гетероциклический фрагмент, или в каждом случае присутствия, -NR2- или -NR2NR3- представляют собой гетероциклоалкильный фрагмент; и
каждый из MP1, MP2, MP3 и MP4 независимо отсутствует или представляет собой фрагмент бионеразлагаемого связующего звена, выбранного из группы, состоящей из алкильного, алкенильного, алкинильного, гетероалкильного, гетероалкенильного, гетероалкинильного, карбоциклического фрагмента, гетероциклического фрагмента и их комбинации, и каждый из MP1, MP2 и MP3 необязательно содержит одно или более -(C=O)-, но не содержит любой указанный фрагмент биоразлагаемого связующего звена;
при условии, что для каждого
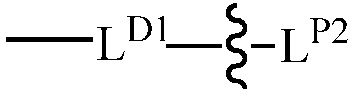
Каждый из MD1 и MP1 независимо представляет собой C1-6 алкил или C1-6 гетероалкил.
каждый из MD2, MD3, MD4, MP2, MP3 и MP4 независимо отсутствует, представляет собой C1-6алкил, циклоалкил, гетероалкил, гетероциклоалкил или их комбинацию.
В каждом



где q представляет собой целое число от 0 до 12, и каждый из p и t независимо представляет собой целое число от 0 до 3.
В объем изобретения также входит способ получения описанной выше каркасной структуры. Способ включает получение полимерного носителя, который замещен с помощью одного или более -LD-D и одного или более -RL1-C(=O)-LD1, и реакцию полимерного носителя с соединением, содержащим LP2 фрагмент, с получением каркасной структуры по пункту 2, включающей полимерный носитель, замещенный как с помощью одного или более -LD-D, так и с помощью одного или более



Изобретение также описывает соединение формулы (XII) или (XIIa):
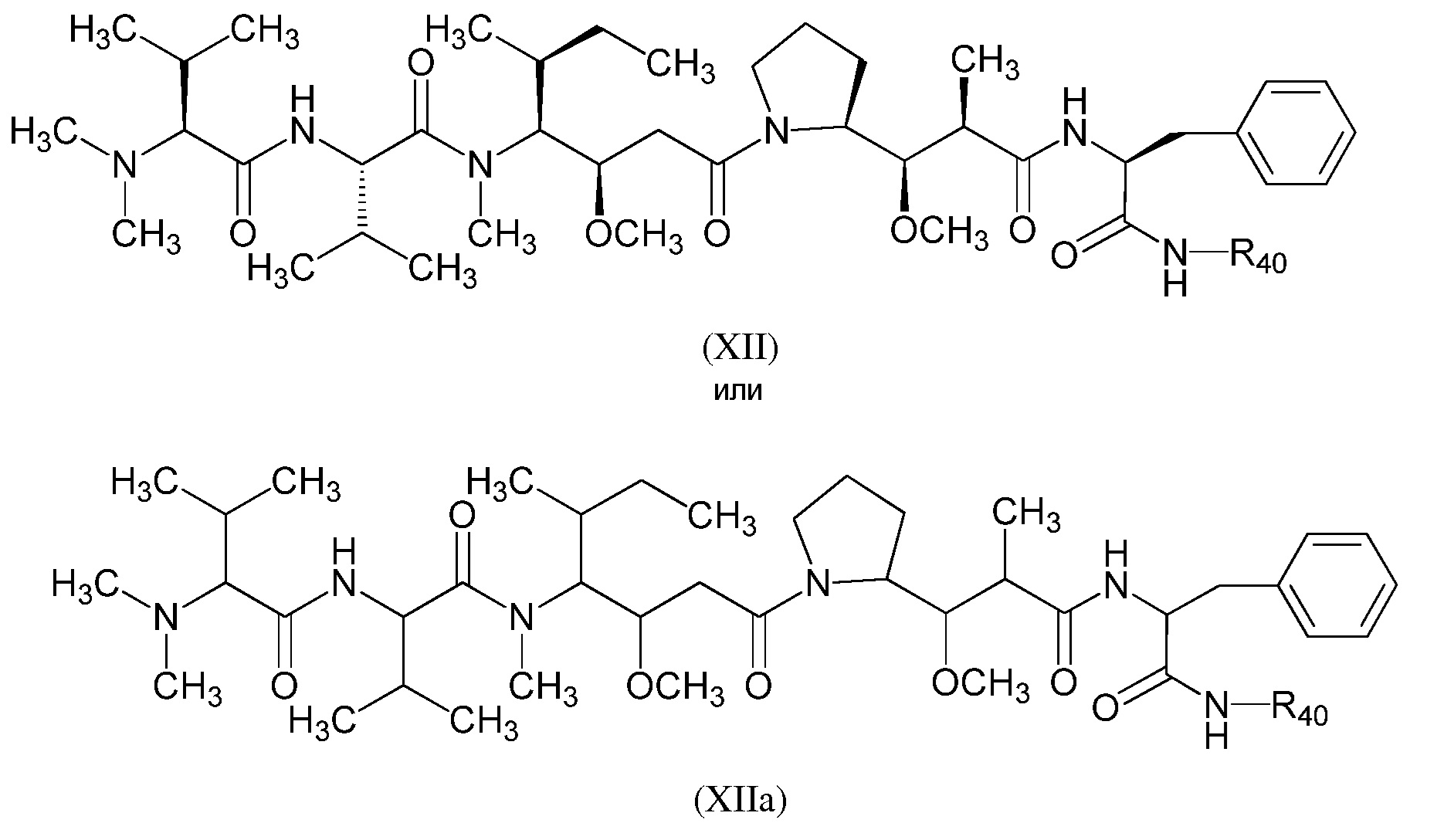
или его фармацевтически приемлемую соль,
где
R40 выбирают из группы, состоящей из
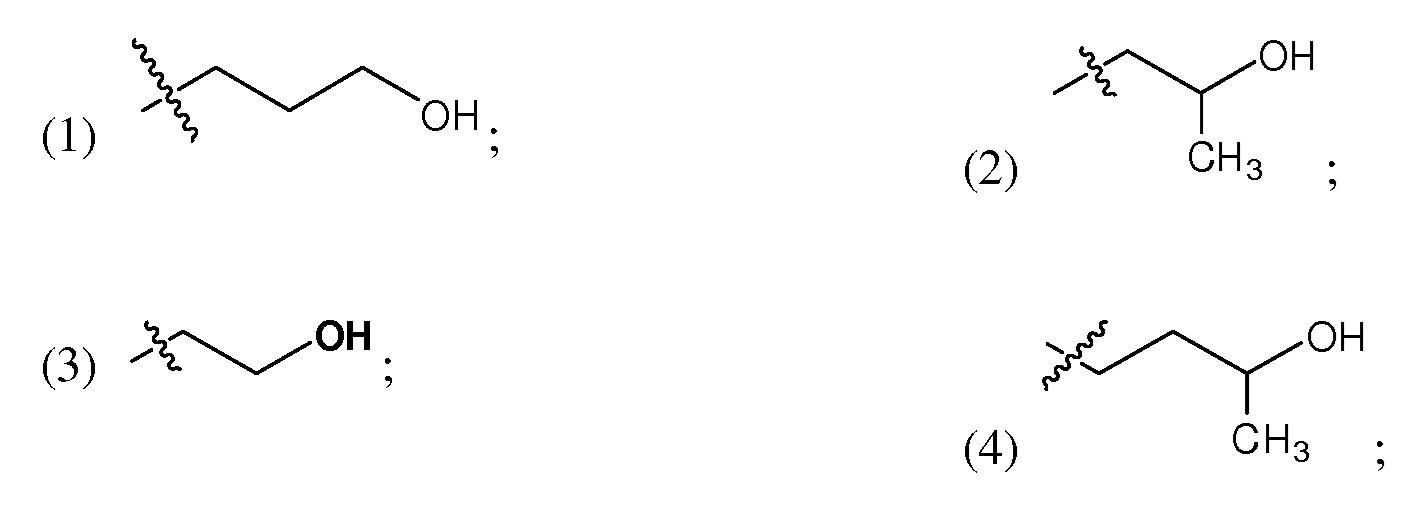
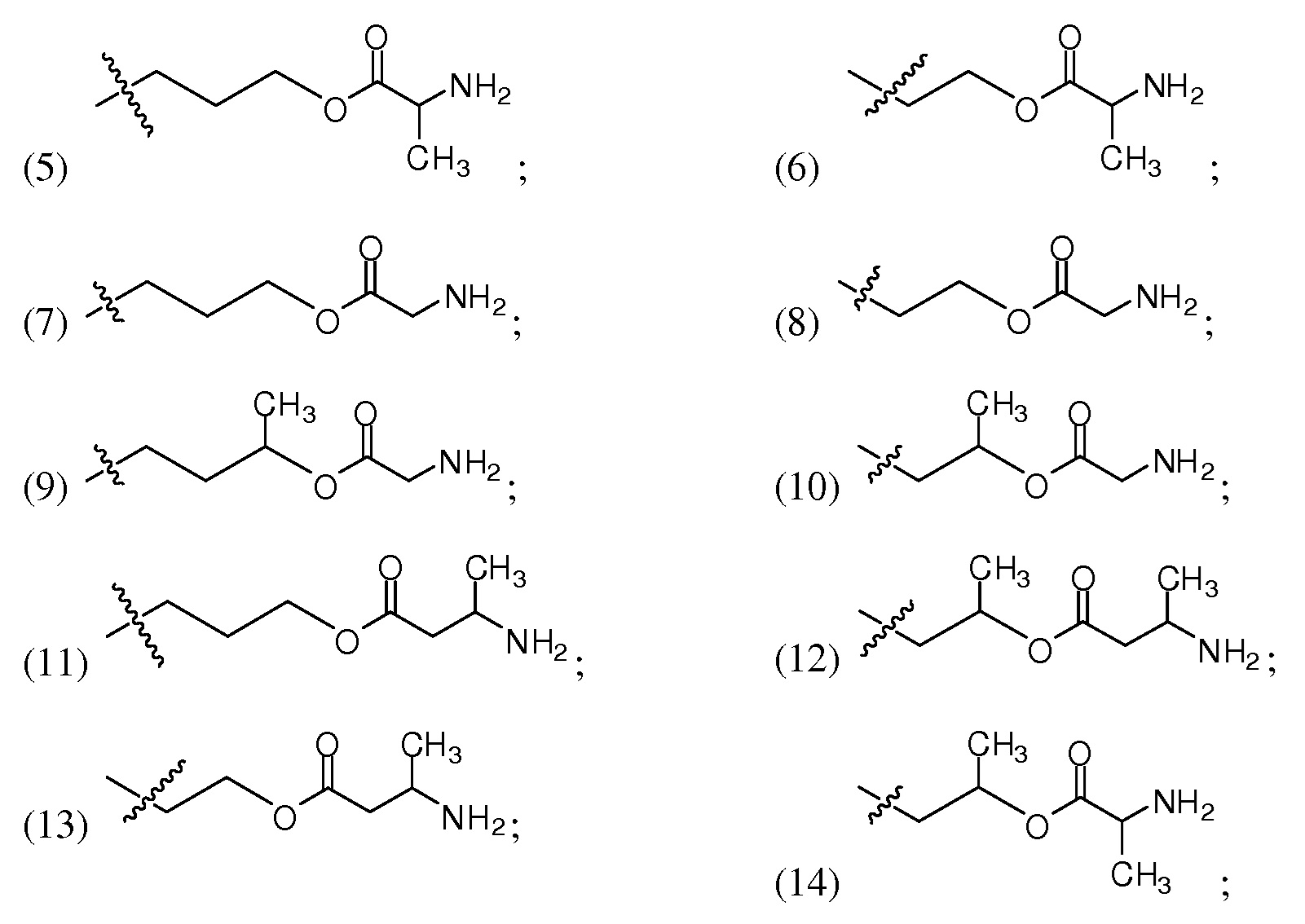

a представляет собой целое число от 1 до 6; и
c представляет собой целое число от 0 до 3.
R40 может представлять собой


В другом аспекте, изобретение описывает полимерную каркасную структуру, применяемую для образования конъюгата с распознающей молекулой на основе белка (PBRM) и терапевтическим средством (D). Каркасная структура (то есть, каркасная структура, не содержащая D) включает полимерный носитель, одно или более LP, соединенное с полимерным носителем, которое используют для соединения PBRM с полимерным носителем, и одно или более -RL1-C(=O)-LD1, соединенное с полимерным носителем через RL1, где:
полимерный носитель представляет собой полиацеталь или поликеталь,
RL1 соединено с атомом кислорода полимерного носителя,
LD1 представляет собой связующее звено, подходящее для присоединения молекулы D к полимерному носителю, где в каждом случае присутствия, D представляет собой независимо терапевтическое средство, имеющее молекулярную массу ≤5 кДа;
LP представляет собой связующее звено, отличающееся от -RL1-C(=O)-LD1 и имеющее структуру: -RL2-C(=O)-LP1, где RL2 присоединен к атому кислорода полимерного носителя, и LP1 используют для присоединения с PBRM;
каждый из RL1 и RL2 независимо отсутствует, представляет собой алкил, гетероалкил, циклоалкил или гетероциклоалкил;
LD1 представляет собой фрагмент, содержащий функциональную группу, которая способна образовывать ковалентную связь с функциональной группой терапевтического средства D, и
LP1 представляет собой фрагмент, содержащий функциональную группу, которая способна образовывать ковалентную связь с функциональной группой PBRM.
Несодержащая D каркасная структура, применяемая для образования конъюгата с PBRM и D может иметь один или более из характерных признаков.
LPпредставляет собой связующее звено, имеющее структуру:


Функциональную группу LP1 или LP2 выбирают из -SRP, -S-S-LG, малеимидо и галогена, где LG представляет собой уходящую группу, и RP представляет собой H или защитную группу для серосодержащей группы.
LD1 включает -X-(CH2)v-C(=O)-, где X непосредственно присоединен к карбонильной группе RL1-C(=O), где X представляет собой CH2, O или NH, и v представляет собой целое число от 1 до 6.
LP1 или LP2 содержит биоразлагаемую химическую связь.
Каждый из RL1 и RL2 отсутствует.
Полимерный носитель несодержащей D каркасной структуры представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу (MW) немодифицированного PHF) от приблизительно 2 кДа до приблизительно 300 кДа.
Для конъюгирования PBRM, имеющей молекулярную массу 40 кДа или более (например, 80 кДа или более), полимерный носитель несодержащей D каркасной структуры представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу (MW) немодифицированного PHF) от приблизительно 2 кДа до приблизительно 40 кДа (например, приблизительно 6-20 кДа или приблизительно 8-15 кДа).
Для конъюгирования PBRM, имеющей молекулярную массу 200 кДа или менее (например, 80 кДа или менее), полимерный носитель несодержащей D каркасной структуры изобретения представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу (MW) немодифицированного PHF) от приблизительно 20 кДа до приблизительно 300 кДа (например, приблизительно 40-150 кДа или приблизительно 50-100 кДа).
Несодержащая D каркасная структура имеет формулу (Id):

где:
m представляет собой целое число от 1 до приблизительно 2200,
m1 представляет собой целое число от 1 до приблизительно 660,
m3 представляет собой целое число от 1 до приблизительно 110, и
сумма m, m1 и m3 составляет от приблизительно 15 до приблизительно 2200.
Когда PHF в формуле (Id) имеет молекулярную массу от приблизительно 2 кДа до приблизительно 40 кДа (то есть, сумма m, m1 и m3 составляет от приблизительно 15 до приблизительно 300), m3 представляет собой целое число от 1 до приблизительно 18 и/или m1 представляет собой целое число от 1 до приблизительно 140 (например, m1 составляет приблизительно 2-120).
Когда PHF в формуле (Id) имеет молекулярную массу от приблизительно 6 кДа до приблизительно 20 кДа (то есть, сумма m, m1 и m3 составляет от приблизительно 45 до приблизительно 150), m3 представляет собой целое число от 1 до приблизительно 9 и/или m1 представляет собой целое число от 1 до приблизительно 75 (например, m1 составляет приблизительно 6-60).
Когда PHF в формуле (Id) имеет молекулярную массу от приблизительно 8 кДа до приблизительно 15 кДа (то есть, сумма m, m1 и m3 составляет от приблизительно 60 до приблизительно 110), m3 представляет собой целое число от 1 до приблизительно 7 и/или m1 представляет собой целое число от 1 до приблизительно 55 (например, m1 составляет приблизительно 6-45).
Когда PHF в формуле (Id) имеет молекулярную массу от 20 кДа до 300 кДа (то есть, сумма m, m1 и m3 составляет от приблизительно 150 до приблизительно 2200), m3 представляет собой целое число от 1 до приблизительно 110 и/или m1 представляет собой целое число от 1 до приблизительно 660 (например, m1 составляет приблизительно 13-550).
Когда PHF в формуле (Id) имеет молекулярную массу от 40 кДа до 150 кДа (то есть, сумма m, m1 и m3 составляет от приблизительно 300 до приблизительно 1100), m3 представляет собой целое число от 1 до приблизительно 75 и/или m1 представляет собой целое число от 1 до приблизительно 330 (например, m1 составляет приблизительно 20-250).
Когда PHF в формуле (Id) имеет молекулярную массу от приблизительно 50 кДа до приблизительно 100 кДа (то есть, сумма m, m1 и m3 составляет от приблизительно 370 до приблизительно 740), m3 представляет собой целое число от 1 до приблизительно 40 и/или m1 представляет собой целое число от 1 до приблизительно 220 (например, m1 составляет приблизительно 20-180).
Несодержащая D каркасная структура дополнительно включает PBRM, присоединенную к полимерному носителю через LP.
Одна или более PBRM присоединены к одному несодержащему D полимерному носителю.
Несодержащая D каркасная структура имеет формулу (Ie):

где:

PBRM имеет молекулярную массу менее чем 200 кДа,
m представляет собой целое число от 1 до 2200,
m1 представляет собой целое число от 1 до 660,
m3 представляет собой целое число от 0 до 110,
m4 представляет собой целое число от 1 до приблизительно 60; и
сумма m, m1, m2, m3 и m4 составляет от приблизительно 150 до приблизительно 2200.
В формуле (Ie), m1 представляет собой целое число от приблизительно 10 до приблизительно 660 (например, приблизительно 14-550).
Когда PHF в формуле (Ie) имеет молекулярную массу от 40 кДа до 150 кДа (то есть, сумма m, m1, m3 и m4 составляет от приблизительно 300 до приблизительно 1100), m3 представляет собой целое число от 1 до приблизительно 75, m4 представляет собой целое число от 1 до приблизительно 30 и/или m1 представляет собой целое число от 1 до приблизительно 330 (например, m1 составляет приблизительно 20-250).
Когда PHF в формуле (Ie) имеет молекулярную массу от приблизительно 50 кДа до приблизительно 100 кДа (то есть, сумма m, m1, m3, и m4 составляет от приблизительно 370 до приблизительно 740), m3 представляет собой целое число от 1 до приблизительно 40, m4 представляет собой целое число от 1 до приблизительно 20 и/или m1 представляет собой целое число от 1 до приблизительно 220 (например, m1 составляет приблизительно 20-180).
В качестве варианта или дополнительно, один или более несодержащих D полимерных носителей соединены с одной PBRM. Каркасная структура включает PBRM с молекулярной массой большей, чем 40 кДа, и один или более полимерных носителей, соединенных с PBRM, где каждый из полимерных носителей независимо имеет формулу (Ih):

где:
терминальное

m представляет собой целое число от 1 до 300,
m1 представляет собой целое число от 1 до 140,
m3 представляет собой целое число от 0 до 18,
m4 представляет собой целое число от 1 до 10; и
сумма m, m1, m3 и m4 составляет от 15 до 300; при условии, что суммарное число LP2,присоединенных к PBRM, составляет 10 или менее.
В формуле (Ih), m1 представляет собой целое число от 2 до приблизительно 130 (например, приблизительно 3-120) и/или m3 представляет собой целое число от 1 до приблизительно 10 (например, приблизительно 1-8).
Когда PHF в формуле (Ih) имеет молекулярную массу от приблизительно 6 кДа до приблизительно 20 кДа (то есть, сумма m, m1, m3 и m4 составляет от приблизительно 45 до приблизительно 150), m3 представляет собой целое число от 1 до приблизительно 9 и/или m1 представляет собой целое число от 6 до приблизительно 75 (например, m1 составляет приблизительно 7-60).
Когда PHF в формуле (Ih) имеет молекулярную массу от приблизительно 8 кДа до приблизительно 15 кДа (то есть, сумма m, m1, m3 и m4 составляет от приблизительно 60 до приблизительно 110), m3 представляет собой целое число от 1 до приблизительно 7 и/или m1 представляет собой целое число от 6 до приблизительно 55 (например, m1 составляет приблизительно 7-45).
Используемые в описании изобретения термины "полимерная каркасная структура" или просто "каркасная структура" и "конъюгат" применяются взаимозаменяемо, когда каркасная структура включает одну или более PBRM и одну или более молекул D.
В еще одном аспекте, изобретение включает в себя конъюгат, содержащий полимерный носитель, один или более -LD-D, соединенный с полимерным носителем, и распознающую молекулу на основе белка (PBRM), соединенную с полимерным носителем через LP, где:
в каждом случае присутствия, D представляет собой независимо терапевтической средство (например, лекарственное средство), имеющее молекулярную массу ≤5 кДа;
полимерный носитель представляет собой полиацеталь или поликеталь,
LD представляет собой связующее звено, имеющее структуру: -RL1-C(=O)-XD-MD1-YD-MD2-ZD-MD3-QD-MD4-, где RL1 соединен с атомом кислорода полимерного носителя, и MD4 соединен с D;
LP представляет собой связующее звено, имеющее структуру: -RL2-C(=O)-XP-MP1-YP-MP2-ZP-MP3-QP-MP4-, где RL2 соединен с атомом кислорода полимерного носителя, и MP4 соединен с распознающей молекулой на основе белка;
каждый из RL1 и RL2 независимо отсутствует, представляет собой алкил, циклоалкил, гетероалкил или гетероциклоалкил;
каждый из XD и XP независимо представляет собой -O-, -S-, -N(R1)- или отсутствует, где R1 представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент, -C(=O)R1B, -C(=O)OR1B, -SO2R1B, или -N(R1)- представляет собой гетероциклоалкильный фрагмент, где R1B представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент;
каждый из YD, YP, ZD, ZP, QD и QP независимо отсутствует или представляет собой фрагмент биоразлагаемого связующего звена, выбранный из группы, состоящей из -S-S-, -C(=O)O-, -C(=O)NR2-, -OC(=O)-, -NR2C(=O)-, -OC(=O)O-, -OC(=O)NR2-, -NR2C(=O)O-, -NR2C(=O)NR3-, -C(OR2)O-, -C(OR2)S-, -C(OR2)NR3-, -C(SR2)O-, -C(SR2)S-, -C(SR2)NR3-, -C(NR2R3)O-, -C(NR2R3)S-, -C(NR2R3)NR4-, -C(=O)S-, -SC(=O)-, -SC(=O)S-, -OC(=O)S-, -SC(=O)O-, -C(=S)S-, -SC(=S)-, -OC(=S)-, -C(=S)O-, -SC(=S)O-, -OC(=S)S-, -OC(=S)O-, -SC(=S)S-, -C(=NR2)O-, -C(=NR2)S-, -C(=NR2)NR3-, -OC(=NR2)-, -SC(=NR2)-, -NR3C(=NR2)-, -NR2SO2-, -NR2NR3-, -C(=O)NR2NR3-, -NR2NR3C(=O)-, -OC(=O)NR2NR3-, -NR2NR3C(=O)O-, -C(=S)NR2NR3-, -NR2NR3C(=S)-, -C(=NR4)NR2NR3-, -NR2NR3C(=NR4)-, -O(N=CR3)-, -(CR3=N)O-, -C(=O)NR2-(N=CR3)-, -(CR3=N)-NR2C(=O)-, -SO3-, -NR2SO2NR3-, -SO2NR2- и полиамида, где в каждом случае присутствия, R2, R3 и R4 независимо представляют собой водород или алифатический, гетероалифатический, карбоциклический или гетероциклический фрагмент, или в каждом случае присутствия, -NR2- или -NR2NR3- представляют собой гетероциклоалкильный фрагмент; и
каждый из MD1, MD2, MD3, MD4, MP1, MP2, MP3 и MP4 независимо отсутствует или представляет собой фрагмент бионеразлагаемого связующего звена, выбранный из группы, состоящей из алкильного, алкенильного, алкинильного, гетероалкильного, гетероалкенильного, гетероалкинильного, карбоциклического фрагмента, гетероциклического фрагмента и их комбинации, и каждый из MD1, MD2, MD3, MP1, MP2 и MP3 необязательно содержит одно или более -(C=O)-, но не содержит любой указанный фрагмент биоразлагаемого связующего звена;
при условии, что для каждого LD, по меньшей мере, один из XD, YD, ZD и QD не отсутствует, и для каждого LP по меньшей мере один из XP, YP, ZP и QPне отсутствует.
Конъюгат может включать один или более из характерных признаков.
Полимерный носитель может представлять собой полиацеталь, например, PHF.
Для каждого LD, MD1 не отсутствует, когда XD отсутствует.
Для каждого LP, MP1 не отсутствует, когда XP отсутствует.
Полимерный носитель может быть дополнительно замещен с помощью одного или более -RL1-C(=O)-XD-MD1-YD-MD2-WD, где каждый WDнезависимо представляет собой:


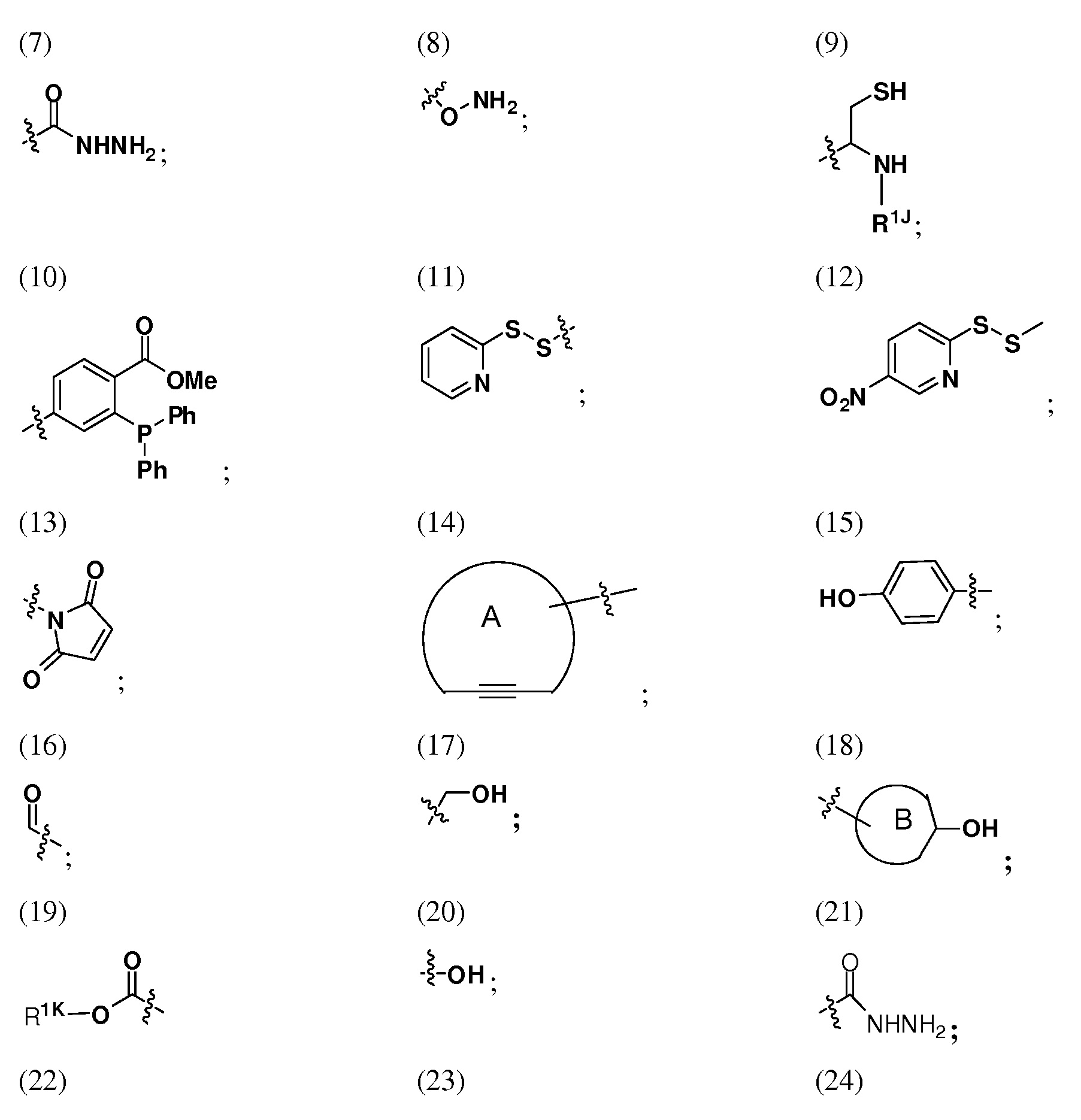


где R1A представляет собой защитную группу для серосодержащей группы, каждое из колец A и B независимо представляет собой циклоалкил или гетероциклоалкил, RW представляет собой алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент; кольцо D представляет собой гетероциклоалкил; R1J представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент; и R1K представляет собой уходящую группу (например, галогенид или RC(O)O-, где R представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент).
Полимерный носитель может быть дополнительно замещен с помощью одного или более -RL2-C(=O)-XP-MP1-YP-MP2-WP, где каждый WP независимо представляет собой:


где R1K представляет собой уходящую группу (например, галогенид или RC(O)O-, где R представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент), R1A представляет собой защитную группу для серосодержащей группы, и кольцо A представляет собой циклоалкил или гетероциклоалкил, и R1J представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент. Например, R1A представляет собой


Кольцо A может представлять собой C3-8 циклоалкил или 5-19-членный гетероциклоалкил.
Кольцо A может представлять собой

Кольцо B может представлять собой C3-8 циклоалкил или 3-12-членный гетероциклоалкил.
Кольцо D может представлять собой пиперазинил или пиперидинил.
Каждый из Rs1, Rs2 и Rs3 может представлять собой водород или C1-6 алкил.
Каждая PBRM независимо может представлять собой пептид, пептидомиметик, антитело или фрагмент антитела.
Каждый из MD1 и MP1 независимо может представлять собой C1-6 алкил или C1-6 гетероалкил.
Каждый из MD2, MD3, MD4, MP2, MP3 и MP4 независимо может отсутствовать, представлять собой C1-6 алкил, циклоалкил, гетероалкил, гетероциклоалкил или их комбинацию.
Для каждого LD, не более чем два из MD2, MD3 и MD4 могут отсутствовать.
Для каждого LP, не более чем два из MP2, MP3 и MP4 могут отсутствовать.
Для каждого LD, не более чем один из MD2 и MD3 может иметь одну из следующих структур:
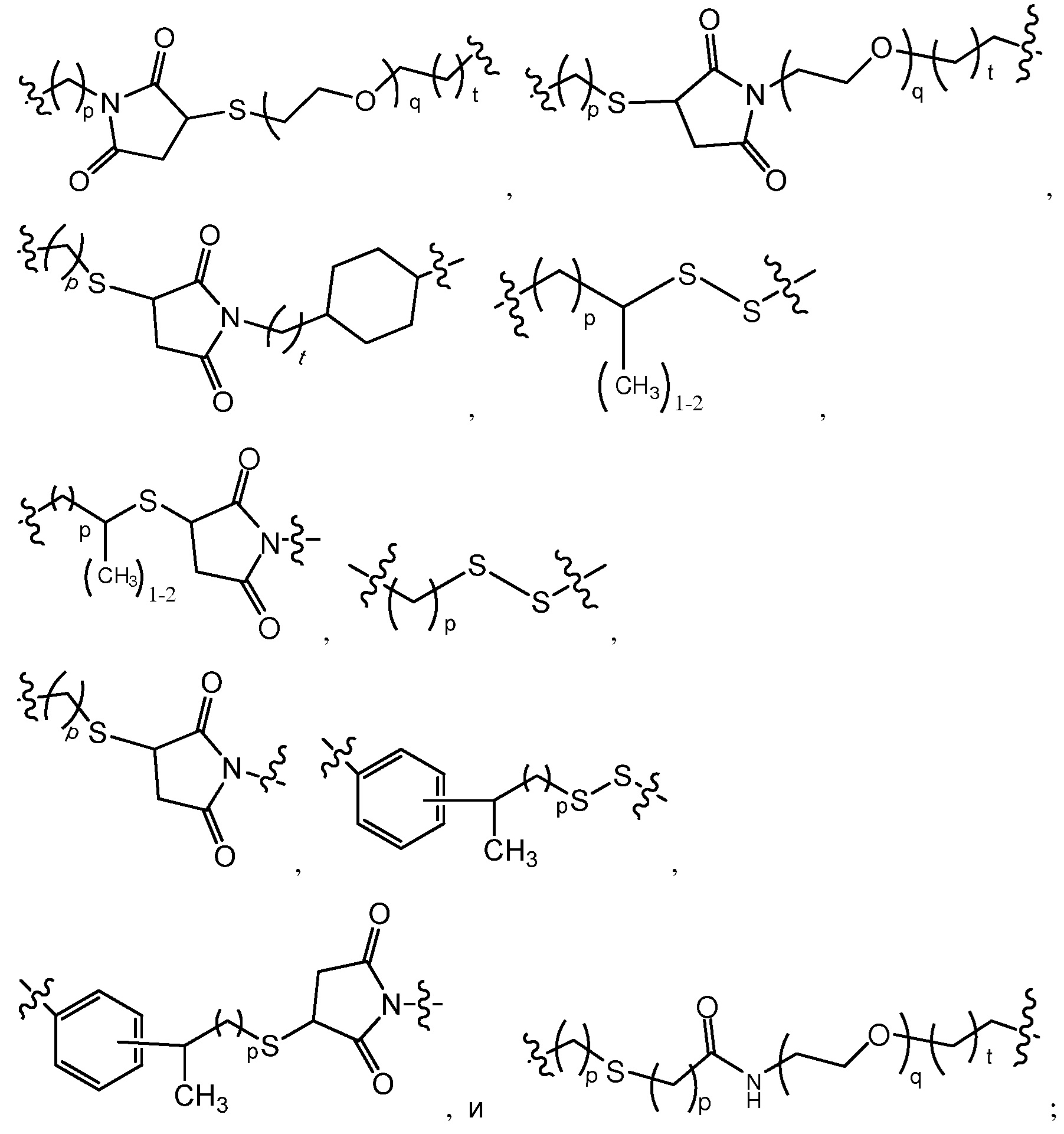
где q представляет собой целое число от 0 до 12, и каждый из p и t независимо представляют собой целое число от 0 до 3.
Для каждого LP, не более чем один из MP2 и MP3 может иметь одну из следующих структур:

где q представляет собой целое число от 0 до 12, и каждый из p и t независимо представляют собой целое число от 0 до 3.
Для каждого LD, каждый из -MD2-ZD-, -ZD-MD3-, -ZD-MD2- и -MD3-ZD- независимо может иметь одну из следующих структур:




где кольцо A или B независимо представляет собой циклоалкил или гетероциклоалкил; RW представляет собой алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент; R1J представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент; и кольцо D представляет собой гетероциклоалкил.
Для каждого LP, каждый из -MP2-ZP-, -ZP-MP3-, -ZP-MP2- и -MP3-ZP- независимо может иметь одну из следующих структур:


где кольцо A представляет собой циклоалкил или гетероциклоалкил, и R1J представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент.
Каждый из XD и XP независимо может отсутствовать.
Каждый из XD и XP независимо может представлять собой O или NH.
Каждый из XD и XP независимо может представлять собой


Каждый из YD и YP независимо может представлять собой -S-S-, -OCO-, -COO-, -CONH- или -NHCO-.
Каждый из QD и QP независимо может отсутствовать, представлять собой -S-S-, -OCO-, -COO-, -CONH-, -NHCO-, OCONHNH- или -NHNHCOO-.
В частности, это изобретение описывает конъюгат формулы (I):

где каждый из n, n1, n2, n3 и n4 представляет собой мольную долю соответствующего полимерного звена, изменяющуюся от 0 до 1; n+n1+n2+n3+n4=1, при условии, что ни один из n, n2 и n4 не равен 0.
В приведенной выше формуле (I), разрыв или промежуток между звеньями полиацеталя указывает, что звенья могут быть соединены друг с другом в любом порядке. Другими словами, присоединяемые группы, которые содержат D, PBRM, WD и WP, могут распределяться вдоль главной цепи полимера случайным образом.
В конъюгате белок-полимер-лекарственное средство формулы (I), каждое D может быть одинаковым или различным фрагментом, и каждое PBRM быть одинаковым или различным фрагментом.
Соотношение между n2 и n4 может составлять величину большую, чем 1:1, и вплоть до 200:1 (например, вплоть до 100:1), например, от 2:1 до 40:1; от 5:1 до 20:1; от 10:1 до 50:1, от 25:1 до 50:1 или от 30:1 до 50:1.
Соотношение между n2 и n4 может составлять приблизительно 50:1, 40:1, 25:1, 20:1, 10:1, 5:1 или 2:1.
В другом аспекте, изобретение предлагает композиции, включающие конъюгаты, способы их получения и способы их применения при лечении различных расстройств, включающих, но этим не ограничивая, рак.
Изобретение также описывает конъюгат лекарственное средство-полимер (например, конъюгат терапевтическое средство-полимер), который является аналогичным описанному выше конъюгату белок-полимер-лекарственное средство за исключением того, что конъюгат лекарственное средство-полимер не содержит PBRM. В этом варианте осуществления, конъюгат полимер-лекарственное средство может включать множество фрагментов лекарственного средства, где каждое D может быть одинаковым или различным. В этом варианте осуществления, в конъюгате формулы (I) n4 равняется 0. В изобретении также рассматриваются и описываются способы получения конъюгатов лекарственное средство-полимер и способы лечения различных расстройств (например, рака).
Изобретение также описывает конъюгат белок-полимер (например, конъюгат PBRM-полимер), который является аналогичным описанному выше конъюгату белок-полимер-лекарственное средство, за исключением того, что конъюгат белок-полимер не содержит лекарственное средство. В этом варианте осуществления, конъюгат белок-полимер может включать множество белковых фрагментов, где каждая PBRM может быть одинаковой или различной. В этом варианте осуществления, в конъюгате формулы (I) n2 равняется 0. В изобретении также рассматриваются и описываются способы получения конъюгатов лекарственное средство-полимер или полимерных каркасных структур и способы лечения различных расстройств (например, рака). Рак, на который направлено лечение, представляет собой рак заднего прохода, астроцитому, лейкоз, лимфому, рак головы и шеи, рак печени, рак яичек, рак шейки матки, саркому, гемангиому, рак пищевода, рак глаза, рак гортани, рак рта, мезотелиому, рак кожи, миелому, рак полости рта, рак прямой кишки, рак горла, рак мочевого пузыря, рак молочной железы, рак матки, рак яичника, рак предстательной железы, рак легкого, рак толстой кишки, рак поджелудочной железы, рак почки или рак желудочно-кишечного тракта.
Изобретение также относится к фармацевтической композиции, включающей описанную в изобретении полимерную каркасную структуру или конъюгат и фармацевтически приемлемый носитель.
В еще одном аспекте, изобретение относится к способу диагностирования расстройства у субъекта, относительно которого существуют подозрения о наличии у него этого расстройства. Способ включает введение эффективного количества описанного в изобретении конъюгата субъекту, относительно которого существуют подозрения о наличии у него расстройства, или проведение анализа для детектирования антигена-мишени/рецептора-мишени во взятом у субъекта образце с целью определения, имеет ли место экспрессия антигена-мишени или рецептора-мишени у субъекта.
Если не определено иначе, то все используемые в описании изобретения технические и научные термины имеют значения, которые являются общепринятыми для специалиста в той области, к которой относится это изобретение. В описании изобретения, формы единственного числа часто включают множественное число, если из текста явно не следует противоположное. Несмотря на то, что при осуществлении или проверке настоящего изобретения могут быть использованы способы и материалы, аналогичные или эквивалентные описанным в изобретении способам и материалам, тем не менее, ниже описаны подходящие способы и материалы. Содержание всех упоминаемых в описании изобретения публикаций, патентных заявок, патентов и других литературных источников приводится в изобретении путем ссылки на них. Предполагается, что приводимые в описании изобретения ссылки не являются прототипом заявляемого изобретения. В случае возникновения противоречий, приоритет следует отдавать настоящему описанию, включая определения. Кроме того, материалы, способы и примеры являются только иллюстрациями, и их не следует считать ограничениями для изобретения.
Одним из преимуществ настоящего изобретения является то, что описанные в изобретении конъюгаты белок-полимер-лекарственное средство или полимерные каркасные структуры значительно повышают биодоступность вводимых лекарственных средств и/или повышают биодоступность белка, присоединенного к полимерному носителю. Другие характерные черты и преимущества изобретения станут очевидными из следующих далее подробного описания и пунктов формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На фигуре 1 приведена графическая зависимость ответной реакции опухоли у мышей, инокулированной под кожу с помощью NCI-N87 клеток (n=10 для каждой группы), после внутривенного введения плацебо, конъюгата PBRM-лекарственное средство-полимер PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12), (пример 8, HPV:трастузумаб приблизительно от 16:1 до 18:1) при 15,6 мг/кг, 5,2 мг/кг, 1,6 мг/кг и 0,5 мг/кг, соответственно, и конъюгата лекарственное средство-полимер PHF-GA-(HPV-аланин)-SH (пример 6) (вводимых при дозе барвинка, которая эквивалентна дозе, применяемой в примере 8 при 15,6 мг/кг), вводимых один раз в неделю в течение 3 недель на 1-ый день, 8-ой день и 15-ый день, соответственно.
На фигуре 2 приведена графическая зависимость ответной реакции опухоли у мышей, инокулированной под кожу с помощью опухолевых клеток BT474 (n=12 для каждой группы), после внутривенного введения плацебо; PBRM (трастузумаба) при 15 мг/кг; конъюгатов PBRM-лекарственное средство-полимер PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (пример 7, HPV:трастузумаб приблизительно от 19:1 до 22:1) при 7,5 мг/кг и PHF-GA-(HPV-аланин)-(ритуксимаб-MCC) (пример 54, HPV:ритуксимаб приблизительно от 12:1 до 15:1) при 20 мг/кг; конъюгата лекарственное средство-полимер PHF-GA-(HPV-аланин)-SH (пример 6) (вводимых при дозе барвинка, которая эквивалентна дозе, применяемой в примере 7 при 15 мг/кг) в комбинации с трастузумабом при 15 мг/кг, вводимых один раз в неделю в течение 3 недель на 1-ый день, 8-ой день и 15-ый день, соответственно.
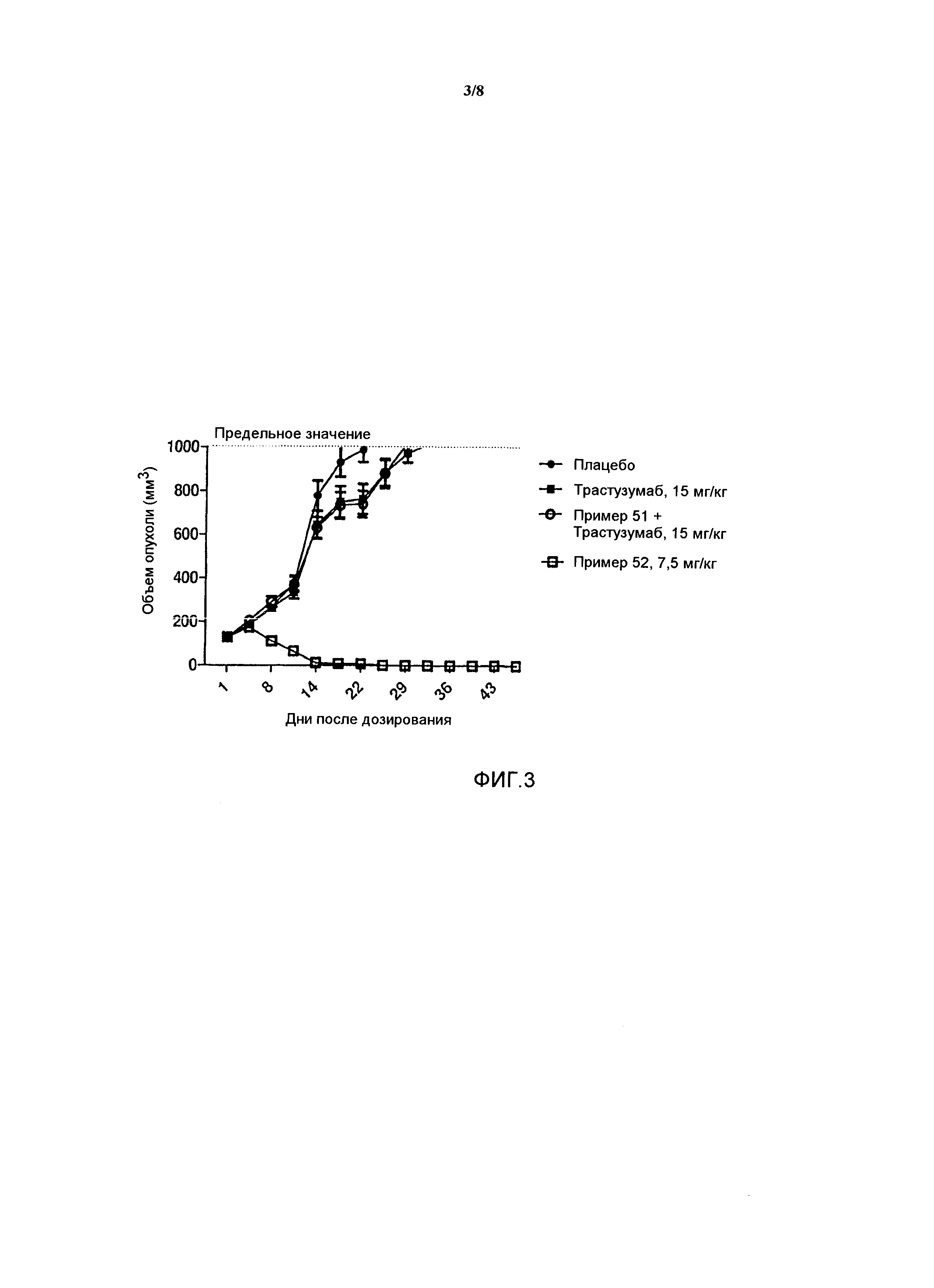
На фигуре 3 приведена графическая зависимость ответной реакции опухоли у мышей, инокулированной под кожу с помощью опухолевых клеток BT474 (n=12 для каждой группы), после внутривенного введения плацебо; PBRM (трастузумаба) при 15 мг/кг; конъюгатов PBRM-лекарственное средство полимер PHF-GA-(ауристатин F-гидроксипропиламид-L-аланин)-(трастузумаб-MCC) (пример 52, ауристатин F:трастузумаб приблизительно от 20:1 до 22:1) при 7,5 мг/кг; конъюгата лекарственное средство-полимер PHF-GA-SH-(ауристатин F-пропиламид-L-аланин) (пример 51) (вводимых при дозе ауристатина, которая эквивалентна дозе, применяемой в примере 52 при 15 мг/кг) в комбинации с трастузумабом при 15 мг/кг, вводимых один раз в неделю в течение 3 недель на 1-ый день, 8-ой день и 15-ый день, соответственно.
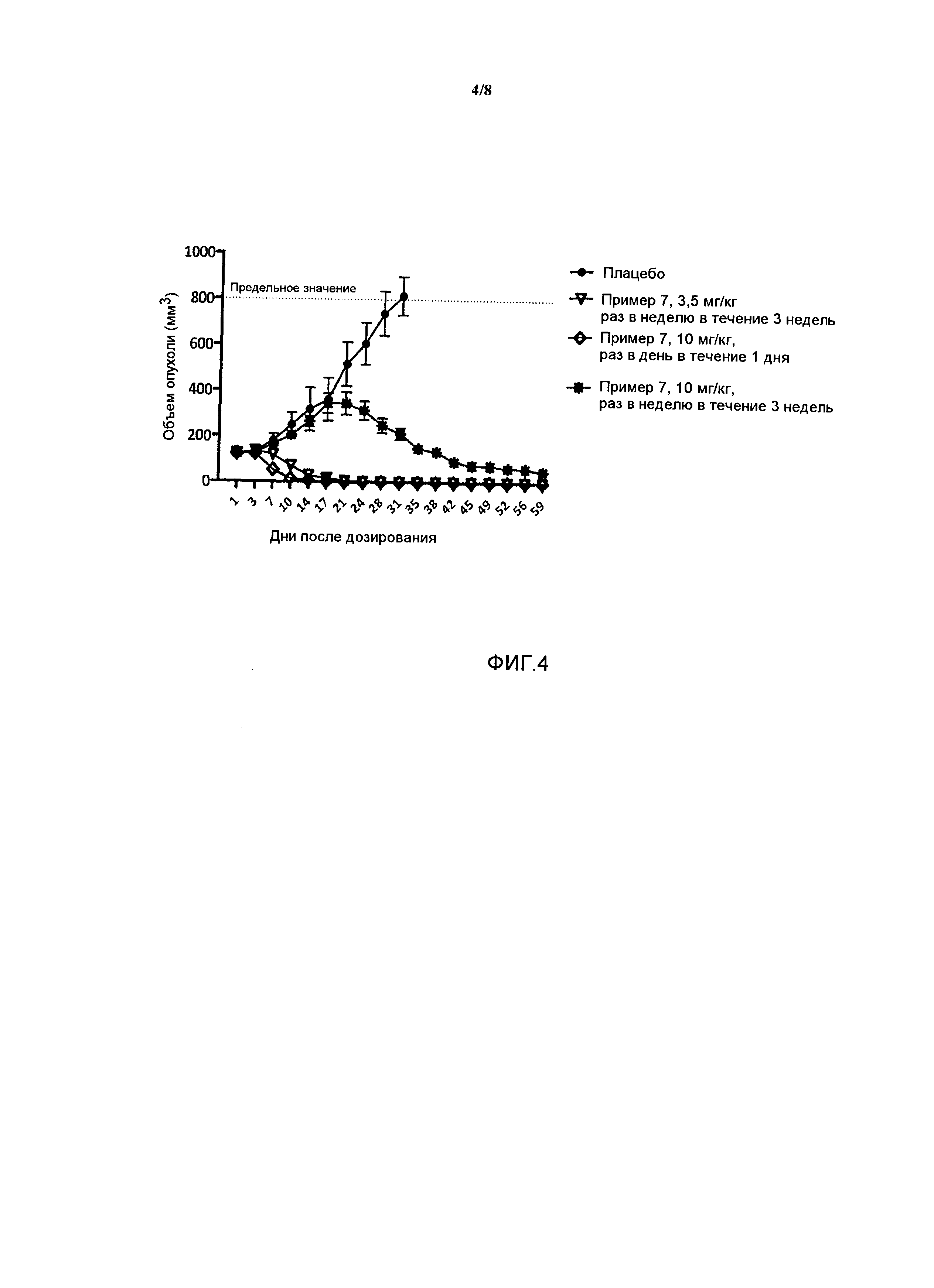
На фигуре 4 приведена графическая зависимость ответной реакции опухоли у мышей, инокулированной под кожу с помощью опухолевых клеток BT474 (n=10 для каждой группы), после внутривенного введения плацебо; конъюгатов PBRM-лекарственное средство-полимер PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (пример 7, HPV:трастузумаб приблизительно от 19:1 до 22:1) при 3,5 мг/кг, вводимых один раз в неделю в течение 3 недель на 1-ый день, 8-ой день и 15-ый день, соответственно; конъюгатов PBRM-лекарственное средство-полимер PHF-GA-(HPV-аланин)- (трастузумаб-MCC) (пример 7, HPV:трастузумаб приблизительно от 19:1 до 22:1) при 10 мг/кг, вводимых в форме разовой дозы на 1-ый день; конъюгатов PBRM-лекарственное средство-полимер PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (пример 7, HPV:трастузумаб приблизительно от 19:1 до 22:1) при 10 мг/кг, вводимых один раз в неделю в течение 3 недель на 17-ый день, 24-ый день и 31-ый день, соответственно.
На фигуре 5 приведена графическая зависимость ответной реакции опухоли у мышей, инокулированной под кожу с помощью опухолевых клеток BT474 (n=10 для каждой группы), после внутривенного введения плацебо или 30 кДа PHF-GA-(HPV-аланин)-(трастузумаб-Fab) (пример 60, HPV:трастузумаб-Fab приблизительно от 10:1 до 14:1) при 7 мг/кг, вводимых один раз в неделю в течение 3 недель на 1-ый день, 8-ой день и 15-ый день, соответственно.
На фигуре 6 приведена графическая зависимость, характеризующая фармакокинетику в плазме для конъюгированных HPV и трастузумаба после внутривенного болюсного введения PBRM-лекарственное средство-конъюгата PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12), как в примере 8 (HPV:трастузумаб приблизительно от 16:1 до 18:1) при 15 мг/кг (в расчете на трастузумаб).
На фигуре 7 приведена графическая зависимость, характеризующая накопление HPV в различных органах мышей после внутривенного болюсного введения PBRM-лекарственное средство-конъюгата PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12), как в примере 8 (HPV:трастузумаб приблизительно от 16:1 до 18:1) при 15 мг/кг (в расчете на трастузумаб).
На фигуре 8 приведена графическая зависимость ответной реакции опухоли у мышей, инокулированной под кожу с помощью опухолевых клеток BT474 (n=10 для каждой группы), после внутривенного введения плацебо; конъюгатов PBRM-лекарственное средство-полимер PHF-GA-(ауристатин F-гидроксипропиламид-L-аланин)-(трастузумаб-MCC) (пример 52, ауристатин F:трастузумаб приблизительно от 24:1 до 28:1) и конъюгата лекарственное средство-полимер PHF-GA-SS-диметил-NO2-(ауристатин F-гидроксипропиламид-L-аланин)-(S-S-трастузумаб) (пример 70, ауристатин F:трастузумаб приблизительно от 9:1 до 13:1) при 2 мг/кг и 4 мг/кг, вводимых один раз в неделю в течение 3 недель на 1-ый день, 8-ой день и 15-ый день, соответственно.
ПОДРОБНОЕ ОПИСАНИЕ КОНКРЕТНЫХ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение предлагает новые конъюгаты белок-полимер-лекарственное средство, полимерные каркасные структуры для получения конъюгатов, способы синтеза конъюгатов или полимерных каркасных структур, содержащие их фармацевтические композиции и различные варианты применения конъюгатов.
Настоящее изобретение также предлагает новые конъюгаты полимер-лекарственное средство, способы синтеза конъюгатов, содержащие их фармацевтические композиции и различные варианты применения конъюгатов.
Настоящее изобретение также предлагает новые производные лекарственных средств, способы синтеза производных, содержащие их фармацевтические композиции и различные варианты применения производных лекарственных средств.
Определение/терминология
В изобретении также более подробно описываются конкретные соединения настоящего изобретения и определения конкретных функциональных групп. Для целей этого изобретения, химические элементы определяются в соответствии с Периодической таблицей элементов по версии службы Chemical Abstracts (CAS), приведенной в Справочнике по химии и физике (Handbook of Chemistry and Physics, 75th Ed.,) на внутренней стороне обложки, а конкретные функциональные группы обычно определяются так, как описано в изобретении. Кроме того, общие принципы органической химии, также как и конкретные функциональные фрагменты и их реакционная способность, описаны в монографии "Organic Chemistry", Thomas Sorrell, University Science Books, Sausalito: 1999, содержания которых приводится в описании изобретения путем ссылки на них. Кроме того, для обычного специалиста в этой области является очевидным, что в описанных в изобретении методах синтеза могут применяться различные защитные группы.
Подразумевается, что в следующем далее описании и пунктах формулы изобретения применение формы единственного числа охватывает как форму единственного числа, так и форму множественного числа, если только в описании изобретения не указано иное или налицо явное противоречие с контекстом. Подразумевается, что термины "включающий", "имеющий", "заключающий" и "содержащий" следует рассматривать как открытые термины (то есть, означающие "включающий, но этим не ограничивая"), если не указано иначе. Кроме того, во всех случаях, когда в варианте осуществления применяется термин "включающий" или другой открытый термин, следует иметь в виду, что аналогичный вариант осуществления может быть заявлен более узко путем применения промежуточного термина "состоящий в основном из" или замкнутого термина "состоящий из".
Предполагается, что перечисление диапазонов величин применяют просто для того, чтобы в сокращенной форме указать индивидуально каждую отдельную величину, попадающую в указанный диапазон, если в описании изобретения не указано иначе, и каждая отдельная величина приводится в описании изобретения, как если бы ее индивидуально упомянули в изобретении. Применяемый в описании изобретения диапазон, если не указано иначе, включает два предела диапазона. Например, выражения "при этом x представляет собой целое число между 1 и 6" и "при этом x представляет собой целое число от 1 до 6" оба означают, что "x представляет собой 1, 2, 3, 4, 5 или 6".
"Защитная группа": используемый в описании изобретения термин защитная группа означает, что конкретный функциональный фрагмент, например, O, S или N, временно блокирован, для того чтобы реакция могла быть селективно проведена в другом реакционно-способном месте в полифункциональном соединении. В предпочтительных вариантах осуществления, защитная группа селективно реагирует с высоким выходом с получением защищенного субстрата, который устойчив в отношении намеченных к проведению реакций; защитная группа должна быть селективно удалена с высоким выходом с помощью легко доступных, предпочтительно, нетоксичных реагентов, которые не взаимодействуют с другими функциональными группами; защитная группа образует легко отделяемое производное (более предпочтительно, без образования новых стереогенных центров); и защитная группа обладает минимумом дополнительных функциональных групп для предотвращения появления дополнительных реакционно-способных мест. Могут применяться подробно описанные в изобретении защитные группы для кислорода, серы, азота и углерода. Например, в конкретных вариантах осуществления, могут применяться конкретные защитные группы для кислорода. Эти защитные группы для кислорода включают, но этим не ограничивая, метиловые эфиры, замещенные метиловые эфиры (например, MOM (метоксиметиловый эфир), MTM (метилтиометиловый эфир), BOM (бензилоксиметиловый эфир) и PMBM (п-метоксибензилоксиметиловый эфир)), замещенные этиловые эфиры, замещенные бензиловые эфиры, силиловые эфиры (например, TMS (триметилсилиловый эфир), TES (триэтилсилиловый эфир), TIPS (триизопропилсилиловый эфир), TBDMS (третбутилдиметилсилиловый эфир), трибензилсилиловый эфир и TBDPS (третбутилдифенилсилиловый эфир), сложные эфиры (например, формиат, ацетат, бензоат (Bz), трифторацетат и дихлорацетат), карбонаты, циклические ацетали и кетали. В других конкретных примерах вариантов осуществления, применяют защитные группы для азота. В технике известны защитные группы для азота, также как и способы установления защиты и снятия защиты. Защитные группы для азота включают, но этим не ограничивая, карбаматы (включая метил-, этил- и замещенные этилкарбаматы (например, Troc), амиды, производные циклических имидов, N-алкил- и N-ариламины, производные иминов и производные енаминов. В еще одних вариантах осуществления, могут применяться конкретные примеры защитных групп для серы. Защитные группы для серосодержащих групп включают, но этим не ограничивая, описанные выше защитные группы для кислорода, также как и алифатическую карбоновую кислоту (например, акриловую кислоту), имид малеиновой кислоты, винилсульфонил и необязательно замещенную малеиновую кислоту. В изобретении подробно описываются и другие конкретные примеры защитных групп, однако, следует иметь в виду, что предполагается, что настоящее изобретения не ограничивается этими защитными группами; и более того, на основе приведенных выше критериев может быть легко найден целый ряд дополнительных эквивалентных защитных групп и использован в настоящем изобретении. Кроме того, различные защитные группы описаны в монографии "Protective Groups in Organic Synthesis" Third Ed. Greene, T.W. and Wuts, P.G., Eds., John Wiley & Sons, New York: 1999, содержание которой приводится в описании изобретения путем ссылки на нее.
"Уходящая группа" относится к молекулярному фрагменту, который уходит с парой электронов при гетеролитическом расщеплении связи. Уходящие группы могут представлять собой анионы или нейтральные молекулы. Уходящие группы включают, но этим не ограничивая, галогениды, такие как Cl-, Br- и I-, сульфонатные эфиры, такие как паратолуолсульфонат ("тозилат", TsO-) и RC(O)O-, где R представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент.
Все описанные в изобретении способы могут быть осуществлены в любом подходящем порядке, если в изобретении не указано иначе или же если это не находится в явном противоречии с контекстом. Приводимые в описании изобретения все без исключения примеры или формулировки иллюстративного типа (например, "такой как") предназначаются только для того, чтобы лучше проиллюстрировать изобретение, и их не следует истолковывать как ограничение объема пунктов формулы изобретения, если только в явной форме не заявлено иное. Ни одну из формулировок в описании изобретения не следует истолковывать как указание на то, что любой незаявленный элемент является существенным для элемента, который заявляется в формуле изобретения.
"Антитело" относится к молекуле иммуноглобулина класса IgG, включающего, но этим не ограничивающего, IgG подклассы (IgG1, 2, 3 и 4), и класса IgM, который способен специфически связывать конкретный эпитоп на антигене. Антитела могут представлять собой интактные иммуноглобулины, полученные из природных источников или из рекомбинантных источников, и могут представлять собой иммунореактивные части интактных иммуноглобулинов. Антитела могут существовать в различных формах, включая, например, поликлональные антитела, моноклональные антитела, камелизированные однодоменные антитела, внутриклеточные антитела ("интратела"), рекомбинантные антитела, антиидиотипические антитела, доменные антитела, линейное антитело, полиспецифическое антитело, фрагменты антител, такие как, Fv, Fab, Fab', Fab'-SH, F(ab')2, одноцепочечные вариабельные фрагменты антител (scFv), Fc, pFc', scFvFc, дисульфид Fv (dsfv), биспецифические антитела (bc-scFv), такие как BiTE антитела; камелизированные антитела, антитела с измененной поверхностью, гуманизированные антитела, полностью человеческие антитела, однодоменное антитело (sdAb, также известное как NANOBODY®), химерные антитела, химерные антитела, включающие по меньшей мере одну человеческую константную область, антитела с двойственным сродством, такие как, ретаргетинговые белки с двойственным сродством (DART™), двухвалентные (или бивалентные) одноцепочечные вариабельные фрагменты (di-scFvs, bi-scFvs), включающие, но этим не ограничивая, минитела, диатела, триатела или тритела, тетратела и другие подобные антитела, и поливалентные антитела. "Фрагмент антитела" относится, по меньшей мере, к части вариабельной области молекулы иммуноглобулина, которая связывает его мишень, то есть, антигенсвязывающей области. Используемый в описании изобретения термин "антитело" относится как к полноразмерному антителу, так и к фрагментам антитела, если не указано иначе.
"Распознающая молекула на основе белка" или "PBRM" относится к молекуле, которая распознает и связывает маркер или рецептор клеточной поверхности, такой как трансмембранный белок, поверхностный иммобилизированный белок или протогликан. Примеры PBRM включают, но этим не ограничивая, антитела (например, трастузумаб, цетуксимаб, ритуксимаб, бевацизумаб, эпратузумаб, велтузумаб, лабетузумаб) или пептиды (пептиды, направленные на LHRH рецептор, EC-1 пептид), липокалины, такие как, например, антикалины, белки, такие как, например, интерфероны, лимфокины, факторы роста, колониестимулирующие факторы и другие подобные, пептиды или мимики пептидов, и другие подобные. Распознающая молекула на основе белка, помимо тагетирования конъюгата модифицированного полимера на конкретную клетку, ткань или область, может также обладать определенной терапевтической активностью, такой как антипролиферативная (цитостатическая и/или цитотоксическая) активность в отношении клетки-мишени или пути. Распознающая молекула на основе белка включает или может быть сконструирована таким образом, чтобы включать по меньшей мере одну химически реакционноспособную группу, такую как, -COOH, первичный амин, вторичный амин -NHR, -SH, или химически реакционно-способный фрагмент или боковые цепи аминокислоты, такой как, например, тирозин, гистидин, цистеин или лизин.
Используемый в описании изобретения термин "биологически совместимые" применяется для описания соединений, которые вызывают минимальные деструктивные эффекты или ответные реакции организма реципиента при контакте с жидкостями организма или живыми клетками или тканями. Так, используемый в описании изобретения термин "биологически совместимая группа" относится к алифатическому, циклоалкильному, гетероалифатическому, гетероциклоалкильному, арильному или гетероарильному фрагменту, который подпадает под приводимое в описание изобретения определение термина "биологически совместимый". Используемый в описании изобретения термин "биологическая совместимость" также означает, что соединения характеризуются минимальными взаимодействиями с распознающими белками, например, природными антителами, клеточными белками, клетками и другими компонентами биологических систем, если только такие взаимодействия специально не являются желательными. Так, вещества и функциональные группы, специально предназначенные оказывать минимальные описанные выше воздействия, например, лекарственные средства и пролекарства, считают биологически совместимыми. Предпочтительно, чтобы (за исключением соединений, которые должны быть цитотоксичными, таких как, например, антинеопластичные средства) соединения считались "биологически совместимыми", если их добавление к нормальным клеткам in vitro при концентрациях, аналогичных предполагаемым системным in vivo концентрациям, приводило бы в результате к гибели клеток в количестве менее чем или равном 1% в течение времени, эквивалентного периоду полувыведения соединения in vivo (например, периода времени, требующегося для того, чтобы было удалено/выведено 50% введенного in vivo соединения), и их введение in vivo вызывало бы минимальные и приемлемые с медицинской точки зрения воспаление, реакцию на чужеродные тела, иммунотоксичность, химическую токсичность и/или другие такие отрицательные воздействия. В приведенном выше предложении, термин "нормальные клетки" относится к клеткам, которые не собираются уничтожить или же значительно повредить с помощью испытуемого соединения.
"Биоразлагаемый": Используемый в описании изобретения термин "биоразлагаемые" полимеры представляют собой полимеры, которые восприимчивы к биологическому превращению in vivo. Используемые в описании изобретения "биоразлагаемые" соединения или фрагменты представляют собой соединения или фрагменты, которые при поглощении клетками могут разрушаться под воздействием лизосомальных или других химических превращений или в результате гидролиза на компоненты, которые клетки могут либо повторно использовать, либо которые могут быть удалены без значительного токсического воздействия на клетки. Используемый в описании изобретения термин "биорасщепляемый" имеет такое же значение как термин "биоразлагаемый". Предпочтительно, чтобы образовавшиеся в результате разрушения фрагменты приводили к небольшой перегрузке или не приводили к перегрузке органа или клеток или к патологическим процессам, вызываемым такой перегрузкой, или к другим отрицательным воздействиям in vivo. Примеры процессов биоразложения включают ферментативный и неферментативный гидролиз, окисление и восстановление. Описанные в изобретении подходящие условия для неферментативного гидролиза конъюгатов биоразлагаемый белок-полимер-лекарственное средство (или их компонентов, например, биоразлагаемого полимерного носителя и связующих звеньев между носителем и антителом или молекулой лекарственного средства), например, включают воздействие воды на биоразлагаемые конъюгаты при температуре и pH лизосомального внутриклеточного компартмента. Биоразложение некоторых конъюгатов белок-полимер-лекарственное средство (или их компонентов, например, биоразлагаемого полимерного носителя и связующих звеньев между носителем и антителом или молекулой лекарственного средства) может быть также интенсифицировано вне клеток, например, в областях организма животного с низкими значениями pH, например, в области воспаления, в непосредственной близости от активированных макрофагов или других клеток, выделяющих факторы, облегчающие разрушение. В конкретных предпочтительных вариантах осуществления, эффективный размер полимерного носителя при pH~7,5 заметно не изменяется в течение от 1 до 7 дней, и сохраняет около 50% своего исходного размера в течение, по меньшей мере, нескольких недель. С другой стороны, предпочтительно, чтобы при pH~5 полимерный носитель заметно разрушался в течение от 1 до 5 дней и полностью превращался в низкомолекулярные фрагменты в течение от двух недель до нескольких месяцев. Целостность полимера при таких испытаниях может быть определена, например, с помощью эксклюзионной высокоэффективной жидкостной хроматографии (ВЭЖХ). Несмотря на то, что в некоторых случаях предпочтительным может быть более быстрое разрушение, тем не менее, обычно более желательно, чтобы полимер разрушался в клетках со скоростью, которая не превышает скорости метаболизации или экскреции фрагментов полимера клетками. В предпочтительных вариантах осуществления, полимеры и побочные продукты биоразложения полимеров являются биологически совместимыми.
"Биодоступность": Термин "биодоступность" относится к системной доступности (то есть, к концентрациям в крови/плазме) данного количества лекарственного средства или соединения, вводимого субъекту. Биодоступность является абсолютным термином, в котором указывается как время (скорость), так и суммарное количество (доля) лекарственного средства или соединения, которое попадает в системное кровообращение из введенной лекарственной формы.
"Гидрофильный": Термин "гидрофильный" при его использовании в отношении заместителей на мономерных звеньях полимера практически не отличается от общепринятого в науке значения этого термина, и он обозначает химические фрагменты, которые содержат ионизируемые, полярные или поляризуемые атомы, или же которые могут быть сольватированы молекулами воды. Так, используемая в описании изобретении гидрофильная группа относится к алифатическому, циклоалкильному, гетероалифатическому, гетероциклоалкильному, арильному или гетероарильному фрагменту, который подпадает под приведенное в описании изобретения определение термина "гидрофильный". Примеры конкретных подходящих гидрофильных органических фрагментов включают, без ограничения, алифатические или гетероалифатические группы, включающие цепочку атомов длиной приблизительно от одного до двенадцати атомов, гидроксил, гидроксиалкил, амин, карбоксил, амид, эфир карбоновой кислоты, тиоэфир, альдегид, нитрил, изонитрил, нитрозо, гидроксиламин, меркаптоалкил, гетероцикл, карбаматы, карбоновые кислоты и их соли, сульфоновые кислоты и их соли, эфиры сульфоновых кислот, фосфорные кислоты и их соли, фосфатные эфиры, полигликолевые эфиры, полиамины, поликарбоксилаты, полиэфиры и политиоэфиры. В предпочтительных вариантах осуществления настоящего изобретения по меньшей мере одно из мономерных звеньев полимера включает карбоксильную группу (COOH), альдегидную группу (CHO), метилольную группу (CH2OH) или гликольную группу (например, CHOH-CH2OH или CH-(CH2OH)2).
Термин "гидрофильный" при его использовании в отношении полимеров изобретения обычно не отличается от общепринятого в науке значения этого термина, и он обозначает полимеры, включающие определенные выше гидрофильные функциональные группы. В предпочтительном варианте осуществления, гидрофильный полимер представляет собой водорастворимый полимер. Гидрофильность полимера может быть непосредственно измерена путем определения энергии гидратации или определена с помощью исследования поведения полимера между двумя жидкими фазами, или путем хроматографии на твердых фазах с известной гидрофобностью, таких как, например, C4 или C18.
"Полимерный носитель": Используемый в описании изобретения термин "полимерный носитель" относится к полимеру или модифицированному полимеру, который подходит для ковалентного связывания или может быть ковалентно связан с одной или более молекул лекарственного средства через специально подобранное связующее звено и/или с одной или более PBRM через специально подобранное связующее звено.
"Физиологические условия": Используемая в описании изобретения фраза "физиологические условия" относится к диапазону химических (например, pH, ионная сила) и биохимических (например, концентрации ферментов) условий, которые характерны для внеклеточных жидкостей живых тканей. Для большинства нормальных тканей, физиологическое значение pH составляет приблизительно от 7,0 до 7,4. Плазма циркулирующей крови и нормальная внутритканевая жидкость представляют собой типичные примеры нормальных физиологических условий.
"Полисахарид", "углевод" или "олигосахарид": Термины "полисахарид", "углевод" или "олигосахарид" являются общеизвестными и относятся, обычно, к веществам, имеющим химическую формулу (CH2O)n, где обычно n>2, и их производным. Углеводы представляют собой полигидроксиальдегиды или полигидроксикетоны или продукты изменения этих веществ в результате простых химических превращений, таких как гидролиз, окисление или восстановление. Обычно, углеводы присутствуют в форме циклических ацеталей или кеталей (таких как, глюкоза или фруктоза). Эти циклические звенья (моносахариды) могут быть соединены друг с другом с образованием молекул с малым числом (олигосахариды) или с некоторым числом (полисахариды) звеньев моносахаридов. Обычно, углеводы с четко определенным числом, типами и расположением моносахаридных звеньев называют олигосахаридами, а углеводы, состоящие из смесей молекул с различным числом и/или расположением моносахаридных звеньев, называют полисахаридами. Термины "полисахарид", "углевод" и "олигосахарид" используются в описании изобретения взаимозаменяемо. Полисахарид может включать природные сахара (например, глюкозу, фруктозу, галактозу, маннозу, арабинозу, рибозу и ксилозу) и/или производные природных сахаров (например, 2'-фторрибозу, 2'-деоксирибозу и гексозу).
"Малая молекула": Используемый в описании изобретения термин "малая молекула" относится к молекулам, либо природным, либо созданным искусственно (например, путем химического синтеза), которые имеют относительно низкую молекулярную массу. Предпочтительные малые молекулы являются биологически активными в том смысле, что они вызывают местный или системный эффект у животных, предпочтительно, у млекопитающих, более предпочтительно, у людей. В конкретных предпочтительных вариантах осуществления, малая молекула является лекарственным средством, и малую молекулу называют "молекулой лекарственного средства" или "лекарственным средством" или "терапевтическим средством". В конкретных вариантах осуществления, молекула лекарственного средства имеет молекулярную массу меньше чем или равную приблизительно 5 кДа. В других вариантах осуществления, молекула лекарственного средства имеет молекулярную массу меньше чем или равную приблизительно 1,5 кДа. В вариантах осуществления, молекулу лекарственного средства выбирают из алкалоидов барвинка, ауристатинов, тубулизинов, дуокармицинов, ингибиторов киназы, ингибиторов MEK, ингибиторов KSP и их аналогов. Предпочтительно, хотя и необязательно, чтобы лекарственное средство представляло собой лекарственное средство, которое уже было признано безопасным и эффективным для применения соответствующим государственным органом или учреждением, например, Федеральным управлением США по контролю качества продуктов питания, напитков и лекарственных препаратов. Например, лекарственные средства для применения на людях перечисляются Федеральным управлением США по контролю качества продуктов питания, напитков и лекарственных препаратов в 21 Своде федеральных нормативных актов в параграфах §§ 330,5, 331-361 и 440-460; лекарственные средства для ветеринарного применения перечисляются Федеральным управлением США по контролю качества продуктов питания, напитков и лекарственных препаратов в 21 Своде федеральных нормативных актов в параграфах §§ 500-589, содержание которых приводится в описании изобретения путем ссылки на них, все считаются подходящими для применения с гидрофильными полимерами настоящего изобретения.
Классы молекул лекарственных средств, которые могут быть использованы при осуществлении настоящего изобретения, включают, но этим не ограничивая, противораковые средства, радионуклиды, витамины, лекарственные средства против СПИДа, антибиотики, иммунодепрессанты, противовирусные средства, ингибиторы ферментов, нейротоксины, опиоиды, снотворные средства, антигистамины, смягчающие компоненты, транквилизаторы, противосудорожные средства, мышечные релаксанты и лекарственные средства против болезни Паркинсона, спазмолитики и мышечные контрактанты, включающие блокаторы каналов, миотические средства и антихолинергические средства, средства против глаукомы, противопаразитарные и/или противопротозойные средства, модуляторы взаимодействий клетка-внеклеточный матрикс, включающие ингибиторы роста клеток и антиадгезионные молекулы, сосудорасширяющие средства, ингибиторы синтеза ДНК, РНК или белка, антигипотензивные средства, анальгетики, жаропонижающие средства, стероидные и нестероидные противовоспалительные средства, антиангиогенные факторы, антисекреторные факторы, антикоагулянты и/или антитромботические средства, местные анестетики, лекарственные средства от глазных болезней, простагландины, антидепрессанты, нейролептики, противорвотные средства, радиофармацевтические препараты. Многие большие молекулы также являются лекарственными средствами.
Более полный, хотя и не исчерпывающий, перечень классов и конкретных лекарственных средств, подходящих для применения в настоящем изобретении, можно найти в монографии "Pharmaceutical Substances: Syntheses, Patents, Applications" by Axel Kleemann and Jurgen Engel, Thieme Medical Publishing, 1999 и энциклопедии "Merck Index: An encyclopedia of Chemicals, Drugs, and Biologicals", Edited by Susan Budavari et ah, CRC Press, 1996, содержание которых приводится в описании изобретения путем ссылки на них. В предпочтительных вариантах осуществления, лекарственное средство, используемое в этом изобретении, представляет собой терапевтическое средство, которое имеет антипролиферативную (цитостатическую и/или цитотоксическую) активность в отношении клетки-мишени или пути. Лекарственное средство может иметь химически реакционно-способную группу, такую как, например, -COOH, первичный амин, вторичный амин -NHR, -OH, -SH, -C(O)H, -C(O)R, -C(O)NHR2b, C(S)OH, -S(O)2OR2b, -P(O)2OR2b, -CN, -NC или -ONO, где R представляет собой алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент, и R2b представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклический фрагмент.
Используемые в описании изобретения "производное лекарственного средства" или "модифицированное лекарственное средство" или другие подобные термины относятся к соединению, которое включает молекулу лекарственного средства, предназначенного для введения с помощью конъюгата изобретения, и функциональную группу, способную связывать молекулу лекарственного средства с полимерным носителем.
Используемый в описании изобретения термин "активная форма" относится к форме соединения, которая проявляет ожидаемую фармацевтическую активность in vivo или in vitro. В частности, когда молекула лекарственного средства, предназначенная для доставки с помощью конъюгата изобретения, высвобождается из конъюгата, активная форма может представлять собой лекарственное средство само по себе или его производные, которые проявляют ожидаемые терапевтические свойства. Высвобождение лекарственного средства из конъюгата может достигаться за счет разрушения биоразлагаемой химической связи связующего звена, которое связывает лекарственное средство с полимерным носителем. Активные производные лекарственного средства могут, соответственно, включать часть связующего звена.
"Диагностическая метка": Используемый в описании изобретения термин "диагностическая метка" относится к атому, группе атомов, фрагменту или функциональной группе, нанокристаллу или другому дискретному элементу рассматриваемой композиции, который может быть детектирован in vivo или ex vivo с помощью известных в науке аналитических методов. Связанные с конъюгатом настоящего изобретения такие диагностические метки позволяют осуществлять мониторинг конъюгата in vivo. В качестве варианта или дополнительно, конструкции и композиции, которые включают диагностические метки, могут применяться для мониторинга биологических функций или структур. Примеры диагностических меток включают, без ограничения, метки, которые могут быть использованы в медицинских диагностических методиках, такие как, радиоактивные изотопы (радионуклиды) для гамма-сцинтиграфии и позитрон-эмиссионной томографии (PET), контрастные вещества для магнитно-резонансной томографии (MRI) (например, парамагнитные атомы и суперпарамагнитные нанокристаллы), контрастные вещества для компьютерной томографии и других рентгеновских методов визуализации, средства для ультразвуковых диагностических методов (сонографии), средства для нейтронной активации (например, бор, гадолиний), флуорофоры для различных оптических методов и, в общем случае, фрагменты, которые могут испускать, отражать, поглощать, рассеивать или иным способом воздействовать на электромагнитные поля или волны (например, гамма-лучи, рентгеновское излучение, радиоволны, микроволновое излучение, видимый свет), частицы (например, альфа-частицы, электроны, позитроны, нейтроны, протоны) или другие формы радиации, например, ультразвук.
"Алифатический": Используемый в описании изобретения термин "алифатический" обычно включает как насыщенные, так и ненасыщенные линейные (то есть, неразветвленные) или разветвленные алифатические углеводороды, которые необязательно замещены одной или более функциональными группами. Для обычного специалиста в этой области является очевидным, что "алифатический", как предполагается в описании изобретения, включает, но этим не ограничивая, алкильные, алкенильные, алкинильные фрагменты. Так, используемый в описании изобретения термин "алкил" включает линейные и разветвленные алкильные группы. Аналогичное обозначение применяется к другим общим терминам, таким как "алкенил", "алкинил" и другим подобным терминам. Кроме того, используемые в описании изобретения термины "алкил", "алкенил", "алкинил" и другие подобные термины охватывают как замещенные, так и незамещенные группы. В конкретных вариантах осуществления, используемые в описании изобретения "низший алкил" применяют для обозначения алкильных групп (замещенных, незамещенных, разветвленных или неразветвленных), имеющих приблизительно 1-6 углеродных атомов.
"Алкенил": термин "алкенил" обозначает одновалентную группу, полученную из углеводородного фрагмента, имеющего, по меньшей мере, одну двойную связь углерод-углерод, в результате удаления одного атома водорода. "Замещенные алкенильные" группы замещены одной или более функциональными группами. Заместители включают, но этим не ограничивая, любой из заместителей, упомянутых ниже, то есть, перечисленных ниже заместителей, приводящих к образованию стабильного соединения. Алкенильные группы включают, например, этенил, пропенил, бутенил, 1-метил-2-бутен-1-ил и другие подобные группы.
"Алкинил": используемый в описании изобретения термин "алкинил" относится к одновалентной группе, полученной из углеводорода, имеющего, по меньшей мере, одну тройную связь углерод-углерод, в результате удаления одного атома водорода. "Замещенные алкенильные" группы замещены одной или более функциональными группами. Заместители включают, но этим не ограничивая, любой из заместителей, упомянутых ниже, то есть, перечисленных ниже заместителей, приводящих к образованию стабильного соединения. Характерные алкинильные группы включают этинил, 2-пропинил (пропаргил), 1-пропинил и другие подобные группы.
В конкретных вариантах осуществления, применяемые в изобретении алкильные, алкенильные и алкинильные группы содержат приблизительно 1-20 алифатических углеродных атомов. В других конкретных вариантах осуществления, применяемые в изобретении алкильные, алкенильные и алкинильные группы содержат приблизительно 1-10 алифатических углеродных атомов. В еще одних вариантах осуществления, применяемые в изобретении алкильные, алкенильные и алкинильные группы содержат приблизительно 1-8 алифатических углеродных атомов. В других вариантах осуществления, применяемые в изобретении алкильные, алкенильные и алкинильные группы содержат приблизительно 1-6 алифатических углеродных атомов. В еще одних вариантах осуществления, применяемые в изобретении алкильные, алкенильные и алкинильные группы содержат приблизительно 1-4 углеродных атомов. Так, иллюстративные примеры алифатических групп включают, но этим не ограничивая, например, метил, этил, н-пропил, изопропил, аллил, н-бутил, вторбутил, изобутил, третбутил, н-пентил, вторпентил, изопентил, третпентил, н-гексил, вторгексил и другие подобные группы, которые в свою очередь могут нести один или более заместителей. Алкенильные группы включают, но этим не ограничивая, например, этенил, пропенил, бутенил, 1-метил-2-бутен-1-ил и другие подобные группы. Типичные алкинильные группы включают, но этим не ограничивая, этинил, 2-пропинил (пропаргил), 1-пропинил и другие подобные группы.
"Алкилен": используемый в описании изобретения термин "алкилен", сам по себе или как часть другого термина, относится к насыщенной, разветвленной или линейной цепи, имеющей два центра из одновалентных радикалов, полученной удалением двух атомов водорода от одного и того же или двух различных углеродных атомов исходного алкана. Алкиленовые радикалы включают, но этим не ограничивая, метилен, 1,2-этилен, 1,3-пропилен и другие подобные радикалы. Подходящие алкилены включают, но этим не ограничивая, метилен, этилен, пропилен, бутилен, пентилен, гексилен, гептилен, октилен, нонилен, декален и другие подобные алкилены. Аналогично, термин "циклоалкилен" относится к двухвалентному циклоалкилу. Циклоалкиленовые радикалы включают, но этим не ограничивая, 1,1-циклопентилен, 1,2-циклопентилен, 1,1-циклобутилен, 1,3-циклобутилен и другие радикалы.
"Гетероалифатический": используемый в описании изобретения термин "гетероалифатический" относится к алифатическим фрагментам, в которых один или более углеродных атомов в главной цепи были замещены гетероатомом. Так, гетероалифатическая группа относится к алифатической цепи, которая содержит один или более атомов кислорода, серы, азота, фосфора или кремния, например, вместо углеродных атомов. Гетероалифатические фрагменты могут быть разветвленными или линейными неразветвленными. В конкретных вариантах осуществления, гетероалифатические фрагменты замещены ("замещенный гетероалифатический") путем независимой замены в них одного или более атомов водорода на один или более фрагментов, включающих, но этим не ограничивая, алифатический, гетероалифатический, циклоалкильный, гетероциклоалкильный, арильный, гетероарильный, алкиларильный, алкилгетероарильный фрагменты, алкокси, арилокси, гетероалкокси, гетероарилокси, алкилтио, арилтио, гетероалкилтио, гетероарилтио, F, Cl, Br, I, -NO2, -CN, -CF3, -CH2CF3; -CHCl2; -CH2OH; -CH2CH2OH; -CH2NH2; -CH2SO2CH3 или -GRG1, где G представляет собой -O-, -S-, -NRG2-, -C(=O)-, -S(=O)-, -SO2-, -C(=O)O-, -C(=O)NRG2-, -OC(=O)-, -NRG2C(=O)-, -OC(=O)O-, -OC(=O)NRG2-, -NRG2C(=O)O-, -NRG2C(=O)NRG2-, -C(=S)-, -C(=S)S-, -SC(=S)-, -SC(=S)S-, -C(=NRG2)-, -C(=NRG2)O-, -C(=NRG2)NRG3-, -OC(=NRG2)-, -NRG2C(=NRG3)-, -NRG2SO2-, -NRG2SO2NRG3- или -SO2NRG2-, где в каждом случае присутствия, RG1, RG2 и RG3 независимо включают, но этим не ограничивая, водород, галоген или необязательно замещенный алифатический, гетероалифатический, циклоалкильный, гетероциклоалкильный, арильный, гетероарильный, алкиларильный или алкилгетероарильный фрагмент. Дополнительные примеры обычно применяемых заместителей иллюстрируются в конкретных вариантах осуществления, приведенных в описанных в изобретении примерах.
"Циклоалкил": используемый в описании изобретения термин "циклоалкил" относится к насыщенной или ненасыщенной неароматической углеводородной моно- или полициклической системе, имеющей от 3 до 30 углеродных атомов (например, C3-C10). Подходящие циклоалкилы включают, но этим не ограничивая, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклопентенил, циклогексенил, циклогептенил, циклогептинил, адамантил и другие подобные группы.
Используемый в описании изобретения термин "гетероциклоалкил" относится к насыщенной или ненасыщенной неароматической 3-8 членной моноциклической, 8-12 членной бициклической или 11-19 членной трициклической кольцевой системе, имеющей один или более гетероатомов (таких как O, N, S или Se), если не указано иначе. В конкретных вариантах осуществления, термин "гетероциклоалкил" относится к неароматическому 5-, 6-, 7- или 8-членному кольцу или полициклической группе, включающей, но этим не ограничивая, би- или трициклическую группу, включающую конденсированные шестичленные кольца, имеющие от одного до трех гетероатомов, независимо выбранных из кислорода, серы и азота, где (i) каждое 5-членное кольцо имеет от 0 до 2 двойных связей, и каждое 6-членное кольцо имеет от 0 до 2 двойных связей, (ii) гетероатомы азот и сера могут быть необязательно окислены, (iii) гетероатом азот может быть необязательно кватернизированным, и (iv) любое из приведенных выше гетероциклоалкильных колец может быть конденсированным с арильным или гетероарильным кольцом. Примеры гетероциклоалкильных групп включают, но этим не ограничивая, пиперидинил, пиперазинил, пирролидинил, диоксанил, тетрагидрофуранил, тетрагидротиенил, изоиндолинил, индолинил, имидазолидинил, пиразолидинил, оксазолидинил, изоксазолидинил, триазолидинил, тетрагидрофуранил, оксиранил, азетидинил, оксетанил, тиетанил, 1,2,3,6-тетрагидропиридинил, тетрагидро-2H-пиранил, 3,6-дигидро-2H-пиранил, морфолинил и другие подобные группы.
Используемый в описании изобретения термин "арил" относится к группам с ароматичностью, включающим "конъюгированные" или полициклические системы, по меньшей мере, с одним ароматическим кольцом, не содержащим ни одного гетероатома в кольцевой системе. Примеры включают фенил, бензил, 1,2,3,4-тетрагидронафталенил и другие группы.
Используемый в описании изобретения термин "гетероарил" относится к определенным выше арильным группам, но содержащим от одного до четырех гетероатомов в кольцевой системе, и, кроме того, гетероарилы могут называть "арилгетероциклами" или "гетероароматическими соединениями". Предполагается, что используемый в описании изобретения термин "гетероарил" включает стабильное 5-, 6- или 7-членное моноциклическое или 7-, 8-, 9-, 10-, 11- или 12-членное бициклическое ароматическое гетероциклическое кольцо, которое состоит из углеродных атомов и одного или более гетероатомов, например, 1 или 1-2, или 1-3, или 1-4, или 1-5, или 1-6 гетероатомов, или, например, 1, 2, 3, 4, 5, или 6 гетероатомов, независимо выбранных из группы, состоящей из азота, кислорода и серы. Атом азота может быть замещенным или незамещенным (то есть, N или NR, где R представляет собой H или другие определяемые заместители). Гетероатомы азот и сера могут быть необязательно окислены (то есть, N→O и S(О)p, где p=1 или 2). Следует отметить, что суммарное число атомов S и O в ароматическом гетероцикле не может быть больше 1. Примеры гетероарила включают пиридил, пиразинил, пиримидинил, пирролил, пиразолил, имидазолил, тиазолил, изотиазолил, тетразолил, оксазолил, изооксазолил, тиадиазолил, оксадиазолил, тиофенил, фуранил, хинолинил, изохинолинил, тетразолил, пиридазинил, хиназолинил, дигидрохиназолил и тетрагидрохиназолил и другие подобные группы.
Кроме того, термины "арил" и "гетероарил" включают полициклические арильные и гетероарильные группы, например, трициклические, бициклические, например, нафталин, бензоксазол, бензодиоксазол, бензотиазол, бензоимидазол, бензотиофен, метилендиоксифенил, хинолин, изохинолин, нафтридин, индол, бензофуран, пурин, бензофуран, деазапурин, индолизин.
В случае полициклических ароматических колец, необходимо, чтобы только одно из колец было ароматическим (например, 2,3-дигидроиндол), хотя все кольца могут быть ароматическими (например, хинолин). Второе кольцо может быть также конденсированным или мостиковым кольцом.
Предполагается, что используемые в описании изобретения термины "карбоцикл" или "карбоциклический фрагмент" включают любое стабильное моноциклическое, бициклическое или трициклическое кольцо, имеющее указанное число углеродных атомов, каждое из которых может быть насыщенным, ненасыщенным или ароматическим. Карбоцикл включает циклоалкил и арил. Например, предполагается, что C3-C14 карбоцикл включает моноциклическое, бициклическое или трициклическое кольцо, имеющее 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 углеродных атомов. Примеры карбоциклов включают, но этим не ограничивая, циклопропил, циклобутил, циклобутенил, циклопентил, циклопентенил, циклогексил, циклогептенил, циклогептил, циклогептенил, циклооктил, циклооктенил, циклооктадиенил, флуоренил, фенил, нафтил, инданил, адамантил и тетрагидронафтил. Мостиковые кольца также подпадают под определение карбоцикла, включая, например, [3.3.0]бициклооктан, [4.3.0]бициклононан, [4.4.0]бициклодекан и [2.2.2]бициклооктан. Образование мостикового кольца происходит тогда, когда один или более углеродных атомов соединяют два несмежных углеродных атома. В одном варианте осуществления, мостиковые кольца находятся на одном или двух углеродных атомов. Следует отметить, что мостик всегда превращает моноциклическое кольцо в трициклическое кольцо. Когда кольцо является мостиковым, на мостике могут также присутствовать заместители, упомянутые для кольца. Эти термины включают также конденсированные кольца (например, нафтил, тетрагидронафтил) и спирокольца.
Используемые в описании изобретения термины "гетероцикл" или "гетероциклический фрагмент" включают любую кольцевую структуру (насыщенную, ненасыщенную или ароматическую), которая содержит, по меньшей мере, один кольцевой гетероатом (например, N, O или S). Гетероцикл включает гетероциклоалкил и гетероарил. Примеры гетероциклов включают, но этим не ограничивая, морфолин, пирролидин, тетрагидротиофен, пиперидин, пиперазин и тетрагидрофуран.
Примеры гетероциклических групп включают, но этим не ограничивая, акридинил, азоцинил, бензимидазолил, бензофуранил, бензотиофуранил, бензотиофенил, бензоксазолил, бензоксазолинил, бензтиазолил, бензтриазолил, бензтетразолил, бензизоксазолил, бензизотиазолил, бензимидазолинил, карбазолил, 4aH-карбазолил, карболинил, хроманил, хроменил, циннолинил, декагидрохинолинил, 2H,6H-1,5,2-дитиазинил, дигидрофуро[2,3-b]тетрагидрофуран, фуранил, фуразанил, имидазолидинил, имидазолинил, имидазолил, 1H-индазолил, индолнил, индолинил, индолизинил, индолил, 3H-индолил, изатиноил, изобензофуранил, изохроманил, изоиндазолил, изоиндолинил, изоиндолил, изохинолинил, изотиазолил, изоксазолил, метилендиоксифенил, морфолинил, нафтиридинил, октагидроизохинолинил, оксадиазолил, 1,2,3-оксадиазолил, 1,2,4-оксадиазолил, 1,2,5-оксадиазолил, 1,3,4-оксадиазолил, 1,2,4-оксадиазол-5(4H)-он, оксазолидинил, оксазолил, оксиндолил, пиримидинил, фенантридинил, фенантролинил, феназинил, фенотиазинил, феноксатинил, феноксазинил, фталазинил, пиперазинил, пиперидинил, пиперидонил, 4-пиперидонил, пиперонил, птеридинил, пуринил, пиранил, пиразинил, пиразолидинил, пиразолинил, пиразолил, пиридазинил, пиридооксазол, пиридоимидазол, пиридотиазол, пиридинил, пиридил, пиримидинил, пирролидинил, пирролинил, 2H-пирролил, пирролил, хиназолинил, хинолинил, 4H-хинолизинил, хиноксалинил, хинуклидинил, тетрагидрофуранил, тетрагидроизохинолинил, тетрагидрохинолинил, тетразолил, 6H-1,2,5-тиадиазинил, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,2,5-тиадиазолил, 1,3,4-тиадиазолил, тиантренил, тиазолил, тиенил, тиенотиазолил, тиенооксазолил, тиеноимидазолил, тиофенил, триазинил, 1,2,3-триазолил, 1,2,4-триазолил, 1,2,5-триазолил, 1,3,4-триазолил и ксантенил. Полициклический гетероцикл может включать конденсированные, мостиковые или спирокольца.
Циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо (или карбоциклическая или гетероциклическая группа) может быть замещено в одном или более положений кольца (например, на образующем кольцо атоме углерода или гетероатоме, таком как N) описанными выше заместителями, например, алифатическими, гетероалифатическими заместителями, циклоалкилом, гетероциклоалкилом, арилом, гетероарилом, алкиларилом, алкилгетероарилом, алкокси, арилокси, гетероалкокси, гетероарилокси, алкилтио, арилтио, гетероалкилтио, гетероарилтио, F, Cl, Br, I, -NO2, -CN, -CF3, -CH2CF3, -CHCl2, -CH2OH, -CH2CH2OH, -CH2NH2, -CH2SO2CH3, - или -GRG1, где G представляет собой -O-, -S-, -NRG2-, -C(=O)-, -S(=O)-, -SO2-, -C(=O)O-, -C(=O)NRG2-, -OC(=O)-, -NRG2C(=O)-, -OC(=O)О-, -OC(=O)NRG2-, -NRG2C(=O)O-, -NRG2C(=O)NRG2-, -C(=S)-, -C(=S)S-, -SC(=S)-, -SC(=S)S-, -C(=NRG2)-, -C(=NRG2)O-, -C(=NRG2)NRG3-, -OC(=NRG2)-, -NRG2C(=NRG3)-, -NRG2SO2-, -NRG2SO2NRG3- или -SO2NRG2-, где в каждом случае присутствия, RG1, RG2 и RG3 независимо включает, но этим не ограничивая, водород, галоген или необязательно замещенный алифатический, гетероалифатический циклоалкильный, гетероциклоалкильный, арильный, гетероарильный, алкиларильный или алкилгетероарильный фрагмент. Арильные и гетероарильные группы могут быть также конденсированными или соединенными мостиком с циклоалкильными или гетероциклическими кольцами, которые не являются ароматическими, с образованием полициклической системы (например, тетралина, метилендиоксифенила).
"Алкокси" (или "алкилокси"): Используемый в описании изобретения термин "алкокси (или алкилокси)" относится к определенной выше алкильной группе, присоединенной к исходному молекулярному фрагменту через атом кислорода ("алкокси"). В конкретных вариантах осуществления, алкильная группа содержит приблизительно 1-20 алифатических углеродных атомов. В других конкретных вариантах осуществления, алкильная группа содержит приблизительно 1-10 алифатических углеродных атомов. В еще одних вариантах осуществления, алкильная группа содержит приблизительно 1-8 алифатических углеродных атомов. В других вариантах осуществления, алкильная группа содержит приблизительно 1-6 алифатических углеродных атомов. В еще одних вариантах осуществления, алкильная группа содержит приблизительно 1-4 алифатических углеродных атомов. Примеры алкоксильных групп включают, но этим не ограничивая, метокси, этокси, пропокси, изопропокси, н-бутокси, третбутокси, неопентокси и н-гексокси.
"Арилокси": Используемый в описании изобретения термин "арилокси" относится к определенной в описании изобретения арильной группе, присоединенной к исходному молекулярному фрагменту через атом кислорода. Примеры арилоксильных групп включают, но этим не ограничивая, фенокси и нафтилокси.
"Гетероарилокси": Используемый в описании изобретения термин "гетероарилокси" относится к определенной в описании изобретения гетероарильной группе, присоединенной к исходному молекулярному фрагменту через атом кислорода. Примеры гетероарилоксильных групп включают, но этим не ограничивая, хинолилокси и изохинолизинилокси.
"Амин": термин "амин" относится к группе, имеющей структуру -N(R)2, где в каждом случае присутствия, R представляет собой независимо водород или алифатический или гетероалифатический фрагмент, или R группы, взятые вместе, могут образовывать гетероциклический фрагмент. В конкретных случаях, аминогруппа может быть заряженной (протонизированной) или кватернизированной, например, -HN+(R)2 или -N+(R)3
"Алкиламино": используемый в описании изобретения термин "алкиламино" относится к группе, имеющей структуру -NHR', где R' представляет собой определенный в описании изобретения алкил. Термин "аминоалкил" относится к группе, имеющей структуру NH2R'-, где R' представляет собой определенный в описании изобретения алкил. В конкретных вариантах осуществления, алкильная группа содержит приблизительно 1-20 алифатических углеродных атомов. В конкретных других вариантах осуществления, алкильная группа содержит приблизительно 1-10 алифатических углеродных атомов. В еще одних вариантах осуществления, применяемые в изобретении алкильные, алкенильные и алкинильные группы содержат приблизительно 1-8 алифатических углеродных атомов. В некоторых других вариантах осуществления, алкильная группа содержит приблизительно 1-6 алифатических углеродных атомов. В еще одних вариантах осуществления, алкильная группа содержит приблизительно 1-4 алифатических углеродных атомов. Примеры алкиламино включают, но этим не ограничивая, метиламино, этиламино, изопропиламино и другие подобные группы.
"Алкилтио" (или "тиоалкил") обозначает определенную в описании изобретения алкильную группу с указанным числом углеродных атомов, присоединенную через атом серы. Предполагается, что C1-6 алкилтио включает C1, C2, C3, C4, C5 и C6 алкилтиогруппы. Предполагается, что C1-8алкилтио включает C1, C2, C3, C4, C5, C6, C7 и C8алкилтиогруппы. Тиоалкильные группы могут быть замещены такими группами, как алкил, алкенил, алкинил, галоген, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, карбоксикислота, алкилкарбонил, арилкарбонил, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил, алкоксил, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметил, циано, азидо, гетероциклический алкиларил или арил или гетероарил.
"Тиокарбонил" или "тиокарбокси" включает соединения и фрагменты, которые содержат атом углерода, соединенный двойной связью с атомом серы.
"Тиоэфир" включает фрагменты, которые содержат атом серы, связанный с двумя углеродными атомами или гетероатомами. Примеры тиоэфиров включают, но этим не ограничивая, алктиоалкилы, алктиоалкенилы и алктиоалкинилы. Термин "алктиоалкилы" включает фрагменты с алкильной, алкенильной или алкинильной группой, связанные с атомом серы, который связан с алкильной группой. Аналогично, термин "алктиоалкенилы" относится к фрагментам, в которых алкильная, алкенильная или алкинильная группа связана с атомом серы, который ковалентно связан с алкенильной группой; и "алктиоалкинилы" относятся к фрагментам, в которых алкильная, алкенильная или алкинильная группа связана с атомом серы, который ковалентно связан с алкинильной группой.
"Арилтио" (или "тиоарил") обозначает определенную в описании изобретения арильную группу с указанным числом углеродных атомов, присоединенную через атом серы.
Используемый в описании изобретения термин "карбоновая кислота" относится к соединению, включающему группу формулы -CO2H.
"Дикарбоновая кислота" относится к соединению, включающему две группы формулы -CO2H.
"Гало, галогенид и галоген": Используемые в описании изобретения термины "гало, галогенид и галоген" относятся к атому, выбранному из фтора, хлора, брома и йода.
"Метилол": Используемый в описании изобретения термин "метилол" относится к спиртовой группе структуры -CH2OH.
"Гидроксиалкил": Используемый в описании изобретения термин "гидроксиалкил" относится к определенной выше алкильной группе, несущей, по меньшей мере, одну OH группу.
"Меркаптоалкил": Используемый в описании изобретения термин "меркаптоалкил" относится к определенной выше алкильной группе, несущей, по меньшей мере, одну SH группу.
"Ацил" включает фрагменты, которые содержат ацильный радикал (-C(O)-) или карбонильную группу. "Замещенный ацил" включает ацильные группы, в которых один или более атомов водорода заменены, например, алкильными группами, алкинильными группами, галогеном, гидроксилом, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилатом, алкилкарбонилом, арилкарбонилом, алкоксикарбонилом, аминокарбонилом, алкиламинокарбонилом, диалкиламинокарбонилом, алкилтиокарбонилом, алкоксилом, фосфатом, фосфонато, фосфинато, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрилом, алкилтио, арилтио, тиокарбоксилатом, сульфатами, алкилсульфинилом, сульфонато, сульфамоилом, сульфонамидо, нитро, трифторметилом, циано, азидо, гетероциклилом, алкиларилом или арильным или гетероарильным фрагментом.
"Углеводород": Используемый в описании изобретения термин "углеводород" относится к любой химической группе, включающей водород и углерод. Углеводород может быть замещенным или незамещенным. Углеводород может быть ненасыщенным, насыщенным, разветвленным, неразветвленным, циклическим, полициклическим или гетероциклическим. Иллюстративные примеры углеводородов включают, например, метил, этил, н-пропил, изопропил, циклопропил, аллил, винил, н-бутил, третбутил, этинил, циклогексил, метокси, диэтиламино, гетероциклоалкил, арил, гетероарил, тиоалкил и другие подобные углеводороды. Любому специалисту в этой области известно, что при осуществлении любых замещений должны соблюдаться все требования к валентностям.
Используемый в описании изобретения термин "алкиларил" относится к арильной группе, замещенной одной или более алкильными группами (например, метилфенил).
Используемый в описании изобретения термин "алкилариламино" относится к -NRG4RG5, где RG4 представляет собой определенный в описании изобретения алкил, и RG5 представляет собой определенный в описании изобретения арил, или, по меньшей мере, один из RG4 и RG5 представляет собой определенный в описании изобретения алкиларил.
"Замещенный": Используемые в описании изобретения термины "замещенный", независимо от того, предшествует ему термин "необязательно" или нет, и "заместитель" относятся к замене водородных радикалов в данной структуре на радикал конкретного заместителя. В случае, когда более чем одно положение в данной структуре может быть замещено более чем одним заместителем, выбранным из указанной группы, в каждом положении заместитель может быть либо одинаковым, либо различным. Предполагается, что используемый в описании изобретения термин "замещенный" включает все допустимые заместители органических соединений. В широком аспекте, допустимые заместители включают ациклические и циклические, разветвленные и неразветвленные, карбоциклические и гетероциклические, ароматические и неароматические заместители органических соединений. Гетероатомы, такие как азот, могут иметь водородные заместители и/или любые допустимые описанные в изобретении заместители органических соединений, которые удовлетворяют требованиям валентностей гетероатомов. Примеры заместителей включают, но этим не ограничивая, алифатический, гетероалифатический, циклоалкильный, гетероциклоалкильный, арильный, гетероарильный, алкиларильный, алкилгетероарильный, алкокси, арилокси, гетероалкокси, гетероарилокси, алкилтио, арилтио, гетероалкилтио, гетероарилтио, F, Cl, Br, I, -NO2, -CN; -CF3, -CH2CF3, -CHCl2, -CH2OH, -CH2CH2OH, -CH2NH2, -CH2SO2CH3, или -GRG1, где G представляет собой -O-, -S-, -NRG2-, -C(=O)-, -S(=O)-, -SO2-, -C(=O)O-, -C(=O)NRG2-, -OC(=O)-, -NRG2C(=O)-, -OC(=O)O-, -OC(=O)NRG2-, -NRG2C(=O)O-, -NRG2C(=O)NRG2-, -C(=S)-, -C(=S)S-, -SC(=S)-, -SC(=S)S-, -C(=NRG2)-, -C(=NRG2)O-, -C(=NRG2)NRG3-, -OC(=NRG2)-, -NRG2C(=NRG3)-, -NRG2SO2-, -NRG2SO2NRG3- или -SO2NRG2-, где в каждом случае присутствия, RG1, RG2 и RG3 независимо включает, но этим не ограничивая, водород, галоген, или необязательно замещенный алифатический, гетероалифатический, циклоалкильный, гетероциклоалкильный, арильный, гетероарильный, алкиларильный или алкилгетероарильный фрагмент. Дополнительные примеры обычно применяемых заместителей иллюстрируются конкретными вариантами осуществления, приводимыми в описанных в изобретении примерах.
Следующие термины, применяемые в изобретении, являются более общими:
"Животное": Используемый в изобретении термин "животное" относится к людям, а также к не относящимся к человеку животным, на любой стадии развития, включающим, например, млекопитающих, птиц, пресмыкающихся, земноводных, рыб, червеобразных и одноклеточных. Клеточные культуры и образцы живых тканей считают материалом, представляющим множества животных. Предпочтительно, чтобы не относящееся к человеку животное представляло собой млекопитающее (например, грызуна, мышь, крысу, кролика, обезьяну, собаку, кошку, примата или свинью). Животным может быть трансгенное животное или человекоподобное существо. Термин "субъект" включает в себя животных.
"Эффективное количество": Вообще, применительно к активному веществу или устройству доставки лекарственного средства, термин "эффективное количество" обозначает количество, необходимое для достижения требуемой ответной биологической реакции. Для специалистов в этой области является очевидным, что эффективное количество средства или устройства может зависеть от таких факторов, как требуемый ожидаемый биологический результат, доставляемое средство, композиция инкапсулирующей матрицы, ткань-мишень и другие факторы. Например, эффективное количество содержащих антиген микрочастиц, вводимых для иммунизации пациента, представляет собой количество, которое приводит в результате к иммунной реакции, достаточной для предотвращения инфицирования организмом, имеющим вводимый антиген.
Используемый в изобретении термин "природная аминокислота" относится к любой одной из обычных природных L-аминокислот, обнаруживаемых в природных белках: глицину (Gly), аланину (Ala), валину (Val), лейцину (Leu), изолейцину (He), лизину (Lys), аргинину (Arg), гистидину (His), пролину (Pro), серину (Ser), треонину (Thr), фенилаланину (Phe), тирозину (Tyr), триптофану (Trp), аспарагиновой кислоте (Asp), глутаминовой кислоте (Glu), аспарагину (Asn), глутамину (Gin), цистеину (Cys) и метионину (Met).
Используемый в изобретении термин "неприродная аминокислота" относится к любой аминокислоте, которая не является природной аминокислотой. Он включает, например, аминокислоты, которые содержат α-, β-, ω-, D-, L-аминоацильные остатки. В более широком смысле, неприродная аминокислота включает остаток общей формулы

"Аминоацил": В более широком смысле, используемый в изобретении термин "аминоацил" включает в себя природные аминокислоты и неприродные аминокислоты.
"Полиамид": относится к гомо- или гетерополимерам природных аминокислот и неприродных аминокислот. Иллюстративные примеры гомополимеров включают, но этим не ограничивая, полилизин, полиаргинин, поли-г-глутаровую кислоту и другие подобные гомополимеры. Иллюстративные примеры гетерополимеров включают, но этим не ограничивая, полимеры, содержащие пептидные фрагменты, выбранные из пептидаз, лизоцимов, металлопротеиназ и других подобных пептидных фрагментов.
"PHF" относится к поли(1-гидроксиметилэтиленгидроксиметил-формалю).
Используемый в описании изобретения термины "полимерное звено", "мономерное звено", "мономер", "звено мономера", "звено", все относятся к повторяющимся структурным звеньям в полимере.
Предполагается, что настоящее изобретение включает все изотопы атомов, входящих в настоящие соединения. Изотопы включают атомы, имеющие одинаковый атомный номер, но различные массовые числа. Общие примеры, без ограничения, изотопов водорода включают тритий и дейтерий. Изотопы углерода включают C-13 и C-14.
Предполагается, что настоящее изобретение включает все изомеры соединения, которые относятся и включают оптические изомеры и таутомерные изомеры, где оптические изомеры включают энантиомеры и диастереомеры, хиральные изомеры и нехиральные изомеры, и оптические изомеры включают выделенные индивидуальные оптические изомеры, так же как и смеси оптических изомеров, включающие рацемические и нерацемические смеси, где изомер может находиться в выделенной форме или в смеси с одним или более другими изомерами.
Полимерные носители
В примерах конкретных вариантов осуществления, конъюгаты изобретения находят применение в биомедицинской области, такой как доставка лекарственного средства и тканевая инженерия, и носитель является биологически совместимым и биоразлагаемым. В конкретных вариантах осуществления, носитель представляет собой растворимый полимер, наночастицу, гель, липосому, мицеллу, шовный материал, имплантат и другие. В конкретных вариантах осуществления, термин "растворимый полимер" охватывает биоразлагаемый биологически совместимый полимер, такой как полиал (например, гидрофильный полиацеталь или поликеталь). В других конкретных вариантах осуществления, носитель представляет собой полностью синтетический, полусинтетический или природный полимер. В других конкретных вариантах осуществления, носитель является гидрофильным.
В конкретных примерах вариантов осуществления, применяемые в настоящем изобретении носители представляют собой биоразлагаемые биологически совместимые полиалы, включающие, по меньшей мере, одну гидролизуемую связь в каждом мономерном звене, расположенном внутри главной цепи. Это гарантирует, что процесс разложения (в результате гидролиза/расщепления мономерных звеньев) будет в результате приводить к фрагментации полимерного конъюгата на мономерные компоненты (то есть, к разложению), и придает полимерным конъюгатам изобретения свойства биоразлагаемости. Свойства (например, растворимость, биоадгезивность и гидрофильность) биоразлагаемых биологически совместимых полимерных конъюгатов могут быть модифицированы путем последующего замещения дополнительных гидрофильных или гидрофобных групп. Примеры биоразлагаемых биологически совместимых полимеров, подходящих для осуществления изобретения, можно найти, в частности, в патентных документах U.S. Patent Nos. 5811510, 5863990, 5958398, 7838619 и 7790150 и U.S. Publication No. 2006/0058512, содержание которых приводится в описании изобретения путем ссылки на них. Указание по значимости, получению и применению этого типа полимеров можно найти в перечисленных выше документах. В конкретных вариантах осуществления, предполагается, что настоящее изобретение будет особенно полезным в комбинации с упомянутыми выше патентными документами, а также с патентными документами U.S. Patent Nos. 5582172 и 6822086, содержание каждого из которых приводится в описании изобретения путем ссылки на него.
Конъюгаты этого изобретения являются гидрофильными, гидролизуемыми и включают молекулы лекарственных средств (например, алкалоиды барвинка или производные, неприродные соединения камптотецина или производные, ауристатины, тубулизины, дуокармицины, PI3 киназы, ингибиторы MEK, ингибиторы KSP и их аналоги) и антитела (например, трастузумаб, цетуксимаб, ритуксимаб, бевацизумаб, эпратузумаб, велтузумаб, лабетузумаб) или пептиды (пептиды, таргетированные на рецептор лютеинизирующего релизинг-гормонаа (LHRH), EC-1 пептид), ковалентно связанные с полимерным носителем с помощью связей, которые содержат одну или более биоразлагаемых химических связей. Так, в конкретных примерах вариантов осуществления, носители, подходящие для осуществления настоящего изобретения, представляют собой полиали, имеющие, по меньшей мере, один ацетальный/кетальный атом кислорода в каждом мономерном звене, расположенном внутри главной цепи. Как уже обсуждалось выше, это гарантирует, что процесс разложения (в результате гидролиза/расщепления ацетальных/кетальных групп полимера) будет в результате приводить к фрагментации полимерного конъюгата на низкомолекулярные компоненты (то есть, к разложению).
В конкретных вариантах осуществления, биоразлагаемые биологически совместимые полимерные носители, используемые для получения полимерных конъюгатов изобретения, представляют собой природные полисахариды, гликополисахариды и синтетические полимеры полигликозида, полиацеталя, полиамида, полиэфира и полимеры полиэфирного происхождения и продукты их окисления, функционализации, модификации, сшивания и конъюгирования.
В других конкретных вариантах осуществления, носитель представляет собой гидрофильный биоразлагаемый полимер, выбранный из группы, состоящей из углеводов, гликополисахаридов, гликолипидов, гликоконъюгатов, полиацеталей, поликеталей и их производных.
В конкретных примерах вариантов осуществления, носитель представляет собой природный линейный и/или разветвленный биоразлагаемый биологически совместимый гомополисахарид, выбранный из группы, состоящей из целлюлозы, амилозы, декстрана, левана, фукоидана, каррагинана, инулина, пектина, амилопектина, гликогена и ликсинана.
В других конкретных примерах вариантов осуществления, носитель представляет собой природный линейный и разветвленный биоразлагаемый биологически совместимый гетерополисахарид, выбранный из группы, состоящей из агарозы, гиалуронана, хондроитинсульфата, дерматансульфата, кератансульфата, альгиновой кислоты и гепарина.
В еще одних примерах вариантов осуществления, полимерный носитель включает сополимер полиацеталя/поликеталя и гидрофильный полимер, выбранный из группы, состоящей из полиакрилатов, поливиниловых полимеров, полиэфиров, полиортоэфиров, полиамидов, полипептидов и их производных.
В еще одном варианте осуществления, полимерный носитель представляет собой декстрин, который получают гидролизом крахмала, приготовленного из различных природных продуктов, таких как, например, пшеница, рис, кукуруза и маниока. В зависимости от структуры исходного крахмалсодержащего материала, декстрин включает специфическое распределение α-1,4 связей и α-1,6 связей. Так как скорость биоразложения α-1,6 связей обычно меньше, чем скорость разложения α-1,4 связей, предпочтительно, чтобы доля α-1,6 связей была бы меньше, чем 10%, и более предпочтительно, меньше, чем 5%. В одном варианте осуществления, молекулярная масса декстрина составляет от приблизительно 1 кДа до приблизительно 200 кДа, более предпочтительно, от приблизительно 2 кДа до приблизительно 55 кДа.
В конкретных вариантах осуществления, носитель включает полисахариды, активированные перед конъюгированием с молекулами лекарственных средств или PBRM путем селективного окисления циклических вицинальных диолов 1,2-, 1,4-, 1,6- и 2,6- пиранозидов и 1,2-, 1,5-, 1,6-фуранозидов, или путем окисления полисахаридов, содержащих латеральный 6-гидрокси и 5,6-диол.
В некоторых других вариантах осуществления, полимерный носитель включает биоразлагаемый биологически совместимый полиацеталь, где, по меньшей мере, подмножество повторяющихся полиацетальных структурных звеньев имеет следующую химическую структуру:
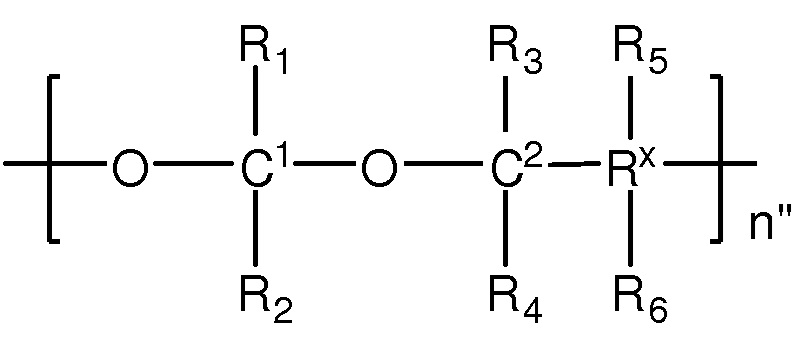
где, в каждом случае присутствия n заключенной в скобки структуры, один из R1 и R2 представляет собой водород, а другой представляет собой биологически совместимую группу и включает углеродный атом, ковалентно связанный с C1; Rx представляет собой углеродный атом, ковалентно связанный с C2; n" представляет собой целое число; в каждом случае присутствия, R3, R4, R5 и R6 представляют собой биологически совместимую группу и являются независимо водородом или органическим фрагментом; и в каждом случае присутствия n заключенной в скобки структуры, по меньшей мере, один из R1, R2, R3, R4, R5 и R6 включает функциональную группу, подходящую для связывания. В конкретных вариантах осуществления, функциональная группа представляет собой гидроксильный фрагмент.
В одном варианте осуществления, полимерный носитель включает активированные гидрофильные биоразлагаемые биологически совместимые полимеры, содержащие от 0,1% до 100% полиацетальных фрагментов, главная цепь которых представлена следующей химической структурой:
(-CH2-CHR7-O-CHR8-O-)o
где:
R7 и R8 представляют собой независимо водород, гидроксил, гидроксиалкил (например, -CH2OH, -CH(OH)-CH2OH), -CHO, -CH(OH)-CHO или -карбонил; и
o представляет собой целое число от 20 до 2000.
В еще одних вариантах осуществления, полимерный носитель включает биоразлагаемый биологически совместимый поликеталь, где, по меньшей мере, подмножество повторяющихся поликетальных структурных звеньев имеет следующую химическую структуру:
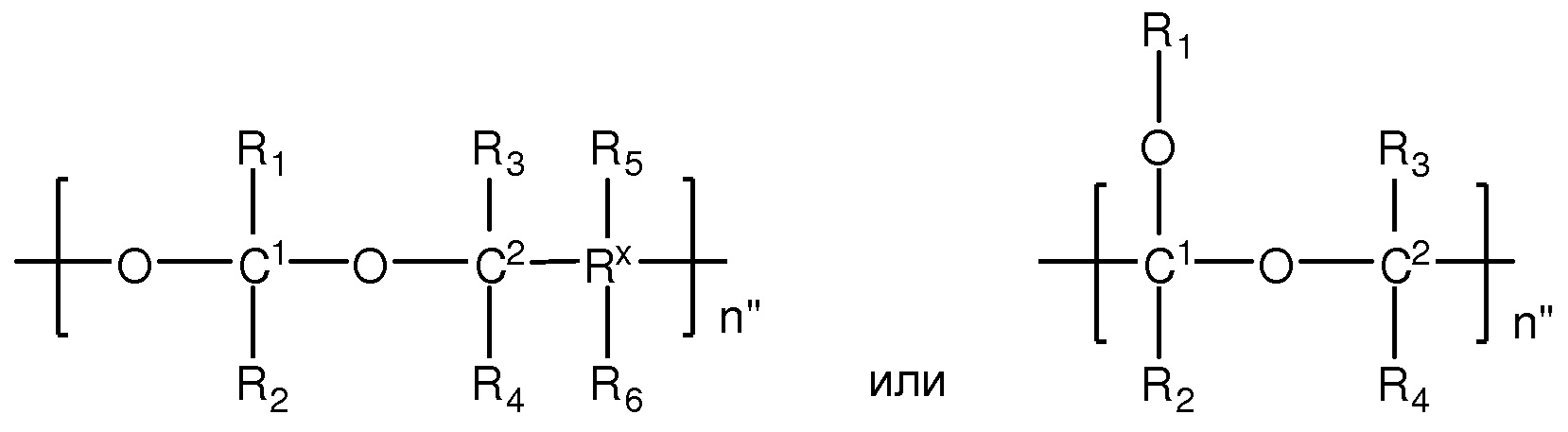
где в каждом случае присутствия, R1 и R2 представляет собой биологически совместимую группу, и Rx, R3, R4, R5, R6 и n" определены в описании изобретения.
В конкретных вариантах осуществления, кетальные звенья представляют собой мономеры формулы (IIa) или (IIb):

Биоразлагаемые биологически совместимые поликетальные полимеры и способы их получения описаны в патентных документах US Patent №№ 5811510, 7790150 и 7838619, содержание которых приводится в описании изобретения путем ссылки на них.
В одном варианте осуществления, полимерный носитель может быть получен из частично окисленного декстрана (β1→6)-D-глюкозы) с последующим восстановлением. В этом варианте осуществления, полимер включает образующуюся случайным образом смесь немодифицированного декстрана (A), звеньев ацетали частично окисленного декстрана (B) и звеньев ацетали полностью окисленного декстрана (C) следующих структур:

В другом варианте осуществления, полимерный носитель включает немодифицированные ацетальные звенья, то есть, полиацетальные сегменты. В некоторых вариантах осуществления, полиацетали могут быть получены из полностью окисленного декстрана с последующим восстановлением. Эти полимеры описаны в патенте США № 5811510, содержание которого приводится в описании изобретения путем ссылки на него, описание полиацеталей приводится от колонки 2, строка 65 до колонки 8, строка 55 и их синтез от колонки 10, строка 45 до колонки 11, строка 14. В одном варианте осуществления, немодифицированный полиацетальный полимер представляет собой полимер поли(гидроксиметилэтилен гидроксиметилформаль) (PHF).
Помимо полимеров поли(гидроксиметилэтиленгидроксиметил- формаля), главная цепь полимерного носителя может также включать сополимеры блоков поли(гидроксиметилэтиленгидроксиметилформаля) и других ацетальных или неацетальных мономеров или полимеров. Например, полимеры полиэтиленгликоля применяют в основной цепи полимера в качестве реагента скрытого действия (stealth agent), так как они могут уменьшать взаимодействия между боковыми цепями присоединенных функциональных групп полимера. Такие группы могут также применяться для ограничения взаимодействий, например, между сывороточными факторами и модифицированным полимером. Другие мономеры скрытого действия для введения в главную цепь полимера включают, например, этиленимин, метакриловую кислоту, акриламид, глутаминовую кислоту и их комбинации.
Ацетальные или кетальные звенья присутствуют в модифицированном полимере в количестве, эффективном для повышения биологической совместимости. Немодифицированное ацетальное или кетальное звено может быть описано как "реагент скрытого действия", который обеспечивает модифицированным полимерам биологическую совместимость и растворимость. Кроме того, конъюгирование с полиацетальным или поликетальным полимером может повышать предрасположенность к метаболизму и разложению присоединенных к нему фрагментов и влиять на биораспределение, выведение и разложение.
Немодифицированные ацетальные звенья представляют собой мономеры формулы (III):

Мольная доля n немодифицированных полиацетальных звеньев представляет собой мольную долю, способную повышать биологическую совместимость, растворимость и увеличивать период полувыведения, от суммарного числа полимерных звеньев в модифицированном полимере. Мольная доля n может представлять собой минимальную долю немодифицированных мономерных ацетальных звеньев, необходимых для обеспечения биологической совместимости, растворимости, стабильности или конкретного периода полувыведения, или может представлять собой некую большую долю. Наиболее желательная степень токсичности - это ее практическое отсутствие, то есть, модифицированный полимер должен быть практически инертным по отношению к субъекту. Однако для обычных специалистов в этой области является очевидным, что некоторая степень токсичности может быть допустима в зависимости от тяжести подвергаемого лечению заболевания или симптома, эффективности лечения, типа и степени ответной иммунной реакции и других подобных соображений.
В одном варианте осуществления, главная цепь модифицированного полимера включает звенья формулы (IV):

где X' обозначает заместитель для гидроксильной группы главной цепи полимера. Как показано в формуле (IV) и других описанных в изобретении формулах, каждое полиацетальное звено имеет единственную гидроксильную группу, присоединенную к глицериновому фрагменту звена, и X' группу (или другой заместитель, такой как -LD-D), присоединенную к гликольальдегидному фрагменту звена. Но это только для удобства, и следует считать, что полимер, имеющий звенья формулы (IV) и других описанных в изобретении формул, может содержать случайное распределение звеньев, имеющих X' группу (или другой заместитель, такой как -LD-D), присоединенную к гликольальдегидному фрагменту звеньев, и звеньев, имеющих единственную X' группу (или другой заместитель, такой как -LD-D), присоединенную к глицериновому фрагменту звеньев, также как звеньев, имеющих две X' группы (или другие заместители, такие как -LD-D), одна из которых присоединена к гликольальдегидному фрагменту, а другая присоединена к глицериновому фрагменту звеньев.
В одном варианте осуществления, биоразлагаемые биологически совместимые полиали, подходящие для осуществления настоящего изобретения, имеют молекулярную массу от приблизительно 0,5 до приблизительно 300 кДа. В предпочтительном варианте осуществления настоящего изобретения, биоразлагаемые биологически совместимые полиали имеют молекулярную массу от приблизительно 1 до приблизительно 300 кДа (например, от приблизительно 1 до приблизительно 200 кДа, от приблизительно 2 до приблизительно 300 кДа, от приблизительно 2 до приблизительно 200 кДа, от приблизительно 5 до приблизительно 100 кДа, от приблизительно 10 до приблизительно 70 кДа, от приблизительно 20 до приблизительно 50 кДа, от приблизительно 20 до приблизительно 300 кДа, от приблизительно 40 до приблизительно 150 кДа, от приблизительно 50 до приблизительно 100 кДа, от приблизительно 2 до приблизительно 40 кДа, от приблизительно 6 до приблизительно 20 кДа или от приблизительно 8 до приблизительно 15 кДа).
В одном варианте осуществления, биоразлагаемые биологически совместимые полиали, подходящие для осуществления настоящего изобретения, подвергают модификации перед конъюгированием с лекарственным средством или PBRM. Например, полиали могут содержать субзвенья связующих звеньев LD или Lp, такие как -C(=O)-X-(CH2)v-C(=O)-, где X представляет собой CH2, O или NH, и v представляет собой целое число от 1 до 6. В таблице A ниже приводятся некоторые примеры модифицированных полиалей, подходящих для конъюгирования с лекарственным средством или PBRM или их производными. Если не указано иначе, то номера ссылок в таблицах A - E ниже соответствуют номерам примеров, описанных в изобретении; термин "ND" означает "не определяли"; и X представляет собой CH2, O или NH.

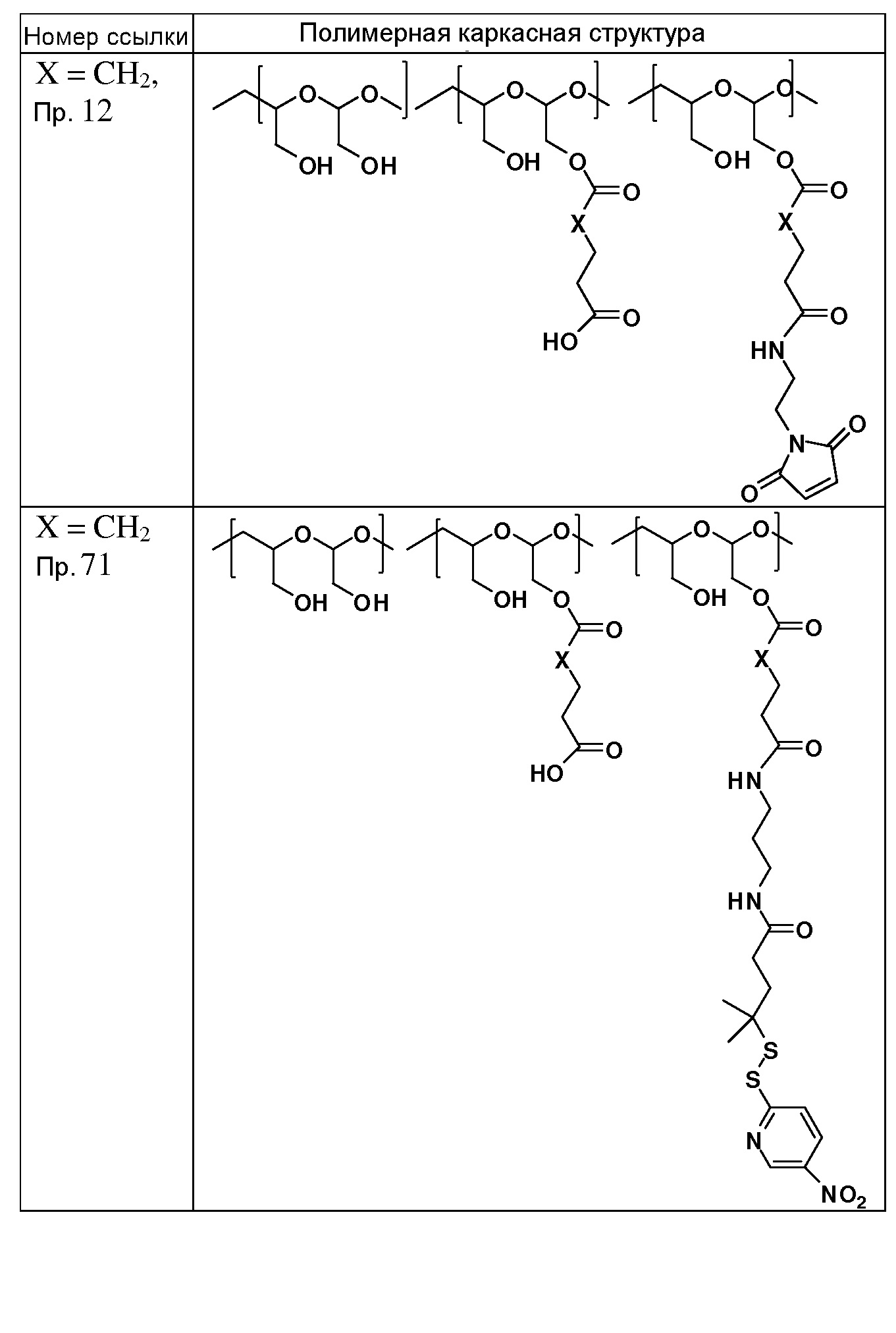



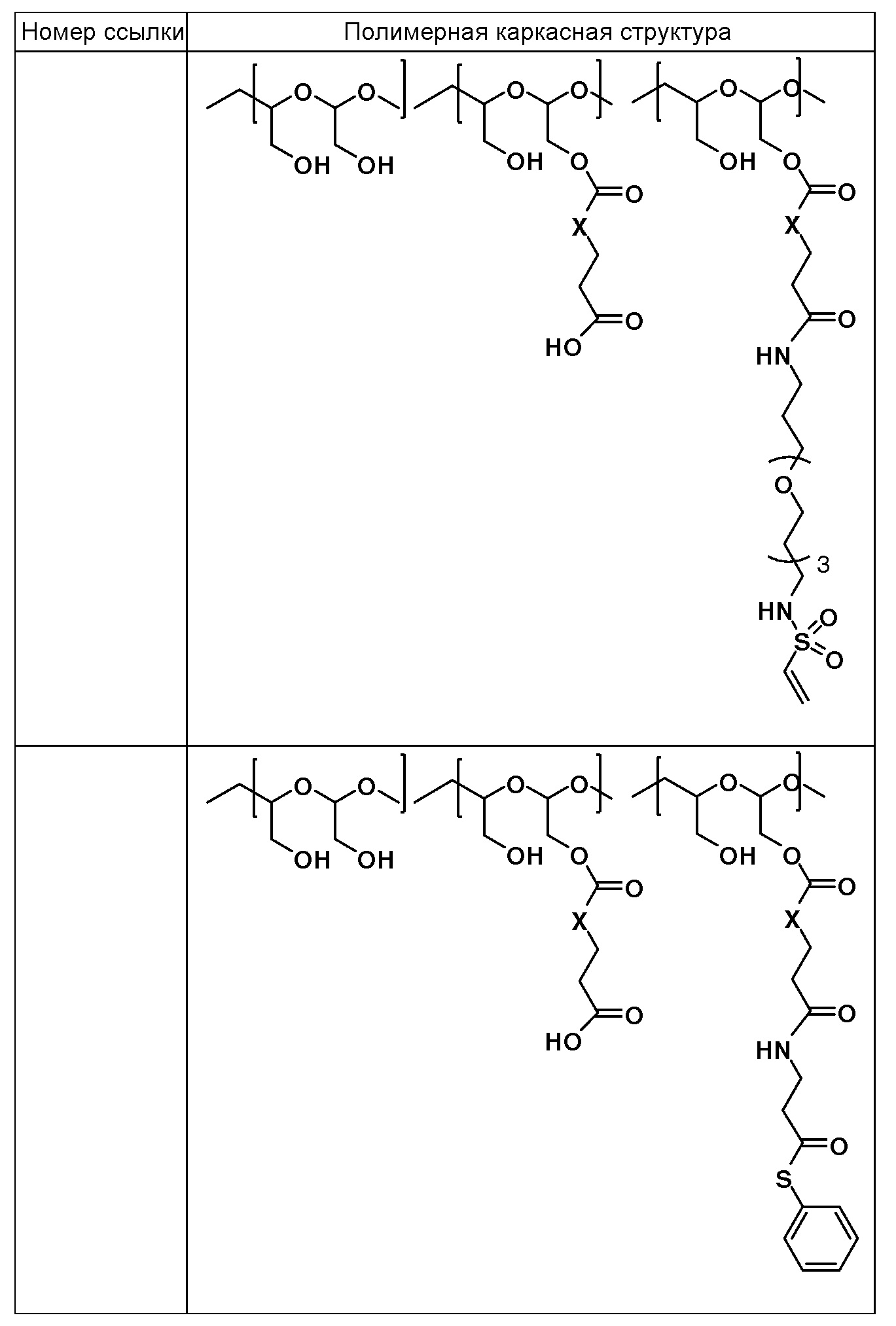
Терапевтические средства
В конкретных вариантах осуществления, терапевтическое средство представляет собой малую молекулу, имеющую молекулярную массу, предпочтительно, ≤ приблизительно 5 кДа, более предпочтительно, ≤ приблизительно 4 кДа, более предпочтительно, ≤ приблизительно 3 кДа, наиболее предпочтительно, ≤ приблизительно 1,5 кДа или ≤ приблизительно 1 кДа.
В конкретных вариантах осуществления, от приблизительно 0,1 до приблизительно 25% мономеров включают терапевтическое средство, более предпочтительно, от приблизительно 0,5 до приблизительно 20%, более предпочтительно, от приблизительно 1 до приблизительно 15%, и еще более предпочтительно, от приблизительно 2 до приблизительно 10%.
Терапевтические средства в виде малой молекулы, используемые в этом изобретении (например, антипролиферативные (цитотоксические и цитостатические) средства, способные образовывать связь с полимерным носителем), включают цитотоксические соединения (например, широкий спектр), ингибиторы ангиогенеза, ингибиторы клеточного цикла, ингибиторы пути PBK/m-TOR/AKT, ингибиторы сигнального пути MAPK, ингибиторы киназы, ингибиторы белков теплового шока, ингибиторы HDAC, ингибиторы PARP, ингибиторы сигнального пути Wnt/Hedgehog и ингибиторы РНК-полимеразы.
Широкий спектр цитоксинов включает, но этим не ограничивая, ДНК-связывающие или алкилирующие лекарственные средства, средства, стабилизирующие или дестабилизирующие микротрубочки, соединения платины и ингибиторы топоизомеразы I.
Примеры ДНК-связывающих или алкилирующих лекарственных средств включают CC-1065 и его аналоги, антрациклины (доксорубицин, эпирубицин, идарубицин, даунорубицин) и их аналоги, алкилирующие средства, такие как калихимицины, дактиномицины, митромицины, пирролобензодиазепины и другие подобные средства.
Примеры аналогов CC-1065 включают дуокармицин SA, дуокармицин C1, дуокармицин C2, дуокармицин B2, DU-86, KW-2189, бизелезин, секо-адолезин и лекарственные средства, описанные в патентах США № 5475092, 5595499, 5846545, 6534660, 6586618, 6756397 и 7049316. Доксорубицин и его аналоги включают лекарственные средства, описанные в патенте США № 6630579. Калихимицины включают лекарственные средства, описанные в патентах США № 5714586 и 5739116. Дуокармицины включают лекарственные средства, описанные в патентах США № 5070092, 5101038, 5187186, 6548530, 6660742 и 7553816 B2; и в публикации Li et al., Tet Letts., 50:2932-2935 (2009). Пирролобензодиазепины включают лекарственные средства, описанные в публикации Denny, Exp. Opin. Ther. Patents., 10(4):459-474 (2000).
Примеры средств, стабилизирующих или дестабилизирующих микротрубочки, включают соединения таксанов, такие как паклитаксел, доцетаксел; майтанзиноиды, ауристатины и их аналоги, производные тубулизина A и B, производные алкалоида барвинка, эпотилоны и криптофицины.
Примеры майтанзиноидов или аналогов майтанзиноидов включают майтанзинол и аналоги майтанзинола, майтанзин или DM-1 и DM-4, которые описаны в патентах США № 5208020, 5416064, 6333410, 6441163, 6716821, RE39151 и 7276497. В конкретных вариантах осуществления, цитотоксическое средство представляет собой майтанзиноид, другую группу антитубулиновых средств (ImmunoGen, Inc.; смотрите также Chari et al., 1992, Cancer Res. 52: 127-131), майтанзиноиды или аналоги майтанзиноидов. Примеры подходящих майтанзиноидов включают майтанзинол и аналоги майтанзинола. Подходящие майтанзиноиды раскрыты в патентах США № 4424219, 4256746, 4294757, 4307016, 4313946, 4315929, 4331598, 4361650, 4362663, 4364866, 4450254, 4322348, 4371533, 6333410, 5475092, 5585499 и 5846545.
Примеры ауристатинов включают ауристатин E (также известный как производное доластатин-10), ауристатин EB (AEB), ауристатин EFP (AEFP), монометилауристатин E (MMAE), монометилауристатин F (MMAF), ауристатин F и доластатин. Подходящие ауристатины также описаны в патентных документах U.S. Publication Nos. 2003/0083263, 2011/0020343, и 2011/0070248; PCT Application Publication Nos. WO 09/117531, WO 2005/081711, WO 04/010957; WO 02/088172 и WO 01/24763, и патентах США № 7498298, 6884869, 6323315, 6239104, 6124431, 6034065, 5780588, 5767237, 5665860, 5663149, 5635483, 5599902, 5554725, 5530097, 5521284, 5504191, 5410024, 5138036, 5076973, 4986988, 4978744, 4879278, 4816444 и 4486414, содержание которых приводится в описании изобретения путем ссылки на них.
Примеры соединений тубулизина включают соединения, описанные в патентах США № 7816377, 7776814, 7754885, патентных документах U.S. Publication Nos. 2011/0021568, 2010/004784, 2010/0048490, 2010/00240701, 2008/0176958 и PCT Application Nos. WO 98/13375, WO 2004/005269, WO 2008/138561, WO 2009/002993, WO 2009/055562, WO 2009/012958, WO 2009/026177, WO 2009/134279, WO 2010/033733, WO 2010/034724, WO 2011/017249, WO 2011/057805, содержание которых приводится в описании изобретения путем ссылки на них.
Примеры алкалоидов барвинка включают винкристин, винбластин, виндезин и навельбин (винорелбин). Подходящие алкалоиды барвинка, которые могут быть использованы в настоящем изобретении, также раскрыты в патентных документах U.S. Publication Nos. 2002/0103136 и 2010/0305149, и в патенте США № 7303749 B1, содержание которых приводится в описании изобретения путем ссылки на них.
Примеры соединений эпотилона включают эпотилон A, B, C, D, E и F и их производные. Подходящие соединения эпотилона и их производные описаны, например, в патентах США № 6956036, 6989450, 6121029, 6117659, 6096757, 6043372, 5969145 и 5886026, и в патентных документах WO 97/19086, WO 98/08849, WO 98/22461, WO 98/25929, WO 98/38192, WO 99/01124, WO 99/02514, WO 99/03848, WO 99/07692, WO 99/27890 и WO 99/28324, содержание которых приводится в описании изобретения путем ссылки на них.
Примеры соединений криптофицина описаны в патентах США № 6680311 и 6747021.
Примеры соединений платины включают цисплатин (PLATINOL®), карбоплатин (PARAPLATIN®), оксалирлатин (ELOXATINE®), ипроплатин, ормаплатин и тетраплатин.
Примеры ингибиторов топоизомеразы I включают камптотецин, производные камптотецина, аналоги камптотецина и неприродные камптотецины, такие как, например, CPT-11 (иринотекан), SN-38, топотекан, 9-аминокамптотецин, рубитекан, гиматекан, каренитецин, силатекан, луртотекан, экзатекан, дифломотекан, белотекан, луртотекан и S39625. Другие соединения камптотецина, которые могут быть использованы в настоящем изобретении, включают соединения, описанные, например, в публикациях J. Med. Chem., 29:2358-2363 (1986); J. Med. Chem., 23:554 (1980); J. Med. Chem., 30:1774 (1987).
Ингибиторы ангиогенеза включают, но этим не ограничивая, ингибиторы MetAP2. Примеры ингибиторов MetAP2 включают аналоги фумагиллола, обозначающие любое соединение, которое содержит ядро со структурой фумагиллина, включая фумагилламин, которые ингибируют способность MetAP-2 удалять NH2-терминальные метионины из белков, как описано в публикациях Rodeschini et al., J. Org. Chem., 69, 357-373, 2004 и Liu, et al., Science 282, 1324-1327, 1998. Неограничивающие примеры "аналогов фумагиллола" раскрыты в публикациях J. Org. Chem., 69, 357, 2004; J.Org. Chem., 70, 6870, 2005; European Patent Application 0 354 787; J. Med. Chem., 49, 5645, 2006; Bioorg. Med. Chem., 11, 5051, 2003; Bioorg. Med. Chem., 14, 91, 2004; Tet. Lett. 40, 4797, 1999; WO 99/61432; патентах США № 6603812, 5789405, 5767293, 6566541 и 6207704.
Примеры ингибиторов клеточного цикла включают ингибиторы CDK, такие как, например, BMS-387032 и PD0332991; ингибиторы Rho-киназ, такие как, например GSK429286; ингибиторы checkpoint киназ, такие как, например, AZD7762; ингибиторы Aurora-киназ, такие как, например, AZD1152, MLN8054 и MLN8237; ингибиторы PLK, такие как, например, BI 2536, BI6727 (воласертиб), GSK461364, ON-01910 (эстибон); и ингибиторы KSP, такие как, например, SB 743921, SB 715992 (испинезиб), MK-0731, AZD8477, AZ3146 и ARRY-520.
Примеры ингибиторов сигнального пути PI3K/m-TOR/AKT включают ингибиторы фосфоинозитид-3-киназы (PI3K), ингибиторы GSK-3, ингибиторы ATM, ингибиторы ДНК-ПК и ингибиторы PDK-1.
Примеры PI3 киназ раскрыты в патенте США № 6608053 и включают BEZ235, BGT226, BKM120, CAL101, CAL263, деметоксивиридин, GDC-0941, GSK615, IC87114, LY294002, паломид 529, перифозин, PF-04691502, PX-866, SAR245408, SAR245409, SF1126, вортманнин, XL147 и XL765.
Примеры ингибиторов AKT включают, но этим не ограничивая, AT7867.
Примеры ингибиторов сигнального пути MAPK включают ингибиторы MEK, Ras, JNK, B-Raf и p38 MAPK.
Примеры ингибиторов MEK раскрыты в патенте США № 7517994 и включают GDC-0973, GSK1120212, MSC1936369B, AS703026, R05126766 и R04987655, PD0325901, AZD6244, AZD 8330 и GDC-0973.
Примеры ингибиторов B-raf включают CDC-0879, PLX-4032 и SB590885.
Примеры ингибиторов B p38 MAPK включают BIRB 796, LY2228820 и SB202190.
Рецепторные тирозинкиназы (RTK) представляют собой рецепторы клеточной поверхности, которые часто связаны с сигнальными путями, стимулирующими неконтролируемую пролиферацию раковых клеток и неоангиогенез. Были идентифицированы многие RTK, которые сверхэкспрессируют или имеют мутации, приводящие к конститутивной активации рецептора, включающие, но этим не ограничивая, рецепторы VEGFR, EGFR, FGFR, PDGFR, EphR и семейство рецепторов RET. Примеры специфических мишеней RTK включают ErbB2, FLT-3, c-Kit, c-Met, HIF.
Примеры ингибиторов рецептора ErbB2 (семейства EGFR) включают, но этим не ограничивая, AEE788 (NVP-AEE 788), BIBW2992, (афатиниб), лапатиниб, эрлотиниб (тарцеву) и гефитиниб (ирессу).
Примеры ингибиторов RTK, действие которых направлено более чем на один сигнальный путь (политаргетные ингибиторы киназы), включают AP24534 (понатиниб), действие которого направлено на рецепторы FGFR, FLT-3, VEGFR-PDGFR и Bcr-Abl; ABT-869 (линифаниб), действие которого направлено на рецепторы FLT-3 и VEGFR-PDGFR; AZD2171, действие которого направлено на рецепторы VEGFR-PDGFR, Flt-1 и VEGF; CHR-258 (довитиниб), действие которого направлено на рецепторы VEGFR-PDGFR, FGFR, Flt-3 и c-Kit.
Примеры ингибиторов белков теплового шока включают ингибиторы HSP90. Примеры ингибиторов HSP90 включают производные 17AAG, BIIB021, BIIB028, SNX-5422, NVP-AUY-922 и KW-2478.
Примеры ингибиторов HDAC включают белиностат (PXD101), CUDC-101, дроксиностат, ITF2357 (гивиностат, гавиностат), JNJ-26481585, LAQ824 (NVP-LAQ824, дациностат), LBH-589 (панобиностат), MC1568, MGCD0103 (моцетиностат), MS-275 (энтиностат), PCI-24781, пироксамид (NSC 696085), SB939, трихостатин A и вориностат (SAHA).
Примеры ингибиторов PARP включают инипариб (BSI 201), олапариб (AZD-2281), ABT-888 (Veliparib), AG014699, CEP 9722, MK 4827, KU-0059436 (AZD2281), LT-673, 3-аминобензамид, A-966492 и AZD2461.
Примеры ингибиторов сигнального пути Wnt/Hedgehog включают висмодегиб (RG3616/GDC-0449), циклопамин (11-деоксоиервин) (ингибиторы пути Hedgehog) и XAV-939 (ингибитор пути Wnt)
Примеры ингибиторов РНК-полимеразы включают аматоксины. Примеры аматоксинов включают α-аманитины, β-аманитины, г-аманитины, е-аманитины, амануллин, амануллиновую кислоту, аманинамид, аманин и проамануллин.
В одном варианте осуществления, лекарственное средство изобретения представляет собой неприродное соединение камптотецина, алкалоид барвинка, ингибитор киназы (например, ингибитор PI3 киназы (GDC-0941 и PI-103)), ингибитор MEK, ингибитор KSP, ингибитор РНК-полимеразы, ингибитор PARP, доцетаксел, паклитаксел, доксорубицин, дуокармицин, тубулизин, ауристатин или соединение платины. В конкретных вариантах осуществления, лекарственное средство представляет собой производное SN-38, виндезин, винбластин, PI-103, AZD 8330, ауристатин E, ауристатин F, соединение дуокармицина, соединение тубулизина или ARRY-520.
В другом варианте осуществления, лекарственное средство, используемое в изобретении, представляет собой комбинацию двух или более лекарственных средств, таких как, например, PI3 киназы и ингибиторы MEK; широкий спектр цитотоксических соединений и соединения платины; ингибиторы PARP и соединения платины; широкий спектр цитотоксических соединений и ингибиторы PARP.
В одном варианте осуществления, алкалоид барвинка представляет собой соединение формулы (V):

где:
R14 представляет собой водород, -C(O)-C1-3 алкил или -C(O)-хлорзамещенный C1-3 алкил;
R15 представляет собой водород, -CH3 или -CHO;
когда R17 и R18 берут независимо, R18 представляет собой водород, и один из R16 или R17 представляет собой этил, а другой представляет собой гидроксил;
когда R17 и R18 берут вместе с углеродом, к которому они присоединены с образованием оксиранового кольца, R16 представляет собой этил;
R19 представляет собой водород, OH, аминогруппу, алкиламино или -[C(R20R21)]a-R22;
каждый из R20 и R21 независимо представляет собой водород, C1-6 алкил, C6-10 арил, гидроксилированный C6-10 арил, полигидроксилированный C6-10 арил, 5-12-членный гетероцикл, C3-8 циклоалкил, гидроксилированный C3-8 циклоалкил, полигидроксилированный C3-8 циклоалкил или боковую цепь природной или неприродной аминокислоты;
R22 представляет собой -OH, -NH2, -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f -N(H)(R23) или -R82-(C(O)-CH(X2)-NH)d-R77;
каждый R23 независимо представляет собой водород, C1-6алкил, C6-10 арил, C3-8 циклоалкил, -COOH или -COO-C1-6 алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащий гетероциклический фрагмент;
R82 представляет собой -NH или кислород;
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3; и
f представляет собой целое число от 1 до 12.
Дополнительные примеры алкалоидов барвинка описаны в патентных документах US 2010/0305149 и US 2002/0103136.
В одном варианте осуществления, алкалоид барвинка формулы (V) представляет собой соединение формулы (VI):

где:
R40 представляет собой водород, -OH, -NH2 или любую из следующих структур:



где:
a представляет собой целое число от 1 до 6; и
c представляет собой целое число от 0 до 3.
В одном варианте осуществления, R40 представляет собой

В другом варианте осуществления, неприродный камптотецин представляет собой соединение формулы (VII):
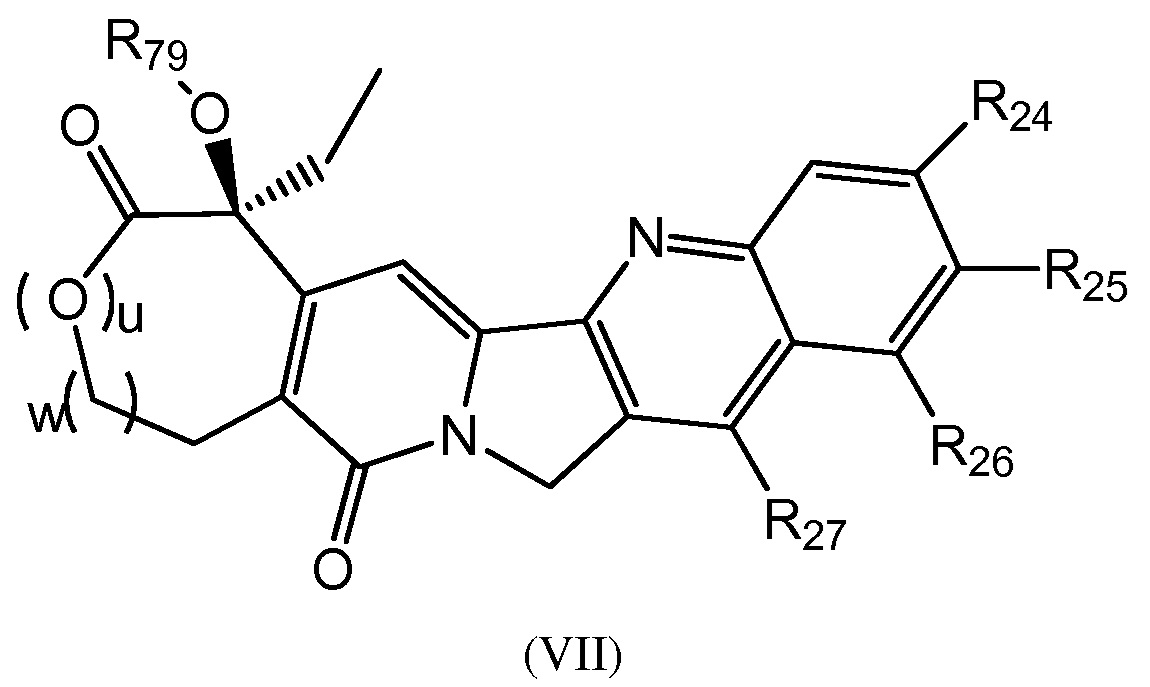
где:
R24 представляет собой -H, -Cl, -F, -OH или алкил; или R24 и R25 могут быть взяты вместе с образованием пяти- или шестичленного кольца;
R25 представляет собой -H, -F, -OH, -CH3, -CH=N-O-третбутил, -CH2CH2Si(CH3)3, -Si((CH3)2)-третбутил, -O-C(O)-R29;
R29 представляет собой -NH2, -R28-C1-6 алкил-R22, 5-12-членный гетероциклоалкил, R28-C5-12 гетероциклоалкил-C1-6 алкил-R22 или -R28-C1-6 алкил-C6-12 арил-C1-6 алкил-R22;
R26 представляет собой -H, -CH2-N(CH3)2, NH2 или NO2;
R27 представляет собой этил, N-метилпиперидин, циклоалкил, -CH2CH2NHCH(CH3)2 или -N-4-метилциклогексиламин;
R79 представляет собой -H или -C(O)-R28-[C(R20R21)]a-R22;
каждый из R20 и R21 независимо представляет собой водород, C1-6 алкил, C6-10 арил, гидроксилированный C6-10 арил, полигидроксилированный C6-10 арил, 5-12-членный гетероцикл, C3-8 циклоалкил, гидроксилированный C3-8 циклоалкил, полигидроксилированный C3-8 циклоалкил или боковую цепь природной или неприродной аминокислоты;
R22 представляет собой -OH, -NH2, -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f-N(H)(R23) или -R82-(C(O)-CH(X2)-NH)d-R77;
каждый R23 независимо представляет собой водород, C1-6 алкил, C6-10 арил, C3-8 циклоалкил, -COOH или -COO-C1-6 алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащее циклическое соединение;
R82 представляет собой -NH или кислород;
или R26 и R27, взятые вместе с двумя углеродными атомами, к которым они присоединены, и третьим углеродным атомом, соединяющим два углеродных атома, образуют необязательно замещенное шестичленное кольцо;
R28 отсутствует, представляет собой NH или кислород;
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3;
f представляет собой целое число от 1 до 12;
u представляет собой целое число 0 или 1;
w представляет собой целое число 0 или 1; и
при условии, что соединение формулы (VII) должно содержать по меньшей мере один из R29 и R79.
В одном варианте осуществления, соединение неприродного камптотецина формулы (VII) представляет собой соединение формулы (VIII) или формулы (XXV):


где R30 представляет собой -NH2, -R28-C1-6 алкил-R22, 5-12-членный гетероциклоалкил, R28-C5-12 гетероциклоалкил-C1-6 алкил-R22 или -R28-C1-6 алкил-C6-12 арил-C1-6 алкил-R22;
R28 отсутствует, представляет собой NH или кислород;
R22 представляет собой -OH, -NH2, -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f -N(H)(R23) или -R82-(C(O)-CH(X2)-NH)d-R77;
каждый R23 независимо представляет собой водород, C1-6 алкил, C6-10 арил, C3-8 циклоалкил, -COOH или -COO-C1-6 алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащее циклическое соединение;
R82 представляет собой -NH или кислород;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3; и
f представляет собой целое число от 1 до 12.
В некоторых вариантах осуществления, R30 представляет собой любую одну из следующих структур:


где:
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3; и
g представляет собой целое число от 2 до 6.
В другом варианте осуществления, PI3 киназа представляет собой соединение формулы (IX):
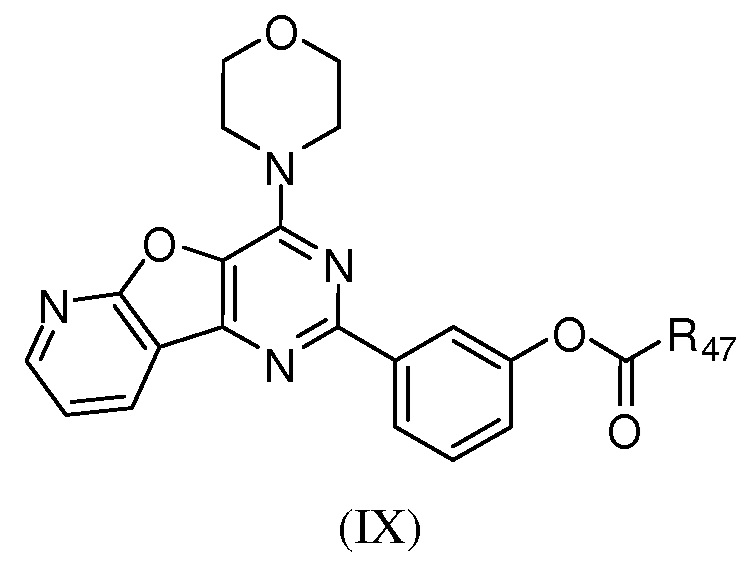
где
R47 представляет собой аминогруппу, -R9-[C(R20R21)]a-R10, -R9-C5-12 гетероциклоалкил-C1-6 алкил-R10 или 5-12-членный гетероциклоалкил;
каждый из R20 и R21 независимо представляет собой водород, C1-6 алкил, C6-10 арил, гидроксилированный C6-10 арил, полигидроксилированный C6-10 арил, 5-12-членный гетероцикл, C3-8циклоалкил, гидроксилированный C3-8 циклоалкил, полигидроксилированный C3-8 циклоалкил или боковую цепь природной или неприродной аминокислоты;
R10 представляет собой -OH, -NHR83, -N-(R83)R11, -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f-N(H)(R23), -R82-(C(O)-CH(X2)-NH)d-R77 или -R82-C(O)-[C(R20R21)]a-R82-R83;
каждый R23 независимо представляет собой водород, C1-6 алкил, C6-10 арил, C3-8 циклоалкил, -COOH или -COO-C1-6алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащее циклическое соединение;
R82 представляет собой -NH или кислород;
R9 отсутствует, представляет собой N-(R83) или кислород;
R83 представляет собой водород или CH;
R11 представляет собой:
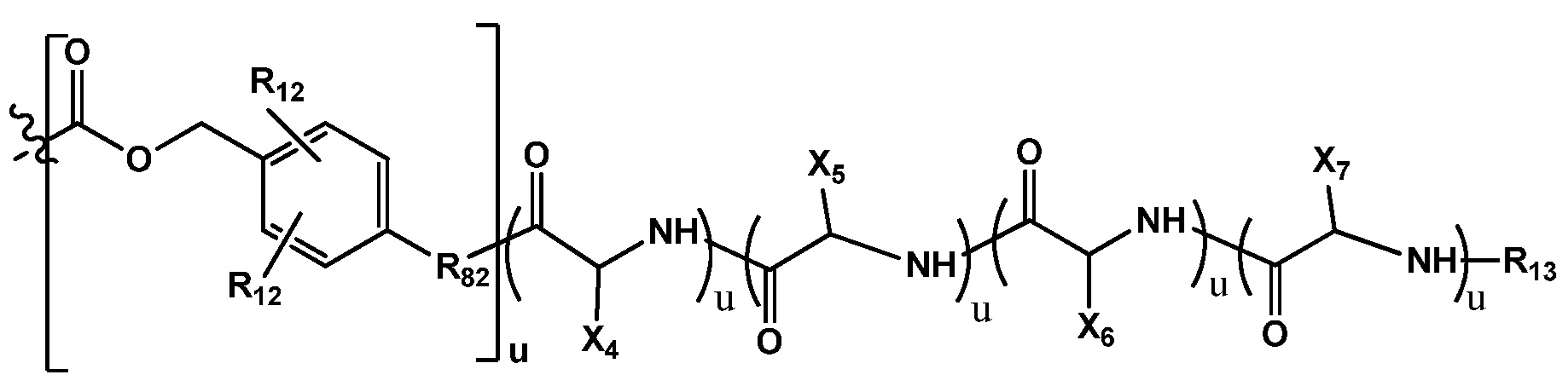
каждый R12 независимо представляет собой водород, хлор, -CH3 или -OCH3;
R13 представляет собой водород или -C(O)-(CH2)d-(O-CH2-CH2)f-NH2;
X4 представляет собой боковую цепь лизина, аргинина, цитруллина, аланина или глицина;
X5 представляет собой боковую цепь фенилаланина, валина, лейцина, изолейцина или триптофана;
каждый из X6 и X7 представляет собой независимо боковую цепь глицина, аланина, серина, валина или пролина;
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3;
f представляет собой целое число от 1 до 12; и
каждый u независимо представляет собой целое число 0 или 1.
В некоторых вариантах осуществления

представляет собой цитруллин-валин; лизин-фенилаланин; цитруллин-фенилаланин; цитруллин-лейцин; цитруллин-валин-глицин-глицин; глицин-фенилаланин-глицин-глицин; валин; пролин; лейцин или изолейцин.
В другом варианте осуществления, R11 представляет собой одну из следующих структур:


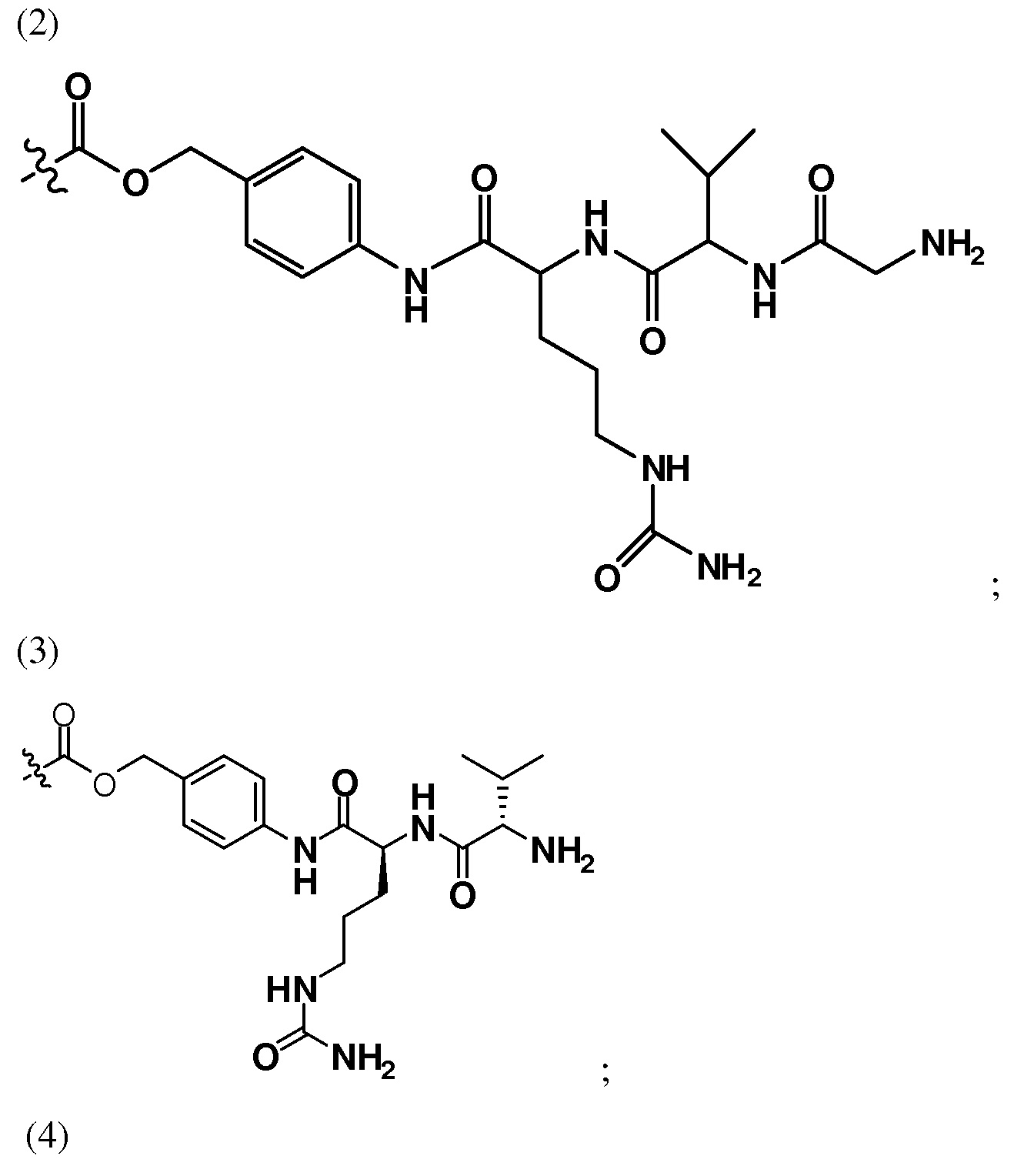

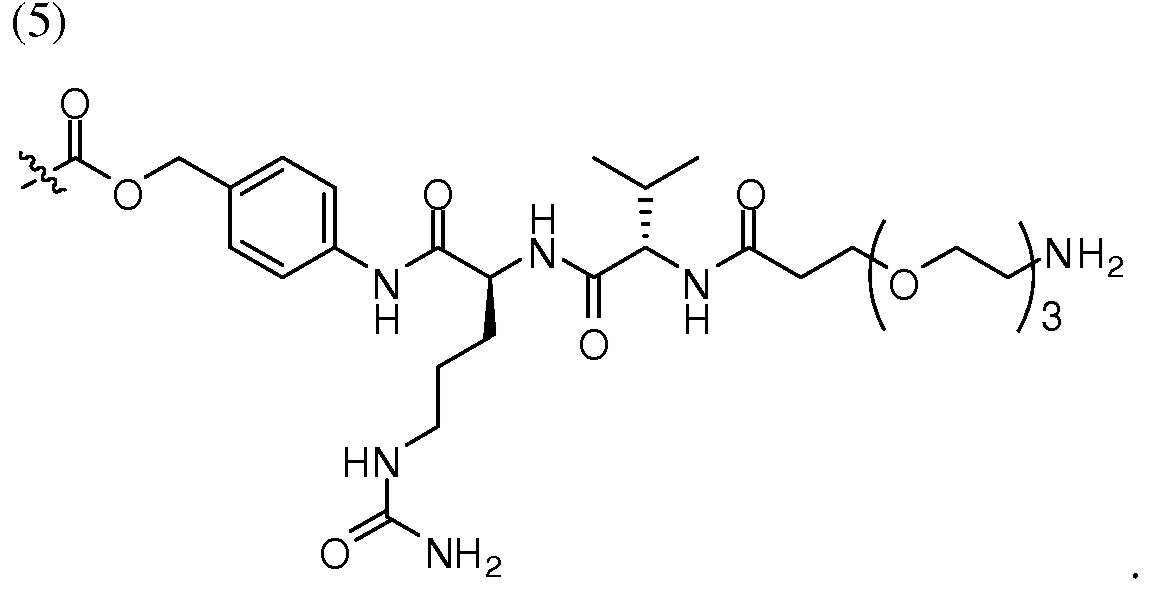
В некоторых вариантах осуществления, R47 представляет собой одну из следующих структур:




где:
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3; и
г представляет собой целое число от 2 до 6.
В другом варианте осуществления, ауристатин представляет собой соединение формулы (X):

где:
каждый из R31 и R32 независимо представляет собой водород или C1-8алкил, и не более чем один их R31 и R32 представляет собой водород;
R33 представляет собой водород, C1-8алкил, C3-8 карбоцикл, C6-10 арил, C1-8 алкил-C6-10 арил, X1-(С3-8карбоцикл), C3-8 гетероцикл или X1-(С3-8гетероцикл);
R34 представляет собой водород, C1-8 алкил, C3-8 карбоцикл, C6-10 арил, X1-С6-10арил, X1-(C3-8 карбоцикл), C3-8 гетероцикл или X1-(C3-8гетероцикл);
R35 представляет собой водород или метил;
или R34 и R35 вместе с углеродным атомом, к которому они присоединены, образуют карбоциклическое кольцо, имеющее формулу -(CR55R41)b-, где каждый из R55 и R41 независимо представляет собой водород или C1-8 алкил, и b представляет собой целое число от 3 до 7;
R36 представляет собой водород или C1-8алкил;
R37 представляет собой водород, C1-8алкил, C3-8 карбоцикл, C6-10 арил, -X1-C6-10арил, -X1-(C3-8 карбоцикл), C3-8 гетероцикл или -X1-(C3-8гетероцикл);
каждый R38 независимо представляет собой водород, OH, C1-8алкил, C3-8 карбоцикл или O-(C1-8 алкил);
R53 представляет собой:

R39 представляет собой H, C1-8 алкил, C6-10 арил, -X1-C6-10арил, C3-8 карбоцикл, C3-8 гетероцикл, -X1-(C3-8гетероцикл), -C1-8 алкилен-NH2, или (CH2)2SCH3
каждый X1 независимо представляет собой C1-10 алкилен или C3-10 циклоалкилен;
R44 представляет собой водород или C1-8 алкил;
R45 представляет собой X3-R42 или NH-R19;
X3 представляет собой O или S;
R19 представляет собой водород, OH, аминогруппу, алкиламино или -[C(R20R21)]a-R22;
R42 представляет собой аминогруппу, C1-6 алкиламино или -[C(R20R21)]a-R22;
каждый из R20 и R21 независимо представляет собой водород, C1-6 алкил, C6-10 арил, гидроксилированный C6-10 арил, полигидроксилированный C6-10 арил, 5-12-членный гетероцикл, C3-8 циклоалкил, гидроксилированный C3-8 циклоалкил, полигидроксилированный C3-8 циклоалкил или боковую цепь природной или неприродной аминокислоты;
R22 представляет собой -OH, -NHR23, -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f-N(H)(R23) или -R82-(C(O)-CH(X2)-NH)d-R77;
каждый R23 независимо представляет собой водород, C1-6 алкил, C6-10арил, C3-8 циклоалкил, -COOH или -COO-C1-6алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащее циклическое соединение;
R82 представляет собой -NH или кислород;
R54 представляет собой -C(R56)2-C(R56)2-C6-10 арил, -C(R56)2-C(R56)2-C3-8 гетероцикл или -C(R56)2-C(R56)2-C3-8 карбоцикл;
R56 независимо выбирают из H, OH, C1-8 алкила, C3-8 карбоцикла, -O-C1-8 алкила, -O C(O)-R29 и -O-R23-O-C1-6 алкил-NH2;
R29 представляет собой аминогруппу, 5-12-членный гетероциклоалкил, -R28-C1-6 алкил-R22, R28-C5-12 гетероциклоалкил-C1-6 алкил-R22, -[C(R20R21)]a-R22, или -R28-C1-6 алкил-C6-12 арил-C1-6алкил-R22;
R28 отсутствует, представляет собой NH или кислород;
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3; и
f представляет собой целое число от 1 до 12.
В некоторых вариантах осуществления, в соединении ауристатина формулы (X):
R39 представляет собой бензил или

R44 представляет собой водород;
В одном варианте осуществления, ауристатин формулы (X) представляет собой соединение формулы (XI), формулы (XII) или формулы (XIII):
где соединение формулы (XI) представляет собой:
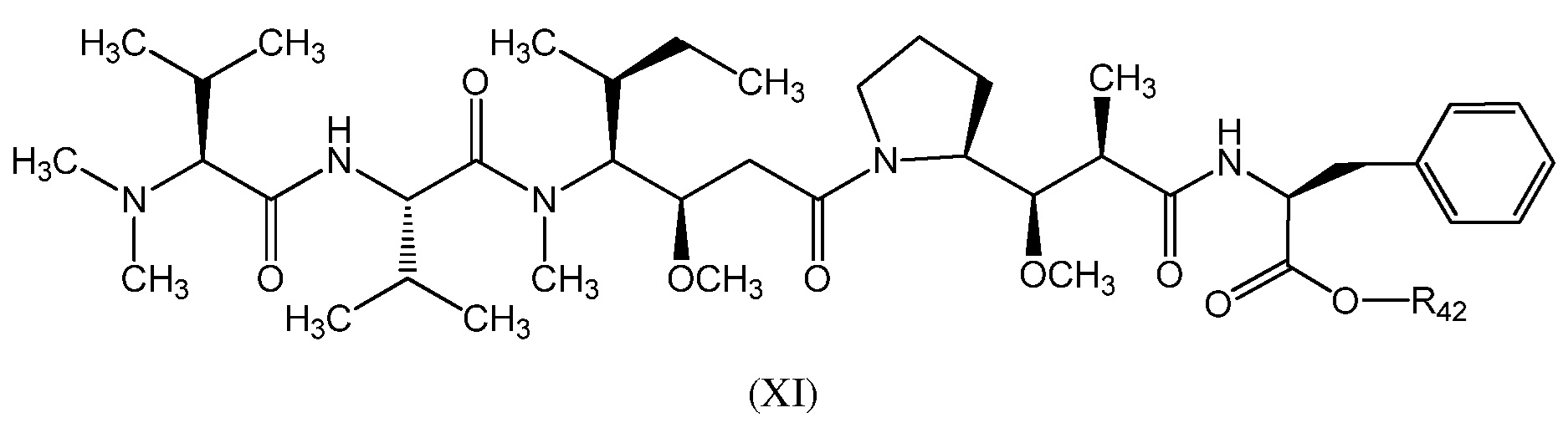
где R42 представляет собой -CH3 или любую одну из следующих структур:


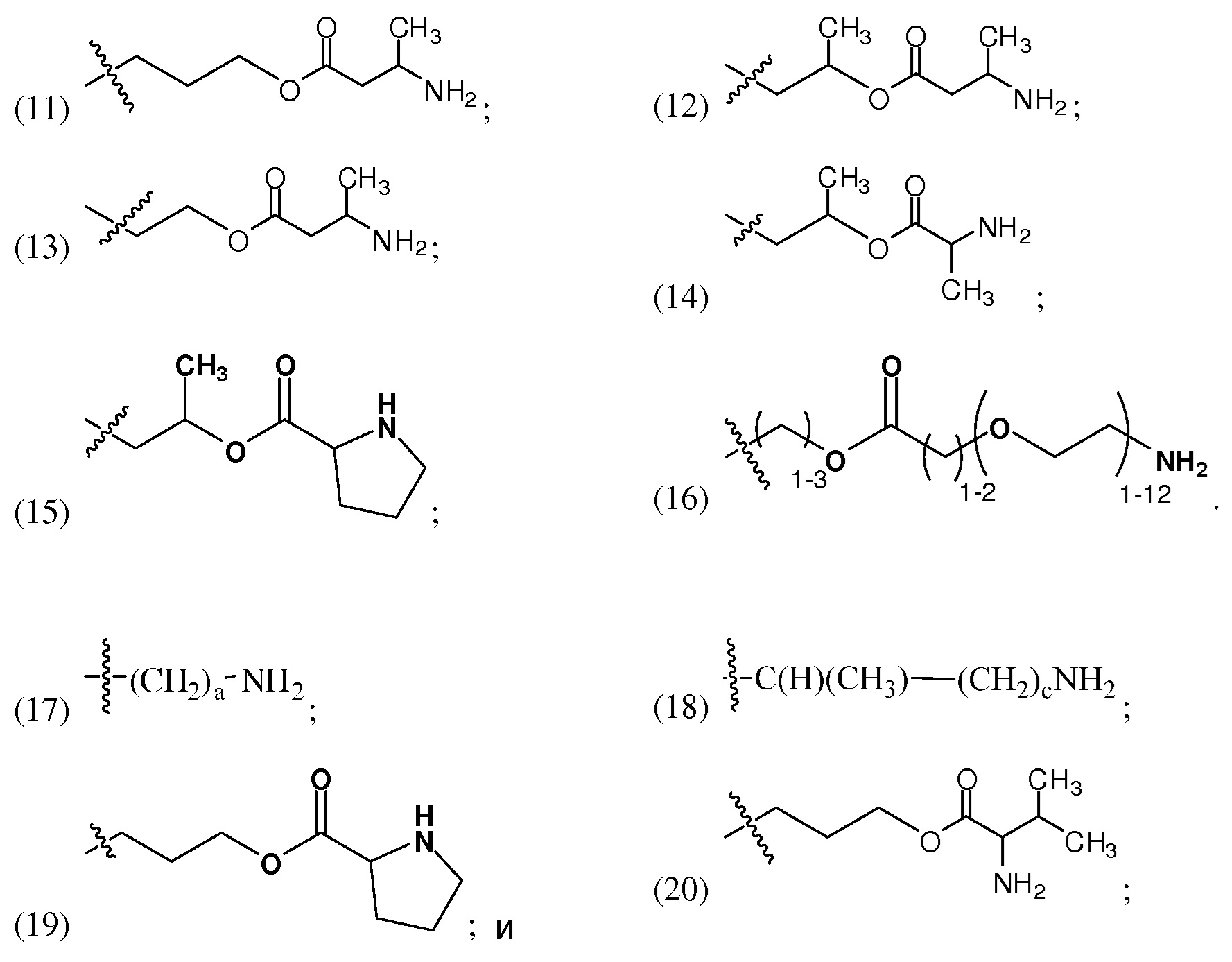
где:
a представляет собой целое число от 1 до 6; и
c представляет собой целое число от 0 до 3;
где соединение формулы (XII) представляет собой:

где R40 представляет собой водород, -OH, -NH2, или любую из следующих структур:


где:
a представляет собой целое число от 1 до 6; и
c представляет собой целое число от 0 до 3.
где соединение формулы (XIII) представляет собой:

где R29 представляет собой аминогруппу, 5-12-членный гетероциклоалкил, -R28-C1-6алкил-R22, R28-C5-12 гетероциклоалкил-C1-6 алкил-R22, -R28-[C(R20R21)]a-R22 или -R28-C1-6 алкил-C6-12 арил-C1-6 алкил-R22;
каждый из R20 и R21 независимо представляет собой водород, C1-6 алкил, C6-10 арил, гидроксилированный C6-10 арил, полигидроксилированный C6-10 арил, 5-12-членный гетероцикл, C3-8 циклоалкил, гидроксилированный C3-8 циклоалкил, полигидроксилированный C3-8 циклоалкил или боковую цепь природной или неприродной аминокислоты;
R22 представляет собой -OH, -NHR2 , -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f -N(H)(R23) или -R82-(C(O)-CH(X2)-NH)d-R77;
каждый R23 независимо представляет собой водород, C1-6 алкил, C6-10 арил, C3-8 циклоалкил, -COOH или -COO-C1-6 алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащее циклическое соединение;
R82 представляет собой -NH или кислород;
R28 отсутствует, представляет собой NH или кислород;
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3; и
f представляет собой целое число от 1 до 12.
В одном варианте осуществления, в формуле (XII), R40 представляет собой



В одном варианте осуществления, в соединении формулы (XIII), R29 представляет собой -NH2, 5-членный гетероциклоалкил, -R28-C1-6 алкил-R22, R28-C5-12 гетероциклоалкил-C1-6 алкил-R22 или -R28-C1-6 алкил-C6-12 арил-C1-6 алкил-R22;
R28 отсутствует, представляет собой NH или кислород;
R22 представляет собой -OH, -NHR23, -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f-N(H)(R23) или -R82-(C(O)-CH(X2)-NH)d-R77;
каждый R23 независимо представляет собой водород, C1-6 алкил, C6-10 арил, C3-8 циклоалкил, -COOH или -COO-C1-6 алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащее циклическое соединение;
R82 представляет собой -NH или кислород;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3; и
f представляет собой целое число от 1 до 12.
В еще одном варианте осуществления, R29 представляет собой любую одну из следующих структур:


где:
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3; и
g представляет собой целое число от 2 до 6.
В одном варианте осуществления, ингибитор MEK представляет собой соединение формулы (XIV):

где R43 представляет собой H или -R46-R47;
каждый из R20 и R21 независимо представляет собой водород, C1-6 алкил, C6-10 арил, гидроксилированный C6-10 арил, полигидроксилированный C6-10 арил, 5-12-членный гетероцикл, C3-8 циклоалкил, гидроксилированный C3-8 циклоалкил, полигидроксилированный C3-8 циклоалкил или боковую цепь природной или неприродной аминокислоты;
R22 представляет собой -OH, -NH2, -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f -N(H)(R23) или -R82-(C(O)-CH(X2)-NH)d-R77;
каждый R23 независимо представляет собой водород, C1-6 алкил, C6-10 арил, C3-8 циклоалкил, -COOH или -COO-C1-6 алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащее циклическое соединение;
R82 представляет собой -NH или кислород;
R46 представляет собой -C(O)-; -C(O)-O-, -C(O)-NH- или отсутствует;
R47 определен в описании изобретения;
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3; и
f представляет собой целое число от 1 до 12.
Дополнительные примеры ингибитора MEK раскрыты в патенте США № 7517994 B2.
В некоторых вариантах осуществления, R43 представляет собой -C(O)-(CH2)a-NH2 или -C(O)-C(H)(CH3)-(CH2)c-NH2; где a представляет собой целое число от 1 до 6; и c представляет собой целое число от 0 до 3.
В другом варианте осуществления, соединение дуокармицина представляет собой соединение формулы (XV):

где:
R47 определен в описании изобретения;
R48 представляет собой водород, -COOC1-6 алкил, -COOH, -NH2 или -CH3;
R49 представляет собой Cl, Br или -OH;
R50 представляет собой водород, -OCH3,

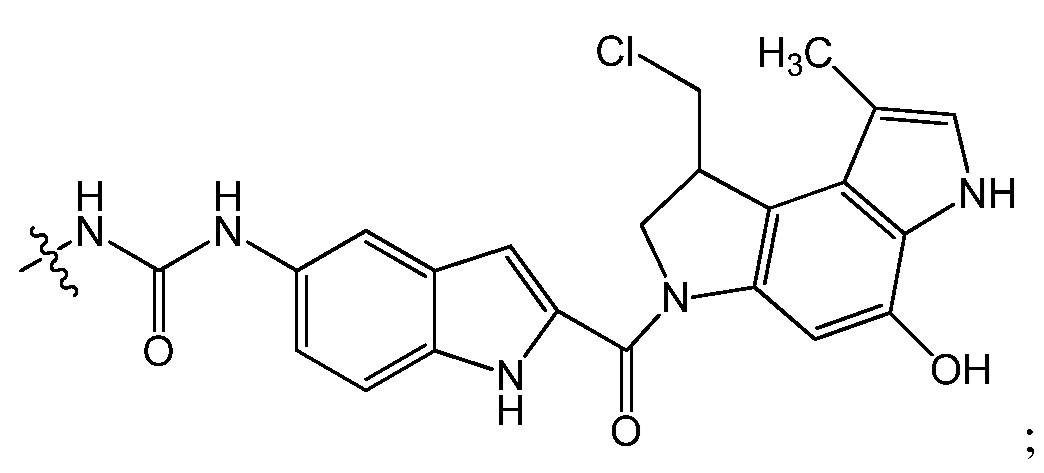
каждый из R51 и R52 независимо представляет собой водород или -OCH3; и
кольцо AA представляет собой либо фенил, либо пирролильное кольцо.
Дополнительные примеры соединений дуокармицина раскрыты в патенте США № 7553816.
В одном варианте осуществления, соединение дуокармицина формулы (XV) представляет собой соединение формулы (XVI), (XVII), (XVIII) или (XIX):



где:
R49 представляет собой Cl, Br или -OH; и
R47 определен в описании изобретения.
В другом варианте осуществления, соединение дуокармицина представляет собой соединение дуокармицина SA формулы (XX): патент США № 5101038; или (XXI):


где:
R42 представляет собой C1-6 алкиламино или -[C(R20R21)]a-R22;
каждый из R20 и R21 независимо представляет собой водород, C1-6 алкил, C6-10 арил, гидроксилированный C6-10 арил, полигидроксилированный C6-10 арил, 5-12-членный гетероцикл, C3-8 циклоалкил, гидроксилированный C3-8 циклоалкил, полигидроксилированный C3-8 циклоалкил или боковую цепь природной или неприродной аминокислоты;
R22 представляет собой -OH, -NH2, -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f-N(H)(R23) или -R82-(C(O)-CH(X2)-NH)d-R77;
каждый R23 независимо представляет собой водород, C1-6 алкил, C6-10 арил, C3-8 циклоалкил, -COOH или -COO-C1-6 алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащее циклическое соединение;
R82 представляет собой -NH или кислород;
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3; и
f представляет собой целое число от 1 до 12.
В некоторых вариантах осуществления, R42 представляет собой любую одну из следующих структур:


где:
a представляет собой целое число от 1 до 6; и
c представляет собой целое число от 0 до 3.
В другом варианте осуществления, тубулизин представляет собой соединение формулы (XXII):

где:
R57 представляет собой C1-4 алкил или -C(O)R58;
R58 представляет собой C1-6алкил, CF3 или C6-10арил;
R59 представляет собой C1-6 алкил;
R60 представляет собой водород, C1-6алкил, C2-7 алкенил, -CH2-фенил, CH2OR65 или CH2OCOR66;
R65 представляет собой водород, C1-6алкил, C2-7 алкенил, C6-10 арил или C(O)R67;
R67 представляет собой C1-6 алкил, C2-7 алкенил, C6-10 арил или гетероарил;
R66 представляет собой C1-6 алкил, -C6H5 или -CH2-фенил;
R61 представляет собой C1-6 алкил;
R62 представляет собой водород, OH, O-C1-4 алкил или O-C(O)-C1-4 алкил;
R63 представляет собой водород, OH, O-C1-4 алкил, O-C(O)-C1-4 алкил, галоген или C1-6 алкил; e представляет собой целое число от 1 до 3 включительно;
R64 представляет собой:

где:
R68 представляет собой водород или C1-C6 алкил;
R69 представляет собой CO2R70, C(O)-R78, CONHNH2, OH, NH2, SH или необязательно замещенную алкильную, циклоалкильную, гетероалкильную или гетероциклоалкильную группу;
R70 представляет собой необязательно замещенную алкильную (то есть C1-6 алкиламин), гетероалкильную или гетероциклоалкильную группу;
каждый из R71 и R73 независимо представляет собой водород, галоген, -NO2, -CN, -NHR74, C1-6 алкил, галогеналкил, алкокси и галогеналкокси;
R72 представляет собой водород, OR43, алкокси, галоген, -NHR74, -O-C(O)-R47, NO2, -CN, C6-10 арил, C1-6 алкил, амино или диалкиламино;
R74 представляет собой водород, -CHO, -C(O)-C1-4 алкил, OH, аминогруппу, алкиламино или -[C(R20R21)]a-R22;
R43 представляет собой H или -R46-R47;
R46 представляет собой -C(O)-; -C(O)-O-, -C(O)-NH- или отсутствует;
R47 определен в описании изобретения;
R78 представляет собой X3-R75 или NH-R19;
X3 представляет собой O или S;
R19 представляет собой водород, OH, аминогруппу, алкиламино или -[C(R20R21)]a-R22;
R75 представляет собой водород, аминогруппу, C1-6 алкиламино или -[C(R20R21)]a-R22;
каждый из R20 и R21 независимо представляет собой водород, C1-6 алкил, C6-10 арил, гидроксилированный C6-10 арил, полигидроксилированный C6-10 арил, 5-12-членный гетероцикл, C3-8 циклоалкил, гидроксилированный C3-8 циклоалкил, полигидроксилированный C3-8 циклоалкил или боковую цепь природной или неприродной аминокислоты;
R22 представляет собой -OH, -NH2, -COOH, -R82-C(O)(CH2)c-C(H)(R23)-N(H)(R23), -R82-C(O)(CH2)d-(OCH2-CH2)f-N(H)(R23) или -R82-(C(O)-CH(X2)-NH)d-R77;
каждый R23 независимо представляет собой водород, C1-6 алкил, C6-10 арил, C3-8 циклоалкил, -COOH или -COO-C1-6 алкил;
X2 представляет собой боковую цепь природной или неприродной аминокислоты;
R77 представляет собой водород или X2, и NR77 образует азотсодержащее циклическое соединение;
R82 представляет собой -NH или кислород;
R47 определен в описании изобретения;
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3;
d представляет собой целое число от 1 до 3;
f представляет собой целое число от 1 до 12; и
при условии, что когда R69 представляет собой C(O)-X3-R75 или C(O)-NH-R19, один или оба R71 и R73 представляют собой -NHR74, и R72 представляет собой OR43, -NHR74 или -O-C(O)-R47, по меньшей мере, один из R19, R43, R74 и R75 не может быть водородом.
В некоторых вариантах осуществления, в соединении формулы (XXII):
R57 представляет собой -CH3;
R59 представляет собой вторбутил;
R60 представляет собой водород, метил, этил, пропил, изопропил или изобутил;
R61 представляет собой изопропил,
R62 представляет собой водород;
R63 представляет собой водород, OH, -O-C3H7, O-C(O)-CH3;
R68 представляет собой водород или -CH3;
R69 представляет собой CO2H, CO2R70 или C(O)-R78;
R70 представляет собой C1-6 алкиламин;
каждый из R71 и R73 независимо представляет собой водород;
R72 представляет собой водород, -OR43, OH, F, -CH3 или -OCH3;
R78 представляет собой OH, -OR75 или -NHR40;
e представляет собой целое число 2;
R40 представляет собой водород, -OH, -NH2, или любую из следующих структур:


где:
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3;
R75 представляет собой любую одну из следующих структур:


где:
a представляет собой целое число от 1 до 6; и
c представляет собой целое число от 0 до 3;
R43 представляет собой водород, -C(O)-(CH2)a-NH2, или -C(O)-C(H)(CH3)-(CH2)c-NH2;
где:
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3; и
R47 представляет собой любую одну из следующих структур:
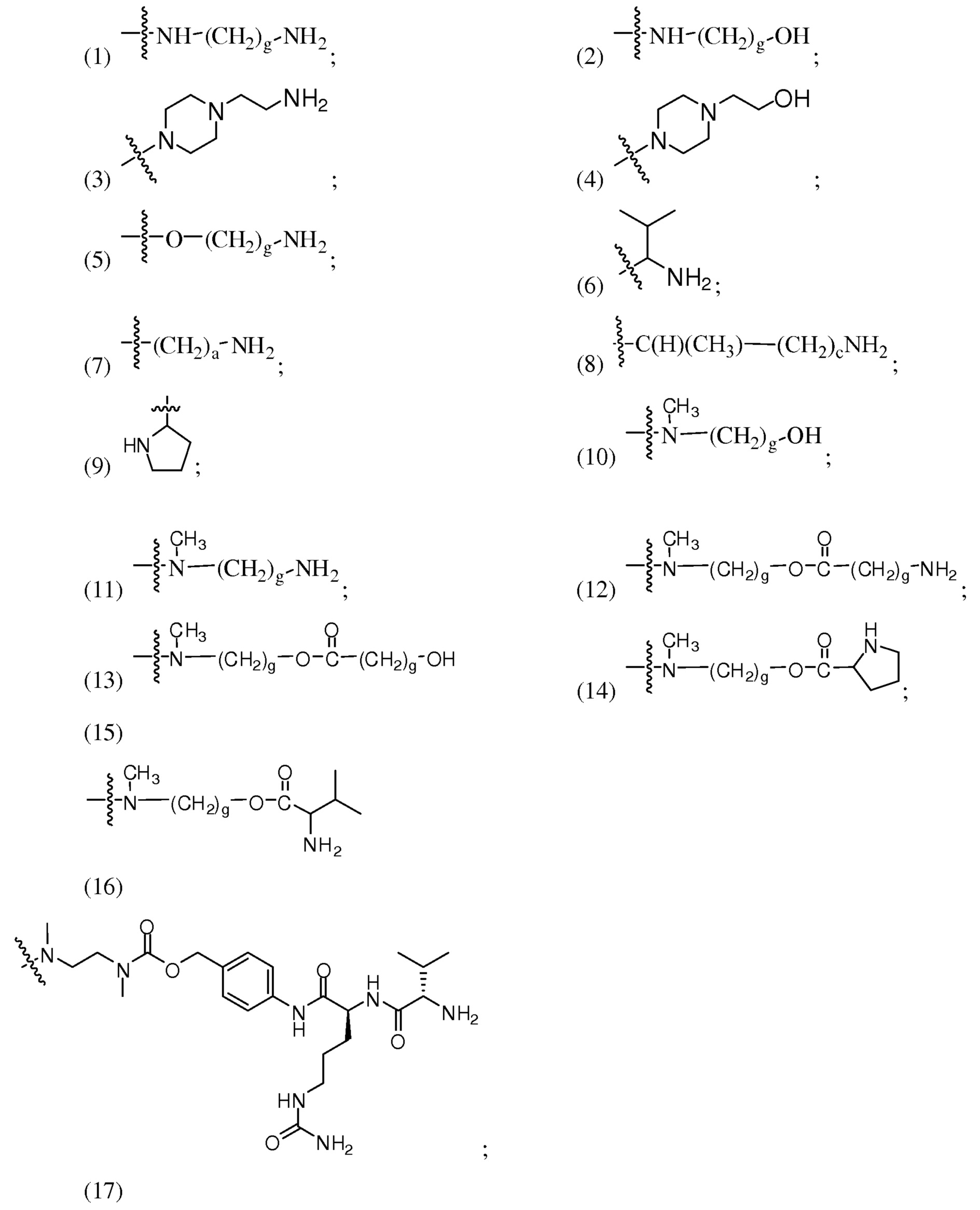

где:
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3; и
g представляет собой целое число от 2 до 6;
при условии, что если R72 представляет собой -OH, то тогда R75 не может быть водородом; если R69 представляет собой COOH, то тогда R72 должен представлять собой -OR43 или -O-C(O)-R47.
В некоторых вариантах осуществления, тубулизин формулы (XXII) представляет собой соединение формулы (XXIII) или (XXIV):

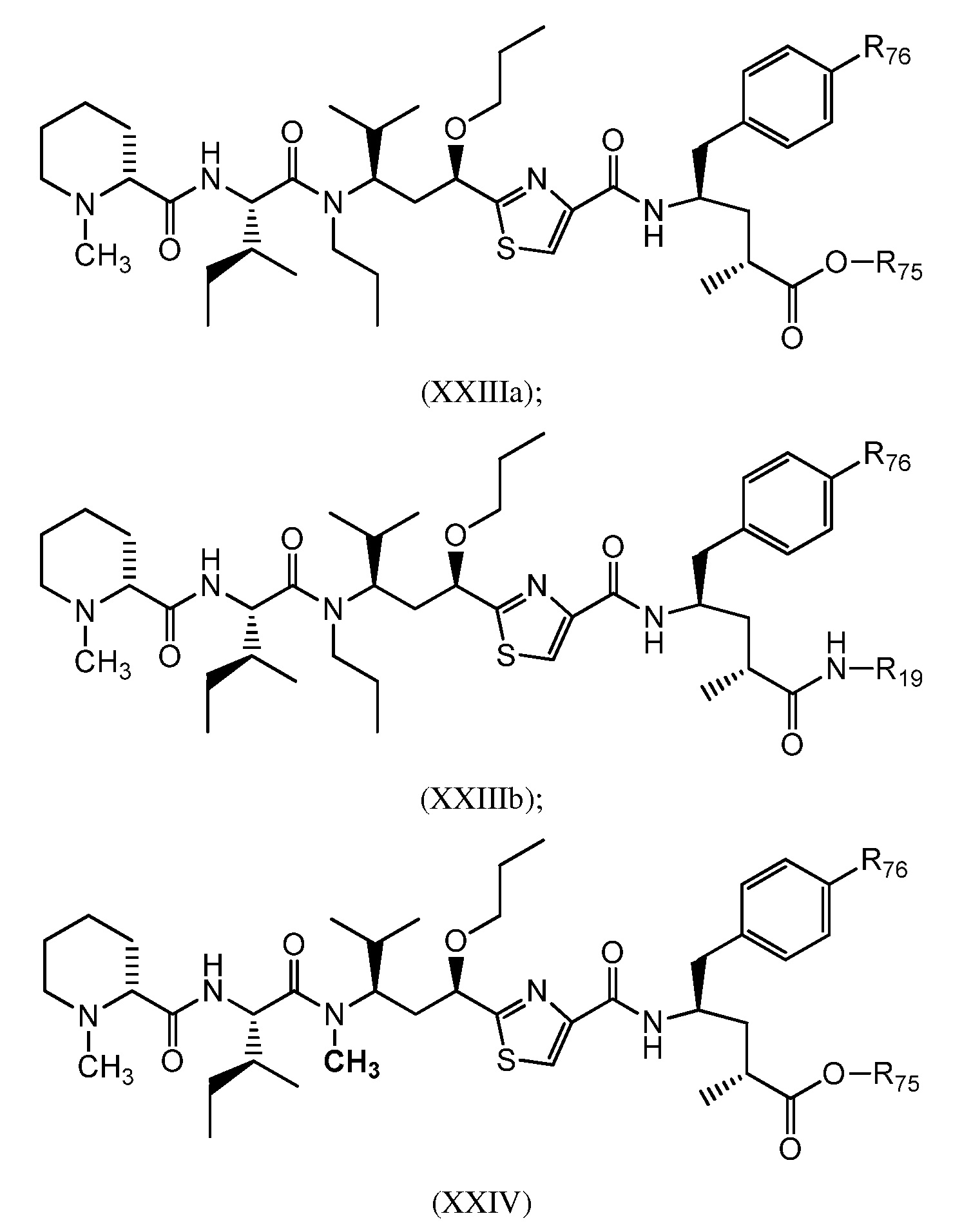
где:
R76 представляет собой водород, OH, OCH3, F, -OR43 или -O-C(O)-R47;
где R78, R75, R19, R47 и R43 определены в описании изобретения; и
при условии, что если R76 представляет собой -OH, OCH3 или F, то тогда R75 и R19 не могут быть водородом.
В одном варианте осуществления, R47 представляет собой

В другом варианте осуществления, соединение ингибитора KSP представляет собой соединение формулы (XXVI):
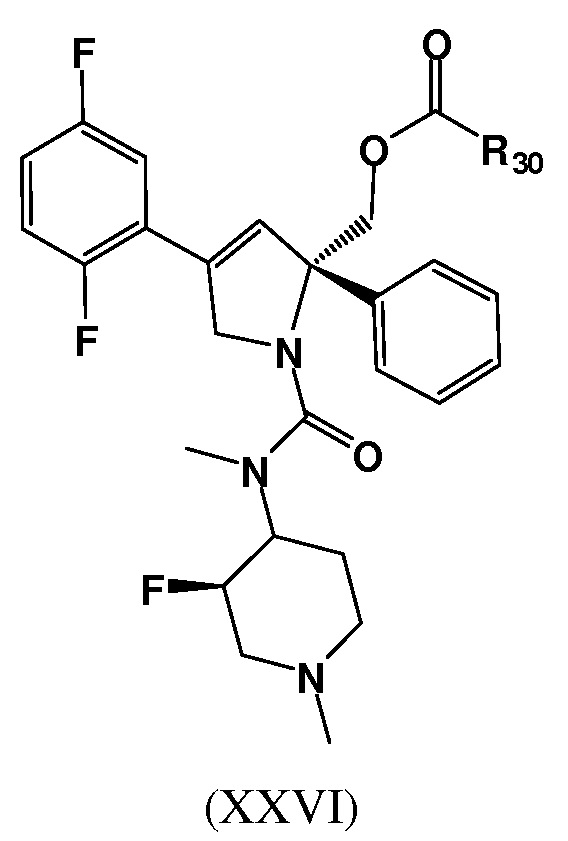
где R30 определен в описании изобретения.
В некоторых вариантах осуществления, R30 представляет собой:

где:
a представляет собой целое число от 1 до 6;
c представляет собой целое число от 0 до 3; и
g представляет собой целое число от 2 до 6.
В другом варианте осуществления, соединение ингибитора KSP представляет собой соединение формулы (XXVII), (XXVIII) или (XXIX):

где:
R11 определен в описании изобретения.
Для любого специалиста в области терапевтических средств является очевидным, что каждое из описанных в изобретении терапевтических средств может быть модифицировано таким образом, что полученное соединение будет сохранять специфичность и/или активность исходного соединения. Для специалиста является также очевидным, что многие из этих модифицированных соединений могут быть использованы вместо описанных в изобретении терапевтических средств. Так, терапевтические средства настоящего изобретения включают аналоги и производные описанных в изобретении соединений.
В таблице B ниже приводится большее количество примеров терапевтических средств и их производных, подходящих для конъюгирования с образованием конъюгатов полимер-лекарственное средство-белок или каркасных структур полимер-лекарственное средство изобретения. Также приводятся спектральные данные конкретных соединений (ND в таблице означает "не определяли"). В этих примерах может также присутствовать активная форма лекарственного средства, когда оно высвобождается из конъюгатов in vitro или in vivo.

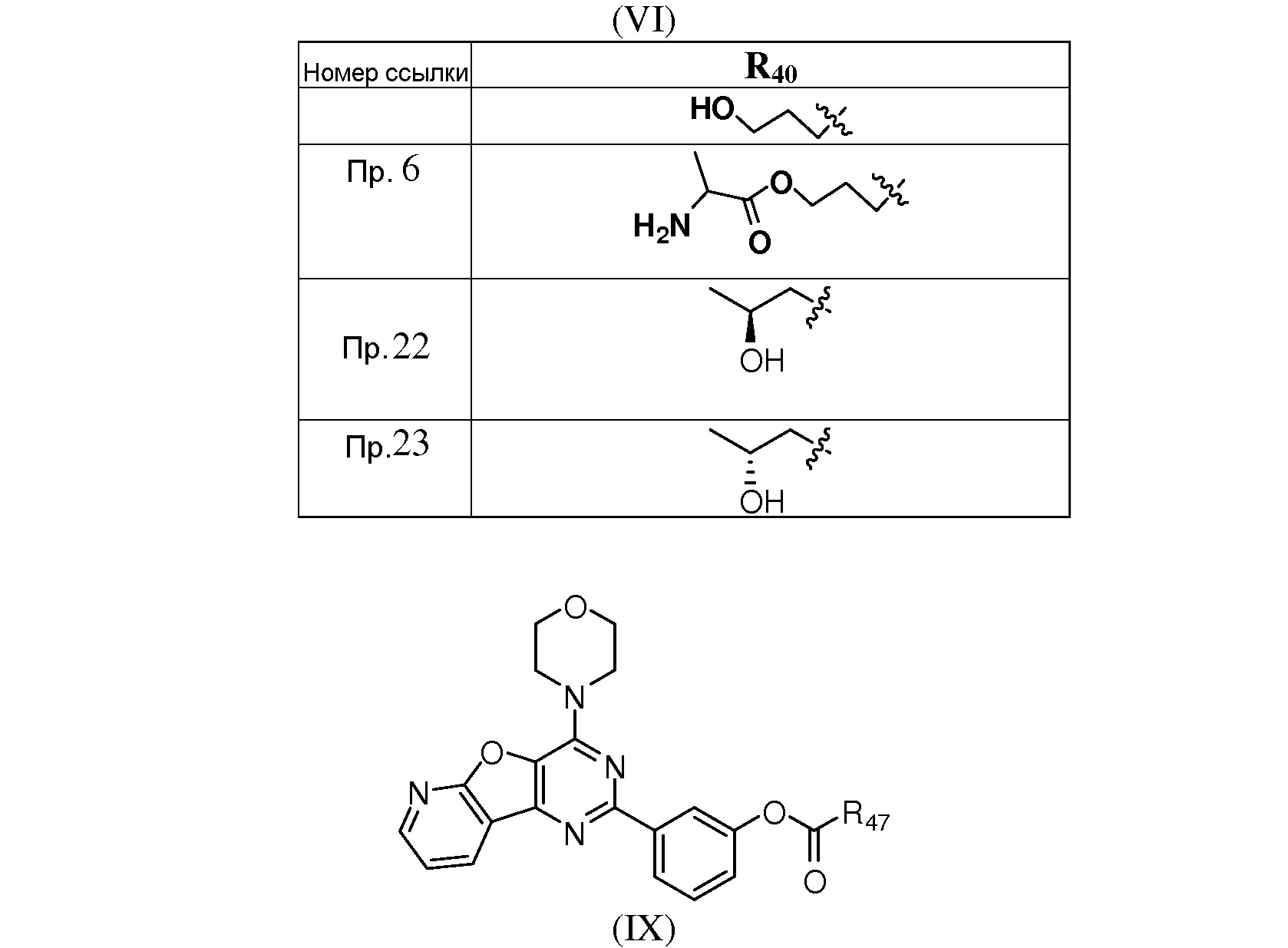











Распознающие молекулы на основе белка (PBRM)
Распознающая молекула на основе белка нацеливает конъюгаты лекарственное средство-полимерный носитель на конкретные ткани, клетки или участки в клетки. Распознающая молекула на основе белка может нацеливать модифицированный полимер на культуру или на целый организм, или и на то, и на другое. В каждом случае, распознающая молекула на основе белка имеет лиганд, который присутствует на поверхности таргетированной клетки (клеток), с которым он связывается с эффективной специфичностью, аффинностью и авидностью. В некоторых вариантах осуществления, распознающая молекула на основе белка нацеливает модифицированный полимер на ткани, отличные от печени. В других вариантах осуществления, распознающая молекула на основе белка нацеливает модифицированный полимер на конкретную ткань, такую как печень, почка, легкое или поджелудочная железа. Распознающая молекула на основе белка может нацеливать модифицированный полимер на клетку-мишень, такую как раковая клетка, на рецептор, экспрессированный на клетке, такой как раковая клетка, на матричную ткань или белок, связанный с раком, такой как опухолевый антиген. В качестве варианта, клетками-мишенями могут быть клетки сосудистой сети опухоли. Распознающие молекулы на основе белка могут нацеливать полимер на конкретные типы клеток, например, специфически нацеливая на гепатоциты в печени, но не затрагивая купферовские клетки. В других случаях, распознающие молекулы на основе белка могут нацеливать полимер на клетки ретикуло-эндотелиальной или лимфатической системы, или на профессиональные фагоциты, такие как макрофаги или эозинофилы. (В таких случаях, сам по себе полимер может также быть эффективной системой доставки, не требующей специфического таргетирования).
В некоторых других вариантах осуществления, распознающая молекула на основе белка может нацеливать модифицированный полимер, например, на участок внутри клетки, такой как ядро, цитоплазма или эндосома. В конкретных вариантах осуществления, распознающая молекула на основе белка может усиливать клеточное связывание с рецепторами или цитоплазматический транспорт в ядро и вход в ядро или выделение из эндосом или других внутриклеточных везикул.
В конкретных вариантах осуществления, распознающие молекулы на основе белка включают антитела, белки и пептиды или пептидные мимики.
Примеры антител или антител, полученных из Fab, Fab2, scFv или фрагментов тяжелых цепей верблюжьего антитела, специфичных к маркерам клеточной поверхности, включают, но этим не ограничивая, 5T4, AOC3, C242, CA-125, CCL11, CCR5, CD2, CD3, CD4, CD5, CD15, CD18, CD19, CD20, CD22, CD23, CD25, CD28, CD30, CD31, CD33, CD37, CD38, CD40, CD41, CD44, CD51, CD52, CD54, CD56, CD62E, CD62P, CD62L, CD70, CD74, CD80, CD125, CD138, CD141, CD147, CD152, CD 154, CD326, CEA, агглютинирующий фактор, CTLA-4, EGFR, ErbB2, ErbB3, EpCAM, рецептор фолиевой кислоты, FAP, GD2, GD3, GPNMB, HGF, HER2, ICAM, IGF-1 рецептор, VEGFR1, EphA2, TRPV1, CFTR, gpNMB, CA9, Cripto, ACE, APP, адренергический рецептор-бета2, клаудин 3, мезотелин, IL-2 рецептор, IL-4 рецептор, IL-13 рецептор, интегрины (включая α4, αvβ3, βvβ5, αvβ6, α1β4, α4β1, α4β7, α5β1, α6β4, αIIbβ3 интегрины), IFN-α, IFN-г, IgE, IgE , IGF-1 рецептор, IL-1, IL-12, IL-23, IL-13, IL-22, IL-4, IL-5, IL-6, рецептор интерферона, ITGB2 (CD18), LFA-1 (CD11a), L-селектин (CD62L), муцин, MUCl, миостатин, NCA-90, NGF, PDGFRα, фосфатидилсерин, клетки рака предстательной железы, синегнойную палочку, вирус бешенства, RANKL, респираторно-синцитиальный вирус, резус-фактор, SLAMF7, сфингозин-1-фосфат, TAG-72, рецептор Т-клетки, тенасцин C, TGF-1, TGF-β2, TGF-β, TNF-α, TRAIL-R1, TRAIL-R2, опухолевый антиген CTAA16.88, VEGF-A, VEGFR2, виментин и другие подобные антитела.
В одном варианте осуществления, антитела или антитело, полученное из Fab, Fab2, scFv или фрагментов тяжелых цепей верблюжьего антитела, специфичных к маркерам клеточной поверхности, включают CA-125, C242, CD3, CD19, CD22, CD25, CD30, CD31, CD33, CD37, CD40, CD44, CD51, CD54, CD56, CD62E, CD62P, CD62L, CD70, CD138, CD141, CD326, CEA, CTLA-4, EGFR, ErbB2, ErbB3, FAP, рецептор фолиевой кислоты, IGF-1 рецептор, GD3, GPNMB, HGF, HER2, VEGF-A, VEGFR2, VEGFR1, EphA2, EpCAM, 5T4, TAG-72, танасцин C, TRPV1, CFTR, gpNMB, CA9, Cripto, ACE, APP, PDGFRα, фосфатидилсерин, клетки рака предстательной железы, адренергический рецептор-бета2, клаудин 3, муцин, MUCl, мезотелин, IL-2 рецептор, IL-4 рецептор, IL-13 рецептор и интегрины (включая αvβ3, αvβ5, αvβ6, α1β4, α4β1, α5β1, α6β4 интегрины), тенасцин C, TRAIL-R2 и виментин.
Примеры антител включают 3F8, абаговомаб, абциксимаб (РЕОПРО), адалимумаб (ХУМИРА), адекатумумаб, афелимомаб, афутузумаб, алацизумаб, ALD518, алемтузумаб (CAMPATH), алтумомаб, аматуксимаб, анатумомаб, анрукинзумаб, аполизумаб, арцитумомаб (CEA-SCAN), аселизумаб, атлизумаб (тоцилизумаб, актемра, роактемра), аторолимумаб, бапинейзумаб, базиликсимаб (симулект), бавитуксимаб, бектумомаб (ЛИМФОСКАН), белимумаб (БЕНЛИСТА), бенрализумаб, бертилимумаб, бензилесомаб (СКИНИТИМУН), бевацизумаб (АВАСТИН), бициромаб (ФИБРИСЦИНТ), биватузумаб, блинатумомаб, брентуксимаб, бриакинумаб, канакитумаб (ИЛАРИС), кантузумаб, капромаб, катумаксомаб (РЕМОВАБ), CC49, цеделизумаб, цертолизумаб, цетуксимаб (ЭРБИТУКС), цитатузумаб, циксутумумаб, кленоликсимаб, кливатузумаб, конатумумаб, CR6261, дацетузумаб, даклизумаб (ЗЕНАПАКС), даратумумаб, деносумаб (ПРОЛИА), детумомаб, дорлимомаб, дорликсизумаб, экромексимаб, экулизумаб (СОЛИРИС), эдобакомаб, эдреколомаб (ПОНОРЕКС), эфализумаб (РАПТИВА), эфунгумаб (МИКОГРАБ), элотузумаб, элсилимомаб, энлимомаб, эпитумомаб, эпратузумаб, эрлизумаб, эртумаксомаб (РЕКСОМУН), этарацизумаб (АБЕГРИН), эксбивирумаб, фанолесомаб (NEUTROSPEC), фаралимомаб, фарлетузумаб, фелвизумаб, фезакинумаб, фигитумумаб, фонтолизумаб (HuZAF), форавирумаб, фрезолимумаб, галиксимаб, гантерерумаб, гавилимомаб, гемтузумаб, гирентуксимаб, глембатумумаб, голимумаб (SEVIPONI), гомиликсимаб, ибализумаб, ибритумомаб, иговомаб (INDIMACIS-125), имциромаб (MYOSCINT), инфликсимаб (РЕМИКЕЙД), интетумумаб, инолимомаб, инотузумаб, ипилимумаб, иратумумаб, келиксимаб, лабетузумаб (CEA-CIDE), лебрикизумаб, лемалесомаб, лерделимумаб, лексатумумаб, либивирумаб, линтузумаб, лукатумумаб, лумиликсимаб, мапатумумаб, маслимомаб, матузумаб, меполизумаб (BOSATRIA), метелимумаб, милатузумаб, минретумомаб, митумомаб, моролимумаб, мотавизумаб (NUMAX), муромонаб-CD3 (ОРТОКЛОН OKT3), наколомаб, наптумомаб, натализумаб (ТИСАБРИ), небакумаб, нецитумумаб, нерелимомаб, нимотузумаб (THERACIM), нофетумомаб, окрелизумаб, одулимомаб, офатумумаб (АРЗЕРРА), оларатумаб, омализумаб (КСОЛАР), онтецизумаб, опортузумаб, ореговомаб (ОВАРЕКС), отеликсизумаб, пагибаксимаб, пализизумаб (СИНАГИС), панитумумаб (ВЕКТИБИКС), панобакумаб, пасколизумаб, пемтумомаб (ТЕРАГИН), пертузумаб (ОМНИТАРГ), пекселизумаб, пинтумомаб, приликсимаб, притумумаб, PRO 140, рафивирумаб, рамуцирумаб, ранибизумаб (ЛУЦЕНТИС), раксибакумаб, регавирумаб, реслизумаб, рилотумумаб, ритуксимаб (РИТУКСАН), робатумумаб, ронтализумаб, ровелизумаб (LEUKARREST), руплизумаб (ANTOVA), сатумомаб пендетид, севирумаб, сибротузумаб, сифалимумаб, силтуксимаб, сиплизумаб, соланезумаб, сонепцизумаб, сонтузумаб, стамулумаб, сулесомаб (ЛЕЙКОСКАН), такатузумаб (AFP-CIDE), тетраксетан, тадоцизумаб, тализумаб, танезумаб, таплитумомаб паптокс, тефибазумаб (AUREXIS), телимомаб, тенатумомаб, тенеликсимаб, теплизумаб, TGN1412, тицилимумаб (тремелимумаб), тигатузумаб, TNX-650, тоцилизумаб (атлизумаб, АКТЕМРА), торализумаб, тоситумомаб (BEXXAR), трастузумаб (ГЕРЦЕПТИН), тремелимумаб, тукотузумаб, тувирумаб, уртоксазумаб, устекинумаб (STELERA), вапаликсимаб, ведолизумаб, велтузумаб, вепалимомаб, визилизумаб (NUVION), волоциксимаб (HUMASPECT), вотумумаб, залутумумаб (HuMEX-EGFr), занолимумаб (HuMAX-CD4), зиралимумаб и золимомаб.
В некоторых вариантах осуществления, антитела нацелены на маркеры клеточной поверхности для 5T4, CA-125, CEA, CD3, CD19, CD20, CD22, CD30, CD33, CD40, CD44, CD51, CTLA-4, EpCAM, HER2, EGFR, FAP, рецептора фолиевой кислоты, HGF, интегрина αvβ3, интегрина α5β1, IGF-1 рецептора, GD3, GPNMB, муцина, MUC1, фосфатидилсерина, клеток рака предстательной железы, PDGFRα, TAG-72, тенасцина C, TRAIL-R2, VEGF-A и VEGFR2. В этом варианте осуществления, антитела представляют собой абаговомаб, адекатумумаб, алацизумаб, алтумомаб, анатумомаб, арцитумомаб, бавитуксимаб, бевацизумаб (АВАСТИН), биватузумаб, блинатумомаб, брентуксимаб, кантузумаб, катумаксомаб, капромаб, цетуксимаб, цитатузумаб, кливатузумаб, конатумумаб, дацетузумаб, эдреколомаб, эпратузумаб, эртумаксомаб, этарацизумаб, фарлетузумаб, фигитумумаб, гемтузумаб, глембатумумаб, ибритумомаб, иговомаб, интетумумаб, инотузумаб, лабетузумаб, лексатумумаб, линтузумаб, лукатумумаб, матузумаб, митумомаб, наптумомаб эстафенотокс, нецитумумаб, опортузумаб, ореговомаб, панитумумаб, пемтумомаб, пертузумаб, притумумаб, ритуксимаб (РИТУКСАН), рилотумумаб, робатумумаб, сатумомаб, сибротузумаб, таплитумомаб, тенатумомаб, тенатумомаб, тицилимумаб (тремелимумаб), тигатузумаб, трастузумаб (ГЕРЦЕПТИН), тоситумомаб, тремелимумаб, тукотузумаб, целмолейкин, волоциксимаб и залутумумаб.
В конкретных вариантах осуществления, антитела, нацеленные на маркеры клеточной поверхности для HER2, представляют собой пертузумаб или трастузумаб, и для EGFR, антитело представляет собой цетуксимаб, и для CD20, антитело представляет собой ритуксимаб, и для VEGF-A, антитело представляет собой бевацизумаб, и для CD-22, антитело представляет собой эпратузумаб или велтузумаб, и для CEA, антитело представляет собой лабетузумаб.
Примеры пептидов или пептидных мимиков включают нацеленные на интегрин пептиды (RGD пептиды), нацеленные на LHRH рецептор пептиды, нацеленные на ErbB2 (HER2) рецептор пептиды, нацеленные на специфический Т-клеточный антиген предстательной железы (PSMA) пептиды, нацеленные на рецептор липопротеина LRP1 полученные из ApoE белка пептиды, пептиды ApoA белка, нацеленные на рецептор соматостатина пептиды, полученные из хлоротоксина пептиды и бомбезин.
В конкретных вариантах осуществления, пептиды или пептидные мимики представляют собой нацеленные на LHRH рецептор пептиды и нацеленные на ErbB2 (HER2) рецептор пептиды.
Примеры белков включают инсулин, трансферрин, фибриноген-гамма фрагмент, тромбоспондин, клаудин, аполипопротеин E, молекулы аффител, таких как, например, ABY-025, белки с анкириновым повтором, белки алкиринподобными повторами и синтетические пептиды.
В некоторых вариантах осуществления изобретения, конъюгаты белок-лекарственное средство-полимер включают широкий спектр цитоксинов в комбинации с маркерами клеточной поверхности для HER2, такие как пертузумаб или трастузумаб; для EGFR, такие как цетуксимаб; для CEA, такие как лабетузумаб; для CD20, такие как ритуксимаб; для VEGF-A, такие как бевацизумаб; или для CD-22, такие как эпратузумаб или велтузумаб.
В других вариантах осуществления изобретения, используемые в изобретении конъюгаты белок-лекарственное средство-полимер или конъюгаты белок-полимер включают комбинации двух или более распознающих молекул на основе белка, такие как, например, комбинация биспецифичных антител, нацеленных на EGF рецептор (EGFR) на опухолевых клетках и на CD3 и CD28 на T-клетках; комбинация антител или антитела, полученного из Fab, Fab2, scFv или фрагментов тяжелых цепей верблюжьего антитела, и пептидов или пептидных мимиков; комбинация антител или антитела, полученного из Fab, Fab2, scFv или фрагментов тяжелых цепей верблюжьего антитела, и белков; комбинация двух биспецифичных антител, таких как CD3 × CD19 плюс CD28 × CD22 биспецифичные антитела.
В таблице C ниже приведено большее количество примеров описанных в изобретении PBRM, которые подходят для конъюгирования с образованием конъюгатов полимер-лекарственное средство-белок или каркасных структур полимер-PBRM изобретения.

Связующие звенья (LD и LP)
Описанное выше лекарственное средство или PBRM соединено с полимерным носителем через связующее звено LD или Lp. В некоторых вариантах осуществления, связующее звено является биорасщепляемым/биоразлагаемым под воздействием условий внутри клетки, и в результате расщепления связующего звена высвобождается лекарственное средство или PBRM из полимерного звена во внутриклеточную среду.
Связующее звено представляет собой любой химический фрагмент, который способен связывать лекарственное средство или PBRM с главной цепью полимера с помощью химических связей, в результате чего лекарственноле средство или PBRM и полимер становятся взаимно химически связаными (например, ковалентно связанными) друг с другом. В некоторых вариантах осуществления, связующее звено включает фрагмент биоразлагаемого связующего звена (например, биоразлагаемую химическую связь, такую как эфирная или амидная связь).
В других вариантах осуществления, связующее звено LD или LP является биоразлагаемым под воздействием мягких условий, то есть, условий внутри клетки, которые отрицательно не влияют на активность лекарственного средства. Примеры подходящего фрагмента биоразлагаемого связующего звена включают дисульфидные связующие звенья, неустойчивые к действию кислот связующие звенья, неустойчивые к действию света связующие звенья, неустойчивые к действию пептидазы связующие звенья и неустойчивые к действию экстеразы связующие звенья.
В некоторых вариантах осуществления, связующее звено LD или LP является биоразлагаемым под воздействием восстановительных условий (например, дисульфидное связующее звено). В этом варианте осуществления, лекарственное средство или фрагмент PBRM связан с полимером через дисульфидную связь. Молекула связующего звена включает реакционно-способную химическую группу, которая может реагировать с лекарственным средством. Предпочтительными реакционно-способными химическими группами для реакции с лекарственным средством или фрагментом PBRM являются N-сукцинимидильные эфиры и N-сульфосукцинимидильные эфиры. Кроме того, молекула связующего звена включает реакционноспособную химическую группу, предпочтительно, дитиопиридильную группу, которая может реагировать с лекарственным средством с образованием дисульфидной связи. В некоторых вариантах осуществления, молекулы связующего звена включают, например, N-сукцинимидил 3-(2-пиридилдитио)пропионат (SPDP), N-сукцинимидил 4-(2-пиридилдитио)бутаноат (SPDB), N-сукцинимидил 4-(2-пиридилдитио)пентаноат (SPP), N-сукцинимидил-S-ацетилтиоацетат (SATA) и N-сукцинимидил-оксикарбонил-альфа-метил-альфа-(2-пиридилдитио)толуол или 2,5-диоксопирролидин-1-ил 4-(1-(пиридин-2-илдисульфанил)этил)бензоат (SMPT).
В других вариантах осуществления, биорасщепляемое связующее звено LD или LP является чувствительным к изменению величины pH, то есть, склонным к гидролизу при конкретных значениях pH. Обычно, чувствительное к изменению величины pH связующее звено является гидролизуемым при кислых условиях. Например, может быть использовано неустойчивое к действию кислот связующее звено, которое является гидролизуемым в лизасоме или эндосоме (например, гидразон, семикарбазон, тиосемикарбазон, цис-аконитовый амид, ортоэфир, ацеталь, кеталь, или другие подобные звенья). Такие связующие звенья являются относительно устойчивыми в условиях с нейтральным значением pH, таких как условия в крови, но являются нестабильными при величине pH ниже 5,5 или 5,0, приблизительной величине pH лизосомы. В конкретных вариантах осуществления, гидролизуемое связующее звено представляет собой тиоэфирное связующее звено (такое как, например, тиоэфир, присоединенный к терапевтическому средству с помощью ацилгидразоновой связи.
В других вариантах осуществления, связующее звено LD или LP является нейстойчивым к действию света и применяется на поверхности тела и во многих полостях тела, которые являются доступными для света. Кроме того, LD или LP является биорасщепляемым под действием инфракрасного излучения, которое может проникать через ткань. Соответственно, LDили LP применяют как на поверхности тела, так и в ткани.
В некоторых вариантах осуществления, связующее звено LD или LPявляется биорасщепляемым под воздействием расщепляющего вещества, которое присутствует во внутриклеточной среде (например, внутри лизосомы или эндосомы или ямки). Связующее звено может представлять собой, например, пептидильное связующее звено, которое расщепляется под воздействием внутриклеточных ферментов пептидазы или протеазы, включая, но этим не ограничивая, лизосомальную или эндосомальную протеазу.
В некоторых вариантах осуществления, связующее звено LD или LP расщепляется эстеразами. Эстеразами, присутстующими внутри или снаружи клеток, могут быть расщеплены только конкретные эфиры. Эфиры образуются путем реакции конденсации карбоновой кислоты и спирта. Простейшими сложными эфирами являются сложные эфиры, полученные с простейшими спиртами, такими как алифатические спирты и некрупные циклические и некрупные ароматические спирты.
В еще одних вариантах осуществления, связующее звено LD или LP не является биорасщепляемым, и лекарственное средство высвобождается в результате разрушения антитела. Смотрите, например, патент США № 7498298, содержание которого приводится в описании изобретения путем ссылки на него.
Обычно, связующее звено LD или LP является практически невосприимчивым к внеклеточной среде. Используемое в описании изобретения выражение "практически невосприимчивое к внеклеточной среде" в отношении связующего звена означает, что не более чем приблизительно 20%, обычно, не более чем приблизительно 15%, более характерно, не более чем приблизительно 10%, и еще более характерно, не более чем приблизительно 5%, не более чем приблизительно 3%, или не более чем приблизительно 1% связующих звеньев в образце конъюгата полимер-лекарственное средство расщепляются при нахождении конъюгата полимер-лекарственное средство во внеклеточной среде (например, в плазме) в течение 24 часов. Является или не является связующее звено практически невосприимчивым к внеклеточной среде, может быть определено, например, путем инкубирования конъюгата полимер-лекарственное средство с плазмой в течение заданного периода времени (например, 2, 4, 8, 16 или 24 часов) и затем определения количества свободного лекарственного средства, присутствующего в плазме.
В вариантах осуществления, связующее звено LD имеет структуру: -RL1-C(=O)-XD-MD1-YD-MD2-ZD-MD3-QD-MD4-, где RL1 соединен с атомом кислорода полимерного носителя и MD4 соединен с доставляемой молекулой лекарственного средства.
В вариантах осуществления, связующее звено LP имеет структуру:
LP представляет собой связующее звено, имеющее структуру: -RL2-C(=O)-XP-MP1-YP-MP2-ZP-MP3-QP-MP4-, где RL2 соединен с атомом кислорода полимерного носителя, и MP4 соединен с PBRM.
Например, каждый из RL1 и RL2 независимо отсутствует, представляет собой алкил, алкенил, алкинил, циклоалкил, гетероалкил, гетероалкенил, гетероалкинил, гетероциклоалкил, арил или гетероарил.
Например, каждый из RL1 и RL2 независимо отсутствует, представляет собой алкил, циклоалкил, гетероалкил или гетероциклоалкил.
Например, RL1 отсутствует.
Например, RL2 отсутствует.
Например, каждый из XD и XP независимо представляет собой -O-, -S-, -N(R1)-, или отсутствует, где R1 представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкил фрагмент, -C(=O)R1B, -C(=O)OR1B, -SO2R1B, или -N(R1)- представляет собой гетероциклоалкильный фрагмент, где R1B представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент.
Например, каждый из YD, YP, ZD, ZP, QD и QP независимо отсутствует или представляет собой фрагмент биоразлагаемого связующего звена, выбранного из группы, состоящей из -S-S-, -C(=O)O-, -C(=O)NR2-, -OC(=O)-, -NR2C(=O)-, -OC(=O)O-, -OC(=O)NR2-, -NR2C(=O)O-, -NR2C(=O)NR3-, -C(OR2)O-, -C(OR2)S-, -C(OR2)NR3-, -C(SR2)O-, -C(SR2)S-, -C(SR2)NR3-, -C(NR2R3)O-, -C(NR2R3)S-, -C(NR2R3)NR4-, -C(=O)S-, -SC(=O)-, -SC(=O)S-, -OC(=O)S-, -SC(=O)O-, -C(=S)S-, -SC(=S)-, -OC(=S)-, -C(=S)O-, -SC(=S)O-, -OC(=S)S-, -OC(=S)O-, -SC(=S)S-, -C(=NR2)O-, -C(=NR2)S-, -C(=NR2)NR3-, -OC(=NR2)-, -SC(=NR2)-, -NR3C(=NR2)-, -NR2SO2-, -NR2NR3-, -C(=O)NR2NR3-, -NR2NR3C(=O)-, -OC(=O)NR2NR3-, -NR2NR3C(=O)O-, -C(=S)NR2NR3-, -NR2NR3C(=S)-, -C(=NR4)NR2NR3-, -NR2NR3C(=NR4)-, -O(N=CR3)-, -(CR3=N)O-, -C(=O)NR2-(N=CR3)-, -(CR3=N)-NR2C(=O)-, -SO3-, -NR2SO2NR3-, -SO2NR2- и полиамида, где в каждом случае присутствия, R2, R3, и R4независимо представляет собой водород или алифатический, гетероалифатический, карбоциклический или гетероциклический фрагмент, или в каждом случае присутствия, -NR2- или -NR2NR3- представляет собой гетероциклоалкильный фрагмент.
Например, каждый из MD1, MD2, MD3, MD4, MP1, MP2, MP3 и MP4 независимо отсутствует или представляет собой фрагмент небиоразлагаемого связующего звена, выбранный из группы, состоящей из алкила, алкенил, алкинила, циклоалкила, гетероалкила, гетероалкенила, гетероалкинила, гетероциклоалкила, арила, гетероарила и их комбинации, и каждый из MD1, MD2, MD3, MP1, MP2 и MP3 необязательно содержит один или более -(C=O)-, но не содержит любой из упомянутых выше фрагментов биоразлагаемого связующего звена.
Например, каждый из MD1, MD2, MD3, MD4, MP1, MP2, MP3 и MP4 независимо представляет собой C1-6 алкил, C1-6 алкил-C(O)-C0-6алкил, C1-6 алкил-NH-C0-6 алкил, C1-6 алкил-O-C0-6 алкил, C1-6 алкил-S-C0-6 алкил, C1-6 алкил-C(O)-C1-6 алкил-NH, C1-6 алкил-C(O)-C1-6 алкил-O, C1-6 алкил-C(O)-C1-6 алкил-S, C3-10 циклоалкил-C(O)-C0-6 алкил, 3-19 членный гетероциклоалкил-C(O)-C0-6 алкил, арил-C(O)-C0-6 алкил, (CH2CH2O)1-12 и другие подобные фрагменты.
Например, для каждого LD, MD1 не отсутствует, когда XD отсутствует.
Например, для каждого LP, MP1 не отсутствует, когда XP отсутствует.
Например, для каждого LD, по меньшей мере, один из XD, YD, ZD и QD не отсутствует.
Например, для каждого LP, по меньшей мере, один из XP, YP, ZP и QP не отсутствует.
Например, каждый из MD1 и MP1 независимо представляет собой C1-6 алкил или C1-6 гетероалкил.
Например, каждый из MD2, MD3, MD4, MP2, MP3 и MP4 независимо отсутствует, представляет собой C1-6 алкил, циклоалкил, гетероалкил, гетероциклоалкил или их комбинацию.
Например, для каждого LD, не более чем два из MD2, MD3 и MD4 отсутствуют.
Например, для каждого LP, не более чем два из MP2, MP3 и MP4 отсутствуют.
Например, для каждого LD, один из MD2 и MD3 имеет одну из следующих структур:



где q представляет собой целое число от 0 до 12, и каждый из p и t независимо представляет собой целое число от 0 до 3, и другой из MD2 или MD3 либо отсутствует, либо представляет собой фрагмент, отличающийся от приведенного выше, такого как C1-6 алкил.
Например, для каждого LP, один из MP2 и MP3 имеет одну из следующих структур:


где q представляет собой целое число от 0 до 12, и каждый из p и t независимо представляет собой целое число от 0 до 3, и другой из MP2 или MP3 либо отсутствует, либо представляет собой фрагмент, отличающийся от приведенного выше, такого как C1-6 алкил.
Например, p представляет собой 2.
Например, q представляет собой 0 или 12.
Например, t представляет собой 0 или 1.
Например, каждый из -MD2-ZD-, -ZD-MD3-, -ZD-MD2- или -MD3-ZD- независимо имеет одну из следующих структур:



где кольцо A или B независимо представляет собой циклоалкил или гетероциклоалкил; RW представляет собой алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент; R1J представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент; и кольцо D представляет собой гетероциклоалкил.
Например, каждый из -MP2-ZP-, -ZP-MP3-, -ZP-MP2- и -MP3-ZP- независимо имеет одну из следующих структур:


где кольцо A представляет собой циклоалкил или гетероциклоалкил, и R1J представляет собой водород, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент.
Например, кольцо A представляет собой 5-19 членный гетероциклоалкил, например,
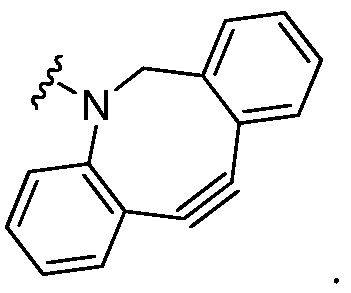
Например, кольцо A представляет собой C3-8 циклоалкил.
Например, кольцо D представляет собой пиперазинил или пиперидинил.
Например, RW представляет собой C1-6 алкил.
Например, R1J представляет собой водород или C1-6 алкил.
Например, ZD представляет собой

Например, ZP представляет собой

Например, XD отсутствует, представляет собой O или NH.
Например, XP отсутствует, представляет собой O или NH.
Например, каждый из XD и XP независимо представляет собой

Например, каждый из YD и YP независимо представляет собой -S-S-, -OCO-, -COO-, -CONH- или -NHCO-.
Например, каждый из QD и QP независимо отсутствует, представляет собой -S-S-, -OCO-, -COO-, -CONH-, -NHCO-, -OCONHNH- или -NHNHCOO-.
Например, -LD-D может иметь одну из приведенных ниже структур, где изображенная волнистой линией связь обозначает, что D (то есть лекарственное средство) либо присоединено к функциональному связующему звену непосредственно, либо через другой фрагмент:
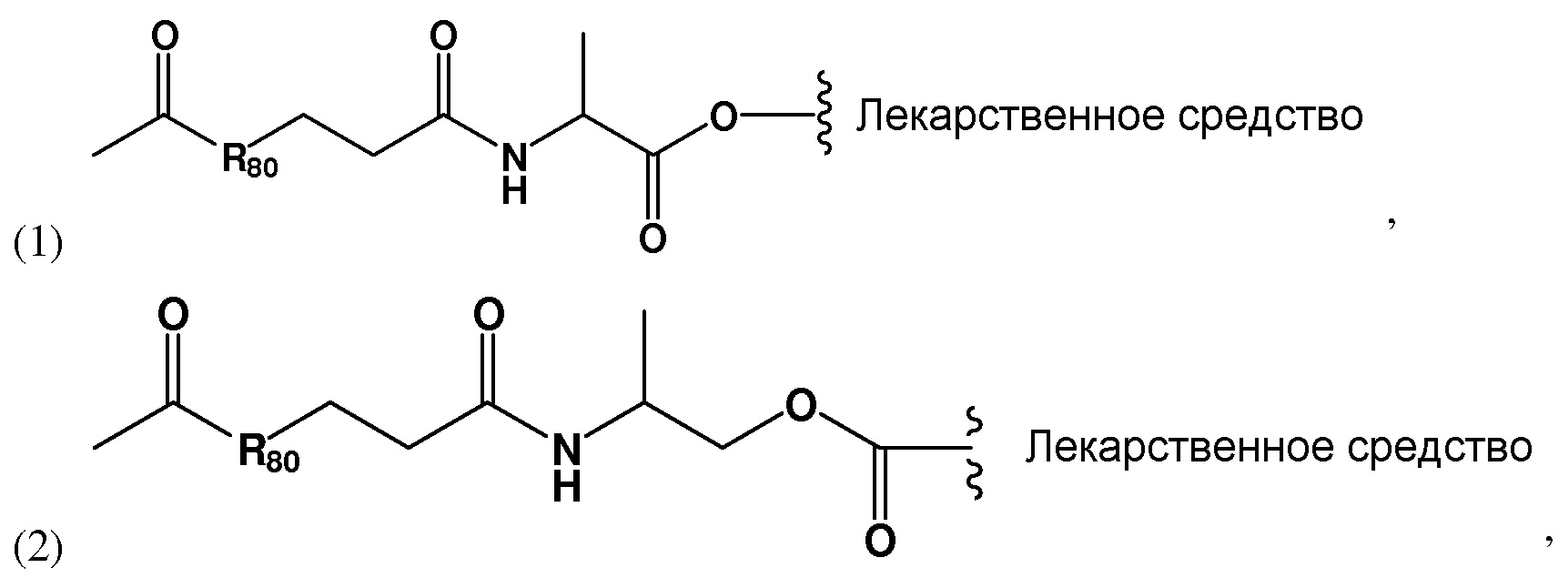
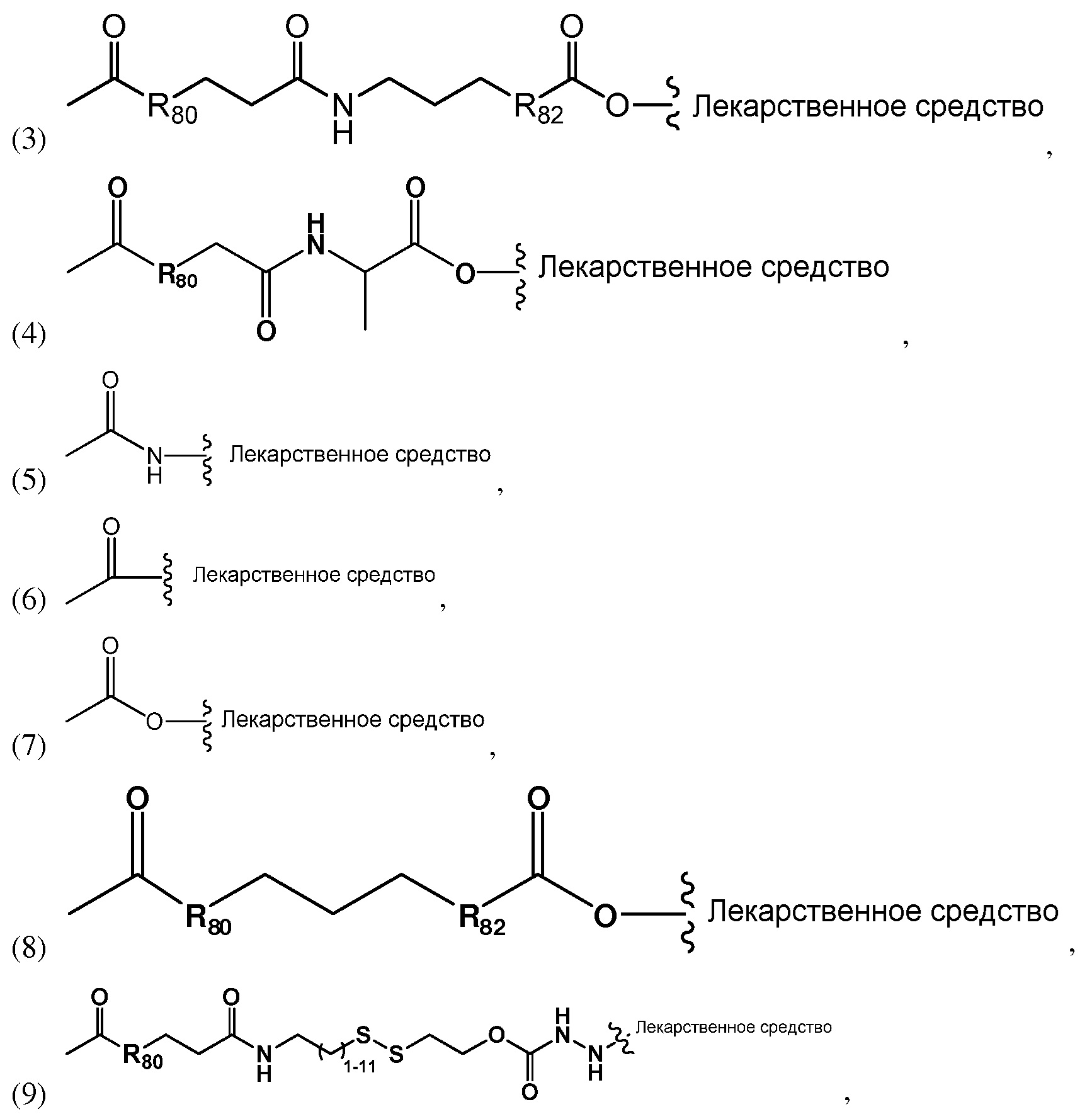




где R80 представляет собой CH2, -NH, или кислород; и
R82 представляет собой -NH или кислород.
Например, полимерный носитель-LP-PBRM может иметь одну из приведенных ниже структур:





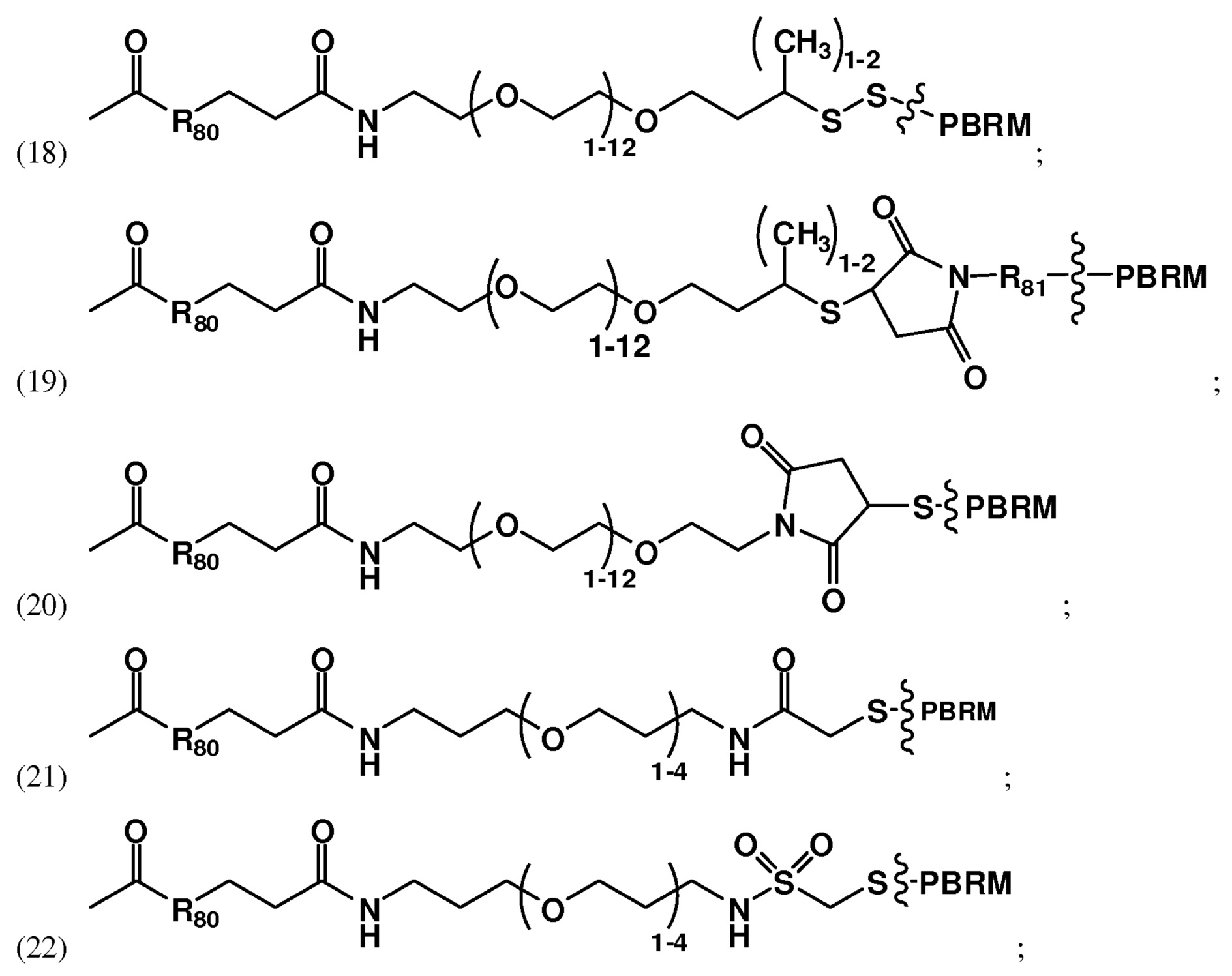
где:
R80 представляет собой CH2, NH или кислород;
R81 представляет собой

Несмотря на то, что в изобретении предпочтительно использовать биорасщепляемые связующие звенья, тем не менее, может быть также использовано и бионерасщепляемое связующее звено для образования описанного выше конъюгата. Бионерасщепляемое связующее звено представляет собой любой химический фрагмент, который способен связывать лекарственное средство или PBRM с полимером устойчивой ковалентной связью. Так, бионерасщепляемые связующие звенья являются практически устойчивыми к расщеплению, вызываемому кислотой, к расщеплению, вызываемому светом, к расщеплению, вызываемому пептидазой, к расщеплению, вызываемому эестеразой, и/или расщеплению дисульфидной связи, в условиях, при которых лекарственное средство или полимер остается активным.
В одном варианте осуществления, существенное количество фрагмента лекарственного средства не высвобождается в результате расщепления из конъюгата до тех пор, пока конъюгат белок-полимер-лекарственное средство не проникнет в клетку с рецептором клеточной поверхности, специфичным для PBRM конъюгата белок-полимер-лекарственное средство, и фрагмент лекарственного средства высвобождается в результате расщепления из конъюгата белок-полимер-лекарственное средство, когда конъюгат белок-полимер-лекарственное средство не проникает в клетку.
В другом варианте осуществления, биодоступность конъюгата белок-полимер-лекарственное средство или внутриклеточного метаболита конъюгата белок-полимер-лекарственное средство у субъекта повышается по сравнению с лекарственным соединением или конъюгатом, включающим фрагмент лекарственного средства конъюгата белок-полимер-лекарственное средство, или по сравнению с соединением, не имеющим фрагмента лекарственного средства.
В другом варианте осуществления, фрагмент лекарственного средства высвобождается в результате расщепления внутри клетки у субъекта из конъюгата белок-полимер-лекарственное средство или внутриклеточного метаболита конъюгата белок-полимер-лекарственное средство.
Конъюгаты или полимерные каркасные структуры
Конъюгаты изобретения включают одно или более присутствующих D, где D представляет собой терапевтическое средство, например, лекарственное средство, где одно или более из присутствующих D могут быть одинаковыми или различными.
В других конкретных вариантах осуществления, одна или более из присутствующих PBRM присоединены к полимерному носителю, где одна или более из присутствующих PBRM могут быть одинаковыми или различными. В других конкретных вариантах осуществления, один или более полимерных носителей, которые содержат одно или более из присутствующих D, соединены с PBRM (например, антителом).
Как уже обсуждалось в более общем виде выше, в конкретных вариантах осуществления, каждый полимерный носитель независимо имеет от приблизительно 0,1 до приблизительно 25% мономеров, включающих D, более предпочтительно, от приблизительно 0,5 до приблизительно 20%, более предпочтительно, от приблизительно 1 до приблизительно 15%, и еще более предпочтительно, от приблизительно 2 до приблизительно 10%.
В конкретных вариантах осуществления, конъюгат этого изобретения имеет формулу (I):
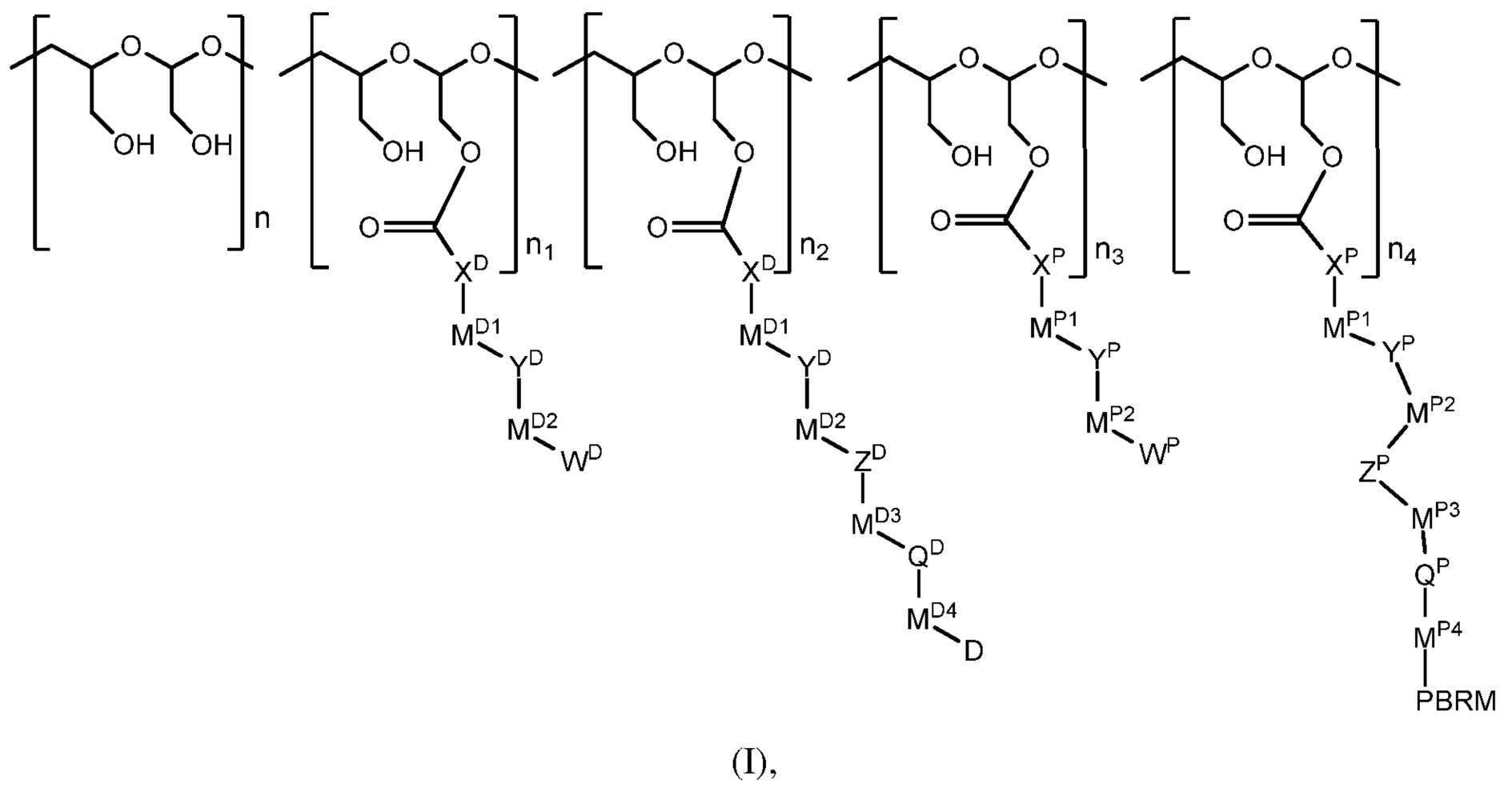
где:
каждый из n, n1, n2, n3 и n4 представляет собой мольную долю соответствующего полимерного звена, изменяющуюся от 0 до 1; n + n1 + n2 + n3+ n4=1; при условии, что ни один из n, n2 и n4 не равен 0.
Например, соотношение между n2 и n4 составляет больше чем 1:1 и ≤200:1.
Например, соотношение между n2 и n4 находится в диапазоне от 10:1 до 50:1.
Например, соотношение между n2 и n4 находится в диапазоне от 30:1 до 50:1.
Например, соотношение между n2 и n4составляет приблизительно 50:1, 25:1, 10:1, 5:1 или 2:1.
В конкретных вариантах осуществления, конъюгаты получают в несколько стадий. Эти стадии включают (1) модифицирование полимера, для того чтобы он содержал функциональную группу, которая может реагировать с функциональной группой лекарственного средства или его производного; (2) реакцию модифицированного полимера с лекарственным средством или его производным для связывания лекарственного средства с полимером; (3) модифицирование конъюгата полимер-лекарственное средство, для того чтобы полимер содержал функциональную группу, которая может реагировать с функциональной группой PBRM или ее производным; и (4) реакцию конъюгата модифицированный полимер-лекарственное средство с PBRM или ее производным с получением конъюгата этого изобретения. Стадия (3) может быть опущена, если модифицированный полимер, полученный на стадии (1), содержит функциональную группу, которая может реагировать с функциональной группой PBRM или ее производным.
В другом варианте осуществления, конъюгаты получают в несколько стадий: (1) модифицированием полимера, для того чтобы он содержал функциональную группу, которая может реагировать с функциональной группой первого лекарственного средства или его производного; (2) реакцией модифицированного полимера с первым лекарственным средством или его производным для связывания первого лекарственного средства с полимером; (3) модифицированием конъюгата полимер-лекарственное средство, для того чтобы он содержал другую функциональную группу, которая может реагировать с функциональной группой второго лекарственного средства или его производным (4) реакцией конъюгата модифицированный полимер-лекарственное средство со вторым лекарственным средством или его производным для связывания второго лекарственного средства с конъюгатом полимер-лекарственное средство; (5) модифицированием конъюгата полимер-лекарственное средство, содержащего 2 различных лекарственных средства, для того чтобы полимер содержал функциональную группу, которая может реагировать с функциональной группой PBRM или ее производным; и (6) реакцией модифицированного конъюгата полимер-лекарственное средство со стадии (5) с PBRM или ее производным с получением конъюгата этого изобретения. Стадии (5) и (6) могут быть повторены, если 2 различных PBRM или их производные конъюгируют для получения конъюгата полимер-лекарственное средство, включающего два различных лекарственных средства и две различных PBRM.
В еще одном варианте осуществления, конъюгаты получают в несколько стадий. Эти стадии включают (1) модифицирование полимера, для того чтобы он содержал функциональную группу, которая может реагировать с функциональной группой лекарственного средства или его производного; (2) дополнительное модифицирование полимера, для того чтобы он также содержал функциональную группу, которая может реагировать с функциональной группой PBRM или ее производным; (3) реакцию модифицированного полимера с лекарственным средством или его производным для связывания лекарственного средства с полимером; и (4) реакцию конъюгата модифицированный полимер-лекарственное средство с PBRM или ее производным с получением конъюгата этого изобретения. Последовательность стадий (1) и (2) или последовательность стадий (3) и (4) может быть изменена. Кроме того, либо стадия (1), либо стадия (2), может быть опущена, если модифицированный полимер содержит функциональную группу, которая может реагировать как с функциональной группой лекарственного средства или его производных, так и с функциональной группой PBRM или ее производной.
В другом варианте осуществления, конъюгаты получают в несколько стадий: (1) модифицированием полимера, для того чтобы он содержал функциональную группу, которая может реагировать с функциональной группой лекарственного средства или его производного; (2) дополнительным модифицированием полимера, для того чтобы он содержал функциональную группу, которая может реагировать с функциональной группой PBRM или ее производным; (3) реакцией модифицированного полимера с первым лекарственным средством или его производным для связывания первого лекарственного средства с полимером; (4) модифицированием конъюгата полимер-лекарственное средство, того чтобы он содержал функциональную группу, которая может реагировать с функциональной группой второго лекарственного средства или его производного (5) реакцией конъюгата модифицированный полимер-лекарственное средство со вторым лекарственным средством или его производным для связывания второго лекарственного средства с конъюгатом полимер-лекарственное средство; (6) реакцией конъюгата модифицированный полимер-лекарственное средство, содержащего 2 различных лекарственных средства, для того чтобы полимер с PBRM или ее производным образовал конъюгат этого изобретения. Стадия (6) может быть повторена, если 2 различных PBRM или их производные конъюгируют для получения конъюгата полимер-лекарственное средство, включающего два различных лекарственных средства и две различных PBRM. Стадия (4) может быть проведена после стадии (1), для того чтобы модифицированный полимер содержал две различных функциональных группы, которые могут реагировать с двумя различными лекарственными средствами или их производными. В этом варианте осуществления, модифицированный полимер, содержащий две различных функциональных группы, которые могут реагировать с двумя различными лекарственными средствами или их производными, может быть дополнительно модифицирован, для того чтобы он содержал функциональную группу, которая может реагировать с функциональной группой PBRM или ее производным; перед реакцией модифицированного полимера либо с двумя различными лекарственными средствами (стадия (3) и стадия (5)), либо с PBRM (стадия (6)).
Биоразлагаемые биологически совместимые конъюгаты изобретения могут быть получены при удовлетворении необходимых требований биоразлагаемости и гидрофильности. Например, при физиологических условиях, может достигаться соотношение между биоразлагаемостью и стабильностью. Например, известно, что в отличие от малых молекул, молекулы с молекулярными массами выше определенной пороговой величины (обычно, выше 40-100 кДа, в зависимости от физической формы молекулы) не выводятся через почки, и могут быть выведены из организма только в результате усвоения клетками и разложения во внутриклеточных компартментах, главным образом, в лизосомах. Это наблюдение является примером того, как могут создаваться функционально стабильные, но и биоразлагаемые материалы путем модулирования их стабильности при обычных физиологических условиях (pH=7,5±0,5) и при лизосомальной величине pH (pH около 5). Например, известно, что гидролиз ацетальных и кетальных групп катализируется кислотами, следовательно, полиали обычно будут менее стабильны в кислотной лизосомальной среде, чем, например, в плазме крови. Можно провести испытание для сравнения профиля разложения полимера, например, при pH=5 и pH=7,5 при 37°C в водной среде, и в результате определить ожидаемое соотношение для стабильности полимера в нормальной физиологической среде и в "дигестивном" лизосомальном компартменте после усвоения клетками. Целостность полимера в таких испытаниях может быть измерена, например, с помощью эксклюзивной ВЭЖХ. Любой специалист в этой области может выбрать другие подходящие методы для изучения различных фрагментов разрушенных конъюгатов этого изобретения.
Во многих случаях будет предпочтительным, если при pH 7,5 эффективный размер полимера не будет заметно изменяться в течение от 1 до 7 дней и оставаться в пределах 50% от исходного размера, по меньшей мере, в течение нескольких недель. С другой стороны, предпочтительно, чтобы при pH 5 полимер заметно разрушался в течение от 1 до 5 дней и полностью превращался в фрагменты с низкой молекулярной массой в течение от двух недель до нескольких месяцев. Несмотря на то, что в некоторых случаях может быть предпочтительным более быстрое разложение полимера, тем не менее, обычно более желательно, чтобы полимер разлагался в клетках со скоростью, которая не превышает скорость метаболизма или экскреции фрагментов полимера клетками. Соответственно, в конкретных вариантах осуществления, ожидается, что конъюгаты настоящего изобретения будут биоразлагаемыми, в частности, при усвоении клетками, и относительно "инертными" в отношении биологических систем. Предпочтительно, чтобы продукты разложения носителя были незаряжены и значительно не изменяли pH среды. Предполагается, что обилие спиртовых групп может обеспечить низкую скорость распознавания полимера клеточными рецепторами, в частности, фагоцитами. Главные цепи полимера настоящего изобретения обычно содержат немного, если они присутствуют, антигенных детерминант (характерных, например, для некоторых полисахаридов и полипептидов) и обычно не включают жесткие структуры, способные участвовать во взаимодействиях типа "ключ-замок" in vivo, если эти взаимодействия не являются желательными. Так, ожидается, что растворимые, сшитые и твердые конъюгаты этого изобретения имеют низкую токсичность и биоадгезию, что делает их подходящими для ряда биомедицинских применений.
В конкретных вариантах осуществления настоящего изобретения, биоразлагаемые биологически совместимые конъюгаты могут образовывать линейные или разветвленные структуры. Например, биоразлагаемые биологически совместимые полиальные конъюгаты настоящего изобретения могут быть хиральными (оптически активными). Необязательно, но биоразлагаемые биологически совместимые полиальные конъюгаты настоящего изобретения могут быть скалемическими.
В конкретных вариантах осуществления, конъюгаты изобретения являются водорастворимыми. В конкретных вариантах осуществления, конъюгаты изобретения являются водонерастворимыми. В конкретных вариантах осуществления, конъюгат изобретения находится в твердой форме. В конкретных вариантах осуществления, конъюгаты изобретения являются коллоидами. В конкретных вариантах осуществления, конъюгаты изобретения находятся в форме частиц. В конкретных вариантах осуществления, конъюгаты изобретения находятся в форме геля.
Это изобретение также раскрывает полимерную каркасную структуру, применяемую для конъюгирования с PBRM для образования описанного в изобретении конъюгата полимер-лекарственное средство-PBRM. Каркасная структура включает полимерный носитель, одие или более -LD-D, соединенный с полимерным носителем, и одно или более LP, соединенное с полимерным носителем, которое подходит для соединения PBRM с полимерным носителем, где:
в каждом случае присутствия, D представляет собой независимо терапевтическое средство, имеющее молекулярную массу ≤5 кДа;
полимерный носитель представляет собой полиацеталь или поликеталь,
LD представляет собой связующее звено, имеющее структуру:


LD1 представляет собой карбонилсодержащий фрагмент;
LP представляет собой связующее звено, отличающееся от LD и имеющее структуру: -RL2-C(=O)-LP1, где RL2 соединен с атомом кислорода полимерного носителя, и LPподходит для прямого или непрямого присоединения к PBRM;
каждый из RL1 и RL2 независимо отсутствует, представляет собой алкил, гетероалкил, циклоалкил, или гетероциклоалкил; и
LP1 представляет собой фрагмент, содержащий функциональную группу, которая способна образовывать ковалентную связь с функциональной группой PBRM.
Например, LP представляет собой связующее звено, имеющее структуру:


Например, функциональную группу для LP1 или LP2 выбирают из -SRP, -S-S-LG, малеимидо и галогена, где LG представляет собой уходящую группу, и RP представляет собой H или защитную группу для серосодержащей группы.
Например, LD1 включает -X-(CH2)v-C(=O)-, где X непосредственно присоединен к карбонильной группе RL1-C(=O), где X представляет собой CH2, O или NH, и v представляет собой целое число от 1 до 6.
Например, LP1 или LP2 содержит биоразлагаемую химическую связь.
Например, каждый из RL1 и RL2 отсутствует.
Например, полимерный носитель каркасной структуры изобретения представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу немодифицированного PHF) от приблизительно 2 кДа до приблизительно 300 кДа. Выбор полимерного носителя с конкретным диапазоном молекулярной массы может зависеть от размера PBRM, которую предполагается конъюгировать.
Например, для конъюгирования PBRM, имеющей молекулярную массу 40 кДа или более (например, 80 кДа или более), полимерный носитель каркасной структуры изобретения представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу немодифицированного PHF) от приблизительно 2 кДа до приблизительно 40 кДа (например, приблизительно 6-20 кДа или приблизительно 8-15 кДа).
Например, для конъюгирования PBRM, имеющей молекулярную массу 200 кДа или менее (например, 80 кДа или менее), полимерный носитель каркасной структуры изобретения представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу немодифицированного PHF) от приблизительно 20 кДа до приблизительно 300 кДа (например, приблизительно 40-150 кДа или приблизительно 50-100 кДа).
Например, каркасная структура имеет формулу (Ia):

где:
m представляет собой целое число от 1 до приблизительно 2200,
m1 представляет собой целое число от 1 до приблизительно 660,
m2 представляет собой целое число от 1 до приблизительно 300,
m3 представляет собой целое число от 1 до приблизительно 110, и
сумма m, m1, m2 и m3 составляет от приблизительно 15 до приблизительно 2200.
Например, когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от приблизительно 2 кДа до приблизительно 40 кДа (то есть, сумма m, m1, m2, и m3 составляет от приблизительно 15 до приблизительно 300), m2 представляет собой целое число от 1 до приблизительно 40, m3 представляет собой целое число от 1 до приблизительно 18, и/или m1 представляет собой целое число от 1 до приблизительно 140 (например, m1 составляет приблизительно 1-90).
Например, когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от приблизительно 6 кДа до приблизительно 20 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 45 до приблизительно 150), m2 представляет собой целое число от 2 до приблизительно 20, m3 представляет собой целое число от 1 до приблизительно 9, и/или m1 представляет собой целое число от 1 до приблизительно 75 (например, m1 составляет приблизительно 4-45).
Например, когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от приблизительно 8 кДа до приблизительно 15 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 60 до приблизительно 110), m2 представляет собой целое число от 2 до приблизительно 15, m3 представляет собой целое число от 1 до приблизительно 7, и/или m1 представляет собой целое число от 1 до приблизительно 55 (например, m1 составляет приблизительно 4-30).
Например, когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от 20 кДа до 300 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 150 до приблизительно 2200), m2 представляет собой целое число от 3 до приблизительно 300, m3 представляет собой целое число от 1 до приблизительно 110, и/или m1 представляет собой целое число от 1 до приблизительно 660 (например, m1 составляет приблизительно 10-250).
Например, когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от 40 кДа до 150 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 300 до приблизительно 1100), m2 представляет собой целое число от 4 до приблизительно 150, m3 представляет собой целое число от 1 до приблизительно 75, и/или m1 представляет собой целое число от 1 до приблизительно 330 (например, m1 составляет приблизительно 15-100).
Например, когда PHF в формуле (Ia) имеет молекулярную массу в диапазоне от приблизительно 50 кДа до приблизительно 100 кДа (то есть, сумма m, m1, m2 и m3 составляет от приблизительно 370 до приблизительно 740), m2 представляет собой целое число от 5 до приблизительно 100, m3 представляет собой целое число от 1 до приблизительно 40, и/или m1 представляет собой целое число от 1 до приблизительно 220 (например, m1 составляет приблизительно 15-80).
Например, каркасная структура дополнительно включает PBRM, соединенную с полимерным носителем через LP.
Например, одну или более PBRM соединяют с одним полимерным носителем, несущим лекарственное средство.
Например, каркасная структура (например, конъюгат PBRM-полимер-лекарственное средство) имеет формулу(Ib):

где:

m представляет собой целое число от 1 до приблизительно 2200,
m1 представляет собой целое число от 1 до приблизительно 660,
m2 представляет собой целое число от 3 до приблизительно 300,
m3 представляет собой целое число от 0 до приблизительно 110,
m4 представляет собой целое число от 1 до приблизительно 60; и
сумма m, m1, m2, m3 и m4 составляет от приблизительно 150 до приблизительно 2200.
Например, в формуле (Ib), m1 представляет собой целое число от приблизительно 10 до приблизительно 660 (например, приблизительно 10-250).
Например, когда PHF в формуле (Ib) имеет молекулярную массу в диапазоне от 40 кДа до 150 кДа (то есть, сумма m, m1, m2, m3 и m4 составляет от приблизительно 300 до приблизительно 1100), m2 представляет собой целое число от 4 до приблизительно 150, m3 представляет собой целое число от 1 до приблизительно 75, m4 представляет собой целое число от 1 до приблизительно 30, и/или m1 представляет собой целое число от 1 до приблизительно 330 (например, m1 составляет приблизительно 10-330 или приблизительно 15-100).
Например, когда PHF в формуле (Ib) имеет молекулярную массу в диапазоне от приблизительно 50 кДа до приблизительно 100 кДа (то есть, сумма m, m1, m2, m3 и m4 составляет от приблизительно 370 до приблизительно 740), m2 представляет собой целое число от 5 до приблизительно 100, m3 представляет собой целое число от 1 до приблизительно 40, m4 представляет собой целое число от 1 до приблизительно 20, и/или m1 представляет собой целое число от 1 до приблизительно 220 (например, m1 составляет приблизительно 15-80).
В качестве варианта или дополнительно, один или более полимерных носителей, несущих лекарственное средство, соединены с одной PBRM. Например, каркасная структура (например, конъюгат PBRM-полимер-лекарственное средство) включает PBRM с молекулярной массой более чем 40 кДа и один или более полимерных носителей, несущих D, соединенных с PBRM, где каждый из полимерных носителей, несущих D, независимо имеет формулу (Ic):

где:
терминальная

m представляет собой целое число от 1 до 300,
m1 представляет собой целое число от 1 до 140,
m2 представляет собой целое число от 1 до 40,
m3 представляет собой целое число от 0 до 18,
m4 представляет собой целое число от 1 до 10; и
сумма m, m1, m2, m3 и m4 изменяется от 15 до 300; при условии, что суммарное число LP2, присоединенных к PBRM, составляет 10 или менее.
Например, в формуле (Ic), m1 представляет собой целое число от 1 до приблизительно 120 (например, приблизительно 1-90) и/или m3 представляет собой целое число от 1 до приблизительно 10 (например, приблизительно 1-8).
Например, когда PHF в формуле (Ic) имеет молекулярную массу в диапазоне от приблизительно 6 кДа до приблизительно 20 кДа (то есть, сумма m, m1, m2, m3 и m4 изменяется от приблизительно 45 до приблизительно 150), m2 представляет собой целое число от 2 до приблизительно 20, m3 представляет собой целое число от 1 до приблизительно 9, и/или m1 представляет собой целое число от 1 до приблизительно 75 (например, m1 составляет приблизительно 4-45).
Например, когда PHF в формуле (Ic) имеет молекулярную массу в диапазоне от приблизительно 8 кДа до приблизительно 15 кДа (то есть, сумма m, m1, m2, m3 и m4 изменяется от приблизительно 60 до приблизительно 110), m2 представляет собой целое число от 2 до приблизительно 15, m3 представляет собой целое число от 1 до приблизительно 7, и/или m1 представляет собой целое число от 1 до приблизительно 55 (например, m1 составляет приблизительно 4-30).
В другом аспекте, изобретение раскрывает каркасную структуру, применяемую для конъюгирования, как с распознающей молекулой на основе белка (PBRM), так и с терапевтическим средством (D). D-несодержащая каркасная структура включает полимерный носитель, одно или более LP, соединенных с полимерным носителем, которые применяют для соединения PBRM с полимерным носителем, и один или более -RL1-C(=O)-LD1, соединенный с полимерным носителем через RL1, где:
полимерный носитель представляет собой полиацеталь или поликеталь,
RL1 соединен с атомом кислорода полимерного носителя,
LD1 представляет собой связующее звено, применяемое для соединения молекулы D к полимерному носителю, где в каждом случае присутствия, D представляет собой независимо терапевтическое средство, имеющее молекулярную массу ≤5 кДа;
LP представляет собой связующее звено, отличающееся от -RL1-C(=O)-LD1 и имеющее структуру: -RL2-C(=O)-LP1, где RL2 соединен с атомом кислорода полимерного носителя, и LP1 применяется для соединения с PBRM;
каждый из RL1 и RL2 независимо отсутствует, представляет собой алкил, гетероалкил, циклоалкил или гетероциклоалкил;
LD1 представляет собой фрагмент, содержащий функциональную группу, которая способна образовывать ковалентную связь с функциональной группой, принадлежащей D, и
LP1 представляет собой фрагмент, содержащий функциональную группу, которая способна образовывать ковалентную связь с функциональной группой, принадлежащей PBRM.
Например, D-несодержащая каркасная структура, применяемая для конъюгирования с PBRM и с D, может иметь одну или более из следующих характерных черт.
Например, LP представляет собой связующее звено, имеющее структуру:


Например, функциональную группу LP1 или LP2 выбирают из -SRP, -S-S-LG, малеимидо и галогена, где LG представляет собой уходящую группу, и RP представляет собой H или защитную группу для серосодержащей группы.
Например, LD1 включает -X-(CH2)V-C(=O)-, где X непосредственно присоединен к карбонильной группе RL1-C(=O), где X представляет собой CH2, O или NH, и v представляет собой целое число от 1 до 6.
Например, LP1 или LP2 содержит биоразлагаемую химическую связь.
Например, каждый из RL1 и RL2 отсутствует.
Например, полимерный носитель D-несодержащей каркасной структуры представляет собой полиацеталь, например, PHF, имеющий молекулярную массу (то есть, молекулярную массу немодифицированного PHF) от приблизительно 2 кДа до приблизительно 300 кДа.
D-несодержащая каркасная структура имеет формулу (Id):

где:
m представляет собой целое число от 1 до приблизительно 2200,
m1 представляет собой целое число от 1 до приблизительно 660,
m3 представляет собой целое число от 1 до приблизительно 110, и
сумма m, m1 и m3 изменяется от приблизительно 15 до приблизительно 2200.
Например, когда PHF в формуле (Id) имеет молекулярную массу в диапазоне от приблизительно 2 кДа до приблизительно 40 кДа (то есть, сумма m, m1 и m3 изменяется от приблизительно 15 до приблизительно 300), m3 представляет собой целое число от 1 до приблизительно 18, и/или m1 представляет собой целое число от 1 до приблизительно 140 (например, m1 составляет приблизительно 2-120).
Например, когда PHF в формуле (Id) имеет молекулярную массу в диапазоне от приблизительно 6 кДа до приблизительно 20 кДа (то есть, сумма m, m1 и m3 изменяется от приблизительно 45 до приблизительно 150), m3 представляет собой целое число от 1 до приблизительно 9, и/или m1 представляет собой целое число от 1 до приблизительно 75 (например, m1 составляет приблизительно 6-60).
Например, когда PHF в формуле (Id) имеет молекулярную массу в диапазоне от приблизительно 8 кДа до приблизительно 15 кДа (то есть, сумма m, m1 и m3 изменяется от приблизительно 60 до приблизительно 110), m3 представляет собой целое число от 1 до приблизительно 7, и/или m1 представляет собой целое число от 1 до приблизительно 55 (например, m1 составляет приблизительно 6-45).
Например, когда PHF в формуле (Id) имеет молекулярную массу в диапазоне от 20 кДа до 300 кДа (то есть, сумма m, m1 и m3 изменяется от приблизительно 150 до приблизительно 2200), m3 представляет собой целое число от 1 до приблизительно 110, и/или m1 представляет собой целое число от 1 до приблизительно 660 (например, m1 составляет приблизительно 13-550).
Например, когда PHF в формуле (Id) имеет молекулярную массу в диапазоне от 40 кДа до 150 кДа (то есть, сумма m, m1 и m3 изменяется от приблизительно 300 до приблизительно 1100), m3 представляет собой целое число от 1 до приблизительно 75, и/или m1 представляет собой целое число от 1 до приблизительно 330 (например, m1 составляет приблизительно 20-250).
Например, когда PHF в формуле (Id) имеет молекулярную массу в диапазоне от приблизительно 50 кДа до приблизительно 100 кДа (то есть, сумма m, m1 и m3 изменяется от приблизительно 370 до приблизительно 740), m3 представляет собой целое число от 1 до приблизительно 40, и/или m1 представляет собой целое число от 1 до приблизительно 220 (например, m1 составляет приблизительно 20-180).
Например, D-несодержащая каркасная структура дополнительно включает PBRM, соединенную с полимерным носителем через LP.
Например, одна или более PBRM соединены с одним D-несодержащим полимерным носителем.
Например, D-несодержащая каркасная структура имеет формулу (Ie):

где:

m представляет собой целое число от 1 до 2200,
m1 представляет собой целое число от 1 до 660,
m3 представляет собой целое число от 0 до 110,
m4 представляет собой целое число от 1 до приблизительно 60; и
сумма m, m1, m2, m3 и m4 изменяется от приблизительно 150 до приблизительно 2200.
Например, в формуле (Ie), m1 представляет собой целое число от приблизительно 10 до приблизительно 660 (например, приблизительно 14-550).
Например, когда PHF в формуле (Ie) имеет молекулярную массу в диапазоне от 40 кДа до 150 кДа (то есть, сумма m, m1, m3 и m4 изменяется от приблизительно 300 до приблизительно 1100), m3 представляет собой целое число от 1 до приблизительно 75, m4 представляет собой целое число от 1 до приблизительно 30, и/или m1 представляет собой целое число от 1 до приблизительно 330 (например, m1 составляет приблизительно 20-250).
Например, когда PHF в формуле (Ie) имеет молекулярную массу в диапазоне от приблизительно 50 кДа до приблизительно 100 кДа (то есть, сумма m, m1, m3 и m4 изменяется от приблизительно 370 до приблизительно 740), m3 представляет собой целое число от 1 до приблизительно 40, m4 представляет собой целое число от 1 до приблизительно 20, и/или m1 представляет собой целое число от 1 до приблизительно 220 (например, m1 составляет приблизительно 20-180).
В качестве варианта или дополнительно, один или более D-несодержащих полимерных носителей соединены с одной PBRM. Например, каркасная структура включает PBRM с молекулярной массой более чем 40 кДа и одним или более полимерными носителями, соединенными с PBRM, где каждый из полимерных носителей независимо имеет формулу (Ih):

где:
терминальная

m представляет собой целое число от 1 до 300,
m1 представляет собой целое число от 1 до 140,
m3 представляет собой целое число от 0 до 18,
m4 представляет собой целое число от 1 до 10; и
сумма m, m1, m3 и m4 изменяется от 15 до 300; при условии, что суммарное число LP2, присоединенных к PBRM, составляет 10 или менее.
Например, в формуле (Ih), m1 представляет собой целое число от 2 до приблизительно 130 (например, приблизительно 3-120) и/или m3 представляет собой целое число от 1 до приблизительно 10 (например, приблизительно 1-8).
Например, когда PHF в формуле (Ih) имеет молекулярную массу в диапазоне от приблизительно 6 кДа до приблизительно 20 кДа (то есть, сумма m, m1, m3 и m4 изменяется от приблизительно 45 до приблизительно 150), m3 представляет собой целое число от 1 до приблизительно 9, и/или m1 представляет собой целое число от 6 до приблизительно 75 (например, m1 составляет приблизительно 7-60).
Например, когда PHF в формуле (Ih) имеет молекулярную массу в диапазоне от приблизительно 8 кДа до приблизительно 15 кДа (то есть, сумма m, m1, m3 и m4 изменяется от приблизительно 60 до приблизительно 110), m3 представляет собой целое число от 1 до приблизительно 7, и/или m1 представляет собой целое число от 6 до приблизительно 55 (например, m1 составляет приблизительно 7-45).
Конъюгаты PBRM-лекарственное средство-полимер, несущие лекарственное средство полимерные каркасные структуры или несущие PBRM полимерные каркасные структуры могут быть очищены (то есть, могут быть удалены остаточные непрореагировавшие лекарственные средства, PBRM или исходные полимерные материалы) путем экстенсивной диафильтрации. В случае необходимости, для удаления любых агрегированных полимерных конъюгатов PBRM-лекарственное средство может быть проведена дополнительная очистка с помощью эксклюзионной хроматографии. Обычно, очищенные полимерные конъюгаты PBRM-лекарственное средство содержат < 5% агрегированных полимерных конъюгатов PBRM-лекарственное средство, определенных с помощью эксклюзионной хроматографии или электрофореза в полиакриламидом геле в присутствии додецилсульфата натрия; <1% конъюгата полимер-лекарственное средство, определенного с помощью эксклюзионной хроматографии, и <2% неконъюгированных PBRM, определенных с помощью высокоэффективной жидкостной хроматографии с обращенной фазой.
В таблицах D и E ниже приводятся примеры несущих лекарственное средство полимерных каркасных структур и конъюгатов полимер-лекарственное средство-белок изобретения, соответственно.











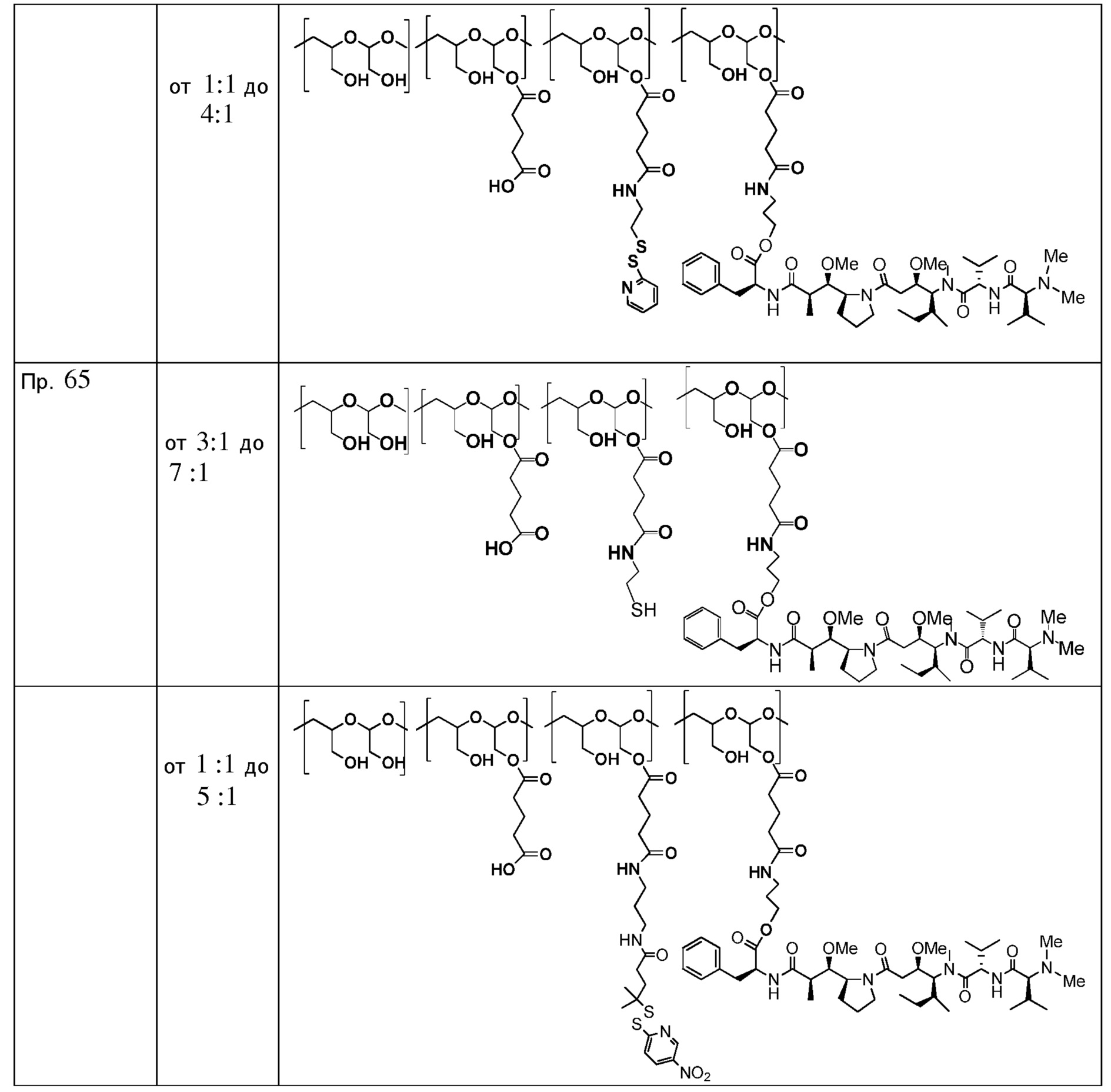













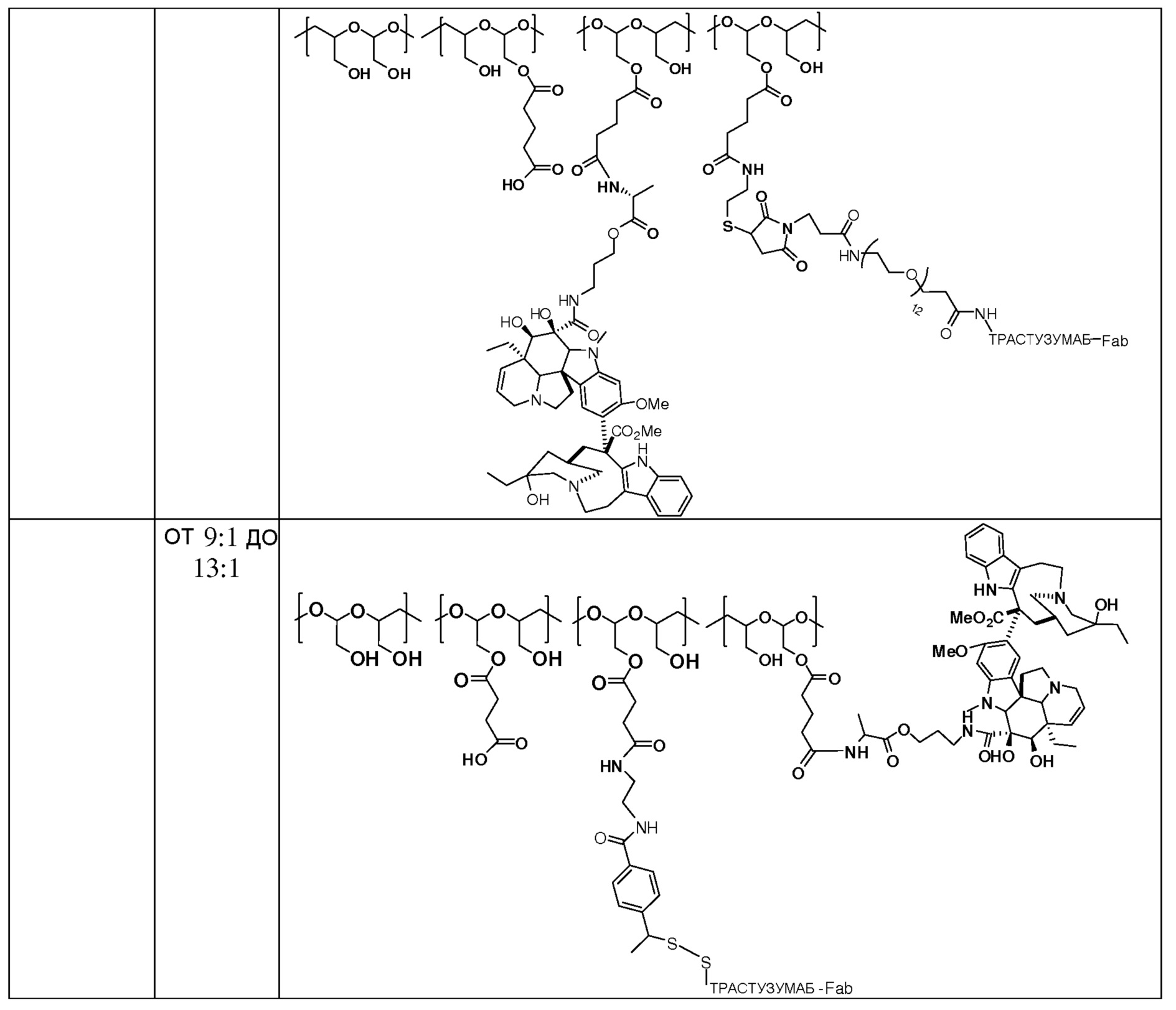
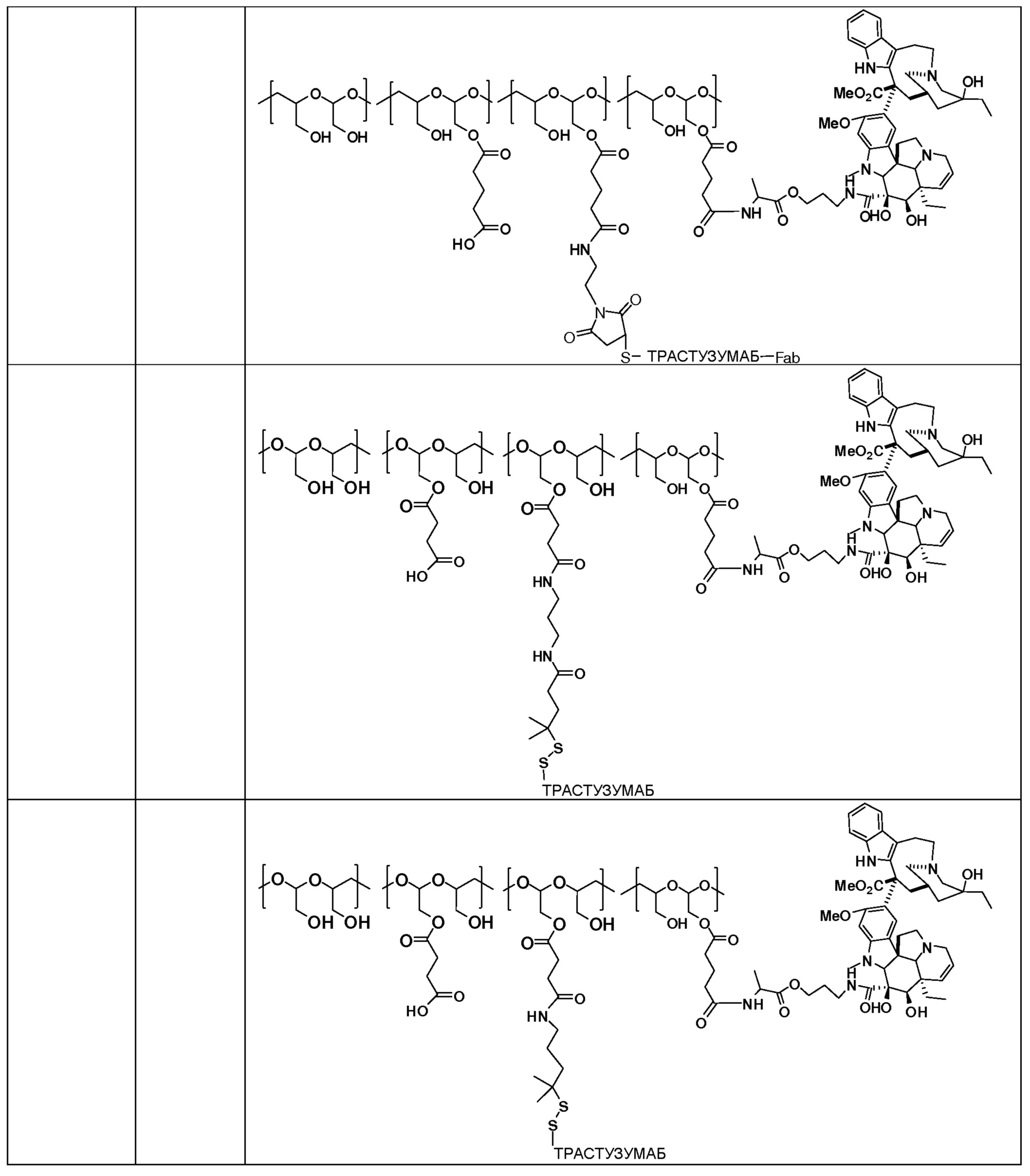







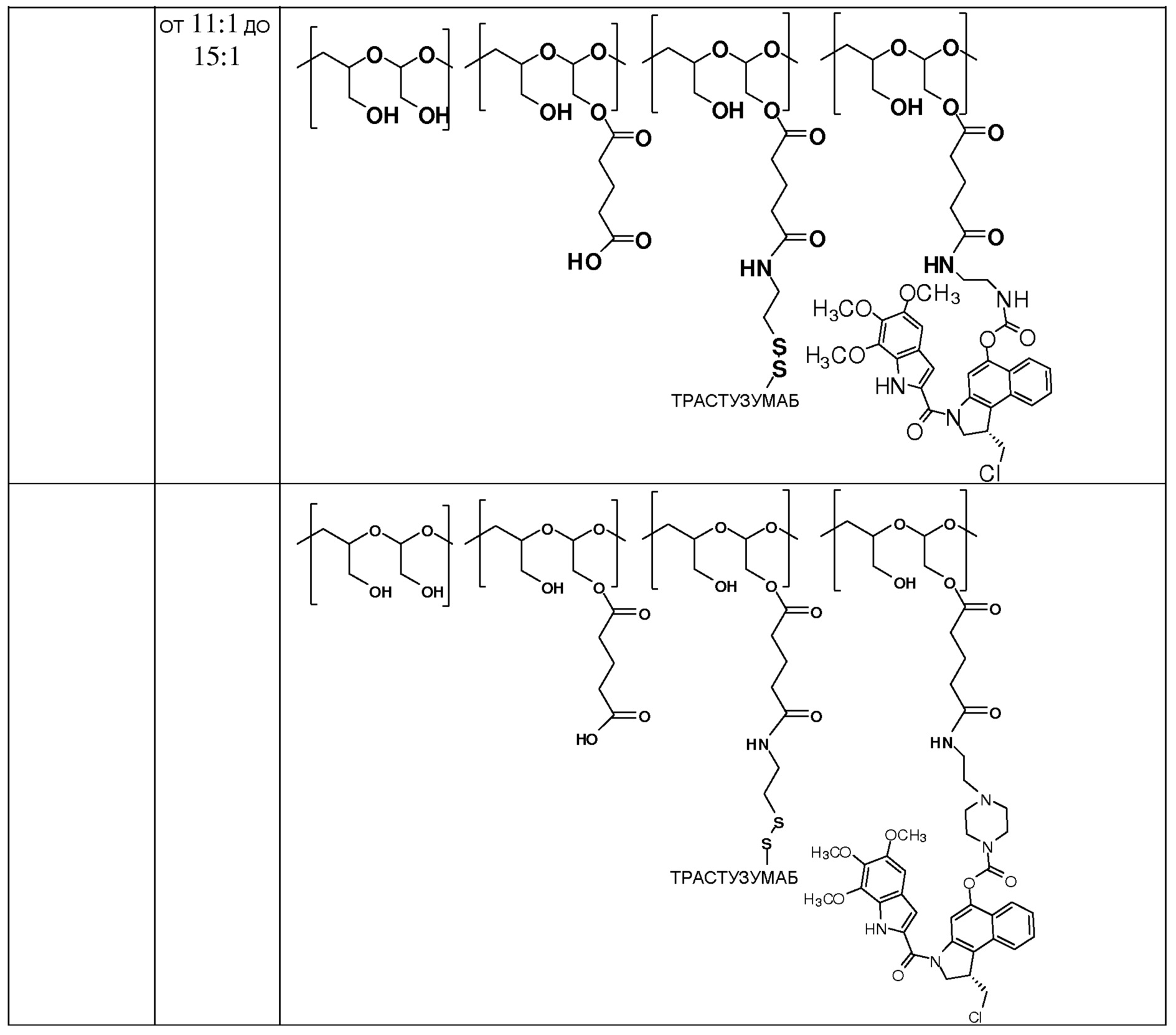
Методы синтеза
Согласно настоящему изобретению, могут быть использованы любые доступные методы для получения конъюгатов изобретения или содержащих их композиций и применяемых для их получения промежуточных соединений и компонентов (например, носителей и модификаторов). Например, могут быть использованы полусинтетические и полностью синтетические методы, такие как методы, подробно обсуждаемые ниже.
Носители
Методы получения полимерных носителей (например, биологически совместимых биоразлагаемых полимерных носителей), применяемых для конъюгирования с модтификаторами, известны в технике. Например, принципы синтеза можно найти в патентах США № 5811510, 5863990, 5958398, 7838619 и 7790150; и в патентном документе U.S. Publication No. 2006/0058512. Для специалиста в области синтеза полимеров является известным, как можно применить эти методы, для того чтобы получить полимерные носители, используемые при осуществлении изобретения.
Например, полусинтетические полиали могут быть получены из полиальдоз и поликетонов путем полного бокового расщепления углеводных колец с помощью периодата в водных растворах с последующей конверсией в гидрофильные фрагменты (например, путем восстановления боргидридом) для конъюгирования гидроксильных групп с одной или более молекулами лекарственного средства или PBRM с помощью связующего звена из дикарбоновой кислоты (например, связующего звена из глутаровой кислоты). В примере варианта осуществления, углеводные кольца подходящего полисахарида могут быть окислены с помощью гликоль-специфичных реагентов, что приводит к расщеплению связей углерод-углерод между углеродными атомами, каждый из которых соединен с гидроксильной группой. Пример применения этой методики к декстрану B-512 показан ниже:


Аналогичный подход может быть использован с леваном:

и инулином:

В приведенных выше схемах, волнистая связь указывает, что WD или WP соединены непосредственно, как показано, или через другой фрагмент, такой как MD2 или MP2, соответственно
В приведенных выше схемах, q' представляет собой целое число от 0 до 4; и в каждом случае присутствия, R2' представляет собой независимо водород, галоген, -CN, NO2, алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент, или -GRG1, где G представляет собой -O-, -S-, -NRG2-, -C(=O)-, -S(=O)-, -SO2-, -C(=O)O-, -C(=O)NRG2-, -OC(=O)-, -NRG2C(=O)-, -OC(=O)O-, -OC(=O)NRG2-, -NRG2C(=O)O-, -NRG2C(=O)NRG2-, -C(=S)-, -C(=S)S-, -SC(=S)-, -SC(=S)S-, -C(=NRG2)-, -C(=NRG2)O-, -C(=NRG2)NRG3-, -OC(=NRG2)-, -NRG2C(=NRG3)-, -NRG2SO2-, -NRG2SO2NRG3- или -SO2NRG2-, где в каждом случае присутствия, RG1, RG2 и RG3 представляет собой независимо водород, галоген или необязательно замещенный алифатический, гетероалифатический, карбоциклический или гетероциклоалкильный фрагмент.
В конкретных вариантах осуществления, в каждом случае присутствия, R2' представляет собой независимо водород, алкил, алкенил, алкинил, циклоалкил, гетероалкил, гетероалкенил, гетероалкинил, гетероциклоалкил, арил, гетероарил, -C(=O)R2A или -ZR2A, где Z представляет собой O, S, NR2B, где в каждом случае присутствия, R2A и R2B представляет собой независимо водород, или алкильный, алкенильный, алкинильный, циклоалкильный, гетероалкильный, гетероалкенильный, гетероалкинильный, гетероциклоалкильный, арильный или гетероарильный фрагмент. В конкретных вариантах осуществления, в каждом случае присутствия, R2 представляет собой водород. В конкретных вариантах осуществления, при одном или более случаях присутствия, R2' представляет собой C1-10алкильный фрагмент. В конкретных вариантах осуществления, при одном или более случаях присутствия, R2' представляет собой низший алкил. В конкретных вариантах осуществления, при одном или более случаях присутствия, R2' представляет собой гидрофобную группу. В конкретных вариантах осуществления, при одном или более случаях присутствия, R2' представляет собой гидрофильную группу. В конкретных вариантах осуществления, при одном или более случаях присутствия, R2' представляет собой анионную группу. В конкретных вариантах осуществления, при одном или более случаях присутствия, R2' представляет собой катаонную группу. В конкретных вариантах осуществления, при одном или более случаях присутствия, R2' представляет собой лиганд рецептора.
В одном варианте осуществления, метод получения биоразлагаемых биологически совместимых полиальных конъюгатов настоящего изобретения включает процесс, с помощью которого подходящий полисахарид смешивают с эффективным количеством гликоль-специфического окислителя с образованием промежуточного альдегидного соединения. Промежуточное альдегидное соединение, которое само по себе является полиалем, может затем быть восстановлено до соответствующего полиола, сукцинолированного и соединенного с одним или более подходящими модификаторами с образованием биоразлагаемого биологически совместимого полиального конъюгата, включающего сукцинамид-содержащие связи.
В другом предпочтительном варианте осуществления, полностью синтетические биоразлагаемые биологически совместимые полиалы для применения в настоящем изобретении могут быть получены реакцией подходящего инициатора с подходящим соединением-предшественником.
Например, полностью синтетические полиалы могут быть получены конденсацией виниловых эфиров с защищенными замещенными диолами. Могут быть использованы другие методы, такие как полимеризация с раскрытием кольца, в которых эффективность метода может зависеть от степени замещения и объемности защитных групп.
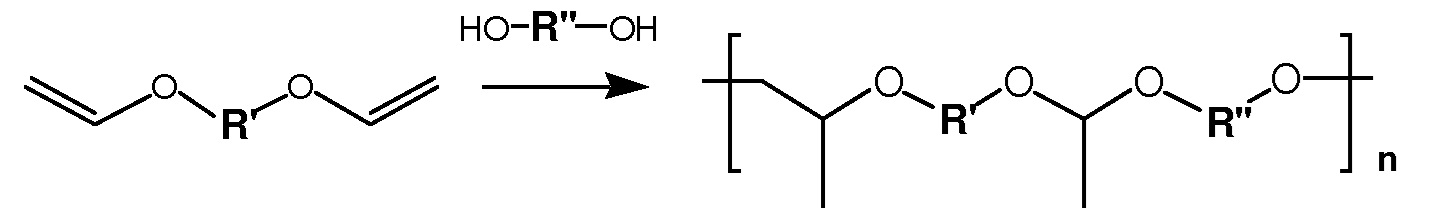
Для любого специалиста в этой области является очевидным, что для получения высокомолекулярных продуктов могут быть оптимизированы системы растворителей, катализаторы и другие факторы.
В конкретных вариантах осуществления, носитель представляет собой PHF.
Лекарственные средства и производные лекарственных средств
В конкретных вариантах осуществления, лекарственное средство может быть модифицировано перед конъюгированием с полимерным носителем. На схемах 1 и 2 показаны методы модифицирования алкалоида барвинка. На схеме 3 показан метод модифицирования производного неприродного камптотецина. На схеме 4 показан метод модифицирования ауристатина F. Большое число методов описаны в патентном документе US 2010/0305149, содержание которого приводится в описании изобретения путем ссылки на него.

Реакция C23 эфира алкалоида барвинка с гидразином и затем обработка с помощью NaNO2 дает в результате активный азидный эфир. Реакция азидного эфира с соединением амина, таким как пропаноламин или 1-аминопропан-2-ол, дает в результате производное алкалоида барвинка с функционализированным гидроксилом, которое может быть далее дериватизировано с помощью аминосодержащих соединений, таких как, например, производные аланина или метилаланина, для конъюгирования с полимерами (смотрите схему 1).
Схема 2

Обработка гидроксильного производного алкалоида барвинка с помощью защищенного аминосодержащего эфира, такого как третбутоксиэтерифицированная аминокислота, и затем гидролиз эфира в трифторуксусной кислоте (TFA) дает трифлатную соль алкалоида барвинка (схема 2). Конъюгирование алкалоида барвинка с функционализированными полимерами дает в результате конъюгаты лекарственное средство-полимер, которые могут быть затем конъюгированы с PBRM или ее производным с получением конъюгатов белок-лекарственное средство-полимер.
Схема 3

10-гидроксигруппу производного неприродного камптотецина, например, SN38, селективно защищают путем реакции производного с третбутилдифенилсилилхлоридом (TBDPSiCl) в присутствии триэтиламина. 20-гидроксигруппа может быть подвергнута реакции с третбутилкарбонилаланином с образованием производного аланина, используя методику, описанную в публикации Sapra, P. et al., Clin. Cancer Res., 14: 1888-1896 (2008). В качестве варианта, могут быть использованы другие аминокислоты, например, глицин. С первичного амина снимают защиту путем удаления Boc-защитной группы в результате обработки трифторуксусной кислотой, затем удаляют TBDPS-защитную группу с помощью фторида тетрабутиламмония (смотрите схему 3). Полученное аминодериватизированное соединение SN38 может быть конъюгировано с функционализированным полимером с образованием конъюгата лекарственное средство-полимер.
Схема 4

Обработка ауристатина F защищенным аминосодержащим эфиром, таким как третбутоксиэтерифицированный 2-гидроксипропиламин и затем гидролиз эфира в HCl дает 2-гидроксипропиламино производное ауристатина F (смотрите схему 4). Конъюгирование производного ауристатина F с функционализированными полимерами дает конъюгаты лекарственное средство-полимер, которые могут быть далее конъюгированы с PBRM или ее производным с образованием конъюгатов белок-полимер-лекарственное средство.
Конъюгаты или полимерные каркасные структуры
Общие методы получения конъюгатов или полимерных каркасных структур этого изобретения были описаны выше. На схемах 5-10 ниже приводятся примеры того, как синтезируют конъюгаты или полимерные каркасные структуры. Переменные (например, XD, XP, LD1 и LP2 и другие) в этих схемах определяются так же, как в описании изобретения, если не указано иначе. Каждый WD1 представляет собой функциональный фрагмент, который способен реагировать с WD с образованием ZD-MD3, и каждый WP1 представляет собой функциональный фрагмент, который способен реагировать с WP с образованием ZP-MP3. -XD-MD1-YD-MD2-WD и -XP-MP1-YP-MP2-WP могут быть различными (такими как в схемах 5 и 5 A) или одинаковыми (такими как в схеме 6). В некоторых вариантах осуществления, -XP-MP1-YP-MP2-WPполучают путем дополнительной модификации -XD-MD1-YD-MD2-WD.
Схема 5

Схема 5A

Схема 6

PBRM может быть связана с конъюгатом лекарственное средство-полимер с образованием конъюгата белок-лекарственное средство- полимер, используя стандартные синтетические методы для конъюгирования белка, включающие, но этим не ограничивая, реакции, основанные на восстановительном аминировании, лигировании по Штаудингеру, образовании оксима, образовании тиазолидина, и описанные в изобретении методы и реакции.
На схеме 7 ниже приведен синтез конъюгата PBRM-лекарственное средство-полимер, в котором PBRM связывают с конъюгатом лекарственное средство-полимер, используя "клик-химию" ("клик-реакции").
Схема 7

На схеме 8 ниже приведен синтез конъюгата PBRM-лекарственное средство-полимер, в котором PBRM связывают с конъюгатом лекарственное средство-полимер с помощью реакции Манниха.
Схема 8

На схеме 9 ниже приведен синтез конъюгата PBRM-лекарственное средство-полимер, в котором PBRM связывают с конъюгатом лекарственное средство-полимер с помощью катализируемой палладием реакции кросс-сочетания.
Схема 9
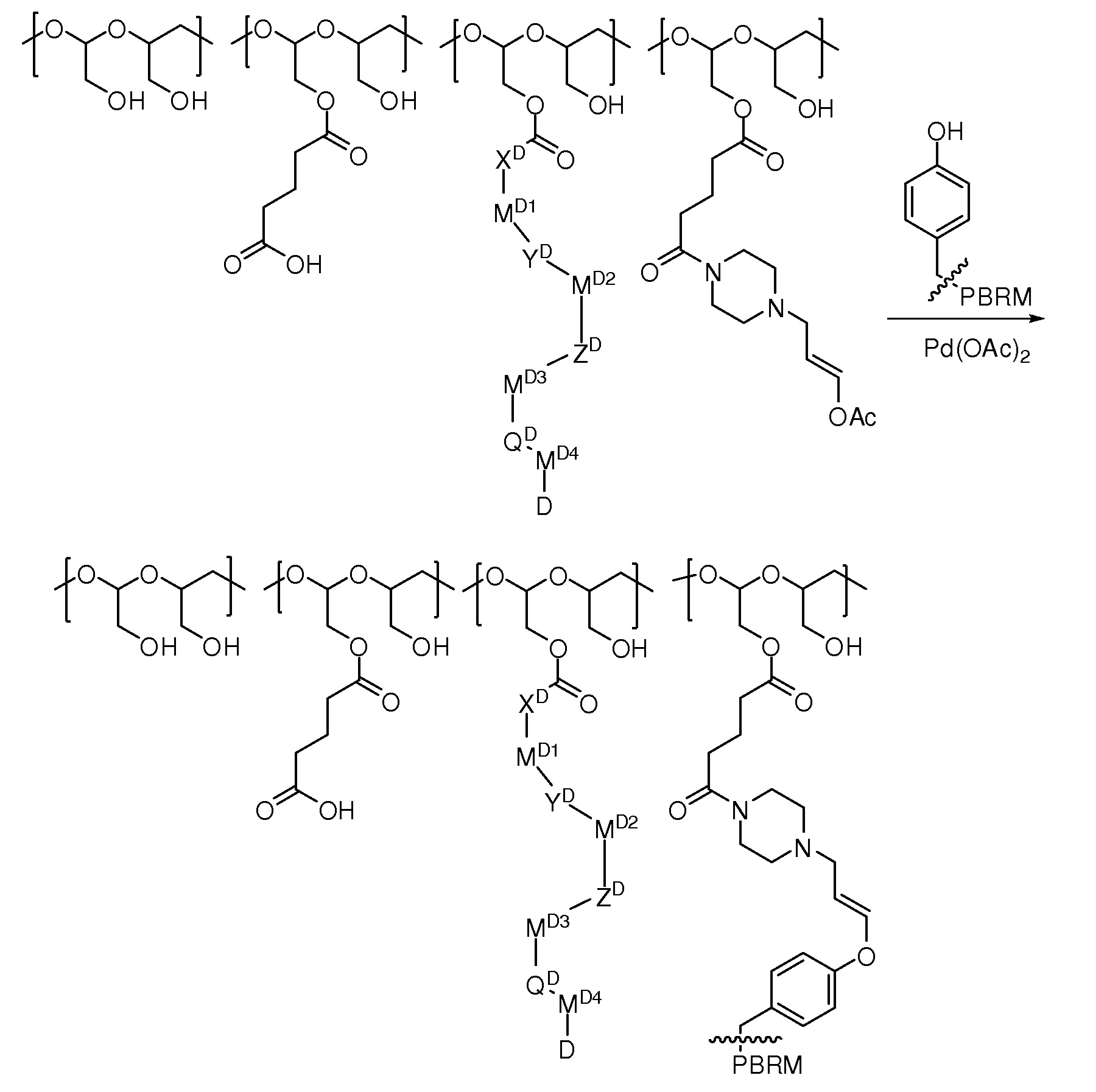
На приведенных выше схемах 7-9, обозначаемая волнистой линией связь указывает, что PBRM либо соединена с функциональным модификатором непосредственно, либо через другой фрагмент, такой как алкил, циклоалкил, арил и другие подобные фрагменты.
На схеме 10 ниже приведена общая схема синтеза получения полимерных каркасных структур изобретения. Обозначаемая волнистой линией связь указывает на наличие непосредственного или косвенного соединения между LD1 и D или LP2.
Схема 10

PBRM может быть присоединена к конъюгату лекарственное средство-полимер с образованием конъюгата белок-лекарственное средство-полимер, используя стандартные синтетические методы для конъюгирования белка, включающие, но этим не ограничивая, реакции, основанные на восстановительном аминировании, лигировании по Штаудингеру, образовании оксима, образовании тиазолидина, и описанные в изобретении методы и реакции.
Фармацевтические композиции
Изобретение также предлагает фармацевтические композиции, включающие один или более описанных в изобретении конъюгатов белок-полимер-лекарственное средство в приемлемом носителе, таком как стабилизатор, буфер и другие подобные вещества. Конъюгаты могут быть введены и внедрены субъекту с помощью стандартных способов вместе или без стабилизаторов, буферов и других подобных веществ, образующих фармацевтическую композицию. Введение может быть местным (в том числе офтальмическим и в мембраны слизистой оболочки, включая вагинальное и ректальное введение), пульмональным, например, путем ингаляции или инсуффляции порошков или аэрозолей, в том числе с помощью небулайзера; интратрахеальным, интраназальным, эпидермальным и трансдермальным, пероральным или парентеральным введением, в том числе внутривенной, внутриартериальной, подкожной, внутрибрюшинной или внутримышечной инъекцией или инфузией, или внутричерепным, например, интратекальным или интравентрикулярным введением. Конъюгаты могут быть приготовлены и применены в виде стерильных растворов и/или суспензий для инъекций, лиофилизированных порошков для растворения перед инъекцией/инфузией, композиций для местного применения, в виде таблеток, капсул или эликсиров для перорального введения, или суппозиториев для ректального введения, и в виде других известных в технике композиций.
Фармакологическая композиция или состав относится к композиции или составу в удобной для введения форме, например, для системного введения, в клетку или субъекту, включая, например, человека. Применение той или иной формы, отчасти, зависит от способа введения, например, перорального, ингаляционного, трансдермального или путем инъекции/инфузии. Такие формы не должны препятствовать достижению композицией или составом клетки-мишени (то есть, клетки, в которую требуется доставить лекарственное средство). Например, фармакологические композиции, инъецируемые в кровоток, должны быть растворимыми. Другими факторами, которые необходимо принимать во внимание, являются токсичность и формы, которые отрицательно влияют на проявление композицией или составом их лечебного действия.
Под "системным введением" подразумевают in vivo системную абсорбцию или аккумулирование модифицированного полимера в кровотоке, и затем распределение его по всему организму. Способы введения, которые приводят к системной абсорбции, включают, без ограничения: внутривенное, подкожное, внутрибрюшинное, ингаляционное, пероральное, внутрилегочное и внутримышечное введение. Каждый из этих способов введения позволяет подвергать доступную ткань, пораженную болезнью, воздействию модифицированных полимеров. Было показано, что скорость попадания активного средства в кровоток зависит от его молекулярной массы или размера. Применение конъюгата этого изобретения позволяет осуществлять целенаправленную доставку лекарственного средства в конкретные клетки, такие как раковые клетки, в результате специфичности PBRM.
"Фармацевтически приемлемый состав" обозначает композицию или состав, которые позволяют осуществлять эффективное распределение конъюгатов в их фактическом месте нахождения наиболее целесообразным образом с точки зрения их ожидаемой активности. В одном варианте осуществления, эффективная доставка происходит до очищения, осуществляемого ретикулоэндотелиальной системой, или продуцирования нецеленоправленного связывания, которое может приводить к снижению эффективности или к токсичности. Неограничивающие примеры средств, применяемых в композициях с конъюгатами, включают: ингибиторы P-гликопротеина (такие как Pluronic P85), которые могут усиливать поступление активных средств в ЦНС; биоразлагаемые полимеры, такие как микросферы поли(DL-лактид-когликолид) для доставки с замедленным высвобождением после интрацеребральной инплантации; и загруженные наночастицы, такие как наночастицы из полибутилцианоакрилата, которые могут доставлять активные средства через гематоэнцефалический барьер и могут изменять механизмы нейронного поглощения.
В объем изобретения также входят приготавливаемые для хранения или введения фармацевтические композиции, которые включают фармацевтически эффективное количество требуемых конъюгатов в фармацевтически приемлемом носителе или разбавителе. Соответствующие носители, разбавители и/или вспомогательные вещества для терапевтического применения хорошо известны в фармацевтике. Например, могут быть использованы буферы, консерванты, наполнители, диспергирующие вещества, стабилизаторы, красители. Помимо этого, могут быть использованы антиоксиданты и суспендирующие средства. Примеры подходящих носителей, разбавителей и/или вспомогательных веществ включают, но этим не ограничивая: (1) физиологический раствор, забуференный фосфатом Дульбекко, pH около 6,5, который может содержать от 1 мг/мл до 25 мг/мл сывороточного альбумина человека, (2) 0,9% физиологический раствор (0,9% масса/объем NaCl) и (3) 5% (масса/объем) декстрозу.
Используемый в изобретении термин "фармацевтически эффективное количество" относится к количеству фармацевтического средства для лечения, облегчения или предотвращения выявленного заболевания или состояния или для оказания заметного терапевтического или ингибирующего эффекта. Эффект может быть обнаружен любым известным методом исследования. Точное эффективное количество для субъекта может зависеть от массы тела, размера и состояния здоровья субъекта, природы и степени тяжести состояния, и лекарственного средста или комбинации лекарственных средств, выбранных для введения. Фармацевтически эффективные количества в конкретном случае могут быть определены с помощью хорошо известной врачам методики. В предпочтительном аспекте, заболевание или состояние может быть подвергнуто лечению путем подавления транскрипции гена.
Для любого конъюгата, фармацевтически эффективное количество может быть определено сначала путем проведения исследований, либо на клеточных культурах, например, культурах неопластических клеток, либо на животных моделях, обычно на крысах, мышах, кроликах, собаках или свиньях. Животная модель может также быть использована для определения соответствующего диапазона концентраций и способа введения. Такая информация может затем быть использована для определения подходящих доз и способов введения для людей. Терапевтическая/профилактическая эффективность и токсичность может быть определена с помощью стандартных фармацевтических методик на клеточных культурах или на экспериментальных животных, например, ED50 (доза, терапевтически эффективная для 50% популяции) и LD50 (доза, летальная для 50% популяции). Соотношение между токсическими и терапевтическими эффектами для дозы LD50/ED50называют терапевтическим индексом. Фармацевтические композиции, которые характеризуются высокими значениями терапевтических индексов, являются предпочтительными. Доза может изменяться внутри этого диапазона в зависимости от используемой лекарственной формы, восприимчивости пациента и способа введения.
В одном варианте осуществления, конъюгаты приготавливают для парентерального введения путем инъекции, в том числе с помощью традиционных методов катетеризации, или инфузии. Композиции для инъекции могут присутствовать в виде дозированной лекарственной формы, например, в ампулах или в упаковках для многократного приема, с добавленным консервантом. Конъюгаты могут быть введены парентерально в стерильной среде. Конъюгат, в зависимости от используемой среды и концентрации, может быть либо суспендирован, либо расстворен в среде. Предпочтительно, чтобы в среде можно было бы растворить вспомогательные вещества, такие как местные анестетики, консерванты и буферные вещества. Используемый в изобретении термин "парентеральный" включает чрескожные, подкожные, внутрисосудистые (например, внутривенные), внутримышечные или интратекальне методы инъекции или инфузии и другие подобные методы. Кроме того, предлагается фармацевтическая композиция, включающая конъюгаты и фармацевтически приемлемый носитель. Один или более из конъюгатов могут присутствовать вместе с одним или более нетоксичными фармацевтически приемлемыми носителями и/или разбавителями и/или вспомогательными веществами, и, в случае необходимости, с другими активными игредиентами.
Стерильный инъецируемый препарат может также представлять собой стерильный инъецируемый раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых сред и растворителей, которые могут быть использованы, находится вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно используют стерильные нелетучие масла. Для этой цели, может быть использовано нераздражающее нелетучее масло, в том числе синтетические моно- или диглицериды. Кроме того, в инъецируемых препаратах находят применение жирные кислоты, такие как олеиновая кислота.
Описываемые в изобретении конъюгаты и композиции могут быть введены в соответствующей форме, предпочтительно, парентерально, более предпочтительно, внутривенно. Для парентерального введения конъюгаты или композиции могут представлять собой водные или неводные стерильные растворы, суспензии или эмульсии. В качестве растворителя или среды могут быть использованы пропиленгликоль, растительные масла и пригодные для инъекций органические эфиры, такие как этилолеат. Композиции могут также содержать вспомогательные вещества, эмульгаторы или диспергирующие вещества.
Для лечения указанных выше состояний применяют величины доз от приблизительно 0,01 мг до приблизительно 140 мг на килограмм массы тела в сутки (от приблизительно 0,05 мг до приблизительно 7 г в сутки на пациента). В некоторых вариантах осуществления, вводимая пациенту доза составляет от приблизительно 0,01 мг/кг до приблизительно 100 мг/кг массы тела субъекта. В некоторых вариантах осуществления, вводимая пациенту доза составляет от приблизительно 0,01 мг/кг до приблизительно 15 мг/кг массы тела субъекта. В некоторых вариантах осуществления, вводимая пациенту доза составляет от приблизительно 0,1 мг/кг до приблизительно 15 мг/кг массы тела субъекта. В некоторых вариантах осуществления, вводимая пациенту доза составляет от приблизительно 0,1 мг/кг до приблизительно 20 мг/кг массы тела субъекта. В некоторых вариантах осуществления, вводимая пациенту доза составляет от приблизительно 0,1 мг/кг до приблизительно 5 мг/кг или от приблизительно 0,1 мг/кг до приблизительно 10 мг/кг массы тела субъекта. В некоторых вариантах осуществления, вводимая доза составляет от приблизительно 1 мг/кг до приблизительно 15 мг/кг массы тела субъекта. В некоторых вариантах осуществления, вводимая доза составляет от приблизительно 1 мг/кг до приблизительно 10 мг/кг массы тела субъекта. Количество конъюгата, которое может быть смешано материалами носителя для получения лекарственной формы с разовой дозой, зависит от подвергаемого лечению пациента и конкретного способа введения. Лекарственной формы с разовой дозой могут обычно содержать от приблизительно 0,01 мг до приблизительно 100 мг; от приблизительно 0,01 мг до приблизительно 75 мг; или от приблизительно 0,01 мг до приблизительно 50 мг; или от приблизительно 0,01 мг до приблизительно 25 мг конъюгата.
Для внутривенного введения, величины доз могут включать от приблизительно 0,01 до приблизительно 200 мг конъюгата на килограмм массы тела животного. В одном аспекте, композиция может включать от приблизительно 1 до приблизительно 100 мг конъюгата на килограмм массы тела животного. В другом аспекте, вводимое количество соединения будет составлять от приблизительно 0,1 до приблизительно 25 мг/кг массы тела животного.
В некоторых вариантах осуществления, конъюгаты могут быть введены следующим образом. Конъюгаты могут вводиться ежедневно в течение 5 дней, либо внутривенно, болюс каждый день в течение около 5 дней, либо путем непрерывной инфузии в течение около 5 дней.
В качестве варианта, конъюгаты могут вводиться один раз в неделю в течение шести недель или более. В качестве другого варианта, конъюгаты могут вводиться один раз каждые две или три недели. Дозы в виде болюса вводят в объеме от приблизительно 50 до приблизительно 400 мл физиологического раствора, в который могут быть добавлены от приблизительно 5 до приблизительно 10 мл человеческого сывороточного альбумина. Непрерывные инфузии осуществляются в объеме от приблизительно 250 до приблизительно 500 мл физиологического раствора, в который могут быть добавлены от приблизительно 25 до приблизительно 50 мл человеческого сывороточного альбумина, в течение периода времени 24 часа.
В некоторых вариантах осуществления, через период времени от приблизительно одной до приблизительно четырех недель после лечения, пациенту может быть проведен второй курс лечения. Конкретные клинические протоколы, учитывающие способ введения, вспомогательные вещества, разбавители, дозы и время, могут быть определены специалистом в форме клинических предписаний.
Следует иметь в виду, что конкретная величина дозы для конкретного субъекта зависит от ряда факторов, включающих активность конкретного конъюгата, возраст, массу тела, общее состояние здоровья, пол, режим питания пациента, время введения, способ введения и скорость выведения, комбинацию с другими активными средствами и тяжесть конкретного заболевания, подвергаемого лечению.
Для введения не относящимуся к человеку животному, конъюгаты могут быть также добавлены в корм для животного или питьевую воду. Может быть удобным готовить корм для животного и питьевую воду так, чтобы животное получало терапевтически достаточное количество конъюгатов в процессе приема пищи. Может быть также удобным, чтобы конъюгаты представляли собой заранее приготовленную смесь для добавления в корм или питьевую воду.
Конъюгаты могут быть также введены субъекту в комбинации с другими терапевтическими соединениями для усиления суммарного терапевтического эффекта. Использование множества соединений для лечения заболевания может увеличивать положительные эффекты, уменьшая при этом побочные эффекты. В некоторых вариантах осуществления, конъюгаты используют в комбинации с химиотерапевтическими средствами, такими как средства, раскрытые в патенте США № 7303749. В других вариантах осуществления, химиотерапевтические средства включают, но этим не ограничивая, летрозол, оксалиплатин, доцетаксел, 5-FU, лапатиниб, капецитабин, лейковорин, эрлотиниб, пертузумаб, бевацизумаб и гемцитабин.
Настоящее изобретение также предлагает фармацевтические наборы, включающие один или несколько контейнеров, заполненных одним или более конъюгатами и/или композициями настоящего изобретения, в том числе, одно или более химиотерапевтических средств. Такие наборы могут также включать, например, другие соединения и/или композиции, устройство(устройства) для введения соединений и/или композиций и письменные инструкции в форме, установленной правительственным учреждением, регулирующим производство, применение или продажу лекарственных препаратов или биологических продуктов.
Способы применения
Способы лечения
В конкретных предпочтительных вариантах осуществления изобретения, конъюгат белок-полимер-лекарственное средство изобретения применяют в способах лечения животных (предпочтительно млекопитающих, наиболее предпочтительно, людей, которые включают мужчин, женщин, младенцев, детей и взрослых). В одном варианте осуществления, конъюгаты настоящего изобретения могут применяться в способе лечения животных, который включает введение животному биоразлагаемого биологически совместимого конъюгата изобретения. Например, конъюгаты согласно изобретению могут быть введены в форме растворимых линейных полимеров, сополимеров, конъюгатов, коллоидов, частиц, гелей, твердых изделий, волокон, пленок и в других формах. Биоразлагаемые биологически совместимые конъюгаты этого изобретения могут быть использованы в качестве носителей лекарственного средства и компонентов носителей лекарственного средств в системах с контролируемым высвобождением лекарственного средства, препаратах для низкоинвазивных хирургических операций и в других случаях. Фармацевтические композиции могут быть инъецируемыми, имплантируемыми и вводимыми другими подобными способами.
В еще одном аспекте, изобретение предлагает способ лечения заболевания или расстройства у субъекта, если он в этом нуждается, включающий введение субъекту эффективного количества, по меньшей мере, одного конъюгата изобретения, где указанный конъюгат высвобождает одно или более терапевтических средств в результате биоразложения.
В другом варианте осуществления, конъюгаты могут быть введены in vitro, in vivo и/или ex vivo для лечения пациентов и/или для модулирования роста выбранных популяций клеток, включающих, например, рак. В некоторых вариантах осуществления, конкретные типы рака, которые могут быть подвергнуты лечению с помощью конъюгатов, включают, но этим не ограничивая: (1) твердые опухоли, включающие, но этим не ограничивая, фибросаркому, миксосаркому, липосаркому, хондросаркому, остеогенную саркому, хордому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, лимфангиоэндотелиальную саркому, синовиому, мезотелиому, опухоль Юинга, лейомиосаркому, рабдомиосаркому, рак толстой кишки, колоректальный рак, рак почки, рак поджелудочной железы, рак костей, рак молочной железы, рак яичников, рак предстательной железы, рак пищевода, рак желудка, рак ротовой полости, рак носовой полости, рак горла, плоскоклеточную карциному, базально-клеточную карциному, аденокарциному, карциному потовых желез, карциному сальных желез, папиллярную карциному, папиллярную аденокарциному, цистаденокарциному, медуллярный рак, бронхогенный рак, гипернефроидный рак, рак печени и желчных путей, хориокарциному, семиному, эмбриональный рак, опухоль Вильмса, рак шейки матки, рак матки, рак яичка, мелкоклеточный рак легкого, рак мочевого пузыря, рак легких, эпителиальный рак, глиому, глиобластому, мультиформную астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, акустическую невриному, олигодендроглиому, менингиому, рак кожи, меланому, нейробластому и ретинобластому; (2) гематологические онкологические заболевания, включающие, но этим не ограничивая, острый лимфобластный лейкоз "ALL", острый лимфобластный В-клеточный лейкоз, острый лимфобластный T-клеточный лейкоз, острый миелобластный лейкоз "AML", острый промиелоцитарный лейкоз "APL", острый монобластный лейкоз, острый эритромиелозный лейкоз, острый мегакариобластный лейкоз, острый миеломоноцитарный лейкоз, острый нелимфоидный лейкоз, острый недифференцированный лейкоз, хронический миелоцитарный лейкоз "CML", хронический лимфоцитарный лейкоз "CLL", волосатоклеточный лейкоз, множественную миелому, острые и хронические лейкозы, например, лимфобластные миелогенные и лимфоцитарные миелоцитарные лейкозы; и (3) лимфомы, такие как болезнь Ходжкина, неходжкинскую лимфому, множественную миелому, макроглобулинемию Вальденстрема, болезнь тяжелых цепей и истинную полицитемию.
В другом варианте осуществления, конъюгаты могут быть введены in vitro, in vivo и/или ex vivo для лечения аутоиммунных заболеваний, таких как системная волчанка, ревматоидный артрит, псориаз и множественный склероз; отторжения трансплантатов, таких как отторжение почечного трансплантата, отторжение трансплантата печени, отторжение трансплантата легкого, отторжение трансплантата сердца и отторжение трансплантата костного мозга; реакция "трансплантат против хозяина"; вирусные инфекции, такие как цитомегаловирусная инфекция, ВИЧ-инфекция и СПИД; и паразитарные инфекции, такие как гиардиоз, амебиаз, шистосоматоз и другие подобные инфекции.
В конкретных вариантах осуществления, конъюгаты могут быть также использованы для приготовления лекарственного препарата, применяемого для лечения или облегчения тяжести расстройств, таких как расстройства, характеризующиеся аномальным ростом клеток (например, рак).
В конкретных вариантах осуществления, терапевтическое средство локализовано доставляется в конкретную клетку-мишень, ткань-мишень или орган-мишень.
В конкретных вариантах осуществления, при реализации способа изобретения, конъюгат дополнительно включает или связан с диагностической меткой. В конкретных примерах вариантов осуществления, диагностическую метку выбирают из группы, состоящей из: радиофармацевтических препаратов или радиоактивных изотопов для гамма-сцинтиграфия и позитронно-эмиссионной томографии, контрастного вещества для магнитно-резонансной томографии (MRI), контрастного вещества для компьютерной томографии, контрастного вещества для метода рентгенологического исследования, вещества для метода ультразвуковой диагностики, вещества для нейтронной активации, фрагмента, который может отражать, рассеивать или подвергать изменению рентгеновское излучение, ультразвук, радиоволны и микроволны и флуорофоры. В конкретных примерах вариантов осуществления, конъюгат дополнительно контролируют in vivo.
Примеры диагностических меток включают, но этим не ограничивая, диагностические радиофармацевтические препараты или радиоактивные изотопы для гамма-сцинтиграфия и позитронно-эмиссионной томографии, контрастное вещество для магнитно-резонансной томографии (MRI) (например, парамагнитные атомы и суперпарамагнитные нанокристаллы), контрастное вещество для компьютерной томографии, контрастное вещество для метода рентгенологического исследования, вещество для метода ультразвуковой диагностики, вещество для нейтронной активации, фрагмент, который может отражать, рассеивать или подвергать изменению рентгеновское излучение, ультразвук, радиоволны и микроволны и флуорофоры в различных оптических методах, и другие вещества. Диагностические радиофармацевтические препараты включают г-излучающие радионуклиды, например, индий-111, технеций-99m и йод-131, и другие. Контрастные вещества для магнитно-резонансной томографии (MRI) включают магнитные соединения, например, парамагнитные ионы, железо, марганец, гадолиний, лантаниды, органические парамагнитные фрагменты и суперпарамагнитные, ферромагнитные и антиферромагнитные соединения, например, коллоидный оксид железа, коллоидные ферриты, и другие соединения. Контрастные вещества для компьютерной томографии и других методов на основе рентгеновского излучения включают соединения, поглощающие рентогеновские лучи, например, йод, барий, и другие вещества. Контрастные вещества для ультразвуковых методов включают соединения, которые могут поглощать, отражать и рассеивать ультразвуковые волны, например, эмульсии, кристаллы, пузырьки газа, и другие вещества. Другие примеры включают вещества, применяемые для нейтронной активации, такие как бор и гадолиний. Кроме того, могут применяться метки, которые способны отражать, преломлять, рассеивать или же подвергать изменению рентгеновское излучение, ультразвук, радиоволны, микроволны и другие виды излучения, применяемые в диагностических методах. Флуоресцентные метки могут применяться для получения изображения. В конкретных вариантах осуществления, модификатор включает парамагнитный ион или группу.
В другом аспекте, изобретение предлагает способ лечения заболевания или расстройства у субъекта, включающий приготовление водной композиции, по меньшей мере, одного конъюгата изобретения и парентеральное инъецирование указанной композиции субъекту.
В другом аспекте, изобретение предлагает способ лечения заболевания или расстройства у субъекта, включающий приготовление импланта, содержащего, по меньшей мере, один конъюгат изобретения, и имплантирование указанного импланта субъекту. В конкретных примерах вариантов осуществления, имплант представляет собой биоразлагаемую гелеобразную матрицу.
В другом аспекте, изобретение предлагает способ лечения животного, если он в нем нуждается, включающий введение конъюгата с помощью описанных выше способов.
В другом аспекте, изобретение предлагает способ инициирования иммунной реакции у животного, включающий введение конъюгата с помощью описанных выше способов.
В другом аспекте, изобретение предлагает способ диагностирования заболевания у животного, включающий стадии:
введения конъюгата с помощью описанных выше способов, где указанный конъюгат включает поддающуюся обнаружению молекулу; и
детектирования поддающейся обнаружению молекулы.
В конкретных примерах вариантов осуществления, стадию детектирования поддающейся обнаружению молекулы осуществляют неинвазивно. В конкретных примерах вариантов осуществления, стадию детектирования поддающейся обнаружению молекулы осуществляют с использованием подходящего оборудования для визуализации.
В одном варианте осуществления, способ лечения животного включает введение животному биоразлагаемого биологически совместимого конъюгата изобретения в виде тампона для хирургической раны, из которой была удалена опухоль или новообразование. Тампон из биоразлагаемого биологически совместимого конъюгата будет заполнять место опухоли в процессе восстановления и разлагаться и исчезать по мере заживления раны.
В конкретных вариантах осуществления, конъюгат связывают с диагностической меткой для in vivo мониторинга.
Описанные выше конъюгаты могут применяться для терапевтического, профилактического лечения и диагностирования животных. Конъюгаты обычно предназначаются для парентерального введения, но в нокоторых случаях они могут быть введены и другими способами.
В одном варианте осуществления, растворимые или коллоидные конъюгаты вводят внутривенно. В другом варианте осуществления, растворимые или коллоидные конъюгаты вводят путем местной (например, подкожной, внутримышечной) инъекции. В другом варианте осуществления, твердые конъюгаты (например, частицы, имплантаты, системы доставки лекарственных средств) вводят путем имплантации или инъекции.
В другом варианте осуществления, конъюгаты, включающие поддающуюся обнаружению метку, вводят для исследования характеристик и динамики распределения метки в организме животного.
В конкретных вариантах осуществления, любой один или более из описанных в изобретении конъюгатов могут быть применены при осуществлении любого из описанных выше способов. В конкретных примерах вариантов осуществления, конъюгат представляет собой конъюгат трастузумаб-PHF-лекарственное средство, ритуксимаб-PHF-лекарственное средство или LHRH-PHF-лекарственное средство.
В описании изобретения, в тех случаях, когда композиции характеризуют как имеющие, содержащие или включающие конкректные компоненты, предполагается, что композиции также состоят в основном или состоят из перечисленных компонентов. Ангалогично, в тех случаях, когда способы или процессы характеризуют как имеющие, содержащие или включающие конкректные стадии, процессы также состоят в основном или состоят из перечисленных стадий. Кроме того, следует иметь в виду, что порядок стадий или порядок осуществления конкретных действий является несущественным при условии, что изобретение остается осуществимым. Более того, две или более стадий или два или более действий могут быть проведены одновременно.
Методы синтеза изобретения допускают использование большого разнообразия функциональных групп; поэтому могут использоваться различные замещенные исходные материалы. Методы синтеза обычно позволяют получать требуемое конечное соединение в конце или почти в конце синтеза в целом, хотя в конкретных случаях может потребоваться дополнительное превращение соединения в его фармацевтически приемлемую соль, эфир или пролекарство.
Лекарственные соединения, применяемые для конъюгатов настоящего изобретения, могут быть получены различными способами, используя производимые промышленностью исходные материалы, описанные в научной литературе соединения или из легко получаемых промежуточных соединений с помощью стандартных методов и методик синтеза, либо являющихся известными для специалистов в этой области, либо очевидными для них в свете идеи изобретения. Стандартные методы и методики синтеза для получения органических молекул и для трансформаций и манипуляций с функциональными группами можно найти в соответствующей научной литературе или в стандартных руководствах в этой области. Не ограничиваясь какой-либо одной или несколькими ссылками на литературные источники, тем не менее, следует отметить, что ценными и общепризнанными руководствами по органическому синтезу являются классические монографии, такие как Smith, M. B., March, J., March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 5th edition, John Wiley & Sons: New York, 2001; и Greene, T.W., Wuts, P.G. M., Protective Groups in Organic Synthesis, 3rd edition, John Wiley & Sons: New York, 1999, содержание которых приводится в описании изобретения путем ссылки на них. Следующие далее описания методов синтеза предназначены только для иллюстрации, и они не являются ограничениями для общих методик получения соединения настоящего изобретения.
Конъюгаты настоящего изобретения и лекарственные соединения, вводимые в них, могут быть удобно получены различными методами, известными специалистам в этой области. Конъюгаты или соединения этого изобретения, имеющие каждую из описанных в изобретении формул, могут быть получены в соответствии со следующими методиками из производимых промышленностью исходных материалов или исходных материалов, которые могут быть получены с использованием методик, описанных в литературе. Эти методики иллюстрируют получение репрезентативных конъюгатов этого изобретения.
После того как разработанные, выбранные и/или оптимизированные с помощью описанных выше методов конъюгаты получены, они могут быть подвергнуты ряду исследований, известных специалистам в этой области, для определения наличия у конъюгатов биологической активности. Например, конъюгаты могут быть подвергнуты традиционным исследованиям, включающим, но этим не ограничивая, описанные ниже исследования для определения наличия у них предполагаемой активности, активности и/или специфичности при связывании.
Кроме того, для ускорения проведения таких исследований может быть использован высокопроизводительный скрининг. В результате, можно быстро провести скрининг описанных в изобретении молекул конъюгатов на активность, имспользуя известные в науке методы. Общая методология проведения высокопроизводительного скрининга описана, например, в монографии Devlin (1998) High Throughput Screening, Marcel Dekker и в патенте США № 5763263. При высокопроизводительных исследованиях могут применяться одна или более различных методик, включающих, но этим не ограничивая, описанные ниже методики.
Содержание всех упоминаемых в изобретении публикаций и патентных документов приводится в описании изобретения путем ссылки на них, также как и содержание каждой конкретно и индивидуально указываемой публикации или документа приводится в описании изобретения путем ссылки на него. Предполагается, что упоминаемые в описании изобретения любые публикации и патентные документы не являются прототипами, то же самое относится и к их содержанию и датам опубликования. Итак, изобретение описано в форме рукописного описания, но для специалистов в этой области является очевидным, что изобретение может быть реализовано в различных вариантах осуществления и что приведенное выше описание и приводимые ниже примеры являются только иллюстрациями и не ограничивают приводимую далее формулу изобретения.
ПРИМЕРЫ
Описанные в изобретении конъюгаты могут быть получены в соответствии со схемами, изображенными в общем виде выше, и в соответствии с методами, описанными в примерах ниже. Используемый в некоторых примерах ниже термин "содержание", если не указано иначе, означает мольную долю полимерных цепей, заменяемых на заданный фрагмент, такой как связующее звено, молекула лекарственного средства или PBRM.
СОКРАЩЕНИЯ
В схемах реакций и примерах синтезов используют следующие сокращения. Этот список не следует считать полным списком сокращений, применяемых в изобретении, так как в схемах синтезов и примерах могут также использоваться дополнительные стандартные сокращения, которые хорошо известны специалистам в области органического синтеза.
ОБЩАЯ ИНФОРМАЦИЯ
Пептиды EC-1-Adoa-NH2 и LTVSPNY-Adoa-NH2 были поставлены фирмой CreoSalus, Louisville, Kentucky.
Связующие звенья M-(PEG)12-NHS и эфир S-ацетил-(PEG)12-NHS были поставлены фирмой Quanta Biodesign, Powell, Ohio.
Очистку методом ВЭЖХ проводили на полупрепаративной колонке Phenomenex Gemini 5 мкм 110 Е, 250 × 10 мм, 5 микрон, используя следующую систему растворителей: растворитель A: вода (0,1% TFA); растворитель B: CH3CN (0,1% TFA).
Содержание HPV в конъюгатах определяли методом LC/MS/MS (жидкостной хроматографии/тандемной масс-спектрометрии) или ВЭЖХ.
Содержание белка в конъюгатах определяли спектрофотометрически при 280 нм.
Содержание дисульфида в -SSPy конъюгатах определяли спектрофотометрически при 340 нм после выделения пиридинтиона (10 мМ DTT, 10 минут, температура окружающей среды).
Содержание SN38 в конъюгатах определяли спектрофотометрически при 370 нм.
Молекулярные массы конъюгатов определяли методом SEC с использованием в качестве эталонов молекулярной массы, либо полисахаридов, либо белков.
Полимерные конъюгаты PBRM-лекарственное средство выделяли из оставшихся непрореагировавшими полимерных конъюгатов лекарственного средства методом экстенсивной диафильтрации. В случае необходимости, проводили дополнительную очистку с помощью гельпроникающей хроматографии для удаления любых агрегированных полимерных конъюгатов PBRM-лекарственное средство. В целом, полимерные конъюгаты PBRM-лекарственное средство обычно содержали <5% агрегированных полимерных конъюгатов PBRM-лекарственное средство, определяемых методом SEC или SDS-PAGE; <1% конъюгата полимер-лекарственное средство, определяемого методом SEC, и <2% неконъюгированной PBRM, определяемой методом ОФ ВЭЖХ.
Восстановленные или частично восстановленные антитела получали, используя описанные в литературе методики, смотрите, например, Francisco et al., Blood 102 (4): 1458-1465 (2003).
Пример 1. Синтез 30 кДа PHF-β-аланина:

PHF (30 кДа, 4,54 г, 33,6 ммоль мономера PHF) растворяли в 150 мл безводного DMF, затем добавляли бис(нитрофенол)карбонат (3,07 г, 10,1 ммоль). Раствор перемешивали при 40°C в течение 4 часов. К смеси PHF добавляли β-аланин (1,50 г, 16,8 ммоль), растворенный в воде (10 мл). Корректировали рН до значения 7,5-8 с помощью TEA, и реакционную смесь перемешивали при 23°C в течение 18 часов, разбавляли до 400 мл водой, и корректировали рН до значения 11 с помощью 5N NaOH. Полученную смесь перемешивали в течение 1 часа при температуре окружающей среды, корректировали рН до значения 6,5 и затем смесь разбавляли до 10% органических веществ водой. Продукт (30 кДа PHF-β-аланин) очищали, используя картридж для ультрафильтрации, снабженный мембранным фильтром 5K Biomax. Очищенный продукт лиофилизировали с получением названного соединения в виде белого твердого вещества (2,07 г, 36% выход). Мольная доля мономерных звеньев PHF, замещенных β-аланином, определенная методом1H ЯМР, составляла 13%.
Пример 2. Синтез 30 кДа PHF-GA

N,N-Диметилпиридин-4-амин (0,268 г, 2,91 ммоль) и глутаровый ангидрид (1,375 г, 12,06 ммоль) добавляли к раствору PHF (30 кДа, 1,48 г, 10,96 ммоль мономера PHF) в DMA (300 мл) и безводного пиридина (33,3 мл). Реакционную смесь перемешивали при 60°C в течение 18 часов. Растворители удаляли при пониженном давлении, и полученное вязкое масло переносили в воду (100 мл). Корректировали рН до значения pH 6,0-6,5 с помощью 5N NaOH. Полученный прозрачный раствор разбавляли до 200 мл водой, фильтровали через фильтр с размером пор 0,2 микрона и очищали диафильтрацией, используя мембранный фильтр с номинальным отсечением по молекулярной массе 5000. Воду удаляли лиофилизацией с получением 30 кДа PHF-GA в виде белого твердого вещества (1,28 г, 48% выход). Доля суммарных мономерных звеньев PHF, замещенных глутаровой кислотой, определенная методом1H ЯМР, составляла 96%.
Пример 3. Синтез производного трастузумаб-MCC

Трастузумаб (10 мг) растворяли в PBS буфере (1 мл, pH 7,0), затем добавляли раствор SMCC в DMSO (5 мкл, 30 мг/мл). Полученный раствор перемешивали при комнатной температуре в течение 2 часов. Трастузумаб-MCC очищали гель-фильтрацией, используя колонку PD-10, приведенную в равновесие с помощью PBS (90% выход). Анализ показал, что в среднем от 5 до 6 групп MCC были связаны с одним трастузумабом.
Описанная выше методика может быть использована для синтеза других производных PBRM.
Пример 4. Синтез производного трастузумаб-M-(PEG)12
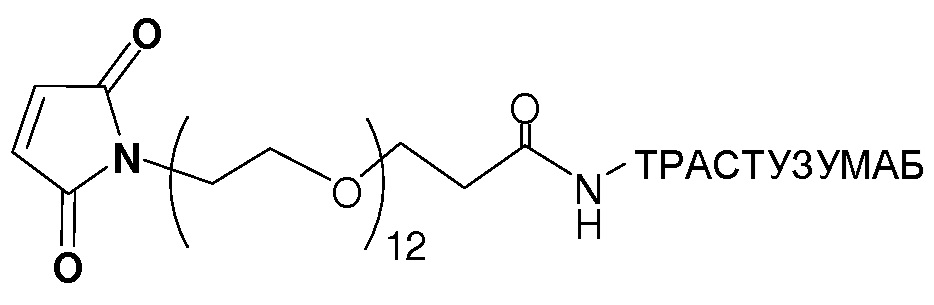
Трастузумаб (10 мг) растворяли в PBS буфере (1 мл, pH 7,0), затем добавляли раствор SM-(PEG)12 в DMSO (4 мкл, 100 мг/мл). Полученный раствор перемешивали при комнатной температуре в течение 2 часов. Трастузумаб-M-(PEG)12 очищали гель-фильтрацией, используя колонку PD-10, приведенную в равновесие с помощью PBS (~90% выход). Анализ показал, что в среднем от 5 до 6 полиэтиленовых групп были связаны с одним трастузумабом.
Описанная методика может быть использована для синтеза других производных PBRM.
Пример 5. Синтез 10 кДа PHF-GA-SSpy

10 кДа PHF-GA (1,63 г 11,12 ммоль, полученный в соответствии с методикой, описанной в примере 2, с PHF 10000 Да, 25% GA) растворяли в воде (10 мл) и добавляли NHS (0,154 г, 1,33 ммоль). Смесь охлаждали до 0°C и затем добавляли водный раствор EDC (0,256 г, 1,33 ммоль), а затем 2-(пиридин-2-илдисульфанил)этанамина гидрохлорид (0,297 г, 1,33 ммоль). Корректировали рН полученной смеси до значения 5,5-6,0, затем перемешивали при 23°C в течение 18 часов, затем очищали диализом через мембрану из регенерированной целлюлозы и лиофилизировали с получением названного соединения (1,66 г, 86%) в виде белого твердого вещества. Содержание SSPy составляло 3%.
Пример 6. Синтез 10 кДа PHF-GA-(HPV-аланин)-SH

10 кДа PHF-GA-SSpy (289,0 мг, 0,023 ммоль, полученного, как описано в примере 5) переносили в смесь воды (8 мл) и ацетонитрила (4 мл) и охлаждали до 0°C. Добавляли NHS (26,4 мг, 0,230 ммоль), затем водный раствор EDC (44,0 мг, 0,230 ммоль) и HPV-аланин (131,45 мг, 0,138 ммоль, полученный, как описано в патентном документе U.S. Publication No. 2010/0305149, Example 1). Корректировали рН полученной смеси до значения 6, и затем смесь перемешивали при комнатной температуре в течение ночи. Корректировали рН до значения 7,5 с помощью 1M NaHCO3 и добавляли DTT (37,8 мг, 0,245 ммоль). Реакционную смесь перемешивали при 23°C в течение 30 минут, разбавляли до 15 мл водой и очищали диализом, используя мембрану из регенерированной целлюлозы (с номинальным отсечением по молекулярной массе 3 кДа). Выход 57% (в расчете на HPV); 7,3 масс.% HPV, определенных с помощью ВЭЖХ.
Путем замены HPV-аланин фрагментами других лекарственных средств или производными лекарственных средств в описанной выше методике, можно синтезировать другие конъюгаты лекарственное средство-полимер.
Пример 7. Синтез 10 кДа PHF-GA-(HPV-аланин)-(трастузумаб-MCC)

К трастузумаб-MCC (20 мг, полученному, как описано в примере 3) в PBS (2 мл, pH 7,0) добавляли 10 кДа PHF-GA-(HPV-Аланин)-SH (11,2 мг, полученному, как описано в примере 6) в воде (0,5 мл). Раствор перемешивали при комнатной температуре в течение 4 часов при pH 7,0. Полученный конъюгат очищали гель-фильтрацией, используя колонку Superpose-6 с PBS в качестве элюента (75% выход). Молекулярная масса PHF-GA-(HPV-аланин)-(трастузумаб- MCC), определенная с помощью SEC, составляла около 170 кДа. Содержание HPV, определенное методом ВЭЖХ, давало среднее мольное отношение HPV к трастузумабу приблизительно от 14:1 до 17:1. Для 10 кДа PHF-GA-(HPV-аланин)-(трастузумаб-MCC), приведенного на фигурах 2 и 4, отношение HPV к трастузумабу составляло приблизительно от 19:1 до 22:1.
Путем замены трастузумаб-MCC другими производными PBRM в описанной выше методике, можно синтезировать другие конъюгаты белок-лекарственное средство. Кроме того, могут быть получены полимерные конъюгаты PBRM-лекарственное средство с различными отношениями лекарственного средства к PBRM путем изменения количества используемых в примерах выше PBRM и лекарственного средства в полимерном конъюгате.
Пример 8. Синтез 10 кДа PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12)

10 кДа PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12) получали, как описано в примере 7, за исключением того, что трастузумаб-MCC заменяли на трастузумаб-M-(PEG)12 (полученный, как описано в примере 4). Молекулярная масса конъюгата PHF-GA-(HPV-аланин)- (трастузумаб-M-(PEG)12), определенная методом SEC, составляла около 200 кДа. Содержание HPV, определенное методом ВЭЖХ, давало среднее мольное отношение HPV к трастузумабу приблизительно от 16:1 до 18:1.
Пример 9. Синтез 70 кДа PHF-GA-SN-38-аланин-SSpy

70 кДа PHF-GA-аланин-SN38 (37,4 мг, 0,254 ммоль, полученный, как описано в патентном документе US 2010/0305149, используя PHF 70000 Да, GA 20%) помещали в пробирку и добавляли 2-(пиридин-2-илдисульфанил)этанамина гидрохлорид (2,83 мг, 0,013 ммоль) и NHS (2,93 мг, 0,025 ммоль), затем EDC (7,32 мг, 0,038 ммоль). Добавляли дополнительные аликвоты EDC (7,32 мг, 0,038 ммоль) в моменты времени 30 минут, 2 часа, 4 часа и 6 часов, и реакционную смесь перемешивали в течение еще 12 часов. Продукт очищали диализом через 10 кДа мембранный фильтр из регенерированной целлюлозы (SSPy 2%; SN38 4,8% (по массе)).
Пример 10. Синтез LHRH-PEG12-SH

LHRH (10 мг) растворяли в смеси ацетонитрил:вода (1:1, 500 мкл) и добавляли исходный раствор PEG12-SATA (9,2 мкл, 0,0025 ммоль, 1,9 мг). Полученную смесь перемешивали в течение 3 часов при температуре окружающей среды. Продукт очищали методом RP-ВЭЖХ, затем лиофилизировали (60% выход).
Очищенный LHRH-PEG12-SH (2 мг) растворяли в воде (400 мкл), корректировали рН до значения 11,8 с помощью TEA, и смесь перемешивали в течение 40 минут в атмосфере аргона и использовали на следующей стадии.
Пример 11. Синтез 70 кДа PHF-GA-SN-38-аланин-(SS-PEG12-LHRH)
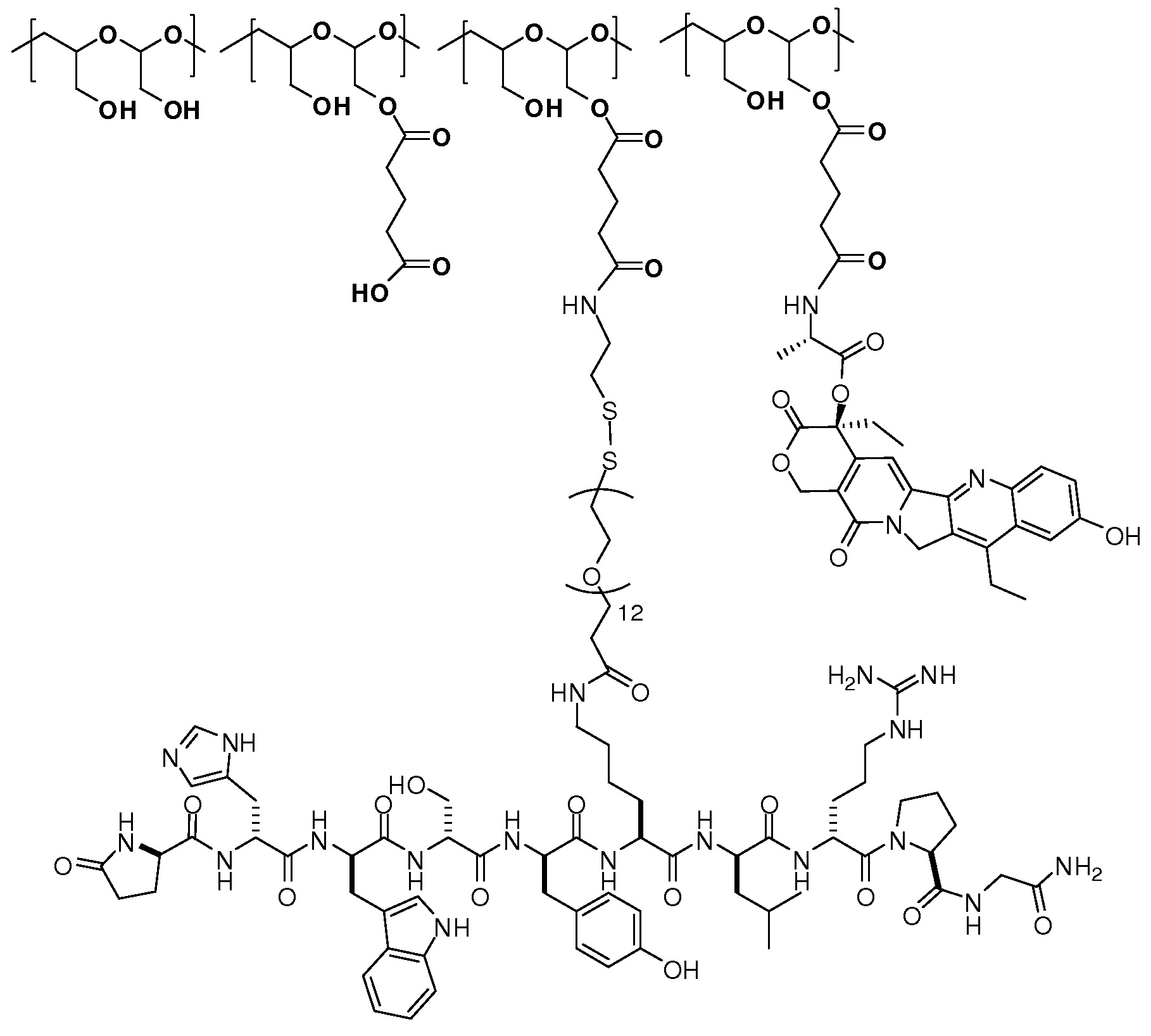
70 кДа PHF-GA-SN-38-аланин-SSpy (2 мг, полученный, как описано в примере 9) растворяли в PBS (0,5 мл, 50 мМ, pH=7,5). Затем добавляли LHRH-PEG12-SH (0,8 мг, полученный, как описано в примере 10). Смесь перемешивали при комнатной температуре в течение 4 часов при pH 7,0. Конъюгат очищали диализом против PBS (pH 7,0), используя мембранный фильтр из регенерированной целлюлозы с номинальным отсечением по молекулярной массе 10 кДа. Содержание LHRH, определенное с помощью HPSEC, составляло 65% с количественным удержанием SN38.
Пример 12. Синтез 30 кДа PHF-GA-малеимида

30 кДа PHF-GA (7,98 г, 50,2 ммоль, полученного как описано в примере 2, GA 15%) переносили в воду (502 мл) и охлаждали до 0°C. Добавляли NHS (0,087 г, 0,752 ммоль), затем водный раствор EDC (0,144 г, 0,752 ммоль). Корректировали рН до значения pH от 7 до 8 с помощью 1N NaOH, и реакционную смесь перемешивали в течение 1 часа при комнатной температуре. Добавляли N-аминоэтил-малеимид (0,080 г, 0,451 ммоль) при 0°C, и реакционную смесь подогревали до комнатной температуры и затем перемешивали в течение ночи. Смесь фильтровали через фильтр с размером пор 2 микрона, концентрировали до 200 мл, очищали диализом через картридж Biomax (полиэфирсульфон) (5K) путем промывания 1 литром воды, затем лиофилизировали с получением названного соединения (2,19 г, 28% выход) в виде белого твердого вещества. Содержание малеимида, определенное с помощью элементного анализа CHN, составляло 2,6%: (CHN среднее): C: 44,81, H: 6,91, N: 0,49.
Пример 13. Синтез 30 кДа PHF-GA-(HPV-аланин)-малеимида

30 кДа PHF-GA-малеимид (271 мг, 7,86 мкмоль, полученный, как описано в примере 12) помещали в смесь воды (8 мл) и CH3CN (4 мл) и охлаждали до 0°C. Добавляли NHS (9,04 мг, 0,079 ммоль), затем водный раствор EDC (15,1 мг, 0,079 ммоль) и HPV-аланин (104 мг, 0,109 ммоль, полученный, как описано в патентном документе U.S. Publication No. 2010/0305149, Example 1) в воде (2 мл). Корректировали рН полученной смеси до значения 6,0 и затем перемешивали при комнатной температуре в течение ночи. Ход реакции постоянно контролировали с помощью ВЭЖХ, детектирование при 245 нм, и добавляли дополнительные аликвоты EDC (15,1 мг, 0,079 ммоль) в воде в момент времени 19 часов и 22 часа. Реакционную смесь разбавляли до 15 мл водой, и полученную смесь очищали диализом через мембрану из регенерированной целлюлозы (5K), элюируя с помощью 5% NaCl/10%CH3CN (3 × 10 мл) и воды (2 × 10 мл). Пробу разбавляли до 10 мл и замораживали с получением 245 мг названного соединения, 93% выход. Мольное отношение HPV к полимеру составляло в среднем приблизительно от 24:1 до 28:1
Пример 14. Синтез EC-1-Adoa-M-(PEG)12

К смеси EC-1-Adoa-NH2 (10 мг, 4 15 мкмоль) в CH3CN/H2O/DMSO (750 мкл, 7:7:1) добавляли исходный раствор (0,064 мг/мл) M-(PEG)12-NHS (63 мкл, 4,1 мг, 4,7 мкмоль) в CH3CN. Корректировали рН до значения 7,4, и затем добавляли DMSO (50 мкл) и NMP (50 мкл) для получения более гомогенной смеси. Смесь перемешивали в атмосфере аргона в течение ночи, защищали от воздействия света. Добавляли дополнительную аликвоту (13 мкл, 1 мг) свежеприготовленного исходного раствора M-(PEG)12-NHS (0,077 мг/мл), и полученную смесь перемешивали в течение 30 минут. Неочищенный продукт очищали с помощью ВЭЖХ (градиент: 10% растворителя B - 90% растворителя B в течение 25 минут). Названное соединение элюировалось на 16 минуте и его концентрировали с получением 2 мг бесцветного твердого вещества. ESI-MS расчетная для C146H209N27O50S2 801,1 (M + 4H+), полученная 802,1.
Пример 15. Синтез 10 кДа PHF-GA-(HPV-аланин)-(EC-1-Adoa-M-(PEG)12)

К раствору 10 кДа PHF-GA-(HPV-аланин)-SH (2 мг, 0,12 мкмоль, полученного, как описано в примере 6, 10 кДа PHF, GA 26%, HPV 7,4%, SH 3%), в 400 мкл воды добавляли раствор пептида EC-1-Adoa-M-(PEG)12 (1 мг, 0,31 мкмоль, полученного как описано в примере 14) в NMP (50 мкл). Корректировали рН до значения 7,4, и реакционную смесь перемешивали в атмосфере аргона до тех пор, пока с помощью HPSEC дополнительно введенный пептид не обнаруживался (2 часа, 37% пептида). Реакционную смесь разбавляли с помощью NaCl (1%, 10 мл) и затем концентрировали до 2 мл путем центробежного фильтрования (мембрана с номинальным отсечением молекулярной массы 3000 Да). Раствор разбавляли с помощью PBS (25 мМ, 8 мл) и концентрировали до 1,5 мл с получением названного соединения, содержащего 0,373 мМ HPV.
Пример 16. Синтез LTVSPNY-Adoa-PEG12-тиоэфира
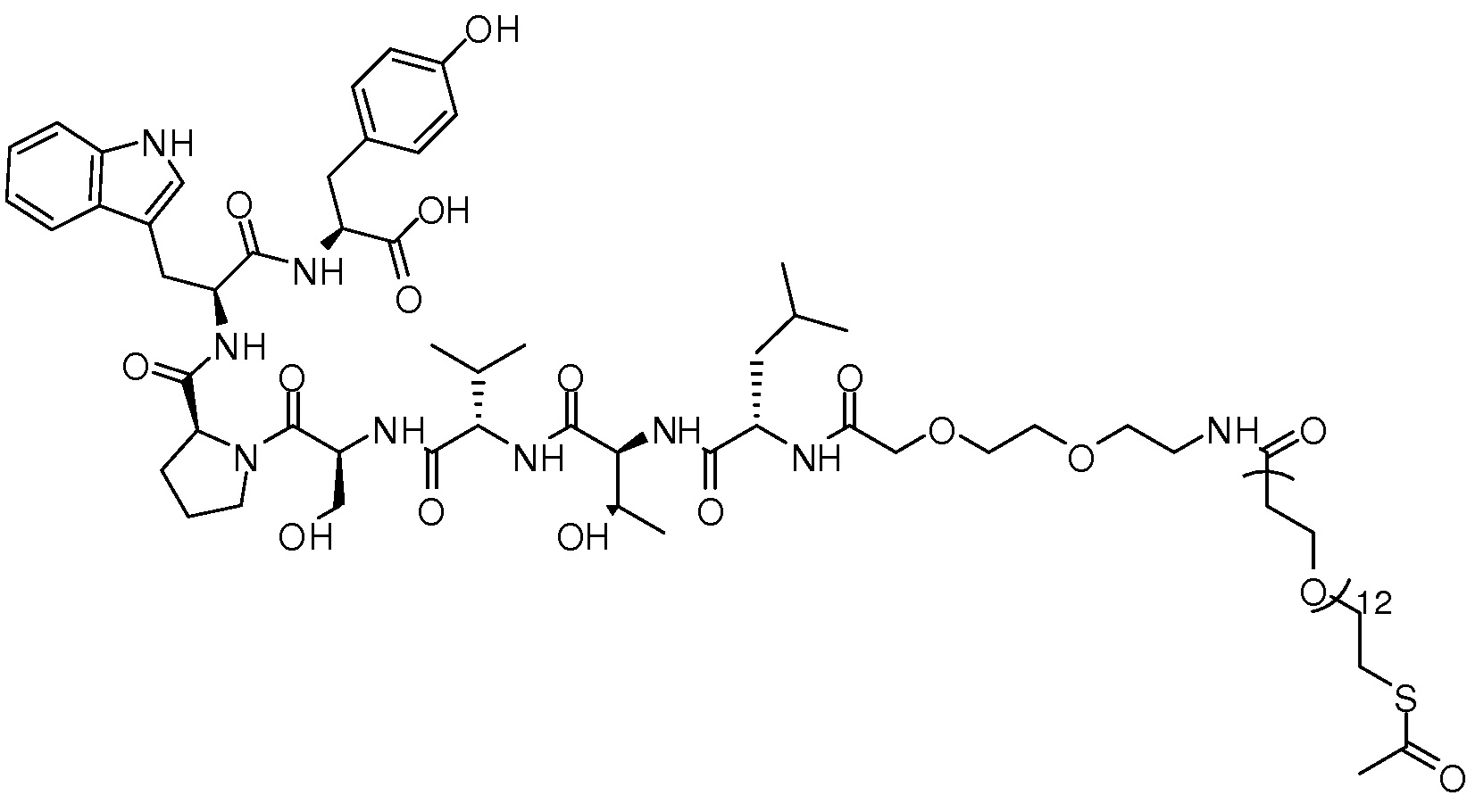
К раствору LTVSPNY-Adoa-NH2 (10 мг, 10,7 мкмоль) в смеси CH3CN/H2O (500 мкл, 1:1) добавляли 46 мкл (20,8 мкмоль, 16,1 мг) свежеприготовленного исходного раствора S-ацетил-PEG12-NHS (350 мг/мл) в DMSO. Корректировали рН до значения 6,5-7,0, и реакционную смесь перемешивали в течение ночи. Затем корректировали pH до значения 7,5-8,0, и реакционную смесь перемешивали в течение ~2 часов. Неочищенный продукт очищали с помощью ВЭЖХ (градиент: 10% растворитель B - 70% растворитель B в течение 25 минут) с получением, после концентрирования, 9 мг названного соединения в виде бесцветного твердого вещества (51% выход). ESI-MS расчетная для C78H126N9NaO28S 845,9, полученная 845,9 (M + H+ + Na+).
Пример 17. Синтез 30 кДа PHF-GA-(HPV-аланин)-(LTVSPNY-Adoa-PEG12)

LTVSPNY-Adoa-PEG12-тиоэфир (0,57 мг, 0,34 мкмоль, полученный, как описано в примере 16) растворяли в воде (500 мкл) и корректировали рН до значения 11,8. Раствор перемешивали в атмосфере аргона в течение 30 минут и значение pH понижали до 5-5,5. Добавляли раствор 30 кДа PHF-GA-(HPV-аланин)-малеимид (2,5 мг, 0,057 ммоль, полученного как описано в примере 13, GA 15%, малеимид 2,6%, HPV 5%) в воде (62,5 мкл). Корректировали рН до значения 7,6, и затем реакционную смесь перемешивали в атмосфере аргона до тех пор, пока с помощью HPSEC дополнительно введенный пептид не обнаруживался (3 часа, 15% введения пептида). Реакционную смесь затем разбавляли с помощью 1% NaCl и фильтровали через шприцевой фильтр 0,2 мкм. Неочищенный материал очищали с помощью перемешиваемой ячеечной фильтрации через мембрану с номинальным отсечением молекулярной массы 5 кДа с получением раствора названного соединения.
Пример 18. Синтез 30 кДа PHF-GA-(HPV-аланин)-SH
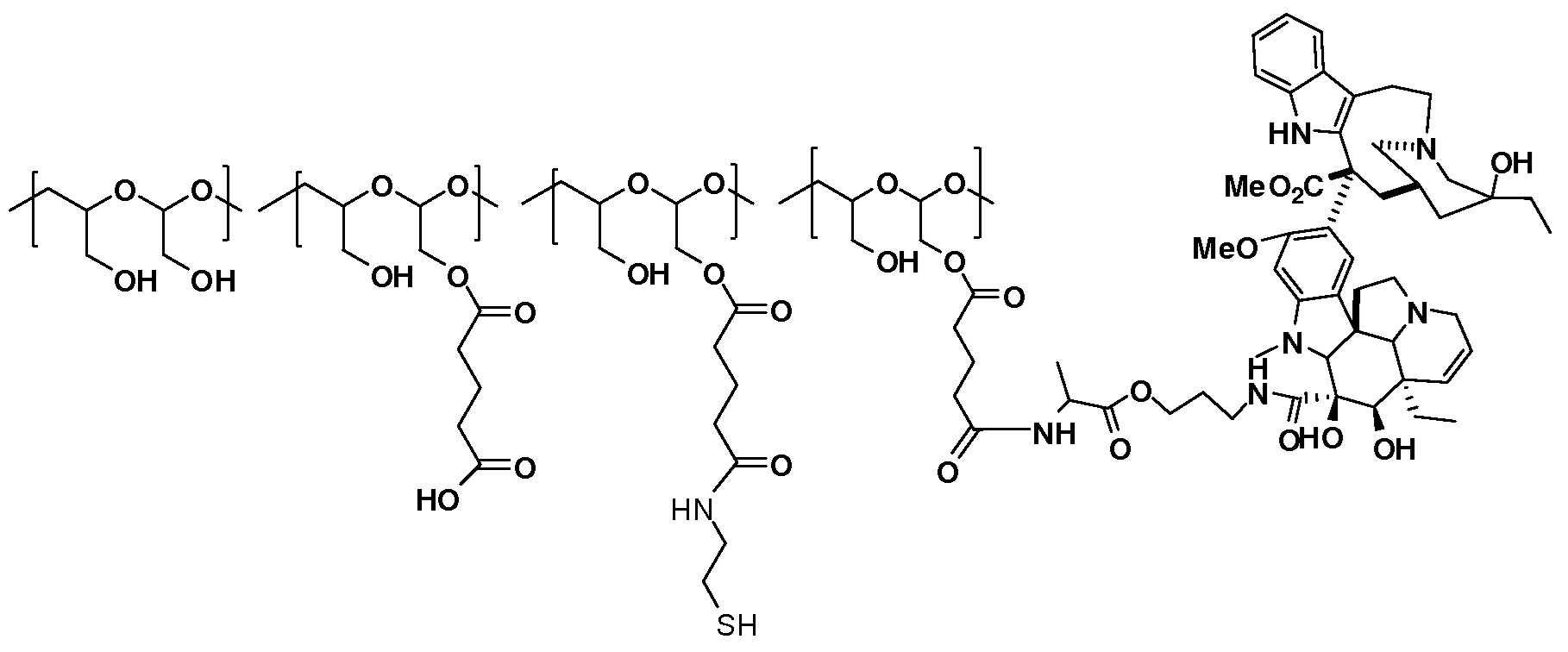
30 кДа PHF-GA-SSpy (26,2 мг, 0,72 мкмоль, полученный как описано в примере 5, используя 30 кДа PHF, GA 10%, SSPy 4,8%) помещали в смесь воды (3 мл) и ацетонитрила (3 мл) и охлаждали до 0°C. Добавляли NHS (0,83 мг, 7,16 мкмоль), затем водный раствор EDC (1,37 мг, 7,16 мкмоль) и HPV-аланин (10,2 мг, 10,7 мкмоль, полученный, как описано в патентном документе U.S. Publication № 2010/0305149, Пример 1). Корректировали рН полученной смеси до значения 6,0, и затем смесь перемешивали при комнатной температуре в течение ночи. Корректировали рН до значения 7,5 с помощью 1M NaHCO3 и добавляли DTT (11,7 мг, 0,076 ммоль). Реакционную смесь перемешивали при 23°C в течение 30 минут, разбавляли до 15 мл водой и очищали диализом, используя мембрану из регенерированной целлюлозы (с номинальным отсечением молекулярной массы 30 кДа). Выход 82% (в расчете на HPV); 20,6% по массе HPV, определенное методом ВЭЖХ.
Пример 19. Синтез 30 кДа PHF-GA-(HPV-аланин)-(трастузумаб-MCC)

К трастузумаб-MCC (20 мг, полученному, как описано в примере 3) в PBS (2 мл, pH 7,0) добавляли 30 кДа PHF-GA-(HPV-аланин)-SH (11,2 мг, полученный, как описано в примере 18) в воде (0,5 мл). Раствор перемешивали при комнатной температуре в течение 4 часов при pH 7,0. Полученный конъюгат очищали гель-фильтрацией, используя колонку Superpose-6 с PBS в качестве элюента. Содержание HPV, определенное методом ВЭЖХ, давало, в среднем, мольное отношение HPV к антителу приблизительно от 10:1 до 12:1.
Пример 20. Синтез 70 кДа PHF-GA-(HPV-аланин)-SH
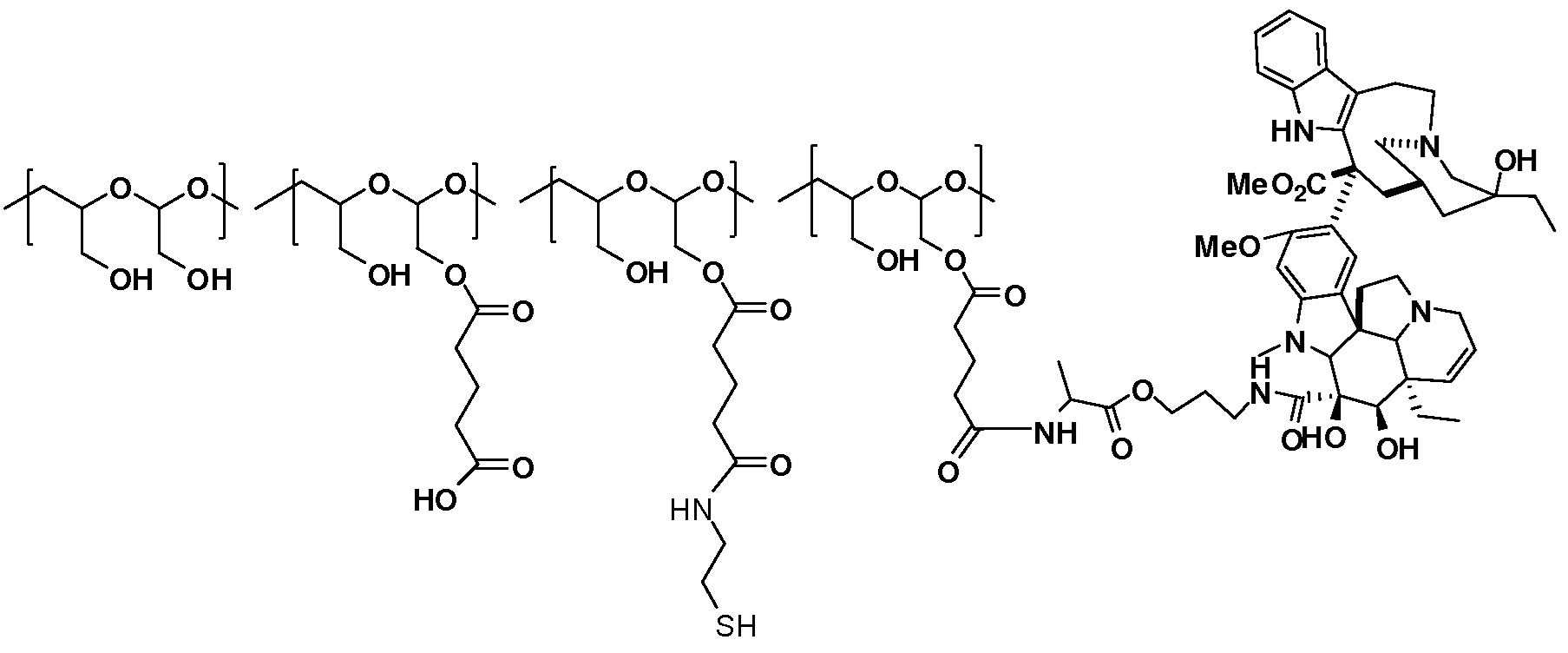
70 кДа PHF-GA-(HPV-аланин)-SH получали, как описано в примере 18, за исключением того, что использовали 70 кДа PHF-GA-SSpy (GA 10%, SSPy 4,8%, 58,2 мг, 0,727 мкмоль, полученный, как описано в примере 5), NHS (0,843 мг, 7,27 мкмоль), EDC (1,39 мг, 7,27 мкмоль) и HPV-аланин (10,4 мг, 10,9 мкмоль). Выход 82% (в расчете на полимер); 10,9% по массе HPV.
Пример 21. Синтез 70 кДа PHF-GA-(HPV-аланин)-(трастузумаб-MCC)

Названное соединение получали, как описано в примере 19, за исключением того, что использовали трастузумаб-MCC (20 мг, полученный, как описано в примере 3) и 70 кДа PHF-GA-(HPV-аланин)-SH (11,2 мг, полученный как описано в примере 20). Содержание HPV, определенное методом ВЭЖХ, давало, в среднем, мольное отношение HPV к антителу приблизительно от 47:1 до 50:1.
Пример 22. Синтез (S)-2HPV
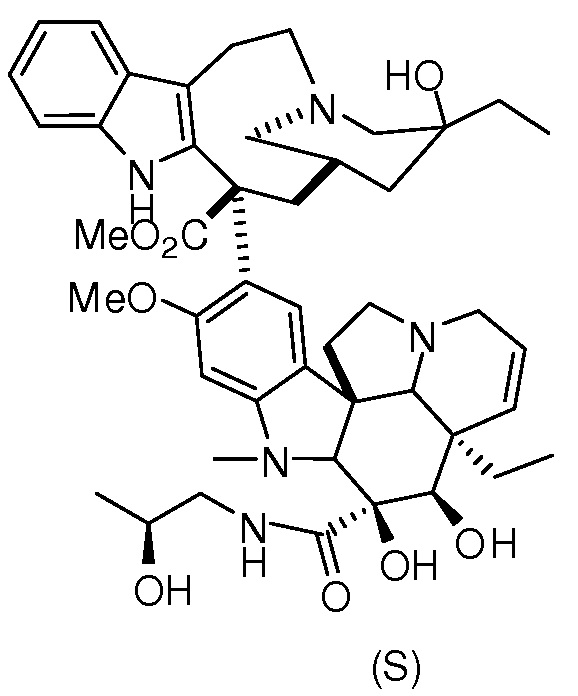
Винбластина дезацетил-гидразид (400 мг, 0,520 ммоль, полученный, как описано в J. Med. Chem., 21, 88-96, 1978) в MeOH (5 мл) смешивали с 1N HCl (15 мл) при 0°C, затем добавляли одной порцией нитрит натрия (93 мг, 1,353 ммоль). Реакционную смесь перемешивали в течение 12 минут, затем корректировали pH до значения 7,6 при 0°C с помощью насыщенного раствора NaHCO3. Реакционную смесь экстрагировали с помощью DCM (3 × 50 мл). Объединенные фракции DCM промывали солевым раствором, сушили над MgSO4 и фильтровали через слой MgSO4. Объем уменьшали до 10 мл, и 5 мл использовали для реакции сочетания с (S)-1-аминопропан-2-олом.
(S)-1-аминопропан-2-ол (205 мкл, 2,6 ммоль) в безводном DCM (2 мл) добавляли по каплям к холодному перемешиваемому раствору винбластина дезацетил-гидразида (полученного, как описано выше) в атмосфере аргона. Реакционную смесь перемешивали при 0°C в течение нескольких часов и затем доводили до комнатной температуры. Метод LC/MS показывал превращение в названное соединение. Неочищенную реакционную смесь загружали непосредственно в колонку CombiFlash (40 g колонка) для очистки.
Колонку CombiFlash предварительно обрабатывали этилацетатом (1% TEA). После введения пробы начальные условия поддерживали в течение 2 минут, затем применяли градиент от 10% MeOH (1% TEA) до этилацетата (1% TEA) в течение 10 минут и затем выдержку. Названное соединение элюировалось на ~12 минуте. Элюированное соединение концентрировали с получением 96 мг (46% выход). m/z(+) 812,4.
Пример 23. Синтез (R)-2HPV

Названное соединение получали, как описано в примере 21, за исключением того, что (R)-1-аминопропан-2-ол (205 мкл, 2,6 ммоль) использовали вместо (S)-1-аминопропан-2-ола, с получением 97 мг (46% выход)
Пример 24. Синтез (PI-103)-4-(2-аминоэтил)пиперазин-1-карбоксилата дигидрохлорида

К смеси PI-103 (50 мг, 0,144 ммоль) и TEA (60 мкл, 0,431 ммоль) в сухом DMF (2,5 мл) добавляли 4-нитрофенилхлорформиат (35 мг, 0,172 ммоль), и полученную смесь перемешивали при комнатной температуре. Через 45 минут добавляли 2-пиперазин-1-илэтилкарбаминовой кислоты третбутиловый эфир (56 мг, 0,244 ммоль), и реакционную смесь затем перемешивали в течение ночи при комнатной температуре, затем удаляли растворитель под высоким вакуумом. Остаток растворяли в DCM (50 мл) и затем промывали последовательно водой (15 мл) и солевым раствором (15 мл). Органическую фазу сушили над Na2SO4 и концентрировали под вакуумом. Неочищенный продукт очищали на силикагеле (4 g колонка CombiFlash, MeOH:DCM (0% MeOH 1-2 минуты, затем градиент до 7% MeOH в течение 15 минут) с получением BOC-защищенного карбамата в виде бесцветной пленки. ESI-MS расчетная для C31H38N7O6 604,3 (M + H+), полученная 604,3.
К очищенному BOC-защищенному карбамату добавляли DCM (5 мл) и 4M HCl в диоксане (5 мл). Смесь перемешивали в течение 1 часа при комнатной температуре и затем концентрировали под вакуумом. Полученный незащищенный PI-103 растворяли в воде и затем лиофилизировали с получением названного соединения в виде бледно-желтого твердого вещества (69 мг, 83% суммарный выход). ESI-MS рассчитанная для C26H30N7O4 504,2 (M + H+), полученная 504,2.
Пример 25. Синтез (PI-103)-4-аминобутилкарбамата гидрохлорида

Названное соединение получали, как описано в примере 24, за исключением того, что синтез проводили на меньшем количестве вещества PI-103 (25 мг), и BOC-1,4-диаминобутан (23 мг, 0,122 ммоль) использовали вместо 2-пиперазин-1-илэтилкарбаминовой кислоты третбутилового эфира с получением названного соединения (13 мг, 36% суммарный выход). ESI-MS рассчитанная для C24H27N6O4 463,2 (M + H+), полученная 463,2.
Пример 26 Синтез 10 кДа PHF-GA-(PI-103)-4-аминобутилкарбамат-SH

К раствору 10 кДа PHF-GA-SSpy (GA 25%, SSPy 3,8%, 30 мг, 2,38 мкмоль, полученного как описано в примере 5) в 1:1 CH3CN/H2O (400 мкл) добавляли NHS (18 мкл исходного раствора 96 мг/мл в CH3CN, 1,7 мг), EDC (78 мкл свежеприготовленного исходного раствора в воде, 37,3 мг/мл, 2,9 мг), затем раствор (PI-103)-4-аминобутилкарбамата гидрохлорида (5,35 мг, 10,7 мкмоль, полученного как описано в примере 25) в 1:1 CH3CN/H2O (200 мкл). Добавляли дополнительное количество CH3CN (100 мкл) для улучшения растворимости. Корректировали рН до значения 5,7-5,8, и смесь перемешивали в течение 1 часа при комнатной температуре. Добавляли дополнительное количество CH3CN (100 мкл) и перемешивание продолжали в течение ночи. Анализ с помощью ВЭЖХ неочищенной реакционной смеси указывал на 92% введение (PI-103)-4-аминобутилкарбамата. Корректировали рН до значения 6,0, и затем неочищенную смесь разбавляли с помощью 1% водного раствора NaCl (10 мл) и фильтровали через шприцевой фильтр 0,2 мкм. Неочищенный продукт очищали путем перемешиваемой ячеечной фильтрации на мембране из регенерированной целлюлозы с номинальным отсечением по молекулярной массе 3 кДа, затем лиофилизировали с получением бесцветного твердого вещества (26 мг, 1,82 мкмоль, 76% выход). Продукт (26 мг, 1,82 мкмоль) растворяли в PBS (25 мМ, pH 7, 1 мл) и затем обрабатывали с помощью DTT (10,4 мг, 0,067 ммоль). Смесь перемешивали в течение приблизительно 1 часа при комнатной температуре и затем очищали путем перемешиваемой ячеечной фильтрации на мембране из регенерированной целлюлозы с номинальным отсечением по молекулярной массе 3 кДа с получением водного раствора названного соединения.
Пример 27. Синтез 10 кДа PHF-GA-(PI-103)-4-аминобутилкарбамат-(трастузумаб-MCC)

Названный конъюгат получали так же, как описано в примере 7, за исключением того, что использовали трастузумаб-MCC (10 мг, полученный, как описано в примере 3) и 10 кДа PHF-GA-(PI-103)-4-аминобутилкарбамат-SH (11,2 мг, полученный, как описано в примере 26).
Пример 28. Синтез 10 кДа PHF-GA-(PI-103)-4-(2-аминоэтил)пиперазин-1-карбамат-SH

Названное соединение получали так же, как описано в примере 26, за исключением того, что использовали 10 кДа PHF-GA-SSpy (GA 25%, SSPy 3,8%, 30 мг, 3,38 мкмоль, полученный, как описано в примере 5), NHS (1,7 мг, 15 мкмоль), EDC (2,88 мг, 15 мкмоль) и (PI-103)-4-(2-аминоэтил)пиперазин-1-карбоксилата дигидрохлорид (5,49 мг, 9,52 мкмоль, полученный, как описано в примере 24). Выход 80%.
Пример 29. Синтез 10 кДа PHF-GA-(PI-103)-4-(2-аминоэтил)пиперазин-1-карбамат-(трастузумаб-MCC)

Названный конъюгат получали так же, как описано в примере 7, за исключением того, что использовали трастузумаб-MCC (10 мг, полученный, как описано в примере 3) и 10 кДа PHF-GA-(PI-103)-4-(2-аминоэтил)пиперазин-1-карбамат-SH (11,2 мг, полученный, как описано в примере 28).
Пример 30. Синтез (PI-103)-4-аминобутилкарбоната гидрохлорида
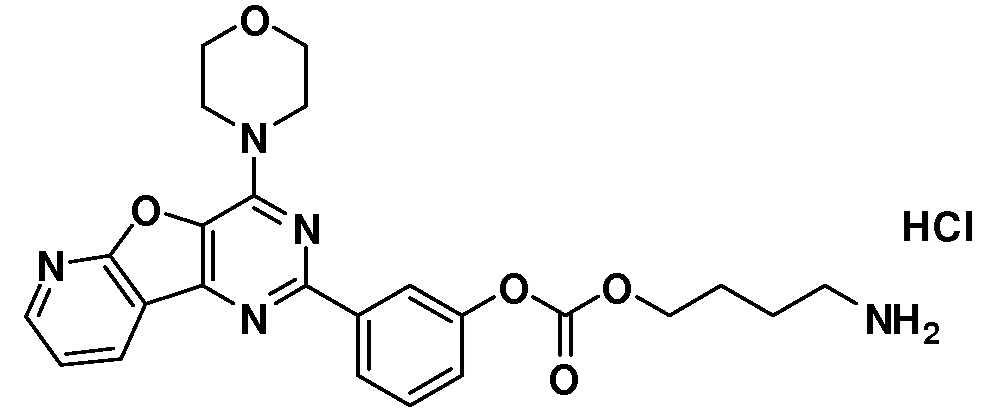
В охлажденный льдом раствор трифосгена (13,6 мг, 0,046 ммоль) в сухом THF (0,5 мл) добавляли раствор третбутил 4-гидроксибутилкарбамата (24,2 мг, 0,128 ммоль) и TEA (18,1 мкл, 0,13 ммоль) в сухом THF (1 мл) в атмосфере аргона. После перемешивания в течение 1 часа при 0°C, неочищенный хлорформиат медленно добавляли к раствору PI-103 (25 мг, 0,072 ммоль) и TEA (15,1 мкл, 0,108 ммоль) в NMP (0,5 мл). Через несколько минут THF удаляли под вакуумом и добавляли NMP (0,5 мл), для того чтобы сделать смесь более гомогенной. Полученную смесь перемешивали в течение ночи при комнатной температуре. Добавляли дополнительное количество хлорформиата (из 45 мг BOC-спирт, полученного, как описано выше) и TEA (15 мкл), и реакционную смесь перемешивали в течение 40 минут, и в этот момент времени метод LC/MS указывал на 95% превращение в требуемый продукт. Реакционную смесь разбавляли с помощью DCM (150 мл) и затем промывали водой (2 × 50 мл) и солевым раствором (50 мл). Органическую фазу сушили над Na2SO4 и концентрировали под вакуумом. Неочищенный продукт очищали на силикагеле (4 g, колонка CombiFlash, EtOAc:Hex, 0% EtOAc 1 минута, затем градиент до 80% EtOAc в течение 16 минут) с получением 26 мг бесцветной пленки. Выход 64%. ESI-MS рассчитанная для C29H34N5O7 564,3 (M + H+), полученная 564,1.
BOC-защищенный карбонат растворяли в DCM (2 мл) и затем обрабатывали с помощью 4M HCl в диоксане (4 мл). Полученную смесь перемешивали в течение 3,5 часов и затем концентрировали под вакуумом. Незащищенный карбонат лиофилизировали из смеси вода:CH3CN с получением названного соединения в виде бледно-желтого твердого вещества (21,9 мг, 96% выход). ESI-MS рассчитанная для C24H26N5O5 464,2 (M + H+), полученная 464,1.
Пример 31. Синтез 10 кДа PHF-GA-(PI-103)-4-аминобутил-карбонат-SH

Названное соединение получали так же, как описано в примере 26, за исключением того, что использовали 10 кДа PHF-GA-SSpy (GA 25%, SSPy 3,8%, 30 мг, 3,38 мкмоль, полученный, как описано в примере 5), NHS (1,7 мг, 15 мкмоль), EDC (2,88 мг, 15 мкмоль) и (PI-103)-4-аминобутилкарбоната гидрохлорид (5,35 мг, 10,7 мкмоль, полученный, как описано в примере 30). Выход 76%.
Пример 32. Синтез 10 кДа PHF-GA-(PI-103)-4-аминобутилкарбонат-(трастузумаб-MCC)
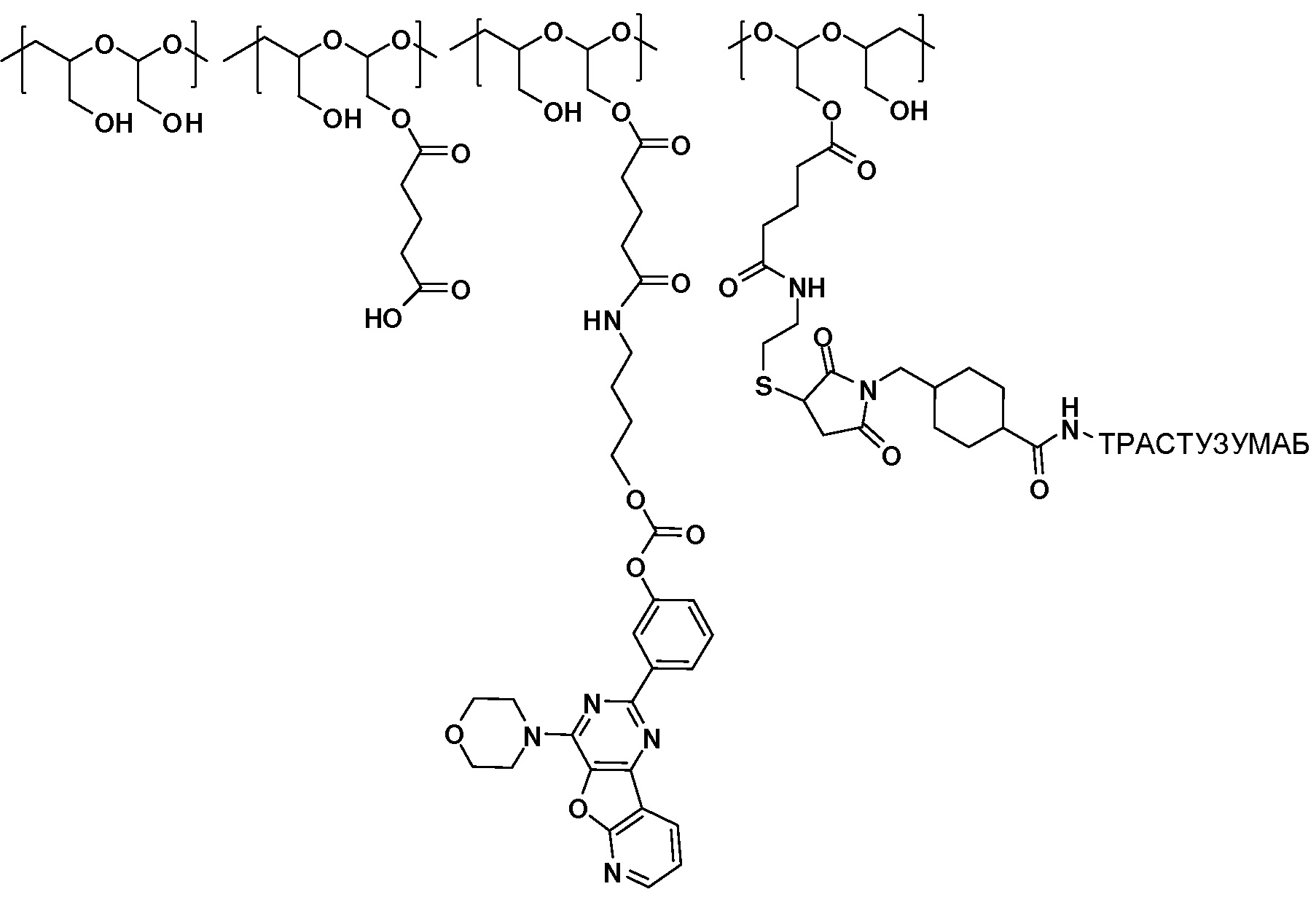
Названный конъюгат получали так же, как описано в примере 7, за исключением того, что использовали трастузумаб-MCC (10 мг, полученный, как описано в примере 3) и 10 кДа PHF-GA-(PI-103)-(4-аминобутилкарбонат)-SH (11,2 мг, полученный, как описано в примере 31). Выход 30%.
Пример 33. Синтез (PI-103)-(S)-2-амино-3-метилбутаноата гидрохлорида

К раствору PI-103 (25 мг, 0,072 ммоль) в NMP (~750 мкл) добавляли смесь HATU (32,7 мг, 0,086 ммоль), DIEA (30,2 мкл, 0,173 ммоль) и BOC-Val-OH (0,086 ммоль, 18,7 ммоль) в NMP. Полученную смесь перемешивали, защищая от воздействия света, в течение 3 дней при комнатной температуре. Затем добавляли раствор BOC-Val-OH (15,6 мг, 0,072 ммоль), HATU (27,4 мг, 0,072 ммоль) и DIEA (25,1 мкл, 0,144 ммоль) в NMP (200 мкл). Реакционную смесь перемешивали в течение ~18 часов при 50°C и затем добавляли DMAP (0,072 ммоль, 8,8 мг). Смесь перемешивали в течение еще 1,5 часов при 50°C, затем реакцию останавливали разбавленной кислотой. Реакционную смесь разбавляли с помощью DCM и затем промывали водой (2 × 50 мл) и солевым раствором (50 мл). BOC-защищенный эфир валина очищали на силикагеле (4 g, колонка Combiflash, EtOAc:Hex, 0% EtOAc, выдержка в течение 1 минуты, затем градиент до 50% EtOAc в течение 16 минут).
BOC-защищенный эфир валина растворяли в DCM (5 мл) и затем обрабатывали с помощью 4M HCl в диоксане (5 мл). Смесь перемешивали в течение 6 часов при комнатной температуре и затем концентрировали досуха под вакуумом. Незащищенный эфир валина лиофилизировали из смеси вода:CH3CN с получением названного соединения в виде бледно-желтого твердого вещества (13,6 мг, суммарный выход 39%). ESI-MS рассчитанная для C24H26N5O4 448,2 (M + H+), полученная 448,2.
Пример 34. Синтез 10 кДа PHF-GA-(PI-103)-(S)-2-амино-3-метилбутаноат-SH

Названное соединение получали так же, как описано в примере 26, за исключением того, что использовали 10 кДа PHF-GA-SSpy (GA 25%, SSPy 3,8%, 41,4 мг, 3,38 мкмоль, полученный, как описано в примере 5), NHS (2,81 мг, 25 мкмоль), EDC (4,85 мг, 25 мкмоль) и (PI-103)-(S)-2-амино-3-метилбутаноата гидрохлорид (6,38 мг, 13 мкмоль, полученный, как описано в примере 33).
Пример 35. Синтез 10 кДа PHF-GA-((PI-103)-(S)-2-амино-3-метилбутаноат-трастузумаб-MCC)

Названный конъюгат получали так же, как описано в примере 7, за исключением того, что использовали трастузумаб-MCC (10 мг, полученный, как описано в примере 3) и 10 кДа PHF-GA-(PI-103)-(S)-2-амино-3-метилбутаноат-SH (11,2 мг, полученный, как описано в примере 34).
Пример 36. Синтез (AZD 8330)-(S)-2-аминопропаноата гидрохлорида

К раствору BOC-Ala-OH (61,5 мг, 0,325 ммоль) в сухом THF (1,5 мл) добавляли DIC (20,5 мг, 0,163 ммоль). Полученную смесь охлаждали до 0°C в атмосфере аргона и перемешивали в течение 10-15 минут. Добавляли смесь AZD 8330 (50 мг, 0,108 ммоль) и DMAP (1,3 мг, 0,0108 ммоль) в сухом THF (1,5 мл), и реакционную смесь перемешивали в течение 1,5 часов при комнатной температуре с защитой от воздействия света. Реакционную смесь разбавляли с помощью EtOAc и затем промывали насыщенным раствором NH4Cl, затем солевым раствором. Органическую фазу сушили над Na2SO4, затем концентрировали под вакуумом. Неочищенный материал очищали на силикагеле (колонка Combiflash, ацетон:DCM, 0% ацетона, выдержка в течение 1-2 минут, затем градиент до 20% ацетона) с получением 37 мг бесцветного твердого вещества. Твердое вещество растворяли в DCM (5 мл) и затем обрабатывали с помощью 4M HCl в диоксане (10 мл). Смесь перемешивали, защищая от воздействия света, при комнатной температуре в течение приблизительно 5 часов. Растворитель удаляли под вакуумом, и остаток лиофилизировали с получением названного соединения в виде бледно-оранжевого твердого вещества (22,4 мг, 39% суммарный выход).
Пример 37. Синтез 10 кДа PHF-GA-(AZD 8330)-(S)-2-амино-пропаноат-SH

Названное соединение получали так же, как описано в примере 26, за исключением того, что использовали 10 кДа PHF-GA-SSpy (GA 25%, SSPy 3,8%, 30 мг, 3,38 мкмоль, полученный, как описано в примере 5), NHS (1,7 мг, 15 мкмоль), EDC (2,88 мг, 15 мкмоль) и (AZD 8330)-(S)-2-аминопропаноата гидрохлорид (6,44 мг, 9,9 мкмоль, полученный, как описано в примере 36).
Пример 38. Синтез 10 кДа PHF-GA-(AZD 8330)-(S)-2-аминопропаноат-(трастузумаб-MCC)

Названное соединение получали так же, как описано в примере 7, за исключением того, что использовали трастузумаб-MCC (10 мг, полученный, как описано в примере 3) и 10 кДа PHF-GA-(AZD 8330)-(S)-2-аминопропаноата гидрохлорид-SH (15,2 мг, полученный, как описано в примере 37). Мольное отношение AZD 8330 к антителу составляло, в среднем, приблизительно от 2:1 до 6:1
Пример 39. Синтез 1-аминопропан-2-ил-ауристатин F трифтор-ацетата

К ауристатину F (150,0 мг, 0,201 ммоль) и HOBt (32,6 мг, 0,241 ммоль) в 5 мл дихлорметана добавляли диизопропил-карбодиимид (68,5 мкл, 0,442 ммоль). Смесь перемешивали при 0°C в течение 10 минут, и в этот момент времени наблюдалось образование осадка. Добавляли третбутил-2-гидроксипропил-карбамат (881,0 мг, 5,03 ммоль) в 2 мл дихлорметана. Реакционную смесь перемешивали при 45°C в герметизированной пробирке, и ход реакции постоянно контролировали методом LCMS. Добавляли дополнительное количество HOBt (30,0 мг, 0,222 ммоль) в момент времени 2,5 часа и 6 часов, и смесь перемешивали в течение 18 часов. Добавляли дополнительное количество HOBt (54,3 мг, 0,402 ммоль) и диизопропилкарбодиимида (43,1 мг, 0,342 ммоль), и смесь перемешивали при 45°C в течение еще 9 часов, и в этот момент времени анализ LCMS показывал полное расходование исходного материала. Растворитель удаляли при пониженном давлении, и остаток растворяли в 3 мл DMF. Пробу очищали с помощью препаративной ВЭЖХ; (градиент 10-90% растворителя B в течение 10 минут, элюируя с помощью 0,1%TFA/вода, 0,1%TFA/CH3CN). Воду удаляли лиофилизацией с получением названного соединения в виде белого твердого вещества.
1-(Третбутоксикарбониламино)пропан-2-ил-ауристатин F (150 мг, 0,166 ммоль) переносили в дихлорметан (5 мл) и добавляли 2,2,2-трифторуксусную кислоту (0,256 мл, 3,32 ммоль). Смесь перемешивали при 23°C в течение 30 минут, и в этот момент времени метод LC/MS указывал на полную конверсию. Объем растворителя уменьшали до 1 мл при пониженном давлении. Добавление по каплям раствора к перемешиваемому диэтиловому эфиру давало названное соединение (27,5 мг, 0,027 ммоль, выход 16%) в виде белого твердого вещества, которое собирали фильтрацией.
Пример 40. Синтез 10 кДа PHF-GA-(1-аминопропан-2-ил- ауристатин F)-SH

10K PHF-GA(28%)-SSPyr(10%) (76,0 мг, 5,93 мкмоль), полученного как описано в примере 5, переносили в воду (5 мл) и ацетонитрил (3 мл) и охлаждали до 0°C. Добавляли NHS (6,82 мг, 0,059 ммоль в 500 мкл воды), затем 1-аминопропан-2-ил-ауристатин F трифторацетат (27,5 мг, 0,027 ммоль, полученный, как описано в примере 39) и EDC (11,4 ммоль, 0,059 ммоль в 500 мкл воды). Корректировали рН до значения 6 с помощью 0,1N NaOH, и реакционную смесь подогревали до комнатной температуры и перемешивали в течение ночи. Корректировали рН до значения 7,5 с помощью 1M NaHCO3 и добавляли (2S,3S)-1,4-димеркаптобутан-2,3-диол (100 мг, 0,648 ммоль). Смесь перемешивали при 23°C в течение 30 минут, разбавляли до 15 мл водой и очищали диализом через 3K мембрану из регенерированной целлюлозы, элюируя с помощью 1% NaCl/вода (3 × 10 мл) и воды (3 × 10 мл). Образец (76 мг) разбавляли до 5 мл и хранили при 2-8°C.
Пример 41. Синтез 10 кДа PHF-GA-(1-аминопропан-2-ил-ауристатин F)-(трастузумаб-MCC)
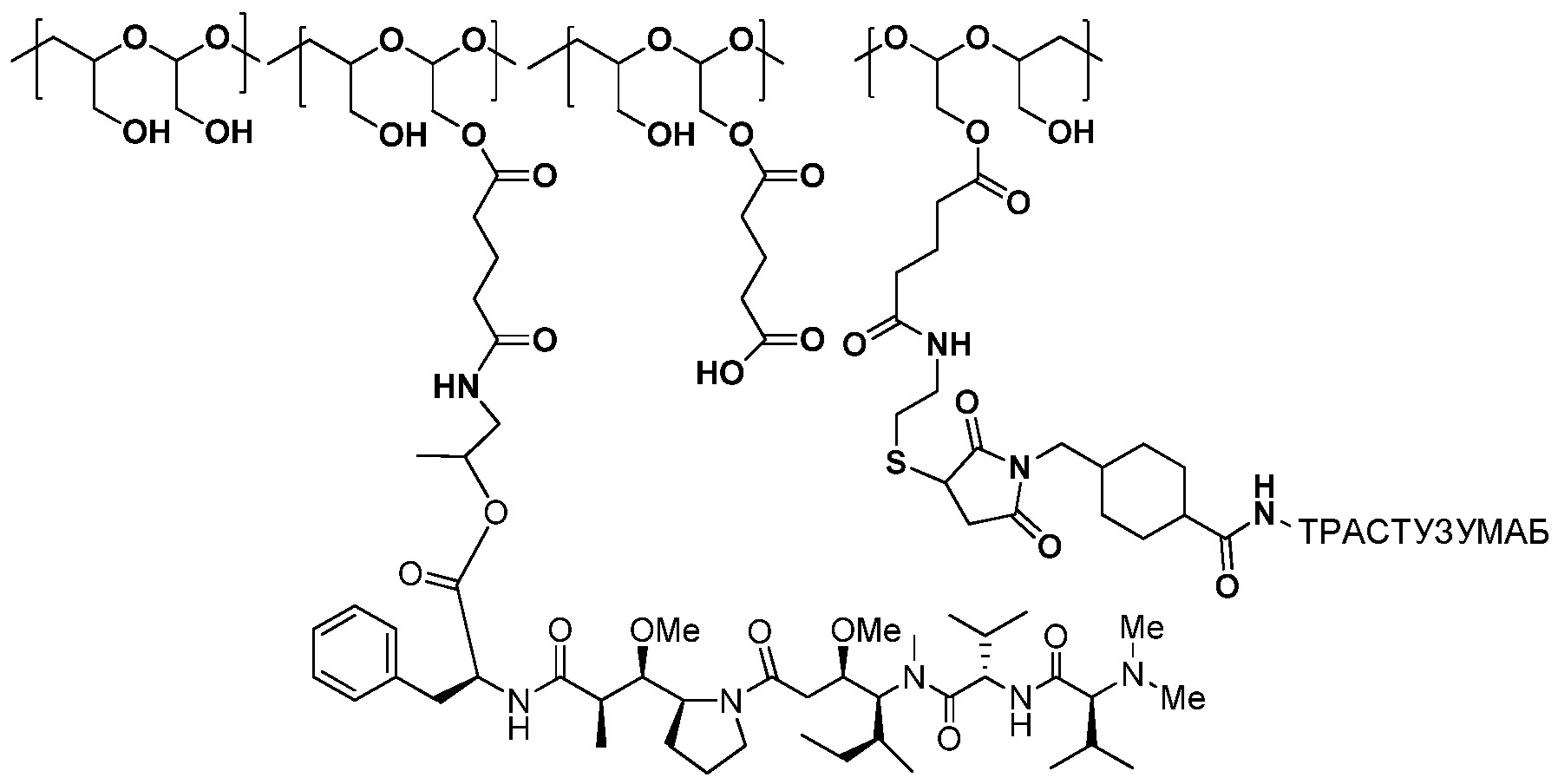
Названный конъюгат получали так же, как описано в примере 7, за исключением того, что использовали трастузумаб-MCC (5 мг, полученный, как описано в примере 3) и 10 кДа PHF-GA-(1-аминопропан-2-ил-ауристатин F)-SH (4,44 мг, полученный, как описано в примере 40, GA 19%, SH 4,8%).
Пример 42. Синтез RD-S1-BOC-амина

RD-S1 (48,5 мг, 0,055 ммоль, полученный в соответствии с методиками, описанными в патентном документе WO 2008/138561) переносили в CH2Cl2 (1 мл) и раствор охлаждали до 0°C. Добавляли EDC (0,127 мл, 0,82 ммоль) и N,N-диметилпиридин-4-амин (33,4 мг, 0,273 ммоль). Реакционную смесь перемешивали при 0°C в течение 20 минут и затем добавляли третбутил 2-гидроксипропилкарбамат (0,094 мл, 0,546 ммоль). Реакционную смесь подогревали до комнатной температуры и перемешивали в течение 24 часов. Образец очищали препаративной ВЭЖХ, элюируя с помощью 0,1% TFA/CH3CN и 0,1% TFA/вода, затем лиофилизировали с получением названного соединения (20,3 мг, 40% выход) в виде бежевого твердого вещества.
Пример 43. Синтез RD-S1-амина

RD-S1-BOC-амин (20,3 мг, 0,022 ммоль, полученный, как описано в примере 42) переносили в CH2Cl2 (0,500 мл) и охлаждали до 0°C. Добавляли по каплям 2,2,2-трифторуксусную кислоту (200 мкл, 2,61 ммоль), затем перемешивали при комнатной температуре в течение 30 минут. Растворитель удаляли при пониженном давлении. Полученное масло переносили в CH2Cl2, затем добавляли эфир с получением названного соединения в виде бежевого твердого вещества (18,1 мг, 100% выход).
Пример 44. Синтез PHF-GA-RD-S1-амин-SH

PHF-GA-SSpy (40,2 мг, 3,19 мкмоль, PHF-GA-SSpy, полученный, как описано в примере 5) переносили в смесь воды (2 мл) и CH3CN (2 мл) и охлаждали до 0°C. Добавляли NHS (3,67 мг, 0,032 ммоль), затем водный раствор EDC (6,12 мг, 0,032 ммоль) и RD-S1-амин (18,1 мг, 0,019 ммоль, полученный, как описано в примере 43) в воде (1 мл). Корректировали рН полученной смеси до значения 6,0-6,5 и затем перемешивали при комнатной температуре в течение ночи. Корректировали рН до значения 7,5 с помощью 1M NaHCO3 и добавляли DTT (10 мг, 0,065 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 30 минут, разбавляли до 15 мл водой, фильтровали через фильтр с размером пор 2 микрона и очищали диализом, используя мембрану из регенерированной целлюлозы (номинальное отсечение по молекулярной массе 3 K), затем промывали 1% NaCl/вода (3 × 10 мл) и затем водой (2 × 10 мл). Названный продукт получали с 61% выходом (в расчете на тубулизин), SH содержание 3,8%.
Путем замены RD-S1-амина другими фрагментами лекарственных средств или производными лекарственных средств в описанных выше методиках, можно синтезировать другие конъюгаты лекарственное средство-полимер.
Пример 45. Синтез XMT-A2

К раствору XMT-A1 (5,03 мг, 6,74 мкмоль) в DMF (33 мкл) при 0°C в атмосфере аргона добавляли TEA (1,88 мкл, 0,013 ммоль). Смесь перемешивали в течение 5 минут и затем добавляли (2-(пиридин-2-илдисульфанил)этил гидразинкарбоксилат (2,48 мг, 10,1 мкмоль) в DMF (20 мкл) и HATU (3,85 мг, 10,1 мкмоль). Реакционную смесь подогревали до комнатной температуры, перемешивали в течение 2,5 часов, разбавляли смесью воды (750 мкл) и CH3CN (1 мл) и затем очищали препаративной ВЭЖХ, элюируя с помощью 0,1% TFA/CH3CN и 0,1% TFA/вода, и затем лиофилизировали с получением названного соединения (8,64 мг, 65,2% выход) в виде белого твердого вещества.
Пример 46. Синтез XMT-A3
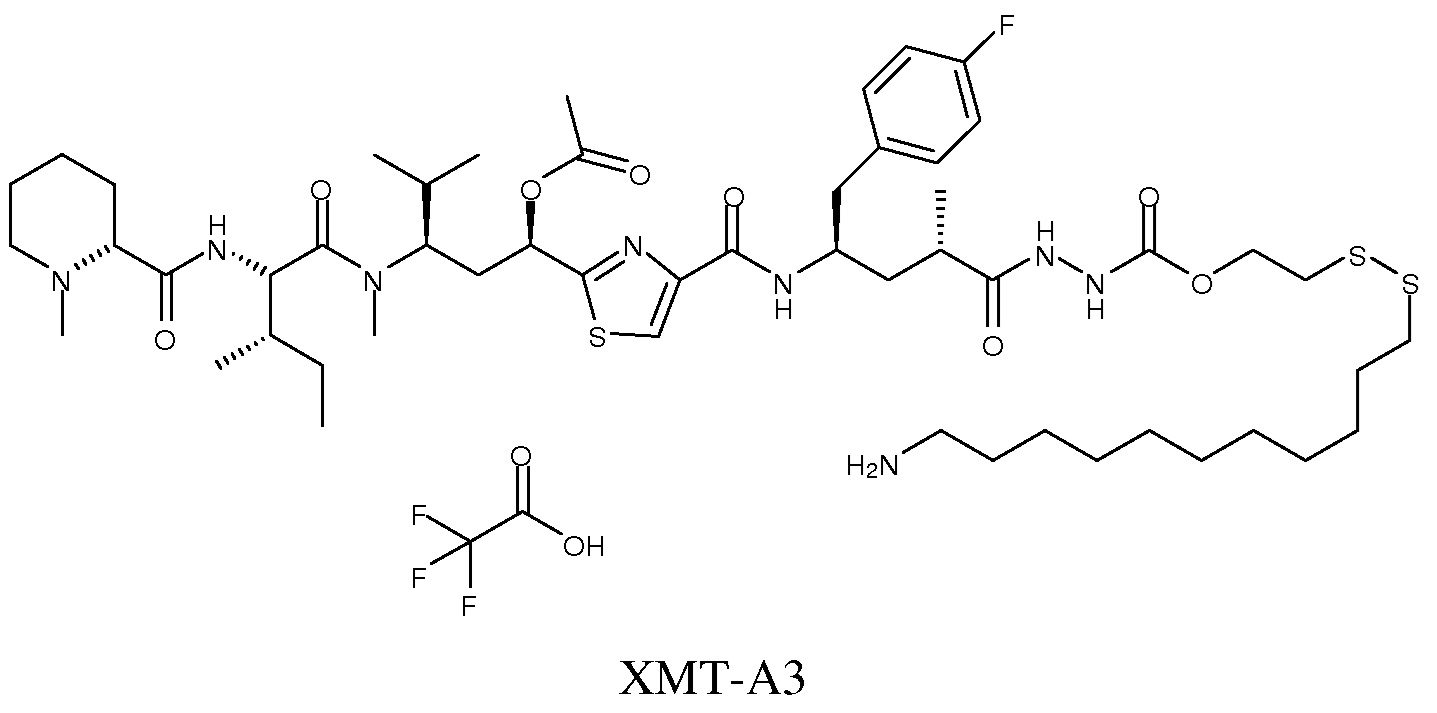
XMT-A2 (11,9 мг, 0,012 ммоль, полученный, как описано в примере 45) растворяли в DMF (0,3 мл) и добавляли 11-амино-ундекан-1-тиола гидрохлорид (29,5 мг, 0,123 ммоль) в DMF (0,3 мл) при 0°C. Реакционную смесь подогревали до комнатной температуры и перемешивали в течение 2 дней, разбавляли водой (2 мл) и очищали препаративной ВЭЖХ, затем лиофилизировали с получением названного соединения (6,02 мг, 46% выход) в виде белого твердого вещества.
Пример 47. Синтез 70 кДа PHF-GA-(XMT-A3)

70 KDa PHF-GA (57,4 мг, 0,217 ммоль, полученный в соответствии с методикой, описанной в примере 2, с 70 KDa PHF, 9% GA) растворяли в смеси воды (2,17 мл) и DMF (0,05 мл). Добавляли XMT-A3 (12,8 мг, 10,9 мкмоль, полученный, как описано в примере 46) в DMF (0,05 мл) и корректировали рН до значения 5-6. Полученный раствор охлаждали до 0°C и добавляли порциями EDC (4,16 мг, 0,022 ммоль) в течение 4 часов. Реакционную смесь перемешивали в течение 6 часов при pH 5,0-6,0. Очистка гельфильтрующей хроматографией с элюированием водой давала названное соединение (40 мг, 5% (по массе) тубулизин).
Пример 48. Синтез ауристатин F-гидроксипропиламида

Ауристатин F (150 мг, 0,201 ммоль), HATU (153,0 мг, 0,402 ммоль) и диизопропилэтиламин (108 мкл, 0,603 ммоль) переносили в DMF (5 мл) и добавляли 3-аминопропан-1-ол (45,9 мкл, 0,603 ммоль). Смесь перемешивали при 23°C в течение 45 минут, и к этому моменту времени LCMS анализ указывал на полное расходование исходного материала. Уменьшали объем до 1,4 мл под высоким вакуумом, затем очищали препаративной ВЭЖХ (градиент 10-90% растворитель B в течение 20 минут, элюируя с помощью 0,1 TFA/вода, 0,1 TFA/CH3CN) с получением названного соединение в виде белого твердого вещества (109 мг, 68% выход).
Пример 49. Синтез ауристатин F-гидроксипропиламид Boc-L-аланина

BOC-L-аланин (117,0 мг, 0,618 ммоль) и DMAP (94,0 мг, 0,772 ммоль) переносили в дихлорметан и затем добавляли диизопропилкарбодиимид (52,6 мкл, 0,340 ммоль). Реакционную смесь охлаждали до 0°C и перемешивали в течение 10 минут, после чего добавляли ауристатин F-гидроксипропиламид (124 мг, 0,154 ммоль, полученный, как описано в примере 48). Реакционную смесь подогревали до 23°C и перемешивали в течение 18 часов. Очистка препаративной ВЭЖХ и затем удаление воды лиофилизацией давала названное соединение в виде бежевого твердого вещества (112 мг, 75% выход).
Пример 50. Синтез ауристатин F-гидроксипропиламид-L-аланина

Ауристатин F-гидроксипропиламид Boc-L-аланин (112 мг, 0,115 ммоль, полученный, как описано в примере 49) переносили в дихлорметан (3 мл) и добавляли избыток трифторуксусной кислоты. Смесь перемешивали при 23°C в течение 1 часа, и растворитель удаляли под высоким вакуумом. Полученное масло переносили в дихлорметан (1,5 мл), и проводили осаждение из диэтилового эфира (30 мл) с получением названного соединения в виде белого твердого вещества (96,2 мг, 85%).
Пример 51. Синтез 10K PHF-GA-SH-(ауристатин F-гидроксипропиламид-L-аланин)

10K PHF-GA(28%)-SSPyr(10%) (135,0 мг, 10,49 мкл, полученный, как описано в примере 5) переносили в воду (8 мл) и ацетонитрил (4 мл) и охлаждали до 0°C. Добавляли 1-NHS (12,07 мг, 0,105 ммоль), затем EDC (20,11 мг, 0,105 ммоль) и ауристатин F-гидроксипропиламид-L-аланин (52,02 мг, 0,047 ммоль, полученный, как описано в примере 50). Корректировали рН до значения 6 с помощью 0,1N NaOH, и смесь перемешивали при 23°C в течение 18 часов. Корректировали рН до значения 7,5 с помощью 1M NaHCO3 и добавляли (2S,3S)-1,4-димеркаптобутан-2,3-диол (90 мг, 0,583 ммоль). Смесь перемешивали при 23°C в течение 30 минут, затем разбавляли до 15 мл водой. Материал очищали диализом через 3K мембрану из регенерированной целлюлозы, элюируя с помощью 1% NaCl/вода (3 × 10 мл) и воды (3 × 10 мл). Образец разбавляли до 5 мл и хранили при 2-8°C. (145,0 мг, ауристатин F 14,06 мг/мл).
Пример 52. Синтез 10 кДа PHF-GA-(ауристатин F-гидроксипропиламид-L-аланин)-(трастузумаб-MCC)

К трастузумаб-MCC (400 мг, полученному, как описано в примере 3) в PBS (20 мл, pH 7,0) добавляли 10 кДа PHF-GA-SH-(ауристатин F-гидроксипропиламид-L-аланин) (106 мг, полученный, как описано в примере 51) в воде (10 мл). Раствор перемешивали при комнатной температуре в течение 4 часов при pH 7,0. Полученный продукт очищали гель-фильтрацией, используя колонку Superpose-6 с PBS в качестве элюента (50% выход). Молекулярная масса PHF-GA-(ауристатин F-гидроксипропиламид-L-аланин)-(трастузумаб-MCC), определенная с помощью SEC, составляла около 170 кДа. Содержание ауристатина F, определенное методом LC-MS, давало, в среднем, мольное отношение ауристатина F к антителу приблизительно от 20:1 до 22:1. Для 10 кДа PHF-GA-(ауристатин F-гидроксипропиламид-L-аланин)-(трастузумаб-MCC), приведенного на фигуре 3, мольное отношение ауристатина F к трастузумабу составляло приблизительно от 20:1 до 22:1, и для приведенного на фигуре 8, мольное отношение ауристатина F к трастузумабу составляло приблизительно от 24:1 до 28:1.
Пример 53. Синтез производного ритуксимаб-MCC

Названное соединение получали, как описано в примере 3. Ритуксимаб использовали вместо трастузумаба. Анализ показал, что в среднем от 5 до 6 групп MCC были связаны с одним ритуксимабом.
Пример 54. Синтез 10 кДа PHF-GA-(HPV-аланин)-(ритуксимаб-MCC)

Названное соединение получали в соответствии с методикой, описанной в примере 7, за исключением того, что ритуксимаб-MCC (полученный, как описано в примере 53) использовали вместо трастузумаб-MCC. Содержание HPV, определенное методом ВЭЖХ, показало, что, в среднем, мольное отношение HPV к ритуксимабу составляет приблизительно от 12:1 до 15:1.
Пример 55. Синтез 10 кДа PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (5:1)

Названное соединение получали в соответствии с методикой, описанной в примере 7, за исключением того, что содержание HPV, определенное методом ВЭЖХ, давало, в среднем, мольное отношение HPV к антителу приблизительно 5:1.
Пример 56. Синтез 10 кДа PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (10:1)

Названное соединение получали в соответствии с методикой, описанной в примере 7, за исключением того, что содержание HPV, определенное методом ВЭЖХ, давало, в среднем, мольное отношение HPV к антителу приблизительно 10:1.
Пример 57. Синтез 10 кДа PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (20:1)

Названное соединение получали в соответствии с методикой, описанной в примере 7, за исключением того, что содержание HPV, определенное методом ВЭЖХ, давало, в среднем, мольное отношение HPV к антителу приблизительно 20:1.
Пример 58. Синтез трастузумаб-F(ab)2
Трастузумаб-F(ab)2 синтезировали из иммобилизированного пепсина (15 мл осажденного геля) и трастузумаба (440 мг, 2,4 мкмоль) в соответствии с инструкциями фирмы-производителя (Pierce) с получением названного соединения (265,2 мг, 100% выход).
Пример 59. Синтез 30 кДа PHF-GA-SSPyr-(HPV-аланин)

К раствору 30 кДа PHF-GA (54 мг, 1,49 мкмоль, полученного, как описано в примере 2) в 2 мл CH3CN:H2O (1:1)) добавляли 69 мкл (37 мкмоль) свежеприготовленного исходного раствора NHS (62,4 мг/мл в CH3CN), затем исходный раствор EDC (150 мкл (37 мкмоль) 47,3 мг/мл в воде). Добавляли раствор HPV-аланина гидрохлорида (21,3 мг, 22 мкмоль, полученного, как описано в патентном документе U.S. Publication No. 2010/0305149, Example 1) в 500 мкл смеси CH3CN:вода (1:1), и затем pH реакционной смеси корректировали до значения 5,8. Ход реакции постоянно контролировали с помощью SEC ВЭЖХ (детектирование при 270 нм), и добавляли дополнительное количество EDC в моменты времени 18 часов (7 мг, 0,037 ммоль) и 19 часов (4,5 мг, 0,023 ммоль). Реакционную смесь разбавляли с помощью 30 мл 1% NaCl для снижения концентрации CH3CN до 4% от суммарного реакционного объема. Неочищенную смесь фильтровали через мембрану 0,2 мкм с помощью шприца и затем очищали путем перемешиваемой ячеечной фильтрации на мембране (регенерированная целлюлоза) с номинальным отсечением по молекулярной массе 5000, промывая с помощью 1% NaCl до тех пор, пока малые молекулы не обнаруживались методом SEC ВЭЖХ. И наконец, очищенный материал концентрировали до 2,5 мл и хранили в виде 1% NaCl раствора при -20°C. Выход 86% (в расчете на HPV). Мольное отношение HPV к полимеру составляло в среднем приблизительно от 11:1 до 15:1
Пример 60. Синтез 30 кДа PHF-GA-(HPV-аланин)-(трастузумаб-Fab)

К трастузумаб-F(ab)2 (3,44 мл, 0,325 мкмоль исходного раствора 10,4 мг/мл, полученному, как описано в примере 58) в PBS, pH 7,4 добавляли аликвоту (138 мкл, 0,467 мг) свежеприготовленного исходного раствора TCEP (3,38 мг/мл в Et3NHOAc буфере). Смесь инкубировали в течение 1 часа при 37°C. Реакционную смесь охлаждали до комнатной температуры и затем очищали на колонке PD10, которая предварительно была приведена в равновесие с EtNHOAc буфером. Добавляли раствор 30 кДа PHF-GA-(HPV-аланин)-SSPyr (600 мкл исходного раствора 6,2 мг HPV эквивалентов/мл, 3,72 мг HPV эквивалентов) в 1% NaCl, и раствор перемешивали при комнатной температуре в течение нескольких часов. Полученный конъюгат сначала очищали центрифугированием на мембране с номинальным отсечением по молекулярной массе 10 кДа и необязательно очищали гель-фильтрацией. Молекулярная масса конъюгата PHF-GA-(HPV-аланин)-(трастузумаб-Fab), определенная с помощью SEC, составляла около 108 кДа, при использовании полисахаридов в качестве эталонов молекулярных масс. Содержание HPV, определенное методом ВЭЖХ, давало, в среднем, мольное отношение HPV к трастузумаб-Fab приблизительно от 5:1 до 8:1. Для 30 кДа PHF-GA-(HPV-аланин)-(трастузумаб-Fab), приведенного на фигуре 5, мольное отношение HPV к трастузумаб-Fab составляло приблизительно от 10:1 до 14:1.
Пример 61. Синтез (S) 2-гидроксипропиламид-ауристатин F

К охлаждаемому льдом раствору ауристатина F (50 мг, 0,067 ммоль) в DMF (4 мл) добавляли HATU (51,0 мг, 0,134 ммоль), и полученную смесь перемешивали при охлаждении в течение 20 минут. К смеси добавляли (S)-1-аминопропан-2-ол (10,07 мг, 0,134 ммоль), затем DIEA (0,035 мл, 0,201 ммоль), и смесь перемешивали при охлаждении в течение 1 часа, и затем в течение ночи при комнатной температуре. Очистка препаративной ВЭЖХ и затем лиофилизация давала названное соединение в виде белого аморфного твердого вещества в форме соли TFA (47 мг, 76% выход) M/z=803,4.
Пример 62. Синтез (R) 2-гидроксипропиламид-ауристатин F

Названное соединение получали, как описано в примере 61, за исключением того, что (R)-1-аминопропан-2-ол (10,07 мг, 0,134 ммоль) использовали вместо (S)-1-аминопропан-2-ола. (49 мг, 80% выход) M/z=803,4.
Пример 63. Синтез XMT-A4 пролинового эфира

К охлаждаемому льдом раствору (S)-1-(третбутоксикарбонил)-пирролидин-2-карбоновой кислоты(2,79 мг, 0,013 ммоль) в DMF (250 мкл) добавляли DIC (2,018 мкл, 0,013 ммоль), и полученную смесь перемешивали в течение 15 минут, и затем к раствору добавляли XMT-A4 (5 мг, 6,48 мкмоль) и DMAP (2,374 мг, 0,019 ммоль) в DMF (250 мкл). Реакционную смесь перемешивали при охлаждении и затем при комнатной температуре. Через 4 часа добавляли еще одну аликвоту (S)-1-(третбутоксикарбонил)пирролидин-2-карбоновой кислоты (2,79 мг, 0,013 ммоль), DIC (2,018 мкл, 0,013 ммоль) в 100 мкл DMF, и перемешивание продолжали в течение ночи при комнатной температуре. Неочищенный продукт очищали с помощью ВЭЖХ, затем лиофилизировали с получением Boc-замещенного XMT-A4 в виде белого аморфного твердого вещества (4,4 мг, 63% выход). M/z=969,4.
К охлаждаемому льдом раствору Boc-замещенного соединения XMT-A4 с 2,2,2-трифторуксусной кислотой (1:1) (4,4 мг, 4,06 мкмоль) в DCM (300 мкл) добавляли TFA (31,3 мкл, 0,406 ммоль), и полученную смесь перемешивали при охлаждении в течение 1 часа, затем перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь концентрировали, растворяли в ацетонитриле и лиофилизировали с получением названного соединения в виде белого твердого вещества (2,3 мг, 58% выход). M/z=869,4.
Пример 64. Синтез ауристатина F гидроксипропиламида

К раствору ауристатина F (100 мг, 0,134 ммоль) в DCM (5 мл), охлаждаемому на ледяной/солевой бане, добавляли DIC (0,052 мл, 0,335 ммоль), третбутил 3-гидроксипропилкарбамат (117 мг, 0,670 ммоль) и DMAP (82 мг, 0,670 ммоль), и полученную смесь перемешивали при охлаждении в течение 2 часов, и затем в течение ночи при комнатной температуре. Реакционную смесь очищали с помощью ВЭЖХ, затем лиофилизировали с получением защищенного третбутилкарбаматом названного соединения в виде белого аморфного твердого вещества (121 мг, 89% выход) M/z=903,5.
К охлаждаемому льдом раствору защищенного третбутилкарбаматом названного соединения в форме 2,2,2-трифторацетата (121 мг, 0,119 ммоль) в DCM (4 мл) добавляли TFA (500 мкл, 6,49 ммоль), и полученную смесь перемешивали при охлаждении в течение 1 часа, и затем при комнатной температуре в течение 1 часа. После удаления избытка TFA, названное соединение выделяли путем осаждения из этилового эфира в виде белого аморфного твердого вещества (109 мг, 93% выход); MZ=803,4.
Пример 65. Синтез 10K PHF-GA-SH-(ауристатин F гидроксипропиламид)
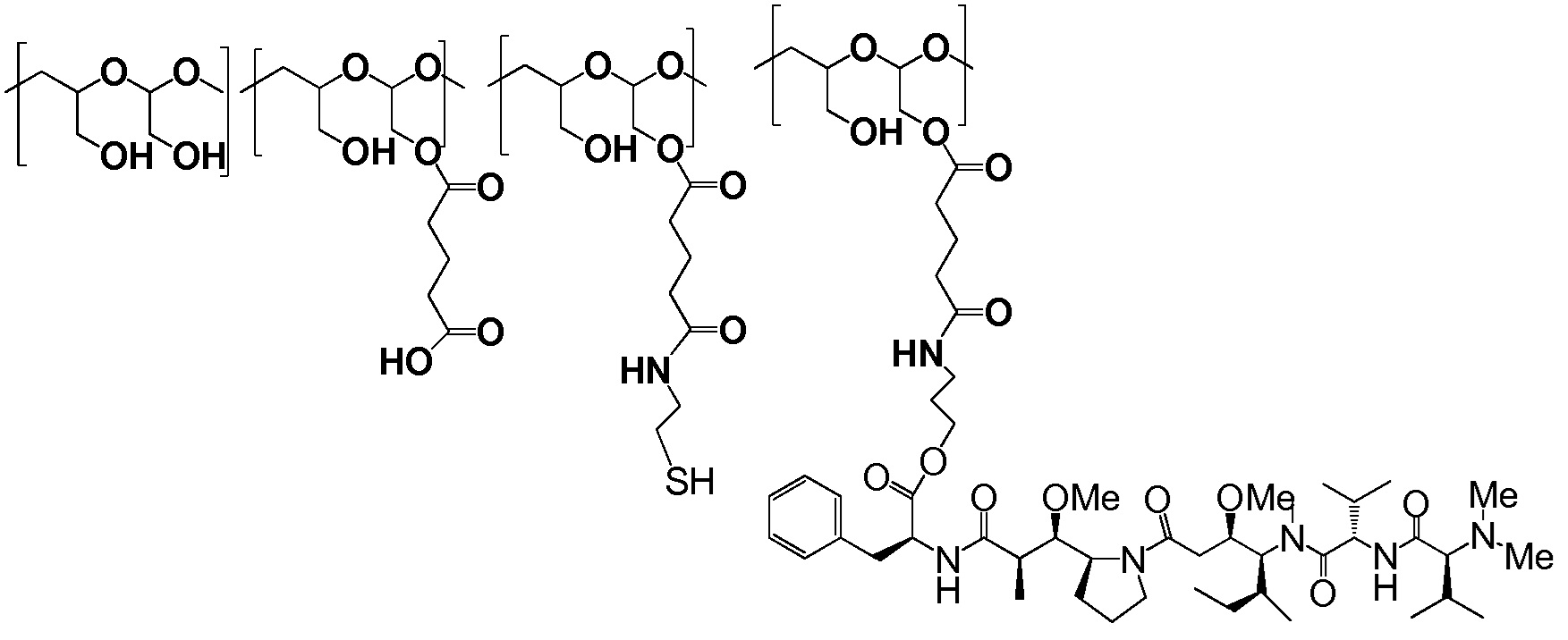
Названное соединение получали, как описано в примере 51, за исключением того, что ауристатин F гидроксипропиламид (пример 64) использовали вместо ауристатин F-гидроксипропиламид-L-аланина (пример 50).
Пример 66. Синтез 10K PHF-GA-SH-(ауристатин F гидроксипропиламид)-(трастузумаб-MCC)

Названное соединение получали, как описано в примере 52, за исключением того, что использовали 10K PHF-GA-SH-(ауристатин F гидроксипропиламид) (пример 66). Содержание ауристатина F, определенное методом LC-MS, давало, в среднем, мольное отношение ауристатина F к антителу приблизительно от 21:1 до 25:1
Пример 67. Синтез N-3(аминопропил)4-метил-4-((5-нитропиридин-2-ил)дисульфанил)пентанамида

К третбутил 3-аминопропилкарбамату (0,437 мл, 2,50 ммоль) в DMF (1 мл) добавляли N-этил-N-изопропилпропан-2-амин (0,437 мл, 2,50 ммоль) и 1H-бензо[d][1,2,3]триазол-1-ол (846 мг, 6,26 ммоль). Реакционную смесь перемешивали в течение 10 минут при 25°C и добавляли 2,5-диоксопирролидин-1-ил-4-метил-4-((5-нитропиридин-2-ил)дисульфанил)пентаноат (500 мг, 1,25 ммоль) в DMF (1 мл). Реакционную смесь перемешивали при 25°C в течение 18 часов. Очистка с помощью ВЭЖХ давала названное соединение в форме его третбутилкарбамата (476,7 мг, 1,04 ммоль, 83%) в виде бежевого твердого вещества: m/z 459 [M+H]+.
К названному соединению в форме его третбутилкарбамата (699,7 мг, 1,53 ммоль) в DMF (5,00 мл) добавляли 2,2,2-трифторуксусную кислоту (2,35 мл, 30,5 ммоль). Смесь перемешивали при 25°C в течение 1 часа. После удаления растворителя, полученное названное соединение использовали без дополнительной очистки: m/z 359 [M+H]+.
Пример 68. 10K PHF-GA (25%)-SS-диметил-NO2 (5%):

10 кДа PHF-GA (2,37 г, 14,5 ммоль, полученный в соответствии с методикой, описанной в примере 2, с PHF 10000 Да, 25% GA) разбавляли до 100 мл водой и добавляли NHS (0,133 г, 1,16 ммоль). Смесь охлаждали до 0°C, корректировали pH до значения 5,5-6,0 и затем добавляли N-3(аминопропил)-4-метил-4-((5-нитропиридин-2-ил)дисульфанил)пентанамид (547,0 мг, 1,16 ммоль, пример 67) в CH3CN (4 мл) и DMF (0,5 мл), затем EDC (0,222 г, 1,16 ммоль). Снова корректировали pH реакционной смеси до значения 5,5-6,0 и перемешивали при комнатной температуре в течение 18 часов. Добавляли дополнительное количество EDC (0,150 мг, 0,782 ммоль), и смесь перемешивали в течение еще 1,5 часов. Образец очищали диализом через мембрану из регенерированной целлюлозы с получением названного соединения (2,05 г).
Пример 69. 10K PHF-GA-SS-диметил-NO2-(ауристатин F-гидроксипропиламид-L-аланин

Названное соединение получали, как описано в примере 51, за исключением того, что 10K PHF-GA(25%)-SS-диметил-NO2(5%) (пример 68) использовали вместо 10K PHF-GA-SS-Pyr (пример 5) и не добавляли (2S,3S)-1,4-димеркаптобутан-2,3-диол (90 мг, 0,583 ммоль).
Пример 70. 10K PHF-GA-SS-диметил-NO2-(ауристатин F-гидроксипропиламид-L-аланин)-(S-S-трастузумаб)

Названное соединение получали из 10K PHF-GA-SS-диметил-NO2-(ауристатин F-гидроксипропиламид-L-аланина) (пример 69), используя методику, описанную в примере 60, за исключением того, что восстановленный трастузумаб использовали вместо трастузумаб-Fab. Содержание ауристатина F, определенное методом LC-MS, давало, в среднем, мольное отношение ауристатина F к антителу приблизительно от 9:1 до 13:1
Пример 71. 10K PHF-GA-SS-диметил-NO2-(ауристатин F-гидроксипропиламид)
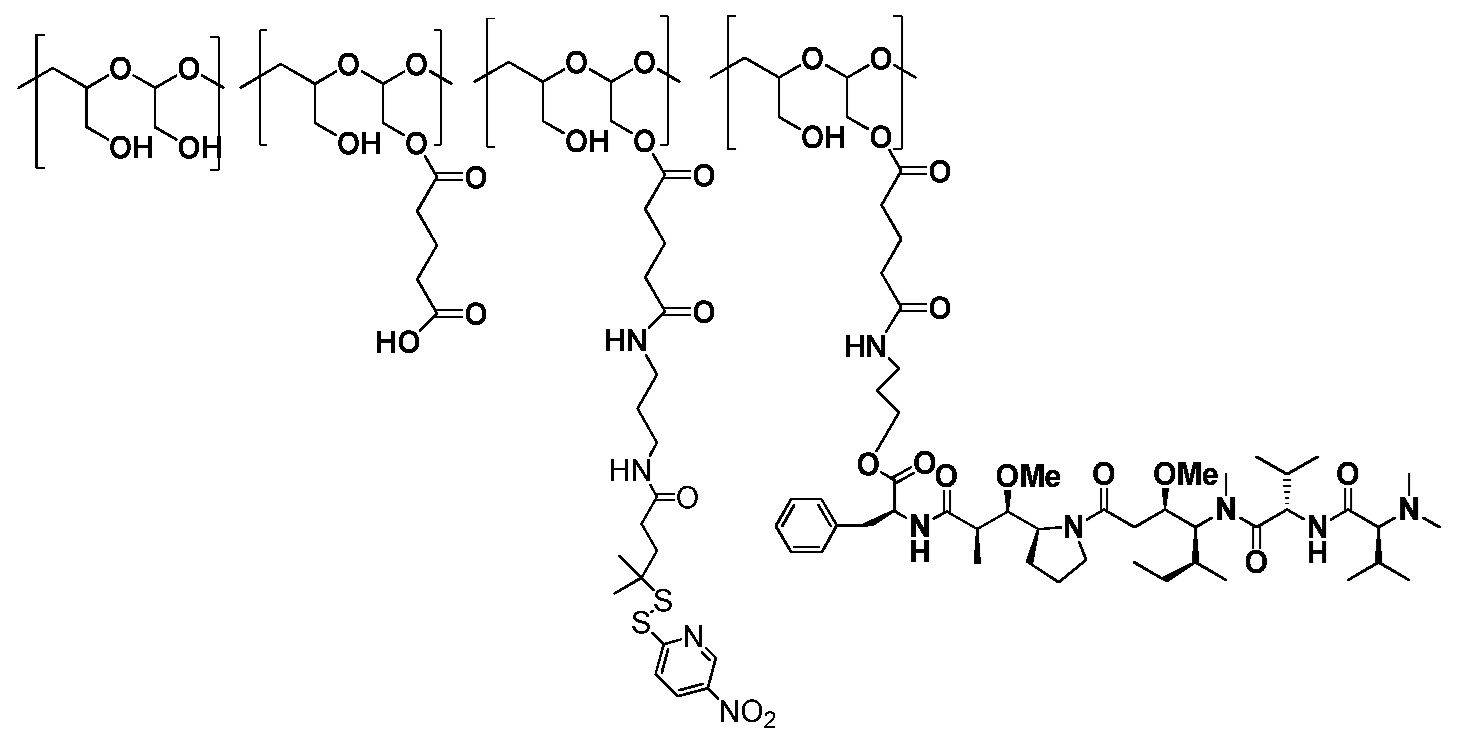
Названное соединение получали, как описано в примере 69, за исключением того, что использовали 10K PHF-GA-SS-диметил-NO2 (пример 68) и ауристатин F-гидроксипропиламид.
Пример 72. 10K PHF-GA-SS-диметил-NO2-(ауристатин F-гидроксипропиламид)-(S-S-трастузумаб)

Названное соединение получали в соответствии с методикой, описанной в примере 70, за исключением того, что использовали 10K PHF-GA-SS-диметил-NO2-(ауристатин F-гидроксипропиламид) (пример 71). Содержание ауристатина F, определенное методом LC-MS, давало, в среднем, мольное отношение ауристатина F к антителу приблизительно от 11:1 до 15:1.
Пример 73. Исследование воздействия полимерных конъюгатов PBRM-лекарственное средство на жизнеспособность клеток
Проводили исследование полимерных конъюгатов PBRM-лекарственное средство по поводу их воздействия на жизнеспособность опухоли с использованием реагента Cell Titer-Glo (Promega Corp). Клетки высевали в 96-луночном планшете с черными стенками и позволяли им прилипнуть в течение ночи при 37°C в увлажненной атмосфере 5% CO2. Клетки SKBR3, BT474, NCI-N87, экспрессирующие HER2, и клетки, эеспрессирующие низкие уровни HER2-MCF7, высевали с плотностью 5000 клеток на лунку. На следующий день заменяли среду на 50 мкл свежей среды, и добавляли в соответствующие лунки 50 мкл разбавленного в 2 раза исходного раствора полимерного конъюгата PBRM-лекарственное средство, полимерного конъюгата лекарственного средства или лекарственного средства, перемешивали и инкубировали в течение 72 часов. Добавляли в лунки реагент Cell Titer-Glo при комнатной температуре, и через 10 минут измеряли люминесцентный сигнал с помощью планшет-ридера SpectraMax M5 (Molecular Devices). Строили кривые зависимостей "доза-эффект", используя программный продукт SoftMax Pro. Значения IC50 получали в результате четырехпараметрической аппроксимации кривых.
Высевали клетки линий Raji и Ramos, экспрессирующие CD20, и проводили исследование, используя такую же методику, как описанная выше методика для клеток, экспрессирующих HER2.
В таблицах I-VII приведены результаты исследования антипролифероативных свойств полимерного конъюгата PBRM-лекарственное средство либо в отношении клеток, экспрессирующих HER2 (таблицы I-IV, VI и VII), либо в отношении клеток, экспрессирующих CD20 (таблица V).
В таблице I приведены результаты исследований для полимерного конъюгата PBRM-лекарственное средство (PHF-GA-(HPV-аланин)-(трастузумаб-MCC), пример 7, (HPV:трастузумаб приблизительно от 14:1 до 17:1) и PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12), пример 8, (HPV:трастузумаб приблизительно от 16:1 до 18:1), полимерного конъюгата лекарственного средства (PHF-GA-(HPV-аланин)-SH, пример 6, и для только одного лекарственного средства (HPV).
Результаты в таблице I показывают, что в случае клеток линии SKBR3 и BT474, экспрессирующих HER2, полимерные конъюгаты PBRM-лекарственное средство (примеры 7 и 8) проявляли повышенную антипролиферативную активность по сравнению с полимерным конъюгатом лекарственного средства (Пример 6) и только одним лекарственным средством (HPV). В случае этих линий клеток, полимерный конъюгат лекарственного средства (пример 6) менее активен, чем только одно лекарственное средство (HPV).
В таблице II приведены результаты исследований для (S)-2HPV (пример 22) и (R)-2HPV (пример 23).
Результаты в таблице II показывают, что в случае клеток линии SKBR3 и BT474, экспрессирующих HER2, производные барвинка (примеры 22 и 23) проявляли аналогичную антипролиферативную активность.
В таблице III приведены результаты исследований для полимерного конъюгата PBRM-лекарственное средство (PHF-GA-SSPyr-(HPV-аланин)), пример 59) и полимерного конъюгата лекарственного средства (PHF-GA-(HPV-аланин)-(трастузумаб-Fab)), пример 60, HPV:трастузумаб-Fab приблизительно от 6:1 до 8:1).
Результаты в таблице III показывают, что в случае клеток линии SKBR3, BT474 и N87, экспрессирующих HER2, полимерный конъюгат PBRM-лекарственное средство (пример 60) проявлял более высокую антипролиферативную активность по сравнению с полимерным конъюгатом лекарственного средства (Пример 59).
В таблице IV приведены результаты исследований для полимерного конъюгата PBRM-лекарственное средство (PHF-GA-(HPV-аланин)-(трастузумаб-MCC)), пример 7 (HPV:трастузумаб приблизительно от 19:1 до 22:1) и PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12), пример 8, HPV:трастузумаб приблизительно от 16:1 до 18:1) и полимерного конъюгата лекарственного средства (PHF-GA-(HPV-аланин)-SH, пример 6).
Результаты в таблице IV показывают, что в случае клеток линии SKBR3, BT474 и N87, экспрессирующих HER2, оба полимерных конъюгата PBRM-лекарственное средство (пример 7 и пример 8) проявляли более высокую антипролиферативную активность по сравнению с полимерным конъюгатом лекарственного средства (пример 6).
В таблице V приведены результаты исследований для полимерного конъюгата PBRM-лекарственное средство (PHF-GA-(HPV-аланин)-(ритуксимаб-MCC), (пример 54, HPV:ритуксимаб приблизительно от 12:1 до 15:1) и полимерного конъюгата лекарственного средства (PHF-GA-(HPV-аланин)-SH, пример 6) в случае клеток линии Raji и Ramos, экспрессирующих CD20.
Результаты в таблице V показывают, что в случае клеток линии Raji и Ramos, экспрессирующих CD20, полимерный конъюгат PBRM-лекарственное средство (пример 54) проявлял более высокую антипролиферативную активность по сравнению с полимерным конъюгатом лекарственного средства (Пример 6).
В таблице VI приведены результаты исследований для полимерных конъюгатов PBRM-лекарственное средство PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (приблизительно 5:1) (пример 55); PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (приблизительно 10:1) (пример 56) и PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (приблизительно 20:1) (Пример 57).
Результаты в таблице VI показывают, что в случае клеток линий SKBR3 и BT474, экспрессирующих HER2, антипролиферативный эффект зависит от количества загружаемого лекарственного средства. Полимерные конъюгаты PBRM-лекарственное средство с более высокой загрузкой лекарственного средства (пример 57) проявляли более высокую антипролиферативную активность по сравнению с конъюгатами с более низкой загрузкой лекарственного средства (пример 56 и пример 55).
В таблице VII приведены результаты исследований для полимерных конъюгатов PBRM-лекарственное средство PHF-GA-(ауристатин F-гидроксипропиламид-L-аланин)-(трастузумаб-MCC) (пример 52, ауристатин F:трастузумаб приблизительно от 20:1 до 22:1); полимерного конъюгата лекарственного средства PHF-GA-SH-(ауристатин F-пропиламид-L-аланин) (пример 51) и ауристатин F-гидроксипропиламид (пример 48)
Результаты в таблице VII показывают, что в случае клеток линии SKBR3, BT474 и N87, экспрессирующих HER2, полимерные конъюгаты PBRM-лекарственное средство (пример 52) и только одно лекарственное средство (пример 48) проявляли более высокую антипролиферативную активность по сравнению с полимерным конъюгатом лекарственного средства (пример 51). Полимерный конъюгат PBRM-лекарственное средство имеет такую же активность, как и только одно лекарственное средство.
Пример 74. Исследование воздействия соединений лекарственных средств на жизнеспособность клеток
Исследовали воздействие лекарственных соединений на жизнеспособность опухоли, используя реагент Cell Titer-Glo (Promega Corp), описанный в примере 73. В таблице VIII приведены результаты исследований антипролиферативных свойств лекарственных соединений в случае клеток, экспрессирующих HER2 ("ND"=не определеляли)
Пример 75. Исследования in vivo эффективности, фармакокинетики и биораспределения
Для того чтобы оценить эффективность и фармакокинетику конъюгата белок-лекарственное средство, использовали модели подкожных и ортотопических ксенотрансплантатов на мышах и крысах.
Испытуемые изделия, вместе с соответствующими элементами управления, вводят внутривенно (IV) путем инъекции в хвостовую вену или внутрибрюшинно. Для оценки циркулирующих уровней испытуемого изделия, собирают пробу крови в заданные моменты времени путем пункции сердца в терминальном состоянии. Пробы выдерживают при комнатной температуре в течение 30 минут для коагуляции, затем центрифугируют в течение 10 минут при 1000 × g при 4°C и быстро замораживают при -80°C. Суммарные концентрации PBRM в пробах плазмы определяют, используя метод ELISA. Циркулирующую концентрацию лекарственного средства (конъюгированного и свободного) определяют методами LC/MS/MS.
Для оценки эффективности полимерного конъюгата PBRM-лекарственное средство, измеряют размер опухоли, используя цифровые штангенциркули. Вычисляют объем опухоли и используют его для определения замедления роста опухоли.
Для определения биораспределения лекарственного средства, вырезают опухоль и важные органы, такие как, например, печень, почки, селезенка, легкие, сердце, мышцы и мозг, быстро замораживают их в жидком азоте, хранят при -80°C. Определяют уровни PBRM и/или лекарственного средства в гомогенатах тканей стандартными методами, такими как, например, методы ELISA или LC/MS/MS, соответственно.
Пример 76. Реакция роста опухоли на введение полимерных конъюгатов PBRM-лекарственное средство
Самок мышей линии CB-17 SCID инокулировали подкожно клетками NCI-N87 (n=10 для каждой группы) или опухолями BT474 (n=12 или n=10 для каждой группы). Испытуемые соединения или плацебо вводили внутривенно в виде разовой дозы в 1-ый день; один раз в неделю в течение 3 недель в 1-ый день, на 8-ой день и на 15-ый день, соответственно; или один раз в неделю в течение 3 недель на 17-ый день, 24-ый день и 31-ый день, соответственно. Дозу полимерного конъюгата лекарственного средства подбирали таким образом, чтобы он доставлял такое же количество лекарственного средства, какое присутствует при самой высокой дозе соответствующего вводимого полимерного конъюгата PBRM-лекарственное средство. Размер опухоли измеряли в моменты времени, указанные на фигурах 1, 2, 3, 4 и 5, используя цифровые штангенциркули. Вычисляли объем опухоли, и использовали его для определения замедления роста опухоли. Мышей умерщвляли, когда опухоли достигали размера 1000 мм3, 800 мм3 или 700 мм3. Объемы опухолей регистрировали как среднее значение (mean) ± стандартная погрешность среднего (SEM) для каждой группы.
На фигуре 1 приведены результаты реакции опухоли у мышей, инокулированных подкожно клетками NCI-N87 (n=10 для каждой группы), после внутривенного введения плацебо, полимерного конъюгата PBRM-лекарственное средство PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12) (пример 8, HPV:трастузумаб приблизительно от 16:1 до 18:1) при 15,6 мг/кг, 5,2 мг/кг, 1,6 мг/кг и 0,5 мг/кг, соответственно, и полимерного конъюгата лекарственного средства PHF-GA-(HPV-аланин)-SH (пример 6) (вводимого при дозе барвинка, которая эквивалентна дозе, присутствующей в примере 8 при 15,6 мг/кг), вводимых один раз в неделю в течение 3 недель в 1-ый день, на 8-ой день и на 15-ый день, соответственно. Результаты иллюстрируют эффект дозы для полимерного конъюгата PBRM-лекарственное средство (пример 8) при самой высокой дозе 15,6 мг/кг, показывая уменьшение объема опухоли с 80% частичным ответом (8/10); с 20% полным ответом (2/10) и с 0% выживаемостью, свободной от опухоли (0/10). Плацебо, конъюгат лекарственное средство-полимер (пример 6) и полимерный конъюгат PBRM-лекарственное средство (пример 8) при дозах 5,2 мг/кг, 1,6 мг/кг и 0,5 мг/кг все характеризовались увеличением объема опухоли.
На фигуре 2 приведены результаты реакции опухоли у мышей, инокулированных подкожно опухолями BT474 (n=12 для каждой группы) после внутривенного введения плацебо; PBRM (трастузумаб) при 15 мг/кг; полимерных конъюгатов PBRM-лекарственное средство PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (пример 7, HPV:трастузумаб приблизительно от 19:1 до 22:1) при 7,5 мг/кг и PHF-GA-(HPV-аланин)-(ритуксимаб-MCC) (пример 54, HPV:ритуксимаб приблизительно от 12:1 до 15:1) при 20 мг/кг; полимерного конъюгата лекарственного средства PHF-GA-(HPV-аланин)-SH (пример 6) (вводимого при дозе барвинка, которая была эквивалентна дозе, присутствующей в примере 7 при 15 мг/кг) в комбинации с трастузумабом при 15 мг/кг, вводимых один раз в неделю в течение 3 недель в 1-ый день, на 8-ой день и на 15-ый день, соответственно. Результаты иллюстрируют уменьшение объема опухоли для примера 7 с 100% полным ответом и с 100% выживаемостью, свободной от опухоли. Плацебо, только один трастузумаб, комбинация примера 6 и трастузумаба; и пример 54 все характеризовались увеличением объема опухоли. Для уменьшения объема опухоли требовалось конъюгирование PBRM, специфичной к HER2 клеткам (трастузумаба), с полимерным конъюгатом лекарственного средства, так как ни полимерный конъюгат лекарственного средства в комбинации с PBRM (пример 6 в комбинации с трастузумабом), ни конъюгирование PBRM, неспецифической к клеткам HER2 (ритуксимаба, пример 54), не приводило к уменьшению объема опухоли).
На фигуре 3 приведены результаты реакции опухоли у мышей, инокулированных подкожно опухолями BT474 (n=12 для каждой группы), после внутривенного введения плацебо; PBRM (трастузумаба) при 15 мг/кг; полимерных конъюгатов PBRM-лекарственное средство PHF-GA-(ауристатин F-гидроксипропиламид-L-аланин)-(трастузумаб-MCC) (пример 52, ауристатин F:трастузумаб приблизительно от 20:1 до 22:1) при 7,5 мг/кг; полимерного конъюгата лекарственного средства PHF-GA-SH-(ауристатин F-пропиламид-L-аланин) (пример 51) (вводимого при дозе ауристатина, которая была эквивалентна дозе, присутствующей в примере 52 при 15 мг/кг) в комбинации с трастузумабом при 15 мг/кг, вводимых один раз в неделю в течение 3 недель в 1-ый день, на 8-ой день и на 15-ый день, соответственно. Результаты иллюстрируют уменьшение объема опухоли для примера 52 с 100% полным ответом (11/11) и с 100% выживаемостью, свободной от опухоли (11/11). Плацебо, только один трастузумаб, комбинация примера 51 и трастузумаба все характеризовались увеличением объема опухоли. Для уменьшения объема опухоли требовалось конъюгирование PBRM с конъюгатом лекарственное средство-полимер, так как ни конъюгат лекарственное средство-полимер в комбинации с PBRM (пример 51 в комбинации с трастузумабом), ни только одна PBRM (трастузумаб), не приводили к уменьшению объема опухоли.
На фигуре 4 приведены результаты реакции опухоли у мышей, инокулированных подкожно опухолями BT474 (n=10 для каждой группы) после внутривенного введения плацебо; полимерных конъюгатов PBRM-лекарственное средство PHF-GA-(HPV-аланин)-(трастузумаб-MCC)(пример 7, HPV:трастузумаб приблизительно от 19:1 до 22:1) при 3,5 мг/кг, вводимых один раз в неделю в течение 3 недель в 1-ый день, на 8-ой день и на 15-ый день, соответственно; полимерных конъюгатов PBRM-лекарственное средство PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (пример 7, HPV:трастузумаб приблизительно от 19:1 до 22:1) при 10 мг/кг, вводимых в форме разовой дозы на 1-ый день; полимерных конъюгатов PBRM-лекарственное средство PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (пример 7, HPV:трастузумаб приблизительно от 19:1 до 22:1) при 10 мг/кг, вводимых один раз в неделю в течение 3 недель в 17-ый день, на 24-ый день и на 31-ый день, соответственно. Результаты иллюстрируют уменьшение объема опухоли для примера 7 для всех исследованных схем дозирования и всех дозируемых концентраций с 100% полным ответом (10/10) и с 100% выживаемостью, свободной от опухоли (10/10), вводимых при 3,5 мг/кг один раз в неделю в течение 3 недель; с 90% частичным ответом (9/10); с 10% полным ответом (1/10) и с 10% выживаемостью, свободной от опухоли (1/10), вводимых при 10 мг/кг один раз в неделю в течение 3 недель у мышей с крупными опухолями; и с 100% полным ответом (10/10) и с 100% выживаемостью, свободной от опухоли (10/10), вводимых при 10 мг/кг в форме разовой дозы. Плацебо характеризовалось увеличением объема опухоли.
На фигуре 5 приведены результаты реакции опухоли у мышей, инокулированных подкожно опухолями BT474 (n=10 для каждой группы) после внутривенного введения плацебо или 30 кДа PHF-GA-(HPV-аланин)-(трастузумаб-Fab) (пример 60, HPV:трастузумаб-Fab приблизительно от 10:1 до 14:1) при 7 мг/кг, вводимых один раз в неделю в течение 3 недель в 1-ый день, на 8-ой день и на 15-ый день, соответственно. Результаты иллюстрируют уменьшение объема опухоли для примера 60 с 100% полным ответом (10/10) и с 100% выживаемостью, свободной от опухоли (10/10), в то время как в случае плацебо происходило увеличение объема опухоли.
На фигуре 8 приведены результаты реакции опухоли у мышей, инокулированных подкожно опухолями BT474 (n=10 для каждой группы) после внутривенного введения плацебо; полимерных конъюгатов PBRM-лекарственное средство PHF-GA-(ауристатин F-гидроксипропиламид-L-аланин)-(трастузумаб-MCC) (пример 52, ауристатин F:трастузумаб приблизительно от 24:1 до 28:1) и полимерного конъюгата лекарственного средства PHF-GA-SS-диметил-NO2-(ауристатин F-гидроксипропиламид-L-аланин)-(S-S-трастузумаб) (пример 70, ауристатин F:трастузумаб приблизительно от 9:1 до 13:1) при 2 мг/кг и 4 мг/кг, вводимых один раз в неделю в течение 3 недель в 1-ый день, на 8-ой день и на 15-ый день, соответственно. Результаты иллюстрируют полное уменьшение объема опухоли для примера 70 при дозах 2 мг/кг и 4 мг/кг и для примера 52 при 4 мг/кг.
Во всех описанных в изобретении in vitro или in vivo экспериментах, если не указано иначе, то все используемые дозы приводились в расчете на PBRM (например, на антитела фрагментов антител) полимерных конъюгатов PBRM-лекарственное средство.
Пример 77. In vitro стабильность полимерных конъюгатов PBRM-лекарственное средство
In vitro стабильность полимерных конъюгатов PBRM-лекарственное средство оценивали путем инкубирования полимерного конъюгата PBRM-лекарственное средство в физиологическом растворе или плазме животных при 37°C, pH 7,4. Скорость разложения полимерного конъюгата PBRM-лекарственное средство определяли путем непрерывного определения количества лекарственного средства, высвобождаемого в матрицу, методом LC/MS/MS после извлечения высвобождаемого лекарственного средства из полимерного конъюгата PBRM-лекарственное средство методом жидкостной экстракции.
В таблице IX приводятся значения периода полуразложения (T1/2) конъюгата PBRM-лекарственное средство, PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12) примера 8 (HPV:трастузумаб приблизительно от 16:1 до 18:1) в плазме мышей, плазме крыс и плазме собак.
Результаты показывают, что полимерный конъюгат PBRM-лекарственное средство примера 8 был стабильным в плазме животных и высвобождал лекарственное средство в заданный период времени.
Пример 78. Исследования связывания лигандов методом поверхностного плазмонного резонанса (SPR) фирмы Biacore
Кинетика связывания полимерного конъюгата PBRM-лекарственное средство с иммобилизированным рецептором определяли методом BIAcore SPR. Константы связывания для PBRM в конъюгате PBRM- лекарственное средство PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12) пример 8 (HPV:трастузумаб приблизительно от 16:1 до 18:1) и для только одной PBRM (то есть, трастузумаба) определяли, используя стандартные методики BIAcore.
Используя стандартную реакцию сочетания амина, hErbB2 иммобилизировали в трех проточных каналах на поверхности сенсорного чипа поверхностного плазмонного резонанса при трех одинаковых плотностях, трастузумаб легко связывался с иммобилизированным hErbB2, тем самым демонстрируя, что оба партнера по связыванию являлись активными. В таблице X приведены параметры связывания ka (константа ассоциации или константа сродства) и KD (константа диссоциации), измеренные при 25°C для конъюгата примера 8 и трастузумаба с использованием оптического биосенсора BioRad ProteOn XPR36, снабженного сенсорным чипом GLC и приведенного в равновесие с помощью подвижного буфера.
Результаты показывают, что PBRM в конъюгате PBRM-лекарственное средство распознавалась PBRM рецептором
Пример 79. Фармакокинетические параметры (PK) стабильности в плазме мышей и распределение в тканях после введения полимерных конъюгатов PBRM-лекарственное средство
Фармакокинетические параметры стабильности в плазме и распределение в тканях PBRM-лекарственное средство-конъюгата определяли после введения PBRM-лекарственное средство-конъюгата самкам мышей линии CB-17 SCID с опухолями NCI-N87 (n=3). Концентрации конъюгированного HPV определяли методом LC/MS/MS. Концентрацию HPV-трастузумаб-конъюгата определяли из данных по конъюгированному HPV. Суммарную концентрацию трастузумаба определяли методом ELISA
Мышам вводили внутривенно болюс PBRM-лекарственное средство-конъюгат PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12) как в примере 8 (HPV:трастузумаб приблизительно от 16:1 до 18:1) при 15 мг/кг (в расчете на трастузумаб).
На фигуре 6 показаны фармакокинетические параметры стабильности в плазме для конъюгированного HPV и трастузумаба после внутривенного введения болюса PBRM-лекарственное средство-конъюгат PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12) как в примере 8 (HPV:трастузумаб приблизительно от 16:1 до 18:1) при 15 мг/кг (в расчете на трастузумаб).
На фигуре 7 показано количество HPV, которое накапливалось в различных органах мышей после внутривенного введения болюса PBRM-лекарственное средство-конъюгат PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12) примера 8 (HPV:трастузумаб приблизительно от 16:1 до 18:1) при 15 мг/кг (в расчете на трастузумаб).
Результаты показывают, что PBRM-лекарственное средство-конъюгат был стабильным в плазме, и что лекарственное средство попадало в опухоль. Максимальное накопление HPV в опухоли наблюдалось между 24 и 72 часами.
Пример 80. Фармакокинетические параметры (PK) стабильности в плазме мышей после введения полимерных конъюгатов PBRM-лекарственное средство
Фармакокинетические параметры (PK) стабильности PBRM-лекарственное средство-конъюгата в плазме мышей определяли после введения PBRM-лекарственное средство-конъюгата самкам мышей линии CB-17 SCID с опухолями N87 (n=3) или опухолями BT474 (n=3). Концентрацию конъюгированного HPV определяли методом LC/MS/MS. Суммарную концентрацию трастузумаба определяли методом ELISA.
В таблице XI приведены значения периода полуразложения (T1/2) и площадь под кривой (AUC) PBRM-лекарственное средство- конъюгата PHF-GA-(HPV-аланин)-(трастузумаб-M-(PEG)12) пример 8 (HPV:трастузумаб приблизительно от 16:1 до 18:1) при 15,6 мг/кг в расчете на трастузумаб в моделе ксенотрансплантата N87 и полимерных конъюгатов PBRM-лекарственное средство PHF-GA-(HPV-аланин)-(трастузумаб-MCC) (Пример 7, HPV:трастузумаб приблизительно от 19:1 до 22:1) при 15,0 мг/кг в расчете на трастузумаб в модели ксенотрансплантата BT474.
Результаты показывают, что полимерные конъюгаты PBRM-лекарственное средство примеров 7 и 8 были стабильными в плазме.
ВКЛЮЧЕНИЕ В ОПИСАНИЕ ИЗОБРЕТЕНИЯ СВЕДЕНИЙ ПУТЕМ ССЫЛКИ
Для всех случаев, содержание каждого из патентных документов и каждой из научных статей приводится в описании изобретения путем ссылки на них.
ЭКВИВАЛЕНТЫ
Изобретение может быть осуществлено в других конкретных формах без отклонения от его сущности или основных характеристик. Поэтому, приведенные выше варианты осуществления следует рассматривать, во всех аспектах, только иллюстрациями, а не ограничениями для описываемого изобретения. Следовательно, объем изобретения определяется прилагаемыми пунктами формулы изобретения, а не приведенным выше описанием изобретения, и предполагается, что все вносимые изменения, не выходящие за рамки значений и диапазона эквивалентности пунктов формулы изобретения, входят в объем настоящего изобретения.
Реферат
Настоящее изобретение относится к конъюгату лекарственного средства. Конъюгат включает распознающую молекулу на основе белка (PBRM) и полимерный носитель, замещенный одним или более -L-D, при этом распознающая молекула на основе белка соединена с полимерным носителем с помощью L. В каждом случае присутствия D представляет собой независимо терапевтическое средство, имеющее молекулярную массу ≤5 кДа. Lи Lпредставляют собой связующие звенья, соединяющие терапевтическое средство и PBRM с полимерным носителем соответственно. Кроме того, раскрываются полимерные каркасные структуры, применяемые для конъюгирования с PBRM с образованием описанного в изобретении конъюгата полимер-лекарственное средство-PBRM; композиции, включающие конъюгаты; способы их получения и способы лечения различных расстройств с помощью конъюгатов или их композиций. 5 н. и 23 з.п. ф-лы, 8 ил., 11 табл., 80 пр.
Формула
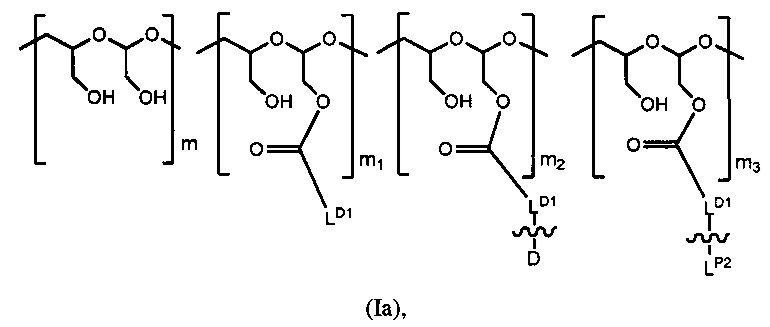
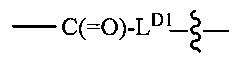









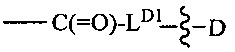




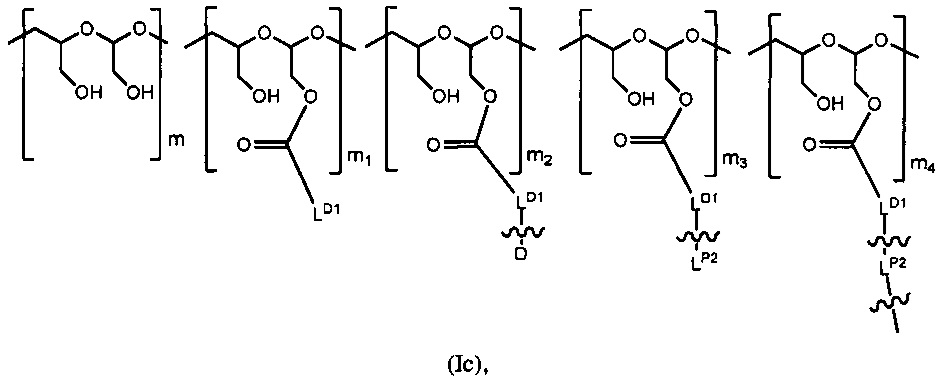
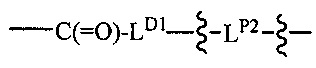























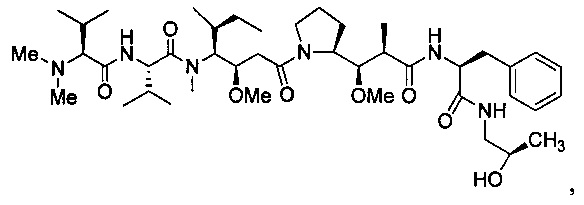


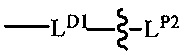




















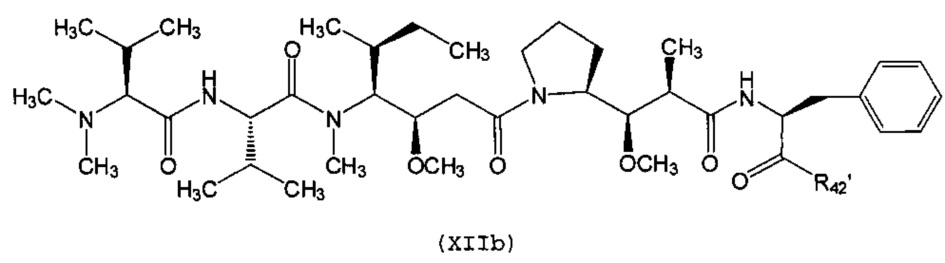





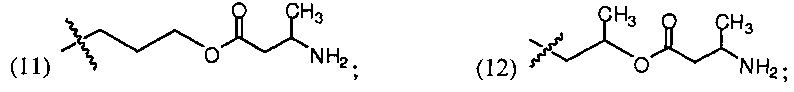

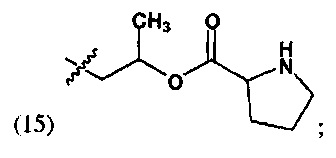


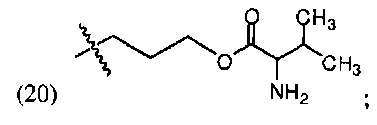









Документы, цитированные в отчёте о поиске
Способ получения полимерных конъюгатов