Способ получения полимерных конъюгатов - RU2401283C2
Код документа: RU2401283C2
Чертежи


Описание
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к улучшенному способу получения полимерных конъюгатов. В особенности, изобретение относится к улучшенному способу получения и очистки полимерных конъюгатов биологически активных молекул, таких как белки.
УРОВЕНЬ ТЕХНИКИ
Конъюгация полимеров с биологически активными молекулами, такими как белки, полипептиды или малые молекулы, со временем стала все более распространенной в качестве способа повышения эффективности, часто при снижении одного или нескольких неблагоприятных свойств, таких молекул. В частности, конъюгация полимеров с использованием полиалкиленоксида (PAO) или, более конкретно, полиэтиленгликоля (PEG) была широко распространена для разработки эффективных производных полутоксичных или иммуногенных лекарственных средств для терапевтического применения.
В патентах США, например, №№ 5643575, 5919455, 5605976 в качестве нескольких примеров описаны неантигенные полимеры, их получение и способы их конъюгации с биологически активными молекулами. Содержание каждого из указанных выше патентов упомянуто здесь полностью для сведения. Хотя в этих патентах представлены важные способы улучшения использования биологически активных молекул, таких как ферменты, белки и другие пептиды и полипептиды, тем не менее еще существует необходимость в улучшенных способах конъюгации.
Например, в указанном выше патенте '575 описаны способы получения разветвленных производных PEG и получаемых вместе с ними белковых конъюгатов. Один из описываемых в нем способов включает использование избытка трехфункциональной молекулы, такой как сложный этиловый эфир лизина, для конъюгации с активированными производными mPEG, такими как карбонат сукцинимидила (SC)-mPEG. Хотя этот способ обеспечивает желаемый активированный разветвленный полимер и получаемый в результате конъюгат, было найдено, что существуют определенные условия, в которых желательно более экономное получение желаемых конъюгатов с более высокой степенью чистоты. Ранее предлагалось для удаления любых не вступивших во взаимодействие исходных веществ или побочных продуктов использовать хроматографию на колонках. См., например, патент США №5932462. Такие способы являются дорогими, неудобными для крупномасштабного производства и могут приводить к значительной потере продукта. Очень желательно удалять или инактивировать остающиеся исходные вещества и побочные продукты, которые могут до получения конечного продукта конкурировать с образованием желаемых конъюгатов разветвленный полимер-лекарственное средство. Это, в свою очередь, приводит к обратному направлению процесса потери продукта. Таким образом, проводили поиски альтернатив, особенно в случаях коммерческого получения и в случае особой важности минимизации потери биологически активной молекулы.
Настоящее изобретение относится к новому и улучшенному способу получения активированных линкеров PEG и их последующей конъюгации с биологически активными молекулами. Также настоящее изобретение относится к неудовлетворенной потребности в предоставлении экономически эффективного способа конъюгации с улучшенной чистотой и выходом продукта в сравнении с известным уровнем техники.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном из вариантов осуществления изобретение относится к новому способу получения активированных полимеров и получаемых вместе с ними полимерных конъюгатов. Первая стадия в этом аспекте изобретения включает взаимодействие активируемого остатка полимера, такого как mPEG-OH, с активирующим веществом, способным предоставлять уходящую группу для активируемого остатка полимера, и дает первую реакционную смесь, содержащую активированный полимерный остаток, такой как mPEG-карбонат сукцинимидила (здесь и далее SC-PEG), и следовое количество предпочтительно активируемого полимерного остатка. В рамках настоящей заявки примеры активирующих средств включают карбонат дисукцинимидила (DSC) или сочетание фосгена (или трифосгена) и N-гидроксисукцинимида (здесь и далее NHS). Дополнительные активирующие средства/уходящие группы описаны ниже в разделе "Подробное описание".
На второй стадии предусмотрено взаимодействие первой реакционной смеси с многофункциональной связывающей группой, обладающей по крайней мере одной защитной группой, т.е. функциональной группой, которая не взаимодействует с активированным полимерным остатком, такой как сложный этиловый эфир лизина. Эту вторую стадию проводят в условиях, где активированный полимерный остаток из первой реакционной смеси присутствует в молярном избытке относительно активных групп многофункциональной связывающей группы, и таким образом формируют вторую реакционную смесь. Эта вторая реакционная смесь содержит первую реакционную смесь и промежуточный полимер, такой как сложный этиловый эфир (PEG)2Lys, получаемый в результате взаимодействия активированного полимерного остатка с многофункциональной связывающей группой.
На следующей стадии вторую реакционную смесь гасят первым гасящим реагентом, таким как фенэтиламин или бензиламин, получая третью реакционную смесь, для инактивации активированного полимерного остатка с образованием третьей реакционной смеси, содержащей, в частности, промежуточные полимерные конъюгаты. Затем к третьей реакционной смеси добавляют второй гасящий реагент, такой как TBDMSiCl, для инактивации в ней активируемого полимерного остатка и, таким образом, образования четвертой реакционной смеси, которая содержит, в частности, промежуточные полимерные конъюгаты. Первый и второй гасящие реагенты можно добавлять в любом порядке при условии, что их не добавляют одновременно. Предпочтительно, однако, первым добавляют первый гасящий реагент, а затем добавляют второй гасящий реагент.
Затем четвертую реакционную смесь обрабатывают снимающим защиту средством для удаления защитной группы, например сильным основанием, таким как LiOH, для устранения защиты в виде сложного этилового эфира, или сильной кислотой, такой как TFA, для устранения защиты в виде сложного трет-бутилового эфира. Затем промежуточный полимер, т.е. PEG-функционализированную многофункциональную связывающую группу, нейтрализуют с образованием пятой реакционной смеси.
Затем пятая реакционная смесь взаимодействует с другим активирующим веществом или соединением, способным активировать в ней промежуточный полимер для связывания с биологически активной молекулой, такой как NHS, образуя шестую реакционную смесь. Затем эта шестая реакционная смесь, содержащая активированный полимер, взаимодействует с биологически активной молекулой, образуя желаемый полимерный конъюгат.
В целях настоящего изобретения способ описан в отношении биологически активных молекул. Однако понятно, что этот термин также включает средства для нацеливания и диагностики. В отличие от способов предшествующего уровня техники эта шестая реакционная смесь содержит желаемый активированный полимер в отсутствие конкурирования без промежуточных соединений, конкурирующих за взаимодействие с биологически активной молекулой.
В другом аспекте изобретения желаемые полимерные конъюгаты выделяют из конечной реакционной смеси, например, диафильтрацией, эксклюзионной хроматографией, на ионообменной колонке, на колонке для аффинной хроматографии или другими способами, хорошо известными специалистам в данной области. Понятно, что выбор способа выделения зависит от конкретных формируемых конечных конъюгатов, и такой выбор можно осуществлять без проведения лишних экспериментов.
В результате изобретения специалист в данной области обеспечен способом, который предоставляет желаемый полимерный конъюгат эффективно и с высоким выходом продукта. Способ легко приспособить для большой порции или промышленного масштаба, избегая дорогой и требующей много времени стадии хроматографии на колонке для выделения желаемого активированного линкера PEG. В одном из особенно предпочтительных вариантов осуществления, в котором получают конъюгаты (PEG)2Lys-полипептид, предпочтительные гасящие реагенты формируют аминокарбамат mPEG и силил-блокированный mPEG, которые инертны в отношении конъюгации полипептидов и легко отделяемы от конечных конъюгатов PEG-полипептид в ходе очистки.
Другие, а также дополнительные преимущества очевидны специалистам в данной области из предоставленного в настоящей заявке описания без проведения лишних экспериментов.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1 схематично представлены стадии реакций, указанные в описании.
На фиг.2-3 схематично представлены схемы реакций, описанные в примерах.
ПОДРОБНОЕ ОПИСАНИЕ
A. Общее представление
Способы по настоящему изобретению эффективны для получения широкого разнообразия полимерных (PEG) конъюгатов. Хотя существует значительный диапазон выбора различных компонентов реакционных смесей, получаемых в ходе настоящего изобретения, характеристики компонентов на каждой стадии являются достаточно сходными для того, чтобы было возможным общее описание способа. Далее приведена ссылка на фиг.1, где представлено схематическое отображение описываемых ниже реакций.
B. Первая реакционная смесь
Первую реакционную смесь формируют с использованием хорошо известных способов активации полимера или PEG. В результате это приводит к раствору, содержащему активируемый полимерный остаток, такой как PEG-OH, и активированный полимерный остаток, такой как SC-PEG. Избыток реагентов в виде малых молекул можно легко удалять с использованием таких известных способов, как перекристаллизация.
В целях настоящего изобретения активируемые полимерные остатки могут включать любые такие известные соединения, однако в предпочтительных аспектах изобретения используют соединения на основе полиалкиленоксида (POA) или полиэтиленгликоля (PEG). Неограничивающий список таких соединений включает mPEG-OH, mPEG-NH2, mPEG-CO2H, mPEG-SH и mPEG-галоген, например Cl. В более предпочтительных вариантах осуществления активируемый полимерный остаток представляет собой mPEG-OH.
Приемлемые уходящие группы, где они упомянуты в связи с синтезом описанных в настоящей заявке полимерных конъюгатов, включают в себя, не ограничиваясь ими, такие молекулы, как N-гидроксибензотриазолил, галоген, N-гидроксифталимидил, п-нитрофеноксигруппу, имидазолил, N-гидроксисукцинимидил, тиазолидинилтион или другие хорошие уходящие группы, как очевидно специалистам в данной области. В целях настоящего изобретения под уходящими группами следует понимать те группы, которые можно заменять нуклеофильной группой, например, NH2, OH, SH или другой реакционно-способной аминогруппой (нуклеофил), которые находятся в многофункциональной молекуле.
Примеры предпочтительных активирующих веществ, способных предоставлять уходящую группу для полимерного остатка, включают в себя, но ими не ограничиваются, DSC/пиридин или NHS/трифосген для получения SC-PEG, 2-меркаптотиозолидин/EDC/DMAP для получения T-PEG (т.е. PEG-2-меркаптотиозолидинилкарбамат), N-гидроксифталамидил/DMAP для получения BSC-PEG (т.е. PEG-N-гидроксифталамидилкарбонат и т.д.).
Примеры некоторых предпочтительных активированных полимерных остатков, эффективных в способе по изобретению, включают остатки, хорошо известные специалистам в области пегилирования. Многие являются коммерчески доступными, например, в Nektar из Huntsville, AL. Неограничивающий список приемлемых активированных полимерных остатков включает






а другие остатки очевидны специалистам в данной области. В более предпочтительных аспектах активированный полимерный остаток представляет собой SC-mPEG. Даже если активированные полимерные остатки покупают у производителя, существует вероятность присутствия некоторых следовых количеств примесей, т.е. mPEG-OH или некоторых из PEG-OH, образующихся в ходе реакции. Таким образом, для реакционных смесей, получаемых с использованием таких соединений, следует применять гашение PEG-OH или другого исходного вещества.
Как правило, реакцию проводят приблизительно при комнатной температуре в инертном растворителе, таком как тетрагидрофуран (THF), толуол (TOL), метиленхлорид (DCM), хлороформ (CHCl3), диметилформамид (DMF) или их смеси.
C. Вторая реакционная смесь
После образования первой реакционной смеси она взаимодействует со многофункциональной связывающей группой, обладающей по крайней мере одной функциональной группой, которая не взаимодействует с активированным полимерным остатком. Реакцию проводят в условиях, в которых активированный полимерный остаток, находящийся в первой реакционной смеси, предпочтительно присутствует в молярном избытке в отношении многофункциональной связывающей группы.
Как правило, реакцию проводят приблизительно при комнатной температуре. Если используют предпочтительный SC-PEG, то при этом формирование второй реакционной смеси предпочтительно проводят при температурах приблизительно от 20°C до приблизительно 50°C, а более предпочтительно - приблизительно от 25°C до приблизительно 35°C.
Хотя лизин и сложные эфиры лизина, такие как сложный этиловый эфир лизина, являются двумя из множества хорошо известных и предпочтительных многофункциональных связывающих групп, обладающих по крайней мере одной защитной группой, т.е. функциональной группой, которая не взаимодействует с активированным полимерным остатком, специалисты в данной области безусловно понимают, что другие соединения также являются эффективными. Например, можно использовать 1,3-диамино-2-пропанол, диэтилентриамин, хлорид малонила и другие вещества. Как правило, неограничивающий список таких альтернатив включает замещенные алкилдиамины, триамины, природные и искусственные производные аминокислот, такие как производные сложного малонового эфира, и дигидроксиалкилы или дитиоалкилы.
В результате реакция приводит к образованию второй реакционной смеси, содержащей первую реакционную смесь и заново образованные промежуточные полимерные конъюгаты, получаемые в результате взаимодействия активированного полимерного остатка с многофункциональной связывающей группой.
D. Третья и четвертая реакционные смеси
После образования промежуточного полимерного конъюгата ко второй реакционной смеси по отдельности добавляют первый и второй гасящие реагенты для образования третьей и четвертой реакционных смесей соответственно.
Конкретно, третью реакционную смесь можно формировать взаимодействием второй реакционной смеси с первым гасящим реагентом для инактивации в ней активированного полимерного остатка. Затем к третьей реакционной смеси добавляют второй гасящий реагент для инактивации в ней активируемого полимерного остатка и формирования четвертой реакционной смеси. Таким образом, четвертая реакционная смесь содержит 1) промежуточный полимер, активируемый для связывания с интересующими мишенями (в ходе последовательных стадий), 2) инактивированные исходные вещества и 3) побочные продукты, которые в ином случае конкурируют с желаемым активированным полимерным линкером, когда с ним взаимодействует биологически активный белок, полипептид и т.д.
В альтернативном варианте осуществления изобретения третью реакционную смесь получают взаимодействием второй реакционной смеси со вторым гасящим реагентом таким образом, что первым в ней инактивируется активируемый полимерный остаток. Затем эта альтернативная третья реакционная смесь взаимодействует с первым гасящим реагентом для инактивации в ней активированного полимерного остатка и образования альтернативной четвертой реакционной смеси.
Используемое количество гасящих реагентов называют достаточным количеством. В целях настоящего изобретения "достаточное" количество веществ в случае первого гасящего реагента представляет собой количество, инактивирующее рассматриваемый здесь активированный полимерный остаток, а в случае второго гасящего реагента представляет собой количество, достаточное для инактивации рассматриваемого здесь активируемого полимерного остатка.
Приемлемые первые гасящие реагенты представляют собой те соединения, которые содержат группы свободного амина, свободного тиола или свободную гидроксильную группу, например цистеин, бензиламин, н-бутиламин, фенилэтиламин, блокированные по C-концу аминокислоты, такие как блокированный глицин или блокированный аланин, и их смеси.
Безусловно, выбор первого гасящего реагента зависит от природы используемого в способе активированного полимерного остатка (т.е. mPEG-SC и т.д.). Приемлемые вторые гасящие реагенты включают те соединения, которые содержат силильную группу или хлорангидрид и способны реагировать с рассматриваемым здесь активируемым полимерным остатком.
Выбор второго гасящего реагента также зависит от природы используемого в способе активируемого полимерного остатка (т.е. mPEG-OH, mPEG-NH2 и т.д.). Неограничивающий список приемлемых веществ включает тетрабутилдиметилсилилхлорид (TBDMSiCl), триметилсилилхлорид (TMSiCl) MeI, MeSO4, CF3SO3Me, Me3OBF4. Например, при использовании mPEG-OH предпочтительным вторым гасящим реагентом является TBDMSiCl.
E. Пятая реакционная смесь
Защитную группу в промежуточном полимере в четвертой реакционной смеси устраняют с использованием эффективного количества устраняющего защитную группу средства, т.е. сильной кислоты или сильного основания. Приемлемые основания включают в себя, но ими не ограничиваются, гидроксид лития, гидроксид калия, трет-бутилат калия, бутиллитий и амид натрия. Приемлемые кислоты можно выбирать из трифторуксусной кислоты (TFA), серной, фосфорной и соляной кислот и т.п. Предпочтительно для снятия защиты добавляют гидроксид лития с последующей нейтрализацией соляной кислотой. Затем четвертую смесь нейтрализуют, формируя пятую реакционную смесь.
Затем пятую реакционную смесь активируют посредством взаимодействия с соответствующим активирующим веществом, т.е. она взаимодействует с соединением, способным активировать в ней промежуточные полимерные конъюгаты для связывания с биологически активной молекулой. Эта стадия приводит к шестой реакционной смеси, содержащей активированный полимер, который надлежит в ней сформировать. Примеры приемлемых соединений, способных активировать промежуточное вещество, включают те "активирующие вещества", которые указаны выше для образования первой реакционной смеси. Если желательно предоставление возможности присоединения активированного полимера к аминогруппам мишени, то предпочтительной уходящей группой является NHS.
F. Полимерные конъюгаты
Шестая реакционная смесь содержит два инактивированных полимерных остатка и один активированный разветвленный полимерный линкер, который далее приемлем для взаимодействия с биологически активным веществом-мишенью без дополнительной очистки и для образования полимерных конъюгатов. Эти активированные разветвленные полимеры могут представлять собой полимеры, описанные в указанных выше, переуступленных в общее пользование патентов США №№ 5643575, 5919455 и 6113906. Одним из особенно предпочтительных активированных разветвленных полимеров является:

Как правило, получаемые способом по изобретению полимерные конъюгаты, содержащие уходящие группы, биологически активные соединения, молекулы для нацеливания или диагностические вещества, имеют формулу:
(R)n-L-D,
где:
R представляет собой полимерный остаток;
L представляет собой многофункциональную связывающую группу, такую как лизин, диаминопропанол, приемлемые аминокислоты, содержащие или не содержащие ароматические группы;
D представляет собой член группы, состоящей из уходящих групп, биологически активных молекул, молекул для нацеливания и диагностических веществ; и
n представляет собой положительное целое число, предпочтительно 2.
Более предпочтительно конъюгаты соответствуют одной из следующих формул:

где
R1-2 представляют собой одинаковые или различные полимерные остатки;
Y1-6 независимо представляют собой O, S или NR3, где R3 выбирают из H (предпочтительно), алкилов и замещенных алкилов C1-6, разветвленных алкилов и замещенных разветвленных алкилов C3-6, а также циклоалкилов C4-8;
J представляет собой бифункциональную связывающую группу; и
D представляет собой уходящую группу, биологически активное соединение, молекулу для нацеливания или диагностическое вещество. Предпочтительно по этому аспекту Y2 и Y4 представляют собой O, тогда как Y1, Y3, Y5 и Y6 представляют собой O, S или NH.
Еще одни полимерные конъюгаты по изобретению включают:




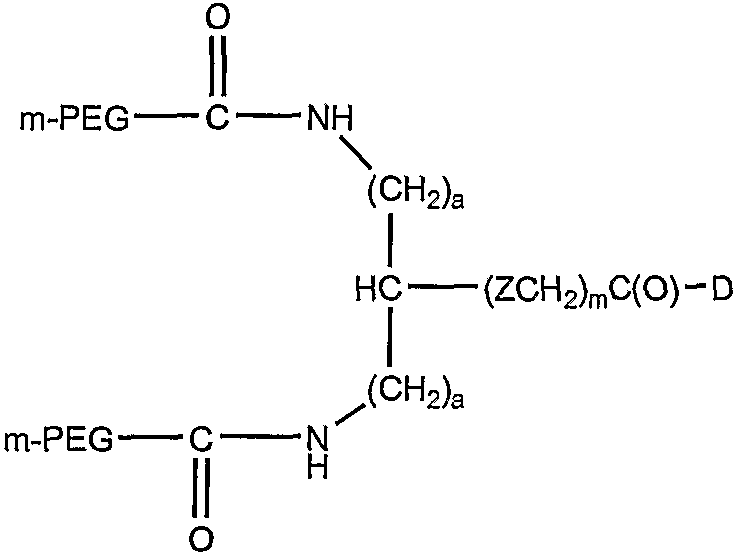
где:
(a) представляет собой целое число приблизительно от 1 до приблизительно 5;
Z представляет собой O, NR4, S, SO или SO2; где R4 представляет собой H, алкил C1-8, разветвленный алкил C1-8, замещенный алкил, арил или аралкил C1-8;
(m) представляет собой 0 или 1;
(p) представляет собой положительное целое число, предпочтительно приблизительно от 1 до приблизительно 6, и
D представляет собой уходящую группу, биологически активное соединение, молекулу для нацеливания или диагностическое вещество.
Полимерные остатки
Как указано выше, R, R1 и R2 представляют собой полимерные остатки. Предпочтительно каждый представляет собой водорастворимый полимерный остаток, предпочтительно практически не являющийся антигенным, например полиалкиленоксид (PAO), а более предпочтительно полиэтиленгликоль. В целях иллюстрации, а не ограничения, фрагмент остатка полиэтиленгликоля (PEG) можно выбирать из:
R6-O-(CH2CH2O)x-,
R6-O-(CH2CH2O)x-CH2C(O)-O-,
R6-O-(CH2CH2O)x-CH2CH2NR5- и
R6-O-(CH2CH2O)x-CH2CH2S-,
где:
x представляет собой степень полимеризации, т.е. приблизительно от 10 до приблизительно 2300;
R5 выбирают из водорода, алкилов C1-6, алкенилов C2-6, алкинилов C2-6, разветвленных алкилов C3-12, циклоалкилов C3-8, замещенных алкилов C1-6, замещенных алкенилов C2-6, замещенных алкинилов C2-6, замещенных циклоалкилов C3-8, арилов, замещенных арилов, аралкилов, гетероалкилов C1-6, замещенных гетероалкилов C1-6, алкоксиалкила C1-6, феноксиалкила и гетероалкокси-C1-6; и
R6 представляет собой блокирующую группу, т.е. метил, этил, бензил и т.д.
В одном из особенно предпочтительных вариантов осуществления R выбирают из
CH3-O-(CH2CH2O)x-, CH3-O-(CH2CH2O)x-CH2C(O)-O-,
CH3-O-(CH2CH2O)x-CH2CH2NH- и CH3-O-(CH2CH2O)x-CH2CH2S-,
где x представляет собой положительное целое число, выбранное таким образом, чтобы общая средневесовая молекулярная масса составляла приблизительно от 200 Да до приблизительно 120000 Да (дальтон). Предпочтительно общая средневесовая молекулярная масса составляет приблизительно от 2000 Да до приблизительно 80000 Да, а более предпочтительно приблизительно от 10000 Да до приблизительно 40000 Да. Во многих аспектах наиболее предпочтительная общая молекулярная масса полимерной части конъюгата составляет приблизительно от 5000 Да до приблизительно 40000 Да в зависимости от требований специалиста в данной области.
Предпочтительно включенные в настоящую заявку полимерные вещества растворимы в воде при комнатной температуре. Неограничивающий список таких полимеров включает гомополимеры полиалкиленоксида, например полиэтиленгликоль (PEG) или полипропиленгликоли, полиоксиэтиленированные полиолы, их сополимеры и их блок-сополимеры при условии, что у блок-сополимеров сохраняется водорастворимость.
Бифункциональные связывающие группы "J"
J может представлять собой любую связывающую группу, в которой облегчено присоединение биологически активной молекулы к алифатической связывающей группе. Неограничивающий список включает:
-NHC(O)CH2OCH2C(O)-;
-NHC(O)CH2NHCH2C(O)-;
-NHC(O)CH2SCH2C(O)-;
-NHC(O)CH2CH2CH2C(O)- или
-NHC(O)CH2CH2C(O)-;
где R7, R8 и R9 выбраны из той же группы, которая определяет R6; а t представляет собой положительное целое число, предпочтительно приблизительно от 1 до приблизительно 12.
G. Отделение полимерных конъюгатов
В другом аспекте указанный выше способ дополнительно включает стадию отделения или выделения полимерного конъюгата из побочных продуктов в смеси 7. Это можно осуществлять с использованием любого приемлемого в данной области способа, который эффективен для достижения результата. Предпочтительно используемый способ представляет собой способ, который можно эффективно использовать в промышленных условиях. Подразумевают, что для достижения желаемого результата наиболее часто используют диафильтрацию или эксклюзионную хроматографию. Однако в зависимости от конкретных потребностей специалиста в данной области можно также использовать ионообменную, аффинную хроматографию и хроматографию на гидрофобной колонке. Например, реакционную смесь можно разводить водой и загружать в колонку, заполненную смолой SP сефароза FF. Затем колонку промывают приемлемым буфером, таким как буфер PBS (фосфатный), для удаления всех инертных PEG вместе с PEG, гидролизованными в ходе реакции. Затем полимерные конъюгаты с двумя или более присоединенными участками вымывают с использованием различного градиента буфера до тех пор, пока не будут элюированы желаемые полимерные конъюгаты с высокой степенью чистоты, например >90-95%.
H. Биологически активные молекулы
В тех аспектах формулы (I), где D представляет собой биологически активное соединение, неограничивающий список таких приемлемых соединений включает остатки органических соединений, ферментов, белков, полипептидов и т.д. Кроме указанного выше, биологически активное соединение может также представлять собой остаток фермента, белка, полипептида, моноклональных антител, олигонуклеотидов, иммуноконъюгатов, например SS1P, одноцепочечных белков, связывающих антиген (SCA), например CC49, а, кроме того, также подразумеваются их фрагменты. Приемлемые белки включают в себя, но ими не ограничиваются, полипептиды, ферменты, пептиды и т.п., обладающие по крайней мере одной доступной группой для присоединения полимера, например ε-амино-, цистинилтио-, N-концевая аминогруппа, включая вещества, которые обладают физиологической или фармакологической активностью, а также вещества, способные катализировать реакции в органических растворителях.
Интересующие белки, полипептиды и пептиды включают в себя, но ими не ограничиваются, гемоглобин, белки сыворотки, такие как факторы крови, в том числе факторы VII, VIII и IX; иммуноглобулины, цитокины, такие как интерлейкины, т.е. от IL-1 до IL-13 и т.д., α-, β- и γ-интерфероны, колониестимулирующие факторы, в том числе гранулоцитарные колониестимулирующие факторы, тромбоцитарные факторы роста и активирующий фосфолипазу белок (PLAP), а также тимозин альфа-1 и секретин. Другие белки, представляющие общий биологический или терапевтический интерес, включают инсулин, растительные белки, такие как лектины и рицины, факторы некроза опухолей и родственные белки, факторы роста, такие как трансформирующие факторы роста, например, TGFα или TGFβ, VEGF, TNFα, вирусные белковые хемокины и эпидермальные факторы роста, гормоны, соматомедины, эритропоэтин, пигментные гормоны, гипоталамические высвобождающие факторы, антидиуретические гормоны, пролактин, хорионический гонадотропин, фолликулостимулирующий гормон, тиреотропный гормон, тканевой активатор плазминогена и т.п. Интересующие иммуноглобулины включают IgG, IgE, IgM, IgA, IgD и их фрагменты.
Некоторые белки, такие как интерлейкины, интерфероны и колониестимулирующие факторы, также существуют в негликозилированной форме, обычно в результате использования рекомбинантных способов. Негликозилированные варианты также входят в число белков по настоящему изобретению.
Интересующие ферменты включают специфичные к углеводам ферменты, протеолитические ферменты, оксидоредуктазы, трансферазы, гидролазы, лиазы, изомеразы и лигазы. Не ограничиваясь конкретными ферментами, примеры интересующих ферментов включают аспарагиназу, аргиназу, аргининдезаминазу, аденозиндезаминазу, супероксиддисмутазу, эндотоксиназы, каталазы, химотрипсин, липазы, уриказы, аденозиндифосфатазы, тирозиназы и билирубиноксидазу. Интересующие ферменты, которые специфичны к углеводам, включают глюкозооксидазы, глюкодазы, галактозидазы, глюкоцереброзидазы, глюкуронидазы и т.д.
Также в настоящую заявку включен любой фрагмент биологического полимера, проявляющий биоактивность in vivo. Они включают в себя аминокислотные последовательности, нуклеиновые кислоты (ДНК, РНК), пептидные нуклеиновые кислоты (ПНК), фрагменты антител, одноцепочечные связывающие белки, см., например, патент США № 4946778, описание которого упомянуто здесь полностью для сведения, связывающие группы, в том числе слитые антитела или фрагменты, поликлональные антитела, моноклональные антитела и каталитические антитела.
Белки или их фрагменты можно получать или выделять с использованием способов, известных специалистам в данной области, например культивированием ткани, экстракцией из животных источников или с использованием способов рекомбинантной ДНК. Также предусмотрены трансгенные источники белков, полипептидов, аминокислотных последовательностей и т.п. Такие вещества получают из трансгенных животных, т.е. мышей, свиней, коров и т.д., где белки экспрессируются в молоке, крови или тканях. Также в качестве источников предусмотрены трансгенные насекомые и бакуловирусные системы экспрессии. Кроме того, в объем изобретения также входят мутантные варианты белков, например мутантные интерфероны.
Другие интересующие белки представляют собой аллергенные белки, такие как амброзия, антиген E, пчелиный яд, клещевой аллерген и т.п. Указанное выше иллюстрирует белки, которые приемлемы по настоящему изобретению. Следует понимать, что эти белки, как указано в настоящей заявке, описанные не конкретно, но обладающие доступной аминогруппой, также предусмотрены и входят в объем настоящего изобретения.
В предпочтительном аспекте изобретения амино- или гидроксилсодержащее соединение представляет собой биологически активное соединение, приемлемое для медицинского или диагностического применения в лечении животных, например млекопитающих, в том числе человека, при таких состояниях, при которых желательно такое лечение. Указанный выше список предназначен для иллюстрации, а не для ограничения соединений, которые можно модифицировать. Специалисты в данной области понимают, что другие такие соединения/композиции можно модифицировать сходным образом без проведения лишних экспериментов. Следует понимать, что эти биологически активные вещества, указанные не конкретно, но обладающие приемлемыми присоединенными группами, также предусмотрены и входят в объем настоящего изобретения.
Диагностические средства
В тех аспектах формулы (I), где D представляет собой диагностическое средство, неограничивающий список приемлемых средств включает красители, хелатобразующие вещества и меченные изотопом соединения, а также другие меченые соединения, например зеленый флуоресцентный белок (GFP).
Молекулы для нацеливания
В тех аспектах формулы (I), где D представляет собой молекулы для нацеливания, неограничивающий список приемлемых средств включает пептиды, такие как пептид TAT и пептид U-7, одноцепочечные антитела, такие как CC49, а также малые молекулы, такие как, например, таурин и биотин.
В предпочтительном аспекте изобретения биологически активное соединение представляет собой соединение, приемлемое для медицинского или диагностического применения в лечении животных, например млекопитающих, в том числе человека, при таких состояниях, при которых желательно такое лечение. Указанный выше список предназначен для иллюстрации, а не для ограничения соединений, которые можно модифицировать. Специалисты в данной области понимают, что другие такие соединения/композиции можно модифицировать сходным образом без проведения лишних экспериментов. Следует понимать, что эти биологически активные вещества, указанные не конкретно, но обладающие приемлемыми присоединенными группами, также предусмотрены и входят в объем настоящего изобретения.
I. Диагностика in vivo
В другом аспекте изобретения диагностическое средство представляет собой метку, выбранную в диагностических целях или в целях получения изображения. Таким образом, приемлемую метку получают связыванием любой приемлемой молекулы, например аминокислотного остатка, с любым общепринятым в данной области излучающим изотопом, рентгеноконтрастной меткой, магнитно-резонансной меткой или другими нерадиоактивными изотопными метками, приемлемыми для получения магнитно-резонансного изображения, метками флуоресцентного типа, метками, проявляющими видимую окраску и/или способными флуоресцировать под воздействием ультрафиолетового излучения, инфракрасного излучения или электрохимической стимуляции, позволяя получать изображение ткани опухоли в ходе хирургических процедур и т.д. Необязательно, диагностическую метку включают в и/или связывают с конъюгированной терапевтической молекулой, что позволяет наблюдать распределение терапевтического биологически активного вещества в пациенте-животном или человеке.
В еще одном аспекте изобретения меченые конъюгаты по изобретению легко получают известными в данной области способами с использованием любой приемлемой метки, в том числе, например, радиоизотопных меток. Только в качестве примера такие метки включают131йод,125йод,99mтехнеций и/или111индий для получения средств для радиоиммуносцинтиграфии для избирательного поглощения опухолевыми клетками in vivo. Например, существует множество известных в данной области способов связывания пептида с Tc-99m, в том числе только в качестве примера способы, которые представлены в патентах США №№ 5328679, 5888474, 5997844 и 5997845, упомянутых здесь полностью для сведения. Также можно использовать другие радиоизотопы, такие как14C,15N и т.д.
В широком смысле для установления анатомического расположения опухолевой ткани у пациента пациенту или животному, у которого предполагают наличие опухоли, вводят метку-конъюгат. Через период времени, достаточный для предоставления возможности меченому иммуноглобулину сосредоточиться в опухолевом участке(-ах), регистрируют вызываемый меткой сигнал, например, визуально, рентгенографией, компьютеризированной трансаксиальной томографией, MRI, регистрацией люминесцентной метки посредством приборов, фотосканирующим устройством, таким как гамма-камера, или любым другим способом или прибором, соответствующим природе выбранной метки.
Затем регистрируемый сигнал преобразуют в изображение или анатомическое и/или физиологическое определение опухолевого участка. Изображение позволяет установить расположение опухоли in vivo и разработать соответствующий лечебный подход. В тех вариантах осуществления, где меченые молекулы сами являются терапевтическим средством, регистрируемый сигнал обеспечивает данные по анатомическому расположению в ходе лечения, обеспечивая исходные данные для последующего диагностического и терапевтического вмешательства.
ПРИМЕРЫ
Следующие примеры предназначены для обеспечения дальнейшего понимания изобретения и не предназначены для какого-либо ограничения эффективного объема изобретения. Ссылки в виде цифр, приведенные жирным шрифтом, соответствуют соединениям, которые представлены на фиг.2-3.
Синтез PEG2
Пример 1
Первая реакционная смесь:
Соединение 1, 20k mPEG-OH (125 г, 6,24 ммоль) в течение двух часов азеотропно кипятили с толуолом (1,88 л) в атмосфере азота для удаления 375 мл растворителя. Раствор охлаждали до 50°C. Добавляли трифосген (1,24 г, 4,18 ммоль) и пиридин (0,99 г, 12,47 ммоль) и перемешивали реакционный раствор в течение трех часов при 50°C. Затем добавляли N-гидроксисукцинимид (1,79 г, 15,59 ммоль) и пиридин (1,23 г, 15,59 ммоль). Реакционный раствор перемешивали в течение двадцати часов при 50°C с последующей фильтрацией для удаления соли пиридина. Растворитель в виде толуола полностью удаляли в вакууме при 40°C. Остаток растворяли в сухом дихлорметане (400 мл). Для осаждения продукта к раствору медленно добавляли простой этиловый эфир (2,50 л). Этот неочищенный продукт повторно растворяли в ацетонитриле (875 мл) с последующим медленным добавлением изопропилового спирта (3,75 л) для осаждения белых твердых веществ. Твердые вещества фильтровали и промывали изопропиловым спиртом и простым эфиром. Выделенные твердые вещества сушили в вакууме при 40°C для получения первой реакционной смеси, содержащей соединения 1 и 2 (112 г, 5,55 ммоль, 89%).13C-ЯМР (75,5 МГц, CDCl3) δ 25,0, 58,6, 67,9-71,4 (PEG), 151, 168,1.
Пример 2
Вторая и третья реакционные смеси:
Первую реакционную смесь из соединений 1 и 2 (5,0 г, 0,25 ммоль) растворяли в безводном хлороформе (50 мл) в атмосфере азота. Добавляли дихлоргидрат сложного 1-лизинэтилового эфира (26 мг, 0,10 ммоль) и триэтиламин (42 мг, 0,41 ммоль). Реакционный раствор нагревали до 30°C и перемешивали в течение двадцати часов при 30°C для получения второй реакционной смеси, содержащей соединения 1, 2 и 4. Эту вторую реакционную смесь охлаждали до комнатной температуры с последующим добавлением бензиламина (53,2 мг, 0,50 ммоль) для гашения избытка активированного PEG из первой реакционной смеси. Этот реакционный раствор перемешивали в течение двадцати часов при комнатной температуре. Растворитель удаляли в вакууме при 30°C. Остаток растворяли в сухом дихлорметане (15 мл). Для осаждения продукта к раствору медленно добавляли простой этиловый эфир (100 мл). Этот неочищенный продукт повторно растворяли в ацетонитриле (10 мл) с последующим медленным добавлением изопропилового спирта (150 мл) для осаждения белых твердых веществ. Твердые вещества фильтровали и промывали изопропиловым спиртом и простым эфиром. Выделенные твердые вещества сушили в вакууме при 40°C для получения третьей реакционной смеси из соединений 1, 4 и 5 (4,5 г, 90% мас.).13C-ЯМР (75,5 МГц, CDCl3) δ 13,84, 21,91, 29,06, 31,70, 40,06, 44,38 (бензиламин), 53,27, 58,55, 60,85, 63,26, 63,71, 68,97-71,41 (PEG), 126,88-127,95 (бензиламин), 155,32, 155,88, 171,60.
Пример 3
Четвертая реакционная смесь:
Третью реакционную смесь, содержащую соединения 1, 4 и 5 (4,23 г), растворяли в безводном дихлорметане (40 мл) с последующим добавлением трет-бутилдиметилсилилхлорида (8 мг, 0,05 ммоль) и триэтиламина (26 мг, 0,26 ммоль). Реакционный раствор перемешивали в течение двадцати часов при комнатной температуре в атмосфере азота. Растворитель удаляли в вакууме. Остаток растворяли в сухом дихлорметане (15 мл). Для осаждения продукта к раствору медленно добавляли простой этиловый эфир (100 мл). Этот неочищенный продукт повторно растворяли в ацетонитриле (10 мл) с последующим медленным добавлением изопропилового спирта (125 мл) для осаждения белых твердых веществ. Твердые вещества фильтровали и промывали изопропиловым спиртом и простым эфиром. Выделенные твердые вещества сушили в вакууме при 40°C для получения четвертой реакционной смеси из соединений 4, 5 и 6 (3,8 г, 93% мас.).13C-ЯМР (75,5 МГц, CDCl3) δ 13,79, 21,85, 28,98, 31,59, 39,99, 44,38 (бензиламин), 53,20, 58,49, 60,76, 63,20, 63,64, 68,91-71,37 (PEG), 126,84-127,89 (бензиламин), 155,29, 155,84, 171,54.
Пример 4
Пятая реакционная смесь:
Четвертую реакционную смесь из соединений 4, 5 и 6 (3,46 г) полностью растворяли в воде (20 мл). Добавляли моногидрат гидроксида лития (5,4 мг, 0,13 ммоль) и реакционный раствор перемешивали при комнатной температуре в течение двадцати часов. Доводили pH раствора до 2-2,5 с последующей двухразовой экстракцией дихлорметаном (100 мл). Объединенный органический слой сушили с использованием сульфата магния. Растворитель удаляли в вакууме. Остаток растворяли в сухом дихлорметане (15 мл). Для осаждения продукта к раствору медленно добавляли простой этиловый эфир (100 мл). Твердые вещества фильтровали и промывали простым эфиром. Выделенные твердые вещества сушили в вакууме при 40°C для получения пятой реакционной смеси, содержащей соединения 5, 6 и 7 (3,0 г, 87% мас.).13C-ЯМР (75,5 МГц, CDCl3) δ 21,8, 28,98, 31,62, 40,06, 44,50 (бензиламин), 52,88, 58,55, 63,23, 63,63, 65,29-72,27 (PEG), 126,87-127,95 (бензиламин), 155,29, 155,84, 172,40.
Пример 5
Шестая реакционная смесь:
Пятую реакционную смесь, содержащую соединения 5, 6 и 7 (2,22 г), N-гидроксисукцинимид (38 мг, 0,33 ммоль) и N,N-диизопропилэтиламин (85 мг, 0,66 ммоль), растворяли в смеси растворителей из безводного дихлорметана и N,N-диметилформамида в атмосфере азота. Раствор охлаждали до 0°C посредством ледяной бани и добавляли хлоргидрат 1-[3-(диметиламин)пропил]-3-этилкарбодиимида. Реакционный раствор в течение ночи перемешивали от 0°C до комнатной температуры. Растворитель удаляли в вакууме. Остаток растворяли в сухом дихлорметане (7 мл). Для осаждения продукта к раствору медленно добавляли простой этиловый эфир (50 мл). Этот неочищенный продукт повторно растворяли в ацетонитриле (4,5 мл) с последующим медленным добавлением изопропилового спирта (70 мл) для осаждения белых твердых веществ. Твердые вещества фильтровали и промывали изопропиловым спиртом и простым эфиром. Выделенные твердые вещества сушили в вакууме при 40°C для получения шестой реакционной смеси, содержащей соединения 5, 6 и 8 (2,07 г, 93% мас.).13C-ЯМР (75,5 МГц, CDCl3) δ 21,46, 25,17, 28,80, 31,38, 39,74, 44,44 (бензиламин), 51,72, 58,55, 63,34, 64,03, 69,12-71,41 (PEG), 126,93-127,95 (бензиламин), 155,07, 155,97, 167,51, 168,19.
Пример 6
PEG2-IFN β-1b (монопегилированный PEG2-интерферон β-1b)
Пегилированный IFN β-1b (монопегилированный PEG2-интерферон β-1b) синтезировали реакцией чистого IFN β-1b (5 мл при 0,45 мг/мл) в 50 мМ фосфате натрия, 50 мМ хлориде натрия, 0,05% Zwittergent 3-14, pH 7,9 с шестой реакционной смесью, содержащей соединения 5, 6 и 8 (38 мг). Реакционную смесь перемешивали в течение 1,5 часа при 25°C. Реакцию пегилирования гасили добавлением глицина (9,5 мкл 1 М раствора глицина), а затем снижением pH до 6,5 посредством 2 н. уксусной кислоты. Монопегилированный конъюгат, соединение 9 (обработанный разветвленным PEG белок), получали с выходом 39% в соответствии с высокоэффективной жидкостной хроматографией с обращенной фазой (RP-HPLC) (см. таблицу 1). Пегилированного IFN β-1b с прямой цепью (1/2 PEG) не наблюдали. Для выделения чистого монопегилированного IFN β-1b, соединения 9, использовали следующую процедуру.
Гашеную реакционную смесь разводили водой, доводя проводимость до ~5 мс, а затем загружали в колонку, заполненную смолой SP сефароза FF, предварительно уравновешенную 20 мМ фосфатом натрия, pH 6,5, при объемной скорости потока 5 мл/мин. Колонку промывали уравновешивающим буфером для удаления из шестой реакционной смеси всех инертных PEG вместе с PEG, гидролизованным в ходе реакции. Олигомеры PEG2-IFN β-1b (HiPEG) вымывали 75 мМ хлоридом натрия в уравновешивающем буфере в течение 10 объемов колонки. Затем желаемый монопегилированный PEG2-IFN β-1b, соединение 9, элюировали с использованием 225 мМ хлорида натрия в уравновешивающем буфере в течение 10 объемов колонки. Основываясь на IFN-β, конечный выход выделенного продукта составлял приблизительно 30%.

Примечание: монопегилированный = монопегилированный PEG2-IFN β-1b; HiPEG = ди/трипегилированный PEG2-IFN β-1b; исходный = IFN β-1b; 1/2 PEG = PEG-IFN β-1b с прямой цепью.
Пример 7
Пегилированный IFN β-1b для сравнения получали с использованием вместо разветвленного активированного PEG 8 PEG2-NHS с той же молекулярной массой из Nektar и шестой реакционной смеси, которую применяли в примере 6, при тех же условиях конъюгации. Перед реакцией с интерфероном этот PEG2-NHS для сравнения очищали с использованием хроматографии на колонках. После пегилирования снова проводили анализ RP-HPLC. Результаты представлены ниже в таблице 2.

Указанные выше результаты показывают, что в сравнении со способами предшествующего уровня техники способ по настоящему изобретению обеспечивает благоприятные результаты без дополнительных расходов, необходимых для очистки PEG2-NHS на колонке перед реакцией с интерфероном. Порция Hi-PEG (мульти-PEG), получаемая в результате способа по изобретению, была значительно меньше, чем порция, которую наблюдали при использовании коммерчески доступного PEG2-NHS. В результате нового способа процентный выход Hi-PEG был снижен приблизительно на половину.
Реферат
Изобретение относится к способам получения полимерных конъюгатов. Предложены варианты способа получения смеси, включающей активированный полимер, который имеет многофункциональную связывающую группу, где активируемым полимером является полиалкиленоксид. Получаемая смесь пригодна к последующей конъюгации с биологически активными молекулами. Технический результат - эффективное получение полимерных конъюгатов, таких как разветвленные конъюгаты PEG-полипептид, в промышленных масштабах без очистки активированных линкеров PEG хроматографией на колонках для удаления примесей. 2 н. и 33 з.п. ф-лы, 3 ил., 2 табл.
Формула
a) взаимодействие активируемого полимерного остатка с активирующим веществом, способным предоставлять для этого уходящую группу, что дает первую реакционную смесь, которая содержит активированный полимерный остаток и активируемый полимерный остаток;
b) взаимодействие указанной первой реакционной смеси с многофункциональной связывающей группой, несущей на себе защитную группу, которая не взаимодействует с указанным активированным полимерным остатком, в условиях, в которых указанный активированный полимерный остаток из первой реакционной смеси присутствует в избытке по отношению к указанной многофункциональной связывающей группе, с образованием второй реакционной смеси, которая включает указанную первую реакционную смесь и содержащий защитную группу промежуточный полимер, получаемый в результате указанного взаимодействия указанного активированного полимерного остатка с указанной многофункциональной связывающей группой;
c) гашение указанной второй реакционной смеси с использованием достаточного количества первого гасящего реагента для инактивации в ней активированного полимерного остатка, с образованием третьей реакционной смеси, которая содержит указанный промежуточный полимер;
d) добавление к указанной третьей реакционной смеси достаточного количества второго гасящего реагента для инактивации в ней активируемого полимерного остатка и образования четвертой реакционной смеси, содержащей указанный промежуточный полимер;
e) удаление защитной группы из промежуточного полимера и нейтрализацию указанной четвертой реакционной смеси с образованием пятой реакционной смеси, содержащей незащищенный промежуточный полимер; и
f) взаимодействие указанной пятой реакционной смеси с соединением, способным активировать в ней незащищенный промежуточный полимер для связывания с биологически активной молекулой, и образование шестой реакционной смеси, которая содержит активированный полимер, который имеет многофункциональную связывающую группу.

где R представляет собой полимерный остаток;
L представляет собой многофункциональную алифатическую связывающую группу;
D представляет собой член группы, состоящей из биологически активных молекул, молекул для нацеливания и диагностических средств; и
n представляет собой положительное целое число.










где R1-2 представляют собой одинаковые или различные полимерные остатки;
Y1-6 независимо представляют собой О, S или NR10, где R10 выбирают из группы, состоящей из Н, алкилов и замещенных алкилов C1-6, разветвленных алкилов и замещенных разветвленных алкилов С3-6, а также циклоалкилов С4-8;
J представляет собой бифункциональную связывающую группу; и
D представляет собой биологически активное соединение, молекулу для нацеливания или диагностическое вещество.
a) взаимодействие активируемого полимерного остатка с активирующим веществом, способным предоставлять для этого уходящую группу, что дает первую реакционную смесь, которая содержит активированный полимерный остаток и активируемый полимерный остаток;
b) взаимодействие указанной первой реакционной смеси с многофункциональной связывающей группой, несущей на себе защитную группу, которая не взаимодействует с указанным активированным полимерным остатком, в условиях, когда указанный активированный полимерный остаток из первой реакционной смеси присутствует в избытке по отношению к указанной многофункциональной связывающей группе, с образованием второй реакционной смеси, которая включает указанную первую реакционную смесь и содержащий защитную группу промежуточный полимер, получаемый в результате указанного взаимодействия указанного активированного полимерного остатка с указанной многофункциональной связывающей группой;
c) гашение указанной второй реакционной смеси с использованием достаточного количества первого гасящего реагента для инактивации в ней активируемого полимерного остатка, с образованием третьей реакционной смеси, которая содержит указанный промежуточный полимер;
d) добавление к указанной третьей реакционной смеси достаточного количества второго гасящего реагента для инактивации в ней активированного полимерного остатка и образования четвертой реакционной смеси, содержащей указанный промежуточный полимер;
e) удаление защитной группы в промежуточном полимере и нейтрализацию указанной четвертой реакционной смеси с образованием пятой реакционной смеси, содержащей незащищенный промежуточный полимер; и
f) взаимодействие указанной пятой реакционной смеси с соединением, способным активировать в ней незащищенный промежуточный полимер для связывания с биологически активной молекулой, и образование шестой реакционной смеси, которая содержит активированный полимер, который имеет многофункциональную связывающую группу.




где (а) представляет собой целое число приблизительно от 1 до приблизительно 5;
Z представляет собой О, NR4, S, SO или SO2; где R4 представляет собой Н, C1-8 алкил, C1-8 разветвленный алкил, C1-8 замещенный алкил, арил или аралкил;
(m) представляет собой 0 или 1;
(р) представляет собой положительное целое число, предпочтительно приблизительно от 1 до приблизительно 6, и
D выбрано из группы, состоящей из биологически активных соединений, молекул для нацеливания или диагностических веществ.



Комментарии