Лекарственный препарат, обладающий иммуномоделирующим, иммунокоррегирующим, противопаразитарным, противосклеротическим, противовирусным, противобактериальным, противогрибковым, противовоспалительным и противоопухолевым действием, и способ его приготовлен - RU2197248C2
Код документа: RU2197248C2
Чертежи


Описание
Изобретение относится к медицине, ветеринарии, фармакологии и химико-фармацевтической промышленности, а более конкретно к иммуномодулирующим, иммунокоррегирующим, противопаразитарным, противосклеротическим, противовирусным, противобактериальным, противогрибковым, противовоспалительным и противоопухолевым препаратам, промышленному способу их приготовления, способу лечения иммунных, паразитарных, вирусных, бактериальных, грибковых, воспалительных и опухолевых заболеваний и новому комплексному применению лекарственных форм лекарственного препарата.
УРОВЕНЬ
ТЕХНИКИ
Известны применяемые в практической медицине лекарственные препараты (лекарственные средства в определенной лекарственной форме) противоинфекционного (противомикробного,
противогрибкового и противовирусного), противовоспалительного и противоопухолевого действия [1-3].
Современными высокоэффективными противомикробными препаратами являются лекарственные средства, включающие в свой состав антибиотики, сульфаниламиды, производные нитрофурана или 8-оксихинолина [4, 5].
К противогрибковым лекарственным препаратам относят антибиотики (гризеофульвин, микосептин, нистатин и др.) и препараты на основе имидазола (клотримазол, миконазол и др.) [3, 4, 6].
В настоящее время широко используются противовирусные лекарственные препараты двух основных групп: препараты на основе аномальных нуклеозодов (например, ацикловир, виразол ), а также интерфероны или их индукторы [5-9].
Группа противовоспалительных фармакологических средств представлена препаратами салициловой (аспирин), фенилпропионовой (ибупрофен) кислот, глюкокортикостероидами (кортизон) [4, 8-10].
Противоопухолевые медицинские препараты это, в первую очередь, химиотерапевтические средства (циклофосфан, фотрин, цитозар и др.) и противоопухолевые антибиотики (брунеомицин, адриомицин) [3-5, 8].
Отдельную, все более важную и наиболее значимую в настоящее время для практической медицины и ветиринарии, группу лекарственных препаратов составляют препараты широкого спектра действия - иммуномодуляторы, изменяющие иммунный ответ организма человека или животного [3, 6, 9].
Особое значение для практической медицины имеют препараты-иммуностимуляторы, например левамизол, тималин, амиксин, а также терафектин (амиприлоз), созданный на основе монозамещенного эфира моносахарида иммуномодулятор, обладающий выраженным противовоспалительным действием [11-13].
Эти препараты увеличивают сопротивляемость пациентов различным инфекциям за счет усиления гуморального или клеточного иммунитета [1-5, 9].
Такие препараты, как правило, обладают относительно широким спектром фармакологического действия, но известные препараты не достаточно эффективны при лечении комплексных заболеваний и поэтому они чаще всего используются в качестве вспомогательных лекарственных средств при лечении отдельных заболеваний различной этиологии.
Известны такие индукторы эндогенного интерферона (один из видов иммуностимуляции), как неовир и циклоферон [14-17]. Эти препараты применяются в медицине в качестве эффективных противовирусных средств.
Известен иммуномодулирующий лекарственный препарат в виде гидрофобных производных N-акридонуксусной кислоты, приготовленный методом микрокапсулирования на фосфолипидном носителе (получение липосом) и методом растворения в воде с эквивалентным количеством гидроксидов щелочных или щелочноземельных металлов и рН-стабилизирующими добавками [19], однако данный препарат обладает ограниченным лечебным действием и не эффективен при лечении комплексных заболеваний.
Известна ранее полученная авторами-заявителями группа химических соединений и способ их получения - соли акридонуксусных кислот и монозамещенных эфиров моносахаридов и их противоинфекционное, противовоспалительное и противоопухлевое действие [20]. По данному способу эти соли перед их применением предварительно синтезируют в твердом виде путем смешивания эквимолекулярных количеств акридонуксусной кислоты или ее производных и монозамещенных эфиров моносахаридов в безводном ацетоне, кипячения с обратным холодильником в течение 20-40 минут с предохранением от попадания влаги, упаривания полученного раствора в вакууме до объема, необходимого для выпадения осадка соли, отделения выпавшего осадка фильтрацией, высушивания и перекристаллизовывания из безводного метанола, высушивания перекристаллизованного осадка в вакууме с получением кристаллической соли акридонуксусных кислот и монозамещенных эфиров моносахаридов и использования этой соли в качестве лекарственного средства противоинфекционного, противовоспалительного и противоопухлевого действия. Получаемые таким образом соли очень гигроскопичны, интенсивно впитывают влагу из воздуха и не пригодны для длительного хранения в обычных для медицинских и ветеринарных препаратов условиях.
Наиболее близким по технической сущности и достигаемому при использованию результату (прототипом), является разработанный ранее при участии авторов-заявителей иммуномодулирующий лекарственный препарат, содержащий в качестве лекарственного вещества производное акридона и моносахаридов различного строения, включенные в фармацевтически приемлемую основу (вспомогательное вещество) [18] . Основным действующим началом этих препаратов являются водорастворимые соли N-акридонуксусной кислоты. При значительной, по сравнению с другими известными препаратами, эффективности противовирусного действия данные лекарственные препараты гидрофильны, что затрудняет проникновение их через липидный слой клеточных мембран. Это в свою очередь существенно ослабляет действие данного лекарственного вещества на внутриклеточных паразитов. Кроме этого, данные препараты обладают ограниченной сферой лечебного действия.
Вышеприведенные аналоги и прототип лекарственного препарата и способы их получения и применения имеют ряд общих существенных недостатков:
- недостаточно широкий спектр фармакологической
активности (специфическое противовирусное или противоопухолевое действие);
- принципиальная невозможность получения ряда лекарственных форм на основе данных лекарственны веществ;
- нестабильность при длительном хранении (разрушение липосом или выпадение осадков из растворов);
- высокая стоимость, трудоемкость и технологическая сложность получения лекарственного
вещества.
ЗАДАЧИ ИЗОБРЕТЕНИЯ
Задачами изобретений и требуемым техническим результатом, достигаемым при использовании изобретений, является разработка и промышленное
изготовление пригодных к использованию в медицине и ветеринарии всех известных в настоящее время лекарственных форм [Государственная Фармакопея ХI, вып.2.] уникального, обладающего высокой активностью
и широким спектром фармакологического действия лекарственного препарата, неспецифического иммуномодулирующего, иммунокоррегирующего, противопаразитарного, противосклеротического, противовирусного,
противобактериального, противогрибкового, противовоспалительного и противоопухолевого действия, разработка нового технологически простого и экономически выгодного промышленного способа приготовления
разнообразных лекарственных форм лекарственного препарата с простым получением различных типов высокоактивных лекарственных форм, содержащих соли акридонуксусной кислоты или ее производных с
монозамещенными эфирами моносахаридов и фармацевтически приемлемые носители (вспомогательные вещества), нового способа лечения иммунных, паразитарных, вирусных, бактериальных, грибковых,
воспалительных и опухолевых заболеваний и нового, не известного ранее применения новых, не известных ранее лекарственных форм лекарственного препарата при одновременном обеспечении максимального
сохранения свойств лекарственного вещества, увеличения сроков хранения препарата, расширении области применения, повышении эффективности против широкого круга смешанных инфекций неизвестной этиологии
и ряда медленных инфекций.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Поставленные задачи решаются и требуемый технический результат достигается тем, что лекарственный препарат, обладающий
иммуномодулирующим, иммунокоррегирующим, противопаразитарным, противосклеротическим, противовирусным, противобактериальным, противогрибковым, противовоспалительным и противоопухолевым действием,
включающий лекарственное вещество и вспомогательное вещество согласно изобретению в качестве лекарственного вещества препарат содержит смесь акридонуксусной кислоты или производных акридонуксусной
кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов общей формулы
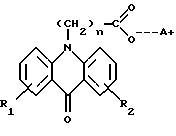
где

или
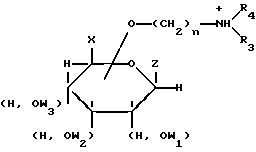
Группа
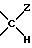
(Н, OW1), (Н, OW2), (Н, OW3) обозначают различные изомеры, отличающиеся положением групп Н и OW относительно плоскости кольца моносахарида.
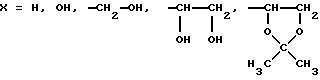
Z= Н, ОН алкил, гидроксиалкил, алкоксил, алкоксиалкил.
W1, W2, W3=Н, алкил, арил, алкенил.
OW1 и Z, OW2 и Z, OW3 и Z, OW1 и X, OW2 и X, OW3 и X, OW1 и OW2, OW1 и OW3, OW2 и OW3 = алкил, арил, бензил, алкенил.
R1, R2=Н, ОН, галоген, алкил, оксиалкил, арил, оксиарил, карбоксигруппа.
R3, R4= Н, алкил, арил или R3 и R4 вместе с атомом азота образуют орфолиновый, пиперидиновый или пиридиновый гетероцикл, n=1-4, при этом в качестве вспомогательного вещества
препарат содержит вещество или вещества, используемое или используемые для приготовления мази, или крема, или пасты, или геля, или линимента, или глазных, или интраназальных капель, или капель для
ушей, или спрея, или аэрозоля, или раствора для парентерального введения, или таблеток, или таблеток с кишечно-растворимым покрытием, или порошка в капсулах, или суппозиториев при соотношении,
мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с
монозамещенными эфирами моносахаридов - 0,05-80
Вспомогательное вещество - 20-99,95
При этом лекарственный препарат содержит смесь акридонуксусной кислоты или производных
акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов, приготовленную путем
смешивания, или смешивания и последующего нагревания, или смешивания при нагревании, или смешивания с нагретым вспомогательным веществом акридонуксусной кислоты, или производных акридонуксусной
кислоты и монозамещенных эфиров моносахаридов непосредственно перед или во время их смешивания с вспомогательным веществом.
При этом лекарственный препарат приготовлен в лекарственной форме мази, или крема, или пасты, или геля, или линимента, или глазных капель, или интраназальных капель, или капель для ушей, или спрея, или аэрозоля, или раствора для парентерального введения, или таблеток, или таблеток с кишечно-растворимым покрытием, или порошка в капсулах, или суппозиториев.
Кроме этого, лекарственный препарат в качестве лекарственного вещества содержит вещество АНАНДИН, имеющее химическую формулу C32H42N2O9 и молекулярную массу, равную 598,76 углеродных единиц, и представляющее собой смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N,N-диметиламино-н-пропил)-1,2:5,6-ди-O-изопропилиден-α,D-глюкофуранозы(диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) с 3-О(N, N-диметиламино-н-пропил)-1,2:5,6-ди-O-изопропилиден-α, D-глюкофуранозой (диметиламинопропилглюкофуранозой), или препарат содержит смесь 3-хлор-10-метиленкарбоксилат-9-акридона и 1,2: 3,4-ди-O-изопропилиден-6-O-(N, N-диэтиламиноэтил)-α, D-галактопиранозы или соль 3-хлор-10-метиленкарбоксилат-9-акридона с 1,2:3, 4-ди-О-изопропилиден-6-О-(N, N-диэтиламиноэтил)-α,D-галактопиранозой, или препарат содержит смесь 3-хлор-6-метил-N-акридонуксусной кислоты и 3-О-(1'-этил-2'-(N-морфолинил)-1, 2-О-изопропилиден-α, D-глюкофуранозы, или соль 3-хлор-6-метил-N-акридонуксусной кислоты с 3-О-(1'-этил-2'-(N-морфолинил)-1,2-О-изопропилиден-α, D-глюкофуранозой, или препарат содержит смесь 3,7-диэтокси-10-метиленкарбоксилат-9-акридона и 3-О-(N,N-диметиламиноэтил)-1,2-О-изопропилиден-α,D-глюкофуранозы, или соль 3,7-диэтокси-10-метиленкарбоксилат-9-акридона с 3-О-(N, N-диметиламиноэтил)-1,2-О-изопропилиден-α, D-глюкофуранозой, или смесь 2-карбокси-N-метиленкарбокси-9-акридона и 3-О-(N, N-диэтиламино-(2'-изобутил)-1,2-О-изопропилиден-α, D-аллофуранозы, или соль 2-карбокси-N-метиленкарбокси-9-акридона с 3-О-(N,N-диэтиламино-(2'-изобутил)-1,2-О-изопропилиден-α,D-аллофуранозой.
Лекарственный препарат в лекарственной форме мази в
качестве лекарственного вещества содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных
акридонуксусной кислоты с монозамещенными эфирами моносахаридов, а в качестве вспомогательного вещества препарат содержит липофильную, или жировую, или гидрофильную основу мази при соотношении,
мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с
монозамещенными эфирами моносахаридов - 0,1-50
Основа мази - 50-99,9
При этом лекарственный препарат в лекарственной форме мази в качестве лекарственного вещества содержит
лекарственное вещество АНАНДИН, имеющее химическую формулу C32H42N2O9 и молекулярную массу, равную 598,76 углеродных единиц, и представляющее собой смесь
N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль
N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) с 3-О(N,N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α,D-глюкофуранозой(диметиламинопропилглюкофуранозой), а в качестве
вспомогательного вещества препарат содержит вазелин, масло касторовое, калий салициловокислый и воду при соотношении, мас.%:
Смесь N-акридонуксусной кислоты (глюкоаминопропилкарб-акридона) и
3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты с 3-О-(N, N-диметиламино-н-пропил)-1,2:5,
6-ди-О-изопропилиден-α,D-глюкофуранозой - 2
Вазелин - 80
Масло касторовое - 5
Калий салициловокислый - 0,1
Вода - 12,9
Кроме этого лекарственный
препарат в лекарственной форме мази в качестве лекарственного вещества содержит лекарственное вещество АНАНДИН, имеющее химическую формулу C32H42N2O9 и
молекулярную массу, равную 598,76 углеродных единиц, и представляющее собой смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2:5,
6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) с 3-О(N,N-диметиламино-н-пропил)-1,2:5,
6-ди-О-изопропилиден-α,D-глюкофуранозой(диметиламинопропилглюкофуранозой), а в качестве вспомогательного вещества препарат содержит ланолин, масло касторовое, калий салициловокислый, спирт и
воду при соотношении, мас.%:
Смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы
(диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты с 3-О-(N,N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-
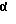
Ланолин - 60
Масло касторовое - 30
Калий салициловокислый - 0,1
Спирт - 3
Вода - 4,9
Лекарственный препарат в лекарственной форме глазных капель или интраназальных капель в качестве лекарственного вещества содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов, а в качестве вспомогательного вещества препарат содержит стерильный водный или масляный растворитель, стабилизатор и/или консервант при соотношении, мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов - 0,1-50
Растворитель, стабилизатор и/или консервант - 50-99,9
При этом лекарственный препарат в лекарственной форме глазных капель или интраназальных капель в качестве лекарственного вещества содержит лекарственное вещество АНАНДИН, имеющее химическую формулу C32H42N2O9 и молекулярную массу, равную 598,76 углеродных единиц, и представляющее собой смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N,N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α,D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) с 3-О-(N,N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α, D-глюкофуранозой (диметиламинопропилглюкофуранозой), а в качестве вспомогательного вещества препарат содержит глицерин и воду при соотношении, мас.%:
Смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты с 3-О-(N, N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α,D-глюкофуранозой - 2
Глицерин - 5
Вода - 93
Кроме этого, лекарственный препарат в лекарственной форме глазных капель в качестве лекарственного вещества содержит смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2:3, 4-ди-О-изопропилиден-6-О-(N,N-диэтиламиноэтил)-α,D-галактопиранозы или соль 3-хлор-10-метиленкарбокси-9-акридона с 1,2:3,4-ди-О-изопропилиден-6-О-(N,N-диэтиламиноэтил)-α, D-галактопиранозой, а в качестве вспомогательного вещества препарат содержит глицерин и воду при соотношении, мас.%:
Смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2:3, 4-ди-О-изопропилиден-6-О-(N,N-диэтиламиноэтил)-α,D-галактопиранозой или соль 3-хлор-10-метиленкарбокси-9-акридона с 1,2: 3,4-ди-О-изопропилиден-6-О-(N,N-диэтиламиноэтил)-α, D-галактопиранозой - 2
Глицерин - 18
Вода - 80
Лекарственный препарат в лекарственной форме интраназальных капель в качестве лекарственного вещества содержит смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2:3,4-ди-О-изопропилиден-6-О(N,N-диэтиламиноэтил)-α,D-галактопиранозы или соль 3-хлор-10-метиленкарбокси-9-акридона с 1,2:3,4-ди-О-изопропилиден-6-О(N, N-диэтиламиноэтил)-α,D-галактопиранозой, а в качестве вспомогательного вещества препарат содержит глицерин, метилпарабен и воду при соотношении, мас.%:
Смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2:3,4-ди-О-изопропилиден-6-О(N, N-диэтиламиноэтил)-α, D-галактопиранозы или соль 3-хлор-10-метиленкарбокси-9-акридона с 1,2:3, 4-ди-О-изопропилиден-6-О-(N,N-диэтиламиноэтил)-α,D-галактопиранозой - 2
Глицерин - 18
Метилпарабен - 0,2
Вода - 79,8
Лекарственный препарат в лекарственной форме капель для ушей в качестве лекарственного вещества содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов, а в качестве вспомогательного вещества препарат содержит стерильный водный или спиртовый или масляный растворитель, стабилизатор и/или консервант при соотношении, мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов - 0,1-50
Растворитель, стабилизатор и/или консервант - 50-99,9
При этом лекарственный препарат в лекарственной форме капель для ушей в качестве лекарственного вещества содержит лекарственное вещество АНАНДИН, имеющее химическую формулу C32H42N2O9 и молекулярную массу, равную 598,76 углеродных единиц, и представляющее собой смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1, 2:5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты с 3-О(N,N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α, D-глюкофуранозой (диметиламинопропилглюкофуранозой), а в качестве вспомогательного вещества препарат содержит масло касторовое, спирт изопропиловый, антибиотик (например, грамицидин) и воду при соотношении, мас.%:
Смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты с 3-О-(N, N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α,D-глюкофуранозой - 1,5-2,5
Масло касторовое - 4
Спирт изопропиловый - 75
Антибиотик (грамицидин С) - 0,005
Вода - Остальное
Лекарственный препарат в лекарственной форме раствора для парентерального введения в качестве лекарственного вещества содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов, а в качестве вспомогательного вещества препарат содержит растворитель, консервант и/или антиоксидант и/или стабилизатор при соотношении, мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов - 0,05-60
Растворитель, консервант и/или антиоксидант и/или стабилизатор - 40-99,95
При этом лекарственный препарат в лекарственной форме раствора для парентерального введения в качестве лекарственного вещества содержит лекарственное вещество АНАНДИН, имеющее химическую формулу C32H42N2O9 и молекулярную массу, равную 598,76 углеродных единиц, и представляющее собой смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N,N-диметиламино-н-пропил)-1,2: 5, 6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) с 3-О(N, N-диметиламино-н-пропил)-1,2:5, 6-ди-О-изопропилиден-α, D-глюкофуранозой (диметиламинопропилглюкофуранозой), а в качестве вспомогательного вещества препарат содержит метиленовый синий, цитрат натрия, лимонную кислоту и апирогенную воду при соотношении, мас.%:
Смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты с 3-О-(N, N-диметиламино-н-пропил)-1,2;5,6-ди-О-изопропилиден-α,D-глюкофуранозой - 10
Метиленовый синий - 0,0005
Цитрат натрия - 0,2
Лимонная кислота - До рН 7,2-8,2
Вода - Остальное
Кроме этого, лекарственный препарат в лекарственной форме раствора для парентерального введения содержит смесь 3,7-диэтокси-10-метиленкарбокси-9-акридона и 3-О-(N,N-диметиламиноэтил)-1,2-О-изопропилиден-α,D-глюкофуранозы или соль 3,7-диэтокси-10-метиленкарбокси-9-акридона с 3-О-(N, N-диметиламиноэтил)-1,2-О-изопропилиден-α, D-глюкофуранозой и апирогенную воду при соотношении, мас.%:
Смесь 3,7-диэтокси-10-метиленкарбокси-9-акридона и 3-О-(N,N-диметиламиноэтил)-1, 2-О-изопропилиден-α, D-глюкофуранозой или соль 3,7-диэтокси-10-метиленкарбокси-9-акридона с 3-О-(N, N-диметиламиноэтил)-1,2-О-изопропилиден-α,D-глюкофуранозой - 25
Апирогенная вода - Остальное
Лекарственный препарат в лекарственной форме спрея в качестве лекарственного вещества содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов, а в качестве вспомогательного вещества препарат содержит растворитель, консервант и/или корригент при соотношении, мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов - 0,1-50
Растворитель, консервант и/или корригент - 50-99,9
При этом лекарственный препарат в лекарственной форме спрея в качестве лекарственного вещества содержит смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3,4-ди-О-изопропилиден-6-О(N, N-диэтиламиноэтил)-α,D-галактопиранозы или соль 3-хлор-10-метиленкарбокси-9-акридона с 1,2:3,4-ди-О-изопропилиден-6-О(N, N-диэтиламиноэтил)-α,D-галактопиранозой, а в качестве вспомогательного вещества препарат содержит апирогенную воду и метилпарабен при соотношении, мас.%:
Смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2:3,4-ди-О-изопропилиден-6-О(N, N-диэтиламиноэтил)-α,D-галактопиранозой или соль 3-хлор-10-метиленкарбокси-9-акридона с 1,2: 3,4-ди-О-изопропилиден--6-O(N,N-диметиламиноэтил)-α,D-галактопиранозой - 2
Метилпарабен - 0,1
Апирогенная вода - Остальное
Лекарственный препарат в лекарственной форме аэрозоля в качестве лекарственного вещества содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов, а в качестве вспомогательного вещества препарат содержит газ-вытеснитель, растворитель и корригент при соотношении, мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с моноземещенными эфирами моносахаридов - 0,1-50
Корригент, растворитель и газ-вытеснитель - 50-99,9
При этом лекарственный препарат в лекарственной форме аэрозоля в качестве лекарственного вещества содержит смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2:3, 4-ди-О-изопропилиден-6-О(N,N- диметиламиноэтил)-α,D-галактопиранозы или соль 3-хлор-10-метиленкарбокси-9-акридона с 1,2:3,4-ди-О-изопропилиден-6-О(N,N-диметиламиноэтил)-α, D-галактопиранозой, корригент, а в качестве вспомогательного вещества препарат содержит апирогенную воду и газ-вытеснитель при соотношении, мас.%:
Смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2:3,4-ди-О-изопропилиден-6-О(N,N-диметиламиноэтил)-α,D-галактопиранозы или соль 3-хлор-10-метиленкарбокси-9-акридона с 1,2: 3,4-ди-О-изопропилиден-6-О(N, N-диметиламиноэтил)-α, D-галактопиранозой - 2
Метилпарабен - 0,1
Апирогенная вода и газ-вытеснитель - Остальное
Лекарственный препарат в лекарственной форме таблеток, или таблеток с кишечно-растворимым покрытием, или порошка в капсулах в качестве лекарственного вещества содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов, а в качестве вспомогательного вещества препарат содержит связующее вещество и кишечнорастворимую оболочку или капсулу при соотношении, мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов - 1,0-80
Связующее вещество и кишечнорастворимая оболочка или капсула - 20-99,0
При этом лекарственный препарат в лекарственной форме таблеток в качестве лекарственного вещества содержит смесь 3-хлор-6-метил-N-акридонуксусной кислоты и 3-О-(1'-этил-2'-(N-морфолинил)-1, 2-О-изопропилиден-α,D-глюкофуранозы или соль 3-хлор-6-метил-N-акридонуксусной кислоты с 3-О-(1'-этил-2'-(N-морфолинил)-1,2-О-изопропилиден-α, D-глюкофуранозой, а в качестве вспомогательного вещества препарат содержит крахмал водорастворимый и кишечнорастворимую оболочку при соотношении, мас.%:
Смесь 3-хлор-6-метил-N-акридонуксусной кислоты и 3-О-(1'-этил-2'-(N-морфолинил)-1,2-О-изопропилиден-α, D-глюкофуранозой или соль 3-хлор-6-метил-N-акридонуксусной кислоты с 3-О-(1'-этил-2'-(N-морфолинил)-1,2-О-изопропилиден-α, D-глюкофуранозой - 50
Крахмал водорастворимый и кишечнорастворимая оболочка - 50
Лекарственный препарат в лекарственной форме суппозиториев в качестве лекарственного вещества содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов, а в качестве вспомогательного вещества препарат содержит плавящуюся при 36,5-37oС основу суппозиториев и консервант при соотношении, мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов - 0,5-40
Основа суппозиториев и консервант - 60-99,5
При этом лекарственный препарат в лекарственной форме суппозиториев в виде ректальных и вагинальных свеч в качестве лекарственного вещества содержит смесь 2-карбокси-N-метиленкарбокси-9-акридона и 3-О-(N,N-диэтиламино-(2'-изобутил)-1,2-О-изопропилиден-α, D-аллофуранозы или соль 2-карбокси-N-метиленкарбокси-9-акридона с 3-О-(N,N-диэтиламино-(2'-изобутил)-1,2-О-изопропилиден-α, D-аллофуранозой, а в качестве вспомогательного вещества препарат содержит сплав масла какао с парафином и гидрогенизированными жирами и тальк при соотношении, мас.%:
Смесь 2-карбокси-N-метиленкарбокси-9-акридона и 3-О-(N,N-диэтиламино-(2'-изобутил)-1,2-О-изопропилиден-α, D-аллофуранозы или соль 2-карбокси-N-метиленкарбокси-9'-акридона с 3-О-(N,N-диметиламино-(2'-изобутил)-1,2-О-изопропилиден-α,D-аллофуранозой - 5
Масло какао с парафином и гидрогенизированными жирами и тальк - 95
Поставленные задачи решаются и требуемый технический результат достигается тем, что по способу приготовления лекарственного препарата, обладающего иммуномодулирующим, иммунокоррегирующим, противопаразитарным, противосклеротическим, противовирусным, противобактериальным, противогрибковым, противовоспалительным и противоопухолевым действием, включающему смешивание лекарственного вещества со вспомогательным веществом с получением лекарственной формы, согласно изобретению препарат приготавливают в лекарственной форме мази, или крема, или пасты, или геля, или линимента, или глазных, или интраназальных капель, или капель для ушей, или спрея, или аэрозоля, или раствора для парентерального введения, или таблеток, или таблеток с кишечно-растворимым покрытием, или порошка в капсулах, или суппозиториев, в качестве лекарственного вещества используют смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов общей формулы

где
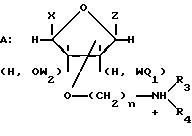
или

Группа
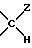
(Н, OW1), (Н, OW2), (Н, OW3) обозначают различные изомеры, отличающиеся положением групп Н и OW относительно плоскости кольца моносахарида.

Z=Н, ОН алкил, гидроксиалкил, алкоксил, алкоксиалкил.
W1, W2, W3=Н, алкил, арил, алкенил.
OW1 и Z, OW2 и Z, OW3 и Z, OW1 и X, OW2 и X, OW3 и X, OW1 и OW2, OW1 и OW3, OW2 и OW3 = алкил, арил, бензил, алкенил.
R1, R2=Н, ОН, галоген, алкил, оксиалкил, арил, оксиарил, карбоксигруппа.
R3, R4= Н, алкил, арил, или R3 и R4
вместе с атомом азота образуют орфолиновый, пиперидиновый или пиридиновый гетероцикл, n=1-4, в качестве вспомогательного вещества используют вещество или вещества, используемое или используемые для
приготовления мази, или крема, или пасты, или геля, или линимента, или глазных, или интраназальных капель, или капель для ушей, или спрея, или аэрозоля, или раствора для парентерального введения, или
таблеток, или таблеток с кишечно-растворимым покрытием, или порошка в капсулах, или суппозиториев, при этом соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными
эфирами моносахаридов смешивают со вспомогательным веществом при соотношении, мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров
моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов - 0,05-80
Вспомогательное вещество - 20-99,95
При этом
смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными
эфирами моносахаридов для ее смешивания со вспомогательным веществом приготавливают в жидком или расплавленном состоянии путем смешивания, или смешивания и последующего нагревания, или смешивания при
нагревании, или смешивания с нагретым вспомогательным веществом акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов непосредственно перед или во время
смешивания со вспомогательным веществом.
Кроме этого, в качестве лекарственного вещества используют лекарственное вещество АНАНДИН, имеющее химическую формулу C32H42N2O9 и молекулярную массу, равную 598,76 углеродных единиц, и представляющее собой смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N,
N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α,D-глюкофуранозы (диметиламинопропилглюкофуранозы) или соль N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) с 3-О(N,
N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α, D-глюкофуранозой (диметиламинопропилглюкофуранозой), которую приготавливают в жидком или расплавленном состоянии непосредственно перед или
во время смешивания со вспомогательным веществом путем смешивания или смешивания и нагревания N-акридонуксусной кислоты и 3-О(N,N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α,
D-глюкофуранозы или
смешивания N-акридонуксусной кислоты и 3-О(N,N-диметиламино-н-пропил)-1,2:5,6-ди-О-изопропилиден-α,D-глюкофуранозы с нагретым вспомогательным веществом.
Кроме этого, в качестве лекарственного вещества используют смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2:3,4-ди-О-изопропилиден-6-О-(N,N-диэтиламиноэтил)-α,D-галактопиранозы или соль 3-хлор-10-метиленкарбокси-9-акридона с 1,2:3,4-ди-О-изопропилиден-6-О-(N,N-диэтиламиноэтил)-α,D-галактопиранозой, которую приготавливают в жидком или расплавленном состоянии непосредственно перед или во время смешивания со вспомогательным веществом путем смешивания или смешивания и нагревания 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3,4-ди-О-изопропилиден-6-О-(N, N-диэтиламиноэтил)-α, D-галактопиранозы или смешивания 3-хлор-10-метиленкарбокси-9-акридона и 1,2:3,4-ди-О-изопропилиден-6-О-(N,N-диэтиламиноэтил)-α,D-галактопиранозы с нагретым вспомогательным веществом.
Кроме этого, в качестве лекарственного вещества используют смесь 3-хлор-6-метил-N-акридонуксусной кислоты и 3-О-(1'-этил-2'-(N-морфолинил)-1, 2-О-изопропилиден-α, D-глюкофуранозы или соль 3-хлор-6-метил-N-акридонуксусной кислоты с 3-О-(1'-этил-2'-(N-морфолинил)-1,2-О-изопропилиден-α,D-глюкофуранозой, которую приготавливают в жидком или расплавленном состоянии непосредственно перед или во время смешивания со вспомогательным веществом путем смешивания и нагревания 3-хлор-6-метил-N-акридонуксусной кислоты и 3-О-(1'-этил-2'-(N-морфолинил)-1,2-О-изопропилиден-α, D-глюкофуранозы или смешивания 3-хлор-6-метил-N-акридонуксусной кислоты и 3-О-(1'-этил-2'-(N-морфолинил)-1,2-О-изопропилиден-α, D-глюкофуранозы с нагретым вспомогательным веществом.
Кроме этого, в качестве лекарственного вещества используют смесь 3,7-диэтокси-10-метиленкарбокси-9-акридона и 3-О-(N, N-диметиламиноэтил)-1,2-О-изопропилиден-α, D-глюкофуранозы или соль 3,7-диэтокси-10-метиленкарбокси-9-акридона с 3-О-(N,N-диметиламиноэтил)-1,2-О-изопропилиден-α,D-глюкофуранозой, которую приготавливают в жидком или расплавленном состоянии непосредственно перед или во время смешивания со вспомогательным веществом путем смешивания или смешивания и нагревания 3, 7-диэтокси-10-метиленкарбокси-9-акридона и 3-О-(N,N-диметиламиноэтил)-1,2-О-изопропилиден-α,D-глюкофуранозы или смешивания 3,7-диэтокси-10-метиленкарбокси-9-акридона и 3-О-(N, N-диметиламиноэтил)-1,2-О-изопропилиден-α,D-глюкофуранозы с нагретым вспомогательным веществом.
При этом смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов и вспомогательного вещества дополнительно нагревают, или стерилизуют, или подвергают иной антибактериальной, или антимикробной, или антивирусной, или антипаразитарной, или антигрибковой обработке и приготавливают препарат описанного выше состава.
Поставленные задачи решаются и требуемый технический результат достигается тем, что по способу лечения иммунных, паразитарных, вирусных, бактериальных, грибковых, воспалительных и опухолевых
заболеваний, включающему применение лекарственного препарата, согласно изобретению при лечении иммунных, паразитарных, вирусных, бактериальных, грибковых, воспалительных и опухолевых заболеваний
применяют лекарственный препарат, содержащий в качестве лекарственного вещества смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль
акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов общей формулы

где
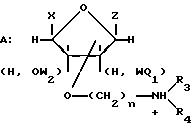
или
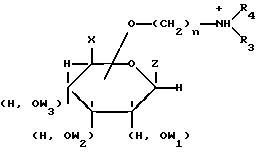
Группа
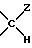
(Н, OW1), (H, OW2), (Н, OW3) обозначают различные изомеры, отличающиеся положением групп Н и OW относительно плоскости кольца моносахарида.

Z=Н, ОН алкил, гидроксиалкил, алкоксил, алкоксиалкил.
W1, W2, W3=Н, алкил, арил, алкенил.
ОW1 и Z, OW2 и Z, OW3 и Z, OW1 и X, OW2 и X, OW3 и X, OW1 и OW2, OW1 и OW3, OW2 и OW3 = алкил, арил, бензил, алкенил.
R1, R2=Н, ОН, галоген, алкил, оксиалкил, арил, оксиарил, карбоксигруппа.
R3, R4= Н, алкил, арил, или R3 и R4 вместе с атомом азота
образуют орфолиновый, пиперидиновый или пиридиновый гетероцикл, n=1-4, при этом в качестве вспомогательного вещества препарат содержит вещество или вещества, используемое или используемые для
приготовления мази, или крема, или пасты, или геля, или линимента, или глазных, или интраназальных капель, или капель для ушей, или спрея, или аэрозоля, или раствора для парентерального введения, или
таблеток, или таблеток с кишечно-растворимым покрытием, или порошка в капсулах, или суппозиториев при соотношении, мас.%:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты
и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов - 0,05-80
Вспомогательное вещество
- 20-99,95
При этом при лечении иммунных, паразитарных, вирусных, бактериальных, грибковых, воспалительных, и опухолевых заболеваний применяют лекарственный препарат описанного выше состава в
качестве иммуномодулирующего средства, иммунокоррегирующего средства, в качестве противопаразитарного средства, в качестве противосклеротического средства, в качестве противовирусного средства, в
качестве противобактериального средства, в качестве противогрибкового средства, в качестве противовоспалительного средства при экзогенных и/или эндогенных повреждающих факторах и в качестве
противоопухолевого (противобластомного) средства.
Поставленные задачи решаются и требуемый технический результат достигается тем, что применяют лекарственный препарат, содержащий смесь
акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами
моносахаридов общей формулы

где

или

Группа
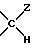
(Н, OW1), (H, OW2), (H, OW3) обозначают различные изомеры, отличающиеся положением групп Н и OW относительно плоскости кольца моносахарида.
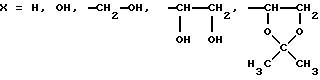
Z=Н, ОН алкил, гидроксиалкил, алкоксил, алкоксиалкил.
W1, W2, W3=Н, алкил, арил, алкенил.
OW1 и Z, OW2 и Z, OW3 и Z, OW1 и X, OW2 и X, OW3 и X, OW1 и OW2, ОW1 и OW3, OW2 и ОW3 = алкил, арил, бензил, алкенил.
R1, R2=Н, ОН, галоген, алкил, оксиалкил, арил, оксиарил, карбоксигруппа.
R3, R4= Н, алкил, арил, или R3 и R4 вместе с атомом азота образуют орфолиновый, пиперидиновый или пиридиновый гетероцикл, n=1-4, и вспомогательное вещество в виде
вещества или веществ, используемого или используемых для приготовления мази, или крема, или пасты, или геля, или линимента, или глазных, или интраназальных капель, или капель для ушей, или спрея, или
аэрозоля, или раствора для парентерального введения, или таблеток, или таблеток с кишечно-растворимым покрытием, или порошка в капсулах, или суппозиториев при соотношении, мас.%:
Смесь
акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами
моносахаридов - 0,05-80
Вспомогательное вещество - 20-99,95
в качестве иммуномодулирующего средства, иммунокоррегирующего средства, в качестве противопаразитарного средства, в
качестве противосклеротического средства, в качестве противовирусного средства, в качестве противобактериального средства, в качестве противогрибкового средства, в качестве противовоспалительного
средства при экзогенных и/или эндогенных повреждающих факторах и в качестве противоопухолевого (противобластомного) средства.
В результате различных испытаний и исследований было экспериментально установлено, что новые лекарственные формы заявляемого лекарственного препарата обладают выраженным иммуномодулирующим, иммунокоррегирующим, противопаразитарным, противосклеротическим, противовирусным, противобактериальным, противогрибковым, противовоспалительным и противоопухолевым действием, низкой токсичностью, высоким индексом терапевтического действия, длительным сроком годности и высокой стабильностью при хранении.
Экспериментально доказано, что лекарственное вещество в силу ряда особенностей строения и физико-химических свойств обладает уникальной способностью растворяться, как в гидрофильных, так и в гидрофобных средах.
Соли акридонуксусных кислот с монозамещенными эфирами моносахаридов являются солями, образованными слабыми кислотами и слабыми основаниями, очень мало диссоциированными в водных растворах и образующих устойчивые ионные пары в спиртах и малополярных растворителях. Между катионом и анионом происходит дополнительное образование водородных связей, что в свою очередь стабилизирует молекулу соединения. Электростатические заряды данных веществ в значительной степени экранированы гидрофобными группами. Все эти факторы, по-видимому, способствуют растворению данных соединений в различных по своей полярности растворителях [22].
Несмотря на ряд существенных технических и изобретательских сложностей, возникших при решении поставленных задач, удалось практически получить на основе изобретения весь набор необходимых в практической медицине лекарственных форм [2, 23].
Характерной новизной изобретения является получение новых, не известных ранее лекарственных форм лекарственного препарата, обладающего уникальной сферой фармацевтической активности, а также новые технологически простые, но эффективные методы получения лекарственных форм лекарственного препарата, включающего получение солей акридонуксусных кислот с монозамещенными эфирами моносахаридов непосредственно перед или во время приготовления лекарственного препарата описанным выше способом.
Как следует из приведенного выше обзора уровня техники, заявляемые способы и устройства для их реализации являются новыми, они не известны из доступных источников информации, не вытекают явным образом из известного уровня техники, т. е. предложенные решения изобретательской задачи не очевидны для среднего специалиста и соответствуют требованиям критерия "изобретательский уровень".
По сравнению с прототипом изобретения группы содержат новую, не известную ранее совокупность существенных признаков, поэтому изобретения группы соответствуют требованиям критерия "новизны".
Некоторые отдельные существенные признаки группы изобретений известны, однако совокупности общих и частных отличительных существенных признаков изобретений среди известных в науке и технике решений в объеме проведенного нами поиска не обнаружено. Кроме этого, отличительные признаки изобретений выполняют новые, не известные ранее функции, то есть обеспечивают возможность получения требуемого нового технического результата.
Совокупность общих и частных существенных признаков изобретений обеспечивает возможность решения поставленных изобретательских задач и достижения цели изобретений (требуемого технического результата при использовании изобретений).
Действительно, как будет дополнительно показано ниже на примерах конкретной реализации изобретений, заявляемые изобретения позволяют не только получить практически все пригодные к использованию в медицине и ветеринарии лекарственные формы уникального, обладающего высокой активностью и широким спектром фармакологического действия лекарственного препарата неспецифического иммуномоделирующего, иммунокоррегирующего, противопаразитарного, противосклеротического, противовирусного, противобактериального, противогрибкового, противовоспалительного и противоопухолевого действия, но и разработать новый, технологически простой и экономически выгодный промышленный способ приготовления разнообразных лекарственных форм лекарственного препарата с технологически простым получением различных типов высокоактивных лекарственных форм, содержащих смесь акридонуксусной кислоты или ее производных и монозамещенных эфиров моносахаридов или соль акридонуксусной кислоты или ее производных с монозамещенными эфирами моносахаридов и фармацевтически приемлемые носители (вспомогательные вещества), использовать новый способ лечения иммунных, паразитарных, вирусных, бактериальных, грибковых, воспалительных и опухолевых заболеваний и применить по новому, не известному ранее назначению новые, не известные ранее лекарственные формы лекарственного препарата, при одновременном обеспечении максимального сохранения свойств лекарственного вещества, увеличении сроков хранения препарата, расширении области применения, повышении эффективности против широкого круга смешанных инфекций неизвестной этиологии и ряда медленных инфекций.
Сущность изобретения поясняется нижеприведенными примерами практического апробирования и промышленной реализации изобретения в Научно-исследовательском обществе "МЕДИТЭР" в Санкт-Петербурге.
ПРИМЕР 1. 5 г акридонуксусной кислоты и 45 г 3-О-(N, N-диметиламино-н-бутил)-1,2:5,6-ди-О-изопропилиден-α,D-аллофуранозы растворяют при нагревании до 90-95oC в 100 мл 50% этанола. Полученный раствор смешивают с 700 мл расплавленного безводного ланолина, 200 мл касторового масла, 10 мл 10% водного раствора салицилата калия. Смесь нагревают до 90oС, доводят вес до 1 килограмма касторовым маслом и медленно охлаждают при интенсивном перемешивании. Полученную гомогенную 5% мазь расфасовывают в тубы и бушоны. Выход 98%.
Мазь эффективна для лечения герпетических поражений кожных покровов, кандидозов половых органов, ран, кожных поражений, вызванных аутоиммунными заболеваниями.
Аналогичным образом готовят кремы, пасты, гели, линименты с различным процентным содержанием биологически активной части и использованием различных фармакологических носителей.
ПРИМЕР 2. 4,5 г 3 -хлор-10-метиленкарбокси-9 -акридона и 5,5 г 1,2: 3,4-ди-О-изопропилиден 6-0(N, N-диметиламиноэтил)-α, D-галакто-пиранозы растворяют при нагревании до 90-100oC в 0,4 л апирогенной воды. Полученный раствор охлаждают, доводят до 500 мл глицерином и фильтруют через бактериальный фильтр. Разливают во флаконы по 5 мл, закрывают резиновыми пробками, обжимают жестяными колпачками, стерилизуют. Выход 97%.
Получают 2% глазные капли, высокоэффективные при лечении конъюнктивитов различной этиологии.
Эти же капли, после введения в раствор 0,1% метилпарабена и розлива в спреи или аэрозольные упаковки, используют в качестве интраназальных при острых респираторных заболеваниях и гриппе А и В для лечения ринитов и воспаления придаточных пазух носа.
ПРИМЕР 3. 270 г 3,7-диэтокси-10-метиленкарбокси-9-акридона и 230 г 3-О-(N, N-диметиламиноэтил)-1,2-О-изопропилиден- α,D-глюкофуранозы растворяют при нагревании до 95-100oC в 1,7 литра апирогенной воды. Полученный раствор охлаждают и фильтруют через бактериальные фильтры, объем доводят до 2 литров, разливают в ампулы по 1 мл, запаивают и стерилизуют. Получают 25% стерильный раствор, предназначенный для парентерального или перорального использования. Выход 97%.
Лекарственная форма предназначена для лечения тяжелых иммунных, вирусных и бактериальных заболеваний, а также в качестве эффективного противоопухолевого средства.
ПРИМЕР 4. 42 г акридонуксусной кислоты и 58 г 3-О-(N,N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы смешивают в 500 мл апирогенной воды. Смесь нагревают при перемешивании до кипения и выдерживают при кипячении 30-40 минут. При этом происходит растворение обоих компонентов. Полученный раствор охлаждают, доводят объем апирогенной водой до 1 литра, фильтруют через бактериальные фильтры и разливают в ампулы по 2 мл. Ампулы запаивают и стерилизуют. Получают 10% стерильный раствор в ампулах для парентерального введения. Выход 95,6%.
Полученное лекарственное средство АНАНДИН в настоящее время имеет разрешение Минздрава РФ 269/2000 на применение в медицине в качестве парентерального средства. Утверждена ВФС 42-3686-00 на 10% стерильный раствор для инъекций. Высокоэффективно в отношении практически всех классов как ДНК-, так и РНК-геномных вирусов (герпес, опоясывающий лишай, вирусные гепатиты, ОРЗ, грипп, энцефаломиелиты, полиэнцефалиты, геморрагические лихорадки), а также стафилококковых инфекций и ряда грибковых поражений.
ПРИМЕР 5. 44 г 3-О-(1'-этил-2'-(N-морфолинил)-1,2-О-изопропилиден-α,D-глюкофуранозы, представляющей собой прозрачную вязкую жидкость смешивают с 39 г 3-хлор-6 -метил-N-акридонуксусной кислоты в 250 мл этанола. Смесь нагревают до кипения и кипятят с обратным холодильником в течение 30 минут. Полученный раствор смешивают с 83 г крахмала водорастворимого и перетирают на шаровой мельнице и высушивают в вакууме 5 мм рт.ст. при температуре 110-120oС. Получают 160 г порошка светло-желтого цвета, из которого по известным технологиям изготавливают таблетки весом 400 мг с содержанием активного препарата 200 мг, которые затем покрывают кишечно-растворимой оболочкой. Выход 93%.
Таблетки эффективны в качестве как профилактического, так и лечебного средства при различных хронических заболеваниях.
ПРИМЕР 6. 45 г 2-карбокси-N-метиленкарбокси-9'-акридона и 5 г 3-О-(N,N, -диэтиламино-(2'-изобутил)-1,2-О-изопропилиден-α, D-аллофуранозы носят в 950 г расплава масла какао с парафином и гидрогенизированными жирами, нагретыми до 95-105oС, при интенсивном перемешивании. Полученный гомогенный расплав выливают в формы для получения суппозиториев весом 4 г охлаждают до 10-15oC, покрывают тонким слоем талька. Выход около 90%.
Получают суппозитории, содержащие 200 мг активного вещества, используемые для введения в полости тела в качестве ректальных (свечи) и вагинальных. Лекарственное средство эффективно для лечения герпетических и кандидозных поражений половых органов, а также в качестве противовоспалительного и ранозаживляющего средства анального канала при геморрое.
Оценка иммуномодулирующего действия заявленного препарата.
Иммуномодулирующая активность лекарственного препарата оценена на 33 больных геморрагической лихорадкой с почечным синдромом (ГЛПС).
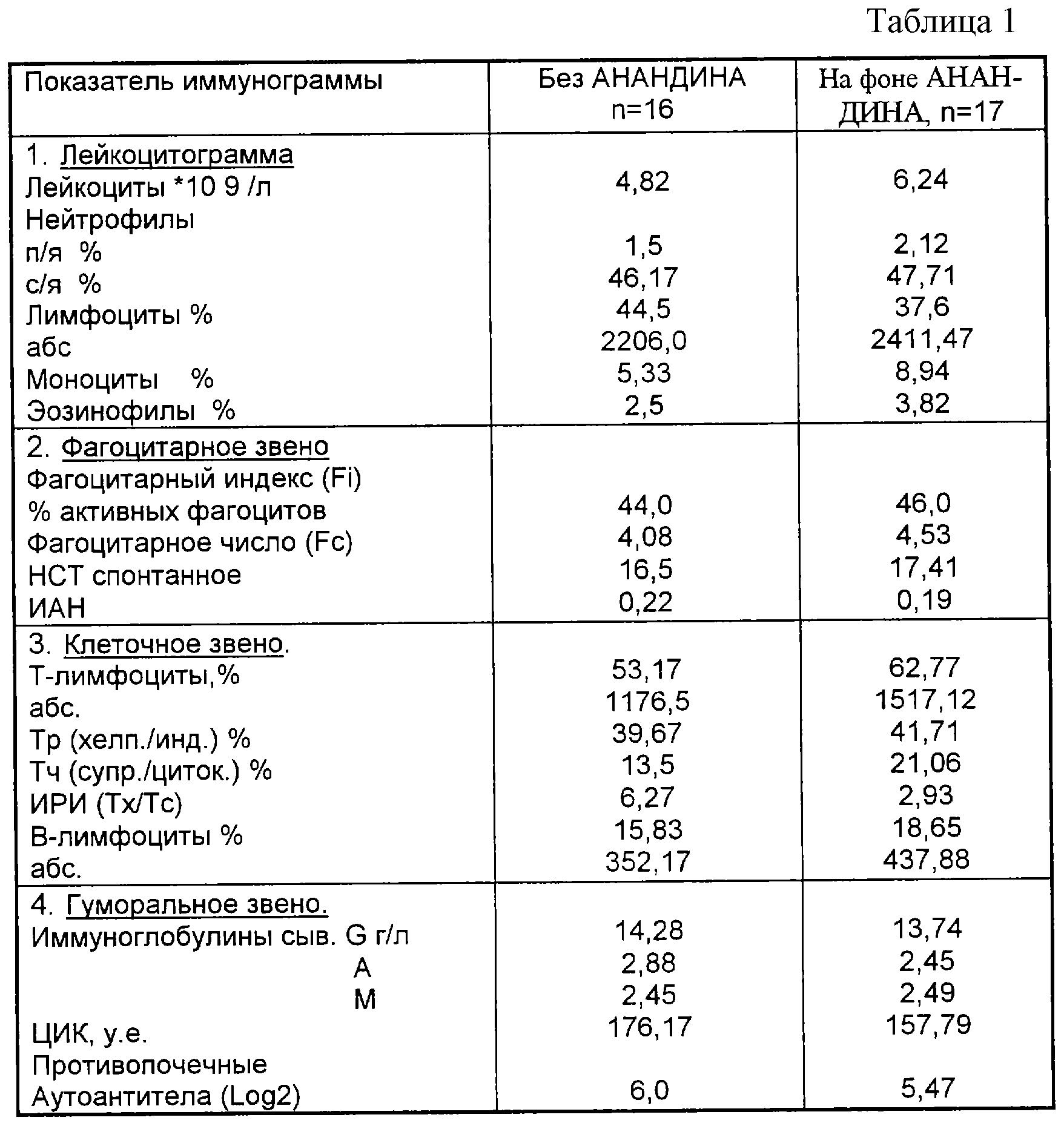
Больным с первичным диагнозом ГЛПС вводили внутримышечно 2 мл 10% стерильного раствора АНАНДИНА (способ получения в примере 4) в течение пяти дней (200 мг препарата в день). Изучены типы иммунного реагирования пациентов на основную патологию ГЛПС на фоне АННДИНА и без него. Результаты анализов приведены в таблице 1.
Из таблицы 1 следует, что на фоне АНАНДИНА основные показатели функциональной активности звеньев иммунитета возрастают. Это свидетельствует о стимуляции системы иммунитета и формировании активного иммуноответа на глубокий воспалительный процесс, при этом также упорядочиваются межклеточные взаимодействия (иммунорегуляторный индекс ИРИ). Т. е. установлено, что АНАНДИН имеет выраженное иммуностимулирующее и иммунокоррегирующее действие.
Оценка противогрибковой активности заявленного препарата.
Для оценки противогрибковой активности заявляемого лекарственного средства в сравнении с прототипом были использованы 140 белых мышей с массой тела 18-20 г. Для получения модели генерализованного кандидоза мышам вводили внутривенно взвесь Candida albicans в дозе 15 млн клеток гриба на мышь (минимум 5 LD50).
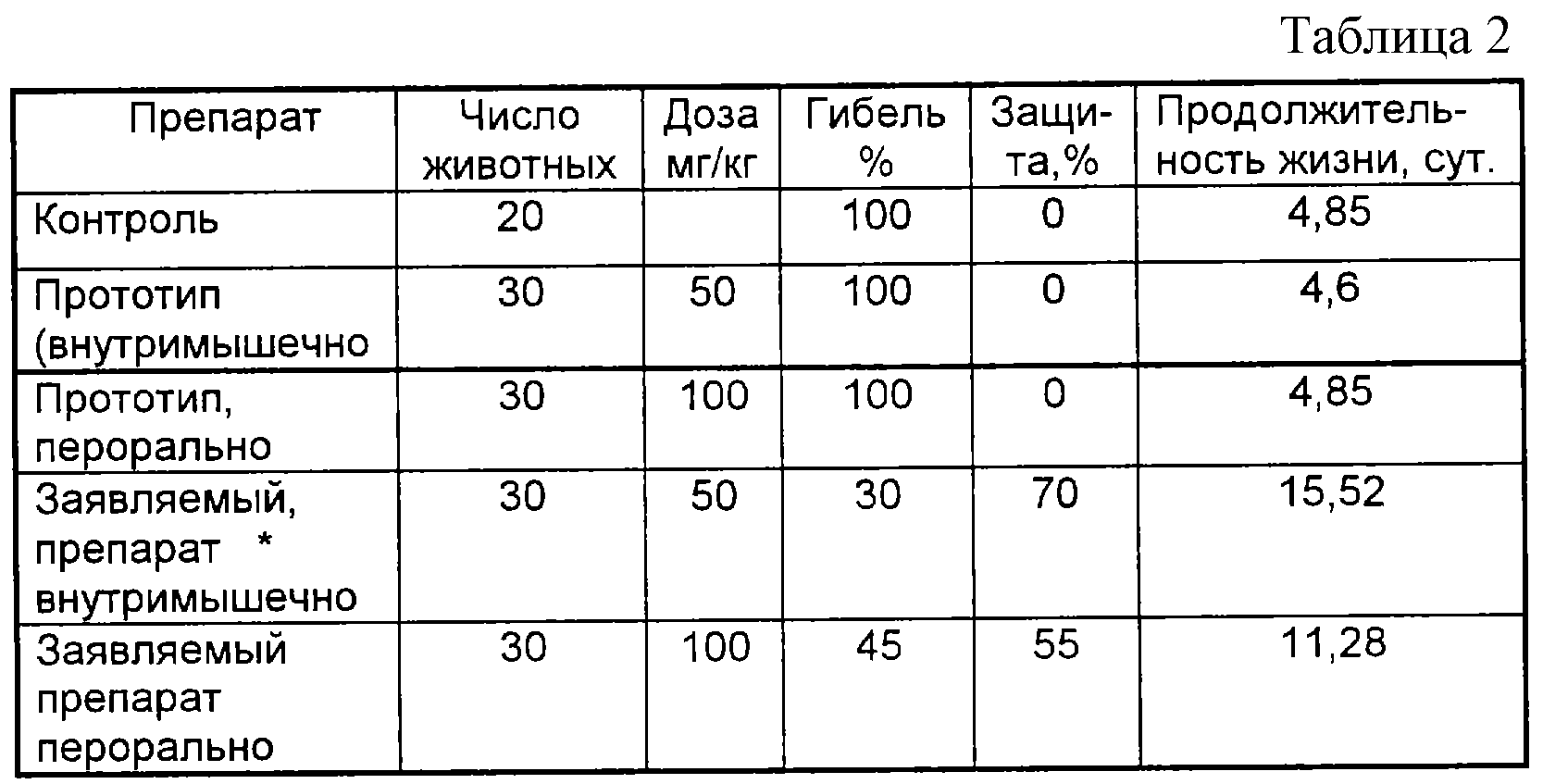
Препараты вводили внутримышечно и перорально в течение 5 дней с момента заражения. Полученные данные представлены в таблице 2.
В таблицах 2-7, приводятся усредненные результаты изучения 3-5 разных составов биологически активной части заявляемого лекарственного препарата.
Как следует из полученных данных таблицы 2, заявляемый лекарственный препарат как при внутримышечной, так и при пероральной формах введения проявил выраженный противогрибковый эффект, в то время как прототип не обладал данным видом активности.
Оценка противовоспалительной активности заявленного препарата.
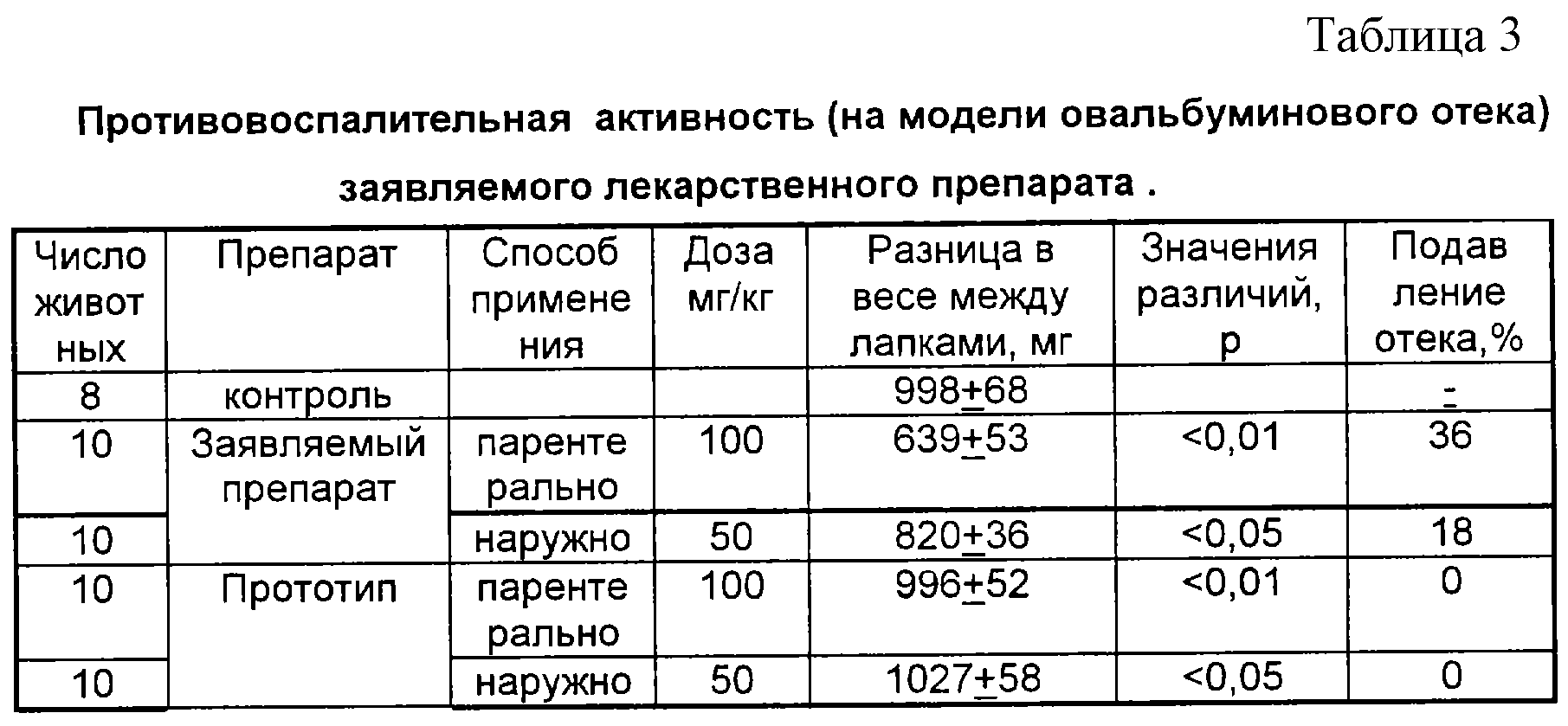
Для сравнительной оценки противовоспалительной активности заявляемого лекарственного препарата и прототипа использована модель асептического экссудативного воспаления лапок крыс. Эксперименты проводились на белых крысах массой 80-90 г, у которых вызывали отек задних лапок подкожным введением яичного белка по методике Селье через 1 ч после введения испытуемых лекарственных форм. Степень подавления отека учитывали по уменьшению прироста в массе отечной лапки крысы, получавшей испытуемые лекарственные препараты по сравнению с животными контрольной группы, которым вводили физиологический раствор. Результаты - в таблице 3.
Результаты, представленные в таблице 3, свидетельствуют о наличии противовоспалительной активности у заявляемой лекарственной формы и
отсутствии ее у прототипа
Оценка противобактериальной активности заявленного препарата.
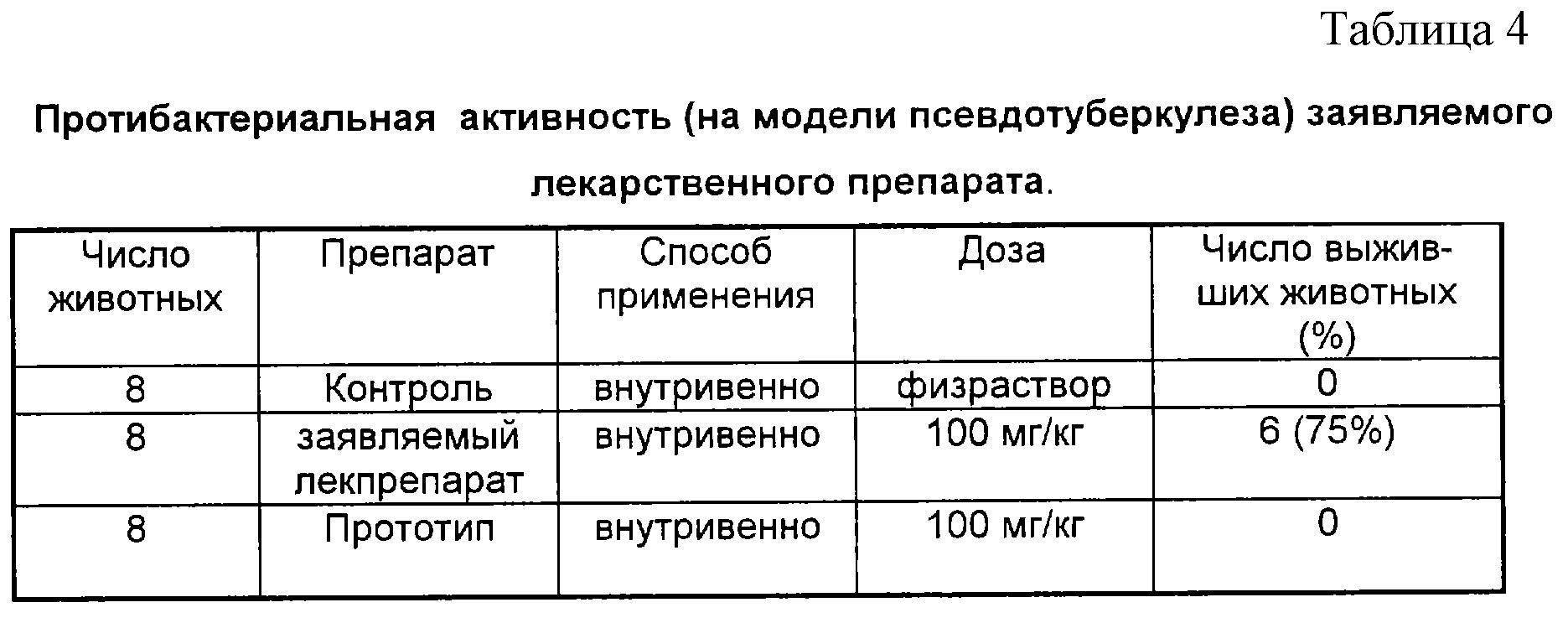
Противобактериальную активность заявляемого лекарственного препарата в сравнении с прототипом оценивали на модели псевдотуберкулеза (Versinia pseudotuberculosis). Морских свинок массой 300-350 г заражали введением подкожно 0,1 мл взвеси, содержащей 1,5•106 клеток штамма псевдотуберкулеза первого серовара, LD-12,6. Препараты вводили через сутки после заражения, в течение 5 дней подряд в дозе 100 мг/кг, внутривенно. Результаты эксперимента - в таблице 4.
Из данных таблицы 4 следует, что заявляемый лекарственный препарат, в отличие от прототипа, обладает выраженной противобактериальной активностью. Следует отметить, что использование прототипа приводило лишь к незначительному увеличению средней продолжительности жизни зараженных животных по сравнению с контролем.
Оценка противовирусной активности заявленного препарата.
Оценку противовирусной активности заявляемого препарата в сравнении с прототипом провели на модели РНК-содержащего вируса (Picomaviridae) Энцефалита Менго (энцефаломиелита мышей), вызывающего заболевание энцефаломиокардит грызунов. Белые мыши весом 18-22 г были заражены дозой вируса 10 LD50, через 1 час после заражения вводили лекарственные препараты однократно в дозах 100 мг/кг внутривенно и перорально.
Из данных таблицы 5 следует, что как заявляемый препарат, так и прототип обладают выраженной противовирусной активностью.
Оценка противоопухолевой активности заявленного препарата.
Оценку противоопухолевой активности заявляемого лекарственного препарата и прототипа осуществили на модели лейкоза Р-388.
Лейкоз Р-388 перевивали внутрибрюшинно мышам-самцам линии ДВА в количестве 106 клеток. Начиная со 2 дня после перевивания мышам контрольной группы вводили 0,1 мл физраствора, а животным опытных групп вводили лекарственные средства 6 по 100 мг/кг ежедневно в течение 7 дней.
Оба испытанных препарата обладают достоверным противоопухолевым действием, однако заявляемый препарат увеличивал продолжительность жизни в 1,5 раза по сравнению с контролем, в то время как в опыте с использованием прототипа наблюдалось увеличение продолжительности жизни в 1,3 раза.
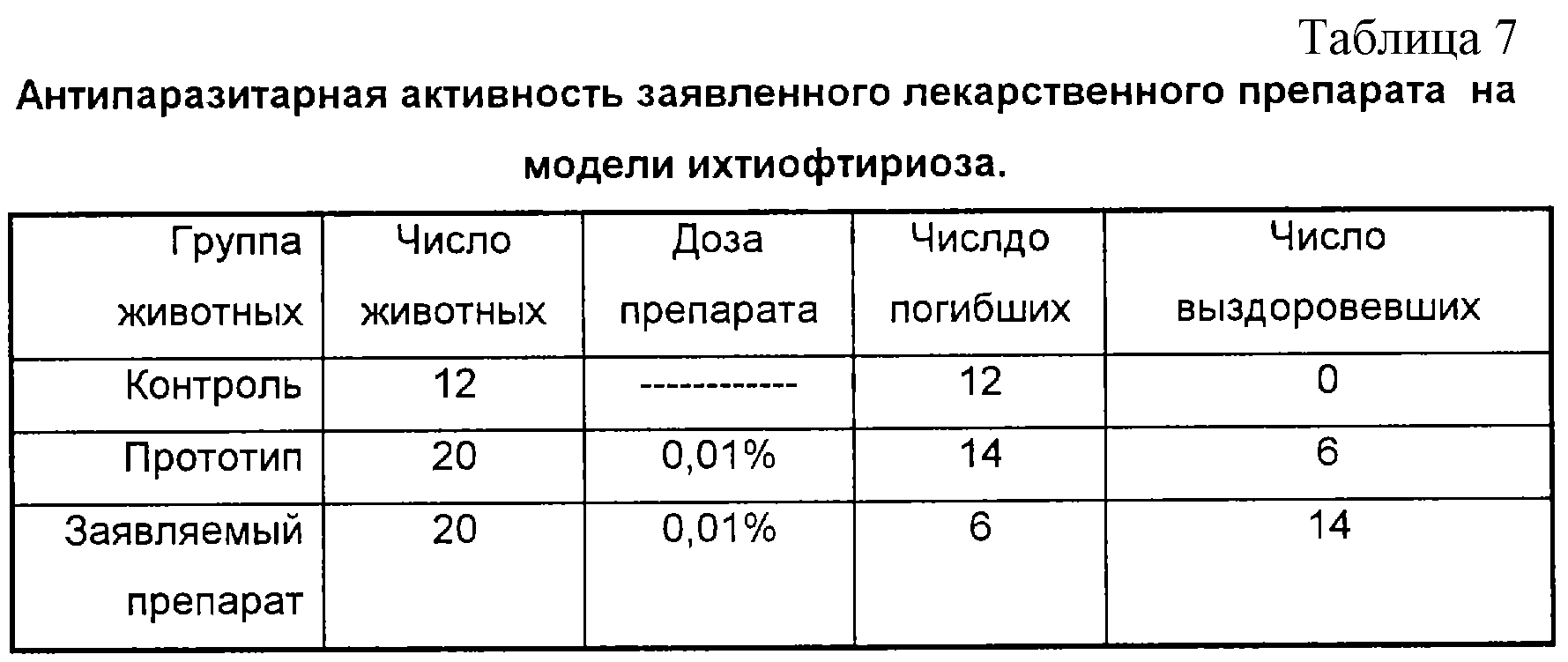
Оценка антипаразитарной активности заявленного препарата.
Оценку антипаразитарной активности проводили на нескольких моделях: токсоплазмоз крыс, криптоспороидоз белых мышей, ихтиофтириоз рыб. Во всех случаях получен выраженный лечебный эффект, значительно превосходящий эффект прототипа.
Ниже приведены данные по испытанию
лекарственного препарата при лечении ихтиофтириоза рыб. В опытах использовали высоковирулентный штамм равнореснитчатой инфузории Ichthyophthius multifiliis. Заражению подвергались беспородные самки
Роесlliа reticulata
Peters в возрасте двух месяцев. На пятый день после заражения появились выраженные признаки заболевания. Для изучения сравнительной эффективности заявляемого лекарственного
препарата в стерильные сосуды с отстоявшейся водой температуры 22-24oС помещали больных рыб
- в первом случае в сосуд вносили гидрофильную лекарственную форму лекарственного
препарата из расчета, чтобы общая концентрация его была 0,01%.
- во втором случае вносили водорастворимую лекарственную форму прототипа в той же концентрации-0,01%.
- в третьем случае вносили стерильный раствор натрия хлорида до концентрации 0,01%.
В сосудах больных рыб выдерживали 5 часов, затем каждую группу переносили в отдельный сосуд с чистой водой.
Лечение проводили в течение 3 дней по той же схеме.
Из данных таблицы 7 следует, что заявляемый лекарственный препарат обладает выраженным лечебным эффектом, в 2,2 раза превосходящим эффективность прототипа.
Кроме того, экспериментально установлено, что предлагаемый лекарственный препарат имеет не только показанную выше уникальную совокупность полезных свойств, но и не обладает раздражающим и сенсибилизирующим действием, не токсичен даже при высоких дозах. Тесты in vitro и in vivo не обнаруживают мутагенной активности.
Представленные экспериментальные результаты показали: заявляемый лекарственный препарат обладает иммуномодулирующим, противопаразитарным, противовирусным, противобактериальным, противогрибковым, противовоспалительным и противоопухолевым действием, что убедительно подтверждает: поставленная цель достигнута - получен новый лекарственный препарат, обладающий высокой активностью и широким спектром фармакологического действия.
Высокая активность заявленного препарата, ее широкий спектр и практически неограниченная растворимость
являются совершенно не очевидными для специалиста. Действительно, используемые для получения биологически активной части препарата ингредиенты
а) акридонуксусная кислота и ее производные
имеют значительно меньшую активность, значительно меньший терапевтический индекс и имеют только противовирусную и иммуномодулирующую активности, мало растворимы в гидрофобных растворителях, причем
часто гигроскопичны и поэтому плохо хранятся.
б) монозамещенные эфиры моносахаридов имеют незначительную активность только против аутоиммунных и воспалительных заболеваний, например Амиприлоз, причем слабо растворимы в гидрофильных фармацевтически приемлемых носителях, таких как водные спирты.
А композиция, созданная их смешиванием с любым фармацевтически приемлемым носителем при нагревании показала активность, несопоставимо большую и широкую, чем сумма активностей ингредиентов, и прекрасную растворимость практически во всех типах основ, используемых в готовых лекарственных средствах. Экспериментально установлено также, что явно выраженное лечебное действие заявляемый лекарственный препарат проявляет во всех заявленных лекарственных формах и во всех пределах заявленных значений содержания отдельных компонентов или ингредиентов.
Выявленные экспериментально и предлагаемые по изобретению предельные значения отдельных ингредиентов лекарственного препарата обусловлены его уникальными физико-химическими и терапевтическими свойствами - растворимостью биологически активной части во всех фармацевтически приемлемых носителях при кратковременном нагревании в течение 20-40 минут до температуры 80-120oC, позволяющим применять в медицине любые лекарственные формы лекарственного препарата, отсутствием осмотического повреждающего давления на ткани лекарственных форм, изотоничностью для глазных, интраназальных, инъекционных лекарственных форм, технологическими особенностями изготовления форм в виде таблеток, суппозиториев порошка и мазей.
Кроме этого, экспериментально установлено, что эффективные терапевтические дозы лекарственного препарата составляют 1-250 мг/кг, терапевтический индекс 100 и более. Низкая токсичность соединений, отсутствие побочного действия и высокая эффективность в низких концентрациях позволяют использовать препарат в широком диапазоне заявленных концентраций и доз.
Исследования и клинические испытания лекарственного препарата для выявления детального биохимического механизма действия и отработки наиболее оптимальных для частных случаев соотношений ингредиентов лекарственных форм продолжаются.
Конкретные параметры и особенности проведения технологических операций могут выбираться в пределах заявленных диапазонов в совокупности с другими известными и широко применяемыми в фармакологической практике технологическими приемами и способами.
ИСТОЧНИКИ ИНФОРМАЦИИ
1. Государственная фармакопея
СССР, Х изд., М.: "Медицина", 1968.
2. Государственная фармакопея СССР, XI изд., вып.1 и 2, М.: "Медицина", 1990.
3. Государственный реестр лекарственных средств (официальное издание), М., 2000.
4. Машковский М. Д. , Лекарственные средства, 14-е изд., ч. 1, 2, М.: "Новая волна", 2000.
5. X. Винтер Гриффит. Новейшие лекарственные средства. - М.: "Крон-пресс", 1998.
6. Харкевич Д.А., Фармакология. - М.: "ГЭОТАР Медицина", 1999.
7. Кленова И.Ф., Яременко Н.А. Ветеринарные препараты в России. Справочник. - М.: "Сельхозиздат", 2000.
8. Лекарственные средства (свойства, применение, противопоказания). Справочник, ред. М.А. Клюев. - М.: "Русская книга", 1993.
9. Chemotherapy and Immunity. Ed. G. Pulverer, J. Jeijaszewicz, Gustav Fisher Verlag, 1985, 245 с.
10. Регистр лекарственных средств России (РЛС), под ред. Крылова Ю.Ф., Москва, "Инфармхим", 1993, 1006 с.
11. Schneiden Н, Levamisole- a general pharmacological perspective. Int. J. Immuno-pharmacological, 1981, v.3, p. 9-13.
12. Gordon G., Minks M.A. The interferone renaissance: molecular aspects of induction and action. Microbiol. Rev., 1981, v. 45, p. 244.
13. Патент США N 4017608, МКИ А 61 К 31\70, НКИ 424\180, 536\129, опубл. 12.04. 1977.
14. Taylor J.L, Grossberg S.E. Тех. Rep. Biol. Med. 1981 82. Vol. 41 p. 158-163;
15. Szulc В. , Piasecki E. Arch. Immun. Ther. Exp., 1988, 36, N
5 р. 537-545.
16. PCT WO 94/22837, приоритет 1.04.1993, опубл. 13.10.1994.
17. Патент США 5658886, (Polysan), приоритет 23.02.1994, опубл. 19.08.1997.
18. Патент РФ 2080108. Травкин О.В., Яковлева Е.В., Буянова Е.В. Иммуномодулирующее лекарственное средство (приоритет от 17.01.1994, зарегистрирован в ГР изобретений 27.05.1997). Прототип.
19. Патент РФ 2103006. Травкин О. В., Генкин Д.Д. Иммуномодулирующее лекарственное средство (приоритет от 23.03.1995, зарегистрирован в ГР изобретений 27.01.1998).
20. Патент РФ 2118532. Травкин О.В., Яковлева Е.В. Противоинфекционное, противовоспалительное и противоопухолевое средство., (приоритет от 10.04.1996, зарегистрирован в ГР изобретений 10.09.1998).
21. Патент Евразии 000632. Травкин О. В., Яковлева Е.В. Средство противоинфекционного, противовоспалительного и противоопухолевого действия (приоритет от 10.04.1996, зарегистрирован 27.10.1999).
22. Новые пути органического синтеза. Ред. Колхаун Х.М. - М.: "Химия", 1989.
23. Грецкий В. М., Хоменок B.C. Руководство к практическим занятиям по технологии лекарственных форм. - М.: "Медицина", 2000.
Реферат
Изобретение относится к медицине и касается улучшенного лекарственного препарата, обладающего иммуномодулирующим, иммунокоррегирующим, противопаразитарным, противосклеротическим, противовирусным, противобактериальным, противогрибковым, противовоспалительным и противоопухолевым действием, включающего смесь акридонуксусной кислоты и монозамещенных эфиров моносахаридов, и способа его получения. Препарат обладает повышенной активностью. 2 с. и 25 з.п. ф-лы, 7 табл.
Формула
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 0,05-80
Вспомогательное вещество - 20-99,95
2. Лекарственный препарат по п. 1, отличающийся тем, что препарат содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов, приготовленную путем смешивания и последующего нагревания или смешивания при нагревании или смешивания с нагретым вспомогательным веществом акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов непосредственно перед или во время их смешивания с вспомогательным веществом.
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 0,1-50
Основа мази - 50-99,9
6. Лекарственный препарат в лекарственной форме мази по п. 5, отличающийся тем, что в качестве лекарственного вещества препарат содержит лекарственное вещество АНАНДИН в виде смеси N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-O(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-O-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы), а в качестве вспомогательного вещества препарат содержит вазелин, масло касторовое, калий салициловокислый и воду при соотношении, мас. %:
Смесь N-акридонуксусной кислоты (глюкоамино пропилкарб-акридона) и 3-O(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) - 2
Вазелин - 80
Масло касторовое - 5
Калий салициловокислый - 0,1
Вода - 12,9
7. Лекарственный препарат в лекарственной форме мази по п. 5, отличающийся тем, что в качестве лекарственного вещества препарат содержит лекарственное вещество АНАНДИН в виде смеси N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы), а в качестве вспомогательного вещества препарат содержит ланолин, масло касторовое, калий салициловокислый, спирт и воду при соотношении, мас. %:
Смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-O(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-O-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) - 2
Ланолин - 60
Масло касторовое - 30
Калий салициловокислый - 0,1
Спирт - 3
Вода - 4,9
8. Лекарственный препарат в лекарственной форме глазных капель или интраназальных капель по п. 3, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов, а в качестве вспомогательного вещества препарат содержит стерильный водный или масляный растворитель, стабилизатор и/или консервант при соотношении, мас. %:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 0,1-50
Растворитель, стабилизатор и/или консервант - 50-99,9
9. Лекарственный препарат в лекарственной форме глазных капель или интраназальных капель по п. 3 или 8, отличающийся тем, что в качестве лекарственного вещества препарат содержит вещество АНАНДИН в виде смеси N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-O-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы), а в качестве вспомогательного вещества препарат содержит глицерин и воду при соотношении, мас. %:
Смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-O(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-O-изопропилиден-α , D-глюкофуранозы (диметиламинопропилглюкофуранозы) - 2
Глицерин - 5
Вода - 93
10. Лекарственный препарат в лекарственной форме глазных капель по п. 3, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3,4-ди-О-изопропилиден-6-О-(N, N-диэтиламиноэтил)-α, D-галактопиранозы, а в качестве вспомогательного вещества препарат содержит глицерин и воду, при соотношении, мас. %:
Смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3,4-ди-О-изопропилиден-6-O-(N, N-диэтиламиноэтил)-α, D-галактопиранозой - 2
Глицерин - 18
Вода - 80
11. Лекарственный препарат в лекарственной форме интраназальных капель по п. 3, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3,4-ди-О-изопропилиден-6-О(N, N-диэтиламиноэтил)-α, D-галактопиранозы, а в качестве вспомогательного вещества препарат содержит глицерин, метилпарабен и воду, при соотношении, мас. %:
Смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3,4-ди-О-изопропилиден-6-О(N, N-диэтиламиноэтил)-α, D-галактопиранозы - 2
Глицерин - 18
Метилпарабен - 0,2
Вода - 79,8
12. Лекарственный препарат в лекарственной форме капель для ушей по п. 3, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов, а в качестве вспомогательного вещества препарат содержит стерильный водный, или спиртовый, или масляный растворитель, стабилизатор и/или консервант при соотношении, мас. %:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 0,1-50
Растворитель, стабилизатор и/или консервант - 50-99,9
13. Лекарственный препарат в лекарственной форме капель для ушей по п. 3 или 12, отличающийся тем, что в качестве лекарственного вещества препарат содержит вещество АНАНДИН в виде смеси N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-O-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы), а в качестве вспомогательного вещества препарат содержит масло касторовое, спирт изопропиловый, антибиотик (например, грамицидин) и воду, при соотношении, мас. %:
Смесь N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы) - 1,5-2,5
Масло касторовое - 4
Спирт изопропиловый - 75
Антибиотик (грамицидин С) - 0,005
Вода - Остальное
14. Лекарственный препарат в лекарственной форме раствора для парентерального введения по п. 3, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов, а в качестве вспомогательного вещества препарат содержит растворитель, консервант, и/или антиоксидант, и/или стабилизатор при соотношении, мас. %:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 0,05-60
Растворитель, консервант, и/или антиоксидант, и/или стабилизатор - 40-99,95
15. Лекарственный препарат в лекарственной форме раствора для парентерального введения по п. 3 или 14, отличающийся тем, что в качестве лекарственного вещества препарат содержит вещество АНАНДИН в виде смеси N-акридонуксусной кислоты (глюкоаминопропилкарбакридона) и 3-О(N, N-диметиламино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропилглюкофуранозы), а в качестве вспомогательного вещества препарат содержит метиленовый синий, цитрат натрия, лимонную кислоту и апирогенную воду при соотношении, мас. %:
Смесь N-акридонуксусной кислоты (глюко- аминопропилкарбакридона) и 3-О(N, N-диметил-амино-н-пропил)-1,2: 5,6-ди-О-изопропилиден-α, D-глюкофуранозы (диметиламинопропил- глюкофуранозы) - 10
Метиленовый синий - 0,0005
Цитрат натрия - 0,2
Лимонная кислота - До рН 7,2-8,2
Вода - Остальное
16. Лекарственный препарат в лекарственной форме раствора для парентерального введения по п. 3 или 14, отличающийся тем, что препарат содержит смесь 3,7-диэтокси-10-метиленкарбокси-9-акридона и 3-О-(N, N-диметиламиноэтил)-1,2-О-изопропилиден-α, D-глюкофуранозы при соотношении, мас. %:
Смесь 3, 7-диэтокси-10-метиленкарбокси-9-акридона и 3-О-(N, N-диметиламиноэтил)-1,2-О-изопропилиден-α, D-глюкофуранозы - 25
Апирогенная вода - Остальное
17. Лекарственный препарат в лекарственной форме спрея по п. 3, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов, а в качестве вспомогательного вещества препарат содержит растворитель, консервант и/или корригент при соотношении, мас. %:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 0,1-50
Растворитель, консервант и/или корригент - 50-99,9
18. Лекарственный препарат в лекарственной форме спрея по п. 3 или 17, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3,4-ди-О-изопропилиден-6-О(N, N-диэтиламиноэтил)-α, D-галактопиранозы, а в качестве вспомогательного вещества препарат содержит апирогенную воду и метилпарабен при соотношении, мас. %:
Смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3, 4-ди-О-изопропилиден-6-О(N, N-диэтиламиноэтил)-α, D-галактопиранозой - 2
Метилпарабен - 0,1
Апирогенная вода - Остальное
19. Лекарственный препарат в лекарственной форме аэрозоля по п. 3, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов, а в качестве вспомогательного вещества препарат содержит газ-вытеснитель, растворитель и корригент при соотношении, мас. %:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 0,1-50
Корригент, растворитель и газ-вытеснитель - 50-99,9
20. Лекарственный препарат в лекарственной форме аэрозоля по п. 3 или 19, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3,4-ди-О-изопропилиден-6-О(N, N-диметиламиноэтил)-α, D-галактопиранозы, корригент, а в качестве вспомогательного вещества препарат содержит апирогенную воду и газ-вытеснитель при соотношении, мас. %:
Смесь 3-хлор-10-метиленкарбокси-9-акридона и 1,2: 3,4-ди-О-изопропилиден-6-О(N, N-диметиламиноэтил)-α, D-галактопиранозы - 2
Метилпарабен - 0,1
Апирогенная вода и газ-вытеснитель - Остальное
21. Лекарственный препарат в лекарственной форме таблеток или таблеток с кишечно-растворимым покрытием или порошка в капсулах по п. 3, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов, а в качестве вспомогательного вещества препарат содержит связующее вещество и кишечно-растворимую оболочку или капсулу при соотношении, мас. %:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 1,0-80
Связующее вещество и кишечно-растворимая оболочка или капсула - 20-99,0
22. Лекарственный препарат в лекарственной форме таблеток по п. 3 или 21, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь 3-хлор-6-метил-N-акридонуксусной кислоты и 3-О-(1'-этил-2'-(N-морфолинил)-1,2-О-изопропилиден-α, D-глюкофуранозы, а в качестве вспомогательного вещества препарат содержит крахмал водорастворимый и кишечно-растворимую оболочку при соотношении, мас. %:
Смесь 3-хлор-6-метил-N-акридонуксусной кислоты и 3-О-(1'-этил-2'-(N-морфолинил)-1, 2-О-изопропилиден-α, D-глюкофуранозой - 50
Крахмал водорастворимый и кишечно-растворимая оболочка - 50
23. Лекарственный препарат в лекарственной форме суппозиториев по п. 3, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов, а в качестве вспомогательного вещества препарат содержит плавящуюся при 36,5-37oС основу суппозиториев и консервант при соотношении, мас. %:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 0,5-40
Основа суппозиториев и консервант - 60-99,5
24. Лекарственный препарат в лекарственной форме суппозиториев в виде ректальных и вагинальных свеч по п. 3 или 23, отличающийся тем, что в качестве лекарственного вещества препарат содержит смесь 2-карбокси-N-метиленкарбокси-9-акридона и 3-О-(N, N-диэтиламино-(2'-изобутил)-1,2-О-изопропилиден-α, D-аллофуранозы, а в качестве вспомогательного вещества препарат содержит сплав масла какао с парафином и гидрогенизированными жирами и тальк при соотношении, мас. %:
Смесь 2-карбокси-N-метиленкарбокси-9-акридона и 3-О-(N, N-диэтиламино-(2'-изобутил)-1,2-О-изопропилиден-α, D-аллофуранозы - 5
Масло какао с парафином и гидрогенизированными жирами и тальк - 95
25. Способ приготовления лекарственного препарата, обладающего иммуномодулирующим, иммунокоррегирующим, противопаразитарным, противосклеротическим, противовирусным, противобактериальным, противогрибковым, противовоспалительным и противоопухолевым действием, включающий смешивание лекарственного вещества со вспомогательным веществом с получением лекарственной формы, отличающийся тем, что препарат приготавливают в лекарственной форме мази, или крема, или пасты, или геля, или линимента, или глазных или интраназальных капель, или капель для ушей, или спрея, или аэрозоля, или раствора для парентерального введения, или таблеток, или таблеток с кишечно-растворимым покрытием, или порошка в капсулах, или суппозиториев, в качестве лекарственного вещества используют смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов, а в качестве вспомогательного вещества используют вещество или вещества, используемое или используемые для приготовления мази, или крема, или пасты, или геля, или линимента, или глазных или интраназальных капель, или капель для ушей, или спрея, или аэрозоля, или раствора для парентерального введения, или таблеток, или таблеток с кишечно-растворимым покрытием, или порошка в капсулах, или суппозиториев, при этом соль акридонуксусной кислоты или производных акридонуксусной кислоты с монозамещенными эфирами моносахаридов смешивают со вспомогательным веществом при соотношении, мас. %:
Смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов - 0,05-80
Вспомогательное вещество - 20-99,95
26. Способ приготовления лекарственного препарата по п. 25, отличающийся тем, что смесь акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов для ее смешивания со вспомогательным веществом приготавливают в жидком или расплавленном состоянии путем смешивания и последующего нагревания, или смешивания при нагревании, или смешивания с нагретым вспомогательным веществом акридонуксусной кислоты или производных акридонуксусной кислоты и монозамещенных эфиров моносахаридов непосредственно перед или во время смешивания со вспомогательным веществом.
Документы, цитированные в отчёте о поиске
Противоинфекционное, противовоспалительное и противоопухолевое лекарственное средство

Комментарии