Производные урацила, обладающие противовирусной активностью в отношении sars-cov-2 - RU2769828C1
Код документа: RU2769828C1
Чертежи













Описание
Область техники
Группа изобретений относится к области молекулярной биологии, вирусологии и медицины, а именно, к новым N1,N3-дизамещенным производным урацила, обладающим противовирусным действием в отношении SARS-CoV-2, и как таковые полезны при лечении и профилактики COVID-19. Это изобретение также относится к применению таких соединений для ингибирования репликации SARS-CoV-2 у млекопитающих, особенно людей, а также к фармацевтической композиции для ингибирования репликации SARS-CoV-2 у млекопитающих.
Уровень техники
Коронавирус SARS-CoV-2, вызвавший глобальную пандемию коронавирус-ассоциированного острого респираторного заболевания (coronavirus-associated acute respiratory disease 19, сокращенно COVID-19), представляет собой третий задокументированный случай проникновения в человеческую популяцию коронавирусов животных. Предыдущие вспышки коронавируса SARS-CoV и MERS хотя и имели угрожающе высокую смертность в 10% и 40% соответственно, но не приводили к гибели более тысячи человек за все время наблюдения. Текущая пандемия с момента проникновения вируса за пределы Китая, насчитывает около 260 млн. заболевших и более 5 млн. погибших. Отсутствие устойчивого коллективного иммунитета в очередной раз привело к лавинообразному росту заболевших и перегрузке систем здравоохранения даже в наиболее развитых странах из-за появления новой генетической линии дельта B.1.617.2.
Действенной мерой, способной разгрузить систему здравоохранения от перегрузки и снизить смертность до формирования коллективного иммунитета, остается режим изоляции. К сожалению, даже среди вакцинированных всегда имеются люди, не защищенные вакциной. В силу особенностей иммунитета на фоне быстрой изменчивости вируса, разработка специфических средств профилактики с широким спектром действия становится особенно актуальной задачей.
Клиническая картина COVID-19 показывает, что по меньшей мере в 80% случаев SARS-CoV-2 вызывает относительно легко протекающее заболевание, которое сводится к воспалению верхних и нижних дыхательных путей, желудочно-кишечного тракта. Тем не менее примерно в 20% случаях развиваются клинически выраженные формы, требующие госпитализации. Описаны и тяжелые формы COVID-19. Для снижения нагрузки на здравоохранение и экономику необходимы как средства терапии, позволяющие сократить период заболевания при легком течении, так и средства, снижающие вероятность развития тяжелого течения, требующего госпитализации.
Известны соединения, обладающие противовирусной активностью и имеющие в своей структуре урацил [1-5]. Для ряда соединений показана активность в отношении аденовируса человека, цитомегаловируса, а также вируса иммунодефицита человека. Их активность в отношении SARS-CoV-2 в настоящий момент не изучена. Таким образом, в настоящее время отсутствуют доступные специфические противовирусные лекарственные средства на основе производных урацила для специфической терапии COVID-19, а доступные неспецифические методы терапии не демонстрируют удовлетворительных результатов в аспектах эффективности и токсичности. В связи с этим, разработка эффективных и малотоксичных препаратов с прямым действием на репликацию SARS-CoV-2 сохраняет свою актуальность.
Раскрытие сущности изобретения
Коронавирусное заболевание 2019 г. (COVID-19) первоначально было описано как новое инфекционное респираторное заболевание в конце 2019 г. Новый патогенный коронавирус, коронавирус тяжелого острого респираторного синдрома 2 (SARS-CoV-2), оказался возбудителем COVID-19. Клинические проявления COVID-19 варьируются от бессимптомной инфекции до пневмонии и острого респираторного дистресс-синдрома (ARDS), цитокинового шторма, коагулопатии, тромбоза и ряда других внелегочных синдромов. В некоторых случаях доброкачественное течение болезни может очень быстро ухудшиться в течение второй недели болезни, что часто требует дополнительной интенсивной терапии. Хотя аберрантные иммунные ответы могут приводить к возникновению некоторых патологий COVID-19, очевидно, что высокий уровень репликации вируса на ранней стадии заболевания связан с серьезностью течения заболевания. Таким образом, существует острая потребность в противовирусном средстве, которое не требует парентерального введения и, следовательно, может быть назначено на ранней стадии заболевания. Учитывая текущее понимание патогенеза COVID-19, такая стратегия, включающая раннюю эффективную противовирусную терапию, должна иметь высокую вероятность успеха.
Задачей предлагаемого изобретения является создание новых, высокоэффективных, селективных и малотоксичных антивирусных агентов действующих непосредственно на SARS-CoV-2 для лечения COVID-19.
Технический результат заявленного изобретения заключается в том, что созданы новые N1,N3- дизамещённые производные урацила, которые обладают противовирусной активностью по отношению к вирусу SARS-CoV-2, в частности способны эффективно ингибировать репликацию SARS-CoV-2.
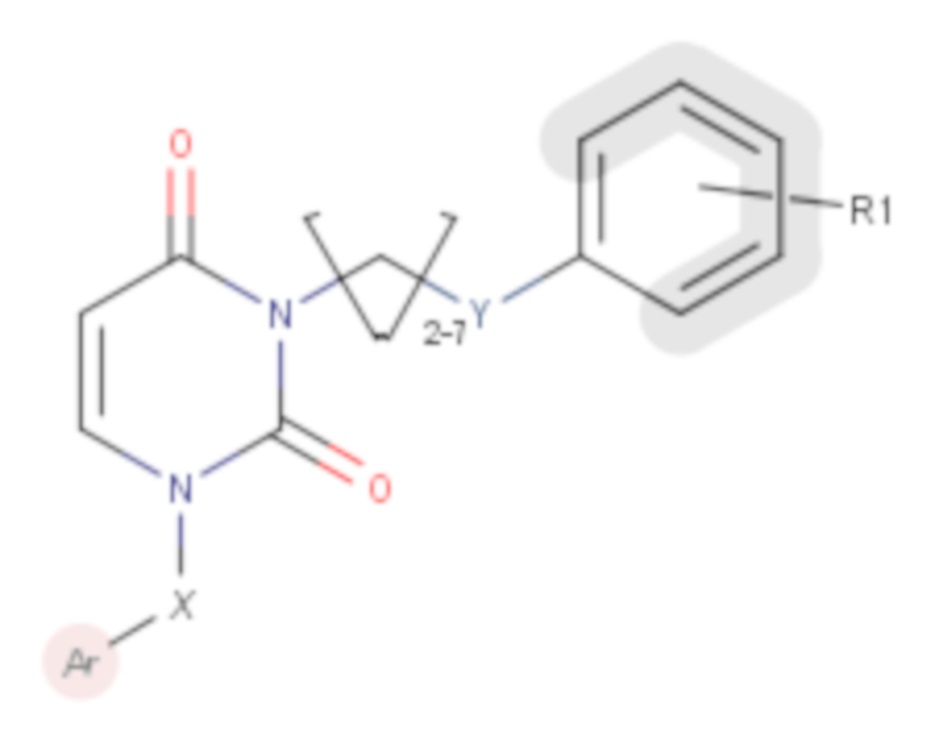
Технический результат достигается за счет того, что синтезировано соединение, представляющее собой N1,N3- дизамещённое производное урацила, отвечающее общей формуле I:

или его фармацевтически приемлемую соль;
где:
X алкил или оксиалкил (С1-С12),
Ar замещенная ароматическая группа,
Ar ароматическая группа,
Y атом кислорода,
R1 карбоксил или галоген,
В N3-положении урацила полиметиленовый линкер может включать от 1 до 12 метиленовых групп.
Также, особо предпочтительные соединения формулы I включают в себя соединения, где наиболее предпочтительными являются:
4-[5-[3-[5-(4-Фторфенокси)пентил]-2,6-диоксо-3,6-дигидропиримидин-1(2H)-ил]пентилокси] бензойной кислоты
или
4-[[5-[3-(Антрацен-9-илметил)-2,6-диоксо-3,6-дигидропиримидин-1(2H)-ил]пентил]окси]бензойной кислоты
или
4-[4-[2,6-Диоксо-3-(4-бромнафтил-1-метил)-3,6-дигидропиримидин-1(2H)-ил]бутокси]бензойная кислота
Кроме того, настоящее изобретение также относится к применению разработанных соединений для ингибирования репликации SARS-CoV-2 у млекопитающего.
Также, настоящее изобретение относится к фармацевтической композиции для ингибирования репликации SARS-CoV-2 у млекопитающего, включающей эффективное количество разработанного соединения или его фармацевтически приемлемой соли и по меньшей мере один фармацевтически приемлемый наполнитель и/или носитель.
В рамках настоящего изобретения признак «фармацевтически приемлемые соли» относится к фармацевтически приемлемым солям, получаемым с помощью присоединения кислоты для соединений из формулы I. Кислоты, которые применяют для получения фармацевтически приемлемых солей для вышеупомянутых основных соединений по этому изобретению, являются такими, которые образуют нетоксичные соли при присоединении кислоты, то есть соли, содержащие фармакологически приемлемые анионы, такие как соли гидрохлорид, гидробромид, гидроиодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, ацетат, лактат, цитрат, кислый цитрат, тартрат, битартрат, сукцинат, малеат, фумарат, глюконат, сахарат, бензоат, метансульфонат, этансульфонат, бензолсульфонат, паратолуолсульфонат и памоат [то есть 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)].
Изобретение также относится к солям присоединения основания к соединениям из формулы I. Химические основания, которые можно применять в качестве реагентов для получения фармацевтически приемлемых солей присоединения основания к соединениям формулы I, имеющих кислую природу, являются те основания, которые образуют нетоксичные основные соли с такими соединениями. Такие нетоксичные основные соли включают в себя, но не ограничиваются ими, производные от фармакологически приемлемых катионов, таких как катионы щелочных металлов (например, калия и натрия) и катионы щелочноземельных металлов (например, кальция и магния), соли аммония или водорастворимые соли присоединения амина, такого как N-метилглюкамин (меглумин), и низшие иные соли фармацевтически приемлемых органических аминов.
Краткое описание чертежей
На фиг. 1 показана схема синтеза N1-замещённых производных урацила (цифры на схеме представляют собой сквозную нумерацию соединений, расшифровка которых приведена в примере 1).
На фиг.2 показана схема синтеза соединений Z870, Z871, Z873 и Z874 (цифры на схеме представляют собой сквозную нумерацию соединений, расшифровка которых приведена в примере 2).
На фиг. 3 показана схема синтез соединения Z876 (цифры на схеме представляют собой сквозную нумерацию соединений, расшифровка которых приведена в примере 3).
На фиг.4 показана схема синтез соединения Z601 (цифры на схеме представляют собой сквозную нумерацию соединений, расшифровка которых приведена в примере 4).
На фиг.5 показана схема синтез соединения Z611. (цифры на схеме представляют собой сквозную нумерацию соединений, расшифровка которых приведена в примере 5).
На фиг. 6 показана схема синтез соединения Z875. (цифры на схеме представляют собой сквозную нумерацию соединений, расшифровка которых приведена в примере 6).
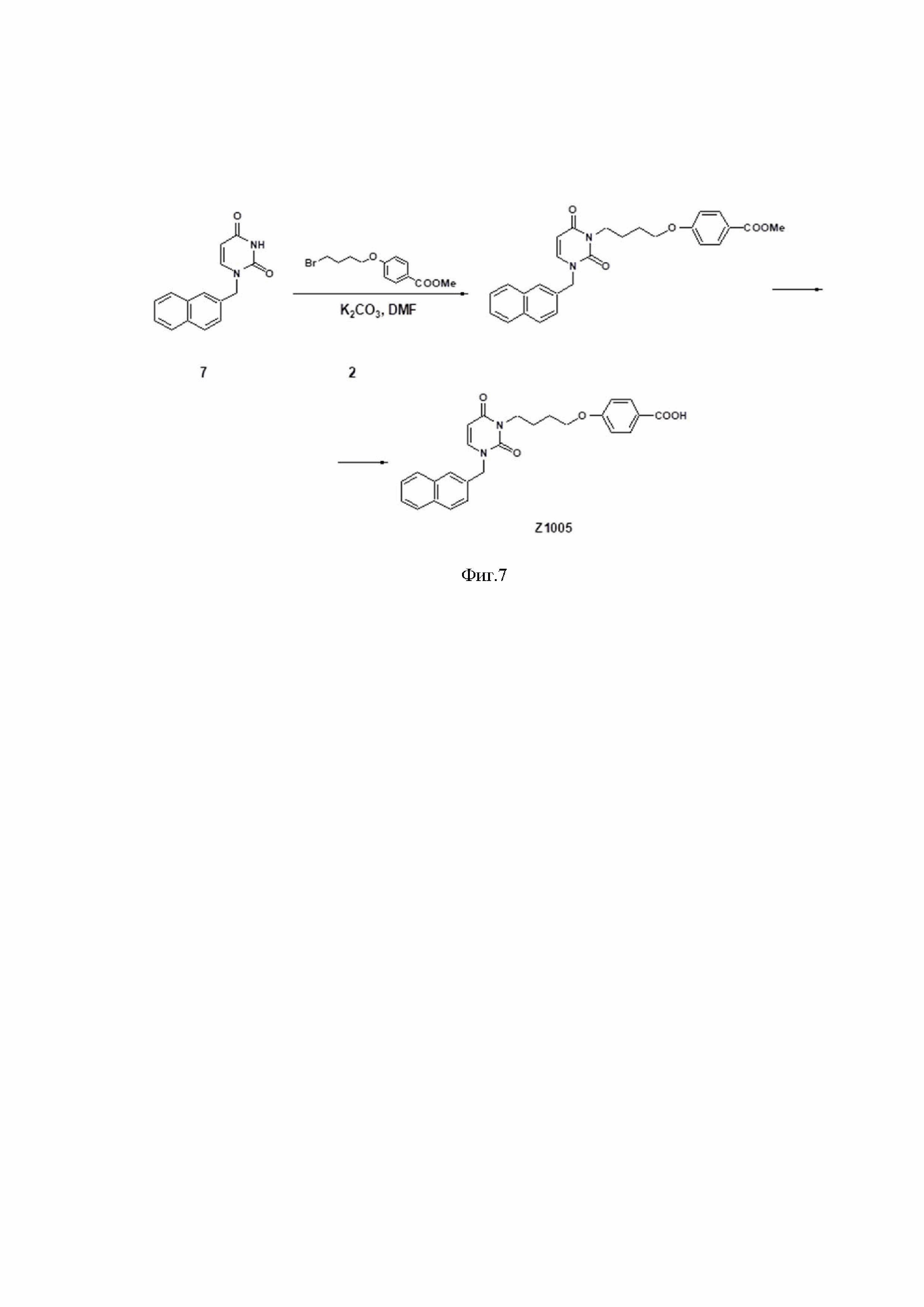
На фиг.7 показана схема синтез соединения Z1005. (цифры на схеме представляют собой сквозную нумерацию соединений, расшифровка которых приведена в примере 7).
На фиг. 8 показана схема синтез соединения Z1006. (цифры на схеме представляют собой сквозную нумерацию соединений, расшифровка которых приведена в примере 8).
На фиг. 9 показаны химические структуры соединений из тестируемой панели.
На фиг 10 представлена оценка жизнеспособности клеток под действием панели соединений.
На фиг. 11 представлена оценка эффективности соединений против SARS-CoV-2 по уровню ингибирования CPE.
На фиг. 12 представлена оценка эффективности соединений против SARS-CoV-2 с помощью кПЦР-ОТ по уровню снижения вирусной нагрузки.
На фиг. 13 представлена оценка эффективности соединений против SARS-CoV-2-индуцированного СРЕ.
На фиг. 14 представлена оценка эффективности соединений на цикл репликации SARS-CoV-2.
Осуществление изобретения
Осуществление изобретения подтверждается следующими примерами.
Пример 1.Общая методика синтеза N1-замещённых производных урацила [1, 3, 4] (фиг.1)]
Смесь урацила (53,53 ммоль) и хлорида аммония (0,3 г, 5,60 ммоль) в гексаметилдисилазане (15 мл) кипятили с обратным холодильником в течение 10 ч в инертной среде до получения прозрачного раствора. Избыток силилирующего агента был удален под вакуумом. Остаточное прозрачное масло 2,4-бис (триметил-силилокси) пиримидина растворяли в 100 мл безводного 1,2-дихлорэтана и добавляли соотвевующий бромида (53,53 ммоль). Реакционную смесь кипятили с обратным холодильником 30 ч, охлаждали до комнатной температуры и обрабатывали 15 мл iPrOH. Выпавший осадок отфильтровывали и дополнительно очищали колоночной хроматографией в смеси EtOH / 1,2-дихлорметан.
Пример 2. Общая методика синтеза кислот Z870, Z871, Z873 и Z874 (фиг.2).
Смесь 1.416 ммоль 1-замещенного урацила (4) и 0.29 г (2.098 ммоль) K2CO3 в растворе 10 мл ДМФА перемешивали при 80°C в течение 1 ч, добавляли 1.40 ммоль метиловый эфир 4-(4-бромбутокси)бензойной кислоты (5) или 4-(5-бромпентилокси)бензойной кислоты (6) и перемешивали при той же температуре в течение 24 ч. Затем реакционную массу упарили в вакууме, остаток экстрагировали 1,2-дихлорэтаном (4 × 25 мл) и экстракт упаривали при пониженном давлении. Остаток очищали флэш-хроматографией с последующим упариванием элюента при пониженном давлении. Остаток растворили в смеси этанол (50 мл) и вода (30 мл), добавили 0.3 г (7.500 ммоль) NaOH и полученную смесь перемешивали при комнатной температуре в течение двух суток. Этанол упарили при пониженном давлении, остаток разбавили водой (200 мл) и подкислили соляной кислотой до значения рН 2. Выпавший осадок отфильтровали, сушили на воздухе и продукт кристаллизовали из смеси этилацетат–гексан (2:1).
Пример 3. Синтез соединения Z876 (фиг.3).
Смесь 0.5 г (1.643 ммоль) 1-(антрацен-9-илметил)урацила (7) [5]и 0.29 г (2.098 ммоль) K2CO3 в растворе 10 мл ДМФА перемешивали при 80°C в течение 1 ч, добавляли 0.48 г (1.594 ммоль) метилового эфира 4-(5-бромпентилокси)бензойной кислоты (6) и перемешивали при той же температуре в течение 24 ч. Затем реакционную массу упарили в вакууме, остаток экстрагировали 1,2-дихлорэтаном (4 × 25 мл) и экстракт упаривали при пониженном давлении. Остаток очищали флэш-хроматографией с последующим упариванием элюента при пониженном давлении. Остаток растворили в смеси этанол (50 мл) и вода (20 мл), добавили 0.3 г (7.500 ммоль) NaOH и полученную смесь перемешивали при 60 °C в течение двух суток. Этанол упарили при пониженном давлении, остаток разбавили водой (200 мл) и подкислили соляной кислотой до значения рН 2. Выпавший осадок отфильтровали, сушили на воздухе и продукт кристаллизовали из смеси этилацетат–гексан (3:1).
Пример 4. Синтез соединения Z601 (фиг.4).
Смесь 0.4 г (1.586 ммоль) 1-(нафтил-1-метил)урацила (1) [1] и 0.35 г (2.532 ммоль) K2CO3 в растворе 10 мл ДМФА перемешивали при 80°C в течение 1 ч, добавляли 0.44 г (1.532 ммоль) метилового эфира 4-(4-бромбутокси)бензойной кислоты (2) и перемешивали при той же температуре в течение 24 ч. Затем реакционную массу упарили в вакууме, остаток обработали 100 мл воды, экстрагировали 1,2-дихлорэтаном (4 × 25 мл) и экстракт упаривали при пониженном давлении. Остаток очищали флэш-хроматографией с последующим упариванием элюента при пониженном давлении. Остаток растворили в смеси этанол (50 мл) и вода (30 мл), добавили 0.35 г (8.750 ммоль) NaOH и полученную смесь перемешивали при комнатной температуре в течение двух суток. Этанол упарили при пониженном давлении, остаток разбавили водой (200 мл) и подкислили соляной кислотой до значения рН 2. Выпавший осадок отфильтровали, сушили на воздухе и продукт кристаллизовали из смеси этилацетат–гексан (2 : 1).
Пример 5. Синтез соединения Z611 (фиг.5)
Смесь 0.5 г (1.643 ммоль) 1-(антрацен-9-илметил)урацила (3) [2] и 0.29 г (2.098 ммоль) K2CO3 в растворе 10 мл ДМФА перемешивали при 80°C в течение 1 ч, добавляли 0.56 г (1.666 ммоль) метилового эфира 1-бром-(6-бромгексилокси)бензола (4) и перемешивали при той же температуре в течение 24 ч. Затем реакционную массу упарили в вакууме, остаток экстрагировали 1,2-дихлорэтаном (4 × 25 мл) и экстракт упаривали при пониженном давлении. Остаток очищали флэш-хроматографией с последующим упариванием элюента при пониженном давлении. Остаток кристаллизовали из смеси этилацетат–гексан (3 : 1).
Пример 6. Синтез соединения Z875 (фиг.6)
Смесь 0.5 г (1.416 ммоль) 1-[5-(4-бромфенокси)пентил]урацила (5) [3] и 0.3 г (2.171 ммоль) K2CO3 в растворе 10 мл ДМФА перемешивали при 80°C в течение 1 ч, охладили до комнатной температуры, добавили 0.32 г (1.397 ммоль) метилового эфира 4-(4-бромбутокси)бензойной кислоты (6) и перемешивали при той же температуре в течение 24 ч. Затем реакционную массу упарили в вакууме, остаток обработали 100 мл воды, экстрагировали 1,2-дихлорэтаном (4 × 25 мл) и экстракт упаривали при пониженном давлении. Остаток очищали флэш-хроматографией с последующим упариванием элюента при пониженном давлении. Остаток растворили в смеси этанол (50 мл) и вода (30 мл), добавили 0.3 г (7.500 ммоль) NaOH и полученную смесь перемешивали при комнатной температуре в течение двух суток. Этанол упарили при пониженном давлении, остаток разбавили водой (200 мл) и подкислили соляной кислотой до значения рН 2. Выпавший осадок отфильтровали, сушили на воздухе и продукт кристаллизовали из смеси этилацетат–гексан (3 : 1).
Пример 7. Синтез соединения Z1005 (фиг.7)
Смесь 0.4 г (1.586 ммоль) 1-(нафтил-2-метил)урацила (7) [1]и 0.35 г (2.532 ммоль) K2CO3 в растворе 10 мл ДМФА перемешивали при 80°C в течение 1 ч, добавляли 0.44 г (1.532 ммоль) метилового эфира 4-(4-бромбутокси)бензойной кислоты (2) и перемешивали при той же температуре в течение 24 ч. Затем реакционную массу упарили в вакууме, остаток обработали 100 мл воды, экстрагировали 1,2-дихлорэтаном (4 × 25 мл) и экстракт упаривали при пониженном давлении. Остаток очищали флэш-хроматографией с последующим упариванием элюента при пониженном давлении. Остаток растворили в смеси этанол (50 мл) и вода (30 мл), добавили 0.35 г (8.750 ммоль) NaOH и полученную смесь перемешивали при комнатной температуре в течение двух суток. Этанол упарили при пониженном давлении, остаток разбавили водой (200 мл) и подкислили соляной кислотой до значения рН 2. Выпавший осадок отфильтровали, сушили на воздухе и продукт кристаллизовали из смеси этилацетат–гексан (2:1).
Пример 8. Синтез соединения Z1006 (фиг.8)
Смесь 0.4 г (1.502 ммоль) 1-(4-бромнафтил-1-метил)урацила (8) [1] и 0.3 г (2.171 ммоль) K2CO3 в растворе 10 мл ДМФА перемешивали при 80°C в течение 1 ч, добавляли 0.43 г (1.497 ммоль) метилового эфира 4-(4-бромбутокси)бензойной кислоты (2) и перемешивали при той же температуре в течение 24 ч. Затем реакционную массу упарили в вакууме, остаток обработали 100 мл воды, экстрагировали 1,2-дихлорэтаном (4 × 25 мл) и экстракт упаривали при пониженном давлении. Остаток очищали флэш-хроматографией с последующим упариванием элюента при пониженном давлении. Остаток растворили в смеси этанол (50 мл) и вода (30 мл), добавили 0.3 г (7.500 ммоль) NaOH и полученную смесь перемешивали при комнатной температуре в течение двух суток. Этанол упарили при пониженном давлении, остаток разбавили водой (200 мл) и подкислили соляной кислотой до значения рН 2. Выпавший осадок отфильтровали, сушили на воздухе и продукт кристаллизовали из смеси этилацетат–гексан (2 : 1).
Пример 9. Методы анализа синтезированных соединений
1Н ЯМР-спектры соединений регистрировали на спектрометре Bruker Avance 400 (400 МГц) в DMSO-d6 с использованием тетраметилсилана в качестве внутреннего стандарта. В описании спектров использованы следующие стандартные сокращения: м.д., миллионные доли; уш., уширенный; с, синглет; д, дублет; дд, дублет дублетов; ддд, дублет дублет дублетов; т, триплет; к, квартет; м, мультиплет). Температуры плавления веществ определяли в стеклянных капиллярах на приборе Mel-Temp 3.0 (Laboratory Devices Inc., US). Тонкослойную хроматографию выполняли на пластинах Merck TLC Silica gel 60 F254 с проявлением в ультрафиолетовом свете с использованием УФ-лампы VL-6.LC (Франция) при длине волны 254 нм.
4-[5-[3-[5-(4-Фторфенокси)пентил]-2,6-диоксо-3,6-дигидропиримидин-1(2H)-ил]пентилокси]бензойная кислота (Z870)
Выход 88%, Т.пл. 133-135 °C, Rf 0.54 (i-PrOH-этилацетат-NH4OH, 9:6:5); Спектр1H ЯМР (ДМСО-d6), d, м.д.: 1.38-1.46 (4H, м, CH2 × 2), 1.60-1.75 (8H, м, CH2 × 4), 3.62-4.08 (8H, м, CH2 × 4), 5.60 (1H, д, J = 7.8 Гц, урацил H-5), 6.87 (2H, д, J = 9 Гц, H-3’, H-5’), 6.91 (2Н, д, J = 8.9 Гц, H-3”, H-5”), 6.99 (2Н, д, J = 7.9 Гц, H-2”, H-6”), 7.40 (2H, д, J = 8.9 Гц, H-2’, H-6’), 7.59 (1H, д, J = 7.8 Гц, урацил H-6).
4-[5-[3-[5-(2-Бромфенокси)пентил]-2,6-диоксо-3,6-дигидропиримидин-1(2H)-ил]пентилокси]бензойная кислота (Z871).
Выход 84%, Т.пл. 91-92 °C, Rf 0.55 (i-PrOH-этилацетат-NH4OH, 9:6:5); Спектр1H ЯМР (ДМСО-d6), d, м.д.: 1.36-1.45 (4H, м, CH2 × 2), 1.61-1.77 (8H, м, CH2 × 4), 3.60-4.07 (8H, м, CH2 × 4), 5.56 (1H, д, J = 7.8 Гц, урацил H-5), 6.86 (1H, т, J = 6.8 Гц, Н-4’), 6.74 (1H, д, J = 8.8 Гц, H-3”, H-5”), 7.07 (1H, д, J = 8.2 Гц, H-6’), 7.01 (2H, д, J = 8.8 Гц, H-2”, H-6”), 7.31 (1H, т, J = 7.0 Гц, H-5’), 7.54 (1H, д, J = 7.9 и 1.4 Гц, H-3’), 7.65 (1H, д, J = 7.8 Гц, урацил H-6).
4-[4-[3-[3-(4-Бромфенокси)пропил]-2,6-диоксо-3,6-дигидропиримидин-1(2H)-ил]бутокси]бензойная кислота (Z873).
Выход 79%, Т.пл. 122-124 °C, Rf 0.51 (i-PrOH-этилацетат-NH4OH, 9:6:5); Спектр1H ЯМР (ДМСО-d6), d, м.д.:1H NMR (DMSO-d6), d, м.д.: 1.58 (2H, кв, J = 7.3 Гц, CH2), 1.66 (2H, кв, J = 7.5 Гц, CH2), 2.01 (2H, кв, J = 6.2 Гц, CH2), 3.69 (2H, т, J = 7.1 Гц, N(1)CH2), 3.89 (2H, т, J = 6.4 Гц, OCH2), 3.99 (2H, т, J = 6.7 Гц, N(3)CH2), 4.09 (2H, т, J = 5.9 Гц, OCH2), 5.53 (1H, д, J = 7.8 Гц, урацил H-5), 6.72 (1H, д, J = 8.8 Гц, H-3”, H-5”), 6.87 (2H, д, J = 9.0 Гц, H-3’, H-5’), 7.04 (2H, д, J = 8.8 Гц, H-2”, H-6”), 7.43 (2H, д, J = 8.9 Гц, H-2’, H-6’), 7.62 (1H, д, J = 7.8 Гц, урацил H-6).
4-[5-[3-[5-(3,5-Диметилфенокси)пентил]-2,6-диоксо-3,6-дигидропиримидин-1(2H)-ил]пентилокси]бензойная кислота (Z874).
Выход 81%, Т.пл. 103.5-105 °C, Rf 0.57 (i-PrOH-этилацетат-NH4OH, 9:6:5); Спектр1H ЯМР (ДМСО-d6), d, м.д.: 1.36-1.44 (4H, м, CH2 × 2), 1.59-1.73 (8H, м, CH2 × 4), 2.24 (6H, с, CH3 × 2), 3.64-4.09 (8H, м, CH2 × 4), 5.55 (1H, д, J = 7.9 Гц, урацил H-5), 6.51 (2H, с, H-2’, H-6’), 6.53 (1H, с, H-4’), 6.74 (1H, д, J = 8.9 Гц, H-3”, H-5”), 6.99 (2H, д, J = 8.8 Гц, H-2”, H-6”), 7.64 (1H, д, J = 7.8 Гц, урацил H-6).
4-[[5-[3-(Антрацен-9-илметил)-2,6-диоксо-3,6-дигидропиримидин-1(2H)-ил]пентил]окси]бензойная кислота (Z876).
Выход 76%, Т.пл. 173-176 °C, Rf 0.52 (i-PrOH-этилацетат-NH4OH, 9:6:5); Спектр1H ЯМР (CDCl3), d, м.д.: 1.31 (2H, квин, J = 6.8 Гц, CH2), 1.59 (2H, квин, J = 7.6 Гц, CH2), 1.67 (2H, квин, J = 7.6 Гц, CH2), 3.54 (2H, т, J = 7.1 Гц, NCH2), 3.77 (2H, т, J = 6.1 Гц, OCH2), 5.68 (1H, д, J = 7.8 Гц, урацил H-5), 6.13 (2Н, с, СН2), 6.72 (1H, д, J = 8.8 Гц, H-3’, H-5’), 6.92 (1H, т, J = 7.6 Гц, урацил H-6), 7.00 (2H, д, J = 8.8 Гц, H-2’, H-6’), 7.45 (2H, т, J = 6.8 Гц, H-3”, H-6”), 7.54 (2H, т, J = 6.8 Гц, H-2”, H-7”), 7.98 (2H, д, J = 8.3 Гц, H-1”, H-8”), 8.41 (1H, c, H-10”), 8.53 (2H, д, J = 9.1 Гц, H-4”, H-5”).
4-[4-[2,6-Диоксо-3-(нафтил-1-метил)-3,6-дигидропиримидин-1(2H)-ил]бутокси]бензойная кислота (Z601)
Выход 76%, Т.пл. 183-184.5 °C, Rf 0.52 (i-PrOH-этилацетат-NH4OH, 9:6:5); Спектр1H ЯМР (CDCl3), d, м.д.: 1.67 (2H, квин, J = 8.2 Гц, CH2), 1.88 (2Н, квин, J = 7.9 Гц, CH2), 4.01-4.08 (4Н, м, СН2 × 2), 5.32 (2Н, с, СН2), 5.64 (1Н, д, J = 8.1 Гц, урацил H-5), 6.91 (1H, д, J = 8.9 Гц, H-3’, H-5’), 6.99 (1H, д, J = 7.9 Гц, урацил H-6), 7.36-7.48 (2Н, м, ароматические Н), 7.50-7.57 (2Н, м, ароматические Н), 7.87-7.95 (3Н, м, ароматические Н), 8.03 (2H, д, J = 8.9 Гц, H-2’, H-6’).
1-(Антрацен-9-илметил)-3-[6-(4-бромфенокси)гексил]урацил (Z611)
Выход 66%, Т.пл. 109.5-111 °C, Rf 0.68 (1,2-дихлорэтан-этилацетат, 1:1); Спектр1H ЯМР (CDCl3), d, м.д.: 1.31 (2H, квин, J = 6.8 Гц, CH2), 1.59 (2H, квин, J = 7.6 Гц, CH2), 1.67 (2H, квин, J = 7.6 Гц, CH2), 3.54 (2H, т, J = 7.1 Гц, NCH2), 3.77 (2H, т, J = 6.1 Гц, OCH2), 5.68 (1H, д, J = 7.8 Гц, урацил H-5), 6.13 (2Н, с, СН2), 6.72 (1H, д, J = 8.8 Гц, H-3’, H-5’), 6.93 (1H, т, J = 7.6 Гц, урацил H-6), 7.37 (2H, д, J = 8.8 Гц, H-2’, H-6’), 7.45 (2H, т, J = 6.8 Гц, H-3”, H-6”), 7.54 (2H, т, J = 6.8 Гц, H-2”, H-7”), 7.98 (2H, д, J = 8.3 Гц, H-1”, H-8”), 8.41 (1H, c, H-10”), 8.53 (2H, д, J = 9.1 Гц, H-4”, H-5”).
4-[[5-[3-[5-(4-бромфенокси)пентил]-2,6-диоксо-3,6-дигидропиримидин-1(2H)-ил]метил]бензойная кислота (Z875)
Выход 77%, Т.пл. 186-187 °C, Rf 0.52 (i-PrOH-этилацетат-NH4OH, 9:6:5); Спектр1H ЯМР (ДМСО-D6), d, м.д.: 1.37 (2H, квин, J = 8.1 Гц, CH2), 1.33-1.74 (4H, м, СН2 × 2), 3.74 (2H, т, J = 7.0 Гц, NCH2), 3.91 (2H, т, J = 6.6 Гц, OCH2), 5.04 (2Н, с, ArСН2), 5.76 (1H, д, J = 7.8 Гц, урацил H-5), 6.76 (1H, д, J = 9.1 Гц, H-3’, H-5’), 7.34 (1H, д, J = 8.3 Гц, H-3”, H-5”), 7.41 (2H, д, J = 8.8 Гц, H-2’, H-6’), 7.76 (1H, д, J = 7.8 Гц, урацил H-6), 7.88 (2H, д, J = 8.3 Гц, H-2”, H-6”).
4-[4-[2,6-Диоксо-3-(нафтил-2-метил)-3,6-дигидропиримидин-1(2H)-ил]бутокси]бензойная кислота (Z1005)
Выход 72%, Т.пл. 143.5-145 °C, Rf 0.52 (i-PrOH-этилацетат-NH4OH, 9:6:5); Спектр1H ЯМР (ДМСО-D6), d, м.д.: 1,47 (2H, квин, J = 7,9 Гц, CH2); 1,70 (2H, квин, J = 7,3 Гц, CH2); 3,75 (2H, т, J = 7,3 Гц, NCH2); 3,89 (2H, т, J = 6,4 Гц, OCH2); 5,15 (2H, c, ArCH2); 5,77 (1H, д, J = 7,9 Гц, урацил H-5); 6,84 (2H, д, J = 9,0 Гц, H-3’, H-5’); 7,40 (2H, д, J = 9,1 Гц, H-2’, H-6’); 7,41-7,48 (3H, ароматические H); 7,73 (1H, c, H-1”); 7,76 (1H, д, J = 7,9 Гц, урацил H-6); 7,82-7,86 (3H, м, ароматические H).
4-[4-[2,6-Диоксо-3-(4-бромнафтил-1-метил)-3,6-дигидропиримидин-1(2H)-ил]бутокси]бензойная кислота (Z1006)
Выход 69%, Т.пл. 195.5-197.5 °C, Rf 0.52 (i-PrOH-этилацетат-NH4OH, 9:6:5); Спектр1H ЯМР (CDCl3), d, м.д.: 1.73 (2H, квин, J = 8.0 Гц, CH2), 1.88 (2Н, квин, J = 7.9 Гц, CH2), 3.92 (2H, т, J = 6.4 Гц, NCH2); 4.03 (2H, т, J = 7.5 Гц, OCH2), 5.34 (2Н, с, ArСН2), 5.63 (1Н, д, J = 8.0 Гц, урацил H-5), 6.75 (1H, д, J = 9.1 Гц, H-3’, H-5’), 6.97 (1Н, д, J = 7.9 Гц, ароматические Н), 7.19 (1Н, д, J = 7.6 Гц, ароматические Н), 7.34 (2H, д, J = 9.0 Гц, H-2’, H-6’), 7.57-7.65 (2Н, м, ароматические Н), 7.76 (1H, д, J = 7.7 Гц, урацил H-6), 7.94 (1Н, дд, J = 7.7 и 1.4 Гц, ароматические Н), 8.32 (1Н, дд, J = 7.8 и 1.4 Гц, ароматические Н).
Пример 10. Определение цитотоксичности in vitro.
Клетки Vero E6 (ATCC CRL-1586) культивировали при 370С и 5% CO2, в полной ростовой среде DMEM (Gibco, США), дополненной 10% эмбриональной бычьей сывороткой (FBS; HyClone, США), 1× GlutaMAX и 1× pen-strep solution (Gibco, США). Оценка токсичности соединений проводили методом скрининга библиотеки соединений (фиг. 9). Для этого клетки Vero E6 высевали в 96-луночные планшеты (2×104клеток/лунку) в полной ростовой среде DMEM за сутки до эксперимента. Затем, раствор, содержащий не более 100 мкМ каждого соединения, добавляли к монослою клеток. Планшеты инкубировали в течение 72 ч при 370С и 5% CO2. После этого, в лунки добавляли раствор МТТ (3-[4,5-dimethylthiazol-2-yl]-2,5 diphenyl tetrazolium bromide, 0.5 мг/мл; ПанЭко, Россия), с последующей инкубацией в течение 4 ч. МТТ метод использовали для измерения клеточной метаболической активности в качестве индикатора жизнеспособности, пролиферации и цитотоксичности клеток. Далее, из лунок отбирали супернатант и растворяли выпавшие кристаллы формазана в ДМСО (диметилсульфоксид; ПанЭко, Россия). Оптическую плотность измеряли при 590 нм с использованием планшетного ридера SPECTROstar Nano microplate reader (BMG LABTECH).
При исследовании жизнеспособности клеток Vero E6 под действием изучаемых аналогов урацила было выяснено, что практически все соединения обладают низкой цитотоксичностью. 50% цитотоксическая концентрация (СС50) находилась выше 100 мкМ (фиг. 10). Незначительное снижение (около 20%) жизнеспособности клеток наблюдали под действием 100 мкМ соединения Z875. Средний цитотоксический эффект проявили соединения Z872 и Z1007, для которых значение СС50 составило ≥ 25 мкМ.
Пример 11. Исследование антивирусного эффекта против SARS-CoV-2.
В работе использовали следующие штаммы SARS-CoV-2 – PMVL-30 (EPI_ISL_872643, B.1.1.141) и “дельта” вариант (B.1.617.2). Вирусы были изолированы из назо/орофарингеального смыва и прошли три последовательных пассажа на клетках Vero E6. Первоначально, проводили скрининговое исследование панели соединений на наличие антивирусного эффекта против «дикого штамма» SARS-CoV-2 PMVL-30. Для этого клетки Vero E6 высевали в 96-луночные планшеты (2×104 клеток/лунку) в полной ростовой среде DMEM за сутки до эксперимента. К клеткам добавляли различные разведения соединений (100, 25, 6.25 мкМ) и инкубировали в течение 1 ч при 370С и 5% CO2. После этого, производили заражение клеток SARS-CoV-2 при 100TCID50 (50% тканевая инфекционная доза). Планшеты инкубировали в течение 72 ч при 370С и 5% CO2. Вирус-индуцированный цитопатический эффект (СРЕ) оценивали с помощью МТТ метода, как описано ранее [11, 12]. После обнаружения соединений, которые активно ингибируют SARS-CoV-2, проводили дополнительные исследования их противовирусной активности в отношении “дельта” варианта SARS-CoV-2 как описано выше. Антивирусный эффект для лидерных соединений был также исследован с помощью ПЦР по уровню снижения вирусной нагрузки SARS-CoV-2.
Для 11 соединений была проведена оценка противовирусного действия против SARS-CoV-2 с использованием клеток Vero E6. Скрининг панели ингибиторов на обнаружение их антивирусной активности проводили с использованием 100 мкМ концентрации соединений, против SARS-CoV-2-индуцированного цитопатического эффекта (СРЕ). Обнаружено, что практически все соединения способны на 90-100% блокировать СРЕ (фиг. 11). Однако, наличие метила в N5 положении урацила в соединении Z872 приводило к полной потери антивирусной активности. Ввиду того, что соединение Z1007 при 100 мкМ обладает наиболее высокой токсичностью по отношению к клеткам Vero E6, его противовирусная активность была оценена при 25 мкМ, для которой ингибирование СРЕ составило в среднем 23,3%.
Дополнительно, противовирусный эффект был подтвержден с помощью ПЦР. Наиболее активные соединения из представленных панелей, приводили к значительному снижению вирусной нагрузки SARS-CoV-2. Соединение Z876 снижало нагрузку примерно на три порядка, в то время как для остальных наблюдалось падение нагрузки в среднем на два порядка в супернатанте SARS-CoV-2 инфицированных клеток Vero E6 (фиг. 12).
Противовирусная активность наиболее активных соединений из исследуемой панели была протестирована в анализе цитопатогенного эффекта (CPE) в культуре клеток Vero E6 против “дельта” варианта SARS-CoV-2 линии B.1.617.2, для определения их полуингибирующих концентраций (IC50). В результате было обнаружено, что соединения активно ингибируют СРЕ SARS-CoV-2, со значениями IC50 от 31.57 до 4.53 мкМ (фиг. 13). Наиболее высокая ингибирующая активность наблюдалась для соединений Z611, Z870 и Z876, для которых значения IC50не превышали 10 мкМ. Соединения Z611 и Z876 имеют родственную структуру с наличием антрацена в линкерной части в положении N1 урацила. Основным отличием соединения Z870 от схожих по структуре соединений из данной панели, являлось наличие фторфеноксипентильного заместителя, в то время как другие соединения содержали бромфеноксипентильный заместитель.
Пример 12. Исследование влияния соединений на стадии цикла репликации SARS-CoV-2
Был проведен анализ по определению на какой стадии жизненного цикла SARS-CoV-2 соединения проявляют эффект [13]. Клетки Vero E6 высевали в 96-луночные планшеты (3×104 клеток/лунку). Клетки инфицировали SARS-CoV-2 PMVL-30 при MOI 0.1 (множественность инфекции), а затем инкубировали еще 1 ч. Далее, вирусный инокулят удаляли, и клетки дважды промывали ростовой средой DMEM. Через 1 ч после инокуляции, к инфицированным клеткам добавляли соединения из исследуемой библиотеки в концентрации 25 мкМ в указанные моменты времени с последующей инкубацией при 370С и 5% СО2 в течение 16 ч после инокуляции (один жизненный цикл вируса). Супернатант из лунок отбирали и анализировали с помощью ОТ-ПЦР в режиме реального времени. Для определения вирусной нагрузки SARS-CoV-2, использовали набор «SARS-CoV-2 FRT» (НИЦЭМ им. Н.Ф. Гамалеи, Россия) с последующей постановкой и анализом на QuantStudio 5 (Applied Biosystems) или CFX96 Touch (Bio-Rad).Относительное количество РНК SARS-CoV-2 определяли с помощью калибровочной прямой, для построения которой при каждой постановке анализа тестировали калибровочные стандарты. Калибровочные стандарты представляли собой рекомбинантные конструкции амплифицируемого фрагмента генома SARS-CoV-2 с известной концентрацией.
Чтобы выяснить противовирусный механизм действия соединений из исследуемой панели, были проведены эксперименты позволяющие определить на какой стадии (стадиях) репликации вируса SARS-CoV-2 они проявляют свою противовирусную активность. Для этого к культуре клеток Vero E6 добавляли 25 мкМ соединений в разные моменты времени репликации вируса, включая прикрепление и проникновение вируса (entry), пост-проникновение и в течение всей вирусной инфекции. Для этого исследования SARS-CoV-2 “дикий тип” был выбран в качестве примера пандемического коронавируса человека. В этом анализе клетки Vero E6 были инфицированы SARS-CoV-2 при MOI равном 0.1, с последующим измерением количества копий вируса через 16 ч после инфекции в супернатанте клеточной культуры методом количественной ПЦР. Результаты ПЦР показали, что исследуемые соединения не подавляют репликацию вируса на стадии прикрепления и проникновения вируса (фиг. 14). Однако, данный анализ показал, что соединения действуют на стадии после проникновения вируса и в течение всей вирусной инфекции, снижая вирусную нагрузку на несколько порядков. Кроме этого, полученные данные свидетельствуют о том, что данные соединения могут быть эффективными в качестве профилактических и лечебных средств при COVID-19.
В результате проведенных исследований открыт новый класс ненуклеозидных ингибиторов репродукции SARS-CoV-2, обладающих высоким противовирусным эффектом in vitro, включая антивирусную активность против “дельта” варианта SARS-CoV-2. Приведенные примеры подтверждают выполнение поставленной задачи, а именно, создание новых, высокоэффективных, селективных и малотоксичных антивирусных агентов для лечения новой коронавирусной инфекции COVID-19.
Список использованных источников информации.
1. Novikov M.S., Babkov D.A., Paramonova M.P., Khandazhinskaya A.L., Ozerov A.A., Chizhov A.O., Andrei G., Snoeck R., Balzarini J., Seley-Radtke K.L. Synthesis and anti-HCMV activity of 1-[ω-(phenoxy)alkyl]uracil derivatives and analogues thereof. Bioorg. Med. Chem., 2013, 21 (14), 4151–4157.
2. Novikov M.S., Babkov D.A., Paramonova M.P., Chizhov A.O., Khandazhinskaya A.L., Seley-Radtke K.L. A highly facile approach to the synthesis of novel 2-(3-benzyl-2,4-dioxo-1,2,3,4-tetrahydropyrimidin-1-yl)-N-phenylacetamides. Tetrahedron Lett., 2013, 54 (6), 576-578.
3. Paramonova M.P., Babkov D.A., Valuev-Elliston V.T., Ivanov A.V., Kochetkov S.N., Pannecouque C., Balzarini J., Novikov M.S. Synthesis and Anti-HIV-1 Activity of 1-[ω-(Phenoxy)alkyl- and -alkenyl]uracil Derivatives. Pharmaceutical Chemistry J. 2013, 47 (9), 459-463.
4. Paramonova M.P., Ozerov A.A., Chizhov A.O., Snoeck R., Andrei G., Khandazhinskaya A.L., Novikov M.S. Synthesis of uracil-coumarin conjugates as potential inhibitors of virus replication. Mendeleev Commun., 2019, 29 (6), 638-639.
5. Malik V., Singh P., Kumar S. Regioselective synthesis of 1-allyl- and 1-arylmethyl uracil and thymine derivatives. Tetrahedron, 2005, 61 (16), 4009-4014.
6. Driouich, JS., Cochin, M., Lingas, G. et al. Favipiravir antiviral efficacy against SARS-CoV-2 in a hamster model. Nat Commun 12, 1735 (2021). https://doi.org/10.1038/s41467-021-21992-w.
7. Suzanne J. F. Kaptein, Sofie Jacobs, at al., Favipiravir at high doses has potent antiviral activity in SARS-CoV-2−infected hamsters, whereas hydroxychloroquine lacks activity. Proceedings of the National Academy of Sciences Oct 2020, 117 (43) 26955-26965; DOI: 10.1073/pnas.2014441117.
8. Williamson, B.N., Feldmann, F., Schwarz, B. et al. Clinical benefit of remdesivir in rhesus macaques infected with SARS-CoV-2. Nature 585, 273–276 (2020). https://doi.org/10.1038/s41586-020-2423-5.
9. Cox, R.M., Wolf, J.D. & Plemper, R.K. Therapeutically administered ribonucleoside analogue MK-4482/EIDD-2801 blocks SARS-CoV-2 transmission in ferrets. Nat Microbiol 6, 11–18 (2021). https://doi.org/10.1038/s41564-020-00835-2.
10. Goldberg E, Ben Zvi H, Sheena L, Sofer S, Krause I, Sklan EH, Shlomai A. A real-life setting evaluation of the effect of remdesivir on viral load in COVID-19 patients admitted to a large tertiary centre in Israel. Clin Microbiol Infect. 2021 Jun;27(6):917.e1-917.e4. doi: 10.1016/j.cmi.2021.02.029. Epub 2021 Mar 9. PMID: 33705849; PMCID: PMC7939997.
11. Altaf, I., Nadeem, M.F., Hussain, N. et al. An in vitro antiviral activity of iodine complexes against SARS-CoV-2. Arch Microbiol 203, 4743–4749 (2021). https://doi.org/10.1007/S00203-021-02430-3.
12. De Meyer S, Bojkova D, Cinatl J, Van Damme E, Buyck C, Van Loock M, Woodfall B, Ciesek S. Lack of antiviral activity of darunavir against SARS-CoV-2. Int J Infect Dis. 2020 Aug;97:7-10. doi: 10.1016/j.ijid.2020.05.085. Epub 2020 May 29. PMID: 32479865; PMCID: PMC7258847. https://doi.org/10.1016/j.ijid.2020.05.085.
13. Yuan, S., Yin, X., Meng, X. et al. Clofazimine broadly inhibits coronaviruses including SARS-CoV-2. Nature 593, 418–423 (2021). https://doi.org/10.1038/s41586-021-03431-4 https://doi.org/10.1038/s41586-021-03431-4.
Реферат
Группа изобретений относится к области молекулярной биологии, вирусологии и медицины, а именно к новым N1,N3-дизамещенным производным урацила и их фармацевтически приемлемым солям, обладающим противовирусным действием в отношении SARS-CoV-2. Предложено соединение общей формулы I или его фармацевтически приемлемая соль, где: X - алкил или оксиалкил (С1-С12), Ar - замещенная ароматическая группа, Ar - ароматическая группа, Y - атом кислорода, R1 - карбоксил или галоген, в N3-положении урацила полиметиленовый линкер может включать от 1 до 12 метиленовых групп. Технический результат: эффективное ингибирование репликации SARS-CoV-2. 3 н. и 1 з.п. ф-лы, 14 ил., 12 пр.
Формула

Документы, цитированные в отчёте о поиске
Производные ди(диазониадиспиро[5.2.5.2]гексадекан)-5-нитропиримидина и их применение для лечения коронавирусных инфекций, в частности вызванных вирусом sars-cov-2

Комментарии