(Аза)индол-, бензотиофен- и бензофуран-3-сульфонамиды - RU2767904C2
Код документа: RU2767904C2
Чертежи
Описание
УРОВЕНЬ ТЕХНИКИ
Связанные с белком G рецепторы (GPCR) образуют самое большое семейство мембранных рецепторов, содержащихся в клетке. Они преобразуют внеклеточные сигналы во внутриклеточные эффекторные системы и участвуют в целом ряде физиологических явлений, поэтому они представляют собой наиболее распространенные мишени для фармацевтических лекарственных средств, хотя имеющихся средства лечения направлены лишь на небольшое количество GPCR.
GPCR отвечает на широкий диапазон лигандов. Благодаря развитию технологий секвенирования генома человека идентифицировано более 400 GPCR (не включая обонятельные рецепторы GPCR), примерно для 25% из которых все еще отсутствует определенный физиологически соответствующий лиганд. Эти рецепторы также известны, как "орфанные GPCR". Предполагается, что их "деорфанизация" и установление их роли in vivo приведут к пониманию новых механизмов регуляции и поэтому к обнаружению новых мишеней для лекарственных средств. Пока не ясно, является ли GPR17 таким орфанным рецептором. С точки зрения филогенетики GPR17 находится в близком родстве с нуклеотидными рецепторами P2Y и цистениллейкотриеновыми рецепторами (CysLT1, CysLT2), при идентичности последовательности аминокислот, составляющей примерно 30 и примерно 35% соответственно.
Анализ множества тканей по методике нозерн-блоттинга и с помощью анализа RT-PCR (полимеразная цепная реакция обратной транскриптазы) указывает на то, что GPR17 экспрессируется главным образом в центральной нервной системе (ЦНС) (Ciana et al., 2006, EMBO J 25(19): 4615; Blasius et al., 1998, J Neurochem 70(4): 1357) и дополнительно в сердце и почках, т.е. в органах, обычно подвергающихся ишемическому повреждению. Идентифицированы две изоформы GPR17 человека, отличающиеся лишь длиной последовательности их аминокислот на N-конце. Короткая изоформа GPR17 кодирует белок, содержащий 339 аминокислотных остатков, при типичных для родопсина семи трансмембранных мотивах. Длинная изоформа кодирует рецептор, содержащий в последовательности аминокислот на N-конце на 28 аминокислот больше (Blasius et al., 1998). GPR17 позвоночных являются весьма сходными (идентичность последовательности аминокислот ортологов у мышей и крыс составляет ~90%), что может являться благоприятной характеристикой в контексте выявления лекарственных средств при разработке малых молекул - лигандов и моделей на животных.
В первоначальном сообщении о деорфанизации GPR17 идентифицировали как двойной рецептор урацилнуклеотидов и цистеинил лейкотриенов (cysLT), LTC4 и LTD4 соответственно, на основании связывания с35SGTPγS и исследования ингибирования сАМР (циклический аденозинмонофосфат), а также визуализации кальция в отдельной клетке (Ciana et al., 2006, тот же источник). Были представлены доказательства функционирования GPR17 в разных клеточных средах, таких как клетки 1321N1, COS7, СНО и HEK293 (Ciana et al., 2006, тот же источник). Затем в независимом исследовании была подтверждена активация GPR17 посредством урацилнуклеотидов, однако не подтверждена активация посредством CysLT (Benned-Jensen and Rosenkilde, 2010, Br J Pharmacol, 159(5): 1092). В недавних независимых сообщениях (Maekawa et al., 2009, PNAS 106(28), 11685; Qi et al., 2013, J Pharmacol Ther 347,1, 38; Hennen et al., 2013, Sci Signal 6, 298) показано отсутствие ответа GPR17 и на урацилнуклеотиды, и на CysLT в разных клеточных средах, стабильно экспрессирующих GPR17 (клетки 1321N1, СНО, HEK293). Также предложена новая регуляторная роль для GPR17: при совместном экспрессировании с CysLT1 GPR17 воспроизводит рецептор CysLT1, невосприимчивый к его эндогенным липидным медиаторам LTC4 и LTD4. Очевидно, что для более подробного изучения фармакологических характеристик и функционирования GPR17 необходимы дополнительные исследования in vitro.
Лекарственные средства, модулирующие активность GPR17, могут обладать нейропротективным, противовоспалительным и противоишемическим воздействиями и поэтому они могут быть полезны для лечения ишемии головного мозга, сердца и почек, и удара (WO 2006/045476), и/или для улучшения восстановления после приступов этих заболеваний (Bonfanti et al., Cell Death and Disease, 2017, 8, e2871).
Полагают, что модуляторы GPR17 также участвуют в потреблении пищи, реакциях инсулина и лептина, и поэтому заявлено, что они играют роль в лечении ожирения (WO 2011/113032).
Кроме того, существует убедительное доказательство того, что GPR17 участвует в процессах нарушения миелинизации, и что негативные модуляторы GPR17 (антагонисты или обратные агонисты) могут представлять собой ценные лекарственные средства, предназначенные для лечения или облегчения протекания миелинизации, таких как рассеянный склероз или повреждение спинного мозга (Chen et al., Nature Neuroscience 2009, 12(11): 1398-406; Ceruti et al.; Brain: Journal of Neurology 2009 132 (Pt 8): 2206-18; Hennen et al., Sci Signal, 6, 2013, 298; Simon et al., J Biol Chem 291, 2016, 705; Fumagalli et al, Neuropharmacology 104, 2016, 82). Показано, что активация GPR17 ингибирует созревание клеток-предшественников олигодендроцитов (ОРС) и, таким образом, эффективно предупреждает нарушение миелинизации (Simon et al., приведенная выше). Таким образом, идентификация активных и селективных антагонистов или обратных агонистов GPR17 является существенно важной для лечения нарушений миелинизации.
Известно, что несколько тяжелых заболеваний, связанных с нарушением миелинизации, вызваны нарушениями миелинизации вследствие уменьшения количества миелина (обычно называющимся демиелинизацией) и/или вследствие неспособности организма надлежащим образом образовывать миелин (иногда называющейся дисмиелинизацией). Заболевания, связанные с нарушением миелинизации, могут быть первичными или вторичными, как ответ на определенные вызывающие их события, такие как, например, травматическое повреждение головного мозга или вирусная инфекция. Заболевания, связанные с нарушением миелинизации, главным образом могут поражать центральную нервную систему (ЦНС), однако также могут затрагивать периферическую нервную систему. Заболевания, связанные с нарушением миелинизации, включают, в частности, рассеянный склероз, нейромиелит зрительного нерва (также известный, как болезнь Девика), лейкодистрофии, синдром Гийена-Барре и многие другие заболевания, дополнительно более подробно описанные ниже (см. например, публикацию Love, J Clin Pathol, 59, 2006, 1151, а также Fumagalli et al., приведенную выше). Недавно установлено, что нейродегенеративные заболевания, такие как болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона, боковой амиотрофический склероз (ALS) и мультисистемная атрофия (МСА) сильно связаны с уменьшенной миелинизацией (см. например, публикации Ettle et al., Mol Neurobiol 53, 2016, 3046; Jellinger and Welling, Movement Disorders, 31, 2016; 1767; Kang et al., Nature Neurosci 6, 2013, 571; Bartzokis, Neurochem Res (2007) 32: 1655).
Рассеянный склероз (MS) является хроническим прогрессирующим нарушением. Он является воспалительным аутоиммунным заболеванием, вызывающим поражение олигодендроцитов, демиелинизацию и, в заключение, потерю аксонов, таким образом, приводящим к возникновению широкого спектра признаков и симптомов, характерных для тяжелого неврологического заболевания, таких как, например, усталость, головокружение, затруднения движения и ходьбы, затруднения с речью и проглатыванием, боль и другие. MS проявляется в нескольких формах, при этом появление новых симптомов происходит или при отдельных приступах (рецидивирующие формы), или путем медленного накопления со временем (прогрессирующие формы). В промежутках между приступами определенные симптомы могут полностью исчезать, однако часто возникает тяжелое неврологическое нарушение, в особенности, если заболевание развивается в более прогрессирующей форме. По данным Американской ассоциации больных рассеянным склерозом в США примерно у 400000 индивидуумов диагностирован MS и во всем мире у 2,5 миллионов, при этом по оценкам ежегодно в США диагностируются 10000 новых случаев. Рассеянный склероз в 2-3 раза чаще встречается у женщин, чем у мужчин.
Не существует известного средства для этиологического лечения или излечивания рассеянного склероза, или многих других заболеваний, связанных с нарушением миелинизации. Лечение обычно является симптоматическим и при этом предпринимаются попытки улучшить функции после приступа и предотвратить новые приступы путем нацеливания лечения на воспалительный компонент заболевания. Такие иммуномодулирующие лекарственные средства обычно обладают лишь умеренной эффективностью, в особенности, если заболевание уже прогрессировало, однако могут приводить к побочным эффектам и плохо переноситься. Кроме того, большинство из имеющихся в продаже лекарственных средств, такие как β-интерфероны, глатирамерацетат или предназначенные для лечения антитела, выпускаются только в форме инъекций и/или направлены только на воспалительный компонент заболевания, а не непосредственно на демиелинизацию. Другие лекарственные средства, такие как кортикостероиды, обладают скорее неспецифическим противовоспалительным и иммунодепрессивным воздействием, таким образом, вероятно, приводящим к возникновению хронических побочных эффектов, таких как проявляющихся, например, в синдроме Кушинга.
Поэтому настоятельно необходимо безопасное и эффективное лекарственное средство, предназначенное для лечения заболеваний, связанных с нарушением миелинизации, таких как MS, предпочтительно лекарственное средство, которое является подходящим для перорального введения. В идеальном случае такое лекарственное средство должно обратить протекание демиелинизации путем уменьшения демиелинизации и/или путем обеспечения повторной миелинизации поврежденных нейронов. Химическое соединение, которое эффективно уменьшает активность рецептора GPR17, может удовлетворить этим требованиям.
Однако известны лишь немногие химические соединения, которые эффективно модулируют активность GPR17.
В WO 2005/103291 предложены эндогенные молекулы, 5-аминолевулиновая кислота (5-ALA) и порфобилиноген (PBG), в качестве активирующих лигандов для GPR17, раскрыто анальгетическое действие агониста GPR17 и предложено применение агонистов GPR17 для лечения невропатической боли и в качестве средств для скрининговых исследований GPR17. Однако указанное сродство 5-ALA и PBG является довольно низким и количества, необходимые для проведения исследований, являются значительными, а именно в случае 5-ALA они составляют сотни микромолей, или в случае PBG составляют даже миллимоли, что делает оба этих соединения не особенно подходящими для применения в систематических скрининговых исследованиях и даже в терапии. Кроме того, PBG является химически нестабильным реакционноспособным соединением, которое быстро разлагается под воздействием воздуха и света, что делает его непригодным к использованию в регулярно проводимых исследованиях. Таким образом, эти соединения не являются перспективными исходными веществами для разработки терапевтически эффективных негативных модуляторов GPR17.
Монтелукаст и пранлукаст изначально были разработаны в качестве антагонистов лейкотриенового рецептора и недавно установлено, что они также воздействуют на рецептор GPR17 (Ciana et al., EMBO J. 2006, 25, 4615-4627). Однако последующие полученные в функциональном исследовании результаты для монтелукаста являлись противоречивыми (Hennen et al., 2013, тот же источник), тогда как фармакологическое ингибирование GPR17 с помощью пранлукаста ускоряет дифференциацию первичных олигодендроцитов у мышей (Hennen et al., 2013, тот же источник) и крыс (Ou et al., J. Neurosci. 36, 2016, 10560-10573). Пранлукаст даже фенокопирует эффект подавления GPR17 в модели фокальной демиелинизации с использованием лизолецитина, поскольку и у мышей с удаленным GPR17, и у мышей дикого типа, которых лечили пранлукастом, наблюдали более раннее возникновение повторной миелинизации (Ou, тот же источник). Эти результаты сильно поддерживают предположение о том, что ингибиторы GPR17 являются перспективными для лечения демиелинизирующих заболеваний человека.
Однако сродство монтелукаста и пранлукаста к GPR17 наблюдается лишь при высоких концентрациях в микромолярном диапазоне (
В US 8623593 раскрыты некоторые индол-2-карбоновые кислоты в качестве агонистов GPR17 и их применение в скрининговых исследованиях. Однако все эти производные являются активными агонистами и не являются подходящими для подавления активности GPR17, которое необходимо для лечения нарушений миелинизации, таких как MS. Кроме того, активаторы GPR17 этого класса не обладают достаточной способностью проникать через гематоэнцефалический барьер вследствие наличия легко ионизируемых карбоксигрупп и поэтому они не являются подходящими основными соединениями для разработки негативных модуляторов GPR17. См. также публикации Baqi et al., Med. Chem. Commun., 2014, 5, 86 и
В WO 2013/167177 описаны некоторые фенилтриазолы и бензодиазепины в качестве антагонистов GPR17. Однако раскрытые соединения были выбраны лишь на основании результатов скрининга, проведенного с помощью компьютерного моделирования, и не приведены никакие результаты биологических исследований. До настоящего времени авторам настоящей заявки не удалось подтвердить, что какой-либо из заявленных лигандов, предложенных авторами предшествующей заявки на патент, обладают модулирующей активностью антагониста GPR17.
Поэтому необходимо идентифицировать активные модуляторы, предпочтительно негативные модуляторы GPR17, которые способны эффективно уменьшать активность GPR17, предпочтительно при пероральном введении.
В публикации Mehra et al. (Eur J Med Chem, 92, 2015, 78-90) раскрыт ряд соединений, обладающих ингибирующей активностью по отношению к ацетилтрансферазе Е. coli, включая четыре фенилзамещенных пирроло[2,3-b]пиридин-3-сульфонамида (соединение 20 [N-(3,4-дифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], 32 [N-(3,5-диметоксифенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], 37 [N-(2,5-дифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид] и 43 [N-(3,5-дифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], приведенные в таблице S7). Структура этих четырех азаиндолов отличается от структуры соединений, раскрытых в настоящем изобретении, тем, что азаиндольное ядро в приведенных в публикации Mehra соединениях не является дополнительно замещенным. Кроме того, в публикации Mehra et al. не описаны какие-либо ингибирующие GPR17 характеристики этих соединений и/или какое-либо применение этих соединений для лечения нарушения миелинизации. Более того, в публикации Mehra et al. раскрыты соединения в качестве потенциальных антибиотиков.
ЧЕРТЕЖИ
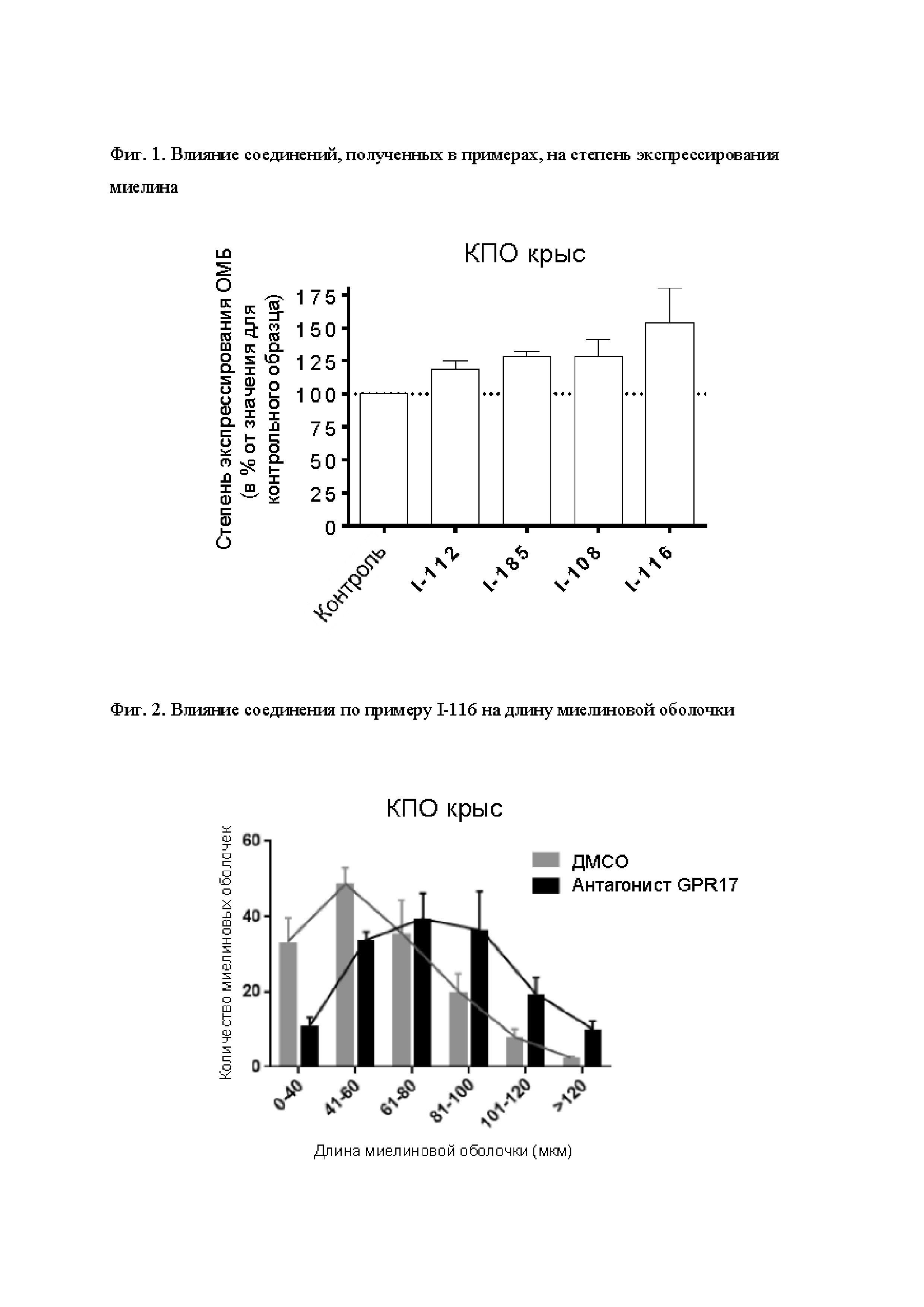
На Фиг. 1 представлена степень экспрессирования основного миелинового белка (МРВ), использующаяся в качестве маркера созревания олигодендроцитов в исследовании по методике вестерн-блоттинга. После добавления в клетки-предшественники олигодендроцитов (ОРС) соединений, предлагаемых в настоящем изобретении, в особенности, соединений I-112, I-185, I-108 и I-116, они стимулируют экспрессию МРВ по сравнению со случаем использования только разбавителя.
На Фиг. 2 представлено влияние соединения, предлагаемого в настоящем изобретении (I-116), на длину миелиновых оболочек, экспрессированных посредством ОРС. После добавления к ОРС соединения I-116 оно индуцирует образование более длинных миелиновых оболочек, чем миелиновые оболочки при добавлении к ОРС только разбавителя.
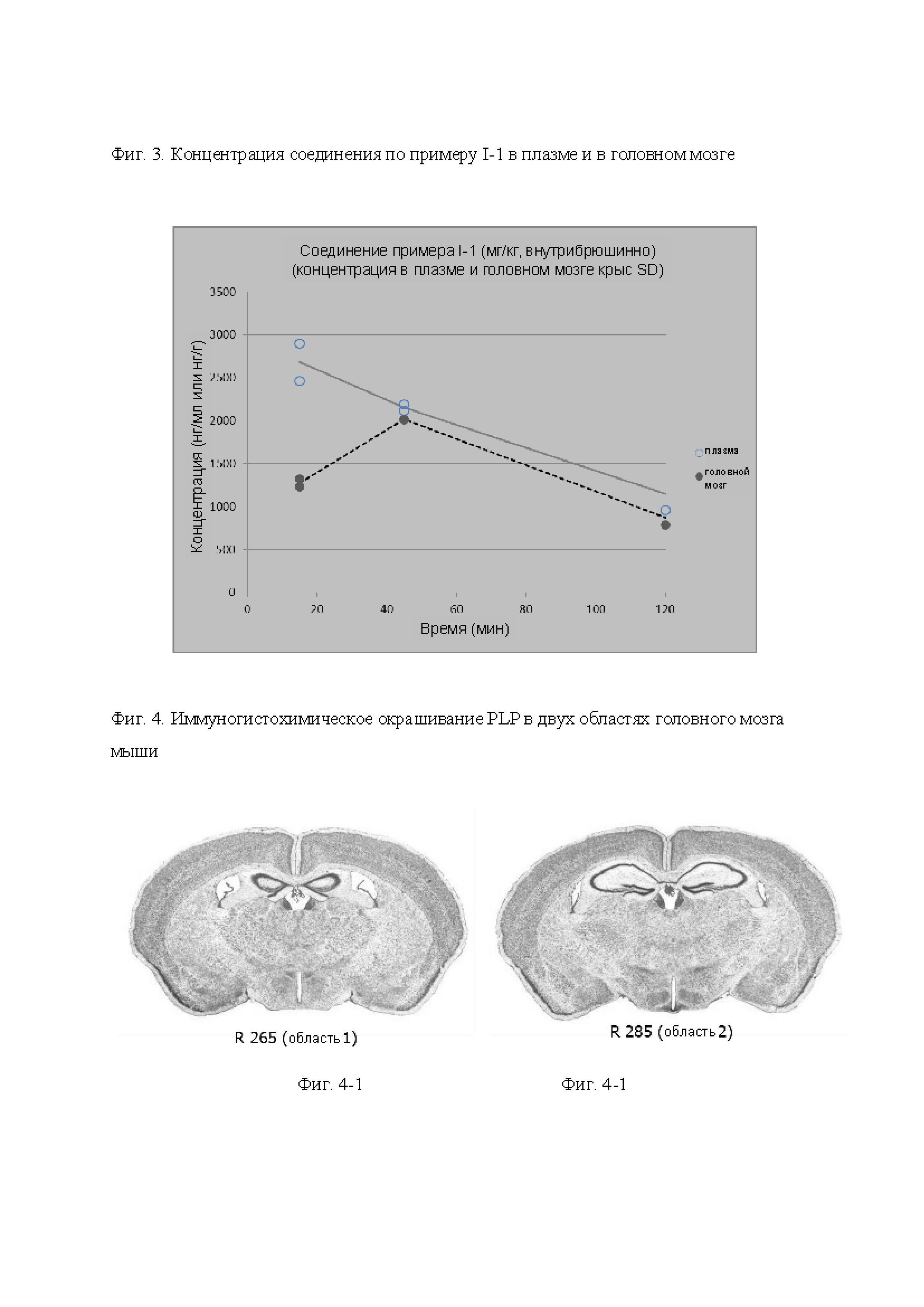
На Фиг. 3 представлена концентрация соединения, предлагаемого в настоящем изобретении I-1, в плазме и головном мозге после внутрибрюшинного введения мышам.
На Фиг. 4 представлено распределение PLP (протеолипидный белок), маркера миелина, в двух соответствующих областях головного мозга мыши, области 1 (Фиг. 4.1) и области 2 (фиг 4.2), после иммуногистохимического окрашивания с помощью антител к PLP. Этот эксперимент использовали для определения влияния соединений, предлагаемых в настоящем изобретении, в модели с использованием купризона (результаты представлены на Фиг. 5).
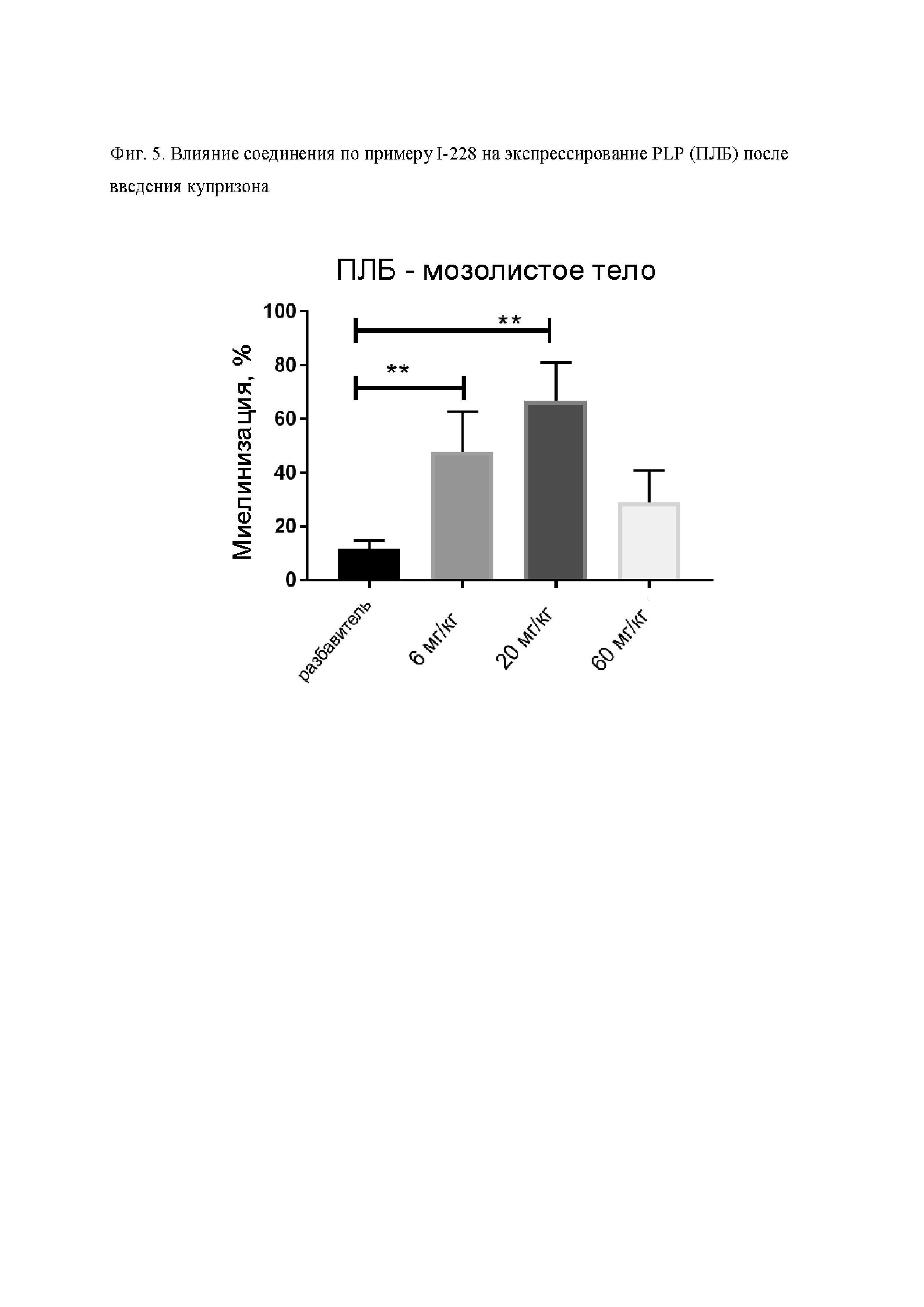
На Фиг. 5 представлено влияние соединения, предлагаемого в настоящем изобретении (I-228), на степень экспрессирования PLP у мыши во время восстановления после введения купризона, определенное с помощью иммуногистохимического окрашивания. После перорального введения мыши соединения I-228 при дозах, равных 6 и 20 мг/кг связанный с миелином белок PLP повторно образуется существенно быстрее в определенных областях головного мозга мыши, чем после введения только разбавителя.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к классу химических соединений, которые являются негативными модуляторами GPR17.
Эти соединения имеют общую структуру формулы I:
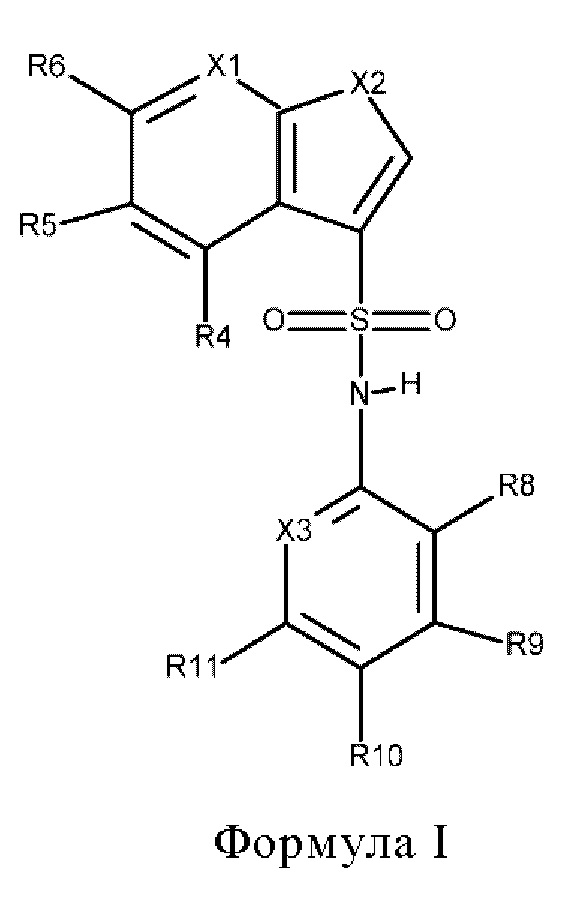
в которой
X1 обозначает N или C(R7),
Х2 обозначает NH, S или О,
Х3 обозначает N или C(R12),
R4 выбран из водорода, метоксигруппы и галогена, включая фтор, и предпочтительно обозначает водород,
R5 выбран из группы, включающей водород, галоген, цианогруппу, C1-С6-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-C6-алкоксигруппу, С1-С3-алкилкарбонил, С1-С3-алкоксикарбонил, С1-С3-алкилсульфинил и С1-С3-алкилсульфонил, где каждый алкил или алкоксигруппа необязательно может содержать один или более заместителей, выбранных из группы, включающей галоген, C1-С3-алкоксигруппу, цианогруппу, азидогруппу, гидроксигруппу, C1-С3-алкиламиногруппу и ди(С1-С3-алкил)аминогруппу, и С1-С3-алкиламинокарбонил (причем предпочтительными необязательными заместителями указанной алкильной группы и алкоксигруппы являются галоген и C1-С6-алкоксигруппа), или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, гидроксигруппу, галоген, цианогруппу, азидогруппу, нитрогруппу, C1-C6-алкил, С2-С6-алкенил, С2-С6-алкинил, C1-С6-алкоксигруппу, С3-С7-циклоалкил, С3-С6-циклоалкенил, С3-С7-гетероциклоалкил, С3-С7-гетероциклоалкенил, фенил, С5-С10-гетероарил, C8-С10-гетероциклил, -ORx, -SRx, -SORx, SO2RX, -пентафторсульфанил, NRyRzz, -NRyCORx, -NRyCO2Rx, -NRxCONRyRz, -NRySORx, -NRySO2Rx, -CORx, -CO2Rx, -CONRyRz, где каждая алкильная, алкенильная, алкинильная группа, алкоксигруппа, циклоалкильная, гетероциклоалкильная, циклоалкенильная, фенильная, гетероарильная или гетероциклильная группа, содержащаяся в R6, может быть незамещенной или замещенной одним или несколькими остатками, предпочтительно выбранными из группы, включающей галоген, гидроксигруппу, оксогруппу, цианогруппу, азидогруппу, нитрогруппу, C1-С6-алкил, галоген(С1-С6)алкил, С1-С6-алкокси(С1-С3)алкил, С3-С7-циклоалкил, С3-С7-гетероциклоалкил, фенил, С5-С10-(предпочтительно С5-С6)гетероарил, ORx, -SRx, -SORx, SO2Rx, -пентафторсульфанил, NRyRz, -NRyCORx, -NRyCO2Rx, -CORx, -CO2Rx, -CONRyRz,
где Rx, Ry, Rz и Rzz независимо выбраны из группы, включающей водород, C1-C6-алкил, С3-С7-циклоалкил, С3-С6-циклоалкенил, С3-С7-циклоалкил(С1-С6)алкил, фенил, фенил(С1-С6)алкил, С3-С7-гетероциклоалкил, С3-С7-гетероциклоалкил(С1-С6)алкил, С5-С6-гетероарил или гетероарил(С1-С6)алкил, причем любая из этих групп может быть незамещенной или содержать один или более заместителей, выбранных из описанных выше, и где Rzz предпочтительно отличается от водорода,
или Ry и Rz, или Ry и Rzz вместе с атомом азота аминогруппы, к которому они оба присоединены, могут образовать ароматический или неароматический, незамещенный или замещенный С5-С6-гетероцикл, где любой заместитель выбран из числа заместителей, описанных выше,
или R6 вместе с R5 или R7 и с атомами углерода, к которым они присоединены, образуют 5- или 6-членное ароматическое или неароматическое кольцо, которое необязательно может содержать один или более гетероатомов, выбранных из S, О и N, и где указанное кольцо может быть незамещенным или содержать один или более заместителей,
где предпочтительно, если (i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель кольца, образованного с помощью R6 и R7, если присутствует, предпочтительно выбран из группы, включающей галоген, гидроксигруппу, цианогруппу, C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С3-С7-циклоалкил, С3-С7-циклоалкил(С1-С3)алкил, С3-С7-гетероциклоалкил(С1-С3)алкил и С1-С6-алкоксигруппу, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из группы, включающей галоген, гидроксигруппу и незамещенные или фторированные C1-С3-алкоксигруппу, С3-С7-циклоалкил и С3-С7-гетероциклоалкил, где любой заместитель фенила, пиридила, циклопентила и циклогексила предпочтительно выбран из группы, включающей фтор, хлор, цианогруппу, гидроксигруппу, метил, фторметил, метоксигруппу и фторметоксигруппу,
или (ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, или
R7, если присутствует, выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, нитрогруппу, аминогруппу, C1-С6-алкил, C1-C6-алкоксигруппу, С2-С6-алкинил, С2-С6-алкенил, С1-С6-алкилкарбонил, C1-C6-алкоксикарбонил, С1-С6-алкилсульфонил, С1-С6-алкилсульфинил, C1-C6-алкилтиогруппу, С1-С3-алкилкарбониламиногруппу, С1-С6-алкиламинокарбонил, ди(С1-С3)алкиламинокарбонил, С3-С7-циклоалкил, С3-С7-циклоалкоксигруппу, С3-С7-гетероциклоалкил, С3-С6-гетероциклоалкоксигруппу, фенил, фенилоксигруппу, фенил(С1-С2)алкил, фенил(С1-С2)алкоксигруппу, фенилсульфонил, фенилсульфинил, С5-С6-гетероарил, С5-С6-гетероарилоксигруппу, С5-С6-гетероарил(С1-С3)алкил, С5-С6-гетероарил(С1-С3)алкоксигруппу, С3-С6-циклоалкил(С1-С2)алкил, С3-С6-циклоалкил(С1-С3)алкоксигруппу, С3-С6-гетероциклоалкил(С1-С2)алкил, С3-С6-гетероциклоалкил(С1-С2)алкоксигруппу, и где каждая группа, содержащаяся в R7, в частности, каждая алкильная, алкенильная, алкинильная группа, алкоксигруппа, циклоалкильная, гетероциклоалкильная, фенильная или гетероарильная группа может быть незамещенной или содержать один или более заместителей, выбранных из галогена, гидроксигруппы, цианогруппы, незамещенного или галогенированного C1-C6-алкила и незамещенной или галогенированной C1-C6-алкоксигруппы,
R8 выбран из группы, включающей водород, C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, C1-C6-алкоксигруппу, С1-С3-алкилсульфинил, С1-С3-алкилсульфонил, C1-С3-алкилтиогруппу, цианогруппу и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и незамещенной или фторированной С1-С3-алкоксигруппы, или вместе с R9 образует кольцевую систему, как здесь описано,
R9 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, C1-С6-алкил, C1-С6-алкоксигруппу, С2-С6-алкенил, С2-С6-алкинил и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и незамещенной или фторированной C1-С3-алкоксигруппы,
или R9 вместе с R8 или R10 и с атомами С, к которым они присоединены, образуют 5- или 6-членное кольцо, которое необязательно может быть дополнительно замещенным и которое может содержать один или более образующих кольцо гетероатомов, выбранных из N, S, О и Se;
где кольцо, образованное с помощью R9 вместе с R8 или R10, и кольцо к которому они присоединены, образуют бициклическую кольцевую систему, предпочтительно выбранную из группы, включающей (а) 2,1,3-бензотиадиазол, (b) 2,1,3-бензоселенадиазол, (с) 2,1,3-бензоксадиазол, (d) 1,3-бензотиазол, (е) 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и незамещенным или замещенным оксогруппой, (f) 1,3-бензодиоксол, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, (g) бензотиофен, который может быть незамещенным или может быть частично гидрированным и незамещенным или содержать один или два заместителя, выбранных из оксогруппы, метила или фтора, где бензотиофен предпочтительно является частично гидрированным с образованием 1,3-дигидро-2-бензотиофена, который предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксидо-2,3-дигидро-1-бензотиофена, который необязательно может быть дополнительно замещенным, (h) бензофуран, который может быть незамещенным или может быть частично гидрированным и незамещенным или замещенным одной или двумя группами, выбранными из оксогруппы, фтора и метила, предпочтительно одной оксогруппой, где бензофуран предпочтительно является частично гидрированным с образованием 1,3-дигидро-2-бензофурана, который предпочтительно замещен оксогруппой с образованием 3-оксо-1,3 дигидробензофурана, который необязательно может быть дополнительно замещенным, например метильной группой, и (i) 2,3-дигидро-1Н-изоиндол, который предпочтительно замещен оксогруппой с образованием 3-оксо-2,3-дигидро-1Н-изоиндола, который необязательно может быть дополнительно замещенным,
R10 выбран из группы, включающей водород, галоген, C1-C6-алкил, C1-C6-алкоксигруппу, С2-С6-алкенил, С2-С6-алкинил, цианогруппу, циано(С1-С6)алкил, циано(С1-С6)алкилоксигруппу,С1-С6-алкилкарбонил, C1-C6-алкоксикарбонил, C1-C6-алкилсульфонил, C1-C6-алкилсульфинил, C1-C6-алкилтиогруппу, С3-C6-циклоалкил, С3-С6-циклоалкилоксигруппу, С3-С6-гетероциклоалкил, С3-С6-гетероциклоалкилоксигруппу, аминогруппу, азидогруппу, пентафторсульфанил, нитрогруппу, С1-С5-алкилкарбониламиногруппу, С1-С5-алкиламинокарбонил, ди(С1-С3)алкиламинокарбонил, C1-С3-алкилсульфинил и C1-С3-алкилсульфонил, где каждый алкил, алкенил, алкинил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из группы, включающей галоген, C1-C6-алкоксигруппу, галоген(С1-С6)алкоксигидрокси(С1-С6)алкоксигруппу, необязательно галогенированную C1-C6-алкилтиогруппу, необязательно галогенированный C1-С3-алкилкарбонил, необязательно галогенированный С1-С3-алкилоксикарбонил, необязательно галогенированный C1-С3-алкилсульфонил, необязательно галогенированный C1-С3-алкилсульфинил, C1-С3-алкилкарбониламиногруппу, С1-С3-алкиламинокарбонил, ди(С1-С3)алкиламинокарбонил, гидроксигруппу, цианогруппу, нитрогруппу, оксогруппу, С3-С6-циклоалкил, С3-C6-циклоалкоксигруппу, С3-С6-гетероциклоалкил, С3-C6-гетероциклоалкоксигруппу, фенил, фенилоксигруппу и С5-С6-гетероарил, где любой С3-С6-циклоалкил, С3-С6-циклоалкоксигруппа, С3-С6-гетероциклоалкил, С3-С6-гетероциклоалкоксигруппа, фенил и гетероарил может быть незамещенным или замещенным одним или несколькими остатками, выбранными из группы, включающей галоген, гидроксигруппу, гидроксиметил, оксогруппу, цианогруппу, нитрогруппу, аминогруппу, необязательно галогенированный или гидроксилированный C1-С3-алкил, необязательно гидроксилированную или галогенированную C1-С3-алкоксигруппу, необязательно галогенированный С1-С3-алкилкарбонил и необязательно галогенированный С1-С3-алкоксикарбонил, где любая аминогруппа может быть замещена одной или двумя группами, выбранными из C1-С3-алкила, С1-С3-алкилсульфонила, С1-С3-алкилкарбонила и С1-С3-алкоксикарбонила, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, C1-С6-алкил, C1-С6-алкоксигруппу, C1-С6-алкилкарбонил, C1-С6-алкоксикарбонил, С1-С6-алкилсульфонил и С1-С6-алкилсульфинил, С2-С6-алкенил и С2-С6-алкинил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и галогенированной, предпочтительно фторированной, или незамещенной C1-С3-алкоксигруппы,
R12, если присутствует, выбран из группы, включающей водород, C1-C6-алкил, C1-С6-алкоксигруппу и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и галогенированной, предпочтительно фторированной, или незамещенной С1-С3-алкоксигруппы,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном варианте осуществления в соединениях формулы I
X1 обозначает N или C(R7),
Х2 обозначает NH или О,
Х3 обозначает N или C(R12),
R4 выбран водорода и фтора, и предпочтительно обозначает водород,
R5 выбран из группы, включающей водород, галоген, цианогруппу, C1-C6-алкил, C1-C6-алкоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, С1-С3-алкилсульфинил и C1-С3-алкилсульфонил, где каждый алкил или алкоксигруппа необязательно может содержать один или более заместителей, выбранных из группы, включающей галоген, C1-С3-алкоксигруппу, С2-С3-алкинил, С2-С3-алкенил, цианогруппу, азидогруппу, гидроксигруппу, и необязательно С1-С3-алкилированную аминогруппу (причем предпочтительными необязательными заместителями указанных алкильной группы и алкоксигруппы являются галоген и C1-C6-алкоксигруппа), или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, гидроксигруппу, галоген, цианогруппу, азидогруппу, C1-C6-алкил, С2-С6-алкенил, С2-С6-алкинил, C1-C6-алкоксигруппу, С3-С7-циклоалкил, С3-С6-циклоалкенил, С3-С7-гетероциклоалкил, С3-С7-гетероциклоалкенил, фенил, С5-С10-гетероарил, C8-С10-гетероциклил, -ORx, -SRx, -SORx, SO2RX, -пентафторсульфанил, NRyRzz, -NRyCORx, -NRyCO2Rx, -NRxCONRyRz, - -CORx, -CO2Rx, -CONRyRz, где каждая алкильная, алкенильная, алкинильная группа, алкоксигруппа, циклоалкильная, гетероциклоалкильная, циклоалкенильная, фенильная, гетероарильная или гетероциклильная группа, содержащаяся в R6, может быть незамещенной или содержать один или более заместителей, предпочтительно выбранных из группы, включающей галоген, гидроксигруппу, оксогруппу, цианогруппу, азидогруппу, нитрогруппу, C1-С6-алкил, C1-С6-алкокси(С1-С3)алкил, С3-С7-циклоалкил, С3-С7-гетероциклоалкил, фенил, С5-С10-(предпочтительно С5-С6)гетероарил, ORx, -SRx, -SORx, SO2RX, -пентафторсульфанил, NRyRz, -NRyCORx, -NRyCO2Rx, -CORx, -CO2Rx, -CONRyRz,
где Rx, Ry, Rz и Rzz независимо выбраны из группы, включающей водород, C1-C6-алкил, С3-С7-циклоалкил, С3-С6-циклоалкенил, С3-С7-циклоалкил(С1-С6)алкил, фенил, фенил(С1-С6)алкил, С3-С7-гетероциклоалкил, С3-С7-гетероциклоалкил(С1-С6)алкил, С5-С6-гетероарил или гетероарил(С1-С6)алкил, любая из этих групп может быть незамещенной или содержать один или более заместителей, выбранных из описанных выше, или Ry и Rz, или Ry и Rzz вместе с атомом азота аминогруппы, к которому они оба присоединены, могут образовать ароматический или неароматический, незамещенный или замещенный С5-С6-гетероцикл, где Rzz предпочтительно отличается от водорода,
или R6 вместе с R5 или R7 и с атомами углерода, к которым они присоединены, образуют 5- или 6-членное ароматическое или неароматическое кольцо, которое необязательно может содержать один или более гетероатомов, выбранных из S, О и N, и где указанное кольцо может быть незамещенным или содержать один или более заместителей,
где предпочтительно, если (i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил, где каждый заместитель, если присутствует, выбран из группы, включающей галоген, С1-С3-алкил, С3-С7-циклоалкил, С3-С7-циклоалкил(С1-С3)алкил, С3-С7-гетероциклоалкил(С1-С3)алкил, C1-С3-алкоксигруппу и С1-С3-алкокси(С1-С3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и С1-С3-алкоксигруппы, или (ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, или
R7 выбран из группы, включающей Н, галоген, цианогруппу, C1-C6-алкил, С1-С6-алкоксигруппу, С2-С6-алкинил, С2-С6-алкенил, C1-C6-алкилкарбонил, С1-С6-алкоксикарбонил, C1-С6-алкилсульфонил, C1-С6-алкилсульфинил, С3-С7-циклоалкил, С3-С7-гетероциклоалкил, фенил, С5-С6-гетероарил, где каждая алкильная, алкенильная, алкинильная группа или алкоксигруппа может быть незамещенной или содержать один или более заместителей, выбранных из галогена и C1-С6-алкоксигруппы,
R8 выбран из водорода, C1-C6-алкила, C1-C6-алкоксигруппы и галогена, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы, или вместе с R9 образует кольцевую систему, как здесь описано,
R9 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, C1-C6-алкил, C1-C6-алкоксигруппу, С2-С6-алкенил, С2-С6-алкинил и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и С1-С3-алкоксигруппы,
или R9 вместе с R8 или R10 и с атомами С, к которым они присоединены, образуют 5- или 6-членное кольцо, которое необязательно может быть дополнительно замещенным и которое может содержать один или более образующих кольцо гетероатомов, выбранных из N, S, О и Se;
где кольцо, образованное с помощью R9 вместе с R8 или R10, и кольцо, к которому они присоединены, предпочтительно образуют бициклическую кольцевую систему, выбранную из группы, включающей (а) 2,1,3-бензотиадиазол, (b) 2,1,3-бензоселенадиазол, (с) 2,1,3-бензооксадиазол, (d) 1,3-бензотиазол, (е) 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и незамещенным или замещенным оксогруппой, (f) 1,3-бензодиоксол, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, (g) бензотиофен, который может быть незамещенным или может быть частично гидрированным и незамещенным или содержать один или два заместителя, выбранных из оксогруппы, метила или фтора, или (h) бензофуран, который может быть незамещенным или может быть частично гидрированным и незамещенным или замещенным одной или двумя группами, выбранными из оксогруппы, фтора и метила, предпочтительно одной оксогруппой,
R10 выбран из группы, включающей водород, галоген, C1-C6-алкил, C1-С6-алкоксигруппу, С2-С6-алкенил, С2-С6-алкинил, цианогруппу, циано(С1-С6)алкил, C1-C6-алкилкарбонил, C1-C6-алкоксикарбонил, C1-C6-алкилсульфонил, C1-С6-алкилсульфинил, азидогруппу, пентафторсульфанил и нитрогруппу, где каждый алкил, алкенил, алкинил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-C6-алкоксигруппы, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, C1-С6-алкил, C1-С6-алкоксигруппу, C1-С6-алкилкарбонил, C1-С6-алкоксикарбонил, С1-С6-алкилсульфонил и С1-С6-алкилсульфинил, С2-С6-алкенил и С2-С6-алкинил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы,
R12 выбран из водорода, C1-С6-алкила, C1-С6-алкоксигруппы и галогена, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
Обычно в соединениях, предлагаемых в настоящем изобретении, в которых R8 и R9 или R9 и R10 вместе образуют бициклическую кольцевую систему, такую как 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, дигидро(1,3)бензоксазол, 1,3-бензотиазол, дигидробензотиофен, дигидробензофуран, дигидроизоиндол или 1,3-бензодиоксол и им подобные, как здесь описано, все фенильные фрагменты этих бициклических групп обычно могут быть замещенными или незамещенными так, как это определено в настоящем изобретении в соответствующих определениях заместителей R8, R10, R11 и R12, тогда как аннелированные фрагменты дигидробензотиофена, дигидробензофурана, дигидробензоксазола или бензодиоксола, образованные с помощью R8 и R9 или R9 и R10 соответственно, необязательно могут быть замещенными, как это специально определено в настоящем изобретении. В качестве неограничивающего примера можно привести следующий: если с помощью R8 и R9 или R9 и R10 образован 1,3-дигидро-2-бензофуран и указано, что кольцо, к которому они присоединены необязательно замещено одной или двумя группами, выбранными из оксогруппы, фтора и метила, то эти конкретные заместители, оксогруппа, фтор или метил, являются заместителями кольца, образованного с помощью R8 и R9 или R9 и R10, и возможно, что фенильное кольцо, к которому присоединены R8 и R9 или R9 и R10, может быть независимо дополнительно замещено, как это определено в настоящем изобретении, остатками R8, R10, R11 и R12. Аналогичным образом, если, например, бензодиоксольная группа определена, как незамещенная, это будет относиться к кольцу, образованному с помощью R8 и R9 или R9 и R10, тогда как фенильное кольцо, к которому они присоединены, может быть замещенным в соответствии с определениями, приведенными в настоящем изобретении для R8, R10, R11 и R12.
В одном предпочтительном варианте осуществления, если R6 в соединениях формулы I обозначает водород и X1 обозначает N, то R5 отличается от водорода; в одном предпочтительном варианте осуществления R5 обозначает йод.
В одном варианте осуществления R5, R6 и R7, если присутствуют, все одновременно не обозначают водород.
В одном варианте осуществления R4, R5, R6 и R7, если присутствуют, все одновременно не обозначают водород.
В одном варианте осуществления R5, R6, R7 (если R7 содержится), R8, R9, R10 и R11 все одновременно не обозначают водород.
В одном предпочтительном варианте осуществления настоящего изобретения в соединении формулы I, или
(a) X1 обозначает CR7 и Х2 обозначает NH, S или О, или
(b) X1 обозначает N и Х2 обозначает NH.
В одном варианте осуществления настоящего изобретения, Х2 в соединении формулы I обозначает NH или О. В этом варианте осуществления X1 предпочтительно обозначает CR7. В одном варианте осуществления настоящего изобретения в соединении формулы I Х2 обозначает S. В этом варианте осуществления X1 предпочтительно обозначает CR7.
В одном варианте осуществления настоящего изобретения, Х2 в соединениях формулы I обозначает NH.
В одном варианте осуществления настоящего изобретения, Х2 в соединениях формулы I обозначает О. В этом варианте осуществления X1 предпочтительно обозначает CR7.
В одном предпочтительном варианте осуществления настоящего изобретения, если X1 в соединениях формулы I обозначает N, то Х2 также обозначает N. В этом варианте осуществления предпочтительно, если по меньшей мере один из R4, R5 и R6 отличается от водорода.
В предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, по меньшей мере один из R8, R9, R10 и R11 отличается от водорода. В другом предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода и незамещенного алкила.
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, не включают такие соединения, как N-3,4-дифторфенил-1Н-пирроло[2,3-b]пиридин-3-сульфонамид, N-(3,5-диметоксифенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид, N-(2,5-дифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид и N-(3,5-дифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид сами по себе, и как предназначенные для применения в качестве лекарственных средств или в качестве активного ингредиента в фармацевтической композиции в целом. В одном варианте осуществления в объем настоящего настоящее изобретения входят эти соединения, предназначенные для применения для предупреждения или лечения нарушения миелинизации, дополнительно определенного в настоящем изобретении, предпочтительно для предупреждения или лечения рассеянного склероза, и/или в способе лечения или предупреждения связанного с GPR17 нарушения, предпочтительно нарушения миелинизации, такого как, в частности, рассеянный склероз.
В одном предпочтительном варианте осуществления соединения, предлагаемые в настоящем изобретении, не включают [N-(4-метилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-[4-метокси-3-(2-метоксиэтокси)-фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-(4-метоксифенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], N-(4-фтор-2-метилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-(2-хлор-4-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-(6-бром-2-пиридинил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-(5-хлор-2-пиридинил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-(2,4-дихлорфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-(3-этилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], N-(2,5-диметилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-[4-(этилсульфонил)фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-(4-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], 1-[N-(3-хлор-4-метоксифенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-(2-этил-6-метилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-(2,4-дифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [N-[2-(трифторметокси)фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид], [6-амино-N-(3-бромфенил)-1Н-индол-3-сульфонамид], [6-амино-N-(2-фторфенил)-1Н-индол-3-сульфонамид], [6-амино-N-(3-бром-2-пиридинил)-1Н-индол-3-сульфонамид], [N-(4-хлор-2-метилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид] и [N-(4-пропилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид сами по себе, тогда как в другом варианте осуществления в объем настоящего изобретения входят эти конкретные соединения, предназначенные для применения (а) для терапии и/или диагностики, (b) для лечения или предупреждения нарушения миелинизации и/или любого другого заболевания или патологического состояния, связанного с GPR17, такого как нарушение функции GPR17, (с) в качестве активного ингредиента в фармацевтической композиции вместе с необязательными фармацевтическими носителями, и/или (d) в способе лечения или предупреждения связанного с GPR17 нарушения, такого как нарушение функции GPR17, предпочтительно нарушения миелинизации, такого как, в частности, рассеянный склероз.
В другом варианте осуществления в соединениях формулы I:
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, нитрогруппу, незамещенный или замещенный С1-С3-алкил, предпочтительно метил, этил, изопропил, моно-, ди- или трифторметил, незамещенный или замещенный С2-С3-алкенил, незамещенный или замещенный С2-С3-алкинил, незамещенный или замещенный С1-С3-алкилкарбонил, незамещенный или замещенный C1-С3-алкоксикарбонил, незамещенный или замещенный С1-С3-алкилсульфинил, предпочтительно метилсульфинил, который может быть дополнительно замещен 1-3 атомами фтора, незамещенный или замещенный C1-С3-алкилсульфонил, предпочтительно метилсульфонил, который может быть дополнительно замещен 1-3 атомами фтора, незамещенный или замещенный бензилсульфонил, незамещенный или замещенный бензилсульфинил, незамещенный или замещенный С3-С7-циклоалкил, предпочтительно циклопропил, незамещенный или замещенный С3-С7-циклоалкил(С1-С3)алкил, предпочтительно циклопропилметил, незамещенную или замещенную С3-С7-циклоалкил(С1-С3)алкилоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный С3-С7-гетероциклоалкил, предпочтительно тетрагидрофуранил, незамещенный или замещенный С3-С7-гетероциклоалкил(С1-С3)алкил, незамещенную или замещенную С3-С7-гетероциклоалкил(С1-С3)алкилоксигруппу, предпочтительно тетрагидрофуранилметоксигруппу, незамещенную или замещенную С1-С3-алкоксигруппу, предпочтительно метоксигруппу или этоксигруппу, каждая из которых необязательно может быть замещена одним или более атомами галогена, предпочтительно атомами фтора, незамещенную или замещенную С3-С6-циклоалкоксигруппу, незамещенную или замещенную С3-С6-гетероциклоалкоксигруппу, незамещенную или замещенную С1-С3-алкокси(С1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, незамещенный или замещенный С1-С3-алкокси(С1-С3)алкил, незамещенную или замещенную (С3-С6)циклоалкил(С1-С3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенную или замещенную (С3-C6)-гетероциклоалкил(С1-С3)алкоксигруппу, предпочтительно тетрагидрофуранилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенилоксигруппу, незамещенный или замещенный тиенил, незамещенный или замещенный пиридил, предпочтительно незамещенный пиридил, незамещенный или замещенный оксазол, незамещенный или замещенный тиазол, незамещенный или замещенный изоксазол, незамещенную или замещенную фенил(С1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, брома, незамещенного0 или фторированного метила, незамещенной или фторированной метоксигруппы, гидроксигруппы и цианогруппы,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из группы, включающей галоген, гидроксигруппу, C1-С3-алкил, С3-С7-циклоалкил, С3-С7-циклоалкил(С1-С3)алкил, С3-С7-гетероциклоалкил(С1-С3)алкил, С1-С3-алкоксигруппу и С1-С3-алкокси(С1-С3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и С1-С3-алкоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
где предпочтительно, что если R6 обозначает водород и X1 обозначает N, то R5 предпочтительно отличается от водорода, и более предпочтительно обозначает йод.
В другом варианте осуществления в соединении формулы I:
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный С1-С3-алкил, предпочтительно метил, этил, изопропил или трифторметил, незамещенный или замещенный С2-С3-алкенил, незамещенный или замещенный С2-С3-алкинил, незамещенный или замещенный С1-С3-алкилкарбонил, незамещенный или замещенный C1-С3-алкоксикарбонил, незамещенный или замещенный С1-С3-алкилсульфинил, предпочтительно метилсульфинил, незамещенный или замещенный C1-С3-алкилсульфонил, предпочтительно метилсульфонил, незамещенный или замещенный С3-С7-циклоалкил, предпочтительно циклопропил, незамещенный или замещенный С3-С7-циклоалкил(С1-С3)алкил, предпочтительно циклопропилметил, незамещенный или замещенный С3-С7-гетероциклоалкил, предпочтительно тетрагидрофуранил, незамещенный или замещенный С3-С7-гетероциклоалкил(С1-С3)алкил, незамещенную или замещенную C1-С3-алкоксигруппу, предпочтительно метоксигруппу, незамещенную или замещенную С3-С6-циклоалкоксигруппу, незамещенную или замещенную С3-С6-гетероциклоалкоксигруппу, незамещенную или замещенную С1-С3-алкокси(С1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, незамещенную или замещенную (С3-С6)циклоалкил(С1-С3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенную или замещенную (С3-С6)гетероциклоалкил(С1-С3)алкоксигруппу, предпочтительно тетрагидрофуранилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенилоксигруппу, незамещенный или замещенный тиенил, незамещенный или замещенный пиридил, предпочтительно незамещенный пиридил, незамещенный или замещенный оксазол, незамещенный или замещенный тиазол, незамещенный или замещенный изоксазол, незамещенную или замещенную фенил(С1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, брома, метила, метоксигруппы и цианогруппы,
или
(iii) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из группы, включающей галоген, C1-С3-алкил, С3-С7-циклоалкил, С3-С7-циклоалкил(С1-С3)алкил, С3-С7-гетероциклоалкил(С1-С3)алкил, С1-С3-алкоксигруппу и С1-С3-алкокси(С1-С3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы,
или
(iv) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
где предпочтительно, что если R6 обозначает водород и X1 обозначает N, то R5 предпочтительно отличается от водорода, и более предпочтительно обозначает йод.
В каждом случае, в котором соединения, предлагаемые в настоящем изобретении, содержат группу R6 и R7, которые вместе с образующими кольцо атомами бициклической кольцевой системы, к которой они присоединены, образуют другой цикл, выбранный из фенила, пиридила, циклопентила и циклогексила, этот цикл вместе с бициклическим фрагментом, с которым он аннелирован, образует трициклический фрагмент, который предпочтительно выбран из группы, включающей 1Н-бензо[g]индол-3-ил, 1Н-пирроло[3,2-h]хинолин-3-ил, 1,6,7,8-тетрагидроциклопента[g]индол-3-ил и 6,7,8,9-тетрагидро-1Н-бензо[g]индол-3-ил. В одном варианте осуществления любой заместитель, содержащийся в 1Н-пирроло[3,2-h]хинолин-3-ильном фрагменте, предпочтительно находится в положении 8 так, что в результате образуется, например, 8-(фторметил)-1Н-пирроло[3,2-h]хинолин.
В одном предпочтительном варианте осуществления в соединениях формулы I:
X1 обозначает N или C(R7),
Х2 обозначает NH, S или О, предпочтительно NH,
Х3 обозначает N или C(R12),
R4 выбран из водорода, метоксигруппы и галогена, и предпочтительно обозначает водород или фтор, наиболее предпочтительно водород,
R5 выбран из группы, включающей водород, галоген, цианогруппу, С1-С3-алкил, C1-С3-алкоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, С1-С3-алкилсульфинил и C1-С3-алкилсульфонил, где каждый алкил или алкоксигруппа необязательно может содержать один или более заместителей, выбранных из группы, включающей галоген, С1-С3-алкоксигруппу, цианогруппу, азидогруппу, C1-С3-алкиламиногруппу и ди(С1-С3-алкил)аминогруппу, предпочтительно метоксигруппы или галогена, или R5 вместе R6 образуют кольцо, как это описано ниже,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, нитрогруппу, незамещенный или замещенный С1-С3-алкил, предпочтительно метил, этил, изопропил, или моно-, ди- или трифторметил, незамещенную или замещенную С1-С3-алкоксигруппу, предпочтительно метоксигруппу, этоксигруппу, моно-, ди- или трифторметоксигруппу и моно-, ди- или трифторэтоксигруппу, незамещенный или замещенный С2-С3-алкенил, незамещенный или замещенный С2-С3-алкинил, незамещенный или замещенный С1-С3-алкилкарбонил, незамещенный или замещенный C1-С3-алкоксикарбонил, незамещенный или замещенный С1-С3-алкилсульфинил, предпочтительно метилсульфинил, незамещенный или замещенный C1-С3-алкилсульфонил, предпочтительно метилсульфонил, незамещенный или замещенный бензилсульфонил, незамещенный или замещенный бензилсульфинил, незамещенный или замещенный С3-С7-циклоалкил, предпочтительно циклопропил, незамещенный или замещенный С3-С7-циклоалкил(С1-С3)алкил, предпочтительно циклопропилметил, незамещенный или замещенный С3-С7-гетероциклоалкил, предпочтительно тетрагидрофуранил и оксетанил, незамещенный или замещенный С3-С7-гетероциклоалкил(С1-С3)алкил, незамещенную или замещенную С3-C6-циклоалкоксигруппу, незамещенную или замещенную С3-C6-гетероциклоалкоксигруппу, незамещенный или замещенный С1-С5-алкокси(С1-С5)алкил, незамещенную или замещенную С1-С3-алкокси(С1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, незамещенную или замещенную (С3-С6)циклоалкил(С1-С3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенную или замещенную (С3-С6)гетероциклоалкил(С1-С3)алкоксигруппу, предпочтительно тетрагидрофуранилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенилоксигруппу, незамещенный или замещенный тиенил, незамещенный или замещенный пиридил, предпочтительно незамещенный пиридил, незамещенный или замещенный оксазол, незамещенный или замещенный тиазол, незамещенный или замещенный изоксазол, незамещенную или замещенную фенил(С1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, где каждый необязательный заместитель, содержащийся в R6, предпочтительно представляет собой один или более заместителей, выбранных из фтора, хлора, брома, незамещенного или фторированного метила, незамещенной или фторированной метоксигруппы, гидроксигруппы и цианогруппы,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из группы, включающей галоген, гидроксигруппу, цианогруппу, C1-C6-алкил, C2-C6-алкенил, С2-С6-алкинил, С3-С7-циклоалкил, С3-С7-циклоалкил(С1-С3)алкил, С3-С7-гетероциклоалкил(С1-С3)алкил, C1-C6-алкоксигруппу и С1-С6-алкокси(С1-С3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и С1-С3-алкоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей Н, галоген, цианогруппу, С1-С3-алкил, С1-С3-алкоксигруппу, С1-С3-алкилкарбонил, С1-С3-алкоксикарбонил, С1-С3-алкилсульфонил, C1-С3-алкилсульфинил, С5-С6-гетероарил, предпочтительно изоксазол, и С5-С6-гетероарил(С1-С3)алкоксигруппу, предпочтительно пиридилметоксигруппу, где каждый алкильный или алкоксильный фрагмент может содержать один или более заместителей, предпочтительно выбранных из галогена, галоген(С1-С6)алкоксигруппы или C1-С3-алкоксигруппы, и где каждый гетероарил может содержать один или более заместителей, предпочтительно выбранных из галогена, метила, гидроксигруппы или метоксигруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из водорода, C1-С3-алкила, C1-С3-алкоксигруппы, цианогруппы и галогена, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, цианогруппы и метоксигруппы, или R8 вместе с R9 образуют кольцевую систему, как здесь описано,
R9 выбран из водорода, C1-С3-алкила, C1-С3-алкоксигруппы, фтора, хлора, брома и йода, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и метоксигруппы,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензотиазол, 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и замещенным оксогруппой с образованием 2-оксо-2,3-дигидро-1,3-бензоксазола, 1,3-бензодиоксол, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, предпочтительно с образованием 2,2-дифтор-1,3-бензодиоксола, 2,3-дигидробензотиофен, который может быть незамещенным или замещенным одной или двумя оксогруппами, предпочтительно с образованием 1,1-диоксидо-2,3-дигидро-1-бензотиофена, 1,3-дигидро-2-бензофуран, который может быть незамещенным или замещенным одной или двумя группами, выбранными из оксогруппы, фтора и метила, предпочтительно по меньшей мере одной оксогруппой, предпочтительно с образованием 3-оксо-1,3-дигидро-2-бензофурана или 1-метил-3-оксо-1,3-дигидро-2-бензофурана, и дигидроизоиндол, который может быть незамещенным или содержать один или два заместителя, выбранных из оксогруппы, фтора и метила, и который предпочтительно представляет собой 3-оксо-2,3-дигидро-1Н-изоиндол,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С5-алкил, предпочтительно C1-С3-алкил, C1-С5-алкоксигруппу, предпочтительно C1-С3-алкоксигруппу, С2-С4-алкенил, С2-С4-алкинил, С3-С4-циклоалкил, С3-С4-гетероциклоалкил, цианогруппу, цианометил, цианометоксигруппу, С1-С3-алкилкарбонил, С1-С3-алкоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, где каждый алкил, алкенил, алкинил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из группы, включающей галоген, незамещенную или фторированную С1-С3-алкоксигруппу, незамещенный или фторированный С1-С3-алкоксикарбонил, незамещенный или фторированный С1-С3-алкилкарбонил, цианогруппу, гидроксигруппу, циклопропил и пиридил, где пиридил необязательно может быть замещен галогеном, незамещенным или фторированным метилом и/или незамещенной или фторированной метоксигруппой, и где любой циклоалкил или гетероциклоалкил может быть незамещенным или замещенным группой, выбранной из галогена, цианогруппы, гидрокси(С1-С2)алкила, С1-С2-алкоксигруппы и С1-С2-алкоксикарбонила, или R10 вместе с R8 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, C1-С3-алкил, С1-С3-алкоксигруппу, фтор, хлор, бром, йод, цианогруппу, С1-С3-алкилкарбонил, С1-С3-алкоксикарбонил, где каждый алкил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора, хлора, брома, йода и С1-С3-алкоксигруппы,
R12, если присутствует, выбран из группы, включающей водород, С1-С3-алкил, C1-С3-алкоксигруппу, фтор, хлор, бром и йод, где каждый алкил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора, хлора, брома, йода и C1-С3-алкоксигруппы,
где в одном предпочтительном варианте осуществления, если R6 обозначает водород и X1 обозначает N, то R5 отличается от водорода и предпочтительно обозначает йод,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода и более предпочтительно, если по меньшей мере один из R8, R9, R10 и R11 также отличается от незамещенного алкила,
и где в другом предпочтительном варианте осуществления по меньшей мере один из R5, R6 и R7, если присутствует, отличается от водорода,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном предпочтительном варианте осуществления в соединениях формулы I:
X1 обозначает N или C(R7),
Х2 обозначает NH или О, предпочтительно NH,
Х3 обозначает N или C(R12),
R4 обозначает водород или фтор, предпочтительно водород,
R5 выбран из группы, включающей водород, галоген, цианогруппу, С1-С3-алкил, С1-С3-алкоксигруппу, С1-С3-алкилкарбонил, С1-С3-алкоксикарбонил, С1-С3-алкилсульфинил и C1-С3-алкилсульфонил, где каждый алкил или алкоксигруппа необязательно может содержать один или более заместителей, выбранных из галогена, C1-С3-алкоксигруппы, цианогруппы, азидогруппы, необязательно алкилированной аминогруппы, предпочтительно метоксигруппы или галогена, или R5 вместе с R6 образуют кольцо, как это описано ниже,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-С3-алкил, предпочтительно метил, этил, изопропил или трифторметил, незамещенную или замещенную C1-С3-алкоксигруппу, предпочтительно метоксигруппу, незамещенный или замещенный С2-С3-алкенил, незамещенный или замещенный С2-С3-алкинил, незамещенный или замещенный С1-С3-алкилкарбонил, незамещенный или замещенный C1-С3-алкоксикарбонил, незамещенный или замещенный C1-С3-алкилсульфинил, предпочтительно метилсульфинил, незамещенный или замещенный C1-С3-алкилсульфонил, предпочтительно метилсульфонил, незамещенный или замещенный С3-С7-циклоалкил, предпочтительно циклопропил, незамещенный или замещенный С3-С7-циклоалкил(С1-С3)алкил, предпочтительно циклопропилметил, незамещенный или замещенный С3-С7-гетероциклоалкил, предпочтительно тетрагидрофуранил, незамещенный или замещенный С3-С7-гетероциклоалкил(С1-С3)алкил, незамещенную или замещенную С3-С6-циклоалкоксигруппу, незамещенную или замещенную С3-С6-гетероциклоалкоксигруппу, незамещенную или замещенную С1-С3-алкокси(С1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, незамещенную или замещенную (С3-С6)циклоалкил(С1-С3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенную или замещенную (С3-С6)гетероциклоалкил(С1-С3)алкоксигруппу, предпочтительно тетрагидрофуранилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенилоксигруппу, незамещенный или замещенный тиенил, незамещенный или замещенный пиридил, предпочтительно незамещенный пиридил, незамещенный или замещенный оксазол, незамещенный или замещенный тиазол, незамещенный или замещенный изоксазол, незамещенную или замещенную фенил(С1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, брома, метила, метоксигруппы и цианогруппы,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из группы, включающей галоген, C1-С3-алкил, С3-С7-циклоалкил, С3-С7-циклоалкил(С1-С3)алкил, С3-С7-гетероциклоалкил(С1-С3)алкил, C1-С3-алкоксигруппу и С1-С3-алкокси(С1-С3)алкил,
где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и С1-С3-алкоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образует 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей Н, галоген, цианогруппу, С1-С3-алкил, C1-С3-алкоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, С1-С3-алкилсульфонил, и C1-С3-алкилсульфинил, где каждый алкильный или алкоксильный фрагмент может содержать один или более заместителей, предпочтительно галоген или C1-С3-алкоксигруппу, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из водорода, C1-С3-алкила, C1-С3-алкоксигруппы и галогена, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, цианогруппы и метоксигруппы, или R8 вместе с R9 образуют кольцевую систему, как здесь описано,
R9 выбран из водорода, C1-С3-алкила, C1-С3-алкоксигруппы, фтора, хлора, брома и йода, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и метоксигруппы,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензооксадиазол, 1,3-бензотиазол, 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и замещенным оксогруппой, 1,3-бензодиоксол, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, 2,3-дигидробензотиофен, который может быть незамещенным или замещенным одной или двумя оксогруппами, и 1,3-дигидро-2-бензофуран, который может быть незамещенным или замещенным одной или двумя группами, выбранными из оксогруппы, фтора и метила, предпочтительно одной оксогруппой,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, C1-С3-алкоксигруппу, С2-С4-алкенил, С2-С4-алкинил, цианогруппу, цианометил, С1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, где каждый алкил, алкенил, алкинил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы, или R10 вместе с R8 образуют кольцевую систему, как здесь описано,
R11 выбран из водорода, C1-С3-алкила, C1-С3-алкоксигруппы, фтора, хлора, брома, йода, C1-С3-алкилкарбонила, C1-С3-алкоксикарбонила, где каждый алкил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора, хлора, брома, йода и C1-С3-алкоксигруппы,
R12 выбран из водорода, C1-С3-алкила, C1-С3-алкоксигруппы, фтора, хлора, брома и йода, где каждый алкил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора, хлора, брома, йода и C1-С3-алкоксигруппы,
где, если R6 обозначает водород и X1 обозначает N, то R5 предпочтительно отличается от водорода, и особенно предпочтительно обозначает йод,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода, и более предпочтительно если по меньшей мере один из R8, R9, R10 и R11 также отличается от незамещенного алкила,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
Другой вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH, S, или О, предпочтительно NH,
Х3 обозначает N или C(R12),
R4 обозначает водород или фтор, предпочтительно водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, незамещенный или фторированный С1-С2-алкил, предпочтительно метил или трифторметил, незамещенную или фторированную С1-С2-алкилоксигруппу, незамещенный или фторированный С1-С2-алкилкарбонил, незамещенный или фторированный С1-С2-алкилоксикарбонил, С1-С2-алкилсульфинил, предпочтительно метилсульфинил, и С1-С2-алкилсульфонил, предпочтительно метилсульфонил, где R5 предпочтительно выбран из водорода, метила, фтора, хлора, брома и йода, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный С1-С3-алкил, предпочтительно метил, этил, изопропил или трифторметил, незамещенный или фторированный С1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный С1-С3-алкоксикарбонил, предпочтительно метоксикарбонил, незамещенный или фторированный(С1-С3)алкилсульфинил, предпочтительно метилсульфинил, незамещенный или фторированный (С1-С3)алкилсульфонил, предпочтительно метилсульфонил, незамещенный или замещенный С3-C6-циклоалкил, предпочтительно циклопропил, незамещенный или замещенный С3-С6-циклоалкил(С1-С3)алкил, предпочтительно циклопропилметил, незамещенный или замещенный С3-С6-гетероциклоалкил, незамещенную или замещенную С3-С6-циклоалкоксигруппу, незамещенную или замещенную С3-C6-гетероциклоалкоксигруппу, незамещенную или замещенную С1-С3-алкоксигруппу, предпочтительно метоксигруппу, этоксигруппу, фторметоксигруппу, и фторэтоксигруппу, незамещенную или замещенную С1-С3-алкокси(С1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, незамещенный или замещенный С1-С3-алкокси(С1-С3)алкил, незамещенную или замещенную С3-С6-циклоалкил(С1-С3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенил(С1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, незамещенную или замещенную фенилоксигруппу, незамещенный или замещенный фенил(С1-С3)алкилсульфонил, предпочтительно бензилсульфонил, незамещенный или замещенный фенил(С1-С3)алкилсульфинил, предпочтительно бензилсульфинил, незамещенный или замещенный тиенил, пиридил, оксазол, тиазол и изоксазол, и где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, незамещенного или фторированного метила, незамещенной или фторированной метоксигруппы, гидроксигруппы и цианогруппы,
при условии, что если R6 обозначает водород и X1 обозначает N, то R5 предпочтительно отличается от водорода, и предпочтительно обозначает йод,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из галогена, гидроксигруппы, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, предпочтительно фтора, и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-С3-алкил, предпочтительно метил, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С3)алкил, предпочтительно моно-, ди- или трифторметил, фтор(С1-С3)алкоксигруппу, предпочтительно моно-, ди- или трифторметоксигруппу и моно-, ди- и трифторэтоксигруппу, незамещенный или фторированный C1-С3-алкилкарбонил, незамещенный или фторированный C1-С3-алкоксикарбонил, метилсульфинил, метилсульфонил, фторированный метилсульфинил, фторированный метилсульфонил, замещенный или незамещенный С5-С6-гетероарил, замещенную или незамещенную С5-С6-гетероарилоксигруппу и С5-С6-гетероарилметоксигруппу, где гетероарил предпочтительно выбран из пиридила, оксазола и изоксазола, и где гетероарил может содержать один или более заместителей, выбранных из галогена, незамещенного или фторированного метила, незамещенной или фторированной метоксигруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, С1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С3)алкоксигруппу, C1-С3-алкил, предпочтительно метил, и фтор(С1-С3)алкил, предпочтительно трифторметил, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 выбран из группы, включающей водород,2 фтор, хлор, бром, йод, С1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С3)алкоксигруппу, С1-С3-алкил, предпочтительно метил, цианогруппу, и фтор(С1-С3)алкил, предпочтительно трифторметил, и предпочтительно обозначает водород, фтор, хлор или бром,
или R9 вместе с R8 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и замещенным оксогруппой (с образованием 2-оксо-2,3-дигидро-1,3-бензоксазола), и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образует бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензотиазол, 3-оксо-2,3-дигидро-1H-изоиндол, 2,3-дигидро-1-бензотиофен, который замещен одной или двумя оксогруппами (предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксо-2,3-дигидро-1-бензотиофена), 3-оксо-1,3-дигидро-2-бензофуран, который необязательно замещен метилом с образованием 1-метил-3-оксо-1,3-дигидро-2-бензофурана, и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, галоген(С1-С3)алкил, предпочтительно фтор(С1-С3)алкил, особенно предпочтительно трифторметил, С2-С3-алкинил, C1-С3-алкилоксигруппу, галоген(С1-С3)алкилоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, циклопропилцианогруппу, цианометил, цианоэтил, незамещенный или фторированный С1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный С1-С3-алкоксикарбонил, предпочтительно метоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, где каждый алкил, циклопропил, алкоксигруппа, алкенил или алкинил, содержащийся R10, если не указано иное, необязательно может дополнительно содержать один или более заместителей, выбранных из группы, включающей фтор, хлор, цианогруппу, гидроксигруппу, C1-С3-алкоксигруппу, предпочтительно метоксигруппу, галоген, C1-С3-алкоксигруппу, и незамещенный или фторированный С1-С3-алкоксикарбонил, где каждый алкил и алкоксигруппа также могут быть замещены циклопропилом, который необязательно может быть замещен, как это определено выше, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, предпочтительно метил, фтор(С1-С3)алкил, предпочтительно фторированный метил, такой как трифторметил, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С3)алкоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, незамещенный или фторированный С1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-С3-алкоксикарбонил, предпочтительно метоксикарбонил, и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкил, предпочтительно метил, фтор(С1-С3)алкил, предпочтительно трифторметил, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С3) алкоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода и более предпочтительно, если по меньшей мере один из R8, R9, R10 и R11 также отличается от незамещенного алкила,
и где в другом предпочтительном варианте осуществления по меньшей мере один из R5, R6 и R7, если присутствует, отличается от водорода и где в одном предпочтительном варианте осуществления, если X1 обозначает N, то Х2 обозначает NH,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH или О, предпочтительно NH,
Х3 обозначает N или C(R12),
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, незамещенный или фторированный С1-С2-алкил, предпочтительно метил или трифторметил, незамещенную или фторированную С1-С2-алкилоксигруппу, незамещенный или фторированный С1-С2-алкилкарбонил, незамещенный или фторированный С1-С2-алкилоксикарбонил, С1-С2-алкилсульфинил, предпочтительно метилсульфинил, и С1-С2-алкилсульфонил, предпочтительно метилсульфонил, предпочтительно обозначает водород, метил или йод, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-С3-алкил, предпочтительно метил, этил, изопропил или трифторметил, незамещенный или фторированный C1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-С3-алкоксикарбонил, предпочтительно метоксикарбонил, (С1-С3)алкилсульфинил, предпочтительно метилсульфинил, (С1-С3)алкилсульфонил, предпочтительно метилсульфонил, С3-С6-циклоалкил, предпочтительно циклопропил, С3-С6-циклоалкил(С1-С3)алкил, предпочтительно циклопропилметил, С3-С6-гетероциклоалкил, С3-С6-циклоалкоксигруппу, С3-C6-гетероциклоалкоксигруппу, незамещенную или замещенную С1-С3-алкоксигруппу, предпочтительно метоксигруппу, незамещенную или замещенную С1-С3-алкокси(С1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, С3-С6-циклоалкил(С1-С3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенил(С1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, незамещенную или замещенную фенилоксигруппу, незамещенный или замещенный тиенил, пиридил, оксазол, тиазол и изоксазол, и где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, метила, метоксигруппы и цианогруппы,
при условии, что если R6 обозначает водород и X1 обозначает N, то R5 предпочтительно отличается от водорода, и предпочтительно обозначает йод,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из галогена, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-С3-алкил, C1-С3-алкилоксигруппу, фтор(С1-С3)алкил, предпочтительно трифторметил, фтор(С1-С3)алкоксигруппу, предпочтительно трифторметоксигруппу, незамещенный или фторированный С1-С3-алкилкарбонил, незамещенный или фторированный С1-С3-алкоксикарбонил, метилсульфинил и метилсульфонил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С3)алкоксигруппу, C1-С3-алкил, предпочтительно метил, и фтор(С1-С3)алкил, предпочтительно трифторметил, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С3)алкоксигруппу, C1-С3-алкил, предпочтительно метил, цианогруппу, и фтор(С1-С3)алкил, предпочтительно трифторметил, и предпочтительно обозначает водород, фтор, хлор или бром,
или R9 вместе с R8 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензооксадиазол, 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и замещенным оксогруппой (с образованием 2-оксо-2,3-дигидро-1,3-бензоксазола), и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензооксадиазол, 1,3-бензотиазол, 2,3-дигидро-1-бензотиофен, который замещен одной или двумя оксогруппами (предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксо-2,3-дигидро-1-бензотиофена), 3-оксо-1,3-дигидро-2-бензофуран, и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, галоген(С1-С3)алкил, предпочтительно фтор(С1-С3)алкил, особенно предпочтительно трифторметил, С2-С3-алкинил, C1-С3-алкилоксигруппу, галоген(C1-С3)алкилоксигруппу, предпочтительно фтор(C1-С2)алкоксигруппу, цианогруппу, цианометил, незамещенный или фторированный С1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный С1-С3-алкоксикарбонил, предпочтительно метоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, предпочтительно метил, фтор(С1-С3)алкил, предпочтительно трифторметил, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, незамещенный или фторированный C1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-С3-алкоксикарбонил, предпочтительно метоксикарбонил, и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкил, предпочтительно метил, фтор(C1-С3)алкил, предпочтительно трифторметил, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3) алкоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода, и более предпочтительно, если по меньшей мере один из R8, R9, R10 и R11 также отличается от незамещенного алкила,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
В одном предпочтительном варианте осуществления в соединениях формулы I, описанной в настоящем изобретении, если Х2 обозначает О, то X1 обозначает C(R7).
Другой вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH, S или О при условии, что, если X1 обозначает N, то Х2 предпочтительно также обозначает N,
Х3 обозначает N или C(R12),
R4 обозначает водород или фтор, предпочтительно водород,
R5 выбран из водорода, метила, фтора, хлора и брома,
или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, галоген, цианогруппу, нитрогруппу, азидогруппу, C1-С3-алкил, C1-С3-алкилсульфинил, предпочтительно метилсульфинил, C1-С3-алкилсульфонил, предпочтительно метилсульфонил, циклопропил, циклопропилметил, циклопропилоксигруппу, C1-С3-алкоксигруппу, предпочтительно метоксигруппу или этоксигруппу, фенил, фенилоксигруппу, бензил, фенил(C1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, бензилсульфинил, бензилсульфонил, тетрагидрофуранил, и 5-6-членный гетероарил, предпочтительно выбранный из тиенила, пиридила, оксазола и изоксазола, и где каждая алкильная группа, алкоксигруппа, циклопропильная, тетрагидрофуранильная, фенильная или гетероарильная группа необязательно может содержать один или более заместителей, выбранных из группы, включающей фтор, хлор, гидроксигруппу, незамещенный или фторированный С1-С2-алкил, незамещенную или фторированную С1-С2-алкоксигруппу и цианогруппу,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из галогена, гидроксигруппы, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, предпочтительно фтора, и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образует 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей водород, галоген, цианогруппу, C1-С3-алкил, C1-С3-алкилоксигруппу, фтор(C1-С3)алкил, предпочтительно моно-, ди- и трифторметил, фтор(C1-С3)алкоксигруппу, предпочтительно моно-, ди- и трифторметоксигруппу или моно-, ди- и трифторэтоксигруппу, незамещенный или фторированный метилсульфинил, незамещенный или фторированный метилсульфонил, С5-С6-гетероарил, С5-С6-гетероарилоксигруппу, C5-C6-гетроарилметил и С5-С6-гетероарилметоксигруппу, где гетероарил (в каждом случае содержащийся в R7) предпочтительно выбран из пиридила, оксазола и изоксазола, и где гетероарил является незамещенным или содержит один или более заместителей, выбранных из галогена, цианогруппы, незамещенного или фторированного метила и незамещенной или фторированной метоксигруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, предпочтительно фторметоксигруппу, и незамещенный или фторированный C1-С3-алкил, предпочтительно фторметил, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 выбран из водорода, фтора, хлора, метоксигруппы, фторметоксигруппы, метила и фторметила,
или R9 вместе с R8 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и замещенным оксогруппой (с образованием 2-оксо-2,3-дигидро-1,3-бензоксазола), и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образует бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензотиазол, 3-оксо-2,3-дигидро-1H-изоиндол, 2,3-дигидро-1-бензотиофен, который замещен одной или двумя оксогруппами (предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксо-2,3-дигидро-1-бензотиофена), 3-оксо-1,3-дигидро-2-бензофуран, который необязательно замещен метилом с образованием 1-метил-3-оксо-1,3-дигидро-2-бензофурана, и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
R10 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, пентафторсульфанил, нитрогруппу, C1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, C1-С3-алкилкарбонил, предпочтительно ацетил, С3-С6-циклоалкил, предпочтительно циклоалкил, С3-С6-циклоалкилоксигруппу, предпочтительно циклоалкилоксигруппу, С3-С6-гетероциклоалкил, С3-С6-гетероциклоалкилоксигруппу, где каждый циклоалкил необязательно содержит один или более заместителей, выбранных из группы, включающей фтор, цианогруппу, незамещенную или фторированную С1-С2-алкоксигруппу и незамещенный или фторированный С1-С2-алкоксикарбонил, и где каждый алкил, алкоксигруппа, алкенил или алкинил, содержащийся в R10, необязательно может дополнительно содержать один или более заместителей, выбранных из группы, включающей циклопропил, галоген предпочтительно фтор, цианогруппу, гидроксигруппу, C1-С3-алкоксигруппу, галоген(C1-С3)алкоксигруппу, предпочтительно фтор(C1-С3)алкоксигруппу, незамещенный или фторированный C1-С3-алкилкарбонил и незамещенный или фторированный C1-С3-алкоксикарбонил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, фтор, хлор, бром, C1-С3-алкил, предпочтительно метил, фтор(C1-С3)алкил, предпочтительно фторметил, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, предпочтительно фторметоксигруппу, и цианогруппу,
R12, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, метил, фторметил, метоксигруппу и фторметоксигруппу, где предпочтительно, если R12 обозначает водород или фтор,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам;
где в предпочтительном варианте осуществления по меньшей мере один, более предпочтительно два из R8, R10 и R11 отличаются от водорода, и более предпочтительно, если по меньшей мере один из R8, R10 и R11 также отличается от незамещенного алкила,
и где в другом предпочтительном варианте осуществления по меньшей мере один из R5, R6 и R7, если присутствует, отличается от водорода,
Другой вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH, S или О, предпочтительно NH или О,
Х3 обозначает N или C(R12),
R4 обозначает водород,
R5 выбран из водорода, фтора, хлора и брома,
R6 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, азидогруппу, аминогруппу, нитрогруппу, метил, этил, н-пропил, изопропил, трифторметил, этенил, этинил, пропаргил, метилсульфинил, метилсульфонил, циклопропил, циклопропилоксигруппу, циклопропилметил, метоксигруппу, этоксигруппу, пропоксигруппу, метоксиэтоксигруппу, этоксиметоксигруппу, циклопропилметоксигруппу, оксетанил, оксетанилметоксигруппу, тетрагидрофуранил, тетрагидрофуранилметоксигруппу, фенил, бензилоксигруппу, фенилоксигруппу, бензилсульфинил, тиенил, пиридил, оксазол, тиазол и изоксазол, где каждый фенил, тиенил, пиридил, оксазол, тиазол и изоксазол необязательно может содержать один или более заместителей, предпочтительно заместителей, выбранных из галогена, метоксигруппы и метила, и где каждая алкильная, алкенильная, алкинильная группа и алкоксигруппа может быть замещена одним или более атомами галогена, предпочтительно фтора, метоксигруппой, фторметоксигруппой и гидроксигруппой,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из фенила, пиридила, циклогексила и циклопентила, каждый из которых может быть незамещенным или дополнительно замещенным одним или несколькими остатками, выбранными из группы, включающей галоген, гидроксигруппу, незамещенный или фторированный метил и незамещенную или фторированную метоксигруппу,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, метилсульфинил, метилсульфонил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, метил, фторметил и фторэтил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, фторметоксигруппу, цианогруппу, метил и фторметил, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 выбран из водорода, фтора и хлора, и предпочтительно обозначает водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол и 1,3-бензодиоксол, который необязательно замещен двумя атомами фтора,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 3-оксо-2,3-дигидро-1H-изоиндол, 2,3-дигидро-1-бензотиофен, который замещен одной или двумя оксогруппами (предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксо-2,3-дигидро-1-бензотиофена), и необязательно метилированный 3-оксо-1,3-дигидро-2-бензофуран,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, этил, н-пропил, изопропил, этенил, н-пропенил, изопропинил, этинил, пропаргил, фтор(C1-С3)алкил, предпочтительно трифторметил, метоксигруппу, этоксигруппу, пропоксигруппу, фтор(C1-С3)алкоксигруппу C1-С3-алкокси(C1-С3)алкил, C1-С3-алкокси(C1-С3)алкоксигруппу, C1-С3-алкокси(С2-С3)алкенил, C1-С3-алкокси(С2-С3)алкинил, C1-С3-алкоксикарбонил(C1-С3)алкил, C1-С3-алкилкарбонил(С1-С3)алкил, С1-С3-алкилкарбонил(С1-С3)алкилоксигруппу, цианогруппу, ацетил, азидогруппу, нитрогруппу, пентафторсульфанил, циклопропил, циклопропилоксигруппу, циклопропилметоксигруппу, и C1-С3-алкоксикарбонил, включая метоксикарбонил, где каждая алкильная, алкенильная, алкинильная группа и алкоксигруппа, содержащаяся в R10, может быть незамещенной или замещенной одним или несколькими остатками, выбранными из галогена, предпочтительно фтора, цианогруппы и/или гидроксигруппы, и где циклопропил необязательно замещен одним или несколькими остатками, выбранными из цианогруппы, необязательно фторированной С1-С2-алкоксигруппы и необязательно фторированного С1-С2-алкоксикарбонила, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, метил, фторметил, метоксигруппу и фторметоксигруппу,
R12, если присутствует, выбран из водорода, фтора, хлора и брома, и предпочтительно обозначает водород или фтор,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11, более предпочтительно по меньшей мере один или по меньшей мере два из них, наиболее предпочтительно все R8, R10 и R11 отличаются от водорода, и по меньшей мере один, предпочтительно по меньшей мере два из R8, R10 и R11 также предпочтительно отличаются от незамещенного алкила,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH, S или О, предпочтительно NH или О,
Х3 обозначает N или C(R12),
R4 обозначает водород,
R5 выбран из водорода, фтора, хлора и брома,
R6 выбран из группы, включающей фтор, хлор, бром, азидогруппу, нитрогруппу, метил, этил, изопропил, трифторметил, метилсульфинил, метилсульфонил, циклопропил, метоксигруппу, фенил, бензилоксигруппу, фенилсульфинил, бензилсульфинил, тиофен-2-ил и тиофен-3-ил, где каждая алкильная группа и алкоксигруппа, содержащаяся R6, может быть замещена одним или более атомами фтора, метоксигруппы, цианогруппы и гидроксигруппы,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из фенила, пиридила, циклогексила и циклопентила, каждый из которых необязательно замещен одной или более группами, выбранными из метила, фторированного метила, метоксигруппы, фторированной метоксигруппы и фтора,
R7 выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, метил, этил, метилсульфонил, метилсульфинил, метоксигруппу, этоксигруппу, моно-, ди- и трифторметоксигруппу, моно-, ди- и трифторэтоксигруппу, моно-, ди- и трифторметил, моно-, ди- и трифторэтил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу, цианогруппу, и моно-, ди- и трифторметил, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 обозначает водород или фтор, предпочтительно водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 1,3-бензодиоксол или 2,2-дифтор-1,3-бензодиоксол,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 3-оксо-2,3-дигидро-1H-изоиндол, 3-оксо-1,3-дигидро-2-бензофуран и 1-метил-3-оксо-1,3-дигидро-2-бензофуран,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, этил, пропил, этенил, пропенил, этинил, пропаргил, метоксигруппу, этоксигруппу, пропилоксигруппу, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, фтор(C1-С3)алкил, включая трифторметил, фторированную и/или гидроксилированную C1-С3-алкоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, незамещенный или фторированный и/или гидроксилированный С1-С2-алкокси(C1-С3)алкил, предпочтительно метоксипропил, этоксиэтил и фторметоксиметил, незамещенную или фторированную и/или гидроксилированную С1-С2-алкокси(C1-С3)алкоксигруппу, предпочтительно фторметоксиэтоксигруппу, незамещенный или фторированный и/или гидроксилированный С1-С2-алкокси(С2-С3)алкенил, предпочтительно метоксипропенил и этоксиэтенил, С1-С2-алкоксициклопропил, С1-С2-алкоксикарбонилциклопропил, циклопропил(С1-С2)алкоксигруппу, ацетил, азидогруппу и пентафторсульфанил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано, и где в предпочтительном варианте осуществления R8 и R10 оба не обозначают водород,
R11 выбран из водорода, фтора, фторметила, хлора, метоксигруппы и фторметоксигруппы,
R12, если присутствует, выбран из водорода и фтора,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам,
где в одном предпочтительном варианте осуществления, если R9 не образуют кольцо вместе с R8, то R10 отличается от водорода.
Один вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH, S или О, предпочтительно NH или О, предпочтительно NH,
R4 обозначает водород,
R5 выбран из водорода, фтора, хлора и брома,
R6 выбран из группы, включающей фтор, бром, хлор, нитрогруппу, азидогруппу, цианогруппу, метил, фторметил, этил, фторэтил, изопропил, циклопропил, циклопропилметил, циклопропилметоксигруппу, метоксигруппу, этоксигруппу, фторметоксигруппу, фторэтоксигруппу, метилсульфинил, метилсульфонил, бензилоксигруппу, тиенил, и предпочтительно обозначает хлор,
R7 выбран из группы, включающей водород, метоксигруппу, фтор, хлор, бром, цианогруппу, фторметоксигруппу, фторэтоксигруппу, и моно-, ди- и трифторметил,
Х3 обозначает N или C(R12),
R8 выбран из водорода, фтора, хлора и метоксигруппы,
R9 обозначает водород или фтор, предпочтительно водород,
R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, азидогруппу, метил, этил, пропил, этенил, пропенил, этинил, пропаргил, моно-, ди- и трифторметил, циклопропилметоксигруппу, циклопропилэтоксигруппу, метоксициклопропил, этоксициклопропил, метоксикарбонилциклопропил, этоксикарбонил-циклопропил, моно-, ди- и трифторметоксигруппу, моно-, ди-, и трифторэтоксигруппу, этоксиметил, метоксиэтил, этоксиэтил, метоксипропил, фторэтоксиметил, фторметоксиэтил, фторэтиксиэтил, фторметоксипропил, этоксиметоксигруппу, метоксиэтоксигруппу, метоксипропоксигруппу, фторэтоксиметоксигруппу, фторметоксиэтоксигруппу, фторметоксипропоксигруппу, метоксиэтенил, метоксипропенил, фторметоксиэтенил, фторметоксиэтенил, этинил, пропаргил и пентафторсульфанил,
R11 выбран из водорода, фтора, хлора, фторметила, метоксигруппы и фторметоксигруппы,
R12, если присутствует, обозначает водород или фтор, предпочтительно водород
где в предпочтительном варианте осуществления по меньшей мере один из R8, и R11 отличается от водорода,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N, или C(R7),
Х2 обозначает NH, S или О, предпочтительно NH,
R4 и R5 оба обозначают водород,
R6 обозначает метоксигруппу, хлор или бром, предпочтительно хлор,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
Х3 обозначает N или C(R12),
R9 вместе с R8 и с фенильным кольцом, к которому R8 и R9 присоединены, образуют 2,1,3-бензотиадиазол, 1,3-бензодиоксол или 2,2-дифтор-1,3-бензодиоксол,
R10 обозначает водород или фтор,
R11 выбран из водорода, фтора, цианогруппы и метоксигруппы, и предпочтительно обозначает водород,
R12, если присутствует, обозначает водород или фтор, предпочтительно водород,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH, S или О,
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, цианогруппу, азидогруппу, метил, этил, изопропил, фторметил, циклопропил, метоксигруппу, фторметоксигруппу, метилсульфинил, метилсульфонил, тиен-2-ил, тиен-3-ил и бензилоксигруппу, и предпочтительно обозначает хлор или бром,
R7 выбран из группы, включающей водород, метоксигруппу, фтор, хлор, бром, цианогруппу, моно-, ди- и трифторметил, метилсульфинил, метилсульфонил и фтор(С1-С2)алкоксигруппу,
Х3 обозначает N или C(R12),
R8 выбран из фтора и метоксигруппы,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, азидогруппу, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, циклопропил(С1-С2)алкил, циклопропил(С1-С2)алкоксигруппу, С1-С2-алкоксициклопропил, С1-С2-алкоксикарбонилциклопропил, незамещенный или фторированный C1-С3-алкил, предпочтительно метил, этил и фторметил, незамещенную или фторированную С1-С3-алкоксигруппу, предпочтительно метоксигруппу, дифторметоксигруппу, дифторэтоксигруппу и трифторэтоксигруппу, незамещенный или фторированный С2-С3-алкенил, незамещенный или фторированный С2-С3-алкинил, незамещенный или фторированный C1-С3-алкокси(C1-С3)алкил, предпочтительно метоксипропил, этоксиэтил и фторметоксиметил, незамещенную или фторированную C1-С3-алкокси(C1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу и фторметоксиэтоксигруппу, незамещенный или фторированный C1-С3-алкокси(С2-С3)алкенил, предпочтительно метоксипропенил, этоксиэтенил и фторметоксипропенил, и пентафторсульфанил,
R11 выбран из водорода, фтора и метоксигруппы,
R12, если присутствует, обозначает водород,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH или О,
Х3 обозначает N или C(R12),
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, азидогруппу, метил, этил, изопропил, трифторметил, метилсульфинил, метилсульфонил, циклопропил, циклопропилметил, метоксигруппу, этоксигруппу, метоксиэтоксигруппу, циклопропилметоксигруппу, фенил, бензилоксигруппу, фенилоксигруппу, тиенил, пиридил, оксазол, тиазол и изоксазол,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из фенила, пиридила и циклопентила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, дифторметоксигруппу, трифторметоксигруппу, метил, дифторметил и трифторметил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, метил и трифторметил, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 выбран из водорода, фтора и хлора, и предпочтительно обозначает водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензооксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол и 1,3-бензодиоксол, который необязательно замещен двумя атомами фтора,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, этинил, пропаргил, фтор(С1-С2)алкил, предпочтительно трифторметил, метоксигруппу, фтор(С1-С2)алкоксигруппу, цианогруппу, цианометил, ацетил, азидогруппу, пентафторсульфанил и метоксикарбонил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из водорода, фтора, хлора, брома и метоксигруппы,
R12 выбран из водорода, фтора, хлора или брома,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода и незамещенного алкила,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH или О,
Х3 обозначает N или C(R12),
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, азидогруппу, метил, изопропил, трифторметил, метилсульфонил, циклопропил, метоксигруппу, фенил, бензилоксигруппу, тиофен-2-ил и тиофен-3-ил,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из фенила, пиридила и циклопентила,
R7 выбран из водорода, фтора, хлора и метоксигруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из водорода, фтора, хлора, брома, метоксигруппы и трифторметила, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 обозначает водород или фтор, предпочтительно водород, или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензооксадиазол, 1,3-бензодиоксол или 2,2-дифтор-1,3-бензодиоксол, R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, этинил, пропаргил, метоксигруппу, цианогруппу, цианометил, трифторметил, фтор(С1-С2)алкоксигруппу, ацетил, азидогруппу и пентафторсульфанил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано, и где в предпочтительном варианте осуществления R8 и R10 оба не обозначают водород,
R11 выбран из водорода, фтора, хлора и метоксигруппы,
R12 выбран из водорода и фтора,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH или О, предпочтительно NH,
R4 и R5 оба обозначают водород,
R6 обозначает бром или хлор, предпочтительно хлор,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
Х3 обозначает N или C(R12),
R8 выбран из водорода, фтора, хлора и метоксигруппы,
R9 обозначает водород или фтор, предпочтительно водород,
R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, трифторметил, дифторэтоксигруппу, трифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, фтора, хлора и метоксигруппы,
R12 обозначает водород или фтор, предпочтительно водород,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N, или C(R7),
Х2 обозначает NH или О, предпочтительно NH,
R4 и R5 оба обозначают водород,
R6 обозначает хлор или бром, предпочтительно хлор,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
Х3 обозначает N или C(R12),
R9 вместе с R8 и с фенильным кольцом, к которому R8 и R9 присоединены, образуют 2,1,3-бензотиадиазол или 2,2-дифтор-1,3-бензодиоксол,
R10 обозначает водород или фтор,
R11 выбран из водорода, фтора и метоксигруппы,
R12 обозначает водород или фтор, предпочтительно водород,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления относится к соединениям формулы I, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH,
R4 и R5 оба обозначают водород,
R6 обозначает хлор или бром, предпочтительно хлор,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
Х3 обозначает N или C(R12),
R8 выбран из фтора и метоксигруппы,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, трифторметил, дифторэтоксигруппу, трифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, фтора и метоксигруппы,
R12 обозначает водород,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
В одном варианте осуществления настоящее изобретение относится к соединениям общей формулы 1-2,
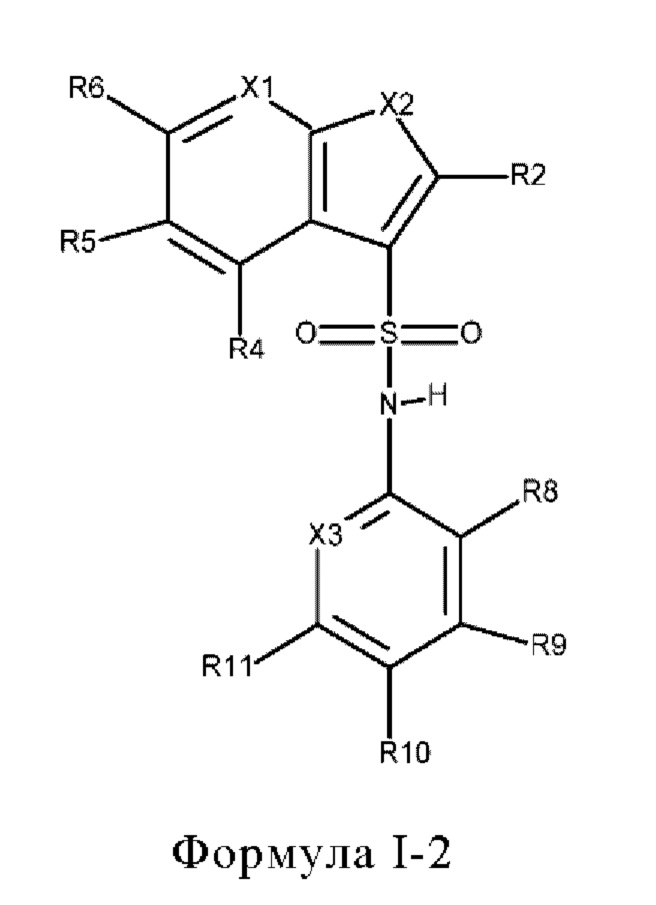
в которой
R2 выбран из водорода, фтора, хлора, брома, йода и метоксигруппы, предпочтительно из водорода и фтора, и в которой R4, R5, R6, R7 если присутствует, R8, R9, R10, R11, X1, Х2, и Х3 являются такими, как описано в настоящем изобретении для соединений формулы I.
Один вариант осуществления относится к соединениям формулы 1-2, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH, S или О, предпочтительно NH или О, более предпочтительно NH,
R2 обозначает водород или фтор,
R4 обозначает водород или фтор,
R5 выбран из водорода и галогена,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, нитрогруппу, незамещенный или фторированный С1-С3-алкил, незамещенную или фторированную C1-С3-алкоксигруппу, метилсульфинил, метилсульфонил, циклопропил, циклопропилметил, циклопропилметоксигруппу, бензилоксигруппу, бензилсульфинил, тиенил и пиридил, и предпочтительно обозначает хлор или бром,
R7 выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, метил, метоксигруппу, фторметил, фторметоксигруппу, метилсульфинил и метилсульфонил,
Х3 обозначает N или C(R12),
R8 выбран из водорода, фтора, хлора, цианогруппы, метоксигруппы и фторметоксигруппы,
R9 обозначает водород или фтор, предпочтительно водород,
R10 выбран из группы, включающей фтор, хлор, бром, йод, азидогруппу, цианогруппу, оксетанил, циано(С1-С2)алкил, циано(С1-С2)алкоксигруппу, циклопропил(С1-С2)алкил, циклобутил(С1-С2)алкил, циклопропил(С1-С2)алкоксигруппу, необязательно фторированный С1-С2-алкоксициклопропил, необязательно фторированный С1-С2-алкоксикарбонилциклопропил, незамещенный или фторированный C1-С3-алкил, предпочтительно метил, этил и фторметил, незамещенную или фторированную C1-С3-алкоксигруппу, предпочтительно метоксигруппу, дифторметоксигруппу, дифторэтоксигруппу и трифторэтоксигруппу, незамещенный или фторированный С2-С3-алкенил, незамещенный или фторированный С2-С3-алкинил, незамещенный или фторированный C1-С3-алкокси(C1-С3)алкил, предпочтительно метоксипропил, этоксиэтил, и фторметоксиметил, незамещенную или фторированную C1-С3-алкокси(C1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу и фторметоксиэтоксигруппу, незамещенный или фторированный C1-С3-алкокси(С2-С3)алкенил, предпочтительно метоксипропенил, этоксиэтенил и фторметоксипропенил, и пентафторсульфанил,
R11 выбран из водорода, фтора, хлора, метоксигруппы, фторметоксигруппы и фторметила,
R12, если присутствует, обозначает водород или фтор, предпочтительно водород
где в предпочтительном варианте осуществления по меньшей мере один из R8 и R11 отличается от водорода,
где в другом предпочтительном варианте осуществления R6 не обозначает водород,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления относится к соединениям формулы 1-2, в которых:
X1 обозначает N, или C(R7),
Х2 обозначает NH, S или О, предпочтительно NH,
R2 обозначает водород,
R4 выбран из водорода и фтора,
R5 выбран из водорода, фтора, хлора и брома,
R6 выбран из группы, включающей галоген, азидогруппу, цианогруппу, бензилоксигруппу, тиенил, предпочтительно тиен-2-ил, незамещенный или фторированный C1-С3-алкил, предпочтительно изопропил и фторметил, циклопропил, циклопропилметил, циклопропилметоксигруппу, незамещенную или фторированную C1-С3-алкоксигруппу, предпочтительно метоксигруппу, фторметоксигруппу и фторэтоксигруппу, метилсульфинил и метилсульфонил, где R6 предпочтительно обозначает хлор или бром,
R7 выбран из группы, включающей водород, фтор, бром, хлор, цианогруппу, метил, фторметил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, метилсульфинил и метилсульфонил,
Х3 обозначает N или C(R12),
R8 выбран из водорода, фтора, метоксигруппы и фторметоксигруппы, и предпочтительно обозначает фтор или метоксигруппу,
R9 выбран из водорода, фтора и метоксигруппы, и предпочтительно обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, азидогруппу, нитрогруппу, пентафторсульфанил, C1-С3-алкил, C1-С3-алкоксигруппу, С2-С3-алкенил, С2-С3-алкинил, циклопропил, циклопропилметоксигруппу и циклопропилэтоксигруппу, где каждая алкильная, алкенильная группа и алкоксигруппа, содержащаяся в R10, может быть замещена одним или несколькими остатками, выбранными из группы, включающей фтор, хлор, цианогруппу, C1-С3-алкилоксигруппу и фтор(C1-С3)алкилоксигруппу, и где каждый циклоалкил может быть незамещенным или замещенным остатком, выбранным из группы, включающей фтор, метил, С1-С2-алкоксигруппу, С1-С2-алкоксикарбонил и цианогруппу,
R11 выбран из водорода, фтора, метила, фторметила, метоксигруппы и фторметоксигруппы,
R12, если присутствует, обозначает водород или фтор, предпочтительно водород,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам,
где в предпочтительном варианте осуществления, если X1 обозначает N, то Х2 также обозначает N, и
где в другом предпочтительном варианте осуществления по меньшей мере один из R8 и R11 отличается от водорода.
Один предпочтительный вариант осуществления относится к соединениям формулы 1-2, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH,
R2, R4 и R5 все обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, азидогруппу, изопропил, циклопропил, метоксигруппу, фторметил, фторметоксигруппу, метилсульфонил, метилсульфинил и бензилоксигруппу, и предпочтительно обозначает хлор или бром,
R7 выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, метил, этил, фторметил, фторэтил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, метилсульфинил и метилсульфонил,
Х3 обозначает N или C(R12),
R8 выбран из фтора и метоксигруппы,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, азидогруппу, цианометил, цианоэтил, цианометоксигруппу, цианоэтоксигруппу, метил, этил, пропил, циклопропил, циклопропилметил, циклопропилэтил, метоксиметил, метоксиэтил, метоксипропил, этоксиметил, этоксиэтил, метоксигруппу, этоксигруппу, пропоксигруппу, циклопропилметоксигруппу, циклопропилэтоксигруппу, метоксиметоксигруппу, метоксиэтоксигруппу, метоксипропоксигруппу, этоксиметоксигруппу, этоксиэтоксигруппу, пропоксиметоксигруппу, этенил, пропенил, метоксиэтенил, метоксипропенил, этинил, пропинил, метоксикарбонилэтил, этоксикарбонилэтил, метоксикарбонилэтенил, этоксикарбонилэтенил и пентафторсульфанил, где каждая алкильная группа или алкоксигруппа, содержащаяся в R10, может быть фторированной и/или гидроксилированной, предпочтительно фторированной, один или более раз, и где каждая циклопропильная группа может содержать заместитель, выбранный из фтора, С1-С2-алкоксигруппы и С1-С2-алкоксикарбонила,
R11 выбран из водорода, фтора, хлора, фторметила, метоксигруппы и фторметоксигруппы,
R12, если присутствует, обозначает водород или фтор,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям формулы I или 1-2, в которых:
X1 обозначает N или C(R7),
Х2 обозначает NH, S или О и предпочтительно обозначает NH,
Х3 обозначает N или CR12,
R2 если он содержатся, R4, R5 и R9 все обозначают водород,
R6 выбран из группы, включающей галоген, цианогруппу, C1-С3-алкоксигруппу, C1-С3-алкил, С3-С6-циклоалкил, предпочтительно С3-С4-циклоалкил, С3-С6-циклоалкилоксигруппу, предпочтительно С3-С4-циклоалкилоксигруппу, С3-С6-гетероциклоалкил, предпочтительно С3-С4-гетероциклоалкил, и С3-С6-гетероциклоалкилоксигруппу, предпочтительно С3-С4-гетероциклоалкилоксигруппу, каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора и незамещенной или фторированной C1-С3-алкоксигруппы,
R7 выбран из группы, включающей водород, галоген, цианогруппу, C1-С3-алкоксигруппу, C1-С3-алкил, С3-С6-циклоалкил, предпочтительно С3-С4-циклоалкил, С3-С6-циклоалкилоксигруппу, предпочтительно С3-С4-циклоалкилоксигруппу, С3-С6-гетероциклоалкил, предпочтительно С3-С4-гетероциклоалкил, и С3-С6-гетероциклоалкилоксигруппу, предпочтительно С3-С4-гетероциклоалкилоксигруппу, каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора и незамещенной или фторированной C1-С3-алкоксигруппы,
R8 выбран из фтора, метоксигруппы и фторметоксигруппы, предпочтительно из фтора и метоксигруппы,
R10 выбран из группы, включающей галоген, С1-С4-алкоксигруппу, С1-С4-алкил, С2-С3-алкенил С2-С3-алкинил, С3-С6-циклоалкил, предпочтительно С3-С4-циклоалкил, С3-С6-циклоалкилоксигруппу, предпочтительно С3-С4-циклоалкилоксигруппу, С3-С6-гетероциклоалкил, предпочтительно С3-С4-гетероциклоалкил, и С3-С6-гетероциклоалкилоксигруппу, предпочтительно С3-С4-гетероциклоалкилоксигруппу, каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора, цианогруппы и незамещенной или фторированной C1-С3-алкоксигруппы,
R11 выбран из водорода, фтора, метоксигруппы и фторметоксигруппы, предпочтительно из фтора и метоксигруппы,
и R12, если присутствует, выбран из водорода, фтора, фторметила, метоксигруппы и фторметоксигруппы.
В одном варианте осуществления настоящее изобретение относится к соединениям формулы I, в которой X1 обозначает CR7 и Х2 обозначает NH, таким образом, имеющим структуру формулы II,
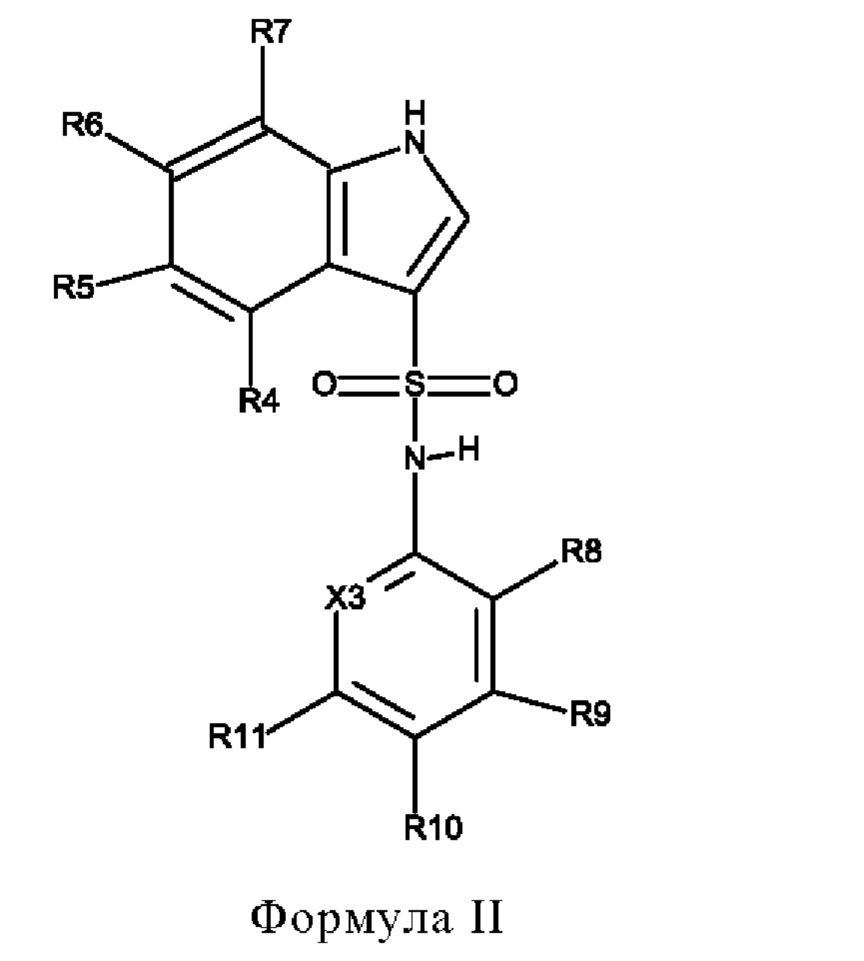
в которой R4, R5, R6, R7, R8, R9, R10, R11, R12 если присутствует, и Х3 являются такими, как описано в настоящем изобретении для формулы I, и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы I, в которой X1 обозначает N и Х2 обозначает NH, таким образом, имеющим структуру формулы III,
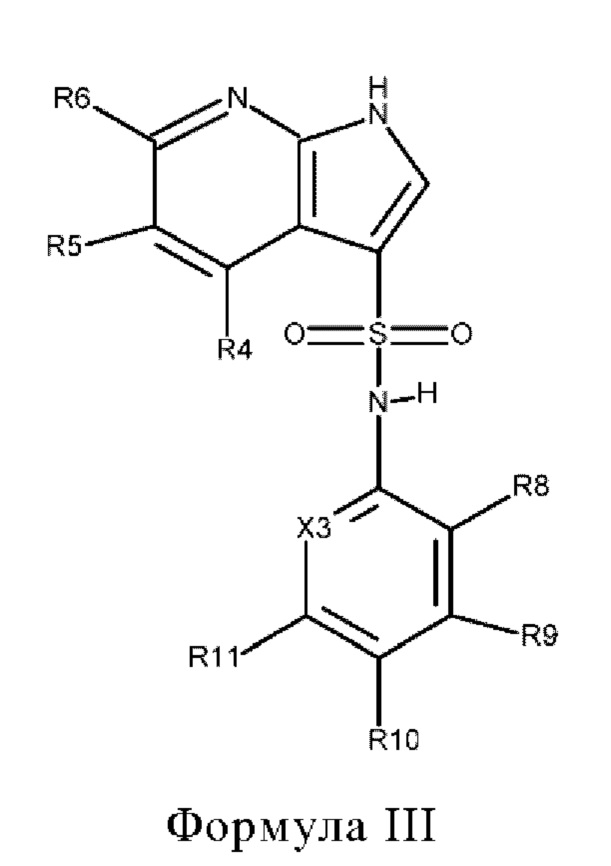
в которой R4, R5, R6, R8, R9, R10, R11, R12 если присутствует, и Х3 являются такими, как описано в настоящем изобретении для формулы I, и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы I, в которой Х2 обозначает О и X1 обозначает C(R7), таким образом, имеющим структуру формулы IV,
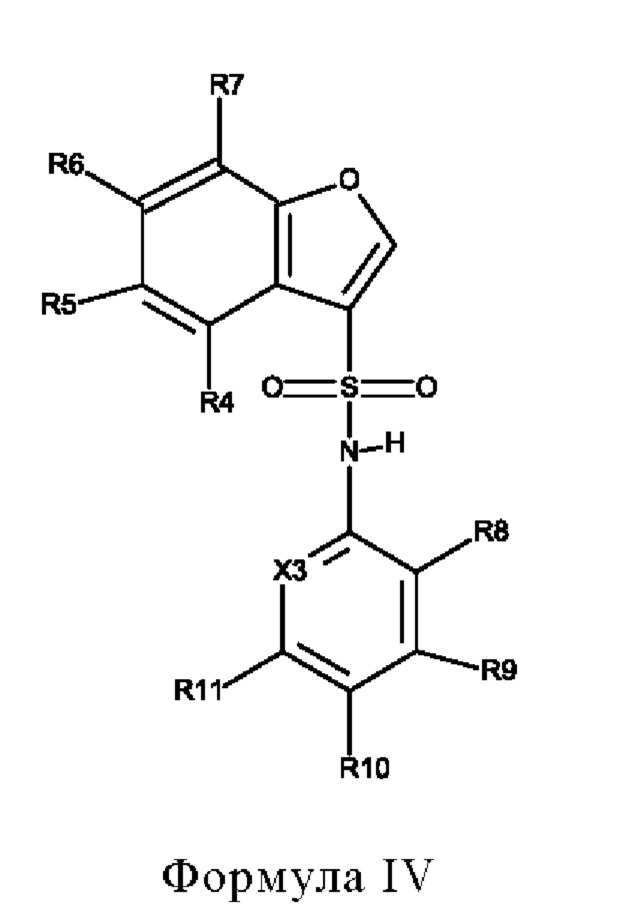
в которой R4, R5, R6, R7, R8, R9, R10, R11, R12 если присутствует, и Х3 являются такими, как описано в настоящем изобретении для формулы I, и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы I, в которой Х2 обозначает S и X1 обозначает C(R7), таким образом, имеющим структуру формулы V,
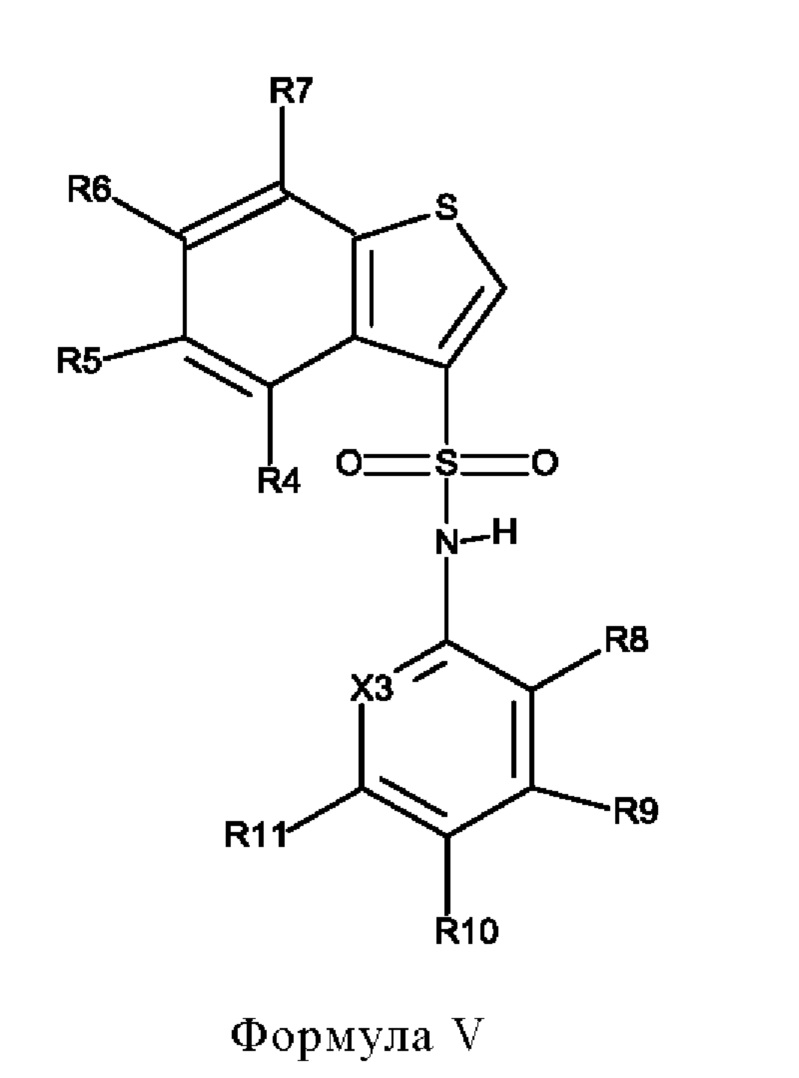
в которой R4, R5, R6, R7, R8, R9, R10, R11, R12 если присутствует, и Х3 являются такими, как описано в настоящем изобретении для формулы I, и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Следует понимать, что ниже в любом определении заместителей соединений формул II, III, IV и V, возможное указание на R7 применимо только для соединений формул II, IV и V, тогда как другие заместители применимы также для соединений формулы III.
В одном варианте осуществления соединений формул I, II, III, IV и V Х3 обозначает C(R12).
В одном варианте осуществления соединений формул I, II, III IV и V, Х3 обозначает N.
В одном варианте осуществления в соединениях формулы III, по меньшей мере один из R4, R5 и R6 отличается от водорода, предпочтительно, если по меньшей мере один из R5 и R6 отличается от водорода.
В одном варианте осуществления, если R6 в соединениях Формулы III обозначает водород, то R5 обозначает галоген; в одном предпочтительном варианте осуществления R5 обозначает йод.
В одном варианте осуществления в соединениях формулы I, II, IV и/или V по меньшей мере один из R5, R6 и R7 отличается от водорода.
В одном варианте осуществления, если R6 в соединениях формулы I, II, III, IV и/или V обозначает водород, то R7 отличается от водорода, и предпочтительно выбран из группы, включающей фтор, хлор, бром, цианогруппу, метоксигруппу, незамещенный или фторированный С1-С2-алкил, незамещенную или фторированную С1-С2-алкоксигруппу, незамещенный или фторированный метилсульфонил и незамещенный или фторированный метилсульфинил, и предпочтительно выбран из группы, включающей фтор, хлор, бром, метил, метоксигруппу, фторметил, фторметоксигруппу, фторэтоксигруппу, метилсульфонил и метилсульфинил.
В одном предпочтительном варианте осуществления, если R10 в соединениях формул I, II, III, IV и V обозначает водород, то R8 и R11 оба отличаются от водорода.
Другой вариант осуществления относится к соединениям формулы II, III, IV или V, в которых:
Х3 обозначает N или C(R12),
R4 обозначает водород,
R5 выбран из водорода, фтора, хлора и брома,
R6 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, азидогруппу, нитрогруппу, метил, этил, н-пропил, изопропил, трифторметил, метилсульфинил, метилсульфонил, циклопропил, циклопропилметил, метоксигруппу, этоксигруппу, метоксиметоксигруппу, метоксиэтоксигруппу, этоксиметоксигруппу, циклопропилметоксигруппу, фенил, бензилоксигруппу, фенилоксигруппу, бензилсульфинил, бензилсульфонил, тиенил, пиридил, оксазол, тиазол и изоксазол, где каждая алкильная группа и алкоксигруппа, содержащаяся в R6, может быть замещена одним или несколькими остатками, выбранными из фтора, цианогруппы и гидроксигруппы, и где каждый фенил, тиенил, пиридил, оксазол, тиазол и изоксазол необязательно может содержать один или более заместителей, предпочтительно заместителей, выбранных из галогена, метоксигруппы, фторметоксигруппы, метила и фторметила, или R6 в соединениях формулы II, IV или V, в частности, в соединениях Формулы II, вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, может образовать кольцо, выбранное из фенила, пиридила, циклогексила и циклопентила, каждое из которых может быть незамещенным или замещенным одной или более группами, выбранными из метила, фторированного метила, метоксигруппы, фторированной метоксигруппы, гидроксигруппы, хлора и фтора,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, метоксигруппу, этоксигруппу, метилсульфинил, метилсульфонил, метил, этил, фторметил, фторэтил и фтор(С1-С2)алкоксигруппу, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, фторметил и фторметоксигруппу, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 выбран из водорода, метила, метоксигруппы, фтора и хлора, и предпочтительно обозначает водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол и 1,3-бензодиоксол, который необязательно замещен двумя атомами фтора,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 3-оксо-2,3-дигидро-1H-изоиндол, 1,1-диоксо-2,3-дигидро-1-бензотиофен, 3-оксо-1,3-дигидро-2-бензофуран, который необязательно может быть метилирован в положении 1,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, незамещенный или фторированный C1-С3-алкенил, включая этенил и пропенил, незамещенный или фторированный C1-С3-алкинил, включая этинил и пропаргил, незамещенный или фторированный и/или гидроксилированный C1-С3-алкил, включая метил, этил, изопропил и трифторметил, незамещенную или фторированную и/или гидроксилированную C1-С3-алкоксигруппу, включая метоксигруппу и фтор(С1-С2)алкоксигруппу, цианогруппу, цианометил, цианометоксигруппу, циклопропил, циклопропилметоксигруппу, циклопропилэтоксигруппу, ацетил, азидогруппу, нитрогруппу, пентафторсульфанил, незамещенный или фторированный и/или гидроксилированный C1-С3-алкокси(C1-С3)алкил, предпочтительно метоксипропил и этоксиэтил, незамещенную или фторированную и/или гидроксилированную C1-С3-алкокси(C1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу и фторметоксиэтоксигруппу, незамещенный или фторированный и/или гидроксилированный C1-С3-алкокси(С2-С3)алкенил, предпочтительно метоксипропенил и этоксиэтенил, незамещенный или фторированный и/или гидроксилированный C1-С3-алкокси(С2-С3)алкинил, незамещенный или фторированный и/или гидроксилированный C1-С3-алкоксикарбонил(C1-С3)алкил, предпочтительно этоксикарбонилэтил, и незамещенный или фторированный и/или гидроксилированный C1-С3-алкоксикарбонил(C1-С3)алкенил, предпочтительно этоксикарбонилэтенил, где каждая циклопропильная группа, содержащаяся в R10, может быть незамещенной или дополнительно содержать один или более заместителей, выбранных из группы, включающей фтор, хлор, цианогруппу, необязательно фторированную С1-С2-алкоксигруппу и необязательно фторированный С1-С2-алкоксикарбонил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, фтор, хлор, бром, незамещенный или фторированный метил и незамещенную или фторированную метоксигруппу,
R12, если присутствует, выбран из водорода, фтора, хлора или брома, и предпочтительно обозначает водород или фтор;
где в предпочтительном варианте осуществления по меньшей мере один, предпочтительно два из R8, R10 и R11, отличаются от водорода и незамещенного алкила,
и где в одном варианте осуществления остатки, содержащиеся в R10, предпочтительно являются незамещенными или фторированными,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям формул II, III IV и V, в которых:
Х3 обозначает N или C(R12),
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор и бром, R6 выбран из группы, включающей фтор, хлор, бром, азидогруппу, цианогруппу, метил, этил, н-пропил, изопропил, трифторметил, метилсульфинил, метилсульфонил, циклопропил, метоксигруппу, фенил, бензилоксигруппу, тиофен-2-ил и тиофен-3-ил, где каждая алкильная и алкоксигруппа, содержащаяся в R6, может быть незамещенной или замещенной одним или несколькими остатками, выбранными из фтора, циклопропила и метоксигруппы, предпочтительно фтором,
R7 выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, метил, этил, метилсульфинил, метилсульфонил, фторметил, фторэтил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу и фторпропоксигруппу,
R8 выбран из водорода, фтора, хлора, брома, метоксигруппы, фторметила и фторметоксигруппы, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 обозначает водород или фтор, предпочтительно водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол, 1,3-бензодиоксол или 2,2-дифтор-1,3-бензодиоксол,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 3-оксо-2,3-дигидро-1H-изоиндол, 1,1-диоксо-2,3-дигидро-1-бензотиофен, 3-оксо-1,3-дигидро-2-бензофуран и 1-метил-3-оксо-1,3-дигидро-2-бензофуран,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, этил, пропил, этенил, пропенил, этинил, пропаргил, фтор(C1-С3)алкил, предпочтительно трифторметил, метоксигруппу, этоксигруппу, фтор(C1-С3)алкоксигруппу, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, ацетил, азидогруппу, незамещенный или фторированный C1-С3-алкокси(C1-С3)алкил, незамещенную или фторированную C1-С3-алкокси(C1-С3)алкоксигруппу, незамещенный или фторированный C1-С3-алкокси(С2-С3)алкенил, незамещенный или фторированный C1-С3-алкокси(С2-С3)алкинил, незамещенный или фторированный C1-С3-алкоксициклопропил, незамещенный или фторированный С1-С3-алкоксикарбонилциклопропил и пентафторсульфанил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано, и где в предпочтительном варианте осуществления R8 и R10 оба не обозначают водород,
R11 выбран из водорода, фтора, хлора, фторированного метила и незамещенной или фторированной метоксигруппы,
R12, если присутствует, выбран из водорода и фтора,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы II, III или IV, в которых:
Х3 обозначает N или C(R12),
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, азидогруппу, метил, этил, изопропил, трифторметил, ацетил, метилсульфинил, метилсульфонил, циклопропил, циклопропилметил, метоксигруппу, этоксигруппу, метоксиэтоксигруппу, циклопропилметоксигруппу, фенил, бензилоксигруппу, фенилоксигруппу, тиенил, пиридил, оксазол, тиазол и изоксазол,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из фенила, пиридила и циклопентила, R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, этоксигруппу, метил, трифторметил и фтор(С1-С2)алкоксигруппу, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из водорода, фтора, хлора, брома, йода, метоксигруппы, метила и трифторметил а, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 выбран из водорода, фтора и хлора, и предпочтительно обозначает водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензооксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол и 1,3-бензодиоксол, который необязательно замещен двумя атомами фтора, R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, этинил, пропаргил, трифторметил, метоксигруппу, фтор(С1-С2)алкоксигруппу, цианогруппу, цианометил, ацетил, азидогруппу, пентафторсульфанил и метоксикарбонил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из водорода, фтора, хлора, брома и метоксигруппы,
R12 выбран из водорода, фтора, хлора или брома,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода и незамещенного алкила,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям формул II, III и IV, в которых:
Х3 обозначает N или C(R12),
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, азидогруппу, метил, изопропил, трифторметил, метилсульфонил, циклопропил, метоксигруппу, фенил, бензилоксигруппу, тиофен-2-ил и тиофен-3-ил,
R7 выбран из водорода, фтора, хлора и метоксигруппы,
R8 выбран из водорода, фтора, хлора, брома, метоксигруппы и трифторметила, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 обозначает водород или фтор, предпочтительно водород, или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензооксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол, 1,3-бензодиоксол или 2,2-дифтор-1,3-бензодиоксол,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, этинил, трифторметил, метоксигруппу, фтор(С1-С2)алкоксигруппу, цианогруппу, цианометил, ацетил, азидогруппу и пентафторсульфанил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано, и где в предпочтительном варианте осуществления R8 и R10 оба не обозначают водород,
R11 выбран из водорода, фтора, хлора и метоксигруппы,
R12 выбран из водорода и фтора,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям формулы II, III IV или V, в которых:
R4 и R5 оба обозначают водород,
R6 обозначает метоксигруппу, трифторметил, бром или хлор, предпочтительно хлор,
R7 обозначает водород, фтор, метоксигруппу, или трифторметил,
Х3 обозначает C(R12),
R9 вместе с R8 или R10 и с фенильным кольцом, к которому R8 и R9 или R9 и R10 присоединены, образует 2,1,3-бензотиадиазол или 2,2-дифтор-1,3-бензодиоксол,
R10 выбран из водорода и фтора,
R11 выбран из водорода, фтора и метоксигруппы, и предпочтительно обозначает водород, и
R12, если присутствует, обозначает водород или фтор,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям формулы II, III или IV, в которых:
R4 и R5 оба обозначают водород,
R6 обозначает бром или хлор, предпочтительно хлор,
R7 обозначает водород, фтор, метоксигруппу, или трифторметил,
Х3 обозначает C(R12),
R9 вместе с R8 или R10 и с фенильным кольцом, к которому R8 и R9 или R9 и R10 присоединены, образуют 2,1,3-бензотиадиазол или 2,2-дифтор-1,3-бензодиоксол,
R10 выбран из водорода и фтора,
R11 выбран из водорода, фтора и метоксигруппы, и
R12 обозначает водород,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления относится к соединениям формулы I, в которых:
R4 и R5 оба обозначают водород,
R6 обозначает хлор или бром, предпочтительно хлор,
R7 обозначает водород, фтор, метоксигруппу или трифторметил,
Х3 обозначает N или C(R12),
R8 выбран из фтора, хлора и метоксигруппы,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, трифторметил и пентафторсульфанил,
R11 выбран из водорода, фтора и метоксигруппы,
R12 обозначает водород
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления настоящего изобретения относится к соединениям формулы II, III IV или V, в которых:
Х3 обозначает N или C(R12),
R4 обозначает водород или фтор, предпочтительно водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, метоксигруппу и фторированный С1-С2-алкил, включая трифторметил, предпочтительно водород, метил, фтор, хлор, бром или йод, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-С3-алкил, предпочтительно метил, этил, изопропил, дифторметил, дифторэтил, трифторэтил и трифторметил, незамещенный или замещенный С2-С3-алкенил, незамещенный или замещенный С2-С3-алкинил, незамещенный или замещенный (C1-С3)алкилсульфинил, предпочтительно метилсульфинил, незамещенный или замещенный C1-С3-алкилсульфонил, предпочтительно метилсульфонил, незамещенный или замещенный С3-С6-циклоалкил, предпочтительно циклопропил, незамещенный или замещенный С3-С6-циклоалкил(C1-С3)алкил, предпочтительно циклопропилметил, незамещенную или замещенную С3-C6-циклоалкил(С1-С3)алкилоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный C3-C6-гетероциклоалкил, незамещенную или замещенную С3-С6-гетероциклоалкил(C1-С3)алкилоксигруппу, предпочтительно гетероциклопропилметоксигруппу, незамещенную или замещенную С3-С6-циклоалкоксигруппу, незамещенную или замещенную С3-С6-гетероциклоалкоксигруппу, незамещенную или замещенную C1-С3-алкоксигруппу, предпочтительно метоксигруппу, дифторметоксигруппу, трифторметоксигруппу, дифторэтоксигруппу, трифторэтоксигруппу незамещенную или замещенную C1-С3-алкокси(C1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, незамещенный или замещенный C1-С3-алкокси(С1-С3)алкил, С3-С6-циклоалкил(С1-С3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный фенил, незамещенный или замещенный фенил(C1-С3)алкил, предпочтительно бензил, незамещенную или замещенную фенил(C1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, незамещенную или замещенную фенилоксигруппу, незамещенный или замещенный фенил(C1-С3)алкилсульфонил, предпочтительно бензилсульфонил, незамещенный или замещенный фенил(C1-С3)алкилсульфинил, предпочтительно бензилсульфинил, незамещенный или замещенный тиенил, незамещенный или замещенный пиридил, незамещенный или замещенный оксазол, незамещенный или замещенный тиазол и незамещенный или замещенный изоксазол, и где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из группы, включающей фтор, хлор, незамещенный или фторированный метил, незамещенную или фторированную метоксигруппу, гидроксигруппу и цианогруппу,
при условии, что если R6 в соединениях формулы III обозначает водород, то по меньшей мере один из R5 и R7 отличается от водорода, где R5 предпочтительно обозначает йод,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из галогена, гидроксигруппы, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, предпочтительно фтора, и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-С3-алкил, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкил, предпочтительно дифторметил или трифторметил, фтор(C1-С3)алкоксигруппу, предпочтительно дифторметоксигруппу, дифторэтоксигруппу, трифторэтоксигруппу и трифторметоксигруппу, метилсульфинил, метилсульфонил, фторированный метилсульфинил, фторированный метилсульфонил, замещенный или незамещенный С3-С6-циклоалкил, замещенный или незамещенный С3-С6-гетероциклоалкил, замещенный или незамещенный С3-С6-циклоалкилоксигруппу, замещенную или незамещенную С3-С6-гетероциклоалкоксигруппу, замещенный или незамещенный С5-С6-гетероарил, замещенную или незамещенную С5-С6-гетероарилоксигруппу и С5-С6-гетероарилметоксигруппу, где гетероарил предпочтительно выбран из группы, включающей пиридил, оксазол и изоксазол, и где гетероарил может содержать один или более заместителей, выбранных из галогена, незамещенного или фторированного метила, незамещенной или фторированной метоксигруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, C1-С3-алкил, предпочтительно метил, и фтор(C1-С3)алкил, предпочтительно трифторметил,
R9 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, C1-С3-алкил, предпочтительно метил, и фтор(C1-С3)алкил, предпочтительно трифторметил, и предпочтительно обозначает водород, метоксигруппу или фтор,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкил, галоген(C1-С3)алкил, предпочтительно фтор(C1-С3)алкил, особенно предпочтительно трифторметил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, галоген(C1-С3)алкилоксигруппу, предпочтительно фтор(C1-С3)алкоксигруппу, цианогруппу, цианометил, цианоэтил, незамещенный или фторированный C1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-С3-алкоксикарбонил, предпочтительно метоксикарбонил, циклопропил, циклопропилоксигруппу, азидогруппу, пентафторсульфанил и нитрогруппу, где любой циклопропильный остаток предпочтительно замещен группой, выбранной из группы, включающей фтор, цианогруппу, C1-С3-алкоксигруппу и C1-С3-алкоксикарбонил, и где каждый алкил, алкоксигруппа, алкенил или алкинил, содержащийся в R10, необязательно может дополнительно содержать один или более заместителей, выбранных из группы, включающей циклопропил, фтор, хлор, бром, йод, цианогруппу, гидроксигруппу, галоген(C1-С3)алкоксигруппу и C1-С3-алкоксигруппу, предпочтительно фтор, метоксигруппу, фторметоксигруппу или фторэтоксигруппу,
R11 выбран из группы, включающей водород, фтор, хлор, цианогруппу, С1-С3-алкил, предпочтительно метил, фтор(C1-С3)алкил, предпочтительно фторметил, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, и более предпочтительно обозначает водород, фтор, хлор, метоксигруппу, фторметоксигруппу или фторметил,
R12, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, C1-С3-алкил, предпочтительно метил, и фтор(C1-С3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор или фторметил,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R10 и R11 отличается от водорода, и более предпочтительно, если по меньшей мере один из R8, R10 и R11 также отличается от незамещенного алкила,
и где предпочтительно, если в соединениях формулы II по меньшей мере один из R5, R6 и R7, если присутствует, не обозначает водород,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления настоящего изобретения относится к соединению формулы II, III или IV, в котором:
Х3 обозначает N или C(R12),
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, метоксигруппу, ацетил, метоксикарбонил и трифторметил, предпочтительно водород, метил или йод, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-С3-алкил, предпочтительно метил, этил, изопропил или трифторметил, незамещенный или фторированный С1-С2-алкилкарбонил, незамещенный или фторированный С1-С2-алкоксикарбонил, (C1-С3)алкилсульфинил, предпочтительно метилсульфинил, C1-С3-алкилсульфонил, предпочтительно метилсульфонил, С3-С6-циклоалкил, предпочтительно циклопропил, С3-С6-циклоалкил(C1-С3)алкил, предпочтительно циклопропилметил, С3-С6-гетероциклоалкил, С3-С6-циклоалкоксигруппу, С3-С6-гетероциклоалкоксигруппу, незамещенную или замещенную C1-С3-алкоксигруппу, предпочтительно метоксигруппу, незамещенную или замещенную C1-С3-алкокси(C1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, С3-С6-циклоалкил(С1-С3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенил(C1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, незамещенную или замещенную фенилоксигруппу, тиенил, пиридил, оксазол, тиазол и изоксазол, и где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, метила, метоксигруппы и цианогруппы,
при условии, что если R6 в соединениях формулы III обозначает водород, то R5 отличается от водорода и предпочтительно обозначает йод,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образует незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из галогена, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образует 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-С3-алкил, C1-С3-алкилоксигруппу, фтор(C1-С3)алкил, предпочтительно трифторметил, фтор(C1-С3)алкоксигруппу, предпочтительно трифторметоксигруппу, незамещенный или фторированный С1-С2-алкилкарбонил, незамещенный или фторированный С1-С2-алкоксикарбонил, метилсульфинил и метилсульфонил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, C1-С3-алкил, предпочтительно метил, и фтор(C1-С3)алкил, предпочтительно трифторметил,
R9 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, C1-С3-алкил, предпочтительно метил, и фтор(C1-С3)алкил, предпочтительно трифторметил, и предпочтительно обозначает водород, фтор, хлор или бром,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкил, галоген(C1-С3)алкил, предпочтительно фтор(C1-С3)алкил, особенно предпочтительно трифторметил, С2-С3-алкинил, C1-С3-алкилоксигруппу, галоген(С1-С3)алкилоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, цианогруппу, цианометил, незамещенный или фторированный C1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный С1-С3-алкоксикарбонил, предпочтительно метоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкил, предпочтительно метил, фтор(C1-С3)алкил, предпочтительно трифторметил, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, незамещенный или фторированный C1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-С3-алкоксикарбонил, предпочтительно метоксикарбонил и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-С3)алкоксигруппу, предпочтительно фтор(С1-С2)алкоксигруппу, C1-С3-алкил, предпочтительно метил, и фтор(C1-С3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор, хлор или бром,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода и более предпочтительно, если по меньшей мере один из R8, R9, R10 и R11 также отличается от незамещенного алкила,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам
Один предпочтительный вариант осуществления настоящего изобретения относится к соединениям формулы II, III IV или V, в которых:
R4 обозначает водород или фтор, более предпочтительно водород,
R5 выбран из водорода, фтора, брома, хлора, йода и метила,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, этил, пропил, предпочтительно изопропил, ацетил, цианогруппу, нитрогруппу, азидогруппу, метилсульфонил, метилсульфинил, фтор(С1-С2)алкил, метоксигруппу, этоксигруппу, фтор(С1-С2)алкоксигруппу, С1-С2-алкоксиметоксигруппу, фторированную (С1-С2)алкоксиметоксигруппу, фторированный (С1-С2)алкоксиметил, фенил, феноксигруппу, бензилоксигруппу, бензилсульфинил, пирид-3-ил, тиен-2-ил, тиен-3-ил, циклопропил, циклопропилоксигруппу, циклопропилметил, и циклопропилметоксигруппу, где каждый фенил, тиенил, пиридил и циклопропил необязательно могут содержать один или большее количество метоксигрупп, атомов фтора и/или хлора, и где R6 предпочтительно не обозначает водород,
или R6 в соединениях формулы II вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, может образовать кольцо, выбранное из группы, включающей незамещенный или замещенный фенил, незамещенный или замещенный пиридил и незамещенный или замещенный циклогексил, и незамещенный или замещенный циклопентил, где любой заместитель такого фенила, пиридила и циклопентила выбран из фтора, хлора, гидроксигруппы, фторированной или незамещенной метоксигруппы и фторированного или незамещенного метила, где кольцо предпочтительно выбрано из незамещенного фенила, пиридила или циклопентила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, метил, метоксигруппу, метилсульфонил, метилсульфинил, фторметил, фторэтил, фторметоксигруппу, фторэтоксигруппу, и необязательно метилированный изоксазол, которым предпочтительно является 3,5-диметил-1,2-оксазол,
Х3 обозначает N или C(R12), и предпочтительно обозначает C(R12),
R8 выбран из группы, включающей водород, метоксигруппу, фторметоксигруппу, цианогруппу, хлор и фтор, и предпочтительно обозначает фтор, метоксигруппу или фторметоксигруппу,
R9 выбран из водорода, метоксигруппы и фтора,
R10 выбран из группы, включающей водород, этенил, пропенил, этинил, пропаргил, цианогруппу, цианометил, ацетил, фтор, хлор, бром, йод, азидогруппу, нитрогруппу, незамещенный или фторированный C1-С3-алкил, предпочтительно метил и трифторметил, гидрокси(C1-С3)алкоксигруппу, предпочтительно гидроксиэтоксигруппу, циано(C1-С3)алкоксигруппу, предпочтительно цианометоксигруппу, циклопропил(С1-С2)алкил, циклопропил(C1-С3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенную или фторированную C1-С3-алкоксигруппу, предпочтительно дифторэтоксигруппу и трифторэтоксигруппу, незамещенный или фторированный С1-С2-алкокси(C1-С3)алкил, предпочтительно метоксипропил и этоксиэтил, незамещенную или фторированную С1-С2-алкокси(C1-С3)алкоксигруппу, предпочтительно метоксиэтоксигруппу и фторметоксиэтоксигруппу, незамещенный или фторированный С1-С2-алкокси(С2-С3)алкенил, предпочтительно метоксипропенил, незамещенный или фторированный С1-С2-алкокси(С2-С3)алкинил и пентафторсульфанил, С1-С2-алкоксициклопропил и С1-С2-алкоксикарбонилциклопропил,
R11 выбран из группы, включающей водород, фтор, хлор, цианогруппу, фторметил, метоксигруппу и фторметоксигруппу,
R12 обозначает водород или фтор,
и где по меньшей мере один, предпочтительно по меньшей мере два из R8, R10 и R11 отличаются от водорода,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления настоящего изобретения относится к соединениям формулы II, III или IV, в которых:
R4 обозначает водород или фтор, более предпочтительно водород,
R5 обозначает водород, йод, или метил,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, этил, изопропил, ацетил, трифторметил, метоксигруппу, этоксигруппу, фтор(С1-С2)алкоксигруппу, (С1-С2)алкоксиметоксигруппу, цианометилсульфонил, фенил, феноксигруппу, бензилоксигруппу, 2-пиридил, 3-пиридил, 4-пиридил, 2-тиенил, 3-тиенил, циклопропил, циклопропилоксигруппу и циклопропилметоксигруппу,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из группы, включающей незамещенный или замещенный фенил, незамещенный или замещенный пиридил, и незамещенный или замещенный циклопентил, где любой заместитель выбран из фтора, метоксигруппы и метила, где кольцо предпочтительно выбрано из незамещенного фенила, пиридила или циклопентила,
и где, если R6 в формуле II обозначает водород, то R5 обозначает йод,
R7 выбран из группы, включающей водород, метил, метоксигруппу, трифторметил, фтор, хлор и бром,
Х3 обозначает N или C(R12) и предпочтительно обозначает C(R12),
R8 выбран из группы, включающей водород, метоксигруппу, цианогруппу, хлор и фтор,
R9 выбран из водорода и фтора,
R10 выбран из группы, включающей водород, этинил, цианогруппу, цианометил, ацетил, фтор, хлор, бром, йод, азидогруппу, нитрогруппу, трифторметил, дифторэтоксигруппу, трифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, фтора, хлора и метоксигруппы,
R12 обозначает водород или фтор,
и где по меньшей мере один из R8, R9, R10 и R11 отличается от водорода
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления настоящего изобретения относится к соединению формулы II, III IV или V, особенно предпочтительно формулы II или III, в котором:
R4 обозначает водород,
R5 выбран из водорода, фтора, хлора и брома, и предпочтительно обозначает водород,
R6 выбран из группы, включающей фтор, хлор, бром, цианогруппу, метил, этил, пропил, предпочтительно изопропил, метилсульфинил, метилсульфонил, циклопропил, циклопропилоксигруппу, бензилоксигруппу, тиенил, метоксигруппу, этоксигруппу, фтор(C1-C3)алкоксигруппу и фтор(C1-C3)алкил, предпочтительно трифторметил,
R7 выбран из группы, включающей водород, метоксигруппу, фтор, хлор, бром, цианогруппу, метилсульфинил, метилсульфонил, C1-C3-алкоксигруппу, фтор(C1-C3)алкоксигруппу, C1-C3-алкил и фтор(C1-C3)алкил, предпочтительно трифторметил,
или R6 и R7 в соединениях формулы II вместе с образующими кольцо атомами С, к которым они присоединены, могут образовать кольцо, выбранное из фенила, циклопентила и пиридила, каждый из которых может быть незамещенным или замещенным одним или несколькими остатками, выбранными из фтора, хлора, гидроксигруппы, фторированной или незамещенной метоксигруппы и фторированного или незамещенного метила, где фенильное, циклопентильное и циклогексильное кольца предпочтительно являются незамещенными, и где пиридильное кольцо предпочтительно является незамещенным или замещенным в положении 8,
Х3 обозначает -C(R12)- или N,
R8 обозначает водород, фтор, метоксигруппу или фторметоксигруппу, и предпочтительно обозначает фтор или метоксигруппу,
R9 обозначает водород,
R10 выбран из группы, включающей галоген, азидогруппу, нитрогруппу, цианогруппу, C1-C3-алкил, C2-C3-алкенил, C2-C3-алкинил, C1-C3-алкоксигруппу, C3-C5-циклоалкил, предпочтительно циклопропил, C3-C5-циклоалкилоксигруппу и пентафторсульфанил, где каждый алкил, алкенил, алкинил и алкоксигруппа могут быть незамещенными или замещенными одним или несколькими остатками, выбранными из группы, включающей галоген, предпочтительно фтор, цианогруппу, циклопропил, C1-C3-алкоксигруппу и фтор-C1-C3-алкоксигруппу, и где любой циклоалкильный фрагмент может быть незамещенным или замещенным одним или несколькими остатками, выбранными из группы, включающей фтор, цианогруппу, незамещенную или фторированную C1-C3-алкоксигруппу и незамещенный или фторированный C1-C3-алкоксикарбонил,
R11 выбран из группы, включающей водород, фтор, хлор, цианогруппу, метоксигруппу, фторметоксигруппу и фторметил, и
R12 выбран из водорода и фтора,
где предпочтительно, если по меньшей мере один из R8 и R11 отличается от водорода и где предпочтительно, если по меньшей мере один из R8 и R11 выбран из фтора, хлора и метоксигруппы,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям формулы II, III IV и V, предпочтительно формулы II и III, в которых:
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей метил, этил, пропил, метилсульфонил, метилсульфинил, метоксигруппу, моно-, ди- и трифторметил, моно-, ди- и трифторэтил, моно-, ди- и трифторметоксигруппу, моно-, ди- и трифторэтоксигруппу, цианогруппу, азидогруппу, фтор, бром и хлор, и предпочтительно выбран из группы, включающей хлор и бром,
R7, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, метил, фторметил, метилсульфинил и метилсульфонил,
Х3 обозначает C(R12),
R8 выбран из водорода, фтора, хлора и метоксигруппы, или вместе с R9 образуют кольцо, как здесь описано,
R9 вместе с R8 или R10 и с фенильным кольцом, к которому R8 и R9 или R9 и R10 присоединены, образуют 2,1,3-бензотиадиазол или 1,3-бензодиоксол, который необязательно замещен двумя атомами фтора,
R10 выбран из водорода и фтора, или R10 вместе с R9 образуют кольцо, как здесь описано,
R11 выбран из водорода, фтора и метоксигруппы,
R12 обозначает водород
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления настоящего изобретения относится к соединению формулы II, III IV или V, особенно предпочтительно формулы II или III, в котором:
R4, R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, метоксигруппу, фторметоксигруппу и фторметил,
R7 выбран из группы, включающей водород, метоксигруппу, фтор, хлор, бром, фторметил, предпочтительно трифторметил, фторметоксигруппу, фторэтоксигруппу, метилсульфинил и метилсульфонил,
Х3 обозначает N или CR12,
R8 обозначает фтор или метоксигруппу,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, незамещенный или фторированный C1-C3-алкил, предпочтительно метил, этил и фторметил, незамещенную или фторированную C1-C3-алкоксигруппу, предпочтительно фторметоксигруппу и фторэтоксигруппу, незамещенный или фторированный C1-C3-алкокси(C1-C3)алкил, предпочтительно метоксипропил, фторированный метоксипропил, этоксиэтил и фторированный метоксиметил, незамещенный или фторированный C1-C2-алкокси(C2-C3)алкенил, включая метоксипропенил и этоксиэтенил, незамещенную или фторированную C1-C2-алкокси(C1-C3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, пентафторсульфанил и циклоалкил, который содержит заместитель, выбранный из группы, включающей C1-C2-алкоксигруппу, фтор(C1-C2)алкоксигруппу, C1-C2-алкоксикарбонил и фтор(C1-C2)алкоксикарбонил,
R11 выбран из водорода, метоксигруппы, фторметоксигруппы, фторметила и фтора,
R12, если присутствует, обозначает водород или фтор,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления настоящего изобретения относится к соединению формулы II, III или IV, особенно предпочтительно формулы II или III, в котором:
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, изопропил, бензилоксигруппу и трифторметил,
R7 обозначает водород, метоксигруппу, фтор или бром, предпочтительно водород,
или R6 и R7 вместе с образующими кольцо атомами С, к которым они присоединены, образуют кольцо, выбранное из фенила, циклопентила и пиридила,
Х3 обозначает -C(R12)-,
R8 обозначает фтор, водород или метоксигруппу,
R9 обозначает водород,
R10 обозначает этинил, трифторметил, дифторэтоксигруппу, цианогруппу, хлор, бром или йод,
R11 выбран из водорода и фтора, и
R12 выбран из водорода и фтора,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям формулы II, III и IV, предпочтительно формулы II и III, в которых:
R4 и R5 оба обозначают водород,
R6 обозначает бром или хлор, предпочтительно хлор,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
Х3 обозначает C(R12),
R8 выбран из водорода, фтора и метоксигруппы, или вместе с R9 образуют кольцо, как здесь описано,
R9 вместе с R8 или R10 и с фенильным кольцом, к которому R8 и R9 или R9 и R10 присоединены, образуют 2,1,3-бензотиадиазол или 1,3-бензодиоксол, который необязательно замещен двумя атомами фтора,
R10 выбран из водорода и фтора, или R10 вместе с R9 образуют кольцо, как здесь описано,
R11 выбран из водорода, фтора и метоксигруппы,
R12 обозначает водород
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления настоящего изобретения относится к соединению формулы II, III или IV, особенно предпочтительно формулы II или III, в котором:
R4, R5 обозначают водород,
R6 обозначает бром, хлор или трифторметил,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
R8 обозначает фтор или метоксигруппу,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, трифторметил, дифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, метоксигруппы и фтора,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
В одном варианте осуществления настоящее изобретение относится к соединениям формулы II, III, IV или V, предпочтительно формулы II или III, в которых:
Х3 обозначает C(R12),
R4 обозначает водород или фтор, предпочтительно водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил и трифторметил, предпочтительно обозначает водород, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-C3-алкил, предпочтительно метил, этил, изопропил или трифторметил, C1-C2-алкилкарбонил, C1-C2-алкоксикарбонил, (C1-C3)алкилсульфинил, предпочтительно метилсульфинил, (C1-C3)алкилсульфонил, предпочтительно метилсульфонил, незамещенный или замещенный бензилсульфонил, незамещенный или замещенный бензилсульфинил, C3-C6-циклоалкил, предпочтительно циклопропил, C3-C6-циклоалкил(C1-C3)алкил, предпочтительно циклопропилметил, C3-C6-гетероциклоалкил, C3-C6-циклоалкоксигруппу, C3-C6-гетероциклоалкоксигруппу, незамещенную или замещенную C1-C3-алкоксигруппу, предпочтительно метоксигруппу, моно ди- и трифторэтоксигруппу, незамещенную или замещенную C1-C3-алкокси(C1-C3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, незамещенный или замещенный C1-C3-алкокси(C1-C3)алкил, (C3-C6)циклоалкил(C1-C3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенил(C1-C3)алкоксигруппу, предпочтительно бензилоксигруппу, незамещенную или замещенную фенилоксигруппу, тиенил, пиридил, оксазол, тиазол и изоксазол, и где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из группы, включающей фтор, хлор, незамещенный или фторированный метил, незамещенную или фторированную метоксигруппу, гидроксигруппу и цианогруппу,
при условии, что если R6 в соединениях формулы III обозначает водород, то R5 предпочтительно обозначает йод,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из галогена, гидроксигруппы, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, предпочтительно фтора, и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-C3-алкил, C1-C3-алкилоксигруппу, фтор(C1-C3)алкил, предпочтительно трифторметил, фтор(C1-C3)алкоксигруппу, предпочтительно фторметоксигруппу или фторэтоксигруппу, C1-C2-алкилкарбонил, C1-C2-алкоксикарбонил, метилсульфинил и метилсульфонил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил,
R9 вместе с R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол, 1,3-бензотиазол, 2,3-дигидро-1-бензотиофен, который замещен одной или двумя оксогруппами (предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксо-2,3-дигидро-1-бензотиофена), 3-оксо-1,3-дигидро-2-бензофуран-5-ил, который может быть незамещенным или замещенным одной или двумя группами, выбранными из оксогруппы, фтора и метила, предпочтительно по меньшей мере одной оксогруппой, предпочтительно с образованием 3-оксо-1,3-дигидро-2-бензофурана или 1-метил-3-оксо-1,3-дигидро-2-бензофурана, и дигидроизоиндол, который может быть незамещенным или содержать один или более заместителей, выбранных из оксогруппы, фтора и метила, и которым предпочтительно является 3-оксо-2,3-дигидро-1H-изоиндол, и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора, предпочтительно с образованием 2,2-дифтор-1,3-бензодиоксола,
R11 выбран из группы; включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, предпочтительно метил, фтор(C1-C3)алкил, предпочтительно трифторметил, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор, хлор или бром,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
В одном варианте осуществления настоящее изобретение относится к соединениям формулы II, III, или IV, предпочтительно формулы II или III, в которых:
Х3 обозначает C(R12),
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил и трифторметил, предпочтительно водород или йод, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-C3-алкил, предпочтительно метил, этил, изопропил или трифторметил, C1-C2-алкилкарбонил, C1-C2-алкоксикарбонил, (C1-C3)алкилсульфинил, предпочтительно метилсульфинил, (C1-C3)алкилсульфонил, предпочтительно метилсульфонил, C3-C6-циклоалкил, предпочтительно циклопропил, C3-C6-циклоалкил(C1-C3)алкил, предпочтительно циклопропилметил, C3-C6-гетероциклоалкил, C3-C6-циклоалкоксигруппу, C3-C6-гетероциклоалкоксигруппу, незамещенную или замещенную C1-C3-алкоксигруппу, предпочтительно метоксигруппу, незамещенную или замещенную C1-C3-алкокси(C1-C3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, (C3-C6)циклоалкил(C1-C3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенил(C1-C3)алкоксигруппу, предпочтительно бензилоксигруппу, незамещенную или замещенную фенилоксигруппу, тиенил, пиридил, оксазол, тиазол и изоксазол, и где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, метила, метоксигруппы и цианогруппы,
при условии, что если R6 в соединениях формулы II обозначает водород, то R5 предпочтительно обозначает йод,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образует незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из галогена, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образует 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-C3-алкил, C1-C3-алкилоксигруппу, фтор(C1-C3)алкил, предпочтительно трифторметил, фтор(C1-C3)алкоксигруппу, предпочтительно трифторметоксигруппу, C1-C2-алкилкарбонил, C1-C2-алкоксикарбонил, метилсульфинил и метилсульфонил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензооксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол, 1,3-бензотиазол, 2,3-дигидро-1-бензотиофен, который замещен одной или двумя оксогруппами (предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксо-2,3-дигидро-1-бензотиофена), 3-оксо-1,3-дигидро-2-бензофуран-5-ил и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, предпочтительно метил, фтор(C1-C3)алкил, предпочтительно трифторметил, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3) алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор, хлор или бром,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления настоящего изобретения относится к соединению формулы II, III или формулы IV, особенно предпочтительно формулы II или III, в котором:
Х3 обозначает C(R12),
R4, R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, метоксигруппу, трифторметил, метилсульфонил и цианогруппу,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из группы, включающей незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклогексил и незамещенный или замещенный циклопентил, где любой заместитель выбран из фтора, метоксигруппы и метила, и где кольцо предпочтительно выбрано из незамещенного фенила, пиридила, циклогексила или циклопентила,
R7 выбран из группы, включающей водород, метил, фторметил, предпочтительно трифторметил, метоксигруппу, фтор, хлор и бром, предпочтительно из группы, включающей водород, фтор и трифторметил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 обозначает водород или фтор,
R9 вместе с R10 и с атомами С, к которым они присоединены, образуют кольцо, выбранное из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 3-оксо-2,3-дигидро-1Н-изоиндол, 3-оксо-1,3-дигидро-2-бензофуран, 1-метил-3-оксо-1,3-дигидро-2-бензофуран и 2,2-дифторзамещенный 1,3-бензодиоксол, предпочтительным является 2,1,3-бензотиадиазол,
R11 обозначает водород или фтор, предпочтительно водород, и
R12 обозначает водород или фтор,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один предпочтительный вариант осуществления настоящего изобретения относится к соединению формулы II, III или формулы IV, особенно предпочтительно формулы II или III, в котором:
Х3 обозначает C(R12),
R4, R5 оба обозначают водород,
R6 обозначает фтор, хлор, бром, трифторметил, метилсульфонил или цианогруппу,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из группы, включающей незамещенный или замещенный фенил, незамещенный или замещенный пиридил, и незамещенный или замещенный циклопентил, где любой заместитель выбран из фтора, метоксигруппы и метила, и где кольцо предпочтительно выбрано из незамещенного фенила, пиридила или циклопентила,
R7 выбран из водорода, метила, трифторметила, метоксигруппы, фтора, хлора и брома, предпочтительно из водорода и брома, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 обозначает водород или фтор,
R9 вместе с R10 и с атомами С, к которым они присоединены, образуют кольцо, выбранное из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензооксадиазол и 2,2-дифторзамещенный 1,3-бензодиоксол, предпочтительным является 2,1,3-бензотиадиазол,
R11 обозначает водород или фтор, и
R12 обозначает водород или фтор,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы II, III IV или V, в которых:
Х3 обозначает C(R12),
R4 обозначает водород или фтор, предпочтительно водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил и фторметил, предпочтительно обозначает водород, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-C3-алкил, предпочтительно метил, этил, пропил, моно-, ди- и трифторметил, незамещенный или замещенный C1-C2-алкилкарбонил, незамещенный или замещенный C1-C2-алкоксикарбонил, (C1-C3)алкилсульфинил, предпочтительно метилсульфинил, (C1-C3)алкилсульфонил, предпочтительно метилсульфонил, C3-C6-циклоалкил, предпочтительно циклопропил, C3-C6-циклоалкил(C1-C3)алкил, предпочтительно циклопропилметил, C3-C6-гетероциклоалкил, C3-C6-циклоалкоксигруппу, C3-C6-гетероциклоалкоксигруппу, незамещенную или замещенную C1-C3-алкоксигруппу, предпочтительно метоксигруппу, моно-, ди- и трифторметоксигруппу, моно-, ди- и трифторэтоксигруппу, незамещенную или замещенную C1-C3-алкокси(C1-C3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, незамещенный или замещенный C1-C3-алкокси(C1-C3)алкил, (C3-C6)циклоалкил(C1-C3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенил(C1-C3)алкоксигруппу, предпочтительно бензилоксигруппу, незамещенную или замещенную фенилоксигруппу, тиенил, пиридил, оксазол, тиазол и изоксазол, и где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, метила, метоксигруппы и цианогруппы,
при условии, что если R6 в соединениях формулы III обозначает водород, то R5 предпочтительно обозначает йод,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образует незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из галогена, гидроксигруппы, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образует 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-C3-алкил, C1-C3-алкилоксигруппу, фтор(C1-C3)алкил, предпочтительно трифторметил, фтор(C1-C3)алкоксигруппу, предпочтительно фторметоксигруппу или фторэтоксигруппу, незамещенный или фторированный C1-C2-алкилкарбонил, незамещенный или фторированный C1-C2-алкоксикарбонил, метилсульфинил, пиридилметоксигруппу, изоксазол и метилсульфонил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R9 вместе с R8 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора;
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, галоген(C1-C3)алкил, предпочтительно фтор(C1-C2)алкил, галогенированный, предпочтительно фториро ванный, или незамещенный C1-C3-алкокси(C1-C3)алкил, С2-С3-алкинил, галогенированный, предпочтительно фторированный, или незамещенный C1-C3-алкокси(C1-C3)алкенил, метоксигруппу, этоксигруппу, галоген(C1-C3)алкилоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, галогенированную, предпочтительно фторированную, или незамещенную C1-C3-алкокси(C1-C3)алкоксигруппу, цианогруппу, цианометил, цианоэтил, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, циклопропилметоксигруппу, (C1-C2)алкоксициклопропил, (C1-C3)алкоксикарбонилциклопропил, азидогруппу, пентафторсульфанил и нитрогруппу, и где в одном варианте осуществления R10 обозначает водород, метоксигруппу или галоген,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, предпочтительно метил, фтор(C1-C3)алкил, предпочтительно трифторметил, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3) алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор, хлор или бром,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы II, III или IV, в которых:
Х3 обозначает C(R12),
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил и трифторметил, предпочтительно водород или йод, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-C3-алкил, предпочтительно метил, этил, изопропил или трифторметил, незамещенный или замещенный C1-C2-алкилкарбонил, незамещенный или замещенный C1-C2-алкоксикарбонил, (C1-C3)алкилсульфинил, предпочтительно метилсульфинил, (C1-C3)алкилсульфонил, предпочтительно метилсульфонил, C3-C6-циклоалкил, предпочтительно циклопропил, C3-C6-циклоалкил(C1-C3)алкил, предпочтительно циклопропилметил, C3-C6-гетероциклоалкил, C3-C6-циклоалкоксигруппу, C3-C6-гетероциклоалкоксигруппу, незамещенную или замещенную C1-C3-алкоксигруппу, предпочтительно метоксигруппу, незамещенную или замещенную C1-C3-алкокси(C1-C3)алкоксигруппу, предпочтительно метоксиэтоксигруппу, (C3-C6)циклоалкил(C1-C3)алкоксигруппу, предпочтительно циклопропилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенил(C1-C3)алкоксигруппу, предпочтительно бензилоксигруппу, незамещенную или замещенную фенилоксигруппу, тиенил, пиридил, оксазол, тиазол и изоксазол, и где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, метила, метоксигруппы и цианогруппы,
при условии, что если R6 в соединении формулы II обозначает водород, то R5 предпочтительно обозначает йод,
или
(iii) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из галогена, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора и метоксигруппы,
или
(iv) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образует 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-C3-алкил, C1-C3-алкилоксигруппу, фтор(C1-C3)алкил, предпочтительно трифторметил, фтор(C1-C3)алкоксигруппу, предпочтительно трифторметоксигруппу, незамещенный или фторированный C1-C2-алкилкарбонил, незамещенный или фторированный C1-C2-алкоксикарбонил, метилсульфинил и метилсульфонил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R9 вместе с R8 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензооксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, галоген(C1-C3)алкил, предпочтительно фтор(C1-C2)алкил, C2-C3-алкинил, метоксигруппу, этоксигруппу, галоген(C1-C3)алкилоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, цианогруппу, цианометил, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, и где в одном варианте осуществления R10 обозначает водород, метоксигруппу или галоген,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, предпочтительно метил, фтор(C1-C3)алкил, предпочтительно трифторметил, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3) алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор, хлор или бром,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы II, III IV или V, особенно предпочтительно формулы II или III, в которых:
Х3 обозначает C(R12),
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, метоксигруппу, фторметоксигруппу, метилсульфинил, метилсульфонил, и фторметил, и предпочтительно обозначает хлор, бром или фторметил,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из группы, включающей незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклогексил и незамещенный или замещенный циклопентил, где любой заместитель выбран из фтора, фторированной или незамещенной метоксигруппы и фторированного или незамещенного метила, и где кольцо предпочтительно выбрано из незамещенного фенила, пиридила, циклогексила или циклопентила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу, метил, ацетил, цианогруппу, фторметил, фторметоксигруппу и фторэтоксигруппу, предпочтительно из водорода и трифторметила, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 вместе с R9 и с атомами С, к которым они присоединены, образуют кольцо, выбранное из группы, включающей 2,1,3-бензоселенадиазол, 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, незамещенный 1,3-бензодиоксол, 2-оксо-2,3-дигидро-1,3-бензоксазол и 2,2-дифтор-1,3-бензодиоксол,
R10 выбран из водорода, фтора, хлора, брома и фторметила,
R11 выбран из водорода, цианогруппы, фтора и хлора, и предпочтительно обозначает водород, и
R12 выбран из водорода, фтора, хлора и фторметила,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы II, III или IV, особенно предпочтительно формулы II или III, в которых:
Х3 обозначает C(R12),
R4 и R5 оба обозначают водород,
R6 выбран из фтора, хлора, брома и трифторметила,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из группы, включающей незамещенный или замещенный фенил, незамещенный или замещенный пиридил и незамещенный или замещенный циклопентил, где любой заместитель выбран из фтора, метоксигруппы и метила, и где кольцо предпочтительно выбрано из незамещенного фенила, пиридила или циклопентила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу, метил, ацетил и трифторметил, предпочтительно из водорода и трифторметила, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 вместе с R9 и с атомами С, к которым они присоединены, образуют кольцо, выбранное из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензооксадиазол, незамещенный 1,3-бензодиоксол, 2-оксо-2,3-дигидро-1,3-бензоксазол и 2,2-дифтор-1,3-бензодиоксол,
R10 обозначает водород или фтор,
R11 выбран из водорода, фтора, хлора, брома и цианогруппы, и
R12 обозначает водород, фтор, хлор и трифторметил
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы II, III IV или V, особенно предпочтительно формулы II или III, в которых:
Х3 обозначает C(R12),
R4 и R5 оба обозначают водород,
R6 выбран из фтора, хлора, брома и фторметила,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из фенила, пиридила, циклогексила и циклопентила,
R7, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу, метил, фторметил, фторметоксигруппу и фторэтоксигруппу, предпочтительно из водорода, фтора и трифторметила, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 вместе с R9 и с атомами С, к которым они присоединены, образуют кольцо, выбранное из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол и 2,2-дифтор-1,3-бензодиоксол,
R10 обозначает водород или фтор,
R11 выбран из водорода, фтора и цианогруппы, и
R12 выбран из водорода, фтора и фторметила,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям общих формул II, III, IV и V, которые необязательно замещены в положении 2 верхнего бициклического кольца, таким образом, имеющих структуры, соответствующие общим формулам II-2, III-2, IV-2 и V-2, представленным ниже:
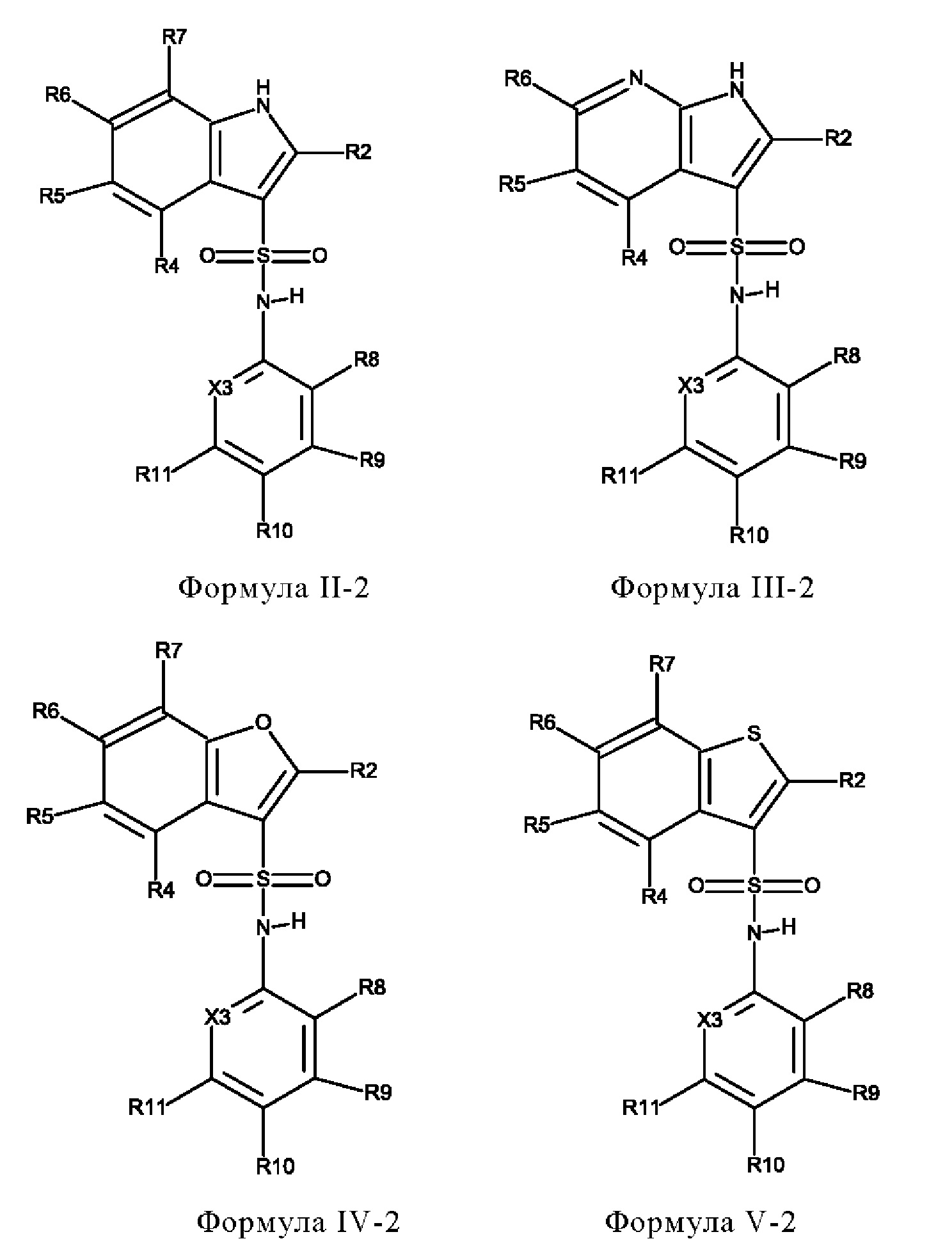
в которых R2 выбран из водорода, фтора, хлора, брома, йода и метоксигруппы, и предпочтительно обозначает водород или фтор, особенно предпочтительно водород,
и в которых R4, R5, R6, R7 если присутствует, R8, R9, R10, R11 и Х3 являются такими, как описано в настоящем изобретении для соответствующих соединений формулы II, III, IV и V.
В одном предпочтительном варианте осуществления настоящего изобретения в соединениях формулы II, II-2, III, III-2, IV, IV-2, V и V-2:
Х3 обозначает N или CR12,
R2, если присутствует, R4, R5 и R9 все обозначают водород,
R6 выбран из группы, включающей галоген, цианогруппу, C1-C3-алкоксигруппу, C1-C3-алкил, C3-C6-циклоалкил, предпочтительно C3-C4-циклоалкил, C3-C6-циклоалкилоксигруппу, предпочтительно C3-C4-циклоалкилоксигруппу, C3-C6-гетероциклоалкил, предпочтительно C3-C4-гетероциклоалкил, и C3-C6-гетероциклоалкилоксигруппу, предпочтительно C3-C4-гетероциклоалкилоксигруппу, каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора и незамещенной или фторированной C1-C3-алкоксигруппы,
R7 выбран из группы, включающей водород, галоген, цианогруппу, C1-C3-алкоксигруппу, C1-C3-алкил, C3-C6-циклоалкил, предпочтительно C3-C4-циклоалкил, C3-C6-циклоалкилоксигруппу, предпочтительно C3-C4-циклоалкилоксигруппу, C3-C6-гетероциклоалкил, предпочтительно C3-C4-гетероциклоалкил, и C3-C6-гетероциклоалкилоксигруппу, предпочтительно C3-C4-гетероциклоалкилоксигруппу, каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора и незамещенной или фторированной C1-C3-алкоксигруппы,
R8 выбран из фтора, метоксигруппы и фторметоксигруппы, предпочтительно из фтора и метоксигруппы,
R10 выбран из группы, включающей галоген, C1-C4-алкоксигруппу, C1-C4-алкил, C2-C3-алкенил C2-C3-алкинил, C3-C6-циклоалкил, предпочтительно C3-C4-циклоалкил, C3-C6-циклоалкилоксигруппу, предпочтительно C3-C4-циклоалкилоксигруппу, C3-C6-гетероциклоалкил, предпочтительно C3-C4-гетероциклоалкил, и C3-C6-гетероциклоалкилоксигруппу, предпочтительно C3-C4-гетероциклоалкилоксигруппу, каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора, цианогруппы и незамещенной или фторированной C1-C3-алкоксигруппы, и
R11 выбран из водорода, фтора, метоксигруппы и фторметоксигруппы, предпочтительно из фтора и метоксигруппы,
и R12, если присутствует, выбран из водорода, фтора, фторметила, метоксигруппы и фторметоксигруппы.
В другом варианте осуществления соединения, предлагаемые в настоящем изобретении, представлены одной из следующих формул IIa - IIc:
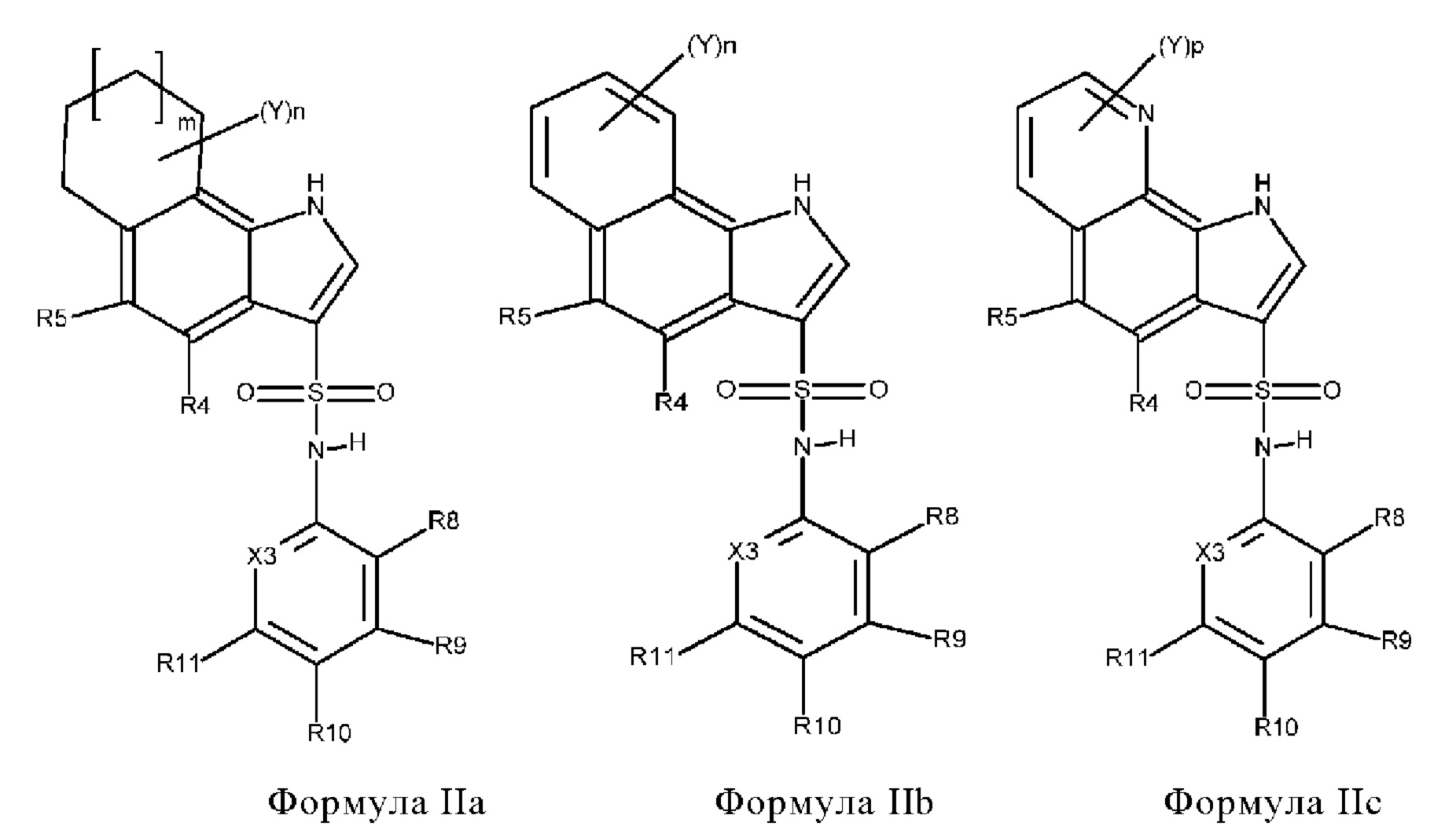
в которой
n обозначает любое число, равное от 0 до 4,
m равно 0 или 1,
р обозначает любое число, равное от 0 до 3, и
любой Y обозначает заместитель, независимо выбранный из группы, включающей галоген, гидроксигруппу, цианогруппу, C1-C6-алкил, C2-C6-алкенил, C2-C6-алкинил, C3-C7-циклоалкил, C3-C7-циклоалкил(C1-C3)алкил, C3-C7-гетероциклоалкил(C1-C3)алкил, C1-C6-алкоксигруппу и C1-C6-алкокси(C1-C3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-C3-алкоксигруппы,
R4, R5, Х3, R8, R9, R10, R11 и R12 являются такими, как описано в настоящем изобретении для соединений формулы I и II.
В одном варианте осуществления в соединениях формулы II(а) - II(с):
m равно 0 или 1, предпочтительно 0,
n обозначает любое число, равное от 0 до 4, предпочтительно от 0 до 2, более предпочтительно 0 или 1,
р обозначает любое число, равное от 0 до 3, предпочтительно от 0 до 2, более предпочтительно 0 или 1,
любой Y обозначает заместитель, независимо выбранный из группы, включающей галоген, гидроксигруппу, цианогруппу, C1-C3-алкил, C1-C3-алкоксигруппу и C1-C3-алкокси(C1-C3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-C3-алкоксигруппы,
R4 обозначает водород или фтор, предпочтительно водород,
R5 выбран из водорода, галогена, C1-C3-алкила и C1-C3-алкоксигруппы, где каждый алкил или алкоксигруппа необязательно может содержать один или более заместителей, предпочтительно метоксигрупп или галогенов,
Х3 обозначает N или C(R12),
R8 выбран из водорода, C1-C3-алкила, C1-C3-алкоксигруппы и галогена, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, цианогруппы и метоксигруппы, или R8 вместе с R9 образуют кольцевую систему, как здесь описано,
R9 выбран из группы, включающей водород, C1-C3-алкил, C1-C3-алкоксигруппу, фтор, хлор, бром и йод, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и метоксигруппы, и где R9 предпочтительно обозначает водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензоксазол, который необязательно может быть частично гидрированным и 2-оксозамещенным, 1,3-бензодиоксол, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, 1,3-бензотиазол, 2,3-дигидро-1-бензотиофен, который замещен одной или двумя оксогруппами (предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксо-2,3-дигидро-1-бензотиофена), 3-оксо-2,3-дигидро-1Н-изоиндол или 1,3 дигидро-2-бензофуран, который может быть незамещенным или замещенным одной или двумя группами, выбранными из оксогруппы, фтора и метила, предпочтительно одной оксогруппой или одной оксогруппой и одной метильной группой,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, C1-C3-алкоксигруппу, C2-C4-алкенил, C2-C4-алкинил, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, C1-C3-алкилкарбонил, C1-C3-алкоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, где каждый алкил, алкенил, алкинил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из группы, включающей галоген, цианогруппу, гидроксигруппу, фтор(C1-C3)алкоксигруппу и C1-C3-алкоксигруппу, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, C1-C3-алкил, C1-C3-алкоксигруппу, C1-C3-алкилкарбонил, C1-C3-алкоксикарбонил, фтор, хлор, бром и йод, где каждый алкил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора, хлора, брома, йода и C1-C3-алкоксигруппы,
R12, если присутствует, выбран из группы, включающей водород, C1-C3-алкил, C1-C3-алкоксигруппу, фтор, хлор, бром и йод, где каждый алкил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора, хлора, брома, йода и C1-C3-алкоксигруппы,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R10 и R11 отличается от водорода и более предпочтительно, если по меньшей мере один из R8, R9, R10 и R11 также отличается от незамещенного алкила,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном предпочтительном варианте осуществления в соединениях формулы IIa, IIb и IIc, Y выбран из группы, включающей водород, галоген, гидроксигруппу, незамещенный или фторированный метил и незамещенную или фторированную метоксигруппу. В одном варианте осуществления Y обозначает фтор, хлор, метоксигруппу или трифторметил. В одном предпочтительном варианте осуществления значениями для n и р независимо являются 0, 1 или 2.
В другом предпочтительном варианте осуществления в соединениях формулы IIa, IIb или IIc, значением для всех m, n и р является 0.
В особенно предпочтительном варианте осуществления, для соединений формулы IIa, IIb и IIc:
m равно 0 или 1,
n и р независимо равны 0, 1 или 2,
Y выбран из галогена, гидроксигрупны, фторированного метила и незамещенной или фторированной метоксигруппы,
R4 обозначает водород,
R5 обозначает водород, метил, метоксигруппу, или галоген, предпочтительно водород,
Х3 обозначает N или C(R12),
R8 выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу, фторметоксигруппу и фторметил, или R8 вместе с R9 образуют кольцевую систему, как здесь описано,
R9 обозначает водород или фтор, предпочтительно водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 1,3-бензодиоксол, 2-оксо-2,3-дигидро-1,3-бензоксазол, 2,2-дифтор-1,3-бензодиоксол и 4-метил-2-оксодигидробензофуран,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, этенил, пропенил, этинил, пропаргил, пентафторсульфанил, незамещенную, фторированную или гидроксилированную C1-C3-алкилоксигруппу, включая моно-, ди- и трифторметоксигруппу и моно-, ди- и трифторэтоксигруппу, незамещенный или фторированный C1-C3-алкилокси(C1-C3)алкил, незамещенную или фторированную C1-C3-алкилокси(C1-C3)алкилоксигруппу, незамещенный или фторированный C1-C3-алкилокси(C2-C3)алкенил, незамещенный или фторированный C1-C3-алкилокси(C2-C3)алкинил, незамещенный или фторированный C1-C3-алкил, включая трифторметил, и циклопропил, который содержит заместитель, выбранный из гидроксигруппы, гидроксиметила, C1-C2-алкоксигруппы и C1-C2-алкоксикарбонила,
или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из водорода, фтора, хлора и метоксигруппы,
R12, если присутствует, выбран из водорода и фтора,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы,
где в одном предпочтительном варианте осуществления, если R9 не образуют кольцо вместе с R8 или R10, то R10 не обозначает водород, и более предпочтительно, если R8 и R10 оба не обозначают водород.
В особенно предпочтительном варианте осуществления, для соединений формулы IIa, IIb и IIc:
значением для всех m, n и р является 0,
R4 обозначает водород,
R5 обозначает водород, метил, метоксигруппу или галоген, предпочтительно водород,
Х3 обозначает N или C(R12),
R8 выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу, фторметоксигруппу и моно-, ди- и трифторметил, и предпочтительно выбран из фтора и метоксигруппы, или R8 вместе с R9 образуют кольцевую систему, как здесь описано,
R9 обозначает водород или фтор, предпочтительно водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 1,3-бензодиоксол, 2-оксо-2,3-дигидро-1,3-бензоксазол, или 2,2-дифтор-1,3-бензодиоксол,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, пентафторсульфанил, фтор(C1-C2)алкоксигруппу, предпочтительно дифторэтоксигруппу или трифторэтоксигруппу, и фтор(C1-C2)алкил, предпочтительно трифторметил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из водорода, фтора, хлора, метоксигруппы и фторметоксигруппы, предпочтительно из фтора и метоксигруппы,
R12, если присутствует, выбран из водорода, метоксигруппы и фтора,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы,
где в одном предпочтительном варианте осуществления, если R9 не образуют кольцо вместе с R8 или R10, то R10 не обозначает водород, и более предпочтительно, если R8 и R10 оба не обозначают водород
В особенно предпочтительном варианте осуществления соединений формулы IIa, IIb и IIc:
значением для всех m, n и р является 0,
R4 обозначает водород,
R5 обозначает водород, метил, метоксигруппу или галоген, предпочтительно водород,
R8 выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу и трифторметил, или R8 вместе с R9 образуют кольцевую систему, как здесь описано,
R9 обозначает водород или фтор, предпочтительно водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензооксадиазол, 1,3-бензодиоксол, 2-оксо-2,3-дигидро-1,3-бензоксазол, или 2,2-дифтор-1,3-бензодиоксол, R10 выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, цианометил, пентафторсульфанил, дифторэтоксигруппу, трифторэтоксигруппу и трифторметил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано, где в предпочтительном варианте осуществления R8 и R10 оба не обозначают водород,
R11 выбран из водорода, фтора, хлора и метоксигруппы,
R12 выбран из водорода и фтора,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
Другой вариант осуществления относится к соединениям формулы IIa - IIc, в которых:
m равно 0 или 1, предпочтительно 0,
n обозначает любое число, равное от 0 до 3, и предпочтительно равное 0 или 1,
р обозначает любое число, равное от 0 до 2, и предпочтительно равное 0 или 1,
любой Y обозначает заместитель, независимо выбранный из галогена, гидроксигруппы, C1-C3-алкила, C1-C3-алкоксигруппы, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-C3-алкоксигруппы,
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, метоксигруппу и трифторметил, и предпочтительно обозначает водород,
Х3 обозначает N или C(R12),
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил,
R9 выбран из водорода, фтора, хлора или брома, и предпочтительно обозначает водород,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, C2-C3-алкенил, C2-C3-алкинил, C1-C3-алкилоксигруппу, цианогруппу, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, где каждый алкил, алкоксигруппа, алкенил или алкинил необязательно может содержать один или более заместителей, выбранных из группы, включающей галоген, цианогруппу, гидроксигруппу, и незамещенную или фторированную и/или гидроксилированную C1-C3-алкоксигруппу,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, предпочтительно метил, фтор(C1-C3)алкил, предпочтительно трифторметил, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3) алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор, хлор или бром,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R10 и R11 отличается от водорода, и предпочтительно по меньшей мере один из R8, R10 и R11 также отличается от незамещенного алкила,
где в одном предпочтительном варианте осуществления R10 отличается от водорода и в особенно предпочтительном варианте осуществления R10 и R8 оба не обозначают водород,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы IIa - IIc, в которых:
m равно 0 или 1, предпочтительно 0,
n обозначает любое число, равное от 0 до 3, и предпочтительно равное 0 или 1,
р обозначает любое число, равное от 0 до 2, и предпочтительно равное 0 или 1,
любой Y обозначает заместитель, независимо выбранный из галогена, C1-C3-алкила, C1-C3-алкоксигруппы, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-C3-алкоксигруппы,
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, метоксигруппу и трифторметил, предпочтительно водород или йод, и предпочтительно обозначает водород,
Х3 обозначает N или C(R12),
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил,
R9 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, C1-C3-алкил, предпочтительно метил, цианогруппу, и фтор(C1-C3)алкил, предпочтительно трифторметил, и предпочтительно обозначает водород, фтор, хлор или бром,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, галоген(C1-C3)алкил, предпочтительно фтор(C1-C3)алкил, особенно предпочтительно трифторметил, C2-C3-алкинил, C1-C3-алкилоксигруппу, галоген(C1-C3)алкилоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, цианогруппу, цианометил, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, предпочтительно метил, фтор(C1-C3)алкил, предпочтительно трифторметил, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор, хлор или бром,
где в предпочтительном варианте осуществления по меньшей мере один из R8, R9, R10 и R11 отличается от водорода, и более предпочтительно, если по меньшей мере один из R8, R9, R10 и R11 также отличается от незамещенного алкила,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой предпочтительный вариант осуществления относится к соединениям формулы IIa, IIb или IIc, в которых:
m равно 0 или 1,
n равно 0, 1 или 2 и предпочтительно равное 0 или 1,
р равно 0 или 1,
любой Y выбран из водорода, галогена, гидроксигруппы, незамещенного или фторированного метила и незамещенной или фторированной метоксигруппы,
R4 и R5 оба обозначают водород,
R8 выбран из водорода, метоксигруппы, фторметоксигруппы, фтора и хлора, и предпочтительно обозначает фтор,
Х3 обозначает N или C(R12),
R9 выбран из водорода, метоксигруппы, фтора и хлора, и предпочтительно обозначает водород,
R10 выбран из группы, включающей водород, этинил, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, этинил, фтор, хлор, бром, йод, азидогруппу, трифторметил, трифторметоксигруппу, дифторэтоксигруппу, трифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, фтора, хлора и метоксигруппы, и
R12, если присутствует, обозначает водород или фтор,
и где по меньшей мере один из R8, R9, R10 и R11 отличается от водорода и где в предпочтительном варианте осуществления по меньшей мере R10 отличается от водорода и где в особенно предпочтительном варианте осуществления R8 и R10 оба отличаются от водорода,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой предпочтительный вариант осуществления относится к соединениям формулы IIa, IIb или IIc, в которых:
m равно 0 или 1,
n равно 0, 1 или 2 и предпочтительно равное 0 или 1,
р равно 0, 1 или 2,
любой Y выбран из водорода, галогена, гидроксигруппы, незамещенного или фторированного метила и незамещенной или фторированной метоксигруппы,
R4 и R5 оба обозначают водород,
R8 обозначает фтор или метоксигруппу,
Х3 обозначает N или C(R12),
R9 выбран из водорода, метоксигруппы, фтора и хлора, и предпочтительно обозначает водород,
R10 выбран из группы, включающей галоген, этинил, пропинил, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, незамещенный или фторированный (C1-C3)алкил, незамещенный или фторированный (C2-C3)алкенил, незамещенный или фторированный (C2-C3)алкинил, незамещенную или фторированную C1-C3-алкилоксигруппу, незамещенный или фторированный метокси(C1-C3)алкил, незамещенную или фторированную метокси(C1-C3)алкилоксигруппу, незамещенный или фторированный метокси(C2-C3)алкенил, незамещенный или фторированный метокси(C2-C3)алкинил и пентафторсульфанил,
R11 выбран из водорода, фтора и метоксигруппы, и
R12, если присутствует, обозначает водород или фтор,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
В одном предпочтительном варианте осуществления, р равно 1 для соединений формулы IIc, a Y присоединен в положении 8 трициклической кольцевой системы, с образованием соединения формулы II-c1, в которой Y предпочтительно выбран из группы, включающей галоген, метил, фторметил, метоксигруппу, фторметоксигруппу и гидроксигруппу, и в которой Х3, R4, R5, R8, R9, R10 и R11 являются такими, как описано в настоящем изобретении для соединений формулы II-с.
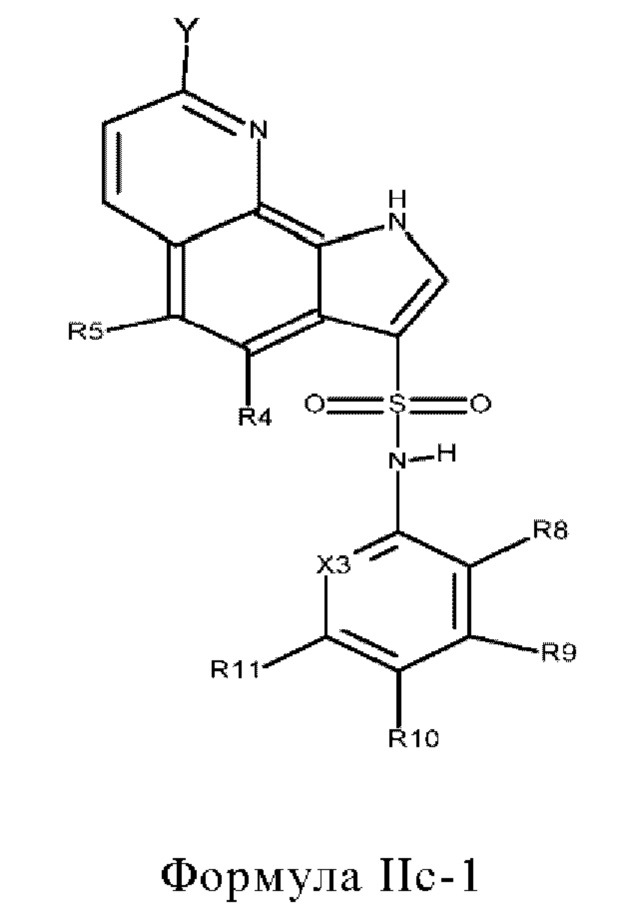
Другой предпочтительный вариант осуществления относится к соединениям формулы IIa, IIb или IIc, в которых
m равно 0 или 1,
n равно 0, 1 или 2 и предпочтительно равное 0 или 1,
р равно 0 или 1 или 2,
любой Y выбран из водорода, галогена, гидроксигруппы, незамещенного или фторированного метила и незамещенной или фторированной метоксигруппы,
R4 и R5 оба выбраны из водорода и фтора,
R8 обозначает фтор или метоксигруппу,
Х3 обозначает N,
R9 выбран из водорода, метоксигруппы, фтора и хлора, и предпочтительно обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, этинил, пропинил, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, незамещенный или фторированный (C1-C3)алкил, незамещенный или фторированный (C2-C3)алкенил, C2-C3-алкинил, незамещенную или фторированную C1-C3-алкилоксигруппу, незамещенный или фторированный C1-C2-алкокси(C1-C3)алкил, незамещенную или фторированную C1-C2-алкокси(C1-C3)алкилоксигруппу, незамещенный или фторированный C1-C2-алкокси(C2-C3)алкенил и пентафторсульфанил,
R11 выбран из группы, включающей водород, фтор, хлор, метоксигруппу, фторметоксигруппу и фторметил,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам,
где в предпочтительном варианте осуществления R10 выбран из группы, включающей хлор, бром, цианометил, цианоэтил, цианометоксигруппу, незамещенный или фторированный (C1-C3)алкил, незамещенную или фторированную C1-C3-алкилоксигруппу, незамещенную или фторированную C1-C2-алкокси(C1-C2)алкилоксигруппу и незамещенный или фторированный метокси(C1-C3)алкил, и в другом предпочтительном варианте осуществления обозначает хлор.
Другой предпочтительный вариант осуществления относится к соединениям формулы IIa, IIb или IIc, в которых R10 выбран из галогена, цианогруппы, цианометила и цианоэтила.
Другой предпочтительный вариант осуществления относится к соединениям формулы IIa, IIb или IIc, в которых:
m равно 0 или 1,
n обозначает любое число, равное от 0 до 3, и предпочтительно равное 0 или 1,
р обозначает любое число, равное от 0 до 2, и предпочтительно равное 0 или 1,
любой Y обозначает заместитель, независимо выбранный из группы, включающей галоген, гидроксигруппу, цианогруппу, C1-C3-алкил, C1-C3-алкоксигруппу, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, гидроксигруппы и C1-C3-алкоксигруппы,
Х3 обозначает C(R12),
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, метоксигруппу и трифторметил, предпочтительно водород или йод,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, предпочтительно метил, и C1-C3-алкоксигруппу, где R8 предпочтительно выбран из фтора и метоксигруппы,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензотиазол, 2,3-дигидро-1-бензотиофен, который замещен одной или двумя оксогруппами (предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксо-2,3-дигидро-1-бензотиофена), необязательно метилированный 3-оксо-1,3-дигидро-2-бензофуран-5-ил и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
R11 выбран из водорода, фтора, хлора, брома, йода и метоксигруппы, и
R12 выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу, фторметоксигруппу, метил и фторметил.
Другой предпочтительный вариант осуществления относится к соединениям формулы IIa, IIb или IIc, в которых:
m равно 0 или 1,
n равно 0, 1 или 2 и предпочтительно равно 0,
р равно 0 или 1, предпочтительно 0,
любой Y выбран из водорода, галогена, незамещенного или фторированного метила и незамещенной или фторированной метоксигруппы,
R4, R5 оба обозначают водород,
Х3 обозначает C(R12),
R8 обозначает водород, метоксигруппу или фтор, и предпочтительно обозначает водород,
R9 вместе с R10 и с атомами С, к которым они присоединены, образуют кольцо, выбранное из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол и 2,2-дифтор-1,3-бензодиоксол, предпочтительно 2,1,3-бензотиадиазол,
R11 обозначает водород или фтор, и
R12 обозначает водород или фтор,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой предпочтительный вариант осуществления относится к соединениям формулы IIa, IIb или IIc; в которых:
m равно 0 или 1,
n обозначает любое число, равное от 0 до 3, и предпочтительно равное 0 или 1,
р обозначает любое число, равное от 0 до 2, и предпочтительно равное 0 или 1,
любой Y обозначает заместитель, независимо выбранный из галогена, гидроксигруппы, C1-C3-алкила, C1-C3-алкоксигруппы, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-C3-алкоксигруппы,
Х3 обозначает C(R12),
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, метоксигруппу, и трифторметил, предпочтительно водород или йод,
R9 вместе с R8 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, галоген(C1-C3)алкил, предпочтительно фтор(C1-C3)алкил, особенно предпочтительно трифторметил, C2-C3-алкинил, C1-C3-алкилоксигруппу, галоген(C1-C3)алкилоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, где R10 предпочтительно обозначает водород, фтор, хлор или бром,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкил, предпочтительно метил, фтор(C1-C3)алкил, предпочтительно трифторметил, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, незамещенный или фторированный C1-C3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-C3-алкоксикарбонил, предпочтительно метоксикарбонил, и цианогруппу, и более предпочтительно обозначает водород, фтор, хлор или бром,
R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-C3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(C1-C3)алкоксигруппу, предпочтительно фтор(C1-C2)алкоксигруппу, C1-C3-алкил, предпочтительно метил, и фтор(C1-C3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор, хлор или бром,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой предпочтительный вариант осуществления относится к соединениям формулы IIa, IIb или IIc, в которых:
m равно 0 или 1,
n равно 0, 1 или 2 и предпочтительно равно 0,
р равно 0 или 1 и предпочтительно равно 0,
любой Y выбран из водорода, галогена, незамещенного или фторированного метила и незамещенной или фторированной метоксигруппы,
Х3 обозначает C(R12)
R4 и R5 оба обозначают водород,
R8 вместе с R9 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 2,1,3-бензоселенадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол, незамещенный 1,3-бензодиоксол и 2,2-дифтор-1,3-бензодиоксол,
R10 выбран из группы, включающей водород, фтор, хлор, бром, трифторметил, трифторметоксигруппу, дифторэтоксигруппу, трифторэтоксигруппу и цианогруппу, и предпочтительно обозначает водород или фтор,
R11 выбран из группы, включающей водород, метоксигруппу, фтор, хлор, бром и цианогруппу, и предпочтительно обозначает водород или фтор,
R12 обозначает водород, фтор, хлор и трифторметил,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой предпочтительный вариант осуществления относится к соединениям, имеющим структуру формулы II,
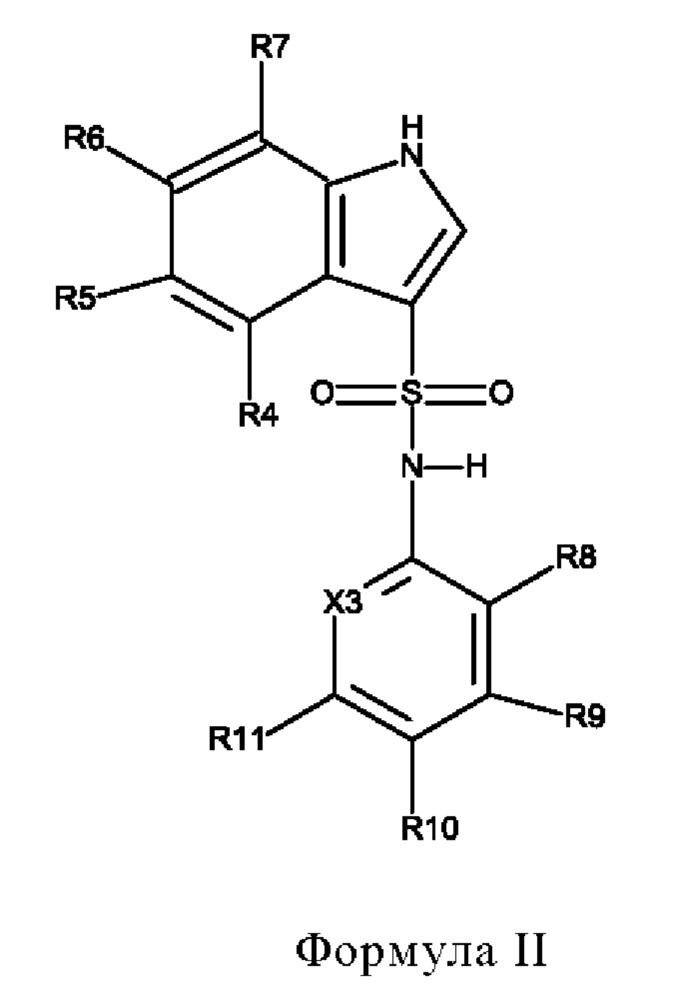
в которой
R4 и R5 оба обозначают водород или фтор;
R6 выбран из группы, включающей фтор, хлор, бром, аминогруппу, нитрогруппу, цианогруппу, азидогруппу, незамещенный или фторированный C1-C3-алкил, предпочтительно выбран из группы, включающей метил, этил, пропил, предпочтительно изопропил, фторметил, предпочтительно трифторметил, незамещенный или фторированный метилсульфонил, незамещенный или фторированный метилсульфинил, незамещенную или фторированную C1-C3-алкилоксигруппу, более предпочтительно выбран из группы, включающей метоксигруппу, фторметоксигруппу и фторэтоксигруппу, незамещенную или фторированную C1-C2-алкилокси(C1-C2)алкилоксигруппу, включая метоксиэтоксигруппу, циклопропил, циклопропилметоксигруппу, фенил, феноксигруппу, бензилоксигруппу, бензилсульфинил, 2-тиенил, 3-тиенил, 3-пиридил, 4-пиридил, тетрагидрофуранил, тетрагидрофуранилметоксигруппу и диметилоксазол, где каждый фенильный, феноксильный, бензилокс ильный, 2-тиенильный, 3-тиенильный, 3-пиридильный, 4-пиридильный остаток необязательно может быть замещен одним или несколькими заместителями, выбранными из фтора, хлора, незамещенного или фторированного метила или незамещенной или фторированной метоксигруппы,
Х3 обозначает C(R12) или N,
R7 выбран из группы, включающей водород, метил, фтор(C1-C2)алкил, предпочтительно моно-, ди- или трифторметил, метилсульфонил, метилсульфинил, метоксигруппу, фтор(C1-C2)алкоксигруппу, цианогруппу, пиридил, пиридилметоксигруппу, феноксигруппу, оксазол, изоксазол, цианогруппу, фтор, хлор или бром, и предпочтительно обозначает водород, метоксигруппу, фтор или бром, где каждый пиридильный, изоксазольный и фенильный остаток необязательно может быть замещен одним или несколькими заместителями, выбранными из фтора, хлора, незамещенного или фторированного метила или незамещенной или фторированной метоксигруппы;
R8 и R11 независимо выбраны из водорода, фтора, хлора и незамещенной или фторированной метоксигруппы;
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, йод, ацетил, азидогруппу, нитрогруппу, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, незамещенный или фторированный C1-C2-алкоксициклопропил, незамещенный или фторированный C1-C2-алкоксикарбонилциклопропил, циклопропилметоксигруппу, циклопропилметил, незамещенный или фторированный C1-C3-алкил, предпочтительно выбран из группы, включающей метил и трифторметил, незамещенную или фторированную и/или гидроксилированную C1-C3-алкоксигруппу, более предпочтительно выбран из группы, включающей метоксигруппу, дифторметоксигруппу, трифторметоксигруппу, дифторэтоксигруппу и трифторэтоксигруппу, незамещенный или фторированный C1-C2-алкокси(C1-C3)алкил, предпочтительно незамещенный или фторированный метоксипропил, незамещенную или фторированную C1-C2-алкокси(C1-C3)алкоксигруппу, включая фторметоксиэтоксигруппу, незамещенный или фторированный C2-C3-алкенил, незамещенный или фторированный C2-C3-алкинил, предпочтительно этинил, незамещенный или фторированный C1-C2-алкокси(C2-C3)алкенил, предпочтительно метоксипропенил, незамещенный или фторированный C1-C2-алкокси(C2-C3)алкинил и пентафторсульфанил;
R12, если присутствует, обозначает водород или фтор,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой предпочтительный вариант осуществления относится к соединениям формулы II, в которых R4 и R5 оба обозначают водород; R6 выбран из группы, включающей фтор, хлор, бром, метил, этил, изопропил, трифторметил, метилсульфонил, метоксигруппу, циклопропил, циклопропилметоксигруппу, фенил, феноксигруппу, бензилоксигруппу, 2-тиенил, 3-тиенил, 3-пиридил, 4-пиридил, тетрагидрофуранил и диметилоксазол, Х3 обозначает C(R12), R9 обозначает водород; R7 выбран из группы, включающей водород, метил, трифторметил, метоксигруппу, фтор, хлор или бром, и предпочтительно обозначает водород, метоксигруппу или бром; R8 и R11 независимо выбраны из водорода, фтора, хлора и метоксигруппы; R10 обозначает фтор, хлор, бром, йод, ацетил, азидогруппу, этинил, цианогруппу, цианометил, трифторметил, дифторэтоксигруппу, трифторэтоксигруппу или пентафторсульфанил; R12 обозначает водород или фтор, и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам
Другой вариант осуществления относится к соединениям формулы II, в которых:
R4 обозначает водород или фтор, предпочтительно водород;
R5 выбран из водорода, фтора, хлора, брома, метоксигруппы и фторметоксигруппы,
R6 выбран из группы, включающей галоген, цианогруппу, аминогруппу, нитрогруппу, незамещенный или фторированный метилсульфонил, незамещенный или фторированный метилсульфинил, C1-C3-алкил, C1-C3-алкилоксигруппу, C2-C3-алкенил, циклопропил, фенил, феноксигруппу, бензилоксигруппу, бензилсульфинил, 2-тиенил, 3-тиенил, 3-пиридил, и 4-пиридил, где каждый фенил, феноксигруппа, бензилоксигруппа, 2-тиенил, 3-тиенил, 3-пиридил, 4-пиридил необязательно может быть замещен одним или большим количеством атомов фтора, хлора, незамещенных или фторированных метилов или незамещенных или фторированных метоксигрупп, и где каждая алкильная, алкенильная группа и алкоксигруппа может быть незамещенной или замещенной одной или более группами, выбранными из галогена, метоксигруппы, фторметоксигруппы, цианогруппы, циклопропила и галогена,
Х3 обозначает C(R12) или N,
R7 выбран из группы, включающей водород, цианогруппу, фтор, хлор, бром, незамещенный или фторированный C1-С3-алкил, предпочтительно выбран из группы, включающей метил, фторметил и фторэтил, и незамещенную или фторированную C1-С3-алкилоксигруппу, более предпочтительно выбран из группы, включающей метоксигруппу, фторметоксигруппу и фторэтоксигруппу,
R8 и R11 независимо выбраны из группы, включающей водород, фтор, хлор, цианогруппу, метил, фторметил, метоксигруппу и фторметоксигруппу;
R9 обозначает водород или фтор, предпочтительно водород,
R10 выбран из группы, включающей галоген, азидогруппу, цианогруппу, циклопропил, нитрогруппу, C1-С3-алкил, C1-С3-алкоксигруппу, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилкарбонил(C1-С3)алкил, C1-С3-алкоксикарбонил(C1-С3)алкил и пентафторсульфанил, где каждая алкильная, алкенильная, алкинильная группа и алкоксигруппа может быть незамещенной или замещенной одним или несколькими остатками, выбранными из группы, включающей фтор, хлор, цианогруппу, циклопропил и незамещенную или фторированную и/или гидроксилированную C1-С3-алкоксигруппу, и где каждая циклопропильная группа может быть замещена одним или несколькими остатками, выбранными из группы, включающей галоген, гидроксигруппу, гидроксиметил, C1-С3-алкоксигруппу, C1-С3-алкоксикарбонил и цианогруппу,
R12, если присутствует, обозначает водород или фтор,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы II, в которых:
R4 обозначает водород,
R5 выбран из водорода, фтора, хлора и брома,
R6 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, нитрогруппу, метил, этил, изопропил, фторметил, предпочтительно трифторметил, фторэтил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, цианогруппу, метилсульфинил, метилсульфонил, циклопропил, фенил, бензилоксигруппу, 2-тиенил и 3-тиенил,
R7 выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, фтор(С1-С2)алкил, предпочтительно трифторметил, и фтор(С1-С2)алкоксигруппу, и предпочтительно обозначает водород, фтор, метоксигруппу, фторметоксигруппу и фторэтоксигруппу,
Х3 обозначает C(R12),
R8 и R11 независимо выбраны из группы, включающей водород, фтор, хлор, цианогруппу, фторметил, метоксигруппу и фторметоксигруппу,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, йод, азидогруппу, незамещенный или фторированный C1-С3-алкил, предпочтительно трифторметил, незамещенную или фторированную C1-С3-алкилоксигруппу, предпочтительно выбран из группы, включающей дифторэтоксигруппу, трифторметоксигруппу и трифторэтоксигруппу, незамещенный или фторированный C1-С3-алкокси(C1-С3)алкил, незамещенную или фторированную C1-С3-алкокси(C1-С3)алкоксигруппу, незамещенный или фторированный C1-С3-алкокси(С2-С3)алкенил, пентафторсульфанил, этинил, пропинил, цианогруппу, цианометоксигруппу и цианометил, и
R12 обозначает водород и фтор,
где предпочтительно, если по меньшей мере один из R8 и R11 обозначает фтор или хлор, более предпочтительно фтор.
Другой вариант осуществления относится к соединениям формулы II, в которых R4 и R5 оба обозначают водород, R6 выбран из группы, включающей фтор, хлор, бром, йод, метил, изопропил, трифторметил, метилсульфонил, циклопропил, фенил, бензилоксигруппу, 2-тиенил и 3-тиенил, Х3 обозначает C(R12), R7 выбран из группы, включающей водород, метил, метоксигруппу, фтор, хлор, бром и трифторметил, предпочтительно из фтора и брома, R8 и R11 независимо выбраны из группы, включающей водород, фтор, хлор и метоксигруппу, R9 обозначает водород, R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, азидогруппу, трифторметил, дифторэтоксигруппу, трифторметоксигруппу, трифторэтоксигруппу, пентафторсульфанил, этинил, цианогруппу и цианометил, R12 обозначает водород и фтор, где предпочтительно, если по меньшей мере один из R8 и R11 обозначает фтор или хлор, более предпочтительно фтор.
Другой вариант осуществления относится к соединениям формулы II, в которых R4 и R5 оба обозначают водород, R6 выбран из группы, включающей фтор, хлор, бром, изопропил, трифторметил, циклопропил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, метилсульфинил и бензилоксигруппу, R7 обозначает водород, метил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, фторметил, цианогруппу, бром или фтор, Х3 обозначает C(R12), R9 обозначает водород, R10 выбран из группы, включающей фтор, бром, хлор, йод, метил, фторметил, предпочтительно трифторметил, фтор(С1-С2)алкоксигруппу, предпочтительно дифторэтоксигруппу и трифторметоксигруппу, пентафторсульфанил, цианогруппу, цианометоксигруппу, цианометил и цианоэтил, R12 обозначает водород или фтор, и R8 и R11 независимо выбраны из группы, включающей водород, фтор, хлор, метоксигруппу и фторметоксигруппу, и в одном предпочтительном варианте осуществления оба отличаются от водорода.
Другой вариант осуществления относится к соединениям формулы II, в которых R4 и R5 оба обозначают водород, R6 выбран из группы, включающей фтор, хлор, бром, изопропил, трифторметил, циклопропил и бензилоксигруппу, R7 обозначает водород, метоксигруппу или фтор, Х3 обозначает C(R12), R9 обозначает водород, R10 выбран из группы, включающей фтор, бром, хлор, йод, трифторметил, дифторэтоксигруппу, трифторметоксигруппу, пентафторсульфанил, цианогруппу и цианометил, R12 обозначает водород или фтор, и R8 и R11 оба отличаются от водорода и предпочтительно обозначают фтор, хлор, метоксигруппу или цианогруппу, более предпочтительно фтор.
Другой предпочтительный вариант осуществления относится к соединениям формулы II, в которых R4 и R5 оба обозначают водород, R6 выбран из группы, включающей фтор, хлор, бром, изопропил, фторметил, метоксигруппу, фторметоксигруппу и фенилоксигруппу, R7 обозначает водород, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, цианогруппу, фтор или хлор, Х3 обозначает C(R12), R9 обозначает водород или фтор, R10 обозначает водород, R12 обозначает водород или фтор, и R8 и R11 оба независимо выбраны из фтора, хлора и метоксигруппы.
Другой предпочтительный вариант осуществления относится к соединениям формулы II, в которых R4, и R5 оба обозначают водород, R6 выбран из группы, включающей фтор, хлор, бром, изопропил, трифторметил и фенилоксигруппу, R7 обозначает водород, метоксигруппу или фтор, Х3 обозначает C(R12), R9 обозначает водород или фтор, R10 обозначает водород, R12 обозначает водород или фтор, и R8 и R11 оба независимо выбраны из фтора, хлора и цианогруппы.
Другой предпочтительный вариант осуществления относится к соединениям формулы II, в которых R4 и R5 оба обозначают водород, R6 выбран из группы, включающей фтор, хлор, бром, йод, метил, этил, изопропил, фторметил, предпочтительно трифторметил, метоксигруппу, метилсульфинил, метилсульфонил, циклопропил, фенил, бензилоксигруппу, 2-тиенил и 3-тиенил, и предпочтительно из фтора, хлора, брома и трифторметила, R7 обозначает водород, метоксигруппу или фтор, предпочтительно водород, Х3 обозначает C(R12), R8 обозначает водород, R9 и R10 вместе с атомами С, к которым они присоединены, образуют 2,1,3-бензотиадиазол, 3-оксо-1,3-дигидро-2-бензофуран или 1-метил-3-оксо-1,3-дигидро-2-бензофуран, и R11 и R12 независимо выбраны из водорода и фтора.
Другой вариант осуществления относится к соединениям формулы II, в которой R4 и R5 оба обозначают водород, R6 выбран из фтора, хлора, брома и метилсульфонила, R7 выбран из группы, включающей водород, фтор, бром, хлор, метоксигруппу и трифторметил, Х3 обозначает C(R12), R8 и R9 вместе с кольцом, к которому они присоединены, образуют 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол или необязательно 2,2-фторзамещенный 1,3-бензодиоксол, R10 обозначает водород, фтор или бром, R11 выбран из водорода, фтора и цианогруппы, и R12 обозначает водород, фтор или трифторметил.
Другой вариант осуществления относится к соединениям формулы II, в которых R4 обозначает водород, R5 выбран из водорода и фтора, R6 выбран из фтора, хлора, брома, метоксигруппы и трифторметила, R7 выбран из группы, включающей водород, галоген, метилсульфонил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу и фторметил, предпочтительно обозначает трифторметил, Х3 обозначает N, R8 обозначает фтор, хлор или метоксигруппу, R9 выбран из группы, включающей водород, фтор, хлор, метил и метоксигруппу, и предпочтительно обозначает водород, R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, цианоэтил, пентафторсульфанил, моно-, ди- и трифторметил, моно-, ди- и трифторметоксигруппу, моно-, ди- и трифторэтоксигруппу, незамещенный или фторированный С1-С2-алкокси(C1-С3)алкил, незамещенную или фторированную С1-С2-алкокси(С1-С2)алкоксигруппу, этинил и цианометил, и R11 выбран из группы, включающей водород, фтор, хлор, фторметил, метоксигруппу и фторметоксигруппу.
Другой вариант осуществления относится к соединениям формулы II, в которых R4, R5 оба обозначают водород, R6 выбран из фтора, хлора, брома и метоксигруппы, R7 выбран из группы, включающей водород, фтор, хлор, бром, фторметил, метоксигруппу и фторметоксигруппу, Х3 обозначает N, R8 обозначает фтор или метоксигруппу, R9 обозначает водород, R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, ацетил, метил, этил, этоксиэтил, метоксипропил, фторированный метоксипропил, фторметил, фторметоксиметил, метоксикарбонилциклопропил, этоксикарбонилциклопропил, этенил, этоксиэтенил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, фторпропоксигруппу, метоксиэтоксигруппу, фторированную метоксиэтоксигруппу, этоксиэтоксигруппу, фторированную этоксиэтоксигруппу, метоксипропоксигруппу, фторированную метоксипропоксигруппу, метоксипропенил и фторметоксипропенил, и R11 обозначает водород, метоксигруппу, фтор или хлор.
Другой вариант осуществления относится к соединениям формулы II, в которых R4 и R5 оба обозначают водород, R6 обозначает хлор или бром, R7 выбран из группы, включающей водород, фтор, хлор, бром и метоксигруппу, и Х3 обозначает C(R12) или N, R8 обозначает фтор, хлор или метоксигруппу, R9 обозначает водород или фтор, предпочтительно водород, R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, C1-С3-алкил, С2-С3-алкенил и C1-С3-алкоксигруппу, где каждый алкил, алкенил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из группы, включающей галоген, предпочтительно фтор, цианогруппу, С1-С2-алкоксигруппу и фтор(С1-С2)алкоксигруппу, и R11 обозначает водород, фтор или метоксигруппу.
Другой вариант осуществления относится к соединениям формулы II(d), II(e), II(f) и II(g),
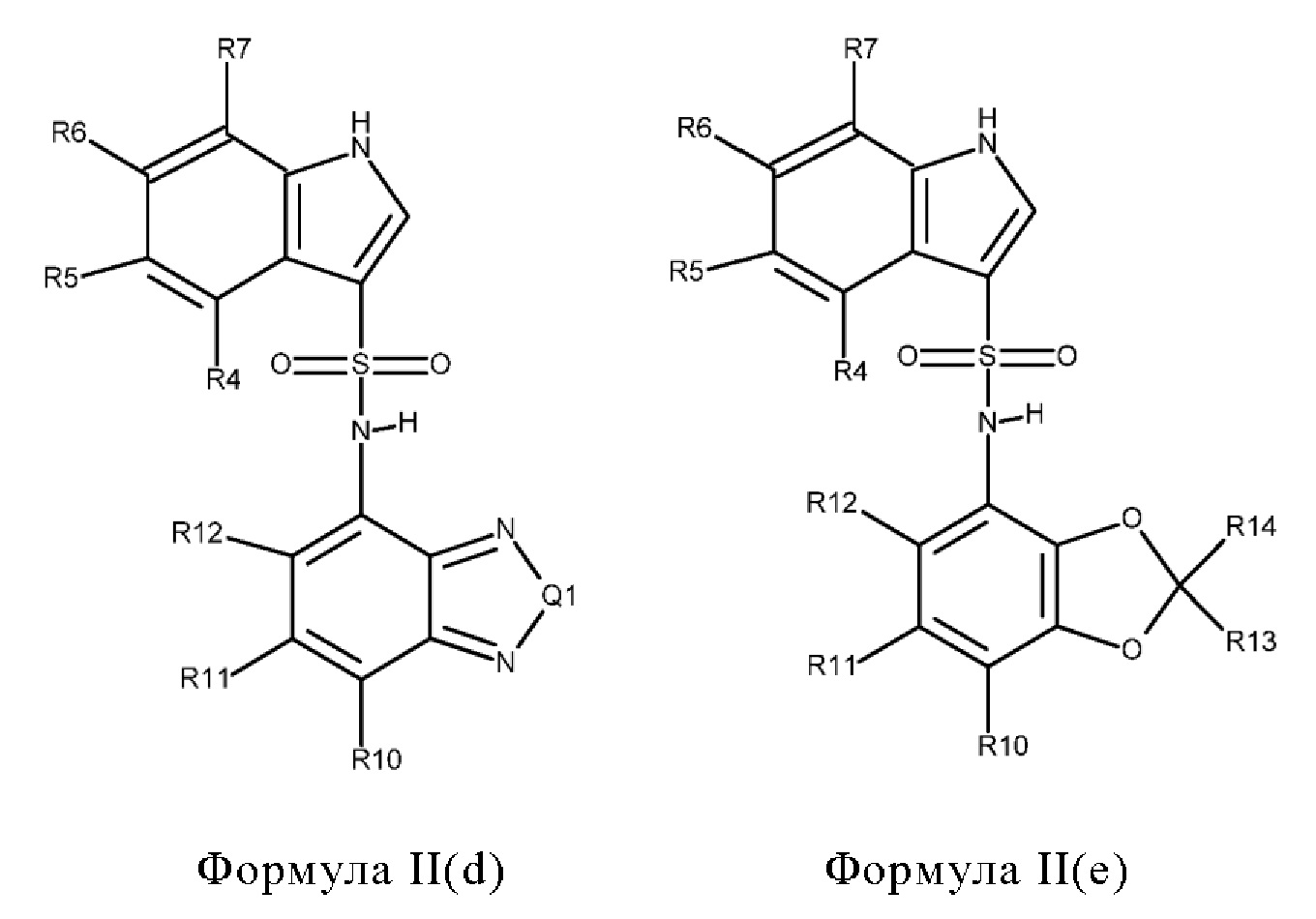
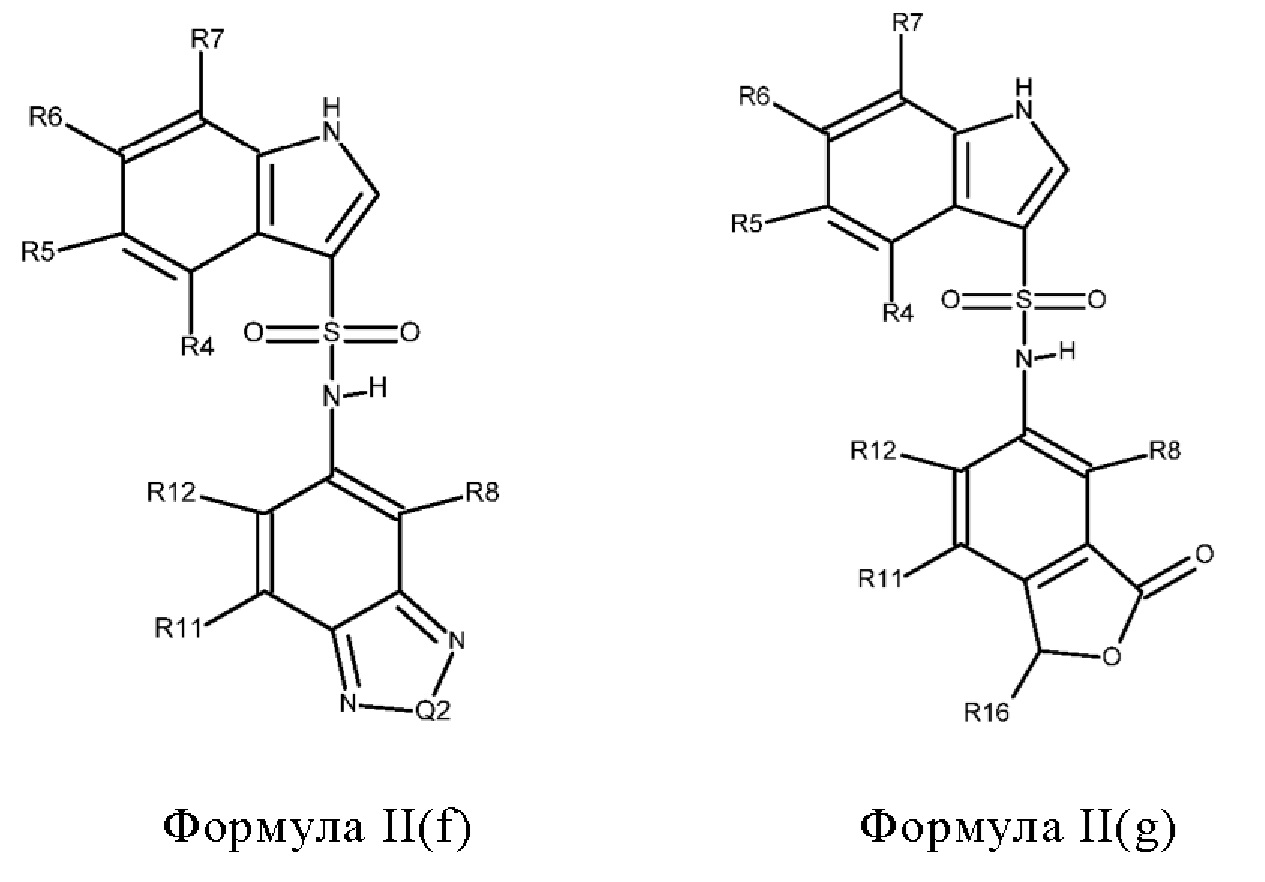
в которой R4, R5, R6, R7, R8, R10, R11 и R12 являются такими, как описано для формул I и II,
где в формуле II(d) Q1 обозначает S или О, и
где в формуле II(е) R13 и R14 выбраны водорода, метила и фтора, и предпочтительно, если они оба обозначают водород или оба обозначают фтор,
где в формуле II(f) Q2 обозначает S или О, предпочтительно S,
и где в формуле II(g) R16 выбран из водорода, фтора, гидроксигруппы, метила, фторметила, метоксигруппы и фторметоксигруппы, и предпочтительно выбран из водорода и метила,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединениям формул II(d), II(е), II(f) и II(g), в которых:
где в формуле II(d) Q1 обозначает S или О, и
где в формуле II(е) R13 и R14 оба выбраны из водорода и фтора,
где в формуле II(f) Q2 обозначает S или О, предпочтительно S,
где в формуле II(g) R16 выбран из водорода и метила,
R4 обозначает водород,
R5 выбран из водорода, фтора, хлора и брома, и предпочтительно обозначает водород,
R6 выбран из группы, включающей фтор, хлор, бром, метил, метоксигруппу, метилсульфонил, метилсульфинил, фторметил, фторметоксигруппу, цианогруппу и бензилоксигруппу, предпочтительно из фтора, хлора, брома и фторметила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу, цианогруппу, метил и фторметил, предпочтительно из водорода и моно-, ди- и трифторметила,
R8, если присутствует, выбран из водорода и галогена, предпочтительно из водорода и фтора, и более предпочтительно обозначает водород,
R10, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, и цианогруппу, предпочтительно обозначает водород или фтор,
R11 выбран из группы, включающей водород, галоген, метоксигруппу, фторметоксигруппу, фторметил и цианогруппу, и предпочтительно обозначает водород или фтор,
R12 выбран из группы, включающей водород, галоген, метоксигруппу, фторметил, предпочтительно из водорода, фтора и фторметила,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
В предпочтительном варианте осуществления, для соединений формулы IId и IIe:
R4 и R5 оба обозначают водород,
R6 выбран из фтора, хлора, брома, трифторметила и фенила,
R7 обозначает водород, фтор, бром, метоксигруппу или трифторметил, предпочтительно водород или трифторметил,
R10 выбран из водорода и галогена, предпочтительно из водорода, фтора и хлора,
R11 выбран из группы, включающей водород, галоген, трифторметил и цианогруппу, предпочтительно из фтора и водорода,
R12 выбран из водорода, галогена и трифторметила, предпочтительно из фтора и водорода,
R13 и R14 в формуле IIe, оба, выбраны из водорода и фтора,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В предпочтительном варианте осуществления, для соединений формулы II(f):
R4 и R5 оба обозначают водород,
R6 выбран из фтора, хлора, брома, трифторметила и фенила,
R7 выбран из водорода, метоксигруппы, фтора и трифторметила,
R8 выбран из водорода и галогена, предпочтительно из водорода и фтора,
R11 выбран из водорода, галогена, трифторметила и цианогруппы, и предпочтительно обозначает водород,
R12 выбран из водорода, галогена и трифторметила, предпочтительно из фтора и водорода,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
Один вариант осуществления относится к соединениям субформул IIa, IIb, IIc, IId, IIe, IIf и IIg, которые дополнительно замещены группой R2, как это показано для приведенной выше общей формулы II-2, таким образом, с образованием соответствующих соединений субформул II-2a, II-2b, II-2c, II-2d, II-2e, II-2f и II-2g, в которых R2 выбран из группы, включающей водород, фтор, хлор, бром, йод и метоксигруппу, и в которых R2 предпочтительно обозначает водород или фтор, и особенно предпочтительно водород, и в которых другие остатки являются такими, как определено в настоящем изобретении для формул II-2a, II-2b, II-2c, II-2d, II-2e, II-2f и II-2g. В качестве неограничивающего примера ниже представлены формулы II-2d и II-2f:
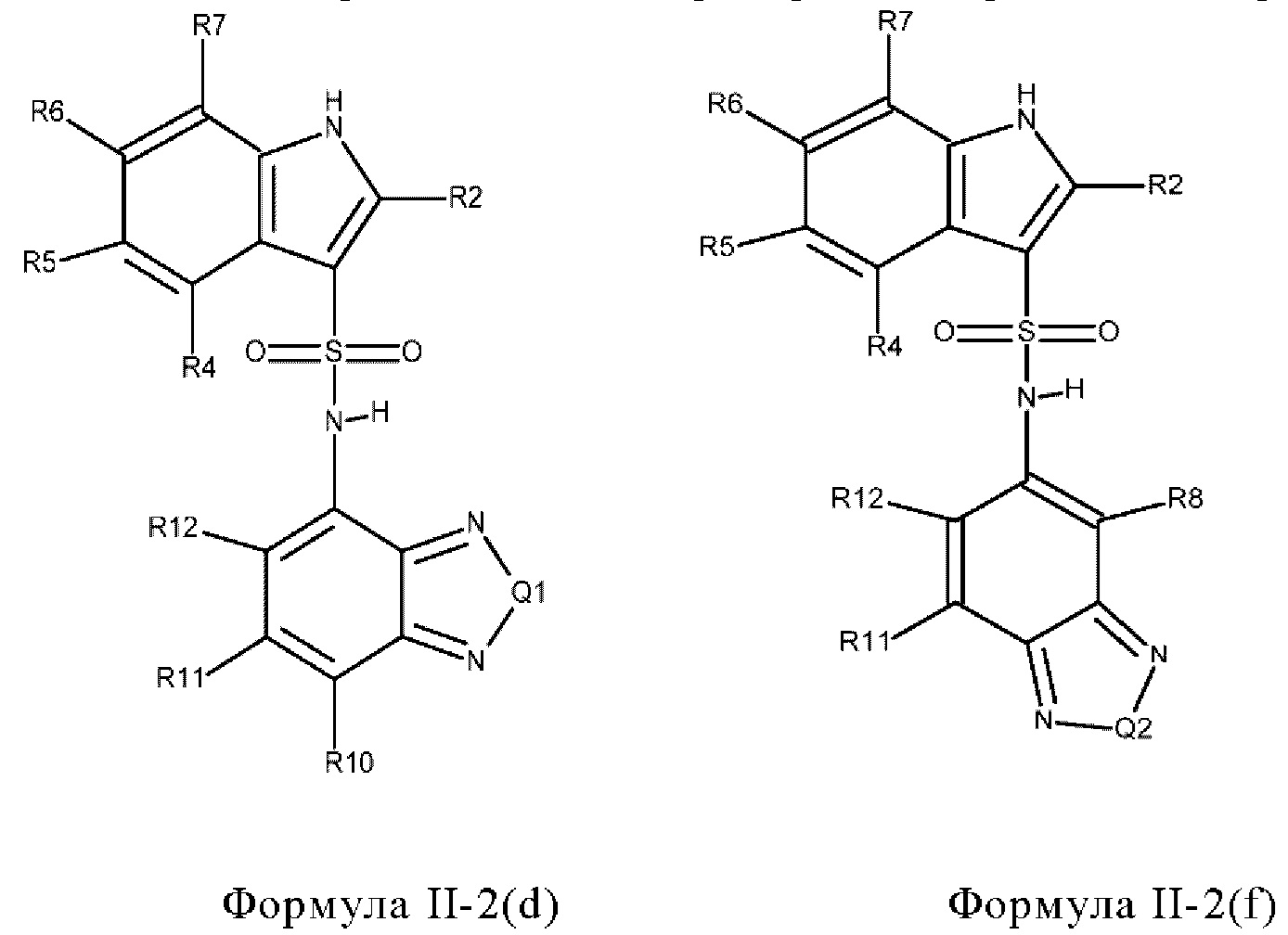
Другой предпочтительный вариант осуществления относится к соединениям формулы III,
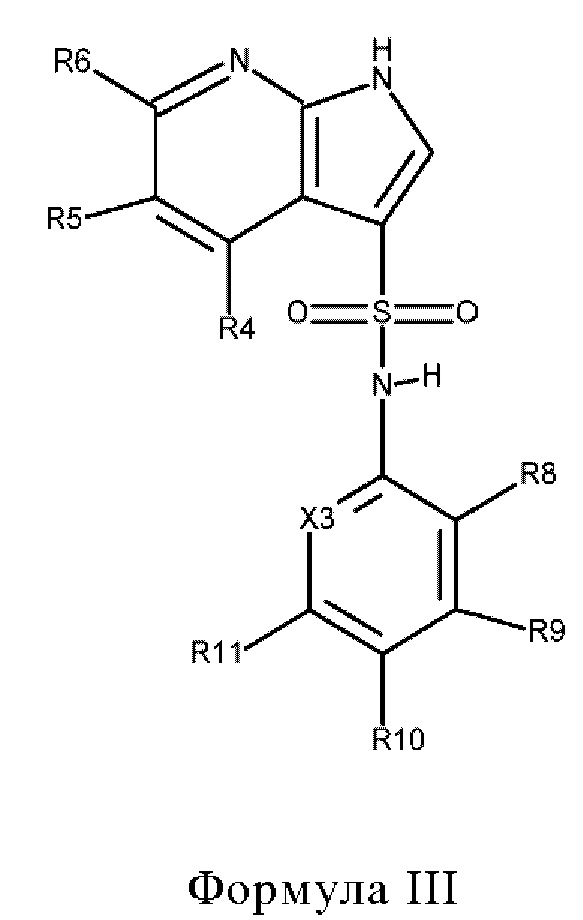
в которой R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей водород, фтор, хлор, бром, фторметил, метоксигруппу, фторметоксигруппу и циклопропил,
Х3 обозначает C(R12) или N,
R8 выбран из водорода, метоксигруппы и галогена, особенно предпочтительно из фтора, хлора, метоксигруппы и водорода,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, бром, хлор, йод, метил, фтор(C1-С3)алкил, предпочтительно трифторметил, незамещенный или фторированный метокси(C1-С3)алкил, незамещенную или фторированную C1-С3-алкилоксигруппу, предпочтительно моно,- ди- и трифторметоксигруппу и моно-, ди- и трифторэтоксигруппу, незамещенную или фторированную метокси(C1-С3)алкилоксигруппу, незамещенный или фторированный С2-С3-алкенил, незамещенный или фторированный метокси(С2-С3)алкенил, этинил, пропаргил, незамещенный или фторированный метокси(С2-С3)алкинил, азидогруппу, пентафторсульфанил, цианометил, цианоэтил и цианогруппу,
R11 обозначает водород, фтор, хлор, или метоксигруппу, особенно предпочтительно водород или фтор,
R12, если присутствует, обозначает водород или фтор,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой вариант осуществления относится к соединениям формулы III, в которых R4 и R5 оба обозначают водород, R6 обозначает хлор или бром, Х3 обозначает C(R12), R12 обозначает водород или фтор, R8 выбран из водорода, метоксигруппы и галогена, особенно предпочтительно из фтора и водорода, R9 обозначает водород, R10 выбран из группы, включающей фтор, бром, хлор, йод, трифторметил, дифторэтоксигруппу, трифторметоксигруппу, трифторэтоксигруппу, этинил, азидогруппу, ацетил, пентафторсульфанил, цианометил и цианогруппу, R11 обозначает водород, фтор, хлор или метоксигруппу, особенно предпочтительно водород или фтор, и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Другой особенно предпочтительный вариант осуществления относится к соединению формулы III, в котором R4 и R5 оба обозначают водород, R6 выбран из группы, включающей метил, фторметил, метоксигруппу, фторметоксигруппу, хлор или бром, Х3 обозначает C(R12), R8 обозначает водород, метоксигруппу или фтор и предпочтительно обозначает фтор, R9 обозначает водород, R10 выбран из группы, включающей фтор, бром, хлор, йод, моно-, ди- и трифторметил, моно-, ди- и трифторметоксигруппу, моно-, ди- и трифторэтоксигруппу, пентафторсульфанил, этинил и цианогруппу, и R11 и R12 независимо выбраны из группы, включающей водород и фтор.
Другой предпочтительный вариант осуществления относится к соединениям формулы III, в которых R4 и R6 обозначают водород, R5 обозначает йод, Х3 обозначает C(R12) или N, R8 и R11 оба независимо выбраны из водорода или фтора, R10 выбран из группы, включающей фтор, бром, хлор, йод, моно-, ди- и трифторметил, моно-, ди- и трифторметоксигруппу, моно-, ди- и трифторэтоксигруппу, пентафторсульфанил и цианогруппу, R9 обозначает водород, и R12, если присутствует, обозначает водород или фтор,
Другой предпочтительный вариант осуществления относится к соединению формулы III, в котором R4 и R5 оба обозначают водород, R6 обозначает хлор или бром, Х3 обозначает C(R12), R8 обозначает водород, R9 и R10 вместе с фенильным кольцом, к которому они присоединены, образуют 2,1,3-бензотиадиазольную кольцевую систему, R11 обозначает водород и R12 обозначает фтор или водород.
Другой предпочтительный вариант осуществления относится к соединению формулы III, в котором R4 и R5 оба обозначают водород, R6 обозначает хлор или бром, Х3 обозначает C(R12), R8 и R9 вместе с фенильным кольцом, к которому они присоединены, образуют 2,1,3-бензотиадиазольную, 2,1,3-бензоксадиазольную, незамещенную 1,3-бензоксолановую или 2,3-дифтор-1,3-бензоксалановую группу, R10 и R11 независимо выбраны из водорода, метоксигруппы, цианогруппы и галогена, предпочтительно из водорода и фтора, и R12 обозначает фтор, трифторметил или водород.
Другой вариант осуществления относится к соединениям формулы III, в которых R4 и R5 оба обозначают водород, R6 выбран из фтора, хлора, брома и моно-, ди- и трифторметила, Х3 обозначает N, R8 обозначает фтор, хлор или метоксигруппу, R9 выбран из водорода, фтора, хлора и метоксигруппы, и предпочтительно обозначает водород, R10 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, моно-, ди и трифторметил, моно-, ди- и трифторметоксигруппу, моно-, ди- и трифторэтоксигруппу, этинил и цианометил, и R11 обозначает водород, фтор или хлор.
Другой вариант осуществления относится к соединениям формулы III, в которых R4 и R5 оба обозначают водород, R6 выбран из хлора, брома, метоксигруппы, моно-, ди- и трифторметила, Х3 обозначает C(R12) или N, R8 выбран из водорода, фтора, хлора, метоксигруппы и фторметоксигруппы, R9 обозначает водород, R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, моно-, ди- и трифторметил, моно-, ди- и трифторметоксигруппу, моно-, ди- и трифторэтоксигруппу, незамещенную или фторированную С1-С2-алкокси(C1-С3)алкоксигруппу, незамещенный или фторированный С1-С2-алкокси(C1-С3)алкил, незамещенный или фторированный С2-С3-алкенил, незамещенный или фторированный С1-С2-алкокси(С2-С3)алкенил и С2-С3-алкинил, R11 обозначает водород, метоксигруппу. фтор или хлор и R12, если присутствует, обозначает водород или фтор.
В одном варианте осуществления соединения имеют структуру, выбранную из формул III(а)-III(с),
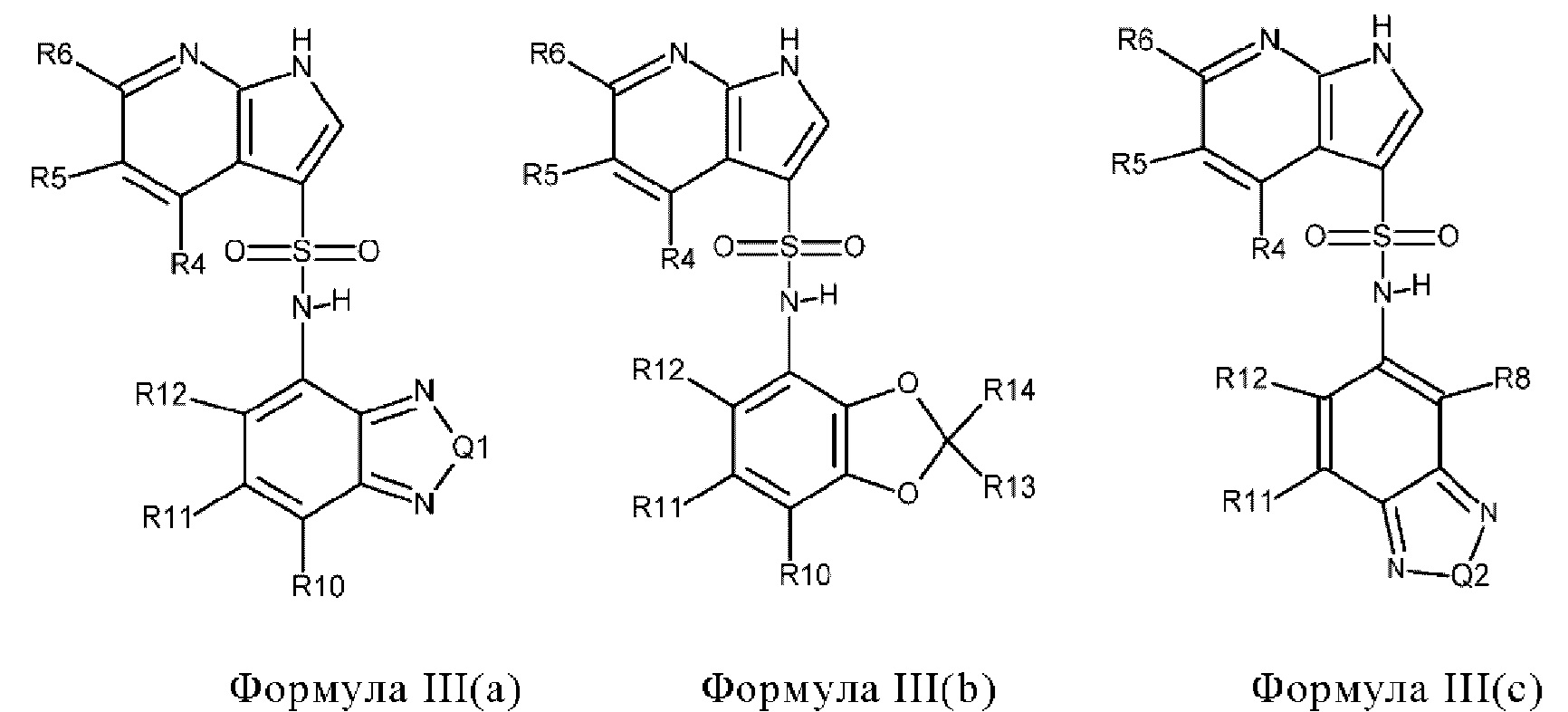
в которых R4, R5, R6, R8, R10, R11 и R12 являются такими, как в настоящем изобретении описано для формул I и III,
где в формуле III(а) Q1 обозначает S или О, и
где в формуле III(b) R13 и R14 выбраны из водорода, метила и фтора, и предпочтительно, если они оба обозначают водород или оба обозначают фтор, и
где в формуле III(с) Q2 обозначает S или О, предпочтительно S,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В предпочтительном варианте осуществления, для соединений формулы III(а)-III(с):
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, моно-, ди- и трифторметил, метоксигруппу и фторметоксигруппу,
R8, если присутствует, обозначает водород или фтор, предпочтительно водород,
R10, если присутствует, выбран из группы, включающей водород и галоген, предпочтительно из группы, включающей водород, фтор и хлор,
R11 выбран из водорода, галогена, трифторметила и цианогруппы, предпочтительно из фтора и водорода,
R12 выбран из водорода, галогена и трифторметила, предпочтительно из водорода и фтора.
Один вариант осуществления относится к соединениям формулы IId, IIe, IIIa и IIIb, в которых:
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, моно-, ди- и трифторметил и метоксигруппу,
R10 выбран из водорода и галогена, предпочтительно из водорода, фтора и хлора,
R11 выбран из водорода, галогена, трифторметила и цианогруппы, предпочтительно из фтора и водорода,
R12 выбран из водорода, галогена и трифторметила,
где в соединениях формулы II(d) и III(а) Q1 обозначает S или О, и
где в формуле II(е) и III(b) R13 и R14 выбраны из водорода и фтора, и предпочтительно, если они оба обозначают водород или оба обозначают фтор.
Один вариант осуществления относится к соединениям формулы IIf и IIIc, в которых:
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, метилсульфонил, моно-, ди- и трифторметил и фенил,
R7, если присутствует, выбран из водорода, метоксигруппы, фтора и трифторметила,
R8 выбран из водорода и галогена, предпочтительно из водорода и фтора,
R11 выбран из водорода, галогена, трифторметила и цианогруппы, и предпочтительно обозначает водород,
R12 выбран из водорода, галогена и трифторметила, предпочтительно из фтора и водорода,
Q2 обозначает О или S, и предпочтительно обозначает S.
Один вариант осуществления относится к соединениям субформул IIIa, IIIb и IIIc, которые дополнительно замещены группой R2, как это показано для приведенной выше общей формулы III-2, таким образом, образуя соответствующие соединения субформул III-2а, III-2b и III-2с, в которых R2 выбран из водорода, фтора, хлора, брома, йода и метоксигруппы, и в которых R2 предпочтительно обозначает водород или фтор и особенно предпочтительно водород, и в которых другие остатки являются такими, как определено в настоящем изобретении для формул IIIa, IIIb и IIIc.
Так, например, если соединение формулы III-с также содержит группу R2, то полученное соединение формулы III-2с является следующим:
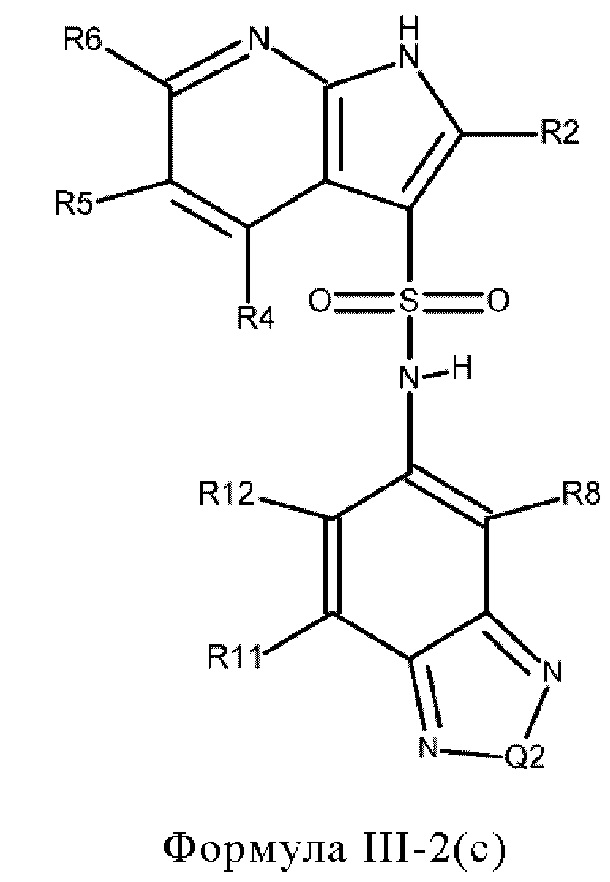
Другим объектом настоящего изобретения являются соединения общей формулой VI, и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы,
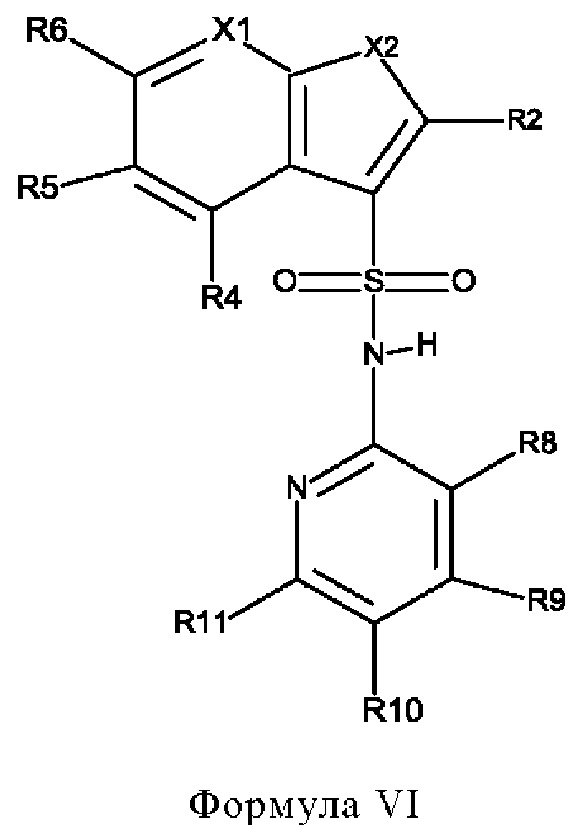
в которой X1, Х2, R2, R4, R5, R6, R8, R9, R10 и R11 имеют значения, описанные выше в настоящем изобретении для соединений формулы I-2, II-2, III-2, IV-2 или V-2, и в которой R2 выбран из водорода, фтора, хлора, брома, йода и метоксигруппы, предпочтительно из водорода и фтора; более предпочтительно, если R2 обозначает водород.
Один вариант осуществления относится к соединению формулы VI, в котором:
X1 обозначает C-R7 или N,
Х2 обозначает NH, S или О, где, если X1 обозначает N, то Х2 предпочтительно обозначает NH,
R2 обозначает водород или фтор, предпочтительно водород,
R4 обозначает водород или фтор,
R5 выбран из группы, включающей водород, галоген, цианогруппу, незамещенный или фторированный C1-С3-алкил, незамещенную или фторированную C1-С3-алкоксигруппу, незамещенный или фторированный C1-С3-алкилкарбонил, незамещенный или фторированный C1-С3-алкилсульфинил и незамещенный или фторированный C1-С3-алкилсульфонил, где R5 предпочтительно выбран из группы, включающей водород, галоген, цианогруппу, метил, метоксигруппу, фторметил и фторметоксигруппу, и более предпочтительно выбран из водорода, фтора, хлора и брома,
или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, нитрогруппу, аминогруппу, C1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкоксигруппу, С3-С6-циклоалкил, С3-C6-гетероциклоалкил, фенил, С5-С6-гетероарил, С3-C6-циклоалкилоксигруппу, С3-C6-гетероциклоалкилоксигруппу, фенилоксигруппу, С5-С6-гетероарилоксигруппу, C1-С3-алкилсульфинил, фенилсульфинил, C1-С3-алкилсульфонил, фенилсульфонил, бензилсульфонил, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, C1-С3-алкиламинокарбонил, ди(С1-С3)алкиламинокарбонил, С3-C6-циклоалкил(С1-С2)алкил, гетероциклоалкил(С1-С2)алкил, фенил(С1-С2)алкил, С5-С6-гетероарил(С1-С2)алкил, С3-C6-циклоалкил(С1-С3)алкоксигруппу, С3-C6-гетероциклоалкил(С1-С2)алкилоксигруппу, фенил(С1-С2)алкоксигруппу, С5-С6-гетероарил(С1-С2)алкоксигруппу, фенил(С1-С2)алкилсульфинил, фенил(С1-С2)алкилсульфонил,
и где каждая группа, содержащаяся в R6, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, фторированного или незамещенного C1-С3-алкила, фторированной или незамещенной C1-С3-алкилоксигруппы, гидроксигруппы и цианогруппы,
или
(i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из гидроксигруппы, галогена, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образует 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, C1-С3-алкил, C1-С3-алкоксигруппу, С2-С3-алкинил, С2-С3-алкенил, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, C1-С3-алкилсульфинил, C1-С3-алкилсульфонил, C1-С3-алкилтиогруппу, С3-C6-циклоалкил, С3-C6-циклоалкилоксигруппу, С3-C6-гетероциклоалкил, С3-C6-гетероциклоалкилоксигруппу, фенил, феноксигруппу, фенилсульфонил, фенилсульфинил, С5-С6-гетероарил, С5-С6-гетероарилоксигруппу, С5-С6-гетероарил(С1-С2)алкил и С5-С6-гетероарил(С1-С2)алкоксигруппу, С3-C6-циклоалкил(С1-С2)алкил, С3-C6-циклоалкил(C1-С3)алкоксигруппу, С3-C6-гетероциклоалкилоксигруппу, С3-C6-гетероциклоалкил(С1-С2)алкил, гетероциклоалкил(С1-С2)алкилоксигруппу, фенил(С1-С2)алкил, фенил(С1-С2)алкоксигруппу,
и где каждая группа, содержащаяся в R7, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, фторированного или незамещенного C1-С3-алкила, фторированной или незамещенной C1-С3-алкилоксигруппы, гидроксигруппы и цианогруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из водорода, необязательно галогенированного, предпочтительно фторированного или незамещенного C1-С3-алкила, необязательно галогенированной, предпочтительно фторированной или незамещенной C1-С3-алкилоксигруппы, цианогруппы и галогена,
R9 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкил, фтор(C1-С3)алкил, C1-С3-алкоксигруппу и фтор(C1-С3)алкоксигруппу, где R9 предпочтительно обозначает водород или фтор,
R10 выбран из группы, включающей водород, галоген, C1-С3-алкил, C1-С3-алкоксигруппу, С2-С3-алкенил, С2-С3-алкинил, цианогруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, C1-С3-алкилсульфинил, C1-С3-алкилсульфонил, C1-С3-алкилтиогруппу, С3-C6-циклоалкил, С3-C6-циклоалкилоксигруппу, С3-C6-гетероциклоалкил, С3-C6-гетероциклоалкилоксигруппу, азидогруппу, пентафторсульфанил, нитрогруппу, C1-С3-алкиламинокарбонил и ди(C1-С3)алкиламинокарбонил, где каждый алкил, алкенил, алкинил или алкоксигруппа, содержащиеся R10, могут быть незамещенными или содержать один или более заместителей, выбранных из группы, включающей галоген, незамещенную или галогенированную C1-С3-алкоксигруппу, незамещенную или галогенированную C1-С3-алкилтиогруппу, незамещенный или галогенированный C1-С3-алкилкарбонил, незамещенный или галогенированный C1-С3-алкилоксикарбонил, незамещенный или галогенированный C1-С3-алкиламинокарбонил, незамещенный или галогенированный ди(C1-С3)алкиламинокарбонил, гидроксигруппу, цианогруппу, С3-C6-циклоалкил, С3-C6-гетероциклоалкил, фенил, и С5-С6-гетероарил, где любой циклоалкил, гетероциклоалкил, фенил и гетероарил может быть незамещенным или замещенным одним или несколькими остатками, выбранными из группы, включающей галоген, гидроксигруппу, гидроксиметил, цианогруппу, нитрогруппу, незамещенный или галогенированный C1-С3-алкил, незамещенную или галогенированную C1-С3-алкоксигруппу, незамещенный или галогенированный C1-С3-алкилкарбонил и незамещенный или галогенированный C1-С3-алкоксикарбонил, и где любой галогенированный заместитель, содержащийся в R10, предпочтительно является фторированным, и где R8 и R10 предпочтительно не обозначают водород,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, незамещенный или фторированный C1-С3-алкил и незамещенную или фторированную С1-С3-алкилоксигруппу, и предпочтительно выбран из водорода, фтора, хлора, метила, фторметила, метоксигруппы и фторметоксигруппы,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
Один вариант осуществления относится к соединению формулы VI, в котором:
X1 обозначает C-R7 или N,
Х2 обозначает NH, S или О, где Х2 предпочтительно обозначает NH
R2 и R4 оба обозначают водород,
R5 выбран из водорода, фтора, хлора и брома,
R6 выбран из группы, включающей водород, фтор, хлор, бром, цианогруппу, азидогруппу, нитрогруппу, C1-С3-алкил, C1-С3-алкилоксигруппу, циклопропил, циклопропилоксигруппу, оксетанил, тетрагидрофуранил, метилсульфонил, метилсульфинил, тиенил, пиридил и бензилоксигруппу, где каждая алкильная группа или алкоксигруппа, содержащаяся в R6, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, незамещенной или фторированной С1-С2-алкилоксигруппы и циклопропила, и где каждая циклопропильная, тиенильная, пиридильная и фенильная группа, содержащаяся в R6, может быть замещена одной или более группами, выбранными из галогена, метоксигруппы, фторметоксигруппы, метила, фторметила и цианогруппы,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил, где каждый заместитель кольца, образованного с помощью R6 и R7, выбран из гидроксигруппы, галогена, цианогруппы, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или фторированными,
R7, если присутствует, выбран из группы, включающей водород, галоген, цианогруппу, C1-С3-алкил, C1-С3-алкоксигруппу, метилсульфинил и метилсульфонил, где алкильная группа или алкоксигруппа, содержащаяся в R7, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, цианогруппы и незамещенной или фторированной С1-С2-алкилоксигруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, незамещенный или фторированный метил и незамещенную или фторированную метоксигруппу,
R9 выбран из группы, включающей водород, фтор, метил, фторметил, метоксигруппу и фторметоксигруппу, и предпочтительно обозначает водород,
R10 выбран из группы, включающей водород, галоген, C1-С3-алкил, C1-С3-алкилоксигруппу, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилкарбонил, С3-С4-циклоалкил и цианогруппу, где каждый алкил, алкенил, алкинил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из группы, включающей фтор, хлор, бром, фторированную или незамещенную C1-С3-алкилоксигруппу, фторированный или незамещенный C1-С3-алкилкарбонил, фторированный или незамещенный C1-С3-алкоксикарбонил, С3-С5-циклоалкил, С3-С5-циклоалкилоксигруппу, С3-С5-гетероциклоалкил, С3-С5-гетероциклоалкилоксигруппу, гидроксигруппу и цианогруппу, где любой циклоалкил, гетероциклоалкил, циклоалкилоксигруппа и гетероциклоалкилоксигруппа могут быть незамещенными или замещенными одним или несколькими остатками, выбранными из группы, включающей галоген, гидроксигруппу, гидроксиметил, цианогруппу, фторированный или незамещенный метил, фторированную или незамещенную C1-С3-алкилоксигруппу, фторированный или незамещенный C1-С3-алкилоксикарбонил и фторированную или незамещенную C1-С3-алкилокси(C1-С3)алкилоксигруппу,
R11 выбран из группы, включающей водород, фтор, хлор, бром, незамещенный или фторированный C1-С3-алкил и незамещенную или фторированную С1-С3-алкилоксигруппу,
и к его фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
В одном предпочтительном варианте осуществления, R6 в соединениях формулы VI не обозначает водород; в более предпочтительном варианте осуществления по меньшей мере один, предпочтительно два из R8, R10 и R11 также отличаются от водорода. В одном варианте осуществления R6 и R10 оба не обозначают водород.
В одном предпочтительном варианте осуществления настоящего изобретения, в соединении формулы VI:
(a) X1 обозначает CR7 и Х2 обозначает NH, S или О, или
(b) X1 обозначает N и Х2 обозначает NH,
Следовательно, предпочтительными субструктурами формулы VI являются формулы VIa, VIb, VIc и VId:
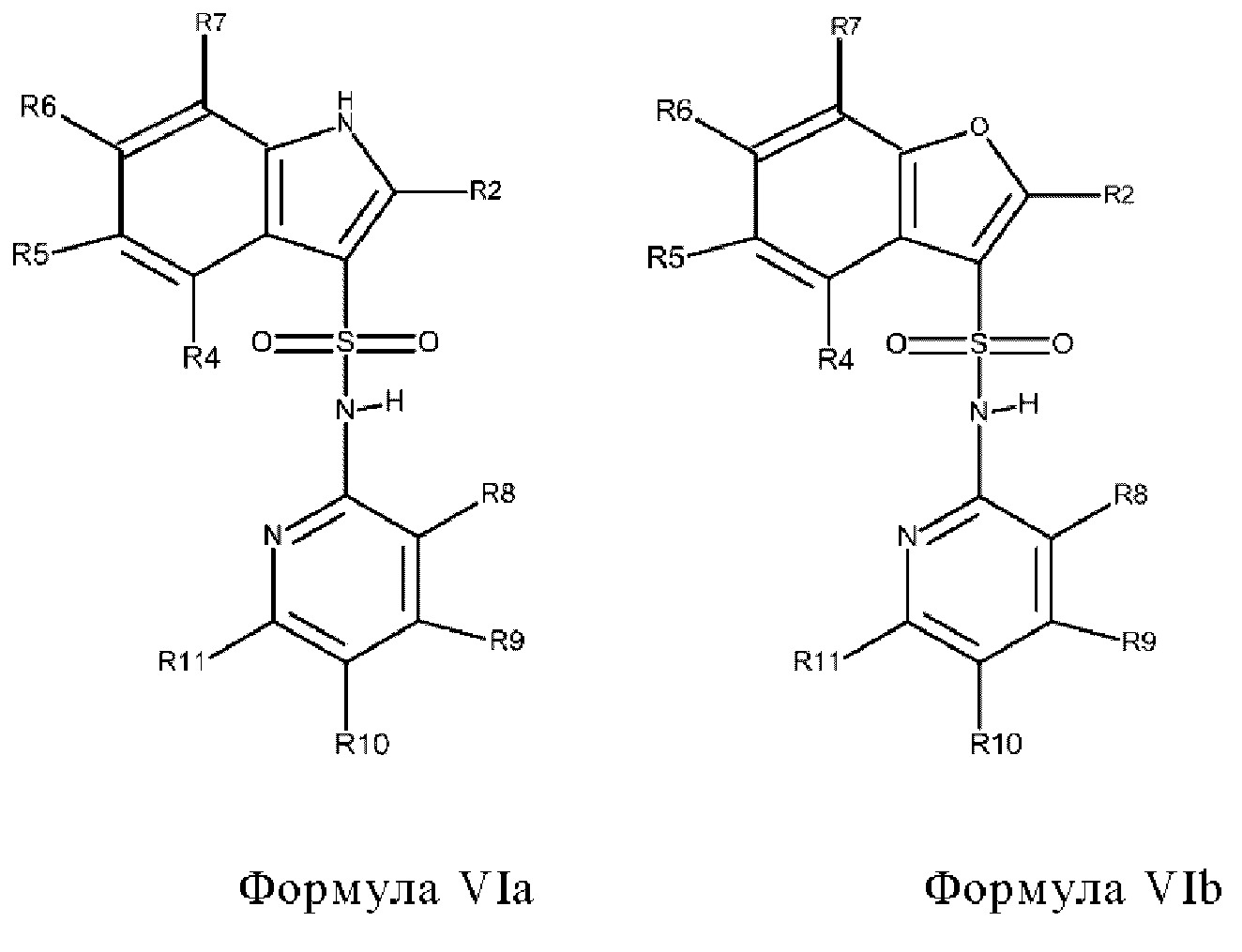
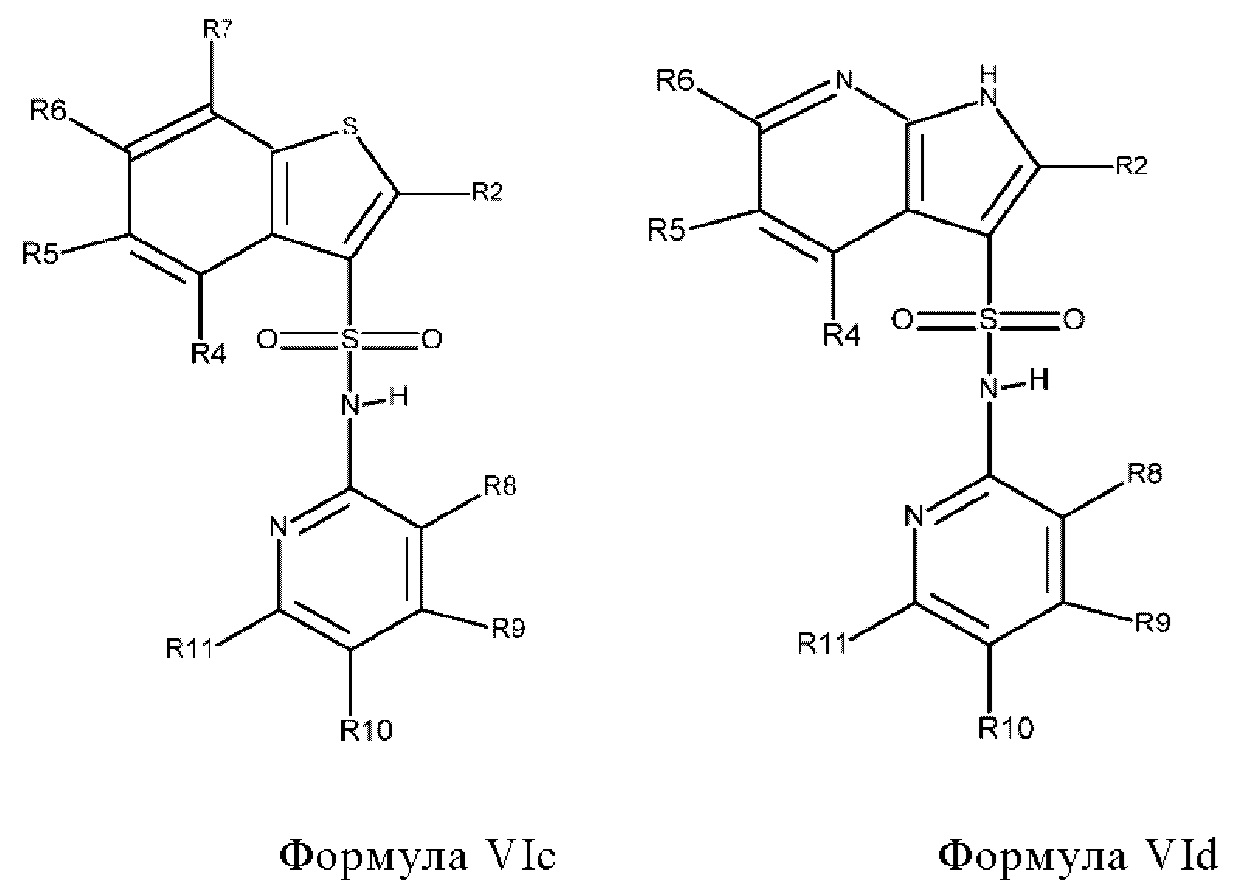
в которых любой R2, R4, R5, R6, R7, если присутствует, R8, R9, R10 и R11 являются такими, как описано в настоящем изобретении для соединений формулы 1-2, II-2, III-2, IV-2, V-2 и VI.
В одном предпочтительном варианте осуществления настоящего изобретения, в соединениях формулы VI и VIa-d:
R2 обозначает водород или фтор,
R4 выбран из водорода, метоксигруппы и фтора, и предпочтительно обозначает водород или фтор, более предпочтительно водород,
R5 выбран из группы, включающей водород, галоген, цианогруппу, C1-С3-алкоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, C1-С3-алкилсульфинил и C1-С3-алкилсульфонил, где каждый алкил или алкоксигруппа необязательно может быть замещена одной или более группами, выбранными из галоген, C1-С3-алкоксигруппу, галоген(C1-С3)алкоксигруппу, цианогруппу, гидроксигруппу, и C1-С3-алкиламиногруппу, причем предпочтительными необязательными заместителями указанных алкильной группы и алкоксигруппы являются галоген и C1-C6-алкоксигруппа, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, гидроксигруппу, галоген, цианогруппу, азидогруппу, нитрогруппу, C1-C6-алкил, С2-С6-алкенил, С2-С6-алкинил, C1-C6-алкоксигруппу, С3-С7-циклоалкил, С3-С7-циклоалкенил, С3-С7-гетероциклоалкил, С3-С7-гетероциклоалкенил, фенил, С5-С10-гетероарил, предпочтительно С5-С6-гетероарил, C8-С10-гетероциклил, -ORx, -SRx, -SORx, SO2Rx, -пентафторсульфанил, NRyRzz, -NRyCORx, -NRyCO2Rx, -NRxCONRyRz, -CORx, -CO2Rx, -CONRyRz, где каждая алкильная, алкенильная, алкинильная группа, алкоксигруппа, циклоалкильная, гетероциклоалкильная, циклоалкенильная, фенильная, гетероарильная или гетероциклильная группа, содержащаяся в R6, может быть незамещенной или содержать один или более заместителей, предпочтительно выбранных из группы, включающей галоген, гидроксигруппу, оксогруппу, цианогруппу, азидогруппу, нитрогруппу, C1-C6-алкил, C1-C6-алкокси(C1-С3)алкил, С3-С7-циклоалкил, С3-С7-гетероциклоалкил, фенил, С5-С10-(предпочтительно С5-С6)гетероарил, ORx, -SRx, -SORx, SO2Rx, -пентафторсульфанил, NRyRz, -NRyCORx, -NRyCO2Rx, -CORx, -CO2Rx, -CONRyRz,
где Rx, Ry, Rz и Rzz независимо выбраны из группы, включающей водород, C1-C6-алкил, С3-С7-циклоалкил, С3-C6-циклоалкенил, С3-С7-циклоалкил(C1-C6)алкил, фенил, фенил(C1-C6)алкил, С3-С7-гетероциклоалкил, С3-С7-гетероциклоалкил(C1-C6)алкил, С5-С6-гетероарил или гетероарил(C1-C6)алкил, любая из этих групп может быть незамещенной или содержать один или более заместителей, выбранных из описанных выше, или Ry и Rz, или Ry и Rzz вместе с атомом азота аминогруппы, к которому они оба присоединены, могут образовать ароматический или неароматический, незамещенный или замещенный С5-С6-гетероцикл, где Rzz предпочтительно отличается от водорода,
или R6 в соединениях формулы VI, VIa, VIb или VIc вместе с R5 или R7 и с атомами углерода, к которым они присоединены, может образовать 5- или 6-членное ароматическое или неароматическое кольцо, которое необязательно может содержать один или более гетероатомов, выбранных из S, О и N, и где указанное кольцо может быть незамещенным или содержать один или более заместителей,
где предпочтительно, если (i) R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил, где каждый заместитель, если присутствует, выбран из группы, включающей галоген, гидроксигруппу, цианогруппу, C1-С3-алкил, С3-С7-циклоалкил, С3-С7-циклоалкил(C1-С3)алкил, С3-С7-гетероциклоалкил(C1-С3)алкил, C1-С3-алкоксигруппу и C1-С3-алкокси(C1-С3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы, или (ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, или
R7, если присутствует, выбран из группы, включающей Н, галоген, цианогруппу, C1-C6-алкил, C1-C6-алкоксигруппу, С2-С6-алкинил, С2-С6-алкенил, C1-C6-алкилкарбонил, C1-C6-алкоксикарбонил, С1-С5-алкилкарбониламиногруппу, C1-С5-алкиламинокарбонил, ди(C1-С3)алкиламинокарбонил, C1-C6-алкилсульфонил, C1-C6-алкилсульфинил, С3-С7-циклоалкил, С3-С7-гетероциклоалкил, фенил, С5-С6-гетероарил, С5-С6-гетероарил(C1-С3)алкил и С5-С6-гетероарил(C1-С3)алкоксигруппу, где каждая алкильная, алкенильная, алкинильная группа или алкоксигруппа может быть незамещенной или содержать один или более заместителей, выбранных из галогена, галоген(C1-C6)алкоксигруппы, предпочтительно фтор(C1-С3)алкоксигруппы и С1-С6-алкоксигруппы,
R8 выбран из группы, включающей водород, C1-C6-алкил, C1-C6-алкоксигруппу и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и необязательно фторированной C1-С3-алкоксигруппы,
R9 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, C1-C6-алкил, C1-C6-алкоксигруппу, С2-С6-алкенил, С2-С6-алкинил и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы,
R10 выбран из группы, включающей водород, галоген, C1-C6-алкил, C1-C6-алкоксигруппу, С2-С6-алкенил, С2-С6-алкинил, цианогруппу, C1-C6-алкилкарбонил, C1-C6-алкоксикарбонил, C1-C6-алкилсульфонил, C1-C6-алкилсульфинил, C1-C6-алкилтиогруппу, C1-С5-алкилкарбониламиногруппу, C1-С5-алкиламинокарбонил, ди(C1-С3)алкиламинокарбонил, С3-С6-циклоалкил, гетеро(С3-C6)циклоалкил, азидогруппу, пентафторсульфанил и нитрогруппу, где каждый алкил, алкенил, алкинил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из группы, включающей галоген, C1-C6-алкоксигруппу, галоген(C1-C6)алкоксигруппу, незамещенный или фторированный C1-С3-алкоксикарбонил, незамещенный или фторированный C1-С3-алкилкарбонил, C1-C6-алкилтиогруппу, незамещенную или фторированную С1-С3-алкилкарбониламиногруппу, незамещенный или фторированный C1-С3-алкиламинокарбонил, незамещенный или фторированный ди(C1-С3)алкиламинокарбонил, незамещенный или фторированный C1-С3-алкилсульфонил, незамещенный или фторированный C1-С3-алкилсульфинил, гидроксигруппу, цианогруппу, цикло(С3-C6)алкил, фенил и С5-С6-гетероарил, где любой циклоалкил, гетероциклоалкил, фенил и гетероарил может быть незамещенным или может быть замещен одним или несколькими остатками, выбранными из группы, включающей галоген, гидроксигруппу, цианогруппу, незамещенный или фторированный C1-С3-алкил, незамещенную или фторированную C1-С3-алкоксигруппу и незамещенный или фторированный C1-С3-алкоксикарбонил,
R11 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, C1-C6-алкил, C1-C6-алкоксигруппу, C1-C6-алкилкарбонил, C1-C6-алкоксикарбонил, C1-C6-алкилсульфонил и C1-C6-алкилсульфинил, C2-C6-алкенил и С2-С6-алкинил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном варианте осуществления в соединениях формулы VI и VIa-d по меньшей мере одна из групп R5, R6 и R7, если она содержится, и по меньшей мере одна, предпочтительно по меньшей мере две из групп R8, R10 и R11, отличаются от водорода, где более предпочтительно, если по меньшей мере один заместитель выбран из фтора, хлора и брома.
В одном варианте осуществления в соединениях формулы VI и VIa-d:
X1, если присутствует, обозначает N или CR7,
Х2, если присутствует, обозначает NH, S или О, где если X1 обозначает N, то Х2 предпочтительно обозначает NH,
R2 обозначает водород или фтор, предпочтительно водород,
R4 обозначает водород или фтор, предпочтительно водород,
R5 выбран из группы, включающей водород, галоген, цианогруппу, С1-С2-алкил, и С1-С2-алкилоксигруппу, где R5 предпочтительно обозначает водород, метил или галоген, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, галоген, цианогруппу, нитрогруппу, аминогруппу, азидогруппу, C1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, C1-С3-алкилкарбониламиногруппу, C1-С3-алкиламинокарбонил, ди(C1-С3)алкиламинокарбонил, (C1-С3)алкилсульфинил, (C1-С3)алкилсульфонил, С3-C6-циклоалкил, С3-C6-циклоалкилоксигруппу, С3-C6-циклоалкил(С1-С2)алкил, С3-C6-циклоалкил(C1-С3)алкоксигруппу, С3-C6-гетероциклоалкил, С3-C6-гетероциклоалкилоксигруппу, С3-C6-гетероциклоалкил(С1-С2)алкил, гетероциклоалкил(С1-С2)алкилоксигруппу, фенил, фенилоксигруппу, фенил(С1-С2)алкил, фенил(С1-С2)алкоксигруппу, фенилсульфонил, фенилсульфинил, фенил(С1-С2)алкилсульфонил, фенил(С1-С2)алкилсульфинил, С5-С6-гетероарил, С5-С6-гетероарилоксигруппу, С5-С6-гетероарил(С1-С2)алкил, и С5-С6-гетероарил(С1-С2)алкоксигруппу, и где каждая группа, содержащаяся в R6, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, фторированного или незамещенного C1-С3-алкила, фторированной или незамещенной C1-С3-алкилоксигруппы, гидроксигруппы и цианогруппы,
или
(i) где R6 в соединениях формулы VI, VIa, VIb или VIc вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, могут образовать незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил,
где каждый заместитель, если присутствует, выбран из гидроксигруппы, галогена, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, предпочтительно фтора, и метоксигруппы,
или
(ii) R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, нитрогруппу, аминогруппу, C1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, C1-С3-алкилкарбониламиногруппу, С1-С3-алкиламинокарбонил, ди(C1-С3)алкиламинокарбонил, C1-С3-алкилсульфинил, C1-С3-алкилсульфонил, C1-С3-алкилтиогруппу, С3-С6-циклоалкил, С3-C6-циклоалкилоксигруппу, С3-C6-циклоалкил(С1-С2)алкил, С3-C6-циклоалкил(С1-С3)алкоксигруппу, С3-C6-гетероциклоалкил, С3-C6-гетероциклоалкилоксигруппу, С3-C6-гетероциклоалкил(С1-С2)алкил, гетероциклоалкил(С1-С2)алкилоксигруппу, фенил, фенилоксигруппу, фенил(С1-С2)алкил, фенил(С1-С2)алкоксигруппу, фенилсульфонил, фенилсульфинил, С5-С6-гетероарил, С5-С6-гетероарилоксигруппу, С5-С6-гетероарил(С1-С2)алкил и С5-С6-гетероарил(С1-С2)алкоксигруппу, и где каждая группа, содержащаяся в R7, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, фторированного или незамещенного C1-С3-алкила, фторированной или незамещенной C1-С3-алкилоксигруппы, гидроксигруппы и цианогруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, галоген, цианогруппу, необязательно галогенированную C1-С3-алкилоксигруппу, необязательно галогенированный C1-С3-алкил, необязательно галогенированный (C1-С3)алкилсульфинил, необязательно галогенированный (C1-С3)алкилсульфонил и необязательно галогенированную (C1-С3)алкилтиогруппу,
R9 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкилоксигруппу, фтор(C1-С3)алкоксигруппу, C1-С3-алкил и фтор(C1-С3)алкил, и предпочтительно обозначает водород,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, нитрогруппу, аминогруппу, азидогруппу, пентафторсульфанил, С1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, C1-С3-алкиламинокарбонил, ди(C1-С3)-алкиламинокарбонил, (C1-С3)алкилсульфинил, (C1-С3)алкилсульфонил, (C1-С3)-алкилтиогруппу, С3-C6-циклоалкил, С3-C6-циклоалкилоксигруппу, С3-C6-циклоалкил(С1-С2)алкил, С3-C6-циклоалкил(C1-С3)алкоксигруппу, С3-C6-гетероциклоалкил, С3-C6-гетероциклоалкилоксигруппу, С3-C6-гетероциклоалкил(С1-С2)алкил, С3-C6-гетероциклоалкил(С1-С2)-алкилоксигруппу, и где каждая группа, содержащаяся в R10, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, фторированного или незамещенного C1-С3-алкила, фторированной или незамещенной C1-С3-алкилоксигруппы, фторированного или незамещенного C1-С3-алкоксикарбонила, фторированного или незамещенного C1-С3-алкилкарбонила, C1-С3-алкиламинокарбонила, ди(C1-С3)-алкиламинокарбонила, гидроксигруппы и цианогруппы,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкил, фтор(C1-С3)алкил, C1-С3-алкилоксигруппу, фтор(C1-С3)алкоксигруппу, незамещенный или фторированный C1-С3-алкилкарбонил, незамещенный или фторированный C1-С3-алкоксикарбонил и цианогруппу,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном предпочтительном варианте осуществления R6 и R10 оба отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном варианте осуществления в соединениях формулы VI и VIa-d:
R2 и R4 оба обозначают водород,
R5 выбран из водорода, фтора, хлора и брома,
R6 выбран из группы, включающей фтор, хлор, бром, азидогруппу, цианогруппу, бензилоксигруппу, метилсульфонил, метилсульфинил, C1-С3-алкил, C1-С3-алкилоксигруппу, циклопропил, циклопропилоксигруппу и циклопропилметоксигруппу, где каждая алкильная группа, алкоксигруппа и циклопропильная группа, содержащаяся в R6, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома и незамещенной или фторированной С1-С2-алкилоксигруппы, где R6 предпочтительно выбран из группы, включающей фтор, хлор, бром, фторированный метил и незамещенную или фторированную метоксигруппу,
или R6 вместе с R7 в соединениях формулы VI, VIa, VIb или VIc, вместе с атомами углерода, к которым R6 и R7 присоединены, могут образовать незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил, где каждый заместитель в R7, если присутствует, выбран из гидроксигруппы, галогена, цианогруппы, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или фторированными и/или гидроксилированными,
R7, если присутствует, выбран из группы, включающей водород, галоген, цианогруппу, C1-С3-алкил, C1-С3-алкилоксигруппу, С3-С6-циклоалкил, С3-C6-циклоалкилоксигруппу, метилсульфинил и метилсульфонил, каждая алкильная группа, алкоксигруппа или циклоалкильная группа, содержащаяся в R7, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, цианогруппы и незамещенной или фторированной С1-С2-алкилоксигруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, незамещенную или фторированную метоксигруппу и незамещенный или фторированный метил,
R9 выбран из водорода, фтора, метила и метоксигруппы, и предпочтительно обозначает водород,
R10 выбран из группы, включающей водород, галоген, цианогруппу, C1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, С3-С4-циклоалкил, С3-С4-циклоалкилоксигруппу, С3-С4-гетероциклоалкил и С3-С4-гетероциклоалкилоксигруппу, где каждая группа алкильная, алкенильная, алкинильная группа и алкилоксигруппа, содержащаяся в R10, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, фторированной или незамещенной C1-С3-алкилоксигруппы, фторированного или незамещенного C1-С3-алкилкарбонила, фторированного или незамещенного С1-С3-алкоксикарбонила, С3-С4-циклоалкила, С3-С4-циклоалкилоксигруппы, С3-С4-гетероциклоалкила, С3-С4-гетероциклоалкилоксигруппы, гидроксигруппы и цианогруппы, и где каждая циклоалкильная и гетероциклоалкильная группа, содержащаяся в R10, может быть замещена остатком, выбранным из группы, включающей фтор, хлор, бром, гидроксигруппу, гидроксиметил, фторированный или незамещенный C1-С3-алкил, фторированную или незамещенную C1-С3-алкилоксигруппу, фторированную или незамещенную С1-С2-алкокси-С1-С2-алкилоксигруппу и фторированный или незамещенный C1-С3-алкоксикарбонил,
R11 выбран из группы, включающей водород, фтор, хлор, бром, незамещенный или фторированный C1-С3-алкил, предпочтительно фторметил, и незамещенную или фторированную С1-С3-алкилоксигруппу, предпочтительно метоксигруппу и фторметоксигруппу, где R11 предпочтительно выбран из группы, включающей водород, фтор, хлор, метоксигруппу и фторметил,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном предпочтительном варианте осуществления, R2 в соединениях формулы VI обозначает водород.
В одном предпочтительном варианте осуществления, R4 в соединениях формулы VI и VIa-d обозначает водород или фтор, особенно предпочтительно водород.
В одном предпочтительном варианте осуществления, R5 в соединениях формулы VI и VIa-d выбран из группы, включающей водород, фтор, хлор, бром, йод и незамещенный или фторированный метил. В особенно предпочтительном варианте осуществления, R5 выбран из группы, включающей водород, фтор, хлор, бром и метил, и особенно предпочтительно из водорода, фтора, хлора и брома. В одном предпочтительном варианте осуществления соединений формулы VI и VIa-d, если R6 не обозначает водород, то R5 обозначает водород.
В одном варианте осуществления соединений формулы VIa-c, в частности, в соединениях формулы VIa, R6 вместе с R7 и с атомами С, к которым R6 и R7 присоединены, образуют кольцо, где кольцо предпочтительно выбрано из фенила, пиридила, циклопентила и циклогексила, каждый из которых может быть незамещенным или содержать один или более заместителей, выбранных из группы, включающей галоген, водород, оксогруппу, C1-С3-алкил, C1-С3-алкоксигруппу, фтор-C1-С3-алкоксигруппу, фтор-C1-С3-алкил, аминогруппу, цианогруппу, ди(C1-С3-алкил)аминогруппу, ацетил, C1-С3-алкилсульфонил, C1-С3-алкилсульфанил, C1-С3-алкилтиогруппу, и где заместитель предпочтительно выбран из группы, включающей фтор, хлор, бром, цианогруппу, гидроксигруппу, метил, фторметил, метоксигруппу и фторметоксигруппу. В предпочтительном варианте осуществления R6 и R7 в соединениях формулы VIa образуют кольцо, которое вместе с аннелированным бициклическим кольцом образует трициклический фрагмент, выбранный из группы, включающей 1Н-бензо[g]индол-3-ил, 1Н-пирроло[3,2-h]хинолин-3-ил, 1,6,7,8-тетрагидроциклопента[g]индол-3-ил и 6,7,8,9-тетрагидро-1Н-бензо[g]индол-3-ил. В одном варианте осуществления, если R6 и R7 образуют пиридильное кольцо с образованием 1Н-пирроло[3,2-h]хинолин-3-ила, то трициклический фрагмент может дополнительно содержать заместитель, выбранный из группы, включающей фтор, хлор, бром, гидроксигруппу, метоксигруппу, фторметил и фторметоксигруппу, предпочтительно в положении 8, с образованием, например, 8-гидрокси-1Н-пирроло[3,2-h]хинолина, 8-(дифторметил)-1Н-пирроло[3,2-h]хинолина или 8-(трифторметокси)-1Н-пирроло[3,2-h]хинолина. В одном варианте осуществления соединений формулы VIa-c, в частности, в соединениях формулы VIa R6 вместе с R7 и с атомами С, к которым R6 и R7 присоединены, образуют кольцо, где кольцо выбрано из фенила, пиридила, циклопентила и циклогексила, которые являются незамещенными или содержат один или более заместителей, выбранных из фтора, хлора, фторметила и фторметоксигруппы, где в одном предпочтительном варианте осуществления кольцо является незамещенным.
В одном предпочтительном варианте осуществления соединений формулы VIa-c, если R6 и R7 образуют необязательно замещенное кольцо, выбранное из фенила, пиридила, циклопентила и циклогексила, то R4 и R5 предпочтительно оба обозначают водород, R8 обозначает водород, галоген или незамещенную или фторированную метоксигруппу, предпочтительно фтор или метоксигруппу, R9 обозначает водород или фтор, предпочтительно водород, R10 выбран из группы, включающей галоген, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, нитрогруппу, азидогруппу, пентафторсульфанил, незамещенный или фторированный и/или гидроксилированный, предпочтительно незамещенный или фторированный C1-С3-алкил, незамещенный или фторированный и/или гидроксилированный, предпочтительно незамещенный или фторированный C1-С3-алкилкарбонил, незамещенную или фторированную и/или гидроксилированную, предпочтительно незамещенную или фторированную C1-С3-алкоксигруппу, незамещенный или фторированный С2-С3-алкенил, С2-С3-алкинил, незамещенный или фторированный и/или гидроксилированный, предпочтительно незамещенный или фторированный С1-С2-алкокси(C1-С3)алкил, незамещенную или фторированную и/или гидроксилированную, предпочтительно незамещенную или фторированную С1-С2-алкокси(C1-С3)алкоксигруппу, R11 выбран из группы, включающей водород, фтор, хлор, бром, незамещенную или фторированную метоксигруппу и незамещенный или фторированный метил.
В одном варианте осуществления R6 и R7 в соединениях формулы VIa образуют пиридин и образованной трициклической системой является необязательно замещенный 1Н-пирроло[3,2-h]хинолин-3-ил, предпочтительно замещенный в положении 8 1Н-пирроло[3,2-h]хинолин.
В одном предпочтительном варианте осуществления R6 и R7 в соединениях формулы VIa образуют необязательно замещенное кольцо, выбранное из фенила, пиридила (предпочтительно с образованием необязательно замещенного в положении 8 1H-пирроло[3,2-h]хинолин-3-ила), циклопентила и циклогексила, R4 и R5 оба обозначают водород, R8 обозначает фтор или незамещенную или фторированную метоксигруппу, R9 обозначает водород или фтор, предпочтительно водород, R10 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, незамещенный или фторированный C1-С3-алкил, незамещенную или фторированную C1-С3-алкоксигруппу, незамещенный или фторированный С2-С3-алкенил, С2-С3-алкинил, незамещенный или фторированный С1-С2-алкокси(C1-С3)алкил и незамещенную или фторированную С1-С2-алкокси(C1-С3)алкоксигруппу, R11 выбран из группы, включающей водород, фтор, хлор, бром, незамещенную или фторированную метоксигруппу и незамещенный или фторированный метил.
В одном предпочтительном варианте осуществления R6 в соединениях формулы VI и VIa-d выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, азидогруппу, аминогруппу, нитрогруппу, C1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, C1-С3-алкилкарбониламиногруппу, C1-С3-алкиламинокарбонил, ди(C1-С3)алкиламинокарбонил, (C1-С3)алкилсульфинил, (C1-С3)алкилсульфонил, С3-С6-циклоалкил, С3-C6-циклоалкилоксигруппу, С3-C6-циклоалкил(С1-С2)алкил, С3-C6-циклоалкил(C1-С3)алкоксигруппу, С3-C6-гетероциклоалкил, С3-C6-гетероциклоалкилоксигруппу, С3-C6-гетероциклоалкил(С1-С2)алкил, гетероциклоалкил(С1-С2)алкилоксигруппу, фенил, фенилоксигруппу, фенил(С1-С2)алкил, фенил(С1-С2)алкоксигруппу, фенилсульфонил, бензилсульфонил, фенилсульфинил, бензилсульфинил, С5-С6-гетероарил, С5-С6-гетероарилоксигруппу, С5-С6-гетероарил(С1-С2)алкил и С5-С6-гетероарил(С1-С2)алкоксигруппу, и где каждая группа, содержащаяся R6, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, фторированного или незамещенного С1-С2-алкила, фторированной или незамещенной С1-С2-алкоксигруппы, гидроксигруппы и цианогруппы.
В одном предпочтительном варианте осуществления R6 в соединениях формулы VI и VIa-d выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, цианометоксигруппу, нитрогруппу, азидогруппу, циклопропил, циклопропилоксигруппу, циклопропилметоксигруппу, незамещенный или замещенный C1-С3-алкил, незамещенный или замещенный C1-С3-алкилоксигруппу, метилсульфинил, метилсульфонил, пиридил, необязательно галогенированный тиенил, и бензилоксигруппу, где каждый заместитель, содержащийся в R6, выбран из галогена, метоксигруппы и фторметоксигруппы, и предпочтительно обозначает фтор. В одном предпочтительном варианте осуществления R6 выбран из группы, включающей хлор, бром, азидогруппу, цианогруппу, циклопропил, метилсульфинил, метилсульфонил, моно-, ди- и трифторметил, метоксигруппу, моно-, ди- и трифторметоксигруппу, и моно-, ди- и трифторэтоксигруппу. В особенно предпочтительном варианте осуществления R6 выбран из группы, включающей фтор, хлор, бром, метоксигруппу, фторметоксигруппу, фторэтоксигруппу и фторметил, и наиболее предпочтительно из группы, включающей фтор, хлор, бром и метоксигруппу.
В одном предпочтительном варианте осуществления соединений формулы VIa-c R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, нитрогруппу, C1-С3-алкил, C1-С3-алкилоксигруппу, C1-С3-алкилсульфинил, C1-С3-алкилсульфонил, C1-С3-алкилтиогруппу, С3-C6-циклоалкил, С3-C6-циклоалкилоксигруппу, С3-C6-гетероциклоалкил, С3-С6-гетероциклоалкилоксигруппу, фенил, фенилоксигруппу, фенил(С1-С2)алкил, фенил(С1-С2)алкоксигруппу, фенилсульфонил, фенилсульфинил, С5-С6-гетероарил, С5-С6-гетероарилоксигруппу, С5-С6-гетероарил(С1-С2)алкил и С5-С6-гетероарил(С1-С2)алкоксигруппу, где каждая группа, содержащаяся в R7, может быть незамещенной или замещенной одним или несколькими остатками, выбранными из группы, включающей фтор, хлор, бром, фторированный или незамещенный метил, фторированную или незамещенную C1-С3-алкилоксигруппу, гидроксигруппу и цианогруппу, и где С5-С6-гетероарил предпочтительно выбран из пиридила, оксазола и изоксазола, каждый из которых может быть замещен, как это описано выше. В одном предпочтительном варианте осуществления R7 выбран из группы, включающей водород, фтор, хлор, бром, метил, фторметил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, метилсульфинил, метилсульфонил и необязательно замещенный изоксазол. В одном предпочтительном варианте осуществления R7 выбран из группы, включающей водород, фтор, хлор, бром, метил, фторметил, метоксигруппу, фторметоксигруппу и метилсульфонил.
В предпочтительном варианте осуществления R8 в соединениях формулы VI и VIa-d выбран из группы, включающей водород, галоген, цианогруппу, незамещенный или фторированный C1-С3-алкил и незамещенную или фторированную C1-С3-алкилоксигруппу, предпочтительно из группы, включающей фтор, хлор, бром, метил, фторметил, метоксигруппу и фторметоксигруппу. В одном предпочтительном варианте осуществления R8 выбран из группы, включающей фтор, метоксигруппу и фторметоксигруппу, и в особенно предпочтительном варианте осуществления R8 обозначает фтор или метоксигруппу.
В одном предпочтительном варианте осуществления R9 в соединениях формулы VI и VIa-d выбран из группы, включающей водород, фтор, хлор, метил, фторметил, метоксигруппу и фторметоксигруппу. В одном предпочтительном варианте осуществления R9 выбран из группы, включающей водород, фтор, метоксигруппу и фторметоксигруппу, и более предпочтительно обозначает водород или фтор и особенно предпочтительно водород,
В одном варианте осуществления R10 в соединениях формулы VI и VIa-d выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, нитрогруппу, аминогруппу, азидогруппу, пентафторсульфанил, C1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, С1-С3-алкилкарбониламиногруппу, C1-С3-алкиламинокарбонил, ди(C1-С3)алкиламинокарбонил, (C1-С3)алкилсульфинил, (C1-С3)алкилсульфонил, (C1-С3)алкилтиогруппу, С3-С4-циклоалкил, С3-С4-циклоалкилоксигруппу, С3-С4-гетероциклоалкил, С3-С4-гетероциклоалкилоксигруппу, С3-С4-гетероциклоалкил(С1-С2)алкил, С3-С4-гетероциклоалкил(С1-С2)алкоксигруппу, С5-С6-гетероарил(С1-С2)алкил и С5-С6-гетероарил(С1-С2)алкоксигруппу, и где каждая алкильная, алкенильная, алкинильная группа и алкоксигруппа, содержащаяся в R10, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, фторированной или незамещенной C1-С3-алкилоксигруппы, C1-С3-алкилоксикарбонила, фенила, фенилоксигруппы, С3-С6-циклоалкила, С3-C6-циклоалкилоксигруппы, С3-C6-гетероциклоалкила, С3-C6-гетероциклоалкилоксигруппы, гидроксигруппы и цианогруппы, и где каждая циклическая группа, содержащаяся в R10, может быть незамещенной или замещенной одним или несколькими остатками, выбранными из группы, включающей фтор, хлор, бром, фторированный или незамещенный C1-С3-алкил, фторированную или незамещенную C1-С3-алкилоксигруппу, фторированный или незамещенный С1-С3-алкилоксикарбонил, гидроксигруппу, гидроксиметил и цианогруппу.
В одном варианте осуществления R10 в соединениях формулы VI и VIa-d выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, нитрогруппу, аминогруппу, азидогруппу, пентафторсульфанил, C1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, (C1-С3)алкилсульфинил, (C1-С3)алкилсульфонил, (С1-С3)алкилтиогруппу, C1-С3-алкилоксициклопропил и C1-С3-алкилоксикарбонилциклопропил, где каждая алкильная группа, алкоксигруппа, алкенильная и алкинильная группа, содержащаяся в R10, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, хлора, брома, фторированного или незамещенного C1-С3-алкила, фторированной или незамещенной С1-С3-алкилоксигруппы, фторированного или незамещенного C1-С3-алкилоксикарбонила, С3-С6-циклоалкила и цианогруппы.
В одном предпочтительном варианте осуществления R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, цианоэтоксигруппу, нитрогруппу, азидогруппу, пентафторсульфанил, C1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, C1-С3-алкилоксигруппу, С1-С2-алкилкарбонил и замещенный циклопропил, где каждая группа, содержащаяся в R10, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, незамещенной или фторированной и/или гидроксилированной, предпочтительно незамещенной или фторированной С1-С2-алкилоксигруппы, незамещенного или фторированного и/или гидроксилированного, предпочтительно незамещенного или фторированного С1-С2-алкилоксикарбонила, незамещенного или замещенного циклопропила и гидроксигруппы, при условии, что любой заместитель циклопропила выбран из группы, включающей галоген, цианогруппу, гидроксиметил, необязательно фторированную С1-С2-алкоксигруппу и необязательно фторированный С1-С2-алкоксикарбонил.
В одном предпочтительном варианте осуществления R10 в соединении, предлагаемом в настоящем изобретении, включая, но не ограничиваясь только ими, соединения формулы VI и VIa-d, выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, цианоэтоксигруппу, нитрогруппу, азидогруппу, пентафторсульфанил, метил, этил, пропил, фторметил, фторэтил, фторпропил, метоксиметил, фторметоксиметил, метоксиэтил, фторметоксиэтил, метоксипропил, фторметоксипропил, этоксиметил, фторэтоксиметил, этоксиэтил, фторэтиксиэтил, пропоксиметил, фторпропоксиметил, метоксигруппу, этоксигруппу, пропоксигруппу, фторметоксигруппу, фторэтоксигруппу, фторпропоксигруппу, метоксиметоксигруппу, фторметоксиметоксигруппу, метоксиэтоксигруппу, фторметоксиэтоксигруппу, метоксипропоксигруппу, фторметоксипропоксигруппу, этоксиметоксигруппу, фторэтоксиметоксигруппу, этоксиэтоксигруппу, фторэтоксиэтоксигруппу, пропоксиметоксигруппу, фторпропоксиметоксигруппу, этенил, пропенил, фторэтенил, фторпропенил, метоксиэтенил, фторметоксиэтенил, метоксипропенил, фторметоксипропенил, этоксиэтенил, фторэтоксиэтенил, этинил, пропинил, метоксиэтинил, фторметоксиэтинил, метоксипропинил, фторметоксипропинил и циклопропилметоксигруппу, где в одном варианте осуществления каждая группа, содержащаяся в R10, предпочтительно может быть дополнительно замещена гидроксигруппой.
В одном предпочтительном варианте осуществления R10 обозначает циклическую группу, выбранную из группы, включающей С3-С5-циклоалкил, С3-С5-циклоалкилоксигруппу, С3-С5-циклоалкил(C1-С3)алкил, предпочтительно циклоалкилметил, С3-С5-циклоалкил(С1-С3)алкоксигруппу, предпочтительно циклоалкилметоксигруппу, С3-С5-гетероциклоалкил, С3-С5-гетероциклоалкилоксигруппу, С3-С5-гетероциклоалкил(С1-С3)алкил, предпочтительно гетероциклоалкилметил, и С3-С5-гетероциклоалкил(C1-С3)алкоксигруппу, предпочтительно гетероциклоалкилметоксигруппу, где каждая циклическая группа может быть незамещенной или содержать один или более заместителей, выбранных из группы, включающей галоген предпочтительно фтор, цианогруппу, гидроксиметил, необязательно фторированную C1-С3-алкоксигруппу, необязательно фторированный С1-С2-алкокси(С1-С2)алкил, необязательно фторированную С1-С2-алкокси(С1-С2)алкоксигруппу и необязательно фторированный С1-С2-алкоксикарбонил. В одном предпочтительном варианте осуществления заместитель предпочтительно выбран из группы, включающей фтор, цианогруппу и необязательно фторированную C1-С3-алкоксигруппу, где циклической группой предпочтительно является циклопропил.
В одном предпочтительном варианте осуществления R10 в соединении, предлагаемом в настоящем изобретении, включая, но не ограничиваясь только ими, соединения формулы VI и VIa-d, выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, цианоэтоксигруппу, пентафторсульфанил, метил, этил, пропил, бутил, фторметил, фторэтил, фторпропил, метоксиметил, фторметоксиметил, метоксиэтил, фторметоксиэтил, метоксипропил, фторметоксипропил, этоксиметил, фторэтоксиметил, этоксиэтил, фторэтиксиэтил, метоксигруппу, этоксигруппу, пропоксигруппу, бутилоксигруппу, фторметоксигруппу, фторэтоксигруппу, фторпропоксигруппу, метоксиметоксигруппу, фторметоксиметоксигруппу, метоксиэтоксигруппу, фторметоксиэтоксигруппу, метоксипропоксигруппу, фторметоксипропоксигруппу, этоксиметоксигруппу, фторэтоксиметоксигруппу, этоксиэтоксигруппу, фторэтоксиэтоксигруппу, этенил, пропенил, фторэтенил, фторпропенил, метоксиэтенил, фторметоксиэтенил, метоксипропенил, фторметоксипропенил, этоксиэтенил, фторэтоксиэтенил, этинил, пропинил, этоксициклопропил, этоксикарбонилциклопропил и циклопропилметоксигруппу.
В одном предпочтительном варианте осуществления R10 в соединении, предлагаемом в настоящем изобретении, включая, но не ограничиваясь только ими, соединения формулы VI и VIa-d, выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, цианоэтил, метил, моно-, ди- и трифторметил, этил, моно-, ди- и трифторэтил, пропил, моно-, ди- и трифторпропил, метоксигруппу, моно-, ди- и трифторметоксигруппу, этоксигруппу, моно-, ди- и трифторэтоксигруппу, пропилоксигруппу, моно-, ди- и трифторпропилоксигруппу, метоксиметил, моно-, ди- и трифторметоксиметил, метоксиэтил, моно-, ди- и трифторметоксиэтил, метоксипропил, моно-, ди- и трифторметоксипропил, метоксиметоксигруппу, моно-, ди- и трифторметоксиметоксигруппу, метоксиэтоксигруппу, моно-, ди- и трифторметоксиэтоксигруппу, метоксипропилоксигруппу, моно-, ди- и трифторметоксипропилоксигруппу, этоксиметоксигруппу, моно-, ди- и трифторэтоксиметоксигруппу, метоксипропенил и моно-, ди- и трифторметоксипропенил.
В одном предпочтительном варианте осуществления R10 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, цианоэтоксигруппу, незамещенный или фторированный C1-С3-алкил, незамещенную или фторированную C1-С3-алкоксигруппу, незамещенный или фторированный С1-С2-алкокси(C1-С3)алкил, незамещенную или фторированную С1-С2-алкокси(C1-С3)алкоксигруппу, и незамещенный или фторированный С1-С2-алкокси(С2-С3)алкенил.
В одном предпочтительном варианте осуществления R10 выбран из группы, включающей галоген, С1-С4-алкоксигруппу, С1-С4-алкил, С2-С4-алкенил, С2-С4-алкинил, С3-С6-циклоалкил, предпочтительно С3-С4-циклоалкил, С3-C6-циклоалкилоксигруппу, предпочтительно С3-С4-циклоалкилоксигруппу, С3-С6-гетероциклоалкил, предпочтительно С3-С4-гетероциклоалкил, и С3-C6-гетероциклоалкилоксигруппу, предпочтительно С3-С4-гетероциклоалкилоксигруппу, каждый из которых необязательно может быть замещен остатком, выбранным из группы, включающей цианогруппу, фтор и незамещенную или фторированную C1-С3-алкоксигруппу.
В одном варианте осуществления R11 в соединениях формулы VI и VIa-d выбран из группы, включающей водород, фтор, хлор, бром, йод, C1-С3-алкил, фтор(C1-С3)алкил, C1-С3-алкилоксигруппу, фтор(C1-С3)алкоксигруппу, незамещенный или фторированный C1-С3-алкилкарбонил и цианогруппу. В предпочтительном варианте осуществления R11 выбран из группы, включающей водород, фтор, хлор, метил, фторметил, метоксигруппу, фторметоксигруппу и цианогруппу, более предпочтительно из водорода, фтора, фторметила, метоксигруппы и фторметоксигруппы.
В одном предпочтительном варианте осуществления в соединениях формулы VI и VIa-d:
R2, R4, R5 и R9 все обозначают водород,
R6 выбран из группы, включающей галоген, цианогруппу, C1-С3-алкоксигруппу, C1-С3-алкил, С3-С6-циклоалкил, предпочтительно С3-С4-циклоалкил, С3-C6-циклоалкилоксигруппу, предпочтительно С3-С4-циклоалкилоксигруппу, С3-C6-гетероциклоалкил, предпочтительно С3-С4-гетероциклоалкил, и С3-C6-гетероциклоалкилоксигруппу, предпочтительно С3-С4-гетероциклоалкилоксигруппу, каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора и незамещенной или фторированной C1-С3-алкоксигруппы,
R7 выбран из группы, включающей водород, галоген, цианогруппу, C1-С3-алкоксигруппу, C1-С3-алкил, С3-C6-циклоалкил, предпочтительно С3-С4-циклоалкил, С3-C6-циклоалкилоксигруппу, предпочтительно С3-С4-циклоалкилоксигруппу, С3-C6-гетероциклоалкил, предпочтительно С3-С4-гетероциклоалкил, и С3-C6-гетероциклоалкилоксигруппу, предпочтительно С3-С4-гетероциклоалкилоксигруппу, каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора и незамещенной или фторированной C1-С3-алкоксигруппы,
R8 выбран из фтора, метоксигруппы и фторметоксигруппы, предпочтительно из фтора и метоксигруппы,
R10 выбран из группы, включающей галоген, С1-С4-алкоксигруппу, С1-С4-алкил, С2-С3-алкенил С2-С3-алкинил, С3-С6-циклоалкил, предпочтительно С3-С4-циклоалкил, С3-С6-циклоалкилоксигруппу, предпочтительно С3-С4-циклоалкилоксигруппу, С3-С6-гетероциклоалкил, предпочтительно С3-С4-гетероциклоалкил, и С3-С6-гетероциклоалкилоксигруппу, предпочтительно С3-С4-гетероциклоалкилоксигруппу, каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора, цианогруппы и незамещенной или фторированной С1-С3-алкоксигруппы, и
R11 выбран из водорода, фтора, метоксигруппы и фторметоксигруппы, предпочтительно из фтора и метоксигруппы.
В предпочтительном варианте осуществления в соединениях формулы VI и VIa-d:
R2 обозначает водород,
R4 обозначает водород или фтор, более предпочтительно водород;
R5 выбран из водорода, фтора, хлора и брома;
R6 выбран из группы, включающей фтор, хлор, бром, азидогруппу, циклопропил, циклопропилоксигруппу, циклопропилметоксигруппу, незамещенный или фторированный С1-С3-алкил, незамещенную или фторированную С1-С3-алкилоксигруппу, метилсульфинил, метилсульфонил, пиридил, необязательно галогенированный тиенил и бензилоксигруппу;
R7, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, метил, фторметил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, метилсульфинил и метилсульфонил;
R8 выбран из группы, включающей водород, фтор, хлор, бром, метил, фторметил, метоксигруппу и фторметоксигруппу;
R9 выбран из группы, включающей водород, фтор, хлор, метил, фторметил, метоксигруппу и фторметоксигруппу, и предпочтительно обозначает водород,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, нитрогруппу, азидогруппу, пентафторсульфанил, С1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, С1-С3-алкилоксигруппу, С1-С3-алкилкарбонил, С1-С3-алкоксикарбонил и циклопропил, где циклопропил необязательно замещен остатком, выбранным из группы, включающей цианогруппу, С1-С2-алкоксигруппу, фтор(С1-С2)алкоксигруппу, С1-С2-алкокси(С1-С2)алкоксигруппу, фтор(С1-С2)алкокси(С1-С2)алкоксигруппу, С1-С2-алкоксикарбонил и фтор(С1-С2)алкоксикарбонил, и где каждая алкильная группа, алкоксигруппа, алкенильная и алкинильная группа, содержащаяся в R10, может быть незамещенной или замещенной одной или более группами, выбранными из галогена, фторированной или незамещенной С1-С2-алкилоксигруппы, цианогруппы, циклопропила и гидроксигруппы, где такой заместитель предпочтительно выбран из фтора, фторированной или незамещенной С1-С2-алкилоксигруппы и цианогруппы;
и R11 выбран из группы, включающей водород, фтор, хлор, метил, фторметил, метоксигруппу, фторметоксигруппу и цианогруппу,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном предпочтительном варианте осуществления R2, если присутствует, в соединениях формулы VI и VIa-d обозначает водород, R4 обозначает водород или фтор, более предпочтительно водород; R5 выбран из водорода, фтора, хлора и брома, и предпочтительно обозначает водород; R6 выбран из группы, включающей фтор, хлор, бром, азидогруппу, метилсульфинил, метилсульфонил, метил, моно-, ди- и трифторметил, метоксигруппу, моно-, ди- и трифторметоксигруппу, и моно-, ди- и трифторэтоксигруппу; R7, если присутствует, выбран из группы, включающей водород, фтор, хлор, бром, метил, фторметил, метоксигруппу, фторметоксигруппу, фторэтоксигруппу, метилсульфинил и метилсульфонил, R8 выбран из группы, включающей водород, фтор, хлор, бром, метил, фторметил, метоксигруппу и фторметоксигруппу, и предпочтительно обозначает фтор или метоксигруппу; R9 выбран из группы, включающей водород, фтор, метоксигруппу и фторметоксигруппу, и предпочтительно обозначает водород; R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, цианоэтоксигруппу, незамещенный или фторированный С1-С3-алкил, незамещенную или фторированную С1-С3-алкилоксигруппу, незамещенный или фторированный С1-С2-алкилокси(С1-С3)алкил,незамещенную или фторированную С1-С2-алкилокси(С1-С3)алкилоксигруппу, незамещенный или фторированный С1-С2-алкилокси(С2-С3)алкенил, циклопропил, циклопропилоксигруппу и циклопропилметоксигруппу, где любой циклопропильный фрагмент необязательно замещен остатком, выбранным из группы, включающей фтор, цианогруппу, С1-С2-алкоксигруппу, фтор(С1-С2)алкоксигруппу, С1-С2-алкокси(С1-С2)алкоксигруппу, фтор(С1-С2)алкокси(С1-С2)алкоксигруппу, С1-С2-алкоксикарбонил, фтор(С1-С2)алкоксикарбонил; и R11 выбран из группы, включающей водород, фтор, хлор, метил, фторметил, метоксигруппу и фторметоксигруппу, где предпочтительно по меньшей мере один заместитель, более предпочтительно два заместителя и более предпочтительно все заместители, содержащиеся в R8, R10 и R11, отличаются от водорода, и где в одном особенно предпочтительном варианте осуществления R8 и R11 оба независимо выбраны из фтора и метоксигруппы.
Другой вариант осуществления относится к соединениям формулы VI и VIa-d, в которых R2, если присутствует, обозначает водород, R4 и R5 оба обозначают водород, R6 выбран из группы, включающей фтор, хлор, бром, метилсульфинил, фторметил, метоксигруппу и фторметоксигруппу, R7 выбран из группы, включающей водород, фтор, хлор, бром, незамещенный или фторированный С1-С2-алкил, незамещенную или фторированную С1-С2-алкоксигруппу, метилсульфинил и метилсульфонил, R8 выбран из группы, включающей водород, фтор, хлор метоксигруппу и фторметоксигруппу, R9 обозначает водород, метоксигруппу или фтор, предпочтительно водород, R10 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, незамещенный или фторированный и/или гидроксилированный С1-С3-алкил, незамещенную или фторированную и/или гидроксилированную С1-С3-алкоксигруппу, незамещенный или фторированный и/или гидроксилированный С1-С2-алкокси(С1-С3)алкил, незамещенную или фторированную и/или гидроксилированную С1-С2-алкокси(С1-С3)алкоксигруппу, незамещенный или фторированный и/или гидроксилированный С1-С2-алкокси(С2-С3)алкенил и незамещенный или фторированный C1-C2-алкоксикарбонилциклопропил, и предпочтительно выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, незамещенный или фторированный С1-С3-алкил, незамещенную или фторированную С1-С3-алкоксигруппу, незамещенный или фторированный С1-С2-алкокси(С1-С3)алкил, незамещенную или фторированную С1-С2-алкокси(С1-С3)алкоксигруппу, незамещенный или фторированный С1-С2-алкокси(С2-С3)алкенил, незамещенный или фторированный С1-С2-алкоксикарбонил-циклопропил и незамещенный или фторированный С1-С3-алкоксициклопропил, и R11 выбран из группы, включающей водород, фтор, хлор, фторметил, метоксигруппу и фторметоксигруппу, где в особенно предпочтительном варианте осуществления по меньшей мере один, более предпочтительно оба R8 и R11 отличаются от водорода.
Другой вариант осуществления относится к соединениям формулы VI и VIa-d, в которых:
R2, R4 и R9 все обозначают водород,
R5 обозначает водород, фтор, хлор или бром, и предпочтительно обозначает водород,
R6 выбран из группы, включающей фтор, хлор, бром, метоксигруппу, фторметоксигруппу, фторметил и азидогруппу,
или R6 вместе с R7 в соединениях формулы VI, VIa, VIb или VIc, вместе с атомами углерода, к которым R6 и R7 присоединены, могут образовать кольцо, выбранное из фенила, пиридила, циклогексила и циклопентила, каждое из которых может быть незамещенным или содержать один или два заместителя, выбранных из группы, включающей фтор, хлор, гидроксигруппу, цианогруппу, метоксигруппу, фторметоксигруппу и фторметил,
R7 выбран из группы, включающей водород, фтор, хлор, бром, незамещенный или фторированный метил, незамещенную или фторированную метоксигруппу и метилсульфинил,
R8 выбран из фтора, хлора, метоксигруппы и фторметоксигруппы,
R10 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, цианометоксигруппу, незамещенный или фторированный С1-С3-алкил, незамещенную или фторированную С1-С3-алкоксигруппу, незамещенный или фторированный С1-С2-алкокси(С1-С3)алкил, незамещенную или фторированную С1-С2-алкокси(С1-С3)алкоксигруппу, и незамещенный или фторированный С1-С2-алкокси(С2-С3)алкенил, где R10 предпочтительно выбран из группы, включающей фтор, хлор, бром, цианометил, цианоэтил, незамещенный или фторированный С1-С3-алкил, незамещенную или фторированную С1-С3-алкоксигруппу, незамещенный или фторированный С1-С2-алкокси(С1-С3)алкил, незамещенную или фторированную С1-С2-алкокси(С1-С3)алкоксигруппу, незамещенный или фторированный С1-С2-алкокси(С2-С3)алкенил, незамещенный или фторированный С1-С3-алкоксициклопропил, незамещенный или фторированный С1-С3-алкоксикарбонилциклопропил и незамещенный или фторированный С1-С2-алкокси(С1-С2)алкоксициклопропил,
R11 выбран из группы, включающей водород, фтор, хлор, метил, фторметил, фторметоксигруппу и метоксигруппу,
и к их фармацевтически приемлемым солям, сольватам, изотопам и совместным кристаллам.
В одном предпочтительном варианте осуществления R6 и R10 в соединениях формулы VI и VIa-d отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления R6, R8 и R10 в соединениях формулы VI и VIa-d все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении
В одном предпочтительном варианте осуществления R6, R8, R10 и R11 в соединениях формулы VI и VIa-d все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном варианте осуществления R7 в соединениях формулы VI и VIa-c не обозначает водород.
В одном предпочтительном варианте осуществления R6, R8 и по меньшей мере один из R10 и R11 в соединениях формулы VI и VIa-d, все, отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном варианте осуществления R6 и R7 в соединениях формулы VI и VIa образуют кольцо, выбранное из фенила, пиридила, циклопентила и циклогексила, и образуют таким образом соединения приведенных ниже формул VIe-VIg:
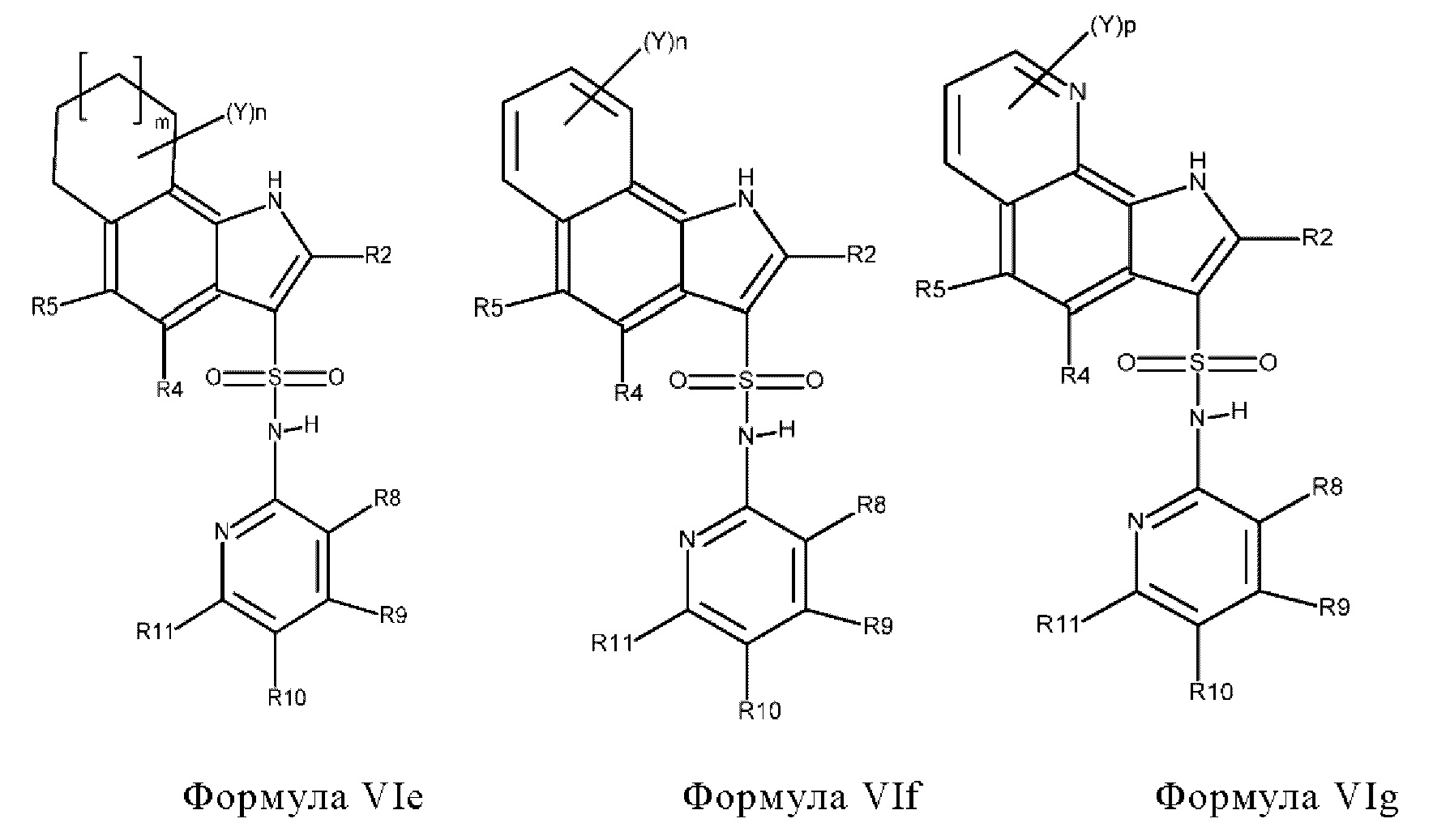
в которых
m равно 0 или 1,
n обозначает любое число, равное от 0 до 4, предпочтительно от 0 до 2, более предпочтительно 0 или 1,
р обозначает любое число, равное от 0 до 3, предпочтительно от 0 до 2, более предпочтительно 0 или 1,
Y выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, гидроксигруппу, метил и метоксигруппу, где метоксигруппа и метильная группа необязательно содержат один или более заместителей, выбранных из группы, включающей фтор, хлор, бром, гидроксигруппу, метоксигруппу и фторметоксигруппу,
R2 и R4 оба обозначают водород,
R5 выбран из водорода, фтора и хлора, более предпочтительно обозначает водород,
R8 выбран из фтора, фторметила, метоксигруппы и фторметоксигруппы,
R9 обозначает водород или фтор,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, цианопропил, цианометоксигруппу, цианоэтоксигруппу, нитрогруппу, азидогруппу, пентафторсульфанил, С1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, С1-С3-алкилоксигруппу, С1-С2-алкилкарбонил, циклопропил, циклопропилметил и циклопропилметоксигруппу, где каждая группа, содержащаяся в R10, может быть незамещенной или замещенной одной или более группами, выбранными из фтора, фторированной или незамещенной С1-С2-алкилоксигруппы, фторированного или незамещенного С1-С2-алкилоксикарбонила и гидроксигруппы,
R11 выбран из группы, включающей водород, фтор, хлор, фторметил, метоксигруппу и фторметоксигруппу,
и их фармацевтически приемлемых солей, сольватов, изотопов и совместных кристаллов.
В одном предпочтительном варианте осуществления в соединениях формулы VIe:
m равно 0 или 1,
n равно 0 или 1, предпочтительно 0,
Y выбран из группы, включающей фтор, хлор, цианогруппу, гидроксигруппу, метил и метоксигруппу, где метоксигруппа и метильная группа необязательно содержат один или более заместителей, выбранных из группы, включающей фтор, хлор, бром, гидроксигруппу, метоксигруппу и фторметоксигруппу,
R2 и R4 обозначают водород,
R5 обозначает водород, фтор, или хлор, предпочтительно водород,
R8 выбран из фтора, фторметила, метоксигруппы и фторметоксигруппы, предпочтительно из фтора и метоксигруппы,
R9 обозначает водород или фтор, предпочтительно водород,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, пентафторсульфанил, С1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, С1-С3-алкилоксигруппу, С1-С2-алкилкарбонил и циклопропил, где каждая алкильная, алкенильная, алкинильная группа, алкилоксигруппа и циклопропильная группа, содержащаяся в R10, может быть незамещенной или предпочтительно замещенной одной или более группами, выбранными из фтора, фторированной или незамещенной С1-С2-алкилоксигруппы, фторированного или незамещенного С1-С2-алкилоксикарбонила и гидроксигруппы, где указанный заместитель предпочтительно выбран из фтора и фторированной или незамещенной С1-С2-алкилоксигруппы,
R11 выбран из группы, включающей водород, фтор, хлор, фторметил, метоксигруппу и фторметоксигруппу,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном предпочтительном варианте осуществления в соединениях формулы VI(f):
n равно 0 или 1, предпочтительно 0,
Y выбран из группы, включающей фтор, хлор, цианогруппу, гидроксигруппу, метил и метоксигруппу, где метоксигруппа и метильная группа необязательно содержат один или более заместителей, выбранных из группы, включающей фтор, хлор, бром, гидроксигруппу, метоксигруппу и фторметоксигруппу,
R2 и R4 оба обозначают водород,
R5 обозначает водород, фтор, или хлор, предпочтительно водород,
R8 выбран из фтора, фторметила, метоксигруппы и фторметоксигруппы,
R9 обозначает водород или фтор, предпочтительно водород,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, пентафторсульфанил, С1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, С1-С3-алкилоксигруппу, С1-С2-алкилкарбонил и циклопропил, где каждая алкильная, алкенильная, алкинильная группа, алкилоксигруппа и циклопропильная группа, содержащаяся в R10, может быть незамещенной или предпочтительно замещенной одной или более группами, выбранными из фтора, фторированной или незамещенной С1-С2-алкилоксигруппы, фторированного или незамещенного С1-С2-алкилоксикарбонила и гидроксигруппы, где указанный заместитель предпочтительно выбран из фтора и фторированной или незамещенной С1-С2-алкилоксигруппы,
R11 выбран из группы, включающей водород, фтор, хлор, фторметил, метоксигруппу и фторметоксигруппу,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном предпочтительном варианте осуществления в соединениях формулы VIg:
р равно 0 или 1,
Y выбран из группы, включающей фтор, хлор, цианогруппу, гидроксигруппу, метил и метоксигруппу, где метоксигруппа и метильная группа необязательно содержат один или более заместителей, выбранных из группы, включающей фтор, хлор, бром, гидроксигруппу, метоксигруппу и фторметоксигруппу,
R4 обозначает водород,
R5 обозначает водород или фтор, предпочтительно водород,
R8 выбран из фтора, фторметила, метоксигруппы и фторметоксигруппы,
R9 обозначает водород или фтор,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, цианометил, цианоэтил, пентафторсульфанил, С1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, С1-С3-алкилоксигруппу, С1-С2-алкилкарбонил и циклопропил, где каждая алкильная, алкенильная, алкинильная группа, алкилоксигруппа и циклопропильная группа, содержащаяся в R10, может быть незамещенной или предпочтительно замещенной одной или более группами, выбранными из фтора, фторированной или незамещенной С1-С2-алкилоксигруппы, фторированного или незамещенного С1-С2-алкилоксикарбонила и гидроксигруппы, где указанный заместитель предпочтительно выбран из фтора и фторированной или незамещенной С1-С2-алкилоксигруппы,
R11 выбран из группы, включающей водород, фтор, хлор, фторметил, метоксигруппу и фторметоксигруппу,
и их фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
В одном предпочтительном варианте осуществления R10 в соединениях формулы VIe-g выбран из группы, включающей хлор, цианогруппу, цианометил, цианоэтил, С1-С3-алкил и С1-С3-алкоксигруппу, где каждый алкил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из группы, включающей фтор, метоксигруппу, фторметоксигруппу, этоксигруппу и фторэтоксигруппу, где в одном варианте осуществления R10 выбран из группы, включающей хлор, бром, незамещенную или фторированную С1-С3-алкоксигруппу, цианогруппу, цианометил и цианоэтил. В одном предпочтительном варианте осуществления соединений формулы VIe-g, R10 обозначает хлор.
В одном предпочтительном варианте осуществления Y, если присутствует, в соединениях формулы VIe-g выбран из группы, включающей фтор, хлор, цианогруппу, гидроксигруппу, метил, фторметил, гидроксиметил, метоксигруппу и фторметоксигруппу. В одном предпочтительном варианте осуществления Y в соединениях формулы VIg выбран из группы, включающей фтор, гидроксигруппу, фторметил, метоксигруппу и фторметоксигруппу.
В одном предпочтительном варианте осуществления R10 в соединениях формулы VIe-VIg выбран из группы, включающей фтор, хлор, бром, фторметил, фторэтил, фторметоксигруппу, фторэтоксигруппу, цианогруппу и цианометил, и особенно предпочтительно обозначает хлор.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R4 обозначает водород, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2c, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R5 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, незамещенный или фторированный С1-С2-алкил, предпочтительно метил или трифторметил, незамещенную или фторированную С1-С2-алкилоксигруппу, незамещенный или фторированный С1-С2-алкилкарбонил, незамещенный или фторированный С1-С2-алкилоксикарбонил, С1-С2-алкилсульфинил, предпочтительно метилсульфинил, и С1-С2-алкилсульфонил, предпочтительно метилсульфонил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, трифторметил, метоксигруппу и трифторметоксигруппу, и особенно предпочтительно выбран из группы, включающей водород, фтор, хлор и бром, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R5 обозначает йод и R6 обозначает водород, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R5 обозначает водород, а другие заместители являются такими, как раскрыто в настоящем изобретении
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7, если присутствует, обозначает водород, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7, если присутствует, обозначает фтор, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7, если присутствует, обозначает C1-С3-алкоксигруппу или фтор(С1-С3)алкоксигруппу, предпочтительно моно-, ди- или трифторметоксигруппу, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7, если присутствует, обозначает метоксигруппу, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7, если присутствует, выбран из группы, включающей водород, цианогруппу, фтор, хлор, бром, метоксигруппу, этоксигруппу, фторметоксигруппу, фторэтоксигруппу, метил, этил, фторметил, фторэтил, метилсульфинил, фторметилсульфинил, метилсульфонил и фторметилсульфонил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7, если присутствует, обозначает метилсульфонил, фторметилсульфонил, метилсульфинил или фторметилсульфинил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7 обозначает трифторметил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7, если присутствует, обозначает цианогруппу, цианометил или цианометоксигруппу, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7 обозначает бром или хлор, предпочтительно бром, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIc, II-2c, IId, II-2d, IIe, II-2е, IIf, II-2f, IIg, II-2g, III, III-2, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, метил и трифторметил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, I, I-2, II, II-2, IIc, II-2c, IId, II-2d, IIe, II-2е, IIf, II-2f, IIg, II-2g, III, III-2, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R8 выбран из группы, включающей фтор, хлор, цианогруппу, метоксигруппу и фторметоксигруппу, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIc, II-2c, IId, II-2d, IIe, II-2е, III, III-2, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R9 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, метил, цианогруппу и трифторметил, и предпочтительно обозначает водород, фтор, хлор или бром, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIc, II-2c, IId, II-2d, IIe, II-2е, III, III-2, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R9 обозначает водород, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2c, IId, II-2d, IIe, II-2е, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, фторметоксигруппу, метил, цианогруппу и фторметил, предпочтительно трифторметил, и более предпочтительно выбран из группы, включающей водород, метоксигруппу, фторметоксигруппу, фторметил, фтор, хлор и бром, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V или V-2, в которых Х3 обозначает C-R12 и R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, метил и фтор(С1-С3)алкил, предпочтительно трифторметил, и более предпочтительно обозначает водород, фтор, хлор или бром, а другие заместители являются такими, как раскрыто в настоящем изобретении. В особенно предпочтительном варианте осуществления R12 обозначает водород или фтор.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc и VId, в которых R6 отличается от водорода, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc и VId, в которых R6 выбран из группы, включающей галоген, циклопропил, циклопропилоксигруппу, циклопропилметил, незамещенный или фторированный C1-С3-алкил, незамещенную или фторированную C1-С3-алкилоксигруппу, незамещенный или фторированный фенил, бензилоксигруппу, тиофен, метилсульфинил, метилсульфонил и циклопропил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc и VId, в которых R6 выбран из группы, включающей фтор, хлор, бром, метоксигруппу, метил, этил, изопропил, циклопропил, фенил, бензилоксигруппу, 2-тиофен, 3-тиофен, трифторметил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc и VId, в которых R6 обозначает хлор или бром, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc и VId, в которых R6 обозначает хлор, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb, VIc и VId, в которых R6 выбран из группы, включающей галоген, цианогруппу, С1-С3-алкил, С1-С3-алкилоксигруппу, С3-С6-циклоалкил и С3-С6-циклоалкилоксигруппу, причем каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора и незамещенной или фторированной С1-С3-алкоксигруппы.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, IV, IV-2, V, V-2, VI, VIa, VIb или VIc, в которых R7 выбран из группы, включающей водород, галоген, цианогруппу, С1-С3-алкил, С1-С3-алкилоксигруппу, С3-С6-циклоалкил и С3-С6-циклоалкилоксигруппу, причем каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора и незамещенной или фторированной С1-С3-алкоксигруппы.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, III, III-2, IV, IV-2, V и V-2, в которых Х3 обозначает C(R12), а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, III, III-2, IV, IV-2, V и V-2, в которых Х3 обозначает N, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, II, IIa, IIb, IIc, III или IV, в которых по меньшей мере один из R8, R10 и R11 отличается от водорода и незамещенного алкила.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, галоген(С1-С3)алкил, предпочтительно фтор(С1-С2)алкил, С2-С3-алкинил, метоксигруппу, этоксигруппу, пропоксигруппу, галоген(С1-С3)алкилоксигруппу, предпочтительно фтор(С1-С2)алкилоксигруппу, незамещенную или фторированную (С1-С2)алкокси(С1-С3)алкоксигруппу, цианогруппу, цианометил, азидогруппу, пентафторсульфанил и нитрогруппу, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 выбран из группы, включающей галоген, цианогруппу, С1-С3-алкил, С2-С3-алкенил, С2-С3-алкинил, С1-С3-алкилоксигруппу, С3-С6-циклоалкил и С3-С6-циклоалкилоксигруппу, причем каждая из этих групп необязательно может быть замещена остатком, выбранным из фтора, цианогруппы и необязательно фторированной С1-С3-алкоксигруппы.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 выбран из группы, включающей цианогруппу, цианометил, галоген, азидогруппу, этинил, пентафторсульфанил, ацетил, дифторэтоксигруппу, трифторэтоксигруппу, трифторметоксигруппу и трифторметил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 обозначает цианогруппу, цианометил, цианоэтил или цианометоксигруппу, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 обозначает фтор, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 обозначает хлор, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 обозначает бром, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 обозначает моно-, ди- или трифторметил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 обозначает дифторэтоксигруппу (-OCH3CHF2), а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 обозначает трифторэтоксигруппу (-OCH3CF3), а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, III, III-2, IIIa, III-2a, IIIb, III-2b, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, в которых R10 обозначает этинил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, в которых R10 выбран из группы, включающей метоксиметил, метоксиэтил, метоксипропил, этоксиметил, этоксиэтил, этоксипропил, пропоксиметил, метоксиэтенил, метоксипропенил, этоксиэтенил, этоксипропенил, метоксиэтинил, метоксипропинил, метоксиметоксигруппу, метоксиэтоксигруппу, метоксипропоксигруппу, этоксиметоксигруппу, этоксиэтоксигруппу, этоксипропоксигруппу и пропоксиметоксигруппу, каждая из которых может быть незамещенной или содержать в качестве заместителей вплоть до 3 атомов фтора, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, в которых R10 обозначает метоксипропил или фторированный метоксипропил, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой особенно предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, дополнительно описанным в настоящем изобретении, в которых R8, R10 и R11 все отличаются от водорода, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой особенно предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, II, III, или IV, дополнительно описанной в настоящем изобретении, в которых R6, R8, и R10 все отличаются от водорода, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой особенно предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, II, III, или IV, дополнительно описанной в настоящем изобретении, в которых R6, R8, R10 и R11 все отличаются от водорода, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, дополнительно описанным в настоящем изобретении, в которых по меньшей мере один из R5, R6 и R7 отличается от водорода, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, дополнительно описанным в настоящем изобретении, в которых по меньшей мере один из R6 и R7 отличается от водорода, а другие заместители являются такими, как раскрыто в настоящем изобретении.
Другой вариант осуществления относится к соединениям формулы III, дополнительно описанным в настоящем изобретении, в которых по меньшей мере один из R6 и R5 отличается от водорода, а другие заместители являются такими, как раскрыто в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R10 и по меньшей мере один из R5, R6 и R7 отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R6 и R10 отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R6, R10 и по меньшей мере один из R8 и R11 отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R6, R8 и R11 все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении,
(a) по меньшей мере один из R5, R6 и R7, если R7 содержится, и
(b) по меньшей мере один из R8, R10 и R11 отличаются от водорода.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R6, R7, если присутствует, R8, R10 и R11 все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R4 обозначает водород и R6, R8, R10 и R11 все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R4, R5 и R9 все обозначают водород и R6, R8, и R10 все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R4, R5, R9 и R12, если присутствует, все обозначают водород и R6, R8 и R10 все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R4 и R12, если присутствует, оба обозначают водород, R5 и R9 независимо обозначают водород или фтор и R6, R8, R10 и R11 все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R4, R5, R9 и R12, если присутствует, все обозначают водород и R6, R8, R10 и R11 все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R4 и R12, если присутствует, оба обозначают водород, R5 и R9 независимо обозначают водород или фтор и R6, R7, R8, R10 и R11 все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
В одном предпочтительном варианте осуществления в соединениях, предлагаемых в настоящем изобретении, R2, R4, R5, R9 и R12, если присутствует, все обозначают водород и R6, R7, R8, R10 и R11 все отличаются от водорода и независимо выбраны из группы, дополнительно определенной в настоящем изобретении.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, II, III, или IV, в которых R4 и R5 оба обозначают водород, R6 обозначает хлор или бром, Х3 обозначает CR12, R8 и R11 оба выбраны из галогена, предпочтительно фтора, и метоксигруппы, R10 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, цианометил, азидогруппу, ацетил, этинил, дифторэтоксигруппу, трифторэтоксигруппу и трифторметил, и R9 и R12 оба обозначают водород.
Другой особенно предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, II, IIa, IIb, IIc, III или IV, дополнительно описанные в настоящем изобретении, в которых R8 и R9 вместе с кольцом, к которому они присоединены, образуют 2,1,3-бензотиадиазол, а другие заместители являются такими, как раскрыто в настоящем изобретении. В одном воплощении этого варианта осуществления R10, R11 и R12 все обозначают водород.
Другой особенно предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, II, IIa, IIb, IIc, III или IV, дополнительно описанные в настоящем изобретении, в которых R10 и R9 вместе с кольцом, к которому они присоединены, образуют 2,1,3-бензотиадиазол, а другие заместители являются такими, как раскрыто в настоящем изобретении. В одном воплощении этого варианта осуществления R10 и R11 оба обозначают водород, а R12 обозначает водород, фтор или хлор.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, и содержащие по меньшей мере один изотоп18F, предпочтительно в положении атома фтора, указанном в одном из соединений, раскрытых в настоящем изобретении. В качестве неограничивающего примера можно привести следующий: в соединении 6-хлор-N-[2-фтор-4-(пентафторсульфанил)фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид, раскрытом в настоящем изобретении, по меньшей мере один из 6 атомов фтора можно заменить на изотоп18F или он может содержать подходящее количество изотопа18F. В качестве другого примера можно привести следующий: атом фтора, содержащийся в соединении 7-бром-6-хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид, может быть представлен изотопом18F или может быть включено количество18F, которое можно измерить с помощью подходящего для PET (позитронная эмиссионная томография) оборудования. Это также относится к другим содержащим фтор соединениям, описанным в настоящем изобретении. Эти содержащие18F соединения предпочтительно можно использовать в качестве предназначенных для PET радиоактивных индикаторов.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, и содержащие по меньшей мере один изотоп11С, предпочтительно в положении атома углерода, указанном в настоящем изобретении. Эти содержащие11С соединения предпочтительно можно использовать в качестве предназначенных для PET радиоактивных индикаторов.
Другой предпочтительный вариант осуществления относится к соединениям, предлагаемым в настоящем изобретении, включая, но не ограничиваясь только ими, формулы I, I-2, II, II-2, IIa, II-2a, IIb, II-2b, IIc, II-2с, IId, II-2d, IIe, II-2e, IIf, II-2f, IIg, II-2g, III, III-2, IIIa, III-2a, IIIb, III-2b, IIIc, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf или VIg, и содержащие по меньшей мере один изотоп123I,125I или131I, предпочтительно в положении атома йода, указанном в настоящем изобретении. В качестве неограничивающего примера можно привести следующий: в соединении N-(4-цианофенил)-5-йод-1Н-пирроло[2,3-b]пиридин-3-сульфонамид, раскрытом в настоящем изобретении, йод может быть представлен изотопом123I,125I или131I. Это также относится к другим содержащим йод соединениям, описанным в настоящем изобретении. Эти содержащие123I,125I или131I соединения предпочтительно можно использовать в качестве предназначенных для SPECT (однофотонная эмиссионная компьютерная томография) радиоактивных индикаторов.
Один вариант осуществления относится к любому из соединений, предлагаемых в настоящем изобретении, которые специально раскрыты в настоящем изобретении.
Предпочтительный вариант осуществления относится к соединению, выбранному из следующих:
6-хлор-N-(4-этинилфенил)-1Н-индол-3-сульфонамид
6-хлор-N-(5-цианопиридин-2-ил)-1H-индол-3-сульфонамид
7-хлор-N-(4-хлор-2,5-дифторфенил)-6-(метилсульфинил)-1Н-индол-3-сульфонамид
6-хлор-N-[3-фтор-5-(метоксиметил)пиридин-2-ил]-1Н-индол-3-сульфонамид
6-хлор-N-(5-йод-3-метилпиридин-2-ил)-1H-индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-(трифторметил)-1H-индол-3-сульфонамид
N-(2,5-дифторфенил)-6-метил-1H-индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-(тетрагидрофуран-3-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(пиридин-3-ил)-1H-индол-3-сульфонамид
N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид
6-циано-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1H-индол-3-сульфонамид
6-хлор-N-(7-циано-2,1,3-бензотиадиазол-4-ил)-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-7-бром-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-6-метокси-1H-индол-3-сульфонамид
6-хлор-N-[2,5-дифтор-4-(пиридин-2-илметокси)фенил]-1H-индол-3-сульфонамид
6-хлор-N-(3-фтор-5-метилпиридин-2-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-(3-гидроксипроп-1-ен-2-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(7-фтор-2,1,3-бензоксадиазол-4-ил)-1H-индол-3-сульфонамид
N-(2,5-дифторфенил)-6-(метилсульфонил)-1H-индол-3-сульфонамид
N-(4-циано-2,5-дифторфенил)-6-(2-метоксиэтокси)-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-6,7,8,9-тетрагидро-1Н-бензо[g]индол-3-сульфонамид
6-хлор-N-{2-фтор-4-[(1Е)-3-метоксипроп-1-ен-1-ил]фенил}-1Н-индол-3-сульфонамид
N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-5-йод-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(4,6-дихлорпиридин-2-ил)-1H-индол-3-сульфонамид
6-хлор-N-(2,3-дифторфенил)-1H-индол-3-сульфонамид
N-(2-фтор-4-йодфенил)-6-(трифторметил)-1H-индол-3-сульфонамид
N-(1,3-бензодиоксол-4-ил)-6-метил-1H-индол-3-сульфонамид
6-хлор-N-(2-хлорфенил)-1H-индол-3-сульфонамид
5-бром-N-(4-цианофенил)-1H-индол-3-сульфонамид
N-(4-бром-2,5-дифторфенил)-6-хлор-1H-индол-3-сульфонамид
6-бром-N-(4-циано-2,5-дифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-1H-пирроло[3,2-h]хинолин-3-сульфонамид
N-(4-бром-2,5-дифторфенил)-1H-пирроло[3,2-h]хинолин-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-[4-(дифторметокси)-2,5-дифторфенил]-1H-индол-3-сульфонамид
N-[4-(цианометил)-2,5-дифторфенил]-1H-пирроло[3,2-h]хинолин-3-сульфонамид
6-бром-N-[3,6-дифтор-5-(3-метоксипропил)пиридин-2-ил]-1H-индол-3-сульфонамид
N-(5-бром-3,6-дифторпиридин-2-ил)-6-хлор-1H-индол-3-сульфонамид
N-(4-бром-2,5-дифторфенил)-6-хлор-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-7-фтор-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-1Н-бензо[g]индол-3-сульфонамид
6-хлор-N-[3,6-дифтор-5-(3-метоксипропил)пиридин-2-ил]-1H-индол-3-сульфонамид
5-бром-6-хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид
6-хлор-N-(5-хлор-3,6-дифторпиридин-2-ил)-1H-индол-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-фтор-1Н-индол-3-сульфонамид
N-(4-циано-2,5-дифторфенил)-1H-бензо[g]индол-3-сульфонамид
N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1Н-бензо[g]индол-3-сульфонамид
7-бром-6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1Н-индол-3-сульфонамид
6-хлор-N-[4-(цианометокси)-2,5-дифторфенил]-1Н-индол-3-сульфонамид
N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид
6-хлор-N-(4-циано-5-фтор-2-метоксифенил)-1Н-индол-3-сульфонамид
6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1Н-индол-3-сульфонамид
6-хлор-N-(5-этил-3,6-дифторпиридин-2-ил)-1Н-индол-3-сульфонамид
6-хлор-N-{5-[(Е)-2-этоксиэтенил]-3,6-дифторпиридин-2-ил}-1Н-индол-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-метокси-1Н-индол-3-сульфонамид
6-хлор-N-(4-хлор-2-фторфенил)-1Н-индол-3-сульфонамид
этил-3-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)пропаноат
6-хлор-N-[2,5-дифтор-4-(трифторметил)фенил]-1Н-индол-3-сульфонамид
6-бром-N-{3,6-дифтор-5-[(1Е)-3-метоксипроп-1-ен-1-ил]пиридин-2-ил}-1Н-индол-3-сульфонамид
6-хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1-бензотиофен-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-6-бром-1Н-индол-3-сульфонамид
6-хлор-N-[4-(2,2-дифторэтокси)-2,5-дифторфенил]-1Н-индол-3-сульфонамид
этил-(2Е)-3-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)проп-2-еноат
N-(5-хлор-3-фторпиридин-2-ил)-1H-бензо[g]индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-8-(дифторметил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-7-метокси-1Н-индол-3-сульфонамид
6-хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-7-фтор-1Н-индол-3-сульфонамид
6-хлор-N-(2,5-дифтор-4-йодфенил)-1Н-индол-3-сульфонамид
N-(4-циано-5-фтор-2-метоксифенил)-1H-бензо[g]индол-3-сульфонамид
N-[4-(цианометокси)-2,5-дифторфенил]-1Н-пирроло[3,2-h]хинолин-3-сульфонамид
N-(4-циано-2,5-дифторфенил)-6-(трифторметил)-1Н-индол-3-сульфонамид
6-хлор-N-(6-фтор-2,1,3-бензотиадиазол-5-ил)-1Н-индол-3-сульфонамид
6-хлор-N-[4-(дифторметокси)-2,5-дифторфенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(2,1,3-бензоселенадиазол-4-ил)-6-хлор-1Н-индол-3-сульфонамид
6-хлор-N-[2,5-дифтор-4-(трифторметил)фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-{3,6-дифтор-5-[(1Е)-3-метоксипроп-1-ен-1-ил]пиридин-2-ил}-1Н-индол-3-сульфонамид
6-хлор-N-(4-циано-2-фторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(2,5-дифтор-4-метилфенил)-1Н-индол-3-сульфонамид
6-хлор-N-[5-(2-этоксиэтил)-3,6-дифторпиридин-2-ил]-1Н-индол-3-сульфонамид
6-хлор-N-(5-хлор-3,6-дифторпиридин-2-ил)-7-метокси-1Н-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(тиофен-2-ил)-1Н-индол-3-сульфонамид
6-хлор-N-(4-этинил-2-фторфенил)-1Н-индол-3-сульфонамид
6-хлор-N-[3-фтор-5-(трифторметил)пиридин-2-ил]-1H-индол-3-сульфонамид
6-хлор-N-[2-фтор-4-(трифторметил)фенил]-1Н-индол-3-сульфонамид
7-бром-6-хлор-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамид
6-бром-N-(4-циано-2-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(4-циано-2,5-дифторфенил)-1Н-индол-3-сульфонамид
6-бром-N-(2-фтор-4-йодфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(5-бром-6-фтор-3-метоксипиридин-2-ил)-6-хлор-1H-индол-3-сульфонамид
6-хлор-N-(2-фтор-4-йодфенил)-1H-индол-3-сульфонамид
6-хлор-N-[5-(цианометил)-6-фтор-3-метоксипиридин-2-ил]-1H-индол-3-сульфонамид
6-бром-7-хлор-N-(4-хлор-2,5-дифторфенил)-1H-индол-3-сульфонамид
6-бром-N-(6-фтор-2,1,3-бензотиадиазол-5-ил)-1H-индол-3-сульфонамид
N-(4-бром-2,5-дифторфенил)-6-метокси-1H-индол-3-сульфонамид
6-бром-N-(4-циано-2-фторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(4-циано-2-фтор-5-метоксифенил)-1H-индол-3-сульфонамид
N-(5-хлор-3,6-дифторпиридин-2-ил)-1H-бензо[g]индол-3-сульфонамид
6-азидо-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1H-индол-3-сульфонамид
6-хлор-N-[3,6-дифтор-5-(2-фторэтокси)пиридин-2-ил]-1H-индол-3-сульфонамид
6-хлор-N-(6-фтор-1-метил-3-оксо-1,3-дигидро-2-бензофуран-5-ил)-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-5Н-[1,3]диоксоло[4,5-f]индол-7-сульфонамид
6-бром-N-(5-хлор-3-фторпиридин-2-ил)-1H-индол-3-сульфонамид
N-[4-(цианометокси)-2,5-дифторфенил]-6-(дифторметил)-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-1H-бензо[g]индол-3-сульфонамид
6-бром-N-(4-хлор-2-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(2,2-дифторэтокси)-1H-индол-3-сульфонамид
6-бром-N-(4-цианофенил)-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-5-ил)-6-бром-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(пропан-2-ил)-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(трифторметил)-1H-индол-3-сульфонамид
N-(4-циано-2,5-дифторфенил)-6-метокси-1H-индол-3-сульфонамид
N-(4-бром-2,5-дифторфенил)-6-метокси-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(5-этенил-3,6-дифторпиридин-2-ил)-1H-индол-3-сульфонамид
N-(4-бром-2,5-дифторфенил)-6-(метилсульфинил)-1H-индол-3-сульфонамид
N-(4-бром-2,5-дифторфенил)-6-хлор-1-бензофуран-3-сульфонамид
N-[4-(дифторметокси)-2,5-дифторфенил]-6-(метилсульфинил)-1H-индол-3-сульфонамид
6-хлор-N-(2,4,5-трифторфенил)-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-8-гидрокси-1Н-пирроло[3,2-h]хинолин-3-сульфонамид
6-хлор-N-(2,5-дифтор-4-метилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-циано-1H-индол-3-сульфонамид
6-хлор-N-[5-(цианометил)-3-метоксипиридин-2-ил]-1H-индол-3-сульфонамид
N-[4-(2-цианоэтил)-2,5-дифторфенил]-1H-пирроло[3,2-h]хинолин-3-сульфонамид
6-хлор-N-[4-(цианометил)-2-фторфенил]-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-1,6,7,8-тетрагидроциклопента[g]индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-1H-пирроло[3,2-h]хинолин-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-6-(трифторметил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-этинил-2-фторфенил)-1H-пирроло[3,2-h]хинолин-3-сульфонамид
N-(4-бром-2-фторфенил)-6-хлор-1H-индол-3-сульфонамид
6-бром-N-(5-хлор-3-фторпиридин-2-ил)-7-метил-1H-индол-3-сульфонамид
6-хлор-N-[4-хлор-5-(дифторметокси)-2-фторфенил]-1H-индол-3-сульфонамид
N-(2,1,3-бензоксадиазол-5-ил)-6-хлор-1H-индол-3-сульфонамид
5-бром-6-хлор-N-(4-циано-2-фторфенил)-1H-индол-3-сульфонамид
6-(бензилокси)-N-(4-циано-2,5-дифторфенил)-1H-индол-3-сульфонамид
N-(6-фтор-2,1,3-бензотиадиазол-5-ил)-1H-бензо[g]индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-6-хлор-1H-индол-3-сульфонамид
6-хлор-N-(3,6-дифтор-5-метилпиридин-2-ил)-1H-индол-3-сульфонамид
6-хлор-N-(4-цианофенил)-1H-индол-3-сульфонамид
6-хлор-N-(5-хлор-3-фторпиридин-2-ил)-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-6-метокси-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-6-(дифторметил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(3-хлор-4-цианофенил)-1H-индол-3-сульфонамид
7-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-6-фтор-1H-индол-3-сульфонамид
6-хлор-N-[2-фтор-4-(пентафтор-лямбда~6~-сульфанил)фенил]-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-цианофенил)-1H-бензо[g]индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид
6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-5,7-дифтор-1H-индол-3-сульфонамид
N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-6-нитро-1H-индол-3-сульфонамид
6-хлор-N-[2-фтор-4-(трифторметил)фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-[4-(цианометокси)-2,5-дифторфенил]-1-бензофуран-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-6-циано-1H-индол-3-сульфонамид
6-хлор-N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-1H-индол-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(метилсульфинил)-1H-индол-3-сульфонамид
6-хлор-N-[3,6-дифтор-5-(пропан-2-ил)пиридин-2-ил]-1H-индол-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-1-бензофуран-3-сульфонамид
7-хлор-N-(4-хлор-2,5-дифторфенил)-6-(метилсульфанил)-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-6-хлор-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-{5-[(дифторметокси)метил]-3-фторпиридин-2-ил}-1H-индол-3-сульфонамид
N-(1,3-бензодиоксол-4-ил)-6-хлор-1Н-индол-3-сульфонамид
6-(бензилокси)-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамид
6-хлор-N-(3,6-дифтор-5-метилпиридин-2-ил)-7-фтор-1H-индол-3-сульфонамид
N-(4-цианофенил)-6-циклопропил-1Н-индол-3-сульфонамид
6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-5-фтор-1H-индол-3-сульфонамид
7-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-6-метокси-1Н-индол-3-сульфонамид
6-хлор-N-(4-циано-5-фтор-2-метоксифенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(6-фтор-3-оксо-1,3-дигидро-2-бензофуран-5-ил)-1H-индол-3-сульфонамид
этил-2-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)циклопропанкарбоксилат
N-(2,1,3-бензоксадиазол-4-ил)-6-хлор-1Н-индол-3-сульфонамид
6-хлор-N-(4-цианофенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(4-хлор-2-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(2,1,3-бензоксадиазол-4-ил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид
6-хлор-N-(4-хлор-5-фтор-2-метоксифенил)-1Н-индол-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-1-бензотиофен-3-сульфонамид
6-хлор-N-[4-(цианометокси)-2,5-дифторфенил]-1-бензотиофен-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-6-бром-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-бром-N-(4-цианофенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(4-циано-2,6-дифторфенил)-1Н-индол-3-сульфонамид
6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(5-бром-3-фторпиридин-2-ил)-6-хлор-1Н-индол-3-сульфонамид
6-хлор-N-(4-циано-2-фторфенил)-5-фтор-1Н-индол-3-сульфонамид
N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-1H-пирроло[3,2-h]хинолин-3-сульфонамид
N-(5-хлор-3,6-дифторпиридин-2-ил)-1H-пирроло[3,2-h]хинолин-3-сульфонамид
N-(4-бром-2-фторфенил)-6-метил-1H-индол-3-сульфонамид
6-бром-N-(4-хлор-2,5-дифторфенил)-4-фтор-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-5-ил)-6-хлор-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-6-метокси-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-6-метокси-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-циано-N-[4-(дифторметокси)-2,5-дифторфенил]-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-6-(метилсульфинил)-1H-индол-3-сульфонамид
6-хлор-N-(6-фтор-2,1,3-бензоксадиазол-5-ил)-1H-индол-3-сульфонамид
6-хлор-N-(3,5-дифтор-6-метоксипиридин-2-ил)-1H-индол-3-сульфонамид
N-(4-циано-5-фтор-2-метоксифенил)-6-метокси-1H-индол-3-сульфонамид
N-[4-(дифторметокси)-2,5-дифторфенил]-6-(дифторметил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(тиофен-3-ил)-1H-индол-3-сульфонамид
N-(4-азидо-2-фторфенил)-6-хлор-1H-индол-3-сульфонамид
6-хлор-N-[2-фтор-4-(трифторметокси)фенил]-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(2-фтор-4-йодфенил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(5-бром-6-хлорпиридин-2-ил)-6-хлор-1H-индол-3-сульфонамид
N-(5-бром-3-метоксипиридин-2-ил)-6-хлор-1H-индол-3-сульфонамид
6-хлор-N-[3-метокси-5-(трифторметил)пиридин-2-ил]-1H-индол-3-сульфонамид
6-хлор-N-(2,5-дифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1-бензотиофен-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(метилсульфонил)-1H-индол-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-5-фтор-1H-индол-3-сульфонамид
N-(2-фтор-4-йодфенил)-5Н-[1,3]диоксоло[4,5-f]индол-7-сульфонамид
N-[4-(цианометокси)-2,5-дифторфенил]-6-фтор-1H-индол-3-сульфонамид
N-[2-фтор-4-(трифторметил)фенил]-6-метокси-1H-индол-3-сульфонамид
6-хлор-N-[2-фтор-4-(пентафтор-лямбда~6~-сульфанил)фенил]-1H-индол-3-сульфонамид
6-бром-N-(2,4,5-трифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(2-фтор-4-йодфенил)-6-(метилсульфонил)-1H-индол-3-сульфонамид
6-хлор-N-(7-фтор-2,1,3-бензотиадиазол-4-ил)-1H-индол-3-сульфонамид
6-хлор-N-(3,6-дифтор-5-метилпиридин-2-ил)-7-(трифторметил)-1H-индол-3-сульфонамид
6-хлор-N-(3,5-дифтор-6-метоксипиридин-2-ил)-7-фтор-1H-индол-3-сульфонамид
6-хлор-N-[2-фтор-4-(трифторметокси)фенил]-1H-индол-3-сульфонамид
6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1-бензофуран-3-сульфонамид
6-хлор-N-(5-хлор-3-фтор-6-метилпиридин-2-ил)-1H-индол-3-сульфонамид
N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-6,7,8,9-тетрагидро-1Н-бензо[g]индол-3-сульфонамид
6-бром-N-(4-этинилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1H-индол-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(3,5-диметил-1,2-оксазол-4-ил)-1H-индол-3-сульфонамид
6-хлор-N-[5-хлор-3-фтор-6-(фторметил)пиридин-2-ил]-1H-индол-3-сульфонамид
6-хлор-N-(3-фтор-5-метилпиридин-2-ил)-1H-индол-3-сульфонамид
6-хлор-N-(2,5-дифтор-4-метоксифенил)-1H-индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-метил-1H-индол-3-сульфонамид
N-(5-хлор-3,6-дифторпиридин-2-ил)-1,6,7,8-тетрагидроциклопента[g]индол-3-сульфонамид
5-бром-6-хлор-N-(4-хлор-2,5-дифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(5-хлор-3,6-дифторпиридин-2-ил)-7-(3,5-диметил-1,2-оксазол-4-ил)-1H-индол-3-сульфонамид
6-бром-N-(2-хлор-3-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(5-хлор-3,6-дифторпиридин-2-ил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-азидо-N-(4-циано-2-фторфенил)-1H-индол-3-сульфонамид
6-(метилсульфонил)-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1H-индол-3-сульфонамид
6-хлор-N-[3,6-дифтор-5-(проп-1-ен-2-ил)пиридин-2-ил]-1H-индол-3-сульфонамид
N-(5-хлор-3-фторпиридин-2-ил)-1H-пирроло[3,2-h]хинолин-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-6-фтор-1H-индол-3-сульфонамид
6-хлор-N-(5-хлор-2-фторфенил)-1H-индол-3-сульфонамид
N-(4-хлор-5-фтор-2-метоксифенил)-1Н-бензо[g]индол-3-сульфонамид
6-хлор-7-(дифторметокси)-N-(3,5-дифтор-6-метоксипиридин-2-ил)-1Н-индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-(метилсульфонил)-1H-индол-3-сульфонамид
6-бром-N-(2,5-дифторфенил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(1,3-бензодиоксол-4-ил)-6-бром-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-6-(трифторметил)-1H-индол-3-сульфонамид
6-хлор-N-(2-хлор-3,5-дифторфенил)-1H-индол-3-сульфонамид
6-амино-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1H-индол-3-сульфонамид
6-амино-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1H-индол-3-сульфонамид
6-(бензилсульфинил)-N-(4-хлор-2,5-дифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(3,6-дифторпиридин-2-ил)-1H-индол-3-сульфонамид
6-хлор-N-(2-фтор-4-метилфенил)-1H-индол-3-сульфонамид
N-(4-бром-2-фторфенил)-6-метокси-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(2,2,2-трифторэтокси)-1H-индол-3-сульфонамид
N-(4-цианофенил)-6-(метилсульфонил)-1H-индол-3-сульфонамид
N-(2,4,5-трифторфенил)-1H-пирроло[3,2-h]хинолин-3-сульфонамид
6-хлор-N-(5-йодпиридин-2-ил)-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(циклопропилметокси)-1Н-индол-3-сульфонамид
N-(4-этинил-2-фторфенил)-6-метокси-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-фтор-N-(2-фтор-4-йодфенил)-1H-индол-3-сульфонамид
6-хлор-N-(5-хлорпиридин-2-ил)-1H-индол-3-сульфонамид
6-хлор-N-(4-циано-2-фторфенил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(4-циано-2-метоксифенил)-1H-индол-3-сульфонамид
6-хлор-N-(3,5-дифтор-6-метоксипиридин-2-ил)-7-(трифторметил)-1Н-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(пиридин-3-ил)-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-5-йод-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-6-(2,2,2-трифторэтокси)-1H-индол-3-сульфонамид
6-хлор-N-(2-оксо-2,3-дигидро-1,3-бензоксазол-7-ил)-1H-индол-3-сульфонамид
6-хлор-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(2,4,5-трифторфенил)-1Н-бензо[g]индол-3-сульфонамид
6-хлор-N-(6-метокси-2,1,3-бензоксадиазол-5-ил)-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-5-ил)-6-хлор-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-этинил-2-фторфенил)-6-метокси-1H-индол-3-сульфонамид
6-хлор-N-[3,6-дифтор-5-(2-метоксиэтокси)пиридин-2-ил]-1H-индол-3-сульфонамид
6-хлор-N-[4-(циклопропилметокси)-2,5-дифторфенил]-1H-индол-3-сульфонамид
N-(4-ацетил-2-фторфенил)-6-хлор-1H-индол-3-сульфонамид
6-хлор-N-(4-циано-3-метоксифенил)-1H-индол-3-сульфонамид
6-хлор-N-(3,5-дифторпиридин-2-ил)-1H-индол-3-сульфонамид
6-хлор-N-(6-циано-2,2-дифтор-1,3-бензодиоксол-4-ил)-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-2-фтор-6-метокси-1H-индол-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-2-фтор-6-метокси-1H-индол-3-сульфонамид
6-хлор-N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-циано-2-фторфенил)-6-фенил-1H-индол-3-сульфонамид
N-(1,3-бензодиоксол-4-ил)-6-хлор-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(4-цианофенил)-1-бензотиофен-3-сульфонамид
6-хлор-N-(4-нитрофенил)-1H-индол-3-сульфонамид
N-(4-цианофенил)-6-(метилсульфинил)-1H-индол-3-сульфонамид
6-(метилсульфонил)-N-(2,4,5-трифторфенил)-1H-индол-3-сульфонамид
N-(4-цианофенил)-5-йод-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(2,4,5-трифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(6-фтор-3-оксо-1,3-дигидро-2-бензофуран-5-ил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(5-фтор-1,3-бензотиазол-6-ил)-1H-индол-3-сульфонамид
6-хлор-N-(7-фтор-2,1,3-бензотиадиазол-4-ил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-хлор-2,5-дифторфенил)-6-(тиофен-3-ил)-1H-индол-3-сульфонамид
6-хлор-N-(2,4-дифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-[3,6-дифтор-5-(3-гидроксипропил)пиридин-2-ил]-1H-индол-3-сульфонамид
6-хлор-N-(2,5-дифторфенил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-метокси-1H-индол-3-сульфонамид
6-хлор-N-(5-фтор-1,1-диоксидо-2,3-дигидро-1-бензотиофен-6-ил)-1H-индол-3-сульфонамид
N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-6-(метилсульфонил)-1H-индол-3-сульфонамид
6-бром-N-(2,4-дифторфенил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(3,5-дихлорпиридин-2-ил)-1H-индол-3-сульфонамид
6-хлор-N-(6-фтор-3-оксо-2,3-дигидро-1Н-изоиндол-5-ил)-1Н-индол-3-сульфонамид
N-(5-бром-3-метоксипиридин-2-ил)-6-хлор-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-циано-1H-индол-3-сульфонамид
6-хлор-N-(2,4,5-трифторфенил)-1-бензофуран-3-сульфонамид
6-хлор-N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-1-бензофуран-3-сульфонамид
6-хлор-N-(4-цианофенил)-1-бензофуран-3-сульфонамид
6-хлор-N-(3-оксо-1,3-дигидро-2-бензофуран-5-ил)-1Н-индол-3-сульфонамид
6-хлор-N-(2-циано-5-фторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(5-хлор-4-метоксипиридин-2-ил)-1Н-индол-3-сульфонамид
6-хлор-N-(3,5-диметоксипиридин-2-ил)-1Н-индол-3-сульфонамид
6-хлор-N-[5-(дифторметокси)-3,6-дифторпиридин-2-ил]-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-5-ил)-6-(трифторметил)-1Н-индол-3-сульфонамид
6-бром-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1H-индол-3-сульфонамид
N-(4-циано-2,5-дифторфенил)-l,6,7,8-тетрагидроциклопента[g]индол-3-сульфонамид
7-бром-6-хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид
N-(4-циано-2,5-дифторфенил)-6-фтор-1Н-индол-3-сульфонамид
N-(4-цианофенил)-6-(трифторметил)-1Н-индол-3-сульфонамид
N-(4-циано-2,5-дифторфенил)-6-метил-1Н-индол-3-сульфонамид
6-бром-N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(2,1,3-бензоселенадиазол-5-ил)-6-хлор-1Н-индол-3-сульфонамид
N-(4-цианофенил)-6-метил-1Н-индол-3-сульфонамид
6-хлор-N-(6-фтор-2,1,3-бензотиадиазол-5-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
7-бром-N-(4-циано-2,5-дифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(3,6-дифтор-5-метилпиридин-2-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид
N-(2,5-дифтор-4-метилфенил)-6-(метилсульфинил)-1H-индол-3-сульфонамид
6-фтор-N-(6-фтор-2,1,3-бензотиадиазол-5-ил)-1H-индол-3-сульфонамид
6-хлор-N-(4-циано-2,5-дифторфенил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-циклопропил-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(2,1,3-бензотиадиазол-4-ил)-6-хлор-7-(трифторметил)-1H-индол-3-сульфонамид
N-(2,l,3-бензотиадиазол-5-ил)-1H-бензо[g]индол-3-сульфонамид
N-(4-циано-3-фторфенил)-1,6,7,8-тетрагидроциклопента[g]индол-3-сульфонамид
6-бром-N-(4-цианофенил)-5-метил-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-4,6-дифтор-1H-индол-3-сульфонамид
N-(4-циано-2,5-дифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(4-циано-3-метилфенил)-1H-индол-3-сульфонамид
N-(4-цианофенил)-6-фтор-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-5-ил)-6-фтор-1H-индол-3-сульфонамид
N-(2,1,3-бензотиадиазол-5-ил)-1,6,7,8-тетрагидроциклопента[g]индол-3-сульфонамид
6-хлор-N-[5-(цианометил)-3-фтор-6-метилпиридин-2-ил]-1H-индол-3-сульфонамид
7-хлор-N-(4-циано-2,5-дифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(пиридин-2-илметокси)-1H-индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-8-(дифторметил)-1H-пирроло[3,2-h]хинолин-3-сульфонамид
N-(4-цианофенил)-5Н-[1,3]диоксоло[4,5-f]индол-7-сульфонамид
N-(5-бром-4-хлор-2-фторфенил)-6-хлор-1H-индол-3-сульфонамид
6-хлор-N-(4-хлор-2,5-дифторфенил)-7-фенокси-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-6-фенокси-1H-индол-3-сульфонамид
6-хлор-N-[4-(2,2-дифторэтокси)-2-фторфенил]-1H-индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-5Н-[1,3]диоксоло[4,5-f]индол-7-сульфонамид
N-(4-бром-2-фтор-5-метилфенил)-6-хлор-1H-индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-(оксетан-3-ил)-1H-пирроло[2,3-b]пиридин-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(3,5-диметил-1,2-оксазол-4-ил)-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(пиридин-4-ил)-1H-индол-3-сульфонамид
N-(7-бром-2,2-дифтор-1,3-бензодиоксол-4-ил)-6-хлор-1H-индол-3-сульфонамид
N-(2,5-дифторфенил)-5-йод-1H-пирроло[2,3-b]пиридин-3-сульфонамид
6-хлор-N-(2-хлор-3-фторфенил)-1H-индол-3-сульфонамид
N-(4-циано-2,5-дифторфенил)-4,6-дифтор-1H-индол-3-сульфонамид
N-(4-циано-2-фторфенил)-1H-индол-3-сульфонамид
N-(5-хлор-3-фторпиридин-2-ил)-6-метокси-1H-индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-8-гидрокси-1H-пирроло[3,2-h]хинолин-3-сульфонамид
N-(4-циано-2-фторфенил)-6-(тетрагидрофуран-2-илметокси)-1H-индол-3-сульфонамид
N-(2,2-дифтор-1,3-бензодиоксол-5-ил)-6-(метилсульфонил)-1H-индол-3-сульфонамид
6-(5-хлортиофен-2-ил)-N-(4-циано-2-фторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(2,2,7-трифтор-1,3-бензодиоксол-4-ил)-1H-индол-3-сульфонамид
6-хлор-7-метокси-N-(2,4,5-трифторфенил)-1H-индол-3-сульфонамид
6-хлор-N-(4-хлор-2-фтор-5-метилфенил)-1H-индол-3-сульфонамид
N-(4-хлор-2-фторфенил)-6-фтор-1H-индол-3-сульфонамид
N-(4-этинилфенил)-6-(метилсульфонил)-1H-индол-3-сульфонамид.
Соединения, предлагаемые в настоящем изобретении, можно получить по методикам, раскрытым в экспериментальном разделе, приведенном в настоящей заявке.
Применение для лечения и диагностики
В одном варианте осуществления настоящее изобретение относится к любому из соединений, описанных в настоящем изобретении, предназначенному для применения для лечения и диагностики, предпочтительно для лечения животных, наиболее предпочтительно людей.
Вследствие их способности модулировать GPR17 соединения, предлагаемые в настоящем изобретении, можно применять в качестве лекарственного средства и их можно применять для лечения и/или предупреждения различных заболеваний ЦНС.
Таким образом одним вариантом осуществления настоящего изобретения является соединение, как здесь описано, предназначенное для применения в качестве лекарственного средства, предпочтительно предназначенное для применения в качестве лекарственного средства для лечения и/или предупреждения связанного с GPR17 заболевания, т.е. заболевания, которое связано с нарушением функции сигнальной системы GPR17, например, с сверхэкспрессированием и/или гиперактивностью рецепторов GPR17. Если не ограничиваться какими-либо теоретическими соображениями, то можно предположить, что активность GPR17 может повыситься, расшириться ее диапазон или она другим образом может измениться в определенных тканях, например, в клетках-предшественниках олигодендроцитов (ОРС) или во время созревания олигодендроцитов, вероятно, благодаря активации эндогенными стимулами, такими как, например, воспалительные факторы. Это может препятствовать дифференциации олигодендроцитов и эффективной миелинизации и, таким образом, способствовать возникновению и развитию нарушения миелинизации (см. публикацию Chen et al., приведенную выше). Таким образом, негативные модуляторы GPR17 могут способствовать миелинизации путем уменьшения или прекращения активности GPR17 и путем поддерживания созревания ОРС с образованием продуцирующих миелин олигодендроцитов (см. например, публикацию Simon et al., приведенную выше).
В одном предпочтительном варианте осуществления настоящее изобретение относится к любому из соединений, описанных в настоящем изобретении, предназначенному для применения для лечения или диагностики, предназначенных для применения для предупреждения или лечения нарушения или синдрома, выбранного из числа нарушений миелинизации и/или связанных с ними, предпочтительно центральной нервной системы.
Нарушения миелинизации можно разделить на три широкие категории:
- демиелинизирующие нарушения, при которых миелин изначально является нормальным, но по определенным причинам разрушился или разложился,
- дисмиелинизирующие нарушения, при которых образовавшийся миелин является аномальным и дисфункциональным (например, вследствие мутаций, влияющих на структуру миелина), и может дегенерировать, и
- гипомиелинизирующие нарушения, которые отличаются аномально низкими количествами миелина.
Примером дисмиелинизирующего нарушения является метахроматическая лейкодистрофия.
Примером гипомиелинизирующих нарушений является болезнь Пелицеуса-Мерцбахера.
Демиелинизирующее нарушение означает уменьшение количества миелина вокруг аксонов вследствие повреждения или разложения в другом случае функционирующего миелина. Причины разложения могут быть разнообразными и в их основе могут лежать, например, воспалительные и/или аутоиммунные процессы (такие как, например, рассеянный склероз), инфекции (такие как, например, прогрессивная мультифокальная лейкоэнцефалопатия, вызванная паповавирусом), метаболические нарушения (например, центральный понтинный миелинолиз), повреждение вследствие воздействия токсинов или механическая травма, и ишемические патологические состояния. Демиелинизирующие нарушения могут возникать в тканях центральной и периферической нервной системы.
Недавно было показано, что нейродегенеративные нарушения связаны с уменьшением миелинизации. Полагают, что сохранение функциональности олигодендроцитов и миелина является важным условием для предупреждения аксональной и нейронной дегенерации (см. например, публикацию Ettle et al., приведенную выше). Таким образом, негативные модуляторы GPR17 могут представлять собой превосходные возможные средства для лечения любых демиелинизирующих нарушений, включая, но не ограничиваясь только ими, нейродегенеративные заболевания, связанные с демиелинизацией и/или нарушенной миелинизацией, таких как, например, ALS, МСА, болезнь Альцгеймера, болезнь Гентингтона или болезнь Паркинсона.
Таким образом, в особенно предпочтительном варианте осуществления соединения, предлагаемые в настоящем изобретении, можно применять для предупреждения и/или лечения нарушения миелинизации периферической или центральной нервной системы, предпочтительно демиелинизирующего нарушения и особенно предпочтительно демиелинизирующего нарушения центральной нервной системы. В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, применяют для лечения и/или предупреждения и/или диагностики нарушения миелинизации, предпочтительно демиелинизирующего нарушения, путем перорального введения.
Примерами таких нарушений миелинизации, которые лечат и/или предупреждают соединениями, раскрытыми в настоящем изобретении, являются, в частности,
- рассеянный склероз (MS), включая его различные субформы,
- нейромиелит зрительного нерва (также известный, как болезнь Девика),
- хронический рецидивирующий воспалительный неврит зрительного нерва, острый рассеянный энцефаломиелит,
- острый геморрагический лейкоэнцефалит (AHL),
- перивентрикулярная лейкомаляция,
- демиелинизация вследствие вирусных инфекций, например, вызванных ВИЧ (вирус иммунодефицита человека), или прогрессивной мультифокальной лейкоэнцефалопатии,
- миелопатии, такие как, например, сухотка спинного мозга (сифилитическая миелопатия),
- центральный понтинный и экстрапонтинный миелинолиз,
- демиелинизация вследствие травматического поражения тканей головного мозга, включая вызванную сжатием демиелинизацию, например, вследствие опухолей,
- демиелинизация в ответ на гипоксию, удар или ишемию, или другие сердечно-сосудистые заболевания,
- демиелинизация вследствие воздействия диоксида углерода, цианида или других токсинов, поражающих ЦНС,
- болезнь Шильдера,
- концентрический склероз Бало,
- перинатальная энцефалопатия,
- нейродегенеративные заболевания, включая, в частности,
◊ боковой амиотрофический склероз (ALS).
◊ болезнь Альцгеймера (AD),
◊ мультисистемную атрофию,
◊ болезнь Паркинсона,
◊ спинально-церебеллярную атаксию (SCA), также известную, как спинально-церебеллярная атрофия,
◊ болезнь Гентингтона,
- психические нарушения, такие как шизофрения и биполярное расстройство (см., например, публикацию Fields, Trends Neurosci 31, 2008, 361; Tkachev et al., Lancet 362, 2003, 798).
- заболевания, связанные с нарушением миелинизации периферической нервной системы, такие как лейкодистрофии, периферические демиелинизирующие невропатии, синдром Дежерина-Соттаса или болезнь Шарко-Мари-Тута.
Кроме того, соединения, предлагаемые в настоящем изобретении, можно применять для лечения или предупреждения нарушения функции тканей, в которых экспрессируется GPR17, таких как, например, сердце или почки, включая, но не ограничиваясь только ими, лечение или предупреждение ишемических нарушений почек и сердца.
Лечение или предупреждение заболевания ЦНС (центральной нервной системы), такого как, в частности, заболевания, связанного с нарушением миелинизации, предпочтительно демиелинизирующего заболевания, также включает лечение признаков и симптомов, связанных с таким заболеванием. Таким образом, соединения, предлагаемые в настоящем изобретении, также можно применять для лечения нарушения или синдрома, связанного с повреждением тканей головного мозга, церебрально-васкулярного нарушения и определенных нейродегенеративных заболеваний, возникающих вследствие демиелинизирующего нарушения или связанных с ним/
В одном варианте осуществления применение соединений, предлагаемых в настоящем изобретении, для лечения и/или предупреждения MS также включает лечение и/или предупреждение признаков и симптомов, связанных с MS, таких как негативные проявления со стороны зрительных нервов (потеря зрения, двойное зрение), задних столбов спинного мозга (потеря чувствительности), корково-спинномозгового пирамидного пути (спастическая слабость), церебеллярных путей (отсутствие координации, дизартрия, вертиго, нарушения познавательной способности), медиального продольного пучка (двойное зрение при боковом взгляде), спинномозгового пути тройничного нерва (онемение лица или боль), мышечная слабость (нарушение глотания, нарушение контроля над мочевым пузырем или кишечником, спазмы), или психологических нарушений, связанных с основным заболеванием, таких как депрессия, состояние тревоги или другие расстройства настроения, общая слабость или бессонница.
Таким образом, соединения, предлагаемые в настоящем изобретении, предназначены для применения для лечения признаков и симптомов заболевания, связанного нарушением миелинизации, такого как рассеянный склероз, где такие признаки и симптомы включают, но не ограничиваются только ими, выбранные из группы, включающей потерю зрения, нарушение зрения, двойное зрение, потерю или нарушение чувствительности, слабость, такую как спастическая слабость, отсутствие моторной координации, вертиго, нарушения познавательной способности, онемение лица, боль в лице, нарушение глотания, нарушение речи, нарушение контроля над мочевым пузырем и/или кишечником, спазмы, депрессию, состояние тревоги, расстройства настроения, бессонницу и усталость.
В одном предпочтительном варианте осуществления соединения, предлагаемые в настоящем изобретении, предназначены для применения для лечения рассеянного склероза. MS является заболеванием, связанным с гетерогенным нарушением миелинизации, и может проявляться в целом ряде разных форм и стадий, включая, но не ограничиваясь только ими, рецидивирующий-ремитирующий MS, вторично-прогрессирующий MS, первично-прогрессирующий MS, прогрессирующий-рецидивирующий MS, каждая из которых зависит от активности и развития заболевания.
В другом варианте осуществления соединение, предлагаемое в настоящем изобретении, можно применять для предупреждения и лечения повреждения спинного мозга, перинатальной энцефалопатии, удара, ишемии или церебрально васкулярного нарушения, или для улучшения восстановления после этих нарушений.
В одном варианте осуществления настоящее изобретение относится к способу предупреждения и/или лечения синдрома или нарушения, связанного с нарушением миелинизации, или синдрома или нарушения, связанного с повреждением тканей головного мозга, который включает введение нуждающемуся в нем пациенту соединения, описанного в настоящем изобретении, в терапевтически эффективном количестве. Нуждающимся в таком лечении пациентом может являться любой пациент, который страдает от повреждения тканей головного мозга, такого как механическое, химическое, вирусное или другое повреждение.
В одном варианте осуществления настоящее изобретение относится к способу предупреждения и/или лечения синдрома или нарушения, связанного с нарушением миелинизации, предпочтительно демиелинизирующего нарушения, или синдрома или нарушения, связанного с ударом или другой ишемией головного мозга, который включает введение нуждающемуся в нем пациенту соединения, описанного в настоящем изобретении, в терапевтически эффективном количестве. Нуждающимся в предупреждении и/или лечении пациентом может являться любой пациент, который подвергся ишемии головного мозга/удару, которые могли быть вызваны, например, непроходимостью мозговой артерии, вызванной эмболом или локальным тромбозом.
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, предназначены для применения для лечения или предупреждения нейромиелита зрительного нерва (также известного, как болезнь Девика или синдром Девика).
Нейромиелит зрительного нерва является гетерогенным нарушением, характеризующимся воспалением и демиелинизацией зрительного нерва и спинного мозга. Многие из связанных с этим нарушением симптомов сходны с симптомами MS и включают мышечную слабость, в особенности, в конечностях, пониженную чувствительность и потерю контроля над мочевым пузырем.
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, предназначены для применения для предупреждения и/или лечения ALS. Недавно показано, что ALS связан с дегенерацией олигодендроцитов и повышенной демиелинизацией, это означает, что ALS является целевым заболеванием для негативных модуляторов GPR17 (см. публикации Kang et al., приведенную выше; Fumagalli et al., Neuropharmacology 104, 2016, 82).
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, предназначены для применения для предупреждения и/или лечения болезни Гентингтона. Подробно описано, что болезнь Гентингтона связана с нарушенной миелинизацией, (см. публикации Bartzokis et al., приведенную выше; Huang et al., Neuron 85, 2015, 1212).
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, предназначены для применения предупреждения и/или лечения мультисистемной атрофии. Недавно показано, что МСА сильно связана с демиелинизацией (см. публикации Ettle, приведенную выше, Jellinger, приведенную выше), на основании чего предполагается, что с помощью повторной миелинизации можно лечить или предупреждать МСА.
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, предназначены для применения предупреждения и/или лечения, болезни Альцгеймера. Недавно установлено, что AD связана с усиленным некрозом клеток-олигодендроцитов и фокальной демиелинизацией и они представляют патологические процессы при AD (Mitew et al., Acta Neuropathol 119, 2010, 567).
Одним вариантом осуществления настоящего изобретения является способ лечения любого из заболеваний или нарушений, описанных в настоящем изобретении, предпочтительно заболеваний, связанных с нарушением миелинизации, таких как MS, нейромиелит зрительного нерва, ALS или другие, путем введения нуждающемуся в нем субъекту, включая являющегося человеком пациента, соединения, предлагаемого в настоящем изобретении, в терапевтически эффективном количестве.
Недавно было показано, что GPR17 также связан с потреблением пищи, регулированием инсулина и ожирением. В разных публикациях описано, что негативные модуляторы GPR17 могут являться полезными для регулирования потребления пищи и для лечения ожирения (см., например, публикацию Ren et al., Diabetes 64, 2015; 3670.) Таким образом, в одном варианте осуществления настоящее изобретение относится к применению соединений, предлагаемых в настоящем изобретении, для предупреждения и/или лечения ожирения, и к способам лечения ожирения.
Пути лечения, предлагаемые в настоящем изобретении, могут включать введение одного из соединений, раскрытых в настоящем изобретении, в качестве "единственного средства" лечения заболевания ЦНС (центральная нервная система), предпочтительно нарушения миелинизации или связанного с ним заболевания, такого как MS или ALS. Альтернативно, соединение, раскрытое в настоящем изобретении, можно вводить вместе с другими полезными лекарственными средствами при проведении комбинированной терапии.
В качестве неограничивающего примера можно привести следующий: соединение, предлагаемое в настоящем изобретении, объединяют с другим лекарственным средством, предназначенным для лечения нарушения миелинизации, такого как MS, указанное другое лекарственное средство обладает другим механизмом воздействия, например, им является противовоспалительное лекарственное средство. Аналогичным образом, соединение, предлагаемое в настоящем изобретении, можно объединить с анальгетическим лекарственным средством. Кроме того, соединение, предлагаемое в настоящем изобретении, можно использовать в комбинации с антидепрессантом для одновременного лечения психологических нарушений, связанных с основным подвергающемуся лечению заболевания, связанного с нарушением миелинизации.
При комбинированной терапии два или большее количество активных веществ могут быть включены в один и тот же препарат или представлять собой "набор компонентов", т.е. находиться в отдельных галеновых препаратах, предназначенных для использования в комбинации. Кроме того, два или большее количество активных веществ, включая соединения, предлагаемые в настоящем изобретении, можно вводить пациенту в одно и то же время или последовательно, например, при интервальной терапии. Дополнительное лекарственное средство можно вводить таким же путем или другим путем введения. Так, например, модулятор GPR17, предлагаемый в настоящем изобретении, можно вводить перорально, тогда как второе лекарственное средство можно вводить путем подкожной инъекции.
Второе лекарственное средство, предназначенное для лечения MS, может быть выбрано из группы, включающей, например, кортикостероиды (например, преднизон, декламетазон), далфампридин, интерферон бета-1а, интерферон бета-1b, глатирамерацетат, пэгинтерферон бета-1а, даклизумаб, терифлуномид, финголимод, сипонимод, диметилфумарат, алемтузумаб, митоксантрон, окрелизумаб, натализумаб и их биологические эквиваленты или биологические аналоги.
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, можно использовать для диагностики и/или мониторинга связанного с GPR17 заболевания, дополнительно описанного в настоящем изобретении, предпочтительно демиелинизирующего заболевания, раскрытого в настоящем изобретении, предпочтительно для диагностики и мониторинга рассеянного склероза.
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, можно использовать для диагностики и/или мониторинга экспрессирования, распределения и/или активации рецептора GPR17 in vivo, например, непосредственно у субъекта, например, с использованием методик молекулярной визуализации, или in vitro, например, путем исследования любых образцов, таких как жидкости или ткани организма, взятые у субъекта. Результаты любого такого определения активности, экспрессирования и/или распределения GPR17 можно использовать для прогнозирования, диагностики и/или мониторинга (а) состояния и развития связанного с GPR17 заболевания, описанного в настоящем изобретении, предпочтительно заболевания, связанного с нарушением миелинизации, включая, но не ограничиваясь только ими, например, рассеянный склероз, и/или (b) эффективности и/или применимости лечения, проводимого в связи с любым таким связанным с GPR17 заболеванием, и/или надлежащей дозировки.
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, можно использовать в качестве предназначенных для PET или SPECT радиоактивных индикаторов, дополнительно описанных в настоящем изобретении, для проведения диагностики и/или мониторинга заболевания in vivo. При этом экспрессирование, активацию и/или распределение рецептора GPR17 можно непосредственно определить у субъекта, например, путем визуализации организма человека после введения предназначенного для PET или SPECT радиоактивного индикатора GPR17, предлагаемого в настоящем изобретении. Это может ускорить надлежащую диагностику заболевания, может способствовать определению применимых возможностей лечения и/или это можно использовать для мониторинга развития заболевания и/или для мониторинга или прогнозирования успеха медицинского вмешательства, включая выбор подходящего пути введения и/или дозировки терапевтического лекарственного средства.
Поэтому одним вариантом осуществления настоящего изобретения является применение предназначенного для PET или SPECT радиоактивного индикатора, предлагаемого в настоящем изобретении, в диагностически эффективном количестве для диагностики связанного с GPR17 нарушения, предпочтительно заболевания, связанного с нарушением миелинизации, включая, но не ограничиваясь только им, MS.
В одном варианте осуществления настоящее изобретение относится к способу диагностики связанного с GPR17 нарушения, предпочтительно заболевания, связанного с нарушением миелинизации, включая, но не ограничиваясь только им, MS, указанный способ включает стадии (а) введения субъекту предназначенного для PET или SPECT радиоактивного индикатора, предлагаемого в настоящем изобретении, в диагностически эффективном количестве, (b) определения количества и/или распределение GPR17 в организме субъекта на основании его связывания с введенным предназначенным для PET или SPECT радиоактивным индикатором и (с) сравнение результатов с результатами, полученными для сравнительного субъекта или группы субъектов.
В одном варианте осуществления предназначенные для PET или SPECT радиоактивные индикаторы, предлагаемые в настоящем изобретении, можно использовать вместе с терапевтическим лекарственным средством, т.е. в качестве дополнительного средства для диагностики, для мониторинга и/или прогнозирования эффективности и/или безопасности указанного терапевтического лекарственного средства для конкретного субъекта или для определения подходящей дозировки лекарственного средства.
Один вариант осуществления относится к предназначенному для PET или SPECT радиоактивному индикатору, предлагаемому в настоящем изобретении, предназначенному для применения в качестве дополнительного лекарственного средства вместе с терапевтическим лекарственным средством. Терапевтическое лекарственное средство, использующееся вместе с предназначенным для PET или SPECT радиоактивным индикатором, предлагаемым в настоящем изобретении, может быть выбрано из группы, включающей (а) немеченое соединение, предлагаемое в настоящем изобретении, (b) модулирующее GPR17 соединение, которое отличается от соединений, предлагаемых в настоящем изобретении, и (с) лекарственное средство, предназначенное для лечения заболевания, связанного с нарушением миелинизации, включая, но не ограничиваясь только им, лекарственное средство, предназначенное для применения для лечения рассеянного склероза, которое не является модулятором GPR17.
Один вариант осуществления относится к набору, включающему
(a) в качестве первого компонента предназначенный для PET или SPECT радиоактивный индикатор, предлагаемый в настоящем изобретении, предпочтительно предназначенный для PET или SPECT радиоактивный индикатор, основанный на соединении, предлагаемом в настоящем изобретении, включая, но не ограничиваясь только ими, соединения, обладающие структурой, соответствующей любой из формул I, II, IIa, IIb, IIc, IId, IIe, III, III, IIIa, IIIb, IIIc или IV, дополнительно определенных в настоящем изобретении, или обладающие структурой любого из соединений, раскрытых в настоящем изобретении, но содержащие включенный по меньшей мере один радионуклид, который является подходящим для визуализации с помощью PET или SPECT, предпочтительно радионуклид, выбранный из группы, включающей18F,11С,123I,125I и131I,
(b) в качестве второго компонента терапевтическое лекарственное средство, выбранное из группы, включающей
i) соединение, предлагаемое в настоящем изобретении, включая, но не ограничиваясь только ими, соединения, обладающие структурой, соответствующей любой из формул I, II, IIa, IIb, IIc, IId, IIe, IIf, III, IIIa, IIIb, IIIc или IV, дополнительно определенных в настоящем изобретении, или обладающие структурой любого из отдельных соединений, раскрытых в настоящем изобретении, и не содержащие включенного радионуклида,
ii) модулирующее GPR17 соединение, которое отличается от соединений, предлагаемых в настоящем изобретении, определенных в (i), и
iii) лекарственное средство, предназначенное для лечения заболевания, связанного с нарушением миелинизации, включая, но не ограничиваясь только им, лекарственное средство, предназначенное для применения для лечения рассеянного склероза, но не способные модулировать активность GPR17.
Альтернативно, соединения, предлагаемые в настоящем изобретении, можно использовать в проводимом in vitro диагностическом исследовании, например, для исследования любой степени экспрессирования, активности и/или распределения GPR17 в подходящих жидкостях организма субъекта, таких как, например, кровь, плазма, моча, слюна или спинномозговая жидкость.
Один вариант осуществления относится к способу лечения связанного с GPR17 заболевания, предпочтительно заболевания, связанного с нарушением миелинизации, предпочтительно демиелинизирующего нарушения, включая, но не ограничиваясь только им, рассеянный склероз, где указанный способ включает стадии (а) определение экспрессирования, активности и/или распределения рецептора GPR17 у субъекта, (b) сравнение экспрессирования, активности и/или распределения рецептора GPR17 у указанного субъекта с экспрессированием, активностью и/или распределением рецептора GPR17 у одного или большего количество здоровых субъектов или у популяции, (с) определение необходимости медицинского лечения или профилактики указанного субъекта на основании отклонения результатов, полученных для экспрессирования, активности и/или распределения рецептора GPR17 у указанного субъекта, от результатов, полученных для здоровых субъектов или популяции, и (d) лечение субъекта, у которого наблюдается отклонение результатов, полученных для экспрессирования, активности и/или распределения рецептора GPR17, путем введения терапевтического лекарственного средства указанному индивидууму, где лекарственное средство является подходящим для лечения связанных с GPR17 заболеваний или нарушений, предпочтительно путем введения модулятора GPR17, предпочтительно путем введения одного или большего количества соединений, предлагаемых в настоящем изобретении. В одном варианте осуществления (а) определение экспрессирования, активности и/или распределения рецептора GPR17 проводят с использованием одного из соединений, предлагаемых в настоящем изобретении, предпочтительно с использованием предназначенного для PET или SPECT радиоактивного индикатора, предлагаемого в настоящем изобретении, или путем проводимого in vitro исследования жидкостей или тканей организма указанного субъекта с использованием предназначенного для PET или SPECT радиоактивного индикатора, предлагаемого в настоящем изобретении.
В одном предпочтительном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение, как здесь описано, и фармацевтически приемлемый носитель.
Для введения в качестве лекарственного средства соединения можно использовать в фармацевтической композиции, содержащей соединение, предлагаемое в настоящем изобретении, и фармацевтически приемлемый носитель, дополнительно определенный в настоящем изобретении. Такая фармацевтическая композиция может быть приспособлена, например, для перорального, внутривенного, внутримышечного, подкожного, назального, ректального, трансбуккального или чрескожного введения и может содержать фармацевтически приемлемые носители, вспомогательные вещества, разбавители, стабилизаторы и т.п.
В одном варианте осуществления соединения, предлагаемые в настоящем изобретении, можно вводить перорально, например, в виде таблетки, капсулы, драже, порошка, гранулята, или в виде жидкости или полужидкого вещества, включая, но не ограничиваясь только ими, например, сиропы, суспензии, эмульсии или растворы.
Так, например, соединения, предлагаемые в настоящем изобретении, можно растворить в маслах, пропиленгликоле или других растворителях, которые обычно используют для приготовления препаратов для инъекции. Примеры подходящих носителей включают, но не ограничиваются только ими, физиологический раствор, полиэтиленгликоль, этанол, растительные масла, изопропилмиристат и т.п. Соединения, предлагаемые в настоящем изобретении, можно приготовить в виде препаратов для инъекций путем растворения, суспендирования или эмульгирования в растворимых в воде растворителях, таких как физиологический раствор и 5% раствор декстрозы, или в нерастворимых в воде растворителях, таких как растительные масла, синтетические глицериды жирных кислот, эфиры высших жирных кислот и пропиленгликоль. Композиции, предлагаемые в настоящем изобретении, могут содержать обычные добавки, такие как растворяющие агенты, изотонические агенты, суспендирующие агенты, эмульгаторы, стабилизаторы и консерванты.
Таблетка может обеспечить немедленное или замедленное высвобождение соединений, предлагаемых в настоящем изобретении.
Препараты для перорального введения, такие как таблетки, могут содержать, без наложения ограничений, агенты, обеспечивающие замедленное высвобождение, разрыхлители, наполнители, смазывающие вещества, стабилизаторы, антиоксиданты, вкусовые вещества, диспергирующие агенты, электролиты, буферы, красители или консерванты. Подходящие инертные наполнители и препараты известны специалистам в данной области техники и описаны в стандартных монографиях, таких как, например, Remington ("The science and practice of pharmacy", Lippincott, Williams & Wilkins, 2000).
Неограничивающие примеры разрыхлителей включают предварительно желатинизированный крахмал, натриевую соль гликолята крахмала, микрокристаллическую целлюлозу, натриевую соль карбоксиметилцеллюлозы (CMC-Na), сшитую CMC-Na и обладающую низкой степенью замещения гидроксипропилцеллюлозу, а также их смеси.
Подходящие наполнители и связующие включают, без наложения ограничений, микрокристаллическую целлюлозу, порошкообразную целлюлозу, лактозу (безводную или ее моногидрат), прессующийся сахар, крахмал (например, кукурузный крахмал или картофельный крахмал), предварительно желатинизированный крахмал, фруктозу, сахарозу, декстрозу, декстраны, другие сахара, такие как маннит, мальтит, сорбит, лактит и сахароза, силифицированную микрокристаллическую целлюлозу, гидрофосфат кальция, дигидрат гидрофосфата кальция, дигидрат дикальцийфосфата, трикальцийфосфат, лактат кальция или их смеси.
Смазывающие вещества, антиадгезивы и/или агенты, придающие скользкость включают стеариновую кислоту, стеарат магния, стеарат кальция, лаурилсульфат натрия, гидрированное растительное масло, гидрированное касторовое масло, стеарилфумарат натрия, макроголы, глицериндибегенат, тальк, кукурузный крахмал, диоксид кремния и т.п., включая их смеси.
Типичными агентами, обеспечивающими замедленное высвобождение, являются, например, такие, которые набухают при соприкосновении с водой, такие как поливинилпирролидон, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, другие простые эфиры целлюлозы, крахмал, предварительно желатинизированный крахмал, полиметакрилат, поливинилацетат, микрокристаллическая целлюлоза, декстраны, и их смеси. Другими агентами, обеспечивающими замедленное высвобождение, могут являться такие, которые можно включить в функциональное покрытие, которое предотвращает быстрое разложение и/или высвобождение активного ингредиента из ядра таблетки. Примерами агентов, которые можно использовать в функциональном покрытии, являются, например, акриловые смолы, производные целлюлозы, такие как гидроксипропилметилацетатфталат целлюлозы, гидроксипропилцеллюлоза или этилцеллюлоза, производные винилацетата, поливинилпирролидон, поливинилацетат, шеллак, метакрилатные полимеры или метакрилатные сополимеры.
Таблетку можно приготовить, например, путем смешивания по меньшей мере одного соединения, предлагаемого в настоящем изобретении, по меньшей мере с одним нетоксичным фармацевтически приемлемым инертным наполнителем, таким как, например, связующее, наполнитель/разбавители, разрыхляющие агенты, пластификатор и т.п., и с необязательным растворителем (водным или неводным), и последующей обработки смеси с получением таблетки по методике, включая, но не ограничиваясь только ими, сухое прессование, сухое гранулирование, влажное гранулирование, распылительную сушку или экструзию расплава. Таблетка может не содержать покрытие или на нее можно нанести покрытие по известным методикам с целью маскировки неприятного вкуса обладающего неприятным вкусом лекарственного средства или с целью замедления распада и всасывания активного ингредиента в желудочно-кишечном тракте.
Соединение, предлагаемое в настоящем изобретении, можно приготовить для парентерального введения путем инъекции, например инъекции ударной дозы вещества или путем вливания. Композиции для инъекции могут поставляться в готовом к применению виде и могут находиться в таких формах, как суспензии, растворы или эмульсии в масле или водных разбавителях, и могут содержать инертные наполнители, такие как суспендирующие, стабилизирующие, консервирующие и/или диспергирующие средства. Альтернативно, активный ингредиент может находиться в порошкообразной форме для проводимого перед применением восстановления с помощью подходящего разбавителя, например, стерильной апирогенной воды.
В случае назального введения или введения путем ингаляции соединения, предлагаемые в настоящем изобретении, обычным образом можно приготовить в виде материалов для распыления с использованием в упаковках под давлением или устройствах типа небулайзер с использованием подходящего пропеллента, например, дихлордифторметана, фтортрихлорметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа или смеси газов.
В случае введения в глаза соединения, предназначенные для применения в настоящем изобретении, обычным образом можно приготовить в виде тонкоизмельченных суспензий в изотоническом, обладающем необходимым значением рН стерильном физиологическом растворе, без добавления или с добавлением консерванта, такого как бактерицидное или фунгицидное средство, например, фенилмеркурнитрат, бензилалконийхлорид или хлоргексидинацетат. Альтернативно, в случае введения в глаза соединения можно приготовить в виде мази, такой как на основе вазелинового масла.
В случае ректального введения соединения, предназначенные для применения в настоящем изобретении, обычным образом можно приготовить в виде суппозиториев. Их можно приготовить путем смешивания активного компонента с подходящим, не оказывающим раздражающего воздействия инертным наполнителем, который является твердым при комнатной температуре, но жидким при ректальной температуре и поэтому плавится в прямой кишке с высвобождением активного компонента. Такие вещества включают, например, масло какао, пчелиный воск и полиэтиленгликоли.
В одном варианте осуществления соединения можно вводить чрескожно. Этот режим введения предотвращает так называемый эффект первого прохождения, возникающий при пероральном введении, и, кроме того, обеспечивает более постоянную концентрацию в плазме, что в некоторых случаях является особенно предпочтительным. Приготовление чрескожных форм, таких как мази или кремы, или других чрескожных систем, таких как, например, пластыри или электрофорезные устройства, обычно известны из предшествующего уровня техники, см., например, публикации Prausnitz and Langer, Nat Biotechnology 2008, Vol 26.11 p 1261; WO 2001/47503; WO 2009/000262; WO 99/49852.
Предпочтительная доза соединений, предлагаемых в настоящем изобретении, зависит от ряда факторов, включая состояние здоровья и массу тела пациента, тяжесть конкретного заболевания, дозированную форму и путь и период введения, но ее могут соответствующим образом выбрать специалисты в данной области техники. В различных вариантах осуществления соединения вводят в количестве, находящемся в диапазоне от 0,001 до 10 мг/(кг массы тела) в сутки или от 0,03 до 1 мг/(кг массы тела) в сутки. Индивидуальные дозы могут находиться в диапазоне примерно от 0,1 до 1000 мг активного ингредиента в сутки, примерно от 0,2 до 750 мг/сутки, примерно от 0,3 до 500 мг/сутки, от 0,5 до 300 мг/сутки или от 1 до 100 мг/сутки. Дозы можно вводить один раз в сутки или несколько раз в сутки, предпочтительно разделенными на порции.
Другим объектом настоящего изобретения является набор, включающий лекарственное средство или фармацевтическую композицию, как здесь описано, и инструкции для ее применения.
ОПРЕДЕЛЕНИЯ
Любое указание на соединение, предлагаемое в настоящем изобретении, также включает указание на фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы таких соединений, если специально не указано иное. "Соединения, предлагаемые в настоящем изобретении", включают соединения, обозначенные общими формулами I, I-2, II, IIa, IIb, IIc, IId, IIe, IIf, IIg, II-2, II-2a, II-2b, II-2c, II-2d, II-2e, II-2f, II-2g, III, IIIa, IIIb, IIIc, III-2, III-2а, III-2b, III-2с, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf и VIg и раскрытые в них, а также отдельные соединения, специально раскрытые в описании и/или в экспериментальном разделе. В любом случае, в котором в отношении "соединений, предлагаемых в настоящем изобретении", определен конкретный заместитель, следует понимать, что это относится только к тем соединениям, которые содержат соответствующий заместитель. Так, например, любое определение R12, содержащегося в "соединениях, предлагаемых в настоящем изобретении", разумеется, не применимо к соединениям, в которых сам по себе R12 не содержится, таким как, например, соединения формулы VI и соответствующих субформул.
Термин "фармацевтически приемлемые соли" означает любые соли, которые соединения, предлагаемые в настоящем изобретении, могут образовать и которые являются подходящими для введения субъектам, предпочтительно субъектам, являющимся людьми. Такие соли включают, но не ограничиваются только ими, соли присоединения с кислотами, образованные с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., или образованные с органическими кислотами, такими как уксусная кислота, пропионовая кислота, гексановая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, 3-(4-гидроксибензоил)бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, 4-хлорбензолсульфоновая кислота, 2-нафталинсульфоновая кислота, 4-толуолсульфоновая кислота, камфорсульфоновая кислота, 4-метилбицикло[2.2.2]окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, 3-фенилпропионовая кислота, триметилуксусная кислота, трет-бутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глутаминовая кислота, гидроксинафтойная кислота, салициловая кислота, стеариновая кислота и муконовая кислота. Другие соли включают 2,2-дихлорацетат, адипат, альгинат, аскорбат, аспартат, 2-ацетамидобензоат, капроат, капринат, камфорат, цикламат, лаурилсульфат, эдизилат, эзилат, изетионат, формиат, галактарат, гентизат, глюцептат, глюкуронат, оксоглутарат, гиппурат, лактобионат, нападизилат, ксинафоат, никотинат, олеат, оротат, оксалат, пальмитат, эмбонат, пидолат, п-аминосалицилат, себацинат, таннат, роданид, ундециленат и т.п.; или соли, образованные с кислым протоном, содержащимся в исходном соединении, замещенным, например, аммиаком, аргинином, бенетамином, бензатином, кальцием, холином, 2-диметиламиноэтанолом, диэтаноламином, диэтиламином, этаноламином, этилендиамином, меглумином, глицином, гидрабамином, имидазолом, лизином, магнием, гидроксиэтилморфолином, пиперазином, калием, эполамином, натрием, троламином, трометамином или цинком.
В объем настоящего изобретения также входят сольваты соединений, определенных в настоящем изобретении. "Сольваты" представляют собой кристаллы, образованные активным соединением и вторым компонентом (растворителем), которые в выделенном виде являются жидкими при комнатной температуре. Такие сольваты можно получить с обычными органическими растворителями, например, углеводородными растворителями, такими как бензол или толуол; хлорированными растворителями, такими как хлороформ или дихлорметан; спиртовыми растворителями, такими как метанол, этанол или изопропанол; простыми эфирными растворителями, такими как диэтиловый эфир или тетрагидрофуран; или сложноэфирными растворителями, такими как этилацетат. Альтернативно, сольваты соединений, предлагаемых в настоящем изобретении, можно получить с водой и в этом случае они будут являться гидратами.
В объем настоящего изобретения также входят совместные кристаллы. Термин "совместный кристалл" используют для описания случая, когда нейтральные молекулярные компоненты содержатся в кристаллическом соединении при определенном стехиометрическом соотношении. Получение фармацевтических совместных кристаллов позволяет модифицировать кристаллическую форму активного фармацевтического ингредиента, что, в свою очередь, может изменить его физико-химические характеристики без ухудшения его необходимой биологической активности. Примеры образующих совместные кристаллы соединений, которые могут содержаться в совместном кристалле вместе с активным фармацевтическим ингредиентом, включают L-аскорбиновую кислоту, лимонную кислоту, глутаровую кислоту, коричную кислоту, миндальную кислоту, мочевину и никотинамид.
В настоящее изобретение также включены все подходящие изотопозамещенные формы соединения, предлагаемого в настоящем изобретении. Изотопозамещенная форма соединения, предлагаемого в настоящем изобретении, определена, соединение, в котором по меньшей мере один атом заменен на атом, обладающий таким же атомным номером, но атомной массой, отличающейся от атомной массы, обычно обнаруживаемой в природе, причем предпочтительным является более часто встречающийся изотоп (изотопы). Примеры изотопов, которые можно вводить в соединения, предлагаемые в настоящем изобретении, включают изотопы водорода, углерода, азота, кислорода, серы, фтора и хлора, такие как2Н,3Н,11С,13С,14С,15N,17О,18О,35S,18F и36Cl соответственно. Следует понимать, что для любого изотопа, который в поддающихся измерению количествах содержится в природе, такого как, например, дейтерия, количество соответствующего радионуклида, которое можно включить в соединения, предлагаемые в настоящем изобретении, для модулирования их характеристик, будет превышать его обычное содержание в природе. Поэтому, например, количество дейтерия, включенного в дейтерированные соединения, предлагаемые в настоящем изобретении, обычно выше, чем количество дейтерия, которое, как ожидается, естественным образом содержится в указанном соединении. Некоторые изотопозамещенные формы соединений, предлагаемых в настоящем изобретении, например, такие, в которые включены такие радиоактивные изотопы, как3Н или14С, применимы для исследования распределения лекарственного средства и/или субстрата в тканях. Соединения, содержащие изотопы тритий, т.е.3Н, и углерод-14, т.е.14С, являются особенно предпочтительными вследствие легкости их получения и детектирования. Кроме того, замещение изотопами, такими как дейтерий, т.е.2Н, может обеспечить некоторые терапевтические преимущества, обусловленные их более высокой метаболической стабильностью, например, увеличенной длительностью полувыведения in vivo, возможностью использования меньших доз и поэтому в некоторых случаях это может являться предпочтительным. Изотопозамещенные формы соединений, предлагаемых в настоящем изобретении, обычно можно получить по обычным методикам с использованием соответствующих изотопозамещенных форм подходящих реагентов.
Частью настоящего изобретения также являются такие соединения, в которых по меньшей мере один атом заменен радиоактивным изотопом (радионуклидом) такого же или другого атома, которые можно использовать in vivo в методиках визуализации, таких как однофотонная эмиссионная компьютерная томография (SPECT), позитронная эмиссионная томография (PET), спектроскопия магнитного резонанса (MRS) или магнитно-резонансная визуализация (MRI).
Примерами таких радиоактивных производных модуляторов GPR17, применимых для исследований с помощью SPECT (в настоящем изобретении такие соединения называются "предназначенными для SPECT радиоактивными индикаторами), являются соединения, в которые включен99mTc,111In,82Rb,137Cs,123I,125I,131I,67Ga,192Ir или201Tl и предпочтительно123I. Так, например, для использования соединений, предлагаемых в настоящем изобретении, в качестве предназначенных для SPECT радиоактивных индикаторов в модулятор GPR17, раскрытый в настоящем изобретении можно включить изотоп123I. В качестве неограничивающего примера можно привести следующий: для использования соединения в качестве предназначенного для SPECT радиоактивного индикатора в соединение, предлагаемое в настоящем изобретении можно включить радионуклид, выбранный из группы, включающей123I,125I и131I, предпочтительным является125I. В одном варианте осуществления предназначенный для SPECT радиоактивный индикатор, предлагаемый в настоящем изобретении, может быть основан на структуре содержащего йод модулятора GPR17, раскрытого в настоящем изобретении, в котором в положении атома йода включен один из следующих радионуклидов:123I,125I и131I, предпочтительно123I.
В соответствии с этим, термин "предназначенный для SPECT радиоактивный индикатор, предлагаемый в настоящем изобретении", означает соединения, предлагаемые в настоящем изобретении, включая обладающие структурой, соответствующей любой из формул I, I-2, II, IIa, IIb, IIc, IId, IIe, IIf, IIg, II-2, III-2a, II-2b, II-2c, II-2d, II-2e, II-2f, II-2g, III, IIIa, IIIb, IIIc, III-2, III-2а, III-2b, III-2с, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf и VIg, дополнительно определенные в настоящем изобретении, или другим образом отдельно раскрытые в настоящем изобретении, в которые включен по меньшей мере один радиоактивный изотоп в количестве, подходящем для визуализации с помощью SPECT. Он включает, но не ограничивается только ими,99mTc,111In,82Rb,137Cs,123I,125I,131I,67Ga,192IR или201T1, и предпочтительным является123I.
Примерами производных модуляторов GPR17, применимых для исследований с помощью PET (в настоящем изобретении такие соединения называются "предназначенными для PET радиоактивными индикаторами"), являются соединения, в которые включен11С,13N,15О,18F,18Br или124I. Так, например, для использования соединения, предлагаемого в настоящем изобретении, в качестве предназначенного для PET радиоактивного индикатора в соединение, предлагаемое в настоящем изобретении, можно включить изотоп18F в количестве, подходящем для визуализации с помощью PET. В одном варианте осуществления предназначенный для PET радиоактивный индикатор может быть основан на структуре содержащего фтор модулятора GPR17, раскрытого в настоящем изобретении, в котором в положении атома включен соответствующий радионуклид8F. В другом варианте осуществления в соединение, предлагаемое в настоящем изобретении, изотоп18F можно включить вместо гидроксигруппы. Это аналогичным образом относится к включению по меньшей мере одного из следующих:11С,13N,15О,76Br или124I, вместо "немеченого" атома углерода, азота, кислорода, брома или йода соответственно или вместо любого другого атома или группы, которая может являться подходящей для замены соответствующим радионуклидом (см., например, публикацию Pimlott and Sutherland, Chem Soc Rev 2011, 40, 149).
В соответствии с этим, термин "предназначенный для PET радиоактивный индикатор, предлагаемый в настоящем изобретении", означает соединения, описанные в настоящей заявке на патент, и обладающие структурой, соответствующей любому из соединений, предлагаемых в настоящем изобретении, включая соединения формул I, I-2, II, IIa, IIb, IIc, IId, IIe, IIf, IIg, II-2, II-2a, II-2b, II-2c, II-2d, II-2e, II-2f, II-2g, III, IIIa, IIIb, IIIc, III-2, III-2a, III-2b, III-2c, IV, IV-2, V, V-2, VI, VIa, VIb, VIc, VId, VIe, VIf и VIg, дополнительно определенные в настоящем изобретении, или другим образом отдельно раскрытые в настоящем изобретении, в которые включен по меньшей мере один радиоактивный изотоп, который является подходящим для визуализации с помощью PET. Он включает, но не ограничивается только ими,11С,13N,15O, 18F,76Br или124I, и предпочтительным является18F.
Соединениями, предназначенными для применения для MRI и MRS, предпочтительно являются соединения, предлагаемые в настоящем изобретении, содержащие подходящее количество включенного магнитного радиоактивного изотопа. Они включают13С,1Н,18F,19F,14N,17О,31Р и33S, где предпочтительными являются19F или13С.
В объем настоящего изобретения входят пролекарства соединений, предлагаемых в настоящем изобретении. Обычно такие пролекарства являются функциональными производными соединений, описанных в настоящем изобретении, которые in vivo, например, с помощью эндогенных ферментов, содержащихся в кишечнике или в крови, легко превращаются в необходимые модулирующие GPR17 соединения, описанные в настоящем изобретении. Обычные методики выбора и получения подходящих пролекарственных производных описаны, например, в публикации Design of Prodrugs, ed. H. Bundgaard, Elsevier, 1985. Так, например, пролекарство может содержать подходящую включенную сложноэфирную группу, которая отщепляется с помощью эстеразы, и происходит выделение активного антагониста GPR17, предлагаемого в настоящем изобретении.
В зависимости от схемы замещения соединения, предлагаемые в настоящем изобретении, могут содержать или не содержать один или большее количество оптических стереоцентров или и могут существовать или не существовать в виде разных энантиомеров или диастереоизомеров. Любые такие энантиомеры, диастереоизомеры или другие оптические изомеры входят в объем настоящего изобретения.
Соединение, предлагаемое в настоящем изобретении, также может находиться в разных кристаллических формах, т.е. в полиморфных формах, все эти формы входят в объем настоящего изобретения.
Соединения, предлагаемые в настоящем изобретении, можно включить в фармацевтическую композицию, которая также может включать фармацевтически приемлемый носитель.
"Фармацевтически приемлемый носитель" означает разбавитель, вспомогательное вещество, инертный наполнитель или носитель, или другой ингредиент, с которым вводят соединение, предлагаемое в настоящем изобретении, и которое для специалиста в данной области техники означает фармацевтически приемлемое, но которое само по себе обычно не является биодинамически активным.
Соединения, предлагаемые в настоящем изобретении, применимы для предупреждения и/или лечения определенных заболеваний, описанных в настоящем изобретении, у животных, предпочтительно у людей.
"Предупреждение" означает уменьшение вероятности возникновения заболевания или нарушения (т.е. обеспечение отсутствия проявления по меньшей мере одного из клинических симптомов заболевания у субъекта, предпочтительно человека, который может быть подвержен заболеванию или предрасположен к нему, но у которого еще не ощущаются или не проявляются симптомы заболевания).
"Лечение" любого заболевания или нарушения в одном варианте осуществления включает улучшение протекания заболевания или нарушения (т.е. остановку или ослабление развития заболевания или по меньшей мере уменьшение проявления одного из его клинических симптомов). В другом варианте осуществления "лечение" означает улучшение по меньшей мере одного физического параметра, который может ощущаться или не ощущаться субъектом, предпочтительно человеком, но который является основой подвергающегося лечению заболевания или нарушения или связан с ним. В еще одном варианте осуществления "лечение" означает изменение протекания заболевания или нарушения, физическое (например, стабилизацию проявляющегося или не проявляющегося симптома), или физиологическое, (например, стабилизацию физиологического параметра), или и то, и другое. В еще одном варианте осуществления "лечение" означает задержку начала или развития, или прогрессирования заболевания или нарушения. Соответственно, лечение" включает любое этиологическое лечение основного заболевания или нарушения (т.е. изменение протекания), а также любое лечение признаков и симптомов заболевания или нарушения (с изменением или без изменения протекания заболевания), а также любое облегчение или ослабление заболевания или нарушения, или его признаков и симптомов.
"Диагностика" или "диагностирование" заболевания или нарушения в одном варианте осуществления включают обнаружение и оценку признаков и симптомов, которые связаны с указанным заболеванием. "Диагностика" или "диагностирование" включают, но не ограничиваются только ими, обнаружение и/или оценку уменьшенного, увеличенного количества рецепторов GPR17 или другим образом неправильно (например, во времени и положении) экспрессированных, активированных или распределенных рецепторов GPR17 по сравнению с наблюдающимися у здоровых субъектов, что является показателем связанного с GPR17 заболевания или нарушения. В одном примере для такой диагностики, включая диагностику нарушения миелинизации, можно использовать лиганды для GPR17 в форме предназначенных для PET или SPECT радиоактивных индикаторов.
Термины "заболевание (заболевания)" и "нарушение (нарушения)" в настоящем изобретении в основном используют взаимозаменяемым образом.
"Мониторинг" означает наблюдение за заболеванием, патологическим состоянием или по меньшей мере одним медицинским показателем в течение определенного промежутка времени. "Мониторинг" также включает наблюдение за воздействием терапевтического лекарственного средства с помощью "дополнительного лекарственного средства".
"Дополнительное средство для диагностики" при использовании в настоящем изобретении означает соединение, которое можно использовать вместе с терапевтическим лекарственным средством для определения применимости (например, безопасности и эффективности) указанного терапевтического лекарственного средства для конкретного пациента. Применение "дополнительного средства для диагностики" может включать стадии диагностики и мониторинга.
Термины "животное (животные)" и "субъект (субъекты)" включают людей. Термины "человек", "пациент" и "являющийся человеком субъект" в настоящем изобретении используют взаимозаменяемым образом.
Настоящее изобретение также относится к способам лечения заболевания или нарушения у животного, предпочтительно заболевания или нарушения у человека, которые включают введение соединений, предлагаемых в настоящем изобретении, в терапевтически эффективных количествах. "Терапевтически эффективное количество" означает такое количество соединения, которое при введении субъекту, предпочтительно человеку, для лечения заболевания является достаточным для проведения такого лечения заболевания. "Терапевтически эффективное количество" может меняться в зависимости от соединения, заболевания и его тяжести, и состояния здоровья, возраста, массы тела, пола и т.п. подвергающегося лечению субъекта, предпочтительно человека.
"Диагностически эффективное количество" означает такое количество соединения, которое при введении субъекту, предпочтительно человеку, для диагностики заболевания является достаточным для проведения такой диагностики.
Термин "рассеянный склероз" при использовании в настоящем изобретении означает заболевание, обозначаемое кодом диагноза G35 в 2016/7 ICD-10-CM (Международная классификация болезней 10-го пересмотра).
Термин "нарушение миелинизации" включает демиелинизирующие нарушения, дисмиелинизирующие нарушения и гипомиелинизирующие нарушения, дополнительно описанные в настоящем изобретении. Подклассом нарушений миелинизации, предпочтительным для лечения или диагностики с помощью соединений, предлагаемых в настоящем изобретении, являются демиелинизирующие нарушения, предпочтительно центральной нервной системы. Нарушением миелинизации, особенно предпочтительным для лечения или диагностики с помощью соединений, предлагаемых в настоящем изобретении, является рассеянный склероз.
Термин "модуляторы GPR17" при использовании в настоящем изобретении описывает соединения, которые способны модулировать активность рецептора GPR17, предпочтительно соединения, которые способность уменьшать активность GPR17. Такие "негативные модуляторы GPR17" включают антагонисты GPR17, которые способны блокировать воздействия агонистов GPR17, а также обратные агонисты GPR17, которые также способны ингибировать обладающие системной активностью рецепторы GPR17 и варианты рецепторов.
Во всех случаях, когда после "С" в виде нижнего индекса указаны числовые значения, эти числовые значения (приведенные в скобках или без них) означают диапазон количества атомов углерода, содержащихся в соответствующей группе, приведенной непосредственно после числовых значений. Так, например, "C1-C6" и "(C1-C6)" оба обозначают группу, дополнительно точно определенную в настоящем изобретении, которая содержат от 1 до 6 атомов С.
"Алкил" включает насыщенные алифатические гидрокарбильные группы. Углеводородная цепь может являться линейной или разветвленной. Примеры "алкила" включают содержащие 1-6 атомов углерода ("C1-C6-алкил"), содержащие 1-5 атомов углерода ("С1-С5-алкил"), 1-4 атома углерода ("С1-С4-алкил") или лишь 1-3 атома углерода ("C1-С3-алкил"). Примерами для этого термина являются такие группы, как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, трет-амил и т.п. Любые количества атомов С, содержащихся в алкилах или в других группах, в настоящем изобретении может быть указано в скобках или без скобок.
"Алкенил" включает одновалентные алифатические гидрокарбильные группы, содержащие по меньшей мере одну двойную связь. Алкенилы могут обладать разветвленной или линейной цепью. Примеры "алкенила" включают содержащие 2-3 атома углерода ("С2-С3-алкенил") или 2-6 атомов углерода ("С2-C3-алкенил"). Примерами для этого термина являются такие группы, как винил (этенил), аллил или бутенил. Термин "пропенил" означает алкенилы, содержащие 3 образующих цепь атома углерода, и включает линейные (н-пропенил), а также разветвленные (изопропинил/метилэтенил) группы.
"Алкинил" включает одновалентные алифатические гидрокарбильные группы, содержащие по меньшей мере одну тройную связь. Алкинилы могут обладать разветвленной или линейной цепью. Примеры "алкинила" включают содержащие 2-6 атомов углерода ("С2-С6-алкинил"). Примерами для этого термина являются такие группы, как этинил, пропаргил и 2-бутинил.
"Алкилоксигруппа" и "алкоксигруппа", использующиеся в настоящем изобретении взаимозаменяемым образом (совместно алк(ил)окси), включают группу -OR, в которой R обозначает "алкил", дополнительно определенный в настоящем изобретении с приведенными примерами. Предпочтительные алк(ил)оксигруппы включают, например, мет(ил)оксигруппу, эт(ил)оксигруппу, н-проп(ил)оксигруппу, изопроп(ил)оксигруппу, н-бут(ил)оксигруппу, трет бут(ил)оксигруппу, втор-бут(ил)оксигруппу, изобут(ил)оксигруппу, н-пент(ил)оксигруппу, 1,2-диметилбут(ил)оксигруппу и т.п.
"Галоген" включает атомы фтора, хлора, брома и йода.
"Азидогруппа" означает группу -N=N=N.
"Цианометил" означает -CH2-C=N.
Термин "галогеналкил" при использовании в настоящем изобретении означает "алкил", описанный в настоящем изобретении (и где числовые значения обозначают количество атомов С, содержащихся в алкильной части), который замещен одним или большим количеством атомов галогенов. Типичные примеры "галоген(С1-С3)алкильных" групп включают, но не ограничиваются только ими, -CF3, -CCl3, -CFCl2, CH2CH2CF3 и CH2CF3.
Термин "фторированная" означает группу, в которой один или большее количество атомов водорода заменены атомами фтора. Так, например, алкильная группа или алкоксигруппа соответственно, для которой указано, что она является незамещенной или фторированной, включает "фторалкил" или "фторалк(ил)оксигруппу" соответственно, определенные в настоящем изобретении. Аналогичным образом, фторированная алкоксиалкильная группа включает такие группы, как фторалкоксиалкил и алкоксифторалкил.
Использующийся термин "фторалкил" означает "алкил", описанный в настоящем изобретении, который замещен одним или большим количеством атомов фтора. Типичные примеры фтор(С1-С3)алкильных групп включают, но не ограничиваются только ими, -CF3, -CH2CHF2 и -CH2CF3. Предпочтительными "фторалкильными" группами являются такие, в которых концевые метальные группы замещены одним или большим количеством атомов фтора; поэтому особенно предпочтительной монофторэтильной группой является -CH2CH2F, особенно предпочтительной дифторэтильной группой является - CH2CHF2, особенно предпочтительной трифторэтильной группой является - CH2CF3, особенно предпочтительной монофторпропильной группой является -CH2CH2CH2F, особенно предпочтительной дифторпропильной группой является -CH2CH2CHF2 и особенно предпочтительной трифторпропильной группой является -CH2CH2CF3.
Термин "моно-, ди- и трифтор", использующийся в качестве приставки для химических групп, таких как алкил или алкоксигруппа, означает сокращение для соответствующих фторированных групп. Так, например, термин "моно-, ди- и трифторэтил" означает такие группы, как монофторэтил, дифторэтил и трифторэтил.
Термин "галогеналк(ил)оксигруппа" при использовании в настоящем изобретении означает "алк(ил)оксигруппу", как здесь описано, которая замещена одним или большим количеством атомов галогенов. Типичные примеры галоген(С1-С3)алкилоксигрупп включают, но не ограничиваются только ими, -OCF3, -OCCl3, -OCFCl2 и -OCH2CF3.
Термины "фторалкилоксигруппа" или "фторалкоксигруппа", использующиеся в настоящем изобретении взаимозаменяемым образом, означают "алк(ил)оксигруппу", как здесь описано, которая замещена одним или большим количеством атомов фтора. Типичные примеры фтор(С1-С3)алк(ил)оксигрупп включают, но не ограничиваются только ими OCF3, OCH2CHF2 и OCF2CHF2. Предпочтительной "монофторэтоксигруппой" является группа -OCH2CH2F. Предпочтительной дифторэтоксигруппой является группа -OCH2CHF2. Предпочтительной трифторэтоксигруппой является группа -OCH2CF3. Предпочтительной монофторпропилоксигруппой является группа -OCH2CH2CH2F. Предпочтительной дифторпропилоксигруппой является группа -OCH2CH2CHF2 и предпочтительной трифторпропилоксигруппой является группа -OCH2CH2CF3.
Термины "фторалк(ил)оксиалкил" или "фторалкоксиалкил", использующиеся в настоящем изобретении взаимозаменяемым образом, означают группу, содержащую алкильную группу, которая замещена алк(ил)оксигруппой, где концевая алкоксигруппа замещена одним или большим количеством атомов фтора. Типичные примеры включают, но не ограничиваются только ими -CH2CH2OCF3, -CH2OCF2CH3 и -CH2OCHFCHF2.
Термины "фторалкилоксиалкилоксигруппа" или "фторалкоксиалкоксигруппа", использующиеся в настоящем изобретении взаимозаменяемым образом, означают группу, в которой алкоксигруппа замещена другой алкоксигруппой, где концевая алкоксигруппа замещена одним или большим количеством атомов фтора. Типичные примеры включают, но не ограничиваются только ими -OCH2OCH2CF3, -OCH2OCF2CH3 и -OCH2CH2OCHF2.
"Алкилкарбонил" означает группу -С(=O)алкил, в которой алкил является таким, как определено в настоящем изобретении. Типичными примерами являются C1-С6-алкилкарбонил и C1-С3-алкилкарбонил и предпочтительным является ацетил (-С(=O)CH3).
"Алк(ил)оксикарбонил" означает радикал -С(=O)-O-алкил, в котором алкильная группа является такой, как определено в настоящем изобретении. Типичными примерами являются C1-С6-алкоксикарбонил и С1-С3-алкоксикарбонил и предпочтительным является метоксикарбонил (-С(=O)OCH3).
"Алкилсульфинил" означает радикал -S(=O)алкил, в котором алкил является таким, как определено в настоящем изобретении. Типичным примером является C1-С3-алкилсульфинил и предпочтительным является метилсульфинил (-S(=O)CH3).
"Алкилсульфонил" означает радикал -S(=O)2-алкил, в котором алкил является таким, как определено в настоящем изобретении. Типичным примером является C1-С3-алкилсульфонил и предпочтительным является метилсульфонил (-S(=O)2CH3).
"C1-С3-Алкокси(C1-С3)алкил" означает группу -C1-С3-алкил-O-(C1-С3)алкил, в которой алкил является таким, как определено в настоящем изобретении.
"C1-С3-Алкокси(C1-С3)алкоксигруппа" означает группу -О-C1-С3-алкил-О-(C1-С3)алкил, в которой алкил является таким, как определено в настоящем изобретении.
Термин "циклоалкил" при использовании в настоящем изобретении означает одновалентную группу, образованную из насыщенного углеводорода, которая может быть незамещенной или содержать один или более заместителей, дополнительно указанных в настоящем изобретении. "Циклоалкил" содержит по меньшей мере 3 и вплоть до, например, 7 образующих кольцо атомов углерода ("С3-С7-циклоалкил") или 6 образующих кольцо атомов ("С3-С6-циклоалкил"). Подходящие циклоалкильные группы включают циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Циклоалкилы предпочтительно являются одновалентными, однако также могут содержать соединенные мостиком бициклические группы, такие как, например, норборнанил. Циклоалкильная группа может являться концевой группой, которая может быть присоединена, например, к кольцевой системе с помощью метиленовой группы или метоксигруппы, в этом случае она будет называться "циклопропилметилом" или "циклопропилметоксигруппой" соответственно. Альтернативно, циклопропильная группа может быть замещенной, например, концевой алкоксигруппой или алкоксикарбонильной группой, в этом случае она будет называться "алкоксициклопропильной" или "алкоксикарбонилциклопропильной" группой. Так, например, "этоксикарбонилциклопропил" обладает структурой CH3CH2-O-С(=O)-циклопропил-, тогда как циклопропилметоксигруппа обладает структурой циклопропил-СН2-O-.
Термин "С3-С7-циклоалкенил" при использовании в настоящем изобретении означает одновалентные группы, содержащие от 3 до 7 атомов углерода, образованные из углеводорода, который содержит по меньшей мере одну двойную связь.
Термин "гетероциклоалкил" при использовании в настоящем изобретении означает насыщенное кольцо, содержащее по меньшей мере два образующих кольцо атома углерода и по меньшей мере один образующий кольцо гетероатом, предпочтительно выбранный из кислорода, серы и азота, где каждое кольцо может быть незамещенным или дополнительно содержать один или более заместителей, описанных в настоящем изобретении. Подходящие гетероциклоалкильные группы включают оксетанил, азетидинил, тетрагидрофуранил, диоксоланил, пирролидинил, оксазолидинил, тиазолидинил, изотиазолидинил, имидазолидинил, тетрагидропиранил, тетрагидротиопиранил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, азепанил, оксазепанил, диазепанил, тиадиазепанил и азоканил. Термин "С3-С7-гетероциклоалкил" означает гетероциклоалкил, содержащий от 3 до 7 образующих кольцо атомов. Гетероциклоалкилы предпочтительно являются моноциклическими, однако также могут соединенные мостиками бициклические молекулы, такие как, например, тропанил.
Термин "гетероциклоалкенил" при использовании в настоящем изобретении означает кольца, содержащие по меньшей мере одну двойную связь, по меньшей мере два образующих кольцо атомов углерода и по меньшей мере один образующий кольцо гетероатом, предпочтительно выбранный из кислорода, серы и азота, где каждое кольцо может быть незамещенным или содержать один или более заместителей, дополнительно определенных в настоящем изобретении. Подходящие гетероциклоалкенильные группы включают тиазолинил, изотиазолинил, имидазолинил, дигидрофуранил, дигидропиранил и дигидротиопиранил. Термин "С3-С7-гетероциклоалкенил" означает гетероциклоалкенил, содержащий от 3 до 7 образующих кольцо атомов. В контексте настоящего изобретения гетероциклоалкенилы предпочтительно являются моноциклическими.
Термин "гетероарил" при использовании в настоящем изобретении означает одновалентные ароматические группы, содержащие по меньшей мере 5 образующих кольцо атомов, образованные из одного кольца, содержащие, например, вплоть до 6 атомов (например, "С5-С6-гетероарил"), или множества конденсированных колец, содержащие, например, вплоть до 10 образующих кольцо атомов (например, "С5-С10-гетероарил"), где один или большее количество атомов углерода заменены одним или большим количеством гетероатомов, предпочтительно выбранных из кислорода, серы и азота. Подходящие гетероарильные группы включают фурил, бензофурил, тиенил, бензотиенил, тиено[2,3-с]пиразолил, пирролил, индолил, пирроло[2,3-b]пиридинил, пирроло[3,2-с]пиридинил, пирроло[3,4-b]пиридинил, пиразолил, пиразоло[1,5-а]пиридинил, пиразоло[3,4-d]пиримидинил, индазолил, 4,5,6,7-тетрагидроиндазолил, оксазолил, бензоксазолил, изоксазолил, тиазолил, бензотиазолил, бензоксадиазолил, бензоселенатиазолил, изотиазолил, имидазолил, бензимидазолил, имидазо[2,1-b]тиазолил, имидазо[1,2-а]пиридинил, имидазо[4,5-b]пиридинил, пуринил, имидазо[1,2-а]пиримидинил, имидазо[1,2-а]пиразинил, оксадиазолил, тиадиазолил, триазолил, [1,2,4]триазоло[1,5-а]-5-пиримидинил, бензотриазолил, тетразолил, пиридинил, хинолинил, изохинолинил, пиридазинил, циннолинил, фталазинил, пиримидинил, хиназолинил, пиразинил, хиноксалинил, птеридинил и триазинил. Как указано выше, термин "С5-С6-гетероарил" означает гетероарил, содержащий 5 или 6 образующих кольцо атомов, хотя некоторые из образующих кольцо атомов не являются атомами углерода, а являются гетероатомами.
Термин "C8-С10-гетероциклил" при использовании в настоящем изобретении означает бициклические группы, содержащие от 8 до 10 образующих кольцо атомов, где один или большее количество образующих кольцо атомов углерода заменены одним или большим количеством гетероатомов, предпочтительно выбранных из кислорода, серы и азота, и где одно из указанных колец является ароматическим и другое является неароматическим. Подходящими C8-С10-гетероциклилами являются бензодиоксолил, дигидробензофуранил, дигидробензотиенил, тетрагидрохинолинил, тетрагидроизохинолинил, тетрагидрохиноксалин и т.п.
Термины "С3-С7-циклоалкил(С1-С6)алкил" или С3-С7-гетероциклоалкил(С1-С6)алкил" означают концевые "С3-С7циклоалкил" или "С3-С7-гетероциклоалкил соответственно, определенные в настоящем изобретении, которые присоединены к С1-С6-алкилу, определенному в настоящем изобретении.
Термины "С3-С7-циклоалкил(С1-С6)алкоксигруппа" или С3-С7-гетероциклоалкил(С1-С6)алкоксигруппа" означают концевые "С3-С7-циклоалкил" или "С3-С7-гетероциклоалкил" соответственно, определенные в настоящем изобретении, которые присоединены к "С1-С6-алкоксигруппе", определенной в настоящем изобретении.
Термин "фенил(С1-С6)алкил" означает С1-С6-алкил, определенный в настоящем изобретении, замещенный фенилом. Примерами являются бензил или фенилэтил.
"Фенил(С1-С6)алкоксигруппа" означает " С1-С6-алкилоксигруппу", замещенную фенилом. Примерами фенилалкилоксигрупп являются фенилэтилоксигруппа и, предпочтительно, бензилоксигруппа.
Термины "пиридил" и "пиридинил" используют в настоящем изобретении взаимозаменяемым образом.
Термин "изоксазол" означает 1,2-оксазол.
Настоящее изобретение дополнительно проиллюстрировано, но ни в коем случае не ограничено, следующими пунктами:
1) Соединение формулы I:
в которой
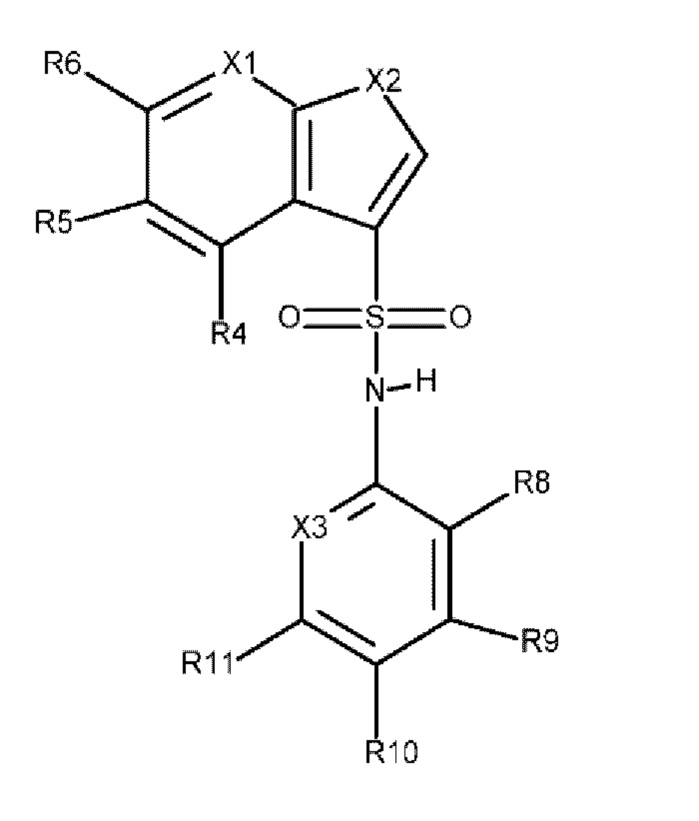
X1 обозначает N или C(R7),
Х2 обозначает NH или О,
Х3 обозначает N или C(R12),
R4 выбран из водорода и фтора,
R5 выбран из группы, включающей водород, галоген, цианогруппу, C1-C6-алкил, C1-C6-алкоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, C1-С3-алкилсульфинил и C1-С3-алкилсульфонил, где каждый алкил или алкоксигруппа необязательно может содержать один или более заместителей, выбранных из группы, включающей галоген, C1-С3-алкоксигруппу, С2-С3-алкинил, С2-С3-алкенил, цианогруппу, азидогруппу, гидроксигруппу, аминогруппу и C1-С3-алкиламиногруппу или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, гидроксигруппу, галоген, цианогруппу, азидогруппу, C1-C6-алкил, С2-С6-алкенил, С2-С6-алкинил, C1-C6-алкоксигруппу, С3-С7-циклоалкил, С3-С6-циклоалкенил, С3-С7-гетероциклоалкил, С3-С7-гетероциклоалкенил, фенил, С5-С10-гетероарил, C8-С10-гетероциклил, -ORx, -SRx, -SORx, SO2RX, -пентафторсульфанил, -NRyRzz, -NRyCORx, -NRyCO2Rx, -NRxCONRyRz, -CORx, -CO2Rx, -CONRyRz, где каждая алкильная, алкенильная, алкинильная группа, алкоксигруппа, циклоалкильная, гетероциклоалкильная, циклоалкенильная, фенильная, гетероарильная или гетероциклильная группа, содержащаяся в R6, может быть незамещенной или содержать один или более заместителей, предпочтительно выбранных из группы, включающей галоген, гидроксигруппу, оксогруппу, цианогруппу, азидогруппу, нитрогруппу, C1-C6-алкил, С1-С6-алкокси(C1-С3)алкил, С3-С7-циклоалкил, С3-С7гетероциклоалкил, фенил, С5-С10-(предпочтительно С5-С6)гетероарил, ORx, -SRx, -SORx, SO2RX, -пентафторсульфанил, NRyRz, -NRyCORx, -NRyCO2Rx, -CORx, -CO2Rx, -CONRyRz,
где Rx, Ry, Rz и Rzz независимо выбраны из группы, включающей водород, C1-С6-алкил, С3-С7-циклоалкил, С3-С6-циклоалкенил, С3-С7-циклоалкил(С1-С6)алкил, фенил, фенил(С1-С6)алкил, С3-С7-гетероциклоалкил, С3-С7-гетероциклоалкил(С1-С6)алкил, С5-С6-гетероарил или гетероарил(С1-С6)алкил, где любая из этих групп может быть незамещенной или содержать один или более заместителей, выбранных из описанных выше, или Ry и Rz, или Ry и Rzz вместе с атомом азота аминогруппы, к которому они оба присоединены, могут образовать ароматический или неароматический, незамещенный или замещенный С5-С6-гетероцикл, и где Rzz отличается от водорода,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образует незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил, где каждый заместитель, если присутствует, выбран из группы, включающей галоген, C1-С3-алкил, С3-С7-циклоалкил, С3-С7-циклоалкил(С1-С3)алкил, С3-С7-гетероциклоалкил(С1-С3)алкил, C1-С3-алкоксигруппу и C1-С3-алкокси(C1-С3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы,
или R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, или
R7 выбран из группы, включающей Н, галоген, цианогруппу, C1-C6-алкил, C1-С6-алкоксигруппу, С2-С6-алкинил, С2-С6-алкенил, C1-С6-алкилкарбонил, C1-C6-алкоксикарбонил, C1-C6-алкилсульфонил, C1-C6-алкилсульфинил, С3-С7-циклоалкил, С3-С7гетероциклоалкил, фенил, С5-С6-гетероарил, где каждая алкильная, алкенильная, алкинильная группа или алкоксигруппа может быть незамещенной или содержать один или более заместителей, выбранных из галогена и C1-C6-алкоксигруппы,
R8 выбран из группы, включающей водород, С1-С6-алкил, C1-C6-алкоксигруппу и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы, или вместе с R9 образует кольцевую систему, как здесь описано,
R9 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, C1-С6-алкил, C1-С6-алкоксигруппу, С2-С6-алкенил, С2-С6-алкинил, и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и С1-С3-алкоксигруппы,
или R9 вместе с R8 или R10, и с кольцом, к которому они присоединены, предпочтительно образуют бициклическую кольцевую систему, выбранную из группы, включающей (а) 2,1,3-бензотиадиазол, (b) 2,1,3-бензоселенадиазол, (с) 2,1,3-бензоксадиазол, (d) 1,3-бензотиазол, (е) 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и незамещенным или замещенным оксогруппой, (f) 1,3-бензодиоксол, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, (g) бензотиофен, который может быть незамещенным или может быть частично гидрированным и незамещенным или содержать один или два заместителя, выбранных из оксогруппы, метила или фтора, или (h) бензофуран, который может быть незамещенным или может быть частично гидрированным и незамещенным или замещенным одной или двумя группами, выбранными из оксогруппы, фтора и метила, предпочтительно одной оксогруппой,
R10 выбран из группы, включающей водород, галоген, C1-C6-алкил, C1-C6-алкоксигруппу, С2-С6-алкенил, С2-С6-алкинил, цианогруппу, циано(С1-С6) алкил, C1-C6-алкилкарбонил, C1-C6-алкоксикарбонил, C1-C6-алкилсульфонил, C1-С6-алкилсульфинил, азидогруппу, пентафторсульфанил и нитрогруппу, где каждый алкил, алкенил, алкинил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С6-алкоксигруппы, или R10 вместе с R9 образует кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу, C1-C6-алкил, C1-C6-алкоксигруппу, C1-C6-алкилкарбонил, C1-C6-алкоксикарбонил, C1-C6-алкилсульфонил и C1-C6-алкилсульфинил, С1-С6-алкенил и С2-С6-алкинил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы,
R12 выбран из группы, включающей водород, C1-C6-алкил, C1-C6-алкоксигруппу и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
2) Соединение по пункту 1, в котором
R4 обозначает водород
R5 выбран из группы, включающей водород, галоген, цианогруппу, С1-С3-алкил, C1-С3-алкоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, C1-С3-алкилсульфинил и C1-С3-алкилсульфонил, где каждый алкил или алкоксигруппа необязательно может содержать один или более заместителей, выбранных из группы, включающей галоген, C1-С3-алкоксигруппу, цианогруппу, азидогруппу и необязательно алкилированную аминогруппу, или R5 вместе с R6 образуют кольцо, как это описано ниже,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-С3-алкил, незамещенную или замещенную C1-С3-алкоксигруппу незамещенный или замещенный С2-С3-алкенил, незамещенный или замещенный С2-С3-алкинил, незамещенный или замещенный C1-С3-алкилкарбонил, незамещенный или замещенный C1-С3-алкоксикарбонил, незамещенный или замещенный С1-С3-алкилсульфинил, незамещенный или замещенный С1-С3-алкилсульфонил, незамещенный или замещенный С3-С7-циклоалкил, незамещенный или замещенный С3-С7-циклоалкил(C1-С3)алкил незамещенный или замещенный С3-С7-гетероциклоалкил незамещенный или замещенный С3-С7-гетероциклоалкил(C1-С3)алкил, незамещенную или замещенную С3-C6-циклоалкоксигруппу, незамещенную или замещенную С3-C6-гетероциклоалкоксигруппу, незамещенную или замещенную C1-С3-алкокси(C1-С3)алкоксигруппу, незамещенную или замещенную (С3-C6)циклоалкил(С1-С3)алкоксигруппу, незамещенную или замещенную (С3-C6)гетероциклоалкил(С1-С3)алкоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенилоксигруппу, незамещенный или замещенный тиенил, незамещенный или замещенный пиридил, незамещенный или замещенный оксазол, незамещенный или замещенный тиазол, незамещенный или замещенный изоксазол, незамещенную или замещенную фенил(C1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, где каждый необязательный заместитель, содержащийся в R6, выбран из группы, включающей фтор, хлор, бром, метил, метоксигруппу и цианогруппу, или
R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образует незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил, где каждый заместитель, если присутствует, выбран из группы, включающей галоген, C1-С3-алкил, С3-С7-циклоалкил, С3-С7-циклоалкил(С1-С3)алкил, С3-С7-гетероциклоалкил(С1-С3)алкил, C1-С3-алкоксигруппу и C1-С3-алкокси(C1-С3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы, или
R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образует 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей Н, галоген, цианогруппу, C1-С3-алкил, C1-С3-алкоксигруппу, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, С1-С3-алкилсульфонил, и C1-С3-алкилсульфинил, где каждый алкильный или алкоксильный фрагмент может содержать один или более заместителей, предпочтительно галоген или C1-С3-алкоксигруппу, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, C1-С3-алкил, С1-С3-алкоксигруппу и галоген, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена, цианогруппы и метоксигруппы, или R8 вместе с R9 образуют кольцевую систему, как здесь описано,
R9 выбран из группы, включающей водород, C1-С3-алкил, С1-С3-алкоксигруппу, фтор, хлор, бром и йод, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и метоксигруппы,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензотиазол, 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и замещенным оксогруппой, 1,3-бензодиоксол, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила, 2,3-дигидробензотиофен, который может быть незамещенным или замещенным одной или двумя оксогруппами, и 1,3-дигидро-2-бензофуран, который может быть незамещенным или замещенным одной или двумя группами, выбранными из оксогруппы, фтора и метила, предпочтительно одной оксогруппой,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, C1-С3-алкоксигруппу, С2-С4 алкенил, С2-С4-алкинил, цианогруппу, цианометил, C1-С3-алкилкарбонил, C1-С3-алкоксикарбонил, азидогруппу, пентафторсульфанил и нитрогруппу, где каждый алкил, алкенил, алкинил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и С1-С3-алкоксигруппы, или R10 вместе с R8 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, C1-С3-алкил, С1-С3-алкоксигруппу, фтор, хлор, бром, йод, C1-С3-алкилкарбонил, С1-С3-алкоксикарбонил, где каждый алкил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора, хлора, брома, йода и С1-С3-алкоксигруппы,
R12 выбран из группы, включающей водород, C1-С3-алкил, С1-С3-алкоксигруппу, фтор, хлор, бром и йод, где каждый алкил и алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора, хлора, брома, йода и С1-С3-алкоксигруппы,
где если R6 обозначает водород и X1 обозначает N, то R5 отличается от водорода и предпочтительно обозначает йод,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
3) Соединение по пункту 1, в котором
X1 обозначает N или C(R7),
Х2 обозначает NH,
Х3 обозначает N или C(R12),
R4 обозначает водород,
R5 выбран из группы, включающей водород, фтор, хлор, бром, йод, незамещенный или фторированный С1-С2-алкил, предпочтительно метил или трифторметил, незамещенную или фторированную С1-С2-алкилоксигруппу, незамещенный или фторированный С1-С2-алкилкарбонил, незамещенный или фторированный С1-С2-алкилоксикарбонил, метилсульфинил и метилсульфонил, или R5 вместе с R6 образуют кольцо, как здесь описано,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, азидогруппу, незамещенный или замещенный C1-С3-алкил, трифторметил, незамещенный или фторированный C1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный С1-С3-алкоксикарбонил, метилсульфинил, метилсульфонил, С3-С6-циклоалкил, предпочтительно циклопропил, С3-С6-циклоалкил(С1-С3)алкил, предпочтительно циклопропилметил, С3-С6-гетероциклоалкил, С3-С6-циклоалкоксигруппу, С3-C6-гетероциклоалкоксигруппу, незамещенную или замещенную С1-С3-алкоксигруппу, предпочтительно метоксигруппу, незамещенную или замещенную С1-С3-алкокси(С1-С3)алкоксигруппу циклопропилметоксигруппу, незамещенный или замещенный фенил, незамещенную или замещенную фенил(С1-С3)алкоксигруппу, предпочтительно бензилоксигруппу, незамещенную или замещенную фенилоксигруппу, незамещенный или замещенный тиенил, пиридил, оксазол, тиазол и изоксазол, и где каждый необязательный заместитель, содержащийся в R6, предпочтительно выбран из фтора, хлора, метила, метоксигруппы и цианогруппы,
при условии, что если R6 обозначает водород и X1 обозначает N, то R5 предпочтительно отличается от водорода и предпочтительно обозначает йод, или
R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенный или замещенный циклопентил или незамещенный или замещенный циклогексил, где каждый заместитель, если присутствует, выбран из галогена, метила или метоксигруппы, где каждый метил или метоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из фтора и метоксигруппы, или
R6 вместе с R5 и с атомами углерода, к которым R6 и R5 присоединены, образуют 1,3-диоксолан, который может быть незамещенным или содержать один или два заместителя, выбранных из фтора и метила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, цианогруппу, С1-С3-алкил, С1-С3-алкилоксигруппу, фтор(С1-С3)алкил, предпочтительно трифторметил, фтор(С1-С3)алкоксигруппу, предпочтительно трифторметоксигруппу, незамещенный или фторированный С1-С3-алкилкарбонил, незамещенный или фторированный С1-С3-алкоксикарбонил, метилсульфинил и метилсульфонил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С3)алкоксигруппу, C1-С3-алкил, предпочтительно метил, и фтор(С1-С3)алкил, предпочтительно трифторметил, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С3)алкоксигруппу, C1-С3-алкил, предпочтительно метил, цианогруппу, и фтор(С1-С3)алкил, предпочтительно трифторметил,
или R9 вместе с R8 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензоксазол, который может быть незамещенным или может быть частично гидрированным и замещенным оксогруппой (с образованием 2-оксо-2,3-дигидро-1,3-бензоксазола) и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора,
или R9 вместе с R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоселенадиазол, 2,1,3-бензоксадиазол, 1,3-бензотиазол 2,3-дигидро-1-бензотиофен, который замещен одной или двумя оксогруппами (предпочтительно замещен двумя оксогруппами с образованием 1,1-диоксо-2,3-дигидро-1-бензотиофена), 3-оксо-1,3-дигидро-2-бензофуран-5-ил и 1,3-бензодиоксол, который необязательно замещен одним или двумя атомами фтора
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, фтор(С1-С3)алкил, предпочтительно трифторметил, С2-С3-алкинил, С1-С3-алкилоксигруппу, фтор(С1-С2)алкоксигруппу, цианогруппу, цианометил, незамещенный или фторированный С1-С3-алкилкарбонил, предпочтительно ацетил, незамещенный или фторированный C1-С3-алкоксикарбонилазидогруппу, пентафторсульфанил и нитрогруппу, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, предпочтительно метил, фтор(С1-С3)алкил, предпочтительно трифторметил, С1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С2)алкоксигруппу, незамещенный или фторированный С1-С3-алкилкарбонил, незамещенный или фторированный C1-С3-алкоксикарбонил и цианогруппу,
R12 выбран из группы, включающей водород, фтор, хлор, бром, йод, С1-С3-алкил, предпочтительно метил, фтор(С1-С3)алкил, предпочтительно трифторметил, С1-С3-алкилоксигруппу, предпочтительно метоксигруппу, фтор(С1-С2)алкоксигруппу и цианогруппу,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
4) Соединение по любому из предыдущих пунктов, в котором
X1 обозначает N или C(R7),
Х2 обозначает NH или О,
Х3 обозначает N или C(R12),
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, азидогруппу, метил, этил, изопропил, трифторметил, метилсульфинил, метилсульфонил, циклопропил, циклопропилметил, метоксигруппу, этоксигруппу, метоксиэтоксигруппу, циклопропилметоксигруппу, фенил, бензилоксигруппу, фенилоксигруппу, тиенил, пиридил, оксазол, тиазол и изоксазол,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из фенила, пиридила и циклопентила,
R7 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, дифторметоксигруппу, трифторметоксигруппу, метил, дифторметил и трифторметил, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, йод, метоксигруппу, метил и трифторметил, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 выбран из водорода, фтора и хлора, и предпочтительно обозначает водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол, 3-оксо-1,3-дигидро-2-бензофуран-5-ил и 1,3-бензодиоксол, который необязательно замещен двумя атомами фтора,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, этинил, пропаргил, фтор(С1-С2)алкил, предпочтительно трифторметил, метоксигруппу, фтор(С1-С2)алкоксигруппу, цианогруппу, цианометил, ацетил, азидогруппу, пентафторсульфанил и метоксикарбонил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано,
R11 выбран из водорода, фтора, хлора, брома и метоксигруппы,
R12 выбран из водорода, фтора, хлора или брома,
где по меньшей мере один из R8, R9, R10 и R11 отличается от водорода и незамещенного алкила,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
5) Соединение по любому из предыдущих пунктов, в котором
X1 обозначает N или C(R7),
Х2 обозначает NH,
Х3 обозначает N или C(R12),
R4 и R5 оба обозначают водород,
R6 выбран из группы, включающей фтор, хлор, бром, азидогруппу, метил, этил, изопропил, трифторметил, метилсульфонил, циклопропил, метоксигруппу, этоксигруппу, трифторметоксигруппу, фенил, бензилоксигруппу, тиофен-2-ил и тиофен-3-ил,
или R6 вместе с R7 и с атомами углерода, к которым R6 и R7 присоединены, образуют кольцо, выбранное из фенила, пиридила и циклопентила,
R7 выбран из водорода, фтора, хлора и метоксигруппы, или R7 вместе с R6 образуют кольцо, как здесь описано,
R8 выбран из группы, включающей водород, фтор, хлор, бром, метоксигруппу и трифторметил, или R8 вместе с R10 образуют кольцевую систему, как здесь описано,
R9 обозначает водород или фтор, предпочтительно водород,
или R9 вместе с R8 или R10 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 1,3-бензодиоксол или 2,2-дифтор-1,3-бензодиоксол,
R10 выбран из группы, включающей водород, фтор, хлор, бром, йод, этинил, пропаргил, метоксигруппу, цианогруппу, цианометил, трифторметил, фтор(С1-С2)алкоксигруппу, ацетил, азидогруппу и пентафторсульфанил, или R10 вместе с R9 образуют кольцевую систему, как здесь описано, и где в предпочтительном варианте осуществления R8 и R10 оба не обозначают водород,
R11 выбран из водорода, фтора, хлора и метоксигруппы,
R12 выбран из водорода и фтора,
его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
6) Соединение по любому из предыдущих пунктов, в котором
X1 обозначает N или C(R7),
Х2 обозначает NH,
R4 и R5 оба обозначают водород,
R6 обозначает бром или хлор,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
Х3 обозначает N или C(R12),
R8 выбран из водорода, фтора, хлора и метоксигруппы,
R9 обозначает водород или фтор,
R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, трифторметил, дифторэтоксигруппу, трифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, фтора, хлора и метоксигруппы,
R12 обозначает водород или фтор,
где по меньшей мере один из R8, R9, R10 и R11 отличается от водорода,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
7) Соединение по любому из предыдущих пунктов, в котором
X1 обозначает N, или C(R7),
Х2 обозначает NH,
R4 и R5 оба обозначают водород,
R6 обозначает хлор или бром,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
Х3 обозначает N или C(R12),
R9 вместе с R8 и с фенильным кольцом, к которому R8 и R9 присоединены, образуют 2,1,3-бензотиадиазол или 2,2-дифтор-1,3-бензодиоксол,
R10 обозначает водород или фтор,
R11 выбран из водорода, фтора и метоксигруппы,
R12 обозначает водород или фтор,
его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
8) Соединение по любому из предыдущих пунктов, в котором XI обозначает N или C(R7),
Х2 обозначает NH,
R4 и R5 оба обозначают водород,
R6 обозначает хлор или бром, предпочтительно хлор,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
Х3 обозначает N или C(R12),
R8 выбран из фтора и метоксигруппы,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, йод, цианогруппу, цианометил, дифторметил, трифторметил, дифторэтоксигруппу, трифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, фтора и метоксигруппы,
R12 обозначает водород,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
9) Соединение по любому из предыдущих пунктов формулы II или III,
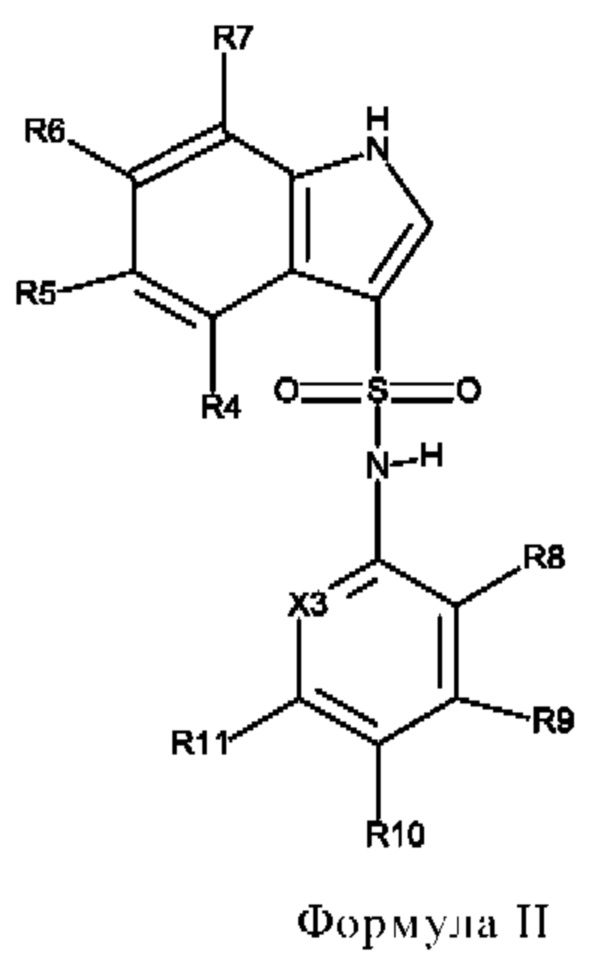
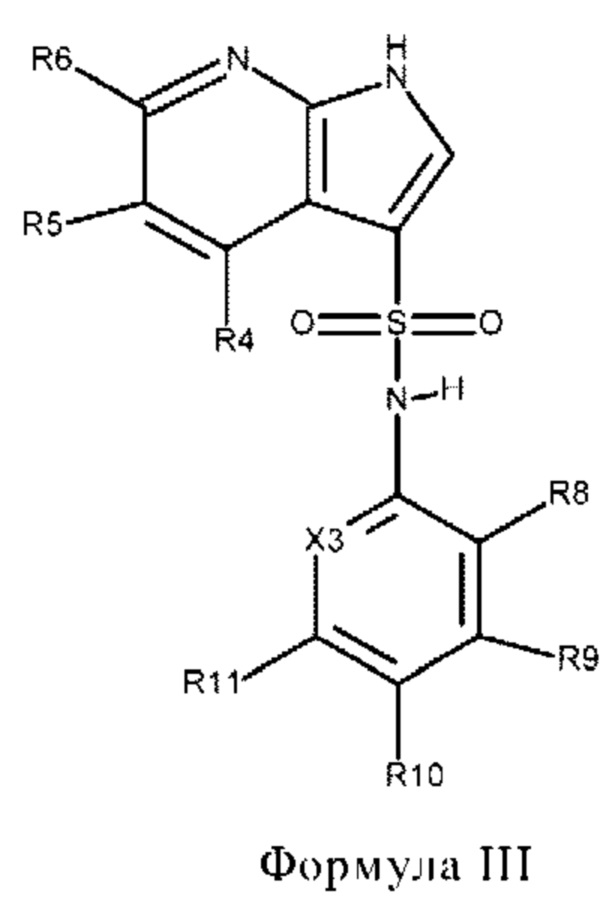
в которой R4, R5, R6, R7 если присутствует, R8, R9, R10, R11 и Х3 являются такими, как определено в любом из предыдущих пунктов.
10) Соединение по пункту 9, в котором
R4 обозначает водород,
R5 обозначает водород, йод, или метил,
R6 выбран из группы, включающей водород, фтор, хлор, бром, йод, метил, этил, изопропил, ацетил, трифторметил, метоксигруппу, этоксигруппу, фтор(С1-С2)алкоксигруппу, (С1-С2)алкоксиметоксигруппу, цианометилсульфонил, фенил, феноксигруппу, бензилоксигруппу, 2-пиридил, 3-пиридил, 4-пиридил, 2-тиенил, 3-тиенил, циклопропил, циклопропилоксигруппу и циклопропилметоксигруппу,
R7 в формуле II выбран из группы, включающей водород, метил, метоксигруппу, трифторметил, фтор, хлор и бром,
Х3 обозначает N или C(R12) и предпочтительно обозначает C(R12),
R8 выбран из водорода, метоксигруппы, цианогруппы, хлора и фтора,
R9 выбран из водорода и фтора,
R10 выбран из группы, включающей водород, этинил, цианогруппу, цианометил, ацетил, фтор, хлор, бром, йод, азидогруппу, нитрогруппу, трифторметил, дифторэтоксигруппу, трифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, фтора, хлора и метоксигруппы,
R12 обозначает водород или фтор,
где по меньшей мере один из R8, R9, R10 и R11 отличается от водорода, и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
11) Соединение по пункту 9, в котором
R4 и R5 оба обозначают водород,
R6 выбран из фтора, хлора, брома, изопропила, бензилоксигруппы и трифторметила,
R7 в формуле II обозначает водород, метоксигруппу, фтор или бром, предпочтительно водород,
Х3 обозначает -C(R12)- или N,
R8 обозначает фтор, водород или метоксигруппу,
R9 обозначает водород,
R10 обозначает этинил, трифторметил, дифторэтоксигруппу, цианогруппу, хлор, бром или йод,
R11 выбран из водорода и фтора, и
R12 выбран из водорода и фтора,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
12) Соединение по пункту 9, в котором
R4, R5 оба обозначают водород,
R6 обозначает бром, хлор или трифторметил,
R7 обозначает водород, метоксигруппу, фтор или трифторметил,
R8 обозначает фтор или метоксигруппу,
R9 обозначает водород,
R10 выбран из группы, включающей фтор, хлор, бром, цианогруппу, цианометил, трифторметил, дифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, метоксигруппы и фтора,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
13) Соединение по любому из пунктов 1-5, одной из следующих формул IIa - IIc,
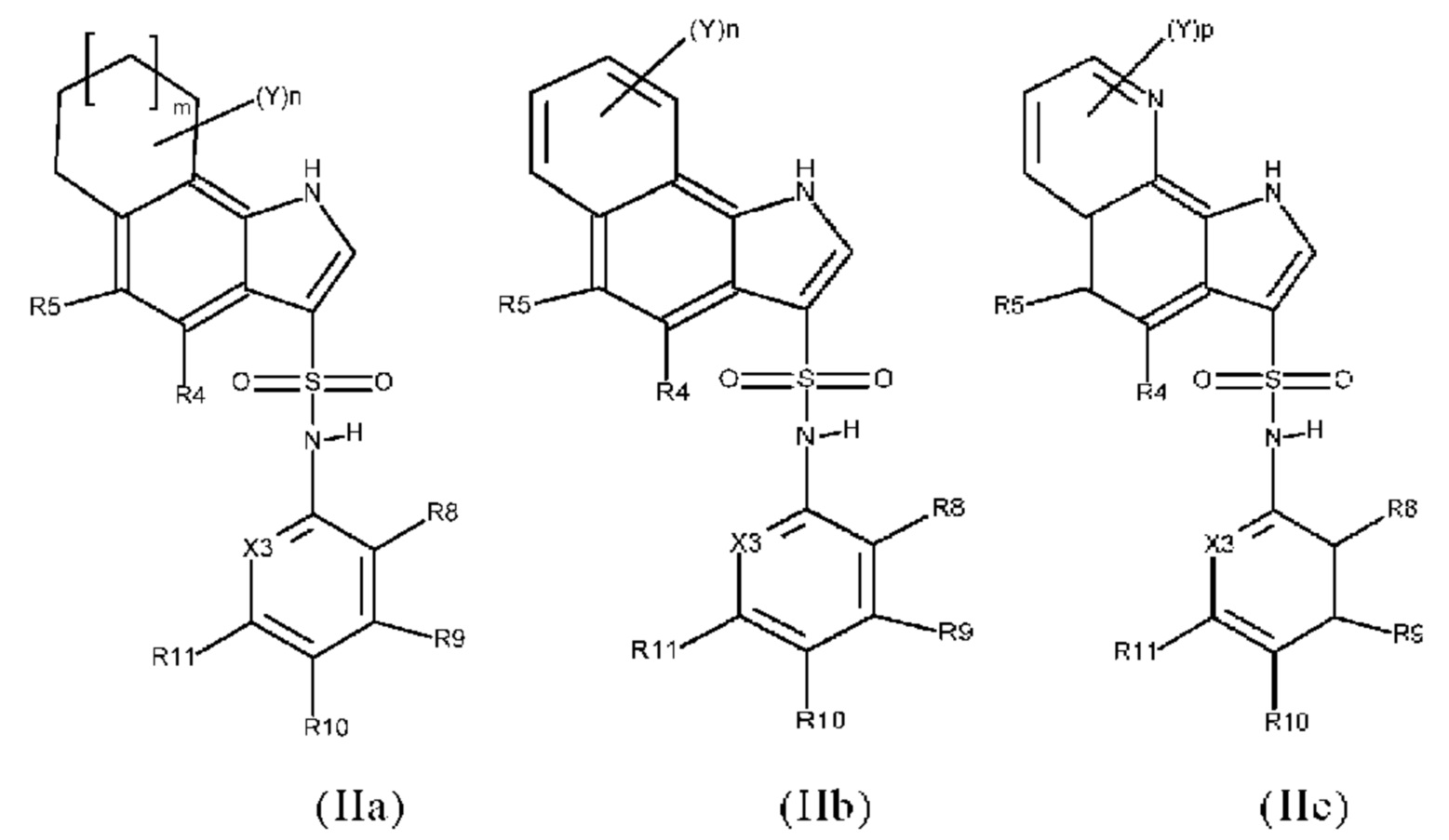
в которых
n обозначает любое число, равное от 0 до 4, предпочтительно 0, 1 или 2,
m равно 0 или 1, р обозначает любое число, равное от 0 до 3, предпочтительно 0, 1 или 2,
любой Y обозначает заместитель, независимо выбранный из группы, включающей галоген, цианогруппу, C1-C6-алкил, С2-С6-алкенил, С2-С6-алкинил, С3-С7-циклоалкил, С3-С7-циклоалкил(С1-С3)алкил, С3-С7-гетероциклоалкил(С1-С3)алкил, C1-С6-алкоксигруппу и С1-С6-алкокси(С1-С3)алкил, где каждый алкил или алкоксигруппа могут быть незамещенными или содержать один или более заместителей, выбранных из галогена и C1-С3-алкоксигруппы, и
R4, R5, Х3, R8, R9, R10, R11 и R12 являются такими, как описано в любом из пунктов 1-5,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
14) Соединение по пункту 13, в котором
m равно 0, n равно 0 или 1, р равно 0 или 1,
любой Y выбран из водорода, галогена, незамещенного или фторированного метила и незамещенной или фторированной метоксигруппы,
R4 и R5 оба обозначают водород,
R8 выбран из водорода, метоксигруппы, фтора и хлора,
Х3 обозначает N или C(R12),
R9 выбран из водорода, метоксигруппы, фтора и хлора, и предпочтительно обозначает водород,
R10 выбран из группы, включающей водород, этинил, цианогруппу, цианометил, фтор, хлор, бром, йод, азидогруппу, трифторметил, трифторметоксигруппу, дифторэтоксигруппу, трифторэтоксигруппу и пентафторсульфанил,
R11 выбран из водорода, фтора, хлора и метоксигруппу, и
R12 обозначает водород или фтор,
и где по меньшей мере один из R8, R9, R10 и R11 отличается от водорода, и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
15) Соединение по пункту 13 и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы, в котором
m равно 0, n равно 0 или 1, р равно 0 или 1,
любой Y выбран из водорода, галогена, незамещенного или фторированного метила и незамещенной или фторированной метоксигруппы,
Х3 обозначает C(R12)
R4 и R5 оба обозначают водород, и
(a) R8 вместе с R9 и с кольцом, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол, 2,1,3-бензоселенадиазол, 2-оксо-2,3-дигидро-1,3-бензоксазол, незамещенный 1,3-бензодиоксол и 2,2-дифтор-1,3-бензодиоксол,
R10 выбран из группы, включающей водород, фтор, хлор, бром, трифторметил, трифторметоксигруппу, дифторэтоксигруппу, трифторэтоксигруппу и цианогруппу, и предпочтительно обозначает водород или фтор,
R11 выбран из водорода, метоксигруппы, фтора, хлора, брома и цианогруппы, и
R12 обозначает водород, фтор, хлор и трифторметил, или
(b) R8 обозначает водород, метоксигруппу или фтор,
R9 вместе с R10 и с атомами С, к которым они присоединены, образуют кольцо, выбранное из группы, включающей 2,1,3-бензотиадиазол, 2,1,3-бензоксадиазол и 2,2-дифтор-1,3-бензодиоксол, R11 обозначает водород или фтор, и
R12 обозначает водород или фтор.
16) Соединение по любому из пунктов 1-5, одной из следующих формул II(d), II(е), II(f), III(а), III(b) или III(с),
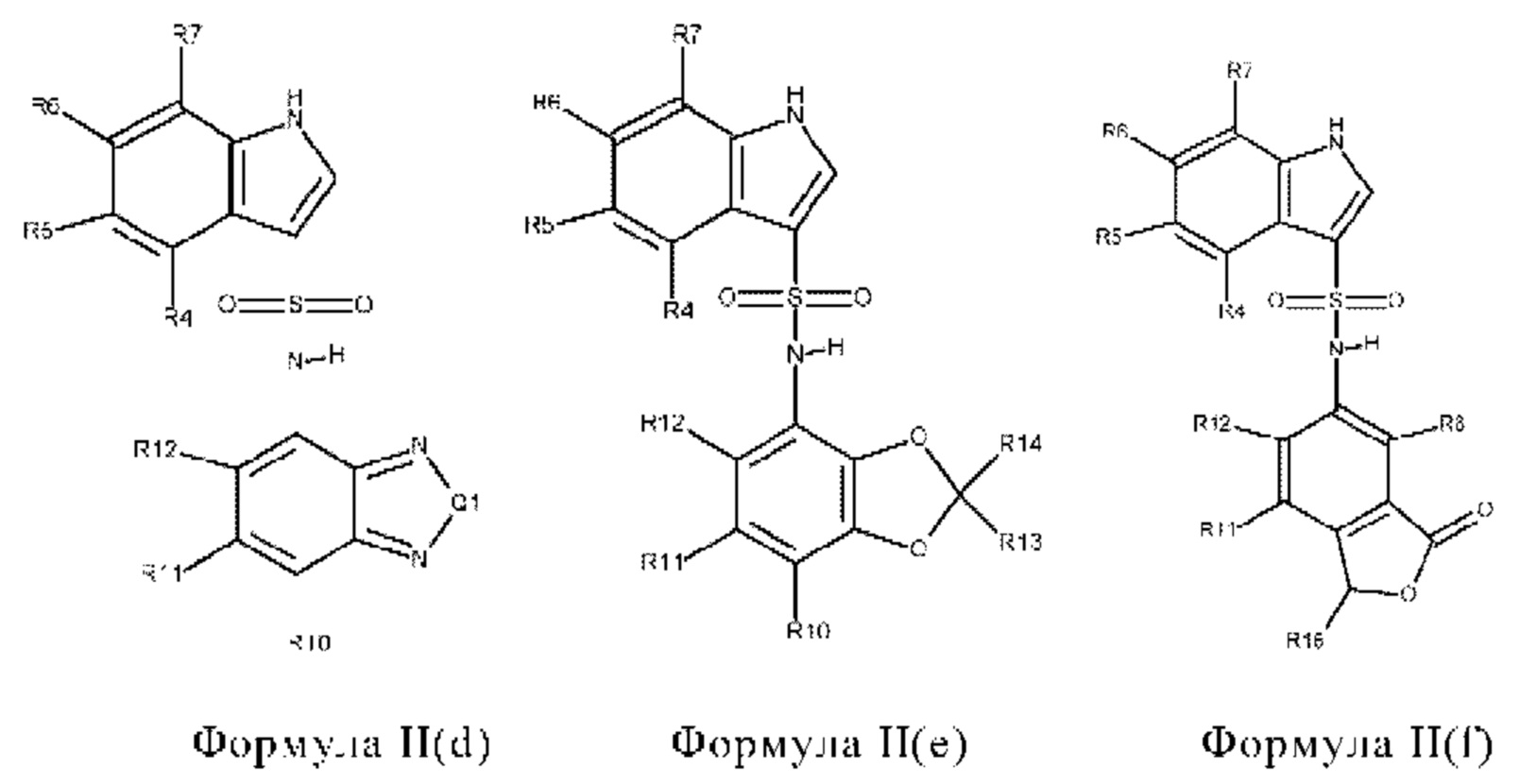
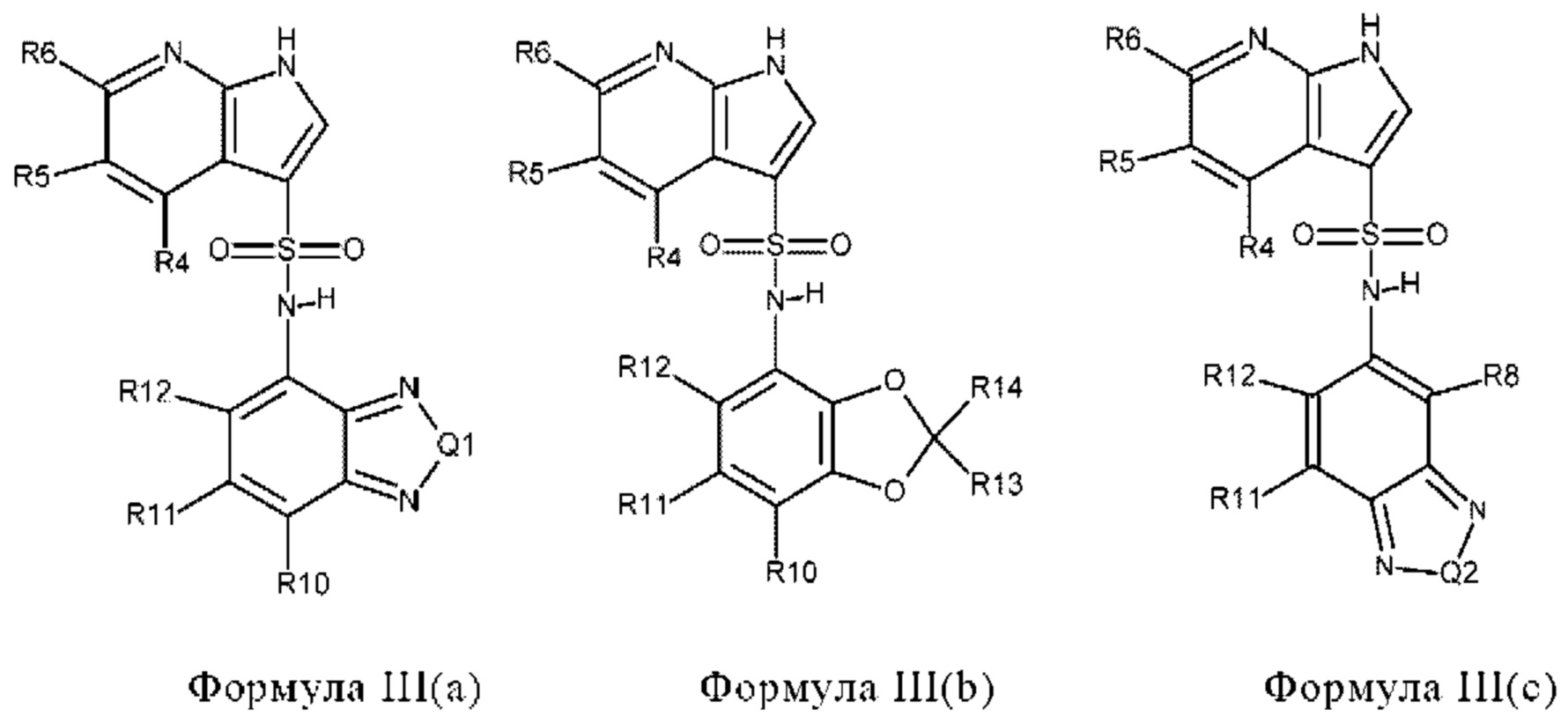
в котором
R4, R5, R6, R7, R8, R10, R11 и R12 являются такими, как описано в любом из пунктов 1-5,
в формулах II(d) и III(а) Q1 обозначает S или О,
в формулах II(е) и III(b) R13 и R14 выбраны из водорода, метила и фтора, и предпочтительно, если они оба обозначают водород или оба обозначают фтор, и
в формулах II(f) и III(с) Q2 обозначает S или О, предпочтительно S,
и его фармацевтически приемлемые соли, сольваты, изотопы и совместные кристаллы.
17) Соединение по пункту 16, одной из формул IId, IIe, IIIa и IIIb, в котором
Q1 обозначает S или О,
R13 и R14 выбраны из водорода и фтора,
R4 и R5 оба обозначают водород,
R6 выбран из фтора, хлора, брома, трифторметила и фенила,
R7, если присутствует, обозначает водород, фтор, бром, метоксигруппу или трифторметил, предпочтительно водород или трифторметил,
R10 выбран из водорода и галогена, предпочтительно из водорода, фтора и хлора,
R11 выбран из группы, включающей водород, галоген, трифторметил и цианогруппу, предпочтительно из фтора и водорода,
R12 выбран из водорода, галогена и трифторметила.
18) Соединение по пункту 16, одной из формул IIf и IIIc, в котором
Q2 обозначает S или О,
R4 и R5 оба обозначают водород,
R6 выбран из фтора, хлора, брома, трифторметила и фенила,
R7, если присутствует, выбран из водорода, метоксигруппы, фтора и трифторметила,
R8 выбран из водорода и галогена, предпочтительно из водорода и фтора,
R11 выбран из водорода, галогена, трифторметила и цианогруппы, и предпочтительно обозначает водород,
R12 выбран из водорода, галогена и трифторметила, предпочтительно из фтора и водорода,
19) Соединение по любому из предыдущих пунктов, содержащее по меньшей мере один изотоп, выбранный из123I,125I,131I,11С,14С,13N,15О,18F,76Br,124I,2H и3H, в увеличенном количестве, превышающем обычное содержание указанного изотопа, если он встречается в природе.
20) Применение соединения по пункту 19, в котором изотоп выбран из123I,125I,131I,11C,13N,15O,18F,76Br и124I, и он содержится в количестве, подходящем для визуализации с помощью PET и/или SPECT, для диагностики или и/или визуализации с помощью PET или SPECT.
21) Соединение по любому из предыдущих пунктов, предназначенное для применения в терапии.
22) Соединение по любому из предыдущих пунктов, предназначенное для применения для предупреждения или лечения нарушения или синдрома, выбранного из нарушения миелинизации и нарушения или синдрома, связанного с повреждением тканей головного мозга.
23) Соединение по пункту 22, где синдром или нарушение выбрано из группы, включающей рассеянный склероз (PC), включая его различные субформы, нейромиелит зрительного нерва (болезнь Девика), хронический рецидивирующий воспалительный неврит зрительного нерва, острый рассеянный энцефаломиелит, острый геморрагический лейкоэнцефалит (AHL), перивентрикулярную лейкомаляцию, демиелинизацию вследствие вирусных инфекций, центральный понтинный и экстрапонтинный миелинолиз, демиелинизацию вследствие травматического поражения тканей головного мозга, демиелинизацию в ответ на гипоксию, удар или ишемию, или другие сердечно-сосудистые заболевания, демиелинизацию вследствие воздействия диоксида углерода, цианида или других токсинов, поражающих ЦНС, болезнь Шильдера, концентрический склероз Бало, перинатальную энцефалопатию, нейродегенеративные заболевания, включая боковой амиотрофический склероз (ALS), болезнь Альцгеймера (AD), мультисистемную атрофию, болезнь Паркинсона, спинально-церебеллярную атаксию (SCA) и болезнь Гентингтона, психические нарушения, такие как шизофрения и биполярное расстройство, и заболевания, связанные с нарушением миелинизации периферической нервной системы, такие как лейкодистрофии, периферические невропатии, синдром Дежерина-Соттаса или болезнь Шарко-Мари-Тута.
24) Соединение по любому из предыдущих пунктов, предназначенное для применения для предупреждения и/или лечения рассеянного склероза (MS).
25) Способ предупреждения и/или лечения синдрома или нарушения, выбранного из нарушения миелинизации и нарушения или синдрома, связанного с повреждением тканей головного мозга, который включает введение нуждающемуся в этом пациенту соединения по любому из предыдущих пунктов в терапевтически эффективном количестве.
26) Способ по пункту 25, в котором симптом или нарушение связано с нарушением миелинизации, выбранным из группы, включающей рассеянный склероз (MS), включая его различные субформы, нейромиелит зрительного нерва (болезнь Девика), хронический рецидивирующий воспалительный неврит зрительного нерва, острый рассеянный энцефаломиелит, острый геморрагический лейкоэнцефалит (AHL), перивентрикулярную лейкомаляцию, демиелинизацию вследствие вирусных инфекций, центральный понтинный и экстрапонтинный миелинолиз, демиелинизацию вследствие травматического поражения тканей головного мозга, демиелинизацию в ответ на гипоксию, удар или ишемию, или другие сердечно-сосудистые заболевания, демиелинизацию вследствие воздействия диоксида углерода, цианида или других токсинов, поражающих ЦНС, болезнь Шильдера, концентрический склероз Бало, перинатальную энцефалопатию, нейродегенеративные заболевания, включая боковой амиотрофический склероз (ALS). болезнь Альцгеймера (AD), мультисистемную атрофию, болезнь Паркинсона, спинально-церебеллярную атаксию (SCA) и болезнь Гентингтона, психические нарушения, такие как шизофрения и биполярное расстройство, и заболевания, связанные с нарушением миелинизации периферической нервной системы, такие как лейкодистрофии, периферические невропатии, синдром Дежерина-Соттаса или болезнь Шарко-Мари-Тута.
27) Фармацевтическая композиция, содержащая соединение по любому из предыдущих пунктов и фармацевтически приемлемый носитель.
ЭКСПЕРИМЕНТАЛЬНЫЙ РАЗДЕЛ
А. ХИМИЧЕСКАЯ СЕКЦИЯ
Соединения, предлагаемые в настоящем изобретении, и пути их синтеза более подробно описаны ниже
Следует понимать, что 1Н-пирроло[2,3-b]пиридины и 1H-индолы, а также их предшественники - анилины обычно содержат атом водорода, присоединенный к кольцу в положении 5, даже если этот атом водорода не всегда явно изображен на чертежах, приведенных в настоящем изобретении.
A-I. Общие методики получения соединений
Соединения формулы I, предлагаемые в настоящем изобретении, можно получить по аналогии с обычными методиками, известными специалисту в области техники синтетической органической химии.
В настоящем изобретении любое описание синтеза соединений общей формулы I также является подходящим для применимых соединений субформул II, IIa, IIb, IIc, IId, IIe, IIf, III, IIIa, IIIb, IIIc и IV и соединений конкретных примеров, раскрытых в настоящем изобретении.
В одном варианте осуществления некоторые соединения общей формулы I можно получить по реакции соединения формулы XI с анилином формулы X по уравнению:
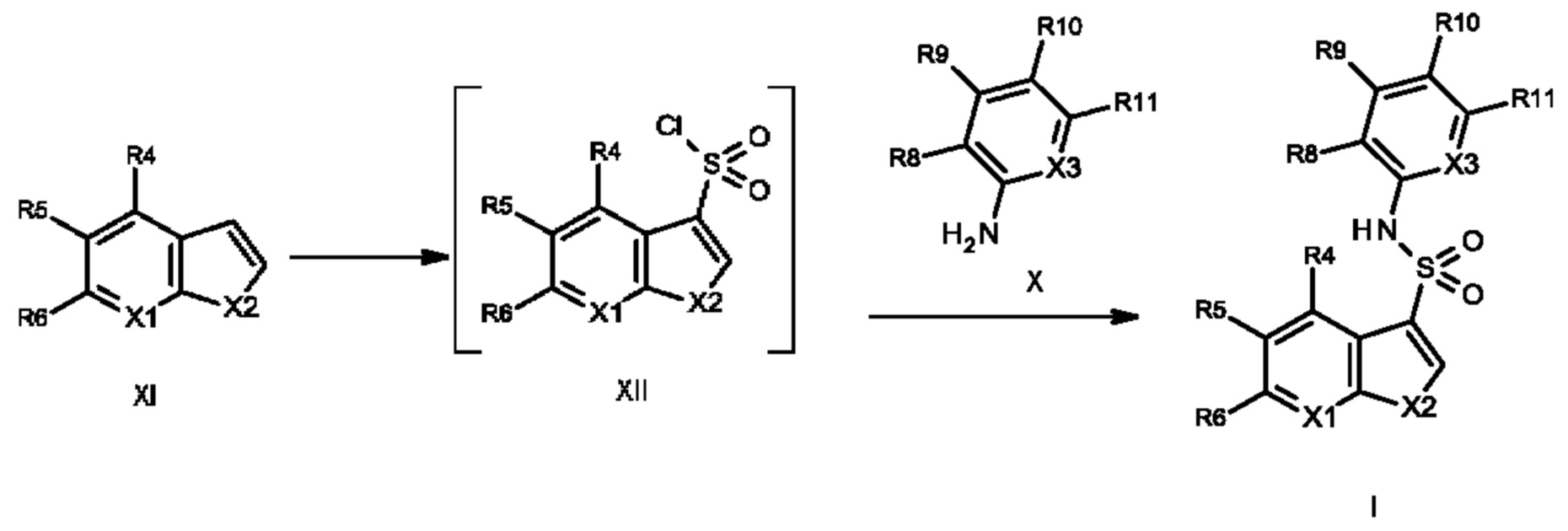
Эту реакцию можно провести с использованием хлорсульфоновой кислоты при температуре, находящейся в диапазоне от 60 до 120°С, в полярном растворителе, таком как ацетонитрил, с получением невыделенного промежуточного сульфонилхлорида XII. Затем промежуточный продукт XII непосредственно вводят в реакцию с анилином X в присутствии основания, такого как пиридин, с использованием или без использования каталитического количества 4-диметиламинопиридина (DMAP), в полярном растворителе, таком как ацетонитрил, при температуре, предпочтительно находящейся в диапазоне от 60 до 80°С.
Альтернативно, промежуточный сульфонилхлорид XII можно получить из соединения XI в присутствии комплекса пиридин-триоксид серы в пиридине при кипячении с обратным холодильником. Промежуточную соль сульфоновой кислоты можно хлорировать в присутствии хлорирующего реагента, такого как трифенилфосфин/трихлорацетонитрил, в растворителе, таком как дихлорметан, при кипячении с обратным холодильником.
Альтернативно, некоторые соединения общей формулы I можно получить по реакции сульфонилхлорида формулы XII с анилином формулы X по уравнению:
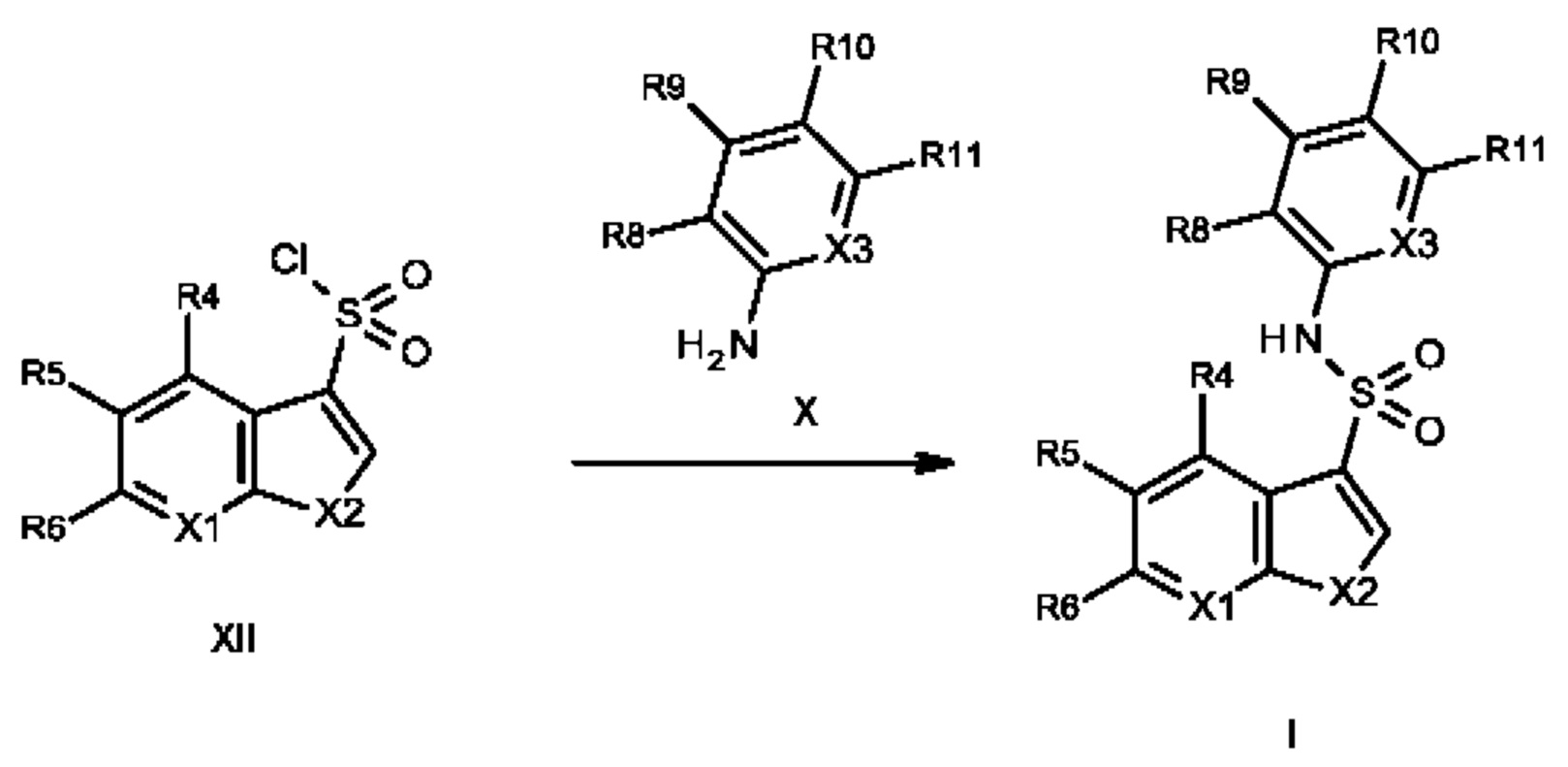
Эту реакцию можно провести в присутствии основания, такого как пиридин, использующегося в качестве растворителя, при комнатной температуре.
Альтернативно, некоторые соединения формулы I, в которой Х3 обозначает N, можно получить по реакции сульфонамида формулы XII-N с фторпиридином формулы X-N.
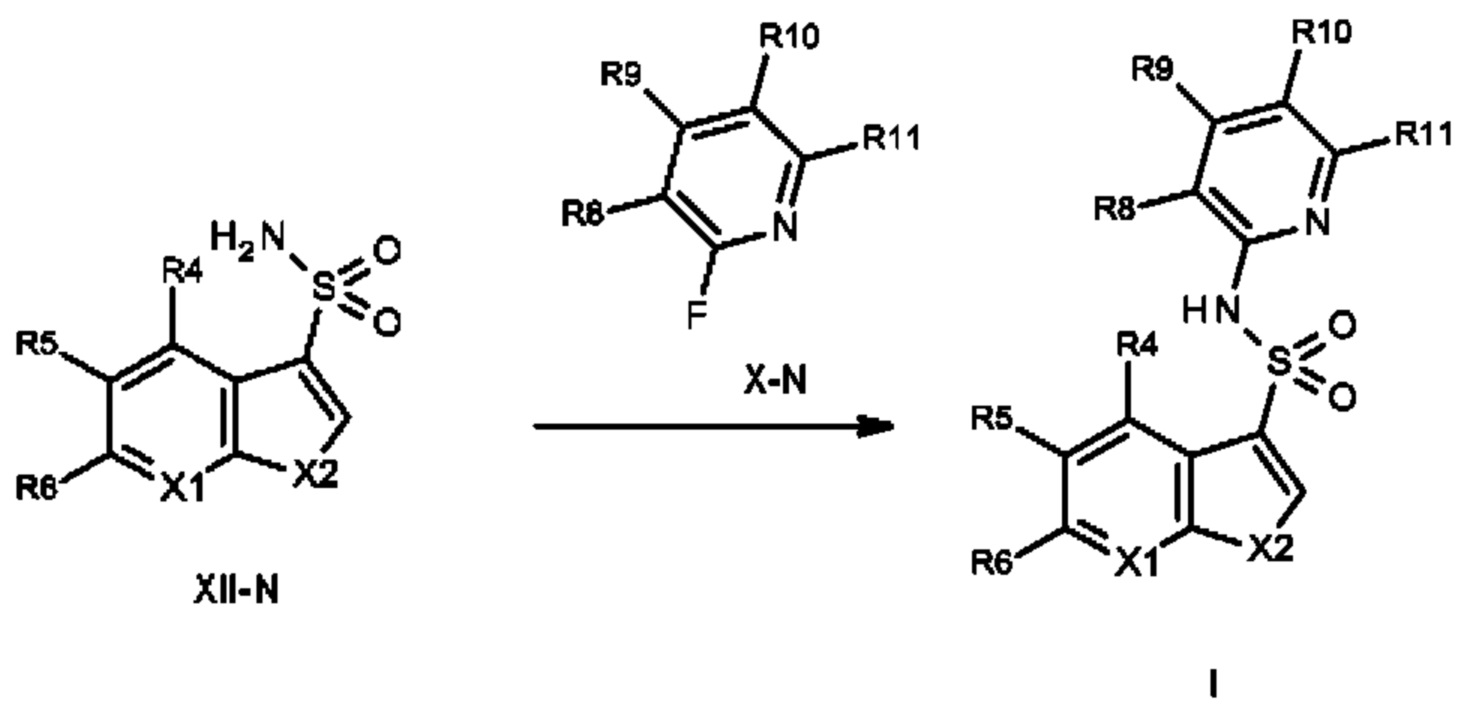
Эту реакцию можно провести в присутствии основания, такого как карбонат калия, в полярном растворителе, таком как диоксан, при высокой температуре.
Соединения формулы XII-N можно получить путем аммонолиза сульфонилхлоридов формулы XII.
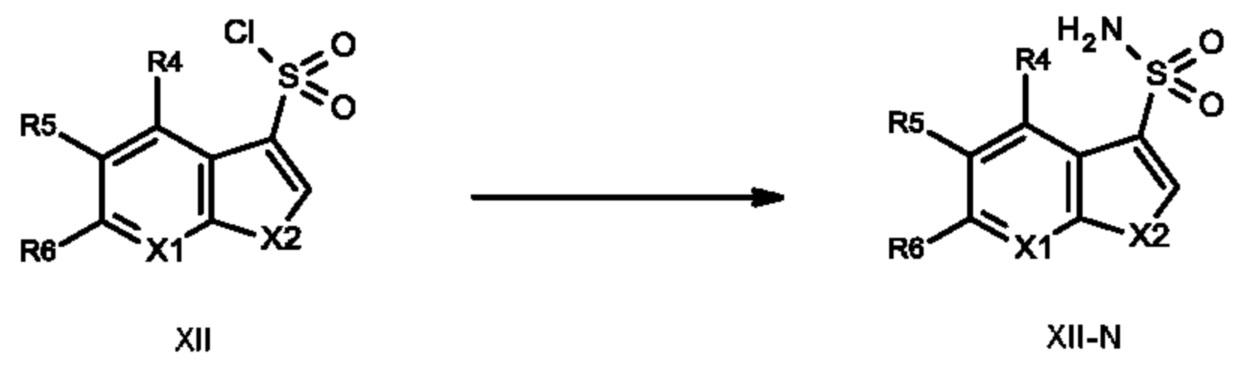
Эту реакцию можно провести с использованием газообразного аммиака в полярном растворителе, таком как тетрагидрофуран, при комнатной температуре.
Альтернативно, некоторые соединения общей формулы I, в которой Х2 = NH, можно получить путем удаления защитной группы из соединения формулы I-P, в которой Р обозначает защитную группу, такую как фенилсульфонил (PhSO2), по уравнению:
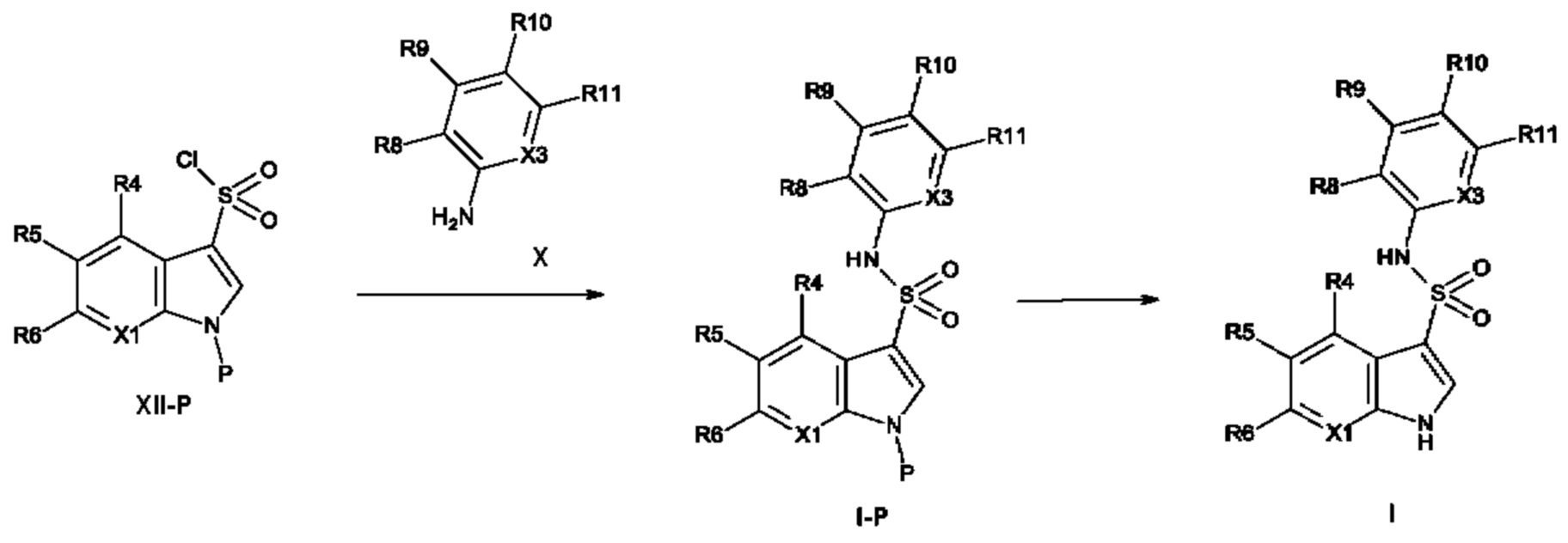
Эту реакцию можно провести в присутствии слабого основания, такого как карбонат калия, в смеси протонных растворителей, таких как метанол и вода, при комнатной температуре.
Соединения формулы I-P можно получить по реакции сульфонилхлорида формулы XII-Р с анилином формулы X. Эту реакцию можно провести в присутствии основания, такого как пиридин, использующегося в качестве растворителя, при комнатной температуре.
Соединения формулы XII можно получить путем хлорирования соединения формулы IX по уравнению:
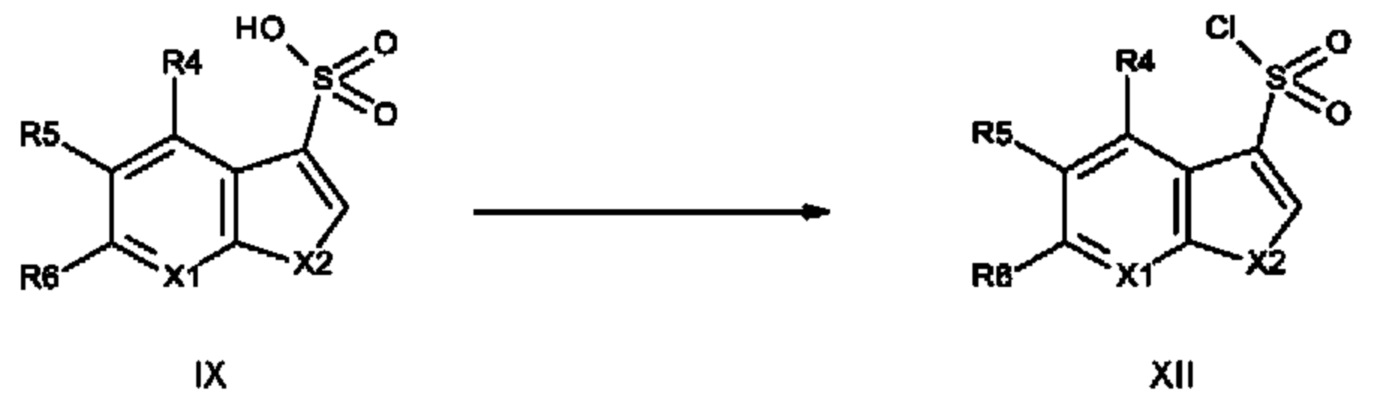
Эту реакцию можно провести в присутствии хлорирующего реагента, такого как оксихлорид фосфора или тионилхлорид, в полярном растворителе, таком как ацетонитрил, при температуре, находящейся в диапазоне от 50 до 100°С.
Соединения формулы IX можно получить путем сульфонилирования соединения формулы XI по уравнению:
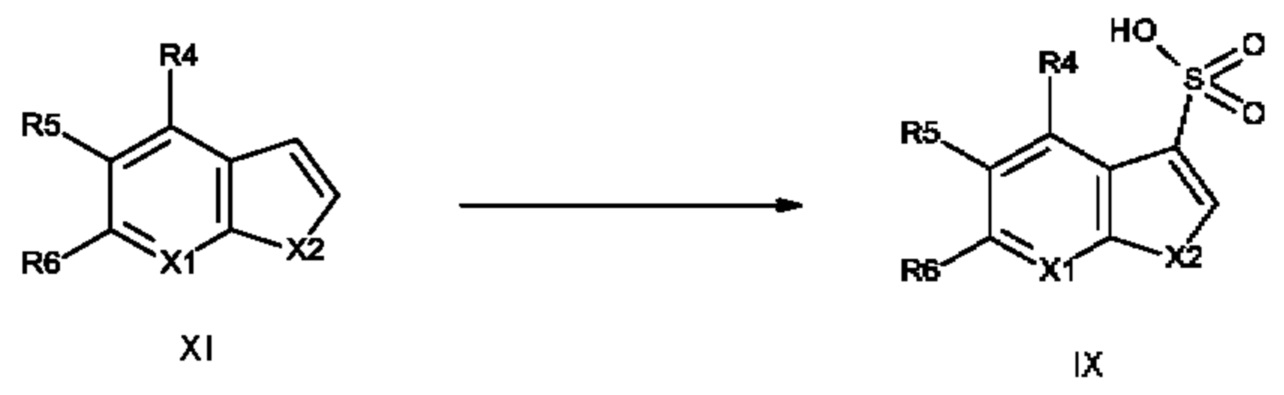
Эту реакцию можно провести в присутствии сульфонилирующего реагента, такого как комплекс пиридин-триоксид серы, в присутствии основания, такого как пиридин, использующегося в качестве растворителя, при кипячении с обратным холодильником.
Альтернативно, некоторые соединения формулы XII, в которой Х2 = О, можно получить путем хлорсульфонилирования соединения формулы XI, в которой Х2 = О по уравнению:
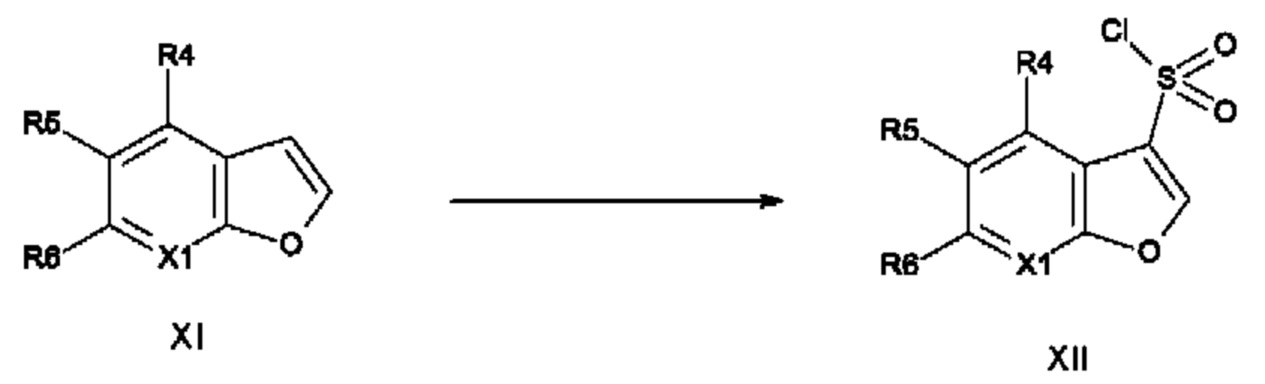
Эту реакцию можно провести в присутствии сульфонилирующего реагента, такого как комплекс триоксид серы-диметилформамид, в растворителе, таком как 1,2-дихлорэтан, при кипячении с обратным холодильником, с последующим добавлением хлорирующего реагента, такого как тионилхлорид, при температуре, находящейся в диапазоне от 60 до 80°С.
Альтернативно, некоторые соединения формулы XII, в которой Х2 = S, можно получить путем хлорсульфонилирования соединения формулы XII, в которой Х2 = S, по уравнению:
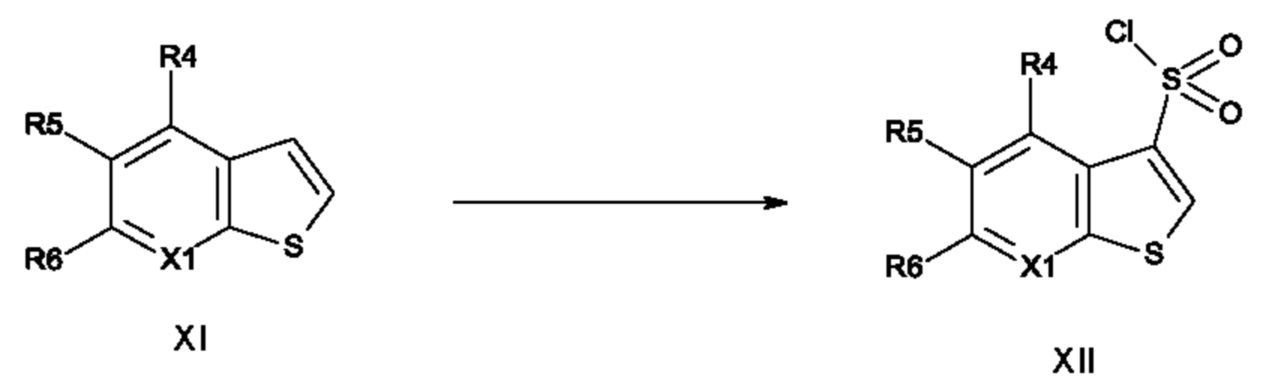
Эту реакцию можно провести в присутствии сульфонилирующего реагента, такого как хлорсульфоновая кислота, в растворителе, таком как дихлорметан, при комнатной температуре.
Соединения формулы XII-Р, в которой Р обозначает защитную группу, такую как фенилсульфонил, можно получить путем хлорсульфонилирования соединения формулы XI-P по уравнению:
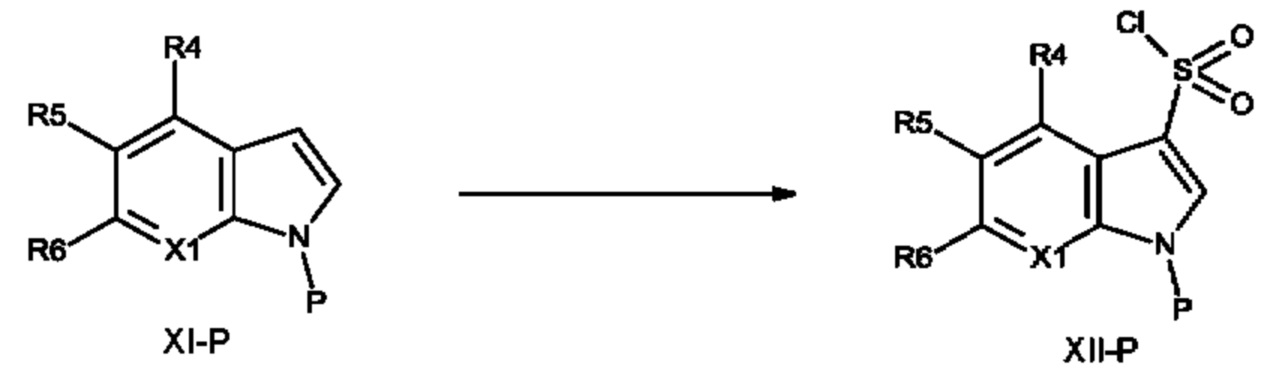
Эту реакцию можно провести в присутствии хлорсульфоновой кислоты в полярном растворителе, таком как ацетонитрил, при комнатной температуре.
Соединения формулы XI-P, в которой Р обозначает защитную группу, такую как фенилсульфонил, можно получить путем удаления защитной группы из соединения формулы XI по уравнению:
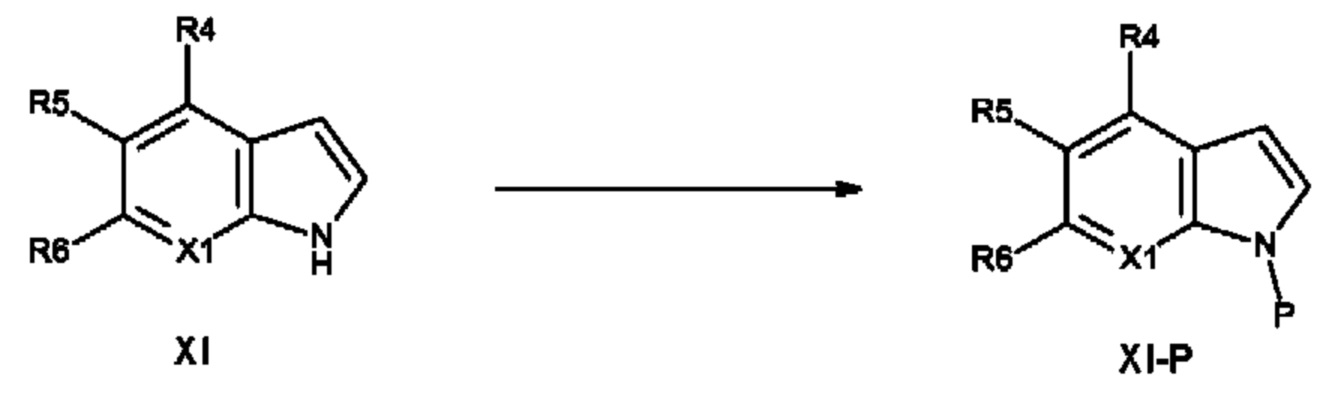
Эту реакцию можно провести по методике, известной специалисту в данной области техники.
Анилины формулы X имеются в продаже или их можно получить по любой методике, известной специалисту в данной области техники, или по методикам, описанным в литературе. Альтернативно, некоторые анилины формулы X можно получить путем восстановления соединения VIII по уравнению:
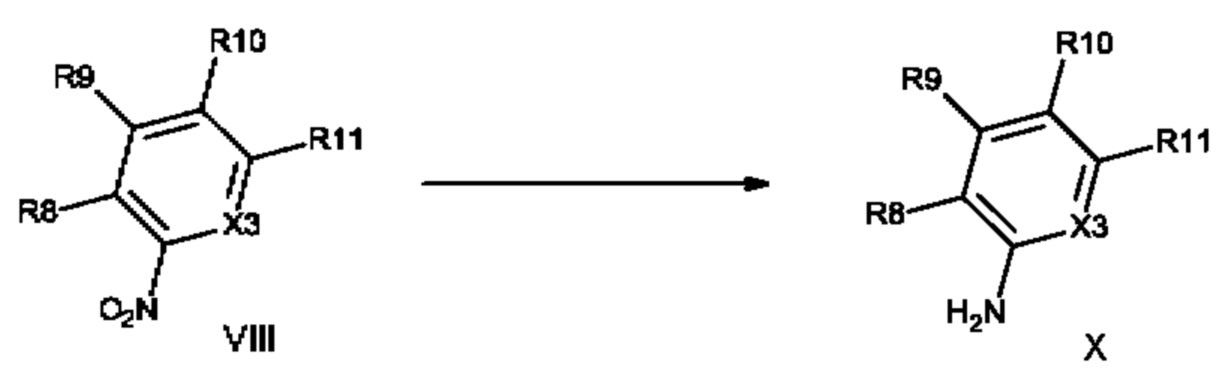
Эту реакцию можно провести с использованием любого восстановительного реагента, такого как дихлорид олова, в присутствии сильной кислоты, такой как хлористоводородная кислота, или водорода, в присутствии каталитического количества палладия на древесном угле в протонном растворителе, таком как этанол, или по любой методике, известной специалисту в данной области техники.
Соединения формулы VIII имеются в продаже или их можно получить по описанным в литературе методикам, или по любым другим методикам, известным специалисту в данной области техники.
Соединения формулы XI имеются в продаже или их можно получить по подходящим методикам, хорошо известным специалисту в данной области техники.
Альтернативно, некоторые соединения формулы XI, в которой X1 = C-R7 и в которой R7 не обозначает водород, можно получить по реакции орто-замещенного нитроарена XII с использованием винилсодержащего реагента Гриньяра XIII (синтез индола по Бартоли) по уравнению:
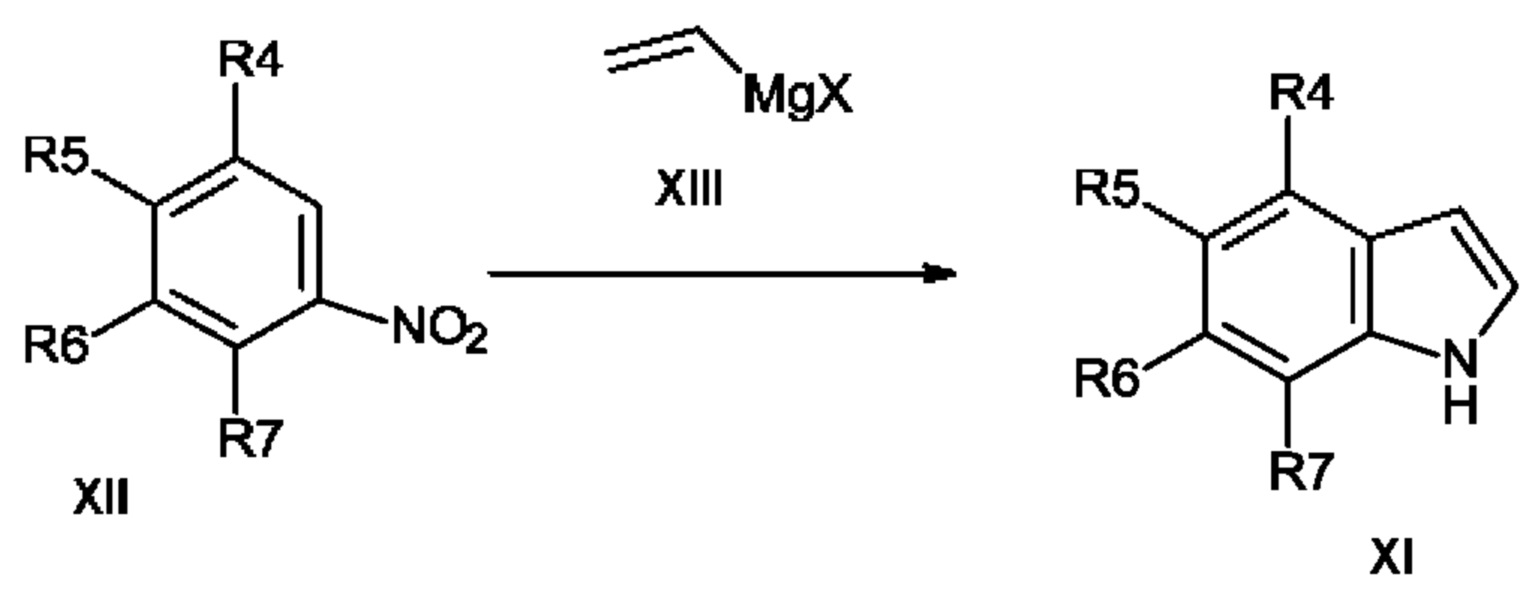
Эту реакцию можно провести с использованием винилсодержащего реагента Гриньяра, такого как винилмагнийбромид, в полярном растворителе, таком как тетрагидрофуран, при низкой температуре, такой как равная -20°С.
Альтернативно, некоторые соединения, описывающиеся общей формулой I, можно получить путем превращения функциональных групп, содержащихся в уже полученных аналогах соединений, описывающихся общей формулой I, по методикам, описанным в литературе или известным специалисту в данной области техники.
В частности, некоторые соединения формулы I, в которой R6 обозначает арильную или гетероарильную группу, можно получить по реакции сочетания типа реакции Судзуки из соединения формулы I, в которой R5 обозначает атом галогена, предпочтительно брома, в присутствии соответствующей бороновой кислоты, соли палладия, такой как [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий, и основания, такого как карбонат калия, в полярном растворителе, таком как диоксан, по методикам, известным специалисту в данной области техники.
Альтернативно, некоторые соединения формулы I, в которой R6 обозначает алкилсульфонильную группу, такую как метилсульфонильная группа, можно получить из соединения формулы I, в которой R5 обозначает атом галогена, предпочтительно брома, в присутствии алкилсульфината, такого как метансульфинат натрия, и соли меди, такой как йодид меди, в полярном растворителе, таком как диметилсульфоксид, при 130°С.
Альтернативно, соединения формулы I, в которой R6 обозначает S(O)Rx и Rx обозначает C1-C6-алкил, можно получить путем окисления соединения формулы I, в которой R6 обозначает SRx, Rx обладает таким же определением, как указанное выше, по любой методике, известной специалисту в данной области техники. Соединение формулы I, в которой R6 обозначает SRx, можно получить из соединения формулы I, в которой R6 обозначает атом галогена, предпочтительно брома, в присутствии алкилтиолята, соли палладия, такой как трис(дибензилидеиацетон)дипалладий(0), фосфинового лиганда, такого как Xantphos, в полярном растворителе, таком как N,N-диметилформамид, при нагревании микроволновым излучением при высокой температуре.
А-II. Аббревиатуры/многократно использовавшиеся реагенты
А-III. Методики анализа
Имеющиеся в продаже растворители и реагенты обычно использовали без дополнительной очистки, включая безводные растворители, когда это являлось целесообразным (обычно продукты Sure-Seal™, выпускающиеся фирмой Aldrich Chemical Company, или AcroSeal™, выпускающиеся фирмой ACROS Organics). Обычно за протеканием реакций следили с помощью тонкослойной хроматографии или жидкостной хроматографии-масс-спектрометрии.
Исследования с помощью масс-спектрометрии в режиме ЖХМС проводили с использованием разных методик и приборов следующим образом:
- ЖХМС в щелочной среде, методика 1:
Для анализа с помощью ЖХМС использовали масс-спектрометр с одной квадрупольной линзой QDA Waters. Этот спектрометр снабжен источником ИЭР и Acquity UPLC H-Class с детектором с диодной матрицей (от 200 до 400 нм). Сбор данных проводили в режиме полного сканирования в МС от 70 до 800 m/z, в режиме положительных ионов и при элюировании в щелочной среде. Разделение с использованием обращенной фазы проводили при 45°C с использованием колонки Waters Acquity UPLC ВЕН С18, 1,7 мкм (2,1×50 мм) для элюирования в щелочной среде. Элюирование в градиентном режиме проводили с использованием смеси вода/ACN/формиат аммония (95/5/63 мг/л) (растворитель А) и смеси ACN/вода/формиат аммония (95/5/63 мг/л) (растворитель В). Инжектируемый объем: 1 мкл. Полнопоточный режим в МС.
Программа для элюирования в щелочной среде "4 мин" (таблица 1).
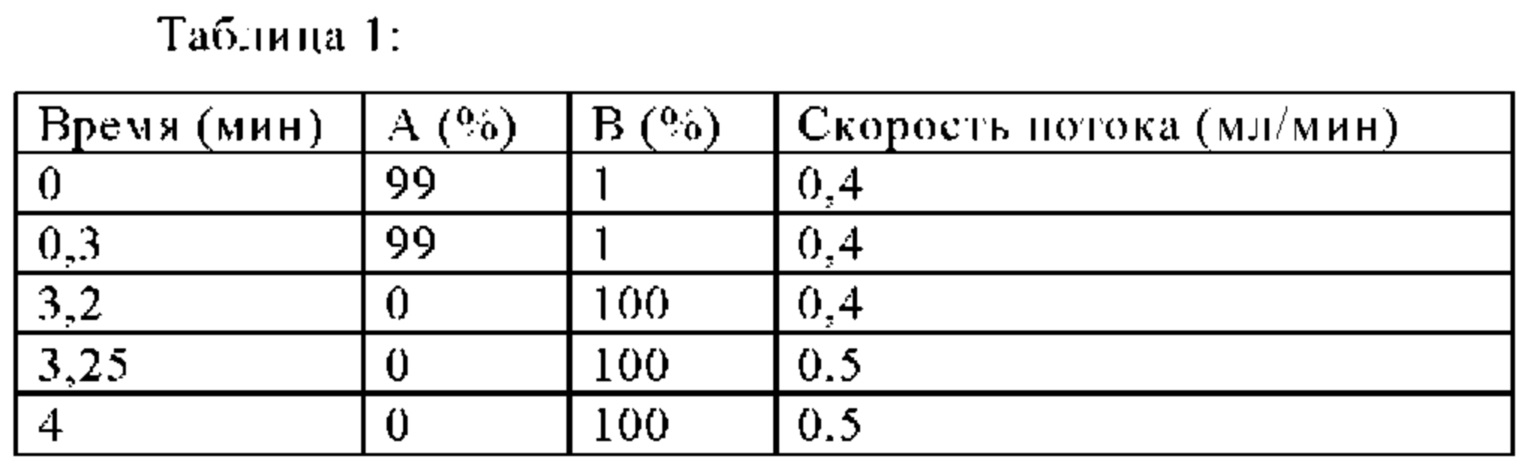
- ЖХМС в щелочной среде, методика 2:
Масс-спектры (МС) снимали с использованием ионизации электрораспылением (ИЭР) на масс-спектрометре для ЖХМС 2010EV (Shimadzu), соединенном с ВЭЖХ (высокоэффективный жидкостный хроматограф) Modular Prominence (Shimadzu), с использованием колонки Xbridge С18, 2,1×30 мм, 2,5 мкм (Waters). Инжектировали раствор образца, обладающий концентрацией, равной примерно 1 мг/мл, объемом 3 мкл. Подвижной фазой в случае щелочной среды являлась смесь А) 5 мМ формиат аммония + 0,1% аммиака в воде и В) 5% подвижной фазы А + 0,1% аммиака в ацетонитриле. Использовавшийся градиентный режим являлся следующим: от 5:95 (В/А) до 95:5 (В/А) за 4 мин и выдерживание при 95:5 (В/А) в течение следующей 1 мин.
- ЖХМС в нейтральной среде, методика 3:
Масс-спектры (МС) снимали на приборе для ЖХМС (Applied Biosystems API 2000, ЖХ/МС/МС, ВЭЖХ Agilent 1100) по следующей методике: соединения растворяли в ACN (растворитель А) или смеси вода (содержащая 2 мМ ацетат аммония):МеОН состава 90:10 (растворитель В) при концентрации, равной 1,0 мг/мл, и при необходимости обрабатывали ультразвуком до обеспечения полного растворения. Затем 10 мкл раствора инжектировали в колонку для ВЭЖХ Phenomenex Luna С18 (50×2,00 мм, размер частиц: 3 мкм) и проводили элюирование в градиентном режиме с использованием смеси вода : АСК (градиентный режим А) или смеси вода : МеОН (градиентный режим В), от смеси состава 90:10 до смеси состава 0:100 за 10 мин, элюирование в градиентном режиме начинали через 1 мин, затем элюировали чистым органическим растворителем в течение 10 мин при скорости потока, равной 300 мкл/мин. Поглощение в УФ-области определяли при длине волны, равной от 220 до 400 нм, с использованием детектора с диодной матрицей (ДДМ).
Неочищенные материалы можно очистить с помощью хроматографии с нормальной фазой, хроматографии с обращенной фазой (в кислой или щелочной среде) или путем перекристаллизации.
Хроматографию с нормальной фазой проводили с использованием колонок с силикагелем (силикагель, 100:200 меш) или картриджей для систем для проведения флэш-хроматографии, таких как Isolera™ Four, выпускающиеся фирмой Biotage®, или CombiFlash®, выпускающиеся фирмой Teledyne Isco.
Препаративную хроматографию с обращенной фазой проводили с использованием двух разных приборов и в соответствии со следующими методиками:
- Препаративная ЖХМС в щелочной среде, методика 1:
Очистку с помощью ЖХМС проводили с использованием масс-спектрометра для МС-детектирования с тремя квадрупольными линзами SQD или QM Waters. Этот спектрометр снабжен источником ИЭР и насосом для подачи четырех компонентов для препаративной ЖХ Waters с детектором с диодной матрицей (от 210 до 400 нм).
Параметры МС: Напряжение на капилляре ИЭР равно 3 кВ. Напряжение на конусе и экстракторе равно 10 В. Температура блока источника равна 120°С. Температура десольватации равна 300°С. Скорость потока газа на конусе равна 30 л/ч (азот). Скорость потока десольватирующего газа равна 650 л/ч. Сбор данных проводили в режиме полного сканирования в МС от 100 до 700 m/z, в режиме положительных ионов при элюировании в кислой среде или в щелочной среде.
Параметры ЖХ: Разделение с использованием обращенной фазы проводили при КТ с использованием колонки XBridge prep OBD С18 (5 мкм, 30×50 мм) (элюирование в щелочной среде). Элюирование в градиентном режиме проводили с использованием воды (растворитель A), ACN (растворитель В), 8 г/л бикарбоната аммония в воде + 500 мкл/л 30% NH4OH (растворитель С) (рН~8,5). ВЭЖХ, скорость потока: от 35 до 60 мл/мин, инжектируемый объем: 1 мл. Отношение деления потока для МС устанавливали равным +/- 1/6000 (таблица 2).
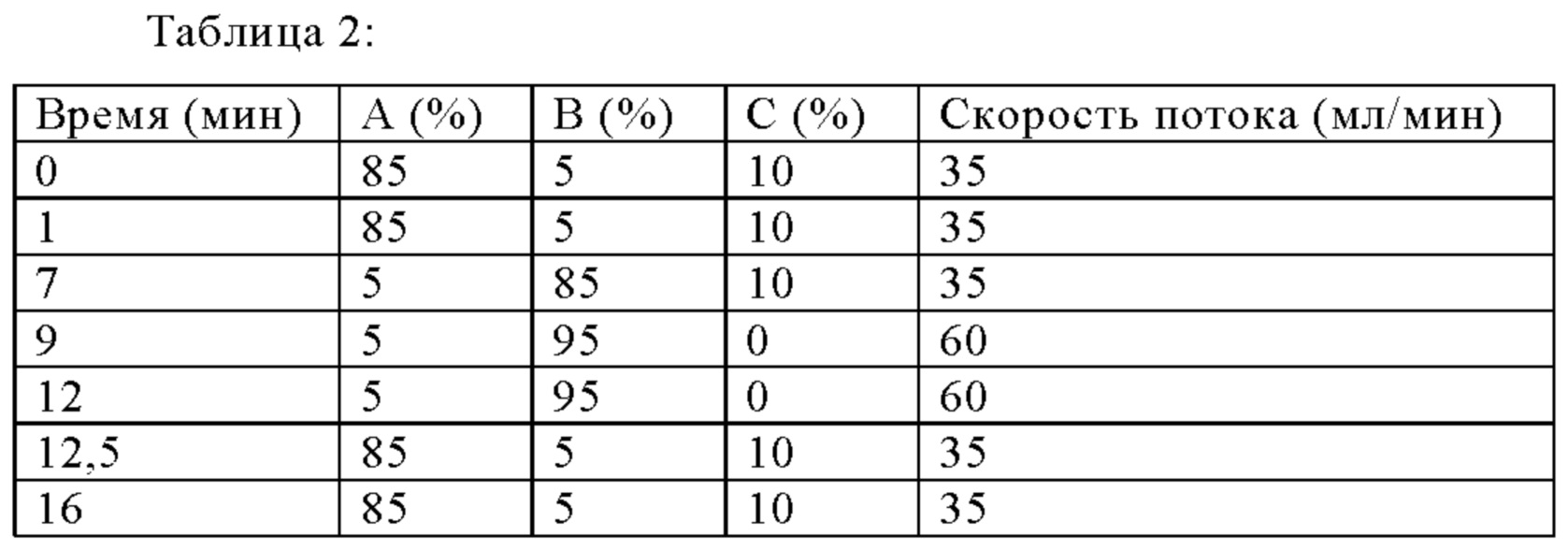
- ОФ-ВЭЖХ (высокоэффективная жидкостная хроматография с обращенной фазой) в нейтральной среде, методика 2:
Очистку конечных продуктов с помощью ВЭЖХ проводили с помощью системы для ВЭЖХ Knauer Smartline 1050, с использованием колонки для ОФ-ВЭЖХ (Knauer, ВД (внутренний диаметр) = 20 мм, Eurospher-100 С18). Продукт растворяли в метаноле (20 мг в 8 мл) и проводили ВЭЖХ с обращенной фазой с использованием градиентного режима и смеси метанола/вода (от 70:30 до 100:0 в течение 24 мин).
Спектры ЯМР снимали с использованием разных приборов:
- тщательно экранированного спектрометра ЯМР BRUKER AVANCE III, 400 МГЦ, снабженном рабочей станцией Windows 7 Professional, использующей программное обеспечение Topspin 3.2, и широкополосным, 5 мм, датчиком двойного резонанса (PABBI 1H/19F-BB Z-GRD Z82021/0075) или датчиком тройного резонанса, 1 мм (PATXI 1H/D-13C/15N Z-GRD Z868301/004).
- спектрометра ЯМР Varian, 400 МГц, при времени накопления (at) = 2,0 с, задержке релаксации (d1) = 2,0 с и уширении линии (1b) = 0,5 Гц,
- спектрометра ЯМР Bruker Avance DRX, 500 МГц,
- спектрометра ЯМР Bruker Avance III, 600 МГц.
Химические сдвиги приведены относительно сигналов остаточных протонов дейтерированных растворителей (DMSO-d6, бензол-d6 или CDCl3). Химические сдвиги приведены в частях на миллион (част./млн) и константы спин-спинового взаимодействия (J) приведены в герцах (Гц). Спиновые мультиплетности указаны следующим образом: широкий (br), синглет (s), дублет (d), триплет (t), квадруплет (q) и мультиплет (m).
Перед проведением окончательных анализов и биологических исследований продуктов их обычно сушили в вакууме.
A-IV: ПРИМЕРЫ СОЕДИНЕНИЙ И СИНТЕЗ
Названия приведенных ниже соединений представляют собой названия, соответствующие нормам IUPAC (Международный союз теоретической и прикладной химии), полученные с помощью программного обеспечения Biovia Draw, Version 16.1, для промежуточных продуктов формулы X, XI, XII и с помощью программного обеспечения ACDlabs, version 14.03, для приведенных в примерах соединений формулы I.
Промежуточные продукты
А. Синтез промежуточных продуктов формулы X
А.1. Синтез 4-фтор-2,1,3-бензотиадиазол-7-амина Х-1:
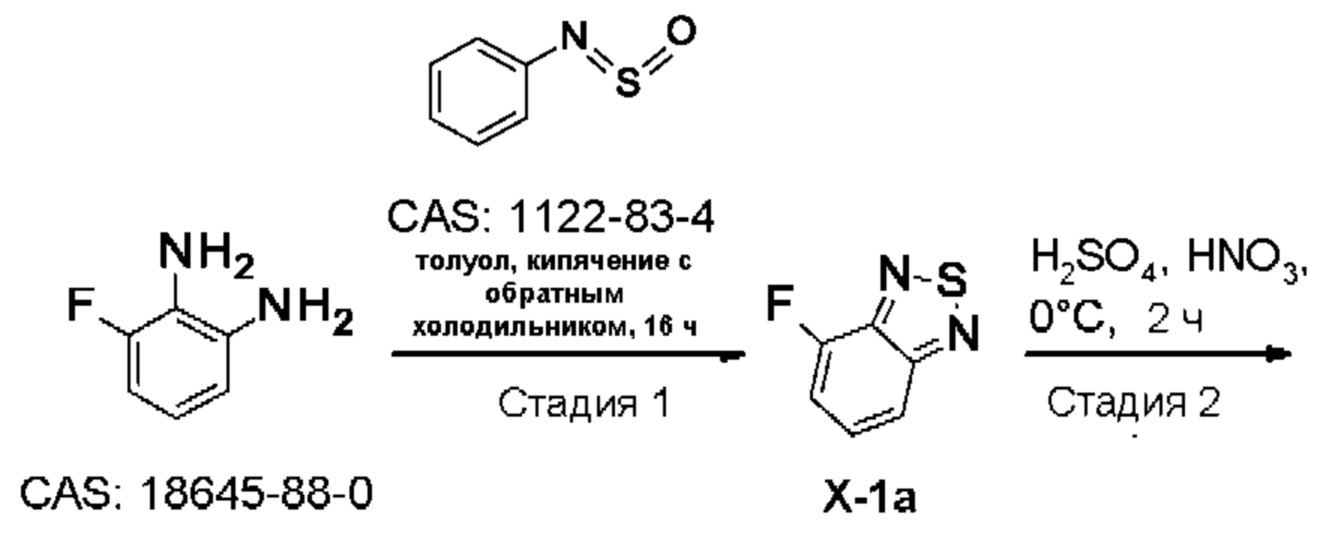
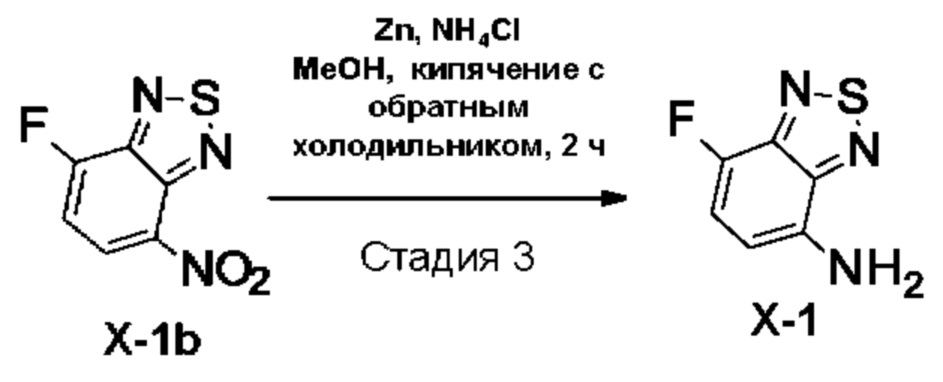
Стадия 1: Синтез 4-фтор-2,1,3-бензотиадиазола Х-1а:
К раствору 3-фторбензол-1,2-диамина (1,00 г, 7,94 ммоля) в толуоле (20 мл) добавляли (сульфиниламино)бензол (10 мл) и реакционную смесь кипятили с обратным холодильником в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь концентрировали в вакууме. Полученную неочищенную смесь очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 2% EtOAc в гексанах) и получали 4-фтор-2,1,3-бензотиадиазол Х-1а (1,06 г) в виде светло-желтой жидкости.
Выход: 87%.
1H ЯМР (400 МГц, CDCl3) δ 7,21-7,25 (m, 1Р) 7,52-7,61 (m, 1H) 7,83 (d, J=8,80 Гц, 1Н).
Стадия 2: Синтез 4-фтор-7-нитро-2,1,3-бензотиадиазола Х-1b:
К H2SO4 (12,0 мл) при 0°С по каплям добавляли дымящую HNO3 (8,00 мл) и реакционную смесь перемешивали при такой же температуре в течение 10 мин. Эту нитрующую смесь при 0°С по каплям добавляли к 4-фтор-2,1,3-бензотиадиазолу Х-1а (0,80 г, 5,19 ммоля). Реакционную смесь перемешивали при 0°С в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакцию останавливали льдом, смесь фильтровали, промывали с помощью Н2О (250 мл) и сушили в вакууме и получали 4-фтор-7-нитро-2,1,3-бензотиадиазол Х-1b (0,80 г, неочищенный) в виде желтого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3) δ 7,43 (t, J=8,56 Гц, 1H) 8,69 (dd, J=8,31, 3,91 Гц, 1Н).
Стадия 3: Синтез 4-фтор-2,1,3-бензотиадиазол-7-амина Х-1:
К раствору 4-фтор-7-нитро-2,1,3-бензотиадиазола Х-1b (0,50 г, 2,51 ммоля) в МеОН (50 мл) добавляли Zn (0,82 г, 12,5 ммоля), затем NH4Cl (1,34 г, 25,1 ммоля). Реакционную смесь кипятили с обратным холодильником в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через слой целита и фильтрат концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 10% EtOAc в гексанах) и получали 0,13 г 4-фтор-2,1,3-бензотиадиазол-7-амина Х-1 в виде желтого твердого вещества.
Выход: 30%.
ЖХМС в щелочной среде, методика 2 (ЭР+): 169,85 (М+Н)+, чистота 97%.
1Н ЯМР (400 МГц, CDCl3) δ 4,53 (brs, 2Н) 6,52 (dd, J=8,07, 3,67 Гц, 1Н) 7,05-7,14 (m, 1H).
А.2. Синтез 7-бром-2,2-дифтор-1,3-бензодиоксол-4-амина Х-2:
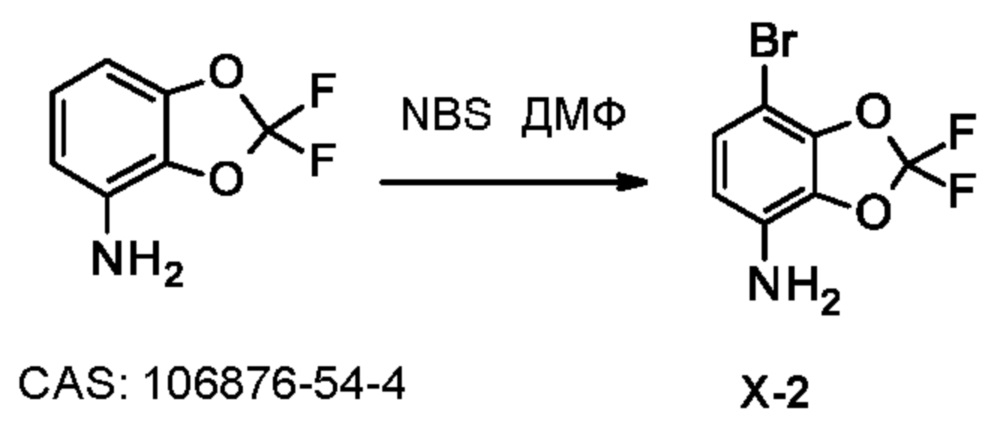
К раствору 2,2-дифтор-1,3-бензодиоксол-4-амина (0,11 г, 0,66 ммоля) в DMF (15 мл) при 0°С порциями добавляли N-бромсукцинимид (0,10 г, 0,59 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали холодной Н2О (15 мл) и смесь экстрагировали с помощью EtOAc (3×10 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 2% EtOAc в гексанах) и получали 0,1 г 7-бром-2,2-дифтор-1,3-бензодиоксол-4-амина Х-2 в виде коричневого твердого вещества.
Выход: 60%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 250,00 (М-Н)-, чистота 99%.
А.3. Синтез 5-фторбензо[с][1,2,5]тиадиазол-4-амина Х-3:
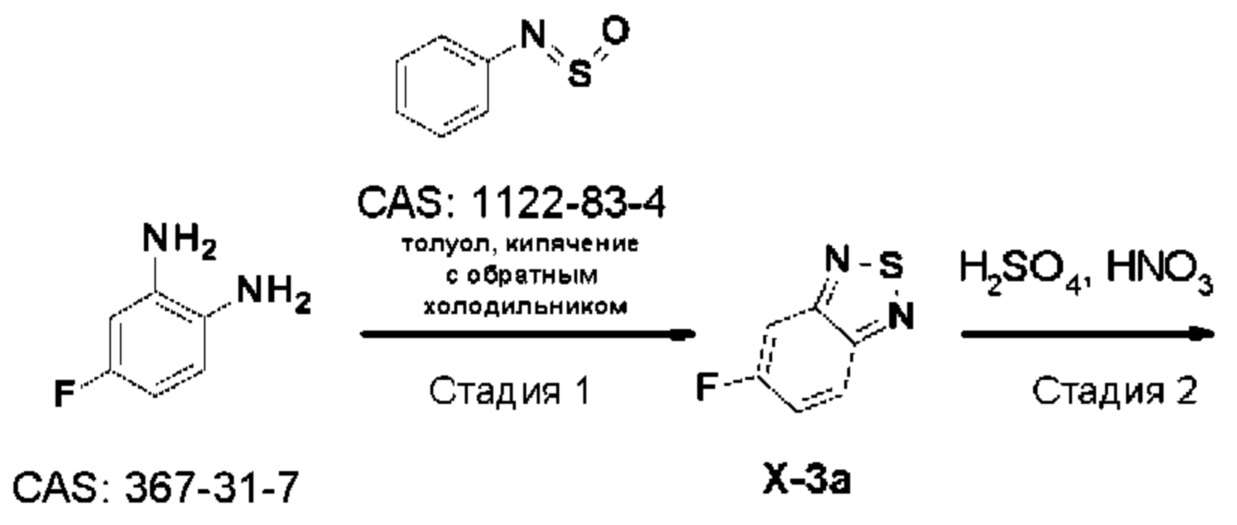
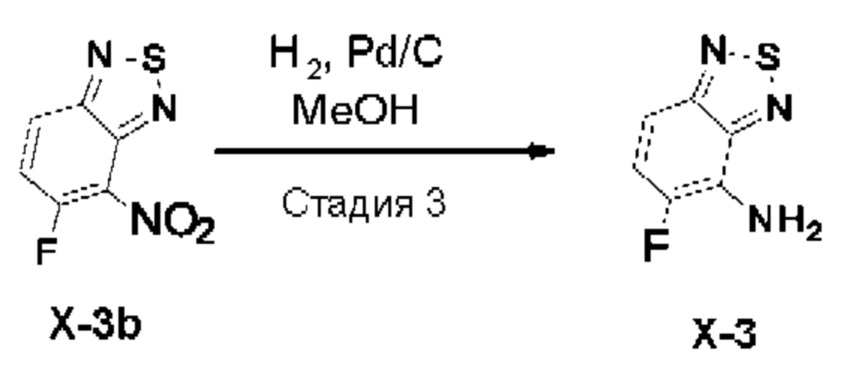
Стадия 1: Синтез 5-фторбензо[с][1,2,5]тиадиазола Х-3а:
К раствору 4-фторбензол-1,2-диамина (1,50 г, 11,9 ммоля) в толуоле (20 мл) добавляли (сульфиниламино)бензол (0,40 мл, 35,7 ммоля) и реакционную смесь кипятили с обратным холодильником в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью Н2О (150 мл) и экстрагировали с помощью EtOAc (3×150 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной флэш-хроматографии (от 0 до 3% EtOAc в гексанах) и получали 1,36 г 5-фтор-2,1,3-бензотиадиазола Х-3а в виде светло-желтой жидкости.
Выход: 74%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,67-7,73 (m, 1H) 7,92-7,95 (m, 1H) 8,15-8,19 (m, 1H).
Стадия 2: Синтез 5-фтор-4-нитро-2,1,3-бензотиадиазола Х-3b:
К раствору 5-фтор-2,1,3-бензотиадиазола Х-3а (1,00 г, 6,49 ммоля) в концентрированной H2SO4 (2 мл) при -10°С добавляли нитрующую смесь (1 мл) и реакционную смесь перемешивали при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали в охлажденную льдом Н2О (50 мл) и экстрагировали с помощью EtOAc (3×50 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной флэш-хроматографии (от 0 до 8% EtOAc в гексанах) и получали 0,66 г 5-фтор-4-нитро-2,1,3-бензотиадиазола Х-3b в виде коричневого твердого вещества.
Выход: 51%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,56 (d, J=9,78 Гц, 1Н) 8,20 (d, J=9,29 Гц, 1H).
Стадия 3: Синтез 5-фтор-2,1,3-бензотиадиазол-4-амина X-3:
К раствору 5-фтор-4-нитро-2,1,3-бензотиадиазола Х-3b (0,65 г, 3,26 ммоля) в МеОН (20 мл) добавляли Pd/C (0,30 г) и реакционную смесь перемешивали при повышенном давлении водорода при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь фильтровали через слой целита и фильтрат концентрировали в вакууме и получали 0,27 г 5-фтор-2,1,3-бензотиадиазол-4-амина Х-3 в виде оранжевого твердого вещества.
Выход: 50%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,09 (brs, 2Н) 7,16-7,20 (m, 1Н) 7,56 (t, J=10,52 Гц, 1H).
A.4. Синтез 7-амино-2,2-дифтор-1,3-бензодиоксол-5-карбонитрила X-4
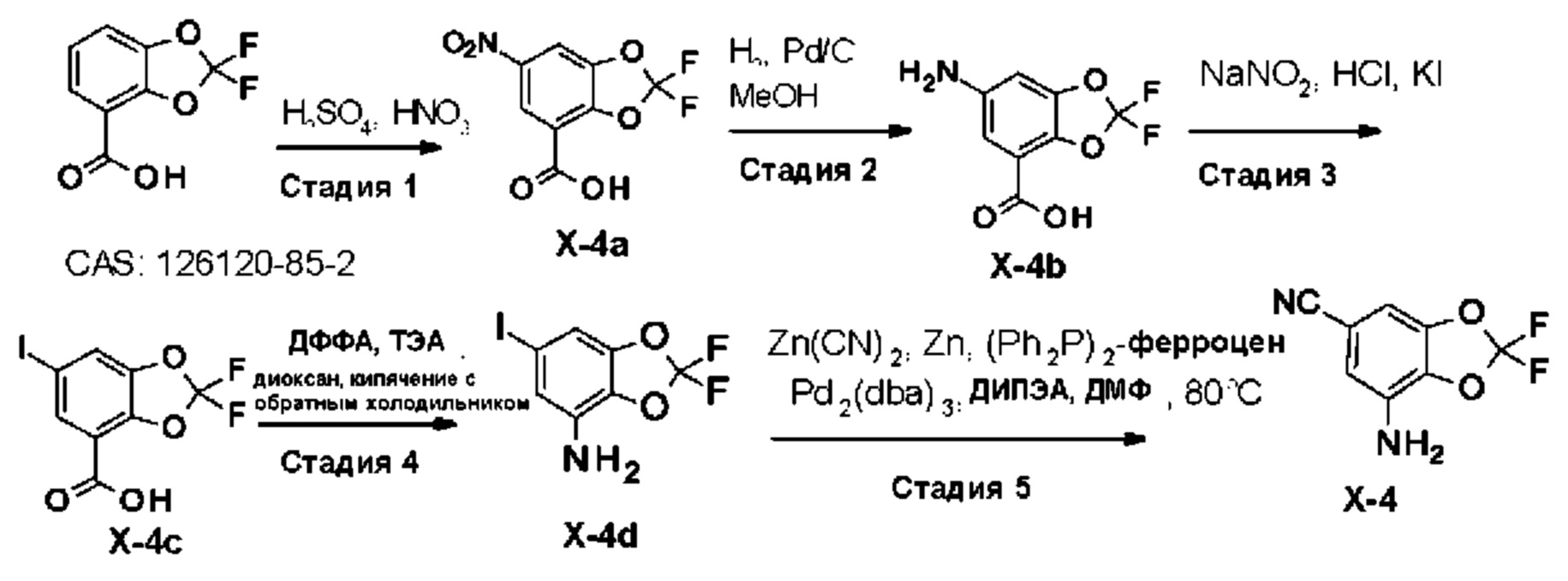
Стадия 1: Синтез 2,2-дифтор-6-нитро-1,3-бензодиоксол-4-карбоновой кислоты Х-4а:
К раствору 2,2-дифтор-1,3-бензодиоксол-4-карбоновой кислоты (10,0 г, 49,5 ммоля) в концентрированной H2SO4 (70 мл) при 0°С добавляли нитрующую смесь (концентрированная. H2SO4 : концентрированная. HNO3, 6:5, 55 мл) и реакционную смесь перемешивали при 0°С в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали на дробленый лед, фильтровали, промывали с помощью Н2О (200 мл) и сушили в вакууме и получали 2,2-дифтор-6-нитро-1,3-бензодиоксол-4-карбоновую кислоту Х-4а (9,80 г, неочищенная) в виде почти белого твердого вещества, которое использовали на следующей стадии без дополнительной очистки.
ЖХМС в щелочной среде, методика 2 (ЭР-): 245,75 (М-Н)-, чистота 73%.
1H ЯМР (400 МГц, DMSO-d6) δ 8,42 (d, J=2,45 Гц, 1Н) 8,62 (d, J=2,45 Гц, 1H) 14,34 (brs, 1H).
Стадия 2: Синтез 6-амино-2,2-дифтор-1,3-бензодиоксол-4-карбоновой кислоты X-4b:
К раствору 2,2-дифтор-6-нитро-1,3-бензодиоксол-4-карбоновой кислоты X-4а (1,00 г, 4,04 ммоля) в МеОН (25 мл) добавляли Pd/C (0,10 г) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через слой целита, промывали с помощью МеОН (40 мл) и фильтрат концентрировали в вакууме и получали 6-амино-2,2-дифтор-1,3-бензодиоксол-4-карбоновую кислоту Х-4b (0,76 г, неочищенная) в виде почти белого твердого вещества.
ЖХМС в щелочной среде, методика 2 (ЭР-): 216,00 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 5,16 (brs, 1Н) 6,48 (s, 1H) 6,70 (s, 1H) 7,28 (brs, 2H).
Стадия 3: Синтез 2,2-дифтор-6-йод-1,3-бензодиоксол-4-карбоновой кислоты Х-4с:
К раствору 6-амино-2,2-дифтор-1,3-бензодиоксол-4-карбоновой кислоты X-4b (0,75 г, 3,45 ммоля) в 6 н. растворе HCl (25 мл) при 0°С добавляли раствор NaNO2 (0,75 г, 10,3 ммоля) в Н2О (10 мл) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. При 0°С по каплям добавляли раствор KI (3,40 г, 20,7 ммоля) в Н2О (5 мл) и реакционную смесь перемешивали при такой же температуре в течение 40 мин. Реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь экстрагировали с помощью EtOAc (2×25 мл). Органический слой отделяли, промывали насыщенным раствором Na2S2O3 (2×20 мл), сушили над безводным Na2SO4 и концентрировали в вакууме и получали 2,2-дифтор-6-йод-1,3-бензодиоксол-4-карбоновую кислоту Х-4с (0,41 г) в виде бледно-желтого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 36%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,70 (d, J=1,60 Гц, 1Н) 7,91 (d, J=1,60 Гц, 1H).
Стадия 4: Синтез 2,2-дифтор-6-йод-1,3-бензодиоксол-4-амина X-4d: К раствору 2,2-дифтор-6-йод-1,3-бензодиоксол-4-карбоновой кислоты Х-4 с (0,40 г, 1,21 ммоля) в диоксане (5 мл) добавляли триэтиламин (0,50 мл, 3,65 ммоля), затем добавляли дифенилфосфорилазид (0,78 мл, 3,65 ммоля). Реакционную смесь кипятили с обратным холодильником в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (20 мл), перемешивали в течение 30 мин и экстрагировали с помощью EtOAc (2×25 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме.
Полученную неочищенную смесь очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 5% EtOAc в гексанах) и получали 0,21 г 2,2-дифтор-6-йод-1,3-бензодиоксол-4-амина X-4d в виде бесцветного полужидкого вещества.
Выход: 57%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 298,00 (М-Н)-, чистота 84%.
Стадия 5: Синтез 7-амино-2,2-дифтор-1,3-бензодиоксол-5-карбонитрила X-4:
К раствору 2,2-дифтор-6-йод-1,3-бензодиоксол-4-амина X-4d (5, 0,20 г, 0,66 ммоля) в DMF (3 мл) добавляли Zn (0,002 г, 0,03 ммоля), Zn(CN)2 (0,08 г, 0,73 ммоля), (Ph2P)2-ферроцен (0,04 г, 0,06 ммоля) и DIPEA (0,11 мл, 0,66 ммоля) и реакционную смесь продували аргоном в течение 10 мин. Добавляли Pd2(dba)3 (0,03 г, 0,04 ммоля) и реакционную смесь нагревали при 80°С в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь разбавляли с помощью EtOAc (25 мл), фильтровали через слой целита и промывали с помощью Н2О (2×25 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество пропускали через диоксид кремния (100-200 меш) с использованием 20% EtOAc в гексанах и получали 0,07 г 7-амино-2,2-дифтор-1,3-бензодиоксол-5-карбонитрила Х-4 в виде бледно-желтого твердого вещества.
Выход: 53%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,72 (s, 2Н) 7,80 (s, 1Н) 7,87 (s, 1H).
A.5. Синтез 5-фтор-2,1,3-бензотиадиазол-6-амина X-5
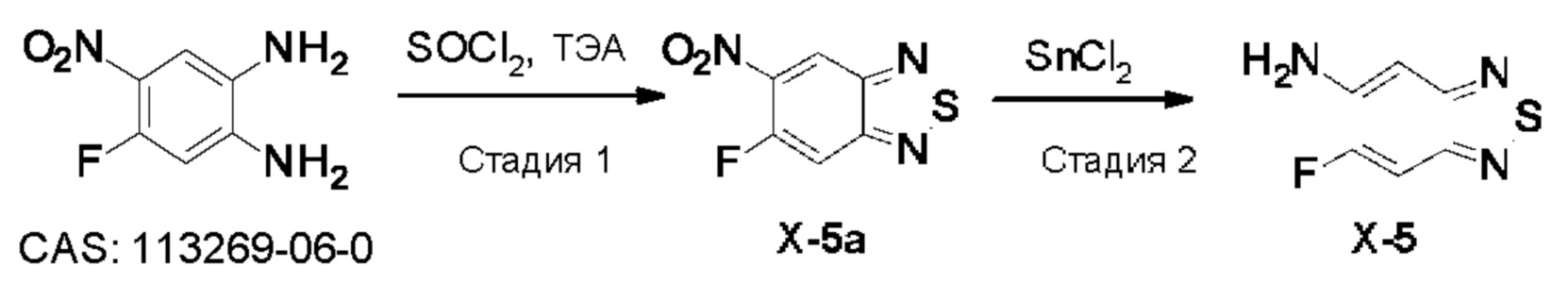
Стадия 1: Синтез 5-фтор-6-нитро-2,1,3-бензотиадиазола Х-5а
В круглодонную колбу добавляли 4-фтор-5-нитробензол-1,2-диамин (0,40 г, 2,30 ммоля), безводный DCM (10 мл) и триэтиламин (TEA, 1,4 мл, 1,00 ммоля). Раствор перемешивали до полного растворения диамина. При 0°С по каплям добавляли тионилхлорид (1 мл, 13,70 ммоля). Затем реакционную смесь нагревали при 40°С в течение 3 ч. Затем смесь охлаждали до комнатной температуры и концентрировали при пониженном давлении. Добавляли воду и затем смесь экстрагировали с помощью DCM (20 мл×3). Органические слои объединяли и сушили над MgSO4. Растворитель выпаривали и получали 5-фтор-6-нитро-2,1,3-бензотиадиазол Х-5а в виде желтого твердого вещества (0,37 г).
Выход: 95%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 200,0 (М+Н)+, чистота 89%.
Стадия 2: Синтез 5-фтор-2,1,3-бензотиадиазол-6-амина Х-5
К раствору 5-фтор-6-нитро-2,1,3-бензотиадиазола Х-5а (0,35 г, 1,75 ммоля) в смеси диоксана (7 мл) и этанола (7 мл) при КТ добавляли твердый SnCl2 (1,8 г, 9,50 ммоля), затем воду (0,35 мл). Реакционную смесь нагревали при 50°С и перемешивали в течение 30 мин, охлаждали до комнатной температуры, концентрировали и подвергали распределению между этилацетатом и 1 н. раствором NaOH. Органический слой промывали 1 н. раствором NaOH, водой и рассолом и затем сушили над MgSO4. Растворитель выпаривали и остаток очищали на силикагеле при элюировании смесью петролейный эфир/EtOAc (3/1) и получали 5-фтор-2,1,3-бензотиадиазол-6-амин Х-5 в виде желтого порошкообразного вещества (0,21 г).
Выход: 68%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 170,1 (М+Н)+, чистота 93%.
А.6. Синтез 4-амино-2,1,3-бензоселенодиазола Х-6
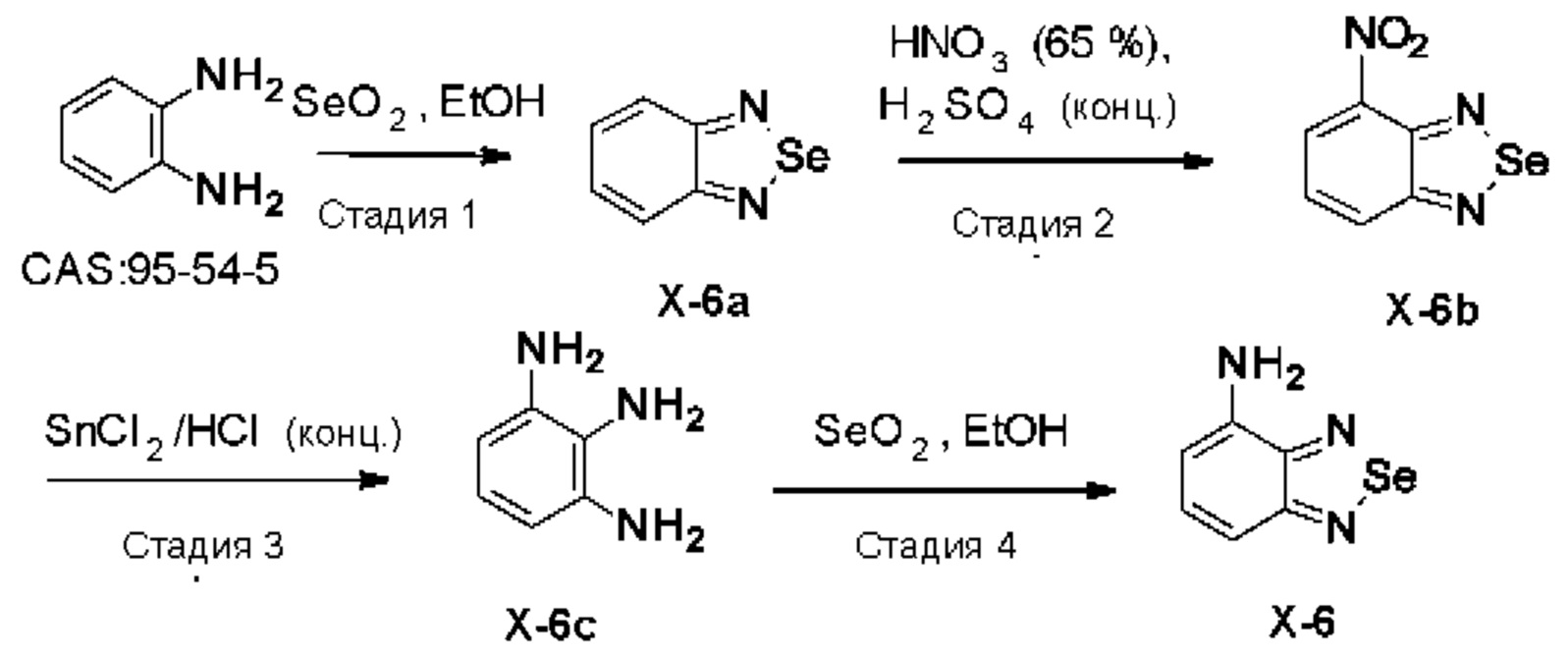
Стадия 1: Синтез 2,1,3-бензоселенадиазола Х-6а
Смесь о-фенилендиамина (10,5 г, 97,1 ммоля) и диоксида селена (11,85 г, 106,8 ммоля) в этаноле (100 мл) кипятили с обратным холодильником в течение 10 мин. Реакционную смесь охлаждали до комнатной температуры и примерно 90% растворителя выпаривали при пониженном давлении. Затем 2,1,3-бензоселенадиазол Х-6а осаждали путем добавления воды (50 мл) и отфильтровывали при пониженном давлении и получали 17,8 г бежевого твердого вещества.
Выход: 85%.
1H ЯМР: (500 МГц, DMSO-d6) δ: 7,99-7,69 (m, 2Н), 7,60-7,43 (m, 2Н).
Чистота > 95%, рассчитана на основании данных1Н ЯМР.
Стадия 2: Синтез 4-нитро-2,1,3-бензоселенадиазола Х-6b
2,1,3-Бензоселенадиазола Х-6а (6,7 г, 36,6 ммоля) растворяли в концентрированной серной кислоте и охлаждали до 0°С. Затем добавляли смесь 65% азотной кислоты (3,8 мл) и концентрированной серной кислоты (7,23 мл). Раствор перемешивали при комнатной температуре в течение 30 мин и затем разбавляли избытком воды со льдом. Желтый осадок (4-нитро-2,1,3-бензоселенадиазол Х-6b) отфильтровывали и промывали водой. Соединение получали с количественным выходом.
Выход: 100%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 8,44 (d, J=7,3 Гц, 1H), 8,27 (d, J=8,8 Гц, 1Н), 7,77-7,68 (m, 1H).
Чистота: 80%, рассчитана на основании данных1Н ЯМР.
Стадия 3: Синтез 1,2,3-триаминобензола Х-6с
Дигидрат хлорида олова(II) (2,22 г, 9,84 ммоля) суспендировали в концентрированной хлористоводородной кислоте. К этой суспензии порциями добавляли 4-нитро-2,1,3-бензоселенадиазол Х-6b (200 мг, 1,11 ммоля). После завершения добавления смесь кипятили с обратным холодильником в течение 5 ч. Затем элементарный селен отфильтровывали в горячем виде. Фильтрат охлаждали до комнатной температуры. Образовавшиеся желтоватые кристаллы (1,2,3-триаминобензолдигидрохлорид Х-6с) отфильтровывали при пониженном давлении, промывали этанолом и сушили и получали 1,11. г. Продукт без обработки и без дополнительной характеризации использовали на следующей стадии.
Выход: 58%.
Стадия 4: Синтез 4-амино-2,1,3-бензоселенодиазола Х-6
К раствору 1 г (5,0 ммоля) 1,2,3-триаминобензолдигидрохлорида Х-6с в воде (10 мл) при комнатной температуре добавляли раствор SeO2 (555 мг, 5,0 ммоля) в воде (15 мл). После завершения добавления реакционную смесь перемешивали в течение 15 мин и затем подщелачивали 30% водным раствором NaOH при охлаждении в бане со льдом. Полученные оранжевые иголки отфильтровывали при пониженном давлении, промывали водой и сушили. Дополнительная очистка с помощью колоночной хроматографии (элюент: чистый дихлорметан) давала 560 мг 4-амино-2,1,3-бензоселенодиазола.
Выход: 56%.
1H ЯМР (600 МГц, DMSO-d6) δ, 7,26 (dd, J=8,9, 7,2 Гц, 1Н), 6,93 (d, J=8,8 Гц, 1H), 6,35 (d, J=7,3 Гц, 1H), 5,98 (s, 2H, NH2).
Чистота > 95%, рассчитана на основании данных1Н ЯМР.
А.7. Синтез 2-(4-амино-3-фторфенил)ацетонитрила Х-7
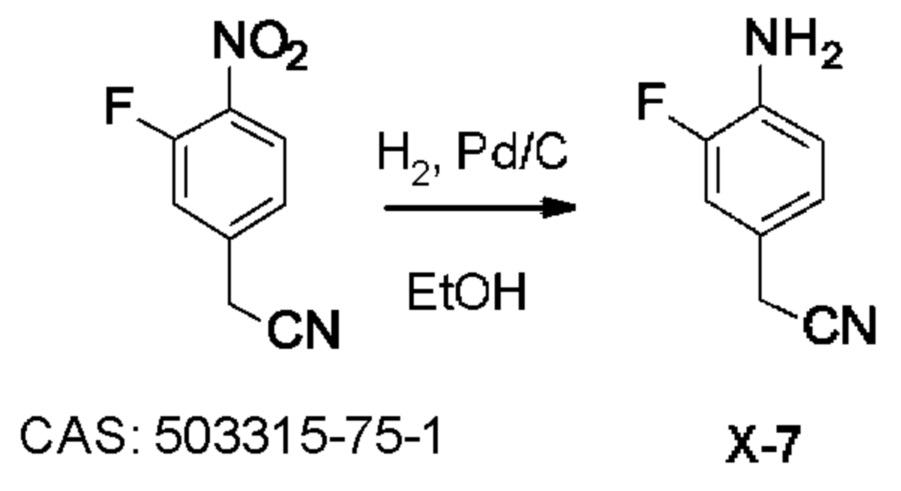
В круглодонную колбу при комнатной температуре добавляли EtOH (5 мл) и 3-фтор-4-нитрофенилацетонитрил (0,05 г, 0,28 ммоля) и 10% палладий на древесном угле (8 мг). Реакционную смесь обрабатывали с помощью Н2 при давлении, равном 35 фунт-сила/дюйм2, в течение 2 ч и затем фильтровали через слой целита и промывали с помощью EtOH. Фильтрат концентрировали в вакууме. Неочищенный продукт, 2-(4-амино-3-фторфенил)ацетонитрил Х-7, использовали на следующей стадии без дополнительной очистки.
Выход: 100%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 151,10 (М+Н)+, чистота 98%.
А.8. Синтез 2-(4-амино-3-фторфенил)пропаннитрила Х-8
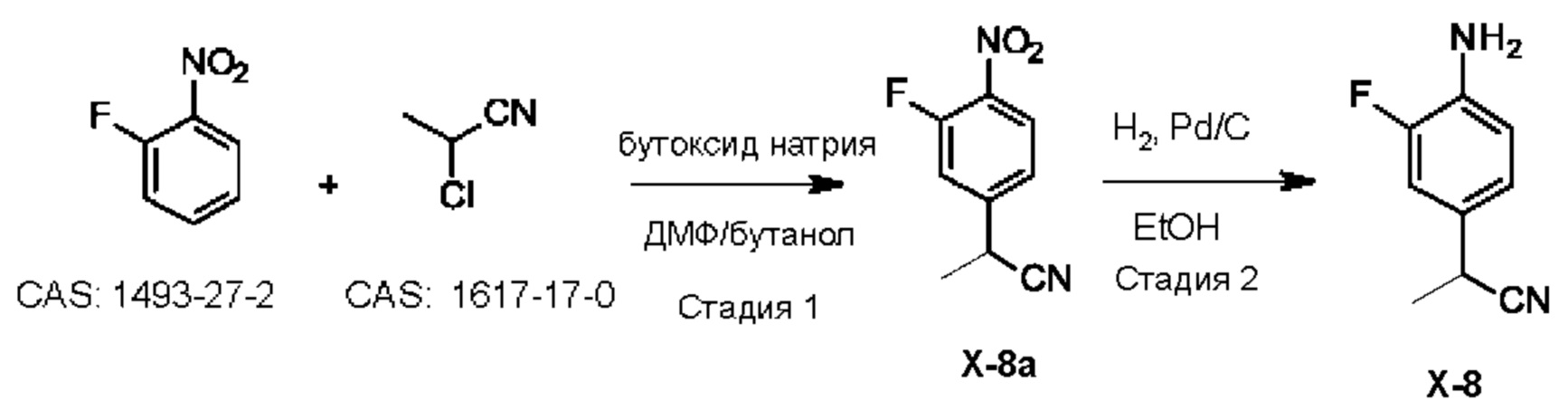
Стадия 1: Синтез 2-(3-фтор-4-нитрофенил)пропаннитрила Х-8а
В высушенную колбу помещали 2,35 г (24,45 ммоля) трет-бутоксида натрия, 5 мл трет-бутанола и 5 мл DMF. Полученный раствор охлаждали в бане из воды со льдом. К холодному раствору по каплям добавляли раствор 1,24 г (8,85 ммоля) 2-фторнитробензола и 1,10 г (12,30 ммоля) 2-хлорпропионитрила в 3 мл DMF. Полученную смеси давали реагировать при -10°С в течение 30 мин и затем выливали в 50 мл 1 н. водного раствора HCl. Водную смесь экстрагировали этилацетатом (50 мл×3) и сушили над сульфатом магния. После выпаривания растворителя остаток очищали на силикагеле при элюировании смесью петролейный эфир/EtOAc (95/5) и получали 2-(4-амино-3-фторфенил)пропионитрил (0,65 г).
1H ЯМР (600 МГц, DMSO-d6) δ 8,22 (t, J=8,2 Гц, 2Н), 7,69 (d, J=14,0 Гц, 1Н) 7,52 (d, J=8,5 Гц, 1H), 4,52 (q, J=7,2 Гц, 2H), 1,59 (d, J=7,3 Гц, 5H).
Чистота > 95%, рассчитана на основании данных1Н ЯМР.
Стадия 2: Синтез 2-(4-амино-3-фторфенил)пропаннитрила Х-8
2-(4-Амино-3-фторфенил)пропаннитрил Х-8 синтезировали по методике, описанной для синтеза соединения Х-7.
Выход: количественный выход.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 165,1 (М+Н)+, чистота 95%.
А.9. Синтез 3-амино-6-цианобензо-2,1,3-тиадиазола Х-9
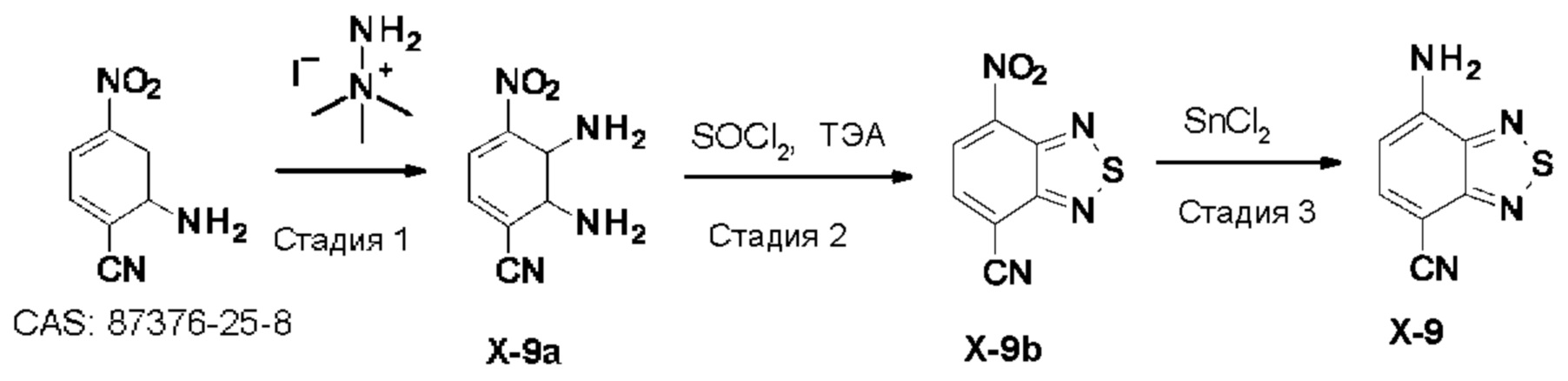
Стадия 1: Синтез 2,3-диамино-4-нитробензонитрила Х-9а
При перемешивании к раствору 2-амино-4-нитробензонитрила (0,1 г, 0,613 ммоля) в DMSO (6 мл) при комнатной температуре одной порцией добавляли 1,1,1-триметилгидразиниййодид (0,124 г, 0,613 ммоля), затем порциями добавляли трет-бутоксид калия (0,21 г, 1,84 ммоля). Реакционную смесь перемешивали при комнатной температуре в атмосфере аргона в течение ночи. Реакционную смесь выливали в смесь лед/вода, подкисляли 10% водным раствором HCl до рН 3 и экстрагировали с помощью DCM (20 мл×3). Объединенные органические слои сушили над MgSO4 и растворитель выпаривали и остаток очищали на диоксиде кремния при элюировании смесью петролейный эфир/EtOAc (2/1) и получали 2,3-диамино-4-нитробензонитрил X-9а в виде белого порошкообразного вещества (0,06 г).
Выход: 58%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 179,1 (М+Н)+, чистота 98%.
Стадии 2 и 3: 4-Амино-2,1,3-бензотиадиазол-7-карбонитрил Х-9
4-Амино-2,1,3-бензотиадиазол-7-карбонитрил Х-9 синтезировали по методике, описанной для синтеза соединения Х-5.
Выход: 42%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 176,9 (М+Н)+, чистота 98%. А. 10. Синтез 2,1,3-бензоселенадиазол-5-амина Х-10
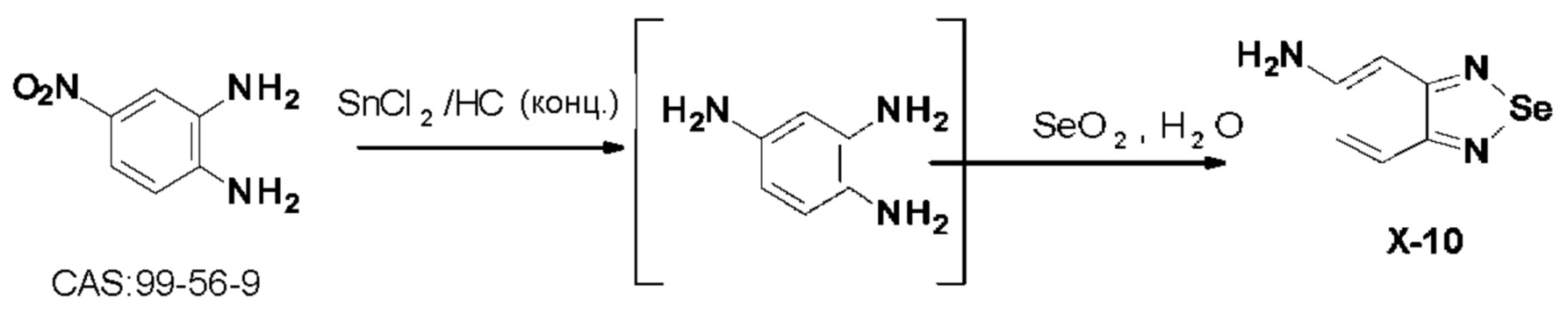
К раствору SnCl2 (5,6 г, 30 ммолей) в 10 мл концентрированной HCl при 50°С добавляли 4-нитро-орто-фенилендиамин (1,0 г, 6,53 ммоля). Смесь перемешивали при 50°С в течение 0,5 ч и охлаждали до комнатной температуры. Затем при энергичном перемешивании добавляли раствор SeO2 (0,73 г, 6,53 ммоля) в воде. Полученную оранжевую суспензию нейтрализовывали концентрированным раствором NaHCO3 (примерно 250 мл) и экстрагировали с помощью DCM (5 раз по 100 мл). Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле 60 (элюент: DCM:MeOH=9,5:0,5) и затем кристаллизовали из диэтилового эфира и получали 912 мг 2,1,3-бензоселенадиазол-5-амина Х-10 в виде оранжевых иголок.
Выход: 71%
1H ЯМР (500 МГц, DMSO-d6) δ: 7,51 (d, J=9,4 Гц, 1Н), 7,12 (dd, J=9,5, 2,2 Гц, 1H), 6,52 (d, J=2,2 Гц, 1H), 6,01 (s, 2H, NH2).
A.11. Синтез 2-(6-амино-5-метокси-3-пиридил)ацетонитрила X-11:
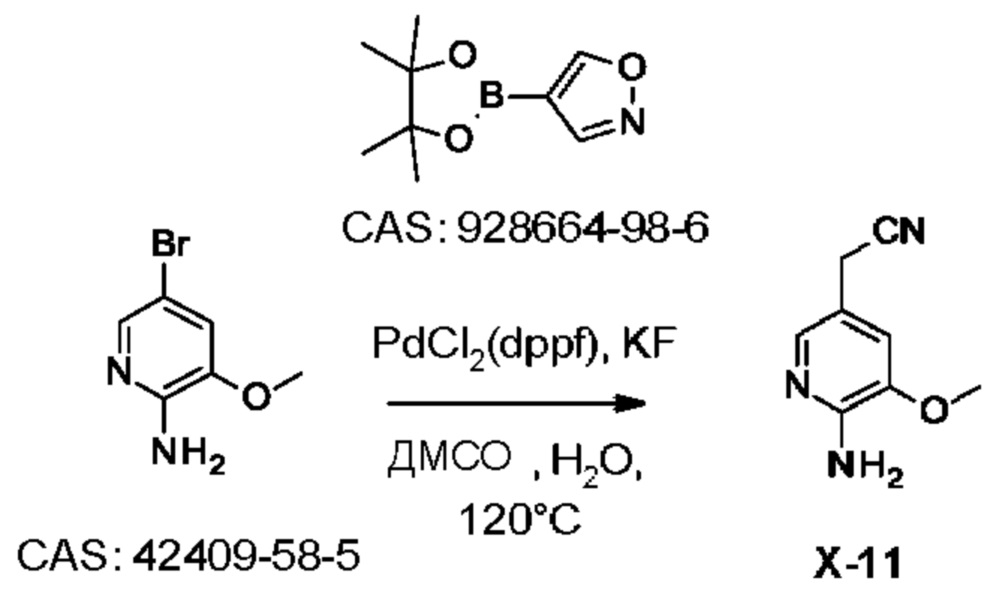
К раствору 5-бром-3-метоксипиридин-2-амина (0,20 г, 0,98 ммоля) и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)изоксазола (0,23 г, 1,18 ммоля) в DMSO (4,8 мл) добавляли раствор KF (0,17 г, 2,96 ммоля) в Н2О (2,9 мл). Реакционную смесь продували аргоном в течение 15 мин, затем добавляли PdCl2(dppf) (0,14 г, 0,19 ммоля). Реакционную смесь нагревали при 120°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через слой целита и фильтрат разбавляли водным раствором NaCl (20 мл). Водный слой экстрагировали с помощью EtOAc (2×60 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 2-(6-амино-5-метокси-3-пиридил)ацетонитрил Х-11 (0,15 г) в виде коричневого твердого вещества.
Выход: 94%
ЖХМС в щелочной среде, методика 2 (ЭР-): 164 (М-Н)-, чистота 58%.
А.12. Синтез 4-хлор-5-(дифторметокси)-2-фторанилина Х-12:
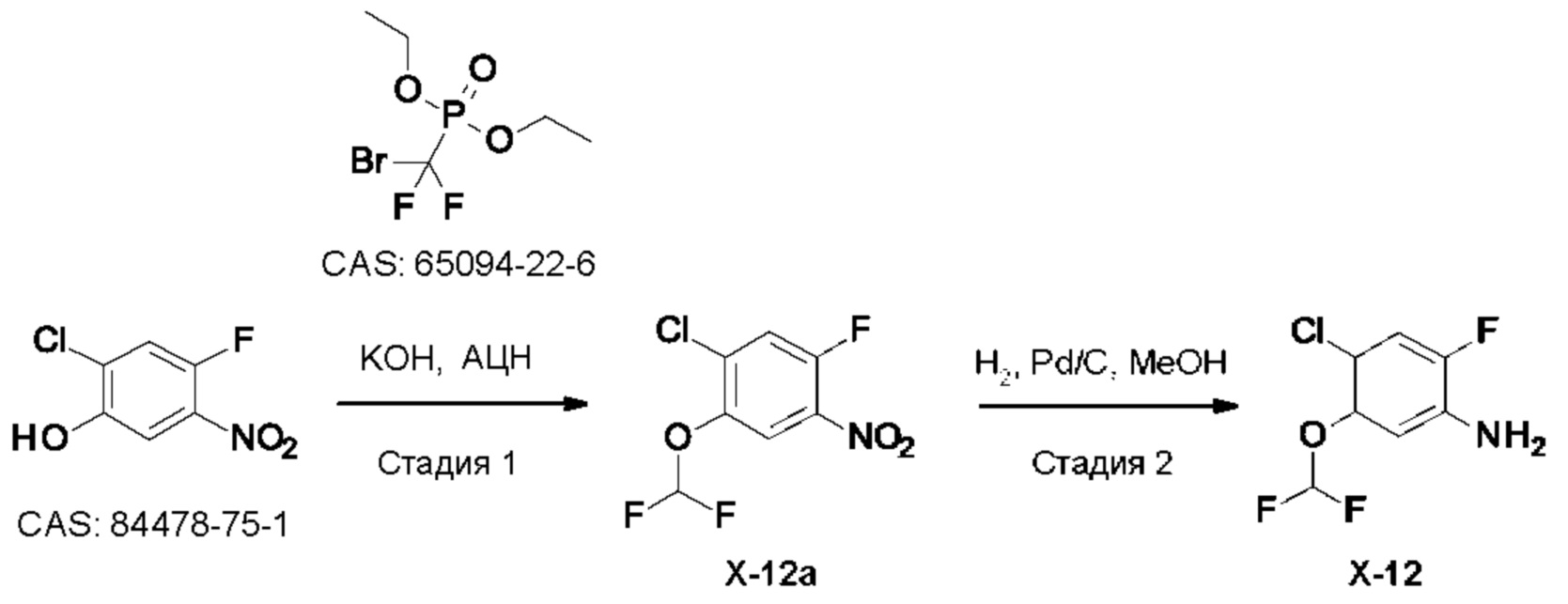
Стадия 1: Синтез 1-хлор-2-(дифторметокси)-5-фтор-4-нитробензола Х-12а:
К раствору 2-хлор-4-фтор-5-нитрофенола (0,50 г, 2,61 ммоля) в CH3CN (10 мл) при 0°С добавляли KOH (0,73 г, 13,0 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. При 0°С по каплям добавляли 1-[[бром(дифтор)метил]этоксифосфорил]оксиэтан (3,48 г, 13,0 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (20 мл) и экстрагировали с помощью EtOAc (20 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, от 0 до 6% EtOAc в гексанах) и получали 1-хлор-2-(дифторметокси)-5-фтор-4-нитробензол Х-12а (0,46 г) в виде бесцветного масла.
Выход: 73%
1H ЯМР (400 МГц, DMSO-d6) δ 7,41 (t, J=72 Гц, 1Н) 8,15 (d, J=6,80 Гц, 1H) 8,21 (d, J=6,80 Гц, 1H).
Стадия 2: Синтез 4-хлор-5-(дифторметокси)-2-фторанилина Х-12:
К раствору 1-хлор-2-(дифторметокси)-5-фтор-4-нитробензола Х-12а (0,15 г, 0,59 ммоля) в МеОН (7 мл) добавляли Pd/C (0,026 г, 0,24 ммоля) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 30 мин. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через целит и промывали с помощью МеОН (10 мл). Фильтрат концентрировали в вакууме и получали 4-хлор-5-(дифторметокси)-2-фторанилин Х-12 (0,13 г) в виде коричневого полужидкого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 80%
ЖХМС в щелочной среде, методика 2 (ЭР-): 210 (М-Н)-, чистота 78%.
А.13. Синтез 4-фтор-2,1,3-бензоксадиазол-7-амина Х-13:
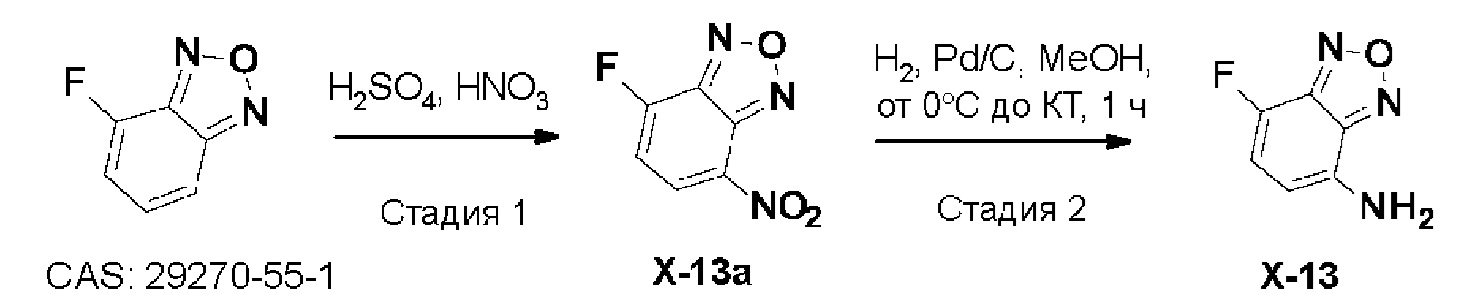
Стадия 1: Синтез 4-фтор-7-нитро-2,1,3-бензоксадиазола Х-13а:
К раствору 4-фтор-2,1,3-бензоксадиазола (1,00 г, 7,24 ммоля) в концентрированной H2SO4 (8 мл) при -10°С по каплям добавляли нитрующую смесь (H2SO4:HNO3, 3:1, 2,40 мл). Реакционную смесь перемешивали при такой же температуре в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали с помощью Н2О (250 мл) и смесь экстрагировали с помощью EtOAc (2×250 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной флэш-хроматографии (от 0 до 10% EtOAc в гексанах) и получали 4-фтор-7-нитро-2,1,3-бензоксадиазол Х-13а (0,39 г) в виде желтого твердого вещества.
Выход: 30%
1H ЯМР (400 МГц, DMSO-d6) δ 7,70 (d, J=8,40 Гц, 1Н) 8,77-8,80 (m, 1H).
Стадия 2: Синтез 4-фтор-2,1,3-бензоксадиазол-7-амина X-13:
К раствору 4-фтор-7-нитро-2,1,3-бензоксадиазола Х-13а (0,13 г, 0,71 ммоля) в МеОН (12 мл) при 0°С добавляли Pd/C (0,04 г) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через слой целита, промывали с помощью МеОН (3×10 мл). Фильтрат концентрировали в вакууме и получали 4-фтор-2,1,3-бензоксадиазол-7-амин Х-13 (0,12 г, неочищенный) в виде коричневого полужидкого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в щелочной среде, методика 2 (ЭР-): 152 (М-Н)-, чистота 80%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,18 (d, J=8,00 Гц, 1Н), 6,40 (brs, 2H), 7,14-7,20 (m, 1H).
A.14. Синтез 5-хлор-3,6-дифторпиридин-2-амина X-14:
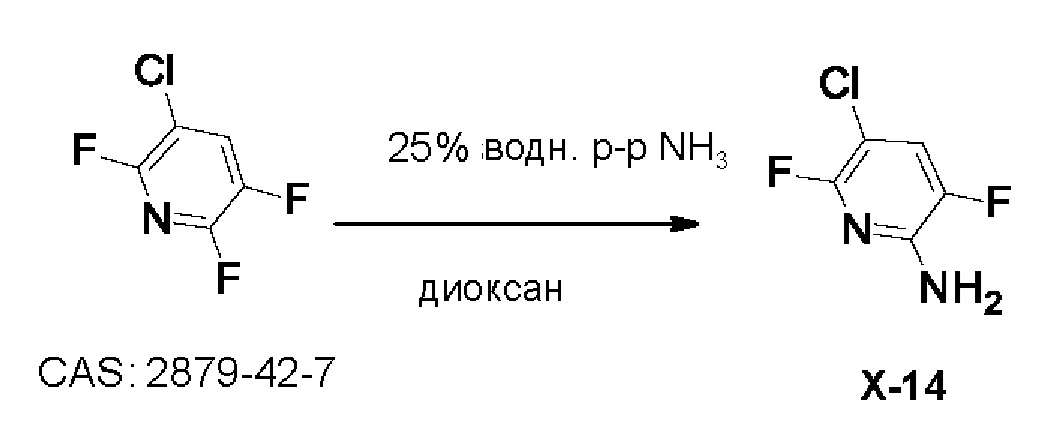
К раствору 3-хлор-2,5,6-трифторпиридина (0,50 г, 2,98 ммоля) в DMSO (10 мл) добавляли 25% водный раствор NH3 (4 мл) и реакционную смесь нагревали в стальном автоклаве при 100°С в течение 12 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (200 мл) и экстрагировали с помощью EtOAc (400 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 5-хлор-3,6-дифторпиридин-2-амин Х-14 (0,41 г, неочищенный) в виде желтого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
1H ЯМР (400 МГц, DMSO-d6) δ 6,85 (s, 2Н), 7,80-7,85 (m, 1Н).
А.15. Синтез 3,6-дифторпиридин-2-амина Х-15:
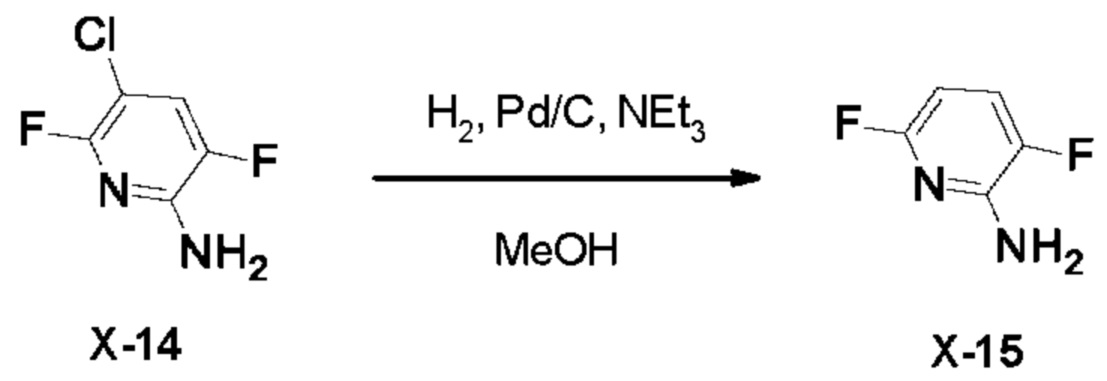
К раствору 5-хлор-3,6-дифторпиридин-2-амина Х-14 (0,50 г, 3,03 ммоля) в МеОН (100 мл) добавляли триэтиламин (5 мл) и Pd/C (0,40 г) и реакционную смесь перемешивали в аппарате Парра со встряхивающим устройством при повышенном давлении водорода, при комнатной температуре в течение 10 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через целит и фильтрат концентрировали в вакууме. Остаток разбавляли с помощью Н2О (200 мл) и экстрагировали с помощью 10% МеОН в DCM (200 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 3,6-дифторпиридин-2-амин Х-15 (0,21 г, неочищенный) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в щелочной среде, методика 2 (ЭР+): 130 (М)+, чистота 91%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,09-6,11 (m, 1Н) 6,57 (brs, 2H) 7,44-7,50 (m, 1H).
A.16. Синтез 5-бром-3,6-дифторпиридин-2-амина X-16:
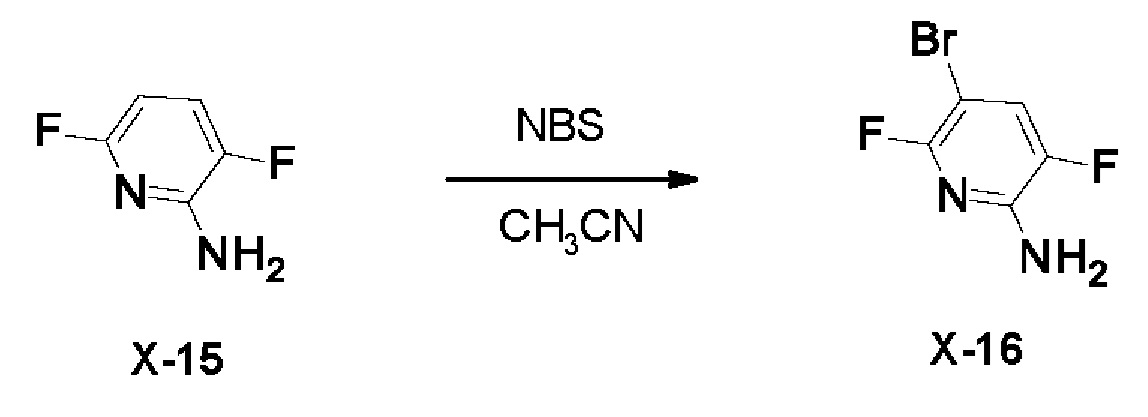
К раствору 3,6-дифторпиридин-2-амина Х-15 (0,60 г, 4,19 ммоля) в CH3CN (40 мл) добавляли NBS (0,52 г, 2,93 ммоля) и реакционную смесь перемешивали при отсутствии света при комнатной температуре в течение 30 мин. Добавляли раствор NBS (0,52 г, 2,93 ммоля) в CH3CN (10 мл) и реакционную смесь перемешивали при комнатной температуре в течение 30 мин. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью EtOAc (160 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, от 5 до 10% EtOAc в гексанах) и получали 5-бром-3,6-дифторпиридин-2-амин Х-16 (0,70 г) в виде почти белого твердого вещества.
Выход: 79%
ЖХМС в щелочной среде, методика 2 (ЭР-): 207 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,86 (brs, 2Н) 7,82-7,91 (m, 1Н).
А.17. Синтез 6-амино-5-фтор-3Н-изобензофуран-1-она Х-17:
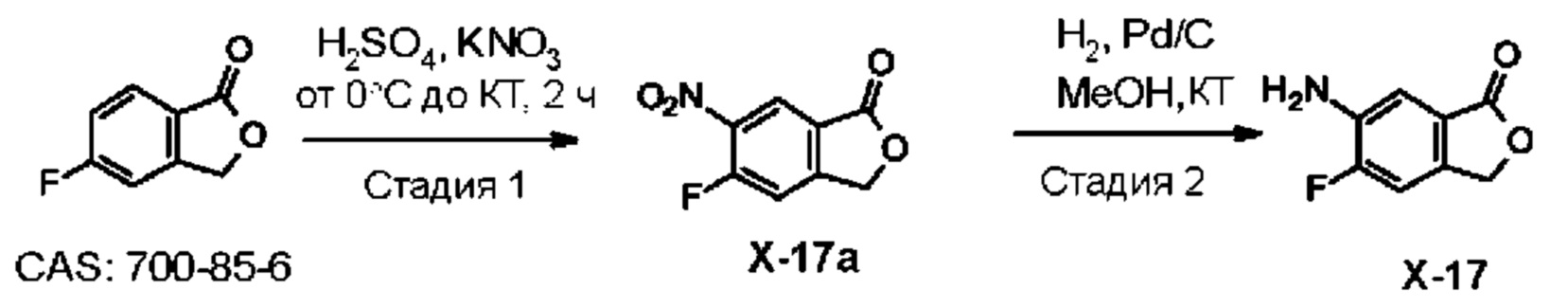
Стадия 1: Синтез 5-фтор-6-нитро-3Н-изобензофуран-1-она Х-17а:
К раствору 5-фтор-3Н-изобензофуран-1-она (0,10 г, 0,65 ммоля) в концентрированной H2SO4 (1 мл) при 0°С добавляли KNO3 (0,13 г, 1,31 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали льдом и смесь экстрагировали с помощью EtOAc (3×30 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии с использованием CombiFlash (от 15 до 20% EtOAc в гексанах) и получали 5-фтор-6-нитро-3Н-изобензофуран-1-он X-17а (0,063 г) в виде почти белого твердого вещества.
Выход: 48%
ЖХМС в щелочной среде, методика 2 (ЭР-): 196 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 5,51 (s, 2Н) 7,95 (d, J=10,27 Гц, 1Н) 8,54 (d, J=6,85 Гц, 1H).
Стадия 2: Синтез 6-амино-5-фтор-3Н-изобензофуран-1-она X-17:
К раствору 5-фтор-6-нитро-3Н-изобензофуран-1-она Х-17а (0,06 г, 0,30 ммоля) в МеОН (10 мл) добавляли Pd/C (0,015 г, 0,02 ммоля) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через целит, промывали с помощью МеОН (3×10 мл). Фильтрат концентрировали в вакууме и получали 6-амино-5-фтор-3Н-изобензофуран-1-он Х-17 (0,054 г, неочищенный) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в щелочной среде, методика 2 (ЭР-): 166 (М-Н)-, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 5,20 (s, 2Н) 5,59 (s, 2Н) 7,12 (d, J=7,83 Гц, 1Н) 7,32 (d, J=10,76 Гц, 1Н).
А.18. Синтез 4-(2,2-дифторэтокси)-2,5-дифторанилина Х-18:
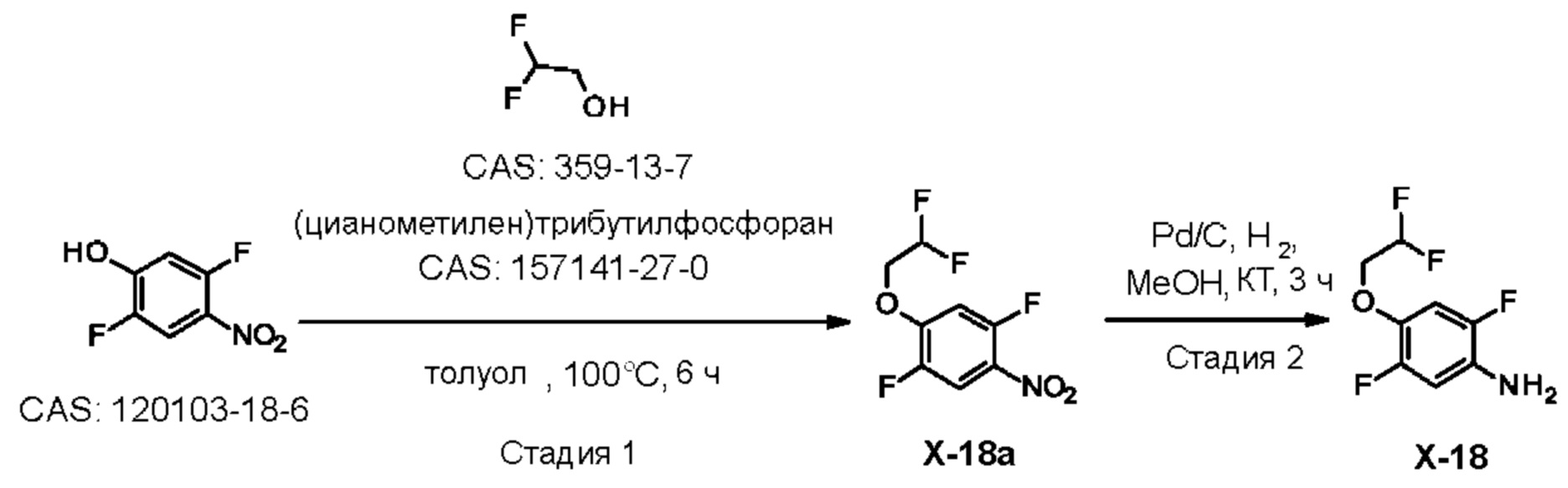
Стадия 1: Синтез 1-(2,2-дифторэтокси)-2,5-дифтор-4-нитробензола Х-18а:
К раствору 2,5-дифтор-4-нитрофенола (0,30 г, 1,71 ммоля) и 2,2-дифторэтанола (0,28 г, 3,43 ммоля) в толуоле (4 мл) добавляли (цианометилен)трибутилфосфоран (0,49 г, 2,06 ммоля) и реакционную смесь нагревали в герметизированной пробирке при 100°С в течение 6 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (30 мл) и экстрагировали с помощью EtOAc (2×30 мл). Органический слой отделяли, промывали рассолом (20 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 10% EtOAc в гексанах) и получали 1-(2,2-дифторэтокси)-2,5-дифтор-4-нитробензол Х-18а (0,20 г) в виде бледно-коричневой жидкости.
Выход: 39%
1H ЯМР (400 МГц, DMSO-d6) δ 4,54-4,68 (m, 2Н) 6,48 (t, J=54 Гц, 1Н) 7,65 (m, 1H) 8,19-8,28 (m, 1H).
Стадия 2: Синтез 4-(2,2-дифторэтокси)-2,5-дифторанилина Х-18:
К раствору 1-(2,2-дифторэтокси)-2,5-дифтор-4-нитробензола Х-18а (0,20 г, 0,67 ммоля) в МеОН (6 мл) добавляли Pd/C (0,014 г, 0,13 ммоля) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через целит, промывали с помощью МеОН (2×20 мл) и фильтрат концентрировали в вакууме и получали 4-(2,2-дифторэтокси)-2,5-дифторанилин Х-18 (0,16 г) в виде бледно-желтой жидкости. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 78%
ЖХМС в щелочной среде, методика 2 (ЭР+): 210 (М+Н)+, чистота 68%.
А.19. Синтез 3,6-дифтор-5-[(Е)-3-метоксипроп-1-енил]пиридин-2-амина Х-19:
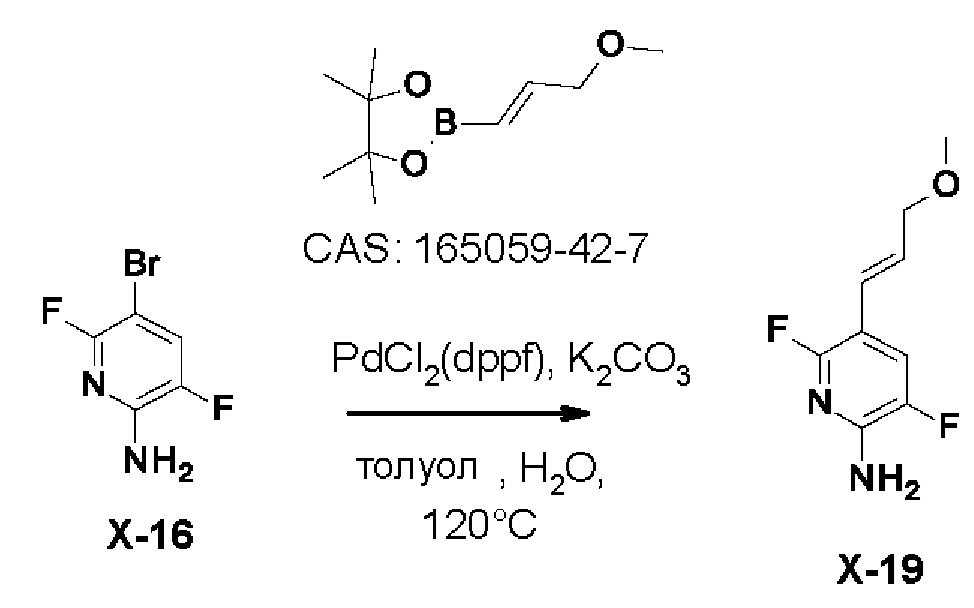
К раствору 5-бром-3,6-дифторпиридин-2-амина Х-16 (1,00 г, 4,68 ммоля) в толуоле (26 мл) и Н2О (4 мл) добавляли пинаколовый эфир транс-3-метокси-1-пропенилбороновой кислоты (1,39 г, 7,02 ммоля) и K2CO3 (1,94 г, 14,0 ммоля). Реакционную смесь продували аргоном в течение 20 мин, затем добавляли PdCl2(dppf) (0,34 г, 0,47 ммоля). Реакционную смесь нагревали при 120°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (250 мл) и экстрагировали с помощью EtOAc (500 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 40% EtOAc в гексанах) и получали 3,6-дифтор-5-[(Е)-3-метоксипроп-1-енил]пиридин-2-амин Х-19 (0,803 г) в виде почти белого твердого вещества.
Выход: 82%
ЖХМС в щелочной среде, методика 2 (ЭР+): 201 (М+Н)+, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,24 (s, 3Н) 3,98 (dd, J=5,62, 1,22 Гц, 2Н) 6,14-6,21 (m, 1H) 6,41 (dd, J=16,14, 0,98 Гц, 1H) 6,74 (s, 2Н) 7,76-7,82 (m, 1H).
А.20. Синтез 3,6-дифтор-5-(3-метоксипропил)пиридин-2-амина Х-20:
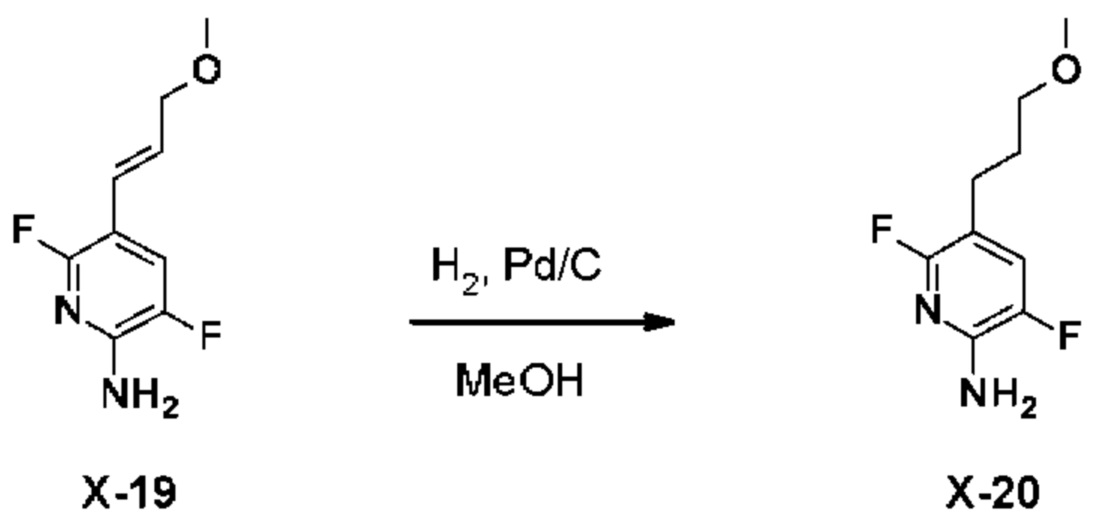
К раствору 3,6-дифтор-5-[(Е)-3-метоксипроп-1-енил]пиридин-2-амина Х-19 (0,39 г, 1,87 ммоля) в МеОН (15 мл) добавляли Pd/C (0,10 г, 0,94 ммоля) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 6 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через целит, промывали с помощью МеОН (20 мл) и фильтрат концентрировали в вакууме и получали 3,6-дифтор-5-(3-метоксипропил)пиридин-2-амин Х-20 (0,368 г) в виде желтой жидкости. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 89%
ЖХМС в щелочной среде, методика 2 (ЭР+): 203 (М+Н)+, чистота 91%.
А.21. Синтез 5-хлор-3-фтор-6-метоксипиридин-2-амина Х-21:
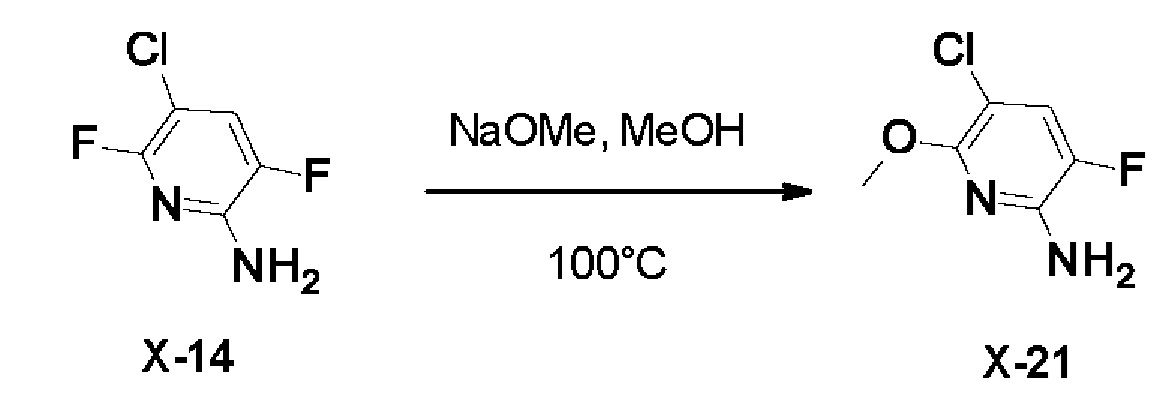
К раствору 5-хлор-3,6-дифторпиридин-2-амина Х-14 (0,50 г, 2,97 ммоля) в МеОН (25 мл) добавляли NaOMe (0,48 г, 8,92 ммоля) и реакционную смесь нагревали при 100°С в течение 24 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью DCM (200 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 5-хлор-3-фтор-6-метоксипиридин-2-амин Х-21 (0,40 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 72%
1H ЯМР (400 МГц, DMSO-d6) δ 3,80 (s, 3Н) 6,35 (s, 2Н) 7,58 (d, J=9,78 Гц, 1Н).
А.22. Синтез 2-(6-амино-5-фтор-2-метокси-3-пиридил)ацетонитрила Х-22:
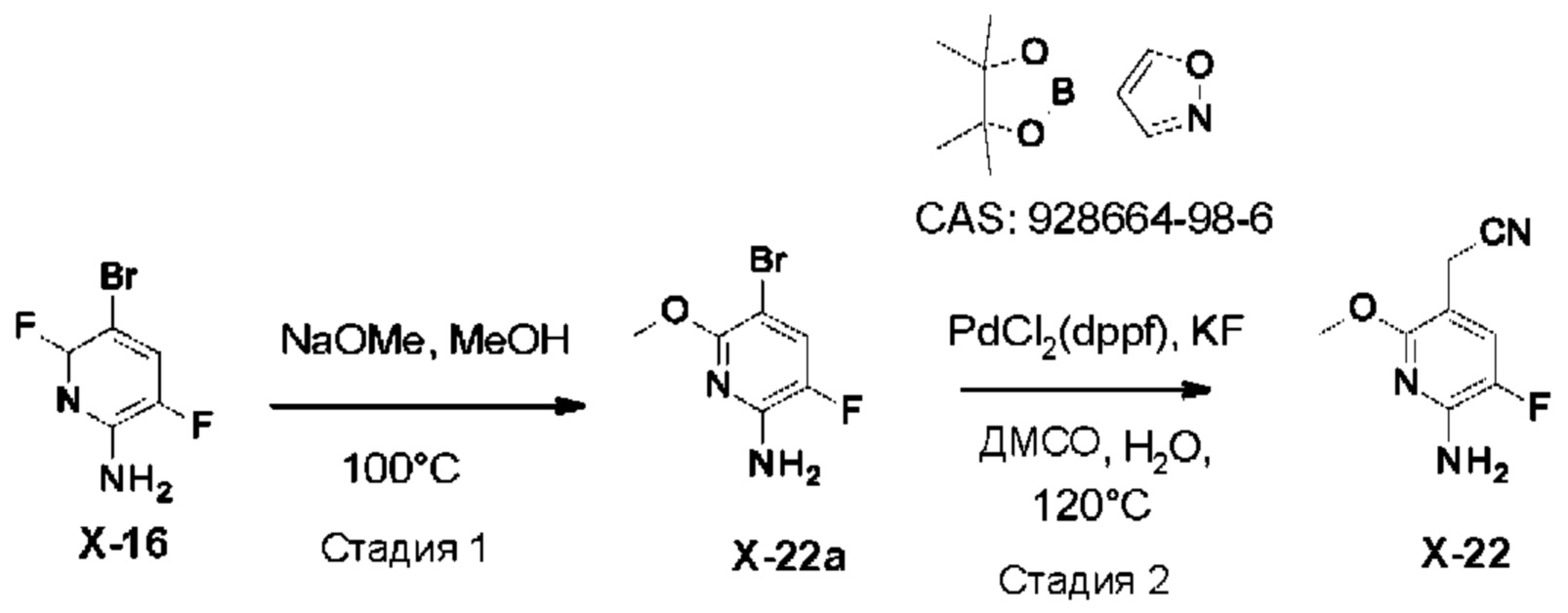
Стадия 1: Синтез 5-бром-3-фтор-6-метоксипиридин-2-амина Х-22а:
К раствору 5-бром-3,6-дифторпиридин-2-амина Х-16 (0,50 г, 2,34 ммоля) в МеОН (25 мл) добавляли NaOMe (0,38 г, 7,02 ммоля) и реакционную смесь нагревали при 100°С в течение 18 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью DCM (200 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, от 5 до 10% EtOAc в гексанах) и получали 5-бром-3-фтор-6-метоксипиридин-2-амин Х-22а (0,403 г) в виде почти белого твердого вещества.
Выход: 71%
ЖХМС в щелочной среде, методика 2 (ЭР+): 221 (М+Н)+, чистота 91%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,79 (s, 3Н) 6,39 (s, 2Н) 7,63-7,69 (m, 1H).
Стадия 2: Синтез 2-(6-амино-5-фтор-2-метокси-3-пиридил)ацетонитрила Х-22:
К раствору 5-бром-3-фтор-6-метоксипиридин-2-амина Х-22а (0,37 г, 1,52 ммоля) и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)изоксазола (0,39 г, 1,97 ммоля) в DMSO (8 мл) и Н2О (4,54 мл) добавляли KF (0,27 г, 4,56 ммоля) и реакционную смесь продували аргоном в течение 20 мин. Добавляли PdCl2(dppf) (0,22 г, 0,30 ммоля) и реакционную смесь нагревали при 110°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью EtOAc (200 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 40% EtOAc в гексанах) и получали 2-(6-амино-5-фтор-2-метокси-3-пиридил)ацетонитрил Х-22 (0,135 г) в виде бледно-желтого твердого вещества.
Выход: 48%
ЖХМС в щелочной среде, методика 2 (ЭР+): 182 (М+Н)+, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,61 (s, 2Н) 3,79 (s, 3Н) 6,22 (s, 2Н) 7,36 (d, J=10,34 Гц, 1Н).
А.23. Синтез 2-(4-амино-2,5-дифторфенокси)ацетонитрила Х-23:
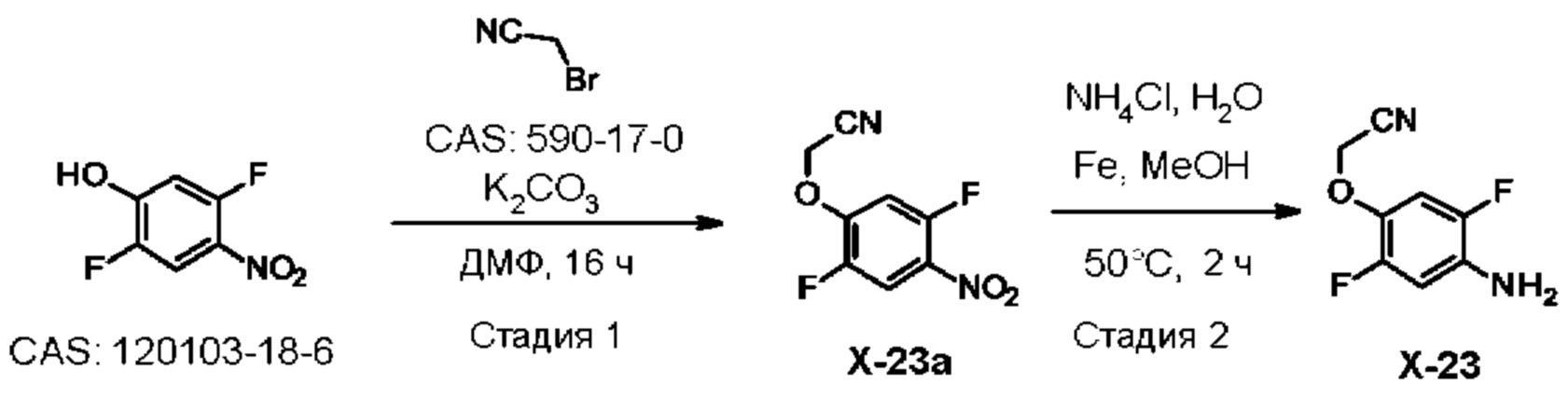
Стадия 1: Синтез 2-(2,5-дифтор-4-нитрофенокси)ацетонитрила Х-23а:
К раствору 2,5-дифтор-4-нитрофенола (0,60 г, 3,43 ммоля) в DMF (6 мл) добавляли K2CO3 (0,95 г, 6,85 ммоля). Реакционную смесь охлаждали до 0-5°С, затем медленно добавляли бромацетонитрил (0,29 мл, 4,11 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали в охлажденную льдом Н2О (35 мл) и экстрагировали с помощью EtOAc (2×50 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 2-(2,5-дифтор-4-нитрофенокси)ацетонитрил Х-23а (0,51 г) в виде коричневого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 70%
1H ЯМР (400 МГц, DMSO-d6) δ 5,93 (s, 2 H) 7,66-7,70 (m, 1 H) 8,23-8,27 (m, 1H).
Стадия 2: Синтез 2-(4-амино-2,5-дифторфенокси)ацетонитрила X-23:
К суспензии NH4Cl (0,63 г, 11,7 ммоля) и Fe (0,39 г, 7,01 ммоля) в H2O (15 мл) добавляли раствор 2-(2,5-дифтор-4-нитрофенокси)ацетонитрила Х-23а (0,50 г, 2,34 ммоля) в МеОН (28 мл). Реакционную смесь нагревали при 50°С в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь фильтровали, промывали с помощью МеОН (20 мл) и фильтрат концентрировали в вакууме. Остаток экстрагировали с помощью EtOAc (2×25 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 30% EtOAc в гексанах) и получали 2-(4-амино-2,5-дифторфенокси)ацетонитрил Х-23 (0,17 г) в виде бледно-желтого твердого вещества.
Выход: 40%
1H ЯМР (400 МГц, DMSO-d6) δ 5,04 (s, 2Н) 5,22 (s, 2Н) 6,62-6,67 (m, 1Н) 7,12-7,17 (m, 1Н).
А.24. Синтез 4-(циклопропилметокси)-2,5-дифторанилина Х-24:
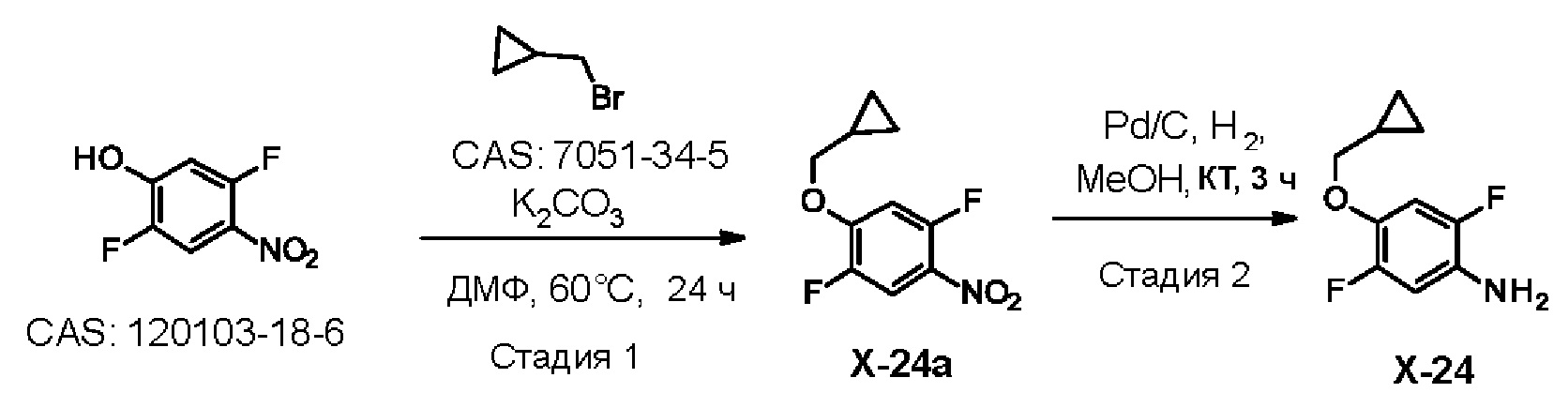
Стадия 1: Синтез 1-(циклопропилметокси)-2,5-дифтор-4-нитробензола X-24а:
К раствору 2,5-дифтор-4-нитрофенола (0,50 г, 2,86 ммоля) в DMF (3 мл) добавляли K2CO3 (1,97 г, 14,3 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 20 мин. При 0°С добавляли циклопропилметилбромид (0,77 г, 5,71 ммоля) и реакционную смесь нагревали при 60°С в течение 24 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (60 мл) и экстрагировали с помощью EtOAc (3×30 мл). Органический слой отделяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4 и концентрировали в вакууме и получали 1-(циклопропилметокси)-2,5-дифтор-4-нитробензол Х-24а (0,584 г) в виде желтой жидкости. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 89%
1H ЯМР (400 МГц, DMSO-d6) δ 0,32-0,41 (m, 2Н) 0,59-0,66 (m, 2Н) 1,22-1,34 (m, 1Н) 4,07 (d, J=7,34 Гц, 2H) 7,46 (dd, J=13,21, 6,85 Гц, 1H) 8,16 (dd, J=11,00, 7,58 Гц, 1H).
Стадия 2: Синтез 4-(циклопропилметокси)-2,5-дифторанилина X-24:
К раствору 1-(циклопропилметокси)-2,5-дифтор-4-нитробензола Х-24а (0,20 г, 0,87 ммоля) в МеОН (10 мл) добавляли Pd/C (0,05 г, 0,09 ммоля) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через целит, промывали с помощью МеОН (3×15 мл) и фильтрат концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии с использованием CombiFlash (от 5 до 10% EtOAc в гексанах) и получали 4-(циклопропилметокси)-2,5-дифторанилин Х-24 (0,127 г) в виде коричневого твердого вещества.
Выход: 62%
ЖХМС в щелочной среде, методика 2 (ЭР+): 200 (М+Н)+, чистота 84%.
А.25. Синтез 3,5-диметоксипиридин-2-амина Х-25:
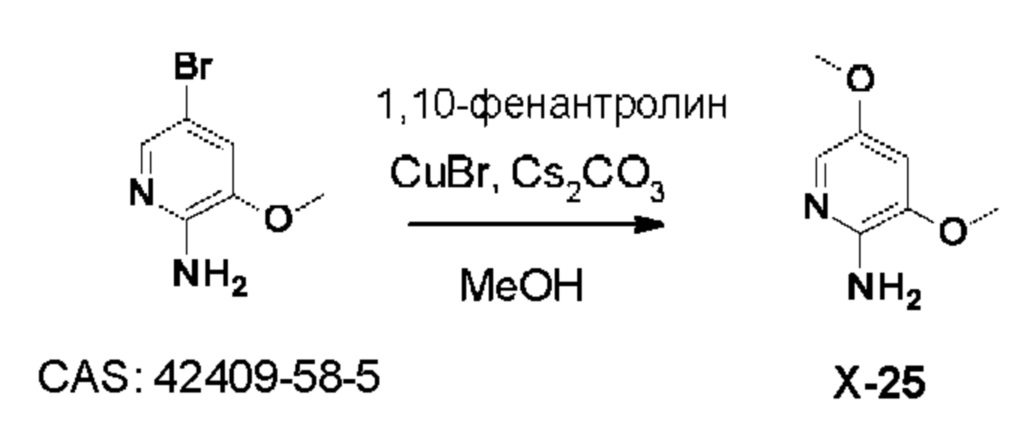
К раствору 5-бром-3-метоксипиридин-2-амина (0,50 г, 2,46 ммоля), 1,10-фенантролина (0,13 г, 0,74 ммоля) и CuBr (0,21 г, 1,48 ммоля) в МеОН (25 мл) добавляли Cs2CO3 (1,61 г, 4,93 ммоля). Реакционную смесь нагревали при 120°С в течение 24 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью H2O (50 мл) и экстрагировали с помощью EtOAc (2×40 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, от 1 до 5% МеОН в DCM) и получали 3,5-диметоксипиридин-2-амин Х-25 (0,27 г) в виде бледно-коричневой жидкости.
Выход: 57%
ЖХМС в щелочной среде, методика 2 (ЭР+): 155 (М+Н)+, чистота 80%.
А.26. Синтез 6-амино-5-фторизоиндолин-1-она Х-26:
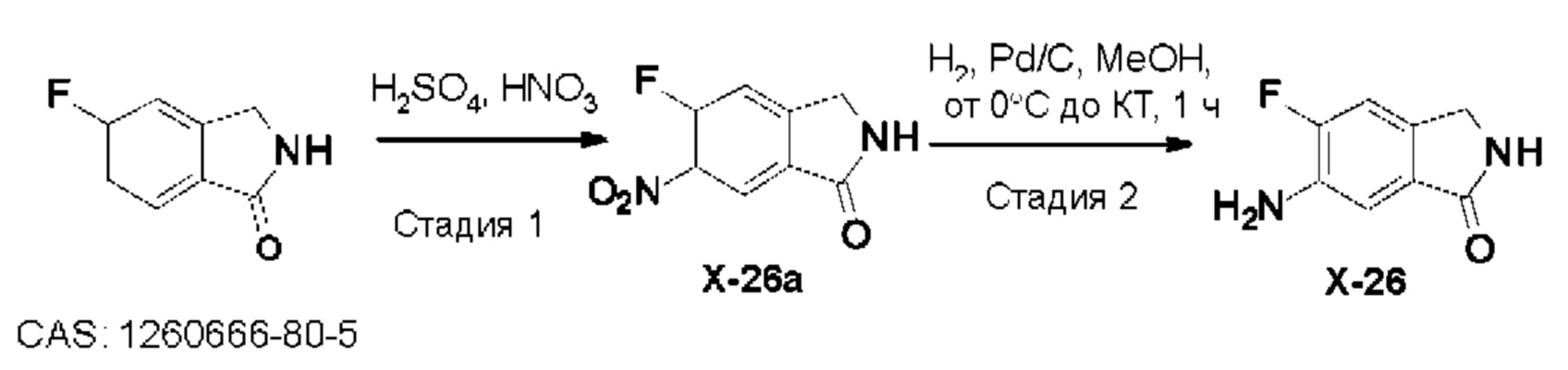
Стадия 1: Синтез 5-фтор-6-нитроизоиндолин-1-она Х-26а:
К раствору 5-фторизоиндолин-1-она (1,00 г, 6,62 ммоля) в H2SO4 (15 мл) при 0°С добавляли KNO3 (1,00 г, 9,92 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли холодной H2O (250 мл) и экстрагировали с помощью EtOAc (250 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали путем промывки с помощью DCM (4 мл) и пентана (10 мл) и сушили в вакууме и получали 5-фтор-6-нитроизоиндолин-1-он Х-26а (0,60 г) в виде почти белого твердого вещества.
Выход: 46%
ЖХМС в щелочной среде, методика 2 (ЭР-): 195 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 4,51 (s, 2Н) 7,86 (d, J=10,88 Гц, 1H) 8,29 (d, J=6,85 Гц, 1Н) 8,95 (brs, 1H).
Стадия 2: Синтез 6-амино-5-фторизоиндолин-1-она Х-26:
К раствору 5-фтор-6-нитроизоиндолин-1-она Х-26а (0,20 г, 1,02 ммоля) в МеОН (10 мл) добавляли Pd/C (0,05 г, 0,47 ммоля) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через целит, промывали с помощью МеОН (10 мл) и фильтрат концентрировали в вакууме и получали 6-амино-5-фторизоиндолин-1-он Х-26 (0,155 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 89%
ЖХМС в щелочной среде, методика 2 (ЭР+): 167 (М+Н)+, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 4,17 (s, 2Н) 5,32 (s, 2Н) 7,02 (d, J=8,31 Гц, 1Н) 7,19 (d, J=10,76 Гц, 1H) 8,33 (brs, 1H).
A.27. Синтез 6-амино-5-фтор-3-метил-3Н-изобензофуран-1-она X-27:
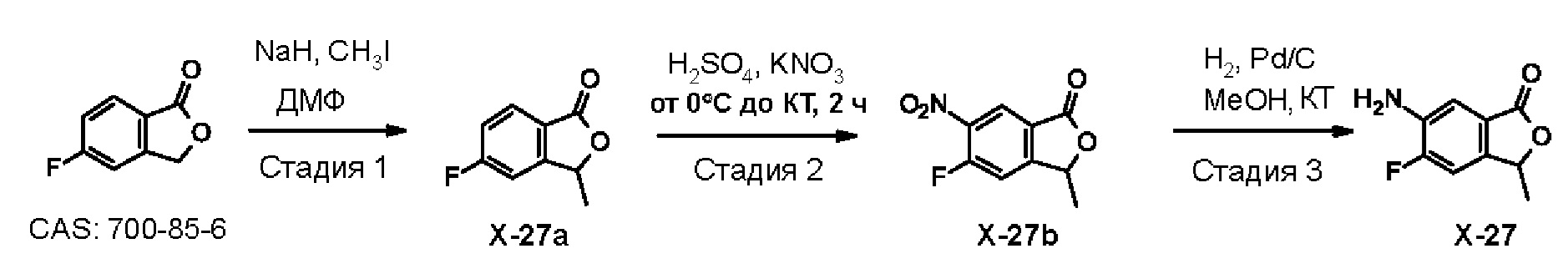
Стадия 1: Синтез 5-фтор-3-метил-3Н-изобензофуран-1-она Х-27а:
К раствору 5-фтор-3Н-изобензофуран-1-она (1,00 г, 6,57 ммоля) в DMF (5 мл) при -20°С добавляли CH3I (0,82 мл, 13,1 ммоля), затем порциями добавляли NaH (0,34 г, 7,89 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли охлажденный льдом насыщенным водным раствором NH4Cl (50 мл) и экстрагировали с помощью EtOAc (2×30 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии с использованием CombiFlash (4% EtOAc в гексанах) и получали 5-фтор-3-метил-3Н-изобензофуран-1-он Х-27а (0,44 г) в виде почти белого твердого вещества.
Выход: 35%
ЖХМС в щелочной среде, методика 2 (ЭР+): 167 (М+Н)+, чистота 87%.
1H ЯМР (400 МГц, DMSO-d6) δ 1,56 (d, J=6,36 Гц, 3Н) 5,68 (q, J=6,36 Гц, 1Н) 7,41-7,48 (m, 1H) 7,62 (dd, J=8,80, 1,96 Гц, 1H) 7,87-7,93 (m, 1H).
Стадия 2: Синтез 5-фтор-6-нитро-3-метил-3Н-изобензофуран-1-она X-27b:
К раствору 5-фтор-3-метил-3Н-изобензофуран-1-она Х-27а (0,40 г, 2,10 ммоля) в концентрированной H2SO4 (4 мл) при 0°С добавляли KNO3 (0,26 г, 2,52 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь разбавляли охлажденной льдом Н2О (25 мл) и экстрагировали с помощью EtOAc (2×20 мл). Органический слой отделяли, промывали холодным насыщенным раствором NaHCO3 (25 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии с использованием CombiFlash (от 12 до 15% EtOAc в гексанах) и получали 5-фтор-6-нитро-3-метил-3Н-изобензофуран-1-он Х-27b (0,145 г, 33%) в виде почти белого твердого вещества.
Выход: 33%
1H ЯМР (400 МГц, DMSO-d6) δ 1,61 (d, J=6,85 Гц, 3Н) 5,82 (q, J=6,85 Гц, 1Н) 8,03-8,07 (m, 1H) 8,53 (d, J=6,85 Гц, 1H).
Стадия 3: Синтез 6-амино-5-фтор-3-метил-3Н-изобензофуран-1-она X-27:
К раствору 5-фтор-6-нитро-3-метил-3Н-изобензофуран-1-она Х-27b (0,14 г, 0,66 ммоля) в МеОН (5 мл) добавляли Pd/C (0,02 г) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь фильтровали через целит, промывали с помощью EtOAc (2×10 мл) и фильтрат концентрировали в вакууме и получали 6-амино-5-фтор-3-метил-3Н-изобензофуран-1-он Х-27 (0,11 г, 92%) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 92%
1H ЯМР (400 МГц, DMSO-d6) δ 1,48 (d, J=6,85 Гц, 3Н) 5,49 (q, J=6,52 Гц, 1Н) 5,60 (s, 2Н) 7,09 (d, J=7,82 Гц, 1H) 7,36 (d, J=10,27 Гц, 1H).
А.28. Синтез 3-метокси-5-(трифторметил)пиридин-2-амина Х-28:
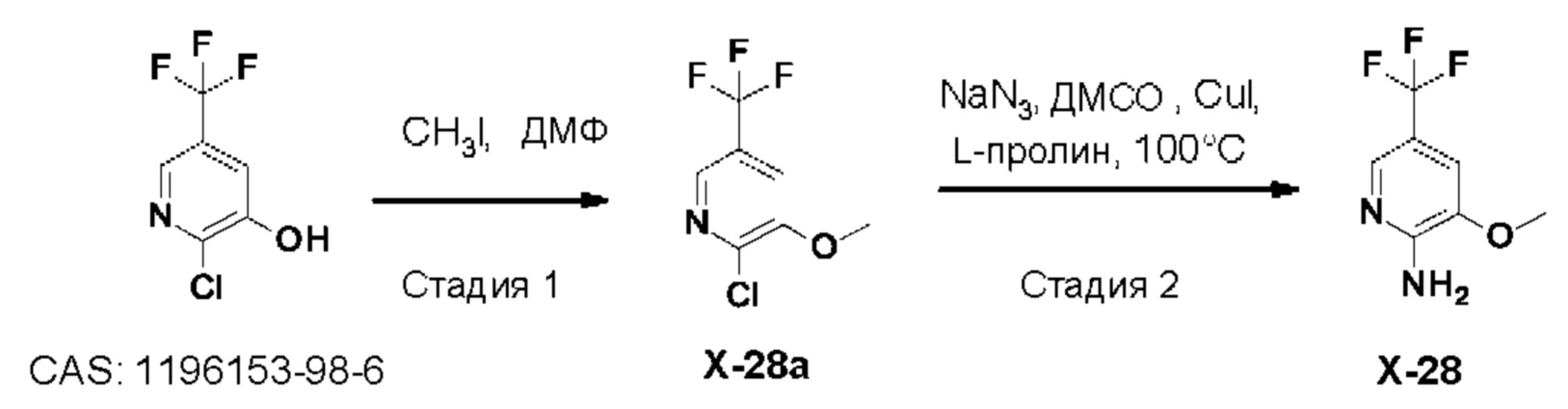
Стадия 1: Синтез 2-хлор-3-метокси-5-(трифторметил)пиридина Х-28а:
К раствору 2-хлор-5-(трифторметил)пиридин-3-ола (0,75 г, 3,80 ммоля) в DMF (15 мл) при 0°С медленно добавляли NaH (0,26 г, 6,45 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 15 мин. При 0°С добавляли CH3I (0,40 мл, 6,45 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 15 мин. Реакционную смесь перемешивали при комнатной температуре в течение 30 мин. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали охлажденной льдом Н2О (100 мл) и смесь экстрагировали с помощью EtOAc (250 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной флэш-хроматографии (диоксид кремния, 230-400 меш, 15% EtOAc в гексанах) и получали 2-хлор-3-метокси-5-(трифторметил)пиридин Х-28а (0,403 г) в виде бледно-желтой жидкости.
Выход: 50%
ЖХМС в щелочной среде, методика 2 (ЭР+): 212 (М+Н)+, чистота 100%.
1H ЯМР (400 МГц, DMSO-d6) δ 4,01 (s, 3Н) 7,91 (s, 1Н) 8,40 (s, 1H).
Стадия 2: Синтез 3-метокси-5-(трифторметил)пиридин-2-амина Х-28
К раствору 2-хлор-3-метокси-5-(трифторметил)пиридина Х-28а (0,35 г, 1,65 ммоля) в DMSO (10 мл) добавляли NaN3 (0,33 г, 5,08 ммоля) и реакционную смесь продували аргоном в течение 10 мин. Добавляли CuI (0,09 г, 0,46 ммоля) и L-пролин (0,09 г, 0,76 ммоля) и реакционную смесь нагревали при 100°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (200 мл) и экстрагировали с помощью EtOAc (300 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 40% EtOAc в гексанах) и получали 3-метокси-5-(трифторметил)пиридин-2-амин Х-28 (0,173 г) в виде бледно-коричневого твердого вещества.
Выход: 54%
ЖХМС в щелочной среде, методика 2 (ЭР+): 193 (М+Н)+, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,84 (s, 3Н) 6,54 (brs, 2Н) 7,16 (s, 1H) 7,84 (s, 1Н).
А.29. Синтез 3,5-дифтор-6-метоксипиридин-2-амина Х-29:
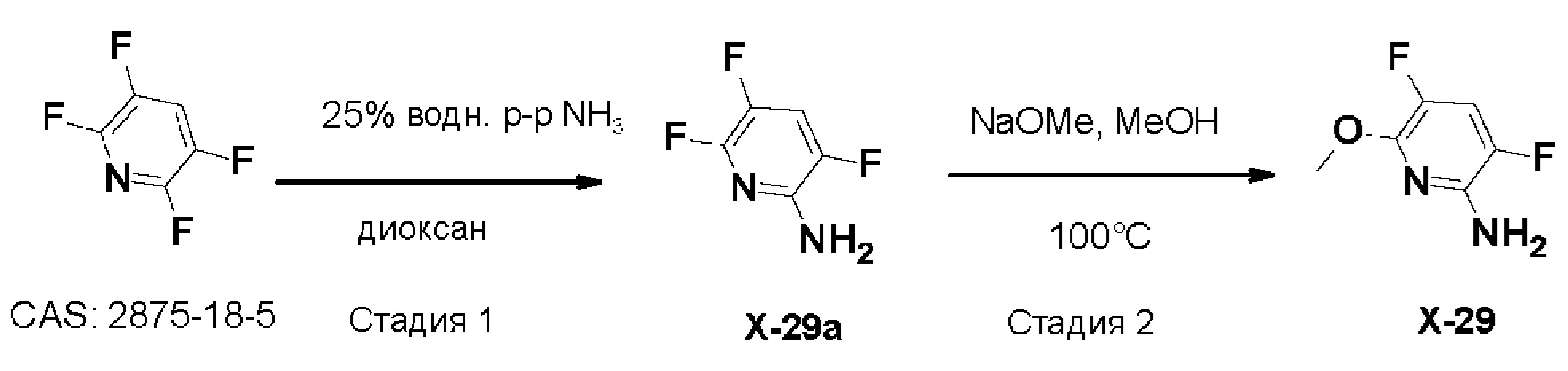
Стадия 1: Синтез 2-хлор-3-метокси-5-(трифторметил)пиридина Х-28а:
К раствору 2,3,5,6-тетрафторпиридина (2,00 г, 13,2 ммоля) в диоксане (100 мл) добавляли NH4OH (25% раствор в воде, 40 мл). Реакционную смесь нагревали при 60°С в течение 48 ч. За протеканием реакции следили с помощью TLC. После завершения реакционную смесь концентрировали в вакууме. Реакционную смесь разбавляли с помощью Н2О (100 мл) и экстрагировали диэтиловым эфиром (2×150 мл). Органические слои отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 1,30 г 3,5,6-трифторпиридин-2-амина Х-29а в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 65%
ЖХМС в щелочной среде, методика 2 (ЭР-): 147 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,52 (br s, 2 Н) 7,85-7,94 (m, 1Н).
Стадия 2: Синтез 3,5-дифтор-6-метоксипиридин-2-амина Х-29:
К раствору 3,5,6-трифторпиридин-2-амина Х-29а (500 мг, 3,38 ммоля) в метаноле (15 мл) добавляли метоксид натрия (547 мг, 10,1 ммоля). Реакционную смесь нагревали при 90-100°С в течение 24 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью Н2О (20 мл) и экстрагировали с помощью EtOAc (50 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 310 мг 3,5-дифтор-6-метоксипиридин-2-амина Х-29 в виде почти белого твердого вещества.
Выход: 52%
ЖХМС в щелочной среде, методика 2 (ЭР+): 161 (М+Н)+, чистота 90%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,81 (s, 3Н) 6,00 (s, 2Н) 7,59 (t, J=10,03 Гц, 1Н).
А.30. Синтез 3,6-дифтор-5-метилпиридин-2-амина Х-30:
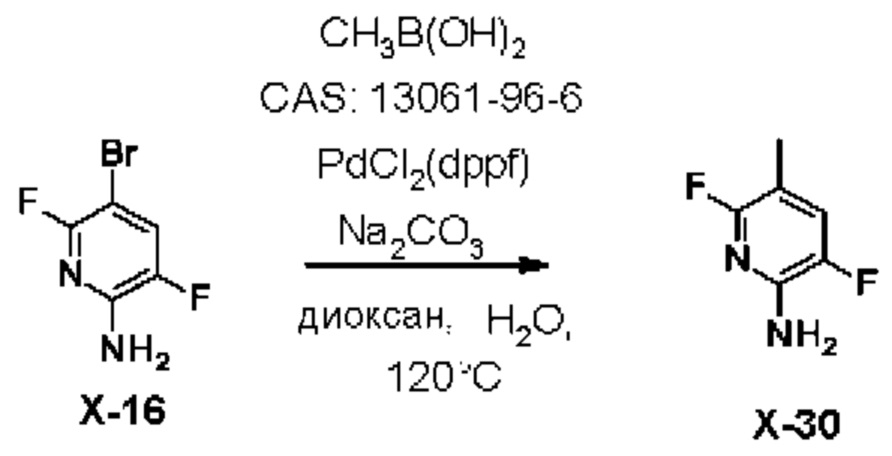
При перемешивании к раствору 5-бром-3,6-дифторпиридин-2-амина Х-16 (0,40 г, 1,91 ммоля) в диоксане (12 мл) добавляли СН3В(ОН)2 (0,23 г, 3,82 ммоля), раствор Na2CO3 (0,51 г, 4,78 ммоля) в Н2О (3 мл). Реакционную смесь продували аргоном в течение 20 мин, затем добавляли PdCl2(dppf) (0,28 г, 0,38 ммоля). Реакционную смесь продували аргоном в течение 10 мин и нагревали при 120°С в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь охлаждали до комнатной температуры, фильтровали через целит, промывали с помощью EtOAc (2×30 мл) и фильтрат концентрировали в вакууме. Полученное неочищенное вещество разбавляли с помощью Н2О (30 мл) и экстрагировали с помощью EtOAc (3×25 мл). Органический слой отделяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 3% EtOAc в гексанах) и получали 3,6-дифтор-5-метилпиридин-2-амин Х-30 (0,145 г) в виде почти белого твердого вещества.
Выход: 32%
ЖХМС в щелочной среде, методика 2 (ЭР+): 145 (М+Н)+, чистота 60%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,79 (s, 3Н) 6,39 (s, 2Н) 7,63-7,69 (m, 1Н).
А.31. Синтез 5-бром-6-фтор-3-метоксипиридин-2-амина Х-31:

Стадия 1: Синтез 5-бром-6-фтор-2-нитропиридин-3-ола Х-31а
К раствору H2SO4 (15 мл) добавляли KNO3 (0,63 г, 6,28 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 20 мин. Добавляли 5-бром-6-фторпиридин-3-ол (0,60 г, 3,14 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь выливали на лед (100 мл) и экстрагировали с помощью EtOAc (3×80 мл). Органический слой отделяли, промывали рассолом (120 мл), сушили над безводным Na2SO4 и концентрировали в вакууме и получали 5-бром-6-фтор-2-нитропиридин-3-ол Х-31а (0,60 г) в виде почти белого твердого вещества.
Выход: 56%
1H ЯМР (400 МГц, DMSO-d6) δ 8,11 (d, J=7,2 Гц, 1Н) 11,83 (brs, 1H).
Стадия 2: Синтез 3-бром-2-фтор-5-метокси-6-нитропиридина X-31b
При перемешивании при 0°С к суспензии NaH (0,11 г, 2,65 ммоля) в DMF (8 мл) добавляли 5-бром-6-фтор-2-нитропиридин-3-ол Х-31а (0,60 г, 1,77 ммоля, в 4 мл DMF) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. При 0°С добавляли CH3I (0,76 г, 5,32 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакцию останавливали льдом, смесь разбавляли с помощью Н2О (60 мл) и экстрагировали с помощью EtOAc (3×40 мл). Органический слой отделяли, промывали рассолом (60 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной флэш-хроматографии (от 12 до 20% EtOAc в гексанах) и получали 3-бром-2-фтор-5-метокси-6-нитропиридин Х-31b (0,30 г) в виде бледно-желтой жидкости.
Выход: 67%
1H ЯМР (400 МГц, CDCl3) δ 4,02 (s, 3Н) 7,86 (d, J=6,4 Гц, 1H).
Стадия 3: Синтез 5-бром-6-фтор-3-метоксипиридин-2-амина Х-31
К раствору 3-бром-2-фтор-5-метокси-6-нитропиридин Х-31b (0,25 г, 1,00 ммоля) в СН3СООН (10 мл) добавляли Fe (0,45 г, 7,97 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через слой целита, промывали с помощью EtOAc (220 мл) и фильтрат концентрировали в вакууме. Остаток выливали в насыщенный водный раствор NaHCO3 (150 мл) и экстрагировали с помощью EtOAc (2×125 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 5-бром-6-фтор-3-метоксипиридин-2-амин Х-31 (0,21 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 87%
ЖХМС в щелочной среде, методика 2 (ЭР+): 221 (М+Н)+, чистота 91%.
1H ЯМР (400 МГц, CDCl3) δ 3,78 (s, 3Н) 6,39 (brs, 2Н) 7,32 (d, J=6,8 Гц, 1Н).
А.32. Синтез 2-(6-амино-2-фтор-5-метокси-3-пиридил)ацетонитрила Х-32:
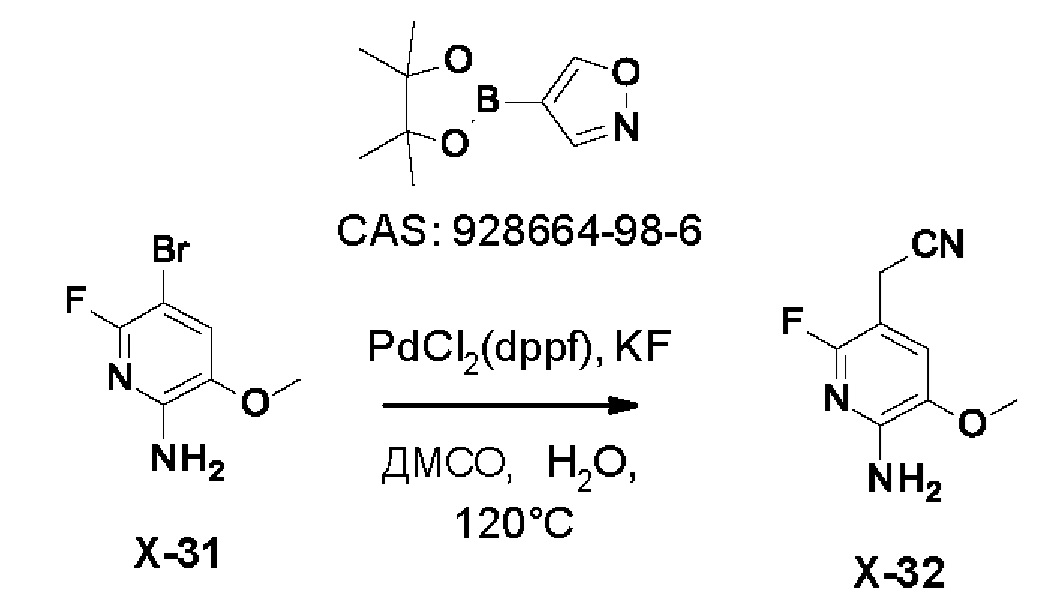
К раствору 5-бром-6-фтор-3-метоксипиридин-2-амина Х-31 (0,24 г, 1,02 ммоля) и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)изоксазола (0,24 г, 1,22 ммоля) в DMSO (12 мл) добавляли раствор KF (0,18 г, 3,05 ммоля) в Н2О (3,05 мл). Реакционную смесь продували аргоном в течение 15 мин, затем добавляли PdCl2(dppf) (0,15 г, 0,20 ммоля). Реакционную смесь нагревали при 120°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали, фильтрат разбавляли рассолом (40 мл) и экстрагировали с помощью EtOAc (2×70 мл). Органический слой отделяли, промывали с помощью Н2О (70 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью флэш-хроматографии (от 40 до 55% EtOAc в гексанах) и получали 2-(6-амино-2-фтор-5-метокси-3-пиридил)ацетонитрил Х-32 (0,10 г) в виде почти белого твердого вещества.
Выход: 54%
ЖХМС в щелочной среде, методика 2 (ЭР-): 180 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,77 (s, 5Н) 6,24 (brs, 2Н) 7,16 (s, 1Н).
А.33. Синтез 2-(4-амино-2,5-дифторфенил)ацетонитрила Х-33:
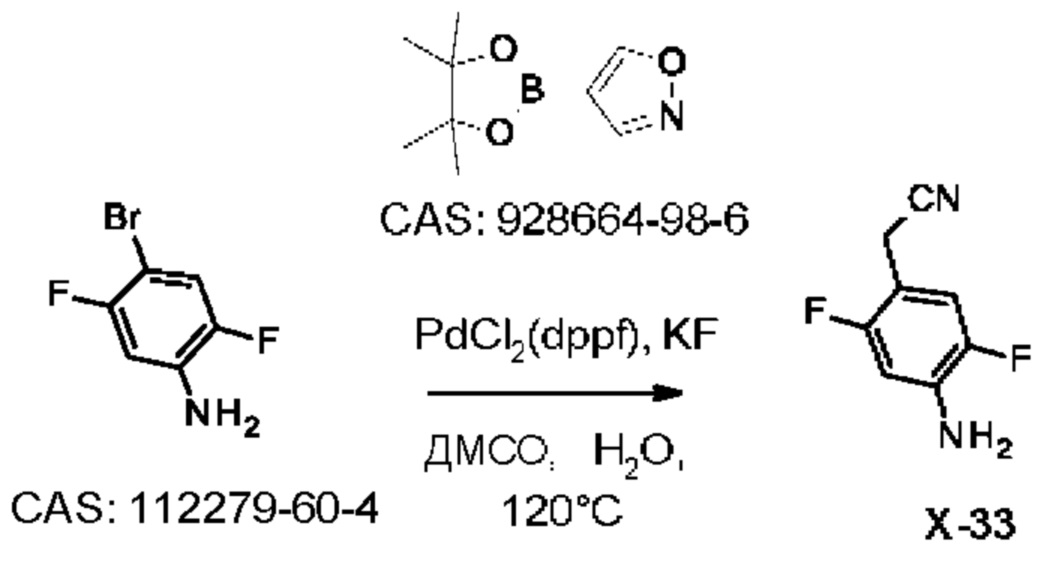
В сосуд помещали 4-бром-2,5-дифторанилин (300 мг, 1,44 ммоля) и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)изоксазол (338 мг, 1,731 ммоля) в диметилсульфоксиде (10 мл). Затем добавляли фторид калия (251 мг, 4,326 ммоля) и воду (78 мкл, 4,32 ммоля). Эту суспензию дегазировали в ультразвуковой ванне путем проводимого в течение 10 мин быстрого пропускания аргона. Затем добавляли [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (106 мг, 1,144 ммоля) и реакционную смесь нагревали в атмосфере аргона при 120°С в течение 19 ч. Затем смесь фильтровали через целит и к фильтрату добавляли рассол и его трижды экстрагировали этилацетатом, сушили над сульфатом магния и выпаривали досуха. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, от 5 до 15% EtOAc в петролейном эфире) и получали 2-(4-амино-2,5-дифторфенил)ацетонитрил Х-33 (87 мг) в виде светло-оранжевого масла.
Выход: 36%
1H ЯМР (400 МГц, DMSO-d6) δ 7,06 (dd, J=11,4, 6,9 Гц, 1H), 6,58 (dd, J=11,6, 7,5 Гц, 1H), 5,53 (s, 2H), 3,80 (s, 2H).
A.34. Синтез 3-(4-амино-2,5-дифторфенил)пропаннитрила X-34:
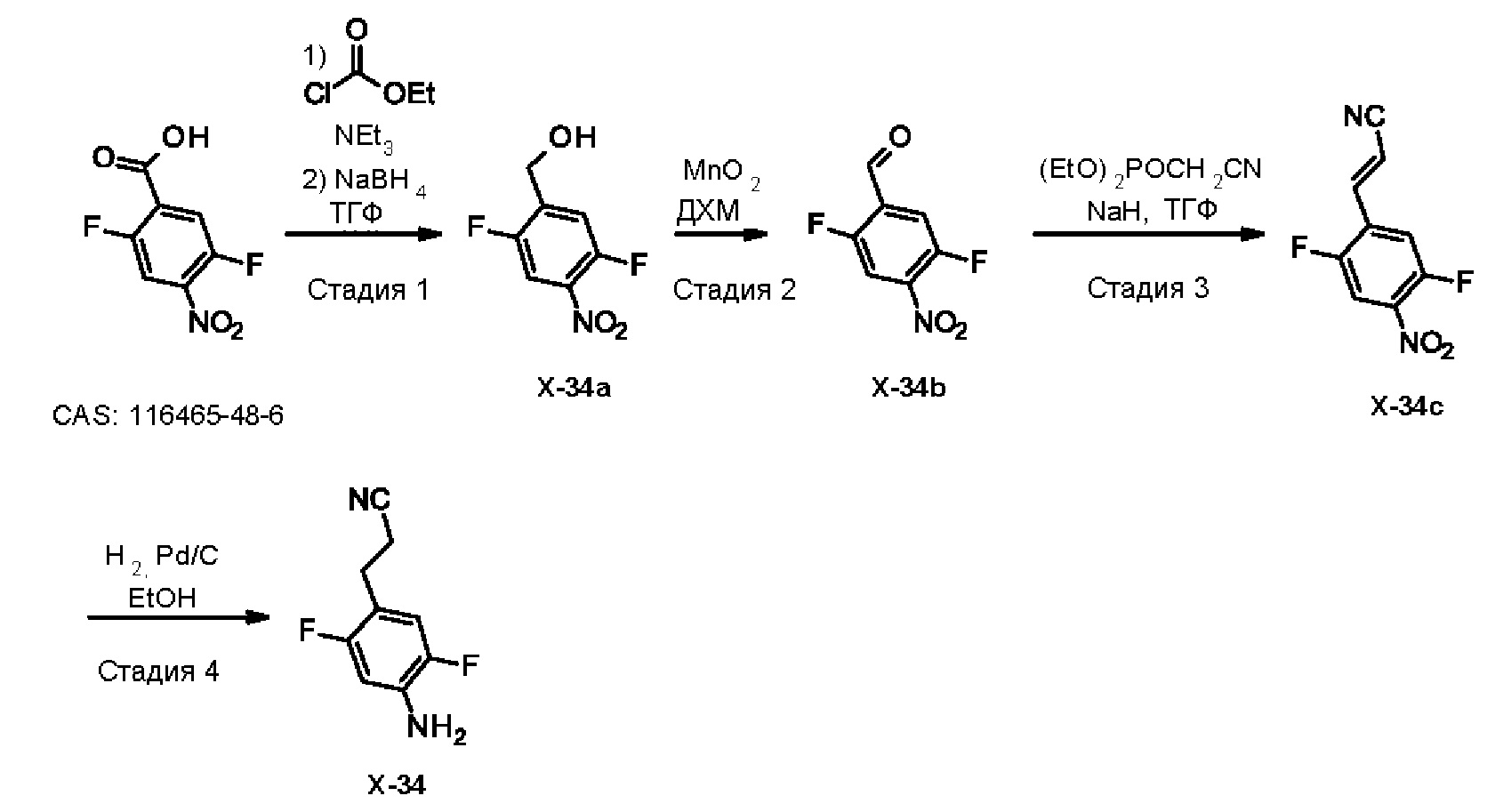
Стадия 1: Синтез (2,5-дифтор-4-нитрофенил)метанола X-34a:
2,5-Дифтор-4-нитробензойную кислоту (2,5 г, 12,3 ммоля) в сухом тетрагидрофуране (10 мл) помещали в атмосферу аргона. Затем добавляли триэтиламин (1,7 мл, 12,3 ммоля) и раствор охлаждали до 0°С. В течение 15 мин добавляли раствор этилхлорформиата (1,2 мл, 12,9 ммоля) в сухом тетрагидрофуране (15 мл) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Осадившийся триэтиламмонийхлорид отфильтровывали и при перемешивании к фильтрату порциями добавляли борогидрид натрия (1,4 г, 3,69 ммоля). Затем по каплям добавляли метанол (15 мл) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем ее подкисляли 1 н. раствором HCl до рН=2 и тетрагидрофуран удаляли в вакууме. Остаток переносили в этилацетат и промывали насыщенным раствором гидрокарбоната натрия. Затем водную фазу трижды экстрагировали этилацетатом. Объединенные органические фазы промывали рассолом, сушили над сульфатом магния и выпаривали досуха. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, DCM) и получали (2,5-дифтор-4-нитрофенил)метанол Х-34а (1,61 г) в виде оранжевого твердого вещества.
Выход: 70%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,77 (dd, J=8,8, 5,8 Гц, 1H), 7,51 (dd, J=11,0, 5,7 Гц, 1H), 4,86 (s, 2H), 2,19 (s, 1H).
Стадия 2: Синтез 2,5-дифтор-4-нитробензальдегида X-34b:
(2,5-Дифтор-4-нитрофенил)метанол X-34a (320 мг, 1,69 ммоля) с активированным оксид марганца (163 г, 169,2 ммоля) при комнатной температуре перемешивали в дихлорметане (10 мл). Через 2 дня реакционную смесь фильтровали через целит и выпаривали досуха и получали 2,5-дифтор-4-нитробензальдегид Х-34b (231 мг) в виде оранжевого твердого вещества.
Выход: 73%.
1H ЯМР (400 МГц, DMSO-d6) δ 10,36 (d, J=2,6 Гц, 1H), 7,93 (dd, J=8,7, 5,4 Гц, 1H), 7,80 (dd, J=9,7, 5,4 Гц, 1Н).
Стадия 3: Синтез (Е)-3-(2,5-дифтор-4-нитрофенил)акрилонитрила Х-34 с:
Диэтилцианометилфосфонат (227 мг, 1,238 ммоля) в сухом тетрагидрофуране (2 мл) помещали в атмосферу аргона. При 0°С добавляли гидрид натрия (60% дисперсия в минеральном масле, 77 мг, 1,925 ммоля). Смесь перемешивали при комнатной температуре в течение 15 мин и при 0°С медленно добавляли раствор 2,5-дифтор-4-нитробензальдегид Х-34b (240 мг, 1,238 ммоля) в сухом тетрагидрофуран (3 мл). Через 1,5 ч реакцию останавливали с помощью насыщенным раствором гидрокарбоната натрия. Затем продукт экстрагировали этилацетатом и органическую фазу один раз промывали насыщенным раствором гидрокарбоната натрия. Объединенные водные слои трижды экстрагировали этилацетатом. Объединенные органические фазы промывали рассолом, сушили над сульфатом магния и выпаривали досуха. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, CombiFlash 24 г, от 2 до 15% EtOAc в петролейном эфире) и получали искомый продукт, (Е)-3-(2,5-дифтор-4-нитрофенил)акрилонитрил Х-34 с (40 мг), в виде желтого твердого вещества.
Выход: 15%.
1H ЯМР (400 МГц, DMSO-d6) δ 8,24 (dd, J=9,8, 6,2 Гц, 1Н), 8,11 (dd, J=11,8, 5,9 Гц, 1H), 7,72 (d, J=16,7 Гц, 1H), 6,77 (d, J=16,7 Гц, 1H).
Стадия 4: Синтез 3-(4-амино-2,5-дифторфенил)пропаннитрила X-34:
(Е)-3-(2,5-Дифтор-4-нитрофенил)акрилонитрил X-34c (65 мг, 0,309 ммоля) в атмосфере аргона растворяли в абсолютном этаноле (8 мл). Затем добавляли палладий на угле (содержание 10 мас. %, 16 мг, 0,015 ммоля) и колбу продували аргоном и затем водородом. Реакционную смесь перемешивали в атмосфере водорода в течение 4 ч. Затем ее фильтровали через целит и выпаривали досуха. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, CombiFlash 4 г, от 2 до 20% EtOAc в петролейном эфире) и получали 3-(4-амино-2,5-дифторфенил)пропаннитрил Х-34 (35 мг) в виде желтого масла, которое кристаллизовалось при выдерживании.
Выход: 63%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,01 (dd, J=11,7, 6,9 Гц, 1H), 6,52 (dd, J=11,6, 7,6 Гц, 1Н), 5,34 (br s, 2H), 2,75 - 2,69 (m, 4H).
A.35. Синтез 3,6-дифтор-5-(2-фторэтокси)пиридин-2-амина X-35:
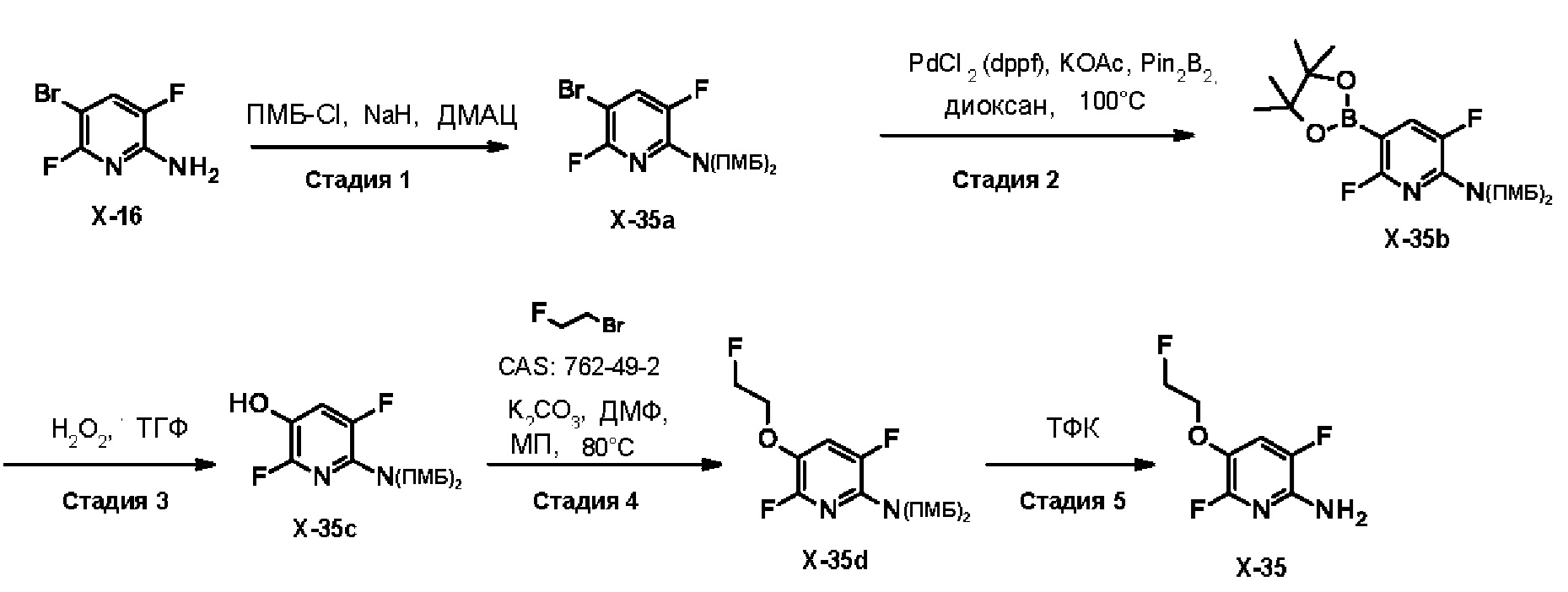
Стадия 1: Синтез 5-бром-3,6-дифтор-N,N-бис[(4-метоксифенил)метил]пиридин-2-амина Х-35а
К раствору 5-бром-3,6-дифторпиридин-2-амина Х-16 (4,00 г, 19,0 ммоля) в DMAC (40 мл) при 0°С порциями добавляли NaH (2,29 г, 57,1 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. При 0°С по каплям добавляли пара-метоксибензилхлорид (5,19 мл, 38,1 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь охлаждали до 0°С, реакцию останавливали насыщенным раствором NH4Cl (20 мл), смесь выливали в Н2О (60 мл) и экстрагировали с помощью EtOAc (3×60 мл). Органический слой отделяли, промывали рассолом (2×80 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 4% EtOAc в гексанах) и получали 5-бром-3,6-дифтор-N,N-бис[(4-метоксифенил)метил]пиридин-2-амин Х-35а (8,2 г, 96%) в виде почти белого твердого вещества.
Выход: 96%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,72 (s, 6Н) 4,57 (s, 4Н) 6,87-6,89 (m, 4Н) 7,16-7,18 (m, 4Н) 7,99-8,07 (m, 1Н).
Стадия 2: Синтез 3,6-дифтор-N,N-бис[(4-метоксифенил)метил]-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амина Х-35b:
К раствору 5-бром-3,6-дифтор-N,N-бис[(4-метоксифенил)метил]пиридин-2-амина Х-35а (4,00 г, 8,90 ммоля) в диоксане (160 мл) при комнатной температуре добавляли бис(пинаколято)дибор (4,52 г, 17,8 ммоля) и KOAc (3,06 г, 31,2 ммоля) и реакционную смесь продували аргоном в течение 20 мин, затем добавляли PdCl2(dppf) (0,65 г, 0,89 ммоля). Реакционную смесь продували аргоном в течение 10 мин и нагревали при 100°С в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь охлаждали, фильтровали через слой целита и промывали с помощью EtOAc (2×80 мл). Фильтрат концентрировали в вакууме, остаток разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью EtOAc (2×80 мл). Органический слой отделяли, промывали рассолом (2×100 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 8% EtOAc в гексанах) и получали 3,6-дифтор-N,N-бис[(4-метоксифенил)метил]-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амин Х-35b (2,60 г) в виде почти белого твердого вещества.
Выход: 59%.
1H ЯМР (400 МГц, DMSO-d6) δ 1,26 (s, 12Н) 3,73 (s, 6Н) 4,64 (s, 4Н) 6,89 (d, J=8,31 Гц, 4H) 7,17 (d, J=8,80 Гц, 4H) 7,51-7,56 (m, 1Н).
Стадия 3: Синтез 6-[бис[(4-метоксифенил)метил]амино]-2,5-дифторпиридин-3-ола Х-35 с:
К раствору 3,6-дифтор-N,N-бис[(4-метоксифенил)метил]-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амина Х-35b (2,50 г, 5,04 ммоля) в THF (30 мл) при 0°С добавляли 30% раствор Н2О2 в Н2О (10 мл) и реакционную смесь перемешивали при такой же температуре в течение 15 мин. Реакционную смесь перемешивали при комнатной температуре в течение 1,5 ч. За протеканием реакции следили с помощью TLC и ЖХМС. Реакционную смесь при 0°С выливали в 5% раствор Na2S2O3 в холодной Н2О (250 мл), разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью EtOAc (2×100 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-[бис[(4-метоксифенил)метил]амино]-2,5-дифторпиридин-3-ол Х-35с (1,74 г, неочищенный) в виде желтого полужидкого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в щелочной среде, методика 2 (ЭР+): 387 (М+Н)+, чистота 93%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,71 (s, 6Н) 4,32 (s, 4Н) 6,86 (d, J=8,80 Гц, 4Н) 7,14 (d, J=8,31 Гц, 4Н) 7,22-7,27 (m, 1H) 9,84 (s, 1Н).
Стадия 4: Синтез 3,6-дифтор-5-(2-фторэтокси)-N,N-бис[(4-метоксифенил)метил]пиридин-2-амина X-35d:
К раствору 6-[бис[(4-метоксифенил)метил]амино]-2,5-дифторпиридин-3-ола Х-35 с (0,70 г, 1,68 ммоля) в DMF (13 мл) при комнатной температуре добавляли K2CO3 (0,70 г, 5,04 ммоля) и 1-бром-2-фторэтан (0,43 г, 3,36 ммоля). Реакционную смесь нагревали в микроволновой печи при 80°С в течение 15 мин. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь охлаждали до комнатной температуры, выливали в Н2О (30 мл) и экстрагировали с помощью EtOAc (3×25 мл). Органический слой отделяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 25% EtOAc в гексанах) и получали 3,6-дифтор-5-(2-фторэтокси)-N,N-бис[(4-метоксифенил)метил]пиридин-2-амин X-35d (0,52 г) в виде коричневой жидкости.
Выход: 71%.
ЖХМС в щелочной среде, методика 2 (ЭР+): 433 (М+Н)+, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,72 (s, 6Н) 4,21-4,25 (m, 1Н) 4,29-4,32 (m, 1H) 4,42 (s, 4H) 4,63-4,66 (m, 1H) 4,75-4,78 (m, 1H) 6,87 (d, J=8,86 Гц, 4H) 7,15 (d, J=8,37 Гц, 4H) 7,69-7,76 (m, 1H).
Стадия 5: Синтез 3,6-дифтор-5-(2-фторэтокси)пиридин-2-амина Х-35:
К 3,6-дифтор-5-(2-фторэтокси)-N,N-бис[(4-метоксифенил)метил]пиридин-2-амину X-35d (0,50 г, 1,15 ммоля) при 0°С добавляли TFA (5 мл) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. Реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью Н2О (25 мл), подщелачивали водным раствором NaHCO3 (10 мл) и экстрагировали с помощью EtOAc (2×25 мл). Органический слой отделяли, промывали рассолом (2×40 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали путем растирания с Et2O (10 мл) и сушили в вакууме и получали 3,6-дифтор-5-(2-фторэтокси)пиридин-2-амин Х-35 (0,258 г) в виде почти белого твердого вещества.
Выход: 80%.
ЖХМС в щелочной среде, методика 2 (ЭР+): 193 (М+Н)+, чистота 69%.
1H ЯМР (400 МГц, DMSO-d6) δ 4,13-4,17 (m, 1Н) 4,20-4,25 (m, 1H) 4,59-4,64 (m, 1H) 4,71-4,76 (m, 1 H) 6,10 (s, 2H) 7,57-7,62 (m, 1H).
A.36. Синтез 3,6-дифтор-5-(2-метоксиэтокси)пиридин-2-амина X-36:
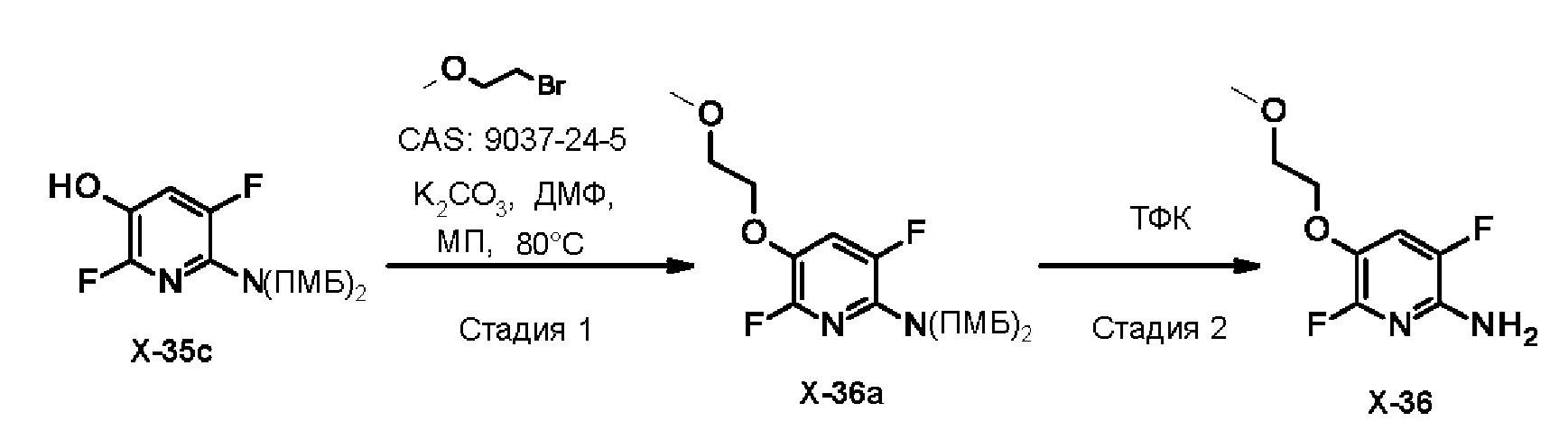
Стадия 1: Синтез 3,6-дифтор-5-(2-метоксиэтокси)-N,N-бис[(4-метоксифенил)метил]пиридин-2-амина Х-36а:
К раствору 6-[бис[(4-метоксифенил)метил]амино]-2,5-дифторпиридин-3-ола Х-35 с (0,60 г, 1,44 ммоля) и 2-бромэтилметилового эфира (0,70 г, 5,04 ммоля) в DMF (10 мл) добавляли K2CO3 (0,90 г, 6,48 ммоля) и реакционную смесь нагревали в микроволновой печи при 80°С в течение 30 мин. Реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью EtOAc (200 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 2% EtOAc в гексанах) и получали 3,6-дифтор-5-(2-метоксиэтокси)-N,N-бис[(4-метоксифенил)метил]пиридин-2-амин Х-36а (0,205 г) в виде коричневого полужидкого вещества.
Выход: 31%.
ЖХМС в щелочной среде, методика 2 (ЭР+): 445 (М+Н)+, чистота 96%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,28 (s, 3Н) 3,59-3,63 (m, 2Н) 3,71 (s, 6Н) 4,09-4,14 (m, 2Н) 4,40 (s, 4Н) 6,85-6,89 (m, 4Н) 7,15 (d, J=8,31 Гц, 4Н) 7,66-7,71 (m, 1H).
Стадия 2: Синтез 3,6-дифтор-5-(2-метоксиэтокси)пиридин-2-амина Х-36:
К 3,6-дифтор-5-(2-метоксиэтокси)-N,N-бис[(4-метоксифенил)метил]пиридин-2-амину Х-36а (0,20 г, 0,43 ммоля) при 0°С добавляли TFA (6 мл) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью Н2О (100 мл), подщелачивали насыщенным раствором NaHCO3 (50 мл) и экстрагировали с помощью EtOAc (200 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 3,6-дифтор-5-(2-метоксиэтокси)пиридин-2-амин Х-36 (0,15 г, неочищенный) в виде коричневого полужидкого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
1H ЯМР (400 МГц, DMSO-d6) δ 3,29 (s, 3Н) 3,53-3,59 (m, 2Н) 4,00-4,04 (m, 2Н) 6,01 (s, 2Н) 7,51-7,57 (m, 1Н).
В. Синтез промежуточных продуктов формулы XI
В.1. Синтез 6-циклопропил-1Н-индола XI-1:
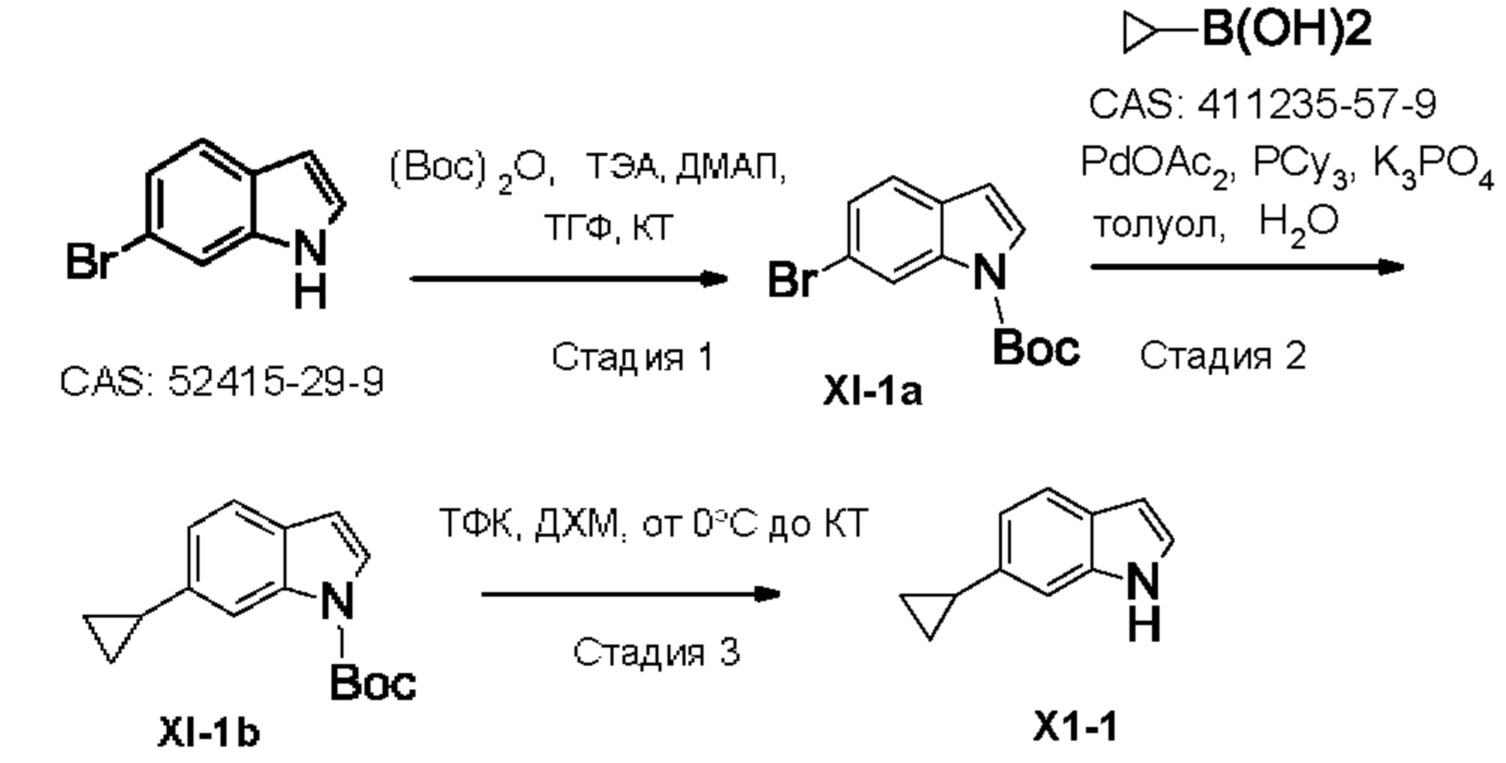
Стадия 1: Синтез трет-бутил-6-броминдол-1-карбоксилата XI-1a:
К раствору 6-бром-1Н-индола (2,70 г, 13,8 ммоля) в THF (30 мл) при 0°С добавляли триэтиламин (2,80 г, 27,6 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 5 мин. При 0°С добавляли DMAP (0,84 г, 6,90 ммоля) и (Вос)2O (4,50 г, 20,7 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакцию останавливали льдом и смесь концентрировали в вакууме. Остаток разбавляли с помощью H2O (100 мл) и экстрагировали с помощью EtOAc (3×100 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 1% EtOAc в гексанах) и получали 3,8 г трет-бутил-6-броминдол-1-карбоксилата XI-1а в виде светло-желтого твердого вещества.
Выход: 92%.
1H ЯМР (400 МГц, DMSO-d6) δ 1,65 (s, 9Н) 6,73 (d, J=3,42 Гц, 1H) 7,20 -7,27 (m, 1H) 7,60 (d, J=8,31 Гц, 1Н) 7,69 (d, J=3,42 Гц, 1Н) 8,23 (s, 1H).
Стадия 2: Синтез трет-бутил-6-циклопропилиндол-1-карбоксилата XI-1b: К раствору трет-бутил-6-броминдол-1-карбоксилата XI-1а (0,70 г, 2,36 ммоля) и циклопропилбороновой кислоты (0,30 г, 3,55 ммоля) в толуоле (15 мл) добавляли K3PO4 (1,00 г, 4,72 ммоля), трициклогексилфосфин (РСу3) (0,13 г, 0,47 ммоля) и H2O (0,70 мл). Реакционную смесь продували аргоном в течение 15 мин, затем добавляли Pd(OAc)2 (0,05 г, 0,24 ммоля). Реакционную смесь нагревали при 100°С в течение 8 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь разбавляли с помощью Н2О (20 мл) и экстрагировали с помощью EtOAc (2×20 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, от 0,5 до 0,8% EtOAc в гексанах) и получали 0,5 г трет-бутил-6-циклопропилиндол-1-карбоксилата XI-1b в виде бесцветной жидкости. Выход: 83%.
1H ЯМР (400 МГц, CDCl3) δ 0,70-0,78 (m, 2Н) 0,96-1,03 (m, 2Н) 1,67 (s, 9Н) 1,98-2,10 (m, 1H) 6,50 (s, 1H) 6,99 (d, J=7,82 Гц, 1H) 7,42 (d, J=8,31 Гц, 1H) 7,50 (d, J=3,42 Гц, 1Н) 7,90 (brs, 1H).
Стадия 3: Синтез 6-циклопропил-1Н-индола XI-1:
К раствору трет-бутил-6-циклопропилиндол-1-карбоксилата XI-1b (1,30 г, 5,10 ммоля) в DCM (25 мл) при 0°С по каплям добавляли TFA (2,5 мл). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью DCM (80 мл) и при 0°С нейтрализовывали триэтиламином (4 мл). Органический слой отделяли, промывали холодным рассолом (20 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, от 4 до 5% EtOAc в гексанах) и получали 0,32 г 6-циклопропил-1Н-индола XI-1 в виде бесцветной жидкости.
Выход: 41%.
1H ЯМР (400 МГц, CDCl3) δ 0,71-0,76 (m, 2Н) 0,93-1,00 (m, 2Н) 1,98-2,08 (m, 1H) 6,51 (s, 1Н) 6,90 (d, J=8,31 Гц, 1H) 7,13-7,18 (m, 2Н) 7,52-7,58 (m, 1Н) 8,03 (brs, 1Н).
В.2. Синтез 6-хлорбензофурана XI-2:
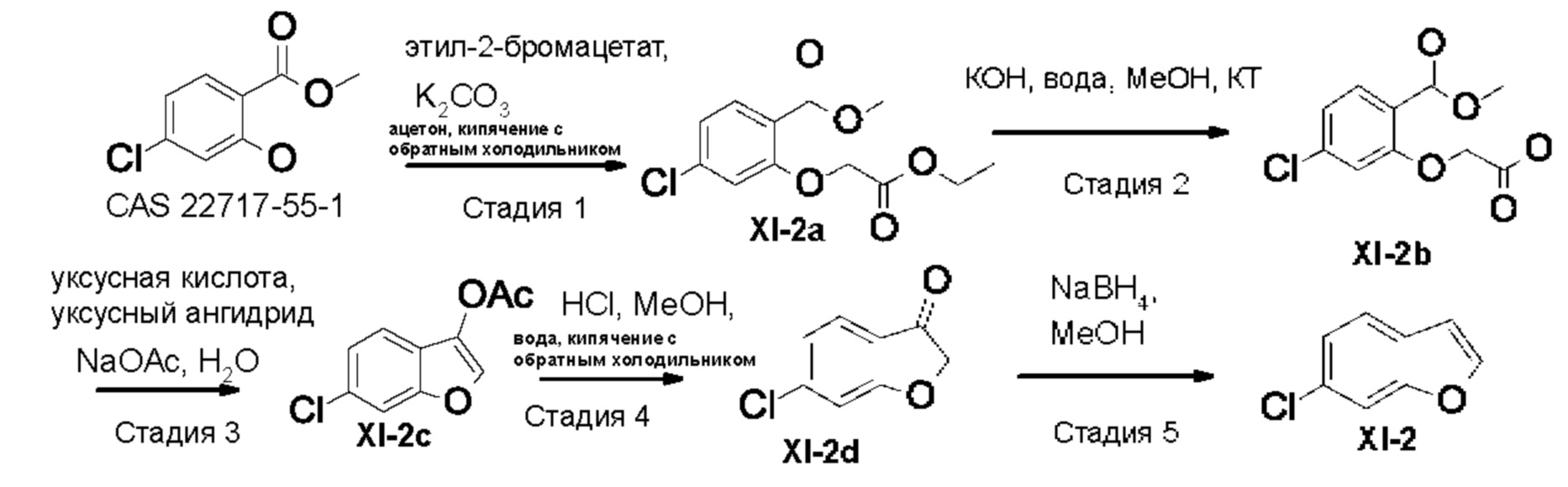
Стадия 1: Синтез метил-4-хлор-2-(2-этокси-2-оксоэтокси)бензоата XI-2а:
К раствору метил-4-хлор-2-гидроксибензоата (5,00 г, 26,7 ммоля) в ацетоне (60 мл) добавляли этил-2-бромацетат (6,72 г, 40,2 ммоля) и K2CO3 (5,56 г, 40,2 ммоля). Реакционную смесь кипятили с обратным холодильником в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток растворяли в петролейном эфире (80 мл), фильтровали и фильтрат концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 20% EtOAc в гексанах) и получали метил-4-хлор-2-(2-этокси-2-оксоэтокси)бензоат XI-2а (6,80 г) в виде красного полужидкого вещества. Получение продукта подтверждали только с помощью TLC.
Выход: 93%.
Стадия 2: Синтез 2-(5-хлор-2-(метоксикарбонил)фенокси)уксусной кислоты XI-2b:
К раствору XI-2а (6,80 г, 24,9 ммоля) в МеОН (180 мл) при 0°С добавляли раствор KOH (3,13 г, 55,8 ммоля) в Н2О (40 мл) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток растворяли в Н2О (100 мл) и подкисляли 2 н. раствором HCl до рН 2. Осадившееся твердое вещество отфильтровывали, сушили в вакууме и получали 2-(5-хлор-2-(метоксикарбонил)фенокси)уксусную кислоту XI-2b (3,80 г) в виде белого твердого вещества.
Выход: 66%.
ЖХМС в щелочной среде, методика 2 (ЭР+): 245,00 (М+Н)+, чистота 16%.
Стадия 3: Синтез 6-хлорбензофуран-3-илацетата XI-2с:
К раствору XI-2b (3,80 г, 16,4 ммоля) в СН3СООН (75 мл) добавляли Ac2O (95 мл), затем добавляли NaOAc (3,19 г, 37,7 ммоля). Реакционную смесь нагревали при 140°С в течение 5 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь разбавляли с помощью Н2О (300 мл) и экстрагировали с помощью EtOAc (60 мл). Органический слой отделяли, промывали насыщенным раствором NaHCO3 (20 мл), сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлорбензофуран-3-илацетат XI-2с (3,00 г, 87%) в виде красной жидкости. Это соединение использовали в следующей реакции без дополнительной очистки.
1H ЯМР (400 МГц, DMSO-d6) δ 2,37 (s, 3Н) 7,34-7,40 (m, 1Н) 7,60 (s, 1H) 7,78-7,82 (m, 1H) 8,24 (s, 1H).
Стадия 4: Синтез 6-хлорбензофуран-3(2Н)-она XI-2d:
К раствору XI-2c (3,00 г, 1,42 ммоля) в МеОН (150 мл) добавляли концентрированную HCl (4 мл) и H2O (35 мл) и реакционную смесь кипятили с обратным холодильником в течение 3 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь охлаждали до комнатной температуры, разбавляли с помощью H2O (20 мл) и фильтровали. Полученное неочищенное вещество промывали с помощью H2O (20 мл) и сушили в вакууме и получали 6-хлорбензофуран-3(2Н)-он XI-2d (2,20 г, 92%) в виде красного твердого вещества.
1H ЯМР (400 МГц, DMSO-d6) δ 2,34 (s, 2Н) 7,23 (d, J=7,83 Гц, 1Н) 7,38 (d, J=7,83 Гц, 1H) 7,70 (t, J=9,05 Гц, 1H).
Стадия 5: Синтез 6-хлорбензофурана XI-2:
К раствору XI-2d (2,20 г, 13,0 ммоля) в МеОН (75 мл) при 0°С порциями добавляли NaBH4 (1,08 г, 28,7 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 4 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакцию останавливали ацетоном (20 мл), смесь разбавляли 3 н. раствором HCl (35 мл) и перемешивали в течение 1 ч. Реакционную смесь экстрагировали с помощью EtOAc (50 мл), сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлорбензофуран XI-2 (1,60 г) в виде бесцветной жидкости. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 80%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,99 (d, J=0,98 Гц, 1Н) 7,30 (d, J=8,31 Гц, 1H) 7,67 (d, J=8,31 Гц, 1H) 7,77 (s, 1H) 8,04 (d, 3=1,96 Гц, 1H).
В.3. Синтез 6-(2-метоксиэтокси)-1Н-индола XI-3:
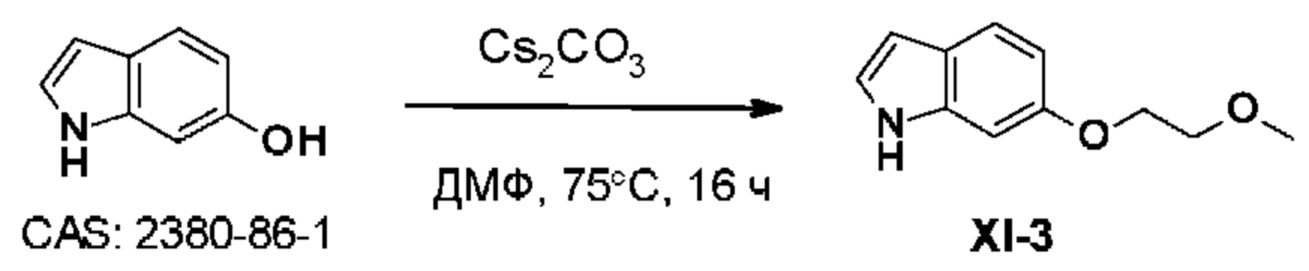
Раствор 1H-индол-6-ола (0,95 г, 7,12 ммоля) в DMF (12 мл) обрабатывали карбонатом цезия (2,79 г, 8,59 ммоля) и перемешивали при 75°С в течение 16 ч (за протеканием реакции следили с помощью TLC). Затем растворитель выпаривали и остаток разбавляли этилацетатом, промывали 1 н. раствором NaOH, водой и рассолом. Объединенные органические экстракты сушили над MgSO4, фильтровали и выпаривали. Остаток очищали с помощью колоночной хроматографии (циклогексан/этилацетат=4:1) и получали 0,88 г 6-(2-метоксиэтокси)-1Н-индола XI-3 в виде белого твердого вещества.
Выход: 65%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 192,0 (М+Н)+, чистота 96%.
В.4. Синтез 6-хлор-7-метокси-1Н-индола XI-4:
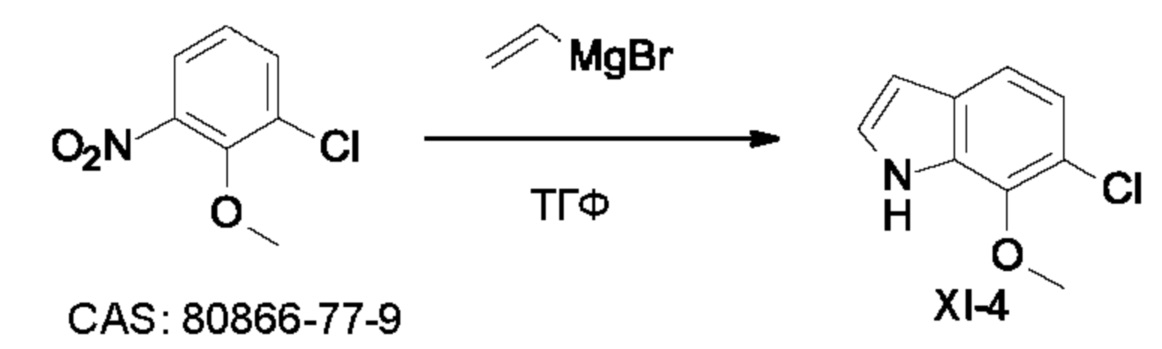
К раствору 1-хлор-2-метокси-3-нитробензола (1,00 г, 5,34 ммоля) в THF (20 мл) при -20°С добавляли винилмагнийбромид (16,0 мл, 16,0 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали льдом и смесь экстрагировали с помощью EtOAc (100 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, от 5 до 10% EtOAc в гексанах) и получали 6-хлор-7-метокси-1Н-индол XI-4 (0,50 г) в виде вязкого масла.
Выход: 51%
1H ЯМР (400 МГц, DMSO-d6) δ 3,91 (s, 3Н) 6,47 (s, 1Н) 6,99 (d, J=8,40 Гц, 1H) 7,29 (d, J=8,00 Гц, 1H) 7,35 (s, 1H) 11,46 (brs, 1H).
B.5. Синтез 6-хлор-7-фтор-1Н-индола XI-5:
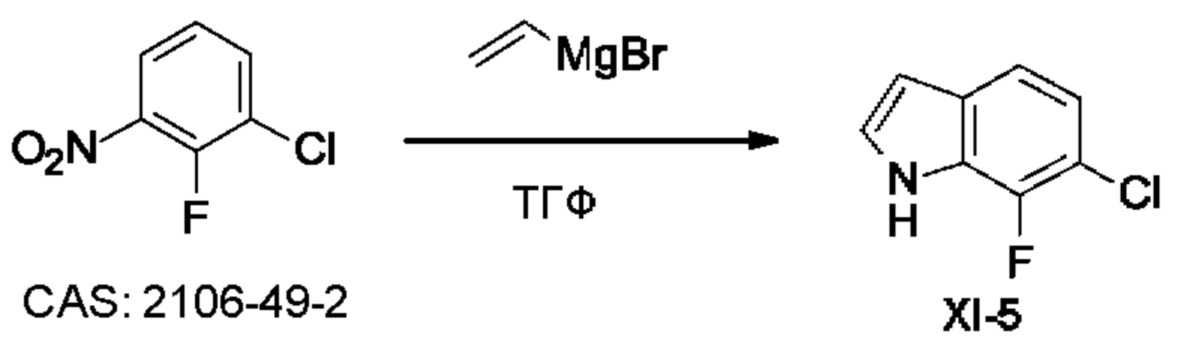
К раствору 1-хлор-2-фтор-3-нитробензола (2,50 г, 14,2 ммоля) в THF (50 мл) при -78°С добавляли винилмагнийбромид (5,61 г, 42,7 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали насыщенным раствором NH4Cl (100 мл), смесь разбавляли с помощью Н2О (400 мл) и экстрагировали с помощью EtOAc (500 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 5% EtOAc в гексанах) и получали 6-хлор-7-фтор-1Н-индол XI-5 (0,60 г) в виде красной жидкости.
Выход: 17%
ЖХМС в щелочной среде, методика 2 (ЭР-): 168,00 (М-Н)-, чистота 66%.
В.6. Синтез 6-(трифторметил)-1Н-пирроло[2,3-b]пиридина XI-6:
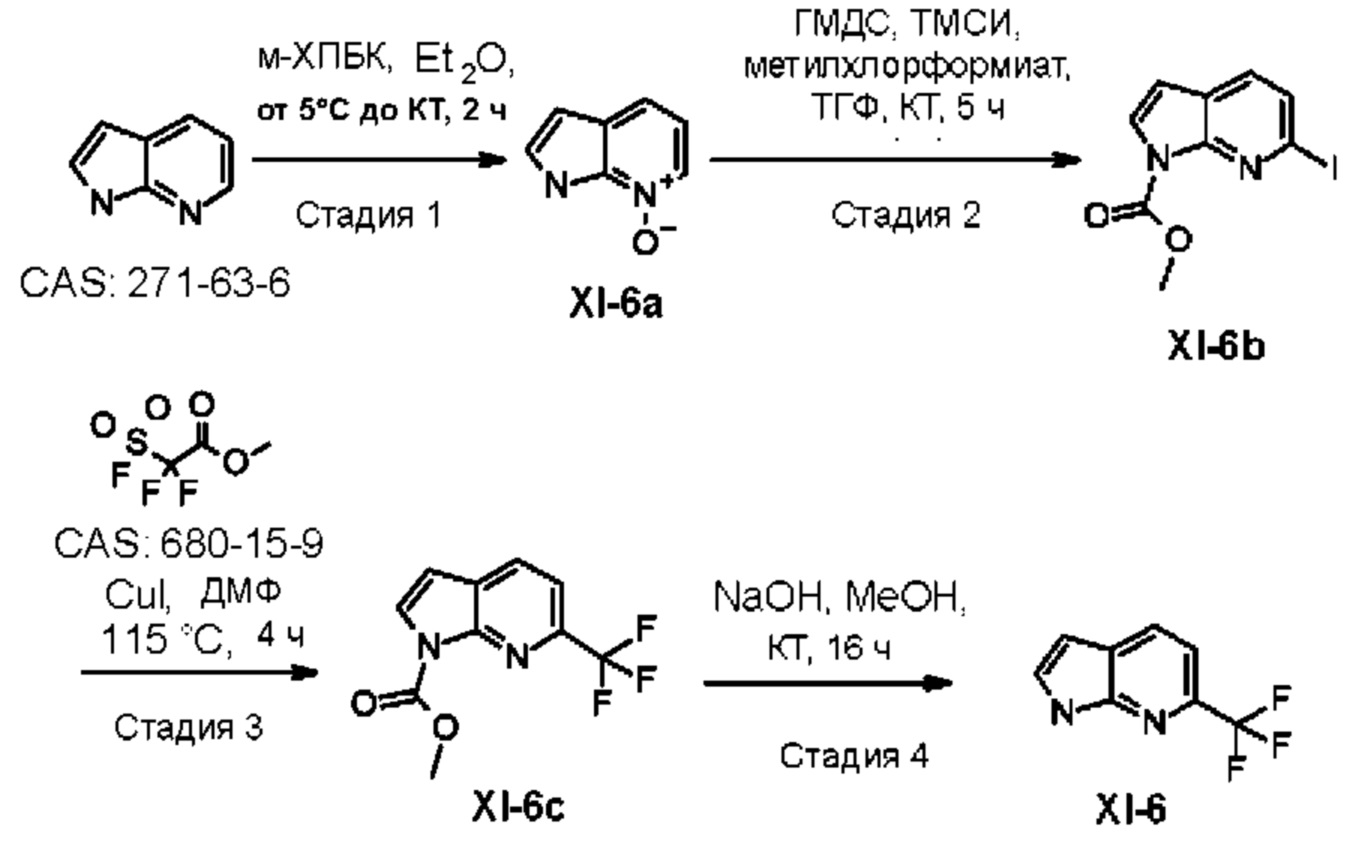
Стадия 1: Синтез 7-оксидо-1Н-пирроло[2,3-b]пиридин-7-ия XI-6а
К раствору 1Н-пирроло[2,3-b]пиридина (2,00 г, 16,9 ммоля) в Et2O (50 мл) при 5°С порциями добавляли м-ХПБК (мета-хлорпероксибензойная кислота) 3,80 г, 22,0 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали, промывали с помощью Et2O (12 мл) и сушили в вакууме и получали 7-оксидо-1H-пирроло[2,3-b]пиридин-7-ий XI-6а (3,75 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 89%
ЖХМС в щелочной среде, методика 2 (ЭР+): 135 (М+Н)+, чистота 54%.
Стадия 2: Синтез метил-6-йодопирроло[2,3-b]пиридин-1-карбоксилата XI-6b
К раствору 7-оксидо-1Н-пирроло[2,3-b]пиридин-7-ия XI-6а (1,60 г, 11,9 ммоля) в THF (100 мл) по каплям добавляли гексаметилдисилазан (ГМДС, 2,31 г, 14,3 ммоля) и триметилсилилйодид (ТМСИ, 4,77 г, 23,9 ммоля), затем по каплям добавляли метилхлорформиат (2,25 г, 23,9 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 5 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью EtOAc (150 мл) и промывали насыщенным раствором NaHCO3 (100 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 10% EtOAc в гексанах) и получали метил-6-йодопирроло[2,3-b]пиридин-1-карбоксилат XI-6b (1,00 г) в виде коричневого твердого вещества.
Выход: 26%
ЖХМС в щелочной среде, методика 2 (ЭР+): 303 (М+Н)+, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 4,12 (s, 3Н) 6,55 (d, J=3,91 Гц, 1Н) 7,54-7,58 (m, 1H) 7,61-7,65 (m, 1H) 7,69 (d, J=3,91 Гц, 1H).
Стадия 3: Синтез метил-6-(трифторметил)пирроло[2,3-b]пиридин-1-карбоксилата XI-6c
К раствору метил-6-йодопирроло[2,3-b]пиридин-1-карбоксилата XI-6b (1,00 г, 3,14 ммоля) в DMF (16,7 мл) добавляли метил-2,2-дифтор-2-фторсульфонилацетат (2,41 г, 12,6 ммоля) и CuI (0,12 г, 0,62 ммоля) и реакционную смесь нагревали при 115°С в течение 4 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью EtOAc (60 мл). Органический слой отделяли, промывали с помощью H2O (25 мл), NH4Cl (25 мл) и рассолом (25 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 10% EtOAc в гексанах) и получали метил-6-(трифторметил)пирроло[2,3-b]пиридин-1-карбоксилат XI-6с (0,65 г) в виде почти белого твердого вещества.
Выход: 71%
ЖХМС в щелочной среде, методика 2 (ЭР+): 245 (М+Н)+, чистота 84%.
1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ 4,14 (s, 3Н) 6,68 (d, J=3,42 Гц, 1H) 7,63 (d, J=8,31 Гц, 1Н) 7,94 (d, J=2,93 Гц, 1H) 8,06 (d, J=7,83 Гц, 1H).
Стадия 4: Синтез 6-(трифторметил)-1Н-пирроло[2,3-Ь]пиридина XI-6
К раствору метил-6-(трифторметил)пирроло[2,3-b]пиридин-1-карбоксилата XI-6 с (0,65 г, 2,23 ммоля) в МеОН (33 мл) добавляли 1 М раствор NaOH (0,26 г, 6,68 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток экстрагировали с помощью DCM (3×15 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-(трифторметил)-1Н-пирроло[2,3-b]пиридин XI-6 (0,45 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 97%
ЖХМС в щелочной среде, методика 2 (ЭР+): 187 (М+Н)+, чистота 89%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,61 (t, J=2,00 Гц, 1H) 7,52 (d, J=7,82 Гц, 1Н) 7,77 (t, J=2,93 Гц, 1Н) 8,21 (d, J=8,31 Гц, 1H) 12,16 (brs, 1Н).
В.7. Синтез 7-бром-6-хлор-1Н-индола XI-7:
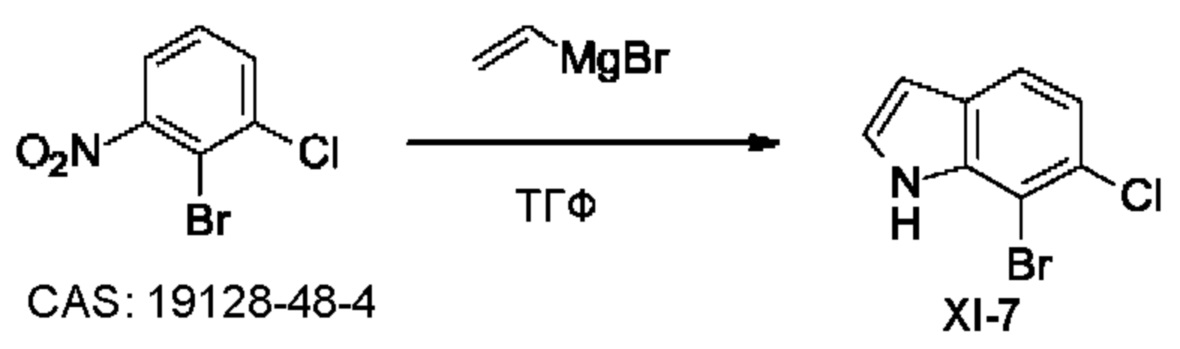
К раствору 2-бром-1-хлор-3-нитробензола (4,50 г, 19,0 ммоля) в THF (90 мл) при -78°С по каплям добавляли винилмагнийбромид (9,99 г, 76,1 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. Реакцию повторяли при количестве, равном 4,5 г, и неочищенные смеси, полученные в 2 реакциях, объединяли. После завершения реакции реакцию останавливали насыщенным раствором NH4Cl (500 мл), смесь разбавляли с помощью H2O (500 мл) и экстрагировали с помощью EtOAc (1000 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 2% EtOAc в гексанах) и получали 7-бром-6-хлор-1Н-индол XI-7 (3,05 г) в виде желтого твердого вещества.
Выход: 33%
ЖХМС в щелочной среде, методика 2 (ЭР-): 228,00 (М-Н)-, чистота 96%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,59 (d, J=1,96 Гц, 1Н) 7,18 (d, J=8,31 Гц, 1Н) 7,41-7,45 (m, 1H) 7,57 (d, J=8,31 Гц, 1H) 11,48 (brs, 1H).
B.8. Синтез 6-хлор-7-(2,2-дифторэтокси)-1Н-индола XI-8:
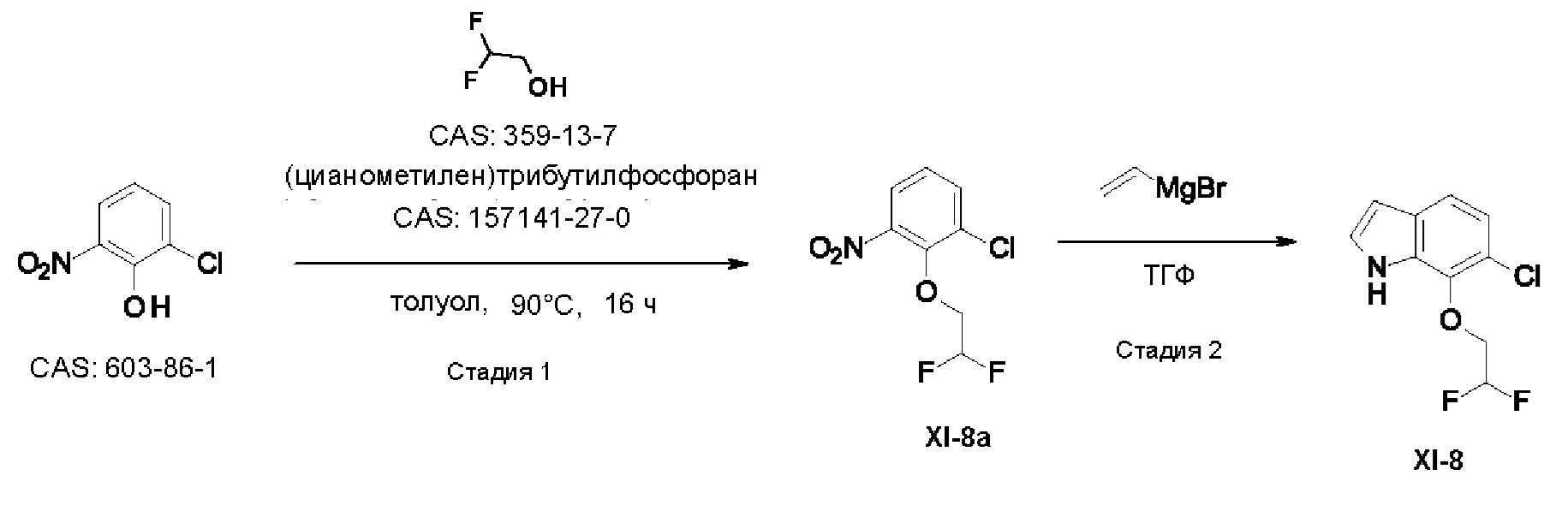
Стадия 1: Синтез 1-хлор-2-(2,2-дифторэтокси)-3-нитробензола XI-8а:
К раствору 2-хлор-6-нитрофенола (0,50 г, 2,88 ммоля) в толуоле (15 мл) добавляли 2,2-дифторэтанол (0,37 мл, 5,76 ммоля), затем добавляли (цианометилен)трибутилфосфоран (0,91 мл, 3,46 ммоля). Реакционную смесь нагревали при 90°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (50 мл) и экстрагировали с помощью EtOAc (3×25 мл). Органический слой отделяли, промывали рассолом (30 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 10% EtOAc в гексанах) и получали 1-хлор-2-(2,2-дифторэтокси)-3-нитробензол XI-8а (0,60 г) в виде бледно-желтого твердого вещества.
Выход: 86%
1H ЯМР (400 МГц, DMSO-d6) δ 4,39-4,43 (m, 2Н) 6,21-6,53 (m, 1Н) 7,41-7,47 (m, 1H) 7,90-7,94 (m, 1H) 7,98 (dd, J=8,31, 1,47 Гц, 1H).
Стадия 2: Синтез 6-хлор-7-(2,2-дифторэтокси)-1Н-индола XI-8:
К раствору 1-хлор-2-(2,2-дифторэтокси)-3-нитробензола XI-8а (0,60 г, 2,46 ммоля) в THF (40 мл) при -78°С по каплям добавляли 1 М раствор винилмагнийбромид (1,29 г, 9,86 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 1 ч. Затем реакционную смесь перемешивали при -40°С в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали насыщенным раствором NH4Cl (35 мл) и смесь экстрагировали с помощью EtOAc (2×50 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 10% EtOAc в гексанах) и получали 6-хлор-7-(2,2-дифторэтокси)-1Н-индол XI-8 (0,13 г) в виде бледно-желтого твердого вещества.
Выход: 23%
ЖХМС в щелочной среде, методика 2 (ЭР-): 230 (М-Н)-, чистота 67%.
В.9. Синтез 6-хлорбензотиофена XI-9:
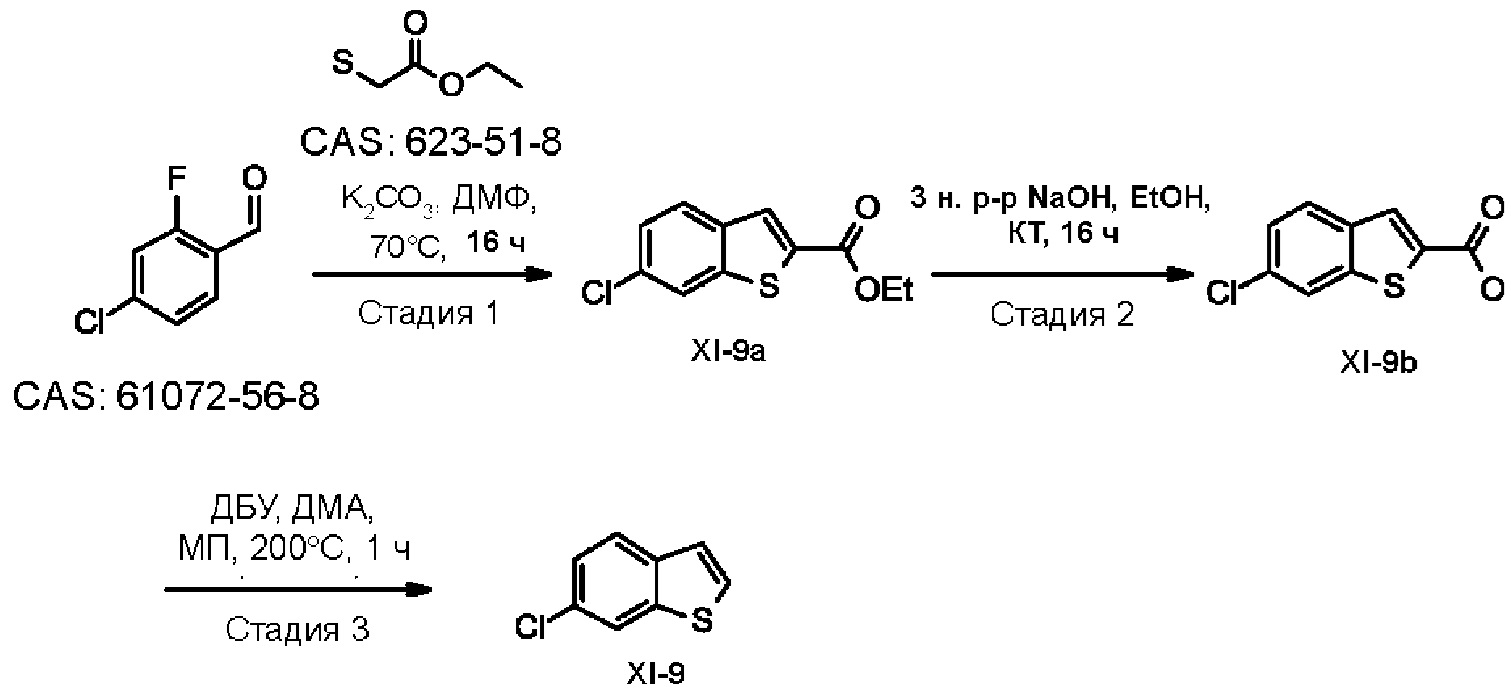
Стадия 1: Синтез этил-6-хлорбензотиофен-2-карбоксилата XI-9а:
К раствору 4-хлор-2-фторбензальдегида (10,0 г, 63,0 ммоля) в DMF (100 мл) добавляли этилтиогликолят (11,3 г, 94,6 ммоля), затем добавляли K2CO3 (26,1 г, 189 ммолей). Реакционную смесь нагревали при 70°С в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь разбавляли с помощью Н2О (300 мл) и экстрагировали с помощью EtOAc (2×300 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали этил-6-хлорбензотиофен-2-карбоксилат XI-9а (9,10 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 60%
1Н ЯМР (400 МГц, DMSO-d6) δ 1,33 (t, J=7,09 Гц, 3Н) 4,35 (q, J=7,01 Гц, 2Н) 7,51 (dd, J=8,56, 1,71 Гц, 1Н) 8,04 (d, J=8,80 Гц, 1H) 8,20 (s, 1H) 8,25 (d, J=0,98 Гц, 1H).
Стадия 2: Синтез 6-хлорбензотиофен-2-карбоновой кислоты XI-9b:
К раствору этил-6-хлорбензотиофен-2-карбоксилата XI-9а (9,00 г, 37,5 ммоля) в EtOH добавляли 3 н. раствор NaOH (24,9 мл, 74,7 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью Н2О (200 мл), подкисляли 2 н. раствором HCl и экстрагировали с помощью EtOAc (2×300 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлорбензотиофен-2-карбоновую кислоту XI-9b (6,10 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 77%
1H ЯМР (400 МГц, DMSO-d6) δ 8,00 (d, J=8,31 Гц, 2Н) 8,10 (s, 1Н) 8,21 (s, 1H) 13,52 (brs, 1H).
Стадия 3: Синтез 6-хлорбензотиофена XI-9:
К раствору 6-хлорбензотиофен-2-карбоновой кислоты XI-9b (1,00 г, 4,70 ммоля) в ДМА (диметилацетамид, 5 мл) добавляли ДБУ (диазабицикло[5.4.0]ундец-7-ен, 2,86 г, 18,8 ммоля) и реакционную смесь нагревали в микроволновой печи при 200°С в течение 1 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь разбавляли с помощью Н2О (30 мл) и экстрагировали с помощью EtOAc (3×20 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлорбензотиофен XI-9 (0,51 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 65%
1H ЯМР (400 МГц, DMSO-d6) δ 7,41 (dd, J=8,56, 1,71 Гц, 1Н) 7,47 (d, J=5,38 Гц, 1H) 7,80 (d, J=5,38 Гц, 1H) 7,89 (d, J=8,80 Гц, 1H) 8,17 (d, J=0,98 Гц, 1H).
B.10. Синтез 6-хлор-5,7-дифтор-1Н-индола XI-10:
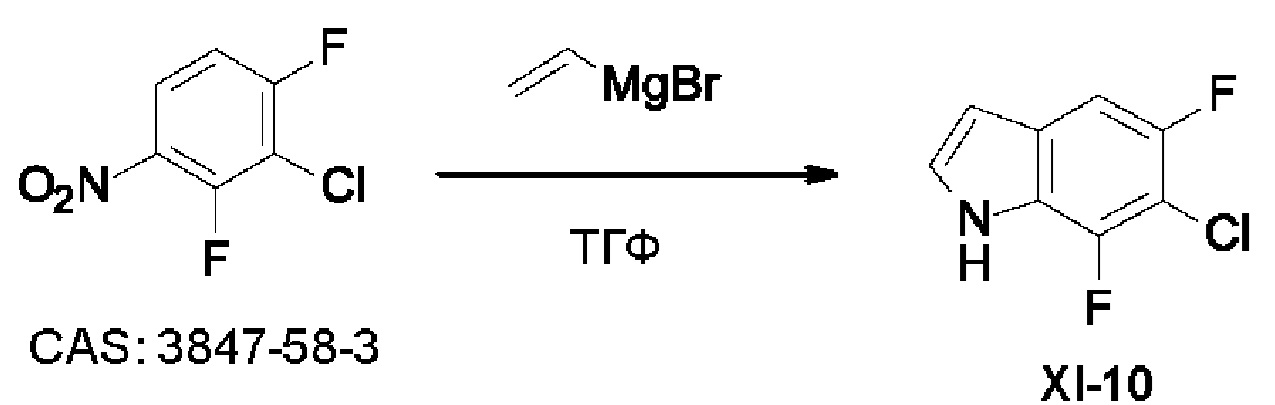
К раствору 2-хлор-1,3-дифтор-4-нитробензола (6 г, 31 ммоль) в THF (120 мл) при -78°С по каплям добавляли винилмагнийбромид (105 мл, 1М, 105 ммолей) и реакционную смесь перемешивали при такой же температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали насыщенным раствором NH4Cl (200 мл), смесь разбавляли с помощью Н2О (300 мл) и экстрагировали с помощью EtOAc (500 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 10% EtOAc в гексанах) и получали 6-хлор-5,7-дифтор-1Н-индол XI-10 (0,71 г) в виде коричневого твердого вещества.
Выход: 12%
ЖХМС в щелочной среде, методика 2 (ЭР-): 186 (М-Н)-, чистота 96%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,54-6,60 (m, 1Н) 7,44 (d, J=9,78 Гц, 1Н) 7,54 (t, J=2,69 Гц, 1Н) 11,92 (br s, 1Н).
В.11. Синтез 6-бром-7-хлор-1Н-индола XI-11:
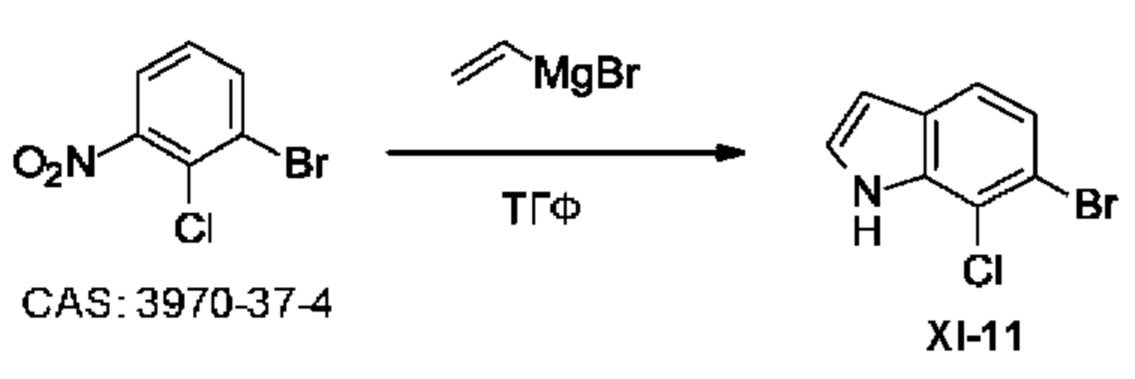
К раствору 1-бром-2-хлор-3-нитробензол (500 мг, 1,9 ммоля) в THF (6 мл) при -78°С по каплям добавляли винилмагнийбромид (7,6 мл, 1М, 7,6 ммоля) и реакционную смесь перемешивали при -78°С в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали насыщенным раствором NH4Cl (60 мл) и смесь экстрагировали с помощью EtOAc (3×50 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 2-5% EtOAc в гексанах) и получали 6-бром-7-хлор-1Н-индол XI-11 (0,15 г) в виде почти белого твердого вещества.
Выход: 32%
ЖХМС в щелочной среде, методика 2 (ЭР-): 228 (М-Н)-, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,59-6,60 (m, 1Н) 7,26 (t, J=2,4 Гц, 1H) 7,34 (d, J=8,4 Гц, 1H) 7,42 (d, J=8,4 Гц, 1H) 8,41 (brs, 1H).
В.12. Синтез 7-хлор-6-метокси-1Н-индола XI-12:
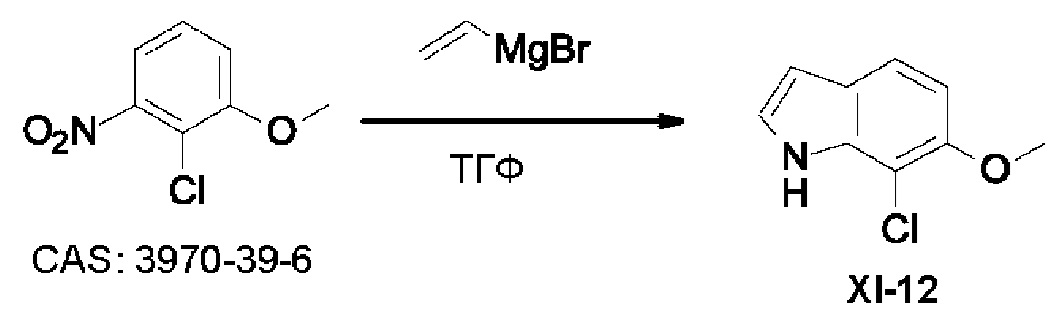
К раствору 2-хлор-1-метокси-3-нитробензола (500 мг, 2,67 ммоля) в THF (10,0 мл) при -78°С добавляли винилмагнийбромид (1,00 М, 8,00 мл, 8,00 ммоля). Реакционную смесь перемешивали при такой же температуре в течение 3 ч. За протеканием реакции следили с помощью TLC. Реакцию останавливали путем добавления насыщенного раствора NH4Cl (15 мл) и смесь экстрагировали этилацетатом (3×30 мл). Органический слой промывали рассолом (30 мл), отделяли и концентрировали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной хроматографии (силикагель, 100-200 меш, 2% EtOAc в гексанах) и получали 7-хлор-6-метокси-1Н-индол XI-12 (0,15 г) в виде белого твердого вещества.
Выход: 30%
1H ЯМР (400 МГц, DMSO-d6) δ 3,86 (s, 3Н) 6,44 (s, 1Н) 6,92 (d, J=8,80 Гц, 1Н) 7,26 (s, 1Н) 7,45 (d, J=8,80 Гц, 1Н) 11,15 (br s, 1Н).
В.13. Синтез 7-хлор-6-фтор-1Н-индола XI-13:
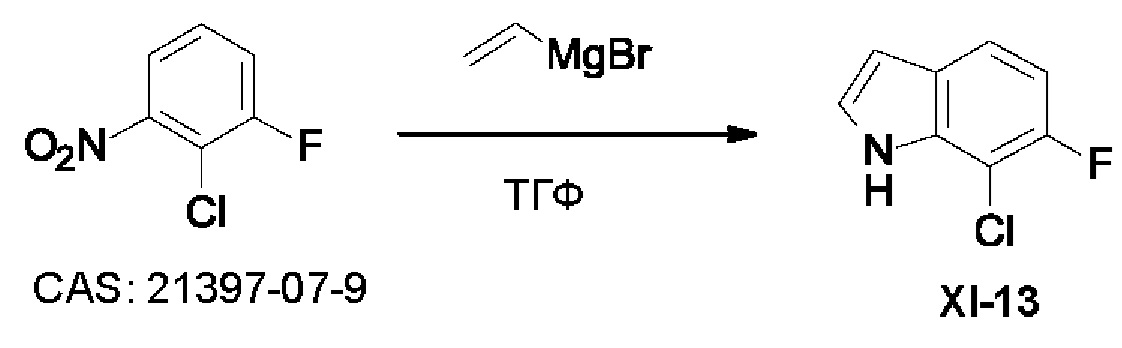
В инертной атмосфере к раствору 2-хлор-1-фтор-3-нитробензола (4,00 г, 22,8 ммоля) в безводном тетрагидрофуране (40,0 мл), охлажденному до -78°С, медленно добавляли винилмагнийбромид (1,00 М, 91,1 мл, 91,1 ммоля). Реакционную смесь перемешивали при -78°С в течение 3 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакцию останавливали путем добавления смеси к холодному насыщенному водному раствору NH4Cl (80 мл). Водный слой экстрагировали этилацетатом (50 мл × 2). Органический слой отделяли, сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали с помощью колоночной хроматографии на силикагеле (100-200 меш) с использованием 5% этилацетата в н-гексане и получали 7-хлор-6-фтор-1H-индол XI-13 (2,0 г) в виде бледно-желтого твердого вещества.
Выход: 45%
1Н ЯМР (400 МГц, DMSO-d6) δ 6,52-6,54 (m, 1Н) 7,00-7,07 (m, 1Н) 7,42 (t, J=2,69 Гц, 1Н) 7,49-7,55 (m, 1Н) 11,60 (br s, 1Н).
В.14. Синтез 6-(дифторметил)-1Н-пирроло[2,3-b]пиридина XI-14:
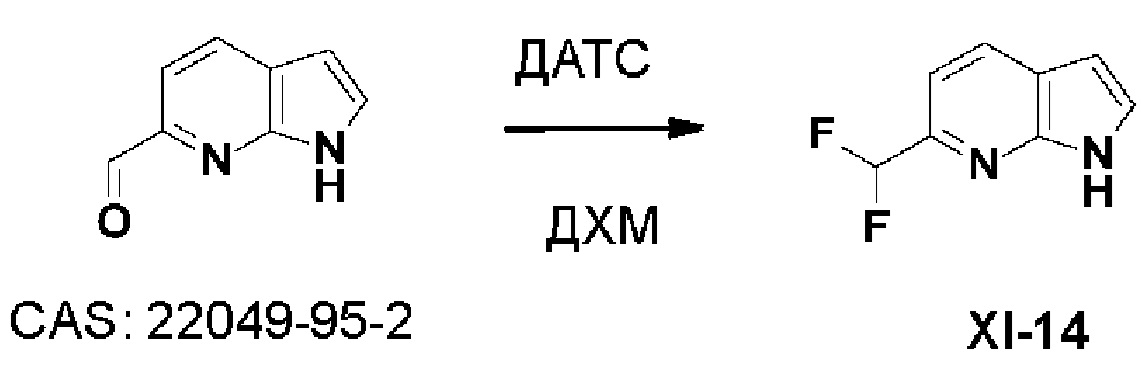
К раствору 1Н-пирроло[2,3-b]пиридин-6-карбальдегида (196 мг, 1,26 ммоля) в дихлорметане (4 мл) при 0°С добавляли диэтиламинотрифторид серы (ДАТС, 260 мкл, 1,91 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 4 ч. Реакционную смесь выливали в смесь льда и NaHCO3 и 3 раза экстрагировали с помощью с помощью DCM. Органическую фазу сушили над Na2SO4 и растворители концентрировали и получали 6-(дифторметил)-1Н-пирроло[2,3-b]пиридин XI-14 (96 мг) в виде коричневого твердого вещества
Выход: 45%.
ЖХМС в щелочной среде, методика 1 (ЭР+): 169 (М+Н)+, чистота 82%.
В.15. Синтез 6-хлор-7-(дифторметокси)-1Н-индола XI-15:
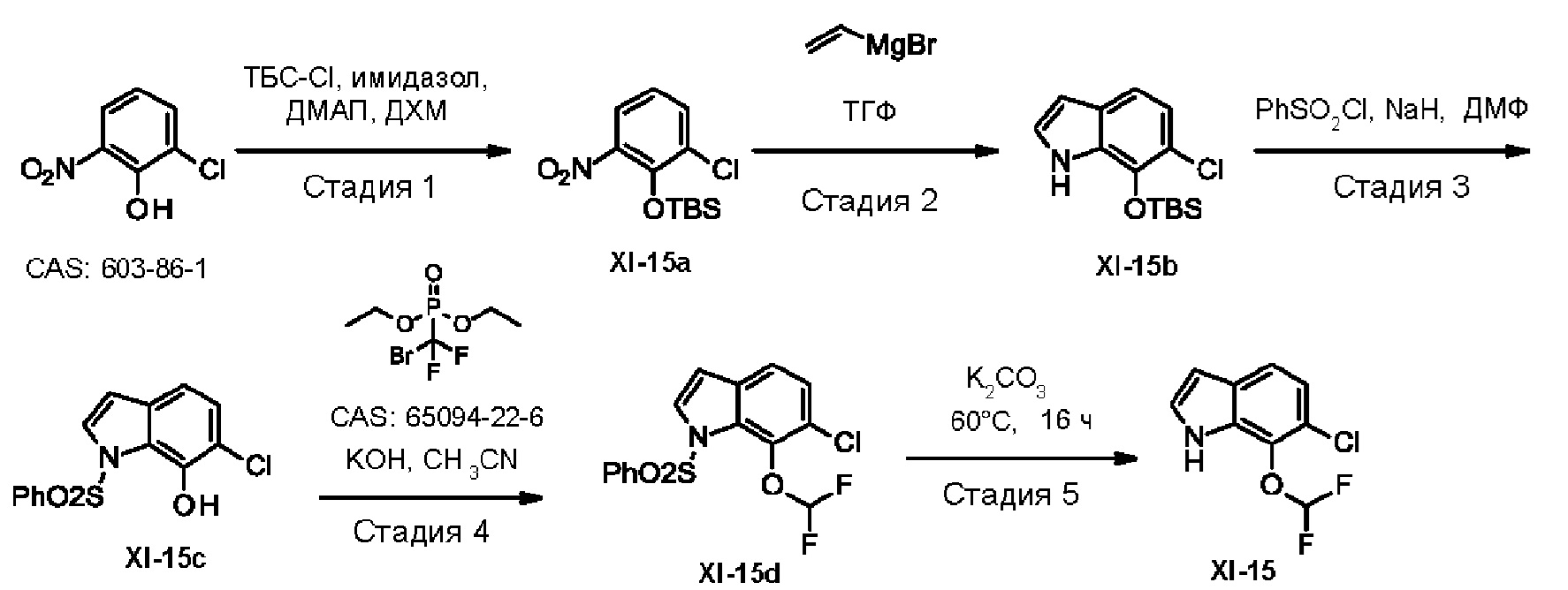
Стадия 1: Синтез трет-бутил(2-хлор-6-нитрофенокси)диметилсилана XI-15а:
К раствору 2-хлор-6-нитрофенола (4,00 г, 23,0 ммоля) в DCM (40 мл) добавляли имидазол (4,71 г, 69,1 ммоля) и TBS-Cl (трибутилсилилхлорид, 3,82 г, 25,4 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 4 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью DCM (2×120 мл). Органический слой отделяли, промывали насыщенным водным раствором NaHCO3 (2×100 мл), сушили над безводным Na2SO4 и концентрировали в вакууме и получали трет-бутил(2-хлор-6-нитрофенокси)диметилсилан XI-15а (7,50 г, неочищенный) в виде бледно-коричневой жидкости. Это соединение использовали в следующей реакции без дополнительной очистки.
1H ЯМР (400 МГц, DMSO-d6) δ 0,15 (s, 6Н) 0,97 (s, 9Н) 7,21 (t, J=8,40 Гц, 1Н) 7,81-7,89 (m, 2H).
Стадия 2: Синтез 7-((трет-бутилдиметилсилил)окси)-6-хлор-1Н-индола XI-15b:
К раствору трет-бутил(2-хлор-6-нитрофенокси)диметилсилана XI-15а (7,49 г, 26,0 ммоля) в THF (60 мл) при -78°С по каплям добавляли винилмагнийбромид (1 М, 104 мл, 104 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 3 ч. Затем реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали насыщенным раствором NH4Cl (150 мл) и смесь экстрагировали с помощью EtOAc (3×120 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью флэш-хроматографии (1,3% EtOAc в гексанах) и получали 7-((трет-бутилдиметилсилил)окси)-6-хлор-1Н-индол XI-15b (2,00 г) в виде бледно-желтой жидкости.
Выход: 21%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 280 (М-Н)-, чистота 77%.
1H ЯМР (400 МГц, DMSO-d6) δ 0,21 (s, 6Н) 1,05 (s, 9Н) 6,43 (dd, J=2,93, 1,96 Гц, 1Н) 6,96 (d, J=8,31 Гц, 1H) 7,17 (d, J=8,31 Гц, 1H) 7,30 (t, J=2,69 Гц, 1H) 10,60 (brs, 1H).
Стадия 3: Синтез 6-хлор-1-(фенилсульфонил)-1Н-индол-7-ола XI-15c:
К раствору 7-((трет-бутилдиметилсилил)окси)-6-хлор-1Н-индола XI-15b (1,69 г, 4,60 ммоля) в DMF (40 мл) порциями при 0°С добавляли NaH (0,92 г, 23,0 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. Добавляли PhSO2Cl (0,98 г, 5,53 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 8 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь медленно выливали в охлажденную льдом Н2О (100 мл) и экстрагировали с помощью EtOAc (2×80 мл). Органический слой отделяли, промывали с помощью Н2О (2×70 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, от 5 до 8% EtOAc в гексанах) и получали 6-хлор-1-(фенилсульфонил)-1Н-индол-7-ол XI-15с (0,71 г) в виде почти белого твердого вещества.
Выход: 41%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 306 (М-Н)-, чистота 81%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,77 (d, J=3,2 Гц, 1Н) 7,07 (d, J=8,4 Гц, 1H) 7,16 (d, J=8,4 Гц, 1H) 7,55-7,60 (m, 2H) 7,65-7,70 (m, 1H) 7,82 (d, J=3,2 Гц, 1H) 7,85-7,88 (m, 2H) 9,70 (brs, 1H).
Стадия 4: Синтез 6-хлор-7-(дифторметокси)-1-(фенилсульфонил)-1Н-индола XI-15d:
К раствору 6-хлор-1-(фенилсульфонил)-1Н-индол-7-ола XI-15c (0,70 г, 1,85 ммоля) в CH3CN (20 мл) при 0°С добавляли раствор KOH (0,52 г, 9,23 ммоля) в Н2О (4 мл) и перемешивали при такой же температуре в течение 15 мин. При 0°С по каплям добавляли бромдифторметилдиэтилфосфонат (1,64 мл, 9,23 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь разбавляли с помощью Н2О (60 мл) и экстрагировали с помощью EtOAc (2×50 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью флэш-хроматографии (от 2 до 6% EtOAc в гексанах) и получали 6-хлор-7-(дифторметокси)-1-(фенилсульфонил)-1H-индол XI-15d (0,41 г) в виде почти белого твердого вещества.
Выход: 53%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 356 (М-Н-), чистота 86%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,97(d, J=4,0 Гц, 1Н) 7,19 (t, J=74 Гц, 1H) 7,42 (d, J=8,0 Гц, 1H) 7,54-7,61 (m, 3H), 7,69 (t, J=7,2 Гц, 1H) 7,77-7,80 (m, 2H) 7,94(d, J=3,2 Гц, 1H).
Стадия 5: Синтез 6-хлор-7-(дифторметокси)-1Н-индола XI-15:
К раствору 6-хлор-7-(дифторметокси)-1-(фенилсульфонил)-1Н-индола XI-15d (0,41 г, 0,97 ммоля) в МеОН (6 мл) добавляли раствор K2CO3 (0,27 г, 1,95 ммоля) в Н2О (2 мл) и реакционную смесь нагревали при 60°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. Реакционную смесь концентрировали в вакууме. Остаток разбавляли с помощью Н2О (40 мл) и экстрагировали с помощью EtOAc (3×30 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью флэш-хроматографии (от 1 до 3% EtOAc в гексанах) и получали 6-хлор-7-(дифторметокси)-1Н-индол XI-15 (0,205 г, 91%) в виде почти белого твердого вещества.
Выход: 91%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 216 (М-Н)-, чистота 93%.
1Н ЯМР (400 МГц, DMSO-d6) δ 6,53-6,55 (m, 1Н) 7,11 (d, J=8,00 Гц, 1H) 7,17 (t, J=74 Гц, 1H) 7,42 (d, J=2,40 Гц, 1H) 7,51 (d, J=8,00 Гц, 1H) 11,52 (brs, 1H).
B.16. Синтез 6-хлор-7-(трифторметил)-1Н-индола XI-16:
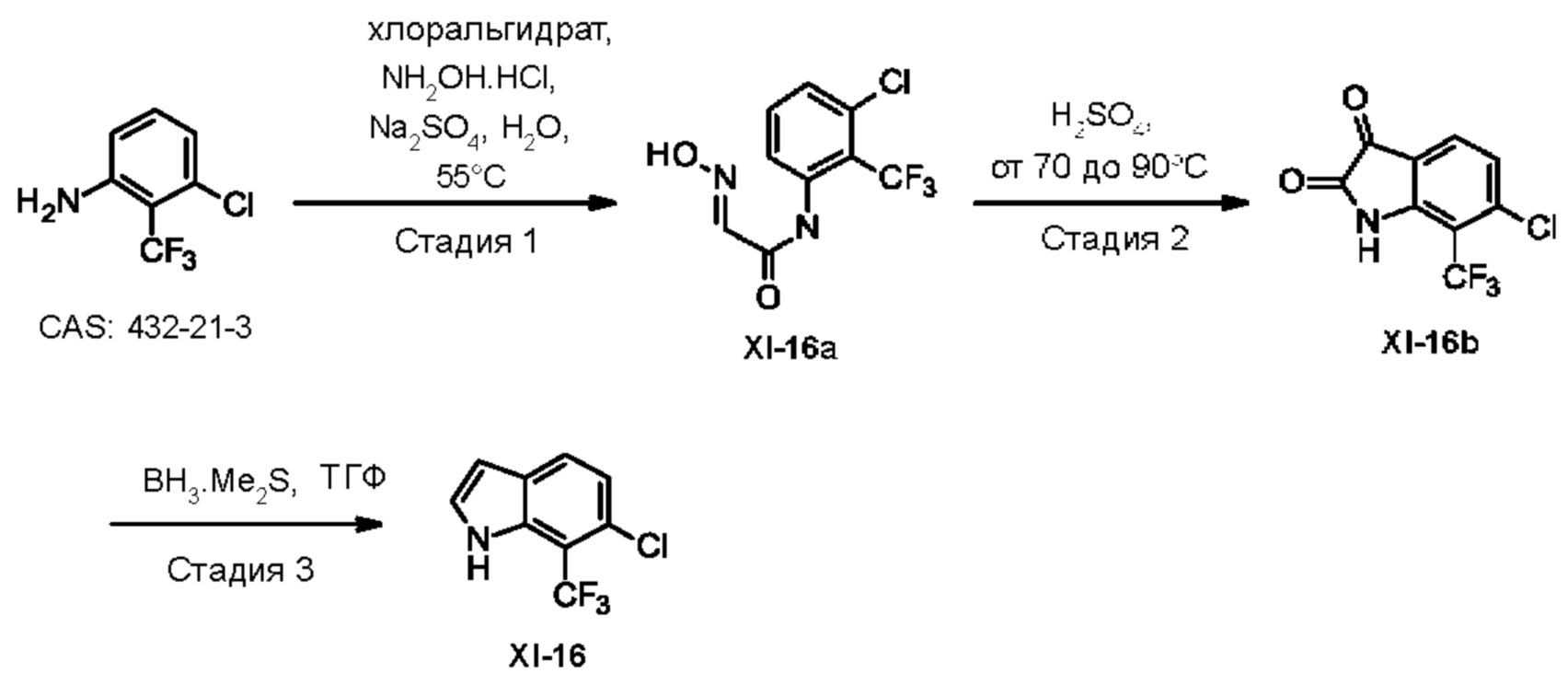
Стадия 1: Синтез (Е)-N-(3-хлор-2-(трифторметил)фенил)-2-(гидроксимино)ацетамида XI-16а:
При перемешивании к раствору хлоральгидрата (2,54 г, 15,3 ммоля) в Н2О (30 мл) добавляли Na2SO4 (0,87 г, 6,14 ммоля) и 3-хлор-2-(трифторметил)анилин (2,00 г, 10,2 ммоля), затем при комнатной температуре добавляли NH2OH⋅HCl (2,13 г, 30,7 ммоля). Реакционную смесь нагревали при 55°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью EtOAc (2×40 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью хроматографии с использованием CombiFlash (от 10 до 20% EtOAc в гексанах) и получали (E)-N-(3-хлор-2-(трифторметил)фенил)-2-(гидроксимино)ацетамид XI-16а (1,25 г) в виде почти белого твердого вещества.
Выход: 44%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 265 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,48 (d, J=7,82 Гц, 1H) 7,61 (s, 1Н) 7,62-7,68 (m, 2H) 10,10 (s, 1H) 12,36 (s, 1H).
Стадия 2: Синтез 6-хлор-7-(трифторметил)индолин-2,3-диона XI-16b:
При перемешивании к раствору H2SO4 (25 мл) при 70°С порциями добавляли (Е)-N-(3-хлор-2-(трифторметил)фенил)-2-(гидроксимино)ацетамид XI-16а (2,50 г, 8,92 ммоля) и реакционную смесь нагревали при 90°С в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали на дробленый лед (150 мл) и экстрагировали с помощью EtOAc (2×40 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлор-7-(трифторметил)индолин-2,3-дион XI-16b (2,31 г, неочищенный) в виде бледно-желтого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в щелочной среде, методика 2 (ЭР-): 248 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,34 (d, J=7,82 Гц, 1Н) 7,72 (d, J=7,82 Гц, 1H) 11,20 (brs, 1H).
Стадия 3: Синтез 6-хлор-7-(трифторметил)-1Н-индола XI-16:
При перемешивании к раствору 6-хлор-7-(трифторметил)индолин-2,3-диона XI-16b (0,90 г, 3,49 ммоля) в THF (20 мл) при 0°С добавляли BH3⋅Me2S (2 М, 5,23 мл, 10,5 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали 2 н. раствором HCl (20 мл), разбавляли с помощью Н2О (60 мл) и экстрагировали с помощью EtOAc (3×40 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Реакцию повторяли с использованием 0,90 г исходного вещества и неочищенные вещества, полученные в 2 реакциях, объединяли в DCM (50 мл) и очищали с помощью хроматографии с использованием CombiFlash (от 0 до 5% EtOAc в гексанах) и получали 6-хлор-7-(трифторметил)-1H-индол XI-16 (0,844 г) в виде бледно-желтой жидкости.
Выход: 53%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 218 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,64-6,65 (m, 1Н) 7,26 (d, J=8,37 Гц, 1H) 7,48-7,50 (m, 1H) 7,85 (d, J=8,37 Гц, 1H) 11,38 (brs, 1H).
С. Синтез промежуточных продуктов формулы XII
С.1. Методика А. Синтез 1Н-пирроло[3,2-h]хинолин-3-сульфоновой кислоты XII-1
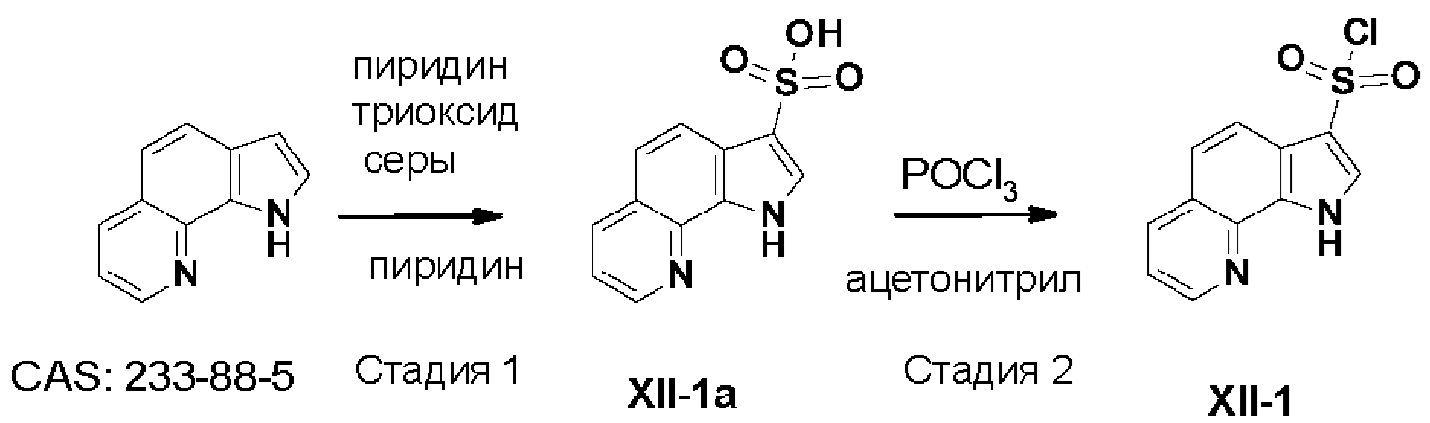
Стадия 1: Синтез 1Н-пирроло[3,2-h]хинолин-3-сульфоновой кислоты ХП-1а
К раствору 1Н-пирроло[3,2-Н]хинолина (400 мг, 2,3 ммоля) в пиридине (6 мл) при 0°С добавляли комплекс пиридин-триоксид серы (1,2 г, 3,5 ммоля). Затем реакционную смесь при перемешивании нагревали при 120°С в течение 2 ч, охлаждали до комнатной температуры и выпаривали досуха. Бежевое твердое вещество растворяли в воде и водную фазу промывали хлороформом (3×). При выдерживании в водной фракции образовывался осадок и его отфильтровывали, промывали водой и сушили в вакууме при 35°С и получали 470 мг 1Н-пирроло[3,2-Н]хинолин-3-сульфоновой кислоты XII-1а в виде бежевого твердого вещества.
Выход: 79%.
ЖХМС в щелочной среде, методика 1 (ЭР+): 249 (М+Н)+, чистота 100%.
Стадия 2: Синтез 1Н-пирроло[3,2-h]хинолин-3-сульфонилхлорида XII-1
В атмосфере аргона к раствору 1Н-пирроло[3,2-h]хинолин-3-сульфоновой кислоты XII-1а (855 мг, 3,44 ммоля) в ацетонитриле (8,5 мл), охлажденному до 0°С, по каплям добавляли оксихлорид фосфора (1,06 г, 6,88 ммоля). Затем реакционную смесь при перемешивании нагревали при 70°С в течение ночи. После охлаждения до комнатной температуры при энергичном перемешивании осторожно добавляли воду со льдом. Осаждалось твердое вещество и его отфильтровывали, промывали водой и сушили в вакууме при 35°С и получали 284 мг 1Н-пирроло[3,2-h]хинолин-3-сульфонилхлорида XII-1 в виде бежевого твердого вещества.
Выход: 27%.
ЖХМС в щелочной среде, методика 1 (ЭР+): 275 (М+Н)+, до проведения анализа реакцию в аликвоте смеси останавливали этиламином.
Приведенные ниже промежуточные продукты можно синтезировать по методике, аналогичной методике А. Если исходные вещества имеются в продаже, то для них указаны регистрационные номера CAS.
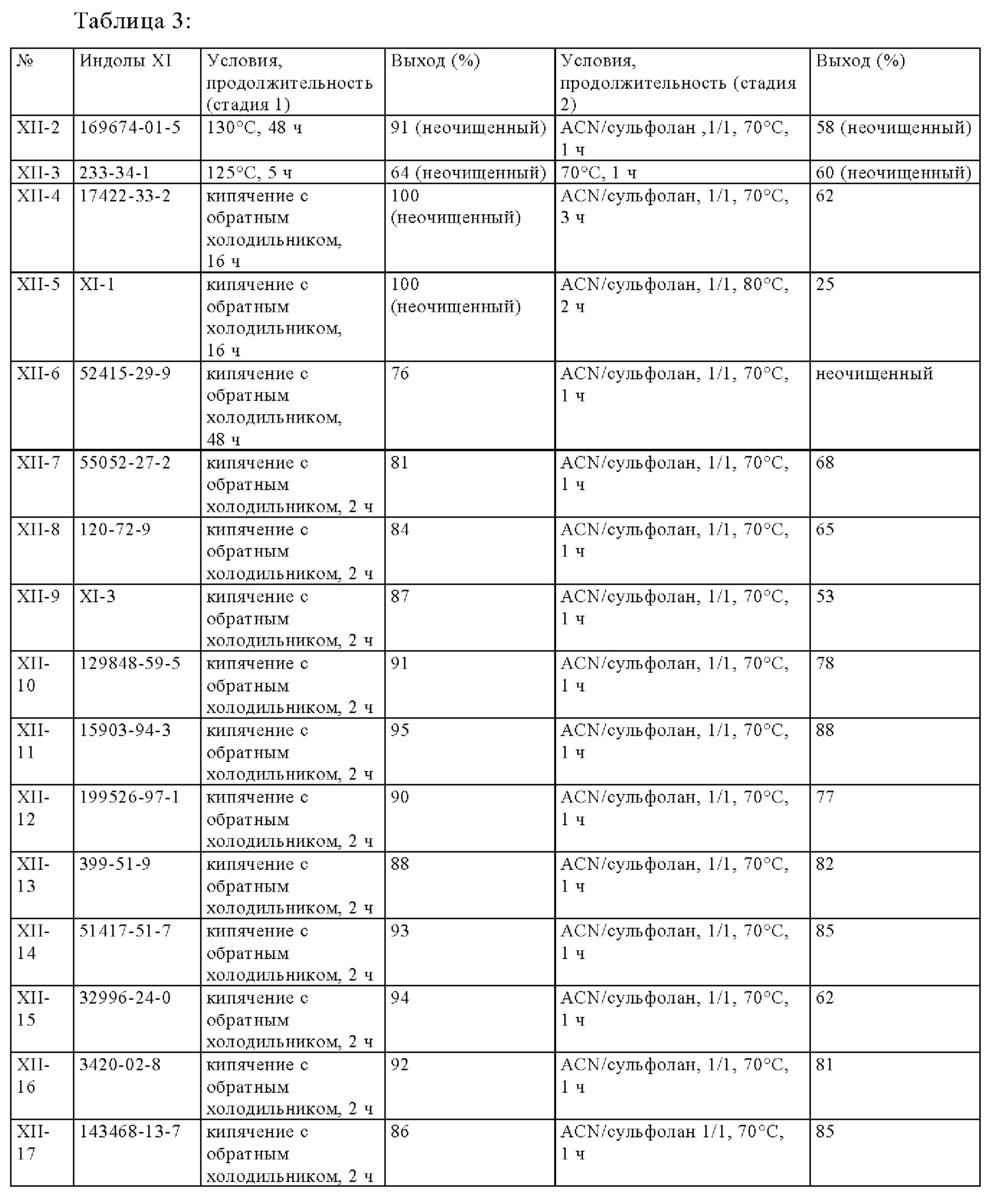
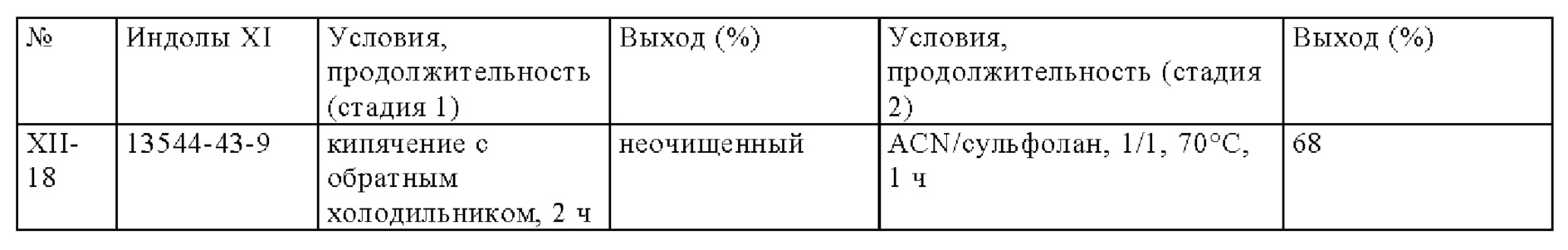
5,6-Дифтор-1H-индол-3-сульфонилхлорид XII-2
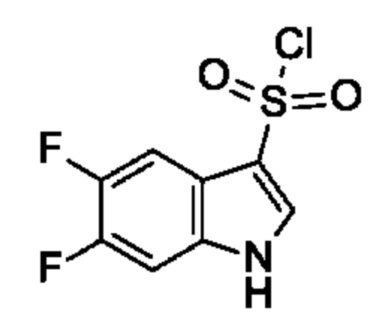
ЖХМС в щелочной среде, методика 2 (ЭР-): 250 (М-Н)-.
1Н-Бензо[g]индол-3-сульфонилхлорид XII-3
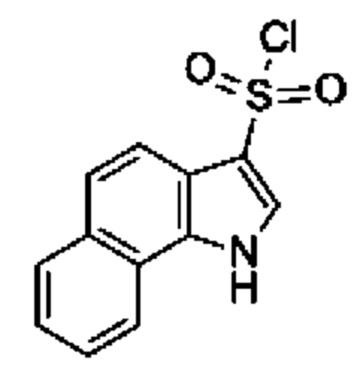
ЖХМС в щелочной среде, методика 1 (ЭР-): 246 (М-Н)-.
6-Хлор-1Н-индол-3-сульфонилхлорид XII-4
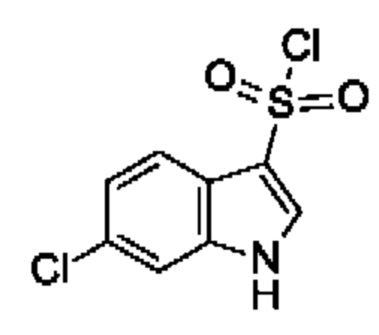
1H ЯМР (400 МГц, DMSO-d6) δ 7,32 (dd, J=8,56, 1,22 Гц, 1Н) 7,71 (s, 1H) 8,03 (d, J=8,80 Гц, 1H) 8,45 (d, J=2,93 Гц, 1H) 12,38 (brs, 1H).
6-Циклопропил-1Н-индол-3-сульфонилхлорид XII-5
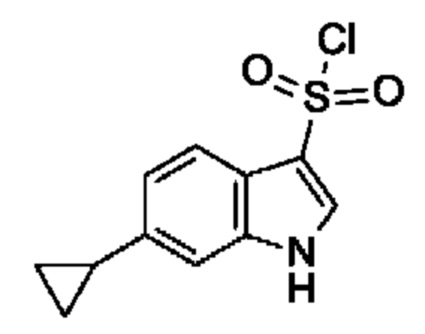
1H ЯМР (400 МГц, DMSO-d6) δ 0,71 (m, 2H) 0,92 (m, 2H) 1,96-2,01 (m, 1H) 7,27 (brs, 1H) 7,31 (s, 1H) 7,60 (d, J=8,31 Гц, 1H) 7,69 (d, J=8,31 Гц, 1H) 10,85 (brs, 1H).
6-Бром-1Н-индол-3-сульфонилхлорид XII-6
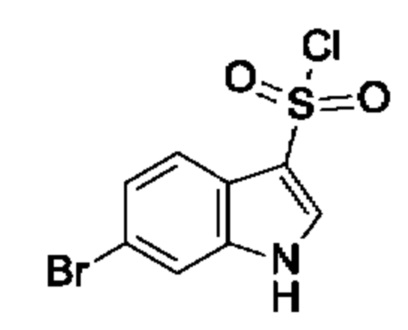
Не характеризовали.
6-Хлор-1Н-пирроло[2,3-b]пиридин-3-сульфонилхлорид XII-7
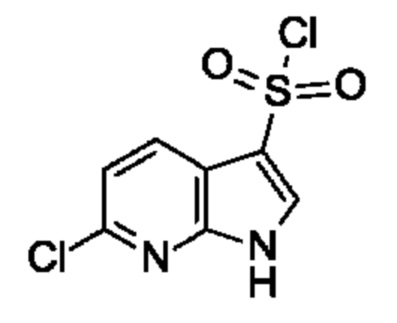
1H ЯМР (500 МГц, DMSO-d6) δ: 11,88 (s, 1H), 8,09 (d, J=8,2 Гц, 1H), 7,51 (s, 1Н), 7,17 (d, J=8,2 Гц, 1Н).
1H-Индол-3-сульфонилхлорид XII-8
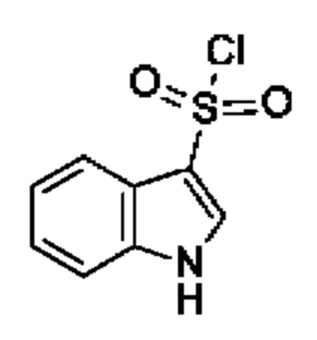
Не характеризовали.
6-(2-Метоксиэтокси)-1H-индол-3-сульфонилхлорид XII-9
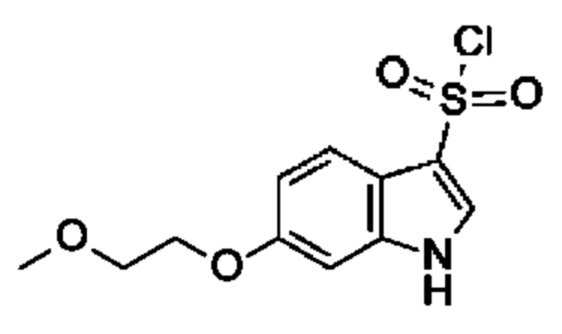
Не характеризовали.
1,6,7,8-Тетрагидроциклопента[g]индол-3-сульфонилхлорид XII-10
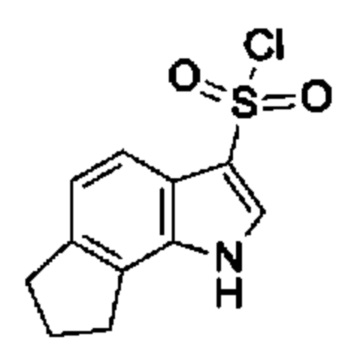
1H ЯМР (600 МГц, бензол-d6) δ:8,05 (d, J=8,2 Гц, 1Н), 7,16 (s, 1Н), 7,02 (d, J=8,1 Гц, 1Н),6,43 (s, 1Н),2,71 (t, J=7,4 Гц, 2Н), 2,38 (t, J=7,4 Гц, 2Н), 1,82-1,85 (m, 2Н).
6-Бензилокси-1H-индол-3-сульфонилхлорид XII-11
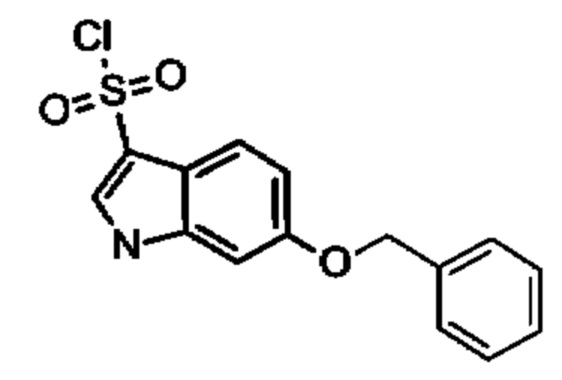
Не характеризовали.
4,6-Дифтор-1H-индол-3-сульфонилхлорид XII-12
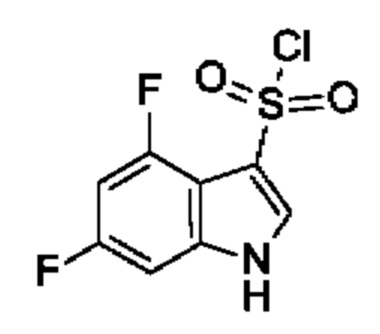
1H ЯМР (600 МГц, бензол-d6) δ: 7,54 (d, J=8,8 Гц, 1Н), 7,04-6,88 (m, 1H, 6,73 (s, 1Н), 6,46 (s, 1H).
6-Фтор-1H-индол-3-сульфонилхлорид XII-13
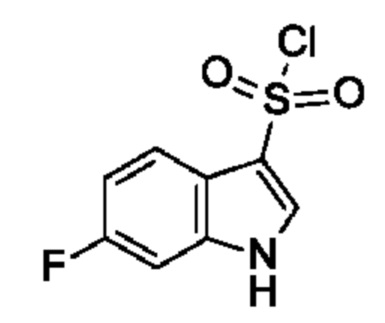
1Н ЯМР (600 МГц, бензол-d6) δ: 7,85 (dd, J=8,9, 5,1 Гц, 1Н), 6,87 (d, J=3,2 Гц, 1H), 6,77-6,78 (m, 1H), 6,37 (dd, J=8,8, 2,2 Гц, 1H), 6,32-6,10 (m, 1Н).
7-Бром-1H-индол-3-сульфонилхлорид XII-14
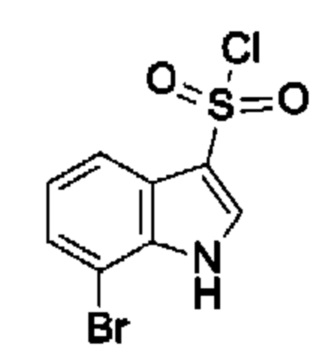
1H ЯМР (600 МГц, бензол-d6) δ: 8,03 (dd, J=8,8, 5,3 Гц, 1H), 7,33 (d, J=2,9 Гц, 1H), 6,88-6,89 (m, 1H), 6,44 (dd, J=9,1, 2,3 Гц, 1H), 6,36 (s, 1H).
6-Изопропил-1H-индол-3-сульфонилхлорид XII-15
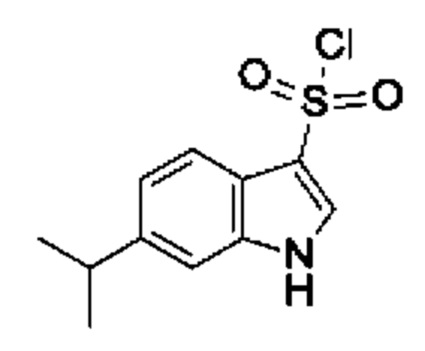
1Н ЯМР (600 МГц, бензол-d6) δ: 8,10 (d, J=8,3 Гц, 1Н), 7,16 (s, 1H), 6,98-6,97 (m, 1H), 6,62 (d, J=1,4 Гц, 1H), 6,50 (s, 1Н), 2,75 (септет, J=6,9 Гц, 1H), 1,15 (d, J=6,9 Гц, 6Н).
6-Метил-1Н-индол-3-сульфонилхлорид XII-16
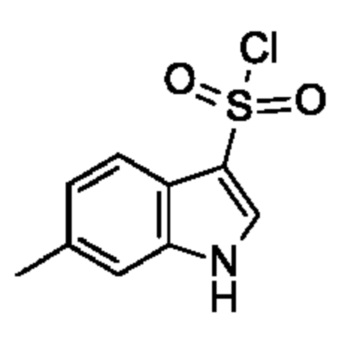
Не характеризовали.
6-Бром-1Н-пирроло[2,3-b]пиридин-3-сульфонилхлорид XII-17
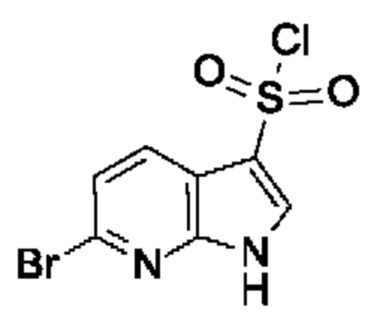
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,86 (s, 1H, NH), 8,09 (d, J=8,2 Гц, 1H), 7,50 (s, 1H), 7,16 (d, J=8,2 Гц, 1H).
6-Трифторметил-1Н-индол-3-сульфонилхлорид XII-18
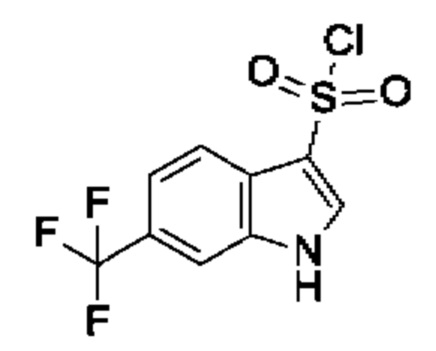
He характеризовали.
С.2. Синтез 1-(бензолсульфонил)-6-хлориндола XII-19
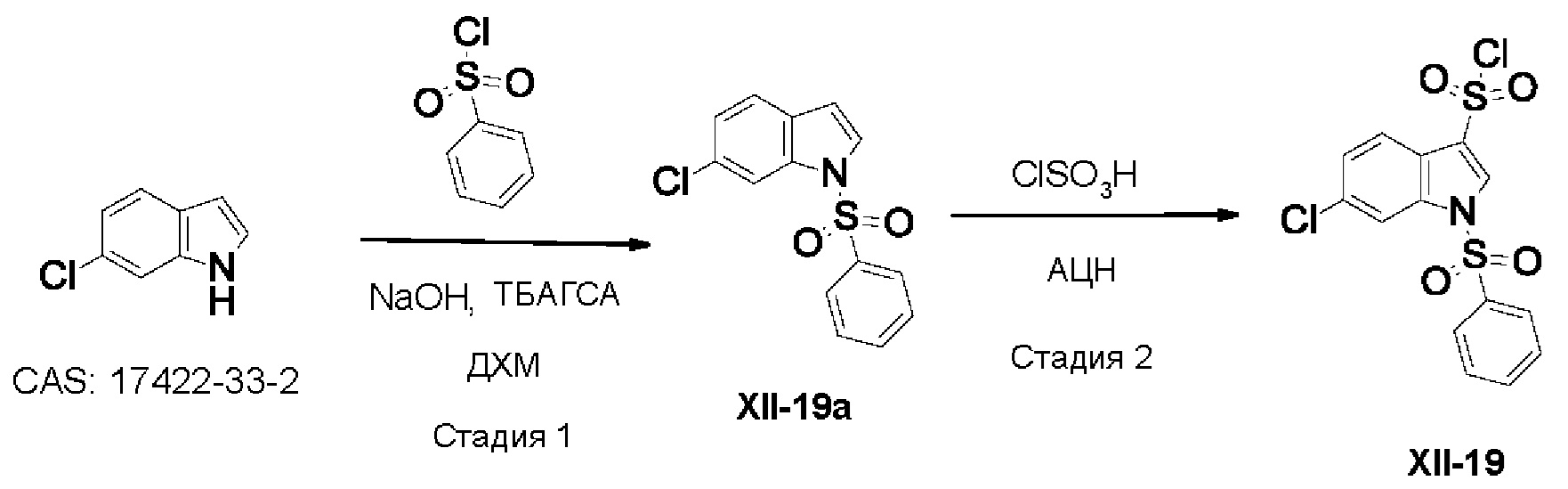
Стадия 1: Синтез 1-(бензолсульфонил)-6-хлориндола XII-19а
Суспензию тонкоизмельченного гидроксида натрия (24,5 г, 613 ммолей) в дихлорметане (300 мл) перемешивали в бане со льдом и одной порцией добавляли 6-хлориндол (30 г, 197 ммолей), затем тетрабутиламмонийгидросульфат (1,75 г, 5,15 ммоля). Затем в течение 20 мин по каплям добавляли бензолсульфонилхлорид (2,2 мл, 218 ммолей) и реакционную смесь перемешивали при 0°С в течение 1 ч. Затем баню со льдом удаляли и смесь перемешивали при комнатной температуре в течение еще 1 ч. После того, как ЖХ/МС указывала на завершение реакции, реакционную смесь фильтровали через слой целита и последний промывали с помощью DCM, объединенный фильтрат и промывочные растворы выпаривали досуха. Продукт растирали с эфиром, фильтровали, промывали небольшим количеством эфира, затем гексаном и сушили, фильтрат концентрировали и получали вторую порцию соединения, всего получали 50,54 г 1-(бензолсульфонил)-6-хлориндола XII-19а в виде светло-коричневого твердого вещества.
Выход: 88%.
1H ЯМР (400 МГц, CDCl3) δ 8,04 (dd, J=1,8, 0,9 Гц, 1Н), 7,91 (t, J=1,4 Гц, 1Н), 7,89 (t, J=1,8 Гц, 1H), 7,67-7,54 (m, 2Н), 7,53-7,48 (m, 2Н), 7,48-7,42 (m, 1Н), 7,23 (dd, J=8,4, 1,9 Гц, 1Н), 6,65 (dd, J=3,7, 0,9 Гц, 1Н).
Стадия 2: Синтез 1-(бензолсульфонил)-6-хлориндол-3-сульфонилхлорида XII-19
Раствор 1-(бензолсульфонил)-6-хлориндола XII-19а (50 г, 171,4 ммоля) в ацетонитриле (500 мл) перемешивали в бане со льдом и в течение 20 мин по каплям добавляли хлорсульфоновую кислоту (100,8 г, 856,8 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 5 дней. Затем ее при перемешивании в течение 20 мин медленно выливали в воду со льдом (2,2 л), фильтровали, несколько раз промывали водой и сушили с отсасыванием и получали 63,77 г 1-(бензолсульфонил)-6-хлориндол-3-сульфонилхлорида XII-19 в виде светло-коричневого твердого вещества.
Выход: 95%.
1H ЯМР (400 МГц, CDCl3) δ 8,36 (s, 1H), 8,07 (d, J=1,8 Гц, 1H), 8,04 (t, J=1,3 Гц, 1H), 8,02 (d, J=1,5 Гц, 1H), 7,91 (d, J=8,6 Гц, 1H), 7,79-7,70 (m, 1H), 7,68-7,59 (m, 2Н), 7,47 (dd, J=8,6, 1,8 Гц, 1Н).
С.3. Синтез 1-(бензолсульфонил)-6-хлорпирроло[2,3-b]пиридин-3-сульфонилхлорида XII-20
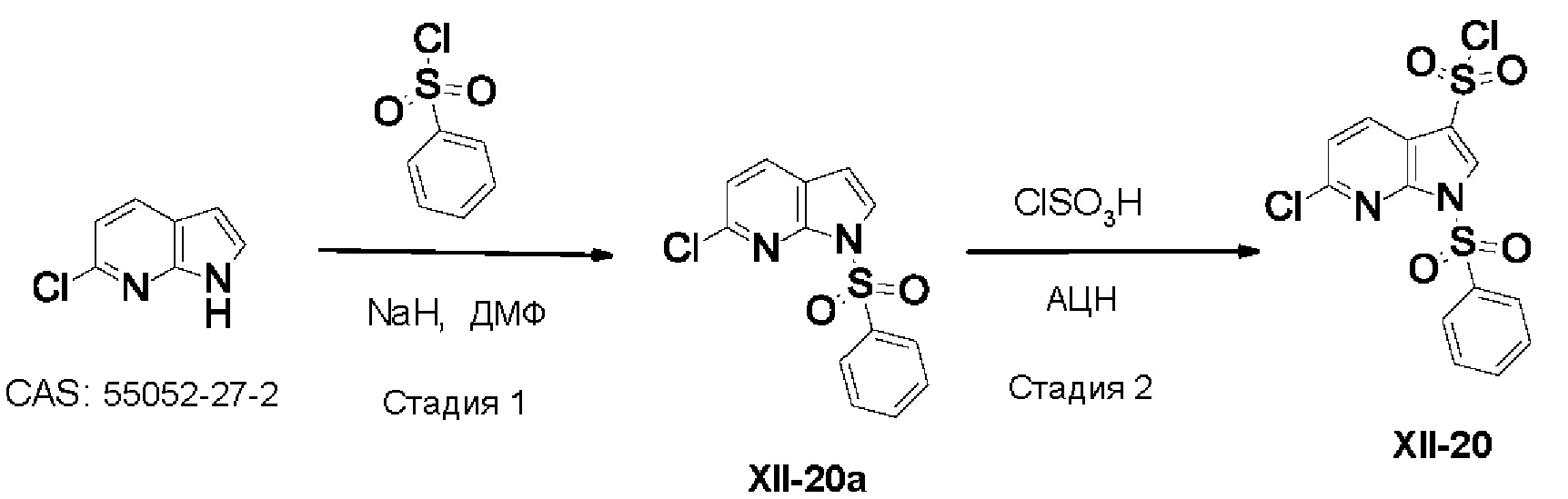
Стадия 1: Синтез 1-(бензолсульфонил)-6-хлорпирроло[2,3-b]пиридина XII-20а
К раствору 6-хлор-1Н-пирроло[2,3-b]пиридина (1,37 г, 8,97 ммоля) в DMF (100 мл) добавляли гидрид натрия (60% в парафине, 1 г, 41 ммоль). Раствор перемешивали в течение 30 мин, давая ему нагреться от 0°С до КТ. Затем по каплям добавляли хлорангидрид бензолсульфоновой кислоты (1,5 мл, 11,8 ммоля). Суспензию перемешивали при комнатной температуре в течение 3 ч и гидролизовали водой со льдом. Полученное твердое вещество отфильтровывали при пониженном давлении, тщательно промывали водой (75 мл) и в заключение петролейным эфиром (15 мл). Полученное вещество сушили при 60°С и очищали с помощью колоночной хроматографии (элюент: чистый дихлор метан) и получали 856 мг 1-(бензолсульфонил)-6-хлорпирроло[2,3-b]пиридина XII-20а в виде коричневатого твердого вещества.
Выход: 32%.
Стадия 2: Синтез 1-(бензолсульфонил)-6-хлорпирроло[2,3-b]пиридин-3-сульфонилхлорида XII-20
Полученный 1-(бензолсульфонил)-6-хлорпирроло[2,3-b]пиридин XII-20а (150 мг, 0,51 ммоля) растворяли в ацетонитриле (5 мл) и по каплям обрабатывали хлорсульфоновой кислотой (2 мл, 2,91 ммоля). Смесь кипятили с обратным холодильником в течение 3 ч, охлаждали до комнатной температуры, гидролизовали водой со льдом (50 мл) и нейтрализовывали насыщенным раствором гидрокарбоната натрия. Неочищенный продукт экстрагировали дихлорметаном (3 раза по 50 мл). Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали. Полученное вещество очищали с помощью колоночной хроматографии (элюент: чистый дихлорметан) и получали 163 мг 1-(бензолсульфонил)-6-хлорпирроло[2,3-b]пиридин-3-сульфонилхлорида XII-20 в виде желтоватого твердого вещества.
Выход: 81%
1H ЯМР (600 МГц, CDCl3) δ: 8,48 (s, 1Н), 8,32 (d, J=7,8 Гц, 2Н), 8,18 (d, J=8,3 Гц, 1H), 7,71 (t, J=7,5 Гц, 1H), 7,60 (t, J=7,9 Гц, 2Н), 7,41 (d, J=8,4 Гц, 1Н).
С.4. Синтез 1-(бензолсульфонил)-6-(циклопропилметокси)индол-3-сульфонилхлорида XII-21
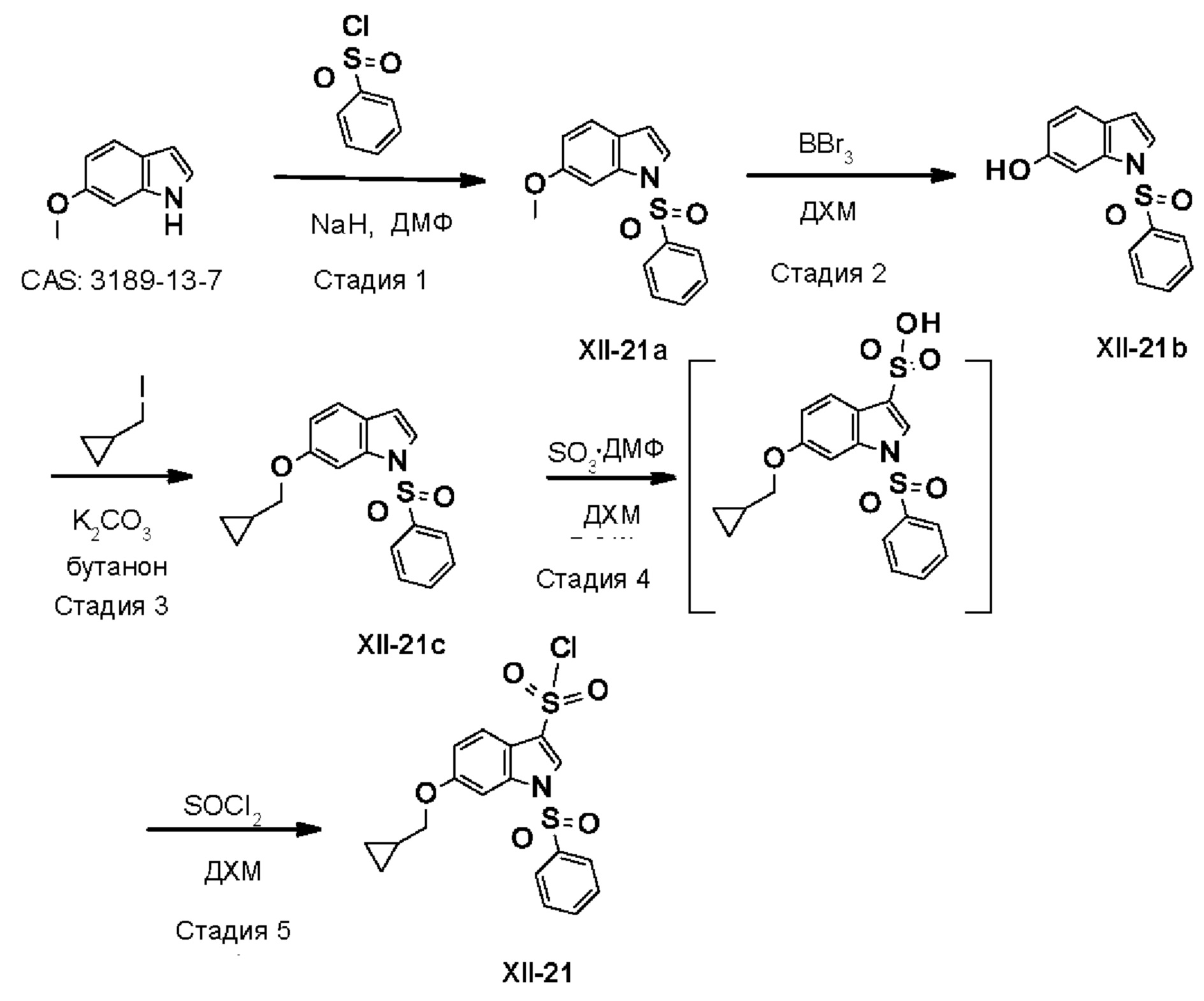
Стадия 1: Синтез 1-(бензолсульфонил)-6-метоксииндола XII-21а
К раствору 6-метоксииндола (2,5 г, 17 ммолей) в DMF (50 мл) при 0°С добавляли гидрид натрия (60% в парафине, 1,7 г, 71 ммоль). Суспензию перемешивали в течение 30 мин, затем нагревали до комнатной температуры. Затем раствор при перемешивании по каплям обрабатывали бензолсульфонилхлоридом (2,8 мл, 3,70 г, 22 ммоля). После перемешивания при комнатной температуре в течение 2,5 ч к реакционной смеси при энергичном перемешивании добавляли воду со льдом. Полученный осадок отфильтровывали при пониженном давлении, тщательно промывали водой (100 мл) и затем петролейным эфиром (10 мл). После сушки при 60°С получали 1-(бензолсульфонил)-6-метоксииндол XII-21а в виде бесцветного твердого вещества (3,2 г).
Выход: 65%
1H ЯМР (600 МГц, CDCl3) δ: 7,87-7,81 (m, 2Н), 7,53-7,48 (m, 2Н), 7,45-7,39 (m, 3Н), 7,36 (d, J=8,5 Гц, 1Н), 6,84 (dd, J=8,6/2,3 Гц, 1Н), 6,56 (dd, J=3,7/0,9 Гц, 1H), 3,85 (s, 3Н).
Стадия 2: Синтез 1-(бензолсульфонил)индол-6-ола XII-21b
К раствору 1-(бензолсульфонил)-6-метоксииндола XII-21а (1 г, 3,5 ммоля) в дихлорметане (30 мл) при комнатной температуре добавляли трибромид бора (2,18 г, 0,83 мл, 8,7 ммоля). После перемешивания при комнатной температуре в течение 30 мин исходное вещество больше не обнаруживали (за протеканием реакции следили с помощью TLC, элюент: чистый дихлорметан). Реакционную смесь гидролизовали путем добавления насыщенного раствора NaHCO3 (70 мл). Добавляли воду (50 мл) и водную фазу экстрагировали дихлорметаном (трижды по 75 мл). Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле 60 (элюент : дихлорметан) и получали 600 мг 1-(бензолсульфонил)индол-6-ола XII-21b в виде бесцветного твердого вещества.
Выход: 63%
1H ЯМР (600 МГц, DMSO-d6) δ 9,58 (s, 1Н, ОН), 7,93-7,85 (m, 2Н), 7,74-7,65 (m, 1H), 7,62-7,56 (m, 2Н), 7,54 (d, J=3,7 Гц, 1H), 7,39-7,29 (m, 2Н), 6,81-6,62 (m, 2Н).
Стадия 3: Синтез 1-(бензолсульфонил)-6-(циклопропилметокси)индола XII-21с
Смесь 1-(бензолсульфонил)индол-6-ола XII-21b (273 мг, 1,0 ммоля), циклопропилметилйодида (224 мг, 1,22 ммоля) и карбоната калия (276 мг, 2,0 ммоля) в бутаноне нагревали при 80°С в течение 16 ч. Затем растворитель удаляли при пониженном давлении и остаток обрабатывали водой (50 мл) и этилацетатом (50 мл). Органическую фазу отделяли и водную фазу дважды экстрагировали этилацетатом (по 50 мл). Объединенные органические экстракты сушили над MgSO4, фильтровали и выпаривали. Остаток очищали с помощью колоночной хроматографии на силикагеле 60 (элюент: чистый дихлорметан) и получали 1-(бензолсульфонил)-6-(циклопропилметокси)индол XII-21с в виде бесцветного твердого вещества (269 мг).
Выход: 82%.
Стадии 4 и 5: Синтез 1-(бензолсульфонил)-6-(циклопропилметокси)индол-3-сульфонилхлорида XII-21
К раствору 1-(бензолсульфонил)-6-(циклопропилметокси)индола XII-21с (130 мг, 0,39 ммоля) в дихлорметане (2 мл) добавляли комплекс SO3⋅DMF (75 мг, 0,49 ммоля). После перемешивания при комнатной температуре в течение 1,5 ч добавляли тионилхлорид (0,04 мл, 66 мг, 0,55 ммоля). После перемешивания при комнатной температуре в течение еще 20 ч растворитель выпаривали и маслообразный остаток очищали с помощью колоночной хроматографии на силикагеле 60 (элюент: чистый дихлорметан) и получали 160 мг 1-(бензолсульфонил)-6-(циклопропилметокси)индол-3-сульфонилхлорида XII-21 в виде бесцветного твердого вещества. Продукт дополнительно не характеризовали, а непосредственно использовали на следующих стадиях.
Выход: 95%.
С.5. Синтез 1-(бензолсульфонил)-6-метоксииндол-3-сульфонилхлорида XII-22
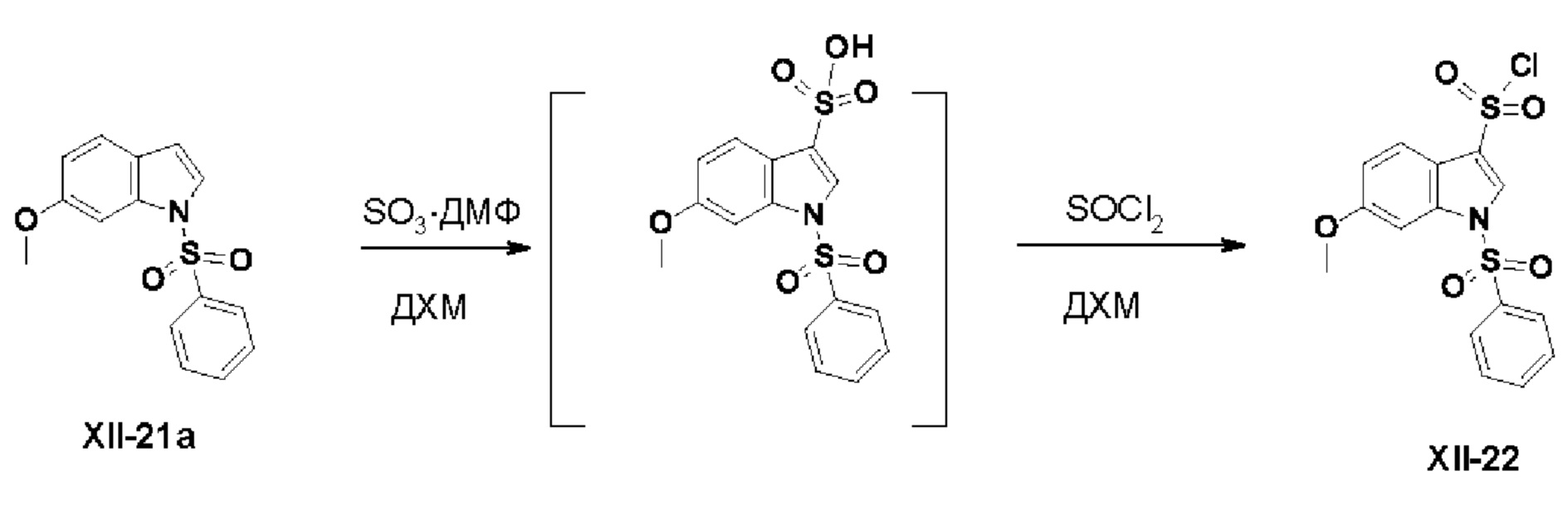
Раствор 1-(бензолсульфонил)-6-метоксииндола XII-21a (500 мг, 1,74 ммоля) в дихлорметане (15 мл) обрабатывали комплексом SO3⋅DMF (1,2 г, 7,8 ммоля) и перемешивали при комнатной температуре в течение 2 ч (за протеканием реакции следили с помощью TLC). Искомую промежуточную индолсульфоновую кислоту не выделяли. Затем добавляли тионилхлорид (1 мл, 14 ммолей) и смесь перемешивали при комнатной температуре в течение 16 ч. Смесь гидролизовали насыщенным раствором NaHCO3 (50 мл) и экстрагировали дихлорметаном (3 раза по 50 мл). Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали путем выпаривания в вакууме. Остаток очищали с помощью колоночной хроматографии (силикагель 60, элюент, дихлорметан/петролейный эфир = 1:1) и получали 1-(бензолсульфонил)-6-метоксииндол-3-сульфонилхлорид XII-22 в виде бесцветного твердого вещества (504 мг).
Выход: 75%
1H ЯМР (600 МГц, CDCl3) δ: 8,23 (s, 1Н), 8,00-7,93 (m, 2Н), 7,80 (d, J=8,8 Гц, 1H), 7,70-7,63 (m, 1H), 7,59-7,53 (m, 2Н), 7,47 (d, J=2,2 Гц, 1H), 7,06 (dd, J=8,8, 2,2 Гц, 1H), 3,89 (s, 3Н).
С.6. Синтез 1-(бензолсульфонил)-6-(тетрагидрофуран-2-илметокси)индол-3-сульфонилхлорида XII-23
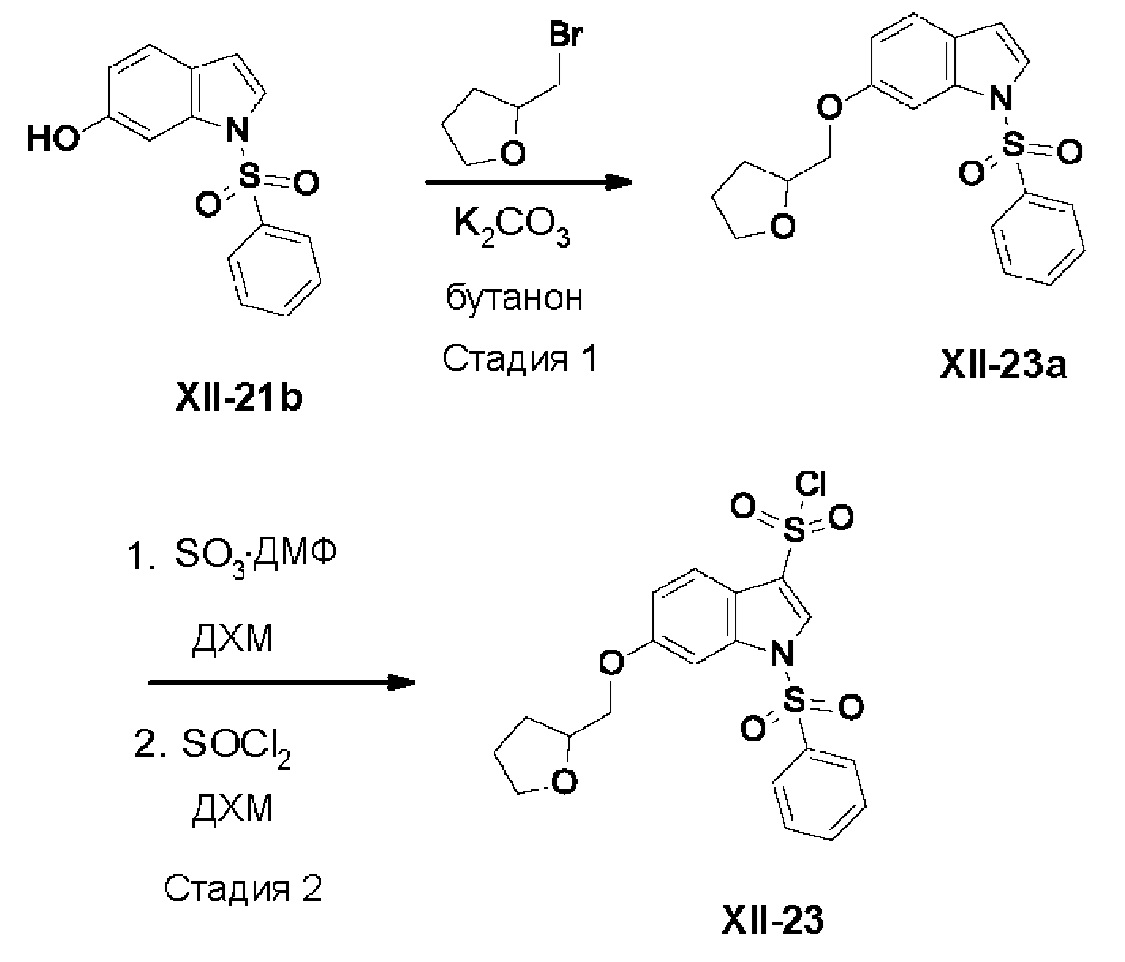
Стадия 1: Синтез 1-(бензолсульфонил)-6-(тетрагидрофуран-2-илметокси)индола XII-21а
Смесь 1-(бензолсульфонил)индол-6-ола XII-21b (273 мг, 1,0 ммоля), 2-бромметилтетрагидрофурана (330 мг, 2,0 ммоля) и K2CO3 (276 мг, 2,0 ммоля) в бутаноне нагревали при 85°С в течение 3 дней. Затем растворитель удаляли при пониженном давлении и остаток обрабатывали водой (50 мл) и этилацетатом (50 мл). Органическую фазу отделяли и водную фазу дважды экстрагировали этилацетатом (по 50 мл). Объединенные органические экстракты сушили над MgSO4, фильтровали и выпаривали. Остаток очищали с помощью колоночной хроматографии на силикагеле 60 (элюент: чистый дихлорметан) и получали 1-(бензолсульфонил)-6-(тетрагидрофуран-2-илметокси)индол XII-23а в виде бесцветного твердого вещества (214 мг).
Выход: 60%.
Стадия 2: Синтез 1-(бензолсульфонил)-6-(тетрагидрофуран-2-илметокси)индол-3-сульфонилхлорида XII-23
К раствору 1-(бензолсульфонил)-6-(тетрагидрофуран-2-илметокси)индола XII-23а (100 мг, 0,28 ммоля) в дихлорметане (2 мл) добавляли комплекс SO3⋅DMF (52 мг, 0,34 ммоля). После перемешивания при комнатной температуре в течение 2 ч добавляли тионилхлорид (0,1 мл, 81 мг, 1,4 ммоля). После перемешивания при комнатной температуре в течение еще 16 ч растворитель выпаривали и маслообразный остаток очищали с помощью колоночной хроматографии на силикагеле 60 (элюент: чистый дихлорметан) и получали 64 мг 1-(бензолсульфонил)-6-(тетрагидрофуран-2-илметокси)индол-3-сульфонилхлорида XII-23 в виде бесцветного твердого вещества. Продукт дополнительно не характеризовали, а непосредственно использовали на следующих стадиях.
Выход: 50%.
С.7. Синтез 6-хлорбензофуран-3-сульфонилхлорида XII-24:
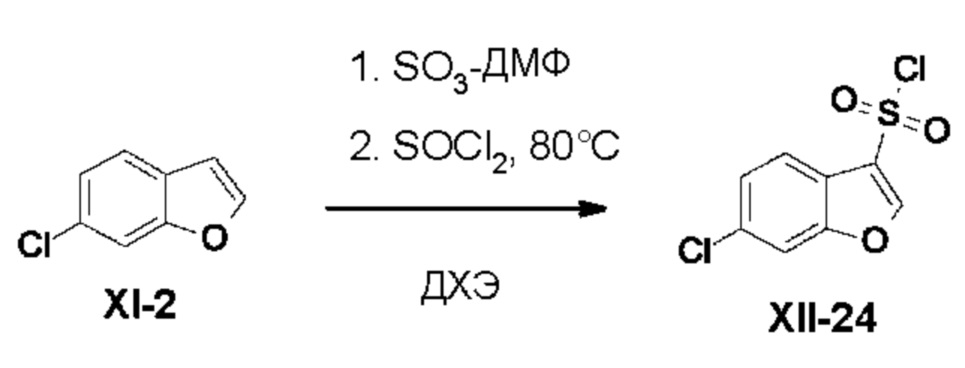
К раствору комплекса SO3-DMF (0,78 г, 4,90 ммоля) в 1,2-дихлорэтане (ДХЭ, 10 мл) добавляли 6-хлорбензофуран XI-2 (0,50 г, 3,27 ммоля) и реакционную смесь нагревали при 70°С в течение 16 ч. Реакционную смесь охлаждали до 0°С, затем добавляли SOCl2 (0,52 мл, 7,16 ммоля). Реакционную смесь нагревали при 80°С в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь концентрировали в вакууме и получали 6-хлорбензофуран-3-сульфонилхлорид XII-24 (0,48 г) в виде красного полужидкого вещества. Получение продукта подтверждали только с помощью TLC.
Выход: 60%.
С.8. Синтез 6-хлор-7-метокси-1Н-индол-3-сульфонилхлорида XII-25:
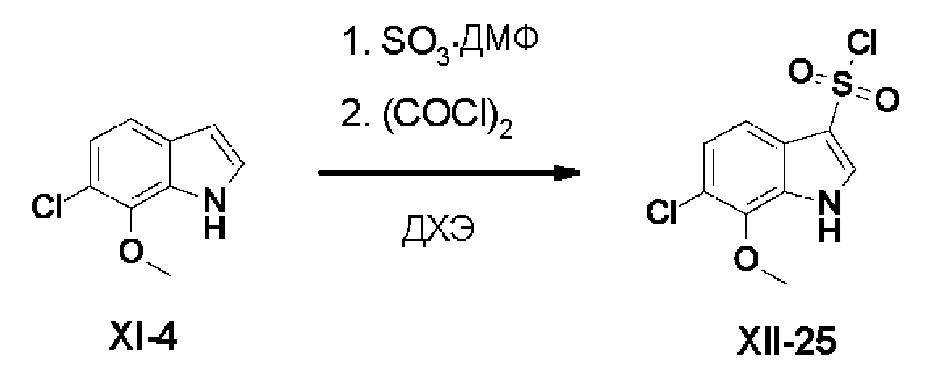
К раствору 6-хлор-7-метокси-1Н-индола XI-4 (0,10 г, 0,55 ммоля) в ДХЭ (5 мл) добавляли комплекс SO3-DMF (0,12 г, 0,82 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакцию останавливали с помощью Н2О (15 мл) и смесь промывали с помощью DCM (2×10 мл). Водный слой концентрировали в вакууме. Полученное неочищенное вещество растворяли в ДХЭ (5 мл), затем при 0°С добавляли оксалилхлорид (0,23 мл, 2,76 ммоля). Реакционную смесь перемешивали при 0°С в течение 10 мин и при комнатной температуре в течение 5 ч. Реакционную смесь концентрировали в вакууме и получали 6-хлор-7-метокси-1Н-индол-3-сульфонилхлорид XII-25 (0,31 г, неочищенный) в виде коричневого масла. Это соединение использовали в следующей реакции без дополнительной очистки.
1H ЯМР (400 МГц, DMSO-d6) δ 3,88 (s, 3Н) 7,02 (d, J=8,80 Гц, 1H) 7,33 (d, J=2,40 Гц, 1Н) 7,48 (d, J=8,80 Гц, 1Н) 7,95 (s, 1H).
С.9. Синтез 6-хлор-7-фтор-1Н-индол-3-сульфонилхлорида XII-26:
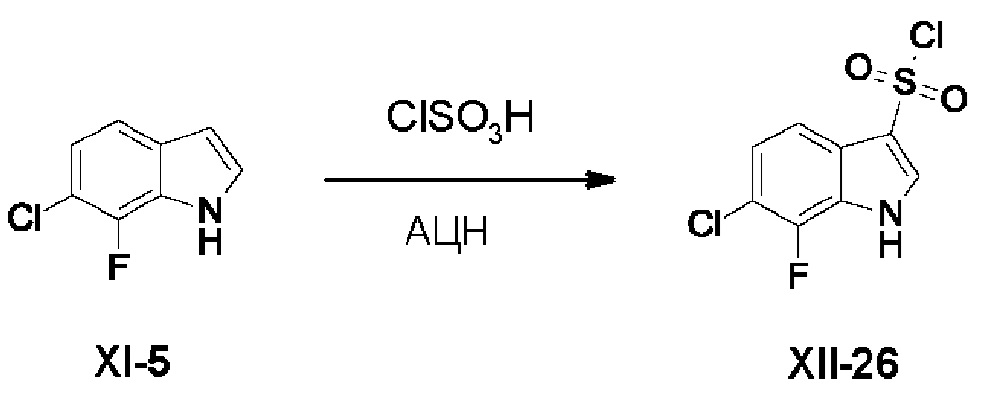
К раствору 6-хлор-7-фтор-1Н-индола XI-5 (0,2 г, 0,78 ммоля) в CH3CN (5 мл) при 0°С добавляли ClSO3H (1 мл) и реакционную смесь перемешивали при комнатной температуре в течение 12 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью EtOAc (2×150 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлор-7-фтор-1Н-индол-3-сульфонилхлорид XII-26 (0,2 г) в виде коричневого полужидкого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 87%
ЖХМС в щелочной среде, методика 2 (ЭР+): 248,00 (М+Н)+ (соответствует сульфоновой кислоте), чистота 89%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,08-7,12 (m, 1Н) 7,41-7,44 (m, 1H) 7,53 (d, J=8,31 Гц, 1H) 11,83 (brs, 1H).
C.10. Синтез 6-(трифторметил)-1Н-пирроло[2,3-b]пиридин-3-сульфонилхлорида XII-27:
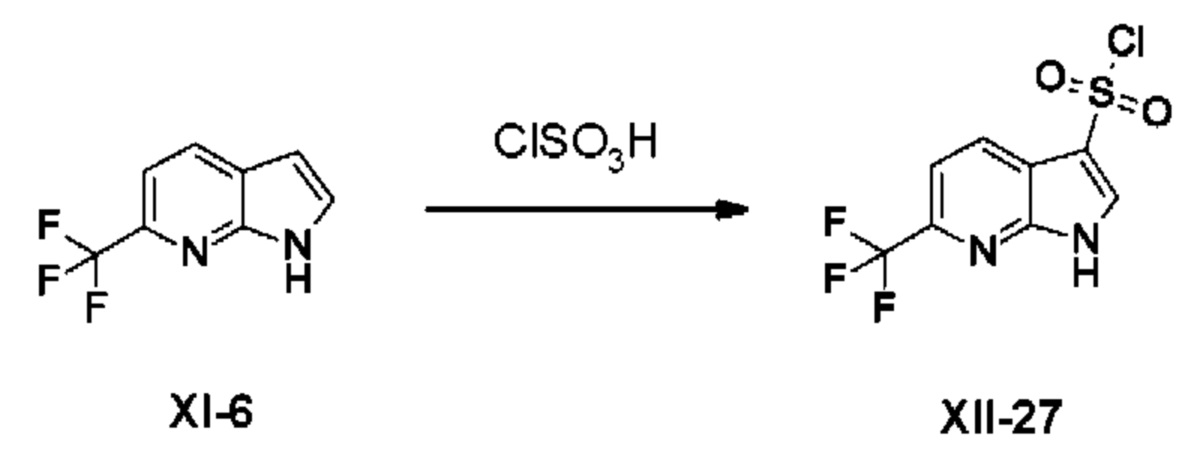
К 6-(трифторметил)-1Н-пирроло[2,3-b]пиридину XI-6 (0,45 г, 2,16 ммоля) при 0°С по каплям добавляли ClSO3H (4,50 мл) и реакционную смесь перемешивали при такой же температуре в течение 10 мин. Затем реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали на лед и экстрагировали с помощью EtOAc (60 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-(трифторметил)-1Н-пирроло[2,3-b]пиридин-3-сульфонилхлорид XII-27 (0,41 г) в виде коричневого полужидкого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 58%
ЖХМС в щелочной среде, методика 2 (ЭР+): 285 (М+Н)+, чистота 83%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,56 (d, J=7,83 Гц, 1Н) 7,71 (s, 1H) 8,29 (d, J=8,31 Гц, 1H) 12,12 (brs, 1H).
C.11. Синтез 5-бром-6-хлор-1Н-индол-3-сульфонилхлорида XII-28:
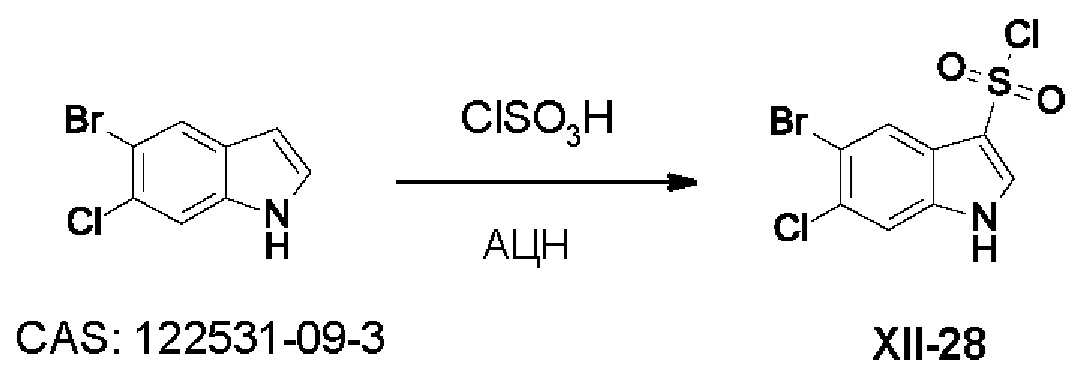
К раствору 5-бром-6-хлор-1Н-индола (2,00 г, 8,68 ммоля) в CH3CN (50 мл) при 0°С добавляли ClSO3H (10,1 г, 86,8 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь разбавляли охлажденной льдом Н2О (100 мл) и экстрагировали с помощью EtOAc (2×50 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 5-бром-6-хлор-1Н-индол-3-сульфонилхлорид XII-28 (2,50 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 88%
1H ЯМР (400 МГц, DMSO-d6) δ 7,91 (s, 1Н) 8,44 (s, 1H) 8,49 (d, J=2,80 Гц, 1H) 12,89 (brs, 1H).
C.12. Синтез 7-бром-6-хлор-1Н-индол-3-сульфонилхлорида XII-29:
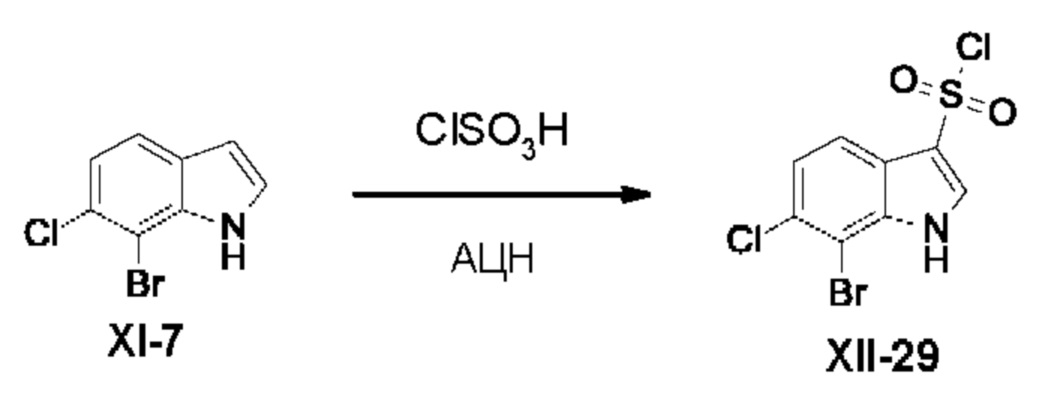
К раствору 7-бром-6-хлор-1Н-индола XI-7 (1,50 г, 6,26 ммоля) в CH3CN (30 мл) при 0°С добавляли ClSO3H (2 мл) и реакционную смесь перемешивали при такой же температуре в течение 15 мин. Затем реакционную смесь перемешивали при комнатной температуре в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью EtOAc (50 мл) и Н2О (100 мл) и водный слой экстрагировали с помощью EtOAc (300 мл). Объединенный органический слой сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали путем промывки пентаном (10 мл) и получали 7-бром-6-хлор-1Н-индол-3-сульфонилхлорид XII-29 (1,40 г) в виде почти белого твердого вещества.
Выход: 67%
ЖХМС в щелочной среде, методика 2 (ЭР-): 308,00 (М-Н)- (соответствует сульфоновой кислоте), чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,23 (d, J=8,80 Гц, 1H) 7,39 (d, J=2,93 Гц, 1Н) 7,73 (d, J=8,31 Гц, 1H) 11,46 (brs, 1H).
C.13. Синтез 6-бром-4-фтор-1Н-индол-3-сульфонилхлорида XII-30:
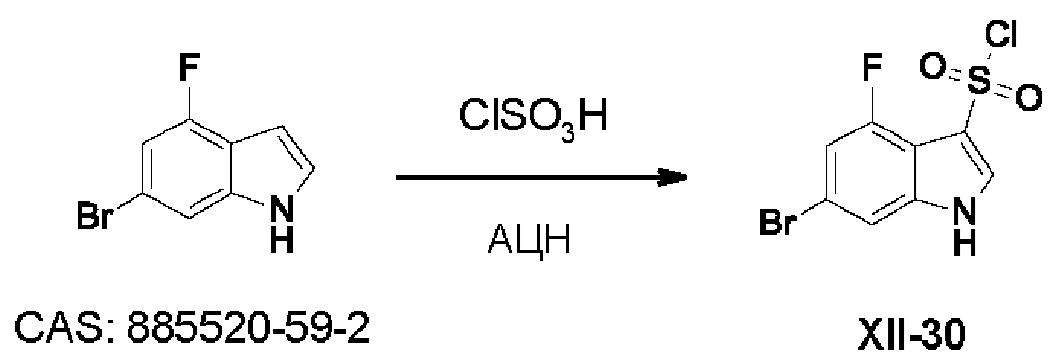
К раствору 6-бром-4-фтор-1Н-индола (0,25 г, 1,17 ммоля) в CH3CN (5 мл) при 0°С добавляли ClSO3H (0,40 мл) и реакционную смесь перемешивали при такой же температуре в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. Реакцию повторяли с использованием 0,25 г исходного вещества и неочищенные смеси, полученные в 2 реакциях, объединяли. После завершения реакции реакцию останавливали охлажденной льдом Н2О (100 мл) и смесь экстрагировали с помощью EtOAc (300 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-бром-4-фтор-1H-индол-3-сульфонилхлорид XII-30 (0,255 г) в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 22%
ЖХМС в щелочной среде, методика 2 (ЭР+): 294,00 (М+Н)+ (соответствует сульфоновой кислоте), чистота 62%.
С.14. Синтез 6-хлор-5-фтор-1Н-индол-3-сульфонилхлорида XII-31:
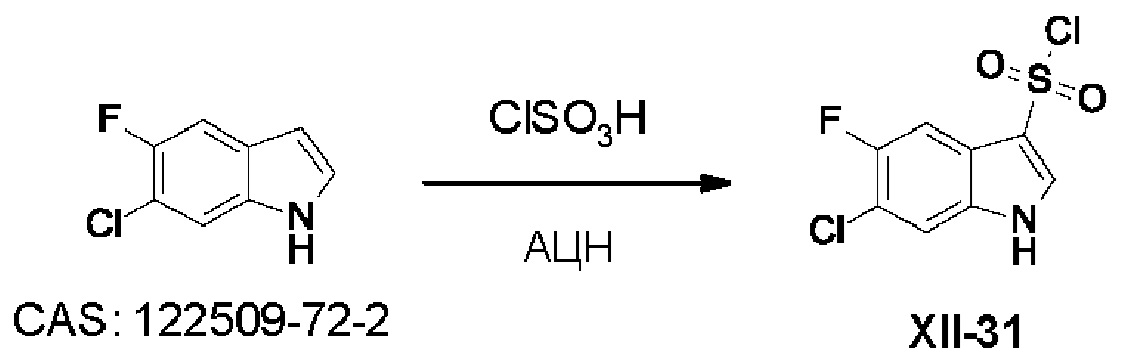
К раствору 6-хлор-5-фтор-1Н-индола (0,50 г, 2,95 ммоля) в CH3CN (5 мл) при 0°С добавляли ClSO3H (0,5 мл) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали охлажденной льдом Н2О (20 мл), смесь фильтровали, промывали с помощью Н2О (25 мл) и сушили в вакууме и получали 6-хлор-5-фтор-1Н-индол-3-сульфонилхлорид XII-31 (0,33 г) в виде бледно-коричневого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 42%
1H ЯМР (400 МГц, DMSO-d6) δ 7,49 (d, J=2,45 Гц, 1Н) 7,52-7,57 (m, 2H) 11,33 (brs, 1H).
С.15. Синтез 6-хлор-7-(2,2-дифторэтокси)-1Н-индол-3-сульфонилхлорида XII-32:
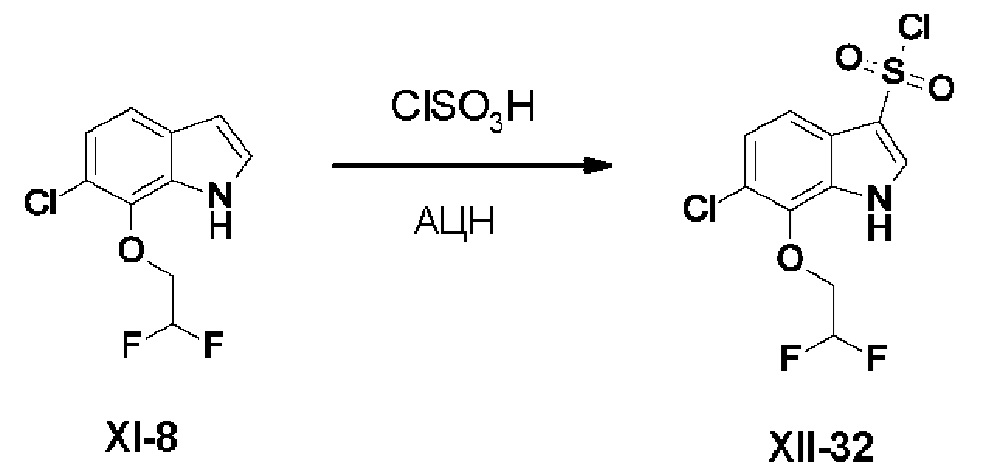
К раствору 6-хлор-7-(2,2-дифторэтокси)-1H-индола XI-8 (0,07 г, 0,30 ммоля) в CH3CN (3 мл) при 0°С добавляли ClSO3H (0,30 мл) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали в охлажденную льдом Н2О (20 мл) и экстрагировали с помощью EtOAc (15 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлор-7-(2,2-дифторэтокси)-1H-индол-3-сульфонилхлорид XII-32 (0,09 г) в виде бледно-коричневого полужидкого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 90%
1H ЯМР (400 МГц, DMSO-d6) δ 4,31-4,46 (m, 2 Н) 6,30-6,57 (m, 1Н) 7,03-7,05 (d, J=8,8 Гц, 1Н) 7,38 (s, 1Н) 7,78-7,80 (d, J=8,0 Гц, 1Н) 11,38 (br s, 1Н).
С.16. Синтез 5-(бензолсульфонил)-[1,3]диоксоло[4,5-f]индол-7-сульфонилхлорида XII-33
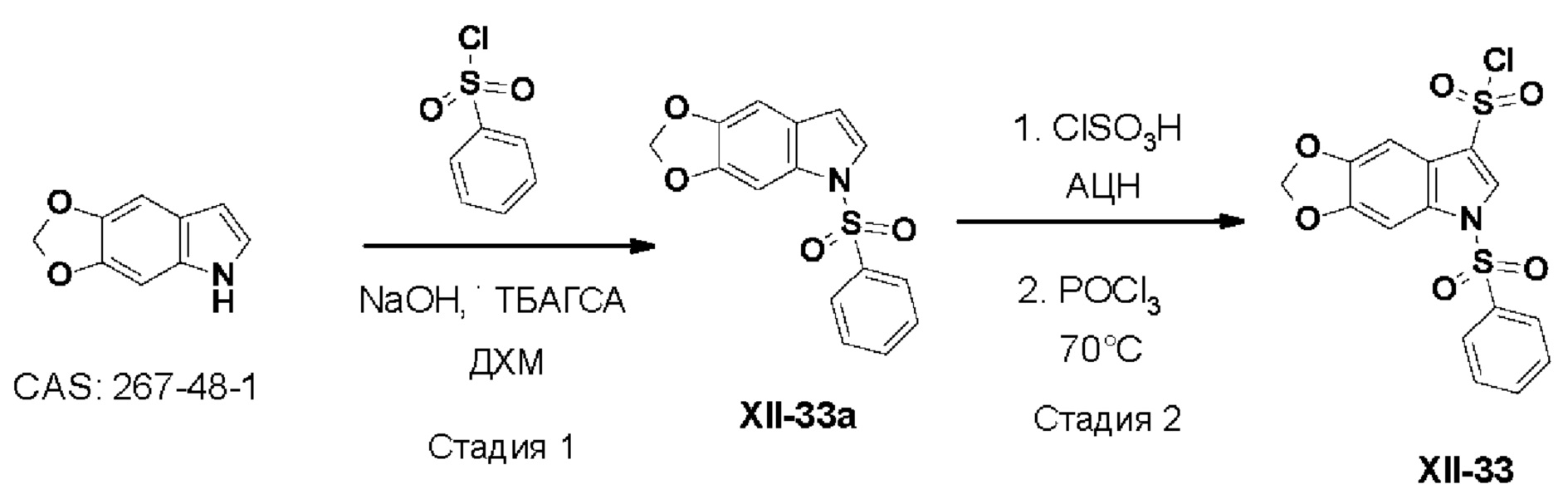
Стадия 1: Синтез 5-(бензолсульфонил)-[1,3]диоксоло[4,5-f]индола XII-33а
Суспензию гидроксида натрия (0,3 г, 7,5 ммоля) в дихлорметане (7 мл) перемешивали в бане со льдом и добавляли 5Н-[1,3]диоксоло[4,5-f]индол (0,5 г, 3 ммоля), затем тетрабутиламмонийгидросульфат (0,3 г, 0,08 ммоля). Затем по каплям добавляли бензолсульфонилхлорид (0,5 мл, 4 ммоля). Затем баню со льдом удаляли и смесь перемешивали при комнатной температуре в течение ночи. После того, как ЖХ/МС указывала на завершение реакции, реакционную смесь выливали в воду со льдом и экстрагировали с помощью DCM (3 раза), объединенные органические фазы сушили над MgSO4 и выпаривали досуха. Продукт очищали с помощью флэш-хроматографии (при элюировании смесью DCM и гептана) и получали 0,9 г 5-(бензолсульфонил)-[1,3]диоксоло[4,5-f]индола XII-33а в виде твердого вещества.
Выход: 100%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 300 (М-Н)-, чистота 100%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,98-7,58 (m, 6Н), 7,44 (s, 1Н), 7,07 (s, 1H), 6,70 (s, 1H), 6,04 (s, 2H).
Стадия 2: Синтез 5-(бензолсульфонил)-[1,3]диоксоло[4,5-f]индол-7-сульфонилхлорида XII-33
Раствор 5-(бензолсульфонил)-[1,3]диоксоло[4,5-f]индола XII-33а (0,4 г, 1 ммоль) в ацетонитриле (4 мл) перемешивали в бане со льдом и добавляли хлорсульфоновую кислоту (90 мкл, 1,31 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем добавляли оксихлорид фосфора (0,5 мл, 5 ммолей) и реакционную смесь нагревали при 70°С в течение ночи. Затем ее при перемешивании выливали в воду со льдом, дважды экстрагировали хлороформом, сушили над MgSO4 и выпаривали и получали 0,25 г 5-(бензолсульфонил)-[1,3]диоксоло[4,5-f]индол-7-сульфонилхлорида XII-33 в виде твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 62%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 398 (М-Н)-, чистота 100%.
С.17. Синтез 1-(бензолсульфонил)-6-метоксипирроло[2,3-b]пиридин-3-сульфонилхлорида XII-34
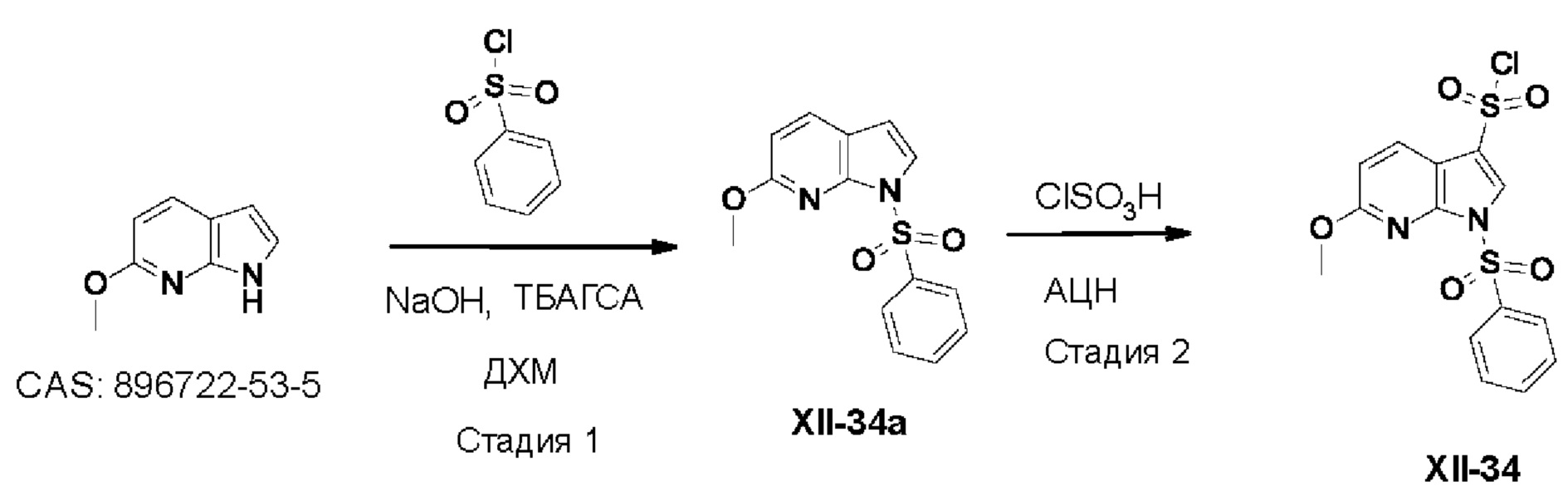
Стадия 1: Синтез 1-(бензолсульфонил)-6-метоксипирроло[2,3-b]пиридина XII-34а
Суспензию гидроксида натрия (0,3 г, 7,5 ммоля) в дихлорметане (6 мл) перемешивали в бане со льдом и добавляли 6-метокси-1Н-пирроло[2,3-b]пиридин (0,45 г, 3 ммоля), затем тетрабутиламмонийгидросульфат (0,3 г, 0,08 ммоля). Затем по каплям добавляли бензолсульфонилхлорид (0,6 мл, 5 ммолей). Затем баню со льдом удаляли и смесь перемешивали при комнатной температуре в течение ночи. После того, как ЖХ/МС указывала на завершение реакции, реакционную смесь выливали в воду со льдом и экстрагировали с помощью DCM (3 раза), объединенные органические фазы сушили над MgSO4 и выпаривали досуха и получали 0,88 г 1-(бензолсульфонил)-6-метоксипирроло[2,3-b]пиридина XII-34а в виде твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 100%.
ЖХМС в щелочной среде, методика 1 (ЭР+): 289 (М+Н)+, чистота 94%.
Стадия 2: Синтез 1-(бензолсульфонил)-6-метоксипирроло[2,3-b]пиридин-3-сульфонилхлорида XII-34
Раствор 1-(бензолсульфонил)-6-метоксипирроло[2,3-b]пиридина XII-34а (0,88 г, 3,1 ммоля) в ацетонитриле (3 мл) перемешивали в бане со льдом и добавляли хлорсульфоновую кислоту (1,5 мл, 22 ммоля). Реакционную смесь перемешивали в течение ночи при 75°С. Затем ее при перемешивании выливали в воду со льдом, дважды экстрагировали хлороформом, сушили над MgSO4 и выпаривали и получали 0,5 г 1-(бензолсульфонил)-6-метоксипирроло[2,3-b]пиридин-3-сульфонилхлорида XII-34 в виде твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 40%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 394 (М-Н)-, чистота 95%.
С.18. Синтез 1-(бензолсульфонил)-6-цианоиндол-3-сульфонилхлорида XII-35
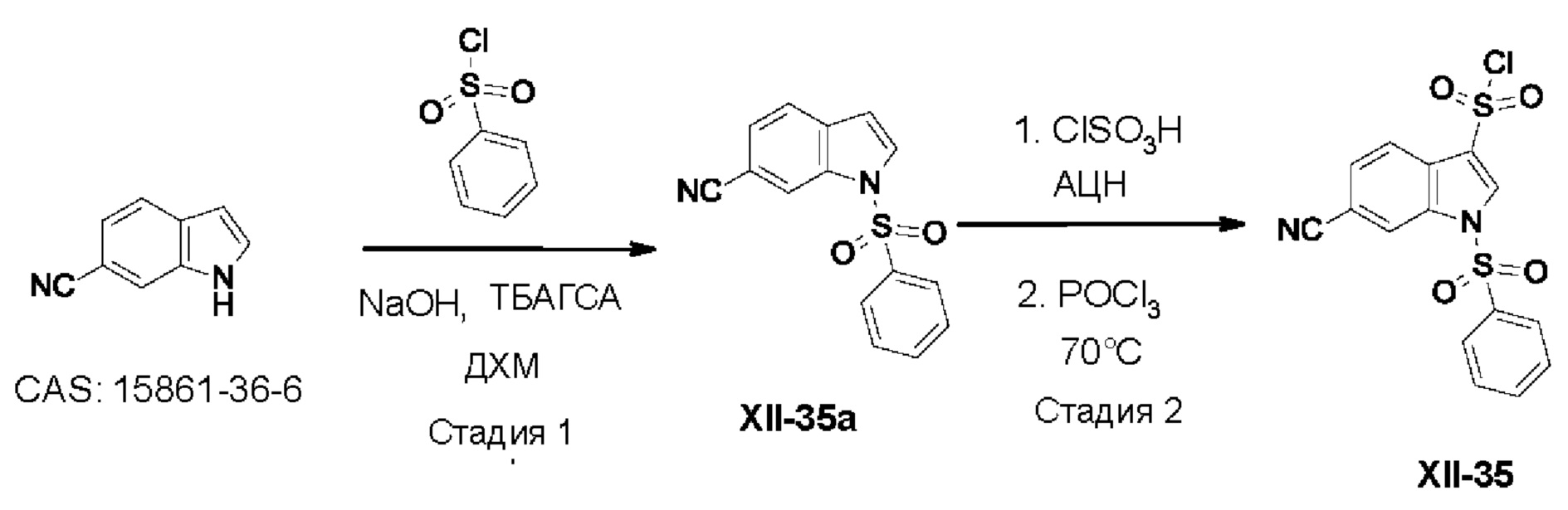
Стадия 1: Синтез 1-(бензолсульфонил)-6-цианоиндола XII-35а
Суспензию гидроксида натрия (0,21 г, 5,25 ммоля) в дихлорметане (6 мл) перемешивали в бане со льдом и добавляли 1Н-индол-6-карбонитрил (0,3 г, 2 ммоля), затем тетрабутиламмонийгидросульфат (0,2 г, 0,06 ммоля). Затем по каплям добавляли бензолсульфонилхлорид (0,33 мл, 2,6 ммоля). Затем баню со льдом удаляли и смесь перемешивали при комнатной температуре в течение ночи. После того, как ЖХ/МС указывала на завершение реакции, реакционную смесь выливали в воду со льдом и экстрагировали с помощью DCM (3 раза), объединенные органические фазы сушили над MgSO4 и выпаривали досуха. Продукт очищали с помощью флэш-хроматографии (при элюировании смесью DCM и гептана) и получали 0,58 г 1-(бензолсульфонил)-6-цианоиндола XII-35а в виде твердого вещества.
Выход: 100%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 281 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 8,38 (s, 1H), 8,14-8,11 (m, 3Н), 7,84-7,61 (m, 5Н), 6,94 (s, 1Н).
Стадия 2: Синтез 1-(бензолсульфонил)-6-цианоиндол-3-сульфонилхлорида XII-35
Раствор 1-(бензолсульфонил)-6-цианоиндола XII-35а (0,3 г, 1 ммоль) в ацетонитриле (2 мл) перемешивали в бане со льдом и добавляли хлорсульфоновую кислоту (140 мкл, 2 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем добавляли оксихлорид фосфора (0,42 мл, 4,5 ммоля) и реакционную смесь нагревали при 70°С в течение ночи. Затем ее при перемешивании выливали в воду со льдом, дважды экстрагировали хлороформом, сушили над MgSO4 и выпаривали и получали 0,42 г 1-(бензолсульфонил)-6-цианоиндол-3-сульфонилхлорида XII-35 в виде твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 100%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 379 (М-Н)-, чистота 100%.
С.19. Синтез 1-(бензолсульфонил)-6-бромпирроло[2,3-b]пиридин-3-сульфонилхлорида XII-36
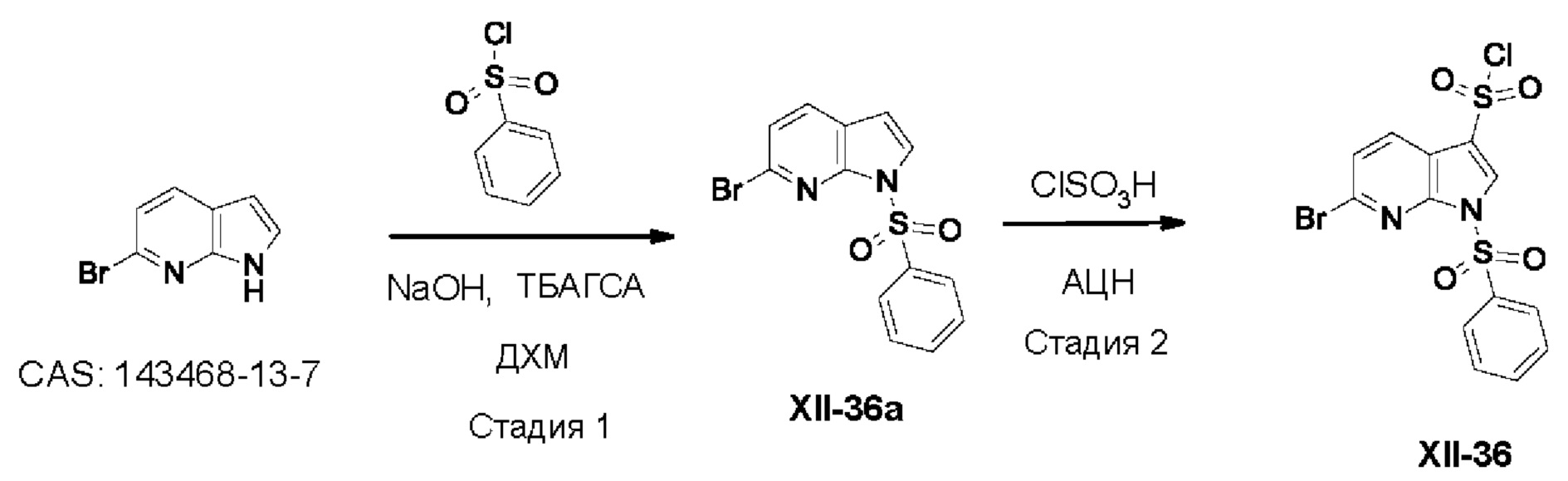
Стадия 1: Синтез 1-(бензолсульфонил)-6-бромпирроло[2,3-b]пиридина XII-36а
Суспензию тонкоизмельченного гидроксида гидроксид натрия (6,3 г, 160 ммолей) в дихлорметане (100 мл) перемешивали в бане со льдом и одной порцией добавляли 6-бромпирроло[2,3-b]пиридин (10 г, 50,7 ммоля), затем тетрабутиламмонийгидросульфат (0,45 г, 1,3 ммоля). Затем в течение 10 мин по каплям добавляли бензолсульфонилхлорид (7,2 мл, 56 ммолей) и реакционную смесь перемешивали при 0°С в течение 2 ч. После того, как ЖХ/МС указывала на завершение реакции, реакционную смесь фильтровали через слой целита и последний промывали с помощью DCM, объединенный фильтрат и промывочные растворы выпаривали досуха. Продукт растирали с эфиром, фильтровали, промывали небольшим количеством эфира, затем гексаном и сушили, фильтрат концентрировали и получали вторую порцию соединения, всего получали 16,8 г 1-(бензолсульфонил)-6-бромпирроло[2,3-b]пиридина XII-36а в виде бледно-желтого твердого вещества.
Выход: 98%.
ЖХМС в щелочной среде, методика 1 (ЭР+): 337 (М+Н)+, чистота 90%.
1H ЯМР (400 МГц, CDCl3) δ 8,28 (t, J=1,4 Гц, 1H), 8,25 (d, J=1,6 Гц, 1Н), 7,77-7,59 (m, 3Н), 7,59-7,49 (m, 2Н), 7,34 (d, J=8,2 Гц, 1H), 6,57 (d, J=4,0 Гц, 1Н).
Стадия 2: Синтез 1-(бензолсульфонил)-6-бромпирроло[2,3-b]пиридин-3-сульфонилхлорида XII-36
Раствор 1-(бензолсульфонил)-6-бромпирроло[2,3-b]пиридина XII-36а (5 г, 14,8 ммоля) в ацетонитриле (50 мл) перемешивали в бане со льдом и в течение 10 мин по каплям добавляли хлорсульфоновую кислоту (1,5 мл, 22 ммоля). Реакционную смесь перемешивали в течение 1 ч, давая температуре медленно повышаться, затем ее перемешивали при 60°С в течение ночи. Затем смесь при перемешивании выливали в воду со льдом, перемешивали в течение 20 мин, дважды экстрагировали этилацетатом. Экстракт промывали водой, насыщенным раствором бикарбоната натрия, сушили над MgSO4 и выпаривали и получали 4,23 г 1-(бензолсульфонил)-6-бромпирроло[2,3-b]пиридин-3-сульфонилхлорида XII-36 в виде почти белого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 65%.
1H ЯМР (400 МГц, CDCl3) δ 8,51 (s, 1H), 8,38 (q, J=1,8 Гц, 1H), 8,35 (t, J=1,7 Гц, 1Н), 8,13 (d, J=8,4 Гц, 1H), 7,81-7,72 (m, 1Н), 7,70-7,62 (m, 2Н), 7,60 (d, J=8,4 Гц, 1Н).
С.20. Синтез 1-(бензолсульфонил)-6-(2,2,2-трифторэтокси)индол-3-сульфонилхлорида XII-37
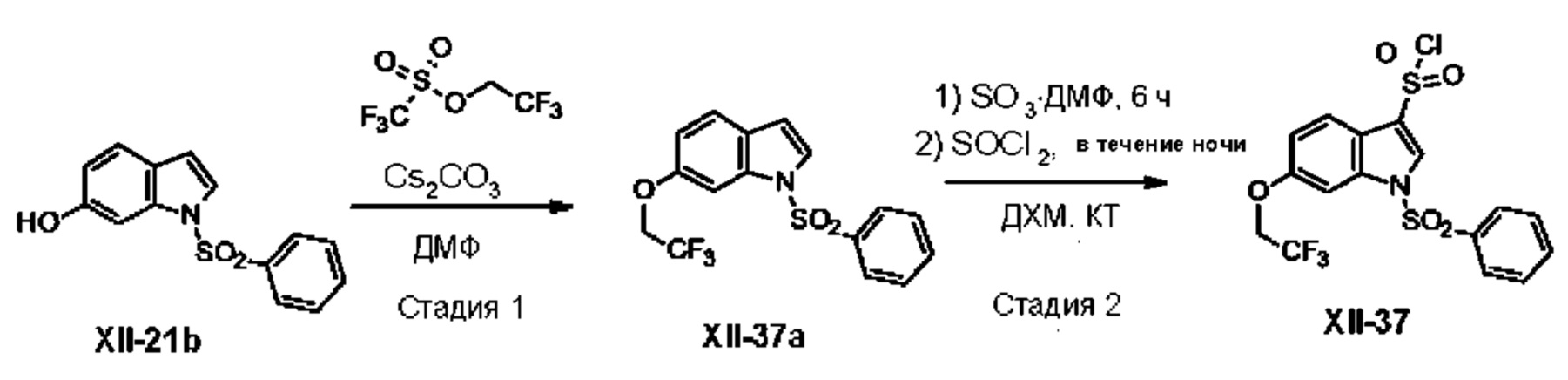
Стадия 1: Синтез 1-(бензолсульфонил)-6-(2,2,2-трифторэтокси)индола XII-37а:
Индол XII-21b (500 мг, 1,8 ммоля) и карбонат цезия (1,19 г, 3,6 ммоля) помещали в 7 мл DMF. Затем добавляли 2,2,2-трифторэтилтрифторметансульфонат (637 мг, 2,7 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Затем добавляли воду для осаждения продукта, который отфильтровывали и получали 1-(бензолсульфонил)-6-(2,2,2-трифторэтокси)индол XII-37а в виде бесцветного твердого вещества (630 мг).
Выход: 97%
1H ЯМР (600 МГц, CDCl3) δ 7,84 (d, J=7,6 Гц, 2Н), 7,63-7,51 (m, 2Н), 7,50-7,39 (m, 4Н), 6,93-6,88 (m, 1Н), 6,59 (d, J=3,8 Гц, 1H), 4,40 (q, J=8,0 Гц, 2Н).
Стадия 2: Синтез 1-(бензолсульфонил)-6-(2,2,2-трифторэтокси)индол-3-сульфонилхлорида XII-37:
Раствор 1-(бензолсульфонил)-6-(2,2,2-трифторэтокси)индола XII-37а (600 мг, 1,689 ммоля) в дихлорметане (10 мл) обрабатывали комплексом SO3⋅DMF (517 мг; 3,377 ммоля) и перемешивали при комнатной температуре в течение 6 ч до израсходования всего исходного вещества (за протеканием реакции следили с помощью TLC). Затем добавляли тионилхлорид (1 мл; 13,78 ммоля) и смесь перемешивали при комнатной температуре в течение ночи. Реакцию в полученной смесь останавливали насыщенным раствором NaHCO3 и смесь дважды экстрагировали дихлорметаном. Органическую фазу выпаривали досуха и очищали с помощью колоночной хроматографии (силикагель 60, элюент: дихлорметан/петролейный эфир = 1:1) и получали 1-(бензолсульфонил)-6-(2,2,2-трифторэтокси)индол-3-сульфонилхлорид XII-37 (306 мг) в виде желтоватого твердого вещества.
Выход: 40%
1H ЯМР (600 МГц, CDCl3) δ 8,28 (s, 1H), 7,97 (d, J=8,0 Гц, 1Н), 7,86 (d, J=8,8 Гц, 1Н), 7,74-7,53 (m, 5Н), 7,11 (dd, J=8,8, 2,2 Гц, 1Н) 4,44 (q, J=7,9 Гц, 2Н).
С.21. Синтез 6-хлорбензотиофен-3-сульфонилхлорида XII-38:
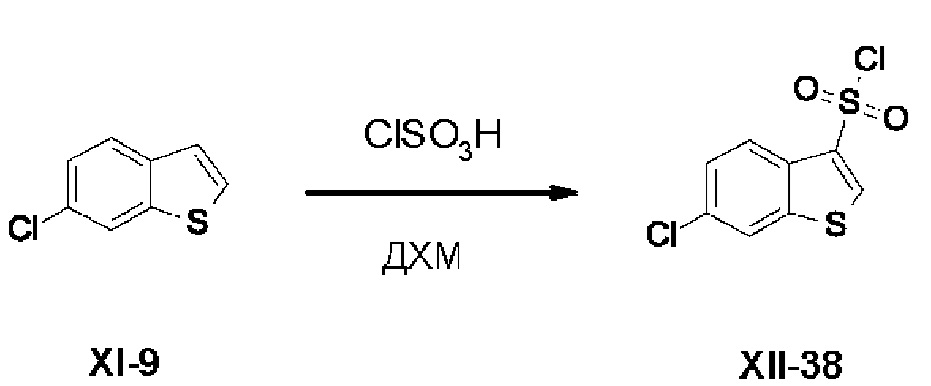
К раствору 6-хлорбензотиофена XI-9 (0,30 г, 1,77 ммоля) в DCM (15 мл) при 0°С добавляли ClSO3H (0,36 мл, 5,33 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 5 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакцию останавливали охлажденной льдом Н2О (50 мл) и смесь экстрагировали с помощью EtOAc (2×50 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлорбензотиофен-3-сульфонилхлорид XII-38 (0,31 г) в виде почти белого твердого вещества.
Выход: 65%
1H ЯМР (400 МГц, DMSO-d6) δ 7,42-7,44 (m, 1Н) 7,81 (s, 1H) 8,05-8,15 (m, 2H).
C.22. Синтез 6-бром-7-метил-1Н-индол-3-сульфонилхлорида XII-39:
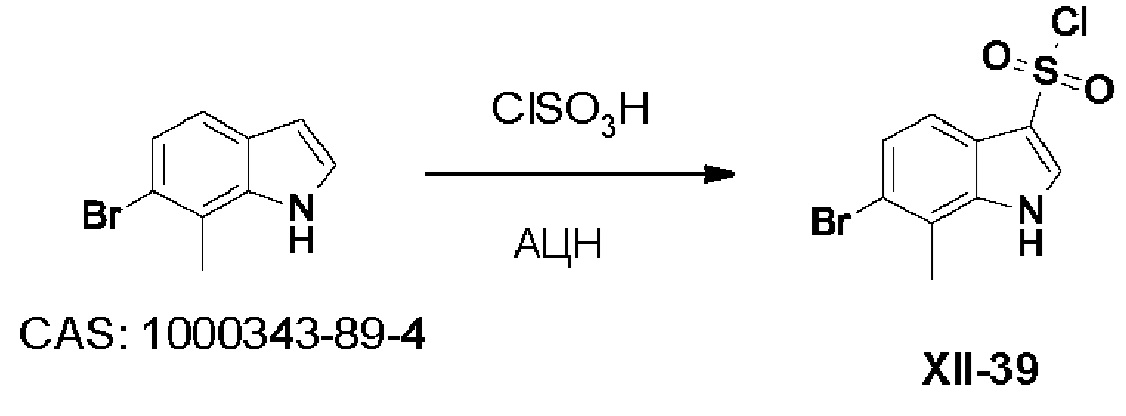
К раствору 6-бром-7-метил-1Н-индола (0,12 г, 0,55 ммоля) в ACN (1,8 мл) при 0°С добавляли ClSO3H (0,15 мл, 2,21 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. После завершения реакции реакцию останавливали с помощью Н2О и смесь экстрагировали с помощью CHCl3 (3×). Органические слои отделяли, сушили над безводным MgSO4 и концентрировали в вакууме и получали 6-бром-7-метил-1Н-индол-3-сульфонилхлорид XII-39 (0,11 г) в виде бежевого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 63%
ЖХМС в щелочной среде, методика 1 (ЭР-): 315 (М-Н)-, до проведения анализа реакцию в аликвоте смеси останавливали этиламином.
С.23. Синтез 6-нитро-1Н-индол-3-сульфонилхлорида XII-40:
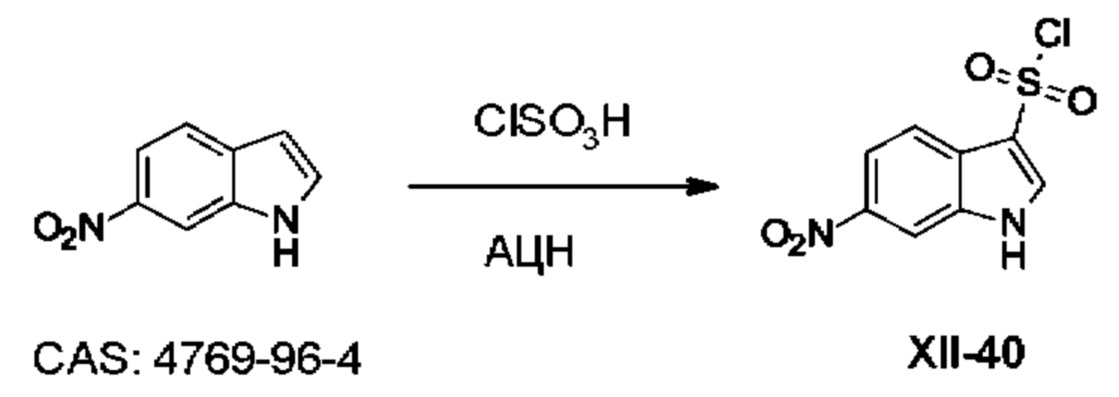
К раствору 6-нитро-1Н-индола (2 г, 12,3 ммоля) в CH3CN (30 мл) при 0°С добавляли ClSO3H (4 мл) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакцию останавливали охлажденной льдом Н2О (150 мл), фильтровали и промывали с помощью Н2О (10 мл). Полученное неочищенное вещество сушили в вакууме и получали 6-нитро-1H-индол-3-сульфонилхлорид XII-40 (2,10 г) в виде бледно-желтого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 64%
1H ЯМР (400 МГц, DMSO-d6) δ 7,78 (s, 1Н) 7,92 (brs, 2H) 8,31 (s, 1H) 11,82 (brs, 1H).
С.24. Синтез 6-хлор-5,7-дифтор-1Н-индол-3-сульфонилхлорида XII-41:
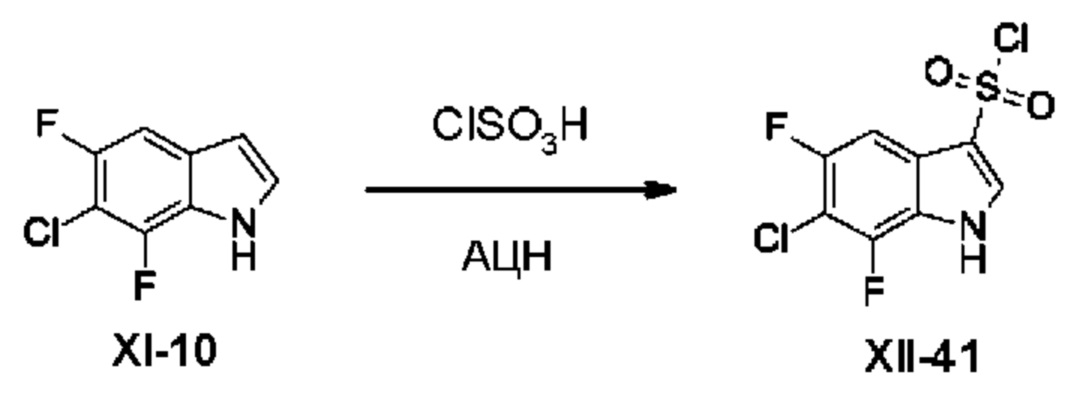
К раствору 6-хлор-5,7-дифтор-1Н-индола XI-10 (700 мг, 3,6 ммоля) в CH3CN (15 мл) при 0°С добавляли ClSO3H (0,8 мл) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли водой (50 мл) и экстрагировали с помощью EtOAc (100 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлор-5,7-дифтор-1H-индол-3-сульфонилхлорид XII-41 (705 мг) в виде коричневого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 64%
ЖХМС в щелочной среде, методика 2 (ЭР-): 266 (М-Н-) (соответствует сульфоновой кислоте), чистота 93%.
С.25. Синтез 6-бром-7-хлор-1Н-индол-3-сульфонилхлорида XII-42:
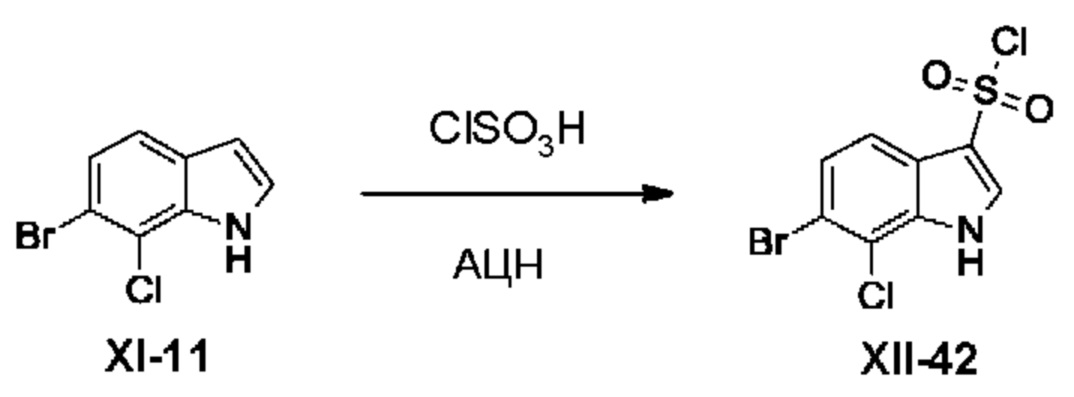
К раствору 6-бром-7-хлор-1Н-индола XI-11 (145 мг, 0,6 ммоля) в CH3CN (3 мл) при 0°С добавляли ClSO3H (0,15 мл) и реакционную смесь перемешивали при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали на дробленый лед (20 мл) и образовавшееся твердое вещество отфильтровывали и сушили и получали 6-бром-7-хлор-1Н-индол-3-сульфонилхлорид XII-42 (90 мг) в виде бледно-коричневого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 44%
ЖХМС в щелочной среде, методика 2 (ЭР-): 308 (М-Н)- (соответствует сульфоновой кислоте), чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,32-7,37 (m, 2Н) 7,64 (d, J=8,8 Гц, 1Н) 11,58 (s, 1Н).
С.26. Синтез 7-хлор-6-метокси-1Н-индол-3-сульфонилхлорида XII-43:
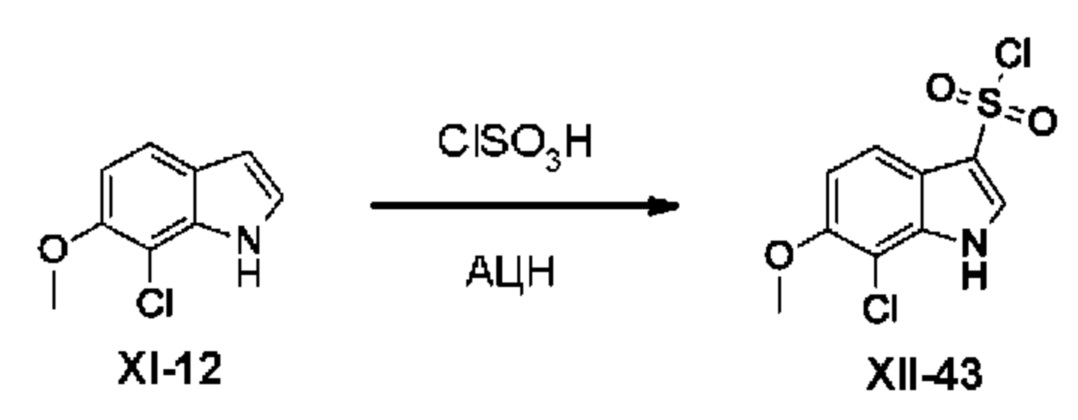
К раствору 7-хлор-6-метокси-1Н-индола XI-12 (600 мг, 3,22 ммоля) в ацетонитриле (15 мл) при температуре, равной от -5 до 0°С, по каплям добавляли хлорсульфоновую кислоту (0,6 мл). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC. Реакционную смесь выливали в смесь воды со льдом (15 мл), экстрагировали с помощью EtOAc (3×15 мл). Объединенные органические слои промывали рассолом (15 мл), Органический слой отделяли, сушили над безводным Na2SO4 (1,00 г) и концентрировали в вакууме. Неочищенное соединение растирали с н-пентаном (15 мл) и получали 7-хлор-6-метокси-1H-индол-3-сульфонилхлорид XII-43 (530 мг) в виде почти белого твердого вещества.
Выход: 58%
1H ЯМР (400 МГц, DMSO-d6) δ 3,86 (s, 3Н) 6,97 (d, J=8,80 Гц, 1Н) 7,27 (d, J=2,45 Гц, 1Н) 7,63 (d, J=8,31 Гц, 1Н) 11,19 (brs, 1Н).
С.27. Синтез 7-хлор-6-фтор-1Н-индол-3-сульфонилхлорида XII-4:
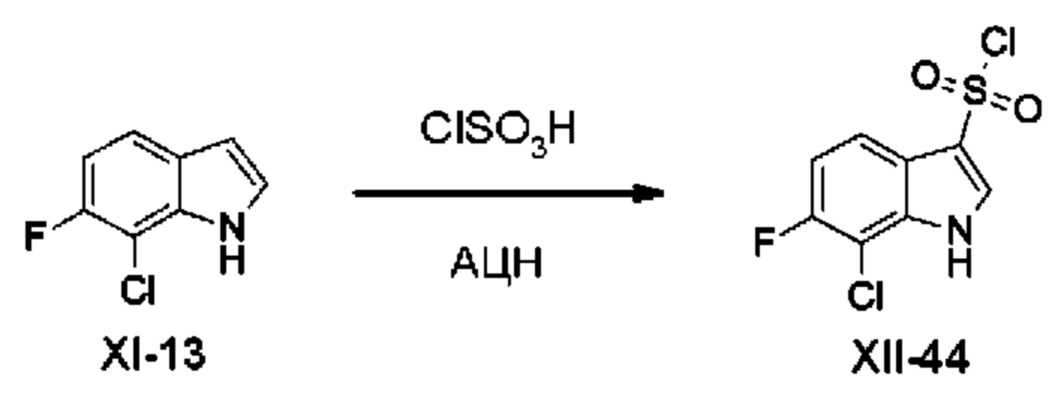
К раствору 7-хлор-6-фтор-1H-индол XI-13 (400 мг, 2,08 ммоля) в ацетонитриле (8 мл) при 0°С медленно добавляли ClSO3H (0,345 мл, 5,19 ммоля). Реакционную смесь перемешивали при 0°С в течение 1 ч и затем при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь выливали в смесь воды со льдом (50 мл). Водный слой экстрагировали этилацетатом (2×25 мл). Органический слой отделяли, сушили над безводным Na2SO4, фильтровали и концентрировали и получали 7-хлор-6-фтор-1H-индол-3-сульфонилхлорид XII-44 (430 мг) в виде коричневого полужидкого вещества. Неочищенный продукт использовали в следующей реакции без дополнительной очистки.
Выход: 62%
1Н ЯМР (400 МГц, DMSO-d6) δ 7,07 (t, J=9,29 Гц, 1 Н) 7,38 (d, J=2,45 Гц, 1 Н) 7,67-7,70 (m, 1 Н) 11,60 (br s, 1 Н).
С.28. Синтез 1-(бензолсульфонил)-6-(дифторметил)пирроло[2,3-b]пиридин-3-сульфонилхлорида XII-45
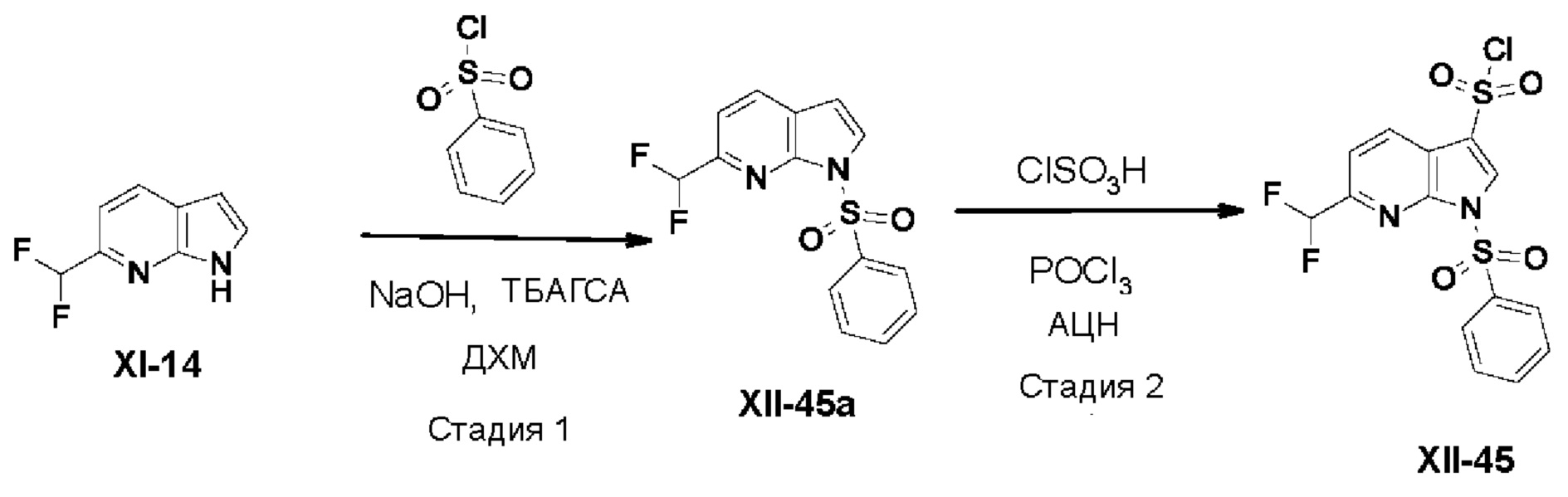
Стадия 1: Синтез 1-(бензолсульфонил)-6-(дифторметил)пирроло[2,3-b]пиридина XII-45а
Суспензию гидроксида натрия (76 мг, 1,88 ммоля) в дихлорметане (1 мл) перемешивали в бане со льдом и добавляли 6-(дифторметил)-1Н-пирроло[2,3-b]пиридин XI-14 (125 мг, 0,74 ммоля), затем тетрабутиламмонийгидросульфат (7,5 г, 0,022 ммоля). Затем по каплям добавляли бензолсульфонилхлорид (105 мкл, 0,81 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение ночи. После завершения реакции смесь фильтровали через слой целита и последний промывали с помощью DCM, объединенный фильтрат и промывочные растворы выпаривали досуха. Неочищенный продукт очищали с помощью хроматографии (SiO2, элюирование дихлорметаном) и получали 1-(бензолсульфонил)-6-(дифторметил)пирроло[2,3-b] пиридин XII-45а (200 мг) в виде светло-коричневого твердого вещества.
Выход: 70%.
ЖХМС в щелочной среде, методика 1 (ЭР+): 309 (М+Н)+, чистота 100%.
Стадия 2: Синтез 1-(бензолсульфонил)-6-(дифторметил)пирроло[2,3-b]пиридин-3-сульфонилхлорида XII-45
Раствор 1-(бензолсульфонил)-6-(дифторметил)пирроло[2,3-b]пиридина XII-45а (76 мг, 0,24 ммоля) в ацетонитриле (10 мл) перемешивали в бане со льдом и по каплям добавляли хлорсульфоновую кислоту (54 мкл, 0,78 ммоля) и реакционную смесь перемешивали при 50°С в течение 4 дней. Затем добавляли оксихлорид фосфора (100 мкл, 1,06 ммоля) и реакционную смесь нагревали при 70°С в течение ночи. Затем после охлаждения ее медленно выливали в воду со льдом и экстрагировали хлороформом (3×). Органические слои сушили над сульфатом магния и выпаривали досуха и получали 1-(бензолсульфонил)-6-хлориндол-3-сульфонилхлорид XII-19 (100 мг) в виде твердого вещества. Неочищенный продукт использовали в следующей реакции без дополнительной очистки.
Выход: 95%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 387 (М-Н)- (соответствует массе сульфоновой кислоты, чистота 88%.
С.29. Синтез 6-хлор-7-(дифторметокси)-1Н-индол-3-сульфонилхлорида XII-46:
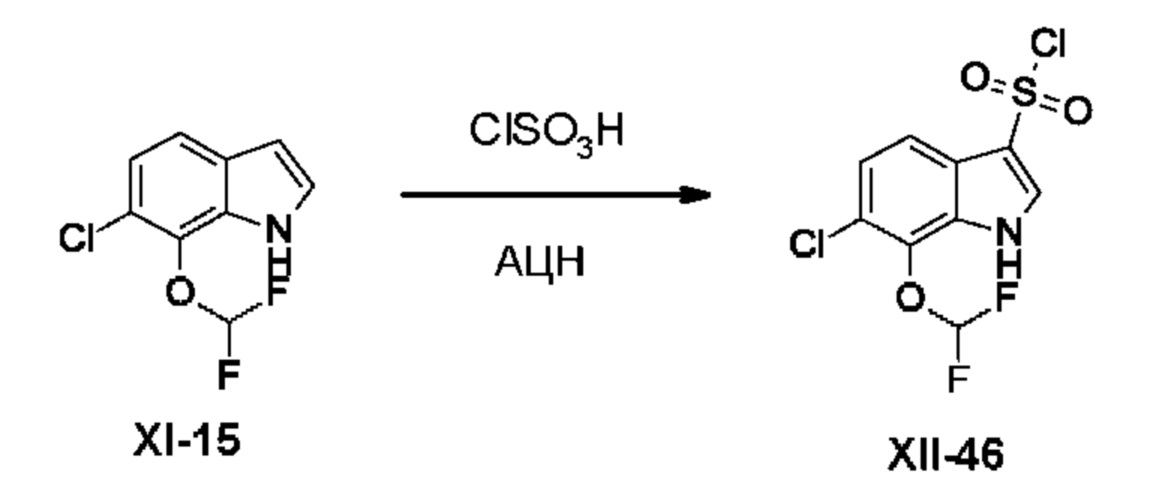
К раствору 6-хлор-7-(дифторметокси)-1Н-индола XI-15 (0,20 г, 0,86 ммоля) в CH3CN (4 мл) при 0°С медленно добавляли ClSO3H (0,20 мл) и реакционную смесь перемешивали при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали на дробленый лед (20 мл) и экстрагировали с помощью EtOAc (3×10 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлор-7-(дифторметокси)-1Н-индол-3-сульфонилхлорид XII-46 (0,23 г, неочищенный) в виде бледно-коричневого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в щелочной среде, методика 2 (ЭР-): 314 (М-Н)-, чистота 55%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,16 (d, J=8,80 Гц, 1Н) 7,16 (t, J=73,6 Гц, 1H) 7,39 (d, J=2,40 Гц, 1H) 7,67 (d, J=8,80 Гц, 1H) 11,53 (brs, 1H).
С.30. Синтез 6-хлор-7-(трифторметил)-1Н-индол-3-сульфонилхлорида XII-47:
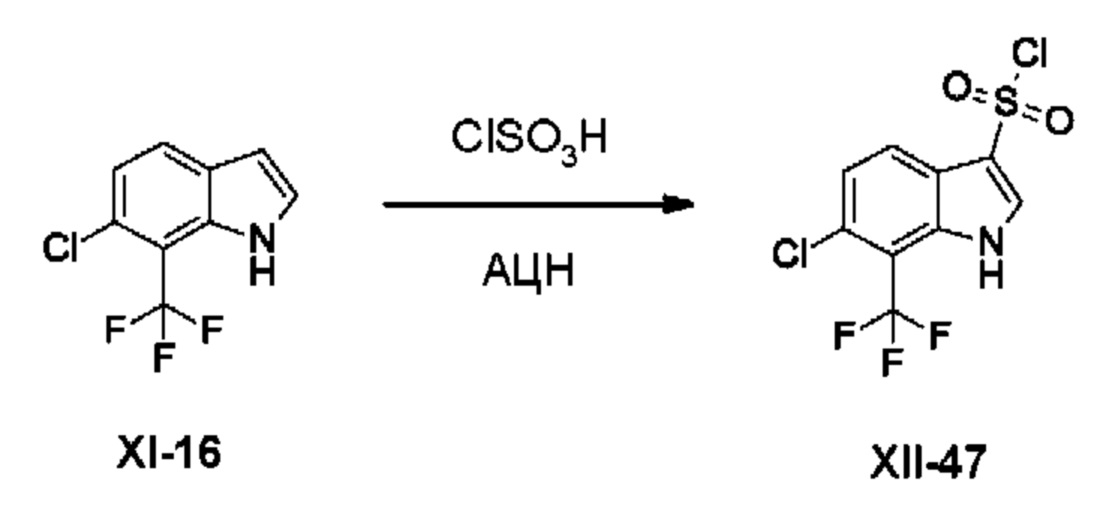
При перемешивании к раствору 6-хлор-7-(трифторметил)-1Н-индола XI-16 (0,52 г, 2,30 ммоля) в CH3CN (10 мл) при 0°С по каплям добавляли ClSO3H (1,50 мл). Реакционную смесь перемешивали при комнатной температуре в течение 2 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали на дробленый лед (100 мл), перемешивали в течение 10 мин и экстрагировали с помощью EtOAc (3×40 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме и получали 6-хлор-7-(трифторметил)-1Н-индол-3-сульфонилхлорид XII-47 (1,01 г, неочищенный) в виде коричневого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в щелочной среде, методика 2 (ЭР-): 298 (М-Н)- (соответствует массе сульфоновой кислоты), чистота 96%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,31 (d, J=8,80 Гц, 1Н) 7,41 (d, J=2,93 Гц, 1H) 8,01 (d, J=8,31 Гц, 1H) 11,27 (brs, 1H).
ПРИМЕРЫ СОЕДИНЕНИЙ
D. Синтез соединений общей формулы I
Все соединения, предлагаемые в настоящем изобретении, специально раскрытые в настоящем изобретении, обозначены, как "I-х", где любой "х" обозначает число, определяющее отдельные соединения. Соответственно, соединения примеров обозначены, как I-1, I-2, I-3 и т.п. Обозначения используют независимо от того, что любое соединение может быть также описано субформулой, предлагаемой в настоящем изобретении, например, формулой II, III или IV и т.п.
D.1. Методика В. Синтез 6-хлор-N-(2,4-дифторфенил)-1Н-индол-3-сульфонамида I-1
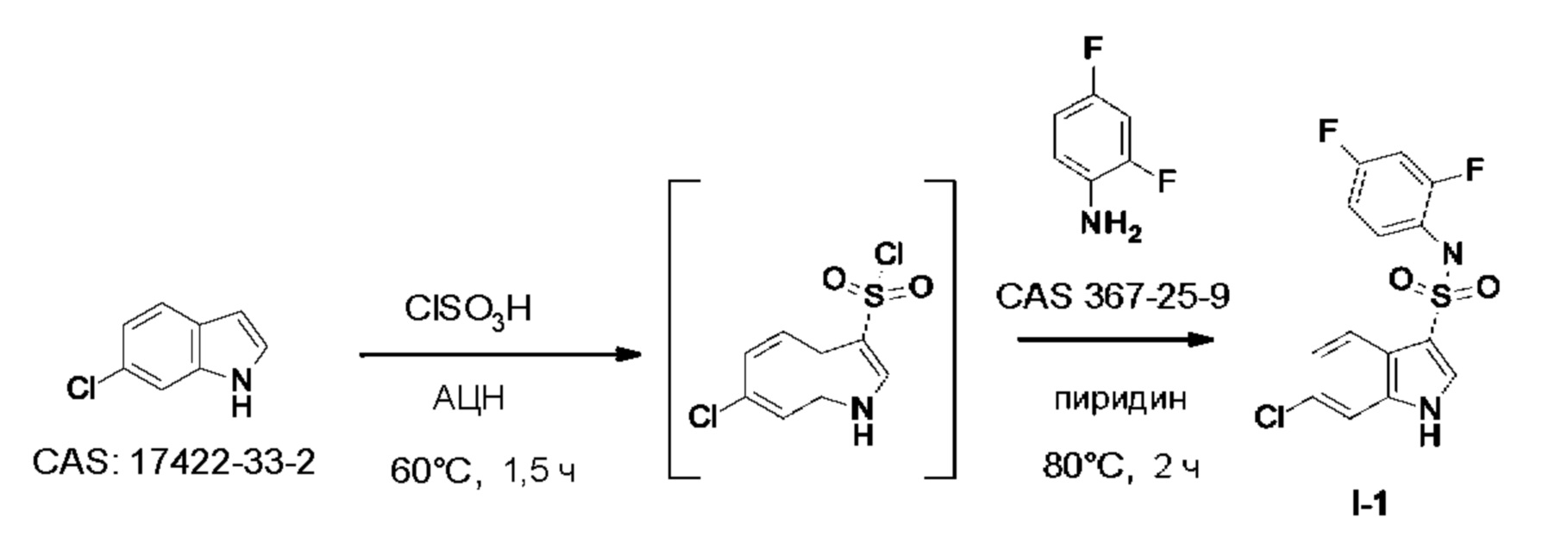
В сосуде, помещенном в баню со льдом, перемешивали раствор 6-хлориндола (630 мг, 4,1 ммоля) в ацетонитриле (25,2 мл) и по каплям добавляли хлорсульфоновую кислоту (714 мкл, 10,7 ммоля) и реакционную смесь перемешивали в течение 30 мин. Баню со льдом удаляли и реакционную смесь нагревали при 60°С в течение 1,5 ч. После охлаждения до комнатной температуры добавляли пиридин (54,6 мл) и раствор становился желтым. Во второй герметизированный сосуд отвешивали 2,4-дифторанилин (25,8 мг, 0,2 ммоля) и добавляли аликвоту полученного выше раствора (1,9 мл, 0,1 ммоля). Реакционную смесь перемешивали при 80°С в течение 2 ч, затем выпаривали в центробежном испарителе. Остаток очищали с помощью хроматографии с обращенной фазой в щелочной среде и с МС-детектированием и получали 11,8 мг 6-хлор-N-(2,4-дифторфенил)-1Н-индол-3-сульфонамида I-1.
Выход: 34%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 341 (М-Н)-, чистота 95%.
Соединения, приведенные ниже в таблице 4, синтезировали в соответствии с методикой В.
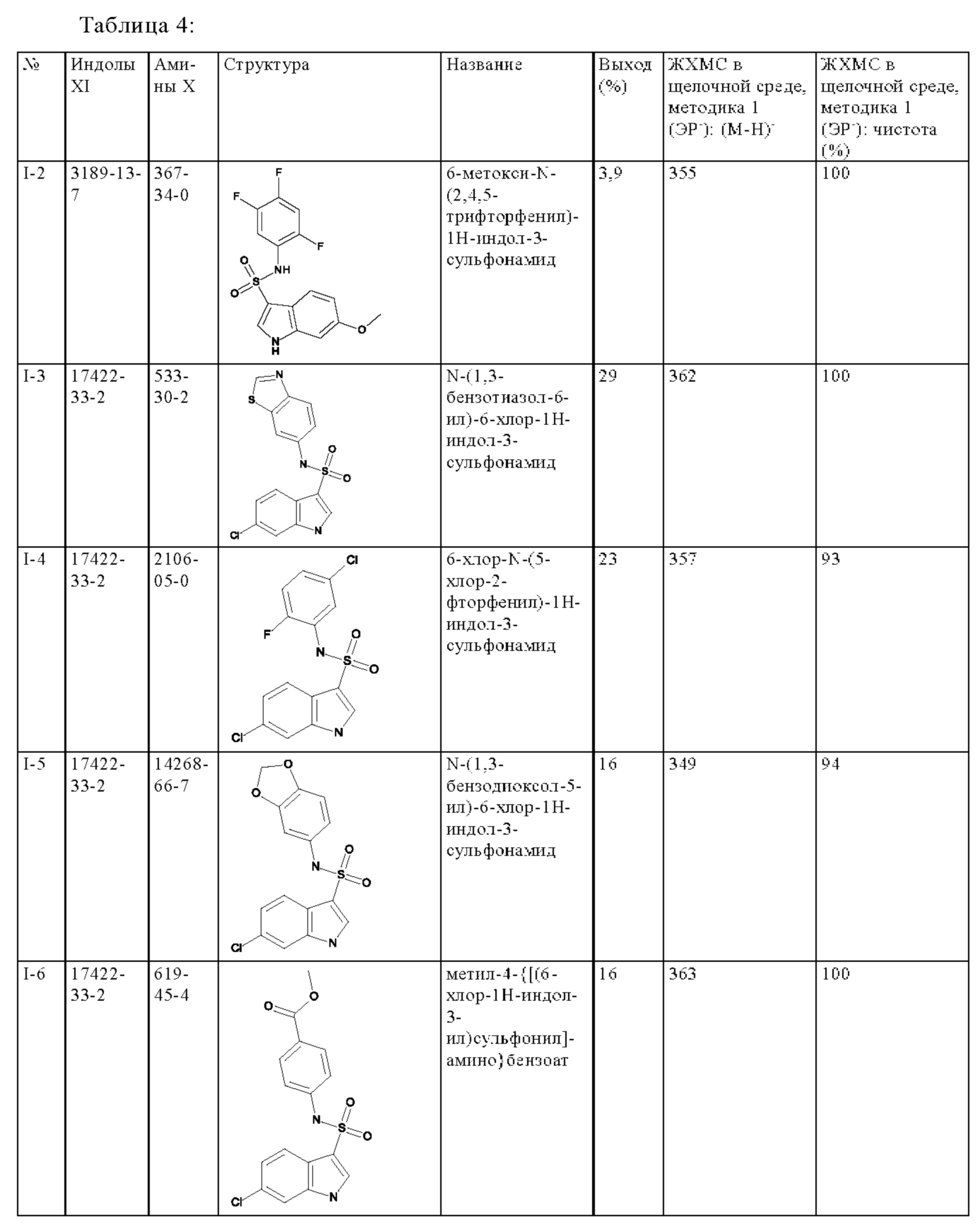
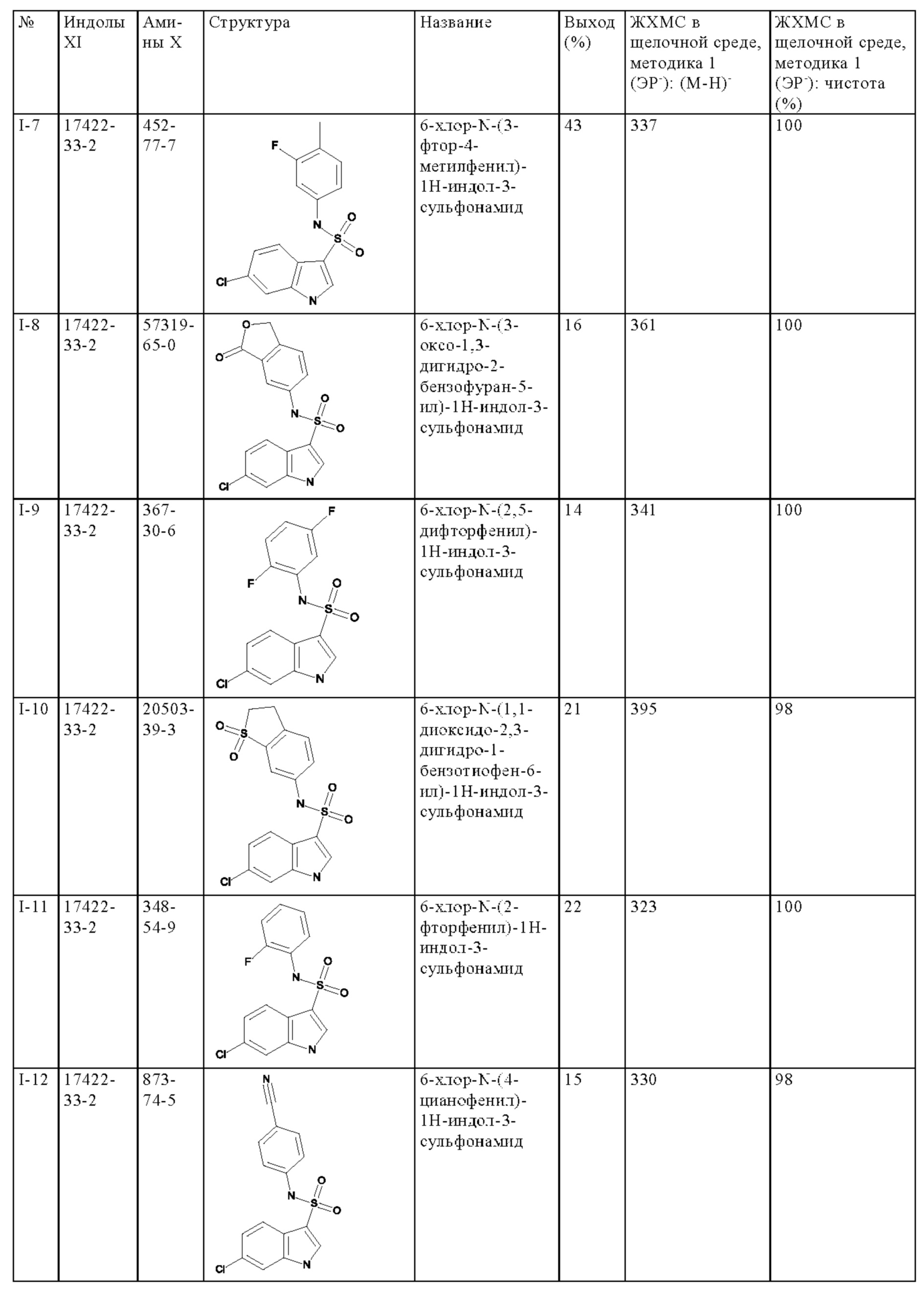
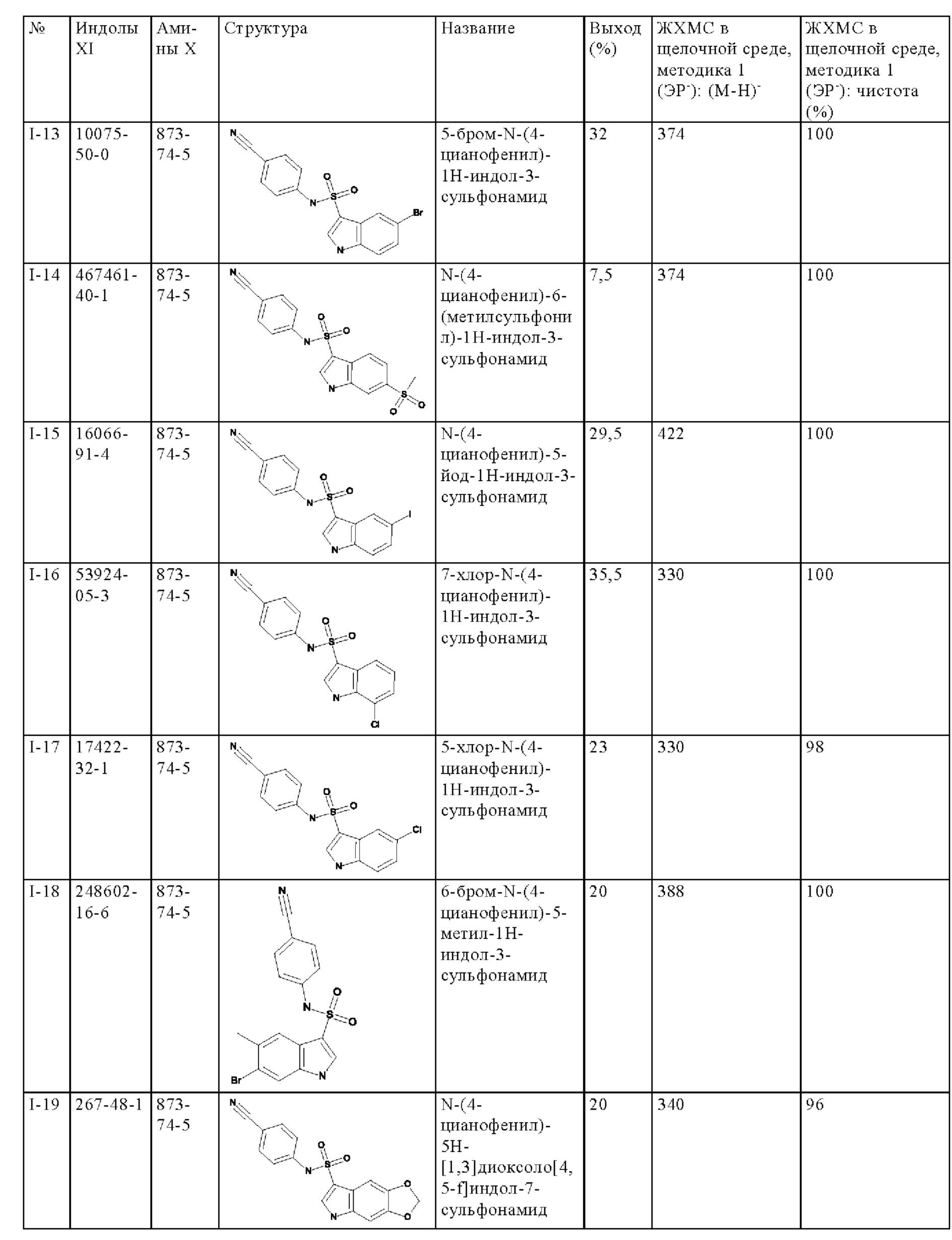
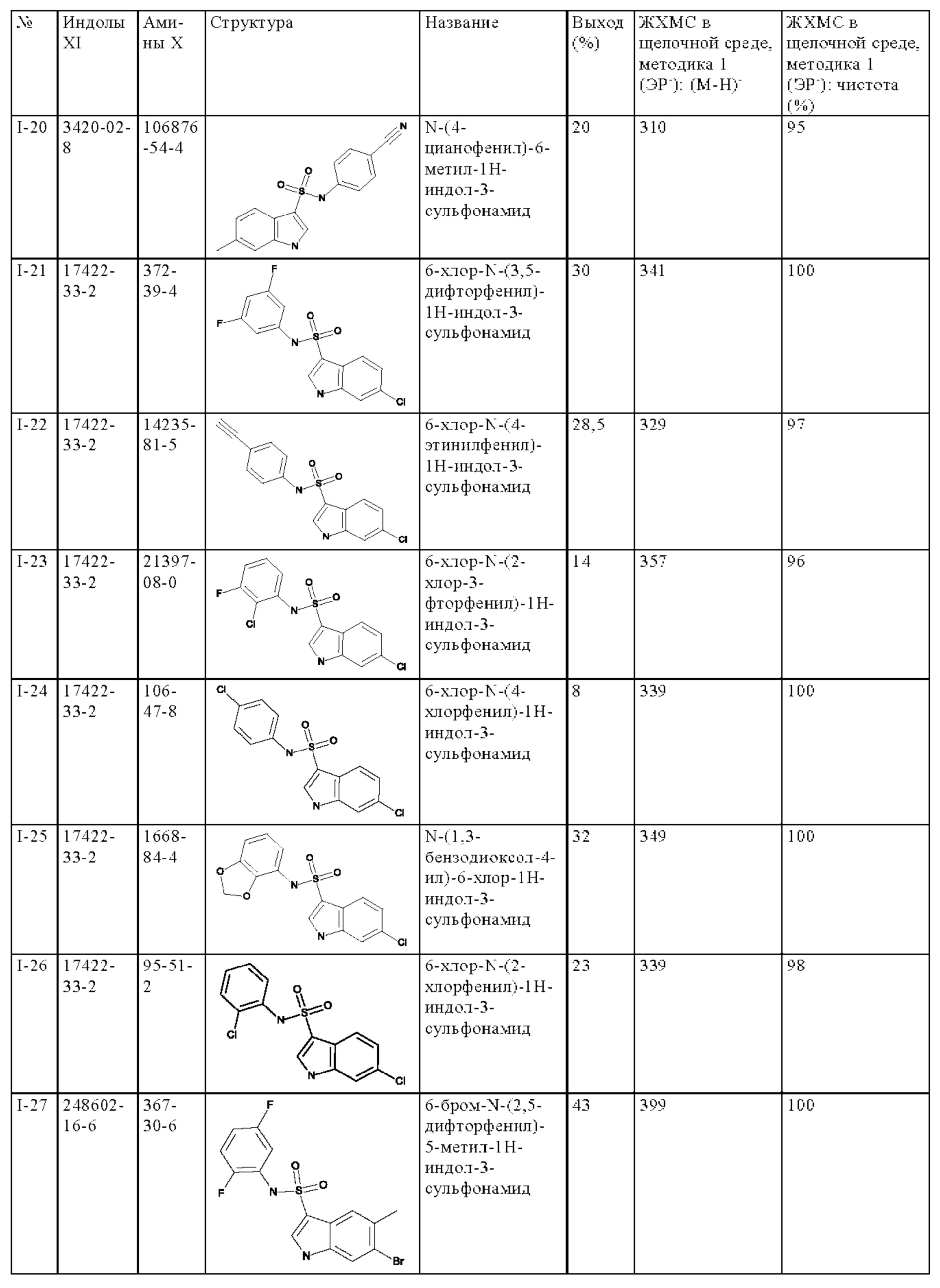
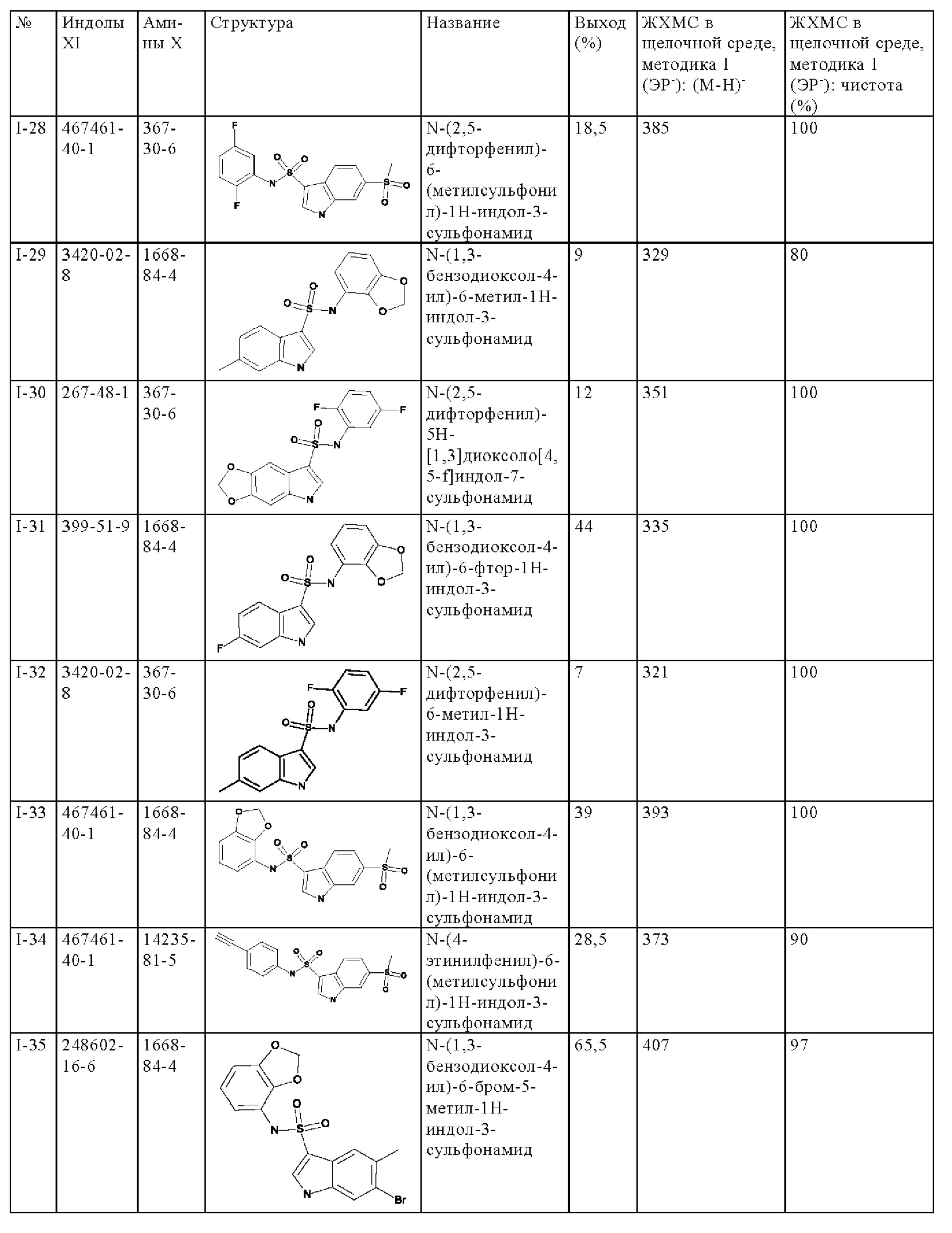
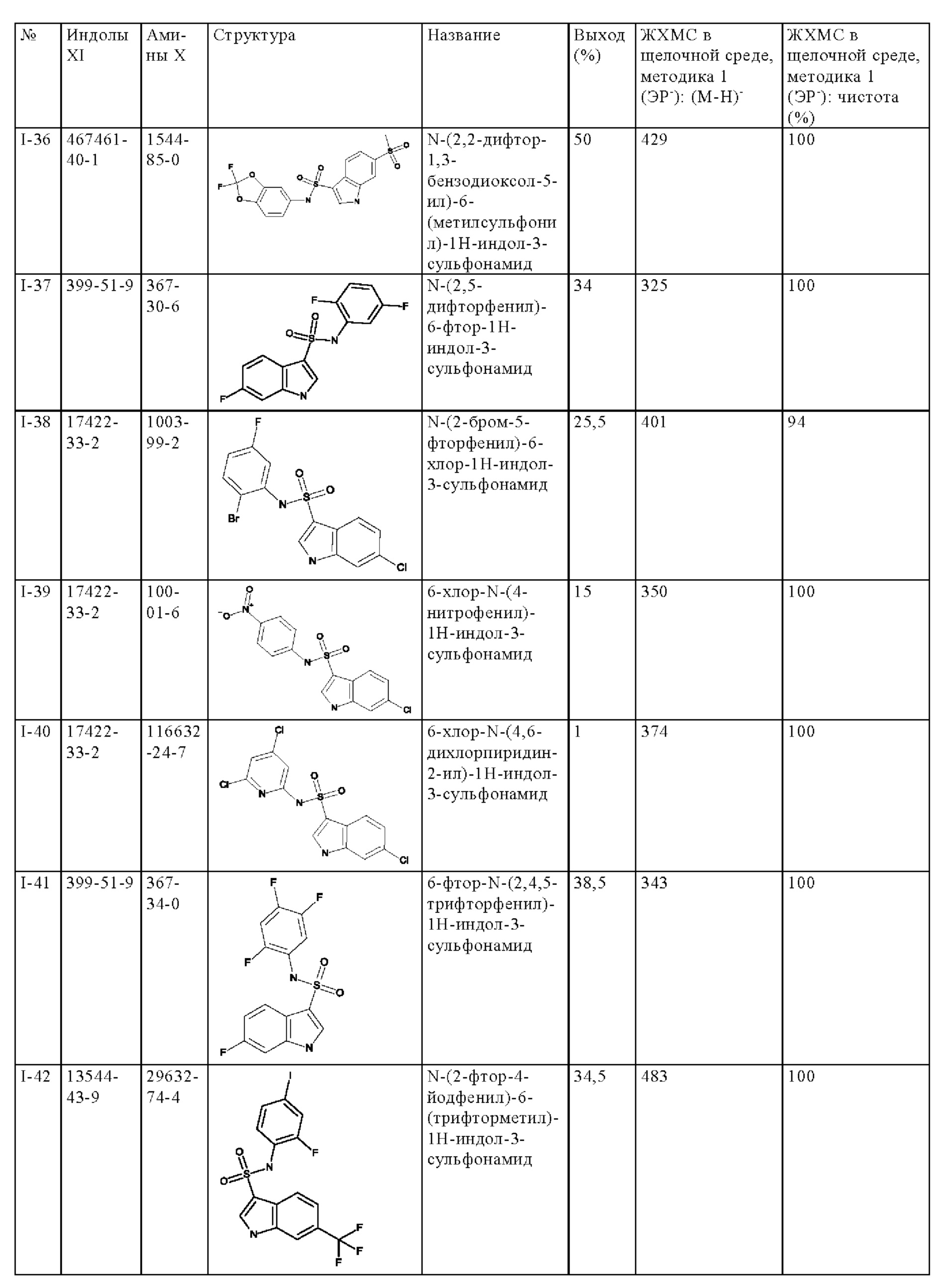
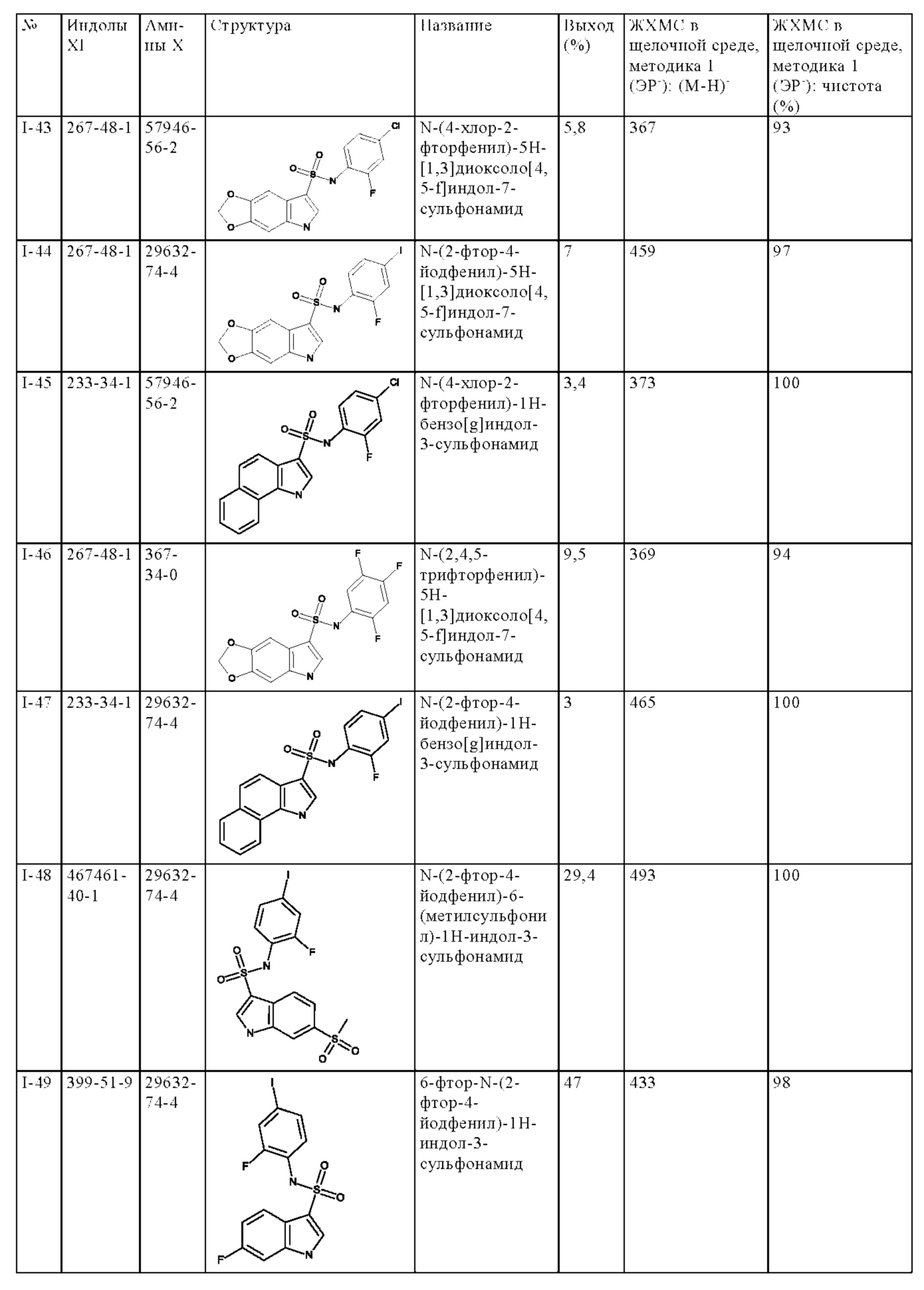
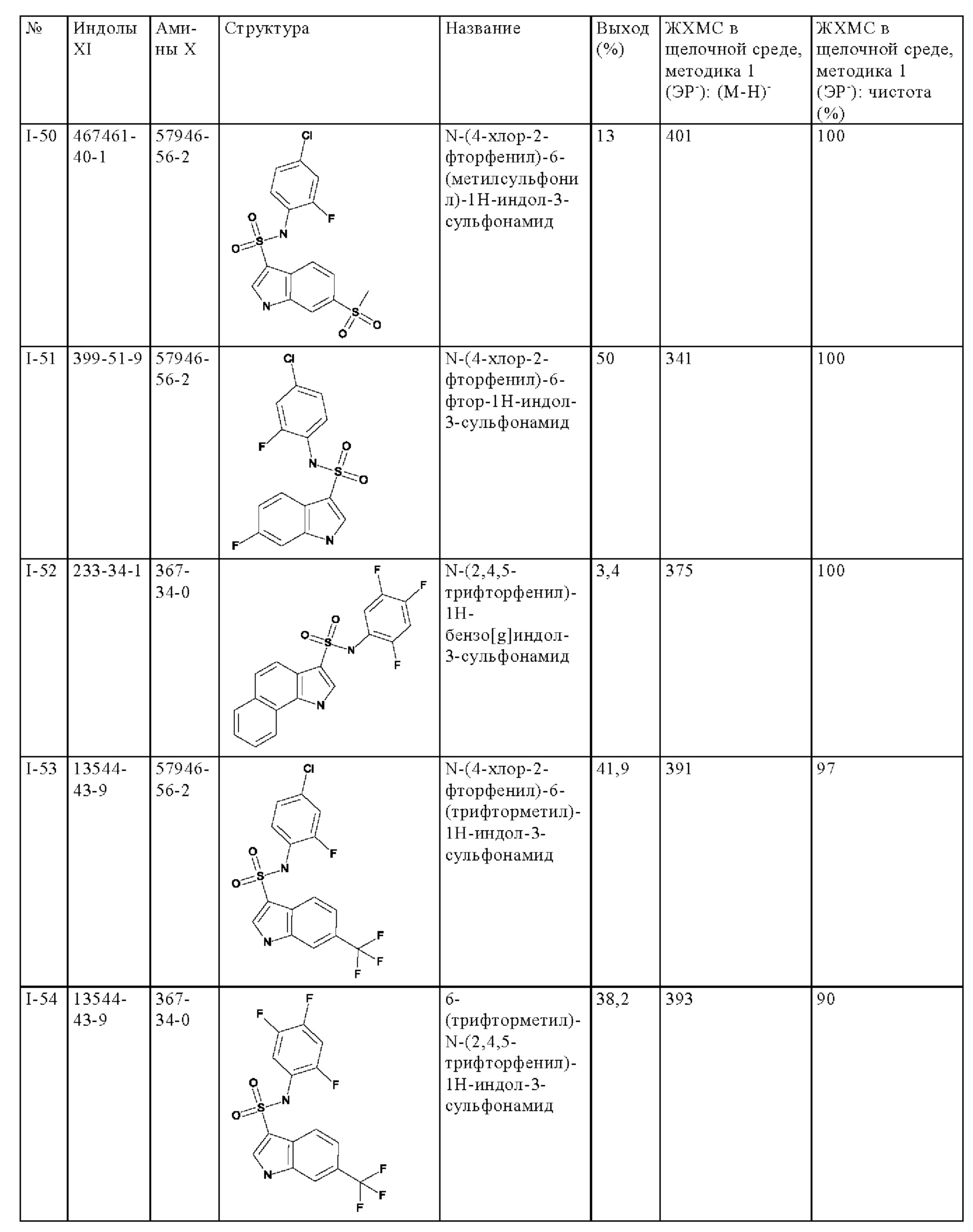
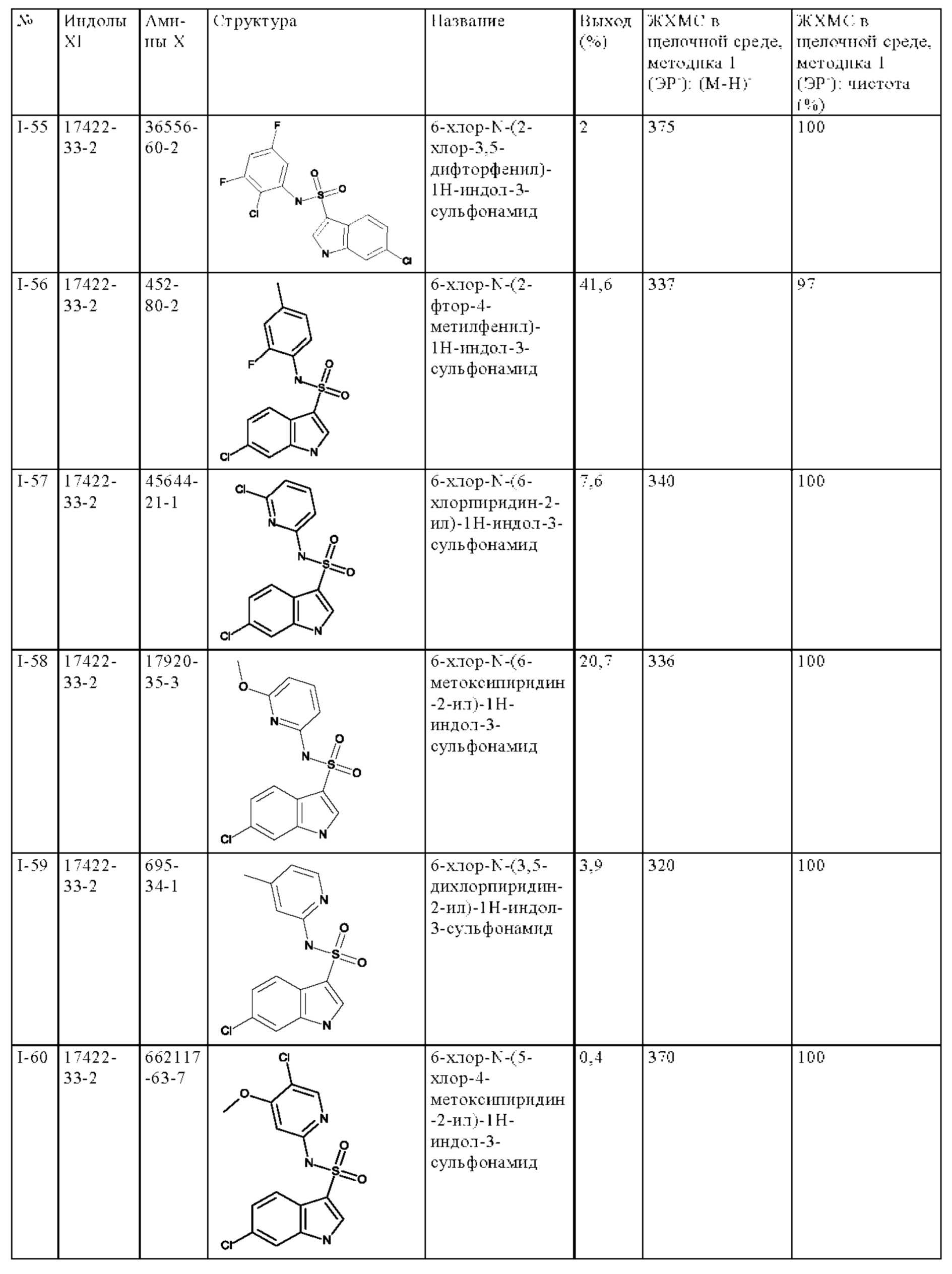
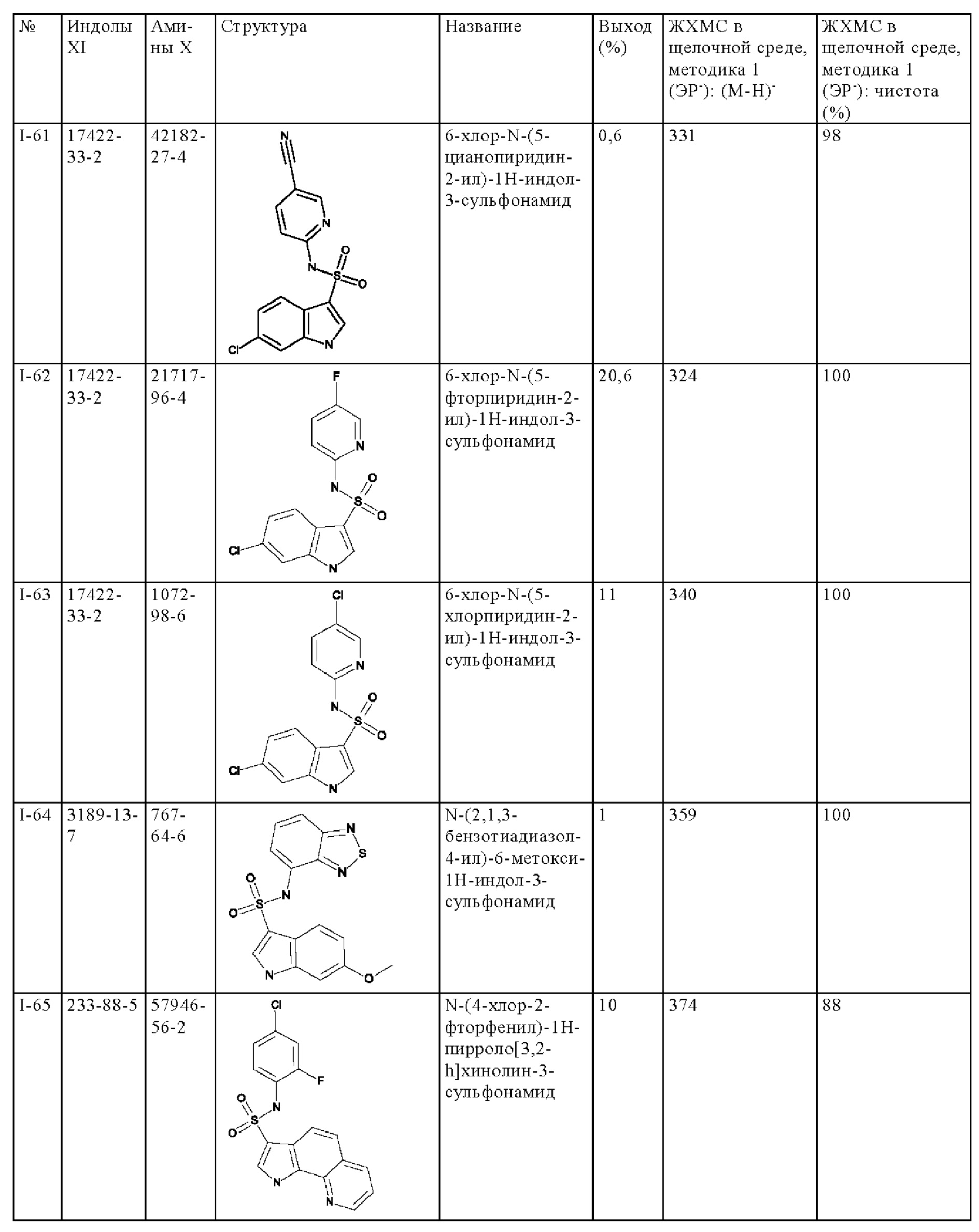
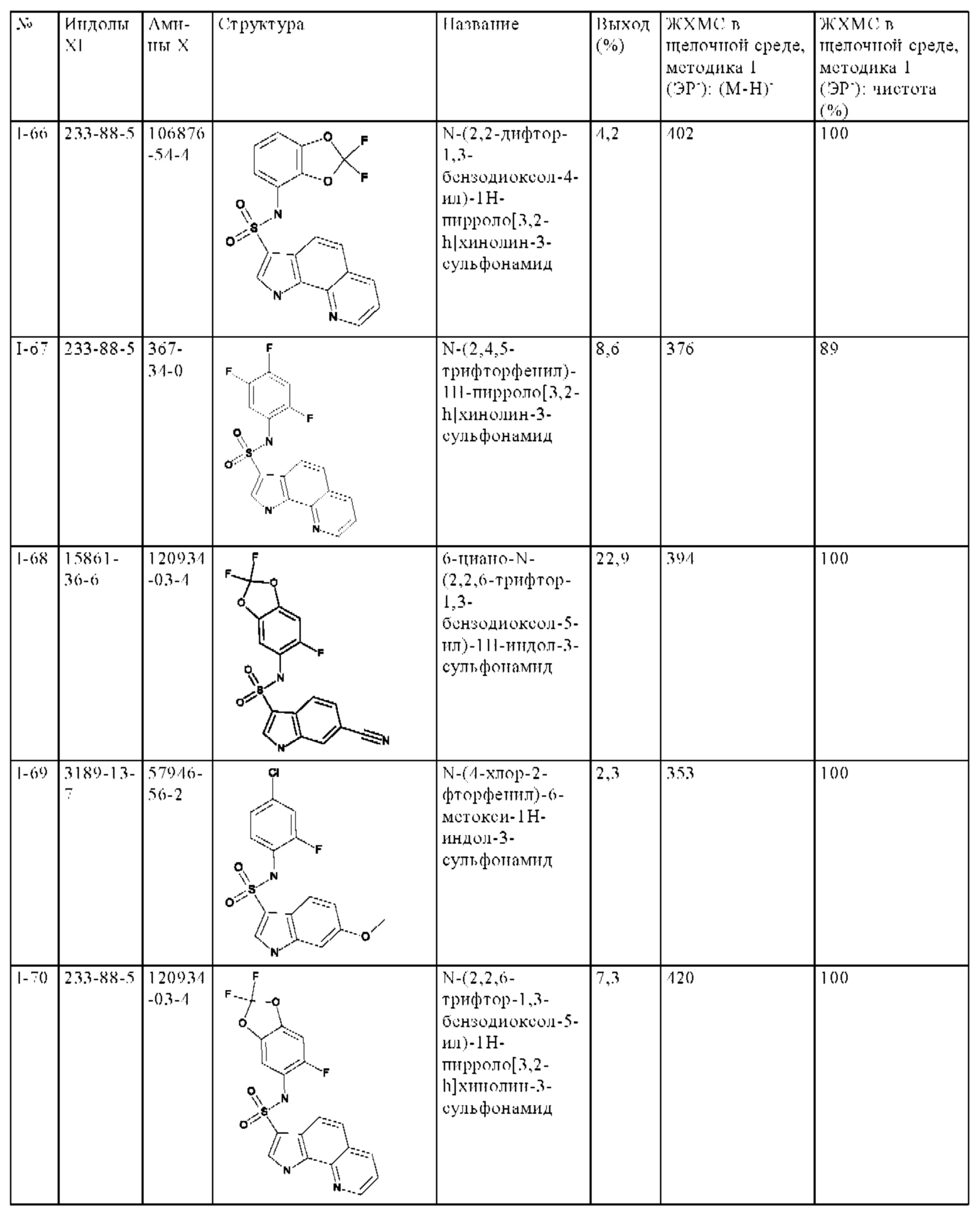
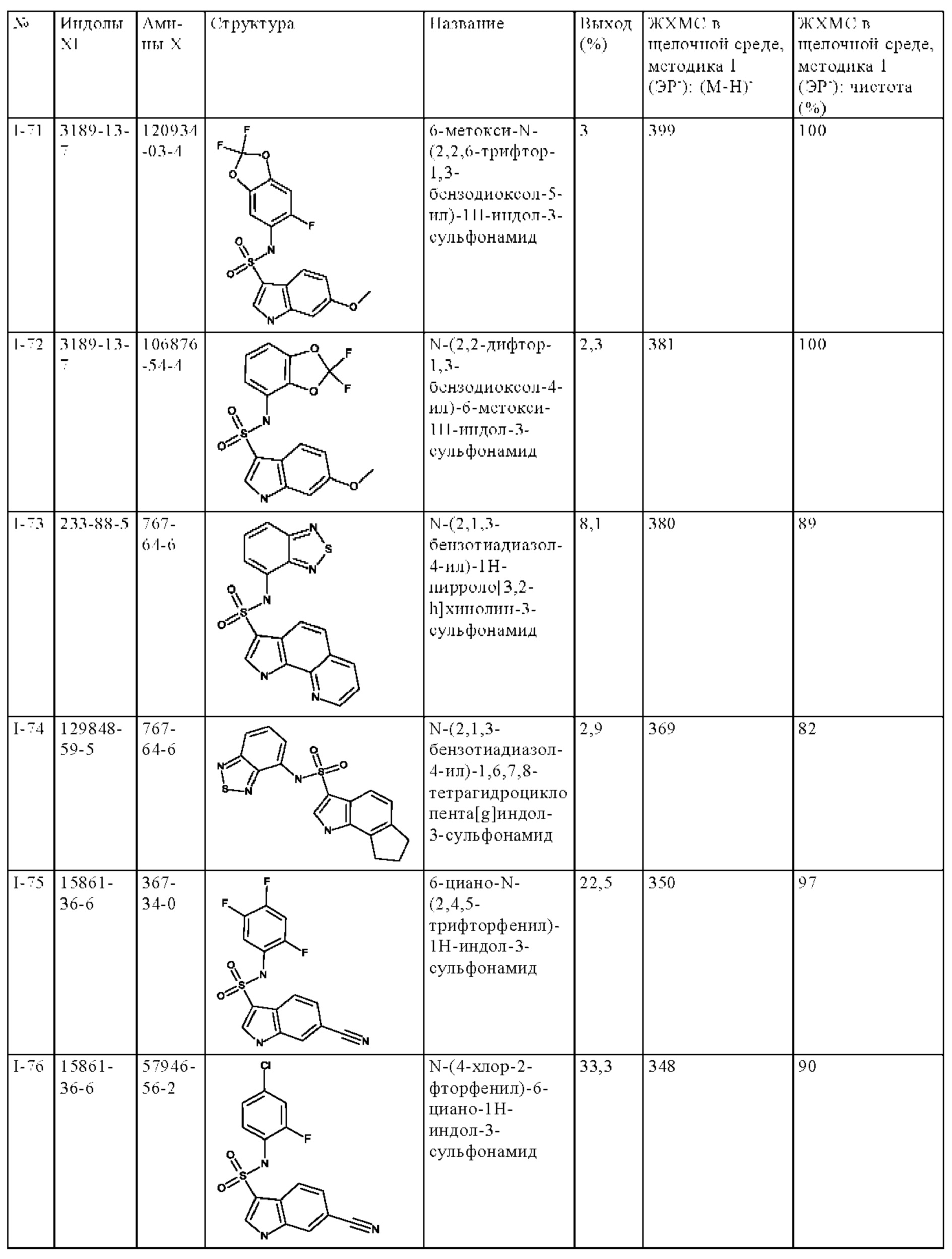
D.2. Методика С. Синтез 5-хлор-N-(4-цианофенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамида I-77
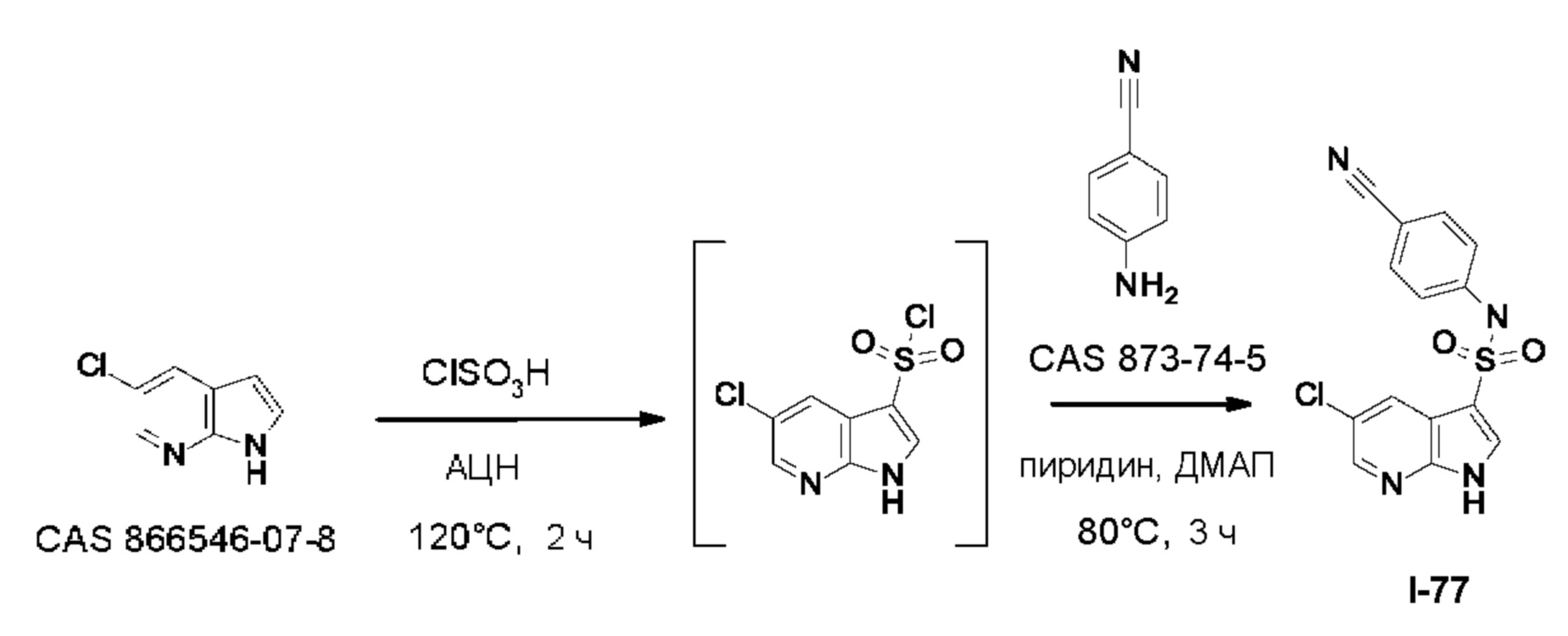
В сосуде перемешивали раствор 5-хлор-1Н-пирроло[2,3-b]пиридина (24 мг, 0,15 ммоля) в ацетонитриле (100 мкл) и по каплям добавляли хлорсульфоновую кислоту (115 мкл, 1,69 ммоля) и реакционную смесь нагревали при 120°С в течение 2 ч. После охлаждения до комнатной температуры добавляли пиридин (1 мл). Затем добавляли раствор 4-аминобензонитрила (35 мг, 0,3 ммоля) и 4-диметиламинопиридина (4 мг, 0,03 ммоля) в ацетонитриле (100 мкл). Реакционную смесь перемешивали при 80°С в течение 3 ч, затем выпаривали в центробежном испарителе. Остаток очищали с помощью хроматографии с обращенной фазой в щелочной среде и с МС-детектированием и получали 5 мг 5-хлор-N-(4-цианофенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамида I-77.
Выход: 10%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 331 (М-Н)-, чистота 100%.
Соединения, приведенные ниже в таблице 5, синтезировали в соответствии с методикой С.
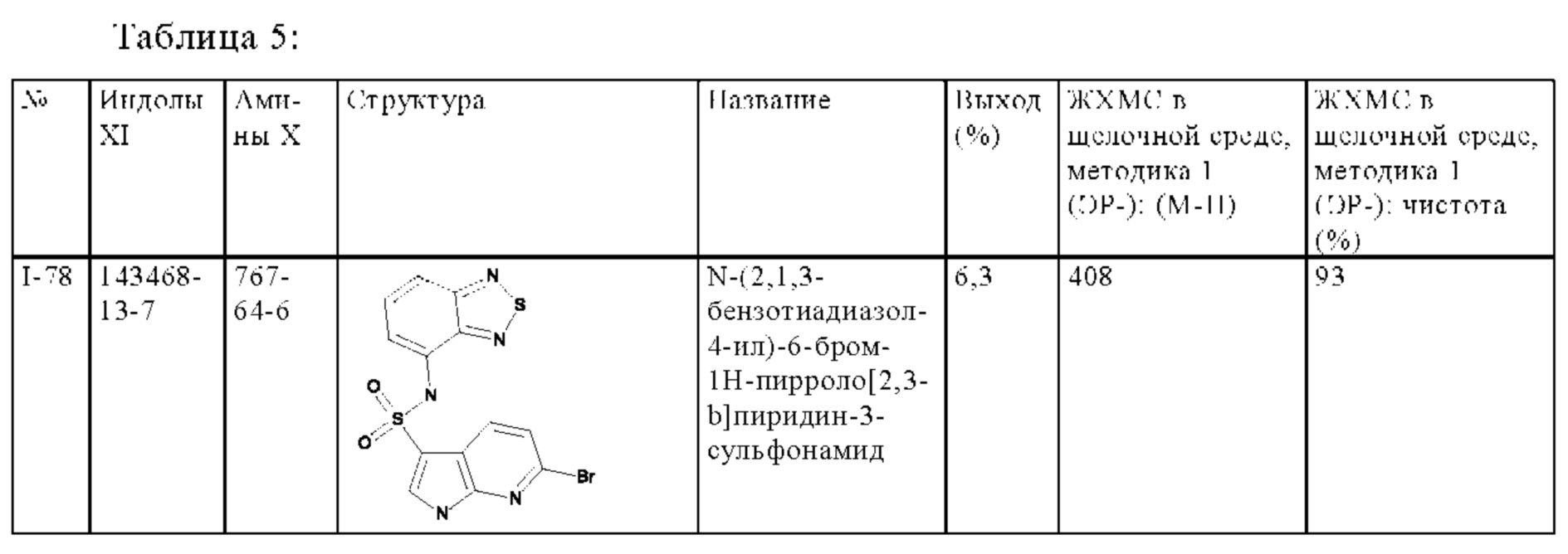
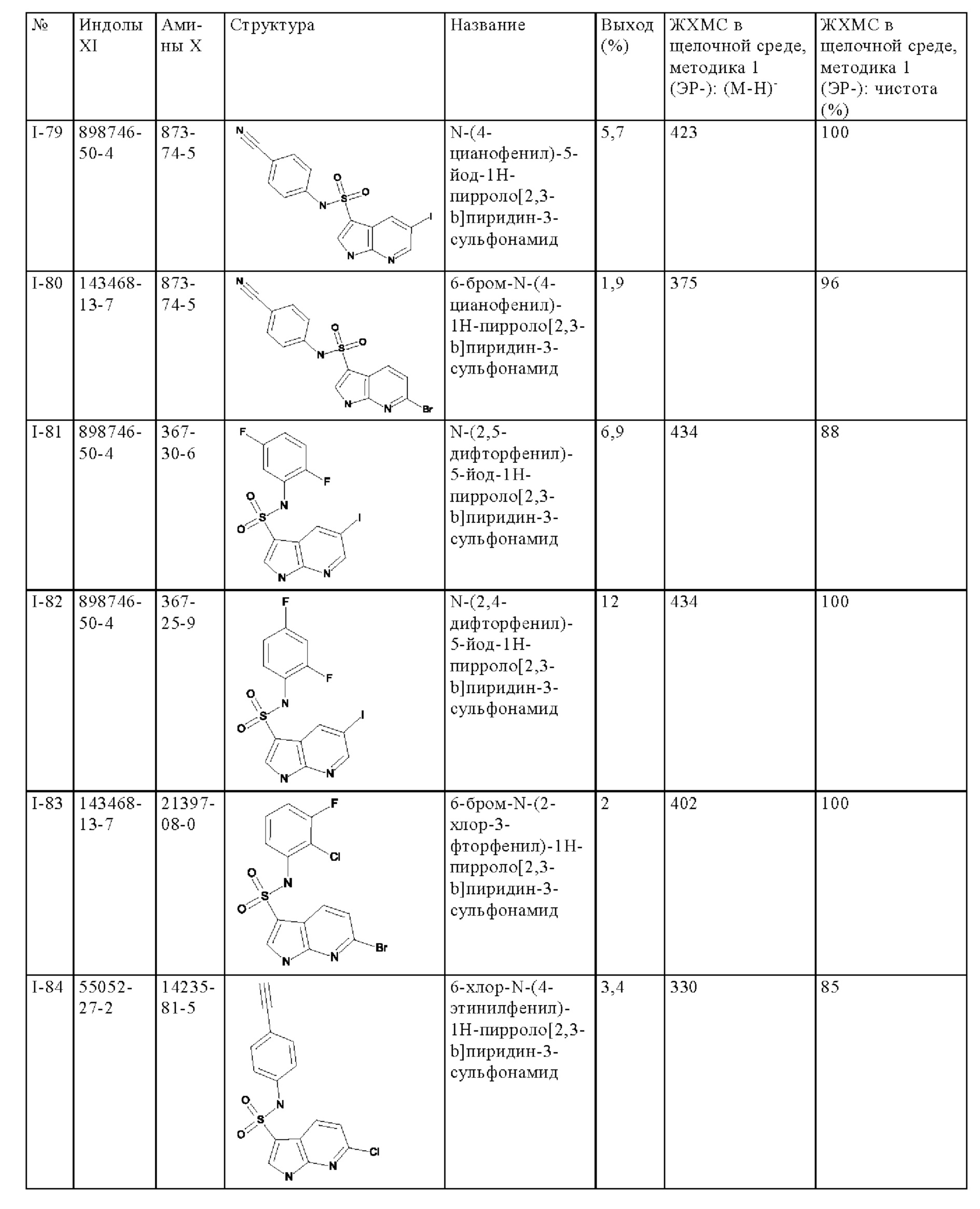
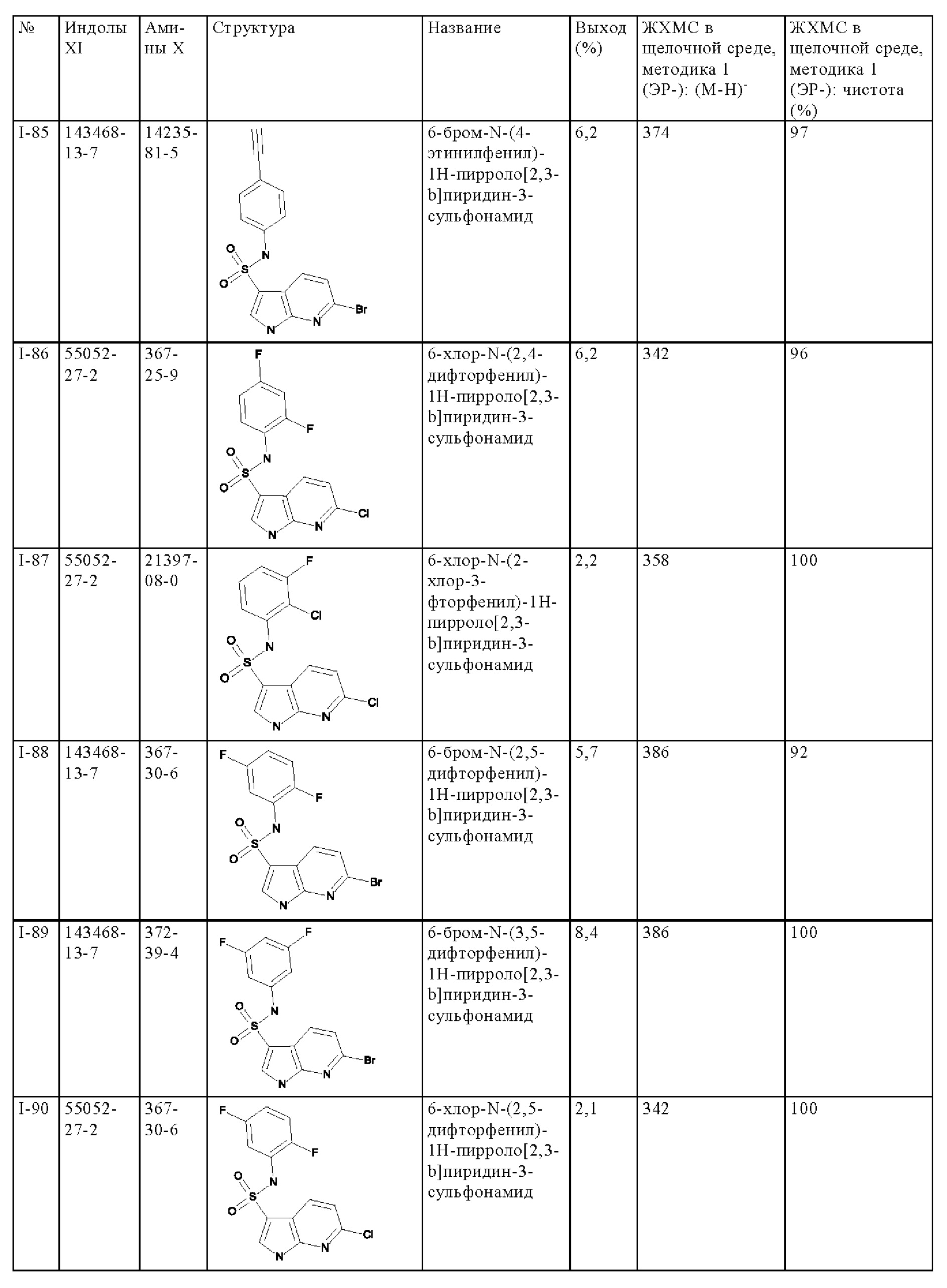

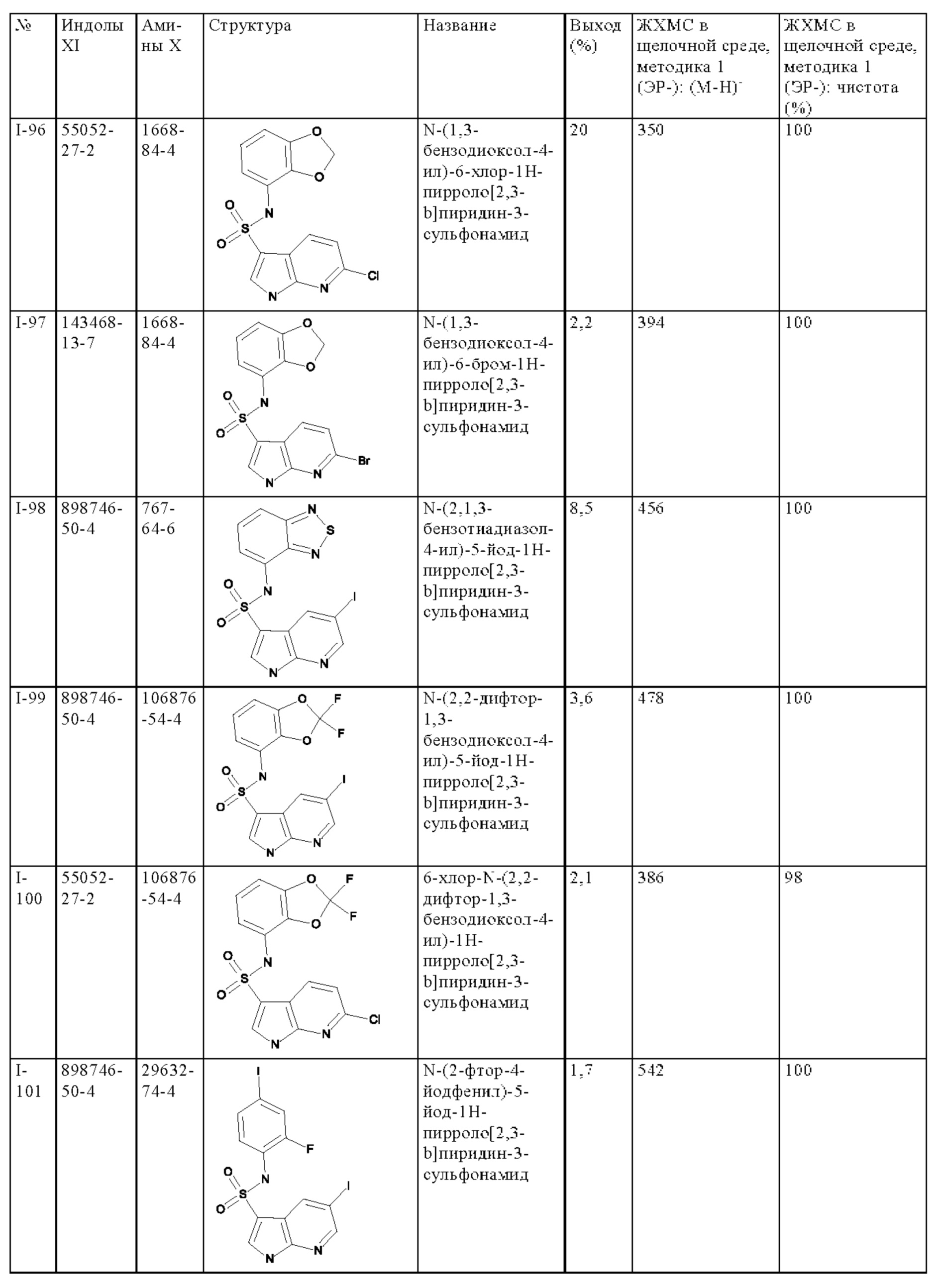
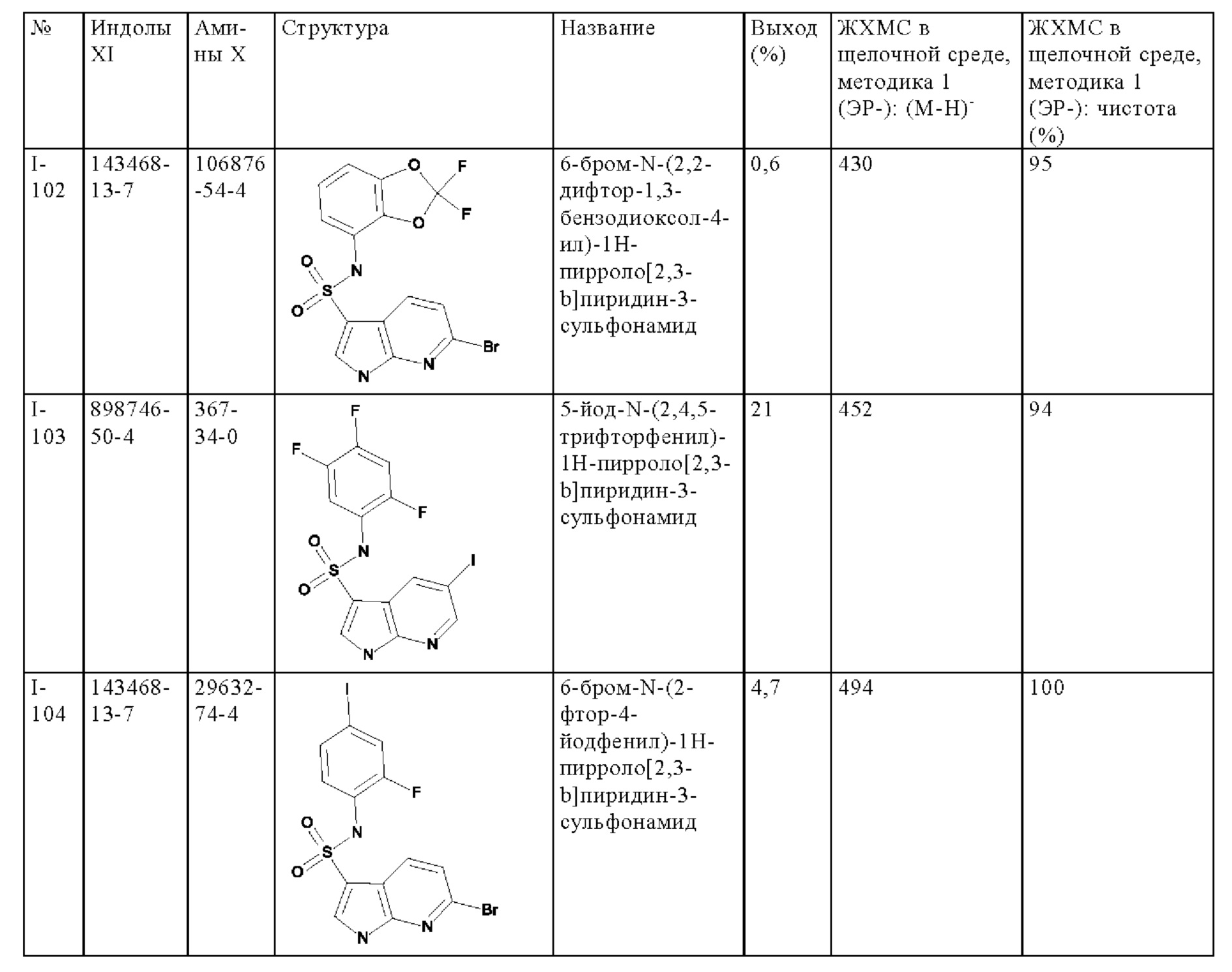
D.3. Методика D. Синтез N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамида I-105
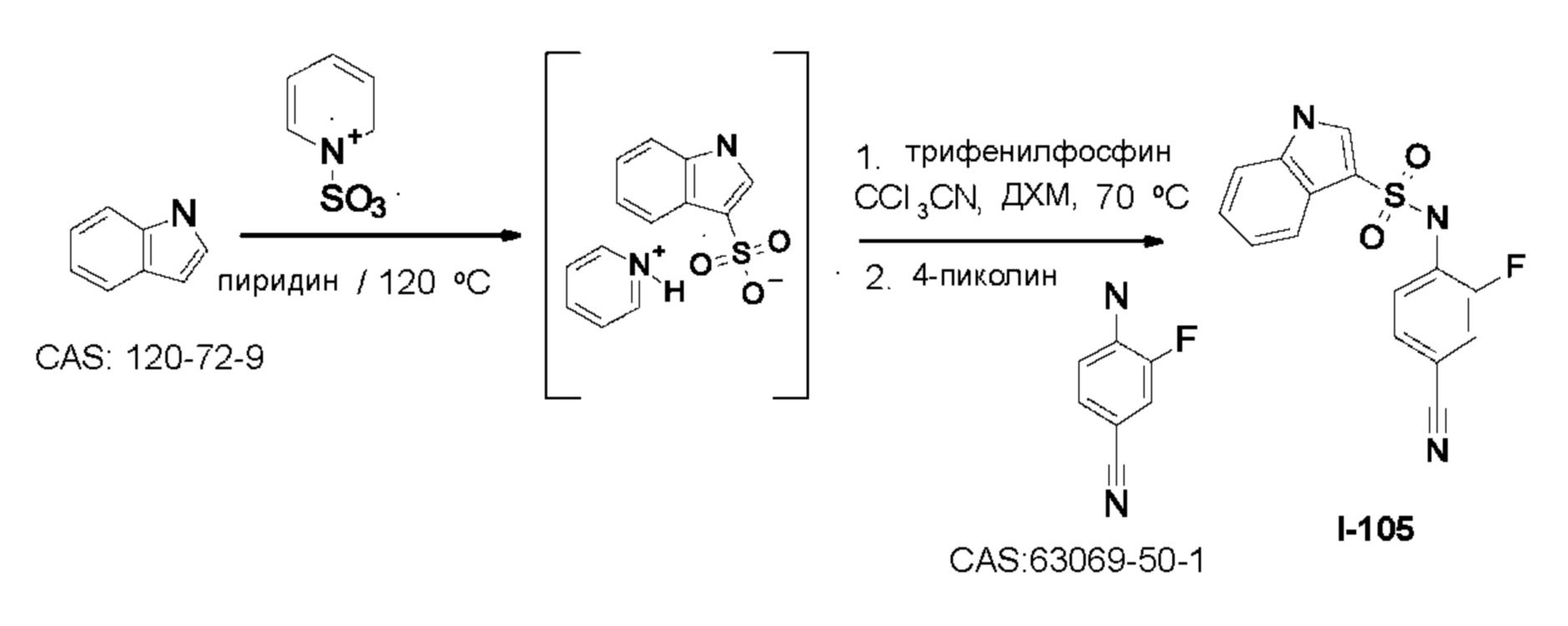
Раствор индола (33,5 мг, 0,29 ммоля), комплекс триоксид серы-пиридин (45,43 мг, 0,29 ммоля) и пиридин (1 мл) кипятили с обратным холодильником при 120°С в течение 1 ч, затем смесь охлаждали до комнатной температуры, затем пиридин выпаривали в вакууме. Полученную суспензию разбавляли водой (10 мл) и затем промывали диэтиловым эфиром (3×30 мл). Затем водную фазу сушили в высоком вакууме (или с помощью лиофилизации) и получали твердый остаток. К сухому остатку добавляли трифенилфосфин (230 мг, 0,86 ммоля), трихлорацетонитрил (123 мг, 0,86 ммоля) и дихлорметан (1 мл) и полученную смесь нагревали при 70°С в течение 1 ч,, затем добавляли 4-амино-3-фторбензонитрил (46,6 мг, 0,34 ммоля) и 4-пиколин (239 мг, 2,57 ммоля). Полученную смесь перемешивали при комнатной температуре в течение ночи. Затем органическую фазу разбавляли с помощью DCM, промывали водой, сушили над безводным сульфатом магния и выпаривали досуха. Продукт очищали с помощью колоночной хроматографии с использованием смеси петролейный эфир (Ткип.=60°С): этилацетат в градиентном режиме от 4:1 до 3:2 и получали бесцветное масло, которое кристаллизовали из ацетона и петролейного эфира и получали 9 мг N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамида I-105, в виде белого порошкообразного вещества.
Выход: 10%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 316,05 (М+Н)+, чистота 97%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,08 (s, 1Н), 10,76 (s, 1H), 8,08 (d, J=3,1 Гц, 1H), 7,83 (d, J=7,9 Гц, 1H), 7,70 (dd, J=10,7, 1,9 Гц, 1H), 7,61-7,48 (m, 2H), 7,49-7,42 (m, 1H), 7,16-7,24 (m, 2H).
Приведенные ниже соединения синтезировали в соответствии с методикой D:
N-(2,1,3-Бензотиадиазол-4-ил)-1Н-индол-3-сульфонамид I-106 получали из 1Н-индола, регистрационный № CAS: 120-72-9, и 2,1,3-бензотиадиазол-4-амина, регистрационный № CAS: 767-64-6.
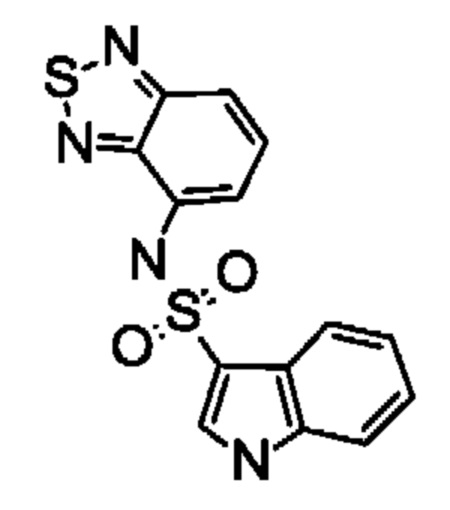
Выход: 15%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 331,02 (М+Н)+, чистота 95%.
1Н ЯМР (600 МГц, DMSO-d6) δ 11,99 (d, J=3,3 Гц, 1H), 10,73 (s, 1H), 8,10 (d, J=3,0 Гц, 1Н), 7,87 (dd, J=8,1, 1,2 Гц, 1H), 7,65 (dd, J=8,8, 0,9 Гц, 1H), 7,57 (dd, J=8,8, 7,4 Гц, 1H), 7,48 (dd, J=7,5, 0,9 Гц, 1H), 7,39-7,40 (m, 1H), 7,14-7,17 (m, 1H), 7,08-7,11 (m, 1H).
N-(2,1,3-Бензотиадиазол-4-ил)-6-фтор-1Н-индол-3-сульфонамид I-107 получали из 6-фтор-1Н-индола, регистрационный № CAS: 399-51-9, и 2,1,3-бензотиадиазол-4-амина, регистрационный № CAS: 767-64-6.
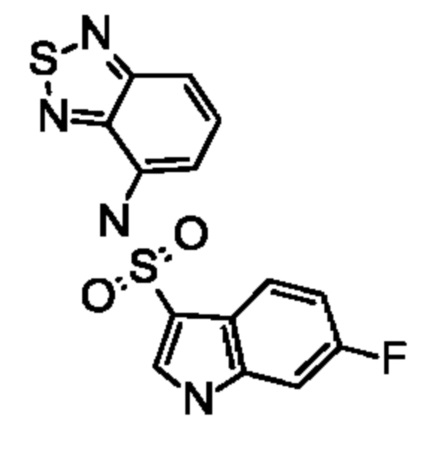
Выход: 13%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 349,02 (М+Н)+, чистота 95%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,02 (s, 1Н), 10,80 (s, 1H), 8,09 (d, J=2,9 Гц, 1H), 7,86 (dd, J=8,9, 5,3 Гц, 1H), 7,71-7,62 (m, 1H), 7,58 (dd, J=8,8, 7,5 Гц, 1H), 7,47 (dd, J=7,4, 1,0 Гц, 1H), 7,19 (dd, J=9,7, 2,4 Гц, 1H), 6,98-7,01 (m, 1H).
6-Хлор-N-(4-циано-2-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-108 получали из 6-хлор-1Н-пирроло[2,3-b]пиридина, регистрационный № CAS: 55052-27-2, и 4-амино-3-фторбензонитрила, регистрационный № CAS: 63069-50-1.
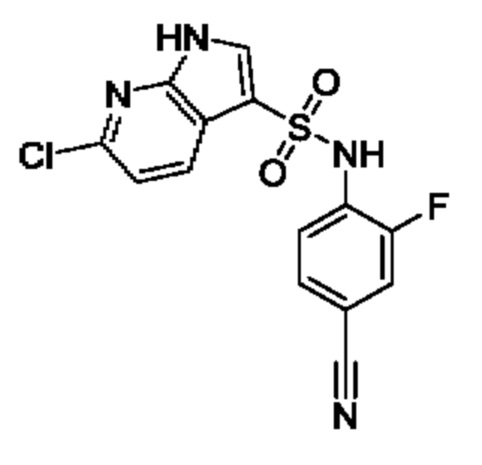
Выход: 5%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 351 (М+Н)+, чистота 95,0%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,92 (d, J=3,4 Гц, 1H), 10,83 (s, 1H), 8,27 (d, J=2,9 Гц, 1Н), 8,22 (d, J=8,3 Гц, 1H), 7,81-7,68 (m, 1H), 7,64-7,50 (m, 2H), 7,37 (d, J=8,3 Гц, 1H).
N-(2,1,3-Бензотиадиазол-4-ил)-6-хлор-1Н-индол-3-сульфонамид I-109 получали из 6-хлор-1H-индола, регистрационный № CAS: 17422-33-2, и 2,1,3-бензотиадиазол-4-амина, регистрационный № CAS: 767-64-6.
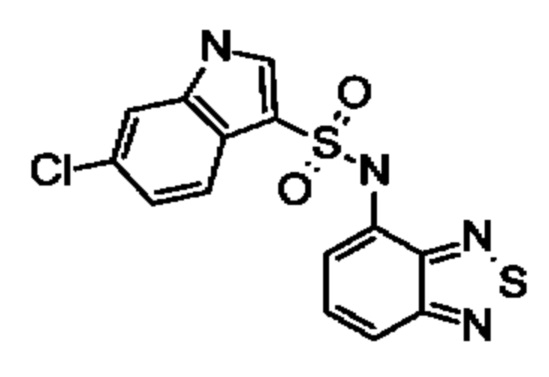
Выход: 31%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 364,99 (М+Н)+, чистота 99,0%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,08 (s, 1Н), 10,80 (s, 1H), 8,12 (d, J=2,4 Гц, 1H), 7,86 (d, J=8,6 Гц, 1H), 7,68 (dd, J=8,8, 0,9 Гц, 1H), 7,58 (dd, J=8,8, 7,4 Гц, 1H), 7,50-7,43 (m, 2H), 7,14 (dd, J=8,6, 1,9 Гц, 1H).
N-(2,1,3-Бензотиадиазол-4-ил)-6-бром-1Н-индол-3-сульфонамид I-110 получали из 6-бром-1Н-индола, регистрационный № CAS: 52415-29-9, и 2,1,3-бензотиадиазол-4-амина, регистрационный № CAS: 767-64-6.
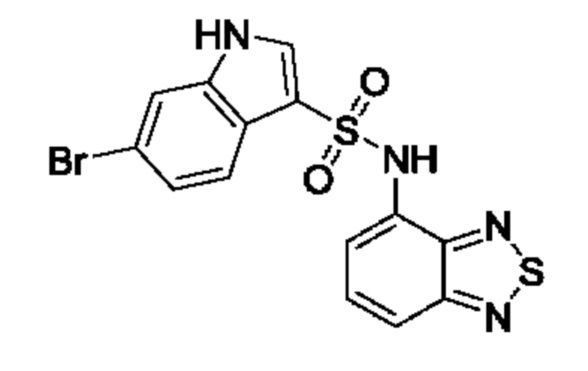
Выход: 27%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 408,94 (М+Н)+, чистота 94,0%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,07 (s, 1Н), 10,80 (s, 1H), 8,10 (d, J=2,6 Гц, 1H), 7,81 (d, J=8,6 Гц, 1H), 7,68 (dd, J=8,8, 0,9 Гц, 1H), 7,65-7,55 (m, 2H), 7,46 (dd, J=7,5, 0,9 Гц, 1H), 7,26 (dd, J=8,6, 1,8 Гц, 1H).
N-(2,1,3-Бензотиадиазол-4-ил)-7-бром-1Н-индол-3-сульфонамид I-111 получали из 7-бром-1Н-индола, регистрационный № CAS: 51417-51-7, и 2,1,3-бензотиадиазол-4-амина, регистрационный № CAS: 767-64-6.
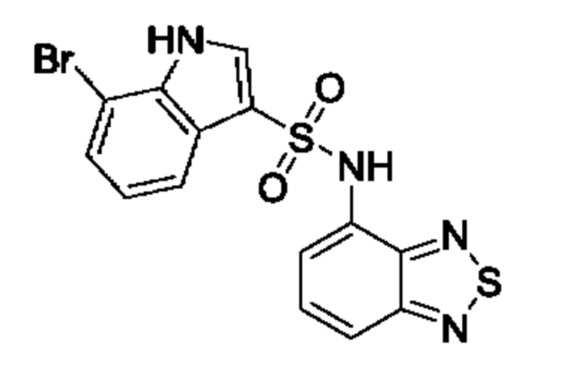
Выход: 25%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 408,94 (М+Н)+, чистота 96,8%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,30 (d, J=3,5 Гц, 1H), 10,86 (s, 1Н), 8,10 (d, J=2,8 Гц, 1H), 7,88 (dd, J=8,0, 0,9 Гц, 1H), 7,68 (dd, J=8,8, 0,9 Гц, 1H), 7,58 (dd, J=8,8, 7,4 Гц, 1H), 7,49 (dd, J=7,4, 0,9 Гц, 1H), 7,41 (dd, J=7,7, 0,9 Гц, 1H), 7,06 (t, J=7,9 Гц, 1H).
N-(4-Циано-2-фторфенил)-6-метокси-1H-индол-3-сульфонамид I-112 получали из 6-метокси-1Н-индола, регистрационный № CAS: 3189-13-7, и 4-амино-3-фторбензонитрила, регистрационный № CAS: 63069-50-1.
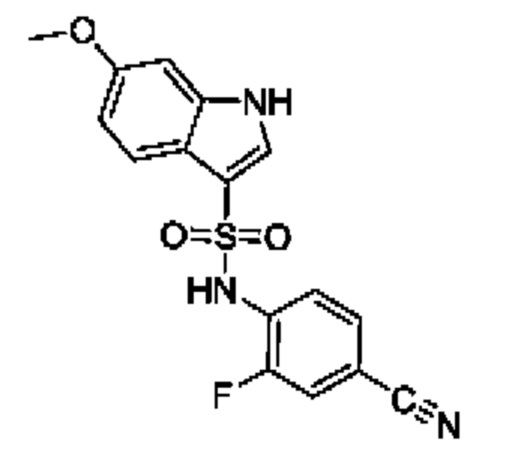
Выход: 18%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 345,3 (М+Н)+, чистота 97,33%.
1H ЯМР (500 МГц, DMSO-d6) δ11,96-11,74 (m, 1Н),10,69 (s, 1Н), 7,93 (d, J=3,0 Гц, 1H), 7,76-7,63 (m, 2H), 7,60-7,46 (m, 2H), 6,93 (dd, J=2,3, 0,6 Гц, 1H), 6,82 (dd, J=8,8, 2,3 Гц, 1H), 3,76 (s, 3H).
N-(4-Циано-2-фторфенил)-6-фтор-1Н-индол-3-сульфонамид I-113 получали из 6-фтор-1Н-индола, регистрационный № CAS: 399-51-9, и 4-амино-3-фторбензонитрила, регистрационный № CAS: 63069-50-1.
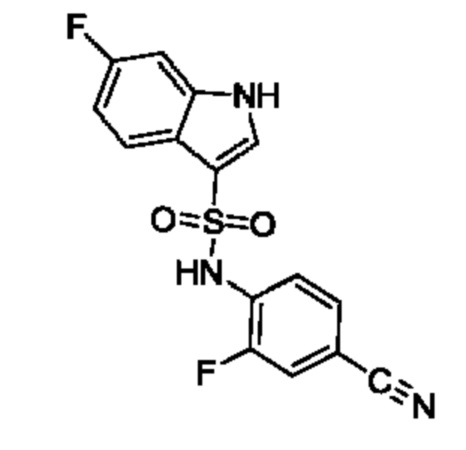
Выход: 21%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 333,3 (М+Н)+, чистота 98,49%.
1H ЯМР (500 МГц, DMSO-d6) δ 11,96-11,74 (m, 1Н),10,69 (s, 1Н), 7,93 (d, J=3,0 Гц, 1H), 7,76-7,63 (m, 2H), 7,60-7,46 (m, 2H), 6,93 (dd, J=2,3, 0,6 Гц, 1H), 6,82 (dd, J=8,8, 2,3 Гц, 1H), 3,76 (s, 3H).
6-Бром-N-(4-циано-2-фторфенил)-1H-индол-3-сульфонамид I-114 получали из 6-бром-1Н-индола, регистрационный № CAS: 52415-29-9, и 4-амино-3-фторбензонитрила, регистрационный № CAS: 63069-50-1.
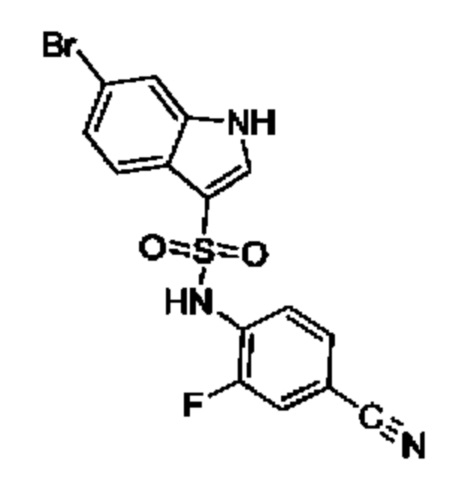
Выход: 25%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 394,2 (М+Н)+, чистота 99,34%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,23-12,10 (m, 1Н), 10,77 (s, 1H), 8,09 (d, J=3,0 Гц, 1H), 7,79-7,70 (m, 2H), 7,66 (d, J=1,8 Гц, 1H), 7,55 (dd, J=3,5, 1,6 Гц, 2H), 7,34 (dd, J=8,6, 1,8 Гц, 1H).
N-(4-Циано-2-фторфенил)-7-метокси-1H-индол-3-сульфонамид I-115 получали из 7-метокси-1Н-индола, регистрационный № CAS: 3189-22-8, и 4-амино-3-фторбензонитрила, регистрационный № CAS: 63069-50-1.
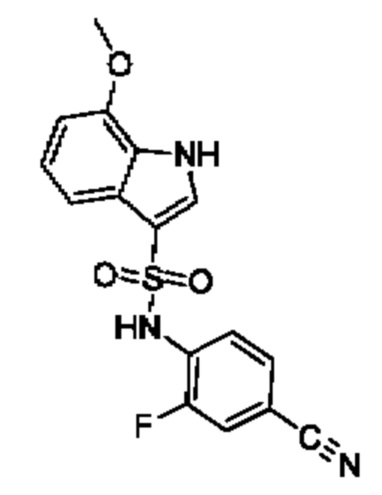
Выход: 17%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 345,3 (М+Н)+, чистота 100%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,46-12,02 (m, 1Н), 10,72 (s, 1H), 7,91 (d, J=3,1 Гц, 1H), 7,70 (dd, J=10,8, 1,8 Гц, 1H), 7,61-7,52 (m, 2H), 7,40 (d, J=8,1 Гц, 1H), 7,10 (t, J=7,9 Гц, 1H), 6,79 (d, J=7,8 Гц, 1H), 3,90 (s, 3H).
6-Хлор-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамид I-116 получали из 6-хлор-1Н-индола, регистрационный № CAS: 17422-33-2, и 4-амино-3-фторбензонитрила, регистрационный № CAS: 63069-50-1.
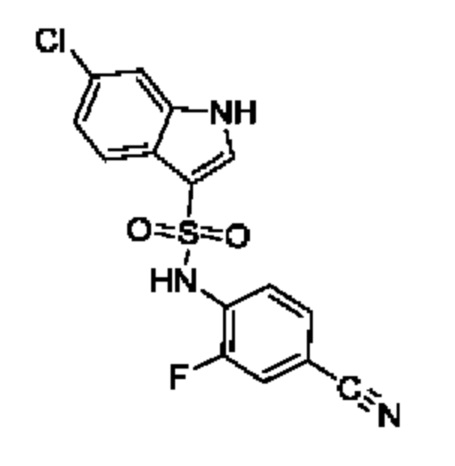
Выход: 28%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 349,7 (М+Н)+, чистота 100%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,17 (d, J=3,3 Гц, 1H), 10,77 (s, 1H), 8,10 (d, J=2,9 Гц, 1Н), 7,82 (d, J=8,6 Гц, 1H), 7,75-7,71 (m, 1H), 7,57-7,53 (m, 2H), 7,52 (s, 1H), 7,23 (dd, J=8,6, 1,9 Гц, 1H).
7-Хлор-N-(4-циано-2,5-дифторфенил)-1Н-индол-3-сульфонамид I-117 получали из 7-хлор-1H-индола, регистрационный № CAS: 53924-05-3, и 4-амино-2,5-дифторбензонитрила, регистрационный № CAS: 112279-61-5.
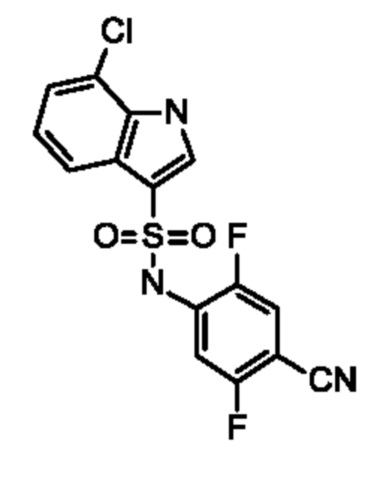
Выход: 42%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 337,99 (М+Н)+, чистота 98%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,65 (s, 1Н), 11,25 (s, 1H), 8,35 (d, J=3,1 Гц, 1H), 7,89-7,80 (m, 2H), 7,49 (dd, J=10,9, 6,3 Гц, 1H), 7,36 (dd, J=7,7, 0,9 Гц, 1H), 7,23 (t, J=7,9 Гц, 1H).
D.4. Методика E. Синтез N-(4-хлор-2,5-дифторфенил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамида I-118
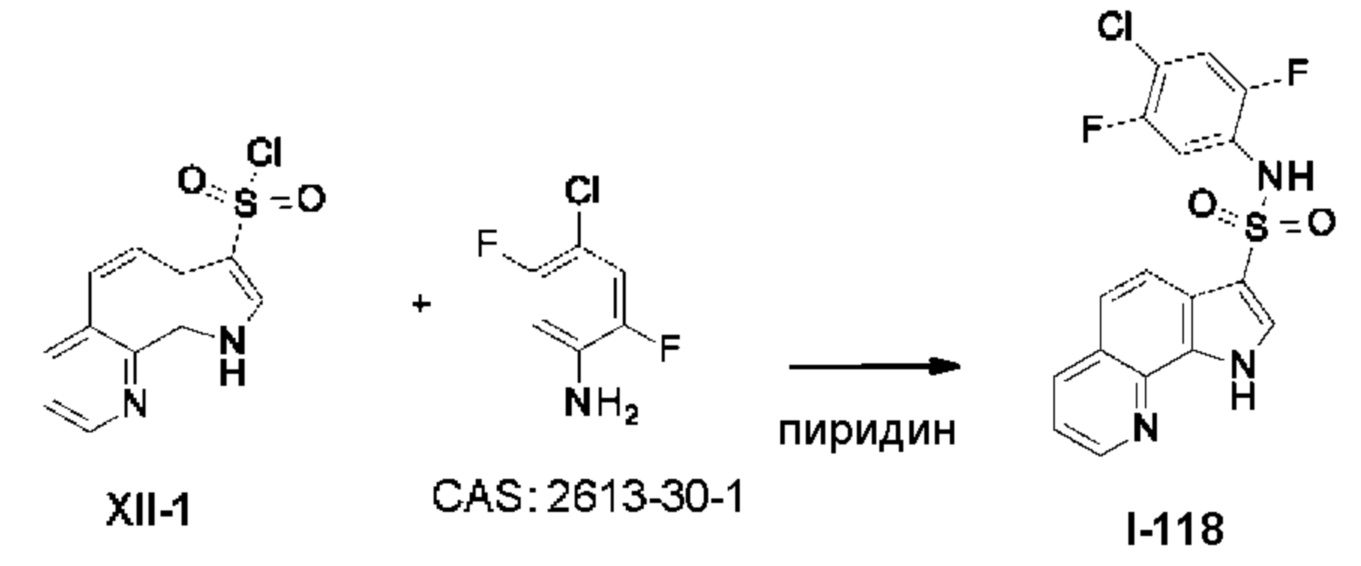
К раствору 1Н-пирроло[3,2-Н]хинолин-3-сульфонилхлорида (140 мг, 0,52 ммоля) в пиридине (1,5 мл) добавляли 4-хлор-2,5-дифторанилин (90 мг, 0,55 ммоля). Реакционную смесь перемешивали при комнатной температуре в течение 4 ч и затем выпаривали досуха. Остаток растирали со смесью вода/ацетонитрил (8/2) и обрабатывали ультразвуком. Твердую суспензию фильтровали, промывали водой, сушили в вакууме при 35°С и получали 105 мг N-(4-хлор-2,5-дифторфенил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамида I-118, в виде бежевого твердого вещества.
Выход: 50%.
ЖХМС в щелочной среде, методика 1 (ЭР+): 394 (М+Н)+, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 13,26 (s, 1Н), 10,51 (s, 1H), 8,93 (dd, J=4,4, 1,6 Гц, 1H), 8,46 (dd, J=8,3, 1,6 Гц, 1H), 8,04-7,65 (m, 3Н), 7,59 (m, 1H), 7,51 (dd, J=9,8, 6,8 Гц, 1H), 7,40 (dd, J=10,4, 7,0 Гц, 1H).
Соединения, приведенные ниже в таблице 6, можно синтезировать по методике, аналогичной методике Е.
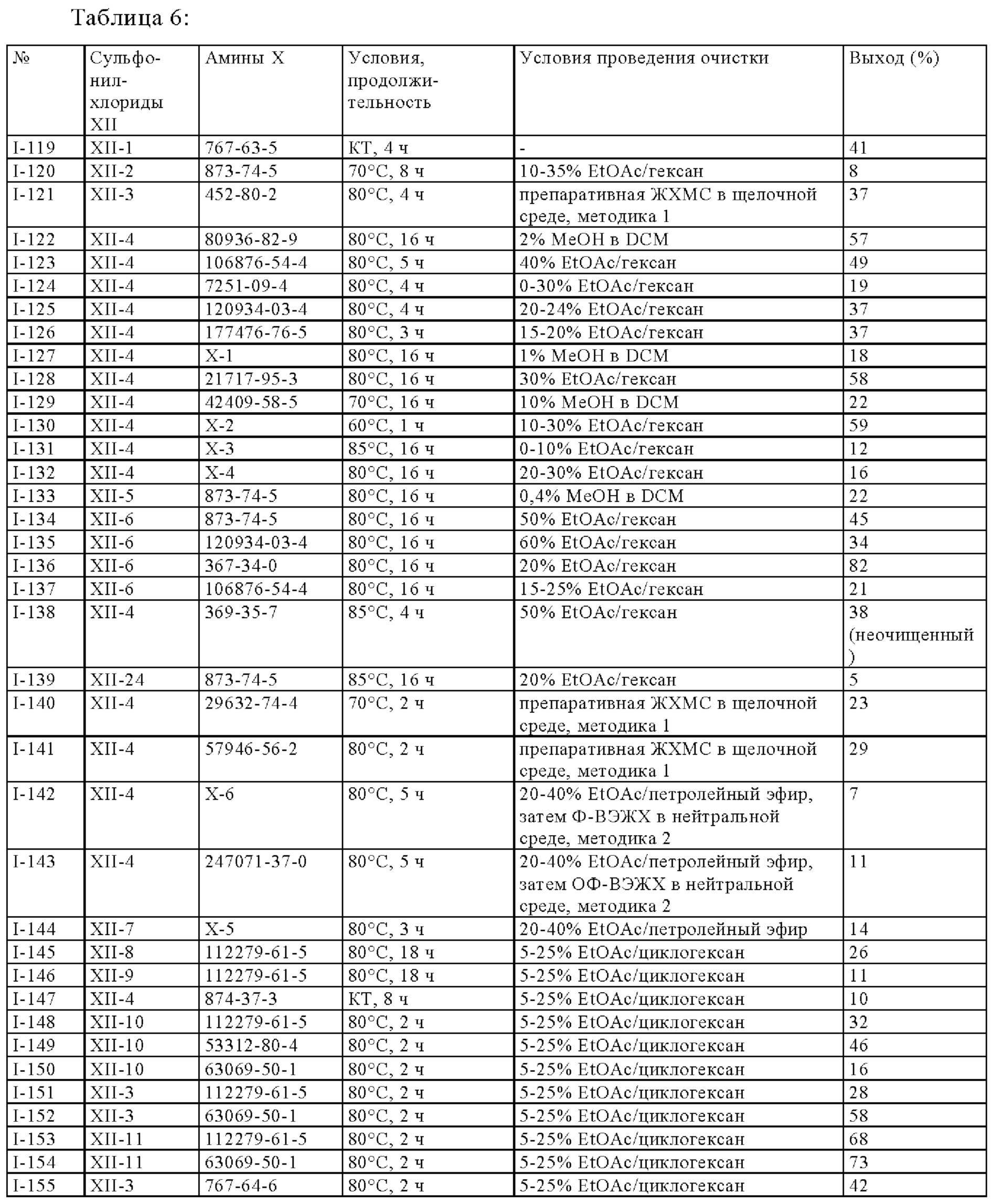
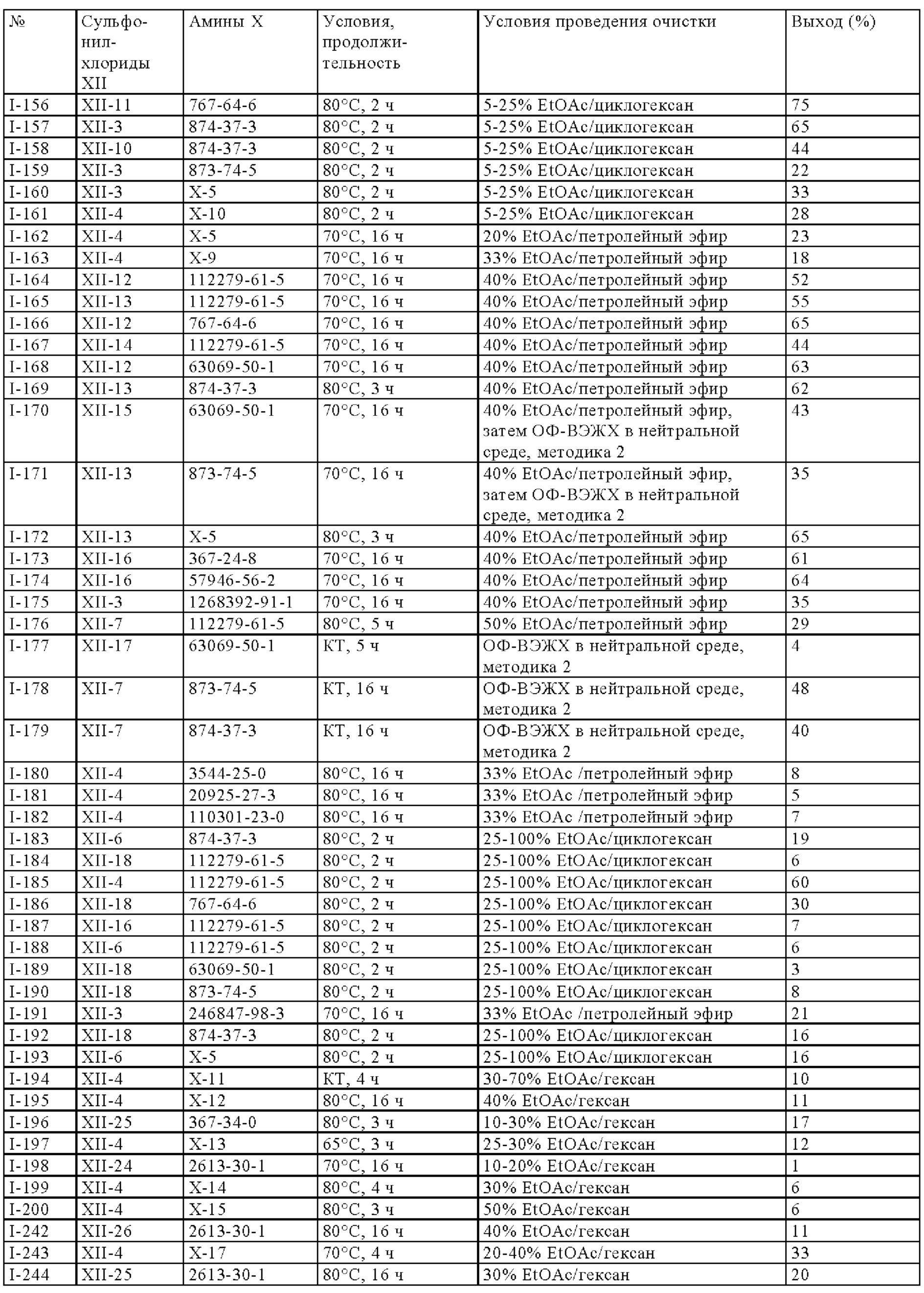
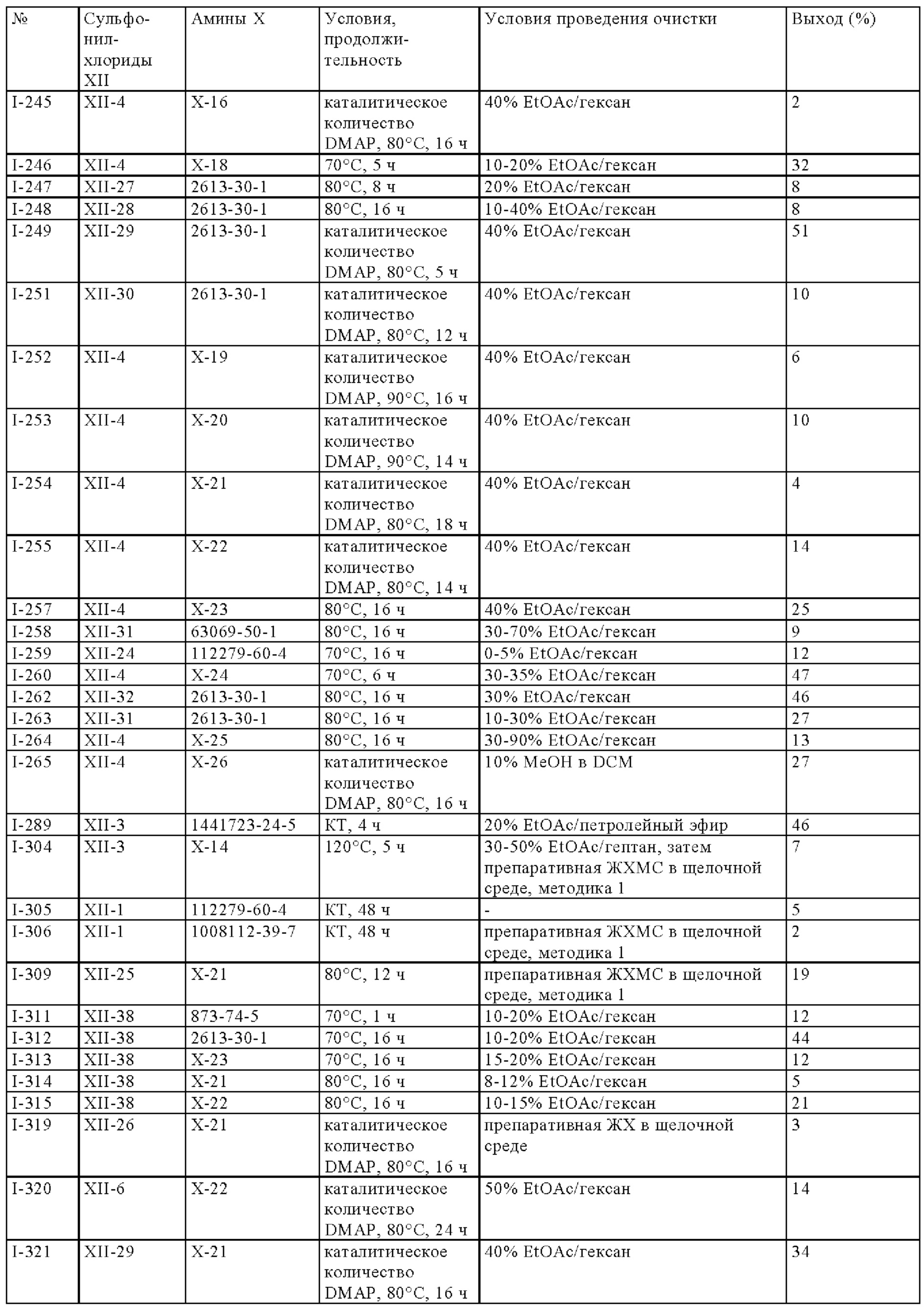
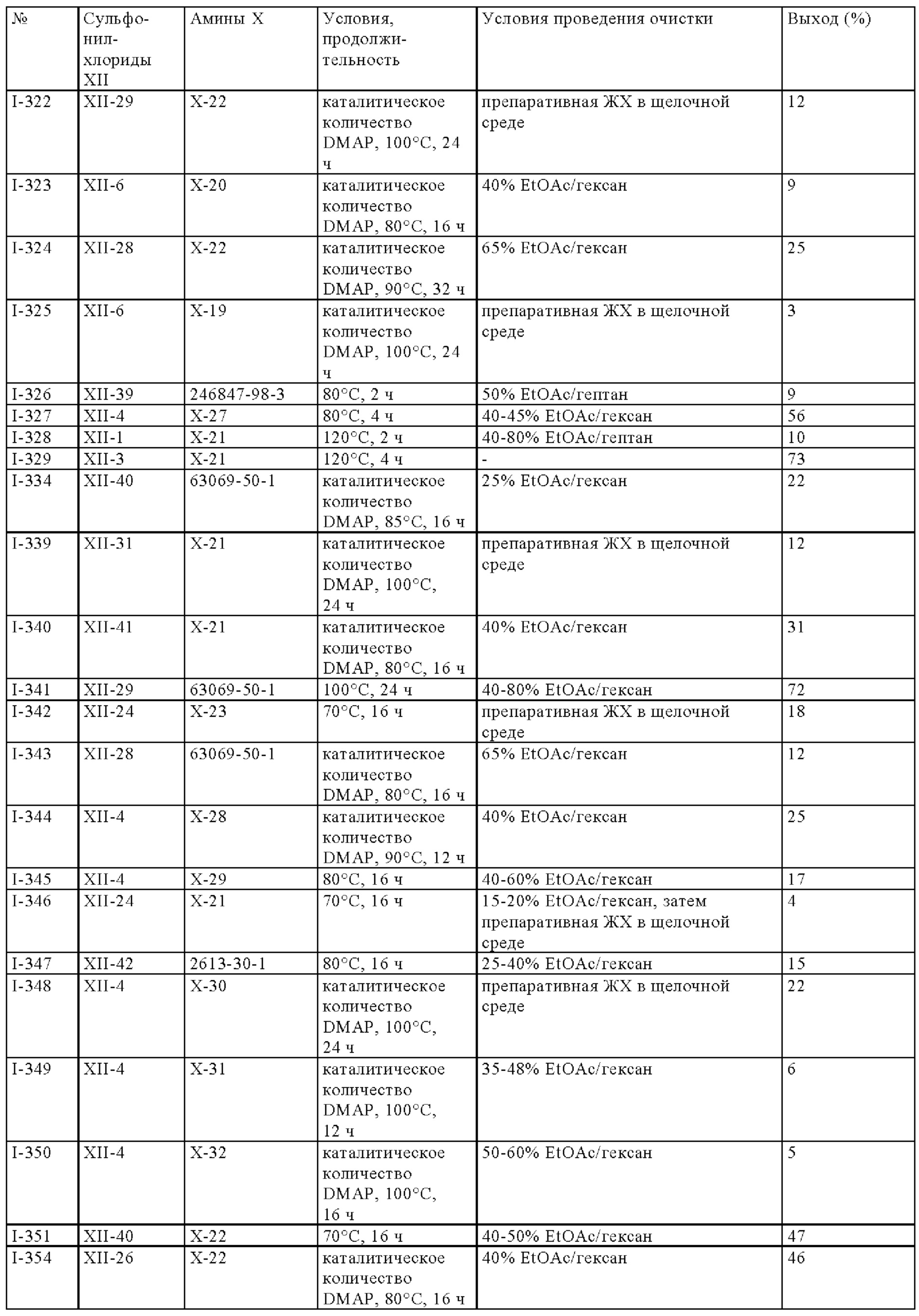
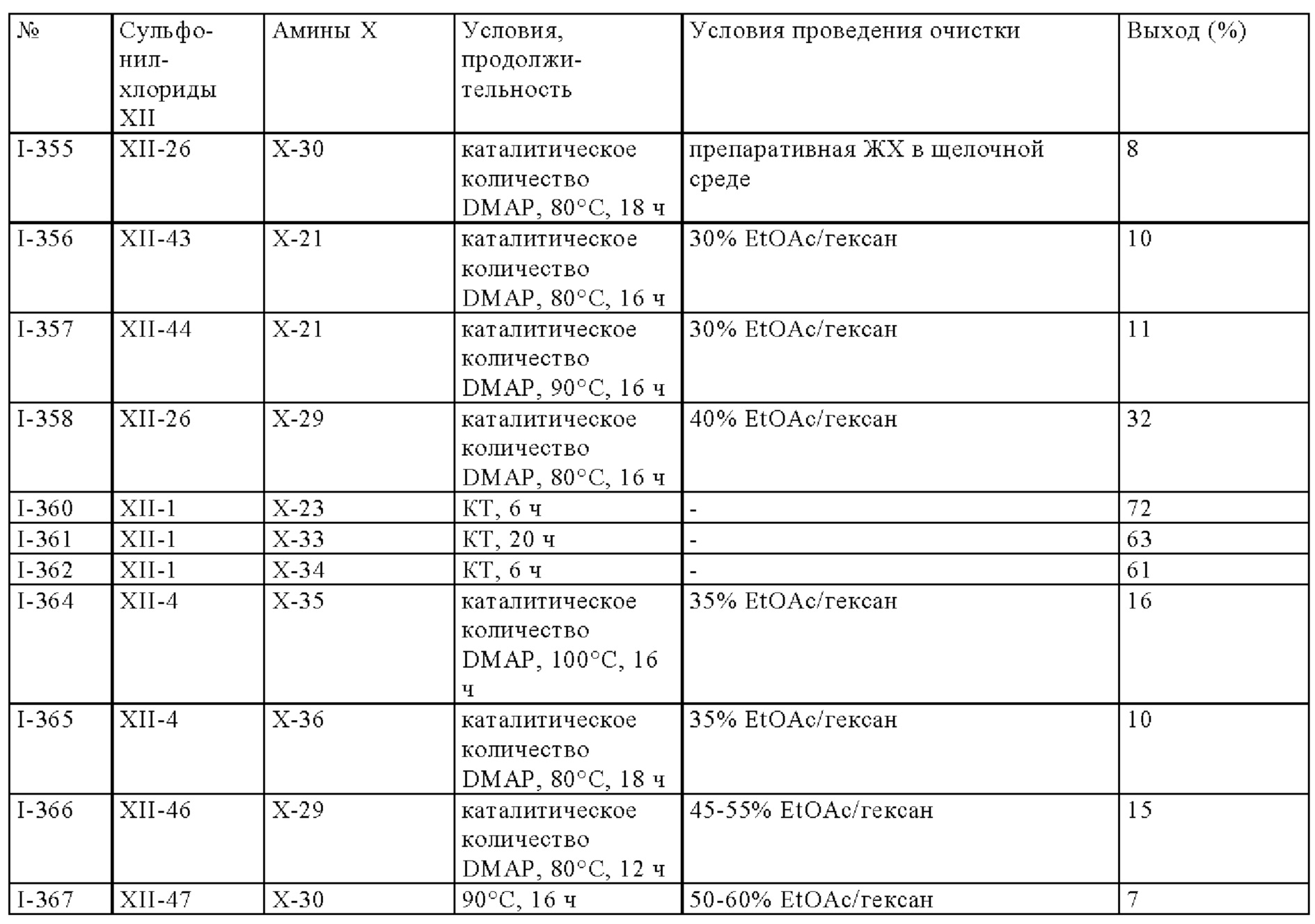
N-(2,1,3-Бензоксадиазол-4-ил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид I-119
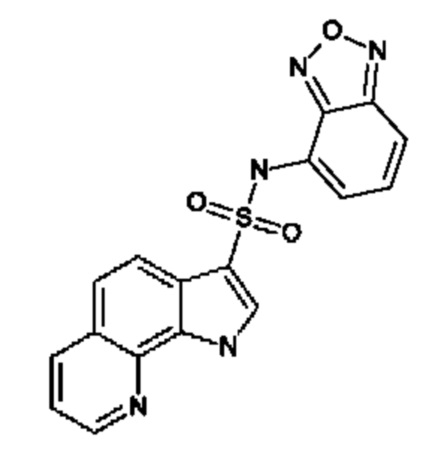
ЖХМС в щелочной среде, методика 1 (ЭР+): 366 (М+Н)+, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 13,29 (s, 1Н), 11,35 (s, 1H), 8,90 (dd, J=4,4, 1,6 Гц, 1H), 8,42 (dd, J=8,3, 1,6 Гц, 1H), 8,14 (s, 1H), 8,08 (d, J=8,7 Гц, 1H), 7,67 (d, J=8,8 Гц, 1H), 7,63-7,42 (m, 3H), 7,32 (d, J=7,2 Гц, 1H).
N-(4-Цианофенил)-5,6-дифтор-1H-индол-3-сульфонамид I-120
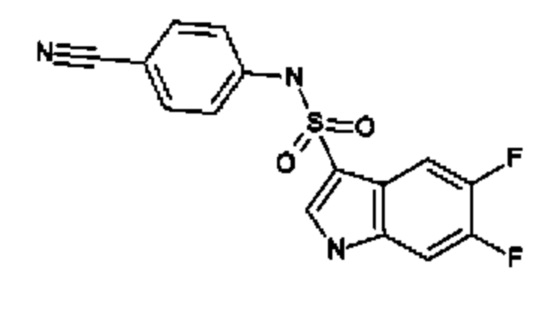
ЖХМС в щелочной среде, методика 2 (ЭР+): 334 (М+Н)+, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,24 (d, J=8,7 Гц, 2Н) 7,52 (dd, J=10,7, 7,0 Гц, 1Н) 7,65 (d, J=8,7 Гц, 2H) 7,74 (dd, J=10,9, 7,9 Гц, 1H) 8,21 (d, J=2,8 Гц, 1H) 10,95 (s, 1H) 12,26 (s, 1H).
N-(2-Фтор-4-метилфенил)-1Н-бензо[g]индол-3-сульфонамид I-121
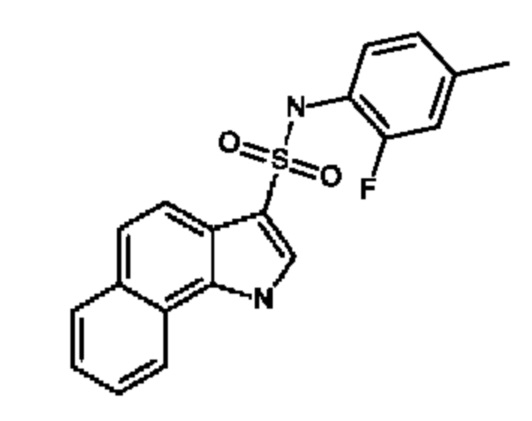
ЖХМС в щелочной среде, методика 1 (ЭР+): 355 (М+Н)+, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 12,83 (s, 1Н), 9,78 (s, 1H), 8,40 (dd, J=8,2, 1,0 Гц, 1H), 7,98 (dd, J=8,2, 1,2 Гц, 1H), 7,83-7,90 (m, 2H), 7,68-7,56 (m, 2H), 7,51 (ddd, J=8,1, 6,9, 1,2 Гц, 1H), 7,15 (t, J=8,2 Гц, 1H), 6,94-6,79 (m, 2H), 2,18 (s, 3H)
6-Хлор-N-(4-(метоксиметил)фенил)-1H-индол-3-сульфонамид I-122
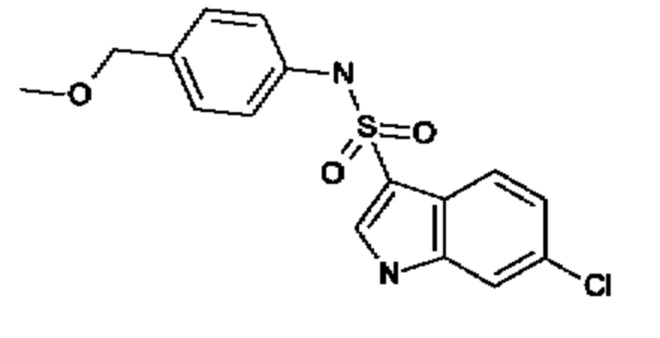
ЖХМС в щелочной среде, методика 2 (ЭР-): 349 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,19 (s, 3Н) 4,22 (s, 2Н) 7,01-7,06 (m, 2Н) 7,08-7,13 (m, 2Н) 7,20 (dd, J=8,56, 1,71 Гц, 1Н) 7,48 (d, J=1,47 Гц, 1H) 7,80 (d, J=8,56 Гц, 1H) 7,98 (s, 1H) 10,19 (brs, 1H) 12,02 (brs, 1H).
6-Хлор-N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-1Н-индол-3-сульфонамид I-123

ЖХМС в щелочной среде, методика 2 (ЭР-): 385 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,95 (d, J=7,82 Гц, 1Н) 7,06 (t, J=8,31 Гц, 1H) 7,11-7,15 (m, 1H) 7,18 (dd, J=8,56, 1,71 Гц, 1H) 7,52 (d, J=1,47 Гц, 1H) 7,64 (d, J=8,80 Гц, 1H) 7,94 (d, J=2,93 Гц, 1H) 10,34 (s, 1H) 12,11 (brs, 1H).
6-Хлор-N-(4-циано-3-метоксифенил)-1H-индол-3-сульфонамид I-124
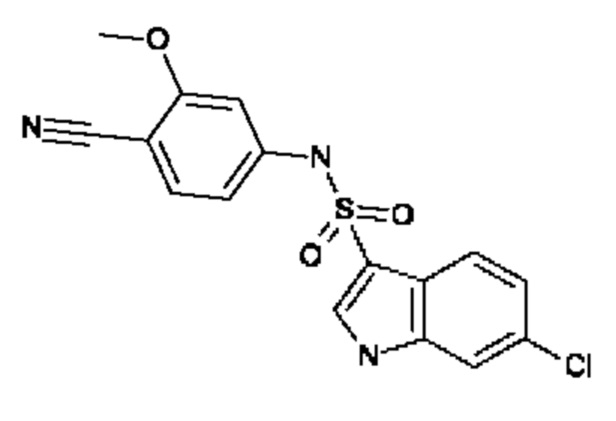
ЖХМС в щелочной среде, методика 2 (ЭР-): 360 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,79 (s, 3Н) 6,76 (d, J=8,31 Гц, 1Н) 6,87 (s, 1H) 7,26 (d, J=8,56 Гц, 1H) 7,44-7,56 (m, 2H) 7,83 (d, J=8,80 Гц, 1H) 8,24 (s, 1H) 10,96 (s, 1H) 12,20 (brs, 1H).
6-Хлор-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1Н-индол-3-сульфонамид I-125
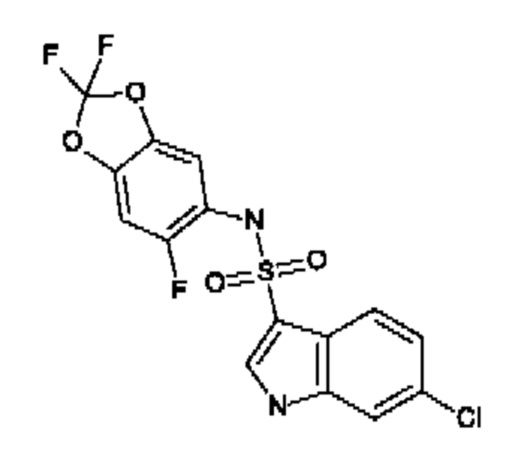
ЖХМС в щелочной среде, методика 2 (ЭР-): 403 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,18 (dd, J=8,56, 1,71 Гц, 1Н) 7,29 (d, J=6,36 Гц, 1H) 7,41 (d, J=8,80 Гц, 1H) 7,50 (s, 1H) 7,68 (d, J=8,80 Гц, 1H) 7,89 (d, J=2,93 Гц, 1H) 10,06 (s, 1H) 12,06 (brs, 1H).
6-Хлор-N-(4-циано-2-метоксифенил)-1H-индол-3-сульфонамид I-126
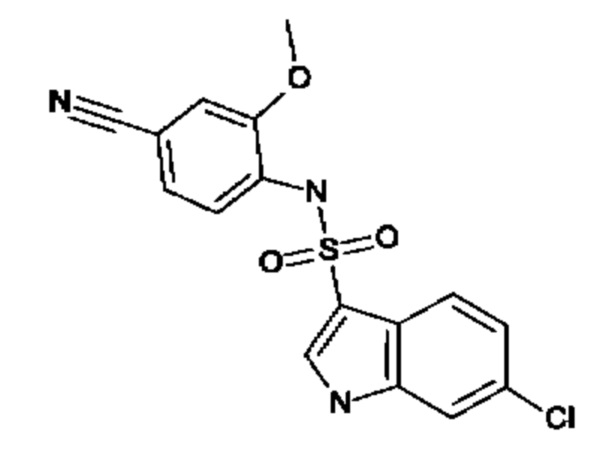
ЖХМС в щелочной среде, методика 2 (ЭР-): 360 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,62 (s, 3Н) 7,22 (dd, J=8,80, 1,47 Гц, 1Н) 7,28-7,33 (m, 2H) 7,46 (d, J=8,31 Гц, 1H) 7,51 (s, 1H) 7,86 (d, J=8,31 Гц, 1H) 8,05 (d, J=2,45 Гц, 1H) 9,85 (s, 1H) 12,10 (brs, 1H).
6-Хлор-N-(7-фтор-2,1,3-бензотиадиазол-4-ил)-1Н-индол-3-сульфонамид I-127
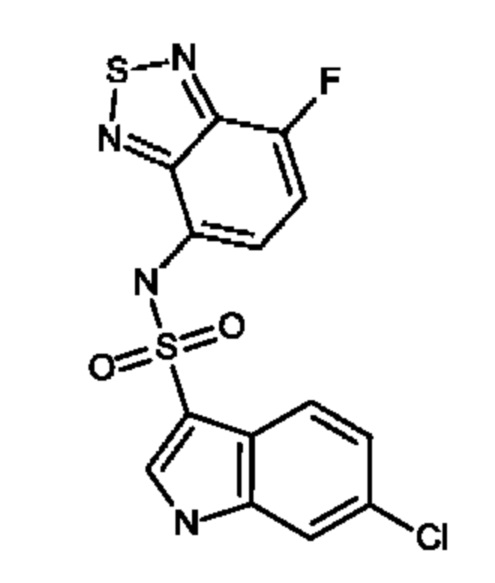
ЖХМС в щелочной среде, методика 2 (ЭР-): 381 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,13 (d, J=8,80 Гц, 1Н) 7,38-7,42 (m, 2H) 7,44 (s, 1H) 7,76 (d, J=8,31 Гц, 1H) 8,02 (brs, 1H) 10,72 (s, 1H) 12,05 (brs, 1H).
6-Хлор-N-(3-фторпиридин-2-ил)-1H-индол-3-сульфонамид I-128
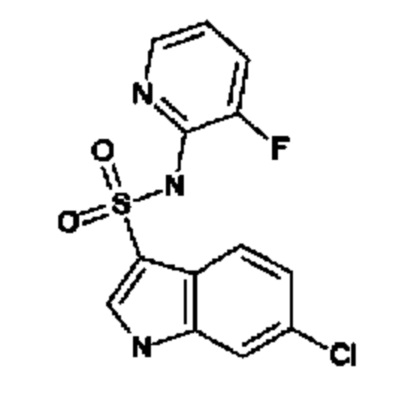
ЖХМС в щелочной среде, методика 2 (ЭР+): 326 (М+Н)+, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,02-7,08 (m, 1Н) 7,22 (d, J=8,31 Гц, 1H) 7,52 (s, 1H) 7,61 (t, J=9,29 Гц, 1H) 7,87 (d, J=7,83 Гц, 1H) 7,96-8,02 (m, 1H) 8,10 (s, 1H) 10,86 (s, 1H) 12,09 (s, 1H).
N-(5-Бром-3-метоксипиридин-2-ил)-6-хлор-1Н-индол-3-сульфонамид I-12
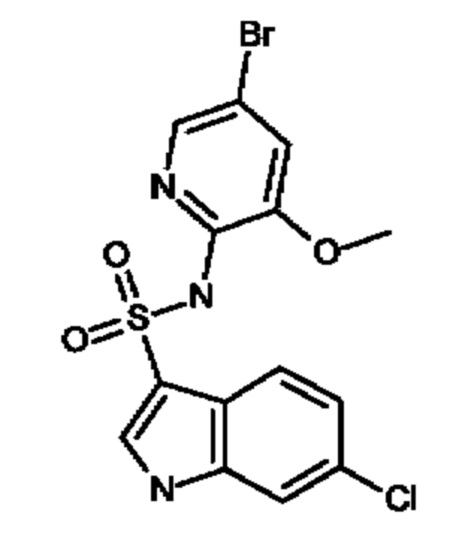
ЖХМС в щелочной среде, методика 2 (ЭР+): 416 (М+Н)+, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,78 (s, 3Н) 7,21 (dd, J=8,56, 1,71 Гц, 1H) 7,50 (s, 2Н) 7,79 (d, J=1,96 Гц, 1H) 7,94 (d, J=8,31 Гц, 1H) 8,09 (d, J=2,45 Гц, 1H) 10,25 (s, 1Н) 12,06 (brs, 1H).
N-(7-Бром-2,2-дифтор-1,3-бензодиоксол-4-ил)-6-хлор-1Н-индол-3-сульфонамид I-130
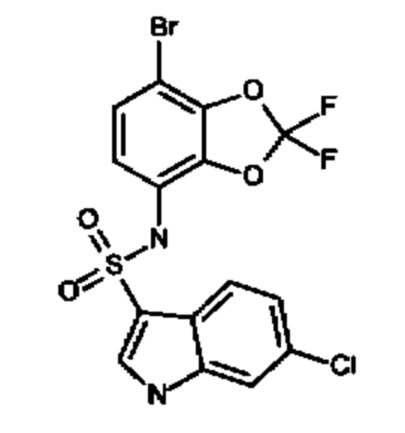
ЖХМС в щелочной среде, методика 2 (ЭР-): 463 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,91 (d, J=8,80 Гц, 1Н) 7,19 (d, J=8,31 Гц, 1H) 7,30 (d, J=9,29 Гц, 1H) 7,48-7,57 (m, 1H) 7,64-7,72 (m, 1H) 7,94 (d, J=2,45 Гц, 1H) 10,44 (brs, 1H) 12,13 (brs, 1H).
6-Хлор-N-(5-фтор-2,1,3-бензотиадиазол-4-ил)-1H-индол-3-сульфонамид I-131
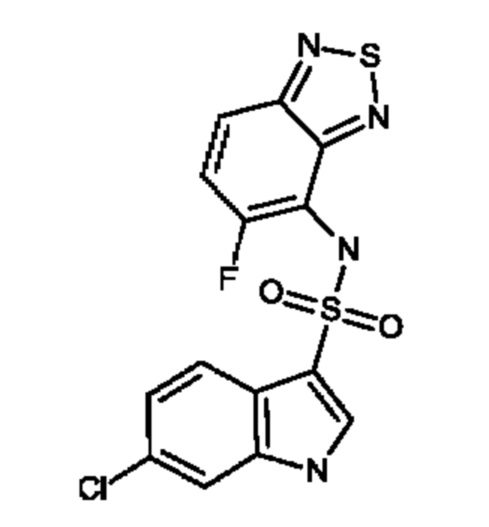
ЖХМС в щелочной среде, методика 2 (ЭР+): 383 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,04 (dd, J=8,80, 1,96 Гц, 1Н) 7,40 (d, J=8,80 Гц, 1H) 7,48 (d, J=1,47 Гц, 1H) 7,72 (t, J=9,78 Гц, 1H) 7,83 (d, J=1,96 Гц, 1H) 8,05 (dd, J=9,29, 4,40 Гц, 1H) 10,13 (s, 1H) 11,98 (brs, 1H).
6-Хлор-N-(6-циано-2,2-дифтор-1,3-бензодиоксол-4-ил)-1H-индол-3-сульфонамид I-132
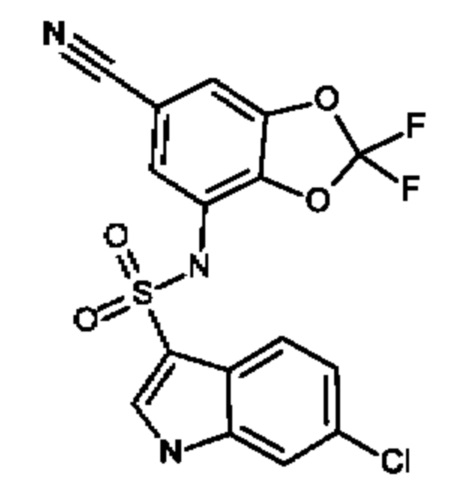
ЖХМС в щелочной среде, методика 2 (ЭР-): 410,00 (М-Н)-, чистота 92%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,21 (dd, J=8,56, 1,71 Гц, 1Н) 7,45 (s, 1H) 7,52 (d, J=1,47 Гц, 1H) 7,65 (d, J=8,80 Гц, 1H) 7,78 (s, 1H) 8,10 (d, J=2,93 Гц, 1H) 10,82 (brs, 1H) 12,20 (brs, 1H).
N-(4-Цианофенил)-6-циклопропил-1Н-индол-3-сульфонамид I-133
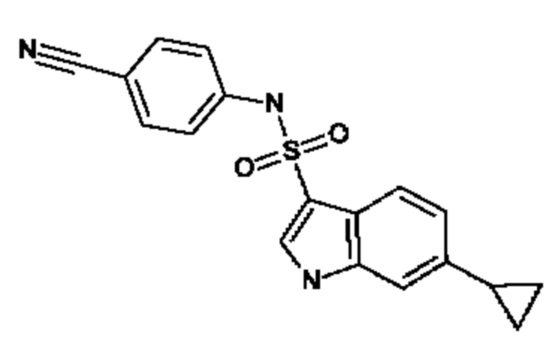
ЖХМС в щелочной среде, методика 2 (ЭР-): 336,00 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 0,58-0,69 (m, 2Н) 0,86-0,98 (m, 2Н) 1,91-2,02 (m, 1Н) 6,90 (d, J=8,31 Гц, 1H) 7,12 (s, 1H) 7,19 (d, J=8,31 Гц, 2H) 7,59 (d, J=8,80 Гц, 2H) 7,67 (d, J=8,31 Гц, 1H) 8,03 (brs, 1H) 10,92 (brs, 1H) 11,87 (brs, 1H).
6-Бром-N-(4-цианофенил)-1Н-индол-3-сульфонамид I-134
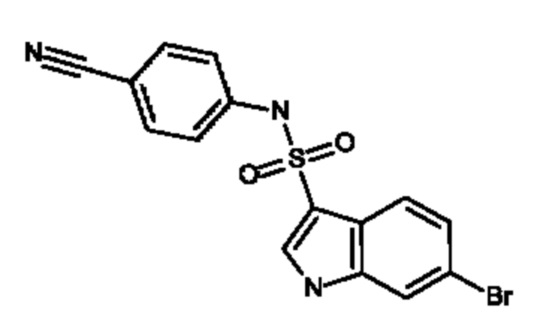
1H ЯМР (400 МГц, DMSO-d6) δ 7,23 (d, J=8,31 Гц, 2H) 7,36 (d, J=8,80 Гц, 1H) 7,59-7,67 (m, 3H) 7,74-7,79 (m, 1H) 8,17 (s, 1H) 10,98 (brs, 1H) 12,19 (brs, 1H).
6-Бром-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1Н-индол-3-сульфонамид I-135
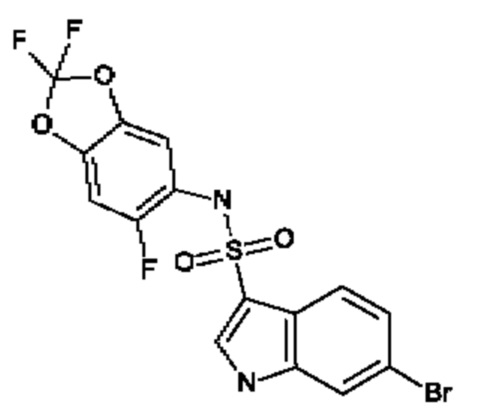
ЖХМС в щелочной среде, методика 2 (ЭР+): 448,80 (М+Н)+, чистота 86%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,34 (d, J=6,40 Гц, 1Н) 7,43 (d, J=8,80 Гц, 1H) 7,71 (d, J=8,80 Гц, 1H) 7,95 (d, J=8,80 Гц, 1H) 8,03 (s, 1H) 8,17 (brs, 1H) 10,20 (brs, 1H) 12,51 (brs, 1H).
6-Бром-N-(2,4,5-трифторфенил)-1Н-индол-3-сульфонамид I-136
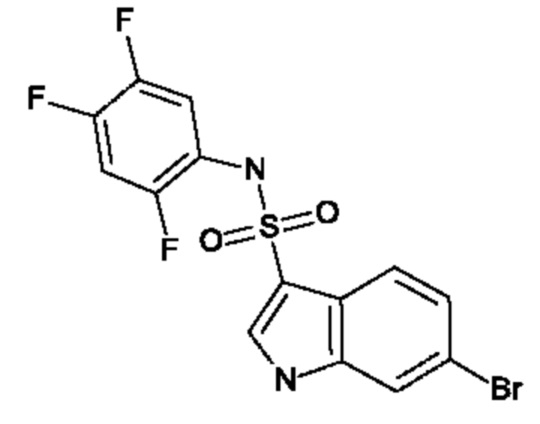
ЖХМС в щелочной среде, методика 2 (ЭР+): 405,00 (М+Н)+, чистота 94%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,31-7,36 (m, 2Н) 7,44-7,51 (m, 1Н) 7,63-7,68 (m, 2H) 7,94 (d, J=2,93 Гц, 1H) 10,21 (s, 1H) 12,11 (brs, 1H).
6-Бром-N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-1Н-индол-3-сульфонамид I-137

ЖХМС в щелочной среде, методика 2 (ЭР+): 431,00 (М+Н)+, чистота 93%.
1Н ЯМР (400 МГц, DMSO-d6) δ 6,94 (dd, J=8,31, 0,98 Гц, 1Н) 7,06 (t, J=8,31 Гц, 1H) 7,11-7,15 (m, 1H) 7,28-7,32 (m, 1H) 7,60 (d, J=8,80 Гц, 1H) 7,66 (d, J=1,47 Гц, 1H) 7,93 (d, J=2,93 Гц, 1H) 10,34 (s, 1H) 12,11 (brs, 1H).
6-Хлор-N-(2-фтор-4-нитрофенил)-1Н-индол-3-сульфонамид I-138
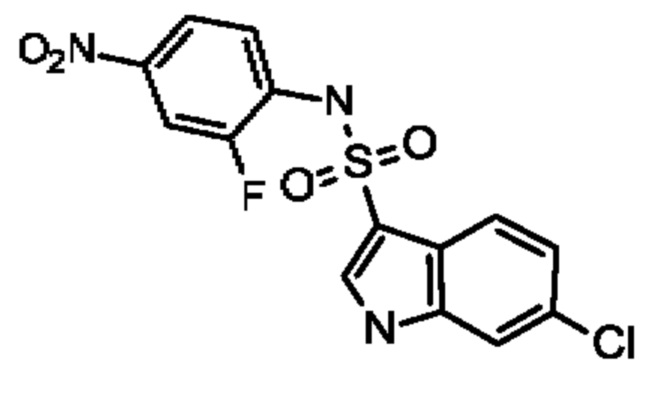
ЖХМС в щелочной среде, методика 2 (ЭР-): 368,00 (М-Н)-, чистота 39%.
6-Хлор-N-(4-цианофенил)-1-бензофуран-3-сульфонамид I-139
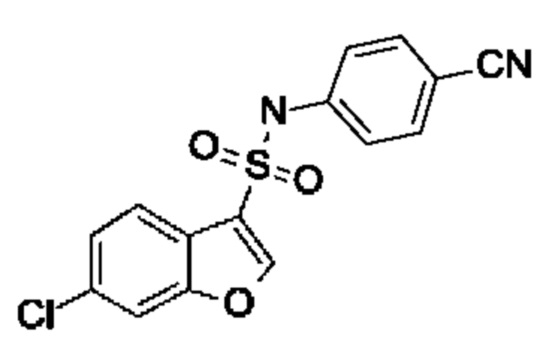
ЖХМС в щелочной среде, методика 2 (ЭР-): 331,00 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,27 (d, J=8,31 Гц, 2Н) 7,48-7,57 (m, 1Н) 7,70 (d, J=8,31 Гц, 2H) 7,84 (s, 1H) 7,96 (s, 1H) 8,93 (s, 1H) 11,44 (brs, 1H).
6-Хлор-N-(2-фтор-4-йодфенил)-1Н-индол-3-сульфонамид I-140
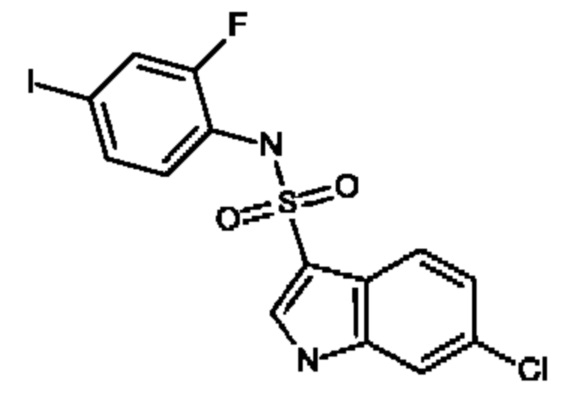
ЖХМС в щелочной среде, методика 1 (ЭР+): 451 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,07 (s, 1Н), 10,11 (s, 1H), 7,91 (d, J=2,4 Гц, 1H), 7,76 (d, J=8,6 Гц, 1H), 7,54-7,47 (s, dd, 2H), 7,44 (dd, J=8,4, 1,8 Гц, 1H), 7,21 (dd, J=8,6, 1,9 Гц, 1H), 7,08 (t, J=8,4 Гц, 1H).
6-Хлор-N-(4-хлор-2-фторфенил)-1Н-индол-3-сульфонамид I-141
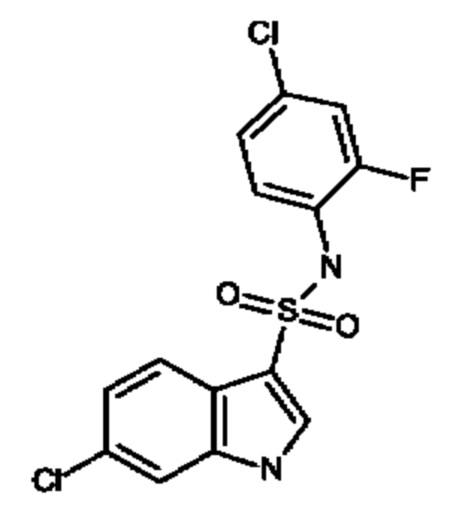
ЖХМС в щелочной среде, методика 1 (ЭР-): 357 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 12,07 (s, 1Н), 10,10 (s, 1H), 7,89 (d, J=2,1 Гц, 1H), 7,73 (d, J=8,6 Гц, 1H), 7,52 (d, J=1,8 Гц, 1H), 7,36-7,25 (m, 2H), 7,24-7,12 (m, 2H).
N-(2,1,3-Бензоселенадиазол-4-ил)-6-хлор-1Н-индол-3-сульфонамид I-142
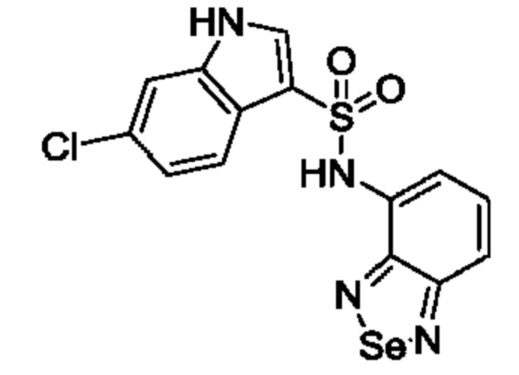
ЖХМС в нейтральной среде, методика 3 (ЭР+): 412,93 (М+Н)+, чистота 98%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,07 (s, 1Н), 10,29 (s, 1H), 8,12 (s, 1H), 7,85 (d, J=8,6 Гц, 1H), 7,46-7,44 (m, 1H), 7,44-7,42 (m, 1H), 7,41 (d, J=9,0 Гц, 1H), 7,27 (dd, J=6,5, 1,7 Гц, 1H), 7,13 (dd, J=8,6, 1,9 Гц, 1H).
6-Хлор-N-(4-циано-2-фтор-5-метоксифенил)-1Н-индол-3-сульфонамид I-143

ЖХМС в нейтральной среде, методика 3 (ЭР+): 379,02 (М+Н)+, чистота 96%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,13 (s, 1Н), 10,83 (s, 1H), 8,15 (d, J=2,3 Гц, 1H), 7,84 (d, J=8,6 Гц, 1H), 7,60-7,46 (m, 2H), 7,23 (dd, J=8,6, 1,9 Гц, 1H), 7,12 (d, J=6,5 Гц, 1H), 3,78 (s, 3H).
6-Хлор-N-(6-фтор-2,1,3-бензотиадиазол-5-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-144
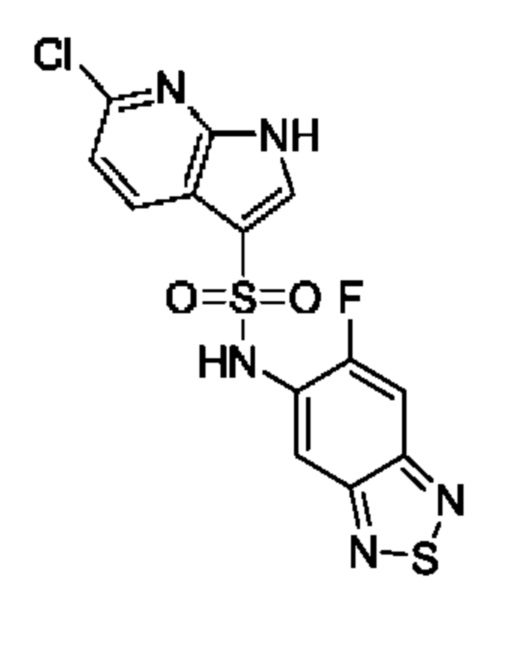
ЖХМС в нейтральной среде, методика 3 (ЭР+): 383,97 (М+Н)+, чистота 99%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,89 (s, 1Н), 10,79 (s, 1H), 8,36 (d, J=2,8 Гц, 1H), 8,29 (d, J=8,3 Гц, 1H), 7,94-7,79 (m, 2H), 7,36 (d, J=8,3 Гц, 1H).
N-(4-Циано-2,5-дифторфенил)-1H-индол-3-сульфонамид I-145
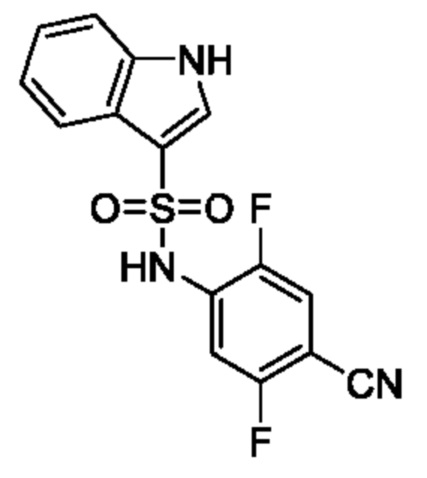
ЖХМС в нейтральной среде, методика 3 (ЭР+): 334,03 (М+Н)+, чистота 99%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,17 (s, 1Н), 11,16 (s, 1H), 8,27 (d, J=3,1 Гц, 1H), 7,90-7,86 (m, 1H), 7,83 (dd, J=10,3, 6,0 Гц, 1H), 7,51-7,42 (m, 2H), 7,23-7,24(m, 2H).
N-(4-Циано-2,5-дифторфенил)-6-(2-метоксиэтокси)-1Н-индол-3-сульфонамид I-146
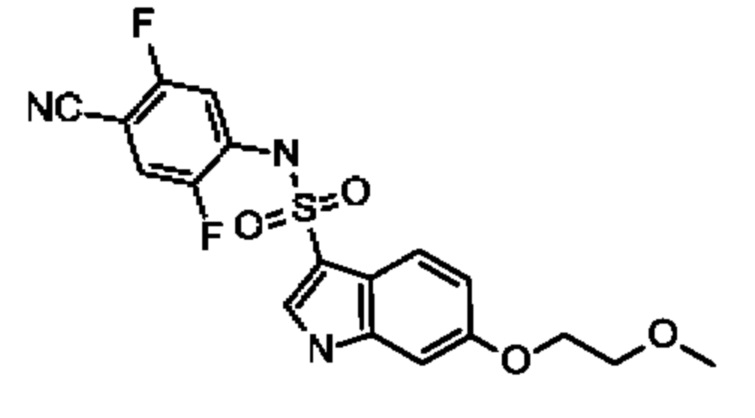
ЖХМС в нейтральной среде, методика 3 (ЭР+): 408,07 (М+Н)+, чистота 99%.
1Н ЯМР (600 МГц, DMSO-d6) δ 11,95 (s, 1Н), 11,13 (s, 1H), 8,12 (d, J=3,0 Гц, 1H), 7,84 (dd, J=10,2, 5,9 Гц, 1H), 7,73 (d, J=8,8 Гц, 1H), 7,43 (dd, J=11,0, 6,3 Гц, 1H), 6,96 (d, J=2,2 Гц, 1H), 6,87 (dd, J=8,8, 2,3 Гц, 1H), 4,19-3,99 (m, 2H, CH2), 3,66 (dd, J=5,6, 3,6 Гц, CH2), 3,30 (s, 3H, CH3).
N-(2,1,3-Бензотиадиазол-5-ил)-6-хлор-1Н-индол-3-сульфонамид I-147
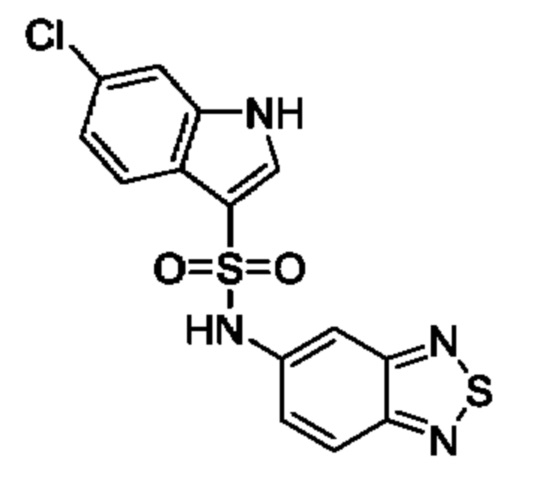
ЖХМС в нейтральной среде, методика 3 (ЭР+): 364,98 (М+Н)+, чистота 99%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,14 (s, 1Н), 10,95-10,90 (m, 1H), 8,25 (s, 1H), 7,92 (dd, J=9,5, 0,7 Гц, 1H), 7,87 (d, J=8,6 Гц, 1H), 7,60 (dd, J=2,1, 0,7 Гц, 1H), 7,52-7,46 (m, 2H), 7,24 (dd, J=8,6, 1,9 Гц, 1H).
N-(4-Циано-2,5-дифторфенил)-1,6,7,8-тетрагидроциклопента[g]индол-3-сульфонамид I-148
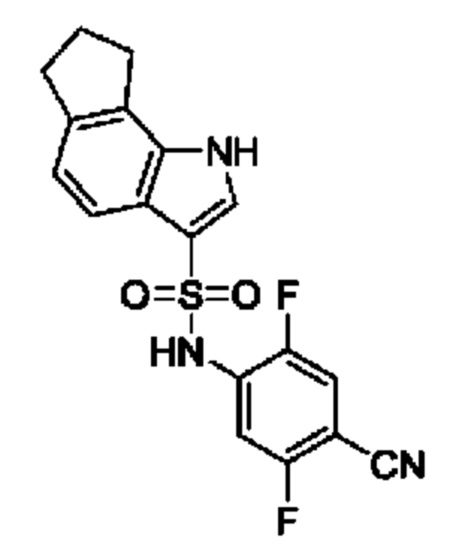
ЖХМС в нейтральной среде, методика 3 (ЭР+): 374,06 (М+Н)+, чистота 98%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,02 (s, 1H), 11,14 (s, 1H), 8,21 (d, J=3,0 Гц, 1H), 7,82 (dd, J=10,3, 5,9 Гц, 1H), 7,66 (d, J=8,1 Гц, 1H), 7,44 (dd, J=11,1, 6,3 Гц, 1H), 7,11 (d, J=8,1 Гц, 1H), 3,01 (t, J=7,4 Гц, 2Н), 2,94 (t, J=7,4 Гц, 2Н), 2,10 (р, J=7,4 Гц, 2Н).
N-(4-Циано-3-фторфенил)-1,6,7,8-тетрагидроциклопента[g]индол-3-сульфонамид I-149
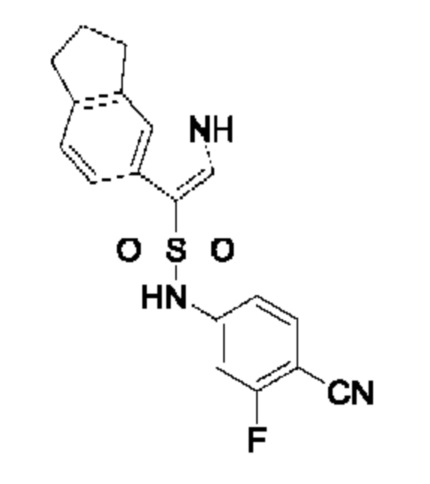
ЖХМС в нейтральной среде, методика 3 (ЭР+): 356,07 (М+Н)+, чистота 95%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,12 (s, 1Н), 11,19 (s, 1H), 8,18 (d, J=3,1 Гц, 1H), 7,68 (dd, J=8,6, 7,6 Гц, 1H), 7,61 (dd, J=8,1, 0,9 Гц, 1H), 7,13-7,07 (m, 2H), 7,04 (dd, J=8,6, 2,1 Гц, 1H), 3,01 (t, J=7,4 Гц, 2H), 2,93 (t, J=7,4 Гц, 2H), 2,09 (p, J=7,4 Гц, 2H).
N-(4-Циано-2-фторфенил)-1,6,7,8-тетрагидроциклопента[g]индол-3-сульфонамид I-150
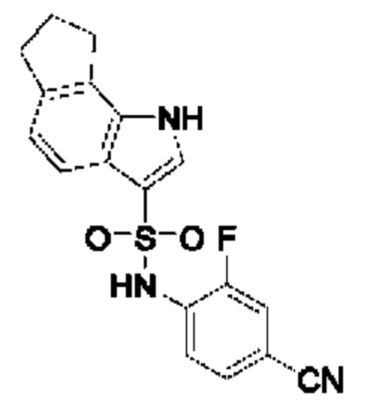
ЖХМС в нейтральной среде, методика 3 (ЭР+): 356,07 (М+Н)+, чистота 98%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,05 (s, 1Н), 10,72 (s, 1H), 8,01 (d, J=3,1 Гц, 1H), 7,71 (dd, J=10,7, 1,8 Гц, 1H), 7,62 (dd, J=8,1, 0,8 Гц, 1H), 7,58 (dd, J=8,6, 7,8 Гц, 1H), 7,55-7,52 (m, 1H), 7,08 (d, J=8,2 Гц, 1H), 3,01 (t, J=7,4 Гц, 2H), 2,94 (t, J=7,4 Гц, 2H), 2,10 (p, J=7,4 Гц, 2H).
N-(4-Циано-2,5-дифторфенил)-1Н-бензо[g]индол-3-сульфонамид I-151
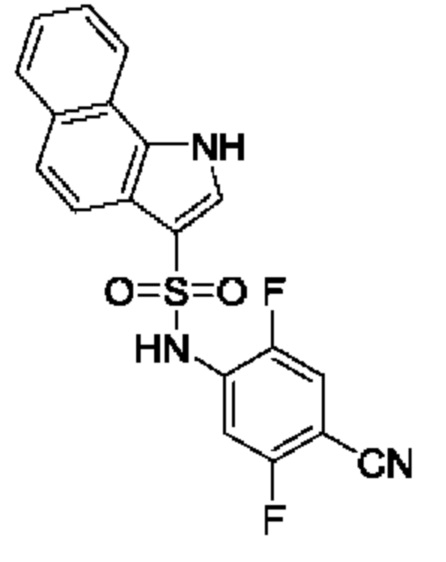
ЖХМС в нейтральной среде, методика 3 (ЭР+): 384,05 (М+Н)+, чистота 96%.
1H ЯМР (500 МГц, DMSO-d6) δ 13,06 (s, 1Н), 11,22 (s, 1H), 8,41 (dd, J=8,3, 1,2 Гц, 1H), 8,36 (d, J=3,1 Гц, 1H), 8,02-7,95 (m, 2H), 7,82 (dd, J=10,3, 5,9 Гц, 1H), 7,69 (d, J=8,7 Гц, 1H), 7,60-7,62 (m, 1H), 7,55-7,47 (m, 2H).
N-(4-Циано-2-фторфенил)-1Н-бензо[g]индол-3-сульфонамид I-152
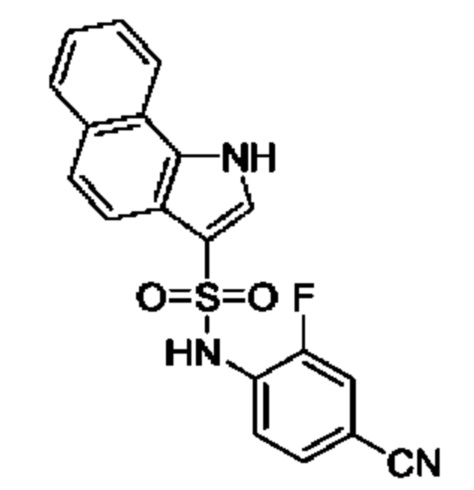
ЖХМС в нейтральной среде, методика 3 (ЭР+): 366,06 (М+Н)+, чистота 99%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,97 (s, 1Н), 10,80 (s, 1H), 8,37-8,39 (m, 1H), 8,16 (d, J=3,1 Гц, 1H), 8,00-7,96 (m, 1H), 7,93 (d, J=8,7 Гц, 1H), 7,70 (dd, J=10,7, 1,8 Гц, 1H), 7,67-7,58 (m, 3H), 7,57-7,46 (m, 2H).
6-(Бензилокси)-N-(4-циано-2,5-дифторфенил)-1H-индол-3-сульфонамид I-153
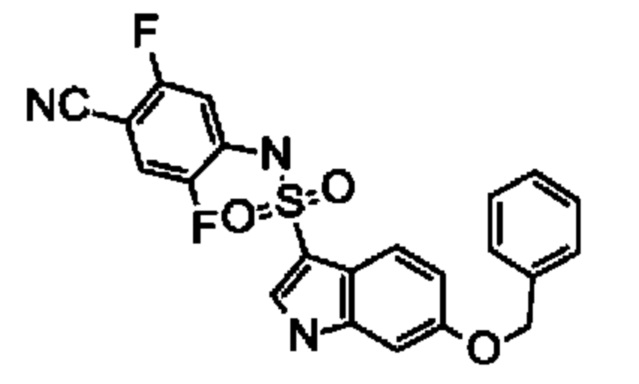
ЖХМС в нейтральной среде, методика 3 (ЭР+): 440,08 (М+Н)+, чистота 98%.
1Н ЯМР (600 МГц, DMSO-d6) δ 11,95 (s, 1Н), 11,13 (s, 1H), 8,12 (d, J=3,0 Гц, 1H), 7,84 (dd, J=10,2, 5,9 Гц, 1H), 7,75 (d, J=8,8 Гц, 1H), 7,47-7,41 (m, 3H), 7,39 (t, J=7,6 Гц, 2H), 7,34-7,30 (m, 1H), 7,02 (d, J=2,2 Гц, 1H), 6,95 (dd, J=8,8, 2,3 Гц, 1H), 5,12 (s, 2H).
6-(Бензилокси)-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамид I-154
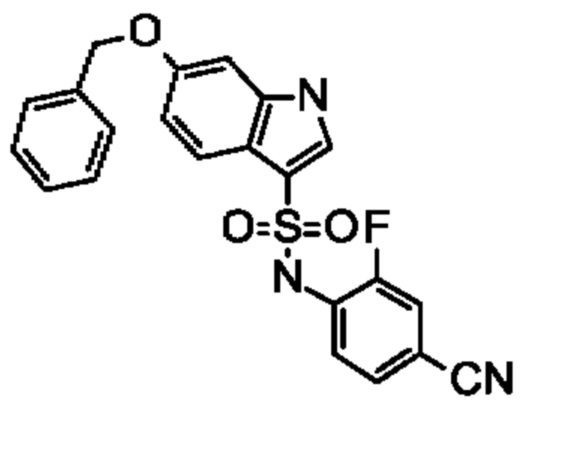
ЖХМС в нейтральной среде, методика 3 (ЭР+): 422,08 (М+Н)+, чистота 97%.
1H ЯМР (500 МГц, DMSO-d6) δ 11,86 (s, 1H), 10,70 (s, 1H), 7,94 (d, J=2,9 Гц, 1H), 7,74-7,69 (m, 2H), 7,60-7,52 (m, 2H), 7,47-7,43 (m, 2H), 7,41-7,37 (m, 2H), 7,35-7,29 (m, 1H), 7,02 (d, J=2,2 Гц, 1H), 6,93 (dd, J=8,8, 2,3 Гц, 1H), 5,12 (s, 2H).
N-(2,1,3-Бензотиадиазол-4-ил)-1H-бензо[g]индол-3-сульфонамид I-155
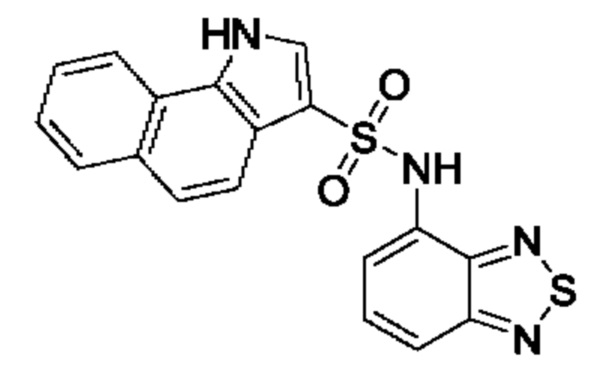
ЖХМС в нейтральной среде, методика 3 (ЭР+): 381,04 (М+Н)+, чистота 95,2%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,88 (s, 1Н), 10,80 (s, 1H), 8,36 (dq, J=8,3, 0,9 Гц, 1H), 8,18 (d, J=3,0 Гц, 1H), 7,98 (d, J=8,8 Гц, 1H), 7,93 (dt, J=8,4, 0,8 Гц, 1H), 7,66 (dd, J=8,7, 1,1 Гц, 1H), 7,55 (m, 3Н), 7,54 (dd, J=7,4, 1,1 Гц, 1H), 7,46-7,48 (m, 1H).
N-(2,1,3-Бензотиадиазол-4-ил)-6-(бензилокси)-1H-индол-3-сульфонамид I-156
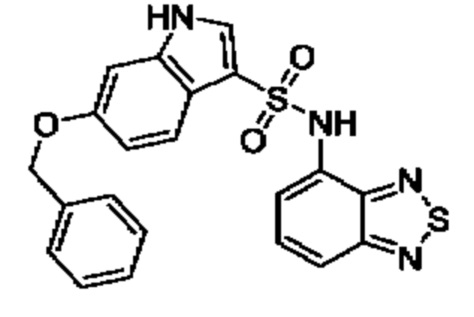
ЖХМС в нейтральной среде, методика 3 (ЭР+): 437,07 (М+Н)+, чистота 99%.
1H ЯМР (600 МГц, DMSO-d6) δ 11,78 (s, 1Н), 10,70 (s, 1H), 7,97 (d, J=2,9 Гц, 1H), 7,77 (d, J=8,8 Гц, 1H), 7,66 (dd, J=8,7, 0,9 Гц, 1H), 7,57 (dd, J=8,8, 7,4 Гц, 1H), 7,47 (dd, J=7,5, 1,0 Гц, 1H), 7,44, 7,40 (m, 2H), 7,37 (t, J=7,6 Гц, 2H), 7,33-7,28 (m, 1H), 6,96 (d, J=2,2 Гц, 1H), 6,85 (dd, J=8,8, 2,3 Гц, 1H), 5,08 (s, 2H).
N-(2,1,3-Бензотиадиазол-5-ил)-1Н-бензо[g]индол-3-сульфонамид I-157
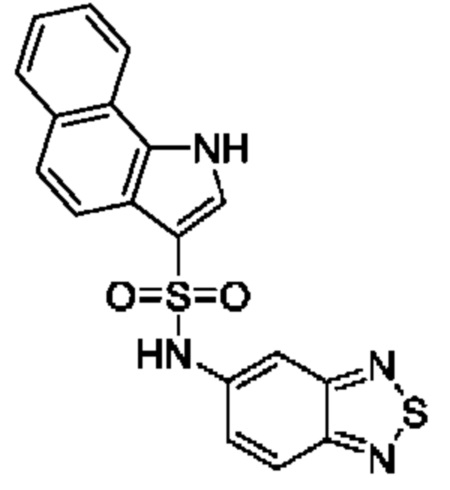
ЖХМС в нейтральной среде, методика 3 (ЭР+): 381,04 (М+Н)+, чистота 97%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,95 (s, 1Н), 10,96 (s, 1H), 8,36 (dd, J=8,3, 1,2 Гц, 1H), 8,31 (d, J=2,8 Гц, 1H), 7,99 (d, J=8,8 Гц, 1H), 7,97-7,94 (m, 1H), 7,90 (dd, J=9,4, 0,7 Гц, 1H), 7,69-7,64 (m, 2H), 7,56-7,58 (m, 1H), 7,53 (dd, J=9,4, 2,2 Гц, 1H), 7,46-7,48 (m, 1H).
N-(2,1,3-Бензотиадиазол-5-ил)-1,6,7,8-тетрагидроциклопента[g]индол-3-сульфонамид I-158
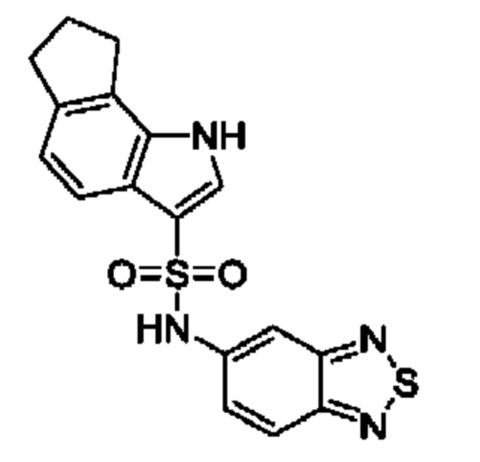
ЖХМС в нейтральной среде, методика 3 (ЭР+): 371,05 (М+Н)+, чистота 100%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,02 (s, 1Н), 10,85 (s, 1H), 8,14 (d, J=3,0 Гц, 1H), 7,89 (dd, J=9,4, 0,7 Гц, 1H), 7,69-7,65 (m, 1H), 7,59 (dd, J=2,2, 0,7 Гц, 1H), 7,50 (dd, J=9,4, 2,2 Гц, 1H), 7,09 (d, J=8,1 Гц, 1H), 2,97 (t, J=7,4 Гц, 2H), 2,90 (t, J=7,4 Гц, 2H), 2,11-2,00 (m, 2H).
N-(4-Цианофенил)-1Н-бензо[g]индол-3-сульфонамид I-159
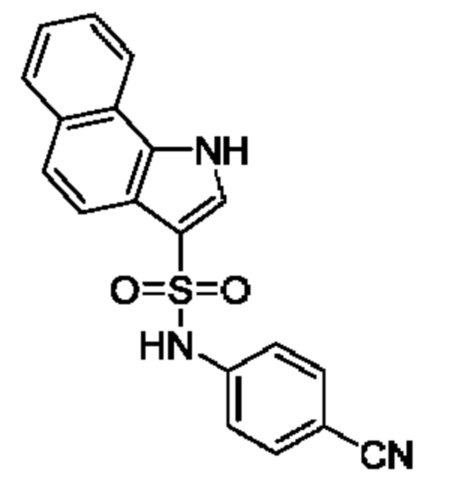
ЖХМС в нейтральной среде, методика 3 (ЭР+): 348,07 (М+Н)+, чистота 98%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,96 (s, 1Н), 10,97 (s, 1H), 8,39 (dd, J=8,3, 1,2 Гц, 1H), 8,22 (d, J=2,9 Гц, 1H), 7,95 (dd, J=19,9, 8,5 Гц, 2H), 7,67 (d, J=8,8 Гц, 1H), 7,64-7,57 (m, 3Н), 7,50-7,52 (m, 1H), 7,32-7,25 (m, 2H).
N-(6-Фтор-2,1,3-бензотиадиазол-5-ил)-1Н-бензо[g]индол-3-сульфонамид I-160
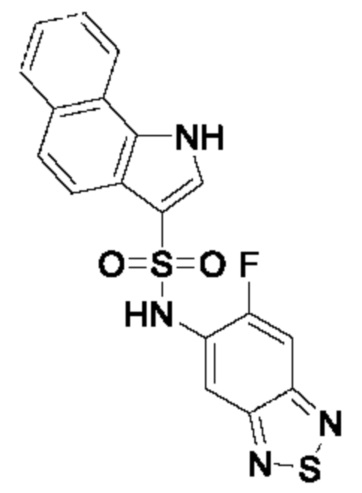
ЖХМС в нейтральной среде, методика 3 (ЭР+): 399,03 (М+Н)+, чистота 97%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,97 (s, 1Н), 10,79 (s, 1H), 8,37-8,39 (m, 1H), 8,27 (d, J=3,1 Гц, 1H), 8,00 (d, J=8,8 Гц, 1H), 7,98-7,94 (m, 1H), 7,90 (d, J=7,8 Гц, 1H), 7,86 (d, J=10,8 Гц, 1H), 7,68-7,64 (m, 1H), 7,57-7,59 (m, 1H), 7,48 7,51 (m, 1H).
N-(2,1,3-Бензоселенадиазол-5-ил)-6-хлор-1Н-индол-3-сульфонамид I-161
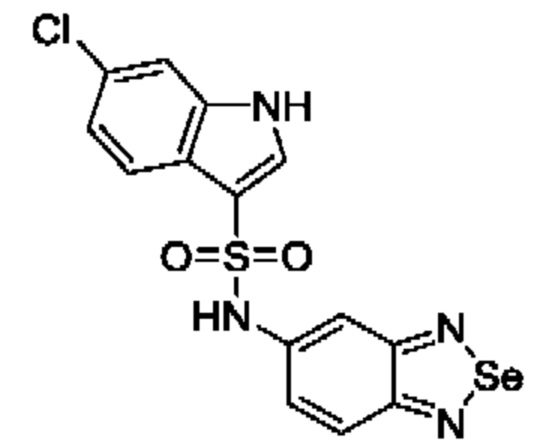
ЖХМС в нейтральной среде, методика 3 (ЭР+): 412,93 (М+Н)+, чистота 98%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,14 (s, 1Н), 10,81 (s, 1H), 8,22 (s, 1H), 7,88 (d, J=8,6 Гц, 1H), 7,67 (d, J=10,3 Гц, 1H), 7,50 (d, J=2,0 Гц, 1H), 7,39-7,33 (m, 2H), 7,25 (dd, J=8,6, 1,9 Гц, 1H).
6-Хлор-N-(6-фтор-2,1,3-бензотиадиазол-5-ил)-1Н-индол-3-сульфонамид I-162
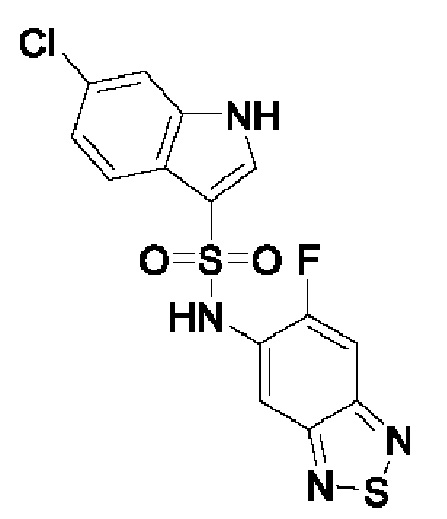
ЖХМС в нейтральной среде, методика 3 (ЭР+): 383,09 (М+Н)+, чистота 97%.
1H ЯМР (500 МГц, DMSO-d6) δ12,16 (s, 1H), 10,76 (s, 1H), 8,22 (s, 1H), 7,80-7,92 (m, 3Н), 7,51 (s, 1Н), 7,18-7,28 (m, 1H).
6-Хлор-N-(7-циано-2,1,3-бензотиадиазол-4-ил)-1Н-индол-3-сульфонамид I-163
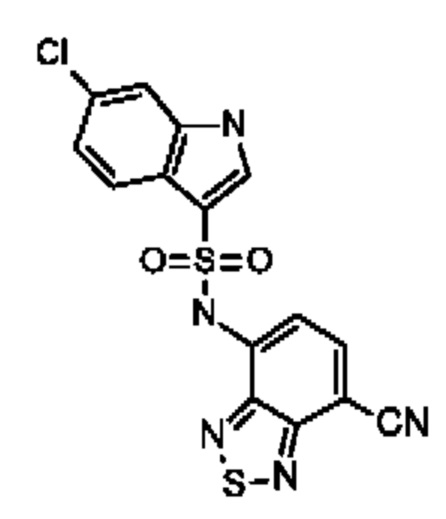
ЖХМС в нейтральной среде, методика 3 (ЭР+): 390,3 (М+Н)+, чистота 95%.
1Н ЯМР (500 МГц, DMSO-d6) δ11,52 (s, 1H), 7,74-7,85 (m, 1Н), 7,68 (d, J=8,5 Гц, 1H), 7,24-7,45 (m, 2H), 7,04 7,11 (m, 1H), 6,94 (d, J=8,4 Гц, 1H).
N-(4-Циано-2,5-дифторфенил)-4,6-дифтор-1Н-индол-3-сульфонамид I-164
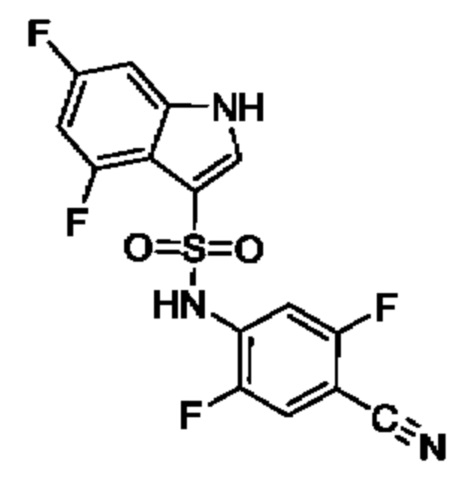
ЖХМС в нейтральной среде, методика 3 (ЭР+): 369,2 (М+Н)+, чистота 95%.
1Н ЯМР (600 МГц, DMSO-d6) δ 12,47 (s, 1Н), 11,04 (s, 1H), 8,25 (d, J=3,0 Гц, 1H), 7,85 (dd, J=10,1, 5,8 Гц, 1H), 7,43 (dd, J=10,9, 6,2 Гц, 1H), 7,16 (dd, J=8,7, 2,1 Гц, 1H), 7,05 (td, J=10,5, 2,2 Гц, 1H).
N-(4-Циано-2,5-дифторфенил)-6-фтор-1Н-индол-3-сульфонамид I-165
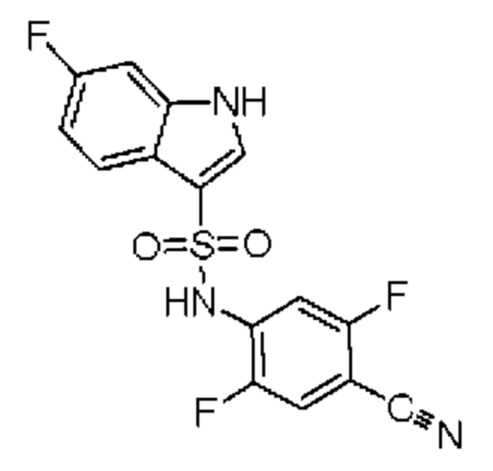
ЖХМС в нейтральной среде, методика 3 (ЭР+): 351,3 (М+Н)+, чистота 98%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,28-12,11 (m, 1Н), 11,18 (s, 1H), 8,26 (d, J=3,0 Гц, 1H), 7,84 (ddd, J=14,4, 9,5, 5,6 Гц, 2H), 7,43 (dd, J=11,0, 6,4 Гц, 1H), 7,27 (dd, J=9,5, 2,4 Гц, 1H), 7,10 (td, J=9,3, 2,4 Гц, 1H).
N-(2,1,3-Бензотиадиазол-4-ил)-4,6-дифтор-1Н-индол-3-сульфонамид I-166
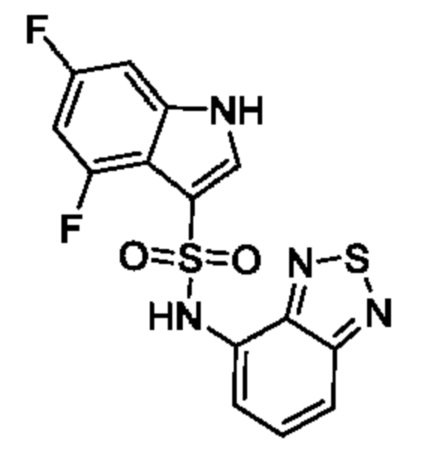
ЖХМС в нейтральной среде, методика 3 (ЭР+): 366,3 (М+Н)+, чистота 99%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,26 (s, 1Н), 10,16 (s, 1H), 8,07 (s, 1H), 7,70 (dd, J=8,9, 0,9 Гц, 1H), 7,58 (dd, J=8,8, 7,4 Гц, 1H), 7,47 (dd, J=7,4, 0,9 Гц, 1H), 7,08 (dd, J=9,0, 2,1 Гц, 1H), 6,96 (td, J=10,4, 2,2 Гц, 1H).
7-Бром-N-(4-циано-2,5-дифторфенил)-1Н-индол-3-сульфонамид I-167
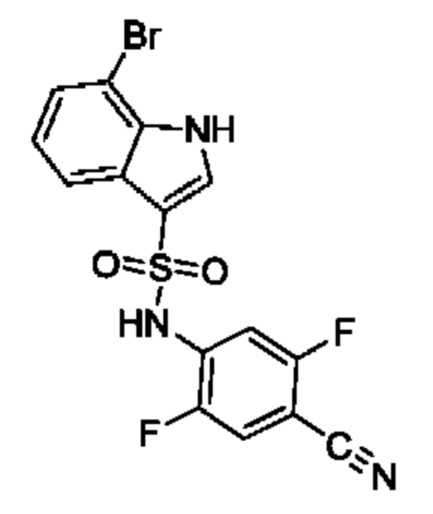
ЖХМС в нейтральной среде, методика 3 (ЭР+): 412,2 (М+Н)+, чистота 99%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,75-12,27 (m, 1Н), 11,22 (s, 1H), 8,30 (d, J=3,1 Гц, 1H), 8,01-7,72 (m, 2H), 7,55-7,38 (m, 2H), 7,17 (t, J=7,8 Гц, 1H).
N-(4-Циано-2-фторфенил)-4,6-дифтор-1Н-индол-3-сульфонамид I-168
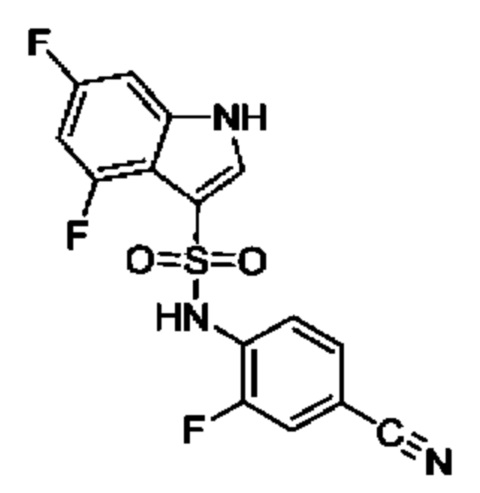
ЖХМС в нейтральной среде, методика 3 (ЭР+): 351,3 (М+Н)+, чистота 98%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,36 (s, 1Н), 10,56 (s, 1H), 8,08 (d, J=2,5 Гц, 1H), 7,80-7,68 (m, 1H), 7,59-7,49 (m, 2H), 7,15 (dd, J=9,0, 2,1 Гц, 1H), 7,03 (m, J=10,8, 10,1, 2,1 Гц, 1H).
N-(2,1,3-Бензотиадиазол-5-ил)-6-фтор-1Н-индол-3-сульфонамид I-169
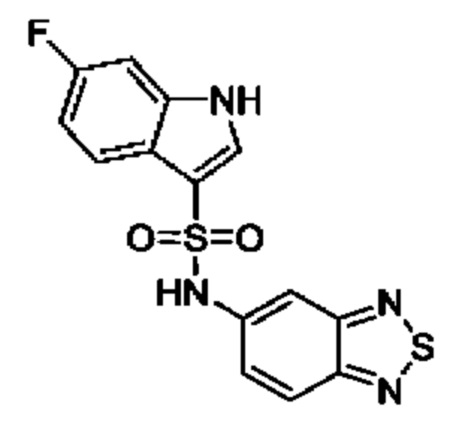
ЖХМС в нейтральной среде, методика 3 (ЭР+): 348,3 (М+Н)+, чистота 97%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,08 (s, 1Н), 10,91 (s, 1H), 8,20 (dd, J=7,1, 2,4 Гц, 1H), 7,91 (dd, J=9,4, 0,7 Гц, 1H), 7,86 (dd, J=8,8, 5,3 Гц, 1H), 7,59 (dd, J=2,2, 0,7 Гц, 1H), 7,48 (dd, J=9,4, 2,2 Гц, 1H), 7,22 (m, J=9,6, 2,4, 0,5 Гц, 1H), 7,08 (m, J=9,7, 8,8, 2,4 Гц, 1H).
N-(4-Циано-2-фторфенил)-6-(пропан-2-ил)-1Н-индол-3-сульфонамид I-170
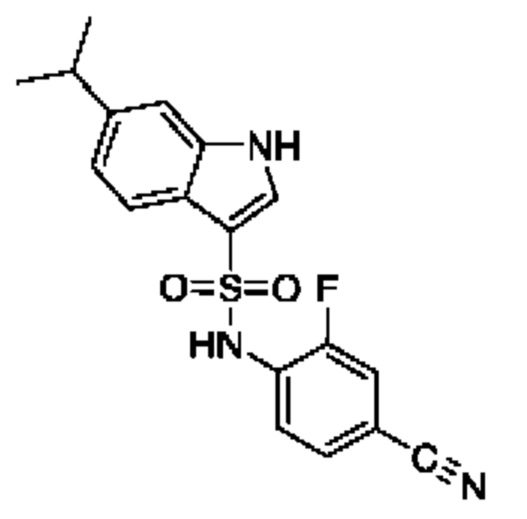
ЖХМС в нейтральной среде, методика 3 (ЭР+): 357,4 (М+Н)+, чистота 95%.
1H ЯМР (500 МГц, DMSO-d6) δ 11,93 (d, J=3,0 Гц, 1H), 10,74 (s, 1Н), 8,02 (d, J=3,0 Гц, 1H), 7,84-7,68 (m, 2H), 7,61-7,44 (m, 2H), 7,27 (t, J=0,9 Гц, 1H), 7,10 (dd, J=8,3, 1,5 Гц, 1H), 2,96 (d, J=6,9 Гц, 1H), 1,21 (d, J=6,9 Гц, 7H).
N-(4-Цианофенил)-6-фтор-1Н-индол-3-сульфонамид I-171
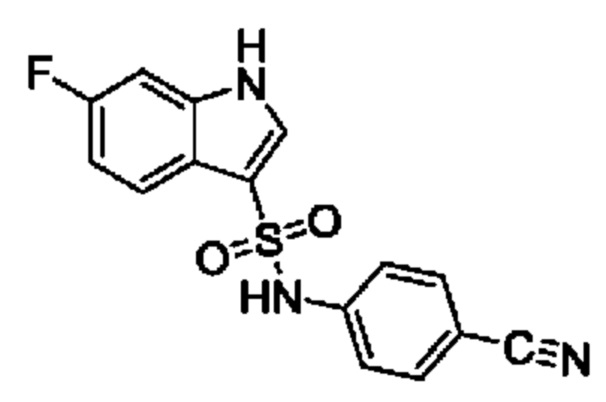
ЖХМС в нейтральной среде, методика 3 (ЭР+): 315,32 (М+Н)+, чистота 97%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,12 (s, 1Н), 10,95 (s, 1H), 8,39-8,06 (m, 1H), 7,80 (dd, J=8,8, 5,2 Гц, 1H), 7,68-7,56 (m, 2H), 7,34-7,14 (m, 3H), 7,08 (m J=9,6, 8,8, 2,4 Гц, 1H).
6-Фтор-N-(6-фтор-2,1,3-бензотиадиазол-5-ил)-1Н-индол-3-сульфонамид I-172
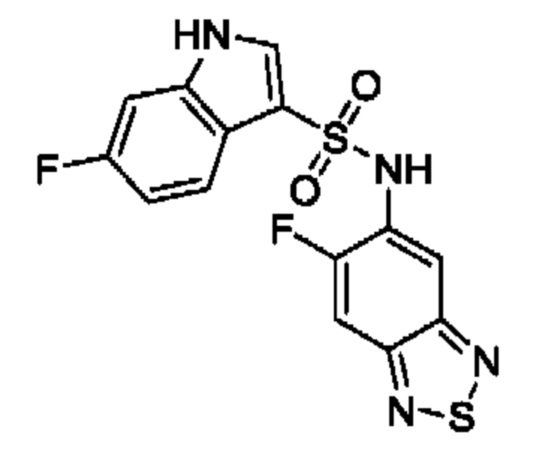
ЖХМС в нейтральной среде, методика 3 (ЭР+): 366,3 (М+Н)+, чистота 99%.
1Н ЯМР (600 МГц, DMSO-d6) δ 12,11 (d, J=3,2 Гц, 1H), 10,76 (s, 1H), 8,19 (d, J=3,0 Гц, 1Н), 8,04-7,69 (m, 3Н), 7,24 (dd, J=9,5, 2,4 Гц, 1H), 7,08 (m, J=9,7, 8,8, 2,4 Гц, 1H).
N-(4-Бром-2-фторфенил)-6-метил-1H-индол-3-сульфонамид I-173
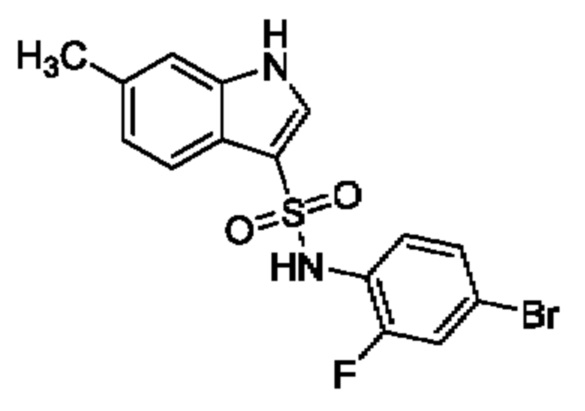
ЖХМС в нейтральной среде, методика 3 (ЭР+): 383,2 (М+Н)+, чистота 95%.
1Н ЯМР (600 МГц, DMSO-d6) δ 11,81 (d, J=3,1 Гц, 1H), 10,01 (s, 1H), 7,77 (d, J=3,0 Гц, 1Н), 7,63 (d, J=8,2 Гц, 1H), 7,40 (dd, J=9,9, 2,1 Гц, 1H), 7,32-7,14 (m, 3H), 6,98 (dd, J=8,3, 1,5 Гц, 1H), 2,38 (s, 3H).
N-(4-Хлор-2-фторфенил)-6-метил-1Н-индол-3-сульфонамид I-174
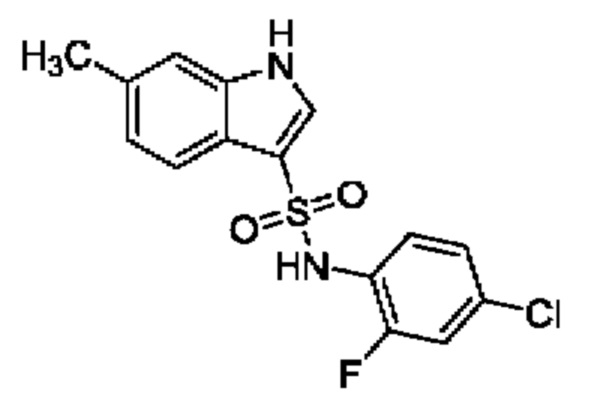
ЖХМС в нейтральной среде, методика 3 (ЭР+): 338,7 (М+Н)+, чистота 95%.
1H ЯМР (600 МГц, DMSO-d6) δ 11,81 (d, J=3,0 Гц, 1H), 9,99 (s, 1H), 7,77 (d, J=2,9 Гц, 1H), 7,62 (d, J=8,1 Гц, 1Н), 7,34-7,22 (m, 3Н), 7,14 (m, J=8,7, 2,4, 1,1 Гц, 1H), 6,98 (dd, J=8,1, 1,4 Гц, 1H), 2,38 (s, 3H).
N-(4-Хлор-5-фтор-2-метоксифенил)-1H-бензо[g]индол-3-сульфонамид I-175
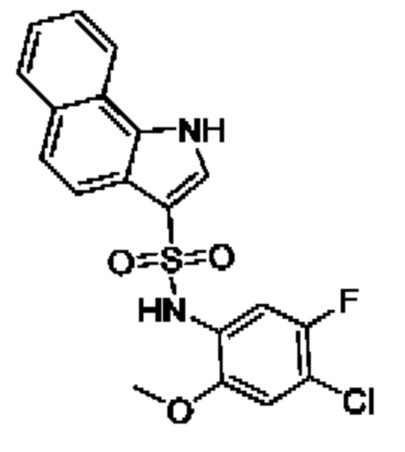
ЖХМС в нейтральной среде, методика 3 (ЭР+): 404,8 (М+Н)+, чистота 95%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,85 (d, J=3,3 Гц, 1H), 9,63 (s, 1Н), 8,38 (d, J=8,2 Гц, 1H), 8,03 (d, J=2,8 Гц, 1H), 7,95 (dd, J=30,6, 8,4 Гц, 2H), 7,70-7,57 (m, 2H), 7,49 (m, J=8,1, 6,8, 1,2 Гц, 1H), 7,31 (d, J=10,6 Гц, 1H), 7,01 (d, J=6,9 Гц, 1H), 3,37 (s, 3Н).
6-Хлор-N-(4-циано-2,5-дифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-176
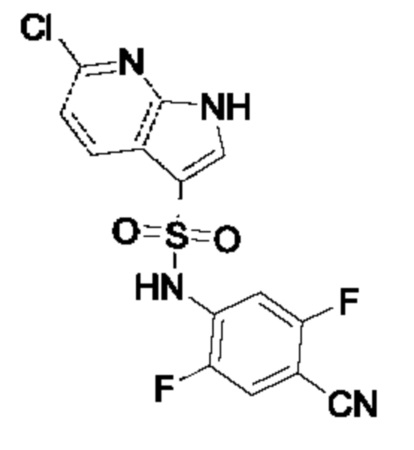
ЖХМС в нейтральной среде, методика 3 (ЭР+): 369,2 (М+Н)+, чистота 98%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,97 (br, 1H, NH), 11,20 (br, 1H, NH), 8,46 (d, J=3,0 Гц, 1Н), 8,28 (d, J=8,3 Гц, 1H), 7,86 (dd, J=10,3, 6,0 Гц, 1H), 7,47 (dd, J=10,8, 6,4 Гц, 1H), 7,40 (d, J=8,2 Гц, 1H).
6-Бром-N-(4-циано-2-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-177

ЖХМС в нейтральной среде, методика 3 (ЭР+): 395,2 (М+Н)+, чистота 99%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,91 (br, 1H, NH), 10,81 (br, 1Н, NH), 8,24 (s, 1H), 8,13 (d, J=8,3 Гц, 1H), 7,70-7,76 (m, 1H), 7,52-7,58 (m, 2H), 7,48 (d, J=8,3 Гц, 1H).
6-Хлор-N-(4-цианофенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-178
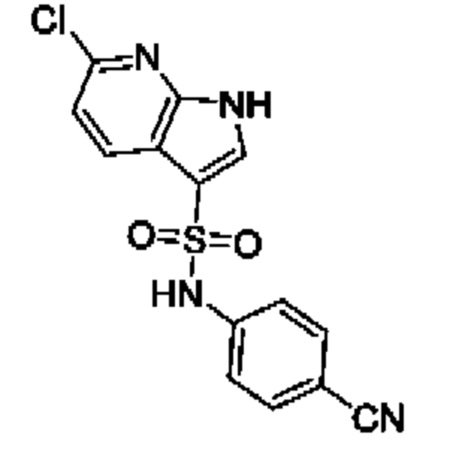
ЖХМС в нейтральной среде, методика 3 (ЭР+): 333,1 (М+Н)+, чистота 97%.
1H ЯМР (500 МГц, DMSO-d6) δ 12,90 (br, 1Н, NH), 11,00 (br, 1H, NH), 8,33 (s, 1H), 8,20 (d, J=8,3 Гц, 1H), 7,64 (d, J=8,8 Гц, 2H), 7,37 (d, J=8,4 Гц, 1H), 7,23 (d, J=8,9 Гц, 2H).
N-(2,1,3-Бензотиадиазол-5-ил)-6-хлор-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-179
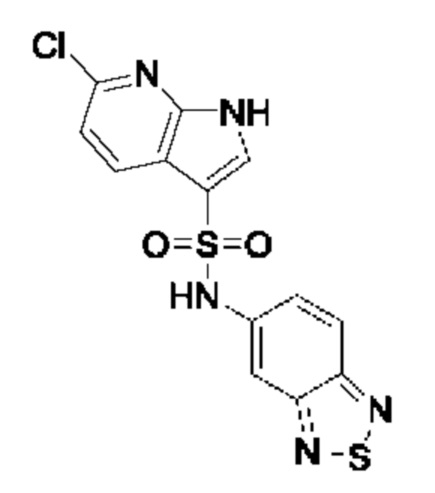
ЖХМС в нейтральной среде, методика 3 (ЭР+): 366,0 (М+Н)+, чистота 96%.
1H ЯМР (500 МГц, DMSO-d6) δ12,87 (br, 1H, NH), 10,97 (br, 1H, NH), 8,41 (s, 1Н), 8,26 (d, J=8,4 Гц, 1H), 7,92 (dd, J=9,4, 0,7 Гц, 1H), 7,61 (dd, J=2,2, 0,6 Гц, 1H), 7,47 (dd, J=9,4, 2,2 Гц, 1H), 7,37 (d, J=8,3 Гц, 1H).
6-Хлор-N-[4-(цианометил)фенил]-1Н-индол-3-сульфонамид I-180
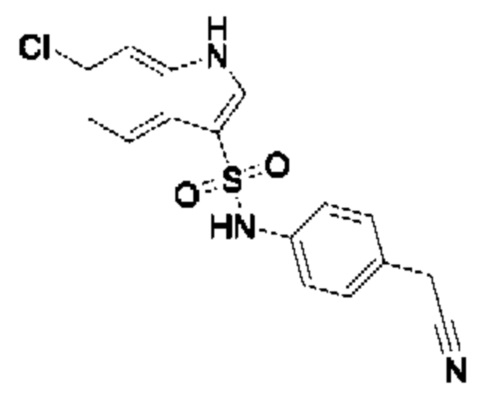
ЖХМС в нейтральной среде, методика 3 (ЭР+): 346,2 (М+Н)+, чистота 98%.
1H ЯМР (500 МГц, DMSO-d6) δ: 12,03 (br, 1H), 10,24 (br, 1Н), 7,79 (dd, J=8,6, 0,5 Гц, 1H), 7,48 (dd, J=1,9, 0,5 Гц, 1H), 7,20 (dd, J=10,5, 8,7 Гц, 2H), 7,15-7,11 (m, 7H), 7,10-7,06 (m, 3H), 3,84 (s, 2H) част./млн.
6-Хлор-N-(3-хлор-4-цианофенил)-1Н-индол-3-сульфонамид I-181
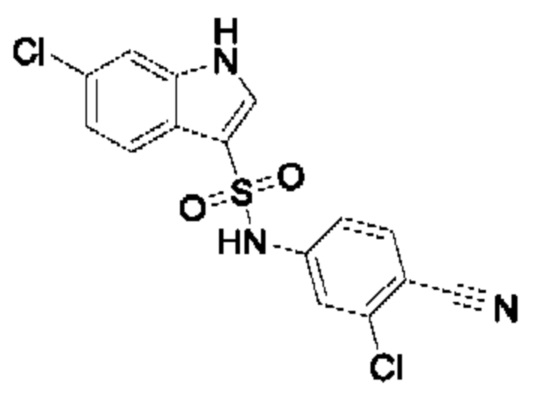
ЖХМС в нейтральной среде, методика 3 (ЭР+): 383,0 (M+NH4)+, чистота 98%.
6-Хлор-N-(4-циано-2,6-дифторфенил)-1Н-индол-3-сульфонамид I-182
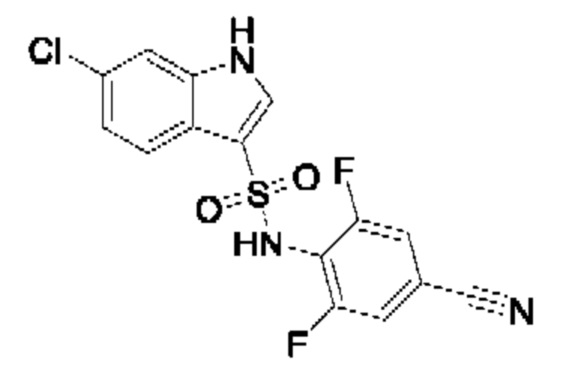
ЖХМС в нейтральной среде, методика 3 (ЭР+): 385,2 (М+Н)+, чистота 92%.
1H ЯМР (500 МГц, DMSO-d6) δ: 12,09 (br, 1H), 10,10 (br, 1H), 7,87 (d, J=3,0 Гц, 1H), 7,78-7,72 (m, 2Н), 7,60 (d, J=8,5 Гц, 1Н), 7,54 (dd, J=1,9, 0,6 Гц, 1H), 7,19 (dd, J=8,6, 1,9 Гц, 1H).
N-(2,1,3-Бензотиадиазол-5-ил)-6-бром-1Н-индол-3-сульфонамид I-183
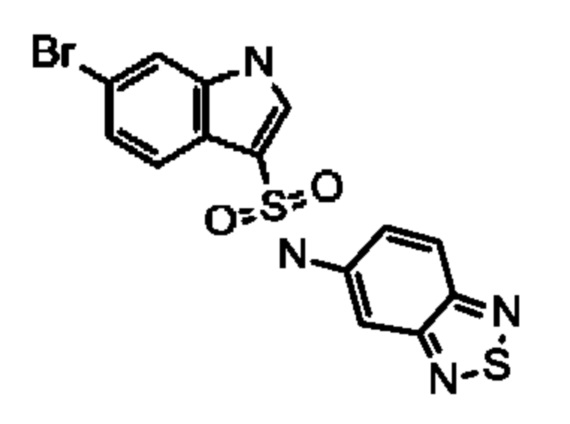
ЖХМС в нейтральной среде, методика 3 (ЭР+): 411,2 (М+Н)+, чистота 97%.
1H ЯМР (600 МГц, DMSO-d6) δ: 12,47 (d, J=3,2 Гц, 1Н), 10,86 (s, 1H), 8,30 (d, J=3,4 Гц, 1H), 8,04 (d, J=8,4 Гц, 1H), 7,82 (s, 1H), 7,75-7,68 (m, 1H), 7,55-7,58 (m, 2H), 7,52 (d, J=8,6 Гц, 1H).
N-(4-Циано-2,5-дифторфенил)-6-(трифторметил)-1Н-индол-3-сульфонамид I-184
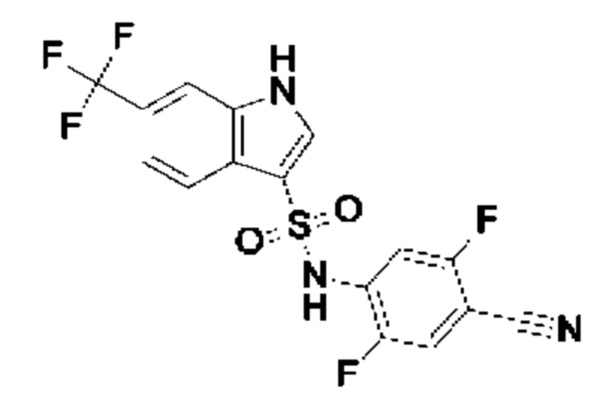
ЖХМС в нейтральной среде, методика 3 (ЭР+): 402,0 (М+Н)+, чистота 99%.
1H ЯМР (600 МГц, DMSO-d6) δ: 12,55 (d, J=3,2 Гц, 1Н), 11,26 (s, 1H), 8,48 (d, J=3,2 Гц, 1H), 8,07 (d, J=8,4 Гц, 1H), 7,88-7,84 (m, 1H), 7,83 (s, 1H), 7,55 (d, J=8,1 Гц, 1H), 7,46 (dd, J=10,9, 6,3 Гц, 1H).
6-Хлор-N-(4-циано-2,5-дифторфенил)-1Н-индол-3-сульфонамид I-185
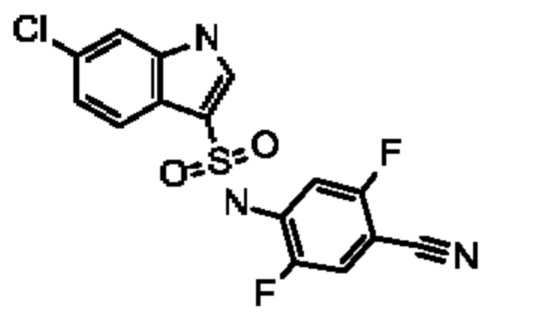
ЖХМС в нейтральной среде, методика 3 (ЭР+): 385,1 (M+NH4)+, чистота 98%.
1H ЯМР (500 МГц, DMSO-d6) δ: 12,26 (d, J=3,0 Гц, 1Н), 11,17 (s, 1H), 8,29 (d, J=3,0 Гц, 1H), 7,86 (d, J=8,6 Гц, 1H), 7,84 (dd, J=11,1, 6,0 Гц, 1H), 7,53 (d, J=2,0 Гц, 1H), 7,44 (dd, J=11,0, 6,4 Гц, 1H), 7,26 (dd, J=8,6, 1,9 Гц, 1H).
N-(2,1,3-Бензотиадиазол-4-ил)-6-(трифторметил)-1Н-индол-3-сульфонамид I-186
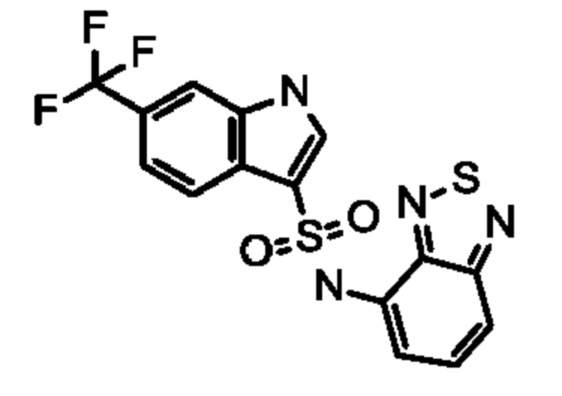
ЖХМС в нейтральной среде, методика 3 (ЭР+): 399,1 (М+Н)+, чистота 92%.
1H ЯМР (500 МГц, DMSO-d6) δ: 12,35 (s, 1H), 10,87 (s, 1H), 8,31 (d, J=2,7 Гц, 1H), 8,06 (d, J=8,5 Гц, 1H), 7,76 (dd, J=1,5, 0,8 Гц, 1Н), 7,69 (dd, J=8,8, 0,9 Гц, 1H), 7,58 (dd, J=8,8, 7,4 Гц, 1H), 7,49 (dd, J=7,4, 0,9 Гц, 1H), 7,43 (dd, J=8,5, 1,6 Гц, 1H).
N-(4-Циано-2,5-дифторфенил)-6-метил-1Н-индол-3-сульфонамид I-187
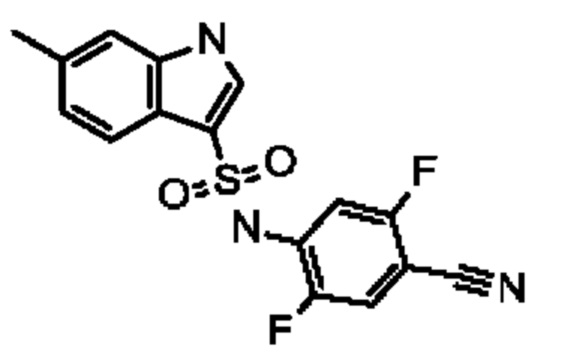
ЖХМС в нейтральной среде, методика 3 (ЭР+): 365,1 (M+NH4)+, чистота 96%.
6-Бром-N-(4-циано-2,5-дифторфенил)-1Н-индол-3-сульфонамид I-188
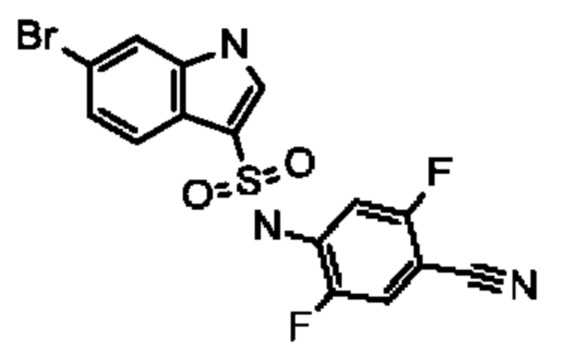
ЖХМС в нейтральной среде, методика 3 (ЭР+): 429,2 (M+NH4)+, чистота 98%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,26 (s, 1H), 11,19 (s, 1H), 8,28 (d, J=3,0 Гц, 1H), 7,84 (dd, J=10,3, 5,9 Гц, 1H), 7,81 (d, J=8,6 Гц, 1Н), 7,67 (s, 1H), 7,43 (dd, J=10,9, 6,3 Гц, 1H), 7,37 (d, J=8,5 Гц, 1H).
N-(4-Циано-2-фторфенил)-6-(трифторметил)-1Н-индол-3-сульфонамид I-189
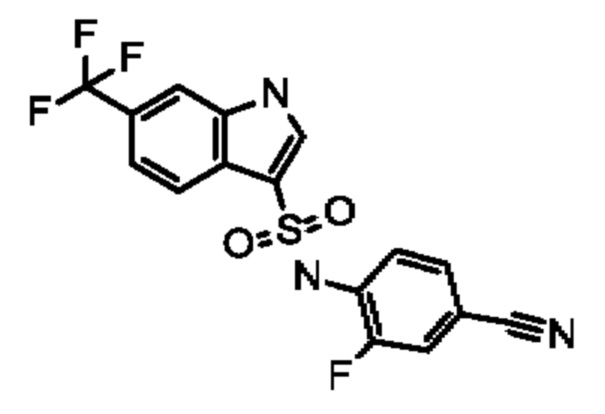
ЖХМС в нейтральной среде, методика 3 (ЭР+): 401,3 (M+NH4)+, чистота 95%.
1H ЯМР (600 МГц, DMSO-d6) δ: 12,46 (d, J=3,4 Гц, 1H), 10,86 (s, 1Н), 8,30 (d, J=3,0 Гц, 1H), 8,03 (d, J=8,5 Гц, 1H), 7,82 (s, 1H), 7,76-7,69 (m, 1H), 7,55-7,58 (m, 2H), 7,52 (dd, J=8,6, 1,6 Гц, 1H).
N-(4-Цианофенил)-6-(трифторметил)-1Н-индол-3-сульфонамид I-190
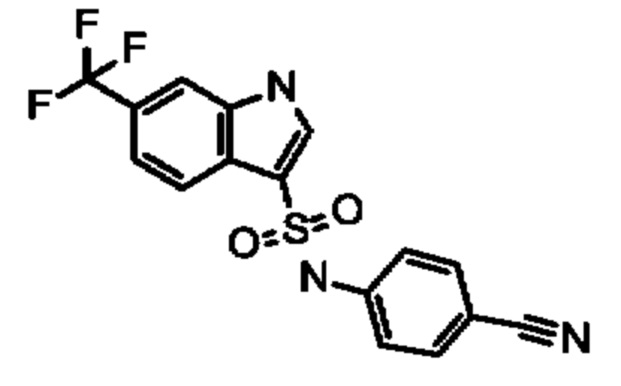
ЖХМС в нейтральной среде, методика 3 (ЭР+): 383,3 (M+NH4)+, чистота 98%.
1H ЯМР (600 МГц, DMSO-d6) δ: 12,46 (s, 1H), 11,04 (s, 1H), 8,37 (s, 1Н), 8,02 (d, J=8,5 Гц, 1H), 7,81 (s, 1H), 7,62 (d, J=8,7 Гц, 2H), 7,53 (d, J=8,7 Гц, 1H), 7,24 (d, J=8,8 Гц, 2H).
N-(5-Хлор-3-фторпиридин-2-ил)-1Н-бензо[g]индол-3-сульфонамид I-191
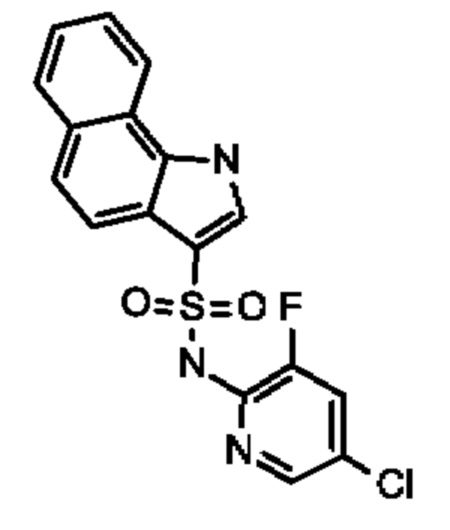
ЖХМС в нейтральной среде, методика 3 (ЭР+): 375,8 (М+Н)+, чистота 96%.
1H ЯМР (600 МГц, DMSO-d6) δ 12,91 (d, J=3,3 Гц, 1H), 11,06 (s, 1H), 8,40 (dd, J=8,2, 1,2 Гц, 1Н), 8,09 (dd, J=31,3, 2,6 Гц, 2H), 8,01-7,86 (m, 3Н), 7,72-7,54 (m, 2H), 7,49 (m, J=8,1, 6,9, 1,2 Гц, 1H).
N-(2,1,3-Бензотиадиазол-5-ил)-6-(трифторметил)-1Н-индол-3-сульфонамид I-192
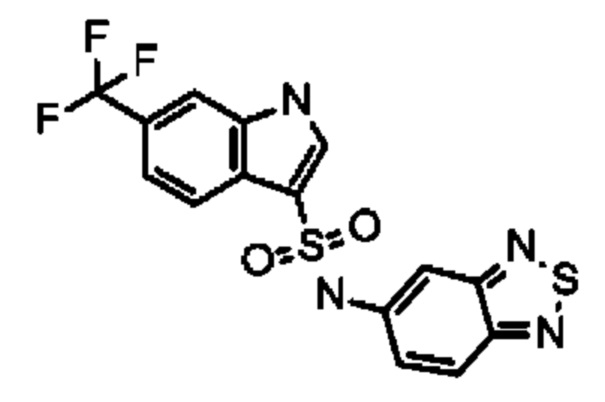
ЖХМС в нейтральной среде, методика 3 (ЭР+): 399 (М+Н)+, чистота 99%.
1H ЯМР (600 МГц, DMSO-d6) δ: 12,43 (s, 1H), 11,02 (s, 1H), 8,45 (s, 1Н), 8,08 (d, J=8,5 Гц, 1H), 7,91 (d, J=9,4 Гц, 1H), 7,78 (s, 1H), 7,61 (d, J=2,5 Гц, 1H), 7,53 (dd, J=8,5, 1,6 Гц, 1H), 7,48 (dd, J=9,4, 2,2 Гц, 1H).
6-Бром-N-(6-фтор-2,1,3-бензотиадиазол-5-ил)-1Н-индол-3-сульфонамид I-193
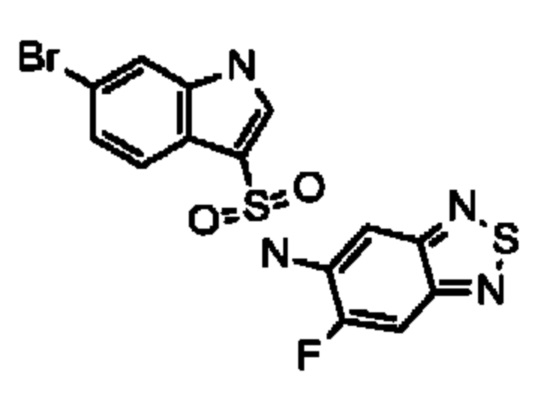
ЖХМС в нейтральной среде, методика 3 (ЭР+): 429,1 (М+Н)+, чистота 99%.
6-Хлор-N-[5-(цианометил)-3-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид I-194
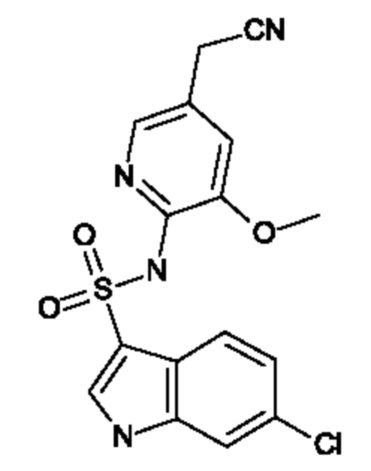
ЖХМС в щелочной среде, методика 2 (ЭР+): 377 (М+Н)+, чистота 100%.
1H ЯМР (600 МГц, DMSO-d6) δ 3,76 (s, 3Н) 3,90 (s, 2Н) 7,20-7,28 (m, 2Н) 7,50 (d, J=1,47 Гц, 1Н) 7,66 (s, 1H) 7,95 (d, J=8,31 Гц, 1H) 8,10 (s, 1H) 10,11 (brs, 1H) 12,03 (brs, 1H).
6-Хлор-N-[4-хлор-5-(дифторметокси)-2-фторфенил]-1H-индол-3-сульфонамид I-195
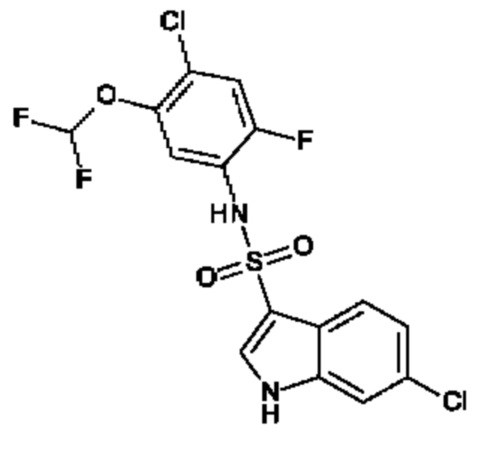
ЖХМС в щелочной среде, методика 2 (ЭР-): 423 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,12 (t, J=72 Гц, 1Н) 7,21 (dd, J=8,8, 2,0 Гц, 1H) 7,28-7,33 (m, 1H) 7,50-7,55 (m, 2H) 7,75 (d, J=8,8 Гц, 1H) 7,94 (d, J=2,45 Гц, 1H) 10,41 (brs, 1H) 12,12 (brs, 1H).
6-Хлор-7-метокси-N-(2,4,5-трифторфенил)-1Н-индол-3-сульфонамид I-196
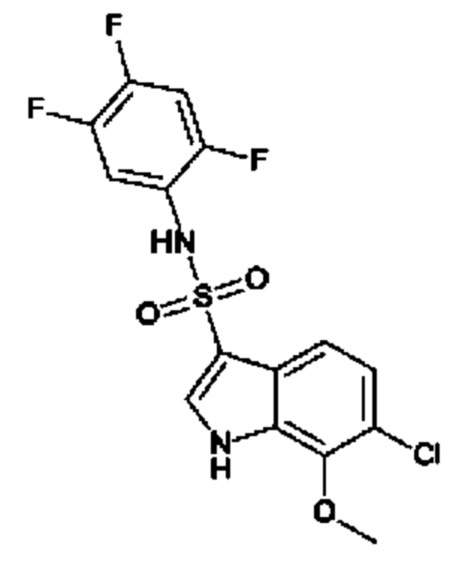
ЖХМС в щелочной среде, методика 2 (ЭР-): 389 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,89 (s, 3Н) 7,20 (d, J=8,00 Гц, 1Н) 7,29-7,36 (m, 1H) 7,42-7,49 (m, 2H) 7,92 (d, J=2,40 Гц, 1H) 10,22 (s, 1H) 12,47 (s, 1H).
6-Хлор-N-(7-фтор-2,1,3-бензоксадиазол-4-ил)-1Н-индол-3-сульфонамид I-197
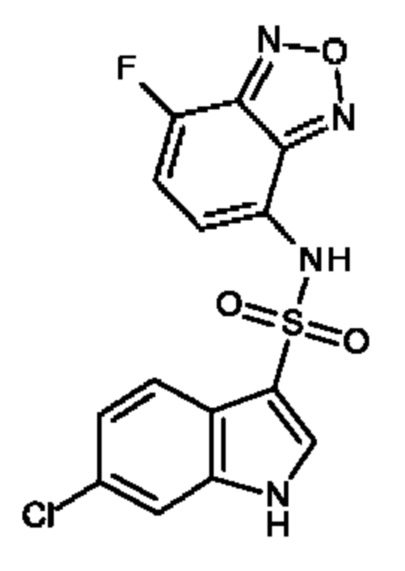
ЖХМС в щелочной среде, методика 2 (ЭР-): 365 (М-Н)-, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,13-7,17 (m, 1Н) 7,21 (d, J=8,8 Гц, 1H) 7,30-7,34 (m, 1H) 7,50 (s, 1H) 7,83 (d, J=9,2 Гц, 1H) 8,2 (d, J=2,8 Гц, 1H) 11,15 (brs, 1H) 12,16 (brs, 1H).
6-Хлор-N-(4-хлор-2,5-дифторфенил)-1-бензофуран-3-сульфонамид I-198
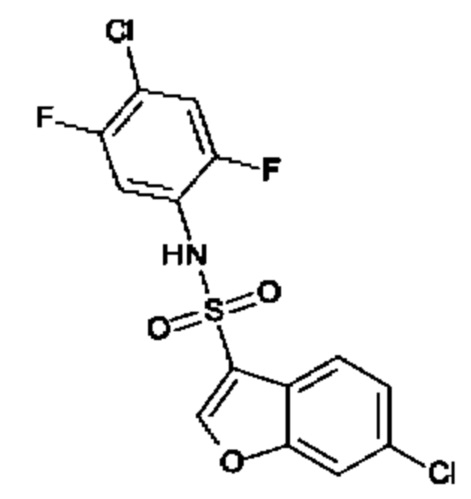
ЖХМС в щелочной среде, методика 2 (ЭР-): 376 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,38-7,44 (m, 1Н) 7,51 (d, J=8,40 Гц, 1H) 7,60 (t, J=8,40 Гц, 1H) 7,78 (d, J=8,00 Гц, 1H) 7,97 (s, 1H) 8,74 (s, 1H) 10,99 (s, 1H).
6-Хлор-N-(5-хлор-3,6-дифторпиридин-2-ил)-1Н-индол-3-сульфонамид I-199
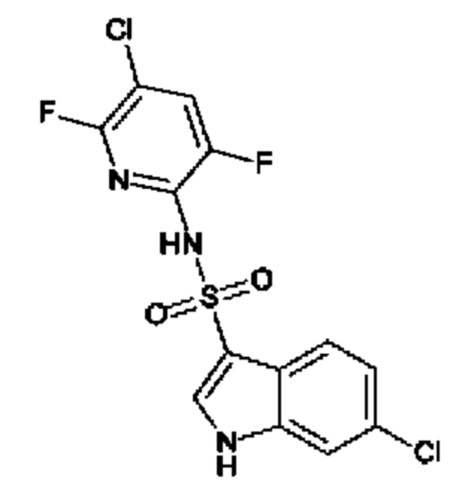
ЖХМС в щелочной среде, методика 2 (ЭР+): 378 (М+Н)+, чистота 96%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,26 (dd, J=8,80, 1,47 Гц, 1Н) 7,55 (d, J=1,47 Гц, 1H) 7,88 (d, J=8,31 Гц, 1H) 8,15 (d, J=2,93 Гц, 1H) 8,21 (t, J=7,83 Гц, 1H) 11,49 (brs, 1H) 12,22 (brs, 1H).
6-Хлор-N-(3,6-дифторпиридин-2-ил)-1Н-индол-3-сульфонамид I-200
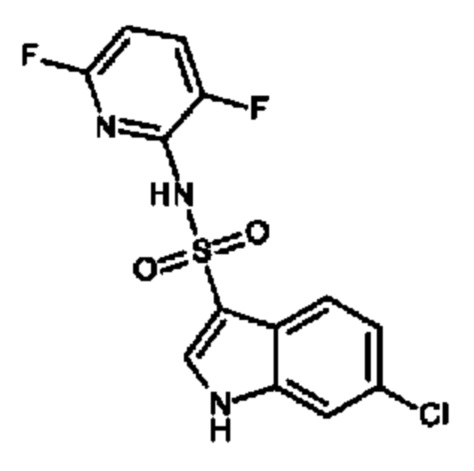
ЖХМС в щелочной среде, методика 2 (ЭР-): 344 (М-Н)-, чистота 93%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,75 (d, J=8,31 Гц, 1Н) 7,24 (dd, J=8,5, 1,71 Гц, 1H) 7,54 (d, J=1,5 Гц, 1H) 7,75-7,83 (m, 1H) 7,88 (d, J=8,3 Гц, 1H) 8,13 (d, J=2,9 Гц, 1H) 11,25 (brs, 1H) 12,18 (brs, 1H).
6-Хлор-N-(4-хлор-2,5-дифторфенил)-7-фтор-1Н-индол-3-сульфонамид I-242
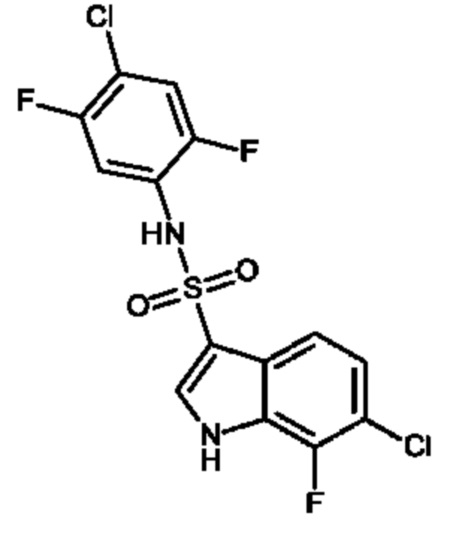
ЖХМС в щелочной среде, методика 2 (ЭР-): 393 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,26-7,39 (m, 2Н) 7,51-7,62 (m, 2Н) 8,13 (s, J=2,45 Гц, 1Н) 10,55 (s, 1H) 12,90 (brs, 1H).
6-Хлор-N-(6-фтор-3-оксо-1,3-дигидро-2-бензофуран-5-ил)-1Н-индол-3-сульфонамид I-243
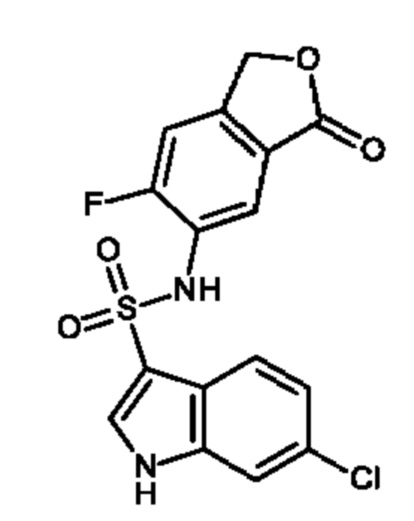
ЖХМС в щелочной среде, методика 2 (ЭР+): 381 (М+Н)+, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 5,28 (s, 2Н) 7,23 (dd, J=8,56, 1,71 Гц, 1Н) 7,46 (d, J=9,29 Гц, 1H) 7,52 (d, J=1,96 Гц, 1H) 7,67 (d, J=6,85 Гц, 1H) 7,77 (d, J=8,80 Гц, 1H) 7,97 (d, J=2,93 Гц, 1H) 10,44 (s, 1H) 12,11 (brs, 1H).
6-Хлор-N-(4-хлор-2,5-дифторфенил)-7-метокси-1Н-индол-3-сульфонамид I-244
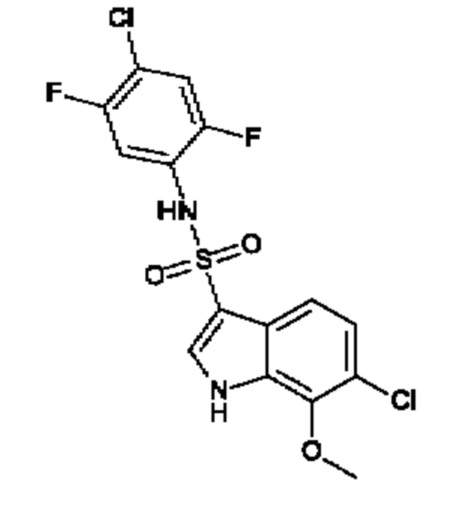
ЖХМС в щелочной среде, методика 2 (ЭР-): 405 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,90 (s, 3Н) 7,24 (d, J=8,31 Гц, 1Н) 7,34-7,40 (m, 1H) 7,52-7,59 (m, 2H) 8,06 (d, J=2,93 Гц, 1H) 10,52 (s, 1H) 12,54 (brs, 1H).
N-(5-Бром-3,6-дифторпиридин-2-ил)-6-хлор-1Н-индол-3-сульфонамид I-245
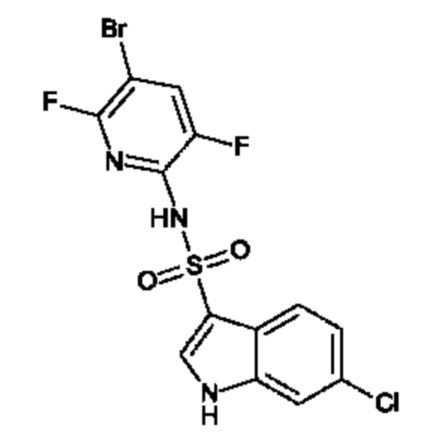
ЖХМС в щелочной среде, методика 2 (ЭР+): 422 (М+Н)+, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,24 (d, J=7,82 Гц, 1Н) 7,54 (s, 1H) 7,87 (d, J=8,31 Гц, 1H) 8,13 (s, 1H) 8,21-8,28 (m, 1H) 11,48 (brs, 1H) 12,18 (brs, 1H).
6-Хлор-N-[4-(2,2-дифторэтокси)-2,5-дифторфенил]-1H-индол-3-сульфонамид I-246
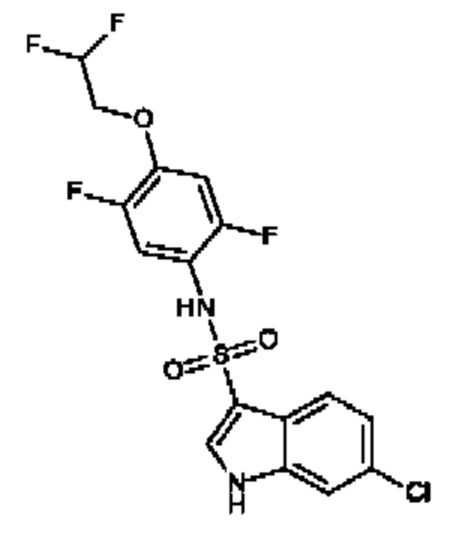
ЖХМС в щелочной среде, методика 2 (ЭР-): 421 (М-Н)-, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 4,26-4,36 (m, 2Н) 6,35 (t, J=54 Гц, 1Н) 7,02-7,18 (m, 2H) 7,20 (dd, J=8,56, 1,71 Гц, 1H) 7,51 (d, J=1,47 Гц, 1H) 7,69 (d, J=8,31 Гц, 1H) 7,86 (d, J=2,45 Гц, 1H) 9,94 (s, 1H) 12,04 (brs, 1H).
N-(4-Хлор-2,5-дифторфенил)-6-(трифторметил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-247
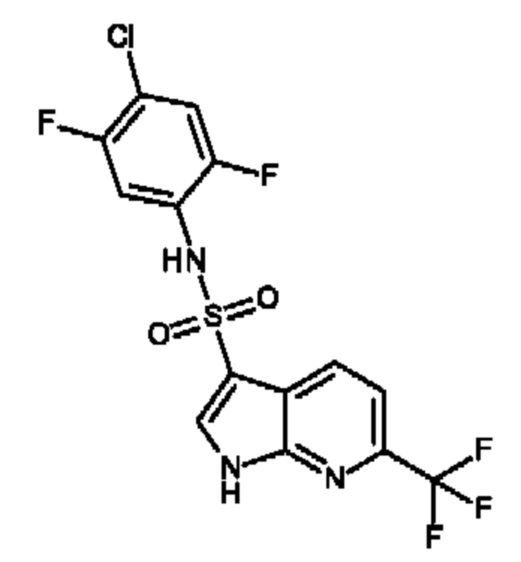
ЖХМС в щелочной среде, методика 2 (ЭР-): 410 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,34-7,39 (m, 1Н) 7,48-7,54 (m, 1H) 7,79 (d, J=8,31 Гц, 1H) 8,41 (d, J=8,31 Гц, 1H) 8,46 (s, 1H) 10,60 (s, 1H) 13,18 (brs, 1H).
5-Бром-6-хлор-N-(4-хлор-2,5-дифторфенил)-1Н-индол-3-сульфонамид I-248

ЖХМС в щелочной среде, методика 2 (ЭР-): 455 (М-Н)-, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,32-7,36 (m, 1Н) 7,50-7,56 (m, 1H) 7,73 (s, 1H) 8,07-8,13 (m, 2H) 10,50 (s, 1H) 12,29 (brs, 1H).
7-Бром-6-хлор-N-(4-хлор-2,5-дифторфенил)-1Н-индол-3-сульфонамид I-249
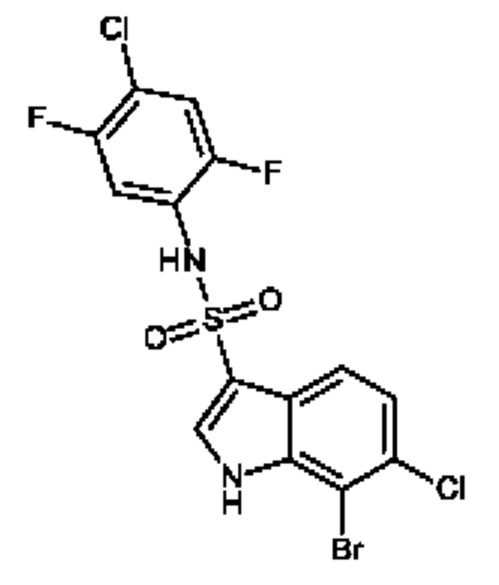
ЖХМС в щелочной среде, методика 2 (ЭР-): 455 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,38 (dd, J=10,03, 7,09 Гц, 1H) 7,43 (d, J=8,31 Гц, 1H) 7,53-7,59 (m, 1H) 7,79 (d, J=8,31 Гц, 1H) 8,07 (d, J=2,93 Гц, 1H) 10,57 (s, 1H) 12,53 (brs, 1H).
6-Бром-N-(4-хлор-2,5-дифторфенил)-4-фтор-1H-индол-3-сульфонамид I-251

ЖХМС в щелочной среде, методика 2 (ЭР+): 439 (М+Н)+, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,26 (d, J=10,29 Гц, 1Н) 7,32-7,39 (m, 1H) 7,52 (d, J=1,25 Гц, 1H) 7,56 (m, 1H) 8,06 (s, 1H) 10,27 (s, 1H) 12,39 (brs, 1H).
6-Хлор-N-{3,6-дифтор-5-[(1Е)-3-метоксипроп-1-ен-1-ил]пиридин-2-ил}-1Н-индол-3-сульфонамид I-252
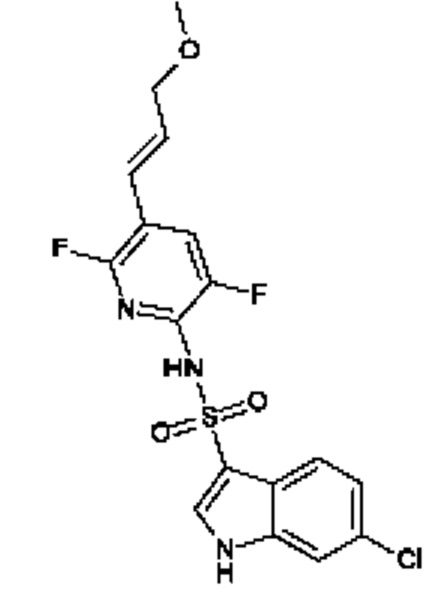
ЖХМС в щелочной среде, методика 2 (ЭР+): 414 (М+Н)+, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,26 (s, 3Н) 4,01 (brs, 2Н) 6,43 (brs, 2Н) 7,20-7,29 (m, 1Н) 7,54 (s, 1H) 7,88 (d, J=8,80 Гц, 1H) 8,08 (t, J=8,80 Гц, 1H) 8,13 (brs, 1H) 11,28 (brs, 1H) 12,18 (brs, 1H).
6-Хлор-N-[3,6-дифтор-5-(3-метоксипропил)пиридин-2-ил]-1Н-индол-3-сульфонамид I-253
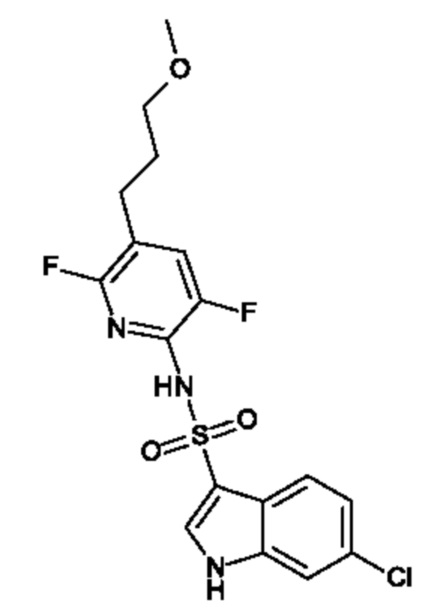
ЖХМС в щелочной среде, методика 2 (ЭР+): 416 (М+Н)+, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 1,65-1,75 (m, 2Н) 3,18 (s, 3Н) 3,26 (t, J=6,11 Гц, 2Н) 7,20-7,27 (m, 1Н) 7,54 (d, J=1,96 Гц, 1H) 7,73 (dd, J=9,29, 7,83 Гц, 1H) 7,84 (d, J=8,80 Гц, 1H) 8,09 (d, J=2,93 Гц, 1H) 11,00 (s, 1H) 12,15 (brs, 1H) (сигналы 2H объединены с пиком растворителя).
6-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1H-индол-3-сульфонамид I-254
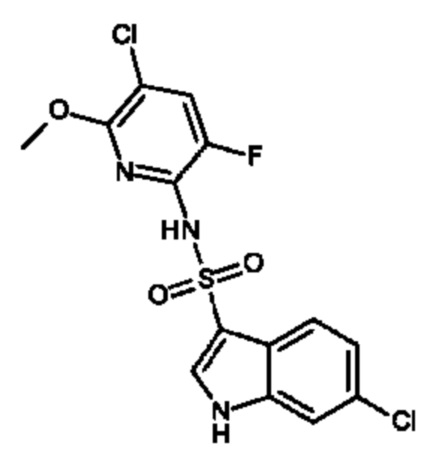
ЖХМС в щелочной среде, методика 2 (ЭР+): 390 (М+Н)+, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,63 (s, 3Н) 7,23 (dd, J=8,56, 1,71 Гц, 1H) 7,54 (d, J=1,96 Гц, 1Н) 7,84 (d, J=8,80 Гц, 1H) 7,94 (d, J=8,80 Гц, 1Н) 8,16 (d, J=2,93 Гц, 1H) 11,11 (s, 1H) 12,11 (brs, 1H).
6-Хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид I-255
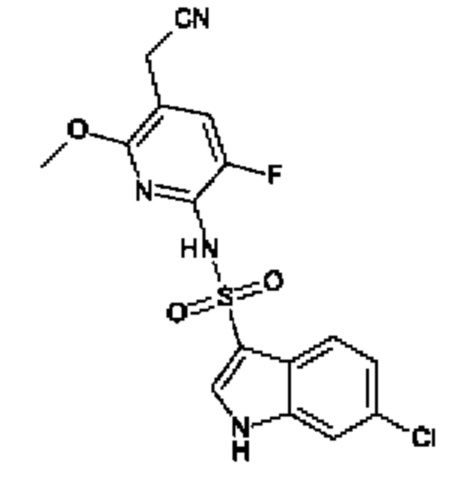
ЖХМС в щелочной среде, методика 2 (ЭР+): 395 (М+Н)+, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,62 (s, 3Н) 3,70 (s, 2Н) 7,22 (dd, J=8,80, 1,96 Гц, 1Н) 7,54 (d, J=1,96 Гц, 1H) 7,62 (d, J=9,78 Гц, 1H) 7,85 (d, J=8,31 Гц, 1H) 8,15 (d, J=2,93 Гц, 1H) 11,02 (s, 1H) 12,08 (brs, 1H).
6-Хлор-N-[4-(цианометокси)-2,5-дифторфенил]-1Н-индол-3-сульфонамид I-257
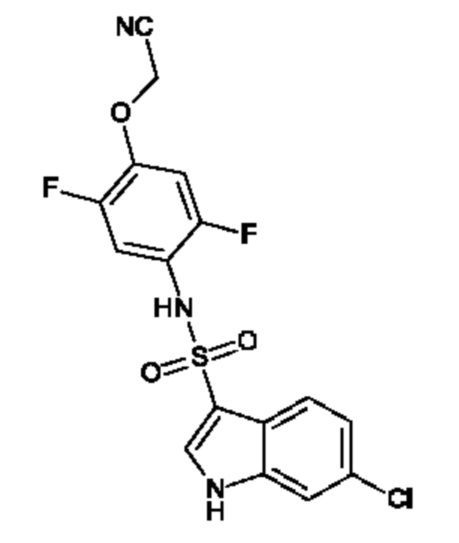
ЖХМС в щелочной среде, методика 2 (ЭР-): 396 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 5,18 (s, 2Н) 7,14-7,27 (m, 3Н) 7,52 (d, J=1,96 Гц, 1H) 7,67 (d, J=8,80 Гц, 1Н) 7,91 (d, J=2,45 Гц, 1Н) 10,05 (s, 1H) 12,07 (brs, 1Н).
6-Хлор-N-(4-циано-2-фторфенил)-5-фтор-1Н-индол-3-сульфонамид I-258
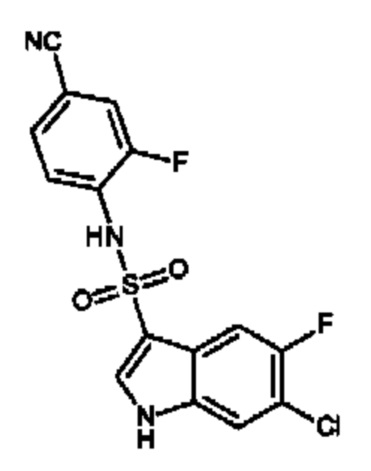
ЖХМС в щелочной среде, методика 2 (ЭР)-: 366 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,57 (d, J=3,91 Гц, 2Н) 7,69 (d, J=6,36 Гц, 1Н) 7,74-7,81 (m, 2H) 8,20 (d, J=2,93 Гц, 1H) 10,81 (s, 1H) 12,31 (brs, 1H).
N-(4-Бром-2,5-дифторфенил)-6-хлор-1-бензофуран-3-сульфонамид I-259
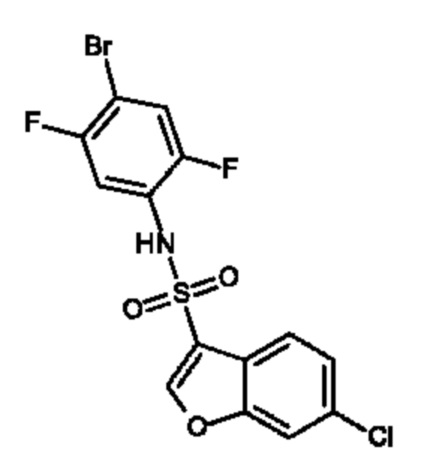
ЖХМС в щелочной среде, методика 2 (ЭР+): 422 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,36-7,40 (m, 1Н) 7,51 (dd, J=8,56, 1,71 Гц, 1H) 7,62-7,66 (m, 1H) 7,78 (d, J=8,31 Гц, 1H) 7,96 (d, J=1,47 Гц, 1H) 8,76 (s, 1H) 11,00 (brs, 1H).
6-Хлор-N-[4-(циклопропилметокси)-2,5-дифторфенил]-1Н-индол-3-сульфонамид I-260
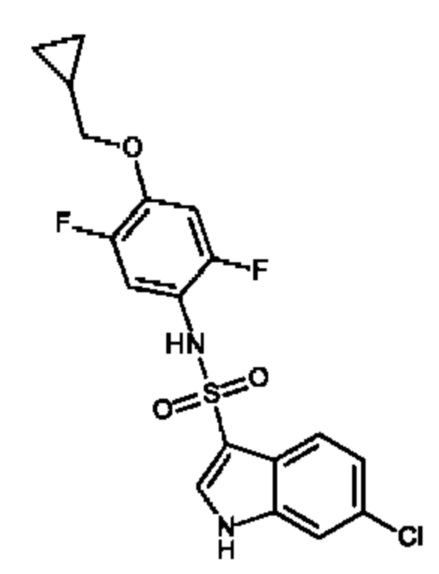
ЖХМС в щелочной среде, методика 2 (ЭР-): 411 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 0,24-0,31 (m, 2Н) 0,50-0,57 (m, 2Н) 1,12-1,21 (m, 1Н) 3,79 (d, J=6,85 Гц, 2H) 6,92-7,05 (m, 2H) 7,20 (dd, J=8,56, 1,71 Гц, 1H) 7,52 (d, J=1,47 Гц, 1H) 7,69 (d, J=8,31 Гц, 1H) 7,84 (d, J=1,96 Гц, 1H) 9,83 (s, 1H) 12,03 (brs, 1H).
6-Хлор-N-(4-хлор-2,5-дифторфенил)-7-(2,2-дифторэтокси)-1Н-индол-3-сульфонамид I-262
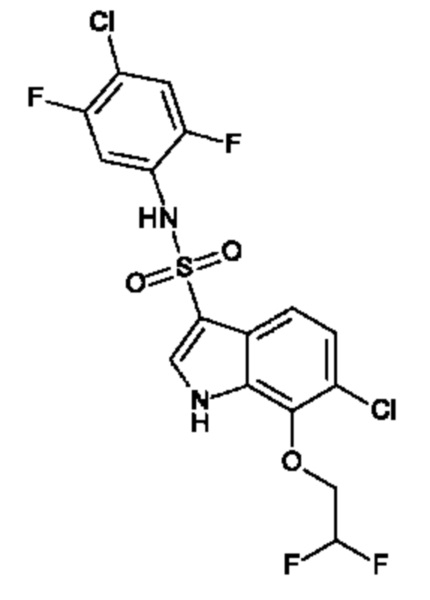
ЖХМС в щелочной среде, методика 2 (ЭР)-: 455 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 4,36-4,41 (m, 2Н) 6,27-6,59 (m, 1Н) 7,26 (d, J=8,68 Гц, 1H) 7,33-7,37 (m, 1H) 7,52-7,56 (m, 1H) 7,58 (d, J=8,68 Гц, 1H) 8,12 (d, J=2,81 Гц, 1H) 10,54 (s, 1H) 12,46 (brs, 1H).
6-Хлор-N-(4-хлор-2,5-дифторфенил)-5-фтор-1Н-индол-3-сульфонамид I-263
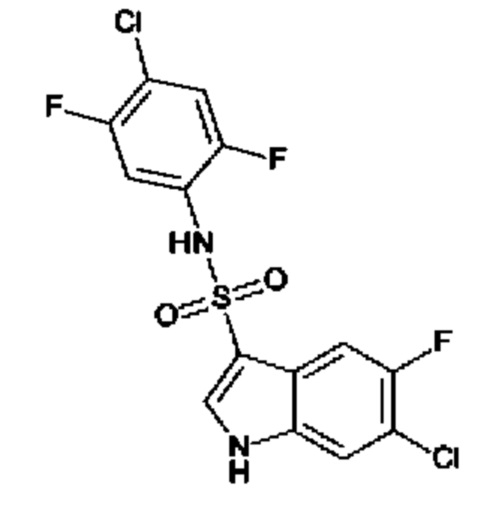
ЖХМС в щелочной среде, методика 2 (ЭР-): 393 (М-Н)-, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,37 (dd, J=10,51, 7,09 Гц, 1Н) 7,56 (dd, J=10,27, 6,85 Гц, 1H) 7,68 (d, J=6,36 Гц, 1H) 7,73 (d, J=10,27 Гц, 1H) 8,13 (d, J=2,93 Гц, 1H) 10,50 (s, 1H) 12,26 (brs, 1H).
6-Хлор-N-(3,5-диметоксипиридин-2-ил)-1Н-индол-3-сульфонамид I-264
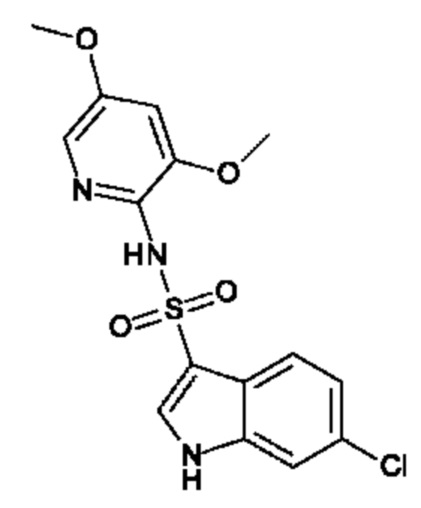
ЖХМС в щелочной среде, методика 2 (ЭР+): 368 (М+Н)+, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,66 (s, 3Н) 3,75 (s, 3Н) 6,94 (d, J=2,45 Гц, 1Н) 7,14-7,24 (m, 1H) 7,46-7,51 (m, 2H) 7,85-7,89 (m, 1H) 7,95 (s, 1H) 9,64 (brs, 1H) 11,95 (brs, 1H).
6-Хлор-N-(6-фтор-3-оксо-2,3-дигидро-1H-изоиндол-5-ил)-1H-индол-3-сульфонамид I-265

ЖХМС в щелочной среде, методика 2 (ЭР+): 380 (М+Н)+, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 4,25 (s, 2Н) 7,21 (dd, J=8,80, 1,96 Гц, 1Н) 7,33 (d, J=9,78 Гц, 1H) 7,49-7,53 (m, 2H) 7,77 (d, J=8,80 Гц, 1H) 7,89 (d, J=2,93 Гц, 1H) 8,59 (s, 1H) 10,21 (s, 1H) 12,07 (d, J=1,96 Гц, 1H).
Т-(4-Циано-5-фтор-2-метоксифенил)-1Н-бензо[g]индол-3-сульфонамид I-289
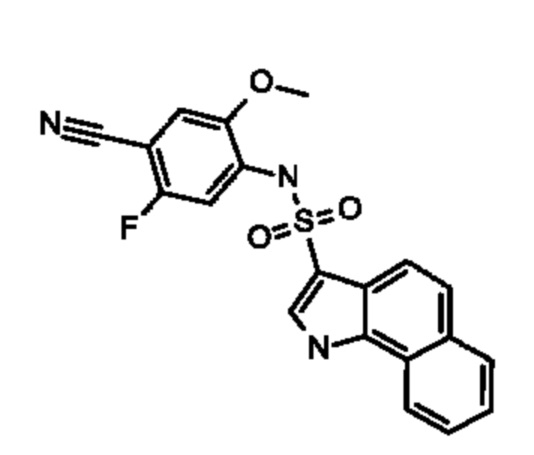
ЖХМС в нейтральной среде, методика 3 (ЭР+): 396,4 (М+Н)+, чистота 95,0%.
1H ЯМР (600 МГц, DMSO-d6) δ: 12,99 (s, 1H), 10,27 (s, 1Н), 8,39 (dd, J=8,3, 1,2 Гц, 1H), 8,30 (d, J=3,0 Гц, 1H), 8,12-7,94 (m, 2H), 7,66 (d, J=8,7 Гц, 1H), 7,62-7,60 (m, 1H), 7,51-7,49 (m, 1H), 7,40 (d, J=11,2 Гц, 1H), 7,34 (d, J=5,9 Гц, 1H), 3,65 (s, 3H).
N-(5-Хлор-3,6-дифторпиридин-2-ил)-1Н-бензо[g]индол-3-сульфонамид I-304
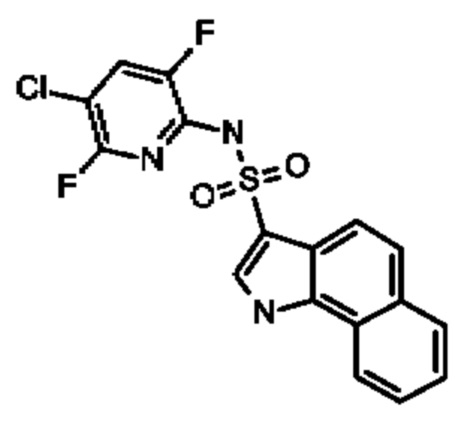
ЖХМС в щелочной среде, методика 1 (ЭР+): 394 (М+Н)+, чистота 100%.
1H ЯМР (400 МГц, DMSO-d6) δ 13,01 (s, 1Н), 11,48 (s, 1H), 8,42 (dd, J=8,2, 1,0 Гц, 1H), 8,18 (d, J=3,2 Гц, 2H), 8,00 (dd, J=8,5, 6,5 Гц, 2H), 7,68 (d, J=8,8 Гц, 1H), 7,57 (dddd, J=54,0, 8,2, 6,9, 1,2 Гц, 2H).
N-(4-Бром-2,5-дифторфенил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид I-305
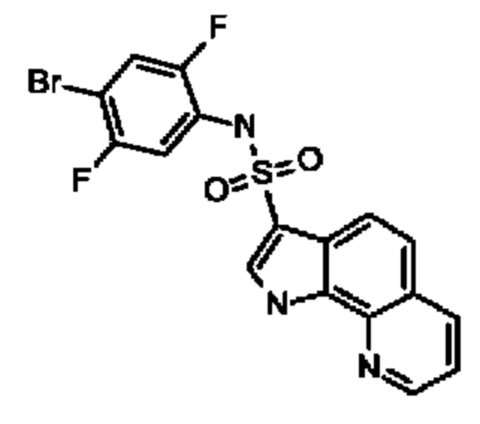
ЖХМС в щелочной среде, методика 1 (ЭР+): 438 (М+Н)+, чистота 95%.
1H ЯМР (400 МГц, DMSO-d6) δ 13,23 (s, 1Н), 10,51 (s, 1H), 8,92 (dd, J=4,4, 1,7 Гц, 1H), 8,44 (dd, J=8,2, 1,7 Гц, 1H), 8,04-7,91 (m, 2H), 7,69 (d, J=8,7 Гц, 1H), 7,57 (dt, J=10,4, 5,2 Гц, 2H), 7,36 (dd, J=10,0, 6,8 Гц, 1H).
N-(4-Этинил-2-фторфенил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид I-306
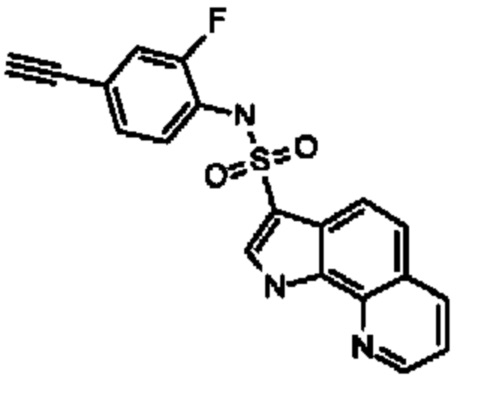
ЖХМС в щелочной среде, методика 1 (ЭР+): 366 (М+Н)+, чистота 97%.
6-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-7-метокси-1Н-индол-3-сульфонамид I-309
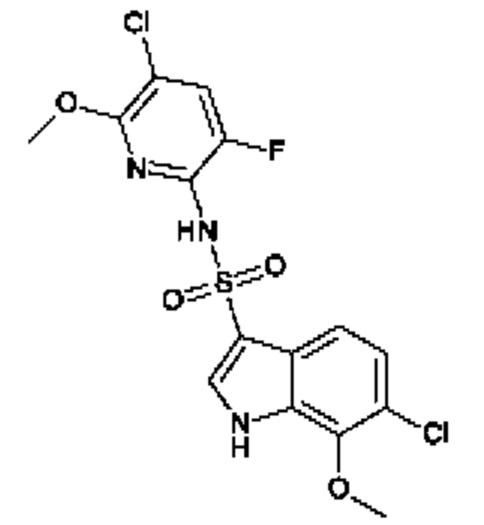
ЖХМС в щелочной среде, методика 2 (ЭР+): 420 (М+Н)+, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,60 (s, 3 Н) 3,90 (s, 3 Н) 7,19 (d, J=8,80 Гц, 1 Н) 7,58 (d, J=8,80 Гц, 1 Н) 7,81 (brs, 1 Н) 8,02 (s, 1 Н) 11,12 (brs, 1 Н) 12,37 (brs, 1 Н).
6-Хлор-N-(4-цианофенил)-1-бензотиофен-3-сульфонамид I-311
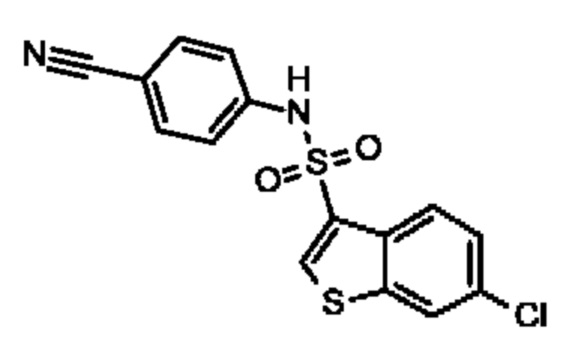
ЖХМС в щелочной среде, методика 2 (ЭР-): 347 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,21 (d, J=8,31 Гц, 2Н) 7,62 (dd, J=8,80, 1,96 Гц, 1Н) 7,66 (d, J=8,80 Гц, 2H) 8,16 (d, J=8,80 Гц, 1H) 8,29 (d, J=1,96 Гц, 1H) 8,78 (s, 1H) 11,40 (s, 1H).
6-Хлор-N-(4-хлор-2,5-дифторфенил)-1-бензотиофен-3-сульфонамид I-312
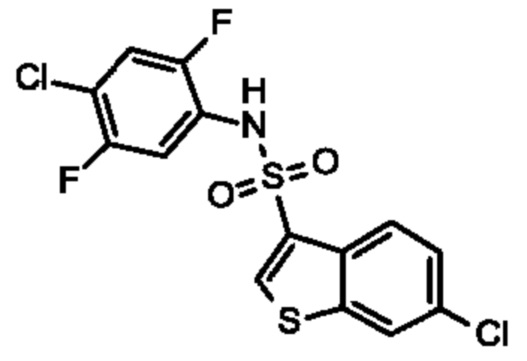
ЖХМС в щелочной среде, методика 2 (ЭР-): 392 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,34-7,39 (m, 1 Н) 7,56-7,63 (m, 2Н) 8,15 (d, J=8,80 Гц, 1 Н) 8,31 (d, J=1,96 Гц, 1 Н) 8,58 (s, 1 Н) 10,91 (br s, 1 Н).
6-Хлор-N-[4-(цианометокси)-2,5-дифторфенил]-1-бензотиофен-3-сульфонамид I-313
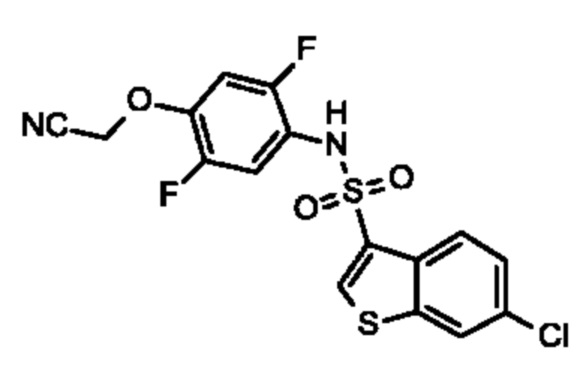
ЖХМС в щелочной среде, методика 2 (ЭР-): 413 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 5,20 (s, 2 Н) 7,17-7,30 (m, 2 Н) 7,59 (dd, J=8,80, 1,96 Гц, 1 Н) 8,06 (d, J=8,80 Гц, 1 Н) 8,31 (d, J=1,96 Гц, 1 Н) 8,46 (s, 1 Н) 10,54 (s, 1 Н).
6-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1-бензотиофен-3-сульфонамид I-314
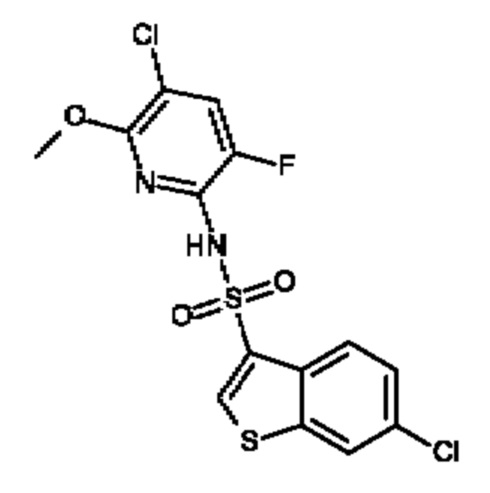
ЖХМС в щелочной среде, методика 2 (ЭР-): 405 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,57 (s, 3 Н) 7,61 (d, J=4,40 Гц, 1 Н) 8,00 (d, J=5,38 Гц, 1 Н) 8,20-8,22 (m, 1 Н) 8,31 (s, 1 Н) 8,77 (s, 1 Н) 11,64 (br s, 1 Н).
6-Хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1-бензотиофен-3-сульфонамид I-315
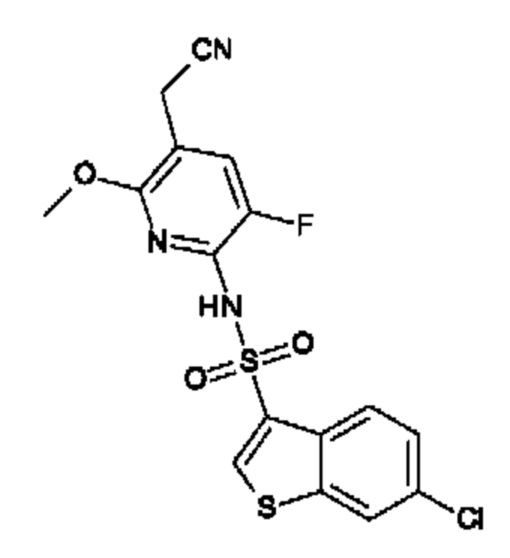
ЖХМС в щелочной среде, методика 2 (ЭР+): 412 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,56 (s, 3 Н) 3,71 (s, 2 Н) 7,60 (dd, J=8,80, 1,96 Гц, 1 Н) 7,68 (d, J=9,29 Гц, 1 Н) 8,23 (d, J=8,31 Гц, 1 Н) 8,31 (d, J=1,96 Гц, 1 Н) 8,77 (s, 1 Н) 11,57 (brs, 1 Н).
6-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-7-фтор-1Н-индол-3-сульфонамид I-319
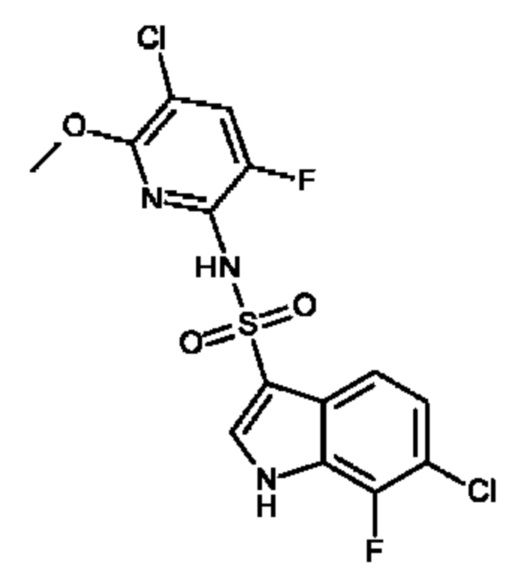
ЖХМС в щелочной среде, методика 2 (ЭР+): 408 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,62 (s, 3 Н) 7,30-7,34 (m, 1 Н) 7,67 (d, J=8,80 Гц, 1 Н) 7,94 (d, J=8,80 Гц, 1 Н) 8,22 (d, J=1,47 Гц, 1 Н) 11,19 (s, 1 Н) 12,85 (br s, 1 Н)
6-Бром-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид I-320
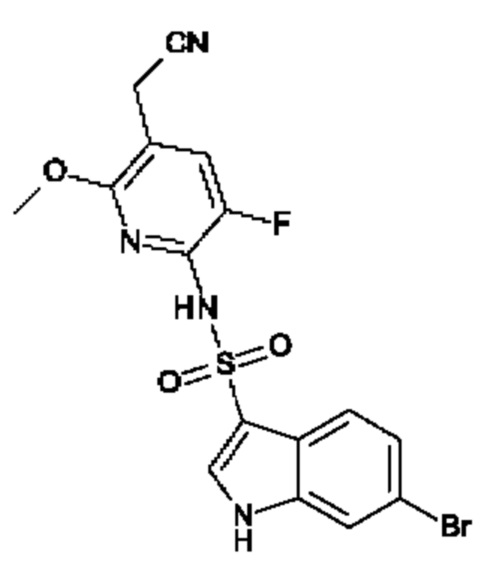
ЖХМС в щелочной среде, методика 2 (ЭР-): 438 (М-Н)-, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,62 (s, 3 Н) 3,70 (s, 2 Н) 7,34 (d, J=8,31 Гц, 1 Н) 7,62 (d, J=9,78 Гц, 1 Н) 7,68 (s, 1 Н) 7,80 (d, J=8,31 Гц, 1 Н) 8,14 (d, J=2,45 Гц, 1 Н) 11,03 (s, 1 Н) 12,09 (br s, 1 Н)
7-Бром-6-хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1Н-индол-3-сульфонамид I-321
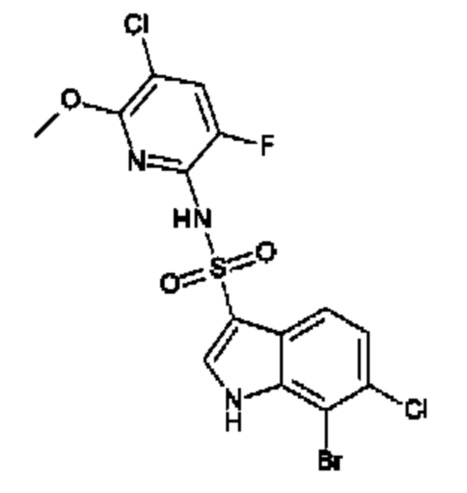
ЖХМС в щелочной среде, методика 2 (ЭР+): 468 (М+Н)+, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,63 (s, 3 Н) 7,42 (d, J=8,31 Гц, 1 Н) 7,85 (d, J=8,31 Гц, 1 Н) 7,95 (d, J=8,80 Гц, 1 Н) 8,14 (d, J=2,93 Гц, 1 Н) 11,20 (s, 1 Н) 12,48 (br s, 1 Н)
7-Бром-6-хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид I-322
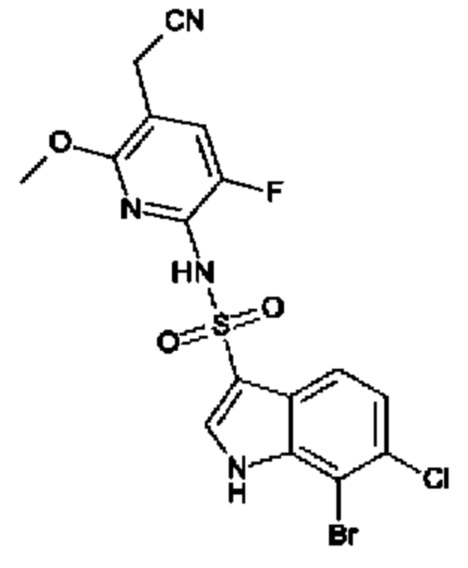
ЖХМС в щелочной среде, методика 2 (ЭР+): 473 (М+Н)+, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,63 (s, 3 Н) 3,70 (s, 2 Н) 7,42 (d, J=8,31 Гц, 1 Н) 7,62 (d, J=9,78 Гц, 1 Н) 7,86 (d, J=8,80 Гц, 1 Н) 8,13 (br s, 1 Н) 11,12 (s, 1 Н) 12,44 (br s, 1 H)
6-Бром-N-[3,6-дифтор-5-(3-метоксипропил)пиридин-2-ил]-1Н-индол-3-сульфонамид I-323
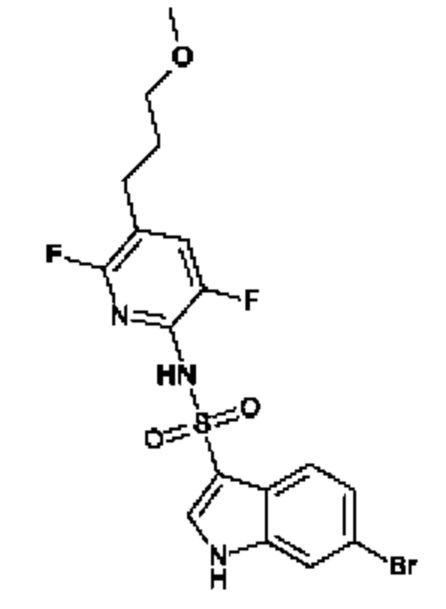
ЖХМС в щелочной среде, методика 2 (ЭР-): 458 (М-Н)-, чистота 96%.
1H ЯМР (400 МГц, Метанол-d4) δ 1,72-1,83 (m, 2 Н) 2,56 (t, J=7,65 Гц, 2 Н) 3,15-3,28 (m, 5 Н) 7,31 (dd, J=8,53, 1,76 Гц, 1 Н) 7,45 (dd, J=9,54, 7,78 Гц, 1 Н) 7,64 (d, J=1,76 Гц, 1 Н) 7,85 (d, J=8,78 Гц, 1 Н) 8,03 (s, 1 Н).
5-Бром-6-хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид I-324
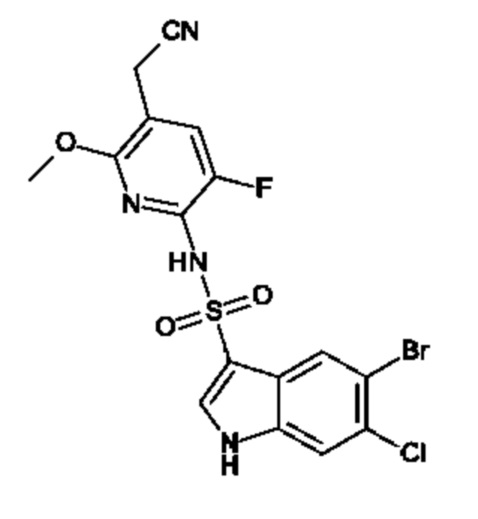
ЖХМС в щелочной среде, методика 2 (ЭР+): 473 (М+Н)+, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,65 (s, 3 Н) 3,71 (s, 2 Н) 7,64 (d, J=9,78 Гц, 1 Н) 7,75 (s, 1 Н) 8,21 (d, J=1,96 Гц, 1 Н) 8,25 (s, 1 Н) 11,03 (br s, 1 Н) 12,22 (br s, 1 H).
6-Бром-N-{3,6-дифтор-5-[(1Е)-3-метоксипроп-1-ен-1-ил]пиридин-2-ил}-1Н-индол-3-сульфонамид I-325
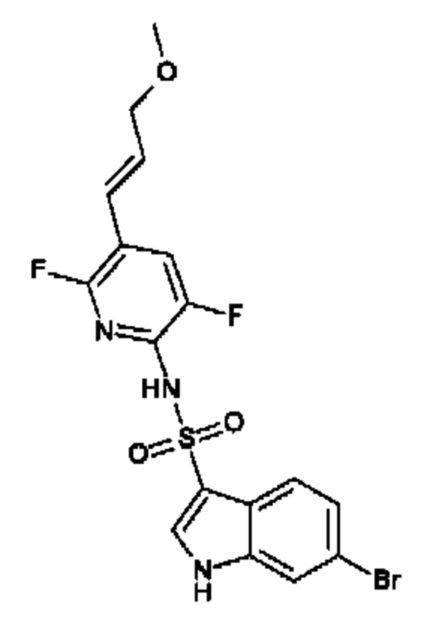
ЖХМС в щелочной среде, методика 2 (ЭР+): 458 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,25 (s, 3 Н) 4,01 (d, J=2,93 Гц, 2 Н) 6,41 (s, 2 Н) 7,34 (d, J=8,80 Гц, 1 Н) 7,67 (s, 1 Н) 7,83 (d, J=8,80 Гц, 1 Н) 8,03-8,13 (m, 2 Н) 11,29 (br s, 1 Н) 12,14 (brs, 1 Н)
6-Бром-N-(5-хлор-3-фторпиридин-2-ил)-7-метил-1Н-индол-3-сульфонамид I-326
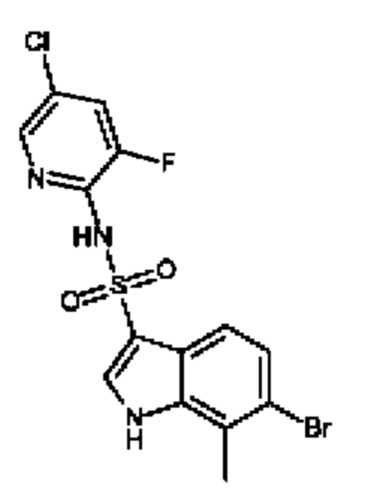
ЖХМС в щелочной среде, методика 1 (ЭР+): 418 (М+Н)+, чистота 90%.
6-Хлор-N-(6-фтор-1-метил-3-оксо-1,3-дигидро-2-бензофуран-5-ил)-1Н-индол-3-сульфонамид I-327
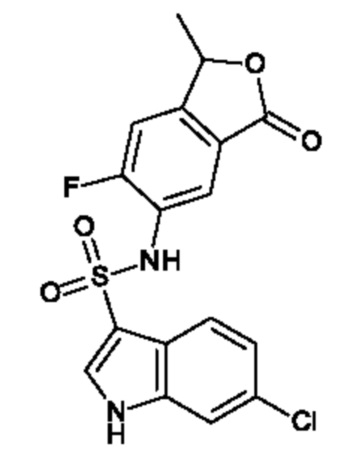
ЖХМС в щелочной среде, методика 2 (ЭР+): 395 (М+Н)+, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 1,48 (d, J=6,85 Гц, 3Н) 5,54-5,61 (m, 1Н) 7,22 (dd, J=8,80, 1,96 Гц, 1H) 7,51-7,55 (m, 2H) 7,65 (d, J=6,85 Гц, 1H) 7,73 (d, J=8,80 Гц, 1H) 7,99 (d, J=2,93 Гц, 1H) 10,43 (s, 1H) 12,12 (brs, 1H).
N-(5-Хлор-3-фтор-6-метоксипиридин-2-ил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид I-328
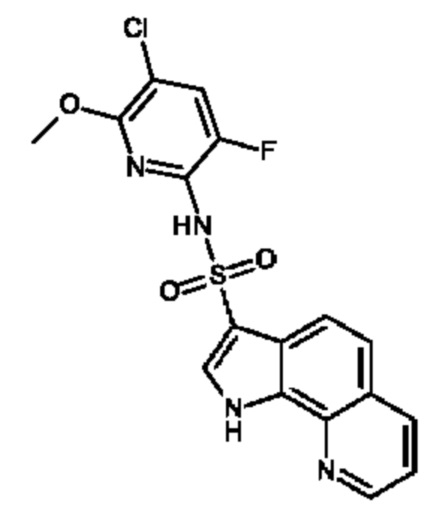
ЖХМС в щелочной среде, методика 1 (ЭР-): 405 (М-Н)-, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 13,21 (s, 1Н), 11,17 (s, 1H), 8,93 (dd, J=4,4, 1,6 Гц, 1H), 8,45 (dd, J=8,3, 1,6 Гц, 1H), 8,14-8,02 (m, 2H), 7,93 (d, J=8,5 Гц, 1H), 7,71 (d, J=8,7 Гц, 1H), 7,58 (dd, J=8,2, 4,4 Гц, 1H), 3,64 (s, 3H).
N-(5-Хлор-3-фтор-6-метоксипиридин-2-ил)-1Н-бензо[g]индол-3-сульфонамид I-329
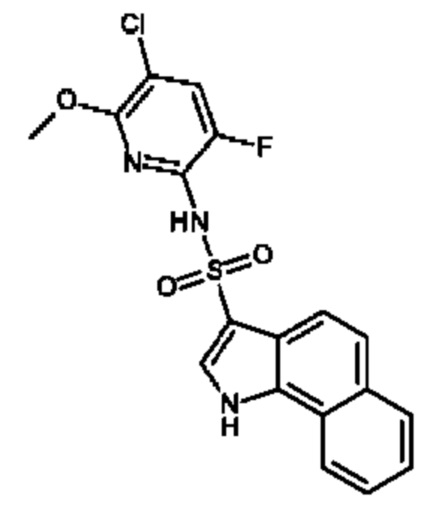
ЖХМС в щелочной среде, методика 1 (ЭР+): 406 (М+Н)+, чистота 96%.
1H ЯМР (400 МГц, DMSO-d6) δ 12,95 (s, 1Н), 11,13 (s, 1Н), 8,43 (d, J=8,3 Гц, 1H), 8,21 (s, 1H), 8,07-7,79 (m, 3H), 7,74-7,36 (m, 3H), 3,67 (s, 3H).
6-Нитро-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамид I-334
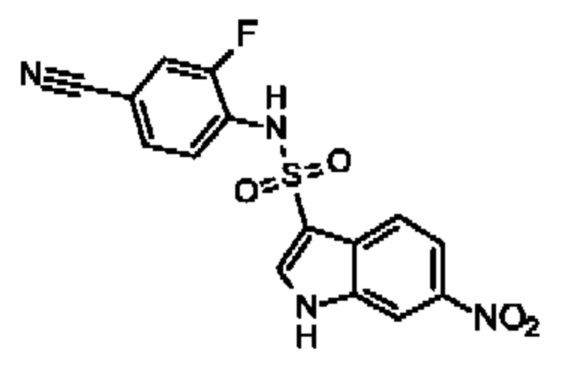
ЖХМС в щелочной среде, методика 2 (ЭР-): 359 (М-Н)-, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,58 (brs, 2Н) 7,76 (d, J=10,27 Гц, 1Н) 7,95-8,03 (m, 1Н) 8,06-8,15 (m, 1H) 8,38-8,44 (m, 2H) 10,94 (brs, 1H) 12,73 (brs, 1H).
6-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-5-фтор-1Н-индол-3-сульфонамид I-339
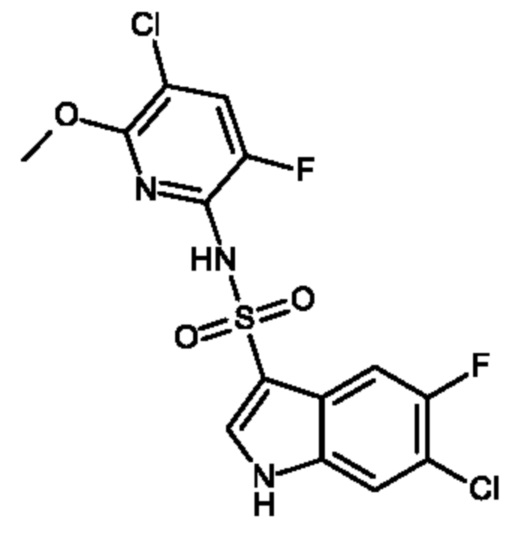
ЖХМС в щелочной среде, методика 2 (ЭР-): 406 (М-Н)-, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,64 (s, 3Н) 7,69 (d, J=6,36 Гц, 1Н) 7,78 (d, J=9,78 Гц, 1Н) 7,94 (d, J=8,80 Гц, 1Н) 8,21 (d, J=2,93 Гц, 1Н) 11,07 (s, 1Н) 12,19 (br s, 1Н).
6-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-5,7-дифтор-1Н-индол-3-сульфонамид I-340
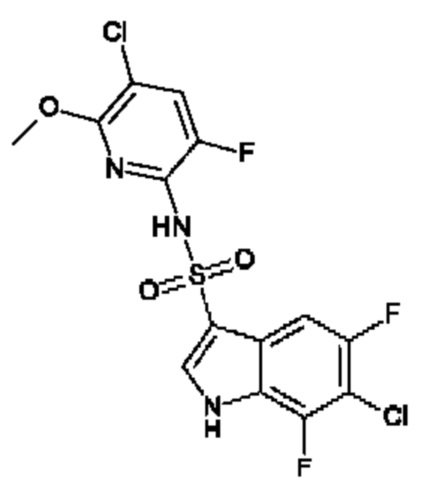
ЖХМС в щелочной среде, методика 2 (ЭР+): 426 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,65 (s, 3Н) 7,70 (d, J=9,78 Гц, 1H) 7,97 (d, J=9,29 Гц, 1H) 8,33 (d, J=1,96 Гц, 1H) 11,17 (s, 1H) 13,00 (br s, 1H).
7-Бром-6-хлор-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамид I-341
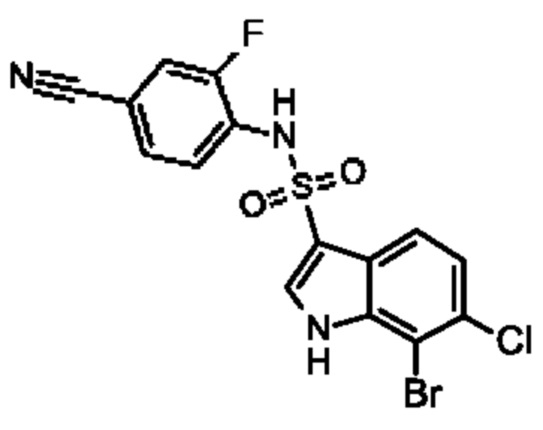
ЖХМС в щелочной среде, методика 2 (ЭР-): 426 (М-Н)-, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,44 (d, J=8,37 Гц, 1Н) 7,56-7,60 (m, 2Н) 7,74-7,79 (m, 1Н) 7,84 (d, J=8,37 Гц, 1Н) 8,14 (d, J=2,95 Гц, 1Н) 10,89 (br s, 1Н) 12,58 (d, J=1,97 Гц, 1Н).
6-Хлор-N-[4-(цианометокси)-2,5-дифторфенил]-1-бензофуран-3-сульфонамид I-342
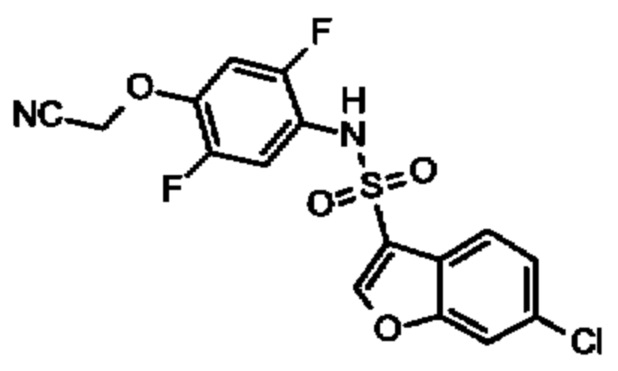
ЖХМС в щелочной среде, методика 2 (ЭР-): 397 (М-Н)-, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 5,21 (s, 2Н) 7,26-7,33 (m, 2Н) 7,49 (dd, J=8,31, 1,47 Гц, 1Н) 7,67 (d, J=8,31 Гц, 1Н) 7,97 (d, J=1,47 Гц, 1Н) 8,66 (s, 1Н) 10,63 (s, 1H).
5-Бром-6-хлор-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамид I-343
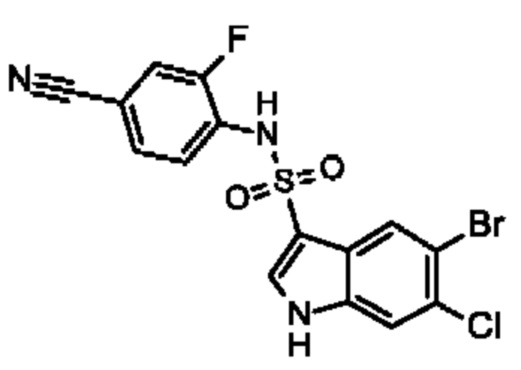
ЖХМС в щелочной среде, методика 2 (ЭР-): 426 (М-Н)-, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,55-7,60 (m, 2Н) 7,71-7,83 (m, 2Н) 8,17-8,21 (m, 2Н) 10,82 (s, 1Н) 12,35 (br s, 1Н).
6-Хлор-N-[3-метокси-5-(трифторметил)пиридин-2-ил]-1Н-индол-3-сульфонамид I-344
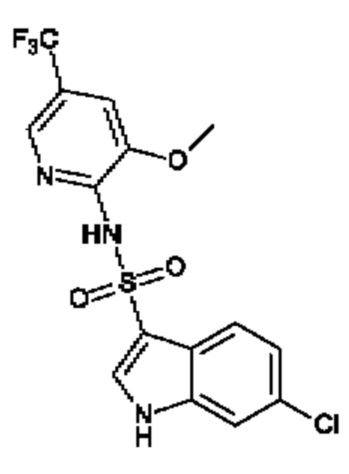
ЖХМС в щелочной среде, методика 2 (ЭР+): 406 (М+Н)+, чистота 96%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,87 (s, 3Н) 7,23 (d, J=8,31 Гц, 1Н) 7,51 (s, 2H) 7,98 (d, J=8,31 Гц, 1Н) 8,06 (s, 1H) 8,18 (s, 1H) 10,67 (brs, 1H) 12,13 (brs, 1H).
6-Хлор-N-(3,5-дифтор-6-метоксипиридин-2-ил)-1Н-индол-3-сульфонамид I-345
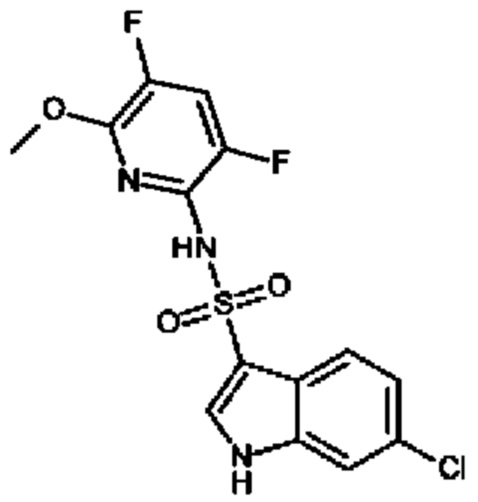
ЖХМС в щелочной среде, методика 2 (ЭР+): 374 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,55 (s, 3Н) 7,19 (dd, J=8,80, 1,96 Гц, 1Н) 7,51 (d, J=1,96 Гц, 1Н) 7,76 (d, J=8,31 Гц, 1Н) 7,86 (t, J=9,29 Гц, 1Н) 8,06 (d, J=2,93 Гц, 1Н) 10,73 (s, 1Н) 12,05 (br s, 1Н).
6-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1-бензофуран-3-сульфонамид I-346
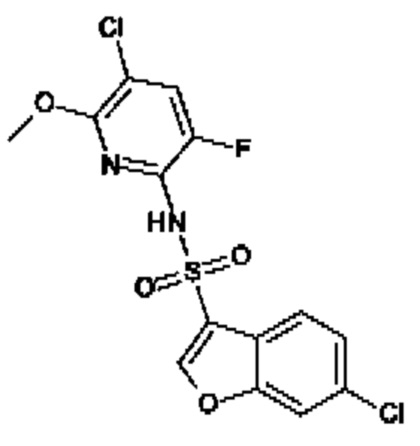
ЖХМС в щелочной среде, методика 2 (ЭР-): 389 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,59 (s, 3Н) 7,52 (dd, J=8,56, 1,71 Гц, 1Н) 7,89 (d, J=8,31 Гц, 1Н) 7,99 (d, J=1,47 Гц, 1Н) 8,03 (d, J=8,80 Гц, 1Н) 8,91 (s, 1Н) 11,66 (br s, 1Н).
6-Бром-7-хлор-N-(4-хлор-2,5-дифторфенил)-1Н-индол-3-сульфонамид I-347
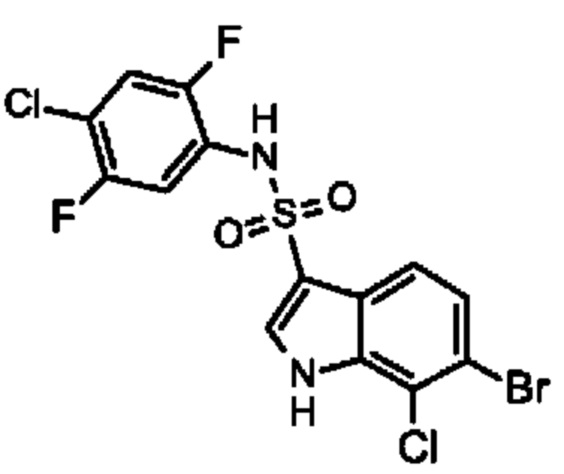
ЖХМС в щелочной среде, методика 2 (ЭР+): 455 (М+Н)+, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 7,36-7,40 (m, 1Н) 7,53-7,58 (m, 2Н) 7,69 (d, J=8,8 Гц, 1Н) 8,09 (d, J=3,2 Гц, 1Н) 10,57 (s, 1Н), 12,69 (brs, 1Н).
6-Хлор-N-(3,6-дифтор-5-метилпиридин-2-ил)-1Н-индол-3-сульфонамид I-348
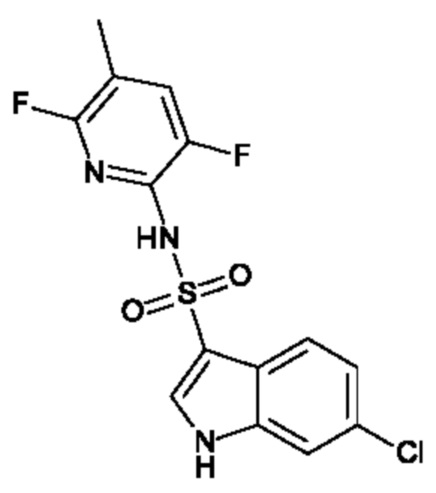
ЖХМС в щелочной среде, методика 2 (ЭР+): 358 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 2,08 (s, 3Н) 7,22 (dd, J=8,56, 1,71 Гц, 1Н) 7,53 (d, J=1,96 Гц, 1H) 7,72 (t, J=8,80 Гц, 1H) 7,84 (d, J=8,31 Гц, 1H) 8,08 (d, J=2,93 Гц, 1H) 10,98 (s, 1H) 12,13 (brs, 1H).
N-(5-Бром-6-фтор-3-метоксипиридин-2-ил)-6-хлор-1Н-индол-3-сульфонамид I-349
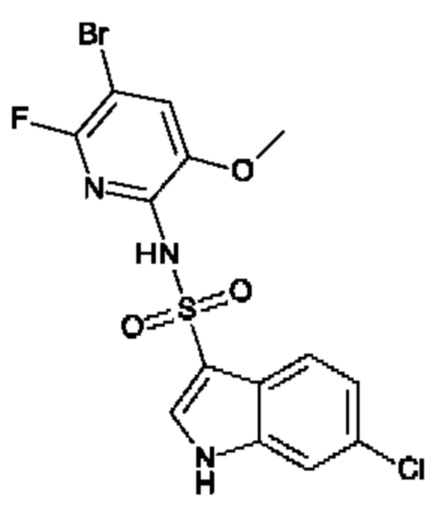
ЖХМС в щелочной среде, методика 2 (ЭР+): 434 (М+Н)+, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,78 (s, 3Н) 7,22 (d, J=8,8 Гц, 1Н) 7,53 (s, 1H) 7,73 (d, J=7,2 Гц, 1H) 7,94 (d, J=8,8 Гц, 1H) 8,11 (d, J=3,2 Гц, 1H) 10,65 (s, 1H), 12,13 (brs, 1H).
6-Хлор-N-[5-(цианометил)-6-фтор-3-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид I-350
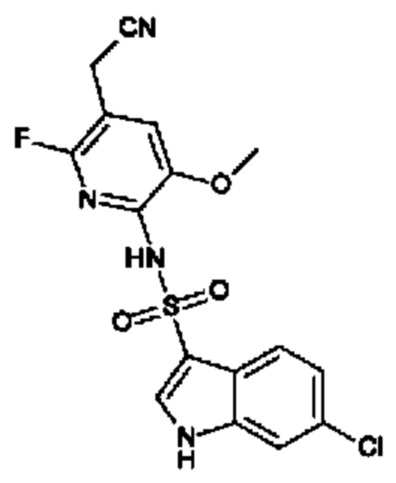
ЖХМС в щелочной среде, методика 2 (ЭР+): 395 (М+Н)+, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,76 (s, 3Н) 3,87 (s, 2Н) 7,21 (dd, J=8,80 Гц, 0,80 Гц, 1Н) 7,47 (d, J=8,40 Гц, 1Н) 7,52 (d, J=0,80 Гц, 1Н) 7,95 (d, J=8,80 Гц, 1Н) 8,10 (d, J=2,80 Гц, 1Н) 10,55 (s, 1Н), 12,12 (brs, 1Н).
N-[5-(Цианометил)-3-фтор-6-метоксипиридин-2-ил]-6-нитро-1Н-индол-3-сульфонамид I-351
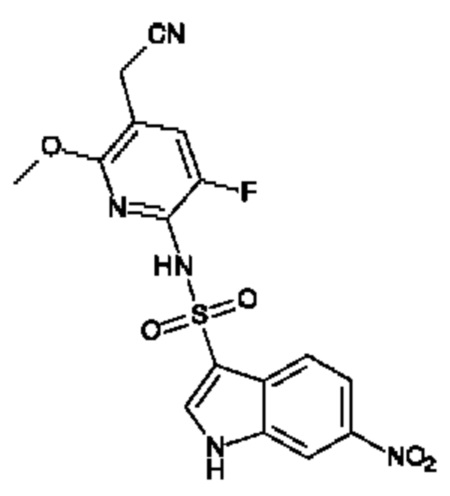
ЖХМС в щелочной среде, методика 2 (ЭР+): 406 (М+Н)+, чистота 88%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,60 (s, 3Н) 3,70 (s, 2Н) 7,64 (d, J=9,78 Гц, 1Н) 8,02-8,06 (m, 1H) 8,07-8,11 (m, 1H) 8,42 (d, J=1,96 Гц, 1H) 8,50 (s, 1H) 11,20 (s, 1H) 12,62 (brs, 1H).
6-Хлор-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-7-фтор-1Н-индол-3-сульфонамид I-354
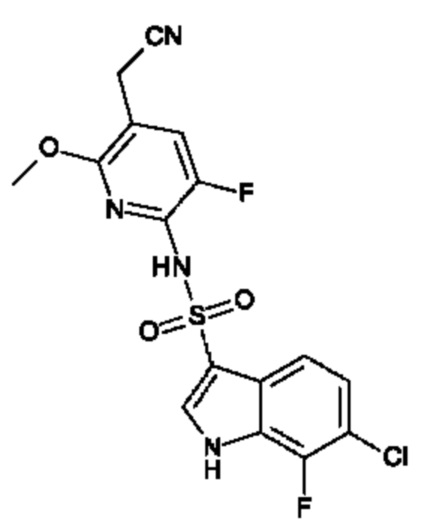
ЖХМС в щелочной среде, методика 2 (ЭР+): 413 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,56 (s, 3Н) 3,61 (s, 2Н) 7,23-7,27 (m, 1Н) 7,55 (d, J=9,84 Гц, 1Н) 7,59 (d, J=8,86 Гц, 1Н) 8,12 (s, 1Н) 11,13 (br s, 1Н) 12,85 (br s, 1Н)
6-Хлор-N-(3,6-дифтор-5-метилпиридин-2-ил)-7-фтор-1Н-индол-3-сульфонамид I-355
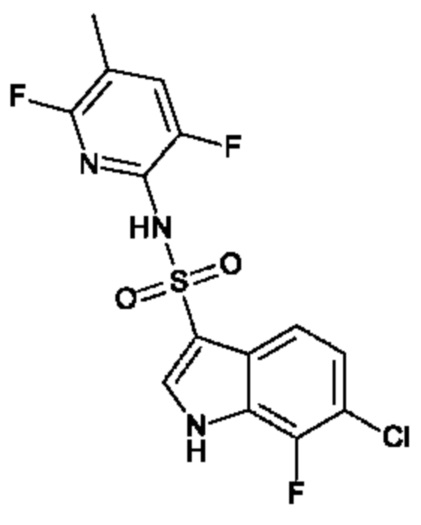
ЖХМС в щелочной среде, методика 2 (ЭР+): 376 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 2,09 (s, 3Н) 7,32 (dd, J=8,56, 6,60 Гц, 1Н) 7,67 (d, J=8,80 Гц, 1Н) 7,71-7,77 (m, 1Н) 8,13 (s, 1Н) 11,07 (br s, 1Н) 12,87 (br s, 1Н)
7-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-6-метокси-1Н-индол-3-сульфонамид I-356
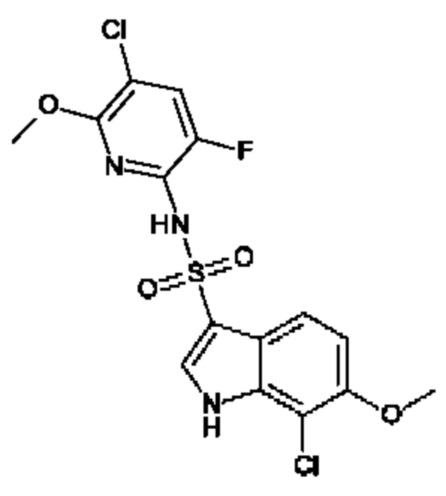
ЖХМС в щелочной среде, методика 2 (ЭР-): 418 (М-Н)-, чистота 96%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,62 (s, 3Н) 3,85 (s, 3Н) 7,09 (d, J=8,80 Гц, 1Н) 7,73 (d, J=8,80 Гц, 1Н) 7,88 (d, J=9,29 Гц, 1Н) 7,95 (s, 1Н) 11,12 (br s, 1Н) 12,14 (br s, 1H)
7-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-6-фтор-1Н-индол-3-сульфонамид I-357
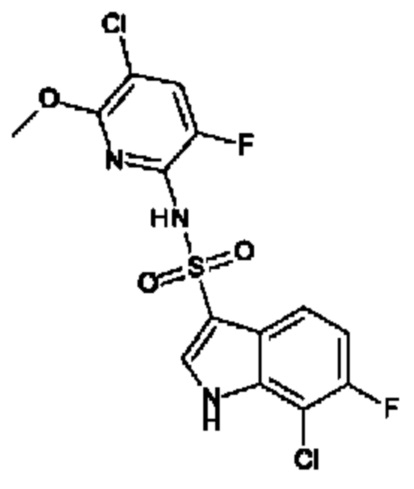
ЖХМС в щелочной среде, методика 2 (ЭР-): 406 (М-Н)-, чистота 95%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,61 (s, 3Н) 7,25 (t, J=9,54 Гц, 1Н) 7,79 (dd, J=8,80, 4,40 Гц, 1Н) 7,91 (d, J=8,80 Гц, 1Н) 8,13 (d, J=2,45 Гц, 1Н) 11,13 (br s, 1Н) 12,61 (br s, 1H)
6-Хлор-N-(3,5-дифтор-6-метоксипиридин-2-ил)-7-фтор-1Н-индол-3-сульфонамид I-358
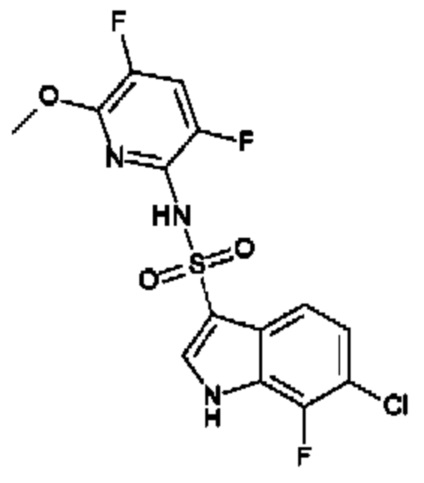
ЖХМС в щелочной среде, методика 2 (ЭР-): 390 (М-Н)-, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,58 (s, 3Н) 7,30 (t, J=7,34 Гц, 1Н) 7,61 (d, J=8,31 Гц, 1Н) 7,90 (t, J=9,29 Гц, 1Н) 8,16 (s, 1Н) 10,84 (s, 1Н) 12,82 (br s, 1Н)
N-[4-(Цианометокси)-2,5-дифторфенил]-1Н-пирроло[3,2-h]хинолин-3-сульфонамид I-360
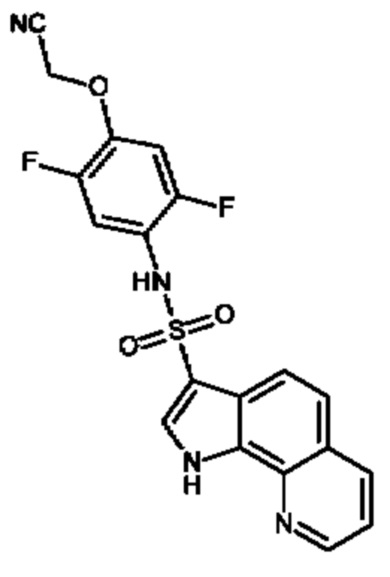
ЖХМС в нейтральной среде, методика 3 (ЭР+): 415 (М+Н)+, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 13,19 (s, 1Н), 10,09 (s, 1Н), 8,91 (d, J=3,0 Гц, 1Н), 8,42 (dd, J=8,5, 1,7 Гц, 1Н), 7,89-7,82 (m, 2H), 7,66 (d, J=8,7 Гц, 1Н), 7,57 (dd, J=8,2, 4,3 Гц, 1H), 7,22 (td, J=11,6, 7,3 Гц, 2H), 5,16 (s, 2H).
N-[4-(Цианометил)-2,5-дифторфенил]-1Н-пирроло[3,2-h]хинолин-3-сульфонамид I-361
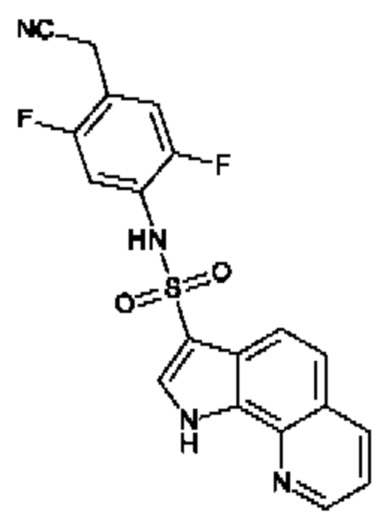
ЖХМС в нейтральной среде, методика 3 (ЭР+): 399 (М+Н)+, чистота 96%.
1Н ЯМР (400 МГц, DMSO-d6) δ 13,24 (s, 1Н), 10,49 (s, 1Н), 8,91 (dd, J=4,3, 1,7 Гц, 1Н), 8,43 (dd, J=8,2, 1,7 Гц, 1Н), 8,02-7,95 (m, 2H), 7,69 (d, J=8,7 Гц, 1H), 7,57 (dd, J=8,2, 4,3 Гц, 1H), 7,30 (dd, J=10,8, 6,5 Гц, 1H), 7,20 (dd, J=10,4, 6,7 Гц, 1H), 3,91 (s, 2H).
N-[4-(2-Цианоэтил)-2,5-дифторфенил]-1Н-пирроло[3,2-h]хинолин-3-сульфонамид I-362
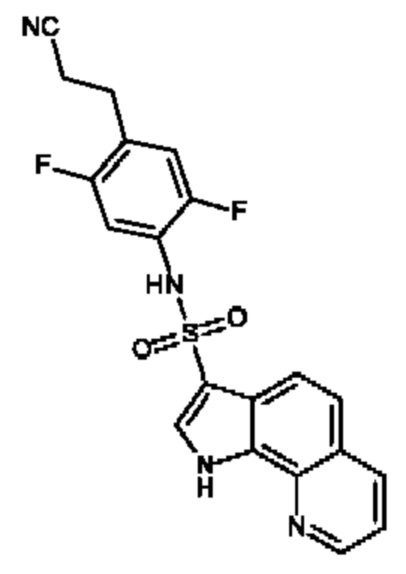
ЖХМС в нейтральной среде, методика 3 (ЭР+): 413 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 13,22 (s, 1Н), 10,33 (s, 1Н), 8,91 (dd, J=4,3, 1,6 Гц, 1Н), 8,43 (dd, J=8,2, 1,7 Гц, 1Н), 7,95 (s, 1H), 7,92 (d, J=8,7 Гц, 1H), 7,67 (d, J=8,7 Гц, 1H), 7,57 (dd, J=8,2, 4,3 Гц, 1H), 7,17 (ddd, J=17,9, 10,7, 6,6 Гц, 2H), 2,79 (t, J=7,2 Гц, 2H), 2,76-2,71 (m, 2H).
6-Хлор-N-[3,6-дифтор-5-(2-фторэтокси)пиридин-2-ил]-1Н-индол-3-сульфонамид I-364
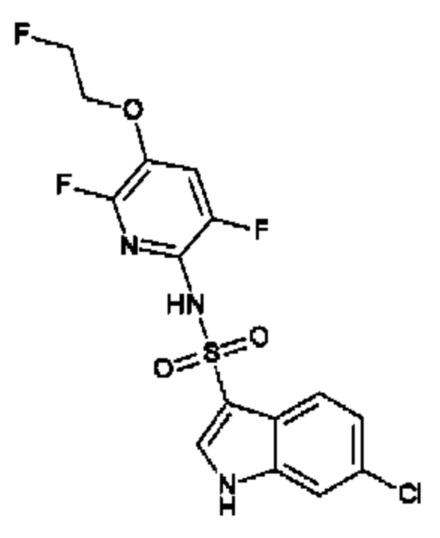
ЖХМС в щелочной среде, методика 2 (ЭР+): 406 (М+Н)+, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 4,24-4,29 (m, 1Н) 4,31-4,36 (m, 1H) 4,60-4,65 (m, 1H) 4,72-4,77 (m, 1H) 7,18 (dd, J=8,61, 1,72 Гц, 1H) 7,51 (d, J=1,48 Гц, 1H) 7,70 (d, J=8,86 Гц, 1H) 7,78 (dd, J=9,84, 8,37 Гц, 1H) 7,95 (d, J=2,95 Гц, 1H) 10,49 (s, 1H) 12,06 (brs, 1H).
6-Хлор-N-[3,6-дифтор-5-(2-метоксиэтокси)пиридин-2-ил]-1Н-индол-3-сульфонамид I-365
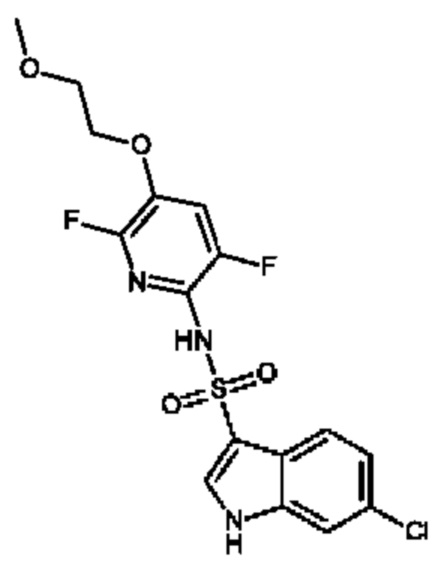
ЖХМС в щелочной среде, методика 2 (ЭР+): 418 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,24 (s, 3Н) 3,58-3,60 (m, 2Н) 4,12-4,17 (m, 2Н) 7,17 (dd, J=8,31, 1,96 Гц, 1Н) 7,50 (d, J=1,96 Гц, 1H) 7,68 (d, J=8,80 Гц, 1H) 7,71-7,77 (m, 1H) 7,93 (d, J=2,45 Гц, 1H) 10,41 (brs, 1H) 12,05 (brs, 1H).
6-Хлор-7-(дифторметокси)-N-(3,5-дифтор-6-метоксипиридин-2-ил)-1Н-индол-3-сульфонамид I-366
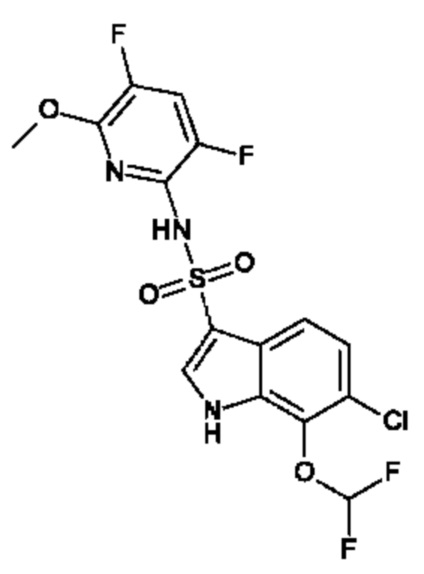
ЖХМС в щелочной среде, методика 2 (ЭР+): 440 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 3,55 (s, 3Н) 7,21 (t, J=73,2 Гц, 1Н) 7,35 (d, J=9,20 Гц, 1H) 7,73 (d, J=8,40 Гц, 1H) 7,90 (t, J=8,80 Гц, 1H) 8,09 (s, 1H) 10,81 (s, 1H), 12,52 (brs, 1H).
6-Хлор-N-(3,6-дифтор-5-метилпиридин-2-ил)-7-(трифторметил)-1Н-индол-3-сульфонамид I-367
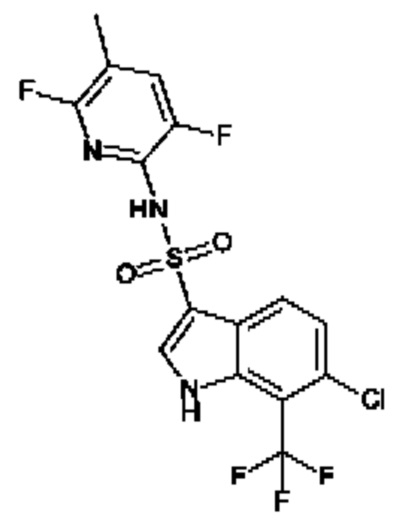
ЖХМС в щелочной среде, методика 2 (ЭР+): 426 (М+Н)+, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 2,09 (s, 3Н) 7,53 (d, J=8,40 Гц, 1Н) 7,69-8,02 (m, 1H) 8,07 (s, 1H) 8,16 (d, J=8,40 Гц, 1H) 11,15 (brs, 1H) 12,25 (brs, 1H).
D.5. Методика F. Синтез N-(2,1,3-бензоксадиазол-5-ил)-6-хлор-1Н-индол-3-сульфонамида I-201
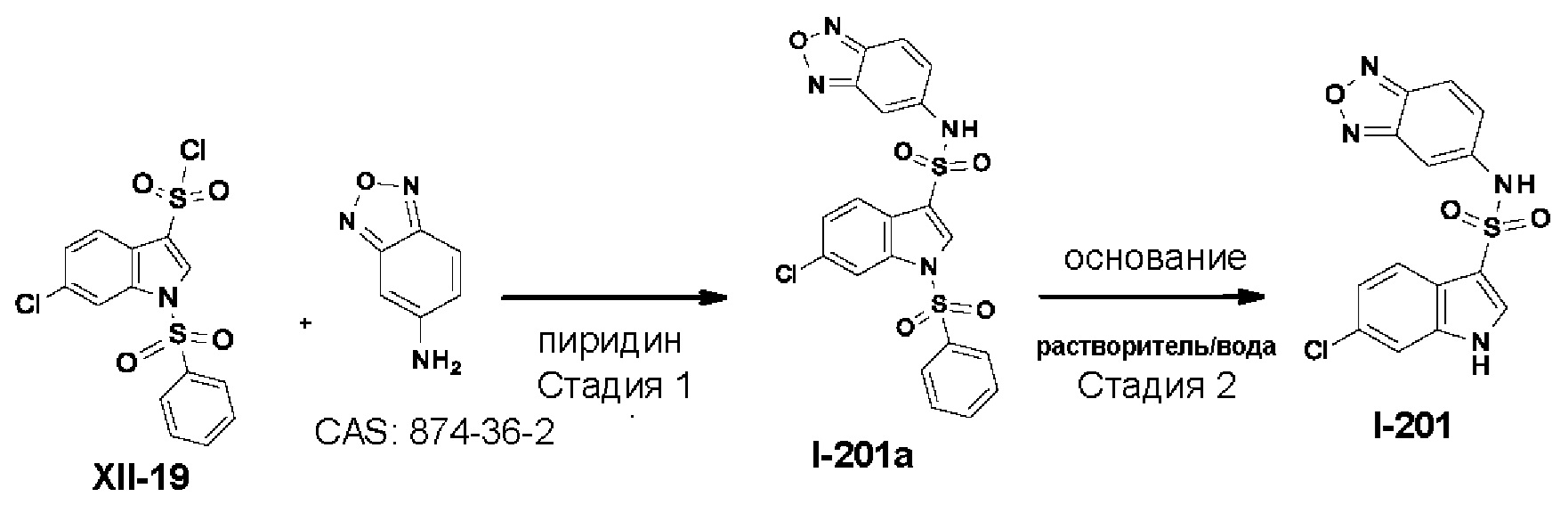
Стадия 1: Синтез 1-(бензолсульфонил)-N-(2,1,3-бензоксадиазол-5-ил)-6-хлориндол-3-сульфонамида I-201а
В герметизированном сосуде в атмосфере аргона 1-(бензолсульфонил)-6-хлориндол-3-сульфонилхлорид XII-19 (192 мг, 0,49 ммоля) растворяли в пиридине (4 мл). Добавляли 2,1,3-бензоксадиазол-5-амин (135 мг, 1 ммоль) и перемешивали при комнатной температуре в течение ночи. Реакционную смесь выпаривали досуха, затем остаток переносили в DCM. Органическую фазу промывали 1 н. раствором HCl и рассолом, сушили над MgSO4 и выпаривали. Оставшееся темное масло затвердевало при выдерживании и затем его растирали со смесью ACN/вода (8/2), обрабатывали ультразвуком и фильтровали, промывали водой и сушили в вакууме и получали 170 мг 1-(бензолсульфонил)-N-(2,1,3-бензоксадиазол-5-ил)-6-хлориндол-3-сульфонамида I-201а в виде желтого твердого вещества.
Выход: 71%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 487 (М-Н)-, чистота 100%.
1Н ЯМР (400 МГц, DMSO-d6) δ 11,52 (s, 1Н), 8,99 (s, 1Н), 8,16-8,10 (m, 2H), 7,98 (d, J=1,8 Гц, 1H), 7,91 (dd, J=9,1, 3,2 Гц, 2H), 7,63 (t, J=7,5 Гц, 1H), 7,56-7,51 (m, 2H), 7,43-7,36 (m, 2H), 7,25 (dd, J=9,6, 1,9 Гц, 1H).
Стадия 2: Синтез N-(2,1,3-бензоксадиазол-5-ил)-6-хлор-1Н-индол-3-сульфонамида I-201
В герметизированной пробирке 1-(бензолсульфонил)-N-(2,1,3-бензоксадиазол-5-ил)-6-хлориндол-3-сульфонамид I-201а (170 мг, 0,34 ммоля) суспендировали в метаноле (4 мл). Добавляли воду (1 мл), затем карбонат калия (200 мг, 1,45 ммоля) и перемешивали при комнатной температуре в течение ночи. Реакционную смесь выпаривали досуха. Остаток растворяли в EtOAc и промывали 1 н. раствором HCl и водой, сушили над MgSO4 и выпаривали. Остаток очищали на диоксиде кремния при элюировании смесью гептан/EtOAc (1/1). После выпаривания получали 170 мг N-(2,1,3-бензоксадиазол-5-ил)-6-хлор-1Н-индол-3-сульфонамида I-201 в виде ярко-желтого твердого вещества.
Выход: 88%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 347 (М-Н)-, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,27 (s, 1Н), 11,22 (s, 1Н), 8,41 (d, J=2,8 Гц, 1Н), 7,94 (d, J=9,5 Гц, 1Н), 7,87 (d, J=8,6 Гц, 1H), 7,54 (d, J=1,8 Гц, 1H), 7,38 (d, J=1,7 Гц, 1H), 7,34 (dd, J=9,5, 1,9 Гц, 1H), 7,29 (dd, J=8,6, 1,9 Гц, 1H).
Соединения, приведенные ниже в таблице 7, можно синтезировать по методикам, аналогичным методике F.
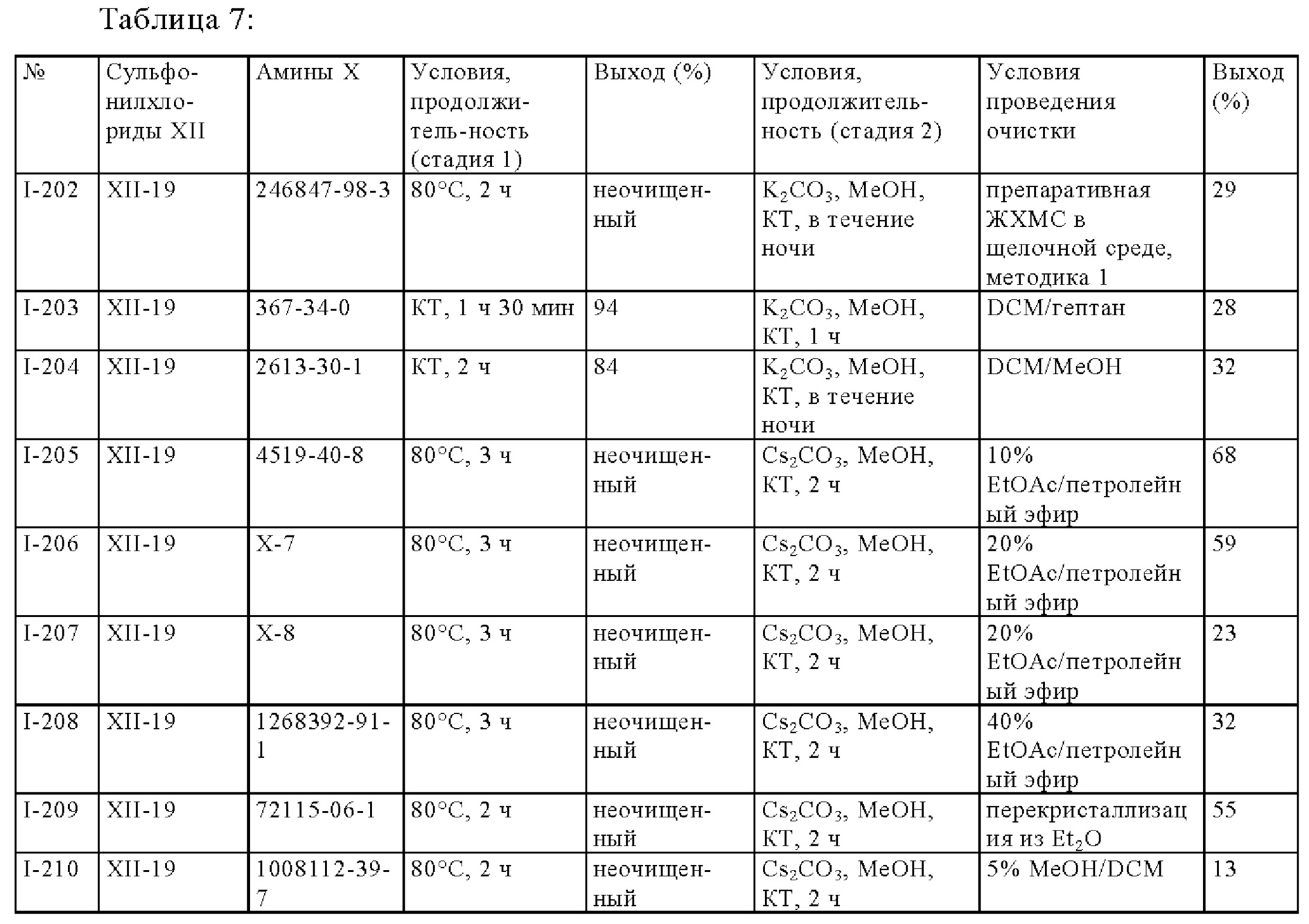
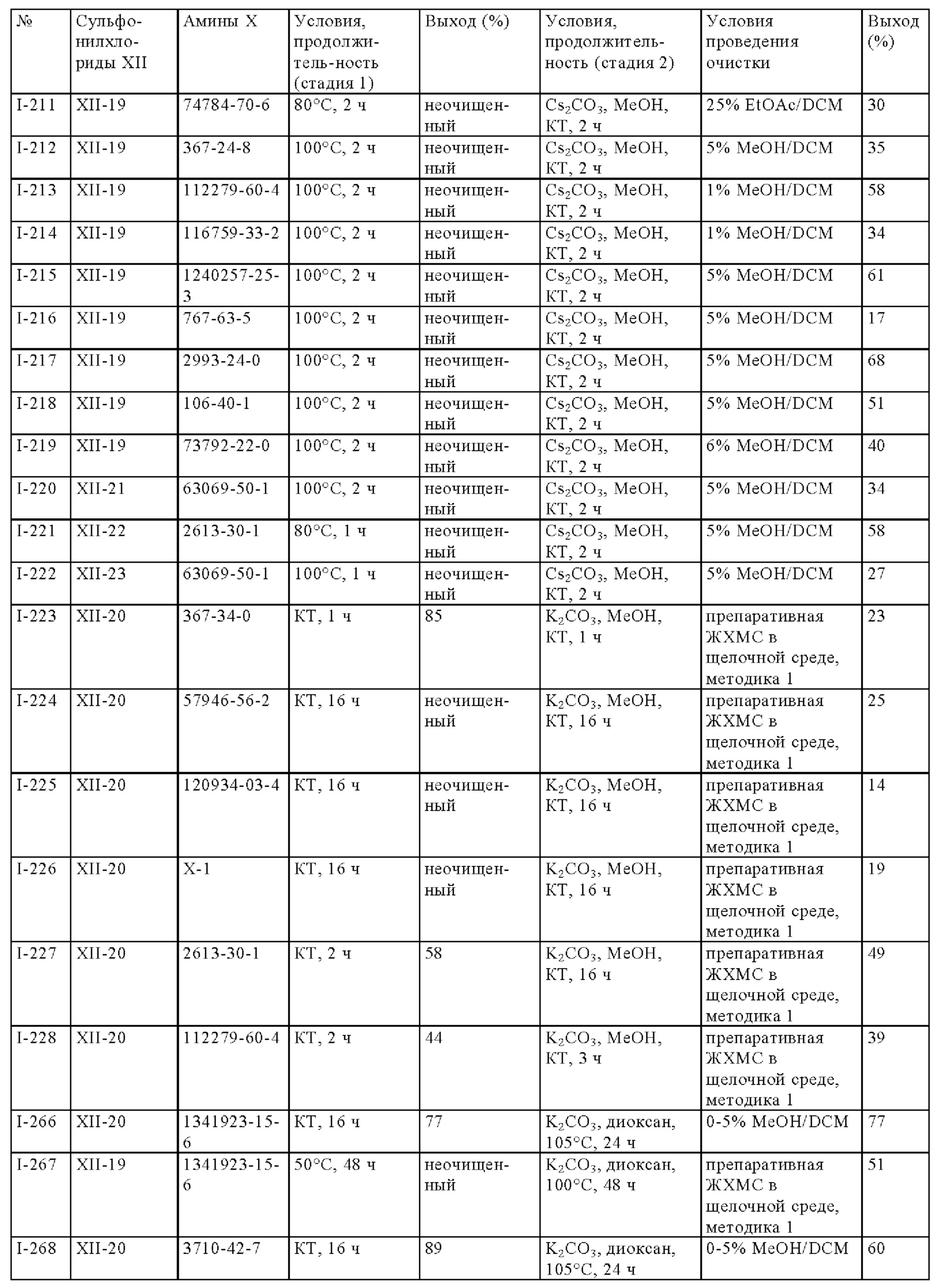
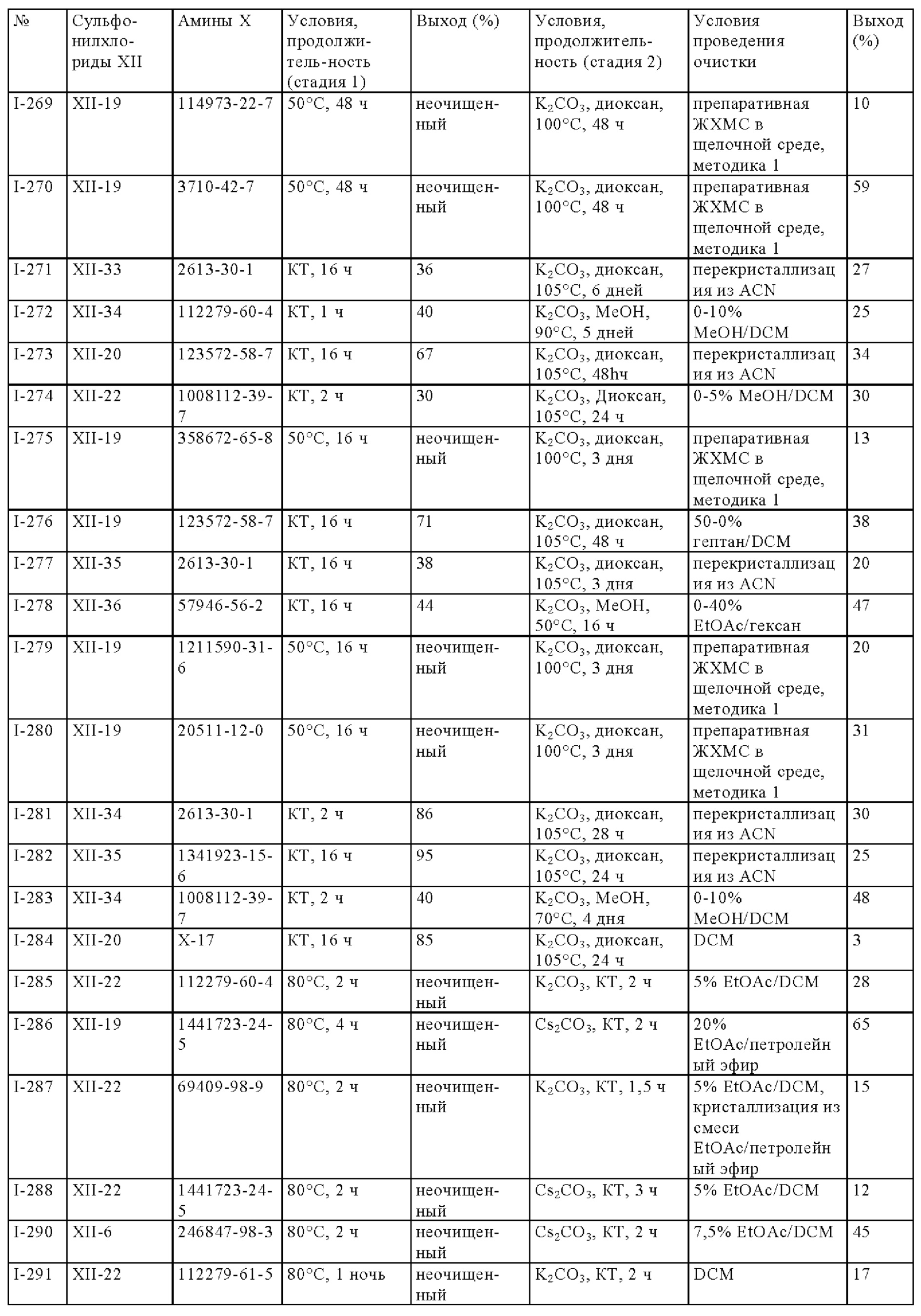
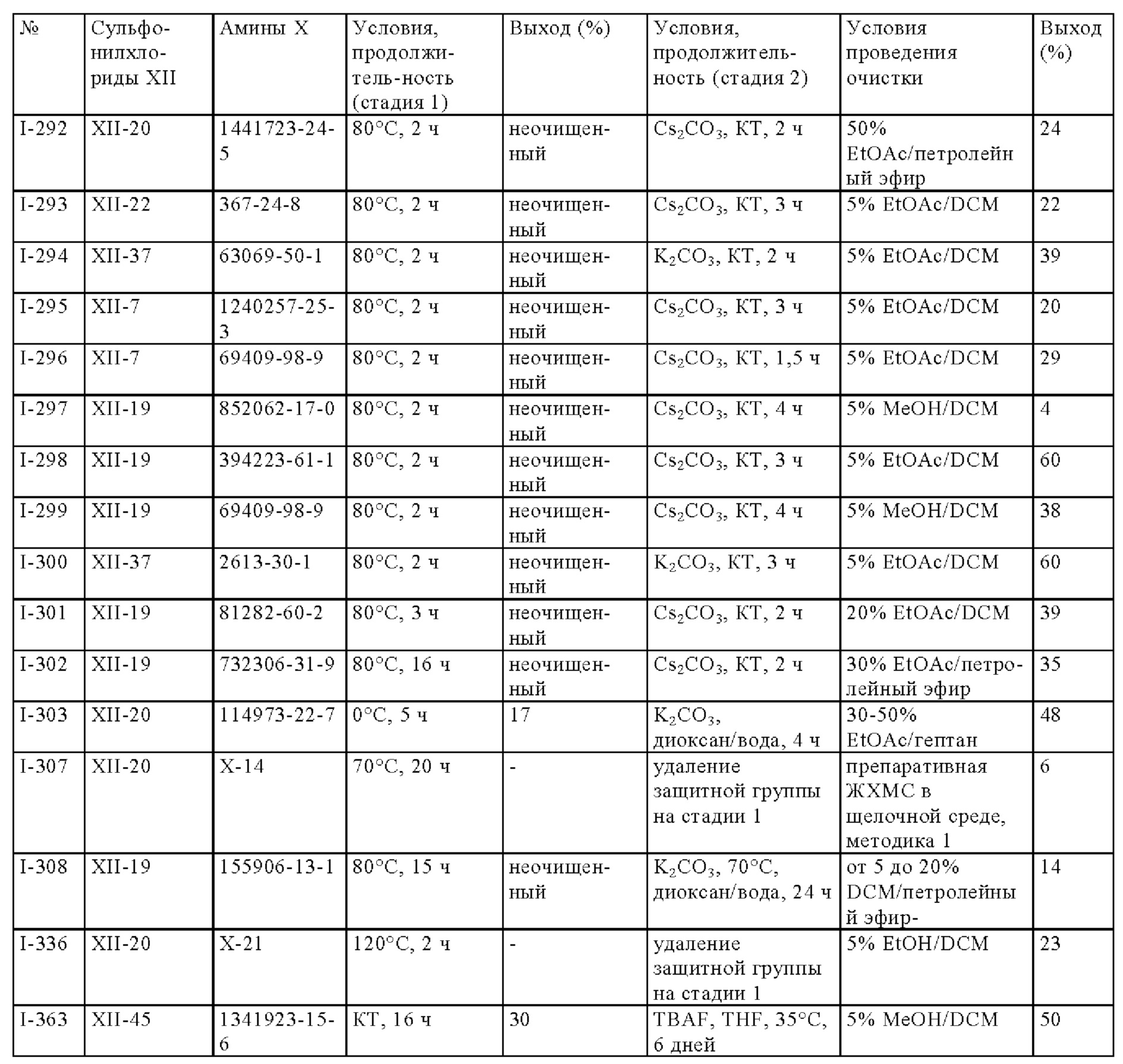
6-Хлор-N-(5-хлор-3-фторпиридин-2-ил)-1Н-индол-3-сульфонамид I-202
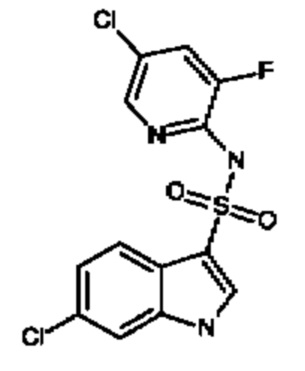
ЖХМС в щелочной среде, методика 1 (ЭР+): 360 (М+Н)+, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,25 (s, 1Н), 11,07 (s, 1Н), 8,08 (d, J=3,5 Гц, 2H), 7,95 (d, J=10,1 Гц, 1H), 7,87 (d, J=8,6 Гц, 1H), 7,55 (s, 1H), 7,23 (m, 1H).
6-Хлор-N-(2,4,5-трифторфенил)-1Н-индол-3-сульфонамид I-203
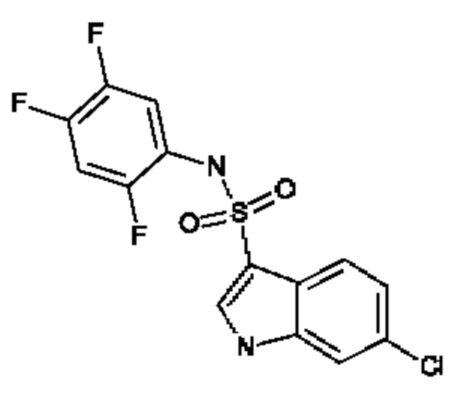
ЖХМС в щелочной среде, методика 1 (ЭР+): 361,2 (М+Н)+, чистота 100%.
1Н ЯМР (400 МГц, DMSO-d6) δ 11,29 (s, 1Н), 7,78 (d, J=8,5 Гц, 1Н), 7,57 (d, J=1,9 Гц, 1Н), 7,37 (d, J=1,9 Гц, 1H), 7,14-7,00 (m, 2H), 6,94 (td, J=11,1, 8,1 Гц, 1H).
6-Хлор-N-(4-хлор-2,5-дифторфенил)-1Н-индол-3-сульфонамид I-204
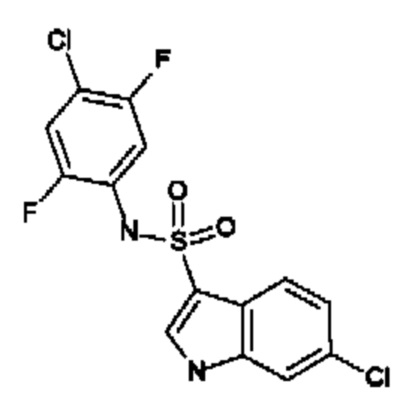
ЖХМС в щелочной среде, методика 1 (ЭР-): 375,2 (М-Н)-, чистота 100%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,13 (s, 1Н), 10,46 (s, 1Н), 8,04 (d, J=2,8 Гц, 1Н), 7,78 (d, J=8,6 Гц, 1H), 7,59-7,47 (m, 2H), 7,34 (dd, J=10,4, 7,0 Гц, 1H), 7,23 (dd, J=8,6, 1,9 Гц, 1H).
6-Хлор-N-(2,3-дифторфенил)-1Н-индол-3-сульфонамид I-205
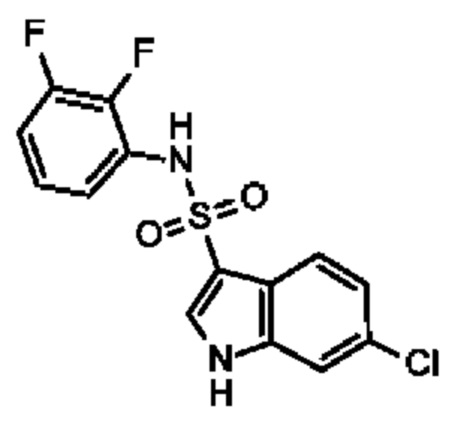
ЖХМС в нейтральной среде, методика 3 (ЭР+): 343,2 (М+Н)+, чистота 97%.
1Н ЯМР (500 МГц, DMSO-d6) δ 12,08 (s, 1Н), 10,24 (s, 1Н), 7,94 (s, 1Н), 7,72 (d, J=8,6 Гц, 1Н), 7,53 (s, 1H), 7,21 (d, J=8,6 Гц, 1H), 7,01-7,17 (m, 3H).
6-Хлор-N-[4-(цианометил)-2-фторфенил]-1Н-индол-3-сульфонамид I-206
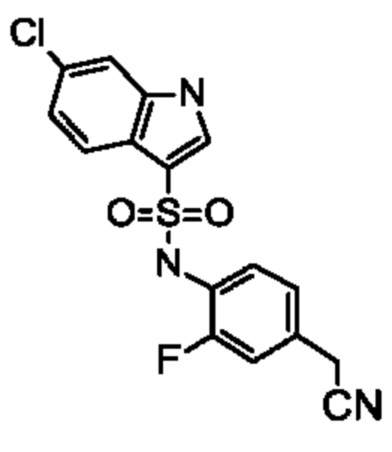
ЖХМС в нейтральной среде, методика 3 (ЭР+): 364,1 (М+Н)+, чистота 98%.
1Н ЯМР (600 МГц, DMSO-d6) δ 12,04 (s, 1Н), 10,04 (s, 1Н), 7,90 (s, 1Н), 7,73 (d, J=8,6 Гц, 1H), 7,52 (s, 1H), 7,32 (s, 1H), 7,19 (d, J=8,6 Гц, 1H), 7,07 (d, J=7,0 Гц, 2H), 3,95 (s, 2H).
6-Хлор-N-[4-(1-цианоэтил)-2-фторфенил]-1Н-индол-3-сульфонамид I-207
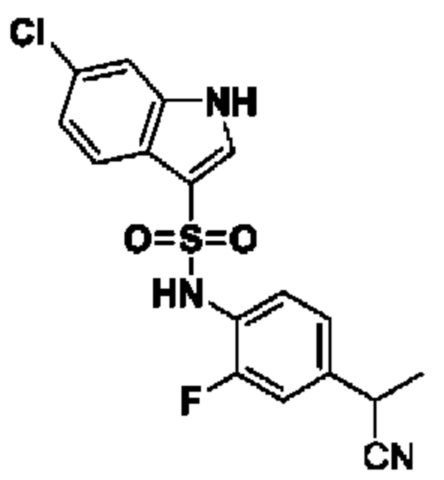
ЖХМС в нейтральной среде, методика 3 (ЭР+): 378,2 (М+Н)+, чистота 94%.
1Н ЯМР (500 МГц, DMSO-d6) δ 10,12 (s, 1Н), 8,01 (s, 1Н), 7,70-7,71 (m, 2H), 7,34-7,36 (m, 1H), 7,09-7,25 (m, 3H), 4,23 (q, J=7,2 Гц, 1H), 1,48 (d, J=7,2 Гц, 3Н).
6-Хлор-N-(4-хлор-5-фтор-2-метоксифенил)-1Н-индол-3-сульфонамид I-208
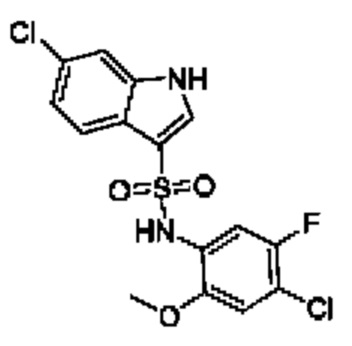
ЖХМС в нейтральной среде, методика 3 (ЭР+): 389,2 (М+Н)+, чистота 95%.
1Н ЯМР (600 МГц, DMSO-d6) δ 12,03 (s, 1Н), 9,63 (s, 1Н), 7,95 (s, 1H), 7,80 (d, J=8,6 Гц, 1H), 7,50 (d, J=1,9 Гц, 1H), 7,34-7,16 (m, 2H), 7,03 (d, J=6,9 Гц, 1H), 3,39 (s, 3H).
6-Хлор-N-(4-циано-3-метилфенил)-1Н-индол-3-сульфонамид I-209
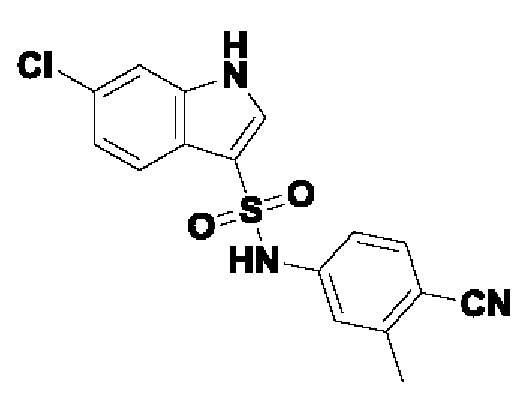
ЖХМС в нейтральной среде, методика 3 (ЭР+): 346 (М+Н)+, чистота 95%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 12,16 (s, 1Н), 10,87 (s, 1Н), 8,20 (s, 1Н), 7,82 (d, J=8,5 Гц, 1Н), 7,68-7,41 (m, 2H), 7,24 (dd, J=8,6, 2,0 Гц, 1H), 7,10 (d, J=2,1 Гц, 1H), 7,06 (dd, J=8,5, 2,2 Гц, 1H), 2,33 (s, 3H).
6-Хлор-N-(4-этинил-2-фторфенил)-1Н-индол-3-сульфонамид I-210
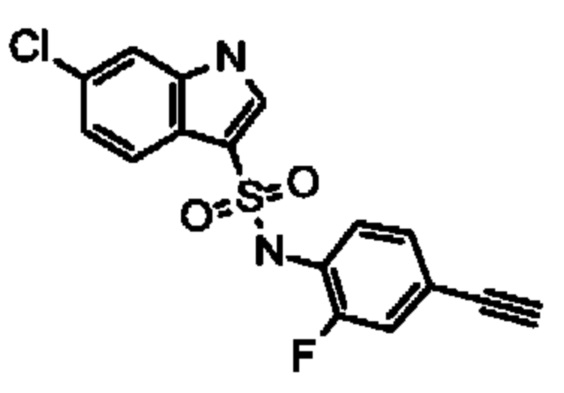
ЖХМС в нейтральной среде, методика 3 (ЭР+): 349 (М+Н)+, чистота 96%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,08 (s, 1Н), 10,25 (s, 1Н), 7,95 (s, 1H), 7,77 (d, J=8,5 Гц, 1H), 7,51 (s, 1H), 7,35-7,32 (m, 1H), 7,23-7,18 (m, 3H), 4,17 (s, 1H).
6-Хлор-N-[5-(трифторметил)пиридин-2-ил]-1Н-индол-3-сульфонамид I-211
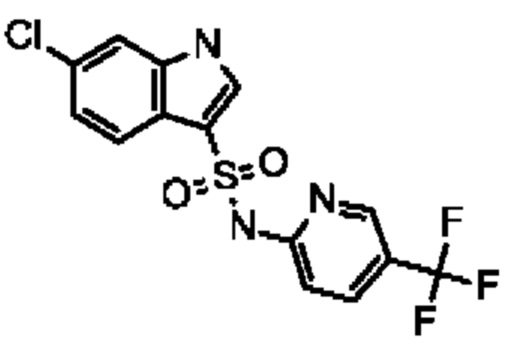
ЖХМС в нейтральной среде, методика 3 (ЭР+): 376,4 (М+Н)+, чистота 84%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,17 (s, 1Н), 11,62 (s, 1Н), 8,49 (d, J=2,6 Гц, 1Н), 8,20 (d, J=2,8 Гц, 1Н), 7,98 (dd, J=8,8, 2,5 Гц, 1Н), 7,88 (d, J=8,6 Гц, 1H), 7,51 (d, J=1,9 Гц, 1H), 7,24 (dd, J=8,7, 2,0 Гц, 1H), 7,22 (d, J=8,9 Гц, 1H).
N-(4-Бром-2-фторфенил)-6-хлор-1Н-индол-3-сульфонамид I-212
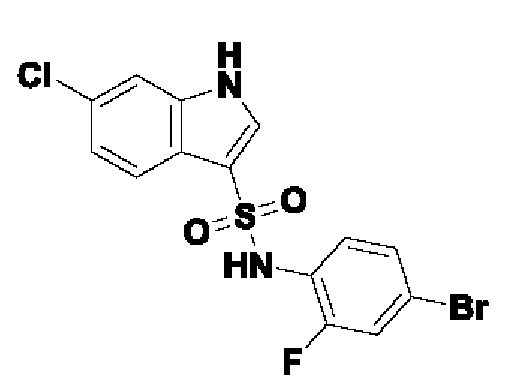
ЖХМС в нейтральной среде, методика 3 (ЭР+): 405 (М+Н)+, чистота 95%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 12,05 (s, 1Н), 10,08 (s, 1Н), 7,89 (d, J=1,5 Гц, 1Н), 7,73 (d, J=8,6 Гц, 1Н), 7,51 (d, J=1,9 Гц, 1Н), 7,41 (dd, J=10,0, 2,2 Гц, 1Н), 7,31-7,26 (m, 1H), 7,23 (t, J=8,5 Гц, 1H), 7,19 (dd, J=8,6, 1,9 Гц, 1H).
N-(4-Бром-2,5-дифторфенил)-6-хлор-1Н-индол-3-сульфонамид I-213
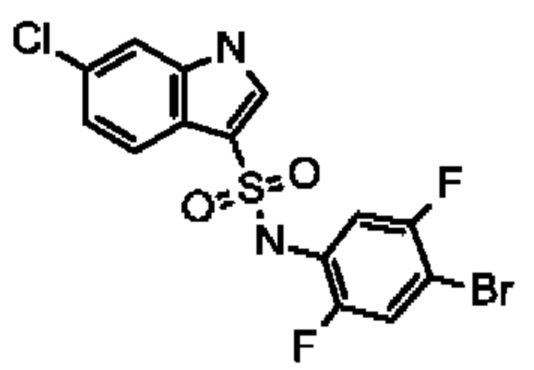
ЖХМС в нейтральной среде, методика 3 (ЭР+): 402,9 (М+Н)+, чистота 97%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 12,12 (s, 1Н), 10,45 (s, 1Н), 8,04 (d, J=2,9 Гц, 1Н), 7,78 (d, J=8,6 Гц, 1Н), 7,59 (dd, J=9,6, 6,4 Гц, 1Н), 7,52 (d, J=1,9 Гц, 1H), 7,30 (dd, J=9,9, 6,8 Гц, 1H), 7,22 (dd, J=8,6, 1,9 Гц, 1H).
6-Хлор-N-(4-хлор-2-фтор-5-метилфенил)-1Н-индол-3-сульфонамид I-214
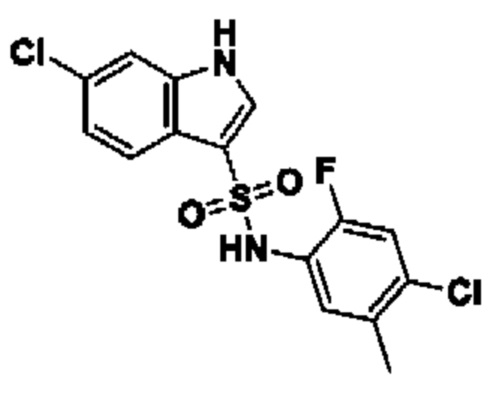
ЖХМС в нейтральной среде, методика 3 (ЭР+): 472,9 (М+Н)+, чистота 98%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 12,03 (s, 1Н), 10,00 (s, 1Н), 7,91 (s, 1Н), 7,73 (d, J=8,6 Гц, 1Н), 7,51 (d, J=1,9 Гц, 1Н), 7,26 (t, J=9,4 Гц, 2H), 7,19 (dd, J=8,6, 1,9 Гц, 1H), 3,29 (s, 3H).
6-Хлор-N-[2-фтор-4-(пентафтор-лямбда~6~-сульфанил)фенил]-1Н-индол-3-сульфонамид
I-215
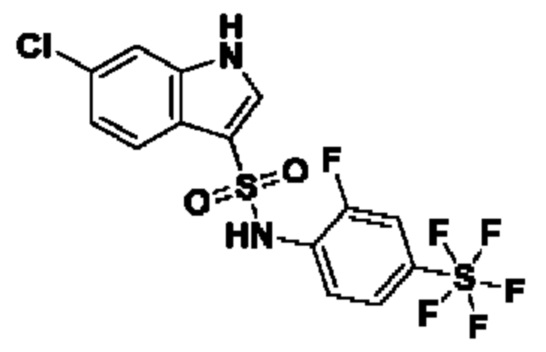
ЖХМС в нейтральной среде, методика 3 (ЭР-): 448,9 (М-Н)-, чистота 96%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 12,16 (s, 1Н), 10,72 (s, 1Н), 8,08 (d, J=3,0 Гц, 1Н), 7,81 (d, J=8,6 Гц, 1Н), 7,80 (dd, J=2,5, 15 Гц, 1Н), 7,64 (dd, J=9,1, 2,5 Гц, 1Н), 7,62-7,57 (m, 1Н), 7,52 (d, J=1,7 Гц, 1Н), 7,22 (dd, J=8,6, 1,9 Гц, 1H).
N-(2,1,3-Бензоксадиазол-4-ил)-6-хлор-1Н-индол-3-сульфонамид I-216
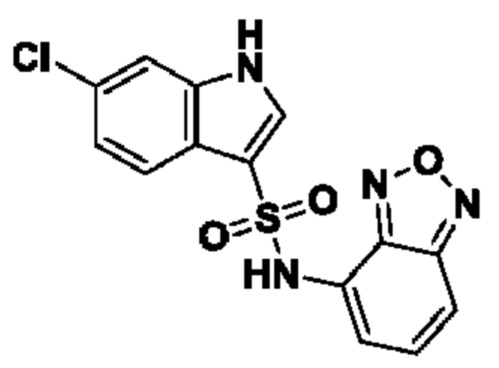
ЖХМС в нейтральной среде, методика 3 (ЭР+): 348,9 (М+Н)+, чистота 95%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,17 (d, J=3,2 Гц, 1Н), 11,28 (s, 1Н), 8,17 (d, J=3,0 Гц, 1H), 7,88 (d, J=8,6 Гц, 1H), 7,59 (d, J=9,0 Гц, 1H), 7,49 (d, J=1,9 Гц, 1H), 7,45 (dd, J=9,0, 7,2 Гц, 1H), 7,24 (d, J=7,2 Гц, 1H), 7,20 (dd, J=8,6, 1,9 Гц, 1H).
6-Хлор-N-[4-(пентафтор-лямбда~6~-сульфанил)фенил]-1Н-индол-3-сульфонамид I-217
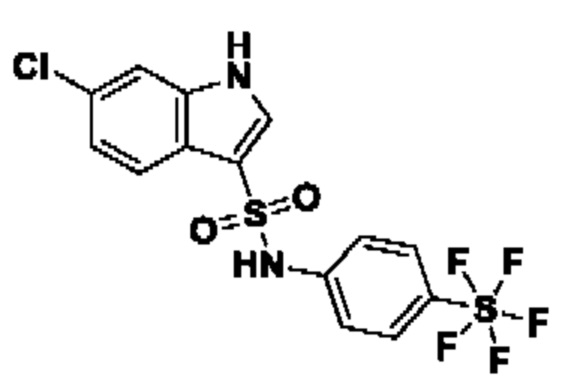
ЖХМС в нейтральной среде, методика 3 (ЭР-): 431 (М-Н)-, чистота 98%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 12,15 (s, 1Н), 10,90 (s, 1Н), 8,14 (s, 1H), 7,82 (d, J=8,6 Гц, 1H), 7,77-7,62 (m, 2H), 7,51 (d, J=1,9 Гц, 1H), 7,29-7,16 (m, 3H).
N-(4-Бромфенил)-6-хлор-1Н-индол-3-сульфонамид I-218
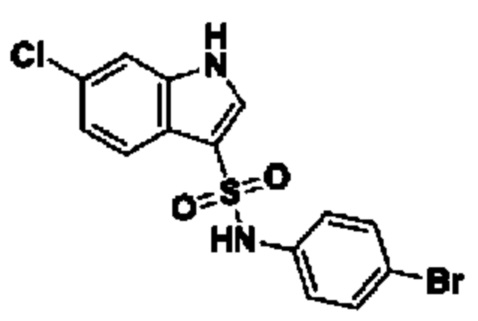
ЖХМС в нейтральной среде, методика 3 (ЭР-): 484,9 (М-Н)-, чистота 95%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,06 (s, 1Н), 10,35 (s, 1Н), 8,00 (s, 1Н), 7,79 (d, J=8,6 Гц, 1Н), 7,49 (d, J=1,9 Гц, 1Н), 7,37-7,30 (m, 2H), 7,21 (dd, J=8,6, 2,0 Гц, 1H), 7,06-6,98 (m, 2H).
N-(4-Ацетил-2-фторфенил)-6-хлор-1Н-индол-3-сульфонамид I-219

ЖХМС в нейтральной среде, методика 3 (ЭР-): 365 (М-Н)-, чистота 99%.
1Н ЯМР (500 МГц, DMSO-d6): δ 12,12 (s, 1Н), 10,58 (s, 1Н), 8,06 (d, J=2,2 Гц, 1Н), 7,84 (d, J=8,6 Гц, 1Н), 7,66 (dd, J=8,5, 2,0 Гц, 1H), 7,60 (dd, J=11,4, 1,9 Гц, 1H), 7,55-7,48 (m, 2H), 7,22 (dd, J=8,6, 1,9 Гц, 1H), 2,46 (s, 3H).
N-(4-Циано-2-фторфенил)-6-(циклопропилметокси)-1Н-индол-3-сульфонамид I-220
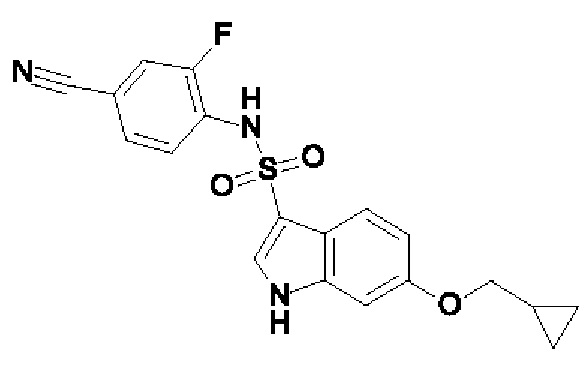
ЖХМС в нейтральной среде, методика 3 (ЭР+): 403 (М+NH4)+, чистота 96%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,81 (d, J=3,0 Гц, 1Н), 10,68 (s, 1Н), 7,91 (d, J=2,9 Гц, 1H), 7,71 (dd, J=10,7, 1,7 Гц, 1H), 7,67 (d, J=8,8 Гц, 1H), 7,61-7,46 (m, 2H), 6,90 (d, J=2,2 Гц, 1H), 6,83 (dd, J=8,8, 2,2 Гц, 1H), 3,80 (d, J=6,9 Гц, 2H), 1,32-1,14 (m, 1H), 0,68-0,51 (m, 2H), 0,37-0,15 (m, 2H).
N-(4-Хлор-2,5-дифторфенил)-6-метокси-1Н-индол-3-сульфонамид I-221
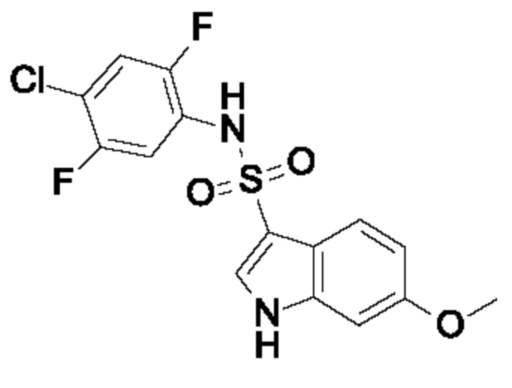
ЖХМС в нейтральной среде, методика 3 (ЭР+): 373 (М+Н)+, чистота 97%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,79 (s, 1Н), 10,35 (s, 1Н), 7,86 (d, J=2,9 Гц, 1Н), 7,64 (d, J=8,8 Гц, 1H), 7,50 (dd, J=9,9, 6,9 Гц, 1H), 7,32 (dd, J=10,5, 6,9 Гц, 1H), 6,93 (d, J=2,2 Гц, 1H), 6,82 (dd, J=8,8, 2,3 Гц, 1H), 3,76 (s, 3H).
N-(4-Циано-2-фторфенил)-6-(тетрагидрофуран-2-илметокси)-1Н-индол-3-сульфонамид I-222
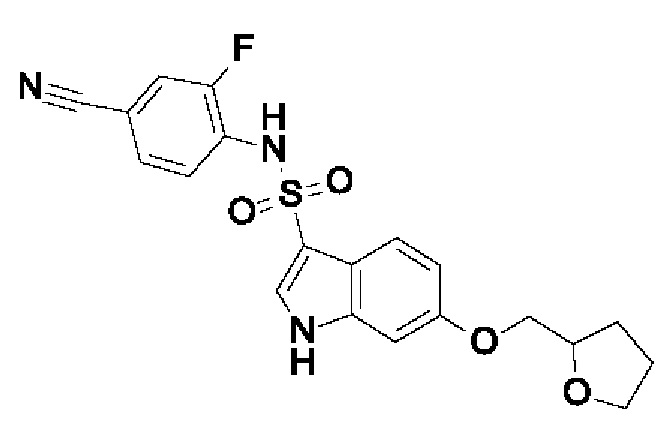
ЖХМС в нейтральной среде, методика 3 (ЭР+): 316 (М+Н)+, чистота 97%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,83 (s, 1Н), 10,68 (s, 1Н), 7,92 (d, J=3,0 Гц, 1Н), 7,71 (dd, J=10,7, 1,7 Гц, 1Н), 7,68 (d, J=8,8 Гц, 1Н), 7,60-7,46 (m, 2Н), 6,94 (d, J=2,3 Гц, 1Н), 6,83 (dd, J=8,8, 2,3 Гц, 1Н), 4,14 (qd, J=6,7, 4,2 Гц, 1Н), 3,92 (qd, J=10,1, 5,1 Гц, 2H), 3,78 (dt, J=8,2, 6,7 Гц, 1H), 3,66 (td, J=7,7, 6,2 Гц, 1H), 1,99 (dddd, J=12,2, 8,5, 7,2, 5,3 Гц, 1H), 1,92-1,74 (m, 2H), 1,67 (ddt, J=12,0, 8,6, 6,9 Гц, 1H).
6-Хлор-N-(2,4,5-трифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-223
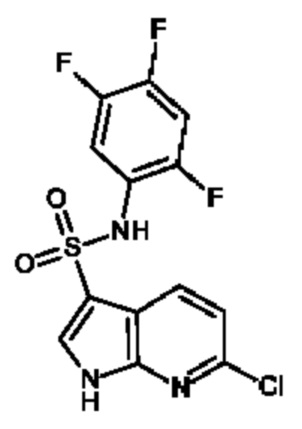
ЖХМС в щелочной среде, методика 1 (ЭР+): 362,2 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,83 (s, 1Н), 10,27 (s, 1Н), 8,19-7,98 (m, 2H), 7,47 (m, J=10,0 Гц, 1H), 7,37 (m, J=9,2 Гц, 2H).
6-Хлор-N-(4-хлор-2-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-224
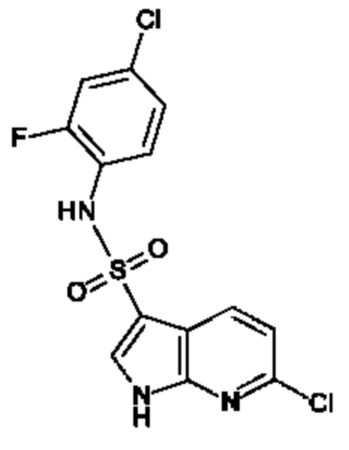
ЖХМС в щелочной среде, методика 1 (ЭР+): 360,2 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,80 (s, 1Н), 10,17 (s, 1Н), 8,12 (d, J=8,3 Гц, 1Н), 8,04 (s, 1Н), 7,34 (m, J=8,8 Гц, 2H), 7,28 (t, J=8,6 Гц, 1Н), 7,18 (d, J=8,6 Гц, 1Н).
6-Хлор-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-225
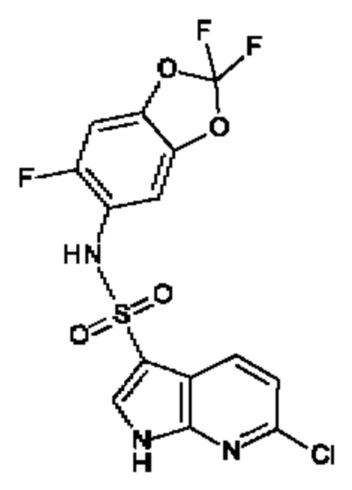
ЖХМС в щелочной среде, методика 1 (ЭР+): 406,2 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,78 (s, 1Н), 10,15 (s, 1Н), 8,10 (d, J=8,4 Гц, 1Н), 8,04 (s, 1Н), 7,43 (d, J=9,1 Гц, 1Н), 7,34 (m, J=7,3, 4,5 Гц, 2H).
6-Хлор-N-(7-фтор-2,1,3-бензотиадиазол-4-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-226
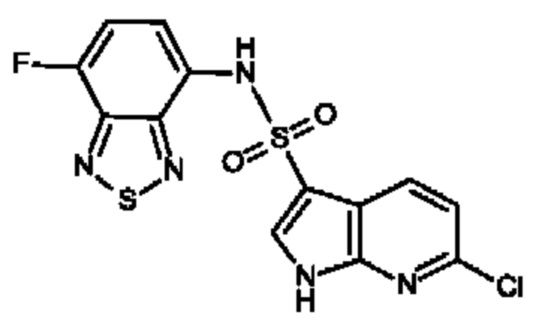
ЖХМС в щелочной среде, методика 1 (ЭР+): 384,2 (М+Н)+, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,78 (s, 1Н), 10,79 (s, 1Н), 8,22-8,12 (m, 2H), 7,51-7,39 (m, 2H), 7,29 (d, J=8,3 Гц, 1H).
6-Хлор-N-(4-хлор-2,5-дифторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-227
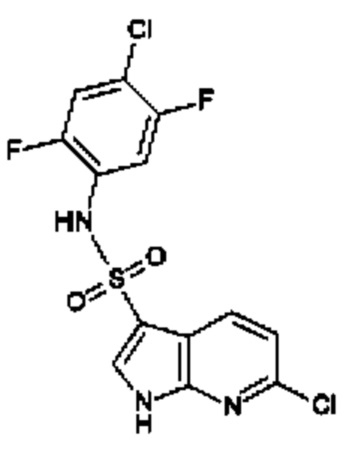
ЖХМС в щелочной среде, методика 1 (ЭР-): 376,2 (М-Н)-, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,87 (s, 1Н), 10,52 (s, 1Н), 8,26-8,12 (m, 2H), 7,55 (dd, J=9,9, 6,8 Гц, 1H), 7,37 (dd, J=9,5, 7,0 Гц, 2H).
N-(4-Бром-2,5-дифторфенил)-6-хлор-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-228
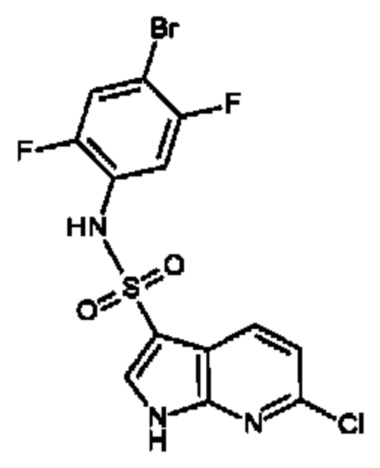
ЖХМС в щелочной среде, методика 1 (ЭР-): 420 (М-Н)-, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,87 (s, 1Н), 10,52 (s, 1Н), 8,25-8,15 (m, 2H), 7,63 (dd, J=9,7, 6,4 Гц, 1H), 7,38 (d, J=8,3 Гц, 1H), 7,34 (dd, J=9,7, 6,8 Гц, 1H).
6-Хлор-N-[4-(дифторметокси)-2,5-дифторфенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-266
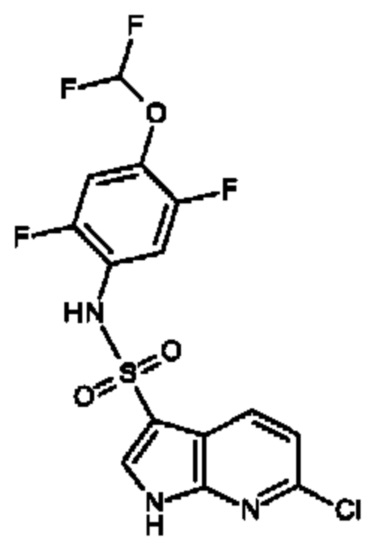
ЖХМС в щелочной среде, методика 1 (ЭР+): 410 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,85 (s, 1Н), 10,38 (s, 1Н), 8,15 (d, 1Н), 8,13 (d, J=8,4 Гц, 1H), 7,38-7,34 (d, 1H), 7,34-7,27 (m, 2H), 7,08 (t, J=72,9 Гц, 1H).
6-Хлор-N-[4-(дифторметокси)-2,5-дифторфенил]-1Н-индол-3-сульфонамид I-267
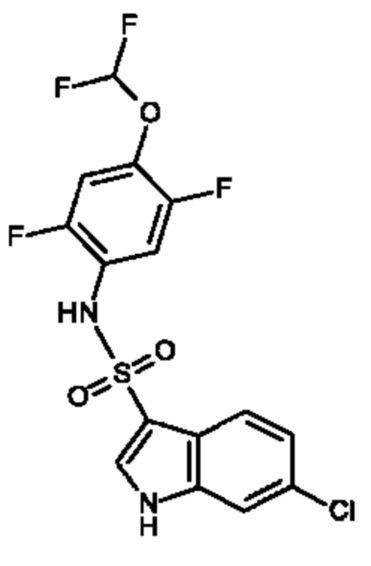
ЖХМС в щелочной среде, методика 1 (ЭР-): 407 (М-Н)-, чистота 97%.
6-Хлор-N-(2,5-дифтор-4-метилфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-268

ЖХМС в щелочной среде, методика 1 (ЭР+): 358 (М+Н)+, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,80 (s, 1Н), 10,19 (s, 1Н), 8,18-8,07 (m, 2H), 7,36 (d, J=8,3 Гц, 1H), 7,06 (ddd, J=11,0, 6,7, 2,2 Гц, 2H), 2,12 (s, J=1,9 Гц, 3Н).
6-Хлор-N-[2,5-дифтор-4-(трифторметил)фенил]-1Н-индол-3-сульфонамид I-269
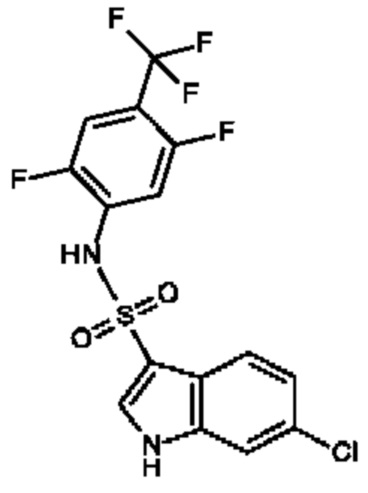
ЖХМС в щелочной среде, методика 1 (ЭР-): 409 (М-Н)-, чистота 100%.
6-Хлор-N-(2,5-дифтор-4-метилфенил)-1Н-индол-3-сульфонамид I-270
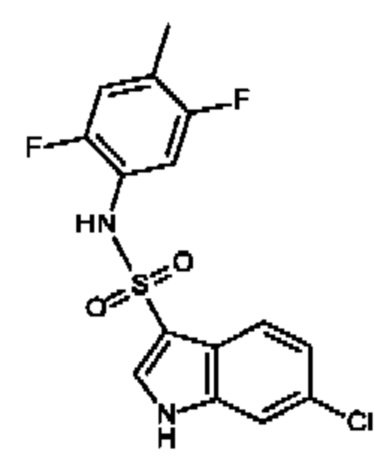
ЖХМС в щелочной среде, методика 1 (ЭР+): 357 (М+Н)+, чистота 99%.
N-(4-Хлор-2,5-дифторфенил)-5Н-[1,3]диоксоло[4,5-f]индол-7-сульфонамид I-271
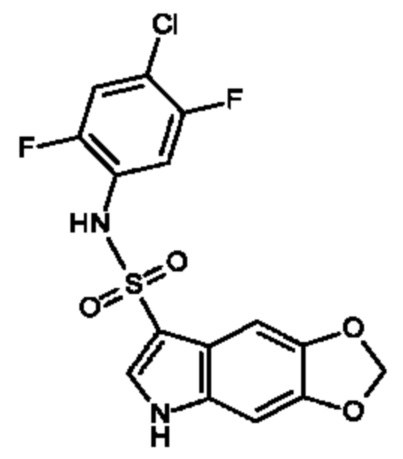
ЖХМС в щелочной среде, методика 1 (ЭР-): 385 (М-Н)-, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 11,81 (s, 1Н), 10,37 (s, 1Н), 7,81 (d, J=3,1 Гц, 1Н), 7,54 (dd, J=10,0, 6,9 Гц, 1H), 7,33 (dd, J=10,6, 7,0 Гц, 1H), 7,25 (s, 1H), 6,97 (s, 1H), 6,00 (s, 2H).
N-(4-Бром-2,5-дифторфенил)-6-метокси-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-272
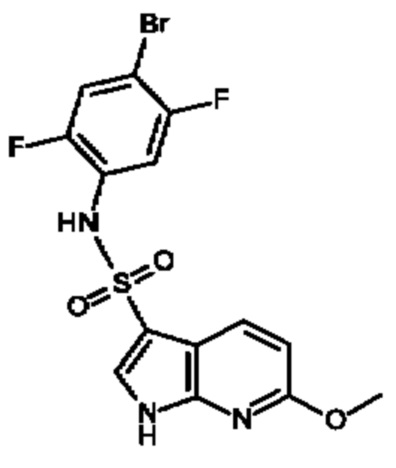
ЖХМС в щелочной среде, методика 1 (ЭР+): 418 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,45 (s, 1Н), 10,43 (s, 1Н), 8,04 (d, J=8,6 Гц, 1Н), 7,88 (d, J=3,0 Гц, 1H), 7,62 (dd, J=9,7, 6,4 Гц, 1H), 7,32 (dd, J=9,9, 6,9 Гц, 1H), 6,73 (d, J=8,6 Гц, 1H), 3,87 (s, 3H).
6-Хлор-N-[2-фтор-4-(трифторметокси)фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-273
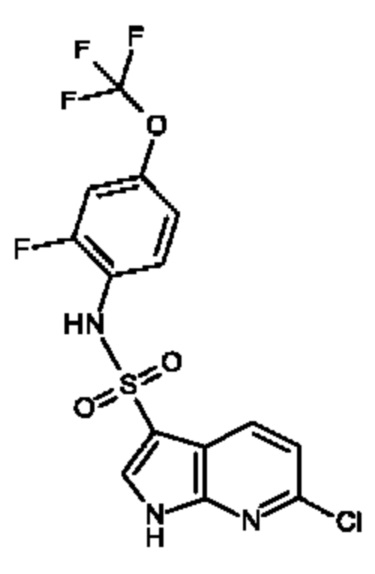
ЖХМС в щелочной среде, методика 1 (ЭР+): 410 (М+Н)+, чистота 99%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,83 (s, 1Н), 10,23 (s, 1Н), 8,08 (d, J=1,6 Гц, 1Н), 8,06 (d, J=8,4 Гц, 1H), 7,39 (t, J=8,9 Гц, 1H), 7,32 (dd, J=8,1, 2,6 Гц, 2H), 7,21-7,13 (m, 1H).
N-(4-Этинил-2-фторфенил)-6-метокси-1Н-индол-3-сульфонамид I-274
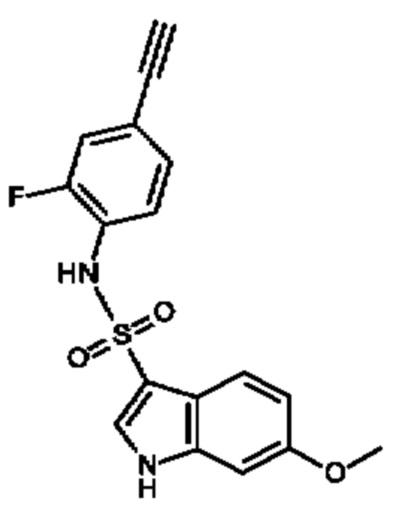
ЖХМС в щелочной среде, методика 1 (ЭР-): 343 (М-Н)-, чистота 96%.
1Н ЯМР (400 МГц, DMSO-d6) δ 11,76 (s, J=3,0 Гц, 1Н), 10,17 (s, 1Н), 7,78 (d, J=2,8 Гц, 1H), 7,64 (d, J=8,8 Гц, 1H), 7,34 (t, J=8,3 Гц, 1H), 7,26-7,13 (m, 2Н), 6,93 (d, J=2,2 Гц, 1H), 6,81 (dd, J=8,8, 2,2 Гц, 1H), 4,18 (s, 1H), 3,77 (s, 3H).
N-(5-Бром-6-хлорпиридин-2-ил)-6-хлор-1Н-индол-3-сульфонамид I-275
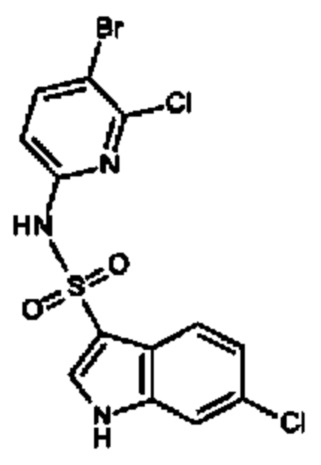
ЖХМС в щелочной среде, методика 1 (ЭР-): 418 (М-Н)-, чистота 96%.
6-Хлор-N-[2-фтор-4-(трифторметокси)фенил]-1Н-индол-3-сульфонамид I-276

ЖХМС в щелочной среде, методика 1 (ЭР-): 407 (М-Н)-, чистота 96%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,08 (s, 1Н), 10,15 (s, 1Н), 7,92 (d, J=2,7 Гц, 1Н), 7,67 (d, J=8,6 Гц, 1H), 7,52 (d, J=1,9 Гц, 1H), 7,39 (t, J=8,9 Гц, 1H), 7,29 (dd, J=10,6, 2,7 Гц, 1H), 7,16 (ddd, J=11,4, 8,9, 2,2 Гц, 2H).
N-(4-Хлор-2,5-дифторфенил)-6-циано-1Н-индол-3-сульфонамид I-277
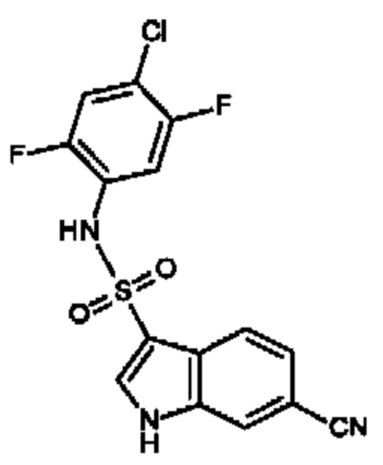
ЖХМС в щелочной среде, методика 1 (ЭР-): 366 (М-Н)-, чистота 100%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,56 (s, 1Н), 10,54 (s, 1Н), 8,26 (d, J=2,4 Гц, 1Н), 8,00 (d, J=1,3 Гц, 1H), 7,94 (d, J=8,4 Гц, 1H), 7,63-7,47 (m, 2H), 7,36 (dd, J=10,3, 6,9 Гц, 1H).
6-Бром-N-(4-хлор-2-фторфенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-278
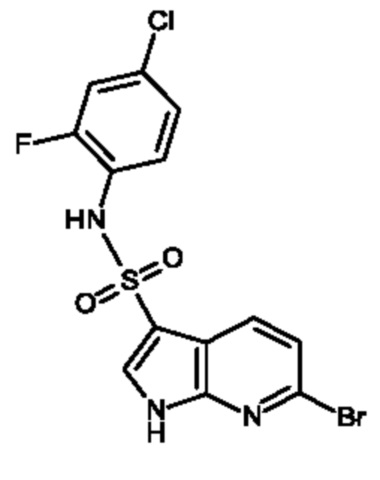
ЖХМС в щелочной среде, методика 1 (ЭР-): 402 (М-Н)-, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,85 (s, 1Н), 10,20 (s, 1H), 8,04 (d, J=8,3 Гц, 2H), 7,48 (d, J=8,3 Гц, 1H), 7,35 (dd, J=10,3, 2,3 Гц, 1H), 7,29 (t, J=8,5 Гц, 1H), 7,19 (ddd, J=8,6, 2,3, 1,0 Гц, 1H).
6-Хлор-N-(3-фтор-5-метилпиридин-2-ил)-1Н-индол-3-сульфонамид I-279
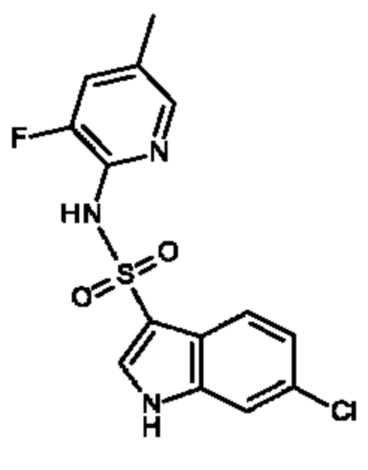
ЖХМС в щелочной среде, методика 1 (ЭР-): 338 (М-Н)-, чистота 99%.
6-Хлор-N-(5-йодпиридин-2-ил)-1Н-индол-3-сульфонамид I-280
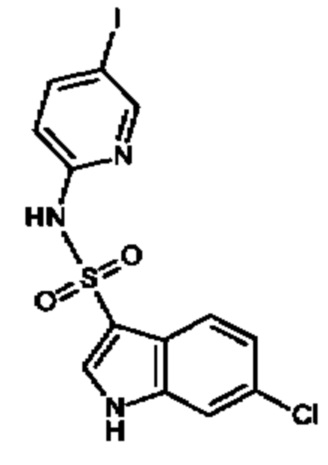
ЖХМС в щелочной среде, методика 1 (ЭР-): 432 (М-Н)-, чистота 91%.
N-(4-Хлор-2,5-дифторфенил)-6-метокси-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-281
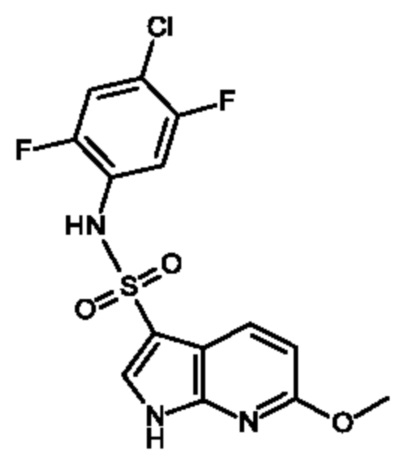
ЖХМС в щелочной среде, методика 1 (ЭР+): 374 (М+Н)+, чистота 100%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,45 (s, J=2,9 Гц, 1Н), 10,42 (s, 1Н), 8,04 (d, J=8,6 Гц, 1H), 7,88 (d, J=2,9 Гц, 1H), 7,54 (dd, J=9,9, 6,8 Гц, 1H), 7,36 (dd, J=10,4, 6,9 Гц, 1H), 6,73 (d, J=8,6 Гц, 1H), 3,88 (s, 3H).
6-Циано-N-[4-(дифторметокси)-2,5-дифторфенил]-1Н-индол-3-сульфонамид I-282
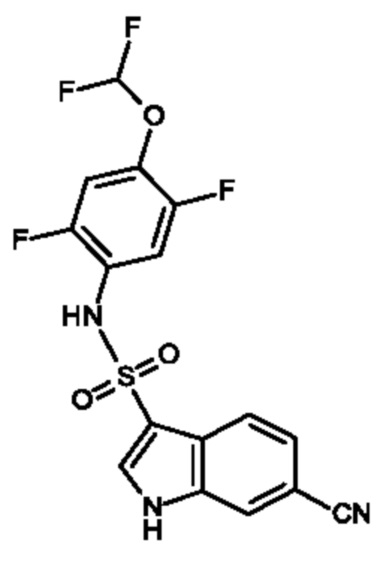
ЖХМС в щелочной среде, методика 1 (ЭР-): 398 (М-Н)-, чистота 100%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,54 (s, 1Н), 10,40 (s, 1Н), 8,22 (d, J=2,8 Гц, 1Н), 8,00 (dd, J=1,4, 0,7 Гц, 1Н), 7,88 (d, J=8,3 Гц, 1Н), 7,55 (dd, J=8,4, 1,4 Гц, 1Н), 7,38-7,25 (m, 2H), 7,16 (s, 1H).
N-(4-Этинил-2-фторфенил)-6-метокси-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-283
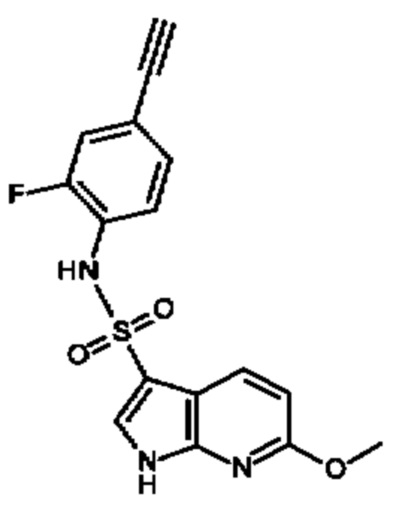
ЖХМС в щелочной среде, методика 1 (ЭР+): 346 (М+Н)+, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,4 (s, 1Н), 10,21 (s, 1Н), 8,00 (d, J=8,7 Гц, 1Н), 7,76 (s, 1H), 7,35 (d, J=8,0 Гц, 1H), 7,20 (m, 2H), 6,70 (d, J=8,6 Гц, 1H) 4,20 (s, 1H), 3,87 (s, 3H).
6-Хлор-N-(6-фтор-3-оксо-1,3-дигидро-2-бензофуран-5-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-284
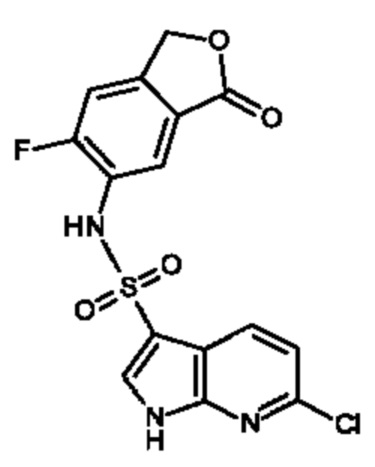
ЖХМС в щелочной среде, методика 1 (ЭР-): 380 (М-Н)-, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,83 (s, 1Н), 10,48 (s, 1Н), 8,15 (d, J=8,3 Гц, 1Н), 8,11 (d, J=2,4 Гц, 1H), 7,68 (d, J=6,9 Гц, 1H), 7,47 (d, J=9,5 Гц, 1H), 7,37 (d, J=8,3 Гц, 1H), 5,30 (s, 2H).
N-(4-Бром-2,5-дифторфенил)-6-метокси-1Н-индол-3-сульфонамид I-285
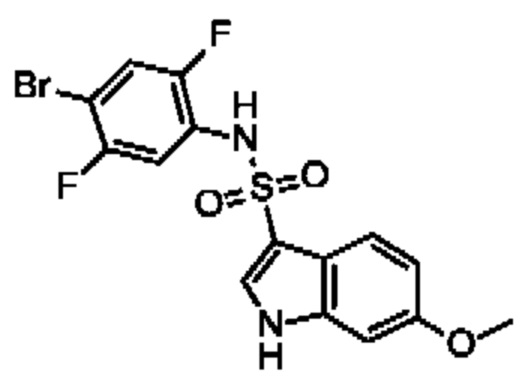
ЖХМС в нейтральной среде, методика 3 (ЭР+): 417 (М+Н)+, чистота 98%
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,79 (d, J=3,0 Гц, 1Н), 10,37 (s, 1Н), 7,87 (d, J=2,9 Гц, 1Н), 7,65 (d, J=8,8 Гц, 1Н), 7,58 (dd, J=9,7, 6,4 Гц, 1H), 7,29 (dd, J=10,0, 6,8 Гц, 1H), 6,93 (d, J=2,2 Гц, 1H), 6,82 (dd, J=8,8, 2,3 Гц, 1H), 3,76 (s, 3H).
6-Хлор-N-(4-циано-5-фтор-2-метоксифенил)-1Н-индол-3-сульфонамид I-286
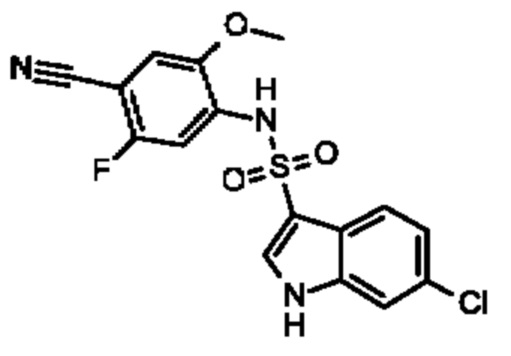
ЖХМС в нейтральной среде, методика 3 (ЭР+): 380,7 (М+Н)+, чистота 97%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,19 (s, 1Н), 10,27 (s, 1Н), 8,23 (s, 1H), 7,90 (d, J=8,6 Гц, 1H), 7,52 (s, 1H), 7,38-7,33 (m, 2H), 7,23 (dd, J=8,6, 1,9 Гц, 1H), 3,65 (s, 3H).
N-(2-Фтор-4-(трифторметил)фенил)-6-метокси-1Н-индол-3-сульфонамид I-287
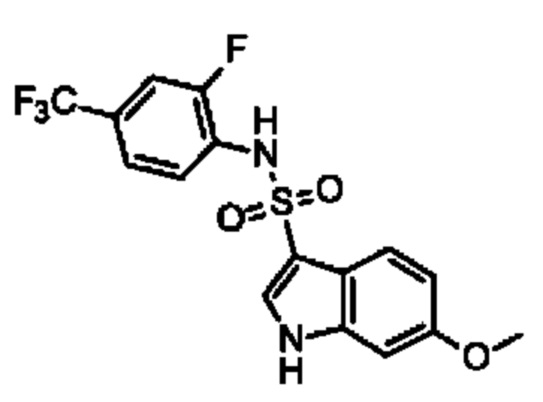
ЖХМС в нейтральной среде, методика 3 (ЭР+): 389 (М+Н)+, чистота 99%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,79 (s, 1Н), 10,48 (s, 1Н), 7,86 (d, J=2,9 Гц, 1Н), 7,67 (d, J=8,8 Гц, 1Н), 7,62-7,50 (m, 2Н), 7,47-7,37 (m, 1Н), 6,92 (d, J=2,2 Гц, 1Н), 6,81 (dd, J=8,8, 2,3 Гц, 1Н), 3,75 (s, 3Н).
N-(4-Циано-5-фтор-2-метоксифенил)-6-метокси-1Н-индол-3-сульфонамид I-288
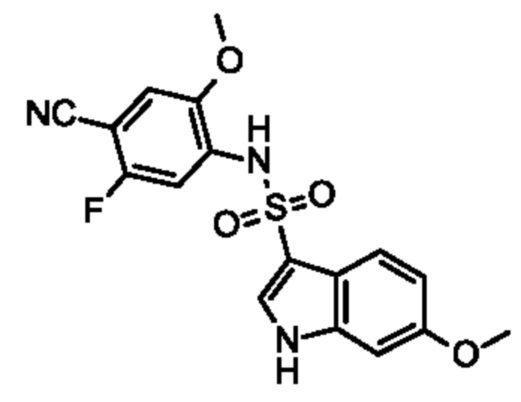
ЖХМС в нейтральной среде, методика 3 (ЭР+): 376 (М+Н)+, чистота 98%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,86 (d, J=3,0 Гц, 1Н), 10,11 (s, 1Н), 8,05 (d, J=2,9 Гц, 1H), 7,75 (d, J=8,8 Гц, 1H), 7,35 (d, J=6,0 Гц, 1H), 7,32 (d, J=11,2 Гц, 1H), 6,93 (d, J=2,3 Гц, 1H), 6,83 (dd, J=8,8, 2,3 Гц, 1H), 3,75 (s, 3H), 3,68 (s, 3H).
6-Бром-N-(5-хлор-3-фторпиридин-2-ил)-1Н-индол-3-сульфонамид I-290
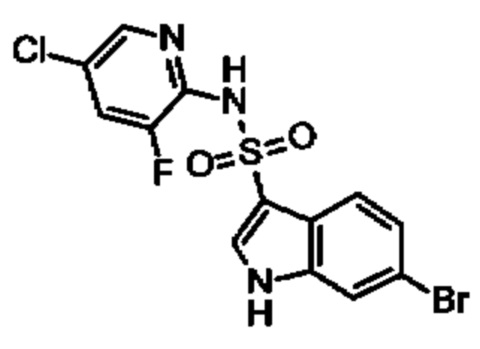
ЖХМС в нейтральной среде, методика 3 (ЭР+): 404 (М+Н)+, чистота 98%.
N-(4-Циано-2,5-дифторфенил)-6-метокси-1Н-индол-3-сульфонамид I-291
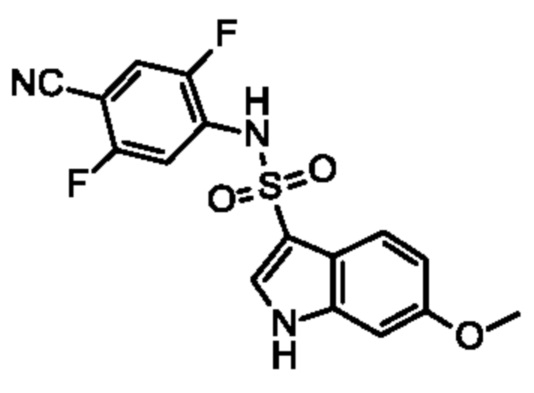
ЖХМС в нейтральной среде, методика 3 (ЭР+): 381 (M+NH4)+, чистота 98%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,93 (br s, 1Н), 11,11 (s, 1H), 8,12 (d, J=3,0 Гц, 1H), 7,83 (dd, J=10,3, 6,0 Гц, 1H), 7,73 (d, J=8,7 Гц, 1H), 7,43 (dd, J=11,1, 6,4 Гц, 1H), 6,95 (d, J=2,3 Гц, 1H), 6,86 (dd, J=8,8, 2,3 Гц, 1H), 3,77 (s, 3H).
6-Хлор-N-(4-циано-5-фтор-2-метоксифенил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-292
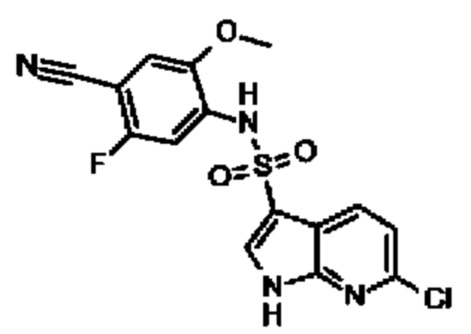
ЖХМС в нейтральной среде, методика 3 (ЭР+): 381 (М+Н)+, чистота 95,0%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,90 (s, 1Н), 10,36 (s, 1Н), 8,40 (d, J=2,3 Гц, 1Н), 8,34 (d, J=8,4 Гц, 1Н), 7,45-7,34 (m, 3Н), 3,63 (s, 3Н).
N-(4-Бром-2-фторфенил)-6-метокси-1Н-индол-3-сульфонамид I-293
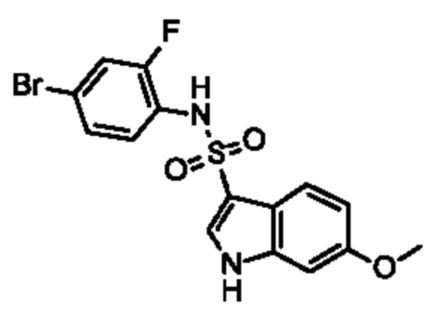
ЖХМС в нейтральной среде, методика 3 (ЭР+): 399 (М+Н)+, чистота 98%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,72 (s, 1Н), 9,97 (s, 1Н), 7,71 (d, J=2,1 Гц, 1Н), 7,61 (d, J=8,8 Гц, 1Н), 7,40 (dd, J=10,0, 2,1 Гц, 1H), 7,32-7,16 (m, 2H), 6,92 (d, J=2,3 Гц, 1H), 6,79 (dd, J=8,8, 2,3 Гц, 1H), 3,76 (s, 3H).
N-(4-Циано-2-фторфенил)-6-(2,2,2-трифторэтокси)-1Н-индол-3-сульфонамид I-294
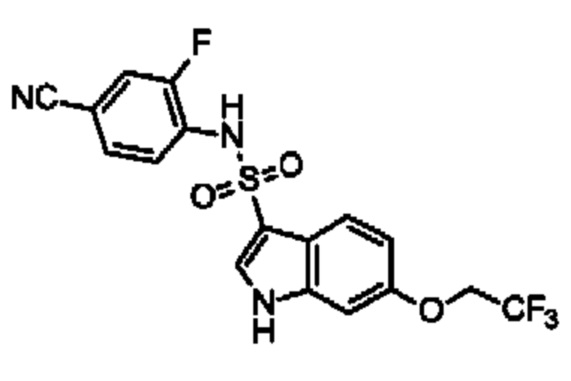
ЖХМС в нейтральной среде, методика 3 (ЭР+): 414 (М+Н)+, чистота 99%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 11,99 (d, J=2,9 Гц, 1Н), 10,71 (s, 1Н), 7,98 (d, J=2,9 Гц, 1H), 7,75 (d, J=8,8 Гц, 1H), 7,71 (dd, J=10,7, 1,7 Гц, 1H), 7,61-7,49 (m, 2H), 7,07 (d, J=2,3 Гц, 1H), 6,95 (dd, J=8,8, 2,3 Гц, 1H), 4,75 (q, J=8,9 Гц, 2H).
6-Хлор-N-[2-фтор-4-(пентафтор-лямбда~6~-сульфанил)фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-295
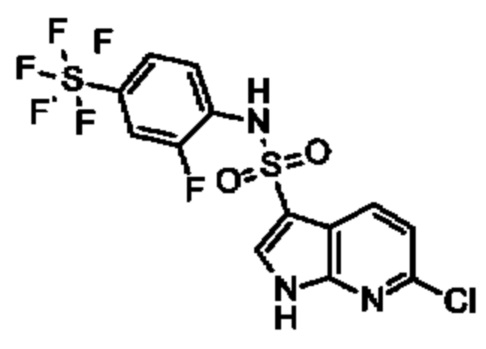
ЖХМС в нейтральной среде, методика 3 (ЭР+): 452 (М+Н)+, чистота 99%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,90 (s, 1Н), 10,80 (s, 1Н), 8,23 (s, 1Н), 8,22 (d, J=8,4 Гц, 1Н), 7,82 (dd, J=10,9, 2,6 Гц, 1H), 7,64 (dd, J=9,2, 2,5 Гц, 1H), 7,61-7,56 (m, 1H), 7,36 (d, J=8,3 Гц, 1H).
6-Хлор-N-[2-фтор-4-(трифторметил)фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-296
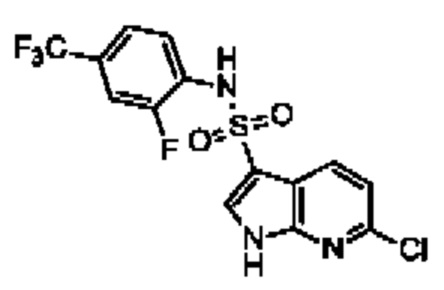
ЖХМС в нейтральной среде, методика 3 (ЭР+): 394 (М+Н)+, чистота 95%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 12,87 (s, 1Н), 10,64 (s, 1Н), 8,20 (d, J=8,4 Гц, 1Н), 8,18 (s, 1H), 7,64-7,52 (m, 2H), 7,50-7,42 (m, 1H), 7,35 (d, J=8,3 Гц, 1H).
6-Хлор-N-[3-фтор-5-(трифторметил)пиридин-2-ил]-1Н-индол-3-сульфонамид I-297
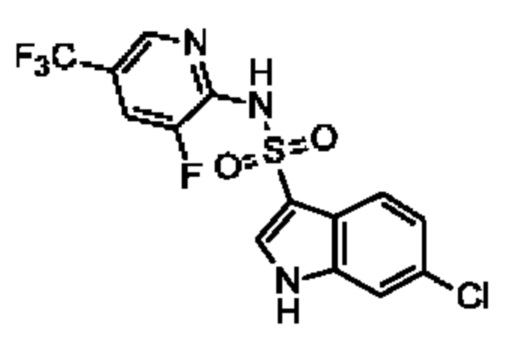
ЖХМС в нейтральной среде, методика 3 (ЭР+): 394 (М+Н)+, чистота 89%
6-Хлор-N-(2,5-дифтор-4-метоксифенил)-1Н-индол-3-сульфонамид I-298
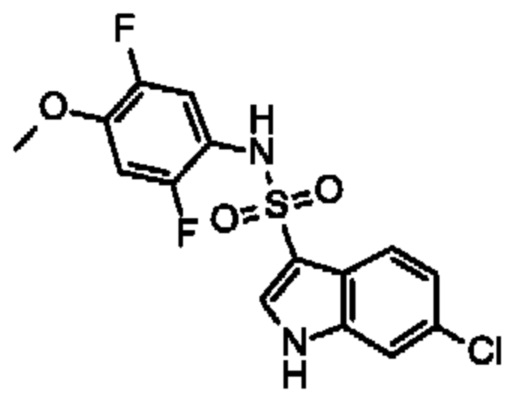
ЖХМС в нейтральной среде, методика 3 (ЭР+): 373 (М+Н)+, чистота 99%.
1Н ЯМР (500 МГц, DMSO-d6) δ: 12,00 (s, 1Н), 9,80 (s, 1Н), 7,83 (s, 1H), 7,69 (d, J=8,5 Гц, 1H), 7,51 (d, J=1,9 Гц, 1H), 7,19 (dd, J=8,6, 1,9 Гц, 1H), 7,00 (ddd, J=11,6, 10,3, 7,7 Гц, 2H), 3,74 (s, 3H).
6-Хлор-N-[2-фтор-4-(трифторметил)фенил]-1Н-индол-3-сульфонамид I-299
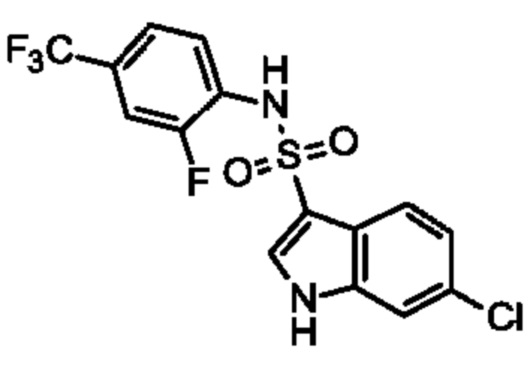
ЖХМС в нейтральной среде, методика 3 (ЭР+): 393 (М+Н)+, чистота 98%.
1Н ЯМР (500 МГц, DMSO-d6) δ 12,13 (d, J=2,9 Гц, 1Н), 10,57 (s, 1Н), 8,04 (d, J=2,9 Гц, 1H), 7,80 (d, J=8,6 Гц, 1H), 7,64-7,54 (m, 2H), 7,52 (d, J=1,9 Гц, 1H), 7,46 (dd, J=8,5, 2,1 Гц, 1H), 7,21 (dd, J=8,6, 1,9 Гц, 1H).
N-(4-Хлор-2,5-дифторфенил)-6-(2,2,2-трифторэтокси)-1H-индол-3-сульфонамид I-300
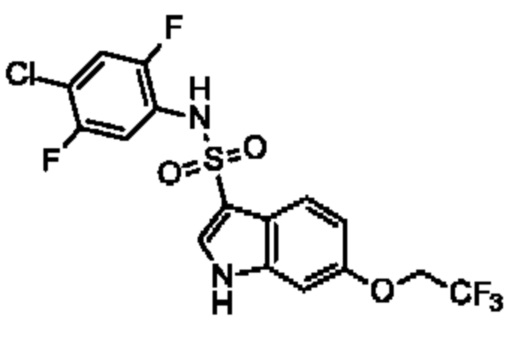
ЖХМС в нейтральной среде, методика 3 (ЭР+): 441 (М+Н)+, чистота 97%.
1H ЯМР (600 МГц, DMSO-d6) δ: 11,95 (d, J=3,1 Гц, 1H), 10,40 (s, 1H), 7,92 (d, J=2,8 Гц, 1H), 7,70 (d, J=8,8 Гц, 1H), 7,50 (dd, J=9,9, 6,8 Гц, 1H), 7,32 (dd, J=10,5, 6,9 Гц, 1H), 7,07 (d, J=2,3 Гц, 1H), 6,94 (dd, J=8,8, 2,3 Гц, 1H), 4,76 (q, J=8,9 Гц, 2H).
6-Хлор-N-(2-оксо-2,3-дигидро-1,3-бензоксазол-7-ил)-1Н-индол-3-сульфонамид I-301
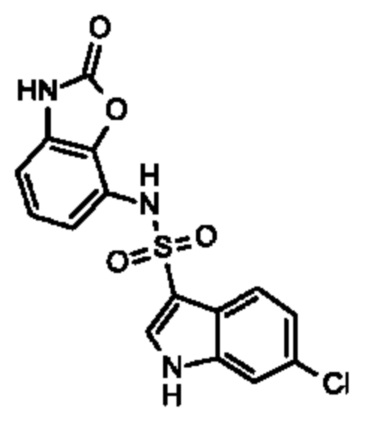
ЖХМС в нейтральной среде, методика 3 (ЭР+): 364 (М+Н)+, чистота 94,0%.
1H ЯМР (500 МГц, DMSO-d6) δ: 12,04 (s, 1Н), 11,55 (s, 1Н), 10,18 (s, 1Н), 7,93 (s, 1Н), 7,68 (d, J=8,6 Гц, 1H), 7,52-7,48 (m, 1H), 7,16 (dd, J=8,6, 1,9 Гц, 1H), 6,98 (dd, J=8,3, 7,8 Гц, 1H), 6,87 (dd, J=8,4, 1,1 Гц, 1H), 6,79 (dd, J=7,7, 1,1 Гц, 1H).
6-Хлор-N-(3,5-дифторпиридин-2-ил)-1Н-индол-3-сульфонамид I-302
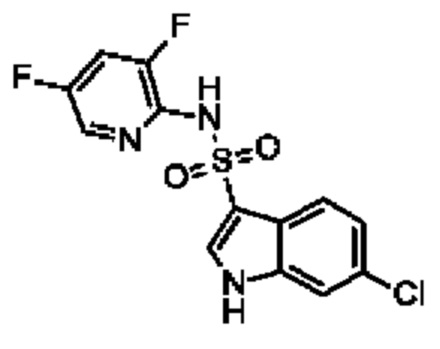
ЖХМС в нейтральной среде, методика 3 (ЭР+): 344 (М+Н)+, чистота 97,8%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,08 (s, 1Н), 10,78 (s, 1Н), 8,10 (s, 1H), 8,04 (s, 1H), 7,89-7,80 (m, 1H), 7,79 (d, J=8,6 Гц, 1H), 7,52 (s, 1H), 7,21 (dd, J=8,6, 1,9 Гц, 1H).
6-Хлор-N-[2,5-дифтор-4-(трифторметил)фенил]-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-303
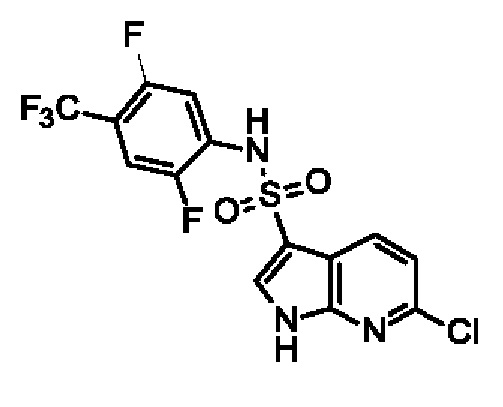
ЖХМС в щелочной среде, методика 1 (ЭР-): 410 (М-Н)-, чистота 97%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,94 (s, 1Н), 11,04 (s, 1Н), 8,40 (d, J=2,9 Гц, 1Н), 8,28 (d, J=8,3 Гц, 1H), 7,71-7,60 (m, 1H), 7,48 (dd, J=12,1, 6,3 Гц, 1H), 7,40 (d, J=8,3 Гц, 1H).
6-Хлор-N-(5-хлор-3,6-дифторпиридин-2-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-307
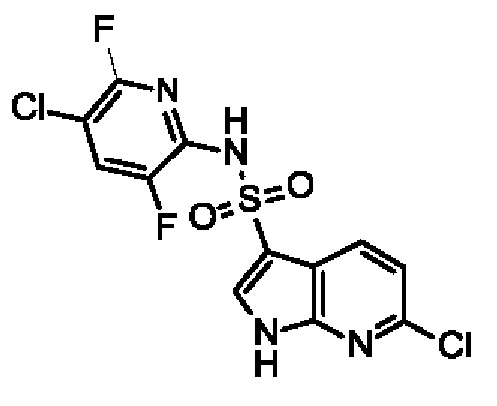
ЖХМС в щелочной среде, методика 1 (ЭР+): 379 (М+Н)+, чистота 100%.
6-Хлор-N-(2,5-дифтор-4-йодфенил)-1Н-индол-3-сульфонамид I-308
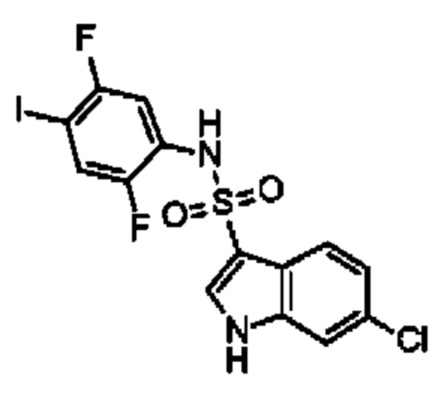
ЖХМС в нейтральной среде, методика 3 (ЭР+): 469 (М+Н)+, чистота 95%.
1Н ЯМР (600 МГц, DMSO-d6) δ: 12,13 (d, J=3,0 Гц, 1Н), 10,45 (s, 1Н), 8,04 (d, J=2,9 Гц, 1H), 7,79 (d, J=8,6 Гц, 1H), 7,63 (dd, J=9,4, 5,7 Гц, 1H), 7,52 (d, J=1,8 Гц, 1H), 7,23 (dd, J=8,6, 1,9 Гц, 1H), 7,20 (dd, J=9,1, 6,5 Гц, 1H).
6-Хлор-N-(5-хлор-3-фтор-6-метоксипиридин-2-ил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-336
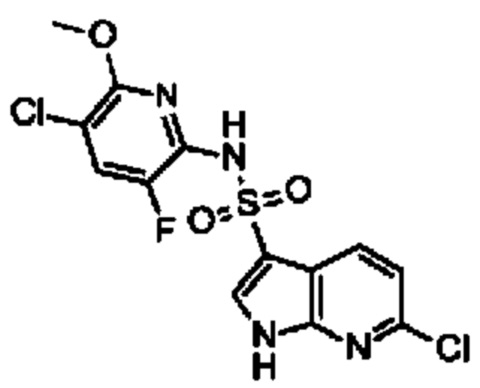
ЖХМС в щелочной среде, методика 1 (ЭР-): 389 (М-Н)-, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,87 (s, 1Н), 11,17 (s, 1Н), 8,29 (dd, J=18,4, 5,6 Гц, 2H), 7,98 (d, J=9,0 Гц, 1Н), 7,39 (d, J=8,4 Гц, 1H), 3,63 (s, 3H).
N-[4-(Дифторметокси)-2,5-дифторфенил]-6-(дифторметил)-1Н-пирроло[2,3-b]пиридин-3-сульфонамид I-363
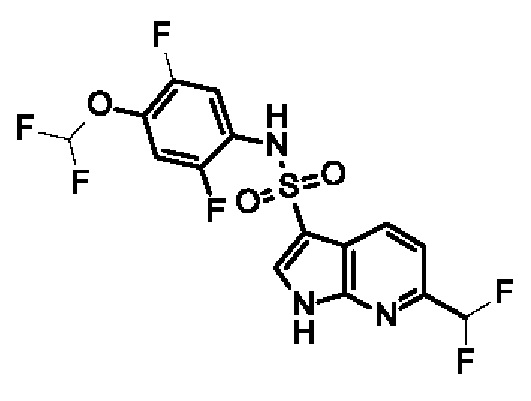
ЖХМС в щелочной среде, методика 1 (ЭР-): 424 (М-Н)-, чистота 95%.
1Н ЯМР (400 МГц, DMSO-d6) δ 12,97 (s, 1Н), 10,44 (s, 1Н), 8,43-8,18 (m, 2H), 7,59 (d, J=8,2 Гц, 1H), 7,43-6,85 (m, 4H)
D.6. Методика G: Синтез N-(4-циано-2-фторфенил)-6-(пиридин-3-ил)-1Н-индол-3-сульфонамида I-229
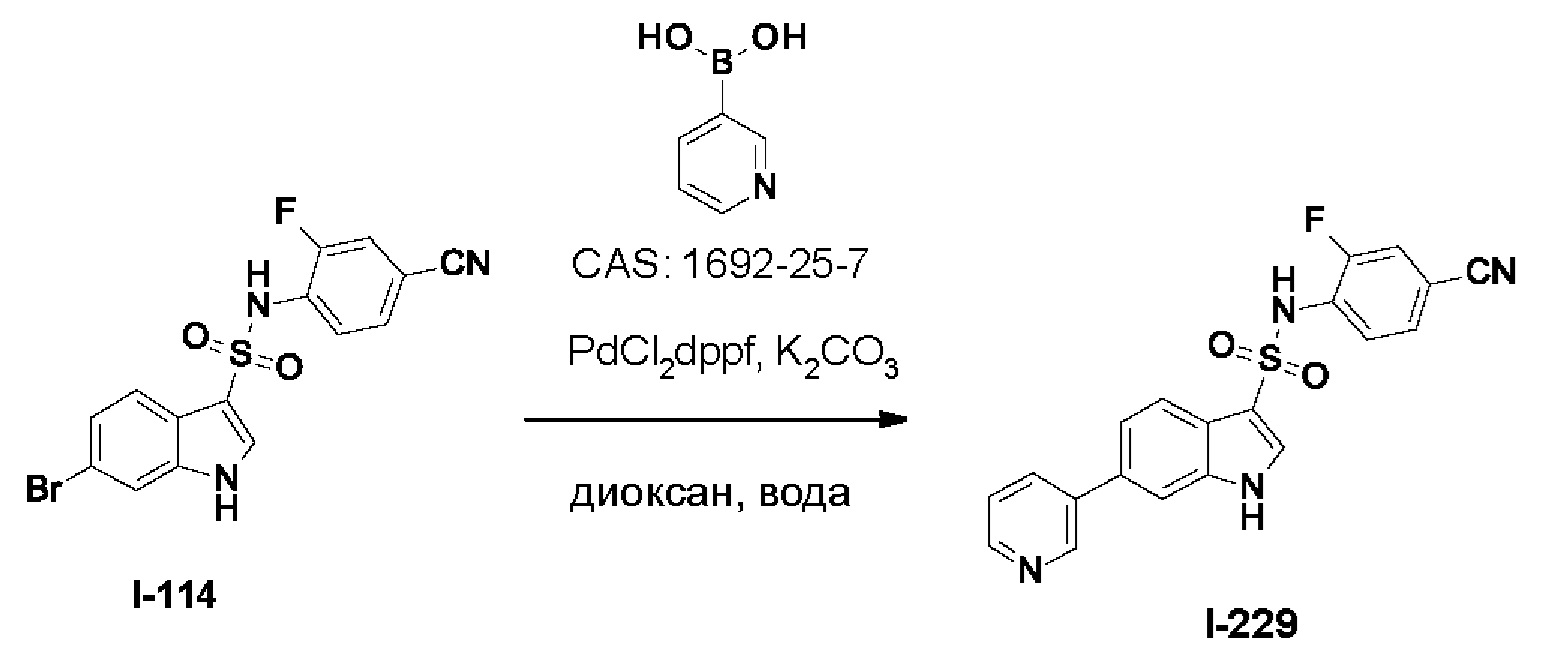
Смесь 6-бром-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамида I-114 (70 мг, 0,18 ммоля), 3-пиридилбороновой кислоты (0,22 ммоля) и карбоната калия (76 мг, 0,55 ммоля) растворяли в смеси диоксан : вода (2,5:1, 5,8 мл) и продували аргоном, подаваемым через мембрану. Затем добавляли [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий (7 мг) и реакционную смесь перемешивали в атмосфере аргона при 95°С в течение 16 ч. Смесь разбавляли водным раствором хлорида аммония и трижды экстрагировали этилацетатом. Объединенные органические слои промывали рассолом, сушили над MgSO4 и концентрировали путем выпаривания в роторном испарителе. Неочищенную смесь очищали с помощью колоночной хроматографии при элюировании с помощью 1% метанола в дихлорметане. Это давало 70 мг N-(4-циано-2-фторфенил)-6-(пиридин-3-ил)-1Н-индол-3-сульфонамида I-229 в виде бежевого твердого вещества.
Выход: 39%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 393,1 (М+Н)+, чистота 99%.
1Н ЯМР (600 МГц, DMSO-d6) δ 12,24 (s, 1Н), 10,83 (s, 1Н), 8,86-8,93 (m, 1Н), 8,55 (d, J=4,5 Гц, 1H), 8,15 (d, J=3,0 Гц, 1H), 8,07 (dt, J=7,9, 1,9 Гц, 1H), 7,95 (d, J=8,4 Гц, 1H), 7,74-7,76 (m, 1H), 7,73 (dd, J=10,7, 1,6 Гц, 1H), 7,59 (t, J=8,2 Гц, 1H), 7,53-7,57 (m, 2H), 7,48 (dd, J=7,9, 4,8 Гц, 1H).
Приведенные ниже соединения синтезировали в соответствии с методикой G:
N-(4-Циано-2-фторфенил)-6-(тиофен-3-ил)-1Н-индол-3-сульфонамид I-230 получали из 3-тиенилбороновой кислоты, регистрационный № CAS: 6165-69-1, очищали с использованием 20% этилацетата в циклогексане.
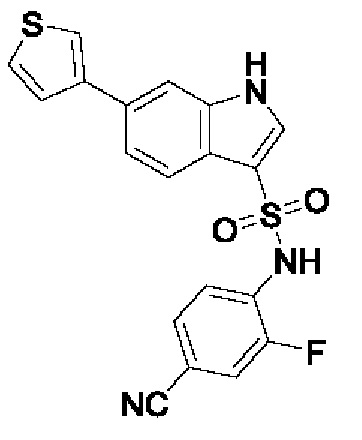
Выход: 69%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 396,0 (М+Н)+, чистота 95%.
1Н ЯМР (500 МГц, DMSO-d6) δ 12,07-12,15 (m, 1Н), 10,77 (s, 1Н), 8,08 (d, J=3,0 Гц, 1Н), 7,81-7,87 (m, 2H), 7,69-7,74 (m, 2H), 7,61-7,64 (m, 1Н), 7,53-7,61 (m, 4H).
N-(4-Циано-2-фторфенил)-6-(пиридин-4-ил)-1Н-индол-3-сульфонамид I-231 получали из 4-пиридилбороновой кислоты, регистрационный № CAS: 1692-15-5.
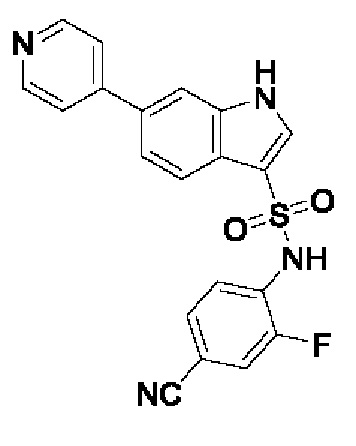
Выход: 25%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 393,1 (М+Н)+, чистота 99%.
1H ЯМР (500 МГц, DMSO-d6) δ12,28 (d, J = 2,4 Гц, 1H), 10,82 (s, 1H), 8,62 (d, J = 5,5 Гц, 2H), 8,17 (d, J = 3,1 Гц, 1H), 7,96 (d, J = 8,4 Гц, 1H), 7,83 - 7,85 (m, 1H), 7,70 - 7,74 (m, 3H), 7,53 - 7,65 (m, 3H).
N-(4-Циано-2-фторфенил)-6-(4-метоксифенил)-1Н-индол-3-сульфонамид I-232 получали из (4-метоксифенил)бороновой кислоты, регистрационный № CAS: 5720-07-0, очищали с использованием 25% этилацетата в циклогексане.
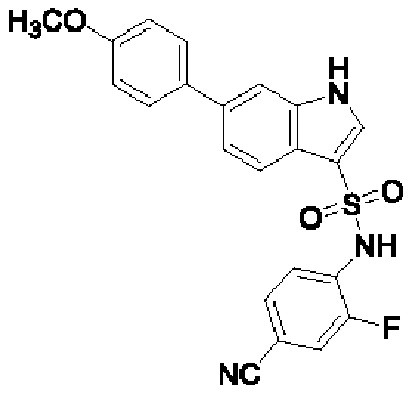
Выход: 24%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 420,1 (М+Н)+, чистота 97%.
1H ЯМР (600 МГц, DMSO-d6) δ12,06 - 12,13 (m, 2Н), 10,79 (s, 2Н), 8,08 (d, J = 2,9 Гц, Ш), 7,87 (d, J = 8,4 Гц, 1H), 7,72 (d, J = 10,1 Гц, 1H), 7,52 - 7,64 (m, 5Н), 7,45 (dd, J = 8,4, 1,4 Гц, 1Н), 7,02 (d, J = 8,8 Гц, 2H), 3,79 (s, 3Н).
N-(4-Циано-2-фторфенил)-6-фенил-1Н-индол-3-сульфонамид I-233 получали из фенилбороновой кислоты, регистрационный № CAS: 98-80-6, очищали с использованием 33% этилацетата в циклогексане.
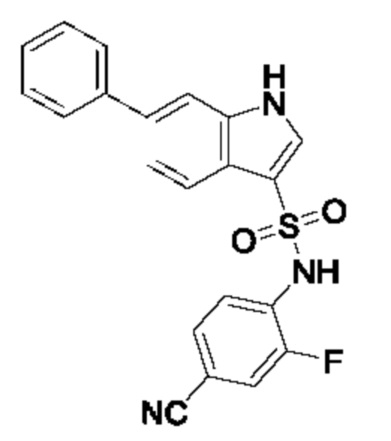
Выход: 57%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 390,1 (М+Н)+, чистота 95%.
1H ЯМР (500 МГц, DMSO-d6) δ12,13 - 12,19 (m, 1Н), 10,79 (s, 1H), 8,12 (d, J = 3,0 Гц, 1H), 7,91 (d, J = 8,4 Гц, 1H), 7,72 (dd, J = 10,7, 1,8 Гц, 1H), 7,64 - 7,69 (m, 3Н), 7,53 - 7,62 (m, 2H), 7,50 (dd, J = 8,4, 1,6 Гц, 1H), 7,43 - 7,48 (m, 2H), 7,32 - 7,37 (m, 1H).
N-(4-Циано-2-фторфенил)-6-(3,5-диметил-1,2-оксазол-4-ил)-1Н-индол-3-сульфонамид I-234 получали из (3,5-диметилизоксазол-4-ил)бороновой кислоты, регистрационный № CAS: 16114-47-9, очищали с использованием 66% этилацетата в петролейном эфире.
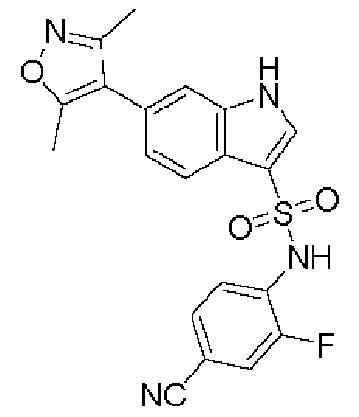
Выход: 34%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 411,2 (М+Н)+, чистота 98%.
1H ЯМР (500 МГц, DMSO-d6) δ12,15 (s, 1H), 10,82 (s, 1H), 8,14 (d, J = 3,0 Гц, 1H), 7,91 (d, J = 8,3 Гц, 1H), 7,73 (d, J = 10,8 Гц, 1Н), 7,61 (t, J = 8,2 Гц, 1H), 7,56 (d, J = 8,5 Гц, 1H), 7,43 (s, 1H), 7,19 (dd, J = 8,3, 1,3 Гц, 1H), 2,21 (s, 3H), 2,39 (s, 3H)
N-(4-Циано-2-фторфенил)-6-(тиофен-2-ил)-1Н-индол-3-сульфонамид I-235 получали из 2-тиенилбороновой кислоты, регистрационный № CAS: 6165-68-0, очищали с использованием 50% этилацетата в петролейном эфире.
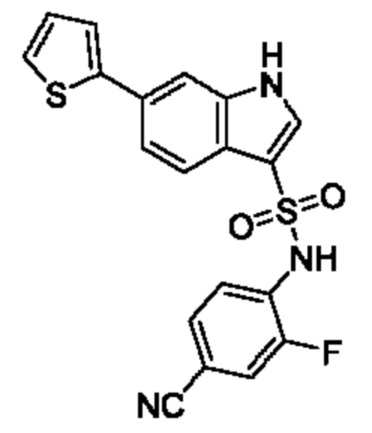
Выход: 94%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 398,1 (М+Н)+, чистота 96%.
1Н ЯМР (500 МГц, DMSO-d6) δ12,12 (d, J = 2,4 Гц, 1Н), 10,82 (s, 1H), 8,11 (d, J = 3,0 Гц, 1H), 7,85 (d, J = 8,4 Гц, 1H), 7,73 (dd, J = 10,8, 1,5 Гц, 1H), 7,67 (d, J = 1,0 Гц, 1H), 7,46 - 7,61 (m, 5H), 7,12 (dd, J = 5,1, 3,7 Гц, 1H).
N-(4-Хлор-2,5-дифторфенил)-6-(тиофен-3-ил)-1Н-индол-3-сульфонамид I-236 получали из 3-тиенилбороновой кислоты, регистрационный № CAS: 6165-69-1, очищали с использованием 33% этилацетата в петролейном эфире.

Выход: 76%.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 425,1 (М+Н)+, чистота 100%.
1H ЯМР (600 МГц, DMSO-d6) δ12,06 (s, 1H), 10,44 (s, 1H), 8,01 (d, J = 3,0 Гц, 1H), 7,83 (dd, J = 2,9, 1,3 Гц, 1H), 7,79 (d, J = 8,4 Гц, 1Н), 7,70 - 7,73 (m, 1H), 7,63 (dd, J = 5,0, 2,9 Гц, 1H), 7,53 - 7,58 (m, 2H), 7,51 (dd, J = 9,9, 6,9 Гц, 1H), 7,35 (dd, J = 10,5, 7,0 Гц, 1H).
D.7. Синтез N-(4-цианофенил)-6-(метилсульфинил)-1Н-индол-3-сульфонамида I-237
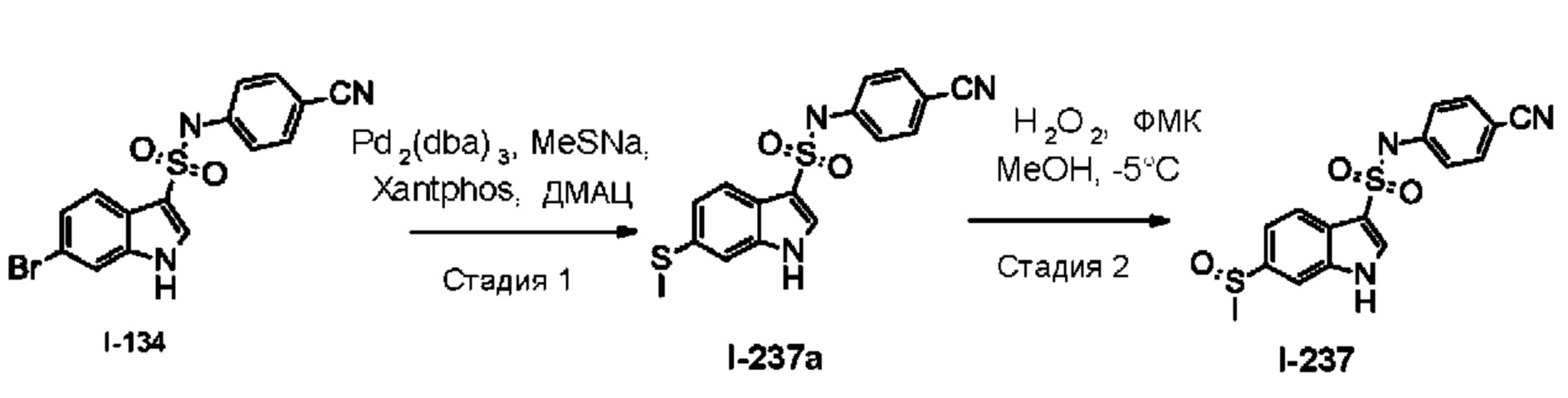
Стадия 1: Синтез N-(4-цианофенил)-6-(метилтио)-1Н-индол-3-сульфонамида I-237а:
К раствору 6-бром-N-(4-цианофенил)-1Н-индол-3-сульфонамида I-134 (0,05 г, 0,13 ммоля) в N,N-диметилацетамиде (2 мл) добавляли Xantphos (0,016 г, 0,03 ммоля) и метантиолат натрия (0,012 г, 0,16 ммоля) и реакционную смесь продували аргоном в течение 5 мин. Добавляли Pd2(dba)3 (0,02 г, 0,03 ммоля) и реакционную смесь повторно продували аргоном в течение 5 мин. Реакционную смесь нагревали в микроволновой печи при 180°С в течение 30 мин. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали насыщенным раствором NH4Cl (50 мл) и насыщенным раствором NaHCO3 (50 мл) и смесь экстрагировали с помощью EtOAc (20 мл). Органический слой отделяли, промывали рассолом (10 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 2% МеОН в DCM) и получали 0,04 г N-(4-цианофенил)-6-(метилтио)-1Н-индол-3-сульфонамида I-237а в виде почти белого твердого вещества.
Выход: 88%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 341,95 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,14 (d, J=8,80 Гц, 1Н) 7,22 (d, J=8,80 Гц, 2H) 7,30 (s, 1H) 7,62 (d, J=8,31 Гц, 2H) 7,74 (d, J=8,80 Гц, 1H) 8,08 (s, 1H) 10,93 (brs, 1H) 11,99 (brs, 1H) (сигналы 3Н объединены с пиком растворителя).
Стадия 2: Синтез N-(4-цианофенил)-6-(метилсульфинил)-1Н-индол-3-сульфонамида I-237
К раствору N-(4-цианофенил)-6-(метилтио)-1Н-индол-3-сульфонамида I-237а (0,12 г, 0,34 ммоля) в МеОН (14 мл) добавляли фосфорномолибденовую кислоту (0,13 г, 0,07 ммоля), затем при -5°С по каплям добавляли Н2О2 (0,004 мл, 0,34 ммоля). Реакционную смесь перемешивали при -5°С в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали насыщенным раствором Na2S2O3 (50 мл) и насыщенным раствором NaHCO3 (10 мл) и смесь экстрагировали с помощью EtOAc (3×50 мл). Органический слой отделяли, промывали рассолом (50 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 3% МеОН в DCM) и получали 0,12 г N-(4-цианофенил)-6-(метилсульфинил)-1Н-индол-3-сульфонамида I-237 в виде светло-коричневого твердого вещества.
Выход: 95%.
ЖХМС в щелочной среде, методика 2 (ЭР ): 360 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 2,71 (s, 3Н) 7,23 (d, J=8,80 Гц, 2Н) 7,45 (d, J=8,80 Гц, 1Н) 7,62 (d, J=8,80 Гц, 2Н) 7,79 (s, 1Н) 7,97 (s, 1H) 8,31 (brs, 1H) 11,03 (s, 1H) 12,41 (brs, 1H).
D.8. Синтез 6-(метилсульфонил)-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1Н-индол-3-сульфонамида I-238
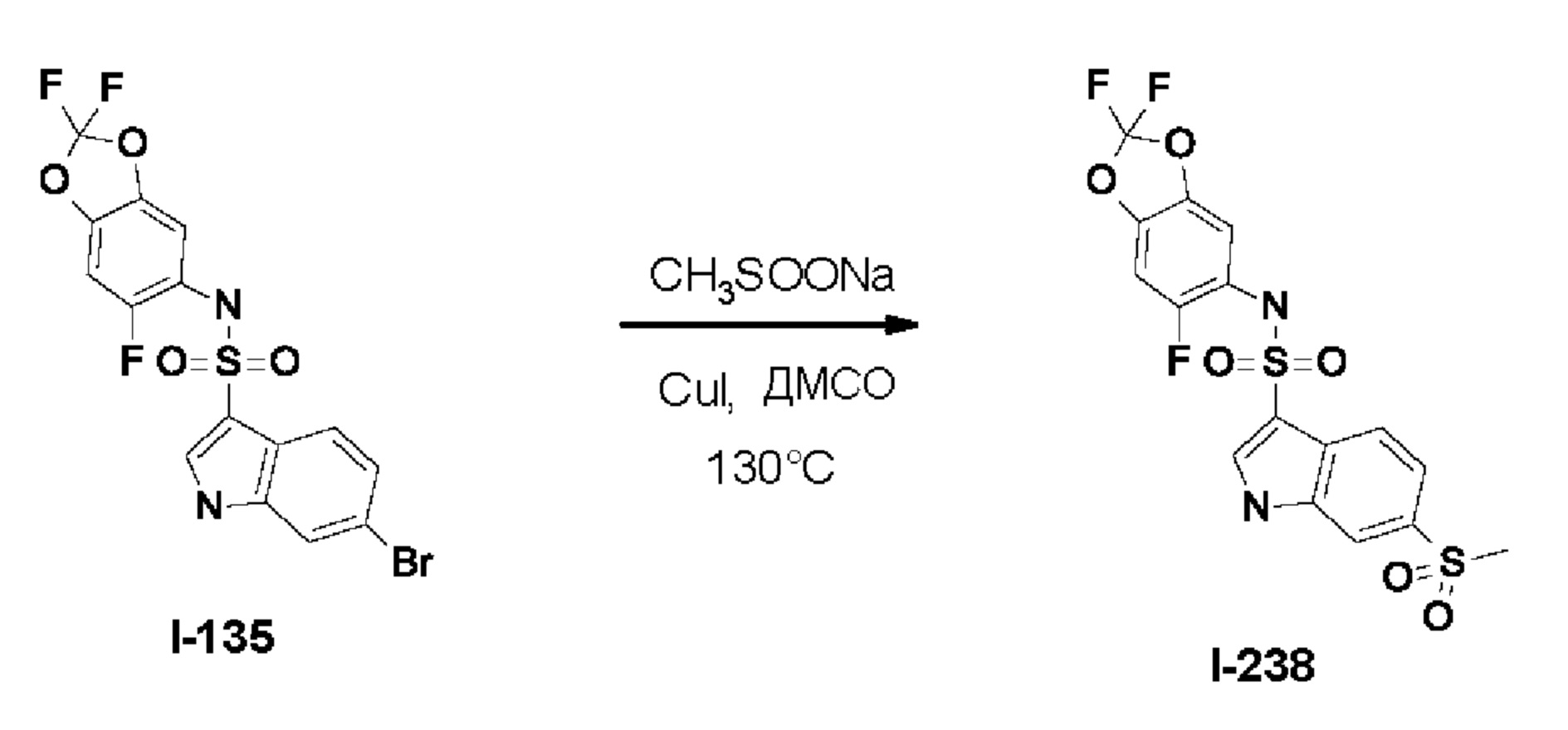
К раствору 6-бром-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1Н-индол-3-сульфонамида I-135 (0,18 г, 0,40 ммоля) в DMSO (4 мл) добавляли метансульфинат натрия (0,18 г, 1,80 ммоля) и CuI (0,34 г, 1,78 ммоля). Реакционную смесь нагревали при 130°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали с помощью Н2О (20 мл) и смесь экстрагировали с помощью EtOAc (30 мл). Органический слой отделяли, промывали рассолом (100 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 5% МеОН в DCM) и получали 0,022 г 6-(метилсульфонил)-N-(2,2,6-трифтор-1,3-бензодиоксол-5-ил)-1Н-индол-3-сульфонамида I-238 в виде почти белого твердого вещества.
Выход: 12%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 447 (М-Н)-, чистота 96%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,22 (s, 3Н) 7,34 (d, J=6,36 Гц, 1Н) 7,44 (d, J=8,80 Гц, 1H) 7,71 (dd, J=8,31, 1,47 Гц, 1H) 7,95 (d, J=8,31 Гц, 1H) 8,03 (s, 1H) 8,17 (d, J=2,93 Гц, 1H) 10,20 (s, 1H) 12,51 (brs, 1H).
D.9. Синтез 6-метилсульфонил-N-(2,4,5-трифторфенил)-1Н-индол-3-сульфонамида I-239
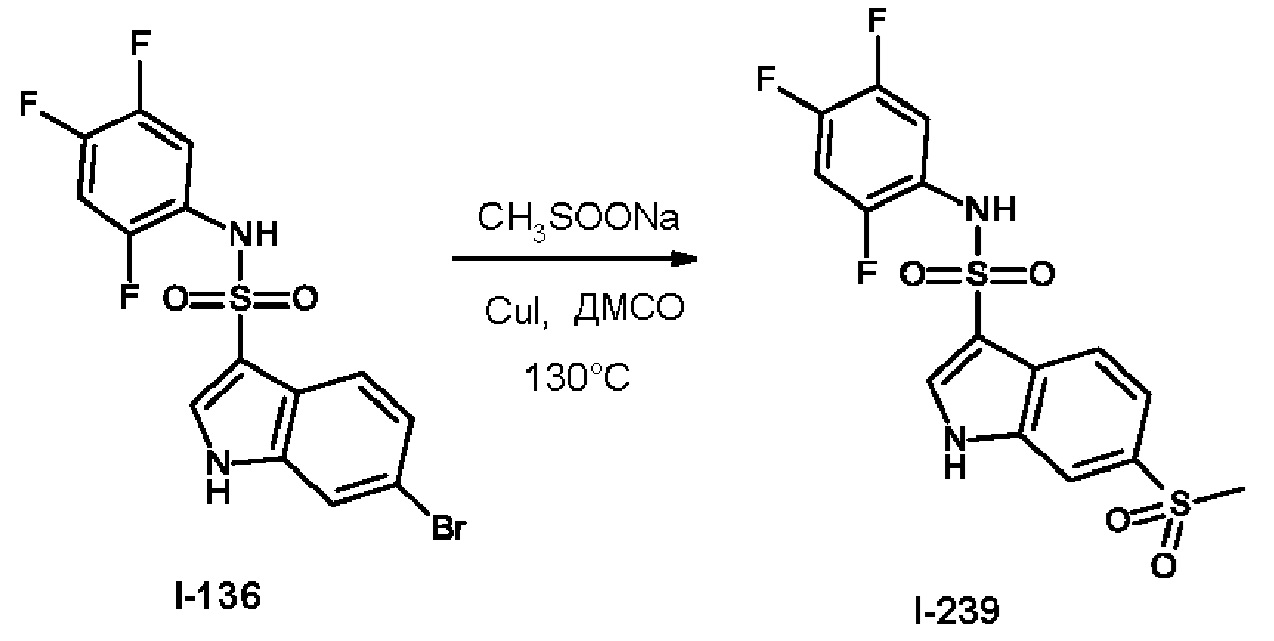
К раствору 6-бром-N-(2,4,5-трифторфенил)-1Н-индол-3-сульфонамида I-136 (0,40 г, 0,98 ммоля) в DMSO (15 мл) добавляли метансульфинат натрия (0,45 г, 4,41 ммоля) и CuI (0,84 г, 4,41 ммоля). Реакционную смесь нагревали при 130°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали насыщенным раствором NH4Cl (30 мл) и насыщенным раствором NaHCO3 (60 мл). Продукт экстрагировали с помощью EtOAc (60 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночная флэш-хроматографии и получали 6-метилсульфонил-N-(2,4,5-трифторфенил)-1Н-индол-3-сульфонамид I-239 (0,02 г, 5%) в виде белого твердого вещества.
Выход: 5%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 403,00 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,22 (s, 3Н) 7,31 - 7,41 (m, 1Н) 7,41 - 7,53 (m, 1H) 7,72 (d, J=8,31 Гц, 1H) 7,96 (d, J=8,31 Гц, 1H) 8,04 (s, 1H) 8,22 (d, J=2,45 Гц, 1H) 10,34 (s, 1H) 12,54 (brs, 1H).
D.10. Синтез N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-6-метилсульфонил-1H-индол-3-сульфонамида I-240
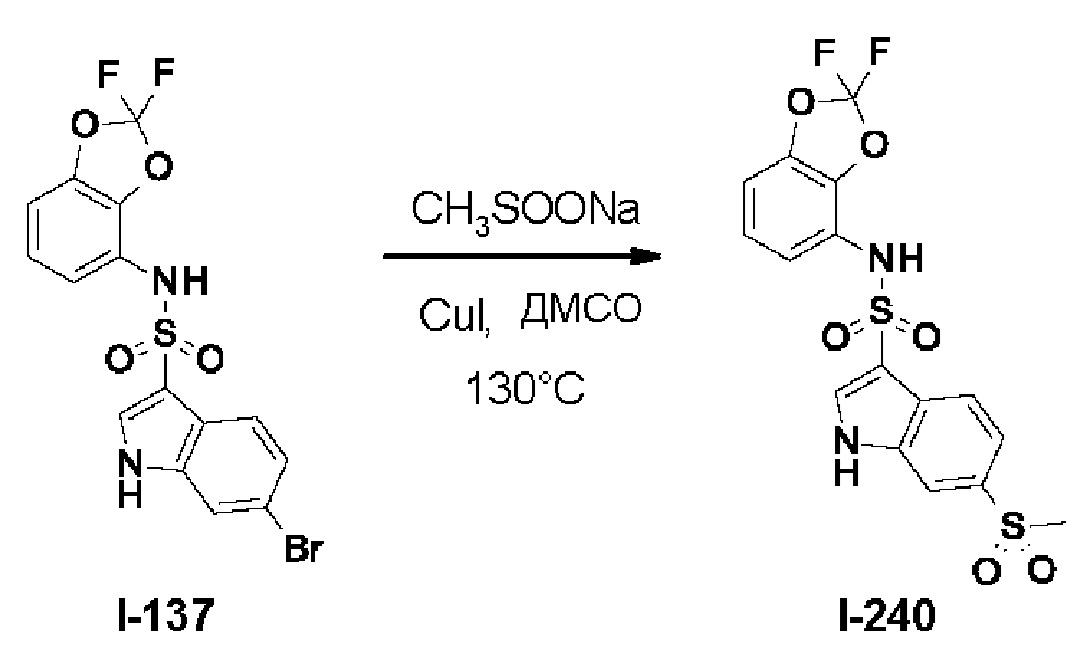
К раствору 6-бром-N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-1Н-индол-3-сульфонамида I-137 (0,13 г, 0,30 ммоля) в DMSO (4 мл) добавляли метансульфинат натрия (0,15 г, 1,50 ммоля) и CuI (0,28 г, 1,50 ммоля). Реакционную смесь нагревали при 130°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакцию останавливали насыщенным раствором NH4Cl (50 мл) и насыщенным раствором NaHCO3 (50 мл). Продукт экстрагировали с помощью EtOAc (4×50 мл). Органический слой отделяли, промывали рассолом (2×50 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, от 55 до 65% EtOAc в гексанах) и получали 0,032 г N-(2,2-дифтор-1,3-бензодиоксол-4-ил)-6-метилсульфонил-1Н-индол-3-сульфонамида I-240 в виде почти белого твердого вещества.
Выход: 25%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 429,00 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,19 (s, 3Н) 6,95 (d, J=8,31 Гц, 1Н) 7,07 (t, J=8,07 Гц, 1H) 7,11 - 7,17 (m, 1H) 7,69 (d, J=8,80 Гц, 1H) 7,88 (d, J=8,31 Гц, 1H) 8,03 (s, 1H) 8,22 (d, J=2,45 Гц, 1H) 10,46 (s, 1H) 12,54 (brs, 1H).
D.11. Синтез N-(4-азидо-2-фторфенил)-6-хлор-1Н-индол-3-сульфонамида I-241
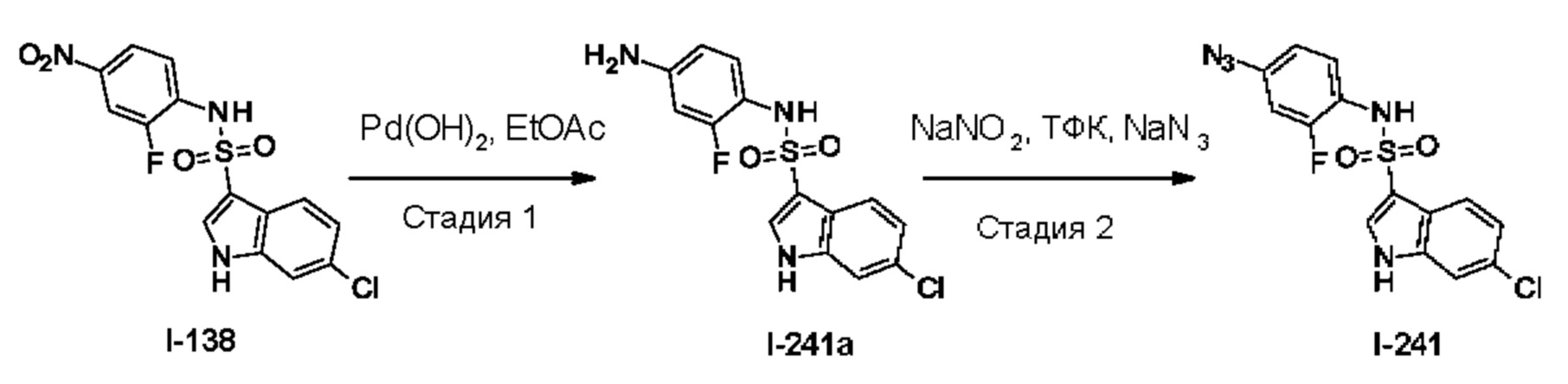
Стадия 1: Синтез N-(4-амино-2-фторфенил)-6-хлор-1Н-индол-3-сульфонамида I-241а:
К раствору 6-хлор-N-(2-фтор-4-нитрофенил)-1Н-индол-3-сульфонамида I-138 (0,32 г, 0,87 ммоля) в EtOAc (15 мл) при 0°С добавляли Pd(OH)2 (0,10 г) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через слой целита, промывали с помощью EtOAc (3×20 мл) и фильтрат концентрировали в вакууме. Полученное неочищенное вещество промывали пентаном (10 мл) и сушили в вакууме и получали N-(4-амино-2-фторфенил)-6-хлор-1H-индол-3-сульфонамид I-241а (0,33 г, неочищенный) в виде серого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в щелочной среде, методика 2 (ЭР-): 338,00 (М-Н)-, чистота 80%.
1H ЯМР (400 МГц, DMSO-d6) δ 5,33 (s, 2Н) 6,12-6,18 (m, 2Н) 6,60 (t, J=8,80 Гц, 1Н) 7,16 (d, J=8,40 Гц, 1H) 7,51 (s, 1H) 7,64-7,69 (m, 2H) 9,14 (s, 1H) 11,92 (s, 1H).
Стадия 2: Синтез N-(4-азидо-2-фторфенил)-6-хлор-1Н-индол-3-сульфонамида I-241
К раствору N-(4-амино-2-фторфенил)-6-хлор-1Н-индол-3-сульфонамида I-241а (0,15 г, 0,44 ммоля) в TFA (3 мл) при 0°С порциями добавляли NaNO2 (0,12 г, 1,77 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. При 0°С порциями добавляли NaN3 (0,09 г, 1,46 ммоля) и реакционную смесь перемешивали при 0°С в течение 30 мин. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь выливали в охлажденную льдом Н2О (10 мл) и экстрагировали с помощью EtOAc (2×10 мл). Органический слой отделяли, промывали рассолом (10 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 30% EtOAc в гексанах) и получали 0,03 г N-(4-азидо-2-фторфенил)-6-хлор-1Н-индол-3-сульфонамида I-241 в виде желтого твердого вещества.
Выход: 19%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 364,00 (М-Н)-, чистота 96%.
1H ЯМР (400 МГц, DMSO-d6) δ 6,83 - 6,99 (m, 2Н) 7,16 - 7,31 (m, 2Н) 7,52 (s, 1Н) 7,68 - 7,77 (m, 1H) 7,84 (brs, 1H) 9,94 (s, 1H) 12,04 (brs, 1H).
D.12. Синтез 6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(3,5-диметил-1,2-оксазол-4-ил)-1Н-индол-3-сульфонамида I-250
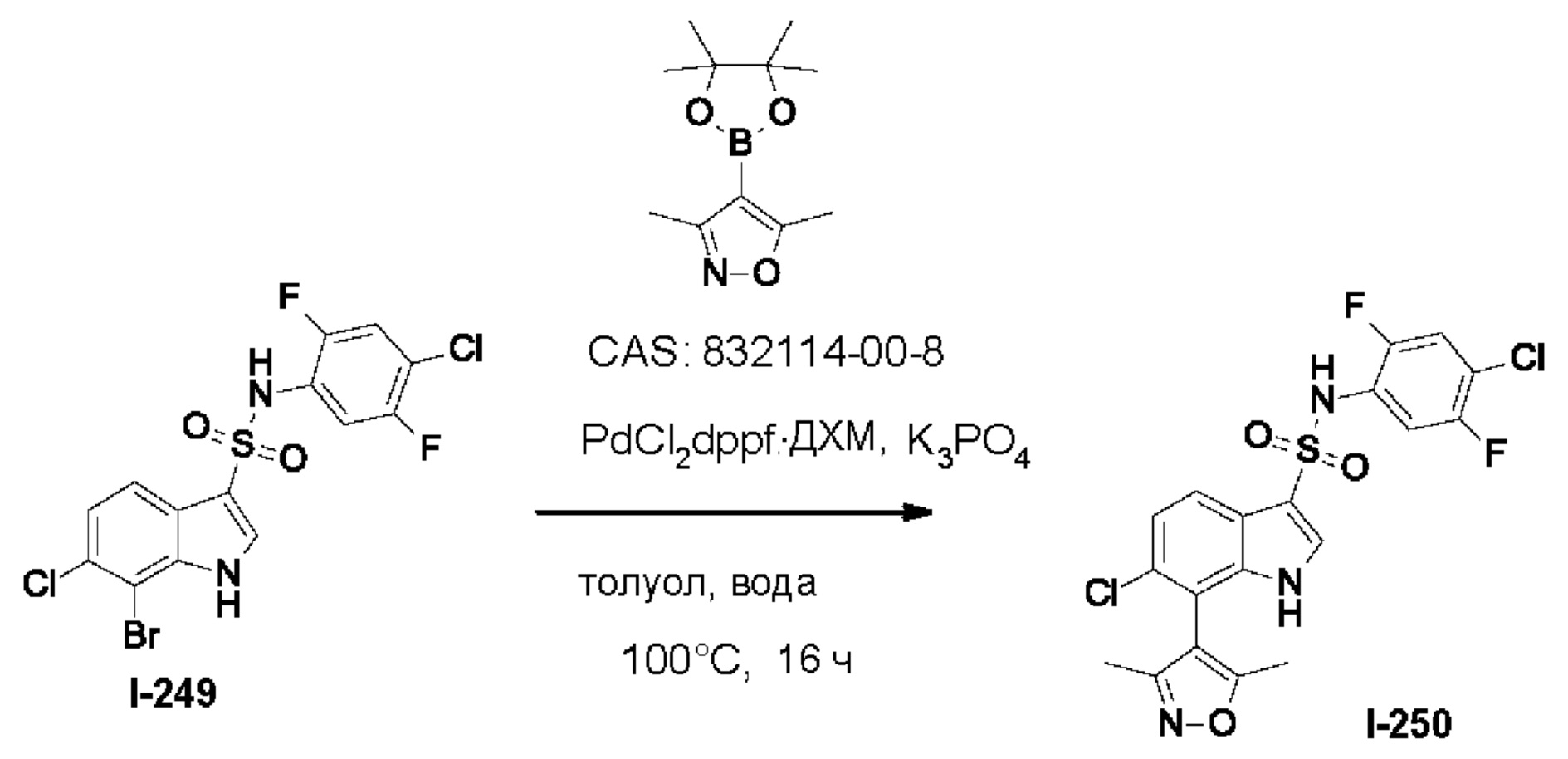
К раствору 7-бром-6-хлор-N-(4-хлор-2,5-дифторфенил)-1H-индол-3-сульфонамида I-249 (0,16 г, 0,35 ммоля) и пинаколового эфира 3,5-диметилизоксазол-4-бороновой кислоты (0,39 г, 1,73 ммоля) в толуоле (8 мл) и Н2О (1 мл) добавляли K3PO4 (0,22 г, 1,04 ммоля). Реакционную смесь продували аргоном в течение 20 мин, затем добавляли PdCl2(dppf)⋅DCM (0,03 г, 0,03 ммоля). Реакционную смесь нагревали при 100°С в течение 16 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (100 мл) и экстрагировали с помощью EtOAc (200 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии с использованием CombiFlash (40% EtOAc в гексанах) и получали 6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(3,5-диметил-1,2-оксазол-4-ил)-1Н-индол-3-сульфонамид I-250 (0,04 г) в виде белого твердого вещества.
Выход: 24%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 470,00 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 1,98 (s, 3Н) 2,15 (s, 3Н) 7,31-7,38 (m, 1Н) 7,41 (d, J=8,80 Гц, 1Н) 7,56 (dd, J=9,78, 6,85 Гц, 1H) 7,85 (d, J=8,80 Гц, 1H) 8,01 (d, J=3,42 Гц, 1H) 10,54 (s, 1H) 12,15 (brs, 1H).
D.13. Синтез 6-хлор-N-(4-хлор-2,5-дифторфенил)-7-циано-1Н-индол-3-сульфонамида I-256
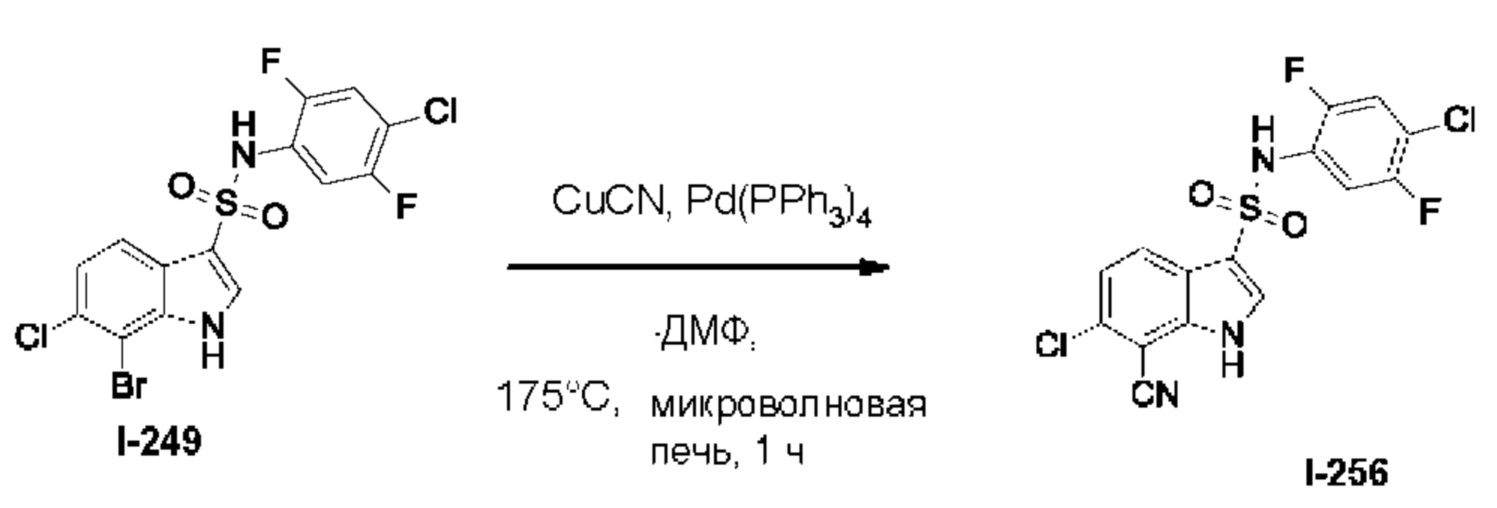
К раствору 7-бром-6-хлор-N-(4-хлор-2,5-дифторфенил)-1H-индол-3-сульфонамида I-249 (0,13 г, 0,28 ммоля) в DMF (9 мл) добавляли CuCN (0,05 г, 0,56 ммоля) и реакционную смесь продували аргоном в течение 20 мин. Добавляли Pd(PPh3)4 (0,03 г, 0,03 ммоля) и реакционную смесь нагревали в микроволновой печи при 175°С в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (100 мл) и EtOAc (100 мл), фильтровали через целит и экстрагировали с помощью EtOAc (100 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью препаративной ВЭЖХ и получали 6-хлор-N-(4-хлор-2,5-дифторфенил)-7-циано-1Н-индол-3-сульфонамид I-256 (0,023 г, 20%) в виде белого твердого вещества.
Выход: 20%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 400 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 7,35 (dd, J=10,27, 6,97 Гц, 1Н) 7,50-7,56 (m, 2H) 8,07 (d, J=8,68 Гц, 1H) 8,16 (s, 1H) 10,58 (brs, 1H) 13,2 (brs, 1H).
D.14. Синтез 6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(метилсульфонил)-1Н-индол-3-сульфонамида I-261
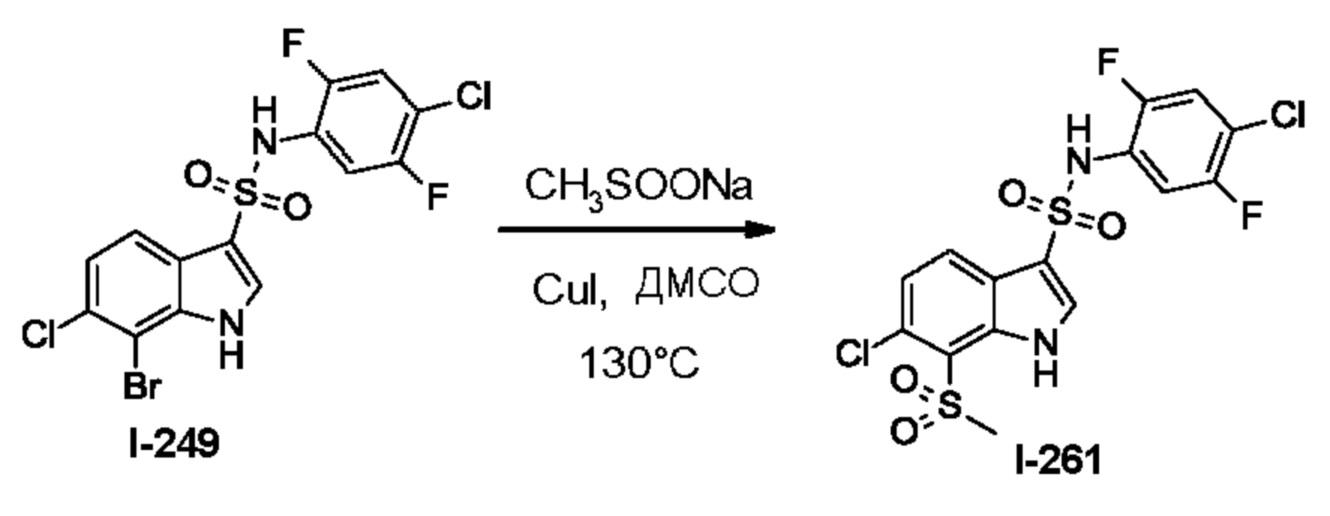
К раствору 7-бром-6-хлор-N-(4-хлор-2,5-дифторфенил)-1Н-индол-3-сульфонамида I-249 (0,15 г, 0,32 ммоля) в DMSO (10 мл) добавляли CuI (0,25 г, 1,29 ммоля) и метансульфонат натрия (0,13 г, 1,29 ммоля). Реакционную смесь нагревали при 130°С в течение 6 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли насыщенным раствором NH4Cl (35 мл), насыщенным раствором NaHCO3 (15 мл) и экстрагировали с помощью EtOAc (2×50 мл). Органический слой отделяли, сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 40% EtOAc в гексанах) и получали 6-хлор-N-(4-хлор-2,5-дифторфенил)-7-(метилсульфонил)-1Н-индол-3-сульфонамид I-261 (0,015 г) в виде почти белого твердого вещества.
Выход: 10%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 453 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,52 (s, 3Н) 7,36-7,40 (m, 1Н) 7,55 (d, J=8,80 Гц, 2H) 7,88 (d, J=3,42 Гц, 1H) 8,10 (d, J=8,80 Гц, 1H) 10,65 (brs, 1H) 11,76 (brs, 1H).
D.15. Методика H: Синтез 6-хлор-N-(5-хлор-3,6-дифторпиридин-2-ил)-7-метокси-1Н-индол-3-сульфонамида I-310
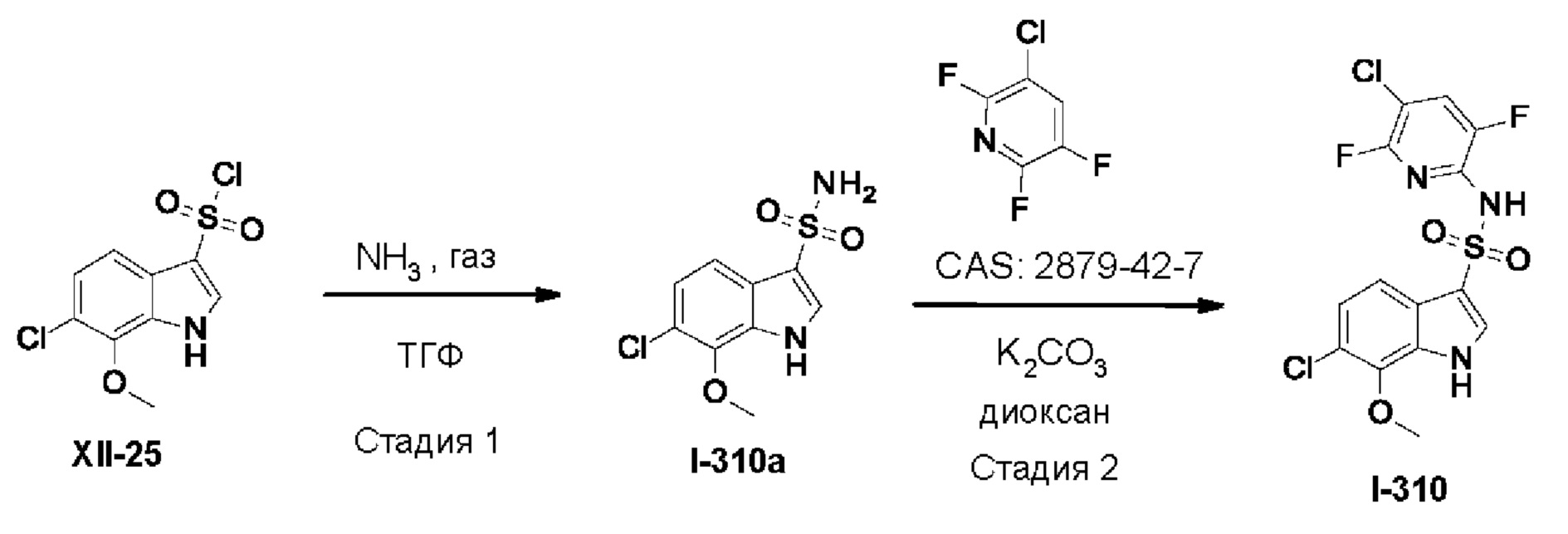
Стадия 1: Синтез 6-хлор-7-метокси-1Н-индол-3-сульфонамида I-310а:
Раствор 6-хлор-7-метокси-1H-индол-3-сульфонилхлорида XII-25 (170 мг, 0,265 ммоля) в THF (10 мл) при 0°С продували газообразным NH3 в течение 10 мин. Реакционную смесь перемешивали при комнатной температуре в течение 30 мин. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь концентрировали в вакууме. Неочищенное вещество промывали смесью DCM:гексан (1:4, 10 мл) и получали 6-хлор-7-метокси-1Н-индол-3-сульфонамид I-310а (150 мг) в виде коричневого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 78%.
ЖХМС в щелочной среде, методика 2 (ЭР+): 259 (МН)+, чистота 36%.
Стадия 2: Синтез 6-хлор-N-(5-хлор-3,6-дифторпиридин-2-ил)-7-метокси-1Н-индол-3-сульфонамида I-310:
При перемешивании к раствору 6-хлор-7-метокси-1Н-индол-3-сульфонамида I-310а (100 мг, 0,384 ммоля) и 3-хлор-2,5,6-трифторпиридина (64,3 мг, 0,384 ммоля) в 1,4-диоксане (10 мл) при КТ добавляли K2CO3 (53 мг, 0,384 ммоля). Реакционную смесь нагревали при 100°С в течение 8 ч. За протеканием реакции следили с помощью TLC. После завершения реакции реакционную смесь фильтровали через слой целита. Фильтрат концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии (диоксид кремния, 100-200 меш, 10-50% EtOAc в гексанах) и получали 60 мг соединения; которое повторно очищали с помощью препаративной TLC с использованием 40% EtOAc в гексане и получали 6-хлор-N-(5-хлор-3,6-дифтор-2-пиридил)-7-метокси-1Н-индол-3-сульфонамид I-310 (14 мг) в виде почти белого твердого вещества.
Выход: 9%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 406 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,91 (s, 3 Н) 7,25 (d, J=8,80 Гц, 1 Н) 7,63 (d, J=8,31 Гц, 1 Н) 8,10 (br s, 1 Н) 8,17 - 8,24 (m, 1 Н) 11,52 (br s, 1 Н) 12,58 (brs, 1 Н).
Соединения, приведенные ниже в таблице 8, можно синтезировать по методикам, аналогичным методике Н.
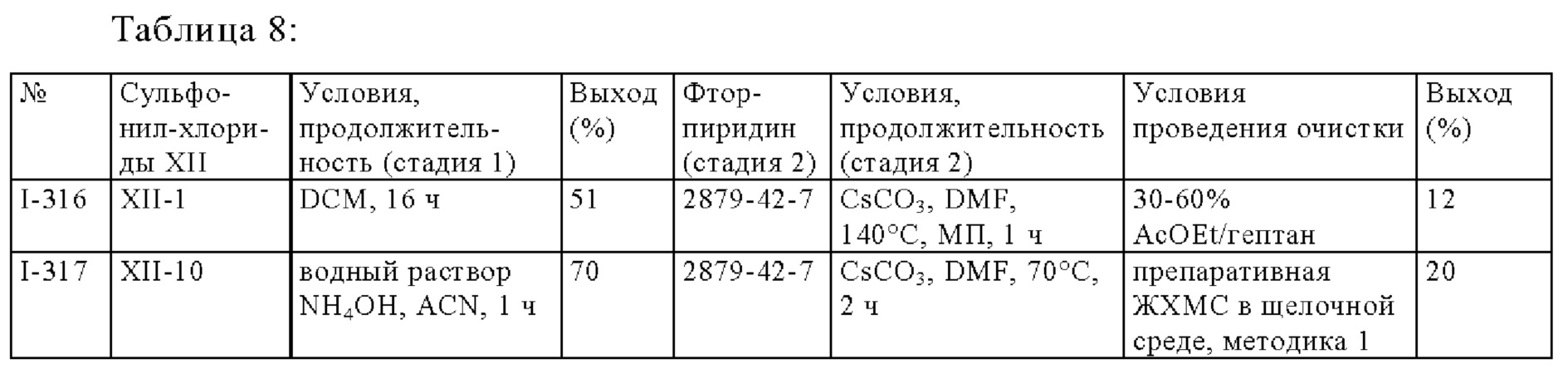
N-(5-Хлор-3,6-дифторпиридин-2-ил)-1Н-пирроло[3,2-h]хинолин-3-сульфонамид I-316
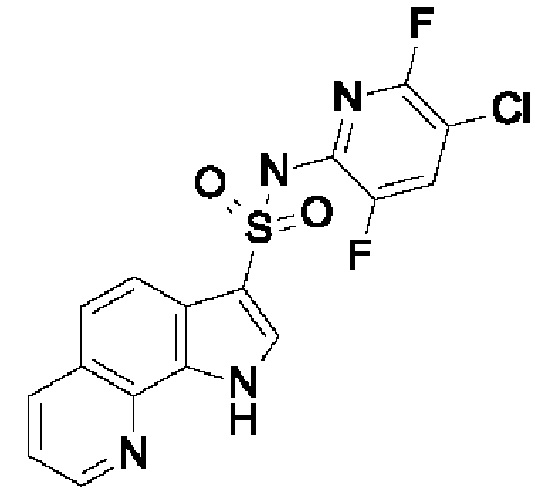
ЖХМС в щелочной среде, методика 1 (ЭР+): 395 (М+Н)+, чистота 98%.
1Н ЯМР (400 МГц, DMSO-d6) δ 13,29 (s, 1Н), 11,52 (s, 1H), 8,92 (dd, J = 4,3, 1,7 Гц, 1H), 8,45 (dd, J = 8,2, 1,7 Гц, 1H), 8,23 - 8,03 (m, 3Н), 7,72 (d, J = 8,8 Гц, 1H), 7,58 (dd, J = 8,2, 4,3 Гц, 1H).
N-(5-Хлор-3,6-дифторпиридин-2-ил)-1,6,7,8-тетрагидроциклопента[g]-индол-3-сульфонамид I-317
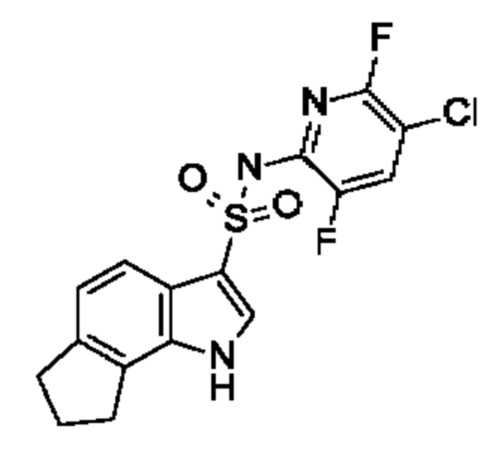
ЖХМС в щелочной среде, методика 1 (ЭР+): 384 (М+Н)+, чистота 93%.
D.16. Синтез N-(4-хлор-2,5-дифторфенил)-2-фтор-6-метокси-1Н-индол-3-сульфонамида I-318
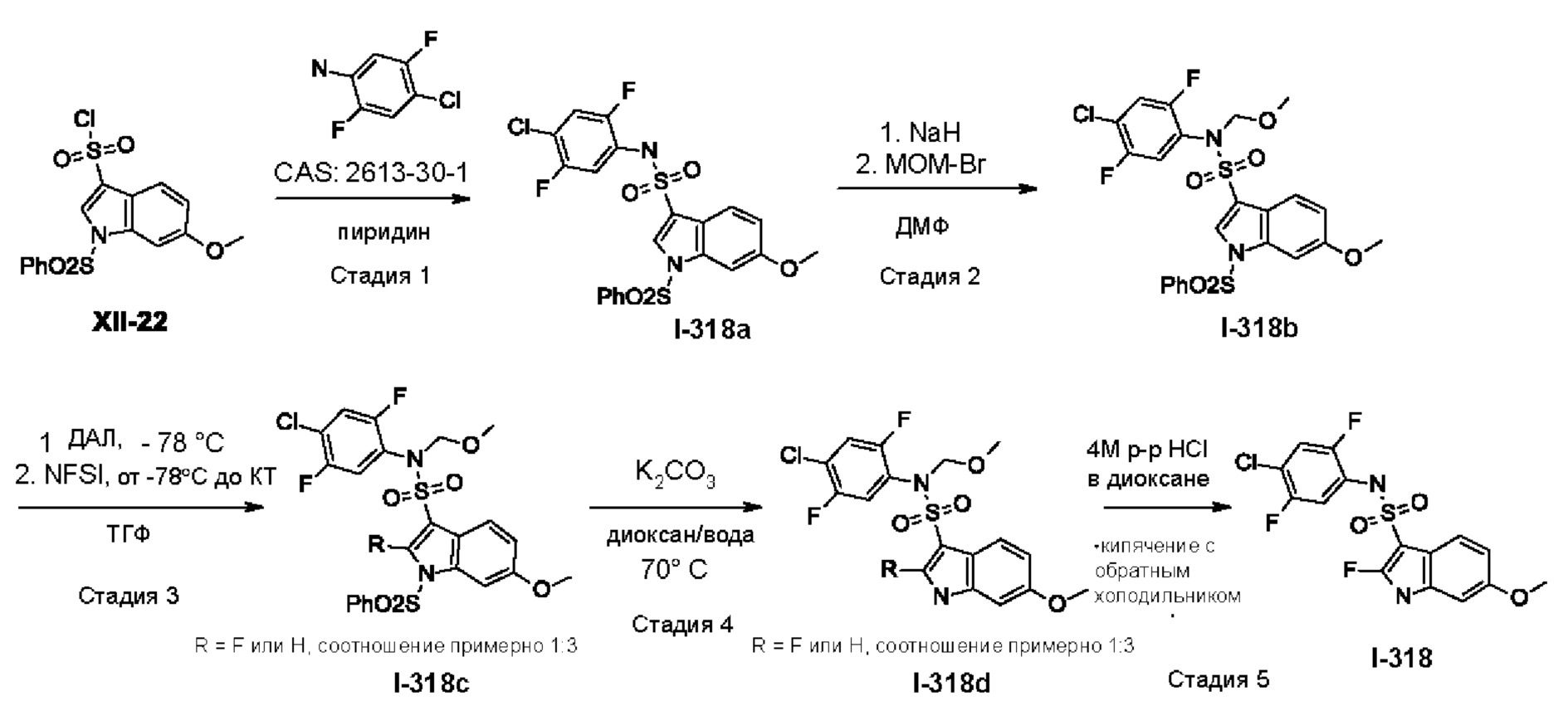
Стадия 1: Синтез N-(4-хлор-2,5-дифторфенил)-6-метокси-1-(фенилсульфонил)-1Н-индол-3-сульфонамида I-318а
Индол XII-22 (1,348 г, 3,49 ммоля) и 4-хлор-2,5-дифторанилин (569 мг, 3,48 ммоля) в пиридине (5 мл) нагревали при 80°С в течение 1 ч. Маслообразный остаток разбавляли этилацетатом, дважды промывали рассолом, сушили над сульфатом магния и выпаривали досуха. Неочищенный остаток затем растворяли в метаноле (150 мл) и кипятили с обратным холодильником до растворения большей части продукта. Затем раствор выпаривали до обеспечения объема, равного примерно 50 мл. После охлаждения до КТ осадок отфильтровывали. Затем его переносили в дихлорметан (12 мл), обрабатывали ультразвуком и повторно отфильтровывали и получали искомый продукт I-318а (763 мг) в виде почти белого твердого вещества. Очистка маточных растворов с помощью флэш-хроматографии (SiO2, дихлорметан) дополнительно давала 273 мг искомого продукта I-318а
Выход: 58%
ЖХМС в нейтральной среде, методика 3 (ЭР+): 512,9 (М+Н)+, чистота 97%.
1Н ЯМР (600 МГц, CDCl3) δ: 8,03 (s, 1Н), 7,84 (d, J = 7,5 Гц, 2Н), 7,63 (t, J = 7,5 Гц, 1H), 7,58 (d, J = 8,8 Гц, 1Н), 7,49 (t, J = 7,8 Гц, 2Н), 7,46 (d, J = 2,2 Гц, 1Н), 7,43 (dd, J = 9,6, 6,8 Гц, 1H), 7,06 (br s, 1H, NH), 6,97 - 6,92 (m, 2H), 3,87 (s, 3H).
Стадия 2: Синтез N-(4-хлор-2,5-дифторфенил)-6-метокси-N-(метоксиметил)-1-(фенилсульфонил)-1Н-индол-3-сульфонамида I-318b
В атмосфере аргона I-318а (200 мг, 0,39 ммоля) и гидрид натрия (60% дисперсия в минеральном масле, 19 мг, 0,47 ммоля) помещали в сухой диметилформамид (2,5 мл). Раствор перемешивали при КТ в течение 15 мин, затем добавляли бромметилметиловый эфир (36 мкл, 0,47 ммоля) в сухом DMF (1,5 мл) и раствор перемешивали при КТ в течение 2,5 ч. Реакцию останавливали водой, смесь трижды экстрагировали этилацетатом, промывали рассолом, сушили над сульфатом магния и выпаривали досуха. Неочищенный остаток очищали с помощью флэш-хроматографии (SiO2, CombiFlash, от 10 до 20% AcOEt в петролейном эфире) и получали искомый продукт I-318b (187 мг) в виде бесцветного масла.
Выход: 86%
1H ЯМР (600 МГц, CDCl3) δ: 7,92 - 7,86 (m, 3Н), 7,65 (t, J = 7,7 Гц, 1H), 7,52 (t, J = 7,9 Гц, 2Н), 7,49 (s, 1Н), 7,42 (d, J = 9,1 Гц, 1H), 7,12 (dd, J = 8,7, 6,3 Гц, 1Н), 7,02 (dd, J = 9,0, 6,4 Гц, 1Н), 6,93 (dd, J = 8,7, 2,4 Гц, 1Н), 5,01 (d, J = 2,2 Гц, 2Н), 3,89 (d, J = 2,1 Гц, 3Н), 3,42 (d, J = 2,1 Гц, 3Н).
ЖХМС в нейтральной среде, методика 3 (ЭР+): 574,1 (M+NH4)+, чистота 98%.
Стадия 3: Синтез N-(4-хлор-2,5-дифторфенил)-2-фтор-6-метокси-N-(метоксиметил)-1-(фенилсульфонил)-1Н-индол-3-сульфонамида I-318с
В атмосфере аргона в колбу помешали I-318b (160 мг, 0,287 ммоля) в сухом тетрагидрофуране (1,5 мл) и раствор охлаждали до -78°С. Затем готовили свежий диизопропиламид лития (ДАЛ) путем проводимого при -78°С и по каплям добавления n-BuLi (1,6 М в гексанах, 341 мкл, 0,545 ммоля) к раствору диизопропиламина (81 мкл, 0,574 ммоля) в сухом тетрагидрофуране (2 мл). Затем этот раствор по каплям добавляли к реакционной смеси, которую затем перемешивали при -78°С в течение 50 мин. Затем добавляли N-фторбензолсульфонимид (136 мг, 0,430 ммоля) в сухом тетрагидрофуране (2 мл) и реакционной смеси в течение ночи давали медленно нагреться до комнатной температуры. Затем реакцию в растворе останавливали водой, смесь трижды экстрагировали дихлорметаном, промывали рассолом, сушили над сульфатом магния и выпаривали досуха. Неочищенный остаток очищали с помощью флэш-хроматографии (SiO2, CombiFlash, от 10 до 20% AcOEt в петролейном эфире) и получали искомый продукт I-318с в виде смеси с исходным веществом I-318b (соотношение равно примерно 1:3, 66 мг), представляющей собой светло-желтое масло. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 592,0 (M+NH4)+.
Стадия 4: Синтез N-(4-хлор-2,5-дифторфенил)-2-фтор-6-метокси-N-(метоксиметил)-1H-индол-3-сульфонамида I-318d
I-318с (смесь с I-318b, соотношение равно примерно 1:3, 60 мг, примерно 0,13 ммоля) и карбонат калия (73 мг, 0,525 ммоля) помещали в диоксан (2 мл) и воду (1 мл) и перемешивали при 70°С в течение 4 ч. Затем реакционную смесь обрабатывали 0,1 М водным раствором хлористоводородной кислоты (4 мл), дважды экстрагировали этилацетатом, промывали рассолом, выпаривали досуха и сушили над сульфатом магния и получали искомое соединение I-318d в виде смеси с соответствующим нефторированным соединением (соотношение равно примерно 1:3, 39 мг), представляющей собой светло-зеленое твердое вещество. Это соединение использовали в следующей реакции без дополнительной очистки.
ЖХМС в нейтральной среде, методика 3 (ЭР+): 452,1 (M+NH4)+.
Стадия 5: Синтез N-(4-хлор-2,5-дифторфенил)-2-фтор-6-метокси-1Н-индол-3-сульфонамида I-318
I-318d (смесь с соответствующим нефторированным соединением, соотношение равно примерно 1:3, 39 мг, примерно 0,09 ммоля) помещали в 4 М раствор хлорида водорода в диоксане (2 мл) и кипятили с обратным холодильником в течение ночи. Затем реакцию останавливали насыщенным водным раствором гидрокарбоната натрия, смесь трижды экстрагировали дихлорметаном, промывали рассолом, сушили над сульфатом магния и выпаривали досуха. Неочищенный остаток очищали с помощью препаративной ВЭЖХ (препаративная ЖХМС в щелочной среде, методика 1) и получали чистый искомый продукт I-318 (4 мг)
Выход: 7% (за 2 стадии)
ЖХМС в щелочной среде, методика 1 (ЭР-): 389 (М-Н)-, чистота 100%.
D.17. Синтез этил-3-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)пропаноата I-331
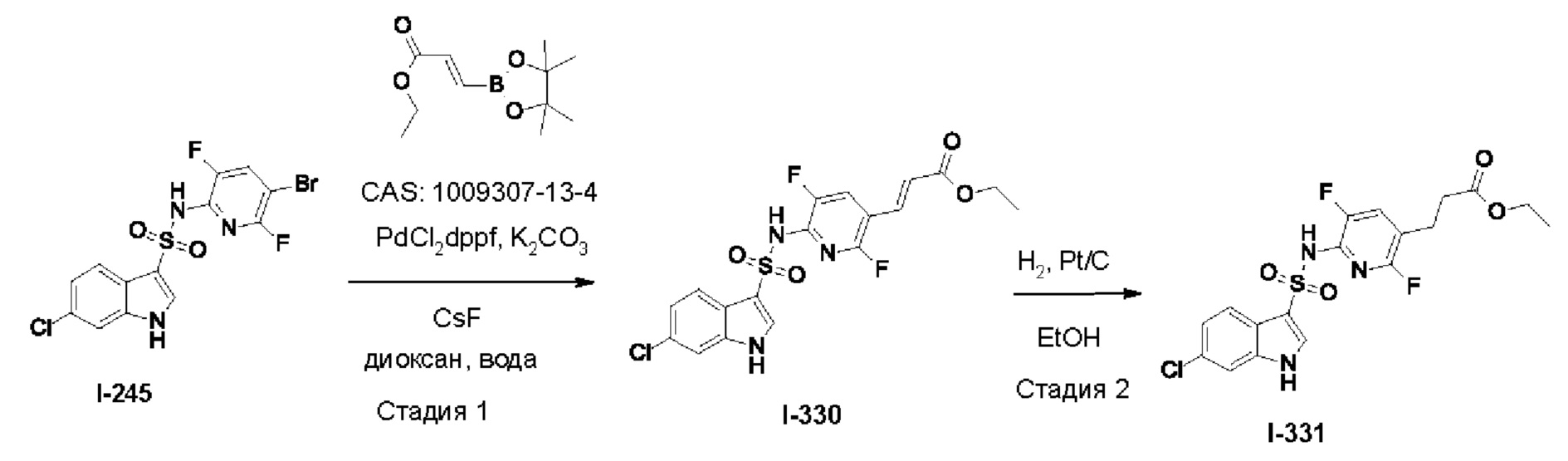
Стадия 1: Синтез этил-(2Е)-3-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)проп-2-еноата I-330
Смесь N-(5-бром-3,6-дифторпиридин-2-ил)-6-хлор-1Н-индол-3-сульфонамида I-245 (100 мг, 0,24 ммоля), пинаколового эфира 2-этоксикарбонилвинилбороновой кислоты (64 мг, 0,28 ммоля), [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (19 мг, 0,024 ммоля), фторида цезия (72 мг, 0,47 ммоля) и карбоната калия (99 мг, 0,71 ммоля) растворяли в смеси диоксан:вода (3:1, 2 мл) и продували аргоном, подаваемым через мембрану. Затем реакционную смесь перемешивали в микроволновой печи при 120°С в течение 20 мин. Смесь разбавляли водой и дважды экстрагировали этилацетатом. Объединенные органические слои сушили над MgSO4 и концентрировали путем выпаривания в роторном испарителе. Неочищенную смесь очищали с помощью препаративной ВЭЖХ (препаративная ЖХМС в щелочной среде, методика 1). Это давало 68 мг этил-(2Е)-3-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)проп-2-еноата I-330 в виде бежевого твердого вещества.
Выход: 65%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 440 (М-Н)-, чистота 98%.
Стадия 2: Синтез этил-3-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)пропаноата I-331
К раствору этил-(2Е)-3-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)проп-2-еноата I-330 (0,65 г, 3,26 ммоля) в EtOH (1,5 мл) добавляли Pt/C (6 мг) и реакционную смесь перемешивали при повышенном давлении водорода (3,5 бар), при комнатной температуре в течение 16 ч. После завершения реакции реакционную смесь фильтровали через слой целита и фильтрат концентрировали в вакууме. Неочищенную смесь очищали путем проведения двух последовательных очисток с помощью ВЭЖХ (в щелочной и в кислой среде) и получали 4 мг 3-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)пропаноата I-331 в виде белого твердого вещества.
Выход: 6%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 442 (М-Н)-, чистота 97%.
1H ЯМР (400 МГц, DMSO-d6) δ 12,14 (s, 1Н), 11,06 (s, 1H), 8,09 (d, J = 2,7 Гц, 1H), 7,84 (d, J = 8,6 Гц, 1H), 7,75 (t, J = 8,6 Гц, 1H), 7,54 (d, J = 1,9 Гц, 1H), 7,22 (dd, J = 8,6, 1,9 Гц, 1H), 3,99 (q, J = 7,1 Гц, 2H), 2,75 - 2,52 (m, 4H), 1,08 (t, J = 7,1 Гц, 3Н).
D.18. Синтез 6-хлор-N-[5-(2-этоксиэтил)-3,6-дифторпиридин-2-ил]-1Н-индол-3-сульфонамида I-333
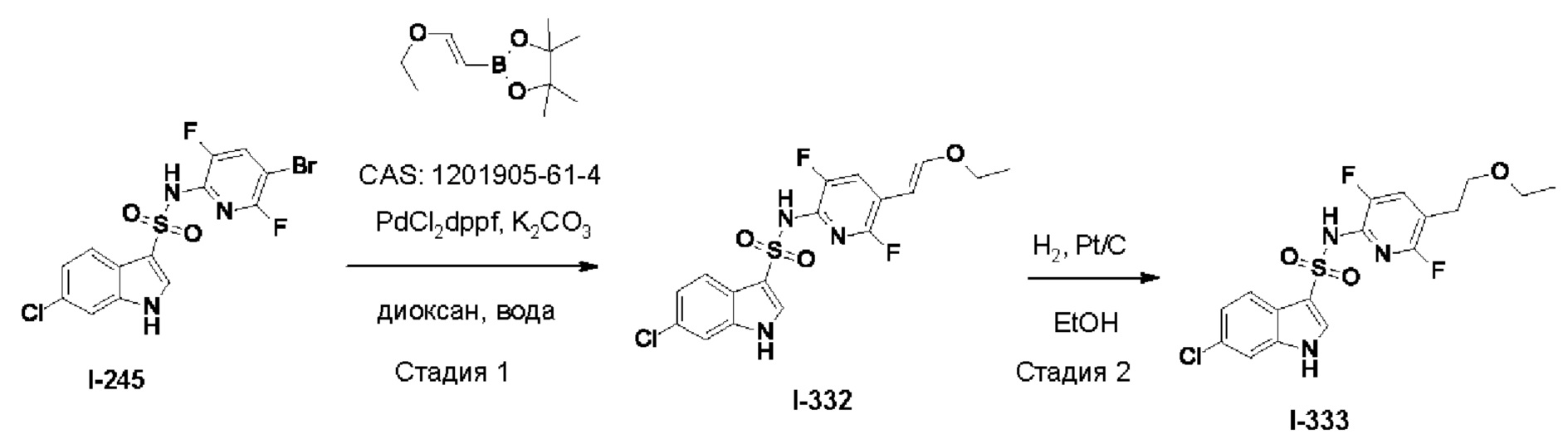
Стадия 1: Синтез 6-хлор-N-{5-[(Е)-2-этоксиэтенил]-3,6-дифторпиридин-2-ил}-1Н-индол-3-сульфонамида I-332
Смесь N-(5-бром-3,6-дифторпиридин-2-ил)-6-хлор-1Н-индол-3-сульфонамида I-245 (100 мг, 0,24 ммоля), пинаколового эфира (Е)-1-этоксиэтен-2-бороновой кислоты (58 мг, 0,28 ммоля), [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (19 мг, 0,024 ммоля) и карбоната калия (99 мг, 0,71 ммоля) растворяли в смеси диоксан:вода (3:1, 2 мл) и продували аргоном, подаваемым через мембрану. Затем реакционную смесь перемешивали в микроволновой печи при 120°С в течение 20 мин. Смесь разбавляли водой и дважды экстрагировали этилацетатом. Объединенные органические слои сушили над MgSO4 и концентрировали путем выпаривания в роторном испарителе. Неочищенную смесь очищали с помощью препаративной ВЭЖХ (препаративная ЖХМС в щелочной среде, методика 1). Это давало 25 мг 6-хлор-Н-{5-[(Е)-2-этоксиэтенил]-3,6-дифторпиридин-2-ил}-1H-индол-3-сульфонамида I-332 в виде бежевого твердого вещества.
Выход: 26%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 412 (М-Н)-, чистота 94%.
Стадия 2: Синтез 6-хлор-N-[5-(2-этоксиэтил)-3,6-дифторпиридин-2-ил]-1H-индол-3-сульфонамида I-333
К раствору 6-хлор-N-{5-[(Е)-2-этоксиэтенил]-3,6-дифторпиридин-2-ил}-1Н-индол-3-сульфонамида I-332 (0,20 г, 0,05 ммоля) в EtOH (0,5 мл) добавляли Pt/C (15 мг) и реакционную смесь перемешивали при повышенном давлении водорода (4 бар), при 50°С в течение 16 ч. После завершения реакции реакционную смесь фильтровали через слой целита и фильтрат концентрировали в вакууме. Неочищенную смесь очищали с помощью препаративной ВЭЖХ (препаративная ЖХМС в щелочной среде, методика 1) и получали 10 мг 6-хлор-N-[5-(2-этоксиэтил)-3,6-дифторпиридин-2-ил]-1Н-индол-3-сульфонамида I-333 в виде белого твердого вещества.
Выход: 50%.
ЖХМС в щелочной среде, методика 1 (ЭР ): 414 (М-Н)-, чистота 98%.
1H ЯМР (400 МГц, DMSO-d6) δ 12,12 (s, 1Н), 11,05 (s, 1H), 8,09 (d, J = 2,9 Гц, 1H), 7,86 (d, J = 8,6 Гц, 1H), 7,73 (t, J = 8,7 Гц, 1H), 7,54 (d, J = 1,9 Гц, 1H), 7,23 (dd, J = 8,6, 1,9 Гц, 1H), 3,50 (t, J = 6,5 Гц, 2H), 3,40 (d, J = 6,9 Гц, 2H), 2,67 (t, J = 6,5 Гц, 2H), 1,04 (t, J = 7,0 Гц, 3H).
D.19. Синтез 6-азидо-N-(4-циано-2-фторфенил)-1H-индол-3-сульфонамида I-335
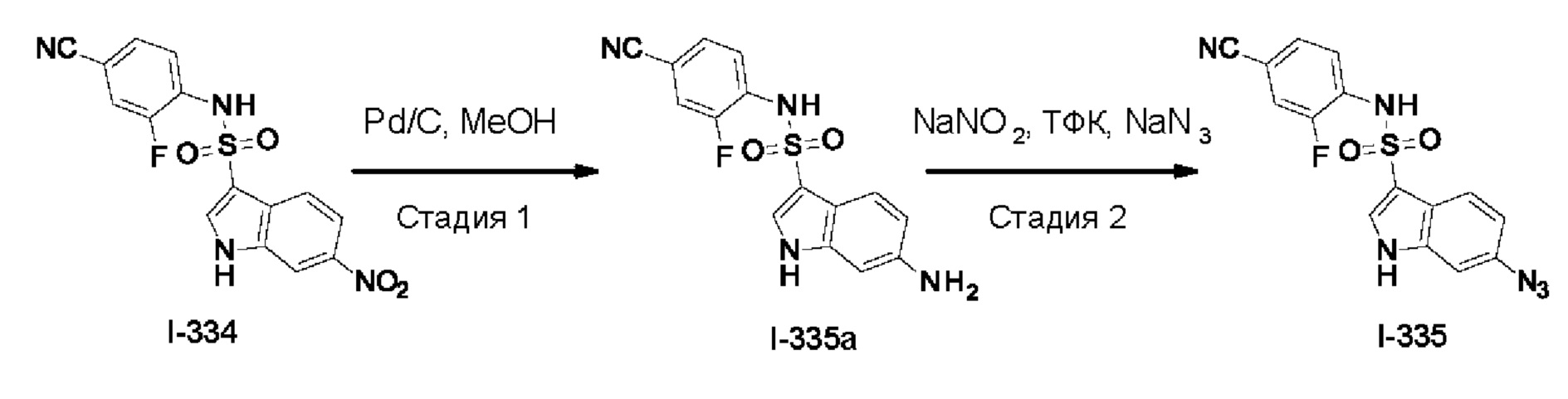
Стадия 1: Синтез 6-амино-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамида I-335а:
К раствору 6-нитро-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамида I-334 (0,50 г, 1,37 ммоля) в МеОН (20 мл) добавляли Pd/C (0,10 г, 1,02 ммоля). Реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 3 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через целит и фильтрат концентрировали в вакууме и получали 6-амино-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамид I-335а (0,40 г) в виде бледно-желтого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 90%.
ЖХМС в щелочной среде, методика 2 (ЭР+): 331 (М+Н)+, чистота 83%.
Стадия 2: Синтез 6-азидо-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамида I-335:
К раствору 6-амино-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамида I-335а (0,20 г, 0,50 ммоля) в TFA (5 мл) при 0°С добавляли NaNO2 (0,14 г, 2,02 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. При 0°С добавляли NaN3 (0,11 г, 1,77 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью H2O (150 мл) и экстрагировали с помощью EtOAc (200 мл). Органический слой отделяли, промывали рассолом (100 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии с использованием CombiFlash (25% EtOAc в гексанах) и получали 6-азидо-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамид I-335 (0,06 г, 31%) в виде желтого твердого вещества.
Выход: 31%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 355 (М-Н)-, чистота 93%.
1Н ЯМР (400 МГц, DMSO-d6) δ 6,99 (dd, J=8,00 Гц, 2,00 Гц, 1H) 7,17 (d, J=2,00 Гц, 1Н) 7,54-7,59 (m, 2Н) 7,74 (d, J=10,0 Гц, 1Н) 7,84 (d, J=8,80 Гц, 1H) 8,07 (d, J=2,80 Гц, 1Н) 10,80 (brs, 1H) 12,06 (brs, 1Н).
D.20. Синтез 6-хлор-N-(5-этил-3,6-дифторпиридин-2-ил)-1Н-индол-3-сульфонамида I-338
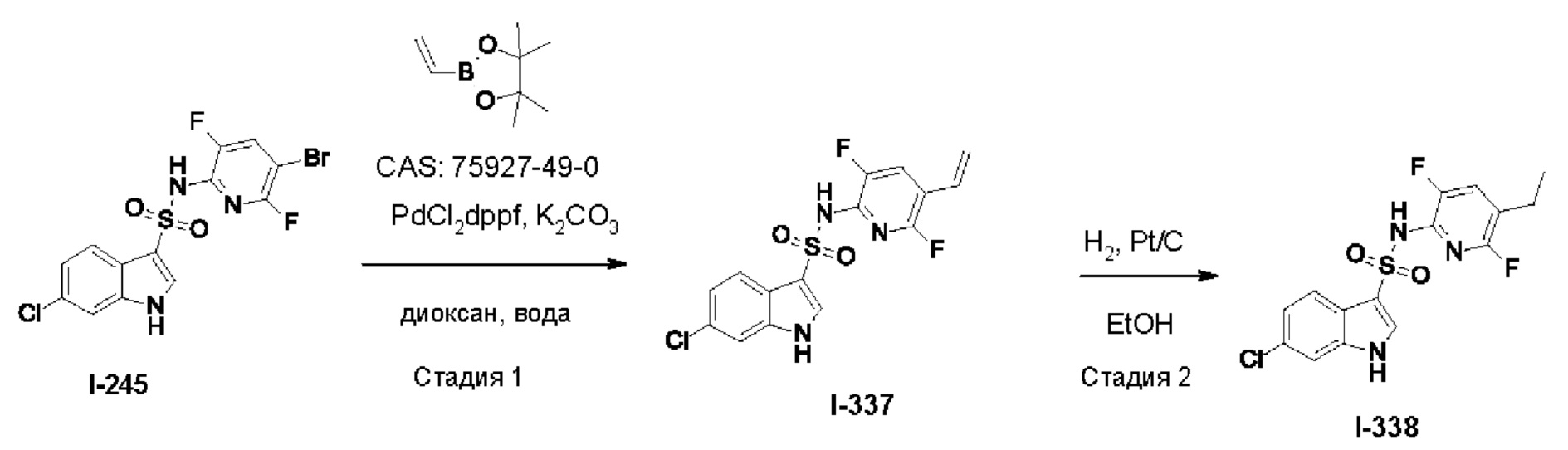
Стадия 1: Синтез 6-хлор-N-{5-[(Е)-2-этоксиэтенил]-3,6-дифторпиридин-2-ил}-1H-индол-3-сульфонамида I-332
Смесь N-(5-бром-3,6-дифторпиридин-2-ил)-6-хлор-1H-индол-3-сульфонамида I-245 (150 мг, 0,35 ммоля), пинаколового эфира винилбороновой кислоты (69 мг, 0,42 ммоля), [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (29 мг, 0,035 ммоля) и карбоната калия (149 мг, 1,06 ммоля) растворяли в смеси диоксан:вода (3:1, 3 мл) и продували аргоном, подаваемым через мембрану. Затем реакционную смесь перемешивали в микроволновой печи при 120°С в течение 40 мин. Смесь разбавляли водой и дважды экстрагировали этилацетатом. Объединенные органические слои сушили над MgSO4 и концентрировали в вакууме. Неочищенную смесь очищали с помощью препаративной ВЭЖХ (препаративная ЖХМС в щелочной среде, методика 1). Это давало 21 мг 6-хлор-N-(5-этенил-3,6-дифторпиридин-2-ил)-1H-индол-3-сульфонамида I-337 в виде бежевого твердого вещества.
Выход: 11%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 368 (М-Н)-, чистота 90%.
Стадия 2: Синтез 6-хлор-N-(5-этил-3,6-дифторпиридин-2-ил)-1H-индол-3-сульфонамида I-338
К раствору 6-хлор-N-(5-этенил-3,6-дифторпиридин-2-ил)-1H-индол-3-сульфонамида I-337 (85 мг, 0,17 ммоля) в EtOH (1,7 мл) добавляли Pt/C (17 мг) и реакционную смесь перемешивали при повышенном давлении водорода (3,5 бар), при комнатной температуре в течение 16 ч. После завершения реакции реакционную смесь фильтровали через слой целита и фильтрат концентрировали в вакууме. Неочищенную смесь очищали с помощью препаративной ВЭЖХ (препаративная ЖХМС в щелочной среде, методика 1) и получали 9 мг 6-хлор-N-(5-этил-3,6-дифторпиридин-2-ил)-1Н-индол-3-сульфонамида I-338 в виде белого твердого вещества.
Выход: 14%.
ЖХМС в щелочной среде, методика 1 (ЭР-): 370 (М-Н)-, чистота 99%.
1H ЯМР (400 МГц, DMSO-d6) δ 12,11 (s, 1Н), 10,99 (s, 1H), 8,08 (s, 1H), 7,85 (s, 1H), 7,73 (s, 1H), 7,55 (d, J = 5,5 Гц, 1H), 7,23 (d, J = 7,7 Гц, 1H), 2,47 (t, 2H), 1,09 (d, J = 7,3 Гц, 3Н).
D.21. Синтез 6-азидо-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамида I-353
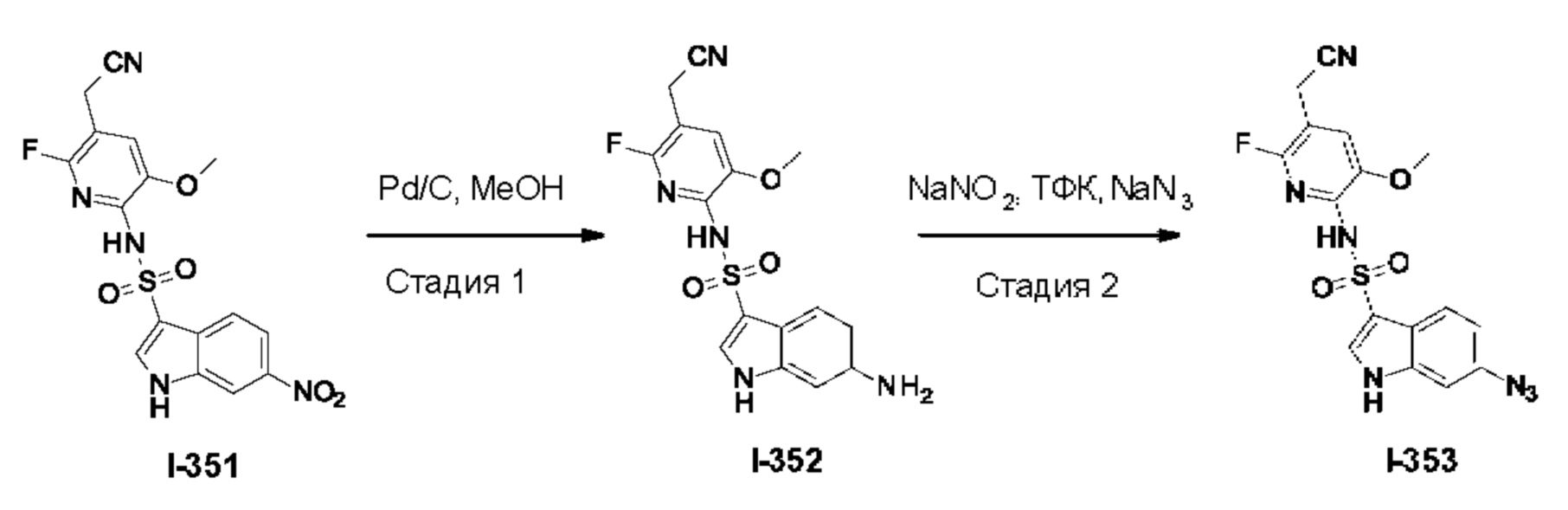
Стадия 1: Синтез 6-амино-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамида I-352:
К раствору N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-6-нитро-1Н-индол-3-сульфонамида I-351 (0,32 г, 0,69 ммоля) в МеОН (20 мл) добавляли 10% Pd/C (0,30 г, 2,82 ммоля) и реакционную смесь перемешивали при повышенном давлении водорода, при комнатной температуре в течение 1 ч. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь фильтровали через слой целита®, промывали с помощью МеОН (3×15 мл) и фильтрат концентрировали в вакууме и получали 6-амино-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид I-352 (0,241 г) в виде бледно-коричневого твердого вещества. Это соединение использовали в следующей реакции без дополнительной очистки.
Выход: 74%.
ЖХМС в щелочной среде, методика 2 (ЭР+): 376 (М+Н)+, чистота 79%.
Стадия 2: Синтез 6-азидо-N-(4-циано-2-фторфенил)-1Н-индол-3-сульфонамида I-353:
К раствору 6-амино-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамида I-352 (0,03 г, 0,06 ммоля) в TFA (2 мл) при 0°С добавляли NaNO2 (0,02 г, 0,25 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. При 0°С добавляли NaN3 (0,01 г, 0,22 ммоля) и реакционную смесь перемешивали при такой же температуре в течение 30 мин. За протеканием реакции следили с помощью TLC и ЖХМС. После завершения реакции реакционную смесь разбавляли с помощью Н2О (40 мл) и экстрагировали с помощью EtOAc (2×30 мл). Органический слой отделяли, промывали рассолом (20 мл), сушили над безводным Na2SO4 и концентрировали в вакууме. Реакцию повторяли с использованием 0,20 г исходного вещества и неочищенные вещества, полученные в 2 реакциях, смешивали в EtOAc (20 мл) и концентрировали в вакууме. Полученное неочищенное вещество очищали с помощью колоночной хроматографии с использованием CombiFlash (25% EtOAc в гексанах) и получали 6-азидо-N-[5-(цианометил)-3-фтор-6-метоксипиридин-2-ил]-1Н-индол-3-сульфонамид I-353 (0,032 г) в виде бледно-коричневого твердого вещества
Выход: 13%.
ЖХМС в щелочной среде, методика 2 (ЭР-): 400 (М-Н)-, чистота 96%.
1H ЯМР (400 МГц, DMSO-d6) δ 3,63 (s, 3Н) 3,70 (s, 2Н) 6,97 (d, J=8,03 Гц, 1Н) 7,20 (s, 1H) 7,62 (d, J=9,54 Гц, 1H) 7,87 (d, J=8,28 Гц, 1Н) 8,12 (s, 1H) 11,03 (brs, 1Н) 11,97 (brs, 1H).
D.22. Синтез этил-2-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)циклопропанкарбоксилата I-359
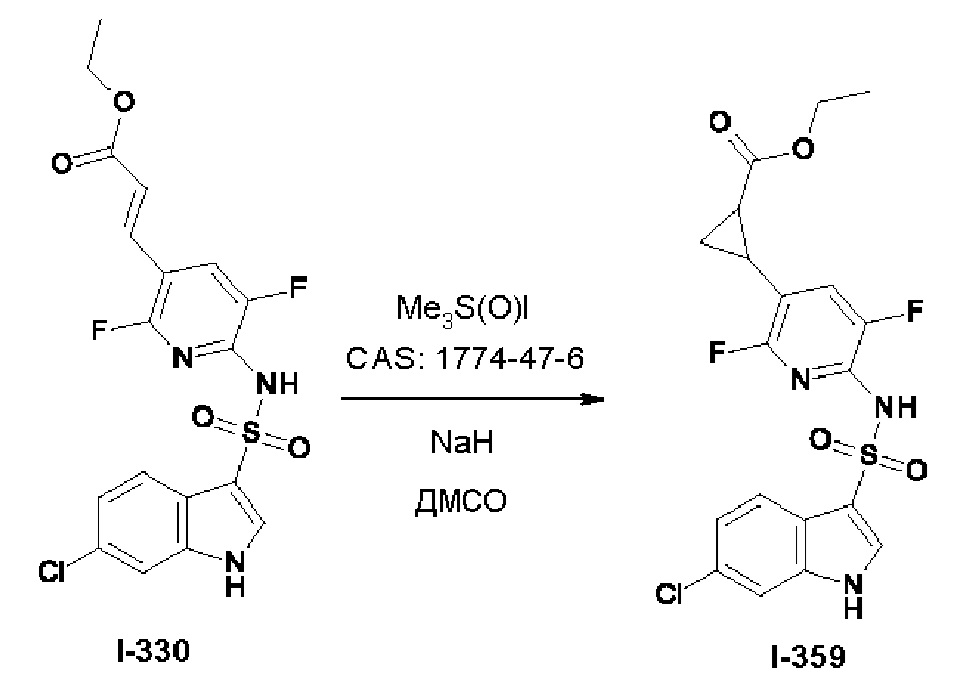
Триметилсульфоксониййодид (66,75 мг, 0,30 ммоля) и гидрид натрия (11,59 мг, 0,29 ммоля) смешивали в диметилсульфоксиде (1,0 мл). Реакционную смесь перемешивали до получения прозрачного бесцветного раствора. Затем добавляли этил-(2Е)-3-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)проп-2-еноат I-330 (100 мг, 0,23 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 20 мин, затем нагревали при 50°С в течение ночи. К реакционной смеси добавляли свежеприготовленные раствор смеси триметилсульфоксониййодида (66,75 мг, 0,30 ммоля) и гидрида натрия (11,59 мг, 0,29 ммоля) в диметилсульфоксиде (1,0 мл) и нагревание продолжали при 50°С в течение 3 ч. Реакционную смесь разбавляли водой и трижды экстрагировали этилацетатом. Органический слой сушили над сульфатом магния, концентрировали в вакууме и неочищенное соединение очищали с помощью хроматографии (препаративная TLC, элюирование смесью дихлорметан/МеОН - 95/5) и получали 12 мг этил-2-(6-{[(6-хлор-1Н-индол-3-ил)сульфонил]амино}-2,5-дифторпиридин-3-ил)циклопропанкарбоксилата I-359, в виде желтого твердого вещества.
Выход: 10%.
ЖХМС в щелочной среде, методика 1 (ЭР+): 456 (М+Н)+, чистота 88%.
Дополнительные соединения примеров, приведенные в таблице 9, получали по описанным выше методикам:
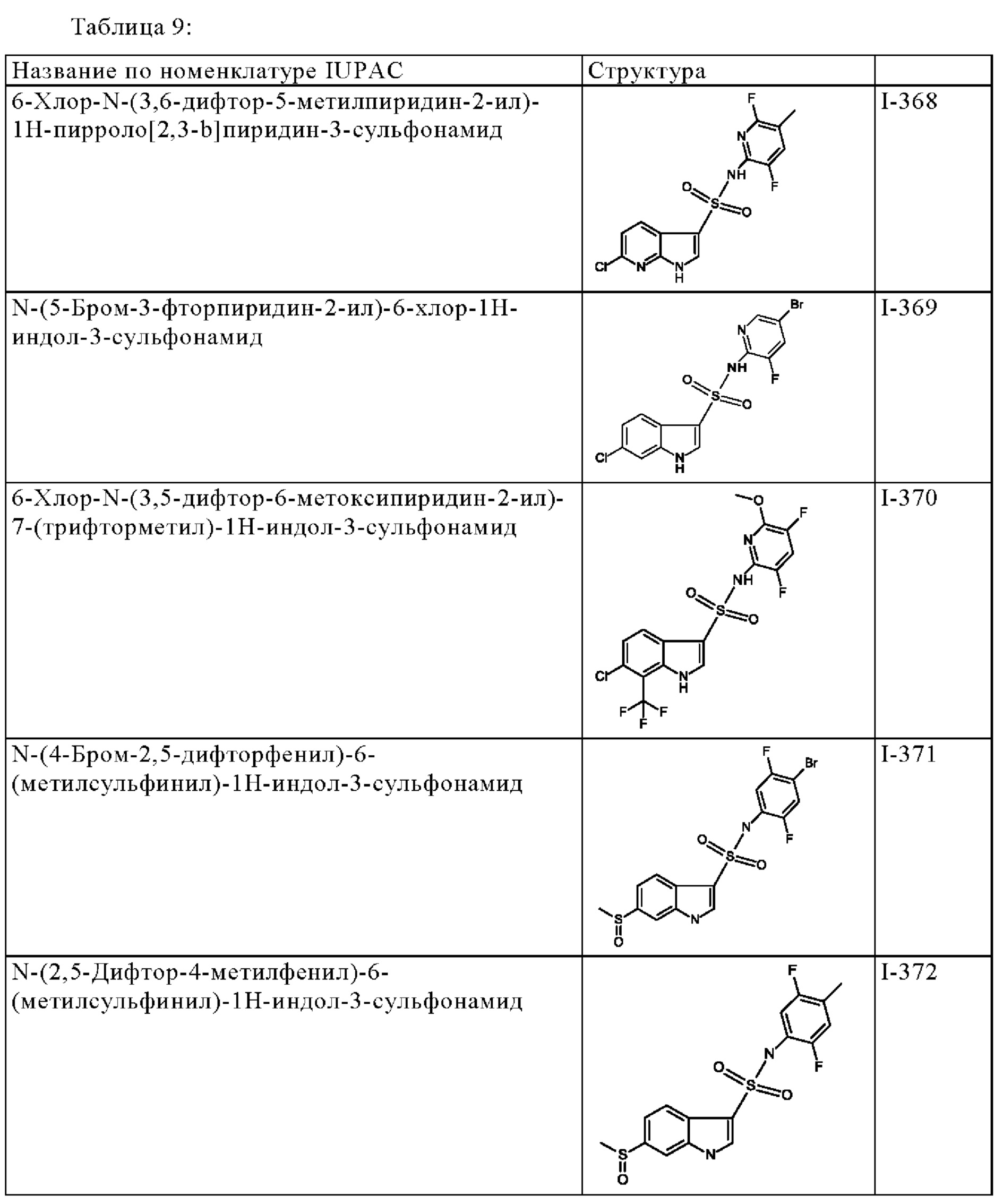
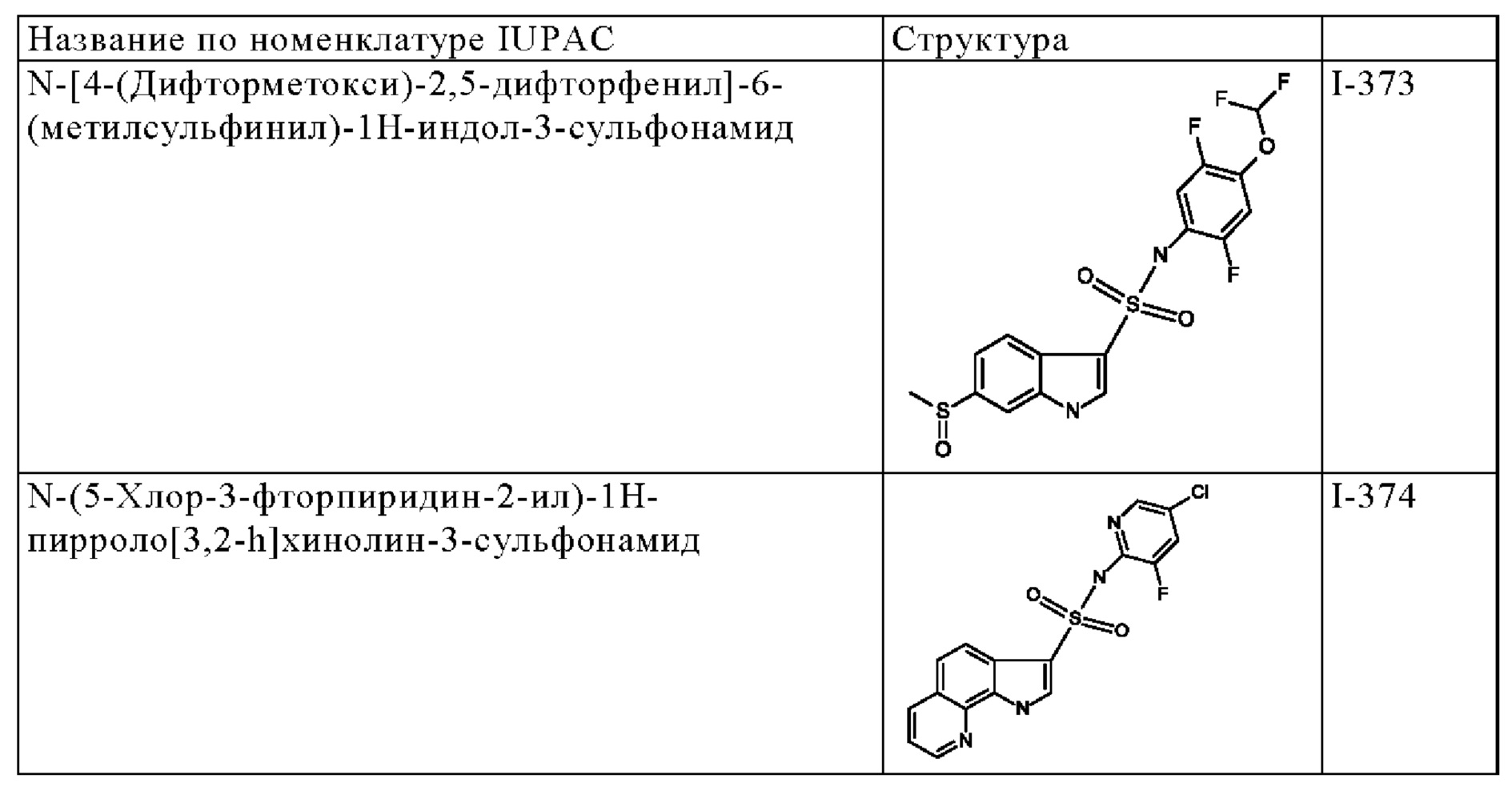
Проводили исследования образцов и их активности по данным исследований Са2+ и сАМР дополнительно приведены в представленной ниже таблице 10.
В. БИОЛОГИЯ/ФАРМАКОЛОГИЯ:
B-I. Культуры клеток
Рекомбинантная линия клеток GPR17:
Клетки Flp-In T-REx СНО, стабильно экспрессирующие рецептор GPR17 (СНО hGPR17), полученные из лаборатории Evi Kostenis (Bonn University, Germany) культивировали при 37°C в увлажненной атмосфере, содержащей 5% СО2. Клетки выращивали в МДСИ (модифицированная по методике Дульбекко среда Игла) с добавлением питательной смеси F-12 и с добавлением гигромицина В (500 мкг/мл) и бластицидина (30 мкг/мл). Экспрессирование из локуса Flp-In индуцировали путем обработки доксициклином (1 мкг/мл) за 16-20 ч до проведения исследований.
Первичные олигодендроциты:
Клетки-предшественники первичных олигодендроцитов (ОРС) выделяли из переднего мозга детенышей крыс Wistar в день 0-2 после рождения. Образцы головного мозга отбирали механически с помощью шприца и двух разных полых игл (сначала 1,2×40 и затем 0,60×30). Не содержащую комков суспензию клеток фильтровали через устройство для просеивания клеток с отверстиями размером 70 мкм и помещали в матрац для клеточных культур площадью 75 см2 не покрытием из поли-D-лизина со средой МДСИ с добавлением 10% (об./об.) термически инактивированной фетальной телячьей сыворотки, пенициллина (100 Ед./мл) и стрептомицина (0,1 мг/мл), причем каждый второй день проводили замену среды. После выдерживания при 37°С в увлажненной атмосфере, содержащей 5% СО2, в течение.8-11 дней смешанные культуры встряхивали при 240 об/мин в течение 14-24 ч для отделения ОРС от астроцитов и микроглии. Для дополнительного обогащения с помощью ОРС суспензию помещали в не содержащие покрытия чашки Петри на 45 мин. Затем ОРС высевали в планшеты с покрытием из поли-L-орнитина и выдерживали при 37°С в увлажненной атмосфере, содержащей 5% СО2, в среде для пролиферации Neurobasal с добавлением 2% (об./об.) В27, 2 мМ GlutaMAX, 100 Ед/мл пенициллина, 0,1 мг/мл стрептомицина, 10 нг/мл PDGF-AA (рецептор тромбоцитарного фактора роста) и 10 нг/мл щелочного раствора FGF (фактор роста фибробластов), проводя замену среды через день.
В-II: Функциональные исследования GPR17 in vitro
В-II-1: Функциональное исследование мобилизации кальция
GPR17 представляет собой рецептор, связанный с белком G. Активация GPR17 запускает передачу сигнала белка G типа Gq, что приводит к выделению кальция (Са2+) из депо - эндоплазматического ретикулума в цитозоль, количество можно определить с помощью красителя Calcium 5, флуоресцентного индикаторного красителя для определения концентрации Са2+ в цитозоле. Все соединения примеров испытывали с использованием исследования Са2+ для GPR17 для определения (скрининга) их способности модулировать GPR17.
Описание исследования Са2+:
Клетки СНО hGPR17 оттаивали и высевали в черные 384-луночные планшеты с прозрачным дном при плотности, равной 20000 клеток/лунка. Клетки инкубировали при 37°С в увлажненной атмосфере, содержащей 5% СО2, в течение ночи. Через 16-22 ч после высевания к клеткам СНО hGPR17 в течение 60 мин добавляли краситель Calcium 5, флуоресцентный индикаторный краситель для определения концентрации Са2+ в цитозоле, в соответствии с инструкциями изготовителя. Зависимость интенсивности флуоресценции от концентрации Са2+ в цитозоле в течение времени определяли при комнатной температуре в помощью устройства для считывания FLIPR Tetra. Клетки сначала инкубировали при комнатной температуре в течение 30 мин в буфере ССРХ (сбалансированный солевой раствор Хенкса) - Hepes (N-2-гидроксиэтилпиперазин-N-2-этансульфоновая кислота), обладающем значением рН, равным 7,4, содержащем исследуемые соединения при увеличивающейся концентрации (обычно от 10-11 до 10-6М). Затем к клеткам добавляли 50 нМ MDL29,951, агониста GPR17. Определяли ингибирующее воздействие исследуемых соединений при разных концентрациях и определяли значения pIC50. Все инкубирования повторяли дважды и результаты сопоставляли с зависимостью концентрация-эффект для эталонных соединений - агониста и антагониста GPR17. Анализ и аппроксимацию зависимости проводили с помощью программного обеспечения ActivityBase ХЕ с использованием 4-параметрического логистического уравнения XLfit: у = А + ((В-A)/(1+((C/x)^D))), где А, В, С и D означают минимальное значение у, максимальное значение у, IC50 и угол наклона соответственно.
Результаты исследования Са2+:
По данным исследования мобилизации Са2+ соединения, приведенные в примерах, предпочтительно обладают значениями pIC50, большими или равными 6,5; более предпочтительно большими или равными 7,5 и еще более предпочтительно большими или равными 8,5. Активности исследованных соединений примеров представлены в таблице в приведенном ниже разделе В-IIB. Диапазоны активностей А, В и С означают следующие значения pIC50, полученные в исследовании Са2+: "А": pIC50 <7,5, "В": pIC50 7,5 < х ≤ 8,5, "С": pIC50 >8,5.
В-IIB. Функциональное исследование накопления сАМР
Активация GPR17 также может обеспечить передачу сигнала белка G типа Gi, что приводит к уменьшению концентрации внутриклеточного циклического аденозинмонофосфата (сАМР). Изменение концентрации внутриклеточного сАМР можно определить с использованием набора для динамического исследования сАМР с помощью ОФРВ, выпускающегося фирмой CisBio (Codolet, France). В исследовании использовали методику однородной флуоресценции с разрешением по времени (ОФРВ) и оно основано на определении конкурентности между нативным сАМР, продуцируемым клетками, и сАМР, меченым с помощью красителя d2. Связывание метки определяли с использованием антител к сАМР, меченых криптатом.
Типичные соединения, которые обладали активностью в исследовании Са2+, также испытывали с помощью этого исследования с AMP для GPR17. Это исследование проводили в качестве подтверждающего исследования с использованием некоторых типичных соединений примеров, а не всех соединений, предлагаемых в настоящем изобретении.
Описание исследования сАМР
Клетки СНО hGPR17 разводили в ЗФФ (забуференный фосфатом физиологический раствор), содержащем ЭДТК (этилендиаминтетрауксусная кислота), и помещали в черные 384-луночные планшеты при плотности, равной 5000 клеток/лунка. Клетки сначала инкубировали при комнатной температуре в течение 30 мин в буфере ССРХ - Hepes (рН 7,4), содержащем разбавитель или исследуемые соединения - антагонисты/обратные агонисты GPR17 при разных концентрациях. Затем к разбавителю и к соединению - антагонисту/обратному агонисту GPR17 при каждой концентрации добавляли агонист GPR17, MDL29,951, в соответствии с зависимостью доза-ответ (обычно от 10-5 до 10-10 М) при конечном объеме буфера ССРХ - Hepes (рН 7,4), содержащего 1% DMSO, 5 мкМ форсколина и 0,1 мМ ИБМК (8-метоксиметил-3-изобутил-1-метилксантин), равном 20 мкл. После инкубирования при комнатной температуре в течение 60 мин реакцию останавливали и клетки лизировали путем добавления реагента для детектирования d2 и содержащего криптат реагента в 10 мкл буфера для лизиса в соответствии с инструкциями изготовителя. После инкубирования в течение 60 мин определяли изменение концентраций сАМР в соответствии с инструкциями изготовителя с использованием устройства для считывания планшетов Envision при возбуждении лазером. Все инкубирования повторяли дважды. Результаты анализировали с помощью программного обеспечения GraphPad Prism с использованием 4-параметрического логистического уравнения для определения pEC50 для MDL29,951 при отсутствии и в присутствии исследуемых соединений - антагонистов/обратных агонистов GPR17. Строили зависимость отношения доз (ОД) от концентрации антагониста и с помощью анализа по методике Шильда получали рассчитанное сродство рА2 для соединений - антагонистов/обратных агонистов GPR17.
Результаты исследования с AMP:
По данным исследования сАМР соединения, приведенные в примерах, обычно обладают значениями рА2, большими или равными 6,5; предпочтительно большими или равными 7,5; более предпочтительно большими или равными 8,5. Активности исследованных соединений примеров приведены в представленной ниже таблице. Диапазоны активностей А, В и С означают следующие значения рА2, полученные в исследовании сАМР: "А": рА2 <7,5, "В": рА2 7,5 < х ≤ 8,5, "С": рА2 >8,5.
В представленной ниже таблице 10 приведены значения pIC50 и рА2 для соединений примеров, изученных с помощью исследований Са2+ и сАМР. Отсутствие результата в столбце со значениями рА2 означает, что соответствующие соединения не исследовали или что результат еще не получен.
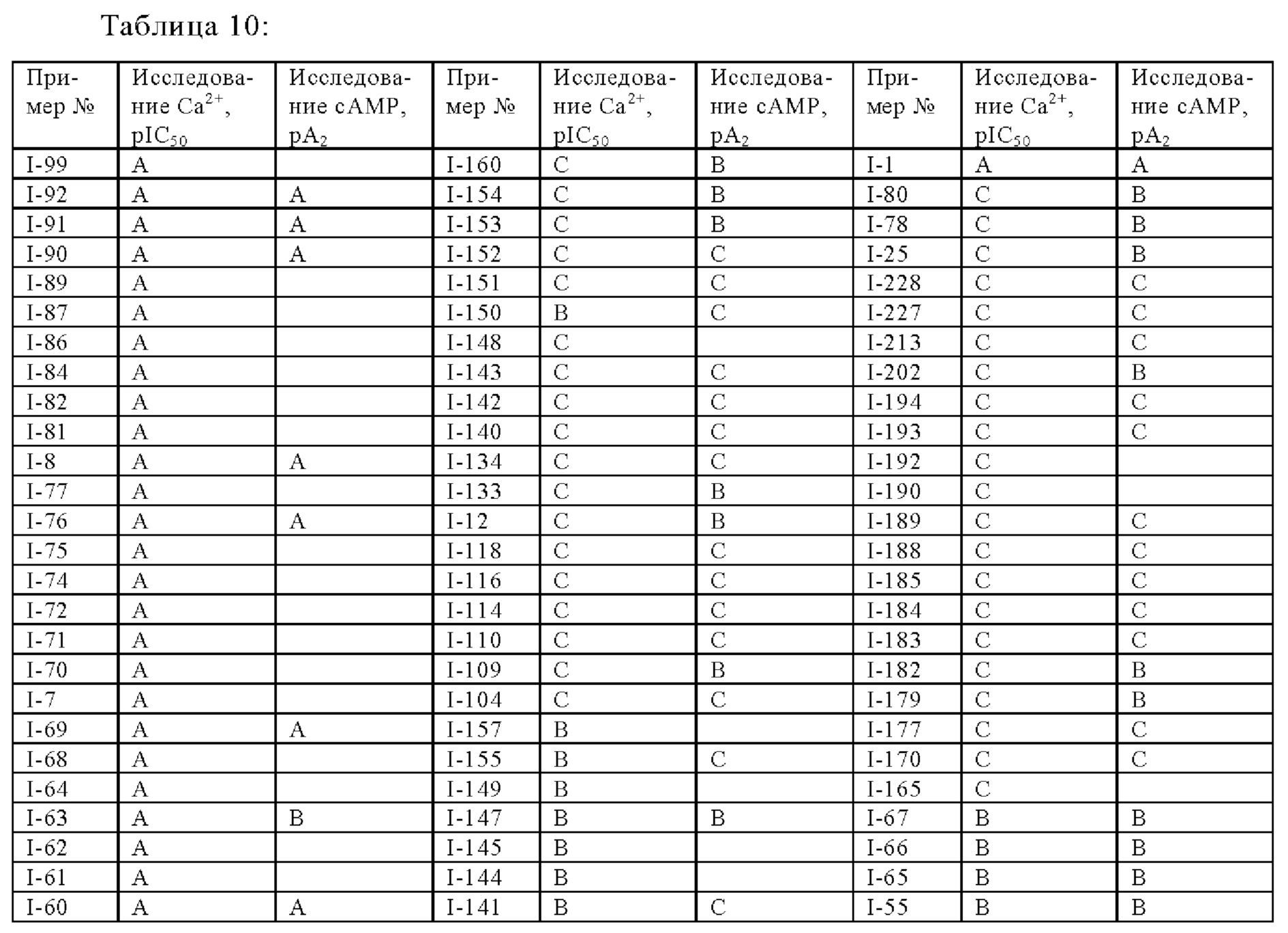
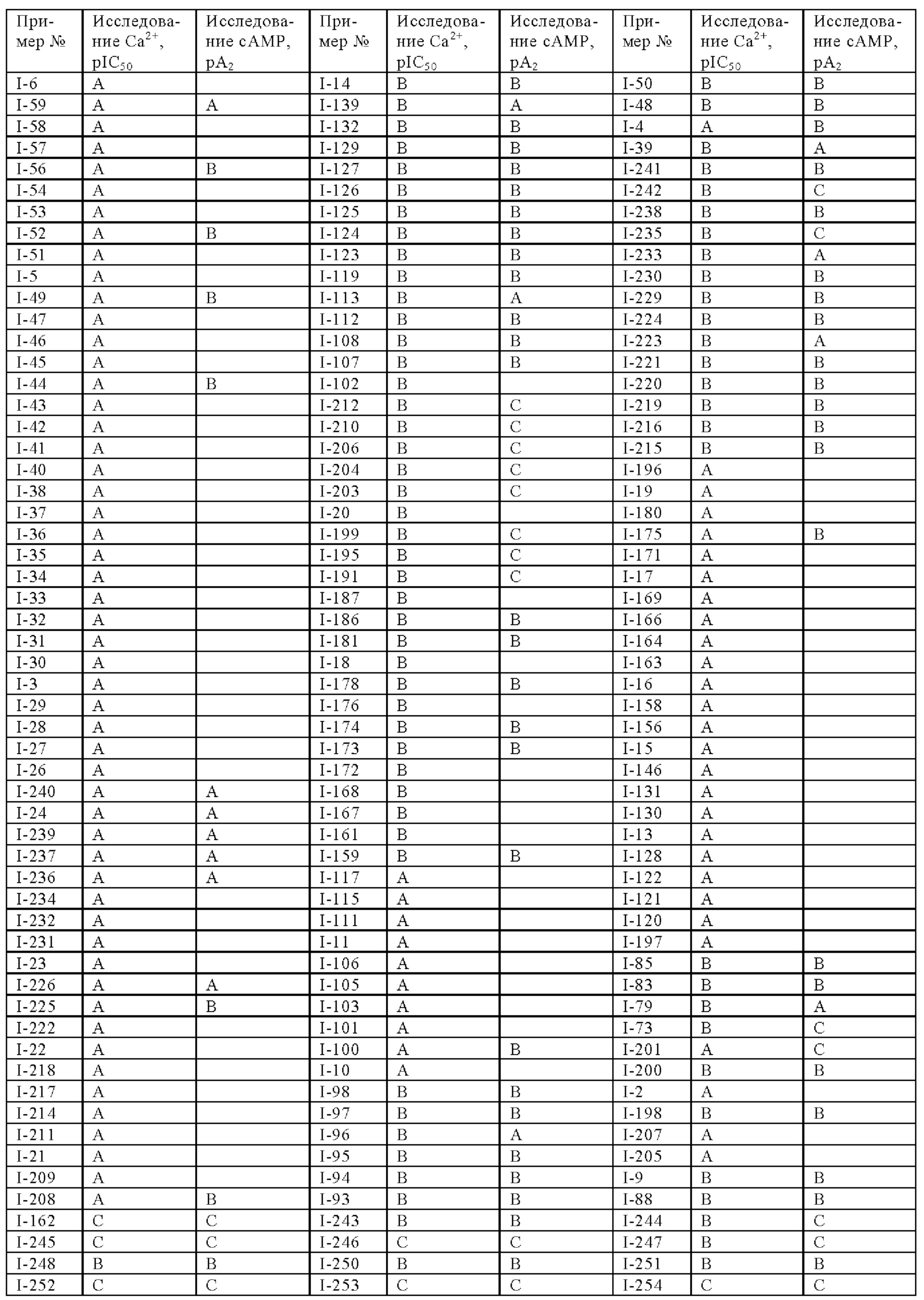
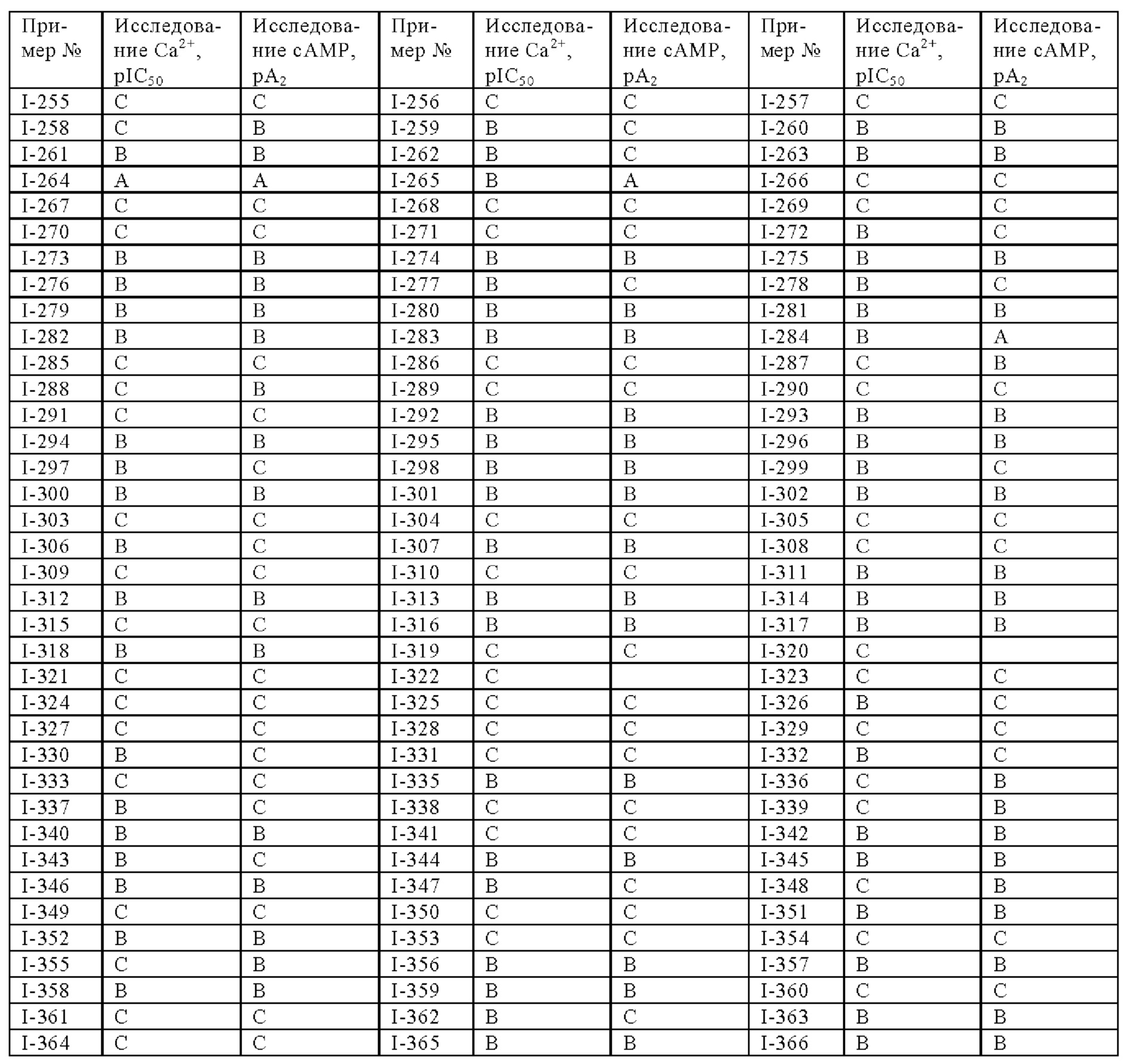
В-IIC: Исследование созревания/миелинизации олигодендроцитов
Воздействие негативных модуляторов GPR17 на созревание/миелинизацию первичных олигодендроцитов можно определить с помощью проводимых in vitro иммунологических исследований с использований антител к основному миелиновому белку (МРВ), использующихся в качестве маркера наличия зрелых олигодендроцитов.
Описание исследования МРВ, вестерн-блоттинг / олигодендроцит / миелинизация
После выдерживания в среде для пролиферации в течение 3-4 дней первичные ОРС высевали в 12-луночные планшеты для выращивания культур тканей при плотности, равной 25000 клеток/см2, и среду заменяли на не содержащую фактора роста среду Neurobasal для индуцирования самопроизвольной дифференциации in vitro и экспрессии белка GPR17. Для конечной дифференциации и количественного анализа экспрессии белка через 24-48 ч в не содержащую фактора роста среду добавляли 0,20 нг/мл трийодтиронина (Т3) и 10 нг/мл цилиарного нейротрофического фактора вместе с исследуемыми соединениями - антагонистами/обратными агонистами GPR17 при концентрации, равной 1 мкМ, или с разбавителем и выдерживали в течение еще 3 дней. После обработки соединением клетки дважды промывали охлажденным льдом ЗФФ и лизировали в охлажденном льдом литическом буфере (25 мМ Tris (трис(гидроксиметиламинометан)), рН 7,4, 150 мМ NaCl, 1 мМ ЭДТК, 1% Triton Х-100, 1% IGEPAL), содержащем смесь ингибитора протеазы. Лизаты перемешивали с вращением при 4°С в течение 20 мин и центрифугировали при скорости, равной 15000×g, при 4°С в течение 10 мин. Концентрацию белка определяли с помощью анализа содержания белка Pierce ВСА в соответствии с инструкциями изготовителя. 7,5-15 мкг Белка разделяли с помощью электрофореза на полиакриламидном геле с использованием 10% ДСН (додецилсульфат натрия) и переносили на нитроцеллюлозную мембрану путем электроблоттинга. После промывки мембраны блокировали с помощью Roti-Block при комнатной температуре в течение 1 ч и инкубировали при 4°С в течение ночи в Roti-Block с добавлением антител к МРВ (1:5000, Lifespan Biosciences). Мембраны 3 раза промывали с помощью ЗФФ, содержащего 0,1% Tween, и затем инкубировали при комнатной температуре в течение 1 ч в Roti-Block с добавлением конъюгированных с пероксидазой хрена козьих антимышиных антител IgG. Иммунореактивные белки визуализировали с помощью хемилюминесценции с использованием реагента для детектирования с помощью вестерн-блоттинга Amersham Biosciences ECL Prime и определяли количество с помощью денситометрии с использованием программного обеспечения Gelscan. Для нормировки на одинаковое содержание и перенос белка мембраны повторно исследовали с использованием антител к β-актину (1:2500, BioLegend; вторичные козьи антикроличьи антитела IgG HRP (ABIN)). Количество экспрессированного МРВ в присутствии исследуемых соединений сопоставляли с количеством экспрессированного МРВ при контрольных условиях.
Описание исследования МРВ, планшеты с волоконным покрытием/созревание/миенилизация олигодендроцита
ОРС высевали в 96-луночные планшеты с волоконным покрытием Mimetix Aligned (Electrospining company) при плотности, равной 16000-22000 клеток/см2. После выдерживания в среде для пролиферации в течение 2 дней и не содержащей фактора роста среде Neurobasal в течение 2 дней для индуцирования самопроизвольной дифференциации in vitro и экспрессии белка GPR17 добавляли разбавитель или исследуемые соединения - антагонисты/обратные агонисты при концентрации, равной 1 мкМ, в среде для конечной дифференциации с добавлением 0,20 нг/мл трийодтиронина и 10 нг/мл цилиарного нейротрофического фактора и выдерживали в течение 6 дней, причем через 3 дня проводили замену среды. Затем клетки фиксировали в 4% параформальдегиде, затем промывали с помощью ЗФФ, обеспечивали проницаемость мембран с помощью 0,1% TritonX-100 в ЗФФ и блокировали с помощью 10% козьей сыворотки и 1% бычьего сывороточного альбумина в забуференном фосфатом физиологическом растворе. Антитела к МРВ разводили в блокирующем буфере (1:2000) и инкубировали при 37°С в течение 1 ч. Клетки повторно промывали с помощью ЗФФ и инкубировали с конъюгированными с Су2 вторичными антимышиными антителами IgG (Millipore, 1:500) в течение 1 ч. После промывки с помощью ЗФФ клетки окрашивали с помощью 0,2 мкг/мл ДАФИ (4,6-диамидино-2-фенилиндол, повторно промывали и закрепляли с помощью Mowiol. Флуоресцентные изображения получали с помощью микроскопа Zeiss AxioObserver.Z1, снабженного системой для визуализации ApoTome и объективом Plan-Apochromat 20×/0,8, с использованием фильтра для eGFP (возбуждение: 470/40 нм; испускание: 525/50 нм) и фильтра для ДАФИ (возбуждение: 365 нм; испускание: 445/50 нм). Получали изображения по меньшей мере для 15 случайно выбранных областей для контрольных образцов (среда для конечной дифференциации с добавлением 0,1% DMSO) и для исследуемых соединений с использованием одинаковых условий, обеспеченных с помощью программного обеспечения Zeiss ZEN2.3. Изменения количеств миелинированных волокон приводили для групп волокон, обладающих разной диной (от 0 до 40 мкм, от 41 до 60 мкм, от 61 до 80, от 81 до 100, от 101 до 120 и >120 мкм) при отсутствии или в присутствии негативного модулятора GPR17.
Результаты исследований созревания/миелинизации олигодендроцитов
Как показано на Фиг. 1 по данным исследования созревания/миелинизации первичных ОРС крыс по методике вестерн-блоттинг типичные соединения, приведенные в примерах, увеличивают степень экспрессирования МРВ, что является маркером зрелых олигодендроцитов.
Влияние соединения примера I-116 на степень экспрессирования МРВ подтверждено с помощью исследования МРВ для созревания/миелинизации олигодендроцита в планшетах с волоконным покрытием. Как показано на приведенном ниже чертеже соединение I-116 способствует образованию более длинных миелиновых оболочек. Эти результаты представлены на Фиг. 2.
В-III: Определение концентрации в плазме и головном мозге
Несколько соединений примеров исследовали для определения концентрации в плазме и головном мозге.
Определение отношения концентрации в головном мозге к концентрации в плазме (Kp в головном мозге)
Самцов крыс Sprague Dawley (n=2 для каждого момента времени) использовали для определения степени проникновения соединений через 15, 45 и 120 мин после внутрибрюшинного введения дозы, равной 3 мг/кг.
В каждый момент времени после анестезии (вдыхание изофлурана) и взятия крови (1 мл образца, полученного путем пункции сердца, помещали в пробирки, содержащие K2-ЭДТК) крыс обескровливали и проводили перфузию головного мозга через левый желудочек (50 мл гепаринизированного 0,9% раствора NaCl (0,15 МЕ/мл), скорость потока 50 мл/мин).
Головной мозг собирали и взвешивали. Плазму получали из образцов крови путем центрифугирования (при 4°С, при 3000×g, в течение 15 мин). Образцы головного мозга и плазмы замораживали до проведения анализа.
В момент анализа образцы головного мозга гомогенизировали в плазме (1:4, об.:об.) и после осаждения белка вместе с образцами плазмы анализировали с помощью ВЭЖХ/МС-МС.
Результаты:
На Фиг. 3 представлены результаты для соединения примера (соединение примера I-1). Через 45 мин после введения соединения I-1 зависимость для его концентрации в головном мозге становится параллельной зависимости для его концентрации в плазме.
B-IV: Исследование соединения примера в модели in vivo острой интоксикации купризоном на мышах
Соединение I-228 исследовали в хорошо известной модели токсической демиелинизации под воздействием купризона на мышах [см. публикации 1-3 в конце этого раздела]. В этой модели кормление молодых мышей купризоном индуцирует гибель клеток-олигодендроцитов и вскоре приводит к активации микроглии и астроцитов. Кормление купризоном в течение 5 недель приводит к сильной и равномерной демиелинизации мозолистого тела, протекание которой можно обратить при прекращении токсического воздействия (фаза повторной миелинизации).
Животные и интоксикация купризоном. Мышей C57B1/6J (Janvier, France) разводили и выдерживали в непатогенных условиях при количестве животных в клетке, равном не более 5. За животными в клетках ухаживали обычным образом и осуществляли микробиологический мониторинг в соответствии с рекомендациями Федерации европейских научных ассоциаций по лабораторным животным. Пища (купризон или стандартный корм) и вода предоставлялись в неограниченном количестве. Демиелинизацию индуцировали путем кормления самцов мышей в возрасте 8 недель (примерно 19-21 г) кормом, содержащим 0,25% купризона [бис(циклогексанон)оксалдигидразон; Sigma-Aldrich, Inc., USA], примешанного к основному стандартному корму для грызунов, в течение 5 недель.
Приготовление образцов тканей и исследование: Для проведения гистологических и иммуногистохимических исследований мышей анестезировали кетамином (100 мг/кг, внутрибрюшинно) и ксилазином (10 мг/кг, внутрибрюшинно), подвергали транскардиальной перфузии охлажденным льдом ЗФФ, затем транскардиальной перфузии 3,7% раствором параформальдегида (рН 7,4). Последующую фиксацию проводили в таком же фиксирующем растворе при 4°С в течение 12 ч. Затем головной мозг закрепляли в парафине и делали коронарные срезы толщиной 5 мкм на уровне 265 (т.е. область 1) и 285 (т.е. область 2) в соответствии с атласом головного мозга мыши Sidman et al. (http://www.hms.harvard.edu/ research/brain/atlas.html). Белок-маркер миелина, PLP (протеолипидный белок), визуализировали с помощью иммуногистохимического анализа. Для этого закрепленные в парафине срезы депарафинировали, повторно гидратировали и промывали с помощью ЗФФ. Неспецифические связывания исключали путем инкубирования предметных стекол с использованием блокирующего раствора при комнатной температуре в течение 1 ч. Предметные стекла инкубировали в течение ночи с первичными антителами, разведенными блокирующим раствором (Immunologic, Netherlands). В день 2 предметные стекла промывали с помощью ЗФФ, блокировали с помощью Н2О2 и повторно промывали с помощью ЗФФ. Для визуализации комплексов эпитоп-первичные антитела использовали полимер со вторичными антителами EnVision® (Dako, Germany). Эта система основана на меченом пероксидазой хрена полимере, сопряженном со вторичными антителами. Меченый полимер не содержит авидин или биотин. В соответствии с этим, устранено или существенно уменьшено неспецифическое окрашивание, возникающее вследствие активности эндогенных авидина-биотина. Кроме того проводили исследование контрольных образцов, при этом или исключали первичные антитела, или предметные стекла инкубировали с субтипами IgG при соответствующих концентрациях. На этих контрольных стеклах не обнаружено специфическое окрашивание.
Интенсивность для продукта реакции, антител к PLP, определяли полуколичественно с использованием микроскопа Nikon Eclipse Е-200 (50×), соединенного с ПЗС-камерой (камера на приборах с зарядовой связью) и снабженного программным обеспечением Image J. Для этого отмечали исследуемую область (т.е. срединная линия мозолистого тела, см. отмеченную на Фиг. 4-1), и изображение преобразовывали в изображение в 8-битной шкале серого. Затем получали бинарное изображение с помощью алгоритма автоматического вычисления порога и определяли соответствующую область сигнала. Для области 1 использовали алгоритм Йена, тогда как для области 2 использовали алгоритм моментов Шанбага соответственно (см. также Фиг. 4-2).
Поскольку предметные стекла с образцами для всех групп окрашивали по отдельности, для непосредственного сопоставления результатов вводили поправочный коэффициент. Этот поправочный коэффициент определяли на основании осмотра предметных стекол под микроскопом. Использовавшиеся поправочные коэффициенты составляли 0,33, 0,75 и 7 соответственно в зависимости от исследуемой области. Для каждой области исследовали два последовательно расположенных среза. Для статистического анализа использовали результаты, полученные для каждого среза.
Для исследования демиелинизации в окрашенных с помощью LFB (Luxol Fast Blue) срезах степень миелинизации в мозолистом теле определяли по шкале от 100 до 0. 100 эквивалентно содержанию миелина у мыши, которой не вводили купризон, тогда как 0 эквивалентен полностью демиелинизированному мозолистому телу. Степень миелинизации определяли путем изучения двух последовательно расположенных предметных стекол и получали одно значение для этой пары.
Схема эксперимента. Мышей кормили купризоном в течение 5 недель и затем до отбора образцов тканей им давали восстановиться после интоксикации в течение 11 дней (т.е. период повторной миелинизации). Через 3 полные недели после кормления купризоном начинали лечение разбавителем или лекарственным средством и его проводили до завершения эксперимента (т.е. вплоть до недели 6,5). Лекарственное средство ежедневно вводили перорально (ПО) при объеме введения, равном 10 мл/кг. Условия проведения эксперимента являлись следующими: 1) разбавитель 2) 6 мг/кг 3) 20 мг/кг и 60 мг/кг, количество животных, использовавшихся для каждого условия равнялось 10.
Литература: 1. Kipp et al, 2009 Acta Neuropathol 118: 723; 2. Kipp et al., 2011, Brain Behav Immun 25: 1554-1568; 3. Slowik et al, 2015, Br J Pharmacol 172: 80-92.
Статистический анализ. Иммуногистохимическое (ИГХ) исследование проводили по слепой методике и при этом и группу, подвергшуюся лечению, выявляли только после контроля качества и статистической обработки. Результаты анализировали с использованием параметрической статистической методики и программного обеспечения Statistica (StatSoft Inc., OK, USA). Зависимой переменной величиной являлось количество PLP, определенное в мозолистом теле. Поскольку целью исследования являлось сравнение четырех доз (0, 6, 20 и 60 мг/кг), использовали односторонний дисперсионный анализ ANOVA. Отличия средних значений определяли с помощью критерия подлинной значимости (КПЗ) Тьюки. При необходимости до статистической обработки проводили логарифмические преобразования для нормировки исходных данных для обеспечения более точного соответствия предположению об однородности дисперсии (тест Левене) и гауссового распределения. Однако для ясности на чертежах приведены средние значения исходных данных. Статистическую значимость устанавливали равной р<0,05. Данные представляли в виде средних значений ± СПС (стандартная погрешность среднего).
Результаты. Полученные с помощью одностороннего дисперсионного анализа ANOVA показали существенное влияние дозы [F(3,70)=3,28, р<0,001] и последующий тест Тьюки показал, что представители двух групп, которым вводили дозу, равную 6 и 20 мг/кг, обладали существенно более высокой концентрацией PLP, чем представители, которым вводили разбавитель (р<0,01), см. Фиг. 5.
Заключение: При исследовании с помощью модели с использованием купризона показано, что соединение I-228 ускоряет повторное образование связанных с миелином белков после перорального введения дозы, равной 6 и 20 мг/кг. Поскольку PLP является маркером миелина, эти результаты показывают, что ингибирование GPR17 соединениями, предлагаемыми в настоящем изобретении, или предупреждает демиелинизацию, или, вероятнее, способствует повторной миелинизации после вызванной купризоном демиелинизации. Это находится в соответствии с недавно опубликованными результатами, полученными для вызванной посредством ЛФХ (лизофосфатидилхолин) демиелинизации с использованием лишенных GPR17 мышей (Ou et al., 2016).
Реферат
Изобретение относится к соединениям или их фармацевтически приемлемым солям, которые обладают модулирующей активностью в отношении GPR17. В формуле I-2 X1 обозначает N или C(R7), Х2 обозначает NH, S или О, Х3 обозначает N или C(R12), R2 выбран из водорода и галогена, R4 выбран из водорода и галогена, R5 выбран из группы, включающей водород, галоген, C1-C6-алкил и т.д., R6 выбран из группы, включающей водород, галоген, цианогруппу, азидогруппу и т.д., R7, если присутствует, выбран из группы, включающей водород, галоген, цианогруппу, C1-C6-алкил, C1-C6-алкоксигруппу, C1-C6-алкилсульфонил, C1-C6-алкилсульфинил и т.д., R8 выбран из группы, включающей водород, галоген, цианогруппу и т.д., R9 выбран из группы, включающей водород, галоген, C1-C6-алкил, C1-C6-алкоксигруппу и т.д., R10 выбран из группы, включающей водород, галоген, C1-C6-алкил, С1-С6-алкоксигруппу, С2-С6-алкенил, С2-С6-алкинил, цианогруппу и т.д., R11 выбран из группы, включающей водород, галоген, цианогруппу, С1-С6-алкил и т.д., R12, если присутствует, выбран из водорода, С1-С6-алкоксигруппы и галогена, при условии, что (a) по меньшей мере один из R5, R6 и R7, если R7 присутствует, и (b) по меньшей мере один из R8, R10 и R11 отличается от водорода. Изобретение относится также к конкретным соединениям, применению указанных соединений для модулирования активности GPR17, для лечения нарушений, связанных с дисфункцией GPR17, в частности рассеянного склероза, способу предупреждения и/или лечения синдрома или нарушения, связанного с дисфункцией GPR17, и фармацевтической композиции. 7 н. и 23 з.п. ф-лы, 5 ил, 10 табл., 374 пр.
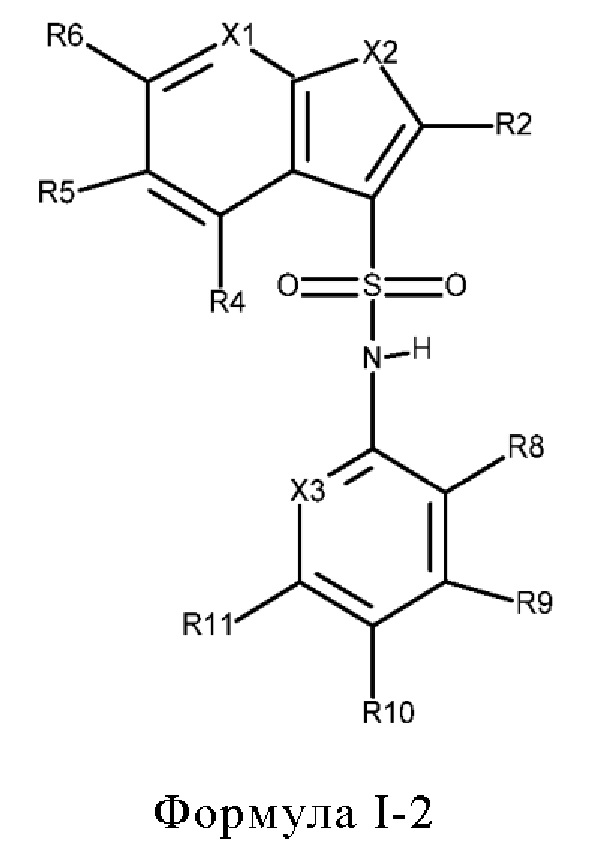
Формула
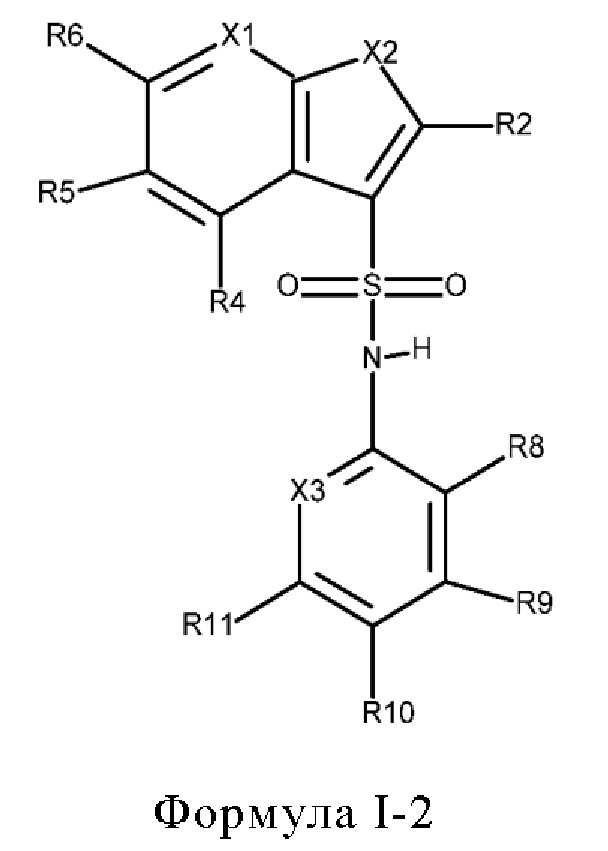
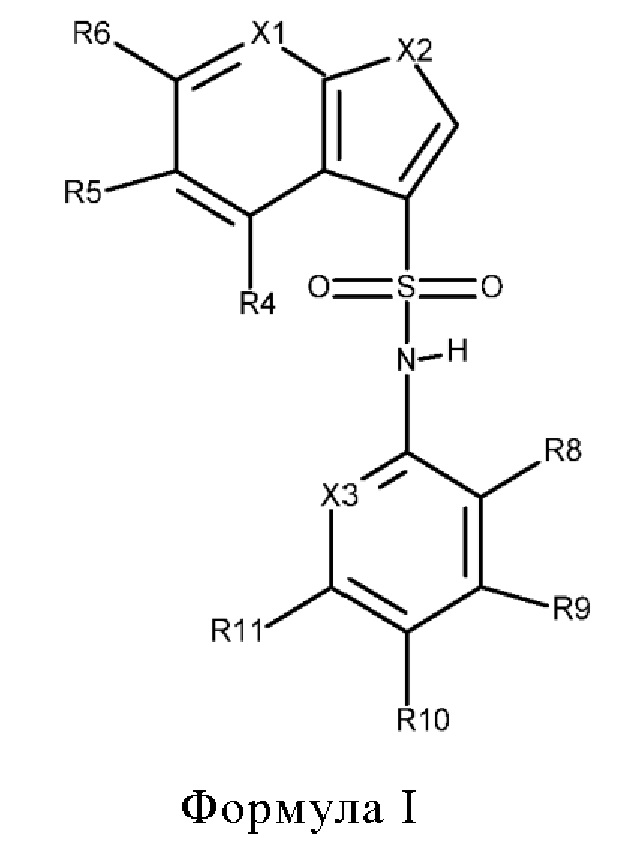
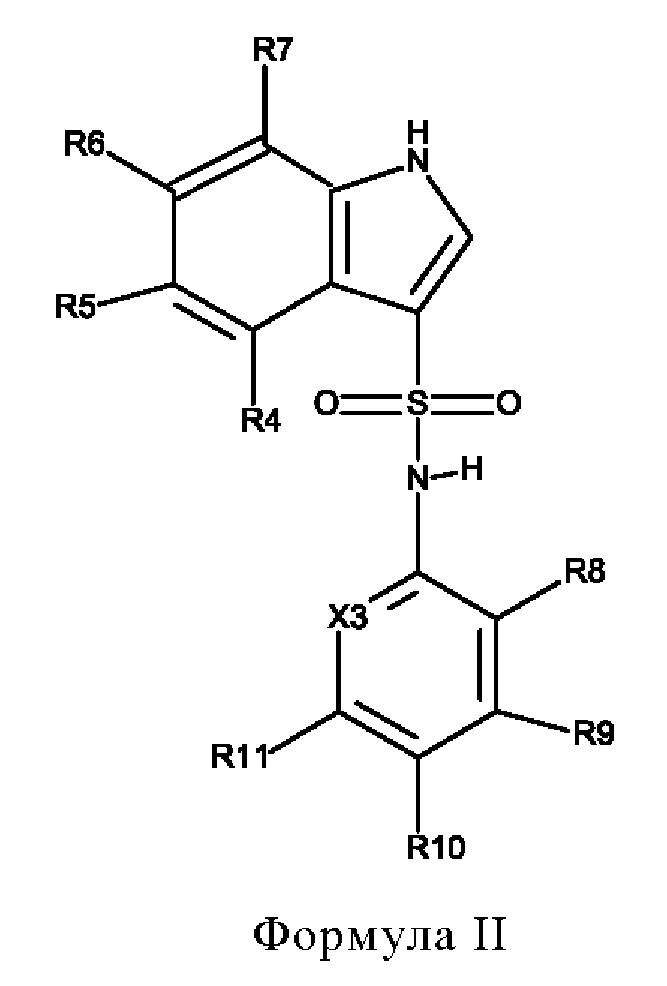
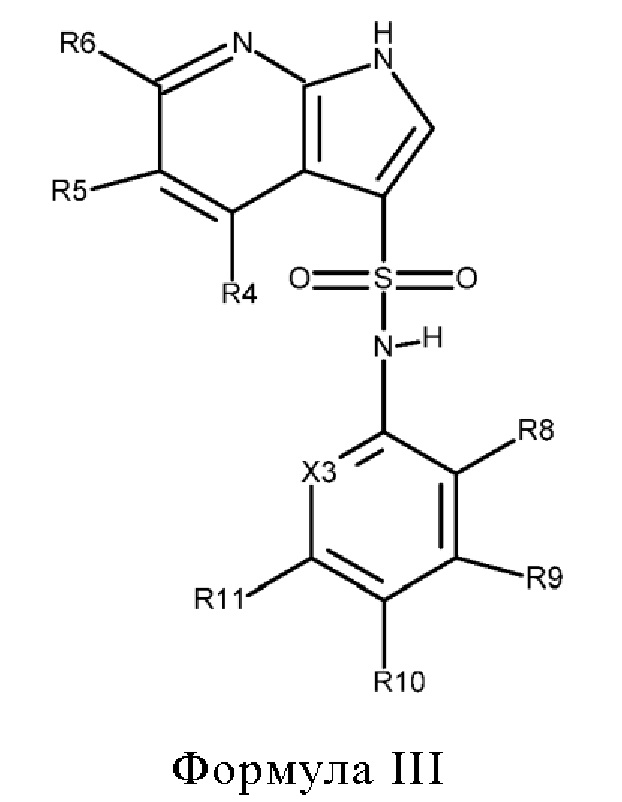
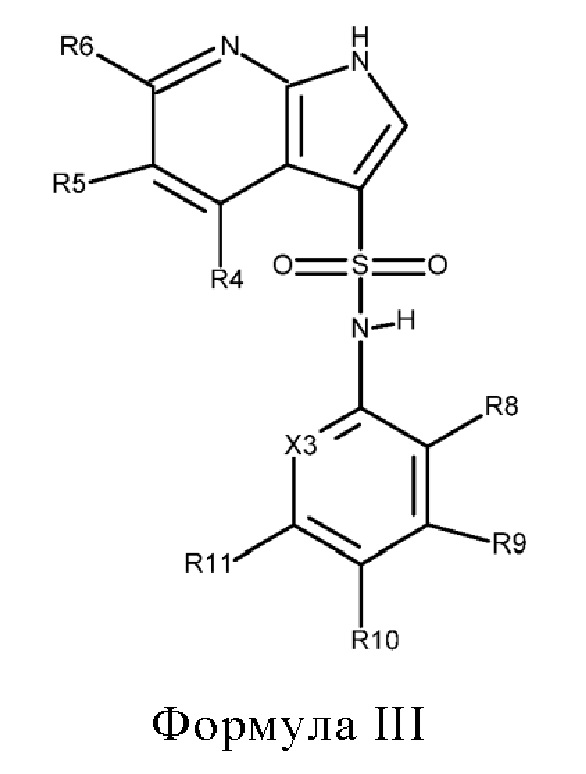
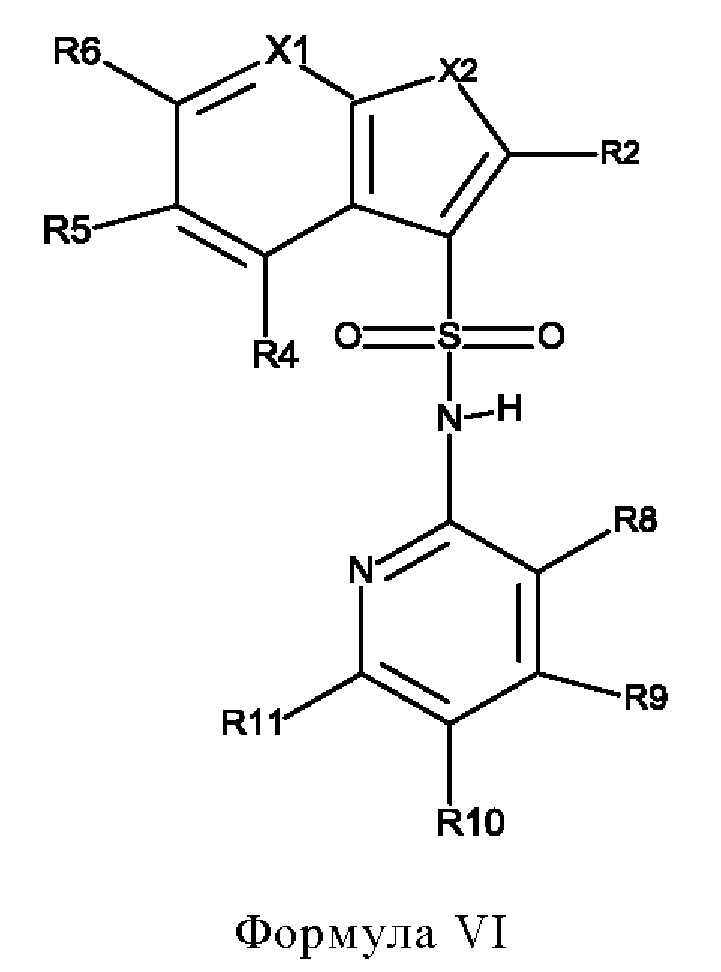
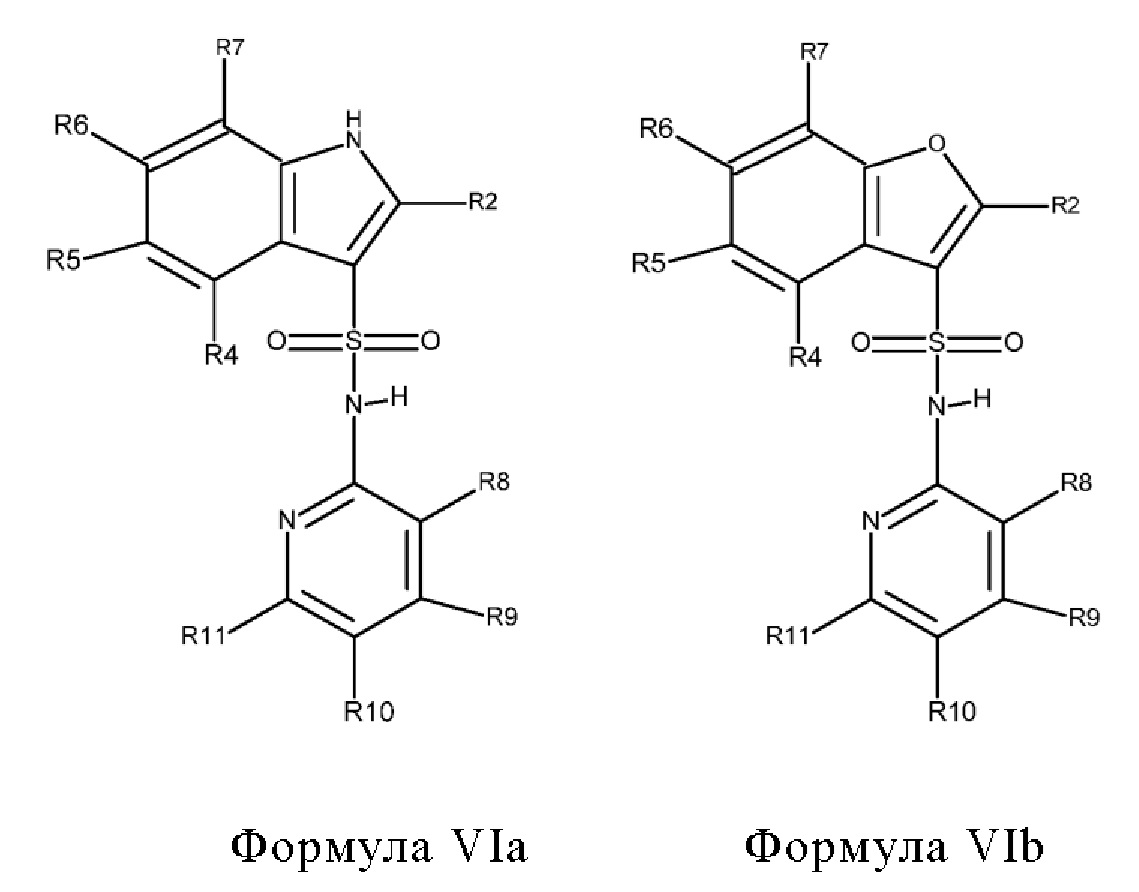
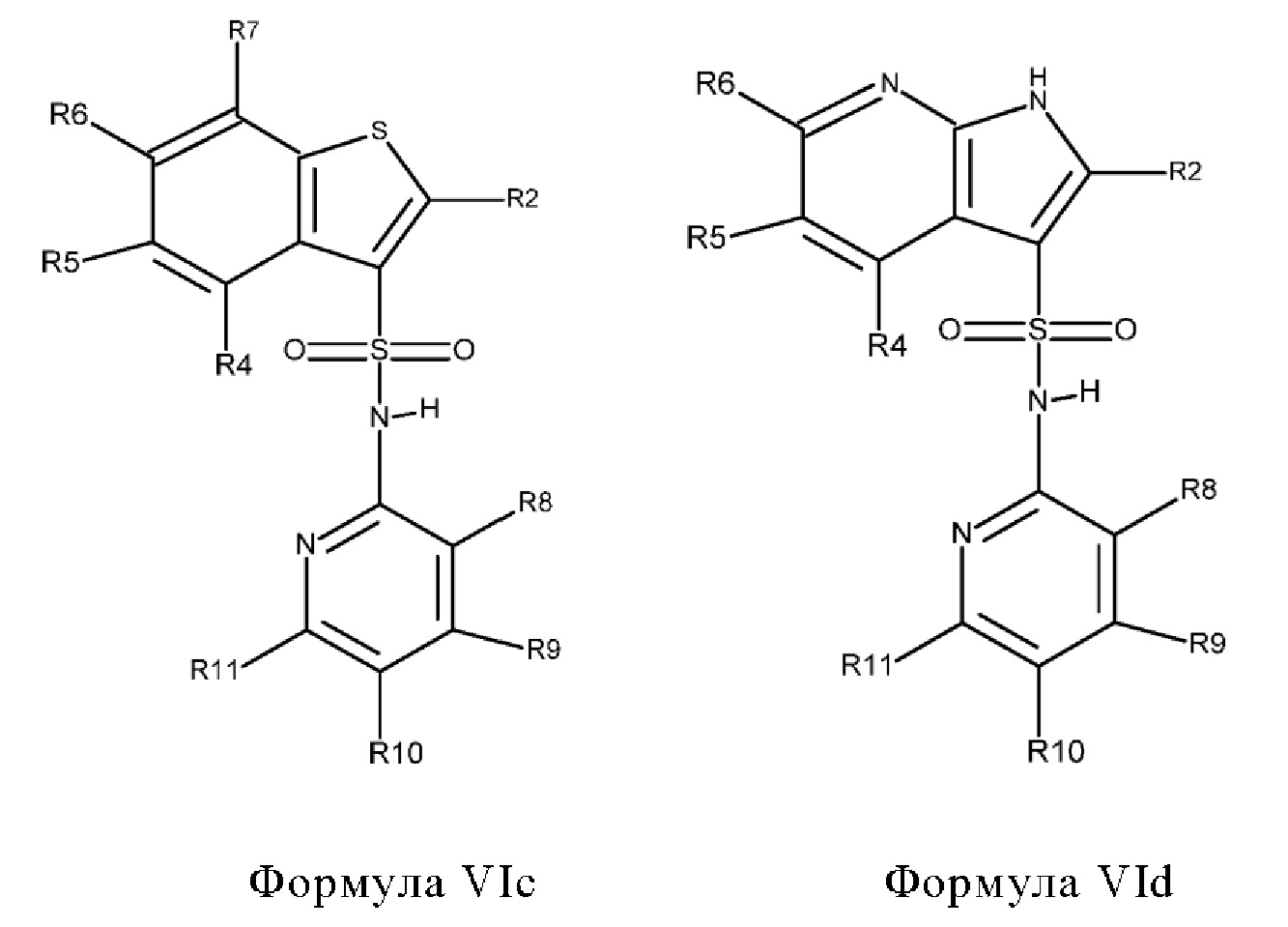
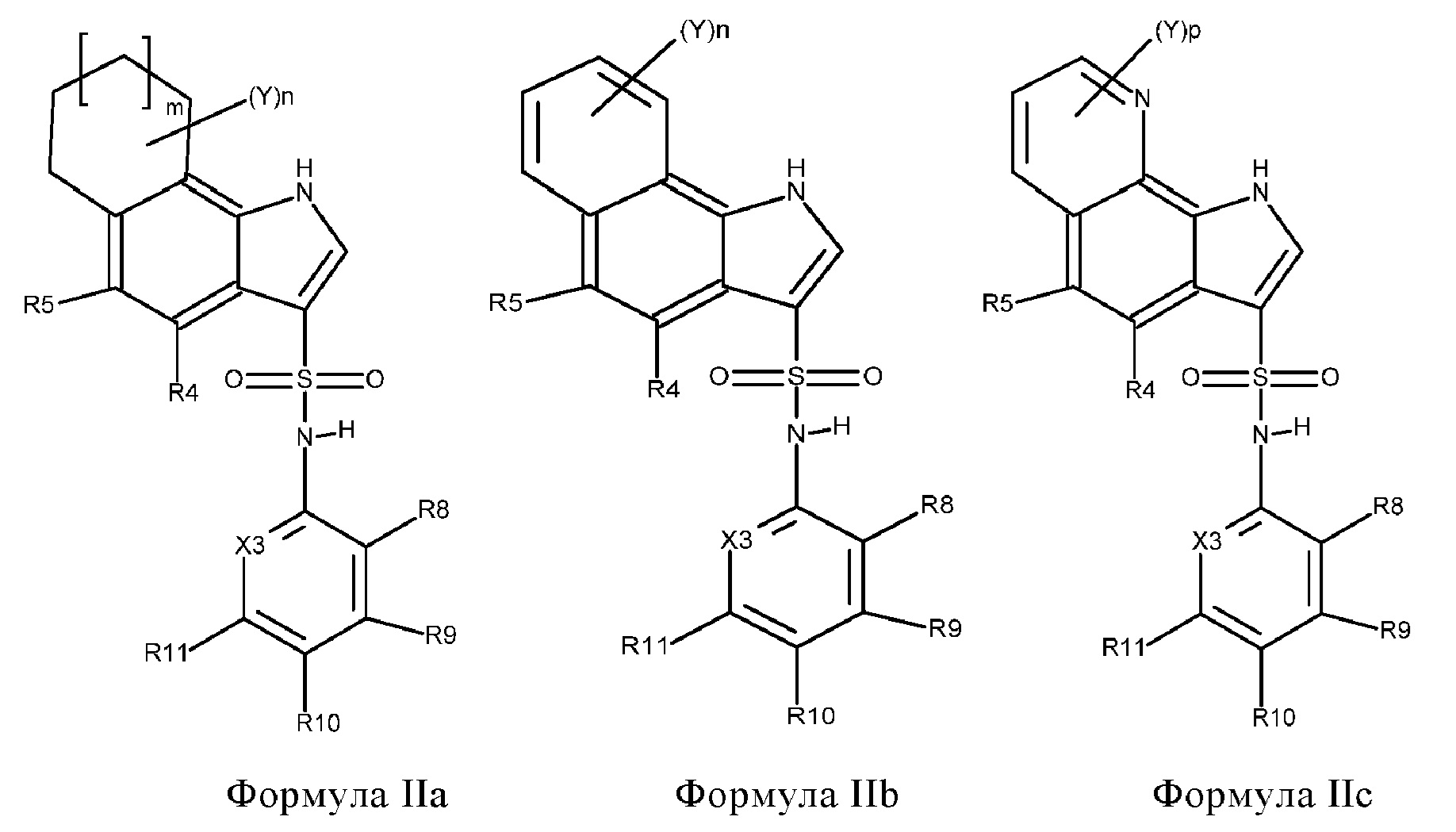
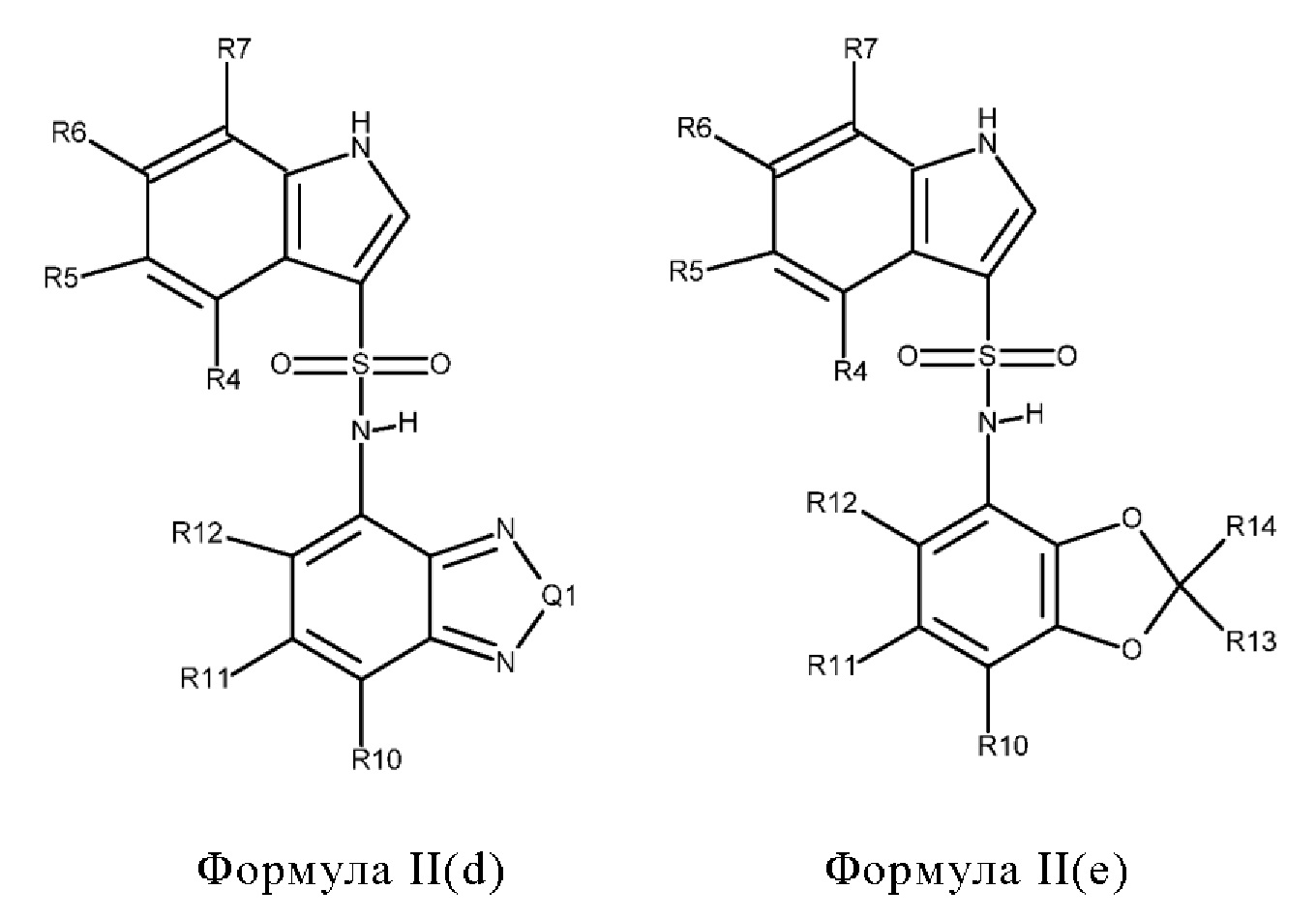
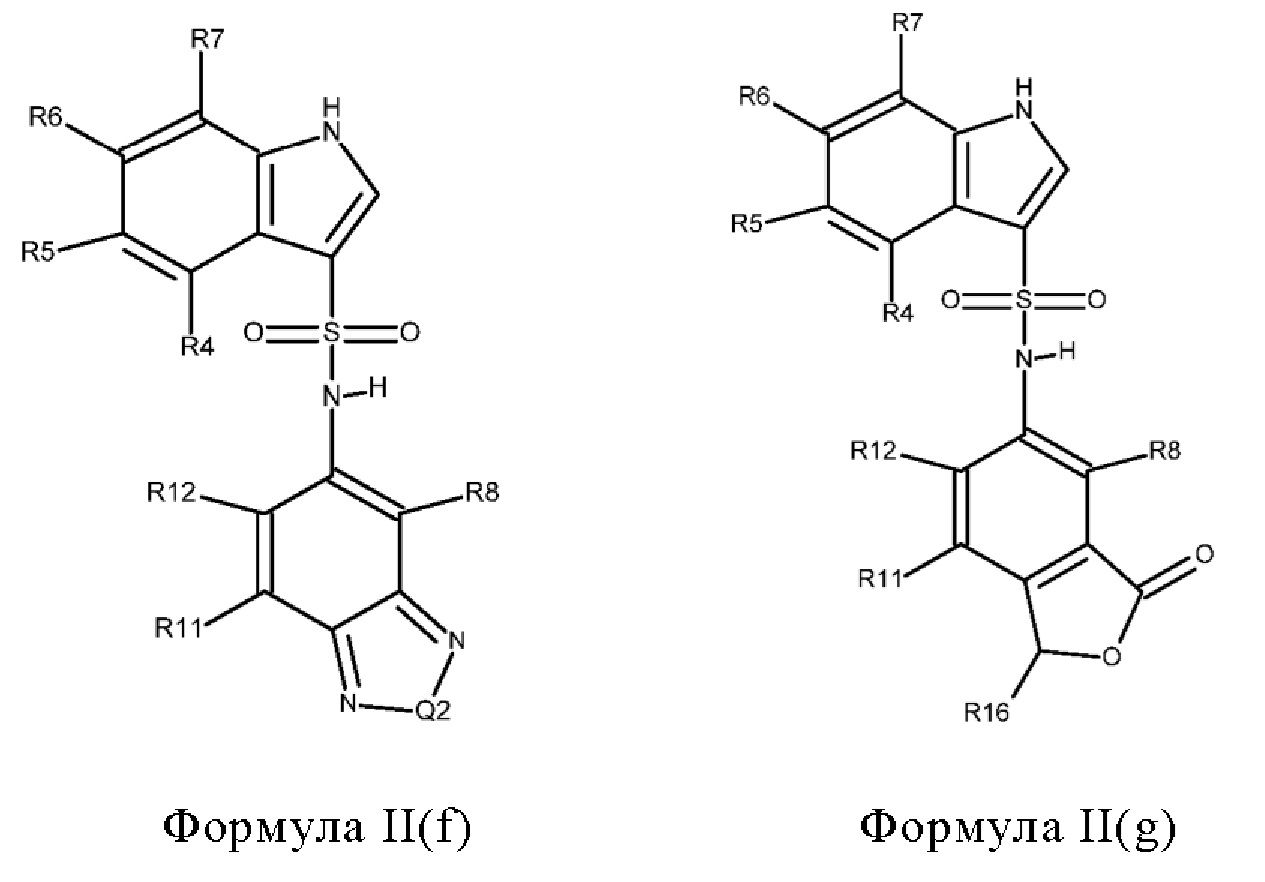
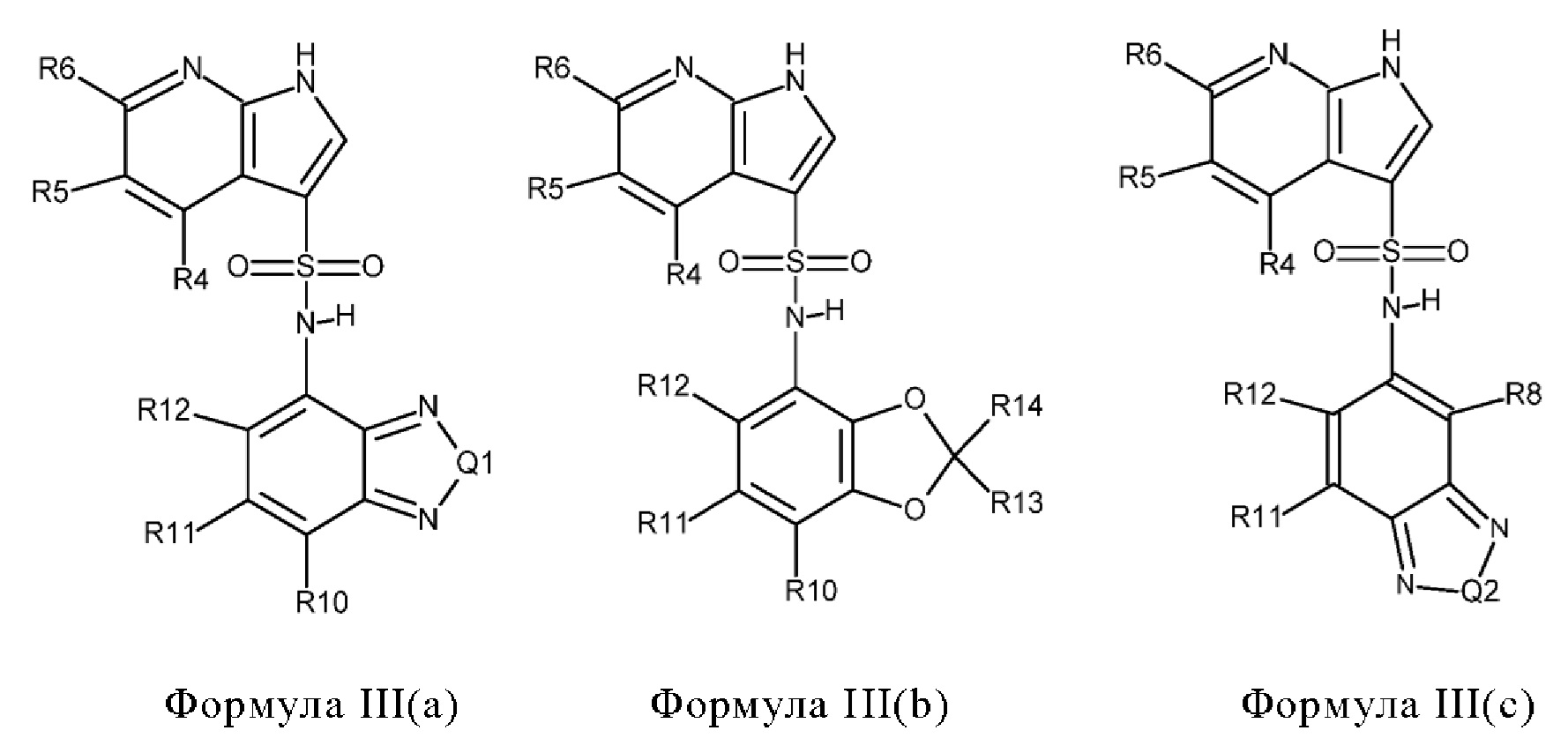
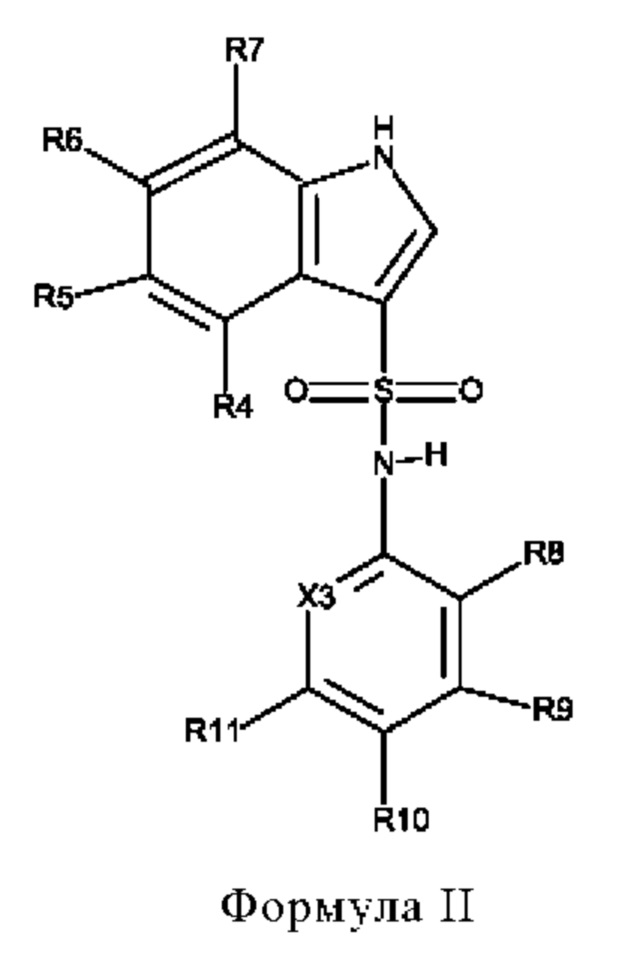

Документы, цитированные в отчёте о поиске
Конъюгаты и малые молекулы, взаимодействующие с рецептором cd16а
Патенты аналоги
Конъюгаты и малые молекулы, взаимодействующие с рецептором cd16а

Комментарии