Производные 1,6-диазабицикло[3.2.1]октан-7-она и их применение для лечения бактериальных инфекций - RU2614418C2
Код документа: RU2614418C2
Описание
Область техники, к которой относится изобретение
Изобретение относится к азотсодержащим соединениям, применению этих соединений в качестве антибактериальных средств, композициям, их содержащим, и способам их получения.
Уровень техники
Возникновение резистентности бактерий к известным антибактериальным средствам становится серьезной проблемой в лечении бактериальных инфекций. Одним из перспективных направлений лечения бактериальных инфекций, и, в частности тех, которые вызваны резистентными бактериями, является разработка новых антибактериальных средств, которые могут преодолеть бактериальную резистентность. Coates и другие исследователи (Br. J. Pharmacol. 2007; 152(8), 1147-1154) изучали новые подходы в разработке новых антибиотиков. Тем не менее, разработка новых антибактериальных средств является сложной задачей. Например, Gwynn и другие исследователи (Annals of the New York Academy of Sciences, 2010, 1213: 5-19) изучали проблемы в открытии антибактериальных средств.
Некоторые антибактериальные средства известны из предшествующего уровня техники (например, см. международные заявки РСТ №№ PCT/US2010/060923, PCT/EP2010/067647, PCT/US2010/052109, PCT/US2010/048109, PCT/GB2009/050609, PCT/EP2009/056178 и PCT/US2009/041200). Тем не менее, сохраняется потребность в мощных антибактериальных средствах для предупреждения и/или лечения бактериальных инфекций, в том числе тех, которые вызываются бактериями, устойчивыми к известным антибактериальным средствам.
Авторы изобретения неожиданно обнаружили азотсодержащие соединения с антибактериальными свойствами.
Сущность изобретения
Таким образом, предложены азотсодержащие соединения, способы получения этих соединений, фармацевтические композиции, содержащие эти соединения, и способ предупреждения или лечения бактериальной инфекции у субъекта с использованием этих соединений.
В одном общем аспекте предложены соединения формулы (I):
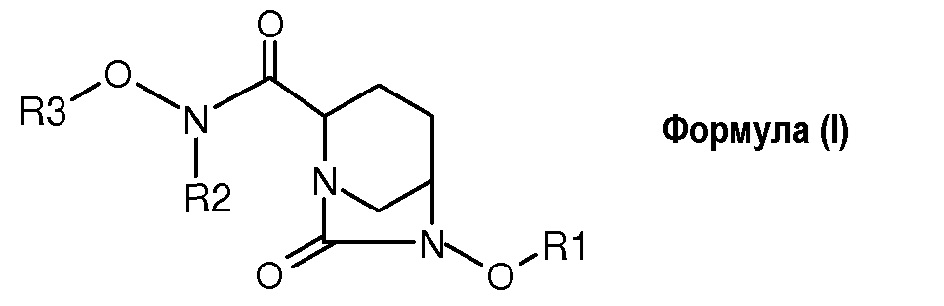
или его стереоизомеры или его фармацевтически приемлемая соль;
где:
R1 представляет собой:
(a) SO3M,
(b) SO2NH2,
(c) PO3M,
(d) CH2COOM,
(e) CF2COOM,
(f) CHFCOOM или
(g) CF3;
М представляет собой водород или катион;
R2 представляет собой:
(a) водород,
(b) (CH2)n-R3 или
(c) COOR3,
n равно 0, 1 или 2;
R3 представляет собой:
(a) водород,
(b) C1-C6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из галогена, OR5, CN, COOR5, CONR6R7, NR6R7, NR5COR8, NR5CONR6R7, гетероциклила, гетероарила, циклоалкила или арила,
(c) CN,
(d) NR6R7,
(e) CONR6R7,
(f) NHCONR6R7,
(g) арил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(h) гетероциклил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(i) гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
j) циклоалкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(k) циклоалкил, замещенный C1-C6 алкилом, где C1-C6 алкил дополнительно замещен одним или несколькими заместителями, независимо выбранными из OR5, NR6R7, галогена, CN или CONR6R7 или
(1) OR8;
R4 представляет собой:
(a) водород,
(b) C1-C6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из галогена, OR5, CN, COOR5, CONR6R7, NR6R7, NR5COR8, гетероциклила, гетероарила, циклоалкила или арила,
(c) арил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(d) гетероциклил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(e) гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7, или
(f) циклоалкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7;
R5 и R8 представляют собой каждый независимо друг от друга:
(a) водород, или
(b) C1-C6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из галогена, CN, CONR6R7, NR6R7, гетероциклила, гетероарила, циклоалкила или арила;
R6 и R7 представляют собой каждый независимо друг от друга:
(a) водород,
(b) C1-C6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из галогена, OR5, CN, COOR5, CONR5R8, NR5R8, NR5COR8, гетероциклила, гетероарила, циклоалкила или арила,
(c) арил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR5R8, галогена, CN, CONR5R8, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR5R8,
(d) гетероциклил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR5R8, галогена, CN, CONR5R8, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR5R8,
(e) гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR5R8, галогена, CN, CONR5R8, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR5R8,
(f) циклоалкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR5R8, галогена, CN, CONR5R8, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR5R8, или
(g) R6 и R7 присоединены друг к другу с образованием семичленного кольца.
В другом общем аспекте предложены фармацевтические композиции, содержащие соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль.
В другом общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, включающий введение указанному субъекту фармацевтически эффективного количества соединения формулы (I) или его стереоизомера, или фармацевтически приемлемой соли.
В другом общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, включающий введение указанному субъекту фармацевтически эффективного количества соединения формулы (I) или его стереоизомера, или фармацевтически приемлемой соли.
В другом общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей соединение формулы (I) или его стереоизомера, или фармацевтически приемлемой соли.
В еще одном общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, включающий введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей соединение формулы (I) или его стереоизомера, или фармацевтически приемлемой соли.
В другом общем аспекте предусмотрены фармацевтические композиции, содержащие: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное.
В другом общем аспекте предусмотрены фармацевтические композиции, содержащие: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль и (b), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В другом общем аспекте предусмотрены фармацевтические композиции, содержащие: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное, и (с), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В другом общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное.
В еще одном общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, включающий введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное.
В другом общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В еще одном общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, включающий введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В другом общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное, и (c), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В еще одном общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное, и (c), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В другом общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, и (b), по меньшей мере, одного ингибитора бета-лактамазы, выбранного из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемого производного.
В еще одном общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, и (b), по меньшей мере, одного ингибитора бета-лактамазы, выбранного из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемого производного.
В другом общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, и (b), по меньшей мере, одного антибактериального средства или его фармацевтически приемлемого производного.
В еще одном общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, и (b), по меньшей мере, одного антибактериального средства или его фармацевтически приемлемого производного.
В другом общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, (b), по меньшей мере, одного ингибитора бета-лактамазы, выбранного из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемого производного, и (c), по меньшей мере, одного антибактериального средства или его фармацевтически приемлемого производного.
В еще одном общем аспекте предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, (b), по меньшей мере, одного ингибитора бета-лактамазы, выбранного из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемого производного, и (c), по меньшей мере, одного антибактериального средства или его фармацевтически приемлемого производного.
В другом общем аспекте предусмотрены способы повышения антибактериальной эффективности антибактериального средства у субъекта, где указанный способ включает совместное введение указанного антибактериального средства или его фармацевтически приемлемого производного с фармацевтически эффективным количеством соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли.
Детали одного или нескольких вариантов осуществления изобретения изложены в приведенном ниже описании. Другие признаки, цели и преимущества настоящего изобретения будут очевидны из следующего описания, включая пункты формулы изобретения.
Подробное описание изобретения
Далее будет сделана ссылка на иллюстративные варианты осуществления, и для их описания в настоящем документе будут использованы конкретные формулировки. Тем не менее, следует понимать, что никакого ограничения объема изобретения, таким образом, не подразумевается. Изменения и дальнейшие модификации признаков изобретения, иллюстрированных в настоящем описании, а также дополнительные применения принципов настоящего изобретения, как показано в настоящем документе, которые осуществлялись бы специалистом в данной области техники и которые приведены в настоящем описании, должны быть рассмотрены в пределах объема изобретения. Следует отметить, что, как используется в настоящем описании и прилагаемой формуле изобретения, формы существительных в единственном числе включают формы существительных во множественном числе, если в описании ясно не указано иное. Все ссылки, включая патенты, патентные заявки и литературу, приведенные в описании, прямо включены в настоящем документе посредством ссылки полностью.
Авторы изобретения неожиданно обнаружили новые азотсодержащие соединения, обладающие антибактериальными свойствами.
Термин "C1-C6 алкил", используемый в настоящем документе, относится к разветвленному или неразветвленному ациклическому углеводородному радикалу, содержащему 1-6 атомов углерода. Типичные не ограничивающие объем изобретения примеры "C1-C6 алкила" включают метил, этил, н-пропил, изо-пропил, н-бутил, изо-бутил, трет-бутил, н-пентил, изо-пентил, н-гексил и тому подобное. "C1-C6-алкил" может быть незамещен или замещен одним или несколькими заместителями. Типичные неограничивающие объем изобретения примеры таких заместителей включают: галоген, алкокси, CN, COOH, CONH2, OH, -NH2, -NHCOCH3, циклоалкил, гетероциклил, гетероарил, арил и тому подобное.
Термин "циклоалкил", используемый в настоящем документе, относится к трех-семичленным циклическим углеводородным радикалам. Циклоалкильная группа необязательно включает одну или несколько двойных или тройных связей, или сочетание двойных связей и тройных связей, но не является ароматической. Типичные неограничивающие примеры циклоалкильных групп включают: циклопропан, циклобутан, циклопентан, циклогексан и циклогептан. Циклоалкил может быть незамещен или замещен одним или несколькими заместителями. Типичные неограничивающие примеры таких заместителей включают: C1-C6 алкил, галоген, алкокси, CN, COOH, CONH2, ОН, NH2, NHCOCH3, гетероциклил, гетероарил, арил, SO2-алкил, SO2-арил, OSO2-алкил, -OSO2-арил и тому подобное.
Термин "гетероциклил", используемый в настоящем документе, относится к четырех-семи членной циклоалкильной группе, содержащей один или несколько гетероатомов, выбранных из азота, кислорода или серы. Гетероциклоалкильная группа, необязательно включает одну или несколько двойных или тройных связей или сочетание двойных связей и тройных связей, но которая не является ароматической. Типичные неограничивающие объем изобретения примеры гетероциклоалкильных групп включают: азетидин, пирролидин, 2-оксо-пирролидин, имидазолидин-2-он, пиперидин, оксазин, тиазин, пиперазин, пиперазин-2,3-дион, морфолин, тиаморфолин, азапан и тому подобное. Гетероциклоалкил может быть незамещен или замещен одним или несколькими заместителями. Типичные неограничивающие объем изобретения примеры таких заместителей включают: C1-C6 алкил, галоген, алкокси, CN, COOH, CONH2, OH, NH2, NHCOCH3, гетероциклил, гетероарил, арил, SO2-алкил, SO2-арил, OSO2-алкил, OSO2-арил и тому подобное.
Термин "арил", используемый в настоящем документе, относится к моноциклическому или полициклическому ароматическому углеводороду. Типичные неограничивающие объем настоящего изобретения примеры арильных групп включают фенил, нафтил, антраценил, флуоренил, фенантренил и тому подобное. Арильная группа может быть не замещена или замещена одним или несколькими заместителями. Типичные неограничивающие объем настоящего изобретения примеры таких заместителей включают C1-C6 алкил, галоген, алкокси, CN, СООН, CONH2, ОН, NH2, NHCOCH3, гетероциклил, гетероарил, арил, SO2-алкил, SO2-арил, OSO2-алкил, OSO2-арил и тому подобное.
Термин "гетероарил", используемый в настоящем документе, относится к моноциклической или полициклической ароматической углеводородной группе, в которой один или несколько атомов углерода заменены на гетероатомы, выбранные из азота, кислорода и серы. Если гетероарильная группа содержит более одного гетероатома, гетероатомы могут быть одинаковыми или различными. Типичные неограничивающие объем настоящего изобретения примеры гетероарильных групп включают: 1,2,4-оксадиазол, 1,3,4-оксадиазол, 1,3,4-тиадиазол, 1,2,3,4-тетразол, 1,3-оксазол, 1,3-тиазол, пиридин, пиримидин, пиразин, пиридазин, фуран, пиррол, тиофен, имидазол, пиразол, бензофуран, бензотиофен, бензимидазол, бензоксазол, бензотиазол, тиазол и тому подобное. Гетероарильная группа может быть не замещена или замещена одним или несколькими заместителями. Типичные неограничивающие объем настоящего изобретения примеры таких заместителей включают: C1-C6 алкил, галоген, алкокси, CN, СООН, CONH2, ОН, NH2, NHCOCH3, гетероциклил, гетероарил, арил, SO2-алкил, SO2-арил, OSO2-алкил, OSO2-арил и тому подобное.
Термин "стереоизомеры", используемый в настоящем документе, относится к соединениям, которые имеют одинаковую химическую конституцию, но отличаются расположением своих атомов или групп в пространстве. Соединения формулы (I) могут содержать асимметричные или хиральные центры и, следовательно, существуют в различных стереоизомерных формах. Подразумевается, если не указано иное, что все стереоизомерные формы соединений формулы (I), а также их смеси, включая рацемические смеси, являются частью настоящего изобретения. Кроме того, настоящее изобретение охватывает все геометрические и позиционные изомеры (включая цис- и транс-формы), а также их смеси, которые включены в объем настоящего изобретения. В общем случае, ссылка на соединение предполагает включение своих стереоизомеров и смесей различных стереоизомеров.
Термин "необязательно замещенный", используемый в настоящем документе, означает, что замещение не является обязательным, и, следовательно, включает как незамещенные, так и замещенные атомы и фрагменты. "Замещенный" атом или фрагмент показывает, что любой атом водорода на определенном атоме или фрагменте может быть заменен выбранным из указанной группы заместителей, при условии, что нормальная валентность указанного атома или фрагмента не превышена, и что замещение обеспечивает стабильное соединение.
Термин "фармацевтически приемлемая соль", используемый в настоящем документе, относится к одной или нескольким солям данного соединения, которые обладают желаемой фармакологической активностью свободного основания и которые ни с биологической точки зрения, ни иным образом являются нежелательными. В общем случае, "фармацевтически приемлемые соли" относятся к солям, которые являются подходящими для использования в контакте с тканями человека и животных без чрезмерной токсичности, раздражения, аллергической реакции и тому подобного, и соизмеримы с разумным соотношением польза/риск. Фармацевтически приемлемые соли хорошо известны в данной области техники. Например, работа С. М. Berge и др. (J. Pharmaceutical Sciences, 66: 1-19 (1977)), включена здесь в качестве ссылки в полном объеме, где подробно описаны различные фармацевтически приемлемые соли.
В общем случае, соединения согласно изобретению, содержат основные (например, атомы азота), а также кислотные фрагменты (например, соединения формулы (I), где М представляет собой водород). Специалисту в данной области техники будет понятно, что такие соединения соответственно могут образовывать кислые соли (образованные с помощью неорганических и/или органических кислот), а также основные соли (образованные с помощью неорганических и/или органических оснований). Такие соли могут быть получены методами, описанными в данной области техники. Например, основной фрагмент может быть превращен в свою соль путем обработки соединения соответствующим количеством кислоты. Типичные неограничивающие объем настоящего изобретения примеры таких подходящих кислот включают хлористоводородную кислоту, трифторуксусную кислоту, метансульфоновую кислоту или тому подобное. Альтернативно, кислотный фрагмент может быть преобразован в свою соль путем обработки подходящим основанием. Типичные неограничивающие объем настоящего изобретения примеры таких оснований включают: карбонат натрия, бикарбонат натрия, карбонат калия, бикарбонат калия или тому подобное. В случае соединений, содержащих более одной функциональной группы, способной к превращению в соль, каждая такая функциональная группа может быть независимо превращена в соль. Например, в случае соединений, содержащих два основных атома азота, один основной атом азота может образовывать соль с помощью одной кислоты, а другой основной атом азота может образовывать соль с другой кислотой. Некоторые соединения по настоящему изобретению содержат как кислотные, так и основные фрагменты, и, таким образом, могут образовывать внутренние соли или соответствующие цвиттерионы. В общем случае, все фармацевтически приемлемые солевые формы соединений формулы (I) в соответствии с изобретением, в том числе кислотно-аддитивные соли, основно-аддитивные соли, цвиттерионы и т.п., рассматриваются как включенные в объем настоящего изобретения, и обычно называются фармацевтически приемлемыми солями.
Термин "галоген" или "гало", используемый в настоящем документе, относится к хлору, брому, фтору или йоду.
Термин "инфекция" или "бактериальная инфекция", используемый в настоящем документе, включает присутствие бактерий в или у субъекта, и в случае подавления их роста может быть обеспечено благоприятное воздействие на субъект. По существу, термин "инфекция", которая является нежелательной, помимо указания на наличие бактерий, также относится к нормальной флоре. Термин "инфекция" включает инфекцию, вызванную бактериями.
Термин «лечить», «лечение» или «терапия», используемый в настоящем документе, относится к введению лекарственного средства, в том числе фармацевтической композиции или одного или нескольких фармацевтически активных ингредиентов, для профилактики и/или в терапевтических целях. Термин "профилактическое лечение" относится к лечению субъекта, который еще не заражен, но который подвержен риску или иным образом имеет риск заражения (предупреждение бактериальной инфекции). Термин "терапевтическое лечение" относится к проведению лечения субъекту, уже страдающему от инфекции.
Термины "лечить", "лечение" или "терапия", используемые в настоящем документе, также относятся к введению композиций или одного или нескольких фармацевтически активных ингредиентов, описанных в настоящем описании, с или без дополнительных фармацевтически активных или инертных ингредиентов, для: (I) снижения или устранения или бактериальной инфекции или одного или несколько симптомов бактериальной инфекции, или (II) замедления прогрессирования бактериальной инфекции или одного или нескольких симптомов бактериальной инфекции, или (III) снижения тяжести бактериальной инфекции или одного или несколько симптомов бактериальной инфекции, или (IV) подавления клинических проявлений бактериальной инфекции, или (V) подавления проявления побочных симптомов бактериальной инфекции.
Термин "фармацевтически эффективное количество" или "терапевтически эффективное количество" или "эффективное количество", используемый в настоящем документе, относится к количеству, которое обеспечивает терапевтический эффект, или является количеством, необходимым для получения терапевтического эффекта у субъекта. Например, терапевтически или фармацевтически эффективное количество антибактериального средства или фармацевтической композиции является количеством антибактериального средства или фармацевтической композиции, необходимым для получения желаемого терапевтического эффекта, что следует из результатов клинических испытаний, исследований инфекции на животной модели и/или in vitro исследований (например, в агаре или бульоне). Фармацевтически эффективное количество зависит от нескольких факторов, включая, но ими не ограничиваясь: микроорганизм, вовлеченный в патологический процесс (например, бактерия), характеристики субъекта (например, рост, вес, пол, возраст и история болезни), тяжесть инфекции и конкретного используемого типа антибактериального средства. Для профилактического лечения, терапевтически или профилактически эффективное количество представляет собой количество, которое будет эффективным в предотвращении микробной (например, бактериальной) инфекции.
Термин "введение" или "применение" включает доставку композиции или одного или нескольких фармацевтически активных ингредиентов субъекту, включая, например, любыми подходящими способами, которые предназначены для доставки композиции или ее активных ингредиентов или других фармацевтически активных ингредиентов к участку локализации инфекции. Способ введения может изменяться в зависимости от различных факторов, таких как, например, компоненты фармацевтической композиции или природа фармацевтически активных или инертных ингредиентов, локализация потенциальной или фактической инфекции, микроорганизма, тяжесть инфекции, возраст и физическое состояние субъекта и тому подобное. Некоторые неограничивающие объем настоящего изобретения примеры способов введения композиции или ее фармацевтически активного ингредиента субъекту, в соответствии с настоящим изобретением, включают: пероральное, внутривенное, местное, интрареспираторное, внутрибрюшинное, внутримышечное, парентеральное, сублингвальное, трансдермальное, интраназальное, аэрозольное, внутриглазное, интратрахеальное, ректальное, вагинальное введение, с помощью генной пушки, кожный пластырь, глазные капли, ушные капли или жидкость для полоскания полости рта. В случае фармацевтической композиции, содержащей более одного ингредиента (активного или инертного), один из способов введения такой композиции заключается в смешивании ингредиентов (например, в виде подходящей единичной дозированной формы, такой как таблетки, капсулы, раствор, порошок и т.п.), и последующем введении лекарственной формы. Альтернативно, ингредиенты могут быть также введены раздельно (одновременно или один за другим), до тех пор, пока эти ингредиенты не достигнут эффективных терапевтических уровней, при которых композиция в целом обеспечивает синергический и/или желаемый эффект.
Термин "рост", используемый в настоящем документе, относится к росту одного или нескольких микроорганизмов, и включает размножение или расширение популяции микроорганизмов (например, бактерий). Термин также включает поддержание постоянных метаболических процессов микроорганизма, включая процессы, которые обеспечивают выживаемость микроорганизма.
Термин "эффективность", используемый в настоящем документе, относится к способности, при лечении с помощью или композиции или одного или нескольких фармацевтически активных ингредиентов, вызывать желаемый биологический эффект у субъекта. Например, термин "антибактериальная эффективность" композиции или антибактериального средства относится к способности композиции или антибактериального средства предотвращать или лечить микробную (например, бактериальную) инфекцию у субъекта.
Термин "синергический" или "синергизм", используемый в настоящем документе, относится к взаимодействию двух или более средств для того, чтобы их совместный эффект был больше, чем их индивидуальные эффекты.
Термин "антибактериальное средство", используемый в настоящем документе, относится к любому веществу, соединению или сочетанию веществ или сочетанию соединений, способному: (I) ингибировать, снижать или предотвращать рост бактерий; (II) ингибировать или снижать способность бактерий вызывать инфекцию у субъекта; или (III) ингибировать или снижать способность бактерий к размножению и сохранению инфекции в окружающей среде. Термин "антибактериальное средство" также относится к соединениям, способным снижать инфективность или вирулентность бактерий.
Термин "бета-лактамное антибактериальное средство", используемый в настоящем документе, относится к соединениям, обладающим антибактериальными свойствами и содержащим бета-лактамное ядро в своей молекулярной структуре.
Термин "бета-лактамаза", используемый в настоящем документе, относится к любому ферменту или белку или любому другому веществу, которое разрушает бета-лактамное кольцо. Термин "бета-лактамаза" включает ферменты, которые продуцируются бактериями и обладают способностью гидролизовать бета-лактамное кольцо в бета-лактамном соединении, либо частично, либо полностью.
Термин "ингибитор бета-лактамазы", используемый в настоящем документе, относится к соединению, способному ингибировать активность одного или нескольких бета-лактамазных ферментов, либо частично, либо полностью.
Термин "фармацевтически инертный ингредиент" или "носитель" или "наполнитель" относится к соединению или веществу, используемому для облегчения введения соединения, включая, например, вещества, которые повышают растворимость соединения. Типичные неограничивающие объем настоящего изобретения примеры твердых носителей включают: крахмал, лактозу, дикальцийфосфат, сахарозу и каолин, и так далее. Типичные неограничивающие объем настоящего изобретения примеры жидких носителей включают: стерильную воду, физиологический раствор, буферы, неионные поверхностно-активные вещества и пищевые масла, такие как масло, арахисовое и кунжутное масла и так далее. Кроме того, могут быть включены различные вспомогательные вещества, обычно используемые в данной области техники. Эти и другие такие вещества описаны в литературе, например, в Merck Index (Merck & Company, Rahway, N.J.). Рекомендации по включению различных компонентов в фармацевтических композициях, которые описаны, например, в работе Gilman et al. (Eds.) (1990); Goodman and Gilman's: The Pharmacological Basis of Therapeutics, 8th Ed., Pergamon Press., которая включена в настоящем документе в качестве ссылки полностью.
Термин "субъект", используемый в настоящем документе, относится к позвоночным и беспозвоночным, включая млекопитающих. Термин "субъект" включает людей, животных, птиц, рыб или амфибий. Типичные неограничивающие объем настоящего изобретения примеры "субъекта" включает людей, кошек, собак, лошадей, овец, крупный рогатый скот, коров, свиней, ягнят, крыс, мышей и морских свинок.
Термин "фармацевтически приемлемое производное", используемый в настоящем документе, относится к и включает любую фармацевтически приемлемую соль, пролекарства, метаболиты, сложные эфиры, простые эфиры, гидраты, полиморфы, сольваты, комплексы, энантиомеры или аддукты соединения, описанного в настоящем документе, которые при введении субъекту способны обеспечить (прямо или косвенно) исходное соединение. Например, термин "антибактериальный агент или его фармацевтически приемлемое производное" включает все производные антибактериального агента (такие как соли, пролекарства, метаболиты, сложные эфиры, простые эфиры, гидраты, полиморфы, сольваты, комплексы, энантиомеры или аддукты), которые, при введении в организм пациента, могут обеспечивать (непосредственно или косвенно) антибактериальное соединение.
В общем случае, термин «катион» включает Na, K, Mg, Ca, NH4+, (CH3CH2)3N+ и т.д.
В одном общем аспекте, предложены соединения формулы (I):

или их стереоизомеры или его фармацевтически приемлемые соли;
где:
R1 представляет собой:
(a) SO3M,
(b) SO2NH2,
(c) PO3M,
(d) CH2COOM,
(e) CF2COOM,
(f) CHFCOOM или
(g) CF3;
М представляет собой водород или катион;
R2 представляет собой:
(a) водород,
(b) (CH2)n-R3 или
(c) COOR3,
n равно 0, 1 или 2;
R3 представляет собой:
(a) водород,
(b) C1-C6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из галогена, OR5, CN, COOR5, CONR6R7, NR6R7, NR5COR8, NR5CONR6R7 гетероциклила, гетероарила, циклоалкила или арила,
(c) CN,
(d) NR6R7,
(e) CONR6R7,
(f) NHCONR6R7,
(g) арил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(h) гетероциклил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(i) гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
j) циклоалкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(k) циклоалкил, замещенный C1-C6 алкилом, где C1-C6 алкил дополнительно замещен одним или несколькими заместителями, независимо выбранными из OR5, NR6R7, галогена, CN или CONR6R7, или
(l) OR8;
R4 представляет собой:
(a) водород,
(b) C1-C6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из галогена, OR5, CN, COOR5, CONR6R7, NR6R7, NR5COR8, гетероциклила, гетероарила, циклоалкила или арила,
(c) арил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(d) гетероциклил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7,
(e) гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7, или
(f) циклоалкил необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR6R7, галогена, CN, CONR6R7, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR6R7;
R5 и R8 представляют собой каждый независимо друг от друга:
(a) водород или
(b) C1-C6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из галогена, CN, CONR6R7, NR6R7, гетероциклила, гетероарила, циклоалкила или арила;
R6 и R7 представляют собой каждый независимо друг от друга:
(a) водород,
(b) C1-C6 алкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из галогена, OR5, CN, COOR5, CONR5R8, NR5R8, NR5COR8, гетероциклила, гетероарила, циклоалкила или арила,
(c) арил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR5R8, галогена, CN, CONR5R8, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR5R8,
(d) гетероциклил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR5R8, галогена, CN, CONR5R8, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR5R8,
(e) гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR5R8, галогена, CN, CONR5R8, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR5R8,
(f) циклоалкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, OR5, NR5R8, галогена, CN, CONR5R8, SO2-алкила, SO2-арила, OSO2-алкила, OSO2-арила или NHCONR5R8, или
(g) R6 и R7 присоединены друг к другу с образованием семичленного кольца.
Типичные неограничивающие объем настоящего изобретения примеры соединений по изобретению включают:
(2S,5R)-7-оксо-N-[(2S)-пирролидин-2-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-[(2R)-пирролидин-2-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-[(3S)-пирролидин-3-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-[(3R)-пирролидин-3-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(2S,4R)-4-гидроксил-пирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(2S,4R)-4-циано-пирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(5R)-5-цианопирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(SR)-5-цианопирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(2S,4R)-4-трифторацетиламино-пирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(2S)-1-карбамимидоил-пирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-{1-[(2S)-пирролидин-2-ил]этилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-{[(2S)-5-оксопирролидин-2-ил]метилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-[(2S)-азетидин-2-илметилокси]-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-[(2R)-азетидин-2-илметилокси]-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-(пиперидин-4-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-((3R,S)-пиперидин-3-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-((2R,S)пиперидин-2-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-((2S)пиперидин-2-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-((2S)пиперидин-2-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-{1-[(2S)-пиперидин-2-ил]этилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-(азепан-2-илметилокси)-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S)-N-(2,3-дигидро-1H-индол-2-илметилокси)-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(2R,S)-1,2,3,4-тетрагидро-хинолин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(3S)-1,2,3,4-тетрагидро-изохинолин-3-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(4S)-1-метил-1,4,5,6-тетрагидропирроло[3,4-c]пиразол-4-ил]метокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(4S)-1H-1,4,5,6-тетрагидропирроло[3,4-c]пиразол-4-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S)-N-[(4,5-дигидрокси-1,4-дигидропиридин-2-ил)метилокси]-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-{[(4S)-2-(2-гидроксифенил)-4,5-дигидро-1,3-оксазол-4-ил]метилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-{[(4S)-2-((2S)-пирролидин-2-ил)-4,5-дигидро-1,3-оксазол-4-ил]метилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-[(3R,S)-пирролидин-3-илокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-[(3S)-пирролидин-3-илокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-7-оксо-N-[(3R)-пирролидин-3-илокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(3R,5S)-5-цианопирролидин-3-ил]окси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(3S,5S)-5-цианопирролидин-3-ил]окси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-{[(3R,5S)-5-карбамоилпирролидин-3-ил]окси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-(азетидин-3-илокси)-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-метилокси-7-оксо-N-(пиперидин-2-илметил)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-метилокси-7-оксо-N-(пиперидин-3-илметил)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-метилокси-7-оксо-N-(пирролидин-2-илметил)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-[(2S)-азетидин-2-илметил]-N-гидрокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-гидрокси-7-оксо-N-[(2S)-пирролидин-2-илметил]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-гидрокси-7-оксо-N-[(2S)-пиперидин-2-илметил]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-[(2S)-азепан-2-илметил]-N-гидрокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-[(2R)-азетидин-2-илметил]-N-гидрокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-гидрокси-7-оксо-N-[(2R)-пирролидин-2-илметил]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-гидрокси-7-оксо-N-[(2R)-пиперидин-2-илметил]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
(2S,5R)-N-[(2R)-азепан-2-илметил]-N-гидрокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамид;
или его стереоизомер или его фармацевтически приемлемую соль.
Типичные неограничивающие объем настоящего изобретения примеры различных солевых форм соединений по изобретению включают:
Натриевую соль (2S,5R)-N-[(2S)-азетидин-2-илметил]-N-гидрокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-гидрокси-7-оксо-N-[(2S)-пирролидин-2-илметил]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-гидрокси-7-оксо-N-[(2S)-пиперидин-2-илметил]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-[(2S)-азепан-2-илметил]-N-гидрокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-[(2R)-азетидин-2-илметил]-N-гидрокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-гидрокси-7-оксо-N-[(2R)-пирролидин-2-илметил]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-гидрокси-7-оксо-N-[(2R)-пиперидин-2-илметил]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-[(2R)-азепан-2-илметил]-N-гидрокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-[(2S)-пирролидин-2-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-[(2R)-пирролидин-2-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-[(3S)-пирролидин-3-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-[(3R)-пирролидин-3-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(2S,4R)-4-гидроксил-пирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(2S,4R)-4-цианопирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(5R)-5-цианопирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(SR)-5-цианопирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(2S,4R)-4-трифторацетиламино-пирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(2S)-1-карбамимидоил-пирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-{1-[(2S)-пирролидин-2-ил]этилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-{[(2S)-5-оксопирролидин-2-ил]метилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-[(2S)-азетидин-2-илметилокси]-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-[(2R)-азетидин-2-илметилокси]-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-(пиперидин-4-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-((3R,S)пиперидин-3-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-((2R,S)пиперидин-2-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-((2S)пиперидин-2-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-((2S)пиперидин-2-илметилокси)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-{1-[(2S)пиперидин-2-ил]этилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-(азепан-2-илметилокси)-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S)-N-(2,3-дигидро-1H-индол-2-илметилокси)-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(2R,S)-1,2,3,4-тетрагидро-хинолин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(3S)-1,2,3,4-тетрагидро-изохинолин-3-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(4S)-1-метил-1,4,5,6-тетрагидропирроло[3,4-c]пиразол-4-ил]метокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(4S)-1H-1,4,5,6-тетрагидропирроло[3,4-c]пиразол-4-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S)-N-[(4,5-дигидрокси-1,4-дигидропиридин-2-ил)метилокси]-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-{[(4S)-2-(2-гидроксифенил)-4,5-дигидро-1,3-оксазол-4-ил]метилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-{[(4S)-2-((2S)пирролидин-2-ил)-4,5-дигидро-1,3-оксазол-4-ил]метилокси}-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-[(3R,S)пирролидин-3-илокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-[(3S)-пирролидин-3-илокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-7-оксо-N-[(3R)-пирролидин-3-илокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(3R,5S)-5-цианопирролидин-3-ил]окси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(3S,5S)-5-цианопирролидин-3-ил]окси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-{[(3R,5S)-5-карбамоилпирролидин-3-ил]окси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-(азетидин-3-илокси)-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-метилокси-7-оксо-N-(пиперидин-2-илметил)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-метилокси-7-оксо-N-(пиперидин-3-илметил)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-метилокси-7-оксо-N-(пирролидин-2-илметил)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
(2S,5R)-N-(2-аминоэтилокси)-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамидную соль трифторуксусной кислоты;
(2S,5R)-N-(2-карбамимидамидоэтилокси)-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамидную соль трифторуксусной кислоты;
(2S,5R)-N-(3-аминопропилокси)-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамидную соль трифторуксусной кислоты;
(2S,5R)-N-{[(2S)-2,5-диаминопентил]окси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамидную соль трифторуксусной кислоты;
(2S,5R)-N-{[(2S,4R)-4-аминопирролидин-2-ил]метилокси}-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамидную соль трифторуксусной кислоты;
(2S,5R)-7-оксо-N-[(2S)-пиперазин-2-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамидную соль трифторуксусной кислоты;
(2S,5R)-N-метилокси-7-оксо-N-(пиперазин-2-илметил)-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамидную соль трифторуксусной кислоты;
Натриевую соль (2S,5R)-N-метокси-N-метил-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-метокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-гидрокси-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-[(1-метил-1H-пиразол-5-ил)метилокси]-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
Натриевую соль (2S,5R)-N-гидрокси-N-метил-7-оксо-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида;
или его стереоизомер.
В общем случае соединения по изобретению могут быть получены в соответствии со следующими процедурами. Специалисту в данной области техники будет понятно, что для обеспечения желаемых и родственных соединений, описанные способы могут быть дополнительно изменены или оптимизированы. В следующих процедурах все переменные имеют значения, указанные выше.
Как показано на схеме 1, транс-6-бензилокси-7-оксо-1,6-диаза-бицикло[3.2.1]октан-2-карбоновую кислоту (1a), которая описана в международной публикации РСТ № WO 2009/091856, подвергают взаимодействию с соответствующими замещенными гидроксиламинами в присутствии подходящего связующего агента, такого как гидрохлорид EDC или дициклогексилкарбодиимид (DCC), в подходящем растворителе, таком как N,N-формамиддиметил; N,N-диметилацетамид; 1,4 диоксан; хлороформ; дихлорметан; или дихлорэтан, при температуре в интервале от -15°С до 60°С в течение приблизительно от 1 до 24 часов с получением промежуточного соединения (1b).
Схема 1

Промежуточное соединение (1b) подвергают гидролизу в присутствии подходящего катализатора (например, 5% или 10% палладий-на-угле или 20% гидроксид палладия на угле) в присутствии источника водорода (такого как газообразный водород, формиат аммония, циклогексен) в подходящем растворителе (таком как метанол, этанол, смесь метанол-дихлорметан или смесь N,N-диметилформамид-дихлорметан) при температуре в интервале от 25°С до 60°С в течение приблизительно от 1 до 14 часов с получением промежуточного соединения (1с).
Промежуточное соединение (1c) сульфонируют взаимодействием с сульфирующим реагентом (таким как комплекс триоксид серы-пиридин или комплекс триоксид серы-N,N-диметилформамид) в подходящем растворителе (таком как пиридин, Ν,Ν-диметилформамид) при температуре в интервале от примерно 25°С до 90°С в течение приблизительно от 1 до 24 часов с получением пиридиновой соли сульфоновой кислоты, которая при обработке тетрабутил сульфат аммония обеспечивает тетрабутиламмониевая соль сульфоновой кислоты в качестве промежуточного соединения (1d).
Некоторые соединения согласно изобретению выделяют в виде цвиттер-ионов, путем обработки промежуточного соединения (1d) трифторуксусной кислотой, в подходящем растворителе (таком как дихлорметан, хлороформ, ацетонитрил) при температуре в интервале от -10°С до 40°С в течение приблизительно 1-14 часов, в частности, когда R в промежуточном соединении (1d) содержит трет-бутоксикарбонил защищенную аминогруппу.
Некоторые другие соединения согласно изобретению выделяют в виде натриевой соли, при пропускании раствора промежуточного соединения (1d) через колонку с натриевой формой смолы Amberlite 200C в смеси тетрагидрофуран-вода с последующим упариванием растворителя в вакууме.
Требуемые замещенные гидроксиламины получают способом, показанным на схеме-2, как описано в Synthesis, 682-4 (1976) и в патенте США 5120849 (1992)
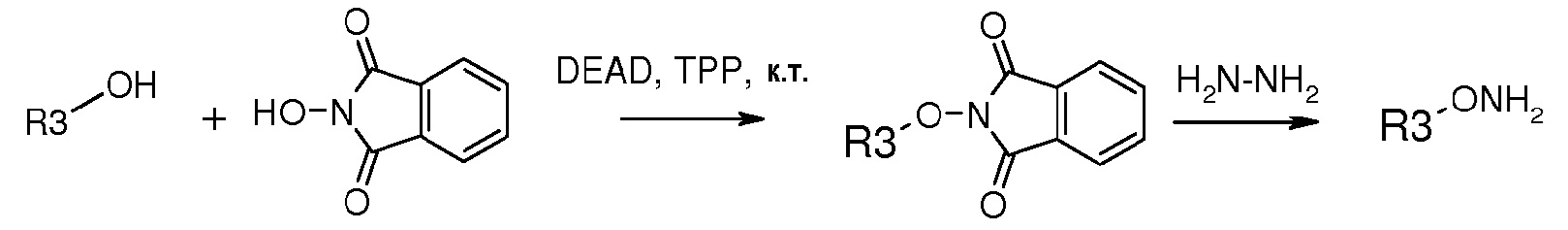
В некоторых вариантах осуществления предусмотрены фармацевтические композиции, содержащие соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль.
В некоторых других вариантах осуществления, предусмотрен способ лечения или предупреждения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли.
В некоторых вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли.
В некоторых других вариантах осуществления предусмотрен способ лечения или предупреждения бактериальной инфекции у субъекта, включающий введению указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей соединение формулы (I) или его стереоизомера или фармацевтически приемлемой соли.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей соединение формулы (I) или его стереоизомера или фармацевтически приемлемой соли.
В некоторых вариантах осуществления, предусмотрены фармацевтические композиции, содержащие: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное.
В некоторых других вариантах осуществления предусмотрены фармацевтические композиции, содержащие: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В некоторых других вариантах осуществления предусмотрены фармацевтические композиции, содержащие: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное, и (c), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В некоторых других вариантах осуществления предложен способ лечения или предупреждения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, и (b), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное, и (c), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества фармацевтической композиции, содержащей: (а) соединение формулы (I) или его стереоизомер или фармацевтически приемлемую соль, (b), по меньшей мере, один ингибитор бета-лактамазы, выбранный из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемое производное, и (c), по меньшей мере, одно антибактериальное средство или его фармацевтически приемлемое производное.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, и (b), по меньшей мере, одного ингибитора бета-лактамазы, выбранного из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемого производного.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, и (b), по меньшей мере, одного ингибитора бета-лактамазы, выбранного из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемого производного.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, и (b), по меньшей мере, одного антибактериального средства или его фармацевтически приемлемого производного.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, и (b), по меньшей мере, одного антибактериального средства или его фармацевтически приемлемого производного.
В некоторых других вариантах осуществления предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, (b), по меньшей мере, одного ингибитора бета-лактамазы, выбранного из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемого производного, и (c), по меньшей мере, одного антибактериального средства или его фармацевтически приемлемого производного.
В некоторых других вариантах осуществления, предложен способ предупреждения или лечения бактериальной инфекции у субъекта, где указанная инфекция вызывается бактерией, продуцирующей один или несколько бета-лактамазных ферментов, где указанный способ включает введение указанному субъекту фармацевтически эффективного количества: (а) соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли, (b), по меньшей мере, одного ингибитора бета-лактамазы, выбранного из сульбактама, тазобактама, клавулановой кислоты, или его фармацевтически приемлемого производного, и (c), по меньшей мере, одного антибактериального средства или его фармацевтически приемлемого производного.
В некоторых вариантах осуществления, предусмотрены способы повышения антибактериальной эффективности антибактериального средства у субъекта, где указанный способ включает совместное введение указанного антибактериального средства или его фармацевтически приемлемого производного с фармацевтически эффективным количеством соединения формулы (I) или его стереоизомера или фармацевтически приемлемой соли.
В некоторых вариантах осуществления композиции и способы согласно изобретению используют соединения формулы (I) или их стереоизомер или фармацевтически приемлемую соль в сочетании с, по меньшей мере, одним антибактериальным средством или его фармацевтически приемлемым производным. Может быть использован широкий ряд антибактериальных агентов. Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств включают одно или несколько антибактериальных соединений, обычно классифицируемых как аминогликозиды, ансамицины, карбацефемы, цефалоспорины, цефамицины, линкозамиды, липопептиды, макролиды, монобактамы, нитрофураны, пенициллины, полипептиды, хинолоны, сульфонамиды, тетрациклины, оксазолидинон и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к аминогликозидам, включают: амикацин, гентамицин, канамицин, неомицин, нетилмицину, тобрамицин, паромомицин, арбекацин, стрептомицин, апрамицин и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к ансамицинам, включают: гелданамицин, гербимицин и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к карбацефемам, включают: лоракарбеф и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к карбапенемам, включают: эртапенем, дорипенем, имипенем, меропенем и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к цефалоспоринам и цефамицинам, включают: цефазолин, цефацетрил, цефадроксил, цефалексин, цефалоглицин, цефалоний, цефалоридин, цефалотин, цефапирин, цефатризин, цефазедон, цефазафлур, цефрадин, цефроксадин, цефтезол, цефаклор, цефамандол, цефминокс, цефоницид, цефоранид, цефотиам, цефпрозил, цефбуперазон, цефуроксим, цефузонам, цефамицин, цефокситин, цетотетан, цефметазол, карбацефема, цефиксим, цефтазидим, цефтриаксон, цефкапен, цефдалоксим, цефдинир, цефдиторен, цефетамет, цефменоксим, цефодизим, цефоперазон, цефотаксим, цефпимизол, Цефпирамид, цефподоксим, цефсулодин, цефтерам, цефтибутен, цефтиолен, цефтизоксим, оксацефем, цефепим, цефозопрам, цефпиром, цефхином, цефтобипрол, цефтиофур, цефхином, цефовецин, CXA-101, цефтаролин, цефтобипрол и т.д.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к линкозамидам, включают: клиндамицин, линкомицин и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к макролидам, включают: азитромицин, кларитромицин, диритромицин, эритромицин, рокситромицин, тролендомицин, телитромицин, спектиномицин, солитромицин и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к монобактамам, включают: азтреонам и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к нитрофуранам, включают: фуразолидон, нитрофурантион и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к пеницилинам, включают: амоксициллин, ампициллин, азлоциллин, карбенициллин, клоксациллин, диклоксациллин, флуклоксациллин, мезлоциллин, метициллин, нафциллин, оксациллин, пенициллин G, пенициллин V, пиперациллин, темоциллин, тикарциллин и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к полипептидам, включают: бацитрацин, колистин, полимиксин B и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к хинолонам, включают: ципрофлоксацин, эноксацин, гатифлоксацин, левофлоксацин, ломефлоксацин, моксифлоксацин, налидиксовая кислота, левонадифлоксацин, норфлоксацин, офлоксацин, тровафлоксацин, грепафлоксацин, спарфлоксацин, темафлоксацин и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к сульфонамидам, включают: мафенид, сульфонамидохризоидин, сульфацетамид, сульфадиазин, сульфаметизол, сульфаметоксазол, сульфасалазин, сульфисоксазол, триметоприн и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к тетрациклинам, включают: демеклоциклин, доксициклин, миноциклин, окситетрациклин, тетрациклин, тигециклин и тому подобное.
Типичные неограничивающие объем настоящего изобретения примеры антибактериальных средств, относящихся к оксазолидинонам, включают: тедизолид, линезолид, ранбезолид, торезолид, радезолид и т.п.
Фармацевтические композиции в соответствии с изобретением могут включать один или несколько фармацевтически приемлемых носителей или наполнителей и т.п. Типичные неограничивающие объем настоящего изобретения примеры таких носителей или инертные наполнители включают: маннит, лактозу, крахмал, стеарат магния, сахарин натрия, тальк, целлюлозу, кроскармелозу натрия, глюкозу, желатин, сахарозу, карбонат магния, смачивающие агенты, эмульгаторы, солюбилизаторы, буферные агенты, регулирующие pH, смазывающие вещества, стабилизаторы, связывающие агенты и т.п.
Фармацевтические композиции по настоящему изобретению могут существовать в различных формах. В некоторых вариантах осуществления фармацевтическая композиция находится в форме порошка или раствора. В некоторых других вариантах осуществления, фармацевтические композиции согласно изобретению находятся в виде порошка, который можно восстанавливать добавлением совместимого восстанавливающего разбавителя до парентерального введения. Неограничивающий объем настоящего изобретения пример такого смешивающегося разбавителя включает воду.
В некоторых других вариантах осуществления, фармацевтические композиции по настоящему изобретению находятся в виде замороженной композиции, которые могут быть разбавлены смешивающимся разбавителем перед парентеральным введением.
В некоторых других вариантах осуществления, фармацевтические композиции по настоящему изобретению находятся в виде готовых к использованию форм для парентерального введения.
В способах согласно изобретению, фармацевтическая композиция и/или другие фармацевтически активные ингредиенты, описанные в настоящем документе, могут быть введены любым подходящим способом, который предназначен для доставки композиции или ее компонентов или активных ингредиентов в желаемый участок. Способ введения может изменяться в зависимости от различных факторов, таких как, например, компонентов в фармацевтической композиции и природы активных ингредиентов, локализации потенциальной или фактической инфекции, микроорганизма (например, бактерии) вовлеченного в патологический процесс, тяжести инфекции, возраста и физического состояния пациента. Некоторые неограничивающие объем настоящего изобретения примеры введения композиции субъекту в соответствии с настоящим изобретением включают пероральный, внутривенный, местный, интрареспираторный, внутрибрюшинный, внутримышечный, парентеральный, сублингвальный, трансдермальный, интраназальный, внутриглазной, аэрозольный, внутритрахиальный, интраректальный, вагинальный способ, генную пушку, кожный пластырь, глазные капели, ушные капли или жидкость для полоскания полости рта.
Композиции согласно изобретению могут быть получены в виде различных дозированных форм, в которых активные ингредиенты и/или инертные наполнители могут присутствовать либо вместе (например, в виде смеси), или в виде отдельных компонентов. Когда различные ингредиенты в композиции объединены в виде смеси, такая композиция может быть доставлена посредством введения такой смеси. Если композиция или дозированная форма, в которой ингредиенты не объединены в виде смеси, но получают в виде отдельных компонентов, то, например, композицию/лекарственную форму можно вводить несколькими способами. В одном из возможных способов, ингредиенты могут быть смешаны в нужных пропорциях, и затем смесь введена при необходимости. Альтернативно, компоненты или ингредиенты (активные или инертные) могут быть введены отдельно (одновременно или один за другим) в соответствующей пропорции, чтобы достичь такого же или эквивалентного терапевтического уровня или эффекта, который был бы достигнут при введении эквивалентной смеси.
Аналогично, в способах согласно изобретению, активные ингредиенты, описанные в настоящем документе, могут быть введены субъекту различными способами в зависимости от требований. В некоторых вариантах осуществления, активные ингредиенты смешивают в соответствующих количествах, и затем смесь вводят субъекту. В некоторых других вариантах осуществления, активные ингредиенты вводят раздельно. Поскольку изобретение предполагает, что активные ингредиенты агенты можно вводить по отдельности, изобретение также относится к объединению отдельных фармацевтических композиций в форме набора. Набор может содержать одну или несколько отдельных фармацевтических композиций, каждая из которых содержит один или несколько активных ингредиентов. Каждая из таких отдельных композиций могут присутствовать в отдельном контейнере, таком как сосуд, ампула, пузырек, шприц, коробки, пакеты и тому подобное. Обычно, набор включает инструкции по введению отдельных компонентов. Форма набора особенно эффективна, когда отдельные компоненты предпочтительно вводят в различных лекарственных формах (например, пероральных и парентеральных) или вводят с различными интервалами введения лекарственных средств. Когда активные ингредиенты вводят раздельно, они могут быть введены одновременно или последовательно.
Фармацевтическая композиция или активные ингредиенты в соответствии с настоящим изобретением могут быть получены в виде различных лекарственных форм. Типичные неограничивающие объем настоящего изобретения примеры лекарственных форм включают: твердые, полутвердые, жидкие и аэрозольные лекарственные формы, такие как таблетки, капсулы, порошки, растворы, суспензии, суппозитории, аэрозоли, гранулы, эмульсии, сиропы, эликсиры и тому подобное.
В общем случае, фармацевтические композиции и способ, описанный в настоящем документе, могут быть использованы для предупреждения или лечения бактериальных инфекций. Предпочтительно, композиции и способы, описанные в настоящем документе, также эффективны в предупреждении или лечении инфекций, вызванных бактериями, которые считаются менее восприимчивыми или не восприимчивыми к одному или нескольким известным антибактериальным средствам или их известным композициям. Некоторые неограничивающие объем настоящего изобретения примеры таких бактерий, обладающих развитой устойчивостью к различным антибактериальным средствам, включают: акинетобактерии, кишечную палочку, синегнойную палочку, золотистый стафилококк, энтеробактерии, клебсиеллу, цитробактерии и тому подобное. Другие неограничивающие объем настоящего изобретения примеры инфекций, которые могут быть предотвращены или вылечены с использованием композиций и/или способов по изобретению, включают: кожные инфекции и инфекции мягких тканей, фебрильную нейтропению, инфекции мочевыводящих путей, интраабдоминальные инфекции, инфекции дыхательных путей, пневмонию (внутрибольничную), бактериальный менингит, хирургические инфекции и т.д.
Неожиданно оказалось, что соединения, композиции и способы по данному изобретению также эффективны в предупреждении или лечении бактериальных инфекций, вызванных бактериями, продуцирующими один или несколько бета-лактамазных ферментов. Способность композиций и способов в соответствии с настоящим изобретением лечить такие резистентные бактерий с помощью типичных бета-лактамных антибиотиков представляет собой значительное улучшение в данной области техники.
В общем случае, соединения формулы (I) или его стереоизомер или фармацевтически приемлемая соль в соответствии с изобретением могут быть также использованы для повышения антибактериальной эффективности антибактериального средства у субъекта. Антибактериальная эффективность одного или нескольких антибактериальных средств может быть повышена, например, путем совместного введения указанного антибактериального средства или его фармацевтически приемлемой соли с фармацевтически эффективным количеством соединения формулы (I) или его стереоизомера или его фармацевтически приемлемой соли в соответствии с изобретением.
Для специалиста в данной области техники будет очевидно, что в изобретении могут быть осуществлены различные замены и модификации, описанные в настоящем документе, без отклонения от объема и сущности настоящего изобретения. Например, специалистам в данной области техники будет понятно, что изобретение может быть осуществлено с использованием ряда различных соединений, в описанных общих описаниях.
Примеры
Следующие примеры иллюстрируют варианты осуществления изобретения, которые в настоящее время являются наиболее известными. Тем не менее, следует понимать, что следующее является только примерами и иллюстрируют применение принципов настоящего изобретения. Многочисленные модификации и альтернативные композиции, способы и системы могут быть разработаны специалистами в данной области техники без отступления от сущности и объема настоящего изобретения. Подразумевается, что прилагаемая формула изобретения охватывает такие модификации и классификации. Таким образом, в то время как настоящее изобретение было описано выше подробно, следующие примеры описаны более подробно в связи с тем, что в настоящее время они рассматриваются в качестве наиболее практичных и предпочтительных вариантов осуществления изобретения.
Пример-1
(2S,5R)-7-оксо-N-[(2S)-пирролидин-2-илметилокси]-6-(сульфоокси)-1,6-диазабицикло-[3.2.1]октан-2-карбоксамид
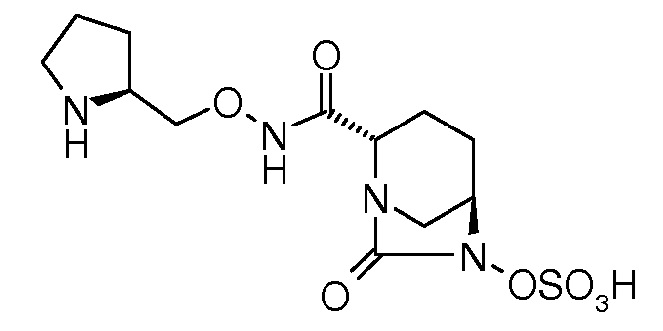
Получение боковой цепи: трет-бутил(2S)-2-[(аминоокси)метил]пирролидин-1-карбоксилат:

Стадия-1
Раствор DEAD (диметилазодикарбоксилат) (17,14 мл, 1,092 моль) в ТГФ (366 мл) охлаждали до -10°C и добавляли медленно раствор TPP (тиаминдифосфат) (22,49 мг, 1,092 ммоль) в THF (ТГФ) (36 мл). После перемешивания в течение 45 минут при температуре ниже -10°C добавляли раствор трет-бутил(2S)-2-(гидроксиметил)пирролидин-1-карбоксилата (12,2 мг, 0,606 моль) в ТГФ (36 мл) и после перемешивания в течение 5 минут добавляли раствор N-гидроксифталимида (9,88 мг, 0,606 моль) в ТГФ (122 мл). Полученную смесь оставляли нагреваться до комнатной температуры и продолжали перемешивание дополнительно. Через 16 часов, растворитель упаривали при пониженном давлении, и остаток разбавляли этилацетатом (250 мл) и слой этилацетата промывали насыщенным водным раствором бикарбоната натрия (1×122 мл), водой (1×122 мл) и насыщенным солевым раствором (1×61 мл). Растворитель упаривали при пониженном давлении и остаток очищали хроматографией на колонке с силикагелем. Элюирование 12% ацетоном в гексане и концентрирование объединенных фракций давали продукт в виде масла светло-желтого цвета, 20,6 мг, с выходом 98%.
Данные анализа:
Масса: 347,3 (M+H) для MW-346,39 и M.F-Cl8H22N2O5
Стадия-II:
К раствору фталимида (4 мг, 0,115 моль) в этаноле (60 мл) и добавляли гидрат гидразина (0,84 мл, 0,173 моль) при комнатной температуре. После перемешивания в течение 1 часа нерастворимые вещества отделяли фильтрованием. Фильтрат концентрировали при пониженном давлении, и остаток разбавляли с помощью DMC (40 мл). Слой DCM промывали водой (2×40 мл) и насыщенным солевым раствором (1×40 мл). Растворитель упаривали при пониженном давлении с получением 2,4 мг остатка. Этот остаток использовали в следующей реакции связывания.
Реакция связывания
Стадия-1: получение трет-бутилового эфира (2S,5R)-2-[(6-бензилокси-7-оксо-1,6-диаза-бицикло[3.2.1]октан-2-карбонил)метилоксикарбамоил]-(2S)-пирролидин-1-карбоновой кислоты:
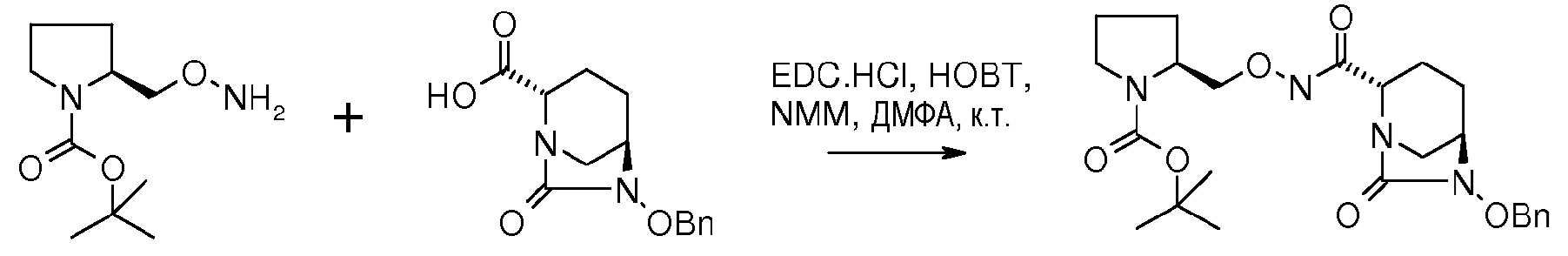
К прозрачному раствору (2S,5R)-6-(бензилокси)-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоновой кислоты (3,06 мг, 0,111 моль) в N,N-диметилформамиде (24 мл), добавляли HOBt (1,49 мг, 0,111 моль), затем гидрохлорид EDC (3,18 мг, 0,166 моль) и NMM (3,39, 0,333 моль) при около 25°C - 35°C при перемешивании. Реакционную смесь перемешивали в течение 15 минут и раствор трет-бутилового эфира 2-аминооксиметил-(S)-пирролидин-1-карбоновой кислоты (2,4 мг, 0,100 моль) растворяли в Ν,Ν-диметилформамиде (15 мл). Реакционную смесь перемешивали при температуре в пределах 25°C - 35°C в течение 16 часов, и полученную смесь выливали в воду (120 мл) и смесь экстрагировали этилацетатом (3×25 мл). Слой этилацетата промывали водой (1×100 мл) и насыщенным солевым раствором (1×50 мл). Растворитель упаривали при пониженном давлении, и остаток очищали хроматографией на колонке с силикагелем. Элюирование 10% ацетоном в гексане и концентрирование объединенных фракций давало продукт в виде твердого вещества белого цвета 2,1 мг, с выходом 64%.
Данные анализа:
Масса: 475,4 (M+H) для MW-474,56 и M.F-C24H34N4O6
1H ЯМР: растворитель (CDCl3): 10,16 (с, 1H), 7,43-7,35 (м, 5H), 5,06-4,88 (дд, 2H), 4,12 (с, 1H), 3,94-3,93 (д, 2H), 3,83 (неразрешаемый с, 1H), 3,75-3,73 (м, 1H), 3,37-3,28 (дт, 2H), 3,02-2,86 (дд, 2H), 2,29-2,25 (м, 1H), 1,99-1,82 (м, 5H), 1,75-1,61 (м, 2H), 1,45 (с, 9H).
Стадия-2: Получение тетрабутиламмониевой соли трет-бутилового эфира (2S,5R)-2-[(6-сульфоокси-7-оксо-1,6-диаза-бицикло[3.2.1]октан-2-карбонил)метилоксикарбамоил]-(2S)-пирролидин-1-карбоновой кислоты:

Раствор соединения бензила (2,1 г, ммоль) в 1:1 смеси DMF:DCM (5 мл) гидрогенизировали над 10% Pd/C (125 мг) при давлении 1 атм. водородом из баллона. После перемешивания в течение 4 часов реакционную смесь фильтровали через целит. Фильтрат концентрировали при пониженном давлении и полученный остаток растворяли в свежеперегнанном ДМФА (2,5 мл) и охлаждали до 10°C. Добавляли комплекс SO3ДМФА (193 мг, 12,6 ммоль) и реакционную смесь оставляли нагреваться до комнатной температуры. После перемешивания реакционной смеси при комнатной температуре в течение 1,5 часов, к реакционной смеси добавляли TBAA (379 мг, 12,6 ммоль) в воде (1,25 мл) и затем продолжали перемешивание в течение 2 часов. Летучие вещества удаляли отгонкой в высоком вакууме, и остаток совместно упаривали с ксиленом (2×25 мл) для удаления остатков ДМФА. Полученный остаток разбавляли водой (20 мл) и экстрагировали DCM (3×20 мл). Объединенный слой DCM промывали водой (2×20 мл). Слой DCM сушили и растворитель упаривали при пониженном давлении. Неочищенный остаток растирали с диэтиловым эфиром (3×25 мл) с получением продукта в виде белого твердого вещества, 610 мг, выход 82%.
Данные анализа:
Масса: 463,4 (M-H) для MW-705,96 и M.F-C33H63N5O9S.
1H ЯМР: Растворитель (CDCl3): 10,2 (с, 1H), 4,35 (с, 1H), 4,14 (с, 1H), 3,91-3,92 (д, 2H), 3,74 (м, 1H), 3,36-3,27 (м, 10H), 2,96-2,88 (дд, 2H), 2,31-2,26 (м, 2H), 2,19-1,98 (м, 2H), 1,95-1,70 (м, 4H), 1,68-1,62 (п, 8H), 1,49-1,40 (м, 17H), 1,02-0,98 (т, 12H) .
Стадия-3: Получение (2S,5R)-7-оксо-N-[(2S)-пирролидин-2-илметилокси]-6-(сульфоокси)-1,6-диазабицикло[3.2.1]октан-2-карбоксамида:

К охлажденному (-10°С) раствору соединения TBA (300 мг, 4,2 ммоль) в DCM (2,5 мл) добавляли ТФА (2,5 мл). После перемешивания в течение 30 мин при -10°C растворитель упаривали при пониженном давлении. Полученный остаток растирали с диэтиловым эфиром с получением белого твердого вещества. Твердое вещество промывали диэтиловым эфиром (3×25 мл), ацетонитрилом (2×25 мл) и DCM (2×25 мл). И оставшееся твердое вещество сушат при пониженном давлении (4 мм рт.ст.) с получением продукта в виде твердого вещества белого цвета 140 мг, выход 91%.
Данные анализа:
Масса: 363,2 (M-H) для MW-364,37 и M.F-C12H20N4O7S.
1H ЯМР: Растворитель (ДМСО-d6): 11,73 (с, 1H), 8,62-8,83 (д, 2H), 3,88-4,00 (м, 3H), 3,74-3,81 (м, 2H), 3,19 (т, 2H), 2,94-3,04 (дд, 2H), 1,96-2,03 (м, 2H), 1,80-1,92 (м, 3H), 1,54-1,73 (м, 3H).
Примеры 2-39 (таблица 1) были получены с использованием процедуры, описанной в примере 1, и используя соответствующий R1CH2ONH2 вместо трет-бутилового эфира 2-аминооксиметил-(S)-пирролидин-1-карбоновой кислоты. Эти соединения были выделены в виде цвиттер-ионов.
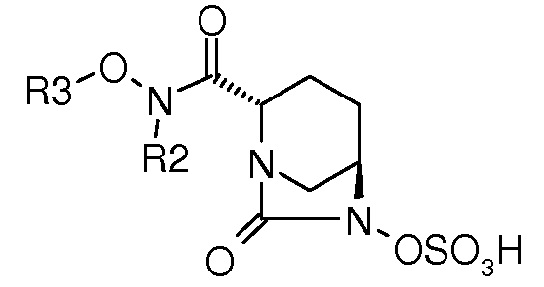
Примеры 40-45 (таблица 2) были получены с использованием процедуры, описанной в примере 1, и используя соответствующий R1CH2ONH2 вместо трет-бутилового эфира 2-аминооксиметил-(S)-пирролидин-1-карбоновой кислоты. Эти соединения выделяли в виде солей трифторуксусной кислоты.

Примеры 46-50 (таблица 3), были получены с использованием процедуры, описанной в примере-1, и используя соответствующий R1CH2ONH2 вместо трет-бутилового эфира 2-аминооксиметил-(S)-пирролидин-1-карбоновой кислоты. Эти соединения выделяли в виде натриевых солей.
Процедура: Раствор промежуточного соединения сульфата (1d), пропускали через колонку с натриевой формой смолы Amberlite 200C в смеси тетрагидрофуран-вода с последующим выпариванием растворителя из объединенных фракций при пониженном давлении (4 мм рт.ст.).
Биологическая активность
Была исследована биологическая активность репрезентативных соединений согласно изобретению в отношении различных бактериальных штаммов. В типичном исследовании, бактериальные культуры, выращиваемые в ночное время, соответствующим образом разбавляли и инокулировали на агаровой среде, содержащей двойные разведения тестируемых соединений. Наблюдение за ростом или отсутствием роста выполняли через 16-20 часов инкубации при 35±2°С в атмосферном воздухе. Всю процедуру выполняли в соответствии с рекомендациями Института клинических и лабораторных стандартов (Clinical and Laboratory Standards Institute (CLSI), Performance Standards for Antimicrobial Susceptibility Testing, 20th Informational Supplement, M 100-S20, Volume 30, № 1, 2010).
В таблице 4 описана антибактериальная активность репрезентативных соединений в соответствии с изобретением в отношении различных мультирезистентных к лекарственным средствам (MDR) грам-отрицательных штаммов бактерий, экспрессирующих различные ESBL. Активности выражены в MIC (мкг/мл). Для сравнения, активность нескольких известных антибактериальных агентов (например, цефтазидим, азтреонам, имипенем, ципрофлоксацин и тигециклин) также включена. Как можно видеть, что типичные соединения по изобретению проявляют антибактериальную активность в отношении различных штаммов MDR.
Реферат
Изобретение относится к области органической химии, а именно к гетероциклическому соединению формулы (I), или к его стереоизомеру, или к его фармацевтически приемлемой соли, где Rпредставляет собой SOM; М представляет собой водород или Na; Rпредставляет собой (a) водород или (b) (CH)-R; n равно 0 или 1; Rпредставляет собой (a) водород, (b) C-Салкил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из (а) 4-10-членного насыщенного или ненасыщенного гетероциклила, содержащего 1-3 гетероатома, выбранных из азота, кислорода и серы, необязательно замещенных одним или более заместителями, независимо выбранными из ОН, CN, NHCOCF, NH, C(=NH)NH, оксо, C-Салкила, СНОН или пирролидина, (b) NHили (с) NHC(=NH)NH, (c) 4-6-членный гетероциклил, содержащий 1 или 2 атома азота, необязательно замещенные одним или несколькими заместителями, независимо выбранными из CN или CONH. Также изобретение относится к фармацевтической композиции на основе соединения формулы (I), способу предупреждения или лечения бактериальной инфекции, основанному на введении как одного соединения формулы (I), так в комбинации с другим антибактериальным агентом. Технический результат: получены новые гетероциклические соединения, полезные при лечении бактериальных инфекций. 14 н. и 4 з.п. ф-лы, 4 табл., 51 пр.
Формула
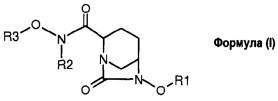
Документы, цитированные в отчёте о поиске
Ингибиторы бета-лактамаз
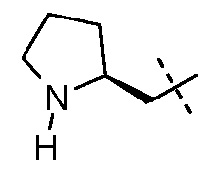



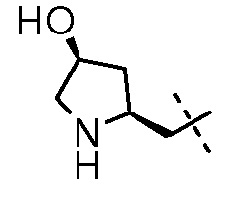
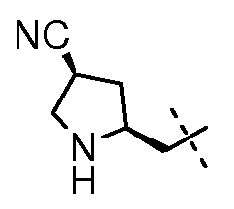



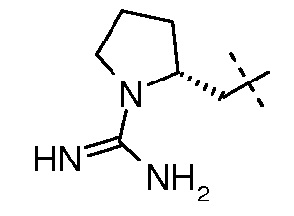




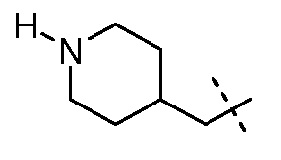


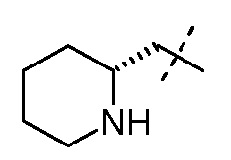









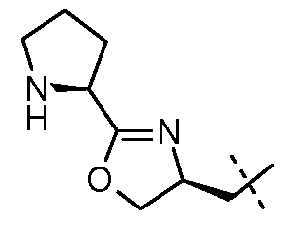
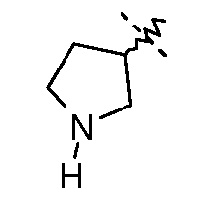



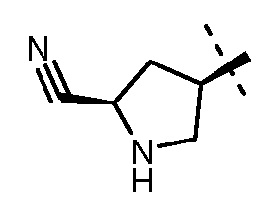



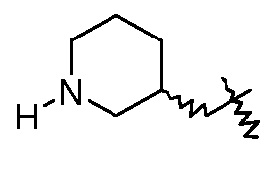
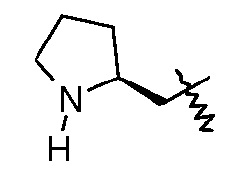
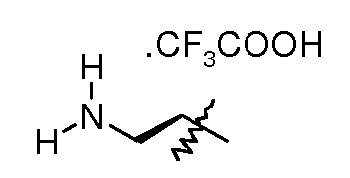




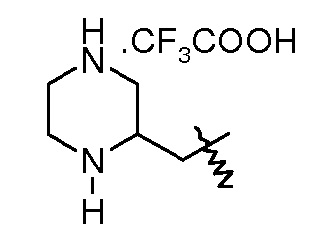
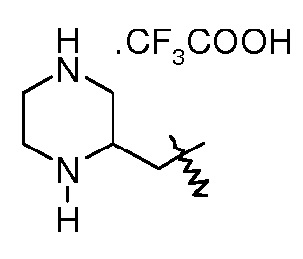


Комментарии