Кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, способ её получения и фармацевтическая композиция на её основе - RU2626877C1
Код документа: RU2626877C1
Чертежи



Описание
Изобретение относится к органической химии и касается новой кристаллической модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата (мирамистин - торговое название), названной β-модификацией, способа ее получения и фармацевтической композиции на ее основе, которая может быть использована в фармацевтической промышленности и медицине в качестве антисептического средства, оказывающего бактерицидное и противовирусное действие.
Известны четвертичные аммониевые соединения и, в частности, бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрат (C26H47ClN2O⋅H2O) - мирамистин (US 2459062 от 11.01.1949 г.).
Сходство заявляемой новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата с известным соединением – мирамистином - заключается в идентичности их химических составов.
Отличие заявляемой новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, от известной кристаллической модификации мирамистина заключается в различии их дифрактограмм рентгенофазового анализа (РФА): определенного набора углов 2θ (град.) - межплоскостных расстояний (d, Å), и их интенсивности (Iотн.=Ii/Imax×100, %), а также кривой дифференциальной сканирующей калориметрии (ДСК) - совокупности эндотермических эффектов при определенных температурах. Отметим, что в литературных источниках результаты РФА, а также данные термоаналитических исследований известной кристаллической модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата отсутствуют.
Известно, что обычно кристаллические модификации характеризуют физико-химическими методами анализа, такими как: ядерным магнитным резонансом (ЯМР) - совокупностью химических сдвигов (м.д.), высокоэффективной жидкостной хроматографией (ВЭЖХ) - временами удерживания (мин) и чистотой исследуемого вещества (%), методом рентгенофазового анализа (РФА) - наборами углов (2θ, град.), межплоскостных расстояний (d, Å) и их интенсивностью (I, имп./мин; Iотн.=Ii/Imax×100, %), термоаналитическими исследованиями - совокупностью тепловых эффектов при определенных температурах и другими.
Известная кристаллическая модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата представляет собой порошок практически белого цвета, без запаха, растворимый в воде, низкомолекулярных спиртах, ацетоне и хлороформе.
Наиболее близким по технической сущности является способ получения известной модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, заключающийся в том, что из исходных компонентов получают раствор целевого продукта, из которого после охлаждения фильтрованием выделяют кристаллиты мирамистина с последующей их сушкой в токе воздуха и далее - в вакуумном эксикаторе (RU 2323923 C2 от 10.05.2008 г.).
Отличие способа получения заявляемой новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата от способа получения известной кристаллической модификации мирамистина состоит в том, что водный раствор мирамистина с концентрацией (0,5-10,0) мас. %, при (25-100)°C, замораживают при скорости охлаждения не ниже 60 град./мин и подвергают сублимационной сушке.
Отличие заявляемой фармацевтической композиции на основе бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата в качестве антисептического средства, оказывающего бактерицидное и противовирусное действие (Регистр Лекарственных Средств России - Инструкция применения препарата Мирамистин®, Мирамистин®-Дарница, Окомистин®), состоит в том, что в качестве действующего вещества используют терапевтически эффективное количество новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
Целью изобретения является получение новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, разработка способа ее получения и применение ее в фармацевтической композиции в качестве антисептического средства, оказывающего бактерицидное и противовирусное действие.
Поставленная цель достигнута настоящим изобретением, а именно получением новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, характеризующейся следующим набором межплоскостных расстояний (d, Å) и соответствующих им интенсивностей (Iотн.=Ii/Imax×100, %): 26,725 - 48,53%; 23,333 - 39,88%; 11,491 - 13,65%; 9,918 - 9,14%; 9,196 - 24,68%; 9,139 - 24,75%; 7,942 - 15,44%; 7,265 - 14,22%; 7,230 - 14,29%; 7,035 - 13,48%; 6,615 - 13,06%; 6,288 - 16,18%; 6,065 - 18,06%; 5,951 - 15,27%; 5,475 - 13,73%; 5,182 - 18,55%; 4,985 - 19,53%; 4,762 - 33,90%; 4,572 - 100,0%; 4,445 - 91,35%; 4,235 - 84,24%; 3,914 - 94,68%; 3,647 - 28,26%; 3,500 - 20,76%; 3,316 - 20,91%; 3,235 - 27,03%; 3,131 - 17,40%; 3,047 - 16,67%; 3,001 - 16,84%; 2,918 - 17,48%; 2,799 - 16,42%; 2,790 - 14,95%; 2,663 - 18,80%; 2,524 - 13,31%; 2,480 - 10,54%; 2,365 -12,01%; 2,352 - 11,52%; 2,231 - 12,92%; 2,162 - 14,71%; 2,100 - 12,57%; 2,032 - 10,37%; 1,991 - 9,31%; 1,955 - 9,80%; 1,908 - 8,58% и совокупностью эндотермических эффектов на кривой ДСК при температурах: (59,6±0,5)°C; (89,9±0,5)°C; (221,3±0,5)°C.
Поставленная цель достигнута также разработкой способа получения новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, который состоит в том, что водный раствор мирамистина с концентрацией (0,5-10,0) мас. %, при (25-100)°C, замораживают при скорости охлаждения не ниже 60 град./мин и подвергают сублимационной сушке.
Кроме того, поставленная цель достигнута применением новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата для приготовления фармацевтической композиции в качестве антисептического средства, оказывающего бактерицидное и противовирусное действие. Указанная композиция содержит кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата в терапевтически эффективном количестве и по крайней мере один фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или наполнитель.
Из патентной и научно-технической литературы не известна кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, способ ее получения и применение ее в фармацевтической композиции в качестве антисептического средства, оказывающего бактерицидное и противовирусное действие.
Авторами изобретения обнаружена новая, не известная ранее, кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, характеризующаяся определенным набором дифракционных максимумов (d, Å) и их интенсивностью (Iотн., %), и совокупностью эндотермических эффектов при определенных температурах на кривой ДСК, предложены способ ее получения и применение ее для приготовления фармацевтической композиции в качестве антисептического средства, оказывающего бактерицидное и противовирусное действие.
Заявляемая новая, не известная ранее, кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата представляет собой порошок практически белого цвета, без запаха, растворимый в воде, низкомолекулярных спиртах, ацетоне и хлороформе.
Для пояснения сущности заявляемого технического решения к описанию приложены следующие таблицы и рисунки:
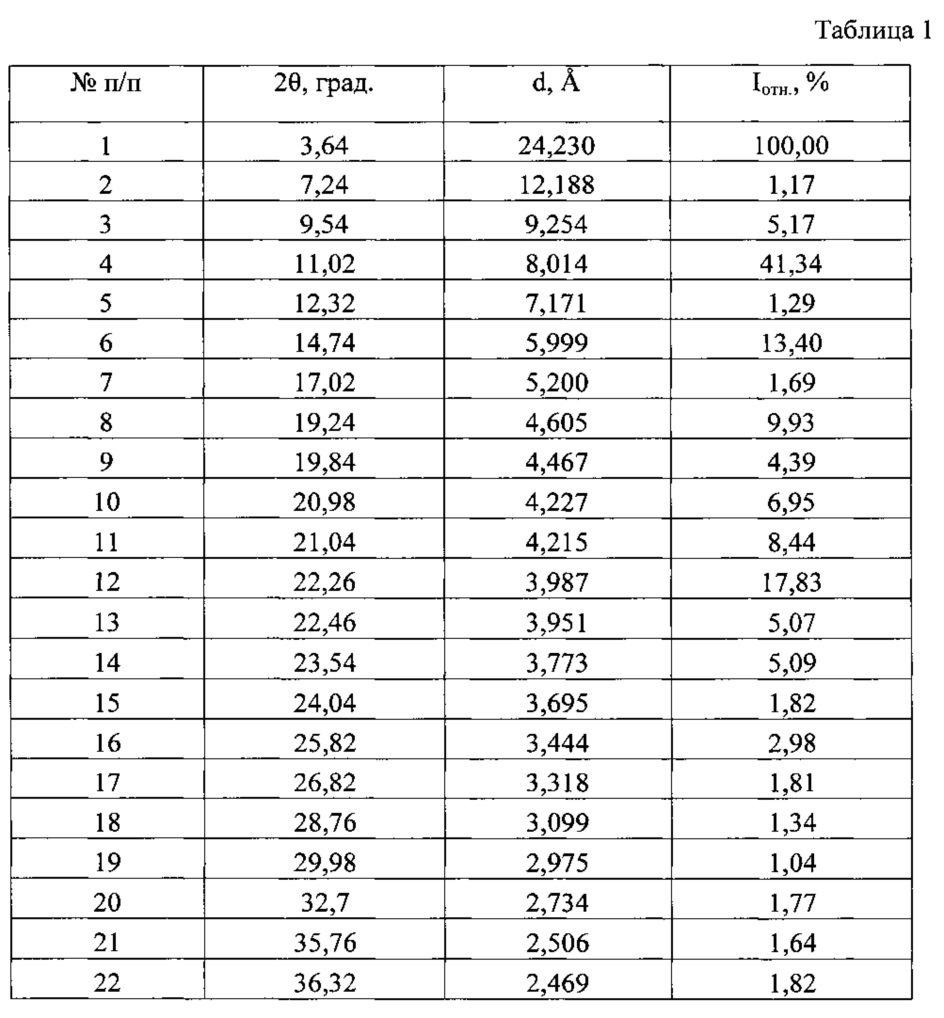
Таблица 1. Углы 2θ, град., межплоскостные расстояния (d, Å) и их интенсивности (Iотн., %) известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества.
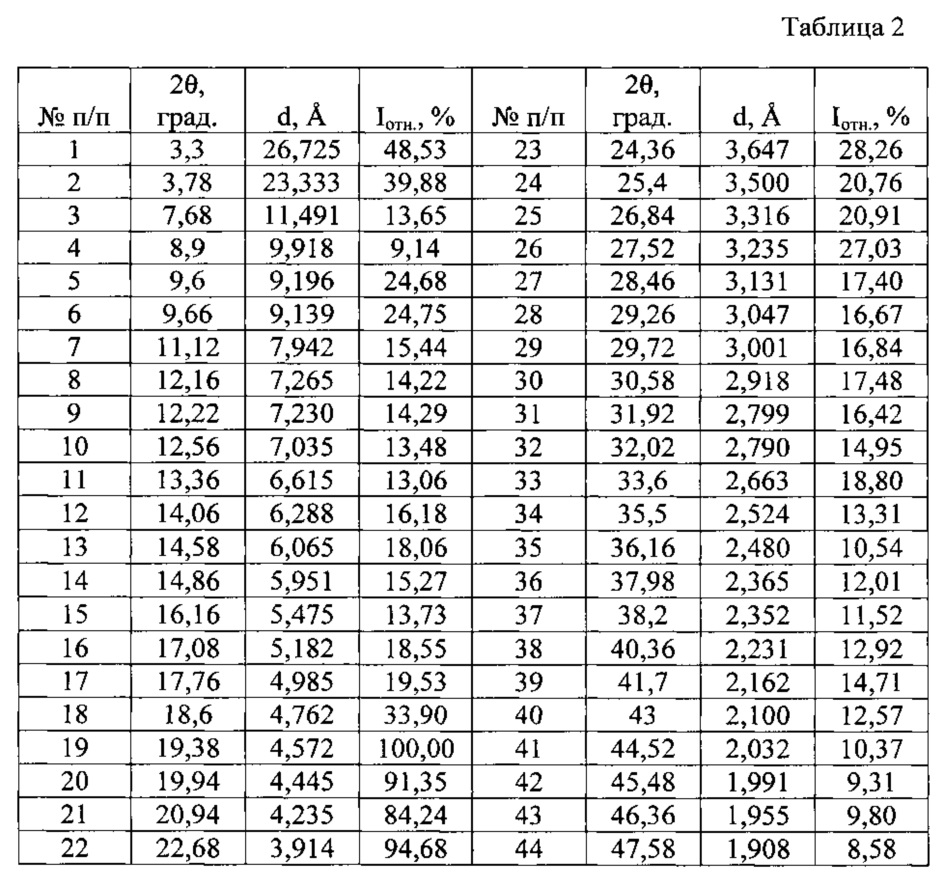
Таблица 2. Углы 2θ, межплоскостные расстояния (d, Å) и их интенсивности (Iотн., %) новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
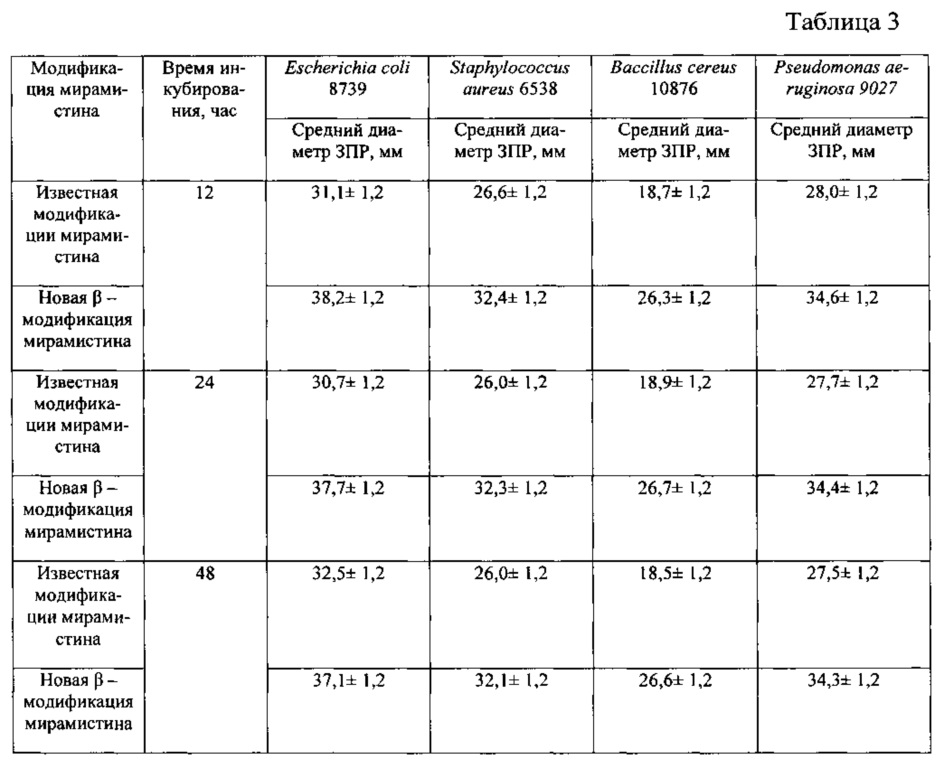
Таблица 3. Величины зон подавления роста тест микроорганизмов при использовании известной кристаллической модификации мирамистина и полученной из нее новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
Таблица 4. Величины зон подавления роста тест микроорганизмов при использовании фармацевтических композиций на основе известной кристаллической модификации мирамистина и полученной из нее новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
Рис. 1. ЯМР1Н - спектр известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества.
Рис. 2. ЯМР1Н - спектр новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
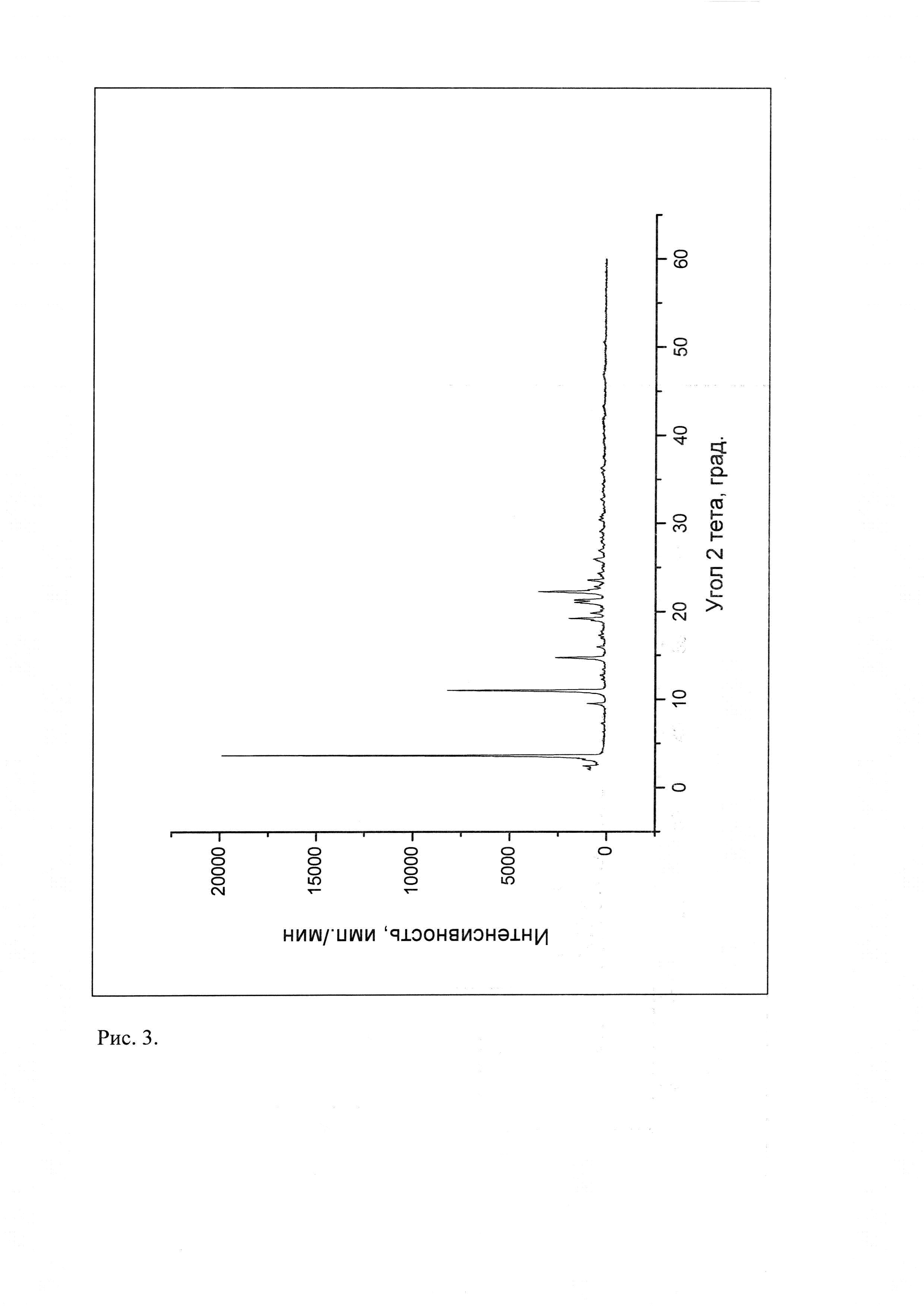
Рис. 3. Дифрактограмма известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества.
Рис. 4. Типичная дифрактограмма новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
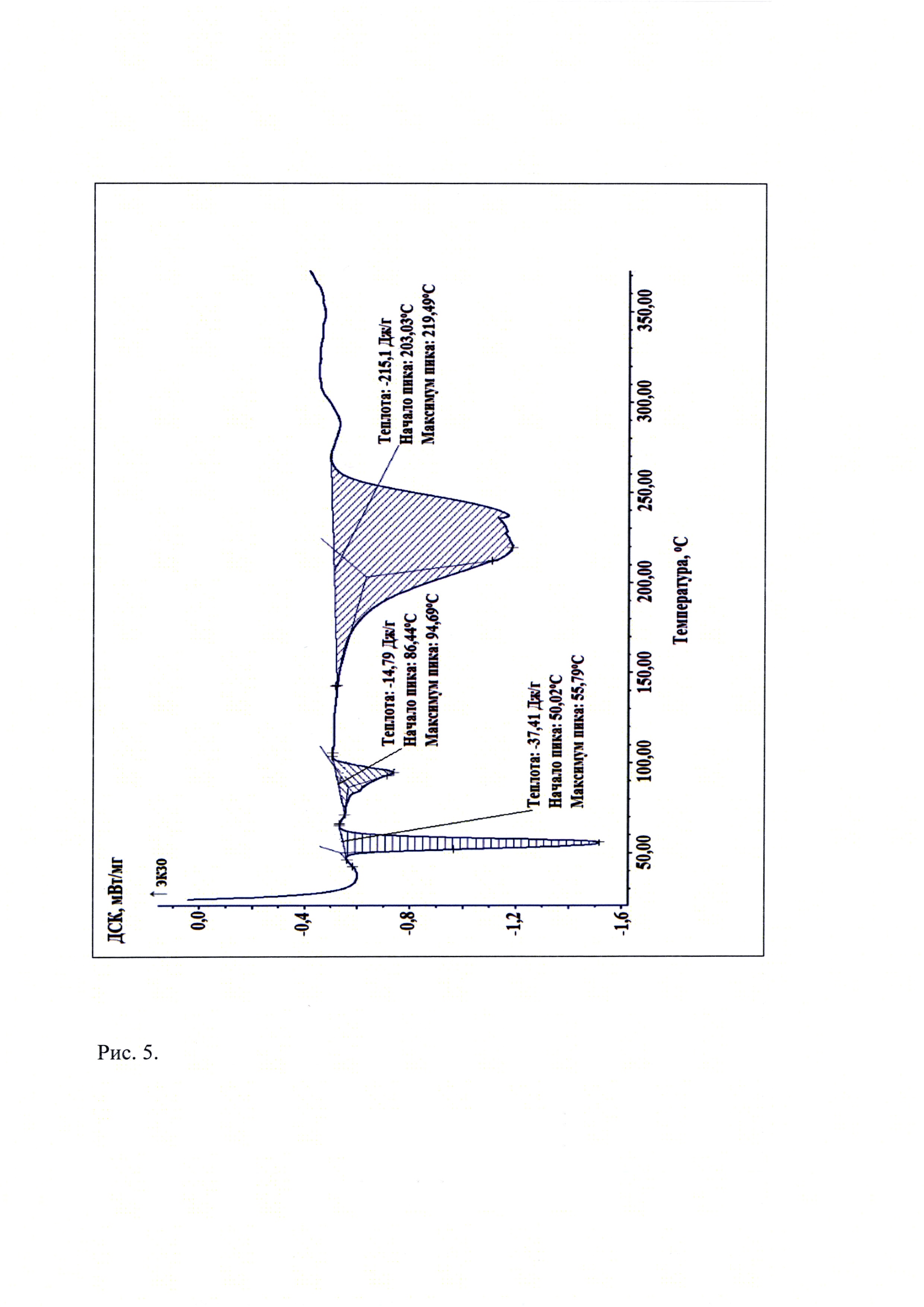
Рис. 5. Кривая дифференциальной сканирующей калориметрии известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества.
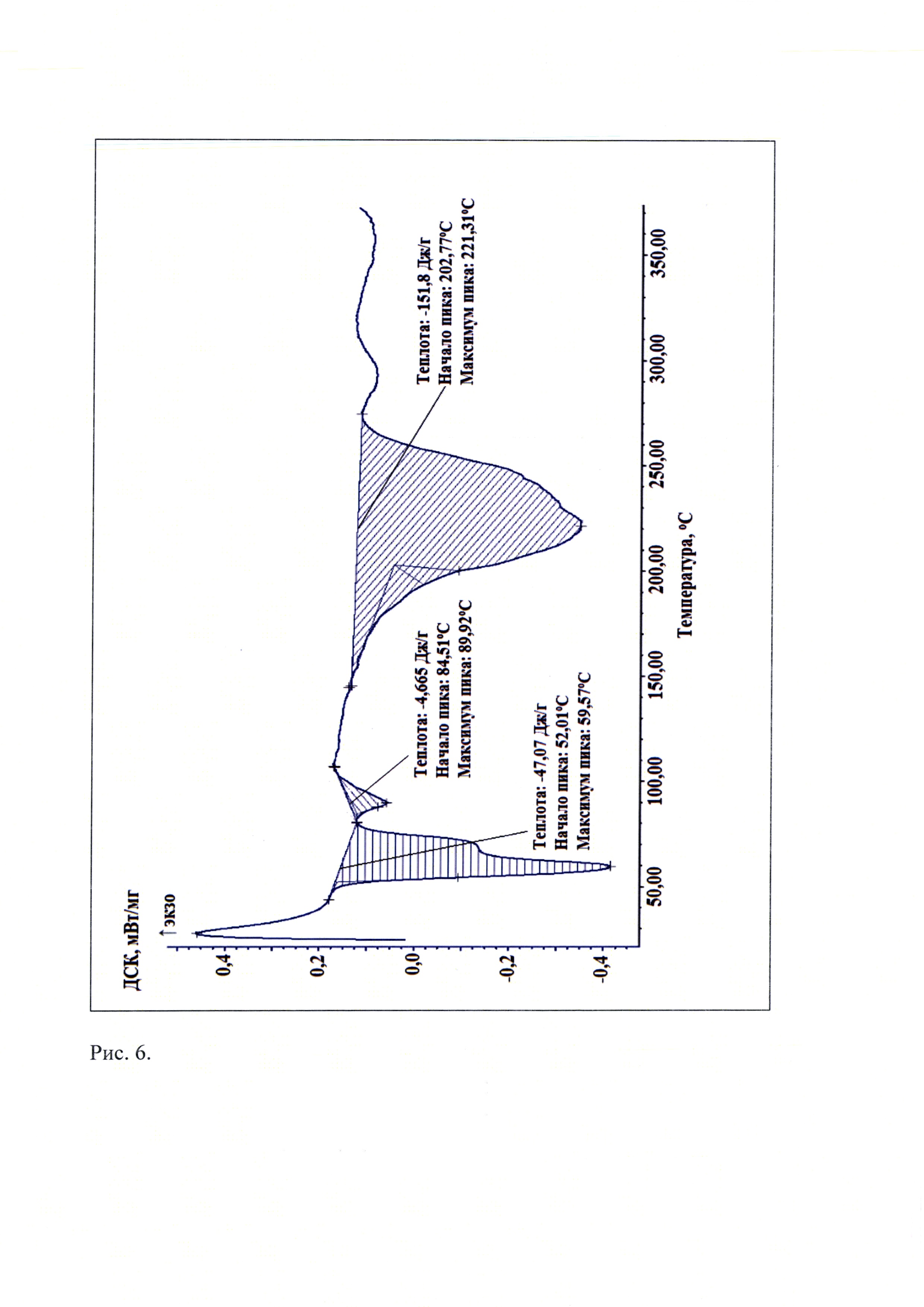
Рис. 6. Типичная кривая дифференциальной сканирующей калориметрии новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
Для идентификации полученного вещества был проведен комплекс физико-химических методов анализа.
Первоначально, методами ядерного магнитного резонанса (ЯМР1Н), высокоэффективной жидкостной хроматографии (ВЭЖХ) и определением воды методом К. Фишера была установлена идентичность химических формул известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества, и новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
Определение химических сдвигов исходного мирамистина и полученного из него вещества было проведено в его насыщенном растворе в дейтерированном диметилсульфоксиде (ДМСО-D6) на ЯМР-спектрометре высокого разрешения VXR-400 фирмы "VARIAN" (США). Полученные данные приведены на рис. 1 и 2 соответственно. Сравнение результатов, представленных на рис. 1 (известная модификация мирамистина), с данными, приведенными на рис. 2 (новая, не известная ранее, кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата), показывает, что ЯМР -1Н - спектры исходного и полученного из него вещества практически идентичны, т.е. полученное вещество является бензилдиметил[3-(миристоиламино)пропил]аммоний хлоридом моногидратом.
Хроматографическую подвижность известной модификации мирамистина и полученного из него вещества определяли методом ВЭЖХ на хроматографе Shimadzu LC - 20А с детектором SPD-M20A и с колонкой длиной 50 мм, сорбентом Grace Apollo С18 "Agilent" (США) с детектированием при длине волны 215,8 нм. В качестве подвижной фазы использовали ацетонитрил и буферный раствор с pH=2,8 (0,1 М NaClO4 + 7% МеОН), температура колонки была равна 30°C, а скорость потока - 1,5 мл/мин. Объем испытуемой пробы составил 3 мкл с концентрацией 2,0 мг/мл. Оказалось, что хроматограммы известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества, и новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата содержат по одному пику основного компонента с характерными временами удерживания 11,952 мин и 11,949 мин соответственно. Эти величины времен удерживания, в пределах ошибки определения, практически одинаковы. Чистота исследованных образцов, определенных методом ВЭЖХ, составили 99,10% (исходное вещество) и 98,57% (новая, не известная ранее, кристаллическая β-модификация).
Проведенные методом ВЭЖХ эксперименты, свидетельствуют о том, что при получении новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата из исходного вещества - известной кристаллической модификации мирамистина, разложения исходного вещества не происходит.
Определение количества воды в известной кристаллической модификации мирамистина и полученной из нее новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата проводили методом кулонометрического титрования по К. Фишеру в автоматическом титраторе C20D «Mettler Toledo» (Швейцария) в соответствии с требованиями ГФ XI. В качестве растворителя использовали метанол безводный («Fluka» категории №34741). Для оценки воспроизводимости опытов определение содержания воды проводили не менее трех раз.
Результаты определения количества воды методом К. Фишера в известной модификации мирамистина и полученного из нее вещества показали, что в мирамистине содержится (3,8±0,3) мас. % воды, а в новой, не известной ранее, кристаллической β-модификации - (4,1±0,3) мас. % воды. Полученные экспериментальные данные свидетельствуют о том, что исследованные образцы (исходный мирамистин и полученной из него кристаллической β-модификации) содержат по одной молекуле воды на молекулу бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида.
Таким образом, экспериментальные результаты ядерного магнитного резонанса (ЯМР-1Н), высокоэффективной жидкостной хроматографии (ВЭЖХ) и определение воды методом К. Фишера однозначно свидетельствуют о том, что полученное из известной модификации мирамистина вещество является бензилдиметил[3-(миристоиламино)пропил]аммоний хлоридом моногидратом.
Для подтверждения того, что полученное из известной модификации мирамистина вещество является новой, не известной ранее, кристаллической β-модификацией бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, были проведены рентгенофазовый анализ (РФА) и термоаналитические исследования.
Рентгенофазовый анализ (РФА) известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества, и полученного из нее вещества проводили на дифрактометре Rigaku D/MAX-2500 (Rigaku, Япония) на CuKα излучении (λ=1,54056 Å). Полученные данные РФА для мирамистина, который использовали в качестве исходного вещества, приведены в табл. 1 и на рис. 3. Результаты рентгенофазового анализа порошка, полученного из известной кристаллической модификации мирамистина, представлены в табл. 2 и на рис. 4. Сравнение полученных данных, представленных в табл. 2, табл. 1, а также на рис. 4 и рис. 3, свидетельствуют о том, что полученный порошок является новой, не известной ранее, кристаллической β-модификацией бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
Таким образом, экспериментальные результаты рентгенофазового анализа однозначно свидетельствуют о том, что полученное вещество является новой, не известной ранее, кристаллической β-модификацией бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата. Она характеризуется отличной от другой кристаллической модификации мирамистина совокупностью межплоскостных расстояний (d, Å) и соответствующих им интенсивностей (Iотн., %): 26,725 - 48,53%; 23,333 - 39,88%; 11,491 - 13,65%; 9,918 - 9,14%; 9,196 - 24,68%; 9,139 - 24,75%; 7,942 - 15,44%; 7,265 - 14,22%; 7,230 - 14,29%; 7,035 - 13,48%; 6,615 - 13,06%; 6,288 - 16,18%; 6,065 - 18,06%; 5,951 - 15,27%; 5,475 - 13,73%; 5,182 - 18,55%; 4,985 - 19,53%; 4,762 - 33,90%; 4,572 - 100,0%; 4,445 - 91,35%; 4,235 - 84,24%; 3,914 - 94,68%; 3,647 - 28,26%; 3,500 - 20,76%; 3,316 - 20,91%; 3,235 - 27,03%; 3,131 - 17,40%; 3,047 - 16,67%; 3,001 - 16,84%; 2,918 - 17,48%; 2,799 - 16,42%; 2,790 - 14,95%; 2,663 - 18,80%; 2,524 - 13,31%; 2,480 - 10,54%; 2,365 - 12,01%; 2,352 - 11,52%; 2,231 - 12,92%; 2,162 - 14,71%; 2,100 - 12,57%; 2,032 - 10,37%; 1,991 - 9,31%; 1,955 - 9,80%; 1,908 - 8,58%.
Термоаналитические исследования известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества и полученной из нее новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата проводили на термоанализаторе DSC 204 Fl Poenix (NETZSCH) в токе аргона при повышении температуры 10 град./мин. В качестве держателей образцов использовали алюминиевые кюветы. Навеска пробы составляла (1,4-4,7) мг. Полученные данные приведены на рис. 5 и рис. 6 соответственно. Видно, что на кривой дифференциальной сканирующей калориметрии известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества (рис. 5), присутствуют три эндотермических эффекта с максимумами при (55,8±0,5)°C; (94,7±0,5)°C; (219,5±0,5)°C, а на кривой ДСК новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата присутствуют также три эндотермических эффекта, но при других температурах, а именно при: (59,6±0,5)°C; (89,9±0,5)°C; (221,3±0,5)°C.
Таким образом, проведенные термоаналитические эксперименты показали, что новая, не известная ранее, кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата характеризуется отличной от другой модификации мирамистина совокупностью эндотермических эффектов на кривой ДСК при температурах: (59,6±0,5)°C; (89,9±0,5)°C; (221,3±0,5)°C.
Определение биологической активности известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества, и полученной из нее новой кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата осуществляли по изучению устойчивости микроорганизмов диско-диффузионным методом [Определение чувствительности к антибактериальным препаратам. Под ред. Онищенко Г.Г. «Клиническая микробиология, антимикробная химиотерапия», 2004 г., том 6, №4, с. 306-359]. В качестве тест-культур использовали бактерии коллекции АТСС (American Type Culture Collection) Escherichia coli 8739; Staphylococcus aureus 6538; Baccillus cereus 10876; Pseudomonas aeruginosa 9027. Эксперименты проводили в стерильных чашках Петри, содержащих по 20 мл агаризованной (ПД - агар) питательной среды (толщина слоя 4 мм), выдержанной в течение суток. Приготовление бактериальной суспензии исследуемого тест микроорганизма и посев ею среды проводили следующим образом. Одну или две полные микробиологические петли с культурой вносили в 5 мл стерильной дистиллированной воды, взбалтывали полученную суспензию в течение 30 секунд и определяли ее концентрацию по оптической плотности при λ=625 нм, сравнивали полученную величину с оптической плотностью приготовленного предварительно 0,5 стандарта МакФарланда (эквивалентна 1,5×108 КОЕ/мл). После этого 100 мкл суспензии культуры помещали на поверхность среды в чашки Петри, тщательно растирали стерильным шпателем и через 15 мин в них вносили известную кристаллической модификации мирамистина или полученную из нее новую кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата в виде дисков диаметром (6,00±0,03) мм, высотой (3,09±0,05) мм и массой (98±3) мг, помещали в термостат и инкубировали при 30°C. Для получения надежных результатов в параллельных сериях опытов использовали не менее 5ти дисков. Контроль результатов роста тест-культур и измерение зон подавления их роста проводили через 12, 24 и 48 часов инкубации. Диаметр зон подавления роста (ЗПР) измеряли линейкой в 3х направлениях для каждого диска, с точностью до ±0,5 мм. Полученные в микробиологических экспериментах результаты приведены в табл. 3. Видно, что зоны подавления роста тест-культур новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата больше при всех временах инкубации, чем при использовании дисков из известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества и, следовательно, полученная новая β модификация мирамистина более активна к процессам подавления роста микроорганизмов.
Приведенные экспериментальные данные рентгенофазового анализа, термоаналитических исследований и определения биологической активности однозначно свидетельствуют о том, что полученная новая, не известная ранее, кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата характеризуется отличной от другой кристаллической модификации мирамистина, совокупностью межплоскостных расстояний и соответствующих им интенсивностей, совокупностью эндотермических эффектов на кривой ДСК при определенных температурах и более активна к процессам подавления роста микроорганизмов по сравнению с известной кристаллической модификацией мирамистина.
Способ получения новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата заключается в том, что водный раствор мирамистина с концентрацией (0,5-10,0) мас. %, при (25-100)°C замораживают при скорости охлаждения не ниже 60 град./мин и подвергают сублимационной сушке.
Отличие способа получения заявляемой новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата от способа получения известной кристаллической формы мирамистина состоит в том, что водный раствор мирамистина с концентрацией (0,5-10,0) мас. %, при (25-100)°C, замораживают при скорости охлаждения не ниже 60 град./мин и подвергают сублимационной сушке.
Предложенный способ получения, заключающийся в том, что водный раствор мирамистина с концентрацией (0,5-10,0) мас. % при (25-100)°C замораживают при скорости охлаждения не ниже 60 град./мин и подвергают сублимационной сушке, позволяет получить новую, не известную ранее, кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
Уменьшение концентрации раствора мирамистина в воде меньше 0,5 мас. % (комнатной температуры) не целесообразно, поскольку не позволяет получать достаточное количество целевого продукта, что удорожает процесс получения новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата.
Увеличение концентрации раствора мирамистина в воде больше 10,0 мас. % приводит к тому, что при замораживании раствора мирамистина система стеклуется - аморфизуется (образуется твердый раствор). Это приводит к тому, что при дальнейшей сублимационной сушке замороженный аморфизованный раствор плавится, из него кристаллизуются уже известная модификация. Получить новую, не известную ранее, кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата в чистом виде не удается.
Уменьшение температуры раствора мирамистина в воде ниже 25°C (комнатной температуры) не целесообразно, поскольку требует дополнительных затрат энергии на охлаждение системы.
Увеличение температуры раствора мирамистина в водном растворе выше 100°C также не целесообразно из-за необходимости применения специального оборудования.
Уменьшение скорости замораживания ниже 60 град./мин приводит к тому, что скорость криокристаллизации раствора мирамистина уменьшается и приближается к равновесному процессу. Это приводит к получению уже известной модификации. Получить новую, не известную ранее, кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата в чистом виде не удается.
Сублимационная сушка замороженного раствора мирамистина необходима для получения новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата. Предпочтительным режимом сублимационной сушки является процесс, который проводят при температурах: на конденсаторе -43°C…-75°C; на продукте -196…+50°C и остаточном давлении в камере (9-3)×10-2 Торр в течение 22-26 ч.
Уменьшение времени сублимационной сушки меньше 22 ч приводит к получению невысохшего продукта: «порошок мирамистина - его замороженный раствор». Система при комнатной температуре плавится, порошок частично растворяется, перекристаллизовывается, образуя известную модификацию мирамистина. Новую, не известную ранее, кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата в чистом виде получить не удается.
Увеличение времени сублимационной сушки нецелесообразно, так как не приводит к увеличению выхода целевого продукта - новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата и лишь удорожает производство.
Возможность осуществления предлагаемого изобретения иллюстрируется следующими примерами, но не ограничивается ими.
Пример 1. 300 мл 10,0 мас. % раствора мирамистина в воде при 100°C, приготовленного из известной кристаллической модификации мирамистина и воды, очищенной по ФС 42-2619-97, замораживают со скоростью 60 град./мин вливанием сразу всего объема раствора в предварительно наполненный жидким азотом (Ткип=-196°C), но не охлажденный предварительно, поддон из нержавеющей стали. Замороженный продукт на поддоне переносят в сублимационную камеру и подвергают сублимационной сушке при температурах: на конденсаторе -71°C…-75°C; на продукте -196°C…+30°C и остаточном давлении в камере (9-5)⋅10-2 Торр в течение 22 ч. Выход продукта сублимационной сушки - порошка практически белого цвета составил 29,25 г (97,5 мас. %). По данным РФА полученное вещество характеризуется типичной дифрактограммой, представленной на рис. 4, и набором межплоскостных расстояний и их интенсивностями, совпадающих с соответствующими значениями для новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, представленными в табл. 2. По данным термоаналитических исследований полученное вещество характеризуется типичной кривой дифференциальной сканирующей калориметрии, представленной на рис. 6 и совпадающей, в пределах ошибки определения, с соответствующими значениями для новой, не известной ранее, кристаллической β-модификацией бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата. Кривая ДСК характеризуется совокупностью трех эндотермических эффектов при температурах: (59,6±0,5)°C; (89,9±0,5)°C; (221,3±0,5)°C. По данным ВЭЖХ чистота полученной новой, не известной ранее, кристаллической β-модификации составляет 98,71%. По данным определения воды методом К. Фишера в полученном веществе содержится (3,9±0,3) мас. % воды, что соответствует в пределах ошибки определения одной молекуле воды на молекулу бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида.
Пример 2. 300 мл 0,50 мас. % раствора мирамистина в воде, приготовленного при 25°C из известной кристаллической модификации мирамистина и воды, очищенной по ФС 42-2619-97, замораживают со скоростью (2-3)×102 град./мин вливанием раствора небольшими порциями в предварительно охлажденный и наполненный жидким азотом (Ткип=-196°C) поддон из нержавеющей стали. Замороженный продукт на поддоне переносят в сублимационную камеру и подвергают сублимационной сушке при температурах: на конденсаторе -52°C…-56°C; на продукте -196°C…+30°C и остаточном давлении в камере (7-4)⋅10-2 Торр в течение 26 ч. Выход продукта сублимационной сушки - порошка почти белого цвета составил 1,41 г (94,0 мас. %). По данным РФА полученное вещество характеризуется типичной дифрактограммой, представленной на рис. 4, и набором межплоскостных расстояний и их интенсивностями, совпадающими с соответствующими значениями для новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, представленными в табл. 2. По данным термоаналитических исследований полученное вещество характеризуется типичной кривой дифференциальной сканирующей калориметрии, представленной на рис. 6 и совпадающей, в пределах ошибки определения, с соответствующими значениями для новой, не известной ранее, кристаллической β-модификацией бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата. Кривая ДСК характеризуется совокупностью трех эндотермических эффектов при температурах: (59,2±0,5)°C; (90,1±0,5)°C; (221,0±0,5)°C. По данным ВЭЖХ чистота полученной новой, не известной ранее, кристаллической β-модификации составляет 98,57%. По данным определения воды методом К. Фишера в полученном веществе содержится (4,3±0,3) мас. % воды, что соответствует, в пределах ошибки определения, одной молекуле воды на молекулу бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида.
Пример 3. 150 мл 2,0 мас. % раствора мирамистина в воде, приготовленного при 25°C из известной кристаллической модификации мирамистина и воды, очищенной по ФС 42-2619-97, замораживают со скоростью примерно 103 град./мин распылением раствора пневматической форсункой при избыточном давлении 0,7 кг/см2 в реактор, наполненный жидким азотом (Ткип=-196°C). Замороженный раствор в виде микрогранул переносят в поддон из нержавеющей стали и подвергают сублимационной сушке при температурах: на конденсаторе -43°C…-48°C; на продукте -196°C…+50°C, и остаточном давлении в камере (6-3)⋅10-2 Торр в течение 24 ч. Выход продукта сублимационной сушки - порошка практически белого цвета составил 2,76 г (92,0 мас. %). По данным РФА полученное вещество характеризуется типичной дифрактограммой, представленной на рис. 4 и набором межплоскостных расстояний и их интенсивностями, совпадающими с соответствующими значениями для новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата, представленными в табл. 2. По данным термоаналитических исследований полученное вещество характеризуется типичной кривой дифференциальной сканирующей калориметрии, представленной на рис. 6 и совпадающей, в пределах ошибки определения, с соответствующими значениями для новой, не известной ранее, кристаллической β-модификацией бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата. Кривая ДСК характеризуется совокупностью трех эндотермических эффектов при температурах: (59,9±0,5)°C; (89,7±0,5)°C; (221,6±0,5)°C. По данным ВЭЖХ чистота полученной новой, не известной ранее, кристаллической β-модификации составляет 98,42%. По данным определения воды методом К. Фишера в полученном веществе содержится (4,1±0,3) мас. % воды, что соответствует, в пределах ошибки определения, одной молекуле воды на молекулу бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида.
Пример 4. Фармацевтическая композиция. Для приготовления 100,00 г композиции, включающей в качестве действующего вещества кристаллическую β-модификациию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата и вспомогательное вещество в соотношении (мас. %):
0,0104 (±0,0002) г порошка новой, не известной ранее, кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата растворяют при перемешивании в 99,9896 (±0,0002) г воды очищенной по ФС 42-0324-09. Полученный раствор подвергают биологическим методам анализа.
Аналогичным способом и идентичной по составу была приготовлена композиция на основе известной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества.
Определение биологической активности фармацевтических композиций, включающих известную кристаллическую модификацию мирамистина, которую использовали в качестве исходного вещества или полученную из нее новую кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата осуществляли по изучению устойчивости микроорганизмов диско-диффузионным методом [Определение чувствительности к антибактериальным препаратам. Под ред. Онищенко Г.Г. «Клиническая микробиология, антимикробная химиотерапия», 2004 г., том 6, №4, с. 306-359]. В качестве тест-культур использовали бактерии коллекции AТСС (American Type Culture Collection) Escherichia coli 8739; Staphylococcus aureus 6538; Baccillus cereus 10876; Pseudomonas aeruginosa 9027. Эксперименты проводили в стерильных чашках Петри, содержащих по 20 мл агаризованной (ПД - агар) питательной среды (толщина слоя 4 мм), выдержанной в течение суток. Приготовление бактериальной суспензии исследуемого тест микроорганизма и посев ею среды проводили следующим образом. Одну или две полные микробиологические петли с культурой вносили в 5 мл стерильной дистиллированной воды, взбалтывали полученную суспензию в течение 30 секунд и определяли ее концентрацию, по оптической плотности, сравнивая полученную величину с оптической плотностью приготовленного предварительно 0,5 стандарта МакФарланда (эквивалентна 1,5×108 КОЕ/мл). После этого 100 мкл суспензии культуры помещали на поверхность среды в чашки Петри, тщательно растирали стерильным шпателем, через 15 мин в них вносили известную кристаллическую модификацию мирамистина, которую использовали в качестве исходного вещества или полученную из нее новую кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата в виде дисков диаметром (6,0±0,1) мм из стерильной фильтровальной бумаги, пропитанных соответствующими растворами, помещали в термостат и инкубировали при 30°C. Для получения надежных результатов в параллельных сериях опытов использовали не менее 5ти дисков. Контроль результатов роста культур и измерение зон подавления их роста проводили через 24 и 42 часов инкубации. Диаметр зон подавления роста измеряли линейкой в 3 направлениях для каждого диска с точностью до 0,5 мм. Полученные в микробиологических экспериментах результаты приведены в табл. 4. Видно, что зоны подавления роста культур дисками, пропитанными фармацевтической композицией, содержащей новую кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорида моногидрата больше, чем при использовании дисков, пропитанных фармацевтической композицией, содержащей известную кристаллическую модификацию мирамистина, которую использовали в качестве исходного вещества и, следовательно, полученная новая β-модификация более активна к процессам подавления роста микроорганизмов.
Таким образом, обнаружена новая, не известная ранее, кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата, предложены способ ее получения и применение ее для приготовления фармацевтической композиции в качестве антисептического средства, оказывающего бактерицидное и противовирусное действие.
Полученная новая, не известная ранее, кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата характеризуется отличным от известной кристаллической модификации мирамистина набором межплоскостных расстояний (d, Å) и соответствующих им интенсивностей (Iотн., %) 26,725 - 48,53%; 23,333 - 39,88%; 11,491 - 13,65%; 9,918 - 9,14%; 9,196 - 24,68%; 9,139 - 24,75%; 7,942 - 15,44%; 7,265 - 14,22%; 7,230 - 14,29%; 7,035 - 13,48%; 6,615 - 13,06%; 6,288 - 16,18%; 6,065 - 18,06%; 5,951 - 15,27%; 5,475 - 13,73%; 5,182 - 18,55%; 4,985 - 19,53%; 4,762 - 33,90%; 4,572 - 100,0%; 4,445 - 91,35%; 4,235 - 84,24%; 3,914 - 94,68%; 3,647 - 28,26%; 3,500 - 20,76%; 3,316 - 20,91%; 3,235 - 27,03%; 3,131 - 17,40%; 3,047 - 16,67%; 3,001 - 16,84%; 2,918 - 17,48%; 2,799 - 16,42%; 2,790 - 14,95%; 2,663 - 18,80%; 2,524 - 13,31%; 2,480 - 10,54%; 2,365 - 12,01%; 2,352 - 11,52%; 2,231 - 12,92%; 2,162 - 14,71%; 2,100 - 12,57%; 2,032 - 10,37%; 1,991 - 9,31%; 1,955 - 9,80%; 1,908 - 8,58% и совокупностью эндотермических эффектов на кривой ДСК при температурах: (59,6±0,5)°C; (89,9±0,5)°C; (221,3±0,5)°C.
Кроме того, новая, не известная ранее, кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата отличается повышенной биологической активностью как в виде спрессованного порошка, так и в составе фармацевтической композиции по сравнению с действием исходной кристаллической модификации мирамистина, которую использовали в качестве исходного вещества.
Из вышеизложенного можно сделать вывод о том, что заявляемая новая, не известная ранее, кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата, способ ее получения и применение ее для приготовления фармацевтической композиции в качестве антисептического средства, оказывающего бактерицидное и противовирусное действие, являются новыми и удовлетворяют критериям «изобретательский уровень» и «промышленная применимость».

Реферат
Изобретение относится к кристаллической безводной модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата (мирамистин - торговое название). Кристаллическая β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата характеризуется следующим набором межплоскостных расстояний (d, Å) и соответствующих им интенсивностей (I, %): 26,725-48,53%; 23,333-39,88%; 11,491-13,65%; 9,918-9,14%; 9,196-24,68%; 9,139-24,75%; 7,942-15,44%; 7,265-14,22%; 7,230-14,29%; 7,035-13,48%; 6,615-13,06%; 6,288-16,18%; 6,065-18,06%; 5,951-15,27%; 5,475-13,73%; 5,182-18,55%; 4,985-19,53%; 4,762-33,90%; 4,572-100,0%; 4,445-91,35%; 4,235-84,24%; 3,914-94,68%; 3,647-28,26%; 3,500-20,76%; 3,316-20,91%; 3,235-27,03%; 3,131-17,40%; 3,047-16,67%; 3,001-16,84%; 2,918-17,48%; 2,799-16,42%; 2,790-14,95%; 2,663-18,80%; 2,524-13,31%; 2,480-10,54%; 2,365-12,01%; 2,352-11,52%; 2,231-12,92%; 2,162-14,71%; 2,100-12,57%; 2,032-10,37%; 1,991-9,31%; 1,955-9,80%; 1,908-8,58% и совокупностью эндотермических эффектов на кривой ДСК при температурах: (59,6±0,5)°C; (89,9±0,5)°C; (221,3±0,5)°C. Способ получения кристаллической β-модификации бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата осуществляют путем замораживания водного раствора бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата с концентрацией 0,5-10 мас. %, при 25-100°C, при скорости охлаждения не ниже 60 град./мин и затем подвергают сублимационной сушке. Сублимационную сушку замороженного раствора проводят при температурах: на конденсаторе (-43…-75)°C; на продукте (-196…+50)°C и остаточном давлении в камере (9-3)×10Торр в течение 22-26 ч. Кристаллическую β-модификацию бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата применяют для приготовления фармацевтической композиции в качестве антисептического средства, оказывающего бактерицидное и противовирусное действие. Технический результат - β-модификация бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрата, более активная к процессам подавления роста микроорганизмов. 3 н. и 1 з.п. ф-лы, 6 ил., 4 табл., 4 пр.
Формула
Документы, цитированные в отчёте о поиске
Лекарственный препарат

Комментарии