Панель для определения предрасположенности к развитию нарушений функционирования тиреоидной системы и ее использование - RU2784603C1
Код документа: RU2784603C1
Описание
Область техники, к которой относится изобретение
Группа изобретений относится к области медицины, а именно к эндокринологии и генетике, и может быть использована для определения вероятности развития функциональных нарушений тиреоидной системы, этиологически вызванных различными полиморфными вариантами в генах, отвечающих за активность ферментов, которые участвуют в биосинтезе, внутриклеточном действии и утилизации тиреоидных гормонов.
С физиологической точки зрения любую патологию щитовидной железы можно классифицировать на два состояния: гипо- и гипертиреоз. Несмотря на разнообразие этиологии и патогенеза развития этих физиологических состояний, используемые в настоящее время принципы их коррекции практически не зависят от механизмов развития этих патологий и сводятся либо к заместительной гормональной терапии (при гипотиреозе), либо к подавлению активности щитовидной железы (ЩЖ) при гипертиреозе (медикаментозная или лучевая терапия, или хирургическое лечение). Но, в настоящее время при масштабном развитии молекулярно-генетических технологий знание характера и роли генетических причин заболеваний щитовидной железы может коренным образом изменить подходы к их лечению.
За последние десятилетия расширилось представление о механизмах функционирования дейодиназ йодтиронинов в норме и при патологических процессах. Основной ролью дейодиназ D1 и D2 является регуляция метаболизма тиреоидных гормонов, в частности они катализируют удаление остатка йода с внешнего или внутреннего кольца молекулы прогормона тироксина (Т4), продуцируя либо активную форму 3,5,3'-1-трийодтиронина (трийодтиронин, Т3), либо неактивную форму (реверсивный Т3, rТ3). По мере углубления нашего понимания метаболизма и действия этих ферментов расширяются возможности применения этих знаний в клинической практике. Это позволит подбирать терапию для лечения щитовидной железы при ее патологии и сопутствующих заболеваниях на основе генетических данных, по всем принципам превентивной и предиктивной медицины.
Уровень техники
В настоящее время оценку функционального состояния щитовидной железы проводят по результатам лабораторного определения уровня тиреотропного гормона (ТТГ) и тиреоидных гормонов (Т4 и Т3), где уровень ТТГ является наиболее чувствительным маркером функции ЩЖ и в комплексе с другими клинико-лабораторными показателями определяет дальнейшую тактику ведения пациента. По результатам гормонального обследования делается вывод о наличии гипотиреоза или гипертиреоза и назначении лечения пациенту. Однако в клинической практике можно столкнуться с ситуацией, когда результаты лабораторных исследований не соответствуют клинической картине и/или нормальному функционированию гипофизарно-тиреоидной оси по принципу отрицательной обратной связи. В ряде случаев патология щитовидной железы и нарушения тиреоидного статуса организма обусловлены генетическими нарушениями в гипоталамо-гипофизарно-тиреоидной системе, начиная с факторов, контролирующих синтез и секрецию гипоталамического тиреотропин-рилизинг-гормона (ТРГ), и завершая факторами, регулирующими периферические эффекты тиреоидных гормонов.
Известно выявление предрасположенностей к заболеваниям, связанным с нарушениями в синтезе гормонов щитовидной железы, которые обусловлены изменениями в регуляции и экспрессии дейодиназ. В работе [R. M. Paragliola, A. Corsello, P. Concolino, F. Frontiersin Bioscience, Landmark, 25, 201-228, Jan 1, 2020] описано влияние патогенных вариантов, детектируемых в генах SECISBP2, DIO1 и DIO2 на механизмы нарушения метаболизма тиреоидных гормонов, что приводит к развитию гипо- или гипертиреоидного состояния.
В статье [Lee KW, Shin Y, Lee S and Lee S (2022) Inherited Disorders of Thyroid Hormone Metabolism Defect Caused by the Dysregulation of Selenoprotein Expression. Front. Endocrinol. 12:803024. doi: 10.3389/fendo.2021.803024] также было описано влияние генетических дефектов, обнаруженных в генах дейодиназ SECISBP2, DIO1 и DIO2, на синтез гормонов щитовидной железы, и были сделаны выводы, что исследование генетических дефектов в участках генов, отвечающих за синтез гормонов щитовидной железы имеют первостепенное диагностическое значение.
Однако, в данных публикациях, прежде всего, описан фундаментальный подход к действию дейодиназ, пониманию молекулярных механизмов действия селена и селенопротеинов и всего процесса метаболизма гормонов щитовидной железы.
Технической проблемой является сложность в выборе сочетания генов/полиморфизмов/генотипов, подходящего для определения предрасположенности к развитию нарушений функционирования тиреоидной системы, о чем свидетельствует практическое отсутствие на рынке диагностических панелей полиморфизмов (SNP), подходящих для диагностики нарушений тиреоидной системы.
Раскрытие сущности изобретения
Технический результат настоящего изобретения заключается в создании панели полиморфизмов и ее использовании для определения предрасположенности к развитию нарушений функционирования тиреоидной системы на основе уникального сочетания полиморфизмов, что позволяет одномоментно выявлять наиболее часто встречающиеся полиморфизмы, дает возможность провести более полный диагностический охват и не пропустить возможные изменения в генотипе.
Достижение указанного технического результата обеспечивается предложенной панелью для определения предрасположенности к развитию нарушений функционирования тиреоидной системы на основе использования уникального сочетания генотипов полиморфизмов генов дейодиназы йодтиронина 1 (DIO1), дейодиназы йодтиронина 2 (DIO2), тиреоидной пероксидазы (TPO), рецептора к тиреотропному гормону (TSHR) и тиреоглобулина (TG).
Предложенная панель включает средства для обнаружения в образце от пациента следующих полиморфизмов:
1) rs2235544 гена дейодиназы йодтиронина 1 (DIO1) генотипа CA или АА;
2) rs11206244 гена DIO1 генотипа CT или ТТ;
3) rs2294512 гена DIO1 генотипа СА или АА;
4) rs4926616 гена DIO1 генотипа TC или СС;
5) rs225014 гена дейодиназы йодтиронина 2 (DIO2) генотипа TC или СС;
6) rs2071403 гена тиреоидной пероксидазы (TPO) генотипа GG;
7) rs732609 гена TPO гомозиготного генотипа CC;
8) rs1126797 гена TPO гомозиготного генотипа TT;
9) rs179247 гена рецептора к тиреотропному гормону (TSHR) генотипа AG или АА;
10) rs2076740 гена тиреоглобулина (TG) генотипа СС в сочетании с аллелью риска rs853326 G>A гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
11) rs853326 гена TG генотипа AA в сочетании с аллелью риска rs2076740 C>T гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
12) rs180223 гена TG генотипа GT или ТТ и
13) rs2069550 гена TG генотипа ТТ.
Предложенная панель может быть использована для определения предрасположенности к развитию такого нарушения щитовидной железы как гипертиреоз или гипотиреоз.
Достижение указанного технического результата обеспечивается также применением панели полиморфизмов для определения предрасположенности к развитию нарушений функционирования тиреоидной системы на основе использования уникального сочетания генотипов полиморфизмов генов дейодиназы йодтиронина 1 (DIO1), дейодиназы йодтиронина 2 (DIO2), тиреоидной пероксидазы (TPO), рецептора к тиреотропному гормону (TSHR) и тиреоглобулина (TG).
Предложенная для применения панель включает средства для обнаружения в образце от пациента следующих полиморфизмов:
1) rs2235544 гена дейодиназы йодтиронина 1 (DIO1) генотипа CA или АА;
2) rs11206244 гена DIO1 генотипа CT или ТТ;
3) rs2294512 гена DIO1 генотипа СА или АА;
4) rs4926616 гена DIO1 генотипа TC или СС;
5) rs225014 гена дейодиназы йодтиронина 2 (DIO2) генотипа TC или СС;
6) rs2071403 гена тиреоидной пероксидазы (TPO) генотипа GG;
7) rs732609 гена TPO гомозиготного генотипа CC;
8) rs1126797 гена TPO гомозиготного генотипа TT;
9) rs179247 гена рецептора к тиреотропному гормону (TSHR) генотипа AG или АА;
10) rs2076740 гена тиреоглобулина (TG) генотипа СС в сочетании с аллелью риска rs853326 G>A гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
11) rs853326 гена TG генотипа AA в сочетании с аллелью риска rs2076740 C>T гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
12) rs180223 гена TG генотипа GT или ТТ и
13) rs2069550 гена TG генотипа ТТ.
Достижение указанного технического результата обеспечивается также предложенным способом определения предрасположенности к развитию нарушений функционирования тиреоидной системы на основе использования уникального сочетания генотипов полиморфизмов генов дейодиназы йодтиронина 1 (DIO1), дейодиназы йодтиронина 2 (DIO2), тиреоидной пероксидазы (TPO), рецептора к тиреотропному гормону (TSHR) и тиреоглобулина (TG).
Предложенный способ характеризуется использованием средств для обнаружения в образце от пациента полиморфизмов генов, ассоциированных с нарушениями функционирования тиреоидной системы, и выявлением по результатам обнаружения полиморфизмов возможной предрасположенности пациента к развитию нарушений функционирования тиреоидной системы.
При этом предложенный способ предусматривает использование указанной панели полиморфизмов, а именно способ включает выявление в образце от пациента следующих полиморфизмов:
1) rs2235544 гена дейодиназы йодтиронина 1 (DIO1) генотипа CA или АА;
2) rs11206244 гена DIO1 генотипа CT или ТТ;
3) rs2294512 гена DIO1 генотипа СА или АА;
4) rs4926616 гена DIO1 генотипа TC или СС;
5) rs225014 гена дейодиназы йодтиронина 2 (DIO2) генотипа TC или СС;
6) rs2071403 гена тиреоидной пероксидазы (TPO) генотипа GG;
7) rs732609 гена TPO гомозиготного генотипа CC;
8) rs1126797 гена TPO гомозиготного генотипа TT;
9) rs179247 гена рецептора к тиреотропному гормону (TSHR) генотипа AG или АА;
10) rs2076740 гена тиреоглобулина (TG) генотипа СС в сочетании с аллелью риска rs853326 G>A гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
11) rs853326 гена TG генотипа AA в сочетании с аллелью риска rs2076740 C>T гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
12) rs180223 гена TG генотипа GT или ТТ и
13) rs2069550 гена TG генотипа ТТ,
где наличие у пациента хотя бы одного из указанных полиморфизмов свидетельствует о возможной предрасположенности к развитию нарушений функционирования тиреоидной системы.
Достижение указанного технического результата обеспечивается также применением панели в указанном способе определения предрасположенности к развитию нарушений функционирования тиреоидной системы, где применение характеризуется выполнением указанных стадий способа, а именно использованием средств для обнаружения в образце от пациента полиморфизмов генов, ассоциированных с нарушениями функционирования тиреоидной системы, и выявлением по результатам обнаружения полиморфизмов возможной предрасположенности пациента к развитию нарушений функционирования тиреоидной системы, где способ включает выявление в образце от пациента следующих полиморфизмов:
1) rs2235544 гена дейодиназы йодтиронина 1 (DIO1) генотипа CA или АА;
2) rs11206244 гена DIO1 генотипа CT или ТТ;
3) rs2294512 гена DIO1 генотипа СА или АА;
4) rs4926616 гена DIO1 генотипа TC или СС;
5) rs225014 гена дейодиназы йодтиронина 2 (DIO2) генотипа TC или СС;
6) rs2071403 гена тиреоидной пероксидазы (TPO) генотипа GG;
7) rs732609 гена TPO гомозиготного генотипа CC;
8) rs1126797 гена TPO гомозиготного генотипа TT;
9) rs179247 гена рецептора к тиреотропному гормону (TSHR) генотипа AG или АА;
10) rs2076740 гена тиреоглобулина (TG) генотипа СС в сочетании с аллелью риска rs853326 G>A гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
11) rs853326 гена TG генотипа AA в сочетании с аллелью риска rs2076740 C>T гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
12) rs180223 гена TG генотипа GT или ТТ и
13) rs2069550 гена TG генотипа ТТ,
где наличие у пациента хотя бы одного из указанных полиморфизмов свидетельствует о возможной предрасположенности к развитию нарушений функционирования тиреоидной системы.
Предложенное изобретение позволяет сделать предположение о физиологическом/патологическом состоянии щитовидной железы и возможном развитии дисфункции щитовидной железы, выражающейся в гипо- или гипертиреозе.
Для поиска подходящего для создания панели сочетания полиморфизмов, позволяющих составить однозначное предположение о состоянии щитовидной железы (риска развития гипо/гипертиреоза) было проведено исследование с учетом следующих факторов, указанных в таблице 1.

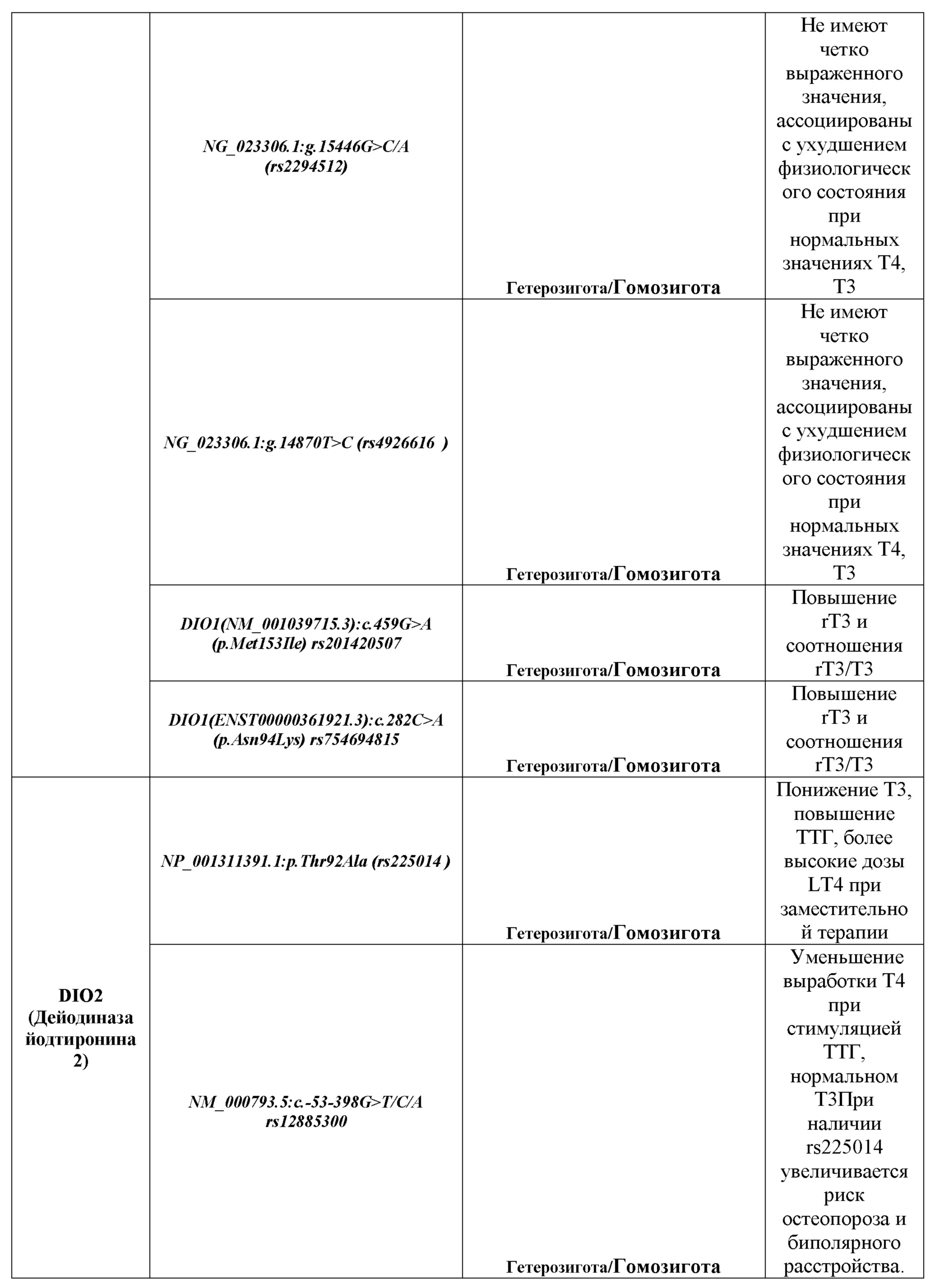
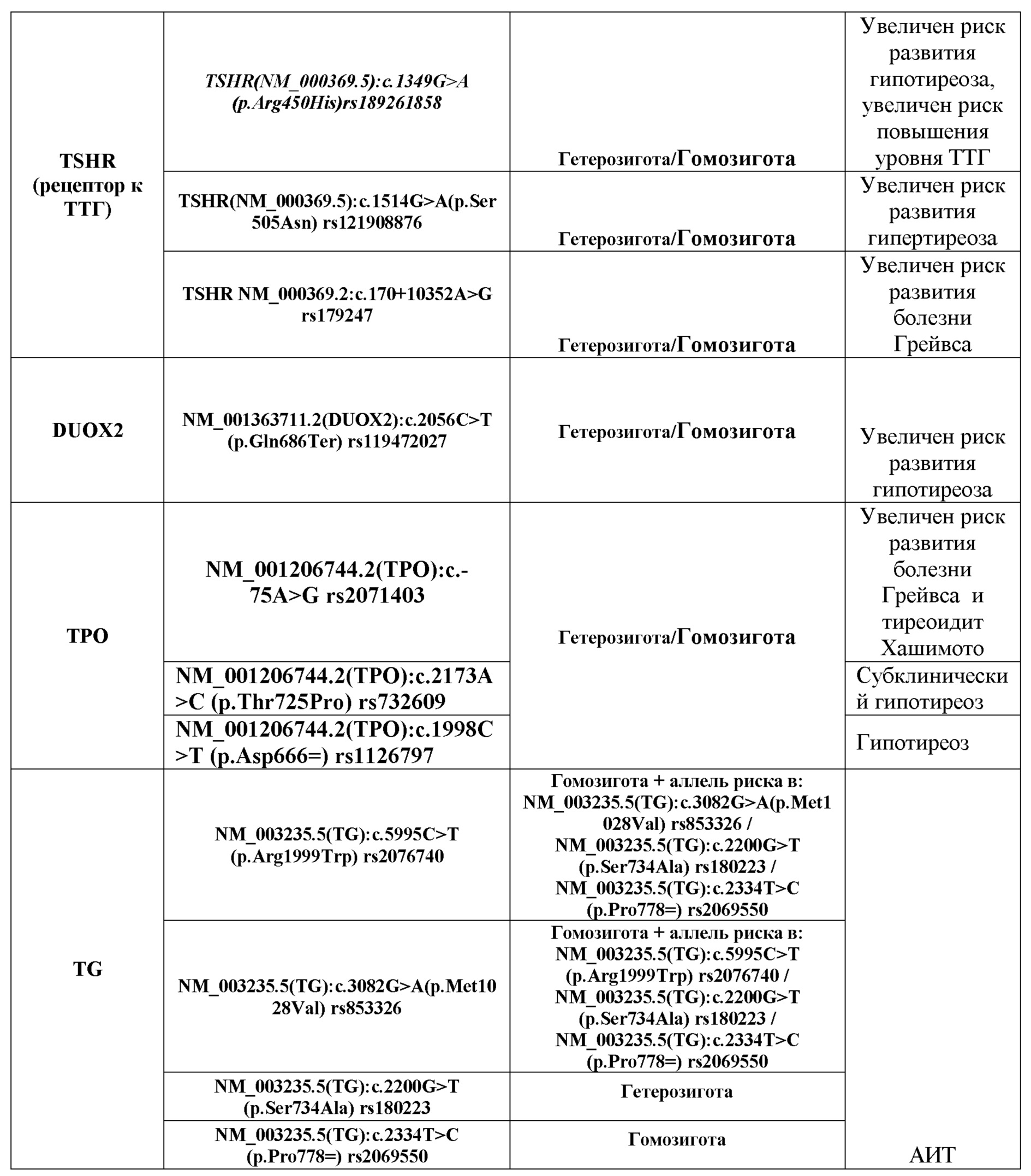
Согласно результатам проведенных исследований, на статистически значимой когорте пациентов были отобраны пять генов, а именно DIO1, DIO2, TPO, TSHR и TG, выявлены определенные полиморфизмы этих генов и установлены наиболее ассоциированные с патологиями тиреоидной системы генотипы указанных полиморфизмов, где наличие у пациента хотя бы одного из следующих полиморфизмов:
1) rs2235544 гена дейодиназы йодтиронина 1 (DIO1) генотипа CA или АА;
2) rs11206244 гена DIO1 генотипа CT или ТТ;
3) rs2294512 гена DIO1 генотипа СА или АА;
4) rs4926616 гена DIO1 генотипа TC или СС;
5) rs225014 гена дейодиназы йодтиронина 2 (DIO2) генотипа TC или СС;
6) rs2071403 гена тиреоидной пероксидазы (TPO) генотипа GG;
7) rs732609 гена TPO гомозиготного генотипа CC;
8) rs1126797 гена TPO гомозиготного генотипа TT;
9) rs179247 гена рецептора к тиреотропному гормону (TSHR) генотипа AG или АА;
10) rs2076740 гена тиреоглобулина (TG) генотипа СС в сочетании с аллелью риска rs853326 G>A гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
11) rs853326 гена TG генотипа AA в сочетании с аллелью риска rs2076740 C>T гена TG, и/или rs180223 G>T гена TG, и/или rs2069550 T>C гена TG;
12) rs180223 гена TG генотипа GT или ТТ и
13) rs2069550 гена TG генотипа ТТ,
свидетельствует о возможной предрасположенности к развитию нарушений функционирования тиреоидной системы.
Определение именно такого сочетания генотипов полиморфизмов указанных генов является диагностически значимым, так как охватывает достаточное количество генов, участвующих в синтезе, внутриклеточном действии и утилизации гормонов щитовидной железы, что позволяет выявить риск на всех этапах функционирования тиреоидной системы.
Осуществление изобретения.
В основе предложенного изобретения лежит молекулярно-генетическое исследование образцов клеток, тканей или физиологических жидкостей от пациентов. В качестве неограничивающего примера приведено исследование образца периферической крови пациентов, в возрасте от 18 лет, на следующие группы мутаций в генах DIO1, DIO2, TPO, TSHR и TG. Процедура молекулярно-генетического исследования осуществляется следующим образом:
Для проведения генотипирования используется ДНК, выделенная из клеток крови человека. Для выделения используется, например, набор "ПРОБА-ГС-ГЕНЕТИКА" (ДНК-технология, Россия) или другой набор реагентов, позволяющий выделить ДНК из периферической крови с концентрацией выше 5 нг/мкл. Процедура выделения происходит по протоколу производителя.
В качестве реактивов для постановки полимеразной цепной реакции в реальном времени (ПЦР-РВ) используется, например, набор "5X ScreenMix-HS" (Евроген, Россия). В полимеразной цепной реакции используются, например, зонды типа TaqMan. Подбор олигонуклеотидов (праймеров и зондов) осуществлялся с помощью, например, ПО Primer Express v3 (Thermo, США). Синтез олигонуклеотидов производится, например, на приборе AppliedBiosistems 3900 (Thermo, США) по заказу в ООО"Люмипроб Рус"(Россия).
Для проведения ПЦР используется, например, амплификатор CFX96 c1000 Touch (BioRad) с детекцией продуктов амплификации в режиме реального времени.
Диагностика осуществляется по данным, полученным по результатам молекулярно-генетического анализа участков генов на наличие аллелей риска (Таблица 2).
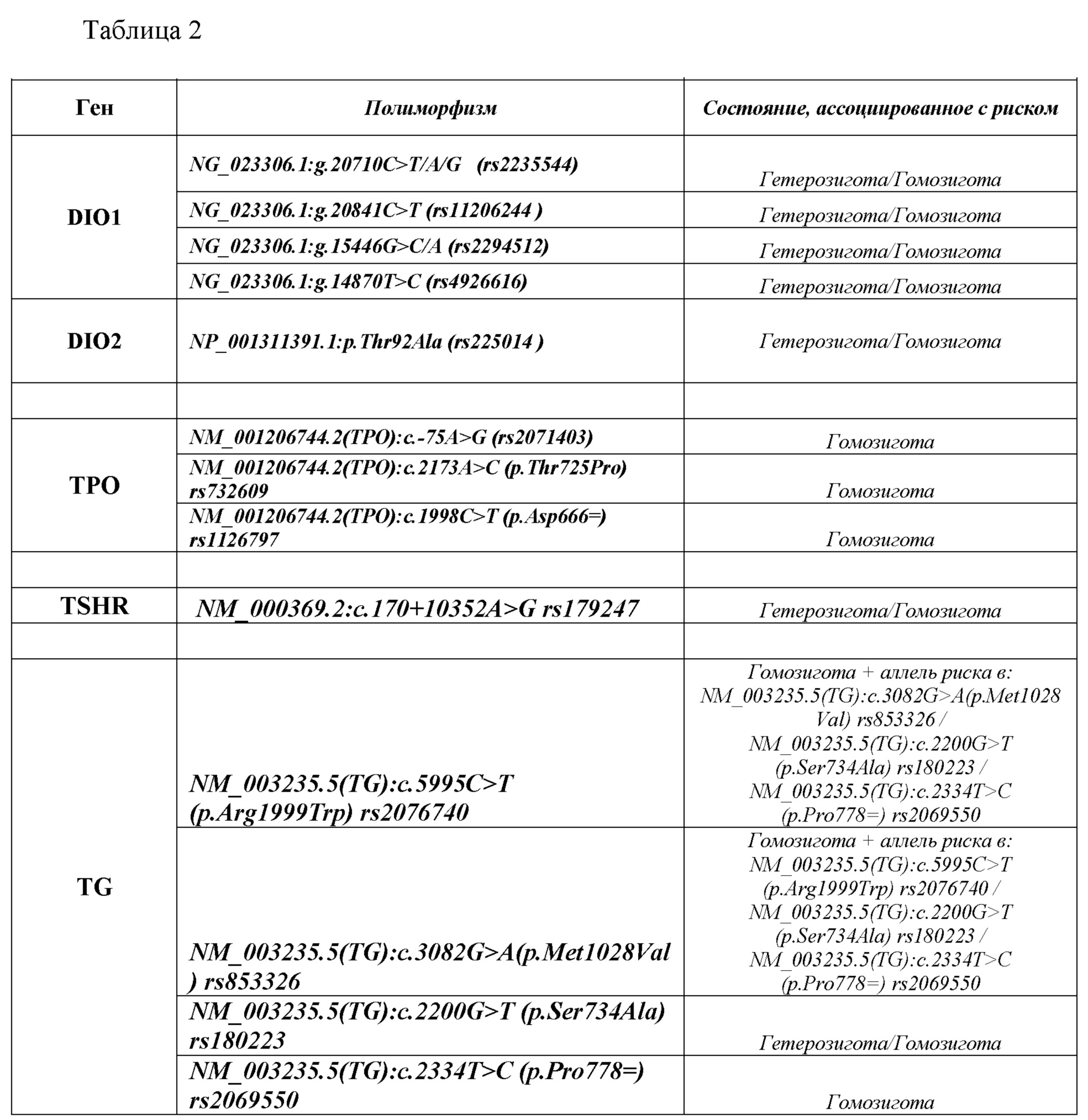
Ниже приведены примеры, демонстрирующие возможность достижения указанного технического результата, в которых показаны результаты исследований образцов от пациентов и подтверждение возможности реализации прогнозирования различий в активности ферментов, которые участвуют в синтезе, внутриклеточном действии и утилизации тиреоидных гормонов, что позволяет сделать предположения о патологическом состоянии щитовидной железы, которые были подтверждены дополнительными клинико-лабораторными исследованиями.
Примеры осуществления изобретения
ПРИМЕР 1: Пациент, 1975 г.р., пол мужской, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что значение св.Т3 стремится к нижней границе референсного диапазона, значение св. Т4 стремиться к верхней границе референсного диапазона, а соотношение св.Т4/св.Т3 ниже РЗ, что указывает на снижение периферической конверсии Т4 в Т3.
ПРИМЕР 2: Пациент, 1969 г.р., пол- женский, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что значение св.Т3 стремится к верхней границе референсного диапазона, значение св. Т4 стремиться к нижней границе референсного диапазона, а соотношение св.Т4/св.Т3 выше РЗ, что указывает на усиление конверсии Т4 в Т3.
ПРИМЕР 3: Пациент, 1970 г.р., пол- мужской, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что значение св.Т3 стремится к нижней границе референсного диапазона, значение св. Т4 выше референсного диапазона, а соотношение св.Т4/св.Т3 ниже РЗ, что указывает на снижение периферической конверсии Т4 в Т3.
ПРИМЕР 4: Пациент, 1946 г.р., пол- женский, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что значение св.Т3 стремится к нижней границе референсного диапазона, значение св. Т4 выше референсного диапазона, а соотношение св.Т4/св.Т3 значительно ниже РЗ, что указывает на снижение периферической конверсии Т4 в Т3.
ПРИМЕР 5: Пациент, 1964 г.р., пол- мужской, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
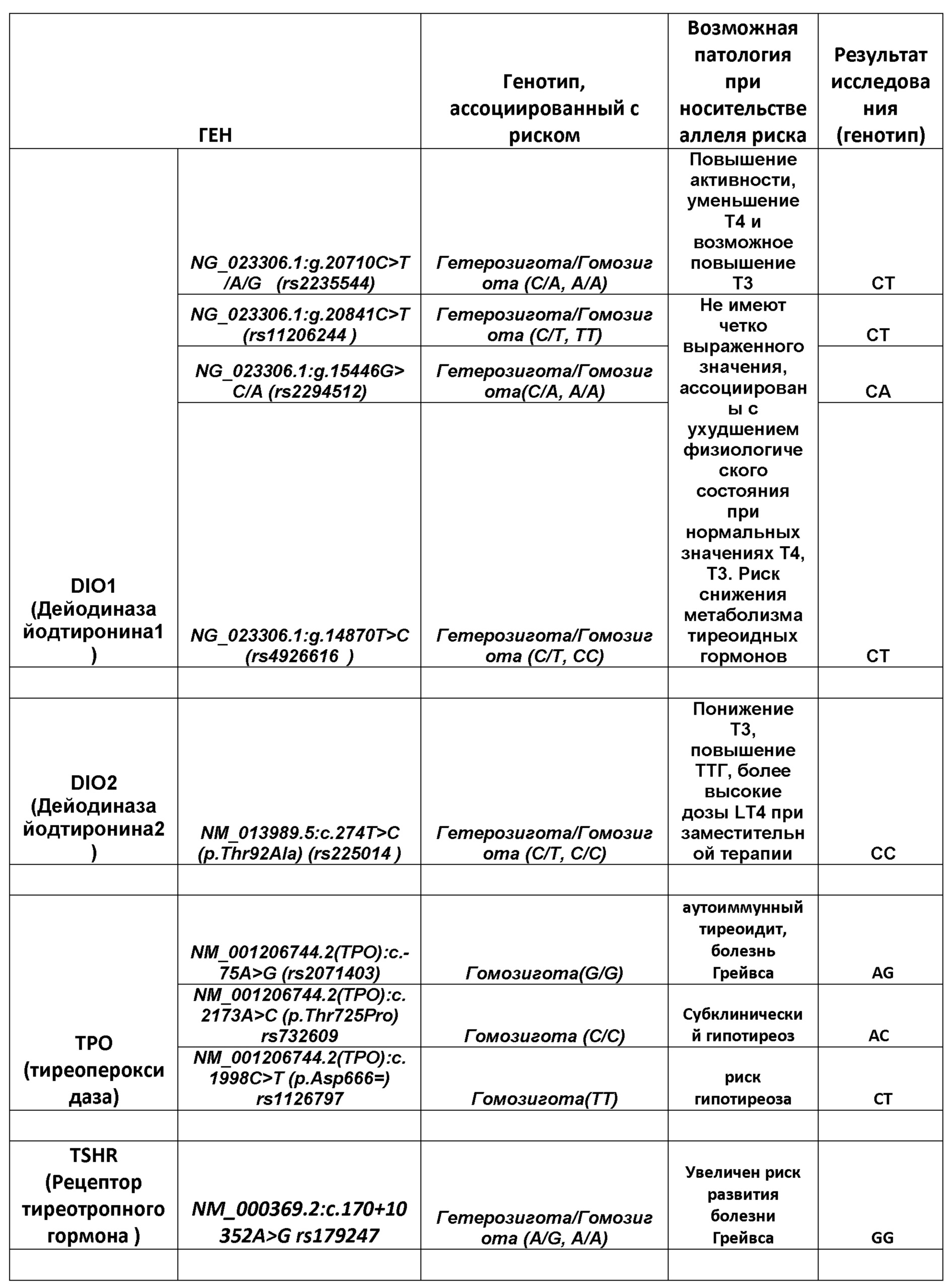

Выявленные изменения в генотипе были подтверждены данными лабораторных исследований на гормоны щитовидной железы, где:
Полученные данные свидетельствуют о том, что значение св.Т3 стремится к нижней границе референсного диапазона, значение ТТГ выше референсного диапазона, а соотношение св.Т4/св.Т3 ниже РЗ, что указывает на снижение периферической конверсии Т4 в Т3.
ПРИМЕР 6: Пациент, 1952 г.р., пол- мужской, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
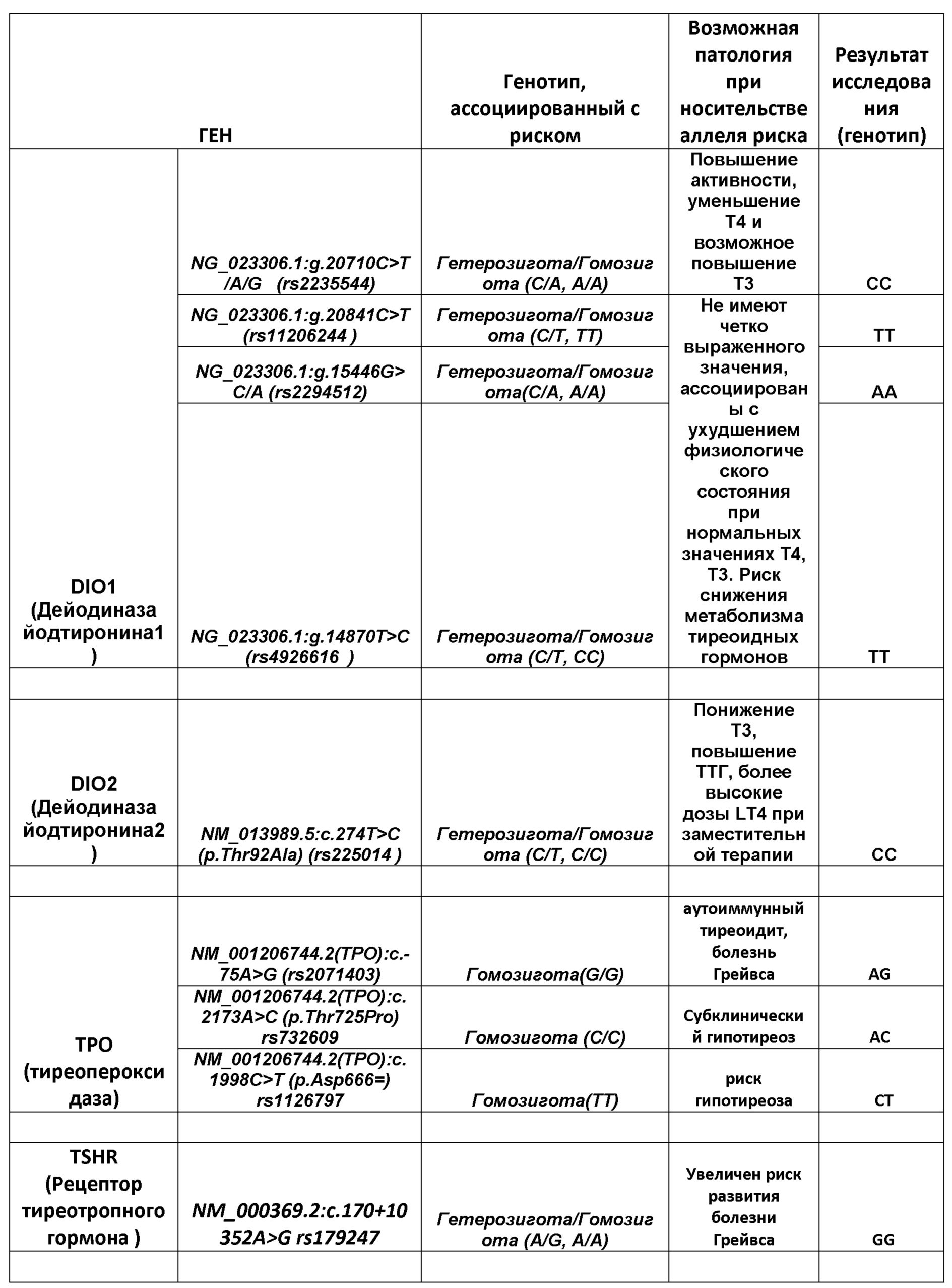

Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что значение св.Т3 стремится к нижней границе референсного диапазона, значение ТТГ выше референсного диапазона, а соотношение св.Т4/св.Т3 ниже РЗ, что указывает на снижение периферической конверсии Т4 в Т3.
ПРИМЕР 7: Пациент, 1985 г.р., пол- женский, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что значение ТТГ выше референсного диапазона, а антитела к ТПО значительно выше нормы, что свидетельствует об аутоиммунном воспалении щитовидной железы.
ПРИМЕР 8: Пациент, 1981 г.р., пол- женский, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что антитела к ТПО значительно выше нормы, что свидетельствует об аутоиммунном воспалении щитовидной железы.
ПРИМЕР 9: Пациент, 1975 г.р., пол- женский, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что значения св. Т3 и Т4 значительно превышают норму, а антитела к рецепторам ТТГ значительно выше нормы, что свидетельствует об избыточной секреции тиреоидных гормонов тканью щитовидной железы.
ПРИМЕР 10: Пациент, 1968 г.р., пол- женский, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что значения св. Т3 и Т4 значительно превышают норму, а ТТГ значительно ниже нормы, что свидетельствует об избыточной секреции тиреоидных гормонов тканью щитовидной железы.
ПРИМЕР 11: Пациент, 1965 г.р., пол- женский, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что значения св. Т3 и Т4 находятся в пределах нормы, значение соотношения св.Т4/св.Т3 ниже РЗ, что указывает на уменьшение периферической конверсии Т4 в Т3, а ТТГ значительно выше нормы, антитела к тиреоглобулину и тиреоидной пероксидазе значительно превышают нормы, что свидетельствует об аутоиммунном воспалении щитовидной железы.
ПРИМЕР 12: Пациент, 1985 г.р., пол- женский, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований:
Полученные данные свидетельствуют о том, что антитела к тиреоглобулину значительно превышает норму, что свидетельствует об аутоиммунном воспалении щитовидной железы.
ПРИМЕР 13: Пациент, 1982 г.р., пол- мужской, результаты анализа на генетические факторы риска развития патологии тиреоидной системы:
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований на гормоны щитовидной железы, где:
Полученные данные свидетельствуют о том, что антитела к тиреоглобулину и ТПО значительно превышают норму, значение ТТГ превышает верхнюю границу нормы, что свидетельствует об аутоиммунном воспалении щитовидной железы.
Приведенные примеры осуществления изобретения наглядно демонстрируют, что выявленные изменения в генотипе у пациентов могут указывать на риск изменения активности ферментов, которые участвуют в биосинтезе, внутриклеточном действии и утилизации тиреоидных гормонов. Предложенная панель на основе уникального сочетания генотипов полиморфизмов генов DIO1, DIO2, TPO, TSHR и TG, ее применение и способ позволяют одномоментно выявлять наиболее часто встречающиеся полиморфизмы, что дает возможность провести более полный диагностический охват и не пропустить возможные изменения в генотипе. Полученные данные могут быть использованы для дальнейшей диагностики состояния щитовидной железы и функционирования тиреоидной системы.
Реферат
Изобретение относится к области медицинской биотехнологии, конкретно к диагностике предрасположенности к развитию нарушений щитовидной железы по выявлению полиморфизмов генов, и может быть использовано для определения вероятности развития функциональных нарушений тиреоидной системы, этиологически вызванных различными полиморфными вариантами в генах, отвечающих за активность ферментов, которые участвуют в биосинтезе, внутриклеточном действии и утилизации тиреоидных гормонов. Предложены панель на основе уникального сочетания генотипов полиморфизмов генов DIO1, DIO2, TPO, TSHR и TG, ее применение и способ для выявления предрасположенности к нарушениям щитовидной железы, например гипер- или гипотиреозу. Предложенные изобретения позволяют одномоментно выявлять наиболее часто встречающиеся полиморфизмы, что дает возможность провести более полный диагностический охват и не пропустить возможные изменения в генотипе. 3 н.п. ф-лы, 2 табл., 13 пр.
Формула
Документы, цитированные в отчёте о поиске
Композиции и способы для диагностики и мониторинга гипертиреоза у животных семейства кошачьих

Комментарии