Препарат для профилактики и лечения воспалительных процессов у животных - RU2725773C1
Код документа: RU2725773C1
Чертежи

Описание
Область техники, к которой относится изобретение
Изобретение относится к ветеринарной фармации, в частности, к препаратам для профилактики и лечения воспалительных процессов у животных и может быть использовано в ветеринарии и животноводстве для профилактики и лечения воспалительных заболеваний у животных.
Уровень техники
Известно нестероидное противовоспалительное лекарственное средство, которое одержит в качестве активного вещества мелоксикам, в качестве вспомогательных веществ - натрия хлорид, глицин, гликофурол (тетрагликоль), полоксамер (лутрол), меглумин, натрия гидроксид и воду для инъекций при следующем соотношении ингредиентов (мас./об. %): мелоксикам - 0,5-1,5; натрия хлорид - 0,1-0,9; глицин - 0,1-1,5; гликофурол (Тетрагликоль) - 1-20; полоксамер (Лутрол) - 0,5-10; меглумин - 0,1-1,5; натрия гидроксид - 0,005-0,1; вода для инъекций - остальное до 100%. Изобретение обеспечивает получение новой лекарственной формы мелоксикама - раствора для внутримышечного введения при комплексном лечении заболеваний суставов, сопровождающихся болевым синдромом. (См. пат. RU №2464984, кл. A61K 31/5415, A61K 47/00, A61K 9/08, А61Р 29/00, опубл. 27.10.2012 г.).
Недостатком данного изобретения является отсутствие в составе компонентов, которые могли бы обеспечить достижение антиоксидантного и иммуностимулирующего эффектов.
Известна комбинация, обладающая антиагрегатной, липидрегулирующей и гастропротекторной активностями, фармацевтическая композиция, твердая дозированная фармацевтическая композиция, содержащая комбинацию ацетилсалициловой кислоты и этилметилгидроксипиридина малата или этилметилгидроксипиридина сукцината, обладающая антиагрегантной, липидрегулирующей и гастропротекторной активностями. (См. пат. RU №2453314, кл. A61K 31/4415, A61K 31/616, A61K 9/20, А61Р 7/02, А61Р 3/06, А61Р 1/04, опубл. 20.06.2012 г.).
Недостатком данной композиции является недостаточный противовоспалительный и иммуностимулирующий эффект, наличие противопоказаний и побочных эффектов, непродолжительный эффект, невозможность инъекционного применения, обусловливающая сложность дозировки и введения при групповом применении животным.
Наиболее близким по технической сущности и достигаемому положительному эффекту и принятый авторами за прототип является антиоксидантный противовоспалительный препарат для животных, содержащий исходные вещества в мас. %, а именно нестероидное противовоспалительное средство, в качестве которого используют флуниксина меглумин 6,0-8,0; этилметилгидроксипиридина сукцинат 10,0-20,0; аскорбиновую кислоту 6,0-8,0; поливинилпирролидон 4,0-6,0; воду для инъекций - остальное. Изобретение обеспечивает выраженное антиоксидантное и противовоспалительное действие, низкую токсичность, высокую эффективность в профилактике и лечении воспалительных заболеваний у животных. (См. пат. RU №2686462, кл. A61K 31/44, A61K 9/08, A61K 45/06, А61Р 29/00, А61Р 39/06, опубл. 26.04.2019 г.).
Недостатком данного препарата является недостаточный иммуностимулирующий эффект, а также то, что входящий в его состав флуниксина меглумин является неселективным ингибитором как фермента циклооксигеназы-2, так и фермента циклооксигеназы-1, что существенно увеличивает риск наступления нежелательных побочных эффектов.
Краткое описание чертежей и иных материалов
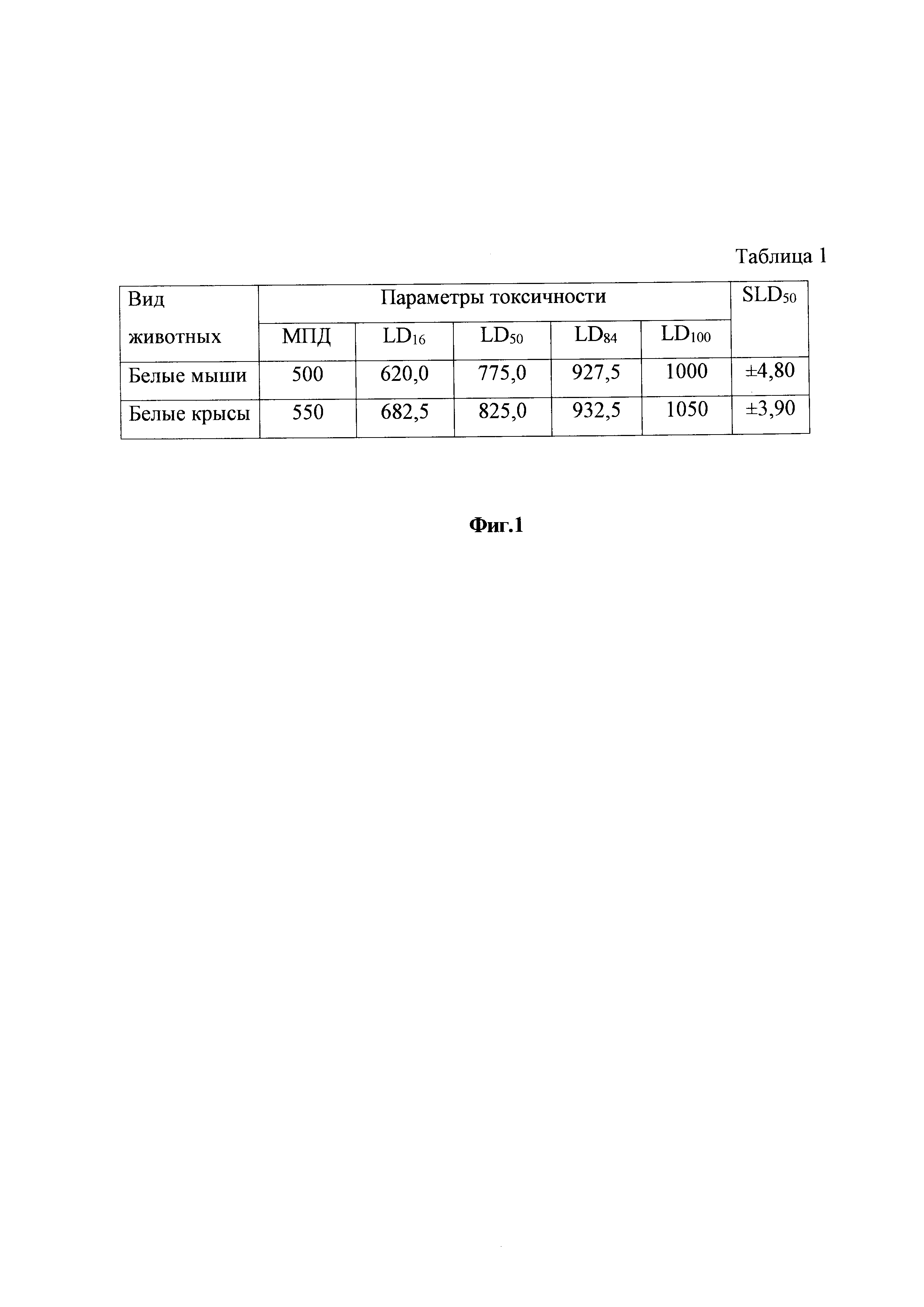
На фиг. 1 дан препарат для профилактики и лечения воспалительных процессов у животных. Острая токсичность препарата для профилактики и лечения воспалительных процессов у животных, табл. 1.
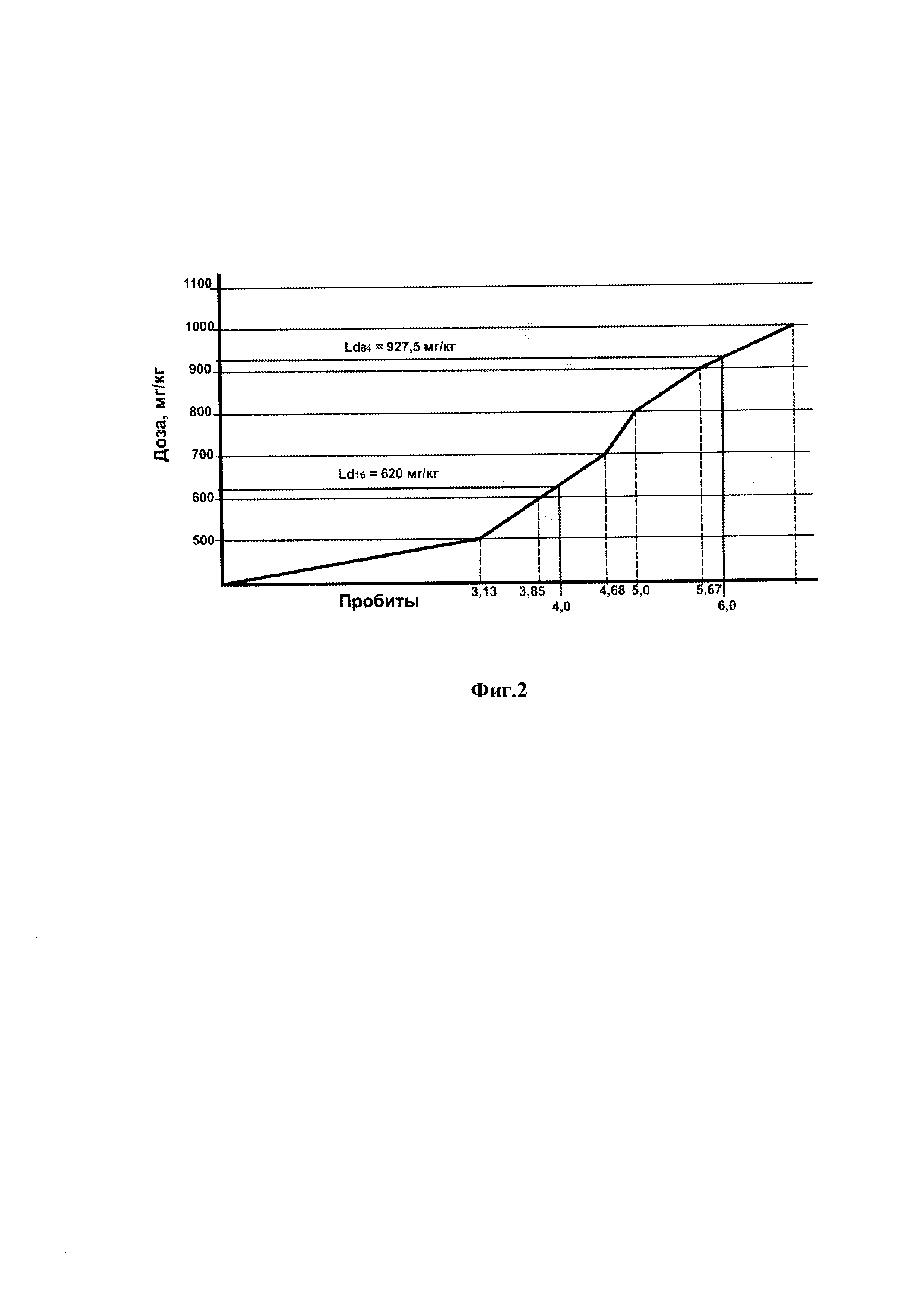
На фиг. 2, тоже, графическое изображение острой токсичности для белых мышей препарата для профилактики и лечения воспалительных процессов у животных, рис. 1.
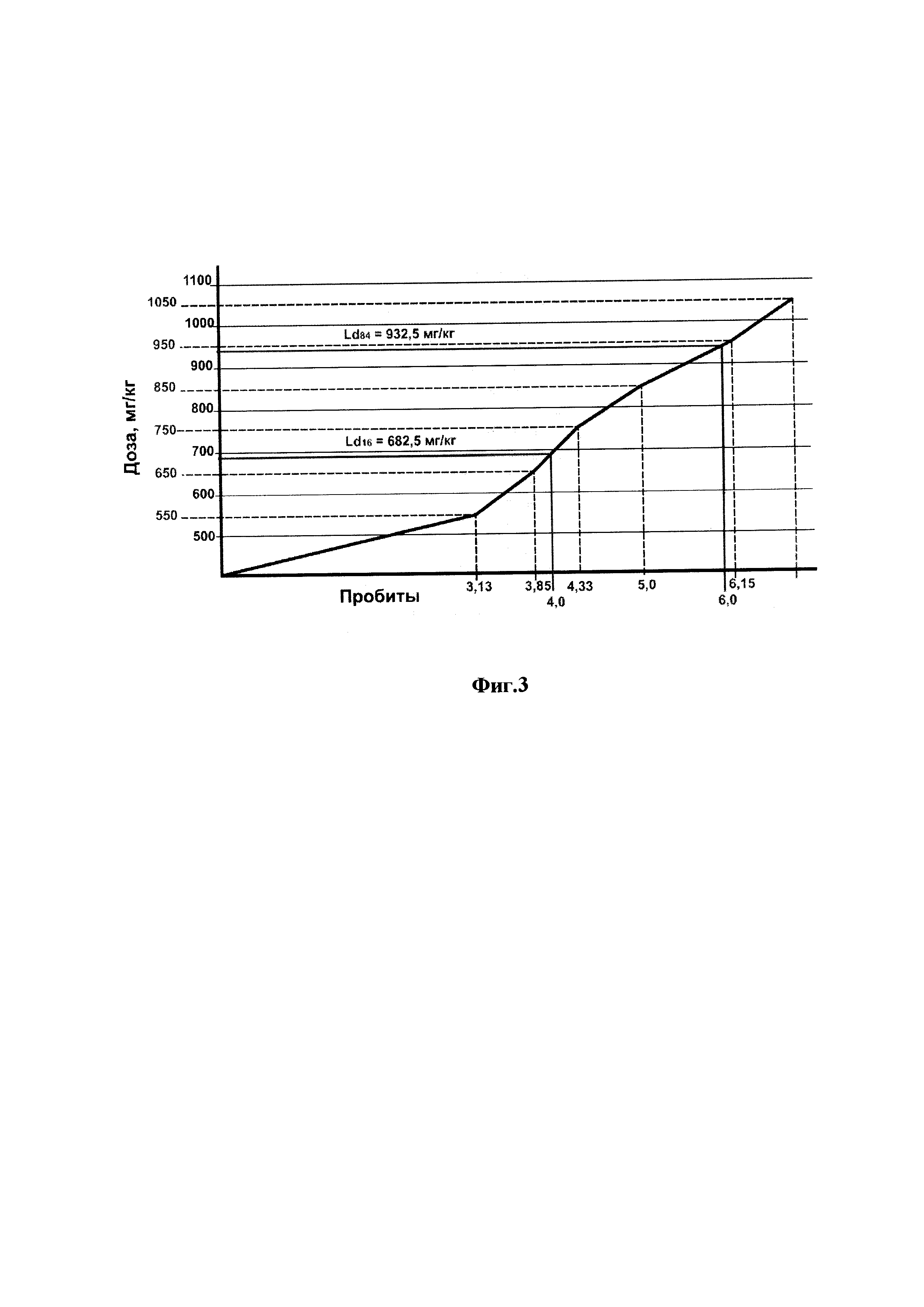
На фиг. 3, тоже, графическое изображение острой токсичности для белых крыс препарата для профилактики и лечения воспалительных процессов у животных, рис. 2.
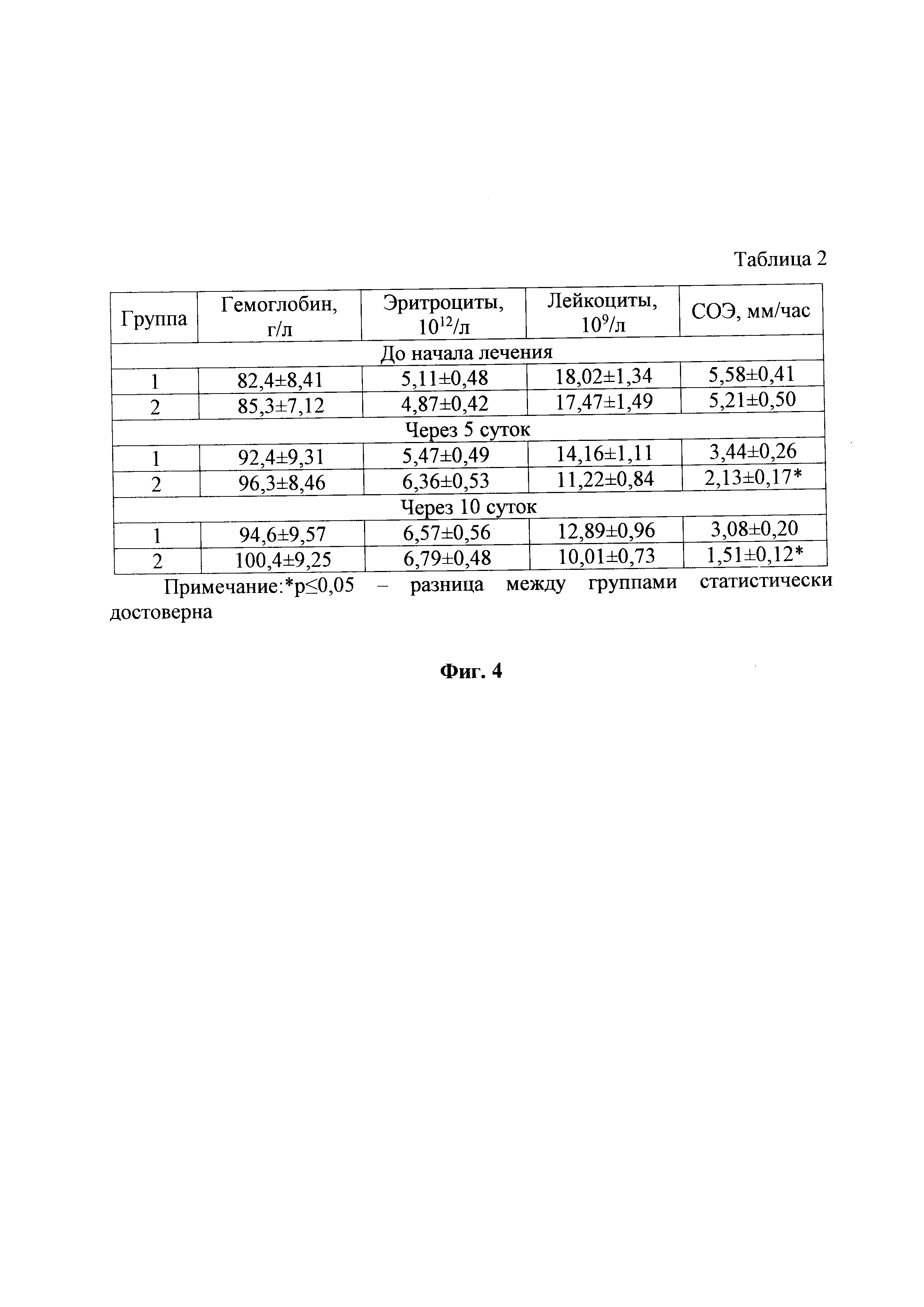
На фиг. 4, тоже, гематологические показатели коров, которым проводили лечение эндометрита, табл. 2.
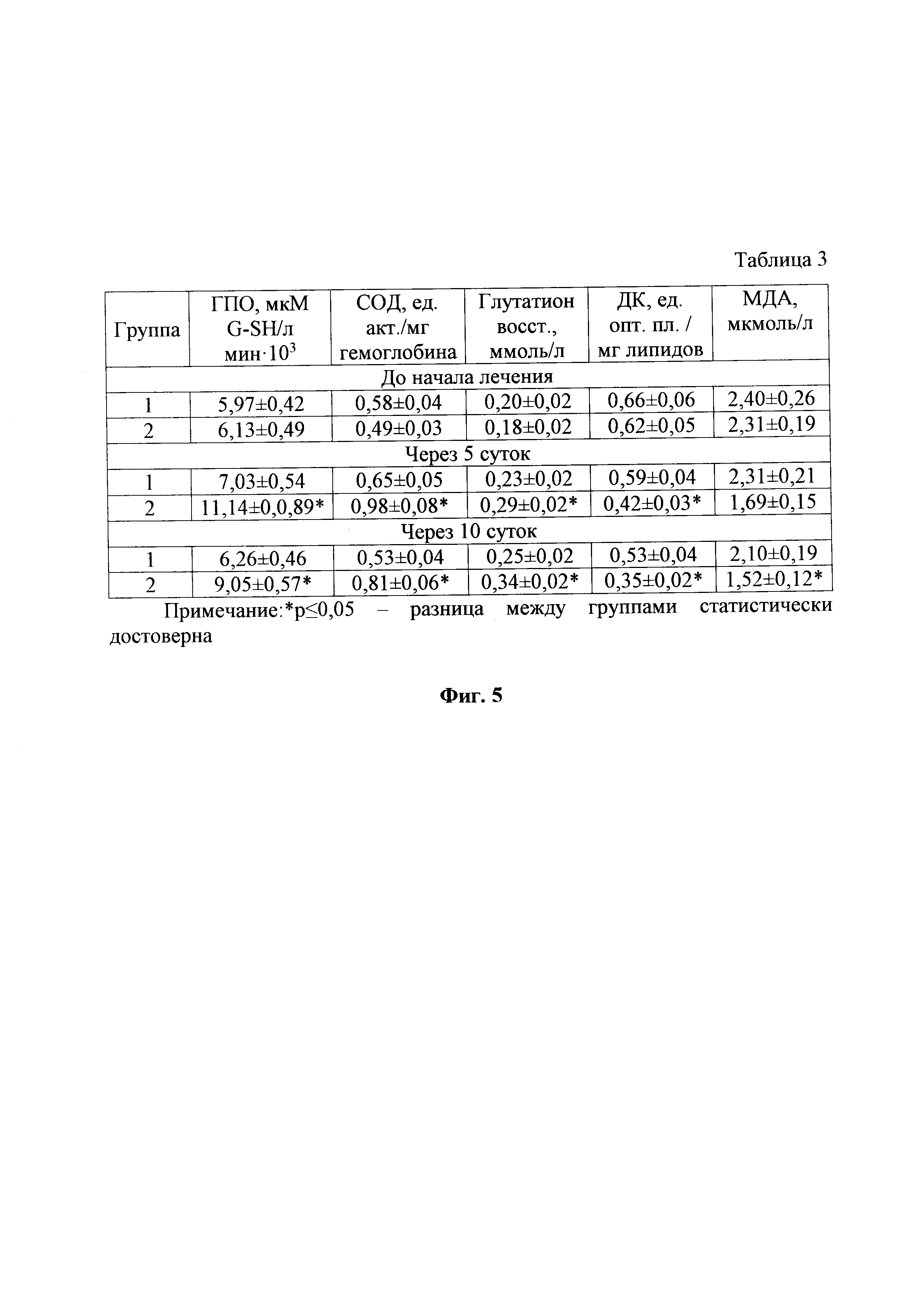
На фиг. 5, тоже, показатели функционирования системы антиоксидантной защиты организма коров, которым проводили лечение эндометрита, табл. 3.
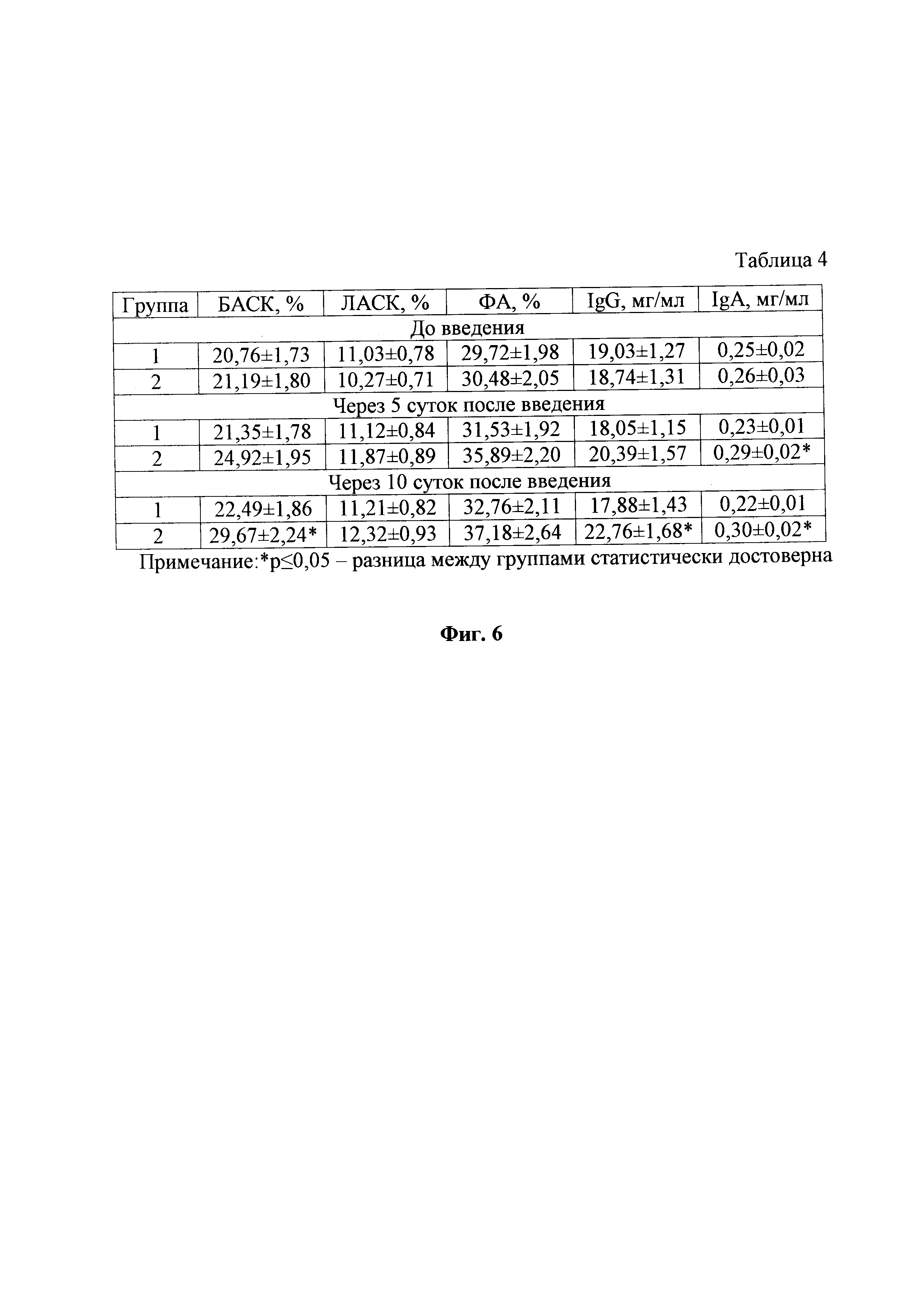
На фиг. 6, тоже, показатели, характеризующие иммунный статус у коров, которым проводили лечение эндометрита, табл. 4.
На фиг. 7, тоже, показатели, характеризующие клинический статус и показатели воспроизводства коров, которым проводили лечение эндометрита, табл. 5.
Раскрытие изобретения
Задачей изобретения является разработка препарата для профилактики и лечения воспалительных процессов у животных, обладающего выраженным противовоспалительным, антиоксидантным и иммуностимулирующим действием, низкой токсичностью, сниженным риском побочных эффектов, высокой эффективностью в профилактике и лечении воспалительных процессов у животных; удобством введения и дозировки.
Технический результат, который может быть достигнут с помощью предлагаемого изобретения, сводится к выраженному противовоспалительному, антиоксидантному и иммуностимулирующему действию, низкой токсичности и частоте развития побочных эффектов, высокой эффективности в профилактике и лечении воспалительных процессов у животных, удобству введения и дозировки.
Технический результат достигается с помощью препарата для профилактики и лечения воспалительных процессов у животных, включающего этилметилгидроксипиридина сукцинат и нестероидное противовоспалительное средство, при этом он дополнительно содержит левамизол основание, поливинилпирролидон и воду для инъекций, а в качестве нестероидного противовоспалительного средства используют мелоксикам, при следующем соотношении компонентов в мас. %:
Общим с заявленным препаратом является наличие в составе нестероидного противовоспалительного средства и этилметилгидроксипиридина сукцината. Отличием от ближайшего аналога, заявляемого препарата для профилактики и лечения воспалительных процессов у животных является использование в качестве нестероидного противовоспалительного средства мелоксикама и присутствие дополнительно левамизола основания, что позволяет достигать более выраженного противовоспалительного эффекта, за счет иммуностимулирующего действия и возможности длительного применения поскольку достигается селективное ингибирование только фермента циклооксигеназы-2 и снижается токсичность и вероятность развития нежелательных побочных эффектов, что дает возможность проводить более эффективно и безопасно лечение и профилактику воспалительных процессов у животных.
Заявляемый препарат для профилактики и лечения воспалительных процессов у животных представляет собой водный прозрачный раствор, без запаха, обладающий выраженным противовоспалительным, иммуностимулирующим и антиоксидантным эффектом, обеспечивает достижение купирования воспалительного процесса, жаропонижающего и обезболивающего действия, малотоксичен, удобен во ведении и дозировании.
Известно, что течение, развитие, появление осложнений и исход воспаления определяется активностью основных эффекторных механизмов, среди которых важное место занимают полиморфноядерные лейкоциты, макрофаги, а также гуморальные факторы воспаления, такие как цитокины, компоненты системы комплемента, лизосомальные ферменты, про- и антиоксидантные системы (См. Маянская Н.Н., Хидирова Л.Д., Маянская С.Д. // Казанский медицинский журнал. - 2013. - Т. 94. - №5. - С. 723-726.).
Сообщается, что при формировании распространенного и генерализованного воспаления наряду с биологическими особенностями флогогенного фактора большое значение имеет нарушение функциональных свойств иммунной системы, в частности выработка нейтрофильных гранулоцитов, а также дисбаланс про- и противовоспалительных цитокинов (См. Кашуба Э.А., Курлович Н.А., Козинец Г.И., Тимохина Т.Х., Дроздова Т.П. // Известия Челябинского научного центра УрО РАН. - 2004. - №S. - С. 76-80.).
Образование активных форм кислорода и активных форм азота долгое время считалось основным фактором, способствующим нарушению регуляции воспалительного ответа. Сообщается, что активные формы кислорода и продуцирование активных форм азота часто связаны с развитием хронических заболеваний и ускорением процесса старения. Механистически эта связь связывает явления окислительного стресса с появлением случайных вредных модификаций макромолекул с прогрессирующим развитием провоспалительных состояний, способствующих возрастным системным заболеваниям (См. Vitetta L., Linnane A.W. // Inflammopharmacology. - 2014. - Vol. 22 (2). - P. 69-72.).
Огромное количество косвенных доказательств указывает на то, что полученные из кислорода свободные радикалы (особенно супероксид и гидроксильный радикал) и высокоэнергетические окислители (такие как пероксинитрит) являются медиаторами воспаления (См. Cuzzocrea S., Riley D.P., Caputi А.Р., Salvemini D. // Pharmacological reviews. - 2001. - Vol. 53 (1). - P. 135-159.).
Известно, что образование свободных радикалов кислорода участвует в развитии синдрома системного воспалительного ответа. В дополнение к своим действиям в качестве вредных медиаторов, генерируемых воспалительными клетками, эти молекулы также играют важную роль, способствуя возникновению и прогрессированию воспаления в отдаленных органах. На ранних стадиях процесса свободные радикалы проявляют свое действие посредством активации ядерных факторов, которые вызывают синтез цитокинов. На более поздних стадиях эндотелиальные клетки активируются благодаря синергии между свободными радикалами и цитокинами, способствующей синтезу медиаторов воспаления и молекул адгезии. Наконец, свободные радикалы проявляют свои токсические эффекты в месте воспаления, реагируя с различными клеточными компонентами, вызывая потерю функции и гибель клеток (См. Closa D., Folch-Puy Е. // IUBMB Life. - 2004. - Vol. 56 (4). - 185-191.).
В последние годы появились доказательства того, что окислительный стресс играет решающую роль в развитии и сохранении воспаления и, таким образом, способствует патофизиологии ряда изнурительных заболеваний. Окислители влияют на все стадии воспалительного ответа, включая высвобождение поврежденными тканями молекул, действующих как эндогенные сигналы опасности, их восприятие врожденными иммунными рецепторами из семейства Toll-подобных и NOD-подобных и активацию сигнальных путей, инициирующих адаптивный клеточный ответ на такие сигналы (См. Lugrin J., Rosenblatt-Velin N., Parapanov R., Liaudet L. // Biological chemistry. - 2014. - Vol. 395 (2). - P. 203-230.).
Уникальность НПВС как класса лекарственных средств обусловлена сочетанием противовоспалительного, обезболивающего, жаропонижающего и антитромботического действия. При болях умеренной и высокой интенсивности анальгетическое действие НПВС сильнее, чем у простых анальгетиков (парацетамола), а у некоторых препаратов по силе сравнимо с опиатами (См. Стуров Н.В., Кузнецов В.И. // Земский врач. - 2011. - №1 (5). - С. 11-14.).
Такое сочетание эффектов обусловлено вмешательством НПВС в метаболизм арахидоновой кислоты. Мишенью действия НПВС является циклооксигеназа (ЦОГ), которая участвует в синтезе простагландинов, простациклинов и тромбоксана (См. Галеева Ж.А., Борисова Е.О., Белоусов Ю.Б., Зырянов С.К. // Лечение заболеваний нервной системы. - 2014. - №1 (13). - С. 17-24.).
Как оказалось, противовоспалительное действие нестероидных противовоспалительных препаратов определяется преимущественно нарастающим и необратимым подавлением активности изофермента циклооксигеназы-2, тогда как побочные эффекты этих препаратов ассоциируются в основном с быстрым, независимым от времени обратимым угнетением другого изофермента - циклооксигеназы-1, контролирующего синтез простагландинов, обладающих цитопротективными свойствами, и тромбоксанзависимую агрегацию тромбоцитов (См. Елисеев М.С. // Современная ревматология. - 2008. - Т. 2. - №4. - С. 54-56.).
Развитие патологии желудочно-кишечного тракта, ассоциированной с приемом нестероидных противовоспалительных препаратов, в основном связывают с блокадой циклооксигеназы-1 и снижением синтеза «цитопротективных» простагландинов. Умеренно селективные нестероидные противовоспалительные средства, типичным представителем которых является мелоксикам, могут иметь определенные преимущества в плане более низкого риска осложнений со стороны желудочно-кишеченого тракта и сердечно-сосудистой системы. Поэтому мелоксикам представляется весьма удачным средством, отличается благоприятной переносимостью и получил признание у российских врачей и пациентов (См. Сатыбалдыев A.M., Каратеев А.Е. // Современная ревматология. - 2017. - Т. 11. - №1. - С. 72-78.).
Одним из средств, положительно влияющим на воспалительные процессы и выраженность болевого синдрома, обладающим антипиретической активностью, является мелоксикам, производное эноликоновой кислоты. Более 99% мелоксикама связывается с белками, причем 40-50% его концентрации в плазме определяется в синовиальной жидкости, что позволяет активно воздействовать на воспалительный процесс в тканях сустава. Период полувыведения его действующего вещества составляет 20 ч, что позволяет однократно вводить его на протяжении суток (См. Корсакова Ю.Л., Бадокин В.В. // Современная ревматология. - 2011. - Т. 5. - №3. - С. 46-51.).
Мелоксикам характеризуется хорошей переносимостью и высокой безопасностью по сравнению с другими нестероидными противовоспалительными средствами, не уступая при этом в противовоспалительной и анальгезирующей активности. Эти свойства привели к широкому внедрению мелоксикама в комплексную терапию различных патологических состояний (См. Бадокин В.В. // РМЖ. - 2016. - Т. 24. - №26. - С. 1772-1776.).
Мелоксикам полностью всасывается при внутримышечном введении, максимальная концентрация его в плазме достигается примерно через 60 минут (См. Бутин А.А. // Трудный пациент. - 2011. - Т. 9. - №11. - С. 20-23.).
Мелоксикам - лекарственное средство, обладающее выраженным противовоспалительным действием, проявившимся при исследовании на всех существующих экспериментальных моделях воспаления. Механизм действия мелоксикама состоит в его способности ингибировать синтез простагландинов - известных медиаторов воспаления (См. Исакова М.Е. // РМЖ. - 2009. - Т. 17. - №13. - С. 862-863.).
Использование инъекционной формы мелоксикама проведении короткого курса терапии также может иметь ряд преимуществ. Так, при внутримышечном введении максимальная сывороточная концентрация достигается в 3-4 раза быстрее, чем при его приеме per os, а периоды полувыведения (20-24 ч) у пероральной и инъекционной форм почти одинаковы, что обусловливает и практически одинаковую продолжительность устойчивого эффекта. Это выгодно отличает инъекционную форму мелоксикама от таковой других нестероидных противовоспалительных средств, обеспечивая оптимальный по продолжительности анальгетический и противовоспалительный эффект, позволяющий применять препарат всего 1 раз в сутки (См. Елисеев М.С., Барскова В.Г., Владимиров С.А. // Современная ревматология. - 2009. - Т. 3. - №3. - С. 53-56.).
Накоплено значительное количество данных о применении в качестве антиоксидантного средства янтарной кислоты и ее солей как самостоятельного средства, так и в составе комплексных лекарственных средств. Показано, что сукцинатсодержащие препараты обладают выраженным антиоксидантным эффектом в различных экспериментальных моделях, снижая интенсивность процессов пероксидации в крови и внутренних органах животных (См. Симонова Н.В., Доровских В.А., Штарберг М.А., Юртаева Е.Ю., Володина И.В., Колесов Б.В. // Бюллетень физиологии и патологии дыхания. - 2018. - №67. - С. 64-69.).
Пристальное внимание фармакологов в качестве перспективных лекарственных средств привлекли соединения гетероароматических фенолов, в частности производные 3-оксипиридина. Они относятся к простейшим гетероциклическим аналогам ароматических фенолов и в этой связи проявляют антиоксидантные и антирадикальные свойства. (См. Новиков В.Е., Лосенкова С.О. // Обзоры по клинической фармакологии и лекарственной терапии. - 2004. - Т. 3. -№1. - С. 2-14.).
На основе этилметилгидроксипиридина сукцинат разработан препарат «Эмицидин» - водорастворимый ветеринарный антиоксидант с выраженным антигипоксическим эффектом. Применяется он при всех видах заболеваний, сопровождающихся усиленной продукцией свободнорадикальных соединений (См. Шатилов А.В. // Ветеринарная патология. - 2008. - №2 (25). - С. 117-119.). Этот антиоксидант ингибирует перекисное окисление липидов, повышает активность антиоксидантной системы организма и оказывает следующие действия: мембранопротекторное, мембраностабилизирующее, улучшает энергетический обмен в клетке, повышает резистентность организма к воздействию различных повреждающих факторов при патологических состояниях, вазопротективное, церебропротективное, кардиопротектное (См. Лаушкина Н.Н. // Вестник Орловского государственного аграрного университета. - 2011. - Т. 31. - №4. - С. 51-52.).
Подтверждено, что препарат «Эмицидин», обладающий ярко выраженным антиоксидантным действием, может использоваться для коррекции окислительного стресса у коров поле родов, сопровождающихся задержанием последа. Применение препарата антиоксиданта-антигипоксанта «Эмицидин» в комплексе с основной схемой лечения помогает восстановить мышечный тонус матки, помогает улучшить общее состояние коров поле родов, в связи с чем инволюция матки у животных с патологией родов проходит быстрее и без осложнений (См. Ярован Н.И., Петрушина М.В., Дементьева Е.С., Лешин В.В. // Вестник Орловского государственного аграрного университета. - 2012. - Т. 34. - №1. - С. 98-100.).
Левамизол - 2,3,5,6-тетрагидро-6-фенилимида-зо-[2,1-Ь]-тиазола гидрохлорид. Белый аморфный или кристаллический порошок. Легко растворим в воде. Он вызывает увеличение числа как Т-, так и В-лимфоцитов, титра естественных антител и активацию процесса антителообразования у интактных животных. Есть сведения о том, что левамизол у интактных животных в основном стимулирует клеточный иммунитет. Данное соединение вызывает быстрый эффект: уже через сутки количество Т-лимфоцитов увеличивается в 2 раза по сравнению с контрольными животными. Возрастающая активность Т-лимфоцитов, наступающая под действием левамизола, очевидно, играет немаловажную роль в способности препарата повышать иммунобиологические свойства организма (См. Даугалиева Э.Х. Филиппов В.В. // Иммунный статус и пути его коррекции при гельминтозах сельскохозяйственных животных. М., ВО «Агропромиздат». - 1991. - 188 с.).
Левамизол является производным имидазола и принадлежит к группе фенилмидотиазолов. Его иммуномодулирующие свойства связаны с изменениями пролифирации, миграции и секреторной функции лимфоцитов, макрофагов и нейтрофилов (См. Хабузов И.П., Александров И.Д. // Ветеринарная патология. - 2012. - №1 (39). - С. 97-105.).
Поливинилпирролидон обладает антитоксическим эффектом, заключающимся в связывании токсинов и их выведении из организма, способствует улучшению микроциркуляции в капиллярах и ликвидации стаза эритроцитов (См. Фрисс С.А. // Медицинская экспертиза и право. - 2011. - №6. - С. 9-11.). Он хорошо растворим в воде, нетоксичен и не имеет высокой склонности к комплексообразованию (См. Сильковская Ф.П. // Химия N-винитпирролидона и его полимеров. - 1970. - С. 134).
Сущность получения препарата для профилактики и лечения воспалительных процессов у животных заключается в следующем: исходные вещества в мас. %, а именно нестероидное противовоспалительное средство, в качестве которого служит мелоксикам - 0,15-0,25; этилметилгидроксипиридина сукцинат - 7,5-12,5; левамизол основание - 5,0-10,0; поливинилпирролидон - 2,5-4,5; вода для инъекций - остальное смешивают в асептических условиях и упаковывают.
Осуществление изобретения
Примеры конкретного выполнения получения и испытания препарата для профилактики и лечения воспалительных процессов у животных.
Пример 1.
Препарат для профилактики и лечения воспалительных процессов у животных готовят путем смешения компонентов в асептических условиях и растворения в воде для инъекций при следующем соотношении компонентов в мас. %:
Данный препарат вводили белым лабораторным крысам, у которых был экспериментально смоделирован асептический скипидарный абсцесс. Проведенный лабораторный анализ крови подопытных животных показал, что его применение приводит к уменьшению скорости оседания эритроцитов на 11,6%, снижению концентрации С-реактивного белка на 19,3%, увеличению бактерицидной активности сыворотки крови на 23,2%, увеличению активности супероксиддисмутазы - на 26,4%, но при этом недостаточно повысился уровень восстановленного глутатиона - всего на 12,3%, недостаточно возросла фагоцитарная активность - только на 14,3% и недостаточно снизилась концентрация малонового диальдегида - всего на 18,2%.
Пример 2.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
Введение полученного препарата белым лабораторным крысам способствовало уменьшению скорости оседания эритроцитов на 31,4%, снижению концентрации С-реактивного белка на 42,8%, увеличению бактерицидной активности сыворотки крови на 34,2%, увеличению активности супероксиддисмутазы - на 33,6%, повышению уровня восстановленного глутатиона - на 29,4%, увеличению фагоцитарной активности - на 24,7% и уменьшению концентрация малонового диальдегида - на 35,1%. При этом, динамика анализируемых показателей положительно коррелировала с клиническими показателями лабораторных животных, что способствовало более быстрой локализации и купированию воспалительного процесса.
Пример 3.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
Введение полученного препарата белым лабораторным крысам способствовало уменьшению скорости оседания эритроцитов на 40,1%, снижению концентрации С-реактивного белка на 46,9%, увеличению бактерицидной активности сыворотки крови на 39,4%, увеличению активности супероксиддисмутазы - на 42,5%, повышению уровня восстановленного глутатиона - на 36,0%, увеличению фагоцитарной активности - на 28,2% и уменьшению концентрация малонового диальдегида - на 37,3%. Применение препарата положительно отразилось на клиническом состоянии лабораторных животных и течении воспалительного процесса.
Пример 4.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
Введение полученного препарата белым лабораторным крысам способствовало уменьшению скорости оседания эритроцитов на 30,2%, снижению концентрации С-реактивного белка на 43,4%, увеличению бактерицидной активности сыворотки крови на 32,8%, увеличению активности супероксиддисмутазы - на 47,2%, повышению уровня восстановленного глутатиона - на 40,2%, увеличению фагоцитарной активности - на 31,1% и уменьшению концентрация малонового диальдегида - на 39,6%. Использование препарата способствовало оптимизации течения воспалительного процесса и нормализации основных клинических показателей.
Пример 5.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
Введение полученного препарата белым лабораторным крысам способствовало уменьшению скорости оседания эритроцитов на 28,5%, снижению концентрации С-реактивного белка на 35,1%, увеличению бактерицидной активности сыворотки крови на 22,6%, увеличению активности супероксиддисмутазы - на 36,1%, повышению уровня восстановленного глутатиона - на 26,8%, увеличению фагоцитарной активности - на 22,6% и уменьшению концентрация малонового диальдегида - на 33,5%. Несмотря на положительную динамику основных маркеров воспалительного процесса, иммунологической резистентности и антиоксидантного статуса она была менее выражена чем в примерах 2, 3 и 4, что коррелировало с клиническими показателями у лабораторных животных и течением воспалительного процесса.
Таким образом, наиболее оптимальными являются примеры 2, 3, 4, поскольку, в результате применения препарата для профилактики и лечения воспалительных процессов у животных в соответствии с ними, получают больший положительный эффект, заключающийся в уменьшению скорости оседания эритроцитов на 30,2-40,1%, снижению концентрации С-реактивного белка на 42,8-46,9%, увеличению бактерицидной активности сыворотки крови на 32,8-39,4%, увеличению активности супероксиддисмутазы - на 33,6-47,2%, повышению уровня восстановленного глутатиона - на 29,4-40,2%, увеличению фагоцитарной активности - на 24,7-31,1% и уменьшению концентрация малонового диальдегида - на 35,1-39,6%. соответственно. При осуществлении этих примеров отмечено положительное влияние введения препарата течение патологического процесса и клиническую картину у белых лабораторных крыс.
Пример 6.
Для проведения оценки препарата для профилактики и лечения воспалительных процессов у животных на острую токсичность берут следующее соотношение компонентов в мас. %:
Исследования по изучению острой токсичности препарата для профилактики и лечения воспалительных процессов у животных проводят на белых лабораторных мышах и лабораторных крысах при однократном внутрижелудочном введении, что позволяет определить летальные дозы, классифицировать препарат по ГОСТ 12.1.007-76 и отнести его к 3 классу опасности «Вещества умеренно опасные» (фиг. 1, 2, 3).
Пример 7.
Эффективность препарата для профилактики и лечения воспалительных процессов у животных изучают на коровах согласно примера 3, являющимся наиболее эффективным, который включает следующее соотношение компонентов в мас. %: мелоксикам - 0,2; этилметилгидроксипиридина сукцинат - 10,0; левамизол основание - 7,5; поливинилпирролидон - 3,5; вода для инъекций - остальное.
Суть эксперимента заключается в том, что используют две группы коров ярославской голштинизированной породы возрастом 4-7 лет и средним весом 410 кг больных гнойно-катаральным эндометритом, по десять особей в каждой. Первая группа животных выступает в качестве контроля и им применяется стандартная схема лечения, включающая внутримышечное введение в 1-4 дни препарата «Амоксигард» (ООО «Нита-Фарм, Россия) в дозе 20 мл, препарата «Утеротон» (ООО «Нита-Фарм, Россия) вечером на 1-3 сутки в дозе 10 мл, препарата «Тривит» (ЗАО «Мосагроген», Россия) и препарата «АСД фракция 2» (ФКП «Армавирская биофабрика», Россия) в дозах 10 мл и 2 мл в 1, 3, 7 и 10 дни лечения. Во второй группе лечение проводят аналогично контроля, но дополнительно в 1-3 сутки вводят внутримышечно препарат для профилактики и лечения воспалительных процессов у животных в дозе 40 мл (из расчета 20,8 мг/кг). Ежедневно регистрируют клинические показатели у больных коров, а также получают кровь для лабораторного исследования на момент начала лечения, на пятые и десятые сутки лечения, при котором определяют гематологические и биохимические показатели.
При анализе результатов гематологического исследования (фиг. 4) установлено, что уровень гемоглобина в крови коров до начала лечения был на уровне нижних границ физиологической нормы. За время проведения эксперимента данный показатель увеличился в первой группе на 14,8%, а во второй - на 17,7% соответственно, но при этом различия между группами не носили статистически достоверного характера. Количество эритроцитов в крови также было низким в начале опыта, что вероятно связано с послеродовой анемией, но за десять суток проводимой терапии наблюдалась тенденция к стабилизации данного параметра. Количество лейкоцитов у коров до введения лекарственных средств значительно превышало физиологический уровень, что соответствует реакции иммунной системы на воспалительный процесс. В результате проводимого лечения происходило постепенное снижение концентрации данных клеток во всех группах, но его степень была неодинакова. Так, за опытный период в первой группе уменьшение составило 28,4%, а во второй - 42,7%, и по завершении лечения в контрольной группе данный показатель был выше чем во второй группе на 22,3%.
Применение препарата для профилактики и лечения воспалительных процессов у животных оказало значимое влияние на динамику скорости оседания эритроцитов (СОЭ). Изначально этот показатель у подопытных животных кратно превышал физиологический уровень. За время наблюдения зафиксировано уменьшение его значений в первой группе на 44,8%, во второй - на 71%. При этом через пять суток после начала лечения в контрольной группе СОЭ была выше чем во второй и третьей на 38,1%, а через десять суток - на 50,9% соответственно, и различия были статистически достоверными. Учитывая, что динамика СОЭ отражает интенсивность воспаления, можно говорить о том, что в первой группе оно протекало интенсивнее чем во второй.
Рассматривая полученные данные об антиоксидантном статусе коров (фиг. 5), используемых в эксперименте, необходимо отметить, что активность глутатионпероксидазы (ГПО), одного из ключевых ферментов антиоксидантной защиты, значительно повысилась во второй группе после применения препарата для профилактики и лечения воспалительных процессов у животных. Так, через пять суток после начала лечения в крови животных, которым вводили этот препарат она была достоверно выше чем в образцах, полученных от коров из первой группы на 58,4%. За время проведения опыта данный показатель увеличился во второй группе на 47,6%, а в первой группе - на 2,1%.
Активность супероксиддисмутазы (СОД) за время исследований увеличилась во второй группе на 65,3%, а в первой - наоборот уменьшилась на 8,6%. В итоге на момент завершения опыта во второй группе значения этого маркера были статистически достоверно выше по сравнению с первой группой на 52,8%. Уровень восстановленного глутатиона в начале лечения был ниже физиологического и увеличивался постепенно в обеих группах. За первые пять суток лечения его повышение в первой группе составило 15,0%, во второй - 61,1%, а за опытный период в целом в контроле увеличение составило 25,0%, а у животных, которым применяли препарат для профилактики и лечения воспалительных процессов у животных - 88,8%. Значения данного показателя во второй группе достоверно было выше чем в первой группе через пять и десять суток после начала лечения.
Концентрация продуктов перекисного окисления в крови коров больных эндометритом существенно превышала референтные показатели, что свидетельствует в пользу того, что воспалительная реакция - это фактор интенсификации свободнорадикального окисления. По мере выздоровления подопытных животных уровень этих метаболитов уменьшался. Так, в первой группе за время наблюдения снижение концентрации диеновых конъюгатов (ДК) составило 19,7%, во второй - 43,5%. Разница между группами характеризовалась статистической достоверностью и составляла через пять суток после начала лечения 28,8%, а через десять суток - 33,9% соответственно. Аналогичная динамика наблюдалась относительно уровня малонового диальдегида (МДА), концентрация которого в крови коров из первой группы в течении опыта снизилась на 12,5%, во второй - 34,2%. Через десять дней после начала лечения разница между первой и второй группами - статистически достоверно составляла 27,6%.
При анализе показателей, характеризующих иммунный статус у коров (фиг. 6) установлено, что за время проведения исследований бактерицидная активность сыворотки крови (БАСК) в первой группе возросла на 8,3%, в то время как во второй - на 40,0%, а по завершению эксперимента в контроле данный показатель был на 31,9% статистически достоверно ниже, чем у животных, которым применяли препарат для профилактики и лечения воспалительных процессов у животных в составе комплексной терапевтической схемы. Лизоцимная активность сыворотки крови (ЛАСК) на за время проведения опыта в первой группе увеличилась на 1,63%, а во второй - на 19,9% и в конце опыта разница между группами составила 9,9% в пользу второй группы. Фагоцитарная активность (ФА) за период наблюдения в первой группе увеличилась на 10,2%, а во второй группе - на 21,9% и в конце опыта была выше во второй группе на 13,5% по сравнению с первой. Уровень иммуноглобулинов класса G (IgG) за время проведения терапии снизился в крови животных из первой группы на 6,0%, а в крови животных из второй группы, наоборот, увеличился на 21,4%, чем была обусловлена достоверная разница по данному показателю между группами, которая на момент завершения эксперимента составила 27,3%. Уровень иммуноглобулинов класса A (IgA) за время проведения опыта снизился в первой группе на 12,0% и увеличился во второй группе - на 15,4%. Достоверная разница между группами по данному показателю на десятые сутки исследования составила 36,3%.
При клиническом наблюдении (фиг. 7) за больными животными установлено, что у животных, которым применяли препарат для профилактики и лечения воспалительных процессов у животных в комплексной схеме лечения, клинические признаки заболевания проявлялись менее продолжительно: в среднем на 2,15 суток короче, чем в первой группе.
Также отмечено, что у коров из второй группы наблюдалась более короткие сроки инволюции матки после лечения. Так, у животных которым применяли препарат для профилактики и лечения воспалительных процессов у животных, данный показатель был меньше чем в контроле на 2,62 суток. Кратность осеменения во второй группе составила в среднем 2,4 раза, в то время как в первой группе - 2,8 раза. Сервис период в контрольной группе был в среднем на 10,5 суток продолжительнее чем в первой группе.
В результате проведенного исследования установлено, что гнойно-катаральный эндометрит у коров протекает на фоне значительной индукции процессов перекисного окисления липидов. Применение при данном заболевании в комплексе со средствами патогенетической терапии препарата для профилактики и лечения воспалительных процессов у животных позволяет добиваться снижения интенсивности воспалительного процесса, что подтверждается динамикой СОЭ и количества лейкоцитов в крови. Это в целом положительно отражается на течении болезни и позволяет уменьшить количество рецидивов заболевания, а также способствует повышению репродуктивного потенциала. Введение в комплексную схему лечения гнойно-катарального эндометрита у коров препарата для профилактики и лечения воспалительных процессов у животных трехкратно в дозе 20 мл на голову в первые трое суток лечения приводит к нормализации антиоксидантного статуса и уменьшению концентрации продуктов перекисного окисления в крови. При этом статистически достоверно повышается уровень активности глутатионпероксидазы, супероксиддисмутазы и восстановленного глутатиона, а также снижается содержание диеновых конъюгатов и малонового диальдегида. Применение препарата для профилактики и лечения воспалительных процессов у животных при лечении эндометрита у коров позволяет повысить у них иммунный статус, что положительно отражается на течении заболевания. Использование данного препарата в дополнение к стандартной терапевтической схеме в сравнительном аспекте сопровождается выраженным повышением терапевтического эффекта.
Преимущества предлагаемого препарата для профилактики и лечения воспалительных процессов у животных в том, что он содержит в комплексе нестероидное противовоспалительное средство, в качестве которого используют мелоксикам, этилметилгидроксипиридина сукцинат, левамизол основание, поливинилпирролидон и воду для инъекций, что значительно повышает его эффективность, а стабильный водный раствор, делает его удобным в дозировании и применении животным.
Предлагаемое изобретение по сравнению с прототипом и другими известными техническими решениями имеет следующие технические преимущества:
- повышенный противовоспалительный эффект;
- наличие иммуностимулирующего эффекта;
- комплексное действие;
- повышение терапевтической эффективности;
- снижение токсичности;
- уменьшение частоты развития побочных эффектов;
- удобство введения и дозирования;
- экономичность в использовании.
Реферат
Изобретение относится к ветеринарии и фармацевтической промышленности, а именно к препарату для профилактики и лечения воспалительных процессов (заболеваний) у животных, который включает (в мас.%): 0,15-0,25% мелоксикама в качестве нестероидного противовоспалительного средства, 7,5-12,5% этилметилгидроксипиридина сукцината, 5,0-10,0% левамизола основания, 2,5-4,5% поливинлпирролидона и воду для инъекций (остальное). Изобретение обеспечивает повышение противовоспалительного терапевтического эффекта при наличии антиоксидантного и иммуностимулирующего действия, а также снижение токсичности и частоты развития побочных эффектов. 7 пр., 7 ил.
Формула
Документы, цитированные в отчёте о поиске
Антиоксидантный противовоспалительный препарат для животных

Комментарии