Антиоксидантный противовоспалительный препарат для животных - RU2686462C1
Код документа: RU2686462C1
Чертежи




Описание
Область техники, к которой относится изобретение
Изобретение относится к ветеринарной фармации, в частности, к антиоксидантным противовоспалительным препаратам для животных и может быть использовано в ветеринарии и животноводстве для профилактики и лечения воспалительных заболеваний у животных.
Уровень техники
Известна инъекционная антибактериальная фармацевтическая композиция, которая может быть использована для лечения инфекций бактериальной этиологии. Композиция содержит флуниксин или одну из его фармацевтически приемлемых солей, азитромицин в форме дигидрата, лимонную кислоту и воду для инъекций при следующем соотношении ингредиентов (мг/мл): азитромицина дигидрат - 60,0-120,0; флуниксин или одна из его фармацевтически приемлемых солей - 38,0-50,0, лимонная кислота - 0,01-1,0, вода для инъекций - до 1 мл. Композиция стабильна при хранении, обладает широким спектром антибактериального действия при внутримышечном введении животным, нетоксична, не вызывает при применении осложнений и побочных эффектов, способствует ускорению выведения из организма остаточных количеств азитромицина и флуниксина и тем самым позволяет сократить срок предубойной выдержки животных. (См. пат. RU №2563826, кл. А61K 31/455, А61K 31/7048, А61K 47/00, А61K 9/08, А61Р 31/04, опубл. 20.09.2015 г.).
Недостатком данной фармацевтической композиции является отсутствие в составе компонентов, которые могли бы обеспечить достижение антиоксидантного эффекта, а также присутствие в составе антибиотика из группы азалидов, чем может быть обусловлен ряд побочных эффектов и противопоказаний, что делает ее применение неоправданным при отсутствии текущих инфекций бактериальной этиологии и с профилактической целью.
Известен препарат для нормализации процессов перекисного окисления липидов у животных, содержащий мас. %: 2-этил-6-метил-3-гидроксипиридина сукцинат 20,0-30,0, кислоту аскорбиновую 5,0-7,0, селен (Se0) 0,3-0,5, поливинилпирролидон 3,0-5,0, воду для инъекций остальное. Препарат обладает антиоксидантным действием, низкой токсичностью и удобством введения, способствует профилактике избыточного образования продуктов перекисного окисления липидов, нормализации функционирования системы антиоксидантной защиты организма животных и процесса перекисного окисления липидов. (См. пат. RU №2538666, кл. А61K 31/4412, А61K 31/375, А61K 33/04, А61Р 3/00, опубл. 10.01.2015 г.).
Недостатком данного препарата является невысокий противовоспалительный эффект.
Наиболее близкой по технической сущности и достигаемому положительному эффекту и принятая авторами за прототип является комбинация, обладающая антиагрегатной, липидрегулирующей и гастропротекторной активностями, фармацевтическая композиция, твердая дозированная фармацевтическая композиция, содержащая комбинацию ацетилсалициловой кислоты и этилметилгидроксипиридина малата или этилметилгидроксипиридина сукцината, обладающая антиагрегантной, липидрегулирующей и гастропротекторной активностями. (См. пат. RU №2453314, кл. А61K 31/4415, А61K 31/616, А61K 9/20, А61Р 7/02, А61Р 3/06, А61Р 1/04, опубл. 20.06.2012 г.).
Недостатком данной композиции является недостаточный противовоспалительный эффект, наличие противопоказаний и побочных эффектов, непродолжительный эффект, невозможность инъекционного применения, обусловливающая сложность дозировки и введения при групповом применении животным.
Краткое описание чертежей и иных материалов
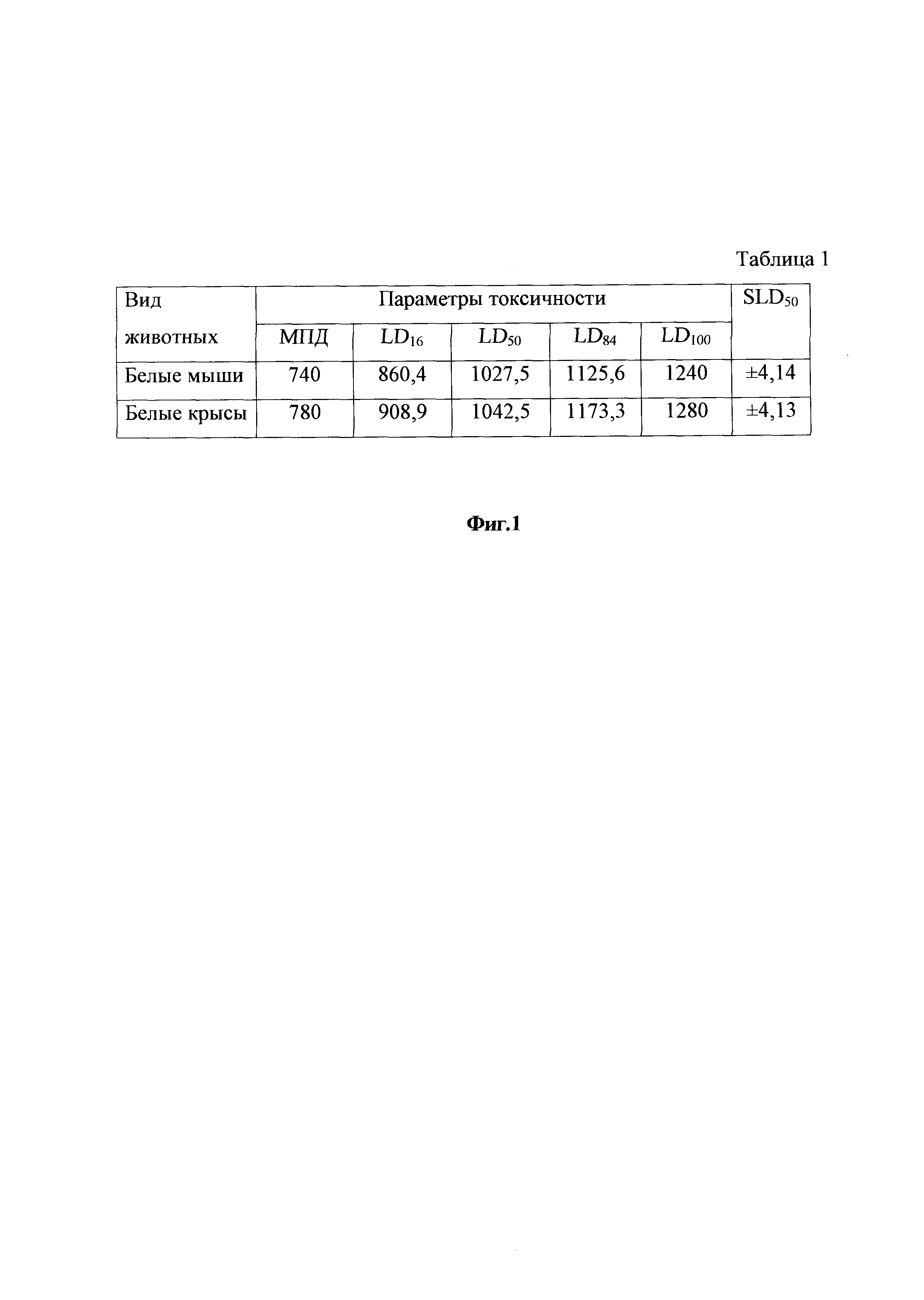
На фиг. 1 дан антиоксидантный противовоспалительный препарат для животных. Острая токсичность антиоксидантного противовоспалительного препарата для животных, табл. 1.
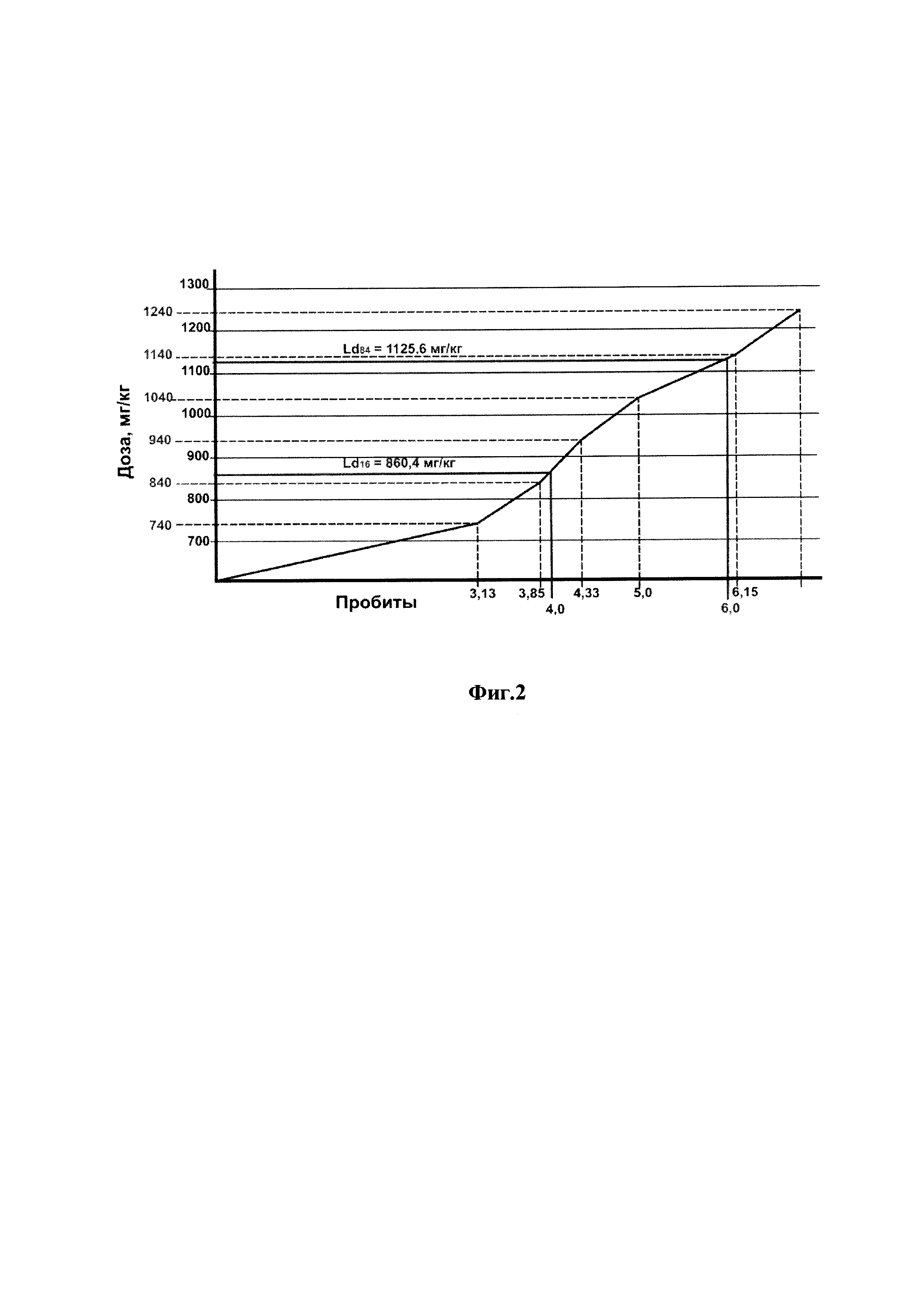
На фиг. 2, тоже, графическое изображение острой токсичности для белых мышей антиоксидантного противовоспалительного препарата для животных.
На фиг. 3, тоже, графическое изображение острой токсичности для белых крыс антиоксидантного противовоспалительного препарата для животных,
На фиг. 4, тоже, гематологические показатели коров, которым проводили профилактику мастита, табл. 2.
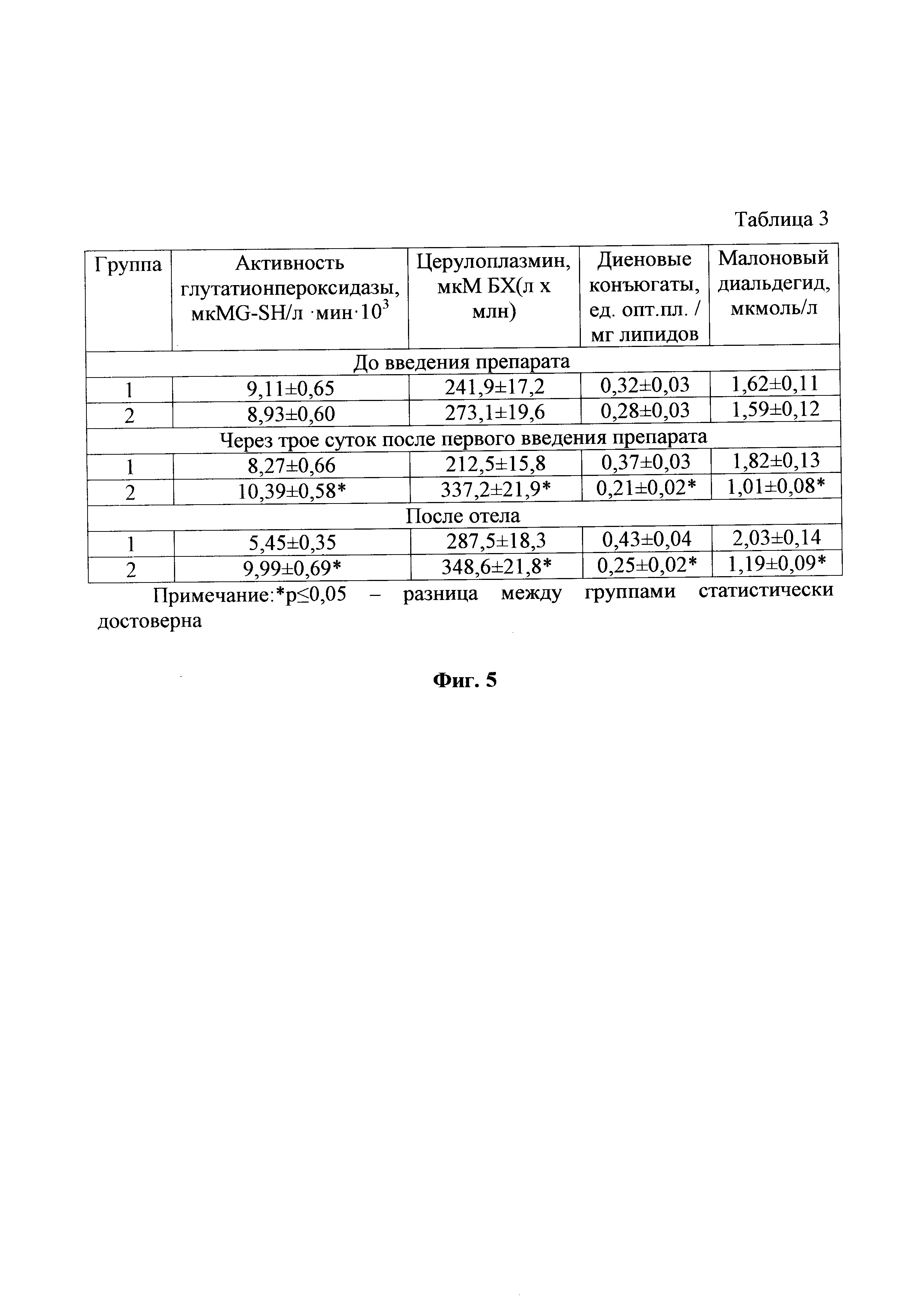
На фиг. 5, тоже, показатели функционирования системы антиоксидантной защиты организма коров, которым проводили профилактику мастита, табл. 3.
На фиг. 6, тоже, заболеваемость коров маститом, табл. 4.
На фиг. 7, тоже, гематологические показатели коров, которым проводили лечение мастита, табл. 5.
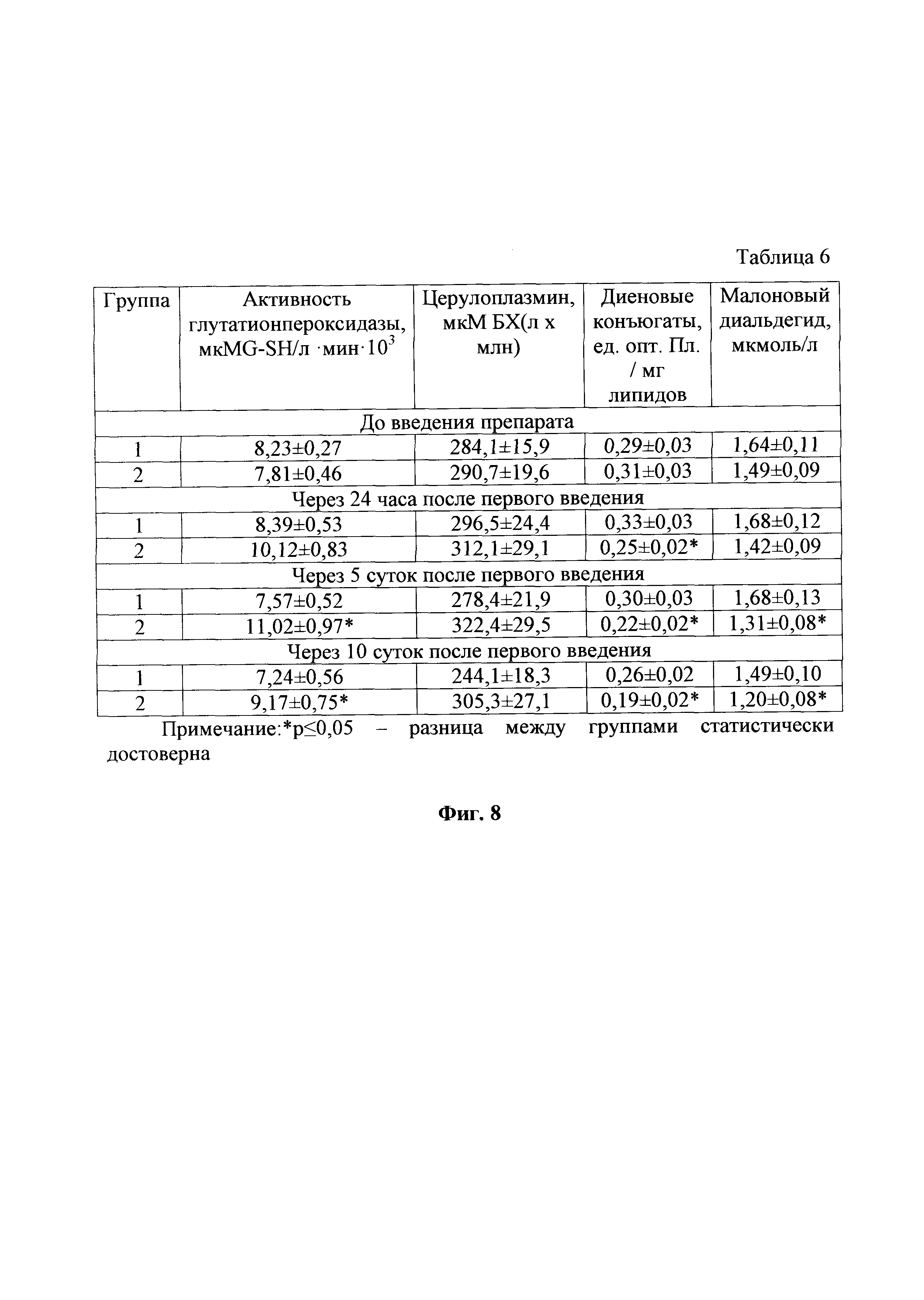
На фиг. 8, тоже, показатели функционирования системы антиоксидантной защиты организма коров, которым проводили лечение мастита, табл. 6.
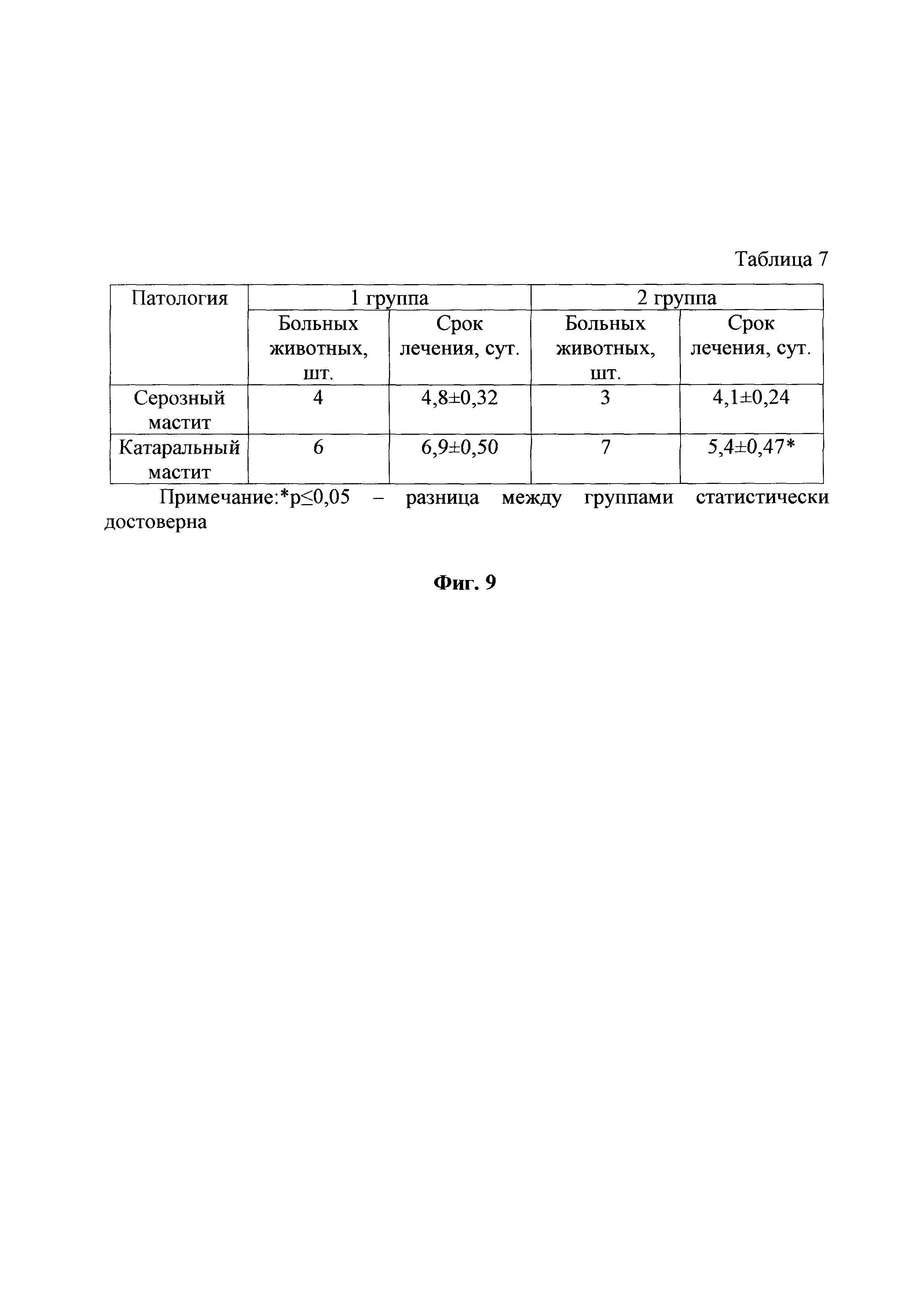
На фиг. 9, тоже, сроки лечения мастита у коров, табл. 7.
Раскрытие изобретения
Задачей изобретения является разработка антиоксидантного противовоспалительного препарата для животных, обладающего выраженным антиоксидантным и противовоспалительным действием, низкой токсичностью, высокой эффективностью в профилактике и лечении воспалительных заболеваний у животных; удобством введения и дозировки.
Технический результат, который может быть достигнут с помощью предлагаемого изобретения, сводится к выраженному антиоксидантному и противовоспалительному действию, низкой токсичности, высокой эффективности в профилактике и лечении воспалительных заболеваний у животных, удобству введения и дозировки.
Технический результат достигается с помощью антиоксидантного противовоспалительного препарата для животных, включающего этилметилгидроксипиридина сукцинат и нестероидное противовоспалительное средство, при этом он дополнительно содержит аскорбиновую кислоту, поливинилпирролидон и воду для инъекций, а в качестве нестероидного противовоспалительного средства используют флуниксина меглумин, при следующем соотношении компонентов в мас. %:
нестероидное противовоспалительное
средство, в качестве которого используют
Общим с заявленным препаратом является наличие в составе этилметилгидроксипиридина сукцината. Отличием от ближайшего аналога, заявляемого антиоксидантного противовоспалительного препарата для животных является содержание нестероидного противовоспалительного средства, в качестве которого используют флуниксин меглумин и присутствие дополнительно аскорбиновой кислоты, поливинилпирролидона и воды для инъекций, позволяющего достигать более высокого противовоспалительного эффекта, увеличить обезболивающий, жаропонижающий и антиоксидантный эффект, что дает возможность проводить более качественно и эффективно профилактику и лечение воспалительных заболеваний у животных.
Заявляемый антиоксидантный противовоспалительный препарат для животных представляет собой водный прозрачный раствор, без запаха, обладающий выраженным антиоксидантным, антигипоксическим, мембранопротекторным и противовоспалительным эффектом, обеспечивает жаропонижающее и обезболивающее действие, удобен в ведении и дозировании.
Воспаление остается одной из важнейших проблем общей патологии и клинической практики, так как представляет собой основной патогенетический компонент многих заболеваний различной этиологии (См. Сафарова М.И., Панфилова М.Н., Панков И.Ю. // Российский ветеринарный журнал. - 2013. - №2. - С. 36-38.).
Воспаление относится к числу наиболее распространенных типовых патологических процессов, протекающих в организме, и одновременно представляет собой важную защитно-приспособительную реакцию. Оно является центральной проблемой общей патологии на протяжении всей истории учения о болезни как процесс, лежащий в основе большинства заболеваний. Общие проявления воспаления включают лихорадку, реакции кроветворной ткани с развитием лейкоцитоза, повышение скорости оседания эритроцитов, ускорение тканевого метаболизма, измененную иммунологическую реактивность, явления интоксикации организма. Рассматривая воспаление, целесообразно коснуться симптома боли, так как практически всегда оба эти фактора сочетаются (См. Овсянникова Е.М., Коровина Н.А. // Медицинский совет. - 2014. - №6. - С. 35-39.).
Нестероидные противовоспалительные средства являются важнейшими симптоматическими лекарственными препаратами современности, которые за счет уникальной комбинации фармакологических свойств - противовоспалительных, анальгетических, жаропонижающих и антитромботических - применяются практически во всех областях медицины (См. Краснюк (мл.) И.И., Овсянникова Л.В., Степанова О.И., Беляцкая А.В., Краснюк И.И., Харитонов Ю.Я., Грих В.В., Кошелева Т.М., Король Л.А. // Разработка и регистрация лекарственных средств. - 2016. - №2 (15). - С. 40-44.).
Флуниксин (2-[[2-метил-3-(трифторметил)-фенил]амино]пиридин-3 карбоновая кислота) относится к нестероидным противовоспалительным, обезболивающим и жаропонижающим средствам, широко используемым в ветеринарии (См. Смирнова Т.Д., Штыков С.Н., Желобицкая Е.А., Сафарова М.И. // Журнал аналитической химии. - 2017. - Т. 72. - №5. - С. 481-485.). Он является одним из наиболее мощных нестероидных противовоспалительных средств и представляет собой действующее вещество, специально разработанное для ветеринарного применения. Ингибируя циклооксигеназу, в результате сокращая синтез простагландинов (медиаторов воспаления), флуниксин приводит к снижению температуры и уменьшению болевой чувствительности, что обеспечивает улучшение состояния животных. В отличие от других нестероидных противовоспалительных средств, в том числе кетопрофена, действие флуниксина отличается безопасностью, длительностью и проявляется при достаточно низких концентрациях в крови, что позволяет обеспечить его начальную противовоспалительную активность в течение 24-36 часов. (См. Сазонов А.А., Новикова С.В. // Молочное и мясное скотоводство. - 2015. - №4. - С. 37-40.).
Флуниксин меглумин угнетает синтез простагландинов Е2-медиаторов воспаления, что обуславливает его анальгезирующее, противовоспалительное, жаропонижающее и антитоксическое действие в отношении эндотоксинов бактерий (Порваткин И.В. Комплексная терапия с одной инъекции // Эффективное животноводство. 2016. №6 (127). С. 38.). В отличие от других нестероидных средств, фармакологическая активность флуниксина меглумина обеспечивается его невысокой концентрацией в крови, быстрым всасыванием и более длительным действием (См. Сафарова М.И., Панфилова М.Н., Панков И.Ю. // Российский ветеринарный журнал. - 2013. - №2. - С. 36-38.).
Окислительный стресс - часть неспецифической генерализованной реакции организма, развивающейся при действии на него повреждающих факторов физической или химической природы. Чрезмерная активация процессов свободнорадикального окисления приводит к развитию целого ряда патологических состояний организма человека и животных (См. Макеев А.А. // Сибирский вестник сельскохозяйственной науки. - 2010. - №2. - С. 69-75.).
Одной из основных причин развития в организме окислительного стресса является гиперпродукция активных форм кислорода, что приводит к разрушению клетки, воспалительным процессам, а на уровне целого организма - к развитию большого числа различных патологий. Цитокины являются ключевыми медиаторами воспаления и активируют синтез бактерицидных активных форм кислорода, для защиты, от действия которых у млекопитающих функционируют различные ферменты-антиоксиданты (каталазы, пероксидазы, супероксиддисмутазы и глутатионзависимые пероксидазы), роль которых состоит в дезактивации активных форм кислорода (См. Бунева В.Н., Блинова Е.А., Невинский Г.А. // Цитокины и воспаление. - 2010. - Т. 9. - №4. - С. 67-69.).
Основная масса воспалительных заболеваний связана с активацией процессов свободнорадикального окисления и перекисного окисления липидов как на местном уровне, так и на уровне целого организма. С другой стороны, длительная прооксидантная нагрузка на организм (стрессы, переохлаждение, перегревание, повышенный фон ультрафиолетового облучения, радиация, излучение и др.) приводит к напряжению в работе антиоксидантной системы, ее дисфункции и, как следствие, инициации неконтролируемых процессов свободнорадикального окисления (См. Мелконян К.И., Быков И.М., Павлюченко И.И., Белкина Н.В. // Кубанский научный медицинский вестник. - 2009. - №3. - С. 74-78.).
В настоящее время известна роль свободнорадикальных реакций перекисного окисления липидов в динамике раневого процесса. В условиях снижения активности системы антиоксидантной защиты гидроксильные радикалы запускают вторичные свободнорадикальные реакции пероксидации липидов мембран клеток не только в зоне раневого дефекта, но и в клетках перифокальной зоны. Процессы активации и элиминации продуктов перекисного окисления липидов неоднократно сменяют друг друга на различных стадиях раневого процесса. В результате наблюдается задержка развития последующих за воспалением фаз раневого процесса. Активация перекисного окисления липидов и снижение антиоксидантной защиты преобладают на этапах воспаления и образования грануляций (См. Олифирова О.С., Козка А.А. // Дальневосточный медицинский журнал. - 2015. - №2. - С. 21-23.).
В норме низкий уровень продукции радикалов-инициаторов и сбалансированная система антиоксидантной защиты приводит к тому, что скорость перекисного окисления клеточных мембран и липопротеидов плазмы крови является крайне малой. Однако в процессе возникновения и развития воспалительных заболеваний этот баланс нарушается. Поэтому применение антиоксидантов в качестве как средств лечения, так и препаратов профилактики данной патологии может иметь высокую эффективность (См. Кабанова А.А., Походенько-Чудакова И.О. // Проблемы здоровья и экологии. - 2010. - №1 (23). - С. 27-31.).
Пристальное внимание фармакологов в качестве перспективных лекарственных средств привлекли соединения гетероароматических фенолов, в частности производные 3-оксипиридина. Они относятся к простейшим гетероциклическим аналогам ароматических фенолов и в этой связи проявляют антиоксидантные и антирадикальные свойства. (См. Новиков В.Е., Лосенкова С.О. // Обзоры по клинической фармакологии и лекарственной терапии. - 2004. - Т. 3. - №1. - С. 2-14.).
2-этил-6-метил-3-гидроксипиридина сукцинат оригинальный отечественный синтетический антиоксидант и антигипоксант, обладающий высокой биологической активностью. (См. Черных И.В., Щулькин А.В., Гацанога М.В., Мыльников П.В. // Российский медико-биологический вестник им. академика И.П. Павлова. - 2015. №1. - С. 62-66.).
Наиболее ярким примером использования таких соединений является применение препарата «Мексидол». Мексидол состоит из 2-х связанных и функционально значимых соединений: 2-этил-6-метил-3-гидрокси-пиридина и сукцината (янтарной кислоты). Наличие 3-гидроксипиридина в структуре данного лекарственного средства обеспечивает комплекс его антиоксидантных и мембранотропных эффектов, способность уменьшать глутаматную эксайтотоксичность, модулировать функционирование рецепторов и ионных каналов, что принципиально отличает Мексидол от других препаратов, содержащих янтарную кислоту. Наличие сукцината в структуре препарата отличает его от других производных 3-гидроксипиридина, поскольку сукцинат функционально значим для многих процессов, протекающих в организме и, в частности, является субстратом для повышения энергетического обмена в клетке. Сочетание в структуре Мексидола двух соединений с уникальными свойствами обеспечивает его хорошую проходимость через гемато-энцефалический барьер, высокую биодоступность и воздействие на различные мишени, следствием чего являются широкий спектр эффектов препарата и высокий терапевтический потенциал. Мексидол - препарат с политаргетным механизмом действия и обладает широким спектром фармакологических эффектов. Он оказывает противоишемическое, нейропротекторное, противогипоксическое, ноотропное, вегетотропное, антистрессорное, анксиолитическое, противосудорожное и другие действия (См. Воронина Т.А. // Российский медицинский журнал. - 2016. - Т. 24. - №7. - С. 434-438).
Эффективным антиоксидантом, предохраняющим эндотелий сосудов от повреждающего действия супероксидных радикалов, является аскорбиновая кислота, которая может устранять толерантность к экзогенным донорам оксида азота и способна высвобождать оксид азота из эндогенных депо (См. Виноградова Т.А. // Журнал Гродненского государственного медицинского университета. - 2003. - №1 (1). - С. 52-58.).
Аскорбиновая кислота - антиоксидант, «фундамент физиологии человека». Благодаря дифенольной группе (-СОН= =СОН-) аскорбиновая кислота обладает сильно выраженными восстановительными свойствами и принимает активное участие в усвоении железа, регуляции углеводного обмена (через синтез триптофана), образовании стероидных гормонов, тормозит избыточную активность протеаз и амилазы поджелудочной железы, способствует накоплению гликогена в печени, усиливает детоксикационную функцию печени и др. Наиболее важными функциями аскорбиновой кислоты являются ее участие в реакциях окислительного фосфорилирования и регенерации убихинона для обеспечения дыхательной функции клеток, а также способность осуществлять репарацию тканей и стабилизацию стенок капилляров путем синтеза проколлагена и коллагена I, III типов (См. Тимен Л.Я., Мачнева Т.В., Трубицына И.Е., Чикунова Б.З. // Экспериментальная и клиническая гастроэнтерология. - 2013. - №5. - С. 89-92.).
Аскорбиновая кислота служит жизненно важным донором электронов. Она выступает в роли ко-фактора 8 ферментов, участвующих в гидроксилировании коллагена, биосинтезе карнитина и норадреналина, метаболизме тирозина и образовании пептидных гормонов. Поскольку аскорбиновая кислота является мощным водорастворимым антиоксидантом, ее концентрация в плазме снижается при патологических состояниях, связанных с острым или хроническим окислительным стрессом (См. Ишунина Т.А. // Фундаментальные и прикладные исследования: проблемы и результаты. - 2014. - №11. - С. 38-43.).
Большое внимание в специальной литературе отводится плазмозаменителям, из которых активнее всего использовался поливинилпирролидон. Препараты на основе поливинилпирролидона оказывают выраженное дезинтоксикационное действие, обусловленное его способностью связывать токсины и быстро выводить их из организма. Эти препараты обладают диуретическим свойством, усиливая почечный кровоток и клубочковую фильтрацию, увеличивают объем циркулирующей крови, что способствует улучшению микроциркуляции в капиллярах и ликвидации стаза эритроцитов. Благодаря своим свойствам препараты на основе поливинилпирролидона применяются при токсических формах острых желудочно-кишечных заболеваний (дизентерии, диспепсии, сальмонеллезе и др.), ожоговой болезни в стадии септикотоксемии, послеоперационной интоксикации, инфекционных заболеваниях, перитоните, сепсисе, гепатитах и других патологических процессах, которые сопровождаются интоксикацией (См. Фрисс С.А. // Медицинская экспертиза и право. - 2011. - №6. - С. 9-11.).
Поливинилпирролидон нашел широкое применение в медицинской практике благодаря своей хорошей растворимости в воде, отсутствию токсичности и высокой склонности к комплексообразованию (См. Сильковская Ф.П. // Химия N-винитпирролидона и его полимеров. - 1970. - С. 134).
Сущность получения антиоксидантного противовоспалительного препарата для животных заключается в следующем: исходные вещества в мас. %, а именно нестероидное противовоспалительное средство, в качестве которого служит флуниксина меглумин 6,0-8,0; этилметилгидроксипиридина сукцинат 10,0-20,0; аскорбиновую кислоту 6,0-8,0; поливинилпирролидон 4,0-6,0; воду для инъекций - остальное смешивают в асептических условиях и упаковывают.
Осуществление изобретения
Примеры конкретного выполнения получения и испытания антиоксидантного противовоспалительного препарата для животных.
Пример 1.
Антиоксидантный противовоспалительный препарат для животных готовят путем смешения компонентов в асептических условиях и растворения в воде для инъекций при следующем соотношении компонентов в мас. %:
нестероидное противовоспалительное
средство, в качестве которого используют
Полученный препарат при введении кроликам, у которых был экспериментально смоделирован воспалительный процесс, приводит к снижению концентрации С-реактивного белка в сыворотке крови на 27,1%, уменьшению скорости оседания эритроцитов на 17,6%, снижению количества лейкоцитов на 21,3%, а также способствовует увеличению активности глутатионпероксидазы - на 24,6%, но при этом произошло недостаточное повышение активности супероксиддисмутазы - всего на 7,1% и недостаточное уменьшение концентрации ТБК-активных продуктов, которая снизилась всего на 16,7%.
Пример 2.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
нестероидное противовоспалительное
средство, в качестве которого используют
Применение полученного препарата кроликам повлияло на уровень С-реактивного белка, который уменьшился на 36,2%, способствует снижению скорости оседания эритроцитов на 24,8% и уменьшению количества лейкоцитов на 32,7%, а также привел к повышению активности глутатионпероксидазы на 39,4% и увеличению активности супероксиддисмутазы на 26,9%. Концентрация ТБК-активных продуктов уменьшилась на 42,1% и находится в пределах физиологической нормы. В целом, наблюдается положительная динамика изменений биохимических и гематологических показателей.
Пример 3.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
нестероидное противовоспалительное
средство, в качестве которого используют
При введении полученного препарата кроликам отмечают, что уровень С-реактивного белка снизился на 40,1%, скорость оседания эритроцитов снизилась на 27,6%, количество лейкоцитов уменьшилось на 35,3%, активность супероксиддисмутазы увеличилась 31,0% и активность глутатионпероксидазы повысилась на 43,1%. Концентрация ТБК-активных продуктов при этом уменьшается на 44,7% и находится в пределах физиологической нормы. У животных наблюдается динамика гематологических и биохимических показателей, свидетельствующая о снижении интенсивности воспалительного процесса.
Пример 4.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
нестероидное противовоспалительное
средство, в качестве которого используют
Введение полученного препарата кроликам привело к уменьшению уровня С-реактивного белка на 38,4%, снижению скорости оседания эритроцитов на 26,3% и сокращению количества лейкоцитов на 33,5%. У кроликов под действием препарата увеличилась активность супероксиддисмутазы на 27,9% и повысилась активность глутатионпероксидазы на 40,2%. Уровень ТБК-активных продуктов уменьшился на 43,4%. Препарат положительно повлиял на динамику основных гематологических и биохимических показателей.
Пример 5.
Проводят аналогично примера 1, но берут следующее соотношение компонентов в мас. %:
нестероидное противовоспалительное
средство, в качестве которого используют
Полученный препарат был применен кроликам, в результате чего уровень С-реактивного белка снизился на 30,9%. Отмечено, что введение препарата способствует снижению скорости оседания эритроцитов на 19,6% и уменьшению концентрации лейкоцитов в крови на 24,8%. Активность глутатионпероксидазы у кроликов возросла после использования препарата на 38,6%, а активность супероксиддисмутазы - на 25,5% соответственно. В крови кроликов уменьшилась концентрация ТБК-активных продуктов на 38,9%. В целом на фоне положительной динамики гематологических и биохимических параметров можно отметить, что результат применения препарата в данном примере показал меньшую эффективность чем в примерах 2, 3 и 4, а также увеличилась себестоимость препарата в связи с повышением расхода основных компонентов.
Таким образом, наиболее оптимальными являются примеры 2, 3, 4, поскольку, в результате применения препарата кроликам, получают больший положительный эффект, заключающийся в уменьшении уровня С-реактивного белка в сыворотке крови - от 36,2% до 40,1%, сокращении скорости оседания эритроцитов - от 24,8% до 27,6%, уменьшении концентрации лейкоцитов в крови - от 32,7% до 35,3, увеличении активности глутатионпероксидазы - от 39,4% до 43,1%, повышении активности супероксиддисмутазы - от 26,9% до 31,0% и снижении концентрации ТБК-активных продуктов - от 42,1% до 44,7% соответственно. При осуществлении этих примеров отмечено положительное влияние введения препарата на основные гематологические и биохимические показатели крови, что подтверждается положительным эффектом, отразившемся на течении патологического процесса и клинической картине.
Пример 6.
Для проведения оценки антиоксидантного противовоспалительного препарата для животных на острую токсичность берут следующее соотношение компонентов в мас. %:
нестероидное противовоспалительное
средство, в качестве которого используют
Исследования по изучению острой токсичности антиоксидантного противовоспалительного препарата для животных проводят на белых лабораторных мышах и лабораторных крысах при однократном внутрижелудочном введении, что позволяет определить летальные дозы, классифицировать препарат по ГОСТ 12.1.007-76 и отнести его к 3 классу опасности «Вещества умеренно опасные» (фиг. 1, 2, 3).
Пример 7.
Эффективность антиоксидантного противовоспалительного препарата для животных изучают на коровах согласно примера 3, являющимся наиболее эффективным, который включает следующее соотношение компонентов в мас. %: нестероидное противовоспалительное средство, в качестве которого используют флуниксина меглумин - 7,0; этилметилгидроксипиридина сукцинат - 15,0; аскорбиновая кислота - 7,0; поливинилпирролидон - 5,0; вода для инъекций - остальное.
Суть эксперимента заключается в том, что его проводят в два этапа. При этом на первом этапе используют две группы стельных сухостойных коров черно-пестрой породы по десять животных в каждой, о сроках стельности судят по записям в журнале техника осеменатора. Коровам из первой группы вводят интрацистернально препарат «Септогель» (ООО «НИТА-ФАРМ», Россиия) двукратно сразу после запуска и сразу после отела в каждую четверть вымени в дозе 10 мл. Во второй группе коров, применяют схему профилактики мастита аналогично первой группе, но дополнительно за 7 суток до предполагаемого отела, за сутки до предполагаемого отела и сразу после отела коровам из второй группы применяют антиоксидантный противовоспалительный препарат для животных, по предлагаемому изобретению, для этого делают внутримышечные инъекции, из расчета 13,6 мг/кг (4 мл на 100 кг живой массы тела животного). На втором этапе исследования проводят с использованием коров черно-пестрой породы больных маститом, которых разделили на две группы по десять животных в каждой. Животным из первой группы итрацистернально вводят препарат «Септогель» сразу после постановки диагноза на мастит трехкратно с интервалом в 12 часов в дозе 10 мл в каждую четверть вымени. Коровам из второй группы проводили терапию аналогичную с первой группой, но дополнительно внутримышечно вводят антиоксидантный противовоспалительный препарат для животных по предлагаемому изобретению из расчета 13,6 мг/кг массы тела животного после постановки диагноза на мастит и через 24 часа. Кровь берут у животных из яремной вены за семь суток до предполагаемого отела, за трое суток до предполагаемого отела и в первые сутки, после отела. В крови и сыворотке, стабилизированной гепарином, определяют уровень гемоглобина, количество эритроцитов и лейкоцитов, скорость оседания эритроцитов, активность глутатионпероксидазы, уровень церулоплазмина, концентрацию продуктов перекисного окисления - диеновых конъюгатов и малонового диальдегида, по клиническим признакам и на основании результатов применения мастотеста проводят диагностику мастита.
На первом этапе эксперимента установлено, что при анализе динамики количества эритроцитов отмечается уменьшение их количества в крови подопытных коров после отела. При этом, в первой группе уменьшение было меньше чем во второй на 11,7% (фиг. 4). Уровень гемоглобина также уменьшился у всех животных после родов, но во второй группе коров данный показатель в завершении эксперимента на 6,2%. Уменьшение количества эритроцитов и уровня гемоглобина может быть связано с послеродовой постгеморрагической анемией.
Количество лейкоцитов у стельных сухостойных коров из обеих групп увеличивалось с приближением родов. Несмотря на то, что увеличение происходило у всех животных, во второй группе данный показатель был значительно ниже, чем в первой, разница за четверо суток до отела составляла 15,2%, а после родов была статистически достоверна и равнялась 25,4%. Скорость оседания эритроцитов (СОЭ) также значительно возросла после родов. При этом в первой группе она увеличилась в 2,2 раза, а во второй - на 29,8%. Разница между первой и второй группой была статистически достоверна и составляла 37,7%. Такая динамика количества лейкоцитов и скорости оседания эритроцитов свидетельствует о развитии воспалительного процесса в организме коров после отела, а достоверная разница между первой и второй группами говорит о выраженном противовоспалительном действии антиоксидантного противовоспалительного препарата для животных.
Уровень активности глутатионпероксидазы уменьшался и его снижение за последнюю неделю до отела составило 40,2% (фиг. 5). Во второй группе наоборот происходило увеличение, и разница относительно первой группы при этом была достоверна уже через трое суток после первого введения и составляла 20,4%, а после родов она была на уровне 45,4%. Уровень церулоплазмина повысился во второй группе и через трое суток после первого введения препаратов был достоверно выше, чем в первой группе на 37%. После родов, повышение по данному показателю отмечалось в обеих опытных группах животных, но несмотря на это во второй группе его значение было достоверно больше на 17,5% чем в первой группе. Увеличение активности ферментативного звена системы антиоксидантной защиты организма во второй группе повлекло за собой уменьшение концентрации продуктов перекисного окисления в крови коров. Так, концентрация диеновых конъюгатов в пробах крови коров из второй группы была достоверно ниже уже через трое суток после первого введения препаратов и составила 43,2%, а после родов также была значительной - на уровне 41,8% и статистически достоверной. В первой группе концентрация диеновых конъюгатов в крови увеличилась и значительно превышала верхние границы физиологической нормы. Аналогично концентрации диеновых конъюгатов во второй группе уменьшалась концентрация малонового диальдегида. Его уровень в крови коров, которым применяли антиоксидантный противовоспалительный препарат для животных, уменьшился и уже через трое суток после его введения и был достоверно меньше на 44,5% чем аналогичный показатель у коров из первой группы, а после родов наблюдалась достоверная разница в 41,4%. При этом, рассматривая динамику по данному показателю в первой группе, можно отметить его значительное повышение с приближением родов и поле отела. Таким образом, при анализе биохимических показателей видно, что токсикоз перед родами и воспалительная реакция после родов провоцируют депрессивное состояние ферментативного звена антиоксидантной защиты, что наряду с воспалением обусловливает увеличение концентрации продуктов перекисного окисления в организме коров. Применение антиоксидантного противовоспалительного препарата для животных, по предлагаемому изобретению, способствовало нормализации активности антиоксидантного фермента глутатионпероксидазы и тем самым обеспечивало уменьшение концентрации малонового диальдегида и диеновых конъюгатов в крови коров.
Рассматривая результаты клинического обследования коров, и применения мастотестов в первую неделю послеродового периода отмечено, что воспаление молочной железы регистрировали у 4 коров из десяти в первой группе, а во второй группе мастит зарегистрирован только у одной коровы (фиг. 6). Таким образом, установлено, что антиоксидантный противовоспалительный препарат для животных обладает выраженным антиоксидантным и противовоспалительным действием и профилактической эффективностью в предупреждении воспалительных заболеваний.
Рассматривая гематологические показатели коров больных маститом (фиг. 7) можно отметить, что уровень эритроцитов после отела был на уровне значений нижних границ физиологической нормы. В последующей динамике за 10 суток данный показатель увеличился в первой группе на 4%, а во второй группе - на 12% и в итоге был на 10,4% больше по завершении эксперимента, но при этом различия не имели статистической достоверности. Количество гемоглобина в течении 10 суток у коров из обоих групп увеличивалось постепенно и значимых отличий в итоговых цифрах не наблюдалось. Количество лейкоцитов в обеих группах после отела существенно превышал референтные показатели, но дальнейшая динамика, наблюдаемая в последующие 10 суток, была направлена на постепенное снижение по данному показателю. В результате, через 10 суток количество лейкоцитов в первой группе за опытный период снизилось на 21,95% и находилось на верхних границах физиологической нормы, а во второй группе за аналогичный промежуток времени уменьшение составило 38,2%. Таким образом, количество лейкоцитов в конце эксперимента во второй группе было меньше на 24,8% чем в первой группе, а разница была статистически достоверна. На момент введения препаратов в крови коров из обеих групп скорость оседания эритроцитов превышала верхнюю границу физиологической нормы более чем в два раза. По ходу проведения опыта значения данного параметра постепенно снижались, но во второй группе нормализация происходила значительно быстрее, на что указывала разница между группами, которая имела статистически значимые различия уже через 24 часа после начала лечения и сохранялась до конца эксперимента. В итоге через 10 суток после введения препаратов разница между первой и второй группами оставила 19,2%.
После отела у всех подопытных животных наблюдалась низкая активность глутатионпероксидазы в крови (фиг. 8). При этом, дальнейшая динамика по данному показателю в перовой и второй группе была неодинакова. Так, в первой группе за время проведения опыта активность глутатионпероксидазы уменьшилась на 12%, в то время как во второй группе она увеличилась на 14,8% соответственно. Через 10 суток после применения препаратов различия между группами были статистически достоверны и составили 20%. Уровень церулоплазмина в крови коров на протяжении опыта статистически достоверных различий между первой и второй группами не имел. Концентрация диеновых конъюгатов в пробах крови коров из обеих групп, полученных после отела, значительно превышала нормальные справочные значения. Применение антиоксидантного противовоспалительного препарата для животных во второй группе привело к значительному сокращению концентрации диеновых конюгатов, которая на момент завершения эксперимента была в данной группе на 26,9% меньше чем в первой группе при условии статистической достоверности различий. Уровень малонового диальдегида в крови также после отела был на много выше физиологической нормы. За время опыта нормализация по данному показателю произошла только во второй группе, чем обусловлены статистически достоверные различия по окончании эксперимента, которые составили 19,4%.
При клиническом исследовании животных, которое подтверждалось результатами применения экспресс-тестов, установлено, что сроки лечения серозного мастита во второй группе были меньше на 0,7 суток или 14,6% меньше чем в первой группе. Сроки лечения катарального мастита были также меньше во второй группе, причем эта разница была статистически достоверна и выразилась в 1,5 суток или 21,7% соответственно (фиг. 9). Таким образом, видно, что схема лечения, примененная во второй группе, обладала большей противовоспалительной эффективностью, что в итоге повлияло на сроки лечения коров.
Результаты проведенного эксперимента свидетельствуют о том, что применение антиоксидантного противовоспалительного препарата для животных является эффективным способом профилактики и лечения воспалительной патологии у животных. Происходит это за счет стимулирования активности ферментативного звена системы антиоксидантной защиты организма и обеспечения выраженного противовоспалительного эффекта.
Преимущества предлагаемого антиоксидантного противовоспалительного препарата для животных в том, что он содержит в комплексе нестероидное противовоспалительное средство, в качестве которого используют флуниксина меглумин, этилметилгидроксипиридина сукцинат, аскорбиновую кислоту, поливинилпирролидон и воду для инъекций, что значительно повышает его эффективность, а стабильный водный раствор, делает его удобным в дозировании и применении животным.
Предлагаемое изобретение по сравнению с прототипом и другими известными техническими решениями имеет следующие технические преимущества:
- повышение антиоксидантного действия;
- наиболее выраженный эффект детоксикации организма;
- повышенный противовоспалительный эффект;
- низкая токсичность;
- комплексное действие;
- удобство введения и дозирования;
- экономичен в использовании.
Реферат
Изобретение относится к ветеринарной фармации, в частности к антиоксидантным противовоспалительным препаратам для животных. Препарат содержит исходные вещества в мас. %, а именно нестероидное противовоспалительное средство, в качестве которого используют флуниксина меглумин 6,0-8,0; этилметилгидроксипиридина сукцинат 10,0-20,0; аскорбиновую кислоту 6,0-8,0; поливинилпирролидон 4,0-6,0; воду для инъекций – остальное. Изобретение обеспечивает выраженное антиоксидантное и противовоспалительное действие, низкую токсичность, высокую эффективность в профилактике и лечении воспалительных заболеваний у животных. 9 ил, 7 табл., 6 пр.

Комментарии