Сконструированные клетки, экспрессирующие множественные иммуномодуляторы, и их применения - RU2573912C2
Код документа: RU2573912C2
Чертежи


















































































Описание
ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет предварительной заявки США, номер 61/103,810, поданной 8 октября 2008 г., которая настоящим полностью включена в данную заявку посредством ссылки.
ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ, ПРИЛОЖЕННЫЙ В ЭЛЕКТРОННОМ ВИДЕ ПОСРЕДСТВОМ СИСТЕМЫ EFS-WEB
[0002] Содержание приложенного в электронном виде перечня последовательностей (название: sequence listing.ST25.txt; размер: 213102 байта; дата создания: 8 октября 2009 г.), поданного вместе с настоящей заявкой, полностью включено в данную заявку посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
Область техники
[0003] Настоящее изобретение относится к области генной терапии, направленной на лечение заболеваний и расстройств, таких как рак. В одном варианте реализации настоящее изобретение обеспечивает конструирование иммунных клеток или вспомогательных клеток для терапии (TSC) таким образом, чтобы они экспрессировали один или более иммуномодуляторов, и применение указанных клеток в качестве лекарственного средства.
Уровень техники
[0004] Интерлейкин-12 (IL-12) представляет собой член семейства цитокинов I типа, который участвует во множестве биологических процессов, включая защитный иммунный ответ и подавление онкогенеза, но не ограничивается ими (Abdi и др., 2006; Adorini, 1999; Adorini, 2001; Adorini и др., 2002; Adorini и др., 1996; Akhtar и др., 2004; Akiyama и др., 2000; Al-Mohanna и др., 2002; Aliberti и др., 1996; Allavena и др., 1994; Alii и Khar, 2004; Alzona и др., 1996; Amemiya и др., 2006; Araujo и др., 2001; Arulanandam и др., 1999; Athie и др., 2000; Athie-Morales и др., 2004; Bertagnolli и др., 1992; Bhardwaj и др., 1996; Biedermann и др., 2006; Brunda и Gately, 1994; Buchanan и др., 1995; Romani и др., 1997; Rothe и др., 1996; Satoskar и др., 2000; Schopfn др., 1999; Thomas и др., 2000; Tsung и др., 1997; Wolf и др., 1994; Yuminamochi и др., 2007). Все большее число полученных данных позволяет предположить, что IL-12 может представлять собой перспективную мишень для борьбы с заболеваниями человека (например, раком).
[0005] Несмотря на тот факт, что IL-12 остается перспективным агентом для терапии рака, благодаря наличию сильного вспомогательного действия на противоопухолевые клетки NK 1 типа, CD4+ Т-клетки и CD8+ Т-клетки (Trinchieri, 2003), описанная токсичность рекомбинантного IL-12 человека (rhIL-12) у пациентов (Atkins и др., 1997), а также ограниченное количество источников, из которых можно получить rhIL-12 со степенью чистоты, удовлетворяющей требованиям GMP для клинического применения, создают препятствия для успешного применения терапевтических подходов, основанных на IL-12. Таким образом, возможно геннотерапевтические подходы могут представлять собой более безопасные, более надежные варианты лечения. Действительно, в I фазе клинических испытаний введение рекомбинантной кДНК IL-12 на основе вируса внутрь опухоли или рядом с ней (Sangro и др., 2004; Triozzi и др., 2005) или плазмиды (Heinzeriing и др., 2005), или аутологических фибробластов, модифицированных геном IL-12 (Kang и др., 2001), оказалась безопасной и хорошо переносимой.
[0006] Тем не менее, объективные клинические ответы пациентов, страдающих меланомой или разнообразными формами карцином, которые получали данные геннотерапевтические средства, были редкими, переменными, временными и преимущественно сосредоточенными в месте введения лекарственного средства (Heinzeriing и др., 2005; Kang и др., 2001; Sangro и др., 2004; Triozzi и др., 2005). В случаях, когда наблюдалось частичное или полное излечение от заболевания, отмечали повышенную встречаемость инфильтрирующих опухоль лимфоцитов (Heinzeriing и др., 2005; Sangro и др., 2004) и повышенные уровни опухолеспецифических CD8+ Т-клеток в кровотоке (Heinzeriing и др., 2005), что согласуется с улучшенным примированием перекрестнореагирующим антигеном антигенспецифических Т-клеток у таких пациентов.
[0007] Поскольку примирование перекрестнореагирующим антигеном специфических Т-клеток лучше всего осуществляют дендритные клетки (DC), которые служат природным, хотя и регулируемым, источником IL-12 (Berard и др., 2000), недавние сообщения о превосходной доклинической эффективности основанной на дендритных клетках генной терапии IL-12 представляли огромный интерес (Satoh и др., 2002; Tatsumi и др., 2003; Yamanaka и др., 2002). Например, было показано, что внутриопухолевая (i.t.) инъекция DC, сконструированных таким образом, что они продуцировали IL-12p70 (путем инфекции рекомбинантным аденовирусом), приводит к значительному улучшению примирования перекрестнореагирующим антигеном набора опухолеспецифических CD8+ Т-клеток широкого спектра действия и к отторжению опухоли в моделях на мышах (Tatsumi и др., 2003). С учетом предыдущего применения рекомбинантного аденовируса, кодирующего mIL-12 под контролем промотора CMV (rAd.cIL12, (Tatsumi и др., 2003)), продуцирование IL-12 сконструированными DC было конститутивным, следовательно, иммунологическое действие данного цитокина, направленное сначала на повреждение опухоли, а затем на дренирующие опухоль лимфатические узлы, невозможно предугадать по отношению к результату терапии. Таким образом, существует потребность в DC, сконструированных для экспрессии IL-12 при определенных условиях, с целью регуляции как уровня экспрессии трансгена, так и момента активации трансгена. Настоящее изобретение обеспечивает многообещающий результат терапии при применении таких клеток.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0008] Настоящее изобретение обеспечивает рекомбинантный вектор, кодирующий белок (белки), обладающий (обладающие) функцией (функциями) одного или нескольких иммуномодуляторов, под контролем одного или нескольких промоторов. В одном варианте реализации настоящего изобретения, один или более промоторов являются промоторами, функционирующими при определенных условиях. В другом варианте реализации настоящего изобретения, один или более промоторов являются конститутивными. В другом варианте реализации настоящего изобретения, вектор представляет собой аденовирусный вектор, кодирующий белок (белки), экспрессия которого (которых) запускается промотором, который может быть активирован при определенных условиях путем обеспечения растворимого низкомолекулярного лиганда, такого как диацилгидразины (например, RG-115819, RG-115830 или RG-115932). Такой вектор позволяет контролировать экспрессию указанного белка (белков) иммунными клетками и TSC.
[0009] В одном варианте реализации, настоящее изобретение обеспечивает вектор для определяемой условиями экспрессии белка(белков), обладающего функцией (функциями) одного или нескольких иммуномодуляторов, содержащий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид, кодирующий генный переключатель, содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий один или более белков, обладающих функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимым фактором транскрипции. В одном варианте реализации настоящего изобретения, иммуномодулятор выбирают из IL-1, IL-2, IL-3, IL-4, IL-5, IL-7, IL-8, IL-9, IL-10R DN или его субъединицы, IL-15, IL-18, IL-21, IL-23, IL-24, IL-27, GM-CSF, IFN-альфа, IFN-гамма, CCL3 (MIP-1a), CCL5 (RANTES), CCL7 (МСР3), ХСL1 (лимфотактина), CXCL1 (MGSA-альфа), CCR7, CCL19 (MIP-3b), CXCL9 (MIG), CXCL10 (IP-10), CXCL12 (SDF-1), CCL21 (6Ckine), OX40L, 4-1BBL, CD40, CD70, GITRL, LIGHT, b-дефензина, HMGB1, Flt3L, IFN-бета, TNF-альфа, dnFADD, TGF-альфа, РНКи PD-L1, антисмыслового олигонуклеотида PD-L1, TGFbRII DN, ICOS-L и S100.
[00010] В другом варианте реализации, настоящее изобретение обеспечивает вектор для экспрессии белка (белков), обладающего функцией (функциями) одного или нескольких иммуномодуляторов, и белка, обладающего функцией IL-12, содержащий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий указанный белок(белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется лиганд-зависимым фактором транскрипции.
[00011] Настоящее изобретение дополнительно обеспечивает способ получения популяции клеток, например, иммунных клеток или TSC, экспрессирующих белок (белки), обладающие функцией (функциями) одного или нескольких иммуномодуляторов, путем модификации (например, трансфекции, электропорации и т.д.) указанных клеток рекомбинантным вектором, при определенных условиях экспрессирующим белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, при этом указанный вектор содержит полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий один или более белков, обладающих функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00012] В другом варианте реализации, настоящее изобретение обеспечивает способ получения популяции клеток, например, иммунных клеток или TSC, экспрессирующих белки, обладающие функцией (функциями) одного или нескольких иммуномодуляторов, и белок, обладающий функцией IL-12, путем модификации клеток рекомбинантным вектором, содержащим полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий указанный белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00013] Настоящее изобретение дополнительно обеспечивает популяцию клеток, например, иммунных клеток или TSC, экспрессирующих белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, которая была модифицирована (например, путем трансфекции, электропорации и т.д.) рекомбинантным вектором, при определенных условиях экспрессирующим белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, при этом указанный вектор содержит полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий один или более белков, обладающих функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00014] В другом варианте реализации, настоящее изобретение обеспечивает популяцию клеток, например, иммунных клеток или TSC, экспрессирующих белки, обладающие функцией(ями) одного или нескольких иммуномодуляторов, и белок, обладающий функцией IL-12, которая была модифицирована рекомбинантным вектором, включающим полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность . фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий указанный белок (белки), обладающий функцией (функциями) одного или нескольких иммуномодуляторов, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00015] В другом варианте реализации, настоящее изобретение обеспечивает композицию, содержащую две или более популяций клеток согласно настоящему изобретению, например, иммунных клеток или TSC, при этом каждая популяция клеток в указанной композиции экспрессирует один или более иммуномодуляторов, которые отличаются от одного или нескольких иммуномодуляторов, экспрессируемых другой популяцией (популяциями) клеток в указанной композиции. В одном варианте реализации, указанная композиция содержит две популяции клеток. В другом варианте реализации, композиция содержит более двух популяций клеток. В другом варианте реализации, композиция содержит три популяции клеток. В другом варианте реализации, композиция содержит четыре популяции клеток.
[00016] В другом варианте реализации, настоящее изобретение обеспечивает сконструированную in vitro клетку, например, иммунную клетку или TSC, содержащую вектор, включающий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий белок, обладающий функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимым фактором транскрипции. В другом варианте реализации, настоящее изобретение обеспечивает сконструированную in vitro клетку, например, иммунную клетку или TSC, содержащую вектор, включающий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий белок, обладающий функцией иммуномодулятора, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется указанным лиганд-зависимым фактором транскрипции.
[00017] В другом варианте реализации, настоящее изобретение обеспечивает композицию, содержащую две или более популяций сконструированных in vitro клеток, например, иммунных клеток или TSC, согласно настоящему изобретению, при этом каждая из популяций сконструированных in vitro клеток в композиции содержит вектор, содержащий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий белок, обладающий функцией иммуномодулятора, связанный с промотором, который активируется указанным лиганд-зависимьм фактором транскрипции, и при этом каждая популяция сконструированных in vitro клеток в композиции экспрессирует один или более иммуномодуляторов, которые отличаются от одного или нескольких иммуномодуляторов, экспрессируемых другой популяцией(ями) сконструированных in vitro клеток в указанной композиции. В одном варианте реализации, настоящее изобретение обеспечивает композицию, содержащую две или более популяций сконструированных т vitro клеток, например, иммунных клеток или TSC, при этом каждая из указанных популяций клеток содержит вектор, включающий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, функционально связанную с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, (2) полинуклеотид, кодирующий белок, обладающий функцией иммуномодулятора, и (3) полинуклеотид, кодирующий белок, обладающий функцией IL-12; при этом по меньшей мере один полинуклеотид из (2) и (3) связан с промотором, который активируется указанным лиганд-зависимым фактором транскрипции. В одном варианте реализации, указанная композиция содержит две популяции сконструированных in vitro клеток. В другом варианте реализации, композиция содержит более двух популяций сконструированных in vitro клеток. В другом варианте реализации, композиция содержит три популяции сконструированных in vitro клеток. В другом варианте реализации, композиция содержит четыре популяции сконструированных in vitro клеток.
[00018] Настоящее изобретение также обеспечивает фармацевтическую композицию, содержащую популяцию клеток, например, иммунных клеток или TSC, описанных в данной заявке.
[00019] В одном варианте реализации настоящего изобретения, полинуклеотид, кодирующий один или более белков, обладающих функциями иммуномодуляторов, находится под контролем промотора генного переключателя и полинуклеотид, кодирующий белок, обладающий функцией IL-12, находится под контролем конститутивного промотора. В другом варианте реализации настоящего изобретения, как полинуклеотид, кодирующий белок (белки), обладающий функцией иммуномодулятора(ов), так и полинуклеотид, кодирующий белок, обладающий функцией IL-12, находятся под контролем мультицистронного промотора генного переключателя. В другом варианте реализации настоящего изобретения, полинуклеотид, кодирующий белок (белки), обладающий функцией(ями) иммуномодулятора(ов), находится под контролем промотора генного переключателя и полинуклеотид, кодирующий белок, обладающий функцией IL-12, находится под контролем промотора, функционирующего в определенных условиях, который отличается от промотора генного переключателя. В дополнительном варианте реализации настоящего изобретения, система регуляции генов для полинуклеотида, кодирующего белок (белки), обладающий функцией(ями) иммуномодулятора(ов), и система регуляции генов для полинуклеотида, обладающего функцией IL-12, являются независимыми. В дополнительном варианте реализации настоящего изобретения, система регуляции генов для каждого полинуклеотида, кодирующего каждый белок, является независимой.
[00020] В одном варианте реализации, настоящее изобретение также обеспечивает лечение рака, такого как, меланомные опухоли, глиомные опухоли, рак почки и раки предстательной железы, а также раков, перечисленных в данной заявке в Таблице 1, но не ограничивается ими. Генотерапия IL-12 продемонстрировала противоопухолевую эффективность в исследованиях моделей на животных в виде вектора рекомбинантной кДНК (Faure и др., 1998; Sangro и др., 2005), но даже более того, в контексте генномодифицированных дендритных клеток (Satoh и др., 2002; Svane и др., 1999; Tatsumi и др., 2003; Yamanaka и др., 2002). На сегодняшний день, тем не менее, I фаза клинических испытаний на человеке генотерапии IL-12 с внедрением плазмид или вирусных векторов не позволила достигнуть длительных, объективных клинических ответов для лечения рака (Heinzerling и др., 2005; Kang и др., 2001; Sangro и др., 2004; Triozzi и др., 2005). Генотерапия, описанная в данной заявке, обеспечивает многообещающее терапевтическое воздействие.
[00021] В одном варианте реализации, настоящее изобретение обеспечивает способ лечения опухоли у млекопитающего, включающий следующие этапы:
(a) введение в микроокружение опухоли популяции иммунных клеток или TSC, которые сконструированы in vitro таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора; и
(b) введение указанному млекопитающему терапевтически эффективного количества активирующего лиганда;
вызывая тем самым экспрессию белка, обладающего функцией иммуномодулятора, и лечение указанной опухоли.
[00022] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения опухоли у млекопитающего, включающий следующие этапы:
(a) введение в микроокружение опухоли двух или более популяций иммунных клеток или TSC, которые сконструированы in vitro таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, при этом каждая популяция иммунных клеток или TSC экспрессирует различный набор одного или нескольких иммуномодуляторов; и
(b) введение указанному млекопитающему терапевтически эффективного количества одного или нескольких активирующих лигандов;
вызывая тем самым экспрессию белков, обладающих функциями иммуномодуляторов, и лечение указанной опухоли.
[00023] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения опухоли у млекопитающего, включающий следующие этапы:
(a) введение в микроокружение опухоли популяции иммунных клеток или TSC, которые сконструированы in vitro таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и белок, обладающий функцией IL-12, при этом по меньшей мере один из белков, обладающих функцией иммуномодулятора или IL-12, находится под контролем функционирующего при определенных условиях промотора, который активируется лигандом; и
(b) введение указанному млекопитающему терапевтически эффективного количества активирующего лиганда;
вызывая тем самым экспрессию белка, обладающего функцией иммуномодулятора, и/или белка, обладающего функцией IL-12, и лечение указанной опухоли.
[00024] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения опухоли у млекопитающего, включающий следующие этапы:
(a) введение в микроокружение опухоли двух или более популяций иммунных клеток или TSC, которые сконструированы in vitro таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и белок, обладающий функцией IL-12, при этом каждая популяция иммунных клеток или TSC экспрессирует различный набор одного или нескольких белков, обладающих функцией иммуномодулятора, при этом по меньшей мере один из белков, обладающих функцией иммуномодулятора или IL-12, находится под контролем функционирующего при определенных условиях промотора, который активируется лигандом; и
(b) введение указанному млекопитающему терапевтически эффективного количества одного или нескольких активирующих лигандов;
вызывая тем самым экспрессию белка, обладающего функциями иммуномодуляторов, и/или белка, обладающего функцией IL-12, и лечение указанной опухоли.
[00025] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения заболевания или расстройства у млекопитающего, включающий следующие этапы:
(a) введение указанному млекопитающему популяции модифицированных клеток, которые модифицированы таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора; и
(b) введение указанному млекопитающему терапевтически эффективного количества активирующего лиганда;
вызывая тем самым экспрессию белка, обладающего функцией иммуномодулятора, и лечение указанного заболевания или расстройства.
[00026] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения заболевания или расстройства у млекопитающего, включающий следующие этапы:
(a) введение указанному млекопитающему двух или более популяций модифицированных клеток, которые модифицированы таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, при этом каждая популяция модифицированных клеток экспрессирует различный набор одного или нескольких иммуномодуляторов; и
(b) введение указанному млекопитающему терапевтически эффективного количества одного или нескольких активирующих лигандов;
вызывая тем самым экспрессию белков, обладающих функциями иммуномодуляторов, и лечение указанного заболевания или расстройства.
[00027] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения заболевания или расстройства у млекопитающего, включающий следующие этапы:
(a) введение указанному млекопитающему популяции модифицированных клеток, которые модифицированы таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и белок, обладающий функцией IL-12, при этом по меньшей мере один из белков, обладающих функцией иммуномодулятора или IL-12, находится под контролем функционирующего при определенных условиях промотора, который активируется лигандом; и
(b) введение указанному млекопитающему терапевтически эффективного количества активирующего лиганда;
вызывая тем самым экспрессию белка, обладающего функцией иммуномодулятора, и/или белка, обладающего функцией IL-12, и лечение указанного заболевания или расстройства.
[00028] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения заболевания или расстройства у млекопитающего, включающий следующие этапы:
(а) введение указанному млекопитающему двух или более популяций модифицированных клеток, которые модифицированы таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и белок, обладающий функцией IL-12, при этом каждая популяция модифицированных клеток экспрессирует различный набор одного или нескольких белков, обладающих функцией иммуномодулятора, при этом по меньшей мере один из белков, обладающих функцией иммуномодулятора или IL-12, находится под контролем функционирующего при определенных условиях промотора, который активируется лигандом; и
(b) введение указанному млекопитающему терапевтически эффективного количества одного или нескольких активирующих лигандов;
вызывая тем самым экспрессию белка, обладающего функциями иммуномодуляторов, и/или белка, обладающего функцией IL-12, и лечение указанного заболевания или расстройства.
[00029] Настоящее изобретение также обеспечивает способ определения эффективности терапии, основанной на сконструированной клетке, например, иммунной клетке или TSC, путем измерения уровня экспрессии или активности IFN-гамма у пациента перед началом терапии, таким образом получая контрольный уровень, затем введения клеток, сконструированных таким образом, что они экспрессируют один или более белков, обладающих функцией иммуномодулятора, и возможно белок, обладающий функцией IL-12, введения эффективного количества активирующего лиганда, а затем измерения уровня экспрессии IFN-гамма, чтобы получить тестовый уровень, и сравнения контрольного уровня с тестовым уровнем, чтобы определить, является ли схема лечения эффективной.
[00030] В одном варианте реализации, настоящее изобретение обеспечивает способ определения эффективности для пациента схемы лечения, основанной на сконструированной in vitro клетке, например, иммунной клетке или TSC, включающий:
(а) измерение уровня экспрессии, или уровня активности, или обоих уровней для интерферона-гамма (IFN-гамма) в первом биологическом образце, полученном из указанного пациента, нуждающегося в лечении, перед введением сконструированных in vitro клеток, таким образом получая контрольный уровень;
(b) введение пациенту, нуждающемуся в этом, сконструированных in vitro клеток, полученных таким образом, что они при определенных условиях экспрессируют один или более белков, обладающих функцией иммуномодулятора, и возможно белок, обладающий функцией IL-12;
(c) введение указанному пациенту, нуждающемуся в этом, эффективного количества активирующего лиганда;
(d) измерение уровня экспрессии, или уровня активности, или обоих уровней IFN-гамма во втором биологическом образце, полученном от указанного пациента, нуждающегося в лечении, после введения сконструированных in vitro иммунных клеток и активирующего лиганда, таким образом получая тестовый уровень; и
(e) сравнение контрольного уровня с тестовым уровнем IFN-гамма, при этом повышение тестового уровня экспрессии, активности или обоих уровней IFN-гамма относительно контрольного уровня указывает на то, что указанная схема лечения эффективна для указанного нуждающегося в лечении пациента.
ПОДРОБНОЕ ОПИСАНИЕ ФИГУР
[00031] На Фиг.1 показана карта плазмиды для системы экспрессии с регулируемого промотора для бицистронного транскрипта, кодирующего hIL-12.
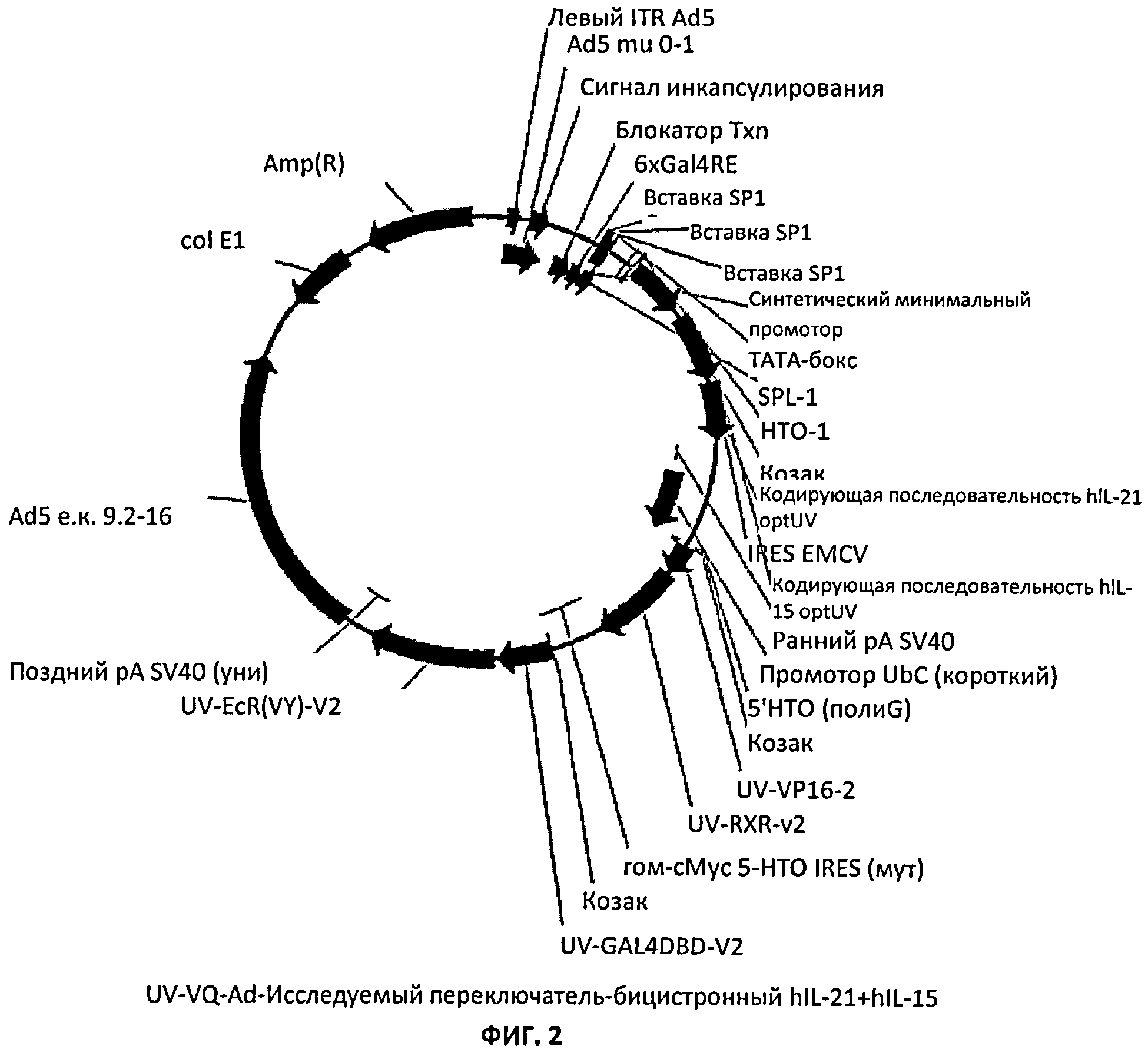
[00032] На Фиг.2 показана карта плазмиды для системы экспрессии с регулируемого промотора для бицистронного транскрипта, кодирующего hIL-21 и hIL-15.
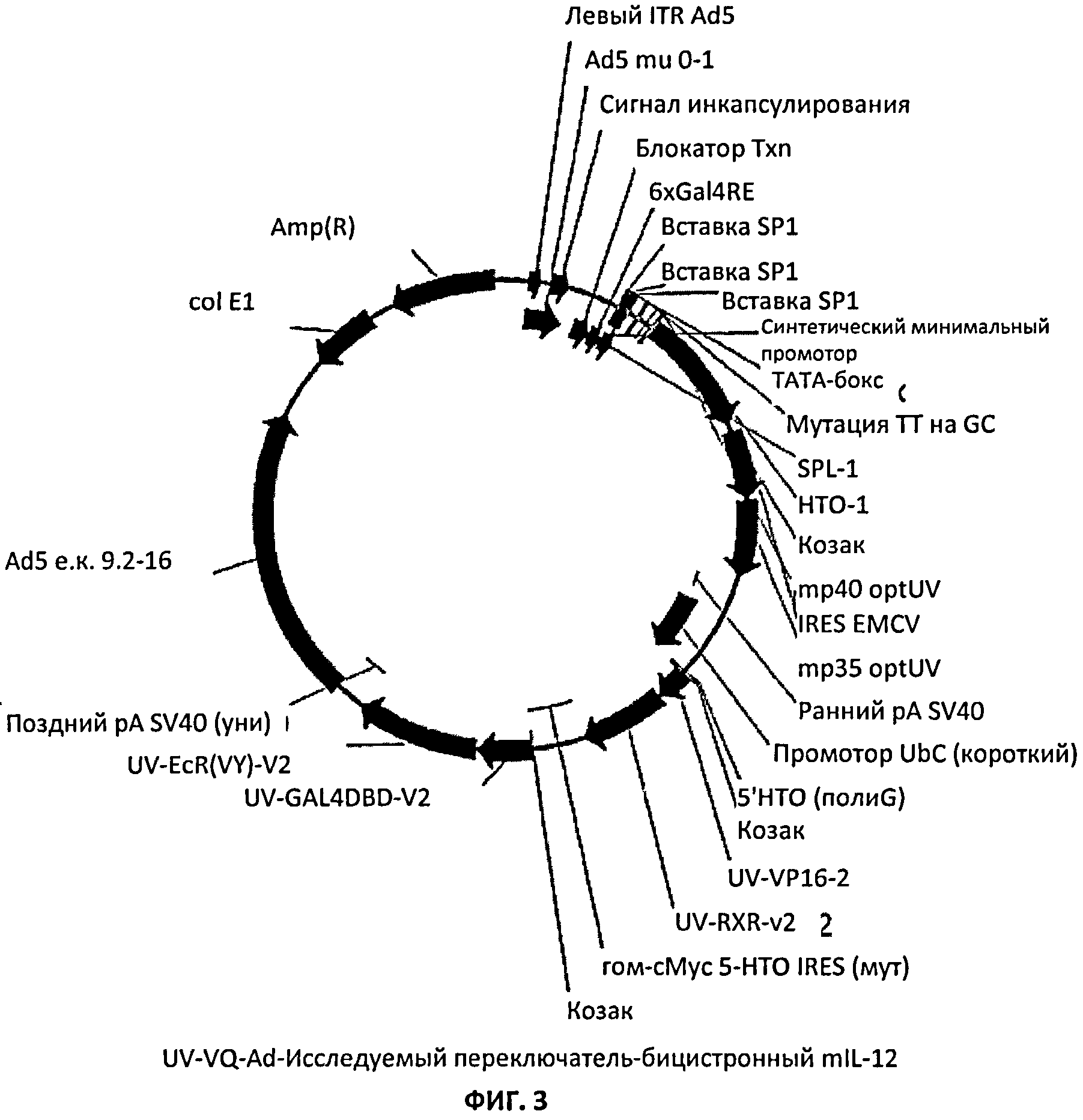
[00033] На Фиг.3 показана карта плазмиды для системы экспрессии с регулируемого промотора для бицистронного транскрипта, кодирующего mIL-12.
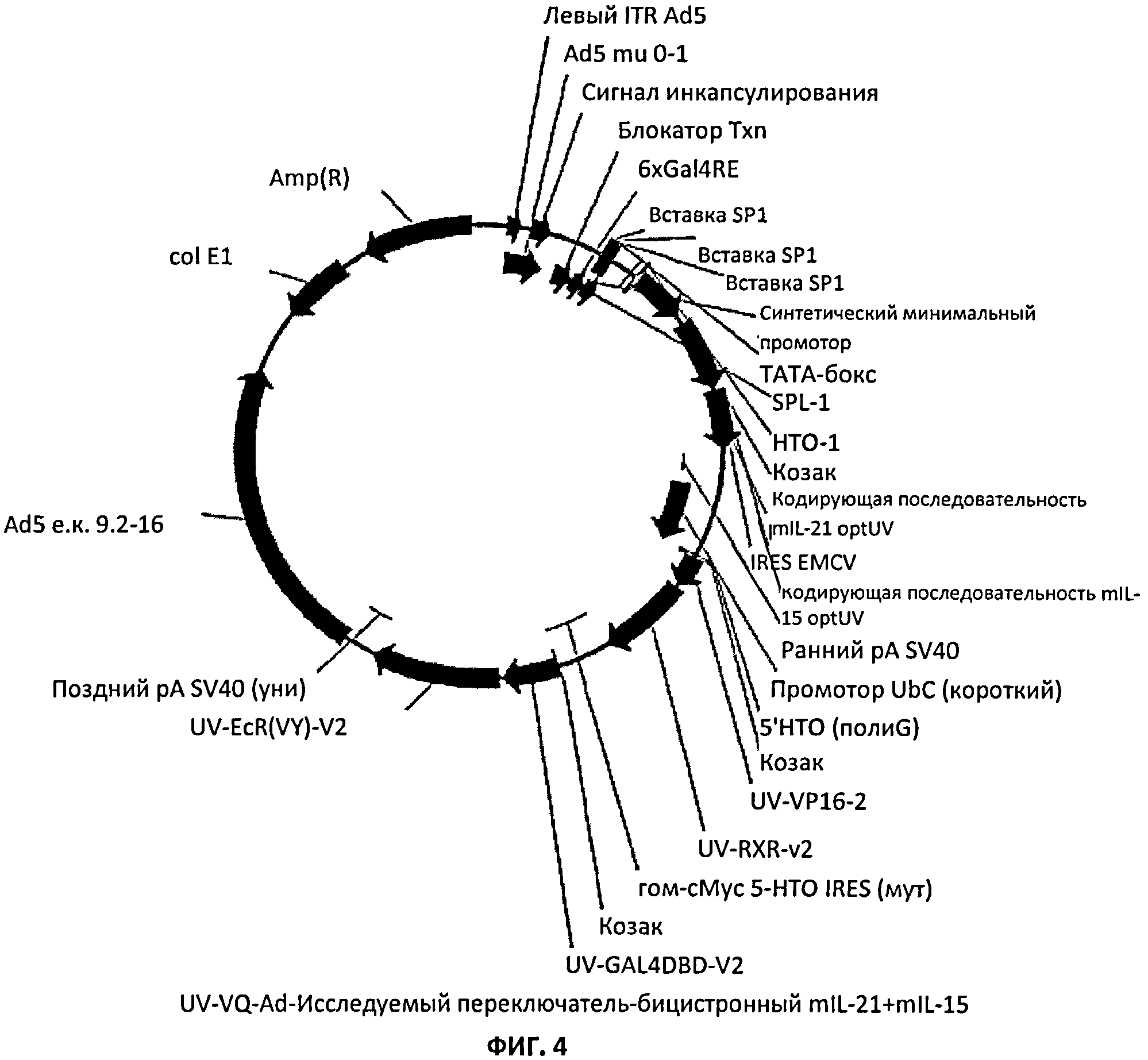
[00034] На Фиг.4 показана карта плазмиды для системы экспрессии с регулируемого промотора для бицистронного транскрипта, кодирующего mIL-21 и mIL-15.
[00035] На Фиг.5 показана карта плазмиды для системы экспрессии с регулируемого промотора hIL-21.
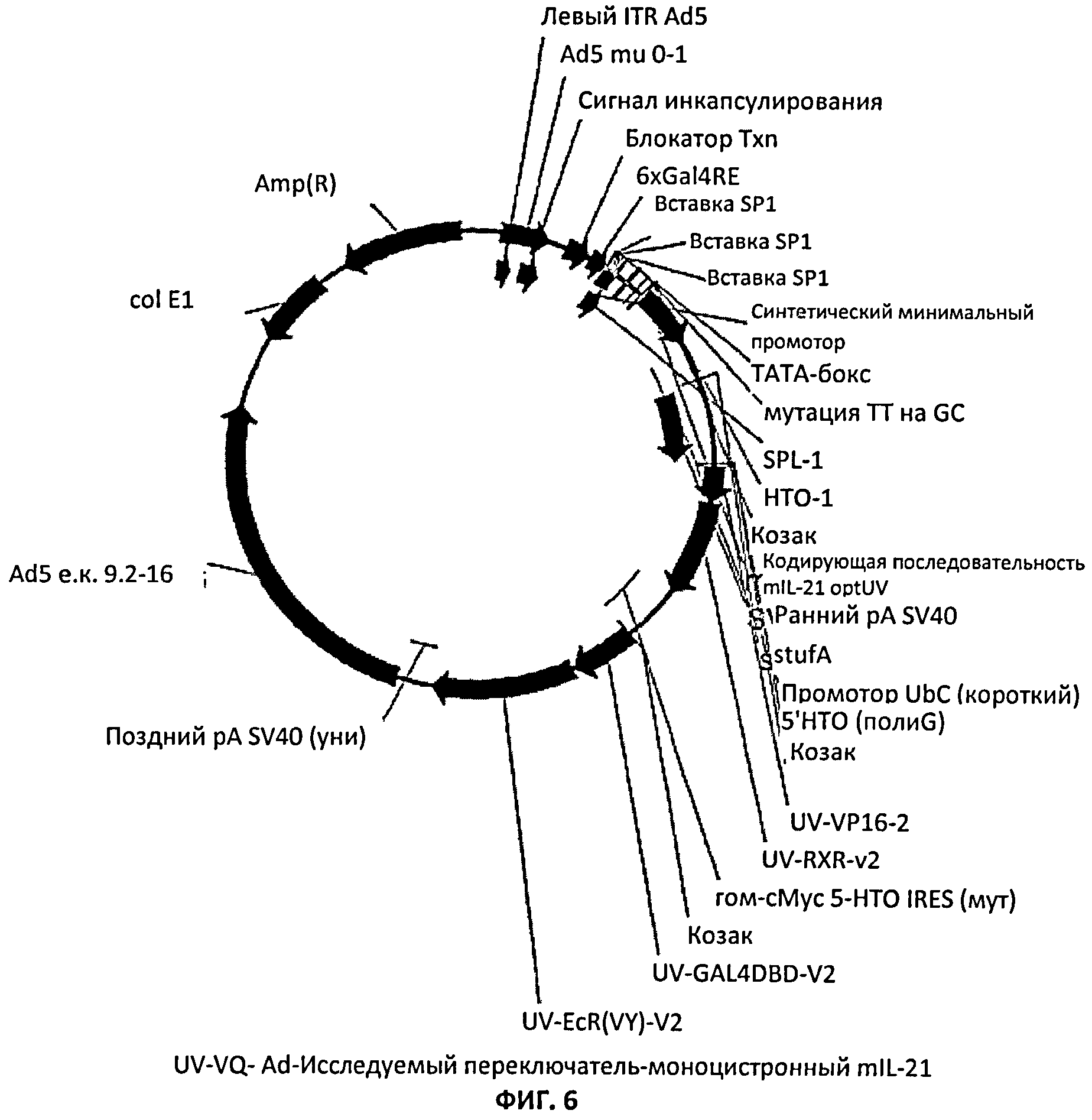
[00036] На Фиг.6 показана карта плазмиды для системы экспрессии с регулируемого промотора mIL-21.
[00037] На Фиг.7 показана карта плазмиды для системы экспрессии с регулируемого промотора трицистронного транскрипта, кодирующего hIL-12 и hIL-21.
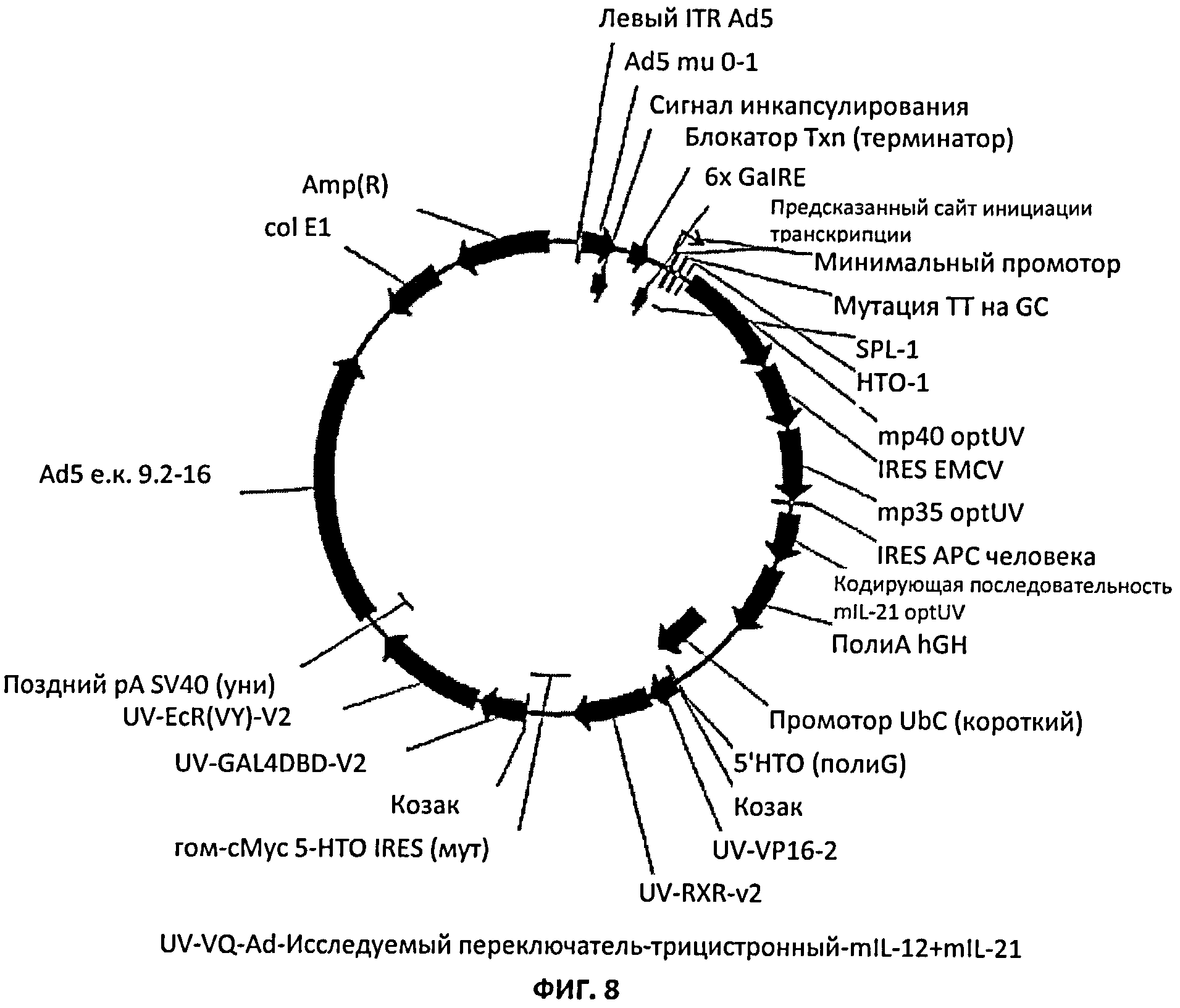
[00038] На Фиг.8 показана карта плазмиды для системы экспрессии с регулируемого промотора трицистронного транскрипта, кодирующего mIL-12 и mIL-21.
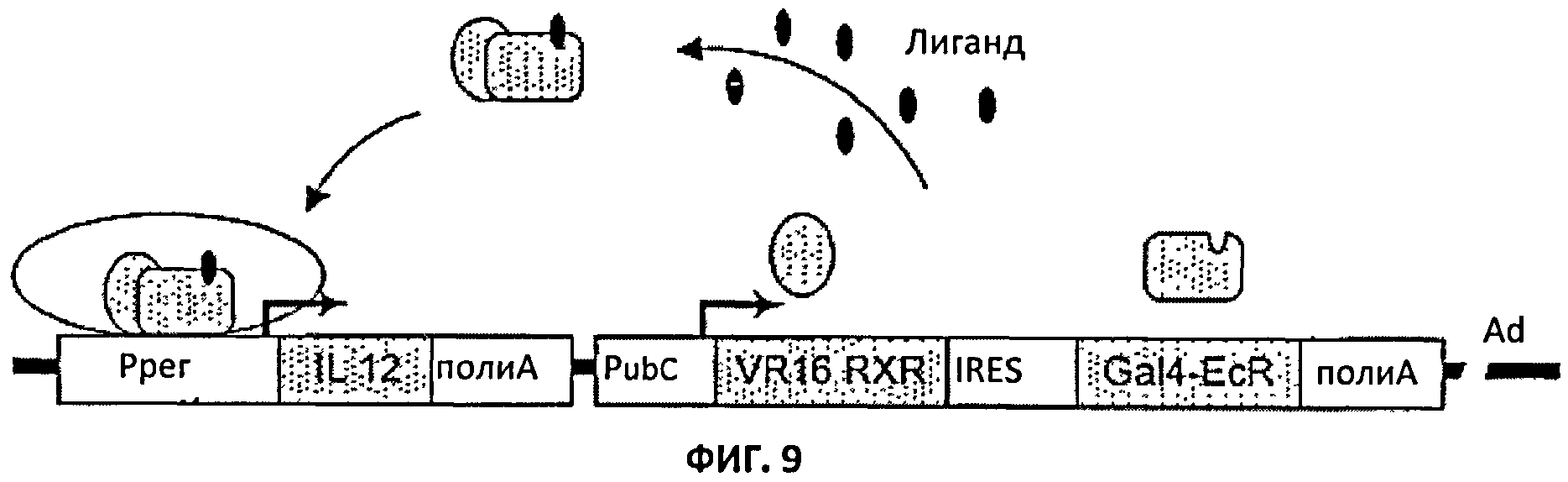
[00039] На Фиг.9 показана структура вектора rAd.RheoIL12, в котором участки Е1 и Е3 были удалены и участок Е1 был заменен на компоненты терапевтической системы RheoSwitch® Therapeutic System (RTS)-IL-12. Прямоугольник с надписью "IL12" представляет собой последовательности, кодирующие IL-12p40 и IL-12p35, разделенные участком внутренней посадки рибосомы (IRES).
ПОДРОБНОЕ ОПИСАНИЕ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Иммуномодуляторы
Цитокины
[00040] Полинуклеотидные последовательности интерлейкина 1 (IL-1), который представляет собой цитокин, важный для воспалительного ответа на инфекцию, доступны в открытых базах данных под номерами доступа: М28983 (IL-1α человека); М15330 (IL-1β человека); AF201830 (IL-1δ человека); AF201831 (IL-1ε человека); AF201832 (1L-1ζ человека); AF201833 (IL-1η человека); NM_010554 (IL-1α мыши); NM_008361 (IL-1β мыши); NM_019451 (L-1δ мыши); NM_019450 (IL-1f6 мыши); NM_027163 (IL-1f8 мыши); NM_53511 (IL-1f9 мыши); NM_204524 (IL-1β цыпленка); NM_017019 (IL-1α крысы) и NM_031512 (IL-1β крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00041] Последовательности аминокислот интерлейкина 1 (IL-1) доступны в открытых базах данных под номерами доступа ААА59134 (IL-1α человека); ААА59135 (IL-1β человека); AAF25210 (IL-1δ человека); AAF25211 (IL-1ε человека); AAF25212 (1L-1ζ человека); AAF25213 (IL-1η человека); NP_034684 (IL-1α мыши); NP_032387 (IL-1β мыши); NP_062324 (L-1δ мыши ); NP_062323 (IL-1f6 мыши); NP_081439 (IL-1f8 мыши); NP_705731 (IL-1f9 мыши); NP_989855 (IL-1β цыпленка); NP_058715 (IL-1α крысы) и NP_113700 (IL-1β крысы), перечисленные последовательности включены в настоящее описание посредством ссылки. Laurent и др., Psychiatr. Genet. 7: 103 (1997) обнаружили полиморфные мутации в гене интерлейкина-1-бета человека.
[00042] Полинуклеотидные последовательности интерлейкина 2 (IL-2), который принадлежит к семейству цитокинов, включающему IL-4, IL-7, IL-9, IL-15 и IL-21, доступны в открытых базах данных под номерами доступа U25676 (человека); NM_008366 (мыши); NM_204153 (цыпленка) и NM_053836 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00043] Последовательности аминокислот интерлейкина 2 (IL-2) доступны в открытых базах данных под номерами доступа ААА70092 (человека); NP_032392 (мыши); NP_989484 (цыпленка) и NP_446288 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00044] Liu и др., Appl. Biochem. Biotechnol. 133: 77 (2006) сконструировали мутантный IL-2 человека, a Lorberboum и др., J. Biol. Chem. 265: 16311 (1990) описали конструирование химерного IL-2.
[00045] Полинуклеотидные последовательности интерлейкина 4 (IL-4), который представляет собой цитокин, который вызывает дифференцировку наивных хелперных Т-клеток в клетки Th2, доступны в открытых базах данных под номерами доступа М23442 (человека); NM_021283 (мыши); NM_001007079 (цыпленка) и NM_201270 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00046] Последовательности аминокислот интерлейкина 4 (IL-4) доступны в открытых базах данных под номерами доступа ААА59150 (человека); NP_067258 (мыши); NP_001007080 (цыпленка) и NP_958427 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00047] Kawashima и др., J. Med. Genet. 35: 502 (1998) описывают полиморфизмы в гене IL-4, которые связаны с атопическим дерматитом.
[00048] Интерлейкин 7 (IL-7) представляет собой цитокин, важный для развития В- и Т-клеток. Полинуклеотидные последовательности IL-7 доступны в открытых базах данных под номерами доступа J04156 (человека); NM_008371 (мыши); NM_001037833 (цыпленка) и NM_013110 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00049] Последовательности аминокислот интерлейкина 7 (IL-7) доступны в открытых базах данных под номерами доступа ААА59156 (человека); NP_032397 (мыши); NP_001032922 (цыпленка) и NP_037242 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00050] Feng и др., Genetics 175:545 (2007) обнаружил точечные мутации в IL-7, которые приводят к функциональному дефекту IL-7.
[00051] Интерлейкин 9 (IL-9) представляет собой цитокин, продуцируемый Т-клетками, и является регулятором гематопоэтических клеток. Полинуклеотидные последовательности IL-9 доступны в открытых базах данных под номерами доступа NM_000590 (человека); NM_008373 (мыши); NM_001037825 (цыпленка) и NM_001105747 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00052] Последовательности аминокислот интерлейкина 9 (IL-9) доступны в открытых базах данных под номерами доступа NP_000581 (человека); NP_032399 (мыши); NP_001032914 (цыпленка) и NP_001099217 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00053] IL-12 представляет собой цитокин, который может действовать как фактор роста для активированных Т- и NK-клеток, повышать литическую активность NK/лимфокин- активированных клеток-киллеров и стимулировать продукцию IFN-гамма покоящимися мононуклеарными клетками периферической крови (РВМС). Полинуклеотидные последовательности IL-12 доступны в открытых базах данных под номерами доступа NM_000882 (IL12A человека); NM_002187 (IL12B человека); NM_008351 (IL12a мыши); NM_008352 (IL12b мыши); NM_213588 (IL12A цыпленка); NM_213571 (IL12B цыпленка); NM_053390 (IL12a крысы) и NM_022611 (IL12b крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00054] Последовательности аминокислот интерлейкина 12 (IL-12) доступны в открытых базах данных под номерами доступа NP_000873 (IL12A человека); NP_002178 (IL12B человека); NP_032377 (IL12a мыши); NP_032378 (IL12b мыши); NP_998753 (IL12A цыпленка); NP_998736 (IL12B цыпленка); NP_445842 (IL12a крысы) и NP_072133 (IL12b крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00055] Интерлейкин 15 (IL-15) представляет собой цитокин, который регулирует активацию и пролиферацию Т-клеток и клеток естественных киллеров. Полинуклеотидные последовательности IL-15 доступны в открытых базах данных под номерами доступа U14407 (человека); NM_008357 (мыши); EU334509 (цыпленка) и AF015719 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00056] Последовательности аминокислот интерлейкина 15 (IL-15) доступны в открытых базах данных под номерами доступа ААА21551 (человека); NP_032383 (мыши); ABY55312 (цыпленка) и ААВ94536 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00057] Интерлейкин 18 (IL-18), цитокин, продуцируемый макрофагом, который вместе с интерлейкином 12 вызывает клеточно-опосредованный иммунитет после инфекции микробными продуктами. Полинуклеотидные последовательности IL-18 доступны в открытых базах данных под номерами доступа U90434 (человека); NM_008360 (мыши); EU747333 (цыпленка) и AY258448 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00058] Последовательности аминокислот интерлейкина 18 (IL-18) доступны в открытых базах данных под номерами доступа ААВ50010 (человека); NP_032386 (мыши); АСЕ79188 (цыпленка) и ААР14669 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00059] Полинуклеотидные последовательности интерлейкина 21 (IL-21), который представляет собой цитокин, который оказывает сильное регуляторное действие на клетки иммунной системы, включая клетки - естественные киллеры и цитотоксические Т-клетки, путем индукции пролиферации клеток, доступны в открытых базах данных под номерами доступа AF254069 (человека); NM_021782 (мыши); NM_001024835 (цыпленка) и NM_001108943 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00060] Последовательности аминокислот интерлейкина 21 (IL-21) доступны в открытых базах данных под номерами доступа, AAG29348 (человека); NP_068554 (мыши); NP_001020006 (цыпленка) и NP_001102413 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00061] Интерлейкин 27 (IL-27) представляет собой цитокин, который играет важную роль в регуляции активности В- и Т-лимфоцитов. Полинуклеотидные последовательности IL-27 доступны в открытых базах данных под номерами доступа AY099296 (человека); NM_145636 (мыши) и ХМ_344962 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00062] Последовательности аминокислот интерлейкина 27 (IL-27) доступны в открытых базах данных под номерами доступа ААМ34498 (человека); NP_663611 (мыши) и ХР_344963 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00063] Полинуклеотидные последовательности интерферона бета-1 (IFNB1), который представляет собой член группы белков-интерферонов, которые связываются с определенными рецепторами на поверхности клетки (IFNAR) и стимулируют как макрофаги, так и клетки - естественные киллеры (NK), чтобы вызвать противовирусный ответ, доступны в открытых базах данных под номерами доступа NM_002176 (человека); NM_010510 (мыши); NM_00102483 6 (цыпленка) и NM_019127 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00064] Последовательности аминокислот интерферона бета 1 (IFNB1) доступны в открытых базах данных под номерами доступа NP_002167 (человека); NP_034640 (мыши); NP_001020007 (цыпленка) и NP_062000 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00065] Интерферон гамма (IFN-гамма) представляет собой растворимый цитокин, который представляет собой единственный интерферон II типа и проявляет противовирусную, иммунорегуляторную и противоопухолевую активность. Полинуклеотидные последовательности IFN-гамма доступны в открытых базах данных под номерами доступа NM_000619 (человека); NM_008337 (мыши) и NM_138880 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00066] Последовательности аминокислот интерферона гамма (IFN-гамма) доступны в открытых базах данных под номерами доступа NP_000610 (человека); NP_032363 (мыши) и NP_620235 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00067] Полинуклеотидные последовательности фактора некроза опухоли (TNF-альфа), который представляет собой многофункциональный провоспалительный цитокин, секретируемый преимущественно моноцитами/макрофагами, который влияет на метаболизм липидов, коагуляцию, устойчивость к инсулину и эндотелиальную функцию, доступны в открытых базах данных под номерами доступа Х02910 (человека); NM_013693 (мыши) и ВС107671 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00068] Последовательности аминокислот TNF-альфа доступны в открытых базах данных под номерами доступа САА26669 (человека); NP_038721 (мыши) и AAI07672 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
Хемокины
[00069] Хемокиновый (С-мотив) лиганд 1 (XCL1, также известный как лимфотактин) является хемотаксическим для CD4+ и CD8+ Т-клеток, но не для моноцитов, и индуцирует повышение количества внутриклеточного кальция в лимфоцитах периферической крови. Полинуклеотидные последовательности XCL1 доступны в открытых базах данных под номерами доступа NM_002995 (человека); NM_008510 (мыши) и NM_134361 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00070] Последовательности аминокислот XCL1 доступны в открытых базах данных под номерами доступа NP_002986 (человека); NP_032536 (мыши) и NP_599188 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки. В патенте США номер 6,022,534 описан лимфотактин и его применение для привлечения цитотоксических Т-клеток и/или NK-клеток, и/или для индукции пролиферации резидентных клеток. В указанном патенте также описаны способы получения и применения антитела против лимфотактина и слитого белка XCL1.
[00071] Полинуклеотидные последовательности СС хемокинового лиганда 3 (CCL3), также известного как воспалительный белок макрофагов-1 (MIP-1), который также называют монокином (тип цитокина, продуцируемого главным образом моноцитами и макрофагами), который участвует в состоянии острого воспаления в привлечении и активации полиморфоядерных лейкоцитов, доступны в открытых базах данных под номерами доступа NM_002983 (человека); NM_011337 (мыши) и NM_013025 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00072] Последовательности аминокислот CCL3 доступны в открытых базах данных под номерами доступа NP_002974 (человека); NP_035467 (мыши) и NP_037157 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00073] Полинуклеотидные последовательности CCL5 (RANTES), который представляет собой провоспалительный цитокин, участвующий в воспалении и развитии астмы, доступны в открытых базах данных под номерами доступа AF043341 (человека); NM_013653 (мыши) и NM_031116 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00074] Последовательности аминокислот CCL5 доступны в открытых базах данных под номерами доступа ААС03541 (человека); NP_038681 (мыши) и NP_112378 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00075] Полинуклеотидные последовательности СС хемокинового лиганда 7 (CCL7), который представляет собой хемокин, вовлеченный в привлечение макрофагов во время воспаления и инвазии рака, доступны в открытых базах данных под номерами доступа NM_006273 (человека); NM_013654 (мыши) и NM_001007612 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00076] Последовательности аминокислот CCL7 доступны в открытых базах данных под номерами доступа NP_006264 (человека); NP_038682 (мыши) и NP_001007613 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00077] Хемокиновый (СХС-мотив) лиганд 9 (CXCL9, также известный как MIG) представляет собой Т-клеточный хемоаттрактант, индуцируемый интерфероном-гамма. Полинуклеотидные последовательности CXCL9 доступны в открытых базах данных под номерами доступа NM_002416 (человека); NM_0108599 (мыши) и NM_145672 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00078] Последовательности аминокислот CXCL9 доступны в открытых базах данных под номерами доступа NP_002407 (человека); NP_032625 (мыши) и NP_663705 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00079] Хемокиновый (С-Х-С-мотив) лиганд 10 (CXCL10) представляет собой малый цитокин, участвующий в хемоаттракции клеток иммунной системы, адгезии Т-клеток к эндотелиальным клеткам, противоопухолевой активности и ангиогенезе. Полинуклеотидные последовательности CXCL10 доступны в открытых базах данных под номерами доступа Х02530 (человека); NM_021274 (мыши) и ВС058444 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00080] Последовательности аминокислот хемокинового (С-Х-С-мотив) лиганда 10 (CXCL10) доступны в открытых базах данных под номерами доступа САА26370 (человека); NP_067249 (мыши) и ААН58444 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00081] Хемокиновый (С-Х-С-мотив) лиганд 12 (CXCL12), также известный как фактор 1, выделенный из стромальных клеток (SDF-1), представляет собой малый цитокин, который принадлежит к семейству интеркринов, члены которого активируют лейкоциты и часто индуцируются провоспалительными стимулами, такими как LPS, TNF или IL1. Подинуклеотидные последовательности CXCL12 доступны в открытых базах данных под номерами доступа NM_000609 (человека); NM_001012477 (мыши); NM_204510 (цыпленка) и NM_001033883 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00082] Последовательности аминокислот CXCL12 доступны в открытых базах данных под номерами доступа NP_000600 (человека); NP_001012495 (мыши); NP_989841 (цыпленка) и NP_001029055 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00083] Hansson и др., Microbes and Infection 5:841 (2006) обсуждают, что взаимодействие между хемокиновым (С-С-мотив) рецептором 7 (CCR7) и хемокиновым (С-С-мотив) лигандом 19 (CCL19, также известным как MIP-3β) важно для выработки первичных иммунных ответов. Полинуклеотидные последовательности CCR7 доступны в открытых базах данных под номерами доступа NM_001838 (человека) и NM_007719 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00084] Последовательности аминокислот CCR7 доступны в открытых базах данных под номерами доступа NP_001829 (человека) и NP_031745 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00085] Полинуклеотидные последовательности CCL19 доступны в открытых базах данных под номерами доступа NM_006274 (человека) и NM_011888 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00086] Последовательности аминокислот CCL19 доступны в открытых базах данных под номерами доступа NP_006265 (человека) и NP_036018 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00087] Полинуклеотидные последовательности СС хемокинового лиганда 21 (CCL21), точно установленного лиганда для CCR7, который необходим для достижения определенного состояния равновесия CD4+, но не CD8+, Т-клетками, при этом нарушения экспрессии CCL21 могут изменять склонность к аутоиммунным реакциям, доступны в открытых базах данных под номерами доступа АВ002409 (человека); NM_011335 (CCL21a мыши); NM_011124 (CCL21b мыши) и NM_023052 (CCL21c мыши); перечисленные последовательности включены в настоящее описание посредством ссылки.
[00088] Последовательности аминокислот CCL21 доступны в открытых базах данных под номерами доступа ВАА21817 (человека); NP_035465 (CCL21a мыши); NP_035254 (CCL21b мыши) и NP_075539 (CCL21c мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00089] Интерлейкин-8 (IL-8), хемокин, также называемый нейтрофил-активирующим пептидом-1 или SCYB8, представляет собой получаемый из ткани пептид, секретируемый несколькими типами клеток в ответ на воспалительные стимулы. В патентах США с номерами 6,133,426 и 6,177,980 описаны аминокислотные и Полинуклеотидные последовательности гуманизированных антител против IL-8. Полинуклеотидная последовательность IL-8 человека доступна в открытой базе данных под номером доступа NM_000584, указанная последовательность включена в настоящее описание посредством ссылки.
[00090] Последовательность аминокислот IL-8 человека доступна в открытой базе данных под номером доступа NP_000575, указанная последовательность включена в настоящее описание посредством ссылки.
Факторы роста
[00091] Колониестимулирующий фактор гранулоцитов/макрофагов (GM-CSF) представляет собой цитокин, который действует как фактор роста белых кровяных клеток, стимулирует стволовые клетки для получения из них гранулоцитов (нейтрофилов, эозинофилов и базофилов) и моноцитов. Полинуклеотидные последовательности GM-CSF доступны в открытых базах данных под номерами доступа M11734 (человека); NM_009969 (мыши); EU520303 (цыпленка); NM_001037660 (Csf2ra крысы) и NM_133555 (Csf2rb крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00092] Последовательности, аминокислот колониестимулирующего фактора гранулоцитов/макрофагов (GM-CSF) доступны в открытых базах данных под номерами доступа ААА52122 (человека); NP_034099 (мыши); АСВ11534 (цыпленка); NP_001032749 (Csf2ra крысы) и NP_598239 (Csf2rb), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00093] Полинуклеотидные последовательности лиганда FMS-подобного рецептора с тирозинкиназной активностью (FLT3/FLK2 лиганда, Flt3L), который может действовать как рецептор фактора роста на гематопоэтических стволовых клетках или клетках-предшественниках, или обоих, доступны в открытых базах данных под номерами доступа U04806 (человека) и NM_013520 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00094] Последовательности аминокислот FLT3/FLK2 лиганда (Flt3L) доступны в открытых базах данных под номерами доступа ААА17999 (человека) и NP_038548 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00095] Полинуклеотидная последовательность трансформирующего фактора роста альфа (TGF-альфа), экспрессия которого повышена при некоторых раках человека, который может обратимо придавать трансформированный фенотип культивируемым клеткам, доступна в открытых базах данных под номером доступа NM_001099691 (человека); NM_031199 (мыши); NM_001001614 (цыпленка) и NM_012671 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[00096] Последовательности аминокислот TGF-альфа доступны в открытых базах данных под номером доступа NP_001093161 (человека); NP_112476 (мыши); NP_001001614 (цыпленка) и NP_036803 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
Адъюванты
[00097] Бета-дефензины представляют собой противомикробные пептиды, участвующие во врожденном иммунном ответе против многих грамотрицательных и грамположительных бактерий, грибков и вирусов. Полинуклеотидные последовательности бета-дефензинов доступны в открытых базах данных под номерами доступа Х92744 (hBD-1 человека); AJ000152 (hBD-2 человека); AF217245 (бета-дефензин-3 человека); AJ314835 (бета-дефензин-4 человека); АВ089180 (hBD-5 человека); AY122466 (бета-дефензин-106 человека, DEFB106); AF540979 (бета-дефензин-107 человека, DEFB107); AF529416 (бета-дефензин-108 человека, DEFB108); DQ012014 (бета-дефензин-110 человека, DEFB110); DQ012015 (бета-дефензин-111 человека, DEFB111); DQ012016 (бета-дефензин-112 человека, DEFB112); DQ012017 (бета-дефензин-113 человека, DEFB113); DQ012018 (бета-дефензин-114 человека, DEFB114); DQ012019 (бета-дефензин-115 человека, DEFB115); DQ012020 (бета-дефензин-116 человека, DEFB116); DQ012021 (бета-дефензин-117 человека, DEFB117); NM_007843 (бета-дефензин-1 мыши); NM_010030 (бета-дефензин-2 мыши, Defb2); NM_013756 (бета-дефензин-3 мыши, Defb3); NM_019728 (бета-дефензин-4 мыши, Defb4); NM_030734 (бета-дефензин-5 мыши, Defb5); NM_054074 (бета-дефензин-6 мыши, Defb6); NM_139220 (бета-дефензин-7 мыши); NM_153108 (бета-дефензин-8 мыши, Defb8); NM_139219 (бета-дефензин-9 мыши, Defb9) и NM_139225 (бета-дефензин-10 мыши, Defb10); перечисленные последовательности включены в настоящее описание посредством ссылки.
[00098] Последовательности аминокислот бета-дефензинов доступны в открытых базах данных под номерами доступа САА63405 (hBD-1 человека); САВ65126 (hBD-2 человека); AAF73853 (бета-дефензин-3 человека); САС85520 (бета-дефензин-4 человека); ВАС10630 (hBD-5 человека); ААМ93908 (бета-дефензин-106 человека, DEFB106); AAN33115 (бета-дефензин-107 человека, DEFB107); AAQ09525 (бета-дефензин человека, DEFB108); AAY59750 (бета-дефензин-110 человека, DEFB110); AAY59751 (бета-дефензин-111 человека, DEFB111); AAY59752 (бета-дефензин-112 человека, DEFB112); AAY59753 (бета-дефензин-113 человека, DEFB113); AAY59754 (бета-дефензин-114 человека, DEFB114); AAY59755 (бета-дефензин-115 человека, DEFB115); AAY59756 (бета-дефензин-116 человека, DEFB116); AAY59757 (бета-дефензин-117 человека, DEFB117); NP_031869 (бета-дефензин-1 мыши); NP_034160 (бета-дефензин-2 мыши, Defb2); NP_038784 (бета-дефензин-3 мыши, Defb3); NP_062702 (бета-дефензин-4 мыши, Defb4); NP_109659 (бета-дефензин-5 мыши, Defb5); NP_473415 (бета-дефензин-6 мыши, Defb6); NP_631966 (бета-дефензин-7 мыши, Defb7); NP_694748 (бета-дефензин-8 мыши, Defb8); NP_631965 (бета-дефензин-9 мыши, Defb9) и NP_631971 (бета-дефензин-10 мыши, Defb10), перечисленные последовательности включены в настоящее описание посредством ссылки. См. также патент США номер 5,242,902 для получения дополнительных последовательностей пептидов дефензинов человека и крысы.
[00099] Белки высокомобильной группы-1 (HMGB1) представляют собой негистонные хромосомные белки, которые действуют как цитокины, опосредуя местный и системный ответы на некротическую гибель клеток и рак, инвазию патогенов, травму и сепсис. Полинуклеотидные последовательности белков HMGB1 доступны в открытых базах данных под номерами доступа NM_002128 (человека); NM_010439 (мыши); NM_204902 (цыпленка) и NM_012963 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000100] Последовательности аминокислот белков высокомобильной группы-1 (HMGB1) доступны в открытых базах данных под номерами доступа NP_002119 (человека); NP_034569 (мыши); NP_990233 (цыпленка) и NP_037095 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000101] Фагоцитарные белки S100 опосредуют воспалительные ответы и привлекают воспалительные клетки в места повреждения ткани, и представляют собой члены семейства молекул молекулярных паттернов, ассоциированных с повреждением (DAMP), которые важны для врожденного иммунитета. См. Foell и др., J. Leucocyte Biol. 81:1 (2006). Полинуклеотидные последовательности белков S100 доступны в открытых базах данных под номерами доступа ВС014392 (S100 А1 человека); ВС002829 (S100 А2 человека); ВС012893 (S100 A3 человека); ВС016300 (S100 А4 человека); Z18954 (S100D человека); ВС001431 (S100 А6 человека); ВС 034687 (S100 А7 человека); ВС005928 (S100 А8 человека); ВС047681 (S100 А9 человека); ВС015973 (S100 А10 человека); D38583 (клагизарин (clagizzarin) человека); NM_011309 (S100a1 мыши); NM_009115 (S100b мыши); NM_013650 (S100a8 мыши); NM_009114 (S100a9 мыши); NM_011310 (S100a3 мыши); NM_011311 (S100a4 мыши) и NM_011312 (S100a5 мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000102] Последовательности аминокислот белков S100 доступны в открытых базах данных под номерами доступа ААН14392 (S100 А1 человека); ААН02829 (S100 А2 человека); ААН12893 (S100 A3 человека); ААН16300 (S100 А4 человека); САА79479 (S100D человека); ААН01431 (S100 А6 человека); ААН34687 (S100 А7 человека); ААН05928 (S100 А8 человека); ААН47681 (S100 А9 человека); ААН15973 (S100 А10 человека); ВАА07597 (клагизарин человека); NP_035439 (S100a1 мыши); NP_033141 (S100b мыши); NP_038678 (S100a8 мыши); NP_033140 (S100a9 мыши); NP_035440 (S100a3 мыши); NP_035441 (S100a4 мыши) и NP_035442 (S100a5 мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000103] Маннан, полисахарид растений, который представляет собой полимер сахара маннозы, используют для выработки иммунного ответа. В патенте США номер 5,807,559 описаны иммуногенные конъюгаты маннана, которые могут быть пригодны для выработки Т-клеточного иммунитета против связанных с опухолью углеводных структур или против углеводных структур, экспрессированных на инфекционных агентах и/или инфицированных клетках-хозяевах. В патенте США номер 5,773,425 описано применение маннана для снятия симптомов и/или излечения от вирусных заболеваний, и для усиления иммунного ответа.
[000104] Бациллу Кальметта-Герена (BCG), живые ослабленные виды микобактерий, применяют в качестве вакцины для предупреждения тяжелого и смертельного туберкулеза. В патенте США номер 7,393,541 описано получение адъювантной вакцины для индукции in vivo опосредованного Т-клетками иммунного ответа на микобактерию у млекопитающего субъекта. См. также Hubbard и Collins, Infect. Immun. 59 (2): 570. В патенте США номер 5,292,513 описан способ примирования макрофагов in vivo у пациентов, нуждающихся в усилении бактерицидной и противовирусной активности, с помощью термоинактивированной BCG. Последовательность полного генома BCG доступна в открытых базах данных под номером доступа NC_008769 (M. bovis BCG str. Pasteur 1173P2, complete genome).
[000105] Бактериальные липополисахариды (LPS) представляют собой эндотоксины, которые вызывают сильный иммунный ответ при инфицировании грамотрицательными бактериями. В патенте США номер 4,148,877 описано фракционирование LPS из бактериальной культуры и применение фракции в качестве лекарственного средства для индукции устойчивости к бактериальной инфекции. В патенте США номер 5,292,513 описан способ примирования макрофагов in vivo у пациентов, нуждающихся в усилении бактерицидной и противовирусной активности, с помощью LPS.
Костимулирующие молекулы (положительный эффект)
[000106] Лиганд OX40 (OX40L) принадлежит к членам 4 суперсемейства лигандов фактора некроза опухоли (Tnfsf4), экспрессируется на дендритных клетках и вызывает дифференцировку Th2-клеток. Полинуклеотидные последовательности лиганда 0Х40 доступны в открытых базах данных под номерами доступа Х79929 (человека); U12763 (мыши) и AF037067 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000107] Последовательности аминокислот лиганда OX40 (OX40L) доступны в открытых базах данных под номерами доступа САА56284 (человека); ААА21871 (мыши) и ААС67236 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000108] Лиганд 4-1ВВ (4-1BBL) принадлежит к членам 9 суперсемейства лигандов фактора некроза опухоли (Tnfsf9), он представляет собой трансмембранный гликопротеин 2 типа и экспрессируется на активированных Т лимфоцитах. Полинуклеотидные последовательности 4-1BBL доступны в открытых базах данных под номерами доступа NM_003811 (человека); NM_009404 (мыши) и AY332409 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000100] Последовательности аминокислот лиганда 4-1ВВ (4-1BBL) доступны в открытых базах данных под номерами доступа NP_003802 (человека); NP_033430 (мыши) и AAQ01228 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000101] Белок CD40 принадлежит к членам 5 суперсемейства рецепторов фактора некроза опухоли, и является ключевым в опосредовании большого разнообразия иммунных и воспалительных реакций, включая зависимое от Т-клеток переключение классов иммуноглобулинов, развитие В-клеток памяти и образование зародышевого центра. Полинуклеотидные последовательности белков CD40 доступны в открытых базах данных под номерами доступа Х60592 (человека); NM_170701 (мыши); NM_204665 (цыпленка) и NM_134360 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000102] Последовательности аминокислот белков CD40 доступны в открытых базах данных под номерами доступа САА43045 (человека); NP_733802 (мыши); P_989996 (цыпленка) и NP_599187 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000103] Белок, родственный семейству индуцируемых глюкокортикоидами рецепторов фактора некроза опухоли, (GITR) может вызывать эффективный иммунитет к развитию опухоли посредством стимуляции Т-клеток. Введение моноклонального антитела против GITR (mAb) может вызвать сильный противоопухолевый иммунитет и уничтожить развившиеся опухоли, не вызывая явных аутоиммунных заболеваний. См. Ко и др., J. Exp. Med. 7: 885 (2005). В патенте США номер 6,503,184 В1 описано антитело против GITR.
[000104] Полинуклеотидные последовательности лиганда GITR (GITRL) доступны в открытых базах данных под номерами доступа AY358868 (человека) и AY359852 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000105] Последовательности аминокислот лиганда GITR (GITRL) доступны в открытых базах данных под номерами доступа AAQ89227 (человека) и AAQ55265 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000106] Лиганд (HSVgD), связывающий медиатор входа в клетку вируса герпеса (HVEM), также называемый р30, или LIGHT, представляет собой член семейства фактора некроза опухоли (TNF), вовлеченный в костимуляцию Т-клеток. Для LIGHT есть два рецептора, медиатор входа в клетку вируса герпеса (HVEM) и рецептор лимфотоксина-β (LT-RR). Являясь лигандом для HVEM, HSVgD активирует Т-клетки, действуя как костимулирующий фактор на Т-клетки, что приводит к пролиферации Т-клеток и секреции цитокинов. См. патент США 7,118,742 для получения полинуклеотидных и аминокислотных последовательностей LIGHT. В патенте США 5,654,174 описан вариант белка gD с делецией карбоксиконцевых остатков.
[000107] CD70 представляет собой цитокин, который связывается с CD27. Он играет роль в активации Т-клеток, индуцирует пролиферацию костимулированных Т-клеток и повышает образование цитолитических Т-клеток. Полинуклеотидные последовательности CD70 доступны в открытых базах данных под номерами доступа NM_001252 (человека); NM_011617 (мыши) и NM_001106878 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000108] Последовательности аминокислот CD70 доступны в открытых базах данных под номерами доступа NP_001243 (человека); NP_035747 (мыши) и NP_001100348 (крысы), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000109] ICOS-L представляет собой лиганд для рецептора клеточной поверхности ICOS, специфичного для Т-клеток, и действует как костимулирующий сигнал для пролиферации Т-клеток и секреции цитокинов. ICOS-L также индуцирует пролиферацию В-клеток и их дифференцировку в плазматические клетки. ICOS-L может играть важную роль в опосредовании местных тканевых ответов на воспалительные состояния, а также в модулировании вторичного иммунного ответа путем костимуляции функции Т-клеток памяти. Полинуклеотидные последовательности ICOS-L доступны в открытых базах данных под номерами доступа NM_015259 (человека) и NM_015790 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000110] Последовательности аминокислот ICOS-L доступны в открытых базах данных под номерами доступа NP_056074 (человека) и NP_056605 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000111] Белок PD-L1 (также известный как CD274) экспрессируется в активированных моноцитах, Т- и В-клетках. Экспрессия PD-L1 в моноцитах повышается при обработке IFN-гамма, а в дендритных клетках и кератиноцитах - при обработке IFN-гамма вместе с другими активаторами. Полинуклеотидные последовательности белков PD-L1 доступны в открытых базах данных под номерами доступа NM_014143 (человека) и NM_021893 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
[000112] Последовательности аминокислот белков PD-L1 доступны в открытых базах данных под номерами доступа NP_054862 (человека) и NP_068693 (мыши), перечисленные последовательности включены в настоящее описание посредством ссылки.
Костимулирующие молекулы (отрицательный эффект)
[000113] Белок 4, связанный с цитотоксическими Т лимфоцитами, (CTLA4) представляет собой член суперсемейства иммуноглобулинов и является костимулирующей молекулой, экспрессируемой в активированных Т-клетках. В патентах США 7,034,121 и 6,984,720 описаны способы получения и применения антител против CTLA4. В патенте США 6,984,720 также описаны последовательности аминокислот тяжелой и легкой цепи антитела против CTLA4.
[000114] Молекулы PD-1 представляют собой члены суперсемейства генов иммуноглобулинов, которые связывают лиганд PD-1 (PD-L1). Связывание PD-L1 с рецептором PD-1 на Т-клетках приводит к передаче костимулирующего сигнала в клетке, который предотвращает прохождение клетки по клеточному циклу и повышает пролиферацию Т-клеток. Ингибирование взаимодействия между PD-L1 и рецептором на Т-клетке с помощью антитела против PD-L1 приводит к снижению иммунного ответа, названного анергией иммунной клетки. В патенте США 7,029,674 описаны способы получения и последовательность антитела против PD-L1.
[000115] PD-L2 в первую очередь известен как лиганд для PD-1 (или гомолог человека - PDCD1). Тем не менее, описывали, что PD-12 участвует в передаче костимулирующего сигнала, необходимого для пролиферации Т-лимфоцитов и продукции IFN-гамма, независимо от PDCD1. Взаимодействие с PDCD1 ингибирует пролиферацию Т-клеток путем блокирования продвижения по клеточному циклу и продукции цитокинов. У Yamazaki и др., J. of Immunol. 169: 5538 (2002) и Ansari и др., J. Exp. Med. 198: 63 (2003) описано получение моноклональных антител против PD-L2.
Молекулы, направленные против иммунных супрессоров (ингибиторы толерантности)
[000116] Трансформирующий фактор роста-бега (TGF-β) представляет собой многофункциональный белок, который регулирует пролиферацию и дифференцировку клеток путем взаимодействия с одним из двух трансмембранных рецепторов с серин/треонинкиназной активностью I типа и II типа. См. Chen и др., Science 28: 1335 (1993). Рецептор TGF II типа (TGFR2) фосфорилирует и активирует рецепторы I типа, которые аутофосфорилируются, затем связывают и активируют регуляторы транскрипции SMAD. У Lynch MA и др., Cancer Res. 58: 4227 (1998) описаны мутации в гене рецептора трансформирующего фактора роста-β II типа (TGFBR2), которые связаны с карциномами яичника человека. У Brand и др., J. Biol. Chem. 265: 11500-11503 (1993) описано, что делеция предсказанного серин/треонинкиназного цитоплазматического домена (нуклеотиды 1172-2036 кДНК TGFβR2 H2-3FF, доступна в открытых базах данных под номером доступа М85079, и последовательность аминокислот, доступная под номером доступа ААА61164) нарушает экспрессию, зависимую от всех трех генов TGF-β (1, 2 и 3). TGF-β продуцируется в большинстве опухолей человека и ингибирует клеточный иммунитет, направленный на опухолевые антигены. У Foster и др., J. Immunother. 31:500 (2008) описано, что экспрессия доминантно отрицательного TGFβR2 в цитотоксических Т-лимфоцитах может приводить к устойчивости к ингибиторному действию TGF-β.
[000117] TGF-β, действуя синергично с TGFα, вызывает трансформацию клеток. Он также действует как негативный аутокринный фактор роста. Нарушенная регуляция активации и передачи сигнала TGFβ может привести к апоптозу. У Ziyadeh и др., Proc. Natl. Acad. Sci. 97: 8015 (2000) описано, что введение антитела против TGF-β может предотвратить почечную недостаточность и гломерулосклероз у мышей db/db, модели диабета II типа, у которых развивается явная нефропатия. Способы получения и применения моноклональных антител против TGFβ описаны в патенте США номер 6,419,928. У Barcellos-Hoff и др., Am J. Pathol. 147:5 (1995) также описан способ получения антитела против TGFβ. Последовательности аминокислот и нуклеотидов конструкций слитого белка TGFβ описаны в патенте США номер 6,756,215.
[000118] IL-10 представляет собой цитокин, продуцируемый активированными Th2-клетками, В-клетками, кератиноцитами, моноцитами и макрофагами. IL-10 ингибирует синтез множества цитокинов, включая IFN-гамма, IL-2, IL-3, TNF и GM-CSF, продуцируемых активированными макрофагами и хелперными Т-клетками. IL-10 используют, чтобы вызвать рост и дифференцировку активированных В-клеток человека, ингибирование Th1-ответов для предотвращения отторжения трансплантата и опосредованных Т-клетками аутоиммунных заболеваний. У O'Farrell и др., EMBO J. 17: 1006 (1998); Kanbayashi и др., Cell Immunol. 171: 153 (1996); Fukushima и др., Br. J. Ophthalmol. 90: 1535 (2006) и van Lent и др., Ann. Rheum. Dis. 66: 334 (2007) описано получение антител против IL-10. В патенте США номер 7,326,567 описана полинуклеотидная последовательность антитела против IL-10. В патенте США номер 5,837,232 описан способ лечения опосредованного В-клетками аутоиммунного расстройства антителами против IL-10.
[000119] Семейство белков-супрессоров передачи сигнала цитокинов (SOCS) образует часть классической системы с отрицательной обратной связью, которая регулирует передачу сигнала цитокинов. У Alexander и др. Cell 98: 597 (1999) описано, что супрессор передачи сигнала цитокинов 1 (SOCS1) представляет собой основной ингибитор передачи сигнала от интерферона-гамма и предотвращает потенциально смертельное действие данного цитокина у новорожденных. У Hilton и др., Proc. Natl. Acad. Sci. USA 95: 114 (1999), обсуждается, что SOCS1 участвует в негативной регуляции цитокинов, которые передают сигнал через путь JAK/STAT3. У Ohya и др. J. Biol. Chem. 272: 27178 (1997) описано, что белки SOCS, похоже, представляют собой основные регуляторы передачи сигнала от интерлейкина 6 (IL-6) и фактора, ингибирующего лейкоз (LIF). В патенте США номер 6,534,277 описан способ получения и применения антитела против SOCS1, в котором последовательность нуклеиновых кислот, кодирующую антитело против SOCS1, вводили в клетки таким образом, что указанное антитело экспрессировалось клетками или их потомством, и рекомбинантные клетки затем вводили in vivo для получения терапевтического эффекта. В патентах США с номерами 6,323,317 и 7,049,418 также описаны антитела против SOCS1.
[000120] TGF-α представляет собой митогенный полипептид, который способен связываться с рецептором EGF и действовать синергично с TGF-β, чтобы вызвать независимую от наличия подложки пролиферацию клеток в мягком агаре. У Ellis и др., N. Engl. J. Med. 317: 158 (1987), описано, что TGF-α играет роль в некоторых паранеопластических проявлениях меланомы. В патенте США номер 4,742,003 и у Xian и др., The J. of Histochem. & Cytochem. 47: 949 (1999) описаны способы получения антител против TGF-α.
[000121] Как рецептор фактора некроза опухоли (TNFR1), так и Fas содержат цитоплазматический Fas-ассоциированный белок с доменом смерти (FADD), который необходим для индуцируемой Fas и TNF передачи сигнала программированной гибели клетки (апоптоза) и олигомеризации рецептора. Был обнаружен белок млекопитающего, обозначенный FADD, обладающий способностью связывать цитоплазматический участок или домен рецептора Fas и ингибировать опосредованный FAS апоптоз. Полинуклеотидная последовательность FADD доступна в открытой базе данных под номером доступа U24231, а последовательность аминокислот доступна под номером доступа ААА86517, обе последовательности включены в настоящее описание посредством ссылки. FADD-фрагмент или нуклеиновая кислота, кодирующая его, который представляет собой доминантно отрицательный ингибитор функционально интактного нативного FADD, описаны в патенте США номер 6,562,797 В1.
ОПИСАНИЕ ПЕРЕЧНЯ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[000122] SEQ ID NO:1 представляет собой полинуклеотидную последовательность конструкции, кодирующей mIL-12 и m-IL21.
[000123] SEQ ID NO:2 представляет собой полинуклеотидную последовательность конструкции, кодирующей hIL-12 и hIL-21.
[000124] SEQ ID NO:3 представляет собой полинуклеотидную последовательность конструкции, кодирующей mIL-21 и mIL-15.
[000125] SEQ ID NO:4 представляет собой полинуклеотидную последовательность конструкции, кодирующей mIL-12.
[000126] SEQ ID NO:5 представляет собой полинуклеотидную последовательность конструкции, кодирующей hIL-21 и hIL-15.
[000127] SEQ ID NO:б представляет собой полинуклеотидную последовательность конструкции, кодирующей hIL-21.
[000128] SEQ ID NO:7 представляет собой полинуклеотидную последовательность конструкции, кодирующей mIL-21.
[000129] SEQ ID NO:8 представляет собой полинуклеотидную последовательность конструкции, кодирующей hIL-21.
[000130] SEQ ID NO:9 представляет собой полинуклеотидную последовательность, кодирующую mIL-21.
[000131] SEQ ID NO:10 представляет собой последовательность аминокислот mIL-21.
[000132] SEQ ID NO:11 представляет собой полинуклеотидную последовательность, кодирующую mIL-15.
[000133] SEQ ID NO:12 представляет собой последовательность аминокислот mIL-15.
[000134] SEQ ID NO:13 представляет собой полинуклеотидную последовательность, кодирующую mp40 mIL-12.
[000135] SEQ ID NO:14 представляет собой последовательность аминокислот mp40 mIL-12.
[000136] SEQ ID NO:15 представляет собой полинуклеотидную последовательность, кодирующую mp35 mIL-12.
[000137] SEQ ID NO:16 представляет собой последовательность аминокислот mp35 mIL-12.
[000138] SEQ ID NO:17 представляет собой полинуклеотидную последовательность, кодирующую hIL-21.
[000139] SEQ ID NO:18 представляет собой последовательность аминокислот hIL-21.
[000140] SEQ ID NO:19 представляет собой полинуклеотидную последовательность, кодирующую hIL-15.
[000141] SEQ ID NO:20 представляет собой последовательность аминокислот hIL-15.
[000142] SEQ ID NO:21 представляет собой полинуклеотидную последовательность, кодирующую р40 hIL-12.
[000143] SEQ ID NO:22 представляет собой последовательность аминокислот р40 hIL-12.
[000144] SEQ ID NO:23 представляет собой полинуклеотидную последовательность, кодирующую р35 hIL-12.
[000145] SEQ ID NO:24 представляет собой последовательность аминокислот р35 hIL-12.
[000146] SEQ ID NO:25 представляет собой последовательность нуклеиновых кислот чувствительного к экдизону элемента, обнаруженного у Drosophila.
[000147] SEQ ID NO:26 представляет собой последовательность нуклеиновых кислот чувствительного к экдизону элемента, обнаруженного у Drosophila melanogaster.
[000148] SEQ ID NO:27 представляет собой последовательность нуклеиновых кислот чувствительного к экдизону элемента, обнаруженного у Drosophila melanogaster.
[000149] SEQ ID NO:28 представляет собой сайт рестрикции для фермента хоуминг-эндонуклеазы (НЕ) I-SceI.
[000150] SEQ ID NO:29 представляет собой последовательность ДНК аденовирусного вектора, включающего последовательность, кодирующую IL-12 человека: Ad-RTS-hIL-12 (SP1-RheoIL-12).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ОПРЕДЕЛЕНИЯ.
[000151] Если не указано иначе, предполагается, что все термины данной области, обозначения и другие научные термины или терминология, используемая в данной заявке, имеют значения, которые обычно понимают специалисты в области, к которой относится настоящее изобретение. В некоторых случаях, определения терминов с общепринятыми значениями приведены в данной заявке для ясности и/или для быстрой справки и понимания, и включение таких определений в настоящее описание не обязательно должно истолковываться как наличие существенного отличия значения термина от обычно подразумеваемого в данной области. Общепринятые определения молекулярно-биологических терминов и/или способов, и/или протоколов можно найти в Rieger и др., Glossary of Genetics: Classical and Molecular, 5-oe издание. Springer-Veriag: Нью-Йорк, 1991; Lewin, Genes V, Oxford University Press: Нью-Йорк, 1994; Sambrook и др., Molecular Cloning, A Laboratory Manual (3-e изд. 2001) и Ausubel и др., Current Protocols in Molecular Biology (1994). В случае необходимости, процедуры, включающие применение доступных для приобретения наборов и/или реагентов, как правило, осуществляют в соответствии с рекомендациями и/или протоколами, и/или параметрами изготовителя, если не указано иначе.
[000152] Термин "изолированный" для целей настоящего изобретения обозначает биологический материал (клетку, нуклеиновую кислоту или белок), который был удален из его естественного окружения (окружения, в котором он находится в природе). Например, полинуклеотид, присутствующий в естественном состоянии в растении или животном, не является изолированным, тем не менее, тот же самый полинуклеотид, отделенный от соседних нуклеиновых кислот, рядом с которыми он находится в природе, считают "изолированным".
[000153] Термин "очищенный", применительно к биологическим материалам, не требует присутствия материала в форме, имеющей абсолютную чистоту, исключающей присутствие других соединений. Это, скорее, относительное определение.
[000154] Термины "нуклеиновая кислота", "молекула нуклеиновой кислоты", "олигонуклеотид", "нуклеотид" и "полинуклеотид" используют взаимозаменяемо, и они относятся к полимерной форме соединенных фосфоэфирными связями рибонуклеозидов (аденозина, гуанозина, уридина или цитидина; "молекул РНК") или дезоксирибонуклеозидов (дезоксиаденозина, дезоксигуанозина, дезокситимидина или дезоксицитидина; "молекул ДНК"), или любых их фосфоэфирных аналогов, таких как фосфоротиоаты и тиоэфиры, либо в одноцепочечной форме, либо в форме двухцепочечной спирали. Возможно образование двухцепочечных ДНК-ДНК, ДНК-РНК и РНК-РНК спиралей. Термин молекула нуклеиновой кислоты, и, в частности, молекула ДНК или РНК, относится только к первичной и вторичной структуре указанной молекулы, и не ограничен какими-либо конкретными третичными формами. Таким образом, данный термин включает двухцепочечную ДНК, обнаруженную, среди прочего, в виде линейных или кольцевых молекул ДНК (например, рестрикционных фрагментов), плазмид, сверхспиральной ДНК и хромосом. При обсуждении структуры конкретных двухцепочечных молекул ДНК, последовательности могут быть описаны в данной заявке согласно стандартной договоренности о написании последовательности только в направлении от 5' к 3' вдоль нетранскрибируемой нити ДНК (т.е., цепи, содержащей последовательность, гомологичную мРНК). "Рекомбинантная молекула ДНК" представляет собой молекулу ДНК, над которой совершили молекулярно-биологические манипуляции. ДНК включает кДНК, геномную ДНК, плазмидную ДНК, синтетическую ДНК и полусинтетическую ДНК, но не ограничена ими.
[000155] Термин "фрагмент", применительно к полинуклеотидным последовательностям, относится к последовательности нуклеотидов, имеющей меньшую длину, чем у исходной нуклеиновой кислоты, и включающей, на протяжении общей части, последовательность нуклеотидов, идентичную исходной нуклеиновой кислоте. Такой фрагмент нуклеиновой кислоты согласно настоящему изобретению может, когда это уместно, быть включен в больший полинуклеотид, частью которого он является. Такие фрагменты включают или в качестве альтернативы состоят из олигонуклеотидов в диапазоне длин от по меньшей мере 6, 8, 9, 10, 12, 15, 18, 20, 21, 22, 23, 24, 25, 30, 39, 40, 42, 45, 48, 50, 51, 54, 57, 60, 63, 66, 70, 75, 78, 80, 90, 100, 105, 120, 135, 150, 200, 300, 500, 720, 900, 1000, 1500, 2000, 3000, 4000, 5000 или более последовательных нуклеотидов нуклеиновой кислоты согласно настоящему изобретению.
[000156] В данной заявке формулировка "изолированный фрагмент нуклеиновой кислоты" относится к полимеру РНК или ДНК, который представляет собой одно- или двухцепочечную молекулу, необязательно содержащую синтетические, неприродные или измененные нуклеотидные основания. Изолированный фрагмент нуклеиновой кислоты в виде полимера ДНК может состоять из одного или нескольких фрагментов кДНК, геномной ДНК или синтетической ДНК.
[000157] Термин "ген" относится к полинуклеотиду, содержащему нуклеотиды, которые кодируют функциональную молекулу, включая функциональные молекулы, полученные только с помощью транскрипции (например, биологически активные виды РНК) или с помощью транскрипции и трансляции (например, полипептид). В объем термина "ген" входят нуклеиновые кислоты кДНК и геномной ДНК. "Ген" также относится к фрагментам нуклеиновой кислоты, которые экспрессируют определенную РНК, белок или полипептид, включая регуляторные последовательности, предшествующие (5'-некодирующие последовательности) и следующие (3'-некодирующие последовательности) за кодирующей последовательностью. Термин "нативный ген" относится к гену в том виде, в котором он находится в природе, с его собственными регуляторными последовательностями. "Химерный ген" относится к любому гену, который не является нативным геном, включающему регуляторные и/или кодирующие последовательности, которые не находятся вместе в природе. Соответственно, химерный ген может включать регуляторные последовательности и кодирующие последовательности, которые получены из различных источников, или регуляторные последовательности и кодирующие последовательности, полученные из одного источника, но расположенные по-другому относительно их расположения в природе. Химерный ген может включать кодирующие последовательности, полученные, из различных источников, и/или регуляторные последовательности, полученные из различных источников. "Эндогенный ген" относится к нативному гену в его природном расположении в геноме организма. Термин "чужеродный" ген или "гетерологичный" ген относится к гену, который обычно не обнаруживается в организме хозяина, но который вводят в организм хозяина путем переноса генов. Чужеродные гены могут включать нативные гены, вставленные в неродной организм, или химерные гены. "Трансген" представляет собой ген, который ввели в геном с помощью процедуры трансформации. Например, ген интерлейкина-12 (IL-12) кодирует белок IL-12. IL-12 представляет собой гетеродимер 35-кДа субъединицы (р35) и 40-кДа субъединицы (р40), связанных дисульфидной связью с получением функционального IL-12p70. Ген IL-12 кодирует как субъединицу р35, так и субъединицу р40.
[000158] "Гетерологичная ДНК" относится к ДНК, не присутствующей в природе в клетке или в хромосомном сайте клетки. Гетерологичная ДНК может содержать ген, чужеродный для данной клетки.
[000159] Термин "геном" включает хромосомную, а также митохондриальную, хлоропластную и вирусную ДНК или РНК.
[000160] Молекула нуклеиновой кислоты "способна к гибридизации" с другой молекулой нуклеиновой кислоты, такой как кДНК, геномная ДНК или РНК, если одноцепочечная форма молекулы нуклеиновой кислоты может отжигаться на другую молекулу нуклеиновой кислоты при подходящих условиях температуры и ионной силы раствора. Условия гибридизации и промывки хорошо известны и проиллюстрированы у Sambrook и др. в Molecular Cloning: A Laboratory Manual, второе издание, Cold Spring Harbor Laboratory Press, Cold Spring Harbor (1989), особенно глава 11 и таблица 11.1 в ней). Условия температуры и ионной силы определяют "жесткости" гибридизации.
[000161] Условия жесткости можно изменять для обнаружения от относительно похожих фрагментов, таких как гомологичные последовательности из состоящих в дальнем родстве организмов, до очень похожих фрагментов, таких как гены, которые повторяют функциональные ферменты из близкородственных организмов. Для предварительного скрининга гомологичных нуклеиновых кислот, можно применять условия низкой жесткости гибридизации, соответствующие Tm, равной 55°, например, в 5Х SSC, 0.1% ДСН, 0.25% молоке и без формамида; или в 30% формамида, 5Х SSC, 0.5% ДСН. Условия умеренной жесткости гибридизации соответствуют более высокой Tm, например, в 40% формамида, с 5Х или 6Х SSC. Условия высокой жесткости гибридизации соответствуют наиболее высокой Tm, например, в 50% формамида, 5Х или 6Х SSC.
[000162] Для гибридизации требуется, чтобы две нуклеиновые кислоты содержали комплементарные последовательности, хотя, в зависимости от жесткости гибридизации, возможны несовпадения между основаниями. Термин "комплементарный" применяют для описания взаимоотношения между нуклеотидными основаниями, которые способны гибридизоваться друг с другом. Например, применительно к ДНК, аденозин комплементарен тимину и цитозин комплементарен гуанину. Соответственно, настоящее изобретение также включает изолированные фрагменты нуклеиновых кислот, которые комплементарны целым последовательностям, как описано или используется в данной заявке, а также по существу сходным последовательностям нуклеиновых кислот.
[000163] В одном варианте реализации настоящего изобретения, полинуклеотиды обнаруживают путем применения условий гибридизации, включающих этап гибридизации при Tm, равной 55°С, и применения условий, указанных выше. В других вариантах реализации, Tm равна 60°С, 63°С или 65°С.
[000164] Послегибридизационные промывки также определяют условия жесткости. В одном наборе условий используют серию промывок, начиная с 6Х SSC, 0.5% ДСН при комнатной температуре в течение 15 минут (мин), затем повторяют промывки в 2X-SSC, 0.5% ДСН при 45°C в течение 30 мин, а затем повторяют дважды промывки в 0.2Х SSC, 0.5% ДСН при 50°С в течение 30 мин. Предпочтительный набор строгих условий включает более высокие температуры, при которых промывки идентичны описанным выше, за исключением того, что температуру двух окончательных 30-мин промывок в 0.2Х SSC, 0.5% ДСН повышают до 60°С. Другой предпочтительный набор очень жестких условий включает две окончательные промывки в 0.1Х SSC, 0.1% ДСН при 65°С.
[000165] Подходящая жесткость для гибридизации нуклеиновых кислот зависит от длины и степени комплементарности нуклеиновых кислот, переменных, хорошо известных в данной области. Чем больше степень подобия или гомологии между двумя последовательностями нуклеотидов, тем больше значения Tm для гибридов нуклеиновых кислот, имеющих данные последовательности. Относительная стабильность (соответствующая более высокой Tm) гибридизации нуклеиновых кислот убывает в следующем порядке: РНК:РНК, ДНК:РНК, ДНК:ДНК. Для гибридов больше 100 нуклеотидов в длину были получены уравнения для вычисления Tm (см. Sambrook и др., выше, 9.50-0.51). Для гибридизации с более короткими нуклеиновыми кислотами, т.е., олигонуклеотидами, положение несовпадений становится более значимым, и длина олигонуклеотида определяет специфичность (см. Sambrook и др., выше, 11.7-11.8).
[000166] В одном варианте реализации настоящего изобретения, полинуклеотиды обнаруживают путем использования условий гибридизации, включающих этап гибридизации в менее чем 500 мМ соли по меньшей мере при 37°С и этап промывки в 2Х SSPE при температуре, равной по меньшей мере 63°С. В другом варианте реализации настоящего изобретения, условия гибридизации включают менее чем 200 мМ соль и по меньшей мере 37°С на этапе гибридизации. В дополнительном варианте реализации, условия гибридизации включают 2Х SSPE и 63°С на обоих этапах гибридизации и промывки.
[000167] В другом варианте реализации настоящего изобретения, длина гибридизующейся нуклеиновой кислоты составляет по меньшей мере приблизительно 10 нуклеотидов. Предпочтительно, минимальная длина гибридизующейся нуклеиновой кислоты составляет по меньшей мере приблизительно 15 нуклеотидов; например, по меньшей мере приблизительно 20 нуклеотидов; например, по меньшей мере 30 нуклеотидов. Более того, для квалифицированного специалиста очевидно, что температуру и концентрацию соли в растворе для промывки при необходимости можно изменять в соответствии с такими факторами, как длина зонда.
[000168] Термин "зонд" относится к одноцепочечной молекуле нуклеиновой кислоты, которая может спариваться с комплементарной одноцепочечной целевой нуклеиновой кислотой с получением двухцепочечной молекулы.
[000169] В данной заявке, термин "олигонуклеотид" относится к короткой нуклеиновой кислоте, которая гибридизуется с молекулой геномной ДНК, молекулой кДНК, молекулой плазмидной ДНК или молекулой мРНК. Олигонуклеотиды могут быть меченными, например,32Р-нуклеотидами или нуклеотидами, с которыми ковалентно конъюгировали метку, такую как биотин. Меченный олигонуклеотид можно применять в качестве зонда для обнаружения присутствия нуклеиновой кислоты. Олигонуклеотиды (один или оба из которых могут содержать метки) можно применять в качестве праймеров для ПЦР, либо для клонирования полноразмерной нуклеиновой кислоты или ее фрагмента, для секвенирования ДНК или для обнаружения присутствия нуклеиновой кислоты. Олигонуклеотид также можно применять для получения тройной спирали с молекулой ДНК. Как правило, Олигонуклеотиды получают синтетическим путем, предпочтительно на синтезаторе нуклеиновых кислот. Соответственно, Олигонуклеотиды можно получить с не встречающимися в природе аналогами фосфоэфирных связей, такими как тиоэфирные связи и т.д.
[000170] "Праймер" относится к олигонуклеотиду, который гибридизуется с целевой последовательностью нуклеиновых кислот с получением двухцепочечного участка нуклеиновой кислоты, который может служить сайтом инициации синтеза ДНК при подходящих условиях. Такие праймеры можно применять в полимеразной цепной реакции или для секвенирования ДНК.
[000171] "Полимеразная цепная реакция" сокращенно называется ПЦР и относится к способу ферментативной амплификации in vitro определенных последовательностей нуклеиновых кислот. ПЦР включает серию повторных температурных циклов, в которой каждый цикл включает три стадии: денатурацию матричной нуклеиновой кислоты для разделения цепей целевой молекулы, отжиг одноцепочечного олигонуклеотидного праймера для ПЦР на матричную нуклеиновую кислоту и удлинение гибридизовавшегося праймера(ов) с помощью ДНК-полимеразы. ПЦР обеспечивает средства для обнаружения присутствия целевой молекулы и, при количественных или полуколичественных условиях, для определения относительного количества данной целевой молекулы в исходном пуле нуклеиновых кислот.
[000172] "Полимеразная цепная реакция с этапом обратной транскрипции" сокращенно называется ОТ-ПЦР и относится к способам ферментативного получения in vitro целевой молекулы или молекул кДНК из молекулы или молекул РНК, а затем ферментативной амплификации конкретной последовательности или последовательностей нуклеиновых кислот из целевой молекулы или молекул кДНК, описанных выше. ОТ-ПЦР также обеспечивает средства обнаружения присутствия целевой молекулы и, при количественных или полуколичественных условиях, определения относительного количества данной целевой молекулы в исходном пуле нуклеиновых кислот.
[000173] "Кодирующая последовательность", ДНК относится к двухцепочечной последовательности ДНК, которая кодирует полипептид и может транскрибироваться и транслироваться в полипептид в клетке in vitro или in vivo, когда она помещена под контроль подходящих регуляторных последовательностей. Формулировка "подходящие регуляторные последовательности" относится к последовательностям нуклеотидов, расположенным перед кодирующей последовательностью (5'-некодирующие последовательности), внутри нее или за ней (3'-некодирующие последовательности), которые влияют на транскрипцию, процессинг или стабильность РНК или трансляцию соответствующей кодирующей последовательности. Регуляторные последовательности могут включать промоторы, трансляционные лидерные последовательности, интроны, последовательности сигналов полиаденилирования, сайты процессинга РНК, сайты связывания эффектора и структуры стебель-петля. Границы кодирующей последовательности определяют по инициирующему кодону на 5'(амино)-конце и трансляционному стоп-кодону на 3'(карбоксильном)-конце. Кодирующая последовательность может содержать прокариотические последовательности, кДНК, полученную из мРНК, геномные последовательности ДНК и даже синтетические последовательности ДНК, но не ограничена ими. Если предполагается, что экспрессия кодирующей последовательности будет осуществляться в эукариотической клетке, сигнал полиаденилирования и последовательность терминации транскрипции будет, как правило, располагаться с 3'-конца кодирующей последовательности.
[000174] "Открытая рамка считывания", сокращенно называемая ОРС, относится к участку последовательности нуклеиновых кислот, любой из ДНК, кДНК или РНК, который содержит сигнал инициации трансляции или инициирующий кодон, такой как ATG или AUG, и терминирующий кодон и потенциально может транслироваться в полипептидную последовательность.
[000175] Термин "голова к голове" используется в данной заявке для описания ориентации двух полинуклеотидных последовательностей по отношению друг к другу. Два полинуклеотида расположены в ориентации голова к голове, когда 5'-конец кодирующей нити одного полинуклеотида расположен рядом с 5'-концом кодирующей нити другого полинуклеотида, в результате чего направление транскрипции каждого полинуклеотида продолжается в противоположную сторону от 5'-конца другого полинуклеотида. Термин "голова к голове" можно сокращенно называть (5') к (5') и можно также обозначать символами (← →) или (3'←5' 5'→3').
[000176] Термин "хвост к хвосту" используется в данной заявке для описания ориентации двух полинуклеотидных последовательностей по отношению друг к другу. Два полинуклеотида расположены в ориентации хвост к хвосту, когда 3'-конец кодирующей нити одного полинуклеотида расположен рядом с 3'-концом кодирующей нити другого полинуклеотида, в результате чего направление транскрипции каждого полинуклеотида продолжается по направлению к другому полинуклеотиду. Термин "хвост к хвосту" можно сокращенно называть (3') к (3') и можно также обозначать символами (→ ←) или (5'→3' 3'←5').
[000177] Термин "голова к хвосту" используется в данной заявке для описания ориентации двух полинуклеотидных последовательностей по отношению друг к другу. Два полинуклеотида расположены в ориентации голова к хвосту, когда 5'-конец кодирующей нити одного полинуклеотида расположен рядом с 3'-концом кодирующей нити другого полинуклеотида, в результате чего направление транскрипции каждого полинуклеотида продолжается в том же направлении, что и для другого полинуклеотида. Термин "голова к хвосту" можно сокращенно называть (5') к (3') и можно также обозначать символами (→ →) или (5'→3' 5'→3').
[000178] Термин "по ходу транскрипции" относится к последовательности нуклеотидов, которая расположена со стороны 3'-конца исходной последовательности нуклеотидов. В частности, последовательности нуклеотидов, расположенные по ходу транскрипции, как правило, относятся к последовательностям, которые следуют за точкой инициации транскрипции. Например, инициирующий кодон трансляции гена расположен по ходу транскрипции от точки инициации транскрипции.
[000179] Термин "против хода транскрипции" относится к последовательности нуклеотидов, которая расположена со стороны 5'-конца исходной последовательности нуклеотидов. В частности, последовательности нуклеотидов, расположенные против хода транскрипции, как правило, относятся к последовательностям, которые расположены на 5'-стороне от кодирующей последовательности или точки инициации транскрипции. Например, большинство промоторов расположено против хода транскрипции от точки инициации транскрипции.
[000180] Термины "эндонуклеаза рестрикции" и "рестрикционный фермент" используют взаимозаменяемо, и они относятся к ферменту, который связывается и расщепляет в сайте внутри конкретной последовательности нуклеотидов в двухцепочечной ДНК.
[000181] Термин "гомологичная рекомбинация" относится к вставке чужеродной последовательности ДНК в другую молекулу ДНК, например, к вставке вектора в хромосому. Предпочтительно, вектор нацелен на конкретный сайт в хромосоме для гомологичной рекомбинации. Для специфичной гомологичной рекомбинации, вектор должен включать достаточно длинные участки, гомологичные последовательностям хромосомы, чтобы позволить комплементарное связывание и включение вектора в хромосому. Более длинные участки гомологии и большие степени подобия последовательностей могут повысить эффективность гомологичной рекомбинации.
[000182] Для увеличения количества полинуклеотида согласно настоящему изобретению можно применять несколько способов, известных в данной области. Как только будут созданы подходящая система хозяина и условия роста, количество рекомбинантных векторов экспрессии можно увеличить и получить их в большом количестве. Как описано в данной заявке, векторы экспрессии, которые можно применять, включают следующие векторы или их производные: вирусы человека или животного, такие как вирус коровьей оспы или аденовирус; вирусы насекомых, такие как бакуловирус; дрожжевые векторы; бактериофаговые векторы (например, лямбда) и плазмидные и космидные ДНК-векторы, как пример из многих подобных, но не ограничиваются ими.
[000183] Термин "вектор" относится к любому носителю для клонирования и/или переноса нуклеиновой кислоты в клетку-хозяина. Вектор может представлять собой репликон, к которому может быть присоединен другой фрагмент ДНК таким образом, чтобы осуществить репликацию присоединенного фрагмента. Термин "репликон" относится к любому генетическому элементу (например, плазмиде, фагу, космиде, хромосоме, вирусу), который действует как автономная единица репликации ДНК in vivo, т.е., способен к репликации под своим собственным контролем. Термин "вектор" содержит как вирусные, так и невирусные носители для введения нуклеиновой кислоты в клетку in vitro, ex vivo или in vivo. Большое количество векторов, известных в данной области, можно применять для осуществления манипуляций над нуклеиновыми кислотами, введения в гены чувствительных элементов и промоторов и т.д. Возможные векторы включают, например, плазмиды или модифицированные вирусы, включая, например, бактериофаги, такие как производные бактериофага лямбда, или плазмиды, такие как производные плазмид pBR322 или pUC, или вектор Bluescript. Другой пример векторов, которые полезны для настоящего изобретения, представляет собой UltraVector™ Production System (Intrexon Corp., Блэксбург, Вирджиния), описанный в WO 2007/038276. Например, вставку фрагментов ДНК, соответствующих чувствительным элементам и промоторам, в подходящий вектор можно осуществить путем лигирования подходящих фрагментов ДНК в выбранный вектор, в котором есть комплементарные липкие концы. В качестве альтернативы, концы молекул ДНК можно ферментативно модифицировать, или можно получить любой сайт путем лигирования последовательностей нуклеотидов (линкеров) с концами ДНК. Такие векторы можно сконструировать таким образом, чтобы они содержали гены селектируемого маркера, который обеспечивает селекцию клеток, в клеточный геном которых включен указанный маркер. Такие маркеры позволяют идентификацию и/или селекцию клеток-хозяев, которые включили и экспрессируют белки, кодируемые маркером.
[000184] Вирусные векторы, и особенно ретровирусные векторы, использовались для множества различных применений, связанных с доставкой генов в клетки, а также в живых субъектов-животных. Вирусные векторы, которые можно применять, включают, но не ограничены перечисленными, ретровирусные, векторы на базе аденоассоциированного вируса, поксвирусные, бакуловирусные, векторы на базе вируса коровьей оспы, вируса простого герпеса, вируса Эпштейна-Барра, аденовирусные, геминивирусные и колимовирусные векторы. Невирусные векторы включают плазмиды, липосомы, электрически заряженные липиды (цитофектины), комплексы ДНК-белок и биополимеры. Вдобавок к нуклеиновым кислотам, вектор также может включать один или более регуляторных участков и/или селектируемых маркеров, полезных для селекции, измерения и контролирования результатов переноса нуклеиновой кислоты (в какие ткани был осуществлен перенос, продолжительность экспрессии и т.д.).
[000185] Термин "плазмида" относится к внехромосомному элементу, часто несущему ген, который не является частью основного метаболизма клетки и обычно находится в виде кольцевых молекул двухцепочечной ДНК. Такие элементы могут представлять собой автономно реплицирующиеся последовательности, встраивающиеся в геном последовательности, фаговые или нуклеотидные последовательности, линейную, кольцевую или сверхспиральную одно- или двухцепочечную ДНК или РНК, полученные из любого источника, в которых множество последовательностей нуклеотидов соединено или вновь объединено в уникальную конструкцию, которая способна вводить в клетку фрагмент промотора и последовательность ДНК выбранного продукта гена вместе с подходящей 3'-нетранслируемой последовательностью.
[000186] Термин "клонирующий вектор" относится к "репликону", который представляет собой единичный участок нуклеиновой кислоты, предпочтительно ДНК, который последовательно повторяется и который содержит точку начала репликации, такому как плазмида, фаг или космида, к которому может быть присоединен другой фрагмент нуклеиновой кислоты для осуществления репликации присоединенного фрагмента. Клонирующие векторы могут быть способны к репликации в одном типе клеток и экспрессии в другом ("челночный вектор"). Клонирующие векторы могут содержать одну или более последовательностей, которые можно использовать для селекции клеток, содержащих указанный вектор, и/или один или более сайтов множественного клонирования для вставки интересующих последовательностей.
[000187] Термин "вектор экспрессии" относится к вектору, плазмиде или носителю, разработанному, чтобы позволить экспрессию вставленной последовательности нуклеиновых кислот после трансформирования ею хозяина. Клонированный ген, т.е., вставленную последовательность нуклеиновых кислот, обычно помещают под контроль регуляторных элементов, таких как промотор, минимальный промотор, энхансер или тому подобные. Существует огромное множество регулирующих инициацию участков или промоторов, которые полезны для запуска экспрессии нуклеиновой кислоты в желательной клетке-хозяине, и они известны специалистам в данной области. В векторе экспрессии можно использовать практически любой промотор, который способен запускать экспрессию данных генов, включая вирусные промоторы, бактериальные промоторы, промоторы животных, промоторы млекопитающих, синтетические промоторы, конститутивные промоторы, тканеспецифичные промоторы, промоторы, связанные с патогенезом или заболеванием, промоторы, специфичные для определенной стадии развития, индуцируемые промоторы, регулируемые светом промоторы; CYC1, HIS3, GAL1, GAL4, GAL10, ADH1, PGK, PH05, GAPDH, ADC1, TRP1, URA3, LEW, ENO, TPI, промоторы щелочной фосфатазы (полезные для экспрессии в Saccharomyces); промотор АОХ1 (полезный для экспрессии в Pichia); р-лактамазный промотор, промоторы lac, ara, tet, trp, lPL, lPR, T7, tac и trc (полезные для экспрессии в Escherichia coli); регулируемые светом, специфичные для семян, специфичные для пыльцы, специфичные для яичника промоторы, промотор 35S вируса мозаики цветной капусты, минимальный 35S CMV, промотор вируса мозаики прожилок листа кассавы (CsVMV), промотор белка, связывающего хлорофилл а/b, рибулозо-1,5-бисфосфаткарбоксилазы, специфичный для ростков, специфичный для корней промотор, хитиназный промотор, индуцируемый стрессом промотор, промотор палочковидного тунгро-вируса риса, суперпромотор растений, промотор картофельной лейцинаминопептидазы, нитратредуктазы, маннопинсинтазы, нопалинсинтазы, убиквитина, белка зеина и антоцианина (полезные для экспрессии в клетках растений); промоторы животных и млекопитающих, известные в данной области, включая ранний промоторный участок SV40 (SV40e), промотор, содержащийся в длинном 3'-концевом повторе (LTR) вируса саркомы Рауса (RSV), промоторы Е1А или гены основных поздних промоторов (MLP) аденовирусов (Ad), ранний промотор цитомегаловируса (CMV), тимидинкиназный (ТК) промотор вируса простого герпеса (HSV), промотор бакуловируса IE1, промотор фактора элонгации 1-альфа (EF1), промотор фосфоглицераткиназы (PGK), промотор убиквитина (Ubc), промотор альбумина, регуляторные последовательности промотора металлотионеина-L мыши и участки, регулирующие транскрипцию, вездесущие промоторы (HPRT, виментина, α-актина, тубулина и тому подобных), промоторы промежуточных филаментов (десмина, нейрофиламентов, кератина, GFAP и тому подобных), промоторы терапевтических генов (MDR, CFTR или фактора VIII и тому подобных), промоторы, связанные с патогенезом или заболеванием, и промоторы, которые проявляют тканеспецифичность и использовались в трансгенных животных, такие как регуляторная область гена эластазы I, которая активна в ацинарных клетках поджелудочной железы; регуляторная область гена инсулина, активная в бета-клетках поджелудочной железы, регуляторная область гена иммуноглобулина, активная в лимфоидных клетках, регуляторная область вируса опухоли молочной железы мыши, активная в тестикулярных клетках, клетках груди, лимфоидных и тучных клетках; промотор гена альбумина, регуляторные области Аро AI и Аро AII, активные в печени, регуляторная область гена альфафетопротеина, активная в печени, регуляторная область гена альфа-1-антитрипсина, активная в печени, регуляторная область гена бета-глобина, активная в миелоидных клетках, регуляторная область гена основного белка миелина, активная в клетках олигодендроцитов в мозге, регуляторная область гена легкой цепи миозина-2, активная в скелетных мышцах, и регуляторная область гена гонадотропин-рилизинг-гормона, активная в гиппокампе, промотор пируваткиназы, промотор виллина, промотор жирной кислоты, связывающей кишечный белок, промотор α-актина клеток гладкой мускулатуры и тому подобные, но не ограничиваются ими. Вдобавок, данные экспрессионные последовательности можно модифицировать путем добавления энхансера или регуляторных последовательностей, и тому подобных.
[000188] Векторы можно вводить в желательные клетки-хозяева с помощью способов, известных в данной области, например, трансфекции, электропорации, микроинъекции, трансдукции, слияния клеток, декстрана DEAE, преципитации фосфатом кальция, липофекции (слияния лизосом), применения генной пушки или переносчика векторной ДНК (см., например, Wu и др., J. Biol. Chem. 267: 963 (1992); Wu и др., J. Biol. Chem. 267: 14621 (1988) и Hartmut и др., заявка на патент Канады номер 2,012,311).
[000189] Полинуклеотид согласно настоящему изобретению также можно ввести in vivo с помощью липофекции. В течение последнего десятилетия, возросло применение липосом для инкапсулирования и трансфекции нуклеиновых кислот in vitro. Синтетические катионные липиды, разработанные для устранения трудностей и опасений, встречающихся при опосредованной липосомами трансфекции, можно применять для получения липосом для трансфекции in vivo гена, кодирующего маркер (Felgner и др., Proc. Natl. Acad. Sci. USA. 84: 7413 (1987); Mackey и др., Proc. Natl. Acad. Sci. USA 55: 8027 (1988) и Ulmer и др., Science 259: 1745 (1993)). Применение катионных липидов может вызывать инкапсулирование отрицательно заряженных нуклеиновых кислот, а также вызывать слияние с отрицательно заряженными клеточными мембранами (Felgner и др., Science 337: 387 (1989)). Особенно полезные соединения и композиции липидов для переноса нуклеиновых кислот описаны в WO 95/18863, WO 96/17823 и в патенте США номер 5,459,127. Применение липофекции для введения экзогенных генов в определенные органы in vivo имеет некоторые практические преимущества. Молекулярное нацеливание липосом на определенные клетки представляет собой одну полезную область. Очевидно, что направление трансфекции на конкретные типы клеток будет особенно предпочтительным для ткани с клеточной гетерогенностью, такой как поджелудочная железа, печень, почка и головной мозг. Липиды можно химически присоединить к другим молекулам для нацеливания (Mackey и др. 1988, выше). Нацеливающие пептиды, например, гормоны или нейромедиаторы, и белки, такие как антитела, или непептидные молекулы можно химически присоединить к липосомам.
[000190] Для облегчения трансфекции нуклеиновой кислоты in vivo также полезны другие молекулы, такие как катионный олигопептид (например, WO 95/21931), пептиды, полученные из белков, связывающих ДНК (например, WO 96/25508), или катионный полимер (например, WO 95/21931).
[000191] Также можно ввести вектор in vivo в виде очищенной ДНК-плазмиды (см. патенты США с номерами 5,693,622, 5,589,466 и 5,580,859). Также можно использовать подходы рецептор-опосредованной доставки ДНК (Curiel и др., Hum. Gene Ther. 3: 147 (1992) и Wu и др., J. Biol. Chem. 262: 4429 (1987)).
[000192] Термин "трансфекция" относится к поглощению клеткой экзогенной или гетерологичной РНК или ДНК. Говорят, что клетка была "трансфицирована" экзогенной или гетерологичной РНК или ДНК, когда такая РНК или ДНК была введена внутрь клетки. Говорят, что клетка была "трансформирована" экзогенной или гетерологичной РНК или ДНК, когда трансфицированная РНК или ДНК влияет на фенотипические изменения. Трансформирующая РНК или ДНК может быть интегрирована (ковалентно связана) в хромосомную ДНК, составляющую геном клетки.
[000193] "Трансформация" относится к переносу фрагмента нуклеиновой кислоты в геном организма хозяина, что приводит к генетически стабильному наследованию. Организмы хозяев, содержащие трансформированные фрагменты нуклеиновых кислот, называют "трансгенными", или "рекомбинантными", или "трансформированными" организмами.
[000194] Вдобавок, рекомбинантный вектор, включающий полинуклеотид согласно настоящему изобретению, может включать одну или более точек начала репликации в клетках-хозяевах, в которых необходима их амплификация или экспрессия, маркеры или маркеры селекции.
[000195] Термин "маркер селекции" относится к фактору идентификации, обычно к антибиотику или гену химической устойчивости, по которому можно проводить селекцию на основании эффекта маркерного гена, т.е., устойчивость к антибиотику, устойчивость к гербициду, колориметрический маркер, ферменты, флуоресцентные маркеры и тому подобные, при этом указанный эффект используют для отслеживания наследования интересующей нуклеиновой кислоты и/или для идентификации клетки или организма, который унаследовал интересующую нуклеиновую кислоту. Примеры генов маркеров селекции, известных и используемых в данной области, включают: гены, обеспечивающие устойчивость к ампициллину, стрептомицину, гентамицину, канамицину, гигромицину, гербициду биалафосу, сульфонамиду и тому подобным; и гены, которые используются как фенотипические маркеры, т.е., регуляторные гены антоцианина, ген изопентанил-трансферазы и тому подобные.
[000196] Термин "репортерный ген" относится к нуклеиновой кислоте, кодирующей фактор идентификации, который можно идентифицировать на основании действия репортерного гена, при этом указанное действие используют для отслеживания наследования интересующей нуклеиновой кислоты, для идентификации клетки или организма, который унаследовал интересующую нуклеиновую кислоту, и/или для измерения индукции экспрессии гена или транскрипции. Примеры репортерных генов, известных и используемых в данной области, включают люциферазу (Luc), зеленый флуоресцентный белок (GFP), хлорамфениколацетилтрансферазу (CAT), β-галактозидазу (LacZ), β-глюкуронидазу (Gus) и тому подобные. Гены маркеров селекции также можно считать репортерными генами.
[000197] Термины "промотор" и "промоторная последовательность" используют взаимозаменяемо, и они относятся к последовательности ДНК, способной контролировать экспрессию кодирующей последовательности или функциональной РНК. Обычно, кодирующая последовательность расположена с 3'-стороны от промоторной последовательности. Промоторы можно получить целиком из нативного гена, или они могут состоять из различных элементов, полученных из различных промоторов, обнаруженных в природе, или даже включать синтетические фрагменты ДНК. Для специалиста в данной области должно быть очевидно, что различные промоторы могут управлять экспрессией гена в различных типах тканей или клеток, или на различных стадиях развития, или в ответ на различное окружение или физиологические условия. Промоторы, которые вызывают экспрессию гена в большинстве типов клеток, в большинстве случаев называют "конститутивными промоторами". Промоторы, которые вызывают экспрессию гена в определенном типе клеток, обычно называют "клеточноспецифичными промоторами" или "тканеспецифичными промоторами". Промоторы, которые вызывают экспрессию гена на определенной стадии развития или дифференцировки клеток, обычно называют "специфичными для стадии развития промоторами" или "специфичными для дифференцировки клеток промоторами". Промоторы, которые индуцируют и вызывают экспрессию гена после воздействия или обработки клетки некоторым агентом, биологической молекулой, химическим соединением, лигандом, светом или тому подобным, что приводит к индуцированию промотора, обычно называют "индуцируемыми промоторами" или "регулируемыми промоторами". Также должно быть очевидно, что поскольку в большинстве случаев точные границы регуляторных последовательностей полностью не определены, фрагменты ДНК с различными длинами могут проявлять идентичную промоторную активность.
[000198] В любом векторе согласно настоящему изобретению, указанный вектор возможно содержит промотор, описанный в данной заявке. В одном варианте реализации настоящего изобретения, указанный промотор представляет собой промотор, выбранный из перечисленных в Таблице 1 в данной заявке.
[000199] В любом векторе согласно настоящему изобретению, указанный вектор возможно содержит тканеспецифичный промотор. В одном варианте реализации, указанный тканеспецифичный промотор представляет собой тканеспецифичный промотор, описанный в данной заявке. В другом варианте реализации, тканеспецифичный промотор представляет собой тканеспецифичный промотор, выбранный из перечисленных в Таблице 2 в данной заявке.
[000200] Промоторная последовательность обычно ограничена на 3'-конце сайтом инициации транскрипции и продолжается против хода транскрипции (в 5'-направлении) таким образом, что она содержит минимальное количество оснований или элементов, необходимых для инициации транскрипции на уровнях, детектируемых выше фоновых значений. Внутри промоторной последовательности находится сайт инициации транскрипции (удобно определяемый, например, путем картирования с помощью нуклеазы S1), а также домены связывания белка (консенсусные последовательности), ответственные за связывание РНК-полимеразы.
[000201] "Промотор терапевтического переключателя" ("TSP") относится к промотору, который контролирует экспрессию компонента генного переключателя. Генные переключатели и различные их компоненты подробно описаны в других местах настоящего описания. В некоторых вариантах реализации настоящего изобретения, TSP является конститутивным, т.е., непрерывно активным. Конститутивный TSP может быть либо повсеместно конститутивным (т.е., в основном функционирующим без необходимости наличия дополнительных факторов или регуляторов, в любой ткани или клетке) или конститутивным ткане- или клеточноспецифичным (т.е., в основном функционирующим без необходимости наличия дополнительных факторов или регуляторов, в определенном типе ткани или типе клеток). В некоторых вариантах реализации, TSP согласно настоящему изобретению активируется при условиях, связанных с заболеванием, расстройством или патологическим состоянием. В некоторых вариантах реализации настоящего изобретения, когда вовлечено два или более TSP, указанные промоторы могут представлять собой комбинацию конститутивного и активируемого промоторов. В данной заявке термин "промотор, активируемый при условиях, связанных с заболеванием, расстройством или патологическим состоянием", включает, без каких-либо ограничений, специфичные для заболевания промоторы, промоторы, отвечающие на конкретные физиологические условия, стадию развития, дифференцировки или патологические состояния, промоторы, отвечающие на определенные биологические молекулы, и промоторы, специфичные для конкретного типа ткани или клеток, связанных с заболеванием, расстройством или патологическим состоянием, например, для опухолевой ткани или злокачественных клеток. TSP могут содержать последовательности встречающихся в природе промоторов, модифицированные последовательности, полученные из встречающихся в природе промоторов, или синтетические последовательности (полученные, например, путем вставки чувствительного элемента в последовательность минимального промотора для изменения отвечаемости указанного промотора).
[000202] Кодирующая последовательность находится "под контролем" контролирующих транскрипцию и трансляцию последовательностей в клетке, когда РНК-полимераза транскрибирует указанную кодирующую последовательность в мРНК, которая затем подвергается транс-сплайсингу РНК (если кодирующая последовательность содержит интроны) и транслируется в белок, кодируемый кодирующей последовательностью.
[000203] "Контролирующие транскрипцию и трансляцию последовательности" относятся к регуляторным последовательностям ДНК, таким как промоторы, энхансеры, терминаторы и тому подобные, которые обеспечивают экспрессию кодирующей последовательности в клетке-хозяине. В эукариотических клетках сигналы полиаденилирования представляют собой контролирующие последовательности.
[000204] Термин "чувствительный элемент" относится к одному или нескольким цис-действующим элементам ДНК, которые наделяют промотор способностью к ответу, опосредованному взаимодействием со связывающими ДНК доменами фактора транскрипции. Такой элемент ДНК может быть либо палиндромным (идеально или неидеально) по последовательности, либо может состоять из мотивов или полусайтов последовательности, разделенных различным числом нуклеотидов. Полусайты могут быть сходными или идентичными и могут располагаться либо в виде прямых или инвертированных повторов, либо в виде отдельного полусайта или мультимеров расположенных последовательно примыкающих полусайтов. Чувствительный элемент может включать минимальный промотор, выделенный из организмов, отличных от природы клетки или организма, в который включили чувствительный элемент. Связывающий ДНК домен фактора транскрипции связывается, в присутствии или отсутствии лиганда, с последовательностью ДНК чувствительного элемента, чтобы инициировать или подавить транскрипцию гена(ов), расположенного по ходу транскрипции, находящегося под регуляцией данного чувствительного элемента. Примеры последовательностей ДНК чувствительных элементов природного рецептора экдизона включают: RRGG/TTCANTGAC/ACYY (SEQ ID NO:25) (см. Cherbas и др., Genes Dev. 5: 120 (1991)); AGGTCAN(n)AGGTCA, где N(n) может представлять собой один или более спейсерных нуклеотидов (SEQ ID NO:26) (см. D'Avino и др., Mol. Cell. Endocrinol. 113:1 (1995)), и GGGTTGAATGAATTT (SEQ ID NO:27) (см. Antoniewski и др., Mol. Cell Biol. 74: 4465 (1994)).
[000205] Термин "функционально связанный" относится к такой связи последовательностей нуклеиновых кислот на одном участке нуклеиновой кислоты, что на функцию одной из них влияет другая. Например, промотор функционально связан с кодирующей последовательностью, когда он способен влиять на экспрессию данной кодирующей последовательности (т.е., данная кодирующая последовательность находится под транскрипционным контролем указанного промотора). Кодирующие последовательности могут быть функционально связаны с регуляторньми последовательностями в смысловой или антисмысловой ориентации.
[000206] Термин "экспрессия" в данной заявке относится к транскрипции и стабильному накоплению смысловой (мРНК) или антисмысловой РНК, полученной из нуклеиновой кислоты или полинуклеотида. Экспрессия также может относиться к трансляции мРНК в белок или полипептид.
[000207] Термины "кассета", "кассета экспрессии" и "кассета экспрессии генов" относятся к фрагменту ДНК, который можно вставить в нуклеиновую кислоту или полинуклеотид в определенных рестрикционных сайтах или путем гомологичной рекомбинации. Указанный фрагмент ДНК содержит полинуклеотид, который кодирует интересующий полипептид, а кассета и сайты рестрикции разработаны таким образом, чтобы они гарантировали вставку кассеты в правильную рамку считывания для транскрипции и трансляции. "Кассета для трансформации" относится к определенному вектору, содержащему полинуклеотид, который кодирует интересующий полипептид, и вдобавок к указанному полинуклеотиду содержит элементы, которые способствуют трансформации определенной клетки-хозяина. Кассеты, кассеты экспрессии, кассеты экспрессии генов и кассеты для трансформации согласно настоящему изобретению также могут включать элементы, которые вызывают усиленную экспрессию полинуклеотида, кодирующего интересующий полипептид, в клетке-хозяине. Данные элементы могут включать последовательность промотора, минимального промотора, энхансера, чувствительного элемента, терминатора, последовательность полиаденилирования и тому подобные последовательности, но не ограничиваются ими.
[000208] Для целей настоящего изобретения, термин "генный переключатель" относится к комбинации чувствительного элемента, связанного с промотором, и системы, основанной на лиганд-зависимом факторе транскрипции, которая, в присутствии одного или нескольких лигандов, модулирует экспрессию гена, в который включены чувствительный элемент и промотор. Термин "полинуклеотид, кодирующий генный переключатель", относится к комбинации чувствительного элемента, связанного с промотором, и полинуклеотида, кодирующего систему, основанную на лиганд-зависимом факторе транскрипции, которая, в присутствии одного или нескольких лигандов, модулирует экспрессию гена, в который включены чувствительный элемент и промотор.
[000209] Промоторы терапевтических переключателей согласно настоящему изобретению могут представлять собой любой промотор, который пригоден для лечения, облегчения или предотвращения определенного заболевания, расстройства или патологического состояния. Примеры включают, без каких-либо ограничений, промоторы генов, которые проявляют повышенную экспрессию только во время определенного заболевания, расстройства или патологического состояния, и промоторы генов, которые проявляют повышенную экспрессию при определенных состояниях клетки (например, пролиферация, апоптоз, изменение рН, состояния окисления, уровня кислорода). В некоторых вариантах реализации настоящего изобретения, когда генный переключатель содержит более чем одну последовательность фактора транскрипции, специфичность терапевтических способов можно повысить путем комбинирования специфичного для заболевания или патологического состояния промотора с промотором, специфичным для типа ткани или клеток, чтобы ограничить ткани, в которых будет экспрессироваться терапевтический продукт. Таким образом, промоторы, специфичные для типа ткани или клеток, входят в объем определения промотора терапевтического переключателя.
[000210] В качестве примера специфичных для заболевания промоторов, к пригодным промоторам для лечения рака относятся промоторы онкогенов. Примеры классов онкогенов включают факторы роста, рецепторы факторов роста, протеинкиназы, регуляторы программированной гибели клетки и факторы транскрипции, но не ограничиваются ими. Конкретные примеры онкогенов включают sis, erb В, erb B-2, ras, abl, myc и bcl-2 и TERT, но не ограничиваются ими. Примеры других связанных с раком генов включают гены опухолеспецифического антигена и другие гены, экспрессия которых повышена в неопластических клетках (например, MAGE-1, раково-эмбриональный антиген, тирозиназа, специфический антиген предстательной железы, специфический мембранный антиген предстательной железы, р53, MUC-1, MUC-2, MUC-4, HER-2/neu, T/Tn, MART-1, gp100, GM2, Tn, sTn и антиген Томпсена-Фриденрайха (TF)).
[000211] Примеры промоторных последовательностей и других регуляторных элементов (например, энхансеров), которые известны в данной области и пригодны в качестве промоторов терапевтического переключателя в настоящем изобретении, описаны в ссылках, перечислены в Таблицах 1 и 2, наряду с заболеванием/расстройством (Таблица 1) или тканеспецифичностью (Таблица 2), связанной с каждым промотором. Промоторные последовательности, описанные в данных ссылках, полностью включены в настоящее описание посредством ссылки.
[000212] Другие гены, которые демонстрируют изменения в уровнях экспрессии во время определенных заболеваний или расстройств и, следовательно, могут обеспечивать промоторы, которые пригодны для настоящего изобретения, включают гены (наряду со связанным с ними заболеванием/расстройством), перечисленные в Таблице 3, но не ограничиваются ими.
[000213] Как только определен ген, паттерн экспрессии которого модулируется во время заболевания, расстройства или патологического состояния, промотор данного гена можно использовать в генном переключателе согласно настоящему изобретению. Последовательности многих генов, включая промоторные участки, известны в данной области и доступны в открытых базах данных, например, в GenBank. Таким образом, как только идентифицирован подходящий ген, можно легко идентифицировать и получить его промоторную последовательность. Другой аспект настоящего изобретения направлен на идентификацию подходящих генов, промотор которых можно выделить и поместить в генный переключатель. Сущность указанного гена, следовательно, может быть не важна для конкретных вариантов реализации настоящего изобретения, при условии, что промотор можно выделить и использовать впоследствии в другой обстановке или окружении. Настоящее изобретение, таким образом, включает применение промоторов из генов, которые еще предстоит идентифицировать. Как только подходящие гены идентифицированы, определение генетических последовательностей, необходимых для промоторной функции, становится вопросом обычных профессиональных навыков или экспериментирования. Действительно, существует несколько коммерческих протоколов, помогающих определить промоторный участок интересующих генов. В качестве примера. Ding и др. недавно выявили промоторную последовательность нового гена Sprouty4 (Am. J. Physiol. Lung Cell. Mol. Physiol. 287: L52 (2004), которая включена посредством ссылки) путем постепенного удаления 5'-фланкирующей последовательности гена Sprouty4 человека. Вкратце, как только определили сайт инициации транскрипции, получили ПЦР-фрагменты, применяя общие ПЦР-праймеры, чтобы клонировать фрагменты 5'-фланкирующего фрагмента в одном направлении. Полученные фрагменты клонировали в люциферазный репортерный вектор и измеряли активность люциферазы, чтобы определить промоторную область гена Sprouty4 человека.
[000214] Другой пример протокола для получения и подтверждения промоторов генов содержит следующие этапы: (1) получение образцов пораженной болезнью и не пораженной болезнью клетки/ткани сходного/того же типа ткани; (2) выделение общей РНК или мРНК из образцов; (3) осуществление дифференциального анализа на микрочипе РНК из пораженного болезнью и не пораженного болезнью материала; (4) идентификацию кандидатов специфичных для заболевания транскриптов; (5) идентификацию геномных последовательностей, связанных со специфичными для заболевания транскриптами; (6) получение или синтез последовательности ДНК против хода транскрипции и по ходу транскрипции от предсказанного сайта инициации транскрипции специфичного для заболевания транскрипта; (7) разработка и получение промоторных репортерных векторов, используя участки ДНК различной длины из этапа 6; и (8) тестирование промоторных репортерных векторов в пораженных болезнью и не пораженных болезнью клетках/тканях, а также в неродственных клетках/тканях.
[000215] Источник, из которого получают промотор, который вставляют в генный переключатель, может быть природным или синтетическим, и источник промотора не должен ограничивать объем настоящего изобретения, описанного в данной заявке. Другими словами, промотор можно непосредственно клонировать из клеток, или промотор может быть клонирован ранее из отличного источника, или промотор может быть синтезирован ранее.
Системы генных переключателей
[000216] Генный переключатель может представлять собой любой генный переключатель, который регулирует экспрессию гена при добавлении или удалении определенного лиганда. В одном варианте реализации настоящего изобретения, генный переключатель представляет собой такой генный переключатель, в котором уровень экспрессии гена зависит от уровня присутствующего лиганда. Примеры комплексов лиганд-зависимых факторов транскрипции, которые можно применять в генных переключателях согласно настоящему изобретению, включают члены суперсемейства ядерных рецепторов, активируемых подходящими лигандами (например, глюкокортикоидом, эстрогеном, прогестином, ретиноидом, экдизоном и их аналогами и миметиками), и rTTA, активируемый тетрациклином, но не ограничиваются ими. В одном аспекте настоящего изобретения, генный переключатель представляет собой основанный на EcR генный переключатель. Примеры таких систем включают системы, описанные в патентах США с номерами 6,258,603, 7,045,315, опубликованных патентных заявках США с номерами 2006/0014711, 2007/0161086 и в опубликованной заявке на международный патент с номером WO 01/70816, но не ограничиваются ими. Примеры систем химерного рецептора экдизона описаны в патенте США номер 7,091,038, опубликованных патентных заявках США с номерами 2002/0110861, 2004/0033600, 2004/0096942, 2005/0266457 и 2006/0100416 и опубликованных международный заявках с номерами WO 01/70816, WO 02/066612, WO 02/066613, WO 02/066614, WO 02/066615, WO 02/29075, WO 2005/108617, каждая из которых полностью включена посредством ссылки. Пример системы, регулируемой нестероидным агонистом экдизона, представляет собой индуцируемую систему экспрессии у млекопитающего RheoSwitch® (New England Biolabs, Ипсвич, Массачусетс). В другом аспекте настоящего изобретения, генный переключатель основан на гетеродимеризации белка, связывающего FK506 (FKBP), с FKBP-рапамицин-связанным белком (FRAP) и регулируется с помощью рапамицина или его неиммуносупрессорных аналогов. Примеры таких систем включают транскрипционную технологию ARGENT™ (ARIAD Pharmaceuticals, Кембридж, Массачусетс) и системы, описанные в патентах США с номерами 6,015,709, 6,117,680, 6,479,653, 6,187,757 и 6,649,595, но не ограничиваются ими.
[000217] В одном варианте реализации настоящего изобретения, указанный генный переключатель содержит одну последовательность фактора транскрипции, кодирующую комплекс лиганд-зависимого фактора транскрипции под контролем промотора терапевтического переключателя. Последовательность фактора транскрипции может кодировать комплекс лиганд-зависимого фактора транскрипции, который представляет собой встречающийся в природе или искусственный комплекс лиганд-зависимого фактора транскрипции. Искусственный фактор транскрипции представляет собой такой фактор транскрипции, в котором природная последовательность фактора транскрипции была изменена, например, путем введения мутации в последовательность или путем объединения доменов из различных факторов транскрипции. В одном варианте реализации, фактор транскрипции содержит лигандсвязывающий домен ядерного рецептора группы Н. В одном варианте реализации настоящего изобретения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона, вездесущего рецептора (UR), сиротского рецептора 1 (OR-1), ядерного рецептора стероидных гормонов 1 (NER-1), белка, взаимодействующего с рецептором ретиноида Х-15 (RIP-15), Х-рецептора-бета печени (LXRβ), белка, подобного рецептору стероидных гормонов (RLD-1), X-рецептора печени (LXR), Х-рецептора-альфа печени (LXRα), фарнезоид-Х-рецептора (FXR), взаимодействующего с рецептором белка 14 (RIP-14) или рецептора фарнезола (HRR-1). В другом варианте реализации настоящего изобретения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
А. Основанный на экдизоне генный переключатель
[000218] EcR и другие ядерные рецепторы группы Н представляют собой члены суперсемейства ядерных рецепторов, все члены которого, как правило, отличаются присутствием аминоконцевого домена трансактивации (AD, также называемого взаимозаменяемо "ТА" или "TD"), возможно слитого с партнером по гетеродимеризации (HP) с получением коактиваторного белка (CAP), связывающего ДНК домена (DBD) и лигандсвязывающего домена, соединенного с DBD с помощью шарнирного участка с получением лиганд-зависимого фактора транскрипции (LTF). В данной заявке, термин "связывающий ДНК домен" включает минимальную полипептидную последовательность связывающего ДНК белка, вплоть до полной длины связывающего ДНК белка, при условии, что функция связывающего ДНК домена состоит в связывании с конкретным чувствительным элементом. Члены суперсемейства ядерных рецепторов также отличаются присутствием четырех или пяти доменов: А/В, С, D, Е и, в некоторых членах семейства, F (см. US 4,981,784 и Evans, Science 240: 889 (1988)). Домен "А/В" соответствует домену трансактивации, "С" соответствует связывающему ДНК домену, "D" соответствует шарнирному участку и "Е" соответствует лигандсвязывающему домену. Некоторые члены указанного семейства также могут содержать другой домен трансактивации на карбоксильном конце лигандсвязывающего домена, соответствующий "F".
[000219] Следующая полипептидная последовательность была описана как полипептидная последовательность рецептора экдизона (экдистероидного рецептора) (рецептора 20-гидроксиэкдизона) (20Е-рецептора) (EcRH) (член 1 группы Н подсемейства 1 ядерных рецепторов) и имеет номер доступа в Genbank Р34021.
[000220] Рецептор экдизона (878 АК) из Drosophila melanogaster (плодовой мушки) (SEQ ID NO:5)


[000221] DBD характеризуется присутствием двух цистеиновых цинковых пальцев, между которыми расположены два аминокислотных мотива, Р-бокс и D-бокс, которые придают специфичность чувствительным элементам. Данные домены могут быть нативными, модифицированными или химерами различных доменов гетерологичных рецепторных белков. EcR, как подгруппа семейства ядерных рецепторов, также содержит менее четко определенные участки, ответственные за свойства гетеродимеризации. Так как домены ядерных рецепторов блочные по своей природе, LBD, DBD и AD можно взаимозаменять.
[000222] В другом варианте реализации настоящего изобретения, фактор транскрипции содержит AD, DBD, который узнает чувствительный элемент, связанный с терапевтическим белком или терапевтическим полинуклеотидом, экспрессию которого нужно модулировать; и LBD ядерного рецептора группы Н. В некоторых вариантах реализации настоящего изобретения, LBD ядерного рецептора группы Н содержит мутацию с заменой.
[000223] В другом варианте реализации настоящего изобретения, генный переключатель содержит первую последовательность фактора транскрипции, например, CAP, под контролем первого промотора терапевтического переключателя (TSP-1), и вторую последовательность фактора транскрипции, например, LTF, под контролем второго промотора терапевтического переключателя (TSP-2), при этом указанные белки, кодируемые указанной первой последовательностью фактора транскрипции и указанной второй последовательностью фактора транскрипции, взаимодействуют с образованием белкового комплекса (LDTFC), т.е., представляет собой генный переключатель, основанный на "двойном переключателе" или на "двухгибридной" системе. Первый и второй TSP могут быть одинаковыми или различными. В данном варианте реализации, присутствие в генном переключателе двух различных TSP, которые необходимы для экспрессии терапевтической молекулы, повышает специфичность указанного способа терапии (см. Фигуру 2). На Фигуре 2 также продемонстрирована возможность модификации терапевтического генного переключателя для лечения любого заболевания, расстройства или патологического состояния путем всего лишь вставки подходящих TSP.
[000224] В дополнительном варианте реализации настоящего изобретения, как первая, так и вторая последовательность фактора транскрипции, например, CAP или LTF, находятся под контролем одного промотора терапевтического переключателя (например, TSP-1 на Фигуре 1). Активация данного промотора приведет к получению обоих CAP и LTF в одной открытой рамке считывания. Этого можно достигнуть, применяя транскрипционный линкер, такой как IRES (участок внутренней посадки рибосомы). В данном варианте реализации настоящего изобретения, обе части комплекса лиганд-зависимого фактора транскрипции синтезируются при активации TSP-1. TSP-1 может представлять собой конститутивный промотор или может активироваться лишь при условиях, связанных с заболеванием, расстройством или патологическим состоянием.
[000225] В дополнительном варианте реализации настоящего изобретения, одна последовательность фактора транскрипции, например, LTF, находится под контролем промотора терапевтического переключателя, активируемого лишь при условиях, связанных с заболеванием, расстройством или патологическим состоянием (например, TSP-2 или TSP-3 на Фигуре 4), и другая последовательность фактора транскрипции, например, CAP, находится под контролем конститутивного промотора терапевтического переключателя (например, TSP-1 на Фигуре 4). В данном варианте реализации настоящего изобретения, одна часть комплекса лиганд-зависимого фактора транскрипции присутствует конститутивно, тогда как вторая часть будет синтезироваться лишь при условиях, связанных с заболеванием, расстройством или патологическим состоянием.
[000226] В другом варианте реализации настоящего изобретения, одна последовательность фактора транскрипции, например, CAP, находится под контролем первого TSP (например, TSP-1 на Фигуре 3) и две или более отличных вторых последовательностей фактора транскрипции, например, LTF-1 и LTF-2, находятся под контролем различных TSP (например, TSP-2 и TSP-3 на Фигуре 3). В данном варианте реализации настоящего изобретения, каждый из LTF может содержать отличные DBD, которые узнают промоторную последовательность, регулируемую отличным фактором (например, DBD-A связывается с чувствительным элементом, связанным с регулируемым фактором промотором-1 (FRP-1), и DBD-B связывается с чувствительным элементом, связанным с регулируемым фактором промотором-2 (FRP-2). Каждый из регулируемых фактором промоторов может быть функционально связан с различными терапевтическими генами. Таким образом, можно обеспечить множество лекарственных средств одновременно.
[000227] В одном варианте реализации настоящего изобретения, первая последовательность фактора транскрипции кодирует полипептид, включающий AD, DBD, который узнает чувствительный элемент, связанный с последовательностью терапевтического продукта, экспрессию которого нужно модулировать; и лигандсвязывающий домен ядерного рецептора группы Н, и вторая последовательность фактора транскрипции кодирует фактор транскрипции, включающий лигандсвязывающий домен ядерного рецептора, выбранного из ретиноид-Х-рецептора (RXR) позвоночного, RXR беспозвоночного, белка ultraspiracle (USP), или химерного ядерного рецептора, включающего по меньшей мере два различных полипептидных фрагмента лигандсвязывающего домена ядерного рецептора, выбранных из RXR позвоночного, RXR беспозвоночного и USP (см. WO 01/70816 А2 и US 2004/0096942 А1). "Партнерский" лигандсвязывающий домен ядерного рецептора может дополнительно включать мутацию укорачивания, делеционную мутацию, мутацию с заменой или другие модификации.
[000228] В другом варианте реализации настоящего изобретения, генный переключатель содержит первую последовательность фактора транскрипции, кодирующую первый полипептид, содержащий лигандсвязывающий домен и DBD ядерного рецептора, который узнает чувствительный элемент, связанный с последовательностью терапевтического продукта, экспрессию которого нужно модулировать, и вторую последовательность фактора транскрипции, кодирующую второй полипептид, содержащий AD и лигандсвязывающий домен ядерного рецептора, при этом один из лигандсвязывающих доменом ядерного рецептора представляет собой лигандсвязывающий домен ядерного рецептора группы Н. В предпочтительном варианте реализации настоящего изобретения, первый полипептид по существу свободен от AD и второй полипептид по существу свободен от DBD. Для целей настоящего изобретения, "по существу свободный" означает, что белок, о котором идет речь, не содержит достаточную последовательность домена, о котором идет речь, чтобы обеспечить активирующую или связывающую активность.
[000229] В другом аспекте настоящего изобретения, первая последовательность фактора транскрипции кодирует белок, содержащий партнера по гетеродимеризации и AD ("CAP"), и вторая последовательность фактора транскрипции кодирует белок, содержащий DBD и лигандсвязывающий домен ("LTF").
[000230] Если один лигандсвязывающий домен (LBD) ядерного рецептора представляет собой LBD группы Н, другой лигандсвязывающий домен ядерного рецептора может быть получен из любого другого ядерного рецептора, который образует димер с LBD группы Н. Например, когда LBD ядерного рецептора группы Н представляет собой LBD EcR, другой "партнер" LBD ядерного рецептора может быть из EcR, RXR позвоночного, RXR беспозвоночного, белка ultraspiracle (USP) или химерного ядерного рецептора, содержащего по меньшей мере два различных полипептидных фрагмента LBD ядерного рецептора, выбранных из RXR позвоночного, RXR беспозвоночного или USP (см. WO 01/70816 А2, международную патентную заявку номер PCT/US02/05235 и US 2004/0096942 A1, полностью включенные в настоящее описание посредством ссылки). "Партнер" LBD ядерного рецептора может дополнительно содержать мутацию укорачивания, делеционную мутацию, мутацию с заменой или другую модификацию.
[000231] В одном варианте реализации настоящего изобретения, LBD RXR позвоночного получают из RXR человека Homo sapiens, мыши Mus musculus, крысы Rattus norvegicus, цыпленка Gallus gallus, свиньи Sus scrofa domestica, лягушки Xenopus laevis, данио Danio rerio, оболочника Polyandrocarpa misakiensis или медузы Tripedalia cysophora.
[000232] В одном варианте реализации настоящего изобретения, LBD RXR беспозвоночного получают из полипептида ultraspiracle саранчи Locusta migratoria ("LmUSP"), гомолога 1 RXR иксодового клеща Amblyomma americanum ("AmaRXRl"), гомолога 2 RXR иксодового клеща Amblyomma americanum ("AmaRXR2"), гомолога RXR манящего краба Celuca pugilator ("CpRXR"), гомолога RXR мучного жука Tenebrio Molitor ("TmRXR"), гомолога RXR медоносной пчелы Apis mellifera ("AmRXR"), гомолога RXR тли Myzus persicae ("MpRXR") или гомолога RXR недвукрылых/нечешуекрылых.
[000233] В одном варианте реализации настоящего изобретения, химерный LBD RXR содержит по меньшей мере два полипептидных фрагмента, выбранных из полипептидного фрагмента RXR позвоночных видов, полипептидного фрагмента RXR беспозвоночных видов или полипептидного фрагмента гомолога RXR беспозвоночных видов недвукрылых/нечешуекрылых. Химерный LBD RXR для применения в настоящем изобретении может содержать по меньшей мере два полипептидных фрагмента RXR различных видов, или, когда виды одинаковые, два или более полипептидных фрагмента могут быть получены из двух или более различных изоформ полипептидного фрагмента RXR указанного вида.
[000234] В одном варианте реализации настоящего изобретения, химерный LBD RXR содержит по меньшей мере один полипептидный фрагмент RXR позвоночных видов и один полипептидный фрагмент RXR беспозвоночных видов.
[000235] В другом варианте реализации настоящего изобретения, химерный LBD RXR содержит по меньшей мере один полипептидный фрагмент RXR позвоночных видов и один полипептидный фрагмент гомолога RXR беспозвоночных видов недвукрылых/нечешуекрылых.
[000236] Лиганд, когда он объединен с LBD ядерного рецептора(ов), который, в свою очередь, связан с чувствительным элементом FRP, связанного с последовательностью терапевтического продукта, обеспечивает внешнюю временную регуляцию экспрессии последовательности терапевтического продукта. Механизм связывания или порядок, в котором различные компоненты настоящего изобретения связываются друг с другом, то есть, например, лиганд с LBD, DBD с чувствительным элементом, AD с промотором и т.д., не важен.
[000237] В конкретном примере, связывание лиганда с лигандсвязывающим доменом (LBD) ядерного рецептора группы Н и с партнером LBD ядерного рецептора приводит к экспрессии последовательности терапевтического продукта. Этот механизм не исключает возможность связывания лиганда с ядерным рецептором группы Н (GHNR) или его партнером, и образование в результате этого активных гомодимерных комплексов (например, GHNR + GHNR или партнер + партнер). Предпочтительно, один или более доменов рецептора изменяют, чтобы получить гибридный генный переключатель. Обычно, один или более из трех доменов, DBD, LBD и AD, можно выбрать из источника, отличного от источника других доменов, для того, чтобы оптимизировать гибридные гены и полученные в результате этого гибридные белки в выбранной клетке-хозяине или организме по трансактивирующей активности, комплементарному связыванию лиганда и узнаванию определенного чувствительного элемента. Вдобавок, сам чувствительный элемент можно модифицировать или заменить на чувствительные элементы к доменам других связывающих ДНК белков, таких как белок GAL-4 из дрожжей (см. Sadowski и др., Nature 335: 563 (1988)) или белок LexA из Escherichia coli (см. Brent и др., Cell 43: 729 (1985)), или на синтетические чувствительные элементы, специфичные для направленных взаимодействий с белками, разработанные, модифицированные и отобранные по таким определенным взаимодействиям (см., например, Kim и др., Proc. Natl. Acad. Sci. USA, 94: 3616 (1997)), чтобы привести чувствительный элемент в соответствие с гибридными рецепторами. Другое преимущество двухгибридных систем состоит в том, что они позволяют выбрать промотор, используемый для запуска экспрессии гена, в соответствии с желательным конечным результатом. Такой двойной контроль может быть особенно важен в области генной терапии, особенно когда продуцируются цитотоксические белки, так как можно контролировать как временной интервал экспрессии, так и вид клеток, в которых будет происходить экспрессия. Когда гены, функционально связанные с подходящим промотором, вводят в клетки субъекта, экспрессию экзогенных генов контролируют с помощью системы согласно настоящему изобретению. Промоторы могут быть конститутивно или индуцибельно регулируемыми, или могут быть тканеспецифичными (то есть, экспрессироваться только в определенном типе клеток), или специфичными для некоторых стадий развития организма.
[000238] Связывающий ДНК домен первого гибридного белка связывается, в присутствии или отсутствии лиганда, с последовательностью ДНК чувствительного элемента, чтобы инициировать или подавить транскрипцию гена (генов), расположенного по ходу транскрипции, находящегося под регуляцией этого чувствительного элемента.
[000239] Функциональный LDTFC, например, комплекс EcR, также может включать дополнительный белок (белки), такой, как иммунофилин. Дополнительные члены семейства белков ядерных рецепторов, известные как транскрипционные факторы (такие как DHR38 или betaFTZ-1), также могут быть лигандзависимыми или независимыми партнерами для EcR, USP и/или RXR. Дополнительно, могут быть необходимы другие кофакторы, такие как белки, широко известные как коактиваторы (также называемые адаптерами или медиаторами). Данные белки не связываются специфично с последовательностью ДНК и не участвуют в основной транскрипции. Они могут оказывать влияние на активацию транскрипции посредством различных механизмов, включая стимуляцию связывания активаторов с ДНК, влияние на структуру хроматина или опосредованно взаимодействий активатора с инициирующим комплексом. Примеры таких коактиваторов включают RIP140, TIF1, RAP46/Bag-1, ARA70, SRC-1/NCoA-1, TIF2/GRIP/NCoA-2, ACTR/AIB1/RACS/pCIP, а также случайный коактиваторный белок, связывающий белок, связывающий цАМФ-чувствительный элемент, СВР/р300 (для обзора см. Glass и др., Curr. Орт. Cell Biol. 9: 222 (1997)). Также, кофакторы белков, широко известные как корепрессоры (также известные как репрессоры, сайленсеры или медиаторы сайленсинга), могут быть необходимы для эффективного ингибирования активации транскрипции в отсутствии лиганда. Данные корепрессоры могут взаимодействовать с не связанным с лигандом EcR, чтобы , подавлять активность на чувствительном элементе. В настоящее время имеются доказательства, которые позволяют предположить, что связывание лиганда изменяет конформацию рецептора, что приводит к высвобождению корепрессора и привлечению описанных выше коактиваторов, тем самым нарушая подавляющую активность. Примеры корепрессоров включают N-CoR и SMRT (для обзора см. Horwitz и др., Mol Endocrinol. 70: 1167 (1996)). Данные кофакторы могут быть либо эндогенными в клетке или организме, либо их можно добавить экзогенно как трансгены, которые будут экспрессироваться либо регулируемым, либо нерегулируемым образом.
В. Основанный на рапамицине генный переключатель
[000240] Настоящее изобретение дополнительно обеспечивает систему генного переключателя, в которой используется FK506-связывающий белок в качестве комплекса лиганд-зависимого фактора транскрипции и рапамицин в качестве лиганда. В одном варианте реализации настоящего изобретения, конструкция, кодирующая генный переключатель, содержит
(a) первый полинуклеотид, кодирующий первый химерный белок, который связывается с рапамицином или его аналогом, и который содержит по меньшей мере один домен РК506-связывающего белка (FKBP) и по меньшей мере один белковый домен, гетерологичный ему, при этом домен FKBP содержит пептидную последовательность, выбранную из:
(1) встречающегося в природе FKBP
(2) варианта встречающегося в природе FKBP, в котором до 10 остатков аминокислот были удалены, вставлены или заменены на заменяющие аминокислоты, и
(3) FKBP, кодируемого последовательностью ДНК, которая избирательно гибридизуется с последовательностью ДНК, кодирующей FKBP по п. (1) или (2);
(b) второй полинуклеотид, кодирующий второй химерный белок, который образует комплекс как с (а) рапамицином или аналогом рапамицина, так и с (b) первым химерным белком, и который содержит по меньшей мере один FKBP: рапамицин-связывающий (FRB) домен и по меньшей мере один белковый домен, гетерологичный ему, при этом домен FRB содержит пептидную последовательность, выбранную из:
(4) встречающегося в природе домена FRB,
(5) варианта встречающегося в природе домена FRB, в котором до 10 остатков аминокислот были удалены, вставлены или заменены на заменяющие аминокислоты, и
(6) домен FRB, кодируемый последовательностью ДНК, которая избирательно гибридизуется с последовательностью ДНК, кодирующей FRB по п. (4) или (5).
[000241] В данной системе генного переключателя, каждый из первого полинуклеотида и второго полинуклеотида находится под контролем одного или нескольких промоторов терапевтических переключателей, как описано в других местах настоящего описания. Более того, в некоторых вариантах реализации настоящего изобретения, по меньшей мере один белковый домен, гетерологичный доменам FKBP и/или FRB в первом и втором химерном белке, может представлять собой один или более доменов "действия" или "эффекторных" доменов. Эффекторные домены можно выбрать из большого разнообразия белковых доменов, включая связывающие ДНК домены, домены активации транскрипции, домены клеточной локализации и домены передачи сигнала (т.е., домены, которые способны при кластеризации или мультимеризации вызывать рост, пролиферацию, дифференцировку, апоптоз клеток, транскрипцию генов и т.д.).
[000242] В некоторых вариантах реализации настоящего изобретения, один слитый белок содержит по меньшей мере один связывающий ДНК домен (например, связывающий ДНК домен GAL4 или ZFHD1) и другой слитый белок содержит по меньшей мере один домен активации транскрипции (например, домен активации транскрипции VP16 или р65). Лиганд-опосредованная ассоциация слитых белков представляет собой образование комплекса факторов транскрипции и приводит к инициации транскрипции целевого гена, связанного с последовательностью ДНК, которая узнается (т.е., способна связываться) связывающим ДНК доменом на одном из слитых белков. Сведения относительно системы экспрессии генов, а также лиганда, приведены в патентах США с номерами 6,187,757 В1, 6,649,595 В1, 6,509,152 В1, 6,479,653 В1 и 6,117,680 В1.
[000243] В других вариантах реализации, настоящее изобретение обеспечивает систему генного переключателя, который содержит полинуклеотиды, кодирующие два слитых белка, которые подвергаются спонтанной агрегации в отсутствии лиганда, в которой (а) первый слитый белок содержит домен агрегации при определенных условиях, который связывается с выбранным лигандом, и домен активации транскрипции, и (b) второй слитый белок содержит домен агрегации при определенных условиях, который связывается с выбранным лигандом и связывающим ДНК доменом, и (с) в отсутствии лиганда, клетки экспрессируют ген, функционально связанный с регуляторной ДНК, с которой связывается указанный связывающий ДНК домен. Модифицированные клетки, содержащие систему генного переключателя, выращивают в присутствии лиганда в количестве, достаточном для репрессирования указанного гена. Удаление лиганда индуцирует экспрессию кодируемого белка, который вызывает гибель клеток. Нуклеиновые кислоты, кодирующие два указанных слитых белка, находятся под контролем по меньшей мере одного промотора, функционирующего в определенных условиях. Система экспрессии генов с применением доменов агрегации при определенных условиях описана в публикации патентной заявки США номер 2002/0048792.
С. Система генного переключателя, основанная на прокариотическом репрессоре/операторе
[000244] В одном варианте реализации, настоящее изобретение обеспечивает систему генного переключателя, содержащую (а) первый полинуклеотид, кодирующий трансактиваторный слитый белок, содержащий прокариотический репрессор тетрациклина ("tet") и домен белка эукариотического транскрипционного активатора; и (b) второй полинуклеотид, кодирующий терапевтический белок или терапевтический полипептид; в которой указанный второй полинуклеотид функционально связан с минимальным промотором и по меньшей мере одной последовательностью оператора tet. Первый полинуклеотид, кодирующий трансактиваторный слитый белок, может содержать промотор терапевтического переключателя, как описано в других местах настоящего описания. Экспрессия летального белка повышена в отсутствии тетрациклина (см., например, Gossen и др. (1992) Proc. Natl. Acad. Sci. 89: 5547-5551; Gossen и др. (1993) TIBS 18: 471-475; Furth и др. (1994) Proc. Natl. Acad. Sci. 91: 9302-9306; и Shockett и др. (1995) Proc. Natl. Acad. Sci. 92: 6522-6526). Система экспрессии TetO описана в патенте США номер 5,464,758 В1.
[000245] В другом варианте реализации настоящего изобретения, система генного переключателя содержит системы репрессора-оператора лактозы ("Lac") из бактерии Escherichia coli. Система генного переключателя согласно настоящему изобретению также может содержать (а) первый полинуклеотид, кодирующий трансактиваторный слитый белок, содержащий прокариотический репрессор lac I и домен белка эукариотического транскрипционного активатора; и (b) второй полинуклеотид, кодирующий терапевтический белок или терапевтический полипептид, в которой указанный второй полинуклеотид функционально связан с промотором терапевтического переключателя. В системе Lac, lac-оперон инактивирован в отсутствии лактозы или ее синтетических аналогов, таких как изопропил-b-D-тиогалактозид.
[000246] Дополнительные системы генных переключателей включают системы, описанные в следующих патентах: US 7,091,038; WO 2004078924; ЕР 1266015; US 20010044151; US 20020110861; US 20020119521; US 20040033600; US 20040197861; US 20040235097; US 20060020146; US 20040049437; US 20040096942; US 20050228016; US 20050266457; US 20060100416; WO 2001/70816; WO 2002/29075; WO 2002/066612; WO 2002/066613; WO 2002/066614; WO 2002/066615; WO 2005/108617; US 6,258,603; US 20050209283; US 20050228016; US 20060020146; EP 0965644; US 7,304,162; US 7,304,161; MX 234742; KR 10-0563143; AU 765306; AU 2002-248500 и AU 2002-306550.
D. Комбинация систем генных переключателей
[000247] Настоящее изобретение обеспечивает композиции нуклеиновых кислот, модифицированные клетки и биореакторы, содержащие две или более систем генных переключателей, содержащие различные комплексы лиганд-зависимых факторов транскрипции, которые активируются эффективным количеством одного или нескольких лигандов, при этом указанные две или более систем генных переключателей содержат первый генный переключатель и второй генный переключатель, оба из которых избирательно индуцируют экспрессию одного или нескольких терапевтических полипептидов или терапевтических полинуклеотидов, при связывании с одним или несколькими лигандами. В объем настоящего изобретения включены любое количество и/или любые комбинации систем генных переключателей.
[000248] В одном варианте реализации настоящее изобретение обеспечивает композицию нуклеиновых кислот, содержащую:
а. первую систему генного переключателя, который содержит:
i первую кассету экспрессии генов, содержащую полинуклеотид, кодирующий первый гибридный полипептид, который содержит:
1. домен трансактивации, который активирует регулируемый фактором промотор, функционально связанный с полинуклеотидом, кодирующим терапевтический полипептид или терапевтический полинуклеотид; и
2. домен партнера по гетеродимеризации,
ii. вторую кассету экспрессии генов, содержащую полинуклеотид, кодирующий второй гибридный полипептид, который содержит:
1. связывающий ДНК домен, который узнает регулируемый фактором промотор, функционально связанный с полинуклеотидом, кодирующим терапевтический полипептид или терапевтический полинуклеотид; и
2. лигандсвязывающий домен; и
iii. третью кассету экспрессии генов, содержащую полинуклеотид, кодирующий терапевтический полипептид или терапевтический полинуклеотид, содержащий:
1. регулируемый фактором промотор, который активируется доменом трансактивации второго гибридного полипептида; и,
2. полинуклеотид, кодирующий терапевтический полипептид или терапевтический полинуклеотид, и
b. вторую систему экспрессии генов, которая содержит:
i. первую кассету экспрессии генов, содержащую полинуклеотид, кодирующий первый гибридный полипептид, который содержит:
1. домен трансактивации, который активирует регулируемый фактором промотор, функционально связанный с полинуклеотидом, кодирующим терапевтический полипептид или терапевтический полинуклеотид; и
2. домен партнера по гетеродимеризации,
ii. вторую кассету экспрессии генов, содержащую полинуклеотид, кодирующий второй гибридный полипептид, который содержит:
1. связывающий ДНК домен, который узнает регулируемый фактором промотор, функционально связанный с полинуклеотидом, кодирующим терапевтический полипептид или терапевтический полинуклеотид; и
2. лигандсвязывающий домен; и
iii. третью кассету экспрессии генов, содержащую полинуклеотид, кодирующий терапевтический полипептид или терапевтический полинуклеотид, содержащий:
1. регулируемый фактором промотор, который активируется доменом трансактивации второго гибридного полипептида; и
2. полинуклеотид, кодирующий терапевтический полипептид или терапевтический полинуклеотид.
[000249] Множество индуцируемых систем экспрессии генов обеспечивают экспрессию данного терапевтического полинуклеотида или терапевтического полипептида в условиях, связанных с различными заболеваниями, расстройствами или патологическими состояниями, или экспрессию множества терапевтических полипептидов или терапевтических полинуклеотидов либо в тех же условиях, связанных с тем же заболеванием, расстройством или патологическим состоянием, или в отличных условиях, отличных от условий, связанных с отличными заболеваниями, расстройствами или патологическими состояниями.
[000250] В некоторых вариантах реализации настоящего изобретения, комбинация двух или более систем генных переключателей может представлять собой (1) систему экспрессии генов, основанную на двойном переключателе рецептора экдизона, и (2) генный переключатель, основанный на одинарном переключателе рецептора экдизона. В других вариантах реализации настоящего изобретения, указанная комбинация может представлять собой (1) генный переключатель, основанный на одинарном или двойном переключателе рецептора экдизона, и (2) генный переключатель, основанный на рапамицине. В качестве альтернативы, комбинация систем генных переключателей может представлять собой две идентичные системы генных переключателей, основанные на рапамицине, как описано выше. Любые возможные комбинации систем генных переключателей входят в объем настоящего изобретения.
Лиганды
[000251] В данной заявке термин "лиганд", применительно к основанным на LDTFC генным переключателям, например, основанным на EcD-комплексе генным переключателям, описывает малые и растворимые молекулы, обладающие способностью активировать генный переключатель, чтобы стимулировать экспрессию полипептида. Лиганд для комплекса лиганд-зависимого фактора транскрипции согласно настоящему изобретению связывается с белковым комплексом, содержащим один или более лигандсвязывающих доменов, домен партнера по гетеродимеризации, связывающий ДНК домен и домен трансактивации. Выбор лиганда для активации комплекса лиганд-зависимого фактора транскрипции зависит от типа используемого генного переключателя.
[000252] Примеры лигандов включают экдистероид, такой как экдизон, 20-гидроксиэкдизон, понастерон А, муристерон А и тому подобные, 9-цис-ретиноевую кислоту, синтетические аналоги ретиноевой кислоты, N,N'-диацилгидразины, такие как описанные в патентах США с номерами 6,013,836; 5,117,057; 5,530,028 и 5,378,726 и публикациях патентных заявок США с номерами 2005/0209283 и 2006/0020146; оксадиазолины, описанные в опубликованной патентной заявке США номер 2004/0171651; дибензоилалкилциангидразины, такие как описанные в европейской заявке номер 461,809; N-алкил-N,N'-диароилгидразины, такие как описанные в патенте США номер 5,225,443; N-ацил-N-алкилкарбонилгидразины, такие как описанные в европейской заявке номер 234,994; N-ароил-N-алкил-N'-ароилгидразины, такие как описанные в патенте США номер 4,985,461; амидокетоны, такие как описанные в опубликованной заявке на патент США номер 2004/0049037; каждая из которых включена в настоящее описание посредством ссылки, и в других аналогичных материалах, включая 3,5-ди-трет-бутил-4-гидрокси-N-изобутилбензамид, 8-O-ацетилгарпагид, оксистерины, 22(R)-гидроксихолестерин, 24(S)-гидроксихолестерин, 25-эпоксихолестерин, Т0901317, 5-альфа-6-альфа-эпоксихолестерин-3-сульфат (ECHS), 7-кетохолестерин-3-сульфат, фамезол, желчные кислоты, 1,1-бифосфонатные эфиры, ювенильный гормон III и тому подобные, но не ограничиваются ими. Примеры диацилгидразиновых лигандов, пригодных в настоящем изобретении, включают RG-115819 (3,5-диметилбензойной кислоты N-(1-этил-2,2-диметилпропил)-N'-(2-метил-3-метоксибензоил)гидразид), RG-115932 ((R)-3,5-диметилбензойной кислоты N-(1-трет-бутилбутил)-N'-(2-этил-3-метоксибензоил)гидразид) и RG-115830 (3,5-диметилбензойной кислоты N-(1-трет-бутилбутил)-N'-(2-этил-3-метоксибензоил)гидразид). См., например, заявку на патент США, серийный номер 12/155,111, и заявку РСТ номер PCT/US2008/006757, обе из которых полностью включены в настоящее описание посредством ссылки.
[000253] Например, лиганд для основанного на рецепторе экдизона генного переключателя можно выбрать из любых подходящих лигандов. в качестве лиганда для генного переключателя согласно настоящему изобретению можно применять как встречающийся в природе экдизон или аналоги экдизона (например, 20-гидроксиэкдизон, муристерон А, понастерон А, понастерон В, понастерон С, 26-иодпонастерон А, инокостерон или 26-мезилинокостерон), так и нестероидные индукторы. В патенте США номер 6,379,945 В1 описан стероидный рецептор насекомого, выделенный из Heliothis virescens ("HEcR"), который способен действовать как генный переключатель, отвечающий как на стероидные, так и на некоторые нестероидные индукторы. Нестероидные индукторы имеют особое преимущество над стероидными, в этой и множестве других систем, которые отвечают как на стероидные, так и на нестероидные индукторы, по многим причинам, включая, например: более низкую стоимость изготовления, метаболическую стабильность, отсутствие у насекомых, растений или млекопитающих и приемлемость для окружающей среды. В патенте США номер 6,379,945 В1 описано применение двух дибензоилгидразинов, 1,2-дибензоил-1-трет-бутилгидразина и тебуфенозида (N-(4-этилбензоил)-N'-(3,5-диметилбензоил)-N'-трет-бутилгидразина), в качестве лигандов для основанного на экдизоне генного переключателя. Также включены в настоящее изобретение в качестве лигандов другие дибензоилгидразины, такие как описанные в патенте США номер 5,117,057 В1. Применение тебуфенозида в качестве химического лиганда для рецептора экдизона из Drosophila melanogaster также описано в патенте США номер 6,147,282. Дополнительные неограничивающие примеры экдизоновых лигандов представляют собой 3,5-ди-трет-бутил-4-гидрокси-N-изобутилбензамид, 8-O-ацетилгарпагид, 1,2-диацилгидразин, N'-замещенный-N,N'-двузамещенный гидразин, дибензоилалкилциангидразин, N-замещенный-N-алкил-N,N-диароилгидразин, N-замещенный-N-ацил-N-алкилкарбонилгидразин или N-ароил-N'-алкил-N'-ароилгидразин (см. патент США номер 6,723,531).
[000254] В одном варианте реализации настоящего изобретения, лиганд для системы генного переключателя, основанной на экдизоне, представляет собой диацилгидразиновый лиганд или хиральный диацилгидразиновый лиганд. Лиганд, используемый в системе генного переключателя, может представлять собой соединения формулы I

где
А представляет собой алкоксил, арилалкилоксил или арилоксил;
В представляет собой возможно содержащий заместители арил или возможно содержащий заместители гетероарил; и
R1 и R2 независимо представляют собой возможно содержащий заместители алкил, арилалкил, гидроксиалкил, галоалкил, возможно содержащий заместители циклоалкил, возможно содержащий заместители алкенил, возможно содержащий заместители алкинил, возможно содержащий заместители гетероцикл, возможно содержащий заместители арил или возможно содержащий заместители гетероарил;
или фармацевтически приемлемые соли, гидраты, кристаллические формы или аморфные формы указанных соединений.
[000255] В другом варианте реализации настоящего изобретения, лиганд может представлять собой энантиомерно обогащенные соединения формулы II

где
А представляет собой алкоксил, арилалкилоксил, арилоксил, арилалкил, возможно содержащий заместители арил или возможно содержащий заместители гетероарил;
В представляет собой возможно содержащий заместители арил или возможно содержащий заместители гетероарил; и
R1 и R2 независимо представляют собой возможно содержащий заместители алкил, арилалкил, гидроксиалкил, галоалкил, возможно содержащий заместители циклоалкил, возможно содержащий заместители алкенил, возможно содержащий заместители алкинил, возможно содержащий заместители гетероцикл, возможно содержащий заместители арил или возможно содержащий заместители гетероарил;
при условии, что R1 не идентичен R2;
при этом абсолютная конфигурация при асимметрическом атоме углерода, несущем R1 и R2; представляет собой преимущественно S;
или фармацевтически приемлемые соли, гидраты, кристаллические формы или аморфные формы указанных соединений.
[000256] В некоторых вариантах реализации настоящего изобретения, лиганд может представлять собой энантиомерно обогащенные соединения формулы III
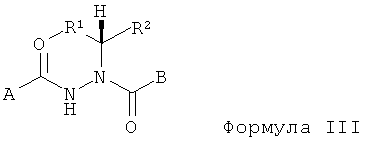
где
А представляет собой алкоксил, арилалкилоксил, арилоксил, арилалкил, возможно содержащий заместители арил или возможно содержащий заместители гетероарил;
В представляет собой возможно содержащий заместители арил или возможно содержащий заместители гетероарил; и
R1 и R2 независимо представляют собой возможно содержащий заместители алкил, арилалкил, гидроксиалкил, галоалкил, возможно содержащий заместители циклоалкил, возможно содержащий заместители алкенил, возможно содержащий заместители алкинил, возможно содержащий заместители гетероцикл, возможно содержащий заместители арил или возможно содержащий заместители гетероарил;
при условии, что R1 не идентичен R2;
при этом абсолютная конфигурация при асимметрическом атоме углерода, несущем R1 и R2, представляет собой преимущественно R;
или фармацевтически приемлемые соли, гидраты, кристаллические формы или аморфные формы казанных соединений.
[000257] В одном варианте реализации настоящего изобретения, лиганд может представлять собой (R)-3,5-диметилбензойной кислоты N-(1-трет-бутилбутил)-N'-(2-этил-3-метоксибензоил)-гидразид, с энантиомерным избытком, равным по меньшей мере 95%, или фармацевтически приемлемую соль, гидрат, кристаллическую форму или аморфную форму указанного соединения.
[000258] Диацилгидразиновые лиганды формулы I и хиральные диацилгидразиновые лиганды формулы II или III, когда они используются в основанной на экдизоне системе генного переключателя, обеспечивают средства для временной регуляции извне экспрессии терапевтического полипептида или терапевтического полинуклеотида согласно настоящему изобретению. См. заявку на патент США номер 12/155,111, поданную 29 мая, 2008 г., которая полностью включена в настоящее описание посредством ссылки.
[000259] Лиганды, используемые в настоящем изобретении, могут образовывать соли. Термин "соль(и)" в данной заявке обозначает кислые и/или основные соли, образованные с неорганическими и/или органическими кислотами и основаниями. Вдобавок, когда соединение формулы I, II или III содержит как основную молекулу, так и кислую молекулу, могут образоваться цвиттерионы ("внутренние соли"), и они также включены в объем термина "соль(и)" в настоящем описании. Используются фармацевтически приемлемые (т.е., нетоксичные, физиологически приемлемые) соли, хотя другие соли также могут быть пригодны, например, на этапах выделения или очистки при получении соединений. Соли соединений формулы I, II или III можно получить, например, путем приведения во взаимодействие соединения с некоторым количеством кислоты или основания, таким как эквивалентное количество, в среде, такой как среда, в которой соль выпадает в осадок, или в водной среде, а затем лиофилизации.
[000260] Лиганды, которые содержат основную молекулу, могут образовывать соли с целым рядом органических и неорганических кислот. Типичные соли присоединения кислоты включают ацетаты (такие как образованные с уксусной кислотой или тригалоуксусной кислотой, например, трифторуксусной кислотой), адипаты, альгинаты, аскорбаты, аспартаты, бензоаты, бензолсульфонаты, бисульфаты, бораты, бутираты, цитраты, камфораты, камфорсульфонаты, циклопентанпропионаты, диглюконаты, додецилсульфаты, этансульфонаты, фумараты, глюкогептаноаты, глицерофосфаты, гемисульфаты, гептаноаты, гексаноаты, гидрохлориды (образованные с соляной кислотой), гидробромиды (образованные с бромистым водородом), гидройодиды, 2-гидроксиэтансульфонаты, лактаты, малеаты (образованные с малеиновой кислотой), метансульфонаты (образованные с метансульфоновой кислотой), 2-нафталинсульфонаты, никотинаты, нитраты, оксалаты, пектинаты, персульфаты, 3-фенилпропионаты, фосфаты, пикраты, пивалаты, пропионаты, салицилаты, сукцинаты, сульфаты (такие как образованные с серной кислотой), сульфонаты (такие как упомянутые в настоящем описании), тартраты, тиоцианаты, толуолсульфонаты, такие как тозилаты, ундеканоаты и тому подобные.
[000261] Лиганды, которые содержат кислую молекулу, могут образовывать соли с целым рядом органических и неорганических оснований. Типичные основные соли включают соли аммония, соли щелочных металлов, такие как соли натрия, лития и калия, соли щелочно-земельных металлов, такие как соли кальция и магния, соли с органическими основаниями (например, органическими аминами), такие как бензатины, дициклогексиламины, гидрабамины (образованные с N,N-бис(дегидроабиетил)этилендиамином), N-метил-D-глюкаминами, N-метил-D-глюкамидами, трет-бутиламинами, и соли с аминокислотами, такими как аргинин, лизин и тому подобные.
[000262] Неограничивающие примеры лигандов для индуцируемой системы экспрессии генов, в которой используется связывающий FK506 домен, представляют собой FK506, циклоспорин А или рапамицин. FK506, рапамицин и их аналоги описаны в патентах США с номерами 6,649,595 В2 и 6,187,757. См. также патенты США с номерами 7,276,498 и 7,273,874.
[000263] Лиганды, описанные в данной заявке, можно вводить отдельно или в составе фармацевтической композиции, содержащей фармацевтически приемлемый носитель. В одном варианте реализации настоящего изобретения, фармацевтическая композиция находится в виде растворов, суспензий, таблеток, капсул, мазей, эликсиров или инъецируемых композиций.
[000264] Термин "основанный на рецепторе экдизона", применительно к генному переключателю, относится к генному переключателю, содержащему по меньшей мере функциональную часть встречающегося в природе или синтетического лигандсвязывающего домена рецептора экдизона, который регулирует экспрессию гена в ответ на лиганд, который связывается с лигандсвязывающим доменом рецептора экдизона. Примеры чувствительных к экдизону систем описаны в патентах США с номерами 7,091,038 и 6,258,603. В одном варианте реализации настоящего изобретения, указанная система представляет собой терапевтическую систему RheoSwitch® (RTS), которая содержит два слитых белка, домены DEF мутагенизированного рецептора экдизона (EcR), слитые со связывающим ДНК доменом Gal4, и домены EF химерного RXR, слитые с доменом активации транскрипции VP16, экспрессируемых под контролем конститутивного промотора, показанного на ФИГ.1.
[000265] Термины "модулируют" и "модулирует" означают индуцирование, уменьшение или ингибирование экспрессии нуклеиновой кислоты или гена, что приводит к соответствующей индукции, уменьшению или ингибированию продукции белка или полипептида.
[000266] Полинуклеотиды или векторы согласно настоящему изобретению могут дополнительно содержать по меньшей мере один промотор, подходящий для запуска экспрессии гена в клетке-хозяине.
[000267] Энхансеры, которые можно применять в вариантах реализации настоящего изобретения, включают энхансер SV40, энхансер цитомегаловируса (CMV), энхансер фактора элонгации 1 (EF1), дрожжевые энхансеры, энхансеры вирусных генов и тому подобные, но не ограничиваются ими.
[000268] Регуляторные области терминации, т.е., терминатор или последовательности полиаденилирования, также можно получить из различных генов, нативных для предпочтительных хозяев. Возможно, сайт терминации может не быть необходимым, тем не менее, наиболее предпочтительно, если он включен. В одном варианте реализации настоящего изобретения, регуляторная область терминации может состоять или быть получена из синтетической последовательности, синтетического сигнала полиаденилирования, сигнала полиаденилирования позднего SV40, сигнала полиаденилирования SV40, бычьего гормона роста (BGH) сигнала полиаденилирования, последовательностей вирусных терминаторов или тому подобных.
[000269] Термины "3'-некодирующие последовательности" или "3'-нетранслируемая область (НТО)" относятся к последовательностям ДНК, расположенным по ходу транскрипции (3') от кодирующей последовательности, и могут содержать последовательности узнавания полиаденилирования [поли(А)] и другие последовательности, кодирующие регуляторные сигналы, способные влиять на процессинг мРНК или экспрессию гена. Сигнал полиаденилирования обычно характеризуется влиянием на добавление участков полиадениловых кислот к 3'-концу предшественника мРНК.
[000270] "Регуляторная область" относится к последовательности нуклеиновых кислот, которая регулирует экспрессию второй последовательности нуклеиновых кислот. Регуляторная область может включать последовательности, которые в природе отвечают за экспрессию определенной нуклеиновой кислоты (гомологичная область), или может включать последовательности различного происхождения, которые отвечают за экспрессию различных белков или даже синтетических белков (гетерологичная область). В частности, указанные последовательности могут представлять собой последовательности прокариотических, эукариотических или вирусных генов, или производные последовательности, которые стимулируют или подавляют транскрипцию гена специфичным или неспецифичным образом и индуцируемым или неиндуцируемым образом. Регуляторные области включают точки начала репликации, сайты сплайсинга РНК, промоторы, энхансеры, последовательности терминации транскрипции и сигнальные последовательности, которые направляют полипептид в секреторные пути целевой клетки.
[000271] Регуляторная область из "гетерологичного источника" относится к регуляторной области, которая в природе не связана с экспрессируемой нуклеиновой кислотой. Среди всех гетерологичных регуляторных областей включены регуляторные области из различных видов, регуляторные области из различных генов, гибридные регуляторные последовательности и регуляторные последовательности, которые не встречаются в природе, но которые разработаны средним специалистом в данной области.
[000272] "РНК-транскрипт" относится к продукту, возникшему в результате катализируемой РНК-полимеразой транскрипции последовательности ДНК. Когда РНК-транскрипт представляет собой идеально комплементарную копию последовательности ДНК, его называют первичным транскриптом, или он может представлять собой последовательность РНК, полученную в результате посттранскрипционного процессинга первичного транскрипта, и называется зрелой РНК. "Информационная РНК (мРНК)" относится к РНК, которая не содержит интронов и которая может транслироваться в белок в клетке. "кДНК" относится к двунитевой ДНК, которую получают из мРНК и которая комплементарна ей. "Смысловая" РНК относится к РНК-транскрипту, который содержит мРНК и, таким образом, может транслироваться в белок в клетке. "Антисмысловая РНК" относится к РНК-транскрипту, который комплементарен всему или части целевого первичного транскрипта или мРНК, и который блокирует экспрессию целевого гена. Комплементарность антисмысловой РНК может быть на любом участке определенного транскрипта гена, т.е., на 5'-некодирующей последовательности, 3'-некодирующей последовательности или кодирующей последовательности. "Функциональная РНК" относится к антисмысловой РНК, РНК рибозима или другой РНК, которая не транслируется, но все же оказывает влияние на клеточные процессы.
[000273] Термины "полипептид", "пептид" и "белок" используют взаимозаменяемо, и они относятся к полимерному соединению, состоящему из ковалентно связанных остатков аминокислот.
[000274] Термины "изолированный полипептид", "изолированный пептид" или "изолированный белок" относятся к полипептиду или белку, который по существу свободен таких соединений, которые обычно с ним связаны в естественном состоянии (например, других белков или полипептидов, нуклеиновых кислот, углеводов, липидов). Термин "изолированный" не подразумевают исключающим искусственные или синтетические смеси с другими соединениями или присутствие примесей, которые не препятствуют его биологической активности и которые могут присутствовать, например, вследствие неполной очистки, добавления стабилизаторов или включения в состав фармацевтически приемлемого состава.
[000275] Термины "мутантный полипептид с заменой" или "мутант с заменой" должны пониматься означающими мутантный полипептид, содержащий замену по меньшей мере одной аминокислоты полипептида дикого типа или встречающегося в природе полипептида на аминокислоту, отличную от аминокислоты полипептида дикого типа или встречающегося в природе полипептида. Мутантный полипептид с заменой может содержать только одну замену аминокислоты полипептида дикого типа или встречающегося в природе полипептида и может называться "точечным мутантным" или "одноточечным мутантным" полипептидом. В качестве альтернативы, мутантный полипептид с заменой может включать замену двух или более аминокислот полипептида дикого типа или встречающегося в природе полипептида на две или более аминокислоты, отличные от аминокислот полипептида дикого типа или встречающегося в природе полипептида. Согласно настоящему изобретению, полипептид лигандсвязывающего домена ядерного рецептора группы Н, содержащий мутацию с заменой, содержит замену по меньшей мере одной аминокислоты полипептида дикого типа или встречающегося в природе полипептида на аминокислоту, отличную от аминокислоты полипептида дикого типа или встречающегося в природе полипептида лигандсвязывающего домена ядерного рецептора группы Н.
[000276] Когда мутантный полипептид с заменой содержит замену двух или более аминокислот полипептида дикого типа или встречающегося в природе полипептида, такая замена может включать либо удаление эквивалентного количества аминокислот полипептида дикого типа или встречающегося в природе полипептида, т.е., 2 аминокислоты полипептида дикого типа или встречающегося в природе полипептида замещают на 2 аминокислоты полипептида не дикого типа или не встречающегося в природе полипептида, либо удаление неэквивалентного количества аминокислот полипептида дикого типа, т.е., 2 аминокислоты полипептида дикого типа замещают на аминокислоту 1 полипептида не дикого типа (мутация замены + делеции), или 2 аминокислоты полипептида дикого типа замещают на 3 аминокислоты полипептида не дикого типа (мутация замены + вставки).
[000277] Мутанты с заменой могут быть описаны с применением системы сокращенной номенклатуры, чтобы указать аминокислотный остаток и количество аминокислот, замещенных в исходной полипептидной последовательности, и новый остаток аминокислоты, на который произвели замену. Например, мутант с заменой, в котором двадцатый (20ый) остаток аминокислоты полипептида замещен, можно сокращенно называть "x20z", где "х" представляет собой аминокислоту, которую замещают, "20" представляет собой положение остатка аминокислоты или ее номер в полипептиде и "z" представляет собой новую аминокислоту, на которую замещают. Следовательно, сокращенное взаимозаменяемое название мутанта с заменой "Е20А" или "Glu20Ala" указывает на то, что данный мутант содержит остаток аланина (обычно сокращенно называемый в данной области "А" или "Ala") на месте глютаминовой кислоты (обычно сокращенно называемой в данной области "Е" или "Glu") в положении 20 полипептида.
[000278] Мутацию с заменой можно осуществить с помощью любого способа мутагенеза, известного в данной области, включая, но не ограничиваясь перечисленными, сайт-направленный мутагенез т vitro (Hutchinson и др., J. Biol. Chem. 253: 6551 (1978); Zoller и др., DNA 3-A79 (1984); Oliphant и др., Gene 44: 177 (1986); Hutchinson и др., Proc. Natl. Acad. Set. USA 83: 710 (1986)), применение линкеров TAB® (Pharmacia), расщепление эндонуклеазами рестрикции/удаление и замену фрагмента, опосредованный ПЦР/олигонуклеотид-направленный мутагенез и тому подобные. Основанные на ПЦР методики являются предпочтительными для сайт-направленного мутагенеза (см. Higuchi, 1989, "Using PCR to Engineer DNA", в PCR Technology: Principles and Applications for DNA Amplification, H.Eriich, ред., Stockton Press, глава 6, стр.61-70).
[000279] Термин "фрагмент", применительно к полипептиду, относится к полипептиду, последовательность аминокислот которого короче, чем таковая у исходного полипептида, и который имеет идентичную данному исходному полипептиду последовательность аминокислот на всем протяжении фрагмента. Такие фрагменты, когда это уместно, могут быть включены в больший полипептид, частью которого они являются. Такие фрагменты полипептида согласно настоящему изобретению могут иметь длину, равную по меньшей мере 2, 3, 4, 5, 6, 8, 10, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 25, 26, 30, 35, 40, 45, 50, 100, 200, 240 или 300 или более аминокислот.
[000280] "Вариант" полипептида или белка относится к любому аналогу, фрагменту, производному или мутанту, который получают из полипептида или белка и который сохраняет по меньшей мере одно биологическое свойство указанного полипептида или белка. В природе могут существовать различные варианты полипептида или белка. Данные варианты могут представлять собой аллельные варианты, характеризуемые различиями в последовательностях нуклеотидов структурного гена, кодирующего белок, или могут включать альтернативный сплайсинг или посттрансляционные модификации. Квалифицированный специалист может получить варианты, содержащие одну или множество замен, делеций, вставок или перестановок аминокислот. Данные варианты могут включать, среди прочего: (а) варианты, в которых один или более остатков аминокислот замещены на консервативные или неконсервативные аминокислоты, (b) варианты, в которых одна или более аминокислот добавлены в полипептид или белок, (с) варианты, в которых одна или более аминокислот содержит замещающую группу, и (d) варианты, в которых полипептид или белок слит с другим полипептидом, таким как сывороточный альбумин. Методики получения данных вариантов, включая генетические (супрессии, делеции, мутации и т.д.), химические и ферментативные методики, известны среднему специалисту в данной области. В одном варианте реализации настоящего изобретения, вариантный полипептид содержит по меньшей мере приблизительно 14 аминокислот.
[000281] Термин "гомология" относится к проценту идентичности между двумя молекулами полинуклеотида или двумя молекулами полипептида. Сходство между последовательностью одной молекулы и другой можно определить с помощью способов, известных в данной области. Например, гомологию можно определить путем непосредственного сравнения информации о последовательности между двумя полипептидными молекулами путем выравнивания информации о последовательности и применения легко доступных компьютерных программ. В качестве альтернативы, гомологию можно определить путем гибридизации полинуклеотидов при условиях, в которых образуются стабильные дуплексы между гомологичными участками, а затем расщепления нуклеазой(ами), специфичной для одной нити, и определения размеров расщепленных фрагментов.
[000282] В данной заявке термин "гомологичный" во всех его грамматических формах и орфографических разновидностях относится к родству между белками, которые имеют "общее эволюционное происхождение", включая белки из суперсемейств (например, суперсемейства иммуноглобулинов) и гомологичные белки из различных видов (например, легкая цепь миозина и т.д.) (Reeck и др., Cell 50: 667 (1987)). Такие белки (и кодирующие их гены) имеют гомологичные последовательности, что отражает высокая степень подобия их последовательностей. Тем не менее, при обычном применении и в настоящей заявке, термин "гомологичный", когда к нему добавлено наречие, такое как "высоко", может относиться к подобию последовательностей, а не к общему эволюционному происхождению.
[000283] Соответственно, термин "подобие последовательностей" во всех его грамматических формах относится к степени идентичности или сходства между последовательностями нуклеиновых кислот или аминокислотными последовательностями белков, которые могут иметь или не иметь общее эволюционное происхождение (см. Reeck и др., Cell 50: 667 (1987)). В одном варианте реализации, две последовательности ДНК являются "по существу гомологичными" или "по существу подобными", когда по меньшей мере приблизительно 50% (например, по меньшей мере приблизительно 75%, 90% или 95%) нуклеотидов совпадают на определенном участке последовательностей ДНК. Последовательности, которые являются по существу гомологичными, можно идентифицировать путем сравнения последовательностей, применяя стандартное программное обеспечение, доступное в базах данных последовательностей, или с помощью эксперимента по гибридизации по Саузерну, например, в жестких условиях, определенных для данной конкретной системы. Определение подходящих условий гибридизации находится в рамках компетенции в данной области (см., например, Sambrook и др., 1989, выше).
[000284] В данной заявке термин "по существу подобные" относится к фрагментам нуклеиновых кислот, в которых изменение одного или нескольких нуклеотидных оснований приводит к замене одной или нескольких аминокислот, но не влияет на функциональные свойства белка, кодируемого последовательностью ДНК. "По существу подобные" также относится к фрагментам нуклеиновых кислот, в которых изменения одного или нескольких нуклеотидных оснований не влияет на способность фрагмента нуклеиновой кислоты опосредовать изменение экспрессии гена с помощью антисмыслового или косупрессорного способа. "По существу подобные" также относится к модификациям фрагментов нуклеиновых кислот согласно настоящему изобретению, таким как делеция или вставка одного или нескольких нуклеотидных оснований, которые по существу не влияют на функциональные свойства полученного транскрипта. Следовательно, должно быть очевидно, что в объем настоящего изобретения входит больше последовательностей, чем определенные последовательности, указанные в примерах. Каждая из предложенных модификаций входит в рамки обычных навыков в данной области, также как и определение сохранения биологической активности кодируемых продуктов.
[000285] Более того, для квалифицированного специалиста должно быть очевидно, что по существу подобные последовательности, входящие в объем настоящего изобретения, также определяют по их способности гибридизоваться в жестких условиях (0.1Х SSC, 0.1% ДСН, 65°С и промывке 2Х SSC, 0.1% ДСН, а затем 0.1Х SSC, 0.1% ДСН) с последовательностями, приведенными в качестве примера в данной заявке. По существу подобные фрагменты нуклеиновых кислот согласно настоящему изобретению представляют собой такие фрагменты нуклеиновых кислот, последовательности ДНК которых по меньшей мере приблизительно на 70%, 80%, 90% или 95% идентичны последовательности ДНК фрагментов нуклеиновых кислот, описанных в данной заявке.
[000286] Две последовательности аминокислот являются "по существу гомологичными" или "по существу подобными", когда более чем приблизительно 40% аминокислот идентичны, или более чем 60% аминокислот подобны (функционально идентичны). Предпочтительно, подобные или гомологичные последовательности идентифицируют путем выравнивания, применяя, например, пакет программ GCG (Genetics Computer Group, руководство по работе с программой пакета GCG, версия 7, Мэдисон, Висконсин).
[000287] Термин "соответствующий" в данной заявке относится к подобным или гомологичным последовательностям, в которых точное положение идентично или отлично от молекулы, подобие или гомологию с которой измеряют. При выравнивании последовательностей нуклеиновых кислот или аминокислот могут быть промежутки. Таким образом, термин "соответствующий" относится к подобию последовательностей, но не к нумерации остатков аминокислот или нуклеотидных оснований.
[000288]. Термин "существенная часть" последовательности аминокислот или нуклеотидов содержит достаточный участок последовательности аминокислот полипептида или последовательности нуклеотидов гена, чтобы предположительно идентифицировать этот полипептид или ген, либо путем оценки последовательности вручную специалистом в данной области, либо путем автоматизированного компьютерного сравнения последовательностей и идентификации с применением алгоритмов, таких как BLAST (основное средство поиска, основанное на локальных выравниваниях; Altschul и др., J. Mol. Biol. 275: 403 (1993)); доступное по ссылке ncbi.nlm.nih.gov/BLAST/). Обычно, необходима последовательность из десяти или более непрерывных аминокислот или из тридцати или более нуклеотидов, чтобы предположительно идентифицировать полипептид или последовательность нуклеиновых кислот как гомологичную известному белку или гену. Более того, применительно к последовательностям нуклеотидов, можно использовать специфичные для гена олигонуклеотидные зонды, содержащие 20-30 непрерывных нуклеотидов, в зависимых от последовательности способах идентификации (например, гибридизации по Саузерну) и выделения генов (например, гибридизации in situ бактериальных колоний или бактериофаговых бляшек). Вдобавок, короткие олигонуклеотиды, состоящие из 12-15 оснований, можно применять в качестве праймеров для амплификации с помощью ПЦР, чтобы получить определенный фрагмент нуклеиновой кислоты, содержащий праймеры. Соответственно, "существенная часть" последовательности нуклеотидов содержит достаточный участок последовательности, чтобы специфично идентифицировать и/или выделить фрагмент нуклеиновой кислоты, включающий указанную последовательность.
[000289] Термин "процент идентичности", известный в данной области, обозначает родство между двумя или более полипептидными последовательностями или двумя или более полинуклеотидными последовательностями, что определяют путем сравнения последовательностей. В данной области термин "идентичность" также означает степень родства последовательностей между полипептидными или полинуклеотидными последовательностями, в зависимости от конкретного случая, что определяют по совпадению между цепочками таких последовательностей. "Идентичность" и "подобие" можно легко рассчитать с помощью известных способов, включая способы, описанные в: Computational Molecular Biology (Lesk, A.M., изд.) Oxford University Press, Нью-Йорк (1988); Biocomputing: Informatics and Genome Projects (Smith, D.W., ред.) Academic Press, Нью-Йорк (1993); Computer Analysis of Sequence Data, часть I (Griffin, A.M., и Griffin, H.G., ред.) Human Press, Нью-Джерси (1994); Sequence Analysis in Molecular Biology (von Heinje, G., ред.) Academic Press (1987) и Sequence Analysis Primer (Gribskov, M. и Devereux, J., ред.) Stockton Press, Нью-Йорк (1991), но не ограничиваясь ими. Предпочтительные способы определения идентичности разработаны таким образом, чтобы можно было получить наилучшее совпадение между тестируемыми последовательностями. Способы определения идентичности и подобия запрограммированы в общедоступных компьютерных программах. Выравнивания последовательностей и вычисление процента идентичности можно осуществить, применяя программное обеспечение для анализа последовательностей, такое как программа Megalign биоинформатического вычислительного комплекса LASERGENE (DNASTAR Inc., Мэдисон, Висконсин). Выравнивание множества последовательностей можно осуществить, применяя способ выравнивания Clustal (Higgins и др., CABIOS. 5: 151 (1989)) с параметрами по умолчанию (штраф за открытие гэпа = 10, штраф за продление гэпа = 10). Можно выбрать следующие параметры по умолчанию для попарного выравнивания с помощью способа Clustal: размер идентичного участка (KTUPLE) 1, штраф за открытие гэпа = 3, за окно = 5 и за сохраненные диагонали = 5.
[000290] Термин "программное обеспечение для анализа последовательностей" относится к любому компьютерному алгоритму или программному обеспечению, которое полезно для анализа последовательностей нуклеотидов или аминокислот."Программное обеспечение для анализа последовательностей" может быть доступно для приобретения или разработано независимо. Обычное программное обеспечение для анализа последовательностей включает, но не ограничено, пакет программ GCG (Wisconsin Package, версия 9.0, Genetics Computer Group (GCG), Мэдисон, Висконсин), BLASTP, BLASTN, BLASTX (Altschul и др., J. Mol. Biol. 215: 403 (1990)) и DNASTAR (DNASTAR, Inc. 1228 S. Park St., Мэдисон, Висконсин 53715, США). В контексте настоящей заявки должно быть очевидно, что когда для анализа применяется программное обеспечение для анализа последовательностей, результаты анализа будут основаны на "значениях по умолчанию" упомянутой программы, если не указано иначе. В данной заявке "значения по умолчанию" будут означать любой набор значений или параметров, который исходно загружается с программным обеспечением, когда оно впервые устанавливается.
[000291] "Химически синтезированный", по отношению к последовательности ДНК, означает, что составляющие ее нуклеотиды были собраны in vitro. Можно осуществить химический синтез ДНК вручную, применяя надежные процедуры, или можно осуществить автоматизированный химический синтез, применяя одно из множества доступных для приобретения устройств. Соответственно, гены можно приспособить для оптимальной экспрессии исходя из оптимизации последовательности нуклеотидов, чтобы она отражала предпочтение кодонов клеткой-хозяином. Для квалифицированного специалиста очевидно, что экспрессия гена будет более успешной, если использование кодонов ориентировано на те кодоны, которые предпочитает хозяин. Определение предпочтительных кодонов может быть основано на исследовании генов, полученных из клетки-хозяина, о последовательности которых есть сведения.
[000292] В данной заявке, две или более отдельно функционирующие системы регуляции генов называют "независимыми", когда: а) модуляция каждой из данных систем соответствующим лигандом, при выбранной концентрации, приводит к измеримому изменению интенсивности экспрессии гена с этой системы, и b) указанное изменение статистически значимо отличается от изменения экспрессии всех других систем, одновременно функционирующих в клетке, ткани или организме, независимо от одновременности или последовательности фактической модуляции. Предпочтительно, модуляция каждой отдельно функционирующей системы регуляции гена влияет на изменение экспрессии этого гена по меньшей мере в 2 раза больше, чем на другие функционирующие системы в клетке, ткани или организме, например, по меньшей мере в 5 раз, в 10 раз, в 100 раз или в 500 раз больше. В идеальной ситуации, модуляция каждой из данных систем соответствующим лигандом при выбранной концентрации приводит к измеримому изменению интенсивности экспрессии гена с данной системы, при этом не происходит измеримого изменения экспрессии всех других систем, функционирующих в клетке, ткани или организме. В таких случаях, множество индуцируемых систем регуляции генов называют "полностью независимыми". Полезные независимые лиганды и независимые основанные на рецепторах системы экспрессии генов описаны в US 2002/0110861 A1.
[000293] Термин "экзогенный ген" означает ген, чужеродный для субъекта, то есть ген, который вводили в субъект с помощью процесса трансформирования, немутированную версию эндогенного мутированного гена или мутированную версию эндогенного немутированного гена. Способ трансформирования не важен для настоящего изобретения и может представлять собой любой способ, известный специалистам в данной области, подходящий для субъекта. Экзогенные гены могут представлять собой либо природные, либо синтетические гены, которые вводят субъекту в виде ДНК или РНК, которая может функционировать через ДНК-посредник, полученный, например, с помощью обратной транскриптазы. Такие гены можно вводить в целевые клетки, непосредственно вводить субъекта или вводить опосредованно путем переноса трансформированных клеток в субъекта.
[000294] Термин "терапевтический продукт" относится к терапевтическому полипептиду или терапевтическому полинуклеотиду, который наделяет полезной функцией клетку-хозяина, в которой такой продукт экспрессируется. Терапевтические полипептиды могут включать, без ограничения, настолько малые пептиды, как имеющие длину три аминокислоты, одно- или многоцепочечные белки и слитые белки. Терапевтические полинуклеотиды могут включать, без ограничения, антисмысловые олигонуклеотиды, малые интерферирующие РНК, рибозимы и внешние вспомогательные последовательности РНК. Терапевтический продукт может включать встречающуюся в природе последовательность, синтетическую последовательность или комбинацию природных и синтетических последовательностей.
[000295] Термин "комплекс лиганд-зависимого фактора транскрипции" или "LDTFC" относится к фактору транскрипции, включающему одну или более белковых субъединиц, комплекс которых может регулировать экспрессию гена, запускаемую с "регулируемого фактором промотора", что определено в настоящем описании. Модель LDTFC представляет собой "рецепторный комплекс экдизона", который, в общем смысле, относится к гетеродимерному белковому комплексу, содержащему по меньшей мере два члена семейства ядерных рецепторов: рецептор экдизона ("EcR") и белок ultraspiracle ("USP") (см. Yao и др., Nature 3 66: 476 (1993)); Yao и др., Cell 71: 63 (1992)). Функциональный LDTFC, такой как комплекс EcR, также может включать дополнительный белок (белки), такой как иммунофилин. Дополнительные члены семейства белков ядерных рецепторов, известные как транскрипционные факторы (такие как DHR38, betaFTZ-1 или другие гомологи у насекомых), также могут быть лигандзависимыми или независимыми партнерами для EcR и/или USP. LDTFC, такой как комплекс EcR, также может представлять собой гетеродимер белка EcR и гомолога у позвоночных белка ultraspiracle, белка Х-рецептора ретиноевой кислоты ("RXR") или химеры USP и RXR. Также в объем терминов "LDTFC" и "комплекс EcR" входят гомодимерные комплексы белка EcR или USP, а также отдельные полипептиды или тримеры, тетрамеры и другие мультимеры, обладающие такой же функцией.
[000296] LDTFC, такой как комплекс EcR, можно активировать активным экдистероидным или нестероидным лигандом, который связывается с одним из белков комплекса, включая EcR, но не исключая другие белки комплекса. LDTFC, такой как комплекс EcR, содержит белки, которые представляют собой члены суперсемейства ядерных рецепторов, в котором все члены характеризуются присутствием одной или нескольких полипептидных субъединиц, включающих аминоконцевой домен трансактивации ("AD", "TD" или "ТА", используемые взаимозаменяемо в данной заявке), связывающий ДНК домен ("DBD") и лигандсвязывающий домен ("LBD"). AD может присутствовать в виде гибридного белка с "партнером по гетеродимеризации" или "HP". Гибридный белок, включающий AD и HP согласно настоящему изобретению, называется в данной заявке "коактиваторным белком" или "CAP". DBD и лигандсвязывающий домен могут экспрессироваться в виде слитого белка, называемого в данной заявке "лиганд-индуцируемым фактором транскрипции" ("LTF"). Партнеры слияния можно разделить с помощью линкера, например, шарнирного участка. Некоторые члены семейства LTF также могут включать другой домен трансактивации на карбоксильном конце LBD. DBD характеризуется присутствием двух цистеиновых цинковых пальцев, между которыми расположены два аминокислотных мотива, Р-бокс и D-бокс, которые придают специфичность к чувствительным к экдизону элементам. Данные домены могут быть нативными, модифицированными или химерами различных доменов гетерологичных рецепторных белков.
[000297] Последовательности ДНК, составляющие экзогенный ген, чувствительный элемент и LDTFC, например, комплекс EcR, можно включить в архебактерии, прокариотические клетки, такие как Escherichia coli. Bacillus subtilis или другие энтеробактерии, или эукариотические клетки, такие как клетки растений или животных. Тем не менее, так как многие белки, экспрессируемые геном, подвергаются некорректному процессингу в бактериях, эукариотические клетки являются предпочтительными. Клетки могут быть в виде отдельных клеток или в виде многоклеточных организмов. Последовательности нуклеотидов для экзогенного гена, чувствительного элемента и рецепторного комплекса также можно ввести в виде молекул РНК, предпочтительно в виде функциональных вирусных РНК, таких как вирус табачной мозаики. Из эукариотических клеток, клетки позвоночных являются предпочтительными, так как в них обычно отсутствуют молекулы, которые придают EcR способность отвечать на лиганды согласно настоящему изобретению. В результате, они "по существу нечувствительны" к лигандам согласно настоящему изобретению. Таким образом, лиганды, полезные для настоящего изобретения, будут оказывать незначительное физиологическое или другое влияние на трансформированные клетки или на весь организм. Следовательно, клетки могут расти и экспрессировать желательный продукт, при этом на них по существу не влияет присутствие самого лиганда.
[000298] Термин "рецепторный комплекс экдизона" в общем смысле относится к гетеродимерному белковому комплексу, содержащему по меньшей мере два элемента из семейства ядерных рецепторов, рецептора экдизона ("EcR") и белков ultraspiracle ("USP") (см. Yao и др., Nature 366: 476 (1993)); Yao и др., Cell 71: 63 (1992)). Функциональный комплекс EcR также может содержать дополнительный белок (белки), такой как иммунофилин. Дополнительные члены семейства белков ядерных рецепторов, известные как транскрипционные факторы (такие как DHR38, betaFTZ-1 или другие гомологи насекомых), также могут быть лигандзависимыми или независимыми партнерами для EcR и/или USP. Комплекс EcR также может представлять собой гетеродимер белка EcR и гомолога у позвоночных белка ultraspiracle, белка Х-рецептора ретиноевой кислоты ("RXR") или химеры USP и RXR. Также в объем термина комплекс EcR входят гомодимерные комплексы белка EcR или USP.
[000299] Комплекс, EcR можно активировать активным экдистероидным или нестероидным лигандом, который связывается с одним из белков комплекса, включая EcR, но не исключая другие белки комплекса. В данной заявке термин "лиганд", применительно к основанным на EcR генным переключателям, описывает малые и растворимые молекулы, обладающие способностью активировать генный переключатель, чтобы стимулировать экспрессию полипептида, кодируемого им. Примеры лигандов включают, без ограничения, экдистероид, такой как экдизон, 20-гидроксиэкдизон, понастерон А, муристерон А и тому подобные, 9-цис-ретиноевую кислоту, синтетические аналоги ретиноевой кислоты, N,N'-диацилгидразины, такие как описанные в патентах США с номерами 6,013,836; 5,117,057; 5,530,028 и 5,378,726 и публикациях патентных заявок США с номерами 2005/0209283 и 2006/0020146; оксадиазолины, описанные в опубликованной заявке на патент США номер 2004/0171651; дибензоилалкилциангидразины, такие как описанные в европейской заявке номер 461,809; N-алкил-N,N'-диароилгидразины, такие как описанные в патенте США номер 5,225,443; N-ацил-N-алкилкарбонилгидразины, такие как описанные в европейской заявке патент номер 234,994; N-ароил-N-алкил-N'-ароилгидразины, такие как описанные в патенте США номер 4,985,461; амидокетоны, такие как описанные в опубликованной заявке на патент США номер 2004/0049037; и другие подобные материалы, включая 3,5-ди-трет-бутил-4-гидрокси-N-изобутилбензамид, 8-O-ацетилгарпагид, оксистерины, 22(R) гидроксихолестерин, 24(S)-гидроксихолестерин, 25-эпоксихолестерин, Т0901317, 5-альфа-6-альфа-эпоксихолестерин-3-сульфат (ECHS), 7-кетохолестерин-3-сульфат, фамезол, желчные кислоты, 1,1-бифосфонатные эфиры, ювенильный гормон III и тому подобные. Примеры диацилгидразиновых лигандов, полезных для настоящего изобретения, включают RG-115819 (3,5-диметилбензойной кислоты N-(1-этил-2,2-диметилпропил)-N'-(2-метил-3-метоксибензоил)-гидразид), RG-115932 ((R)-3,5-диметилбензойной кислоты N-(1-трет-бутилбутил)-N'-(2-этил-3 -метоксибензоил)-гидразид) и RG-115 83 0 (3,5-диметилбензойной кислоты N-(1-трет-бутилбутил)-N'-(2-этил-3-метоксибензоил)-гидразид). См. заявку на патент США номер 12/155,111, поданную 29 мая, 2008 г., и PCT/US2008/006757, поданную 29 мая, 2008 г., чтобы найти дополнительные диацилгидразины, которые полезны для осуществления настоящего изобретения.
[000300] Комплекс EcR содержит белки, которые представляют собой члены суперсемейства ядерных рецепторов, в котором все члены характеризуются присутствием аминоконцевого домена трансактивации ("ТА"), связывающего ДНК домена ("DBD") и лигандсвязывающего домена ("LBD"), разделенных шарнирным участком. Некоторые члены указанного семейства также могут включать другой домен трансактивации на карбоксиконцевой стороне LBD. DBD характеризуется присутствием двух цистеиновых цинковых пальцев, между которыми расположены два аминокислотных мотива, Р-бокс и D-бокс, которые придают специфичность к чувствительным к экдизону элементам. Данные домены могут быть нативными, модифицированными или химерами различных доменов гетерологичных рецепторных белков.
[000301] Последовательности ДНК, составляющие экзогенный ген, чувствительный элемент и комплекс EcR, можно включить в архебактерии, прокариотические клетки, такие как Escherichia coli. Bacillus subtilis или другие энтеробактерии, или эукариотические клетки, такие как клетки растений или животных. Тем не менее, так как многие белки, экспрессируемые геном, подвергаются некорректному процессингу в бактериях, эукариотические клетки являются предпочтительными. Клетки могут быть в виде отдельных клеток или в виде многоклеточных организмов. Последовательности нуклеотидов для экзогенного гена, чувствительного элемента и рецепторного комплекса также можно ввести в виде молекул РНК, предпочтительно в виде функциональных вирусных РНК, таких как вирус табачной мозаики. Из эукариотических клеток, клетки позвоночных являются предпочтительными, так как в них обычно отсутствуют молекулы, которые придают EcR отвечаемость на лиганды согласно настоящему изобретению. В результате, они "по существу нечувствительны" к лигандам согласно настоящему изобретению. Таким образом, лиганды, полезные для настоящего изобретения, будут оказывать незначительное физиологическое или другое влияние на трансформированные клетки или на весь организм. Следовательно, клетки могут расти и экспрессировать желательный продукт, при этом на них по существу не влияет присутствие самого лиганда.
[000302] Лиганды EcR, когда их используют совместно с комплексом EcR, который, в свою очередь, связан с чувствительным элементом, связанным с экзогенным геном (например, IL-12), обеспечивают средства для внешней временной регуляции экспрессии экзогенного гена. Порядок, в котором различные компоненты связываются друг с другом, то есть, лиганд с рецепторным комплексом и рецепторный комплекс с чувствительным элементом, не важен. Обычно, модуляция экспрессии экзогенного гена происходит в ответ на связывание комплекса EcR со специфичным контролирующим, или регуляторным, элементом ДНК. Белок EcR, как и другие члены семейства ядерных рецепторов, содержат по меньшей мере три домена: домен трансактивации, связывающий ДНК домен и лигандсвязывающий домен. Этот рецептор, как и подгруппа семейства ядерных рецепторов, также имеет менее четко определенные участки, ответственные за гетеродимеризационные свойства. Связывание лиганда с лигандсвязывающим доменом белка EcR, после гетеродимеризации с белком USP или RXR, позволяет ДНК-связывающим доменам гетеродимерных белков связаться с чувствительным элементом в активированной форме, что, таким образом, приводит к экспрессии или супрессии экзогенного гена. Данный механизм не исключает потенциальное связывание лиганда с любым из EcR или USP и образование в результате этого активных гомодимерных комплексов (например, EcR+EcR или USP+USP). В одном варианте реализации настоящего изобретения, один или более доменов рецептора можно изменить, чтобы получить химерный генный переключатель. Обычно, один или более из трех доменов можно выбрать из источника, отличного от источника других доменов, чтобы оптимизировать химерный рецептор в выбранной клетке-хозяине или организме по трансактивирующей активности, комплементарному связыванию лиганда и узнаванию определенного чувствительного элемента. Вдобавок, сам чувствительный элемент можно модифицировать или заменить на чувствительные элементы к доменам других связывающих ДНК белков, таких как белок GAL-4 из дрожжей (см. Sadowski и др., Nature 335: 563 (1988)) или белок LexA из Е. coli (см. Brent и др., Cell 43: 729 (1985)), в химерных комплексах EcR. Другое преимущество химерных систем состоит в том, что они позволяют выбирать промотор, используемый для запуска экспрессии экзогенного гена, в соответствии с желательным конечным результатом. Такой двойной контроль может быть особенно важным в областях генной терапии, особенно когда продуцируются цитотоксические белки, так как в этом случае можно контролировать как время осуществления экспрессии, так и тип клеток, в которых происходит экспрессия. Когда экзогенные гены, функционально связанные с подходящим промотором, вводят в клетки субъекта, экспрессия экзогенных генов контролируется присутствием лиганда согласно настоящему изобретению. Промоторы могут быть конститутивно или индуцибельно регулируемыми или могут быть тканеспецифичными (то есть, экспрессироваться лишь в конкретном типе клеток), или специфичными к некоторым стадиям развития организма.
[000303] В некоторых вариантах реализации настоящего изобретения, промотор терапевтического переключателя, описанный в способах, является конститутивным. В некоторых вариантах реализации настоящего изобретения, промотор терапевтического переключателя активируется при условиях, связанных с заболеванием, расстройством или патологическим состоянием, например, указанный промотор активируется в ответ на заболевание, в ответ на конкретное физиологическое состояние, стадию развития, дифференцировку или патологическое состояние, и/или в ответ на одну или более определенных биологических молекул; и/или указанный промотор активируется в определенных типах ткани или клеток. В некоторых вариантах реализации настоящего изобретения, указанное заболевание, расстройство или патологическое состояние реагирует на действие терапевтического полипептида или полинуклеотида. Например, в некоторых неограничивающих вариантах реализации настоящего изобретения, терапевтический полинуклеотид или полипептид полезен для лечения, предупреждения, снижения выраженности, уменьшения симптомов, предотвращения прогрессирования или излечения от заболевания, расстройства или патологического состояния, но не обязательно осуществляет любое или все из перечисленных действий. В некоторых вариантах реализации настоящего изобретения, первый и второй полинуклеотиды вводят, чтобы осуществить экспрессию комплекса лиганд-зависимого фактора транскрипции при условиях, связанных с заболеванием, расстройством или патологическим состоянием. В одном варианте реализации, терапевтические способы осуществляют таким образом, чтобы терапевтический полипептид или терапевтический полинуклеотид экспрессировался и распространялся у субъекта на уровне, достаточном для лечения, снижения выраженности или предупреждения указанного заболевания, расстройства или патологического состояния. В данной заявке термин "распространяется" означает, что указанный полипептид экспрессируется и высвобождается из модифицированной клетки в достаточном количестве, чтобы оказывать влияние или проявлять активность у субъекта. Распространение может быть системным, местным или промежуточным вариантом распространения. Например, терапевтический полипептид или терапевтический полинуклеотид может системно распространяться через кровоток или лимфатическую систему. В качестве альтернативы, терапевтический полипептид или терапевтический полинуклеотид может распространяться местно в ткани или органе, который лечат.
[000304] Множество геномных и кДНК-последовательностей нуклеиновых кислот, кодирующих множество полипептидов, таких как факторы транскрипции и репортерные белки, хорошо известны в данной области. Специалисты в данной области имеют доступ к сведениям о последовательностях нуклеиновых кислот практически всех известных генов и могут получить молекулу нуклеиновой кислоты непосредственно из общедоступного депозитария, учреждения, которое опубликовало последовательность, либо использовать обычные способы для получения указанной молекулы. См., например, описание номеров доступа последовательностей, ниже.
[000305] Генный переключатель может представлять собой любую систему генного переключателя, которая регулирует экспрессию гена при добавлении или удалении определенного лиганда. В одном варианте реализации настоящего изобретения, указанный генный переключатель представляет собой такой генный переключатель, уровень экспрессии гена с которого зависит от уровня присутствующего лиганда. Примеры лиганд-зависимых факторов транскрипции, которые можно применять в генных переключателях согласно настоящему изобретению, включают члены суперсемейства ядерных рецепторов, активируемых соответствующими лигандами (например, глюкокортикоидом, эстрогеном, прогестином, ретиноидом, экдизоном и их аналогами и миметиками), и rTTA, активируемый тетрациклином, но не ограничиваются ими. В одном аспекте настоящего изобретения, указанный генный переключатель представляет собой основанный на EcR генный переключатель. Примеры таких систем включают системы, описанные в патентах США с номерами 6,258,603, 7,045,315, опубликованных заявках на патент США с номерами 2006/0014711, 2007/0161086 и опубликованной международной заявке WO 01/70816, но не ограничиваются ими. Примеры систем с химерным рецептором экдизона описаны в патенте США номер 7,091,038, опубликованных заявках на патент США с номерами 2002/0110861, 2004/0033600, 2004/0096942, 2005/0266457 и 2006/0100416 и опубликованных международных заявках WO 01/70816, WO 02/066612, WO 02/066613, WO 02/066614, WO 02/066615, WO 02/29075 и WO 2005/108617. Пример системы, регулируемой нестероидным агонистом экдизона, представляет собой индуцируемую систему экспрессии у млекопитающего RheoSwitch® (New England Biolabs, Ипсвич, Массачусетс).
[000306] В одном варианте реализации настоящего изобретения, полинуклеотид, кодирующий генный переключатель, содержит одну последовательность фактора транскрипции, кодирующую лиганд-зависимый фактор транскрипции, под контролем промотора. Последовательность фактора транскрипции может кодировать лиганд-зависимый фактор транскрипции, который представляет собой встречающийся в природе или искусственный фактор транскрипции. Искусственный фактор транскрипции представляет собой такой фактор транскрипции, в котором природная последовательность указанного фактора транскрипции была изменена, например, путем мутирования последовательности или путем объединения доменов из различных факторов транскрипции. В одном варианте реализации настоящего изобретения, указанный фактор транскрипции содержит лигандсвязывающий домен ядерного рецептора группы Н (LBD). В одном варианте реализации настоящего изобретения, LBD ядерного рецептора группы Н получают из EcR, вездесущего рецептора, сиротского рецептора 1, NER-1, ядерного рецептора стероидных гормонов 1, белка, взаимодействующего с рецептором ретиноида Х-15, Х-рецептора-бета печени, белка, подобного рецептору стероидных гормонов, Х-рецептора печени, Х-рецептора-альфа печени, фарнезоид-Х-рецептора, взаимодействующего с рецептором белка 14 или рецептора фарнезола. В другом варианте реализации настоящего изобретения, LBD ядерного рецептора группы Н получают из рецептора экдизона.
[000307] EcR и другие ядерные рецепторы группы Н представляют собой члены суперсемейства ядерных рецепторов, все члены которого как правило характеризуются присутствием аминоконцевого домена трансактивации (TD), связывающего ДНК домена (DBD) и лигандсвязывающего домена, отделенного от DBD шарнирным участком. В данной заявке термин "связывающий ДНК домен" содержит минимальную полипептидную последовательность связывающего ДНК белка, вплоть до полной длины связывающего ДНК белка, при условии, что функция связывающего ДНК домена состоит в связывании с конкретным чувствительным элементом. Члены суперсемейства ядерных рецепторов также отличаются присутствием четырех или пяти доменов: А/В, С, D, Е и, в некоторых членах семейства, F (см. US 4,981,784 и Evans, Science 240-М9 (1988)). Домен "А/В" соответствует домену трансактивации, "С" соответствует связывающему ДНК домену, "D" соответствует шарнирному участку и "Е" соответствует лигандсвязывающему домену. Некоторые члены указанного семейства также могут содержать другой домен трансактивации на карбоксильном конце лигандсвязывающего домена, соответствующий "F".
[000308] DBD характеризуется присутствием двух цистеиновых цинковых пальцев, между которыми расположены два аминокислотных мотива, Р-бокс и D-бокс, которые придают специфичность чувствительным элементам. Данные домены могут быть нативными, модифицированными или химерами различных доменов гетерологичных рецепторных белков. EcR, как подгруппа семейства ядерных рецепторов, также содержит менее четко определенные участки, ответственные за свойства гетеродимеризации. Так как домены ядерных рецепторов блочные по своей природе, LBD, DBD и TD, могут быть взаимозаменяемыми.
[000309] В другом варианте реализации настоящего изобретения, фактор транскрипции содержит TD, DBD, который узнает чувствительный элемент, связанный с экзогенным геном, экспрессию которого нужно модулировать; и LBD ядерного рецептора группы Н. В некоторых вариантах реализации настоящего изобретения, LBD ядерного рецептора группы Н содержит мутацию с заменой.
[000310] В другом варианте реализации настоящего изобретения, полинуклеотид, кодирующий генный переключатель, содержит первую последовательность фактора транскрипции под контролем первого промотора и вторую последовательность фактора транскрипции под контролем второго промотора, при этом указанные белки, кодируемые указанной первой последовательностью фактора транскрипции и указанной второй последовательностью фактора транскрипции, взаимодействуют с образованием белкового комплекса, который функционирует как лиганд-зависимый фактор транскрипции, т.е. представляет собой генный переключатель, основанный на "двойном переключателе" или на "двухгибридной" системе. Первый и второй промоторы могут быть одинаковыми или различными.
[000311] В некоторых вариантах реализации настоящего изобретения, полинуклеотид, кодирующий генный переключатель, содержит первую последовательность фактора транскрипции и вторую последовательность фактора транскрипции под контролем промотора, при этом указанные белки, кодируемые указанной первой последовательностью фактора транскрипции и указанной второй последовательностью фактора транскрипции, взаимодействуют с образованием белкового комплекса, который функционирует как лиганд-зависимый фактор транскрипции, т.е. представляет собой "одиночный генный переключатель". Первую последовательность фактора транскрипции и вторую последовательность фактора транскрипции можно соединить с помощью участка внутренней посадки рибосомы (IRES). IRES может представлять собой IRES EMCV.
[000312] В одном варианте реализации настоящего изобретения, первая последовательность фактора транскрипции кодирует полипептид, включающий TD, DBD, который узнает чувствительный элемент, связанный с экзогенным геном, экспрессию которого нужно модулировать; и LBD ядерного рецептора группы Н, и вторая последовательность фактора транскрипции кодирует фактор транскрипции, включающий LBD ядерного рецептора, выбранный из LBD RXR позвоночного, LBD RXR беспозвоночного, LBD белка ultraspiracle и химерного лигандсвязывающего домена, включающего два полипептидных фрагмента, при этом первый полипептидный фрагмент получен из LBD RXR позвоночного, LBD RXR беспозвоночного или LBD белка ultraspiracle, а второй полипептидный фрагмент получен из отличного LBD RXR позвоночного, LBD RXR беспозвоночного или LBD белка ultraspiracle.
[000313] В другом варианте реализации настоящего изобретения, указанный генный переключатель, содержит первую последовательность фактора транскрипции, кодирующую первый полипептид, включающий LBD и DBD ядерного рецептора, который узнает чувствительный элемент, связанный с экзогенным геном, экспрессию которого нужно модулировать, и вторую последовательность фактора транскрипции, кодирующую второй полипептид, включающий TD и LBD ядерного рецептора, при этом один из LBD ядерного рецептора представляет собой LBD ядерного рецептора группы Н. В предпочтительном варианте реализации настоящего изобретения, первый полипептид по существу свободен от TD и второй полипептид по существу свободен от DBD. Для целей настоящего изобретения, термин "по существу свободный" означает, что белок, о котором идет речь, содержит недостаточную последовательность домена, о котором идет речь, чтобы обеспечить активацию или связывающую активность.
[000314] В другом аспекте настоящего изобретения, первая последовательность фактора транскрипции кодирует белок, включающий партнер по гетеродимеризации и TD, и вторая последовательность фактора транскрипции кодирует белок, включающий DBD и LBD.
[000315] Когда только один LBD ядерного рецептора представляет собой LBD группы Н, другой LBD ядерного рецептора можно получить из любого другого ядерного рецептора, который образует димер с LBD группы Н. Например, когда LBD ядерного рецептора группы Н представляет собой LBD EcR, другой "партнер" LBD ядерного рецептора можно получить из EcR, RXR позвоночного, RXR беспозвоночного, белка ultraspiracle (USP) или химерного ядерного рецептора, содержащего по меньшей мере два различных полипептидных фрагмента LBD ядерного рецептора, выбранного из RXR позвоночного, RXR беспозвоночного и USP (см. WO 01/70816 А2, международную заявку на патент номер PCT/US02/05235 и US 2004/0096942 А1). "Партнерский" лигандсвязывающий домен ядерного рецептора может дополнительно включать мутацию укорачивания, делеционную мутацию, мутацию с заменой или другую модификацию.
[000316] В одном варианте реализации настоящего изобретения, LBD RXR позвоночного получают из RXR человека Homo sapiens, мыши Mus musculus, крысы Rattus norvegicus, цыпленка Gallus gallus, свиньи Sus scrofa domestica, лягушки Xenopus laevis, данио Danio rerio, оболочника Polyandrocarpa misakiensis или медузы Tripedalia cysophora.
[000317] В одном варианте реализации настоящего изобретения, лигандсвязывающий домен RXR беспозвоночного получают из полипептида ultraspiracle саранчи Locusta migratoria ("LmUSP"), гомолога 1 RXR иксодового клеща Amblyomma americanum ("AmaRXR1"), гомолога 2 RXR иксодового клеща Amblyomma americanum ("AmaRXR2"), гомолога RXR манящего краба Celuca pugilator ("CpRXR"), гомолога RXR мучного жука Tenebrio Molitor ("TmRXR"), гомолога RXR медоносной пчелы Apis mellifera ("AmRXR"), гомолога RXR тли Myzus persicae ("MpRXR") или гомолога RXR недвукрылых/нечешуекрылых.
[000318] В одном варианте реализации настоящего изобретения, химерный LBD RXR содержит по меньшей мере два полипептидных фрагмента, выбранных из полипептидного фрагмента RXR позвоночных видов, полипептидного фрагмента RXR беспозвоночных видов и полипептидного фрагмента гомолога RXR беспозвоночных видов недвукрылых/нечешуекрылых. Химерный лигандсвязывающий домен RXR для применения в настоящем изобретении может включать по меньшей мере два полипептидных фрагмента RXR различных видов, или, когда виды одинаковые, два или более полипептидных фрагмента могут быть получены из двух или более различных изоформ полипептидного фрагмента RXR указанного вида.
[000319] В одном варианте реализации настоящего изобретения, химерный лигандсвязывающий домен RXR содержит по меньшей мере один полипептидный фрагмент RXR позвоночных видов и один полипептидный фрагмент RXR беспозвоночных видов.
[000320] В другом варианте реализации настоящего изобретения, химерный лигандсвязывающий домен RXR содержит по меньшей мере один полипептидный фрагмент RXR позвоночных видов и один полипептидный фрагмент гомолога RXR-беспозвоночных видов недвукрылых/нечешуекрылых.
[000321] Лиганд, когда он объединен с LBD ядерного рецептора(ов), который, в свою очередь, связан с чувствительным элементом, связанным с экзогенным геном, обеспечивает внешнюю временную регуляцию экспрессии экзогенного гена. Механизм связывания или порядок, в котором различные компоненты настоящего изобретения связываются друг с другом, то есть, например, лиганд с LBD, DBD с чувствительным элементом, TD с промотором и т.д., не важен.
[000322] В конкретном примере, связывание лиганда с LBD ядерного рецептора группы Н и с партнером LBD ядерного рецептора позволяет экспрессию экзогенного гена. Этот механизм не исключает возможности связывания лиганда с ядерным рецептором группы Н (GHNR) или его партнером, и образования в результате этого активных гомодимерных комплексов (например, GHNR+GHNR или партнер + партнер). Предпочтительно, один или более доменов рецептора изменяют, чтобы получить гибридный генный переключатель. Обычно, один или более из трех доменов, DBD, LBD и AD, можно выбрать из источника, отличного от источника других доменов, для того, чтобы оптимизировать гибридные гены и полученные в результате этого гибридные белки в выбранной клетке-хозяине или организме по трансактивирующей активности, комплементарному связыванию лиганда и узнаванию определенного чувствительного элемента. Вдобавок, сам чувствительный элемент можно модифицировать или заменить на чувствительные элементы к доменам других связывающих ДНК белков, таких как белок GAL-4 из дрожжей (см. Sadowski и др., Nature 335: 563 (1988)) или белок LexA из Escherichia coli (см. Brent и др., Cell 43: 729 (1985)), или на синтетические чувствительные элементы, специфичные для направленных взаимодействий с белками, разработанные, модифицированные и отобранные по таким определенным взаимодействиям (см., например, Kim и др., Proc. Natl. Acad. Sci. USA, 94: 3616 (1997)), чтобы привести чувствительный элемент в соответствие с гибридными рецепторами.
[000323] Функциональный комплекс EcR также может содержать дополнительный белок (белки), такой как иммунофилин. Дополнительные члены семейства белков ядерных рецепторов, известные как транскрипционные факторы (такие как DHR38 или betaFTZ-1), также могут быть лигандзависимыми или независимыми партнерами для EcR, USP и/или RXR. Дополнительно, могут быть необходимы. другие кофакторы, такие как белки, широко известные как коактиваторы (также называемые адаптерами или медиаторами. Данные белки не связываются специфично с последовательностью ДНК и не участвуют в основной транскрипции. Они могут оказывать влияние на активацию транскрипций посредством различных механизмов, включая стимуляцию связывания активаторов с ДНК, влияние на структуру хроматина или опосредование взаимодействий активатора с инициирующим комплексом. Примеры таких коактиваторов включают RIP140, TIF1, RAP46/Bag-1, ARA70, SRC-1/NCoA-1, TIF2/GRIP/NCoA-2, ACTR/AIB1/RAC3/pCIP, а также случайный коактиваторный белок, связывающий белок, связывающий цАМФ-чувствительный элемент, СВР/р300 (для обзора см. Glass и др., Curr. Opin. Cell Biol. 9: 222 (1997)). Также, кофакторы белков, широко известные как корепрессоры (также известные как репрессоры, сайленсеры или медиаторы сайленсинга), могут быть необходимы для эффективного ингибирования активации транскрипции в отсутствии лиганда. Данные корепрессоры могут взаимодействовать с не связанным с лигандом EcR, чтобы подавлять активность на чувствительном элементе. В настоящее время имеются доказательства, которые позволяют предположить, что связывание лиганда изменяет конформацию рецептора, что приводит к высвобождению корепрессора и привлечению описанных выше коактиваторов, нарушая тем самым подавляющую активность. Примеры корепрессоров включают N-CoR и SMRT (для обзора см. Horwitz и др., Mol Endocrinol. 10: 1167 (1996)). Данные кофакторы могут быть либо эндогенными в клетке или организме, либо их можно добавить экзогенно в виде трансгенов, которые будут экспрессироваться либо регулируемым, либо нерегулируемым образом.
[000324] Экзогенный ген функционально связан с промотором, содержащим по меньшей мере один чувствительный элемент, который узнается DBD лиганд-зависимого фактора транскрипции, кодируемого генным переключателем. В одном варианте реализации настоящего изобретения, указанный промотор содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более копий чувствительного элемента. Промоторы, содержащие желательные чувствительные элементы, могут представлять собой встречающиеся в природе промоторы или искусственные промоторы, созданные с помощью методик, которые хорошо известны в данной области, например, один или более чувствительных элементов функционально связаны с минимальным промотором.
[000325] Чтобы ввести полинуклеотиды в клетки, можно использовать вектор. Указанный вектор может представлять собой, например, плазмидный вектор или вирусный вектор из одно- или двухцепочечной РНК или ДНК. Такие векторы можно вводить в клетки с помощью хорошо известных способов введения ДНК и РНК в клетки. Вирусные векторы могут быть репликационно-компетентными или репликационно-дефектными. В последнем случае, воспроизведение вируса, как правило, будет происходить только в комплементарных клетках-хозяевах. В данной заявке термин "клетка-хозяин" или "хозяин" используется для обозначения клетки согласно настоящему изобретению, которая содержит один или более полинуклеотидов согласно настоящему изобретению.
[000326] Таким образом, как минимум, векторы должны включать полинуклеотиды согласно настоящему изобретению. Другие компоненты вектора могут включать селектируемые маркеры, домены модификации хроматина, дополнительные промоторы, запускающие экспрессию других полипептидов, которые также могут присутствовать на векторе (например, летального полипептида), сайты встраивания в геном, сайты рекомбинации и молекулярные элементы вставки, но не ограничиваются ими. Векторы могут содержать любое количество данных дополнительных элементов, либо внутри, либо снаружи указанных полинуклеотидов таким образом, что вектор можно приспособить для определенных целей желательных терапевтических способов.
[000327] В одном варианте реализации настоящего изобретения, векторы, которые вводят в клетки, дополнительно содержат "селектируемый маркерный ген", который, когда он экспрессируется, указывает на то, что конструкция генного переключателя согласно настоящему изобретению встроилась в геном клетки-хозяина. Таким образом, селектируемый ген может быть положительным маркером встраивания в геном. Хотя его наличие не является крайне необходимым для способов согласно настоящему изобретению, присутствие селектируемого маркерного гена позволяет специалисту отобрать популяцию живых клеток, если векторная конструкция встроилась в геном указанных клеток. Таким образом, некоторые варианты реализации настоящего изобретения включают отбор клеток, в которые вектор успешно встроился. В данной заявке термин "отбирать" или его варианты," когда они применяются в сочетании с клетками, предполагают означающими стандартные, хорошо известные способы отбора клеток с определенным генетическим составом или фенотипом. Обычные способы включают культивирование клеток в присутствии антибиотиков, таких как G418, неомицин и ампициллин, но не ограничиваются ими. Другие примеры селектируемых маркерных генов включают гены, которые придают устойчивость к дигидрофолатредуктазе, гигромицину или микофенольной кислоте, но не ограничиваются ими. Другие способы селекции включают селектируемый маркерный ген, который позволяет использовать в качестве селекционных агентов тимидинкиназу, гипоксантин-гуанин фосфорибозилтрансферазу или аденин фосфорибозилтрансферазу, но не ограничиваются ими. Клетки, содержащие векторную конструкцию, содержащую ген или гены устойчивости к антибиотику, затем способны расти при наличии антибиотика в культуре. Аналогично, клетки, не содержащие векторную конструкцию, содержащую ген или гены устойчивости к антибиотику, не способны расти при наличии антибиотика в культуре.
[000328] В данной заявке термин "домен модификации хроматина" (CMD) относится к последовательности нуклеотидов, которая взаимодействует с множеством белков, связанных с поддержанием и/или изменением структуры хроматина, таких как ДНК-инсуляторы, не ограничиваются ими. См. Ciavatta и др., Proc. Nati Acad. Sci. U.S.A., 103: 9958 (2006). Примеры CMD включают инсулятор β-глобулина цыпленка и гиперчувствительный сайт 4 (cHS4) цыпленка, но не ограничиваются ими. Использование различных последовательностей. CMD между одной или несколькими генными программами (т.е., промотор, кодирующая последовательность и 3'-регуляторная область), например, может способствовать применению последовательностей ДНК различных CMD в качестве "мини плеч гомологии" в комбинации с различными микроорганизмами или рекомбинантными способами in vitro, чтобы "обменять" друг с другом генные программы имеющихся мультигенных и моногенных челночных векторов. Другие примеры доменов модификации хроматина известны в данной области, или их можно легко идентифицировать.
[000329] Конкретные векторы для применения в настоящем изобретении представляют собой векторы экспрессии, которые кодируют белки или полинуклеотиды. Как правило, такие векторы включают цис-действующие регуляторные области, эффективные для экспрессии в хозяине, функционально связанные с полинуклеотидом, экспрессию которого нужно осуществить. Подходящие транс-действующие факторы обеспечивает хозяин, дополняющий вектор или сам вектор при его введении в хозяина.
[000330] Для экспрессии белков или полинуклеотидов можно применять большое разнообразие векторов экспрессии. Такие векторы включают хромосомные векторы, эписомные векторы и векторы на основе вирусов, например, векторы, полученные из бактериальных плазмид, из бактериофага, из эписом дрожжей, из хромосомных элементов дрожжей, из вирусов, таких как аденоассоциированные вирусы, лентивирусы, бакуловирусы, паповавирусы, такие как SV40, вирусы коровьей оспы, аденовирусы, вирусы оспы птиц, вирусы псевдобешенства и ретровирусы, и векторы, полученные из комбинации перечисленных, например, полученные из генетических элементов плазмиды и бактериофага, такие как космиды и фагмиды. Все перечисленные векторы можно применять для экспрессии в соответствии с данным аспектом настоящего изобретения. Как правило, в этом отношении можно применять для экспрессии любой вектор, подходящий для сохранения, передачи по наследству или экспрессирования полинуклеотидов или белков в хозяине.
[000331] Полинуклеотидная последовательность в векторе экспрессии функционально связана с подходящей последовательностью(ями), контролирующей экспрессию, включая, например, промотор для прямой транскрипции мРНК. Типичные дополнительные промоторы включают конститутивные промоторы и тканеспецифичные или индуцируемые промоторы, но не ограничиваются ими. Примеры конститутивных эукариотических промоторов включают промотор гена металлотионеина I мыши (Hamer и др., J. Mol. Appl. Gen. 7: 273 (1982)); промотор ТК вируса герпеса (McKnight, Cell 31: 355 (1982)); ранний промотор SV40 (Benoist и др., Nature 290: 304 (1981)) и промотор вируса коровьей оспы, но не ограничиваются ими. Дополнительные примеры промоторов, которые можно применять для запуска экспрессии белка или полинуклеотида, включают тканеспецифичные промоторы и другие эндогенные промоторы для конкретных белков, такие как промотор альбумина (гепатоциты), промотор проинсулина (бета-клетки поджелудочной железы) и тому подобные, но не ограничиваются ими. Обычно, экспрессионные конструкции содержат сайты инициации и терминации транскрипции и, в транскрибируемом участке, сайт связывания рибосомы для трансляции. Кодирующая часть зрелых транскриптов, экспрессируемых конструкциями, может содержать инициирующий трансляцию кодон AUG в начале и терминирующий кодон (UAA, UGA или UAG), расположенный подходящим образом, на конце транслируемого полипептида.
[000332] Вдобавок, конструкции могут содержать регуляторные области, которые регулируют, а также вызывают экспрессию. Как правило, такие участки функционируют путем контролирования транскрипции, как, например, сайты связывания репрессоров и энхансеров, среди прочих.
[000333] Примеры эукариотических векторов включают pW-LNEO, pSV2CAT, pOG44, pXT1 и pSG, доступные от Stratagene; pSVK3, pBPV, pMSG и pSVL доступные от Amersham Pharmacia Biotech; и pCMVDsRed2-express, pIRES2-DsRed2, pDsRed2-Mito и pCMV-EGFP, доступные от Clontech, но не ограничиваются ими. Многие другие векторы хорошо известны и доступны для приобретения.
[000334] Особенно пригодные векторы, которые содержат молекулярные элементы вставки для быстрой вставки и удаления элементов генных программ, описаны в опубликованной патентной заявке США номер 2004/0185556, патентной заявке США номер 11/233,246 и опубликованных международных заявках WO 2005/040336 и WO 2005/116231. Примером таких векторов является UltraVector™ Production System (Intrexon Corp., Блэксбург, Вирджиния), описанный в WO 2007/038276. В данной заявке термин "генная программа" представляет собой комбинацию генетических элементов, содержащих промотор (Р), экспрессируемую последовательность (Е) и 3'-регуляторную последовательность (3), таким образом, что "РЕ3" представляет собой генную программу. Можно легко заменить элементы внутри генной программы между молекулярными элементами, которые фланкируют каждый из элементов генной программы. Молекулярный элемент в данной заявке определен как полинуклеотид, содержащий по меньшей мере два неизменчивых редких или малораспространенных сайта рестрикции, расположенных линейно. В одном варианте реализации настоящего изобретения, молекулярный элемент содержит по меньшей мере три неизменчивых редких или малораспространенных сайта рестрикции, расположенных линейно. Обычно, любой молекулярный элемент не будет содержать редкий или малораспространенный сайт рестрикции любого другого молекулярного элемента внутри одной генной программы. Узнаваемые последовательности размером больше 6 нуклеотидов, на которых действует рестрикционный фермент, называют "редкими" сайтами рестрикции. Тем не менее, существуют сайты рестрикции размером 6 п.о., которые встречаются реже, чем это предсказывают статистически, и такие сайты, и эндонуклеазы, которые их расщепляют, называют "малораспространенными". Примеры редких или малораспространенных рестрикционных ферментов включают AsiS I, Рас I, Sbf I, Fse I, Asc I, Mlu I, SnaB I, Not I, Sal I, Swa I, Rsr II, BSiW I, Sfo I, Sgr AI, AflIII, Pvu I, Ngo MIV, Ase I, Flp I, Pme I, Sda I, Sgf I, Srf I, Nru I, Acl I, Cla I, Csp45 I, Age I, Bst1107 I, BstB I, Hpa I, Aat II, EcoR V, Nhe I, Spe I, Avi II, Avr II, Mfe I, Afe I, Fsp I, Kpn I, Sca I, BspE I, Nde I, Bfr I, Xho I, Pml I, ApaL I, Kas I, Xma I, BsrB I, Nsi I, Sac II, Sac I, Blp I, PspoM I, Pci I, Stu I, Sph I, BamH I, Bsu36 I, Xba I, BbvC I, Bgl II, Nco I, Hind III, EcoR I, BsrG I и Sse8781 I, но не ограничиваются ими.
[000335] Вектор также может содержать сайты рестрикции для второго класса рестрикционных ферментов, называемых ферментами хоуминг-эндонуклеазами (НЕ). У ферментов НЕ большие асимметричные сайты рестрикции (12-40 пар оснований), и их сайты рестрикции редко встречаются в природе. Например, у НЕ, известного как I-SceI, сайт. рестрикции размером 18 п.о. (5'-TAGGGATAACAGGGTAAT-3' (SEQ ID NO:28)), и теоретически он должен встречаться один раз на каждые 7×1010 пар оснований в произвольной последовательности. Такая частота встречаемости эквивалентна лишь одному сайту в геноме, который в 20 раз больше генома млекопитающего. Редкая встречаемость в природе сайтов НЕ сильно повышает вероятность того, что специалист в области генной инженерии сможет разрезать генную программу, не нарушая целостности генной программы, если сайты НЕ введены в подходящие положения клонирующей векторной плазмиды.
[000336] Отбор подходящих векторов и промоторов для экспрессии в клетке-хозяине представляет собой хорошо известную процедуру, и необходимые методики конструирования вектора и введения его в хозяина, а также его экспрессии в хозяине, находятся в рамках средней компетенции в данной области.
[000337] Введение полинуклеотидов в клетки можно осуществить путем временной трансфекции, стабильной трансфекции или локус-специфической вставки вектора. Временную и стабильную трансфекцию векторами клетки-хозяина можно осуществить путем кальций-фосфатной трансфекции, опосредованной DEAE-декстраном трансфекции, опосредованной катионным липидом трансфекции, электропорации, трансдукции, инфекции или с помощью других способов. Такие способы описаны во многих стандартных лабораторных руководствах, таких как Davis и др., Basic Methods in Molecular Biology (1986); Keown и др., 1990, Methods Enzymol. 185: 527-37; Sambrook и др., 2001, Molecular Cloning, A Laboratory Manual, третье издание. Cold Spring Harbor Laboratory Press, Нью-Йорк. Данные способы стабильной трансфекции приводят к произвольному встраиванию вектора в геном клетки. Дополнительно, число копий и ориентация векторов, по большому счету, также произвольны.
[000338] В одном варианте реализации настоящего изобретения, вектор встраивают в биологически нейтральный сайт в геноме. Биологически нейтральный сайт представляет собой сайт в геноме, вставка полинуклеотидов в который практически не нарушает, если вообще нарушает, нормальное функционирование клетки. Биологически нейтральные сайты можно выявить, применяя доступные способы биоинформатики. В данной области известно множество биологически нейтральных сайтов, например, эквивалентный ROSA локус. Другие биологически нейтральные сайты можно идентифицировать, применяя обычные методики, хорошо известные в данной области. Описание сайта(ов) встраивания в геном осуществляют, применяя способы, известные в данной области. Для контролирования положения, числа копий и/или ориентации полинуклеотидов при введении вектора в клетки можно применять способы локус-специфической вставки. Способы локус-специфической вставки хорошо известны в данной области и включают, но не ограничены перечисленными, гомологичную рекомбинацию и опосредованное рекомбиназой встраивание в геном. Разумеется, если в способах согласно настоящему изобретению нужно применять методы локус-специфической вставки, указанные векторы могут включать элементы, которые способствуют локус-специфической вставке, например, но не ограничиваясь, гомологичной рекомбинации. Например, векторы могут включать один, два, три, четыре или более сайтов встраивания в геном (GIS). В данной заявке термин "сайт встраивания в геном" определен как часть последовательности вектора, последовательность нуклеотидов которой идентична или практически идентична областям генома в клетках, которая позволяет встраивание вектора в геном. В частности, указанный вектор может включать два сайта встраивания в геном, которые фланкируют по меньшей мере указанные полинуклеотиды. Разумеется, GIS может фланкировать дополнительные элементы или даже все элементы, присутствующие на векторе.
[000339] В другом варианте реализации, локус-специфическую вставку можно осуществить путем вставки гена в определенный сайт рекомбиназы. Вкратце, бактериальные ферменты рекомбиназы, такие как интеграза PhiC31, но не ограничиваясь ей, могут действовать на "псевдо"-сайтах рекомбинации в геноме человека. Данные псевдосайты рекомбинации могут представлять собой мишени для локус-специфической вставки с помощью рекомбиназ. Вставка гена в определенный сайт рекомбиназы описана у Thyagarajan и др., Mol. Cell Biol. 21: 3926 (2001). Другие примеры рекомбиназ и соответствующих их сайтов, которые можно применять для вставки гена в определенный сайт рекомбиназы, включают сериновые рекомбиназы, такие как R4 и ТР901-1, и рекомбиназы, описанные в WO 2006/083253, но не ограничиваются ими.
[000340] В дополнительном варианте реализации настоящего изобретения, указанный вектор может включать ген устойчивости к химическим веществам, например, ген множественной лекарственной устойчивости mdr1, дигидрофолатредуктазу или О6-алкилгуанин-ДНК-алкилтрансферазу. Ген устойчивости к химическим веществам может находиться под контролем конститутивного (например, CMV) или индуцируемого (например, RheoSwitch®) промотора. В данном варианте реализации настоящего изобретения, если требуется лечение заболевания у субъекта с сохранением модифицированных клеток в субъекте, практикующий врач может применять химиотерапевтический агент для разрушения пораженных болезнью клеток, при этом модифицированные клетки будут защищены от агента в результате экспрессии подходящего гена устойчивости к химическим веществам, и можно будет продолжать применять его для лечения, снижения выраженности или предупреждения заболевания или расстройства. Путем помещения гена устойчивости к химическим веществам под контроль индуцируемого промотора, можно избежать нежелательной экспрессии указанного гена устойчивости к химическим веществам, при этом он будет доступен в случае необходимости длительного лечения. Если сами модифицированные клетки становятся пораженными болезнью, их можно будет уничтожить путем индукции экспрессии летального полипептида, как описано ниже.
[000341] Способы согласно настоящему изобретению осуществляют путем введения полинуклеотидов, кодирующих генный переключатель и экзогенный ген, в клетки субъекта. Можно применять любой способ введения полинуклеотида в клетку, известный в данной области, такой как описанные выше.
[000342] Когда полинуклеотиды нужно вводить в клетки ex vivo, клетки можно получить из субъекта с помощью любого способа, известного в данной области, включая биопсии, соскобы и хирургическое удаление ткани, но не ограничиваясь ими. Выделенные клетки можно культивировать в течение достаточного количества времени, чтобы позволить полинуклеотидам войти в клетки, например, в течение 2, 4, 6, 8, 10, 12, 18, 24, 36, 48 часов или более. Способы культивирования первичных клеток на протяжении небольших промежутков времени хорошо известны в данной области. Например, клетки можно культивировать в планшетах (например, в микролуночных планшетах), либо присоединенными, либо в суспензии.
[000343] Для терапевтических способов ех vivo, клетки выделяют из субъекта и культивируют при условиях, подходящих для введения полинуклеотидов в клетки. Как только полинуклеотиды были введены в клетки, указанные клетки инкубируют в течение достаточного периода времени, чтобы позволить экспрессироваться лиганд-зависимому фактору транскрипции, например, в течение 0.5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 18 или 24 часов или более. В некоторый момент времени после введения полинуклеотидов в клетки (либо перед, либо после того, как экспрессировались значительные уровни лиганд-зависимого фактора транскрипции), клетки вводят обратно субъекту. Это введение можно осуществить с помощью любого способа, известного в данной области, например, путем внутривенной инфузии или непосредственной инъекции в ткань или полость. В одном варианте реализации настоящего изобретения, присутствие полинуклеотидов в клетках определяют перед введением клеток обратно субъекту. В другом варианте реализации настоящего изобретения, клетки, содержащие полинуклеотиды, отбирают (например, на основании присутствия селектируемого маркера в полинуклеотидах) и только такие клетки, содержащие указанные полинуклеотиды, вводят субъекту. После того как клетки ввели обратно субъекту, субъекту вводят лиганд, чтобы индуцировать экспрессию терапевтического полипептида или терапевтического полинуклеотида. В альтернативном варианте реализации, лиганд можно добавить в клетки даже перед тем, как клетки вводят обратно субъекту, таким образом, что терапевтический полипептид или терапевтический полинуклеотид экспрессируется перед введением клеток. Лиганд можно вводить с помощью любого подходящего способа, либо системно (например, перорально, внутривенно), либо местно (например, интраперитонеально, интратекально, интравентрикулярно или путем непосредственной инъекции в ткань или орган, куда были введены клетки). Оптимальное время введения лиганда можно определить для каждого типа клеток и заболевания или расстройства, применяя только обычные способы.
[000344] Терапевтические способы in vivo согласно настоящему изобретению включают непосредственное введение in vivo полинуклеотидов в клетки субъекта. Полинуклеотиды можно вводить субъекту системно или местно (например, в место проявления заболевания или расстройства). Как только полинуклеотиды были введены субъекту, можно вводить лиганд для индукции экспрессии терапевтического полипептида или терапевтического полинуклеотида. Лиганд можно вводить с помощью любого подходящего способа, либо системно (например, перорально, внутривенно), либо местно (например, интраперитонеально, интратекально, интравентрикулярно или путем непосредственной инъекции в ткань или орган, где проявилось заболевание или расстройство). Оптимальное время введения лиганда можно определить для каждого типа клеток и заболевания или расстройства, применяя только обычные способы.
[000345] Для применения in vivo, лиганды, описанные в данной заявке, можно принимать в фармацевтически приемлемых носителях, таких как, например, растворы, суспензии, таблетки, капсулы, мази, эликсиры и инъецируемые композиции. Фармацевтические композиции могут включать от 0.01% до 99% лиганда по весу. Композиции могут быть в виде лекарственных форм, содержащих одну либо множество доз. Количество лиганда в любой конкретной фармацевтической композиции будет зависеть от эффективной дозы, то есть дозы, необходимой для индукции экспрессии или супрессии желательного гена.
[000346] Подходящие пути введения фармацевтических препаратов включают пероральный, ректальный, топический (включая дермальный, буккальный и сублингвальный), вагинальный, парентеральный (включая подкожный, внутримышечный, внутривенный, внутриопухолевый, внутрикожный, интратекальный и эпидуральный) путь введения и введение с помощью назогастрального зонда. Для специалистов в данной области должно быть очевидно, что предпочтительный путь введения будет зависеть от состояния, которое лечат, и может изменяться в зависимости от таких факторов, как состояние реципиента.
[000347] В данной заявке термин "rAD.RheoIL12" относится к аденовирусному полинуклеотидному вектору, несущему ген IL-12 под контролем генного переключателя терапевтической системы RheoSwitch® (RTS), который способен продуцировать белок IL-12 в присутствии активирующего лиганда. В данной заявке термин "rAd.cIL12" относится к аденовирусному полинуклеотидному контрольному вектору, включающему ген IL-12 под контролем конститутивного промотора.
[000348] В данной заявке термин "IL-12p70" относится к белку IL-12, который обычно содержит две субъединицы, как правило, называемые р40 и р35. В объем термина IL-12p70 входят гибридные белки, содержащие две субъединицы IL-12 (р40 и р35), при этом указанный гибридный белок может содержать линкерные аминокислоты между субъединицами.
[000349] В данной заявке термин "белок, обладающий функцией иммуномодулятора", относится к белку, который обладает по меньшей мере 20% (например, по меньшей мере 30%, 40%, 50%, 60%, 70%, 80% или 90%) любой биологической активности иммуномодулятора, выбранного из IL-1, IL-2, IL-3, IL-4, IL-5, IL-7, IL-8, IL-9, IL-10R или его субъединицы DN, IL-15, IL-18, IL-21, IL-23, IL-24, IL-27, GM-CSF, IFN-альфа, IFN-гамма, CCL3 (MIP-1a), CCL5 (RANTES), CCL7 (МСР3), XCL1 (лимфотактина), CXCL1 (MGSA-альфа), CCR7, CCL19 (MIP-3b), CXCL9 (MIG), CXCL10 (IP-10), CXCL12 (SDF-1), CCL21 (6Ckine), OX40L, 4-1BBL, CD40, CD70, GITRL, LIGHT, b-дефензина, HMGB1, Flt3L, IFN-бета, TNF-альфа, dnFADD, BCG, TGF-альфа, PD-L1, TGFbRII DN, ICOS-L и S100. Аналогично, термин "белок, обладающий функцией IL-12", относится к белку, который обладает по меньшей мере 20% (например, по меньшей мере 30%, 40%, 50%, 60%, 70%, 80% или 90%) любой биологической активности IL-12 человека. Биологические активности таких иммуномодуляторов хорошо известны. См. следующую таблицу.
[000350] Биологические активности IL-12 также хорошо известны и включают дифференцировку наивных Т-клеток в Th1-клетки, стимуляцию роста и функционирования Т-клеток, продукцию интерферона-гамма (IFN-гамма) и фактора некроза опухоли-альфа (TNF-α) Т-клетками и клетками - естественными киллерами (NK), снижение опосредованного IL-4 подавления IFN-гамма, усиление цитотоксической активности NK-клеток и цитотоксических CD8+ Т-лимфоцитов, стимуляцию экспрессии IL-12R-β1 и IL-12R-β2, содействие презентации опухолевых антигенов с помощью повышения регуляции молекул МНС I и II класса и анти-ангиогенную активность, но не ограничиваются ими. В объем термина "белок, обладающий функцией IL-12" входят мутанты последовательности IL-12 дикого типа, в которых последовательность дикого типа была изменена путем одной или нескольких вставок, делеций или замен аминокислот, а также не относящиеся к IL-12 белки, которые имитируют одну или более биологических активностей IL-12.
[000351] В данной заявке термины "активация" или "активируют" относятся к любому измеримому повышению клеточной активности генного переключателя, приводящему к экспрессии интересующего гена (например, выбранного из IL-1, IL-2, IL-3, IL-4, IL-5, IL-7, IL-8, IL-9, IL-10R или его субъединицы DN, IL-15, IL-18, IL-21, IL-23, IL-24, IL-27, GM-CSF, IFN-альфа, IFN-гамма, CCL3 (MIP-1a), CCL5 (RANTES), CCL7 (МСР3), XCL1 (лимфотактина), CXCL1 (MGSA-альфа), CCR7, CCL19 (MIP-3b), CXCL9 (MIG), CXCL10 (IP-10), CXCL12 (SDF-1), CCL21 (6Ckine), OX40L, 4-1BBL, CD40, CD70, GITRL, LIGHT, b-дефензина, HMGB1, Flt3L, IFN-бета, TNF-альфа, dnFADD, TGF-альфа, РНКи PD-L1, антисмыслового олигонуклеотида PD-L1, TGFbRII DN, ICOS-L и S100.
[000352] В данной заявке термины "лечить" или "лечение" заболевания относятся к выполнению протокола, который может включать введение одного или нескольких лекарственных средств или сконструированных т vitro клеток млекопитающему (человеку или не относящемуся к человеку млекопитающему), с целью смягчить признаки или симптомы заболевания. Таким образом, "лечить" или "лечение" не должны обязательно толковаться как требующие полного смягчения признаков или симптомов, они не требуют излечения и, в частности, включают протоколы, которые оказывают лишь незначительное влияние на субъекта.
[000353] В данной заявке термин "иммунные клетки" содержит дендритные клетки, макрофаги, нейтрофилы, тучные клетки, эозинофилы, базофилы, клетки - естественные киллеры и лимфоциты (например. В- и Т-клетки).
[000354] В данной заявке термины "дендритные клетки" и "DC" используются взаимозаменяемо.
[000355] В данной заявке термин "вспомогательные клетки для терапии" (TSC) описывает клетки, которые можно модифицировать (например, трансфицировать, электропорировать и т.д.) вектором согласно настоящему изобретению, чтобы доставить один или более белков, обладающих функцией иммуномодулятора, и, возможно, белок, обладающий функцией IL-12, в микроокружение опухоли. Такие TSC включают стволовые клетки, фибробласты, эндотелиальные клетки и кератиноциты, но не ограничены ими.
[000356] В данной заявке термины "сконструированные in vitro иммунные клетки", или "популяция сконструированных in vitro иммунных клеток", или "популяция сконструированных иммунных клеток", или "иммунные клетки, экспрессирующие иммуномодулятор", или "иммунные клетки, экспрессирующие IL-12", относятся к иммунным клеткам, например, дендритным клеткам, при определенных условиях экспрессирующим иммуномодулятор и/или IL-12, в зависимости от конкретного случая, под контролем генного переключателя, который можно активировать с помощью активирующего лиганда.
[000357] В данной заявке термины "сконструированные in vitro TSC", или "сконструированная in vitro популяция TSC", или "популяция сконструированных TSC", или "TSC, экспрессирующие иммуномодулятор", или "TSC, экспрессирующие IL-12", относятся к вспомогательным клеткам для терапии, например, стволовым клеткам, фибробластам, эндотелиальным клеткам и кератиноцитам, при определенных условиях экспрессирующим иммуномодулятор и/или IL-12, в зависимости от конкретного случая, под контролем генного переключателя, который можно активировать с помощью активирующего лиганда.
[000358] В данной заявке термин "модифицированная клетка" относится к клеткам, которые были изменены с помощью процесса, включающего трансфекции, электропорации, микроинъекции, трансдукции, слияния клеток, применения декстрана DEAE, преципитации фосфатом кальция и липофекции (слияния лизосом), но не ограничивающегося ими.
[000359] В данной заявке термины "МОI" или "множественность заражения" относятся к среднему количеству аденовирусных частиц, которые заражают отдельную клетку в конкретном эксперименте (например, рекомбинантного аденовируса или контрольного аденовируса).
[000360] В данной заявке термин "опухоль" относится ко всему доброкачественному или злокачественному росту и пролиферации клеток, либо in vivo, либо in vitro, либо к предраковым, либо к раковым клеткам и/или тканям.
[000361] Примеры раков, которые можно лечить согласно настоящему изобретению, включают рак молочной железы, рак предстательной железы, лимфому, рак кожи, рак поджелудочной железы, рак толстой кишки, меланому, злокачественную меланому, рак яичников, рак мозга, первичную карциному мозга, рак головы и шеи, глиому, глиобластому, рак печени, рак мочевого пузыря, немелкоклеточную карциному легкого, карциному головы и шеи, карциному груди, карциному яичника, карциному легкого, мелкоклеточную карциному легкого, опухоль Вильмса, карциному шейки матки, тестикулярную карциному, карциному мочевого пузыря, карциному поджелудочной железы, карциному желудка, карциному толстой кишки, карциному предстательной железы, карциному мочеполовой системы, рак щитовидной железы, карциному пищевода, миелому, множественную миелому, карциному надпочечников, почечноклеточную карциному, карциному эндометрия, карциному коры надпочечников, злокачественную инсулиному поджелудочной железы, злокачественную карциноидную карциному, хориокарциному, фунгоидный микоз, злокачественную гиперкальцемию, гиперплазию шейки матки, лейкемию, острую лимфоцитарную лейкемию, хроническую лимфоцитарную лейкемию, острую миелогенную лейкемию, хроническую миелогенную лейкемию, хроническую гранулоцитарную лейкемию, острую гранулоцитарную лейкемию, волосатоклеточную лейкемию, нейробластому, рабдомиосаркому, саркому Капоши, истинную полицитемию, эссенциальный тромбоцитоз, болезнь Ходжкина, неходжкинскую лимфому, саркому мягких тканей, мезотелиому, остеогенную саркому, первичную макроглобулинемию и ретинобластому, и тому подобные раки.
[000362] Настоящее изобретение обеспечивает конструирование клеток, например, иммунных клеток и TSC таким образом, что они при определенных условиях экспрессируют белок, обладающий функцией иммуномодулятора, и возможно IL-12, и терапевтическое использование и/или применение для лечения рака или опухолей, или обоих. Сконструированные in vitro иммунные клетки и TSC, которые при определенных условиях экспрессируют белок, обладающий функцией иммуномодулятора, и возможно IL-12, представляют собой безопасное усовершенствование конститутивной продукции белка (белков). Дополнительно, возможность контролировать время и уровень экспрессии иммуномодулятора и возможно экспрессии IL-12 обеспечивает улучшенный контроль эффективности лечения. Следовательно, сконструированные in vitro иммунные клетки и TSC могут входить в состав фармацевтических композиций как лекарства для лечения рака или опухоли у человека или не относящегося к человеку организма. В качестве альтернативы, сконструированные in vitro популяции иммунных клеток, TSC или их субпопуляции можно применять в качестве носителей для доставки при определенных условиях иммуномодулятора и возможно белка IL-12 для их продукции в определенной области (нормальная ткань, рак или опухоль) организма человека или не относящегося к человеку организма. Указанные иммунные клетки могут представлять собой аутологические или неаутологические дендритные клетки. Дендритные клетки можно выделить из костного мозга или из периферического кровообращения. У пациентов-людей популяции дендритных клеток можно выделить с помощью процедуры лейкафереза, при которой выделяют и удаляют фракцию белых кровяных клеток и вводят обратно пациенту другие компоненты крови.
[000363] В другом варианте реализации настоящего изобретения, указанные дендритные клетки можно получить путем трансфекции гематопоэтических стволовых клеток человека вектором согласно настоящему изобретению, экспрессирующим белок, обладающий функцией иммуномодулятора, и возможно белок, обладающий функцией IL-12, и дифференцировки трансфицированной стволовой клетки с получением дендритной клетки. См. патент США 6,734,014.
[000364] В одном варианте реализации настоящего изобретения, обеспечен аденовирусный вектор нуклеиновых кислот, содержащий генный переключатель, в котором кодирующие последовательности для VP16-RXR и Gal4-EcR, разделенные последовательностью участка внутренней посадки рибосомы (IRES) EMCV, вставлены в аденовирусный челночный вектор под контролем промотора С убиквитина человека. Кодирующие последовательности для субъединиц р40 и р35 IL12, разделенные последовательностью IRES и помещенные под контроль синтетического индуцируемого промотора, вставляют против хода транскрипции от промотора С убиквитина.
[000365] В другом варианте реализации, настоящее изобретение обеспечивает челночный вектор, несущий единицы транскрипции (VP16-RXR и Gal4-EcR) для двух гибридных белков и индуцируемые субъединицы IL-12, рекомбинированные с аденовирусным остовом (AdEasy1) в клетках Е. coli BJ5183. После проверки рекомбинантного клона, плазмиду, несущую геном rAd.RheoIL12, растят в клетках XL10-Gold, а затем очищают от них, расщепляют плазмидный остов и упаковывают путем трансфекции в клетки НЕК 293.
[000366] В конкретном варианте реализации настоящего изобретения, полученный в результате этого первичный вирусный сток амплифицируют путем повторной инфекции клеток НЕК 293 и очищают с помощью центрифугирования в градиенте плотности CsCl.
[000367] В одном варианте реализации настоящего изобретения, последовательность гена иммуномодулятора и/или гена IL-12 представляет собой последовательность гена дикого типа. В другом варианте реализации настоящего изобретения, последовательность гена иммуномодулятора и/или гена IL-12 представляет собой модифицированную последовательность гена, например, химерную последовательность или последовательность, которая была модифицирована таким образом, чтобы использовались предпочтительные кодоны.
[000368] В одном варианте реализации настоящего изобретения, последовательность гена иммуномодулятора и/или гена IL-12 представляет собой последовательность дикого типа человека. В другом варианте реализации настоящего изобретения, последовательность по меньшей мере на 85% идентична последовательности дикого типа человека, например, по меньшей мере на 90%, 95% или 99% идентична последовательности дикого типа человека. В дополнительном варианте реализации настоящего изобретения, последовательность гена кодирует полипептид человека. В другом варианте реализации настоящего изобретения, ген кодирует полипептид, который по меньшей мере на 85% идентичен полипептиду дикого типа человека, например, по меньшей мере на 90%, 95% или 99% идентичен полипептиду дикого типа человека.
[000369] В одном варианте реализации настоящего изобретения, ген IL-12 представляет собой последовательность дикого типа IL-12 мыши. В другом варианте реализации настоящего изобретения, указанная последовательность по меньшей мере на 85% идентична последовательности дикого типа IL-12 мыши, например, по меньшей мере на 90%, 95% или 99% идентична последовательности дикого типа IL-12 мыши. В дополнительном варианте реализации настоящего изобретения, последовательность гена IL-12 кодирует полипептид IL-12 мыши. В другом варианте реализации настоящего изобретения, указанный ген кодирует полипептид, который по меньшей мере на 85% идентичен полипептиду дикого типа IL-12 мыши, например, по меньшей мере на 90%, 95% или 99% идентичен полипептиду дикого типа IL-12 мыши.
[000370] Дендритные клетки (DC) можно выделить из костного мозга людей, мышей или других млекопитающих. Дендритные клетки можно выделить из крови людей, мышей или других млекопитающих. У пациентов-людей, популяции дендритных клеток можно выделить с помощью процедуры лейкафереза, известной в данной области, при которой выделяют и удаляют фракцию белых кровяных клеток и вливают обратно пациенту другие компоненты крови. В одном варианте реализации настоящего изобретения, DC получают из костного мозга мыши, как описано ранее (Tatsumi и др., 2003). Вкратце, костный мозг (ВМ) Tg мыши дикого типа или EGFP культивируют в кондиционированной среде (СМ), дополненной 1000 ед./мл рекомбинантного колониестимулирующего фактора гранулоцитов/макрофагов мыши и рекомбинантным mIL-4 (Peprotech, Роки Хилл, Нью-Джерси) при 37°С в увлажненном термостате при 5% СО2 в течение 7 дней. Затем выделяют CD11c+ DC, например, применяя специфичные гранулы MACSTM, следуя инструкциям изготовителя (Miltenyi Biotec, Оберн, Калифорния). Полученные таким образом CD11c+ DC были >95% чистыми, что выявили на основании морфологии и одновременной экспрессии CD11b, CD40, CD80 и антигенов МНС I класса и II класса.
[000371] Один вариант реализации настоящего изобретения обеспечивает сконструированные иммунные клетки и TSC, при определенных условиях экспрессирующие белок, обладающий функцией иммуномодулятора, и возможно IL-12, подходящие для терапевтического применения для лечения рака или опухоли, или обоих, в качестве генной терапии у человека или не относящегося к человеку организма. В некотором варианте реализации настоящего изобретения, настоящее изобретение обеспечивает сконструированные иммунные клетки и TSC, содержащие генный переключатель.
[000372] В другом варианте реализации, настоящее изобретение обеспечивает сконструированные иммунные клетки и TSC, содержащие по меньшей мере часть рецептора экдизона. В другом варианте реализации, настоящее изобретение обеспечивает сконструированные иммунные клетки и TSC, содержащие генный переключатель, основанный на рецепторе экдизона. В другом варианте реализации, настоящее изобретение обеспечивает сконструированные иммунные клетки и TSC, содержащие RheoSwitch. В другом варианте реализации, настоящее изобретение обеспечивает набор, включающий сконструированные иммунные клетки и TSC, содержащие генный переключатель, и лиганд, который модулирует генный переключатель. В другом варианте реализации настоящего изобретения, наборы дополнительно содержат лиганд диацилгидразин. В другом варианте реализации настоящего изобретения, набор дополнительно содержит RG-115830 или RG-115932.
[000373] В одном варианте реализации, настоящее изобретение обеспечивает сконструированную популяцию иммунных клеток и TSC. В одном варианте реализации настоящего изобретения, культивированные DC на 7 день обрабатывают рекомбинантным аденовирусом, кодирующим иммуномодулятор и/или IL-12, экспрессия которых запускается с конститутивного или индуцируемого промотора, или инфицируют проверочным, контрольным аденовирусным вектором (rAchψ5), в диапазоне множественностей заражения (MOI). Через 48 ч. инфицированные DC собирают и анализируют их фенотип и продукцию иммуномодулятора и/или IL-12, применяя специальный набор ELISA (BD-PharMingen, Сан-Диего, Калифорния), с нижним порогом детектирования, составляющим 62.5 пг/мл.
[000374] В другом варианте реализации, настоящее изобретение обеспечивает сконструированную in vitro популяцию иммунных клеток и TSC, содержащих вектор, например, ДНК-вектор, включающий генный переключатель, способный при определенных условиях экспрессировать белок, обладающий функцией иммуномодулятора и/или IL-12, и дополнительно содержащих активирующий, лиганд.
[000375] В дополнительном варианте реализации, настоящее изобретение обеспечивает способ лечения рака, например, меланомы или глиомы, путем введения сконструированных DC пациенту, а затем введения активирующего лиганда, такого как RG-115819, RG-115830 или RG-115932, указанному пациенту. Пациент может представлять собой человека или животного, страдающего от рака. Способы лечения и продукты, сконструированные клетки, наборы и лиганды находят применение в терапии человека и в терапии домашних животных. Следовательно, продукты и способы предполагают для применения у человека и для ветеринарных целей у животного.
[000376] В одном аспекте, настоящее изобретение обеспечивает фармацевтическую композицию, подходящую для введения человеку или не относящемуся к человеку субъекту, содержащую популяцию сконструированных in vitro иммунных клеток или TSC, экспрессирующих белок, обладающий функцией иммуномодулятора и/или IL-12, при этом указанная лекарственная форма подходит для введения внутрь опухоли. Настоящее изобретение дополнительно обеспечивает фармацевтическую композицию, содержащую активирующий лиганд, такой как RG-115819, RG-115830 или RG-115932, при этом указанная композиция подходит для введения интраперитонеальным, пероральным или подкожным путем.
[000377] В конкретном варианте реализации, описанном в данной заявке, настоящее изобретение обеспечивает способ лечения опухоли, включающий следующие этапы по порядку:
а. введение внутрь опухоли млекопитающего популяции сконструированных in vitro иммунных клеток или TSC; и
b. введение указанному млекопитающему терапевтически эффективного количества активирующего лиганда.
[000378] В одном варианте реализации настоящего изобретения, активирующий лиганд вводят по существу в то же время, что и сконструированные in vitro иммунные клетки или TSC, например, в течение одного часа перед или после введения клеток. В другом варианте реализации настоящего изобретения, активирующий лиганд вводят через или менее чем через приблизительно 24 часа после введения сконструированных in vitro иммунных клеток или TSC. В еще одном варианте реализации настоящего изобретения, активирующий лиганд вводят через или менее чем через приблизительно 48 часов после введения сконструированных in vitro иммунных клеток или TSC. В другом варианте реализации настоящего изобретения, лиганд представляет собой RG-115932. В другом варианте реализации настоящего изобретения, лиганд вводят в дозе, равной приблизительно от 1 до 50 мг/кг/день. В другом варианте реализации настоящего изобретения, лиганд вводят в дозе, равной приблизительно 30 мг/кг/день. В другом варианте реализации настоящего изобретения, лиганд вводят ежедневно в течение периода от 7 до 28 дней. В другом варианте реализации настоящего изобретения, лиганд вводят ежедневно в течение 14 дней. В другом варианте реализации настоящего изобретения, вводят приблизительно от 1×106 до 1×108 клеток. В другом варианте реализации настоящего изобретения, вводят приблизительно 1×107 клеток.
[000379] В одном варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они при определенных условиях экспрессируют IL-2 и IL-12. IL-2 оказывает эффективное иммунорегуляторное действие на эффекторные и регуляторные Т-, NK- и NK-T-клетки. Ожидается, что экспрессия IL-2 и IL-12 в клетках приведет к взаимному повышению экспрессии рецепторов друг друга и индуцирует различные биологические эффекты посредством отдельных путей передачи сигналов. Также ожидается, что комбинация IL-2 и IL-12 увеличит продолжительность иммунной стимуляции и позволит снизить эффективную дозу клеток, которая может быть лучше переносима животными. См. Dietrich 2002, Wigginton 2002, 2001, 1996 и Koyama, 1997, McDermott и Atkins 2008; Bemtsen и др. 2008; Tarhim и др. 2008; Heemskerk и др. 2008; Horton и др. 2008. Полинуклеотидные последовательности IL-2 доступны под номерами доступа U25676 (человека); NM_008366 (мыши); NM_204153 (цыпленка) и NM_053836 (крысы). Полинуклеотидные последовательности IL-12 доступны под номерами доступа NM_000882 (IL12A человека); NM_002187 (IL12B человека); NM_008351 (IL12a мыши); NM_008352 (IL12b мыши); NM_213588 (IL12A цыпленка); NM_213571 (IL12B цыпленка); NM_053390 (IL12a крысы) и NM_022611 (IL12b крысы). SEQ ID NOS:13, 15, 21 и 23 кодируют IL-12 человека и мыши и их субъединицы.
[000380] В другом варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они при определенных условиях экспрессируют IL-18 и IL-12. IL-18 индуцирует продукцию IFN-гамма и вызывает развитие Т-хелперных клеток и активацию NK-клеток. Вдобавок, IL-18 может повысить продукцию GM-CSF и понизить продукцию IL-10. Ожидается, что экспрессия IL-18 и IL-12 позволит преодолеть ограничения, наблюдаемые, когда каждый цитокин вводят отдельно. Ожидается, что экспрессия IL-12 и IL-18 в дендритных клетках будет стимулировать более интенсивные Th1-ответы против опухолевого антигена, чем когда дендритные клетки трансфицируют каждым цитокином отдельно.
[000381] Внутриопухолевая инъекция DC, сконструированных таким образом, что они секретируют как IL-12, так и IL-18, вызывала наиболее высокие уровни продукции INF-γ и полное отторжение опухоли (Tatsumi 2003). См. Vujanovic, 2006. См. также Coughlin, 1998, Subleski, 206, Tatsumi, 2003, и Sabel, 2007; Shiratori и др. 2007; Lian и др. 2007; linuma и др. 2006. Полинуклеотидные последовательности IL-12 см. выше. Полинуклеотидные последовательности IL-18 доступны под номерами доступа U90434 (человека); NM_008360 (мыши); EU747333 (цыпленка) и AY258448 (крысы).
[000382] В другом варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они при определенных условиях экспрессируют IL-15 и IL-12. IL-15 разделяет некоторые биологические активности с IL-2, что также делает его потенциально полезным для лечения рака. IL-15 стимулирует пролиферацию NK-клеток и активированных Т-клеток и поддерживает экспансию эффекторных Т-клеток. Сообщали, что IL-15 действовал синергично с IL-12 с повышением продукции IFN-гамма NK-клетками. Koka, 2004; Basak 2008; Lasek и др. 2004. Внутриопухолевая доставка IL-15 и IL-12 вызывает существенную регрессию опухоли в модели меланомы (Lasek 1999). Полинуклеотидные последовательности IL-12 см. выше. SEQ ID NOS:11 и 19 кодируют IL-15 человека и мыши. На ФИГ.2 и 4 приведены карты плазмид для систем экспрессии, которые можно использовать для экспрессии IL-12 и IL-15 человека и мыши.
[000383] В другом варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они при определенных условиях экспрессируют IL-21 и IL-12. IL-21 и его рецептор разделяют гомологию последовательностей с IL-2 и IL-15. IL-21 вызывает экспансию и созревание NK-клеток. Биологическое действие IL-21 потенциально синергично с IL-12, так как обработка NK-клеток IL-21 приводит к существенному повышению экспрессии рецептора IL-12. Вдобавок, IL-21 может повышать передачу сигнала IL-12 и содействовать ему в повышении продукции IFN-гамма. Полинуклеотидные последовательности IL-12 см. выше. Полинуклеотидные последовательности IL-21 доступны под номерами доступа AF254069 (человека); NM_021782 (мыши); NM_001024835 (цыпленка) и NM_001108943 (крысы). SEQ ID NOS:6, 7, 8, 9, и 17 кодируют IL-21 человека и мыши. SEQ ID NOS:1 и 2 представляют собой Полинуклеотидные конструкции, которые кодируют IL-12 и IL-21 мыши и человека. На ФИГ.7 и 8 приведены карты плазмид для систем экспрессии, которые можно использовать для экспрессии IL-12 и IL-21 человека и мыши, соответственно.
[000384] В другом варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они при определенных условиях экспрессируют TNF-альфа и IL-12. TNF-альфа представляет собой эффективный активатор иммунных клеток, и он опосредует противоопухолевые свойства. Вдобавок, TNF-альфа может действовать синергично с IL-12 с повышением экспрессии IFN-гамма и рецептора IL-12 на Т-клетках. В исследовании на животных, применение как IL-12, так и TNF-альфа привело к инфильтрации опухоли DN8+ Т-клетками, существенной продукции IFN-гамма и последующей регрессии опухоли. См. Sabel, 2003, 2004, 2007, Taniguchi, 1998, Lasek, 2000; и Xia и др. 2008. Полинуклеотидные последовательности IL-12 см. выше. Полинуклеотидные последовательности, кодирующие TNF-альфа, доступны под номерами доступа Х02910 (человека); NM_013693 (мыши) и ВС107671 (крысы).
[000385] В другом варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они при определенных условиях экспрессируют IL-7 и IL-12. IL-7 представляет собой член семейства IL-2, и он важен для лимфопоэза Т-клеток и В-клеток. IL-7 регулирует гомеостаз выживаемости и пролиферации наивных Т-клеток и CD8+ Т-клеток памяти. Было показано, что IL-7 повышает образование CTL против опухолей. Вдобавок, IL-12 направленно действует на CD8+ Т-клетки с повышением опосредованной IL-7 пролиферации. Дополнительно, сообщали, что IL-7 и IL-12 синергично повышают цитотоксичность CD8+ T-клеток. Mehrotra, 1995; Sharma и др. 2003; Tirapu и др. 2002. Таким образом, ожидается, что совместная экспрессия IL-7 и IL-12 обеспечит оптимальные противоопухолевые ответы. Полинуклеотидные последовательности, кодирующие IL-12, см. выше. Полинуклеотидные последовательности, кодирующие IL-7, доступны под номерами доступа J04156 (человека); NM_008371 (мыши); NM_001037833 (цыпленка) и NM_013110 (крысы).
[000386] В другом варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они при определенных условиях экспрессируют GM-CSF и IL-12. GM-CSF регулирует дифференцировку и пролиферацию гематопоэтических клеток-предшественников и играет особенно важную роль в созревании специальных антигенпрезентирующих клеток (АРС), таких как дендритные клетки. GM-CSF также повышает способность дендритных клеток процессировать и представлять антигены. GM-CSF функционирует иначе, чем IL-12, и оба вызывают существенные противоопухолевые ответы в исследованиях на животных. Ожидают, что комбинация IL-12 (активация Т-клеток) и GM-CSF (активация дендритных клеток) приведет к более эффективному противоопухолевому иммунитету. В исследованиях на животных, лечение GM-CSF в комбинации с IL-12 значительно подавляло рост опухоли во множестве моделей рака. Wang, 2001; Chang, 2007; Jean, 2004; Nair, 2006; Hill 2002; Small и др. 2007. В испытаниях на человеке, GM-CSF + IL-12 успешно применяли для лечения пациентов, страдающих миеломой, у которых комбинированное действие обоих цитокинов приводило к уменьшению количества В-клеток в кровотоке. Rasmussen, 2003; Hansson, 2007; Abdalla, 2007. Ожидается, что совместная экспрессия GM-CSF и IL-12 в одной клетке поможет избежать нежелательных системных эффектов, таких как уменьшение количества В-клеток в кровотоке. Полинуклеотидные последовательности, кодирующие IL-12, см. выше. Полинуклеотидные последовательности GM-CSF доступны под номерами доступа M11734 (человека); NM_009969 (мыши); EU520303 (цыпленка); NM_001037660 (Csf2ra крысы) и NMJ 33555 (Csf2rb крысы).
[000387] В другом варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они при определенных условиях экспрессируют хемокин (например, CCL3 (MIP-1a), CCL5 (RANTES), CCL7 (МСР3), XCL1 (лимфотактин), CCL19 (MIP-3b), CXCL9 (MIG), CXCL10 (IP-10), CXCL12 (SDF-1) или CCL21 (6Ckine)) и JL-2. Хемокины представляют, собой, хемоаттракторные цитокины, которые регулируют направленную миграцию и активацию лейкоцитов и других типов клеток при множестве воспалительных и невоспалительных состояний. Воспалительные цитокины контролируют привлечение лейкоцитов при воспалении и повреждении ткани. Гомеостатические хемокины осуществляют функции домашнего хозяйства, такие как управление перемещением лейкоцитов (например, дендритных клеток) к вторичным лимфоидным органам и внутри них, а также в костном мозге и тимусе во время гематопоэза. В исследованиях на животных, совместная внутриопухолевая инъекция двух отдельных аденовирусов, экспрессирующих IL-12 и CXCL10, привела к 100% регрессии опухолевых узелков, произошедших от линии клеток колоректальной аденокарциномы мыши СТ26. Narvaiza и др., 2000, Emtage и др., 1999, описали два дважды рекомбинантных аденовирусных вектора, экспрессирующих либо IL2 и XCL1 (лимфотактин), либо IL-12 и XCL1. Внутриопухолевая инъекция указанных векторов в аденокарциномные опухоли груди у мышей вызвала эффективные противоопухолевые реакции и защитный иммунитет. В других исследованиях на животных, совместная трансдукция аденовирусных векторов, экспрессирующих IL-12 и CCL27, привела к регрессии опухоли и длительному специфичному иммунитету. Gao и др., 2007. Таким образом, ожидается, что совместная экспрессия хемокина и IL-12 согласно настоящему изобретению приведет к синергичной противоопухолевой активности.
[000388] В другом варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они при определенных условиях экспрессируют антиангиогенный цитокин (например, IP-10 и Mig) и IL-12. IP-10 и Mig представляют собой хемоаттрактанты для Т-клеток и NK-клеток, и их способность ингибировать ангиогенез зависит от NK-клеток. Исследования на животных показали, что комбинированная терапия двумя аденовирусами, один из которых экспрессирует IP 10, а другой экспрессирует IL-12, привела к заметному совместному противоопухолевому действию. Narvaiza и др., 2000. В других исследованиях, аденовирусные векторы, экспрессирующие IP 10 или MIG и/или IL-12, вводили внутрь опухоли в модели на мышах аденокарциномы и фибросаркомы молочной железы. Обнаружили, что введение IP-10 или MIG в комбинации с IL-12 привело к значительной регрессии опухоли и повышенной выживаемости несущих опухоль животных по сравнению с животными, которым вводили IP 10, MIG, IL-12 отдельно, или с контрольными животными, при этом комбинация IP-10, IL12 была наиболее эффективной. Palmer, 2001. См. также Mazzolini, 2003; и Huang 2004. Таким образом, ожидается, что совместная экспрессия антиангиогенного цитокина и IL-12 приведет к синергичной противоопухолевой активности.
[000389] Чтобы продемонстрировать эффективную опосредованную IL-12 генную терапию, использовали кондиционную систему экспрессии кДНК, которая позволяет запускать продукцию иммуномодулятора и/или IL-12 иммунными клетками или TSC в различные моменты времени после внутриопухолевой инъекции. На основании результатов для модели агрессивной меланомы В 16 у мышей C57BL/6 были сделаны следующие выводы: 1) повышенные уровни IL-12 секретируются DC.RheoIL12 в присутствии активирующего лиганда RG-115830, но не в отсутствии указанного лиганда; 2) внутриопухолевая основанная на DC.RheoIL12 терапия также эффективна, как и внутриопухолевая основанная на DC.cIL12 терапия, при условии, что RG-115830 вводят животным, которых лечат, в течение 24 ч после инъекции DC (а в более поздние моменты времени предоставления лиганда терапия RG-115830 терпит неудачу); 3) экспрессия IL-12 в DC, похоже, продлевает выживаемость данных клеток в микроокружении опухоли и связана с более высоким количеством DC, инъецированных внутрь опухоли, которые мигрируют в дренирующие опухоль лимфатические узлы; и 4) наиболее сильный иммунный коррелят результата терапии представляет собой уровень опухолеспецифических CD8+ Т-клеток, перекрестно примированных терапией, а не количество инъецированных DC, оставшихся в микроокружении опухоли. В целом, полученные результаты позволяют предположить, что основанные на DC.IL12 методы лечения, вероятно, успешны благодаря положительному влиянию на афферентные события (перекрестное примирование) эффекторов CD8+ Т-клеток 1 типа, но не на более поздние эфферентные события, такие как опосредованное инъецированными DC привлечение противоопухолевых Т-клеток в микроокружение опухоли и т.д.
[000390] Перед внутриопухолевой инъекцией, клетки (иммунные клетки или TSC) можно обработать некоторым фактором, чтобы стимулировать активность клеток. Например, клетки можно обработать костимулирующей молекулой, такой как положительно костимулирующая молекула, включая OX40L, 4-1BBL, CD40, CD40L, GITRL, CD70, LIGHT или ICOS-L, или отрицательно. костимулирующей молекулой, такой как антитела против CTLA4, антитела против PD-L1 или антитела против PD-L2. Например, клетки (например, иммунные клетки или TSC) можно инкубировать с клеткой, экспрессирующей одну или более костимулирующих молекул, например, с клетками лимфомы J588, экспрессирующими молекулу лиганда CD40. В другом варианте реализации настоящего изобретения, клетки (иммунные клетки или TSC) можно обработать молекулой, направленной против иммунных супрессоров (ингибитором толерантности), такой как антитела против TGF-бета (для ингибирования передачи сигнала TGF в микроокружении), антитела против IL-10, TGFbRII DN (для ингибирования передачи сигнала TGF в генномодифицированных клетках), DN IL-10R, dnFADD (для ингибирования путей клеточной гибели внутри клеток), антитела против SOCS1, миРНК или рецепторы-ловушки (для ингибирования передачи супрессорного сигнала цитокинов внутри клеток) или антитела против TGFa.
[000391] Получали рекомбинантные аденовирусы, несущие полинуклеотидные последовательности, показанные на Фигурах 1-8. Например, hIL-21 получали путем совместной трансфекции вектора экспрессии hIL-21, линеаризованного с помощью рестрикционного расщепления в сайте, расположенном против хода транскрипции от левого ITR, и подходящего (например, с удаленным ЕЗ) аденовирусного остова в пермиссивную линию клеток, такую как клетки НЕК293. Аденовирусный вектор, несущий иммуномодуляторные гены мыши, использовали для трансдукции дендритных клеток или TSC мыши для применения в терапевтических моделях на мышах. Для терапевтических применений у человека, полинуклеотид, кодирующий человеческий гомолог иммуномодуляторного гена, вставляли в подходящий вектор. Аденовирусный вектор для терапевтического применения у человека получали при условиях GMP (надлежащей производственной практики). Пример схемы лечения (клинического испытания) пациентов, страдающих меланомой III/IV стадии, описан далее. Лечение в данном случае включало внутриопухолевую инъекцию трансфицированных аденовирусом дендритных клеток и ежедневное пероральное введение в течение 14 дней активаторного средства (лиганда). Субъектов подвергали скринингу от 30 дней до одной недели до клинического испытания. Каждого субъекта просили подписать информированное согласие перед началом проведения каких-либо процедур. Исследователь информировал субъектов о природе, целях, продолжительности, потенциальной опасности и процедурах, которые будут выполняться во время испытания, и о вероятности того, что их медицинские карты может проверять FDA (Управление по контролю качества продовольствия и медикаментов). Субъектов (всего от 16 до 20) произвольно разделили на 4 группы. Все группы получали внутриопухолевую инъекцию до 5×107 трансфицированных дендритных клеток, приблизительно через 3 часа после перорального введения первой дозы лиганда. 4 группы отличались по получаемой ежедневно пероральной дозе лиганда: например, группа 1 = 0.01 мг/кг; группа 2 = 0.3 мг/кг; группа 3 = 1 мг/кг; группа 4 = 3 мг/кг. Во время курса лечения, отбирали кровь в определенные промежутки времени для оценки однократной дозы и стационарной фармакокинетики активаторного лекарственного средства и его основных метаболитов. Также, кровь отбирали в определенные моменты времени для оценки гуморального и клеточного иммунных ответов против вирусного вектора, компонентов RTS и опухоли. Собирали мочу и отбирали кровь в определенные моменты времени для химического анализа сыворотки, анализа мочи и гематологии (показатели безопасности). Биопсии опухоли и/или дренирующего опухоль лимфатического узла брали в определенные моменты времени для оценки экспрессии трансгена и иммунного ответа на опухоль в результате терапии. Для пациентов устанавливали критерии раннего прекращения испытания в случае возникновения нежелательных явлений, и нежелательные явления регистрировали. За пациентами наблюдали в течение 1, 2, 3 и 4 месяцев для обнаружения нежелательных явлений и результата терапии.
[000392] В другом варианте реализации настоящего изобретения, субъекту, нуждающемуся в лечении опухоли, (а) вводят дендритные клетки, сконструированные таким образом, что они экспрессируют иммуномодулятор, например, иммуномодулятор, описанный в данной заявке, либо конститутивно, либо при определенных условиях, и (b) вектор, экспрессирующий иммуномодулятор, например, иммуномодулятор, описанный в данной заявке, либо конститутивно, либо при определенных условиях; путем внутриопухолевой инъекции субъекту. В предпочтительном варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они экспрессируют вектор Ad-иммуномодулятор и, в частности, вектор Ad-RTS-иммуномодулятор. В другом предпочтительном варианте реализации настоящего изобретения, вектор, который вводят путем внутриопухолевой инъекции субъекту, представляет собой вектор Ad-иммуномодулятор и, в частности, вектор Ad-RTS-иммуномодулятор.
[000393] В другом варианте реализации настоящего изобретения, субъекту, нуждающемуся в лечении опухоли, (а) вводят дендритные клетки, сконструированные таким образом, что они экспрессируют IL-12, либо конститутивно, либо при определенных условиях, и (b) вектор, экспрессирующий IL-12, либо конститутивно, либо при определенных условиях, путем внутриопухолевой инъекции субъекту. В предпочтительном варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они экспрессируют вектор Ad-IL-12, и, в частности, вектор Ad-RTS-IL-12. В другом предпочтительном варианте реализации настоящего изобретения, вектор, который вводят путем внутриопухолевой инъекции субъекту, представляет собой вектор Ad-IL-12, и, в частности, вектор Ad-RTS-IL-12.
[000394] В другом варианте реализации настоящего изобретения, субъекту, нуждающемуся в лечении опухоли, (а) вводят дендритные клетки, сконструированные таким образом, что они экспрессируют IL-12, либо конститутивно, либо при определенных условиях, и (b) субъекту вводят один или более противораковых химиотерапевтических агентов. В предпочтительном варианте реализации настоящего изобретения, сконструированные дендритные клетки сконструированы таким образом, что они экспрессируют вектор Ad-IL-12, и, в частности, вектор Ad-RTS-IL-12. Указанный один или более противораковых химиотерапевтических агентов можно вводить перед введением сконструированных дендритных клеток, после введения сконструированных дендритных клеток или одновременно с введением сконструированных дендритных клеток. В предпочтительном варианте реализации настоящего изобретения, указанный противораковый химиотерапевтический агент представляет собой паклитаксел, производное или аналог паклитаксела, темозоломид, производное или аналог темозоломида, сунитиниб, производное или аналог сунитиниба, гемцитабин, или производное или аналог гемцитабина.
[000395] В другом варианте реализации настоящего изобретения, субъекту, нуждающемуся в лечении опухоли, (а) вводят дендритные клетки, сконструированные таким образом, что они экспрессируют IL-12, либо конститутивно, либо при определенных условиях, (b) вектор, экспрессирующий IL-12, либо конститутивно, либо при определенных условиях, путем внутриопухолевой инъекции субъекту, и (с) указанному субъекту вводят один или более противораковых химиотерапевтических агентов. В предпочтительном варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они экспрессируют вектор Ad-IL-12, и, в частности, вектор Ad-RTS-IL-12. В другом предпочтительном варианте реализации настоящего изобретения, вектор, который вводят путем внутриопухолевой инъекции субъекту, представляет собой вектор Ad-IL-12, и, в частности, вектор Ad-RTS-IL-12. Указанный один или более противораковых химиотерапевтических агентов можно вводить перед введением сконструированных дендритных клеток и вектора, экспрессирующего IL-12, после введения сконструированных дендритных клеток и вектора, экспрессирующего IL-12, или одновременно с введением сконструированных дендритных клеток и вектора, экспрессирующего IL-12. В предпочтительном варианте реализации настоящего изобретения, указанный противораковый химиотерапевтический агент представляет собой паклитаксел, производное или аналог паклитаксела, темозоломид, производное или аналог темозоломида, сунитиниб, производное или аналог сунитиниба, гемцитабин, или производное или аналог гемцитабина.
[000396] В другом варианте реализации настоящего изобретения, субъекту, нуждающемуся в лечении опухоли, (а) вводят дендритные клетки, сконструированные таким образом, что они экспрессируют иммуномодулятор, например, иммуномодулятор, описанный в данной заявке, либо конститутивно, либо при определенных условиях, и (b) вектор, экспрессирующий иммуномодулятор, например, иммуномодулятор, описанный в данной заявке, либо конститутивно, либо при определенных условиях, путем внутриопухолевой инъекции субъекту. В предпочтительном варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они экспрессируют вектор Ad-иммуномодулятор и, в частности, вектор Ad-RTS-иммуномодулятор. В другом предпочтительном варианте реализации настоящего изобретения, вектор, который вводят путем внутриопухолевой инъекции субъекту, представляет собой вектор Ad-IL-иммуномодулятор, и, в частности, вектор Ad-RTS-иммуномодулятор.
[000397] В другом варианте реализации настоящего изобретения, субъекту, нуждающемуся в лечении опухоли, (а) вводят дендритные клетки, сконструированные таким образом, что они экспрессируют иммуномодулятор, например, иммуномодулятор, описанный в данной заявке, либо конститутивно, либо при определенных условиях, и (b) указанному субъекту вводят один или более противораковых химиотерапевтических агентов. В предпочтительном варианте реализации настоящего изобретения, сконструированные дендритные клетки сконструированы таким образом, что они экспрессируют вектор Ad-иммуномодулятор и, в частности, вектор Ad-RTS-иммуномодулятор. Указанный один или более противораковых химиотерапевтических агентов можно вводить перед введением сконструированных дендритных клеток, после введения сконструированных дендритных клеток или одновременно с введением сконструированных дендритных клеток. В предпочтительном варианте реализации настоящего изобретения, противораковый химиотерапевтический агент представляет собой паклитаксел, производное или аналог паклитаксела, темозоломид, производное или аналог темозоломида, сунитиниб, производное или аналог сунитиниба, гемцитабин или производное или аналог гемцитабина.
[000398] В другом варианте реализации настоящего изобретения, субъекту, нуждающемуся в лечении опухоли, (а) вводят дендритные клетки, сконструированные таким образом, что они экспрессируют иммуномодулятор, например, иммуномодулятор, описанный в данной заявке, либо конститутивно, либо при определенных условиях, (b) вектор, экспрессирующий иммуномодулятор, например, иммуномодулятор, описанный в данной заявке, либо конститутивно, либо при определенных условиях, путем внутриопухолевой инъекции субъекту, и (с) субъекту вводят один или более противораковых химиотерапевтических агентов. В предпочтительном варианте реализации настоящего изобретения, дендритные клетки сконструированы таким образом, что они экспрессируют вектор Ad-иммуномодулятор и, в частности, вектор Ad-RTS-иммуномодулятор. В другом предпочтительном варианте реализации настоящего изобретения, вектор, который вводят путем внутриопухолевой инъекции субъекту, представляет собой вектор Ad-иммуномодулятор и, в частности, вектор Ad-RTS-иммуномодулятор. Указанный один или более противораковых химиотерапевтических агентов можно вводить перед введением сконструированных дендритных клеток и вектора, экспрессирующего иммуномодулятор, после введения сконструированных дендритных клеток и вектора, экспрессирующего иммуномодулятор, или одновременно с введением сконструированных дендритных клеток и вектора, экспрессирующего иммуномодулятор. В предпочтительном варианте реализации настоящего изобретения, противораковый химиотерапевтический агент представляет собой паклитаксел, производное или аналог паклитаксела, темозоломид, производное или аналог темозоломида, сунитиниб, производное или аналог сунитиниба, гемцитабин или производное или аналог гемцитабина.
[000399] В любом из способов согласно настоящему изобретению, указанное заболевание или расстройство может представлять собой заболевание или расстройство, описанное в настоящей заявке. В одном варианте реализации настоящего изобретения, указанное заболевание или расстройство представляет собой заболевание или расстройство, приведенное в Таблице 1 в данной заявке. В другом варианте реализации настоящего изобретения, указанное заболевание или расстройство представляет собой заболевание или расстройство, приведенное в Таблице 3 в данной заявке.
[000400] В любом из способов согласно настоящему изобретению, рак или опухоль может представлять собой заболевание или расстройство, описанное в настоящей заявке. В одном варианте реализации настоящего изобретения, рак или опухоль представляет собой рак или опухоль, приведенные в Таблице 1 в данной заявке. В другом варианте реализации настоящего изобретения, рак или опухоль представляет собой рак или опухоль, приведенные в Таблице 3 в данной заявке.
[000401] Можно измерить влияние экспрессии иммуномодулятора и/или IL-12 на популяцию клеток путем измерения уровня экспрессии или активности цитокина типа Th1/Tc1, IFN-гамма, в биологическом образце из пациента.
[000402] Для целей настоящего изобретения, настоящее изобретение обеспечивает способ определения эффективности схемы лечения ракового пациента, основанной на сконструированных in vitro иммунных клетках или TSC, включающий:
а. измерение уровня экспрессии, или уровня активности, или обоих уровней для интерферона-гамма (IFN-гамма) в первом биологическом образце, полученном из пациента-человека, перед введением сконструированных in vitro клеток, например, иммунных клеток или TSC, таким образом получая контрольный уровень;
b. введение внутрь опухоли указанного пациента сконструированных in vitro клеток;
с. введение указанному пациенту эффективного количества активирующего лиганда;
d. измерение уровня экспрессии, или уровня активности, или обоих уровней для IFN-гамма во втором биологическом образце, полученном от указанного пациента в некоторый момент времени после введения указанного активирующего лиганда, таким образом получая результаты для | тестового уровня; и
е. сравнение контрольного уровня с тестовым уровнем IFN-гамма, при этом результаты, указывающие на повышение уровня экспрессии, активности, или обоих уровней для IFN-гамма в тестовом уровне относительно контрольного уровня, указывают на то, что схема лечения эффективна для указанного пациента. Настоящее изобретение также возможно может включать дополнительные этапы, перечисленные далее:
f. проведение биопсии и подсчет инфильтрирующих опухоль лимфоцитов (TIL) и/или
g. наблюдение регрессии опухоли в ответ на лечение.
[000403] Термин "субъект" означает интактное насекомое, растение или животное. Также ожидается, что лиганды будут работать в равной степени хорошо, когда субъект будет представлять собой грибок или дрожжи. Животные, в которых используют настоящее изобретение, включают позвоночных, например, млекопитающих, таких как люди, грызуны, обезьяны и другие животные, но не ограничены ими, при этом люди или мыши наиболее предпочтительны. Другие животные включают домашних животных, таких как собаки, коты, лошади, крупный рогатый скот, овцы, козы, свиньи и тому подобные.
[000404] Без привязки к какой-либо теории, ожидается, что настоящее изобретение будет содействовать применению генной терапии вводимыми внутрь опухоли сконструированными т vitro иммунными клетками и TSC в клинической практике, уделяя особое внимание объективным клиническим ответам как первостепенному ожидаемому результату исследования и примированным противоопухолевым CD8+ Т-клеткам (продуцирующим IFN-гамма) как второстепенному ожидаемому результату исследования. Возможность включать и выключать экспрессию иммуномодулятора и/или IL-12 in vivo повышает безопасность и терапевтический контроль над лечением, поскольку как время, так и уровень экспрессии белка можно контролировать с помощью введения лиганда, и дополнительно поскольку ожидают, что время экспрессии иммуномодулятора и/или IL-12 крайне важно для терапевтической эффективности указанного способа.
[000405] Настоящее изобретение дополнительно способствует терапевтическому применению сконструированных in vitro клеток со вставленными генами, экспрессируемыми при определенных условиях, как инновационному подходу для эффективного и действенного лечения заболеваний человека.
[000406] В случае противоречия между какой-либо идеей или предположением в любом из ссылочных материалов, цитируемых в них и настоящем описании, последнее должно иметь приоритетное значение для целей настоящего изобретения.
[000407] Все патенты, заявки на патент и публикации, цитированные в данной заявке, полностью включены в настоящую заявку посредством ссылки.
[000408] Должно быть очевидно, что описанные выше варианты реализации и пояснительные примеры не предполагаются ограничивающими в каком-либо отношении объем настоящего изобретения, и что подразумевается, что в объем формулы изобретения, приведенной в данной заявке, входят все варианты реализации и пояснительные примеры, независимо от того, представлены они явным образом в данной заявке или нет.
[000409] Патентная заявка США номер 12/247,738 с названием "Engineered Dendritic Cells And Uses For Treatment Of Cancer", поданная 8 октября 2008 г., настоящим полностью включена посредством ссылки. Патентная заявка США номер 12/241,018 с названием "Therapeutic Gene-Switch Constructs And Bioreactors For The Expression Of Biotherapeutic Molecules, And Uses Thereof, поданная 29 сентября 2008 г., также настоящим полностью включена посредством ссылки.
ПРИМЕР 1
[000410] Исследование предпринимали, чтобы определить дозу дендритных клеток и наиболее эффективный цитокин, который способен вызвать опухолеспецифические иммунные ответы и противоопухолевую активность в опухолевой модели почечноклеточного рака Renca.
[000411] В данном исследовании использовали две линии опухолевых клеток: Renca и Renca-HA. Последнюю линию клеток получали путем трансфекции клеток Renca гемагглютинином вируса гриппа (НА). Преимущество модели Renca-HA состоит в возможности отслеживать антигенспецифические Т-клетки, так как оба полученных из НА CD 8- и CD4-специфичных эпитопа известны и уже использовались.
[000412] Конкретная цель состояла в определении индукции НА-специфичных иммунных ответов после внутриопухолевого введения дендритных клеток.
[000413] Формировали подкожную опухоль Renca-HA у BALB/c мышей. Когда опухоль становилась пальпируемой, дендритные клетки инъецировали внутрь опухоли. Введение дендритных клеток повторяли дважды с 7-дневными промежутками времени, всего осуществляли 3 введения.
[000414] Использовали следующие группы мышей (в каждой группе находилось 3 мыши):
1. Мыши, которым ничего не вводили;
2. Мыши, которым вводили 5×105 дендритных клеток, трансдуцированных контрольной плазмидой;
3. Мыши, которым вводили 106 дендритных клеток, трансдуцированных контрольной плазмидой;
4. Мыши, которым вводили 5×106 дендритных клеток, трансдуцированных контрольной плазмидой;
5. Тех же, что и в группах 2-4, применяя дендритные клетки, трансдуцированные IL-12;
6. Тех же, что и в группах 2-4, применяя дендритные клетки, трансдуцированные IL-15; и
7. Тех же, что и в группах 2-4, применяя дендритные клетки, трансдуцированные IL-21.
Для тестирования влияния комбинации различных цитокинов, мышам одновременно вводили:
8. 5×105 дендритных клеток, трансдуцированных IL-12, и 5×105дендритных клеток, трансдуцированных IL-15,
9. 5×105 дендритных клеток, трансдуцированных IL-12, и 5×105дендритных клеток, трансдуцированных IL-21, и
10. 5×105 дендритных клеток, трансдуцированных IL-15, и 5×105дендритных клеток, трансдуцированных IL-21.
[000415] Через четыре дня после последнего введения, лимфатические узлы несущих опухоль мышей удаляли и клетки стимулировали либо подходящим для МНС I класса пептидом (для обнаружения ответов CD8+ Т-клеток), либо подходящим для МНС II класса пептидом (для обнаружения ответов CD4+ Т-клеток).
[000416] Проводили следующие анализы:
[000417] 1. ELISPOT IFN-γ и IL-2;
2. Анализ пролиферации Т-клеток;
3. Обнаружение высвобождения TNFα, IL-10, IL-4 и GM-CSF клетками лимфатических узлов.
[000418] Вдобавок, NK-активность клеток лимфатических узлов оценивали, применяя клетки YAC в качестве мишеней.
[000419] Параллельно, клетки стимулировали антителами против CD3/CD28, чтобы оценить неспецифический ответ Т-клеток.
[000420] Определили наиболее эффективную дозу дендритных клеток, способную вызвать антигенспецифические иммунные ответы.
[000421] Конкретная цель 2 - оценить противоопухолевую активность дендритных клеток, трансдуцированных генами цитокинов.
[000422] В дальнейших экспериментах использовали только такие трансдуцированные цитокинами дендритные клетки, для которых продемонстрировали статистически значимую индукцию иммунных ответов.
[000423] Лечение несущих опухоль Renca-HA мышей осуществляли, как описано в конкретной цели 1. Использовали одну дозу DC, трансдуцированных цитокинами, которые проявили специфическую активность в предшествующих экспериментах. В качестве контроля использовали дендритные клетки, трансфицированные контрольным аденовирусом. Чтобы достигнуть статистической значимости, в каждую группу включали по 10 мышей.
[000424] Оценивали рост опухоли. Опухоль Renca-HA содержит иммуногенный эпитоп, который полезен для иммунологического контроля и предварительного тестирования противоопухолевого действия. Тем не менее, чтобы проверить потенциальную противоопухолевую активность лечения, нужно использовать нетрансфицированные опухолевые клетки. Следовательно, эксперименты, описанные выше, повторяли с применением модели опухоли Renca.
ПРИМЕР 2
[000425] Безопасность, переносимость, функционирование трансгена и иммунологическое действие внутриопухолевой инъекции(й) трансдуцированных аденовирусом аутологических дендритных клеток, сконструированных таким образом, что они экспрессируют hIL-12 и один или более других иммуномодуляторов под контролем RTS, у субъектов с меланомой на стадиях III и IV оценивали с помощью таких способов, как описанные ниже.
[000426] Исследование с участием субъектов исследования с меланомой на стадиях III и IV осуществляли на 4 когортах (группах) субъектов, при этом каждый субъект получал одну внутриопухолевую инъекцию (в меланомную опухоль) трансдуцированных аденовирусом аутологических (введенных обратно тому же субъекту, от которого они произошли) дендритных клеток (DC), сконструированных таким образом, что они экспрессируют интерлейкин-12 человека (ML-12) и один или более других иммуномодуляторов, в дозе, равной 5×107, в комбинации с ежедневным пероральным введением доз активаторного средства (активирующего лиганда). В исследовании применяли инъекции дендритных клеток, трансдуцированных ex vivo (после того, как клетки удаляли из субъектов) аденовирусным вектором, для индуцируемой экспрессии IL-12 человека и одного или нескольких других иммуномодуляторов. Продукцию IL-12 и одного или нескольких других иммуномодуляторов инъецированными DC "запускали" (индуцировали) с помощью активации RTS путем перорального введения активирующего средства (RG-115932). Безопасность и переносимость оценивали с помощью физического обследования (включая функциональный статус по ECOG), измерения показателей жизнедеятельности, химического анализа сыворотки, анализа мочи, гематологии, возникновения нежелательных "побочных эффектов" и антител и клеточного иммунного ответа на аденовирус, компоненты RTS и активирующее средство. Чтобы оценить улучшение, измеряли однодозовую и стационарную фармакокинетику/ADME (всасывание, распределение, метаболизм и выведение) перорального активирующего средства и его основных метаболитов, осуществляли анализ уровней hIL-12, уровней других иммуномодуляторов и клеточного иммунного ответа (Т-клетки) в биоптатах целевых опухолей, дренирующих опухоли лимфатических узлах и периферическом кровообращении, а также измеряли профиль цитокинов в сыворотке.
[000427] Например, 16 субъектов с меланомой на стадиях III и IV разделяли на четыре группы, при этом группы 1 и 2 включали по три субъекта и группы 3 и 4 включали по 5 субъектов. Все субъекты получали однократную внутриопухолевую инъекцию 5×107 аутологических DC, трансфицированных аденовирусным вектором, кодирующим IL-12 человека и один или более других иммуномодуляторов под контролем RTS. Например, субъектам осуществляли внутриопухолевую инъекцию аутологических DC, трансдуцированных аденовирусным вектором, кодирующим IL-12 человека под контролем RTS и иммуномодулятор, такой как IL-15 или IL-21.
[000428] Субъекты получали однократную ежедневную пероральную дозу активирующего средства (группа 1: 0.01 мг/кг, группа 2: 0.1 мг/кг, группа 3: 1.0 мг/кг или группа 4: 3 мг/кг), при этом первую дозу вводили приблизительно за 3 часа до инъекции DC в день 1 и продолжали введение в течение 13 следующих дней. Дополнительную инъекцию(и) трансдуцированных аденовирусом аутологических дендритных клеток в комбинации с 14 однократными (один раз) ежедневными пероральными дозами активирующего средства можно осуществлять подходящим субъектам, которые удовлетворяют критериям для повторного лечения. Безопасность, переносимость и функционирование дендритных клеток оценивают для всех субъектов в каждой группе, начиная с группы 1, в течение вплоть до одного месяца после инъекции сконструированных in vitro дендритных клеток, перед включением в исследование следующих субъектов, получающих более высокие дозы активирующего средства. Оценку безопасности продолжали для всех субъектов в течение 3 месяцев после первоначальной инъекции сконструированных дендритных клеток, с возможностью продлить период наблюдения до шести месяцев, чтобы проконтролировать безопасность для субъекта, если наблюдается токсичность или субъект получает дополнительную инъекцию(и) дендритных клеток.
[000429] Такое исследование демонстрирует безопасность и переносимость однократной или многократной внутриопухолевой инъекции(й) трансдуцированных аденовирусом аутологических дендритных клеток в комбинации с пероральным активирующим средством у субъектов с меланомой. Исследование позволяет получить стационарную фармакокинетику/ADME перорального активирующего средства. Данное исследование демонстрирует функциональность RTS у субъектов с помощью измерения экспрессии hIL-12 и экспрессии одного или нескольких других иммуномодуляторов трансдуцированными аденовирусом аутологическими дендритными клетками в целевой опухоли и/или дренирующих опухоль лимфатических узлах в ответ на активацию RTS посредством перорального введения активирующего средства. Более того, данное исследование демонстрирует иммунологическое действие трансдуцированных аденовирусом аутологических дендритных клеток в отношении клеточного иммунного ответа в целевой опухоли, дренирующих ее лимфатических узлах и периферическом кровообращении после перорального введения активирующего средства.
[000430] Меланому выбрали в качестве примера рака. Было показано, что меланома, в частности, среди солидных опухолей, отвечает на иммунотерапевтические подходы, и меланомные опухоли легко доступны для внутриопухолевой инъекции и биопсии. Субъекты, включенные в исследование, имели неоперабельную меланому III или IV стадии, которая была по меньшей мере 0.5 см в диаметре, с любой толщиной опухоли, любым количеством вовлеченных лимфатических узлов, транзитными метастазами или отдаленными метастазами.
Получение аденовируса, несущего терапевтическую систему RheoSwitch, ML-12 и один или более других иммуномодуляторов.
[000431] Рекомбинантную ДНК переносили в дендритные клетки (DC) путем трансдукции аденовирусного вектора ex vivo. Рекомбинантную ДНК применяли для экспрессии IL-12 человека (р70) и одного или нескольких других иммуномодуляторов инъецированными внутрь опухоли незрелыми дендритными клетками, что придавало выживаемость и стимулировало созревание DC в окружении опухоли и приводило к их последующей миграции в дренирующие опухоль лимфатические узлы. Это приводило к смещению дифференцировки Т-хелперных клеток в тип Th1, а также к активации опухолеспецифических цитотоксических Т-клеток путем примирования перекрестнореагирующими опухолевыми антигенами.
[000432] Рекомбинантная ДНК, используемая в виде рекомбинантного аденовирусного вектора, позволяет экспрессию IL-12 человека и одного или нескольких других иммуномодуляторов под контролем терапевтической системы RheoSwitch® (RTS). RTS содержит бицистронную информационную последовательность, экспрессируемую с промотора С убиквитина человека и кодирующую два слитых белка: Gal4-EcR и VP16-RXR. Gal4-EcR представляет собой слитые связывающий ДНК домен (аминокислоты 1-147) Gal4 дрожжей и DEF-домены рецептора экдизона насекомого Choristoneura fumiferana. В другом варианте реализации настоящего изобретения, RTS состоит из бицистронной информационной последовательности, экспрессируемой с промотора С убиквитина человека и кодирующей два слитых белка: Gal4-EcR и VP16-RXR. Gal4-EcR представляет собой слитые связывающий ДНК домен (аминокислоты 1-147) Gal4 дрожжей и DEF-домены рецептора экдизона насекомого Choristoneura fumiferana. VP16-RXR собой слитые домен активации транскрипции HSV-VP16 и EF-домены химерного RXR, полученного из последовательностей человека и саранчи. Данные последовательности Gal4-EcR и VP16-RXR разделены участком внутренней посадки рибосомы (IRES) из EMCV. Данные два слитых белка димеризуются, когда Gal4-EcR связывается с низкомолекулярным лекарственным средством (RG-115932) и активирует транскрипцию ML-12 и одного или нескольких других иммуномодуляторов с чувствительного к Gal4 промотора, который содержит шесть сайтов связывания Gal4 и синтетический минимальный промотор. Единицу транскрипции RTS, описанную выше, помещают по ходу транскрипции от единиц транскрипции hIL-12 и одного или нескольких других иммуномодуляторов. Всю эту кассету RTS-hIL12-иммуномодулятор включают в геном аденовируса 5 в сайт, где участок Е1 был удален. В аденовирусном остове также отсутствует ген Е3. Карта для аденовирусного вектора Ad-RTS-hIL-12 показана на ФИГ.8 в US 2009/0123441 Al.
[000433] Рекомбинантный аденовирусный вектор, применяемый в данном исследовании, содержит следующие типичные регуляторные элементы, вдобавок к последовательностям вирусного вектора: промотор С убиквитина человека, участок внутренней посадки рибосомы, полученный из EMCV, индуцируемый промотор, включающий 6 копий сайта связывания Gal4, 3 копии сайта связывания SP-1 и последовательность синтетического минимального промотора, сайты полиаденилирования SV40 и последовательность терминатора транскрипции, полученную из гена альфа-глобина человека. Должно быть очевидно, что можно использовать другие регуляторные элементы в качестве альтернативы.
[000434] Типичный рекомбинантный аденовирусный вектор Ad-RTS-hIL-12-иммуномодулятор(ы) получают следующим способом. Кодирующие последовательности для рецепторных слитых белков, VP16-RXR и Gal4-EcR, разделенные IRES (участком внутренней посадки рибосомы) EMCV, вставляли в аденовирусный челночный вектор под контролем промотора С убиквитина человека (конститутивного промотора). Затем, кодирующие последовательности для субъединиц р40 и р35 hIL-12, разделенных IRES, и одного или нескольких других иммуномодуляторов помещали под контроль синтетического индуцируемого промотора, включающего 6 копий сайта связывания Gal4, и вставляли против хода транскрипции от последовательностей промотора С убиквитина и рецептора. Челночный вектор включал последовательности аденовируса серотипа 5 с левого конца по единицу картирования 16 (е.к. 16), из которого последовательности Е1 были удалены и замещены на RTS, IL-12 и одну или более последовательностей других иммуномодуляторов (RTS-hIL-12). Челночный вектор, несущий RTS-hIL-12-иммуномодулятор(ы), тестировали, с помощью временной трансфекции им клеток НТ-1080, на зависимую от присутствия активирующего средства экспрессию IL-12 и другого иммуномодулятора(ов). Челночный вектор затем объединяли с аденовирусным остовом путем совместной трансфекции ими клеток НЕК 293 с получением рекомбинантного аденовируса Ad-RTS-hIL-12-иммуномодулятор(ы). В аденовирусном остове удалены последовательности с 0 по 9.2 е.к. с левого конца генома и ген Е3. Челночный вектор и аденовирусный остов содержат перекрывающуюся последовательность с е.к. 9.2 по е.к. 16, которая позволяет рекомбинацию между ними и получение рекомбинантного аденовирусного вектора. Так как в рекомбинантном аденовирусном векторе отсутствуют участки Е1 и Е3, вирус не может реплицироваться в нормальных клетках млекопитающих. Тем не менее, вирус может реплицироваться в клетках НЕК 293, которые содержат участок Е1 аденовируса-5 и, следовательно, обеспечивают функционирование Е1 в трансположении.
[000435] Типичный рекомбинантный аденовирусный вектор получали следующим способом. Линеаризованным челночным вектором, несущим элементы ДНК для индуцируемой экспрессии IL-12 человека и одного или нескольких Других иммуномодуляторов, и аденовирусным остовом совместно трансфицировали клетки НЕК293. Рекомбинация между перекрывающимися последовательностями на челночном векторе и вирусном остове приводила к получению рекомбинантного аденовируса и его упаковыванию в вирусные частицы в клетках НЕК293. Клетки НЕК293 выращивали в среде DMEM, содержащей фетальную бычью сыворотку.
[000436] Вирус, используемый для предложенного исследования, очищали путем центрифугирования в градиенте плотности CsCl. Рекомбинантный аденовирус подвергали двум раундам очистки бляшек и полученный в результате этого материал для посева использовали для получения основного вирусного банка (MVB) путем амплификации в клетках НЕК293 из полностью охарактеризованного основного клеточного банка. MVB подвергали комплексным выпускным испытаниям согласно cGMP/GLP (текущие правила надлежащей производственной практики/надлежащей лабораторной практики), включая репликационную компетентность аденовируса (RCA), стерильность, присутствие микоплазмы, случайных вирусов, ретровируса, вирусов человека HIV1/2, HTLV1/2, HAV, HBV, HCV, EBV, В 19, CMV, HHV-6, 7 и 8, бычьих и свиных" вирусов, полное секвенирование вектора и функциональное тестирование путем индуцируемой AD экспрессии IL-12 и одного или нескольких-других иммуномодуляторов в линиях клеток человека.
[000437] Вирус из MVB можно применять для получения очищенного вируса в лаборатории cGMP, который можно снова подвергнуть выпускным испытаниям, включая идентичность, RCA, стерильность, присутствие микоплазмы, случайных вирусов, соотношение вирусных частиц к инфекционным дозам, контаминацию с ДНК, эндотоксином и белками клетки-хозяина, и функциональное тестирование путем индуцируемой AD экспрессии IL-12 и одного или нескольких других иммуномодуляторов в линиях клеток человека.
Трансдукция аутологических дендритных клеток аденовирусом, включающим трансген hiL-12 и один или более других иммуномодуляторов и терапевтическую систему Rheoswitch® (RTS)
[000438] Дендритные клетки, полученные из людей, трансдуцировали ex vivo и инъецировали в опухоль. DC перед вирусной трансдукцией охарактеризовали по жизнеспособности, чистоте (как правило, >80% клеток проявляли DC-фенотип), стерильности, отсутствию микоплазмы и эндотоксина. После вирусной трансдукции, клетки промывали повторно, чтобы удалить любой непоглощенный вирус. Супернатант с последней промывки тестировали на содержание остаточного вируса с помощью ПЦР. Так как DC трансдуцировали ех vivo с помощью аденовирусного вектора (невстраивающийся вирус) и время жизни DC после внутриопухолевой инъекции и последующей миграции в дренирующие опухоль лимфатические узлы мало, не ожидали, что вирусная ДНК может включиться в какие-либо нецелевые клетки. Ожидали, что протокол, используемый для аденовирусной трансдукции DC, позволит получить 80-90% трансдукции, и считали его очень эффективным.
[000439] Сбор РВМС (мононуклеаров периферической крови) путем лейкафереза: Субъектов подвергали стандартному лейкаферезу от 90 до 120 минут на устройстве для афереза от UPCI Outpatient. Процедура лейкафереза включала удаление крови из вены одной руки; пропускание крови через центрифугу (разделитель клеток), в которой компоненты разделялись и один или более компонентов удалялись; и возвращение оставшихся компонентов в вену субъекта на той же или другой руке. Отбирали не более чем 15% общего объема крови субъекта единовременно, когда кровь пропускалась через устройство для разделения клеток. В разделителе клеток, кровь разделяли на плазму, тромбоциты, белые кровяные клетки и красные кровяные клетки. Белые кровяные клетки (WBC) удаляли, а все другие компоненты возвращали в кровообращение субъекта. Использовали каждую возможность применить два периферических венозных катетера для этой процедуры. Если это невозможно, может быть необходимо применение центрального венозного катетера. Лечащий врач должен сначала все разъяснить субъекту перед проведения ему лейкафереза, и должен подвергнуть его обычному скринингу на показатели жизнедеятельности (включая кровяное давление) перед этой процедурой.
[000440] Обработка: После сбора, пакет с лейкоцитами доставляли вручную на CPL и немедленно обрабатывали путем элютриационного центрифугирования в ELHTOA™. Это закрытая система, утвержденная для клинического применения. Получали фракцию моноцитов, и после получения и проверки жизнеспособности клеток их переносили в картридж Aastrom для культивирования в течение 6 дней в присутствии IL-4 и GM-CSF. Все процедуры обработки и промывки осуществляли в стерильных условиях.
[000441] Исходный посев: Моноциты, полученные из одного пакета с лейкоцитами, подсчитывали в присутствии красителя трипановый синий, чтобы определить количество жизнеспособных клеток. Моноциты оценивали по чистоте с помощью проточной цитометрии. Моноциты ресуспендировали при концентрации от 5 до 10×106 клеток/мл в бессывороточной и свободной от антибиотиков среде CellGenix, содержащей 1000 МЕ/мл IL-4 и 1000 МЕ/мл GM-CSF на SOP-CPL-0166, и помещали в картридж Aastrom. Для инокуляции кассеты необходим минимальный загрузочный объем 50 мл и минимальное количество клеток.
[000442] Культура: Картридж Aastrom помещали в термостат в Replicell System - полностью закрытое, cGMP-совместимое автоматизированное культуральное устройство для получения незрелых DC.
[000443] Сбор незрелых DC: В день 6, картридж Aastrom удаляли из термостата и собирали незрелые DC. Клетки получали с помощью центрифугирования при 1500 об/мин, промывали в среде CellGenix, подсчитывали в присутствии красителя трипановый синий и проверяли на морфологические и фенотипические свойства.
[000444] Жизнеспособность: Жизнеспособность определяли путем осуществления гемоцитометрического подсчета клеток в присутствии трипанового синего. Как правило, >95% собранных клеток были жизнеспособными, т.е., не включали краситель трипановый синий. Если жизнеспособность была менее 70%, незрелые DC отбрасывали.
[000445] Определение фенотипа: Клетки, полученные в культуре, подсчитывали путем исследования под микроскопом на гемоцитометре, и предварительную лейкоцитарную формулу (DC против лимфоцитов) получали, применяя краситель трипановый синий. Подтверждение полученной лейкоцитарной формулы получали с помощью проточной цитометрии, устанавливая дискриминационное окно на DC против лимфоцитов и используя свойства сильного прямого и бокового рассеяния незрелых DC в качестве критерия для их идентификации. Незрелые DC обычно содержат >80% клеток с морфологией дендритных клеток и имеют фенотип DC.
[000446] Анализ эффективности IL-12p70: Было установлено, что зрелые DC (mDC) способны продуцировать IL-12p70 самопроизвольно или при активации CD40L с добавлением или без сигналов врожденного иммунитета (например, LPS). Недавно учредили стандартизированный анализ продукции IL-12p70, который пригоден для малых образцов или больших партий вакцин DC, полученных при множестве условий. Современный анализ эффективности состоит из двух отдельных этапов, первый этап включает совместное инкубирование реактивных DC с клетками лимфомы J588, стабильно трансфицированными геном лиганда CD40 человека в качестве стимулятора. Второй этап включает тестирование супернатантов из данных совместных культур на уровни IL-12p70, секретируемого DC, стимулированными J558/CD40L +/- LPS, в системе Luminex. Данный анализ эффективности имеет коэффициент вариации для серии анализов 18.5% (n=30) и широкий динамический диапазон, что способствует оценке продуктов различных DC, характеризуемых сильно различающимися уровнями продукции IL-12p70. Стандартный диапазон для учрежденного анализа, в котором используют продукты DC, полученные из моноцитов 13 здоровых доноров, составлял 8-999 пг/мл, со средним значением 270 пг/мл.
Критерии продукции и высвобождения для дендритных клеток.
[000447] Каждую партию полученных in vitro дендритных клеток тестировали на присутствие микробных контаминантов (аэробных и анаэробных бактерий, грибков и микоплазмы), а также эндотоксина, и описывали фенотипически и функционально. Все дендритные клетки для инъецирования субъектам должны быть свежими и не должны подвергаться криоконсервированию.
[000448] Проверка гарантии качества DC: DC, полученные как описано выше, оценивали на стерильность, жизнеспособность, чистоту, эффективность и стабильность. Устанавливали критерии выпуска клеточного продукта и строго следовали им.
[000449] Жизнеспособность: Клетки, полученные в культуре, подсчитывали с помощью исследования под микроскопом на гемоцитометре, и получали лейкоцитарную формулу (DC против лимфоцитов), применяя краситель трипановый синий. Эта формула позволяла получать процент жизнеспособных клеток в тестируемой культуре. Для удовлетворения этого критерия выпуска требовалось более 70% жизнеспособных клеток после исключения трипановым синим и минимум 70% клеток, экспрессирующих HLA-DR и CD86 в качестве моноцитарных маркеров DC. В пробный анализ можно включить дополнительные маркеры, такие как CD83 и CCR7 для оценки статуса созревания DC и CD3 и CD 19 для оценки контаминации лимфоцитами.
[000450] Чистота: Анализ методом проточной цитометрии с использованием двухцветовой маркировки клеток, окрашенных FITC- и РЕ-конъюгированными MAT, использовали для определения того, что популяция DC, идентифицированная морфологически, экспрессирует поверхностные антигены, определенные для DC, и не экспрессирует антигены моноцитарных линий клеток и линий Т- и В-клеток. Для получения вакцины, полученные DC должны экспрессировать HLA-DR и CD86 и не должны экспрессировать CD3, CD19 или CD14. Чтобы считать их mDC, клетки должны экспрессировать CD83+ и CCR7+.
[000451] Эффективность: Чтобы определить меру эффективности DC, мы определили их способность продуцировать IL-12p70, как описано выше.
[000452] Стерильность: DC тестировали с помощью бактериальных (аэробных и анаэробных) и грибковых культур, применяя систему BD Bactec (Becton Dickinson Co., Спаркс, Мэриленд), в микробиологической лаборатории медицинского центра университета Питтсбурга. Окончательные результаты ведения микробных культур получали через 14 дней. Перед выпуском DC для применения в качестве вакцины, осуществляли окрашивание по Граму, которое должно быть отрицательным по присутствию микроорганизмов.
[000453] С помощью IMCPL проверяют на наличие микоплазмы, применяя систему быстрого определения микоплазмы в культуре ткани Gen-Probe Mycoplasma Tissue Culture Rapid Detection System (Gen-Probe, Inc. Сан-Диего, Калифорния), которая основана на способе гибридизации нуклеиновых кислот. Тестирование на наличие эндотоксина осуществляли, применяя анализ Limulus Amoebocyte Lysate Pyrogen Plus (Bio Whittaker, Inc., Уолкервиль, Мэриленд). Тестирование на наличие эндотоксина осуществляли на культуре клеток в момент сбора и перед выпуском конечного продукта. Приемлемый уровень эндотоксина составлял <5 ЕЭ/кг массы тела. Нетрансдуцированные и трансдуцированные дендритные клетки подвергали криоконсервированию для дальнейшего анализа.
[000454] Ожидали, что все трансдуцированные клетки будут экспрессировать трансген. Ожидали, что более чем 80% DC трансдуцированы. Продукт должен быть биологически активным, так как в трансгене сохраняется нативная кодирующая последовательность. Трансдуцированные вирусом DC, инъецированные в опухоль, имели незрелый фенотип DC и не экспрессировали IL-12 и один или более других иммуномодуляторов до тех пор, пока их не подвергли созреванию, и, следовательно, на этой стадии экспрессия IL-12 и одного или нескольких других иммуномодуляторов преимущественно осуществлялась с трансгена. Так как экспрессия трансгена, содержащего IL-12 и один или более других иммуномодуляторов, индуцировалась низкомолекулярным активирующим средством RG-115932 зависимым от дозы образом, можно было поддерживать уровень экспрессии трансгена в трансдуцированных DC на желательных уровнях. Небольшую часть трансдуцированных DC, полученных для введения людям, можно тестировать in vitro на зависимую от активирующего средства индукцию экспрессии IL-12 и одного или нескольких других иммуномодуляторов. Экспрессию IL-12 и одного или нескольких других иммуномодуляторов можно проанализировать с помощью ELISA с чувствительностью 4 нг/мл.
[000455] Ожидается, что индукция in vitro IL-12 и одного или нескольких других иммуномодуляторов в клетках, трансдуцированных вектором, применяемым в предложенном исследовании, позволяет получить приблизительно 500 нг IL-12 и одного или нескольких других иммуномодуляторов из 106 клеток за 24 часа, что определяли с помощью ELISA. В доклинических исследованиях с использованием модели меланомы на мышах, внутриопухолевая инъекция 106 или более трансдуцированных DC показала свою эффективность. Тем не менее, ожидается, что необходимая внутриопухолевая инъекция может проявить эффективность на уровнях ниже этого количества и, следовательно, можно осуществлять инъекции 5×107 трансдуцированных DC в качестве исходной точки, чтобы определить, требуются ли меньшие или большие количества.
[000456] Например, in vitro, линии клеток человека и мыши и первичные дендритные клетки, Трансдуцированные рекомбинантным аденовирусным вектором, несущим гены IL-12 и одного или нескольких других иммуномодуляторов, проявили индукцию экспрессии IL-12 в ответ на активирующее средство зависимым от дозы образом.
6.3. Лекарственная форма активирующего средства
[000457] Активирующее средство, применяемое в данной заявке, входит в состав любой из следующих лекарственных форм:
(1) 100% лабразол;
(2) Ароматизированный листерином лабразол (Latitude Pharmaceuticals Inc., США) содержащий (а) ментол, (b) тимол, (с) эвкалиптол, (d) аспартам, (е) сахаринат натрия, (f) лимонную кислоту, (g) ароматизатор мяты перечной, (h) ароматизатор сливок, (i) лабразол;
(3) Миглиол 812 и фосфолипон 90G (Latitude Pharmaceuticals Inc., США); или
(4) Миглиол 812, фосфолипон 90G и витамин Е (токоферола полиэтиленгликольсукцинат) (Latitude Pharmaceuticals Inc., США).
Доставка
[000458] Несмотря на то, что можно предположить множество концентраций и определенных протоколов, один пример лечения пациентов будет включать осуществление пациентам внутриопухолевой инъекции(й) трансдуцированных аутологических дендритных клеток (AdDC) в концентрации 5×107, суспендированных в стерильном солевом растворе, сконструированных таким образом, что они экспрессируют hIL-12 (интерлейкин-12 человека) и один или более других иммуномодуляторов под контролем RTS, в комбинации с пероральным введением активирующего средства (RG-115932).
[000459] Первоначальное лечение
[000460] День 1 приема стационарного пациента: В день 1, осуществляли базовое физическое обследование (включая показатели жизнедеятельности, вес и статус ECOG). Собирали мочу и отбирали кровь для базового химического анализа сыворотки, анализа мочи и гематологии (показателей безопасности). Приблизительно за 3 часа до внутриопухолевой инъекции сконструированных in vitro дендритных клеток, каждому субъекту вводили дозу активирующего средства (группа 1 - 0.01 мг/кг, 0.3 мг/кг, 1.0 мг/кг, и 3 мг/кг) незамедлительно после приема пищи. Отбирали кровь в определенные промежутки времени (перед введением дозы, через 0.5, 1, 1.5, 2, 4, 6, 8, 12, 16 и 24 часа после введения дозы AD) в день 1 для оценки фармакокинетики однократной дозы активирующего средства и его основных метаболитов. Каждый субъект получал однократную внутриопухолевую инъекцию трансдуцированных аденовирусом аутологических дендритных клеток в концентрации 5×107 клеток, сконструированных таким образом, что они экспрессируют hIL-12 и один или более других иммуномодуляторов под контролем RTS. За субъектами тщательно наблюдали на предмет возникновения реакций в месте инъекции и/или реакций гиперчувствительности. В дни с 2 по 14 приема стационарного пациента: В дни с 2 по 14, каждому субъекту вводили дозу активирующего средства незамедлительно после приема пищи. Показатели жизнедеятельности и нежелательные явления отслеживали ежедневно в дни с 2 по 14. В день 4±24 часа, биопсии опухоли и/или дренирующих опухоль лимфатических узлов осуществляли у приблизительно 50% субъектов для измерения уровня hIL-12 и клеточного иммунного ответа. В день 8 измеряли вес. В день 8±24 часа, биопсии опухоли и/или дренирующих опухоль лимфатических узлов осуществляли у субъектов, которым не осуществляли биопсию в день 4, для измерения уровня hIL-12 и одного или нескольких других иммуномодуляторов и клеточного иммунного ответа. Кровь отбирали в день 4±24 часа и в день 8±24 часа для анализа на присутствие антител и клеточных иммунных ответов против аденовируса и/или компонентов RTS. Также получали профиль цитокинов в сыворотке, чтобы определить, влияет ли на экспрессию других цитокинов лечение трансгеном hIL-12 и одного или нескольких других иммуномодуляторов. В день 8 собирали мочу и отбирали кровь для базового химического анализа сыворотки, анализа мочи и гематологии (показателей безопасности). В день 8 отбирали кровь в определенные промежутки времени (перед введением дозы, через 0.5, 1, 2, 4, 6, 8, 12, 16 и 24 часа после введения дозы AD) для оценки стационарной фармакокинетики/ADME активирующего средства и его основных метаболитов.
[000461] День 14 приема стационарного пациента: В день 14 каждому субъекту вводили дозу активирующего средства незамедлительно после приема пищи. Каждому субъекту проводили физическое обследование (включая показатели жизнедеятельности, рост, вес и статус ECOG). Собирали мочу и отбирали кровь для химического анализа сыворотки, анализа мочи и гематологии (показателей безопасности). Кровь отбирали в день 14±24 часа для анализа на наличие антител и клеточного иммунного ответа против аденовируса и/или компонентов RTS. Также получали профиль цитокинов в сыворотке, чтобы определить, изменилась ли экспрессия других цитокинов.
[000462] Кровь собирали у субъектов в определенные приемы стационарных пациентов и амбулаторных пациентов, чтобы измерить наличие антител и клеточного иммунного ответа на аденовирус и компоненты RTS. Кровь получали для измерения базового профиля цитокинов в сыворотке. Для обнаружения гуморального ответа на аденовирусный вектор применяли анализ блокирования инфицирующей способности AdVeGFP (Gambotto, Robins и др. 2004). Гуморальный ответ на компоненты RTS оценивали с помощью анализа вестерн-блот и/или ELISA, используя сыворотку из пациента и белки RTS, продуцированные вектором экспрессии. Вдобавок, осуществляли мультиплексное тестирование цитокинов в сыворотке с помощью Luminex для IL-12, IFN-гамма, IP-10 и других ТЫ/ТЫ цитокинов, таких как IL-2, TNF-альфа, IL-4, IL-5 и IL-10. Для данных анализов на антитела и цитокины требуется приблизительно 10 мл крови.
[000463] Возможный гуморальный и клеточный иммунный ответ на аденовирус и/или компоненты RTS: Кровь собирали у субъектов в определенные приемы стационарных пациентов и амбулаторных пациентов, чтобы оценить возможный гуморальный и клеточный иммунный ответ на аденовирус и компоненты RTS, и на опухолевые антигены. Для обнаружения гуморального ответа на аденовирусный вектор применяли анализ блокирования инфицирующей способности AdVeGFP (Nwanegbo, и др. 2004). Гуморальный ответ на компоненты RTS оценивали с помощью анализа вестерн-блот и/или ELISA, используя сыворотку из субъектов и белки RTS, продуцированные вектором экспрессии. Вдобавок, осуществляли мультиплексное тестирование цитокинов в сыворотке с помощью Luminex для IL-12, IFN-гамма, IP-10 и других Th1/Th2 цитокинов, таких как IL-2, TNF-альфа, IL-4, IL-5 и IL-10. Для данных анализов на антитела и цитокины требуется приблизительно 10 мл крови.
[000464] Для анализов клеточного иммунного ответа требовалось приблизительно 50-60 мл крови, из которой отделяли CD4 и CD8 субпопуляции Т-клеток. Отделенные Т-клетки смешивали с аутологическими DC, трансдуцированными пустым вектором AdV, векторами AdV-RTS или AdV-RTS-hIL12-иммуномодулятор(ы), и анализировали с помощью ELISPOT на продукцию IFN-гамма Т-клетками, активированными антигенами, полученными из AdV и RTS, при наличии таковых. Подобные анализы осуществляли, используя опухолевые клетки сами по себе и/или DC, экспрессирующие общие меланомные антигены, для оценки раннего иммунного ответа на опухоль. При необходимости также можно осуществить дополнительные анализы.
[000465] ТЕСТ НА ОПРЕДЕЛЕНИЕ БЕРЕМЕННОСТИ: Женщинам детородного периода проводили тест на определение беременности по моче на первом скрининге и перед первым приемом стационарного пациента для повторной фазы лечения. Тестирование осуществляли по меньшей мере за 72, 48, 24 или 12 часов до введения активирующего средства во время как первоначального лечения, так и всех повторных периодов лечения. Если тест на определение беременности по моче был положительным, то его подтверждали с помощью теста на определение беременности по сыворотке. Если беременность подтверждали, субъекту не позволяли начинать испытание или продолжать повторную фазу лечения. Тест на определение беременности можно осуществлять столько раз, сколько это необходимо.
[000466] ОПРОС О СОПУТСТВУЮЩЕМ ПРИЕМЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ: На этапе скрининга и перед первым приемом стационарного пациента для повторной фазы лечения, каждого субъекта опрашивали, чтобы получить перечень принимаемых одновременно лекарственных средств, для определения любой возможной взаимосвязи с нежелательными явлениями, которые возникают во время испытания и периода последующего наблюдения.
[000467] КРИТЕРИИ ДОПУСКА К ПОВТОРНОМУ ЛЕЧЕНИЮ: Если субъект переносил предшествующее введение AdDC без возникновения нежелательных реакций, которые ограничивали прием лекарственного средства, и проявил отсутствие прогрессирования заболевания или уменьшение симптомов к моменту возможного повторного лечения, считали, что он подходит для повторного лечения. Если по мнению научного руководителя и лечащего врача была возможна клиническая польза от дополнительной внутриопухолевой инъекции(й) AdDC в комбинации с активирующим средством (максимально переносимая доза из группы 1) в течение 14 следующих дней, субъекту предлагали повторное лечение, при условии, что удовлетворялись следующие критерии:
1. Отсутствовала ограничивающая токсичность,
2. Заболевание субъекта было стабильным или проявило клинические или субъективные признаки улучшения, и
3. Отсутствовали признаки гуморального или клеточного иммунного ответа на аденовирусные компоненты терапевтической системы RheoSwitch®.
[000468] ОЦЕНКА ФУНКЦИОНИРОВАНИЯ ТРАНСГЕНА И ИММУНОЛОГИЧЕСКИХ ЭФФЕКТОВ: Пункционные или хирургические биопсии опухоли и дренирующих опухоль лимфатических узлов осуществляли во время скрининга (с дня -12 по день -7), в день 4, день 8 и день 14 испытания и в 1 месяц последующего наблюдения (см. Таблицы 3-5) для оценки in vivo экспрессии трансгена hIL-12 и одного или нескольких других иммуномодуляторов, и клеточного иммунного ответа. Тонкоигольные пункционно-аспирационные биопсии опухоли и дренирующих опухоль лимфатических узлов осуществляли с дня -12 по день -7 и в день 14 повторного лечения для оценки in vivo экспрессии трансгена hIL-12 и одного или нескольких других иммуномодуляторов, и клеточного иммунного ответа. Биоптаты оценивали с помощью стандартной световой микроскопии и иммуногистохимии для оценки Т-клеточной инфильтрации опухоли и дренирующих опухоль лимфатических узлов. Биопсийные срезы изучал патоморфолог, не знающий исходные; данные исследуемого субъекта. Чтобы отличить эндогенную и индуцированную экспрессию IL-12 дендритными клетками в опухоли и дренирующих опухоль лимфатических узлах, применяли ОТ-ПЦР на РНК со специально разработанными праймерами. Отбирали кровь для получения профиля цитокинов в сыворотке при скрининге, в день 4, день 8 и день 14 испытания, в 1 месяц последующего наблюдения и в дни с -12 по -7, в день 8 и день 14 повторного лечения (см. Таблицы 3-5). Получали профиль цитокинов в сыворотке, чтобы определить, влияло ли на экспрессию других цитокинов лечение трансгеном hIL-12. Осуществляли мультиплексное тестирование цитокинов в сыворотке с помощью Luminex для IL- 12, IFN-гамма, IP-10 и других Th1/Th2 цитокинов, таких как IL-2, TNFa, IL-4, IL-5 и IL-10. Для данных анализов на антитела и цитокины требовалось приблизительно 10 мл крови.
[000469] ОДНОДОЗОВАЯ И СТАЦИОНАРНАЯ ФАРМАКОКИНЕТИКА АКТИВИРУЮЩЕГО СРЕДСТВА: Кровь отбирали, в определенные промежутки времени (перед введением дозы, через 0.5, 1, 1.5, 2, 4, 6, 8, 12, 16 и 24 часа после утреннего введения дозы) в день 1 испытания для оценки однодозовой фармакокинетики и в день 8 испытания для измерения стационарной фармакокинетики/ADME активирующего средства и его основных метаболитов. Плазму оценивали с помощью ВЭЖХ, чтобы получить следующие критические точки стационарной фармакокинетики активирующего средства и основных метаболитов: Cmax (максимальная наблюдаемая концентрация в плазме), Tmax (время достижения максимальной наблюдаемой концентрации в плазме), Ctrough (минимальная наблюдаемая концентрация в плазме, вычисленная как средняя концентрация в промежутке времени от 0 и 24 часов), C24h (концентрация в плазме через 24 часа), AUC24h (площадь под кривой зависимости концентрации в плазме от времени в промежутке времени от 0 до 24 часов), Ке (видимая скорость выведения) и Т112 (видимое время полужизни).
[000470] Должно быть очевидно, что описанные выше варианты реализации и пояснительные примеры не предполагаются ограничивающими в каком-либо отношении объем настоящего изобретения, и что подразумевается, что в объем формулы изобретения, приведенной в данной заявке, входят все варианты реализации и пояснительные примеры, независимо от того, представлены они явным образом в данной заявке или нет.
Литература
Abdalla, 2007.
Abdi К, Singh N, Matzinger P (2006). T-cell control of IL-12p75 production. Scand J Immunol 64: 83-92.
Adorini L (1999). Interleukin-12, a key cytokine in Th1-mediated autoimmune diseases. Cell Mol Life Sci 55: 1610-25.
Adorini L (2001). Interleukin 12 and autoimmune diabetes. Nat Genet 27: 131-2.
Adorini L, Gregori S, Harrison LC (2002). Understanding autoimmune diabetes: insights from mouse models. Trends Mol Med 8: 31-8.
Adorini L, Gregori S, Magram J, Trembleau S (1996). The role of IL-12 in the pathogenesis of Th1 cell-mediated autoimmune diseases. Ann N Y Acad Sci 795: 208-15.
Akhtar N, Padilla ML, Dickerson EB, Steinberg H, Breen M, Auerbach R et al (2004). Interleukin-12 inhibits tumor growth in a novel angiogenesis canine hemangiosarcoma xenograft model. Neoplasia 6: 106-16.
Akiyama Y, Watanabe M, Maruyama K, Ruscetti FW, Wiltrout RH, Yamaguchi К (2000). Enhancement of antitumor immunity against В16 melanoma tumor using genetically modified dendritic cells to produce cytokines. Gene Ther 7: 2113-21.
Al-Mohanna F. Saleh S, Parhar RS, Collison К (2002). IL-12-dependent nuclear factor-kappaB activation leads to de novo synthesis and release of IL-8 and TNF-alpha in human neutrophils. J Leukoc Biol 72: 995-1002.
Aliberti JC, Cardoso MA, Martins GA, Gazzinelli RT, Vieira LQ, Silva JS (1996). Interleukin-12 mediates resistance to Trypanosoma cruzi in mice and is produced by murine macrophages in response to live trypomastigotes. Infect Immun 64: 1961-7.
Allavena P, Paganin C, Zhou D, Bianchi G, Sozzani S, Mantovani A (1994). Interleukin-12 is chemotactic for natural killer cells and stimulates their interaction with vascular endothelium. Blood 84: 2261-8.
Alii RS, Khar A (2004). Interleukin-12 secreted by mature dendritic cells mediates activation of NK cell function. FEBS Lett 559: 71-6.
Alzona M, Jack HM, Simms PE, Ellis TM (1996). Interleukin-12 activates interferon-gamma production by targeted activation of CD30+ Т cells. Ann N Y Acad Sci 795: 127-36.
Amemiya К, Meyers JL, Trevino SR, Chanh TC, Norris SL, Waag DM (2006). Interleukin-12 induces a Th1-like response to Burkholderia mallei and limited protection in BALB/c mice. Vaccine 24: 1413-20.
Araujo MI, Bliss SK, Suzuki Y, Alcaraz A, Denkers EY, Pearce EJ (2001). Interleukin-12 promotes pathologic liver changes and death in mice coinfected with Schistosoma mansoni and Toxoplasma gondii. Infect Immun 69: 1454-62.
Arulanandam BP, Van Cleave VH, Metzger DW (1999). IL-12 is a potent neonatal vaccine adjuvant. Eur J Immunol 29: 256-64.
Athie MV, Flotow H, Hilyard KL, Cantrell DA (2000). IL-12 selectively regulates STAT4 via phosphatidylinositol 3-kinase and Ras-independent signal transduction pathways. Eur J Immunol 30: 1425-34.
Athie-Morales V, Smits HH, Cantrell DA, Hilkens CM (2004). Sustained IL-12 signaling is required for Th1 development. J Immunol 172: 61-9.
Atkins MB, Robertson MJ, Gordon M, Lotze MT, DeCoste M, DuBois JS et al (1997). Phase I evaluation of intravenous recombinant human interleukin 12 in patients with advanced malignancies, Clin Cancer Res 3: 409-17.
Berard F, Blanco P, Davoust J, Neidhart-Berard EM, Nouri-Shirazi M, Taquet N et al (2000). Cross-priming of naive CD8 Т cells against melanoma antigens using dendritic cells loaded with killed allogeneic melanoma cells. J Exp Med 192: 1535-44.
Bertagnolli MM, Lin BY, Young D, Herrmann SH (1992). IL-12 augments antigen-dependent proliferation of activated Т lymphocytes. J Immunol 149: 3778-83.
Bhardwaj N, Seder RA, Reddy A, Feldman MV (1996). IL-12 in conjunction with dendritic cells enhances antiviral CD8+ CTL responses in vitro. J Clin Invest 98: 715-22.
Biedermann Т, Lametschwandtner G, Tangemann K, Kund J, Hinteregger S, Carballido-Perrig N et al (2006). IL-12 instructs skin homing of human Th2 cells. J Immunol 177: 3763-70.
Brunda MJ, Gately MK. (1994). Antitumor activity of interleukin-12. Clin Immunol Immunopathol 71: 253-5.
Buchanan JM, Vogel LA, Van Cleave VH, Metzger DW (1995). Interleukin 12 alters the isotype-restricted antibody response of mice to hen eggwhite lysozyme. Int Immunol 7: 1519-28.
Chang, 2007.
Coughlin, 1998.
Dietrich 2002.
Emtage et al., "Adenoviral Vectors Expressing Lymphotactin and Interleukin 2 or Lymphotactin and Interleukin 12 Synergize to Facilitate Tumor Regression in Murine Breast Cancer Models," Hum. Gene Ther. 10: 697 (1999).
Faure F, Even J, Kourilsky P (1998). Tumor-specific immune response: current in vitro analyses may not reflect the in vivo immune status. Crit Rev Immunol 18: 77-86.
Gao et al., "Cotransduction of CCL27 gene can improve the efficacy and safety of IL-12 gene therapy for cancer," Gene Ther. 14: 491-502 (2007)
Hansson, 2007.
Heinzerling L, Burg G, Dummer R, Maier T, Oberholzer PA, Schultz J et al (2005). Intratumoral injection of DNA encoding human interieukin 12 into patients with metastatic melanoma: clinical efficacy. Hum Gene Ther 16: 35-48.
Hill 2002.
Itoh T, Storkus WJ, Gorelik E, Lotze MT (1994). Partial purification of murine tumor-associated peptide epitopes common to histologically distinct tumors, melanoma and sarcoma, that are presented by H-2Kb molecules and recognized by CD8+ tumor-infiltrating lymphocytes. J Immunol 153: 1202-15.
Jean, 2004.
Kang WK, Park C, Yoon HL, Kim WS, Yoon SS, Lee MH et al (2001). Interleukin 12 gene therapy of cancer by peritumoral injection of transduced autologous fibroblasts: outcome of a phase I study. Hum Gene Ther 12: 671-84.
Koka, 2004.
Koyama, 1997
Lasek, 2000.
Mehrotra, 1995.
Narvaiza et al., "Intratumoral coinjection of two adenoviruses, one encoding the chemokine IFN-gamma-inducible protein-10 and another encoding IL-12, results in marked antitumoral synergy," J. Immunol. 164: 3112 (2000).
Nair, 2006.
Narvaiza et al., Intratumoral Coinjection of Two Adenoviruses, One Encoding the Chemokine IFN-γ-Inducible Protein-10 and Another Encoding IL-12, Results in Marked Antitumoral Synergy," J. Immunol. 164: 3112-3122 (2000).
Palmer et al., "Combined CXC chemokine and interleukin-12 gene transfer enhances antitumor activity," Gene Ther. 5: 282-290 (2001).
Rasmussen, 2003.
Romani L, Puccetti P, Bistoni F (1997). Interleukin-12 in infectious diseases, Clin Microbiol Rev 10: 611-36.
Rothe H, Burkart V, Faust A, Kolb H (1996). Interleukin-12 gene expression mediates the accelerating effect of cyclophosphamide in autoimmune disease. Ann N Y Acad Sci 795: 397-9.
Sabel, 2003, 2004, 2007.
Sangro В, Mazzolini G, Ruiz J, Herraiz M, Quiroga J, Herrero I et al (2004). Phase I trial of intratumoral injection of an adenovirus encoding interleukin-12 for advanced digestive tumors. J Clin Oncol 22: 1389-97.
Sangro B, Melero I, Qian C, Prieto J (2005). Gene therapy of cancer based on interieukin 12. Curr Gene Ther 5: 573-81.
Satoh Y, Esche C, Gambotto A, Shurin GV, Yurkovetsky ZR, Robbins PD et al (2002). Local administration of IL-12-transfected dendritic cells induces antitumor immune responses to colon adenocarcinoma in the liver in mice. J Exp Ther Oncol 2: 337-49.
Satoskar AR, Rodig S, Telford SR, 3rd, Satoskar AA, Ghosh SK, von Lichtenberg F et al (2000). IL-12 gene-deficient C57BL/6 mice are susceptible to Leishmania donovani but have diminished hepatic immunopathology. Eur J Immunol 30: 834-9.
Schopf LR, Bliss JL, Lavigne LM, Chung CL, Wolf SF, Sypek JP (1999). Interleukin-12 is capable of generating an antigen-specific Th1-type response in the presence of an ongoing infection-driven Th2-type response. Infect Immun 67: 2166-71.
Subleski, 2006.
Svane IM, Boesen M, Engel AM (1999). The role of cytotoxic T-lymphocytes in the prevention and immune surveillance of tumors-lessons from normal and immunodeficient mice. Med Oncol 16: 223-38.
Taniguchi, 1998.
Tatsumi T, Huang J, Gooding WE, Gambotto A, Robbins PD, Vujanovic NL et al (2003). Intratumoral delivery of dendritic cells engineered to secrete both interleukin (IL)-12 and IL-18 effectively treats local and distant disease in association with broadly reactive Tc1-type immunity. Cancer Res 63: 6378-86.
Thomas GR, Chen Z, Enamorado I, Bancroft C, Van Waes С (2000). IL-12- and IL-2-induced tumor regression in a new murine model of oral squamous-cell carcinoma is promoted by expression of the CD80 co-stimulatory molecule and interferon-gamma. Int J Cancer 86: 368-74.
Trinchieri G (2003). Interleukin-12 and the regulation of innate resistance and adaptive immunity. Nat Rev Immunol 3: 133-46.
Triozzi PL, Alien КО, Carlisle RR, Craig M, LoBuglio AF, Conry RM (2005). Phase I study of the intratumoral administration of recombinant canarypox viruses expressing B7.1 and interleukin 12 in patients with metastatic melanoma, Clin Cancer Res 11: 4168-75.
Tsung К, Meko JB, Peplinski GR, Tsung YL, Norton JA (1997). IL-12 induces T helper 1-directed antitumor response. J Immunol 158: 3359-65.
Vujanovic, 2006.
Wang, 2001.
Wigginton 2002, 2001, 1996
Wolf SF, Sieburth D, Sypek J (1994). Interleukin 12: a key modulator of immune function. Stem Cells 12: 154-68.
Yamanaka R, Zullo SA, Ramsey J, Yajima N, Tsuchiya N, Tanaka R et al (2002). Marked enhancement of antitumor immune responses in mouse brain tumor models by genetically modified dendritic cells producing Semliki Forest virus-mediated interleukin-12. J Neurosurg 97: 611-8.
Yuminamochi E, Koike T, Takeda K, Horiuchi I, Okumura К (2007). Interleukin-12- and interferon-gamma-mediated natural killer cell activation by Agaricus blazei Murill. Immunology.
McDermott, D.F. and Atkins, M.B. (2008) Immunotherapy of metastatic renal cell carcinoma.
Cancer J. 14, 320-324.
Bemtsen, A., Trepiakas, R., Wenandy, L., Geertsen, P.F., thor Straten, P., Andersen, M.H., Pedersen, A.E., Claesson, M.H., Lorentzen, Т., Johansen, J.S. and Svane, I.M. (2008) Therapeutic dendritic cell vaccination of patients with metastatic renal cell carcinoma: a clinical phase 1/2 trial. J. Immunother. 31, 771-780.
Tarhini, A.A., Kirkwood, J.M., Gooding, W.E., Moschos, S. and Agarwala, S.S. (2008) A phase 2 trial of sequential temozolomide chemotherapy followed by high-dose interleukin 2 immunotherapy for metastatic melanoma. Cancer. 113, 1632-1640.
Heemskerk, В., Liu, К., Dudley, M.E., Johnson, L.A., Kaiser, A., Downey, S., Zheng, Z., Shelton, Т.Е., Matsuda, K., Robbins, P.P., Morgan, R.A., Rosenberg, S.A. (2008) Adoptive cell therapy for patients with melanoma, using tumor-infiltrating lymphocytes genetically engineered to secrete interieukin-2. Hum Gene Ther. 19, 496-510.
Horton, H.M., Lalor, P.A. and Rolland, A.P. (2008) IL-2 plasmid electroporation: from preclinical studies to phase I clinical trial. Methods Mol Biol. 423, 361-372.
Shiratori, I., Suzuki, Y., Oshiumi, H., Begum, N.A., Ebihara, Т., Matsumoto, M., Hazeki, K., Kodama, K., Kashiwazaki, Y. and Seya, T. (2007) Recombinant interleukin-12 and interleukin-18 antitumor therapy in a guinea-pig hepatoma cell implant model.
Cancer Sci. 98, 1936-1942.
Lian H, Jin N, Li X, Mi Z, Zhang J, Sun L, Li X, Zheng H, Li P. (2007) Induction of an effective anti-tumor immune response and tumor regression by combined administration of IL-18 and Apoptin. Cancer Immunol Immunother. 56, 181-192.
Iinuma, H., Okinaga, K., Fukushima, R., Inaba, Т., Iwasaki, K., Okinaga, A., Takahashi, I. and Kaneko, M. (2006) Superior protective and therapeutic effects of IL-12 and IL-18 gene-transduced dendritic neuroblastoma fusion cells on liver metastasis of murine neuroblastoma. J. Immunol. 176, 3461-3469.
Basak, G.W., Zapala, L., Wysocki, PJ., Mackiewicz, A., Jakóbisiak, M. and Lasek, W. (2008) Interleukin 15 augments antitumor activity of cytokine gene-modified melanoma cell vaccines in a murine model. Oncol Rep. 19, 1173-1179.
Lasek, W., Basak, G., Switaj, Т., Jakubowska, A.B., Wysocki, P.J., Mackiewicz, A., Drela, N., Jalili, A., Kamiński, R., Kozar, K. and Jakóbisiak, M. (2004) Complete tumour regressions induced by vaccination with IL-12 gene-transduced tumour cells in combination with IL-15 in a melanoma model in mice. Cancer Immunol Immunother. 53, 363-372.
Xia, Y., Dai, J., Lu, P., Huang, Y., Zhu, Y. and Zhang, X. (2008) Distinct effect of CD40 and TNF-signaling on the chemokine/chemokine receptor expression and function of the human monocyte-derived dendritic cells. Cell Mol Immunol. 5, 121-131.
Sharma, S., Batra, R.K., Yang, S.C., Hillinger, S., Zhu, L., Atianzar, K., Strieter, R.M., Riedl, K., Huang, M. and Dubinett, S.M. (2003) Interleukin-7 gene-modified dendritic cells reduce pulmonary tumor burden in spontaneous murine bronchoalveolar cell carcinoma. Hum Gene Ther. 14, 1511-1524.
Tirapu, I., Rodriguez-Calvillo, M., Qian, C., Duarte, M., Smerdou, C., Palencia, В., Mazzolini, G., Prieto, J. and Melero, I. (2002) Cytokine gene transfer into dendritic cells for cancer treatment. Curr. Gene Ther. 2, 79-89.
Small, E.J., Sacks, N., Nemunaitis, J., Urba, W.J., Dula, E., Centeno, A.S., Nelson, W.G., Ando, D., Howard, C., Borellini, F., Nguyen, M., Hege, K. and Simons, J.W. (2007) Granulocyte macrophage colony-stimulating factor-secreting allogeneic cellular immunotherapy for hormone-refractory prostate cancer. Clin Cancer Res. 13, 3883-3891.
Huang, H. and Xiang, J. (2004) Synergistic effect of lymphotactin and interferon gamma-inducible protein-10 transgene expression in T-cell localization and adoptive T-cell therapy of tumors. Int. J. Cancer. 109, 817-825.
Реферат
Настоящее изобретение относится к области биотехнологии и может быть использовано для рекомбинантной экспрессии иммуномодуляторных белков. Конструируют вектор, содержащий полинуклеотид, кодирующий генный переключатель, при этом указанный полинуклеотид содержит (1) по меньшей мере одну последовательность фактора транскрипции, которая функционально связана с промотором, при этом указанная по меньшей мере одна последовательность фактора транскрипции кодирует лиганд-зависимый фактор транскрипции, и (2) полинуклеотид, кодирующий полипептид IL-12 и один или более иммуномодуляторных полипептидов, выбранных из IL-2, IL-7, IL-15, IL-18, IL-21, GM-CSF, CCL3 (MIP-1a), CCL5 (RANTES), CCL7 (MCP3), XCL1 (лимфотактин), CCL19 (MIP-3b), CXCL9 (MIG), CXCL10 (IP-10), CXCL12 (SDF-1), CCL21 (6Ckine) или TNF-альфа. Изобретение позволяет использовать вектор для управляемой экспрессии иммуномодуляторных белков. 4 н. и 8 з.п. ф-лы, 9 ил., 4 табл., 2 пр.
Формула
Документы, цитированные в отчёте о поиске
Фармацевтическая композиция для индукции иммуннойреакции у человека

Комментарии