Опосредованный аденоассоциированным вирусом перенос генов в центральную нервную систему - RU2692251C2
Код документа: RU2692251C2
Чертежи














Описание
Ссылка на родственные заявки
По настоящей заявке испрашивается приоритет согласно дате подачи предварительной заявки на патент США с серийным номером 61/823757, поданной 15 мая 2013 г., раскрытие которой включено в настоящий документ посредством ссылки.
Заявление о правах правительства
Настоящее изобретение было выполнено при правительственной поддержке согласно HD 032652 и DK 094538, предоставленными Национальными институтами здравоохранения. Правительство обладает определенными правами на настоящее изобретение.
Предшествующий уровень техники настоящего изобретения
Мукополисахаридозы (MPS) представляют собой группу из 11 заболеваний накопления, вызванных нарушениями в катаболизме гликозаминогликана (ГАГ), приводя к его накоплению в лизосомах (Muenzer, 2004; Munoz-Rojas et al., 2008). Проявления различной степени тяжести включают в себя органомегалии, скелетные дисплазии, сердечную и легочную обструкцию и неврологическую деградацию. Для MPS I, дефицита идуронидазы (IDUA), тяжесть варьирует от легкой (синдром Шейе) до умеренной (Гурлера-Шейе) и до тяжелой (синдром Гурлера), причем последняя приводит к неврологической деградации и смерти к 15 годам (Muenzer, 2004; Munoz-Rojas et al., 2008). Способы лечения MPS были по большей части паллиативными. Тем не менее, существует несколько заболеваний MPS, включая в себя синдром Гурлера, для которых была эффективна трансплантация аллогенных гемопоэтических стволовых клеток (HSCT) (Krivit, 2004; Orchard et al., 2007; Peters et al., 2003). Кроме того, для все большего и большего числа заболеваний MPS становится доступной заместительная ферментная терапия (ERT) (Brady, 2006). В общем, HSCT и ERT приводят к очищению от накапливаемых веществ и усовершенствованию периферийных состояний, хотя некоторые проблемы после лечения сохраняются (скелетные, сердечные, помутнение роговицы). Основная проблема этих клеточных и ферментных способов лечения заключается в эффективности в направленном воздействии на неврологические проявления, поскольку периферически введенный фермент не проникает через гематоэнцефалический барьер, и было обнаружено, что HSCT полезна для некоторых, но не всех MPS.
MPS I был одним из самых широко изученных заболеваний MPS для развития клеточных и молекулярных способов лечения. Эффективность аллогенной HSCT, скорее всего, представляет собой результат метаболической перекрестной коррекции, в результате чего отсутствующий фермент высвобождается из полученных от донора клеток и впоследствии захватывается клетками-хозяевами и переносится в лизосомы, где фермент способствует лизосомальному метаболизму (Fratantoni et al., 1968). Впоследствии наблюдается очистка от накопленных веществ ГАГ в периферических органах, таких как печень и селезенка, наблюдается освобождение от сердечной обструкции и улучшение помутнения роговицы (Orchard et al., 2007). Особым значением характеризуется влияние трансплантации аллогенных стволовых клеток на возникновение неврологических проявлений при заболеваниях MPS. В связи с этим, для нескольких заболеваний MPS существуют свидетельства, что индивидуумы с введенными аллогенными стволовыми клетками характеризуются улучшенными результатами в сравнении с пациентами без трансплантации (Bjoraker et al., 2006; Krivit, 2004; Orchard et al., 2007; Peters et al., 2003). Основная гипотеза, объясняющая неврологическое преимущество аллогенной трансплантации гемопоэтических стволовых клеток, заключается в проникновении полученных от доноров гемопоэтических клеток (скорее всего микроглии) (Hess et al., 2004; Unger et al., 1993) в центральную нервную систему, где отсутствующий фермент экспрессируется введенными клетками, из которых указанный фермент проникает в ткани ЦНС и участвует в освобождении от накопленных веществ. Содержание фермента, полученного тканями ЦНС, таким образом, ограничивается этим количеством, экспрессированным и высвобожденным из полученных от донора клеток, введенных в головной мозг. В то время как такие введения приносят большую пользу для MPS I, тем не менее реципиенты продолжают демонстрировать IQ ниже нормального и нарушенную нейрокогнитивную способность (Ziegler and Shapiro, 2007).
Явление метаболической перекрестной коррекции также объясняет эффективность ERT для нескольких лизосомных болезней накопления (Brady, 2006), особенно MPS I. Однако, из-за потребности в проникновении через гематоэнцефалический барьер (ГЭБ) фермента, отсутствующего при конкретной лизосомной болезни накопления (ЛБН) для того, чтобы эффективно достичь ЦНС, эффективность ферментной терапии для неврологических проявлений лизосомной болезни накопления (ЛБН) не наблюдалась (Brady, 2006). Ферменты почти всегда слишком большие и, как правило, слишком заряженные, чтобы эффективно проникать через ГЭБ. Это вызвало появление исследований в области инвазивного интратекального введения фермента (Dickson et al., 2007), эффективность которого была продемонстрирована на собачьей модели MPS I (Kakkis et al., 2004) и клинические испытания на человеке которого начинаются для MPS I (Pastores, 2008; Munoz-Rojas et al., 2008). Основные недостатки ферментной терапии заключаются в ее большой стоимости (>$ 200000 в год) и потребности в повторных инфузиях рекомбинантного белка. Текущие клинические испытания интратекального введения IDUA разрабатываются для введения фермента только один раз каждые три месяца, поэтому эффективность этого режима дозирования остается неясной.
Краткое раскрытие настоящего изобретения
Описаны способы предотвращения, ингибирования и/или лечения одного или нескольких симптомов, связанных с заболеванием центральной нервной системы (ЦНС) у нуждающегося в этом млекопитающего. Способы включают доставку в ЦНС нуждающемуся в лечении млекопитающему композиции, содержащей эффективное количество рекомбинантного вектора на основе аденоассоциированного вируса (rAAV), содержащего открытую рамку считывания, кодирующую генный продукт, например, терапевтический генный продукт. Продукты генов-мишеней, которые могут кодироваться с помощью вектора rAAV, включают в себя без ограничения альфа-L-идуронидазу, идуронат-2-сульфатазу, гепарансульфат сульфатазу, N-ацетил-альфа-D-глюкозаминидазу, бета-гексозаминидазу, альфа-галактозидазу, бета-галактозидазу, бета-глюкуронидазу или глюкоцереброзидазу. Заболевания, которые можно предотвращать, ингибировать или лечить с использование раскрытых в настоящем документе способов, включают в себя без ограничения нарушение мукополисахаридоз типа I, нарушение мукополисахаридоз типа II или нарушение мукополисахаридоз типа VII. Вектор AAV можно вводить в различных формах, чтобы убедиться, что он поступает в ЦНС/головной мозг и что трансген успешно трансдуцирует в ЦНС/головном мозге субъекта. Пути доставки к ЦНС/головному мозгу включают в себя без ограничения интратекальное введение, интракраниальное введение, например, интрацеребровентрикулярное введение или введение в боковые желудочки головного мозга), интраназальное введение, эндоваскулярное введение и интрапаренхиматозное введение.
Согласно одному варианту осуществления способы включают доставку в ЦНС нуждающегося в лечении взрослого млекопитающего композиции, содержащей эффективное количество вектора rAAV-9, содержащего открытую рамку считывания, кодирующую ген. Согласно одному варианту осуществления способы включают доставку в ЦНС нуждающегося в лечении взрослого млекопитающего композиции, содержащей эффективное количество вектора rAAV-9, содержащего открытую рамку считывания, кодирующую IDUA. Эти способы основаны, в частности, на том открытии, что вектор AAV-9 может эффективно трансдуцировать терапевтический трансген в головном мозге/ЦНС взрослых субъектов, восстанавливая содержание фермента до содержания у субъектов дикого типа (смотрите фиг. 15, ниже). Результаты, достигнутые с использованием AAV-9, представляют собой удивительные ввиду предыдущей работы, которая показала, что внутрисосудистая доставка AAV-9 у взрослых мышей не достигала широкого прямого нейронального направленного воздействия (смотрите Foust et al., 2009), а также дополнительных данных, показывающих, что прямая инъекция AAV8-IDUA в ЦНС взрослых дефицитных по IDUA мышей приводила к плохой экспрессии трансгена (фиг. 18). В качестве доказательства принципа описанные в настоящем документе действующие примеры используют доклиническую модель для лечения MPS1, наследуемого метаболического нарушения, вызванного дефицитом лизосомального фермента альфа-L-идуронидазы (IDUA). Действующие примеры показывают, что прямая инъекция AAV9-IDUA в ЦНС иммунокомпетентных взрослых дефицитных по IDUA мышей приводила к экспрессии и активности фермента IDUA, которая была такой же или выше, чем экспрессия и активность фермента IDUA у взрослых мышей дикого типа (фиг. 15, ниже).
Согласно дополнительному варианту осуществления настоящего изобретения действующие примеры показывают также, что совместная терапия для индукции иммуносупрессии или приобретения иммунологической толерантности, или лечения животных с иммунодефицитом может достичь даже более высоких уровней экспрессии и активности фермента IDUA. Согласно одному варианту осуществления пациентов с генотипами, которые способствуют иммунному ответу, который нейтрализует активность фермента (смотрите, например, Barbier et al., 2013), подвергают воздействию иммунодепрессанта в дополнение к вектору rAAV, содержащему открытую рамку считывания, кодирующую генный продукт, такой как IDUA.
Новорожденные мыши IDUA-/- характеризуются отсутствием иммунокомпетентности. Однако введение экспрессирующего IDUA AAV-8 новорожденным мышам IDUA-/- приводит к экспрессии IDUA (Wolf et al., 2011), таким образом, вызывая толерантность животных к IDUA. Как описано в настоящем документе, применимость опосредованного AAV переноса генов взрослым (иммунокомпетентным) мышам путем прямой инфузии AAV в центральную нервную систему была показана с использованием различных путей введения. Например, AAV-IDUA серотипа 9 вводили путем прямой инъекции в боковые желудочки взрослых дефицитных по IDUA мышей, которые были либо иммунокомпетентными, иммунодефицитными (NODSCID/IDUA-/-), подвергнуты иммуносупрессии циклофосфамидом (CP), либо подвергнуты иммунологической толерантности с помощью еженедельных инъекций белка идуронидазы человека (альдуразима), начиная с рождения. Иммуносупрессированным CP животным также вводили AAV9-IDUA путем интраназальной инфузии, путем интратекального введения и путем эндоваскулярной инфузии с маннитолом и без него, чтобы нарушить гематоэнцефалический барьер. Животных умерщвляли через 8 недель после введения вектора и собирали головной мозг, и подвергали микропрепарированию для оценки ферментативной активности IDUA, тканевых гликозаминогликанов и векторных последовательностей IDUA в сравнении с нормальными и подвергнутыми воздействию контрольными мышами. Результаты этих исследований показывают, что могут быть использованы многочисленные пути для введения вектора AAV непосредственно в ЦНС, например, с тем, чтобы достичь более высокого содержания доставляемых белков и/или ферментативной активности в ЦНС. Кроме того, хотя головной мозг представляет собой иммунопривилегированный сайт, введение иммунодепрессанта или обеспечение иммунологической толерантности может повышать активность, обнаруженную в головном мозге, после введения AAV. Более высокие уровни экспрессии в расчете на одно введение и/или малоинвазивные способы введения представляют собой клинически более приемлемые для пациентов.
Таким образом, в настоящем изобретении предусмотрено использование рекомбинантных векторов AAV (rAAV), которые кодируют генный продукт с терапевтическим эффектом при экспрессии в ЦНС млекопитающих. Согласно одному варианту осуществления млекопитающее представляет собой иммунокомпетентное млекопитающее с заболеванием или нарушением центральной нервной системы (неврологическим заболеванием). Используемый в настоящем документе термин "иммунокомпетентное" млекопитающее представляет собой млекопитающее в таком возрасте, когда возникает как клеточный, так и гуморальный иммунный ответ после контакта с антигенным стимулом путем усиления активности функций Th1 или производства IFN-гамма в ответ на поликлональные стимулы, в отличие от новорожденного, который характеризуется врожденным иммунитетом и иммунитетом, полученным от матери, например, во время беременности или кормления грудью. Взрослое млекопитающее, которое не характеризуется наличием иммунодефицита, представляет собой пример иммунокомпетентного млекопитающего. Например, иммунокомпетентный человек, как правило, представляет собой человека, возрастом по меньшей мере 1, 2, 3, 4, 5 или 6 месяцев и включает в себя взрослых людей без иммунодефицита. Согласно одному варианту осуществления AAV вводят интратекально. Согласно одному варианту осуществления AAV вводят интракраниально (например, интрацеребровентрикулярно). Согласно одному варианту осуществления AAV вводится интраназально, с усилителем проницаемости или без него. Согласно одному варианту осуществления AAV вводят эндоваскулярно, например, введение в сонную артерию, с усилителем проницаемости или без него. Согласно одному варианту осуществления млекопитающее, которому вводят AAV, представляет собой млекопитающее с иммунодефицитом или подвергнутое иммунологической толеризации или иммуносупрессии, например, чтобы индуцировать более высокие уровни экспрессии терапевтического белка по отношению к соответствующему млекопитающему, которому вводят AAV, но не подвергают иммунологической толеризации или иммуносупрессии. Согласно одному варианту осуществления вводят средство иммуносупрессии, чтобы индуцировать подавление иммунитета. Согласно одному варианту осуществления млекопитающее, которому вводят AAV, не подвергают иммунологической толеризации или иммуносупрессии (например, введение одного AAV обеспечивает терапевтический эффект).
В настоящем изобретении предусмотрен способ предотвращения, ингибирования или лечения одного или нескольких симптомов, связанных с заболеванием или нарушением центральной нервной системы, у нуждающегося в этом млекопитающего. Способ включает интратекальное, например, в поясничную область, или интрацеребровентрикулярное, например, в боковой желудочек, введение млекопитающему композиции, содержащей эффективное количество вектора rAAV, содержащего открытую рамку считывания, кодирующую генный продукт, экспрессия которого в центральной нервной системе млекопитающего предотвращает, ингибирует или лечит один или несколько симптомов. Согласно одному варианту осуществления генный продукт представляет собой связанный с накоплениями лизосомальный фермент. Согласно одному варианту осуществления млекопитающее представляет собой иммунокомпетентное взрослое млекопитающее. Согласно одному варианту осуществления вектор rAAV представляет собой вектор AAV-1, AAV-2, AAV-3, AAV-4, AAV-5, AAV-6, AAV-7, AAV-8, AAV rh10 или AAV-9. Согласно одному варианту осуществления млекопитающее представляет собой человека. Согласно одному варианту осуществления вводят многократные дозы. Согласно одному варианту осуществления композицию вводят еженедельно, ежемесячно или через каждые два или более месяца.
Согласно одному варианту осуществления способ включает интратекальное, например, в области поясницы, введение млекопитающему композиции, содержащей эффективное количество вектора rAAV, содержащего открытую рамку считывания, кодирующую генный продукт, экспрессия которого в центральной нервной системе млекопитающего предотвращает, ингибирует или лечит один или несколько симптомов, и не обязательное введение усилителя проницаемости. Согласно одному варианту осуществления усилитель проницаемости вводят перед введением композиции. Согласно одному варианту осуществления композиция содержит усилитель проницаемости. Согласно одному варианту осуществления усилитель проницаемости вводят после введения композиции. Согласно одному варианту осуществления продукт гена представляет собой связанный с накоплениями лизосомальный фермент. Согласно одному варианту осуществления млекопитающее представляет собой иммунокомпетентное взрослое млекопитающее. Согласно одному варианту осуществления вектор rAAV представляет собой вектор AAV-1, AAV-2, AAV-3, AAV-4, AAV-5, AAV-6, AAV-7, AAV-8, AAV rh10 или AAV-9. Согласно одному варианту осуществления млекопитающее представляет собой человека. Согласно одному варианту осуществления вводят многократные дозы. Согласно одному варианту осуществления композицию вводят еженедельно, ежемесячно или через каждые два или более месяца. Согласно одному варианту осуществления млекопитающее, которому интратекально вводят AAV, не подвергается иммунологической толеризации или иммуносупрессии (например, введение одного AAV обеспечивает терапевтический эффект). Согласно одному варианту осуществления млекопитающее, которому интратекально вводят AAV, представляет собой млекопитающее с иммунодефицитом или оно подвергается иммунологической толеризации или иммуносупрессии, например, чтобы индуцировать более высокие уровни экспрессии терапевтического белка, по сравнению с соответствующим млекопитающим, которому интратекально вводят AAV, но не подвергают иммунологической толеризации или иммуносупрессии.
Согласно одному варианту осуществления способ включает интрацеребровентрикулярное, например, в боковой желудочек, введение иммунокомпетентному млекопитающему композиции, содержащей эффективное количество rAAV, содержащего открытую рамку считывания, кодирующую генный продукт, экспрессия которого в центральной нервной системе млекопитающего предотвращает, ингибирует или лечит один или несколько симптомов. Согласно одному варианту осуществления генный продукт представляет собой связанный с накоплениями лизосомальный фермент. Согласно одному варианту осуществления вектор rAAV представляет собой вектор AAV-1, AAV-2, AAV-3, AAV-4, AAV-5, AAV-6, AAV-7, AAV-8, AAV rh10 или AAV-9. Согласно одному варианту осуществления, вектор rAAV не представляет собой вектор rAAV-5. Согласно одному варианту осуществления млекопитающее представляет собой человека. Согласно одному варианту осуществления вводят многократные дозы. Согласно одному варианту осуществления композицию вводят еженедельно, ежемесячно или через каждые два или более месяца. Согласно одному варианту осуществления млекопитающее, которому интрацеребровентрикулярно вводят AAV, не подвергается иммунологической толеризации или иммуносупрессии (например, введение одного AAV обеспечивает терапевтический эффект). Согласно одному варианту осуществления млекопитающее, которому интрацеребровентрикулярно вводят AAV, представляет собой млекопитающее с иммунодефицитом или его подвергают иммунологической толеризации или иммуносупрессии, например, чтобы индуцировать более высокие уровни экспрессии терапевтического белка, по сравнению с соответствующим млекопитающим, которому интрацеребровентрикулярно вводят AAV, но не подвергают иммунологической толеризации или иммуносупрессии. Согласно одному варианту осуществления млекопитающее приобретает иммунологическую толерантность к генному продукту перед введение содержащей AAV композиции.
Дополнительно в настоящем изобретении предусмотрен способ предотвращения, ингибирования или лечения одного или нескольких симптомов, связанных с заболеванием или нарушением центральной нервной системы у нуждающегося в этом млекопитающего. Способ включает эндоваскулярное введение млекопитающему композиции, содержащей эффективное количество вектора rAAV, содержащего открытую рамку считывания, кодирующую генный продукт, экспрессия которого в центральной нервной системе млекопитающего предотвращает, ингибирует или лечит один или несколько симптомов, и эффективное количество усилителя проницаемости. Согласно одному варианту осуществления композиция содержит усилитель проницаемости. Согласно одному варианту осуществления усилитель проницаемости содержит маннитол, гликохолат натрия, таурохолат натрия, дезоксихолат натрия, салицилат натрия, каприлат натрия, капрат натрия, лаурилсульфат натрия, полиоксиэтилен-9-лауриловый эфир или ЭДТА. Согласно одному варианту осуществления генный продукт представляет собой связанный с накоплениями лизосомальный фермент. Согласно одному варианту осуществления млекопитающее представляет собой иммунокомпетентное взрослое млекопитающее. Согласно одному варианту осуществления вектор rAAV представляет собой вектор AAV-1, AAV-2, AAV-3, AAV-4, AAV-5, AAV-6, AAV-7, AAV-8, AAV rh10 или AAV-9. Согласно одному варианту осуществления вектор rAAV не представляет собой вектор rAAV-5. Согласно одному варианту осуществления млекопитающее представляет собой человека. Согласно одному варианту осуществления вводят многократные дозы. Согласно одному варианту осуществления композицию вводят еженедельно. Согласно одному варианту осуществления композицию вводится еженедельно, ежемесячно или через каждые два или более месяца. Согласно одному варианту осуществления млекопитающее, которому эндоваскулярно вводят AAV, не подвергается иммунологической толеризации или иммуносупрессии (например, введение AAV обеспечивает терапевтический эффект). Согласно одному варианту осуществления млекопитающее, которому эндоваскулярно вводят AAV, представляет собой млекопитающее с иммунодефицитом или его подвергают иммунологической толеризации или иммуносупрессии, например, чтобы индуцировать более высокие уровни экспрессии терапевтического белка, по сравнению с соответствующим млекопитающим, которому эндоваскулярно вводят AAV, но не подвергают иммунологической толеризации или иммуносупрессии.
Согласно одному варианту осуществления способ включает интраназальное введение млекопитающему композиции, содержащий эффективное количество вектора rAAV-9, содержащего открытую рамку считывания, кодирующую генный продукт, экспрессия которого в центральной нервной системе млекопитающего предотвращает, ингибирует или лечит один или несколько симптомов, и не обязательное введение усилителя проницаемости. Согласно одному варианту осуществления интраназальная доставка может быть достигнута, как описано в патенте США №8609088, раскрытие которого включено в настоящий документ посредством ссылки. Согласно одному варианту осуществления усилитель проницаемости вводят перед введением композицией. Согласно одному варианту осуществления композиция содержит усилитель проницаемости. Согласно одному варианту осуществления усилитель проницаемости вводят после введения композиции. Согласно одному варианту осуществления генный продукт представляет собой связанный с накоплениями лизосомальный фермент. Согласно одному варианту осуществления млекопитающее представляет собой иммунокомпетентное взрослое млекопитающее. Согласно одному варианту осуществления млекопитающее представляет собой человека. Согласно одному варианту осуществления вводят многократные дозы. Согласно одному варианту осуществления композицию вводят еженедельно, ежемесячно или каждые два или более месяца. Согласно одному варианту осуществления млекопитающее, которому вводят интраназально AAV, не подвергается иммунологической толеризации или иммуносупрессии. Согласно одному варианту осуществления млекопитающее, которому вводят интраназально AAV, подвергается иммунологической толеризации или иммуносупрессии, например, чтобы вызвать более высокие уровни экспрессии белка IDUA, по сравнению с соответствующим млекопитающим, которому вводят интраназально AAV, но не подвергают иммунологической толеризации или иммуносупрессии.
Также предусмотрен способ предотвращения, ингибирования или лечения одного или нескольких симптомов, связанных с заболеванием центральной нервной системы у нуждающегося в этом млекопитающего. Способ включает введение млекопитающему композиции, содержащей эффективное количество вектора rAAV, содержащего открытую рамку считывания, кодирующую генный продукт, экспрессия которого в центральной нервной системе млекопитающих предотвращает, ингибирует или лечит один или несколько симптомов, и иммунносупрессанта. Согласно одному варианту осуществления иммунносупрессант содержит циклофосфамид. Согласно одному варианту осуществления иммунносупрессант содержит глюкокортикоид, цитостатические средства, включающие в себя алкилирующее средство, или антиметаболит, такой как метотрексат, азатиоприн, меркаптопурин или цитотоксический антибиотик, антитело или средство, активное к иммунофилину. Согласно одному варианту осуществления иммунносупрессант содержит азотистый иприт, нитрозомочевину, соединение платины, метотрексат, азатиоприн, меркаптопурин, фторурацил, дактиномицин, антрациклин, митомицин С, блеомицин, митрамицин, направленные на рецептор ИЛ-2 (CD25-) или CD3- антитела, антитела к ИЛ-2, циклоспорин, такролимус, сиролимус, IFN-β, интерферон-γ, опиоид или связывающие TNF-α (фактор некроза опухоли-альфа) средства, такие как инфликсимаб (Ремикейд), этанерцепт (Энбрел) или адалимумаб (Хумира). Согласно одному варианту осуществления rAAV и иммунносупрессант вводят совместно. Согласно одному варианту осуществления rAAV вводят перед введением и необязательно после введения иммунносупрессанта. Согласно одному варианту осуществления иммунносупрессант вводят перед введением rAAV. Согласно одному варианту осуществления rAAV и иммунносупрессант вводят интратекально. Согласно одному варианту осуществления rAAV и иммунносупрессант вводят интрацеребровентрикулярно. Согласно одному варианту осуществления rAAV вводят интратекально и иммунносупрессант вводят внутривенно. Согласно одному варианту осуществления генный продукт представляет собой связанный с накоплениями лизосомальный фермент. Согласно одному варианту осуществления млекопитающее представляет собой взрослое млекопитающее. Согласно одному варианту осуществления вектор rAAV представляет собой вектор AAV-1, AAV-2, AAV-3, AAV-4, AAV-5, AAV-6, AAV-7, AAV-8, AAV rh10 или AAV-9. Согласно одному варианту осуществления млекопитающее представляет собой человека. Согласно одному варианту осуществления вводят многократные дозы. Согласно одному варианту осуществления композицию вводят еженедельно. Согласно одному варианту осуществления композицию вводят еженедельно, ежемесячно или каждые два или более месяца.
В настоящем изобретении также предусмотрен способ предотвращения, ингибирования или лечения одного или нескольких симптомов, связанных с заболеванием центральной нервной системы, у нуждающегося в этом млекопитающего. Млекопитающее с приобретенной иммунологической толерантностью к генному продукту, который связан с заболеванием, вводят композицию, содержащую эффективное количество вектора rAAV, содержащего открытую рамку считывания, кодирующую генный продукт, экспрессия которого в центральной нервной системе млекопитающего предотвращает, ингибирует или лечит один или несколько симптомов. Согласно одному варианту осуществления генный продукт представляет собой связанный с накоплениями лизосомальный фермент. Согласно одному варианту осуществления млекопитающее представляет собой взрослое млекопитающее. Согласно одному варианту осуществления вектор rAAV представляет собой вектор AAV-1, AAV-2, AAV-3, AAV-4, AAV-5, AAV-6, AAV-7, AAV-8, AAV rh10 или AAV-9. Согласно одному варианту осуществления млекопитающее представляет собой человека. Согласно одному варианту осуществления вводят многократные дозы. Согласно одному варианту осуществления композицию вводится еженедельно.
Генные продукты, которые могут кодироваться векторами rAAV, включают в себя без ограничения альфа-L-идуронидазу, идуронат-2-сульфатазу, гепарансульфат сульфатазу, N-ацетил-альфа-D-глюкозаминидазу, бета-гексозаминидазу, альфа-галактозидазу, бета-галактозидазу, бета-глюкуронидазу, глюкоцереброзидазу, фактор роста фибробластов-2 (FGF-2), фактор роста головного мозга (BDGF), нейротурин, глиальный фактор роста (GDGF), тирозингидроксилазу, дофамин декарбоксилазу или декарбоксилазу глутаминовой кислоты.
Заболевания, которые характеризуются одним или несколькими неврологическими симптомами, которые можно предотвращать, ингибировать или лечить с использованием описанных в настоящем документе способов, включают в себя без ограничения следующие: адренолейкодистрофия, болезнь Альцгеймера, боковой амиотрофический склероз, синдром Ангельмана, синдром атаксии телеангиэктазии, синдром Шарко-Мари-Тута, синдром Коккейна, глухота, мышечная дистрофия Дюшенна, эпилепсия, эссенциальный тремор, синдром фрагильной X-хромосомы, атаксия Фридрейха, болезнь Гоше, болезнь Хантингтона, синдром Леша-Нихана, болезнь мочи с запахом кленового сиропа, синдром Менкеса, миотоническая дистрофия, нарколепсия, нейрофиброматоз, болезнь Ниманна-Пика, болезнь Паркинсона, фенилкетонурия, синдром Прадера-Вилли, болезнь Рефсума, синдром Ретта, спинальная мышечная атрофия, спиноцеребеллярная атаксия, болезнь Танжер, болезнь Тея-Сакса, туберозный склероз, синдром Гиппеля-Линдау, синдром Вильямса, болезнь Вильсона или синдром Зеллвегер. Согласно одному варианту осуществления заболевание представляет собой лизосомную болезнь накопления, например, отсутствие или недостаток связанного с накоплениями лизосомального фермента. Лизосомные болезни накопления включают в себя без ограничения заболевание мукополисахаридоз (MPS), например, мукополисахаридоз типа I, например, синдром Гурлера и варианты синдрома Шейе и синдрома Гурлера-Шейе (дефицит альфа-L-идуронидазы); синдром Хантера (дефицит идуронат-2-сульфатазы); мукополисахаридоз типа III, например, синдром Санфилиппо (А, В, С или D; дефицит гепарансульфат сульфатазы, N-ацетил-альфа-D-глюкозаминидазы, ацетил-СоА:альфа-глюкозаминид-N-ацетил-трансферазы или N-ацетилглюкозамин-6-сульфат сульфатазы); мукополисахаридоз типа IV например, например, синдром Моркио (дефицит галактозамин-6-сульфат сульфатазы или бета-галактозидазы); мукополисахаридоз типа VI, например, синдром Марото-Лами (дефицит арилсульфатазы В); мукополисахаридоз типа II; мукополисахаридоз типа III (А, В, С или D; дефицит гепарансульфат сульфатазы, N-ацетил-альфа-D-глюкозаминидазы, ацетил-СоА:альфа-глюкозаминид-N-ацетилтрансферазы или N-ацетилглюкозамина-6-сульфат сульфатазы); мукополисахаридоз типа IV (А или В; дефицит галактозамин-6-сульфатазы и бета-галактозидазы); мукополисахаридоз типа VI (дефицит арилсульфатазы В); мукополисахаридоз типа VII (дефицит бета-глюкуронидазы); мукополисахаридоз типа VIII (дефицит глюкозамин-6-сульфат сульфатазы); мукополисахаридоз типа IX (дефицит гиалуронидазы); болезнь Тея-Сакса (дефицит в альфа-субъединице бета-гексозаминидазы); болезнь Сандгоффа (дефицит в обеих альфа и бета-субъединицах бета-гексозаминидазы); ганглиозидоз GM1 (типа I или типа II); болезнь Фабри (дефицит альфа-галактозидазы); метахроматическую лейкодистрофию (дефицит арильной сульфатазы А); болезнь Помпе (недостаток кислоты мальтазы); фукозидоз (дефицит фукозидазы); альфа-маннозидоз (дефицит альфа-маннозидазы); бета-маннозидоз (дефицит бета-маннозидазы), нейронный восковидный липофусциноз и болезнь Гоше (типов I, II и III; дефицит глюкоцереброзидазы), а также такие нарушения, как синдром Германского-Пудлака; амавротическую идиотию; болезнь Танжер; аспартилглюкозаминурию; врожденное нарушение гликозилирования, тип Ia; синдром Чедиака-Хигаси; макулярную дистрофию роговицы, 1; цистиноз, нефропатический; синдром Фанкони-Бикель; липогранулематоз Фарбера; фиброматоз; гелеофизическую дисплазию; связанное с накоплением гликогена заболевание I; связанное с накоплением гликогена заболевание Ib; связанное с накоплением гликогена заболевание Iс; связанное с накоплением гликогена заболевание III; связанное с накоплением гликогена заболевание IV; связанное с накоплением гликогена заболевание V; связанное с накоплением гликогена заболевание VI; связанное с накоплением гликогена заболевание VII; связанное с накоплением гликогена заболевание 0; иммуно-остеоидную дисплазию, тип Шимке; липидоз; липазу b; муколипидоз II; муколипидоз II, включая в себя вариантную форму; муколипидоз IV; дефицит нейраминидазы с дефицитом бета-галактозидазы; муколипидоз I; болезнь Ниманна-Пика (дефицит сфингомиелиназы); болезнь Ниманна-Пика без дефицита сфингомиелиназы (дефицит гена npc1, кодирующего метаболизирующий холестерин фермент); болезнь Рефсума; болезнь голубых гистиоцитов; инфантильную форму заболевания накопления сиаловых кислот; сиалурию; множественную сульфатазную недостаточность; болезнь накопления триглицеридов с нарушенным окислением длинноцепочечных жирных кислот; болезнь Винчестера; болезнь Вольмана (дефицит гидролазы эфира холестерина); подобное дезоксирибонуклеазе I нарушение 1; нарушение арилсульфатазы Е; нарушение АТФазы, транспортировки Н+, лизосомальной, субъединицы 1; заболевание накопления гликогена IIb; нарушение ассоциированного с Ras белка rab9; точечную эпифизарную дисплазию 1, связанное с Х-хромосомой рецессивное нарушение; заболевание накопления гликогена VIII; нарушение связанного с лизосомой мембранного белка 2; синдром Менкеса; врожденный порок гликозилирования, типа Iс; и сиалурию. Замена менее чем 20%, например, менее чем 10% или приблизительно от 1% до 5%, содержания связанного с накоплениями лизосомального фермента, обнаруженного у млекопитающих без заболевания, может предотвращать, ингибировать или лечить неврологические симптомы, такие как неврологические дегенерации у млекопитающих.
Согласно одному варианту осуществления описанные в настоящем документе способы включают доставку в ЦНС нуждающегося в таком лечении иммунокомпетентного человека композиции, содержащей эффективное количество вектора rAAV-9, содержащего открытую рамку считывания, кодирующую IDUA. Пути введения к ЦНС/головному мозгу включают в себя без ограничения интратекальное введение, интракраниальное введение, например, интрацеребровентрикулярное введение или введение в боковые желудочки головного мозга, интраназальное введение, эндоваскулярное введение и интрапаренхиматозное введение.
В способах согласно настоящему изобретению могут быть использованы другие вирусные векторы, например, такие вирусные векторы, как векторы ретровируса, лентивируса, аденовируса, вируса леса Семлики или вируса простого герпеса.
Краткое описание графических материалов
Фигура 1. Экспериментальная разработка для дефицитных по идуронидазе мышей, которым вводили IDUA-AAV либо интрацеребровентрикулярно (ICV), либо интратекально. Для предотвращения иммунного ответа животных либо подвергали иммуносупрессии с циклофосфамидом (CP), вызывали иммунологическую толерантность при рождении путем внутривенного введения белка идуронидазы человека (альдуразима), либо проводили инъекции у NOD-SCID мышей с иммунодефицитом, которые также характеризовались дефицитом идуронидазы. Животных умерщвляли в указанное время после воздействия, головной мозг подвергали микропрепарированию и в экстрактах анализировали активность идуронидазы.
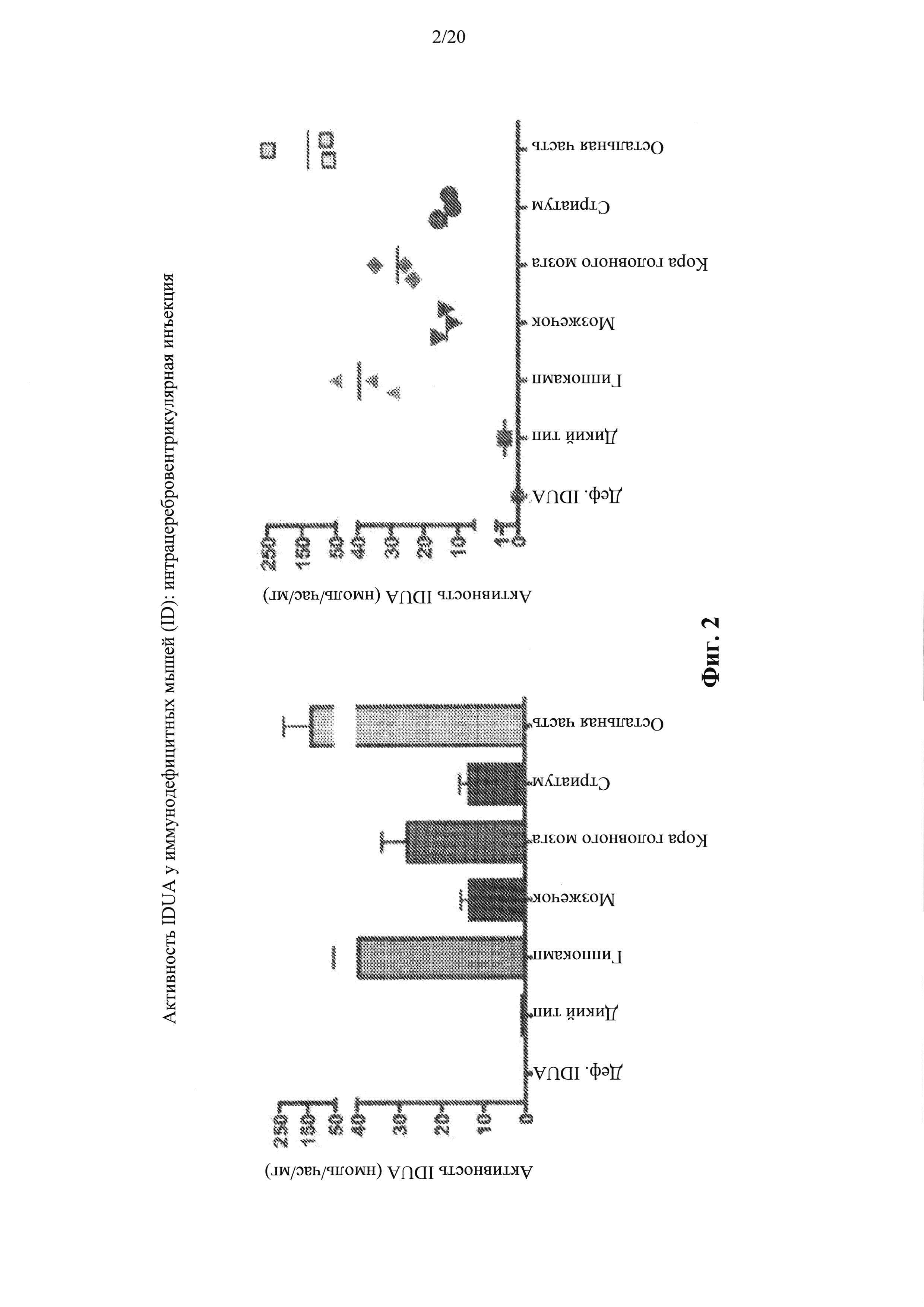
Фигура 2. Активность IDUA у иммунодефицитных, дефицитных по IDUA животных.
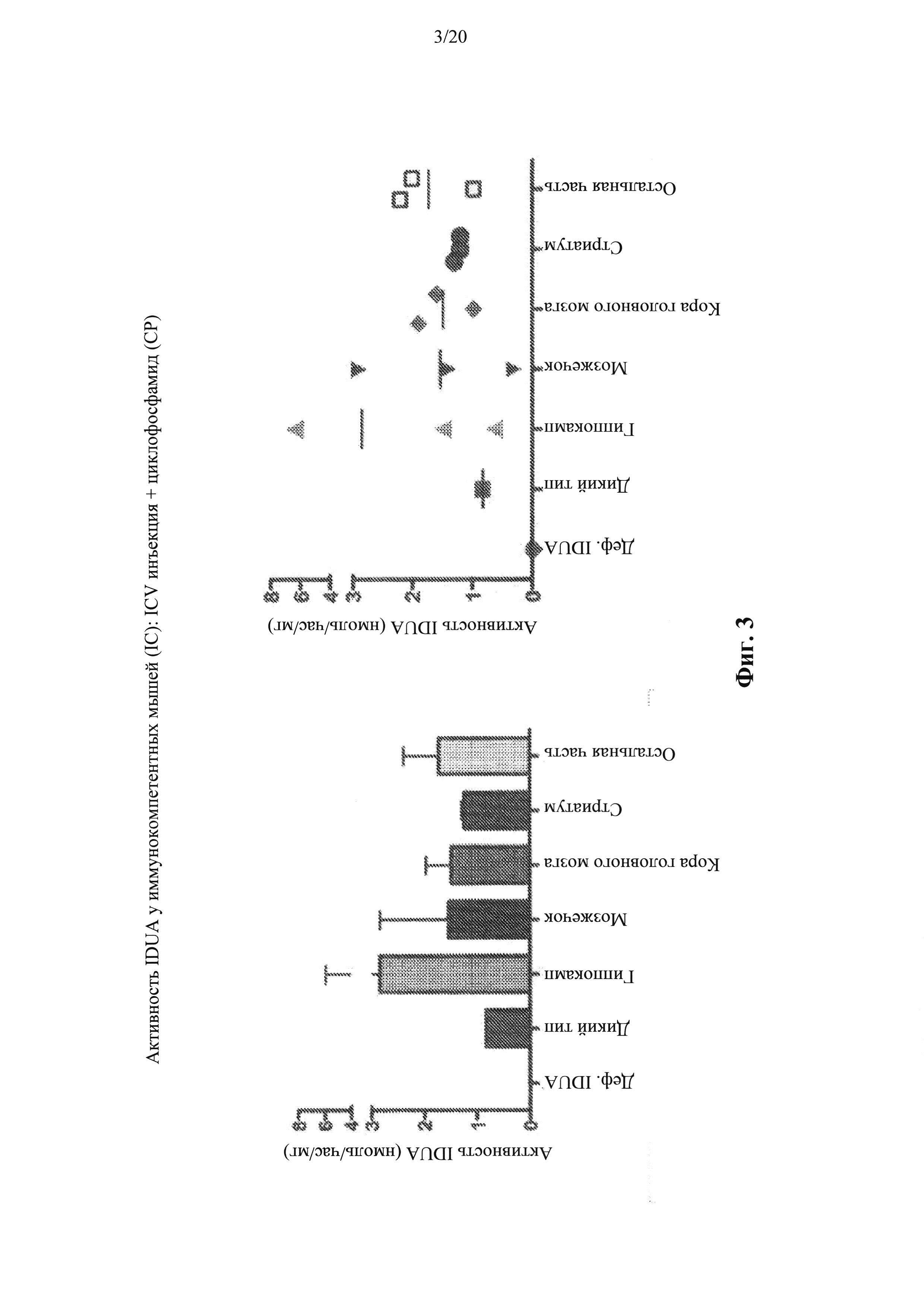
Фигура 3. Активность IDUA у иммуносупрессированных животных, которым вводили вектор AAV путем ICV.
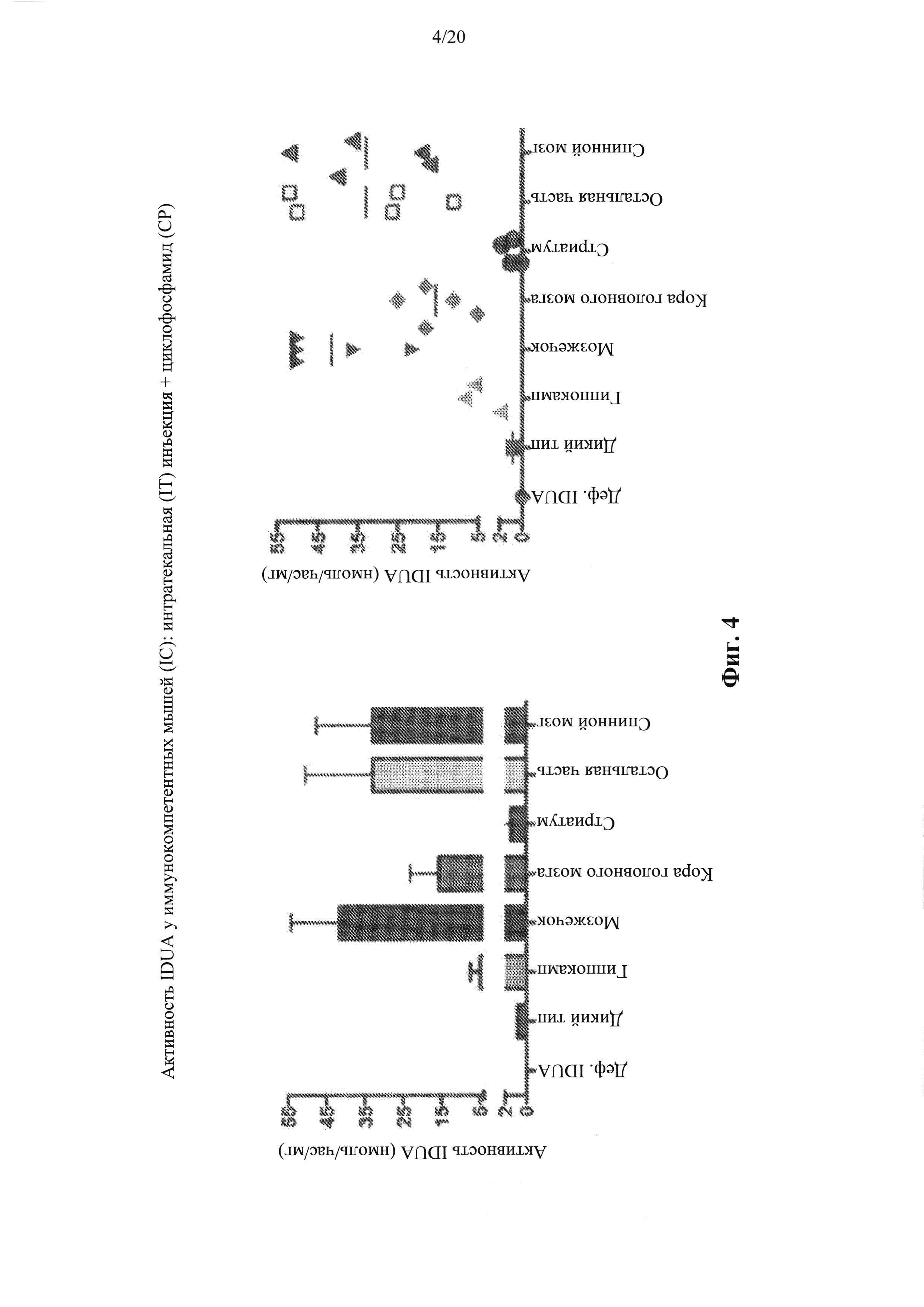
Фигура 4. Активность IDUA у иммуносупрессированных животных, которым вводили вектор AAV путем IT.
Фигура 5. Активность IDUA у животных с приобретенной иммунологической толерантностью, которым вводили вектор AAV ICV.
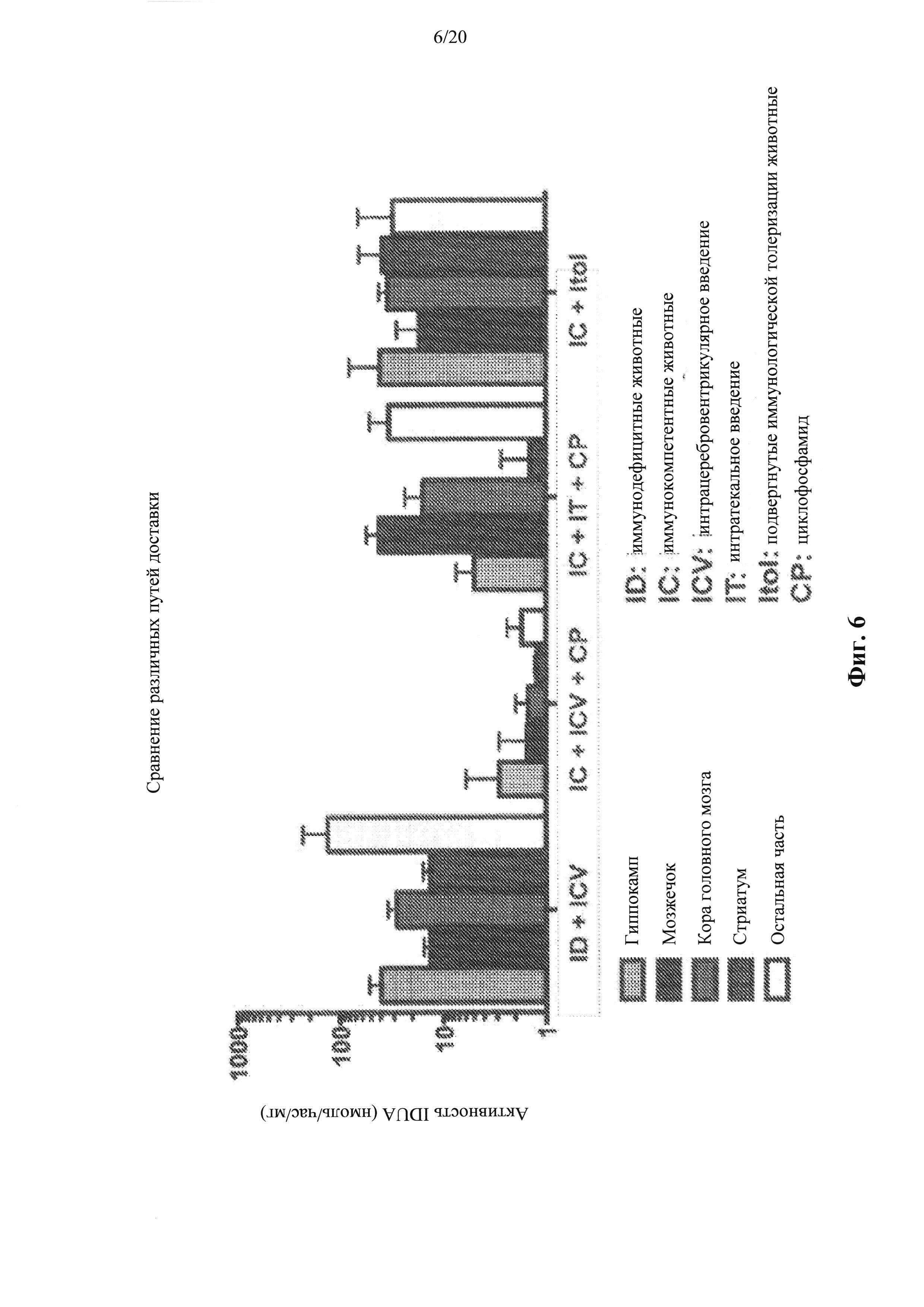
Фигура 6. Сопоставление всех средних уровней активности IDUA для сравнения.
Фигура 7. Данные сгруппированы в соответствии с областью головного мозга.
Фигура 8. Анализ вещества накопления ГАГ в различных отделах головного мозга для всех четырех исследуемых групп.
Фигура 9. Схема эксперимента.
Фигура 10. Интракраниальная инфузия AAV9IDUA иммунодефицитным мышам с MPS I. Взрослым животным вводили 1011 векторных геномов и оценивали экспрессию идуронидазы в головном мозге через 10 недель. Уровни ферментативной активности в головном мозге были значительно выше, чем в головном мозге животных дикого типа, и варьировали в пределах, которые были от 30 до 300 раз выше, чем у животных дикого типа.
Фигура 11. Интракраниальное введение AAV9IDUA иммунокомпетентным, дефицитным по IDUA мышам. Взрослым животным вводили 1011 векторных геномов и подвергали иммуносупрессии путем еженедельной инъекции циклофосфамида (CP). Инъекции CP прекращали через 6 недель после инъекции вектора из-за неудовлетворительного состояния здоровья и животных умерщвляли через 8 недель после инъекции. Головной мозг подвергали микропрепарированию и анализировали активность фермента IDUA.
Фигура 12. Интракраниальная инфузия AAV9IDUA мышам с MPS I с приобретенной иммунологической толерантностью. У мышей с MPS 1 вызывали толерантность либо одной дозой альдуразима при рождении, либо многократными дозами, вводимыми еженедельно, начиная с рождения. Мышам вводили вектор в 4 месяца и умерщвляли через 11 недель после инъекции. Головной мозг подвергали микропрепарированию и анализировали экспрессию идуронидазы. Активности ферментов варьировали в диапазоне, который был в среднем от 10 до 1000 раз выше, чем уровни у животных дикого типа.
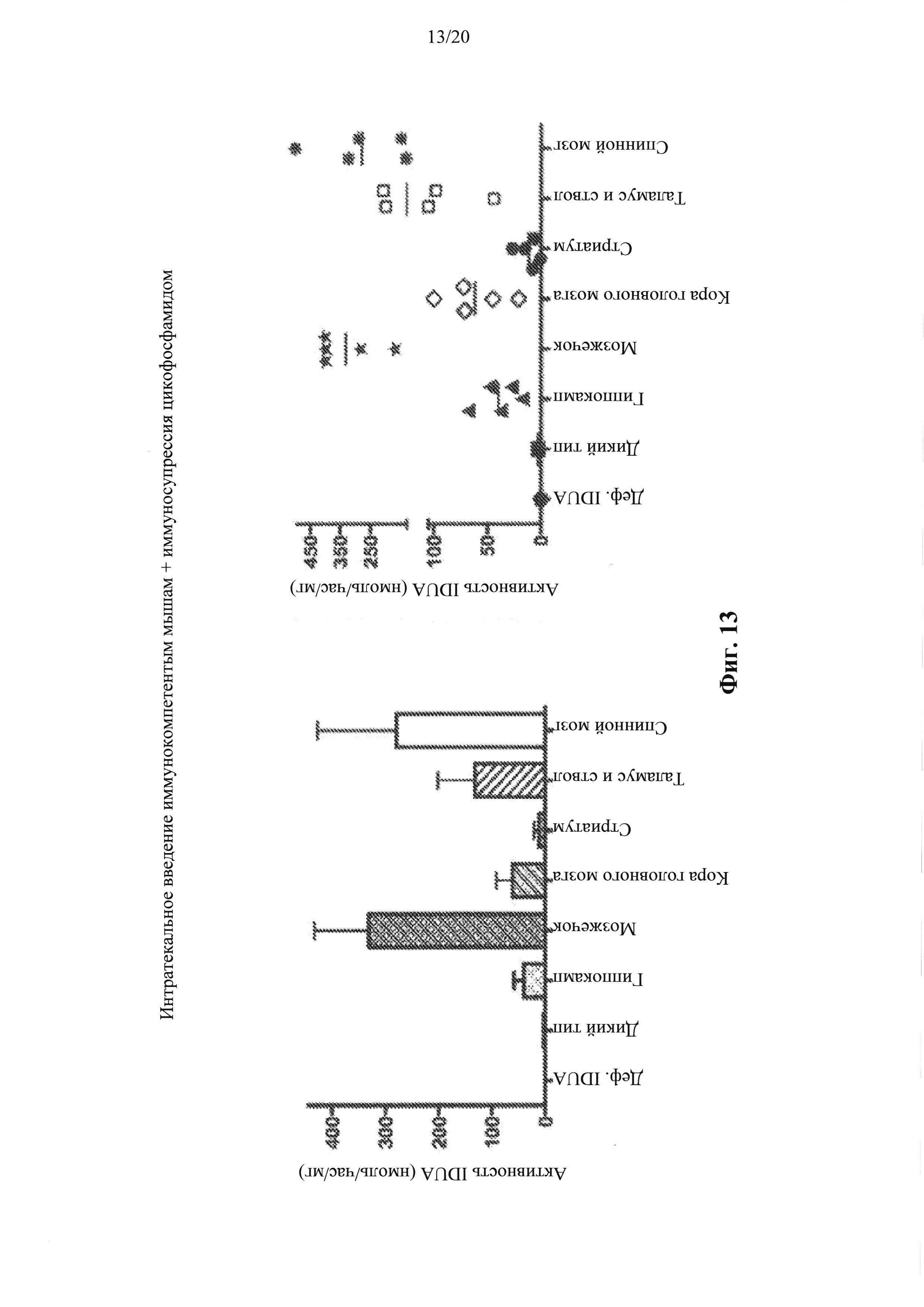
Фигура 13. Интратекальное введение AAV9IDUA иммунокомпетентным, дефицитным по IDUA животным. Взрослым мышам с MPS I вводили AAV9IDUA интратекально, а затем раз в неделю иммуносупрессивную схему циклофосфамида. Животных умерщвляли через 11 недель после инъекции, а затем в головном мозге и спинном мозге анализировали активность фермента IDUA.
Фигура 14. Интратекальная инфузия AAV9IDUA мышам с MPS I с приобретенной иммунологической толерантностью. У дефицитных по IDUA животных вызывали толерантность при рождении одной дозой альдуразима или многократными дозами, вводимыми еженедельно, начиная с рождения. В возрасте 4 месяца животным вводили интратекально вектор AAV9IDUA и через 10 недель после инъекции животных умерщвляли, головной мозг подвергали микропрепарированию и анализировали активность идуронидазы. Наблюдалось восстановление активности фермента во всех частях головного мозга, с активностью в мозжечке, варьировавшей в пределах, которые от 200- до 1500 раз выше, чем уровни у животных дикого типа. Уровни активности фермента в обонятельной луковице и мозжечке (справа от пунктироной линии) соответствуют правой оси ординат.
Фигура 15. Интратекальная инфузия AAV9IDUA иммунокомпетентным животным с MPS I. Контрольным животным с MPS I вводили вектор AAV9IDUA, но не подвергали ни иммуносупрессии, ни иммунологической толеризации. Животных умерщвляли через 11 недель после инъекции вектора, а затем в их головном мозге анализировали активность идуронидазы. Содержание ферментов восстанавливалось до содержания у животных дикого типа во всех частях мозга, но было значительно ниже, чем у животных, которые были подвергнуты либо иммуносупрессии, либо иммунологической толеризации.
Фигура 16. Нормализация содержания гликозаминогликанов (ГАГ) после интракраниальной или интратекальной инфузии AAV9. AAV9IDUA вводили интракраниально или интратекально мышам с MPS I с иммунодефицитом, подвергнутым иммуносупрессии или иммунологической толеризации, как указано.
Животных умерщвляли через 8-11 недель после инъекции, а затем головной мозг подвергали микропрепарированию и анализировали содержание ГАГ. Накопление ГАГ восстанавливалось до содержания, соответствующего животным дикого типа или близкого животным дикого типа во всех проанализированных группах.
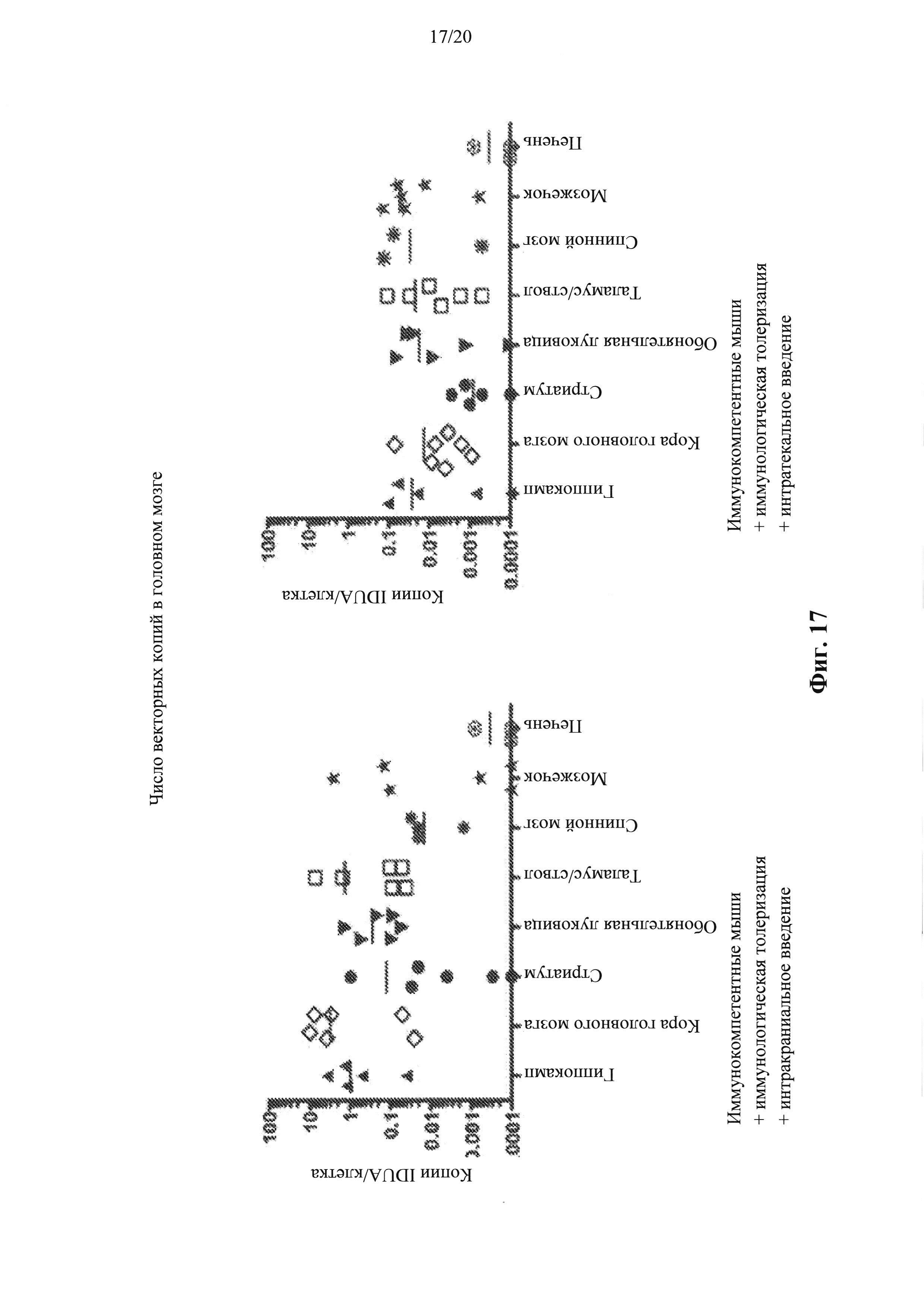
Фигура 17. Векторные копии IDUA в головном мозге. В подвергнутом микропрепарированию головном мозге анализировали векторные последовательности IDUA с помощью количественной ПЦР. Число копий у мышей, которым их вводили интракраниально и интратекально, коррелировало с уровнем активности фермента, изображенным на фиг. 11 и 13.
Фигура 18. Инфузия ICV AAV8-MCI взрослым животным.
Фигура 19. Интраназальное введение AAV9/IDUA иммунокомпетентным, дефицитным по IDUA животным. Взрослым мышам с MPS I вводили AAV9/IDUA интраназально, а затем еженедельно иммуносупрессивную схему циклофосфамида. Животных умерщвляли через 12 недель после инъекции и в головном мозге анализировали активность фермента IDUA.
Фигура 20. Векторные копии IDUA в головном мозге. В подвергнутом микропрепарированию головном мозге анализировали векторные последовательности IDUA с помощью количественной ПЦР. Число копий у мышей, которым их вводили интраназально, коррелировало с содержанием фермента на фиг. 19.
Подробное описание настоящего изобретения
Определения
Используемый в настоящем документе термин "индивидуум" (как в субъекте лечения) означает млекопитающее. Млекопитающие включают в себя, например, людей, нечеловекообразных приматов, например, обезьян и мартышек; и не приматов, например, собак, кошек, крыс, мышей, крупный рогатый скот, лошадей, овец и коз. Отличные от млекопитающих животные включают в себя, например, рыб и птиц.
Термины "заболевание" или "нарушение" используются взаимозаменяемо и используются для обозначения заболеваний или состояний, при которых отсутствие или снижение количества конкретного генного продукта, например, связанного с накоплениями лизосомального фермента, играет важную роль при заболевании, таким образом, что терапевтически полезный эффект может быть достигнут путем дополнения, например, по меньшей мере 1% нормального содержания.
Используемый в настоящем документе термин "по существу" означает полностью или почти полностью; например, композиция, которая "по существу свободна" от компонента либо не содержит ни одного компонента, либо содержит такое незначительное количество, что любое соответствующее функциональное свойство композиции не зависит от присутствия следовых количеств, или соединение представляет собой "по существу чистое", если есть только незначительные следы присутствующих примесей.
"Лечение" или "воздействие" по смыслу в настоящем документе относится к облегчению симптомов, связанных с нарушением или заболеванием, "ингибирование" означает торможение дальнейшего прогрессирования или ухудшения симптомов, связанных с нарушением или заболеванием, и "предотвращение" относится к предупреждению симптомов, связанных с нарушением или заболеванием.
Используемое в настоящем документе "эффективное количество" или "терапевтически эффективное количество" средства согласно настоящему изобретению, например, рекомбинантного AAV, кодирующего генный продукт, относится к количеству средства, которое облегчает, в целом или частично, симптомы, связанные с нарушением или состоянием, или останавливает или замедляет дальнейшее прогрессирование или ухудшение этих симптомов, или предотвращает или обеспечивает профилактику нарушения или состояния, например, количеству, которое эффективно для предотвращения, ингибирования или лечения у индивидуума одного или нескольких неврологических симптомов.
В частности, "терапевтически эффективное количество" относится к количеству, эффективному в дозах и в течение периодов времени, необходимых для достижения желаемого терапевтического результата. Терапевтически эффективное количество также представляет собой таковое, при котором любые токсические или вредные эффекты соединений согласно настоящему изобретению перевешиваются терапевтически благоприятными эффектами.
Используемый в настоящем документе "вектор" относится к макромолекуле или комплексу макромолекул, который содержит или связан с полинуклеотидом и который может быть использован для того, чтобы опосредовать доставку полинуклеотида в клетке, либо in vitro, либо in vivo. Иллюстративные векторы включают в себя, например, плазмиды, вирусные векторы, липосомы и другие средства доставки генов. Доставляемый полинуклеотид, иногда называемый как "полинуклеотид-мишень" или "трансген", может содержать представляющую интерес кодирующую последовательность в генной терапии (такую как ген, кодирующий представляющий терапевтический интерес белок) и/или селективный или обнаруживаемый маркер.
"AAV" представляет собой аденоассоциированный вирус и может быть использован для обозначения самого вируса или его производных. Этот термин охватывает все подтипы, серотипы и псевдотипы и как встречающиеся в природе, так и рекомбинантные формы, за исключением случаев, когда требуется иное. Используемый в настоящем документе термин "серотип" относится к AAV. который идентифицирован с помощью и отличается от других AAV на основании его связывающих свойств, например, существует одиннадцать серотипов AAV, AAV-1-AAV-11, включая в себя AAV-2, AAV-5, AAV-8, AAV-9 и AAV rh10, и термин охватывает псевдотипы с теми же связывающими свойствами. Так, например, серотипы AAV-5 включают в себя AAV со связывающими свойствами AAV-5, например, псевдотипированный AAV, содержащий капсид AAV-5 и геном rAAV, который не происходит или его не получают от AAV-5, или чей геном представляет собой химерный. Сокращение "rAAV" относится к рекомбинантному аденоассоциированному вирусу, также называемому рекомбинантный вектор AAV (или "вектор rAAV").
Термин "вирус AAV" относится к вирусной частице, состоящей по меньшей мере из одного капсидного белка AAV и заключенного в капсид полинуклеотида. Если частица содержит гетерологичный полинуклеотид (т.е. полинуклеотид, отличный от генома AAV дикого типа, такой как трансген для доставки к клетке млекопитающего), то, как правило, его называют "rAAV". "Капсидный белок" AAV включает в себя капсидный белок AAV дикого типа, а также модифицированные формы капсидного белка AAV, которые структурно и/или функционально способны к упаковке генома rAAV и связываются по меньшей мере с одним специфическим клеточным рецептором, который может отличаться от рецептора, используемого AAV дикого типа. Модифицированный капсидный белок AAV включает в себя химерный капсидный белок AAV, такой как тот, который содержит аминокислотные последовательности от двух или более серотипов AAV, например, капсидный белок, образованный из части капсидного белка из AAV-5, слитого или связанного с участком капсидного белка из AAV-2, и капсидный белок AAV, содержащий метку или другой обнаруживаемый капсидный белок не-AAV или белок, слитый или связанный с капсидным белком AAV, например, часть молекулы антитела, которая связывается с рецептором трансферрином, может быть рекомбинантно слита с капсидным белком AAV-2.
"Псевдотипированный" rAAV представляет собой инфекционный вирус, содержащий любую комбинацию капсидного белка AAV и генома AAV. Капсидные белки из любого серотипа AAV могут быть использованы с геномом rAAV, который происходит из генома AAV дикого типа другого серотипа или который представляет собой химерный геном, т.е. образован из ДНК AAV от двух или более различных серотипов, например химерный геном, содержащий 2 инвертированных концевых повтора (ITR), каждый ITR от различных серотипов или химерных ITR. Использование химерных геномов, таких как те, которые содержат ITR от двух серотипов AAV или химерных ITR, может приводить к направленной рекомбинации, которая может дополнительно повысить производство транскрипционно активных межмолекулярных конкатемеров. Таким образом, 5' и 3' ITR в пределах вектора rAAV согласно настоящему изобретению могут быть гомологичными, т.е. от одного серотипа, гетерологичными, т.е. от различных серотипов, или химерными, т.е. ITR, который содержит последовательности ITR от более чем одного серотипа AAV.
Векторы rAAV
Аденоассоциированные вирусы любого серотипа пригодны для получения rAAV, так как различные серотипы функционально и структурно связаны даже на генетическом уровне. Все серотипы AAV, по-видимому, обладают похожими свойствами репликации, опосредованными гомологичными генами rep; и все, как правило, несут три взаимосвязанных капсидных белка, такие как те, которые экспрессированы в AAV2. Степень родства далее подтверждается с помощью гетеродуплексного анализа, который показывает обширную перекрестную гибридизацию между серотипами по длине генома; и наличия аналогичных сегментов самоотжига на концах, которые соответствуют ITR. Подобные паттерны инфекционности также предполагают, что функции репликации в каждом серотипе находятся под аналогичным регулирующим контролем. Среди различных серотипов AAV наиболее часто используется AAV2.
Вектор AAV согласно настоящему изобретению, как правило, содержит полинуклеотид, который гетерологичен AAV. Полинуклеотид, как правило, представляет интерес из-за способности обеспечивать функцию к клетке-мишени в контексте генной терапии, такую, как активация или подавление экспрессии определенного фенотипа. Такой гетерологичный полинуклеотид или "трансген" в основном характеризуется достаточной длиной, чтобы обеспечить требуемую функцию или кодирующую последовательность.
Там, где желательна транскрипция гетерологичного полинуклеотида в предназначенной клетке-мишени, он может быть функционально связан с собственным или гетерологичным промотором, в зависимости, например, от желаемого уровня и/или специфичности транскрипции внутри клетки-мишени, как известно в настоящей области техники. Различные типы промоторов и энхансеров пригодны для использования в данном контексте. Конститутивные промоторы обеспечивают постоянный уровень транскрипции гена и могут быть предпочтительными, когда желательно, чтобы терапевтический или профилактический полинуклеотид экспрессировался на постоянной основе. Индуцируемые промоторы, как правило, характеризуются низкой активностью в отсутствие индуктора и активируются в присутствии индуктора. Они могут быть предпочтительными, когда экспрессия желательна только в определенное время или в определенных местах или когда желательно титрование уровня экспрессии с использованием индуцирующего средства. Промоторы и энхансеры могут быть также тканеспецифическими: т.е. обладать активностью только в определенных типах клеток, предположительно из-за генных регулирующих элементов, найденных только в этих клетках.
Иллюстративные примеры промоторов представляют собой поздний промотор из вируса 40 обезьян ОВ40, промоторный/энхансерный элемент полиэдра бакуловируса, тимидинкиназу вируса простого герпеса (HSV tk), непосредственный ранний промотор из цитомегаловируса (CMV) и различные ретровирусные промоторы, включая в себя элементы LTR. Индуцируемые промоторы включают в себя индуцируемые промоторы - ионы тяжелых металлов (например, промотор вируса опухоли молочной железы мыши (MMTV) или различные промоторы гормона роста) и промоторы из фага Т7, которые активны в присутствии РНК-полимеразы Т7. В качестве иллюстрации примеры тканеспецифических промоторов включают в себя различные промоторы сурфактина (для экспрессии в легких), промоторы миозина (для экспрессии в мышцах) и промоторы альбумина (для экспрессии в печени). Большое разнообразие других промоторов известно и общедоступно в настоящей области техники, и последовательности многих таких промоторов доступны в базах данных последовательностей, таких как база данных GenBank.
Там, где трансляция также желательна в предназначенной клетке-мишени, гетерологичный полинуклеотид предпочтительно будет также содержать элементы контроля, которые облегчают трансляцию (например, сайт связывания рибосом или "RBS" и сигнал полиаденилирования). Соответственно, гетерологичный полинуклеотид, как правило, содержит по меньшей мере один кодирующий участок, функционально связанный с подходящим промотором, и может также содержать, например, функционально связанный энхансер, сайт связывания рибосом и поли-А сигнал. Гетерологичный полинуклеотид может содержать одну кодирующую область или более чем одну кодирующую область под контролем одних и тех же или различных промоторов. Весь блок, содержащий комбинацию контрольных элементов и кодирующей области, часто упоминается как экспрессионная кассета.
Гетерологичный полинуклеотид встраивают с помощью рекомбинантных способов в или в месте геномной кодирующей области AAV (т.е. в месте генов rep и cap AAV), но, как правило, окружают по обе стороны областями инвертированных концевых повторов (ITR) AAV. Это означает, что ITR появляется как выше против хода, так и ниже по ходу транскрипции от кодирующей последовательности, либо в непосредственном соприкосновении, например, (но не обязательно), без какой-либо промежуточной последовательности происхождения AAV, с тем, чтобы уменьшить вероятность рекомбинации, которая может регенерировать репликацию генома AAV. Тем не менее, одного ITR может быть достаточно, чтобы выполнять функции, обычно связанные с конфигурациями, содержащими два ITR (смотрите, например, WO 94/13788), и векторные конструкты только с одним ITR, таким образом, можно использоваться вместе со способами упаковки и производства согласно настоящему изобретению.
Природные промоторы для rep представляют собой саморегулирующиеся и могут ограничивать количество произведенных частиц AAV. Ген rep также может быть функционально связан с гетерологичным промотором, независимо от того предусмотрен ли rep в виде части векторной конструкции или отдельно. Подходит любой гетерологичный промотор, который не сильно подавляется с помощью генной экспрессии rep; но индуцируемые промоторы могут быть предпочтительными, поскольку конститутивная экспрессия гена rep может оказывать отрицательное воздействие на клетку-хозяина. В настоящей области техники известно большое разнообразие индуцируемых промоторов; включая в себя, в качестве иллюстрации, индуцируемые промоторы - ионы тяжелых металлов (например, промоторы металлотионеина); индуцируемые промоторы стероидных гормонов (такие как промотор MMTV или промоторы гормона роста); и такие промоторы, как из фага Т7, которые активны в присутствии РНК-полимеразы Т7. Один подкласс индуцируемых промоторов представляют собой те промоторы, которые индуцируются с помощью вируса-помощника, который используется для дополнения репликации и упаковки вектора rAAV. Также был описан ряд индуцируемых с помощью вирусов-помощников промоторов, включая в себя ранний генный промотор аденовируса, который индуцируется белком Е1А аденовируса; основной поздний промотор аденовируса; промотор вируса герпеса, который индуцируется с помощью белков вируса герпеса, таких как VP16 или 1СР4; а также индуцируемые промоторы вируса осповакцины или поксвируса.
Способы идентификации и исследования индуцируемых с помощью вирусов-помощников промоторов были описаны (смотрите, например, WO 96/17947). Таким образом, в настоящей области техники известны способы определения того, представляют ли собой кандидатные промоторы индуцируемые с помощью вируса-помощника и будут ли они или нет полезны при получении упаковочных клеток с высокой эффективностью. Кратко, один такой способ включает замену промотора р5 гена rep AAV на предполагаемый индуцируемый с помощью вирусов-помощников промотор (либо известный в настоящей области техники, либо идентифицированный с использованием хорошо известных техник, таких как связывание с "репортерными" генами без промоторов). Гены rep-cap AAV (замененные р5), например, связанные с положительным селективным маркером, таким как ген резистентности к антибиотику, затем стабильно интегрируют в подходящую клетку-хозяина (такую как клетки HeLa или А549, примеры которых приведены ниже). Клетки, которые способны расти относительно хорошо в условиях отбора (например, в присутствии антибиотика), затем исследуют на их способность экспрессировать гены rep и cap при добавлении вируса-помощника. В качестве первого исследования на экспрессию rep и/или cap, клетки можно легко подвергнуть скринингу с использованием иммунофлюоресценции для обнаружения белков Rep и/или Сар. Подтверждение возможности и эффективности упаковки может быть определено с помощью функциональных исследований на репликацию и упаковку поступающих векторов rAAV. С использованием этой методики, индуцируемый вирусом-помощником промотор получают из мышиного гена металлотионеина, который был идентифицирован в качестве подходящего для замены промотора р5 и используется для производства высоких титров частиц rAAV (как описано в WO 96/17947).
Удаление одного или нескольких генов AAV в любом случае нежелательно для уменьшения вероятности получения компетентного к репликации AAV ("RCA"). Соответственно, кодирующие или промоторные последовательности для rep, cap или и того и другого могут быть удалены, так как функции, обеспечиваемые этими генами, могут быть предусмотрены в trans.
Полученный в результате вектор относится к "дефектному" в отношении этих функций. Для того чтобы реплицировать и упаковать вектор, недостающие функции дополняются геном упаковки или их множеством, которые вместе кодируют необходимые функции для различных утерянных генных продуктов rep и/или cap. Гены или генные кассеты упаковки согласно одному варианту осуществления не находятся в окружении ITR AAV и согласно одному варианту осуществления не разделяют любую существенную гомологию с геномом rAAV. Таким образом, чтобы свести к минимуму гомологичную рекомбинацию в процессе репликации между векторной последовательностью и отдельно предусмотренными генами упаковки, желательно избежать перекрытия двух полинуклеотидных последовательностей. Уровень гомологии и соответствующей частоты рекомбинации увеличивается с увеличением длины гомологичных последовательностей и с уровнем их общей идентичности. Уровень гомологии, который будет представлять затруднение в данной системе, может быть определен теоретически и подтвержден экспериментально, как известно в настоящей области техники. Как правило, однако, рекомбинация может быть существенно уменьшена или устранена, если перекрывающаяся последовательность составляет менее чем приблизительно последовательность из 25 нуклеотидов, если она по меньшей мере на 80% идентична по всей ее длине, или менее чем приблизительно последовательность из 50 нуклеотидов, если она по меньшей мере на 70% идентична по всей ее длине. Конечно, предпочтительны даже более низкие уровни гомологии, так как они будут еще больше снижать вероятность рекомбинации. Похоже, что даже без перекрывающейся гомологии, существуют некоторые остаточные частоты производства RCA. Даже дополнительное сокращение частоты производства RCA (например, с помощью негомологичной рекомбинации) может быть получено путем "расщепления" репликации и капсидирования функций AAV, как описано Allen с соавт., WO 98/27204).
Векторный конструкт rAAV и комплементарные генные конструкты упаковки могут быть реализованы в настоящем изобретении в ряде различных форм. Вирусные частицы, плазмиды и стабильно трансформированные клетки-хозяева могут все быть использованы для введения таких конструктов в упаковочную клетку, либо временно, либо стабильно.
Согласно некоторым вариантам осуществления настоящего изобретения вектор AAV и комплементарный ген(ы) упаковки, если таковые имеются, предусмотрены в виде бактериальных плазмид, частиц AAV или любой их комбинации. Согласно другим вариантам осуществления либо последовательность вектора AAV, ген(ы) упаковки, либо и то и другое представлены в виде генетически измененных (предпочтительно измененных с возможностью передаваться по наследству) эукариотических клеток. Развитие клеток-хозяев, измененное с возможностью передаваться по наследству, чтобы экспрессировать векторную последовательность AAV, упаковочные гены AAV или и то и другое, включает установленный источник материала, который экспрессируется на надежном уровне.
Множество различных генетически измененных клеток может быть, таким образом, использовано в контексте настоящего изобретения. В качестве иллюстрации, клетка-хозяин млекопитающих может быть использована по меньшей мере с одной интактной копией стабильно интегрированного вектора rAAV. Упаковочная плазмида AAV, содержащая по меньшей мере ген rep AAV, функционально связанный с промотором, может быть использована для обеспечения функции репликации (как описано в патенте США №5658776). Кроме того, стабильная клеточная линия млекопитающих с геном rep AAV, функционально связанным с промотором, может быть использована для обеспечения функции репликации (смотрите, например, Trempe et al., WO 95/13392); Burstein et al. (WO 98/23018) и Johnson et al. (США №5656785). Ген cap AAV, обеспечивающий инкапсулирование белков, как описано выше, может быть предусмотрен вместе с геном rep AAV или отдельно (смотрите, например, упомянутые выше заявки и патенты, а также Allen et al. (WO 98/27204). Другие комбинации возможны и включены в объем настоящего изобретения.
Пути доставки
Несмотря на огромную сеть мозговой сосудистой системы, системная доставка лекарственных средств к центральной нервной системе (ЦНС) не эффективна для более, чем 98% малых молекул и почти 100% крупных молекул (Partridge, 2005). Отсутствие эффективности обусловлено наличием гематоэнцефалического барьера (ГЭБ), который предотвращает поступление в головной мозг из циркулирующей крови большинства посторонних веществ, даже многих полезных лекарственных средств. В то время как некоторые низкомолекулярные, пептидные и белковые терапевтические средства, получаемые системно, достигают паренхимы головного мозга, пересекая ГЭБ (Banks, 2008), как правило, необходимы высокие системные дозы для достижения терапевтического содержания, что может привести к неблагоприятным последствиям в организме. Лекарственные средства могут быть введены непосредственно в ЦНС путем интрацеребровентрикулярных или интрапаренхимальных инъекций. Интраназальная доставка обходит ГЭБ и направляет лекарственные средства непосредственно к ЦНС, используя пути по обонятельным и тройничным нервам, иннервирующим носовые проходы (Frey II, 2002; Thorne et al., 2004; Dhanda et al., 2005).
Может быть использован любой путь введения rAAV при условии, что этот путь и вводимое количество представляет собой профилактически или терапевтически полезное. В одном примере пути введения в ЦНС включают в себя интратекальный и интракраниальный пути. Интракраниальное введение может осуществляться в мостомозжечковую цистерну или желудочек. Термин "мостомозжечковая цистерна" предназначен для включения доступа к пространству вокруг и ниже мозжечка через отверстие между черепом и верхней частью позвоночника. Термин "желудочек головного мозга" предназначен для включения полостей в головном мозге, которые непрерывно связаны с центральным каналом спинного мозга. Интракраниальное введение осуществляется путем инъекции или инфузии, и подходящие диапазоны доз для внутричерепного введения, как правило, варьируют в диапазоне приблизительно от 103 до 1015 инфекционных единиц вирусного вектора на микролитр, поставляемый в дозе от 1 до 3000 мкл одного объема инъекции. Например, вирусные геномы или инфекционные единицы вектора на микролитр, как правило, содержат приблизительно 104, 105, 106, 107, 108, 109, 1010, 1011, 1012, 1013 или 1014 вирусных геномов или инфекционных единиц вирусного вектора, доставляемых приблизительно в 10, 50, 100, 200, 500, 1000 или 2000 мкл. Следует понимать, что вышеупомянутая дозировка представляет собой лишь иллюстративную дозировку, и специалистам в настоящей области техники будет понятно, что эта дозировка может варьировать. Эффективные дозы могут быть экстраполированы из кривых доза-чувствительность, полученных из тест-систем in vitro или in vivo.
AAV, доставляемый интратекальными способами лечения согласно настоящему изобретению, может быть введен любым удобным путем, обычно используемым для интратекального введения. Например, интратекальное введение может осуществляться путем медленной инфузии состава в течение приблизительно часа. Интратекальное введения осуществляется путем инъекции или инфузии, и применимый диапазон доз для интратекального введения, как правило, варьирует от 103 до 1015 инфекционных единиц вирусного вектора на микролитр, поставляемые, например, в объеме от 1 до 3000 микролитров или от 0,5 до 15 миллилитров вводимого объема. Например, вирусные геномы или инфекционные единицы вектора на микролитр, как правило, будут содержать приблизительно 104, 105, 106, 107, 108, 109, 1010, 1011, 1012, 1013 или 1014 вирусных геномов или инфекционных единиц вирусного вектора.
Терапия, если экспрессируется такой связанный с накоплениями лизосомальный фермент, как IDUA, приводит к нормализации лизосомальных гранул накопления в нейрональной ткани и/или ткани мозговых оболочек субъектов, как описано выше. Предполагается, что отложение гранул накопления уменьшается в нейронах и ткани глии, тем самым уменьшая задержку развития и регрессию, наблюдаемую у людей, страдающих от лизосомальной болезни накопления. Другие эффекты терапии могут включать в себя нормализацию лизосомальных гранул накопления в оболочках головного мозга возле арахноидальной грануляции, присутствие которых при лизосомальной болезни накопления приводит к гидроцефалии высокого давления. Способы согласно настоящему изобретению также могут быть использованы при лечении компрессии спинного мозга, которая представляет собой результат наличия лизосомальных гранул накопления в оболочках шейного отдела возле позвоночника в положении С1-С5 или в другом месте в спинном мозге. Способы согласно настоящему изобретению также направлены на лечение кист, которые вызваны периваскулярным накоплением лизосомальных гранул накопления вокруг сосудов головного мозга. Согласно другим вариантам осуществления терапия также может преимущественно приводить к нормализации объема печени и экскреции гликозаминогликанов с мочой, уменьшению размера селезенки и апноэ/гипопноэ событий, увеличению роста и скорости роста в препубертатном возрасте субъектов, увеличению сгибания плеча и разгибания локтя и колена и снижению трикуспидальной регургитации или легочной регургитации.
Интратекальное введение согласно настоящему изобретению может включать введение композиции в поясничную область. Любое такое введение может осуществляться путем болюсной инъекции. В зависимости от тяжести симптомов и восприимчивости субъекта к терапии, болюсную инъекцию можно вводить один раз в неделю, раз в месяц, раз в 6 месяцев или раз в год. Согласно другим вариантам осуществления интратекальное введение достигается путем использования инфузионного насоса. Специалистам в настоящей области техники известны устройства, которые могут быть использованы для осуществления интратекального введения композиции. Композиция может быть введена интратекально, например, путем однократной инъекции или путем непрерывной инфузии. Следует понимать, что дозированное лечение может осуществляться в виде однократного введения дозы или многократных доз.
Используемый в настоящем документе термин "интратекальное введение" предназначен для включения доставки фармацевтической композиции непосредственно в спинномозговую жидкость субъекта с помощью техник, включающих в себя инъекцию в боковые желудочки головного мозга через трепанационное отверстие или путем цистернальной или люмбальной пункции или т.п. Термин "поясничная область" предназначен для включения области между третьим и четвертым поясничными (нижняя часть спины) позвонками и, более конкретно, области L2-S1 позвоночника.
Введение композиции в соответствии с настоящим изобретением в любое из указанных выше мест может быть достигнуто путем прямой инъекции композиции или с применением инфузионных насосов. Для инъекции композиция может быть составлена в жидких растворах, например, в физиологически совместимых буферах, таких как раствор Хэнкса, раствор Рингера или фосфатный буфер. Кроме того, фермент может быть составлен в твердой форме и повторно растворен или суспендирован непосредственно перед использованием. Лиофилизированные формы также включены. Инъекции могут осуществляться, например, путем болюсной инъекции или непрерывной инфузии (например, с использованием инфузионных насосов) фермента.
Согласно одному варианту осуществления настоящего изобретения rAAV вводят путем инъекции в боковые желудочки головного мозга субъекта. Инъекция может быть выполнена, например, через выполненное в черепе субъекта трепанационное отверстие. Согласно другому варианту осуществления фермент и/или другой фармацевтический состав вводят через шунт, хирургически вставленный в желудочек головного мозга субъекта. Например, могут быть сделаны инъекции в боковые желудочки, которые больше, хотя также могут быть сделаны инъекции в третий и четвертый желудочки меньшего размера. Согласно еще одному варианту осуществления используемые в настоящем изобретении композиции вводят с помощью инъекции в мостомозжечковую цистерну или поясничную область субъекта.
Хотя точные механизмы, лежащие в основе интраназальной доставки лекарственных средств в ЦНС, не полностью понятны, накопленный объем данных показывает, что важны пути, включающие в себя нервы, соединяющие носовые проходы с головным мозгом и спинным мозгом. Кроме того, пути, включающие в себя сосудистую систему, спинномозговую жидкость и лимфатическую систему, были вовлечены в транспорт молекул из носовой полости в ЦНС. Вполне вероятно, что ответственно за это сочетание указанных путей, хотя один путь может преобладать, в зависимости от свойств используемого лекарственного средства, характеристик состава и устройства доставки.
Лекарственные средства могут быстро получить доступ к ЦНС после интраназального введения через пути обонятельного нерва, ведущие из носовой полости непосредственно к ЦНС. Пути обонятельного нерва представляют собой основной компонент интраназальной доставки, о чем свидетельствует тот факт, что флуоресцентно меченые вещества связаны с обонятельными нервами, поскольку они проходят решетчатую пластину (Jansson et al., 2002), концентрации лекарственных средств в обонятельных луковицах, как правило, одни из самых высоких из наблюдаемых концентраций в ЦНС (Thorne et al., 2004; Banks et al., 2004; Graff et al., 2005a); Nonaka et al., 2008; Ross et al., 2004; Ross et al., 2008; Thorne et al., 2008), и существует сильная, положительная корреляция между концентрациями в обонятельном эпителии и обонятельных луковицах (Dhuria et al., 2009а).
Обонятельные пути восходят в верхней части носовых проходов, в обонятельной области, где обонятельные рецепторные нейроны (ORN) перемежаются поддерживающими клетками, микровиллярными клетками и базальными клетками. ORN опосредуют обоняние путем передачи сенсорной информации от периферийного окружения в ЦНС (Clerico et al., 2003). Под эпителием собственная пластинка слизистой оболочки содержит слизь секретирующих желез Боумена, аксоны, кровеносные сосуды, лимфатические сосуды и соединительную ткань. Дендриты ORN распространяются в слизистый слой обонятельного эпителия, в то время как аксоны этих биполярных нейронов распространяются по направлению к центру через собственную пластинку слизистой оболочки и через отверстия в решетчатой пластинке решетчатой кости, которая отделяет носовую и черепную полости. Аксоны ORN проходят через субарахноидальное пространство, содержащее ЦСЖ, и останавливаются на митральных клетках в обонятельных луковицах. Оттуда нейронные проекции распространяются к нескольким областям головного мозга, включая в себя обонятельный тракт, переднее обонятельное ядро, грушевидную кору, миндалину и гипоталамус (Buck, 2000). В дополнение к ORN хемосенсорные нейроны, расположенные в переднем отделе дистальной части носовой полости в ганглии Грюнеберг, ведут к обонятельным луковицам (Fuss et al., 2005; Koos et al., 2005).
Уникальные характеристики ORN способствуют динамическому клеточному окружению для критической интраназальной доставки в ЦНС. Из-за прямого контакта с токсинами во внешней окружающей среде ORN регенерируют каждые 3-4 недели из базальных клеток, находящихся в обонятельном эпителии (Mackay-Sim, 2003). Специальные подобные клеткам Шванна клетки, называемые обонятельные оболочечные клетки (ООК), окружают аксоны ORN и играют важную роль в регенерации, отрастании и ремиелинизации аксонов (Field et al., 2003; Li et al., 2005a; Li et al., 2005b). ООК создают непрерывные, заполненные жидкостью периневральные каналы, которые, что интересно, остаются открытыми, несмотря на дегенерацию и регенерацию ORN (Williams et al., 2004).
Учитывая уникальную среду обонятельного эпителия, для интраназально введенных лекарственных средств существует возможность достичь ЦНС с помощью внеклеточных или внутриклеточных механизмов транспорта вдоль обонятельных нервов. Внеклеточные транспортные механизмы включают в себя быстрое движение молекул между клетками в назальном эпителии, занимая у лекарственного средства всего от нескольких минут до 30 минут для досжения обонятельных луковиц и других областей ЦНС после интраназального введения (Frey II, 2002; Balin et al., 1986). Транспорт, вероятно, включает в себя механизмы массового передвижения (Thorne et al., 2004; Thorne et al., 2001) в каналах, созданных с помощью ООК. Лекарственные средства могут также продвигаться в этих каналах с помощью структурных изменений, которые происходят во время деполяризации и аксонального распространения потенциала действия в соседних аксонах (Luzzati et al., 2004). Внутриклеточные механизмы транспорта включают в себя захват молекул в ORN путем пассивной диффузии, опосредованного рецепторами эндоцитоза или адсорбционного эндоцитоза, с последующим более медленным аксональным транспортом, занимающим у лекарственного средства от нескольких часов до нескольких дней для появления в обонятельных луковицах и других областях мозга (Baker et al., 1986; Broadwell et al., 1985; Kristensson et al., 1971). Внутриклеточный транспорт в ORN был продемонстрирован для малых, липофильных молекул, таких как частицы золота (de Lorenzo, 1970; Gopinath et al., 1978), соли алюминия (Perl et al., 1987), а также для веществ с рецепторами на ORN, таких как WGA-HRP (Thorne et al., 1995; Baker et al., 1986; Itaya et al., 1986; Shipley, 1985). Внутриклеточные механизмы, несмотря на то, что они важны для некоторых лекарственных средств, не могут быть преобладающим видом транспорта в ЦНС. В то время как некоторые крупные молекулы, такие как подобный галанину пептид (GALP), проявляют насыщаемые транспортные пути в ЦНС (Nonaka et al., 2008), для других крупных молекул, таких как NGF и инсулиноподобный фактор роста-I (IGF-I), интраназальная доставка в головной мозг нененасыщаема и опосредована не рецептором (Thorne et al., 2004; Chen et al., 1998; Zhao et al., 2004).
Часто упускаемый из виду, но важный путь, соединяющий носовые проходы с ЦНС, включает в себя тройничный нерв, который иннервирует респираторный и обонятельный эпителии носовых ходов и входит в ЦНС в варолиевом мосте (Clerico et al., 2003; Graff et al., 2003). Интересно, что небольшая часть тройничного нерва также заканчивается в обонятельных луковицах (Schaefer et al., 2002). Клеточный состав респираторной области носовых ходов отличается от обонятельной области с реснитчатыми эпителиальными клетками, распределенными среди слизи секретирующих бокаловидных клеток. Эти клетки способствуют мукоцилиарным механизмам очистки, которые удаляют слизь вместе с чужеродными веществами из полости носа в носоглотку. Тройничный нерв передает сенсорную информацию от носовой полости, ротовой полости, век и роговицы в ЦНС через глазничную ветвь (V1), верхнечелюстную ветвь (V2) или нижнечелюстную ветвь (V3) тройничного нерва (Clerico et al., 2003; Gray, 1978). Ветви от глазничной ветви тройничного нерва обеспечивают иннервацию задней слизистой оболочки носа и передней части носа, в то время как ветви верхнечелюстной ветви обеспечивают иннервацию боковых стенок слизистой оболочки носа. Нижнечелюстная ветвь тройничного нерва простирается до нижней челюсти и зубов без прямых нервных входов в полость носа. Три ветви тройничного нерва приходят вместе к тройничному ганглию и продолжаются к центру до входа в головной мозг на уровне варолиевого моста, заканчиваясь в спинномозговых тройничных ядрах в стволе мозга. Уникальная особенность тройничного нерва заключается в том, что он входит в мозг от респираторного эпителия носовых ходов в двух местах: (1) через переднее рваное отверстие в области варолиевого моста и (2) через решетчатую пластинку решетчатой кости вблизи обонятельных луковиц, создавая точки входа, как в каудальную, так и ростральную области мозга после интраназального введения. Также вероятно, что другие нервы, которые иннервируют лицо и голову, например, лицевой нерв, или других сенсорные структуры в полости носа, такие как ганглий Грюнеберга, могут обеспечивать точки входа в ЦНС для интраназально применяемых лекарственных средств.
Традиционно, интраназальный путь введения был использован для доставки лекарственных средств в системную циркуляцию с помощью абсорбции в капиллярные кровеносные сосуды, лежащие под слизистой оболочкой носа. Слизистая оболочка носа высоко васкуляризована, получая свое кровоснабжение от ветвей верхнечелюстной, глазной и лицевой артерий, которые отходят от сонной артерии (Clerico et al., 2003; Cauna, 1982). Слизистая оболочка обонятельной области получает кровь от мелких ветвей глазной артерии, тогда как респираторная слизистая оболочка получает кровь от крупной артериальной ветви верхнечелюстной артерии (DeSesso, 1993). Относительная плотность кровеносных сосудов больше в респираторной слизистой оболочке, по сравнению с обонятельной слизистой оболочкой, делая вышеупомянутую область идеальным местом для поглощения в кровь (DeSesso, 1993). Сосудистая система в респираторной области содержит смесь сплошного и фенестрированного эндотелия (Grevers et al., 1987; Van Diest et al., 1979), позволяя как малым, так и большим молекулам входить в системное кровообращение после назального введения.
Доставка в ЦНС после абсорбции в системный кровоток и последующей транспортировки через ГЭБ возможна, особенно для малых, липофильных лекарственных средств, которые легче проникают в кровеносный поток и пересекают ГЭБ, по сравнению с крупными, гидрофильными лекарственными средствами, такими как пептиды и белки.
Появляющееся все большее количество доказательств предполагает, что механизмы, включающие в себя каналы, связанные с кровеносными сосудами, или периваскулярные каналы, участвуют в интраназальной доставке лекарственных средств в ЦНС. Периваскулярные пространства связаны наружным слоем кровеносных сосудов и базальной мембраной окружающей ткани (Pollock et al., 1997). Эти периваскулярные пространства выступают в качестве лимфатической системы для головного мозга, где полученные из нейронов вещества выводятся из межклеточной жидкости головного мозга путем входа в периваскулярные каналы, связанные с кровеносными сосудами головного мозга. Периваскулярный транспорт происходит благодаря механизмам объемного потока, в отличие от одиночной диффузии (Cserr et al., 1981; Groothuis et al., 2007), и артериальные пульсации представляют собой также движущую силу для периваскулярного транспорта (Rennels et al., 1985; Rennels et al., 1985). Применяемые интраназально лекарственные средства могут двигаться в периваскулярные пространства в носовых проходах или после достижения головного мозга, и широкое распределение, наблюдаемое в ЦНС, может быть связано с периваскулярными транспортными механизмами (Thorne et al., 2004).
Пути, соединяющие субарахноидальное пространство, содержащее цереброспинальную жидкость, периневральные пространства, охватывающие обонятельные нервы, и назальная лимфатическая система важны для дренажа ЦСЖ и эти же пути обеспечивают доступ для применяемых интраназально лекарственных средств к ЦСЖ и другим областям ЦНС. Несколько исследований свидетельствуют о том, что меченые вещества, введенные в спинномозговую жидкость в желудочках мозга или субарахноидальное пространство перетекают к нижней стороне обонятельных луковиц в каналы, связанные с обонятельными нервами, проходящими решетчатую пластинку решетчатой кости, и достигают назальной лимфатической системы и шейных лимфатических узлов (Bradbury et al., 1983; Hatterer et al., 2006; Johnston et al., 2004a); Kida et al., 1993; Walter et al., 2006a; Walter et al., 2006b). Лекарственные средства могут получить доступ к ЦНС с помощью этих же путей после интраназального введения, двигаясь из носовых ходов к спинномозговой жидкости к интерстициальным пространствам и периваскулярным пространствам головного мозга для распространения по всему головному мозгу. Эти дренажные пути характеризуются важным значением для ряда видов животных (овцы, кролики и крысы), составляя приблизительно 50% очищения ЦСЖ (Bradbury et al., 1981; Boulton et al., 1999; Boulton et al., 1996; Cserr et al., 1992). Пути между носовыми проходами и ЦСЖ все еще важны и функциональны у людей, о чем свидетельствует тот факт, что лекарственные средства доставляются в ЦСЖ после интраназальной доставки, не проникая в существенной степени в кровь (Born et al., 2002). Ряд интраназальных исследований показывает, что лекарственные средства получают прямой доступ к ЦСЖ из носовой полости с последующим распределением к головному и спинному мозгу. Многие применяемые интраназально молекулы быстро проникают в ЦСЖ, и этот транспорт зависит от липофильности, молекулярной массы и степени ионизации молекул (Dhanda et al., 2005; Born et al., 2002; Kumar et al., 1974; Sakane et al., 1995; Sakane et al, 1994; Wang et al., 2007). Оценка распределения в ЦСЖ может предоставить информацию о механизме интраназальной доставки.
Оптимальная доставка к ЦНС по нервным путям связана с доставкой средства к верхней трети носовой полости (Hanson et al., 2008). Хотя может быть использовано положение "лежа на спине", другое положение для направленного воздействия на обонятельную область представляет собой позу "молящегося Мекке" с положением головы вниз и вперед. Лежачее положение на спине с углом головы в 70° или 90° может быть пригодным для эффективной доставки к ЦСЖ с использованием трубки, вставленной в ноздри, чтобы доставить лекарство путем интраназального введения (van den Berg et al., (2002)).
Для интраназального введения лекарственного средства капли в нос можно вводить в течение 10-20 минут попеременно в каждую ноздрю каждые 1-2 минут, чтобы позволить раствору всасываться в назальный эпителий (Thorne et al., 2004; Capsoni et al., 2002; Ross et al., 2004; Ross et al., 2008; Dhuria et al., 2009a; Dhuria et al., 2009b; Francis et al., 2008; Martinez et al., 2008). Этот неинвазивный способ не предполагает установки устройства в ноздрю. Вместо этого, капли помещаются в отверстии ноздри, что позволяет человеку вдыхать каплю в носовую полость. Другие способы введения анестизированному индивидууму включают в себя герметизацию пищевода и вставку дыхательной трубки в трахею, чтобы предотвратить проглатывание назального состава и устранить проблемы, связанные с дыхательной недостаточностью (Chow et al., 1999; Chow et al., 2001; Fliedner et al., 2006; Dahlin et al., 2001). Гибкая трубка может быть вставлена в ноздри для локализованной доставки небольшого объема лекарственной раствора к респираторному или обонятельному эпителию, в зависимости от длины трубка (Chow et al., 1999; Van den Berg et al., 2003; van den Berg et al., 2004a; Banks et al., 2004; van den Berg et al., 2002; Vyas et al., 2006a; Charlton et al., 2007a; Gao et al., 2007a).
Назальные устройства доставки, такие как спреи, назальные капельницы или шприцы без игл, могут быть использованы для направленного воздействия средства на различные области носовой полости. OptiMist™ представляет собой активируемое вдохом устройство, которое направляет жидкие или порошкообразные назальные составы в носовую полость, включая в себя обонятельную область, без осаждения в легких или пищеводе (Djupesland et al., 2006). Устройство ViaNase™ также может быть использовано для направленного воздействия назального спрея на обонятельный и респираторный эпителий носовой полости. Носовые капли, как правило, оседают на дно носовой полости и подвергаются быстрому мукоцилиарному клиренсу, в то время как назальные спреи распределяются в средней части носового хода слизистой оболочки носа (Scheibe et al., 2008).
Иммунносупрессанты или вызывающие иммуннологическую толерантность средства могут быть введены любым путем, включающим в себя парентеральный. Согласно одному варианту осуществления иммунносупрессант или вызывающее иммуннологическую толерантность средство можно вводить с помощью подкожной, внутримышечной или внутривенной инъекции, перорально, интратекально, интракраниально или интраназально, или путем замедленного высвобождения, например, с использованием подкожного имплантата. Иммунносупрессант или вызывающее иммуннологическую толерантность средство может быть растворено или диспергировано в жидком носителе. Для парентерального введения активный материал может быть подходящим образом смешан с приемлемым носителем, например, с растительным маслом, таким как арахисовое масло, хлопковое масло и т.п. Также могут быть использованы другие парентеральные носители, такие как органические композиции с использованием солкеталя, глицерина, формаля и водных парентеральных составов. Для парентерального применения путем инъекции композиции могут содержать водный раствор водорастворимой фармацевтически приемлемой соли активных кислот согласно настоящему изобретению, предпочтительно в концентрации 0,01-10% и, необязательно, также стабилизирующее средство и/или буферные вещества в водном растворе. Дозированные единицы раствора могут быть преимущественно заключены в ампулы.
Композиция, например, содержащая rAAV композиция, содержащая иммунносупрессант композиция или вызывающая иммунологическую толерантность композиция, может быть в форме инъекционной единичной дозы. Примеры носителей или разбавителей, подходящие для приготовления таких инъекционных доз, включают в себя такие разбавители, как воду, этиловый спирт, макрогол, пропиленгликоль, этоксилированный изостеариловый спирт, полиоксиизостеариловый спирт и эфиры жирных кислот полиоксиэтиленсорбитана, такие регулирующие рН средства или буферы, как цитрат натрия, ацетат натрия и фосфат натрия, такие стабилизаторы, как пиросульфит натрия, ЭДТА, тиогликолевая кислота и тиомолочная кислота, такие изотонические средства, как хлорид натрия и глюкоза, такие местных анестетики, как прокаина гидрохлорид и лидокаина гидрохлорид. Кроме могут быть добавлены обычные солюбилизирующие средства и анальгетики. Инъекции могут быть приготовлены путем добавления таких носителей к ферменту или другим биологически активным соединениям после процедур, хорошо известных специалистам в настоящей области техники. Подробное обсуждение фармацевтически приемлемых вспомогательных веществ доступно в REMINGTON'S PHARMACEUTICAL SCIENCES (Mack Pub. Co., N.J. 1991). Фармацевтически приемлемые составы могут быть легко суспендированы в водных наполнителях и введены с помощью обычных игл для подкожных инъекций или с использованием инфузионных насосов. Перед введением составы могут быть стерилизованы, предпочтительно с помощью гамма-излучения или электронным пучком.
Когда иммунносупрессант или вызывающее иммуннологическую толерантность средство вводят в виде подкожного импланта, соединение суспендируют или растворяют в медленно диспергируемом материале, известном специалистам в настоящей области техники, или вводят в устройство, которое медленно высвобождает активное вещество путем использования постоянной движущей силы, такой как осмотический насос. В таких случаях возможно введение в течение длительного периода времени.
Дозировка, в которой вводят композицию, содержащую иммунносупрессант или вызывающее иммуннологическую толерантность средство, может варьировать в широком диапазоне и будет зависеть от различных факторов, таких как тяжесть заболевания, возраст пациента и т.д., и, возможно, будет нуждаться в индивидуальной корректировке. Возможный диапазон количества, которое может быть введено в день, составляет приблизительно от 0,1 мг до 2000 мг или приблизительно от 1 мг до 2000 мг. Композиции, содержащие иммунносупрессант или вызывающее иммунную толерантность средство, соответственно могут быть составлены таким образом, чтобы они обеспечивали дозы в указанных пределах, либо в виде отдельных дозированных единиц, либо в виде многократных дозированных единиц. В дополнение к иммунносупрессанту рассматриваемые составы могут содержать один или несколько кодирующих rAAV терапевтических генных продуктов.
Описанные в настоящем документе композиции могут быть использованы в комбинации с другим лекарственным средством. Композиции могут появляться в обычных формах, например, аэрозолях, растворах, суспензиях или для местного применения, или в лиофилизированной форме.
Типичные композиции включают в себя rAAV, иммунносупрессант, усилитель проницаемости или их комбинацию, и фармацевтически приемлемое вспомогательное вещество, которое может представлять собой носитель или разбавитель. Например, активное средство(а) может быть смешано с носителем или разбавлено носителем, или заключено в носитель. Когда активное средство смешивают с носителем или когда носитель служит разбавителем, он может представлять собой твердый, полутвердый или жидкий материал, который выступает в роли наполнителя, вспомогательного вещества или среды для активного средства. Некоторые примеры подходящих носителей представляют собой воду, растворы солей, спирты, полиэтиленгликоли, полигидроксиэтоксилированное касторовое масло, арахисовое масло, оливковое масло, желатин, лактозу, каолин, сахарозу, декстрин, карбонат магния, сахар, циклодекстрин, амилозу, стеарат магния, тальк, желатин, агар, пектин, аравийскую камедь, стеариновую кислоту или низшие алкиловые эфиры целлюлозы, кремниевую кислоту, жирные кислоты, амины жирных кислот, моноглицериды и диглицериды жирных кислот, сложные эфиры пентаэритрита жирных кислот, полиоксиэтилен, гидроксиметилцеллюлозу и поливинилпирролидон. Аналогично, носитель или разбавитель может включать в себя любой материал с замедленным высвобождением, известный в настоящей области техники, такой как глицерилмоностеарат или глицерилдистеарат, отдельно или в смеси с воском.
Составы могут быть смешаны со вспомогательными средствами, которые не реагируют вредным образом с активным средством(ами). Такие добавки могут включать в себя смачивающие средства, эмульгаторы и суспендирующие средства, соли для воздействия на осмотическое давление, буферы и/или красители, консерванты, подсластители или ароматизаторы. Композиции также могут быть стерилизованы при необходимости.
Если используется жидкий носитель, препарат может быть в форме жидкости, такой как водная жидкая суспензия или раствор. Приемлемые растворители или носители включают в себя стерильную воду, раствор Рингера или изотонический водный раствор соли.
Средство(а) может быть представлено в виде порошка, пригодного для восстановления с соответствующим раствором, как описано выше. Примеры этого включают в себя без ограничения высушенные вымораживанием, высушенные в барабанной сушке или высушенные распылением порошки, аморфные порошки, гранулы, преципитаты или частицы. Композиция может необязательно содержать стабилизаторы, модификаторы рН, поверхностно-активные вещества, модификаторы биодоступности и их комбинации. Форма дозированной единицы может представлять собой отдельные контейнеры или многодозовые контейнеры.
Рассматриваемые в настоящем изобретении композиции могут включать в себя, например, мицеллы или липосомы или какую-либо другую инкапсулированную форму, или могут быть введены в форме пролонгированного высвобождения, чтобы обеспечить эффект длительного накопления и/или доставки, например, с использованием биоразлагаемых полимеров, например, полилактид-полигликолида. Примеры других биоразлагаемых полимеров включают в себя поли(ортоэфиры) и поли(ангидриды).
Полимерные наночастицы, например, состоящие из гидрофобного ядра полимолочной кислоты (PLA) и гидрофильной оболочки метокси-поли (этиленгликоля) (MPEG), могут характеризоваться улучшенной растворимостью и направленным воздействием на ЦНС. Региональные различия в направленном воздействии между микроэмульсией и составами наночастиц могут быть из-за различий в размере частиц.
Липосомы представляют собой очень простые структуры, состоящие из одного или нескольких липидных бислоев амфифильных липидов, т.е. фосфолипидов или холестерина. Липофильный фрагмент бислоев повернут по отношению один к другому и создает внутреннюю гидрофобную среду в мембране. Липосомы представляют собой подходящие носители лекарственных средств для некоторых липофильных лекарственных средств, которые могут быть связаны с неполярными частями липидных бислоев, если они соответствуют по размеру и геометрии. Размер липосом варьирует от 20 нм до нескольких мкм.
Смешанные мицеллы представляют собой эффективные содержащие поверхностно активные вещества структуры, которые состоят из солей желчных кислот, фосфолипидов, три-, ди- и моноглицеридов, жирных кислот, свободного холестерина и жирорастворимых питательных микроэлементов. Поскольку длинноцепочечные фосфолипиды, как известно, образуют двойные слои при диспергировании в воде, предпочтительная фаза короткоцепочечных аналогов представляет собой сферическую мицеллярную фазу. Мицеллярный раствор представляет собой термодинамически стабильную систему, образованную самопроизвольно в воде и органических растворителях. Взаимодействие между мицеллами и гидрофобными/липофильными лекарственными средствами приводит к образованию смешанных мицелл (СМ), которые часто также называют набухшими мицеллами. В человеческом организме они заключают в себя гидрофобные соединения с низкой растворимостью в воде и выступают в роли резервуара для продуктов пищеварения, например, моноглицеридов.
Липидные микрочастицы включает в себя липидные нано- и микросферы. Микросферы, как правило, определяются как небольшие сферические частицы, полученные из любого материала, которые характеризуются размерами от приблизительно 0,2 до 100 мкм. Сферы меньшего размера до 200 нм, как правило, называют наносферы. Липидные микросферы представляют собой однородные микроэмульсии масло/вода, подобные коммерчески доступным жировым эмульсиям, и их получают с помощью процедуры интенсивной обработки ультразвуком или способов эмульгирования высоким давлением (способы шлифования). Естественное поверхностно-активное вещество лецитин снижает поверхностное натяжение жидкости, таким образом, действуя как эмульгатор, с образованием стабильной эмульсии. Структура и состав липидных наносфер похож на таковой липидных микросфер, но с меньшим диаметром.
Полимерные наночастицы служат в качестве носителей для широкого разнообразия ингредиентов. Активные компоненты могут быть либо растворены в полимерном матриксе, либо захвачены или адсорбированы на поверхности частиц. Полимеры, применимые для получения органических наночастиц, включают в себя производные целлюлозы и такие сложные полиэфиры, как поли(молочная кислота), поли(гликолевая кислота) и их сополимер. Из-за их небольшого размера, их большого соотношения площади поверхности/объема и возможности функционализации интерфейса, полимерные наночастицы представляют собой идеальные носители и системы высвобождения. Если размер частиц менее 50 нм, они больше не распознаются в качестве частиц многими биологическими, а также синтетическими барьерными слоями, но действуют подобно молекулярно дисперсным системам.
Таким образом, композиция согласно настоящему изобретению может быть составлена, чтобы обеспечить быстрое, пролонгированное, контролируемое или замедленное высвобождение или любую комбинацию высвобождений активного средства после введения индивидууму с использованием процедур, хорошо известных в настоящей области техники. Согласно одному варианту осуществления фермент находится в изотоническом или гипотоническом растворе. Согласно одному варианту осуществления для ферментов, которые не растворимы в воде, может быть использовано основанное на липидах средство доставки, например, такая микроэмульсия, как описана в WO 2008/049588, раскрытие которой включено в настоящий документ посредством ссылки, или липосомы.
Согласно одному варианту осуществления препарат может содержать средство, растворенное или суспендированное в жидком носителе, таком как водный носитель, для аэрозольного применения. Носитель может содержать добавки, такие как солюбилизирующие средства, например, пропиленгликоль, поверхностно-активные вещества, усилители абсорбции, такие как лецитин (фосфатидилхолин) или циклодекстрин, или консерванты, такие как парабены. Например, в дополнение к растворимости, эффективная доставка в ЦНС после интраназального введения может зависеть от проницаемости мембраны. Для ферментов, где парацеллюлярный транспорт затруднен из-за размера и полярности, повышение проницаемости мембран может улучшить внеклеточные механизмы транспорта в ЦНС по обонятельному и тройничному нерву. Один из подходов к модификации проницаемости мембраны в назальном эпителии заключается в использовании таких усилителей проницаемости, как поверхностно-активные вещества, например, лауроилкарнитин (LC), соли желчных кислот, липиды, циклодекстрины, полимеры или модификаторов плотных контактов.
Как правило, активные средства распределяют на единичные дозированные формы, включающие в себя активный ингредиент вместе с фармацевтически приемлемым носителем на единичную дозу. Как правило, дозированные формы, подходящие для назального введения, включают в себя приблизительно от 125 мкг до приблизительно 125 мг, например, от приблизительно 250 мкг до приблизительно 50 мг или от приблизительно 2,5 мг до приблизительно 25 мг соединений в смеси с фармацевтически приемлемым носителем или разбавителем.
Дозированные формы могут быть введены один раз в день или чаще, чем один раз в день, например, два или три раза в день. Альтернативно, дозированные формы могут быть введены реже, чем каждый день, например, через день или раз в неделю, если лечащим врачом установлена целесообразность.
Настоящее изобретение будет описано с помощью следующих неограничивающих примеров.
ПРИМЕРЫ
Пример I
Опосредованная вектором AAV доставка генов идуронидазы в мышиной модели мукополисахаридоза типа I: сравнение различных путей доставки к ЦНС
Мукополисахаридоз типа I (MPS I) представляет собой наследственное нарушение обмена веществ, вызванное дефицитом лизосомального фермента альфа-L-идуронидазы (IDUA). Системное и ненормальное накопление гликозаминогликанов связано с задержкой роста, органомегалией, скелетной дисплазией и сердечно-легочными заболеваниями. Индивидуумы с наиболее тяжелой формой заболевания (синдром Гурлера) страдают от нейродегенерации, умственной отсталости и ранней смерти. Два современных способы лечения MPS I (трансплантация гемопоэтических стволовых клеток и ферментная заместительная терапия) не могут эффективно лечить все проявления этого заболевания в центральной нервной системе (ЦНС).
Что касается генной терапии, ранее было показано, что внутрисосудистая доставка AAV-9 у взрослых мышей не добилась широкого прямого нейронального направленного воздействия (смотрите Foust et al, 2009). В предыдущей работе также показали, что прямая инъекция AAV8-IDUA в ЦНС взрослых дефицитных по IDUA мышей приводила к низкой частоте или слабому уровню экспрессии трансгена (смотрите фиг. 18). Следующие примеры, которые используют доклиническую модель для лечения MPS1, на удивление показывают, что прямая инъекция AAV9-IDUA в ЦНС иммунокомпетентных взрослых дефицитных по IDUA мышей приводила к экспрессии и активности фермента IDUA, которая представляет собой такую же или выше, чем экспрессия и активность фермента IDUA у взрослых мышей дикого типа (фиг. 15, ниже).
Способы
Получение AAV9-IDUA. Векторный конструкт AAV-IDUA (MCI) был описан ранее (Wolf et al., 2011) (промотор mCags). ДНК плазмиды AAV-IDUA упаковывали в вирионы AAV9 в векторное ядро университета Флориды, получая титр, равный 3×1013 векторных геномов на миллилитр.
Инфузии ICV Взрослых мышей Idua-/- анестезировали с использованием коктейля кетамина и ксилазина (100 мг кетамина + 10 мг ксилазина на кг) и помещали на стереотаксическую рамку. Десять мкл AAV9-IDUA вводили в правый боковой желудочек (стереотаксические координаты АР 0,4, ML 0,8, DV 2,4 мм от брегмы) с использованием шприца Гамильтона. Животных возвращали в их клетки на грелки для восстановления.
Интратекальные инфузии. Инфузии молодым взрослым мышам проводили путем инъекции 10 мкл содержащего вектор AAV раствора между L5 и L6 позвонками через 20 минут после внутривенной инъекции 0,2 мл 25% маннитола.
Иммунологическая толеризация. Новорожденным дефицитным по IDUA мышам вводили через лицевую височную вену 5 мкл раствора, содержащего 5,8 мкг рекомбинантного белка идуронидазы (альдуразима), и затем животных возвращали в клетки.
Иммуносупрессия циклофосфамидом. Для иммуносупрессии животным вводили циклофосфамид один раз в неделю в дозе 120 мг/кг, начиная через один день после инфузии вектора AAV9-IDUA.
Животные. Животных анестезировали кетамином/ксилазином (100 мг кетамина+10 мг ксилазина на кг) и осуществляли транскардиальную перфузию с помощью PBS в объеме 70 мл перед умерщвлением. Головной мозг собирали и подвергали микропрепарированию на льду на мозжечок, гиппокамп, стриатум, кору и ствол головного мозга/таламус ("остальная часть"). Образцы замораживали на сухом льду и хранили при -80°С. Образцы размораживали и гомогенизировали в 1 мл PBS с использованием автоматического растирания пестиком и пермеабилизировали путем добавления 0,1% раствора Тритон Х-100. Активность IDUA определяли с помощью флуориметрического анализа с использованием 4MU-идуронида в качестве субстрата. Активность выражают в единицах (процентах субстрата, превращенного в продукт в минуту) на мг белка, как определено с помощью анализа Бредфорда (BioRad).
Ткани. Гомогенаты тканей осветляли центрифугированием в течение 3 мин при 13000 оборотах в минуту с использованием настольной центрифуги Eppendorf модели 5415D (Eppendorf) и инкубировали в течение ночи с протеиназой К, ДНКазой1 и РНКазой. Концентрацию ГАГ определяли с использованием анализа сульфатированных гликозаминогликанов Blyscan (Accurate Chemical) в соответствии с инструкциями изготовителя.
Результаты
На фиг. 1 показаны результаты для дефицитных по идуронидазе мышей, которым вводили AAV либо интрацеребровентрикулярно (ICV), либо интратекально (IT). Для предотвращения иммунного ответа животных подвергали либо иммуносупрессии с циклофосфамидом (CP), иммунологической толеризации при рождении путем внутривенного введения белка идуронидазы человека (альдуразима), либо осуществляли инъекции NOD-SCID мышам с иммунодефицитом, которые также испытывали дефицит по идуронидазе. Животных умерщвляли в указанное время после воздействия и головной мозг подвергали микропрепарированию, и в экстрактах анализировали активность идуронидазы.
На фиг. 2 показаны данные для иммунодефицитных, дефицитных по IDUA животных, которым вводили ICV с вектором AAV-IDUA. Эти животные показали высокие уровни экспрессии IDUA (от 10 до 100 раз выше, чем у животных дикого типа) во всех областях головного мозга, с наибольшим уровнем, наблюдаемым в стволе головного мозга и таламусе ("остальная часть").
Подвергнутые иммуносупрессии животные, которым вводили вектор AAV путем ICV, характеризовались относительно низким содержанием фермента в головном мозге, по сравнению с животными с иммунодефицитом (фиг. 3). Обратите внимание, что иммуносупрессия может быть у этих животных аномальной, потому что CP был отменен за 2 недели до умерщвления из-за неудовлетворительного состояния здоровья.
На фиг. 4 показаны данные для иммуносупрессированных животных, которым вводили вектор AAV путем IT. Животные с иммунологической толерантностью, которым вводили вектор AAV путем ICV, проявляли широкую активность IDUA во всех частях головного мозга (фиг. 5), аналогично той, которая наблюдается у животных с иммунодефицитом, что свидетельствует об эффективности процедуры иммунологической толеризации.
Фиг. 6 представляет собой сведение всех средних уровней активности IDUA для сравнения, а фиг. 7 представляет собой данные, сгруппированные в соответствии с областью головного мозга.
Накопление ГАГ анализировали в различных отделах головного мозга для всех четырех исследуемых групп. Для каждой группы среднее каждой части головного мозга показано слева, значения для каждого отдельного животного показаны справа (фиг. 8). Животные с дефицитом IDUA (крайние слева) характеризовались высоким содержанием ГАГ по сравнению с животными дикого типа (пурпурный столбик). Содержание ГАГ было на уровне дикого типа или ниже, чем у животных дикого типа для всех участков головного мозга во всех группах обработанных AAV животных. Содержание ГАГ было небольшим, хотя не значительно выше, чем у животных дикого типа, в коре головного мозга и стволе головного мозга животных, которым вводили AAV9-IDUA интратекально.
Выводы
Результаты показывают высокое и широкое распространение IDUA в головном мозге независимо от пути доставки (ICV или IT), хотя экспрессия IDUA в стриатуме и гиппокампе была ниже у животных, которым вводили IT путем, по сравнению с ICV путем. Похоже, наблюдается иммунная реакция, так как мыши с иммуннодефицитом характеризуются более высокими уровнями экспрессии, чем иммунокомпетентные мыши. Что касается инъекции ICV, когда CP отменили рано, экспрессия IDUA была ниже. Кроме того, приобретение иммунологической толерантности было эффективным для восстановления высокой активности фермента. Также содержание ГАГ восстанавливалось до нормального во всех экспериментальных группах подвергнутых воздействию мышей.
Пример II
Способы
Получение AAV9IDUA. Плазмиды AAV-IDUA упаковывали в вирионы AAV9 либо в векторное ядро университета Флориды, либо в векторное ядро университета Пенсильвании, получая титр, равный 1-3×1013 векторных геномов на миллилитр.
Инфузии ICV. Смотрите пример I.
Интратекальные инфузии. Смотрите пример I.
Иммунологическая толеризация. Как и в примере I, за исключением следующего: для нескольких толеризаций новорожденным мышам с дефицитом IDUA вводили первую дозу альдуразима в лицевую височную вену с последующими 6 еженедельными инъекциями, вводимыми внутрибрюшинно.
Иммуносупрессия циклофосфамидом. Смотрите пример I.
Животные. Животных анестезировали кетамином/ксилазином (100 мг кетамина + 10 мг ксилазина на кг) и осуществляли транскардиальную перфузию с помощью PBS в объеме 70 мл перед умерщвлением. Головной мозг собирали и подвергали микропрепарированию на льду на мозжечек, гиппокамп, стриатум, кору и ствол головного мозга/таламус ("остальная часть"). Образцы замораживали на сухом льду и хранили при -80°С.
Активность IDUA тканей. Образцы тканей размораживали и гомогенизировали в физиологическом растворе в тканевом гомогенизаторе. Гомогенаты тканей осветляли центрифугированием при 15000 оборотах в минуту с использованием настольной центрифуги Eppendorf при 4°С в течение 15 мин. Тканевые лизаты (супернатант) собирали и в них анализировали активность IDUA и содержание накоплений ГАГ.
Содержание ГАГ в тканях. Тканевые лизаты инкубировали в течение ночи с протеиназой К, РНКазой и ДНКазой. Содержание ГАГ анализировали с использованием анализа сульфатированных гликозаминогликанов Blyscan (Accurate Chemical) в соответствии с инструкциями изготовителя.
Копии вектора IDUA. Гомогенаты тканей использовали для выделения ДНК и последующей количественной ПЦР, как описано в Wolf с соавт. (2011).
Результаты
На фиг. 9 показана постановка эксперимента и группы. Животным вводили вектор AAV9IDUA путем инфузии либо интрацеребровентрикулярно (ICV), либо интратекально (IT). Введение вектора проводили NOD-SCID мышам с иммунодефицитом (ID), которые характеризовались также дефицитом IDUA, или мышам с дефицитом IDUA, которых подвергали либо иммуносупрессии циклофосфамидом (CP), либо иммунологической толеризации при рождении с помощью одной или многократных инъекций белка идуронидазы человека (альдуразима). Время воздействия вектором и умерщвления соответствует показанному на фиг. 9. Все введения вектора проводили взрослым животным в возрасте от 3-4,5 месяцев. Животным вводили 10 мкл вектора в дозе 3×1011 векторных геномов на 10 мкл.
На фиг. 10 показана ферментативная активность IDUA у мышей с иммунодефицитом и дефицитом IDUA с интракраниальной инфузией. Высокие уровни активности фермента наблюдались во всех областях головного мозга, варьируя в диапазоне, который от 30 до 300 раз выше, чем уровень у животных дикого типа. Самая высокая экспрессия фермента наблюдалась в таламусе и стволе головного мозга, а также в гиппокампе.
Животные, которых подвергали интракраниальному введению и иммуносупрессии циклофосфамидом (CP), показали значительно более низкие уровни активности фермента по сравнению с другими группами (фиг. 11). Тем не менее, введение CP в данном случае пришлось отменить за 2 недели до умерщвления из-за неудовлетворительного состояния здоровья животных.
Содержание фермента IDUA у животных, толеризованных при рождении белком IDUA (альдуразимом) и подвергнутых интракраниальному введению вектора, показано на фиг. 12. Все животные показали высокое содержание фермента во всех частях головного мозга, которое варьировало в диапазоне, который от 10 до 1000 раз выше, чем содержание у животных дикого типа, схожее на содержание, достигаемое у животных с иммунодефицитом, указывая на эффективность процедуры иммунологической толеризации.
На фиг. 13 показано содержание фермента IDUA у мышей, которых подвергали интратекальному введению и вводили CP на еженедельной основе. Повышенное содержание IDUA наблюдали во всех частях головного мозга, особенно в мозжечке и спинном мозге. Содержание фермента было самым низким в стриатуме и гиппокампе с активностью на уровне животных дикого типа.
Мышей с дефицитом IDUA подвергали толеризации альдуразимом, как описано выше, и интратекальному введению вектора (фиг. 14). Наблюдалась повсеместная активность фермента IDUA во всех частях головного мозга, с самым высоким уровнем активности в стволе мозга и таламусе, обонятельной луковице, спинном мозге и мозжечке. Подобно данным на фиг. 13, самые низкие уровни активности фермента наблюдались в стриатуме, коре и гиппокампе.
Контрольным иммунокомпетентным животным с дефицитом IDUA проводили интратекальную инфузию вектора без иммуносупрессии или иммунологической толеризации (фиг. 15). Результаты показывают, что, хотя активность фермента была на уровне дикого типа или немного выше, содержание фермента было значительно ниже, чем наблюдалось у животных, подвергнутых иммуномодуляции. Снижение содержания фермента было особенно значительным в мозжечке, обонятельной луковице и таламусе, и стволе мозга, областях, которые экспрессировали самые высокие уровни фермента у животных, подвергнутых иммуномодуляции.
Животных исследовали на наличие вещества накопления ГАГ, как показано на фиг. 15. Все группы продемонстрировали очищение от накопления ГАГ, с содержанием ГАГ, близким к наблюдаемому у животных дикого типа. Животные, которые были подвергнуты иммуносупрессии и интратекальному введению вектора AAV-IDUA, характеризовались таким содержанием ГАГ в коре, которое было немного выше, чем у животных дикого типа, но по-прежнему значительно ниже, чем у мышей с дефицитом IDUA без воздействия.
Наличие вектора AAV9IDUA у животных, которые были подвергнуты иммунологической толеризации и либо интратекальному, либо интракраниальному введению вектора, оценивали с помощью количественной ПЦР, как показано на фиг. 16. Количество копий IDUA на клетку было выше у животных, подвергнутых интракраниальной инфузии, по сравнению с животными, подвергнутыми интратекальной инфузии, что согласуется с более высоким уровнем активности фермента, показанным у животных, подвергнутых интракраниальному введению.
Выводы
Высокое, распространенное и терапевтическое содержание IDUA наблюдалось во всех областях головного мозга после интрацеребровентрикулярного и интратекального пути введения AAV9IDUA у взрослых мышей. Активности ферментов восстанавливались до уровней у животных дикого типа или чуть выше у иммунокомпетентных животных с дефицитом IDUA, которые получали инфузию AAV-IDUA интратекально. Значительно более высокое содержание фермента IDUA наблюдалось для обоих путей инъекции вектора у животных, подвергнутых иммунологической толеризации, начиная с рождения путем введения белка IDUA.
Пример III
Взрослых иммунокомпетентных дефицитных по IDUA мышей (возраст 12 недель) анестезировали кетамином/ксилазином, а затем проводили интраназальную инфузию вектора AAV9IDUA. Вектор вводили путем внесения восьми капель по 3 мкл микропипеткой в интраназальную полость, чередуя ноздри, с 2-минутными интервалами между каждым внесением. В общей сложности каждому взрослому животному вводили 2,4-7×1011 векторных геномов, в зависимости от источника вектора. Животных иммуносупрессировали с помощью еженедельного введения 120 мг/кг циклофосфамида, начиная со следующего дня после введения вектора. Мышей умерщвляли через 12 недель после инфузии вектора, животных исследовали на экспрессию фермента IDUA и векторные копии в головном мозге.
Ссылки
Al-Ghananeem et al., AAPS Pharm. Sci. Tech., 3: E5 (2002).
Bagger et al., Eur. J. Pharm. Sci., 21: 235-242 (2004b).
Bagger et al., Int. J. Pharm., 269: 311-322 (2004a).
Baker et al., Exp. Brain Res., 63: 461 (1986).
Balin et al., J. Comp. Neurol., 251: 260-280 (1986).
Banks et al., J. Drug Target, 17: 91-97 (2009).
Banks et al., J. Pharmacol. Exp. Ther., 309: 469 (2004).
Banks, Biopolymers, 90: 589 (2008).
Barakat et al., J. Pharm. Pharmacol., 58: 63 (2006).
Barbier et al., Mol. Genet. Metab., 110: 303 (2013).
Baumgartner et al., Neuron., 58: 639 (2008).
Benedict et al., Neuroendocrinology, 86: 136 (2007b).
Benedict et al., Neuropsychopharmacology. 32: 239 (2007a).
Benedict et al., Psychoneuroendocrinology, 29: 1326 (2004).
Bjoraker et al., J. Dev. Behav. Ped., 27: 290 (2006).
Blits et al., J. Neuros. Methods, 185: 257 (2010).
Born et al., Nat. Neurosci., 5: 514 (2002).
Boulton et al., Am. J. Physiol., 276: R818 (1999).
Boulton et al., Neuropathol. Appl. Neurobiol., 22: 325 (1996).
Bradbury et al., Am. J. Physiol., 240: F329 (1981).
Bradbury et al., J. Physiol., 339: 519 (1983).
Brady, Ann. Rev. Med., 57: 283 (2006).
Broadwell et al., J. Comp. Neurol., 242: 632 (1985).
Broekman et al., Neuroscience, 138: 501 (2006).
Buck, In: Kandel ER, Schwartz JH, Jessell TM, editors. Principles of neural science. 4th edition. New York: McGraw-Hill Companies. pp. 625-652 (2000).
Buxer et al., J. Neurochem., 56: 1012 (1991).
Cai et al., Sichuan Da Xue Xue Bao Yi Xue Ban, 39: 438 (2008).
Capsoni et al., Proc. Natl. Acad. Sci. USA, 99: 12432 (2002).
Carare et al., Neuropathol. Appl. Neurobiol., 34: 131 (2008).
Cauna, In: Proctor DF, Andersen I, editors. Amsterdam: Elsevier Biomedical Press. pp. 45-69 (1982).
Charlton et al., Int. J. Pharm., 338: 94 (2007b).
Charlton et al, J. Drug Target, 15: 370 (2007a).
Charlton et al., Pharm. Res., 25: 1531 (2008).
Chen et al., J. Alzheimers Dis., 1: 35 (1998).
Chen et al., J. Pharm. Sci., 95: 1364 (2006).
Chow et al., J. Pharm. Sci., 88: 754 (1999).
Chow et al., J. Pharm. Sci., 90: 1729 (2001).
Clerico et al., In: Doty RL, editor. Handbook of olfaction and gustation. 2nd edition. New York: Marcel Dekker, Inc. pp. 1-16 (2003).
Costantino et al., Int. J. Pharm., 337: 1 (2007).
Cserr et al., Am. J. Physiol., 240: F319 (1981).
Cserr et al., Brain Pathol., 2: 269 (1992).
Dahlin et al., Eur. J. Pharm. Sci., 14: 75 (2001).
Danhof et al., American Association of Pharmaceutical Scientists Annual Meeting, Atlanta, GA (2008).
Danielyan et al., Eur. J. Cell. Biol., 88: 315 (2009).
Davis et al., Clin. Pharmacokinet., 42: 1107 (2003).
de Lorenzo, In: Wolstenholme GEW, Knight J, editors. Taste and smell in vertebrates. London: Churchill, pp. 151-175 (1970).
De Rosa et al., Proc. Natl. Acad. Sci. USA. 102: 3811 (2005).
DeSesso, Oual. Assur., 2: 213 (1993).
deSouza et al., Eur. Neuropsychopharmacol., 19: 53 (2009).
Dhanda et al., Drug Del. Tech., 5: 64 (2005).
Dhuria et al., J. Pharm. Sci., 98: 2501 (2009b).
Dhuria et al., J. Pharmaceutical Sciences, 99: 1654 (2010).
Dhuria et al., J. Pharmacol. Exp. Ther., 328: 312 (2009a).
Diano et al., J. Clin. Invest., 118: 26 (2008).
Dickson et al., Mol. Gen. Metab., 91: 61 (2007).
Djupesland et al., Laryngoscope. 116: 466 (2006).
Domes et al., Biol. Psychiatry. 61: 731 (2007b).
Domes et al., Biol. Psychiatry. 62: 1187 (2007a).
Dufes et al., Int. J. Pharm., 255: 87 (2003).
Einer-Jensen et al., Exp. Brain Res., 130: 216 (2000b).
Einer-Jensen et al., Pharmacol. Toxicol., 87: 276 (2000a).
Einer-Jensen et al., Reproduction, 129: 9 (2005).
Ellinwood et al., Mol. Genet. Metab., 91: 239 (2007).
Fehm et al., J. Clin. Endocrinol. Metab., 86: 1144 (2001).
Field et al., J. Neurocytol., 32: 317 (2003).
Fliedner et al., Endocrinology., 17: 2088 (2006).
Foust et al., Nat. Biotech., 27: 5 (2009)).
Francis et al., Brain, 131: 3311 (2008).
Fratantoni et al., Science, 162: 570 (1968).
Frey et al., Drug Delivery, 4: 87 (1997).
Frey II, Drug Del. Tech., 2: 46 (2002).
Fuss et al., Eur. J. Neurosci., 22: 2649 (2005).
Gao et al., Biomaterials, 27: 3482 (2006).
Gao et al., Int. J. Pharm., 340: 207 (2007a).
Gao et al., J. Control Release, 121: 156 (2007b).
Gopinath et al., Current Ther. Res., 23: 596 (1978).
Gozes et al., Curr. Alzheimer Res., 4: 507 (2007).
Graff et al., Pharm. Res., 20: 1225 (2003).
Graff et al., Pharm. Res., 22: 235 (2005a).
Graff et al., Pharm. Res., 22: 86 (2005b).
Gray, 15th revised edition (Classic Collectors edition). New York: Bounty Books (1978).
Grevers et al., Arch. Otorhinolaryngol., 244: 55 (1987).
Groothuis et al., J. Cereb. Blood Flow Metab., 27: 43 (2007).
Gross et al., J. Anat, 135: 83 (1982).
Guastella et al., Biol. Psychiatry, 63: 3 (2008).
Hadaczek et al., Mol. Ther., 14: 69 (2006).
Hallschmid et al., Regul. Pept, 149: 79 (2008).
Han et al., J. Mol. Med., 85: 75 (2007).
Hanson et al., BMC Neurosci., 9: S5 (2008).
Hanson et al., Drug Del. Tech., 4: 66 (2004).
Hanson et al., San Diego, CA: Society for Neuroscience (2007).
Hanson et al., In: EPO, editor. Biopharm and HealthPartners Research Foundation (2008).
Hartung et al., J. Am. Soc. Gene Ther., 9: 866 (2004).
Hartung et al., Mol. Thera., 9: 869 (2004).
Hashizume et al., Neuro. Oncol., 10: 112 (2008).
Hatterer et al., Blood, 107: 806 (2006).
Herati et al., J. Gene Med., 10: 972 (2008).
Hess et al., Exp. Neuro., 186: 134(2004).
Horvat et al., Eur. J. Pharm. Biopharm., 72: 252 (2009).
Hussar et al., Chem. Senses, 27: 7 (2002).
Illum, J. Control Release, 87: 187 (2003).
Illum, J. Pharm. Pharmacol., 56: 3 (2004).
Itaya et al., Brain Res., 398: 397 (1986).
Jansson et al., J. Drug Target, 10: 379 (2002).
Jogani et al., Alzheimer Dis. Assoc. Disord., 22: 116 (2008).
Johnston et al., Cerebrospinal Fluid Res., 1: 2 (2004).
Kakkis et al., Mol. Gen. Met., 83: 163 (2004).
Kandimalla et al., J. Pharm. Sci., 94: 613 (2005b).
Kandimalla et al., Pharm. Res., 22: 1121 (2005a).
Kida et al., Neuropathol. Appl. Neurobiol. 19: 480 (1993).
Kirsch et al., J. Neurosci., 25: 11489 (2005).
Klein et al., J. Am. Soc. Gene Ther., 13: 517 (2006).
Koos et al., Neuroreport, 16: 1929 (2005).
Kosfeld et al., Nature. 435: 673 (2005).
Kristensson et al., Acta Neuropathol (Berl), 19: 145 (1971).
Krivit, Springer Seminars in Immunopathology, 26: 119 (2004).
Kumar et al., Curr. Sci., 43: 435 (1974).
Kumar et al., Int. J. Pharm., 358: 285 (2008).
Li et al., Chin. J. Physiol., 48: 7 (2005c).
Li et al., Glia, 52: 245 (2005a).
Li et al., J. Neurocytol., 34: 343 (2005b).
Loftus et al., Neuroscience, 139: 1061 (2006).
Luzzati et al., J. Mol. Biol., 343: 199 (2004).
Mackay-Sim, In: Doty RL, editor. Handbook of olfaction and gustation. 2nd edition. New York: Marcel Dekker, Inc. pp. 93-113 (2003).
Martinez et al., Neuroscience, 157: 908 (2008).
Minn et al., J. Drug Target, 10: 285 (2002).
Miragall et al., J. Comp. Neurol., 341: 433 (1994).
Muenzer, J. Pediatrics, 144: S27 (2004).
Munoz-Rojas et al., Am. J. Med. Gen., 146A: 2538 (2008).
Neufeld and Muenzer, In A. L. B. C.R. Scriver, W.S. Sly, et al (ed.), McGraw Hill, NY, pg. 3421 (2001).
Nonaka et al., J. Pharmacol. Exp. Ther., 325: 513 (2008).
Ohlfest et al., Blood, 105: 2691 (2005).
Orchard et al., J. Pediatrics. 151: 340 (2007).
Owens et al., Diabet. Med., 20: 886 (2003).
Pan et al., Brain Res., 1188: 241 (2008).
Pardridge, NeuroRx, 2: 3 (2005).
Parker et al., Psychoneuroendocrinology, 30: 924 (2005).
Pastores, Exp. Opin. Biol. Ther., 8: 1003 (2008).
Perl et al., Lancet, 1: 1028 (1987).
Peters et al., Bone Marrow Transpl., 31: 229 (2003).
Pollock et al., J. Anat., 191: 337 (1997).
Raghavan et al., J. Laryngol. Otol., 114: 456 (2000).
Reger et al., J. Alzheimers Dis., 13: 323 (2008a).
Reger et al., Neurobiol. Aging. 27: 451 (2006).
Reger et al., Neurology, 70: 440 (2008b).
Rennels et al., Adv. Neurol., 52: 431 (1990).
Rennels et al., Brain Res., 326: 47 (1985).
Reolon et al., Brain Res., 1076: 225 (2006).
Rimmele et al., J. Neurosci., 29: 38 (2009).
Ross et al., J. Neuroimmunol., 151: 66 (2004).
Ross et al., Neurosci. Lett., 439: 30 (2008).
Sakane et al., J. Pharm. Pharmacol., 46: 378 (1994).
Sakane et al., J. Pharm. Pharmacol., 47: 379 (1995).
Sarkar, Pharm. Res., 9: 1 (1992).
Schaefer et al., J. Comp. Neurol., 444: 221 (2002).
Scheibe et al., Arch. Otolaryngol. Head Neck Surg., 134: 643 (2008).
Schley et al., J. Theor. Biol., 238: 962 (2006).
Schulz et al., Endocrinology, 145: 2696 (2004).
Scott et al., Am. J. Hum. Genet., 53: 973 (1993).
Shimizu et al., Int. J. Obes. (Lond), 29: 858 (2005).
Shipley, Brain Res. Bull., 15: 129 (1985).
Skipor et al., Reprod. Biol., 3: 143 (2003).
Steen et al., J. Alzheimers Dis., 7: 63 (2005).
Stefanczyk-Krzymowska et al., Exp. Physiol., 85: 801 (2000).
Takano et al., J. Histochem. Cytochem., 53: 611 (2005).
Thorne et al., Brain Res., 692: 278 (1995).
Thorne et al., Clin. Pharmacokinet., 40: 907 (2001).
Thorne et al., Neuroscience, 127: 481 (2004).
Thorne et al., Neuroscience, 152: 785 (2008).
Thorne, RG. 2002. The nasal pathways for drug delivery to the central nervous system: Studies with protein tracers and therapeutics. Doctoral Dissertation, University of Minnesota.
Unger et al., J. Neuropath. Exp. Neuro., 52: 460 (1993).
van den Berg et al., Eur. J. Pharm. Biopharm., 58: 131 (2004b).
Van den Berg et al., J. Drug Target. 11: 325 (2003).
van den Berg et al., J. Neurosci. Methods, 116: 99 (2002).
van den Berg et al., Pharm. Res., 21: 799 (2004a).
Van Diest et al., J. Anat., 128: 293 (1979).
Vyas et al., AAPS PharmSciTech., 7: E1 (2006c).
Vyas et al., Crit. Rev. Ther. Drug Carrier Syst., 23: 319 (2006b).
Vyas et al., J. Drug Target, 13: 317 (2005).
Vyas et al., J. Pharm. Sci., 95: 570 (2006a).
Walter et al., Arch. Histol. Cytol., 69: 37 (2006a).
Walter et al., Neuropathol. Appl. Neurobiol., 32: 388 (2006b).
Wang et al., Cancer Chemother. Pharmacol., 57: 97 (2006a).
Wang et al., Eur. J. Pharm. Biopharm., 70: 735 (2008).
Wang et al., Int. J. Pharm., 317: 40 (2006b).
Wang et al., Int. J. Pharm., 341: 20 (2007).
Watson et al., Gene Therapy, 16 February 2006, doi: 10.1038/sj.gt.3302735.
Weller et al., Neurol. Res., 25: 611 (2003).
Westin et al., Eur. J. Pharm. Sci., 24: 565 (2005).
Westin et al., Pharm. Res., 23: 565 (2006).
Williams et al., J. Comp. Neurol., 470: 50 (2004).
Wioland et al., J. Histochem. Cytochem., 48: 1215 (2000).
Wolf et al., Neurobio. Dis., 43: 123 (2011).
Xu et al., J. Clin. Invest., 118: 272 (2008).
Yamada et al., Am. J. Physiol., 261: H1197 (1991).
Yang et al., J. Pharm. Sci., 94: 1577 (2005).
Zhang et al., Acta Neuropathol. (Berl), 83: 233 (1992).
Zhang et al., Acta Pharmacol. Sin., 25: 522 (2004a).
Zhang et al., Int. J. Pharm., 275: 85 (2004b).
Zhang et al., J. Drug Target, 14: 281 (2006).
Zhao et al., Acta Pharmacol. Sin., 28: 273 (2007).
Zhao et al., Chin. Med. Sci. J., 19: 257 (2004).
Zheng et al., Mol. Genet. Metab., 79: 233 (2003).
Ziegler and Shapiro, In J. Donders and S. Hunter (ed.), Cambridge University Press, p. 427 (2007).
Все публикации, патенты и патентные заявки включены в настоящий документ посредством ссылки. В то время как в предшествующем описании настоящее изобретение было описано в отношении некоторых предпочтительных вариантов его осуществления и многие детали были изложены для целей иллюстрации, специалистам в настоящей области техники будет очевидно, что настоящее изобретение допускает дополнительные варианты осуществления и что некоторые из деталей в настоящем документе могут значительно изменяться без отступления от основных принципов настоящего изобретения.
Реферат
Изобретение относится к области медицины. Предложен способ предотвращения, ингибирования или лечения одного или нескольких симптомов мукополисахаридоза типа I (MPS I) у человека, включающий интратекальное введение нуждающемуся в этом человеку композиции, содержащей эффективное количество вектора на основе рекомбинантного аденоассоциированного вируса (rAAV), содержащего открытую рамку считывания, кодирующую альфа-L-идуронидазу, причем rAAV представляет собой rAAV9 или rAAVrh10. Изобретение обеспечивает эффективный способ предотвращения, ингибирования или лечения одного или нескольких симптомов MPS I у человека, имеющего отсутствие или недостаток связанного с накоплениями лизосомального фермента. 16 з.п. ф-лы, 20 ил., 3 пр.
Формула
Документы, цитированные в отчёте о поиске
Медленная внутрижелудочковая доставка

Комментарии