Фотолюминесцентный полимерный композиционный материал для светоизлучающих систем - RU2583267C2
Код документа: RU2583267C2
Чертежи
Описание
Изобретение относится к химии и физикохимии полимерных материалов, а именно к полученным впервые композиционным полимерным материалам, содержащим функциональный компонент - полифенилхинолин (ПФХ) в полимерных матрицах. ПФХ обеспечивает настройку координат цветности благодаря варьированию взаимодействия между донорными и акцепторными фрагментами, что отражается в спектрах фотолюминесценции. Материал может быть использован для создания светоизлучающих систем (светодиодов, светоизлучающих информационных панелей, осветительных систем, фото- и переизлучающих покрытий).
В настоящее время для получения белого свечения с хорошим индексом цветопередачи (CRI>80) в светодиодах используют люминесцентные композитные материалы. Эффект получают за счет использования синих полупроводниковых кристаллов (в светодиодах), покрытых люминофорной композицией желтого свечения, совместно излучающих белый свет [RU 2405804, опубл. 10.12.2010, Бюл. №34. 7 с]. Однако данная технология имеет недостатки, например высокую нагрузку на люминофор, находящийся на полупроводниковом кристалле, что приводит к снижению эффективности светового прибора.
Для получения белого света с помощью синего светодиода могут наносить желтый люминофор (иттрий-алюминиевый гранат Y3Al5O12 - ИАГ или гранатит) или смесь красного и желто-зеленого люминофоров на поверхность синего светодиода с целью их последовательного перепоглощения и выравнивания цвета. Однако такие системы с одним люминофором имеют низкий CRI (<75), что снижает их качество при использовании с целью внутреннего освещения. Использование нескольких люминофоров сопряжено с вопросами оптимизации устройства, кроме того, смешение люминофоров не всегда приводит к эффективному преобразованию света.
Другой подход связан с использованием полимерных люминофоров, обладающих рядом преимуществ по сравнению с предыдущим. Во-первых, он позволяет включать в полимерную цепь люминофоры с разной полосой испускания в видимом диапазоне. С целью разработки полимерных светоизлучающих материалов с белой электролюминесценцией для светодиодных осветительных систем синтезирована серия люминофорсодержащих сополифлуоренов, содержащих фрагменты нильского красного в боковой цепи. Максимальная яркость электролюминесценции достигала 3870 кд/м2. В ряде случаев получены светоизлучающие устройства с индексами цветности, близкими к белому свету, и яркостью 380-2380 кд/м2 [Г.И. Носова и др. / Синтез, фото- и электролюминесцентные свойства сополифлуоренов с фрагментами Нильского красного в боковой цепи // Высокомолекулярные соединения, Polymer Science Series В, Added to Web of Sci. Library: 08 Apr 2014]. Недостатком такого подхода является сложность используемой химической реакции в связи с настройкой координат цветности по системе МКО 1931 г.
Во-вторых, в качестве люминесцирующих материалов используют металлполимерные комплексы, где в качестве испускающих центров используют ионы (III) лантанидов (тербия, европия, самария), а полимер играет роль высокомолекулярного лиганда, обеспечивающего антенный эффект [Якиманский А.В. и др. / Люминесценция комплексов лантанидов Ln3+ в полимерных матрицах // Высокомолекулярные соединения. 2012. Т. 54. №12. С. 1699]. Недостатком таких систем является невысокий индекс передачи цвета, поскольку полоса люминесценции лантанидных ионов состоит из квазимонохроматических линий, которые не обеспечивают полного перекрытия видимого диапазона, если речь идет об источниках освещения.
В-третьих, одним из перспективных классов полимерных материалов для создания молекулярных оптоэлектронных устройств являются полимеры, содержащие в мономерном звене донорные и акцепторные группы, образующие донорно-акцепторные (Д-А) комплексы. Люминесценция от таких Д-А молекул может быть результатом взаимодействия близко расположенных донорных и акцепторных фрагментов с образованием внутримолекулярного комплекса с переносом заряда (ВКПЗ). Перенос энергии электронного возбуждения (ЭЭВ), образование внутри- и межмолекулярных эксимеров и эксиплексов также позволяет контролировать спектральный состав испускаемого света за счет соответствующего подбора Д-А фрагментов [Jenekhe S.A., Liangde L., Maksudul M.A. // Macromolecules. 2001. V. 34. P. 7315]. Так в работе [Александрова Е.Л. и др. / Сополимеры карбазол- и индолокарбазолсодержащих фенилхинолинов - новые материалы для электролюминесцентных устройств // Физика и техника полупроводников. 2013. Т. 47. №8. С. 1055-1064]. Авторы синтезировали сополимеры фенилхинолинов (ФХ), содержащие звенья карбазола (Кз) и индолокарбазола. Получаемый материал обладает люминесцентными свойствами в широком видимом диапазоне благодаря образованию внутри- и межмакромолекулярных донорно-акцепторных комплексов. При включении гибкой -О- развязки между элементарными повторяющимися фрагментами ФХ-Кз-ФХ происходит нарушение сопряжения в карбазолсодержащих ПФХ, что уменьшает эффективную миграцию ЭЭВ и сохраняет полосу люминесценции 454 нм (синее свечение). Это позволило получить систему с фотолюминесценцией, близкой к белой, с координатами цвета по шкале МКО 1931 г. (0.322, 0.355).
В настоящее время не известны технические решения, позволяющие настраивать координаты цветности спектров фотолюминесценции полимеров путем варьирования длины бокового алкильного радикала в повторяющейся структурной единице полимера, являющейся ВКПЗ, при помещении их в полимерную матрицу, обладающую фотоактивными или электропроводящими свойствами либо инертную.
Прототипом заявляемого изобретения является композиционный материал на основе полимера с мономерным звеном, включающий карбазол и фенилхинолин, помещенного в полимерные матрицы ПММА и ПВКз. Строение и фотофизические свойства такого полимера и его полимер-полимерных композитов раскрыты [Светличный В.М. и др. / Карбазолсодержащие полифенилхинолины как основа оптоэлектронных материалов с белой люминесценцией // Физика и техника полупроводников. 2012. Т. 46. №4. С. 512-519]. Эти композиционные материалы не обладают во всем видимом диапазоне возможностями по настройке координат цветности фотолюминесценции, поскольку не варьировалась длина бокового алкильного радикала в карбазольном фрагменте ПФХ, что необходимо для регулировки донорно-акцепторного взаимодействия.
Технической задачей и положительным результатом данного изобретения является создание полимерного композиционного материала, обладающего спектром фотолюминесценции с настраиваемыми координатами цветности в системе Международной комиссии по освещению. Указанная задача и технический результат достигаются за счет варьирования длины бокового алкильного радикала от 12 до 18 атомов углерода в ПФХ и химической природы полимерной матрицы, что позволяет благодаря настройке координат цветности люминесценции использовать эти композиционные материалы в фото- и электролюминесцентных устройствах, информационных люминесцирующих панелях, осветительных приборах, декоративных люминесцирующих устройствах.
Заявленным объектом патентования является фотолюминесцентный полимерный композиционный материал для светоизлучающих систем, включающий 1,6 масс. % полифенилхинолина - поли[2,2′-(9-додецилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолина)] или поли[2,2′-(9-окта-децилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолина)] формулы:
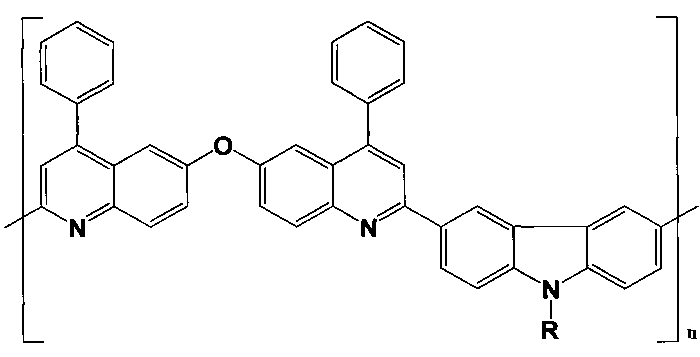
где n - число повторяющихся звеньев; R - C12H25 или С18Н37,
и 98,4 масс. % полимерной матрицы, выбранной из группы, включающей полистирол, сополимер винилового спирта с винилацетатом, поли-N-винилкарбазол или полиметилметакрилат - матрицы разной функциональной направленности - фотоинертные, фотоактивные - поглощающие и люминесцирующие, обладающие дырочной или электронной проводимостью, а также способные к межмакромолекулярному взаимодействию с функциональными группами вводимого компонента либо вызывающие его сегрегацию.
Существенное отличие заявляемого изобретения от прототипа заключается в том, что использованы два полифенилхинолина (ПФХ): поли[2,2′-(9-додецилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолин)] - ПФХ{O-K12} и поли[2,2′-(9-октадецилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолин)] - ПФХ{O-K18}, имеющие разную длину бокового алифатического радикала при карбазольном фрагменте. Причем ПФХ{O-K18} синтезирован впервые. Цель варьирования бокового радикала - обеспечить, во-первых, растворимость ПФХ в широком ряду растворителей, что важно для технологического использования, во-вторых, различное взаимодействие люминесцирующих макромолекул с полимерной матрицей, а также между собой в случае сегрегирующей матрицы.
В заявляемом изобретении использован широкий набор матриц с различными свойствами: ПСт, сополимер ВС-ВА, ПВКз и ПММА; некоторые из них совместно с ПФХ ранее не использовались.
Полученный композиционный материал ПФХ в полимерных матрицах обладает широким спектром люминесценции в видимом диапазоне. Возможна тонкая подстройка координат цветности (в стандарте МКО 1931), которая осуществима двумя способами: во-первых, использованием ПФХ с разной длиной боковых радикалов; во-вторых, варьированием природы использованной матрицы.
Заявляемый материал получали в несколько стадий: i) синтез мономеров; ii) синтез гомополимеров ПФХ на основе полученных мономеров; iii) получение пленок композиционного материала из растворов ПФХ - полимерная матрица в диметилформамиде или в хлороформе.
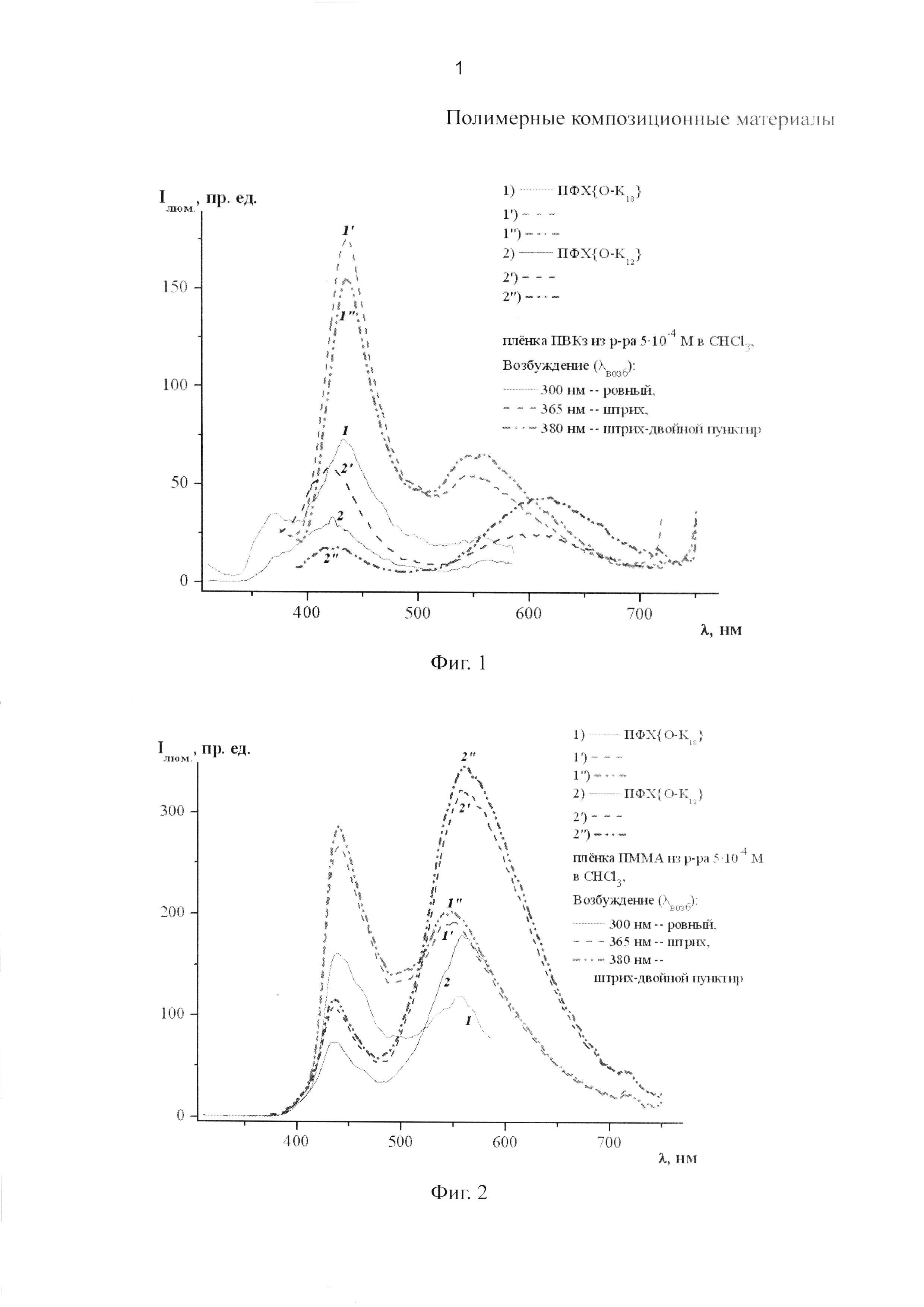
Спектры люминесценции пленок из заявляемого полимерного композицонного материала снимали на люминесцентном спектрофотометре LS-100, фирмы PTI, Канада. Фиг. 1 представляет спектры люминесценции ПФХ{O-K18} и ПФХ{O-K12} в ПВКз. Использование ПВКз обусловлено тем, что эта матрица обладает дырочной проводимостью. Для доказательства межмакромолекулярного взаимодействия использовано возбуждение на трех длинах волн: 300, 365 и 380 нм, чтобы были затронуты последовательно в сравнении все поглощающие осцилляторы в макромолекулах ПФХ и матрицы: гетероароматическое ядро карбазола, фенилхинолиновый высокоэнергетический КПЗ и ФХ-карбазольный низкоэнергетический КПЗ, соответственно. Длина волны 300 нм выбрана для возбуждения карбазольного ядра, чтобы показать перенос энергии с этого фрагмента по цепи. Длины волн 365 и 380 нм использованы, чтобы продемонстрировать перенос энергии при первичном поглощении фенилхинолинового фрагмента.
В результате данного эксперимента получен материал с высокой эффективностью фотолюминесценции в синей области видимого спектра (кр. 1′ и 1′′): координаты цветности (0.227, 0.218), и эффективной чистотой цвета pE0.539 (пример №5, табл. 1).
Фиг. 2 представляет спектры люминесценции ПФХ{O-K18} и ПФХ{O-K12} в ПММА. Использование ПММА обусловлено тем, что эта матрица фотоинертна после 300 нм. Анализ спектров люминесценции при возбуждении при всех трех длинах волн - 300, 365 и 380 нм - показывает полное отсутствие полосы люминесценции, связанной с мономерными карбазольными фрагментами (λмакс. люм.=350 нм), высокоэнергетическими (λмакс. люм.=370 нм) и низкоэнергетическими (λмакс. люм.=410 нм) эксимерами карбазола.
Несмотря на разную химическую природу матриц ПВКз и ПММА наблюдают взаимодействие ПФХ-ПФХ. Оказывается, что уменьшение длины бокового радикала усиливает взаимодействие Д-А фрагментов в обеих матрицах, хотя ПВКз является хорошим «твердым» растворителем для ПФХ, а ПММА - сегрегирующим.
В результате получен материал с голубым оттенком (примеры №7, табл. 1, кр. 1′ и 1′′) либо с желтым цветом люминесценции и высокой ее интенсивностью (примеры №8, табл. 1, кр. 2′ и 2′′).
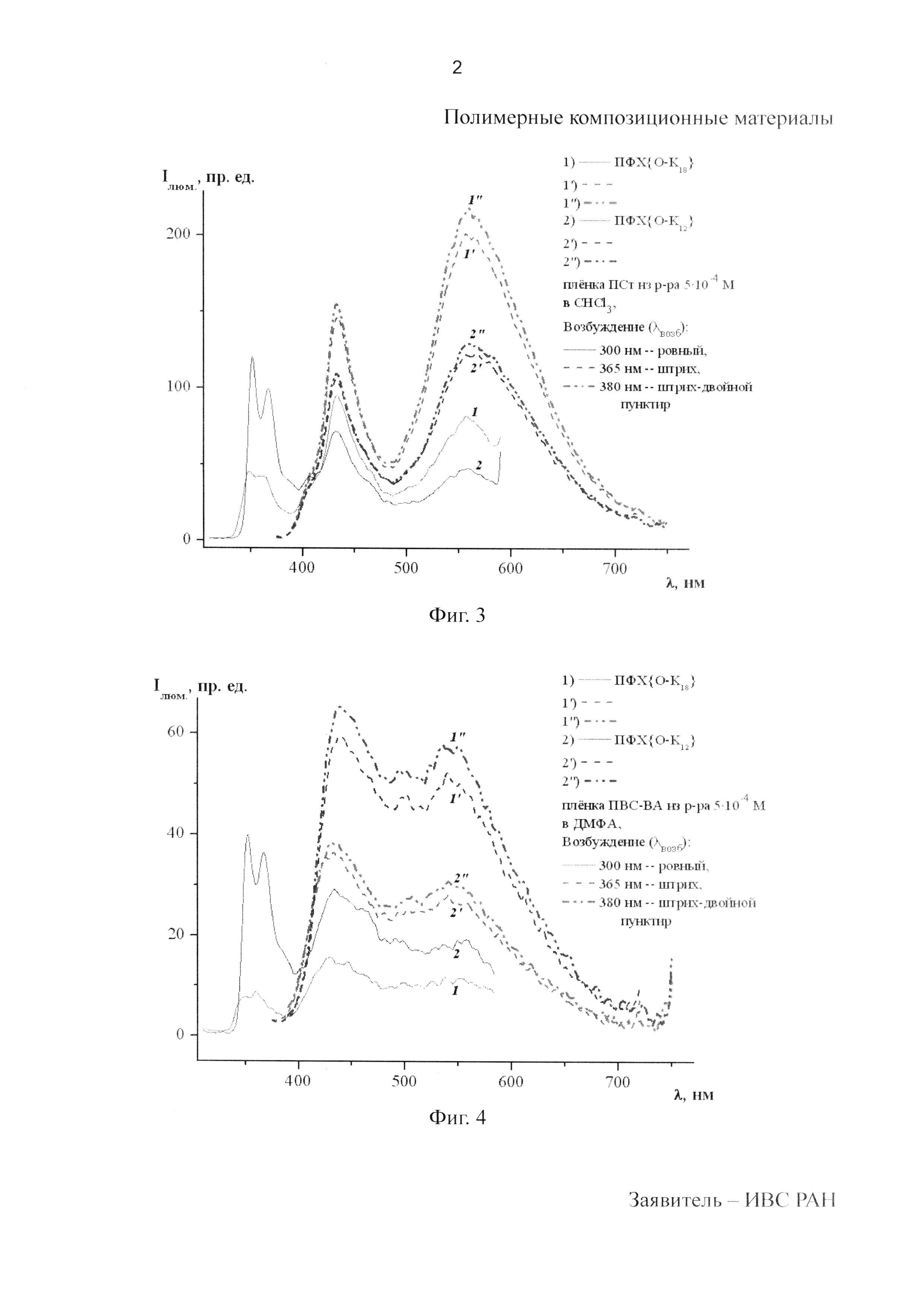
Фиг. 3 представляет спектры люминесценции ПФХ{O-K18} и ПФХ{O-K12} в ПСт. Использование ПСт обусловлено тем, что эта матрица, с одной стороны, обладает дырочной проводимостью, а с другой, - она люминесцирует в области 300 нм.
При переходе к композиционным материалам - ПФХ в матрице ПСт - наблюдают такую же тенденцию, как и в матрице ПММА по сравнению с матрицей ПВКз. Это может указывать на незначительное усиление взаимодействия ПФХ-матрицы ПСт при увеличении длины бокового радикала, возможно, за счет лучшего «растворения» макромолекул ПСт в более длинных алифатических радикалах. При увеличении длины бокового радикала усиливается взаимодействие ПФХ-ПФХ в отличие от матриц ПВКз и ПММА.
В результате получен материал (кр. 2′) с приближающимися к белому координатами цветности (0.358, 0.370) и эффективной чистотой цвета pE0.057 (пример №2, табл. 1).
Фиг. 4 представляет спектры люминесценции ПФХ{O-K18} и ПФХ{O-K12} в П(ВС-ВА). Использование П(ВС-ВА) обусловлено тем, что эта матрица фотоинертна в области ближнего ультрафиолета, а с другой стороны, подвержена структурообразованию при нагревании.
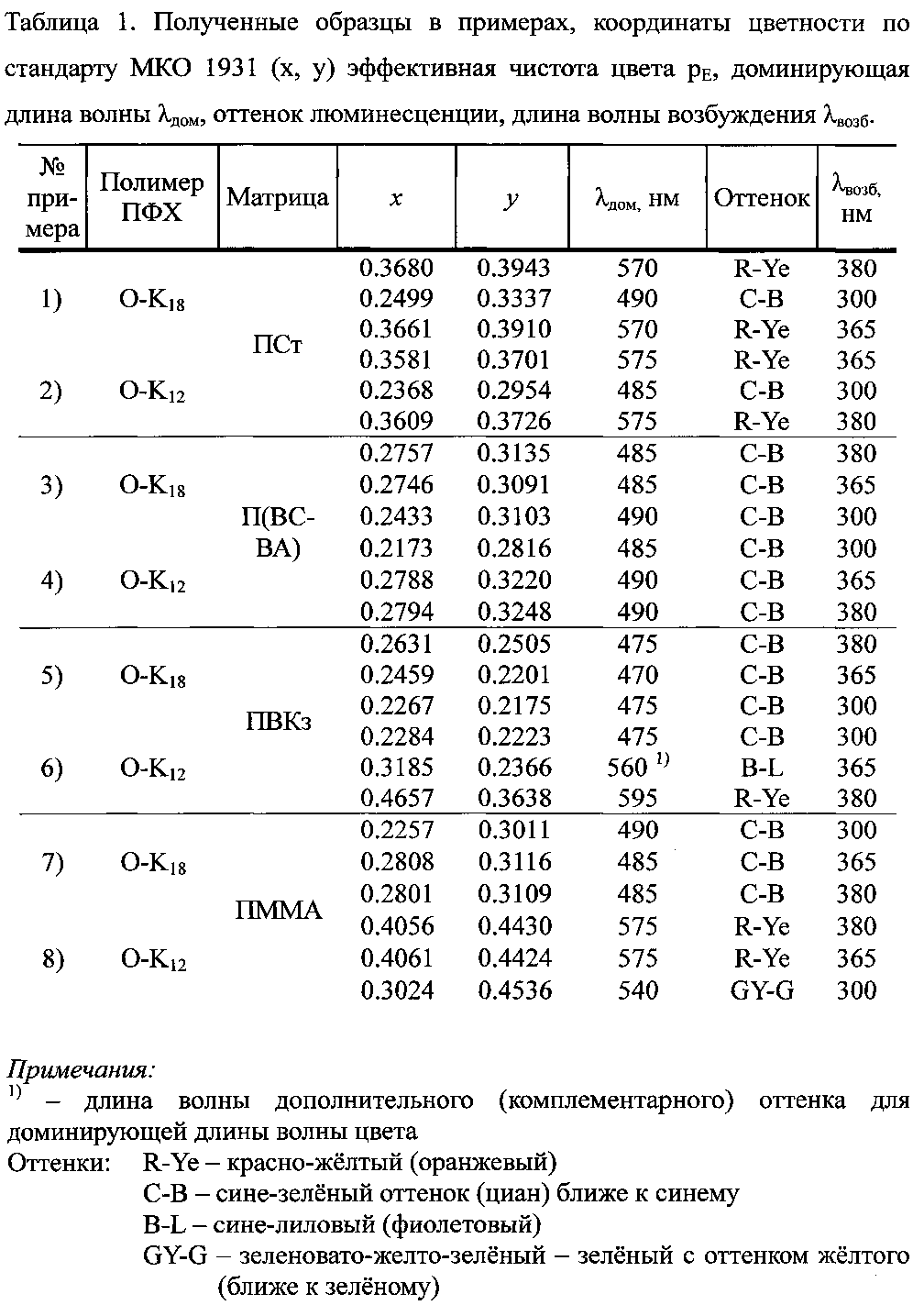
Полученные характеристики подтверждены фигурами и таблицами: Таблица 1 представляет образцы композиционного материала, полученного в примерах 1-8, координаты цветности по стандарту МКО 1931 (х, у), доминирующую длину волны λдом, оттенок люминесценции, длину волны возбуждения λвозб.
Фигура 1 представляет спектры люминесценции ПФХ{O-K18 или K12} в матрице ПВКз.
Фигура 2 представляет спектры люминесценции ПФХ{O-K18 или K12} в матрице ПММА.
Фигура 3 представляет спектры люминесценции ПФХ{O-K18 или K12} в матрице ПСт.
Фигура 4 представляет спектры люминесценции ПФХ{O-K18 или K12} в матрице ПВС-ВА.
Для подтверждения соответствия заявленного изобретения такому условию патентоспособности как «промышленная применимость» и для лучшего понимания сущности заявленного изобретения приведены примеры конкретной реализации изобретения, которыми не может исчерпываться его сущность.
i) Стадия синтеза мономеров
Синтез 3,6-диацетил-9-додецилкарбазола (мономер 1)
В трехгорлой круглодонной колбе, снабженной обратным холодильником, верхнеприводной мешалкой, в атмосфере аргона растворяли 9-додецилкарбазол (1,2 г; 3,58 ммоль) в хлористом метилене (10,79 г), затем добавляли хлорид алюминия (1,465 г; 11 ммоль) и при тщательном перемешивании по каплям вводили ацетилхлорид (0,91 г; 11,54 ммоль). Реакцию проводили в течение 5 часов при комнатной температуре. Реакционный раствор обрабатывали смесью хлористого метилена (86,3 г) и дистиллированной воды (38 г). Отделяли органический слой, промывали дистиллированной водой (2×100 г) и сушили в течение 15-17 часов прокаленным сульфатом магния. Хлористый метилен удаляли на ротационном испарителе. Полученный твердый продукт перекристаллизовывали из этилового спирта. Сушили под вакуумом при температуре 75°С. Выход - 0,82 г (54,6%). Температура плавления 97,5-98,5°С.
По данным элементного анализа для C28H37NO2:
Вычислено, %: С - 80,15; Н - 8,89; N - 3,34.
Найдено, %: С - 80,06; 80,05; Н - 9,00; 9,12; N - 3,44; 3,48.
1Н ЯМР (CDCl3), δ (м.д.): 8,85 (2Н); 8,20 (2Н); 7,54 (2Н); 4,37 (2Н); 2,71 (6Н); 1,90 (2Н); 1,37-1,25 (18Н); 0,87 (3Н).
Синтез 3,6-диацетил-9-октадецилкарбазола (мономер 2)
Для синтеза мономера 2 использовали 1,679 г (4 ммоль) 9-октадецилкарбазола, 12,1 г хлористого метилена, 1,64 г (12,3 моль) хлорида алюминия и 1,01 г (12,8 ммоль) ацетилхлорида. Процесс проводили аналогично синтезу мономера 1. Выход продукта - 1,12 г (55,5%). Температура плавления 108,3-109,4°С.
1Н ЯМР (CDCl3), δ (м.д.): 8,80 (2Н); 8,17 (2Н); 7,48 (2Н); 4,34 (2Н); 2,76 (6Н); 1,84 (2Н); 1,34-1,23 (30Н); 0,89 (3Н).
ii) Стадия синтеза гомополимеров ПФХ на основе полученных мономеров.
Синтез поли[2,2′-(9-додецилкарбазол-3,6-диил)-6,6′-окси(бис)(4-фенил-хинолина)] (полимер 1)
В трехгорлой круглодонной колбе, снабженной верхнеприводной мешалкой и обратным холодильником, в атмосфере аргона растворяли 0,85 г пентоксида фосфора в 3,09 г м-крезола в течение 3 часов при температуре 140°С. В полученный светло-желтый раствор при комнатной температуре загружали 0,2042 г (0,5 ммоль) 4,4′-диамино-3,3′-дибензоилдифенилового эфира и 0,21 г (0,5 ммоль) мономера 1. Реакцию проводили при перемешивании в атмосфере аргона при температуре 140°С в течение 24 часов. По окончании реакции полимер высаживали при интенсивном перемешивании в смесь этанола (59,3 г) с триэтиламином (5,84 г). Затем выделенный полимер промывали от м-крезола этанолом с триэтиламином (10%) на аппарате Сокслета в течение 24 часов и сушили под вакуумом при t=100°С в течение 5 часов. Выход продукта - 75%.
1Н ЯМР (CDCl3), δ (м.д.): 9,03 (2Н); 8,45 (2Н); 8,30 (2Н); 8,04 (2Н); 7,58-7,44 (16Н); 4,41 (2Н); 1,96 (2Н); 1,33-1,24 (18Н); 0,87 (3Н).
Синтез поли[2,2′-(9-октадецилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолина) (полимер 2)
Синтез полимера 2 отличается от синтеза полимера 1 тем, что использовался мономер 2 вместо мономера 1. Выход продукта - 65%.
1Н ЯМР (CDCl3), δ (м.д.): 9,04 (2Н); 8,46 (2Н); 8,29 (2Н); 8,02 (2Н); 7,57-7,46 (16Н); 4,31 (2Н); 1,92 (2Н); 1,33-1,22 (ЗОН); 0,91 (3Н).
Молекулярная масса синтезированных полимеров 1 и 2 была оценена по данным гельпроникающей хроматографии и составила для ПФХ{O-K12} MW=5·104, а для ПФХ{O-K18} MW=4,5·104.
iii) Стадия (основная) получения пленок композиционного материала
Пример 1. Полимерный композиционный материал готовили из синтезированного ПФХ{O-K18} (см. ранее Стадии i и ii) путем смешения 1,25 г его раствора в хлороформе (концентрация 0,067 масс. %), с 0,77 г раствора ПСт в хлороформе (концентрация 6,7 масс. %) и 0.24 г хлороформа. Из полученного композиционного полимерного раствора (2,26 г) формовали покрытие на ровной стеклянной поверхности площадью 4 см2. Удаляли растворитель сушкой при 70°С в течение 2 часов. Толщина пленки составляла 40-50 мкм. (См. табл. 1, пример №1).
Пример 2. Полимерный композиционный материал готовили из синтезированного ПФХ{O-K12} (см. ранее Стадии i и ii) путем смешения 1,62 г его раствора в хлороформе (концентрация 0,052 масс. %) с 0,77 г раствора ПСт в хлороформе (концентрация 6,7 масс. %) и 0.34 г хлороформа. Полученные (2,73 г) композиционного полимерного раствора выливали на ровную стеклянную поверхность площадью 4 см2. Удаляли растворитель сушкой при 70°С в течение 2 часов. Толщина пленки составляла 40-50 мкм. (См. табл. 1, пример №2).
Пример 3. Полимерный композиционный материал готовили из синтезированного ПФХ{O-K18} (см. ранее Стадии i и ii) путем смешения 0,76 г его раствора в диметилформамиде (концентрация 0,106 масс. %) с 0,47 г раствора П(ВС-ВА) в диметилформамиде (концентрация 10,6 масс. %) и 0,15 г ДМФА. Полученные 1,4 г композиционного полимерного раствора выливали на ровную стеклянную поверхность площадью 4 см2. Удаляли растворитель сушкой при 70°С в течение 5 часов. Толщина пленки составляла 40-50 мкм. (См. табл. 1, пример №3).
Пример 4. Полимерный композиционный материал готовили из синтезированного ПФХ{O-K12} (см. ранее Стадии i и ii) путем смешения 0,99 г его раствора в диметилформамиде (концентрация 0,082 масс. %) с 0,47 г раствора П(ВС-ВА) в диметилформамиде (концентрация 10,6 масс. %) и 0,22 г ДМФА. Полученные 1,68 г композиционного полимерного раствора выливали на ровную стеклянную поверхность площадью 4 см2. Удаляли растворитель сушкой при 70°С в течение 5 часов. Толщина пленки составляла 40-50 мкм. (См. табл. 1, пример №4).
Пример 5. Полимерный композиционный материал готовили из синтезированного ПФХ{O-K18} (см. ранее Стадии i и ii) путем смешения 1,25 г его раствора в хлороформе (концентрация масс. 0,067%) с 0,77 г раствора ПВКз в хлороформе (концентрация 6,7 масс. %) и 0,24 г хлороформа. Полученные 2,26 г композиционного полимерного раствора выливали на ровную стеклянную поверхность площадью 4 см2. Удаляли растворитель сушкой при 70°С в течение 2 часов. Толщина пленки составляла 40-50 мкм. (См. табл. 1, пример №5).
Пример 6. Полимерный композиционный материал готовили из синтезированного ПФХ{O-K12} (см. ранее Стадии i и ii) путем смешения 1,62 г его раствора в хлороформе (концентрация 0,052 масс. %) с 0,77 г раствора ПВКз в хлороформе (концентрация 6,7 масс. %) и 0,34 г хлороформа. Полученные 2,73 г композиционного полимерного раствора выливали на ровную стеклянную поверхность площадью 4 см2. Удаляли растворитель сушкой при 70°С в течение 2 часов. Толщина пленки составляла 40-50 мкм. (См. табл. 1, пример №6).
Пример 7. Полимерный композиционный материал готовили из синтезированного ПФХ{O-K18} (см. ранее Стадии i и ii) путем смешения 1,25 г его раствора в хлороформе (концентрация 0,067 масс. %) с 0,77 г раствора ПММА в хлороформе (концентрация 6,7 масс. %) и 0,24 г хлороформа. Полученные 2,26 г композиционного полимерного раствора выливали на ровную стеклянную поверхность площадью 4 см2. Удаляли растворитель сушкой при 70°С в течение 2 часов. Толщина пленки составляла 40-50 мкм. (См. табл. 1, пример №7).
Пример 8. Полимерный композиционный материал готовили из синтезированного ПФХ{O-K12} (см. ранее Стадии i и ii) путем смешения 1,62 г его раствора в хлороформе (концентрация 0,052 масс. %) с 0,77 г раствора ПММА в хлороформе (концентрация 6,7 масс. %) и 0,34 г хлороформа. Полученные 2,73 г композиционного полимерного раствора выливали на ровную стеклянную поверхность площадью 4 см2. Удаляли растворитель сушкой при 70°С в течение 2 часов. Толщина пленки составляла 40-50 мкм. (См. табл. 1, пример №8).
В примерах 1-8 получаемый композиционный материал включает 1,6 масс. % ПФХ и 98,4 масс. % полимерной матрицы, выбранной из группы, включающей полистирол, сополимер винилового спирта с винилацетатом, поли-N-винилкарбазол, или полиметилметакрилат.
В табл. 1 приведены полученные композиционные материалы с указанием их цветовых характеристик, полученных из спектров фотолюминесценции, и условий их получения.
Впервые также синтезирован поли[2,2′-(9-октадецилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолин)] - ПФХ{O-K18} - полимер, имеющий боковой алкильный радикал из 18 атомов углерода. Использование в заявляемом изобретении ПФХ с разной длиной бокового радикала позволило получить полимерный композиционный материал с настраиваемыми координатами цветности фотолюминесценции в системе МКО 1931 г.
Анализ научно-технического уровня не позволил обнаружить опубликованное решение, полностью совпадающее по совокупности существенных признаков с заявленным изобретением. Это подтверждает вывод о соответствии предлагаемого решения такому условию патентоспособности как «новизна».
Обнаруженные нами два эффекта позволяют сделать вывод о соответствии заявляемого решения в целом такому условию патентоспособности как «изобретательский уровень»: i) «растворяющая» способность матрицы ПВКз, обладающей некоторым сродством к ПФХ; ii) «экранирующая» роль алифатических радикалов, длина которых влияет на вероятность внутри- и межмакромолекулярного переноса энергии электронного возбуждения в макромолекулярных цепях ПФХ и при взаимодействии между собой и полимерной матрицей. В результате, не очевидным, во-первых, стал тот факт, что в матрице ПВКз происходит усиление интенсивности люминесценции ПФХ (строка 15, табл. 1) в области 410-490 нм, что дает синее свечение (λдом=475 нм) с координатами цветности (0.227, 0.218) и эффективной чистотой цвета pE0.539. Во-вторых, оказалось, что параметры цветности для ПФХ с разной длиной бокового радикала в матрице ПСт (строки 1, 3, 4, 6, табл. 1) близки к белому, что обусловлено сродством этой матрицы по сравнению с ПВКз и с ПММА при полученной формуле композиционного материала:
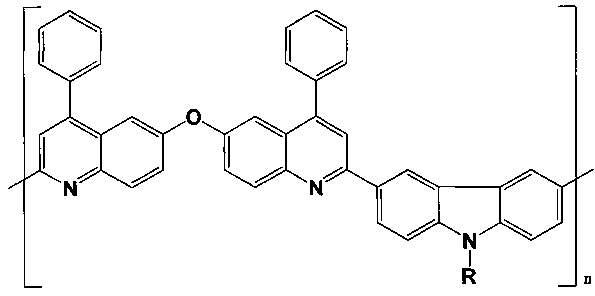
где n - число повторяющихся звеньев; R - С12Н25 или С18Н37
Таким образом, как изложено в описании, предлагаемые композиты позволяют настраивать координаты цветности (по стандарту МКО 1931) получаемого материала благодаря изменению в химической природе структурного звена ПФХ и использованию полимерных матриц с разными фотофизическими и физико-химическими свойствами. Полученный материал может использоваться в конструировании фото- и электролюминесцирующих устройств, информационных люминесцирующих панелей, осветительных приборов, декоративных люминесцирующих устройств.
Реферат
Изобретение относится к новым композиционным полимерным материалам для светоизлучающих систем. Предложен фотолюминесцентный полимерный композиционный материал, включающий 1,6 мас.% полифенилхинолина (ПФХ) - поли[2,2′-(9-додецилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолина)] или поли[2,2′-(9-окта-децилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолина)] и 98,4 мас.% полимерной матрицы. Полимерную матрицу выбирают из группы, включающей полистирол, сополимер винилового спирта с винилацетатом, поли-N-винилкарбазол и полиметилметакрилат. Варьирование длины бокового радикала при карбазольном фрагменте ПФХ обеспечивает растворимость ПФХ в широком ряду растворителей, что важно для технологического использования, а также обеспечивает варьирование взаимодействия между донорными и акцепторными фрагментами в полимерном композите, что позволяет настраивать координаты цветности фотолюминесцентного материала. 4 ил., 1 табл., 8 пр.
Формула
1,6 мас.% полифенилхинолина - поли[2,2′-(9-додецилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолина)] или поли[2,2′-(9-окта-децилкарбазол-3,6-диил)-6,6′-(окси)бис(4-фенилхинолина)] формулы:
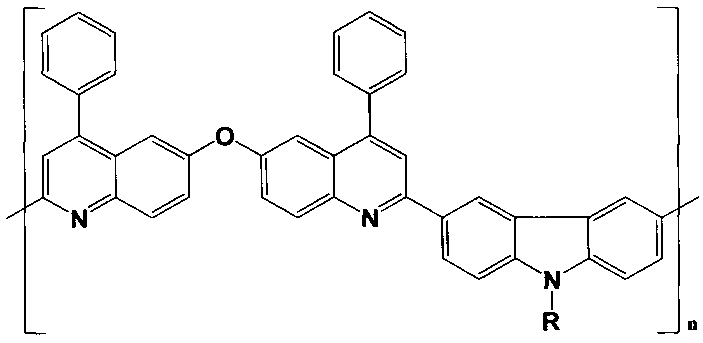
где R - С12Н25 или C18H37, и
98,4 мас.% полимерной матрицы, выбранной из группы, включающей полистирол, сополимер винилового спирта с винилацетатом, поли-N-винилкарбазол или полиметилметакрилат - матрицы разной функциональной направленности - фотоинертные, фотоактивные - поглощающие и люминесцирующие, обладающие дырочной или электронной проводимостью, а также способные к межмакромолекулярному взаимодействию с функциональными группами вводимого компонента либо вызывающие его сегрегацию.
Документы, цитированные в отчёте о поиске
Полимеры, производные бензобис(силолотиофена), и их применение в качестве органических полупроводников
Состав для получения инжектирующих дырки или транспортирующих дырки слоев в электролюминесцентных устройствах, органических элементах солнечных батарей, органических лазерных диодах, органических тонкопленочных транзисторах или органических полевых транзи

Комментарии