Композиция для раневых повязок - RU2748184C2
Код документа: RU2748184C2
Чертежи







Описание
Настоящее изобретение относится к композиции, которая может быть использована в качестве или как часть раневой повязки и к раневым повязкам, включающим указанную композицию. Точнее, настоящее изобретение относится к композиции, которая разрушает и уничтожает бактерии в биопленке и также предотвращает образование биопленки.
Описание биопленок представлено Philips PL, et al., Biofilms Made Easy, Wounds International 2010, 1(3) и суммировано в настоящем описании. Биопленка представляет собой любую группу микроорганизмов, в которой клетки эффективно прилипают друг к другу на поверхности. Биопленкой может быть комплексное микробное сообщество, содержащее бактерии и грибы. Микроорганизмы часто встраиваются в самопродуцируемую матрицу внеклеточных полимерных веществ (EPS). EPS биопленки, которые также называют как слизь (хотя необходимо понимать, что не все называемое слизью является биопленкой), представляет собой полимерный конгломерат, обычно состоящий из внеклеточной ДНК, белков и полисахаридов. Матрица EPS может крепко прикреплять биопленку к живым или неживым поверхностям.
Известно, что биопленки образуются на поверхностях медицинских устройств, таких как мочевые катетеры, импланты и швы. Это представляет собой проблему, т.к. они участвуют в заболеваниях, которые характеризуются лежащей в основе бактериальной инфекцией и хроническим воспалением.
Областью настоящего изобретения принципиально является уход за ранами. Биопленки обычно обнаруживают в ранах, но только относительно недавно их приняли, как вызывающие замедленное заживление ран. Даже предполагали, что почти все хронические раны имеют сообщества биопленки на по меньшей мере части раневого ложа.
Биопленки могут образовываться на живых или неживых поверхностях и могут преобладать в естественном, промышленном и госпитальном окружении. В естественных условиях микроорганизмы, такие как бактерии, могут прикрепляться к поверхностям и образовывать биопленки. Когда бактерии размножаются, они становятся тесно прикрепленным к поверхности. После прикрепления бактерии секретируют EPS с образованием защитной матрицы. Это затем приводит к образованию небольших бактериальных колоний, образующих исходную биопленку. С течением времени биопленка может диспергироваться и прикрепляться к другим частям раневого ложа, образуя новые колонии биопленки.
Образование биопленок может развиваться относительно быстро, биопленка, способна образовываться в течение менее 24 часов.
Считают, что биопленки стимулируют хронический воспалительный ответ в попытке очистить рану от биопленки. Такой ответ приводит к обилию нейтрофилов и макрофагов, окружающих биопленки. Такие воспалительные клетки секретируют большое количество реактивных форм кислорода (ROS) и протеаз (матриксные металлопротеиназы (MMP) и эластазу). Протеазы могут помочь разрушить прикрепление между биопленками и тканью, вытесняя биопленку из раны. Однако ROS и протеазы также повреждают нормальные и заживляющие ткани, белки и иммунные клетки. Хронический воспалительный ответ не всегда успешен в удалении биопленки, и предположили, что в ответе участвует биопленка. Путем индукции неэффективного воспалительного ответа, биопленка защищает микроорганизмы, которые содержит, и увеличивает продукцию экссудата, что обеспечивает источник питания и помогает сохранять биопленку.
В настоящее время одним из наиболее эффективных методов для уменьшения нежелательных эффектов биопленок является физическое удаление биопленки, известное как хирургическая обработка раны. Хирургическая обработка раны включает удаление мертвых и зараженных тканей из раны. Однако такой процесс имеет ограничения, так как никакая форма хирургической обработки раны не может удалить всю биопленку. Следовательно, биопленка имеет возможность восстановиться в течение короткого периода времени. В результате этого, пациент часто должен подвергаться хирургической обработке раны.
Также изучали попытки предотвратить повторное образование биопленки. Преимущественно, в таких методах используют антимикробные средства для уничтожения микроорганизмов. Однако существуют некоторые ограничения этого метода, в том смысле, что антимикробные средства могут быть использованы различными путями и необходимо рассматривать чувствительность и аллергию пациента.
Следовательно, существует необходимость разработать улучшенные методы уничтожения бактерий в биопленке и также предотвращать повторное образование биопленки.
Настоящее изобретение было осуществлено из рассмотрения вышеупомянутых ограничений и проблем.
В соответствии с первым аспектом настоящего изобретения обеспечивают композицию, включающую первый компонент, выбираемый из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина и любых их комбинаций, по меньшей мере одну трехосновную кислоту и по меньшей мере одну растворяющую кислоту.
Неожиданно было обнаружено, что композиция, включающая первый компонент, по меньшей мере одну трехосновную кислоту и по меньшей мере одну растворяющую кислоту, способна разрушать и предотвращать образование биопленки и обладает антимикробным эффектом в отношении микроорганизмов в биопленке.
Биопленкой, описанной в настоящем описании, предпочтительно является биопленка на основе микробов, хотя изобретение не ограничено таковой.
Термин 'трехосновная кислота' (которая также может называться, как 'трехосновная кислота') используют в настоящем описании для обозначения кислоты, которая имеет три иона водорода для отдачи основанию в кислотно-основной реакции. Иными словами, трехосновная молекула имеет три заменяемых атома водорода.
Композиция может включать одну или более трехосновных кислот. Следовательно, композиция может включать две, три, четыре или более трехосновных кислот. Типично композиция включает одну трехосновную кислоту.
Трехосновная кислота может быть выбрана из группы, состоящей из лимонной кислоты, фосфорной кислоты или их смесей.
Предпочтительно, трехосновной кислотой является лимонная кислота.
Трехосновная кислота может находиться в форме гранул, хлопьев, порошков или растворов. Типично, трехосновная кислота поставляется в форме порошка.
В получении композиции по настоящему изобретению трехосновная кислота обычно находится в форме кислого раствора. Такой раствор получают путем растворения некоторого количества трехосновной кислоты, обычно в форме порошка, в некотором объеме воды и/или растворителя. Растворитель может быть водным или неводным, но предпочтительно является неводным.
Композиция может включать смесь первого компонента и трехосновной кислоты. Трехосновная кислота может находиться в контакте с первым компонентом.
Типично, трехосновная кислота абсорбируется в, или наносится на по меньшей мере часть первого компонента. Предпочтительно трехосновную кислоту наносят на по меньшей мере часть поверхности первого компонента. Более предпочтительно, трехосновную кислоту наносят на по существу всю поверхность первого компонента.
Антимикробными средствами обычно называют вещества, которые уничтожают или ингибируют рост микроорганизмов. Обычно принято в заживлении ран, что чтобы вещество проявляло антимикробную эффективность, оно должно демонстрировать степень уничтожения бактерий Log4.
Термин 'антимикробный' используется в настоящем описании для описания средства или вещества, способного демонстрировать степень уничтожения бактерий Log4 в течение 24 часов. Наоборот, термин 'не-антимикробный' используют в настоящем описании, как относящийся к средству или веществу, которое демонстрирует менее чем Log4 степень уничтожения бактерий в течение 24 часов
Первый компонент может быть не-антимикробным.
Соотношение первого компонента к по меньшей мере одной трехосновной кислоте может составлять по меньшей мере 2:1.
Соотношение по меньшей мере одной трехосновной кислоты к по меньшей мере одной растворяющей кислоте составляет по меньшей мере 1:1.
Первый компонент может находиться в форме волокон, гранул, хлопьев, порошка или их комбинаций.
Первый компонент может быть полностью или частично покрыт трехосновной кислотой.
Типично, первый компонент включает волокна. Волокна могут быть ткаными или неткаными. Предпочтительно волокна являются неткаными. Волокна могут быть полностью или частично покрыты трехосновной кислотой.
Альтернативно, композиция может включать отдельные части первого компонента и трехосновной кислоты. Например, первый компонент может быть в форме волокон, гранул, хлопьев, порошка, одного или более листов или их комбинаций и трехосновная кислота может находиться в форме гранул, хлопьев или порошка, посредством чего первый компонент и трехосновная кислота располагаются в отдельных частях композиции. Отдельные части могут, например, быть представлены в форме слоев. Альтернативно, трехосновная кислота и первый компонент могут быть смешаны.
Дополнительно или альтернативно, трехосновная кислота может быть ассоциирована с материалом носителем. Следовательно, композиция может включать первый компонент, выбираемый из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина и их комбинаций; и по меньшей мере одну трехосновную кислоту, где трехосновная кислота ассоциирована с материалом носителем.
Трехосновная кислота может быть абсорбирована в или нанесена на материал носитель. Материал носитель может действовать как носитель для трехосновной кислоты. В таких вариантах осуществления изобретения трехосновная кислота не должна реагировать или необратимо связываться с материалом носителем. Материал носитель может включать любой подходящий материал, который может абсорбировать, получать или действовать как носитель для трехосновной кислоты. Типичные материалы включают, без ограничения, полимеры, такие как целлюлоза, производные целлюлозы (например, этилцеллюлоза, метилцеллюлоза и др.), хлопок, альгинат, вискоза, полипропилен, полиэтилен или любая комбинация таких материалов. Предпочтительно материалом носителем является вискоза.
Типично, материал носитель является волокнистым. В некоторых вариантах осуществления изобретения первый компонент и материал носитель могут быть смешаны вместе для получения нетканого изделия. Первый компонент и материал носитель могут быть прикреплены или сшиты вместе.
Предпочтительно, однако, композиция не включает материал носитель. Трехосновная кислота предпочтительно нанесена на по меньшей мере часть первого компонента, как объяснено ранее.
Трехосновная кислота может быть нанесена на первый компонент и/или материал носитель любыми подходящими средствами, известными в области техники.
Обычно трехосновная кислота, как правило в форме порошка, растворяется в воде с образованием кислого раствора. Кислый раствор затем может быть смешан с растворителем. Первый компонент затем смешивают со смесью кислого раствора/растворителя. Растворитель и необязательно часть воды могут быть удалены путем выпаривания, например, для получения твердой композиции по настоящему изобретению. Типично, композиция включает трехосновную кислоту, нанесенную на первый компонент.
Альтернативно, трехосновная кислота может быть смешана с водой и/или растворителем, как объяснено выше, и распылена на первый компонент.
Предпочтительно, первый компонент не растворяют в растворителе во время получения композиции. Предпочтительно, первый компонент является нерастворимым в кислом растворе или смеси кислого раствора/растворителя.
Наблюдали, что получение исходной композиции первого компонента и трехосновной кислоты без начального растворения первого компонента в растворителе, и/или когда первый компонент не растворяется в смеси кислого раствора/растворителя, допускает эффективное получение композиции, имеющей большее количество первого компонента, которое может быть доставлено в рану. При использовании первого компонента, который исходно растворяется в растворителе, является предпочтительным, когда общее количество доступного первого компонента растворяется в присутствии растворителя. Более того, в ситуациях, когда первый компонент растворяется при получении, конечная композиция не может находиться в форе волокон, гранул или порошка, что ограничивает потенциальное применение и формы композиции. Первый компонент, следовательно, является нерастворимым в воде и растворителе.
В случаях, когда первый компонент включает волокна хитозана, растворителем предпочтительно является неводный растворитель, такой как изопропиловый спирт.
Трехосновную кислоту предпочтительно доставляют в форме кислого раствора. Кислый раствор (кислота в воде) может иметь концентрацию от около 5-80%, предпочтительно от около 20-60% и наиболее предпочтительно от около 40-50%.
Трехосновная кислота может присутствовать в композиции в количестве, более чем около 2% первого компонента, предпочтительно более чем около 5% первого компонента, более предпочтительно более чем около 10% первого компонента и наиболее предпочтительно более чем около 25% первого компонента. Трехосновная кислота может присутствовать в композиции в количестве по меньшей мере около 2% первого компонента, предпочтительно по меньшей мере около 5% первого компонента, более предпочтительно по меньшей мере около 10% первого компонента и наиболее предпочтительно по меньшей мере около 25% первого компонента.
Трехосновная кислота может присутствовать в количестве около 2-75% первого компонента, предпочтительно около 10-75% первого компонента, более предпочтительно около 20-75% первого компонента и наиболее предпочтительно в количестве около 25-60% первого компонента. Хорошие результаты наблюдали с трехосновной кислотой, присутствующей в количестве около 60% первого компонента. Процентное значение кислоты относится к относительным количествам трехосновной кислоты по сравнению с общим количеством первого компонента в композиции. Например, если общее количество первого компонента в композиции составило 1 г, композиция, включающая 20% трехосновной кислоты, содержит 0,2 г трехосновной кислоты.
Первый компонент выбирают из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина и любых их комбинаций.
Термин 'производное' используют в настоящем описании для обозначения соединения, которое происходит из хитозана или хитина после одной или более химических реакций или модификаций. Одна или более химических реакций или модификаций могут включать замену одного или более амино или гидроксильных протонов в хитозане или хитине; или частичное деацетилирование хитина. Например, производное хитина может включать частично деацетилированный хитин, который может иметь различный процент деацетилирования, если желательно. Типично, частично деацетилированный хитин, подходящий для применения в настоящем изобретении, имеет степень деацетилирования по меньшей мере около 50%, более типично по меньшей мере около 75% и наиболее типично по меньшей мере около 85%. Также включают в термины 'производные хитозана или хитина' продукты реакции хитозана или хитина с другими соединениями. Такие продукты реакции включают, без ограничения, карбоксиметилхитозан, гидроксилбутилхитин, N-ацилхитозан, O-ацилхитозан, N-алкилхитозан, O-алкилхитозан, N-алкилиденхитозан, N-арилиденхитозан, O-сульфонилхитозан, сульфатированный хитозан или хитин, фосфорилированый хитозан или хитин, нитрированный хитозан или хитин, деоксигалохитозан, алкалихитин, алкалихитозан, или хелаты металлов с хитозаном, органические соли и др. Производные хитина или хитозана, включая таковые, на которые ссылаются в настоящем описании, также могут содержать функциональные группы, связанные с ними посредством ковалентных или нековалентных связей.
Типично, первым компонентом является хитозан или производное хитозана. Предпочтительно первым компонентом является хитозан.
Хитозаном является производное твердых отходов обработки моллюсков и он может быть экстрагирован из культуры грибов. Он является катионным полимерным материалом, который является нерастворимым в воде. Хитозан является известным кровоостанавливающим средством для применения в перевязке ран. Термин 'кровоостанавливающее средство' используют в настоящем описании, как относящееся к любому средству, которое способно давать сгусток или пробку, которая останавливает или уменьшает кровотечение, когда она контактирует с кровью или другими жидкостями тела, такими как раневой экссудат, из физиологического целевого участка или области раны человека или животного.
Существует множество различных типов хитозана, которые могут быть использованы в качестве материала в раневых повязках, с различными свойствами абсорбции. Различные типы хитозана могут иметь различную молекулярную массу, различные степени деацетилирования, различное расположение β-(1-4)-связанного D-глюкозамина и мономеров N-ацетил-D-глюкозамина, различные хиральные формы или они могут быть получены из различных видов или источников (и грибов), или могут быть обработаны различным образом во время производства. Каждый и все из таких различных вариаций материалов хитозана используются для применения в настоящем изобретении.
Первый компонент хитозан может иметь степень деацетилирования более чем 70%, предпочтительно более чем 80% и более предпочтительно более чем 85%.
Материалы хитозана могут проявлять гелеобразующие свойства, когда находятся в форме соли. Для получения соли хитозана, хитозан обычно смешивают с соответствующей кислотой. Гелеобразующие свойства солей хитозана делают их желательными для применения в качестве материалов в раневых повязках.
Хитозан и/или производное хитозана могут находиться в любой подходящей форме, такой как, например, волокна, гранулы, порошок, хлопья, лист, пена, лиофилизированная пена, прессованная пена, пленка, перфорированная пленка, шарики и комбинации двух или более из вышесказанного. Типично, хитозан и/или производное хитозана находятся в форме волокон. Предпочтительно волокна являются неткаными. Волокна могут быть любого желаемого диаметра или длины и могут быть сформированы в текстильное изделие или подушечку для применения.
Типично, молекулярная масса первого компонента, используемого в композиции по настоящему изобретению, составляет менее чем около 2000000, более типично менее чем около 1000000, и еще более типично менее чем около 500000, и наиболее типично менее чем около 175000.
Первый компонент в 1% растворе уксусной кислоты может иметь вязкость более чем 150 сП.
Композиция по настоящему изобретению включает растворяющую кислоту.
Термин 'растворяющая кислота' используется в настоящем описании как относящийся к кислоте, которая, при нанесении на или ассоциации с первым компонентом делает первый компонент более растворимым в водных жидкостях организма.
Композиция может включать одну или более растворяющих кислот. Композиция может, следовательно, включать две, три, четыре или более растворяющих кислот. Типично композиция включает одну растворяющую кислоту.
Растворяющая кислота может быть выбрана из группы, состоящей из янтарной кислоты, яблочной кислоты, серной кислоты, акриловой кислоты, молочной кислоты, муравьиной кислоты, уксусной кислоты, соляной кислоты, азотной кислоты и смесей любого одного или более из них.
Растворяющей кислотой может предпочтительно быть одноосновная кислота.
Термин 'одноосновная кислота' (который также может называться здесь 'моноосновная кислота') используют в настоящем описании как относящийся к кислоте, которая имеет один ион водорода, чтобы отдавать основанию в кислотно-основной реакции. Иными словами, одноосновная молекула имеет один замещаемый атом водорода.
Одноосновная кислота может быть выбрана из группы, состоящей из молочной кислоты, муравьиной кислоты, уксусной кислоты, соляной кислоты, азотной кислоты и смесей любой одной или более из них.
Предпочтительно, одноосновной кислотой является молочная кислота, уксусная кислота или их смесь. Наиболее предпочтительно, одноосновной кислотой является молочная кислота.
Растворяющая кислота может находиться в форме гранул, порошка или раствора. Типично, растворяющая кислота находится в форме раствора. Такой раствор получают путем растворения некоторого количества растворяющей кислоты в объеме воды и/или растворителя.
Композиция включает смесь первого компонента, по меньшей мере одной трехосновной кислоты и по меньшей мере одной растворяющей кислоты.
Растворяющая кислота может быть смешана с трехосновной кислотой и контактировать с первым компонентом таким образом, как описано выше в отношении трехосновной кислоты отдельно. Альтернативно, трехосновная и растворяющая кислоты могут контактировать с отдельными частями первого компонента и затем объединяться в композицию. Например, когда первый компонент находится в форме волокон, выбор волокон может быть частично или полностью покрыт трехосновной кислотой и отдельный выбор волокон может быть частично или полностью покрыт растворяющей кислотой.
Типично, растворяющая кислота смешивается с трехосновной кислотой и контактирует с первым компонентом.
По меньшей мере одна растворяющая кислота или смесь по меньшей мере одной растворяющей кислоты и по меньшей мере одной трехосновной кислоты могут быть абсорбированы в, или нанесены оболочкой на, по меньшей мере часть первого компонента. Предпочтительно, по меньшей мере одна растворяющая кислота или смесь по меньшей мере одной растворяющей кислоты и по меньшей мере одной трехосновной кислоты наносят на по существу всю поверхность первого компонента. В некоторых вариантах осуществления изобретения трехосновная кислота может быть абсорбирована в, или нанесена на, по меньшей мере часть первого компонента, и растворяющая кислота может затем быть абсорбирована в или нанесена на, по меньшей мере часть такового или наоборот.
Альтернативно, композиция может включать отдельные части первого компонента, по меньшей мере одну трехосновную кислоту и по меньшей мере одну растворяющую кислоту. Например, первый компонент может находиться в форме волокон, гранул, хлопьев, порошка, листа или их комбинаций, и трехосновная и растворяющая кислоты могут находиться в форме гранул, хлопьев и/или порошка, посредством чего первый компонент и кислоты располагаются в различных частях композиции. Например, отдельные части могут, например, находиться в форме слоев. Альтернативно, первый компонент, трехосновная кислота и растворяющая кислота могут быть смешаны.
В некоторых вариантах осуществления изобретения по меньшей мере одна трехосновная кислота и по меньшей мере одна растворяющая кислота могут быть ассоциированы с одним и тем же или с отдельными материалами носителями. Композиция, следовательно, может включать первый компонент, выбираемый из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина, и их комбинаций; по меньшей мере одной трехосновной кислоты и по меньшей мере одной растворяющей кислоты, где трехосновная кислота и/или растворяющая кислота ассоциированы с одним или отдельными материалами носителями.
Растворяющая кислота может быть ассоциирована с материалом носителем тем же образом, как описано в настоящем описании в отношении трехосновной кислоты.
Растворяющая кислота может быть нанесена на первый компонент и трехосновная кислота может быть нанесена на материал носитель, или наоборот.
Первый компонент может включать волокна, покрытые растворяющей кислотой, и материал носитель может быть покрыт трехосновной кислотой. Материалом носителем может быть вискоза.
По меньшей мере одна растворяющая кислота может быть нанесена на первый компонент и/или материал носитель теми же средствами, как описано для трехосновной кислоты.
Первый компонент может быть частично или полностью покрыт оболочкой из растворяющей кислоты.
Растворяющая кислота предпочтительно поступает в форме кислого раствора. Кислый раствор (кислота в воде) может иметь концентрацию по меньшей мере около 40%, предпочтительно по меньшей мере около 60% и наиболее предпочтительно по меньшей мере около 80%.
По меньшей мере одна растворяющая кислота может присутствовать в количестве, большем чем около 2% первого компонента, предпочтительно более чем 5% первого компонента и более предпочтительно более чем около 10% первого компонента. По меньшей мере одна растворяющая кислота может присутствовать в количестве по меньшей мере около 2% первого компонента, предпочтительно по меньшей мере около 5% первого компонента, более предпочтительно по меньшей мере около 10% первого компонента и наиболее предпочтительно по меньшей мере около 25% первого компонента.
По меньшей мере одна растворяющая кислота может присутствовать в количестве около 2-50% первого компонента, предпочтительно около 10-40% первого компонента или более предпочтительно около 20-30% первого компонента. Предпочтительно по меньшей мере одна растворяющая кислота может присутствовать в количестве около 25% первого компонента. Тем же образом как для трехосновной кислоты процентные значения относятся к относительным количествам растворяющей кислоты по сравнению с общим количеством первого компонента.
Было обнаружено, что при отсутствии растворяющей кислоты более высокое количество трехосновной кислоты в композиции приводит к большей эффективности в отношении микроорганизмов. Такая композиция может включать трехосновную кислоту в количестве по меньшей мере около 25%, предпочтительно по меньшей мере около 35%, более предпочтительно по меньшей мере около 50% и наиболее предпочтительно по меньшей мере около 60% первого компонента.
Однако было обнаружено в исследованиях, что композиция, имеющая содержание растворяющей кислоты около 15-30% первого компонента может уменьшать количество трехосновной кислоты, требуемое для оказания желаемого эффекта. Например, было показано, что композиция, имеющая содержание трехосновной кислоты более чем 20%, дает сравнимые результаты относительно композиции, имеющей содержание растворяющей кислоты 15-20%, но сниженное количество трехосновной кислоты около 5% или менее.
Следовательно, вариант осуществления настоящего изобретения включает композицию, включающую первый компонент, выбираемый из группы, состоящей их хитозана, хитина, производных хитозана, производных хитина и их комбинаций; 20-75% по меньшей мере одной трехосновной кислоты и 10-40% по меньшей мере одной растворяющей кислоты.
Хорошие результаты наблюдали для композиции, имеющей содержание растворяющей кислоты от 20-35%, особенно 25-30%, первого компонента и содержание трехосновной кислоты от 25-45%, особенно 30-40%, первого компонента.
Комбинированная кислота может присутствовать в композиции в количестве по меньшей мере около 4% первого компонента, предпочтительно по меньшей мере около 10% первого компонента, более предпочтительно по меньшей мере около 25% первого компонента и наиболее предпочтительно по меньшей мере около 45% первого компонента.
Композиция по настоящему изобретению может находиться в форме гранул, хлопьев, волокон, порошка, нетканого текстиля, или сшитого текстиля, геля, гидрогелевого листа, гидрогеля и/или пленки. Волокна могут быть ткаными или неткаными. Предпочтительно волокна являются неткаными.
Типично, композиция находится в форме волокон. Более типично, композиция находится в форме нетканых волокон или нетканого текстиля.
Альтернативно, композиция может находиться в форме геля, гидрогеля или жидкости. Находясь в указанных формах, композиция может быть использована без дополнительной модификации (например, она может быть нанесена непосредственно на рану) или композиция может быть нанесена на средство доставки.
Гидрогель получают путем получения раствора трехосновной кислоты и растворяющей кислоты в воде, необязательно, смешивая раствор с растворителем и добавляя первый компонент к раствору. Первый компонент абсорбирует раствор и гель. Степень гелеобразования и прочность геля может варьироваться посредством количества первого компонента, добавленного к раствору. Чем больше количество первого компонента в растворе, тем плотнее гель и наоборот. Затем гель может быть высушен в различной степени в зависимости от формы желаемой композиции.
Альтернативно, гидрогель получают путем получения композиции по настоящему изобретению в сухой форме, например, гранул, хлопьев, волокон, порошка, текстиля, и смешивания с водой. Композиция абсорбирует воду и гель. Также степень гелеобразования и плотность геля может варьироваться от количества композиции, смешанной с водой, или от количества воды, смешанной с композицией. Чем больше количество композиции относительно воды, тем плотнее гель и наоборот. Затем гель может быть высушен в различной степени в зависимости от формы желаемой композиции.
Например, гидрогелевый лист может быть получен путем переноса гидрогеля в шаблон, такой как кювета, и сушки гидрогеля в такой степени, чтобы не удалить всю воду, но оставить достаточно воды для получения геля.
Альтернативно, сухая пленка может быть получена путем переноса гидрогеля в шаблон, такой как кювета, и сушки гидрогеля с такой степени, чтобы удалить по существу всю воду. Полученная композиция находится в форме сухой пленки. Пленка предпочтительно является гибкой.
Средство доставки может включать полиуретановую пену, полиуретановую пленку, тканый текстиль, суперабсорбирующий материал, медицинское устройство, такое как катетер, стент и подобное. Средство доставки может включать более чем один из каждого из вышеуказанных компонентов и/или может включать комбинацию одного или более из вышеуказанного.
Например, средство доставки может включать одну или более из полиуретановых пен и полиуретановой пленки. Альтернативно, средство доставки может включать тканый вискозный текстиль.
Термин 'суперабсорбирующий материал' используют в настоящем описании, как относящийся к гидрофильному материалу, который является набухающим в воде, но не водорастворимым, и который способен абсорбировать жидкость до более чем 2000% с удержанием жидкости более чем 85%. Предпочтительно суперабсорбирующий материал способен абсорбировать жидкость до более чем 2500% с удержанием жидкости более чем 90%.
Термин 'разбухающий в воде' используют в настоящем описании как относящийся к материалу, который, при контакте с водой или жидкостью, содержащей воду, будет абсорбировать жидкость и набухать, но по существу не растворяется в такой жидкости.
Термин 'водорастворимый' используют в настоящем описании, как относящийся к материалу, который при контакте с водой или жидкостью, содержащей воду, растворяется в такой жидкости.
Суперабсорбирующий материал может быть выбран из полимерных материалов, таких как поли(виниловый) спирт (PVA), поли(этиленоксид) (PEO) и поли(акриловая кислота). Суперабсорбирующий материал может быть химически модифицирован. Например, суперабсорбирующим материалом может быть полимерный материал, полученный путем графт-полимеризации акриловой кислоты на цепи карбоксиметилцеллюлозы. Суперабсорбирующий материал может включать химически модифицированный материал, выбираемый из крахмала, целлюлозы и полимерных материалов, таких как поли(виниловый спирт) (PVA), поли(этиленоксид) (PEO), и поли(акриловая кислота). Поли(акриловая кислота) может быть частично нейтрализованной, немного сшитой поли(акриловой кислотой).
Термины ʺперекрестная сшивкаʺ и ʺперекрестно сшитыйʺ используют в настоящем описании как относящиеся к двум или более полимерным цепям, связанным первичной связью, такой как ковалентная связь. Термин ʺнемного перекрестно сшитыйʺ используется в настоящем описании, как относящийся к вариантам осуществления изобретения, где ряд сшивающих первичных связей в суперабсорбирующем материале равен менее чем общему количеству возможных сшивающих связей.
В некоторых вариантах осуществления изобретения суперабсорбирующий материал выбирают из полимерных материалов, таких как PVA, PEO, и поли(акриловая кислота), предпочтительно, частично нейтрализованной, немного перекрестно сшитой поли(акриловой кислоты). Типично, суперабсорбирующий материал является частично нейтрализованной, немного перекрестно сшитой поли(акриловой кислотой).
Суперабсорбирующий материал может находиться в форме волокон. Типично, суперабсорбирующий материал находится в форме нетканых волокон. Длина волокон может составлять до 100 мм, и составляет типично от 20-75 мм, более типично от 32 до 51 мм.
Средством доставки может быть раневая повязка, известная в области техники.
Композиция по настоящему изобретению может наноситься на средство доставки любыми подходящими средствами, известными в области техники.
Композиция по настоящему изобретению может включать первый компонент, выбираемый из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина и их комбинаций; по меньшей мере одну трехосновную кислоту и по меньшей мере одну растворяющую кислоту, где первый компонент является по меньшей мере частично покрыт трехосновной кислотой и растворяющей кислотой.
Композиция может включать первый волокнистый компонент, выбираемый из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина и их комбинаций; и по меньшей мере одну трехосновную кислоту и по меньшей мере одну растворяющую кислоту, где волокна первого компонента являются по меньшей мере частично покрытыми оболочкой из трехосновной кислоты и растворяющей кислоты.
Типично, композиция включает волокнистый хитозановый первый компонент, по меньшей мере частично покрытый оболочкой из трехосновной кислоты и растворяющей кислоты. Предпочтительно, композиция включает нетканый волокнистый хитозановый первый компонент, по меньшей мере частично покрытый оболочкой из лимонной кислоты и молочной кислоты. Предпочтительно еще композиция включает нетканый волокнистый хитозановый первый компонент, по существу полностью покрытый оболочкой из смеси лимонной кислоты и молочной кислоты.
В соответствии с дополнительным аспектом настоящего изобретения обеспечивают раневые повязки, включающие композицию, как описано в настоящем описании.
Раневой повязкой может быть раневая повязка, которая образует гель при контакте с жидкостью, такой как раневой экссудат. В области гелеобразующих раневых повязок, которые сфокусированы на задержке кровотечения из кровоточащей раны, особенно неожиданно для композиции по настоящему изобретению, что трехосновная кислота на нетканых раневых повязках не имеет тенденции к гелеобразованию и оказывает отрицательное влияние на поглощение и удержание воды.
Раневая повязка может включать композицию, как описано в настоящем описании, и средство доставки, как описано в настоящем описании. Композиция может наноситься на средство доставки путем нанесения оболочки или подобным. Композиция и средство доставки могут образовывать многослойные раневые повязки.
Композиция по настоящему изобретению или раневая повязка, включающая такую композицию, также может включать дополнительные компоненты. Такие дополнительные компоненты включают, без ограничения, антимикробные средства; фармацевтические средства; комплексообразующие средства; увлажняющие средства, такие как поверхностно-активные вещества; факторы роста; цитокины; средства, которые абсорбируют средства, которые замедляют заживление, такие как MMP (матриксные металллопротеиназы) и эластаза; и/или другие компоненты раневых повязок, такие как кальций, витамин K, фибриноген, тромбин, фактор VII, фактор VIII, глины, такие как каолин, окисленная регенерированная целлюлоза, желатин или коллаген и др.
Подходящие антимикробные средства могут быть выбраны из списка, включающего серебро, полигексаметилен бигуанид (PHMB), йод, октенидин, медь, хлоргексидина глюконат (CHG), миконазол, метронидазол и комбинации одного или более из них.
Антимикробное средство может быть нанесено на или абсорбировано в первый компонент и/или материал носитель таким же образом, как описано в настоящем описании в отношении трехосновной и/или растворяющих кислот.
Композиция по настоящему изобретению может быть смешана с другими композициями, применимыми в уходе за ранами. В некоторых вариантах осуществления изобретения композиция по настоящему изобретению может быть смешана или перемешана с одним или более кровоостанавливающими средствами. Кровоостанавливающие средства могут находиться в форме волокон, гранул, хлопьев, порошка или любой их комбинации. Предпочтительно, кровоостанавливающее средство находится в форме гранул.
Например, композиция по настоящему изобретению, как описано в настоящем описании, может быть перемешана с кровоостанавливающим средством, таким как гранулы Celox®, коммерчески доступное кровоостанавливающее средство на основе хитозана.
В соответствии с дополнительным аспектом настоящего изобретения обеспечивают композицию, как описано в настоящем описании, для применения в качестве терапевтического средства.
В соответствии с дополнительным аспектом настоящего изобретения обеспечивают композицию, как описано в настоящем описании, для применения в лечении ран.
В соответствии с дополнительным аспектом настоящего изобретения обеспечивают композицию, как описано в настоящем описании, для применения в разрушении и уничтожении бактерий в биопленке.
В соответствии с дополнительным аспектом настоящего изобретения обеспечивают композицию, как описано в настоящем описании, для применения в профилактике образования биопленки.
В соответствии с дополнительным аспектом настоящего изобретения обеспечивают способ получения композиции, включающей первый компонент, выбираемый из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина и их комбинаций; по меньшей мере одну трехосновную кислоту и по меньшей мере одну растворяющую кислоту, способ включает стадии:
(a) покрытия оболочкой по меньшей мере части первого компонента с помощью смеси, включающей по меньшей мере одну трехосновную кислоту и по меньшей мере одну растворяющую кислоту; и/или
(b) абсорбции в по меньшей мере одну часть первого компонента смеси, включающей по меньшей мере одну трехосновную кислоту и по меньшей мере одну растворяющую кислоту.
В соответствии с дополнительным аспектом настоящего изобретения обеспечивают способ получения композиции, включающей первый компонент, выбираемый из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина и их комбинаций; по меньшей мере одну трехосновную кислоту и по меньшей мере одну растворяющую кислоту, способ включает стадии:
(а) смешивание трехосновной кислоты с водой и/или растворителем для получения раствора трехосновной кислоты;
(b) смешивание раствора трехосновной кислоты с раствором растворяющей кислоты, полученным путем смешивания растворяющей кислоты с водой и/или растворителем, для получения раствора смешанной кислоты;
(c) необязательно смешивание раствора смешанной кислоты с растворителем; и
(d) добавление первого компонента к раствору, полученному на стадии (c).
Способ может дополнительно включать стадию (e) сушки смеси, полученной на стадии (d). Стадия сушки может удалять некоторое количество или весь растворитель и/или количество воды в композиции.
Для композиций, где первый компонент включает волокна хитозана, растворитель стадий (a)-(c) обычно является неводным.
Дополнительные аспекты настоящего изобретения могут включать любую или все характеристики, описанные в отношении первого аспекта настоящего изобретения, при желании или если необходимо.
Варианты осуществления настоящего изобретения далее будут дополнительно описаны со ссылками на следующие неограничивающие примеры и сопутствующие чертежи, в которых:
Фиг. 1: представляет собой график, показывающий результаты тестирования с использованием анализа MBEC для Pseudomonas aeruginosa ATCC 13359;
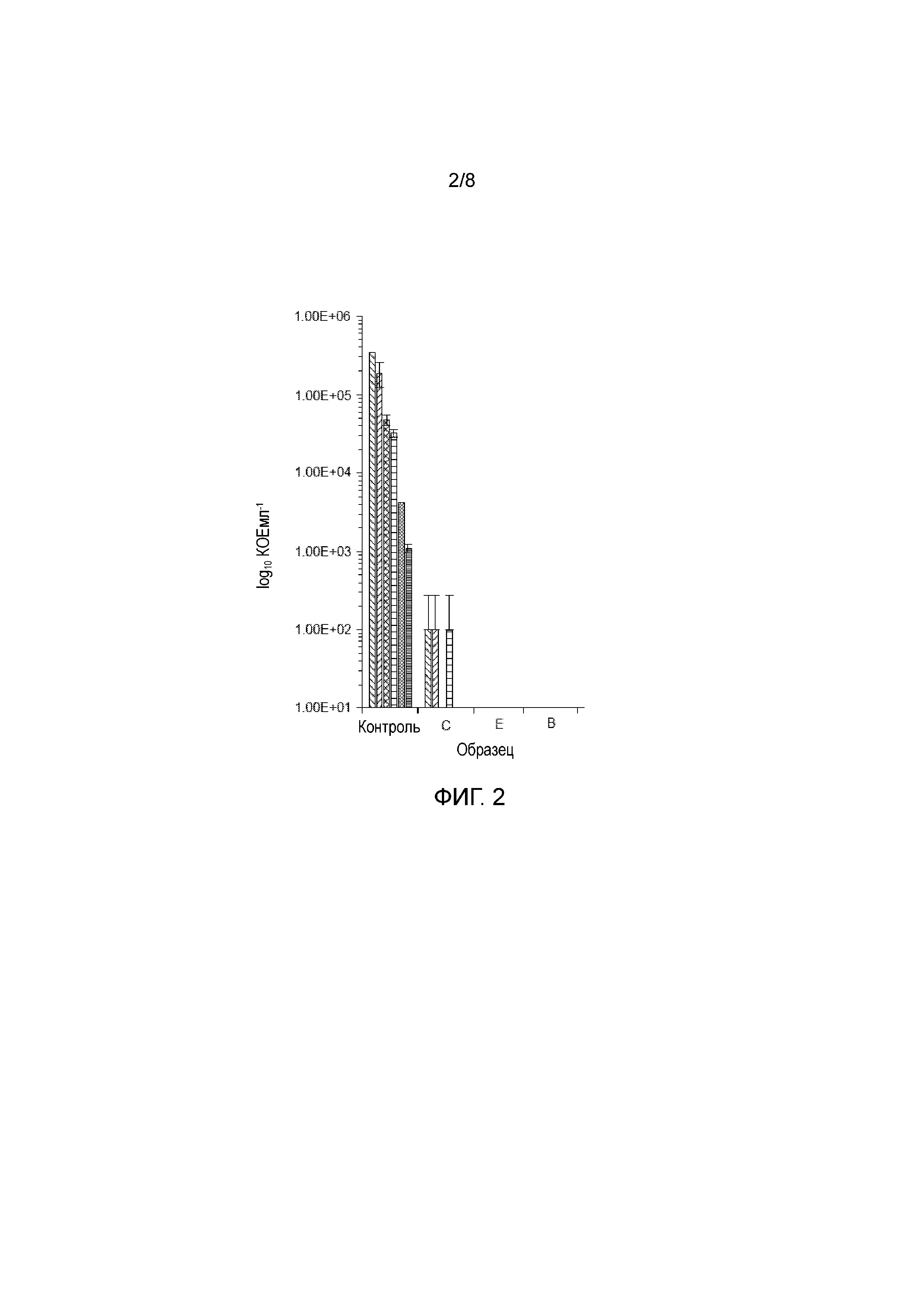
Фиг. 2: представляет собой график, показывающий результаты тестирования с использованием анализа MBEC для Staphylococcus haemolyticus;
Фиг. 3: представляет собой график, показывающий результаты тестирования с использованием анализа MBEC для MRSA 308;
Фиг. 4: представляет собой график, показывающий результаты тестирования с использованием реакторной модели CDC для Pseudomonas aeruginosa ATCC 10434;
Фиг. 5: представляет собой график, показывающий результаты тестирования с использованием реакторной модели CDC для Staphylococcus haemolyticus NCTC 11042;
Фиг. 6: представляет собой график, показывающий результаты тестирования с использованием реакторной модели CDC для метициллин-резистентного Staphylococcus aureus 308;
Фиг. 7: представляет собой график, показывающий результаты тестирования с использованием реакторной модели CDC для Pseudomonas aeruginosa ATCC 10434;
Фиг. 8: представляет собой график, показывающий результаты тестирования с использованием реакторной модели CDC для Pseudomonas aeruginosa ATCC 10434;
Фиг. 9: представляет собой график, показывающий результаты тестирования с использованием реакторной модели CDC для Staphylococcus aureus;
Фиг. 10: представляет собой график, показывающий результаты тестирования с использованием реакторной модели CDC для Staphylococcus aureus;
Фиг. 11: представляет собой график, показывающий количество жизнеспособного Staphylococcus aureus, восстановленного из ранее образованной 24-часовой биопленки после 24 часов обработки каждым средством;
Фиг. 12: представляет собой количество жизнеспособного Staphylococcus aureus, восстановленного из заранее образованной 72-часовой биопленки через 24 часа после обработки каждым средством.
Общие методы получения образца
Общий метод 1: Первый компонент и трехосновная кислота
Порошок трехосновной кислоты (например, лимонной кислоты) растворяли в деионизированной воде и затем смешивали с неводным растворителем (например, IPA). Первый компонент, обычно в форме нетканых волокон, помещали в раствор трехосновной кислоты и позволяли абсорбировать раствор. Затем раствор сушили с использованием термической сушки, оставляя твердый хитозан, хитин или их производные, покрытые трехосновной кислотой.
Общий метод 2: Первый компонент с трехосновной кислотой и одноосновной кислотой
Порошок трехосновной кислоты (например, лимонной кислоты) растворяли в деионизированной воде и затем смешивали с раствором растворяющей кислоты (например, молочной кислоты). Его затем смешивали с неводным растворителем (например, IPA). Первый компонент, обычно в форме нетканых волокон, помещали в смешанный раствор кислоты и позволяли абсорбировать раствор. Затем раствор сушили с использованием термической сушки, чтобы оставить твердый хитозан, хитин или их производные, покрытыми смесью трехосновной кислоты и растворяющей кислоты.
Примерные композиции
Далее представлены примеры композиций, полученные в соответствии с настоящим изобретением.
Пример 1 (контроль)
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,439 г) для получения номинальной 32,5% композиции.
Пример 2 (контроль)
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,027-0,068 г) для получения номинальной 2-5% композиции.
Пример 3 (контроль)
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,27-0,41 г) для получения номинальной 20-30% композиции.
Пример 4 (контроль)
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,81-0,94 г) для получения номинальной 60-70% композиции.
Пример 5:
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,027-0,068 г) и молочной кислотой (0,34 г) для получения номинальной композиции 2-5% трехосновной кислоты и 25% одноосновной кислоты.
Пример 6:
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,27-0,41 г) и молочной кислотой (0,34 г) для получения номинальной композиции 20-30% трехосновной кислоты и 25% одноосновной кислоты.
Пример 7:
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,81-0,94 г) и молочной кислотой (0,41 г) для получения номинальной композиции 60-70% трехосновной кислоты и 30% одноосновной кислоты.
Пример 8:
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,04 г) и молочной кислотой (0,2 г) для получения номинальной композиции 3% трехосновной кислоты и 15% одноосновной кислоты.
Пример 9:
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,34 г) и молочной кислотой (0,2 г) для получения номинальной композиции 25% трехосновной кислоты и 15% одноосновной кислоты.
Пример 10:
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,81 г) и молочной кислотой (0,27 г) для получения номинальной композиции 60% трехосновной кислоты и 20% одноосновной кислоты.
Пример 11:
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,41 г) и молочной кислотой (0,34 г) для получения номинальной композиции 30% трехосновной кислоты и 25% одноосновной кислоты.
Пример 12:
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,54 г) и молочной кислотой (0,34 г) для получения номинальной композиции 40% трехосновной кислоты и 25% одноосновной кислоты.
Пример 13:
Нетканые волокна 100% хитозана (1,35 г) покрывали лимонной кислотой (0,54 г) и молочной кислотой (0,41 г) для получения номинальной композиции 40% трехосновной кислоты и 30% одноосновной кислоты.
Примеры раневых повязок
Пример 14 (контроль)
Получали композицию по настоящему изобретению, содержащую номинально 2 г 100% нетканых волокон хитозана в 8 г деионизированной воды с 0,6 г лимонной кислоты. Композицию наносили на поверхность несетчатой полиуретановой пены и позволяли высохнуть. Пену, содержащую сухую композицию по настоящему изобретению, затем адгезивно связывали с полиуретановой пеной, дистально по отношению к связанному слою полиуретановой пленки, для получения слоя, контактирующего с раной.
Пример 15 (контроль)
Получали композицию по настоящему изобретению, содержащую номинально 2 г 100% нетканых волокон хитозана в 8 г деионизированной воде с 0,6 г лимонной кислоты. Композицию наносили на поверхность тканевого вискозного текстиля и позволяли высохнуть.
Анализ MBEC 1
Для определения эффективности антимикробных агентов в отношении биопленок из различных микроорганизмов, использовали анализ MBEC (минимальная концентрация эрадикации биопленки).
Анализ MBEC представляет собой скрининговый анализ с высоким выходом, используемый для определения эффективности антимикробных средств в отношении биопленок из различных микроорганизмов. Инокулятор биопленок MBEC состоит из пластиковой крышки с 96 штифтами и соответствующим основанием. Существуют два типа оснований, которые могут быть использованы с крышкой MBEC. Одно основание содержит 96 отдельных ячеек. Отдельные ячейки позволяют расти множеству микроорганизмов на тех же штифтах крышки. Другой тип основания является профилированным через основание, которое может содержать только единственный микроорганизм. Биопленки устанавливаются на штифтах в общих условиях (отсутствие тока питательных веществ в или из отдельной ячейки) с аккуратным перемешиванием. Образовавшуюся биопленку переносили в новый 96 луночный планшет для исследования эффективности антимикробных средств. Дизайн исследования позволяет одновременное тестирование множества биоцидов в множестве концентраций с повторными образцами, делая его эффективным скрининговым средством.
Тестируемые микроорганизмы
Pseudomonas aeruginosa ATCC 13359
Staphylococcus haemolyticus
MRSA 308
Сравнительные тестируемые образцы
Контроль: Фосфатный буферный раствор (PBS)
Образец A: 100% нетканые волокна хитозана с Ag (номинально 1%) и молочная кислота для получения номинальной композиции 25% одноосновной кислоты
Образец B: Нетканые волокна карбоксиметилированной целлюлозы с Ag (номинально 1%) (Aquacel Ag®)
Образец C: 100% Нетканые волокна хитозана с молочной кислотой для получения номинальной композиции 25% одноосновной кислоты
Образец D: 100% Нетканые волокна хитозана с уксусной кислотой для получения номинальной композиции 25% одноосновной кислоты
Образец E: 100% Нетканые волокна хитозана с лимонной кислотой для получения номинальной композиции 25% трехосновной кислоты
Получение бактериального инокулята
24 часовую культуру каждого микроорганизма собирали с планшета с триптон соевым агаром (TSA) или планшета с агаром с сердечно-мозговым экстрактом (BHIA) и суспендировали или в 20 мл триптон-соевого бульона (TSB) или 20 мл бульона с сердечно-мозговым экстрактом (BHIB). Полученную бактериальную суспензию разводили для получения исходной ОП590=0,10±0,03, что соответствует бактериальной концентрации 108 КОЕмл-1. Такой исходный инокулят серийно разводили дополнительно шесть раз с целью получения прогрессивно более низкой бактериальной нагрузки (т.е. 107, 106, 105, 104, 103 КОЕмл-1). Исходная бактериальная концентрация для каждого организма составила типично 1×108±5×107 КОЕмл-1.
Анализ MBEC
Биопленку каждого микроорганизма выращивали на проекциях штифтов на крышке планшета микротитратора в течение 48 часов при 37°C, 50 об/мин. Через 48 часов крышки штифтов удаляли, промывали коротко в фосфатном буферном растворе (PBS) для удаления планктонных бактерий и затем помещали в планшет выбора агента в течение 24 часов. Для получения планшета выбора для раневых повязок, кусочки 1 см2 нарезали с использованием стерильных ножниц и помещали в обозначенные ячейки планшета микротитратора. Планшет выбора для теста гранул агента получали путем взвешивания 30 мг±3 мг каждой композиции гранул в ячейках планшета микротитратора. Раневые повязки и гранулы затем активировали 150 мкл PBS. После обработки проекции штифтов на крышке промывали дважды в PBS, затем переносили в 200 мкл нейтрализатора и помещали в ультразвуковую водную баню в течение 5 минут с целью восстановления оставшихся прикрепленных бактерий. Серийные разведения проводили на полученной восстановленной среде, и капельные планшеты использовали для количественной оценки восстановленных бактерий. Все образцы тестировали три раза, если не указано иначе.
Результат показан в таблице 1 и фиг. 1-3. Результаты на фиг. 1-3 относятся к образцам B, C и E.
Очевидно из графиков, показанных на фиг. 1-3, что образец E, включающий хитозан, покрытый трехосновной кислотой, является эффективным против всех трех тестируемых микроорганизмов. Образец C, включающий хитозановые волокна, покрытые одноосновной кислотой, продемонстрировал концентрации микроорганизмов для всех трех тестируемых микроорганизмов. Наконец, образец B, включающий карбоксиметилированную целлюлозу с серебром, показал хорошие результаты в отношении Staphylococcus haemolyticus, но не был эффективным против или Pseudomonas aeruginosa ATCC 13359 или MRSA 308.
Таблица 1: Результаты теста после анализа MBEC
Реакторная модель CDC 1
Для определения способности удаления биопленки семи раневых повязок, против трех бактериальных образцов, с использованием реакторного метода CDC.
Тестируемые микроорганизмы
Staphylococcus haemolyticus NCTC 11042
Pseudomonas aeruginosa ATCC 10434
Метициллин-резистентный Staphylococcus aureus 308
Тестируемые образцы
Контроль: фосфатный буферный раствор (PBS)
Образец F: 100% нетканые волокна хитозана с 15% молочной кислотой и 3% лимонной кислотой. Это соответствует 1,35 г хитозана, 0,2 г молочной кислоты и 0,04 г лимонной кислоты (пример 8).
Образец G: 100% нетканые волокна хитозана с 15% молочной кислотой 25% лимонной кислотой. Это соответствует 1,35 г хитозана, 0,2 г молочной кислоты и 0,34 г лимонной кислоты (пример 9).
Образец H: 100% нетканые волокна хитозана с 20% молочной кислоты и 60% лимонной кислоты. Это соответствует 1,35 г хитозана, 0,27 г молочной кислоты и 0,81 г лимонной кислоты (пример 10).
Образец I: 100% нетканые волокна хитозана с 3% лимонной кислотой. Это соответствует 1,35 г хитозана и 0,04 г лимонной кислоты (сравнительный пример 2).
Образец J: 100% нетканые волокна хитозана с 25% лимонной кислотой. Это соответствует 1,35 г хитозана и 0,34 г лимонной кислоты (сравнительный пример 3).
Образец K: 100% нетканые волокна хитозана с 60% лимонной кислотой. Это соответствует 1,35 г хитозана и 0,81 г лимонной кислоты (сравнительный пример 4).
Образцы получали, следуя методам, описанным ранее.
Образцы повязок нарезали до применения на куски приблизительно 1,5 см2. Фосфатный буферный раствор (PBS) использовали в качестве контроля.
Получение бактериального инокулята
24 часовую культуру тестируемых бактерий собирали из планшета с триптон-соевым агаром (TSA) с использованием стерильной губки и ресуспендировали в 20 мл триптон-соевого бульона (TSB). Бактериальную суспензию разводили для получения OП590= 0,10±0,03, что соответствует бактериальной концентрации 108±5×107 КОЕмл-1. Ее дополнительно разводили в TSB и использовали в качестве инокулята для реактора CDC, содержащего пробные образцы. Реактор CDC инкубировали в течение 48 часов при 37°C, встряхивали при 50 об/мин с целью стимуляции роста биопленки.
Обработка биопленки
Через 48 часов пробные образцы удаляли из реактора CDC и промывали 3 раза в стерильном PBS с целью удаления планктонных бактерий. Промытые образцы затем обрабатывали путем размещения образца между двумя образцами повязки 1,5 см2. Повязки активировали до тестирования путем добавления к каждому 1,5 см2 куску 350 мкл PBS (75% насыщение). Контрольные образцы погружали в 2 мл PBS для P. aeruginosa (или в случае S. haemolyticus и MRSA в 2 мл PBS+0,1% TSB). Все образцы тестировали в трех экземплярах. Микроорганизмы восстанавливали из образцов через 24 часа обработки и оценивали количественно путем использования серийных разведений и капельных планшетов.
Результаты показаны на фиг. 4-6.
Очевидно из графиков, показанных на фиг. 4-6, что образцы G, H и K оказались эффективными против всех трех тестируемых микроорганизмов. Образцы G и H включают хитозановые волокна, покрытые трехосновной кислотой и одноосновной кислотой. Образец K включает хитозановые волокна, покрытые большим количеством трехосновной кислоты. Тогда как образцы F, I и J были эффективными против метициллин-резистентного Staphylococcus aureus 308, они были менее эффективными против и Staphylococcus haemolyticus NCTC 11042 и Pseudomonas aeruginosa ATCC 10434.
Результаты реакторной модели CDC показали, что хитозан, покрытый большими количествами трехосновной кислоты, например, около 60%, оказался более эффективным против микроорганизмов, чем меньшим количеством около 25% или менее. Также, результаты показывают, что включение одноосновной кислоты с трехосновной кислотой может быть эффективным в уменьшении количества требуемой трехосновной кислоты, например, уменьшения количества трехосновной кислоты до около 25%.
Реакторная модель CDC 2
Для определения способности удаления биопленки шести раневых повязок, в отношении двух бактериальных образцов, с использованием реакторного метода CDC.
Тестируемые микроорганизмы
Staphylococcus haemolyticus NCTC 8325
Pseudomonas aeruginosa ATCC 10434
Тестируемые образцы
Контроль: фосфатный буферный раствор (PBS)
Образец L: 100% нетканые волокна хитозана с 25% молочной кислоты и 30% лимонной кислоты. Это соответствует 1,35 г хитозана, 0,34 г молочной кислоты и 0,41 г лимонной кислоты (образец 11).
Образец M: 100% нетканые волокна хитозана с 25% молочной кислоты и 40% лимонной кислоты. Это соответствует 1,35 г хитозана, 0,34 г молочной кислоты и 0,54 г лимонной кислоты (пример 12).
Образец N: 100% нетканые волокна хитозана с 30% молочной кислоты и 40% лимонной кислоты. Это соответствует 1,35 г хитозана, 0,41 г молочной кислоты и 0,54 г лимонной кислоты (пример 13).
Пример O: 100% Нетканые волокна хитозана.
Образец P: 55% волокна хитозана/45% нетканые волокна вискозы с 25% молочной кислоты. Это соответствует 0,74 г волокон хитозана, 0,61 г волокон вискозы и 0,34 г молочной кислоты
Образец Q: Нетканая карбоксиметилцеллюлоза с ионной композицией против формирования биопленки, содержащей серебро.
Образцы получали, следуя способам, описанным ранее.
Образцы повязок нарезали до применения на кусочки приблизительно 1,5 см2. Фосфатный буферный раствор (PBS) использовали в качестве контроля.
Получение бактериального инокулята
24 часовую культуру каждого микроорганизма собирали с планшета с триптон-соевым агаром (TSA) и ресуспендировали в 20 мл триптон-соевого бульона (TSB). Полученную бактериальную суспензию разводили для получения исходной OП590=0,10±0,03, что соответствовало бактериальной концентрации 108±5×107 КОЕмл-1. Ее дополнительно разводили до приблизительно 107 КОЕмл-1в TSB и использовали в качестве исходного инокулята для реактора CDC. Реактор CDC инкубировали в течение 24 и 72 часов при 37°C, встряхивая при 50 об/мин с целью облегчения роста биопленки.
Обработка биопленки
Через 24 часа и 72 часа пробные образцы удаляли из реактора CDC и промывали 3 раза в стерильном фосфатном буферном растворе (PBS) с целью удаления планктонных бактерий. Промытые образцы затем обрабатывали путем размещения каждого образца между двумя кусками материала раневых повязок. Повязки активировали перед тестированием путем добавления 350 мкл PBS, содержащего 1% TSB. Контрольные образцы погружали в 2 мл PBS, содержащего 1% TSB. После периода обработки 24 часа образцы помещали в 2 мл нейтрализатора и обрабатывали ультразвуком в течение 15 минут для восстановления оставшихся прикрепленных бактерий. Проводили серийные разведения полученной восстановленной среды и капельные планшеты использовали для количественной оценки восстановленных бактерий. Все образцы тестировали в тройном экземпляре.
Результаты показаны на фиг. 7-10.
На фиг. 7 показано количество жизнеспособных Pseudomonas aeruginosa, восстановленных из заранее образованных 24-часовых биопленок после 24 часовой обработки образцами раневых повязок. Контроль обрабатывали PBS+1% TSB.
На фиг. 8 показано количество жизнеспособных Pseudomonas aeruginosa, восстановленных из заранее образованных 72-часовых биопленок, после 24 часовой обработки образцами раневых повязок. Контроль обрабатывали PBS+1% TSB.
На фиг. 9 показано количество жизнеспособных Staphylococcus aureus, восстановленных из заранее образованных 24-часовых биопленок после 24 часовой обработки образцами раневых повязок. Контроль обрабатывали PBS+1% TSB.
На фиг. 10 показано количество жизнеспособных Staphylococcus aureus, восстановленных из заранее образованных 72-часовых биопленок после 24 часовой обработки образцами раневых повязок. Контроль обрабатывали PBS+1% TSB.
Очевидно из графиков, показанных на фиг. 7-10, что образцы L, M и N по настоящему изобретению являются эффективными против обоих тестируемых микроорганизмов. Тогда как образцы Q и P были эффективными против Staphylococcus aureus, они были менее эффективными против Pseudomonas aeruginosa ATCC 10434.
Анализ MBEC 2
Тестируемый микроорганизм
Staphylococcus aureus NCTC 8325
Тестируемые агенты
Все тестируемые агенты получали путем покрытия оболочкой гранул хитозана, имеющего степень деацетилирования >75%, специфической кислотой(ами) с использованием неводного растворителя. Это давало твердые соли хитозана в форме гранул. Затем гранулы смешивали в гелевой композиции с использованием деионизированной воды с гелем, содержащим между 5-10% соли хитозана.
Анализ MBEC
Биопленку S. aureus выращивали на проекциях штифтов на крышке планшета микротитратора в течение 24 часов и 72 часов при 37°C. Через 24 часа и 72 часа крышки штифтов удаляли, промывали коротко в стерильном фосфатном буферном растворе (PBS) для удаления планктонных бактерий и затем помещали на планшет выбора агента в течение 24 часов. Для получения планшета выбора некоторое количество каждой гелевой композиции помещали в ячейки планшета микротитратора. Проекции штифтов на крышке положительного и отрицательного контроля помещали в PBS+1% TSB. После обработки проекции штифтов на крышке промывали дважды в PBS и затем помещали в нейтрализатор. Планшеты обрабатывали ультразвуком. Серийные разведения проводили на полученной восстановленной среде, и капельные планшеты использовали для количественной оценки восстановленных бактерий. Все образцы тестировали в трех экземплярах.
Двадцати-четырех-часовая биопленка
Все тестируемые агенты успешно уменьшали количество жизнеспособных бактерий, восстановленных из заранее образованных 24-часовых биопленок S. aureus после обработки в течение 24 часов при 37°C, как показано на фиг. 11. Это представлено 5,84 ± 0,53 log уменьшением жизнеспособных бактерий по сравнению с необработанным контролем.
Семидесяти-двух-часовая биопленка
Все тестируемые агенты успешно снижали количество жизнеспособных бактерий, восстановленных из заранее образованных 72-часовых биопленок S. aureus после обработки в течение 24 часов при 37°C, как показано на фиг. 12. Для каждого агента это представлено 5,52±0,22 log уменьшением жизнеспособных бактерий по сравнению с необработанным контролем.
Конечно, необходимо понимать, что настоящее изобретение не предназначено быть ограниченным вышеописанными примерами, которые описаны только в качестве примера.
Реферат
Группа изобретений относится к области медицины, а именно к композиции для применения для разрушения и уничтожения бактерий в биопленке и для предупреждения образования биопленки, включающей первый компонент, выбираемый из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина, и любой их комбинации; трехосновную кислоту и растворяющую кислоту, где трехосновная кислота присутствует в количестве по меньшей мере 10 мас.% от первого компонента и где трехосновная кислота представляет собой лимонную кислоту и где растворяющая кислота представляет собой молочную кислоту, также относится к раневой повязке, и к способу получения композиции для применения для разрушения и уничтожения бактерий в биопленке и для предупреждения образования биопленки, включающей первый компонент, выбираемый из группы, состоящей из хитозана, хитина, производных хитозана, производных хитина и их комбинаций; трехосновную кислоту и растворяющую кислоту, где трехосновная кислота присутствует в количестве по меньшей мере 10 мас.% от количества первого компонента и где трехосновная кислота представляет собой лимонную кислоту и где растворяющая кислота является молочной кислотой, где способ, включает стадии: a) покрытия оболочкой по меньшей мере одной части первого компонента с помощью смеси, включающей лимонную кислоту и молочную кислоту; и/или b) абсорбции в по меньшей мере части первого компонента смеси, включающей лимонную кислоту и молочную кислоту. Группа изобретений обеспечивает получение улучшенных средств для уничтожения бактерий в биопленке, а также для предотвращения повторного образования биопленки, при этом средства характеризуются увеличенной антимикробной эффективностью. 3 н. и 24 з.п. ф-лы, 1 табл., 15 пр., 12 ил.

Комментарии