Связанная с респираторным заболеванием ген-специфическая мирнк, двуспиральная конструкция олиго-рнк, содержащая мирнк, и содержащая ее композиция для предупреждения или лечения респираторного заболевания - RU2656154C2
Код документа: RU2656154C2
Чертежи



















































































































Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к связанной с респираторным заболеванием ген-специфической миРНК и высокоэффективной конструкции, представляющей собой двуспиральную олиго-РНК («двуспиральную конструкцию олиго-РНК»), содержащую миРНК. Двуспиральная конструкция олиго-РНК представляет собой структуру, в которой гидрофильный материал и гидрофобный материал конъюгированы с обоими концами двуспиральной РНК (миРНК) посредством простой ковалентной связи или опосредованной линкером ковалентной связи для эффективной доставки в клетки, при этом конструкция может быть превращена в форму наночастицы путем гидрофобных взаимодействий двуспиральной конструкции олиго-РНК в водном растворе. миРНК, включенная в двуспиральную конструкцию олиго-РНК, предпочтительно представляет собой миРНК, специфическую к CTGF, Cyr61 или Plekhol (далее в настоящем документе называемая CTGF-, Cyr61- или Plekhol-специфическая миРНК), который представляет собой ген, связанный с респираторными заболеваниями, в частности, идиопатическим легочным фиброзом и хроническим обструктивным заболеванием легкого (COPD).
Кроме того, настоящее изобретение относится к способу получения двуспиральной конструкции олиго-РНК и фармацевтической композиции, содержащей двуспиральную конструкцию олиго-РНК, для предупреждения или лечения респираторных заболеваний, в частности, идиопатического легочного фиброза и COPD.
Предпосылки создания изобретения
Технологии ингибирования экспрессии генов являются важными инструментами при разработке терапевтического агента и валидации мишени для лечения заболеваний. Среди этих технологий есть технологии на основе РНК-интерференции (далее в настоящем документе называемая «RNAi»), после обнаружения ее действия на последовательность-специфическую мРНК в различных видах клеток млекопитающих (Silence of the transcripts: RNA interference in medicine. J. Mol. Med. (2005) 83: 764-773). При доставке в клетку длинная двухцепочечная РНК превращается в малую интерферирующую РНК (далее в настоящем документе называемую «миРНК»), которая процессируется до 21-23 пар оснований (по) под действием эндонуклеазы дайсер. миРНК связывается с РНК-индуцированным комплексом сайленсинга (RISC), где руководящая (антисмысловая) цепь узнает и расщепляет целевую мРНК для последовательность-специфического ингибирования экспрессии целевого гена (NUCLEIC-ACID THERAPEUTICS: BASIC PRINCIPLES AND RECENT APPLICATIONS. Nature Reviews Drug Discovery. 2002. 1, 503-514).
Bertrand et al. обнаружили, что по сравнению с антисмысловым олигонуклеотидом (ASO) на том же самом целевом гене миРНК обладает эффектом значительного ингибирования экспрессии мРНК in vitro и in vivo, и соответствующий эффект сохраняется в течение длительного времени (Comparison of antisense oligonucleotides and siRNAs in cell culture and in vivo. Biochem. Biophys. Res. Commun. 2002. 296: 1000-1004). Кроме того, поскольку миРНК комплементарно связана с целевой мРНК для последовательность-специфического регулирования экспрессии целевого гена, механизм действия миРНК имеет преимущество, состоящее в том, что направленное воздействие может быть значительно увеличено по сравнению с существующими медицинскими продуктами или химическими фармацевтическими препаратами на основе антител (низкомолекулярными лекарственными средствами) (Progress Towards in Vivo Use of siRNAs. MOLECULAR THERAPY. 2006 13(4): 664-670).
Для разработки миРНК в качестве терапевтического агента с превосходным эффектом и различным диапазоном использования миРНК необходима эффективная доставка миРНК в клетку-мишень с улучшенной стабильностью и более эффективная доставка миРНК в клетку (Harnessing In Vivo siRNA Delivery for Drug Discovery and Therapeutic Development. Drug Discov. Today. 2006 Jan; 11(1-2): 67-73.
Для решения указанных проблем предпринимались активные исследования в отношении модификации некоторых нуклеотидов или основной цепи миРНК, для придания устойчивости нуклеиновой кислоты к действию лиазы, или использования носителей, таких как вирусные векторы, липосомы или наночастицы и т.п. для улучшения стабильности in vivo.
Системы доставки с использованием вирусных векторов, таких как аденовирус, ретровирус и т.п., обладают высокой эффективностью трансфекции, а также высокой иммуногенностью и онкогенностью. При этом невирусная система доставки, включая наночастицы, обладает низкой эффективностью доставки в клетку по сравнению с вирусной системой доставки, но обладает высокой стабильность in vivo и может быть доставлена мишень-специфически, обладает значительно улучшенными эффектами доставки олигонуклеотида RNAi в клетки или ткани, такими как поглощение, интернализация и т.п., и редко обладает цитотоксичностью и стимуляцией иммунной системы, таким образом, невирусная система доставки оценивается в настоящее время как перспективный способ доставки по сравнению с вирусными системами доставки (Nonviral delivery of synthetic siRNA s in vivo. J Clin Invest. 2007 December 3; 117(12): 3623-3632).
В способе с использованием наноносителя в невирусных системах доставки для формирования наночастиц используются различные полимеры, такие как липосомы, катионные полимерные композиты и т.п., и для доставки в клетки миРНК загружают на наночастицы, то есть наноноситель. Среди способов с использованием наноносителей в основном применяют способ с использованием полимерной наночастицы, полимерной мицеллы, липоплекса или т.п., при этом липоплекс состоит из катионного липида для взаимодействия с анионным липидом эндосомы клетки, вызывая тем самым дестабилизирующий эндосому эффект для доставки миРНК в клетку (Proc. Natl. Acad. Sci. 15; 93(21): 11493-8, 1996).
Кроме того, известно, что химические материалы и т.п. соединены с концевыми участками сопровождающей (смысловой) цепи миРНК для обеспечения улучшенных фармакокинетических характеристик, таким образом, что может быть индуцирована высокая эффективность in vivo (Nature 11; 432(7014): 173-8, 2004). В настоящем документе стабильность миРНК может варьировать в зависимости от свойств химических материалов, соединенных с концами смысловой («сопровождающей») или антисмысловой («направляющей») цепи миРНК. Например, миРНК, с которой конъюгировано полимерное соединение, такое как полиэтиленгликоль (PEG), взаимодействует с анионной фосфатной группой миРНК в присутствии катионных материалов с образованием комплекса, являясь таким образом носителем, обладающим улучшенной стабильностью миРНК (J. Control Release 129(2): 107-16, 2008). В частности, мицелла, состоящая из полимерных комплексов, характеризуется чрезвычайно малым размером, высокооднородным распределением и спонтанным образованием, тем самым являясь легкой в отношении управления качеством состава и обеспечения воспроизводимости по сравнению с другими системами, используемыми в качестве носителей для доставки лекарственных средств, такими как микросферы, наночастицы и т.п.
Кроме того, для улучшения эффективности внутриклеточной доставки миРНК разработана технология использования конъюгата миРНК, в котором гидрофильный материал, представляющий собой биосовместимый полимер (например, полиэтиленгликоль (PEG)), конъюгирован с миРНК посредством простой ковалентной связи или опосредованной линкером ковалентной связи, для обеспечения стабильности миРНК и эффективной проницаемости клеточной мембраны (смотри публикацию корейского патента №883471). Однако химическая модификация миРНК и конъюгирование с полиэтиленгликолем (PEG) (пегилирование) все же имеют недостатки, связанные с низкой стабильностью in vivo и неравномерной доставкой в орган-мишень. Для устранения указанных недостатков была разработана двуспиральная конструкция олиго-РНК, в которой гидрофильный материал и гидрофобный материал соединены с олигонуклеотидами, в частности, двуспиральной РНК, такой как миРНК, при этом двуспиральная конструкция олиго-РНК формирует самособирающуюся наночастицу, названную Self-Assembled-Micelle-irihibitory-RNA (SAMiRNA™), путем гидрофобного взаимодействия гидрофобного материала (смотри публикацию корейского патента №1224828), при этом технология SAMiRNA™ обладает преимуществом, состоящим в возможности получения гомогенных наночастиц чрезвычайно малого размера по сравнению с существующими технологиями доставки.
Конкретным примером технологии SAMiRNA™ является использование PEG (полиэтиленгликоля) в качестве гидрофильного материала, при этом PEG представляет собой синтетический полимер, используемый для увеличения растворимости фармацевтических средств, в частности, белка и для контроля фармакокинетики. PEG представляет собой полидисперсный материал, при этом полимер в одной партии состоит из суммы различного числа мономеров, молекулярная масса показана на кривой Гаусса, и значения индекса полидисперсности (Mw/Mn) выражают степень гомогенности материала. То есть, когда PEG имеет низкую молекулярную массу (от 3 до 5 кДа), индекс полидисперсности составляет около 1,01, и когда PEG имеет высокую молекулярную массу (20 кДа), индекс полидисперсности является высоким и составляет около 1,2, то есть при более высокой молекулярной массе гомогенность материала является сравнительно низкой (F.М. Veronese. Peptide and protein PEGylation: a review of problems and solutions. Biomaterials (2001) 22: 405-417). Таким образом, при комбинировании PEG с фармацевтическими средствами показатель полидисперсности PEG отражается на конъюгате, таким образом, затруднительно выполнить верификацию одного материала, и поэтому возрастает тенденция получения материалов с низким показателем полидисперсности путем синтеза PEG и улучшения способов очистки, но при этом имеются проблемы, связанные с характеристикой полидисперсности материала, в частности, при комбинировании PEG с материалом с низкой молекулярной массой имеются трудности, связанные с подтверждением легкости получения комбинации и т.д. (Francesco М. Veronese and Gianfranco Pasut. PEGylation, successful approach to drug delivery. DRUG DISCOVERY TODAY (2005) 10(21): 1451-1458).
Таким образом, недавно в качестве улучшенной технологии SAMiRNA™, которая представляет собой существующие самособирающиеся наночастицы, была разработана технология получения новой формы носителя, имеющего чрезвычайно малый размер по сравнению с существующими SAMiRNA™ и значительно улучшенную полидисперсность, путем объединения гидрофильного материала двуспиральной конструкции РНК, формирующей SAMiRNA™, в блоки, основная единица которых включает от 1 до 15 однородных мономеров, имеющих предварительно определенную молекулярную массу, и при необходимости линкер, и использования по необходимости соответствующего количества блоков гидрофильных материалов.
При этом, поскольку биофармацевтические препараты специфически действуют на последовательность целевого гена или структуру белка, для оценки эффективности и безопасности в неклинической суррогатной модели дополнительно требуется материал, действующий по такому же механизму, как соответствующие биофармацевтические препараты у человека, даже в разновидностях суррогатной модели. Таким образом, для того, чтобы избежать трудностей, связанных с дополнительным поиском материала, имеющего такой же механизм действия, как у человека, необходимо разработать материал, действующий по одинаковому механизму у человека (подвергаемая лечению мишень) и мышей (неклиническая суррогатная модель).
Идиопатический легочный фиброз (далее в настоящем документе называемый сокращенно «IPF») представляет собой заболевание, в котором хронические воспалительные клетки проникают в стенку альвеол (альвеола легких), делая легкие более твердыми, вызывая тяжелое структурное изменение в легочной ткани, такое, что функция легких постепенно снижается, приводя к смерти. Однако до сих пор не существует эффективного лечения, и идиопатический легочный фиброз обычно диагностируется после появления симптомов и имеет чрезвычайно плохой прогноз, поскольку медиана выживаемости составляет примерно от трех до пяти лет. Имеются сообщения о том, что частота случаев в различных странах составляет примерно 3-5 человек на 100000 и известно, что частота возникновения обычно является более высокой в возрасте старше 50 лет, и частота возникновения у мужчин в два раза выше, чем у женщин.
Причина IPF до сих пор до конца не установлена и имеются лишь сообщения о том, что высокая частота возникновения наблюдается у курильщиков, принимающих антидепрессанты, имеющих хроническую легочную дисфункцию вследствие гастроэзофагеального рефлюкса, после вдыхания металлической пыли, древесной пыли, растворителей и т.п., которые рассматриваются как факторы риска, связанные с возникновением IPF. Однако у большинства пациентов конкретные причинные факторы не могут быть выявлены.
Известно, что IPF непрерывно ухудшается при отсутствия лечения, и около 50% пациентов умирают в течение 3-5 лет, и после того как легкие полностью затвердевают путем фиброза по мере прогрессирования заболевания улучшение не наступает несмотря на любое лечение, и поэтому можно предположить, что раннее лечение повышает эффективность. В настоящее время известен способ комбинированной терапии с использованием в качестве терапевтического агента стероида и азатиоприна или циклофосфамида, но трудно сказать о наличии особых эффектов, и попытки использования нескольких ингибиторов фиброза в экспериментах на животных и малых группах пациентов не показали четких эффектов. В частности, отсутствует другое эффективное лечение для пациентов с конечной стадией IPF, дополнительно к трансплантации легких. Таким образом, существует острая потребность в разработке более эффективного терапевтического агента против IPF.
При этом COPD, одно из типичных заболеваний легких, наряду с астмой, отличается от астмы тем, что сопровождается необратимой обструкцией дыхательных путей и представляет собой респираторное заболевание, сопровождающееся ненормальным воспалительным ответом легких на повторную инфекцию, вредные частицы, выхлопные газы или курение, и не является полностью обратимым, демонстрируя возрастающее прогрессирующее ограничение воздушного потока (Pauwels et al, AmJRespir Crit Care Med, 163: 1256-1276, 2001). COPD представляет собой заболевание, вызванное патологическими изменениями бронхиол и легочной паренхимы путем воспаления дыхательного пути и паренхимы легких, и характеризуется обструктивным бронхиолитом и эмфиземой (разрушением легочной паренхимы). Типы COPD включают хронический обструктивный бронхит, хронический бронхиолит и эмфизему. COPD характеризуется увеличенным количеством нейтрофилов и повышенной секрецией цитокинов, таких как GM-CSF, TNF-α, IL-8 и MIP-2. Кроме того, наблюдается воспаление дыхательного пути, утолщенная стенка бронхов и закупорка бронхов вследствие увеличенной секреции слизи. Когда бронхи закупориваются, альвеолы расширяются и повреждаются, таким образом, происходит нарушение обмена кислорода и двуокиси углерода, приводя к дыхательной недостаточности.
По степени тяжести заболевание COPD в 1990 году занимало 6-е место среди причин смерти от заболеваний, но прогнозируется, что в 2020 году будет занимать третье место, и является единственным заболеванием, частота случаев возникновения которого выросла в 10 раз. COPD имеет высокий показатель распространенности, вызывает респираторные нарушения и требует больших прямых медицинских затрат для диагностики и лечения, а также значительных непрямых затрат, таких как потери вследствие одышки и вынужденный отпуск или потери вследствие преждевременной смерти, что является социальной и экономической проблемой в мире (Chronic obstructive pulmonary disease (COPD) treatment guidelines 2005. Chronic obstructive airway disease Clinical Research Center, p. 30-31).
Существующие терапевтические лекарственные средства не были подтверждены в качестве лекарственных средств, которые на длительное время уменьшают сокращение функции легких, что является характеристикой COPD. Таким образом, главной целью лечения COPD лекарственными средствами является уменьшение симптомов или осложнений. Бронходилатор является типичным аллопатическим средством для лечения COPD из терапевтических средств, и обычно назначают противовоспалительное лекарственное средство или кортикостероид, но эффект является незначительным, область применения является узкой и существует большая вероятность побочных эффектов. Известно, что в качестве других лекарственных средств только вакцина против гриппа уменьшает серьезные симптомы и вероятность смертельного исхода примерно на 50% у пациентов с COPD (chronic obstructive pulmonary disease (COPD) treatment guidelines 2005. Chronic obstructive airway disease Clinical Research Center, p. 52-58).
Между тем, установлено множество генетических факторов, которые повышают (или понижают) риск возникновения COPD у индивидуума. Генетическим фактором риска, который был продемонстрирован на сегодняшний день, является генетический дефицит альфа-1-антитрипсина. Курильщики значительно повышают риск возникновения COPD, однако возникновение панлобулярной эмфиземы и сокращение функции легких, которые быстро прогрессируют в молодом возрасте, продемонстрировано как курильщиками, так и не курящими людьми, имеющими значительный генетический дефицит. Хотя было получено подтверждение того, что другие гены связаны с COPD, до сих пор отсутствует мнение о патогенезе дополнительно к альфа-1-антитрипсину, и предпринимаются попытки идентифицировать биомаркеры заболевания в диагностических целях путем исследования клеточных, молекулярных и генетических ненормальных состояний, которые преимущественно наблюдаются у пациентов с COPD, или найти новый способ лечения (P.J. Barnes and R.A. Stockely. COPD: current therapeutic interventions and future approaches. Eur Respir J. (2005) 25: 1084-1106). В частности, было проведено исследование с целью диагностики COPD и отбора мишени для лечения методами, такими как микрочипы для идентификации генов, протеомика и т.д., и в основном выполняли анализы генетических факторов для получения данных по чувствительности (подверженности) к COPD и причинам ухудшения симптомов COPD, вызванных курением (Peter J. Castaldi et al. The COPD genetic association compendium. Human Molecular Genetics, 2010, Vol. 19, No. 3 526-534).
CTGF (фактор роста соединительной ткани; CCN2), который является одним из матриксно-клеточных белков, включенных в семейство CCN, известен как секретируемый цитокин, вовлеченный в различные биологические процессы, такие как клеточная адгезия, миграция, пролиферация, ангиогенез, заживление ран и т.п. Сверхэкспрессия CTGF рассматривается как основная причина симптомов, таких как склеродерма, фиброзирующее заболевание и формирование шрамов (Brigstock DR. Connective tissue growth factor (CCN2, CTGF) and organ fibrosis: lessons from transgenic animals. J Cell Commun Signal (2010) 4 (1): 1-4). В частности, в отношении фиброза известно, что CTGF вызывает устойчивый фиброз вместе с TGF-β (трансформирующий фактор роста-β) или стимулирует выработку ЕСМ (внеклеточного матрикса) под действием условий, которые вызывают формирование волокон, и недавно стало известно о возможности лечить нарушения зрения или дистрофию мышц, вызванную ненормальной экспрессией CTGF путем обработки образцов или материалов, которые препятствуют экспрессии CTGF или ингибируют его действие, но актуальность в отношении респираторного заболевания не была описана (патент США No. 7,622,454 и публикация заявки на патент США No. 20120164151).
CYR61 (обогащенный цистеином ангиогенный индуктор 61) представляет собой сигнальный белок, ассоциированный с внеклеточным матриксом (ЕСМ), включенный в семейство CCN, который, как известно, контролирует различные клеточные события, такие как клеточная адгезия, миграция, пролиферация, дифференцировка, апоптоз и т.п. Очищенный CYR61 стимулирует прикрепление и распространение эндотелиальных клеток подобно действию фибронектина, и не обладает митогенной активностью, но усиливает митогенный эффект фактора роста фибробластов (MARIA L. KIREEVA et al. Cyr61, a Product of a Growth Factor-Inducible Immediate-Early Gene, Promotes Cell Proliferation, Migration, and Adhesion. MOLECULAR AND CELLULAR BIOLOGY, Apr. 1996, p. 1326-1334).
Имеются сообщения о том, что Plekho1 (семейство О, первый член семейства, содержащий плекстрин-гомологичный домен) присутствует в плазматической мембране или ядре, действует в качестве неферментного регулятора протеинкиназы CK2α1 (казеинкиназа 2, альфа 1) и вовлечен в апоптоз путем ингибирования действия АР-1 посредством С-концевого участка, образующегося при расщеплении каспазой 3 (Denis G. Bosc et al. Identification and Characterization of CKIP-1, a Novel Pleckstrin Homology Domain-containing Protein That Interacts with Protein Kinase CK2. The Journal of Biological Chemistry(2000) 275, 14295-14306; Lingqiang Zhang et al. Role for the pleckstrin homology domain containing protein CKIP-1 in AP-1 regulation and apoptosis. The EMBO Journal (2005) 24, 766-778).
Как описано выше, уровень распространения респираторных заболеваний, в частности, идиопатического легочного фиброза и COPD увеличился, но до сих пор отсутствуют терапевтические агенты, способные предупреждать или лечить идиопатический легочный фиброз и COPD. Таким образом, в настоящее время на рынке имеется острая потребность в терапевтическом агенте, который обладает высокой эффективностью по предупреждению и лечению идиопатического легочного фиброза и COPD без вызывания побочных эффектов.
Описание изобретения
Целью настоящего изобретения является обеспечение новой миРНК, специфической к CTGF, Cyr61 или Plekho1 (далее в настоящем документе называемой CTGF-, Cyr61- или Plekho1-специфическая миРНК), которая способна ингибировать их экспрессию с высокой эффективностью, двуспиральной конструкции олиго-РНК, содержащей миРНК, и способа получения двуспиральной конструкции олиго-РНК.
Еще одной целью настоящего изобретения является обеспечение фармацевтической композиции, включающей в качестве эффективного компонента CTGF-, Cyr61- или Plekho1-специфическую миРНК или двуспиральную конструкцию олиго-РНК, содержащую миРНК, для предупреждения или лечения респираторных заболеваний, в частности, идиопатического легочного фиброза и COPD.
Еще одной целью настоящего изобретения является обеспечение способа предупреждения или лечения респираторных заболеваний, в частности, идиопатического легочного фиброза и COPD, путем использования CTGF-, Cyr61- или Plekho1-специфической миРНК или двуспиральной конструкции олиго-РНК, содержащей миРНК.
Краткое описание чертежей
На фигуре 1 представлена схематическая диаграмма наночастицы, образованной двуспиральной структурой олиго-полимера в соответствии с настоящим изобретением.
На фигуре 2 представлены диаграммы, демонстрирующие величину ингибирования экспрессии целевого гена, подтвержденную после трансформации клеточной линии фибробластов человека миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 1 по 10, с 101 по 110, и с 201 по 210, в соответствии с настоящим изобретением.
А: Диаграмма, демонстрирующая величину экспрессии CTGF после лечения 5 или 20 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 1 по 10.
В: Диаграмма, демонстрирующая величину экспрессии Cyr61 после лечения 5 или 20 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 101 по 110.
С: Диаграмма, демонстрирующая величину экспрессии Plekho1 после лечения 5 или 20 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 201 по 210.
На фигуре 3 представлены диаграммы, демонстрирующие величину ингибирования экспрессии целевого гена, подтвержденную после трансформации клеточной линии фибробластов человека миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 1, 3, 4, 8, 9, 10, 102, 104, 105, 106, 107, 108, 109, 204, 206, 207, 208, 209 или 210, в соответствии с настоящим изобретением.
А: Диаграмма, демонстрирующая величину экспрессии CTGF после лечения 0,2 или 1 нМ миРНК, имеющей последовательность, представленную в SEQ ID NO: 1, 3, 4, 8, 9 или 10, в качестве смысловой цепи.
В: Диаграмма, демонстрирующая величину экспрессии Cyr61 после лечения 0,2 или 1 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 102, 104, 105, 106, 107, 108 или 109.
С: Диаграмма, демонстрирующая величину экспрессии Plekho1 после лечения 0,2 или 1 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 204, 206, 207, 208, 209, или 210.
На фигуре 4 представлены диаграммы, демонстрирующие величину ингибирования экспрессии целевого гена, подтвержденную после трансформации клеточной линии рака легких человека миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 35, 42, 59, 602, 603, 604, 124, 153, 166, 187, 197, 212, 218, 221 или 223, в соответствии с настоящим изобретением.
А: Диаграмма, демонстрирующая величину экспрессии CTGF после лечения 0,04, 0,2 или 1 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 35, 42, 59, 602, 603, или 604.
В: Диаграмма, демонстрирующая величину экспрессии Cyr61 после лечения 0,5, 1 или 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 124, 153, 166, 187, или 197.
С: Диаграмма, демонстрирующая величину экспрессии Plekho1 после лечения 0,5, 1 или 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 212, 218, 221 или 223.
На фигуре 5 представлена диаграмма, демонстрирующая величину ингибирования экспрессии целевого гена, подтвержденную после трансформации клеточной линии рака легких человека SAMiRNA, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 42, 59 или 602, в соответствии с настоящим изобретением.
На фигуре 6 представлены диаграммы, демонстрирующие величину ингибирования экспрессии целевого гена, подтвержденную после трансформации клеточной линии фибробластов мышей миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 301 по 330, с 401 по 430, с 501 по 530, в соответствии с настоящим изобретением.
А: Диаграмма, демонстрирующая величину экспрессии CTGF после лечения 20 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 301 по 330.
В: Диаграмма, демонстрирующая величину экспрессии Cyr61 после лечения 20 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 401 по 430.
С: Диаграмма, демонстрирующая величину экспрессии Plekho1 после лечения 20 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 501 по 530.
На фигуре 7 представлены диаграммы, демонстрирующие величину ингибирования экспрессии целевого гена, подтвержденную после трансформации клеточной линии фибробластов мышей миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 404 по 406, с 408 по 410, с 414 по 418, с 420 по 422, 424, 427, 429, 430, с 503 по 509, с 514 по 517, 519, с 521 по 526 или 528, в соответствии с настоящим изобретением.
А: Диаграмма, демонстрирующая величину экспрессии Cyr61 после лечения 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 404 по 406, с 408 по 410, с 414 по 418, с 420 по 422, 424, 427, 429 или 430.
В: Диаграмма, демонстрирующая величину экспрессии Plekho1 после лечения 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 503 по 509, с 514 по 517, 519, с 521 по 526 или 528.
На фигуре 8 представлены диаграммы, демонстрирующие величину ингибирования экспрессии целевого гена, подтвержденную после трансформации клеточной линии фибробластов мышей миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 301, 303, 307, 323, 410, 422, 424, 507, 515 или 525, в соответствии с настоящим изобретением.
А: Диаграмма, демонстрирующая величину экспрессии CTGF после лечения 0,2, 1 или 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 301, 303, 307 или 323.
В: Диаграмма, демонстрирующая величину экспрессии Cyr61 после лечения 0,2, 1 или 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 410, 422 или 424.
С: Диаграмма, демонстрирующая величину экспрессии Plekho1 после лечения 0,2, 1 или 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 507, 515 или 525.
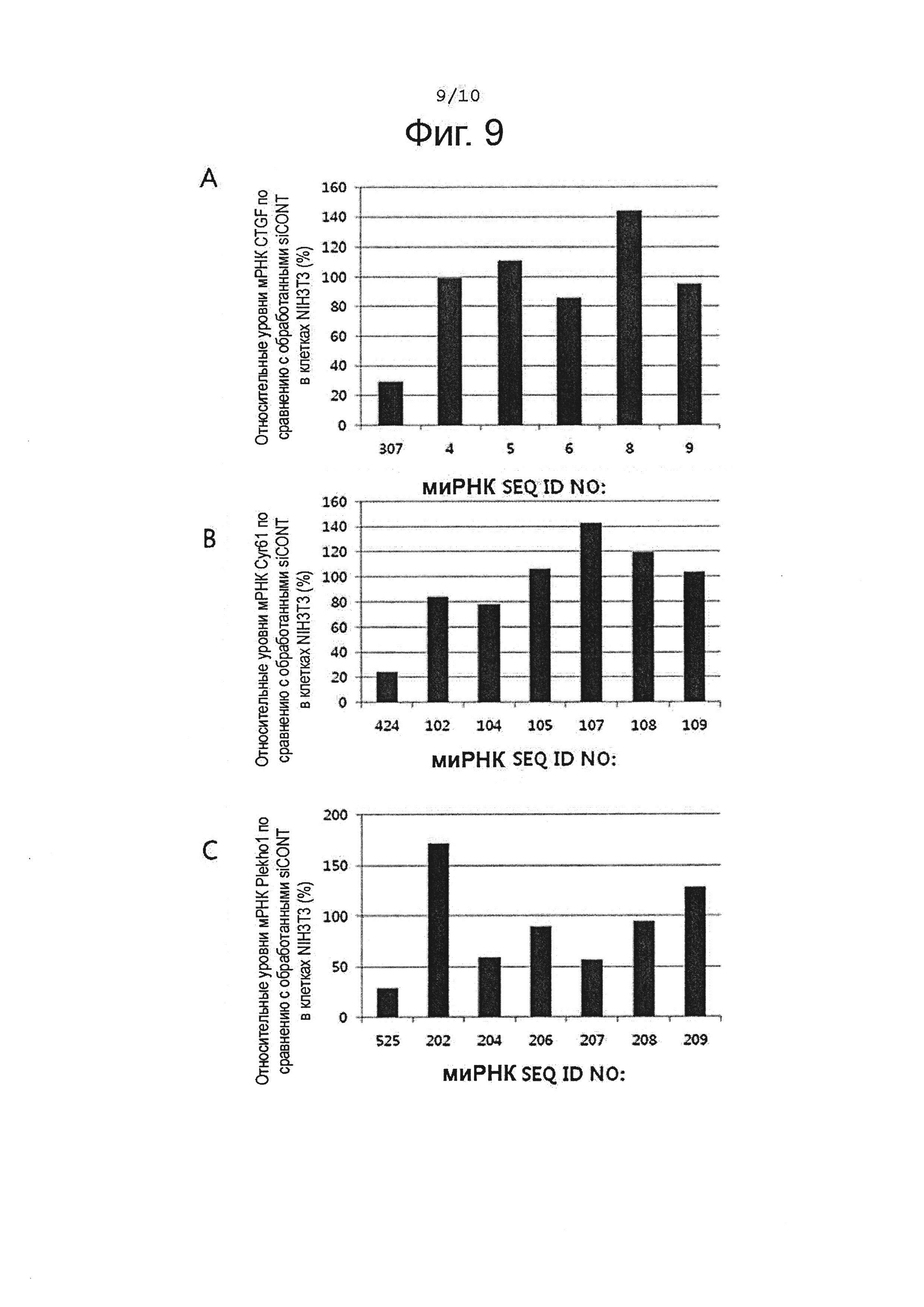
На фигуре 9 представлены диаграммы, демонстрирующие величину ингибирования экспрессии целевого гена, подтвержденную после трансформации клеточной линии фибробластов мышей миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 4, 5, 6, 8, 9, 102, 104, 105, 107, 108, 109, 202, 204, с 206 по 209, 307, 424 или 525, в соответствии с настоящим изобретением.
А: Диаграмма, демонстрирующая величину экспрессии CTGF после лечения 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 4, 5, 6, 8, 9 или 307.
В: Диаграмма, демонстрирующая величину экспрессии Cyr61 после лечения 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 102, 104, 105, 107, 108, 109 или 424.
С: Диаграмма, демонстрирующая величину экспрессии Plekho1 после лечения 5 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 202, 204, с 206 по 209 или 525.
На фигуре 10 представлены диаграммы, демонстрирующие величину ингибирования экспрессии целевого гена, подтвержденную после трансформации клеточной линии фибробластов мышей миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 6, 8, 102, 104, 105, 204, 207, 208, 307, 424 или 525, в соответствии с настоящим изобретением.
А: Диаграмма, демонстрирующая величину экспрессии CTGF после лечения 5 или 20 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 6, 8 или 307.
В: Диаграмма, демонстрирующая величину экспрессии Cyr61 после лечения 5 или 20 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 102, 104, 105 или 424.
С: Диаграмма, демонстрирующая величину экспрессии Plekho1 после лечения 5 или 20 нМ миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 204, 207, 208 или 525.
Лучший способ осуществления изобретения
Для достижения указанных выше целей, настоящее изобретение обеспечивает CTGF-, Cyr61- или Plekho1- (гены, связанные с респираторными заболеваниями)-специфическую миРНК, состоящую из первого олигонуклеотида, который представляет собой смысловую цепь, имеющую любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 1 по 600 и с 602 по 604, и второго олигонуклеотида, который представляет собой антисмысловую цепь, имеющую комплементарную смысловой цепи последовательность.
В настоящем изобретении миРНК включает все материалы, обладающие общим действием RNAi (РНК-интерференции) и, таким образом, специалисту в данной области будет очевидно, что CTGF-, Cyr61- или Plekho1-специфическая миРНК включает CTGF-, Cyr61- или Plekho1-специфическую короткую шпилечную РНК (кшРНК) и т.п.
SEQ ID NO: с 1 по 100 или с 602 по 604 представляют собой последовательности смысловой цепи CTGF (Homo sapiens)-специфической миРНК, SEQ ID NO: с 101 по 200 представляют собой последовательности смысловой цепи Cyr61 (Homo sapiens)-специфической миРНК, SEQ ID NO: с 201 по 300 представляют собой последовательности смысловой цепи Plekho1 (Homo sapiens)-специфической миРНК, SEQ ID NO: с 301 по 400 представляют собой последовательности смысловой цепи CTGF (Mus musculus)-специфической миРНК, SEQ ID NO: с 401 по 500 представляют собой последовательности смысловой цепи Cyr61 (Mus musculus)-специфической миРНК, и SEQ ID NO: с 501 по 600 представляют собой последовательности смысловой цепи Plekho1 (Mus musculus)-специфической миРНК.
В соответствии с настоящим изобретением миРНК предпочтительно представляет собой CTGF-специфическую миРНК, имеющую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 1 по 10, 35, 42, 59, 602, 603, 604, с 301 по 303, с 305 по 307, 309, 317, 323 и 329;
Cyr61-специфическую миРНК, имеющую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 101 по 110, 124, 153, 166, 187, 197, 409, 410, 415, 417, 418, 420, 422, 424, 427 и 429;
Plekho1-специфическую миРНК, имеющую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 201 по 210, 212, 218, 221, 223, с 504 по 507, 514, 515 и с 522 по 525.
Более предпочтительно, миРНК в соответствии с настоящим изобретением представляет собой CTGF-специфическую миРНК, имеющую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 4, 5, 8, 9, 35, 42, 59, 601, 602, 604, 301, 303, 307 и 323;
Cyr61-специфическую миРНК, имеющую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 102, 104, 107, 108, 124, 153, 166, 187, 197, 410, 422 и 424;
Plekho1-специфическую миРНК, имеющую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 206 по 209, 212, 218, 221, 223, 507, 515 и 525.
Наиболее предпочтительно, миРНК в соответствии с настоящим изобретением представляет собой CTGF-специфическую миРНК, имеющую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 42, 59, 602 и 323;
Cyr61-специфическую миРНК, имеющую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 124, 153, 187, 197 и 424; или Plekho1-специфическую миРНК, имеющую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 212, 218, 221, 223 и 525.
В частности, было получено подтверждение того, что некоторые из CTGF-, Cyr61- или Plekhol-специфических миРНК человека в соответствии с настоящим изобретением могут одновременно ингибировать экспрессию CTGF, Cyr61 или Plekho1 мышей.
миРНК, способная одновременно ингибировать экспрессию CTGF, Cyr61 или Plekho1 человека и мышей, предпочтительно включает смысловую цепь CTGF-специфической миРНК в соответствии с SEQ ID NO: 6 или 8, смысловую цепь Cyr61-специфической миРНК в соответствии с SEQ ID NO: 102, 104 или 105, или смысловую цепь Plekho1-специфической миРНК в соответствии с SEQ ID NO: 204, 207 или 208.
Наиболее предпочтительно, миРНК включает смысловую цепь CTGF-специфической миРНК в соответствии с SEQ ID NO: 6, смысловую цепь Cyr61-специфической миРНК в соответствии с SEQ ID NO: 102 или смысловую цепь Plekho1-специфической миРНК в соответствии с SEQ ID NO: 207.
Смысловая цепь или антисмысловая цепь миРНК в соответствии с настоящим изобретением предпочтительно содержит от 19 до 31 нуклеотида, и миРНК включает смысловую цепь, имеющую любую последовательность, выбранную из SEQ ID NO: с 1 по 604, и комплементарную ей антисмысловую цепь.
Поскольку CTGF-, Cyr61- или Plekho1-специфическая миРНК в соответствии с настоящим изобретением содержит последовательность оснований, которая разработана таким образом, что может комплементарно соединяться с мРНК, кодирующей соответствующий ген, экспрессия соответствующего гена может быть эффективно ингибирована. Кроме того, CTGF-, Cyr61- или Plekho1-специфическая миРНК в соответствии с настоящим изобретением может включать «свисающий конец», который представляет собой конструкцию, включающую один или два или более непарных нуклеотидов на 3'-конце миРНК, и может включать различные модификации миРНК для обеспечения устойчивости нуклеиновой кислоты к действию лиазы и уменьшения неспецифического иммунного ответа для улучшения стабильности in vivo. Модификация первого олигонуклеотида или второго олигонуклеотида, образующих миРНК, может представлять собой одну или более комбинаций, выбранных из модификации, в которой группа -ОН при 2'-атоме углерода в структуре сахара в одном или нескольких нуклеотидах заменена на -СН3(метил), -ОСН3(метокси), -NH2, -F(фтор), -O-2-метоксиэтил, -О-пропил, -O-2-метилтиоэтил, -О-3-аминопропил, -О-3-диметиламинопропил, -O-N-метилацетамидо или -О-диметиламидооксиэтил; модификации, в которой кислород в структуре сахара в нуклеотидах заменен на серу; и модификацию нуклеотидных связей на фосфоротиоатные или боранофосфатные, метил-фосфонатные связи, или может представлять собой модификацию пептидо-нуклеиновой кислоты (PNA), модификацию замкнутой нуклеиновой кислоты (LNA) или модификацию незамкнутой нуклеиновой кислоты (UNA) (Ann. Rev. Med. 55, 61-65 2004; US 5,660,985; US 5,958,691; US 6,531,584; US 5,808,023; US 6,326,358; US 6,175,001; Bioorg. Med. Chem. Lett. 14: 1139-1143, 2003; RNA, 9: 1034-1048, 2003; Nucleic Acid Res. 31: 589-595, 2003; Nucleic Acids Research, 38(17) 5761-5773, 2010; Nucleic Acids Research, 39(5) 1823-1832, 2011).
CTGF-, Cyr61- и/или Plekho1-специфическая миРНК в соответствии с настоящим изобретением может ингибировать экспрессию соответствующего гена и значительно ингибировать экспрессию соответствующего белка.
Настоящее изобретение также обеспечивает конъюгат, в котором гидрофильный материал и гидрофобный материал конъюгированы к обоим концам миРНК, для эффективной доставки in vivo и улучшения стабильности миРНК, специфической к гену, связанному с респираторными заболеваниями, в частности, CTGF-, Cyr61- или Plekho1-специфической миРНК.
В конъюгате миРНК, в котором гидрофильный материал и гидрофобный материал соединены с миРНК, самособирающаяся наночастица образуется путем гидрофобного взаимодействия гидрофобного материала (смотри публикацию корейского патента №1224828), при этом самособирающаяся наночастица обладает преимуществами, состоящими в том, что эффективность внутренней доставки и стабильность in vivo являются исключительно высокими, и однородность размера частиц является превосходной, что обеспечивает легкое прохождение контроля качества (QC), облегчая тем самым процесс изготовления лекарственных средств.
В одном предпочтительном иллюстративном варианте осуществления двуспиральная конструкция олиго-РНК, содержащая CTGF-, Cyr61- или Plekho1-специфическую миРНК в соответствии с настоящим изобретением, предпочтительно имеет структуру, представленную следующей структурной формулой (1):
Структурная формула 1

В структурной формуле (1) А представляет собой гидрофильный материал, В представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой CTGF-, Cyr61- или Plekho1-специфическую миРНК.
Более предпочтительно, двуспиральная конструкция олиго-РНК, содержащая CTGF-, Cyr61- или Plekhol-специфическую миРНК в соответствии с настоящим изобретением, предпочтительно имеет структуру, представленную следующей структурной формулой (2):
Структурная формула 2

В структурной формуле (2) А, В, X и Y являются такими же, как определено в структурной формуле (1), S представляет собой смысловую цепь CTGF-, Cyr61- или Plekho1-специфической миРНК, и AS представляет собой антисмысловую цепь CTGF-, Cyr61- или Plekho1-специфической миРНК.
Более предпочтительно, двуспиральная конструкция олиго-РНК, содержащая CTGF-, Cyr61- или Plekho1-специфическую миРНК в соответствии с настоящим изобретением, имеет структуру, представленную следующей структурной формулой (3) или (4):
Структурная формула 3

Структурная формула 4

В структурных формулах (3) и (4) А, В, S, AS, X и Y являются такими же, как определено в структурной формуле (1), и 5' и 3' означают 5'-конец и 3'-конец смысловой цепи CTGF-, Cyr61- или Plekho1-специфической миРНК.
Специалисту в данной области будет очевидно, что в структурных формулах с (1) по (4) от одной до трех фосфатных групп может быть присоединено к 5'-концу антисмысловой цепи двуспиральной конструкции олиго-РНК, содержащей CTGF-, Cyr61- или Plekho1-специфическую миРНК, и вместо миРНК можно использовать короткую шпилечную РНК (кшРНК).
Гидрофильный материал в структурных формулах с (1) по (4) предпочтительно представляет собой катионный или неионный полимерный материал, имеющий молекулярную массу от 200 до 10000, более предпочтительно неионный полимерный материал, имеющий молекулярную массу от 1000 до 2000. Например, неионные гидрофильные полимерные соединения, такие как полиэтиленгликоль, поливинилпирролидон, полиоксазолин и т.п., предпочтительно используют в качестве гидрофильного полимерного материала, но настоящее изобретение не обязательно ими ограничивается.
В частности, гидрофильный материал (А) в структурных формулах с (1) по (4) может быть использован в форме блока гидрофильного материала, представленного следующей структурной формулой (5) или (6), и проблемы, вызванные полидисперсностью, которые могут возникать при использовании общепринятого синтетического полимерного материала и т.п., могут быть в значительной мере уменьшены путем использования по необходимости соответствующего числа (n в структурной формуле (5) или (6)) блоков гидрофильного материала.
Структурная формула 5

Структурная формула 6

В структурной формуле (5) А' представляет собой мономер гидрофильного материала, J представляет собой линкер для соединения мономеров гидрофильного материала (сумма равна m) или линкер для соединения мономеров гидрофильного материала (сумма равна m) с миРНК, m представляет собой целое число от 1 до 15, n представляет собой целое число от 1 до 10, и повторяющаяся единица, представленная (A'm-J) или (J-A'm), соответствуют основной единице блока гидрофильного материала.
Когда блок гидрофильного материала представлен структурной формулой (5) или (6), двуспиральная конструкция олиго-РНК, содержащая CTGF-, Cyr61- или Plekho1-специфическую миРНК в соответствии с настоящим изобретением, может иметь структуру, представленную следующей структурной формулой (7) или (8):
Структурная формула 7

Структурная формула 8
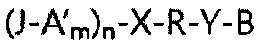
В структурных формулах (7) и (8) X, R, Y и В являются такими же, как определено в структурной формуле (1), и A', J, m и n являются такими же, как определено в структурных формулах (5) и (6).
В структурных формулах (5) и (6) мономер гидрофильного материала А' можно использовать без ограничения при условии, что он отвечает целям настоящего изобретения, из числа мономеров неионного гидрофильного полимера. Мономер гидрофильного материала А' предпочтительно представляет собой мономер, выбранный из следующих соединений с (1) по (3), представленных в таблице 1, более предпочтительно мономер соединения (1), и G в соединении (1) может быть предпочтительно выбран из СН2, О, S и NH.
В частности, из мономеров гидрофильного материала мономер соединения (1), который является особенно подходящим для получения конструкции в соответствии с настоящим изобретением, может содержать различные введенные в него функциональные группы и обладать удовлетворительной аффинностью in vivo, индуцировать незначительный иммунный ответ, обладая, таким образом, превосходной биосовместимостью, и, кроме того, может увеличивать стабильность in vivo олигонуклеотида, включенного в конструкцию структурной формулы (7) или (8), и повышать эффективность доставки.

В частности, гидрофильный материал в структурных формулах с (5) по (8) предпочтительно имеет общую молекулярную массу от 1000 до 2000. Таким образом, например, когда в структурных формулах (7) и (8) используется гексаэтиленгликоль, представленный соединением (1), то есть материал, в котором G представляет собой О, и m равно 6, молекулярная масса спейсера гексаэтиленгликоля равна 344, так что повторяющееся число (n) предпочтительно равно от 3 до 5. В частности, повторяющаяся единица гидрофильной группы, то есть блока гидрофильного материала, представленного (A'm-J) или (J-A'm)n в структурных формулах (5) и (6), может быть использована по необходимости в подходящем количестве, представленном n. А, который представляет собой мономер гидрофильного материала, и J, который представляет собой линкер, включенный в каждый блок гидрофильного материала, могут быть независимо одинаковыми или отличаться друг от друга. То есть, при использовании 3 блоков гидрофильного материала (n=3), мономер гидрофильного материала соединения (1) используется в первом блоке, мономер гидрофильного материала соединения (2) используется во втором блоке, мономер гидрофильного материала соединения (3) используется в третьем блоке, и т.д. То есть можно использовать различные мономеры гидрофильного материала для всех блоков гидрофильного материала, и любой мономер гидрофильного материала, выбранный из мономеров гидрофильного материала соединений с (1) по (3), можно также в равной степени использовать во всех блоках гидрофильного материала. Аналогичным образом, линкеры, опосредующие связывание мономера гидрофильного материала, могут быть также одинаковыми или отличаться друг от друга для всех блоков гидрофильного материала. Кроме того, m, представляющее собой число мономеров гидрофильного материала, может быть одинаковым или различаться для всех блоков гидрофильного материала. То есть, 3 мономера гидрофильного материала (m=3) соединены в первом блоке гидрофильного материала, 5 мономеров гидрофильного материала (m=5) соединены во втором блоке гидрофильного материала, 4 мономера гидрофильного материала (m=4) соединены в третьем блоке гидрофильного материала, и т.д. То есть мономеры гидрофильного материала, каждый, имеющий различное количество, или имеющие одинаковое количество, могут быть использованы во всех блоках гидрофильного материала.
Кроме того, в настоящем изобретении линкер (J) предпочтительно выбран из группы, состоящей из РО3-, SO3 и СО2, но настоящее изобретение ими не ограничивается. Специалисту в данной области будет очевидно, что может быть использован любой линкер в зависимости от используемого мономера гидрофильного материала, и т.п., при условии, что он отвечает целям настоящего изобретения.
Гидрофобный материал (В) в структурных формулах с (1) по (4), (7) и (8) служит для формирования наночастицы, образованной олигонуклеотидными структурами в соответствии со структурными формулами с (1) по (4), (7) и (8), посредством гидрофобного взаимодействия. Гидрофобный материал предпочтительно имеет молекулярную массу от 250 до 1000 и может включать производное стероида, производное глицерида, эфир глицерина, полипропиленгликоль, ненасыщенный или насыщенный С12-С50 углеводород, диацилфосфатидилхолин, жирную кислоту, фосфолипид, липополиамин и т.п., но настоящее изобретение ими не ограничивается. Специалисту в данной области будет очевидно, что может быть использован любой гадрофобный материал при условии, что он отвечает целям настоящего изобретения.
Производное стероида может быть выбрано из группы, состоящей из холестерина, холестанола, холевой кислоты, формиата холестерила, формиата холестанила и амина холестерила, и производное глицерида может быть выбрано из моно-, ди- и триглицерида, и т.п., при этом жирная кислота глицерида предпочтительно представляет собой ненасыщенную или насыщенную жирную кислоту от С12 до С50.
В частности, из числа гидрофобных материалов предпочтительным является насыщенный или ненасыщенный углеводород или холестерин благодаря его способности легко присоединяться на стадии синтеза олигонуклеотидной конструкции в соответствии с настоящим изобретением, и наиболее предпочтительным является С24 углеводород, в частности, тетрадокозан, содержащий дисульфидную связь.
Гидрофобный материал присоединен к дистальному концу гидрофильного материала и не имеет значения, присоединен гидрофобный материал к какому-либо положению смысловой цепи или антисмысловой цепи миРНК.
Гидрофильный материал или гидрофобный материал в структурных формулах с (1) по (4), (7) и (8) в соответствии с настоящим изобретением присоединен к CTGF-, Cyr61- или Plekho1-специфической миРНК посредством простой ковалентной связи или опосредованной линкером ковалентной связи (X или Y). Кроме того, линкер, опосредующий ковалентную связь, ковалентно присоединен к гидрофильному материалу или гидрофобному материалу на конце CTGF-, Cyr61- или Plekho1-специфической миРНК, и конкретным образом не ограничен при условии, что по необходимости обеспечена связь, которая может разрушаться в специфической среде. Таким образом, в качестве линкера для связывания может быть использовано любое соединение для активации CTGF-, Cyr61- или Plekho1-специфической миРНК и/или гидрофильный материал (или гидрофобный материал) для получения двуспиральной конструкции олиго-РНК в соответствии с настоящим изобретением. Ковалентная связь может представлять собой любую расщепляемую связь или нерасщепляемую связь. В настоящем документе примеры нерасщепляемой связи могут включать амидную связь или фосфатную связь, и примеры расщепляемой связи могут включать дисульфидную связь, расщепляемую кислотой связь, сложноэфирную связь, ангидридную связь, биорасщепляемую связь или расщепляемую ферментом связь и тому подобное, но настоящее изобретение ими не ограничивается.
Кроме того, любую CTGF-, Cyr61- или Plekho1-специфическую миРНК, представленную R (или S и AS) в структурных формулах с (1) по (4), (7) и (8), можно использовать без ограничения при условии, что миРНК специфически связывается с CTGF, Cyr61 или Plekho1. Предпочтительно, CTGF-, Cyr61- или Plekhol-специфическая миРНК состоит из смысловой цепи, имеющей любую последовательность, выбранную из SEQ ID NO: с 1 по 600 и с 602 по 604, и антисмысловой цепи, имеющей комплементарную смысловой цепи последовательность.
В частности, миРНК, включенная в структурные формулы с (1) по (4), (7) и (8), в соответствии с настоящим изобретением предпочтительно представляет собой CTGF-специфическую миРНК, содержащую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 1 по 10, 35, 42, 59, с 602 по 604 или с 301 по 303, с 305 по 307, 309, 317, 323 и 329,
Cyr61-специфическую миРНК, содержащую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 101 по 110, 124, 153, 166, 187, 197, 409, 410, 415, 417, 418, 420, 422, 424, 427 и 429, или
Plekho1-специфическую миРНК, содержащую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 201 по 210, 212, 218, 221, 223, с 504 по 507, 514, 515 и с 522 по 525.
Более предпочтительно, миРНК в соответствии с настоящим изобретением представляет собой CTGF-специфическую миРНК, содержащую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 4, 5, 8, 9, 35, 42, 59, 602, 603, 604, 301, 303, 307 и 323,
Cyr61-специфическую миРНК, содержащую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 102, 104, 107, 108, 124, 153, 166, 187, 197, 410, 422 и 424, или
Plekhol-специфическую миРНК, содержащую в качестве смысловой цепи любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 206 по 209, 212, 218, 221, 223, 507, 515 и 525.
Более предпочтительно, миРНК в соответствии с настоящим изобретением представляет собой CTGF-специфическую миРНК, содержащую в качестве смысловой цепи любую последовательность, представленную в SEQ ID NO: 42, 59, 602 или 323,
Cry61-специфическую миРНК, содержащую в качестве смысловой цепи любую последовательность, представленную в SEQ ID NO: 124, 153, 187, 197 или 424, или
Plekho1-специфическую миРНК, содержащую в качестве смысловой цепи любую последовательность, представленную в SEQ ID NO: 212, 218, 221, 223 или 525.
Кроме того, миРНК, включающая смысловую цепь CTGF-специфической миРНК человека и мышей в соответствии с SEQ ID NO: 6 или 8, миРНК, содержащая смысловую цепь Cyr61-специфической миРНК человека и мышей в соответствии с SEQ ID NO: 102, 104 или 105, и миРНК, включающая смысловую цепь Plekho1-специфической миРНК человека и мышей в соответствии с SEQ ID NO: 204, 207 или 208, являются особенно предпочтительными, так как миРНК, имеющая последовательность в качестве смысловой цепи, обладает эффектом одновременного ингибирования экспрессии CTGF, Cyr61 или Plekhol человека и мышей, таким образом, миРНК, включающая смысловую цепь CTGF-специфической миРНК человека и мышей в соответствии с SEQ ID NO: 6, миРНК, включающая смысловую цепь Cyr61-специфической миРНК человека и мышей в соответствии с SEQ ID NO: 102, и миРНК включающая смысловую цепь Plekho1-специфической миРНК человека и мышей в соответствии с SEQ ID NO: 207, являются наиболее предпочтительными.
В двуспиральной конструкции олиго-РНК, содержащей CTGF-, Cyr61- или Plekho1-специфическую миРНК в соответствии с настоящим изобретением, аминогруппа или полигистидиновая группа может быть дополнительно введена в участок дистального конца, соединенного с миРНК гидрофильного материала в конструкции.
Это облегчает выполнение межклеточного введения и выхода из эндосомы двуспиральной конструкции олиго-РНК, содержащей CTGF-, Cyr61- или Plekho1-специфическую миРНК в соответствии с настоящим изобретением, и сообщается о возможности введения аминогруппы и использования полигистидиновой группы для облегчения выполнения межклеточного введения и выхода из эндосомы носителей, таких как квантовые точки, дендример, липосома и т.п., и их эффекте.
В частности, известно, что первичная аминогруппа, экспрессирующаяся на конце или снаружи носителя, протонирована in vivo с формированием конъюгата с отрицательно заряженным геном путем электростатического взаимодействия, и выход из эндосомы легко выполняется за счет внутренних третичных аминов, обладающих буферным эффектом при низком рН эндосомы после введения в клетки, тем самым способна защитить носитель от разложения лизосомы (gene delivery and expression inhibition using a polymer-based hybrid material. Polymer Sci. Technol, Vol. 23, No. 3, pp 254-259).
Кроме того, известно, что гистидин, который является одной из незаменимых аминокислот, имеющий имидазольное кольцо (pKa3 6,04) при остатке (-R), увеличивает буферную емкость в эндосоме и лизосоме, поэтому экспрессию гистидина можно использовать для увеличения эффективности выхода из эндосомы в невирусных носителях для генов, включая липосому (Novel histidine-conjugated galactosylated cationic liposomes for efficient hepatocyte selective gene transfer in human hepatoma HepG2 cells. J. Controlled Release 118, pp 262-270).
Аминогруппа или полигистидиновая группа может быть связана с гидрофильным материалом или блоком гидрофильного материала посредством, по меньшей мере, одного линкера.
При введении аминогруппы или полигистидиновой группы в гидрофильный материал двуспиральной конструкции олиго-РНК, представленной структурной формулой (1), двуспиральная конструкция олиго-РНК может иметь структуру, представленную ниже структурной формулой (9):
Структурная формула 9

В структурной формуле (9) А, В, R, X и Y являются такими же, как определено в структурной формуле (1),
Р представляет собой аминогруппу или полигистидиновую группу. J1 и J2 представляют собой линкеры, и каждый может быть независимо выбран из простой ковалентной связи, РО3-, SO3, СО2, С2-12-алкила, алкенила и алкинила, но настоящее изобретение ими не ограничивается. Специалисту в данной области будет очевидно, что любой линкер может быть использован в качестве J1 и J2 при условии, что он отвечает целям настоящего изобретения, в зависимости от используемого гидрофильного материала.
Предпочтительно, чтобы при введении аминогруппы J2 предпочтительно представлял собой простую ковалентную связь или РО3-, и J1 предпочтительно представлял собой С6-алкил, но настоящее изобретение ими не ограничивается.
Кроме того, при введении полигистидиновой группы в структурной формуле (9) J2 предпочтительно представляет собой простую ковалентную связь или РО3-, и J1 предпочтительно представляет собой следующее соединение (4), но настоящее изобретение им не ограничивается.
Соединение 4
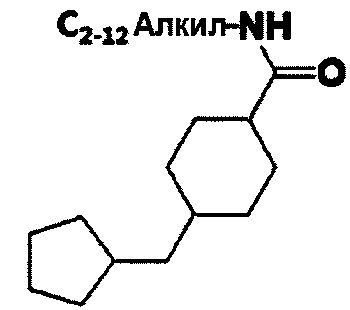
Кроме того, когда гидрофильный материал двуспиральной конструкции олиго-РНК, представленный структурной формулой (9), представляет собой блок гидрофильного материала, представленного структурной формулой (5) или (6), и вводится аминогруппа или полигистидиновая группа, двуспиральная конструкция олиго-РНК может быть представлена структурной формулой (10) или (11):
Структурная формула 10

Структурная формула 11

В структурных формулах (10) и (11) X, R, Y, В, A', J, m и n являются такими же, как определено в структурной формуле (5) или (6), и Р, J1 и J2 являются такими же, как определено в структурной формуле (9).
В частности, в структурных формулах (10) и (11) гидрофильный материал предпочтительно соединен с 3'-концом смысловой цепи CTGF-, Cyr61- или Plekho1-специфической миРНК, и в этом случае структурные формулы с (9) по (11) могут быть представлены следующими структурными формулами с (12) по (14):
Структурная формула 12

Структурная формула 13

Структурная формула 14

В структурных формулах с (12) по (14) X, R, Y, В, A, A' J, m, n, Р, J1 и J2 являются такими же, как определено в структурных формулах с (9) по (11), и 5' и 3' означают 5'-конец и 3'-конец смысловой цепи CTGF-, Cyr61- или Plekho1-специфической миРНК.
Аминогруппа, которая может быть введена в настоящем изобретении, может представлять собой аминогруппу от первичной до третичной, и первичная аминогруппа является особенно предпочтительной. Введенная аминогруппа может присутствовать в виде амина. Например, соль первичной аминогруппы может находиться в форме NH3+.
Кроме того, полигистидиновая группа, которая может быть введена в настоящем изобретении, предпочтительно включает от 3 до 10 гистидинов, более предпочтительно от 5 до 8 гистидинов, и наиболее предпочтительно 6 гистидинов. В дополнение к гистидину, может быть дополнительно включен, по меньшей мере, один цистеин.
При этом, когда направленно воздействующий фрагмент обеспечен в двуспиральной структуре олиго-РНК, содержащей CTGF-, Cyr61- или Plekho1-специфическую миРНК в соответствии с настоящим изобретением, и наночастица, образованная из нее, доставка в клетку-мишень эффективно стимулируется для достижения доставки даже при относительно низком уровне дозы, демонстрируя тем самым высокий контроль экспрессии целевого гена, и предотвращая неспецифическую доставку CTGF-, Cyr61- или Plekho1-специфической миРНК в другие органы и клетки.
Таким образом, настоящее изобретение обеспечивает двуспиральную конструкцию олиго-РНК, в которой лиганд (L), в частности, лиганд, специфически связанный с рецептором, который стимулирует интернализацию в клетку-мишень посредством рецептор-опосредованного эндоцитоза (RME), дополнительно связан со структурой в соответствии со структурными формулами с (1) по (4), (7) и (8). Например, форма, в которой лиганд связан с двуспиральной структурой олиго-РНК в соответствии со структурной формулой (1), имеет конструкцию, представленную следующей структурной формулой (15):
Структурная формула 15

В структурной формуле (15) А, В, X и Y являются такими же, как определено в структурной формуле (1), L представляет собой лиганд, специфически связанный с рецептором, который стимулирует интернализацию в клетку-мишень посредством рецептор-опосредованного эндоцитоза (RME), и i представляет целое число от 1 до 5, предпочтительно целое число от 1 до 3.
Лиганд в структурной формуле (15) может быть предпочтительно выбран из группы, состоящей из специфического к целевому рецептору антитела или аптамера, пептида, который обладает свойствами RME для стимуляции интернализации в клетку специфическим к клетке-мишени образом; или фолата (как правило, фолат и фолевая кислота используются взаимозаменяемо, и фолат в настоящем изобретении означает фолат в природном состоянии или в активированном состоянии в организме человека), химических веществ, таких как сахар, карбогидрат, и т.п., включая гексоамины, такие как N-ацетилгалактозамин (NAG), и т.п., глюкоза, манноза, но настоящее изобретение ими не ограничивается.
Кроме того, гидрофильный материал А в структурной формуле (15) может быть использован в форме блока гидрофильного материала, представленного структурными формулами (5) и (6).
Настоящее изобретение также обеспечивает способ получения двуспиральной конструкции олиго-РНК, содержащей CTGF-, Cyr61- или Plekho1-специфическую миРНК.
Способ получения двуспиральной конструкции олиго-РНК, содержащей CTGF-, Cyr61- или Plekho1-специфическую миРНК в соответствии с настоящим изобретением, может включать следующие стадии:
(1) связывание гидрофильного материала с твердой подложкой;
(2) синтез одноцепочечной РНК на твердой подложке, содержащей связанный с ней гидрофильный материал;
(3) ковалентное связывание гидрофобного материала с 5'-концом одноцепочечной РНК;
(4) синтез одноцепочечной цепи РНК, имеющей последовательность, комплементарную последовательности одноцепочечной РНК;
(5) отделение и очистка конструкции РНК-полимер и одноцепочечной РНК от твердой подложки после завершения синтеза одноцепочечной РНК; и
(6) получение двуспиральной конструкции олиго-РНК путем гибридизации конструкции РНК-полимер и одноцепочечной РНК, содержащей комплементарную ей последовательность.
Твердая подложка в настоящем изобретении предпочтительно представляет собой стекло с контролируемым размером пор (CPG), полистирол, силикагель, бумагу из целлюлозы и т.п., но настоящее изобретение ими не ограничивается. В CPG диаметр составляет предпочтительно от 40 до 180 мкм, и размер пор предпочтительно составляет от 500
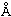
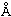
Кроме того, одноцепочечная РНК, содержащая последовательность, комплементарную последовательности одноцепочечной РНК, синтезированной на стадии (2), может содержать фосфатную группу, присоединенную к ее 5'-концу.
При этом настоящее изобретение обеспечивает способ получения двуспиральной конструкции олиго-РНК, в которой лиганд дополнительно присоединен к двуспиральной структуре олиго-РНК, содержащей CTGF-, Cyr61- или Plekho1-специфическую миРНК.
Способ получения двуспиральной конструкции олиго-РНК, содержащей лиганд-присоединенную CTGF-, Cyr61- или Plekho1-специфическую миРНК в соответствии с настоящим изобретением, может включать следующие стадии:
(1) связывание гидрофильного материала с твердой подложкой, содержащей присоединенную к ней функциональную группу;
(2) синтез одноцепочечной РНК на твердой подложке, содержащей присоединенную к ней функциональную группу-гидрофильный материал;
(3) ковалентное связывание гидрофильного материала с 5'-концом одноцепочечной РНК;
(4) синтез одноцепочечной РНК, имеющей последовательность, комплементарную последовательности одноцепочечной РНК;
(5) отделение конструкции функциональная группа-РНК-полимер и одноцепочечной РНК, содержащей комплементарную последовательность, от твердой подложки после завершения синтеза одноцепочечной РНК;
(6) получение одноцепочечной конструкции лиганд-РНК-полимер путем связывания лиганда с концом гидрофильного материала с использованием функциональной группы; и
(7) получение конструкции лиганд-двуспиральная олиго-РНК путем гибридизации конструкции лиганд-РНК-полимер и одноцепочечной РНК, содержащей комплементарную ей последовательность.
После стадии (6), указанной выше, после завершения процесса получения проводят подтверждение получения желаемой конструкции лиганд-двуспиральная олиго-РНК и желаемой одноцепочечной РНК, содержащей комплементарную ей последовательность, путем отделения и очистки конструкции лиганд-РНК-полимер и одноцепочечной РНК, содержащей комплементарную ей последовательность, и измерения молекулярной массы при помощи масс-спектрометра MALDI-TOF. Конструкция лиганд-двуспиральная олиго-РНК может быть получена путем гибридизации полученной конструкции лиганд-РНК-полимер и одноцепочечной РНК, содержащей комплементарную ей последовательность. В способе получения стадия (4), которая представляет собой стадию синтеза одноцепочечной РНК, содержащей последовательность, комплементарную последовательности одноцепочечной РНК, синтезированной на стадии (3), представляет собой независимый процесс синтеза, и может быть выполнена перед стадией (1) или на любой стадии с (1) по (6).
Настоящее изобретение также обеспечивает наночастицу, включающую двуспиральную конструкцию олиго-РНК, содержащую CTGF-, Cyr61- или Plekho1-специфическую миРНК.
Как описано выше, двуспиральная конструкция олиго-РНК, содержащая CTGF-, Cyr61- или Plekho1-специфическую миРНК, представляет собой амфипатическую конструкцию, содержащую гидрофобные материалы и гидрофильные материалы, при этом гидрофильные материалы обладают аффинностью к присутствующим в организме молекулам воды посредством взаимодействия, такого как водородная связь и т.п., и обращены наружу, и гидрофобные материалы обращены внутрь посредством гидрофобного взаимодействия между ними, формируя тем самым термодинамически стабильную наночастицу. То есть гидрофобные материалы расположены в центре наночастицы, и гидрофильные материалы расположены в направлении наружу CTGF-, Cyr61- или Plekho1-специфической миРНК с формированием наночастиц, защищающих CTGF-, Cyr61- или Plekho1-специфическую миРНК. Эти сформированные наночастицы улучшают внутриклеточную доставку CTGF-, Cyr61- или Plekho1-специфической миРНК и улучшают эффект миРНК.
Наночастицы в соответствии с настоящим изобретением могут быть образованы только двуспиральной структурой олиго-РНК, содержащей миРНК, которые имеют одинаковые последовательности, или могут быть образованы двуспиральной структурой олиго-РНК, содержащей миРНК, которые имеют отличающиеся друг от друга последовательности, при этом в настоящем изобретении предполагается, что миРНК, которые имеют отличающиеся друг от друга последовательности, включают миРНК, обладающую специфичностью к различным целевым генам, например, CTGF-, Cyr61- или Plekho1-специфическая миРНК, или миРНК, обладающую специфичностью к одному и тому же целевому гену, но имеющую отличающуюся последовательность.
Кроме того, двуспиральная конструкция олиго-РНК, содержащая другую связанную с респираторными заболеваниями ген-специфическую миРНК дополнительно к CTGF-, Cyr61- или Plekho1-специфической миРНК, может быть также включена в наночастицу в соответствии с настоящим изобретением.
Кроме того, настоящее изобретение обеспечивает композицию для предупреждения или лечения респираторных заболеваний, в частности, идиопатического легочного фиброза и COPD, включающую: CTGF-, Cyr61- или Plekho1-специфическую миРНК, двуспиральную конструкцию олиго-РНК, содержащую миРНК, и/или наночастицу, образованную двуспиральной конструкцией олиго-РНК.
Композиция, включающая в качестве эффективных компонентов CTGF-, Cyr61- или Plekho1-специфическую миРНК в соответствии с настоящим изобретением, двуспиральную конструкцию олиго-РНК, содержащую миРНК, и/или наночастицу, образованную двуспиральной конструкцией олиго-РНК, ингибирует ремоделирование легочной артерии и ремоделирование дыхательных путей, таким образом, CTGF-, Cyr61- или Plekhol-специфическая миРНК или композиция, содержащая миРНК, обладает эффектом предупреждения или лечения респираторных заболеваний.
В частности, композиция для предупреждения или лечения респираторных заболеваний, содержащая двуспиральную конструкцию олиго-РНК в соответствии с настоящим изобретением, может включать:
двуспиральную конструкцию олиго-РНК, включающую CTGF-специфическую миРНК, которая содержит смысловую цепь, имеющую любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 1 по 100 или с 602 по 604 и с 301 по 400, предпочтительно любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 1 по 10, 35, 42, 59, с 602 по 604, с 301 по 303, с 305 по 307, 309, 317, 323 и 329, более предпочтительно любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 4, 5, 8, 9, 35, 42, 59, с 602 по 604, 301, 303, 307 и 323, наиболее предпочтительно любую последовательность, представленную в SEQ ID NO: 42, 59, 602 или 323, и антисмысловую цепь, имеющую последовательность, комплементарную смысловой цепи;
двуспиральную конструкцию олиго-РНК, включающую Cyr61-специфическую миРНК, которая содержит смысловую цепь, имеющую любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 101 по 200 и с 401 по 500, предпочтительно любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 101 по 110, 124, 153, 166, 187, 197, 409, 410, 415, 417, 418, 420, 422, 424, 427 и 429, более предпочтительно любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 102, 104, 107, 108, 124, 153, 166, 187, 197, 410, 422 и 424, наиболее предпочтительно любую последовательность, представленную в SEQ ID NO: 124, 153, 187, 197 или 424, и антисмысловую цепь, имеющую последовательность, комплементарную смысловой цепи; или
двуспиральную конструкцию олиго-РНК, включающую Plekho1-специфическую миРНК, которая содержит смысловую цепь, имеющую любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 201 по 300 и с 501 по 600, предпочтительно любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 201 по 210, 212, 218, 221, 223, с 504 по 507, 514, 515 и с 522 по 525, более предпочтительно любую последовательность, выбранную из группы, состоящей из SEQ ID NO: с 206 по 209, 212, 218, 221, 223, 507, 515 и 525, наиболее предпочтительно любую последовательность, представленную в SEQ ID NO: 212, 218, 221, 223 или 525, и антисмысловую цепь, имеющую последовательность, комплементарную смысловой цепи.
Кроме того, композиция для предупреждения или лечения респираторных заболеваний, включающая двуспиральную конструкцию олиго-РНК в соответствии с настоящим изобретением, может включать: двуспиральную конструкцию олиго-РНК, включающую CTGF-специфическую миРНК, которая содержит смысловую цепь CTGF-специфической миРНК человека и мышей в соответствии с последовательностью SEQ ID NO: 6 или 8, предпочтительно SEQ ID NO: 6, и антисмысловую цепь, имеющую последовательность, комплементарную смысловой цепи;
двуспиральную конструкцию олиго-РНК, включающую Cyr61-специфическую миРНК, которая содержит смысловую цепь Cyr61-специфической миРНК человека и мышей в соответствии с любой последовательностью, представленной в SEQ ID NO: 102, 104 и 105, предпочтительно SEQ ID NO: 102, и антисмысловую цепь, имеющую последовательность, комплементарную смысловой цепи; или
двуспиральную конструкцию олиго-РНК, включающую Plekho1-специфическую миРНК, которая содержит смысловую цепь Plekho1-специфической миРНК человека и мышей в соответствии с любой последовательностью, представленной в SEQ ID NO: 204, 207 и 208, предпочтительно SEQ ID NO: 207, и антисмысловую цепь, имеющую последовательность, комплементарную смысловой цепи.
Кроме того, двуспиральная конструкция олиго-РНК, содержащая CTGF-специфическую миРНК, двуспиральная конструкция олиго-РНК, содержащая Cyr61-специфическую миРНК, и/или двуспиральная конструкция олиго-РНК, содержащая Plekho1-специфическую миРНК, могут быть смешаны и включены в композицию, и, кроме того, миРНК, специфическая к другому связанному с респираторными заболеваниями гену дополнительно к CTGF, Cry61 или Plekho1, или двуспиральная конструкция олиго-РНК, содержащая другую, связанную с респираторными заболеваниями, ген-специфическую миРНК, может быть также включена в композицию в соответствии с настоящим изобретением.
При использовании композиции для предупреждения или лечения респираторных заболеваний, которая дополнительно включает двуспиральную конструкцию олиго-РНК, содержащую другую связанную с респираторными заболеваниями ген-специфическую миРНК вместе с CTGF-, Cyr61- и/или Plekho1-специфической миРНК, или двуспиральную конструкцию олиго-РНК, содержащую CTGF-, Cyr61- и/или Plekho1-специфическую миРНК, может быть получен синергический эффект, сходный с синергическим эффектом комбинированной терапии.
Примеры респираторных заболеваний, которые можно предупредить или лечить с помощью композиции согласно настоящему изобретению, включают идиопатический легочный фиброз, астму, хроническое обструктивное заболевание легких (COPD), острый или хронический бронхит, аллергический ринит, кашель и мокроту, острую инфекцию нижних дыхательных путей, бронхит и бронхиолит, тонзилит, ларингит и т.д., но настоящее изобретением ими не ограничивается.
Кроме того, наночастица, включенная в композицию для предупреждения или лечения респираторного заболевания, в том числе наночастица, образованная двуспиральной структурой олиго-РНК в соответствии с настоящим изобретением, может состоять только из одной конструкции, выбранной из двуспиральной конструкции олиго-РНК, содержащей CTGF-, Cyr61- или Plekho1-специфическую миРНК, или может быть образована в форме, в которой смешаны два или более видов двуспиральных структур олиго-РНК, содержащих CTGF-, Cyr61- или Plekho1-специфическую миРНК.
Композиция согласно настоящему изобретению может быть получена путем дополнительного включения, по меньшей мере, одного фармацевтически приемлемого носителя в дополнение к эффективным компонентам. Фармацевтически приемлемый носитель должен быть совместим с эффективными компонентами настоящего изобретения и может быть использован путем смешивания одного или более компонентов, выбранных из солевого раствора, стерильной воды, раствора Рингера, буферного солевого раствора, раствора декстрозы, раствора мальтодекстрина, глицерина и этанола, и по необходимости могут быть добавлены другие общепринятые добавки, такие как антиоксидант, буфер, фунгистатическое вещество и тому подобное. Кроме того, композиция может быть получена в виде состава для инъекции, такого как водный раствор, суспензия, эмульсия и тому подобное, путем дополнительного добавления разбавителя, диспергирующего вещества, поверхностно-активного вещества, связующего вещества и скользящего вещества. В частности, предпочтительно обеспечить композицию, полученную в виде лиофилизированного состава. Для приготовления лиофилизированного состава можно использовать любой способ, который, как правило, известен в области техники, к которой относится настоящее изобретение, при этом может быть добавлен стабилизатор для лиофилизации. Кроме того, соответствующие способы в данной области или способ, раскрытый в Remington's pharmaceutical Science, Mack Publishing Company, или Easton PA, может быть предпочтительно использован для составления в зависимости от заболевания или компонента.
Доза и способ введения эффективных компонентов, и т.п., включенных в фармацевтическую композицию согласно настоящему изобретению, могут быть определены специалистами в данной области исходя из симптомов пациента и тяжести заболевания. Кроме того, композиция может быть составлена в различной форме, такой как порошок, таблетка, капсула, раствор, инъекция, мазь, сироп и тому подобное, и может быть обеспечена в виде единичной дозы или контейнере для множества доз, например, герметично запечатанной ампуле, бутылке и тому подобное.
Фармацевтическую композицию согласно настоящему изобретению можно вводить перорально или парентерально. Примеры путей введения фармацевтической композиции в соответствии с настоящим изобретением могут включать пероральное, внутривенное, внутримышечное, внутриартериальное, интрамедуллярное, интрадуральное, внутрисердечное, трансдермальное, подкожное, интраперитонеальное, интестинальное, сублингвальное или местное введение, но настоящее изобретение ими не ограничивается. В частности, для лечения респираторных заболеваний способ введения может также включать введение в легкие путем капельного введения в дыхательные органы. Вводимое количество композиции может изменяться в различных диапазонах в зависимости от массы тела, возраста, пола, состояния здоровья, диеты, времени приема, способа введения, скорости выведения из организма, тяжести заболевания пациента и тому подобное, и может быть легко определено специалистом в данной области. Кроме того, композиция согласно настоящему изобретению может быть формулирована в подходящую лекарственную форму путем использования известных технологий для клинического введения.
Кроме того, настоящее изобретение обеспечивает способ предупреждения или лечения респираторных заболеваний, в частности, идиопатического легочного фиброза и COPD, включающий: введение двуспиральной конструкции олиго-РНК в соответствии с настоящим изобретением и наночастицы, включающей двуспиральную конструкцию олиго-РНК, пациенту, нуждающемуся в таком лечении.
Примеры
Далее в настоящем документе настоящее изобретение будет описано более подробно при обращении к следующим примерам. Эти примеры представлены только для иллюстрации настоящего изобретения, и специалисту в данной области будет очевидно, что объем настоящего изобретения не предполагается быть ограниченным этими примерами.
Пример 1. Дизайн целевой последовательности CTGF, Cyr61 или Plekho1 и получение миРНК
Было разработано 604 типа целевых последовательностей (смысловых цепей), способных связываться с последовательностью мРНК гена CTGF (Homo sapiens) (NM_001901), последовательностью мРНК гена Cyr61 (Homo sapiens) (NM_001554), последовательностью мРНК гена Plekho1 (Homo sapiens) (NM_016274), последовательностью мРНК гена CTGF (Mus musculus) (NM_010217), последовательностью мРНК гена Cyr61 (Mus musculus) (NM_010516) или последовательностью мРНК гена Plekho1 (Mus musculus) (NM_023320), и были получены миРНК антисмысловых цепей, имеющие последовательности, комплементарные целевым последовательностям.
Сначала использовали программу для дизайна генов (Turbo si-Designer), разработанную фирмой Bioneer Co., для дизайна целевой последовательности, с которой может связываться миРНК, из последовательностей мРНК соответствующих генов. Для связанных с респираторным заболеванием генов миРНК в соответствии с настоящим изобретением имеет двухцепочечную структуру, включающую смысловую цепь, состоящую из 19 нуклеотидов, и комплементарную ей антисмысловую цепь. Кроме того, получали siCONT (имеющую последовательность, представленную в SEQ ID NO: 601, в качестве смысловой цепи), которая представляет собой миРНК, имеющую последовательность, в которой экспрессия любого гена не является ингибированной. миРНК получали путем связывания фосфодиэфирных связей, формирующих структуру основной цепи РНК, с использованием β-цианоэтилфосфорамидита (Nucleic Acids Research, 12: 4539-4557, 1984). В частности, продукт реакции, содержащий РНК желательной длины, получали путем повторного проведения серий процессов разблокирования, связывания, окисления и кэппирования на твердой подложке, к которой прикреплен нуклеотид, с использованием РНК-синтезатора (384 Synthesizer, BIONEER, Korea). РНК продукта реакции отделяли и очищали с использованием высокоэффективной жидкостной хроматографии (HPLC) на жидкостном хроматографе LC918 (Japan Analytical Industry, Japan), оснащенном колонкой Daisogel Cig (Daiso, Japan), и подтверждали соответствие очищенной РНК целевой последовательности при помощи масс-спектрометра MALDI-TOF (Shimadzu, Japan). После этого желаемую двухцепочечную миРНК (SEQ ID NO: с 1 по 604) получали путем связывания смысловой цепи РНК с антисмысловой цепью РНК.
Пример 2. Получение двуспиральной конструкции олиго-РНК (PEG-SAMiRNA)
Двуспиральная конструкция олиго-РНК (PEG-SAMiRNA), полученная в настоящем изобретении, имеет структуру, представленную следующей структурной формулой (16):
Структурная формула 16

В структурной формуле (16) S представляет собой смысловую цепь миРНК; AS представляет собой антисмысловую цепь миРНК; PEG представляет собой гидрофильный материал, а именно, полиэтиленгликоль; С24 представляет собой гидрофобный материал и тетрадокозан, содержащий дисульфидную связь; и 5' и 3' означают направления конца двуспиральной олиго-РНК.
Смысловую цепь миРНК структурной формулы (16) получали путем синтеза структуры смысловой цепи двуспиральная олиго-РНК-гидрофильный материал, в которой полиэтиленгликоль присоединен к 3'-концу описанным выше способом, в котором фосфодиэфирные связи, формирующие структуру основной цепи РНК, связаны путем использования β-цианоэтилфосфорамидита на основе 3' полиэтиленгликоля (PEG, Mn=2000)-CPG, полученного в примере 1 публикации корейского патента №10-2012-0119212, в качестве подложки, и связывания тетрадокозана, содержащего дисульфидную связь, с 5'-концом, получая тем самым смысловую цепь желаемой конструкции РНК-полимер. Что касается антисмысловой цепи, которую гибридизуют со смысловой цепью, то антисмысловую цепь, имеющую последовательность, комплементарную смысловой цепи, получали с помощью описанной выше реакции.
После завершения синтеза одноцепочечную РНК и конструкцию РНК-полимер, синтезированную путем обработки 28% (об/об) раствором аммиака в водяной ванне при 60°С отделяли от CPG, и защитные группы удаляли путем реакции снятия защиты, соответственно. Одноцепочечную РНК и конструкцию РНК-полимер, из которой были удалены защитные группы, обрабатывали N-метилпирролидоном, триэтиламином и триэтиламинтригидрофторидом при объемном соотношении 10:3:4 в печи при 70°С для удаления 2' TBDMS (трет-бутилдиметилсилила).
РНК продукта реакции отделяли и очищали с помощью HPLC на жидкостном хроматографе LC918 (Japan Analytical Industry, Japan), оснащенном колонкой Daisogel C18(Daiso, Japan), и подтверждали соответствие очищенной РНК целевой последовательности при помощи масс-спектрометра MALDI-TOF (Shimadzu, Japan). Затем для получения двуспиральной конструкции олиго-РНК смысловую цепь и антисмысловую цепь смешивали в одинаковых количествах, помещали в буфер для гибридизации 1X (30 мМ HEPES, 100 мМ ацетата калия. 2 мМ ацетата магния, рН 7,0 ~7,5), и реакция протекала в водяной ванне при постоянной температуре 90°С в течение 3 минут, затем при 37°C с получением двуспиральной конструкции олиго-РНК, содержащей миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 42, 59, 602, 124, 153, 187, 197, 212, 218, 221, 223, 323, 424, 525 или 601 (далее в настоящем документе называемую SAMiRNALP-hCTGF, SAMiRNALP-hCyr, SAMiRNALP-hPlek, SAMiRNALP-mCTGF, SAMiRNALP-mCyr и SAMiRNALP-mPlek SAMiRNALP-CONT, соответственно). Подтверждали, что полученная двуспиральная конструкция олиго-РНК была прогибридизована с помощью электрофореза.
Пример 3. Получение улучшенной двуспиральной конструкции олиго-РНК (Mono-HEG-SAMiRNA)
Улучшенная двуспиральная конструкция олиго-РНК согласно настоящему изобретению (далее в настоящем документе называемую «Mono-HEG-SAMiRNA», смотри структурную формулу (17)), полученная с использованием [РО3--гексаэтиленгликоля]4, который представляет собой блок гидрофильного материала, вместо PEG, который представляет собой гидрофильный материал, имеет следующую структурную формулу (17):
Структурная формула 17

В структурной формуле (17) S представляет собой смысловую цепь миРНК; AS представляет собой антисмысловую цепь миРНК; [Гексаэтиленгликоль]4 представляет собой мономер гидрофильного материала; С24 представляет собой гидрофобный материал и тетрадокозан, содержащий дисульфидную связь; и 5' и 3' означают направления конца смысловой цепи двуспиральной олиго-РНК.
Конструкция Mono-HEG SAMiRNA в соответствии со структурной формулой (17) может быть представлена следующей структурной формулой (18):
Структурная формула 18
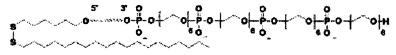
РНК продукта реакции отделяли и очищали с помощью HPLC на жидкостном хроматографе LC918 (Japan Analytical Industry, Japan), оснащенном колонкой Daisogel C18(Daiso, Japan), и подтверждали соответствие очищенной РНК целевой последовательности при помощи масс-спектрометра MALDI-TOF (Shimadzu, Japan). Затем для получения двуспиральной конструкции олиго-РНК смысловую цепь и антисмысловую цепь смешивали в одинаковом количестве, помещали в буфер 1X для гибридизации (30 мМ HEPES, 100 мМ ацетата калия. 2 мМ ацетата магния, рН 7,0 ~7,5), и реакция протекала в водяной ванне при постоянной температуре 90°С в течение 3 минут, затем при 37°С, с получением двуспиральной конструкции олиго-РНК, содержащей миРНК, имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 42, 59, 602, 124, 153, 187, 197, 212, 218, 221, 223, 323, 424, 525 или 601 (далее в настоящем документе называемую Mono-HEG-SAMiRNALP-hCTGF, Mono-HEG-SAMiRNALP-hCyr, Mono-HEG-SAMiRNALP-hPlek, Mono-HEG-SAMiRNALP-mCTGF, Mono-HEG-SAMiRNALP-mCyr, Mono-HEG-SAMiRNALP-mPlek и Mono-HEG-SAMiRNALP-CONT, соответственно). Подтверждали, что полученная двуспиральная конструкция олиго-РНК прогибридизоваласьу с помощью электрофореза.
Пример 4. Получение наночастиц, образованных из улучшенной двуспиральной конструкции олиго-РНК (Mono-HEG-SAMiRNA), и измерение их размера
Двуспиральная конструкция олиго-РНК (Mono-HEG-SAMiRNA), полученная в примере 3, формирует наночастицу, а именно, мицеллу путем гидрофобного взаимодействия между гидрофобными материалами, присоединенными к концу двуспиральной олиго-РНК (фигура 1).
Получение наночастицы (SAMiRNA), образованной соответствующей Mono-HEG-SAMiRNA, подтверждали с помощью анализа PDI (индекса полидисперсности) наночастиц, образованных из Mono-HEG-SAMiRNA-hCTGF, Mono-HEG-SAMiRNA-hCyr, Mono-HEG-SAMiRNA-hPlek, Mono-HEG-SAMiRNA-mCTGF, Mono-HEG-SAMiRNA-mCyr, Mono-HEG-SAMiRNA-mPlek и Mono-HEG-SAMiRNA-CONT.
Пример 4-1. Получение наночастицы
Mono-HEG-SAMiRNA-hCTGF растворяли в 1,5 мл DPBS (фосфатно-буферный солевой раствор Дульбекко) при концентрации 50 мкг/мл, полученную смесь сушили лиофилизацией при -75°С и в условиях 5 мм.рт.ст. (Torr) в течение 48 часов с получением наночастиц в виде порошка, и порошок растворяли в DPBS, который представляет собой растворитель, с получением гомогенизированных наночастиц. Таким же способом получали наночастицы, образованные из Mono-HEG-SAMiRNA-hCyr, Mono-HEG-SAMiRNA-hPlek, Mono-HEG-SAMiRNA-mCTGF, Mono-HEG-SAMiRNA-mCyr, Mono-HEG-SAMiRNA-mPlek, и Mono-HEG-SAMiRNA-CONT.
Пример 4-2. Измерение размера и индекса полидисперсности (PDI) наночастицы
Размер наночастицы определяли путем измерения зета-потенциала. Размер гомогенизированных наночастиц, полученных в примере 4-1, определяли путем измерения зета-потенциала (Nano-ZS, MALVERN, England) в условиях, в которых показатель преломления материала составляет 1,459, показатель поглощения равен 0,001, температура растворителя DPBS равна 25°С, и соответствующие вязкость и показатель преломления составляют 1,0200 и 1,335, соответственно. После выполнения измерения размера, которое включало 15 повторов, измерение затем повторяли шесть раз.
С уменьшением величины PDI соответствующие частицы становятся однородно распределенными и, таким образом, предпочтительно, чтобы наночастицы согласно настоящему изобретению имели в высокой степени однородный размер.
Пример 5. Подтверждение ингибирования экспрессии целевого гена с использованием специфической к целевому гену миРНК для человека в клеточной линии фибробластов человека (MRC-5).
Фибробласты человека (MRC-5), который представляют собой клеточную линию фибробластов, трансформировали миРНК, имеющими в качестве смысловой цепи последовательности, представленные в SEQ ID NO: с 1 по 10, с 101 по 110, с 201 по 210 и 601, полученные в примере 1, и экспрессию целевого гена анализировали в трансформированной клеточной линии фибробластов (MRC-5).
Пример 5-1. Культура клеточной линии фибробластов человека
Клеточную линию фибробластов человека (MRC-5), полученную от Korean Cell line bank (KCLB), выращивали в культуральной среде RPMI-1640 (GIBCO/Invitrogen, США, 10% (об/об) фетальной бычьей сыворотки, 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина) при 37°С и 5% (об/об) СО2.
Пример 5-2. Трансфекция целевой миРНК в клеточную линию фибробластов человека
1,8×105 клеток клеточной линии фибробластов (MRC-5), культивированных в примере 5-1, выращивали в среде RPMI 1640 в течение 18 часов в 6-луночном планшете при 37°С и 5% (об/об) СО2, и среду удаляли, и в каждую лунку вносили 500 мкл среды Opti-MEM (GIBCO, USA).
Затем 3,5 мкл Lipofectamine™ RNAi Max (Invitrogen, USA) смешивали с 246,5 мкл среды Opti-MEM с получением смешанного раствора, и реакция в смешанном растворе протекала при комнатной температуре в течение 5 минут. Растворы миРНК, каждый из которых имеет конечную концентрацию 5 или 20 нМ, готовили путем добавления 5 или 20 мкл миРНК (1 пмоль/мкл), имеющих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: с 1 по 10, с 101 по 110, с 201 по 210 и 601, полученные в примере 1, в 230 мкл среды Opti-MEM. Смесь Lipofectamine™ RNAi Мах и раствор миРНК смешивали, и реакция протекала при комнатной температуре в течение 15 минут с получением раствора для трансфекции.
Затем 500 мкл каждого раствора для трансфекции вносили в каждую лунку опухолевой клеточной линии, содержащей внесенную в нее среду Opti-MEM, и культивировали в течение 6 часов, после чего среду Opti-MEM удаляли. Затем вносили 1 мл культуральной среды Opti-MEM и культивировали при 37°С и 5% (об/об) СО2 в течение 24 часов.
Пример 5-3. Количественный анализ мРНК целевого гена
кДНК получали путем экстракции тотальной РНК из трансфицированной клеточной линии, полученной в примере 5-2, и величину экспрессии мРНК целевого гена определяли путем сравнительного количественного анализа методом PCR в режиме реального времени.
Пример 5-3-1. Отделение РНК от трансфицированной клетки и получение кДНК
Тотальную РНК экстрагировали из трансфицированной клеточной линии, полученной в примере 5-2, с помощью набора для экстракции РНК (AccuPrep Cell total RNA extraction kit, BIONEER, Korea), и экстрагированную РНК использовали для получения кДНК с помощью обратной транскриптазы РНК (AccuPower CycleScript RT Premix/dT20, Bioneer, Korea) согласно следующему способу. В частности, 1 мкг экстрагированной РНК на каждую пробирку добавляли в AccuPower CycleScript RT Premix/dT20(Bioneer, Korea), содержащийся в пробирке Эппендорфа объемом 0,25 мл, и дистиллированную воду, обработанную DEPC (диэтилпирокарбонатом), добавляли до получения общего объема 20 мкл. Процесс гибридизации РНК и праймеров при 30°С в течение 1 минуты при помощи амплификатора генов (MyGenie™ 96 Gradient Thermal Block, BIONEER, Korea), и процесс получения кДНК при 52°С в течение 4 минут повторяли 6 раз, и затем реакцию амплификации останавливали путем инактивации фермента при 90°С в течение 5 минут.
Пример 5-3-2. Сравнительный количественный анализ мРНК целевого гена
Относительное количество мРНК связанного с респираторным заболеванием гена количественно определяли следующим способом посредством PCR в режиме реального времени, используя в качестве матрицы кДНК, полученную в примере 5-3-1. Полученную в примере 5-3-1 кДНК разбавляли в 5 раз дистиллированной водой в каждой лунке 96-луночного планшета. Затем добавляли 3 мкл разбавленной кДНК, 25 мкл 2× GreenStar™ PCR master mix (BIONEER, Korea), 19 мкл дистиллированной воды и 3 мкл праймеров qPCR (таблица 2; каждый F и R имеет концентрацию 10 пмоль/мкл; BIONEER, Korea) с получением смешанного раствора. При этом RPL13A (рибосомальный белок L13a), который представляет собой ген домашнего хозяйства (далее в настоящем документе называемый как ген НК), определяли как эталонный ген для нормализации величины экспрессии мРНК целевого гена. Последующую реакцию выполняли на 96-луночном планшете, содержащем смесь, с помощью Exicycler™ 96 Real-Time Quantitative Thermal Block (BIONEER, Korea). После реакции при 95°C в течение 15 минут для активации фермента и удаления вторичной структуры кДНК, 42 раза повторяли четыре процесса, в том числе процесс денатурации при 94°С в течение 30 секунд, процесс гибридизации при 58°С в течение 30 секунд, процесс удлинения при 72°С в течение 30 секунд и процесс сканирования с использованием красителя SYBR green, и конечное удлинение выполняли при 72°С в течение 3 минут. Затем температуру поддерживали при 55°С в течение 1 минуты, и кривую плавления анализировали в интервале от 55°С до 95°С. После завершения PCR рассчитывали значение Ct (порогового цикла) каждого полученного целевого гена, то есть значения Ct целевого гена корректировали на значение Ct гена домашнего хозяйства GAPDH, и затем разницу (ΔCt) получали путем использования в качестве контрольной группы тестируемой группы, обработанной миРНК (SEQ ID NO: 601, siCONT), содержащей контрольную последовательность, предотвращающую ингибирование экспрессии гена.
Величину экспрессии целевого гена клетки, обработанной CTGF (Homo sapiens)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 1 по 10) определяли путем сравнительного количественного анализа, используя величину ΔCt и расчетную формулу 2(-ΔCt)×100 (фигура 2А). Кроме того, величину экспрессии целевого гена клетки, обработанной Cyr61 (Homo sapiens)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 101 по 110), определяли путем сравнительного количественного анализа (фигура 2 В), и величину экспрессии целевого гена клетки, обработанной Plekho1 (Homo sapiens)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 201 по 210), определяли путем сравнительного количественного анализа (фигура 2С).
В результате может быть подтверждено, что несколько видов миРНК согласно настоящему изобретению показали высокий уровень ингибирования экспрессии целевого гена. Кроме того, для отбора миРНК, обладающей высокой эффективностью, были отобраны миРНК, имеющие в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 1, 3, 4, 8, 9, 10, 102, 104, 105, 106, 107, 108, 109, 204, 206, 207, 208, 209 и 210, в которых величина экспрессии мРНК для каждого гена при концентрации 5 нМ является значительно уменьшенной.


Пример 6. Отбор специфической к целевому гену миРНК для человека, обладающей высокой эффективностью в клеточной линии фибробластов человека (MRC-5)
Клеточную линию фибробластов человека (MRC-5) трансформировали с использованием миРНК, имеющих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 1, 3, 4, 8, 9, 10, 102, 104, 105, 106, 107, 108, 109, 204, 206, 207, 208, 209, 210 и 601, отобранные в примере 5-3-2, и экспрессию целевого гена анализировали в трансформированной клеточной линии фибробластов (MRC-5) для отбора миРНК, обладающей высокой эффективностью.
Пример 6-1. Культура клеточной линии фибробластов человека
Клеточную линию фибробластов человека (MRC-5), полученную из Korean Cell line bank (KCLB, Korea), культивировали в таких же условиях, как описано в Примере 5-1.
Пример 6-2. Трансфекция целевой миРНК в клеточную линию фибробластов человека
1,8×105 клеток клеточной линии фибробластов (MRC-5), культивированных в примере 6-1, культивировали в среде RPMI 1640 в течение 18 часов в 6-луночном планшете в условиях 37°С и 5% (об/об) СО2, и среду удаляли, и в каждую лунку вносили 500 мкл среды Opti-MEM.
Затем 3,5 мкл Lipofectamine™ RNAi Max (Invitrogen, USA) смешивали с 246,5 мкл среды Opti-MEM с получением смешанного раствора, и реакция в смешанном растворе протекала при комнатной температуре в течение 5 минут. Готовили растворы миРНК, каждый из которых имел конечную концентрацию 0,2 нМ или 1 нМ, путем добавления 0,2 мкл или 1 мкл миРНК (1 пмоль/мкл), имеющих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 1, 3, 4, 8, 9, 10, 102, 104, 105, 106, 107, 108, 109, 204, 206, 207, 208, 209, 210 и 601, полученные в примере 1, в 230 мкл среды Opti-MEM. Смесь Lipofectamine™ RNAi Мах и раствор миРНК смешивали, и реакция протекала при комнатной температуре в течение 15 минут с получением раствора для трансфекции.
Затем 500 мкл каждого раствора для трансфекции вносили в каждую лунку опухолевой клеточной линии, содержащей внесенную в нее среду Opti-MEM, и культивировали в течение 6 часов, после чего среду Opti-MEM удаляли. Затем вносили 1 мл культуральной среды RPMI 1640 и культивировали в условиях 37°С и 5% (об/об) СО2 в течение 24 часов.
Пример 6-3. Количественный анализ целевого гена мРНК
кДНК получали путем экстракции тотальной РНК из трансфицированной клеточной линии, полученной в примере 6-2, таким же способом, как описано в примере 4-3, и величину экспрессии мРНК целевого гена определяли путем сравнительного количественного анализа методом PCR в режиме реального времени. Наблюдаемая величина ингибирования экспрессии целевого гена после обработки миРНК при низкой концентрации ясно подтверждает эффективность каждой миРНК, и что миРНК, имеющие в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 8, 107 и 206, демонстрируют сравнительно высокий уровень ингибирования экспрессии целевого гена даже при значительно низкой концентрации (фигура 3).
Пример 7. Подтверждение ингибирования экспрессии целевого гена с использованием специфической к целевому гену миРНК для человека в клеточной линии рака легких человека (А549)
Клеточную линию рака легких человека (А549), которая представляет собой клеточную линию опухоли легкого, трансформировали с помощью миРНК, имеющих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 35, 42, 59, 602, 603, 604, 124, 153, 166, 187, 197, 212, 218, 221, 223 и 601, полученные в примере 1, и экспрессию целевого гена анализировали в трансформированной клеточной линии рака легкого (А549).
Пример 7-1. Культура клеточной линии рака легкого человека
Клеточную линии рака легкого человека (А549), полученную из Американской коллекции типовых культур (American Type Culture Collection, АТСС), культивировали в культуральной среде DMEM (GIBCO/Invitrogen, США, 10% (об/об) фетальной бычьей сыворотки, 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина) в условиях 37°С и 5% (об/об) CO2.
Пример 7-2. Трансфекция целевой миРНК в клеточную линию рака легкого человека
1,2×105 клеток клеточной линии рака легкого (А549), культивированных в примере 7-1, культивировали в среде DMEM в течение 18 часов в 6-луночном планшете в условиях 37°С и 5% (об/об) СО2, и среду удаляли, и в каждую лунку вносили 500 мкл среды Opti-MEM (GIBCO, США).
Затем 3,5 мкл Lipofectamine™ RNAi Max (Invitrogen, USA) смешивали с 246,5 мкл среды Opti-MEM с получением смешанного раствора, и реакция в смешанном растворе протекала при комнатной температуре в течение 5 минут. Готовили растворы миРНК, каждый из которых имел конечную концентрацию 5 нМ, 1 нМ, 0,5 нМ, 0,2 нМ или 0,04 нМ, путем добавления 1 мкл миРНК (1 пмоль/мкл), имеющих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 35, 42, 59, 602, 603, 604, 124, 153, 166, 187, 197, 212, 218, 221 и 223, полученные в примере 1, в 230 мкл среды Opti-MEM. Смесь Lipofectamine™ RNAi Мах и раствор миРНК смешивали, и реакция протекала при комнатной температуре в течение 15 минут с получением раствора для трансфекции.
Затем 500 мкл каждого раствора для трансфекции вносили в каждую лунку опухолевой клеточной линии, содержащую внесенную в нее среду Opti-MEM, и культивировали в течение 6 часов, после чего среду Opti-MEM удаляли. Затем вносили 1 мл культуральной среды RPMI 1640 и культивировали в условиях 37°С и 5% (об/об) СО2 в течение 24 часов.
Пример 7-3. Количественный анализ целевого гена мРНК
кДНК получали путем экстракции тотальной РНК из трансфицированной клеточной линии, полученной в примере 7-2, и величину экспрессии мРНК целевого гена определяли путем сравнительного количественного анализа методом PCR в режиме реального времени.
Пример 7-3-1. Отделение РНК от трансфицированной клетки и получение кДНК
Тотальную РНК экстрагировали из трансфицированной клеточной линии, полученной в примере 5-2, с помощью набора для экстракции РНК (AccuPrep Cell total RNA extraction kit, BIONEER, Korea), и экстрагированную РНК использовали для получения кДНК с помощью обратной транскриптазы РНК (AccuPower CycleScript RT Premix/dT20, Bioneer, Korea) согласно следующему способу. В частности, 1 мкг экстрагированной РНК на каждую пробирку добавляли в AccuPower CycleScript RT Premix/dT20(Bioneer, Korea), содержащийся в пробирке Эппендорфа объемом 0,25 мл, и добавляли дистиллированную воду, обработанную DEPC (диэтилпирокарбонатом) таким образом, чтобы получить общий объем 20 мкл. Процесс гибридизации РНК и праймеров при 30°С в течение 1 минуты с помощью амплификатора генов (MyGenie™ 96 Gradient Thermal Block, BIONEER, Korea) и процесс получения кДНК при 52°С в течение 4 минут повторяли 6 раз и затем реакцию амплификации останавливали путем инактивации фермента при 90°С в течение 5 минут.
Пример 7-3-2. Сравнительный количественный анализ целевого гена мРНК
Относительное количество связанного с респираторным заболеванием гена мРНК количественно определяли следующим способом посредством PCR в режиме реального времени, при этом в качестве темплата использовали кДНК, полученную в примере 7-3-1. кДНК, полученную в примере 6-3-1, разбавляли 5 раз дистиллированной водой в каждой лунке 96-луночного планшета. Затем добавляли 3 мкл разбавленной кДНК, 25 мкл 2× GreenStar™ PCR master mix (BIONEER, Korea), 19 мкл дистиллированной воды и 3 мкл праймеров qPCR (таблица 2; каждый F и R содержит 10 пмоль/мкл; BIONEER, Korea) с получением смешанного раствора. При этом RPL13A (рибосомальный белок L13a), который представляет собой конститутивный ген (далее в настоящем документе называемый как НК ген) определяли в качестве эталонного гена для нормализации величины экспрессии целевого гена мРНК. Последующую реакцию выполняли на 96-луночном планшете, содержащем смесь, с помощью Exicycler™ 96 Real-Time Quantitative Thermal Block (BIONEER, Korea). После протекания реакции при 95°С в течение 15 минут для активации фермента и удаления вторичной структуры кДНК, четыре процесса, включающие процесс денатурации при 94°С в течение 30 секунд, процесс гибридизации при 58°С в течение 30 секунд, процесс удлинения при 72°С в течение 30 секунд и процесс сканирования с использованием красителя SYBR green повторяли 42 раза, и конечное удлинение выполняли при 72°С в течение 3 минут. Затем температуру поддерживали при 55°С в течение 1 минуты и кривую плавления анализировали в интервале от 55°С до 95°С. После завершения PCR рассчитывали значение Ct (порогового цикла) каждого полученного целевого гена, то есть значения Ct целевого гена корректировали на значение Ct гена домашнего хозяйства GAPDH, и затем разницу (ΔCt) получали путем использования в качестве контрольной группы тестируемой группы, обработанной миРНК (SEQ ID NO: 601, siCONT), содержащей контрольную последовательность, предотвращающую ингибирование экспрессии гена.
Величину экспрессии целевого гена клетки, обработанной CTGF (Homo sapiens)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 132, 42, 59, 602, 603, 604) определяли путем сравнительного количественного анализа с использованием значения ΔCt и расчетной формулы 2(-ΔCt)×100 (фигура 4А). Затем величину экспрессии целевого гена клетки, обработанной Cyr61 (Homo sapiens)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 124, 153, 166, 187 и 197) определяли путем сравнительного количественного анализа (фигура 4В), и величину экспрессии целевого гена клетки, обработанной Plekho1 (Homo sapiens)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 212, 218, 221 и 223) определяли путем сравнительного количественного анализа (фигура 4С).
В результате можно подтвердить, что некоторые типы миРНК согласно настоящему изобретению продемонстрировали высокий уровень ингибирования экспрессии целевого гена. Кроме того, для отбора миРНК, обладающей высокой эффективностью, были отобраны миРНК, имеющие в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 42, 59, 602, 124, 153, 187, 197, 212, 218, 221 и 223, в которых величина экспрессии мРНК для каждого гена при концентрации 5 нМ является значительно сниженной.
Пример 8. Ингибирование экспрессии целевого гена в клеточной линии рака легкого человека (А549) наночастицей (SAMiRNA), образованной двуспиральной структурой олиго-полимера
Клеточную линию рака легкого человека (А549) трансформировали путем использования наночастицы, образованной из SAMiRNA LP, включающей миРНК, имеющей в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 42, 59, 602, 124, 153, 187, 197, 212, 218, 221 и 223, отобранные в примере 7-3-2, и экспрессию целевого гена анализировали в трансформированной клеточной линии рака легкого (А549).
Пример 8-1. Культура клеточной линии рака легкого человека
Клеточную линию рака легкого человека (А549), полученную из Американской коллекции типовых культур (American Type Culture Collection, АТСС), культивировали в таких же условиях, как описано в примере 7-1.
Пример 8-2. Трансфекция целевой SAMiRNA в клеточную линию рака легкого человека
1,2×105 клеток клеточной линии рака легкого (А549), культивированных в примере 8-1, культивировали в среде RPMI 1640 в течение 18 часов в 12-луночном планшете в условиях 37°С и 5% (об/об) СО2, и среду удаляли, и в каждую лунку вносили такое же количество среды Opti-MEM (GIBCO, США). 100 мкл среды Opti-MEM и SAMiRNALP и monoSAMiRNALP, полученные в примере 4-2, добавляли в DPBS при концентрации 50 мкг/мл, полученную смесь сушили вымораживанием при -75°С и в условиях 5 мм.рт.ст. (Torr) в течение 48 часов таким же способом, как описано в примере 5-1, с получением гомогенизированных наночастиц. Затем каждую лунку с опухолевой клеточной линией, в которую внесена среда Opti-MEM, обрабатывали раствором для трансфекции при концентрации 200 нМ, и культивировали при 37°С и 5% (об/об) CO2 в течение 48 часов.
Пример 8-3. Сравнительный количественный анализ мРНК целевого гена
кДНК получали путем экстракции тотальной РНК из трансфицированной клеточной линии, полученной в примере 8-2, таким же способом, как описано в пример 6-3, и величину экспрессии мРНК целевого гена определяли путем сравнительного количественного анализа методом PCR в режиме реального времени. Наблюдаемая величина ингибирования экспрессии целевого гена после обработки миРНК при низкой концентрации ясно подтверждала эффективность каждой миРНК, и что миРНК, содержащие в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 42, 59 и 602, демонстрируют сравнительно высокий уровень ингибирования экспрессии целевого гена даже при крайне низкой концентрации (фигура 5).
Пример 9. Подтверждение ингибирования экспрессии целевого гена с использованием специфической к целевому гену миРНК для мышей в клеточной линии фибробластов мышей (NIH3T3)
Фибробласт мышей (NIH3T3), который представляет собой клеточную линию фибробластов, трансформировали с помощью миРНК, содержащих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: с 301 по 330, с 401 по 430, с 501 по 530 и 601, полученные в примере 1, и экспрессию целевого гена анализировали в трансформированной клеточной линии фибробластов (NIH3T3).
Пример 9-1. Культура клеточной линии фибробластов мышей
Клеточную линию фибробластов мышей (NIH3T3), полученную из Американской коллекции типовых культур (American Type Culture Collection, АТСС), культивировали в культуральной среде RPMI-1640 (GIBCO/Invitrogen, США, 10% (об/об) фетальной бычьей сыворотки, 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина) в условиях 37°С и 5% (об/об) CO2.
Пример 9-2. Трансфекция целевой миРНК в клеточную линию фибробластов мышей
1×105 клеток клеточной линии фибробластов (NIH3T3), культивированную в примере 9-1, культивировали в среде RPMI 1640 в течение 18 часов в 12-луночном планшете в условиях 37°С и 5% (об/об) СО2, и среду удаляли, и в каждую лунку вносили 500 мкл среды Opti-MEM (GIBCO, США).
Затем 1,5 мкл Lipofectamine™ RNAi Max (Invitrogen, USA) смешивали с 248,5 мкл среды Opti-MEM с получением смешанного раствора, и реакция в смешанном растворе протекала при комнатной температуре в течение 5 минут. 5 мкл или 20 мкл миРНК (1 пмоль/мкл), содержащих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: с 301 по 330, с 401 по 430, с 501 по 530 и 601, полученные в примере 1, добавляли в 230 мкл среды Opti-MEM с получением растворов миРНК с конечной концентрацией 5 нМ или 20 нМ. Смесь Lipofectamine™ RNAi Мах и раствор миРНК смешивали, и реакция протекала при комнатной температуре в течение 20 минут с получением раствора для трансфекции.
Затем 500 мкл каждого раствора для трансфекции вносили в каждую лунку опухолевой клеточной линии, содержащей внесенную в нее среду Opti-MEM, и культивировали в течение 6 часов, после чего среду Opti-MEM удаляли. Затем вносили 1 мл культуральной среды RPMI 1640 и культивировали в условиях 37°С и 5% (об/об) СО2 в течение 24 часов.
Пример 9-3. Количественный анализ мРНК целевого гена
кДНК получали путем экстракции тотальной РНК из трансфицированной клеточной линии, полученной в примере 9-2, таким же способом, как описано в примере 5-3, и величину экспрессии мРНК целевого гена определяли путем сравнительного количественного анализа методом PCR в режиме реального времени.
Величину экспрессии целевого гена клетки, обработанной CTGF (Mus musculus)-специфической миРНК (содержащей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 301 по 330) (фигура 6А) определяли путем сравнительного количественного анализа. Кроме того, величину экспрессии целевого гена клетки, обработанной Cyr61 (Mus musculus)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 401 по 430) определяли путем сравнительного количественного анализа (фигура 6В), и величину экспрессии целевого гена клетки, обработанной Plekho1 (Mus musculus)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: с 501 по 530) определяли путем сравнительного количественного анализа (фигура 6С).
В результате можно подтвердить, что некоторые виды миРНК согласно настоящему изобретению продемонстрировали высокий уровень ингибирования экспрессии целевого гена. Кроме того, для отбора миРНК, обладающей высокой эффективностью, была отобрана миРНК, имеющая в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 301, 302, 303, 305, 306, 307, 309, 317, 323 или 329, в которой величина экспрессии мРНК для CTGF (Mus musculus) при концентрации 20 нМ является значительно сниженной, миРНК, имеющая в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 409, 410, 415, 417, 418, 420, 422, 424, 427 или 429, в которой величина экспрессии мРНК для Cyr61 (Mus musculus) при концентрации 20 нМ является значительно сниженной, и миРНК, имеющая в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 504, 505, 506, 507, 514, 515, 522, 523, 524 или 525, в которой величина экспрессии мРНК для Plekho1 (Mus musculus) при концентрации 20 нМ является значительно сниженной.
Кроме того, для отбора миРНК, обладающей более предпочтительной эффективностью, была отобрана миРНК, имеющая в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 301, 303, 307 или 323, в которой величина экспрессии мРНК для CTGF (Mus musculus) при концентрации 5 нМ является значительно сниженной, миРНК, имеющая в качестве смысловой цепи последовательность, представленную SEQ ID NO: 410, 422 или 424, в которой величина экспрессии мРНК для Cyr61 (Mus musculus) при концентрации 5 нМ является значительно сниженной, и миРНК, имеющая в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 507, 515 или 525, в которой величина экспрессии мРНК для Plekho1 (Mus musculus) при концентрации 5 нМ является значительно сниженной (фигура 7).
Пример 10. Отбор специфической к целевому гену миРНК для мышей, обладающей высокой эффективностью в клеточной линии фибробластов мышей (NIH3T3)
Для отбора миРНК, обладающей высокой эффективностью экспрессию целевого гена анализировали в клеточной линии фибробластов мышей (NIH3T3) с использованием миРНК, имеющих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 301, 303, 307, 323,410, 422, 424, 507, 515, 525 и 601, отобранные в примере 9-3.
Пример 10-1. Культура клеточной линии фибробластов мышей
Клеточную линию фибробластов мышей (NIH3T3), полученную из Американской коллекции типовых культур (American Type Culture Collection, АТСС), культивировали в таких же условиях, как в примере 9-1.
Пример 10-2. Трансфекция целевой миРНК в клеточную линию фибробластов мышей
1×105 клеток клеточной линии фибробластов (NIH3T3), культивированную в примере 10-1, культивировали в среде RPMI 1640 в течение 18 часов в 12-луночном планшете в условиях 37°С и 5% (об/об) CO2, и среду удаляли, и в каждую лунку вносили 500 мкл среды Opti-MEM (GIBCO, США).
Затем 1,5 мкл Lipofectamine™ RNAi Max (Invitrogen, USA) смешивали с 248,5 мкл среды Opti-MEM с получением смешанного раствора, и реакция в смешанном растворе протекала при комнатной температуре в течение 5 минут. 0,2 мкл, 1 мкл или 5 мкл миРНК (1 пмоль/мкл), содержащих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 301, 303, 307, 323, 410, 422, 424, 507, 515, 525 и 601, полученные в примере 1, добавляли в 230 мкл среды Opti-MEM, получая тем самым растворы миРНК с конечной концентрацией 0,2 нМ, 1 нМ или 5 нМ. Смесь Lipofectamine™ RNAi Мах и раствор миРНК смешивали, и реакция протекала при комнатной температуре в течение 20 минут с получением раствора для трансфекции.
Затем 500 мкл каждого раствора для трансфекции вносили в каждую лунку опухолевой клеточной линии, содержащей внесенную в нее среду Opti-MEM, и культивировали в течение 6 часов, после чего среду Opti-MEM удаляли. Затем вносили 1 мл культуральной среды RPMI 1640 и культивировали в условиях 37°С и 5% (об/об) CO2 в течение 24 часов.
Пример 10-3. Количественный анализ мРНК целевого гена
кДНК получали путем экстракции тотальной РНК из трансфицированной клеточной линии, полученной в примере 10-2, таким же способом, как описано в примере 5-3, и величину экспрессии мРНК целевого гена определяли путем сравнительного количественного анализа методом PCR в режиме реального времени. Величину экспрессии целевого гена клетки, обработанной CTGF (Mus musculus)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 301, 303, 307 и 323) определяли путем сравнительного количественного анализа (фигура 8А). Кроме того, величину экспрессии целевого гена клетки, обработанной Cyr61 (Mus musculus)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 410, 422 и 424) определяли путем сравнительного количественного анализа (фигура 8В), и величину экспрессии целевого гена клетки, обработанной Plekho1 (Mus musculus)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 507, 515 и 525) определяли путем сравнительного количественного анализа (фигура 8С).
В результате, для отбора миРНК, обладающей высокой эффективностью, было подтверждено, что каждая специфическая к целевому гену миРНК ингибирует экспрессию целевого гена зависимым от концентрации образом, и было подтверждено, что миРНК, имеющие в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 307, 424 и 525, продемонстрировали сравнительно высокий уровень ингибирования экспрессии целевого гена даже при значительно низкой концентрации.
Пример 11. Подтверждение ингибирования экспрессии целевого гена с использованием специфической к целевому гену миРНК для человека в клеточной линии фибробластов мышей (NIH3T3)
Так как биофармацевтические средства содержат участки специфического к разновидностям действия, такие как структура белка или последовательность гена, идентичность используемого для лечения лекарственного средства имеет важное значение для обеспечения эффективности при разработке нового биофармацевтического средства. Гомология последовательностей генов между специфической к целевому гену миРНК для человека и специфической к целевому гену миРНК для мышей, разработанных в примере 1, анализировали для отбора последовательностей миРНК, которые могут подтвердить эффект ингибирования экспрессии целевого гена в клетках фибробластов мышей.
Отобранные последовательности миРНК представляют собой миРНК, имеющие в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 4, 5, 6, 8, 9, 102, 104, 105, 107, 108, 109, 202, 204, 206, 207, 208 и 209, которые представляют собой специфические к целевому гену миРНК для человека, полученные в примере 1, миРНК, имеющие в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 307, 424 и 525, которые представляют собой специфические к целевому гену миРНК для мышей, и миРНК, имеющая в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 601, которая представляет собой контрольную группу. Экспрессию целевого гена анализировали в клеточной линии фибробластов мышей (NIH3T3) с использованием этих отобранных миРНК, и их эффективность подтверждали в мышиной клетке миРНК, разработанной на основе гена человека.
Пример 11-1. Культура клеточной линии фибробластов мышей
Клеточную линию фибробластов мышей (NIH3T3), полученную из Американской коллекции типовых культур (American Type Culture Collection, АТСС), культивировали в таких же условиях, как описано в примере 9-1.
Пример 11-2. Трансфекция целевой миРНК в клеточную линию фибробластов мышей
1,8×105 клеток клеточной линии фибробластов (NIH3T3), культивированных в примере 11-1, культивировали в среде RPMI 1640 в течение 18 часов в 6-луночном планшете в условиях 37°С и 5% (об/об) СО2, и среду удаляли, и в каждую лунку вносили 500 мкл среды Opti-MEM (GIBCO, США).
Затем 3,5 мкл Lipofectamine™ RNAi Max (Invitrogen, USA) смешивали с 246,5 мкл среды Opti-MEM с получением смешанного раствора, и реакция в смешанном растворе протекала при комнатной температуре в течение 5 минут. Растворы миРНК с конечной концентрацией 5 или 20 нМ готовили путем добавления 5 или 20 мкл миРНК (1 пмоль/мкл), содержащих в качестве смысловой цепи последовательности, представленные в SEQ ID NO: 4, 5, 6, 8, 9, 102, 104, 105, 107, 108, 109, 202, 204, 206, 207, 208, 209, 307, 424, 525 и 601, полученные в примере 1, в 230 мкл среды Opti-MEM. Смесь Lipofectamine™ RNAi Мах и раствор миРНК смешивали, и реакция протекала при комнатной температуре в течение 15 минут с получением раствора для трансфекции.
Затем 500 мкл каждого раствора для трансфекции вносили в каждую лунку опухолевой клеточной линии, содержащей внесенную в нее среду Opti-MEM, и культивировали в течение 6 часов, после чего среду Opti-MEM удаляли. Затем вносили 1 мл культуральной среды RPMI 1640 и культивировали в условиях 37°С и 5% (об/об) СО2 в течение 24 часов.
Пример 11-3. Количественный анализ мРНК целевого гена
кДНК получали путем экстракции тотальной РНК из трансфицированной клеточной линии, полученной в примере 11-2, таким же способом, как описано в примере 5-3, и величину экспрессии мРНК целевого гена определяли путем сравнительного количественного анализа методом PCR в режиме реального времени. Величину экспрессии целевого гена клетки, обработанной CTGF (Mus musculus)-специфической миРНК (SEQ ID NO: 307) или обработанной CTGF (Homo sapiens)-специфической миРНК (SEQ ID NO: 4, 5, 6, 8 или 9) определяли путем сравнительного количественного анализа (фигура 9А). Величину экспрессии целевого гена клетки, обработанной Cyr61 (Mus musculus)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 424) или обработанной Cyr61 (Mus musculus)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 102, 104, 105, 107, 108 или 109) определяли путем сравнительного количественного анализа (фигура 9В), и величину экспрессии целевого гена клетки, обработанной Plekhol (Mus musculus)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 525), или обработанной Plekho1 (Mus musculus)-специфической миРНК (имеющей в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 202, 204, 206, 207, 208 или 209, определяли путем сравнительного количественного анализа (фигура 9С).
В результате было подтверждено, что каждая специфическая к целевому гену миРНК для человека ингибирует экспрессию целевого гена в соответствии с гомологией последовательностей, и было подтверждено, что миРНК, содержащая в качестве смысловой цепи последовательность, представленную в SEQ ID NO: 6, 8, 102, 104, 105, 204, 207 и 208, продемонстрировала сравнительно высокий уровень ингибирования экспрессии целевого гена при 20 нМ, и помимо этого, величина IC50 (концентрация, вызывающая 50% ингибирования) составила меньше, чем 20 нМ в миРНК, имеющих последовательности, представленные в SEQ ID NO: 6, 102 и 207, даже в мышиных клеточных линиях. Таким образом, было получено подтверждение того, что сравнительно высокий уровень ингибирования экспрессии целевого гена сохранялся даже при низкой концентрации, то есть эти миРНК обладали высокой эффективностью (фигура 10).
Благоприятные эффекты
CTGF-, Cyr61- или Plekho1-специфическая миРНК в соответствии с настоящим изобретением, двуспиральная конструкция олиго-РНК, содержащая миРНК, и фармацевтическая композиция, предназначенная для лечения, содержащая двуспиральную конструкцию олиго-РНК, могут ингибировать экспрессию CTGF, Cyr61 или Plekho1 с высокой эффективностью без вызывания побочных эффектов с обеспечением эффектов лечения респираторных заболеваний, в частности, идиопатического легочного фиброза и хронического обструктивного заболевания легких (COPD), и могут быть использованы с высокой эффективностью для лечения респираторных заболеваний, для которых в настоящее время не существует подходящего терапевтического агента, в частности, идиопатического легочного фиброза и хронического обструктивного заболевания легких (COPD).
Исходя из указанного выше, специалисту в области, к которой относится настоящее изобретение, будет понятно, что настоящее изобретение может быть воплощено в других конкретных вариантах осуществления без изменения его технической сущности или существенных признаков. В этом отношении должно быть понятно, что указанные выше примеры во всех аспектах являются иллюстративными, но не ограничивающими. Объем настоящего изобретения должен рассматриваться как включающий смысл и объем прилагаемых пунктов формулы изобретения, и все изменения и модифицированные формы, которые получены скорее из его эквивалентной концепции, чем подробного описания.
Реферат
Группа изобретений относится к области биотехнологии. Предложены конструкция и наночастица, содержащая указанную конструкцию, предназначенные для эффективной доставки в клетки CTGF-специфической миРНК, а также фармацевтическая композиция и состав, содержащий лиофилизированную указанную фармацевтическую композицию, для предупреждения или лечения респираторных заболеваний, и способ предупреждения или лечения респираторных заболеваний. Указанная конструкция состоит из гидрофильного и гидрофобного материалов, связанных напрямую через простую ковалентную связь или с помощью линкеров с различными концами смысловой или антисмысловой цепи CTGF-специфической миРНК. Строение предложенной конструкции обеспечивает самопроизвольную сборку содержащих указанную конструкцию наночастиц, которые имеют низкие индексы полидисперсности и однородные размеры. Контроль строения гидрофильного фрагмента предложенной конструкции обеспечивает возможность регулирования индекса полидисперсности и размера наночастиц. Предложенная группа изобретений обеспечивает эффективную доставку CTGF-специфической миРНК в клетки и может быть использована в медицине для предупреждения или лечения респираторных заболеваний. 5 н. и 18 з.п. ф-лы, 25 ил., 2 табл., 11 пр.
Формула




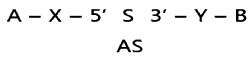

Документы, цитированные в отчёте о поиске
Комбинации, содержащие противомускариновые средства и ингибиторы pde4

Комментарии