Способ трехмерного картирования камер сердца с использованием навигационной системы "астрокард" для лечения пациентов с нарушением ритма сердца - RU2724191C1
Код документа: RU2724191C1
Чертежи


Описание
Область техники, к которой относится изобретение
Изобретение относится к области медицины, а именно кардиохирургии, интервенционной аритмологии и может быть использовано в системе электроанатомического картирования, например, «Астрокард», для повышения точности, эффективности, снижения времени проведения интервенционных вмешательств.
Уровень техники
Из уровня техники известен способ картирования камер сердца, реализуемый системой инвазивного электроанатомического картирования «Carto merge system» [Kuklik P. et al. Integration of the data from electroanatomical mapping system and CT imaging modality // The international journal of cardiovascular imaging. - 2009. - T. 25. - №. 4. - C. 425-432.], использующей технологию магнитной локализации для определения положения небольших датчиков, которые встроены в наконечники различных диагностических и аблационных электрофизиологических катетеров. При реализации способа на пациента в рентгеноперационной накладывают шесть референтных датчиков, устанавливают специальный магнит под операционным столом. Далее с использованием навигационного электрода с магнитным датчиком выполняют построение электроанатомической модели камеры сердца, которую интегрируют в КТ/МРТ-изображение. Интеграцию производят ручным способом, опираясь на несколько произвольных точек на электроанатомической модели, либо посредством сдвига модели и КТ/МРТ-изображения относительно друг друга, после чего выполняют радиочастотную аблацию.
Система обеспечивает построение электроанатомических, активационных, вольтажных карт только специальными электродами с магнитными датчиками. Наибольшая точность совпадения достигается при малом промежутке времени между выполненным КТ/МРТ исследованием и интервенционным вмешательством. Однако так как используется ручное совмещение/сопоставление изображений, точность и достоверность получаемого изображения камеры сердца снижается.
Из уровня техники известен также способ картирования камер сердца, реализуемый системой Rhythmia (Boston Scientific) (Practical Guide to Catheter Ablation of Atrial Fibrillation. Авторы: Jonathan S. Steinberg, Pierre Jais, Hugh Calkins), который также использует методику магнитной локализации электродов, в которых размещены небольшие магнитные датчики, и методику, основанную на регистрации импеданса с использованием электродов без магнитных датчиков. Согласно способу на спину пациента накладывают один магнитный датчик, который визуализируется в магнитном поле специальным магнитом, установленным под операционным столом, затем на грудную клетку пациента накладывают дополнительные референтные электроды, которые позволяют визуализировать электроды в импендансном поле без магнитного датчика. С использованием специального навигационного электрода выполняют построение электроанатомической модели камеры сердца. После чего ее сопоставляют с КТ/МРТ изображением. Интеграция также производится ручным способом, опираясь на несколько произвольных точек на электроанатомической модели. По полученному изображению выполняют радиочастотную аблацию.
Однако первоначальное построение электроанатомической модели для последующего совмещения с КТ/МРТ моделью выполняют только специальными электродами, имеющими магнитные датчики. При работе с КТ/МРТ моделью на нее не проецируются карты активации и вольтажные карты, которые используют в качестве информационной поддержки при диагностике и лечении пациентов с нарушением ритма сердца. Кроме того, известный способ характеризуется низкой достоверностью получаемых результатов, так как требуется постоянная корректировка изображения во время работы, что может повлечь за собой снижение точности и эффективности проведения интервенционного вмешательства у пациента.
Известен способ картирования камер сердца, реализуемый системой EnSite (Abbott, USA), в котором принцип анатомической реконструкции основан на регистрации импеданса, что позволяет производить реконструкцию интересующей камеры сердца электродами без использования специальных магнитных датчиков с последующим слиянием полученной электроанатомической модели с КТ/МРТ моделью камеры сердца по произвольно выбранным референтным точкам [Kettering K. et al. Catheter ablation of atrial fibrillation using the Navx-/Ensite-system and a CT-/MRI-guided approach // Clinical research in cardiology. - 2009. - T. 98. - №. 5. - C. 285-296. Shu L., Wang J. A valid registration algorithm for electroanatomic map and CT surface // 2017 First International Conference on Electronics Instrumentation & Information Systems (EIIS). - IEEE, 2017. - С.1-4.]
Однако система Ensite не всегда способна распознать КТ/МРТ изображения при недостаточном количестве срезов, что делает невозможным выполнение слияния анатомической модели с КТ/МРТ моделью. Кроме того, референтные точки в данной системе берутся произвольно, а не в конкретных плоскостях, что увеличивает время сопоставления электроанатомической реконструкции и модели КТ/МРТ, снижает точность получаемой модели.
Наиболее близким к заявляемому решению является способ картирования камер сердца с использованием навигационной системы «Astrocard» для лечения пациентов с нарушением ритма сердца [Яшков М.В. и др. Использование новой навигационной системы картирования «Астрокард» (Россия) с возможностью интеграции компьютерной модели левого предсердия для лечения фибрилляции и трепетания предсердий // Сибирский медицинский журнал. - 2019. - Т. 34. - №. 2. - С. 33-38.]. Для реализации способа в условиях рентгеноперационной выполняют электрофизиологическое исследование (ЭФИ). Для чего ЭКГ в 12 отведениях (в диапазоне 0,05-160 Гц) и интракардиальные электрограммы (с фильтром 30-700 Гц) регистрируют и записывают на 128-канальном комплексе для проведения внутрисердечных ЭФИ («Астрокард», Россия). Электроанатомическое инвазивное картирование осуществляют с использованием навигационной системы «Астрокард» (Россия), основанной на регистрации электрического импеданса, для чего на грудную клетку устанавливают 6 навигационных электродов. В последующем всем пациентам выполняют РЧА. Для картирования камер сердца проводят МСКТ или КТ или МРТ сердца с получением 3D изображения сердца, которую интраоперационно совмещают с электроанатомической моделью камеры сердца, полученной с помощью системы навигационного картирования «Астрокард». Однако для совмещения построенной электроанатомической модели с обработанным КТ/МРТ изображением на полученных изображениях выбирают референтные точки в разных плоскостях произвольно, что увеличивает время сопоставления электроанатомической реконструкции и модели КТ/МРТ, снижает точность и достоверность получаемого изображения камеры сердца по сравнению с заявляемым решением.
Технической проблемой является сохранение во время совмещения КТ/МРТ изображения камер сердца (КТ/МРТ модели) с изображением электроанатомической модели, соответствия размеров камер сердца КТ/МРТ и электроанатомической моделей, а также возможность достоверной визуализации положения электрофизиологических катетеров на получаемой модели в реальном времени по отношению к структурам сердца. Решение данной технической проблемы позволит сократить время на обработку полученных изображений с повышением точности совмещения, и как следствие, повышением точности и эффективности проведения интервенционного вмешательства у пациента и снижение времени флюороскопии.
Раскрытие сущности изобретения
Техническим результатом, на достижение которого направлено заявленное изобретение, является возможность получения достоверного представления анатомических особенностей камеры сердца на компьютерной модели камеры сердца, позволяющей повысить эффективность проведения интервенционного лечения при нарушениях ритма сердца (радиочастотной аблации), снизить время флюороскопии. Совмещение МСКТ/МРТ с электроанатомической реконструкцией по заявляемому способу может с высокой точностью отображать истинную трехмерную анатомию камер сердца и дает возможность визуализировать истинные анатомические отношения между структурами средостения. Заявляемый способ позволяет выполнять манипуляции в сердце во время проведения инервенционных вмешательств у пациентов с нарушениями ритма сердца с уменьшением общего времени флюороскопии и времени оперативного вмешательства.
Технический результат обеспечивается посредством реализации способа картирования камер сердца с использованием навигационной системы «Астрокард» при лечении пациентов с нарушением ритма сердца, включающего следующие этапы:
- проведение МСКТ или КТ или МРТ сердца с получением 3D изображения сердца,
- получение интраоперационно электроанатомической модели камеры сердца с помощью системы навигационного картирования «Астрокард»,
- совмещение полученной электроанатомической модели камер сердца с обработанным изображением МСКТ или КТ или МРТ сердца, для чего
на полученных изображениях выбирают, по меньшей мере, две пары референтных точек, расположенных попарно в разных плоскостях,
при этом точки каждой пары на полученных изображениях выбирают на участках, на которых визуализируются анатомические структуры, и удаленных друг от друга на расстояние не менее 2 см, при этом выбранные точки на изображении МСКТ или КТ или МРТ соответствуют точкам на электроанатомической модели, а пары точек располагают таким образом, чтобы линии, проведенные через упомянутые точки в проекции на плоскость располагались по углом не менее 45, после чего производят совмещение изображений по выбранным точкам и корректируют положение изображений по анатомическим ориентирам, при этом в качестве первого ориентира используют бифуркацию правых вен, в качестве второго - бифуркацию левых легочных вен, в качестве третьего - крышу левого предсердия, в качестве четвертого - основание ушка левого предсердия.
Точность совмещения электроанатомической модели и КТ модели может быть повышена за счет выбора дополнительных пар референтных точек (от одной до пяти), при этом точки каждой пары на полученных изображениях выбирают на участках, на которых визуализируются анатомические структуры, и удаленные друг от друга на расстояние не менее 2 см, при этом точки на изображении МСКТ или КТ или МРТ выбирают в соответствии с анатомическими ориентирами на электроанатомической модели: в качестве первого ориентира может быть использована область риджа (зона между впадением в левое предсердие ушка левого предсердия и левой верхней легочной веной), в качестве остальных - области впадения легочных вен (на верхнем сегменте правой и левой верхней легочной вены, и нижнем сегменте правой и левой нижней легочной вены). При этом дополнительные пары точек располагают аналогично описанному выше способу (таким образом, чтобы линии, проведенные через упомянутые точки в проекции на плоскость располагались по углом не менее 45°).
Использование заявляемого способа особенно актуально в случае атипичной анатомии сердца.
Краткое описание чертежей
Изобретение поясняется чертежами.
На фиг. 1 представлена схема расположения навигационных электродов на поверхности тела пациента системы «Астрокард» (Россия). Позициями на фигуре обозначены: 1 и 2 - электроды, которые накладываются в левой надключичной области, и на левом бедре, соответственно; 3 и 4 - по средней подмышечной линии слева и справа, соответственно; 5 и 6 - на переднюю и заднюю поверхность грудной клетки в области сердца.
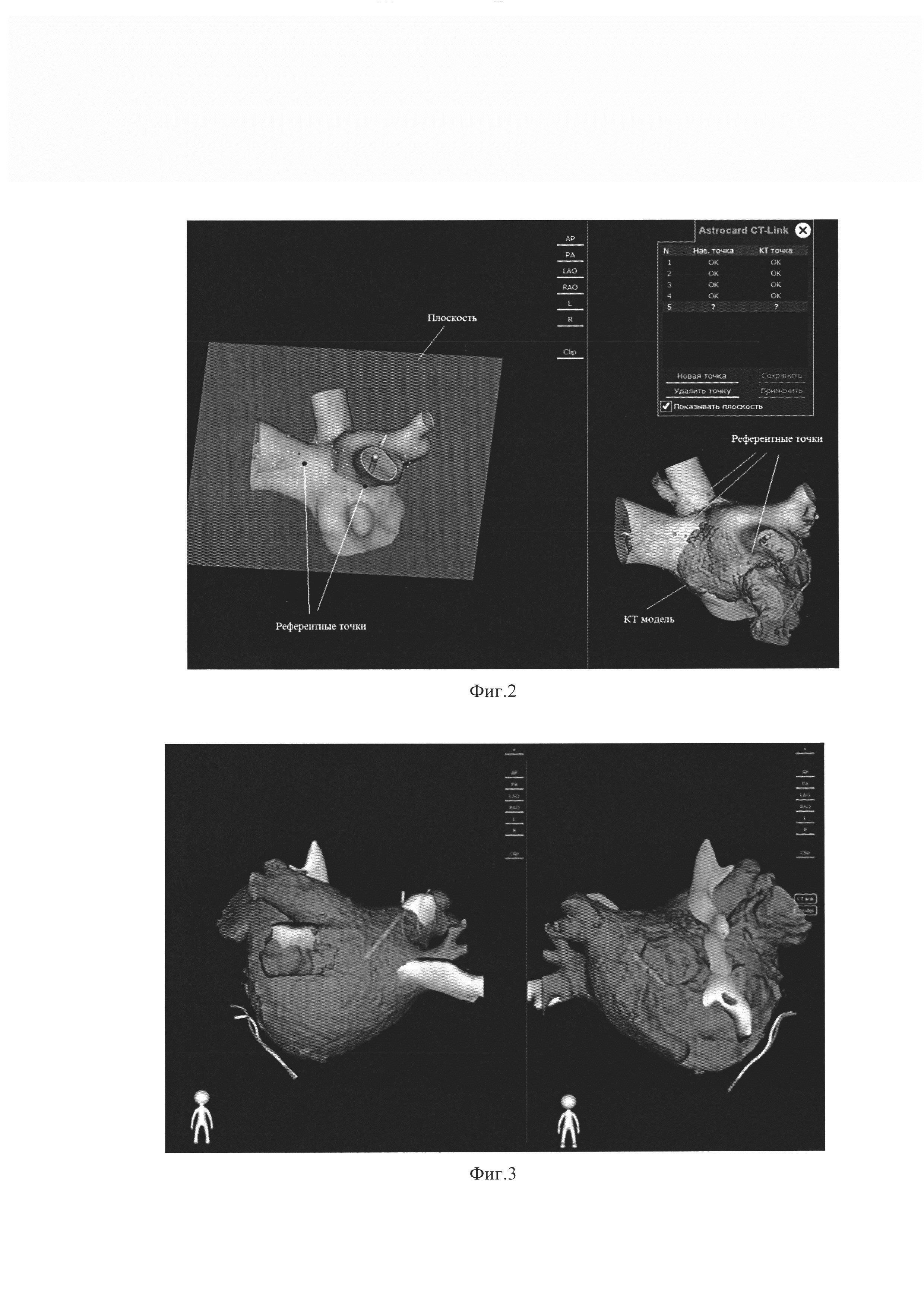
На фиг. 2 изображение, полученное интраоперационно на мониторе системы «Астрокард», на котором представлен вариант выбора точек для совмещения КТ изображения с реконструированной электроанатомической моделью. Слева на изображении представлена электроанатомическая модель с выделенной плоскостью, построенной по референтным точкам. Справа представлены совмещенные изображения электроанатомической модели и КТ - модели (Astrocard СТ - Link). Astrocard CTLink - меню взятия референтных точек и информация об их количестве. КТ - модель компьютерной томографии левого предсердия. Реконструкция - электроанатомическая модель. Референтные точки - точки для интеграции модели КТ и электроанатомической модели.
На фиг. 3 - изображение, полученное интраоперационно на мониторе системы «Астрокард», на котором представлен результат сопоставления КТ модели и электроанатомической реконструкции (модели).
На фиг. 4 - изображение КТ модели левого предсердия, полученное интраоперационно на мониторе системы «Астрокард», после антральной аблации у пациента, на котором визуализируется диагностический электрод, расположенный в коронарном синусе, а также выделены аблационные точки. ПВЛВ - правая верхняя легочная вена, ПНЛВ - правая нижняя легочная вена, Ушко ЛП - ушко левого предсердия.
Осуществление изобретения
Ниже представлено более подробное описание осуществления изобретения.
Перед оперативным вмешательством пациенту выполняют КТ/МРТ сердца. Данные загружают на электронный носитель. Далее в операционной, для интервенционных вмешательств на грудную клетку пациента устанавливают 6 дополнительных навигационных электродов, как показано на фиг. 1. Электроды 5 и 6 накладывают на переднюю и на заднюю поверхность грудной клетки в области сердца. Электроды 3 и 4 - по средней подмышечной линии слева и справа. Электрод 1 - в левой надключичной области, электрод 2 - на левом бедре. В последующем для позиционирования внутрисердечных электродов выполняют пункцию сосудов по методике Сельдингера. Далее устанавливают диагностический электрод в коронарный синус. Данный электрод является референтным для последующего построения электроанатомической модели левого предсердия (ЛП).
Далее на программном комплексе «Астрокард» выполняют обработку МСКТ/МРТ изображения. С использованием системы навигации «Астрокард» (Россия) производят анатомическую реконструкцию изображения любым электродом с построением активационных и амплитудных карт. Типы используемых катетеров определяются навигационной системой автоматически. После выполнения электроанатомической реконструкции ЛП, выполняют совмещение построенной модели с обработанным МСКТ изображением. Для этого на электроанатомической реконструкции и модели КТ выбирают референтные точки в разных плоскостях по описанному выше алгоритму. Дальнейшие манипуляции по лечению пациента с нарушением ритма сердца выполняют с использованием полученной совмещенной модели.
Ниже представлено обоснование выбранных референтных точек и анатомических ориентиров, необходимых для построения совмещенной КТ/МРТ модели сердца и электроанатомической модели.
Выбирают K - систему координат (x,y,z), связанную с KT моделью, N - систему координат (α, β, γ), связанную с навигационным изображением. Система координат навигационного изображения является неортогональной и, в общем случае, криволинейной. Для произвольной точки с заданными координатами α,β,γ в навигационном изображении вычисляют координаты x,y,z в системе K, для чего пользователь указывает референтные точки в системе координат K и соответствующие им точки в системе N. По реперным точкам, определяют закон преобразования координат α,β,γ в x,y,z. Точность такого преобразования пользователь оценивает визуально путем сопоставления КТ модели и построенной навигационной модели (электроанатомической модели), отображенной в системе координат К. Если точность недостаточна, возможно добавление новой пары реперных точек или корректировка уже существующей.
Переход из системы координат N, в систему координат K может осуществляться с использованием следующей формулы:
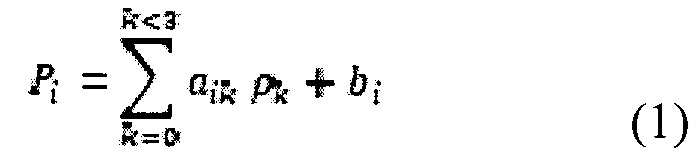
где aik - компоненты квадратной матрицы размера 3×3, bi - компоненты 3-х мерного вектора, ρk - координаты (α,β,γ) точки в системе N, Pi - координаты (x,y,z) в системе K.
В случае, если система координат N не является криволинейной, а только неортогональной, значения aik и bi являются постоянными величинами. Если N является криволинейной, то aik и bi являются функциями координат ρk. Таким образом, для решения поставленной задачи находят постоянные значения aik и bi для линейного случая или значения aik и bi как функции координат в общем случае.
При использовании линейной системы координат навигационного изображения (но неортогональной), где Pin и ρkn координаты n-й реперной точки в системах координат K и N, соответственно, переход из системы координат N, в систему координат K может осуществляться с использованием следующей формулы:

Уравнения (2) являются системой линейных уравнений относительно 12 неизвестных aik и bi. Из линейной алгебры известно, что для того, чтобы система линейных уравнений с 12 неизвестными была однозначно разрешима, необходимо, чтобы она состояла из 12 линейно независимых уравнений. Каждая пара реперных точек Pin и ρkn добавляет 3 уравнения (т.к. у каждой точки 3 координаты). Таким образом, для нахождения неизвестных aik и bi используют 4 реперные точки Pin и 4 соответствующие им реперные точки ρkn. В этом случае система уравнений (2) с 12-ю неизвестными будет иметь вид в виде 3-х систем уравнений с 4-мя неизвестными:

n=0, 1, 2, 3
Или в матричном виде:

где ai и Pi - векторы, М - матрица:
Вектор а0=(a00, a01, a02, b0)
Вектор a1=(a10, a11, a12, b1)
Вектор a2=(a20, a21, a22, b2)
Вектор P0=(P00, P01, P02, 1)
Вектор P1=(P10, P11, P12, 1)
Вектор P2=(P20, P21, P22, 1)

Чтобы системы уравнений (3) имели единственное решение, необходимо и достаточно, чтобы детерминант матрицы М был отличен от нуля. Геометрически это равнозначно тому, что 4-е реперных точки ρkn не должны принадлежать одной плоскости.
Таким образом, на первом этапе в предлагаемом способе пользователь должен указать по 2-е пары референтных точек - на КТ модели и электроанатомической модели, не лежащих в одной плоскости. Если визуальное совмещение навигационной модели и КТ изображения достаточно хорошее, то система координат навигационной модели близка к линейной, на этом поиск закона преобразования координат можно остановить. Если совпадение недостаточное, то система координат навигационной модели существенно нелинейна, и требуется дальнейшее уточнение закона преобразования координат путем добавления новых пар референтных точек.
Если количество (Nr) реперных точек больше 4, система уравнений (2) является переопределенной и не может быть точно решена. Однако она может быть решена приближенно методом наименьших квадратов (МНК) путем минимизации ошибок:
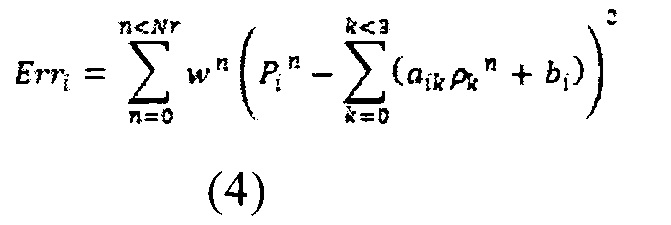
где wn - вес ошибки для точки n, Erri - суммарная ошибка для координаты i. Если для некоторой заданной точки m вес ошибки wm больше, чем для остальных точек, то решение, полученное с помощью МНК будет таково, что совпадение в окрестности этой точки будет точнее, ценой ослабления совпадения в остальных точках. При выборе веса во всех точках, кроме заданной, равными 1, а в заданной точке много больше единицы:
wm=w>>1, wn=1, n≠m,
получают коэффициенты aik и bi такие, что совпадение в окрестности заданной точки будет сколь угодно точным. Увеличивая W, увеличивают точность совпадения в точке m, однако уменьшают совпадение в остальных точках. Повторив эту процедуру для каждой пары реперных точек, получают набор из Nr решений aikn и bin. Каждое из решений aikn и bin обеспечивает достаточно точное совпадение в окрестности реперной точки n.
Для получения значений aik и bi в произвольной точке применяют интерполяцию. В качестве узлов интерполяции используют реперные точки, а в качестве значений в узлах - значения aikn и bin, вычисленные ранее. В качестве метода интерполяции может быть использован любой известный метод многомерной (в данном случае трехмерной) интерполяции.
После выполнения интерполяции получают aik и bi как функции координат в системе N: aik= aik(α,β,γ), bi=bi(α,β,γ)
Преобразование (2), выполненное с использованием этих коэффициентов, обеспечивает точное совпадение в реперных точках и приближенное в других. Как и ранее, если визуальное совмещение навигационной модели и КТ изображения достаточно хорошее, то на этом поиск закона преобразования координат останавливают. Если совпадение недостаточное, то добавляют еще одну пару референтных точек в том месте, где совпадение плохое, и повторяют описанную процедуру еще раз.
Радиочастотная изоляция легочных вен с применением известного и нового алгоритма интеграции с КТ изображением в навигационной системе «Астрокард» (Россия) была выполнена 33 пациентам по поводу нарушения ритма сердца, которым планировалось интервенционное вмешательство. При сравнении результатов реализации двух способов (по прототипу, в соответствии со способом, описанным в авторской статье, с произвольным выбором референсных точек, и по заявляемому способу), заявляемый способ продемонстрировал следующие преимущества:
- возможность более достоверной визуализации положения электрофизиологических катетеров на получаемой модели в реальном времени по отношению к структурам сердца, что оценивалось моментами выхода электрофизиологических катетеров за пределы камеры сердца и их неточное положение при флюороскопическом контроле, что наблюдалось в прототипе и чего не наблюдалось в заявленном способе;
- сокращение времени обработки полученных изображений с повышением точности совмещения (время, потраченное на обработку, заявляемым способом составило 7±1,8 мин и способом по прототипу 10±1,9 мин),
- снижение времени флюороскопии, за счет более достоверной визуализации электрофизиологических катетеров в моделях и снижения времени на совмещения и последующую корректировку моделей, по сравнению со способом прототипа (прототип время флюороскопии 58±14,5 мин, заявленный способ 44±11,3 мин);
- снижение общего времени оперативного вмешательства, за счет сокращение времени обработки полученных изображений с повышением точности совмещения, достоверной визуализации положения электрофизиологических катетеров (прототип время операции 95±13,7 мин, заявленный способ 78±11,3 мин);
- снижение погрешности получаемых моделей, которое оценивалось по положению электрофизиологических катетеров в сердце при флюороскопическом контроле с положением данных в модели.
Реферат
Изобретение относится к области медицины, а именно кардиохирургии, интервенционной аритмологии, и может быть использовано для трехмерного картирования камер сердца с использованием навигационной системы «Астрокард» при лечении пациентов с нарушением ритма сердца. Проводят МСКТ, или КТ, или МРТ сердца с получением 3D изображения сердца. Получают интраоперационно электроанатомическую модель камеры сердца с помощью системы навигационного картирования «Астрокард». Совмещают полученную электроанатомическую модель камер сердца с обработанным изображением МСКТ, или КТ, или МРТ сердца, для чего на полученных изображениях выбирают, по меньшей мере, две пары референтных точек, расположенных попарно в разных плоскостях. При этом точки каждой пары на полученных изображениях выбирают на участках, на которых визуализируются анатомические структуры и удаленных друг от друга на расстояние не менее 2 см. При этом выбранные точки на изображении МСКТ, или КТ, или МРТ соответствуют точкам на электроанатомической модели, а пары точек располагают таким образом, чтобы линии, проведенные через упомянутые точки в проекции на плоскость, располагались под углом не менее 45°. Далее производят совмещение изображений по выбранным точкам и корректируют положение изображений по анатомическим ориентирам. При этом в качестве первого ориентира используют бифуркацию правых вен, в качестве второго - бифуркацию левых легочных вен, в качестве третьего - крышу левого предсердия, в качестве четвертого - основание ушка левого предсердия. Способ позволяет получать точную компьютерную модель камеры сердца, обеспечивая повышение точности и эффективности проведения интервенционного лечения при нарушениях ритма сердца за счет выбора дополнительных пар референтных точек. 4 ил.

Комментарии