Слитый белок, наночастица, состоящая из множества мономеров указанного слитого белка, и их применение - RU2714155C2
Код документа: RU2714155C2
Чертежи

Описание
Настоящее изобретение относится к слитому белку, к наночастицам, состоящим из множества мономеров указанного слитого белка, к нуклеиновым кислотам, кодирующим указанный слитый белок, и к их диагностическому и терапевтическому применению.
Селективное высвобождение терапевтических средств в пораженной области является одной из самых важных задач по улучшению текущей терапии. В этом контексте применение наночастиц в качестве носителей (нановекторов) терапевтических средств обеспечивает возможность как обойти биологические барьеры, которые могут присутствовать на пути от места введения до конечной цели, так и, в частности, обеспечить накопление лекарственного средства селективным образом в пораженной области, предпочтительнее, чем в нормальных тканях. В качестве основополагающей предпосылки нановектор должен обладать способностью связывать большое количество лекарственного средства эффективным образом.
Среди известных носителей для целевого высвобождения лекарственного средства наночастицы на основе ферритинов (FTS) привлекают все большее внимание благодаря их исключительным характеристикам биосовместимости, способности проникать сквозь биологические барьеры, функционализационной универсальности и возможности связывать определенные виды лекарственных средств (Vannucci, L., Falvo, E., Ceci, P. Multifunctional Protein-Based Nanoparticles for Cancer Theranosis. 2014, A. Prokop et al. (eds.), Intracellular Delivery II, Fundamental Biomedical Technologies 7). FTS представляют собой высоко симметричные мультимерные белковые структуры, состоящие из 24 субъединиц, которые собираются в молекулярную структуру по существу со сферической оболочкой, окружающей полость, которая физиологически используется для хранения железа. Наружный диаметр и внутренний диаметр составляют 12 и 8 нм, соответственно. Такая молекулярная структура по типу оболочки обозначается далее как «наночастица» или «HFt наночастица».
Наночастицы на основе тяжелой цепи ферритина человека (HFt) демонстрируют ряд преимуществ по сравнению с другими системами высвобождения лекарственных средств, особенно в связи с применением in vivo у человека. Фактически, молекулы HFt предназначены для прохождения сквозь биологические барьеры (20 нм малого диаметра), и в физиологических условиях они присутствуют как в клетках, так и в крови, хотя и в низких концентрациях (приблизительно 20 мкг/л).
Являясь природными элементами, они обладают меньшей вероятностью вызывать сильный аутоиммунный (внешний) гуморальный и/или Т-клеточный иммунный ответ.
Кроме того, HFt являются одними из нескольких природных наночастиц, которые сами по себе способны связываться с опухолевыми клетками эффективным и селективным путем. Действительно, с использованием одной из самых привлекательных молекул для таргетной терапии злокачественных новообразований, рецептор трансферрина 1 (TfR1), было показано, что HFt интернализируется. TfR1 действительно активирован на поверхности многих типов злокачественных опухолей (вплоть до в 100 раз выше, чем на нормальных клетках) и эффективно интернализируется. Для более 474 образцов клинических тканей, HFt, но не из легких цепей ферритина человека (Lft), была доказана интернализация TfR1 и специфическое распознание многих типов опухолей (т.е. рак печени, легких, поджелудочной железы, толстой кишки, шейки матки, яичников, простаты, молочной железы, саркомы и тимуса) по сравнению с неопухолевыми тканями, с 98% чувствительностью и 95% специфичностью (Fan K, Cao C, Pan Y, Lu D, Yang D, Feng J, et al. Magnetoferritin nanoparticles for targeting and visualizing tumour tissues. Nat Nanotechnol. 2012;7:459-64).
Однако, нативная HFt имеет несколько недостатков. Во-первых, выходы, с которыми она способна связываться с определенными типами лекарственных средств, такими как, например, доксорубицин (один из противоопухолевых препаратов с широким спектром противоопухолевой активности), являются низкими, и это может ограничить их возможное применение и клинические разработки. Во-вторых, нативная HFt при системном пути введения имеет очень короткий период полураспада в плазме, примерно 2-3 часа. И, наконец, ее природная ферроксидазная активность может ингибировать развитие и созревание остеобластов человека и приводить к снижению минерализации, к остеопении и остеопорозу (Zarjou A, Jeney V, Arosio P, Poli M, Zavaczki E, Balla G, Balla J. Ferritin ferroxidase activity: a potent inhibitor of osteogenesis. J Bone Miner Res. 2010,25:164-72). По этой причине целесообразно использовать вариант HFt с отсутствием ферроксидазной активности, приобретенной в результате сайт-специфической мутации (в настоящем документе обозначена как vHFt), который не вызывает ингибирования.
Для того, чтобы одновременно устранить все недостатки, перечисленные выше в отношении нативной HFt, авторы настоящего изобретения решили генетически модифицировать тяжелую цепь ферритина человека (HFt), действуя непосредственно на наружную поверхность белка. При этом способность инкапсулировать лекарственное средство доксорубицин в полость белка значительно и неожиданно улучшилась, а полураспад в плазме увеличился, не влияя на способность белка распознавать опухолевые клетки.
Эти и другие цели достигаются благодаря слитому белку, как охарактеризовано в прилагаемой формуле изобретения в пункте 1. Другие независимые пункты и зависимые пункты относятся к дополнительным аспектам и конкретным вариантам осуществления настоящего изобретения, которые являются неотъемлемой частью настоящего описания.
Дополнительные признаки и преимущества настоящего изобретения станут очевидны из следующего далее подробного описания, которое предназначено только для иллюстративных целей, а не для ограничения, со ссылками на прилагаемые чертежи, на которых:
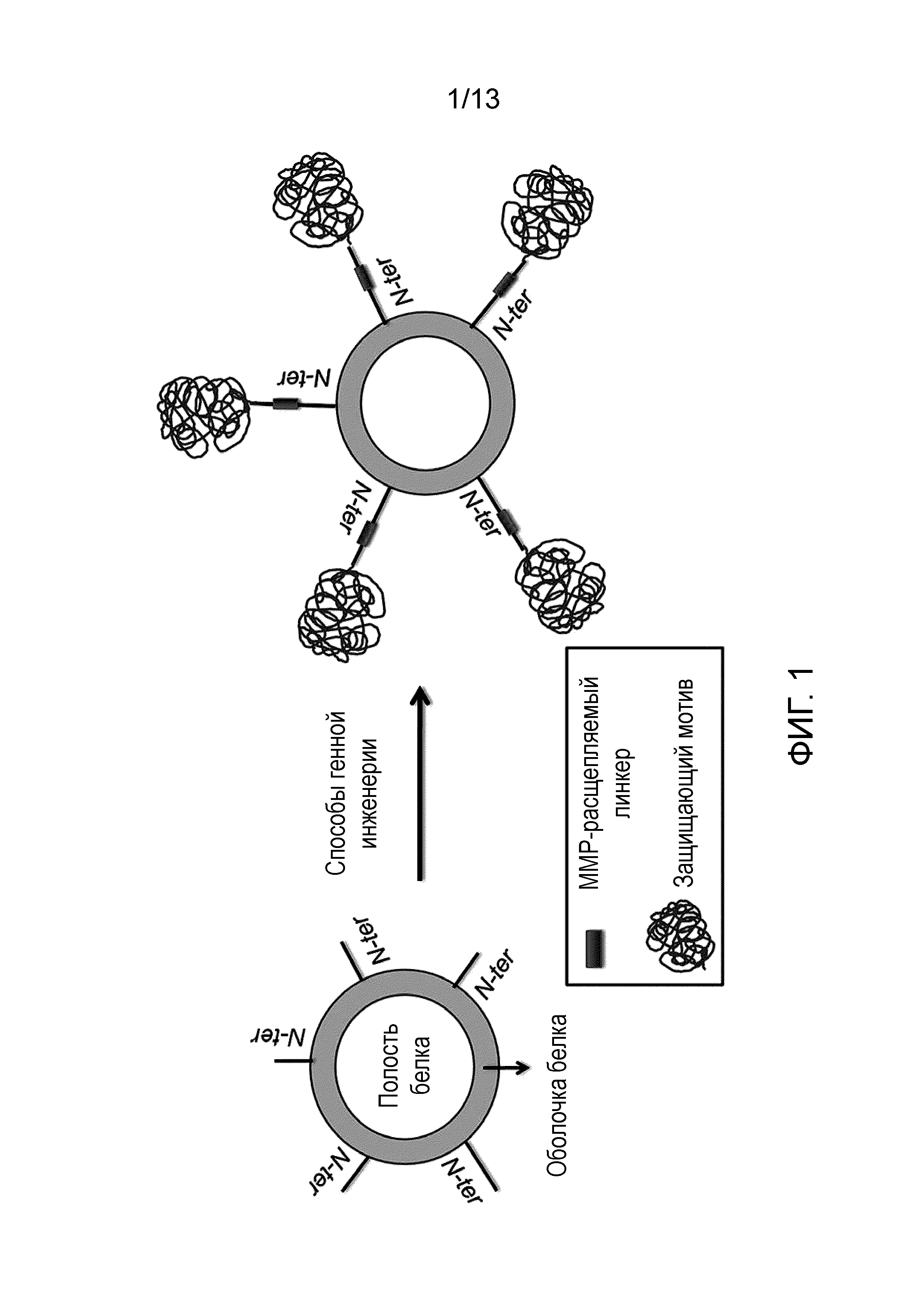
На Фигуре 1схематически представлено получение наночастиц HFt, в которых N-конец каждого из 24 мономеров генетически связан с расщепляемыми пептидными последовательностями и с последовательностями, по существу состоящими из пролина, аланина и серина (PAS). Для ясности показано только 5 из 24 N-концов.
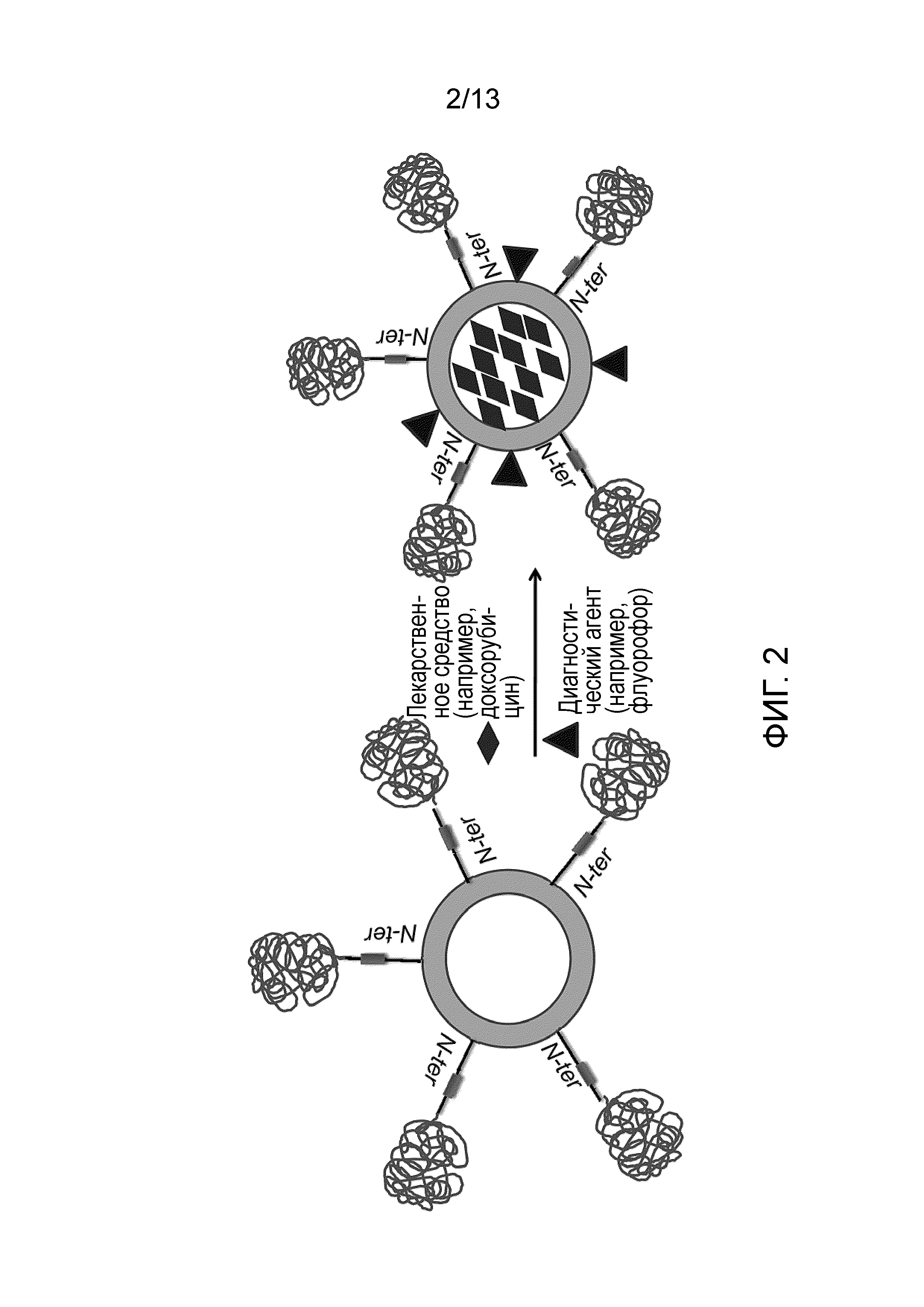
На Фигуре 2схематически представлено получение наночастиц HFt, которые несут терапевтические и/или диагностические молекулы. Они могут быть загружены во внутреннюю полость или связан с внешней поверхностью белка.
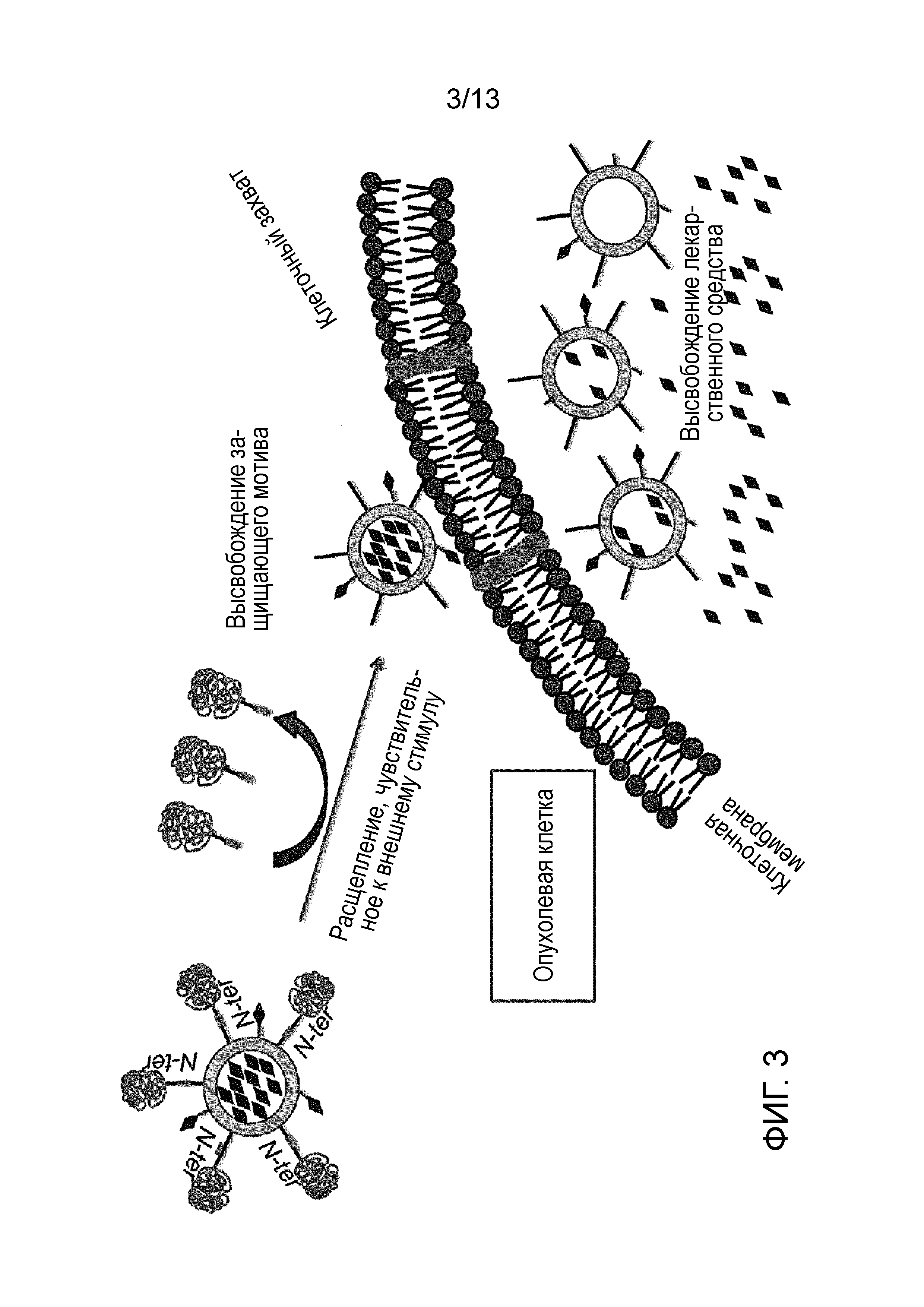
На Фигуре 3 изображена общая диаграмма, которая описывает способ действия наночастиц HFt на опухолевые клетки.
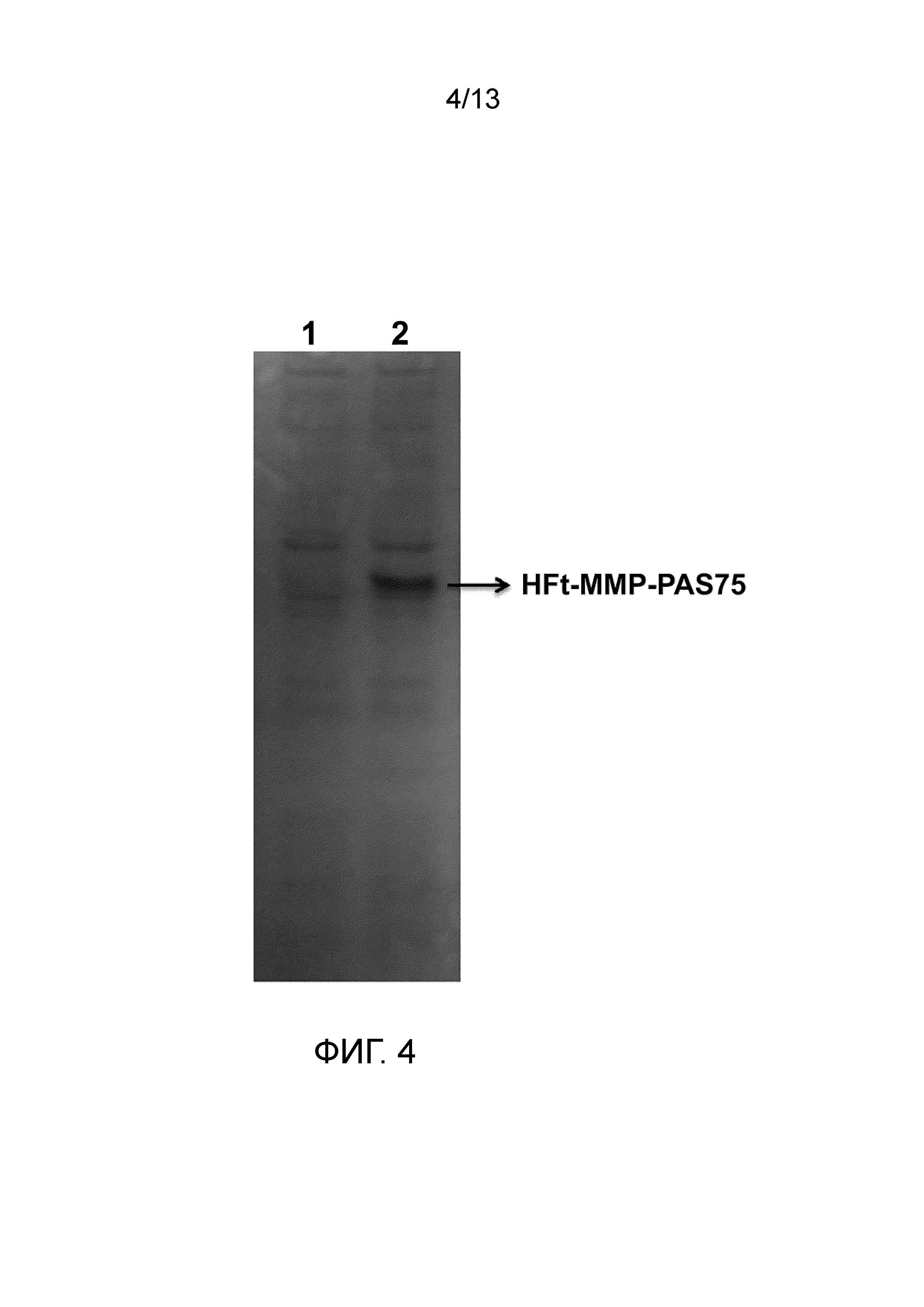
На Фигуре 4 показан белковый профиль экспрессии одной из полученных конструкций, HFt-ММР-PAS75 (длина PAS: 75 остатков), с помощью SDS-PAGE с последующим окрашиванием Кумасси синим R-250. Рекомбинантный белок получали в E. Coli BL21DE3, используя IPTG-индуцируемую плазмиду, pet-11A, и очищали, как описано в разделе, относящемся к примерам. Дорожка 1: SDS-PAGE растворимых и нерастворимых фракций, отличных от IPTG-индуцированных клеток. Дорожка 2: SDS-PAGE растворимых и нерастворимых фракций клеток, индуцированных 0,5 мМ IPTG. Полоса HFt-ММР-PAS обозначена черной стрелкой и перемещается приблизительно при 40 кДа, в отличие от вычисленной массы, равной 28,5 кДа. Это явление согласуется с другими сообщениями для PASилированных белков и обусловлено пониженным связыванием SDS последовательностей PAS. Кроме того, последовательности PAS слабо окрашиваются Кумасси синим, что приводит к заниженной оценке белковой полосы в геле.
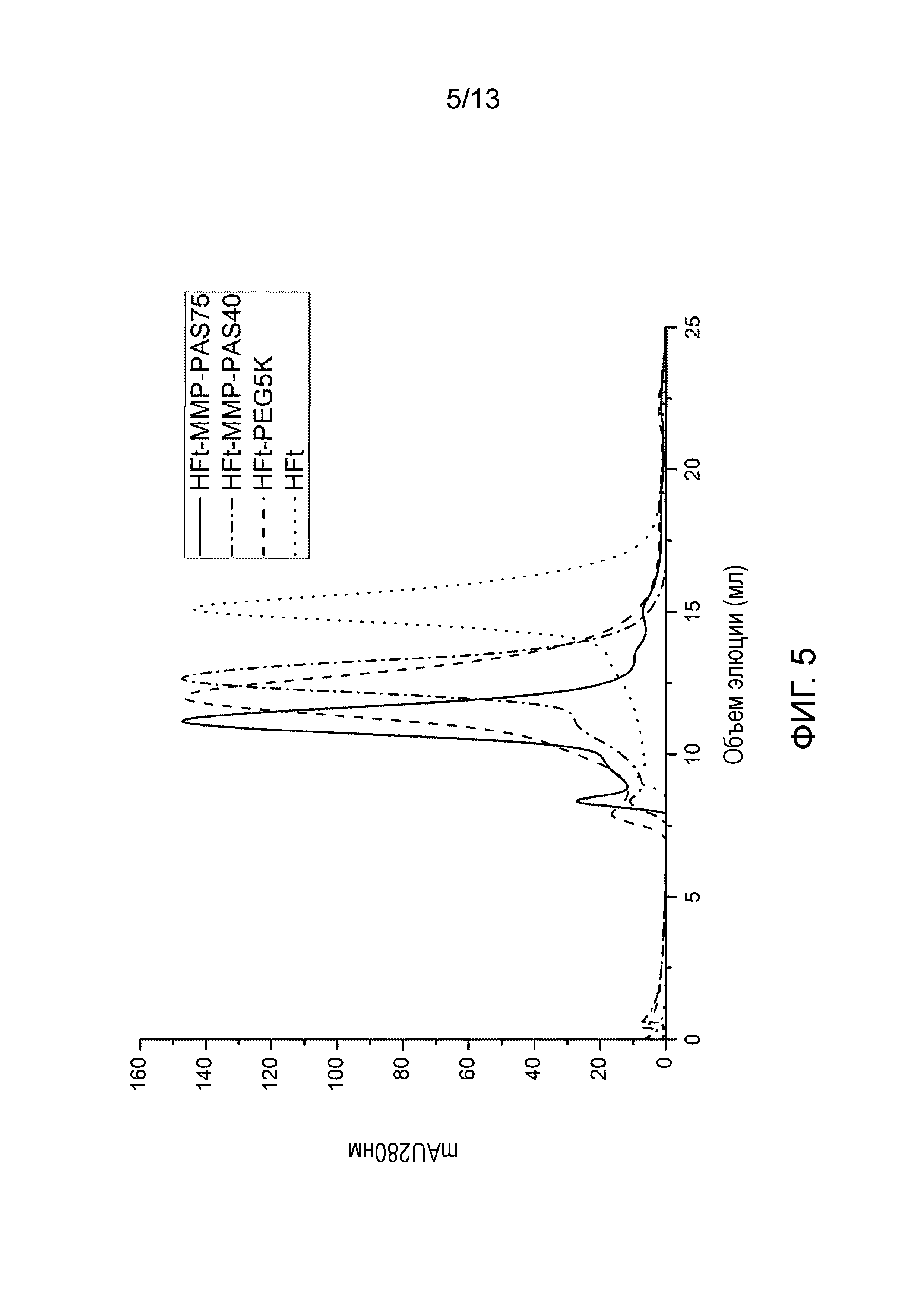
На Фигуре 5 показаны профили эксклюзионной хроматографии нативной HFt (пунктирные линии) и конструкций слитого белка HFt-ММР-PAS75 (сплошные линии), HFt-ММР-PAS40 (прерывистые и пунктирные линии) или HFt с функциональной группой полиэтиленгликоля (REG) 5 кДа (HFT-PEG5K, прерывистые линии).
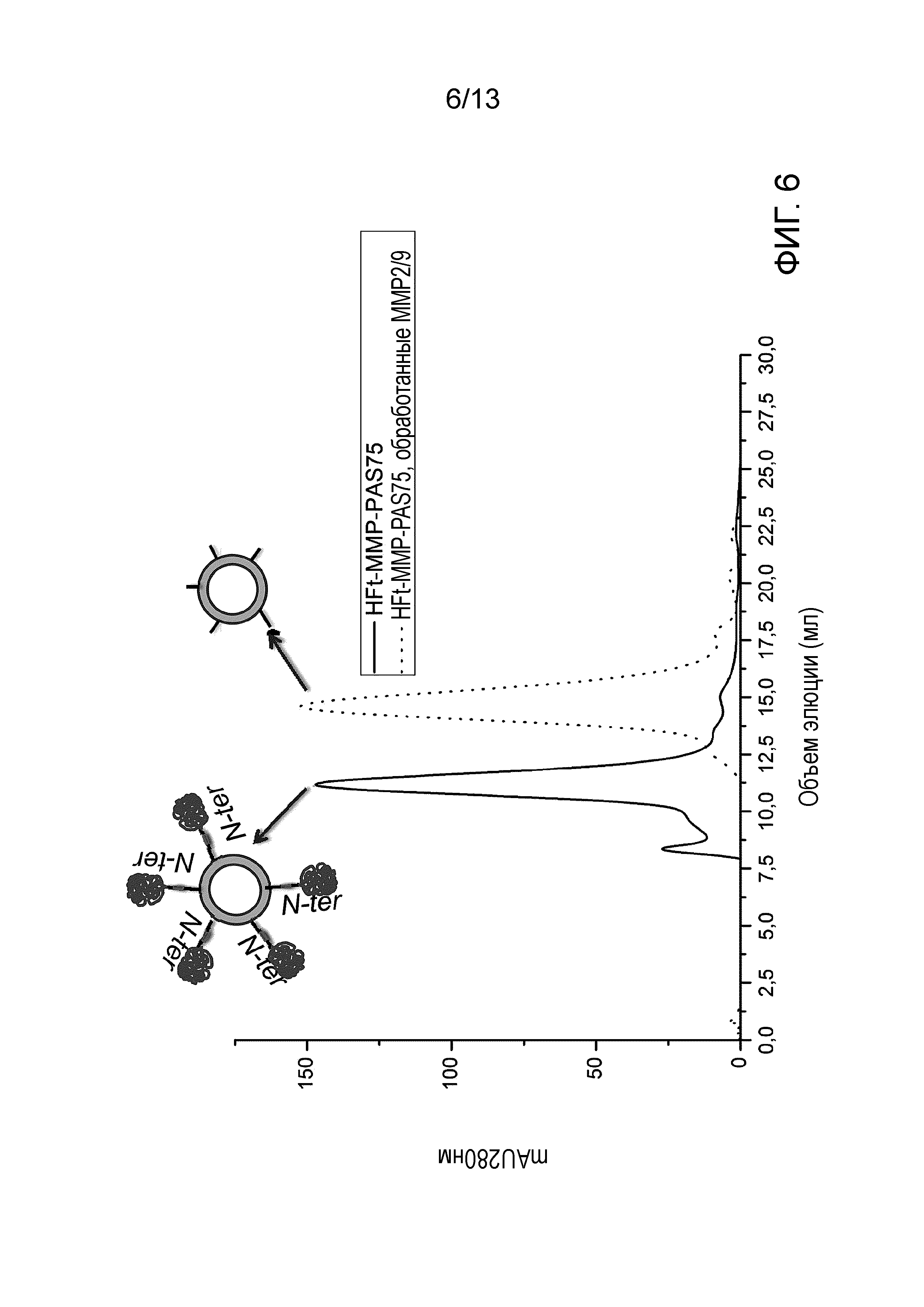
На Фигуре 6 показаны типичные профили эксклюзионной хроматографии HFt-MMP-PAS75 до (сплошные линии) и после (пунктирные линии) удаления PAS протеазой ММР-2/9 (коллагеназа IV) in vitro.
На Фигуре 7 показаны профили перемещения полос HFt-ММР-PAS75 до и после удаления PAS под действием протеазы ММР-2/9 (коллагеназа IV) in vitro. SDS-PAGE окрашивали Кумасси синим R-250. Дорожка 1: маркерный белок; Дорожка 2: HFt (1 мг/мл); Дорожка 3: HFt-ММР-PAS75 (2 мг/мл) после расщепления in vitro с помощью 0,2 мг/мл протеазы ММР-2/9 (коллагеназа IV); Дорожка 4: HFt-ММР-PAS75 (2 мг/мл) после расщепления in vitro с помощью 0,2 мг/мл протеазы ММР-2/9 (коллагеназа IV).
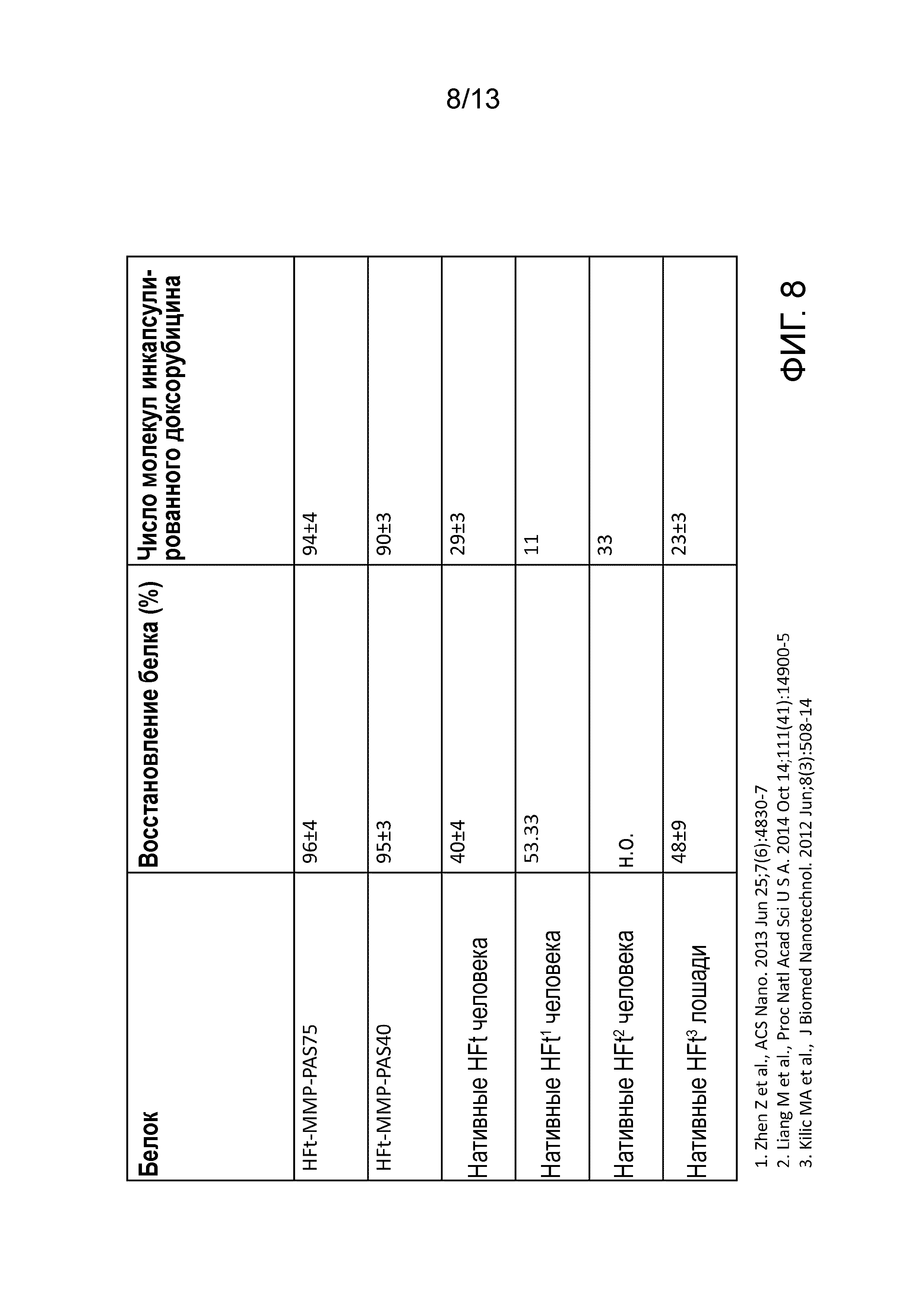
На Фигуре 8 показана способность инкапсулировать доксорубицин у двух из полученных конструкций (HFt-ММР-PAS40 и HFt-ММР-PAS75) по сравнению с нативным белком HFt и другими данными из литературы. Величины относительного выхода указаны в единицах % восстановления белка и числа инкапсулированных молекул доксорубицина. Можно видеть, что эти конструкции, являющиеся объектом этого патента, неожиданно и непредвиденно приобрели улучшенную способность инкапсулировать лекарственное средство доксорубицин, по крайней мере, в 6 раз по сравнению с нативной HFt.
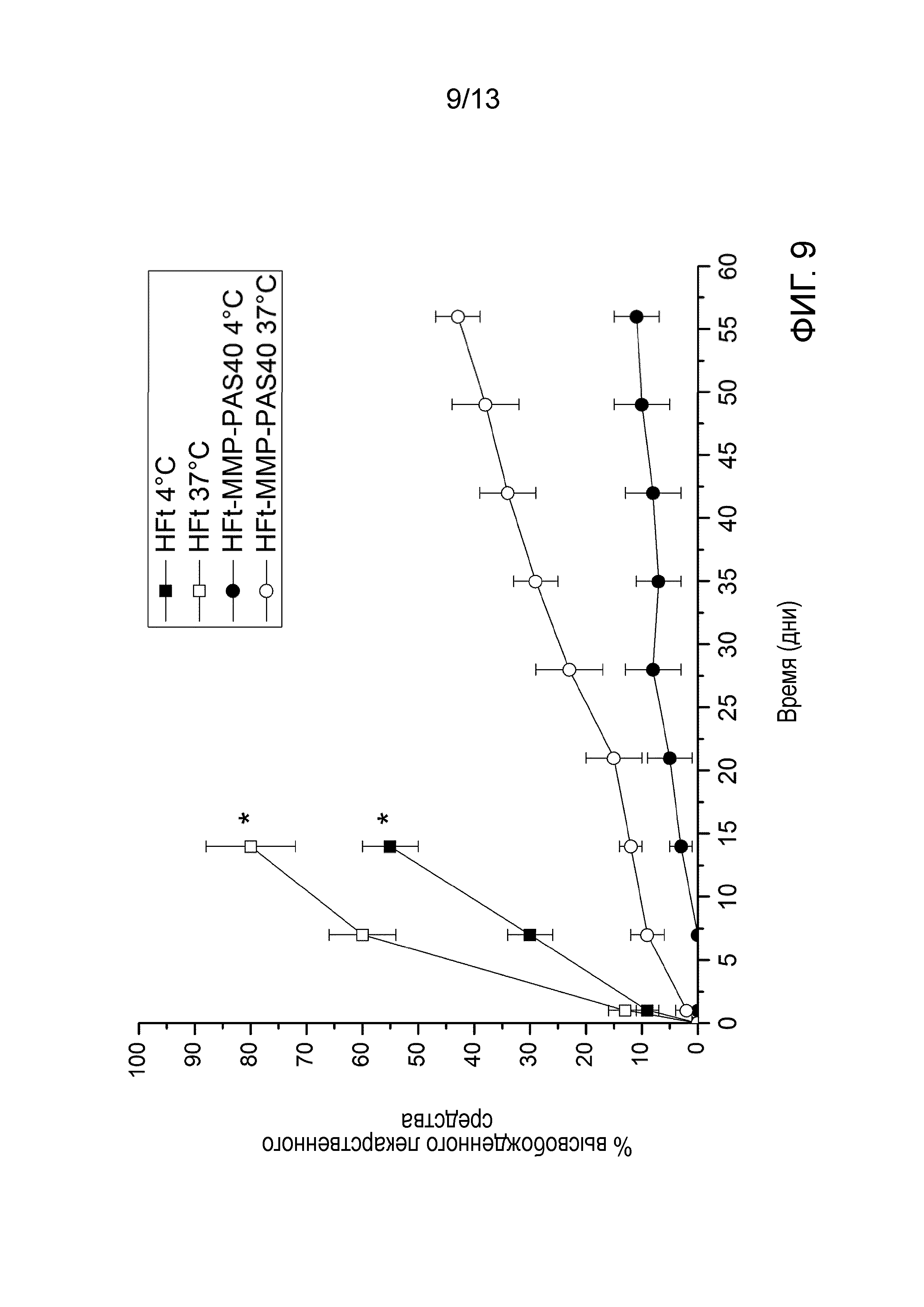
На Фигуре 9 показана стабильность комплексов ферритин-доксорубицин (HFt-DOXO, HFt-ММР-PAS40-DOXO и HFt-ММР-PAS75-DOXO) при 4°С и 37°С в единицах % высвобождения лекарственного средства в течение времени. Из-за изменений, проведенных в HFt, как описано в этом патенте, конструкция HFt-ММР-PAS40 (те же результаты были получены также с HFt-ММР-PAS75) является гораздо более стабильной (низкий % высвобождения лекарственного средства в течение времени при хранении при 4 или 37°С) в связанной с лекарством форме по сравнению с соответствующей нативной конструкцией HFt. Звездочка (*) указывает на то, что количество высвобожденного лекарственного вещества не может быть определено в течение этого периода времени в образцах нативной HFt, поскольку вещество, как правило, становится мутным и выпадает в осадок.
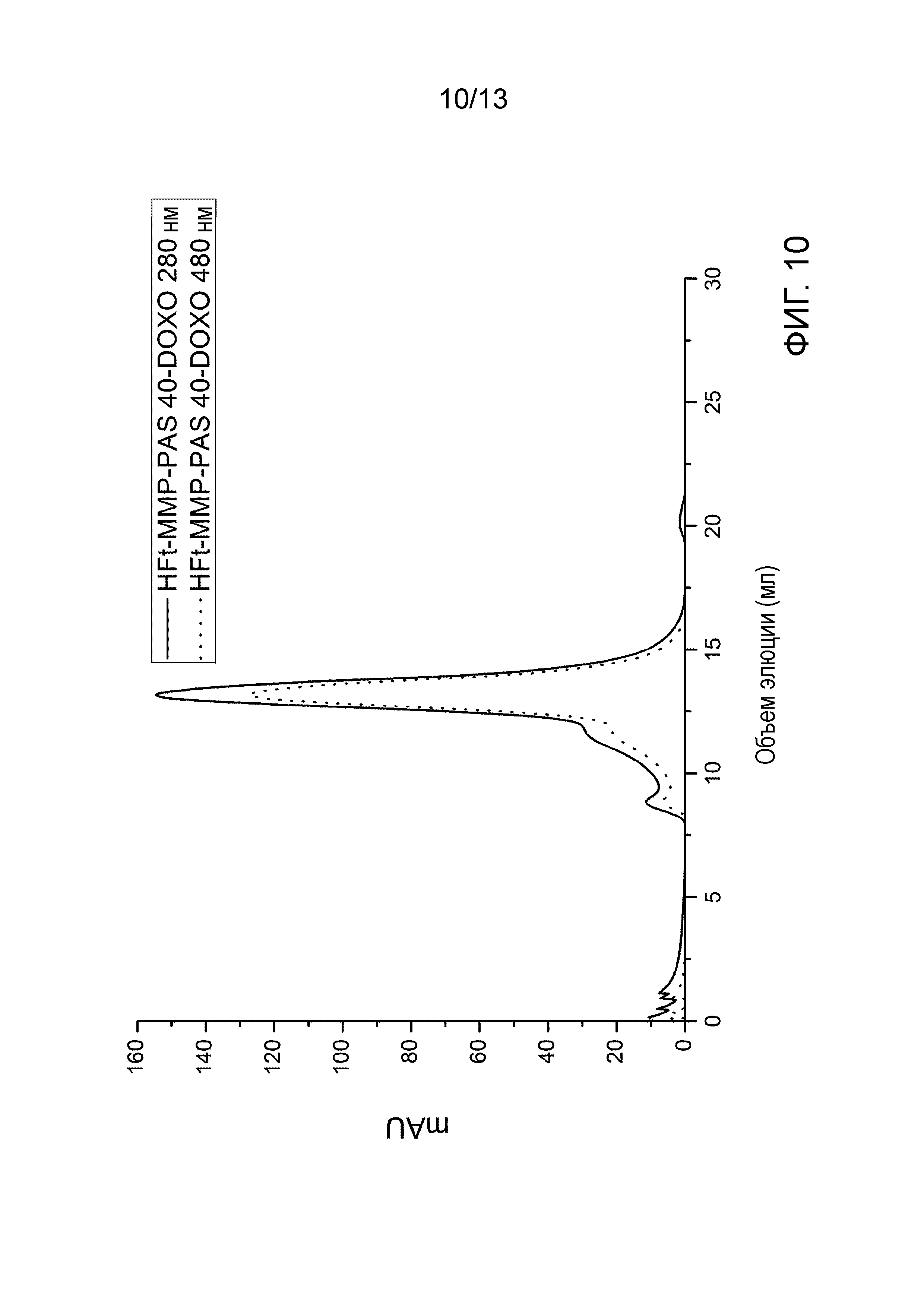
На Фигуре 10 показан типичный профиль эксклюзионной хроматографии HFt-MMP-PAS40-DOXO с показаниями при длине волны 280 нм (сплошные линии) и 485 нм (пунктирные линии).
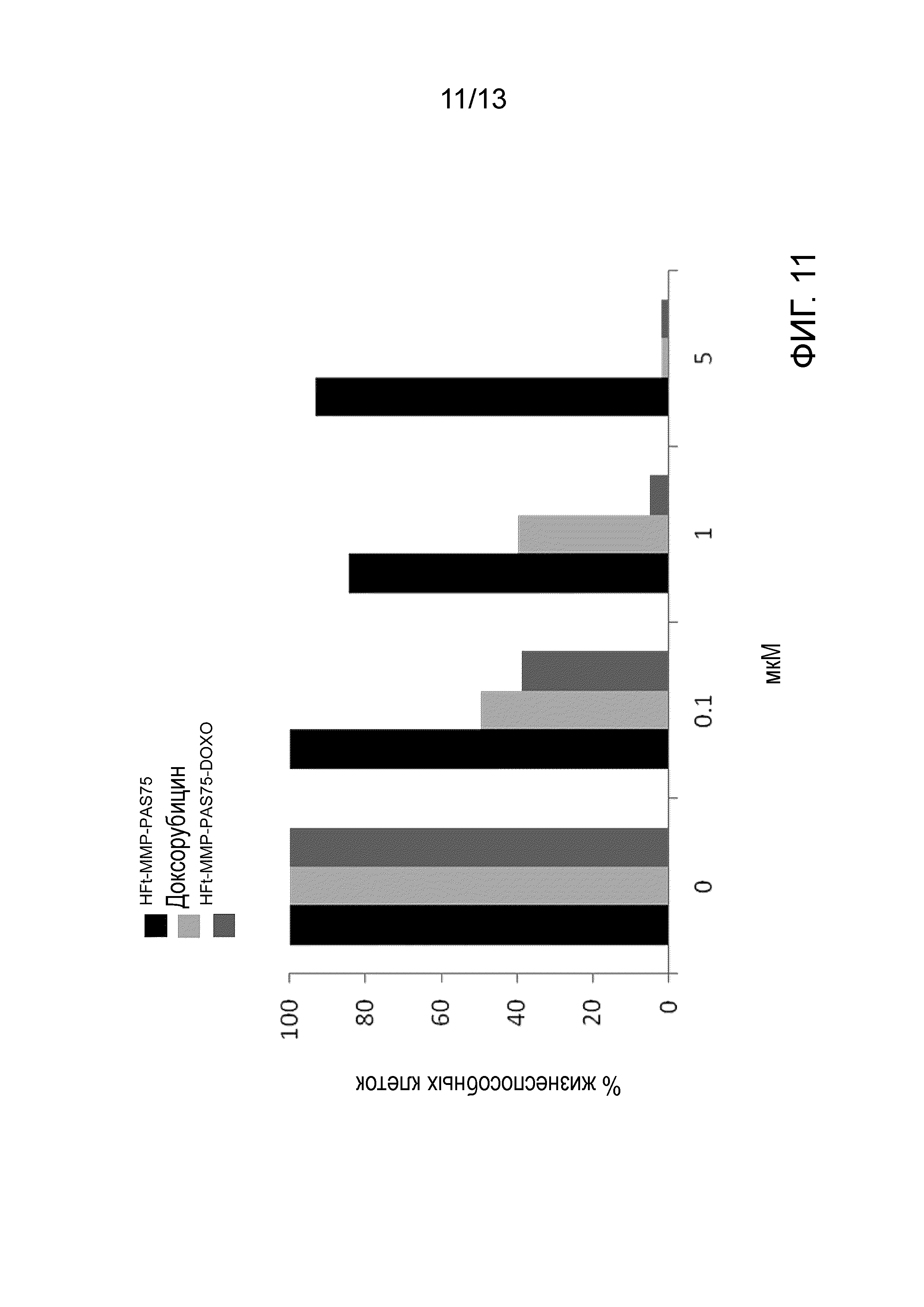
На Фигуре 11 показано антипролиферативное действие доксорубицина, HFtT-MMP-PAS75 и HFt-MMP-PAS75-DOXO в отношении клеток саркомы HT-1080.
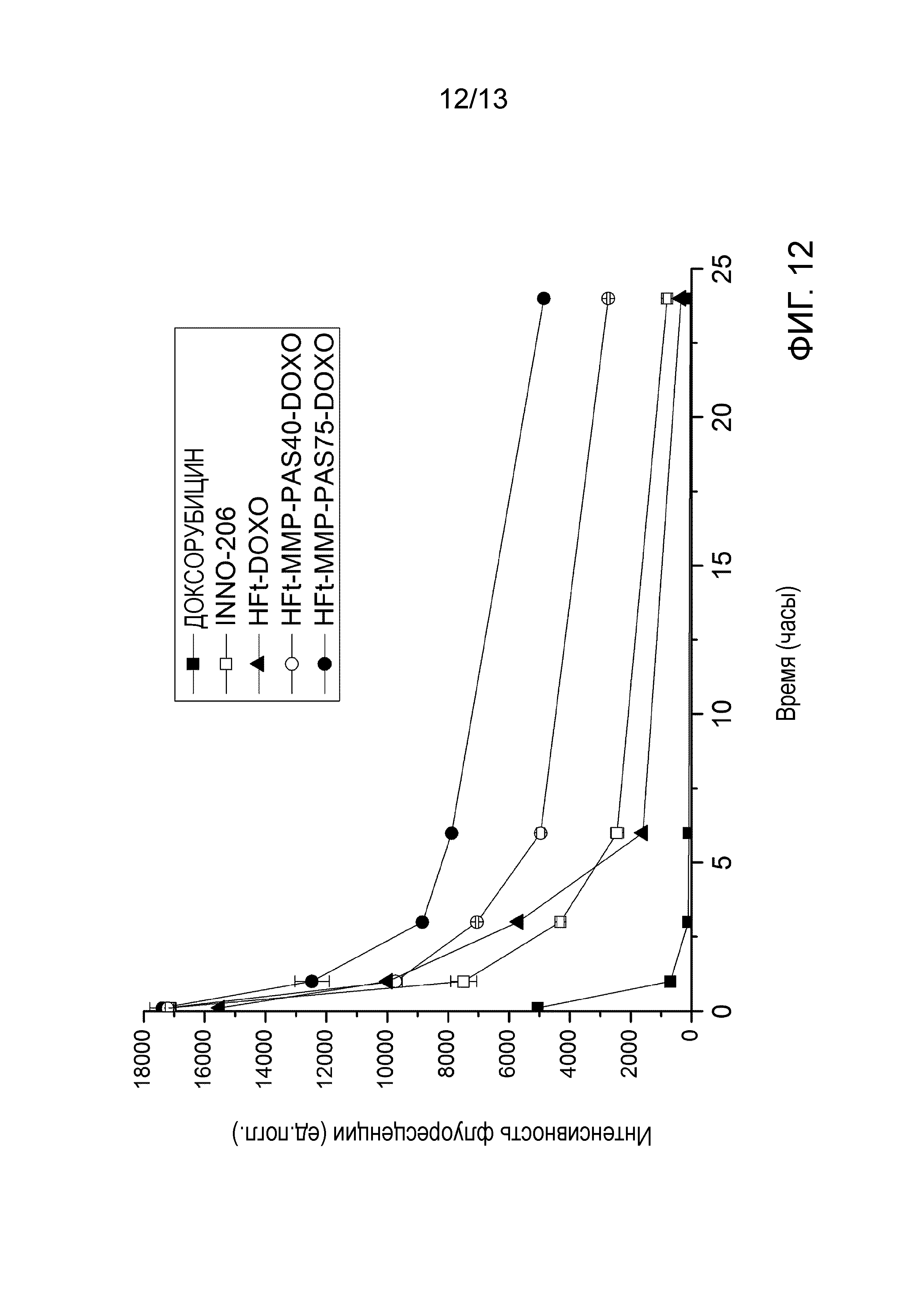
На Фигуре 12 показаны результаты фармакокинетических экспериментов на доксорубицин-содержащих соединениях. Величины концентрация доксорубицина в плазме были рассчитаны в разное время (10, 60, 180, 360 и 1440 минут) после внутривенной инъекции здоровым мышам чистого лекарственного средства доксорубицина и INNO-206 (новый и более активный состав доксорубицина) или доксорубицина, инкапсулированного в соединения на основе ферритина: нативная HFt, HFt-ММЗ-PAS40 и HFt-ММЗ-PAS75.
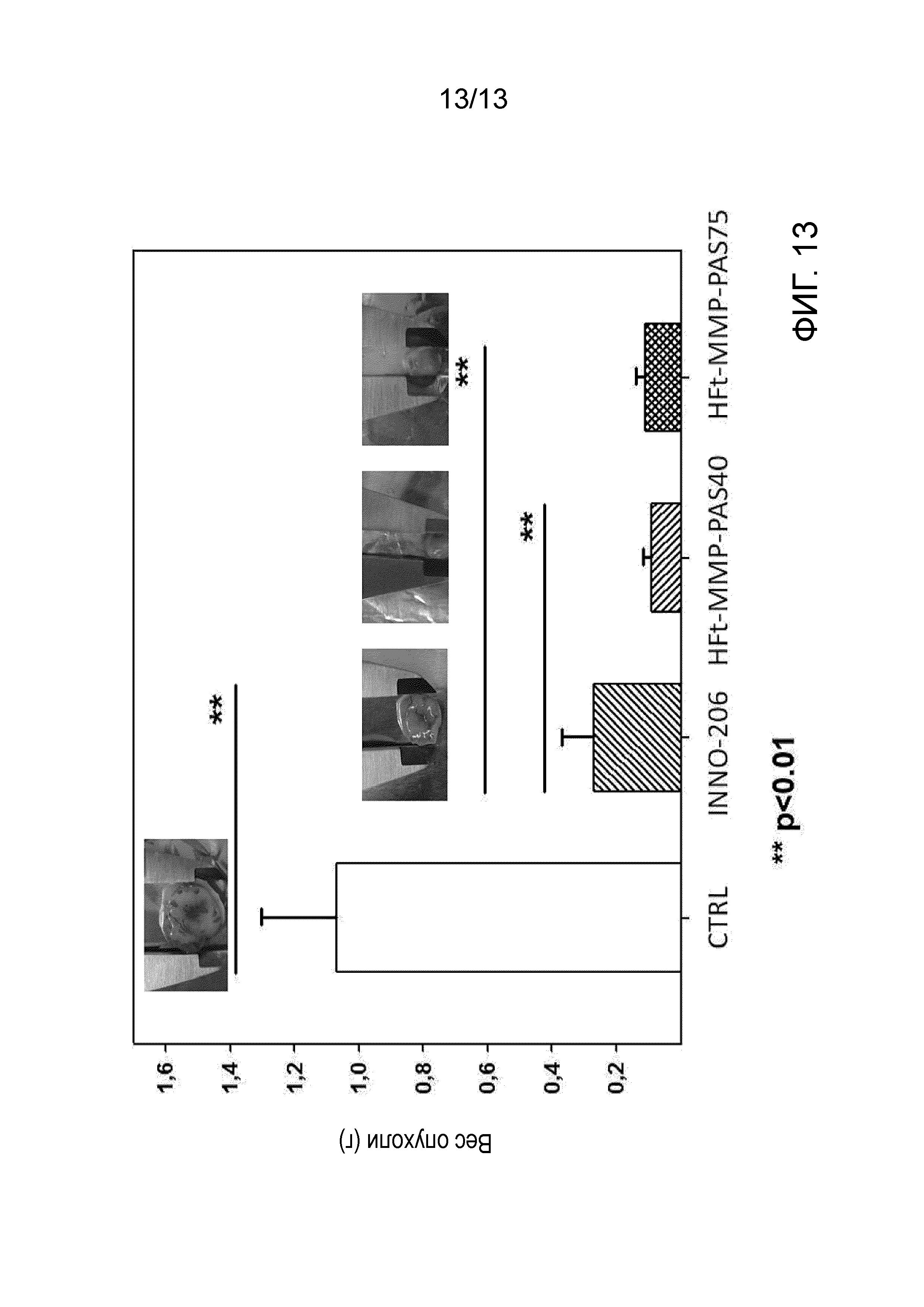
На Фигуре 13 показан типичный эксперимент для оценки терапевтического эффекта у мышей с опухолью поджелудочной железы человека (ксенотрасплантаты). Группы мышей (n=6), после того как размер опухоли достигал примерно 100 мм3, обрабатывали 4 раза (каждые 4 дня) одной дозой 5 мг/кг доксорубицина. Тестируемыми соединениями были: INNO-206, HFt-ММЗ-PAS40-DOXO и HFt-ММЗ-PAS75-DOXO. На фигуре вес опухоли (и характерные изображения) регистрировали через примерно 3 недели после начала лечения.
Слитый белок, который является объектом настоящего изобретения, содержит по крайней мере три домена.
Первый домен содержит аминокислотную последовательность тяжелой цепи ферритина человека. Такая аминокислотная последовательность представляет собой нативную последовательность или вариант нативной последовательности, которая по крайней мере на 90% идентична по последовательности. Так как длина тяжелой цепи ферритина человека составляет 183 аминокислоты (SEQ ID NO:1), то вариант, который по крайней мере на 90% идентичен по последовательности, содержит до 19 аминокислотных замен по сравнению с нативной последовательностью. Это определение включает, кроме прочего, аминокислотную последовательность SEQ ID NO:2 вышеуказанного варианта vHFt, не имеющего активность ферроксидазы, который является альтернативным вариантом. Аминокислотная последовательность vHFt характеризуется двумя аминокислотными заменами: лизин вместо глутамата 62 и глицин вместо гистидина 65.
Второй домен слитого белка по настоящему изобретению содержит аминокислотную последовательность по меньшей мере одного сайта расщепления матричной металлопротеиназы (ММР), в частности, ММР-2, ММР-3, ММР-7 или ММР-9. В качестве неограничивающего примера в описании перечислено несколько пептидов, которые моделируют последовательность расщепления цепи коллагена и расщепляются особенно эффективным образом под действием ММР-2 и ММР-9:
Gly-Pro-Leu-Gly-Ile-Ala-Gly-Gln (SEQ ID NO:3)
Gly-Pro-Gln-Gly-Ile-Trp-Gly-Gln (SEQ ID NO:4)
Pro-Leu-Gly-Leu-Ala-Gly (SEQ ID NO:5)
Pro-Val-Gly-Leu-Ile-Gly (SEQ ID NO:6)
Cys-Gly-Leu-Asp-Asp (SEQ ID NO:7).
Аминокислотные последовательности, которые содержат сайт расщепления для предполагаемого для использования фермента, также могут быть сконструированы таким образом, чтобы участок расщепления повторялся несколько раз, например, так, как это показано в последовательности ниже:
Gly-Pro-Leu-Gly-Ile-Ala-Gly-Gln-Gly-Pro-Leu-Gly-Ile-Ala-Gly-Gln (SEQ ID NO:8).
Все ранее указанные аминокислотные последовательности являются характерными, но не ограничивающими примерами получения слитых белков и наночастиц согласно настоящему изобретению.
Третий домен слитого белка по изобретению, связанный с N-концом, состоит из аминокислотной последовательности полипептида, которая богата пролином, серином и аланином (для краткости указан как «PAS») для повышения стабильности белка во время процесса инкапсулирования лекарственного средства, предпочтительно, лекарственного средства доксорубицина, и повышения стабильности комплекса белок-лекарственное средство. Наличие PAS способно также маскировать поверхность белка и таким образом увеличивать время полужизни из плазмы.
Полипептид PAS состоит в основном из аминокислотных последовательностей, богатых Pro, Ala и Ser, которые образуют неструктурированный полимер, длина которого, предпочтительно, меньше 80 аминокислотных остатков, более предпочтительно, от 20 до 80 аминокислотных остатков, еще более предпочтительно, от 40 до 75 аминокислотных остатков. В предпочтительном варианте осуществления количество пролиновых остатков вышеуказанного полипептида PAS составляет 10-40% от общего количества аминокислотных остатков полипептида PAS.
Примеры полипептидов PAS, особенно подходящие для применения в рамках настоящего изобретения и поэтому являющиеся предпочтительными, представляют собой полипептиды PAS из 40 или 75 аминокислотных остатков, например следующие:
ASPAAPAPASPAAPAPSAPAASPAAPAPASPAAPAPSAPA (SEQ ID NO:9)
ASPAAPAPASPAAPAPSAPAASPAAPAPASPAAPAPSAPAASPAAPAPASPAAPAPSAPAASPAAPAPASPAAPA (SEQ ID NO:10).
Стабилизирующий и маскирующий полипептид PAS добавляли к поверхности HFt на всем протяжении короткой пептидной последовательности, которая, как ранее указывалось, содержит один или более сайтов расщепления металлопротеиназы, получая таким образом слитый белок по изобретению с замещаемой маскировкой. Действительно, полипептид PAS может быть селективно удален в тканях-мишенях посредством внеклеточной матриксной металлопротеиназы (MMP). В частности, было показано, что ММP-2 и MMP-9 являются ключевыми металлопротеиназами, которые сверхэкспрессированы в опухолевом микроокружении и участвуют в ангиогенезе, инвазии и опухолевых метастазах.
Применение полипептидов PAS на мультимерной поверхности ферритина в рамках настоящего изобретения дает несколько преимуществ по сравнению с известными из уровня техники. Для того, чтобы инкапсулировать лекарственное средство или низкомолекулярные молекулы в белковую полость ферритина, до настоящего времени были предприняты самые очевидные действия, которые непосредственно модифицируют лекарственное средство или внутреннюю полость белка. Таким образом, взаимосвязь между лекарственным средством (или низкомолекулярной молекулой) и связывающими сайтами во внутренней полости ферритина является более предпочтительной. Например, с доксорубицином был заранее был получен комплекс с медью (II) для повышения инкапсуляционного выхода (Zhen Z et al., ACS Nano. 2013 Jun 25;7(6):4830-7). Наночастицы золота инкапсулировали, генетически модифицируя внутреннюю полость ферритина золото-связывающим пептидом (Zheng B et al. Nanotechnology. 2010 Jan 29;21(4):045305). Однако авторы настоящего изобретения решили воздействовать непосредственно на внешнюю поверхность белка, используя инертные полимеры PAS с целью стабилизации белка во время резкого изменения рН, который обычно используется для диссоциации (рН 2,0) и повторной ассоциации (рН 7,5) HFt в присутствии лекарственного средства. Присутствие полимера PAS может также ограничить неспецифическое связывание лекарственного средства на поверхности.
Кроме того, присутствие PAS также может быть способом увеличения периода полураспада белка в плазме, как было недавно предложено компанией XL-protein Gmbh для ряда белков. В самом деле, эта технология, обозначенная как «PASилирование», способна увеличить период полураспада в плазме био-фармацевтических препаратов, используя природную неструктурированную аминокислотную цепь в качестве биологической альтернативы PEG (Schlapschy M, Binder U, Börger C, Theobald I, Wachinger K, Kisling S, Haller D, Skerra A. PASylation: a biological alternative to PEGylation for extending the plasma half-life of pharmaceutically active proteins. Protein Eng Des Sel. 2013, 26:489-501). Используя эту технологию биологически активный белок генетически слит с полипептидной последовательностью, содержащей несколько сотен остатков низкомолекулярных аминокислот пролина, серина и аланина (PAS). Как правило, последовательность PAS состоит из 100-3000 остатков (предпочтительно 400-600 остатков), слитых с биологически активным белком. Биологически активные белки, указанные в патенте WO 2008/155134, подпадают под следующие категории: связывающие белки, фрагменты антител, цитокины, факторы роста, ферменты, гормоны. Тяжелая цепь ферритина человека не указывается и, особенно в форме vHFt, не относится к перечисленным категориям. Согласно результатам тестирования, проведенного авторами настоящего изобретения, которые будут описаны более подробно далее, для тяжелой цепи ферритина человека (нативной или варианта) последовательность PAS может быть значительно короче, чем описанная в публикации WO 2008/155134, например, меньше 80 аминокислотных остатков. Другими словами, за счет использования конкретной способности HFt образовывать наночастицу, состоящую из 24 мономеров, оказалось, что значительно более короткие последовательности PAS эффективны для увеличения периода полураспада HFt в плазме in vivo. Выбор длины маскирующего полипептида PAS является важной стадией при разработке HFt, снабженной желаемыми характеристиками. На самом деле, с одной стороны, in vivo период полураспада должен быть достаточно длинным, чтобы позволить HFt накапливаться в желаемом месте. С другой стороны, HFt должна быть способна высвобождаться из маскирующего полимера в средах, богатых металлопротеиназой (ММР). Если последовательность PAS слишком короткая, то конструкция может быть выведена из организма слишком быстро. Если последовательность PAS слишком длинная, то это может препятствовать проникновению через биологические барьеры, которые отделяют ее от целевой ткани и клеток (то есть, кровеносные сосуды, непроницаемые перегородки, опухоли стромы и тому подобное) и/или маскировке сайта или сайтов расщепления MMP.
Кроме того, получение конечного белкового продукта, который сверхэкспрессируется, полностью растворим, и который имеет правильную укладку и сборку, не является очевидным заранее, если N-конец белка модифицирован, как и в случае слитого белка по настоящему изобретению. Действительно, хорошо известно, что N-концевая модификация белка может привести к ухудшению экспрессии, растворимости и/или правильной укладки и сборки.
Все эти результаты, в частности, улучшение выхода инкапсулирования лекарственного средства доксорубицина, были неожиданно получены авторами настоящего изобретения, которые сконструировали наночастицы на основе тяжелой цепи ферритина человека (HFT) в нативной форме или в виде варианта (предпочтительно vHFt), используя как технологию слитых генов, так и технологию получения рекомбинантных белков. В частности, как будет подробно описано в разделе, относящемся к примерам, были сделаны генетические конструкции, которые, в одной последовательности нуклеиновой кислоты (например, ДНК), кодируют три последовательности, приведенные на Фигуре 1: i) HFt (или vHFt); ii) короткие пептидные последовательности (ММР), расщепляемые ММР-2/9; iii) неструктурированные полипептидные последовательности, богатые Pro, Ser и Ala (PAS), предпочтительно, с длиной, составляющей от 20 до 80 остатков. Последовательности ii) и iii) связаны с N-концом HFt для обратимой маскировки.
В некоторых вариантах осуществления изобретения слитый белок HFT по настоящему изобретению содержит первую и/или вторую линкерную аминокислотную(ые) последовательность(и), соответственно, связывающую(ие) первый домен со вторым доменом и/или второй домен с третьим доменом. Первая и/или вторая аминокислотные последовательности могут быть одинаковыми или отличаться друг от друга.
Как уже было указано выше, слитые белки HFt, полученные авторами настоящего изобретения, спонтанно образуют наночастицы HFt, способные нести терапевтические (химические соединения, моноклональные антитела, пептиды и тому подобное) и/или диагностические молекулы (Фигура 2). В предпочтительном варианте осуществления по меньшей мере 5 терапевтических и/или диагностических молекул инкапсулированы во внутреннюю полость наночастицы HFt или ковалентно связаны с поверхностью наночастицы HFt. Количество связанного препарата и стабильность комплекса белок-лекарственное средство значительно увеличиливалась по сравнению с немодифицированным белком благодаря наличию полипептидов PAS. Как используется в настоящем описании, термин «стабильность комплекса белок-лекарственное средство» относится к способности слитого белка HFt удерживать лекарственное средство в полости и не высвобождать его в течение времени хранения комплекса. Высвобождение лекарственного средства из белка HFt перед его конечным использованием может привести к нежелательным эффектам, таким как выпадение в осадок, кластеризация и потеря конечного продукта.
Наночастицы HFt по настоящему изобретению, которые выступают как системы нацеленного связывания и высвобождения лекарственных средств и диагностических агентов, будут временно неактивными в циркуляции и в тканях, которые не экспрессируют ММР или которые экспрессируют их недостаточно, и впоследствии будет активированы, когда достигнут ткани-мишени, богатой ММР (ММP-2/9), где лекарственная нагрузка может быть высвобождена (Фигура 3). Терапевтическая молекула представляет собой, например, фармацевтический активный ингредиент. Как используется в настоящем описании, термин "фармацевтический активный ингредиент" или просто "активный ингредиент" относится к любой фармацевтически активной молекуле (химическое соединение, моноклональное антитело, пептид и тому подобное), например, к молекуле, которая может быть использована для лечения злокачественного новообразования. Предпочтительные активные ингредиенты для использования в настоящем изобретении представляют собой, например, но ими не ограничиваются, доксорубицин, паклитаксел, гемцитабин и активные ингредиенты на основе платины. Также может быть использован предшественник активных ингредиентов, перечисленных выше.
Диагностическая молекула представляет собой, например, визуализирующий агент. Как используется в настоящем описании, термин "визуализирующий агент" относится к молекуле, которая обеспечивает возможность визуализации органов, тканей или систем организма. Примеры визуализирующих агентов включают парамагнитные агенты, оптические зонды и радионуклиды. Термин "оптический зонд" относится к флуоресцентному соединению, которое может быть обнаружено путем возбуждения при первой длине волны и считывании при второй длине волны. Примеры оптических зондов включают флуоресцеин изотиоцианат и 5- (и 6)-карбокситетраметилродамин, сукцинимидиловый эфир.
При диагностическом и терапевтическом применении наночастицы HFt по настоящему изобретению, которые действуют как нацеленные системы носителей, могут быть введены индивиду или пациенту посредством любого подходящего пути введения, например перорально, парентерально, внутривенно, внутрибрюшинно, внутримышечно, в виде суппозиториев, внутриочагово, интраназально или подкожно, интратекально, интралимфатически, путем ингаляции микрокапель или путем имплантации устройства замедленного высвобождения, например осмотического насоса. Как используется в настоящем описании, термин «индивид» относится к животным, таким как млекопитающие, включая человека, коров, овец, коз, лошадей, собак, кошек, кроликов, крыс, мышей и тому подобное.
Как используется в настоящем описании, термин «лечение» относится к свидетельству успешного или улучшенного лечения определенного заболевания, поражения, состояния или симптома, или, при определенных обстоятельствах, к профилактике возникновения симптома или состояния.
При терапевтическом применении наночастицы HFt по изобретению используются для введения терапевтически эффективной дозы фармацевтически активного ингредиента. "Терапевтически эффективная доза" означает дозу, которая дает терапевтический эффект, для достижения которого ее вводят. Точная доза будет зависеть от ряда факторов, в том числе цели лечения, индивида, заболевания, на которое направлено лечение, и тому подобное, и может быть легко определена средним специалистом в данной области, используя известные per se методики (см, например, Lieberman, Pharmaceutical Dosage Forms (vols. 1-3, 1992); Lloyd, The Art, Science and Technology of Pharmaceutical Compounding (1999); Pickar, Dosage Calculations (1999); and Remington: The Science and Practice of Pharmacy, 20th Edition, 2003, Gennaro, Ed., Lippincott, Williams & Wilkins).
Наночастицы HFt по изобретению могут быть использованы для лечения любого заболевания, которое требует введения фармацевтического ингредиента, например, путем изолирования активного ингредиента в полости наночастицы или путем его ковалентного связывания с поверхностью наночастиц. Наночастицы могут быть также использованы для диагностики, более конкретно, для визуализации заболеваний, путем изолирования активного ингредиента в полости наночастицы или путем его ковалентного связывания с поверхностью наночастиц.
Наночастицы HFt по настоящему изобретению могут быть введены индивиду для лечения любого заболевания, предпочтительно, гиперпролиферативного заболевания, включая злокачественное новообразование, например: карцинома, глиома, мезотелиома, меланома, саркома, лимфома, лейкоз, аденокарцинома, рак молочной железы, рак яичников, рак шейки матки, глиобластома, лейкоз, лимфома, рак предстательной железы, лимфома Беркитта, рак головы и шеи, рак толстой кишки, колоректальный рак, немелкоклеточный рак легкого, мелкоклеточный рак легкого, рак пищевода, рак желудка, рак поджелудочной железы, гепатобилиарный рак, рак мочевого пузыря, мелкоклеточный рак кишечника, рак прямой кишки, рак почки, рак желчного пузыря, рак полового члена, рак уретры, рак яичка, рак шейки матки, рак влагалища, рак матки рак щитовидной железы, паратиреоидный рак, рак надпочечников, эндокринный рак поджелудочной железы, карциноидная опухоль, рак кости, рак кожи, ретинобластома, множественная меланома, лимфома Ходжкина, неходжкинская лимфома (см CANCER: PRINCIPLES AND PRACTICE (DeVita, V. T. et al. 2008 Edition) для другие виды злокачественного новообразования).
Следующие примеры приведены с целью иллюстрации, но не в качестве ограничения объема настоящего изобретения, определенного в прилагаемой формуле изобретения.
ПРИМЕРЫ
Пример 1
Конструирование экспрессионных векторов для слитных белков HFt-ММЗ-PAS40 и HFt-ММЗ-PAS75
В качестве первой стадии создания конструкции HFt-MMP-PAS (или vHFt-MMP-PAS) конструировали несколько молекулярных моделей на основе трехмерной структуры HFt, которая была определена экспериментально с помощью рентгеновской кристаллографии и является доступной в Protein Data Bank (PDB) под кодом 3AJO. Для того, чтобы модифицировать эту структуру вычислительным образом, использовали программное обеспечение InsightII molecular modelling software (Accelrys Inc.)
i) для того, чтобы сконструировать модель варианта HFt, описанную Vannucci et al. (2012), которая имеет подходящий гидродинамический объем, использовали полимер, содержащий 110 единиц PEG, который был связан с группами -SH, представленными на поверхности HFt. Полимеры PEG создавали по образцу в плотно упакованной конформации на поверхности белка для того, чтобы отразить гидродинамический объем, который был экспериментально измерен для замедленной циркуляции PEGилированной HFt (PEG 5 кДа) (см Vannucci et al., 2012).
ii) для того, чтобы сконструировать модель новой HFt, выбранную последовательность расщепления ММР (SEQ ID NO:5) связывали с экспонированным N-концом каждой субъединицы HFt (SEQ ID NO:1) и конструировали ряд полимеров PAS различной длины. Эти полимеры PAS присоединяли к последовательности расщепления MMP посредством трех остатков глицина, и их объем был сравним с объемом PEGлированной HFt. Сначала выбирали две длины PAS, так как они отражали два разных сценария, то есть расширенную конформацию (PAS40) и более упакованную конформацию (PAS75), принимая во внимание, что из-за наличия пептидных связей и остатков пролина полимеры PAS значительно снижают степень свободы по сравнению с очень гибким PEG.
Ген HFt-ММР-PAS40 получали путем объединения трех различных последовательностей в одну последовательность: HFt (SEQ ID NO:1), ММР (SEQ ID NO:5) и PAS (SEQ ID NO:9). Линкер, состоящий из трех остатков глицина, встраивали между HFt и ММР и между ММР и PAS.
Ген HFt-ММР-PAS75 получали путем объединения трех различных последовательностей в одну последовательность: HFt (SEQ ID NO:1), ММР (SEQ ID NO:5) и PAS (SEQ ID NO:10). Линкер, состоящий из трех остатков глицина, встраивали между HFt и ММР и между ММР и PAS.
Вектор экспрессии, рЕТ-11а, содержащий ген HFt-ММР-PAS40 или ген HFT-ММР-PAS75, синтезировали, используя GENEART AG (Germania). Синтез гена проводили с учетом оптимизации кодонов для высоких уровней экспрессии в E.coli.
Пример 2
Бактериальная экспрессия и очистка слитого белка HFt-MMP-PAS40 и HFt-MMP-PAS75
Векторы экспрессии pET-11a, содержащие HFt-ММР-PAS40 или HFt-ММР-PAS75 из Примера 1, вводили в E.coli BL21 (DE3) и секвенировали с помощью метода дидезокси-секвенирования, чтобы подтвердить наличие правильного гена. Клетки E. coli BL21 (DE3), содержащие рекомбинантную плазмиду, культивировали до OD600 со значением 0,6 при 37°C в 1 л жидкой среды Terrific Broth (TB), содержащей ампициллин (23,6 г/л дрожжевого экстракта, 11,8 г/л триптона, 9,4 г/л K2HPO4,2,2 г/л KH2PO4). Генную экспрессию индуцировали, добавляя 0,5 мМ изопропил тио-β-D-галактозида (IPTG), и культуру дополнительно инкубировали в течение 3 часов. Клетки собирали центрифугированием (15000 оборотов в минуту в течение 20 минут), суспендировали в 50 мМ Трис-HCl (рН 7,5), 0,5 мМ дитиотреитола, 1 мМ ЭДТА и 300 мМ NaCl и разрушали ультразвуком. Лизат центрифугировали при 15000 оборотах в минуту в течение 40 минут, и супернатант, содержащий растворимую фракцию, обрабатывают в течение 30 минут при температуре 37°С 0,1 мг/мл ДНКазой, обогащенной 5 мМ MgCl2, нагревали до 75°С в течение 10 мин, охлаждали на льду, а затем центрифугировали для удаления денатурированных белков. Извлеченный супернатант осаждали, используя концентрацию 65% насыщенного (масс/объем) сульфата аммония. Осадок ресуспендировали и подвергали диализу в течение ночи против 30 мМ Tris-HCl, рН 7,5, 0,25 М NaCl, а затем нагружали на колонку Superdex 200 HiLoad 26/600 (GE Healthcare), предварительно уравновешенную фосфатным буфером (PBS). Фракции собирали, концентрировали, фильтровали в стерильных условиях и хранили при температуре 4°С. Чистоту всех препаратов оценивали, окрашивая Кумасси синим 15% PAGE геля в присутствии SDS. Концентрацию белка определяли спектрофотометрически при длине волны 280 нм, используя коэффициент молярной экстинкции, полученный с помощью программного обеспечения ProtParam (www.expasy.org).
Бактериальный профиль экспрессии для конструкции HFt-ММР-PAS75 показан на Фигуре 4.
Пример 3
Получение PEGилированного варианта белка HFt
Нативная HFt была PEGилирована с помощью PEG 5 кДа, и ее использовали в качестве эталона в экспериментах с эксклюзионной хроматографией (SEC). Растворы (2 мг/мл) инкубировали вместе с 1,0 мМ метоксиполиэтиленгликоль малеимида 5 кДа (Sigma-Aldrich) в PBS при рН 7,0 и при комнатной температуре в течение приблизительно 2 часов при перемешивании. Затем образцы отфильтровывали и заменяли 5 раз H2Оdd, используя 30 кДа спиновое фильтрационное устройство от компании Amicon Ultra-15 (Millipore Corporate) для удаления избытка реагентов. Образец PEGилированного (HFt-PEG5K) стерильно фильтровали и хранили при температуре 4°С.
Пример 4
Оценка гидродинамического объема для HFt, HFt-MMP-PAS40, HFt-MMP-PAS75 и HFt-PEG5K с помощью эксклюзионной хроматографии (SEC)
Эксперименты SEC проводили с помощью гель-фильтрации на колонке Superose 6, уравновешенной фосфатным буфером (PBS) при рН 7,5. Все образцы получали в концентрации 1 мг/мл в фильтрованном PBS.
Все профили элюции SEC анализировали с помощью Origin 8.0 (OriginLab Corporation, Northampton, MA). Профили элюции для HFt и ее слитого белка или функционализированных вариантов показаны на Фигуре 5. Эти результаты указывают и на то, что оба PASилированных варианта имеют гидродинамические объемы, которые выше по сравнению с нативным белком, и то, что они сравнимы с PEGилированным вариантом (PEG 5 кДа) HFt, где HFt-MMP-PAS75 немного выше, а HFt-MMP-PAS40 немного ниже. Кроме того, оба PASилированных варианта более однородны и имеют монодисперсный профиль по сравнению с PEGилированным вариантом. Эти гидродинамические объемы рассматривают как подходящие значения для целей настоящего изобретения, и оба слитых белка HFt-MMP-PAS75 и HFt-ММР-PAS40 были дополнительно охарактеризованы и использованы для инкапсулирования лекарственных средств и в качестве наноносителей при лечении злокачественного новообразования.
Пример 5
Удаление защитной PAS из слитого белка HFt-ММР-PAS75 в присутствии протеазы ММР2/9 in vitro
Для анализа ферментативно расщепляемых ММР-чувствительных конъюгатов, было изучено расщепление HFt-MMP-PAS75 в присутствии ММР-2/9. Раствор HFt-MMP-PAS75 смешивали с коллагеназой IV (содержащей ММР2 и 9) и инкубировали при 37°С в течение 2 часов. Затем образцы исследовали в экспериментах SEC, используя гель-фильтрацию на колонке Superose 6, уравновешенную фосфатным буфером (PBS) при рН 7,5 (Фигура 6), и с помощью гель-хроматографии на SDS (Фигура 7).
Пример 6
Получение HFt-MMP-PAS40 и HFt-MMP-PAS75, несущих химиотерапевтическое средство
В качестве химиотерапевтического средства авторы настоящего изобретения привели пример, в котором использовали лекарственное средство доксорубицин (DOXO). DOXO был инкапсулирован внутрь белковой полости двух слитых белков, используя процесс соединения-рассоединения белка как функцию рН. Реакцию проводили, используя предпочтительную концентрацию 1,5 мМ DOXO и предпочтительную концентрацию 5 мкМ белка. Реакцию инкапсулирования проводили путем осторожного перемешивания DOXO и белка в темноте в кислой среде при рН в интервале от 1,8 до 2,5, более предпочтительно, 2,0. Температура реакции, как правило, находилась в диапазоне от 10°С до 40°С, предпочтительно, при +25°С, в течение периода от 5 до 30 минут, предпочтительно, в течение 10 минут. После этого раствор быстро доводили до рН в интервале от 6,5 до 9,0, более предпочтительно, до рН 7,5, используя концентрированный NaOH, и перемешивали в течение дополнительных 30 минут. Затем раствор центрифугировали при 15000 оборотах в минуту в течение 30 минут при 4°С, и супернатант подвергали диализу в фосфатном буфере с рН 7,4 (PBS) в течение периода между 10 и 16 часов в темноте при температуре 4°С. На конечной стадии раствор доводили до нужной концентрации с помощью 30 кДа спинового устройства Amicon Ultra-15 (Millipore Corporate). Наночастицы HFt (NP), содержащие DOXO (HFt-ММР-PAS40-DOXO и HFt-ММР-PAS75-DOXO), стерильно фильтровали и хранили при 4°С в темноте.
Пример 7
Тестирование инкапсулирующего выхода лекарственного средства доксорубицина
Способность инкапсулировать доксорубицин двумя полученными конструкциями (HFt-ММР-PAS40 и HFt-ММР-PAS75) исследовали и сравнивали с нативным белком HFt и с другими данными из литературы. Количество доксорубицина определяли после того, как образцы инкубировали с кислым изопропанолом (2н HCl) при температуре 25°C в течение 30 минут. Оценку проводили с помощью УФ-видимого спектрофотометра с показаниями при длине волны 485 нм и коэффициенте экстинкции для DOXO 9250 М-1см-1.
Величины относительного выхода указывали в единицах % восстановления белка и числа инкапсулированных молекул доксорубицина (Фигура 8). Можно видеть, что эти конструкции, являющиеся объектом изобретения по данному патенту, неожиданно и непредвиденно приобретали улучшенную способность инкапсулировать лекарственное средство доксорубицин, по крайней мере, в 6 раз по сравнению с нативной HFt.
Пример 8
Тестирование стабильности комплексов ферритин-доксорубицин
Стабильность комплексов ферритин-доксорубицин тестировали при температуре 4°С и 37°С в единицах % высвобождения лекарственного средства в течение времени. % высвобождения доксорубицина оценивали с помощью эксклюзионной хроматографии (SEC), используя гель-фильтрацию на колонке Superose 6, уравновешенной фосфатным буфером (PBS) при рН 7,5. Все образцы получали при 1 мг/мл в фильтрованном PBS, после поглощения при 280 и 485 нм. Типичный профиль элюции для HFt-MMP-PAS40-DOXO показан на Фигуре 9.
Как показано на Фигуре 10, из-за изменений, проведенных в HFt, как описано в этом патенте, конструкция HFt-ММР-PAS40 (те же результаты были получены также с HFt-ММР-PAS75) является гораздо более стабильной в лекарственно-связанной форме по сравнению с соответствующей нативной конструкцией HFt.
Пример 9
Анти-пролиферативные эффекты HFt-MMP-PAS75-DOXO in vitro
Для тестирования пролиферации клетки саркомы человека (HT-1080) высевали на 96-луночные планшеты в количестве приблизительно от 5×103/лунка в 200 мкл полной среды при 37°С. На следующий день в лунки добавляли PBS, HFt-ММР-PAS75, доксорубицин или HFt-ММР-PAS75-DOXO, трехкратно, при различных концентрациях доксорубицина, и клетки культивировали в течение 72 часов. В течение последних 4 часов в культуре добавляли [3Н]-тимидин (1 мкКю/лунка; 1 мКю=37 МБк), и включение оценивали путем лизиса клеток и подсчета TCA-выделяемой радиоактивности.
Антипролиферативные эффекты HFt-MMP-PAS75-DOXO на культивированные злокачественные клетки показаны на Фигуре 11. Полученные результаты свидетельствуют о том, что HFt-ММР-PAS75-DOXO эффективно ингибирует клетки саркомы, выросшие in vivo зависимым от концентрации образом, причем значения IC50 одинаковые или ниже по сравнению с неинкапсулированным доксорубицином. Эти результаты имеют важное значение в свете потенциального терапевтического применения.
Пример 10
Фармакокинетические исследования доксорубицин-содержащих соединений
Для того, чтобы оценить стабильность в плазме и фармакокинетику, доксорубицин-содержащие соединения вводили внутривенно здоровым мышам. Затем отбирали образцы крови в разные моменты времени (10, 60, 180, 360 и 1440 минут), разбавляли подкисленным изопропанолом (0,75 н HCl) в соотношении 1:10 и замораживали при -20°C. На следующий день извлеченный доксорубицин количественно измеряли, измеряя флуоресценцию при возбуждении 485 нм и излучении 590 нм, используя многорежимный сканирующий считивающий ридер. Оценивали следующие образцы: доксорубицин, INNO-206 (новый и более активный препарат доксорубицина), HFt-DOXO, HFt-ММР-PAS40-DOXO и HFt-ММР-PAS75-DOXO. Результаты показаны на Фигуре 12.
Пример 11
Оценка терапевтического эффекта доксорубицин-содержащих соединений на животных моделях
Типичный эксперимент по оценке терапевтического эффекта доксорубицин-содержащих соединений проводили на мышах с опухолью поджелудочной железы человека (ксенотрансплантаты). Группы мышей (n=6) после того, как размер опухоли достигал примерно 100 мм3, обрабатывали 4 раза (каждые 4 дня) одной дозой 5 мг/кг доксорубицина. Тестированными соединениями были: INNO-206, HFt-ММЗ-PAS40-DOXO и HFt-ММЗ-PAS75-DOXO. Результат типичного эксперимента массы опухоли (и характерных изображений) через приблизительно 3 недели после начала лечения приведен на Фигуре 13. Как показано на фигуре, доксорубицин-содержащие конструкции, полученные авторами настоящего изобретения, обладают более высокой терапевтической активностью по сравнению с новым составом лекарственного средства доксорубицина (INNO-206) в тестированных дозах.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Consiglio Nazionale delle Ricerche
<120> Слитый белок, наночастица, состоящая из множества мономеров
указанного слитого белка, и их применение
<130> I0160220-EC
<160> 10
<170> PatentIn version 3.5
<210> 1
<211> 183
<212> Белок
<213> Homo sapiens
<400> 1
Met Thr Thr Ala Ser Thr Ser Gln Val Arg Gln Asn Tyr His Gln Asp
1 5 10 15
Ser Glu Ala Ala Ile Asn Arg Gln Ile Asn Leu Glu Leu Tyr Ala Ser
20 25 30
Tyr Val Tyr Leu Ser Met Ser Tyr Tyr Phe Asp Arg Asp Asp Val Ala
35 40 45
Leu Lys Asn Phe Ala Lys Tyr Phe Leu His Gln Ser His Glu Glu Arg
50 55 60
Glu His Ala Glu Lys Leu Met Lys Leu Gln Asn Gln Arg Gly Gly Arg
65 70 75 80
Ile Phe Leu Gln Asp Ile Lys Lys Pro Asp Cys Asp Asp Trp Glu Ser
85 90 95
Gly Leu Asn Ala Met Glu Cys Ala Leu His Leu Glu Lys Asn Val Asn
100 105 110
Gln Ser Leu Leu Glu Leu His Lys Leu Ala Thr Asp Lys Asn Asp Pro
115 120 125
His Leu Cys Asp Phe Ile Glu Thr His Tyr Leu Asn Glu Gln Val Lys
130 135 140
Ala Ile Lys Glu Leu Gly Asp His Val Thr Asn Leu Arg Lys Met Gly
145 150 155 160
Ala Pro Glu Ser Gly Leu Ala Glu Tyr Leu Phe Asp Lys His Thr Leu
165 170 175
Gly Asp Ser Asp Asn Glu Ser
180
<210> 2
<211> 183
<212> Белок
<213> Искусственная последовательность
<220>
<223> Вариант тяжелой цепи ферритина человека (vHFt)
<400> 2
Met Thr Thr Ala Ser Thr Ser Gln Val Arg Gln Asn Tyr His Gln Asp
1 5 10 15
Ser Glu Ala Ala Ile Asn Arg Gln Ile Asn Leu Glu Leu Tyr Ala Ser
20 25 30
Tyr Val Tyr Leu Ser Met Ser Tyr Tyr Phe Asp Arg Asp Asp Val Ala
35 40 45
Leu Lys Asn Phe Ala Lys Tyr Phe Leu His Gln Ser His Glu Lys Arg
50 55 60
Glu Gly Ala Glu Lys Leu Met Lys Leu Gln Asn Gln Arg Gly Gly Arg
65 70 75 80
Ile Phe Leu Gln Asp Ile Lys Lys Pro Asp Cys Asp Asp Trp Glu Ser
85 90 95
Gly Leu Asn Ala Met Glu Cys Ala Leu His Leu Glu Lys Asn Val Asn
100 105 110
Gln Ser Leu Leu Glu Leu His Lys Leu Ala Thr Asp Lys Asn Asp Pro
115 120 125
His Leu Cys Asp Phe Ile Glu Thr His Tyr Leu Asn Glu Gln Val Lys
130 135 140
Ala Ile Lys Glu Leu Gly Asp His Val Thr Asn Leu Arg Lys Met Gly
145 150 155 160
Ala Pro Glu Ser Gly Leu Ala Glu Tyr Leu Phe Asp Lys His Thr Leu
165 170 175
Gly Asp Ser Asp Asn Glu Ser
180
<210> 3
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Пептид, имитирующий сайт расщепления MMP
<400> 3
Gly Pro Leu Gly Ile Ala Gly Gln
1 5
<210> 4
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Пептид, имитирующий сайт расщепления MMP
<400> 4
Gly Pro Gln Gly Ile Trp Gly Gln
1 5
<210> 5
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Пептид, имитирующий сайт расщепления MMP
<400> 5
Pro Leu Gly Leu Ala Gly
1 5
<210> 6
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Пептид, имитирующий сайт расщепления MMP
<400> 6
Pro Val Gly Leu Ile Gly
1 5
<210> 7
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Пептид, имитирующий сайт расщепления MMP
<400> 7
Cys Gly Leu Asp Asp
1 5
<210> 8
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Пептид с повторяющимися сайтами расщепления MMP
<400> 8
Gly Pro Leu Gly Ile Ala Gly Gln Gly Pro Leu Gly Ile Ala Gly Gln
1 5 10 15
<210> 9
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Последовательность PAS
<400> 9
Ala Ser Pro Ala Ala Pro Ala Pro Ala Ser Pro Ala Ala Pro Ala Pro
1 5 10 15
Ser Ala Pro Ala Ala Ser Pro Ala Ala Pro Ala Pro Ala Ser Pro Ala
20 25 30
Ala Pro Ala Pro Ser Ala Pro Ala
35 40
<210> 10
<211> 75
<212> Белок
<213> Искусственная последовательность
<220>
<223> последовательность PAS
<400> 10
Ala Ser Pro Ala Ala Pro Ala Pro Ala Ser Pro Ala Ala Pro Ala Pro
1 5 10 15
Ser Ala Pro Ala Ala Ser Pro Ala Ala Pro Ala Pro Ala Ser Pro Ala
20 25 30
Ala Pro Ala Pro Ser Ala Pro Ala Ala Ser Pro Ala Ala Pro Ala Pro
35 40 45
Ala Ser Pro Ala Ala Pro Ala Pro Ser Ala Pro Ala Ala Ser Pro Ala
50 55 60
Ala Pro Ala Pro Ala Ser Pro Ala Ala Pro Ala
65 70 75
<---
Реферат
Изобретение относится к биотехнологии, конкретно к рекомбинантным слитым белкам, и может быть использовано в медицине. Получен слитый белок, основанный на тяжелой цепи ферритина человека, который содержит на N-конце белка по меньшей мере одну последовательность расщепления матриксной металлопротеиназы (ММР) и неструктурированного полипептида, состоящего по существу из пролина, серина и аланина (PAS), действующего в качестве маскирующего полимера. Получена также наночастица, состоящая из нескольких мономеров указанного слитого белка. Наночастица или слитый белок входят в состав противоопухолевой фармацевтической композиции совместно с доксорубицином. Изобретение позволяет повысить стабильность комплекса белок-лекарственное средство. 6 н. и 7 з.п. ф-лы, 13 ил., 11 пр.
Формула
Документы, цитированные в отчёте о поиске
Система магнитного распознавания

Комментарии