Растворимый универсальный усиливающий adcc синтетический слитный ген, пептидная технология и их применение - RU2725807C2
Код документа: RU2725807C2
Чертежи














Описание
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] По настоящей заявке испрашивается приоритет по одновременно рассматриваемым предварительным патентным заявкам США № 62/089097, зарегистрированной 8 декабря 2014 года, и 62/200557, зарегистрированной 3 августа 2015 года, включенным в настоящее описание в качестве ссылок в полном объеме.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к синтетическим биологическим продуктам и способам, которые можно использовать, чтобы позволить иммунным эффекторным клеткам, в частности T-клеткам, опосредовать антителозависимую клеточную цитотоксичность (ADCC), а также способам их применения в лечении и профилактике злокачественных новообразований, инфекционных, воспалительных, аутоиммунных и других заболеваний.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0003] У млекопитающих, в частности, высших позвоночных, включая человека, развилась очень сложная иммунная система, в которой используется множество механизмов и эффекторов для детекции, деструкции или, по меньшей мере, заключения чужеродных патогенов, а также пораженных или находящихся в условиях стресса аутологичных клеток. Эти пораженные клетки могут инфицироваться вирусом или бактериями или становиться злокачественными.
[0004] Одним из механизмов иммунной системы для распознавания и элиминации пораженных клеток-хозяев и инвазирующих внутриклеточных микроорганизмов (например, вирусов, бактерий или паразитов) является клеточно-опосредованная цитотоксичность, которую может осуществлять ряд лейкоцитов и белков. Эти потенциально цитотоксические эффекторы включают: из лимфоидного ростка: естественные киллеры (NK) и цитотоксические T-лимфоциты (CTL); и из миелоидного ростка: макрофаги, нейтрофилы и эозинофилы.
[0005] Важный путь осуществления иммунной системой клеточно-опосредованной цитотоксичности основан на антителах. За последнее десятилетие моноклональные антитела (mAb), направленно воздействующие на опухолеспецифичные белки поверхности клетки, стали популярным терапевтическим подходом против злокачественных новообразований. Некоторые mAb внедрены в рутинную клиническую практику, включая ритуксимаб (ритуксан, мабтера), трастузумаб (герцептин) и цетуксимаб (эрбитукс). Популярность mAb является результатом их бифункциональной природы. Один конец антитела (Fab) можно делать высокоспецифическим для конкретного опухолевого белка без изменения другого конца (Fc), рекрутирующего множество эффекторных клеток и белков, уничтожающих опухолевую клетку.
[0006] В частности, после распознавания и связывания антигенов на поверхности клетки-мишени антитела сначала действуют в качестве адаптера и переходят к активации цитотоксической способности иммунных эффекторных клеток посредством вторичного связывания с конкретными рецепторами на этих эффекторных клетках. Это явление названо антителозависимой клеточной цитотоксичностью (ADCC). Например, что касается врожденного иммунитета против злокачественных новообразований, ADCC, главным образом, опосредована естественными киллерами (NK) (и, в меньшей степени, нейтрофилами, моноцитами и макрофагами), экспрессирующими относительно низкоаффинный Fc-рецептор (FcγRIIIa, также известный как CD16a), активирующийся только после его связывания с Fc-фрагментами антител, покрывающих поливалентный антиген на пораженной клетке-мишени (например, опухолевой клетке). Это связывание запускает высвобождение цитотоксических гранул, подобных перфорину и гранзиму (а также многих цитокинов, включая ИФНγ), что приводит к лизису клетки-мишени. Важность ADCC показана в исследованиях in vitro, а также в исследованиях на животных. Кроме того, в нескольких клинических исследованиях показано, что пациенты, несущие вариант CD16 с более низкой аффинностью (F158), имеют худший клинический исход.
[0007] Однако, эффективность ADCC, главным образом, опосредуемой эндогенными естественными киллерами (NK), в организме ограничена по ряду физиологических, а также патологических причин, как описано ниже (в случае, когда эндогенные цитотоксические T-лимфоциты участвуют в элиминации опухоли в целом, также обнаруживают, что их эффективность очень ограничена и является недостаточной).
[0008] Во-первых, большинство клеток, участвующих в ADCC, таких как макрофаги и нейтрофилы, не имеют тенденции к пролиферации, когда они активированы. NK-клетки также обладают ограниченным пролиферативным потенциалом в ответ на активацию, и они также быстро погибают. Таким образом, природный ADCC-ответ в организме рискует быть преодоленным прогрессированием заболевания (например, вирусной инфекции, злокачественного новообразования), даже если эффекторы ADCC распознают антитела, покрывающие пораженные клетки.
[0009] Во-вторых, многие из эффекторных клеток ADCC также экспрессируют ингибиторные рецепторы, ослабляющие их иммунологическую реактивность, таким образом, образуя систему балансов и проверок. Эти рецепторы включают ингибиторные KIR (киллерные иммуноглобулин-подобные рецепторы) в случае CD56low NK-клеток, FcγRIIb на моноцитах и B-клеток, и CTLA-4 (CD152) и PD-1 (белок программируемой гибели 1, CD279) в случае T-клеток. Злокачественные клетки и вирусы противодействуют системе защиты организма на основе ADCC, аномально усиливая такие ингибиторные пути.
[00010] В-третьих, основной Fc-рецептор на эффекторных клетках ADCC, FcγRIIIa (CD16a), обладает относительно низкой аффинностью (Kd≈10-6 M) для антител, даже вариант рецептора V158 обладает лишь в два раза более высокой аффинностью по сравнению с неэффективной формой рецептора F158. Это является одним из механизмов, посредством которого злокачественные клетки становятся резистентными к некоторым терапевтическим моноклональным антителам (mAb), т.к. плотность мишеней на поверхности клеток снижается ниже конкретного уровня.
[00011] В свете природных ограничений пролиферации и аффинности, а также дальнейшего подавления посредством ингибиторных Fc-рецепторов в условиях заболевания, таких как злокачественное новообразование или другие заболевания, функция ADCC организма обладает значительным потенциалом, никогда полностью не реализованным. Таким образом, синтетическое биологическое средство представляет собой новый и крайне желательный подход для высвобождения полного потенциала активности ADCC при профилактике и лечении заболеваний человека.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[00012] Настоящее изобретение положит начало новым подходам для улучшения иммунной защиты против злокачественных новообразований, инфекций и других заболеваний. Настоящее изобретение относится к новому, свободно ассоциированному, адаптер-подобному энхансеру ADCC, объединяющему цитотоксичность и пролиферативный потенциал T-клеток с терапией на основе антител.
[00013] Настоящее изобретение относится к слитому белку в виде свободно ассоциированного и циркулирующего адаптера, приводящего антитела против пораженной клетки (например, опухолевой клетки) в контакт с CD3+ T-клетками. Эта новая адаптерная молекула является растворимой, и ее можно инъецировать в кровь пациента для достижения большинства тканевых компартментов. Этот адаптер-подобный энхансер ADCC имеет два следующих компонента: (a) высокоаффинный Fc-связывающий домен; и (b) высокоаффинный CD3-связывающий домен. Принцип, лежащий в основе этого подхода, является следующим: этот адаптер-подобный энхансер ADCC будет связываться с опухолевой клеткой, уже покрытой одним или несколькими терапевтическими антителами, и энхансер также будет связываться с CD3+ T-клетками. При нахождении в непосредственной близости или в контакте с T-клеткой антитела, покрывающие опухолевую клетку, будут вызывать перекрестную сшивку CD3 на поверхности T-клетки и приводить к активации T-клетки и, в конечном итоге, лизису опухолевой клетки.
[00014] Энхансер ADCC по настоящему изобретению можно использовать в комбинации с терапией антителами или самостоятельно для направленного воздействия на пораженные клетки, распознаваемые или связываемые природным антителом.
[00015] В первом аспекте настоящее изобретение относится к получению высокоаффинных Fc-рецепторов или фрагментов антител, таких как антитела с более высокой аффинностью к природному антителу, чем CD16 человека дикого типа (например, наиболее распространенной формой CD16 человека, т.е. распространенному варианту F158). Рецептор (далее в настоящем описании этот термин используют для включения вариантов осуществления, похожих на более традиционный рецептор поверхности клетки, и вариантов осуществления на основе фрагментов антитела), частично или полностью, можно получать из другой макромолекулы, существующей в иммунной системе или сконструированной de novo. Высокоаффинный Fc-рецептор делает возможным эффективное связывание с общим Fc-фрагментом антител, воздействующих на широкий спектр антигенов поверхности клетки и, таким образом, широкий спектр заболеваний и показаний. Это является большим преимуществом по сравнению с антиген-зависимой иммунотерапией, при которой необходимо получать разные антитела против каждого конкретного антигена.
[00016] В другом аспекте, относящемся к получению растворимого, адаптер-подобного энхансера ADCC, высокоаффинный CD3-связывающий домен подвергают слиянию с высокоаффинным Fc-связывающим доменом или рецептором, описываемым в первом аспекте. Примеры таких высокоаффинных CD3-связывающих доменов включают OKT3 и новый scFv против CD3. В различных вариантах осуществления высокоаффинный Fc-связывающий домен можно выбирать из группы, состоящей из эктодомена CD64, высокоаффинного варианта CD16 и фрагмента антитела с высокой аффинностью для Fc человека.
[00017] В другом аспекте изобретение относится к фармацевтической композиции, включающей слитый белок по изобретению, который, в свою очередь, содержит высокоаффинный Fc-связывающий домен и высокоаффинный CD3-связывающий домен. Фармацевтическая композиция дополнительно включает фармацевтически приемлемый эксципиент.
[00018] В родственном аспекте изобретение относится к способу терапевтического лечения нуждающегося в этом индивидуума от состояния, включающему введение указанному индивидууму терапевтически эффективного количества фармацевтической композиции по изобретению. Способ может дополнительно включать стадию введения терапевтического антитела против по меньшей мере одного антигена поверхности клетки, свидетельствующего об указанном состоянии. В одном из вариантов осуществления антитело содержит Fc-область, по существу, схожую с IgG4 человека. Подвергаемое лечению состояние может являться злокачественным новообразованием, воспалительным заболеванием, аутоиммунным заболеванием, отторжением трансплантата, инфекцией и т.д.
[00019] В еще одном аспекте изобретение относится к способу профилактического лечения нуждающегося в этом индивидуума от схожих состояний, включающему введение указанному индивидууму профилактически эффективного количества фармацевтической композиции по изобретению. Способ может дополнительно включать стадию введения вакцины против указанного состояния. В одном из вариантов осуществления состояние является злокачественным новообразованием.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[00020] На фигуре 1 схематически изображен адаптер-подобный энхансер ADCC по настоящему изобретению.
[00021] На фигуре 2 схематически изображены экзоны CD64 и CD16. CD64 содержит дополнительную иммуноглобулиновую складку и таким образом, экзон во внеклеточной области. Эта дополнительная складка вносит вклад в более высокую аффинность CD64 для Fc.
[00022] На фигуре 3 приведена аминокислотная последовательность (SEQ ID NO: 1) Fc-связывающего домена адаптер-подобного энхансера ADCC по варианту осуществления настоящего изобретения. В частности, домен в этом варианте осуществления включает эктодомен CD64 с учетом границ экзона.
[00023] На фигуре 4 приведена аминокислотная последовательность (SEQ ID NO: 2) домена против CD3 адаптер-подобного энхансера ADCC по варианту осуществления настоящего изобретения. В частности, домен в этом варианте осуществления включает две спейсерные/линкерные последовательности (подчеркнуты) и гуманизированную версию последовательности OKT3.
[00024] На фигуре 5 приведена аминокислотная последовательность (SEQ ID NO: 3) целого адаптер-подобного энхансера ADCC по варианту осуществления, представленного на фиг. 3 и 4.
[00025] На фигуре 6 приведена последовательность ДНК (SEQ ID NO: 4) целого адаптер-подобного энхансера ADCC по варианту осуществления, представленного на фиг. 5.
[00026] Фигура 7 является фотографией иммуноблота (вестерн-блоттинг), на которой показана динамика гиперэкспрессии двух версий растворимого, адаптер-подобного энхансера ADCC в клетках Expi293. Обе версии содержали одинаковую последовательность слитого белка CD64-OKT3 и отличались только соответствующими нуклеотидными последовательностями (дорожки 1 и 2). Белок секретировался в среды. Предсказанная молекулярная масса составляла 58 кДа; антитело против CD64 соответствовало полосе 75 кДа, вероятно, в результате гликозилирования.
[00027] Фигура 8 представляет собой фотографии окрашенных кумаси гелей, на которых показана очистка растворимого энхансера ADCC с использованием коммерческой колонки с IgG человека (GE Life Sciences). Трансфицированные клетки полностью удаляли из супернатанта культуры с помощью множественных стадии центрифугирования с последующей ультрафильтрацией. Колонку уравновешивали нейтральным буфером и нагружали супернатант, а затем элюат (для обеспечения полного связывания). Белок очищали с помощью поэтапного градиента снижающегося pH. Очищенный белок сразу нейтрализовали высокомолярным буфером Трис. Очищенный белок подвергали обмену на PBS посредством последовательного диализа или повторной ультрафильтрации с использованием центрифужных фильтров Amicon® Ultra. Дорожки в геле на правой стороне представляют собой различные фракции элюата, когда промывочный буфер находился при pH 3,05.
[00028] На фигуре 9 схематически изображен анализ с использованием клеток Jurkat для тестирования способности адаптер-подобного энхансера ADCC по настоящему изобретению связываться с CD3+ иммунными эффекторными клетками.
[00029] На фигуре 10 проиллюстрированы данные FACS, демонстрирующие связывание между клетками Jurkat и энхансером ADCC по изобретению до очистки ("нагружаемый образец") и после очистки ("очищенный белок") в анализе с фиг. 9. Незакрашенная кривая представляет собой отрицательный контроль. В этом случае и во всех последующих экспериментах очищенный энхансер ADCC используют в количестве 10-20 нг/микролитров, если не указано иначе.
[00030] На фигура 11 проиллюстрированы данные FACS, демонстрирующие титрование связывания между клетками Jurkat и энхансером ADCC по изобретению в различных концентрациях. Объем энхансера в микролитрах указан в верхнем правом углу верхних шести диаграмм как: 50, 25, 12,5, 6,25, 3,13 и 1,56 микролитров. На нижней диаграмме данные объединены. CD3+ клетки Jurkat инкубировали с различными количествами энхансера, избыток энхансера удаляли посредством промывания клеток PBS, и связанные белки-энхансеры определяли с использованием флуоресцентного антитела против CD64 человека.
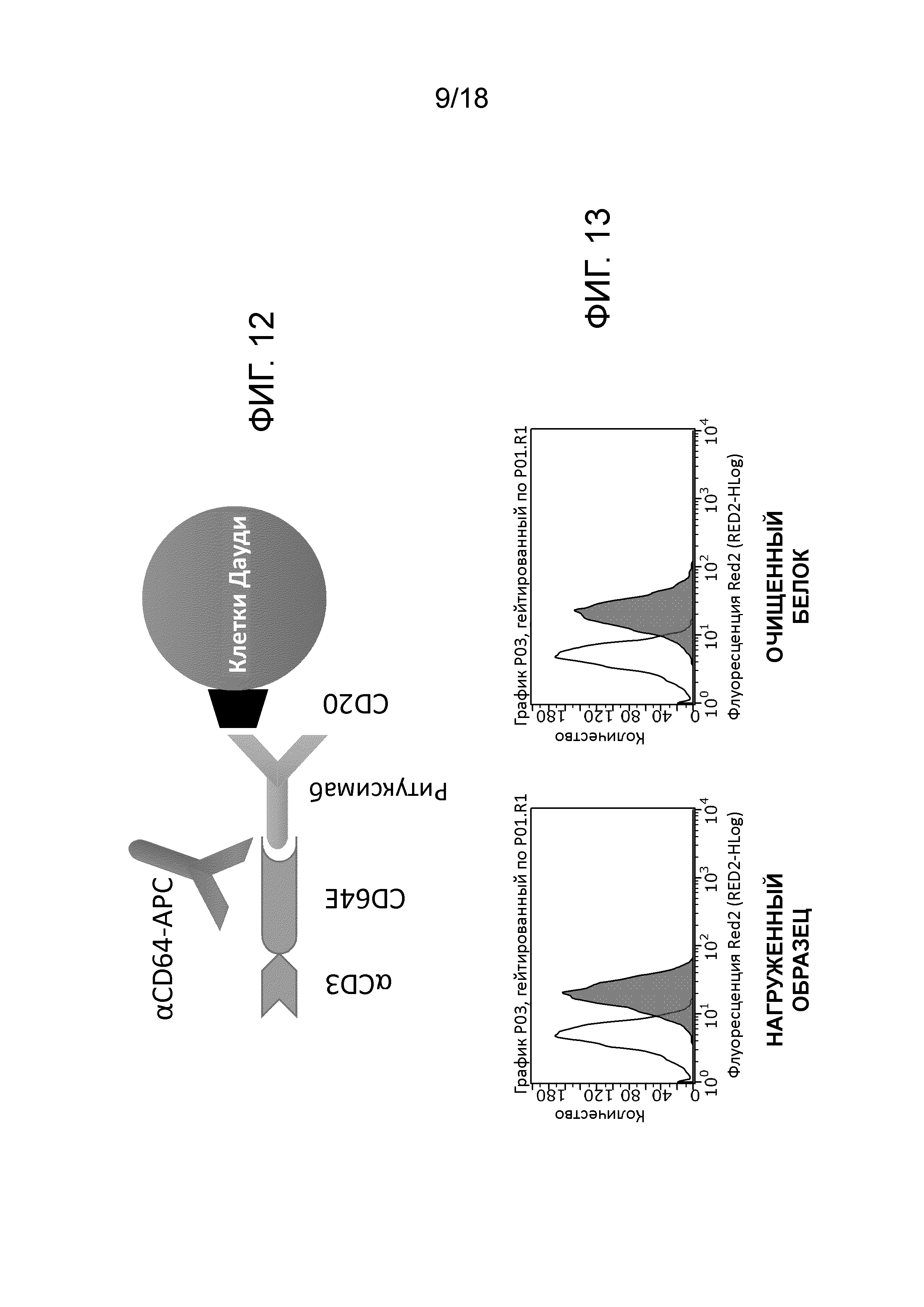
[00031] На фигуре 12 схематически изображен анализ с использованием клеток Дауди для тестирования способности адаптер-подобного энхансера ADCC по настоящему изобретению связываться с CD20+ клетками-мишенями, покрытыми ритуксаном.
[00032] На фигуре 13 проиллюстрированы данные FACS, демонстрирующие связывание между клетками Дауди и энхансером ADCC по изобретению перед очисткой ("нагружаемый образец") и после очистки ("очищенный белок") в анализе с фиг. 12.
[00033] На фигуре 14 проиллюстрированы данные FACS, демонстрирующие титрование связывания между клетками Дауди и энхансером ADCC по изобретению в различных концентрациях. Объем энхансера в микролитрах указан в верхнем правом углу верхних шести диаграмм как: 50, 25, 12,5, 6,25, 3,13 и 1,56 микролитров. На нижней диаграмме данные объединены. CD20+ клетки Дауди покрывали ритуксаном (антителом против CD20) и избыток ритуксана удаляли посредством промывания клеток PBS. Покрытые ритуксаном клетки инкубировали с различными количествами энхансера и избыток энхансера удаляли посредством промывания клеток PBS. Связанные белки-энхансеры определяли с использованием флуоресцентного антитела против CD64 человека. Наблюдали приблизительно в 30 раз более высокую аффинность для антитела в случае энхансера ADCC по сравнению с CD20.
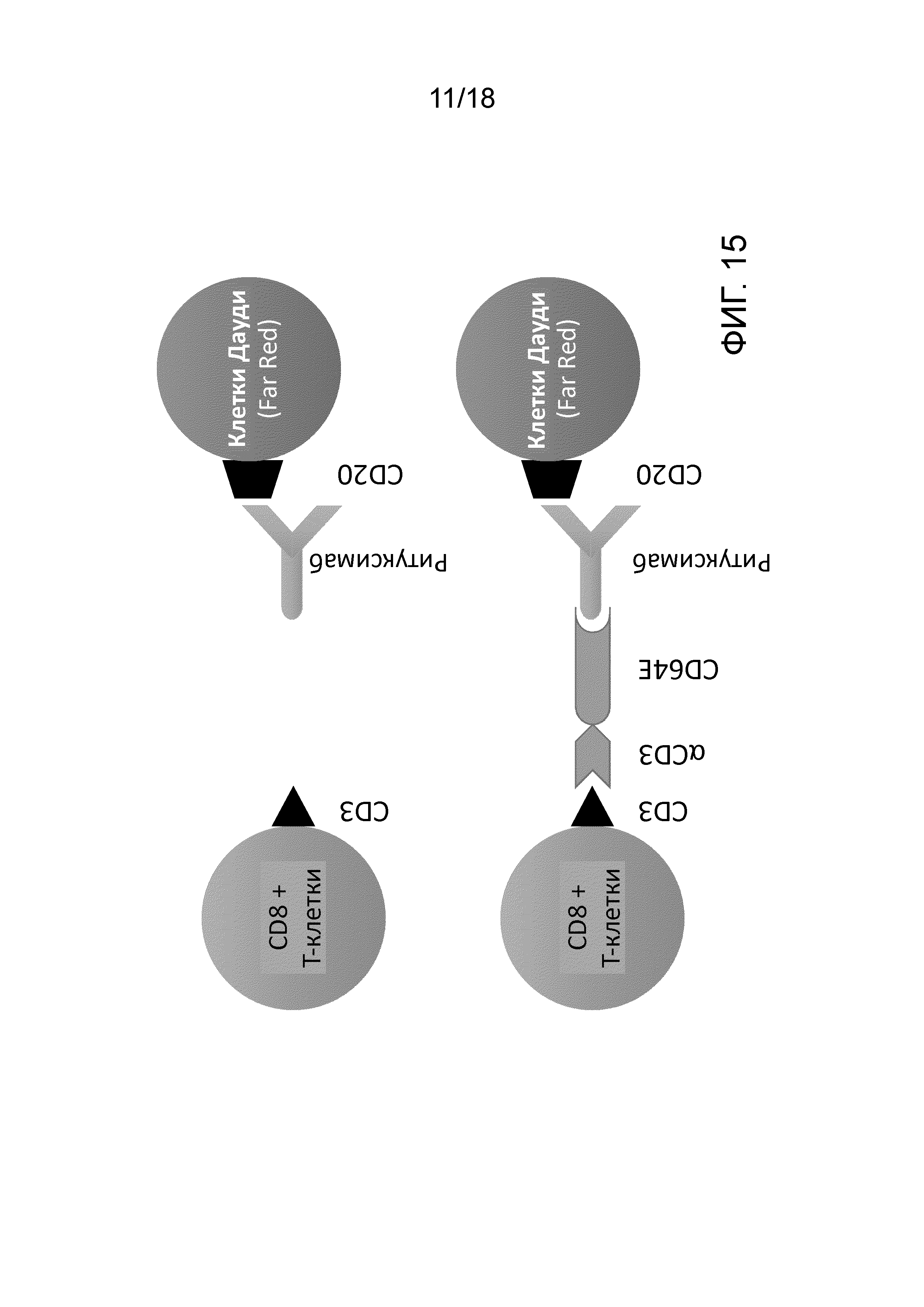
[00034] На фигуре 15 схематически изображен анализ с использованием клеток Дауди, покрытых ритуксаном, и CD8+ T-клеток для тестирования способности адаптер-подобного энхансера ADCC по настоящему изобретению опосредовать и усиливать цитотоксичность против злокачественных клеток-мишеней.
[00035] На фигуре 16 проиллюстрированы данные FACS, демонстрирующие детекцию клеток-мишеней (клеток Дауди) (верхний кластер) и эффекторных T-клеток (нижний кластер) в анализе с фиг. 15. Данные свидетельствуют о том, что энхансер по изобретению способен рекрутировать T-клетки для лизиса большей части популяции клеток Дауди без снижения жизнеспособности T-клеток (правая диаграмма). В этом и всех последующих экспериментах соотношение E:T (эффекторных клеток и клеток-мишеней) составляло 10.
[00036] На фигуре 17 проиллюстрированы данные экспериментов по цитотоксичности, включающих две концентрации ритуксана (против CD20), CD20+ клеток Дауди, CD8+ T-клеток и энхансера по изобретению. Данные свидетельствуют о том, что энхансер повышал цитолиз T-клетками клеток-мишеней, и что цитолиз зависел от концентрации ритуксана и энхансера. Как свидетельствуют данные для периода между днем 1 и днем 2, цитолиз также повышался при более длительном воздействии (зависящая от времени ADCC). Ритуксан использовали в количестве 0,1 мкг/мл (1-кратном) или 0,01 мкг /мл (1-кратном). Энхансер использовали в количестве 12,5 микролитров (+) или 50 микролитров (+++).
[00037] На фигуре 18 проиллюстрированы данные экспериментов по цитотоксичности, включающих две концентрации ритуксана, клеток Раджи, CD8+ T-клеток и энхансера по изобретению. Данные свидетельствуют о результатах, схожих с представленными на фиг. 17, при одинаковых концентрациях ритуксана и энхансера.
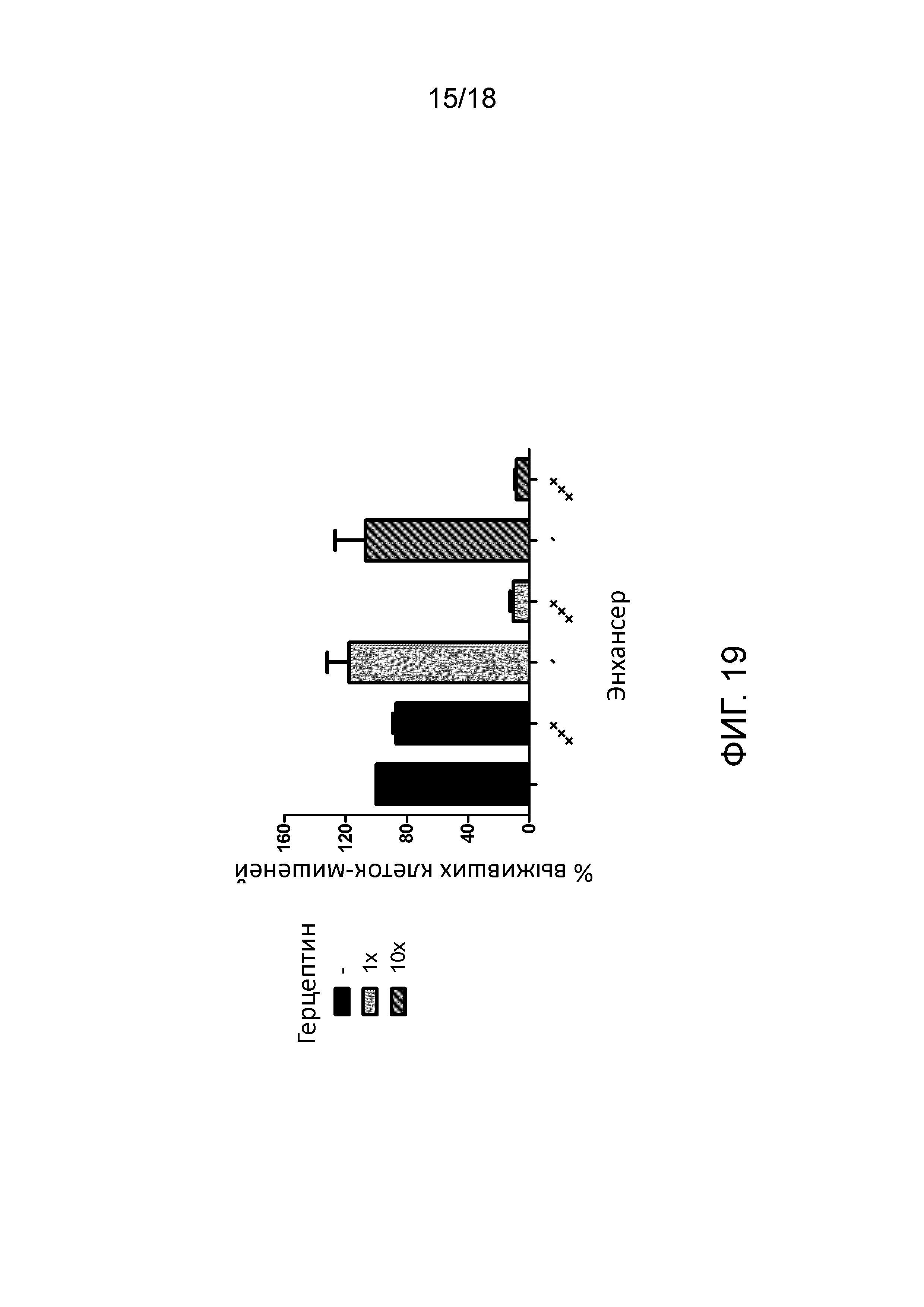
[00038] На фигуре 19 проиллюстрированы данные экспериментов по цитотоксичности, включающих две концентрации герцептина, HER+ SK-BR3 клеток, CD8+ T-клеток и энхансера по изобретению. Данные свидетельствуют о даже более выраженном цитотоксическом эффекте (по сравнению с результатами, представленными на фиг. 18) при добавлении энхансера. Герцептин использовали в количестве 1 мкг/мл (10-кратном) или 0,1 мкг /мл (1-кратном). Энхансер использовали в количестве 50 микролитров (+++).
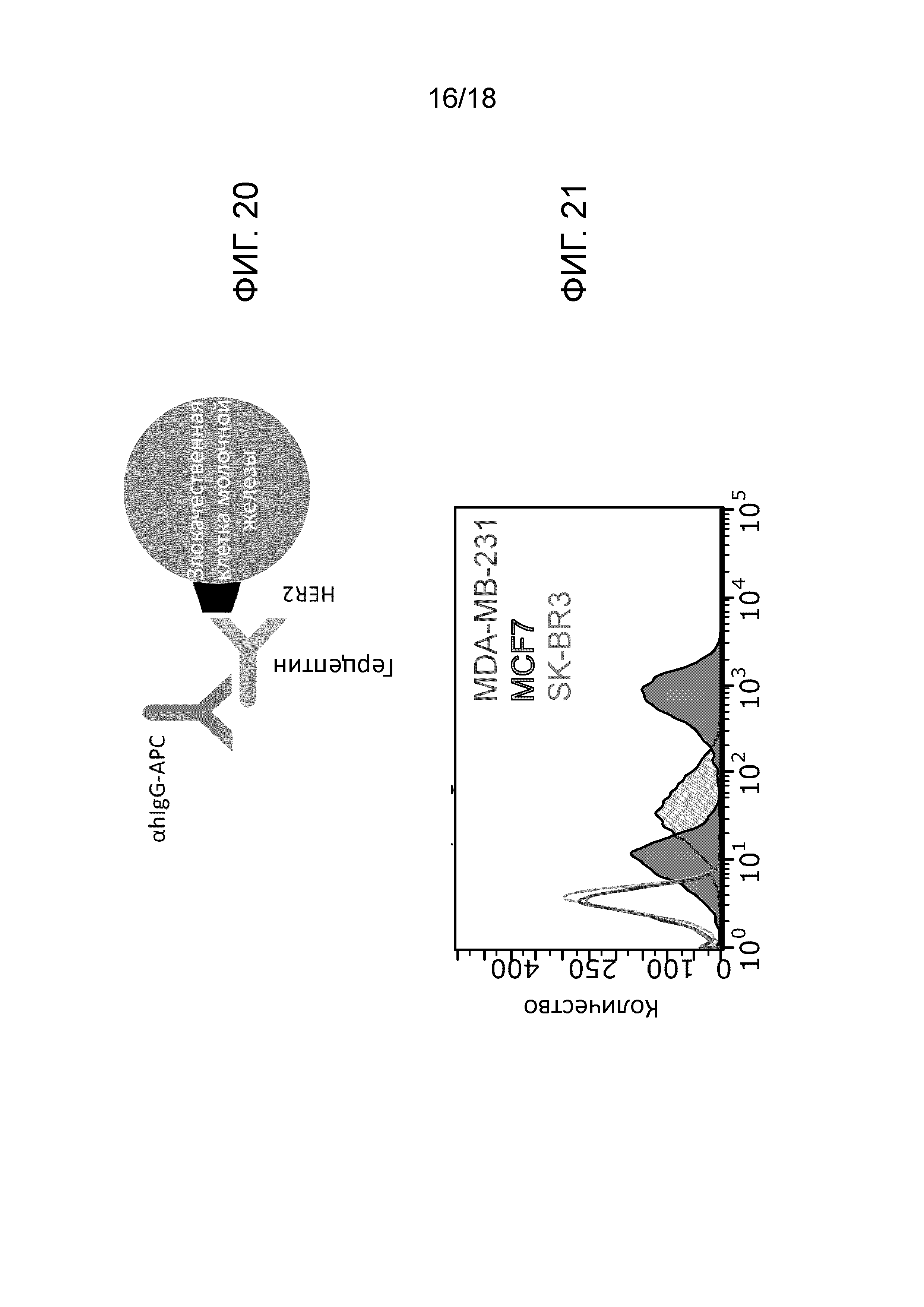
[00039] На фигуре 20 схематически изображено измерение экспрессии HER2 в различных злокачественных клетках молочной железы в соответствии с примером по изобретению.
[00040] На фигуре 21 сравнивают уровни экспрессии HER2 среди трех разных линий клеток рака молочной железы: MDA-MB-231, MCF7 и SK-BR3. Крайний левый пик представляет неокрашенный контроль, последующие пики представляют собой MDA-MB-231, MCF7 и SK-BR3 клетки, соответственно. Данные свидетельствуют о том, что среди трех линий SK-BR3 имела наиболее высокий уровень экспрессии HER2, в то время как MDA-MB-231 - наиболее низкий.
[00041] На фигуре 22 проиллюстрированы данные экспериментов по цитотоксичности, включающие герцептин, HER-hi клетки SK-BR3, HER-lo клетки MDA-MB-231 и энхансер по изобретению. Данные свидетельствуют о способности энхансера усиливать способность герцептина вызывать цитолиз обоих типов злокачественных клеток молочной железы. Данные также свидетельствуют о более выраженном эффекте в клетках SK-BR3, что свидетельствует о том, что эффект зависит от уровня экспрессии HER2. Однако способность уничтожать клетки MDA-MB-231 свидетельствует о том, что энхансер по изобретению можно использовать для сенсибилизации опухолей даже с низкой экспрессией HER2 к герцептину. В этих экспериментах энхансер использовали в количестве 50 микролитров.
[00042] На фигуре 23 проиллюстрированы данные экспериментов по цитотоксичности, включающие ниволумаб (против PD1), клетки HEK-293T, трансгенно экспрессирующие PD1 ("293T-PD1"), CD8+ T-клетки и энхансер по изобретению. Родительские немодифицированные клетки HEK-293T ("293T"), а также контрольный IgG4 включали в качестве контролей. Значительный лизис клеток-мишеней наблюдали только тогда, когда клетки, экспрессирующие PD-1, подвергали воздействию ниволумаба в присутствие энхансера. CD8+ T-клетки находились во всех изображенных образцах, включая крайний левый контроль.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
I. Определения
[00043] Если не указано иначе, технические термины используют в соответствии с общепринятым употреблением. Определения распространенных терминов молекулярной биологии можно найти, например, в Benjamin Lewin, Genes VII, опубликованной Oxford University Press, 2000 (ISBN 019879276X); Kendrew et al. (eds.); The Encyclopedia of Molecular Biology, опубликованной Blackwell Publishers, 1994 (ISBN 0632021829); и Robert A. Meyers (ed.), Molecular Biology and Biotechnology: a Comprehensive Desk Reference, опубликованной Wiley, John & Sons, Inc., 1995 (ISBN 0471186341), и других схожих технических источниках.
[00044] В рамках изобретения термин в единственном числе может означать один или несколько. В рамках изобретения, при использовании в комбинации с термином "содержащий" термины в единственном числе могут означать один или несколько. В рамках изобретения, термин "другой" может означать, по меньшей мере, второй или иной. Кроме того, если контекст четко не указывает на иное, термины в единственном числе включают термины во множественном числе, и термины во множественном числе включают термины в единственном числе.
[00045] В рамках изобретения, термин "приблизительно" относится к числовому значению, включая, например, целые части, доли и процентные доли, указано ли это конкретно или нет. Термин "приблизительно", как правило, относится к диапазону числовых значений (например, ±5-10% от указанного значения), которые специалист в этой области будет считать эквивалентными указанному значению (например, имеющему ту же функцию или результат). В некоторых случаях, термин "приблизительно" может включать числовые значения, округленные до ближайшего значимого знака.
[00046] В рамках изобретения, термин "антитело" или "Ab" в широком смысле относится к любой молекуле иммуноглобулина (Ig), состоящей из четырех полипептидных цепей, двух тяжелых цепей (H) и двух легких цепей (L), или любому его функциональному фрагменту, мутанту, варианту или производному, сохраняющему необходимые связывающие эпитоп признаки молекулы Ig. Такие форматы мутантов, вариантов или производных антитела известны в этой области и включают, в качестве неограничивающих примеров, одноцепочечный Fv(scFv), Fab, F(ab'), F(ab')2, однодоменное антитело и т.п. Их неограничивающие варианты осуществления описаны ниже.
[00047] CD16 экспрессируется в двух разных формах, CD16a и CD16b, являющихся продуктами двух разных высокогомологичных генов. CD16a является полипептид-заякоренным трансмембранным белком, в то время как CD16b является гликозилфосфатидилинозитол-заякоренным белком. В рамках изобретения, CD16 относится к обеим формам белка, если иное не будет очевидно специалистам в этой области.
[00048] Эффекторные клетки, применимые в практическом осуществлении настоящего изобретения, могут являться аутологичными, сингенными или аллогенными, при этом их выбор зависит от заболевания, подлежащего лечению, и доступных средств.
II. Композиции
[00049] Настоящее изобретение относится к технологии растворимого универсального белка-энхансера ADCC (SUAEP), относящейся к готовым к использованию, адаптер-подобным, растворимым универсальным белкам, усиливающим ADCC, которые, теоретически, можно использовать универсально для повышения терапевтической эффективности антител. Механизмы усиления могут включать, по меньшей мере, следующие аспекты:
[00050] 1. ADCC важна для эффективности способов терапии на основе антител (например, лечения Rituxan® или Herceptin®). В нескольких исследованиях показано, что пациенты, гомозиготные по низкоаффинному варианту CD16 (158F), имеют менее благоприятный прогноз.
[00051] 2. Даже в случае пациентов с относительно высокоаффинным вариантом CD16, ADCC может супрессироваться, как описано выше, по некоторым причинам, например, из-за иммуносупрессорного окружения, вовлечения ингибиторных рецепторов или неспособности эффекторных клеток пролиферировать.
[00052] 3. Система комплемента также важна для эффективности Rituxan® (ритуксимаба). Например, хотя CLL являются рефрактерными B-клеточными злокачественными новообразованиями, пациенты часто являются рефрактерными к Rituxan® по причине дефицита комплемента или из-за истощения комплемента вскоре после лечения Rituxan® (Xu et al., 2011, International Journal of Cancer 128: 2193-2201; Kennedy et al., 2004, Journal of Immunology 172 (5) 3280-3288).
[00053] Во всех этих случаях добавление энхансера ADCC поможет преодолеть эту проблему и рекрутировать цитотоксические T-клетки к злокачественным клеткам.
[00054] Кроме того, технология SUAEP по настоящему изобретению будет применима в снижении количеств антител, которые необходимо использовать для терапии, и, таким образом, минимизировать (a) неспецифические побочные эффекты антитела и (b) снижать вероятность развития ответа против антитела. Следует отметить, что даже полностью человеческое антитело содержит уникальные CDR3, которые могут запускать иммунный ответ. Снижение количества антитела, используемого в терапии, будет снижать вероятность запуска этого ответа.
Адаптер для T-клеток
[00055] По варианту осуществления настоящего изобретения, слитый белок, функционирующий в виде циркулирующего, свободно ассоциированного адаптер-подобного энхансера ADCC, имеет два компонента: высокоаффинный Fc-связывающий домен, соединяющийся с антителами, и высокоаффинный CD3-связывающий домен, рекрутирующий T-клетки (фиг. 3).
(a) Fc-связывающий домен
[00056] Fc-связывающий домен для адаптер-подобного энхансера ADCC можно получать из множества источников, включая:
[00057] (i) Эктодомен CD64 (FcγR1):
[00058] FcγR1 является высокоаффинным Fc-рецептором (Kd≈10-9 M для IgG1 и IgG3), присутствующим на макрофагах и нейтрофилах и отвечающим за антитело-опосредованный фагоцитоз и высвобождение медиаторов. FcγRI включает гликопротеиновую α-цепь, внеклеточный домен которой состоит из трех иммуноглобулиновых доменов, отвечающих за связывание с антителами.
[00059] По варианту осуществления изобретения части или весь эктодомен CD64 (FcγRI) подвергают слиянию с подходящим CD3-связывающим доменом для получения адаптер-подобного энхансера, опосредующего ADCC. Преимущественно, если эктодомен является нативным для организма, энхансер в этом варианте осуществления является сингенным и, таким образом, неиммуногенным.
[00060] (ii) Высокоаффинный вариант CD16:
[00061] В другом варианте осуществления изобретения Fc-связывающий домен адаптер-подобного энхансера ADCC по настоящему изобретению включает части или весь эктодомен варианта CD16 (FcγRIII) с улучшенной аффинностью к Fc-фрагменту антител. В варианте осуществления последовательность Fc-связывающего домена получают посредством случайного мутагенеза связывающей области FcγRIIIa и подвергают селекции с использованием наиболее распространенного варианта CD16 (F158) в качестве сравнительного контроля.
[00062] (iii) Высокоаффинный ScFv:
[00063] В дополнительном варианте осуществления Fc-связывающий домен по настоящему изобретению включает фрагмент антитела, сконструированный с высокой аффинностью к Fc (предпочтительно, Fc человека). В варианте осуществления фрагмент антитела является ScFv (одноцепочечным вариабельным фрагментом). В альтернативном варианте осуществления фрагмент является Fab (антигенсвязывающим фрагментом). Фрагмент антитела должен проявлять более высокую аффинность к Fc, чем контрольный рецептор, например, CD16. Способы конструирования таких фрагментов антител хорошо известны специалисту в этой области, например, использование коммерчески доступных гибридом. Например, Fc-домен человека инъецируют лабораторным животным (например, мышам) в течение периода времени. B-клетки, выделенные из селезенок животных, подвергают слиянию с миеломными клетками и подвергают скринингу на клоны, продуцирующие высокоаффинные моноклональные антитела против Fc-домена. Эти антитела-кандидаты можно гуманизировать, деиммунизировать и/или преобразовывать в Fab или версии ScFv стандартными способами. Альтернативно, полностью человеческие антитела можно получать посредством скрининга библиотек (например, на основе фагового дисплея, дрожжей или клеток млекопитающих) на высокоаффинные клоны или моноклональные антитела из животных с гуманизированными иммунными системами.
(b) CD3-связывающий домен
[00064] CD3-связывающий домен, предпочтительно с высокой аффинностью, также можно получать из множества источников.
[00065] Например, этот домен можно получать из OKT3, являющегося моноклональным антителом против CD3, являвшегося первым моноклональным антителом, одобренным для использования на людях в 1986 году. Оно является моноклональным антителом мыши, и со временем его множество раз модифицировали для его гуманизации, и чтобы сделать его менее иммуногенным (деиммунизировать). В одном из вариантов осуществления CD3-связывающий домен содержит scFv-часть антитела OKT3, предпочтительно, деиммунизированной, гуманизированной версии (dhOKT3).
[00066] В других вариантах осуществления настоящего изобретения новый scFv против CD3 можно получать способами, схожими с описанным в разделе (a) (iii) выше в отношении высокоаффинного Fc-связывающего scFv.
[00067] В предпочтительном варианте осуществления адаптер-подобный энхансер ADCC является слитым белком, в котором эктодомен CD64 соединяют с scFv dhOKT3.
[00068] Следует отметить, что это терапевтическое средство можно использовать для повышения эффективности коммерчески доступных противораковых антител. Однако это терапевтическое средство также можно использовать в качестве монотерапии для повышения эффективности природных антител организма, неспособных элиминировать опухоли из-за характерной низкой активности ADCC пациента.
III. Терапевтические средства и вакцины
[00069] Клинические аспекты энхансеров ADCC для лечения злокачественных новообразований можно тестировать с использованием злокачественных клеток человека в комбинации с коммерчески доступными терапевтическими антителами. Например, клетки Дауди обрабатывают (1) ритуксимабом (торговое название Rituxan®), антителом против CD20, вовлеченного в лимфому, аутоиммунные заболевания и отторжение трансплантата, приводящим к активации, дегрануляции и пролиферации эффекторных клеток, (2) CD8+ цитотоксическими T-клетками, и (3) адаптер-подобным энхансером ADCC по настоящему изобретению. В одном из вариантов осуществления энхансер ADCC по изобретению используют в комбинации с существующим терапевтическим антителом, таким как ритуксимаб. Также наблюдают цитолиз клеток-мишеней. Тестирование in vivo осуществляют с использованием коммерчески доступных мышей NOD.scid. IL2Rγ-/-, имеющих очень низкое количество T- и B-клеток и не имеющих NK-клетки. Альтернативно, используют мышей NOD.Scid, имеющих очень низкое количество T- и B-клеток и сниженное количество NK-клеток. Этим мышам пересаживали меченые клетки Дауди, наблюдали рост опухоли и измеряли его любым подходящим способом визуализации. У мышей, которым вводили ритуксимаб и иммунные эффекторные клетки, трансдуцированные энхансером ADCC по настоящему изобретению, наблюдают длительные периоды ремиссии, регрессии опухолей или длительное отсутствие прогрессирования.
[00070] В другом примере SK-BR-3 или MDA-MB-231 обрабатывают (1) CD8+ цитотоксическими T-клетками, (2) адаптер-подобным энхансером ADCC по настоящему изобретению, и (3) трастузумабом (торговое название Herceptin®) против HER2/neu, вовлеченного в рак молочной железы, что приводит к активации, дегрануляции и пролиферации эффекторных клеток. Также наблюдают цитолиз клетки-мишени. Противоопухолевую активность энхансера ADCC in vivo наблюдают в мышиных моделях, схожих с описываемым выше примером.
[00071] Клиническое применение энхансера ADCC по настоящему изобретению в случае аутоиммунности можно тестировать с использованием одной из хорошо известных мышиных моделей для каждого конкретного заболевания. Например, показано, что антитело-опосредованное истощение B-клеток предотвращает и даже реверсирует диабет типа 1 у мышей NOD. Однако, этот эффект ограничен низкой аффинностью Fc-рецепторов (Hu et al. J Clin Invest. 2007, 117(12): 3857-67; Xiu et al. J Immunol. 2008, 180(5):2863-75). Контрольных мышей сравнивали с мышами, которым вводили антитела против CD19 или против CD20 в отдельности или в комбинации с энхансером ADCC по настоящему изобретению. У мышей, которым вводили энхансер ADCC, наблюдали задержку дебюта заболевания или длительное реверсирование симптомов.
[00072] Аналогичные эксперименты можно осуществлять на других мышиных моделях, в которых показано, что антитело-опосредованное истощение влияет на заболевания, такие как рассеянный склероз или экспериментальный аутоиммунный энцефаломиелит (Barr et al. J Exp Med. 2012, 209(5): 1001-10)), артрит (Yanaba et al. J Immunol. 2007, 179(2): 1369-80) и т.д.
[00073] Клиническое применение энхансеров ADCC при вирусных инфекциях, таких как инфекция ВИЧ, можно тестировать с использованием хорошо известной гуманизированной мышиной модели, в которой показано, что с помощью комбинации антител контролируют репликацию ВИЧ (Nature, 2012, 492(7427): 118-22). Гуманизированных мышей получали, сначала воспроизводя мышей NOD.RAG1-/-.IL2Rγ-/- с эмбриональными, полученными из печени CD34+ гематопоэтическими стволовыми клетками человека. Эти мыши имеют полностью человеческую иммунную систему, их можно инфицировать ВИЧ, и они не реагируют отрицательно на антитела человека. Инфицированных контрольных мышей сравнивают с мышами, которым вводили смесь нейтрализующих антител в отдельности или в комбинации с иммунными эффекторными клетками человека вместе с адаптер-подобным энхансером ADCC по настоящему изобретению. У мышей, которым вводили энхансер ADCC, наблюдали длительное снижение виремии и восстановление количества T-клеток.
[00074] Альтернативной модельной системой для тестирования клинической эффективности энхансера ADCC является модель новорожденных макак-резусов, инфицированных вирусом иммунодефицита обезьян (SHIV), в которой показано, что нейтрализующие антитела предотвращают быстрый дебют заболевания (Jaworski et al. J Virol. 2013, 87(19): 10447-59). Инфицированных контрольных макак сравнивают с макаками, которым вводили смесь нейтрализующих антител в отдельности или в комбинации с адаптер-подобным энхансером ADCC по настоящему изобретению. Аналогично, у макак, которым вводили энхансер ADCC, наблюдали длительное снижение виремии и восстановление количества T-клеток.
[00075] Конструкции ДНК и РНК, кодирующие усиливающую ADCC систему по настоящему изобретению, можно составлять для введения индивидууму способами, известными специалистам в этой области. Составы, содержащие конструкции ДНК и РНК, кодирующие усиливающую ADCC систему, могут включать фармацевтически приемлемые эксципиенты. Эксципиенты, включенные в составы, будут иметь разное предназначение в зависимости, например, от типа генной конструкции или используемых эффекторных клеток и способа введения. Неограничивающие примеры часто используемых эксципиентов включают: физиологический раствор, забуференный физиологический раствор, декстрозу, воду для инъекций, глицерин, этанол и их комбинации, стабилизирующие средства, солюбилизаторы и поверхностно-активные вещества, буферы и консерванты, регуляторы тоничности, наполнители и смазки.
[00076] В другом варианте осуществления изобретения пациенту вводят фармацевтический состав адаптер-подобного энхансера ADCC по изобретению. Неограничивающие примеры способов введения включают внутривенную инъекцию. Другие способы включают, в качестве неограничивающих примеров, внутриопухолевый, внутрикожный, подкожный (s.c., s.q., sub-Q, Hypo), внутримышечный (i.m.), интраперитонеальный (i.p.), внутриартериальный, интрамедуллярный, внутрисердечный, внутрисуставной (сустав), интрасиновиальный (синовиальная жидкость), внутричерепной, интраспинальный и интратекальный (спинномозговая жидкость). Для осуществления такого введения можно использовать любое известное устройство, применимое для парентеральной инъекции или инфузии составов. В рамках изобретения, термины "лечить" и "лечение" имеют свое общепринятое значение и включают одно или несколько из: блокирования, улучшения или снижения тяжести и/или количества симптомов заболевания (например, злокачественного новообразования) у индивидуума, и/или ингибирования роста, деления, распространения или пролиферации злокачественных клеток, или прогрессирования злокачественного новообразования (например, появления новых опухолей) у индивидуума. Лечение означает блокирование, улучшение, снижение или ингибирование на приблизительно от 1% до приблизительно 100% относительно индивидуума, в отношении которого не использовали способы по настоящему изобретению. Предпочтительно, блокирование, улучшение, снижение или ингибирование составляет приблизительно 100%, 99%, 98%, 97%, 96%, 95%, 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20%, 10%, 5% или 1% относительно индивидуума, в отношении которого не использовали способы по настоящему изобретению.
[00077] Клиническую активность энхансера ADCC по настоящему изобретению, как в качестве терапевтического средства, так и профилактического средства, необязательно, можно повышать с использованием дендритных клеток (DC). В лимфоидных органах DC презентируют антиген T-хелперным клетками, в свою очередь, регулирующим иммунные эффекторы, включая CTL, B-клетки, макрофаги, эозинофилы и NK-клетки. Сообщают, что аутологичные DC, сконструированные для экспрессии антигена ВИЧ или активированные экзогенным белком ВИЧ, способны примировать CTL in vitro против ВИЧ (Wilson et al., J Immunol., 1999, 162:3070-78). Таким образом, в варианте осуществления настоящего изобретения DC сначала выделяли из пациента, а затем примировали ex vivo посредством инкубации с источником антигенов-мишеней, например, конкретных опухоле-ассоциированных антигенов или других поверхностных маркеров заболевания, которые можно получать из пациента или чужеродного источника. Эти DC, в конечном итоге, инфузировали обратно пациенту перед лечением аутологичными CTL и/или другими эффекторными клетками, трансфицированными с использованием усиливающей ADCC системы по настоящему изобретению, или составами, содержащими конструкции ДНК и РНК, кодирующие усиливающую ADCC систему. Это представляет собой модель усиленного лечения, а также вакцину с использованием энхансера ADCC и DC.
[00078] Изобретение также относится к набору, содержащему один или несколько контейнеров, содержащих количества генных конструкций, кодирующих адаптер-подобный энхансер ADCC, с фармацевтически приемлемыми эксципиентами. Набор также может включать инструкции по использованию. Набор также можно дополнять уведомлением в форме, предписанной государственным органом, регулирующим производство, использование или продажу фармацевтических средств или биологических продуктов, в котором отображено одобрение государственным органом, регулирующим производство, использование или продажу для введения человеку.
IV. ПРИМЕРЫ
(1) Конструирование T-клеточного адаптера
[00079] По различным вариантам осуществления настоящего изобретения разрабатывали и тестировали адаптер-подобные энхансеры ADCC, т.е. слитые белки с высокоаффинным Fc-связывающим доменом, соединенным с высокоаффинным CD3-связывающим доменом.
[00080] В частности, синтетическую ДНК CD64-dhOKT3 сначала получали посредством химического синтеза в виде генетического материала для получения адаптер-подобного энхансера ADCC (или растворимого, свободно ассоциированного, циркулирующего T-клеточного адаптера), в котором Fc-связывающий эктодомен CD64 подвергают слиянию с деиммунизированной и гуманизированной версией scFv ортоклона OKT3 (также известного как муромонаб-CD3), являющегося антителом против CD3.
[00081] Другие Fc-связывающие домены, например, на основе эктодоменов, т.е. внеклеточных доменов, других Fc-рецепторов (например, CD32 и CD16), также можно использовать в других вариантах осуществления изобретения. Однако, CD64 (т.е. FcγRI) обладает приблизительно в 100-1000 раз более высокой аффинностью к Fc-области антител, чем CD16, что делает эктодомен CD64, часть CD64, отвечающую за связывание антитела, предпочтительным кандидатом для Fc-связывающего домена в слитом белке.
[00082] Соединения частей слитого белка соответствовали границам экзонов исходного белка (см. фиг. 2). Домен CD64, полученный, таким образом, для слитого белка, включал два экзона, кодирующих секреторный сигнал, а затем три экзона, кодирующих эктодомен, и представлен на фиг. 3 как SEQ ID NO: 1. Однако секреторную сигнальную последовательность можно получать не из CD64 и ее можно заменять другими подходящими секреторными сигнальными последовательностями. Кроме того, в альтернативном варианте осуществления соединения частей слитого белка основаны на предсказанной границе аминокислотной последовательности между эктодоменом и трансмембранным доменом исходного белка. По сравнению со слиянием на основе экзонов, в этом подходе к слитому белку добавляли части линкерной последовательности, например, между двумя исходными доменами.
[00083] Остальная часть слитого белка (SEQ ID NO: 2), включая две спейсерные последовательности и последовательность OKT3, представлена на фиг. 4. OKT3 исходно получали из клеток мыши, но впоследствии гуманизировали, т.е. преобразовывали или подвергали мутагенезу так, чтобы оно было более похожим на антитело человека по многим группам. Гуманизация антитела или фрагмента антитела является стандартным способом, известным специалисту в этой области. Полная последовательность (SEQ ID NO: 3) адаптер-подобного энхансера ADCC, в которой внеклеточную часть CD64 подвергали слиянию с деиммунизированным и гуманизированным OKT3 (dhOKT3) с помощью гибкого серин-глицинового линкера, представлена на фиг. 5. В альтернативных вариантах осуществления можно использовать другие агонистические последовательности против CD3, такие как гуманизированный TR66.
[00084] Что касается фиг. 6, слитый белок CD64-dhOKT3 подвергали обратной трансляции и оптимизации последовательности для получения последовательности ДНК (SEQ ID NO: 4), представленной на фигуре. Оптимизация основана на комбинации выбора кодонов для отдельных аминокислот, чаще встречающихся у людей, а также удаления областей повторов, а также областей, которые потенциально могут образовывать вторичные структуры.
[00085] Альтернативные варианты осуществления изобретения включают добавление метки (например, Myc или His) для облегчения очистки. В другом варианте метку делают расщепляемой таким образом, что очищенный белок можно использовать в терапии без помех со стороны метки. Оба варианта осуществления можно осуществлять на практике стандартными способами, хорошо известными специалисту в этой области и не представленными подробно в настоящем описании.
(2) Экспрессия и очистка
[00086] Синтетический ген для слитого белка CD64-dhOKT3 химически синтезировали и клонировали в экспрессирующий вектор млекопитающих. Использовали вектор pVITRO2-MCS, коммерчески доступный в Invivogen®, но есть множество распространенных векторов, которые могут выполнять ту же функцию. Для экспрессии рекомбинантный экспрессирующий вектор трансфицировали в клетки Expi293 (коммерчески доступные в Thermo Fisher Scientific) по инструкциям производителя. Полученная линия клеток продуцировала растворимый секретируемый белок (фиг. 7 и 8). В кратком изложении, клетки Expi293 выращивали в средах для экспрессии Expi293 и трансфицировали с использованием реагента для трансфекции ExpiFectamine 293. Синтезированные энхансеры ADCC 1 и 2 (фиг. 7) добавляли в культуру через 16-20 часов после трансфекции и собирали супернатант через 2-7 дней после трансфекции. В альтернативных вариантах осуществления изобретения используют другие системы экспрессии, например, клетки CHO. В альтернативном варианте осуществления экспрессирующую кассету можно стабильно встраивать в геном линии клеток для получения стабильного производного, продуцирующего слитый белок.
[00087] Белок-энхансер ADCC подвергали аффинной очистке общепринятыми способами, такими как использование коммерчески доступных колонок с сефарозой и IgG (GE Healthcare Life Sciences) (фиг. 8). В кратком изложении, супернатант трансфицированных клеток нагружали на колонку, упакованную частицами сефарозы, поперечно сшитой с IgG человека. Затем колонку промывали буфером с нейтральным pH и поэтапным градиентом цитрат-фосфатного буфера с более низким pH. Белок-энхансер ADCC элюировали при низком pH (~pH 3) и сразу нейтрализовали в 1 M Трис-HCl (pH 7,4). Буфер подвергали замене посредством диализа или ультрафильтрации.
[00088] Также можно использовать другие общепринятые способы очистки, подобные использованию колонок для высаливания. В другом альтернативном варианте осуществления используют аффинную колонку с протеином L. Протеин L связывается с каппа-цепью многих видов, включая каппа-цепь scFv, такую как OKT3-часть слитого белка. В настоящем изобретении также можно использовать другие общепринятые способы очистки немеченого белка, например, ионообменный, эксклюзионный и т.д., в отдельности или в комбинации. Альтернативно, и как указано выше, слитый белок можно метить стандартными метками для облегчения очистки с использованием подходящих аффинных колонок. Эти стадии также можно использовать в тандеме для получения белка с более высокой чистотой.
[00089] (3) Аффинность связывания
[00090] Способность слитого белка CD64-против-CD3 связываться с Fc и CD3 можно тестировать напрямую с использованием супернатанта или очищенного белка несколькими способами. Например, как показано на фиг. 9, клетки Jurkat можно использовать для тестирования такой аффинности, т.к. клетки Jurkat являются T-лимфоцитами, экспрессирующими CD3. По одному из примеров, 2×105 клеток Jurkat промывали PBS и инкубировали в течение 30 минут при 4°C в 50 мкл супернатанта культуры (от клеток Expi293, трансфицированных экспрессирующим вектором в течение нескольких дней) или очищенных слитых белков. Клетки дважды промывали PBS, а затем связанный энхансер ADCC определяли с использованием коммерчески доступного флуоресцентно меченого антитела против CD64 (фиг. 10). Как показано на фиг. 11, осуществляли титрование связывания с клетками Jurkat, и результаты свидетельствуют о корреляции между связыванием и концентрацией энхансера.
[00091] При использовании меченого белка аффинность связывания также можно определять с помощью флуоресцентно меченого антитела против метки. Этот подход также можно использовать для детекции связывания домена CD64 покрытыми ритуксимабом CD20+ клетками Дауди (см. фиг. 12). В кратком изложении, 106 клеток Дауди собирали, промывали PBS и инкубировали в течение 30 минут при 4°C с 0,1 мкг/мл ритуксимаба (антитела против CD20, также известного как ритуксан, мабтера и Zytux). Клетки снова промывали PBS, а затем инкубировали с супернатантом или очищенным белком, как описано выше (фиг. 13). Как показано на фиг. 14, осуществляли титрование связывания с клетками Дауди, и результаты свидетельствовали о существенной корреляции между связыванием и концентрацией энхансера. Фактически, связывание Fc или антитела адаптер-подобным энхансером ADCC, по-видимому, является приблизительно в 30 более высоким, чем связывание CD3 с другого конца энхансера.
[00092] В альтернативных вариантах осуществления исследовали гетерологичную агрегацию между покрытыми ритуксимабом клетками Дауди и клетками Jurkat в системах совместных культур как признак аффинностей связывания. Клетки Дауди и клетки Jurkat соответствующим образом метили витальными красителями, такими как CFSE или CellTrace Far Red, общепринятыми способами и/или конструировали для экспрессии флуоресцентных белков, таких как GFP. Затем клетки инкубировали с ритуксимабом и растворимым энхансером ADCC по настоящему изобретению. Данные FACS исследовали на предмет дуплетов, положительных по обоим цветам. Как понятно специалисту в этой области, выбор линий клеток в вариантах осуществления, представленных в настоящем описании, не ограничен клетками Jurkat и клетками Дауди, настоящее изобретение относится к применению различных линий клеток или первичных клеток в комбинации с подходящими антителами.
[00093] Способность слитого белка CD64-antiCD3 связываться с Fc и CD3 также можно тестировать с помощью поверхностного плазмонного резонанса или других стандартных биохимических или клеточных анализов.
(4) Усиление цитотоксичности
[00094] Наивные первичные CD8+ T-клетки выделяли из донорской крови общепринятым способом, например, с использованием набора RosetteSep CD8 T Cell Enrichment Kit (Stem Cell Technology) с последующей экспансией против CD3/CD28. Альтернативно, аналогичные эксперименты можно осуществлять с использованием тотальных T-клеток или PBMC. Используя любые из этих клеток, тестировали способность энхансера по изобретению вызывать активацию, пролиферацию и запускать цитотоксичность, в частности, ADCC. В частности, пролиферацию T-клеток можно измерять с помощью проточной цитометрии или других общепринятых способов, например, включения тимидиновой метки, разведения CFSE и т.д. Активацию можно измерять посредством детекции множества известных маркеров активации, например, HLA-DR, CD25, CD69 и т.д. Как правило, в случае этих экспериментов энхансер может функционировать самостоятельно, но дополнительные эксперименты осуществляли с:
[00095] (A) 50 МЕ/мл ИЛ-2;
[00096] (B) клетками-мишенями; и/или
[00097] (C) соответствующими антителами;
или без них.
[00098] При включении клеток-мишеней, их можно предварительно обрабатывать митомицином C для прекращения пролиферации и минимизации эффектов перенасыщения. Кроме того, лизосомально-ассоциированный мембранный белок-1 (LAMP-1 или CD107a) описан в качестве маркера дегрануляции CD8+ T-клетками и NK-клетками литических гранул после стимуляции. Таким образом, В описываемых выше экспериментах по сокультивированию, можно анализировать уровень CD107a+ T-клеток в качестве показателя дегрануляции посредством проточной цитометрии.
[00099] Для оценки цитотоксичности T-клетки сокультивировали в течение одного или двух дней с мечеными CellTrace клетками-мишенями в присутствие соответствующего терапевтического антитела. Результаты и условия нескольких примеров представлены на фигурах 15-23, и свидетельствуют об исключительной способности адаптер-подобного энхансера запускать, усиливать или увеличивать антитело-зависимую цитотоксичность против множества злокачественных клеток. Данные, представленные на этих фигурах, включают эффективный цитолиз B-лимфобластных клеток (Дауди и Раджи), злокачественных клеток молочной железы (SK-BR3 и MDA-MB-231) и клеток, экспрессирующих PD-1 (293-PD1).
[000100] Например, данные и механизмы, представленные на фиг. 15 и 16 свидетельствуют о том, что энхансер по изобретению способен уничтожать значительную часть популяции CD20+ клеток Дауди в присутствие ритуксана посредством рекрутирования T-клеток для осуществления ADCC. В качестве другого примера, данные, представленные на фиг. 19, свидетельствуют о том, что энхансер по изобретению запускает способность герцептина, антитела, сконструированного против рецепторов HER2 на злокачественных клетках молочной железы, к уничтожению злокачественных клеток молочной железы SK-BR3, предположительно, т.к. T-клетки рекрутировались энхансером для усиления ADCC.
[000101] Можно осуществлять дополнительное тестирование с использованием других антител на других линиях злокачественных клеток и в других условиях, например: (a) CD33+ линиях AML (например HL-60, MOLM-13 и THP-1), обработанных антителом против CD33 (WM-53); (b) CD19+ линиях (например, NALM-6 и MEC-1), обработанных антителом против CD19 (HIB19); и (c) EpCAM+ линиях (например SW480), обработанных против антителом EpCAM (HEA-125).
[000102] Что касается фиг. 23, эксперименты по цитотоксичности включали использование ниволумаба (антитела против PD1), клеток HEK-293T (эмбриональных клеток почки человека, экспрессирующих крупный антиген T), трансгенно экспрессирующих PD1 ("293T-PD1"), CD8+ T-клеток, и энхансера по изобретению. Родительские немодифицированные клетки HEK-293T ("293T"), а также контрольный IgG4 включали в качестве контролей. Ниволумаб разрабатывали в качестве антитела IgG4 таким образом, что он не имеет какой-либо активности ADCC. Однако последующие эксперименты показали, что ADCC и антитела против PD1 могут лучше действовать совместно. В отличие от CD16, CD64 обладает способностью связываться с IgG4 и преобразовывать исходно ADCC-отрицательные, антитела, такие как ниволумаб, в ADCC-положительные антитела для рекрутирования дополнительной поддержки со стороны других иммунных эффекторных клеток, таких как T-клетки. Как показано на фигуре, сам по себе ниволумаб, даже при повышении его концентрации в 10 раз, все равно обладает лишь ограниченной способностью к цитолизу в отношении клеток-мишеней 293T-PD1, при этом наблюдают приблизительно 75% выживаемости мишеней. Однако при добавлении адаптер-подобного энхансера по изобретению в смесь коэффициент выживаемости клетки-мишени уменьшался до менее 5%. Это представляет собой основу для перспективного терапевтического применения энхансера по изобретению в комбинации или соединении с антителами IgG4 или другими иммунными эффекторными клетками, в ином случае не обладающими способностью к ADCC.
[000103] Данные, представленные в настоящем описании, подтверждают возможность применения адаптер-подобного энхансера ADCC с антителами, такими как ритуксан и герцептин, для усиления их функции, для снижения дозы антител, снижения побочных эффектов и ответа против антитела.
[000104] Это работает не только при лечении злокачественного новообразования, но также и аутоиммунных заболеваний. Например, в случае ритуксана или ритуксимаба получали смешанные результаты при лечении пациентов с аутоиммунными заболеваниями: он хорошо действует при RA, но лишь незначительно при SLE. Одной из причин этого является то, что опосредованное макрофагами истощение B-клеток у пациеок на T-клетки с использованием энхансера ADCC в качестве T-клеточного адаптера позволит преодолеть эту проблему.
[000105] Кроме того, энхансер можно использовать для пациентов с низкоаффинной версией CD16 (158F), или пациентов, у которых ADCC/CDC каким-либо образом супрессирована, например, пациентов с хроническим лимфоцитарным лейкозом (CLL) и других пациентов, подвергаемых лечению злокачественных опухолей.
[000106] Существует множество антител, в случае которых роль ADCC непонятна до их использования в клинической практике, например, трастузумаба, антитела против PD-1, против PD-L1, против CTLA4 и т.д. Многие из этих антител являются антителами IgG4. Как описано выше, CD64-часть энхансера может связываться с IgG4 и преобразовывать исходно ADCC-отрицательные антитела в ADCC-положительные антитела.
[000107] Специалистам в этой области очевидно, что можно осуществлять различные модификации и варианты настоящего изобретения без отклонения от объема или сущности изобретения. Другие варианты осуществления изобретения будут очевидны специалистам в этой области при прочтении описания и практическом осуществлении представленного в настоящем описании изобретения. Следует понимать, что описание и примеры представлены исключительно в иллюстративных целях, при этом объем и сущность изобретения указаны в представленной ниже формуле изобретения.
[000108] На всем протяжении настоящей заявки различные публикации, патенты и/или патентные заявки процитированы для более полного описания уровня техники в той области, к которой относится изобретение. Описания этих публикаций, патентов и/или патентных заявок включено в настоящее описание в качестве ссылки в полном объеме в той же степени, как если бы каждая независимая публикация, патент и/или патентная заявка была конкретно и отдельно включена в качестве ссылок.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> 1GLOBE HEALTH INSTITUTE LLC
LI, Chiang J.
UNNIRAMAN, Shyam
<120> РАСТВОРИМЫЙ УНИВЕРСАЛЬНЫЙ УСИЛИВАЮЩИЙ ADCC СИНТЕТИЧЕСКИЙ СЛИТЫЙ ГЕН, ПЕПТИДНАЯ ТЕХНОЛОГИЯ И ИХ ПРИМЕНЕНИЕ
<130> GHI-003PCT1
<140> PCT/US 15/064572
<141> 2015-12-08
<150> US 62/089,097
<151> 2014-12-08
<150> US 62/200,557
<151> 2015-08-03
<160> 4
<170> PatentIn version 3.5
<210> 1
<211> 281
<212> Белок
<213> Homo sapiens
<400> 1
Met Trp Phe Leu Thr Thr Leu Leu Leu Trp Val Pro Val Asp Gly Gln
1 5 10 15
Val Asp Thr Thr Lys Ala Val Ile Thr Leu Gln Pro Pro Trp Val Ser
20 25 30
Val Phe Gln Glu Glu Thr Val Thr Leu His Cys Glu Val Leu His Leu
35 40 45
Pro Gly Ser Ser Ser Thr Gln Trp Phe Leu Asn Gly Thr Ala Thr Gln
50 55 60
Thr Ser Thr Pro Ser Tyr Arg Ile Thr Ser Ala Ser Val Asn Asp Ser
65 70 75 80
Gly Glu Tyr Arg Cys Gln Arg Gly Leu Ser Gly Arg Ser Asp Pro Ile
85 90 95
Gln Leu Glu Ile His Arg Gly Trp Leu Leu Leu Gln Val Ser Ser Arg
100 105 110
Val Phe Thr Glu Gly Glu Pro Leu Ala Leu Arg Cys His Ala Trp Lys
115 120 125
Asp Lys Leu Val Tyr Asn Val Leu Tyr Tyr Arg Asn Gly Lys Ala Phe
130 135 140
Lys Phe Phe His Trp Asn Ser Asn Leu Thr Ile Leu Lys Thr Asn Ile
145 150 155 160
Ser His Asn Gly Thr Tyr His Cys Ser Gly Met Gly Lys His Arg Tyr
165 170 175
Thr Ser Ala Gly Ile Ser Val Thr Val Lys Glu Leu Phe Pro Ala Pro
180 185 190
Val Leu Asn Ala Ser Val Thr Ser Pro Leu Leu Glu Gly Asn Leu Val
195 200 205
Thr Leu Ser Cys Glu Thr Lys Leu Leu Leu Gln Arg Pro Gly Leu Gln
210 215 220
Leu Tyr Phe Ser Phe Tyr Met Gly Ser Lys Thr Leu Arg Gly Arg Asn
225 230 235 240
Thr Ser Ser Glu Tyr Gln Ile Leu Thr Ala Arg Arg Glu Asp Ser Gly
245 250 255
Leu Tyr Trp Cys Glu Ala Ala Thr Glu Asp Gly Asn Val Leu Lys Arg
260 265 270
Ser Pro Glu Leu Glu Leu Gln Val Leu
275 280
<210> 2
<211> 250
<212> Белок
<213> Искусственная
<220>
<223> Линкерные последовательности с гуманизированной последовательностью OKT3
<400> 2
Ser Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Gly
1 5 10 15
Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Lys Ser Ser
20 25 30
Gly Tyr Thr Phe Thr Arg Tyr Thr Met His Trp Val Arg Gln Ala Pro
35 40 45
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Ile Asn Pro Ser Arg Gly Tyr
50 55 60
Thr Asn Tyr Asn Gln Lys Val Lys Asp Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ser Lys Asn Thr Ala Phe Leu Gln Met Asp Ser Leu Arg Pro Glu
85 90 95
Asp Thr Gly Val Tyr Phe Cys Ala Arg Tyr Tyr Asp Asp His Tyr Cys
100 105 110
Leu Asp Tyr Trp Gly Gln Gly Thr Pro Val Thr Val Ser Ser Val Glu
115 120 125
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Val Asp
130 135 140
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
145 150 155 160
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
165 170 175
Asn Trp Tyr Gln Gln Thr Pro Gly Lys Ala Pro Lys Arg Trp Ile Tyr
180 185 190
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
195 200 205
Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro Glu
210 215 220
Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
225 230 235 240
Phe Gly Gln Gly Thr Lys Leu Gln Ile Thr
245 250
<210> 3
<211> 531
<212> Белок
<213> Искусственная
<220>
<223> Последовательность слитого белка для варианта осуществления «подобный адаптеру энхансер ADCC»
<400> 3
Met Trp Phe Leu Thr Thr Leu Leu Leu Trp Val Pro Val Asp Gly Gln
1 5 10 15
Val Asp Thr Thr Lys Ala Val Ile Thr Leu Gln Pro Pro Trp Val Ser
20 25 30
Val Phe Gln Glu Glu Thr Val Thr Leu His Cys Glu Val Leu His Leu
35 40 45
Pro Gly Ser Ser Ser Thr Gln Trp Phe Leu Asn Gly Thr Ala Thr Gln
50 55 60
Thr Ser Thr Pro Ser Tyr Arg Ile Thr Ser Ala Ser Val Asn Asp Ser
65 70 75 80
Gly Glu Tyr Arg Cys Gln Arg Gly Leu Ser Gly Arg Ser Asp Pro Ile
85 90 95
Gln Leu Glu Ile His Arg Gly Trp Leu Leu Leu Gln Val Ser Ser Arg
100 105 110
Val Phe Thr Glu Gly Glu Pro Leu Ala Leu Arg Cys His Ala Trp Lys
115 120 125
Asp Lys Leu Val Tyr Asn Val Leu Tyr Tyr Arg Asn Gly Lys Ala Phe
130 135 140
Lys Phe Phe His Trp Asn Ser Asn Leu Thr Ile Leu Lys Thr Asn Ile
145 150 155 160
Ser His Asn Gly Thr Tyr His Cys Ser Gly Met Gly Lys His Arg Tyr
165 170 175
Thr Ser Ala Gly Ile Ser Val Thr Val Lys Glu Leu Phe Pro Ala Pro
180 185 190
Val Leu Asn Ala Ser Val Thr Ser Pro Leu Leu Glu Gly Asn Leu Val
195 200 205
Thr Leu Ser Cys Glu Thr Lys Leu Leu Leu Gln Arg Pro Gly Leu Gln
210 215 220
Leu Tyr Phe Ser Phe Tyr Met Gly Ser Lys Thr Leu Arg Gly Arg Asn
225 230 235 240
Thr Ser Ser Glu Tyr Gln Ile Leu Thr Ala Arg Arg Glu Asp Ser Gly
245 250 255
Leu Tyr Trp Cys Glu Ala Ala Thr Glu Asp Gly Asn Val Leu Lys Arg
260 265 270
Ser Pro Glu Leu Glu Leu Gln Val Leu Ser Ser Gly Gly Gly Gly Ser
275 280 285
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
290 295 300
Ser Leu Arg Leu Ser Cys Lys Ser Ser Gly Tyr Thr Phe Thr Arg Tyr
305 310 315 320
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
325 330 335
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Val
340 345 350
Lys Asp Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Ala Phe
355 360 365
Leu Gln Met Asp Ser Leu Arg Pro Glu Asp Thr Gly Val Tyr Phe Cys
370 375 380
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
385 390 395 400
Thr Pro Val Thr Val Ser Ser Val Glu Gly Gly Ser Gly Gly Ser Gly
405 410 415
Gly Ser Gly Gly Ser Gly Gly Val Asp Asp Ile Gln Met Thr Gln Ser
420 425 430
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
435 440 445
Arg Ala Ser Ser Ser Val Ser Tyr Met Asn Trp Tyr Gln Gln Thr Pro
450 455 460
Gly Lys Ala Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys Val Ala Ser
465 470 475 480
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr
485 490 495
Phe Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys
500 505 510
Gln Gln Trp Ser Ser Asn Pro Leu Thr Phe Gly Gln Gly Thr Lys Leu
515 520 525
Gln Ile Thr
530
<210> 4
<211> 1596
<212> ДНК
<213> Искусственная
<220>
<223> Последовательность ДНК для варианта осуществления «слитый белок»
<400> 4
atgtggtttc tgactacact gctgctgtgg gtgcccgtgg atggacaggt ggatactaca 60
aaagccgtga ttacactgca gcccccttgg gtgtctgtct tccaggagga aaccgtgaca 120
ctgcactgcg aggtcctgca tctgccaggc agctcctcta cccagtggtt tctgaacgga 180
actgctaccc agacatctac tcccagttac cgcatcacaa gcgcatccgt gaatgacagc 240
ggcgagtatc gatgccagcg ggggctgtca ggtcgaagcg atccaatcca gctggaaatt 300
caccgggggt ggctgctgct gcaggtgagt tcaagggtct tcaccgaggg tgaacccctg 360
gcactgaggt gtcacgcctg gaaggacaaa ctggtgtaca acgtcctgta ctatagaaat 420
ggcaaggcct tcaagttctt tcattggaac agcaatctga ctatcctgaa gaccaacatt 480
tctcacaatg gaacctacca ttgcagcgga atggggaagc atcgctatac ttctgctggg 540
atcagtgtga ccgtcaaaga actgttccca gctcccgtgc tgaacgcatc cgtcacatct 600
cctctgctgg aggggaatct ggtgacactg tcctgtgaaa ctaagctgct gctgcagcgg 660
ccaggactgc agctgtactt ctccttttat atgggctcta aaaccctgag aggacgcaac 720
acaagctccg agtaccagat tctgactgcc cggagggaag acagcgggct gtattggtgc 780
gaggccgcta ccgaagatgg taatgtgctg aagaggtccc ccgagctgga actgcaggtg 840
ctgtctagtg gcggaggggg tagtcaggtg cagctggtcc agtccggagg aggagtggtc 900
cagcctggca ggtcactgag actgagctgt aagtcaagcg gatacacctt cacaagatat 960
actatgcact gggtgcgcca ggctcctggt aaaggactgg agtggatcgg gtacattaac 1020
cctagcagag gttacacaaa ctataatcag aaggtgaaag accgcttcac aatctcccga 1080
gataactcta aaaatactgc ctttctgcag atggactccc tgagacctga ggataccggc 1140
gtgtactttt gcgctcgcta ctatgacgat cattactgtc tggattattg gggacagggg 1200
accccagtga cagtctcctc tgtggaaggt ggcagtggag ggtcaggtgg cagcggaggg 1260
tccggtggag tggacgatat ccagatgacc cagtctccca gttcactgtc tgccagtgtg 1320
ggcgaccggg tcactattac ctgcagggct agctcctctg tgagctacat gaattggtat 1380
cagcagaccc ctggcaaggc accaaaacga tggatctacg ataccagtaa ggtggcctca 1440
ggagtcccaa gccggttctc aggtagcggc tccggaacag actatacctt caccatcagt 1500
tcactgcagc ctgaggatat tgccacttac tattgtcagc agtggagtag taatcctctg 1560
acattcggac agggaaccaa actgcagatc acataa 1596
<---
Реферат
Изобретение относится к области биотехнологии, конкретно к пептидным энхансерам антителозависимой клеточной цитотоксичности (ADCC), и может быть использовано в медицине для усиления ADCC в комбинации с терапевтическим антителом против антигена поверхности клетки, свидетельствующего о злокачественном новообразовании. Получают слитый белок, состоящий из высокоаффинного Fc-связывающего домена, высокоаффинного CD3-связывающего домена и гибкого серин-глицинового линкера. Настоящее изобретение обеспечивает повышение терапевтической эффективности антител за счет применения технологии растворимого универсального белка-энхансера ADCC (SUAEP), т.е. готового к использованию адаптер-подобного, растворимого универсального белка, усиливающего ADCC. 2 н. и 4 з.п. ф-лы, 23 ил., 4 пр.
Формула
Документы, цитированные в отчёте о поиске
Способ направления (индукции) иммунного ответа, днк, вектор, способ лечения

Комментарии