Новые производные арилимидазола, их препараты и их терапевтические применения - RU2323216C2
Код документа: RU2323216C2
Описание
Изобретение относится к новым производным арилимидазола, которые могут быть использованы в качестве ингибиторов NO синтазы (NOS) и в качестве модуляторов натриевых каналов.
Обусловлено потенциальной ролью NO и натриевых каналов в физиопатологии, новые производные, описанные в соответствии с общей формулой (I), описанные ниже, могут оказывать полезные или благоприятные эффекты:
• в лечении или предотвращении боли и в частности:
◆ нейропатической боли и в частности:
- нейропатической боли метаболического происхождения (такой как, например, диабетические нейропатии),
- нейропатической боли инфекционного происхождения, такой как таковая, связанная с вирусными или ретровирусными заболеваниями (такими как, например, боль, связанная с герпесом, такая как пост-герпетическая боль, боль, связанная с синдромом приобретенного иммунодефицита (СПИД), или боль, связанная с опоясывающим герпесом),
- нейропатическая боль травматического происхождения (такая как, например, таковая, связанная с фантомом конечности),
◆ языкоглоточная невралгия, вторичные метастатические инфильтрационные радикулопатии и нейропатии, ожирение болезненное и боль, связанная с ожогами,
◆ мигрень,
◆ послеоперационная боль,
◆ центральная боль в результате церебральных сосудистых случаев, повреждения таламуса или рассеянного склероза,
◆ хроническая боль и
◆ боль, связанная с раком;
◆ в лечении рассеянного склероза;
◆ в лечении расстройств центральной или периферической нервной системы и в частности:
◆ эпилепсии,
◆ нейродегенеративных заболеваний, из которых в частности может быть упомянуто старческое слабоумие, включая болезнь Альцгеймера, хорея Геттингтона, болезнь Паркинсона, амиотрофический боковой склероз, атаксия Фредерика и прионовые заболевания (в частности, болезнь Крейтцфельда-Якоба),
◆ ишемия головного мозга и травмы головного и спинного мозга,
◆ депрессия и биполярные расстройства,
◆ энцефалопатии, включая энцефалопатии вирусного или токсического происхождения,
◆ пристрастие к опиатам, алкоголю и вызывающим привыкание веществам,
◆ эректильные и репродуктивные расстройства,
◆ когнитивные расстройства,
◆ тревожность, шизофрения, расстройства сна и расстройства пищевого поведения (анорексия, булимия и др.);
• в лечении сердечно-сосудистых заболеваний, таких как инфаркт миокарда или нарушение сердечного ритма, в частности аритмии;
• в лечении расстройств скелетных мышц и нервно-мышечных соединений, таких как миопатии;
• в лечении воспалительных заболеваний, таких как, например, псориаз, артроз и ревматоидный артрит, воспаления желудочно-кишечной системы (колит, болезнь Крона) или легочной системы и дыхательных путей (астма, синусит, ринит), а также контактной или отложенной гиперчувствительности и, в частности, артроза и ревматоидного артрита;
• в лечении потери слуха травматического, акустического или токсического происхождения и звона в ушах,
• в лечении осложнений, связанных с аутоиммунными и вирусными заболеваниями, такими как, например, волчанка, СПИД, паразитарные и вирусные инфекции, осложнения диабета, включая ретинопатии, нефропатии и полинейропатии;
• в лечении неврологических заболеваний, связанных с интоксикацией (отравление кадмием, вдыхание н-гексана, пестициды, гербициды), с лечением (радиотерапия) или расстройства генетического происхождения (болезнь Вилсона);
• и чаще в лечении всех патологий, характеризующихся избыточной продукцией монооксида азота и/или дисфункцией натриевых каналов.
Заявитель описывал в заявке WO 01/26656 производные имидазола, которые могут модулировать натриевые каналы, а именно, соединения с общей формулой (А1)

в которой
А представляет собой (в частности) необязательно замещенный фенильный или бифенильный радикал;
В представляет собой (в частности), атом водорода или алкильный радикал;
Х представляет собой (в частности) NR38, R38 представляет собой в частности атом водорода или алкильный или аралкильный радикал;
n является целым числом от 0 до 6;
Ω представляет собой один из радикалов NR46R47 или OR48, в которых R46 и R47 представляют собой (в частности) независимо, атом водорода или алкильный, арильный, аралкильный, циклоалкильный или циклоалкилалкильный радикал и R48 представляет собой атом водорода или алкильный радикал.
Данные соединения, однако, не имеют какой-либо активности в отношении NOS, как таковая соединений по изобретению.
Более того, предметом заявки WO 95/05363 являются соединения, ингибирующие NOS с общей формулой (А2)
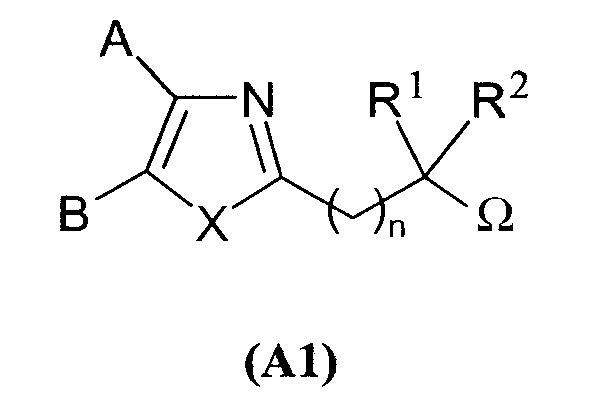
в которой:
D представляет собой фенил, пиридинил или ароматический гетероцикл с 5 членами, содержащими от 1 до 4 гетероатомов, выбираемых из О, N и S, данные три группы являются необязательно замещенными одной или более группами, выбираемыми из (С1-С6)алкила, (С1-С6)алкокси, галогена, (С1-С6)перфторалкила, или D представляет собой (С1 -С6)перфторалкил;
R1 представляет собой водород;
R2 представляет собой -Х(СН2)nZCONR3R4, -X(CH2)nNHCO(CH2)sNR3R4, -X(CH2)pNR3R4, -X(CH2)nNHCOR5 или -(CH2)qNHC(NH)R6,
R3 и R4 представляют независимо водород, (С1-С6)алкил, -(СН2)r-A, -(CH2)mOA или -CH(CH3)(CH2)tA;
или группа NR3R4 представляет собой 1-инданил, пиперониламино, пиперидинил, морфолинил, пирролидинил, 1,2,3,4-тетрагидроизохинолинил или пиперазинил, необязательно замещенные в положении 4 (С1-С6)алкилом;
R5 представляет собой (С1-С6)алкил, (С1-С6)перфторалкил, -(СН2)r-A или -O(CH2)wA;
А представляет собой фенил, пиридинил, пиримидинил или ароматический гетероцикл с 5 членами, содержащий от 1 до 4 гетероатомов, выбираемых из O, N и S, данные 4 группы необязательно замещенные одной или более группами, выбираемыми из (С1-С6)алкила, галогена, нитро, циано и трифторметила;
R6 представляет собой фенил, пиридинил или ароматический гетероцикл с 5 членами, содержащий от 1 до 4 гетероатомов, выбираемых из O, N и S, данные три группы, необязательно замещенные одной или более группами, выбираемыми из (С1-С6)алкила, (С1-С6 )алкокси, галогена, (С1-С6)перфторалкила, или R6 представляет собой (С1-С6)перфторалкил;
n и r представляют собой независимо целое число от 0 до 6;
р и w представляют собой независимо целое число от 1 до 5;
m представляет собой целое число от 2 до 5;
q и t представляют собой независимо целое число от 0 до 5;
s представляет собой целое число от 1 до 3;
Х представляет собой О или связь;
Z представляет собой О, NR7 или связь;
R7 представляет собой водород или (С1-С6)алкил;
понимают, что
(а) D, когда он содержит гетероатом, не связан с остатком соединения по формуле (А2) гетероатомом;
(b) когда R2 представляет собой -Х(СН2)nZCONR3R4 и ни Х ни Z не являются связью, тогда n представляет собой целое число от 2 до 6;
(с) когда R2 представляет собой -X(CH2)nNHCO(CH2)sNR3R4, или -X(CH2)nNHCOR5 и Х представляет собой О, тогда n представляет собой целое число от 2 до 6;
(d) когда R2 представляет собой -X(CH2)pNR3R4 и Х представляет собой О, тогда р представляет собой целое число от 2 до 5;
(е) когда R2 представляет собой -(CH2 )qNHC(NH)R6, R1 представляет собой водород, D представляет собой фенил и R6 представляет собой фенил, тогда q не является 0;
(f) когда R2 представляет собой -(CH2)qNHC(NH)R6, R1 представляет собой водород, D и R6 представляют собой 2-хлорфенил, тогда q не является 0;
(g) когда R2 представляет собой -(CH2)qNHC(NH)R6, R1 представляет собой водород, D и R6 представляют собой 3-пиридинил, тогда q не является 0; и
(h) когда R2 представляет собой -(CH2)qNHC(NH)R6, R1 представляет собой водород, D и R6 представляют собой 4-пиридинил, тогда q не является 0.
Однако не было описано активности по отношению натриевых каналов для соединений с общей формулой (А2).
Заявитель к настоящему времени разработал новый класс производных арилимидазола, которые соответствуют общей формуле (I)

в которой
R1 представляет собой атом водорода или алкильный, циклоалкильный, циклоалкилалкильный радикал или также один из арильного или аралкильного радикалов, ароматический цикл которых необязательно замещен от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
R2 представляет собой атом водорода или алкильный радикал;
R3 представляет собой атом водорода или алкильный или аралкильный радикал;
Х представляет собой связь или линейный или разветвленный алкиленовый радикал, содержащий от 1 до 5 атомов углерода;
Y представляет собой атом водорода, циклоалкильный радикал, NR4R5, OR14 или SR15 радикал или
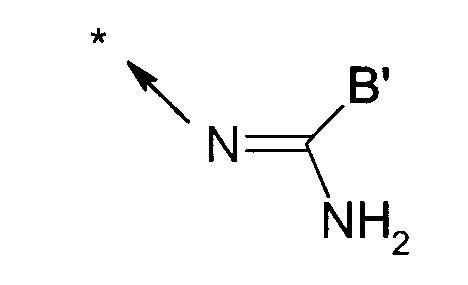
радикал, или также Y представляет собой арильный радикал, необязательно замещенный от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
А представляет собой связь или фениленовый радикал;
В и В' выбирают независимо из алкильного радикала, циклоалкильного радикала, NR6R7 или SR8 радикала, карбоциклического арильного радикала или гетероциклического арильного радикала с 5 или 6 членами, содержащими от 1 до 4 гетероатомов, выбираемых из O, S и N (в частности, тиофеновый, фурановый, пиррольный или тиазоловый радикалы и, в частности, 2-тиениловый радикал), указанные карбоциклические и гетероциклические арильные радикалы, необязательно замещенные одной - тремя группами, выбираемыми независимо из алкильного, алкенильного или алкокси радикалов (и, в частности, радикала, выбираемого из метилового и метокси радикалов),
R4 представляет собой атом водорода или алкильный, циклоалкильный, циклоалкилалкильный, -С(О)R9, -С(О)OR9, -С(О)NHR9 или -SO2R9 радикал или также один или арильный или аралкильный радикал, ароматический цикл которых необязательно замещен от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала, или R4 представляет собой бис-фенилалкильный радикал,
R5 представляет собой атом водорода или алкильный, арильный или аралкильный радикал,
или также R4 и R5 образуют с атомом азота, который их несет, неароматический гетероцикл с пятью или семью членами, содержащий 1-2 гетероатома, элементы для завершения гетероцикла независимо выбирают из группы, содержащей -CHR10-, -NR11-, -O- и -S-;
R6 и R7 представляют собой независимо атом водорода или алкильный, алкенильный или алкинильный радикал,
или R6 представляет собой нитро радикал и R7 представляет собой атом водорода,
или также R6 и R7 образуют с атомом азота, который их несет, неароматический гетероцикл с пятью-шестью членами, элементы для завершения гетероцикла выбирают независимо из группы, содержащей -СН2-, -NR12-, -O- и -S-;
R8 представляет собой линейный или разветвленный алкильный радикал, имеющий от 1 до 6 атомов углерода, необязательно замещенный от одного до 3 раз (и, в частности, от одного до двух) одним или более заместителями, выбираемыми независимо из атома галогена и -ОН, амино, циано и арильного радикалов;
R9 представляет собой алкильный, галоалкильный, циклоалкильный или циклоалкилалкильный радикал или также один из карбоциклического или гетероциклического аралкильного или арильного радикалов, ароматический цикл которых независимо замещен от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
R10 представляет собой атом водорода или алкильный или арильный радикал, необязательно замещенный от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома водорода и алкильного или алкокси радикала (R10 предпочтительно выбирают из атома водорода или метилового или фенильного радикала),
R11 представляет собой атом водорода, алкильный радикал, циклоалкильный радикал, циклоалкилалкильный радикал, -С(О)R13 радикал, -С(О)OR13 радикал, -SO2R13 радикал, -С(О)NHR13 радикал или также один из арильного или аралкильного радикалов, ароматический цикл которых необязательно замещен от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
R12 представляет собой атом водорода или алкильный радикал;
R13 представляет собой алкильный радикал, галоалкильный радикал или также один из карбоциклического или гетероциклического аралкильного или арильного радикалов, ароматический цикл которых необязательно замещен от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
R14 представляет собой алкильный радикал, фенильный радикал или аралкильный радикал; и наконец
R15 представляет собой алкильный радикал, фенильный радикал или аралкильный радикал;
или фармацевтически приемлемые соли соединений общей формулы (I).
Указанные соединения общей формулы (I) или их фармацевтически приемлемые соли могут быть использованы для получения лекарственного средства, предназначенного для ингибирования NOS и для модулирования натриевых каналов.
В частности, соединения общей формулы (I) или фармацевтически приемлемые соли соединений общей формулы (I) являются соединениями общей формулы (I')
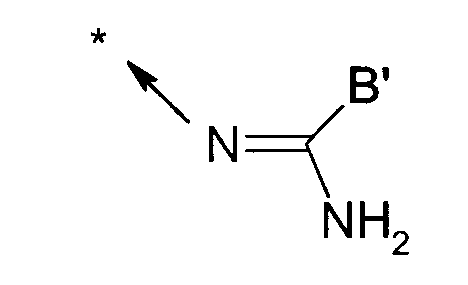
в которой
R1 представляет собой атом водорода или алкильный, циклоалкильный, циклоалкилалкильный радикал или также один из арильного или аралкильного радикалов, ароматический цикл которых необязательно замещен от одного до 3 раз (и в частности от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
R2 представляет собой атом водорода или алкильный радикал;
R3 представляет собой атом водорода или алкильный или аралкильный радикал;
Х представляет собой связь или линейный или разветвленный алкиленовый радикал, содержащий от 1 до 5 атомов углерода;
Y представляет собой атом водорода, циклоалкильный радикал, NR4R5 или

радикал, или также Y представляет собой арильный радикал, необязательно замещенный от одного до 3 раз (и, в частности, от одного до двух раз) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
А представляет собой связь или фениленовый радикал;
В и В' выбирают независимо из алкильного радикала, циклоалкильного радикала, NR6R7 или SR8 радикала, карбоциклического арильного радикала или гетероциклического арильного радикала с 5 или 6 членами, содержащими от 1 до 4 гетероатомов, выбираемых из O, S и N (в частности, тиофеновый, фурановый, пирроловый или тиазоловый радикалы и в частности, 2-тиениловый радикал), указанные карбоциклические и гетероциклические арильные радикалы необязательно замещены одной или тремя группами, выбираемыми независимо из алкильного, алкенильного или алкокси радикалов (и, в частности, радикала, выбираемого из метилового и метокси радикалов),
R4 представляет собой атом водорода или алкильный, циклоалкильный, циклоалкилалкильный, -С(О)R9, -С(О)OR9, -С(О)NHR9 или -SO2R9 радикалов или также один из или арильного или аралкильного радикалов, ароматический цикл которых необязательно замещен от одного до 3 раз (и, в частности, от одного до двух раз) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала,
R5 представляет собой атом водорода или алкильный, арильный или аралкильный радикал,
или также R4 и R5 образуют с атомом азота, который их несет, неароматический гетероцикл с пятью-семью членами, содержащий 1-2 гетероатома, элементы для завершения гетероцикла независимо выбирают из группы, содержащей -CHR10-, -NR11-, -O- и -S-;
R6 и R7 представляют собой независимо атом водорода или алкильный, алкенильный или алкинильный радикал,
или R6 представляет собой нитро радикал и R7 представляет собой атом водорода,
или также R6 и R7 образуют с атомом азота, который их несет, неароматический гетероцикл с пятью-шестью членами, элементы для завершения гетероцикла выбирают независимо из группы, содержащей -СН2-, -NR12-, -O- и -S-;
R8 представляет собой линейный или разветвленный алкильный радикал, имеющий от 1 до 6 атомов углерода, необязательно замещенный от одного до 3 раз (и в частности, от одного до двух) одним или более заместителями, выбираемыми независимо из атома галогена и -ОН, амино, циано и арильного радикалов;
R9 представляет собой алкильный, галоалкильный, циклоалкильный или циклоалкилалкильный радикал или также один из карбоциклического или гетероциклического аралкильного или арильного радикалов, ароматический цикл которых необязательно замещен от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
R10 представляет собой атом водорода или алкильный или арильный радикал, необязательно замещенный от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала (R10 предпочтительно выбирают из атома водорода или метилового или фенильного радикала),
R11 представляет собой атом водорода, алкильный радикал, циклоалкильный радикал, циклоалкилалкильный радикал, -С(О)R13 радикал, -С(О)OR13 радикал, -SO2R13 радикал, -С(О)NHR13 радикал или также один из арильного или аралкильного радикалов, ароматический цикл которых необязательно замещен от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
R12 представляет собой атом водорода или алкильный радикал; и наконец
R13 представляет собой алкильный радикал, галоалкильный радикал или также один из карбоциклического или гетероциклического аралкильного или арильного радикалов, ароматический цикл которых необязательно замещен от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикала;
или фармацевтически приемлемые соли соединений общей формулы (I').
Под алкилом, если не указано иначе, обозначают линейный или разветвленный алкильный радикал, содержащий от 1 до 12 атомов углерода, предпочтительно от 1 до 8 атомов углерода и еще более предпочтительно от 1 до 6 атомов углерода. Под циклоалкилом, если не указано иначе, обозначают циклоалкильный радикал, содержащий от 3 до 7 атомов углерода. Под алкокси, если не указано иначе, обозначают алкокси радикал, углеродная цепь которого является линейной или разветвленной и включает от 1 до 6 атомов углерода. Под алкенилом, если не указано иначе, обозначают линейный или разветвленный углеводородный радикал, содержащий от 2 до 6 атомов углерода и, по меньшей мере, одну двойную связь. Под алкинилом, если не указано иначе, обозначают линейный или разветвленный углеводородный радикал, содержащий от 2 до 6 атомов углерода и, по меньшей мере, одну тройную связь. Под галоалкилом обозначают алкильный радикал, по меньшей мере, один (и необязательно все) атомы водорода которого замещены атомом галогена. Под галоалкокси обозначают алкокси радикал, по меньшей мере, один (и необязательно все) атомы водорода которого замещены атомом галогена. Карбоциклическим или гетероциклическим арилом, если не указано иначе, обозначают карбоциклическую или гетероциклическую систему, включающую от одного до трех конденсированных циклов, по меньшей мере, один из которых является ароматическим циклом и все являются циклами с 5-7 членами, система называется гетероциклической, когда, по меньшей мере, один из циклов, которые ее составляют, включает один или более гетероатомов (O, N или S). Арилом, если не указано иначе, обозначают карбоциклический арильный радикал. Наконец атомом галогена обозначают атом, выбираемый из атомов фтора, хлора, брома и йода.
Циклоалкилалкильный, аралкильный, алкоксикарбонильный, галоалкоксикарбонильный или аралкоксикарбонильный радикалы обозначают соответственно циклоалкилалкильный, аралкильный, алкоксикарбонильный, галоалкоксикарбонильный или аралкоксикарбонильный радикалы, в которых алкильный, алкокси, галоалкильный, циклоалкильный и арильный радикалы, которые их составляют, имеют значения, указанные ранее.
Линейным или разветвленным алкилом, имеющим от 1 до 6 атомов углерода, обозначают, в частности, метиловый, этиловый, пропиловый, изопропиловый, бутиловый, изобутиловый, втор-бутиловый и трет-бутиловый, пентиловый, неопентиловый, изопентиловый, гексиловый, изогексиловый радикалы. Циклоалкилом обозначают, в частности, циклопропиловый, циклобутиловый, циклопентиловый и циклогексиловый радикалы. Алкокси обозначают предпочтительно метокси, этокси, пропокси, изопропокси, изобутокси, втор-бутокси и трет-бутокси радикалы и более предпочтительно метокси и этокси радикалы. Галоалкилом обозначают, в частности, трифторметиловый радикал. Галоалкокси обозначают, в частности, трифторметокси радикал. Карбоциклическим арилом обозначают, в частности, фениловый, нафтиловый и фенантриловый радикалы, предпочтительно, фениловый и нафтиловый радикалы и более предпочтительно фениловый радикал. Гетероциклическим арилом обозначают, в частности, пирролиловый, фураниловый, тиениловый, пиридиловый, пиримидиниловый, триазиниловый, имидазолиловый, оксазолиловый, тиазолиловый, индолиловый и хинолиловый радикалы. Аралкилом обозначают, в частности, феналкильный радикал и предпочтительно бензиловый радикал.
Фармацевтически приемлемыми солями обозначают, в частности, аддитивные соли с неорганическими кислотами, такие как гидрохлорид, гидробромид, гидройодид, сульфат, фосфат, дифосфат и нитрат, или с органическими кислотами, такие как ацетат, малеат, фумарат, тартрат, сукцинат, цитрат, лактат, метансульфонат, п-толуолсульфонат, памоат и стеарат. Для других примеров фармацевтически приемлемых солей могут быть сделаны ссылки на «Salt selection for basic drugs», Int. J. Pharm. (1986), 33, 201-217.
Кроме того, когда существует стрелка, выходящая из химической структуры, показывающая на звездочку (*), указанная стрелка показывает точку крепления. Например:
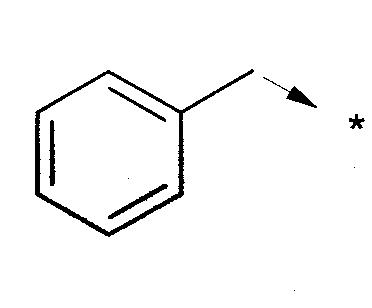
Как правило, случай, в котором А представляет собой связь, является предпочтительным. Подобно соединения, в которых R3 представляет собой атом водорода или метиловый или бензиловый радикал (и, в частности, соединения, в которых R3 представляет собой атом водорода), являются, как правило, предпочтительными.
Предпочтительно, кроме того, чтобы соединения с общей формулой (I) по изобретению являлись таковыми, что они включают, по меньшей мере, одну из следующих характеристик:
- Х представляет собой связь или линейный или разветвленный алкиленовый радикал, содержащий от 1 до 5 атомов углерода (и предпочтительно от 1 до 3 атомов углерода) и Y представляет собой NR4R5 радикал;
- Х представляет собой связь или линейный или разветвленный алкиленовый радикал, содержащий от 1 до 5 атомов углерода (и предпочтительно от 1 до 3 атомов углерода) и Y представляет собой

радикал;
- Х представляет собой связь или линейный или разветвленный алкиленовый радикал, содержащий от 1 до 5 атомов углерода (и предпочтительно от 1 до 3 атомов углерода) и Y представляет собой циклоалкильный радикал или арильный радикал, необязательно замещенный от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атомов галогена и алкильного или алкокси радикала;
- Х представляет собой связь и Y представляет собой атом водорода, при, по меньшей мере, одном из R1 и R2, представляющем собой радикал, выбираемый из алкильного, циклоалкильного или циклоалкилалкильного радикалов.
В соответствии с одним из предпочтительных вариантов, а именно, когда Х представляет собой связь или линейный или разветвленный алкиленовый радикал, содержащий от 1 до 5 атомов углерода (и предпочтительно от 1 до 3 атомов углерода и еще более предпочтительно от 1 до 2 атомов углерода), и Y представляет собой NR4 R5 радикал, является более того предпочтительным для соединений с общей формулой (I) по изобретению, быть таковыми, чтобы они включали по меньшей мере одну из следующих характеристик:
- R4 представляет собой алкильный, циклоалкильный, циклоалкилалкильный радикал или также один из арильного или аралкильного радикалов, ароматический цикл которых необязательно замещен от одного до 3 раз заместителями, выбираемыми независимо из атома галогена и алкильного или алкокси радикалов (R4 также представляет более предпочтительно радикал, выбираемый из алкильного и циклоалкильного радикалов и еще более предпочтительно циклоалкильный радикал) и R5 представляет собой атом водорода или алкильный радикал (и более предпочтительно атом водорода или метиловый радикал);
- R4 представляет собой -С(О)R9, -C(O)OR9, -C(O)NHR9 или SO2R9 радикал (и совершенно особенно -C(O)OR9 радикал) и R5 представляет собой атом водорода или метиловый или этиловый радикал (и предпочтительно атом водорода или метиловый радикал).
В соответствии с другим предпочтительным вариантом, а именно, когда Х представляет собой связь или линейный или разветвленный алкиленовый радикал, содержащий от 1 до 5 атомов углерода (и предпочтительно от 1 до 3 атомов углерода), и Y представляет собой

радикал,
является более того предпочтительным для соединений с общей формулой (I) по изобретению быть такими, что они включают, по меньшей мере, одну из следующих характеристик:
- Х представляет собой связь или -СН2- или -(СН2)2- радикал;
- R1 и R2 представляют собой атомы водорода.
Еще в соответствии с одним из предпочтительных вариантов, а именно, когда Х представляет собой связь или линейный или разветвленный алкиленовый радикал, содержащий от 1 до 5 атомов углерода (и предпочтительно от 1 до 3 атомов углерода) и Y представляет собой циклоалкильный радикал или арильный радикал, необязательно замещенный от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атомов галогена и алкильного или алкокси радикала, является более того предпочтительным для соединений с общей формулой (I) по изобретению быть таковыми, чтобы они включали, по меньшей мере, одну из следующих характеристик:
- Y является циклогексильным радикалом;
- Y является фенильным радикалом, необязательно замещенным от одного до 3 раз (и, в частности, от одного до двух) заместителями, выбираемыми независимо из атомов галогена и алкильного или алкокси радикала (и предпочтительно из атома галогена и метилового или метокси радикала);
- R1 и R2, представляющие собой атомы водорода.
В соответствии со следующим предпочтительным вариантом, а именно, когда Х представляет собой связь и Y представляет собой атом водорода, тогда как, по меньшей мере, один из R1 и R2 представляют собой радикал, выбираемый из алкильного, циклоалкильного или циклоалкилалкильного радикалов, является более того предпочтительным для соединений с общей формулой (I) по изобретению быть таковыми, чтобы они включали по меньшей мере одну из следующих характеристик:
- по меньшей мере, один из R1 и R2 представляет собой алкильный радикал, включающий, по меньшей мере, 4 атома углерода, тогда как другой представляет собой атом водорода;
- R1 и R2 оба представляют собой алкильные радикалы, включающие, по меньшей мере, 3 атома углерода каждый;
- R1 представляет собой циклоакильный или циклоалкилалкильный радикал и R2 затем предпочтительно представляет собой атом водорода или метиловый радикал (и более предпочтительно атом водорода).
Обычно соединения общей формулы (I) являются предпочтительными, в которых В представляет собой циклоалкильный радикал (в частности, циклопропиловый радикал), карбоциклический арильный радикал (в частности, фенильный радикал), гетероциклический арильный радикал с 5 членами, содержащий от 1 до 2 гетероатомов, выбираемых из O, S и N (в частности, тиофеновый, фурановый, пирроловый или тиазоловый радикалы и, в частности, 2-тиениловый радикал) или также NH-NO2 радикал.
Соединения общей формулы (I) являются особенно предпочтительными, в которых В представляет собой гетероциклический арильный радикал с 5 членами, содержащими от 1 до 2 гетероатомов, выбираемых из O, S и N (в частности, тиофеновый, фурановый, пирроловый или тиазоловый радикалы и, в частности, 2-тиениловый радикал), или NH-NO2 радикал. Соединения общей формулы (I) также являются особенно более предпочтительными, в которых В представляет собой 2-тиениловый радикал или NH-NO2 радикал. Такие же предпочтения являются подходящими с соответствующими изменениями к В', когда данный радикал присутствует в соединениях общей формулы (I).
Также обычно, когда R4 и R5 формируют с атомом азота, который их несет, неароматический гетероцикл с пятью-семью членами, содержащий от 1 до 2 гетероатомов, элементы для завершения гетероцикла выбирают независимо из группы, включающей -CHR10-, -NR11-, -O- и -S-, образующийся гетероцикл (который является необязательно замещенным R10 и R11радикалами) предпочтительно выбирают из группы, включающей пирролидиновый, пиперидиновый, пиперазиновый, морфолиновый, тиоморфолиновый, азепиновый и гомопиперазиновый циклы и более предпочтительно из группы, включающей пирролидиновый, пиперидиновый, пиперазиновый, морфолиновый и тиоморфолиновый циклы.
Более того, R13 предпочтительно представляет собой алкильный радикал или галоалкильный радикал.
Более того, R15 предпочтительно представляет собой фенильный радикал, как R14.
В частности, соединение относится к следующим соединениям с общей формулой (I), описанным далее в виде примеров (иногда в форме солей):
- бутил-2-[4-(4-{[(1Z)-амино(тиен-2-ил)метилен]амино}фенил)-1Н-имидазол-2-ил]этилкарбамат;
- бутил-2-[4-(3-{[(1Е)-амино(тиен-2-ил)метилен]амино}фенил)-1Н-имидазол-2-ил]этилкарбамат;
- бутил-2-[4-(4'-{[(1Z)-амино(тиен-2-ил)метилен]амино}-1,1'-бифенил-4-ил)-1Н-имидазол-2-ил]этилкарбамат;
- N'-(4-{2-[(циклогексиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-(4-{2-[2-(циклогексиламино)этил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-(3-{2-[(циклогексиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-[4-(2-{[циклогексил(метил)амино]метил}-1Н-имидазол-4-ил)фенил]тиофен-2-карбоксимидамид;
- N'-(4-{2-[(дибензиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-(4-{2-[(бензиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-{3-[2-(аминометил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
- N'-{3-[2-({[(1Е)-амино(тиен-2-ил)метилен]амино}метил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
- N'-{4-[2-({[(1Е)-амино(тиен-2-ил)метилен]амино}метил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
- N-{3-[2-(2-циклогексилэтил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
- N'-{3-[2-(1-пентилгексил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
- N'-{4-[2-(2-циклогексилэтил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
- N'-{3-[2-(циклогексилметил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
- N'-{3-[2-(3-циклогексилпропил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
- N'-[3-(2-гексил-1Н-имидазол-4-ил)фенил]тиофен-2-карбоксимидамид;
- N-{4-[2-(2-циклогексилэтил)-1Н-имидазол-4-ил]фенил}-N"-нитрогуанидин;
- N'-(4-{2-[(циклогептиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-(4-{2-[(метиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-(4-{2-[(циклобутиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-[4-(2-{[(2,2-дифенилэтил)амино]метил}-1Н-имидазол-4-ил]фенил)тиофен-2-карбоксимидамид;
- N'-{3-[2-(2-{[(1Е)-амино(тиен-2-ил)метилен]амино}этил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
- N'-(3-{2-[(фенилтио)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-(4-{2-[(фенилтио)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид;
- N'-{3-[2-(4-изобутилбензил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид;
и соли последнего.
Изобретение также относится к лекарственным средствам, соединениям с общей формулой (I), как определено ранее, или фармацевтически приемлемым солям таких соединений. Также оно относится к фармацевтическим композициям, содержащим, в качестве активного ингредиента, соединения с общей формулой (I), как определено ранее, или фармацевтически приемлемые соли таких соединений, с фармацевтически приемлемым вспомогательным веществом или вспомогательными веществами.
Более того, целью изобретения также является применение соединений с общей формулой (I), как определено ранее, или фармацевтически приемлемые соли таких соединений для получения лекарственного средства, предназначенного для лечения или предотвращения расстройства/заболевания, выбираемого из следующих расстройств/заболеваний: боль, рассеянный склероз, расстройства центральной или периферической нервной системы, сердечно-сосудистые расстройства, расстройства скелетной мускулатуры и нервномышечных соединений, воспалительных заболеваний, потери слуха травматического, акустического или токсического происхождения и звона в ушах, осложнений, связанных с аутоиммунными и вирусными заболеваниями и неврологических заболеваний, связанных с интоксикацией, лечением или расстройствами генетического происхождения. Предпочтительно изобретение относится к применению соединений с общей формулой (I), как определено ранее, или фармацевтически приемлемых солей таких соединений для получения лекарственного средства, предназначенного для лечения расстройства/заболевания, выбираемого из следующих расстройств/заболеваний: боль, расстройства центральной или периферической нервной системы. В особенности, изобретение относится к применению соединений с общей формулой (I), как определено ранее, или фармацевтически приемлемых солей таких соединений для получения лекарственного средства, предназначенного для лечения или предотвращения боли, в частности боли нейропатического происхождения.
Изобретение также относится к способам лечения вышеупомянутых заболеваний, включающим введение пациенту, получающему лечение, терапевтически эффективной дозы соединения общей формулы (I).
Для лекарственных средств, фармацевтические композиции, применения для получения лекарственных средств или терапевтических средств, предпочтения, указанные для соединений общей формулы (I), применяют с соответствующими изменениями.
В определенных случаях, соединения общей формулы (I) по настоящему изобретению могут содержать асимметричные атомы углерода. В результате такие соединения имеют две возможные энантиомерные формы, т.е. «R» и «S» конфигурации. Настоящее изобретение включает две энантиомерные формы соединений с общей формулой (I) и все комбинации таких форм, включая «RS» рацемические смеси. В попытке упростить предмет, когда не указана специфическая конфигурация в структурных формулах или названиях соединений, необходимо понимать, что представлены две энантиомерные формы и их смеси.
Фармацевтические композиции, содержащие соединение по изобретению, могут быть в твердой форме, например, порошки, гранулы, таблетки, желатиновые капсулы, липосомы, суппозитории или пластыри. Соответствующей твердой основой может быть, например, фосфат кальция, стеарат магния, тальк, сахара, лактоза, декстрин, крахмал, желатин, целлюлоза, метилцеллюлоза, карбоксиметилцеллюлоза натрия, поливинилпирролидин и воск.
Фармацевтические композиции, содержащие соединение по изобретению, также могут быть представлены в жидкой форме, например, растворы, эмульсии, суспензиии или сиропы. Соответствующими жидкими основами могут быть, например, вода, органические растворители, такие как глицерин или гликоли, так же их смеси, в различных соотношениях, в воде.
Введение лекарственного средства по изобретению может быть выполнено местным путем, пероральным путем, парентеральным путем, путем внутримышечной инъекции, путем подкожной инъекции, путем внутривенной инъекции и др.
Доза продукта по настоящему изобретению для обеспечения лечения вышеупомянутых заболеваний или расстройств, варьируется в зависимости от способа введения, возраста и массы тела субъекта, получающего лечение, а также состояния последнего, и окончательно определяется лечащим врачом или ветеринаром. Подобное количество, определенное лечащим врачом или ветеринаром, в данном описании называют «терапевтически эффективное количество».
В качестве указания, вводимая доза, предусматриваемая для лекарственного средства по изобретению, включает от 0,1 мг до 10 г в зависимости от типа используемого активного соединения.
В соответствии с изобретением, соединение общей формулы (I) может быть получено способами, описанными ниже.
ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ПО ИЗОБРЕТЕНИЮ:
Получение соединений общей формулы (I):
Соединения общей формулы (I) могут быть получены, например, из промежуточных продуктов с общими формулами (I)P, (I)AP, (I)AD, (I)D, (II)1, (II)1A, (III)1, (III)1A, (IV), (IV'), (V), (VI), (VI'), (VII) и (VII') в соответствии с методиками, описанными ниже.
ВАРИАНТ №1: R3 представляет собой атом водорода:
Путь №1:
Y представляет собой Н или необязательно замещенный циклоалкильный или арильный радикал, или также Y представляет собой OR14, SR15 или NR4R5 радикал, в котором R4 представляет собой -C(O)R9, -C(O)OR9, -C(O)NHR9 или -SO2R9 или в котором R4 представляет собой необязательно замещенный алкильный, циклоалкильный, циклоалкилалкильный или бис-фенилалкильный или арильный или аралкильный радикал и R5 не является Н, или также в котором R4 и R5 образуют вместе с атомом азота, который их несет, гетероцикл:
Когда Y представляет собой атом водорода, циклоалкильный радикал, необязательно замещенный арильный радикал или OR14, SR15 или NR4R5 радикал, в котором R4 представляет собой -C(O)R9, -C(O)OR9, -C(O)NHR9 или -SO2R9 радикал или в котором R4 представляет собой алкильный, циклоалкильный, циклоалкилалкильный или бис-фенилалкильный радикал или арильный или аралкильный радикал, необязательно замещенный на ароматическом цикле, и R5 не является атомом водорода или также в котором R4 и R5 образуют с атомом азота, который их несет, необязательно замещенный гетероцикл, соответствующие соединения с общей формулой (I), далее называемые соединениями с общей формулой (I)1, могут быть получены, диаграмма 1, из промежуточных соединений общей формулы (II)1, в которой Х, R1, R2 и А имеют такое же значение, что в общей формуле (I), W представляет собой NO2 или N3 группу и Y представляет собой атом водорода, циклоалкильный радикал или NR4R5 радикал, в котором R4 и R5 имеют такое же значение, что и выше. Указанные промежуточные продукты общей формулы (II)1 подвергают, в протонном полярном растворителе, таком как этанол (необязательно в смеси с дихлорметаном), гидрогенизации, катализируемой палладием на углероде (или любой другой соответствующей реакцией) с целью получения промежуточных продуктов общей формулы (III)1. Соединения общей формулы (I)1 затем получают реакцией, в растворителе, таком как изопропанол, промежуточных продуктов общей формулы (III)1 с одним из соединений общей формулой (IV), (V), (VI) или (VII) (депротектирование в кислой среде соединения, полученного в виде промежуточного продукта, также необходимо в случае реакции с соединением общей формулы (VII)) или с бензоилизотиоцианатом, затем с галогеналкилом общей формулы R8-Hal.
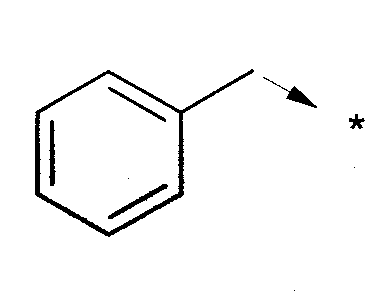
Диаграмма 1
Следовательно, в определенном случае, когда В представляет собой алкильный радикал, циклоалкильный радикал, NR6R7 радикал, в котором R6 и R7 образуют с атомом азота, который их несет, неароматический гетероцикл с пятью-шестью членами, карбоциклический арильный радикал или гетероциклический арильный радикал, реакция соединения общей формулы (III)1 с соединением общей формулы (IV) может проводиться, как представлено на диаграмме 1.
В определенном случае, когда В представляет собой NHNO2, соединение общей формулы (III)1реагирует с соединением формулы (V), как представлено на диаграмме 1.
В определенном случае, когда В представляет собой NR6R7 радикал, в котором R6 представляет собой атом водорода или алкильный, алкенильный или алкинильный радикал и R7 представляет собой атом водорода или алкильный радикал, соединение общей формулы (III)1 может реагировать с соединением общей формулы (VI), в которой L представляет собой, например, пиразольный цикл, или также с соединением общей формулы (VII), в котором, например, L представляет собой пиразольный цикл и Gp группы Boc ( Tetrahedron Lett. (1993) 34 (21), 3389-3392) или L представляет собой группу -N-SO2-CF3 и Gp группы Boc (J. Org. Chem. (1998) 63, 3804-3805). В случае, когда используют соединение общей формулы (VII), затем проводят депротектирование гуанидиновой функциональной группы, например, в присутствии сильной кислоты, такой как, например, трифторуксусная кислота, с целью получения соединения общей формулы (I).
Наконец, в определенном случае, когда В представляет собой SR8 радикал, тиомочевина общей формулы (I)1 может быть получена в 3 стадии. Реакция бензоилизотиоцианата на анилине общей формулы (III)1 в растворителе, таком как, например, ацетон, приводит к промежуточному соединению бензоил-тиомочевине, которую затем гидролизуют стандартным образом путем нагревания в основной среде. Полученную таким образом тиомочевину затем алкилируют с использованием, например, галогенированного производного общей формулы R8-Hal, нагреванием в инертном растворителе с целью получения соединения общей формулы (I)1.
Путь №2:
Y представляет собой Н или необязательно замещенный циклоалкильный или арильный радикал или также NR4R5 радикал, в котором R4 не является -С(О)R9, -C(O)OR9, -C(O)NHR9 или -SO2R9 или в котором R4 представляет собой алкильный, циклоалкильный, циклоалкилалкильный или бис-фенилалкильный радикал или также необязательно замещенный арил или аралкил и R5 представляет собой Н:
Когда Y представляет собой NR4R5 радикал, в котором R4 не является -С(О)R9, -C(O)OR9, -C(O)NHR9 или -SO2R9 радикалом или необязательно замещенным арильным радикалом, или в котором R4 представляет собой алкильный, циклоалкильный, циклоалкилалкильный или бис-фенилалкильный радикал или арильный или аралкильный радикал, необязательно замещенный на ароматическом цикле, и R5 представляет собой атом водорода, соответствующие соединения общей формулы (I), далее называемые соединениями общей формулы (I)2, могут быть получены, диаграмма 2, из соединений общей формулы (I)P, в которой Х, R1, R2, R5, A и В имеют такие же значения, что и в общей формуле (I) и Gp представляет собой стандартную аминную защитную группу (такую как трет-бутоксикарбонильная группа). Указанные соединения общей формулы (I)P депротектируют с целью получения соединений общей формулы (I)D, реакцию проводят в условиях, стандартных для специалиста в области техники (см. Protective groups in organic synthesis, 2nd ed., (John Wiley & Sons Inc., 1991)); следовательно такое депротектирование проводят, например, в кислой среде (в частности, с использованием соляной кислоты; реакцию проводят в растворителе, таком как этилацетат). Соединения общей формулы (I)D затем алкилируют в соответствии с методиками, известными специалисту в области техники, с целью получения соединений общей формулы (I)2; например, в случае, когда R4 представляет собой алкильный или циклоалкилалкильный радикал, соединения общей формулы (I)D реагируют с галидами общей формулы R4Hal, в которой Hal является атомом галогена, или также в случае, когда R4 представляет собой циклоалкильный радикал или радикал общей формулы R-CH2-, в которой R представляет собой алкильный, аралкильный или бис-фенилалкильный радикал, реакцию конденсации соединений общей формулы (I)D проводят с соответствующими кетонами или альдегидом общей формулы R-CHO в присутствии восстанавливающего агента, такого как триацетоксиборогидрид натрия или борогидрид натрия в низшем алифатическом спирте, таком как метанол, и необязательно в присутствии молекулярного сита, данную реакцию предпочтительно проводят при температуре окружающей среды.
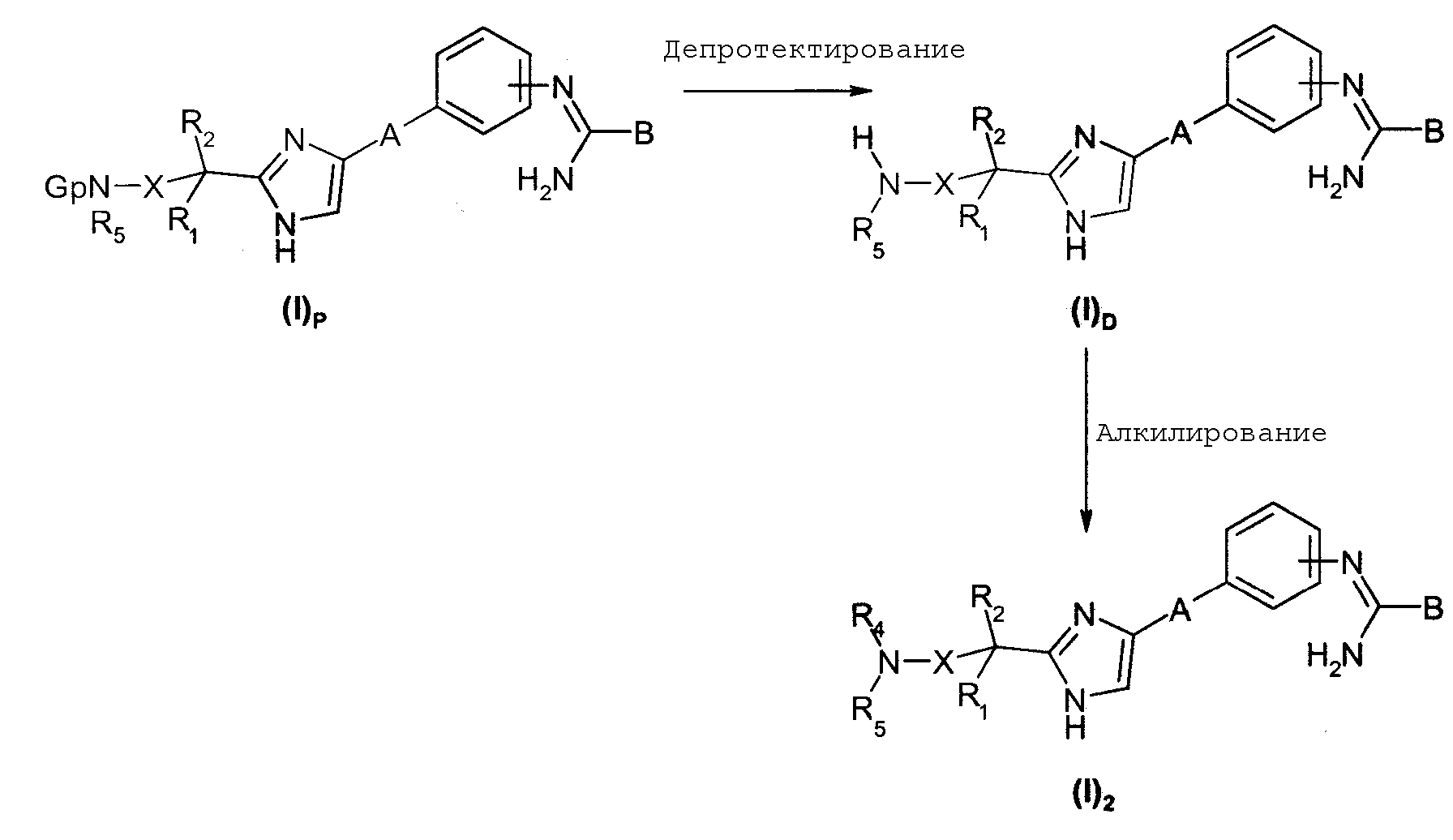
Диаграмма 2
Путь № 3:
Y представляет собой радикал амидинового типа:
Когда Y представляет собой радикал типа

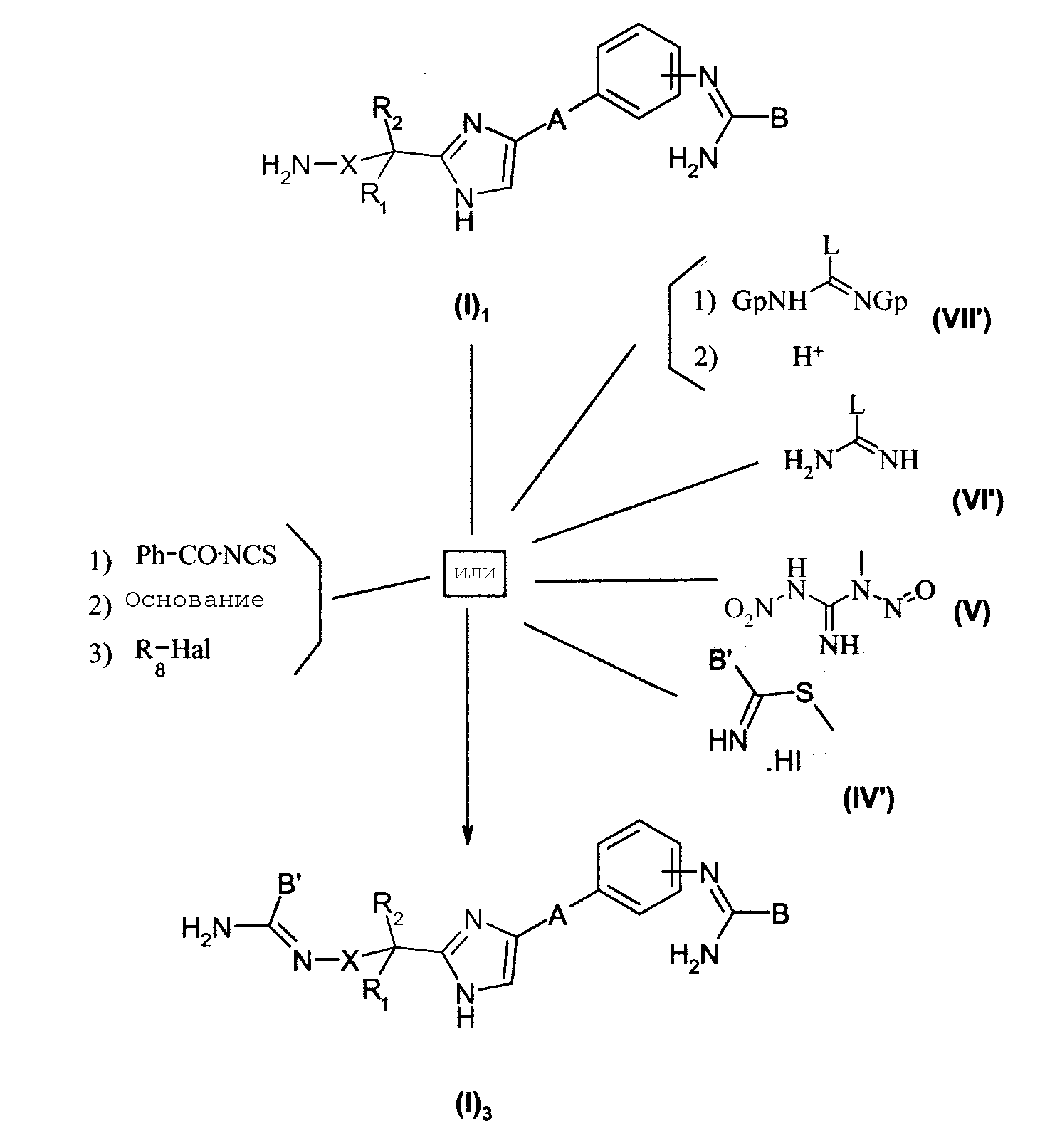
Диаграмма 3
ВАРИАНТ № 2: R3 не является атомом водорода:
Путь № 1:
Y представляет собой Н или необязательно замещенный циклоалкильный или арильный радикал, или также Y представляет собой OR14, SR15 или NR4R5 радикал, в котором R4 представляет собой -C(O)R9, -C(O)OR9, -C(O)NHR9 или -SO2R9 или в котором R4 представляет собой алкильный, циклоалкильный, циклоалкилалкильный или бис-фенилалкильный радикал или необязательно замещенный арильный или аралкильный радикал и R5 не является Н или также в котором R4 и R5 образуют, с атомом азота, который их несет, гетероцикл;
Когда R3 представляет собой алкильный или аралкильный радикал и Y представляет собой атом водорода, циклоалкильный радикал, необязательно замещенный арильный радикал или OR14, SR15 или NR4R5 радикал, в котором R4 представляет собой -C(O)R9, -C(O)OR9, -C(O)NHR9 или -SO2R9 радикал или в котором R4 представляет собой алкильный, циклоалкильный, циклоалкилалкильный или бис-фенилалкильный радикал или арильный или аралкильный радикал, необязательно замещенный на ароматическом цикле, и R5 не является атомом водорода, или также в котором R4 и R5 образуют с атомом азота, который их несет, необязательно замещенный гетероцикл, стадия может просто быть добавлена к пути синтеза № 1 ВАРИАНТА 1. Атом азота в положении 1 имидазольного цикла алкилируют перед проведением катализируемой гидрогенизации, затем используют обычные стадии пути № 1 ВАРИАНТА 1 с целью получения соединений общей формулы (I)1A, иными словами, соединений общей формулы (I)1, в которых R3 представляет собой алкильный или аралкильный радикал и Х, Y, R1 , R2, A и В имеют такие же значения, что и в общей формуле (I)1. Данный способ синтеза суммирован на диаграмме 1а далее.
Соединения общей формулы (I)1А могут быть получены, диаграмма 1а, из промежуточных продуктов общей формулы (II)1, в которой Х, R1, R2 и А имеют такие же значения, что и в общей формуле (I), W представляет собой NO2 или N3 группу, Y представляет собой атом водорода, циклоалкильный радикал, необязательно замещенный арильный радикал, OR14 или SR15 радикал или NR4R5 радикал, в котором R4 представляет собой -C(O)R9, -C(O)OR9, -C(O)NHR9 или -SO2R9, или необязательно замещенный арильный радикал, или в котором R4 представляет собой алкильный, циклоалкильный, циклоалкилалкильный или бис-фенилалкильный радикал или также необязательно замещенный аралкильный радикал и R5 не является атомом водорода. Указанные промежуточные продукты общей формулы (II)1 сначала алкилируют по методикам, известным специалисту в области техники, например, посредством галогенированного производного общей формулы R3Hal, в которой Hal является атомом галогена. Промежуточные продукты общей формулы (II)1A затем подвергают, в протонном полярном растворителе, таком как этанол (необязательно в смеси с дихлорметаном), гидрогенизации, катализируемой палладием на углероде с целью получения промежуточных продуктов общей формулы (III)1А. Соединения общей формулы (I)1А затем получают реакцией, в растворителе, таком как изопропанол, промежуточных продуктов общей формулы (III)1A с соединениями с общей формулой (IV), (V),(VI) или (VII) (депротектирование в кислой среде соединения, полученного в виде промежуточного продукта, также является необходимым в случае реакции с соединением общей формулы (VII)), или с бензоилизотиоцианатом, затем галогеналкилом общей формулы R8-Hal (см. ВАРИАНТ №1, путь № 1).
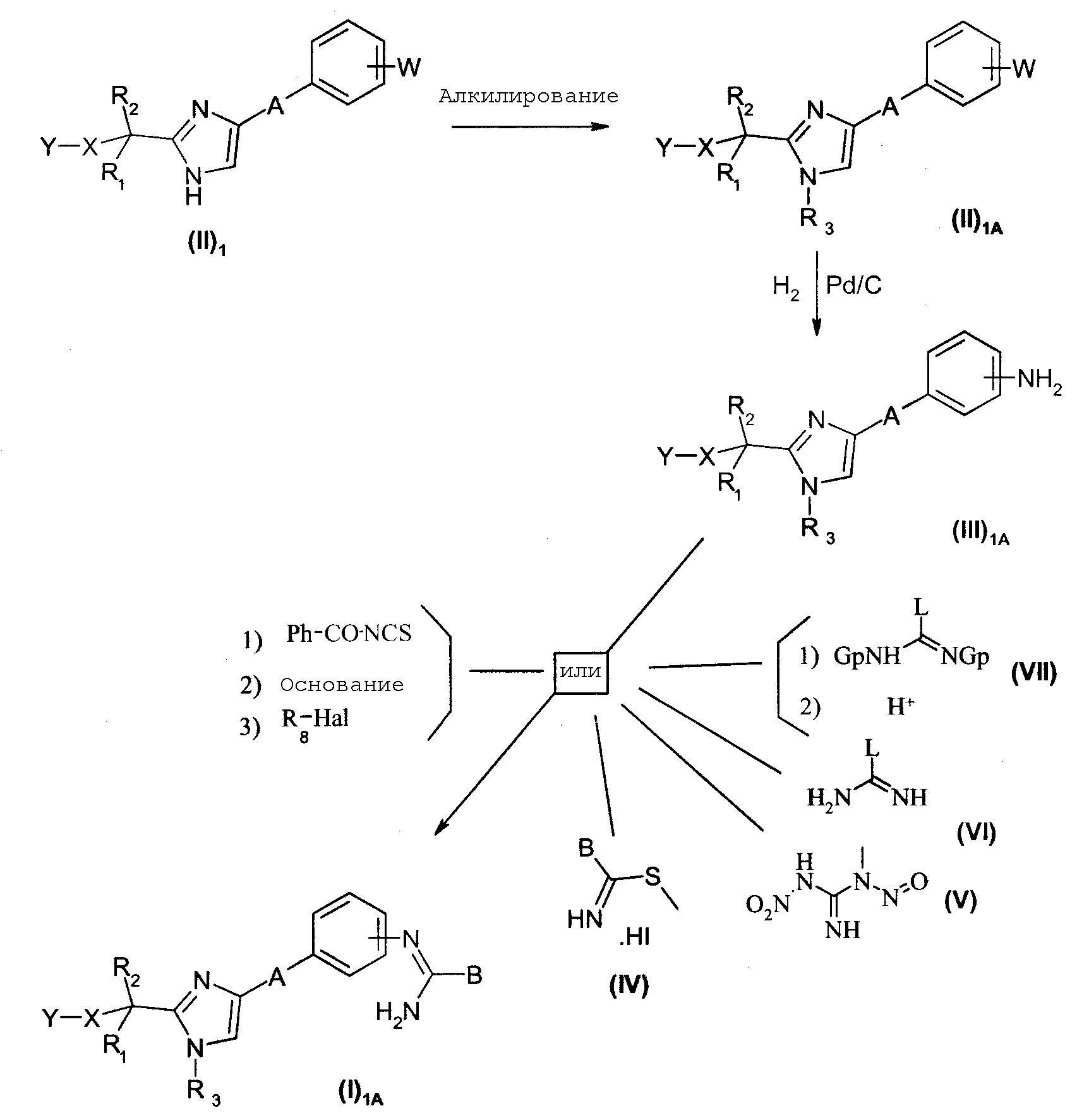
Диаграмма 1 а
Путь № 2:
Y представляет собой Н или циклоалкил или необязательно замещенный арильный радикал или также NR4R5 радикал, в котором R4 не является -C(O)R9, -C(O)OR9, -C(O)NHR9 или -SO2R9 или в котором R4 представляет собой алкильный, циклоалкильный, циклоалкилалкильный или бис-фенилалкильный радикал или также необязательно замещенный арильный или аралкильный радикал, и R5 представляет собой Н.
Когда R3 представляет собой алкильный или аралкильный радикал и Y представляет собой NR4R5 радикал, в котором R4 не является -C(O)R9, -C(O)OR9, -C(O)NHR9 или -SO2R9 или в котором R4 представляет собой алкильный, циклоалкильный, циклоалкилалкильный или бис-фенилалкильный радикал или арильный или аралкильный радикал, необязательно замещенный на ароматическом цикле, и R5 представляет собой атом водорода, стадия может просто быть добавлена к пути синтеза № 2 ВАРИАНТА №1. Атом азота в положении 1 имидазольного цикла алкилируют, тогда как аминную функциональную группу в боковой цепи в положении 2 имидазольного цикла защищают, затем используют обычные стадии пути № 2 ВАРИАНТА № 1 с целью получения соединений общей формулы (I)2А, иными словами соединений общей формулы (I)2, в которых R3 представляет собой алкильный или аралкильный радикал и А, В, Х, R1, R2, R4 и R5 имеют такие же значения, что и в общей формуле (I)2 . Данный способ синтеза суммирован на диаграмме 2а далее.
Соединения общей формулы (I)P сначала алкилируют в соответствии с методиками, известными специалисту в области техники, например, посредством галогенированного производного общей формулы R3Hal, в которой Hal является атомом галогена. Полученные соединения общей формулы (I)AP затем депротектируют с целью получения соединений общей формулы (I)AD, реакцию проводят в стандартных условиях для специалиста в области техники (см. Protective groups in organic synthesis, 2nd ed., (John Wiley & Sons Inc., 1991)); следовательно такое депротектирование проводят, например, в кислой среде (в частности, с использованием соляной кислоты; реакцию можно проводить в растворителе, таком как этилацетат). Соединения общей формулы (I)AD затем алкилируют в соответствии с методиками, известными специалисту в области техники, с целью получения соединения общей формулы (I)2A; например, в случае, когда R4 представляет собой алкильный или циклоалкилалкильный радикал, соединения общей формулы (I)AD реагируют с галидами общей формулы R4Hal, в которой Hal является атомом галогена, или также в случае, когда R4 представляет собой циклоалкильный радикал или радикал общей формулы R-CH2-, в которой R представляет собой алкильный, аралкильный или бис-фенилалкильный радикал, реакцию конденсации соединений общей формулы (I)AD проводят с соответствующими циклоалкилкетонами или альдегидом общей формулы R-CHO в присутствии восстанавливающего агента, такого как триацетоксиборогидрид натрия или борогидрид натрия в низшем алифатическом спирте, таком как метанол и необязательно в присутствии молекулярного сита, данную реакцию предпочтительно проводят при температуре окружающей среды.
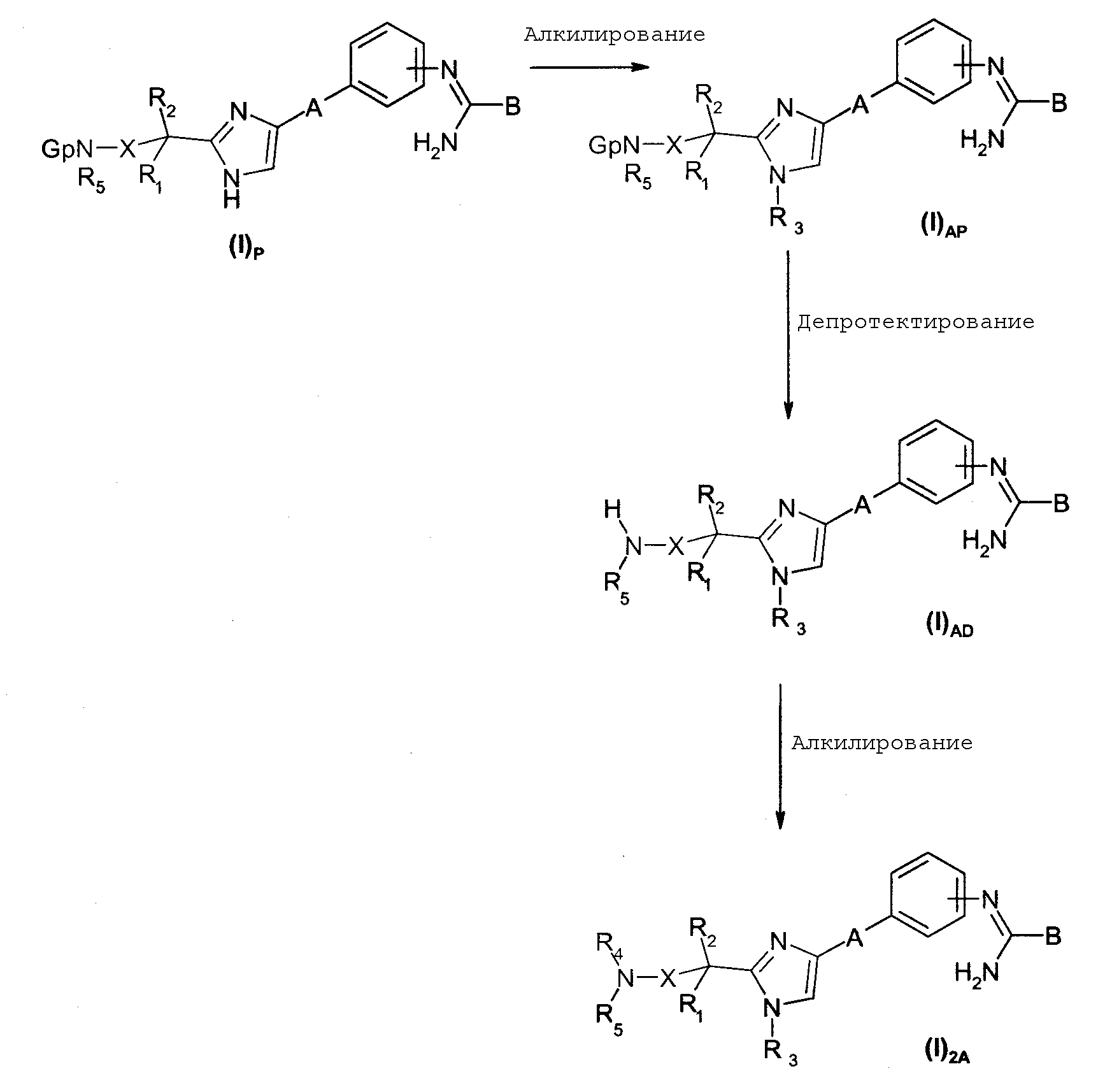
Диаграмма 2а
Путь № 3:
Y представляет собой радикал типа амидина:
Когда Y представляет собой радикал типа

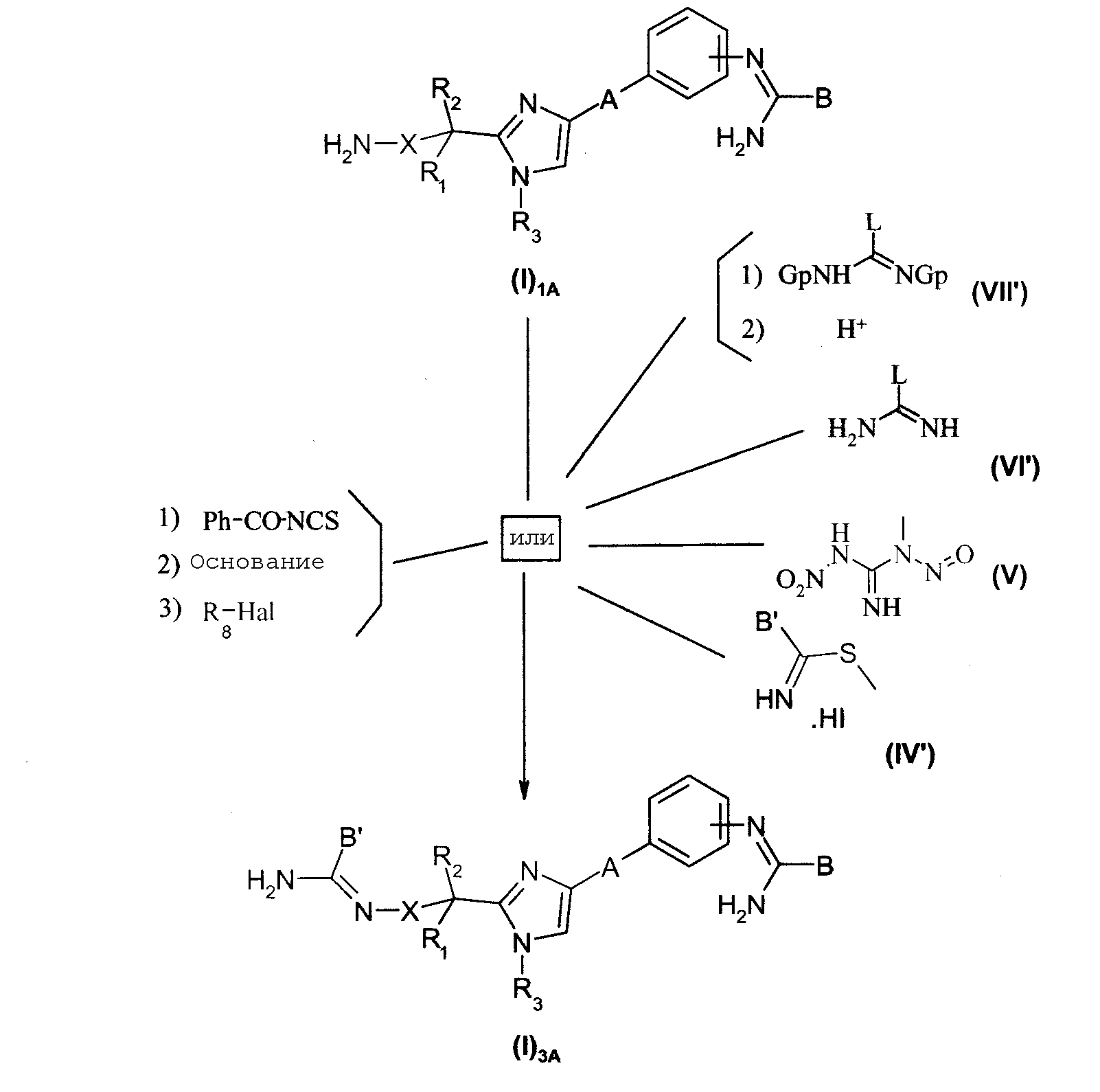
Диаграмма 3а
Получение определенных некоммерческих промежуточных продуктов синтеза:
Получение соединений общей формулы (I)P
Данные соединения фактически также являются соединениями общей формулы (I), в которой Y представляет собой группу NR4R5, в которой R4 представляет собой определенную алкоксикарбонильную группу (такую как трет-бутоксикарбонильная группа). Следовательно, они могут быть получены в соответствии с методикой, описанной для соединений общей формулы (I) выше (см. путь 1).
Получение соединений общей формулы (II)1
Соединения общей формулы (II)1 получают реакцией циклоконденсации кислоты общей формулы (VIII)1с α-галогенкетоном общей формулы (IX)1. Например, диаграмма 4, карбонат цезия добавляют к кислоте общей формулы (VIII)1. Полученный промежуточный продукт конденсируют с α-галогенкетоном общей формулы (IX)1, затем добавляют большой избыток ацетата аммония (например, 15 или 20 эквивалентов на эквивалент кислоты общей формулы (VIII)1). Данную реакцию предпочтительно проводят в смеси ксилолов и при нагревании (если целесообразно, вода, образующаяся в течение реакции, также может удаляться одновременно).
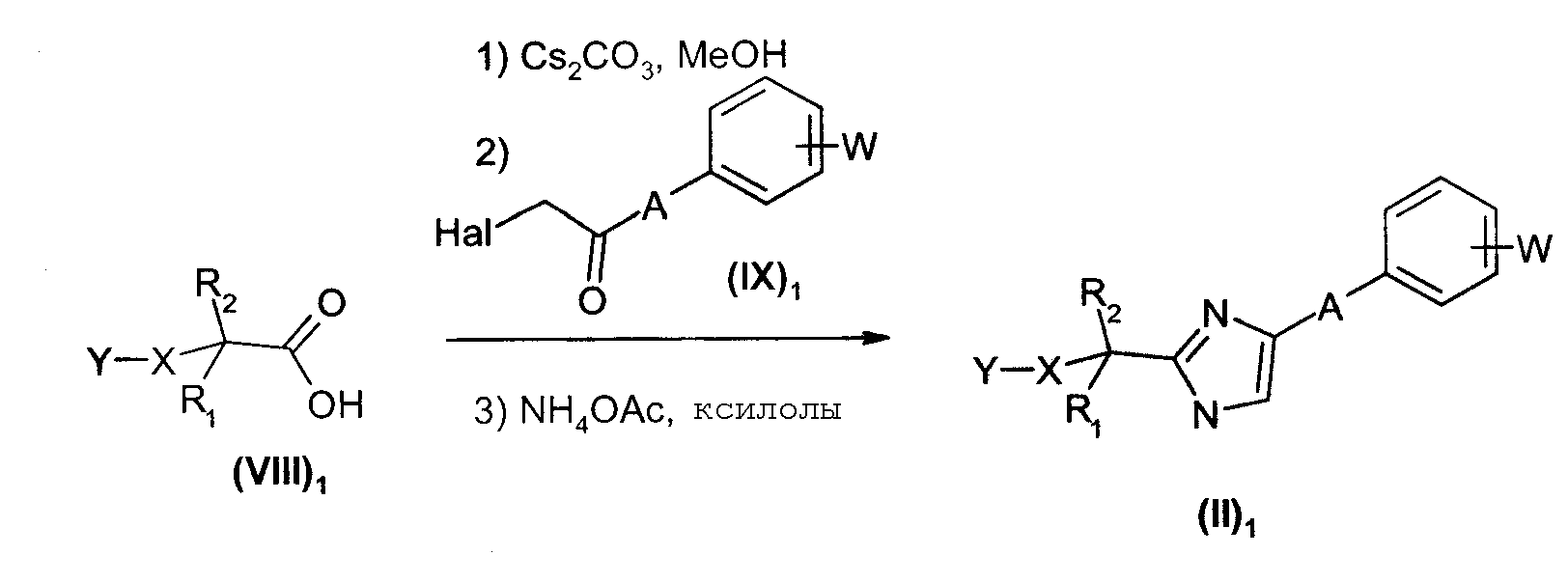
Диаграмма 4
Получение соединений общей формулы (IV) или (IV')
Соединения общей формулы (IV), в которой В представляет собой алкильный радикал, карбоциклический арильный радикал или гетероциклический арильный радикал могут быть получены, например, диаграмма 5, реакцией тиоамидов общей формулы (IV).1 с метилйодидом в растворителе, таком как ацетон. Синтез является идентичным для соединений общей формулы (IV')((IV').1 и В' замещая (IV).1 и В соответственно на диаграмме 5)
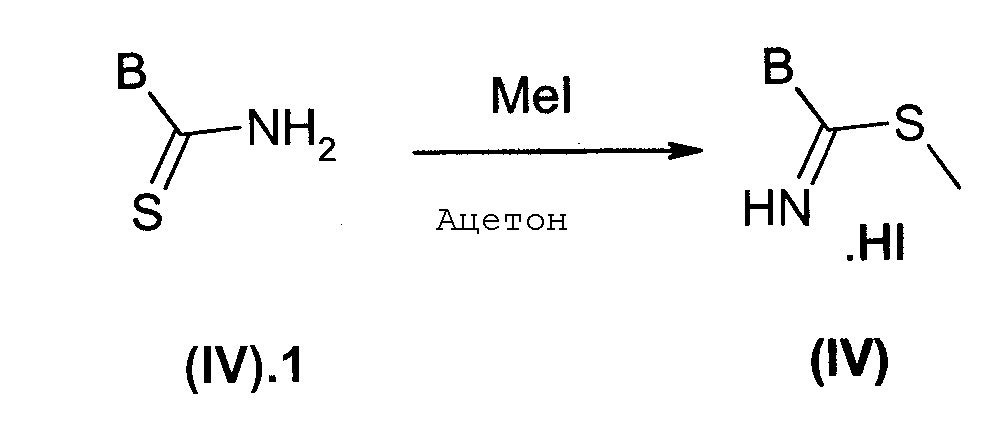
Диаграмма 5
Получение соединений формулы (V)
Получение данных соединений может проводиться в соответствии со способами, известными специалисту в области техники, такими как, например, таковые, описанные в следующей публикации: J. Amer. Chem. Soc. (1947), 69, 3028-3030).
Получение определенных соединений общей формулы (VIII)1
Соединения общей формулы (VIII)1, в которой R4 представляет собой -C(O)OR9 радикал, и Х, R1, R2, R5 и R9 имеют такое же значение, как в общей формуле (I), получают, диаграмма 6, реакцией, в основных условиях (создаваемых, например, путем добавления гидроксида натрия и воды или в присутствии органического основания, такого как триэтиламин), аминокислоты общей формулы (X)1 с галогенированным производным общей формулы R9-OC(O)-Hal, в которой Hal представляет собой атом галогена. Когда реакцию терминируют, среду подкисляют (например, добавлением соляной кислоты) с целью получения аминокислоты общей формулы (VIII)1.
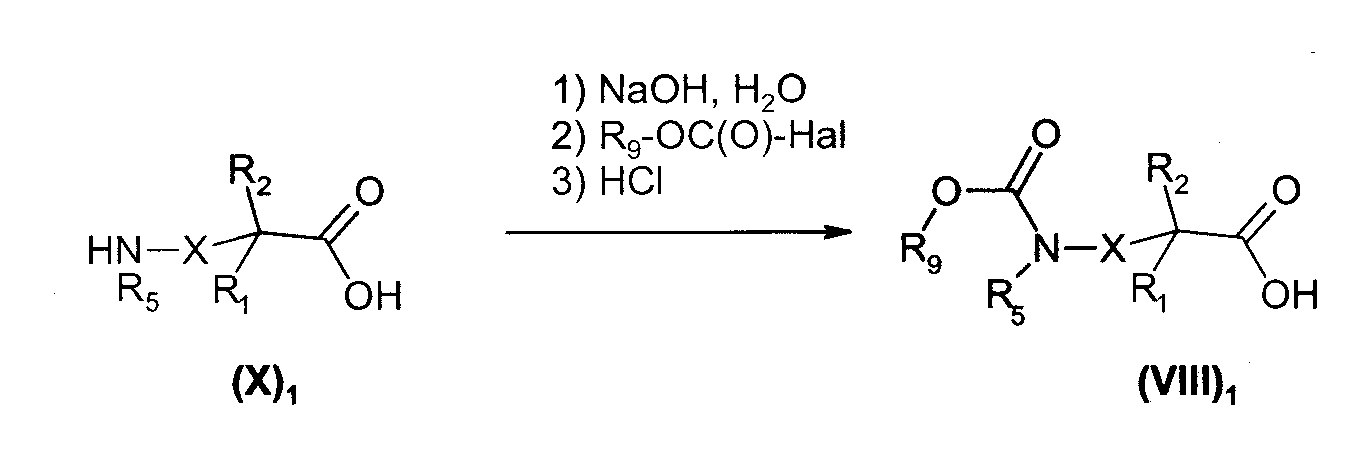
Диаграмма 6
Соединения общей формулы (VIII)1, в которой R4 представляет собой -С(О)R9 радикал, и Х, R1, R2 и R5 имеют такое же значение, что и в общей формуле (I), получают, диаграмма 7, конденсацией аминокислот общей формулы (X)1 с карбоновыми кислотами (или соответствующими кислыми хлоридами) общей формулы R9-COOH в стандартных условиях пептидного синтеза (M. Bodanszky and A. Bodanszky, The Practice of Peptide Synthesis, 145 (Springer-Verlag, 1984)) в полярном растворителе, таком как тетрагидрофуран, дихлорметан или диметилформамид в присутствии связующего реагента, такого как дициклогексилкарбодиимид (DCC), 1,1'-карбонилдиимидазол (CDI) (J. Med. Chem (1992), 35 (23), 4464-4472) или гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (EDC или WSCI) (John Jones, The chemical synthesis of peptides, 54 (Clerendon Press, Oxford, 1991)).
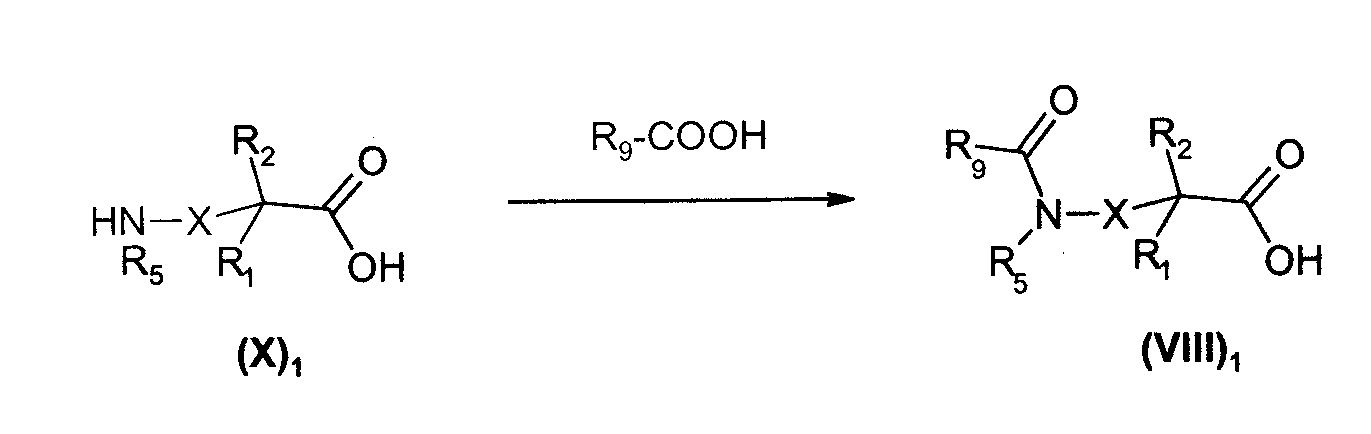
Диаграмма 7
Соединения общей формулы (VIII)1, в которой R4 представляет собой -C(O)NHR9 радикал, и Х, R1, R2 и R5 имеют такое же значение, как в общей формуле (I), получают, диаграмма 8, реакцией аминокислот общей формулы (X)1 с изоцианатами общей формулы R9-NCO; реакцию можно проводить при температуре окружающей среды в растворителе, таком как хлороформ.
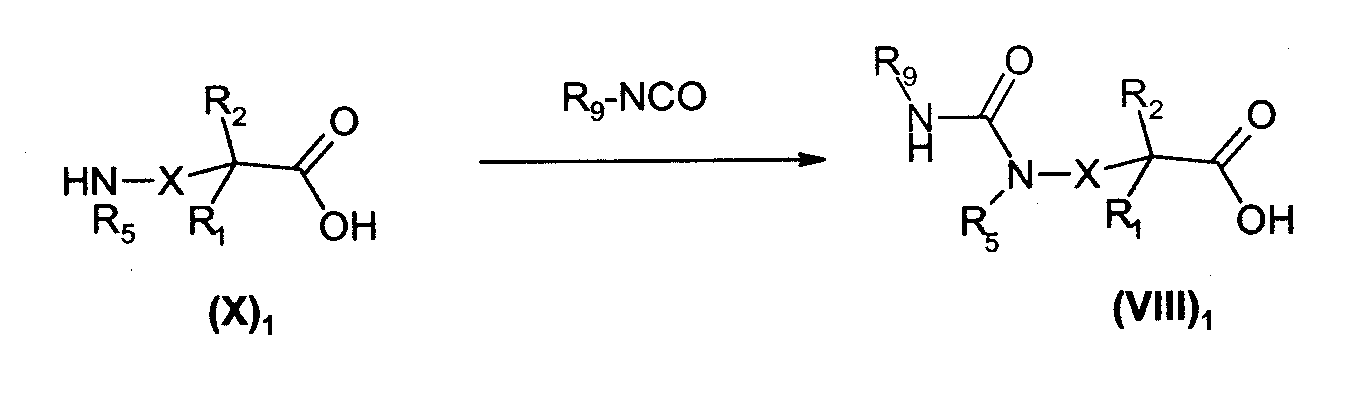
Диаграмма 8
Соединения общей формулы (VIII)1, в которой R4 представляет собой -C(O)NHR9 радикал, и Х, R1, R2 и R5 имеют такое же значение, как общей формулы (I), получают, диаграмма 9, реакцией аминокислот общей формулы (X)1 с сульфохлоридами общей формулы R9-SO2Cl в стандартных условиях; реакцию можно, например, проводить при температуре окружающей среды в растворителе, таком как диметилформамид в присутствии основания, такого как триэтиламин.
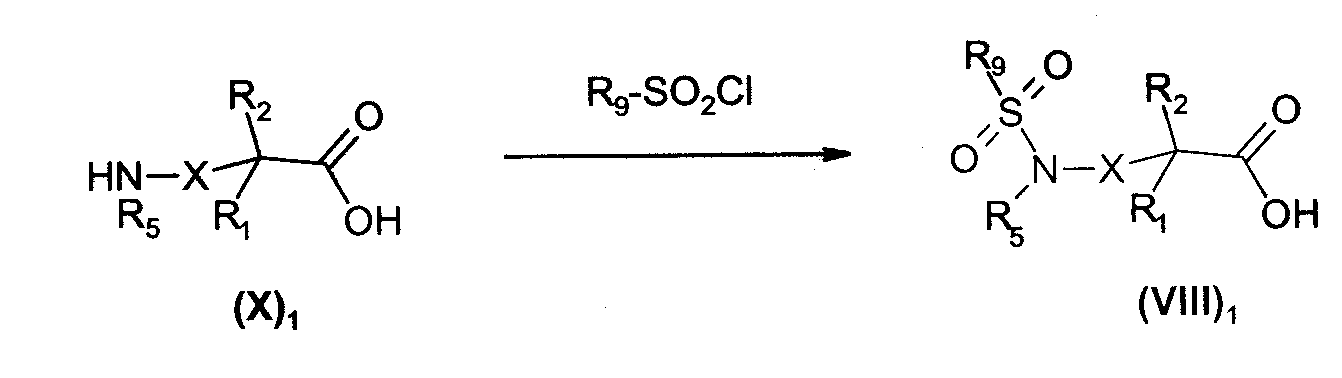
Диаграмма 9
Получение соединений общей формулы (IX)1
Соединения общей формулы (IX)1, в которой Hal представляет собой атом галогена (например, атом хлора или брома), W представляет собой NO2 или N3 группу и А имеет такое же значение, что и в общей формуле (I), получают, диаграмма 10, реакцией кетона общей формулы (XI)1 с галогенирующим агентом. Например, в определенном случае бромирования, реакцию можно проводить с агентом бромирования, таким как CuBr2 (J. Org. Chem. (1964), 29, 3459), бром (J. Het. Chem. (1988), 25 , 337), N-бромсукцинимид (J. Amer. Chem. Soc. (1980), 102, 2838) в присутствии уксусной кислоты в растворителе, таком как этилацетат или дихлорметан, HBr или Br2 в эфире, этаноле или уксусной кислоте (Biorg. Med. Chem. Lett. (1996), 6(3), 253-258; J. Med. Chem. (1988), 31(10), 1910-1918; J. Am. Chem. Soc. (1999), 121, 24) или также с использованием бромирующей смолы (J. Macromol. Sci. Chem. (1977), A11, (3) 507-514).

Диаграмма 10
Получение других промежуточных продуктов
Получение других некоммерческих промежуточных продуктов описано в литературе или в рамках специалиста в области техники посредством стандартных способов синтеза.
Если не указано иначе, все технические и научные термины, используемые в данном описании, имеют такое же значение, как таковое, обычно понимаемое обычным специалистом в области, к которой относится настоящее изобретение. Подобно, все публикации, патентные заявки, все патенты и все другие ссылки, упомянутые в данном описании, включены в виде ссылки.
Следующие примеры представлены с целью иллюстрации вышеуказанных методик и ни в каком случае не должны расцениваться как ограничение диапазона изобретения.
ПРИМЕРЫ:
Способ, используемый для измерения времени удерживания (в.у.) и молекулярного пика (МН+)
Соединения характеризуются их временем удерживания (в.у.), выражаемым в минутах, определяемым жидкостной хроматографией (ЖХ), и их молекулярным пиком (МН+), определяемым масс-спектрометрией (МС), отдельный квадрупольный масс-спектрометр (Micromass, Platform model), снабженный источником электроразбрызгивания, используют с разрешением 0,8 да при 50% канале.
В примерах ниже условия элюции, соответствующие показанным результатам, следующие: прохождение из смеси ацетонитрила-воды-трифторуксусной кислоты 50-950-0,2 (А) в смесь ацетонитрила-воды 950-50 (В) через линейный градиент в течение периода 8,5 минут, затем элюция чистой смесью В в течение 10,5 минут.
Пример 1: гидрохлорид бутил-2-[4-(4-{[(1Z)-амино(тиен-2-ил)метилен]амино}фенил)-1Н-имидазол-2-ил]этилкарбамата:
1.1) бутил-2-[4-(4-азидофенил)-1Н-имидазол-2-ил]этилкарбамат:
Смесь, содержащую N-(бутоксикарбонил)-β-аланин (3 г; 15,1 ммоль) и карбонат цезия (2,43 г; 7,55 ммоль) в 50 мл безводного метанола, перемешивали в течение одного часа. Данную смесь выпаривали досуха, затем разводили 60 мл диметилформамида. Добавляли бромид 4-азидофенацила (3,64 г; 15,1 ммоль), затем полученную смесь перемешивали в течение 2 часов. Растворитель выпаривали с использованием лопастного насоса. Добавляли 80 мл этилацетата и бромид цезия фильтровали на фритте. После выпаривания фильтрата, добавляли 200 мл ксилолов. Затем добавляли ацетат аммония (23 г; 0,3 моль) и смесь нагревали с обратным холодильником в течение 1 часа 30 минут перед помещением в ледяную воду, к которой добавлено 80 мл этилацетата. После декантации, органическую фазу промывали насыщенным раствором хлорида натрия. Затем органическую фазу сушили над сульфатом магния и выпаривали растворитель. Полученное масло очищали на колонке из диоксида кремния (элюент: этилацетат-гептан/8-2). Ожидаемый продукт получали в форме черного масла с выходом 65%.
1.2) 2-[4-(4-аминофенил)-1Н-имидазол-2-ил]этилкарбамат:
Промежуточный продукт 1.1 (3 г; 9,15 ммоль) растворяли в 50 мл этанола в присутствии палладия на углероде (приблизительно 10 мас%). Данную смесь гидрогенизировали под двумя крышками в течение 18 часов. Затем реакционную смесь фильтровали на фильтре Millipore®, затем промывали в этаноле. После выпаривания растворителя, получали пену светло-коричневого цвета с выходом 88%.
1Н ЯМР (δ ч/млн, ДМСО): 0,84 (т, 3Н), 1,27-1,29 (м, 2Н), 1,45-1,48 (м, 2Н), 3,05 (м, 2Н), 3,42 (м, 2Н), 3,90 (м, 2Н), 5,5-6,2 (ушир.м, 1Н), 6,67-6,69 (д, 2Н), 7,34 (ушир. с, 1Н), 7,47-7,49 (д, 2Н), 7,70 (с, 1Н), 14,33 (ушир. с, 2Н). МН+=303,2.
1.3) Метилтиофен-2-карбимидотиоат:
Метилйодид (66 г; 0,46 моль) добавляют по каплям при 0°С к раствору тиофен-2-карботиоамида (50 г; 0,33 моль) в 500 мл ацетона. После добавления перемешивание поддерживали в течение двух часов при 23°С. Образующийся осадок фильтровали на фритте и промывали дважды 100 мл ацетона перед сушкой в вакууме (в вакуумном колпаке). Получали желтый порошок с выходом 97%.
1Н ЯМР (δ ч/млн, ДМСО): 2,8 (с, 3Н), 7,42 (м, 1Н), 8,125 (д, 1Н), 8,27 (д, 1Н), 10-12 (ушир. м, 1Н).
1.4) бутил-2-[4-(4-{[(1Z)-амино(тиен-2-ил)метилен]амино}фенил)-1Н-имидазол-2-ил]этилкарбамат:
Промежуточный продукт 1.2 (2,5 г; 8,2 моль) суспендировали в 30 мл 2-пропанола в присутствии промежуточного продукта 1.3 (1,2 экв.). Реакционную смесь выдерживали при 50°С в течение 18 часов перед концентрированием досуха. Осадок помещали в 50 мл этилацетата и 50 мл насыщенного раствора карбоната натрия. Смесь перемешивали в течение 30 минут перед декантацией. Затем органическую фазу промывали насыщенным раствором хлорида натрия, затем сушили над сульфатом натрия. Растворители выпаривали и полученную пену очищали на колонке из диоксида кремния (элюент: CH2Cl2-MeOH/97-3 до 90-10). Получали порошок светло-желтого цвета с выходом 57%. Температура плавления: 146,2°С.
МН+ = 412,2.
1.5) гидрохлорид бутил-2-[4-(4-{[(1Z)-амино(тиен-2-ил)метилен]амино}фенил)-1Н-имидазол-2-ил]этилкарбамата:
Промежуточный продукт 1.4 (1 г; 2,43 ммоль) растворяли в этаноле (20 мл). 1Н соляную кислоту в растворе эфира (9,7 мл; 9,7 ммоль). Смесь перемешивали в течение одного часа. После концентрирования досуха, осадок помещали в эфир (15 мл) и смесь перемешивали в течение 15 минут. После фильтрации на фритте и промывания эфиром полученного твердого вещества, последний сушили в вакууме (вакуумный колпак). Получали ожидаемый продукт в форме твердого вещества кремового цвета с выходом 100%.
Температура плавления: > 260°С.
МН+ = 412,2.
Соединения примеров 2 и 3 получали в соответствии с методикой, аналогичной таковой, описанной для соединения примера 1.
Пример 2:гидрохлорид бутил-2-[4-(3-{[(1Е)-амино(тиен-2-ил)метилен]амино}фенил)-1Н-имидазол-2-ил]этилкарбамата:
Температура плавления: 210-212°С.
МН+ = 412,2.
Пример 3:гидрохлорид бутил-2-[4-(4'-{[(1Z)-амино(тиен-2-ил)метилен]амино}-1, 1'-бифенил-4-ил)-1Н-имидазол-2-ил]этилкарбамата:
Температура плавления: 97-98°С.
МН+ = 488,2.
Пример 4: гидрохлорид N'-(4-{2-[(циклогексиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
4.1) Трет-бутил[4-(4-азидофенил)-1Н-имидазол-2-ил]метилкарбамат:
Смесь, содержащую N-(трет-бутоксикарбонил)глицин (5 г; 28,5 ммоль) и карбонат цезия (4,6 г; 14,2 ммоль) в 30 мл безводного метанола, перемешивали в течение одного часа. Данную смесь выпаривали досуха, затем разводили 60 мл диметилформамида. Добавляли бромид 4-азидофенацила (6,84 г; 28,5 ммоль), затем полученную смесь перемешивали в течение 2 часов. Растворитель выпаривали с использованием лопастного насоса. Добавляли 80 мл этилацетата и бромид цезия фильтровали на фритте. После выпаривания фильтрата, добавляли 200 мл ксилолов, затем ацетат аммония (44 г; 0,57 моль) и смесь нагревали с обратным холодильником в течение 1 часа 30 минут перед помещением в ледяную воду, к которой было добавлено 80 мл этилацетата. После декантации, органическую фазу нейтрализовали насыщенным раствором бикарбоната натрия с последующей фильтрацией на стеклянном микроволокнистом фильтре (GF/A, Whatman). Органическую фазу промывали насыщенным раствором хлорида натрия, затем сушили над сульфатом натрия и растворитель выпаривали. Полученное черное масло очищали на колонке из диоксида кремния (элюент: этилацетат-гептан/6-4 до 3-7). Получали порошок коричневого цвета, который, после промывания изопропиловым эфиром, давал порошок светло-коричневого цвета с выходом 48%.
1Н ЯМР (δ ч/млн, ДМСО): 1,39 (с, 9Н), 4,16 (м, 2Н), 7,06 (д, 2Н), 7,24 (ушир. с, 1Н), 7,48 (с, 1Н), 7,77 (д, 2Н), 11,8 (ушир. с, 1Н).
4.2) Трет-бутил[4-(4-аминофенил)-1Н-имидазол-2-ил]метилкарбамат:
Промежуточный продукт 4.1 (4,3 г; 13,6 ммоль) растворяли в 50 мл смеси этанола-CH2Cl2 2-1 в присутствии палладия на углероде (приблизительно 10 мас%). Данную смесь гидрировали под давлением 2 бар водорода в течение 24 часов. Затем реакционную смесь фильтровали на стеклянном микроволокнистом фильтре (GF/A, Whatman), затем промывали в этаноле. После выпаривания растворителя, остаток перемешивали в эфире. Затем смесь фильтровали на фритте, затем промывали в эфире и изопентане. Получали порошок бледно-желтого цвета с выходом 100%.
1Н ЯМР (δ ч/млн, ДМСО): 1,39 (с, 9Н), 4,17 (м, 2Н), 6,54 (д, 2Н), 7,16-7,19 (ушир. с, 2Н), 7,35 (д, 2Н).
4.3) трет-бутил-[4-(4-{[(1Е)амино(тиен-2-ил)метилен]амино}фенил)-1Н-имидазол-2-ил]метилкарбамат:
Промежуточный продукт 4.2 (3,9 г; 13,6 моль) суспендировали в 30 мл пропанола-2 в присутствии промежуточного продукта 1.3. Смесь нагревали до температуры 60°С в течение 48 часов. После концентрирования досуха смеси, остаток помещали в 50 мл этилацетата и 50 мл насыщенного раствора кислого карбоната натрия. Смесь перемешивали в течение 30 минут перед декантацией. Полученную органическую фазу промывали насыщенным раствором хлорида натрия, затем сушили над сульфатом натрия. Растворители выпаривали и полученную пену очищали на колонке из диоксида кремния (элюент: CH2Cl2-EtOH/98-2 до 90-10). Получали масло светло-желтого цвета, которое кристаллизовали из эфира. После фильтрования на фритте и промывания эфиром, получали порошок бледно-желтого цвета с выходом 59%.
1Н ЯМР (δ ч/млн, ДМСО): 1,39 (с, 9Н), 4,17 (м, 2Н), 6,4 (м, 2Н), 6,82 (м, 2Н), 7,07-7,36 (м, 3Н), 7,59-7,73 (м, 4Н), 11,7 (ушир. с, 1Н).
4.4) гидрохлорид N'-{4-[2-(аминометил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Промежуточный продукт 4.3 (3,1 г; 7,79 ммоль) суспендировали в 20 мл этилацетата. Добавляли соляную кислоту в концентрации 4,4 М в этилацетате (80 мл; 0,35 моль) и полученную смесь перемешивали при 22°С в течение 18 часов. После концентрирования досуха, остаток помещали в эфир перед повторным концентрированием досуха. После перемешивания в изопентане, затем фильтрации на фритте и промывания твердого вещества в изопентане, получали порошок кремового цвета с выходом 95%. Температура плавления: > 260°С
1Н ЯМР (δ ч/млн, ДМСО): 4,47 (с, 2Н), 7,37-7,39 (м, 1Н), 7,59 (м, 2Н), 8,05 (м, 2Н), 8,18 (м, 3Н), 9,08 (ушир. м, 3Н), 9,94 (ушир. с, 1Н), 11,6-11,8 (ушир. с, 1Н).
4.5) N-(4-{2-[(циклогексиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамид:
Промежуточный продукт 4.4 (800 мг; 1,96 ммоль) суспендировали в 30 мл метанола в присутствии триэтиламина (0,83 мл; 5,88 ммоль). Затем добавляли циклогексанон (0,25 мл; 2,35 ммоль), затем смесь перемешивали в течение трех часов при 23°С. После добавления триацетоксиборогидрида натрия (500 мг; 2,35 ммоль) смесь еще раз перемешивали при 23°С в течение двух часов. Затем добавляли насыщенный раствор кислого сульфата калия, затем воду с целью растворения осадка, который образуется. Наконец, добавляли насыщенный раствор бикарбоната натрия к полученной смеси, перед пятикратной экстракцией этилацетатом. Затем органическую фазу сушили над сульфатом натрия. Растворители выпаривали и полученную пену очищали на колонке из диоксида кремния (элюент: CH2Cl2-EtOH-NH4OH/92,5-5,5-2 до 90-7,5-2,5). Получали масло светло-желтого цвета, которое кристаллизовали из эфира. После фильтрации на фритте и промывания твердого вещества эфиром, получали порошок бледно-желтого цвета с выходом 64%.
1Н ЯМР (δ ч/млн, ДМСО): 1,02-1,22 (с, 5Н), 1,52-1,84 (м, 5Н), 2,37-2,42 (м, 1Н), 3,75 (с, 2Н), 6,41 (м, 2Н), 6,82 (м, 2Н), 7,08 (м, 1Н), 7,36 (м, 1Н), 7,59-7,74 (м, 4Н), 11,7 (ушир. с, 1Н).
МН+=380,2.
4.6) гидрохлорид N-(4-{2-[(циклогексиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
Данное соединение получали из промежуточного продукта 4.5 в соответствии с методикой, аналогичной таковой стадии 1.5 примера 1. Температура плавления: 234-235°С.
МН+ = 394,2.
Соединения примеров 5-9 получали в соответствии с методикой, аналогичной таковой, описанной для соединения примера 4.
Пример 5: гидрохлорид N'-(4-{2-[2-(циклогексиламино)этил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
Температура плавления: 185-186°С.
МН+ = 394,2.
Пример 6: гидрохлорид N'-(3-{2-[(циклогексиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
Температура плавления: >225°С.
МН+ = 380,2.
Пример 7: гидрохлорид N'-[4-(2-{[циклогексил(метил)амино]метил}-1Н-имидазол-4-ил)фенил]тиофен-2-карбоксимидамида:
Температура плавления: 240-241°С.
Пример 8: гидрохлорид N'-(4-{2-[(дибензиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
Температура плавления: 150-151°С.
МН+ = 478,2.
Пример 9: гидрохлорид N'-(4-{2-[(бензиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
Температура плавления: 228-229°С.
МН+ = 388,1.
Пример 10: гидрохлорид N'-{3-[2-(аминометил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
10.1) Трет-бутил[4-(3-нитрофенил)-1Н-имидазол-2-ил]метилкарбамат:
Данное соединение получают в соответствии с методикой, аналогичной таковой, описанной для стадии 4.1 примера 4, с бромидом 3-нитрофенацила, замещающим бромид 4-азидофенацила. Ожидаемое соединение получали в форме порошка кремового цвета с выходом 44%.
1Н ЯМР (δ ч/млн, ДМСО): 4,96 (с, 2Н), 7,69-7,75 (м, 4Н), 7,90 (дд, 2Н), 8,08 (дд, 2Н).
МН+=319,2.
10.2) Трет-бутил[4-(3-аминофенил)-1Н-имидазол-2-ил]метилкарбамат:
Данное соединение получают в соответствии с методикой, аналогичной таковой, описанной для стадии 4.2 примера 4, с промежуточным продуктом 10.1, замещающим промежуточный продукт 4.1. Ожидаемое соединение получали в форме порошка кремового цвета с выходом 89%.
1Н ЯМР (δ ч/млн, ДМСО): 1,39 (с, 9Н), 4,2 (с, 2Н), 6,43 (м, 1Н), 6,84-7,01 (м, 3Н), 7,26-7,34 (м, 2Н).
МН+=289,2.
10.3) Трет-бутил[4-(3-{[(1E)-амино(тиен-2-ил)метилен]амино}фенил)-1Н-имидазол-2-ил]метилкарбамат:
Данное соединение получают в соответствии с методикой, аналогичной таковой, описанной для стадии 4.3 примера 4, с промежуточным продуктом 10.2, замещающим промежуточный продукт 4.2. Ожидаемое соединение получали в форме белого порошка с выходом 68%.
1Н ЯМР (δ ч/млн, ДМСО): 1,39 (с, 9Н), 4,15 (м, 2Н), 6,34-6,62 (м, 3Н), 7,08-7,74 (м, 8Н), 11,77 (с, 1Н).
10.4) гидрохлорид N'-{3-[2-(аминометил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Данное соединение получают в соответствии с методикой, аналогичной таковой, описанной для стадии 4.4 примера 4, с промежуточным продуктом 10.3, замещающим промежуточный продукт 4.3. Ожидаемое соединение получали в форме белого порошка с выходом 98%. Температура плавления: >265°С.
1Н ЯМР (δ ч/млн, ДМСО): 4,40 (с, 2Н), 7,38-7,45 (м, 2Н), 7,64-7,68 (м, 1Н), 7,95 (м, 2Н), 8,12-8,23 (м, 3Н), 9,06 (ушир. с, 4Н), 9,96 (с, 1Н), 11,81 (ушир. с, 1Н).
Пример 11: гидрохлорид N'-{3-[2-({[(1Е)-амино(тиен-2-ил)метилен]амино}метил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
11.1) N'-{3-[2-({[(1Е)-амино(тиен-2-ил)метилен]амино}метил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид:
Данное соединение получают в соответствии с методикой, аналогичной таковой, описанной для стадии 4.3 примера 4, с соединением примера 10, замещающим промежуточный продукт 4.2. Ожидаемое соединение получали в форме порошка кремового цвета с выходом 80%.
МН+ = 407,2.
11.2) гидрохлоридN'-{3-[2-({[(1Е)амино(тиен-2-ил)метилен]амино}метил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Данное соединение получали из промежуточного продукта 11.1 в соответствии с методикой, аналогичной таковой по стадии 1.5 примера 1. Температура плавления: >300°С.
МН+ = 407, 2.
Соединение примера 12 получали в соответствии с методикой, аналогичной таковой, описанной для соединения примера 11.
Пример 12:гидрохлорид N'-{4-[2-({[(1Е)-амино(тиен-2-ил)метилен]амино}метил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Температура плавления: 227-228°С.
МН+ = 407,2.
Пример 13:гидрохлорид N-{3-[2-(2-циклогексилэтил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
13.1) 2-(2-циклогексилэтил)-4-(3-нитрофенил)-1Н-имидазол:
Данное соединение получают в соответствии с методикой, аналогичной таковой, описанной для стадии 4.1 примера 4, с циклогексилэтилкарбоновой кислотой и бромидом 3-нитрофенацила, замещающими N-(трет-бутоксикарбонил)глицин и бромид 4-азидофенацила. Ожидаемое соединение получали в форме желтого порошка с выходом 26%.
МН+ = 300,2.
13.2) 3-[2-(2-циклогексилэтил)-1Н-имидазол-4-ил]анилин:
Данное соединение получают в соответствии с методикой, аналогичной таковой, описанной для стадии 4.2 примера 4, с промежуточным продуктом 13.1, замещающим промежуточный продукт 4.1. Ожидаемое соединение получали в форме белого порошка с выходом 93%.
МН+ = 270,2.
13.3) N-{3-[2-(2-циклогексилэтил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамид:
Данное соединение получают в соответствии с методикой, аналогичной таковой, описанной для стадии 4.3 примера 4, с промежуточным продуктом 13.2, замещающим промежуточный продукт 4.2. Ожидаемое соединение получали в форме белого порошка с выходом 20%.
МН+ = 379,2.
13.4) гидрохлорид N-{3-[2-(2-циклогексилэтил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Данное соединение получали из промежуточного продукта 13.3 в соответствии с методикой, аналогичной таковой стадии 1.5 примера 1. Температура плавления: > 191-193°С.
МН+ = 379,2.
Соединения примеров 14-20 получают в соответствии с методикой, аналогичной таковой, описанной для соединения примера 13.
Пример 14:гидрохлорид N'-{3-[2-(1-пентилгексил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Температура плавления: 163,3°С.
МН+ = 423,2.
Пример 15:гидрохлорид N'-{4-[2-(2-циклогексилэтил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Температура плавления: 196,2°С.
МН+ = 379,2.
Пример 16:гидрохлорид N'-{3-[2-(циклогексилметил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Бледно-желтая пена.
МН+ = 365,2; в.у. = 7,40 мин.
Пример 17:гидрохлорид N'-{3-[2-(3-циклогексилпропил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Температура плавления: 180-181°С.
МН+ = 393,2.
Пример 18:гидрохлорид N'-[3-(2-гексил-1Н-имидазол-4-ил)фенил]тиофен-2-карбоксимидамида:
Бледно-желтая пена.
МН+ = 353,2; в.у. = 7,40 мин.
Пример 19:гидрохлорид N-{4-[2-(2-циклогексилэтил)-1Н-имидазол-4-ил]фенил}-N"-нитрогуанидина:
Температура плавления: 185-186°С.
МН+ = 357,2.
Соединения примеров 20-23 получают в соответствии с методикой, аналогичной таковой, описанной для соединения примера 4.
Пример 20:гидрохлорид N'-(4-{2-[(циклогептиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
Температура плавления: 264-265°С.
Пример 21:гидрохлорид N'-(4-{2-[(метиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
Температура плавления: >250°С.
Пример 22:гидрохлорид N'-(4-{2-[(циклобутиламино)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
Температура плавления: 263-264°С.
Пример 23:гидрохлорид N'-[4-(2-{[(2,2-дифенилэтил)амино]метил}-1Н-имидазол-4-ил)фенил]тиофен-2-карбоксимидамида:
Температура плавления: >250°С реагент, используемый на последней стадии, 3, 3-дифенилпропанал, получают из коммерческих соединений, адаптированных в соответствии с протоколом, подобным таковому, описанному в J. Org. Chem. (1990), 55(17), 5078-88].
Соединение по примеру 24 получают в соответствии с методикой, аналогичной таковой, описанной для соединения примера 11.
Пример 24:гидрохлорид N'-{3-[2-(2{[(1E)-амино(тиен-2-ил)метилен]амино}этил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Температура плавления: >245°С.
Соединения примеров 25-27 получают в соответствии с методикой, аналогичной таковой, описанной для соединения примера 13.
Пример 25:гидрохлорид N'-(3-{2-[(фенилтио)метил]-1Н-имидазол-4-ил}фенил)тиофен-2-карбоксимидамида:
Данное соединение получают в форме бледно-желтой пены.
МН+ = 391,1; в.у. = 7, 30 мин.
Пример 26:гидрохлорид N'-(4-{2-[(фенилтио)метил]-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Данное соединение получают в форме бледно-желтой пены.
МН+ = 391,1; в.у. = 7,30 мин.
Пример 27:гидрохлорид N'-{3-[2-(4-изобутилбензил)-1Н-имидазол-4-ил]фенил}тиофен-2-карбоксимидамида:
Температура плавления: 214-216°С получение исходного соединения, (4-изобутилфенил)уксусной кислоты, было описано в РСТ заявке WO02/102375 - см. пример 1, стадия 1 данного документа].
Фармакологическое исследование продуктов по изобретению
Тест связывания натриевых каналов коры головного мозга крыс
Тест состоит в измерении взаимодействия соединений по сравнению со связыванием меченного тритием батрахотоксина с потенциалозависимыми натриевыми каналами в соответствии с протоколом, описанным Brown (J. Neurosci. (1986), 6, 2064-2070).
Получение гомогенатов коры головного мозга крыс
Кору головного мозга крыс Sprague-Dawley 230-250 г (Charles River, France) удаляли, взвешивали и гомогенизировали с использованием размолочной машины Поттера, снабженной тефлоновым клапаном (10 обратных ходов) в 10 объемах буфера для выделения, композиция которого следующая (сахароза 0,32 М; K2HPO4 5 мМ; рН 7,4). Гомогенат подвергали первому центрифугированию при 1000 g в течение 10 минут. Супернатант удаляли и центрифугировали при 20000 g в течение 15 минут. Осадок помещали в буфер для выделения и центрифугировали при 20000 g в течение 15 минут. Полученный осадок ресуспендировали в инкубационном буфере (50 мМ HEPES; 5,4 мМ KCl; 0,8 мМ MgSO4; 5,5 мМ глюкозы; 130 мМ хлорида холина, рН 7,4), затем делили на аликвоты и хранили при -80°С до дня исследования. Окончательная концентрация белка составляла от 4 до 8 мг/мл. Анализ белка проводили с использованием набора, продаваемого BioRad (France).
Измерение связывания меченного тритием батрахотоксина
Реакцию связывания проводили путем инкубирования в течение 1 часа 30 минут при 25°С 100 мкм гомогената коры головного мозга крыс, содержащего 75 мкг белка со 100 мкл [3H] бензоата батрахотоксина-А 20 альфа (37,5 Ки/ммоль, NEN) при 5 нМ (окончательная концентрация) 200 мкл тетродотоксина при 1 мкМ (окончательная концентрация) и ядом скорпиона при 40 мкг/мл (окончательная концентрация) и 100 мкл инкубационного буфера отдельно или в присутствии тестируемых продуктов в различных концентрациях. Неспецифическое связывание определяли в присутствии 300 мкМ вератридина и значение этого неспецифического связывания вычитали из всех других значений. Затем образцы фильтровали с использованием Brandel (Gaithersburg, Maryland, USA) с использованием планшетов Unifilter GF/C, заранее инкубированных с 0,1% полиэтиленимином (20 мкл/ячейку) и промытых дважды 2 мл фильтрационного буфера (5 мМ HEPES; 1,8 мМ CaCl2; 0,8 мМ MgSO4; 130 мМ хлорида холина; рН 7,4). После добавления 20 мкл Microscint 0® радиоактивность рассчитывали с использованием жидкостного сцинтилляционного счетчика (Topcount, Packard). Измерение проводили в двух экземплярах. Результаты выражаются в % специфического связывания меченного тритием батрахотоксина по отношению к контролю.
Результаты
Соединения по примерам 1-9, 11-20 и 22-27, описанные выше, все имели ИК50, менее или равную 10 мкМ.
Исследование эффектов на нейрональную конститутивную NO синтазу мозжечка крыс
Ингибирующую активность продуктов по изобретению определяли путем измерения их эффектов на превращение NO-синтазой [3H]L-аргинина в [3H]L-цитруллин в соответствии с модифицированным методом Bredt and Snyder (Proc. Natl. Acad. Sci. USA, (1990) 87: 682-685).
Получение гомогенатов мозжечков крыс
Мозжечки крыс Sprague-Dawley (300 г - Charles River) быстро удаляли, взвешивали и гомогенизировали в 5 объемах экстракционного буфера (50 мМ HEPES; 1 мМ ЭДТА; рН 7,4, пепстатин А 10 мг/мл, лейпептин 10 мг/мл). Затем гомогенаты центрифугировали при 35000 g в течение 1 часа при 4°С. Затем супернатант пропускали через колонку из смолы DOWEX 50W-X8, натриевую форму помещали в экстракционный буфер, с целью удаления эндогенного аргинина. Полученные препараты делили на аликвоты и хранили при -80°С.
Исследование активности нейрональной NOS
Инкубационный буфер состоял из 100 мМ HEPES (рН 7,4), 2 мМ ЭДТА, 2,5 мМ CaCl2, 2мМ дитиотреитола, 2 мМ восстановленного НАДФН, 10 мкг/мл кальмодулина, 10 мкМ FAD, 10 мкМ FMN и 10 мкМ BH4. Тестируемые продукты растворяли в этом буфере. Реакцию проводили инкубированием в течение 15 минут при 37°С 100 мкл инкубационного буфера, содержащего ингибиторы, 25 мкл раствора, содержащего 62,5 нМ [3H]L-аргинина (специфическая активность: 56,4 Ки/ммоль, Perkin-Elmer) и 25 мкМ нерадиоактивного L-аргинина, 25 мкл инкубационного буфера и 50 мкл препарата фермента, разведенного в 10 раз в 50 мМ буфера HEPES. Реакцию останавливали 2 мл 20 мМ буфера HEPES, рН 5,5, содержащего 2 мМ ЭДТА. Все образцы пропускали через колонку из 1 мл смолы DOWEX 50W-X8, натриевую форму, вложенную в останавливающий буфер. После добавления 16 мл сцинтилляционной жидкости (Ultima Gold, Packard), определяли количество радиоактивности жидкостным сцинтилляционным счетчиком (Winspectral 1410, Wallac). Измерения проводили в двух экземплярах. Каждая серия измерений включала 2 пробирки, не содержащие фермент (реакция гасила значение, которое вычитали из каждого измерения), и 2 пробирки, не содержащие ингибитор (контрольная реакция). Результаты выражали как процент реакции ингибирования ферментом (контрольное значение реакции).
Результаты
Соединения по примерам 1-13, 15, 16 и 18-26, описанные выше, все имели ИК50, менее или равную 10 мкМ.
Реферат
Описывается соединение общей формулы (I), в которой R1 и R2 представляют собой атом водорода или алкильный радикал, R3 обозначает атом водорода, Х представляет собой связь или линейный или разветвленный алкиленовый радикал, Y обозначает атом водорода, циклоалкильный радикал, NR4R5, OR14 или SR15 радикал или
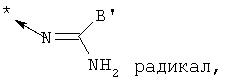
где В' обозначает тиенил, или также Y обозначает возможно замещенный арильный радикал; А представляет собой связь или фениленовый радикал; В обозначает NR6R7 радикал или тиенил. Описывается также применение арилимидазола общей формулы (I) в качестве лекарственного препарата, предназначенного для лечения или предотвращения боли. Соединения формулы (I) могут быть использованы в качестве ингибиторов NO синтазы и в качестве модуляторов натриевых каналов. 2 н. и 5 з.п. ф-лы.
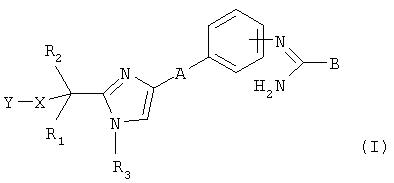
Формула
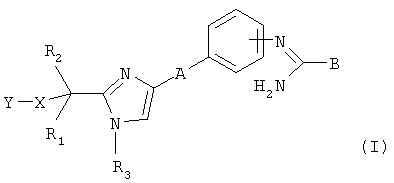
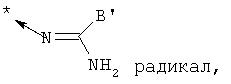
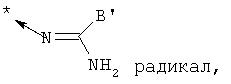
Документы, цитированные в отчёте о поиске
Производные 2-(иминометил)аминофенила, способ их получения, фармацевтическая композиция на их основе и промежуточные вещества

Комментарии