Замещенные хроман-6-илоксициклоалканы, их применение в качестве лекарственных средств - RU2666350C2
Код документа: RU2666350C2
Описание
Настоящее изобретение относится к замещенным хроман-6-илоксициклоалканам формулы I,
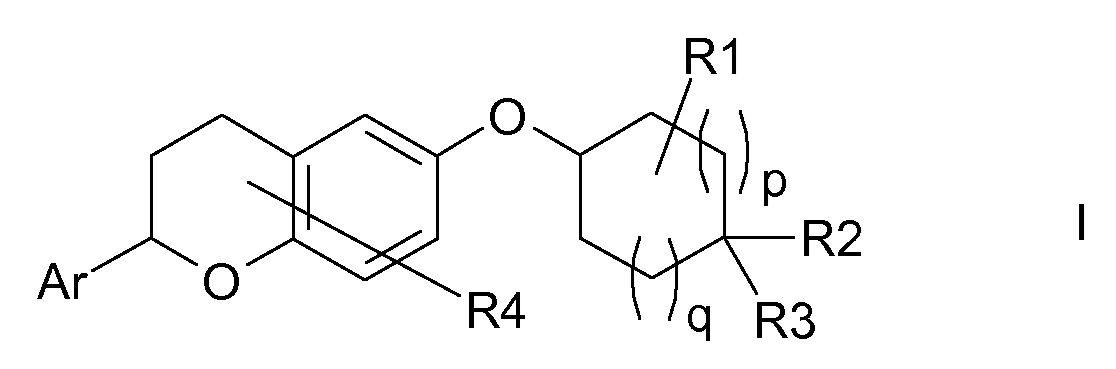
в которой Ar, R1-R4, p и q являются такими, как определено ниже. Соединения формулы I являются ингибиторами натрий-кальциевого обмена (NCX), в особенности натрий-кальциевого обмена подтипа 1 (NCX1), и являются подходящими для лечения различных нарушений, при которых нарушен внутриклеточный кальциевый гомеостаз, таких как аритмии, сердечная недостаточность и удар. Кроме того, настоящее изобретение относится к способам получения соединений формулы I, к их применению в качестве лекарственных средств и к содержащим их фармацевтическим композициям.
За последнее десятилетие достигнуты большие успехи в фармакологической терапии сердечной недостаточности (HF) или застойной сердечной недостаточности (CHF). Установлено, что бета-блокаторы и ингибиторы системы ренин-ангиотензин-альдостерон оказывают благоприятное влияние при CHF с точки зрения смертности и улучшения симптомов (K. Dickstein et al., Eur. J. Heart Fail. 10 (2008): 933-989). Тем не менее, заболеваемость и смертность остаются неприемлемо высокими. Количество пациентов, страдающих CHF, и, в частности, более тяжелыми формами CHF, даже увеличивается, отчасти парадоксально, вследствие успеха этих методик лечения. Таким образом, необходимы средства, которые способствуют улучшению результата лечения CHF и улучшают качество жизни. Блокаторы натрий-кальциевого обмена (NCX), транспортного бела, который участвует в регуляции содержания кальция и натрия в клетках, перспективны для улучшения прогноза при CHF и качества жизни.
Функцией NCX является выведение кальция из кардиомиоцитов и клеток других типов, таких как нейроны. Показано, что при CHF NCX характеризуется повышенной регуляцией и поэтому выводит кальций из клеток и дополнительно уменьшает сократительную способность миокарда (M. Flesch et al., Circulation 94 (1996): 992-1002; G. Hasenfuss et al., Circulation 99 (1999): 641-648). Недостаточность нагнетательной функции сердца при CHF обусловлена не только необратимыми структурными изменениями и утратой миокарда, но и неблагоприятными функциональными изменениями, включающими нарушение внутриклеточного кальциевого гомеостаза. Последнее можно лечить ингибированием NCX. Описаны три подтипа NCX. В сердце экспрессируется преимущественно подтип 1.
При NCX кальций заменяется на натрий и внеклеточный натрий является движущей силой для обмена. Стехиометрия обмена является такой, что три иона натрия поступают в клетку для выведения одного иона кальция. Эта стехиометрия приводит к направленному внутрь потоку, который по своей природе является деполяризующим. Деполяризующий поток, если он достаточно велик, может вызвать следовые деполяризации желудочкового и предсердного потенциала действия. Следовые деполяризации являются колебаниями электрического мембранного потенциала и могут происходить во время (ранние следовые деполяризации, EAD) или после (запаздывающие следовые деполяризации, DAD) потенциала действия сердца. Возникновение EAD связывают с пролонгированным желудочковым потенциалом (наблюдается в виде увеличенного интервала QT на электрокардиограмме (ECG)), что является обычной особенностью сердечной недостаточности. Предполагается, что следовые деполяризации являются основной причиной аритмии сердца и поэтому их также называют триггерной активностью (D. M. Bers et al., Ann. N. Y. Acad. Sci. 1080 (2006): 165-177; K. R. Sipido et al., Pflugers Arch. 430 (1995): 871-878; A. O. Verkerk et al., Circulation 104 (2001): 2728-2733; C. Pott et al., Current Drug Targets 12 (2011): 737-747; G. Antoons et al., Pharmacol. Ther. 134 (2012): 26-42). Ранние экстрасистолы, возникающие вследствие индуцированных посредством NCX деполяризующих потоков, могут привести к появлению более комплексных и необратимых аритмий, таких как приступы тахикардии, трепетания желудочков или фибрилляции желудочков.
Пациенты, страдающие недостаточностью нагнетательной функции сердца, или сердечной недостаточностью, обычно страдают от аритмий и подвержены смерти от аритмии. Примерно 50% случаев смерти от заболеваний сердца при CHF составляют смерти от аритмии. Поэтому блокада NCX является средством уменьшения недостаточности нагнетательной функции сердца и связанных с ней симптомов, а также снижения количества смертей от аритмии. Современные лекарственные средства с положительным инотропным воздействием характеризуются проаритмическими воздействиями, которые или увеличивают смертность, как в случае ингибиторов фосфодиэстеразы, или устраняют благоприятные воздействия, обеспечиваемые уменьшением недостаточности нагнетательной функции сердца положительными инотропными воздействиями (J. T. Parissis et al., Curr. Opin. Crit. Care 16 (2010): 432-441). С другой стороны, целый ряд клинически применяющихся противоаритмических лекарственных средств оказывают неблагоприятное инотропное воздействие на сердце, ухудшая симптомы сердечной недостаточности. Блокаторы NCX являются терапевтически уникальными, поскольку они могут решить две основные задачи при CHF, недостаточность нагнетательной функции сердца и аритмии.
Блокада NCX представляет особый интерес для запущенных стадий CHF, таких как относящихся к классам III и IV NYHA (Нью-Йоркская кардиологическая ассоциация) в соответствии с функциональной классификацией сердечной недостаточности, при которых терапевтические средства, т.е. бета-блокаторы, ингибиторы системы ренин-ангиотензин-альдостерон, диуретики и сосудорасширяющие средства, уже полностью использованы. Новой появившейся группой являются пожилые пациенты с прогрессированием на конечную стадию HF. На этой поздней стадии для значительной части пациентов больше не является желательным сосудорасширяющий эффект, поскольку артериальное давление уже снижено вследствие недостаточности нагнетательной функции сердца. Недостатками ингибиторов фосфодиэстеразы, как средств с положительным инотропным действием, является не только то, что они проаритмические, но и то, что они обладают сосудорасширяющим действием.
Фибрилляция предсердий (AF) является наиболее часто встречающейся аритмией. От AF страдает примерно 6,8 миллионов пациентов в США и Европейском Союзе и ее распространенность сильно возрастает вследствие старения населения и успешного лечения инфаркта миокарда, заболевания коронарной артерии и застойной сердечной недостаточности. AF приводит примерно к 25% всех случаев удара и к увеличению смертности. Кроме того, показано, что при AF наблюдается повышенная регуляция NCX (U. Schotten et al., Cardiovasc. Res. 53 (2002): 192-201). Повышенная регуляция NCX может участвовать в индуцировании AF вследствие аритмогенной активности NCX и ее поддержания и, следовательно, блокаторы NCX оказывают терапевтически благоприятные воздействия при терапии и предупреждении AF. Поскольку частота заболевания AF увеличивается у стареющего населения и она часто связана с сердечной недостаточностью у достигающего примерно 45% количества пациентов (I. Savelieva et al., Europace 5 Suppl 1 (2004): S5-S19), блокаторы NCX особенно благоприятны для пациентов, страдающих AF и CHF.
Поскольку блокаторы NCX также оказывают положительное инотропное воздействие на предсердия, они могут быть особенно полезны при диастолической сердечной недостаточности, при которой наполнение желудочков является главной проблемой вследствие увеличения жесткости желудочков. Более энергичное сокращение предсердий должно улучшить наполнение желудочков при диастолической сердечной недостаточности.
Поскольку уменьшенный минутный сердечный выброс оказывает вредное влияние на кровоток в органах, таких как почки, головной мозг и сердце, ингибирование NCX, которое приводит к увеличению сократительной способности сердца, может привести к улучшению кровотока в головном мозге, сердце и почках с целью лечения или предупреждения удара, слабоумия и болезни Альцгеймера, почечной недостаточности и ишемии сердца. Поскольку NCX также участвует в чувствительной к солям гипертензии, его ингибирование также применимо для лечения гипертензии.
Ингибиторы NCX также применимы для лечения или предупреждения опасных для жизни патологических состояний, при которых инотропная поддержка необходима для обеспечения достаточного кровоснабжения. Они включают все формы шока, гемодинамический шок, кардиогенный шок и септический шок. Ингибиторы NCX являются особенно подходящими для лечения этих патологических состояний, поскольку они не влияют на частоту сердечных сокращений и не оказывают проаритмические или сосудорасширяющие воздействия, как другие инотропные лекарственные средства.
При ударе блокаторы NCX могут улучшать результаты лечения, поскольку при гипоксии нейронов, происходящей при ударе, NCX обращает направление переноса и вводит в клетки кальций, что приводит к перегрузке кальцием. Это приводит к ускоренной гибели клеток вследствие избыточных внутриклеточных концентраций кальция. Кроме того, низкий минутный сердечный выброс может привести к ишемии головного мозга, благоприятствующей удару. Блокаторы NCX увеличивают минутный сердечный выброс и улучшают кровоток в головном мозге. Следовательно, блокаторы NCX перспективны для лечения или предупреждения удара (T. Matsuda et al., J. Pharmacol. Exp. Ther. 298 (2001): 249-256).
Некоторые соединения, способные ингибировать NCX, уже описаны, например, в EP 0978506, JP 2008/189592, WO 2004/000813, WO 2004/063191, WO 03/006452, WO 02/32883, WO 97/09306. Однако необходимы дополнительные соединения, которые ингибируют NCX и являются подходящими для применения в качестве лекарственных средств для лечения указанных выше патологических состояний. Установлено, что соединения формулы I являются превосходными ингибиторами натрий-кальциевого обмена (NCX), в особенности натрий-кальциевого обмена подтипа 1 (NCX1), и обладают профилем характеристик, благоприятным для такого применения.
Таким образом, объектом настоящего изобретения являются соединения формулы I в любых из их стереоизомерных форм и смеси стереоизомерных форм в любом соотношении и их фармацевтически приемлемые соли,
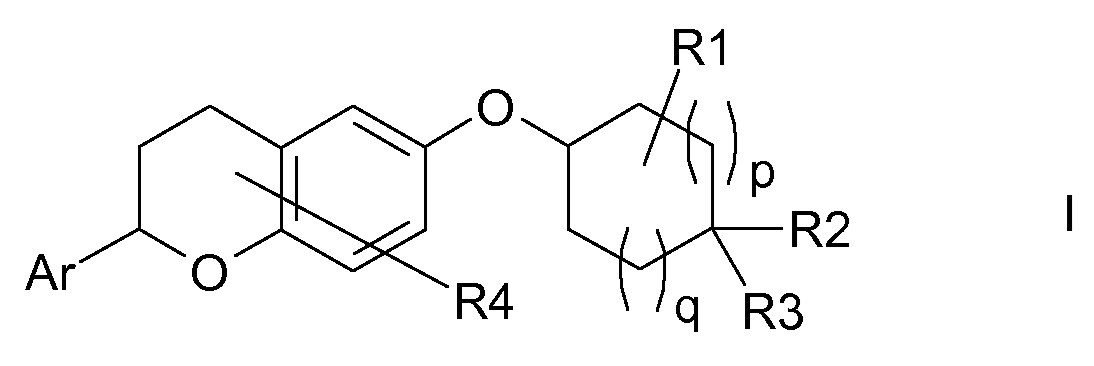
в которой
Ar означает фенил, который является незамещенным или содержит один или несколько одинаковых или разных заместителей R0;
R0 выбран из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O- и (C3-C7)-циклоалкил-(C1-C4)-алкил-O-, и две группы R0, связанные с соседними кольцевыми атомами углерода в Ar, вместе с атомами углерода, с которыми они связаны, могут образовать 5-7-членное мононенасыщенное кольцо, которое содержит 0, 1 или 2 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу, и которое является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
R1 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
R2 выбран из группы, включающей водород, (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, (C1-C6)-алкил-C(O)-O-, фенил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20;
R3 выбран из группы, включающей водород и (C1-C6)-алкил, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей (C3-C7)-циклоалкил, фенил, HO- и (C1-C4)-алкил-O-;
или группы R2 и R3 вместе означают оксогруппу;
R4 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-;
R5 и R6 независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, фенил, Het1 и Het2, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и фенил и Het1 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R22,
или группы R5 и R6 вместе с атомом азота, с которыми они связаны, образуют 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который в дополнение к атому азота, с которым связаны R5 и R6, содержит 0 или 1 дополнительный кольцевой гетероатом, выбранный из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей R21;
R7 выбран из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, фенил, Het1 и Het2, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и фенил и Het1 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R22;
R8 выбран из группы, включающей водород и (C1-C4)-алкил;
R9 выбран из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, фенил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-;
R10 выбран из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, фенил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-;
R20 выбран из группы, включающей R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, (C3-C7)-циклоалкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-;
R21 выбран из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, R34-O-C(O)-(C1-C4)-алкил-, R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, (C3-C7)-циклоалкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-;
R22 выбран из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, (C3-C7)-циклоалкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, R33-O-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, NC-, R33-C(O)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-;
R24 означает 3-10-членное моноциклическое или бициклическое кольцо, которое является насыщенным, частично ненасыщенным или ароматическим и содержит 0, 1, 2, 3 или 4 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу, и которое является незамещенным или содержит один или несколько одинаковых или разных заместителей R22;
R30 и R33 независимо друг от друга выбраны из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, фенил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-;
R31 и R32 независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, фенил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-,
или группы R31 и R32 вместе с атомом азота, с которыми они связаны, образуют 4-7-членный моноциклический насыщенный гетероцикл, который в дополнение к атому азота, с которым связаны R31 и R32, содержит 0 или 1 дополнительный кольцевой гетероатом, выбранный из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
R34 выбран из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, фенил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-;
Het1 означает 5-членный или 6-членный моноциклический ароматический гетероцикл, который содержит 1, 2 или 3 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-, если не указано иное;
Het2 означает 4-10-членный моноциклический или бициклический насыщенный или частично ненасыщенный гетероцикл, который содержит 1 или 2 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу;
n выбран из группы, включающей 0, 1 и 2, где все числа не зависят друг от друга;
p и q независимо друг от друга выбраны из группы, включающей 0 и 1;
где все фенильные группы являются незамещенными или содержат один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-, если не указано иное;
где все циклоалкильные и бициклоалкильные группы независимо от любых других заместителей, которые могут содержаться в циклоалкильной или бициклоалкильной группе, могут содержать один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
где все алкильные группы независимо от любых других заместителей, которые могут содержаться в алкильной группе, могут содержать один или несколько фторидных заместителей.
Если группа R1 означает водород, то к атомам углерода циклоалканового кольца в соединениях формулы I и во всех других соединениях, в которых содержится R1, присоединены атомы водорода, только за исключением групп R2 и R3 и атома кислорода, связывающего циклоалкановое кольцо с хромановым кольцом. Группы R1 в соединениях формулы I и во всех других соединениях, в которых содержится R1, которые отличаются от водорода, т.е. фтор и (C1-C4)-алкильные заместители, представляющие собой R1, могут быть связаны с любым из кольцевых атомов углерода циклоалканового кольца, представленных в формуле I, который содержит свободный центр связывания, т.е. с любым кольцевым атомом углерода циклоалканового кольца кроме кольцевого атома углерода, содержащего группы R2 и R3, что указано связью, исходящей из R1, которая не направлена на конкретный атом углерода. Аналогичным образом, если группа R4 означает водород, то хромановое кольцо в соединениях формулы I и во всех других соединениях, в которых содержится R4, содержит атомы водорода, только за исключением группы Ar и атома кислорода, связывающего хромановое кольцо с циклоалкановым кольцом. Группы R4 в соединениях формулы I и во всех других соединениях, в которых содержится R4, которые отличаются от водорода, т.е. галоген, (C1-C4)-алкил и (C1-C4)-алкил-O- заместители, представляющие собой R4, могут быть связаны с любым из атомов углерода хроманового кольца, представленных в формуле I, который содержит свободный центр связывания, т.е. с атомами углерода, находящимися в положениях 2, 3, 4, 5, 7 и 8 хроманового кольца, как показано в формуле I', что указано связью, исходящей из R4, которая не направлена на конкретный атом углерода хроманового кольца.
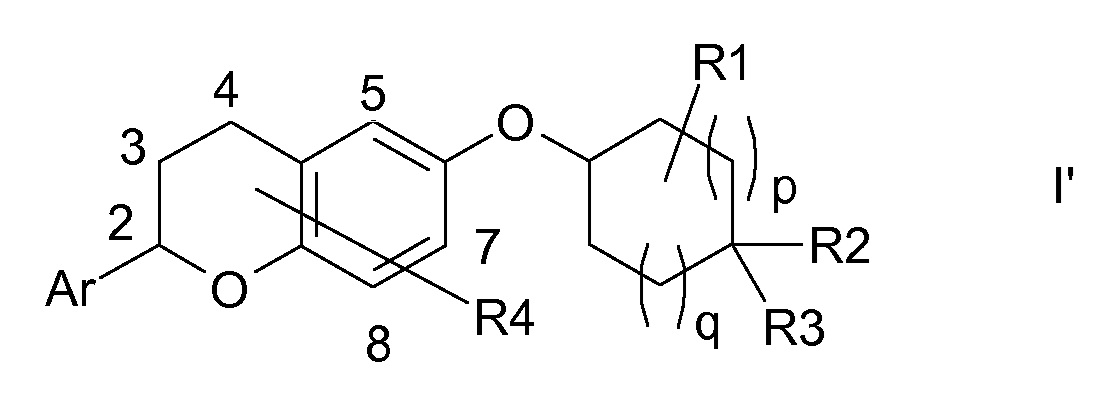
Во всех свободных центрах связывания атомов углерода в положениях 2, 3, 4, 5, 7 и 8 хроманового кольца, которые не заняты группами R4, отличающимися от водорода, а также во всех свободных центрах связывания циклоалканового кольца, которые не заняты группами R1, отличающимися от водорода, содержится атом водорода. Т.е., если в соединении формулы I не содержится группа R4, которая отличается от водорода, атомы углерода, находящиеся в положениях 2, 5, 7 и 8 хроманового кольца, содержат один атом водорода и атомы углерода, находящиеся в положениях 3 и 4 хроманового кольца, содержат два атома водорода. Если в соединении формулы I не содержится группа R1, которая отличается от водорода, кольцевой атом углерода циклоалканового кольца, который содержит атом кислорода, связанный с хромановым кольцом, содержит один атом водорода и другие кольцевые атомы углерода кроме атома, содержащего R2 и R3, содержат два атома водорода. Соединения формулы I, в которых не содержится группа R4 и/или не содержится группа R1, которая отличается от водорода, альтернативно можно представить модифицированной формулой I, в которой R4 и/или R1 и начинающиеся на них связи опущены. Если содержатся заместители R4 и/или R1, т.е. атомы или группы, представляющие собой R4 и/или R1, которые отличаются от водорода, один или несколько указанных атомов водорода заменены заместителями.
Если структурные элементы, например, такие как группы, заместители или числа, могут содержаться в соединениях формулы I несколько раз, все они независимы друг от друга и в каждом случае могут обладать любым из указанных значений и в каждом случае они могут быть идентичны любому другому такому элементу или отличаться от него. Например, в диалкиламиногруппе алкильные группы могут быть одинаковыми или разными.
Алкильные группы, т.е. насыщенные углеводородные остатки, могут быть линейными (обладающими линейной цепью) или разветвленными. Это также относится к случаю, когда эти группы являются замещенными или являются частью другой группы, например, -O-алкильной группы (алкилоксигруппы, алкоксигруппы) или HO-замещенной алкильной группы (-алкил-OH, гидроксиалкильная группа). В зависимости от соответствующего определения количество атомов углерода в алкильной группе может равняться 1, 2, 3, 4, 5 или 6, или 1, 2, 3 или 4, или 1, 2 или 3, или 1 или 2, или 1. Примерами алкилов являются метил, этил, пропил, включая н-пропил и изопропил, бутил, включая н-бутил, втор-бутил, изобутил и трет-бутил, пентил, включая н-пентил, 1-метилбутил, изопентил, неопентил и трет-пентил и гексил, включая н-гексил, 3,3-диметилбутил и изогексил. Примерами -O-алкильных групп являются метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, изобутоксигруппа, трет-бутоксигруппа, н-пентоксигруппа. Примерами алкил-S(O)n- являются метилсульфанил- (CH3-S-), метансульфинил- (CH3-S(O)-), метансульфонил (CH3-S(O)2-), этилсульфанил- (CH3-CH2-S-), этансульфинил- (CH3-CH2-S(O)-), этансульфонил (CH3-CH2-S(O)2-), 1-метилэтилсульфанил- ((CH3)2CH-S-), 1-метилэтансульфинил- ((CH3)2CH-S(O)-), 1-метилэтансульфонил ((CH3)2CH-S(O)2-). В одном варианте осуществления настоящего изобретения число n выбрано из группы, включающей 0 и 2, где все числа n независимы друг от друга и могут быть одинаковыми или разными. В другом варианте осуществления число n в любом из его случаев появления независимо от его значений в других случаях появления равно 0. В другом варианте осуществления число n в любом из его случаев появления независимо от его значений в других случаях появления равно 2.
Замещенная алкильная группа может быть замещена в любых положениях при условии, что соответствующее соединение является достаточно стабильным и применимым в качестве фармацевтически активного соединения. Обязательным является условие о том, чтобы конкретная группа и соединение формулы I были достаточно стабильными и применимыми в качестве фармацевтически активного соединения, которое в целом относится к определениям всех групп, содержащихся в соединениях формулы I. В качестве примеров замещенных алкильных групп, в особенности HO-(C1-C4)-алкильных групп, можно отметить, например, гидроксиметил, 1-гидроксиэтил, 2-гидроксиэтил, 1-гидроксипропил, 2-гидроксипропил, 3-гидроксипропил, 1-гидрокси-1-метилэтил, 2-гидрокси-1-метилэтил, 1-гидроксибутил, 4-гидроксибутил, 2-гидрокси-1-метилпропил или 2-гидрокси-1-метилпропил.
Независимо от любых других заместителей, которые могут находиться в алкильной группе, и, если не указано иное, алкильные группы могут быть замещены одним или несколькими фторидными заместителями, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или 11 фторидными заместителями, или 1, 2, 3, 4 или 5 фторидными заместителями, или 1, 2 или 3 фторидными заместителями, которые могут находиться в любых положениях. Т.е. независимо от любых других заместителей, которые могут находиться в алкильной группе, алкильная группа может не быть замещена фторидными заместителями, т.е. не содержать фторидные заместители или содержать фторидные заместители, где все алкильные группы в соединениях формулы I независимы друг от друга применительно к необязательному замещению фторидными заместителями. Например, во фторзамещенной алкильной группе одна или несколько метильных групп могут содержать три фторидных заместителя каждая и находиться в виде трифторметильных групп и/или одна или несколько метиленовых групп (CH2) может содержать два фторидных заместителя каждая и находиться в виде дифторметиленовых групп. Пояснения о замещении группы фтором также относятся к случаю, когда группа дополнительно содержит другие заместители и/или является частью другой группы, например, -O-алкильной группы. Примерами фторзамещенных алкильных групп являются трифторметил, 2-фторэтил, 1-фторэтил, 1,1-дифторэтил, 2,2,2-трифторэтил, пентафторэтил, 3,3,3-трифторпропил, 2,2,3,3,3-пентафторпропил, 4,4,4-трифторбутил и гексафторизопропил. Примерами фторзамещенных -O-алкильных групп являются трифторметоксигруппа (-OCF3), 2,2,2-трифторэтоксигруппа, пентафторэтоксигруппа и 3,3,3-трифторпропоксигруппа. Примерами фторзамещенных групп алкил-S(O)n- являются трифторметилсульфанил- (CF3-S-), трифторметансульфинил - (CF3-S(O)-) и трифторметансульфонил (CF3-S(O)2-). Применительно ко всем группам или заместителям в соединениях формулы I, которыми может быть алкильная группа, которая обычно может содержать один или несколько фторидных заместителей, в качестве примера групп или заместителей, содержащих фторзамещенный алкил, который можно включить в определение группы или заместителя, можно отметить группу CF3 (трифторметил) или соответствующие группы, такие как CF3-O- или CF3-S-.
Приведенные выше пояснения для алкильных групп соответственно относятся к алкильным группам, которые в соответствии с определением группы в соединениях формулы I связаны с двумя соседними группами или соединены с двумя группами, и могут рассматриваться, как двухвалентные алкильные группы (алкандиильные группы), как в случае алкильного фрагмента замещенной алкильной группы. Таким образом, такие группы также могут быть линейными или разветвленными, связи с соседними группами могут находиться в любых положениях и могут исходить из одного и того же атома углерода или из разных атомов углерода, и они могут быть незамещенными или замещенными фторидными заместителями независимо от любых других заместителей. Примерами таких двухвалентных алкильных групп являются -CH2-, -CH2-CH2-, -CH2-CH2-CH2-, -CH2-CH2-CH2-CH2-, -CH(CH3)-, -C(CH3)2-, -CH(CH3)-CH2-, -CH2-CH(CH3)-, -C(CH3)2-CH2-, -CH2-C(CH3)2-. Примерами фторзамещенных алкандиильных групп, которые могут содержать 1, 2, 3, 4, 5 или 6 фторидных заместителей, например, являются -CHF-, -CF2-, -CF2-CH2-, -CH2-CF2-, -CF2-CF2-, -CF(CH3)-, -C(CF3)2-, -C(CH3)2-CF2-, -CF2-C(CH3)2-.
Приведенные выше пояснения для алкильных групп соответственно относятся к ненасыщенным углеводородным остаткам, т.е. алкенильным группам, которые в одном варианте осуществления настоящего изобретения содержат одну двойную связь. Так, например, алкенильные группы также могут быть линейными или разветвленными. Двойные связи могут находиться в любых положениях. Количество атомов углерода в алкенильной группе может равняться, например, 2, 3, 4, 5 или 6, или 2, 3, 4 или 5, или 3, 4 или 5. Примерами алкенила являются этенил (винил), проп-1-енил, проп-2-енил (аллил), бут-2-енил, бут-3-енил, 2-метилпроп-2-енил, 3-метилбут-2-енил, гекс-3-енил, гекс-4-енил, 4-метилпент-3-енил. В одном варианте осуществления настоящего изобретения алкенильные группы содержат по меньшей мере 3 атома углерода и связаны с остальной части молекулы через атом углерода, который не является частью двойной связи.
Количество кольцевых атомов углерода в (C3-C7)-циклоалкильной группе может равняться 3, 4, 5, 6 или 7. Примерами циклоалкилов являются циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Количество кольцевых атомов углерода в (C6-C10)-бициклоалкильной группе может равняться 6, 7, 8, 9 или 10. Два цикла в бициклоалкильной группе могут содержать 1, 2 или несколько общих кольцевых атомов углерода и она может быть конденсированной или образовать мостиковый бицикл или спироцикл. Примерами бициклоалкила являются бицикло[2.1.1]гексил, бицикло[2.2.1]гептил, бицикло[3.1.1]гептил, бицикло[2.2.2]октил, бицикло[3.2.1]октил, бицикло[3.2.2]нонил и бицикло[4.4.0]децил. Бициклоалкильные группы могут быть присоединены через любой кольцевой атом углерода. Независимо от любых других заместителей, которые могут содержаться в циклоалкильной группе или бициклоалкильной группе, и, если не указано иное, циклоалкильные группы и бициклоалкильные группы могут быть замещены одним или большим количество (C1-C4)-алкильных заместителей, например, 1, 2, 3 или 4 одинаковыми или разными (C1-C4)-алкильными заместителями, например, метильными группами, которые могут находиться в любых положениях. Т.е. независимо от любых других заместителей, которые могут содержаться в циклоалкильной группе или бициклоалкильной группе, циклоалкильные группы и бициклоалкильные группы могут не быть замещены (C1-C4)-алкильными заместителями, т.е. не содержать (C1-C4)-алкильные заместители или быть замещены (C1-C4)-алкильными заместителями, где все циклоалкильные группы и бициклоалкильные группы в соединениях формулы I не зависят друг от друга применительно к необязательному замещению (C1-C4)-алкильными заместителями. Примерами таких алкилзамещенных циклоалкильных групп и бициклоалкильных групп являются 1-метилциклопропил, 2,2-диметилциклопропил, 1-метилциклопентил, 2,3-диметилциклопентил, 1-метилциклогексил, 4-метилциклогексил, 4-изопропилциклогексил, 4-трет-бутилциклогексил, 3,3,5,5-тетраметилциклогексил, 7,7-диметилбицикло[2.2.1]гептил, 6,6-диметилбицикло[3.1.1]гептил и 1,7,7-триметилбицикло[2.2.1]гептил.
Независимо от любых других заместителей, включая (C1-C4)-алкильные заместители, которые могут находиться в циклоалкильной группе или бициклоалкильной группе, и, если не указано иное, циклоалкильные группы и бициклоалкильные группы могут дополнительно быть замещены одним или несколькими фторидными заместителями, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или 11 фторидными заместителями, или 1, 2, 3, 4 или 5 фторидными заместителями, или 1, 2 или 3 фторидными заместителями, которые могут находиться в любых положениях и также могут находиться в (C1-C4)-алкильном заместителе. Т.е. независимо от любых других заместителей, которые могут содержаться в циклоалкильной группе или бициклоалкильной группе, циклоалкильные группы и бициклоалкильные группы могут не быть замещены фторидными заместителями, т.е. не содержать фторидные заместители, или могут быть замещены фторидными заместителями, где все циклоалкильные группы и бициклоалкильные группы в соединениях формулы I независимы друг от друга применительно к необязательному замещению фторидными заместителями. Примерами фторзамещенных циклоалкильных групп и бициклоалкильных групп являются 1-фторциклопропил, 2,2-дифторциклопропил, 3,3-дифторциклобутил, 1-фторциклогексил, 4,4-дифторциклогексил, 3,3,4,4,5,5-гексафторциклогексил, 1-фторбицикло[2.2.2]октил и 1,4-дифторбицикло[2.2.2]октил. Циклоалкильные группы также могут быть одновременно замещены фтором и алкилом. Примерами группы (C3-C7)-циклоалкил-(C1-C4)-алкил- являются циклопропилметил-, циклобутилметил-, циклопентилметил-, циклогексилметил-, циклогептилметил-, 1-циклопропилэтил-, 2-циклопропилэтил-, 1-циклобутилэтил-, 2-циклобутилэтил-, 1-циклопентилэтил-, 2-циклопентилэтил-, 1-циклогексилэтил-, 2-циклогексилэтил-, 1-циклогептилэтил-, 2-циклогептилэтил-. В одном варианте осуществления настоящего изобретения группа (C3-C7)-циклоалкил-(C1-C4)-алкил- в любом одном или большем количестве случаев появления такой группы независимо от любых других случаев появления, представляет собой группу (C3-C7)-циклоалкил-(C1-C2)-алкил-, в другом варианте осуществления группу (C3-C7)-циклоалкил-CH2-. В группе (C3-C7)-циклоалкил-(C1-C4)-алкил- и аналогично во всех других группах концевой дефис означает свободную связь, с помощью которой присоединена группа, и, таким образом, показывает, с помощью какой подгруппы присоединена группа, состоящая из подгрупп.
В замещенных фенильных группах, включая фенильные группы, представляющие собой Ar и R24, заместители могут находиться в любых положениях. В монозамещенных фенильных группах заместитель может находиться в положении 2, в положении 3 или в положении 4. В дизамещенных фенильных группах заместители могут находиться в положениях 2 и 3, в положениях 2 и 4, в положениях 2 и 5, в положениях 2 и 6, в положениях 3 и 4, или в положениях 3 и 5. В тризамещенных фенильных группах заместители могут находиться в положениях 2, 3 и 4, в положениях 2, 3 и 5, в положениях 2, 3 и 6, в положениях 2, 4 и 5, в положениях 2, 4 и 6, или в положениях 3, 4 и 5. Если фенильная группа содержит четыре заместителя, часть них может быть атомами фтора, например, заместители могут находиться в положениях 2, 3, 4 и 5, в положениях 2, 3, 4 и 6, или в положениях 2, 3, 5 и 6. Если полизамещенная фенильная группа или любая другая полизамещенная группа содержит разные заместители, то каждый заместитель может находиться в любом подходящем положении и настоящее изобретение включает все изомеры положения. Количество заместителей в замещенной фенильной группе может равняться 1, 2, 3, 4 или 5. В одном варианте осуществления настоящего изобретения количество заместителей в замещенной фенильной группе и аналогично в других вариантах осуществления количество заместителей в любой другой замещенной группе, которая может содержать один или несколько заместителей, равно 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1, где количество заместителей в любом случае появления такой замещенной группы не зависит от количества заместителей в других случаях появления.
В гетероциклических группах, включая группы Het1 и Het2 и гетероциклические группы R24 и другие гетероциклические кольца, которые могут содержаться в соединениях формулы I, такие как кольца, образованные двумя группами вместе с атомом или атомами, к которым они присоединены, элементы гетероатомного кольца могут содержаться в любой комбинации и находиться в любых подходящих положениях при условии, что полученная группа и соединение формулы I являются подходящими и достаточно стабильными в качестве фармацевтически активного соединения. В одном варианте осуществления настоящего изобретения два атома кислорода в любом гетероциклическом кольце в соединениях формулы I не могут находиться в соседних положениях кольца. В другом варианте осуществления настоящего изобретения два элемента гетероатомного кольца, выбранные из группы, включающей атомы кислорода и атомы серы, не могут находиться в соседних положениях кольца в любом гетероциклическом кольце в соединениях формулы I. В другом варианте осуществления настоящего изобретения два элемента гетероатомного кольца, выбранные из группы, включающей атомы азота, содержащие экзоциклическую группу, такую как атом водорода или заместитель, атомы серы и атомы кислорода, не могут находиться в соседних положениях кольца в любом гетероциклическом кольце в соединениях формулы I. Выбор элементов гетероатомного кольца в ароматическом гетероциклическом кольце ограничивается предварительным условием о том, что кольцо является ароматическим, т.е. оно представляет собой циклическую систему, содержащую 6 делокализованных пи-электронов в случае, если она является моноциклической, или 10 делокализованных пи-электронов в случае, если она является бициклической. Моноциклические ароматические гетероциклы представляют собой 5-членные или 6-членные кольца и в случае 5-членного кольца содержат один кольцевой гетероатом, выбранный из группы, включающей кислород, серу и азот, где этот кольцевой атом азота содержит экзоциклическую группу, такую как атом водорода или заместитель, и необязательно один или несколько дополнительных кольцевых атомов азота, и в случае 6-членного кольца содержат один или несколько атомов азота в качестве кольцевых гетероатомов, но не содержат атомы кислорода и атомы серы в качестве кольцевых гетероатомов. Гетероциклические группы в соединениях формулы I могут быть присоединены через любой подходящий кольцевой атом, т.е. любой кольцевой атом, который содержит атом водорода или заместитель, включая кольцевые атомы углерода или кольцевые атомы азота, если в определении группы не указано иное. В одном варианте осуществления настоящего изобретения любая из гетероциклических групп, содержащаяся в соединениях формулы I в любом из ее случаев появления независимо от ее других случаев появления и независимо от любых других гетероциклических групп присоединена через кольцевой атом углерода, и в другом варианте осуществления через кольцевой атом азота, если это возможно. В замещенных гетероциклических группах заместители могут находиться в любых положениях.
Количество кольцевых гетероатомов, которые могут содержаться в гетероциклической группе в соединениях формулы I, количество циклов, т.е. может ли гетероциклическая группа быть моноциклической и/или бициклической, количество элементов кольца, которые могут содержаться, и степень насыщенности, т.е. является ли гетероциклическая группа насыщенной и не содержит двойной связи в кольце, или она является частично ненасыщенной и содержит одну или несколько, например, одну или две двойные связи в кольце, но не является ароматической, или она является ароматической и таким образом содержит две двойные связи в кольце в случае 5-членного моноциклического ароматического гетероцикла, три двойные связи в кольце в случае 6-членного моноциклического ароматического гетероцикла, четыре двойные связи в кольце в случае 9-членного бициклического ароматического гетероцикла и пять двойных связей в кольце в случае 10-членного ароматического гетероцикла, задано в определениях отдельных групп в соединениях формулы I. Два цикла в бициклической гетероциклической группе могут содержать 1, 2 или несколько общих кольцевых атомов углерода и она может быть конденсированной или образовать мостиковый бицикл или спироцикл. Примерами гетероциклических кольцевых систем, которые можно отметить и из которых можно образовать гетероциклические группы в соединениях формулы I и из любой одной или большего количества которых любая из гетероциклических групп в соединениях формулы I независимо от любой другой гетероциклической группы выбрана в одном варианте осуществления настоящего изобретения при условии, что кольцевая система представляет собой то, что соответствует определению группы, являются оксетан, тиетан, азетидин, фуран, тетрагидрофуран, тиофен, тетрагидротиофен, пиррол, пирролин, пирролидин, 1,3-диоксол, 1,3-диоксолан, изоксазол ([1,2]оксазол), изоксазолин, изоксазолидин, оксазол ([1,3]оксазол), оксазолин, оксазолидин, изотиазол ([1,2]тиазол), изотиазолин, изотиазолидин, тиазол ([1,3]тиазол), тиазолин, тиазолидин, пиразол, пиразолин, пиразолидин, имидазол, имидазолин, имидазолидин, [1,2,3]триазол, [1,2,4]триазол, [1,2,4]оксадиазол, [1,3,4]оксадиазол, [1,2,5]оксадиазол, [1,2,4]тиадиазол, 1H-тетразол, пиран, тетрагидропиран, тиопиран, тетрагидротиопиран, 2,3-дигидро[1,4]диоксин, 1,4-диоксан, пиридин, 1,2,5,6-тетрагидропиридин, пиперидин, морфолин, тиоморфолин, пиперазин, пиридазин, пиримидин, пиразин, [1,2,4]триазин, оксепан, тиепан, азепан, [1,3]диазепан, [1,4]диазепан, [1,4]оксазепан, [1,4]тиазепан, азокан, 3-азабицикло[3.1.0]гексан, октагидроциклопента[b]пиррол, октагидроциклопента[c]пиррол, 2-азаспиро[4.4]нонан, 7-азабицикло[2.2.1]гептан, 2,7-диазаспиро[4.4]нонан, октагидропирроло[3,4-b]пиррол, 6,7-дигидро-5H-пирроло[2,1-c][1,2,4]триазол, имидазо[2,1-b]тиазол, 6,7-дигидро-5H-тиазоло[3,2-a]пиримидин, бензофуран, изобензофуран, бензотиофен (бензо[b]тиофен), 1H-индол, 2,3-дигидро-1H-индол, октагидроиндол, 2H-изоиндол, октагидроизоиндол, бензо[1,3]диоксол, бензоксазол, бензтиазол, 1H-бензимидазол, имидазо[1,2-a]пиридин, [1,2,4]триазоло[4,3-a]пиридин, хроман, изохроман, тиохроман, бензо[1,4]диоксан, 3,4-дигидро-2H-бензо[1,4]оксазин, 3,4-дигидро-2H-бензо[1,4]тиазин, 2-азаспиро[4.5]декан, 3-азабицикло[3.2.2]нонан, хинолин, 1,2,3,4-тетрагидрохинолин, 5,6,7,8-тетрагидрохинолин, изохинолин, 1,2,3,4-тетрагидроизохинолин, 5,6,7,8-тетрагидроизохинолин, 2,7-диазаспиро[4.5]декан, 2,8-диазаспиро[4.5]декан, циннолин, хиназолин, хиноксалин, фталазин и [1,8]нафтиридин, которые все могут быть замещенными или замещены в любых подходящих положениях так, как указано в определении соответствующей группы в соединениях формулы I, где указанная степень ненасыщенности приведена только для примера, и в отдельных группах также могут находиться кольцевые системы, характеризующиеся большей или меньшей степенью насыщенности или гидрирования, или ненасыщенности, как это указано в определении группы.
Как отмечено выше, гетероциклические группы могут быть присоединены через любой подходящий кольцевой атом. Например, наряду с другими положениями оксетановое и тиетановое кольцо может быть присоединено через положения 2 и 3, азетидиновое кольцо через положения 1, 2 и 3, фурановое кольцо, тетрагидрофурановое кольцо, тиофеновое кольцо и тетрагидротиофеновое кольцо через положения 2 и 3, пиррольное кольцо и пирролидиновое кольцо через положения 1, 2 и 3, изоксазольное кольцо и изотиазольное кольцо через положения 3, 4 и 5, пиразольное кольцо через положения 1, 3, 4 и 5, оксазольное кольцо и тиазольное кольцо через положения 2, 4 и 5, имидазольное кольцо и имидазолидиновое кольцо через положения 1, 2, 4 и 5, 1H-тетразольное кольцо через положения 1 и 5, тетрагидропирановое и тетрагидротиопирановое кольцо через положения 2, 3 и 4, 1,4-диоксановое кольцо через положение 2, пиридиновое кольцо через положения 2, 3 и 4, пиперидиновое кольцо через положения 1, 2, 3 и 4, морфолиновое кольцо и тиоморфолиновое кольцо через положения 2, 3 и 4, пиперазиновое кольцо через положения 1 и 2, пиримидиновое кольцо через положения 2, 4 и 5, пиразиновое кольцо через положение 2, азепановое кольцо через положения 1, 2, 3 и 4, 3-азабицикло[3.1.0]гексановое кольцо через положения 3 и 6, октагидроциклопента[b]пиррольное и октагидроциклопента[c]пиррольное кольцо через положение 1, 2-азаспиро[4.4]нонановое кольцо через положение 2, 7-азабицикло[2.2.1]гептановое кольцо через положение 7, октагидропирроло[3,4-b]пиррольное кольцо через положения 1 и 5, 6,7-дигидро-5H-пирроло[2,1-c][1,2,4]триазольное кольцо через положение 3, имидазо[2,1-b]тиазольное кольцо через положения 2, 5 и 6, 6,7-дигидро-5H-тиазоло[3,2-a]пиримидиновое кольцо через положение 3, бензофурановое кольцо и бензотиофеновое кольцо через положения 2, 3, 4, 5, 6 и 7, 1H-индольное кольцо, 2,3-дигидро-1H-индольное и октагидроиндольное кольцо через положения 1, 2, 3, 4, 5, 6 и 7, бензо[1,3]диоксольное кольцо через положения 4, 5, 6 и 7, бензоксазольное кольцо и бензтиазольное кольцо через положения 2, 4, 5, 6 и 7, 1H-бензимидазольное кольцо через положения 1, 2, 4, 5, 6 и 7, имидазо[1,2-a]пиридиновое кольцо через положения 2 и 3, [1,2,4]триазоло[4,3-a]пиридиновое кольцо через положение 3, бензо[1,4]диоксановое кольцо через положения 5, 6, 7 и 8, 3-азабицикло[3.2.2]нонановое кольцо через положение 3, хинолиновое кольцо через положения 2, 3, 4, 5, 6, 7 и 8, 1,2,3,4-тетрагидрохинолиновое кольцо через положения 1, 5, 6, 7 и 8, 5,6,7,8-тетрагидрохинолиновое кольцо через положения 2, 3 и 4, изохинолиновое кольцо через положения 1, 3, 4, 5, 6, 7 и 8, 1,2,3,4-тетрагидроизохинолиновое кольцо через положения 2, 5, 6, 7 и 8, 5,6,7,8-тетрагидроизохинолиновое кольцо через положения 1, 3, 4 и 5, 2,7-диазаспиро[4.5]декановое кольцо через положения 2 и 7, 2,8-диазаспиро[4.5]декановое кольцо через положения 2 и 8, где образованные остатки гетероциклических групп все могут быть незамещенными или замещенными в любых подходящих положениях, как это указано в определении соответствующей группы в соединениях формулы I.
Галоген означает фтор, хлор, бром или йод. В одном варианте осуществления настоящего изобретения галоген в любых случаях его появления означает фтор, хлор или бром, в другом варианте осуществления фтор или хлор, в другом варианте осуществления фтор, в другом варианте осуществления хлор, где все случаи появления галогена независимы друг от друга.
Оксогруппа, т.е. присоединенный двойной связью атом кислорода, когда он является заместителем атома углерода, заменяет два атома водорода у атома углерода исходной системы. Таким образом, если группа CH2 замещена оксогруппой, она становится карбонильной группой (C(O), C=O). Так, если группы R2 и R3 вместе означают оксогруппу, то группа C(R2)-R3 в циклоалкановом кольце, представленном в формуле I, становится карбонильной группой. Оксогруппы также могут находиться у атомов серы, например, у кольцевых атомов серы в насыщенных и частично ненасыщенных гетероциклах, в которых обычно кроме кольцевых атомов серы в качестве гетероатомных элементов кольца могут содержаться группа S(O) (S(=O)) и S(O)2 группа (S(=O)2). Оксогруппа не может быть заместителем у атома углерода в ароматическом кольце, таком как фенильная группа.
Настоящее изобретение включает все стереоизомерные формы соединений формулы I, например, все энантиомеры и диастереоизомеры, включая цис/транс-изомеры. Настоящее изобретение также включает смеси двух или большего количества стереоизомерных форм, например, смеси энантиомеров и/или диастереоизомеров, включая цис/транс-изомеры, во всех соотношениях. Асимметрические центры, содержащиеся в соединениях формулы I, например, атом углерода в положении 2 хроманового кольца или в незамещенных или замещенных алкильных группах, все независимо друг от друга могут обладать S-конфигурацией или R-конфигурацией. Настоящее изобретение относится к энантиомерам, к левовращающим и правовращающим антиподам, в энантиомерно чистой форме и в основном в энантиомерно чистой форме, например, при молярном отношении этих двух энантиомеров, составляющем 98:2 или 99:1, или более, и в форме их рацемата, т.е. смеси этих двух энантиомеров в молярном отношении 1:1, и в форме смесей этих двух энантиомеров во всех соотношениях. Настоящее изобретение также относится к диастереоизомерам в форме чистых и в основном чистых диастереоизомеров и в форме смесей двух или большего количества диастереоизомеров во всех соотношениях. Настоящее изобретение также включает все цис/транс-изомеры соединений формулы I в чистом виде и в основном в чистом виде, например, при молярном отношении цис/транс изомеров, составляющем 98:2 или 99:1, или более, и в форме смесей цис-изомера и транс-изомера во всех соотношениях. Цис/транс-изометрия может наблюдаться в замещенных кольцах. Получение отдельных стереоизомеров при необходимости можно провести путем разделения смеси по обычным методикам, например, с помощью хроматографии или кристаллизации, или путем использования в синтезе стереохимически однородных исходных соединений, или с помощью стереоселективных реакций. До разделения стереоизомеров необязательно можно получить их производные. Разделение смеси стереоизомеров можно провести во время синтеза на стадии получения соединения формулы I или на стадии получения промежуточного продукта. Например, в случае соединения формулы I, содержащего асимметрический центр, отдельные энантиомеры можно получить путем приготовления рацемата соединения формулы I и его разделения на энантиомеры с помощью высокоэффективной жидкостной хроматографии на хиральной фазе по стандартным методикам, или разделения рацемата любого промежуточного продукта во время синтеза с помощью такой хроматографии или с помощью кристаллизации его соли с оптически активным амином или кислотой и превращения энантиомеров промежуточного продукта в энантиомерные формы конечного соединения формулы I, или путем проведения энантиоселективной реакции во время синтеза. Настоящее изобретение также включает все таутомерные формы соединений формулы I.
Наряду со свободными соединениями формулы I, т.е. соединениями, в которых кислотные и основные группы не находятся в форме соли, настоящее изобретение также включает соли соединений формулы I, в частности, их физиологически или токсикологически приемлемые соли или их фармацевтически приемлемые соли, которые можно образовать с помощью одной или большего количества кислотных или основных групп, содержащихся в соединениях формулы I, например, основных гетероциклических фрагментов. Таким образом, соединения формулы I можно депротонировать по кислотной группе и использовать, например, в виде солей со щелочными металлами, например, солей натрия или калия, или в виде солей аммония, например, в виде солей с аммиаком или органическими аминами или аминокислотами. Соединения формулы I, содержащие по меньшей мере одну основную группу, также можно получить и использовать в виде их солей присоединения с кислотами, например, в форме фармацевтически приемлемых солей с неорганическими кислотами и органическими кислотами, таких как соли с хлористоводородной кислотой, и в этом случае они содержатся, например, в виде гидрохлоридов. Обычно соли можно получить из кислотных и основных соединений формулы I по реакции с кислотой или основанием в растворителе или разбавителе по обычным методикам. Если в молекуле соединения формулы I одновременно содержится кислотная и основная группы, то в дополнение к указанным солевым формам настоящее изобретение также включает внутренние соли (бетаины, цвиттерионы). Настоящее изобретение также включает все соли соединений формулы I, которые вследствие плохой физиологический переносимости непосредственно непригодны для применения в качестве лекарственного средства, но являются подходящими для применения в качестве промежуточных продуктов для химических реакций или для получения физиологически приемлемых солей, например, с помощью анионного обмена или катионного обмена.
В одном варианте осуществления настоящего изобретения группа Ar означает фенил, который является незамещенным или замещен 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2 одинаковыми или разными заместителями R0. В другом варианте осуществления Ar означает фенил, который является незамещенным или замещен 1 заместителем R0. В другом варианте осуществления Ar означает незамещенный фенил. В другом варианте осуществления Ar означает фенил, который замещен 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2 одинаковыми или разными заместителями R0. В другом варианте осуществления Ar означает фенил, который замещен 1 заместителем R0. Если в Ar содержится один заместитель R0, то в одном варианте осуществления он находится в положении 2, в другом варианте осуществления в положении 3, в другом варианте осуществления в положении 4 фенильной группы. Если содержатся два заместителя R0, которые не образуют кольцо вместе с атомами углерода, с которыми они связаны, то в одном варианте осуществления они находятся в положениях 2 и 3, в другом варианте осуществления в положениях 2 и 4, в другом варианте осуществления в положениях 2 и 5, в другом варианте осуществления в положениях 2 и 6, в другом варианте осуществления в положениях 3 и 4, и в другом варианте осуществления в положениях 3 и 5 фенильной группы.
Двойная связь, которая содержится в мононенасыщенном кольце, которое могут образовать два заместителя R0, связанные с соседними кольцевыми атомами углерода в Ar, вместе с атомами углерода, с которыми они связаны, содержится между указанными двумя соседними кольцевыми атомами углерода в ароматическом кольце Ar, которая является общей для кольца Ar и кольца, образованного этими двумя группами R0, и в соответствии с правилами номенклатуры для конденсированных колец ее считают двойной связью, содержащейся в обоих кольцах. Случай, когда две группы R0, связанные с соседними кольцевыми атомами углерода в Ar, вместе с атомами углерода, с которыми они связаны, образуют 5-7-членное мононенасыщенное кольцо, которое является моноциклическим кольцом, другими словами можно описать, как случай, когда две группы R0 вместе образуют двухвалентный остаток, включающий цепь, содержащую от 3 до 5 атомов, из которых 0, 1 или 2 являются одинаковыми или разными гетероатомами, выбранными из группы, включающей азот, кислород и серу, концевые атомы которого, которые связаны с двумя соседними кольцевыми атомами углерода в Ar, отделены друг от друга с помощью от 1 до 3 атомов. Примерами таких двухвалентных остатков, из любого одного или большего количества которых выбраны две группы R0, связанные с соседними кольцевыми атомами углерода в Ar, в одном варианте осуществления настоящего изобретения являются остатки -CH2-CH2-CH2-, -CH2-CH2-CH2-CH2-, -CH2-CH2-CH2-CH2-CH2-, -O-CH2-CH2-,-CH2-CH2-O-, -O-CH2-O-, -O-CH2-CH2-O-, -O-CH2-CH2-CH2-O-, -NH-CH2-CH2-O-, -O-CH2-CH2-NH-, -S-CH2-CH2-NH- и -NH-CH2-CH2-S-, которые все могут быть замещены по атомам углерода и атомам азота заместителями, выбранными из группы, включающей фтор и (C1-C4)-алкил, например, фтор и метил, и, таким образом, также могут содержаться, например, в виде двухвалентных остатков -O-CF2-O-, -O-C(CH3)2-O-, -N(CH3)-CH2-CH2-O-, -O-CH2-CH2-N(CH3)-, -S-CH2-CH2-N(CH3)- и -N(CH3)-CH2-CH2-S-. В одном варианте осуществления настоящего изобретения кольцо, которое могут образовать две группы R0, связанные с соседними кольцевыми атомами углерода в Ar вместе с атомами углерода, с которыми они связаны, является 5-членным или 6-членным, в другом варианте осуществления 5-членным, в другом варианте осуществления 6-членным кольцом. В одном варианте осуществления настоящего изобретения количество заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил, которые могут содержаться в кольце, образованном двумя группами R0, связанными с соседними кольцевыми атомами углерода в Ar вместе с атомами углерода, с которыми они связаны, равно 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления - 1. В одном варианте осуществления настоящего изобретения заместители, которые могут содержаться в кольце, образованном двумя группами R0, связанными с соседними кольцевыми атомами углерода в Ar вместе с атомами углерода, с которыми они связаны, являются фторидными заместителями, и в другом варианте осуществления они являются (C1-C4)-алкильными заместителями, например, метильными заместителями, и в другом варианте осуществления они являются заместителями в таком кольце, связанными с кольцевым атомом азота, выбранными из группы, включающей (C1-C4)-алкил.
В одном варианте осуществления настоящего изобретения группа R0 выбрана из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, HO- и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, HO- и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил- и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C1-C6)-алкил-O- и (C3-C7)-циклоалкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, HO- и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей галоген, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, и в другом варианте осуществления из группы, включающей (C1-C6)-алкил-O-, и во всех этих вариантах осуществления две группы R1, связанные с соседними атомами углерода в Ar, вместе с атомами углерода, с которыми они связаны, могут образовать 5-7-членное мононенасыщенное кольцо, которое содержит 0, 1 или 2 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу, и которое является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил.
В одном варианте осуществления R0 выбран из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O- и (C3-C7)-циклоалкил-(C1-C4)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, HO- и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, HO- и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил- и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C1-C6)-алкил-O- и (C3-C7)-циклоалкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил, HO- и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген, (C1-C6)-алкил и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей галоген, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, и в другом варианте осуществления из группы, включающей (C1-C6)-алкил-O-.
В одном варианте осуществления (C1-C6)-алкильная группа, которая представляет собой R0 или содержится в группе (C1-C6)-алкил-O-, представляющей собой R0, является (C1-C4)-алкильной группой, в другом варианте осуществления (C1-C3)-алкильной группой, в другом варианте осуществления (C1-C2)-алкильной группой, в другом варианте осуществления метильной группой. В одном варианте осуществления настоящего изобретения (C3-C7)-циклоалкильная группа, которая представляет собой R0 или содержится в группе R0, является (C3-C6)-циклоалкильной группой, в другом варианте осуществления (C3-C4)-циклоалкильной группой, в другом варианте осуществления циклопропильной группой. В одном варианте осуществления галоген, представляющий собой R0, выбран из группы, включающей фтор и хлор, в другом варианте осуществления он представляет собой фтор.
Примерами групп Ar, включая необязательные заместители R0, из любого одного или нескольких которых выбран Ar, в одном варианте осуществления настоящего изобретения являются фенил, т.е. незамещенный фенил, 2-фторфенил, 3-фторфенил, 4-фторфенил, 2-хлорфенил, 3-хлорфенил, 4-хлорфенил, 2-метилфенил (о-толил), 3-метилфенил (м-толил), 4-метилфенил (п-толил), 2-этилфенил, 3-этилфенил, 4-этилфенил, 2-метоксифенил, 3-метоксифенил, 4-метоксифенил, 2-этоксифенил, 3-этоксифенил, 4-этоксифенил, 2-пропоксифенил, 3-пропоксифенил, 4-пропоксифенил, 2-изопропоксифенил, 3-изопропоксифенил, 4-изопропоксифенил, 2,3-дифторфенил, 2,4-дифторфенил, 2,5-дифторфенил, 2,6-дифторфенил, 3,4-дифторфенил, 3,5-дифторфенил, 2,3-дихлорфенил, 2,4-дихлорфенил, 2,5-дихлорфенил, 2,6-дихлорфенил, 3,4-дихлорфенил, 3,5-дихлорфенил, 2-хлор-3-фторфенил, 2-хлор-4-фторфенил, 2-хлор-5-фторфенил, 2-хлор-6-фторфенил, 3-хлор-2-фторфенил, 3-хлор-4-фторфенил, 3-хлор-5-фторфенил, 4-хлор-2-фторфенил, 4-хлор-3-фторфенил, 5-хлор-2-фторфенил, 2,3-диметилфенил, 2,4-диметилфенил, 2,5-диметилфенил, 2,6-диметилфенил, 3,4-диметилфенил, 3,5-диметилфенил, 2-фтор-3-метилфенил, 2-фтор-4-метилфенил, 2-фтор-5-метилфенил, 2-фтор-6-метилфенил, 3-фтор-2-метилфенил, 3-фтор-4-метилфенил, 3-фтор-5-метилфенил, 4-фтор-2-метилфенил, 4-фтор-3-метилфенил, 5-фтор-2-метилфенил, 2-хлор-3-метилфенил, 2-хлор-4-метилфенил, 2-хлор-5-метилфенил, 2-хлор-6-метилфенил, 3-хлор-2-метилфенил, 3-хлор-4-метилфенил, 3-хлор-5-метилфенил, 4-хлор-2-метилфенил, 4-хлор-3-метилфенил, 5-хлор-2-метилфенил, 2-фтор-3-метоксифенил, 2-фтор-4-метоксифенил, 2-фтор-5-метоксифенил, 2-фтор-6-метоксифенил, 3-фтор-2-метоксифенил, 3-фтор-4-метоксифенил, 3-фтор-5-метоксифенил, 4-фтор-2-метоксифенил, 4-фтор-3-метоксифенил, 5-фтор-2-метоксифенил, 2-метокси-3-метилфенил, 2-метокси-4-метилфенил, 2-метокси-5-метилфенил, 2-метокси-6-метилфенил, 3-метокси-2-метилфенил, 3-метокси-4-метилфенил, 3-метокси-5-метилфенил, 4-метокси-2-метилфенил, 4-метокси-3-метилфенил, 5-метокси-2-метилфенил.
В одном варианте осуществления настоящего изобретения группа R1 означает водород или один или несколько фторидных заместителей. Т.е. в этом варианте осуществления циклоалкановое кольцо, представленное в формуле I, является незамещенным или замещено одним или несколькими фторидными заместителями за исключением групп R2 и R3 и атома кислорода, связывающего циклоалкановое кольцо с хромановым кольцом. В другом варианте осуществления группа R1 означает водород или один или несколько (C1-C4)-алкильных заместителей. Т.е. в этом варианте осуществления циклоалкановое кольцо, представленное в формуле I, является незамещенным или замещено одним или несколькими (C1-C4)-алкильными заместителями за исключением групп R2 и R3 и атома кислорода, связывающего циклоалкановое кольцо с хромановым кольцом. В другом варианте осуществления группа R1 означает водород. Т.е. в этом варианте осуществления циклоалкановое кольцо, представленное в формуле I, является незамещенным, или другими словами содержит атомы водорода, только за исключением групп R2 и R3 и атома кислорода, связывающего циклоалкановое кольцо с хромановым кольцом. В одном варианте осуществления количество атомов фтора и/или (C1-C4)-алкильных групп, представляющих собой R1, равно 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1. В одном варианте осуществления (C1-C4)-алкил, представляющая собой R1, означает (C1-C3)-алкил, в другом варианте осуществления (C1-C2)-алкил, в другом варианте осуществления метил. В одном варианте осуществления кольцевой атом углерода циклоалканового кольца, представленного в формуле I, которое содержит атом кислорода, связывающий кольцо с хромановым кольцом, не содержит группу R1, которая означает фтор или (C1-C4)-алкил, т.е. в этом варианте осуществления указанный кольцевой атом углерода содержит атом водорода.
В одном варианте осуществления настоящего изобретения группа R2 выбрана из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, (C1-C6)-алкил-C(O)-O-, фенил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, (C1-C6)-алкил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, (C1-C6)-алкил-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, (C1-C6)-алкил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, R5-N(R6)-, R7-C(O)-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, R5-N(R6)-, R7-C(O)-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, R5-N(R6)-, R7-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, (C1-C6)-алкил-C(O)-O-, фенил-C(O)-O- и Het1-C(O)-O-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-C(O)-O и Het1-C(O)-O-, в другом варианте осуществления из группы, включающей HO-, (C1-C6)-алкил-O-, (C1-C6)-алкил-C(O)-O- и Het1-C(O)-O-, в другом варианте осуществления из группы, включающей HO-, (C1-C6)-алкил-C(O)-O- и Het1-C(O)-O-, где во всех этих вариантах осуществления (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, или во всех этих вариантах осуществления R2 и R3 вместе означают оксогруппу.
В одном варианте осуществления R2 выбран из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, HO-, R5-N(R6)-, R7-C(O)-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, R5-N(R6)-, R7-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, R5-N(R6)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей R5-N(R6)-, R7-C(O)-N(R8)- и R7-S(O)2-N(R8)-, в другом варианте осуществления из группы, включающей R5-N(R6)-, R7-C(O)-N(R8)- и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил и R5-N(R6)-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил и R5-N(R6)-C(O)-, в другом варианте осуществления из группы, включающей R5-N(R6)- и R5-N(R6)-C(O)-, где во всех этих вариантах осуществления (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20.
В одном варианте осуществления R2 означает (C1-C6)-алкил, который является незамещенным или содержит один или несколько одинаковых или разных заместителей R20. В другом варианте осуществления R(2) означает R5-N(R6)- и, таким образом, соединения формулы I являются соединениями формулы Ia.
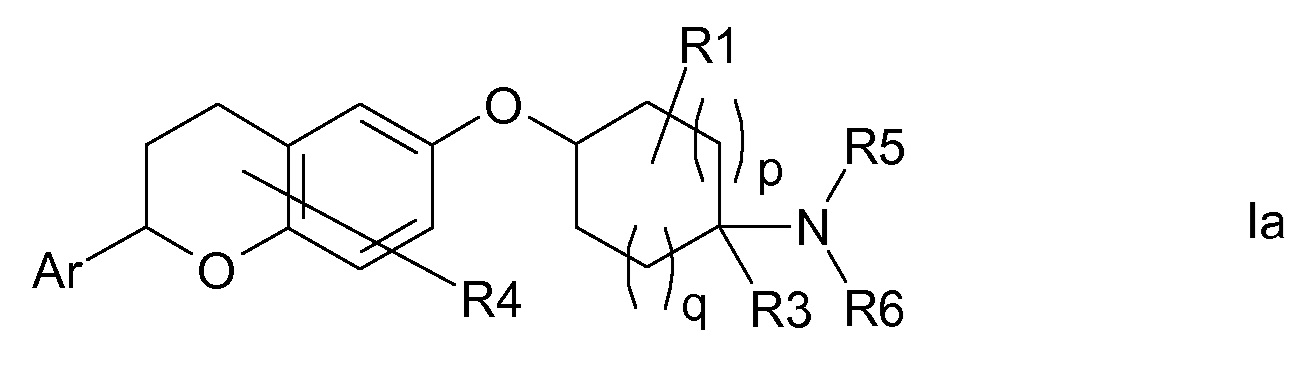
В другом варианте осуществления R(2) означает R7-C(O)-N(R8)- и, таким образом, соединения формулы I являются соединениями формулы Ib.
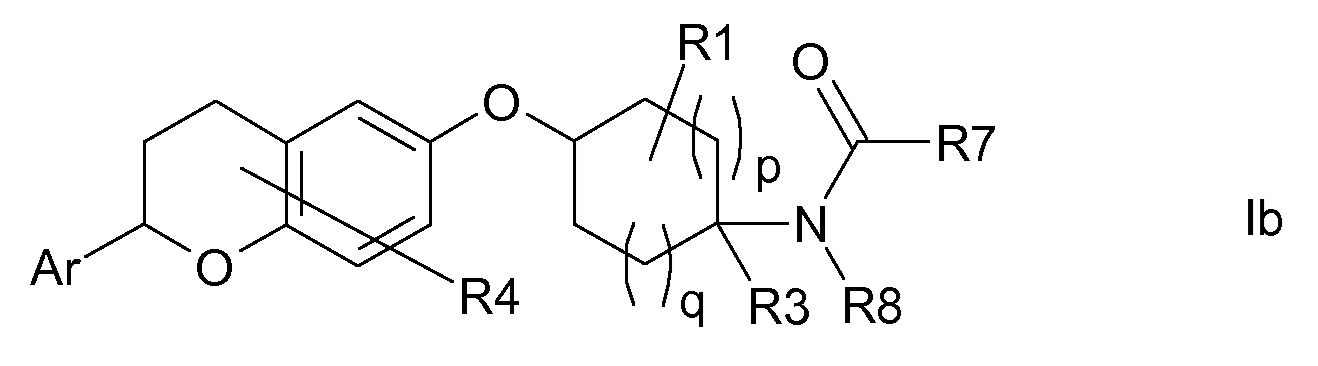
В другом варианте осуществления R(2) означает R7-S(O)2-N(R8)- и, таким образом, соединения формулы I являются соединениями формулы Ic.
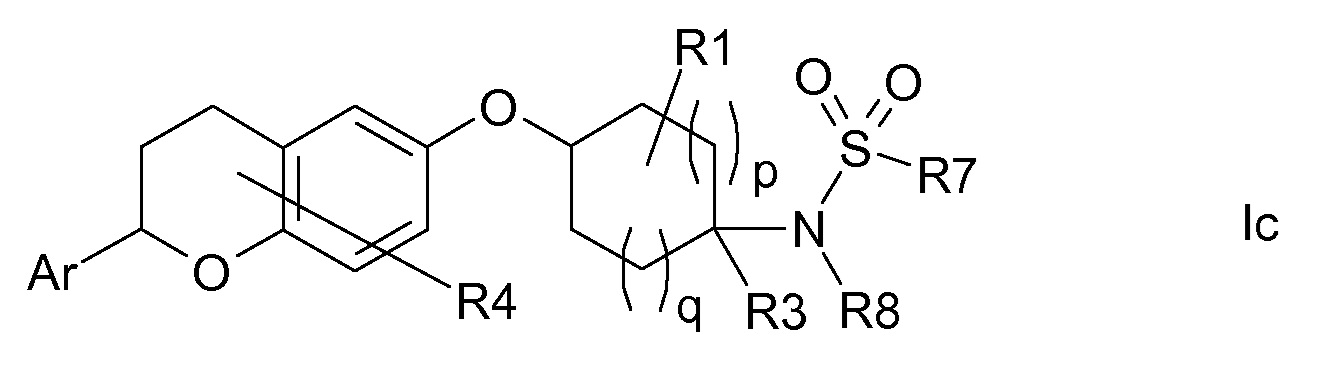
В другом варианте осуществления R(2) означает R5-N(R6)-C(O)- и, таким образом, соединения формулы I являются соединениями формулы Id.
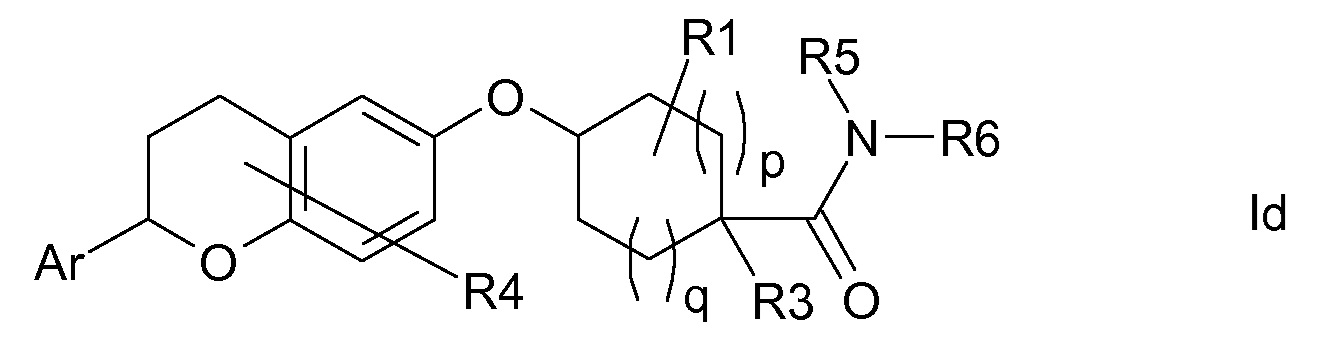
Группы Ar, R1, R3-R8 и числа p и q в соединениях формул Ia, Ib, Ic и Id определены так, как в соединениях формулы I.
В одном варианте осуществления количество заместителей R20 в замещенной (C1-C6)-алкильной группе, которая представляет собой R2 или содержится в группах (C1-C6)-алкил-O- или (C1-C6)-алкил-C(O)-O-, представляющих собой R2, равно 1, 2, 3 или 4, в другом варианте осуществления 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1. В одном варианте осуществления (C1-C6)-алкильная группа, которая представляет собой R2, замещена одним или несколькими одинаковыми или разными заместителями R20, т.е. не является незамещенной. В одном варианте осуществления (C1-C6)-алкильная группа, которая представляет собой R2, замещена одним или несколькими одинаковыми или разными заместителями R20, один из которых связан с атомом углерода алкильной группы, которая связана с циклоалкановым кольцом, представленным в формуле I, т.е. в положении 1 алкильной группы. В одном варианте осуществления (C1-C6)-алкильная группа, которая представляет собой R2 или содержится в группах (C1-C6)-алкил-O- или (C1-C6)-алкил-C(O)-O-, представляющих собой R2, представляет собой (C1-C4)-алкильную группу, в другом варианте осуществления (C1-C3)-алкильную группу, в другом варианте осуществления (C1-C2)-алкильную группу, в другом варианте осуществления метильную группу, которые все являются незамещенными или замещены одним или несколькими одинаковыми или разными заместителями R20, и в одном варианте осуществления замещены одним или несколькими одинаковыми или разными заместителями R20, где в одном варианте осуществления количество заместителей R20 равно 1, 2 или 3, в другом варианте осуществления 1 или 2, и в другом варианте осуществления 1. В одном варианте осуществления (C1-C6)-алкильная группа, которая представляет собой R2, представляет собой метильную группу, которая замещена одним заместителем R20, и, таким образом, в этом варианте осуществления группа R2 представляет собой группу R20-CH2-.
В одном варианте осуществления настоящего изобретения группа R3 означает водород, в другом варианте осуществления она означает (C1-C6)-алкил, который является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей (C3-C7)-циклоалкил, фенил, HO- и (C1-C4)-алкил-O-, где алкильные группы, представляющие собой R3, как и алкильные группы в общем случае, независимо от этих указанных заместителей, могут быть замещены одним или несколькими фторидными заместителями. В одном варианте осуществления количество заместителей, выбранных из группы, включающей (C3-C7)-циклоалкил, фенил, HO- и (C1-C4)-алкил-O-, в замещенной алкильной группе, представляющей собой R3, равно 1. В одном варианте осуществления алкильная группа, представляющая собой R3, не содержит заместители, выбранные из группы, включающей (C3-C7)-циклоалкил, фенил, HO- и (C1-C4)-алкил-O-. В одном варианте осуществления заместители в алкильной группе, представляющей собой R3, выбраны из группы, включающей (C3-C7)-циклоалкил, фенил и (C1-C4)-алкил-O-, в другом варианте осуществления из группы, включающей (C3-C7)-циклоалкил и фенил, и в другом варианте осуществления они являются фенильными группами. В одном варианте осуществления (C1-C6)-алкильная группа, представляющая собой R3, представляет собой (C1-C4)-алкильную группу, в другом варианте осуществления (C1-C3)-алкильную группу, в другом варианте осуществления (C1-C2)-алкильную группу, в другом варианте осуществления метильную группу. В одном варианте осуществления R2 и R3 обладают разными значениями, но вместе не представляют собой оксогруппу. В другом варианте осуществления R2 и R3 вместе представляют собой оксогруппу.
Как указано выше, в свободных центрах связывания хроманового кольца, т.е. в центрах связывания в положениях 2, 3, 4, 5, 7 и 8 хроманового кольца, которые не заняты связями с кольцом или связью с группой Ar, могут содержаться атомы водорода или заместители, выбранные из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-, которые представляют собой R4. В одном варианте осуществления настоящего изобретения в свободном центре связывания в положении 2 хроманового кольца, т.е. в свободном центре связывания кольцевого атома углерода, который содержит группу Ar, содержится атом водорода, и в свободных центрах связывания в положениях 3, 4, 5, 7 и 8 хроманового кольца содержатся атомы водорода или заместители, выбранные из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-. В другом варианте осуществления настоящего изобретения в свободных центрах связывания в положениях 2, 3 и 4 хроманового кольца содержатся атомы водорода и в свободных центрах связывания в положениях 5, 7 и 8 хроманового кольца содержатся атомы водорода или заместители, выбранные из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-. В другом варианте осуществления настоящего изобретения в свободных центрах связывания в положениях 2 и 5 хроманового кольца содержатся атомы водорода и в свободных центрах связывания в положениях 3, 4, 7 и 8 хроманового кольца содержатся атомы водорода или заместители, выбранные из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-. В другом варианте осуществления настоящего изобретения в свободных центрах связывания в положениях 2, 5, 7 и 8 хроманового кольца содержатся атомы водорода и в свободных центрах связывания в положениях 3 и 4 хроманового кольца содержатся атомы водорода или заместители, выбранные из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-. В одном варианте осуществления количество групп R4, которые отличаются от водорода, т.е. количество заместителей R4, которые выбраны из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-, равно 1, 2 или 3, в другом варианте осуществления оно равно 1 или 2, в другом варианте осуществления оно равно 1, и в другом варианте осуществления оно равно 0 и, таким образом, в этом последнем варианте осуществления группы R4, которые отличаются от водорода, не содержатся в хромановом кольце и атомы водорода находятся во всех его свободных центрах связывания. В одном варианте осуществления R4 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген и (C1-C4)-алкил, в другом варианте осуществления R4 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор, хлор и (C1-C4)-алкил. В одном варианте осуществления R4 в свободных центрах связывания в положениях 2, 3 и 4 хроманового кольца означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил, в другом варианте осуществления R4 в свободных центрах связывания в положениях 2, 3 и 4 хроманового кольца означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей (C1-C4)-алкил, и R4 в свободных центрах связывания в положениях 5, 7 и 8 хроманового кольца означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-, в другом варианте осуществления R4 в свободных центрах связывания в положениях 5, 7 и 8 хроманового кольца означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген и (C1-C4)-алкил, в другом варианте осуществления R4 в свободных центрах связывания в положениях 5, 7 и 8 хроманового кольца означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген. В одном варианте осуществления настоящего изобретения (C1-C4)-алкильная группа, представляющая собой R4 или содержащаяся в R4, представляет собой (C1-C2)-алкил, в другом варианте осуществления она представляет собой метил.
В одном варианте осуществления настоящего изобретения R5 и R6 независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C6-C10)-бициклоалкил, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей водород и (C1-C6)-алкил, где во всех этих вариантах осуществления (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20 и (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и Het1 является незамещенным или содержит один или несколько одинаковых или разных заместителей R22, или группы R5 и R6 вместе с атомом азота, с которыми они связаны, образуют 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который в дополнение к атому азота, с которым связаны R5 и R6, содержит 0 или 1 дополнительный кольцевой гетероатом, выбранный из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей R21.
В одном варианте осуществления R5 и R6 независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C6-C10)-бициклоалкил, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей водород и (C1-C6)-алкил, где во всех этих вариантах осуществления (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и Het1 является незамещенным или содержит один или несколько одинаковых или разных заместителей R22.
В одном варианте осуществления настоящего изобретения одна из групп R5 и R6 выбрана из группы, включающей водород и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C4)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C2)-алкил, в другом варианте осуществления из группы, включающей водород и метил, и другим вариантом осуществления является водород и вторая из групп R5 и R6 выбрана из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, фенил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C6-C10)-бициклоалкил, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей водород и (C1-C6)-алкил, где во всех этих вариантах осуществления (C1-C6)-алкил, (C1-C4)-алкил, (C1-C2)-алкил и метил, представляющий собой R5 или R6, является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и Het1 является незамещенным или содержит один или несколько одинаковых или разных заместителей R22, или группы R5 и R6 вместе с атомом азота, с которыми они связаны, образуют 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который в дополнение к атому азота, с которым связаны R5 и R6, содержит 0 или 1 дополнительный кольцевой гетероатом, выбранный из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей R21.
В одном варианте осуществления настоящего изобретения одна из групп R5 и R6 выбрана из группы, включающей водород и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C4)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C2)-алкил, в другом варианте осуществления из группы, включающей водород и метил, и в другом варианте осуществления она означает водород и вторая из групп R5 и R6 выбрана из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, фенил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C6-C10)-бициклоалкил, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей водород и (C1-C6)-алкил, где во всех этих вариантах осуществления (C1-C6)-алкил, (C1-C4)-алкил, (C1-C2)-алкил и метил, представляющий собой R5 или R6, является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и Het1 является незамещенным или содержит один или несколько одинаковых или разных заместителей R22. В одном варианте осуществления R5 и R6 оба означают водород.
В одном варианте осуществления настоящего изобретения одна из групп R5 и R6 выбрана из группы, включающей водород и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C4)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C2)-алкил, в другом варианте осуществления из группы, включающей водород и метил, и другим вариантом осуществления является водород, и вторая из групп R5 и R6 выбрана из группы, включающей (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, фенил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и (C6-C10)-бициклоалкил, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, где во всех этих вариантах осуществления (C1-C6)-алкил, (C1-C4)-алкил, (C1-C2)-алкил и метил, представляющий собой R5 или R6, является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и Het1 является незамещенным или содержит один или несколько одинаковых или разных заместителей R22, или группы R5 и R6 вместе с атомом азота, с которыми они связаны, образуют 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который в дополнение к атому азота, с которым связаны R5 и R6, содержит 0 или 1 дополнительный кольцевой гетероатом, выбранный из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей R21.
В одном варианте осуществления настоящего изобретения одна из групп R5 и R6 выбрана из группы, включающей водород и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C4)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C2)-алкил, в другом варианте осуществления из группы, включающей водород и метил, и другим вариантом осуществления является водород и вторая из групп R5 и R6 выбрана из группы, включающей (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, фенил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и (C6-C10)-бициклоалкил, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, где во всех этих вариантах осуществления (C1-C6)-алкил, (C1-C4)-алкил, (C1-C2)-алкил и метил, представляющий собой R5 или R6, является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил, (C6-C10)-бициклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и Het1 является незамещенным или содержит один или несколько одинаковых или разных заместителей R22.
В одном варианте осуществления настоящего изобретения (C1-C6)-алкильная группа, представляющая собой R5 или R6, представляет собой (C1-C4)-алкильную группу, в другом варианте осуществления (C1-C3)-алкильную группу, в другом варианте осуществления (C1-C2)-алкильную группу, в другом варианте осуществления любую одну или несколько групп, выбранных из группы, включающей бутил, пропил, изопропил, этил и метил, например, выбранных из группы, включающей метил, этил и пропил, которые все являются незамещенными или замещены одним или несколькими, например, 1, 2 или 3, или 1 или 2, или 1 одинаковыми или разными заместителями R20, и эти заместители могут находиться в любых положениях, например, в положении 1 и/или в положении 2 этильной группы, представляющей собой R5 или R6, или в положении 1 и/или в положении 2 и/или в положении 3 пропильной группы, представляющей собой R5 или R6.
В одном варианте осуществления настоящего изобретения количество одинаковых или разных заместителей R20, которые необязательно содержатся в (C1-C6)-алкильной группе, представляющей собой R5 или R6, равно 1, 2, 3 или 4, в другом варианте осуществления оно равно 1, 2 или 3, в другом варианте осуществления оно равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп R24, представляющих собой заместители R20, которые необязательно содержатся в (C1-C6)-алкильной группе, представляющей собой R5 или R6, кроме любых других заместителей R20, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0 (нулю), т.е. в этом последнем варианте осуществления R20 является таким, как определено, но не представляет собой R24. В одном варианте осуществления количество оксогрупп, представляющих собой заместители R20, которые необязательно содержатся в (C1-C6)-алкильной группе, представляющей собой R5 или R6, кроме любых других заместителей R20, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп, выбранных из группы, включающей R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, представляющих собой заместители R20, которые необязательно содержатся в (C1-C6)-алкильной группе, представляющей собой R5 или R6, кроме любых других заместителей R20, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0.
В одном варианте осуществления настоящего изобретения количество одинаковых или разных заместителей R21, которые необязательно содержатся в (C3-C7)-циклоалкильной, (C6-C10)-бициклоалкильной и Het2 группах, представляющих собой R5 или R6, независимо друг от друга равно 1, 2, 3 или 4, в другом варианте осуществления оно равно 1, 2 или 3, в другом варианте осуществления оно равно 1 или 2, в другом варианте осуществления оно равно 1. В одном варианте осуществления количество групп R24, представляющих собой заместители R21, которые необязательно содержатся в (C3-C7)-циклоалкильной, (C6-C10)-бициклоалкильной и Het2 группах, представляющих собой R5 или R6, кроме любых других заместителей R21, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество оксогрупп, представляющих собой заместители R21, которые необязательно содержатся в (C3-C7)-циклоалкильной, (C6-C10)-бициклоалкильной и Het2 группах, представляющих собой R5 или R6, кроме любых других заместителей R21, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп, выбранных из группы, включающей R34-O-C(O)-(C1-C4)-алкил-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, представляющие собой заместители R21, которые необязательно содержатся в (C3-C7)-циклоалкильной, (C6-C10)-бициклоалкильной и Het2 группах, представляющих собой R5 или R6, кроме любых других заместителей R21, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0.
В одном варианте осуществления настоящего изобретения количество одинаковых или разных заместителей R22, которые необязательно содержатся в фенильной и Het1 группах, представляющих собой R5 или R6, независимо друг от друга равно 1, 2, 3 или 4, в другом варианте осуществления оно равно 1, 2 или 3, в другом варианте осуществления оно равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп, выбранных из группы, включающей R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, представляющие собой заместители R22, которые необязательно содержатся в фенильной и Het1 группах, представляющих собой R5 или R6, кроме любых других заместителей R22, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0.
Моноциклический гетероцикл, который могут образовать группы R5 и R6 вместе с атомом азота, с которым они связаны, и, таким образом, гетероцикл, присоединенный через кольцевой атом азота, может быть 4-членным, 5-членным, 6-членным или 7-членным. В одном варианте осуществления настоящего изобретения этот гетероцикл является 4-6-членным, в другом варианте осуществления он является 5-6-членным, в другом варианте осуществления он является 5-членным, в другом варианте осуществления он является 6-членным. В одном варианте осуществления гетероцикл, образованный группами R5 и R6 вместе с атомом азота, с которым они связаны, является насыщенным или содержит в кольце одну двойную связь, в другом варианте осуществления он является насыщенным. В одном варианте осуществления дополнительный кольцевой гетероатом, который необязательно содержится в гетероцикле, образованном группами R5 и R6 вместе с атомом азота, с которым они связаны, выбран из группы, включающей азот и кислород, в другом варианте осуществления он является атомом азота и в другом варианте осуществления он является атомом кислорода. Примерами гетероциклических групп, из любой одной или большего количества которых выбрана гетероциклическая группа, образованная группами R5 и R6 вместе с атомом азота, с которым они связаны, в одном варианте осуществления настоящего изобретения являются азетидин-1-ил, пирролидин-1-ил, пиперидин-1-ил, азепан-1-ил, имидазолидин-1-ил, оксазолидин-3-ил, тиазолидин-3-ил, пиперазин-1-ил, морфолин-4-ил и тиоморфолин-4-ил, которые все могут быть незамещенными или содержать один или несколько одинаковых или разных заместителей R21.
В одном варианте осуществления настоящего изобретения количество одинаковых или разных заместителей R21, которые необязательно содержатся в гетероцикле, образованном группами R5 и R6 вместе с атомом азота, с которым они связаны, равно 1, 2, 3 или 4, в другом варианте осуществления оно равно 1, 2 или 3, в другом варианте осуществления оно равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп R24, представляющих собой заместители R21, которые необязательно содержатся в гетероцикле, образованном группами R5 и R6 вместе с атомом азота, с которым они связаны, кроме любых других заместителей R21, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество оксогрупп, представляющих собой заместители R21, которые необязательно содержатся в гетероцикле, образованном группами R5 и R6 вместе с атомом азота, с которым они связаны, кроме любых других заместителей R21, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп, выбранных из группы, включающей R34-O-C(O)-(C1-C4)-алкил-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, представляющие собой заместители R21, которые необязательно содержатся в гетероцикле, образованном группами R5 и R6 вместе с атомом азота, с которым они связаны, кроме любых других заместителей R21, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0.
В одном варианте осуществления настоящего изобретения R7 в любом из его случаев появления независимо от других случаев появления выбран из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C3-C7)-циклоалкил, Het1 и Het2, в другом варианте осуществления из группы, включающей (C1-C6)-алкил и Het2, в другом варианте осуществления из группы, включающей (C3-C7)-циклоалкил и Het2, в другом варианте осуществления из группы, включающей фенил и Het1, в другом варианте осуществления им является (C1-C6)-алкил, в другом варианте осуществления им является (C3-C7)-циклоалкил, в другом варианте осуществления им является фенил, в другом варианте осуществления им является Het1 и в другом варианте осуществления им является Het2, где все группы (C1-C6)-алкил являются незамещенными или замещены одним или несколькими одинаковыми или разными заместителями R20, все группы (C3-C7)-циклоалкил и Het2 являются незамещенными или замещены одним или несколькими одинаковыми или разными заместителями R2 и все группы фенил и Het1 являются незамещенными или замещены одним или несколькими одинаковыми или разными заместителями R22.
В одном варианте осуществления настоящего изобретения количество одинаковых или разных заместителей R20, которые необязательно содержатся в (C1-C6)-алкильной группе, представляющей собой R7, равно 1, 2, 3 или 4, в другом варианте осуществления оно равно 1, 2 или 3, в другом варианте осуществления оно равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп R24, представляющих собой заместители R20, которые необязательно содержатся в (C1-C6)-алкильной группе, представляющей собой R7, кроме любых других заместителей R20, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0 (нулю), т.е. в этом последнем варианте осуществления R20 является таким, как определено, но не представляет собой R24. В одном варианте осуществления количество оксогрупп, представляющих собой заместители R20, которые необязательно содержатся в (C1-C6)-алкильной группе, представляющей собой R7, кроме любых других заместителей R20, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп, выбранных из группы, включающей R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, представляющие собой заместители R20, которые необязательно содержатся в (C1-C6)-алкильной группе, представляющей собой R7, кроме любых других заместителей R20, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0.
В одном варианте осуществления настоящего изобретения количество одинаковых или разных заместителей R21, которые необязательно содержатся в (C3-C7)-циклоалкильной и Het2 группах, представляющих собой R7, независимо друг от друга равно 1, 2, 3 или 4, в другом варианте осуществления оно равно 1, 2 или 3, в другом варианте осуществления оно равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп R24, представляющих собой заместители R21, которые необязательно содержатся в (C3-C7)-циклоалкильной и Het2 группах, представляющих собой R7, кроме любых других заместителей R21, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество оксогрупп, представляющих собой заместители R21, которые необязательно содержатся в (C3-C7)-циклоалкильной и Het2 группах, представляющих собой R7, кроме любых других заместителей R21, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп, выбранных из группы, включающей R34-O-C(O)-(C1-C4)-алкил-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, представляющие собой заместители R21, которые необязательно содержатся в (C3-C7)-циклоалкильной и Het2 группах, представляющих собой R7, кроме любых других заместителей R21, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0.
В одном варианте осуществления настоящего изобретения количество одинаковых или разных заместителей R22, которые необязательно содержатся в фенильной и Het1 группах, представляющих собой R7, независимо друг от друга равно 1, 2, 3 или 4, в другом варианте осуществления оно равно 1, 2 или 3, в другом варианте осуществления оно равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп, выбранных из группы, включающей R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, представляющие собой заместители R22, которые необязательно содержатся в фенильной и Het1 группах, представляющих собой R7, кроме любых других заместителей R22, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0.
В одном варианте осуществления настоящего изобретения R8 в любом из его случаев появления независимо от других случаев его появления выбран из группы, включающей водород и (C1-C3)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C2)-алкил, в другом варианте осуществления из группы, включающей водород и метил, и в другом варианте осуществления R8 означает водород.
В одном варианте осуществления настоящего изобретения R9 выбран из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, и в другом варианте осуществления из группы, включающей (C1-C4)-алкил.
В одном варианте осуществления настоящего изобретения R10 выбран из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей водород, (C1-C6)-алкил и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей водород и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C4)-алкил, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, и (C3-C7)-циклоалкил-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, и в другом варианте осуществления из группы, включающей (C1-C4)-алкил.
В одном варианте осуществления настоящего изобретения R20 выбран из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, (C3-C7)-циклоалкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)- и R31-N(R32)-S(O)2-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)- и R34-O-C(O)-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)- и (C1-C6)-алкил-S(O)2-N(R32)-, в другом варианте осуществления из группы, включающей R31-N(R32)-, R33-C(O)-N(R32)- и (C1-C6)-алкил-S(O)2-N(R32)-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n- и R31-N(R32)-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O- и (HO)2P(O)-O-CH2-O-C(O)-O-, в другом варианте осуществления из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, HO-S(O)2-O- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей HO-, (C1-C6)-алкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей HO-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей HO-, HO-S(O)2-O- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей HO- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей R24, HO- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей R24 и HO-, и в другом варианте осуществления R20 означает HO-, и в другом варианте осуществления R20 означает R24, где в случае, когда содержится более, чем один заместитель R20, заместители R20 независимо друг от друга определены так, как в любом из этих вариантов осуществления.
В одном варианте осуществления настоящего изобретения R21 выбран из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, R34-O-C(O)-(C1-C4)-алкил-, R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, (C3-C7)-циклоалкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)- и R34-O-C(O)-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, R31-N(R32)-, R33-C(O)-N(R32)- и (C1-C6)-алкил-S(O)2-N(R32)-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O- и R31-N(R32)-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O- и R31-N(R32)-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O- и (HO)2P(O)-O-CH2-O-C(O)-O-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, R34-O-C(O)-(C1-C4)-алкил-, R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, R34-O-C(O)-(C1-C4)-алкил-, R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, R31-N(R32)-, R33-C(O)-N(R32)- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, R31-N(R32)-, R33-C(O)-N(R32)- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, фтор, HO-, оксогруппу, HO-S(O)2-O-, (HO)2P(O)-O- и (HO)2P(O)-O-CH2-O-C(O)-O-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, фтор, HO-, оксогруппу, HO-S(O)2-O- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, фтор, HO-, оксогруппу и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, фтор, HO- и оксогруппу, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, фтор, HO-, (C1-C6)-алкил-O-, HO-S(O)2-O- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, фтор, HO-, HO-S(O)2-O- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, фтор, HO-, HO-S(O)2-O- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, фтор, HO- и (HO)2P(O)-O-, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, фтор и HO-, где в случае, когда содержится более, чем один заместитель R21, заместители R21 независимо друг от друга определены так, как в любом из этих вариантов осуществления. В одном варианте осуществления заместители R21, которые связаны с кольцевым атомом азота, что может быть в случае, группы Het2 или кольца, которое могут образовать R5 и R6 вместе с атомом азота, с которым они связаны, выбраны из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил- и R24, где R24 присоединен через кольцевой атом углерода, в другом варианте осуществления из группы, включающей (C1-C4)-алкил.
В одном варианте осуществления настоящего изобретения R22 выбран из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, оксогруппу, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, R33-O-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, NC-, R31-N(R32)-C(O)- и R31-N(R32)-S(O)2-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, оксогруппу, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, NC- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, HO-, оксогруппу, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, NC- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, HO-, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, R31-N(R32)-, NC- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, R33-O-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, NC-, R33-C(O)- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, NC-, R33-C(O)- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)- и R31-N(R32)-C(O)-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, HO-, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, R31-N(R32)- и NC-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, HO-, (C1-C6)-алкил-O-, HO-S(O)2-O-, (HO)2P(O)-O- и NC-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, HO-, (C1-C6)-алкил-O-, (HO)2P(O)-O- и NC-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил, (C1-C6)-алкил-O- и NC-, в другом варианте осуществления из группы, включающей галоген, (C1-C4)-алкил и (C1-C6)-алкил-O-, в другом варианте осуществления из группы, включающей галоген и (C1-C4)-алкил, где в случае, когда содержится более, чем один заместитель R22, заместители R22 независимо друг от друга определены так, как в любом из этих вариантов осуществления. В одном варианте осуществления заместители R22, которые связаны с кольцевым атомом азота, что может быть в случае группы Het1 и R24, выбраны из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил- и (C3-C7)-циклоалкил, в другом варианте осуществления из группы, включающей (C1-C4)-алкил.
Моноциклическая или бициклическая группа R24 может быть 3-членной, 4-членной, 5-членной, 6-членной, 7-членной, 8-членной, 9-членной или 10-членной. В одном варианте осуществления настоящего изобретения моноциклическая группа R24 является 3-членной, 4-членной, 5-членной, 6-членной или 7-членной, и бициклическая группа R24 является 6-членной, 7-членной, 8-членной, 9-членной или 10-членной. В одном варианте осуществления настоящего изобретения R24 представляет собой моноциклическое кольцо, в другом варианте осуществления 3-7-членное моноциклическое кольцо, в другом варианте осуществления 3-6-членное моноциклическое кольцо, в другом варианте осуществления 4-6-членное моноциклическое кольцо, в другом варианте осуществления 5-членное или 6-членное моноциклическое кольцо, в другом варианте осуществления бициклическое кольцо, в другом варианте осуществления 6-10-членное бициклическое кольцо, в другом варианте осуществления 7-10-членное бициклическое кольцо, в другом варианте осуществления 7-9-членное бициклическое кольцо. Два цикла в бициклической группе R24 могут быть конденсированными или образовать мостиковый бицикл или спироцикл. Моноциклическое или бициклическое кольцо R24 может быть насыщенным, т.е. не содержать двойную связь в кольцевой системе, или может быть частично ненасыщенным, т.е. содержать одну или несколько двойных связей в кольцевой системе, например, 1, 2, 3 или 4 двойные связи, или 1, 2 или 3 двойные связи, или 1 или 2 двойные связи, или 1 двойную связь, но не является полностью ароматическим, т.е. оно не содержит циклическую систему из 6 делокализованных пи-электронов в случае моноцикла или из 10 делокализованных пи-электронов в случае бицикла, или оно может быть ароматическим. Количество двойных связей, которые могут содержаться в кольце, зависит от типа кольцевой системы и размера кольца. Частично ненасыщенные кольца R24 также включают бициклические кольцевые системы, в которых один из двух циклов является ароматическим и второй не является ароматическим. В одном варианте осуществления R24 представляет собой насыщенное или ароматическое кольцо, в другом варианте осуществления насыщенное кольцо, в другом варианте осуществления ароматическое кольцо.
Кольцо R24 может быть карбоциклическим, т.е. содержать 0 (ноль) кольцевых гетероатомов, или гетероциклическим, т.е. содержать 1, 2, 3 или 4 одинаковых или разных кольцевых гетероатома. В одном варианте осуществления количество кольцевых гетероатомов, которые содержатся в R24, равно 0, 1, 2 или 3, в другом варианте осуществления 0, 1 или 2, в другом варианте осуществления 0 или 1. В одном варианте осуществления настоящего изобретения R24 в любом из его случаев появления независимо от других случаев его появления представляет собой карбоциклическое кольцо, и в другом варианте осуществления он представляет собой гетероциклическое кольцо. В бициклическом кольце R24 кольцевые гетероатомы могут содержаться в одном из двух циклов или в обоих циклах в любых подходящих положениях. В мостиковых и конденсированных бициклических кольцах кольцевые атомы азота также могут содержаться в мостиковых положениях и в конденсированных положениях. В одном варианте осуществления настоящего изобретения 3-членное кольцо R24 представляет собой карбоциклическое кольцо, предпочтительно циклопропановое кольцо, т.е. в этом случае группа R24 представляет собой циклопропильную группу. В одном варианте осуществления кольцевые гетероатомы, которые содержатся в R24, выбраны из группы, включающей азот и кислород, в другом варианте осуществления из группы, включающей азот и серу, и в другом варианте осуществления они являются атомами азота. R24 может быть присоединен через любой кольцевой атом углерода и любой кольцевой атом азота, который содержит свободный центр связывания. В бициклической группе R24 кольцевой атом, через который присоединен R24, может содержаться в насыщенном кольце, частично ненасыщенном кольце или в ароматическом кольце. В одном варианте осуществления настоящего изобретения R24 в любом из его случаев появления независимо от других случаев его появления присоединен через кольцевой атом углерода, в другом варианте осуществления через кольцевой атом азота.
Типами циклических групп, которые содержатся по определению R24, являются циклоалкильные группы, бициклоалкильные группы, фенильные группы, нафтильные группы, включая нафталин-1-ильные группы и нафталин-2-ильные группы, частично гидрировали нафтильные группы, такие как 1,2,3,4-тетрагидронафталинильные группы, моноциклические и бициклические ароматические гетероциклические группы, такие как, например, группа Het1 и насыщенные и частично ненасыщенные моноциклические и бициклические гетероциклические группы, такие как группа Het2. Приведенные выше и ниже пояснения для таких групп соответственно относятся к таким группам, представляющим собой R24, как и пояснения, приведенные выше для гетероциклических групп в целом. Примерами групп, из любой одной или большего количества которых выбрана группа R24, в одном варианте осуществления настоящего изобретения, являются группы следующих формул
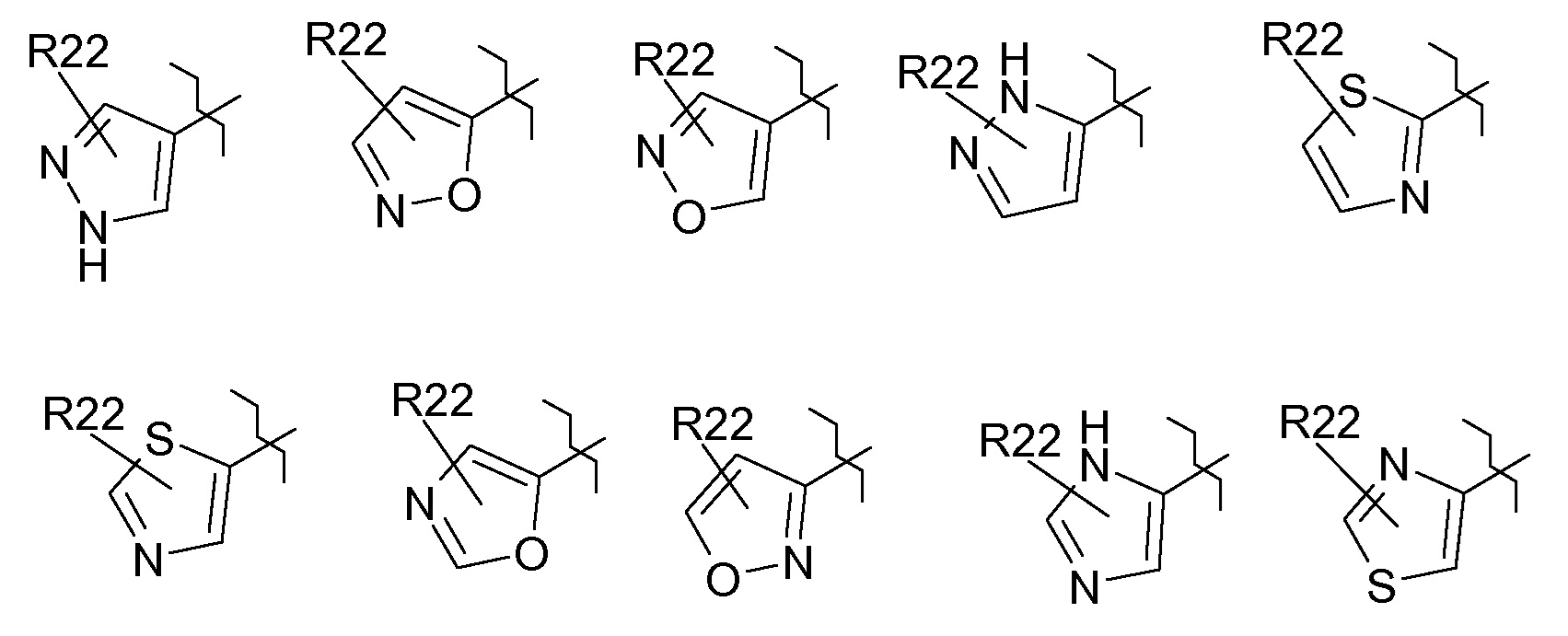
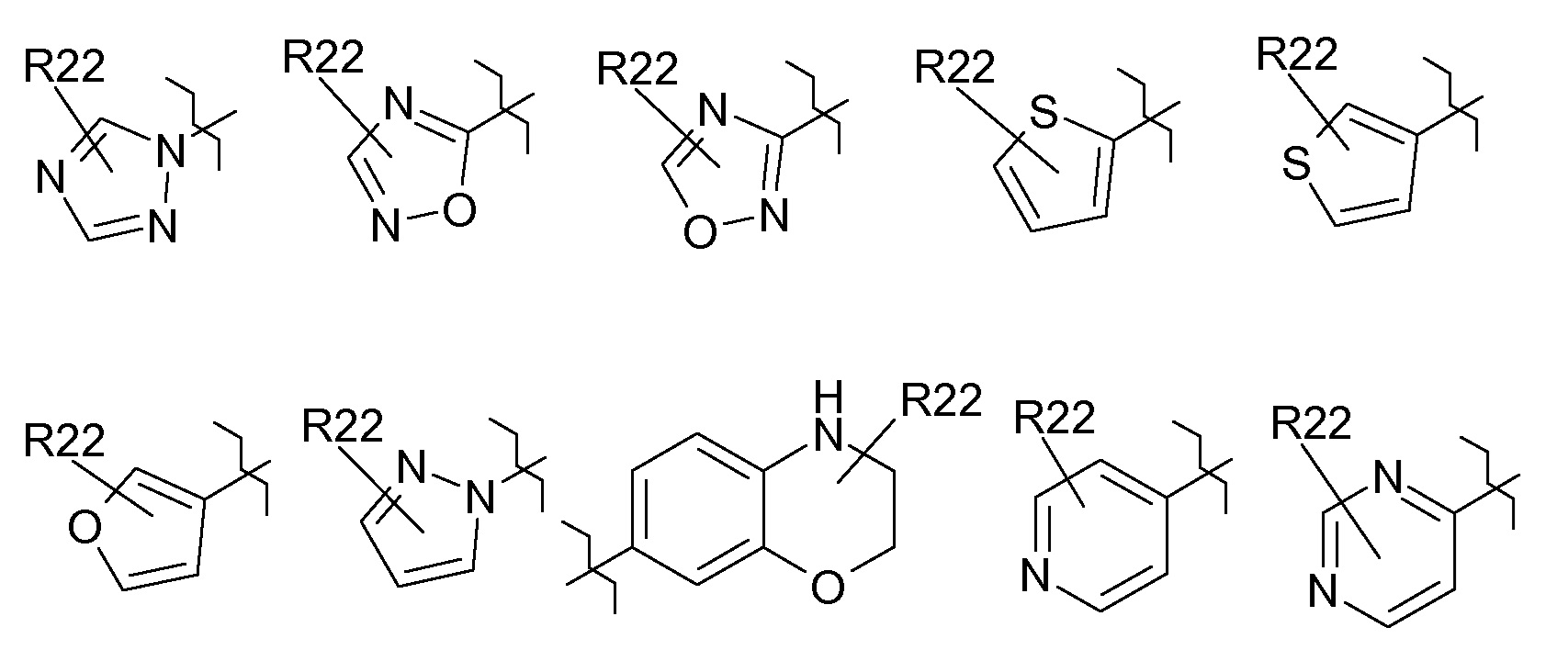
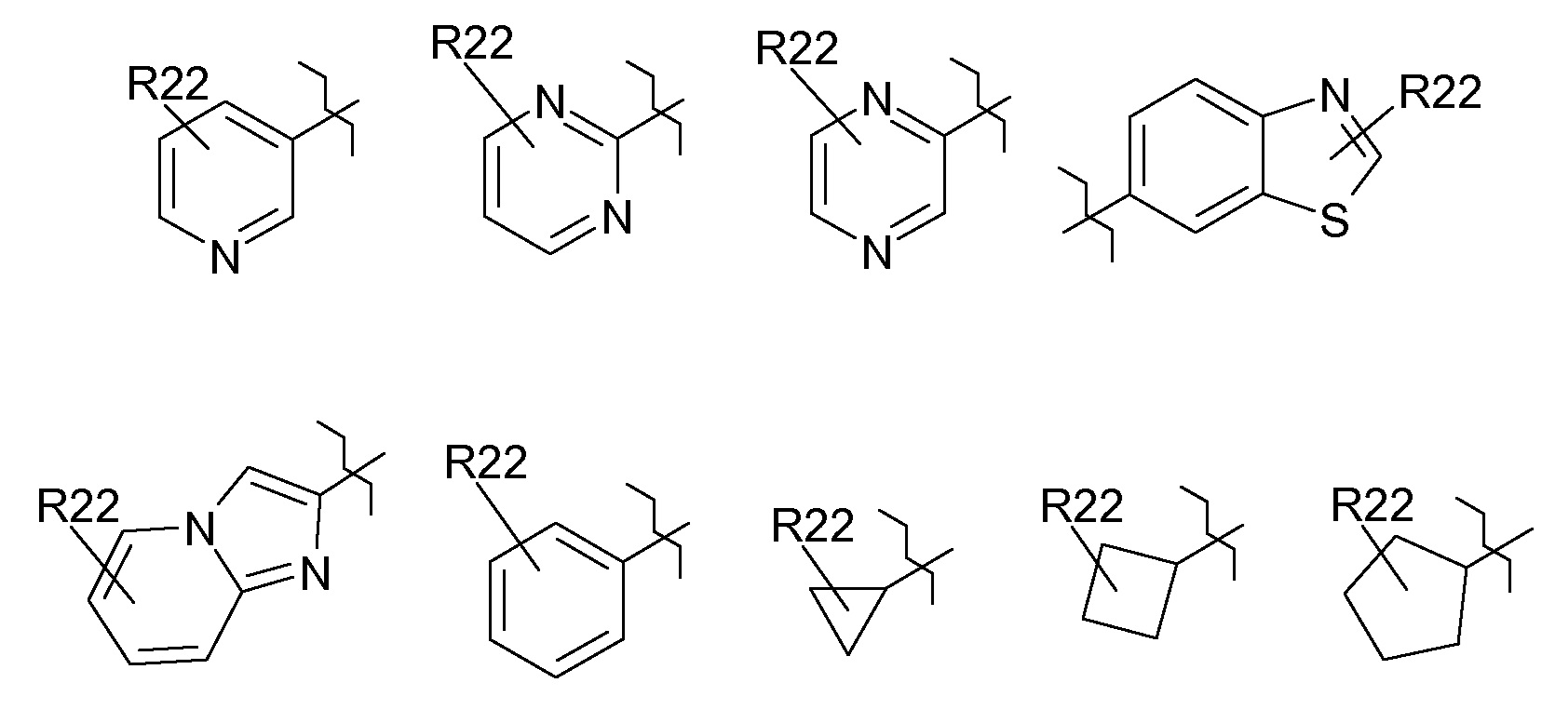
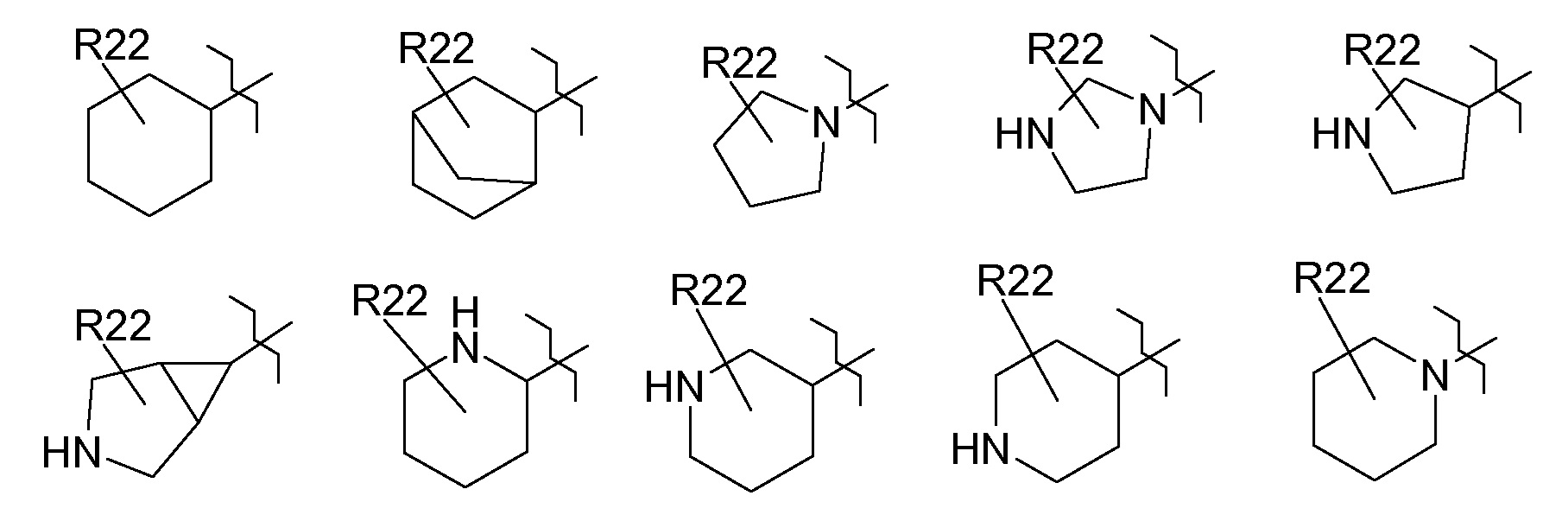
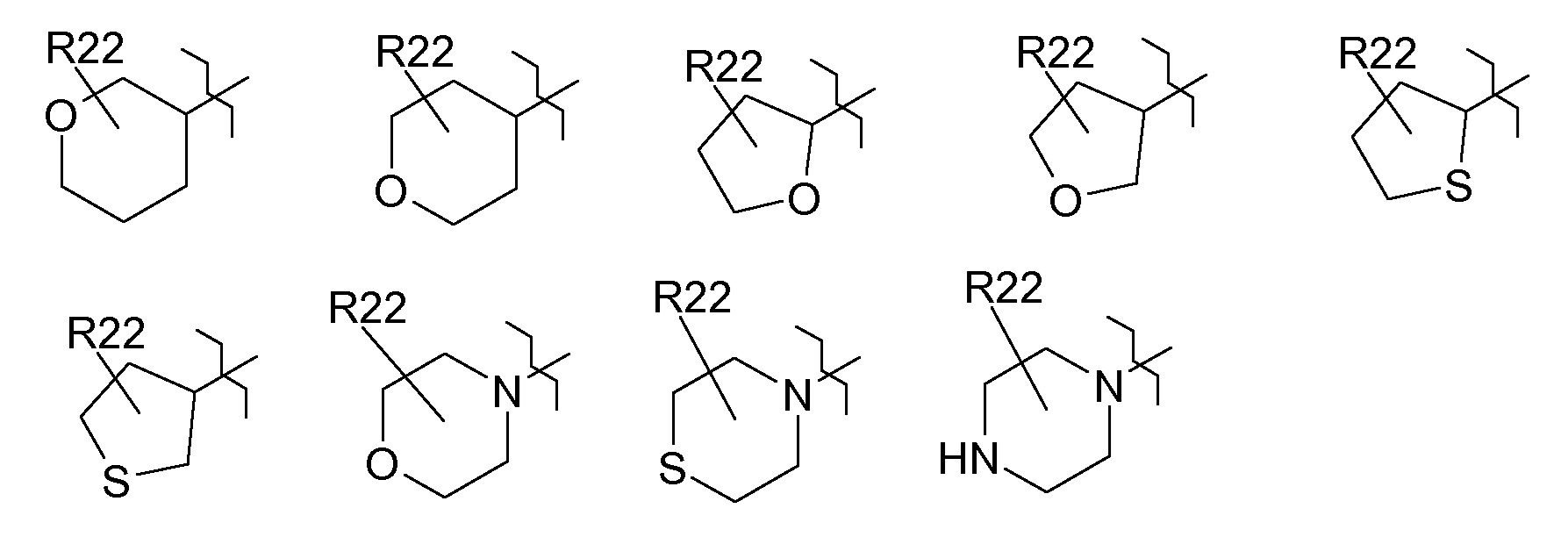
в которых линия, пересеченная значком
В одном варианте осуществления настоящего изобретения количество одинаковых или разных заместителей R22, которые необязательно содержатся в группе R24, равно 1, 2, 3 или 4, в другом варианте осуществления оно равно 1, 2 или 3, в другом варианте осуществления оно равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество оксогрупп, представляющих собой заместители R22, которые необязательно содержатся в R24, кроме любых других заместителей R22, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления количество групп, выбранных из группы, включающей R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-, представляющие собой заместители R22, которые необязательно содержатся в R24, кроме любых других заместителей R22, равно 1 или 2, в другом варианте осуществления оно равно 1, в другом варианте осуществления оно равно 0.
В одном варианте осуществления настоящего изобретения R30 в любом из его случаев появления независимо от других случаев его появления выбран из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, в другом варианте осуществления из группы, включающей (C1-C3)-алкил, в другом варианте осуществления из группы, включающей (C1-C2)-алкил, и в другом варианте осуществления R30 означает метил.
В одном варианте осуществления настоящего изобретения R31 и R32 в любых из их случаев появления независимо от других случаев появления и независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей водород и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C4)-алкил, в другом варианте осуществления из группы, включающей водород и метил, или группы R31 и R32 вместе с атомом азота, с которыми они связаны, образуют 4-7-членный моноциклический насыщенный гетероцикл, который в дополнение к атому азота, с которым связаны R31 и R32, содержит 0 или 1 дополнительный кольцевой гетероатом, выбранный из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил. В другом варианте осуществления R31 и R32 в любых из их случаев появления независимо от других случаев появления и независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей водород и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C4)-алкил, в другом варианте осуществления из группы, включающей водород и метил.
Моноциклический гетероцикл, который могут образовать группы R31 и R32 вместе с атомом азота, с которым они связаны, и, таким образом, гетероцикл, присоединенный через кольцевой атом азота, может быть 4-членным, 5-членным, 6-членным или 7-членным. В одном варианте осуществления настоящего изобретения гетероцикл, образованный группами R31 и R32 вместе с атомом азота, с которым они связаны, является 5-членным или 6-членным, в другом варианте осуществления он является 6-членным. В одном варианте осуществления дополнительный кольцевой гетероатом, который необязательно содержится в гетероцикле, образованном группами R31 и R32 вместе с атомом азота, с которым они связаны, выбран из группы, включающей азот и кислород, в другом варианте осуществления он является атомом азота и в другом варианте осуществления он является атомом кислорода. В одном варианте осуществления настоящего изобретения количество заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил, которые могут содержаться в кольце, образованном группами R31 и R32 вместе с атомом азота, с которым они связаны, равно 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1, в другом варианте осуществления оно равно 0. В одном варианте осуществления настоящего изобретения заместители, которые могут содержаться в кольце, образованном группами R31 и R32 вместе с атомом азота, с которым они связаны, являются фторидными заместителями, и в другом варианте осуществления они являются (C1-C4)-алкильными заместителями, например, метильными заместителями, и в другом варианте осуществления они являются заместителями в таком кольце, связанными с кольцевым атомом азота, выбранными из группы, включающей (C1-C4)-алкил. Примерами гетероциклических групп, из любой одной или большего количества которых выбраны гетероциклические группы, образованные группами R31 и R32 вместе с атомом азота, с которым они связаны, в одном варианте осуществления настоящего изобретения являются азетидин-1-ил, пирролидин-1-ил, пиперидин-1-ил, морфолин-4-ил, тиоморфолин-4-ил, и 4-метилпиперазин-1-ил.
В одном варианте осуществления настоящего изобретения R33 в любом из его случаев появления независимо от других случаев его появления выбран из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей (C1-C6)-алкил, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, в другом варианте осуществления из группы, включающей (C1-C3)-алкил, в другом варианте осуществления из группы, включающей (C1-C2)-алкил, и в другом варианте осуществления R33 означает метил.
В одном варианте осуществления настоящего изобретения R34 в любом из его случаев появления независимо от других случаев его появления выбран из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-, в другом варианте осуществления из группы, включающей водород и (C1-C6)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C4)-алкил, в другом варианте осуществления из группы, включающей водород и (C1-C3)-алкил, в другом варианте осуществления из группы, включающей (C1-C4)-алкил, в другом варианте осуществления из группы, включающей (C1-C3)-алкил, и в другом варианте осуществления R34 означает водород.
В одном варианте осуществления настоящего изобретения ароматическая группа Het1 в любом из ее случаев появления независимо от других случаев появления, представляет собой 5-членный гетероцикл, который содержит один кольцевой гетероатом, который выбран из группы, включающей азот, кислород и серу, и дополнительный кольцевой гетероатом, которым является кольцевой атом азота, или она представляет собой 6-членный гетероцикл, который содержит 1 или 2 кольцевых атома азота, в другом варианте осуществления Het1 выбран из группы, включающей ароматические гетероциклы пиразол, имидазол, изоксазол, оксазол, тиазол, пиридин, пиримидин и пиразин, в другом варианте осуществления из группы, включающей пиразол, изоксазол, оксазол, тиазол, пиридин и пиримидин, в другом варианте осуществления из группы, включающей пиразол, изоксазол, оксазол, тиазол и пиридин, в другом варианте осуществления из группы, включающей пиразол, изоксазол, тиазол и пиридин, в другом варианте осуществления из группы, включающей пиразол, изоксазол и пиридин, в другом варианте осуществления из группы, включающей пиразол, изоксазол и тиазол, которые все являются незамещенными или замещенными, как указано. В одном варианте осуществления группа Het1 присоединена через кольцевой атом углерода. В одном варианте осуществления количество заместителей, которые необязательно содержатся в группе Het1, равно 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1, в другом варианте осуществления оно равно 0. В случае, если некоторая группа Het1 необязательно содержит заместители, выбранные из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-, и для этой группы Het1 не указано другое замещение, в одном варианте осуществления такая группа Het1 необязательно содержит заместители, выбранные из группы, включающей галоген и (C1-C4)-алкил, и в другом варианте осуществления заместитель в такой группе Het1, который связан с кольцевым атомом азота, таким как содержащийся в пиррольном, пиразольном или имидазольном кольце, выбран из группы, включающей (C1-C4)-алкил.
Гетероциклическая группа Het2 может быть 4-членной, 5-членной, 6-членной, 7-членной, 8-членной, 9-членной или 10-членной. В одном варианте осуществления настоящего изобретения моноциклическая группа Het2 является 4-членной, 5-членной, 6-членной или 7-членной, и бициклическая группа Het2 является 6-членной, 7-членной, 8-членной, 9-членной или 10-членной. В одном варианте осуществления настоящего изобретения Het2 в любом из его случаев появления независимо от других случаев появления представляет собой моноциклическое кольцо, в другом варианте осуществления 4-7-членное моноциклическое кольцо, в другом варианте осуществления 4-6-членное моноциклическое кольцо, в другом варианте осуществления 5-членное или 6-членное моноциклическое кольцо, в другом варианте осуществления бициклическое кольцо, в другом варианте осуществления 6-10-членное бициклическое кольцо, в другом варианте осуществления 7-10-членное бициклическое кольцо, в другом варианте осуществления 7-9-членное бициклическое кольцо. Два цикла в бициклической группе Het2 могут быть конденсированными или образовать мостиковый бицикл или спироцикл. В одном варианте осуществления группа Het2 является насыщенной или содержит одну двойную связь в кольце, в другом варианте осуществления она является насыщенной. В одном варианте осуществления дополнительный кольцевой гетероатом, который необязательно содержится в группе Het2, выбран из группы, включающей азот и кислород, в другом варианте осуществления он является атомом азота и в другом варианте осуществления он является атомом кислорода. Het2 моет быть присоединен через любой кольцевой атом углерода и через любой кольцевой атом азота, который содержит свободный центр связывания. В одном варианте осуществления настоящего изобретения Het2 в любом из его случаев появления независимо от других случаев его появления присоединен через кольцевой атом углерода, в другом варианте осуществления через кольцевой атом азота. Примерами гетероциклических групп, из любой одной или большего количества которых выбран Het2, в одном варианте осуществления настоящего изобретения являются оксетанил, азетидинил, тетрагидрофуранил, тетрагидротиофенил, пирролидинил, тетрагидропиранил, тетрагидротиопиранил, пиперидинил, азепанил, морфолинил, тиоморфолинил, пиперазинил и 3-азабицикло[3.1.0]гексил, которые в одном варианте осуществления присоединены через кольцевой атом углерода и, например, представляют собой остатки оксетан-3-ил, азетидин-2-ил, азетидин-3-ил, тетрагидрофуран-2-ил, тетрагидрофуран-3-ил, тетрагидротиофен-2-ил, тетрагидротиофен-3-ил, пирролидин-2-ил, пирролидин-3-ил, тетрагидропиран-2-ил, тетрагидропиран-3-ил, тетрагидропиран-4-ил, тетрагидротиопиран-2-ил, тетрагидротиопиран-3-ил, тетрагидротиопиран-4-ил, пиперидин-2-ил, пиперидин-3-ил, пиперидин-4-ил и 3-азабицикло[3.1.0]гекс-6-ил.
Если одно или оба числа p и q равны 0 (нулю), то один или оба заключенных в скобки углов циклоалканового кольца, представленного в формуле I, не содержатся и кольцевой атом углерода, к которому присоединены группы R2 и R3, связан ординарной связью с одним или обоими кольцевыми атомами углерода, соседними с атомом, к которому присоединен атом кислорода, который связывает циклоалкановое кольцо с хромановым кольцом. В одном варианте осуществления настоящего изобретения одно из чисел p и q, например, p, выбрано из группы, включающей 0 и 1, и другое из чисел p и q, например, q, равно 0. В другом варианте осуществления оба числа p и q равны 0 и соответствующие соединения являются соединениями формулы Ie. В другом варианте осуществления настоящего изобретения одно из чисел p и q равно 0 и второе равно 1 и соответствующие соединения являются соединениями формулы If. В другом варианте осуществления настоящего изобретения оба числа p и q равны 1 и соответствующие соединения являются соединениями формулы Ig. Группы Ar и R1-R4 в соединениях формул Ie, If и Ig определены так, как в соединениях формулы I.
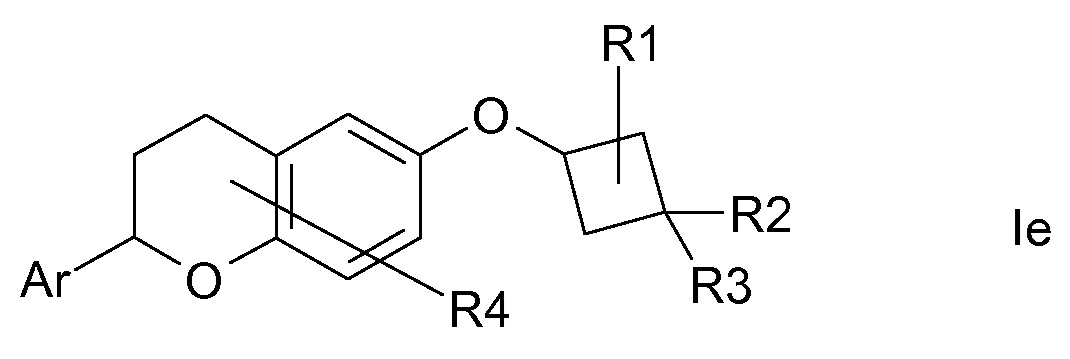
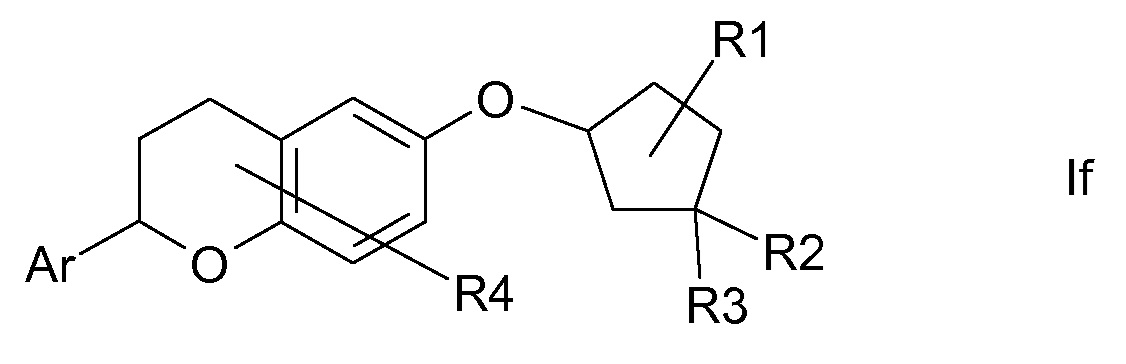
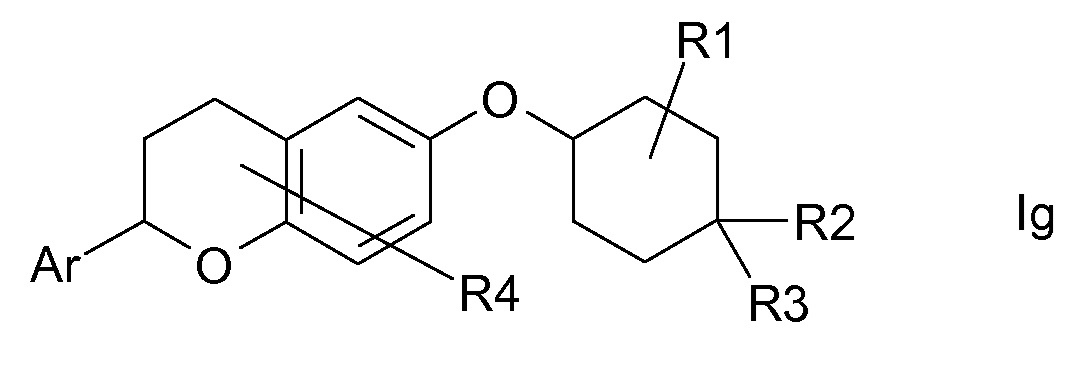
В одном варианте осуществления настоящего изобретения заместители в фенильной группе в любом случае появления в соединении формулы I независимо от любых других случаев появления выбраны из группы, включающей галоген и (C1-C4)-алкил, если не указано иное. В одном варианте осуществления количество заместителей в фенильной группе равно 1, 2 или 3, в другом варианте осуществления 1 или 2, в другом варианте осуществления 1, в другом варианте осуществления оно равно 0, если не указано иное.
В одном варианте осуществления настоящего изобретения хиральный атом углерода в положении 2 хроманового кольца в соединении формулы I содержится или в основном содержится, например, при молярном соотношении двух изомеров, составляющем 98:2 или 99:1 или более, в одной конфигурации, в R-конфигурации или в S-конфигурации, что указано волнистой формой клиновидной связи в соединении формулы Ih. В другом варианте осуществления настоящего изобретения хиральный атом углерода в положении 2 хроманового кольца в соединении формулы I содержится или в основном содержится, например, при молярном соотношении двух изомеров, составляющем 98:2 или 99:1 или более, в конфигурации, представленной в формуле Ik, т.е. в соответствующем соединении формулы I группа Ar расположена над плоскостью, которая, как можно допустить, образована хромановым кольцом, расположенным, как представлено в формуле Ik, конфигурация которой является R-конфигурацией в случае, когда все группы R4 означают водород. В другом варианте осуществления настоящего изобретения хиральный атом углерода в положении 2 хроманового кольца в соединении формулы I содержится или в основном содержится, например, при молярном соотношении двух изомеров, составляющем 98:2 или 99:1 или более, в конфигурации, представленной в формуле Im, т.е. в соответствующем соединении формулы I группа Ar расположена под плоскостью, которая, как можно допустить, образована хромановым кольцом, расположенным, как представлено в формуле Im, конфигурация которой является S-конфигурацией в случае, когда все группы R4 означают водород.
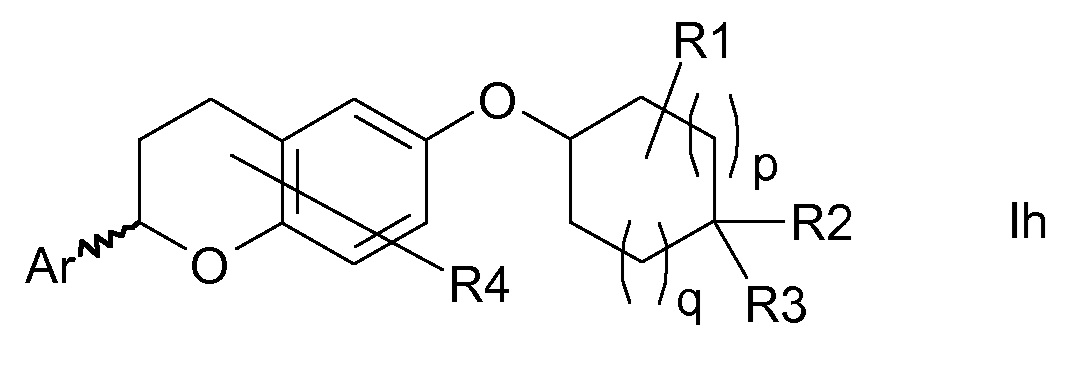
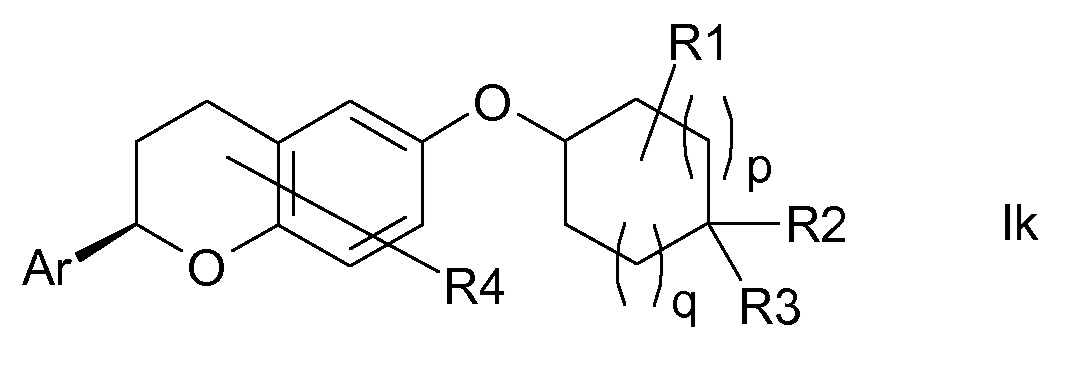

Группы Ar, R1-R4 и числа p и q в соединениях формул Ih, Ik и Im определены так, как в соединениях формулы I.
В одном варианте осуществления настоящего изобретения группа R2 и атом кислорода, который связывает циклоалкановое кольцо, представленное в формуле I, с хромановым кольцом, находятся в цис-положении друг по отношению к другу, т.е. они находятся с одной и той же стороны плоскости, например, над плоскостью, которая, как можно допустить, образована циклоалкановым кольцом, расположенным, как представлено в формуле In, и соответствующие соединения являются соединениями формулы In. В другом варианте осуществления настоящего изобретения группа R2 и атом кислорода, который связывает циклоалкановое кольцо, представленное в формуле I, с хромановым кольцом, находятся в транс-положении друг по отношению к другу, т.е. они находятся с разных сторон от плоскости, которая, как можно допустить, образована циклоалкановым кольцом, расположенным, как представлено в формуле Io, и соответствующие соединения являются соединениями формулы Io.
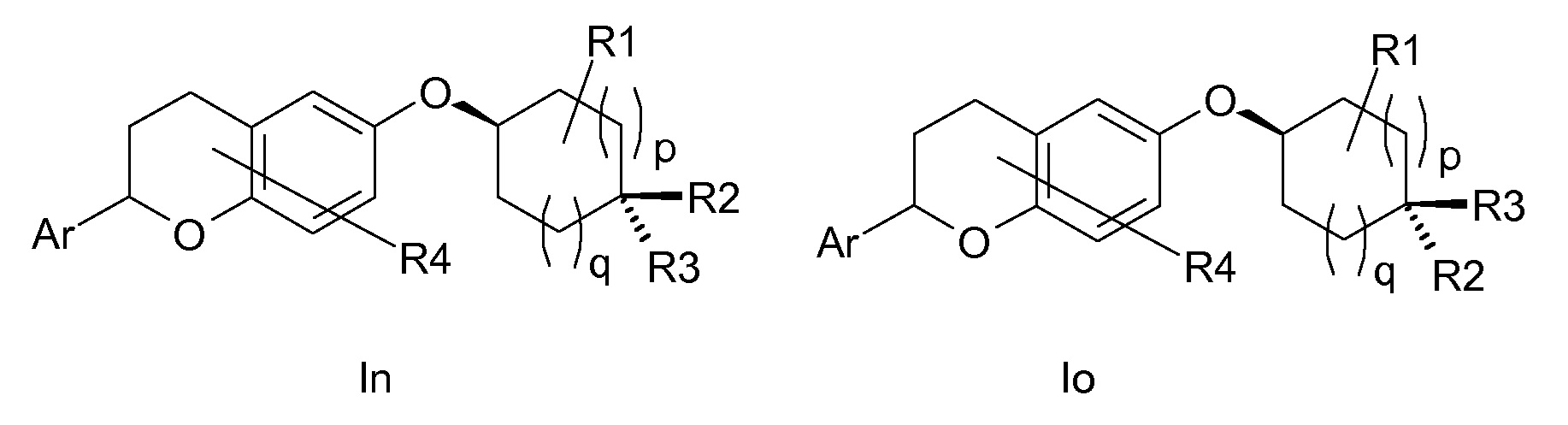
Объектом настоящего изобретения являются все соединения формулы I, в которой любой один или несколько структурных элементов, таких как группы, остатки, заместители, числа и стереохимические конфигурации, определены, как в любом из указанных вариантов осуществления или определений элементов, или обладают одним или несколькими заданными значениями, которые указаны в настоящем изобретении в качестве примеров элементов, где все комбинации одного или нескольких определений соединений или элементов и/или указанных вариантов осуществления, и/или конкретных значений элементов, являются объектом настоящего изобретения. Также применительно ко всем таким соединениям формулы I все их стереоизомерные формы и смеси стереоизомерных форм в любом соотношении и их фармацевтически приемлемые соли являются объектом настоящего изобретения.
В качестве примера соединений, предлагаемых в настоящем изобретении, которые применительно к любым структурным элементам определены, как в указанных вариантах осуществления настоящего изобретения или в определениях таких элементов, можно отметить соединения формулы I, в которой
Ar означает фенил, который является незамещенным или содержит один или несколько одинаковых или разных заместителей R0;
R0 выбран из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O- и (C3-C7)-циклоалкил-(C1-C4)-алкил-O;
R1 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
R2 выбран из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, (C1-C6)-алкил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20;
R3 выбран из группы, включающей водород и (C1-C6)-алкил, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей (C3-C7)-циклоалкил и фенил;
или группы R2 и R3 вместе означают оксогруппу;
R4 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-;
R5 и R6 независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C2-C6)-алкенил, (C3-C7)-циклоалкил, Het1 и Het2, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и Het1 является незамещенным или содержит один или несколько одинаковых или разных заместителей R22,
или группы R5 и R6 вместе с атомом азота, с которыми они связаны, образуют 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который в дополнение к атому азота, с которым связаны R5 и R6, содержит 0 или 1 дополнительный кольцевой гетероатом, выбранный из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей R21;
R7 выбран из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, фенил, Het1 и Het2, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и фенил и Het1 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R22;
R8 выбран из группы, включающей водород и (C1-C4)-алкил;
R9 выбран из группы, включающей (C1-C6)-алкил и (C3-C7)-циклоалкил;
R10 выбран из группы, включающей водород, (C1-C6)-алкил и (C3-C7)-циклоалкил;
R20 выбран из группы, включающей R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (HO)2P(O)-O-CH2-O-C(O)-O-, (C1-C6)-алкил-S(O)n-, (C3-C7)-циклоалкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-;
R21 выбран из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, R34-O-C(O)-(C1-C4)-алкил-, R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)- и R31-N(R32)-C(O)-;
R22 выбран из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, R33-O-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, NC-, R33-C(O)- и R31-N(R32)-C(O)-;
R24 означает 3-7-членное моноциклическое кольцо, которое является насыщенным, частично ненасыщенным или ароматическим и содержит 0, 1, 2 или 3 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу, и которое является незамещенным или содержит один или несколько одинаковых или разных заместителей R22;
R30 и R33 независимо друг от друга выбраны из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, фенил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-;
R31 и R32 независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, фенил-(C1-C4)-алкил- и Het1-(C1-C4)-алкил-;
R34 выбран из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-;
Het1 означает 5-членный или 6-членный моноциклический ароматический гетероцикл, который содержит 1, 2 или 3 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-, если не указано иное;
Het2 означает 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который содержит 1 или 2 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу;
n выбран из группы, включающей 0, 1 и 2, где все числа не зависят друг от друга;
p и q независимо друг от друга выбраны из группы, включающей 0 и 1;
где все фенильные группы являются незамещенными или содержат один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-, если не указано иное;
где все циклоалкильные группы независимо от любых других заместителей, которые могут содержаться в циклоалкильной группе, могут содержать один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
где все алкильные группы независимо от любых других заместителей, которые могут содержаться в алкильной группе, могут содержать один или несколько фторидных заместителей;
в любой из их стереоизомерных форм или смесь стереоизомерных форм в любом соотношении и их фармацевтически приемлемая соль.
В качестве другого такого примера можно отметить соединения формулы I в которой
Ar означает фенил, который является незамещенным или содержит один или несколько одинаковых или разных заместителей R0;
R0 выбран из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкил-, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O- и (C3-C7)-циклоалкил-(C1-C4)-алкил-O-;
R1 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
R2 выбран из группы, включающей (C1-C6)-алкил, HO-, (C1-C6)-алкил-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20;
R3 выбран из группы, включающей водород и (C1-C6)-алкил, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из группы, включающей (C3-C7)-циклоалкил и фенил;
или группы R2 и R3 вместе означают оксогруппу;
R4 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-;
R5 и R6 независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21,
или группы R5 и R6 вместе с атомом азота, с которыми они связаны, образуют 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который в дополнение к атому азота, с которым связаны R5 и R6, содержит 0 или 1 дополнительный кольцевой гетероатом, выбранный из группы, включающей азот, кислород и серу, и который является незамещенным или содержит один или несколько одинаковых или разных заместителей R21;
R7 выбран из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21;
R8 выбран из группы, включающей водород и (C1-C4)-алкил;
R9 выбран из группы, включающей (C1-C6)-алкил и (C3-C7)-циклоалкил;
R10 выбран из группы, включающей водород, (C1-C6)-алкил и (C3-C7)-циклоалкил-;
R20 выбран из группы, включающей R24, фтор, HO-, оксогруппу, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, R30-C(O)-O-, R30-NH-C(O)-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)2-;
R21 выбран из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, R34-O-C(O)-(C1-C4)-алкил-, R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)- и R31-N(R32)-C(O)-;
R22 выбран из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, NC-, R33-C(O)- и R31-N(R32)-C(O)-;
R24 означает 3-7-членное моноциклическое кольцо, которое является насыщенным, частично ненасыщенным или ароматическим и содержит 0, 1, 2 или 3 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу, и которое является незамещенным или содержит один или несколько одинаковых или разных заместителей R22;
R30 и R33 независимо друг от друга выбраны из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-;
R31 и R32 независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-;
R34 выбран из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-;
Het2 означает 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который содержит 1 или 2 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу;
n выбран из группы, включающей 0, 1 и 2, где все числа не зависят друг от друга;
p и q независимо друг от друга выбраны из группы, включающей 0 и 1;
где все фенильные группы являются незамещенными или содержат один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген, (C1-C4)-алкил и (C1-C4)-алкил-O-, если не указано иное;
где все циклоалкильные группы независимо от любых других заместителей, которые могут содержаться в циклоалкильной группе, могут содержать один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
где все алкильные группы независимо от любых других заместителей, которые могут содержаться в алкильной группе, могут содержать один или несколько фторидных заместителей;
в любой из их стереоизомерных форм или смесь стереоизомерных форм в любом соотношении и их фармацевтически приемлемая соль.
В качестве другого такого примера можно отметить соединения формулы I в которой
Ar означает фенил, который является незамещенным или содержит один или несколько одинаковых или разных заместителей R0;
R0 выбран из группы, включающей галоген, (C1-C6)-алкил, (C3-C7)-циклоалкил, (C1-C6)-алкил-O- и (C3-C7)-циклоалкил-O-;
R1 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
R2 выбран из группы, включающей (C1-C6)-алкил, HO-, R5-N(R6)-, R7-C(O)-N(R8)- и R5-N(R6)-C(O)-, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20;
R3 означает водород;
R4 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген и (C1-C4)-алкил;
одна из групп R5 и R6 выбрана из группы, включающей водород и (C1-C6)-алкил, и вторая из групп R5 и R6 выбрана из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, где (C1-C6)-алкил все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21;
R7 выбран из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, где (C1-C6)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21;
R8 выбран из группы, включающей водород и (C1-C4)-алкил;
R20 выбран из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)-, R31-N(R32)-C(O)- и R31-N(R32)-S(O)2-;
R21 выбран из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, R31-N(R32)-, R33-C(O)-N(R32)- и R31-N(R32)-C(O)-;
R22 выбран из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)- и R31-N(R32)-C(O)-;
R24 означает 3-7-членное моноциклическое кольцо, которое является насыщенным, частично ненасыщенным или ароматическим и содержит 0, 1, 2 или 3 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу, и которое является незамещенным или содержит один или несколько одинаковых или разных заместителей R22;
R33 выбран из группы, включающей (C1-C6)-алкил;
R31 и R32 независимо друг от друга выбраны из группы, включающей водород, (C1-C6)-алкил, (C3-C7)-циклоалкил и (C3-C7)-циклоалкил-(C1-C4)-алкил-;
Het2 означает 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который содержит 1 или 2 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу;
n выбран из группы, включающей 0, 1 и 2, где все числа не зависят друг от друга;
p и q равны 1;
где все циклоалкильные группы независимо от любых других заместителей, которые могут содержаться в циклоалкильной группе, могут содержать один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
где все алкильные группы независимо от любых других заместителей, которые могут содержаться в алкильной группе, могут содержать один или несколько фторидных заместителей;
в любой из их стереоизомерных форм или смесь стереоизомерных форм в любом соотношении и их фармацевтически приемлемая соль.
В качестве другого такого примера можно отметить соединения формулы I в которой
Ar означает фенил, который является незамещенным или содержит 1 или 2 одинаковых или разных заместителя R0;
R0 выбран из группы, включающей галоген, (C1-C6)-алкил и (C1-C6)-алкил-O-;
R1 означает водород;
R2 означает R5-N(R6)-C(O)-;
R3 означает водород;
R4 означает водород;
одна из групп R5 и R6 выбрана из группы, включающей водород и (C1-C6)-алкил, и вторая из групп R5 и R6 выбрана из группы, включающей (C1-C6)-алкил, (C3-C7)-циклоалкил и Het2, где (C1-C6)-алкил все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R20, и (C3-C7)-циклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21;
R20 выбран из группы, включающей R24, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)-, (C1-C6)-алкил-S(O)2-N(R32)- и R31-N(R32)-C(O)-;
R21 выбран из группы, включающей (C1-C4)-алкил, HO-(C1-C4)-алкил-, R31-N(R32)-(C1-C4)-алкил-, фтор, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, R31-N(R32)-, R33-C(O)-N(R32)- и R31-N(R32)-C(O)-;
R22 выбран из группы, включающей галоген, (C1-C4)-алкил, HO-(C1-C4)-алкил-, (C3-C7)-циклоалкил, HO-, (C1-C6)-алкил-O-, (C3-C7)-циклоалкил-O-, HO-S(O)2-O-, (HO)2P(O)-O-, (C1-C6)-алкил-S(O)n-, R31-N(R32)-, R33-C(O)-N(R32)- и R31-N(R32)-C(O)-;
R24 означает 3-7-членное моноциклическое кольцо, которое является насыщенным, частично ненасыщенным или ароматическим и содержит 0, 1 или 2 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу, и которое является незамещенным или содержит один или несколько одинаковых или разных заместителей R22;
R33 выбран из группы, включающей (C1-C6)-алкил;
R31 и R32 независимо друг от друга выбраны из группы, включающей водород и (C1-C6)-алкил;
Het2 означает 4-7-членный моноциклический насыщенный или частично ненасыщенный гетероцикл, который содержит 1 или 2 одинаковых или разных кольцевых гетероатома, выбранных из группы, включающей азот, кислород и серу;
n выбран из группы, включающей 0, 1 и 2, где все числа не зависят друг от друга;
p и q равны 1;
где все циклоалкильные группы независимо от любых других заместителей, которые могут содержаться в циклоалкиле, могут содержать один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C1-C4)-алкил;
где все алкильные группы независимо от любых других заместителей, которые могут содержаться в алкильной группе, могут содержать один или несколько фторидных заместителей;
в любой из их стереоизомерных форм или смесь стереоизомерных форм в любом соотношении и их фармацевтически приемлемая соль.
Объектом настоящего изобретения также является соединение формулы I, которое выбрано из числа любых конкретных соединений формулы I, которые раскрыты в настоящем изобретении, или является любым из конкретных соединений формулы I, которые раскрыты в настоящем изобретении, независимо от того, раскрыты ли они в виде свободного соединения и/или в виде конкретной соли, или его фармацевтически приемлемой соли, где соединение формулы I является объектом настоящего изобретения в любой из его стереоизомерных форм или смеси стереоизомерных форм в любом соотношении, а также любые конкретные соли и стереоизомерные формы, раскрытые в настоящем изобретении. Например, объектом настоящего изобретения является соединение формулы I, которое выбрано из группы, включающей:
транс-4-(2-о-толилхроман-6-илокси)-циклогексиламин,
N-(Изоксазол-5-илметил)-4-(2-о-толилхроман-6-илокси)-циклогексанкарбоксамид,
2-Амино-N-[транс-4-((S)-2-фенилхроман-6-илокси)-циклогексил]-ацетамид,
4-(2-о-толилхроман-6-илокси)-N-(1,3,5-триметилпиразол-4-илметил)-циклогексиламин,
(S)-N-[транс-4-(2-Фенилхроман-6-илокси)-циклогексил]-пирролидин-2-карбоксамид,
(2-гидроксиэтил)-амид транс-4-((R)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты,
(2-гидроксиэтил)-амид транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты,
(2-гидроксиэтил)-амид цис-4-((R)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты,
(2-гидроксиэтил)-амид цис-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты и
динатриевую соль моно-(2-{[транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбонил]-амино}- этилового) эфира фосфорной кислоты,
или которое является любым из этих соединений и их фармацевтически приемлемых солей, где соединение формулы I является объектом настоящего изобретения в любой из его стереоизомерных форм или смесь стереоизомерных форм в любом соотношении, если не указана конкретная стереоизомерная форма для любых атомов углерода в соответствующем соединении.
Другим объектом настоящего изобретения являются способы получения соединений формулы I, которые описаны ниже и с помощью которых можно получить соединения формулы I и промежуточные продукты, образующиеся при их синтезе. Например, один такой способ относится к синтезу соединений формулы I из хроман-6-олов формулы II и циклоалканолов формулы III и включает образование простой эфирной связи между циклоалкановым кольцом и хромановым кольцом с получением соединений формулы IV и, в зависимости от значений групп X и Y в соединении формулы III и групп R2 и R3 в конечном соединении формулы I, последующее превращение групп X и Y в группы R2 и R3 и/или другие превращения групп.
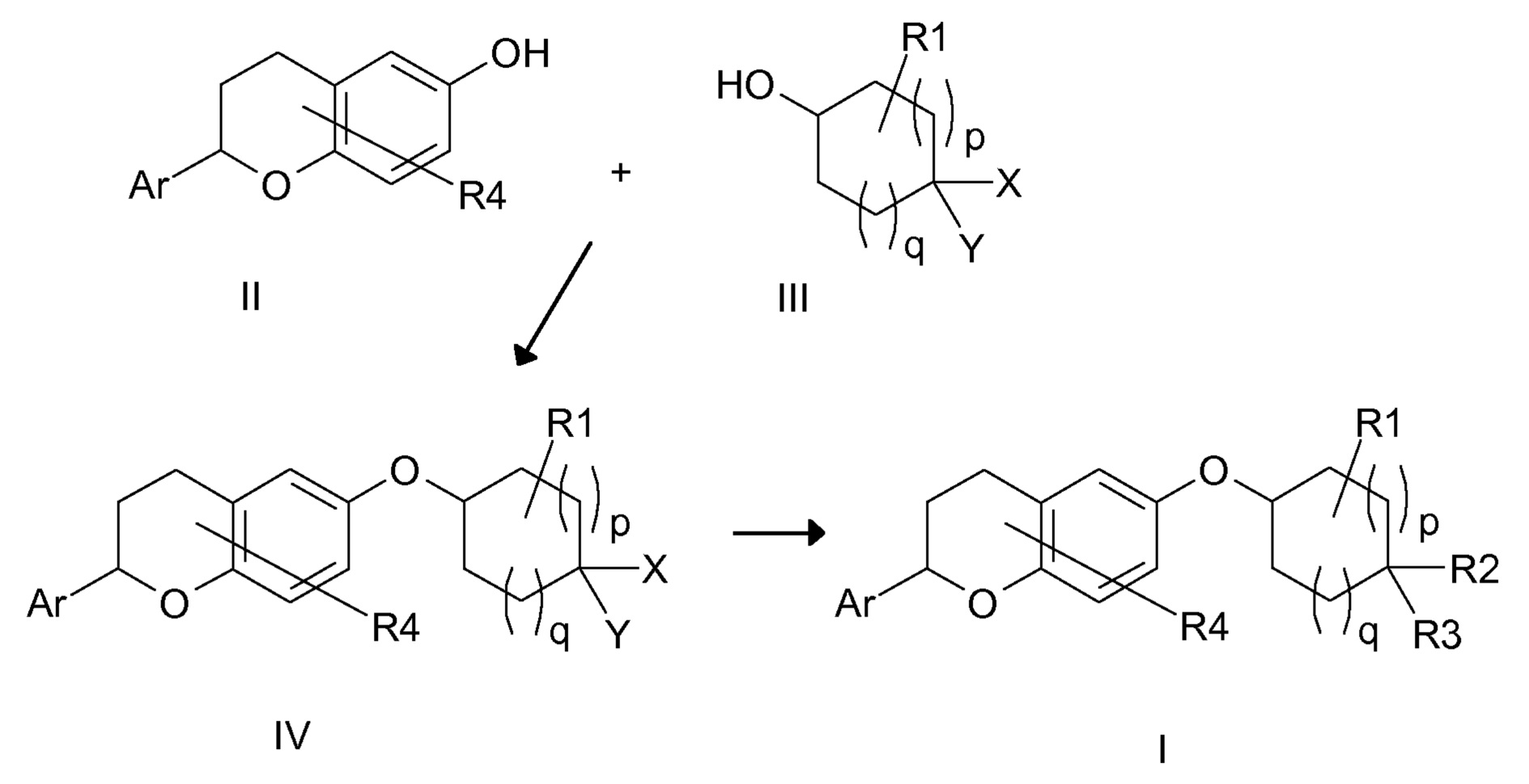
Группы Ar, R1 и R4 и числа p и q в соединениях формул II, III и IV определены так, как в соединениях формулы I, и дополнительно функциональные группы могут содержаться в защищенной форме или в форме группы-предшественника, которую затем превращают в конечную группу. Одна или обе группы X и Y в соединениях формул III и IV могут представлять собой группы R2 и R3, которые содержатся в конечном соединении формулы I, и, таким образом, в некоторых случаях соединение формулы IV уже является соединением формулы I, или одна или обе группы X и Y могут представлять собой защищенные формы или группы-предшественники групп R2 и R3 или исходные группы для образования групп R2 и R3. Например, в этом случае группы R2 и R3 в соединении формулы I не мешают образованию простой эфирной связи, как в случае, когда R2 означает водород или алкил, который может быть незамещенными или замещенным нереакционноспособными заместителями, или, например, алкил-O- и/или R3 означает водород или алкил, которые могут быть незамещенными или замещенным нереакционноспособными заместителями, группы X и Y в соединении формулы III уже могут обладать значениями соответствующих групп R2 и R3. Для синтеза соединений формулы I, в которой R2 означает HO-, алкил-O-, алкил-C(O)-O-, фенил-C(O)-O- или Het1-C(O)-O-, и R3 означает водород или алкил, или R2 и R3 вместе означают оксогруппу, можно использовать соединения формулы III, в которой X означает защищенную гидроксигруппу и Y означает водород или алкил, или X и Y вместе представляют собой защищенную оксогруппу, и из полученных соединений формулы IV удаляют защитную группу и их вводят в различные дополнительные реакции. Аналогичным образом, для синтеза соединений формулы I, в которой R2 означает R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)2-N(R8)- или R9-N(R10)-C(O)-N(R8)-, можно использовать соединения формулы III, в которой X означает защищенную аминогруппу и Y означает водород или алкил, и из полученных соединений формулы IV удаляют защитную группу и их вводят в различные дополнительные реакции. Для синтеза соединений формулы I, в которой R2 означает амидную группу R5-N(R6)-C(O)-, соединения формулы III можно использовать, в которой X означает сложноэфирную группу, такую как алкил-O-C(O)- и Y означает водород или алкил, и полученные соединения формулы IV прямо или через соответствующие карбоновые кислоты превращают в амиды формулы I. Дополнительное подробное описание таких стратегий синтеза приведено ниже и в примерах. Большое количество подходящих исходных циклоалканолов формулы III имеются в продаже или их можно получить по методикам или аналогично методикам, описанным в литературе, и это также относится к другим исходным соединениям, использующимся при синтезе соединений формулы I.
Реакцию соединений формул II и III, т.е. образование простой эфирной связи, удобно проводить с помощью хорошо известной реакции Мицунобу в присутствии третичного фосфина, такого как триарилфосфин, такого как трифенилфосфин, или триалкилфосфина, такого как трибутилфосфин, и производного азодикарбоновой кислоты, такого как диэфир азодикарбоновой кислоты, такой как диэтилазодикарбоксилат (ДЭАД) и диизопропилазодикарбоксилат (ДИАД) или диамид азодикарбоновой кислоты, такой как дипиперидид азодикарбоновой кислоты (АДДП). Реакцию Мицунобу, которая протекает с обращением конфигурации у атома углерода в соединении формулы III, которое содержит гидроксигруппу, представленную в формуле III, проводят в безводной среде в инертном растворителе, таком как углеводород, такой как бензол и толуол, хлорированный углеводород, такой как дихлорметан или хлороформ, простой эфир, такой как диэтиловый эфир, тетрагидрофуран (ТГФ) или диоксан, нитрил, такой как ацетонитрил, или амид, такой как диметилформамид (ДМФ), обычно при температурах, равных от примерно -50°C до примерно 100°C, предпочтительно от примерно 0°C до примерно 30°C. Дополнительные подробности приведены в различной литературе о реакции Мицунобу, такой как обзорные статьи O. Mitsunobu, Synthesis (1981): 1-28; D. L. Hughes, Organic Reactions 42 (1992): 335-656; K. C. Kumara Swamy et al., Chemical Reviews 109 (2009): 2551-2651.
В качестве примера синтеза типов соединений формулы I из соединений формул II и III через соединения формулы IV, указанные выше, на следующей схеме проиллюстрирован синтез соединений формулы Id, т.е. соединений формулы I, в которой R2 означает R5-N(R6)-C(O)-.
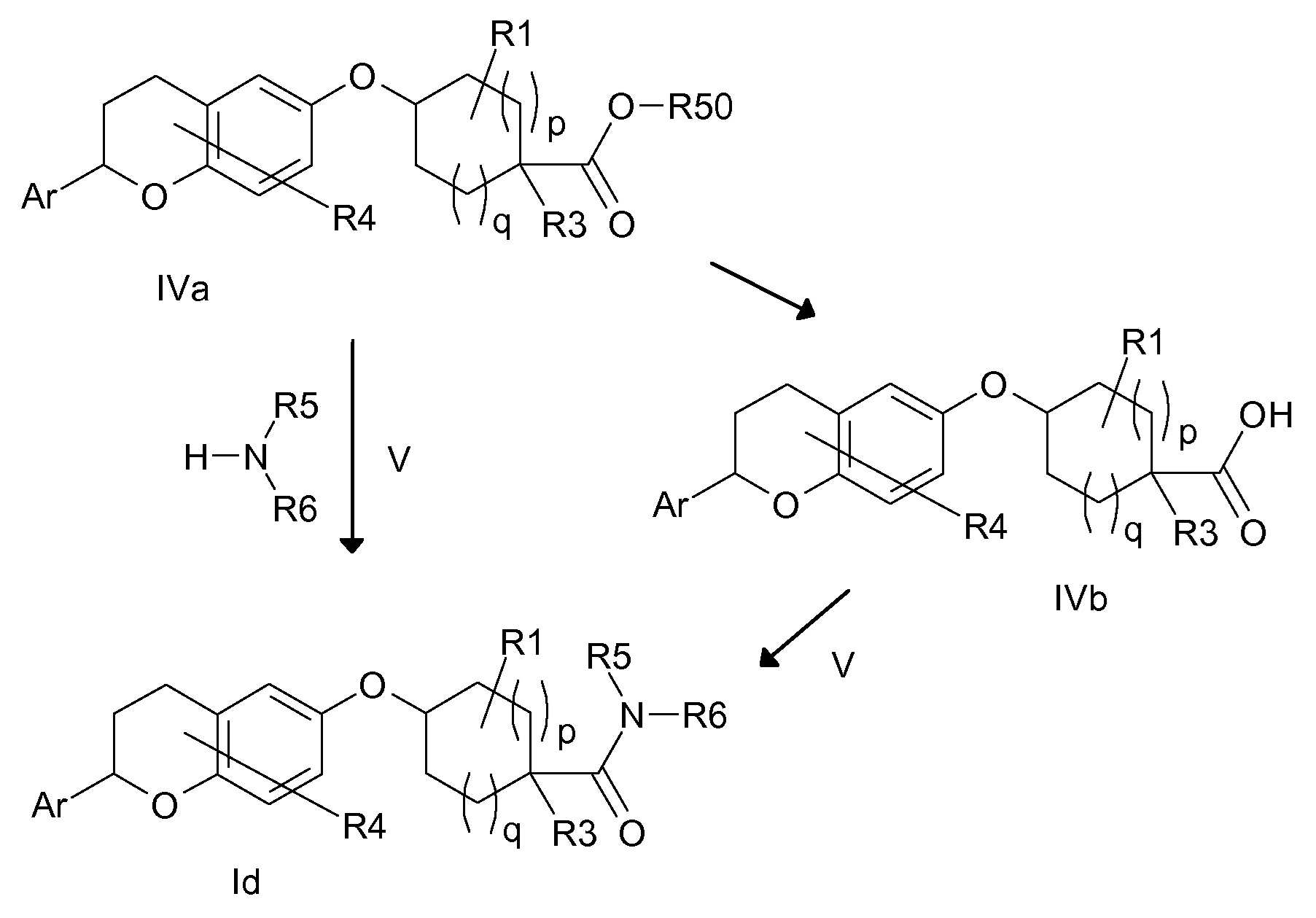
Как отмечено выше, соединения формулы III, в которых X означает сложноэфирную группу, можно ввести в реакцию с соединениями формулы II и получить соединения формулы IV, такие как соединения формулы IVa, в которой R50 означает (C1-C4)-алкил, например. Соединения формулы IVa, предпочтительно соединения формулы IVa, в которой R50 означает (C1-C2)-алкил, можно ввести в реакцию с аминами формулы V при стандартных условиях аминолиза сложных эфиров, например, в растворителе, таком как углеводород, такой как толуол, хлорированный углеводород, такой как дихлорметан, 1,2-дихлорэтан или хлорбензол или простой эфир, такой как ТГФ, диоксан или 1,2-диметоксиэтан (ДМЭ) при температурах, равных от примерно 20°C до примерно 120°C, и получить соединения формулы Id. Соединения формулы IVa также можно превратить в соединения формулы Id удобным образом с помощью проводимого сначала превращения соединения формулы IVa в соответствующую карбоновую кислоту формулы IVb или ее соль, и введения в реакцию соединения формулы IVb или его соли с амином формулы V при стандартных условиях образования амидов из карбоновых кислот. Группы Ar, R1, R3, R4, R5 и R6 и числа p и q в соединениях формул IVa, IVb и V определены так, как в соединениях формулы I, и дополнительно функциональные группы могут содержаться в защищенной форме или в форме группы-предшественника, которую затем превращают в конечную группу.
Соединения формулы IVa можно превратить в соединения формулы IVb путем обработки кислотой или основанием, например, путем обработки гидроксидом щелочного металла, таким как гидроксид лития, гидроксид натрия или гидроксид калия, в растворителе, таком как простой эфир, такой как ТГФ, диоксан или ДМЭ или спирт, такой как метанол или этанол, или смеси растворителей, предпочтительно в водном растворителе или смеси растворителей, или путем обработки хлористоводородной кислотой или трифторуксусной кислотой в растворителе, таком как хлорированный углеводород, такой как дихлорметан, простой эфир или спирт, в частности, в случае трет-бутилового эфира при температурах, равных от примерно 20°C до примерно 100°C, с последующим использованием стандартных процедур обработки, таких как подкисление, в случае, если сложный эфир формулы IVa гидролизуют в присутствии основания и необходимо получить свободную карбоновую кислоту формулы IVb, где конкретные условия, как обычно, зависят от условий в конкретном случае и их легко выбирает специалист в данной области техники. Для реакции с соединением формулы V карбоксигруппу HO-C(O)- в соединении формулы IVb обычно активируют in situ с помощью обычного амидного реагента сочетания или превращают в реакционноспособное производное карбоновой кислоты, которое можно получить in situ или выделить. Например, соединение формулы IVb можно превратить в галогенангидрид кислоты, например, путем обработки тионилхлоридом, пентахлоридом фосфора или оксалилхлоридом, или обработать алкилхлорформиатом, таким как этилхлорформиат или изобутилхлорформиат, и получить смешанный ангидрид. Обычными реагентами сочетания, которые можно использовать, являются ангидрид пропансульфоновой кислоты, N,N'-карбонилдиазолы, такие как N,N'-карбонилдиимидазол (CDI), карбодиимиды, такие как 1,3-диизопропилкарбодиимид (DIC), 1,3-дициклогексилкарбодиимид (DCC) или 1-(3-диметиламинопропил)-3-этилкарбодиимидгидрохлорид (EDC), карбодиимиды вместе с добавками, такими как 1-гидроксибензотриазол (HOBT) или 1-гидрокси-7-азабензотриазол (HOAT), реагенты сочетания на основе урония, такие как O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуронийгексафторфосфат (HATU), O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийгексафторфосфат (HBTU) или O-(циано(этоксикарбонил)метиленамино)-N,N,N',N'-тетраметилуронийтетрафторборат (TOTU), и реагенты сочетания на основе фосфония, такие как (бензотриазол-1-илокси)трис(диметиламино)фосфонийгексафторфосфат (BOP), (бензотриазол-1-илокси)трипирролидинфосфонийгексафторфосфат (PyBOP) или бромтрипирролидинофосфонийгексафторфосфат (PyBroP). Реакцию активированного соединения формулы IVb или реакционноспособного производного соединения формулы IVb обычно проводят в инертном растворителе, например, углеводороде, таком как толуол, хлорированном углеводороде, таком как дихлорметан, простом эфире, таком как ТГФ, диоксан или ДМЭ, сложном эфире, таком как этилацетат или бутилацетат, нитриле, таком как ацетонитрил, амиде, таком как ДМФ или N-метилпирролидин-2-он (NMP), или воде, или в смеси растворителей, при температурах, равных от примерно -10°C до примерно 100°C, предпочтительно при температурах, равных от примерно 0°C до примерно 60°C. Реакцию предпочтительно проводят в присутствии основания, такого как третичный амин, такой как триэтиламин, этилдиизопропиламин, N-метилморфолин или пиридин, или неорганического основания, такого как гидроксид, карбонат или гидрокарбонат щелочного металла, такой как гидроксид натрия, гидроксид калия, карбонат натрия или гидрокарбонат натрия.
В качестве другого примера на следующей схеме проиллюстрирован синтез соединений формулы I, в которых R2 и R3 вместе означают оксогруппу, т.е. соединений формулы Ip, и их применение для синтеза других соединений формулы I.
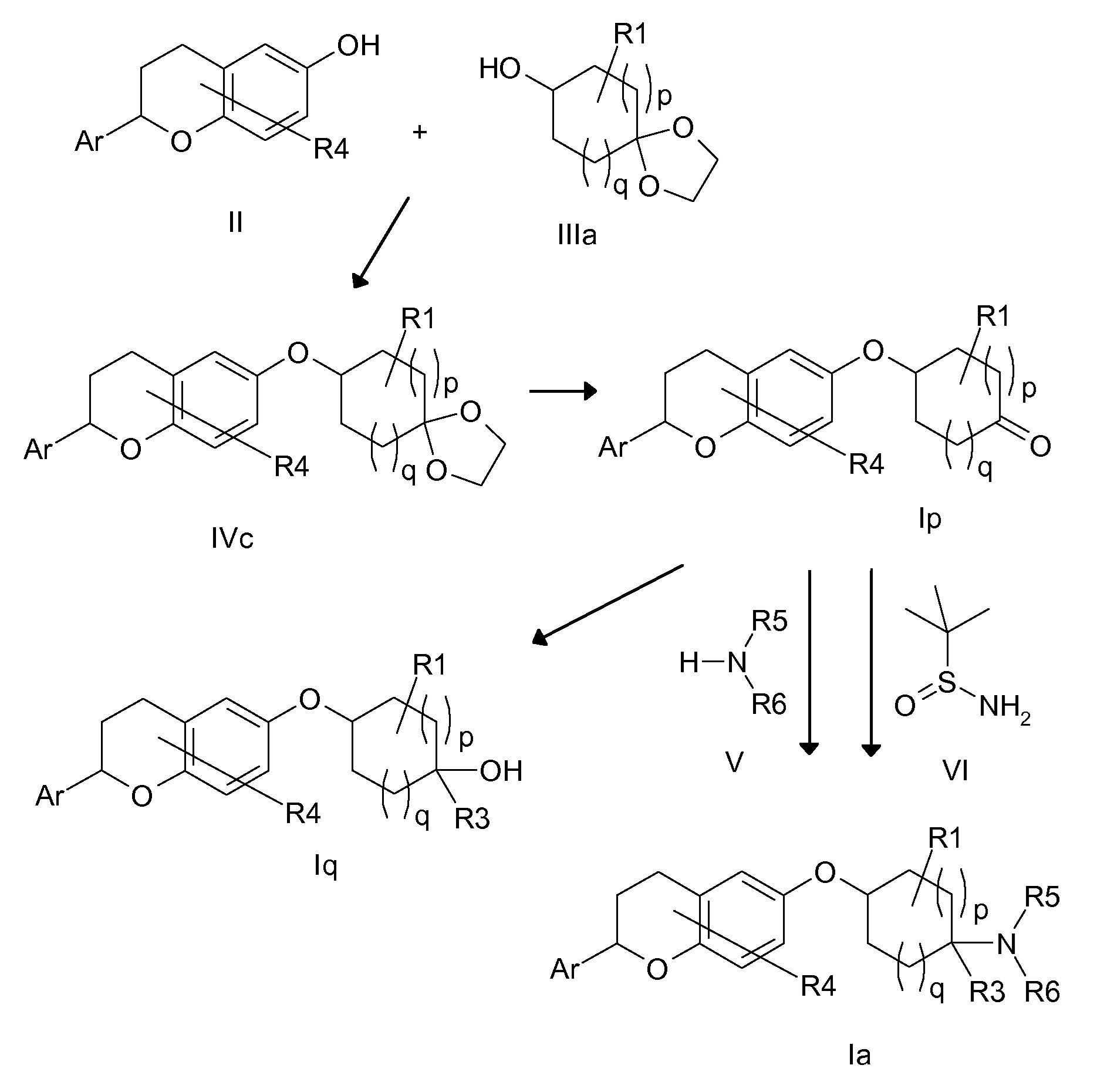
Соединения формулы II можно ввести в реакцию с соединениями формулы III, в которой группы X и Y вместе представляют собой двухвалентную 1,2-этилендиоксигруппу (-O-CH2-CH2-O-), т.е. 1,4-диоксаспироциклоалканолами формулы IIIa, которые являются защищенной формой соответствующих гидроксициклоалканонов, в которых оксогруппа кетализирована этиленгликолем. Из полученных соединений формулы IVc можно удалить защитную группу при стандартных условиях, например, путем обработки хлористоводородной кислотой при температурах, равных от примерно 20°C от примерно 30°C, и получить соответствующие кетоны, т.е. соединения формулы Ip, которые уже являются конечными соединениями формулы I. Соединения формулы Ip легко можно превратить в другие соединения формулы I при стандартных условиях. Например, их можно превратить в соединения формулы I, в которой R2 означает HO-, т.е. соединения формулы Iq, восстановлением комплексным гидридным восстановительным реагентом, таким как боргидрид натрия, и получить соединения формулы Iq, в которой R3 означает водород, или путем обработки реагентом Гриньяра получить соединения формулы Iq, в которой R3 означает необязательно замещенную алкильную группу. Соединения формулы Ip также можно ввести в реакцию с аминами формулы V, предпочтительно с аминами, в которых по меньшей мере одна из групп R5 и R6 отличается от водорода, в реакцию восстановительного аминирования, например, с комплексным боргидридом в качестве восстановительного реагента, таким как цианоборгидрид натрия или триацетоксиборгидрид натрия, и получить соединения формулы I, в которой R2 означает группу R5-N(R6)-, т.е. соединения формулы Ia, и R3 означает водород. По реакции с трет-бутилсульфинамидом формулы VI и затем с реагентом Гриньяра соединения формулы Ip можно превратить в соединения формулы Ia, в которой R3 означает необязательно замещенную алкильную группу и R5 и R6 означают водород, эти соединения можно дополнительно модифицировать по атому азота, например, алкилировать с помощью реакции восстановительного аминирования, или ацилировать или сульфонилировать при стандартных условиях. Группы Ar, R1 и R4 и числа p и q в соединениях формул IIIa и IVc определены так, как в соединениях формулы I, и дополнительно функциональные группы могут содержаться в защищенной форме или в форме группы-предшественника, которую затем превращают в конечную группу.
В качестве другого примера на следующей схеме проиллюстрировано превращение соединений формулы IV, в которой группа X представляет собой защищенную аминогруппу и группа Y означает группу R3, например, водород, в соединения формулы I.
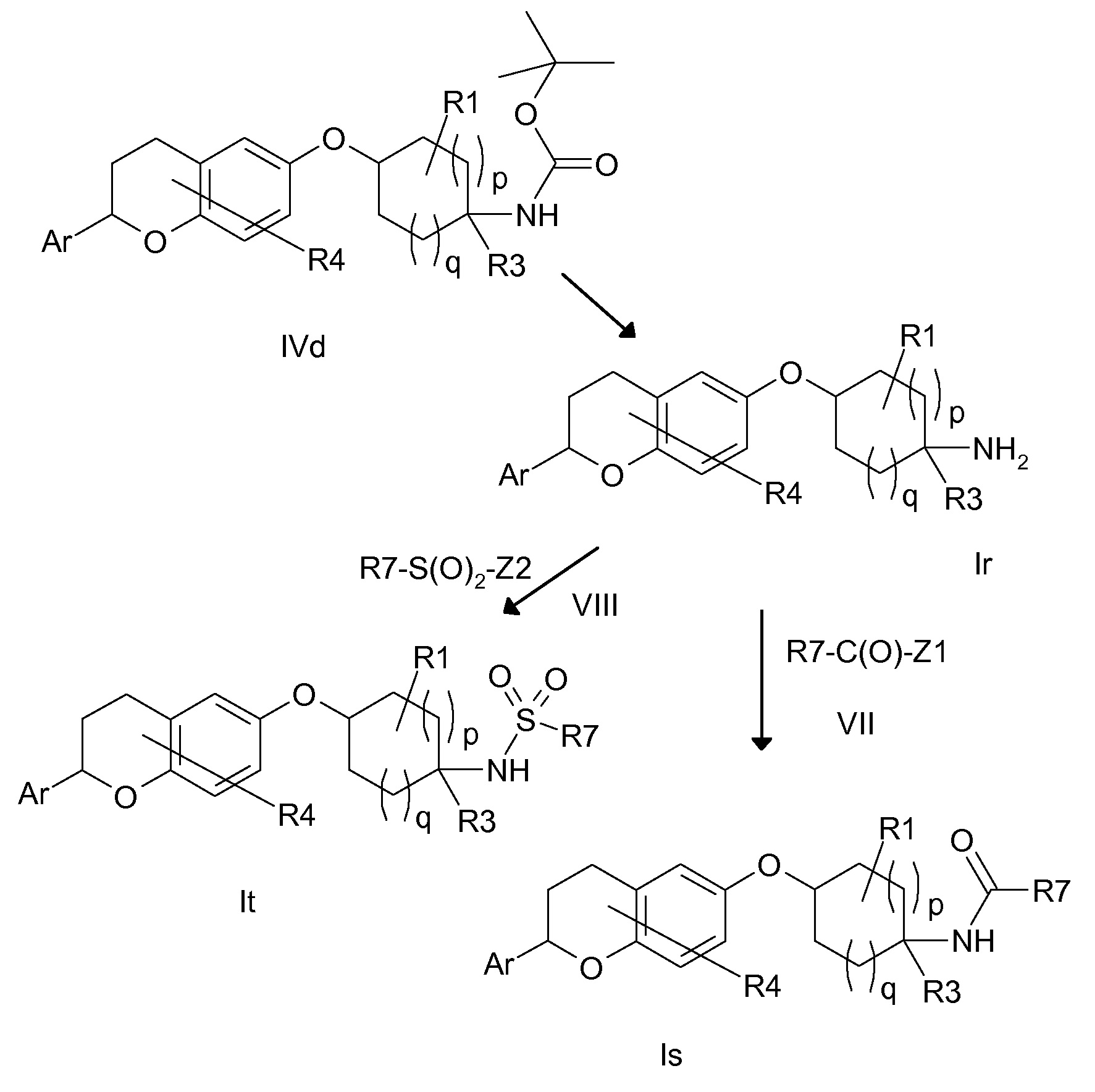
Из соединений формулы IVd, которые можно получить из соединений формулы II и легко доступных аминоциклоанканолов формулы III, которые защищены по атому азота трет-бутилоксигруппой (Boc), защитную группу можно удалить путем обработки кислотой, например, трифторуксусной кислотой, при температурах, равных от примерно 20°C до примерно 30°C, и получить соединения формулы Ir, которые уже являются конечными соединениями формулы I. Соединения формулы Ir можно легко превратить в другие соединения формулы I, например, ацилировать соединениями формулы VII и сульфонилировать соединениями формулы VIII и получить соединения формулы I, в которой R2 означает группу R7-C(O)-NH- и группу R7-S(O)2-NH соответственно и R8 означает водород, т.е. соединения формул Is и It. Соединения формулы Ir можно легко алкилировать по аминогруппе, например, с помощью реакции восстановительного аминирования и получить соответствующие соединения формулы Ir, в которой атом азота содержит одну или две алкильные группы, и последние соединения, содержащие одну алкильную группу, ацилировать соединениями формулы VII и сульфонилировать соединениями формулы VIII и получить соответствующие соединения формул Is и It, в которых R8 означает алкил. Группы Ar, R1, R3, R4 и R7 и числа p и q в соединениях формул IVd, VII и VIII определены так, как в соединениях формулы I, и дополнительно функциональные группы могут содержаться в защищенной форме или в форме группы-предшественника, которую затем превращают в конечную группу. Группы Z1 и Z2 в соединениях формул VII и VIII представляют собой способные к нуклеофильному замещению отщепляющиеся группы, предпочтительно хлор, и в этом последнем случае соединения формул VII и VIII являются хлорангидридами карбоновых кислот и хлорангидридами сульфоновых кислот. Группы Z1 и Z2 также могут быть гидроксигруппами и в этом случае соединения формул VII и VIII представляют собой карбоновые кислоты и сульфоновые кислоты, которые обычно активируют in situ с помощью обычного амидного реагента сочетания или превращают в реакционноспособное производное карбоновой кислоты, такое как соединение, в котором Z1 или Z2 означает хлор, для реакции с соединением формулы Ir. Описание активирующих реагентов и условий проведения реакции, приведенное выше применительно к реакции соединений формулы IVb с соединениями формулы V с получением карбоксамидов, применимо соответственно к реакционной смеси соединений формул VII и VIII с соединениями формулы Ir с получением карбоксамидов и сульфонамидов.
Для получения других соединений формулы I в соединениях формулы I полученных, как описано выше, или в промежуточных продуктах или исходных соединениях для синтеза соединений формулы I при стандартных условиях можно провести различные превращения функциональных групп. Например, гидроксигруппу можно ввести в реакцию с карбоновой кислотой или ее реакционноспособным производным по методике, аналогичной описанной выше для реакции карбоновой кислоты с амином, и получить эфир карбоновой кислоты. Этерификацию гидроксигрупп можно провести алкилированием соответствующим галогенсодержащим соединением, например, бромидом или йодидом, в присутствии основания, такого как гидрид щелочного металла, такой как гидрид натрия или карбонат щелочного металла, такой как карбонат калия или карбонат цезия, в инертном растворителе, таком как амид, такой как ДМФ или NMP, или кетон, такой как ацетон или бутан-2-он, или соответствующим спиртом при условиях проведения реакции Мицунобу в присутствии фосфина, такого как трифенилфосфин или трибутилфосфин, и производного азодикарбоновой кислоты, такого как диэтилазодикарбоксилат или диизопропилазодикарбоксилат. По реакции с изоцианатом гидроксигруппу можно превратить в N-замещенный эфир карбаминовой кислоты. Путем обработки подходящим галогенирующим реагентом гидроксигруппу можно превратить в галогенид. Путем обработки триоксидом серы в присутствии пиридина гидроксигруппу можно превратить в моноэфир серной кислоты. Путем обработки подходящим фосфорамидитом, таким как дибензил-N,N-диизопропилфосфорамидит, диаллил-N,N-диизопропилфосфорамидит или ди-трет-бутил-N,N-диизопропилфосфорамидит формулы (изопропил)2N-P(O-R55)2, в которой R55 означает бензил, аллил или трет-бутил, например, в присутствии тетразола и с последующим окислением, например, надкислотой, такой как 3-хлорпербензойная кислота, гидроксигруппу можно превратить в ее дибензиловый эфир фосфорной кислоты, диаллиловый эфир фосфорной кислоты и ди-трет-бутиловый эфир фосфорной кислоты соответственно, который можно расщепить и получить моноэфир фосфорной кислоты гидроксигруппы, т.е. соединение, которое содержит группу (HO)2P(O)-, присоединенную к атому кислорода гидроксигруппы, с помощью каталитического гидрирования в присутствии палладиевого катализатора в случае дибензилового сложного эфира, с помощью катализируемого палладием нуклеофильного замещения в случае диаллилового сложного эфира и путем обработки кислотой, такой как трифторуксусная кислота, в случае ди-трет-бутилового эфира. Путем обработки хлорметилхлорформиатом и затем дибензилфосфатом серебра гидроксигруппу можно превратить в дибензилоксифосфорилоксиметиловый эфир угольной кислоты, который можно расщепить и получить фосфонооксиметиловый эфир угольной кислоты гидроксигруппы, т.е. соединение, которое содержит группу (HO)2P(O)-O-CH2-O-C(O)-, присоединенную к атому кислорода гидроксигруппы, с помощью каталитического гидрирования в присутствии палладиевого катализатора (см. WO 2010/039474). Атом галогена можно заменить различными группами с помощью реакции замещения, которая также может быть катализируемой переходным металлом реакцией. Аминогруппу можно модифицировать при стандартных условиях алкилирования, например, по реакции с галогенсодержащим соединением или путем восстановительного аминирования карбонильного соединения, или для ацилирования или сульфонилирования, например, по реакции с активированной карбоновой кислотой или производным карбоновой кислоты, таким как хлорангидрид или ангидрид кислоты. Сложноэфирную группу карбоновой кислоты можно гидролизовать в кислой или щелочной среде и получить карбоновую кислоту. Карбоксигруппу можно активировать или превратить в реакционноспособное производное, как описано выше, и ввести в реакцию со спиртом или амином или аммиаком и получить сложный эфир или амид. Первичный амид можно дегидратировать и получить нитрил. Атом серы группе в алкил-S- или в гетероциклическом кольце можно окислить пероксидом, таким как пероксид водорода или надкислота, и получить сульфоксидный фрагмент (S(O)) или сульфоновый фрагмент (S(O)2). Карбоксигруппу, сложноэфирную карбоксигруппу и кетонную группу можно восстановить с получением спирта, например, комплексным гидридом, таким как алюмогидрид лития, боргидрид лития или боргидрид натрия. Гидроксигруппу можно окислить с образованием оксогруппы, например, пиридинийхлорхроматом или реагентом периодинан Десса-Мартина. Все такие реакции при получении соединений формулы I общеизвестны и их можно провести по методикам, известным специалисту в данной области техники, или аналогично методикам, которые описаны в стандартной литературе, например, в публикациях Houben-Weyl, Methods of Organic Chemistry, Thieme; или Organic Reactions, John Wiley & Sons; или R. C. Larock, Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2. ed. (1999), John Wiley & Sons, и цитированной в них литературе.
Хроман-6-олы формулы II, которые используются для синтеза соединений формулы IV, описанных выше, можно получить по различным методикам. По одной из них ацетофенон формулы IX, который замещен в бензольном кольце гидроксигруппой и группой G1 и может дополнительно быть замещен в бензольном кольце и ацетильной группе заместителями R4 конденсируют с альдегидом формулы X в присутствии основания и получают хроман-4-он формулы XII и/или халькон формулы XI и затем полученный халькон формулы XI циклизуют и получают хроман-4-он формулы XII.
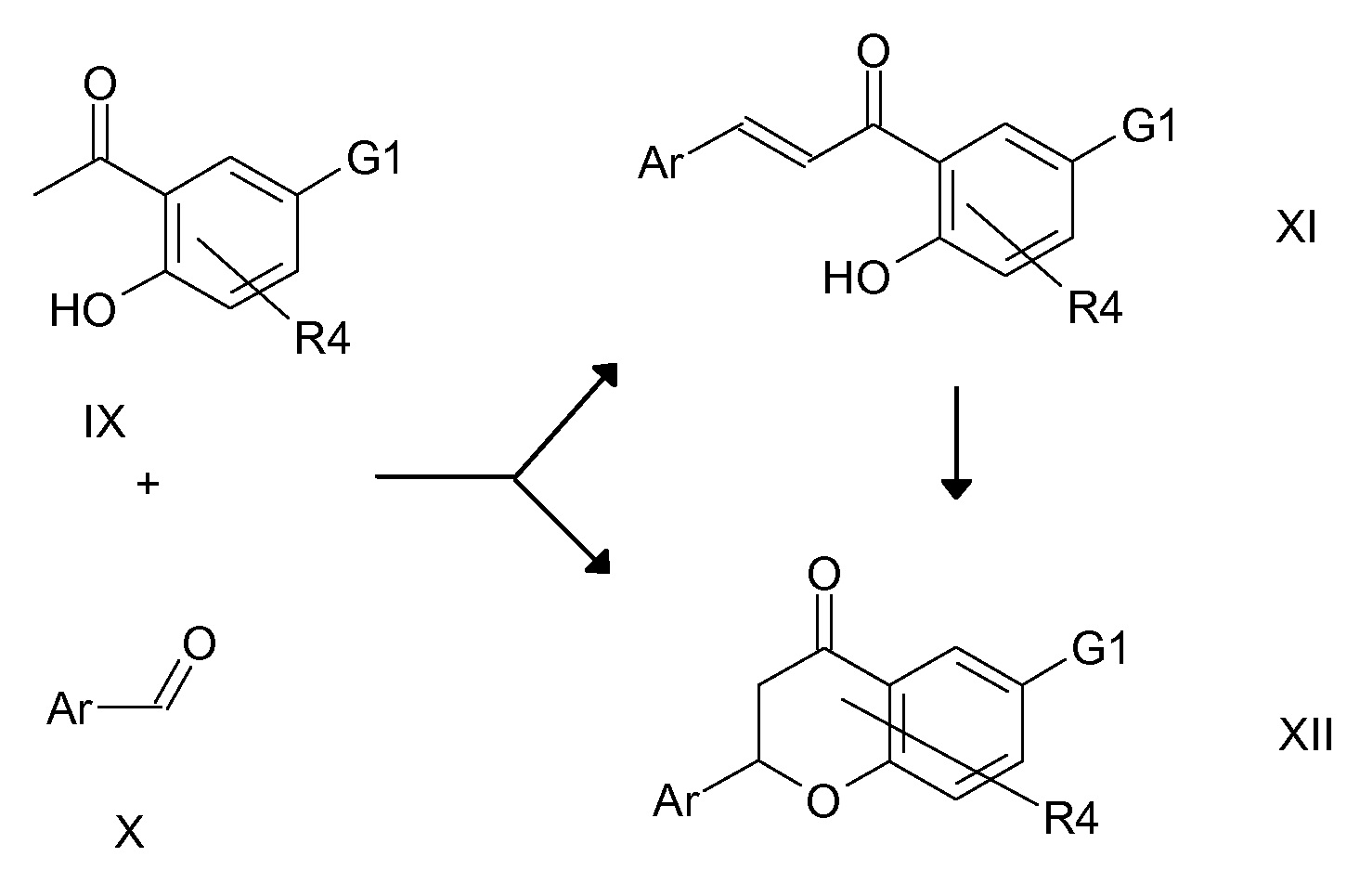
Группы Ar и R4 в соединениях формул IX, X, XI и XII определены так, как в соединениях формулы I, и дополнительно функциональные группы могут содержаться в защищенной форме или в форме группы-предшественника, которую затем превращают в конечную группу. Группа G1 в соединениях формул IX, XI и XII представляет собой гидроксигруппу или бром. При проведении реакции соединений формул IX и X в присутствии гидроксида щелочного металла, такого как гидроксид калия, в качестве основания, в растворителе, таком как спирт, такой как метанол или этанол, при температурах, равных от примерно 30°C до примерно 70°C, полученным продуктом является халькон формулы XI. При проведении реакции соединений формул IX и X в присутствии соли слабой кислоты, такой как ацетат аммония, например, в растворителе, таком как уксусная кислота, при температурах, равных от примерно 100°C до примерно 120°C, полученным продуктом является смесь халькона формулы XI и хроман-4-она формулы XII. Соединение формулы XI, а также смесь соединений формул XI и XII можно использовать в реакции циклизации и получить соединение формулы XII, что можно выполнить путем обработки исходного вещества кислотой, такой как хлористоводородная кислота, или амином, таким как этилдиизопропиламин, и фторидом калия в растворителе, таком как спирт, такой как метанол или этанол, при температурах, равных от примерно 60°C до примерно 100°C.
Затем оксогруппу в положении 4 цикла соединений формулы XII восстанавливают с получением группы CH2 и получают соединения формулы XIV, предпочтительно постадийно через производные 4-гидроксихромана формулы XIII.
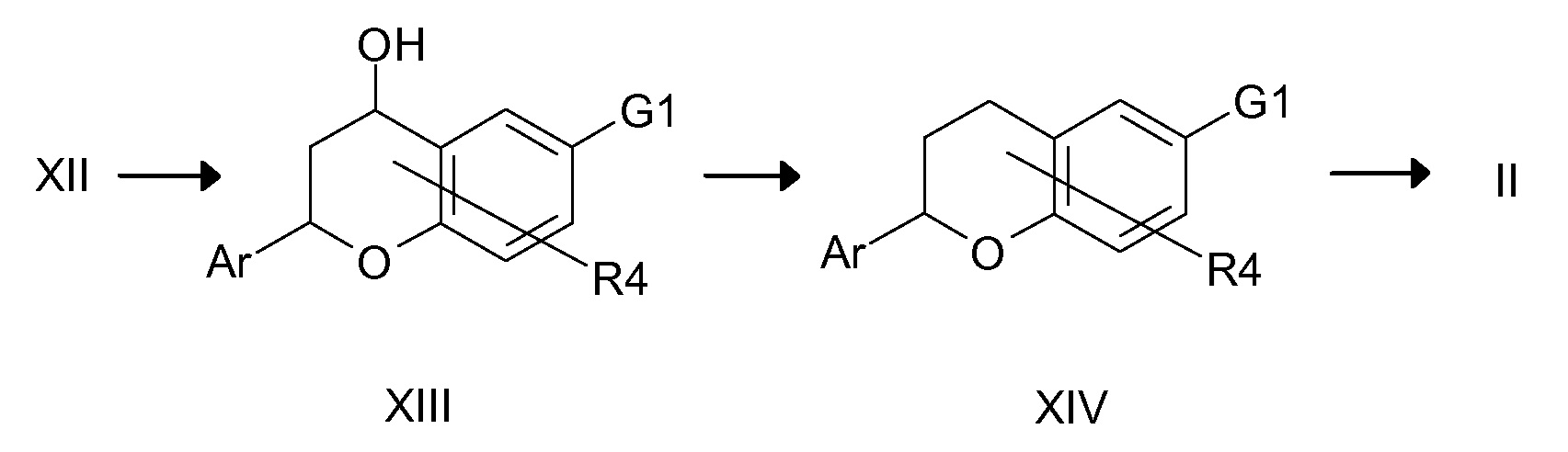
Группы Ar и R4 в соединениях формул XIII и XIV определены так, как в соединениях формулы I, и дополнительно функциональные группы могут содержаться в защищенной форме или в форме группы-предшественника, которую затем превращают в конечную группу. Группа G1 в соединениях формул XIII и XIV представляет собой гидроксигруппу или бром. Восстановление соединений формулы XII с образованием соединений формулы XIII можно провести при стандартных условиях восстановления кетона в спирт, например, с помощью комплексного гидрида в качестве восстановительного реагента или производного борана, такого как комплекс боран-тетрагидрофуран, в растворителе, таком как простой эфир, такой как ТГФ или диоксан, при температурах, равных от примерно 30°C до примерно 80°C. Восстановление соединений формулы XIII с образованием соединений формулы XIV можно провести, например, путем обработки силановым восстановительным реагентом, таким как триалкилсилан, такой как триэтилсилан, и кислотой, такой как трифторуксусная кислота, в растворителе, таком как хлорированный углеводород, такой как дихлорметан, при температурах, равных от примерно 0°C до примерно 40°C. В случае, если группа G1 в соединении формулы XIII и его соединениях-предшественниках представляет собой гидроксигруппу, полученное соединение формулы XIV уже является соединением формулы II. В случае, если группа G1 в полученном соединении формулы XIV представляет собой бром, ее можно превратить в гидроксигруппу металированием соединения формулы XIV литийорганическим соединением, таким как бутиллитий, и обработкой триалкилборатом, таким как триизопропилборат, в растворителе, таком как углеводород, такой как гептан или циклогексан, или простой эфир, такой как ТГФ или диоксан, при температурах, равных от примерно -80°C до примерно 0°C, с последующим окислительным расщеплением, например, с помощью пероксида водорода, в присутствии основания, такого как гидроксид натрия.
Другие методики получения хроман-6-олов формулы II включают циклизацию 3-гидроксипропилзамещенного производного бензола формулы XV, которое замещено в бензольном кольце двумя подходящими группами G2 и G3 и может дополнительно быть замещено в бензольном кольце и пропильной группе заместителями R4, и получить производное хромана формулы XVI, в которой группу G3 затем превращают в гидроксигруппу содержащуюся в соединениях формулы II.
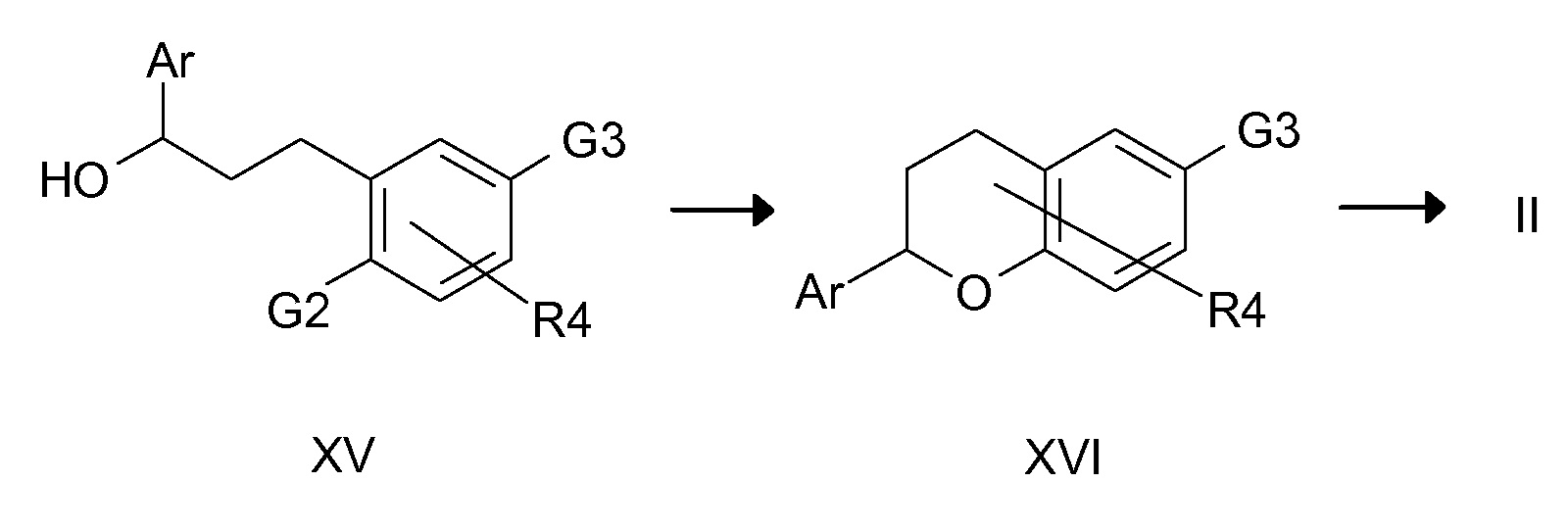
Группы Ar и R4 в соединениях формул XV и XVI определены так, как в соединениях формулы I, и дополнительно функциональные группы могут содержаться в защищенной форме или в форме группы-предшественника, которую затем превращают в конечную группу. Группа G2 в соединениях формулы XV может представлять собой гидроксигруппу или способные к нуклеофильному замещению отщепляющиеся группы, например, фтор. Группа G3 в соединениях формул XV и XVI может представлять собой бром или (C1-C4)-алкил-O-, такой как, например, метоксигруппа. В случае, если G3 означает бром, превращение группы G3 в соединении формулы XVI в гидроксигруппу в соединении формулы II можно провести, как описано выше для превращения соединений формулы XIV в соединения формулы II. В случае, если G3 означает (C1-C4)-алкил-O-, превращение в гидроксигруппу можно провести по стандартный методикам расщепления простой эфирной связи, например, путем обработки трибромидом бора в хлорированном углеводороде, таком как дихлорметан, при температурах, равных от примерно -20°C до примерно 10°C, в случае метоксигруппы. В случае, если группа G2 представляет собой гидроксигруппу, циклизацию соединения формулы XV с образованием соединения формулы XVI удобно можно провести при условиях проведения реакции Мицунобу путем обработки фосфином, таким как трифенилфосфин или трибутилфосфин, и производным азодикарбоновой кислоты, таким как диэтилазодикарбоксилат или диизопропилазодикарбоксилат, в растворителе, таком как простой эфир, такой как ТГФ или диоксан, при температурах, равных от примерно 0°С до примерно 30°C. В случае если бензольное кольцо, содержащее G2 в соединении формулы XV, способно к нуклеофильному ароматическому замещению и G2 означает отщепляющуюся группу, такую как фтор, циклизацию можно провести с помощью обработки соединения формулы XV основанием, что увеличивает нуклеофильность гидроксигруппы в положении 3 пропильной группы, например, амидом щелочного металла или гидридом щелочного металла, таким как гидрид натрия, в инертном растворителе, таком как простой эфир, такой как ТГФ или диоксан, или амид, такой как ДМФ или NMP, при температурах, равных от примерно -20°C до примерно 100°C.
С помощью циклизации соединений формулы XV также с удобством можно получить отдельные стереоизомерные формы соединений формулы XVI и II и конечные соединения формулы I, в которых хиральный атом углерода в положении 2 хроманового кольца находится в R-конфигурации или в S-конфигурации. Для синтеза таких отдельных стереоизомеров, которые другим образом можно получить, например, хроматографическим разделением смеси стереоизомеров конечных соединений формулы I на хиральной фазе или на любой стадии синтеза, используют отдельные стереоизомерные формы 3-гидроксипропилзамещенного бензола формулы XV, т.е. соединения формулы XVa. В зависимости реакции циклизации и выбранных условий циклизация может протекать с сохранением или обращением конфигурации хирального атома углерода и дает отдельные стереоизомерные формы соединений формулы XVI, т.е. соединения формулы XVIa, которые можно ввести в последующую реакцию и получить отдельные стереоизомерные формы соединений формул II и I. В соединениях формул XVa и XVIa содержатся группы Ar, R4, G2 и G3, определенные, как в соединениях формулы XV и XVI соответственно, и представленный хиральный атом углерода содержится или в основном содержится в R-конфигурации или в S-конфигурации, что указано волнистой формой клиновидной связи.
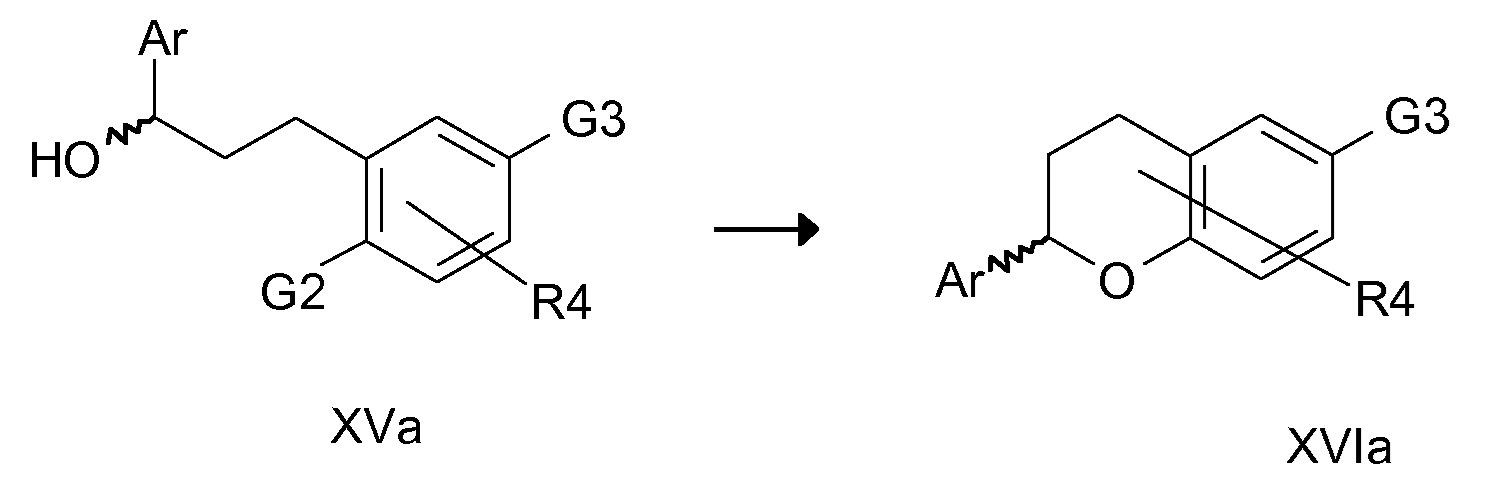
в одном варианте осуществления настоящее изобретение относится к способу получения соединения формулы I,
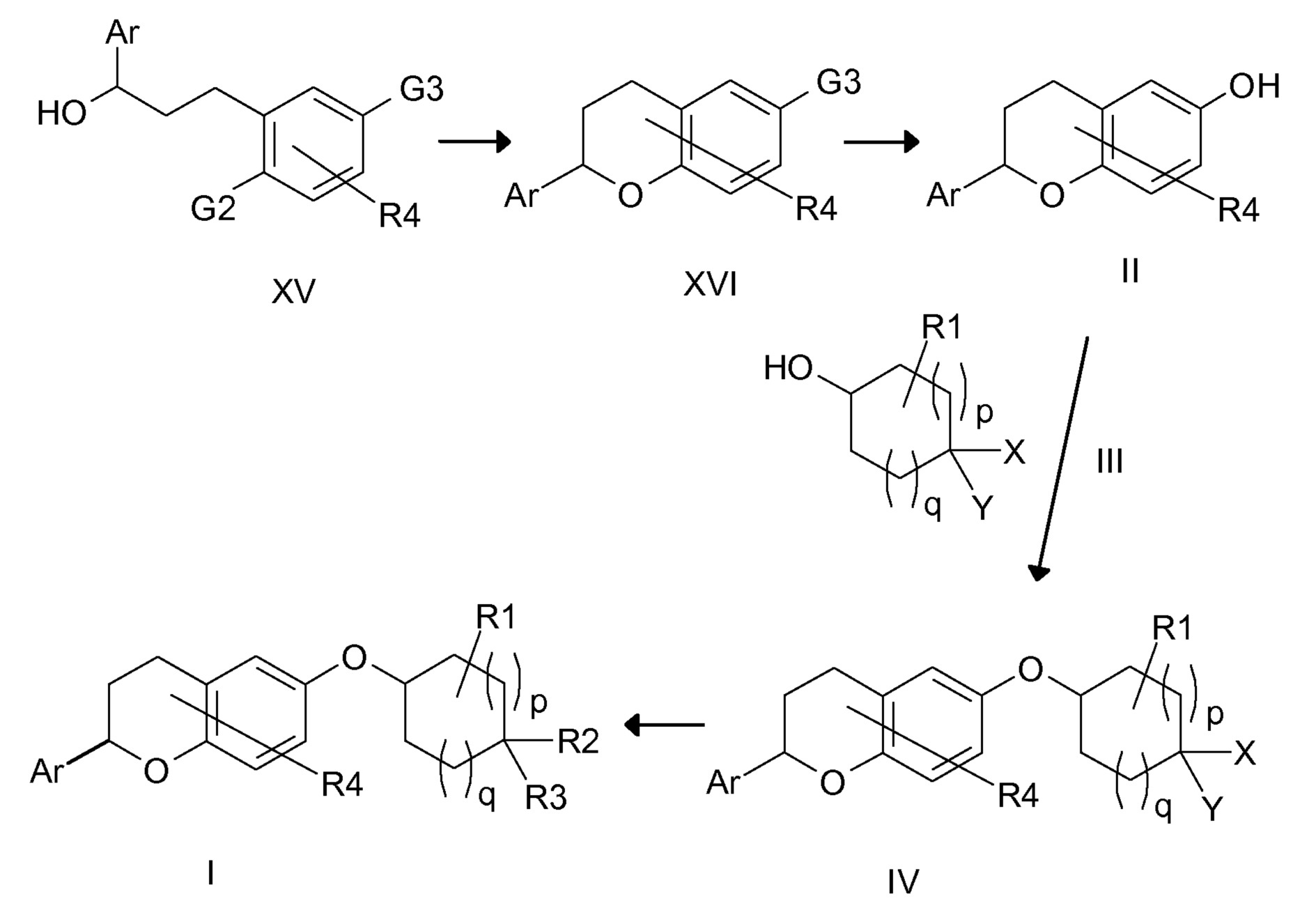
который включает циклизацию соединения формулы XV с образованием соединения формулы XVI, превращение соединения формулы XVI в соединение формулы II, введение в реакцию соединения формулы II с соединением формулы III с получением соединения формулы IV и превращение соединения формулы IV в соединение формулы I.
Другой вариант осуществления настоящего изобретения относится к описанному выше способу, в котором хиральный атом углерода, содержащий группу Ar в соединениях формул II, IV, XV и XVI, содержится или в основном содержится в одной конфигурации, в R-конфигурации или в S-конфигурации, т.е. к способу получения соединения формулы Ih,
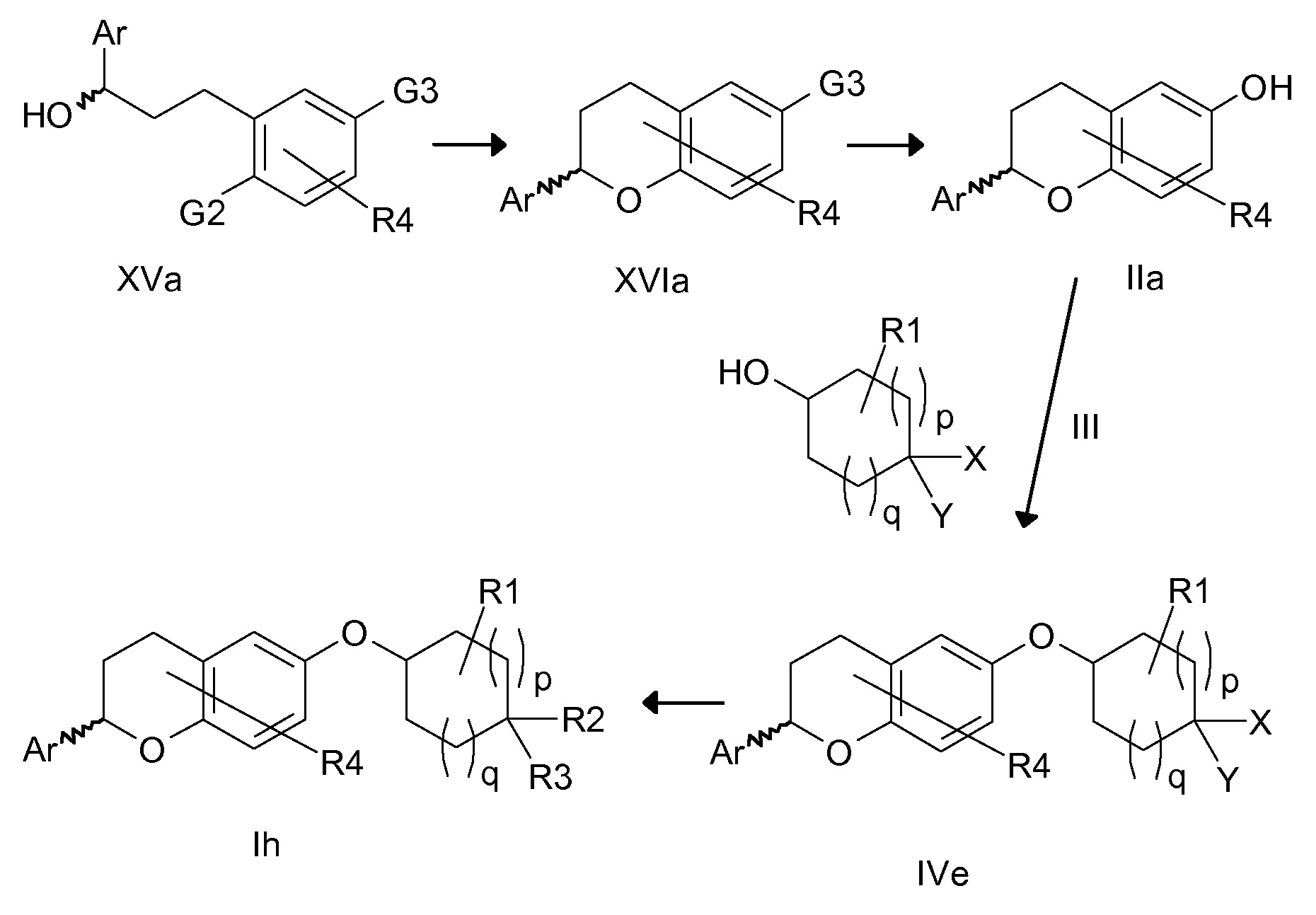
который включает циклизацию соединения формулы XVa с образованием соединения формулы XVIa, превращение соединения формулы XVIa в соединение формулы IIa, введение в реакцию соединения формулы IIa с соединением формулы III с получением соединения формулы IVe и превращение соединения формулы IVe в соединение формулы Ih. В соединениях формул IIa и IVe содержатся группы Ar, R1, R4, X и Y и числа p и q, определенные, как соединениях формулы II и IV соответственно.
Соединения формулы XV, включая стереоизомерные формы формулы XVa, которые используются в реакции циклизации с образованием соединений формул XVI и XVIa, описанных выше, можно получить по различным методикам, описанным в литературе, или по аналогичным методикам. Например, эфир 3-оксопропионовой кислоты формулы XVII можно алкилировать бензилгалогенидом формулы XVIII и получить 3-оксопропилзамещенное производное бензола формулы XIX, в которой затем кетонную группу восстанавливают в гидроксигруппу и получают соединение формулы XV.
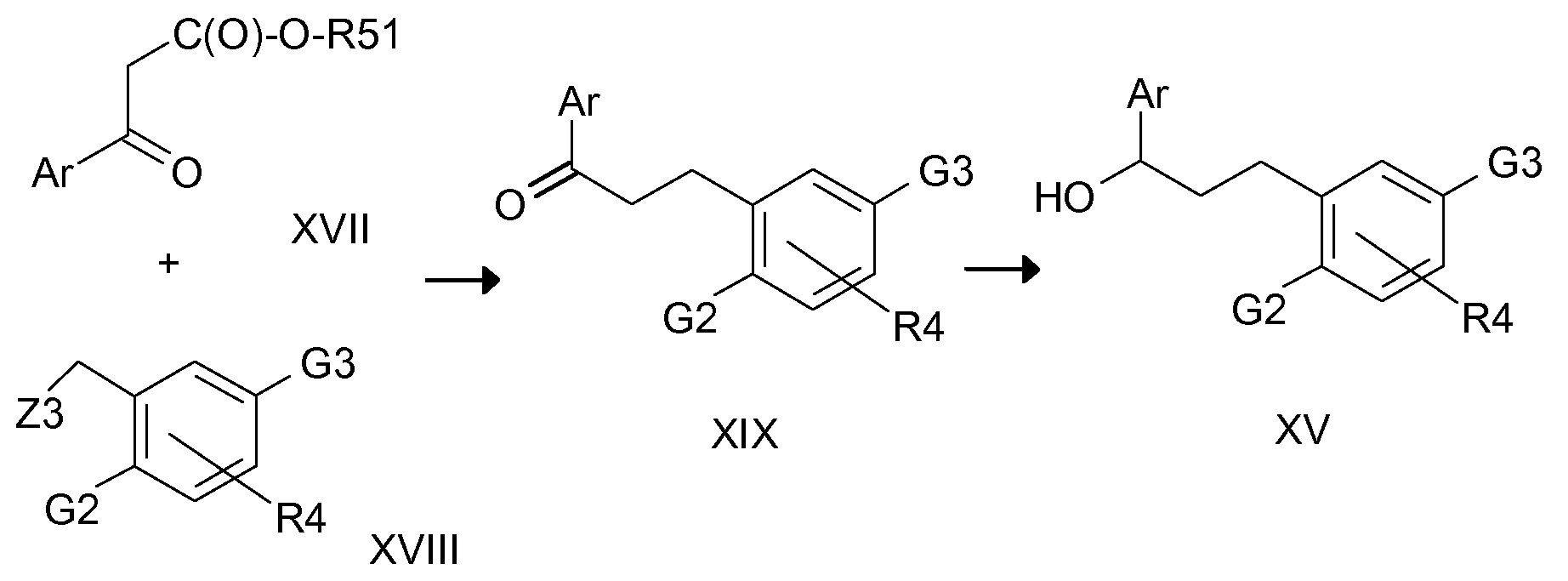
Группы Ar и R4 в соединениях формул XVII, XVIII и XIX определены так, как в соединениях формулы I, и дополнительно функциональные группы могут содержаться в защищенной форме или в форме группы-предшественника, которую затем превращают в конечную группу. При получении соединений формулы XV по этой методике группа G2 в соединениях формул XVIII и XIX предпочтительно представляет собой способную к нуклеофильному замещению отщепляющуюся группу, например, фтор, и группа G3 в соединениях формул XVIII и XIX предпочтительно представляет собой бром. Группа R51 в соединениях формулы XVII представляет собой (C1-C4)-алкил, например, метил или этил. Группа Z3 в соединениях формулы XVIII представляет собой способную к нуклеофильному замещению отщепляющуюся группу, например, хлор или бром. Реакцию соединений формул XVII и XVIII с получением соединений формулы XIX проводят в инертном растворителе, таком как простой эфир, такой как ТГФ, диоксан или ДМЭ, в присутствии основания, такого как алкоксид щелочного металла или гидрид щелочного металла, например, гидрид натрия, при температурах, равных от примерно 0°C до примерно 50°C. С помощью обработки полученного бензилированного эфира 3-оксопропионовой кислоты кислотой, например, хлористоводородной кислотой, в водном растворителе, таком как простой эфир, такой как диоксан, или кислота, такая как уксусная кислота или смесь растворителей, при температурах, равных от примерно 60°C до примерно 120°C сложноэфирный фрагмент затем омыляют и декарбоксилируют и получают кетон формулы XIX. Для восстановления кетонного фрагмента в соединениях формулы XIX с образованием соединений формулы XV можно использовать различные восстановительные реагенты, например, комплексный гидрид металла, такой как боргидрид натрия или боргидрид лития, в растворителе, таком как простой эфир или спирт. По реакции асимметрического восстановления с использованием хирального восстановительного реагента, например, энантиомерной формы хирального комплексного гидрида металла или хирального борана, такого как органоборан на основе альфа-пинена, такой как B-хлордиизопинокамфеилборан, который обычно сокращенно обозначают, как (-)-Ipc2BCl или (-)-DipCl, и (+)-Ipc2BCl или (+)-DipCl соответственно, в инертном растворителе, таком как простой эфир, такой как ТГФ или диоксан при температурах, равных от примерно -40°C до примерно 30°C, с удобством можно получить отдельные стереоизомерные формы соединений формулы XV, т.е. соединения формулы XVa, которые можно циклизовать с образованием энантиомерных форм соединений формулы XVI, т.е. соединений формулы XVIa, как описано выше.
В другом способе получения соединений формулы XV индан-1-он формулы XX вводят в реакцию расширения цикла с получением хроман-2-она формулы XXI, в которой лактонный фрагмент можно восстановить в альдегидный фрагмент, который находится в форме циклического гемиацеталя формулы XXII и который можно ввести в реакцию с подходящим металлоорганическим соединением формулы XXIII.

Группы Ar и R4 в соединениях формул XX, XXI, XXII и XXIII определены так, как в соединениях формулы I, и дополнительно функциональные группы могут содержаться в защищенной форме или в форме группы-предшественника, которую затем превращают в конечную группу. При получении соединений формулы XV по этой методике группа G3 в соединениях формул XX, XXI и XXII предпочтительно представляет собой (C1-C4)-алкил-O- группу. Группа M в соединениях формулы XXIII представляет собой металл или эквивалент металла, например, литий. Превращение соединения формулы XX в соединение формулы XXI можно провести путем обработки надкислотой, такой как 3-хлорпербензойная кислота, в растворителе, таком как хлорированный углеводород, такой как дихлорметан, при температурах, равных от примерно -10°C до примерно 30°C. Для восстановления лактонного фрагмента в соединении формулы XXI с образованием замаскированного альдегидного фрагмента в соединении формулы XXII, можно использовать комплексный содержащий металл восстановительный реагент, такой как диизобутилалюминийгидрид, в растворителе, таком как углеводород, такой как циклогексан или толуол, или хлорированный углеводород, такой как дихлорметан, или простой эфир, такой как ТГФ или диоксан, или смесь растворителей, при температурах, равных от примерно -80°C до примерно 30°C. Для последующей стадии соединение формулы XXIII обычно получают in situ из соответствующего подходящего бензола или галогензамещенного бензола металированием, например, литийорганическим соединением, таким как бутиллитий или амид лития, такой как диизопропиламид лития или 2,2,6,6- тетраметилпиперидид лития, и вводят в реакцию с соединением формулы XXII в инертном растворителе, таком как углеводород, такой как гептан или циклогексан, или простой эфир, такой как ТГФ, или смесь растворителей при температурах, равных от примерно -80°C до примерно 30°C.
Как уже отмечено, во всех реакциях, которые проводят во время получения соединений формулы I, может быть предпочтительно или необходимо временно защищать функциональные группы или они должны изначально содержаться в виде групп-предшественников и позднее из них удалить защитную группу или превратить ее в необходимые группы. Соответствующие стратегии синтеза и защитные группы и группы-предшественники, которые являются подходящими для соответствующего случая, известны специалисту в данной области техники и описаны, например, в публикации P. G. M. Wuts and T. W. Greene, Greene's Protective Groups in Organic Synthesis, 4. ed. (2007), John Wiley & Sons. Примерами защитных групп, которые можно отметить, являются бензильные защитные группы, например, бензиловые эфиры гидроксисоединений и бензиловые эфиры карбоновых кислот, из которых бензильную группу можно удалить с помощью каталитического гидрирования в присутствии палладиевого катализатора, трет-бутильные защитные группы, например, трет-бутиловые эфиры карбоновых кислот, из которых трет-бутильную группу можно удалить путем обработки трифторуксусной кислотой, ацильные защитные группы, например, сложные эфиры и амиды гидроксисоединений и аминов, которые можно повторно расщепить с помощью кислотного или щелочного гидролиза, или алкоксикарбонильные защитные группы, например, трет-бутоксикарбонильные производные аминов, которые можно повторно расщепить путем обработки трифторуксусной кислотой. Примерами предшественников, которые можно отметить, являются атомы галогенов, которые можно заменить многими другими группами, или нитрогруппы, которые можно превратить, например, с помощью каталитического гидрирования, в аминогруппы, которые можно диазотировать и превратить в большое количество групп.
Соответствующие подробные описания условий, использующихся в конкретном способе получения, включая растворитель, основание или кислоту, температуру, порядок добавления, молярные соотношения и другие параметры которые являются обычными и используются во всех реакциях при синтезе соединения формулы l, специалист в данной области техники выбирает стандартным образом с учетом характеристик исходных соединений и искомых соединений и других особенностей конкретного случая. Как также известно специалисту в данной области техники, не все способы, описанные в настоящем изобретении, в одинаковой степени могут быть применимы для получения всех соединений формулы I и их промежуточных продуктов и необходимо вносить изменения. Во всех способах получения соединений формулы I обработку реакционной смеси и очистку продукта проводят по стандартным методикам, известным специалисту в данной области техники, которые включают, например, остановку реакции водой, регулирование некоторых значений pH, осаждение, экстракцию, сушку, концентрирование, кристаллизацию, перегонку и хроматографию. Для характеризации продуктов также используют обычные методики, такие как ЯМР, ИК и масс-спектроскопия.
Другим объектом настоящего изобретения являются новые исходные соединения и промежуточные продукты, образующиеся при синтезе соединений формулы I, включая соединения формул II, IIa, III, IIIa, IV, IVa, IVb, IVc, IVd, IVe, V, VI, VII, VIII, IX, X, XI, XII, XIII, XIV, XV, XVa, XVI, XVIa, XVII, XVIII, XIX, XX, XXI, XXII и XXIII, в которых группы Ar, R1-R7, R50, R51, G1, G2, G3, M, X, Y и Z1-Z3 и числа p и q являются такими, как определено выше, в любой из их стереоизомерных форм или смесь стереоизомерных форм в любом соотношении и их соли, и их применение в качестве промежуточных продуктов для синтеза или исходных соединений. Все общие пояснения, описания вариантов осуществления и определения чисел и групп, приведенные выше применительно к соединениям формулы I, соответственно применимы к указанным промежуточным продуктам и исходным соединениям. Объектом настоящего изобретения являются, в частности, новые особые исходные соединения и промежуточные продукты, описанные в настоящем изобретении. Независимо от того, описаны ли они, как свободные соединения и/или как конкретная соль, они являются объектом настоящего изобретения и в форме свободных соединений, и в форме их солей, и, если описана конкретная соль, дополнительно в форме этой конкретной соли.
Соединения формулы I ингибируют натрий-кальциевый обмен (NCX), в особенности натрий-кальциевый обмен подтипа 1 (NCX1), как можно показать с помощью фармакологических исследований, описанных ниже, и других фармакологических исследований, которые известны специалисту в данной области техники, например, с помощью моделей на животных, посредством которых можно исследовать влияние на функцию сердца ex vivo или in vivo. Поэтому соединения формулы I и их фармацевтически приемлемые соли являются ценными фармацевтически активными соединениями. Соединения формулы I и их фармацевтически приемлемые соли можно использовать для лечения сердечной недостаточности, включая острую и хроническую застойную сердечную недостаточность (CHF), систолическую сердечную недостаточность, диастолическую сердечную недостаточность, сердечную недостаточность с сохранившейся фракцией выброса, диабетическую сердечную недостаточность и декомпенсированную сердечную недостаточность и терапию сердечной недостаточности в комбинации с использованием устройства, аритмий сердца, включая предсердные аритмии, фибрилляции предсердий, фибрилляции предсердий у пациентов, страдающих CHF, вентрикулярных аритмий, желудочковой тахикардии, мономорфной желудочковой тахикардии, полиморфной желудочковой тахикардии, Тахикардии с трепетанием - мерцанием предсердий и вентрикулярных аритмий у пациентов, страдающих CHF, удара, слабоумия, включая болезнь Альцгеймера, гипертензии, ишемии сердца, почечной недостаточности, шока, включая гемодинамический шок, кардиогенный шок и септический шок, возрастных нарушений и заболеваний, которые, например, проявляются, как вторичные после связанного с NCX поражения. Лечение заболеваний следует понимать, как включающее и терапию имеющихся патологических изменений или нарушений функций организма, или имеющихся симптомов с целью ослабления, смягчения или излечивания, и профилактику или предупреждение патологических изменений или нарушений функций организма, или симптомов у людей или животных, которые восприимчивы к ним и нуждаются в такой профилактике или предупреждении, с целью предупреждения или подавления их возникновения или ослабления в случае их возникновения. Например, у пациентов, которые вследствие своего анамнеза подвержены аритмии сердца или декомпенсации сердца, с помощью профилактического или предупредительного лекарственного лечения можно предупредить возникновение или повторное возникновение аритмий или декомпенсации или уменьшить их тяжесть и осложнения. Лечение заболеваний можно проводить и в острых случаях, и в хронических случаях. Соединения формулы I и их фармацевтически приемлемые соли также можно использовать при различных нарушениях для обеспечения улучшения кровотока в сердце, головном мозге и почках, и в целом при нарушениях, при которых нарушен внутриклеточный кальциевый гомеостаз, или NCX активируется нежелательным образом, или врач предполагает, что ингибирование NCX необходимо для улучшения состояния пациента, где соединения формулы I и их фармацевтически приемлемые соли также можно использовать в случаях, когда предполагается только некоторое частичное ингибирование NCX, например, при использовании низкой дозы.
Поэтому соединения формулы I и их фармацевтически приемлемые соли можно применять для животных, предпочтительно млекопитающих и в особенности людей, в качестве лекарственного средства или лекарственного препарата по отдельности, в смесях друг с другом или в форме фармацевтических композиций. Объектом настоящего изобретения также являются соединения формулы I и их фармацевтически приемлемые соли, предназначенные для применения в качестве лекарственного средства. Объектом настоящего изобретения также являются фармацевтические композиции и лекарственные средства, которые содержат по меньшей мере одно соединение формулы I и/или его фармацевтически приемлемую соль в качестве активного ингредиента в дозе, эффективной для предназначенного применения, и фармацевтически приемлемый носитель, т.е. один или несколько фармацевтически нетоксичных или неопасных разбавителей и/или инертных наполнителей и необязательно одно или несколько других фармацевтически активных соединений. Объектом настоящего изобретения также являются соединения формулы I и их фармацевтически приемлемые соли, предназначенные для применения в качестве противоаритмического средства. Объектом настоящего изобретения также являются соединения формулы I и их фармацевтически приемлемые соли, предназначенные для применения для лечения заболеваний, указанных выше или ниже, включая лечение любого из указанных заболеваний, например, сердечной недостаточности, аритмии сердца, удара, слабоумия, гипертензии, ишемии сердца, почечной недостаточности, шока, возрастных нарушений или заболеваний, которые проявляются, как вторичные после связанных с NCX поражений, где лечение заболеваний включает их терапию и профилактику, как отмечено выше, или предназначенные для применения в качестве ингибитора NCX. Объектом настоящего изобретения также является применение соединений формулы I и их фармацевтически приемлемых солей для приготовления лекарственного средства для лечения заболеваний, указанных выше или ниже, включая лечение любого из указанных заболеваний, например, сердечной недостаточности, аритмии сердца, удара, слабоумия, гипертензии, ишемии сердца, почечной недостаточности, шока, возрастных нарушений или заболеваний, которые проявляются, как вторичные после связанных с NCX поражений, где лечение заболеваний включает их терапию и профилактику, как отмечено выше, лекарственное соединение для ингибирования NCX. Объектом настоящего изобретения также являются способы лечения заболеваний, указанных выше или ниже, включая лечение любого из указанных заболеваний, например, сердечной недостаточности, аритмии сердца, удара, слабоумия, гипертензии, ишемии сердца, почечной недостаточности, шока, возрастных нарушений или заболеваний, которые проявляются, как вторичные после связанного с NCX поражения, где лечение заболеваний включает их терапию и профилактику, как отмечено выше, и способ ингибирования NCX, который включает введение эффективного количества по меньшей мере одного соединения формулы I и/или его фармацевтически приемлемой соли человеку или животному, которое в нем нуждается. Соединения формулы I и их фармацевтически приемлемые соли, и содержащие их фармацевтические композиции и лекарственные средства можно вводить энтерально, например, путем перорального или ректального введения, парентерально, например, путем внутривенной, внутримышечной или подкожной инъекции или вливания, или с помощью другого пути введения, такого как местное, подкожное, чрескожное, назальное, фарингеальное или ингаляционное введение, предпочтительный путь введения зависит от условий в конкретном случае. Соединения формулы I и их фармацевтически приемлемые соли также можно использовать в комбинации с другими фармацевтически активными соединениями.
Фармацевтические композиции и лекарственные средства, предлагаемые в настоящем изобретении, обычно содержат от примерно 0,5 до примерно 90 масс.% соединения или соединений формулы I или их фармацевтически приемлемых солей и количество активного ингредиента формулы I и/или его фармацевтически приемлемой соли, которое в разовой дозе обычно составляет от примерно 0,1 мг до примерно 1 г, предпочтительно от примерно 0,2 мг до примерно 500 мг, например, от примерно 1 мг до примерно 300 мг. В зависимости от типа фармацевтической композиции и других условий в конкретном случае количество может отклоняться от указанных значений. Получение фармацевтические композиции и лекарственных средств можно провести по известным методикам и это известно специалисту в данной области техники. Для этого соединения формулы I и/или их фармацевтически приемлемые соли смешивают с одним или несколькими твердыми или жидкими разбавителями и/или инертных наполнителей, при желании также в комбинации с одним или несколькими другими фармацевтически активными соединениями и готовят в форме, подходящей для дозирования и введения, которую затем можно использовать в медицине или ветеринарии.
В качестве носителей, которые также можно рассматривать, как разбавители или растворители, или агенты, увеличивающие объем, и инертных наполнителей можно использовать подходящие органические и неорганические вещества, которые не взаимодействуют нежелательным образом с соединениями формулы I. В качестве примеров типов инертных наполнителей, или добавок, которые могут содержаться в фармацевтических композициях и лекарственных средствах, можно отметить смазывающие вещества, консерванты, гелеобразователи, загустители, стабилизаторы, разрыхлители, смачивающие агенты, эмульгаторы, диспергирующие средства, противовспенивающие агенты, соли, буферные вещества, красители, вкусовые добавки и антиоксиданты. Примерами носителей и инертных наполнителей являются вода, физиологический раствор, растительные масла, такие как подсолнечное масло, животные масла, такие как рыбий жир, воска, спирты, такие как этанол, изопропанол, 1,2-пропандиол, глицерин, полиолы, полиэтиленгликоли, поливинилпирролидон, желатин, гуммиарабик, целлюлоза, углеводы, такие как глюкоза, лактоза, или крахмал, такой как кукурузный крахмал, карбонат магния, фосфат калия, хлорид натрия, стеариновая кислота и ее соли, такие как стеарат магния, тальк, ланолин, вазелиновое масло или их смеси, например, смеси воды или физиологического раствора с одним или несколькими органическими растворителями, такими как смеси воды со спиртами.
Для перорального или ректального применения можно использовать фармацевтические формы, такие как, например, таблетки, таблетки с покрытием, таблетки с покрытием из сахара, гранулы, капсулы из твердого и мягкого желатина, суппозитории, растворы, включая масляные, спиртовые или водные растворы или капли, кроме того суспензии или эмульсии. Для парентерального применения, например, путем инъекции или вливания, можно использовать фармацевтические формы, такие как растворы, например, водные растворы, можно использовать. Для местного применения можно использовать фармацевтические формы, такие как мази, кремы, пасты, лосьоны, гели, спреи, пенки, аэрозоли, растворы или порошки. Фармацевтические составы, такие как, например, аэрозоли и спреи, могут включать растворы, суспензии или эмульсии активного ингредиента в фармацевтически приемлемом растворителе, таком как этанол или вода, или смеси таких растворителей. Составы также могут включать другие фармацевтически инертные наполнители, такие как поверхностно-активные вещества, эмульгаторы и стабилизаторы, и газообразный пропеллент. Такая фармацевтическая форма обычно содержит активный ингредиент в концентрации, равной от примерно 0,1 до примерно 10%, предпочтительно от примерно 0,3 до примерно 3 масс.%.
Обычно доза соединений формулы I и частота введения зависит от условий в конкретном случае и врач выбирает ее в соответствии с обычными правилами и процедурами. Она зависит, например, от вводимого соединения формулы I и его активности и продолжительности действия, от характера и тяжести конкретного синдрома, от пола, возраста, массы и индивидуальной восприимчивости подвергающегося лечению человека или животного, от того, является ли лечение кратковременным или длительным, или профилактическим, и от того, вводят ли другие фармацевтически активные соединения в дополнение к соединению формулы I. Обычно в случае введения взрослому, обладающего массой, равной примерно 75 кг, достаточной является доза, равная от примерно 0,1 мг до примерно 100 мг/кг/сутки, предпочтительно от примерно 1 мг до примерно 10 мг/кг/сутки (в каждом случае в миллиграммах в пересчете на килограмм массы тела). Суточную дозу можно вводить в виде разовой дозы или разделить на несколько отдельных доз, например, 2, 3 или 4 отдельные дозы. Введение также можно проводить непрерывно, например, с помощью непрерывной инъекции или вливания. В зависимости от поведения индивидуума в конкретном случае может потребоваться отклонение от указанных доз в большую или меньшую сторону.
Кроме использования в качестве фармацевтически активного соединения в медицине и ветеринарии соединения формулы I также можно использовать в качестве средств в биохимических исследованиях или в качестве средств для научных исследований и для диагностики, например, биологических образцов для диагностики in vitro, если предполагается ингибирование NCX. Соединения формулы I и их соли также можно использовать в качестве промежуточных продуктов для получения других фармацевтически активных веществ.
Приведенные ниже примеры иллюстрируют настоящее изобретение.
Когда соединения примеров, содержащие основную группу, очищали с помощью препаративной высокоэффективной жидкостной хроматографии (ВЭЖХ) на материале колонки с обращенной фазой (ОФ) и, как обычно, элюент использовали в градиентном режиме в виде смеси воды и ацетонитрила, содержащей трифторуксусную кислоту, в зависимости от особенностей обработки, таких как условия выпаривания или лиофилизации, их частично получали в виде их солей присоединения с трифторуксусной кислотой. В названиях соединений примеров и структурных формулах такая содержащаяся трифторуксусная кислота не указана.
Полученные соединения обычно характеризовали с помощью спектроскопических данных и хроматографических данных, в частности, с помощью масс-спектров (МС) и времен удерживания (Rt; в мин) ВЭЖХ, которые получали с помощью объединенного исследования посредством аналитической ВЭЖХ/МС (ЖХ/МС) (ЖХ - жидкостная хроматография) и/или спектров ядерного магнитного резонанса (ЯМР).1H-ЯМР спектры регистрировали при 500 МГц в D6-ДМСО в качестве растворителя при 298 K, если не указано иное. При исследовании с помощью ЯМР для пиков приведены представленные на распечатках химический сдвиг δ (в м.д.), количество атомов водорода (H) и мультиплетность (s: синглет, d: дублет, dd: двойной дублет, t: триплет, m: мультиплет; br: широкий). При исследовании с помощью МС приведены массовое число (m/z) пика молекулярного ион [M], например, [M+], или родственного иона, такого как ион [M+1], например, [(M+1)+], т.е. протонированного молекулярного иона [(M+H)+] ([MH+]) или иона [M-1], например, [(M-1)‾], т.е. депротонированного молекулярного иона [(M-H)‾], который образовался в соответствии с использованной методикой ионизации. Обычно методикой ионизации являлась ионизация электрораспылением (ESI+). Длина волны УФ-излучения при детектировании в ВЭЖХ обычно равнялась 220 нм. Для методики ЖХ/МС использовали следующие аббревиатуры. "АЦН" означает ацетонитрил, "ТФУК" означает трифторуксусную кислоту, и "МК" означает муравьиную кислоту.
Методика A
Колонка: Waters UPLC BEH C18, 1,7 мкм, 2,1×50 мм; температура: 55°C; скорость потока: 0,9 мл/мин; элюент A: вода + 0,1% МК; элюент B: АЦН + 0,08% МК; градиентный режим: от 95% A + 5% B (0 мин) до 5% A + 95% B (1,1 мин) до 5% A + 95% B (1,7 мин) до 95% A + 5% B (1,8 мин) до 95% A + 5% B (2,0 мин)
Методика B
Колонка: Waters XBridge C18, 2,5 мкм, 4,6×50 мм; температура: 30°C; скорость потока: 1,3 мл/мин; элюент A: вода + 0,1% МК; элюент B: АЦН + 0,1% МК; градиентный режим: от 97% A + 3% B (0 мин) до 40% A + 60% B (3,5 мин) до 2% A + 98% B (4,0 мин) до 2% A + 98% B (5,0 мин) до 97% A + 3% B (6,5 мин)
Методика C
Колонка: Waters Atlantis T3 C18, 3 мкм, 3×100 мм; температура: 55°C; скорость потока: 1,0 мл/мин; элюент A: вода + 0,05% ТФУК; элюент B: АЦН + 0,05% ТФУК; градиентный режим: от 95% A + 5% B (0 мин) до 5% A + 95% B (5,0 мин) до 95% A + 5% B (7,0 мин)
Методика D
Колонка: Waters Atlantis T3 C18, 3 мкм, 3×50 мм; температура: 55°C; скорость потока: 0,6 мл/мин; элюент A: вода + 0,05% ТФУК; элюент B: АЦН + 0,05% ТФУК; градиентный режим: от 95% A + 5% B (0 мин) до 5% A + 95% B (4,0 мин) до 2% A + 98% B (6,5 мин) до 95% A + 5% B (9,0 мин)
Методика E
Колонка: Waters UPLC BEH C18, 1,7 мкм, 2,1×50 мм; температура: 55°C; скорость потока: 0,9 мл/мин; элюент A: вода + 0,05% МК; элюент B: АЦН + 0,035% МК; градиентный режим: от 95% A + 5% B (0 мин) до 5% A + 95% B (1,1 мин) до 5% A + 95% B (1,7 мин) до 95% A + 5% B (1,8 мин) до 95% A + 5% B (2,0 мин)
Методика F
Колонка: Waters UPLC BEH C18, 1,7 мкм, 2,1×50 мм; температура: 55°C; скорость потока: 0,9 мл/мин; элюент A: вода + 0,05% МК; элюент B: АЦН + 0,035% МК; градиентный режим: от 95% A + 5% B (0 мин) до 5% A + 95% B (1,1 мин) до 5% A + 95% B (1,7 мин) до 95% A + 5% B (1,9 мин) до 95% A + 5% B (2,0 мин)
Примеры типичных синтезов
Пример A
(E)-1-(5-Бром-2-гидроксифенил)-3-о-толилпропенон и 6-бром-2-о-толилхроман-4-он
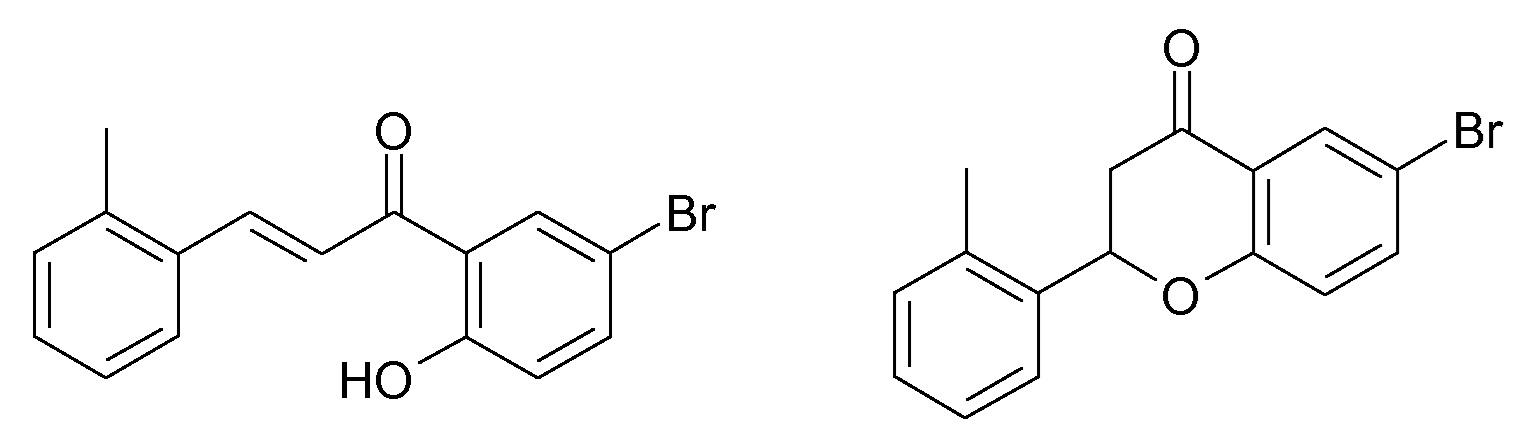
К раствору о-толуилового альдегида (4,1 г, 33,7 ммоль, 1,1 экв.) и 5-бром-2-гидроксиацетофенона (6,9 г, 32,1 ммоль) в этаноле (100 мл) при комнатной температуре добавляли порошкообразный гидроксид калия (5,2 г, 93 ммоль, 5 экв.) и суспензию перемешивали при 50°C в течение 3 ч и образовывался красный раствор. Раствору давали охладиться до комнатной температуры и выливали на лед. Значение pH водной смеси устанавливали равным < 7 водным раствором хлористоводородной кислоты. Полученную желтую суспензию перемешивали, пока не образуется желтое твердое вещество, и осадок отфильтровывали, промывали водой и сушили. Желтый (E)-1-(5-бром-2-гидроксифенил)-3-о-толилпропенон (9,6 г, 94%) использовали в реакции циклизации без дополнительной очистки.
К раствору (E)-1-(5-бром-2-гидроксифенил)-3-о-толилпропенона (9,6 г, 30,3 ммоль) в этаноле (130 мл) добавляли концентрированный водный раствор хлористоводородной кислоты (1,5 мл). Раствор кипятили с обратным холодильником в течение 5 ч. Затем раствор охлаждали до комнатной температуры и растворители удаляли при пониженном давлении. Полученный красный 6-бром-2-о-толилхроман-4-он (9,5 г, 100%) использовали на следующей стадии без дополнительной очистки.
По описанной методике также синтезировали следующие хроманоны:
6-Бром-2-(5-фтор-2-метилфенил)-хроман-4-он
6-Бром-2-(2,6-диметилфенил)-хроман-4-он
2-(3-Фтор-2-метоксифенил)-6-гидроксихроман-4-он
6-Гидрокси-7-метил-2-о-толилхроман-4-он
2-(2-Фтор-3-метоксифенил)-6-гидроксихроман-4-он
6-Гидрокси-3-метил-2-фенилхроман-4-он
2-(2-Фторфенил)-6-гидроксихроман-4-он
2-(3-Фтор-2-метилфенил)-6-гидроксихроман-4-он
Пример B
6-Бром-2-о-толилхроман-4-ол и 6-бром-2-о-толилхроман
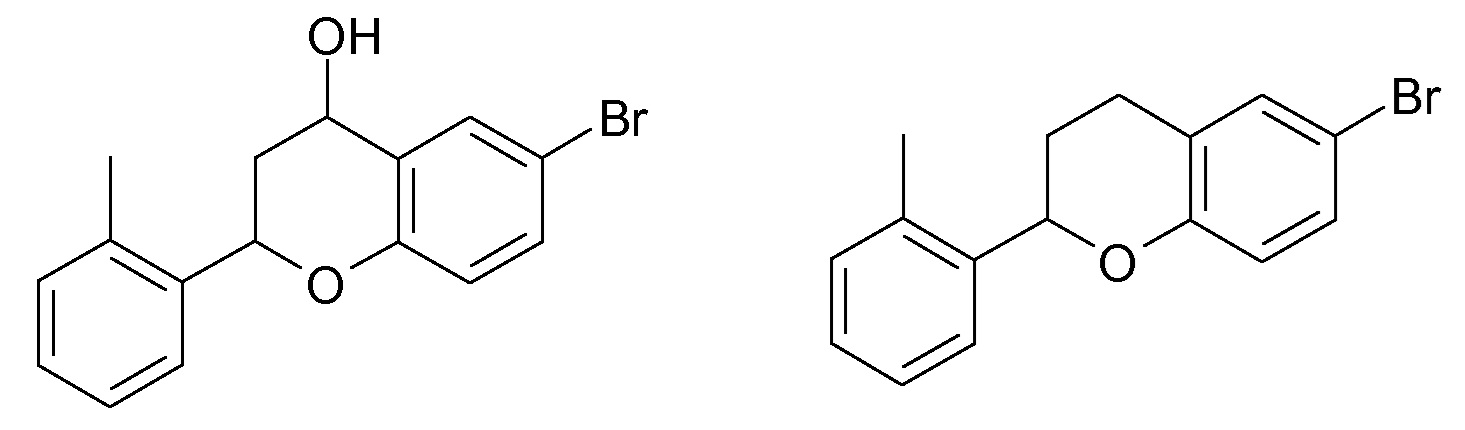
К раствору 6-бром-2-о-толилхроман-4-она (11,0 г, 34,7 ммоль) в тетрагидрофуране (100 мл) при комнатной температуре по каплям добавляли раствор аддукта борана с тетрагидрофураном (1M в тетрагидрофуране, 86,7 мл, 2,5 экв.). Раствор кипятили с обратным холодильником в течение 1 ч, охлаждали до комнатной температуры и его осторожно добавляли к смеси воды со льдом и 1 н водного раствора хлористоводородной кислоты. Водный слой экстрагировали дихлорметаном и объединенные органические слои промывали водой, сушили над сульфатом натрия и фильтровали и растворитель удаляли при пониженном давлении. 6-Бром-2-о-толилхроман-4-ол получали в виде желтого масла (11,1 г, 100%) и использовали для восстановления в хроман без дополнительной очистки.
К раствору 6-бром-2-о-толилхроман-4-ола (11,9 г, 37,3 ммоль) в дихлорметане (130 мл) при 0°C добавляли триэтилсилан (29,6 г, 255 ммоль, 6,8 экв.) и трифторуксусную кислоту (75 мл, 27 экв.). Раствор перемешивали при комнатной температуре в течение 2,5 ч. Растворитель удаляли при пониженном давлении и остаток подвергали распределению между водой и этилацетатом. Водный слой экстрагировали этилацетатом и объединенные органические слои промывали водой и насыщенным водным раствором гидрокарбоната натрия, сушили над сульфатом натрия и фильтровали, и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали с помощью колоночной хроматографии (силикагель; градиентный режим этилацетат/гептан). 6-Бром-2-о-толилхроман получали в виде бледно-желтого масла (7,10 г, 63%).
По описанной методике также синтезировали следующие производные хромана:
7-Метил-2-о-толилхроман-6-ол
6-Бром-2-(2,6-диметилфенил)-хроман
2-(2-Фтор-3-метоксифенил)-хроман-6-ол
6-Бром-2-(5-фтор-2-метилфенил)-хроман
2-(3-Фтор-2-метоксифенил)-хроман-6-ол
2-(2-Фторфенил)-хроман-6-ол
2-(3-Фтор-2-метилфенил)-хроман-6-ол
3-Метил-2-фенилхроман-6-ол
Пример C
(S)-6-Бром-2-о-толилхроман
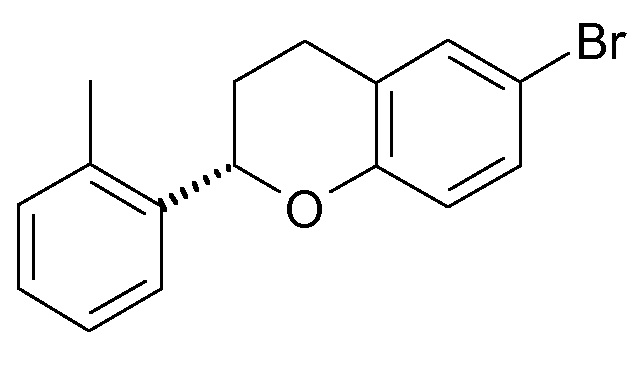
a) 3-(5-Бром-2-фторфенил)-1-о-толилпропан-1-он
Гидрид натрия (60% в масле, 2,1 г, 52 ммоль) и метил 3-оксо-3-о-толилпропаноат (10 г, 52 ммоль) суспендировали в тетрагидрофуране и 4-бром-2-(бромметил)-1-фторбензол (15,3 г, 57 ммоль) добавляли. После завершения превращения реакцию останавливали льдом и насыщенным раствором хлорида аммония и экстрагировали с помощью н-гептан. Объединенные органические слои один раз промывали насыщенным раствором хлорида аммония, водой и солевым раствором. Органический слой сушили над сульфатом магния и выпаривали досуха. Полученное желтое масло растворяли в 25 мл уксусной кислоты, 25 мл концентрированной хлористоводородной кислоты и 20 мл 1,4-диоксана и кипятили с обратным холодильником в течение 4 ч, пока ЖХ/МС не указывала на израсходование исходного вещества. Добавляли 50 мл воды и 100 мл трет-бутилметилового эфира и продукт экстрагировали. Объединенные органические слои один раз промывали насыщенным раствором хлорида аммония, водой и солевым раствором. Органический слой сушили над сульфатом магния и выпаривали досуха. Остаток очищали с помощью колоночной хроматографии (силикагель, градиентный режим гептан/этилацетат) и получали 11,2 г 3-(5-бром-2-фторфенил)-1-о-толилпропан-1-она в виде бесцветного масла.
b) (S)-3-(5-Бром-2-фторфенил)-1-о-толилпропан-1-ол
3-(5-Бром-2-фторфенил)-1-о-толилпропан-1-он (14 г, 43,6 ммоль) разбавляли с помощью 20 мл сухого тетрагидрофурана и по каплям добавляли к раствору (−)-B-хлордиизопинокамфенилборан-((-)-DipCl, 27,96 г, 87,2 ммоль) в 100 мл сухого тетрагидрофурана, поддерживая температуру находящейся в диапазоне от -30°C до -25°C. Через 6 ч ЖХ/МС указывала на полное превращение исходного вещества. Реакцию в холодной смеси останавливали с помощью 10 мл метанола и 10 г гидрокарбоната натрия и смеси давали нагреться до комнатной температуры. Растворители удаляли в вакууме и полученное желтое масло растворяли в 200 мл этилацетата и насыщенного раствора хлорида аммония. Фазы разделяли и органический слой один раз промывали с помощью 50 мл солевого раствора, сушили над сульфатом магния и выпаривали и получали 45 г желтого масла. Это масло очищали с помощью колоночной хроматографии (силикагель, градиентный режим гептан/этилацетат) и получали 11,2 г (S)-3-(5-бром-2-фторфенил)-1-о-толилпропан-1-ола в виде бесцветного масла.
Соотношение энантиомеров (ВЭЖХ; колонка: Chiralcel OJ-H, 250×4,6 мм; элюент гептан/этилацетат/метанол 20:1:1): (S):(R) = 99,4:0,6
c) (S)-6-Бром-2-о-толилхроман
3-(5-Бром-2-фторфенил)-1-о-толилпропан-1-ол (10,5 г) растворяли в 10 мл сухого N-метилпирролидин-2-она и раствор по каплям добавляли к суспензии гидрида натрия (60% в масле, 1,56 г, 39 ммоль) в 20 мл сухого N-метилпирролидин-2-она при 60°C. После завершения добавления смесь перемешивали при 60°C для обеспечения полного израсходования исходного вещества через 12 ч. Затем реакцию в смеси останавливали льдом и насыщенным раствором хлорида аммония и экстрагировали н-гептаном. Объединенные органические слои один раз промывали насыщенным раствором хлорида аммония, водой и солевым раствором. Органический слой сушили над сульфатом магния и выпаривали и получали 12 г прозрачного масла. Это масло очищали с помощью колоночной хроматографии (силикагель, градиентный режим гептан/этилацетат) и получали 7,7 г (S)-6-бром-2-о-толилхромана в виде бесцветного масла.
Пример D
2-о-толилхроман-6-ол
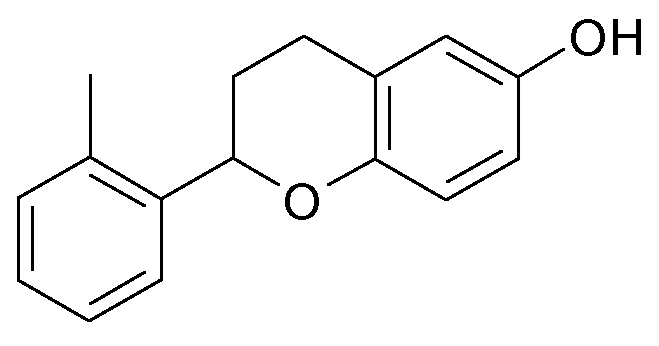
К раствору 6-бром-2-о-толилхромана (1 г, 3,3 ммоль) в тетрагидрофуране (3 мл) при -78°C медленно добавляли н-бутиллитий (2,2 M в циклогексане, 1,8 мл, 1,2 экв.) и смесь выдерживали при -78°C в течение 30 мин. Добавляли триизопропилборат (1,9 г, 2,3 мл, 9,9 ммоль, 3 экв.) и перемешивание продолжали при такой же температуре в течение 1 ч. Холодный раствор выливали в раствор этанола (1,1 мл), воды (3,0 мл) и водного раствора гидроксида натрия (8 M, 1,6 мл). К этому раствору медленно добавляли пероксид водорода (35% водный раствор, 0,9 мл, 3,1 экв.), поддерживая температуру ниже <30°C. Перемешивание при комнатной температуре продолжали в течение 15 мин, суспензию охлаждали до 0°C и значение pH устанавливали равным < 7 водным раствором хлористоводородной кислоты. К полученному раствору добавляли насыщенный водный раствор сульфита натрия (4 мл) и водный слой экстрагировали этилацетатом. Объединенные органические слои сушили над сульфатом натрия и фильтровали, и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали с помощью колоночной хроматографии (силикагель; градиентный режим этилацетат/гептан). 2-о-толилхроман-6-ол получали в виде бледно-желтого твердого вещества (480 мг, 60%).
По описанной методике также синтезировали следующие хроманолы:
2-(5-Фтор-2-метилфенил)-хроман-6-ол
2-(2,6-Диметилфенил)-хроман-6-ол
(S)-2-о-толилхроман-6-ол
Пример E
5-Хлор-2-фенилхроман-6-ол
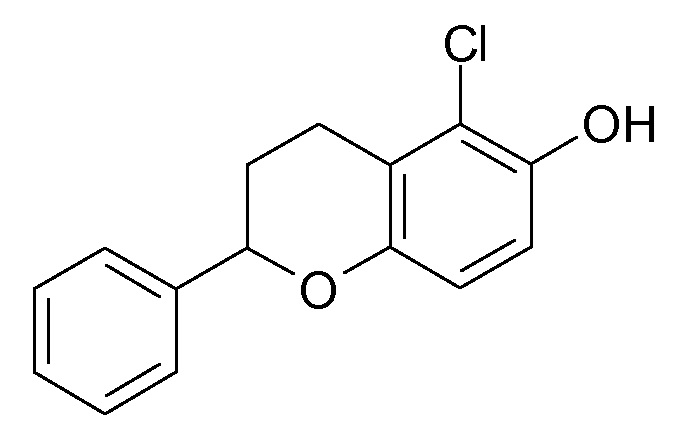
К суспензии 200 мг 2-фенилхроман-6-ола (0,88 ммоль) и 142 мг хлорида железа(III) (0,88 ммоль) в 15 мл ацетонитрила при комнатной температуре одной порцией добавляли 118 мг N-хлорсукцинимида (0,88 ммоль) и перемешивание продолжали в течение 16 ч. Летучие компоненты удаляли при пониженном давлении. Полученный остаток очищали с помощью ВЭЖХ с обращенной фазой. Получали 127 мг искомого соединения в виде бледно-желтого твердого вещества (55%).
Пример F
трет-Бутиловый эфир [4-транс-(2-о-толилхроман-6-илокси)-циклогексил]-карбаминовой кислоты
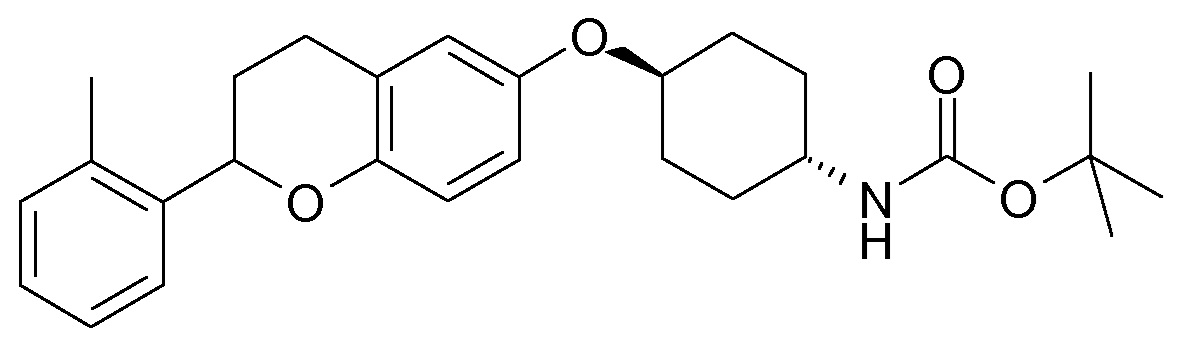
6,5 г (27 ммоль) 2-о-толилхроман-6-ола, 8,16 г (31,1 ммоль) трифенилфосфина и 6,7 г (31,1 ммоль) трет-бутил-цис-4-гидроксициклогексилкарбамата растворяли в 50 мл сухого тетрагидрофурана. К раствору добавляли 6,5 мл (31,1 ммоль) диизопропилазодикарбоксилата и реакционную смесь перемешивали при комнатной температуре в течение 48 ч. Растворитель удаляли путем выпаривания и полученное масло очищали с помощью хроматографии на силикагеле с использованием смеси гептан/этилацетат 4:1 в качестве элюента. Фракции продукта собирали и выпаривали и получали 6 г искомого соединения.
1H-ЯМР (400 МГц): δ (м.д.) = 1,29-1,33 (4H, м), 1,38 (9H, с), 1,79 (2H, м), 1,82 (1H, м), 2,12 (1H, м), 2,35 (3H, с), 2,73 (1H, дд), 3,02 (1H, м), 3,28 (1H, м),4,13 (1H, м), 5,17 (1H, дд), 6,69 (1H), 6,74 (1H), 6,79 (1 H), 7,21 (3H), 7,43 (1H).
По описанной методике также синтезировали следующие соединения:
6-(1,4-Диоксаспиро[4.5]дец-8-илокси)-2-о-толилхроман
трет-бутиловый эфир [цис-4-(2-о-толилхроман-6-илокси)-циклогексилметил]-карбаминовой кислоты
этиловый эфир 4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты
этиловый эфир цис-4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты
этиловый эфир транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты
этиловый эфир транс-4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты
трет-бутиловый эфир [цис-4-(2-фенилхроман-6-илокси)-циклогексил]-карбаминовой кислоты
трет-бутиловый эфир [транс-4-(2-фенилхроман-6-илокси)-циклогексил]-карбаминовой кислоты
трет-бутиловый эфир [цис-4-(2-фенилхроман-6-илокси)-циклогексилметил]-карбаминовой кислоты
трет-бутиловый эфир {1-[1-этил-4-(2-фенилхроман-6-илокси)-циклогексил]-пропил}-карбаминовой кислоты
6-(1,4-диоксаспиро[4.5]дец-8-илокси)-2-фенилхроман
этиловый эфир цис-4-(2-фенилхроман-6-илокси)-циклогексанкарбоновой кислоты
этиловый эфир 4-(2-фенилхроман-6-илокси)-циклогексанкарбоновой кислоты
трет-бутиловый эфир [4-(2-фенилхроман-6-илокси)-1-пропилциклогексил]-карбаминовой кислоты
этиловый эфир 4-[2-(2,6-диметилфенил)-хроман-6-илокси]-циклогексанкарбоновой кислоты
трет-бутиловый эфир {транс-4-[2-(2,6-диметилфенил)-хроман-6-илокси]-циклогексил}-карбаминовой кислоты
2-(2,6-диметилфенил)-6-(1,4-диоксаспиро[4.5]дец-8-илокси)-хроман
этиловый эфир 4-[2-(3-фтор-2-метилфенил)-хроман-6-илокси]-циклогексанкарбоновой кислоты
6-(1,4-диоксаспиро[4.5]дец-8-илокси)-2-(3-фтор-2-метилфенил)-хроман
6-(1,4-диоксаспиро[4.5]дец-8-илокси)-2-(2-фторфенил)-хроман
этиловый эфир 4-[2-(2-фторфенил)-хроман-6-илокси]-циклогексанкарбоновой кислоты
трет-бутиловый эфир {транс-4-[2-(5-фтор-2-метилфенил)-хроман-6-илокси]-циклогексил}-карбаминовой кислоты
трет-бутиловый эфир {транс-4-[2-(2-фторфенил)-хроман-6-илокси]-циклогексил}-карбаминовой кислоты
этиловый эфир 4-(7-метил-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты
этиловый эфир 4-(5-хлор-2-фенилхроман-6-илокси)-циклогексанкарбоновой кислоты
этиловый эфир 4-[2-(2-фтор-3-метоксифенил)-хроман-6-илокси]-циклогексанкарбоновой кислоты
этиловый эфир 4-(3-метил-2-фенилхроман-6-илокси)-циклогексанкарбоновой кислоты
этиловый эфир 4-[2-(3-фтор-2-метоксифенил)-хроман-6-илокси]-циклогексанкарбоновой кислоты
Пример G
транс-4-(2-о-толилхроман-6-илокси)-циклогексиламингидрохлорид
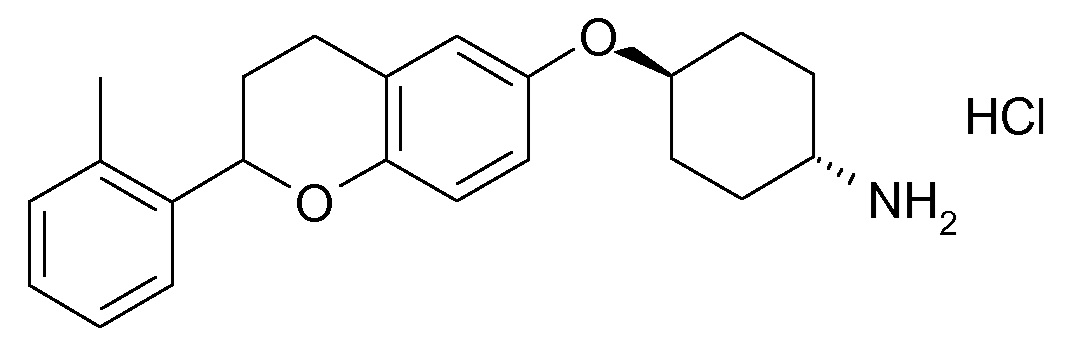
6 г (13,7 ммоль) трет-бутилового эфира [транс-4-(2-о-толилхроман-6-илокси)-циклогексил]-карбаминовой кислоты растворяли в 50 мл 1,4-диоксана и 25 мл 2 н раствора хлорида водорода в диэтиловом эфире. Диэтиловый эфир удаляли путем выпаривания и оставшийся раствор кипятили с обратным холодильником, пока исходное вещество не переставало обнаруживаться с помощью ОФ-ВЭЖХ. Полученную суспензию охлаждали до 0°C и кристаллы собирали фильтрованием, один раз промывали холодным метил-трет-бутиловым эфиром и сушили в вакууме при 25°C и получали 3,6 г искомого соединения.
1H-ЯМР (400 МГц): δ (м.д.) = 1,42 (4H, м), 1,88 (1H, м), 1,95 (2H, м), 2,08 (3H, м), 2,35 (3H, с), 2,73 (1H, дд), 3,02 (2H, м), 4,13 (1H, м), 5,17 (1H, дд), 6,74 (2H), 6,79 (1H), 7,21 (3H), 7,43 (1H), 8,08 (3H, с).
По описанной методике также синтезировали следующие соединения:
цис-4-(2-Фенилхроман-6-илокси)-циклогексиламин
транс-4-(2-Фенилхроман-6-илокси)-циклогексиламин
[цис-4-(2-Фенилхроман-6-илокси)-циклогексилметил]амин
4-(2-Фенилхроман-6-илокси)-1-пропилциклогексиламин
1-[1-Этил-4-(2-фенилхроман-6-илокси)-циклогексил]-пропиламин
[цис-4-(2-о-толилхроман-6-илокси)-циклогексилметил]амин
транс-4-[2-(2,6-Диметилфенил)-хроман-6-илокси]-циклогексиламин
транс-4-[2-(2-Фторфенил)-хроман-6-илокси]-циклогексиламин
транс-4-[2-(5-Фтор-2-метилфенил)-хроман-6-илокси]-циклогексиламин
Пример H
транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбоновая кислота
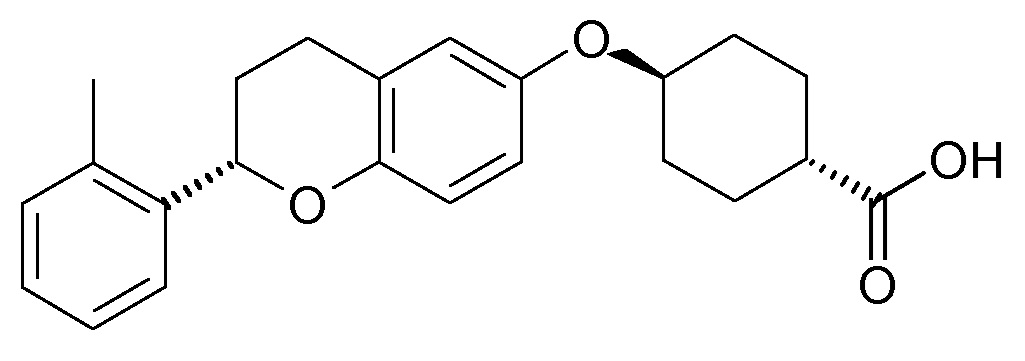
0,75 г (1,9 ммоль) этилового эфира транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты растворяли в 10 мл тетрагидрофурана. Добавляли 94 мг (3,9 ммоль) гидроксида лития (растворенного в 2 мл воды). Раствор перемешивали при комнатной температуре в течение ночи, пока исходное вещество не переставало обнаруживаться с помощью ОФ-ВЭЖХ. Раствор разбавляли метил-трет-бутиловым эфиром и добавляли 2 н хлористоводородную кислоту до pH, равного 2. После разделения фаз органический слой сушили над сульфатом магния и растворитель выпаривали. Полученный продукт кристаллизовался при выдерживании и получали 0,65 г искомого соединения.
1H-ЯМР (400 МГц): δ (м.д.) = 1,36 (2H, м), 1,48 (2H, м), 1,85-2,11 (6H, м), 2,35 (3H, с), 2,38 (1H, м), 2,73 (1H, дд), 3,02 (1H, м), 4,18 (1H, м), 5,17 (1H, дд), 6,72 (3H), 7,21 (3H), 7,43 (1H), 12,10 (1H, с).
По описанной методике также синтезировали следующие соединения:
цис-4-(2-Фенилхроман-6-илокси)-циклогексанкарбоновая кислота
4-(2-Фенилхроман-6-илокси)-циклогексанкарбоновая кислота
4-(7-Метил-2-о-толилхроман-6-илокси)-циклогексанкарбоновая кислота
4-(5-Хлор-2-фенилхроман-6-илокси)-циклогексанкарбоновая кислота
4-[2-(2-Фтор-3-метоксифенил)-хроман-6-илокси]-циклогексанкарбоновая кислота
4-(3-Метил-2-фенилхроман-6-илокси)-циклогексанкарбоновая кислота
4-[2-(3-Фтор-2-метоксифенил)-хроман-6-илокси]-циклогексанкарбоновая кислота
4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновая кислота
транс-4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновая кислота
цис-4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновая кислота
4-[2-(2,6-Диметилфенил)-хроман-6-илокси]-циклогексанкарбоновая кислота
4-[2-(3-Фтор-2-метилфенил)-хроман-6-илокси]-циклогексанкарбоновая кислота
4-[2-(2-Фторфенил)-хроман-6-илокси]-циклогексанкарбоновая кислота
Пример J
4-(2-Фенилхроман-6-илокси)-циклогексанон
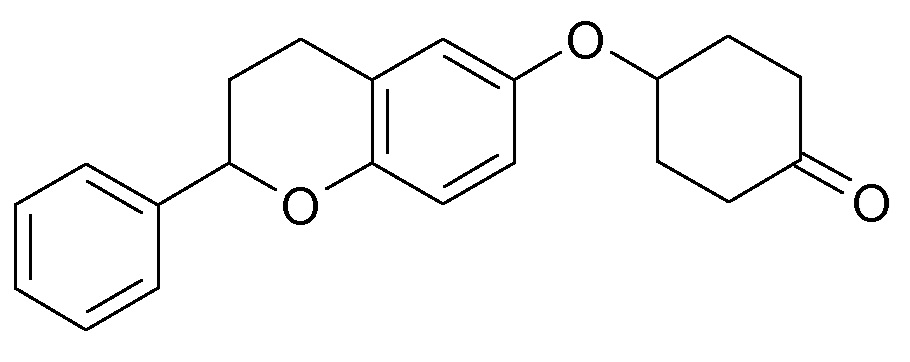
430 мг 6-(1,4-диоксаспиро[4.5]дец-8-илокси)-2-фенилхромана растворяли при комнатной температуре в 5 мл тетрагидрофурана. Добавляли 5 мл 10% водного раствора хлористоводородной кислоты и перемешивание при комнатной температуре продолжали в течение 16 ч. Реакционную смесь разбавляли этилацетатом и органический слой промывали насыщенным водным раствором гидрокарбоната натрия. Органический слой сушили над сульфатом натрия и фильтровали, и летучие компоненты удаляли при пониженном давлении. Получали 357 мг искомого соединения в виде бледно-желтого твердого вещества.
По описанной методике также синтезировали следующие соединения:
4-(2-о-толилхроман-6-илокси)-циклогексанон
4-[2-(2,6-Диметилфенил)-хроман-6-илокси]-циклогексанон
4-[2-(3-Фтор-2-метилфенил)-хроман-6-илокси]-циклогексанон
4-[2-(2-Фторфенил)-хроман-6-илокси]-циклогексанон
Пример K
[4-(2-о-толилхроман-6-илокси)-циклогексил]-(1,3,5-триметил-1H-пиразол-4-илметил)-амин
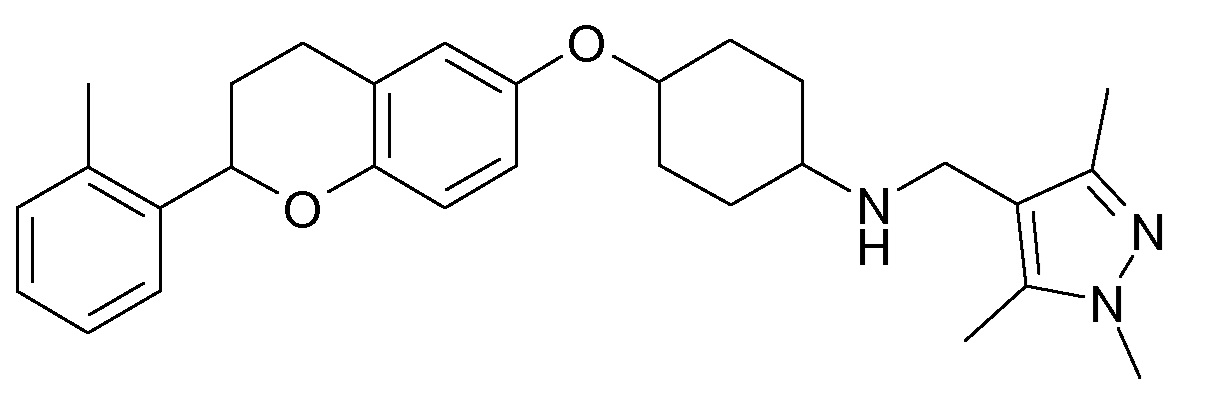
К раствору 100 мг 4-(2-о-толилхроман-6-илокси)-циклогексанона (0,30 ммоль) в 2 мл метанола и 0,15 мл уксусной кислоты при комнатной температуре одной порцией добавляли 124 мг (1,3,5-триметил-1H-пиразол-4-илметил)амина (0,89 ммоль) и 56 мг цианоборгидрида натрия (0,89 ммоль) и перемешивание при комнатной температуре продолжали в течение 2 ч. Летучие компоненты удаляли при пониженном давлении и полученный остаток растворяли в дихлорметане. Органический слой промывали 2 н водным раствором гидроксида натрия и насыщенным водным раствором хлорида натрия. Органический слой сушили над сульфатом натрия и фильтровали, и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали с помощью ВЭЖХ с обращенной фазой. 132 мг искомого соединения выделяли.
Пример L
(Тетрагидрофуран-3-илметил)-[транс-4-(2-о-толилхроман-6-илокси)-циклогексил]-амин и бис-(тетрагидрофуран-3-илметил)-[транс-4-(2-о-толилхроман-6-илокси)-циклогексил]-амин
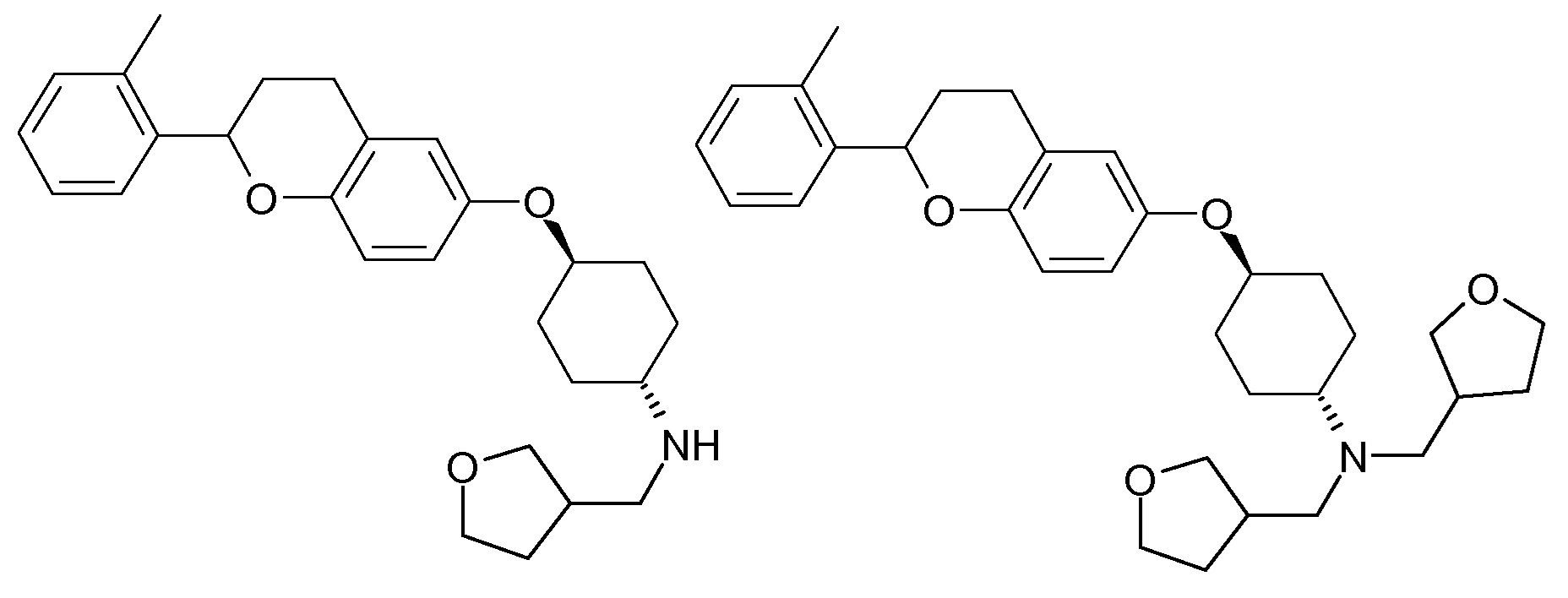
К раствору 61 мг транс-4-(2-о-толилхроман-6-илокси)-циклогексиламина (0,18 ммоль) в 3 мл метанола и 0,2 мл уксусной кислоты при комнатной температуре добавляли 39 мг тетрагидрофуран-3-карбоксальдегида (0,20 ммоль) в 3 мл метанола и затем одной порцией добавляли 12 мг цианоборгидрида натрия (0,89 ммоль (0,20 ммоль). Перемешивание при комнатной температуре продолжали в течение 16 ч. Раствор разбавляли насыщенным водным раствором гидрокарбоната натрия и водный слой экстрагировали дихлорметаном. Объединенные органические слои сушили над сульфатом натрия и фильтровали, и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали с помощью ОФ-ВЭЖХ. Выделяли 23 мг (тетрагидрофуран-3-илметил)-[транс-4-(2-о-толилхроман-6-илокси)-циклогексил]-амина и 19 мг бис-(тетрагидрофуран-3-илметил)-[транс-4-(2-о-толилхроман-6-илокси)-циклогексил]-амина.
Пример M
трет-Бутиловый эфир ({[цис-4-(2-о-толилхроман-6-илокси)-циклогексилметил]-карбамоил}-метил)-карбаминовой кислоты
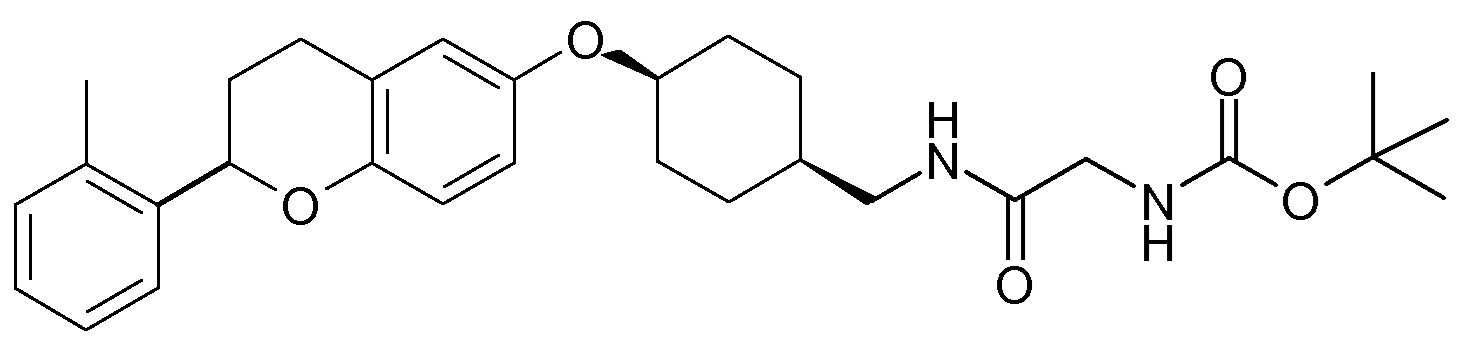
К суспензии 110 мг [цис-4-(2-о-толилхроман-6-илокси)-циклогексилметил]амингидрохлорида (0,28 ммоль), 75 мг N-трет-бутоксикарбонилглицина (0,43 ммоль), 76 мг 1-(3-диметиламинопропил)-3-этилкарбодиимидгидрохлорида (0,40 ммоль) и 54 мг гидроксибензотриазола (0,40 ммоль) в 2 мл диметилформамида при комнатной температуре добавляли 0,16 мл N-метилморфолина (1,42 ммоль) и перемешивание при комнатной температуре продолжали в течение 16 ч. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Объединенные органические слои промывали разбавленным водным раствором карбоната натрия, сушили над сульфатом натрия и фильтровали, и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали с помощью колоночной хроматографии с использованием смеси этилацетат/гептан/метанол 5:10:1 в качестве элюента. Выделяли 95 мг искомого соединения.
Пример N
N-[цис-4-(2-Фенилхроман-6-илокси)-циклогексилметил]-метансульфонамид
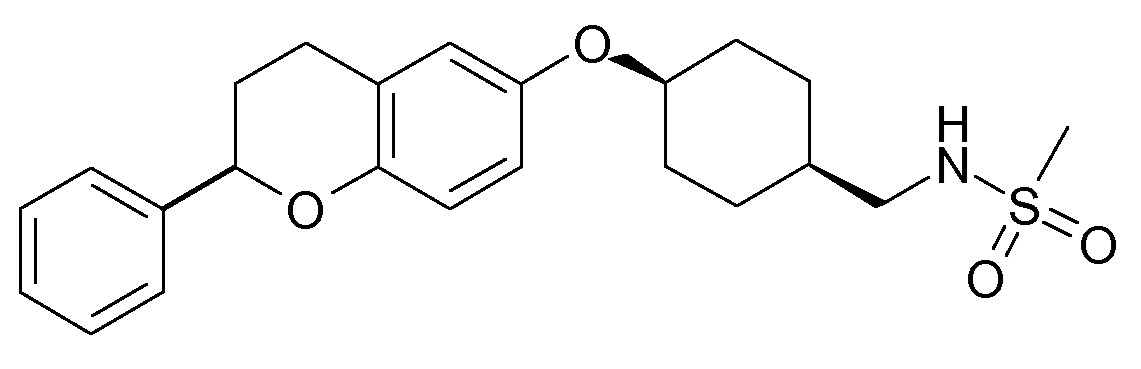
К раствору 150 мг [цис-4-(2-фенилхроман-6-илокси)-циклогексилметил]амингидрохлорида (0,40 ммоль) в 4 мл пиридина при комнатной температуре добавляли 47 мкл метансульфонилхлорида (0,60 ммоль) и перемешивание при комнатной температуре продолжали в течение 16 ч. Реакционную смесь разбавляли водой и экстрагировали дихлорметаном Объединенные органические слои промывали с помощью разбавленный водный раствор хлористоводородной кислоты, сушили над сульфатом натрия и фильтровали, и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали с помощью ВЭЖХ с обращенной фазой. Выделяли 97 мг искомого соединения в виде белого твердого вещества.
Пример O
(2-Гидроксиэтил)-амид 4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты
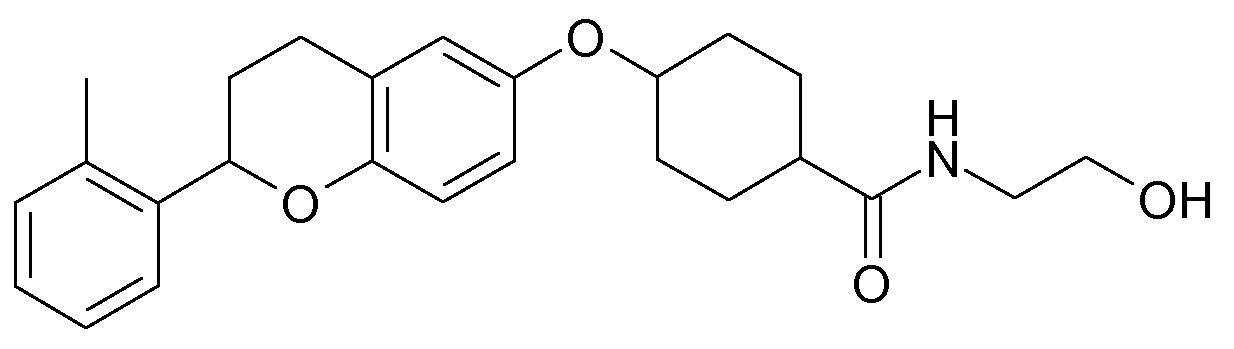
К раствору 100 мг 4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты (0,40 ммоль) в 25 мл дихлорметана при комнатной температуре добавляли 103 мг 1-(3-диметиламинопропил)-3-этилкарбодиимидгидрохлорида (0,54 ммоль), 73 мг гидроксибензотриазола (0,54 ммоль), 0,12 мл триэтиламина (0,88 ммоль) и 11 мкл 2-аминоэтанола (0,19 ммоль) и перемешивание при комнатной температуре продолжали в течение 16 ч. Реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Объединенные органические слои сушили над сульфатом натрия и фильтровали, и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали с помощью ВЭЖХ с обращенной фазой. Выделяли 42 мг белого твердого вещества, которое представляло собой смесь четырех стереоизомеров искомого соединения.
Стереоизомеры разделяли с помощью препаративной ВЭЖХ на хиральной фазе (колонка: Chiralpak AS-H, 250×30 мм; температура: 30°C; скорость потока: 40 мл/мин; элюент: гептан/этанол/метанол 20:1:1) и получали (2-гидроксиэтил)-амид транс-4-((R)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты, (2-гидроксиэтил)-амид транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты, стереоизомер 1 (2-гидроксиэтил)-амида цис-4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты и стереоизомер 2 (2-гидроксиэтил)-амида цис-4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты. Конфигурация хирального атома углерода в положении 2 хроманового кольца для стереоизомеров 1 и 2 (2-гидроксиэтил)-амида цис-4-(2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты неизвестна; одним из них является (2-гидроксиэтил)-амид цис-4-((R)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты и другим является (2-гидроксиэтил)-амид цис-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты.
Пример P
4-(2-Фенилхроман-6-илокси)-1-пропилциклогексанол
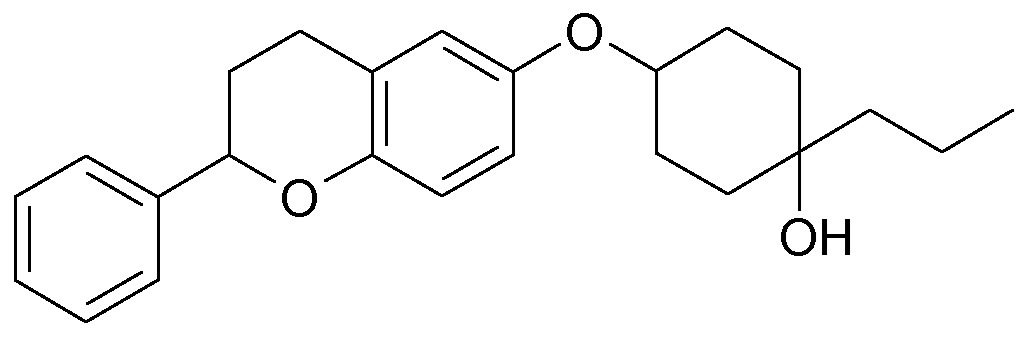
100 мг 4-(2-фенилхроман-6-илокси)-циклогексанона при комнатной температуре растворяли в 5 мл тетрагидрофурана. Добавляли 2M раствор пропилмагнийхлорида в диэтиловом эфире (0,31 мл, 2 экв.) и перемешивание при комнатной температуре продолжали в течение 4 ч. Реакцию останавливали путем осторожного добавления насыщенного водного раствора хлорида аммония. Водный слой экстрагировали метил-трет-бутиловым эфиром. Органический слой сушили над сульфатом натрия и фильтровали, и растворитель удаляли путем выпаривания. Полученное масло хроматографировали на силикагеле с использованием смеси гептан/этилацетат 20:1 в качестве элюента. Выделяли 54 мг искомого соединения в виде бледно-желтого масла (48%).
Пример Q
4-(2-Фенилхроман-6-илокси)-циклогексанол
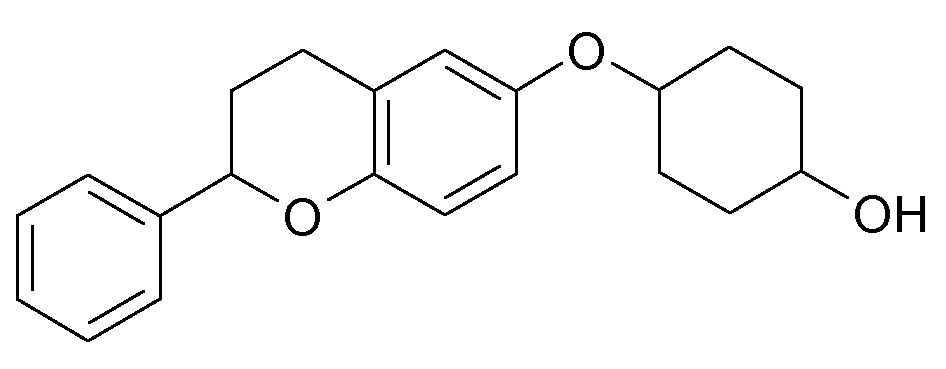
500 мг 4-(2-Фенилхроман-6-илокси)-циклогексанона (1,6 ммоль) растворяли при 0°C в 2,5 мл этанола. Порциями добавляли 30 мг боргидрида натрия (0,78 ммоль) и перемешивание при комнатной температуре продолжали в течение 2 ч. Растворитель удаляли при пониженном давлении и остаток подвергали распределению между насыщенным водным раствором гидрокарбоната натрия и дихлорметаном. Водный слой экстрагировали дихлорметаном. Объединенные органические слои сушили над сульфатом натрия и фильтровали, и летучие компоненты удаляли при пониженном давлении. 500 мг искомого соединения получали в виде бледно-желтого твердого вещества.
Пример R
4-(2-Фенилхроман-6-илокси)-циклогексиловый эфир 3-фторизоникотиновой кислоты
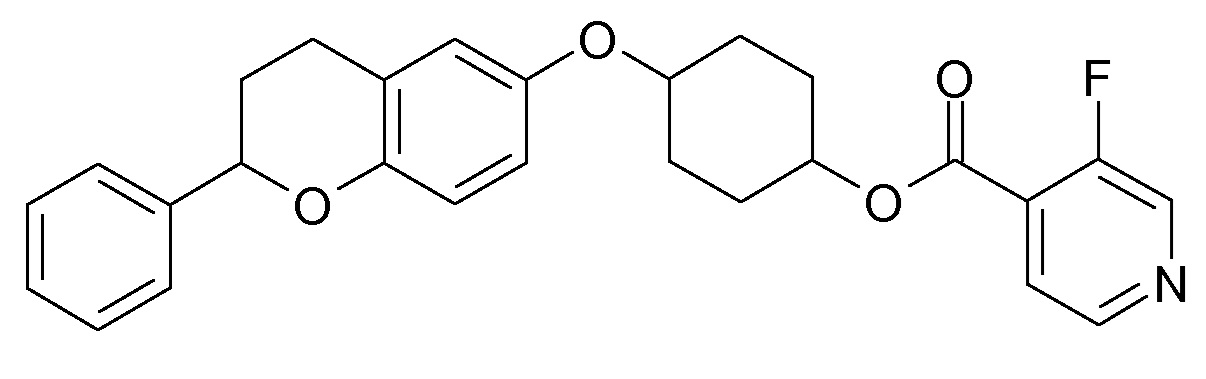
К раствору 158 мг 3-фторизоникотиновой кислоты (1,12 ммоль) и 156 мкл триэтиламина (1,12 ммоль) в 16 мл дихлорметана при 15°C по каплям добавляли 138 мкл пивалоилхлорида (1,12 ммоль). Раствор перемешивали в течение 30 мин. Добавляли раствор 110 мг 4-(2-фенилхроман-6-илокси)-циклогексанола (0,34 ммоль) в 4 мл дихлорметана и одной порцией добавляли 82 мг 4-диметиламинопиридина (0,68 ммоль). Перемешивание при комнатной температуре продолжали в течение 16 ч. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия и водный слой экстрагировали дихлорметаном. Объединенные органические слои сушили над сульфатом натрия и фильтровали, и растворитель удаляли путем выпаривания. Полученное масло очищали с помощью ВЭЖХ с обращенной фазой. Выделяли 104 мг искомого соединения в виде твердого вещества (69%).
Пример S
1-Бензил-4-(2-фенилхроман-6-илокси)-циклогексиламин
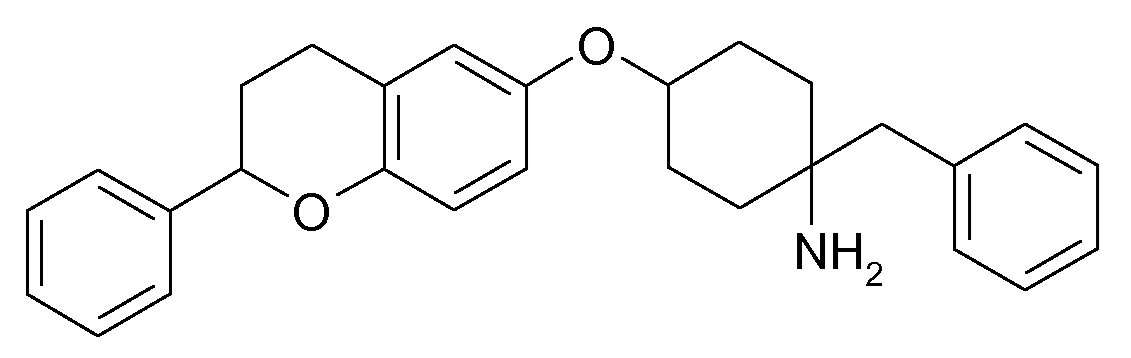
a) К раствору 352 мг 4-(2-фенилхроман-6-илокси)-циклогексанона (1,1 ммоль) в 10 мл тетрагидрофурана при комнатной температуре добавляли 0,46 мл этоксида титана(IV) (2,18 ммоль) и 139 мг трет-бутилсульфинамида (1,15 ммоль) и полученный раствор кипятили с обратным холодильником в течение 16 ч. Раствор охлаждали до 0°C и добавляли 1,09 мл бензилмагнийхлорида (2M в тетрагидрофуране, 2,18 ммоль). Смесь перемешивали при комнатной температуре в течение 16 ч и добавляли еще 1,09 мл раствора бензилмагнийхлорида. После перемешивания в течение еще 16 ч реакцию останавливали путем осторожного добавления воды. Суспензию фильтровали и осадок на фильтре промывали дихлорметаном. Водный слой экстрагировали дихлорметаном. Объединенные органические слои сушили над сульфатом натрия и фильтровали, и растворитель удаляли путем выпаривания. Полученное масло очищали с помощью хроматографии на силикагеле в градиентном режиме с использованием смеси гептан/этилацетат (от 0% этилацетата до 25% этилацетата). Выделяли 248 мг [1-бензил-4-(2-фенилхроман-6-илокси)-циклогексил]-амида 2-метилпропан-2-сульфиновой кислоты в виде смеси диастереоизомеров (44%).
b) 120 мг [1-бензил-4-(2-фенилхроман-6-илокси)-циклогексил]-амида 2-метилпропан-2-сульфиновой кислоты (0,23 ммоль) растворяли в 2 мл трифторуксусной кислоты в герметизированной пробирке для микроволновой печи и нагревали в микроволновом реакторе в течение 1 ч при 130°C. Растворитель удаляли при пониженном давлении и полученный остаток очищали с помощью ВЭЖХ с обращенной фазой. Получали 21 мг 1-бензил-4-(2-фенилхроман-6-илокси)-циклогексиламина в виде твердого вещества (17%).
Пример T
Динатриевая соль моно-(2-{[транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбонил]-амино}-этилового) эфира фосфорной кислоты
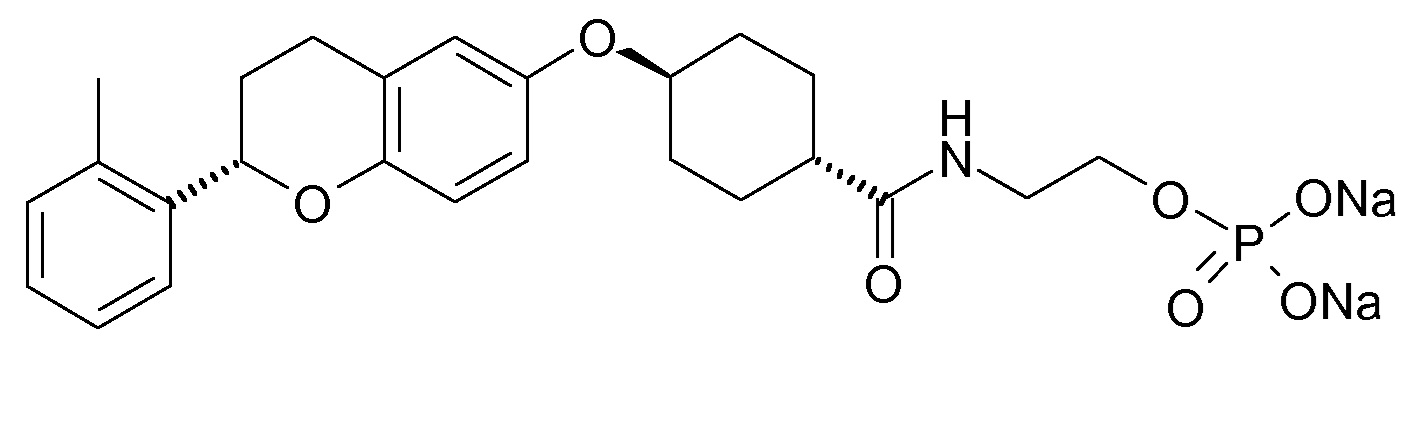
a) Дибензиловый эфир,(2-{[транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбонил]-амино}-этиловый) эфир фосфорной кислоты
К суспензии (2-гидроксиэтил)-амида транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбоновой кислоты (0,5 г, 1,22 ммоль) и тетразола (102 мг, 1,47 ммоль, 1,2 экв.) в дихлорметане (7 мл) и ацетонитриле (7 мл) при 0°C добавляли дибензил-N,N-диизопропилфосфорамидит (0,46 г, 1,34 ммоль, 1,1 экв.) и смесь перемешивали при 0°C в течение 60 мин (контроль с помощью ТСХ (тонкослойная хроматография). К полученному раствору одной порцией добавляли 3-хлорпербензойную кислоту (65%, 390 мг, 1,47 ммоль, 1,2 экв.) и энергичное перемешивание при 0°C продолжали в течение 30 мин (контроль с помощью ТСХ). Смесь разбавляли дихлорметаном и органический слой промывали насыщенным водным раствором гидрокарбоната натрия и затем насыщенным водным раствором хлорида аммония. Объединенные органические слои сушили над сульфатом натрия и фильтровали, и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали с помощью колоночной хроматографии (силикагель, градиентный режим этилацетат/метанол). Получали дибензиловый эфир, (2-{[транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбонил]-амино}-этиловый) эфир фосфорной кислоты в виде бесцветного масла (0,66 г, 81%).
b) Динатриевая соль моно-(2-{[транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбонил]-амино}-этилового) эфира фосфорной кислоты
Дибензиловый эфир, (2-{[транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбонил]-амино}-этиловый) эфир фосфорной кислоты (0,33 г, 0,49 ммоль) растворяли в метаноле (10 мл) и добавляли палладий на древесном угле (10% Pd, 54% воды, 0,3 г). Суспензию энергично перемешивали в течение 1,5 ч в атмосфере водорода. Смесь фильтровали и осадок на фильтре промывали метанолом. Фильтрат выпаривали при пониженном давлении и полученный неочищенный продукт очищали с помощью препаративной ВЭЖХ с обращенной фазой (градиентный режим вода/ацетонитрил (+ 0,1% трифторуксусной кислоты)). Полученный моно-(2-{[транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбонил]-амино}-этиловый) эфир фосфорной кислоты суспендировали в воде и превращали в динатриевую соль путем добавления 2 экв. 0,5 н водного раствора гидроксида натрия. Полученный водный раствор лиофилизировали и получали динатриевую соль моно-(2-{[транс-4-((S)-2-о-толилхроман-6-илокси)-циклогексанкарбонил]-амино}-этилового) эфира фосфорной кислоты в виде белого твердого вещества (113 мг, 43%).
По аналогии с методиками, описанными выше в примерах синтеза, получали соединения примеров формулы I приведенные в таблице 1. В таблице 1 "Пример №" означает номер соединения примера; "ЖХ/МС" означает методику ЖХ/МС, описанную выше, которую использовали при исследовании с помощью ВЭЖХ и МС соединений примеров; "МС" означает массовое число (в атомных единицах массы) для пика молекулярного иона или родственного иона, такого как M+1 в масс-спектре, в случае соли означает массовое число исходного соединения, т.е. свободной кислоты или основания, если не указан другой ион; "Rt" означает время удерживания в ВЭЖХ (в мин); и "NCX1rv IC50" означает значение IC50 (в мкМ (микромоль/литр) для ингибирования NCX1 в обратном режиме, определенное с помощью анализа ингибирования притока Ca2+ в клетки (обратный режим), описанного ниже).
(1) Наблюдающийся ион [M+H]+, если не указано иное,
(2) В случае, если соединение было получено в виде стереоизомера 1 и стереоизомера 2, один из них обладает R-конфигурацией и второй S-конфигурацией по отношению к положению 2 в хромановом кольце.
(3) Ингибирование в % при 10 мкМ; значение IC50 не определено.
Типичные данные ЯМР для соединений примеров.
Пример № 156
1H-ЯМР (400 МГц): δ (м.д.) = 1,41 (4H, м), 1,98 (3H, м), 2,11 (3H, м), 2,35 (3H, с), 2,75 (1H, м), 3,02 (2H, м), 4,12 (1H, м), 5,15 (1H, дд), 6,74 (3H, м), 7,24 (3H, м), 7,41 (1H, м).
Пример № 158
1H-ЯМР (400 МГц): δ (м.д.) = 1,28 (2H, м), 1,54 (2H, м), 1,88 (3H, м), 2,11 (3H, м), 2,22 (1H, м), 2,32 (3H, с), 2,75 (1H, м), 2,96 (1H, м), 4,12 (1H, м), 4,42 (2H, д), 5,17 (1H, тт), 6,28 (1H, с), 6,72 (3H, м), 7,21 (3H, м), 7,43 (1H, м), 8,48 (2H, м).
Пример № 159
1H-ЯМР: δ (м.д.) = 1,47 (4H, м), 1,90 (2H, м), 2,00 (3H, м), 2,15 (1H, м), 2,70 (1H, м), 2,95 (1H, м), 3,54 (2H, м), 3,67 (1H, м), 4,16 (1H, м), 5,05 (1H, дд), 6,72 (3H, м), 7,38 (1H, м), 7,41 (4H, м), 8,48 (1H, д).
Пример № 177
1H-ЯМР: δ (м.д.) = 1,40 (1H, м), 1,58 (2H, м), 1,78, (1H, м), 1,98 (3H, м), 2,18 (7H, м), 2,25 (3H, с), 2,35 (3H, с), 2,77 (1H, м), 3,03 (1H, м), 3,19, (1H, м), 3,97 (2H, м), 4,13 (0,5H, м), 4,48 (0,5H, м), 5,17 (1H, дд), 6,73 (3H, м), 7,22 (3H, м), 7,40 (1H, м).
Пример № 180
1H-ЯМР: δ (м.д.) = 1,48 (4H, м), 1,95 (8H, м), 2,15 (1H, м), 2,28 (1H, м), 2,70 (1H, м), 2,93 (1H, м), 3,22 (1H, м), 3,51 (2H, м), 3,65 (1H, м), 4,10 (1H, т), 4,18 (1H, м), 5,05 (1H, дд), 6,73 (3H, м), 7,42 (1H, м), 7,40 (4H, м), 8,45 (1H, д).
Пример № 268
1H-ЯМР (400 МГц): δ (м.д.) = 1,28 (2H, м), 1,48 (2H, м), 1,74 (2H, м), 1,88 (1H, м), 2,11 (4H, м), 2,32 (3H, с), 2,38 (1H, м), 2,73 (1H, дд), 2,96 (1H, м), 3,12 (2H, дт), 3,38 (4H, м), 4,12 (1H, м), 4,68 (1H, т), 5,17 (1H, дд), 6,72 (3H), 7,21 (3H), 7,43 (1H), 7,79 (1H, т).
Пример № 303
1H-ЯМР (400 МГц, D2O): δ (м.д.) = 1,45 (4H, м), 1,93 (2H, м), 2,08 (1H, м), 2,18 (3H, м) 2,30 (1H, м) 2,81 (1H, м), 3,02 (1H, м), 3,35 (2H, т), 3,80 (2H, м), 4,42 (1 H, м), 5. 30 (1H, дд), 6,81 (2H, м), 6,90 (1H, м), 7,29 (3H, м), 7,48 (1H, м).
Фармакологические примеры
A) Методика исследования для определения ингибирующей активности NCX1
Натрий-кальциевый обмен NCX1 может переносить ионы кальция и ионы натрия через мембрану клетки. Этот перенос является обменом Ca2+ и Na+ в двух направлениях в зависимости от мембранного потенциала и градиентов ионов. В первом направлении, называющемся "прямым режимом" или "режимом выведения кальция", Ca2+ переносится из клетки и Na+ переносится в клетку. Во втором направлении, называющемся "обратным режимом" или "режимом введения кальция", перенос происходит в обратном направлении. Влияние соединений, предлагаемых в настоящем изобретении, на NCX1 определяли в клетках CHO, стабильно экспрессирующих NCX1 человека (обозначение гена: SLC8A1; см. WO 2009/115238). Исследование основано на мониторинге внутриклеточных концентраций Ca2+ с использованием чувствительного по отношению к кальцию флуоресцентного красителя, который регистрируют с помощью устройства FLIPR (Fluorimetric Imaging Plate Reader, Molecular Devices).
Методика исследования - обратный режим
Исследование основано на мониторинге внутриклеточных концентраций Ca2+ с использованием чувствительного по отношению к кальцию красителя Fluo-4. В клетки CHO, экспрессирующие NCX1, вводили краситель с помощью ацетоксиметилового эфира Fluo-4 AM (Invitrogen, F14202), который внутри клеток расцепляется вследствие активности эстеразы с образованием заряженных частиц свободного Fluo-4. После периода предварительной инкубации с исследуемым соединением добавляли грамицидин (Sigma, G5002). Грамицидин является ионофором для ионов Na+, опосредующим увеличение содержания внутриклеточных ионов Na+. Следовательно, внутриклеточные ионы Na+ обмениваются на внеклеточные ионы Ca2+ (приток Ca2+, обратный режим). Увеличение содержания внутриклеточных ионов Ca2+ регистрировали путем измерения интенсивности флуоресценции Fluo-4 при длине волны, равной 520 нм, с помощью устройства FLIPR.
Вкратце, методика заключалась в следующем: при исследовании переноса в обратном режиме по 18000 клеток/лунка высевали в 96-луночный микропланшет (Corning COSTAR 3904) и инкубировали в течение ночи в культуральной среде (1X Nut Mix F12 (Ham) (Gibco, 21765-029); 10% (об./об.) фетальной телячьей сыворотки (PAA Gold, A15-649); 450 мкг/мл генетицина (Gibco, 10131-027)). Использовали полный объем, составляющий 100 мкл среды/лунка. Для проведения исследования с помощью FLIPR из планшетов удаляли культуральную среду и в каждую лунку добавляли 100 мкл раствора красителя (2 мкМ Fluo-4 AM; 0,02% (об./об.) Pluronic F-127 (20%, Invitrogen, P3000MP); 0,1% (об./об.) раствора бычьего альбумина (30% (об./об.), Sigma, A9205) в буфере для анализа (133,8 мМ NaCl (Sigma, S5886); 4,7 мМ KCl (Sigma, P3911); 1,25 мМ MgCl2 (Merck, 1.05833.0250); 3,5 мМ CaCl2 (Merck, 1.02083.0250); 5 мМ глюкозы (Sigma, G7021); 10 мМ Hepes (Sigma, H4034); 0,01% (об./об.) Pluronic F-127 (5%, Sigma, P2443); 2,5 мМ пробенецида (Maybridge, SB00915EB); pH 7,4)). Планшеты инкубировали в темноте при комнатной температуре в течение 80 мин. После инкубационного периода раствор красителя удаляли и лунки промывали с помощью 100 мкл буфера для анализа. Затем в лунки добавляли 80 мкл раствора исследуемого соединения в буфере для анализа в разных концентрациях. Планшеты инкубировали при 16°C в течение 45 мин. При этом 60 мкМ раствор грамицидина в буфере для анализа (4°C) готовили и хранили в лунках 96-луночного микропланшета (96-луночный микропланшет, полипропиленовый, U-образной формы (Greiner Bio-One, 650201)) при 4°C до начала измерений. Мониторинг флуоресценции проводили с помощью 240 измерений с промежутками в 2 с. После пятого измерения в каждую лунку планшетов для исследования добавляли 40 мкл раствора грамицидина и получали конечную концентрацию грамицидина, равную 20 мкМ. Для определения значений IC50 минимальное значение интенсивности флуоресценции вычитали из максимального значения интенсивности флуоресценции для всех измерений. Расчет значений IC50 с помощью выраженного в процентах ингибирования притока Ca2+ в клетки (обратный режим), вызванного исследуемым соединением, проводили с помощью Biost@t Speed 2.0. Результаты, полученные для соединений, предлагаемых в настоящем изобретении, приведены в таблице 1.
Методика исследования - прямой режим
Исследование основано на мониторинге внутриклеточных концентраций Ca2+ с использованием набора PBX Calcium Assay Kit, выпускающегося фирмой BD (Becton, Dickinson and Company), с индикаторным красителем для кальция 51-9000177BKa (BD, 640177). В клетки CHO, экспрессирующие NCX1, вводили краситель и после периода предварительной инкубации с исследуемым соединением добавляли иономицин (Calbiochem, 407950). Иономицин является ионофором для ионов Ca2+, опосредующим увеличение содержания внутриклеточных ионов Ca2+. Следовательно, внутриклеточные ионы Ca2+ обмениваются на внеклеточные ионы Na+ (отток Ca2+, прямой режим). Уменьшение содержания внутриклеточных ионов Ca2+ регистрировали путем измерения интенсивности флуоресценции индикаторного красителя для кальция при длине волны, равной 520 нм, с помощью устройства FLIPR.
Вкратце, аналогично методике для обратного режима методика для прямого режима заключалась в следующем: при исследовании переноса по 18000 клеток/лунка высевали в 96-луночный микропланшет (Corning COSTAR 3904) и инкубировали в течение ночи в культуральной среде (см. выше). Использовали полный объем, составляющий 100 мкл среды/лунка. Для проведения исследования с помощью FLIPR из планшетов удаляли культуральную среду и в каждую лунку на стадии промывки добавляли 100 мкл буфера для анализа (133,8 мМ NaCl (Sigma, S5886); 4,7 мМ KCl (Sigma, P3911); 1,25 мМ MgCl2 (Merck, 1.05833.0250); 3,5 мМ CaCl2 (Merck, 1.02083.0250); 5 мМ глюкозы (Sigma, G7021); 10 мМ Hepes (Sigma, H4034); pH 7,4)). Буфер для анализа удаляли и в лунки добавляли 100 мкл раствора исследуемого соединения в буфере для анализа в разных концентрациях. Затем в каждую лунку добавляли 100 мкл раствора красителя (0,09% (об./об.) индикаторного красителя для кальция, 9,1% (об./об.) усилителя сигнала (выпускающегося фирмой PBX Calcium Assay Kit); в буфере для анализа). Планшеты инкубировали в темноте при комнатной температуре в течение 60 мин. При этом 10 мкМ раствор иономицина в буфере для анализа (дополнительно содержащий 0,05% фетальной телячьей сыворотки (см. выше); 4°C) готовили и хранили в лунках 96-луночного микропланшета (96-луночный микропланшет, полипропиленовый, U-образной формы (Greiner Bio-One, 650201)). Мониторинг флуоресценции проводили с помощью 60 измерений с промежутками в 2 с. После пятого измерения в каждую лунку планшетов для исследования добавляли 50 мкл раствора иономицина и получали конечную концентрацию иономицина, равную 2 мкМ. Для определения значений IC50 минимальное значение интенсивности флуоресценции вычитали из максимального значения интенсивности флуоресценции для пятнадцатого - пятьдесят пятого измерений. Расчет значений IC50 с помощью выраженного в процентах ингибирования оттока Ca2+ кальция из клеток (прямой режим), вызванного исследуемым соединением, проводили с помощью Biost@t Speed 2.0. Результаты, полученные для соединений, предлагаемых в настоящем изобретении, приведены в таблице 2. "NCX1fw IC50" в таблице 2 означает значение IC50 (в мкМ (микромоль/литр)) для ингибирования NCX1 в прямом режиме.
B) Методика in vivo для исследования влияния на сократительную способность сердца
Взрослых самцов крыс Sprague-Dawley (Harlan Winkelmann, Borchen, Germany) массой от 340 до 370 г анестезировали пентобарбиталом (100 мг/кг внутрибрюшинно) и им давали дышать смесью кислорода (40%) и комнатного воздуха (60%) при дыхательном объеме, равном 1 мл/100 г при 60 вдох/мин. Температуру тела поддерживали равной 36,5±0,3°C с помощью нагревательной лампы и за ней следили с помощью ректального термодатчика. Системное артериальное давление измеряли в левой сонной артерии датчиком давления (Combitrans; B. Braun Melsungen AG, Melsungen, Germany), соединенным с мостовым усилителем постоянного тока (PLUGSYS/ADC Type 663; Harvard Apparatus GmbH, March-Hugstetten, Germany). Электрокардиограмму снимали в виде отведения II с помощью подкожно введенных пластинчатых электродов, соединенных с модулем для измерения частоты сердечных сокращений (PLUGSYS/HRM Type 669; Harvard Apparatus GmbH, March-Hugstetten, Germany). В правую сонную артерию в левом желудочке помещали катетер с микронаконечником (2 French, SPR-320; Millar Instruments, Houston, TX, USA) и непрерывно измеряли давление в левом желудочке (LVP) и конечно-диастолическое давление (EDP). Регистрацию гемодинамических данных проводили с помощью аналогово-цифрового преобразователя, соединенного с персональным компьютером, с использованием программного обеспечения Notocord (HEM version 3.5). Сократительную способность (dp/dtmax) и релаксацию (dp/dtmin) левого желудочка рассчитывали по сигналу LVP. Для внутривенного введения исследуемых соединений вскрывали левую яремную вену и вводили катетер PP-50. Исследуемые соединения вводили с помощью внутривенной болюсной инъекции или с помощью внутривенного вливания с использованием насоса для вливаний (Unita; B. Braun Melsungen AG, Melsungen, Germany). Исследуемые соединения растворяли в смеси гликофурола (75%) и кремофора (25%) и раствор дополнительно разбавляли дистиллированной водой (1:4). В типичном эксперименте последовательно вводили несколько доз исследуемого соединения с увеличением дозы. Статистическую значимость полученных данных по сравнению с контрольными экспериментами, при которых вводили растворитель, определяли с использованием двустороннего критерия ANOVA (программа Everstat). Данные по увеличению сократительной способности левого желудочка (увеличение в процентах) соединениями примеров приведены в таблице 3 при сопоставлении с контрольными экспериментами, при которых вводили растворитель.
Реферат
Изобретение относится к соединению формулы I в любой из его стереоизомерных форм или смеси стереоизомерных форм в любом соотношении, или его фармацевтически приемлемым солям, которые обладают свойством ингибирования натрий-кальциевого обмена (NCX). В формуле I Ar означает фенил, который является незамещенным или содержит один или несколько одинаковых или разных заместителей R0; R0 выбран из группы, включающей галоген, (C-C)-алкил, (C-C)-алкил-O-, (C-C)-циклоалкил-O- и (C-C)-циклоалкил-(C-C)-алкил-O-; R1 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей фтор и (C-C)-алкил; R2 выбран из группы, включающей (C-C)-алкил, HO-, (C-C)-алкил-C(O)-O-, Het1-C(O)-O-, R5-N(R6)-, R7-C(O)-N(R8)-, R7-S(O)-N(R8)-, R9-N(R10)-C(O)-N(R8)- и R5-N(R6)-C(O)-, где (C-C)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20; R3 выбран из группы, включающей водород и (C-C)-алкил, где (C-C)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей, выбранных из фенила; или группы R2 и R3 вместе означают оксогруппу; R4 означает водород или один или несколько одинаковых или разных заместителей, выбранных из группы, включающей галоген и (C-C)-алкил; R5 и R6 независимо друг от друга выбраны из группы, включающей водород, (C-C)-алкил, (C-C)-алкенил, (C-C)-циклоалкил, Het1 и Het2, где (C-C)-алкил является незамещенным или содержит один или несколько одинаковых или разных заместителей R20, и (C-C)-циклоалкил и Het2 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R21, и фенил и Het1 все являются незамещенными или содержат один или несколько одинаковых или разных заместителей R22; R7 выбран из группы, включающей (C-C)-алкил, (C-C)-циклоалкил, фенил, Het1 и Het2; R8 выбран из водорода; R9 выбран из (C-C)-алкила; R10 выбран из водорода и (C-C)-алкила; R20 выбран из группы, включающей R24, фтор, HO-, (C-C)-алкил-O-, (C-C)-циклоалкил-O-, (HO)P(O)-O-, (C-C)-алкил-S(O)-, (C-C)-циклоалкил-S(O)-, R31-N(R32)-, R33-C(O)-N(R32)-, (C-C)-алкил-S(O)-N(R32)-, R31-N(R32)-C(O)-, R34-O-C(O)- и R31-N(R32)-S(O)-; R21 выбран из (C-C)-алкила, фтора, HO- и оксогруппы; R22 выбран из галогена, (C-C)-алкила, HO- и оксогруппы; R24 означает 3-6-членное кольцо, которое содержит 0-4 одинаковых или разных гетероатома, выбранных из азота, кислорода и серы; R33 выбран из (C-C)-алкила; R31, R32, R34 выбраны из водорода и (C-C)-алкила; Het1 означает 5-6-членный ароматический гетероцикл, содержащий 1-3 гетероатома, выбранных из азота, кислорода и серы; Het2 означает 4-6-членный гетероцикл, содержащий 1 или 2 гетероатома, выбранных из азота, кислорода и серы; n выбран из 0, 1 и 2; p и q выбраны из 0 и 1. Изобретение относится также к фармацевтической композиции и применению указанных соединений для приготовления лекарственного средства для ингибирования NCX. 3 н. и 10 з.п. ф-лы, 3 табл., 306 пр.
Формула
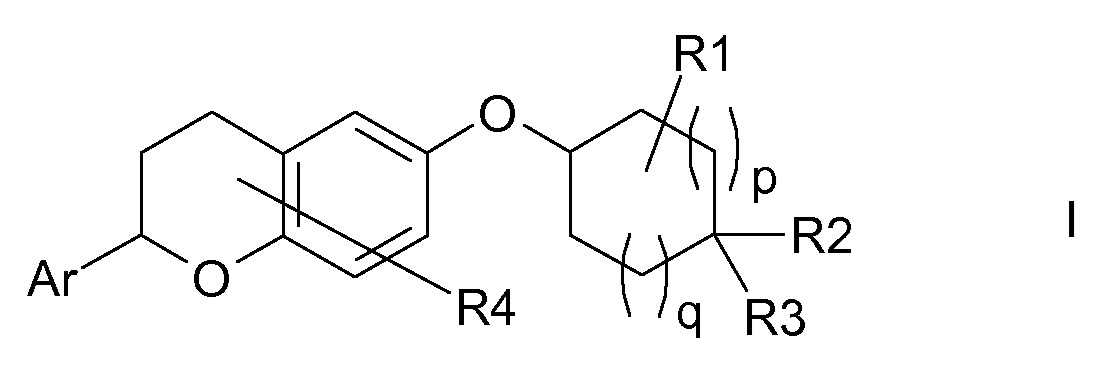
Документы, цитированные в отчёте о поиске
Бензопирановое соединение

Комментарии