Замещенные арилтиоалкилтиопиридины, способ их получения, лекарственное средство на их основе и способ получения лекарственного средства. - RU2154062C2
Код документа: RU2154062C2
Чертежи
















Описание
Изобретение относится к соединениям, которые должны применяться в фармацевтической промышленности в качестве биологически активных веществ для получения лекарственных средств.
Известный уровень техники
В европейской патентной заявке 150586 закрываются 2-(пиридилметилтио-, соответственно, -сульфинил) бензимидазолы, которые в пиридиновой части молекулы в положении
4, среди прочего, могут быть
замещены алкилтио- или арилтиоостатками. Для описанных соединений указывается длительное подавление выделения кислоты желудочного сока.
В международной патентной заявке ВОИС-89/03830 описывается, что те же самые, а также другие подобные по структуре соединения должны быть пригодны для лечения остеопороза.
В международной патентной заявке ВОИС -92/12976 описываются определенным образом замещенные 2-(пиридилметилтио-, соответственно, -сульфинил) бензимидазолы, которые должны быть эффективны против Helicobacter - бактерий, и далее для них раскрыто, что они должны быть пригодны для предотвращения и лечения целого ряда заболеваний желудка.
Описание изобретения
Предметом изобретения являются
соединения формулы (I) (см. прилагаемый
формульный лист), где
R1 обозначает водород, (C1-C4)-алкил или (C1-C4)-алкоксил;
R2 обозначает
водород, (C1-C4
)-алкил, (C1-C4)-алкоксил, галоген, трифторметил, полностью или преобладающе замещенный фтором (C1-C4)-алкоксил,
хлордифторметокси-группу, 2-хлор-1,1,
2-трифторэтокси-группу или вместе с R3 при желании обозначает целиком или частично замещенную фтором (C1-C2)-алкилендиокси- или
хлортрифторэтилендиокси-группу;
R3
обозначает водород, полностью или преобладающе замещенный фтором (C1-C4)-алкоксил, хлордифторметокси-группу, 2-хлор-1,1,
2-трифторэтокси-группу или вместе с R2 при желании
обозначает целиком или частично замещенную фтором (C1-C2)-алкилендиокси- или хлортрифторэтилендиокси-группу;
R4
обозначает водород, (C1-C4)-алкил;
R5 обозначает водород, (C1-C4)-алкил или (C1-C4)- алкоксил;
R6 обозначает
замещенный с помощью R8 и R9 цикл или бицикл, который выбирает
из группы, состоящей из бензола, фурана, тиофена, пиррола, оксазола, изоксазола, тиазола, тиазолина, изотиазола, имидазола, имидазолина,
пиразола, триазола, тетразола, тиадиазола, оксадиазола,
пиридина, пиpидин-N-oкcидa, пиримидина и бензимидазола;
R7 обозначает водород, (C1-C4)-алкил или (C1
-C4)-алкоксил;
R8 обозначает водород,
(C1-C4)-алкил, гидроксил, (C1-C4)-алкоксил, галоген, нитро-группу, карбоксил, (C1
-C4)-алкоксикарбонил, гуанидино-группу, замещенный с
помощью R10 (C1-C4)-алкил или -N(R11)R12;
R9 обозначает водород, (C1-C4)-алкил,
(C1-C4)-алкоксил, фтор или трифторметил;
R10 обозначает гидроксил, (C1-C4)-алкоксил, карбоксил, (C1-C4)-алкоксикарбонил или
-N(R11)R12, причем
R11 обозначает водород, (C1
-C4)-алкил или -CO- R13 и
R12 обозначает водород или (C1-C4)-алкил, или причем
R11 и R12 вместе и при включении атома азота, с которым оба связаны,
представляют собой пиперидиновый или морфолиновый остаток;
R13 обозначает водород, (C1-C4)-алкил
или (C1-C4)-алкоксил;
"m" обозначает
число 2 - 7;
"n" обозначает число 0 или 1;
"p" обозначает число 0 или 1 и
"q" обозначает число 0 или 1
и их соли;
(C1-C4)-алкил обозначает
линейные или разветвленные алкильные остатки с 1-4 C-атомами. В качестве примера следует назвать бутильный, изобутильный, втор.
-бутильный, трет. -бутильный, пропильный, изопропильный, этильный и
метильный остаток.
(C1-C4)-алкоксил обозначает остаток, который наряду с атомом кислорода содержит один из вышеуказанных (C1-C4)-алкильных остатков. В качестве примера следует назвать метокси- и этокси-остаток.
Галогеном в смысле настоящего изобретения является бром, хлор и фтор.
В качестве полностью или преобладающе замещенного фтором (C1-C4)-алкоксила следует назвать, например, 1,2, 2-трифторэтокси-, 2,2,3,3,3-пентафторпропокси-, перфторэтокси- и в особенности 1,1,2,2, -тетрафторэтокси-, трифторметокси-, 2,2,2-трифторэтокси- и дифторметокси-остаток.
В качестве целиком или частично замещенной фтором (C1-C2)-алкилендиокси-группы следует, например, назвать метилендиокси- (-O-CH2-O-), этилендиокси-(-O-CH2-CH2-O-), 1,1-дифторэтилендиокси-(-O-CF2-CH2-O-), 1,1,2, 2- тетрафторэтилендиокси-(-O-CF2-CF2-O-) и в особенности дифторметилендиокси-(-O-CF2 -O-) остаток.
Если R2 и R3 при желании вместе обозначают целиком или частично замещенный фтором (C1-C2)-алкилендиокси- или хлортрифторэтилендиокси-остаток, то заместители R2 и R3 в соседних положениях - предпочтительно в положениях 5 и 6 - связаны с бензольной частью бензимидазольного кольца.
Группа -S(O)q связана с атомом углерода соответствующего цикла, соответственно бицикла R6, так что в качестве остатков R6, например, следует назвать остатки: фенил, 2-фурил, 3-фурил, 2-тиенил, 3-тиенил, 3-пирролил, 2-оксазолин, 4-оксазолил, 4-изоксазолил, 5-изоксазолил, 2-тиазолил, 3-изотиазолил, 2-имидазолил, 3-пиразолил, 4-пиразолил, 1,2,3-триазол-4-ил, 1,2,5-тиадиазол-4-ил, 1,2,4-триазол-3-ил, тетразол-5-ил, 1,3, 4-тиадиазол-2-ил, 1,2,3-тиадиазол-4-ил, 1,3,4-оксадиазол-2-ил, 2-пиридил, 4-пиридил, 2-пиримидинил и 2-бензимидазолил.
Заместители R8 и в случае необходимости R9 в циклах, соответственно, бициклах R6 могут быть связаны с любым возможным положением. В качестве, например, замещенных остатков R6 следует назвать: 4-метилфенил, 3-диметиламинометилфенил, 3-пиперилинометилфенил, 3-карбоксиметилфенил, 2-диметиламинометил-5-метил-3-фурил, 1-метилпиррол-3-ил, 4, 5-диметил-оксазол-2-ил, 3,5-диметил-изоксазол-4-ил, 4,5-диметил-тиазол-2-ил, 4-метил-5-карбоксиметил-тиазол-2-ил, 1-метил-имидазол-2-ил, 1-метил-пиразол-3-ил, 1-(2-диметиламиноэтил)-пиразол-3-ил, 5-метил-1,3,4-оксадиазол-2-ил, 1-метил-1,2,3-триазол-4-ил, 1-метил-1,2, 4-триазол-3-ил, 1-(2-диметиламиноэтил)-1,2,3-триазол-4-ил, 1-метил-тетразол-5-ил, 1-(2-диметиламиноэтил)-тетразол-5-ил, 1-карбоксиметил-тетразол-5-ил, 5-метил-1,3,4-тиадиазол-2-ил, 5-трифторметил-1, 3,4-диадиазол-2-ил, 1-(2-гидроксиэтил)-тетразол-5-ил, 2-амино-1,3,4-тиадиазол-2-ил, 3-амино-1,2,4-триазол-5-ил, 4-метил-5-трифторметил-1,2,4-триазол-3-ил и 4-амино-пиримидин-2-ил.
В
качестве остатков -CmH2m, которые замещены с помощью
R6-S(O)q-, принимают во
внимание линейные или разветвленные остатки. В качестве примера следует назвать
гептильный, изогептильный (2-метил-гексильный), гексильный, изогексильный
(2-метил-пентильный), неогексильный (2,
2-диметилбутильный), пентильный, изопентильный (3-метил-бутильный), неопентильный (2,
2-диметилпропильный), бутильный, изобутильный, втор.-бутильный,
трет.-бутильный, пропильный, изопропильный и
этильный остаток. В качестве, например, остатков R6-S(O)q-CmH2m следует назвать:
фенилтиопентил; фенилтиоэтил;
фенилтиопропил; фенилтиобутил;
4-метил-фенилтиоэтил; 4-метил-фенилтиопропил; 3-диметиламинометил-фенил-тиоэтил;
3-диметил-аминометил-фенил-тиопропил; 3-пиперидинометил-фенил-тиоэтил;
3-пиперидинометил-фенилтиопропил;
3-пиперидино-метил-фенил-тиобутил; 1-метил-пиррол-3-тиоэтил; 4,
5-диметилоксазол-метил-фенил-тиобутил; 1-метил-пиррол-3-тиоэтил; 4,5-диметилоксазол-2-тиопропил; 3,
5-диметил-изоксазол-5-тиоэтил; 3,
5-диметил-изоксазол-5-тиопропил; тиазол-2-тиоэтил;
тиазол-2-тиопропил; тиазол-2-тиобутил; 4-метил-5-карбоксиметил-тиазол-2-тиопропил; 1-метил-имидазол-2-тиоэтил;
1-метилимидазол-2-тиопропил;
1-метилимидазол-2-тиобутил; имидазол-2-тиоэтил;
имидазол-2-тиопропил; пиразол-3-тиопропил; 1-(2-диметиламиноэтил)-пиразол-2-тиоэтил; 1,3,4-оксадиазол-2-тиоэтил; 1,3,
4-оксадиазол-2-тиопропил; 1,2,
3-триазол-4-тиоэтил; 1,2,3-триазол-тиопропил; 1,2,
3-триазол-4-тиобутил; 1-метил-1,2,3-триазол-4-тиоэтил; 1-метил-1,2,3-триазол-4-тиопропил; 1,2,3-триазол-4-тиоэтил; 1,2,
4-триазол-3-тиопропил;
3-амино-1,2,4-триазол-5-тиоэтил; 3-амино-1,2,
4-триазол-5-тиопропил; 4-метил-5-трифторметил-1,264-триазол-3-тиоэтил; 4-метил-5-трифторметил-1,2,4-триазол-3-тиопропил; 1-метил-1,
2,4-триазол-3-тиоэтил;
1-метил-1,2,4-триазол-3-тиопропил; 1-метил 1,
2,4-триазол-3-тиобутил; тетразол-5-тиоэтил; тетразол-5-тиопропил; тетразол-5-тиобутил; 1-метил-тетразол-5-тиоэтил;
1-метил-тетразол-5-тиопропил;
1-метил-тетразол-5-тиобутил;
1-(2-диметиламиноэтил)-тетразол-5-тиоэтил; 1-(2-диметиламиноэтил)-тетразол-5-тиопропил; 1-(2-гидроксиэтил)-тетразол-5-тиоэтил;
1-(2-гидроксиэтил)-тетразол-5-тиопропил; 1,3,
4-тиадиазол-2-тиоэтил; 1,3,
4-тиадиазол-2-тиопропил; 5-метил-1,3,4-тиадиазол-2-тиоэтил; 5-метил-1,3,4-тиадиазол-2-тиопропил; 5-метил-1,3,
4-тиадиазол-2-тиобутил; 5-трифторметил-1,3,4-тиадиазол-2-тиоэтил;
5-трифторметил-1,3,
4-тиадиазол-2-тиопропил; 1,2,3-тиа-диазол-4-тиоэтил; 1,2,3-тиадиазол-4-тиопропил;
1-карбоксиметил-тетразол-5-тиоэтил; 1-карбоксиметил-тетразол-5-тиопропил; 2-пиридил-тиоэтил;
2-пиридил-тиопропил;
2-пиридил-тиобутил; 4-пиридил-тиоэтил; 4-пиридил-тиопропил; 4-пиридил-тиобутил;
2-пиримидин-тиоэтил; 2-пиримидин-тиопропил; 2-пиримидин-тиобутил; 4-амино-пиримидин-2-тиоэтил;
4-амино-пиримидин-2-тиопропил; 2-бензимидазол-тиоэтил; 2-бензимидазол-тиопропил;
4-метил-тиазол-5-тиоэтил; 4-метил-тиазол-5-тиопропил; 4-метил-тиазол-5-тиобутил;
1-метоксикарбонилметилтетразол-5-тиоэтил; 1-метоксикарбонилметилтетразол-5-тиопропил;
1-метоксикарбонилметилтетразол-5-тиобутил; 5-нитроимидазол-1-тиоэтил; 5-нитроимидазол-1-тиопропил;
5-нитроимидазол-1-тиобутил; 2-метил-5-нитроимидазол-1-тиоэтил; 2-метил-5-нитроимидазол-1-тиопропил и
2-метил-5-нитроимидазол-1-тиобутил.
В качестве солей для соединений формулы (I), в которых "n" обозначает число, равное нулю, принимают во внимание любые соли присоединения кислот. Особо следует упомянуть фармакологически приемлемые соли обычно применяемых в галеновой промышленности неорганических и органических кислот. Фармокологически неприемлемые соли, которые, например, можно получать прежде всего при получении предлагаемых согласно изобретению соединений в промышленном масштабе в качестве технологических продуктов, с помощью известных специалисту способов переводят в фармакологически приемлемые соли. В качестве таковых пригодны водорастворимые и водонерастворимые соли присоединения кислот, как, например, соляная кислота, бромводородная кислота, фосфорная кислота, азотная кислота, серная кислота, уксусная кислота, лимонная кислота, D-глюконовая кислота, бензойная кислота, 2-(4-гидроксибензоил) бензойная кислота, масляная кислота, сульфосалициловая кислота, малеиновая кислота, лауриновая кислота, яблочная кислота, фумаровая кислота, янтарная кислота, щавелевая кислота, винная кислота, эмбоновая кислота, стеариновая кислота, толуолсульфокислота, метансульфокислота или 3-гидрокси-2-нафтойная кислота, причем, в зависимости от того, идет ли речь об одно- или многоосновной кислоте, и в зависимости от того, какая кислота желательна, кислоты при получении солей используют в эквимолярном или отклоняющемся от него количественном соотношении.
Для соединений формулы (I), в которых "n" обозначает число, равное 1, в качестве солей принимают во внимание также соли с основаниями. В качестве примеров основных солей следует упомянуть соли лития, натрия, калия, кальция, алюминия, магния, титана, аммония, меглумина или гуанидиния, причем также здесь при получении солей используют основания в эквимолярном или отклоняющемся от него количественном соотношении.
Предпочтительными соединения формулы (I) являются
такие, в которых:
R1 обозначает водород;
R2
обозначает водород, галоген или
метокси-группу;
R3 обозначает водород; R4 обозначает водород;
R5 обозначает водород,
(C1-C4)-алкил или (C1-C4)-алкоксил;
R6
обозначает замещенный с помощью R8 и R9 цикл, который выбирают из группы, состоящей из бензола, изоксазола,
тиазола, имидазола, триазола, тетразола, тиадиазола,
пиридина, пиридин-N-оксида, пиримидина
и бензимидазола;
R7 обозначает водород или (C1-C4)-алкил;
R8
обозначает водород, (C1-C4)-алкил,
гидроксил, нитро-, гуанидино-группу,
карбоксил, (C1-C4)-алкоксикарбонил, замещенный с помощью R10 (C1-C4)-алкил или амино-группу;
R9 обозначает
водород или (C1-C4
)-алкил;
R10 обозначает гидроксил, карбоксил, (C1-C4)-алкоксикарбонил
или -N(R11) R12, причем
R11 обозначает водород,
(C1-C4)-алкил или
-CO-R13; и
R12 обозначает водород или (C1-C4)-алкил или причем
R11 и R12 вместе и при включении атома азота, с которым
оба связаны, представляют собой
пиперидиновый остаток;
R13 обозначает водород, (C1-C4)-алкил или (C1
-C4)-алкоксил;
"m" обозначает число
2 - 4;
"n" обозначает
число 0 или 1;
"p" обозначает число 0 и
"q" обозначает число 0;
и их соли.
Особенно предпочтительными соединениями формулы
(I) являются такие, в которых
R1 обозначает водород;
R2 обозначает водород, фтор или метокси-группу;
R3 обозначает
водород;
R4 обозначает водород;
R5
обозначает (C1-C4
)-алкил или (C1-C4-алкоксил;
R6 обозначает замещенный с помощью R8 и R9 цикл,
который выбирают из группы, состоящей из бензола,
тиазола, имидазола, триазола, тетразола,
тиадиазола, пиридина, пиримидина и бензимидазола;
R7 обозначает водород;
R8 обозначает
водород, (C1-C4)-алкил,
гидроксил, нитро-, гуанидино-группу, карбоксил,
(C1-C4)-алкоксикарбонил или замещенный с помощью R10 метил или этил;
R9
обозначает водород или (C1-C4)-алкил;
R10 обозначает гидроксил,
карбоксил или -N(R11)R12,
причем
R11 обозначает (C1-C4)-алкил
и
R12 обозначает (C1
-C4)-алкил, или причем
R11 и R12
вместе и при включении атома азота, с которым оба связаны, представляют собой пиперидиновый остаток;
"m" обозначает число 2-4;
"n" обозначает число, равное 0;
"p" обозначает
число, равное 0;
"q" обозначает число, равное 0,
и их соли.
Другими
предпочтительными соединениями формулы
(I) являются такие, в которых
R1 обозначает
водород;
R2 обозначает водород или фтор;
R3 обозначает водород;
R4 обозначает
водород;
R5 обозначает (C1-C4)-алкил или (C1-C4)-алкоксил;
R6 обозначает замещенный с помощью R8 и R9 цикл, который выбирают из группы,
состоящей из бензола, тиазола,
имидазола, триазола, тетразола, тиадиазола, пиридина, пиримидина
и бензимидазола;
R7 обозначает водород;
R8 обозначает водород, метил, нитро-группу,
(C1-C4
)-алкоксикарбонил или замещенный с помощью R10 метил или этил;
R9 обозначает водород;
R10 обозначает гидроксил, карбоксил или - N(R11)R12, причем
R11 обозначает метил и
R12 обозначает метил, или причем
R11 и R12 вместе и при
включении атома азота, с которым оба связаны, представляют собой пиперидиновый остаток;
"m"
обозначает число 2-4;
"n" обозначает число, равное 0;
"p" обозначает число,
равное 0;
"q" обозначает число, равное 0,
и их соли.
Другими особенно
предпочтительными
соединениями формулы (I) являются такие, в которых
R1 обозначает
водород;
R2 обозначает водород;
R3 обозначает водород;
R4 обозначает водород;
R5
обозначает (C1-C4)-алкил или (C1-C4
)-алкоксил;
R6 обозначает замещенный с помощью R8 и R9 цикл, который выбирают из группы, состоящей из
бензола,
тиазола, имидазола, триазола, тетразола, тиадиазола, пиридина, пиримидина;
R7 обозначает водород;
R8 обозначает водород, метил или замещенный с помощью R10-метил или этил;
R9 обозначает водород;
R10 обозначает карбоксил или -N(R11) R12,
причем
R11 обозначает метил и;
R12 обозначает метил;
"m" обозначает число 2-4;
"n"
обозначает число, равное 0;
"p" обозначает число, равное 0; и
"q" обозначает число, равное 0,
и их соли.
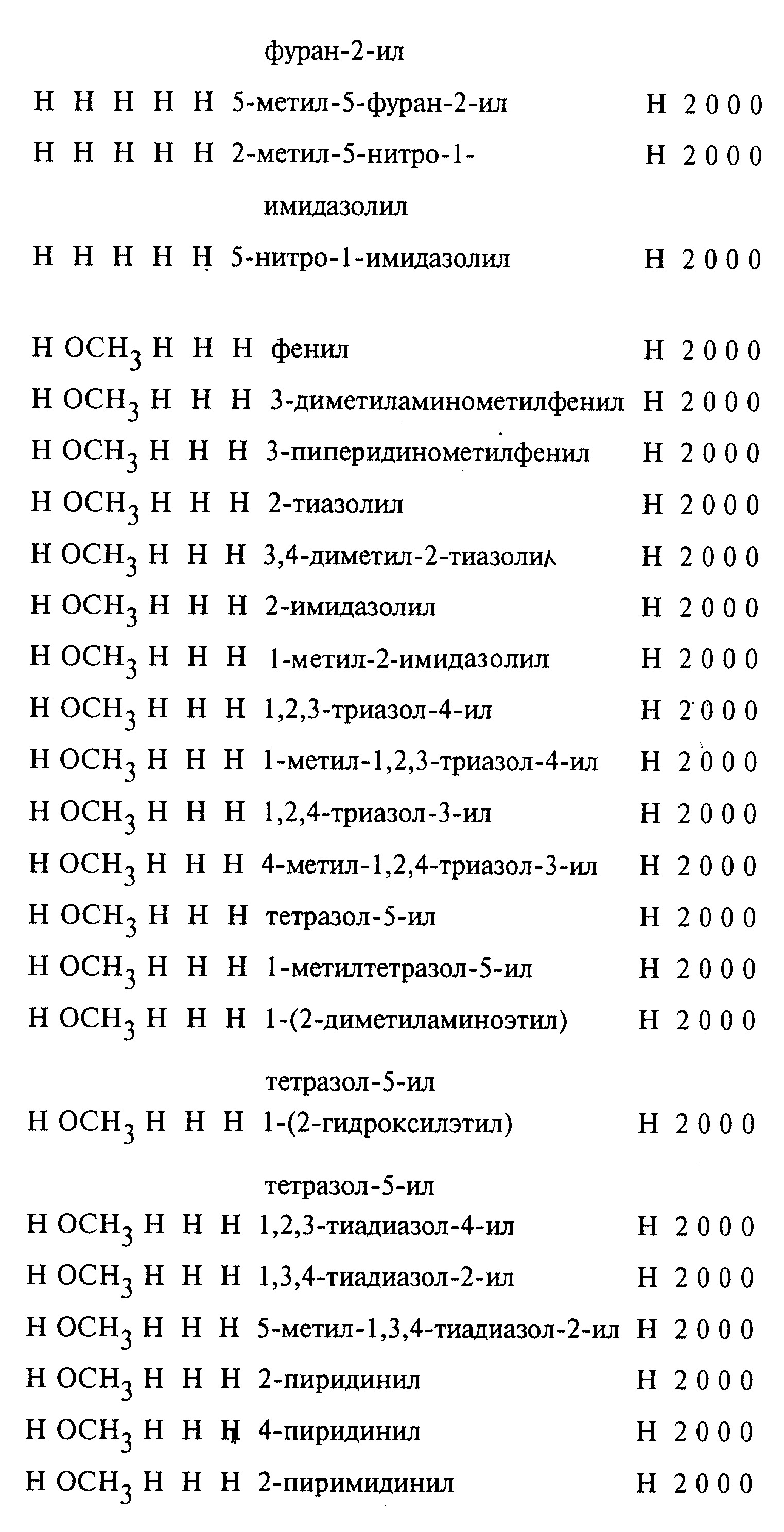
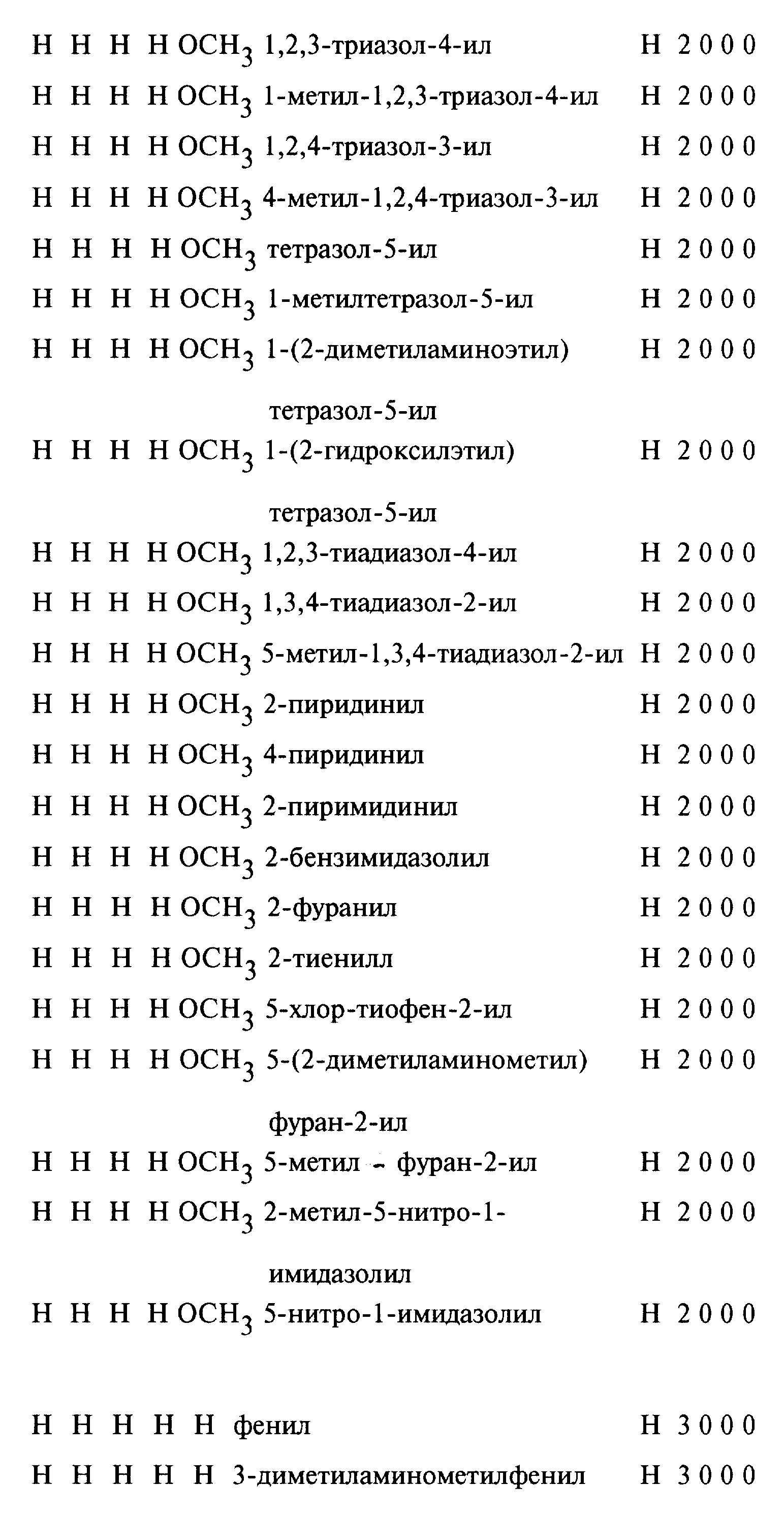
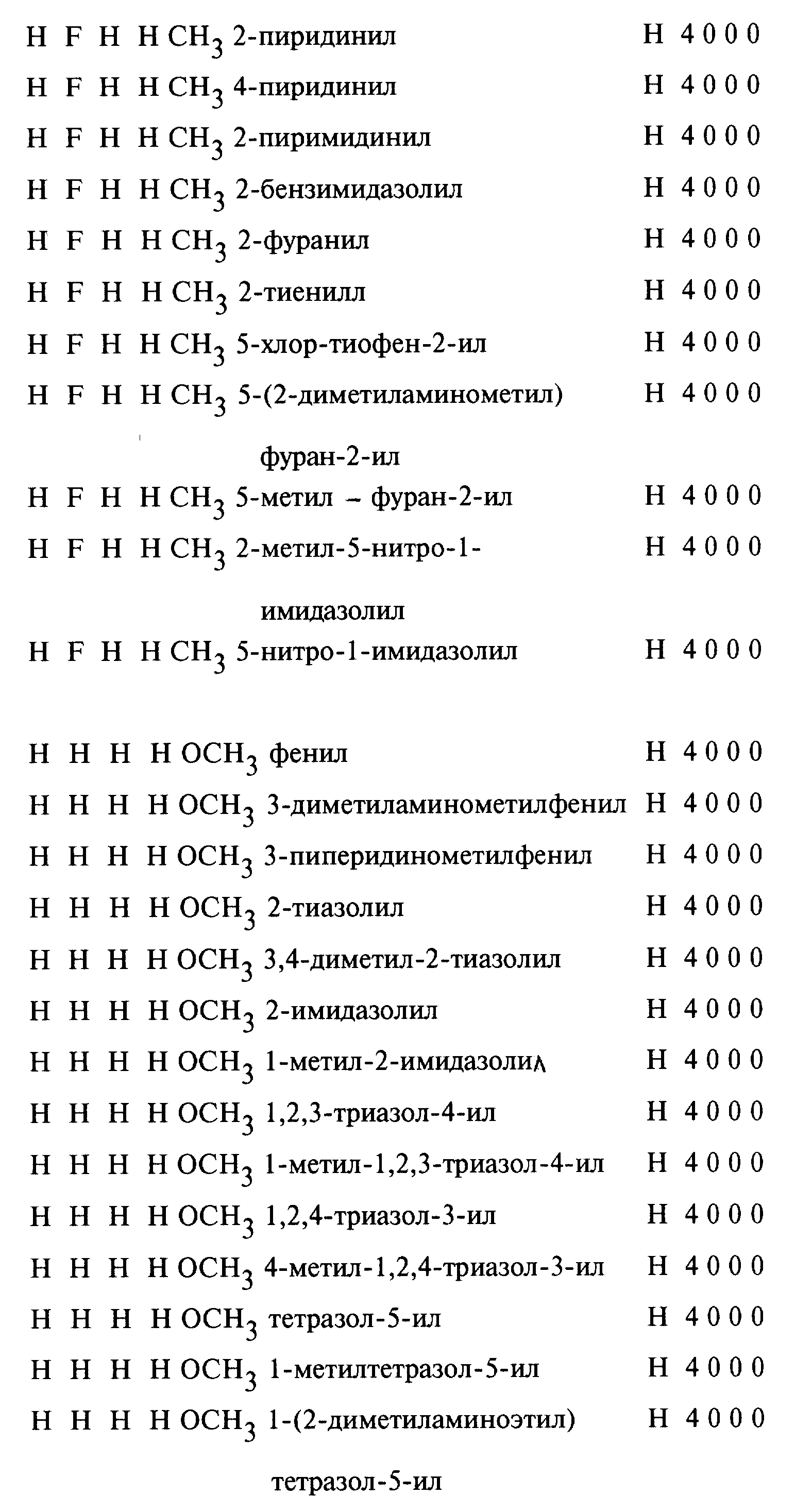
Предлагаемые согласно изобретению, приводимые в качестве примеров соединения представлены в Таблице 1 (в конце описания), причем заместитель R1 находится в положении 5, соответственно 6, а заместитель R2 находится в положении 6, соответственно 5 (из-за таутомерии в бензимидазольном кольце в случае R4=H положения 5 и 6 не различаются).
Другим предметом изобретения является способ получения соединений формулы (I), где R1, R2, R3 и R4, R5, R6, R7, "m", "n", "p" и "q" имеют вышеуказанные значения, и их солей.
Способ отличается тем, что
а) меркаптобензимидазолы формулы (II (см. прилагаемый
формульный
лист), где R1, R2, R3 и R4 имеют указанные значения, вводят во
взаимодействие с пиколиновыми производными формулы (III) (см. прилагаемый формульный лист), где R5, R6, R7 и "m", "p" и "q"
имеют
вышеуказанные значения и X представляет собой пригодную удаляемую
группу; или
б) соединения формулы (IV) (см. прилагаемый формульный лист), где R1, R2, R3, R4, R5, R7 и "m" имеют
вышеуказанные значения, "n" и "p" обозначают числа, равные 0, и Y представляет
собой пригодную удаляемую группу, вводят во взаимодействие с тиолами R6 - SH; и (в случае, если соединения формулы (I)
с
"n"=1, соответственно, "p" = 1 и/или "q"= 1 представляют собой желательные
целевые продукты) затем полученные по п. п. а) или б) соединения с "n" = 0 и/или "p" = 0 и/или "o" = 0 окисляют;
и/или полученные соединения при желании затем переводят в соли;
и/или
полученные соли при желании затем переводят в свободные соединения.
При вышеуказанном взаимодействии исходные соединения можно применять как таковые или в случае необходимости в форме их солей.
В качестве пригодных удаляемых групп X, соответственно Y, например, следует назвать атомы галогенов, в особенности хлор, или активированные за счет этерификации до сложного эфира (например, с помощью n-толуолсульфокислоты) гидроксильные группы.
Взаимодействие соединения формулы (II) с соединением формулы (III) осуществляют в пригодных, предпочтительно полярных протонных или апротонных растворителях (как метанол, этанол, изопропанол, диметилсульфоксид, ацетон, диметилформамид или ацетонитрил) при добавке или при исключении воды. Это взаимодействие осуществляют, например, в присутствии акцептора протонов. В качестве таковых пригодны гидроксиды щелочных металлов, как гидроксид натрия; карбонаты щелочных металлов, как карбонат калия; или третичные амины, как пиридин, триэтил, амин или этилдиизопропиламин. Альтернативно, взаимодействие также можно осуществлять без акцептора протонов, причем - в зависимости от рода исходных соединений - в случае необходимости прежде всего могут выделяться соли присоединения кислот в особенно чистой форме. Температура реакции может составлять 0-150oC, причем в присутствии акцепторов протонов предпочтительны температуры в пределах 20-80oC, а без акцепторов протонов - 60-120oC, в особенности температура кипения используемых растворителей. Времена реакций составляют 0, 5-30 часов.
Взаимодействие соединений формулы (IV) с тиолами R6-SH осуществляют подобным образом, как и взаимодействие соединений формулы (II) с соединениями формулы (III).
Окисление сульфидов (соединения формулы (I) с "n"=0) до сульфоксидов (соединения формулы (I) с "n" = 1) осуществляют в условиях, которые известны специалисту для окисления сульфидов до сульфоксидов (см. на этот счет, например, J. Drabowicz и М. Mikolajczyk, Organic preparations and procedures int. 14 (1-2), 45-89 (1982) или E.Block в S.Patal, The Chemistry of Functional Groups, дополнение E. , часть I, с. 539-608, John Wiley and Sons (Международная публикация, 1980). В качестве окислителей принимают во внимание все обычно применяемые для окисления сульфидов до сульфоксидов реагенты, в особенности надкислоты, как, например, надуксусная кислота, трифторнадуксусная кислота, 3, 5-динитро-надбензойная кислота, надмалеиновая кислота, перосифталат магния или предпочтительно м-хлор-надбензойная кислота.
Температура реакции (в зависимости от реакционноспособности окислителя и степени разбавления) составляет от -70oC до температуры кипения применяемого растворителя, предпочтительно, однако, от -30oC до +20oC. Как предпочтительное также оказывается окисление с помощью галогенов, соответственно, с помощью гипогалогенитов (например, с помощью водного раствора гипохлорита натрия), которое целесообразно осуществляют при температурах 0 - 50oC. Реакцию целесообразнее осуществлять в инертных растворителях, например, в ароматических или хлорированных углеводородах, как бензол, толуол, дихлорметан или хлороформ, предпочтительно в сложных или простых эфирах, как этилацетат, изопропилацетат или диоксан, или в спиртах, предпочтительно в изопропаноле.
Предлагаемые согласно изобретению сульфоксиды представляют собой оптически активные соединения. В зависимости от рода заместителей в молекуле могут быть еще другие центры хиральности. Изобретение поэтому охватывает как энантиомеры и диастереомеры, так и их смеси и рацематы. Энантиомеры само по себе известным образом (например, путем получения и разделения соответствующих диастереоизомерных соединений) можно разделять (см., например, ВОИС-92/08716).
Соединения формулы (II) известны, например, из ВОИС-86/02646, европейского патента 134400 или европейского патента 127763. Соединения формулы (III) с "p" = 0, соответственно, "q" = 0 можно получать, например, так как описывается в нижеследующих примерах.
Для получения соединений формулы (III) с "p" = 1, соответственно "q" = 1, соответствующие 2-гидрокси-метил-4-меркаптозамещенные пиридины, например, окисляют с помощью м-хлорнадбензойной кислоты до сульфоксидов и затем хлорируют, например, с помощью тионилхлорида. Взаимодействие с 2-меркаптобензимидазорами дает соединения формулы (1) с "p" = 1 и "q" = 1.
В зависимости от рода заместителей R6 сульфоксиды с "q" = 1 получают также при окислении до сульфоксидов с "n" = 1. Впрочем, соответствующие сульфиды, соответственно сульфоксиды, можно получать путем выбора пригодных исходных соединений, соответственно, благодаря применению селективных окислителей.
Необходимые для получения соединений формулы (III) тиолы R6-CmH2m - SH можно получать, например, из соответствующих галоидных соединений аналогично J. Med. Chem. 14 (1971) 349.
Следующие примеры поясняют подробнее изобретение, не ограничивая его объема охраны. Предлагаемые согласно изобретению соединения и исходные соединения можно получать аналогичным путем, как описывается в примерах.
ПРИМЕРЫ
Целевые продукты
1. 2-{ /[3-Метил-4-(3-(5-метил-1,3,
4-тиадиазол-2-ил-тио)пропилтио)-2-пиридинил]метил/тио}-1H-бензимидазол
К раствору 5-метил-1,3,4-тиадиазол-2-тиола (0,16 г; 1,2
ммоль) в 10 мл этанола и 1,4 мл 1н. раствора гидроксида натрия
добавляют 2-{/[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил/тио}-1H-бензимидазол (36 г, 1,0 моль) и кипятят с обратным холодильником в
течение 20-30 часов. Прикапывают 12 мл H2O,
оставляют охлаждаться, отфильтровывают выделившееся твердое вещество, промывают водой и сушат в вакууме при 50oC. Получают 0,38 г (83%
от теории) целевого соединения в виде бесцветного
твердого вещества с т. пл. 76-77oC.
2. 2-{ /[3-Метил-4-(3-(4-метил-1,2,
3-триазол-3-ил-тио)пропилтио)-2-пиридинил]метил/тио}-1H-бензимидазол
Согласно указанной в
примере 1 методике путем взаимодействия 4-метил-1,2,4-триазол-3-тиола (0,19 г; 1,6 ммоль) с
2-{/[4-(3-хлор-пропилтио)-3-метил-2-пиридинил] метил/тио} -1Н- бензимидазолом (0,36 г, 1,0 ммоль) и 1,7
ммоль 1н. раствора гидроксида натрия получают неочищенное целевое соединение (содержащее воду).
После кристаллизации из смеси этилацетата с диизопропиловым эфиром получают целевое соединение в виде
бесцветного твердого вещества с т. пл. 98-99oC (выход 58% от теории).
3. 2-{ /[3-Метил-4-(3-(1-метилимидазол-2-ил-тио)пропилтио)-2-пиридинил] метил/тио}-1H-бензимидазол
Согласно указанной в примере 1 методике, путем взаимодействия 2-меркапто-1-метилимидазола с
2-{ /[4-(3-хлорпропилтио)-3- метил-2-пиридинил] метил/тио}-1Н-бензимидазолом и NaOH, после
кристаллизации из этилацетата с диизопропиловым эфиром получают целевое соединение (68% от теории) в виде
бесцветного твердого вещества с т.пл. 97-99oC.
4.
2-{/[4[3-(3-Амино-1,2,4-триазол-5-ил-тио)пропилтио)-3- метил-2-пиридинил]метил/тио}-1H-бензимидазол
Согласно
указанной в примере 1 методике, путем взаимодействия 3-амино-5-меркапто-1,2,
4-триазола с 2-{/[4-(3-хлорпропилтио)-3-метил-2- пиридинил] метил/тио}-1Н-бензимидазолом и NaOH получают целевое соединение
(82% от теории) в виде бесцветного твердого вещества с т. пл. 94-96oC.
5. 2-{/[4[3-(5-Амино-1,3,
4-тиадиазол- 2-ил-тио)пропилтио]-3-метил-2-пиридинил]метил/тио}-1H-бензимидазол
Согласно указанной в примере 1 методике, путем
взаимодействия 2-амино-5-меркапто-1,3,4-тиадиазола с
2-{/[4-(3- хлорпропилтио)-3-метил-2-пиридинил] метил/тио}-1Н- бензимидазолом и NaOH получают неочищенное целевое соединение в виде масла. Путем
растворения в изопропаноле, смешивания с
концентрированной соляной кислотой (примерно 5 эквивалентов), полного концентрирования и растирания с ацетоном получают целевое соединение в виде
тригидрохлорида; бесцветное твердое вещество; при
105oC газовыделение; выше 240oC разложение.
6. 2-{ /[4-(3-Имидазол-2-ил-тио-пропилтио)-3-метил-2- пиридинил]
метил/тио}-1H-бензимидазол
Согласно
указанной в примере 1 методике, путем взаимодействия 2-меркаптоимидазола с 2-{ /[4-(3-
хлорпропилтио)-3-метил-2-пиридинил]метил/тио}-1H- бензимидазолом
и
NaOH, после кристаллизации из смеси метанола
с толуолом получают целевое соединение (62% от теории); бесцветное твердое вещество с т. пл. 195oC (разложение).
7.
2-{/[3-Метил-4-(3-(3-1,2,
4-триазол-3-ил-тио)пропилтио)-2-пиридинил] метил/тио}-1H-бензимидазол
Согласно указанной в примере 1 методике, путем взаимодействия 3-меркапто-1,2,4-триазола с 2-{
/[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил/тио} -1Н- бензимидазолом и NaOH, получают целевое соединение (76% от теории); бесцветное твердое вещество с т. пл. 80-82oC.
8.2-{ /[3-Метил-4-(3-(1-метил-тетразол-5-ил-тио)пропилтио)-2-пиридинил] метил/тио}-1H-бензимидазол
Согласно указанной в примере 1 методике, путем взаимодействия 1
метил-5-меркапто-тетразола
с
2-{ /[4-(3- хлорпропилтио)-3-метил-2-пиридинил]метил/тио} -1H- бензимидазолом и NaOH получают целевое соединение (68% от теории); бесцветное твердое вещество с т. пл.
99-100oC.
9. 2-{/[3-Метил-4-(3-(тиазол-2-ил-тио)пропилтио)-2-пиридинил] метил/тио} -1H-бензимидазол
Согласно указанной в примере 1 методике, путем взаимодействия 2
меркаптотиазола с 2-{
/[4-(3-хлорпропилтио)-3- метил-2-пиридинил]метил/тио}-1H-бензимидазолом и NaOH получают целевое соединение (63% от теории); бесцветное твердое вещество с т. пл. 121-123oC.
10. 2-{ /[3-Метил-4-(3-(пиридин-2-ил-тио)пропилтио)-2-пиридинил] метил/тио}-1H-бензимидазол
Согласно указанной в примере 1 методике, путем взаимодействия 2
меркаптопиридина с 2-{
/[4-(3-хлорпропилтио)-3-метил-2-пиридинил]метил/тио}-1H-бензимидазолом и NaOH получают целевое соединение (87% от теории); бесцветное твердое вещество с т. пл. 97-99oC.
11.
2-{/[3-Метил-4-(3-(пиримидин-2-ил-тио)пропилтио)-2-пиридинил]метил/ тио}-1H-бензимидазол
Согласно указанной в примере 1 методике, путем взаимодействия 2
меркаптопиримидина с
2-{/[4-(3-хлорпропилтио)-3-метил-2-пиридинил]метил/тио}-1H-бензимидазолом и NaOH получают целевое соединение в виде моногидрата (92% от теории); бесцветное твердое вещество с т.
пл. 118-119o
C.
12. 2-{ /[4-/(3-Бензимидазол-2-ил тио)пропилтио/-3-метил-2-пиридинил] метил/тио}-1H-бензимидазол
Согласно указанной в примере 1 методике, путем
взаимодействия 2
меркаптобензимидазола с 2-{ /[4-(3-хлорпропилтио)-3-метил-2- пиридинил] метил/тио} -1H-бензимидазолом и NaOH получают целевое соединение (62% от теории); бесцветное твердое вещество
с т. пл.
177-180oC (разложение).
13. 2-{ /[3-Метил-4-(3-фенилтио-пропилтио)-2-пиридинил] метил/тио} -1H- бензимидазол
Согласно указанной в примере 1 методике,
путем
взаимодействия тиофенола с 2-{/[4-(3-хлорпропилтио)-3-метил-2- пиридинил]метил/тио}-1H-бензимидазолом и NaOH получают целевое соединение (95% от теории); бесцветное твердое вещество с т. пл.
141-143oC.
14. 2-{/[3-Метил-4-(3-(пиридин-1-оксо-2-ил-тио)пропилтио)-2-пиридинил] метил/тио} -1H-бензимидазол-дигидрохлорид
Согласно указанной в примере 1
методике,
путем взаимодействия 2-меркаптопиридин-N-оксида с 2-{/[4-(3- хлорпропилтио)-3-метил-2-пиридинил]метил/тио} -1H- бензимидазолом и NaOH получают целевое соединение в виде вязкого масла.
Экстрагируют
дихлорметаном, сушат над карбонатом калия, полностью концентрируют (досуха), остаток растворяют в изопропаноле, смешивают с 3 эквивалентами концентрированной соляной кислоты и
перегоняют.
Образовавшееся твердое вещество отфильтровывают и сушат в вакууме над KOH. Получают целевое соединение (66% от теории); бесцветное твердое вещество с т. пл. 71-73oC
(разложение).
15. 2-{/[3-Метил-4-(2-(пиридин-2-ил-тио)этилтио)-2-пиридинил] метил/тио} -1H-бензимидазол
Согласно указанной в примере 1 методике, путем взаимодействия
2-меркаптопиридина с
2-{/[4-(2- хлорэтилтио)-3-метил-2-пиридинил/метил/тио}-1H- бензимидазолом и раствором гидроксида натрия, после кристаллизации из изопропанола, получают целевое соединение (72%
от теории) в виде
бесцветного твердого вещества с т. пл. 145-147oC.
16. 2-{
/[3-Метил-4-(3-(4-метил-пиримидин-2-ил-тио)пропилтио)- 2-пиридинил]метил/тио}-1H-бензимидазол
Согласно
указанной в примере 1 методике, путем взаимодействия с 2-меркапто-4-метилпиримидином,
получают целевое соединение; бежевого цвета твердое вещество; т. пл. 70-72oC; выход = 77% от
теории.
17.
2-{/[4/3-(1-(2-Диметиламииноэтил)тетразол-5-ил-тио)пропилтио)-3- метил-2-пиридинил]метил/тио}-1H-бензимидазол-тригидрохлорид
Согласно описанной в примерах 14 и 1
методике,
путем
взаимодействия с 1-(2-диметиламино)-2-меркаптотетразолом, получают целевое соединение с т. пл. 131-133oC (разложение); выход = 40% от теории.
18.
2-{/[3-Метил-4-(3-(1,
3,
4-тиадиазол-2-ил-тио)пропилтио)-2-пиридинил] метил/тио}-1H-бензимидазол-тригидрохлорид
Согласно описанной в примерах 14 и 1 методике, путем взаимодействия с
2-меркапто-1,3,4-тиадиазолом,
получают целевое соединение с т. пл. 167-170oC; выход составляет 53% от теории.
19. 2-{
/[3-Метил-4-(3-(пиридин-4-ил-тио)пропилтио)-2-пиридинил]
метил/ тио}-1H-беизимидазол
Согласно описанной в примере 1 методике, путем взаимодействия с 4-меркаптопиридином, получают целевое
соединение; бесцветный порошок; т. пл. 164-166; выход = 92%
от теории.
20. 2-{
/[3-Метокси-4-(3-(1-метил-тетразол-5-ил-тио)пропилтио)-2- пиридинил]метил/тио}-1H-бензимидазол-тригидрохлорид
Согласно описанной в примерах 14 и 1
методике,
путем взаимодействия 2-{
/[4-(3-xлopпpoпилтиo)-3-метoкcи 2-пиридинил] метил/тио}-1Н-бензимидазола с 1-метил-5-меркаптотетразолом, получают целевое соединение в виде бесцветного
кристаллизата; т. пл.
135oC
(разложение); выход составляет 84% от теории.
21. 2-{/[3-Метокси-4-(3-(пиримидин-2-ил-тио)пропилтио)-2-пиридинил]метил/ тио}-1H-бензимидазол
Согласно
описанной в примере 1
методике, путем взаимодействия 2-меркаптопиримидина с 2-{/[4-(3-хлорпропилтио)-3 метокси-2-пиридинил]метил/тио} -1Н-бензимидазолом, получают целевое соединение в
виде бежевого
порошка; т. пл.
88-90oC; выход = 77% от теории.
22. 5-{5-/2-(1Н-Бензимидазол-2-ил-тиометил)-3-метил-4- пиридинил/-1,5-дитиа-пент-1-ил}-тетразол-1-ацетат
натрия
Согласно описанной
в примере 1 методике, путем взаимодействия 2-меркаптотетразол-1-уксусной кислотой и раствором гидроксида натрия, после осаждения с помощью ацетона и
перекристаллизации из смеси
метанола с
диизопропиловым эфиром, получают целевое соединение; бежевый порошок; т. пл.: начиная со 180oC разложение; выход = 34% от теории.
23. 2-{
/[3-Метил-4-(2-(1-метил-тетразол-5-ил-тио)этилтио)-2-пиридинил] метил/тио}-1H-бензимидазол
Согласно указанной в примере 1 методике, путем взаимодействия 1-метил-5-меркапто-тетразола
с
2-{/[4-(2-хлорпропилтио)-3 метил-2-пиридинил/метил/тио}-1Н-бензимидазолом и NaOH, получают целевое соединение (82% от теории) в виде бесцветного твердого вещества. Т. пл. 204-208oC.
24. 2-{/[3-Метил-4-(4-(1-метил-тетразол-5-ил-тио)бутилтио)-2-пиридинил] метил/тио} -1H-бензимидазол
Согласно указанной в примере 1 методике, путем взаимодействия
1-метил-5-меркаптотетразола с 2-{ /[4-(4-хлорпропилтио)-3-метил-2-пиридинил] метил/тио} -1Н-бензимидазолом и NaOH, получают целевое соединение (48% от теории) в виде бесцветного твердого вещества.
Т.
пл. 208-210oC.
Исходные соединения
А 1. 2-{/[4-(3-хлорпропилтио)-3 метил-2-пиридинил]метил/тио} -1Н-бензимидазол
К раствору
2-меркапто-1Н-бензимидазола (1,
5 г/10 ммоль) в 40 мл этанола и 21 мл 1н. раствора гидроксида натрия в течение 20 минут при 40oC прикалывают один эквивалент
2-хлорметил-4-(3-хлорпропилтио)-23-метилпиридин-гидрохлорида
(растворенный в 10 мл воды). Затем перемешивают в течение 2-3-х часов при 50-60oC и следующие 3-4 часа при комнатной
температуре, отгоняют этанол на ротационном испарителе (1 кПа/40oC), экстрагируют 3 раза по 20 мл дихлорметаном, промывают с помощью 0,1 н. раствора гидроксида натрия, сушат над
карбонатом калия и концентрируют в вакууме досуха. Для очистки сырой продукт
хроматографируют на силикагеле (дихлорметан 20:1 - 3:1); собранные чистые фракции все вместе концентрируют в вакууме и
кристаллизуют из смеси дихлорметана с толуолом. Выход: 2,67 г (74%) целевого
соединения в виде бесцветного твердого вещества с т. пл. 112-114oC.
А 2.
2-Хлорметил-4-(3-хлорпропилтио)-3-метилпиридин-гидрохлорид
а) 2,
3-Диметил-4-(3-гидроксипропилтио)пиридин-N-оксид
К 50 мл безводного (высушенного) N-метилпирролидона (NМП) порциями
добавляют 6 г (60%-ного) NaH, перемешивают 15 минут, в течение 20 минут
добавляют 9,5 г (0,11 моль) 3-гидроксипропилмеркаптана и снова перемешивают в течение 30 минут вплоть до прекращения выделения
газа. После этого в течение 20 минут прикапывают раствор 14,4 г (0,1
моль) 4-хлор-2,3-диметилпиридин-N-оксида в 100 мл NMП, реакционную смесь перемешивают в течение 1 часа при комнатной температуре,
затем 1 час при 70oC и затем еще 1 час при 100o
C.
По окончании взаимодействия оставляют охлаждаться, разбавляют с помощью 500 мл воды и экстрагируют 4 раза по 300 мл дихлорметаном. Объединенные органические фазы промывают водой, сушат над сульфатом магния и концентрируют. Маслянистый остаток [10,0 г сырого 2, 3-диметил-4-(3-гидроксипропилтио)- пиридин-N-оксида] прямо используют в следующей стадии.
б)
2-Гидроксиметил-4-(3-гидроксипропилтио)-3-метил-пиридин
Полученное в п. а)
желтого цвета масло растворяют в 100 мл уксусного ангидрида и перемешивают в течение 2-х часов при 100o
C.
После концентрирования в вакууме коричневого цвета маслянистый остаток перегоняют
в аппаратуре для перегонки, включающей трубку с шаровым расширением, и вводят во взаимодействие далее без
очистки.
Маслянистый дистиллят в 100 мл 2 н. раствора гидроксида натрия и 100 мл изопропанола кипятят с обратным холодильником при перемешивании в течение 2-х часов. Изопропанол отгоняют, остаток экстрагируют 3 раза по 100 мл дихлорметаном, объединенные органические фазы промывают водой, сушат над карбонатом калия и концентрируют в вакууме. Получают 5,0 г 2-гидроксиметил-4-(3-гидроксипропилтио)-3-метилпиридина, который без очистки вводят во взаимодействие далее.
в) 2-Хлорметил-4-(3-хлорпропилтио)-3-метил-пиридин-гидрохлорид
5,
0
г масла из примера б) растворяют в дихлорметане (100 мл), прикапывают в полученный раствор 4 эквивалента
тионилхлорида и перемешивают 20 часов при комнатной температуре. Полностью концентрируют и
получают 4,5 г целевого соединения в виде маслянистого, постепенно кристаллизирующегося остатка, который в
желательном случае также можно применять в виде раствора в этаноле прямо для введения во
взаимодействие в случае необходимости с замещенными 2-меркаптобензимидазолами.
Б 1.
2-{/[4-(2-Хлорэтилтио)-3-метил-2-пиридинил]метил/тио}-1H-бензимидазол
Согласно указанной в
примере А 1. методике, путем взаимодействия 2-меркапто-1Н-бензимидазола с
4-(2-хлорэтилтио)-2-хлорметил-3- метилпиридин-гидрохлоридом и NaOH, после кристаллизации из этилацетата, получают целевое
соединение (62% от теории) в виде бесцветного твердого вещества с т. пл.
178-180oC.
Б 2. 4-(2-Хлорэтилтио)-2-хлорметил-3-метилпиридин-гидрохлорид
а) 2,
3-Диметил-4-(2-гидроксиэтилтио)пиридин-N-оксид
Согласно указанной в примере
А 2.а) методике, путем взаимодействия 4-хлор-2,3-диметил-пиридин-N-оксида с 2-меркаптоэтанолом и гидридом натрия,
получают целевое соединение в виде маслянистого остатка, который без дальнейшей
очистки используют в следующей стадии.
б) 4(2-гидроксиэтилтио)-2-гидроксиметил-3-метилпиридин
Согласно указанной в примере А 2.б) методике, путем взаимодействия полученного
в п.а) масла с уксусным ангидридом и последующего омыления с помощью NaOH, получают целевое соединение в виде
маслянистого остатка, который без дальнейшей очистки используют в следующей стадии.
в) 4-(2-Хлорэтилтио)-2-хлорметил-3-метилпиридин-гидрохлорид
Согласно указанной в примере А
2.в) методике, путем взаимодействия полученного в п. б) масла с тионилхлоридом,
получают целевое соединение в виде маслянистого остатка, который в виде раствора в этаноле используют прямо для
введения
во взаимодействие с 2-меркаптобензимидазолом.
В 1.
2-{/[[4-(4-Хлорбутилтио)-3-метил-2-пиридинил]метил/тио}-1Н-бензимидазол
Согласно указанной в примере А1 методике,
путем
взаимодействия 2-меркапто-1Н-бензимидазола с
4-(4-хлорбутилтио)-2-хлорметил-3- метил-пиридин-гидрохлоридом и NaOH, после кристаллизации и смеси этилацетата с диизопропиловым эфиром, получают
целевое
соединение (82% от теории) в виде слабо
желтого твердого вещества с т.пл. 151-153oC.
В 2. 4-(4-Хлорбутилтио)-2-хлорметил-3-метилпиридин-гидрохлорид
а) 2,
3-Диметил-4-(4-гидроксиэтилтио)пиридин-N-оксид
Согласно указанной в примере А 2.а) методике, путем взаимодействия 4-хлор-2,3-диметил-пиридин-N-оксида с 4-меркаптоэтанолом и гидридом натрия,
получают целевое соединение в виде маслянистого
остатка, который без дальнейшей очистки используют в следующей стадии.
б) 4-(4-Гидроксибутилтио)-2-гидроксиметил-3-метилпиридин
Согласно указанной в примере А 2.б) методике,
путем взаимодействия полученного в п.а) масла с уксусным ангидридом и последующего омыления с помощью NaOH, получают целевое соединение в виде
маслянистого остатка, который без дальнейшей очистки
используют в следующей стадии.
в) 4-(2-Хлорбутилтио)-2-хлорметил-3-метилпиридин-гидрохлорид
Согласно указанной в примере
А
2.в) методике, путем взаимодействия полученного в
п. б) масла с тионилхлоридом, получают целевое соединение в виде маслянистого остатка, который в виде раствора в этаноле прямо используют для
введения
во взаимодействие с
2-меркаптобензимидазолом.
Г1. 2-{/[4-(3-Хлорпропилтио)-3-метокси-2-пиридинил]метил/тио}- 1H-бензимидазол-дигидрохлорид
2-Меркапто-1Н-бензимидазол
(10 г) и
2-хлорметил-4-(3-хлорпропилтио)-3-метоксипиридин-гидрохлорид (1 эквивалент) в 150 мл изопропанола и 15 мл воды перемешивают в течение 5 часов при 80oC, охлаждают, отфильтровывают
выделившееся твердое вещество и перекристаллизовывают из смеси изопропанола с водой. Получают целевое соединение в виде порошка светло-коричневого цвета; т. пл. 117-119oC (разложение).
Выход = 67% от теории.
Г 2. 2-Хлорметил-4-(3-хлорпропилтио)-3-метокси-пиридин-гидрохлорид
Согласно описанному в примере А 2 а), б) и в) способу работы, исходя из
4-хлор-3-метокси-2-метилпиридин-N-оксида, получают целевое соединение в виде медленно кристаллизующегося масла, которое прямо используют далее.
Промышленная применимость
Превосходная эффективность соединений формулы (1) и их солей против Helicobacter-бактерий позволяет использовать их в медицине в качестве биологически активных веществ для лечения заболеваний,
которые
основаны на действии Helicobacter-бактерий.
Другим предметом изобретения поэтому является способ лечения млекопитающих, в частности людей, которые страдают заболеваниями, основанными на действии Helicobacter-бактерий. Способ отличается тем, что заболевшим индивидуумам вводят терапевтически эффективное и фармакологически приемлемое количество одного или нескольких соединений формулы (1) и/или их фармакологически приемлемых солей.
Предметом изобретения, кроме того, являются соединения формулы (I) и их фармакологически приемлемые соли для применения при лечении заболеваний, которые основаны на действии Helicobacter-бактерий.
Изобретение также охватывает применение соединений формулы (I) и их фармакологически приемлемых солей при приготовлении лекарственных средств, которые используют для борьбы с такими заболеваниями, которые основаны на действии Helicobacter-бактерий.
Следующим предметом изобретения являются лекарственные средства для борьбы с Helicobacter-бактериями, которые содержат одно или несколько соединений общей формулы (I) и/или их фармакологически приемлемых солей.
Из Helicobacter-штаммов, по отношению к которым соединения формулы (I) оказываются эффективными, следует в особенности упомянуть штамм Helicobacter pylori.
Лекарственные средства получают само по себе известными, доступными специалисту способами. В качестве лекарственных средств фармакологически активные соединения формулы (I) и их соли (=биологически активные вещества) применяют либо как таковые, либо предпочтительно в комбинации с пригодными фармацевтическими вспомогательными веществами, например, в форме таблеток, драже, капсул, эмульсий, суспензий, гелей или растворов, причем содержание биологически активного вещества предпочтительно составляет 0,1 - 95%.
Какие вспомогательные вещества пригодны для желательных формулировок лекарственных средств, специалисту известно на основании его специального знания. Наряду с растворителями, гелеобразующими агентами, вспомогательными веществами для изготовления таблеток и другими носителями биологически активных веществ, можно применять, например, антиоксиданты, диспергаторы, эмульгаторы, антивспениватели; вещества, корригирующие неприятный вкус лекарственного средства; консерванты, агенты растворения, красители или промоторы проницаемости и комплексообразователи (например, циклодекстрины).
Биологически активные вещества можно вводить, например, парентерально (например, внутривенно) или в особенности орально.
В общем, в медицине биологически активные вещества вводят в суточной дозе примерно 0,2-50, предпочтительно 1-30 мг/кг веса тела, в случае необходимости в форме нескольких, предпочтительно 2-6, разовых доз, для достижения желательного результата.
В этой связи, в качестве существенного согласно изобретению аспекта, особенно нужно упомянуть, что соединения формулы (I), в которых "n" обозначает число, равное 0, по отношению к Helicobacter-бактериям оказываются уже эффективными при введении таких доз, которые ниже таковых, которые необходимо использовать для достижения достаточного для терапевтических целей подавления выделения кислоты желудочного сока.
Соединения формулы (I), в которых "n" обозначает число, равное 1, наряду со своей эффективностью против Helicobacter-бактерий, также обладают отчетливым, подавляющим выделение кислоты желудочного сока действием. Соответственно, эти соединения используют также для лечения таких заболеваний, которые основаны на повышенном выделении кислоты желудочного сока.
Предлагаемые согласно изобретению соединения можно вводить также в фиксированной или свободной комбинации с нейтрализующим кислоту желудочного сока и/или подавляющим выделение кислоты желудочного сока веществом и/или с веществом, пригодным для классической борьбы с Helicobacter pylori.
В качестве нейтрализующих кислоту желудочного сока веществ, например, следует назвать гидрокарбонат натрия или другие антацидные средства (как гидроксид алюминия, алюминат магния или магалдрат). В качестве подавляющих выделение кислоты желудочного сока веществ следует назвать, например, H2 -блокирующие средства (например, циметидин, ранитидин), H+/К+ - АТФ - ингибиторы (например, лансопразол, омепразол или в особенности пантопразол), а также так называемые периферические антихолинергические средства (например, пирензепин, телензепин).
В качестве веществ, пригодных для классической борьбы с Helicobacter pylori, в особенности следует назвать антимикробно/эффективные вещества, как, например, пенициллин G, гентамицин, эритромицин, нитрофуразон, тинидазол, нитрофурантоин, фуразолидин, метронидазол и в особенности амоксициллин, или, однако, также соли висмута, как, например, цитрат висмута.
Биологические исследования
Соединения формулы (I) исследуют относительно их
активности (эффективности против
Helicobacter pylori, руководствуясь описанной Tomoyuki Iwahi и др. (Antimicrobial
Agents and Chemotherapy, 1991, 490-496) методикой при применении Columbia-агара
(оксид) и при периоде роста 4 дня.
Для исследованных соединений при этом получаются указанные в нижеследующей таблице 2
примерные MIC 50 - значения (указанные номера соединений совпадают с номерами
соединений в описании).
Реферат
Замещенные арилтиоалкилтиопиридины формулы I, где R1-R4 обозначает водород, R5 - водород, (C1-C4)алкил или (C1-C4 )алкоксил, R6 обозначает замещенный с помощью R8 и R9 цикл, который выбирают из группы, состоящей из бензола, тиазола, имидазола, триазола, тетразола, тиадиазола, пиридина, пиридин-N-оксида, пиримидина и бензимидазола; R7, R9, R11, R12 - водород или (С1-С4)алкил; R8 - водород, NH2 -группа или (С1-С4)алкил, возможно замещенный R10, m = 2-4; n, р, q = 0, и их соли эффективны для борьбы с Helicobacter-бактериями. 4 с. и 6 з.п. ф-лы, 2 табл.
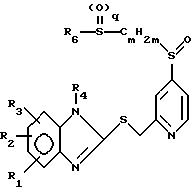
Формула
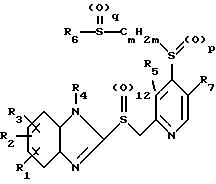
где R1, R2, R3, R4 каждый обозначает водород;
R5 обозначает водород, (C1-C4)алкил или (C1-C4)алкоксил;
R6 обозначает замещенный с помощью R8 и R9 цикл, который выбирают из группы, состоящей из бензола, тиазола, имидазола, триазола, тетразола, тиадиазола, пиридина, пиридин-N-оксида, пиримидина и бензимидазола,
R7 обозначает водород или (C1-C4)алкил;
R8 обозначает водород, NH2-группу или (C1-C4)алкил, возможно замещенный R10;
R9 обозначает водород или (C1-C4)алкил; R10 обозначает карбоксил или -N(R11)R12, причем R11 обозначает водород или (C1-C4)алкил и
R12 обозначает водород или (C1-C4)алкил,
m = 2 - 4; n = 0; p =0; q =0;
и их соли.
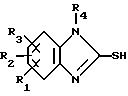
где R1, R2, R3 и R4 имеют указанные в п.1 значения, вводят во взаимодействие с пиколиновым производным формулы III:
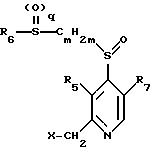
где R5, R6, R7, m и q имеют указанные в п.1 значения;
X обозначает пригодную удаляемую группу,
и/или полученные соли при желании переводят в свободные соединения.
Документы, цитированные в отчёте о поиске
Способ получения производных пиридина

Комментарии