Алкилирование n'-фенил-n-алкилфенилендиаминов в ионной жидкости - RU2422435C2
Код документа: RU2422435C2
Описание
УРОВЕНЬ ТЕХНИКИ
Данная заявка является продолжением находящейся на рассмотрении заявки США №11/3046829, поданной 14 декабря 2005, г., включенной здесь в качестве ссылки в полном объеме.
N'-фенил-N-алкилфенилендиамины нашли применение в качестве антиоксидантов для смазочных масел, композиций каучуков и антиозонантов. В патенте США №5232614 раскрывается применение N,N'-диалкилзамещенных п-фенилендиаминов в качестве антиоксидантов в смазочных маслах.
Алкилирование производных N'-фенил-N-фенилендиамина по методу Фриделя-Крафтса с использованием альфа-олефинов и в качестве катализатора кислоты Льюиса, такой как хлорид алюминия, приводит к получению алкилированного продукта с небольшим выходом или не дает алкилированного продукта. Вместо указанных условий для алкилирования N'-фенил-N-фенилендиаминов можно использовать алкил алюминия в качестве катализатора, а также высокое давление.
Однако применение алкилов алюминия для алкилирования N'-фенил-N-фенилендиаминов имеет, по меньшей мере, два недостатка: соединения непригодны к переработке для повторного использования и могут самопроизвольно воспламеняться на воздухе. Кроме того, реакция алкилирования обычно проходит по незамещенному фенильному кольцу. Таким образом, например, применение хлорида триэтилалюминия, нагрева и давления для алкилирования N'-фенил-N-изогексилфенилендиамина с помощью 1-децена приводит к получению, главным образом, N'-2-метилнонилфенил-N-изогексилфенилендиамина.
Ионная жидкость состоит из неорганических и/или органических катионов и анионов и обычно имеет очень низкое давление паров, широкий интервал температур жидкого состояния и является невоспламеняемой. Ионные жидкости могут выступать в качестве катализатора и/или растворителя, и проводились исследования возможности их применения в качестве растворителей, электролитов, в способах разделения и в качестве добавок к жидкостям, таким как смазки (см. Holbrey, “Industrial Applications of Ionic Liquids”, Chemistry Today 35 (June 2004); Parkinson, “Ionic Liquids Make an Environmental Splash”, 100 Chemical Engineering Progress 7 (September 2004); Drake et al., “Structural Effects on the Physical Properties of Ionic Liquids”, Air Force Research Laboratory Report No. AFRL-PR-ED-VG-2003-12 (May 2003).
Применение ионных жидкостей в алкилировании по Фриделю-Крафтсу обсуждалось в публикациях Wilkes, “Friedel-Crafts Reactions in Chloroaluminate Molten Salts”, Molten Salt Chemistry: An Introduction and Selected Application 405 (Mamantov and Marassi Eds. 1987), и Earle et al., “Organic Synthesis”, Ionic Liquids in Synthesis 174 (Wasserschied & Welton Eds. 2003). Однако исследований, относящихся к реакции алкилирования, которая позволяет дополнительно замещать фениленовый цикл производного N'-фенил-N-алкилфенилендиамина, не проводилось.
Предметом настоящего изобретения является предоставление способа синтеза, который позволяет осуществлять алкилирование фениленового цикла производного N'-фенил-N-фенилендиамина.
Отличительным признаком настоящего изобретения является применение ионной жидкости в качестве растворителя и катализатора реакции алкилирования.
Преимущество настоящего изобретения заключается в том, что применение ионной жидкости обычно позволяет удобно выделять N'-фенил-N-алкил(алкилфенилен)диамин из реакционной смеси.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В соответствии с одним аспектом настоящее изобретение относится к способу алкилирования N'-фенил-N-алкилфенилендиамина, который включает в себя
взаимодействие N'-фенил-N-алкилфенилендиамина формулы I
Формула I
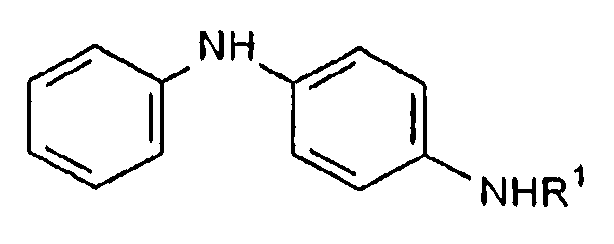
где R1 представляет собой алкильную группу или арилалкильную группу,
с алкилирующим агентом в присутствии ионной жидкости, включающей в себя кислоту Льюиса и четвертичный катион,
для получения N'-фенил-N-алкил(алкилфенилен)диамина формулы II
Формула II
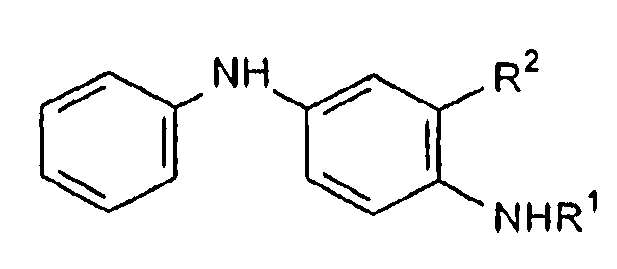
где R1 принимает значения, определенные выше,
R2 представляет собой замещенную или незамещенную линейную, разветвленную или циклическую алкильную группу или алкиларильную группу.
В соответствии с другим аспектом настоящее изобретение относится к N'-фенил-N-алкил(алкилфенилен)диамину формулы II
Формула II
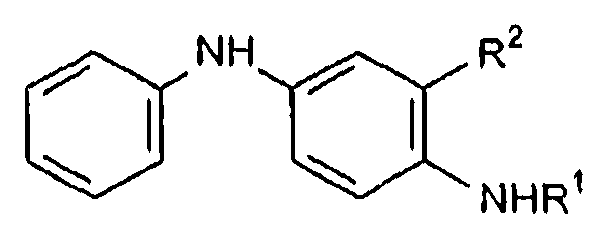
где R1 представляет собой алкильную группу или арилалкильную группу;
R2 представляет собой замещенную или незамещенную линейную, разветвленную или циклическую алкильную группу или алкиларильную группу, полученному способом, который включает в себя:
взаимодействие N'-фенил-N-алкилфенилендиамина формулы I
Формула I
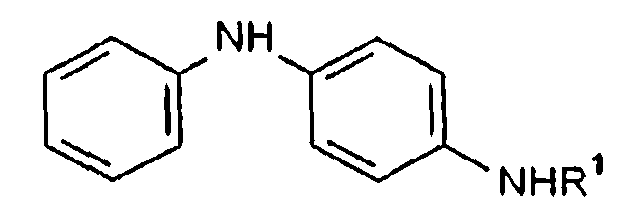
где R1 представляет собой алкильную группу или арилалкильную группу;
с алкилирующим агентом в присутствии ионной жидкости, включающей в себя кислоту Льюиса и четвертичный катион.
В соответствии с еще одним аспектом настоящее изобретение относится к композиции смазки, включающей в себя смазочное масло и N'-фенил-N-алкил(алкилфенилен)диамин формулы II
Формула II
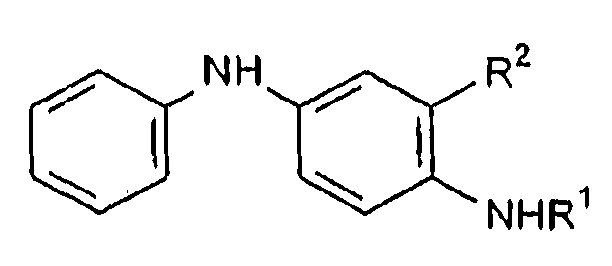
где R1 представляет собой алкильную группу или арилалкильную группу;
R2 представляет собой замещенную или незамещенную линейную, разветвленную или циклическую алкильную группу или алкиларильную группу.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ
ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Как указано выше, настоящее изобретение относится к алкилированию по Фриделю-Крафтсу N'-фенил-N-алкилфенилендиамина в присутствии неорганической жидкости.
Алкилирующий агент может представлять собой замещенный или незамещенный линейный, разветвленный или циклический олефин или арилалкен. Подходящие линейные олефины включают 1-гексен, 1-нонен, 1-децен и 1-додецен. Подходящие циклические олефины включают циклогексен, циклопентен и циклооктен. Подходящие разветвленные олефины включают пропиленовый тример (нонены), пропиленовый тетрамер (додецены), пропиленовый пентамер и диизобутилен. Подходящие арилалкилены включают стирол, метилстирол, 3-фенилпропен и 2-фенил-2-бутен.
Ионная жидкость может состоять полностью из анионов и катионов и может быть удобно получена смешением кислоты Льюиса и алкильной четвертичной соли металла, предпочтительно при нагревании.
Кислота Льюиса может представлять собой галогенид металла, алкиларил или сложный алкилсульфонатный эфир. Подходящие кислоты Льюиса в форме галогенидов металлов включают хлорид алюминия, бромид алюминия, трихлорид индия, трихлорид галлия, петнахлорид ниобия, пентахлорид тантала, тетрахлорид титана, трифторид бора, эфират трехфтористого бора, трихлорид бора, хлорид железа (III) и хлорид циркония. Типичные примеры алкилгалогенидов включают метилхлорид, метилбромид, метилйодид, этилхлорид, этилбромид, этилйодид, н-пропилхлорид, н-пропилбромид, н-пропилйодид, изопропилхлорид, изопропилбромид, изопропилиодид, н-бутилхлорид, н-бутилбромид, н-бутилйодид, изобутилхлорид, изобутилбромид, изобутилйодид, трет-бутилхлорид, трет-бутилбромид, трет-бутилйодид, н-пентилхлорид, н-пентилбромид, н-пентилйодид, неопентилбромид, неопентилхлорид, неопентилйодид, октилхлорид, октилбромид и октилйодид. Типичные примеры алкиларилгалогенидов включают бензилбромид, бензилхлорид, бензилйодид, α-фенилэтилхлорид, α-фенилэтилбромид, α-фенилэтилйодид, β-фенилэтилхлорид, β-фенилэтилбромид и β-фенилэтилйодид. Подходящие сложные алкилсульфонатные эфиры включают алкилтозилаты, алкилмезилаты и алкилтрифлаты.
Алкильная четвертичная соль металла может представлять собой четвертичную соль аммония, соль алкилфосфония, соль алкилимидазолия, соль алкилтриазолия и соль алкилпиридиния. Подходящие четвертичные соли аммония могут включать в качестве катионов катионы, выбранные из группы, включающей бензилтриметиламмоний, бутилтриметиламмоний, метилтриэтиламмоний, этилтриметиламмоний, тетра-н-бутиламмоний, н-гексилтриметиламмоний, н-гептилтриметиламмоний, н-октилтриметиламмоний, н-гексилтриэтиламмоний, н-гептилтриэтиламмоний, н-октилтриэтиламмоний, н-гексилтри-н-бутиламмоний, н-гептилтри-н-бутиламмоний, н-октилтри-н-бутиламмоний, трис-(н-пропил)ундециламмоний, тетра-н-пентиламмоний, N-децил-н-октилдиметиламмоний и N-тетрадецилтриэтиламмоний.
Подходящие четвертичные соли алкилфосфония могут включать в качестве катионов катионы, выбранные из группы, включающей бензилтриметилфосфоний, бутилтриметилфосфоний, метилтриэтилфосфоний, этилтриметилфосфоний, тетра-н-бутилфосфоний, н-гексилтриметилфосфоний, н-гептилтриметилфосфоний, н-октилтриметилфосфоний, н-гексилтриэтилфосфоний, н-гептилтриэтилфосфоний, н-октилтриэтилфосфоний, н-гексилтри-н-бутилфосфоний, н-гептилтри-н-бутилфосфоний, н-октилтри-н-бутилфосфоний, трис-(н-пропил)ундецилфосфоний, тетра-н-пентилфосфоний, N-децил-н-октилдиметилфосфоний и N-тетрадецилтриэтилфосфоний.
Подходящие соли алкилимидазолия могут включать в качестве катионов катионы, выбранные из группы, включающей 1-метил-3-метилимидазолий, 1-этил-3-метилимидазолий, 1-бутил-3-метилимидазолий, 1-додецил-5-метилимидазолий, 1-(2,2,2-трифторэтил)-3-метилимидазолий, 1-(этоксиметил)-3-метилимидазолий, 3-этил-1-этилимидазолий, 3-этил-1-бутилимидазолий, 1-этил-2,3-диметилимидазолий, 1,2-диэтил-3-метилимидазолий, 1-этил-3,5-диметилимидазолий и 1,3-диэтил-5-метилимидазолий.
Подходящие соли алкилтриазолия могут включать в качестве катионов катионы, выбранные из группы, включающей 1-(3',3',3'-трифтор-н-пропил)-3-н-бутил-1,2,4-триазолий, 1-(2'-фторэтил)-3-н-гептил-1,2,4-триазолий, 1-(2'-фторэтил)-3-н-децил-1,2,4-триазолий, 1-(1Н,1Н,2Н,2Н-перфтор-н-гексил)-3-н-бутил-1,2,4-триазолий, 1-н-пропил-4-амино-1,2,4-триазолий, 1-н-бутил-4-амино-1,2,4-триазолий и 1-н-гексил-4-амино-1,2,4-триазолий.
В предпочтительном варианте осуществления изобретения ионная жидкость получена in situ непосредственно перед добавлением алкилирующего агента. Кислота Льюиса, алкильная четвертичная соль металла и N'-фенил-N-алкилфенилендиамин могут загружаться в подходящую реакционную емкость, предпочтительно в сухой инертной атмосфере, при нагревании до температуры не выше 200°С и с перемешиванием, например, со скоростью от 200 до 300 об./мин до образования жидкой ионной фазы и органической фазы. Инертная атмосфера служит для защиты ионной жидкости от окисления и предпочтительно выбрана из группы, включающей атмосферу аргона, атмосферу гелия и атмосферу азота. Инертная атмосфера также должна быть сухой во избежание разложения ионной жидкости.
Алкилирующий агент может добавляться в реакционную емкость непосредственно после образования ионной жидкости одной порцией сразу или в виде множества небольших порций.
Реакция алкилирования может предпочтительно проводиться при температуре в интервале от 80 до 200°С в течение периода времени в интервале от 1 часа до 24 часов.
Реакция алкилирования приводит к получению смеси моно-, ди- и три-алкилированных N'-фенил-N-алкилфенилендиаминов. Продукты реакции могут выделяться из смеси реагентов стандартными методами разделения с помощью аппаратуры, хорошо известной специалисту данной области техники, например с помощью делительной воронки. Аналогично, выделенная реакционная смесь может разделяться на компоненты с использованием стандартных методов разделения и аппаратуры, хорошо известной специалисту данной области техники, такими как, например, жидкостная хроматография высокого давления.
Алкилирование по Фриделю-Крафтсу N'-фенил-N-алкилфенилендиамина в ионной жидкости, которая описана выше, неожиданно приводит к получению N'-фенил-N-алкил(алкилфенилен)диамина формулы II:
Формула II
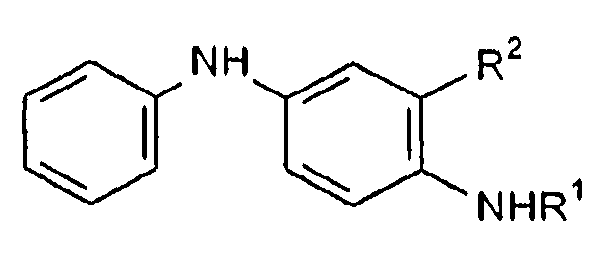
где R1 представляет собой алкильную группу или арилалкильную группу;
R2 представляет собой замещенную или незамещенную линейную, разветвленную или циклическую алкильную группу или алкиларильную группу, предпочтительно содержащую от 1 до 30 атомов углерода.
Предпочтительные N'-фенил-N-алкил(алкилфенилен)диамины включают соединения, в которых R1 и R2 оба представляют н-2-децил, в которых R1 представляет собой 2-изогексил и R2 представляет собой н-2-децил и в которых, по меньшей мере, один из R1 и R2 представляет собой арилалкильную группу.
N'-фенил-N-алкил(алкилфенилен)диамины, полученные способом согласно настоящему изобретению, как полагают, подходят для применения в качестве антиоксидантов в композициях смазок, например, описанных в патенте США № 5232614, содержание которого введено в данное описание во всей полноте в виде ссылки. Обычно композиция смазки будет включать, по меньшей мере, смазочное масло и, по меньшей мере, один N'-фенил-N-алкил(алкилфенилен)диамин в качестве антиоксиданта. Однако композиция может также включать в себя один или несколько компонентов, выбранных из группы, включающей дисперсант, детергент, противоизносную присадку, присадку, снижающую температуру застывания масла, ингибитор коррозии и модификатор трения.
Смазочное масло может представлять собой углеводородное масло, полученное из нефти, или углеводород с длинной цепью, замещенный альфа- или бета-ненасыщенной карбоновой кислотой. Детергент, когда присутствует, может представлять собой сульфонат щелочного металла, сульфонат щелочно-земельного металла или металлическую соль серосодержащего алкилфенольного соединения.
Противоизносная присадка, когда присутствует, может представлять собой органический сульфид, полисульфид, сложный эфир бета-тиодипропионовой кислоты, сложный фосфорсодержащий эфир или соль металла дигидрокарбилдитиофосфата.
Ингибитор коррозии, когда присутствует, может представлять собой производное бензотриазола, производное тиадиазола, производное меркаптобензотиазола в форме аминной соли, сульфонамид, тиосульфонамид, продукт реакции конденсации меркаптобензотиазола с амином и формальдегидом, диалкилфосфит, триалкилфосфит или триарилфосфит.
Модификатор трения, когда присутствует, может представлять собой сложный глицериловый моноэфир высшей жирной кислоты или производное оксазолина.
Как полагают заявители, ионная жидкость может подвергаться вторичному рециркулированию для применения в последующих реакциях алкилирования с помощью простого фазового разделения, при котором растворимый в углеводородах продукт реакции декантируется и таким образом отделяется от более плотной фазы ионной жидкости. После этого ионная жидкость сама по себе или в сочетании со свежим катализатором может использоваться для катализа другой реакции алкилирования.
ПРИМЕРЫ
Приведенные далее примеры более подробно иллюстрируют варианты практического осуществления изобретения. Конкретные условия, приведенные в примерах, являются только иллюстративными и не предназначены для ограничения области настоящего изобретения.
Пример 1
В круглодонную четырехгорлую колбу объемом 1 л, снабженную рубашкой, терморегулятором, термопарой и капельной воронкой равновесного давления, в атмосфере азота избыточного давления загружают твердый N'-фенил-N-2-изогексил-п-фенилендиамин (53,38 г, 0,1989 моль, коммерчески доступен как Flexzone 7P от Chemtura Corp.), хлорид алюминия (13,37 г, 0,100 моль, 50,4% (мол.) относительно N'-фенил-N-2-изогексил-п-фенилендиамина) и бромид тетра-н-бутиламмония (21,34 г, 0,0661 моль, 33,3% (мол.) относительно N'-фенил-N-2-изогексил-п-фенилендиамина). Перемешивание начинают со скоростью 200-300 об./мин и смесь нагревают сначала до 160°С.
Когда температура реакционной смеси, приобретающей окраску от темно-коричневой до черной, достигает 160°С, начинают добавление 94% 1-децена (97,64 г, 0,696 моль, 3,5 экв. относительно N'-фенил-N-2-изогексил-п-фенилендиамина), которое осуществляют в течение 2 часов. После завершения добавления реакционную смесь нагревают до 170°С и выдерживают при данной температуре в течение 25 часов.
Реакционной смеси дают возможность охладиться до температуры окружающей среды и смесь разбавляют 300 мл н-гептана. Реакционная смесь, имеющая окраску от темно-коричневой до черной, делится на две фазы: нижнюю твердую фазу и верхнюю жидкую фазу, которую декантируют в делительную воронку объемом 2 л, промывают водой (2х500 мл), затем разбавленным раствором аммиака (смесь 400 мл воды и 100 мл конц. водного гидроксида аммония) и сушат над безводным сульфатом натрия. Масса твердой фазы на дне колбы составляет 50,74 г.
Осушитель удаляют фильтрацией с подсосом через диск диаметром 9,0 см из фильтровальной бумаги со стекловолокном 934 АН. Фильтрат, имеющий темную окраску, конденсируют в вакууме (роторный испаритель, температура водяной бани 95°С, конечный вакуум <6 мм), получая продукт в виде масла темно-коричневого -черного цвета (49,49 г).
ГХ-анализ показывает, что данный продукт представляет собой смесь (% площади) непрореагировавшего N'-фенил-N-2-изогексил-п-фенилендиамина (17,1%), монодециклированного N'-фенил-N-2-изогексил-п-фенилендиамина (71,8%), мультидециклированного N'-фенил-N-2-изогексил-п-фенилендиамина (7,5%). Монодециклированный продукт представляет собой смесь двух изомеров (8,2% и 63,6%). Основной изомер выделяют колоночной хроматографией.
Основной изомер идентифицируют как N'-фенил-N-2-изогексил-[2-(2-изодецил)-п-фенилен]диамин (GREE) в соответствии с его временем удерживания в ГХ-анализе, а также в соответствии с ИК- и ЯМР спектром, которые соответствуют времени удерживания в ГХ, а также ИК- и ЯМР спектру истинного образца (GRFE), полученного с использование другого способа синтеза, например, из 1-децена c использованием хлорида диэтилалюминия в качестве катализатора, а также нагрева и высокого давления.
Заявители полагают, что ионная жидкость может рециркулироваться для применения в последующих реакциях алкилирования, например, посредством простого фазового разделения, при котором растворимый(е) в углеводородах продукт(ы) реакции декантируют и таким образом отделяют от более плотной фазы ионной жидкости. Ионная жидкость может затем использоваться для катализа другой реакции алкилирования сама по себе и в сочетании со свежим катализатором.
Реферат
Изобретение относится к улучшенному способу орто-алкилирования в фенильное кольцо N'-фенил-N-алкил-п-фенилендиаминов. Способ заключается во взаимодействии N'-фенил-N-алкилфенилендиамина формулы I: ! ! где R1 представляет собой алкильную группу, с алкилирующим агентом, выбранным из незамещенного линейного олефина, в инертной атмосфере в присутствии ионной жидкости, включающей кислоту Льюиса, представляющую собой галогенид металла, и четвертичный катион, выбранный из четвертичного катиона аммония, для получения N'-фенил-N-алкил(алкилфенилен)диамина формулы II: ! ! где R1 принимает значения, определенные выше, R2 представляет собой незамещенную линейную алкильную группу. Способ позволяет упростить выделение целевого продукта из реакционной массы. 7 з.п. ф-лы.
Формула
формула I

где R1 представляет собой алкильную группу,
с алкилирующим агентом, выбранным из незамещенного линейного олефина, в инертной атмосфере в присутствии ионной жидкости, включающей кислоту Льюиса, представляющую собой галогенид металла, и четвертичный катион, выбранный из четвертичного катиона аммония,
для получения N'-фенил-N-алкил(алкилфенилен)диамина формулы II
формула II

где R1 принимает значения, определенные выше,
R2 представляет собой незамещенную линейную алкильную группу.
Документы, цитированные в отчёте о поиске
Иммобилизованные ионные жидкости

Комментарии