Соединения, включающие связанные гетероарильные фрагменты, и их применение в качестве новых модификаторов вкусо-аромата умами, тастантов (стимуляторов сенсорных клеток вкусовых сосочков языка) и усилителей вкуса в пищевых композициях - RU2410383C2
Код документа: RU2410383C2
Описание
Родственные заявки
Настоящая заявка имеет приоритет предварительной заявки на патент США №60/650029, заявленной 4 февраля 2005 года, полное описание которой включено в качестве ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к открытию вещества, придающего вкус и аромат, или модификаторам вкуса, таким как ароматизаторы или агенты, придающие вкус и аромат, и усилителям вкусо-аромата или усилителям вкуса, а именно модификаторам острого вкуса («умами»), агентам, придающим острый вкусо-аромат, и усилителям острого вкусо-аромата для пищевых продуктов, напитков и других пищевых композиций.
Уровень техники, предшествующий изобретению
На протяжении столетий в пищевые продукты, напитки и/или пищевые композиции (употребляемые в пищу) для улучшения их вкуса вводили различные, натуральные и искусственные композиции и/или соединения. Хотя давно известны только пять основных типов «вкуса» (сладкий, кислый, горький, соленый и «умами»/острый), были мало понятны биологические и биохимические основы восприятия вкуса, и большинство улучшителей вкуса или агентов, модифицирующих вкус, были открыты случайно или по ошибке.
Например, одним из пяти известных вкусов является «острый» или «умами» вкусо-аромат глютамата натрия («MSG»), который в настоящее время повсеместно добавляют в композиции многих пищевых продуктов и напитков для желательного улучшения их «острого» вкусо-аромата. MSG известен тем, что вызывает побочные реакции у некоторых людей, но в поиске искусственных заменителей MSG не достигнут значительный прогресс. Известно, что очень небольшое количество веществ натурального происхождения могут повышать или усиливать эффективность MSG как агента, придающего острый вкусо-аромат, таким образом, чтобы снизить количество MSG для придания вкусо-аромата. Например, нуклеотидные соединения натурального происхождения монофосфат инозина (IMP) или монофосфат гуанозина (GMP) известны как оказывающие синергетическое и/или усиливающее воздействие на острый вкус MSG. Однако выделение IMP и GMP из натуральных источников и очистка или их синтез является очень трудоемким и дорогим процессом, таким образом, ограничивается их практическое коммерческое применение во многих пищевых композициях. Недорогие соединения, которые могли бы обеспечить вкусо-аромат MSG и/или заменить вкусо-аромат MSG или увеличить эффективность любого присутствующего MSG, избавляя, таким образом, от необходимости введения добавок IMP или GMP, могли бы быть очень ценными, в частности, если использовать такие соединения в максимально низких концентрациях, сводя к минимуму, таким образом, стоимость и возможность любого риска для здоровья.
В последние десятилетия в биологии в общем был достигнут существенный прогресс и лучшее понимание биологических и биохимических феноменов, лежащих в основе восприятия вкуса. Например, недавно были идентифицированы белки вкусовых рецепторов у млекопитающих, которые вовлечены в восприятие вкуса. В частности, два различных семейства G белков, связанных с рецепторами, вовлеченных в восприятие вкуса, идентифицированные как T2Rs и T1Rs. (См., например, Nelson, et al., Cell (2001) 106(3):381-390; Adler, et al., Cell (2000) 100(6):693-702; Chandrashekar, et al.,Cell (2000) 100:703-711; Matsunami, et al., Number (2000) 404:601-604; Li, et al., Proc. Natl. Acad. Sci. USA (2002) 99:4962-4966; Montmayeur, et al.,Nature Neuroscience (2001) 4(S):492-498: патент США 6462148; и PCT публикации WO 02/06254, WO 00/63166 art, WO 02/064631 и WO 03/001876, и заявка на патент США US 2003-0232407 A1). Полное содержание статей, заявок на патенты и выданных патентов, приведенных здесь выше, включено сюда в качестве ссылки, включая раскрытие в них выявления и структуры белков T2Rs и T1Rs вкусовых рецепторов млекопитающих и способов искусственной экспрессии этих рецепторов в линиях клеток и использования полученных в результате линий клеток для отбора соединений в качестве потенциальных агентов, придающих «острый» вкусо-аромат.
Следует иметь в виду, что семейство T2R представляет собой семейство, состоящее из более 25 генов, вовлеченных в восприятие горького вкуса, семейство T1Rs включает только три члена T1R1, T1R2 и T1R3. (См. Li, et al.,Proc. Natl. Acad. Sci. USA (2002) 99:4962-4966.) В WO 02/064631 и/или WO 03/001876 недавно было описано, что когда определенные члены T1R коэкспрессированы подходящими линиями клеток млекопитающих, они объединяются с получением функциональных вкусовых рецепторов. В частности, было открыто, что коэкспрессия T1R1 и T1R3 в подходящей клетке-хозяине приводит в результате к получению функционального T1R1/T1R3 рецептора острого («умами») вкуса, отвечающего за стимуляцию острого вкуса, включая глютамат натрия. (См. Li, et al. (Id.) Приведенная выше ссылка также раскрывает анализы и/или ускоренный скрининг для измерения активности T1R1/T1R3 или T1R2/T1R3 рецепторов флуорометрическим изображением в присутствии целевых соединений.
Совсем недавно заявителями были поданы определенные заявки на патент США и международные заявки, в которых описывается использование определенных амидных соединений в качестве стимуляторов сенсорных клеток вкусовых сосочков языка (тастанта) к восприятию умами/или сладкого вкуса, и/или синергетических усилителей «Умами» вкуса MSG, и/или сладкого вкуса различных натуральных и искусственных подсластителей. См., например, заявку на патент США №60/494071, поданную 6 августа 2003 года, заявку на патент США №60/552064, поданную 9 марта 2004 года, заявку на полезную модель США №10/913303, поданную 6 августа 2004 года и опубликованную в США под № US-2005-0084506-A1 21 апреля 2005 года, и международную заявку № PCT/US04/25419, поданную 6 августа 2004 года и опубликованную как WO2005/041684 12 мая 2005 года, и WO2005/015158, опубликованную 17 февраля 2005 года. Полное содержание статей, заявок на патенты и выданных патентов, приведенных здесь выше, включены сюда в качестве ссылки, включая раскрытие в них выявления и структуры амидных соединений, которые могут использоваться в качестве потенциальных агентов, придающих «острый» или сладкий вкусо-аромат, или усилителей. Таким образом, сохраняется необходимость в новых и улучшенных соединениях, усиливающих вкус.
Авторы разработали вышеописанные методы анализов и/или способы ускоренного скрининга для идентификации из очень большого числа начальных соединений очень небольшого числа связанных гетероарильных соединений, модулирующих активность T1R1/T1R3 рецепторов «острого» вкуса, начали продолжительный комплексный циклический процесс исследования, оценки и проверки и оптимизацию химической структуры, создавая, таким образом, различные изобретения, описанные ниже.
Краткое описание изобретения
Настоящее изобретение относится ко многим аспектам, каждый из которых относится к определенным искусственным соединениям, содержащим связанные гетероарильные фрагменты, которые имеют общую структуру, показанную ниже в формуле (I), способам синтеза этих соединений и применению этих соединений и употребляемых в пищу их солей и/или композициям из них в качестве агентов, придающих острый вкус и аромат пищевым композициям или одному или более их компоненту предшественнику. В большинстве вариантов воплощения настоящее изобретение относится к способам модулирования острого вкуса пищевых продуктов, включающим:
a) обеспечение, по меньшей мере, одного пищевого продукта или одного или более его предшественника, и
b) смешивание пищевого продукта или одного или более его предшественника с, по меньшей мере, одним соединением формулы (I) или употребляемой в пищу его приемлемой солью в, по меньшей мере, количестве, модулирующем острый вкус и аромат, с получением модифицированного пищевого продукта;
где соединение формулы (I) имеет формулу:

где
i) Ar представляет собой арильный или гетероарильный радикал, необязательно имеющий, по меньшей мере, один заместитель;
ii) Y представляет собой O, S, S(O), SO2, CR1R2, или NR5;
iii) m равно 0 или 1;
iv) hAr1 представляет собой необязательно замещенное гетероарильное кольцо;
v) X представляет собой O, S, S(O), SO2, CR8R9 или NR10;
vi) n равно 0, 1, 2 или 3;
vii) hAr2 представляет собой необязательно замещенное гетероарильное кольцо.
Что касается вариантов воплощения изобретения с соединениями формулы (I), hAr2может представлять собой необязательно замещенный арильный радикал, такой как фенильный радикал.
В других вариантах воплощения настоящее изобретение относится к соединениям формулы (I), обеспечивающим модифицирование пищевых продуктов или композиций, содержащих одно или более соединений формулы (I), или его различным подклассам или группам соединений, или употребляемым в пищу их приемлемым солям, или продуктам, полученным по способам, приведенным выше или ниже. Например, другие варианты воплощения настоящего изобретения, описанные здесь, относятся к пищевым композициям с модифицированным вкусом, содержащим:
а) по меньшей мере, один пищевой продукт или один или более его предшественник, и
b) по меньшей мере, одно соединение, по меньшей мере, в количестве, модулирующем острый вкус и аромат, имеющее формулу:
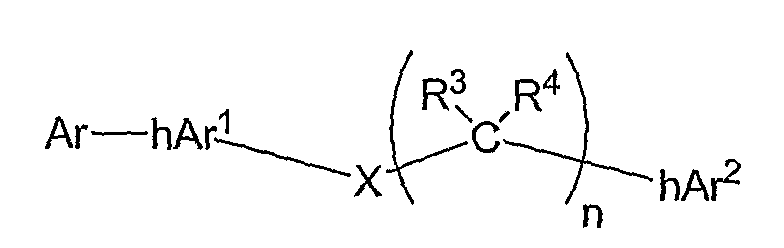
где
i) Ar представляет собой моноциклический или бициклический арильный или гетероарильный радикал, включающий одно или два ароматических кольца, независимо выбранных из бензольных колец и пяти- или шестичленных гетероарильных колец, каждое ароматическое кольцо необязательно имеет один, два или три R20замещающих радикалов, где каждый R20 радикал независимо выбран из гидроксила, NH2, NO2, SH, SO3H, P(O)(OH)2, галогена или органического радикала C1-C4;
ii) hAr1 представляет собой необязательно замещенный пяти- или шестичленный гетероарильный кольцевой радикал, имеющий от 1 до 4 гетероатомов, независимо выбранных из кислорода, серы и/или азота, где любой из оставшихся членов гетероароматического кольца независимо выбран из CR6, N, NR7;
iii) X представляет собой O, S, S(O), SO2, CR8R9 или NR10;
iv) n равно 0, 1, 2 или 3;
v) R3, R4, R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, SH, галогена или органического радикала C1-C4, R7 и R10 независимо выбраны из водорода, гидроксила или органического радикала C1-C4 и R6 независимо выбран из водорода, гидроксила, NH2, NO2, SH, SO3H, P(O)(OH)2, галогена или органического радикала C1-C4;
vi) hAr2 представляет собой необязательно замещенное пяти- или шестичленное гетероарильное кольцо, имеющее, по меньшей мере, один атом углерода в кольце и, по меньшей мере, один атом азота в кольце, и где оставшиеся члены гетероарильного кольца независимо выбраны из CR30, N, NR31, O и S, где каждый R30независимо выбран из водорода, гидроксила, NH2, NO2, SH, SO3H, P(O)(OH)2, галогена или органического радикала C1-C4 и каждый R31независимо выбран из водорода или органического радикала C1-C4;
или их пищевую приемлемую соль.
В некоторых вариантах воплощения настоящее изобретение относится к подклассу связанных гетероарильных соединений формулы (I) и их применению в способах модулирования острого вкуса пищевых композиций. Например, один подкласс связанных гетероарильных соединений имеет структуру, показанную ниже формулой (IА):

где
i) n` равно 0, 1, 2 или 3 и каждый R20 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
ii) n`` равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
iii) X представляет собой NH, O, S, S(O), SO2 или СН2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила, пирролила, бензофуранила, бензотиофуранила или бензопирролила;
v) hAr1 имеет структуру:



(1) X1 представляет собой NH, O или S,
(2) X2 представляет собой N или CR6, где R6 представляет собой водород, галоген или органический радикал C1-C4,
(3) X3 представляет собой N или CR6, где R6 представляет собой водород, галоген или органический радикал C1-C4, и
vi) hAr2 представляет собой кольцо пиридила, пиразинила или пиримидинила;
или их пищевую приемлемую соль.
Другие относятся к подклассу связанных гетероарилов формулы (I), используемых в качестве агентов, придающих острый вкус и аромат, представляющих собой триазольные соединения, имеющие структуру, показанную ниже формулой (IВ):

где
i) n` равно 0, 1, 2 или 3 и каждый R20 независимо выбран из гидрокси, SH, NH2, галогена и органического радикала C1-C4, выбранного из алкила, алкоксила, алкокси-алкила, гидроксиалкила, галогеналкила, CN, CO2H, CHO, COR21, NHR21, NR21R21 или SR21 радикалов, где R21 представляет собой алкил;
ii) n`` равно 0, 1, 2 или 3 и каждый R30 независимо выбран из гидрокси, SH, NH2, галогена или органического радикала C1-C4, выбранного из алкила, алкоксила, алкокси-алкила, гидроксиалкила, галогеналкила, CN, CO2H, CHO, COR32, NHR32, NR32R32 или SR32 радикала, где R32 представляет собой алкил;
iii) X представляет собой NH, O, S, S(O), SO2 или СН2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила или пирролила;
или их пищевую приемлемую соль.
Другие соединения относятся к подклассу связанных гетероарилов формулы (I), представляющих собой триазольные соединения, имеющие структуру, показанную ниже в формуле (IС), где X и Y представляют линкерные группы:

где
i) n` равно 0, 1, 2 или 3 и каждый R20 независимо выбран из группы, состоящей из гидроксила, SH, NH2, галогена или органического радикала C1-C4;
ii) n`` равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из ОН, SH, NH2, галогена или органического радикала C1-C4;
iii) X представляет собой NH, O, S, S(O), SO2 или СR8R9, где R8и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, галогена или органического радикала C1-C4;
iv) Y представляет собой NH, O, S, S(O), SO2 или СR8R9, где R8и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, галогена или органического радикала C1-C4;
v) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила или пирролила;
или их пищевую приемлемую соль.
Следующие соединения относятся к подклассу связанных гетероарилов формулы (I), представляющих собой соединения, имеющие hAr1гетероарильные кольца, которые представляют собой шестичленные азотные гетероарилы, как показано в формуле (ID):
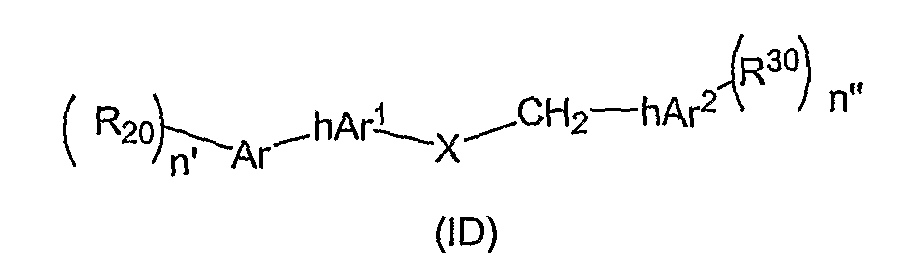
где
i) n` равно 0, 1, 2 или 3 и каждый R20 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
ii) n`` равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
iii) X представляет собой NH, O, S, S(O), SO2 или СН2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила, пирролила, бензофуранила, бензотиофуранила или бензопирролила;
v) hAr1 имеет структуру:

где R6 и R6' независимо выбраны из водорода, галогена или органического радикала C1-C4, и
vi) hAr2 представляет собой кольцо пиридила, пиразинила или пиримидинила.
Связанные гетероарильные соединения формул (I), (IA), (IB), (IC) и (ID) и группы соединений, входящие в них, могут связываться и/или активировать in vitro белки T1R1/T1R3 рецептора острого («умами») вкуса при неожиданно очень низких концентрациях, порядка микромолей или менее. Предполагается также, что связанные гетероарильные соединения также или подобным образом взаимодействуют in vivo с рецепторами острого вкуса у животных или людей, что было подтверждено подлинным вкусовым тестированием людей соединениями, выбранными из формулы (I), которые приведены ниже.
Таким образом, многие из подклассов и групп связанных гетероарильных соединений формулы (I), далее описанных здесь ниже, могут быть использованы в неожиданно низких концентрациях в качестве агентов, придающих острый вкус и аромат, или усилителей острого вкуса и аромата, которые заменяют и/или синергетически усиливают острый вкус и аромат MSG.
Дополнительные необязательные ограничения химических и физических характеристик гетероциклических соединений формулы (I) и их замещающих радикалов или групп будут описаны ниже. Некоторые из гетероциклических соединений со структурой, подпадающей под формулу (I), были синтезированы способами, известными из уровня техники для различных целей, но авторы изобретения не предполагали, что такие связанные гетероарильные соединения могут быть использованы в качестве агентов, придающих острый вкус и аромат, или усилителей острого вкуса и аромата. Кроме того, многие из гетероциклических соединений формулы (I), описанные здесь, являются новыми соединениями, которые до этого вообще не были синтезированы, и обладают неожиданным свойством выступать в роли агентов, придающих вкус и аромат, или усилителей вкуса.
Также изобретение относится к пищевым продуктам с модифицированным вкусо-ароматом, таким как пищевые продукты и напитки, полученные взаимодействием соединений по настоящему изобретению с пищевыми продуктами или их предшественниками.
Во многих вариантах воплощения настоящего изобретения одно или более связанное гетероарильное соединение формулы (I), идентифицированное, описанное и/или заявленное далее, или его пищевые приемлемые соли может быть использовано в смесях или комбинациях с известными соединениями, придающими острый вкусо-аромат, такими как MSG, в качестве усилителей острого вкусо-аромата в пищевых продуктах и композициях напитков или их предшественниках для потребления человеком или животными.
Во многих вариантах воплощения изобретения связанные гетероарильные соединения формулы (I) и их различные подклассы являются агонистами рецепторов T1R1/T1R3 и, таким образом, предположительно способны индуцировать или усиливать восприятие острого вкуса людьми. Многие из гетероциклических соединений формулы (I) и/или их различные подклассы гетероциклических соединений при использовании совместно с MSG или отдельно повышают или модулируют ответ in vitro и восприятие людьми острого вкуса при неожиданно низких концентрациях.
В некоторых вариантах воплощения настоящее изобретение относится к новым соединениям, агентам, придающим вкус и аромат, усилителям вкусо-аромата, соединениям, модифицирующим вкусо-аромат, и/или композициям, включающим соединения формулы (I), и различным группам и подгруппам этих соединений.
В некоторых вариантах воплощения настоящее изобретение относится к пищевым или медицинским композициям или их предшественникам, подходящим для потребления человеком или животным, содержащим, по меньшей мере, одно соединение формулы (I) или его пищевую приемлемую соль.
Подводя итог всем приведенным аспектам настоящего изобретения, не следует их считать ограничивающими настоящее изобретение.
Подробное описание изобретения
Настоящее изобретение может стать более ясным для понимания благодаря последующему подробному описанию различных вариантов его воплощения, включенным в него примерам, химическим формулам, таблицам и предшествующему и последующему их описанию. Перед представлением соединений, композиций и/или способов, раскрытых и описанных, для лучшего понимания без иных специальных указаний в пунктах формулы настоящее изобретение не ограничивается определенными пищевыми продуктами или способами получения пищевых продуктов, определенными пищевыми носителями или рецептурами или особыми способами составления соединений по настоящему изобретению с пищевыми продуктами или композициями для орального введения, поскольку для специалиста в данной области техники ясно, что такие вещи могут иметь варианты. Терминология используется только для описания конкретных вариантов воплощения настоящего изобретения и не ограничивает объем притязаний.
Определения
«Носитель, приемлемый для пищевых продуктов, или инертный наполнитель» представляет собой твердую или жидкую среду и/или композицию, которая используется для получения требуемой диспергируемой формы дозировки для соединения по настоящему изобретению, чтобы максимизировать биологическую эффективность соединения по настоящему изобретению в диспергируемой/растворимой форме. Носитель, приемлемый для пищевых продуктов, включает многие традиционные пищевые ингредиенты, такие как вода, при нейтральном, кислом или щелочном рН, фруктовые или овощные соки, уксус, маринады, пиво, вино, природная вода/жировые эмульсии, такие как молоко или сгущенное молоко, пищевые масла и шортенинги, жирные кислоты и их алкильные эфиры, низкомолекулярные олигомеры пропиленгликоля, глицериновые эфиры жирных кислот и дисперсии или эмульсии таких гидрофобных веществ в водной среде, соли, такие как хлорид натрия, пшеничная мука, растворители, такие как этанол, твердые пищевые наполнители, такие как растительные порошки или мука, или другие жидкие носители, диспергирующие или суспендирующие агенты, поверхностно-активные агенты, изотонические агенты, загущающие или эмульгирующие агенты, консерванты, отвердители, лубриканты и т.д.
«Вкусо-аромат» используется здесь для описания восприятия субъектом вкуса и/или запаха, куда входят сладкий, кислый, соленый, горький, умами и другие. Под субъектом понимается человек или животное.
«Агент, придающий вкус и аромат» используется здесь для описания соединения или его биологически приемлемой соли, которые индуцируют аромат или вкус у животного или человека.
«Модификатор вкуса и аромата» используется здесь для описания соединения или его биологически приемлемой соли, которые модулируют, включая усиление или потенцирование и индуцирование вкусов и/или запахов натурального или синтетического агента, придающего вкус и аромат у животного или человека.
«Усилитель вкусо-аромата» используется здесь для описания соединения или биологически приемлемой соли, которые усиливают и/или приумножают вкус и/или запах натурального или синтетического агента, придающего вкус и аромат или пищевой композиции, включающей усилитель вкусо-аромата.
«Острый вкусо-аромат» используется здесь для описания острого «умами» вкуса, индуцированного, как правило, MSG (глютаматом натрия) у животного или человека.
«Агент, придающий острый вкусо-аромат», «соединение, придающее острый вкусо-аромат», или «соединение, активирующее рецептор острого вкусо-аромата» используется здесь для описания соединения или его биологически приемлемой соли, которые вызывают у субъекта способность воспринимать острый вкусо-аромат, например MSG (глютамат натрия) или соединение, активирующее in vitro рецептор T1R1/T1R3. Под субъектом понимается человек или животное.
«Модификатор острого вкусо-аромата» используется здесь для описания соединения или биологически приемлемой соли, которые модулируют, включая усиление или потенцирование, индуцирование и блокирование острого вкуса натуральных или синтетических агентов, придающих острый вкус и аромат, например, MSG (глютамат натрия) у животного или человека.
«Усилитель острого вкусо-аромата» используется здесь для описания соединения или его биологически приемлемой соли, которые усиливают и/или потенцируют острый вкус натурального или синтетического агента, придающего острый вкусо-аромат, например, MSG (глютамат натрия) у животного или человека.
«Соединение, активирующее рецептор умами» используется здесь для описания соединения, которое активирует рецептор умами, такой как рецептор T1R1/T1R3.
«Соединение, модулирующее рецептор умами» используется здесь для описания соединения, которое модулирует (активирует, усиливает или блокирует) рецептор умами.
«Соединение, усиливающее рецептор умами», используется здесь для описания соединения, которое усиливает или потенцирует воздействие натурального или синтетического соединения, активирующего рецептор умами, например MSG (глютамат натрия).
«Количество, модулирующее острый вкусо-аромат» используется здесь для описания количества соединения формулы (I), которое достаточно для изменения (как повышение, так и понижение) острого вкуса в пищевом или медицинском продукте или композиции, или их предшественнике, достаточное, чтобы быть воспринятым человеком. Во многих вариантах воплощения настоящего изобретения гетероциклическое соединение должно присутствовать, по меньшей мере, в количестве около 0,001 частей на миллион, чтобы большинство людей ощутило модуляцию острого вкусо-аромата пищевой композиции, содержащей гетероциклическое соединение. Большой диапазон концентрации, которую необходимо, как правило, использовать для экономичного обеспечения требуемой степени модуляции острого вкусо-аромата, может составлять от около 0,001 частей на миллион до 100 частей на миллион или в более узких пределах от около 0,1 частей на миллион до 10 частей на миллион. Альтернативные пределы количеств, модулирующих острый вкусо-аромат, могут составлять от около 0,01 частей на миллион до около 30 частей на миллион, от около 0,05 частей на миллион до около 15 частей на миллион, от около 0,1 частей на миллион до около 5 частей на миллион или от около 0,1 частей на миллион до около 3 частей на миллион.
«Количество, усиливающее острый вкусо-аромат» используется здесь для описания количества соединения, которое достаточно для усиления вкуса натуральных или синтетических агентов, придающих вкус и аромат, например MSG (глютамат натрия) в пищевом или медицинском продукте или композиции, достаточное, чтобы быть воспринятым человеком или животным. Большой диапазон количества вещества, усиливающего острый вкусо-аромат, может составлять от около 0,001 частей на миллион до 100 частей на миллион или в более узких пределах от около 0,1 частей на миллион до 10 частей на миллион. Альтернативные пределы количеств, усиливающих острый вкусо-аромат, могут составлять от около 0,01 частей на миллион до около 30 частей на миллион, от около 0,05 частей на миллион до около 15 частей на миллион, от около 0,1 частей на миллион до около 5 частей на миллион или от около 0,1 частей на миллион до около 3 частей на миллион.
«Количество, модулирующее рецептор умами» используется здесь для описания количества соединения, достаточного для модуляции (активации, усиления или блокирования) белков рецептора умами. Во многих вариантах воплощения настоящего изобретения количество, модулирующее рецептор умами, составляет, по меньшей мере, около 1 пМ, или, по меньшей мере, около 1 нМ, или, по меньшей мере, около 10 нМ, по меньшей мере, около 100 нМ (т.е. около 0,1 мкМ). «Количество, модулирующее или активирующее рецептор T1R1/T1R3», используется здесь для описания количества соединения, достаточного для модуляции или активации рецептора T1R1/T1R3. Эти количества предпочтительно равны количествам, модулирующим рецептор умами.
«Рецептор умами» используется здесь для описания рецептора вкуса, который может регулироваться соединением с острым вкусо-ароматом. Предпочтительно рецептор умами представляет собой G белок, связанный с рецепторами, и более предпочтительно рецептор умами представляет собой рецептор T1R1/T1R3.
Соединения по настоящему изобретению модулируют рецептор умами и предпочтительно являются агонистами рецептора T1R1/T1R3. Агонист этого рецептора оказывает активирующее воздействие на каскадный механизм передачи сигнала. В большинстве случаев агонистическое воздействие соединения на рецептор также порождает острый вкусо-аромат во время проведения тестов на вкус. Таким образом, соединение по настоящему изобретению подходит для использования в качестве заместителя или усилителя MSG, который недостаточно хорошо переносится некоторыми людьми, например, в пищевых продуктах.
Кроме того, это агонистическое воздействие оказывает синергетическое воздействие на восприятие острого вкуса, это происходит, когда соединение по настоящему изобретению комбинируют с другим агентом, придающим острый вкусо-аромат, таким как MSG. Нуклеотиды IMP или GMP, как правило, вводят в MSG для интенсификации острого вкусо-аромата MSG, таким образом, для обеспечения одного и того же уровня вкуса необходимо меньшее количество MSG по сравнению с применением только одного MSG. Таким образом, комбинирование соединений по настоящему изобретению с другим агентом, придающим острый вкусо-аромат, таким как MSG, существенно снижает необходимость во введении дорогих нуклеотидов, таких как IMP, в качестве усилителей вкусо-аромата, в то же время попутно сокращая вводимое количество соединения, придающего острый вкусо-аромат, такого как MSG, для обеспечения такого же уровня вкуса по сравнению с применением только одного MSG.
«Синергетический эффект» используется здесь для описания усиленного вкусо-аромата комбинации из соединений с острым вкусо-ароматом или соединений, активирующих рецептор, по сравнению с суммированным вкусовым воздействием или вкусо-ароматическим воздействием, связанным с каждым отдельным соединением. В случае соединений, усиливающих острый вкусо-аромат, синергетическое воздействие на эффективность MSG может быть указано для соединений формулы (I), имеющих соотношение ЕС50 (определение приведено здесь ниже) 2,0 или более, или предпочтительно 5,0 или более, или 10,0 или более, или 15,0 или более.
Когда соединения, описанные здесь, включают один или более хиральный центр, стереохимия таких хиральных центров может независимо представлять собой R или S конфигурацию или смесь двух. Кроме того, хиральные центры могут быть обозначены как R или S или R,S или d,D, l,L или d,l, D,L. Соответственно соединения по настоящему изобретению, если они могут быть представлены необязательно в активной форме, могут быть представлены в форме рацемической смеси энантиомеров или в форме, по существу в выделенной и очищенной форме как отдельных энантиомеров, так и в смеси, включающей любые относительные пропорции энантиомеров. В случае, если указано в пунктах формулы, что единственный энантиомер из описанных потенциально оптически активных гетероциклических соединений является приемлемым по причинам здоровья или эффективности, то он предпочтительно присутствует в энантиомерном избытке, по меньшей мере, около 80% или, по меньшей мере, около 90%, или, по меньшей мере, около 95%, или, по меньшей мере, около 98%, или, по меньшей мере, около 99%, или, по меньшей мере, около 99,5%.
Термин «углеводородный остаток» используется здесь для описания химической подгруппы или радикала, находящегося в составе сложного химического соединения, которое содержит только атомы углерода и водорода. Углеводородный остаток может быть алифатическим или ароматическим, с нормальной неразветвленной цепью, циклическим, разветвленным, насыщенным или ненасыщенным. В большинстве вариантов воплощения настоящего изобретения углеводородные остатки представляют собой структуру с ограниченным пространственным размером и молекулярной массой и могут включать от 1 до 18 атомов углерода, от 1 до 16 атомов углерода, от 1 до 12 атомов углерода, от 1 до 10 атомов углерода, от 1 до 8 атомов углерода, от 1 до 6 атомов углерода или от 1 до 4 атомов углерода.
Углеводородный остаток, описанный здесь как «замещенный», содержит или замещен одним или более независимо выбранными гетероатомами, такими как O, S, N, P, или галогены (фтор, хлор, бром и йод) или одну или более замещающие группы, содержащие гетероатомы (OH, NH2, NO2, SO3H и т.п.) и дополнительно атомы углерода и водорода замещающего остатка. Замещенные углеводородные остатки также могут содержать карбонильные группы, аминогруппы, гидроксильные группы и тому подобное или содержат гетероатомы, встроенные в «основу» углеводородного остатка.
Термин «неорганическая» группа или остаток используется здесь для описания нейтральных, катионных или анионных радикалов заместителей органических молекул, описанных или заявленных здесь, которые имеют от 1 до 16 атомов, которые не включают углерод, но содержат другие гетероатомы из периодической таблицы, которые предпочтительно включают один или более атомов, независимо выбранных из H, O, N, S, один или более галоген или ионы щелочноземельного металла. Примеры неорганических металлов включают, но не ограничиваются H, Na+, Ca++ и K+, галогены, которые включают фтор, хлор, бром и йод, OH, SH, SO3H, SO3-, PO3H, PO3-, NO, NO2 или NH2 и тому подобное.
Используемый здесь термин «алкил», «алкенил» и «алкинил» включает заместители с прямой и разветвленной цепью и циклические моновалентные заместители, которые соответственно представляют насыщенные и ненасыщенные, по меньшей мере, с одной двойной связью, и ненасыщенные, по меньшей мере, с одной тройной связью.
«Алкил» используется здесь для описания углеводородной группы, которая по существу может быть образована из алкана удалением водорода из структуры нециклического углеводородного соединения с прямыми или разветвленными углеродными цепями и замещением атома водорода другим атомом или органической или неорганической замещающей группой. В некоторых вариантах воплощения настоящего изобретения алкильные группы представляют собой «С1-С6 алкил», такой как метил, этил, пропил, изопропил, н-бутил, изо-бутил, втор-бутил, трет-бутил, амил, трет-амил, гексил и т.п. Большинство вариантов воплощения настоящего изобретения включают «С1-С4 алкильные» группы (в качестве альтернативы называемые «низшие алкилы»), которые включают метил, этил, пропил, изо-пропил, н-бутил, изо-бутил, втор-бутил и т-бутил группы. Некоторые из предпочтительных алкильных групп по настоящему изобретению имеют три или более атомов углерода, предпочтительно от 3 до 16 атомов углерода, от 4 до 14 атомов углерода или от 6 до 12 атомов углерода.
Используемый здесь термин «алкенил» относится к структурным аналогам алкильной группы или остатку, который включает, по меньшей мере, одну двойную связь углерод-углерод. В некоторых вариантах воплощения настоящего изобретения алкенильные группы представляют собой «С2-С7 алкенилы», примерами которых являются винил, аллил, 2-бутенил, 3-бутенил, 2-пентенил, 3-пентенил, 4-пентенил, 2-гексенил, 3-гексенил, 4-гексенил, 5-гексенил, 2-гептенил, 3-гептенил, 4-гептенил, 5-гептенил, 6-гептенил наряду с диенами и триенами с прямой и разветвленной цепью. В других вариантах воплощения настоящего изобретения алкенилы могут быть ограничены от двух до четырех атомами углерода.
Термин «алкинил» относится к структурным аналогам алкильной группы или радикала, которые включают по меньшей мере одну тройную связь углерод-углерод. Предпочтительные алкинильные группы представляют собой «С2-С7 алкинилы», такие как этинил, пропинил, 2-бутинил, 2-пентинил, 3-пентинил, 2-гексинил, 3-гексинил, 4-гексинил, 2-гептинил, 3-гептинил, 4-гептинил, 5-гептинил наряду с ди- и триинами с прямой или разветвленной цепью, включая ен-ины.
Термины «замещенный алкил», «замещенный алкенил», «замещенный алкинил» и «замещенный алкилен» определяют алкильные, алкенильные или алкинильные группы или радикалы, как описано выше, где один или более атом водорода по существу замещен одним или более и предпочтительно одной или двумя независимо выбранными органическими или неорганическими замещающими группами или радикалами, которые могут включать галоген, гидрокси, амино, SH, C1-C7 алкокси или алкокси-алкил, оксо, C3-C7 циклоалкил, нафтил, амино, (монозамещенные)амино, (двузамещенные)амино, гуанидино, гетероциклические, замещенные гетероциклические, имидазолил, индолил, пирролидинил, C1-C7 ацил, C1-C7 ацилокси, нитро, карбокси, карбамоил, карбоксамид, N-(C1-C6алкил)карбоксамид, N,N-ди(C1-C6 алкил)карбоксамид, циано, метилсульфониламино, тиол, C1-C4алкилтио или C1-C4алкилсульфонильные группы. Замещенные алкильные группы могут быть замещены одним или более, предпочтительно единожды или дважды одними и теми же или разными заместителями. В большинстве вариантов воплощения настоящего изобретения предпочтительной группой из замещающих групп для большинства алкилов являются гидрокси, фтор, хлор, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метил, этил, изопропил, винил, трифторметил, метокси, этокси, изопропокси и трифторметокси группы. В большинстве вариантов воплощения настоящего изобретения, которые включают приведенные выше замещающие группы, более предпочтительной группой из замещающих групп являются гидрокси, SEt, SCH3, метил, этил, изопропил, трифторметил, метокси, этокси и трифторметокси группы.
Примеры приведенных выше замещенных алкильных групп включают 2-оксопроп-1-ил, 3-оксобут-1-ил, цианометил, нитрометил, хлорметил, трифторметил, гидроксиметил, тетрагидропиранилоксиметил, тритилоксиметил, пропионилоксиметил, аминометил, карбоксиметил, аллилоксикарбонилметил, аллилоксикарбониламинометил, метоксиметил, этоксиметил, т-бутоксиметил, ацетоксиметил, хлорметил, трифторметил, 6-гидроксигексил, 2,4-дихлор(н-бутил), 2-аминопропил, 1-хлорэтил, 2-хлорэтил, 1-бромэтил, 2-хлорэтил, 1-фторэтил, 2-фторэтил, 1-йодэтил, 2-йодэтил, 1-хлорпропил, 2-хлорпропил, 3-хлорпропил, 1-бромпропил, 2-бромпропил, 3-бромпропил, 1-фторпропил, 2-фторпропил, 3-фторпропил, 2-аминоэтил, 1-аминоэтил, N-бензоил-2-аминоэтил, N-ацетил-2-аминоэтил, N-бензоил-1-аминоэтил, N-ацетил-1-аминоэтил и т.п.
Примеры замещенных алкенильных групп включают стиренил, 3-хлорпропен-1-ил, 3-хлорбутен-1-ил, 3-метоксипропен-2-ил, 3-фенилбутен-2-ил, 1-цианобутен-3-ил и т.д. Геометрическая изомерия не является решающей, и для проведения замещения двойных связей могут быть использованы все геометрические изомеры.
Примеры замещенных алкинильных групп воключают фенилацетилен-1-ил, 1-фенил-2-пропин-1-ил и т.д.
Галогеналкилы представляют собой замещенные алкильные группы или остатки, где один или более атомов водорода соответствующей алкильной группы замещен атомом галогена (фтора, хлора, брома и йода). Предпочтительные галогеналкилы могут иметь от одного до четырех атомов углерода. Примеры предпочтительных галогеналкильных групп включают трифторметил и пентафторэтил.
Галогеналкокси группы представляют собой алкокси группы или остатки, где один или более атомов водорода из R группы алкокси группы представляет собой атом галогена (фтора, хлора, брома и йода). Предпочтительные галогеналкокси группы могут иметь от одного до четырех атомов углерода. Примеры предпочтительных галогеналкокси групп включают трифторметиокси и пентафторэтокси группы.
Термин «оксо» определяет атом углерода, связанный с двумя дополнительными атомами углерода, замещенный атомом кислорода, связанным двойной связью с атомом углерода с образованием кетонового радикала или остатка.
«Алкокси» или «алкоксил» используется здесь для обозначения -OR радикала или группы, где R представляет собой алкильный радикал. В некоторых вариантах воплощения настоящего изобретения алкокси группы могут быть C1-C8 и в других вариантах воплощения настоящего изобретения алкокси группы могут быть C1-C4, где R представляет собой низший алкил, такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси, т-бутокси и подобные алкокси группы. Термин «замещенный алкокси» обозначает, что R группа представляет собой замещенную алкильную группу или остаток. Примеры замещенных алкокси групп включают трифторметокси, гидроксиметил, гидроксиэтил, гидроксипропил и алкоксиалкил, такие как метоксиметил, метоксиэтил, полиоксоэтилен, полиоксопропилен и им подобные.
«Алкоксиалкил» используется здесь для обозначения -R-O-R' группы или радикала, где R и R' представляют собой алкильные группы. В некоторых вариантах воплощения настоящего изобретения алкоксиалкильные группы могут быть C1-C8 и в других вариантах воплощения настоящего изобретения могут быть C1-C4. В большинстве вариантов воплощения настоящего изобретения как R, так и R' представляют собой низший алкил, такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси, т-бутокси и подобные алкокси группы. Примеры алкоксиалкильных групп включают метоксиметил, этоксиэтил, метоксипропил, метоксибутил и им подобные.
«Ацилокси» используется здесь для определения RCO2- эфирной группы, где R представляет собой алкильную, циклоалкильную, арильную, гетероарильную, замещенную алкильную, замещенную циклоалкильную, замещенную арильную или замещенную гетероарильную группу или радикал, где R радикал включает от одного до семи или от одного до четырех атомов углерода. В большинстве вариантов воплощения настоящего изобретения R представляет собой алкильный радикал, и такие ацилокси радикалы, как, например, формилокси, ацетокси, пропионилокси, бутирилокси, пивалоилокси, пентаноилокси, гексаноилокси, гептаноилокси и подобные. В других вариантах воплощения настоящего изобретения R группы представляют собой С1-С4 алкилы.
Используемый здесь термин «ацил» включает в себя алкильные, алкенильные, алкинильные и родственные гетероформы, которые связаны с дополнительным органическим остатком через карбонильную группу с образованием кетонового радикала или группы. Предпочтительные ацильные группы представляют собой «С1-С7 ацилы», такие как формил, ацетил, пропионил, бутирил, пентаноил, пивалоил, гексаноил, гептаноил, бензоил и им подобные. Более предпочтительные ацильные группы представляют собой ацетил и бензоил.
Термин «замещенный ацил» определяет ацильную группу, где R группа замещена одним или более и предпочтительно одним или двумя галогеном, гидрокси, оксо, алкилом, циклоалкилом, нафтилом, амино, (монозамещенным)амино, (двузамещенным)амино, гуанидино, гетероциклическим кольцом, замещенным гетероциклическим кольцом, имидазолилом, индолилом, пирролидинилом, C1-C7 алкокси, алкокси-алкилом, C1-C7 ацилом, C1-C7 ацилокси, нитро, C1-C6 алкил эфиром, карбокси, алкоксикарбонилом, карбамоилом, карбоксамидом, N-(C1-C6алкил)карбоксамидом, N,N-ди(C1-C6 алкил)карбоксамидом, циано, метилсульфониламино, тиолом, C1-C4алкилтио или C1-C4алкилсульфонильными группами. Замещенные ацильные группы могут быть замещены одним или более, предпочтительно единожды или дважды одними и теми же или разными заместителями.
Примеры C1-C7 замещенных ацильных групп включают 4-фенилбутироил, 3-фенилбутироил, 3-фенилпропаноил, 2-циклогексанилацетил, циклогексанкарбонил, 2-фураноил и 3-диметиламинобензоил.
Циклоалкильные остатки или группы представляют собой структурно родственные циклическим, а именно циклическим или бициклическим углеводородным соединениям, где один или более атом водорода замещен органической или неорганической замещающей группой. Циклоалкилы по настоящему изобретению включают, по меньшей мере, от 3 до 12 или более предпочтительно от 3 до 8 атомов углерода в кольце или более предпочтительно от 4 до 6 атомов углерода в кольце. Примеры таких циклоалкильных остатков включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и насыщенные бициклические или конденсированные полициклические циклоалканы, такие как декалиновые группы, полициклические норборнильные или адамантильные группы и им подобные.
Предпочтительные циклоалкильные группы включают «C3-C7 циклоалкилы», такие как кольца циклопропила, циклобутила, циклопентила, циклогексила или циклогептила. Аналогично, термин «C5-C7 циклоалкилы» включает кольца циклопентила, циклогексила или циклогептила.
«Замещенный циклоалкил» относится к циклоалкильным кольцам таким, как описано выше, замещенным от одного до четырех, предпочтительно одним или двумя заместителями, независимо выбранными из галогена, гидрокси, C1-C4 алкилтио, C1-C4 алкилсульфоксида, C1-C4 алкилсульфонила, C1-C4 замещенного алкилтио, C1-C4 замещенного алкилсульфоксида, C1-C4 замещенного алкилсульфонила, C1-C4 алкила, C1-C4 алкокси, C1-C6 замещенного алкила, C1-C4 алкокси-алкила, оксо, (монозамещенным)амино, (двузамещенным)амино, трифторметила, карбокси, фенила, замещенного фенила, фенилтио, фенилсульфоксида, фенилсульфонила, амино. В большинстве вариантов воплощения замещенных циклоалкильных групп замещенная циклоалкильная группа может иметь 1, 2, 3 или 4 замещенные группы, независимо выбранные из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3,метила, этила, изопропила, винила, трифторметила, метокси, этокси, изопропокси и трифторметокси.
Термин «циклоалкилен» относится к циклоалкилу, как описано выше, где циклоалкильный радикал связан в двух позициях, соединяя вместе две отдельные дополнительные группы. Аналогично, «замещенный циклоалкилен» относится к циклоалкилену, у которого циклоалкильный радикал связан в двух позициях, соединяя вместе две отдельные дополнительные группы, несущий дополнительно, по меньшей мере, один дополнительный заместитель.
Термин «циклоалкенил» означает предпочтительно 1, 2 или 3-циклопентенильное кольцо, 1, 2, 3 или 4-циклогексенильное кольцо или 1, 2, 3, 4 или 5-циклогептенильное кольцо, при этом термин «замещенный циклоалкенил» относится к описанным выше циклоалкенильным кольцам, замещенным заместителем, предпочтительно C1-C6 алкилом, галогеном, гидрокси, C1-C7 алкокси, алкокси-алкилом, трифторметилом, карбокси, алкоксикарбонилом, оксо, (монозамещенным)амино, (двузамещенным)амино, фенилом, замещенным фенилом, амино или защищенным амино.
Термин «циклоалкенилен» означает циклоалкенильное кольцо, как описано выше, где циклоалкенильный радикал связан в двух позициях, соединяя вместе две отдельные дополнительные группы. Аналогично, «замещенный циклоалкенилен» относится к циклоалкенилену, дополнительно замещенному предпочтительно галогеном, гидрокси, C1-C4 алкилтио, C1-C4 алкилсульфоксидом, C1-C4 алкилсульфонилом, C1-C4 замещенным алкилтио, C1-C4 замещенным алкилсульфоксидом, C1-C4 замещенным алкилсульфонилом, C1-C6 алкилом, C1-C7 алкокси, C1-C6 замещенным алкилом, C1-C7 алкокси-алкилом, оксо, (монозамещенным)амино, (двузамещенным)амино, трифторметилом, карбокси, алкоксикарбонилом, фенилом, замещенным фенилом, фенилтио, фенилсульфоксидом, фенилсульфонилом, амино или замещенной амино группой.
Термин «гетероцикл» или «гетероциклическое кольцо» относится к необязательно замещенным 3-8-членным кольцам, имеющим один или более атомов углерода, связанных в кольце, которые также включают от 1 до 5 гетероатомов в кольце, таких как кислород, сера и/или азот, входящих в кольцо. Эти гетероциклические кольца могут быть насыщенными, ненасыщенными или частично ненасыщенными, но предпочтительны насыщенные. Предпочтительные ненасыщенные гетероциклические кольца включают фуранил, тиофуранил, пирролил, пиридил, пиримидил, пиразинил, бензоксазол, бензтиазол, хинолинил и подобные гетероатомные кольца. Предпочтительные насыщенные гетероциклические кольца включают пиперидил, азиридинил, пиперидинил, пиперазинил, тетрагидрофурано, пирролил и тетрагидротиофенил.
Термин «замещенный гетероцикл» или «замещенное гетероциклическое кольцо» относится к описанному выше гетероциклическому кольцу замещенному, например, одним или более и предпочтительно одним или двумя заместителями, теми же или другими заместителями, предпочтительно, представляющими собой галоген, гидрокси, тио, алкилтио, циано, нитро, C1-C4 алкил, C1-C4 алкокси, С1-С4 замещенный алкокси, алкокси-алкил, С1-С4 ацил, С1-С4 ацилокси, карбокси, алкоксикарбонил, карбоксиметил, гидроксиметил, алкокси-алкиламино, (монозамещенный)амино, (двузамещенный)амино карбоксамид, N-(C1-C6 алкил)карбоксамид, N,N-ди(C1-C6 алкил)карбоксамид, трифторметил, N-((C1-C6 алкил)сульфонил)амино, N-(фенилсульфонил)амино группы, или замещенные конденсированным кольцом, таким как бензокольцо. В большинстве вариантов воплощения настоящего изобретения замещенные гетероциклические группы, замещенные циклоалкильные группы могут иметь 1, 2, 3 или 4 замещающих группы, независимо выбранные из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, винила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп.
«Арильная» группа используется здесь для описания моноциклического, связанного бициклического или конденсированного бициклического радикала или группы, включающей, по меньшей мере, одно шестичленное ароматическое «бензольное» кольцо. Арильные группы предпочтительно включают от 6 до 12 атомов углерода в кольце, например, фенил, бифенил, нафтил, инданил и тетрагидронафтил. Арильные группы могут быть необязательно замещены различными органическими и/или неорганическими замещающими группами, где замещенная арильная группа в комбинации со всеми ее заместителями включает от 6 до 18 или, предпочтительно, от 6 до 16 атомов углерода. Предпочтительные необязательные замещающие группы включают 1, 2, 3 или 4 замещающих группы, независимо выбранных из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, винила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп.
Термин «гетероарильный» относится к производному гетероциклического арила, предпочтительно, включающему пяти- или шестичленную конъюгированную или ароматическую кольцевую систему, имеющую от 1 до 4 гетероатомов, независимо выбранных из кислорода, серы и/или азота, встроенных в ненасыщенное и конъюгированное гетероциклическое кольцо. Гетероарильные группы включают моноциклические гетероароматические, связанные бициклические гетероароматические или конденсированные бициклические гетероароматические фрагменты. Примеры гетероарилов включают пиридинил, пиримидинил и пиразинил, пиридазинил, пирролил, фуранил, тиофуранил, оксазолил, изоксазолил, фталимидо, тиазолил, хинолинил, изохинолинил, индолил или фуран или тиофуран непосредственно/прямо с фенилом, пиридилом или пирролилом и подобными ненасыщенными и конъюгированными гетероароматическими кольцами. В это определение включается любая моноциклическая, связанная бициклическая или конденсированная бициклическая гетероарильная кольцевая система, обладающая характеристиками ароматичности, включая распределение электронов в кольцевой системе. Как правило, гетероароматические кольцевые системы содержат 3-12 атомов углерода в кольце и от 1 до 5 гетероатомов в кольце, независимо выбранных из атомов кислорода, азота и серы.
Термин «замещенный гетероарил» относится к описанному выше гетероарилу замещенному, например, одним или более и предпочтительно одним или двумя заместителями теми же или другими, предпочтительно представляющими собой галоген, гидрокси, защищенный гидрокси, тио, алкилтио, циано, нитро, C1-C6 алкил, C1-C7 замещенный алкил, C1-C7 алкокси, C1-C7 замещенный алкокси, алкокси-алкил, C1-C7 ацил, C1-C7 замещенный ацил, C1-C7 ацилокси, карбокси, алкоксикарбонил, карбоксиметил, гидроксиметил, амино, (монозамещенный)амино, (двузамещенный)амино, карбоксамид, N-(C1-C6 алкил)карбоксамид, N,N-ди(C1-C6 алкил)карбоксамид, трифторметил, N-((C1-C6 алкил)сульфонил)амино, N-(фенилсульфонил)амино группы. В большинстве вариантов воплощения замещенные гетероарильные группы, замещенная циклоалкильная группа будет иметь 1, 2, 3 или 4 замещающих группы, независимо выбранные из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, винила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп.
Аналогично «арилалкил» и «гетероарилалкил» относятся к ароматическим и гетероароматическим системам, соединенным с другим остатком углеродной цепью, включая замещенные или незамещенные, насыщенные или ненасыщенные углеродные цепи, как правило, с 1-6 С. Эти углеродные цепи также могут включать карбонильную группу, что делает их, таким образом, способными взаимодействовать с заместителями, такими как ацильный фрагмент. Предпочтительно арилалкил или гетероарилалкил представляет собой алкильную группу, замещенную в любом положении арильной группой, замещенным арилом, гетероарилом или замещенным гетероарилом. Предпочтительные группы также включают бензил, 2-фенилэтил, 3-фенилпропил, 4-фенил-н-бутил, 3-фенил-н-амил, 3-фенил-2-бутил, 2-пиридинилметил, 2-(2-пиридинил)этил и им подобные.
Термин «замещенный арилалкил» относится к арилалкильной группе, замещенной в положении алкила одной или более и предпочтительно одной или двумя группами, предпочтительно выбранными из галогена, гидрокси, оксо, амино, (монозамещенный)амино, (двузамещенный)амино, гуанидино, гетероциклического кольца, замещенного гетероциклического кольца, C1-C6 алкила, C1-C6 замещенного алкила, C1-C7 алкокси, C1-C7 замещенного алкокси, алкокси-алкила, C1-C7 ацила, C1-C7 замещенного ацила, C1-C7 ацилокси, нитро, карбокси, алкоксикарбонила, карбамоила, карбоксамида, N-(C1-C6 алкил)карбоксамида, N,N-(C1-C6 диалкил)карбоксамида, циано, N-(C1-C6 алкилсульфонил)амино, тиола, C1-C4 алкилтио, C1-C4 алкилсульфонильных групп; и/или фенильная группа может быть замещена одним или более и предпочтительно одним или двумя заместителями, предпочтительно выбранными из галогена, гидрокси, защищенного гидрокси, тио, алкилтио, циано, нитро, C1-C6 алкила, C1-C6 замещенного алкила, C1-C7 алкокси, C1-C7 замещенного алкокси, алкокси-алкила, C1-C7 ацила, C1-C7 замещенного ацила, C1-C7 ацилокси, карбокси, алкоксикарбонила, карбоксиметила, гидроксиметила, амино, (монозамещенного)амино, (двузамещенного)амино, карбоксамида, N-(C1-C6 алкил)карбоксамида, N,N-ди(C1-C6 алкил)карбоксамида, трифторметила, N-((C1-C6 алкил)сульфонил)амино, N-(фенилсульфонил)амино, циклического C2-C7 алкилена или фенильной группы, замещенной или незамещенной с получением в результате бифенильной группы. Замещенная алкильная или фенильная группы могут быть замещены одним или более и предпочтительно одним или двумя заместителями, теми же или другими.
Примеры термина «замещенный арилалкил» включают группы, такие как 2-фенил-1-хлорэтил, 2-(4-метоксифенил)этил, 4-(2,6-дигидроксифенил)-н-гексил, 2-(5-циано-3-метоксифенил)-н-пентил, 3-(2,6-диметилфенил)пропил, 4-хлор-3-аминобензил, 6-(4-метоксифенил)-3-карбокси-н-гексил, 5-(4-аминометилфенил)-3-(аминометил)-н-пентил, 5-фенил-3-оксо-н-пент-1-ил и т.п.
Термин «арилалкилен» относится к арилалкилу, как описано выше, где арилалкильный радикал связан в двух позициях, соединяя вместе две отдельные дополнительные группы. Определение включает группы, имеющие формулу: -фенил-алкил- и алкил-фенил-алкил-. В фенильном кольце могут быть замещения 1,2, 1,3 или 1,4. Термин «замещенный арилалкилен» относится к арилалкилену, как описано выше, который дополнительно замещен предпочтительно галогеном, гидрокси, защищенным гидрокси, C1-C4 алкилтио, C1-C4 алкилсульфоксидом, C1-C4 алкилсульфонилом, C1-C4 замещенным алкилтио, C1-C4 замещенным алкилсульфоксидом, C1-C4 замещенным алкилсульфонилом, C1-C6 алкилом, C1-C7 алкокси, C1-C6 замещенным алкилом, C1-C7 алкокси-алкилом, оксо, (монозамещенный)амино, (двузамещенный)амино, трифторметилом, карбокси, алкоксикарбонилом, фенилом, замещенным фенилом, фенилтио, фенилсульфоксидом, фенилсульфонилом, амино или защищенной амино группой в фенильном кольце или в алкильной группе.
Термин «замещенный фенил» относится к фенильной группе, замещенной одним или более и предпочтительно одним или двумя фрагментами, предпочтительно выбранными из группы, включающей галоген, гидрокси, защищенный гидрокси, тио, алкилтио, циано, нитро, C1-C6 алкил, C1-C6 замещенный алкил, C1-C7 алкокси, C1-C7 замещенный алкокси, алкокси-алкил, C1-C7 ацил, C1-C7 замещенный ацил, C1-C7 ацилокси, карбокси, алкоксикарбонил, карбоксиметил, гидроксиметил, амино, (монозамещенный)амино, (двузамещенный)амино, карбоксамид, N-(C1-C6 алкил)карбоксамид, N,N-ди(C1-C6 алкил) карбоксамид, трифторметил, N-((C1-C6 алкил)сульфонил)амино, N-(фенилсульфонил)амино или фенил, где фенил представляет замещенный или незамещенный, такой как, например, полученный в результате бифенил. В большинстве вариантов воплощения замещенные фенильные группы, замещенная циклоалкильная группа имеют 1, 2, 3 или 4 замещающих группы, независимо выбранные из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, винила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп.
Термины «гало» и «галоген» относятся к атомам или ионам фтора, хлора, брома или йода или ионами. Предпочтительные галогены представляют фтор и хлор. Хотя многие соединения по настоящему изобретению содержат атомы галогена в качестве заместителей, они проявляют высокую эффективность в связывании с рецепторами, отвечающими за распознавание вкуса умами, такие галогенированные органические соединения в некоторых случаях могут проявлять нежелательные токсические свойства при введении животным in vivo. Таким образом, в различных вариантах соединений формулы (I), если атом галогена (включая атом фтора, хлора, брома или йода) включен в список в качестве возможного заместителя, в качестве альтернативы и предпочтительной группы заместителей, а именно как предполагаемый, то не следует туда включать галогенные группы.
Термин «(монозамещенный)амино» относится к амино (NHR) группе, где R группа выбрана из группы, состоящей из фенила, C6-C10 замещенного фенила, C1-C6 алкила, C1-C6 замещенного алкила, C1-C7 ацила, C1-C7 замещенного ацила, C2-C7 алкенила, C2-C7 замещенного алкенила, C2-C7 алкинила, C2-C7 замещенного алкинила, C7-C12 фенилалкила, C7-C12 замещенного фенилалкила и гетероциклического кольца. (Монозамещенный)амино может иметь дополнительно аминозащищающую группу, которая подпадает под термин «защищенный (монозамещенный)амино».
Термин «(двузамещенный)амино» относится к амино (NR2) группе с двумя заместителями, независимо выбранными из группы, состоящей из фенила, C6-C10 замещенного фенила, C1-C6 алкила, C1-C6 замещенного алкила, C1-C7 ацила, C2-C7 алкенила, C2-C7 алкинила, C7-C12 фенилалкила и C7-C12 замещенного фенилалкила. Оба заместителя могут быть одинаковыми или различными.
Термин «алкилтио» относится к -SR группам, где R представляет собой необязательно замещенную C1-C7 или C1-C4органическую группу, предпочтительно алкил, циклоалкил, арил или гетероциклическую группу, такую как метилтио, этилтио, н-пропилтио, изопропилтио, н-бутилтио, т-бутилтио и им подобные.
Термин «алкилсульфоксид» относится к -SO2R группам, где R представляет собой необязательно замещенную C1-C7 или C1-C4органическую группу, предпочтительно алкил, циклоалкил, арил или гетероциклическую группу, такую как метилтио, этилтио, н-пропилтио, изопропилтио, н-бутилтио, т-бутилтио и им подобные группы, такие как метилсульфоксид, этилсульфоксид, н-пропилсульфоксид, изопропилсульфоксид, н-бутилсульфоксид, втор-бутилсульфоксид и им подобные.
Термин «алкилсульфонил» относится к -S(O)R группам, где R представляет собой необязательно замещенную C1-C7 или C1-C4органическую группу, которая включает, например, группы, такие как метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, т-бутилсульфонил и им подобные.
Термины «фенилтио», «фенилсульфоксид» и «фенилсульфонил» определяют сульфоксид (-S(O)-R) или сульфон (-SO2R), где R группа представляет собой фенильную группу. Термины «замещенный фенилтио», «замещенный фенилсульфоксид» и «замещенный фенилсульфонил» означают, что фенил этих групп может быть замещен, как описано выше в отношении «замещенного фенила».
Термин «алкоксикарбонил» обозначает, что «алкокси» группа связана с карбонильной группой (например, эфир карбоновой кислоты) -C(O)-OR, где R представляет собой предпочтительно алкильную группу, предпочтительно C1-C4 алкильную группу. Термин «замещенный алкоксикарбонил» относится к замещенному алкокси, связанному с карбонильной группой, алкокси может быть замещен, как описано выше в отношении замещенного алкила.
Термин «фенилен» обозначает фенильную группу, где фенильный радикал связан в двух позициях, соединяя вместе две отдельные дополнительные группы. Примеры «фенилена» включают 1,2-фенилен, 1,3-фенилен и 1,4-фенилен.
Термин «замещенный алкилен» обозначает алкильную группу, где алкильный радикал связан в двух позициях, соединяя вместе две отдельные дополнительные группы, и несет дополнительный заместитель. Примеры «замещенного алкилена» включают аминометилен, 1-(амино)-1,2-этил, 2-(амино)-1,2-этил, 1-(ацетамидо)-1,2-этил, 2-(ацетамидо)-1,2-этил, 2-гидрокси-1,1-этил, 1-(амино)-1,3-пропил.
Одно или более соединений по настоящему изобретению могут представлять собой соль. Термин «соль» включает соли, образованные анионами карбоксилата и азота аминогруппы, и включают соли, образованные органическими и неорганическими анионами и катионами, приведенными ниже. Кроме того, термин включает соли, которые образуются в результате стандартных кислотно-основных реакций с основными группами (такими как азот, включающий гетероциклы или аминогруппы), и органические или неорганические кислоты. Такие кислоты включают соляную, плавиковую, трифторуксусную, серную, фосфорную, уксусную, янтарную, лимонную, молочную, яблочную, муравьиную, пальмитиновую, холевую, памовую, муциновую, D-глютаминовую, D-камфорную, глутаровую, фталиевую, винную, лауриновую, стеариновую, салициловую, метансульфоновую, бензолсульфоновую, сорбиновую, пикриновую, бензойную, коричную и подобные кислоты.
Термин «органический или неорганический катион» относится к положительно заряженным ионам для карбоксилатного аниона карбоксилатной соли. Неорганические положительно заряженные ионы включают, но не ограничиваются щелочными и щелочноземельными металлами (такими как литий, натрий, калий, кальций, магний и т.п.) и другими двухвалентными и трехвалентными катионами металлов, такими как барий, алюминий и подобные, и катионами аммония (NH4)+. Органические катионы включают катионы аммония, полученные при обработке кислотой или алкилтио первичных, вторичных или третичных аминов, таких как триметиламин, циклогексиламин; и органические катионы, такие как дибензиламмоний, бензиламмоний, 2-гидроксиэтиламмоний, бис(2-гидроксиэтил)аммоний, фенилэтилбензиламмоний, дибензилэтилендиаммоний и им подобные катионы. См., например, Pharmaceutical Salts,” Berge, et al.,J. Pharm. Sci. (1977) 66:1-19, включенную в качестве ссылки. Другие катионы, подходящие под вышеуказанный термин, включают протонированные формы прокаина, хинина и N-метилглюкозамин и протонированные формы основных аминокислот, таких как глицин, орнитин, гистидин, фенилглицин, лизин и аргинин. Кроме того, любая цвиттер-ионная форма растворимых соединений, образованных карбоновой кислотой и аминогруппой, также относится к этому термину. Например, катион для карбоксилатного аниона будет существовать, когда R2 или R3 замещен (четвертичный аммоний) метильной группой. Предпочтительным катионом для карбоксилатного аниона является катион натрия.
Соединения по настоящему изобретению также могут присутствовать как растворители и гидраты. Таким образом, эти соединения могут кристаллизоваться, например, гидратационной водой или одной молекулой или целым рядом молекул, или любой фракцией исходного раствора растворителя. В объем настоящего изобретения входят растворители и гидраты таких соединений.
Термин «аминокислота» включает любую одну из двадцати аминокислот природного происхождения или D-форму любой одной из аминокислот природного происхождения. Дополнительно термин «аминокислота» также включает другие аминокислоты неприродного происхождения, помимо D-аминокислот, которые представляют собой функциональные эквиваленты аминокислот природного происхождения. Такие аминокислоты неприродного происхождения включают, например, норлейцин (“Nle”), норвалин (“Nva”), L- или D-нафталанин, орнитин (“Orn”), гомоаргинин (homoArg) и другие пептиды, хорошо известные из уровня техники, такие как описанные в M. Bodanzsky, “Principles of Peptide Synthesis,” 1st and 2nd revised ed., Springer-Verlag, New York, NY, 1984 and 1993, и Stewart and Young, “Solid Phase Peptide Synthesis,” 2nd ed., Pierce Chemical Co., Rockford, IL, 1984, оба включены в качестве ссылки. Аминокислоты и аналоги аминокислот могут быть закуплены (Sigma Chemical Co.; Advanced Chemtech) или синтезированы по способам, известным из уровня техники.
Остатки химических веществ, приведенные в описании и формуле, относятся к структурным фрагментам или фрагментам, которые являются конечным продуктом химических веществ, участвующих в специфических химических реакциях или последующих химических реакциях или химических продуктах, независимо от структуры фрагментов или фрагментов, фактически полученных из химических веществ. Таким образом, этиленгликольный остаток в полиэфире относится к одной или более -OCH2CH2O- повторяющимся единицам полиэфира, независимо от того, какой этиленгликоль использовался для получения полиэфира.
Термин «органический остаток» или «органический радикал» относится к остатку или радикалу, содержащему углерод, включающему, по меньшей мере, один атом углерода. Органические остатки могут содержать один или более гетероатомов или быть связанными с другими молекулами через гетероатом, включая кислород, азот, серу, фосфор или им подобные. Примеры органических остатков включают, но не ограничиваются, алкил или замещенные алкилы, алкоксилы или замещенные алкоксилы, гидроксиалкилы и алкоксиалкилы, циклоалкил или замещенные циклоалкилы, циклоалкенил или замещенные циклоалкенилы, гетероциклы или замещенные гетероциклы, арилы или замещенные арилы, гетероарилы или замещенные гетероарилы, моно или дизамещенные амино, амидные группы, CN, CO2H, CHO, COR6, CO2R6, SR6, где R6 представляет собой алкил или ему подобные. Примеры веществ органических групп или органических остатков включают, но не ограничиваются, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метил, этил, изопропил, винил, трифторметил, метокси, этокси, изопропокси, трифторметокси, фенил, феноксил и пиридильные группы или остатки и им подобные. Органические остатки могут включать от 1 до 18 атомов углерода, от 1 до 15 атомов углерода, от 1 до 12 атомов углерода, от 1 до 8 атомов углерода или от 1 до 4 атомов углерода.
Под термином «эффективное количество» соединения, описанного здесь, понимается количество, достаточное для обеспечения требуемой регуляции требуемой функции, такой как генная экспрессия, белковая функция или индукция определенного типа вкусового восприятия. Как указано ниже, точное количество варьирует от субъекта к субъекту, в зависимости от специфики, возраста, общего состояния субъекта, от специфических особенностей и рецептурного состава пищевой композиции и т.п. Таким образом, не представляется возможным точно указать «эффективное количество». Однако соответствующее эффективное количество может быть определено специалистом в данной области техники, использующим только рутинные эксперименты.
Следует отметить, что использованные в описании и формуле изобретения артикли единственного числа “a,” “an” и “the” включают понятие множественного числа, несмотря на контекст. Так, например, ссылка «ароматическое соединение» включает смесь ароматических соединений.
Как правило, пределы выражают здесь от «около» одного частного значения и/или до «около» другого частного значения. Когда пределы выражены таким образом, то один из вариантов воплощения настоящего изобретения включает от одного частного значения и/или до другого частного значения. Аналогично, когда показатели выражены, как приблизительные значения с использованием антецедента «около», следует понимать, что частное значение составляет еще один вариант воплощения изобретения. Кроме того, следует понимать, что крайние значения пределов оба являются важными показателями от одного предела до другого.
«Необязательный» или «необязательно» обозначает, что последующее событие или обстоятельства могут произойти или могут не произойти, и описание включает примеры, в которых указанное событие или обстоятельства происходят, и примеры, в которых указанное событие или обстоятельства не происходят. Например, фраза «необязательно замещенный низший алкил» подразумевает группу низшего алкила замещенного или незамещенного, и описание включает как незамещенный низший алкил, так и замещенный низший алкил.
Связанные гетероарильные соединения по настоящему изобретению
Предположительно связанные гетероарильные соединения, описанные здесь, являются агонистами и/или аллостерическими модификаторами белков рецепторов вкуса умами, однако авторы не хотели бы быть ограниченными определенной теорией. Кроме того, разумно предположить, что связанные гетероарильные соединения имеют ядро из связанных структурных элементов, которое предположительно является целым, и, несмотря на некоторую возможность изменения отдельных структурных элементов или их периферийных заместителей, имеют размер, форму и/или полярность, которые обуславливают сильное и специфическое взаимное притяжение с белками рецепторов вкуса умами, таким образом, связанные гетероарильные соединения могут модифицировать, улучшать и/или усиливать вкус умами пищевых продуктов, потребляемых в пищу животными и/или человеком. Таким образом, связанные гетероарильные соединения хотя и могут отличаться в некоторых аспектах, но несмотря на это имеют одинаковые структурные признаки, что позволяет варьировать до некоторой степени, усиливая желаемое агонистическое и/или аллостерическое связующее взаимодействие с белками рецепторов вкуса умами.
Таким образом, соединения по настоящему изобретению включают, по меньшей мере, две ароматические «арильные» или «гетероарильные» группы hAr1 и hAr2 и третью арильную или гетероарильную кольцевую группу Ar, все три из этих ароматических кольцевых групп могут быть необязательно замещены различными периферийными заместителями. Кроме того, hAr1, hAr2и Ar кольцевые группы связаны вместе мостиковыми или связующими группами X, Y и/или CR3R4, как описано далее ниже, которые могут быть представлены определенным, но варьирующим числом или в некоторых случаях необязательно отсутствовать. А именно соединения по настоящему изобретению («связанные гетероарильные соединения») представляют собой класс соединений, которые участвуют в структурных признаках ядра, как показано ниже в формуле (I):

где различные группы могут быть заданы и/или выбраны альтернативным и вариабельным путем, как описано выше или ниже краткого описания изобретения.
В некоторых вариантах воплощения связанных гетероарильных соединений формулы (I):
i) Ar представляет собой моноциклический или бициклический арильный или гетероарильный радикал, включающий одно или два ароматических кольца, независимо выбранных из бензольных колец и пяти- или шестичленных гетероарильных колец, каждое ароматическое кольцо необязательно имеет один или два R20замещающих радикала, где каждый R20 радикал независимо выбран из гидроксила, NH2, SH, галогена или органического радикала C1-C4;
ii) Y представляет собой O, S, S(O), SO2, CR1R2 или NR5;
iii) m равно 0 или 1;
iv) hAr1 представляет собой пяти- или шестичленный гетероарильный кольцевой радикал, содержащий, по меньшей мере, два атома углерода в кольце и от одного до трех гетероатомов в кольце, независимо выбранных из O, N или S, где любой из оставшихся членов гетероароматического кольца независимо выбран из CR6, N, NR7;
v) X представляет собой O, S, S(O), SO2, CR8R9 или NR10;
vi) n равно 0, 1, 2 или 3;
vii) R1, R2, R3, R4, R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, SH, галогена или органического радикала C1-C4 и R5, R7 и R10 независимо выбраны из водорода, гидроксила или органического радикала C1-C4 и R6 представляет собой водород, галоген или органический радикал C1-C4;
viii) hAr2 представляет пяти- или шестичленное гетероарильное кольцо, имеющее, по меньшей мере, два атома углерода в кольце и, по меньшей мере, один атом азота в кольце, и где оставшиеся члены гетероароматического кольца независимо выбраны из CR30, N, NR31, O и S, где каждый R30независимо выбран из водорода, галогена или органического радикала C1-C4 и каждый R31независимо выбран из водорода или органического радикала C1-C4;
или их пищевую приемлемую соль.
В других вариантах воплощения связанных гетероарильных соединений формулы (I), где hAr2 представляет собой арильное кольцо:
i) Ar представляет собой моноциклический или бициклический арильный или гетероарильный радикал, включающий одно или два ароматических кольца, независимо, выбранных из бензольных колец и пяти- или шестичленных гетероарильных колец, каждое ароматическое кольцо необязательно имеет один или два R20замещающих радикала, где каждый R20 радикал независимо выбран из гидроксила, NH2, SH, галогена или органического радикала C1-C4;
ii) Y представляет собой O, S, S(O), SO2, CR1R2 или NR5;
iii) m равно 0 или 1;
iv) hAr1 представляет собой пяти- или шестичленный гетероарильный кольцевой радикал, содержащий, по меньшей мере, два атома углерода в кольце и от одного до трех гетероатомов в кольце, независимо выбранных из O, N или S, где любой из оставшихся членов гетероароматического кольца независимо выбран из CR6, N, NR7;
v) X представляет собой O, S, S(O), SO2, CR8R9 или NR10;
vi) n равно 0, 1, 2 или 3;
vii) R1, R2, R3, R4, R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, SH, галогена или органического радикала C1-C4 и R5, R7 и R10 независимо выбраны из водорода, гидроксила или органического радикала C1-C4 и R6 представляет собой водород, галоген или органический радикал C1-C4;
viii) hAr2 представляет собой фенильное кольцо, необязательно замещенное 0, 1, 2 или 3 R30радикалами, независимо выбранными из водорода, галогена или органического радикала C1-C4;
или их пищевую приемлемую соль.
Другие конкретные варианты воплощения настоящего изобретения обеспечивают модифицированный вкус пищевых композиций, содержащих, по меньшей мере, одно соединение формулы (I) в количестве, модулирующем острый вкусо-аромат, где соединение формулы (I) не содержит группы Y и, таким образом, имеет формулу:

где
i) Ar представляет собой моноциклический или бициклический арильный или гетероарильный радикал, включающий одно или два ароматических кольца, независимо выбранных из бензольных колец и пяти- или шестичленных гетероарильных колец, каждое ароматическое кольцо необязательно имеет один, два или три R20замещающих радикала, где каждый R20 радикал независимо выбран из гидроксила, NH2, NO2, SH, SO3H, P(O)(OH)2, галогена, или органического радикала C1-C4;
ii) hAr1 представляет собой пяти- или шестичленный гетероарильный кольцевой радикал, имеющий от 1 до 4 гетероатомов, независимо выбранных из кислорода, серы и/или азота, где любой из оставшихся членов гетероароматического кольца независимо выбран из CR6, N, NR7;
iii) X представляет собой O, S, S(O), SO2, CR8R9 или NR10;
iv) n равно 0, 1, 2 или 3;
v) R3, R4, R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, SH, галогена или органического радикала C1-C4, R7 и R10 независимо выбраны из водорода, гидроксила или органического радикала C1-C4 и R6 представляет собой водород, галоген или органический радикал C1-C4;
vi) hAr2 представляет собой пяти- или шестичленное гетероарильное кольцо, имеющее, по меньшей мере, один атом углерода в кольце и, по меньшей мере, один атом азота в кольце, и где оставшиеся члены гетероарильного кольца независимо выбраны из CR30, N, NR31, O и S, где каждый R30независимо выбран из водорода, гидроксила, NH2, NO2, SH, SO3H, P(O)(OH)2, галогена или органического радикала C1-C4 и каждый R31независимо выбран из водорода или органического радикала C1-C4;
или их пищевую приемлемую соль.
В другом варианте воплощения настоящего изобретения соединения формулы I включают соединения, имеющие формулу (IА), показанную ниже, которая включает hAr1 радикалы, которые представляют собой пятичленные гетероарильные радикалы:

где
i) n` равно 0, 1, 2 или 3 и каждый R20 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
ii) n`` равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
iii) X представляет собой NH, O, S, S(O), SO2 или СН2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила, пирролила, бензофуранила, бензотиофуранила или бензопирролила;
v) hAr1 имеет структуру:

(1) X1 представляет собой NH, O или S,
(2) X2 представляет собой N или CR6, где R6 представляет собой водород, галоген или органический радикал C1-C4,
(3) X3 представляет собой N или CR6, где R6 представляет собой водород, галоген или органический радикал C1-C4, и
vi) hAr2 представляет собой кольцо пиридила, пиразинила или пиримидинила;
или их пищевую приемлемую соль.
Класс и подкласс связанных гетероарильных соединений, описанных выше, включают многие ранее неизвестные подклассы соединений и/или группы соединений и также включают некоторые соединения, которые могут быть известны из уровня техники в связи с другим их использованием. Несмотря на знания и предположения заявителей, из уровня техники не известно, что соединения, приведенные выше, и различные их классы и подклассы используются в неожиданно низких концентрациях, как здесь описано, для модификации, улучшения и/или усиления вкусо-аромата умами пищевых композиций.
Ar радикал и его заместители
Ar радикал соединений формулы (I) и его различные подклассы необязательно могут быть замещены моноциклическими или бициклическими арильными или гетероарильными радикалами (как описано где-либо здесь), включающими одно или два ароматических кольца, независимо выбранных из бензольных колец и пяти- или шестичленных гетероарильных колец с одним, двумя или тремя необязательными R20заместителями, которые могут присоединяться в любое из положений арильного или гетероарильного кольцевого радикала, иное, чем положение, которое обеспечивает связь с Y или hAr1 радикалом.
Во многих вариантах воплощения соединений формулы (I) и их подклассов Ar представляет собой моноциклический или бициклический арильный радикал, который включает, по меньшей мере, одно бензольное кольцо. Когда Ar представляет собой моноциклический арил, например, Ar радикалы могут включать следующие структуры:

В некоторых вариантах воплощения соединений формулы I и их подклассов Ar имеет формулу:

Когда Ar представляет собой бициклический арильный радикал, например, Ar радикалы могут включать следующие структуры:


Во многих вариантах воплощения соединений формулы (I) и их подклассов Ar представляет собой необязательно замещенный моноциклический или бициклический гетероарильный радикал, включающий одно или два ароматических кольца, независимо выбранных из пяти- или шестичленных гетероарильных колец. Моноциклические гетероарильные Ar кольца с шестичленным кольцом включают необязательно замещенные кольца пиридила, пиразинила или пиримидинила, которые включают, но не ограничиваются следующими структурами, приведенными в качестве примера:

Моноциклические гетероарильные Ar кольца с пятичленными кольцами включают необязательно замещенные кольца фуранила, тиофуранила, пирролила, пиразолила, оксазолила или изоксазолила, которые включают, но не ограничиваются следующими структурами, приведенными в качестве примера:

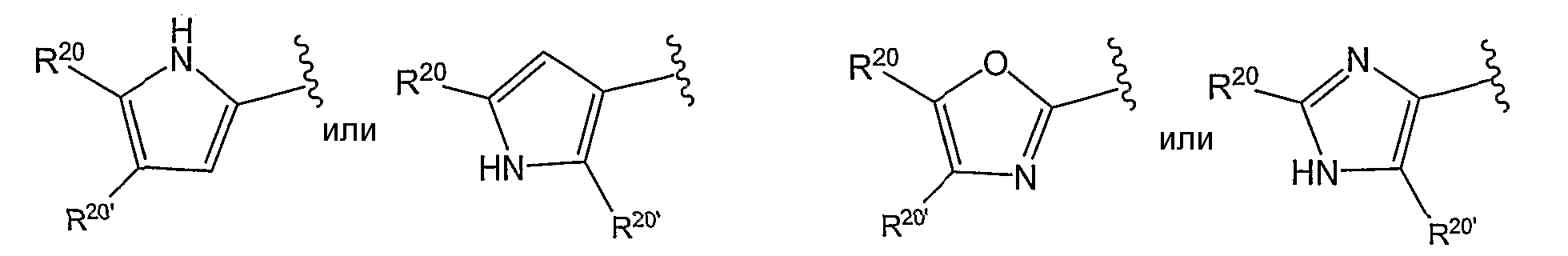
Бициклические гетероарильные Ar кольца могут включать необязательно замещенные кольца, такие как радикалы бензофуранила, бензотиофуранила или бензопирролила или другие гетероарильные радикалы, такие как следующие:

В различных вариантах воплощения соединений формулы I и их различных подклассов, описанных здесь, Ar радикал может быть необязательно замещен одним, двумя или тремя R20замещающими радикалами, где каждый R20 радикал независимо выбран из гидроксила, NH2, SH, галогена или органического радикала C1-C4. Подходящие подклассы органических радикалов C1-C4включают алкил, алкоксил, алкокси-алкил, гидроксиалкил, галогеналкил, CN, CO2H, CHO, COR21, CO2R21, NHR21, NR21R21`, SR21, S(О)R21и SO2R21 радикалы, где R21 и R21` представляют собой независимо выбранные алкилы. В некоторых вариантах воплощения соединений формулы (I) R20 и/или R20` радикалы независимо выбраны из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп. В других дополнительных вариантах воплощения настоящего изобретения R20 и/или R20` независимо выбраны из группы метила, метокси и этила.
Во многих вариантах воплощения соединений формулы (I) желательно, чтобы Ar кольцевой радикал имел ограниченный предел размера и молекулярной массы. Таким образом, в некоторых вариантах воплощения настоящего изобретения Ar радикал включает от 4 до 16 атомов углерода или от 5 до 12 атомов углерода или от 6 до 10 атомов углерода.
Во многих вариантах воплощения соединений формулы (I) hAr1 представляет собой необязательно замещенный пяти- или шестичленный гетероарильный кольцевой радикал. Гетероарильные радикалы hAr1 включают, по меньшей мере, два атома углерода в кольце, образующие связи, которые связывают гетероарильное кольцо радикала hAr1 с другими радикалами соединений формулы (I). Гетероарильные радикалы hAr1включают также от одного до трех гетероатомов в кольце, независимо выбранных из O, N или S, где любой из оставшихся членов гетероароматического кольца независимо выбран из CR6, N и NR7, где R6 и R7 радикалы представляют собой описанные ниже. Таким образом, hAr1 радикалы могут иметь, как минимум, ноль, как максимум, три R6 и R7 радикалов. Понятно, что в объем притязаний настоящего изобретения входят всевозможные схемы замещения атомов углерода, азота и серы гетероарильных колец и их необязательные заместители достаточно химически стабильны и могут быть применены в пищевых продуктах.
Радикал hAr1
hAr1 радикал соединений формулы (I) и его различные подклассы необязательно могут быть замещены моноциклическим или бициклическим гетероарильным радикалом (как описано где-либо здесь), включающим одно или два пяти- или шестичленных гетероарильных кольца с одним, двумя или тремя необязательными R6 или R7 заместителями, которые могут присоединяться в любое из положений гетероарильного кольцевого радикала hAr1, иное чем положение, которое обеспечивает связь hAr1с Ar и/или Y радикалом и также с Х радикалом.
В некоторых вариантах воплощения соединений формулы (I) и их подклассов hAr1 радикалы представляют собой необязательно замещенный шестичленный гетероарильный радикал, такой как hAr1, представляющий собой радикал пиридила, пиразинила, пиридазинила или пиримидинила, имеющий структуру:

где R6 и R6' замещающие радикалы могут быть заданы, как описано ниже. Во многих вариантах воплощения соединений формулы (I) радикалы пиридила, пиразинила, пиридазинила или пиримидинила представляют собой незамещенные, но могущие иметь соединения с соседними группами любой структуры, как показано ниже:

В частности, радикалы пиридила, пиразинила, пиридазинила или пиримидинила включают, но не ограничиваются следующими структурами, приведенными в качестве примера:

В некоторых вариантах воплощения соединений формулы (I) и их подклассов hAr1 радикалы представляют собой необязательно замещенный пятичленный гетероарильный радикал, такой как радикал фуранила, тиофуранила или пирролила, включающий, но не ограничивающиеся следующими структурами, приведенными в качестве примера:

В hAr1 структурах, описанных выше, R6 радикалы могут быть галогеном или органическим радикалом C1-C4. Подходящие подклассы органических радикалов C1-C4включают алкил, алкоксил, алкокси-алкил, гидроксиалкил, галогеналкил, CN, CO2H, CHO, COR21, CO2R21, NHR21, NR21R21`, SR21, S(О)R21и SO2R21 радикалы, где R21 и R21` независимо выбраны алкилы. В некоторых вариантах воплощения настоящего изобретения R6представляет собой водород или радикал C1-C4 алкил или алкоксил. В некоторых вариантах воплощения настоящего изобретения R6 радикалы независимо выбраны из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп. Во многих вариантах воплощения настоящего изобретения R6 представляет собой водород. В hAr1 структурах, описанных выше, R7 может представлять собой водород или алкильный радикал C1-C4, во многих вариантах воплощения настоящего изобретения R7 представляет собой водород.
Во многих вариантах воплощения соединений формулы (I) hAr1представляет собой необязательно замещенный диазол или триазол, имеющий структуру:

где R7 является таким, как описано выше. В большинстве таких вариантов воплощения настоящего изобретения R7 представляет собой водород или C1-C4 алкил или более предпочтительно водород. В предпочтительных вариантах воплощения соединений формулы (I) hAr1представляет собой необязательно замещенный триазол, имеющий структуру:

Следует понимать, что при определенных температурных условиях, рН и других изменяемых показателях большинство гетероарильных соединений, описанных здесь, включающих ароматическую NH или OH группы, включая триазольные соединения, такие, как описанные здесь выше, могут иметь и имеют таутомеры, которые уравновешивают три структуры, показанные выше и которые в этих вариантах воплощения соединений формулы (I) представляют собой реальный образец соединения, которое может включать и часто включает смесь таких таутомеров. Таким образом, если в описании и/или формуле показан только один таутомер, следует понимать, что в объем притязаний входят и другие таутомеры, если не указано иное.
В некоторых вариантах воплощения соединений формулы (I) и их подклассов hAr1 радикал может быть тетразолом, имеющим структуру:
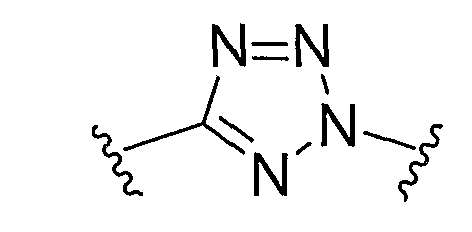

В некоторых вариантах воплощения соединений формулы (I) и их подклассов hAr1 представляет собой незамещенный гетероарильный радикал, имеющий одну из следующих показанных ниже структур:
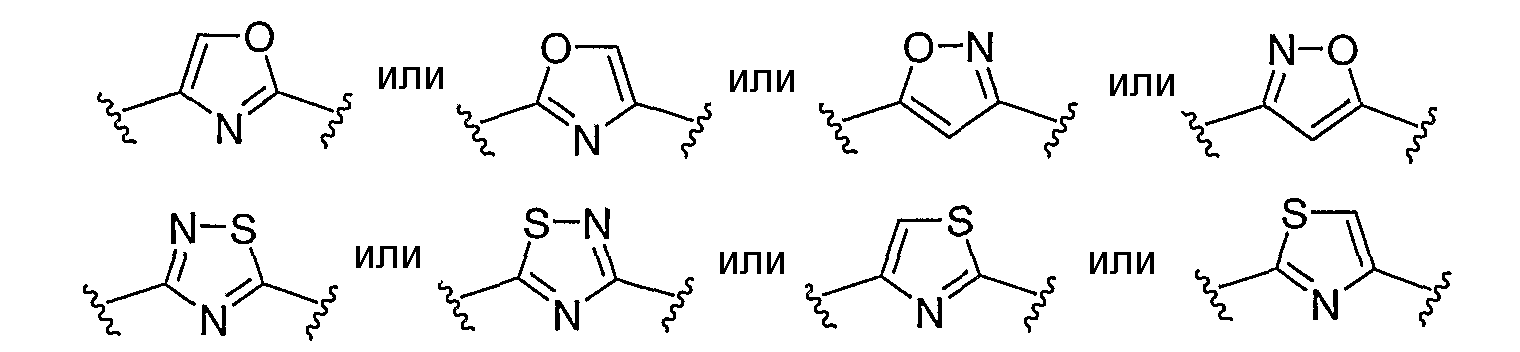

Радикал hAr2
Во многих вариантах воплощения соединений формулы (I) hAr2 представляет собой необязательно замещенный фенильный радикал или необязательно замещенный пяти- или шестичленный гетероарильный кольцевой радикал, который связан через Х и/или одну или более CR3R4 группы с hAr1 радикалом, как описано выше.
В некоторых вариантах воплощения аналогов соединений формулы I hAr2 представляет собой фенильное кольцо, необязательно замещенное 0, 1, 2 или 3 R30радикалами, независимо выбранными из водорода, галогена или органического радикала C1-C4. В некоторых вариантах воплощения соединений формулы (I) hAr2 радикал представляет собой гетероарильный радикал в соответствии с термином, описанным здесь, и hAr2 гетероарильный радикал имеет, по меньшей мере, один атом углерода в кольце, который связан с Х и необязательно CR3R4 группами и, по меньшей мере, один дополнительный атом углерода в кольце и, по меньшей мере, один атом азота в кольце. Оставшиеся кольцевые члены пяти- или шестичленного гетероарильного кольца могут быть независимо выбраны из CR30, N, NR31, O и S, при условии, что валентность CR30, N, NR31, O и S радикалов выбрана в комбинации таким образом, что в результате образуется полно конъюгированное ароматическое и делокализованное гетероарильное кольцо, имеющее 4n+2 “π” электроны, выбор и/или условия могут быть легко определены специалистом в данной области органической химии.
В таких вариантах воплощения hAr2 каждый R30радикал может быть независимо выбран из водорода, галогена или органического радикала C1-C4, и каждый R31радикал может быть независимо выбран из водорода или органического радикала C1-C4. Подходящие подклассы органических радикалов C1-C4включают алкил, алкоксил, алкокси-алкил, гидроксиалкил, галогеналкил, CN, CO2H, CHO, COR21, CO2R21, NHR21, NR21R21`, SR21, S(О)R21и SO2R21 радикалы, где R21 и R21` представляют собой независимо выбранные алкилы. В некоторых вариантах воплощения настоящего изобретения R30 независимо выбран из водорода или C1-C4 алкила или алкоксильного радикала. В некоторых вариантах воплощения настоящего изобретения каждый R30 радикал может быть независимо выбран из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп. В некоторых вариантах воплощения настоящего изобретения каждый R30 представляет собой группу, являющуюся водородом. В hAr2 структурах, описанных выше, R31 может быть водородом или C1-C4 алкильным радикалом, и в большинстве вариантов воплощения настоящего изобретения R30 представляет собой водород.
В некоторых вариантах воплощения настоящего изобретения hAr2 представляет собой пятичленный гетероарильный радикал, имеющий одну из следующих структур, приведенных в качестве примера ниже:

Во многих вариантах воплощения настоящего изобретения hAr2 представляет собой шестичленный гетероарильный радикал, такой как радикал пиридила, пиразинила или пиримидинила, где необязательные R30 радикалы независимо выбраны из гидроксила, SH, NH2, галогена, алкила, алкоксила, алкокси-алкила, гидроксиалкила, галогеналкила, CN, CO2H, CHO, COR32, CO2R32, NHR32, NR32R32` или SR32радикала, где R32 и R32` представляют собой независимо выбранные алкилы. Примеры структур радикалов пиридила, пиразинила или пиримидинила показаны ниже:

В предпочтительных вариантах воплощения настоящего изобретения hAr2 представляет собой 2-пиридил, 2-пиразинил или 2-пиримидинил радикал, как показано ниже:

В некоторых вариантах воплощения настоящего изобретения каждый R30 и/или R30` радикал hAr2 радикала независимо выбран из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп. Во многих вариантах воплощения настоящего изобретения каждый R30 представляет собой водород (т.е. n`` равно 0).
В предпочтительных вариантах воплощения настоящего изобретения hAr2 представляет собой незамещенный 2-пиридил радикал, как показано ниже:

Линкерные группы Х, Y и (CR3R4)
Как описано выше, hAr1, hAr2и Ar кольцевые группы могут быть связаны вместе мостиковыми или связующими группами Х, Y и/или CR3R4, как те, которые будут описаны ниже. Ar и hAr1 группы могут быть необязательно связаны (где m=1) двухвалентным “Y” атомом или группой, которая образует мостик с Ar и hAr1. Y группа, как правило, содержит атом с одной связью к Ar кольцу и другой связью к hAr1 радикалу, и необязательно другие замещающие группы, которые могут иметь множество структур, включающих, но не ограничивающихся O, S, S(O), SO2, CR1R2 или NR5, образуя таким образом соединения формулы (I), имеющие следующие структуры:

В качестве альтернативы во многих вариантах воплощения соединений по настоящему изобретению m=0, таким образом, Y группа отсутствует и Ar и hAr1 кольца непосредственно соединены/связаны одно с другим, как показано ниже:

В отличие от «Y» группы «Х» группа присутствует, как правило, в соединениях формулы (I) и связана с hAr1 группой и, по меньшей мере, образует соединение или связь с CR3R4 и/или hAr2 гетероарильной кольцевой группой. Х группа, как правило, включает двухвалентный атом или группу с одной связью к hAr1 кольцу и другой связью к CR3R4 и/или hAr2 гетероарильной кольцевой группе и необязательно другие замещающие группы, таким образом образуя связь или мостик между hAr1 и CR3R4 и/или hAr2 гетероарильной кольцевой группой. Х группа может иметь множество структур, включающих, но не ограничивающихся O, S, S(O), SO2, CR8R9 или NR10, образуя, таким образом, соединения формулы (I), имеющие следующие структуры:
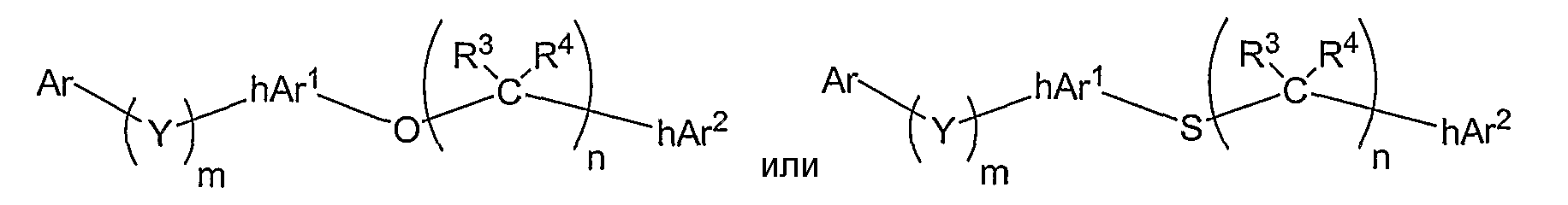

В некоторых вариантах воплощения настоящего изобретения Х представляет собой S, NH или O, в предпочтительных вариантах воплощения настоящего изобретения Х представляет собой S.
CR3R4 группы представляют собой необязательные (т.е. n равно 0, 1, 2 или 3) мостиковые группы, которые связаны с Х группой и соединяют или связывают ее с hAr2 гетероарильным кольцом. Следует понимать, что если в формуле не указано иное, то если присутствует более чем одна CR3R4 группа в данной молекуле, R3 и R4заместители могут быть независимо выбраны для каждой CR3R4присутствующей группы. В некоторых вариантах воплощения настоящего изобретения n=2 и в результате полученные соединения имеют следующую структуру:

Во многих вариантах воплощения настоящего изобретения n=1, и полученный в результате подкласс соединений формулы (I) имеет следующую структуру:

Во многих вариантах воплощения настоящего изобретения m=0 и n=1, и полученный в результате подкласс соединений формулы (I) имеет следующую структуру:

В приведенном выше описании определенные R1-R10 замещающие группы были заданы в связи с признаками связанных гетероарильных соединений формулы (I). Как правило, каждая из замещающих групп может быть независимо выбрана из других групп, в частности, R1, R2, R3, R4, R8 и R9 может быть независимо выбрана из неорганических радикалов или групп, включающих водород, кислород, гидрокси, NH2, SH или галоген (фтор, хлор, бром или йод) или органического радикала C1-C4. R7 и R10 независимо выбраны из водорода, гидроксила или органического радикала C1-C4, и R6 представляет собой водород, галоген или органический радикал C1-C4. Подходящие органические радикалы C1-C4включают, но не ограничиваются определенными подклассами органических радикалов, таких как алкил, алкоксил, алкокси-алкил, гидроксиалкил, галогеналкил, CN, CO2H, CHO, CORх, CO2Rх,NHRх, NRхRх`, SRх, S(О)Rхи SO2Rх, где Rх представляет собой алкил. В некоторых вариантах воплощения настоящего изобретения органические радикалы C1-C4выбраны из NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп. Во многих вариантах воплощения настоящего изобретения один или все R1-R10 представляют собой водород.
В предпочтительных вариантах воплощения настоящего изобретения связанные гетероарильные соединения формулы (I), m=0 (т.е. Y группа отсутствует), n=1 и R3 и R4 группы представляют собой водород, таким образом образуя единичную метиленовую группу, которая связывает X и hAr2 кольца, и Ar, hAr1 и hAr2 ограничены определенными предпочтительными ароматическими кольцевыми системами с образованием предпочтительного подкласса связанного гетероарильного соединения, имеющего формулу (IA), как показано ниже:

где
i) n` равно 0, 1, 2 или 3 и каждый R20 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
ii) n`` равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
iii) X представляет собой NH, O, S, S(O), SO2 или СН2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила, пирролила, бензофуранила, бензотиофуранила или бензопирролила;
v) hAr1 имеет структуру:

(1) X1 представляет собой NH, O или S,
(2) X2 представляет собой N или CR6, где R6 представляет собой водород, галоген или органический радикала C1-C4,
(3) X3 представляет собой N или CR6, где R6 представляет собой водород, галоген или органический радикал C1-C4, и
vi) hAr2 представляет собой кольцо пиридила, пиразинила или пиримидинила.
Как следует из приведенного выше описания соединений формулы (IA), hAr1 кольцевой радикал, относящийся к подклассу пятичленных гетероарилов, как определено выбором/сродством X1, X2 и X3 атомов, радикалов или групп. В определенных более узких подклассах X1 представляет собой NH. В других более узких подкласса X2 может быть N или CH, при этом X3 представляет собой независимо N или CH. В предпочтительных подклассах X2 и X3 представляют собой N.
В других предпочтительных подклассах, X1 представляет собой NH, а X2 и X3 представляют собой N, таким образом, полученное в результате hAr1 кольцо представляет собой триазольный кольцевой радикал, имеющий структуру, показанную ниже:

которая демонстрирует, что таутомеризм может иметь место, по меньшей мере, при определенных условиях в результате смешения трех триазольных групп в соединениях формулы (IA).
Кроме того, в некоторых вариантах воплощения соединений формулы (IA) Ar представляет собой предпочтительно радикалы фенил или фуранил и X группа представляет собой S, NH или O, или более предпочтительно S или O. В других предпочтительных вариантах воплощения соединений формулы (IA) hAr2 представляет собой 2-пиридинил радикал, имеющий структуру:

где n`` предпочтительно равно 1 или 0.
В большинстве вариантов воплощения соединений формулы (IA) R20 и/или R30 радикалы независимо выбраны из гидрокси, SH, NH2, галогена, алкила, алкоксила, алкокси-алкила, гидроксиалкила, галогеналкила, CN, CO2H, CHO, CORх, CO2Rх, NHRх, NRхRх` или SRх радикала, где Rх представляет собой алкил или даже более предпочтительно R20 и/или R30 радикалы независимо выбраны из группы, состоящей из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси группы.
Другие предпочтительные подклассы соединений формулы (I) представляют собой триазольные соединения формулы (IВ), показанные ниже:

где
i) n` равно 0, 1, 2 или 3 и каждый R20 независимо выбран из гидрокси, SH, NH2, галогена и радикала C1-C4, выбранного из алкила, алкоксила, алкокси-алкила, гидроксиалкила, галогеналкила, CN, CO2H, CHO, COR21, CO2R21, NHR21, NR21R21`или SR21 радикала, где R21 и R21` представляют собой алкил,
ii) n`` равно 0, 1, 2 или 3 и каждый R30 независимо выбран из гидрокси, SH, NH2, галогена и радикала C1-C4, выбранного из алкила, алкоксила, алкокси-алкила, гидроксиалкила, галогеналкила, CN, CO2H, CHO, COR32, CO2R32 или SR32 радикала, где R32 и R32` представляют собой алкил,
iii) X представляет собой NH, O, S, S(O), SO2 или СН2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила или пирролила;
или их пищевую приемлемую соль.
В других вариантах воплощения настоящего изобретения, относящихся к подклассу соединений формулы (I), где hAr1 представляет собой триазольное кольцо, а обе X и Y линкерные группы присутствуют, как показано ниже на соединениях формулы (IC):

где
i) n` равно 0, 1, 2 или 3 и каждый R20 независимо выбран из группы, состоящей из гидроксила, SH, NH2, галогена или органического радикала C1-C4;
ii) n`` равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из ОН, SH, NH2, галогена или органического радикала C1-C4;
iii) X представляет собой NH, O, S, S(O), SO2 или CR8R9, где R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, галогена или органического радикала C1-C4;
iv) Y представляет собой NH, O, S, S(O), SO2, или CR8R9, где R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, галогена или органического радикала C1-C4;
v) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила или пирролила;
или их пищевую приемлемую соль.
В других вариантах воплощения настоящего изобретения, относящихся к подклассу соединений формулы (I), где hAr1 представляет собой шестичленный гетероарил, содержащий один или два атома азота, как показано ниже на соединениях формулы (ID):

и где
i) n` равно 0, 1, 2 или 3 и каждый R20 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
ii) n`` равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена или органического радикала C1-C4;
iii) X представляет собой NH, O, S, S(O), SO2 или СН2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила, пирролила, бензофуранила, бензотиофуранила или бензопирролила;
v) hAr1 имеет структуру:

где R6 и R6' независимо выбраны из водорода, галогена или органического радикала C1-C4, и
vi) hAr2представляет собой кольцо пиридила, пиразинила или пиримидинила.
В некоторых вариантах воплощения соединений формулы (ID) Ar представляет собой кольцо фенила, n` равно 1 или 2 и каждый R20 независимо выбран из группы, состоящей из метила, этила, изопропила, трифторметила, метокси, трифторметокси и этокси. В других вариантах воплощения соединений формулы (ID) Ar представляет собой кольцо фенила, конденсированное с алкилендиокси кольцом, такие Ar группы имеют структуру:

В некоторых вариантах воплощения соединений формулы (ID) Ar представляет собой кольцо фуранила, n` равно 1 или 2 и каждый R20 независимо выбран из группы, состоящей из метила, этила, изопропила, трифторметила, метокси, трифторметокси и этокси.
В некоторых вариантах воплощения соединений формулы (ID) hAr1 представляет собой незамещенный радикал пиридила, пиразинила, пиридазинила или пиримидинила, имеющий структуру:

В некоторых вариантах воплощения соединений формулы (ID) hAr2 представляет собой необязательно замещенный радикал пиридила, имеющий структуру:

где каждый R30 независимо выбран из группы, состоящей из гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, CO2CH3, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси. Предпочтительно пиридинильный радикал представляет собой 2-пиридинил радикал, имеющий структуру:

где n'' равно 0 или 1 и более предпочтительно n”=0.
В большинстве вариантов воплощения настоящего изобретения, относящихся к соединениям формулы (I) и их подклассам (IА), (IB), (IC) и (ID), описанным выше, связанные гетороарильные соединения представляют собой так называемые «малые молекулы» в сравнении с большинством биологических молекул и могут иметь варьирующие ограничения по абсолютному физическому размеру, молекулярному весу, физическим характеристикам, таким образом, они могут быть до некоторой степени растворимы в водной среде и имеют подходящий размер для эффективного соединения с соответствующими гетеродимерами T1R1/T1R3 рецепторов вкуса.
Таким образом, в большинстве вариантов воплощения соединений формулы (I) и/или их различных подклассов молекулярная масса соединений формулы (I) должна составлять менее около 800 грамм на моль или в других вариантах воплощения настоящего изобретения менее или равна около 700 грамм на моль, 600 грамм на моль, 500 грамм на моль, 450 грамм на моль, 400 грамм на моль, 350 грамм на моль или 300 грамм на моль. Аналогично соединения формулы (I) предпочтительно могут иметь молекулярную массу в пределах, таких как, например, от около 175 до около 500 грамм на моль, от около 200 до около 450 грамм на моль, от около 225 до около 400 грамм на моль, от около 250 до около 350 грамм на моль.
Молекулярная масса и/или гидрофильный характер соединений также может быть модифицирован ограничением числа атомов углерода в соединениях по настоящему изобретению. Соответственно, в некоторых вариантах воплощения настоящего изобретения соединения формулы (I) имеют от 10 до 22 атомов углерода или в качестве альтернативы от 12 до 20 атомов углерода.
Кроме того, желательно, чтобы соединения формулы (I) и их подклассы и группы имели достаточную полярность и/или достаточное количество полярных функциональных групп, таким образом, они, по меньшей мере, до некоторой степени будут растворимы в водных биологических жидкостях, таких как слюна. Хорошо известным индикатором такой водной растворимости является log10 коэффициента распределения данного соединения между н-октанолом и водой, параметр которого может быть легко и быстро рассчитан с использованием компьютерных вычислений, исходя из структуры соединения, с помощью большого количества современного программного обеспечения в области химии, таким образом, «создаются» соединения с оцененной в достаточной степени водной растворимостью, в настоящее время, как правило, не требуется реально синтезировать соединения, хотя желательно проводить экспериментальное подтверждение водной растворимости реально синтезированных соединений-кандидатов. Соответственно в некоторых вариантах воплощения настоящего изобретения log10 коэффициента распределения данного соединения между н-октанолом и водой составляет менее 5,5, предпочтительно менее 5,0 или менее 4,5.
Для вариантов воплощения настоящего изобретения и/или подклассов соединений формулы (I) предполагается, таким образом, что любой из представителей подклассов и/или групп соединений формулы (I), описанных ниже, может быть смешан в эффективном количестве с пищевым продуктом или его предшественником как в его конкретной форме, так и в форме пищевой приемлемой соли с использованием процессов или способов, описанных в данной заявке, или любыми другими способами, известными специалисту в области получения пищевых или медицинских продуктов или их предшественников для получения пищевого продукта или его предшественника с модифицированным острым вкусо-ароматом.
Используемые в пищу приемлемые соединения, их соли и/или пищевые композиции
Многие из связанных гетероарильных соединений формулы (I) или их различные подклассы включают кислотную или основную группу, исходя из того, что в результате эти кислотные или основные группы могут быть нейтрализованы соответствующими используемыми в пищу приемлемыми кислотами или основаниями с получением используемых в пищу приемлемых солей, и соединения формулы (I) могут быть введены в форме используемых в пищу приемлемых солей, многие из которых признаны как GRAS (признаны полностью безвредными).
Кроме того, кислотный или основной характер («рН») пищевых композиций зависит от состава введенных соединений формулы (I), которые могут присутствовать в форме солей, предпочтительно представляющих собой пищевые приемлемые соли. Соединения формулы (I), имеющие кислые замещающие группы, такие как карбоновых кислот, будут стремиться (при нейтральном физиологическом рН) присутствовать в растворе в форме анионов карбоксилатов и, таким образом, в предпочтительных вариантах воплощения настоящего изобретения будут связываться с пищевыми приемлемыми и/или фармацевтически приемлемыми катионами, многие из которых известны специалисту в данной области техники. Такие пищевые приемлемые катионы включают катионы щелочных металлов (катионы лития, натрия и калия), катионы щелочноземельных металлов (магний, кальций и им подобные) или аммония (NH4)+ или катионы органически замещенного аммония, такие как катионы (R-NH3)+.
Соединения формулы (I), имеющие основные замещающие группы, такие как аминогруппы или гетероциклические кольца, содержащие атомы азота, будут стремиться (при нейтральном физиологическом рН или при кислом рН, как правило, в большинстве пищевых продуктов) присутствовать в растворе в форме катионов групп аммония и, таким образом, в предпочтительных вариантах воплощения настоящего изобретения будут связываться с пищевыми приемлемыми анионами, многие из которых известны специалисту в данной области техники. Такие пищевые анионные группы включают анионные формы различных карбоновых кислот (ацетаты, цитраты, тартраты, анионы солей жирных кислот и т.п.), галиды (в частности, фториды или хлориды), нитраты, фосфаты, сульфаты и им подобные.
Связанные гетероарильные соединения формулы (I) или их различные подклассы и их соли предпочтительно должны быть пищевыми приемлемыми, т.е. считаться подходящими для использования в пищевом продукте или напитке для придания данным немодифицированным пищевым композициям улучшенного и/или приятного острого вкуса и не должны быть токсичными или быть причиной неприятного или нежелательного фармакологического или токсикологического воздействия на животное или человека при применении в качестве агентов, придающих вкус и аромат пищевым композициям, как правило, в низких концентрациях.
Типичным способом демонстрации того, что соединение, придающее вкус и аромат, относится к пищевым приемлемым, является его тестирование и/или оценка Экспертной группой Ассоциации промышленных производителей вкусовых и ароматических соединений и экстрактов (FEMA) и признание «полностью безвредными» (“GRAS”). Способ оценки вкусовых и ароматических соединений FEMA/GRAS представляет собой комплекс, хорошо известный специалисту в области получения пищевых продуктов, описанный Smith, et al. в статье, озаглавленной “GRAS Flavoring Substances 21,” Food Technology, 57(5), pgs 46-59, May 2003, полное содержание которой включено в качестве ссылки.
При оценке способом FEMA/GRAS нового вкусового и ароматического соединения, как правило, проводят тестирование на нежелательные токсические воздействия на лабораторных крысах, при котором крыс кормят, по меньшей мере, около 90 дней при концентрации, по меньшей мере, в 100 раз выше или в 1000 раз выше максимально допустимых концентраций соединения в каждой категории тестируемых пищевых продуктов. Например, такое тестирование соединений формулы (I) может проводиться смешиванием соединения с крысиным кормом и скармливаться лабораторным крысам, таким как Crl:CD(SD)IGS BR крысы в концентрации около 100 мг/кг массы тела в день в течение 90 дней, и затем крыс умерщвляют и проводят оценку с использованием различных известных процедур медицинского тестирования для того, чтобы показать, что соединение формулы (I) не оказывает токсического воздействия на крыс.
Для соединений формулы (I) на данный момент, по меньшей мере, в большинстве вариантов воплощения настоящего изобретения не известна индивидуальная фармацевтическая или биологическая активность для лечения заболеваний у животных или людей, или возможность введения или реализации в качестве фармацевтически активных агентов. Связанные гетероарильные соединения формулы (I) и их различные подклассы, тем не менее, в некоторых вариантах воплощения настоящего изобретения могут быть использованы и реализованы в качестве агентов, придающих вкус и аромат для модификации или улучшения вкуса определенных типов «фармацевтических» или «нутрицевтических» композиций, таких как пищевые композиции, обогащенные витаминами, таких как супы, и во многих таких вариантах воплощения соединений по настоящему изобретению, как правило, могут быть введены в рецептуру с MSG или другими соединениями - тастантами острого вкуса для усиления острого вкусо-аромата таких нутрицевтических композиций.
Принимая во внимание все описанное выше, если уже открыто или будет открыто позднее, что одно или более соединений формулы (I) или фармацевтическая композиция с этим соединением имеет фармацевтическую и/или биологическую активность для лечения заболеваний, тогда в связи с заявляемыми способами модификации острого вкуса пищевых композиций, которые включают использование таких известных соединений, и связанных с заявляемыми пищевыми композициями, полученными вышеописанными способами, дополнительные варианты воплощения таких способов или пищевых композиций по настоящему изобретению могут включать перечисление способов или композиций, заявленных здесь, а также должны включать MSG.
Соединения по настоящему изобретению, усиливающие острый вкус
Связанные гетероарильные соединения формулы (I) и их различные подклассы и группы, как описано выше, обладают способностью придавать острый вкус и аромат и модифицировать острый вкус и аромат пищевых продуктов. Как следует из теоретических выкладок и примеров, многие соединения формулы (I) являются агонистами рецептора hT1R1/hT1R3 «острого» вкуса, по меньшей мере, в концентрациях 100 мкM или менее. Соответственно многие из амидных соединений формулы (I) имеют сильный индивидуальный острый вкусо-аромат в присутствии или отсутствии MSG и, таким образом, могут быть использованы в качестве самостоятельных ароматизаторов острого вкусо-аромата или усилителей вкусо-аромата.
Кроме того, предпочтительно использование таких искусственных ароматизаторов в минимально возможных концентрациях, минимизируя, таким образом, как стоимость, так и любое побочное воздействие при введении соединений формулы (I) в больших концентрациях. Соответственно желательно тестировать соединения формулы (I) на их эффективность в качестве агонистов рецепторов вкуса в низких концентрациях, выявляя таким образом лучшие и самые эффективные связанные гетероарильные соединения формулы (I). Как описано в WO03/001876 и патентной публикации США 2003-0232407 А1, включенных в качестве ссылки, и как описано здесь ниже, сейчас существуют лабораторные процедуры для измерения активности соединений агонистов рецептора hT1R1/hT1R3 «острого» вкуса. При таких способах, как правило, измеряют “EC50”, т.е. концентрацию, при которой соединение вызывает активацию 50% релевантного рецептора.
Предпочтительно связанные гетероарильные соединения формулы (I), являющиеся модификаторами острого вкусо-аромата, имеют EC50для рецептора hT1R1/hT1R3 менее чем около 10 мкM. Более предпочтительно, такие соединения имеют EC50 для рецептора hT1R1/hT1R3 менее чем около 5 мкM, 3 мкM, 2 мкM, 1 мкM или 0,5 мкM.
В некоторых вариантах воплощения настоящего изобретения соединения формулы (I) являются модуляторами или усилителями агонистической активности острого вкусо-аромата глютамата натрия для рецептора hT1R1/hT1R3. Здесь ниже описана опытная процедура для так называемых соотношений EC50, т.е. для растворения соединения формулы (I) в воде, содержащей MSG и измерения уровня, до которого амидное соединение понижает количество MSG, требуемое для активации 50% доступных рецепторов. Предпочтительно, соединения формулы (I) при растворении в водном растворе содержат около 1 мкM связанного гетероарильного соединения, понижающего наблюдаемый EC50 глютамата натрия для рецептора hT1R1/hT1R3, экспрессированного в клеточной НЕК линии клеток 293-Gα15, по меньшей мере, на 50%, т.е. соединение имеет соотношение EC50, по меньшей мере, 2,0 или предпочтительно 3,0, 5,0 или 7,0.
Вышеописанные анализы, используемые для выявления самых сильных соединений формулы (I), используемых в качестве модификатора или усилителя острого вкусо-аромата, и результаты таких анализов считаются хорошо коррелируемыми с существующим восприятием острого вкусо-аромата у животных и человека, но в конечном счете результаты анализов могут быть подтверждены, по меньшей мере, для самых сильных соединений формулы (I) проведением вкусового тестирования с участием людей. Такое экспериментальное вкусовое тестирование с участием людей может быть эффективно проконтролировано с использованием количественных и качественных показателей для водных растворов соединений-кандидатов в сравнении с контрольным водным раствором или, альтернативно, определением вкусовых показателей соединений по настоящему изобретению в используемых в настоящее время вкусовых композициях.
Для выявления более сильных модификаторов или агентов, придающих острый вкус, в водный раствор вводят соответственно любое индивидуальное гетероарильное соединение формулы (I) или представителя одного из его подклассов, которое должно иметь острый вкус согласно большинству из представителей комиссии, состоящей, по меньшей мере, из 8 человек, оценивающих вкус, в количестве, модифицирующем острый вкусо-аромат.
Соответственно для выявления более сильных усилителей, придающих острый вкус, в водный раствор вводят соединение формулы (I) в количестве, модифицирующем острый вкусо-аромат, и 12 мМ глютамата натрия, что должно усилить острый вкус по сравнению с контрольным водным раствором, содержащим 12 мМ глютамата натрия согласно большинству из представителей комиссии, состоящей, по меньшей мере, из 8 человек, оценивающих вкус. Предпочтительно для выявления более сильных усилителей, придающих острый вкус, в водный раствор вводят соединение формулы (I) в количестве, модифицирующем острый вкусо-аромат (предпочтительно около 30, 10, 5 или 2 частей на миллион), и 12 мМ глютамата натрия, что должно усилить острый вкус по сравнению с контрольным водным раствором, содержащим 12 мМ глютамата натрия и 100 мкM монофосфата инозина, согласно большинству из представителей комиссии, оценивающих вкус, состоящей, по меньшей мере, из 8 человек.
Применение соединения формулы (I) для получения пищевых композиций
Ароматизаторы, модификаторы вкусо-аромата, агенты, придающие вкусо-аромат, усилители вкусо-аромата, агенты, придающие острый («умами») вкусо-аромат и/или усилители острого («умами») вкусо-аромата, полученные из соединений формулы (I) и их подклассов и групп и их пищевых приемлемых солей и композиций с их использованием, могут быть использованы в пищевых продуктах, напитках и других пищевых композициях, где, как правило, используют соединения, придающие острый вкусо-аромат, в частности MSG, IMP или GMP. Эти композиции включаются в композиции для потребления человеком и животными. К ним относятся пищевые продукты или напитки (жидкие) для потребления сельскохозяйственными животными, домашними животными и животными, содержащимися в зоопарках.
Специалист в области получения и реализации пищевых композиций (т.е. пищевых продуктов или напитков или их предшественников или модификаторов их вкусо-аромата) хорошо представляет большое количество вариантов классов, подклассов и групп пищевых композиций, их использование в данной области техники, которое хорошо известно в отношении этих пищевых композиций, их получение и реализацию различных вариантов этих пищевых композиций. Такой список в рамках настоящего уровня техники приведен здесь ниже, а именно предполагается, что различные подклассы и группы соединений формулы (I) могут быть использованы для модификации и усиления острых вкусо-ароматов, представленных в следующем списке пищевых композиций, как отдельных, так и всех возможных комбинаций или смесей из них.
Одно или более кондитерское изделие, шоколадное кондитерское изделие, плитки, штучные шоколадосодержащие изделия типа батончиков, расфасованный шоколад с начинкой /без начинки, шоколад в коробках, шоколадные конфеты в коробках, миниатюры в обертке вперекрутку, фигурный шоколад, шоколад с игрушками, альфахорес (вид испанских медовых пряников), другие штучные шоколадные изделия, стандартная мятная леденцовая карамель, мятная леденцовая карамель с усиленным мятным вкусо-ароматом, леденцовая карамель, пастила, конфеты с жевательной резинкой, желейный и жевательный мармелад, карамель и нуга, медицинские кондитерские изделия, леденцы, лакричная карамель, другие вареные кондитерские изделия, жевательная резинка, жевательная резинка с сахаром, жевательная резинка без сахара, жевательная резинка медицинского назначения, жевательная резинка, образующая при жевании пузыри, хлеб, упакованный хлеб промышленного производства, неупакованный хлеб ручной выпечки, мучные кондитерские изделия, пирожные промышленного производства, пирожные ручной выпечки, печенье, печенье, покрытое шоколадом, печенье типа сандвичей, печенье с начинкой, печенье с пряностями и крекеры, заменители хлеба, зерновые завтраки, готовые к употреблению завтраки, семейные зерновые завтраки, хлопья, мюсли, другие готовые к употреблению завтраки, детские зерновые завтраки, горячие зерновые завтраки, мороженое, мягкое мороженое, порционное сливочное мороженое, порционное молочное мороженое, сливочное мороженое в брикетах, сливочное мороженое домашнего приготовления, мороженое домашнего приготовления, мороженое-десерт, молочные продукты, молоко свежее/пастеризованное, молоко цельное свежее/пастеризованное, молоко обезжиренное свежее/пастеризованное, молоко с длительным сроком хранения/УВТ, молоко цельное с длительным сроком хранения/УВТ, обезжиренное молоко с длительным сроком хранения/УВТ, молоко с пониженным содержанием жира с длительным сроком хранения/УВТ, козье молоко, сгущенное обезжиренное молоко, концентрированное обезжиренное молоко, сгущенное молоко, концентрированное молоко, сгущенное молоко с вкусовыми добавками, концентрированное молоко с вкусовыми добавками, функциональное и другие виды концентрированного молока, молочные напитки с вкусо-ароматическими добавками, молоко с вкусо-ароматическими добавками, молочные напитки с фруктовыми соками и вкусо-ароматическими добавками, соевое молоко, кисломолочные напитки, ферментированные молочные напитки, забеливатели для кофе, сухое молоко, сухие молочные напитки с вкусо-ароматическими добавками, сливки, сыры, плавленые сыры, пастообразные плавленые сыры, сырье для плавленых сыров, сырки, сырье для сыров, твердые сыры, расфасованные твердые сыры, нерасфасованные твердые сыры, йогурт, йогурт без добавок/натуральный, йогурт с вкусо-ароматическими добавками, йогурт с фруктами, пробиотический йогурт, питьевой йогурт, питьевой йогурт без добавок, пробиотический питьевой йогурт, охлажденные десерты с длительным сроком хранения, десерты на молочной основе, десерты на соевой основе, охлажденные снеки, домашний сыр и творог, домашний сыр и творог без добавок, домашний сыр и творог с вкусо-ароматическими добавками, пикантные домашний сыр и творог, сладкие и острые снеки, фруктовые снеки, чипсы/криспы, формованные снеки, тарталетки, кукурузные хлопья, поп-корн, крендель с солью, орешки, другие сладкие и острые снеки, батончики для перекусывания, зерновые батончики, батончики для завтрака, энергетические батончики, фруктовые батончики, другие батончики для перекусывания, продукты - заменители еды, продукты для похудения, диетические напитки, готовые блюда, готовые консервированные блюда, готовые замороженные блюда, концентраты готовых блюд, охлажденные готовые блюда, смеси для обеда, замороженная пицца, охлажденная пицца, суп, консервированный суп, суповые концентраты, суп быстрого приготовления, охлажденный суп, суп УВТ-обработки, замороженный суп, консервированная паста, сухая паста, охлажденная/свежая паста, лапша, обычная лапша, лапша быстрого приготовления, лапша быстрого приготовления в емкости для еды, лапша быстрого приготовления в мелкой расфасовке, охлажденная лапша, снеки из лапши, консервированные пищевые продукты, консервированное мясо и мясопродукты, консервированная рыба и морепродукты, консервированные овощи, консервированные томаты, консервированные бобы, консервированные фрукты, консервированные готовые к употреблению блюда, консервированный суп, консервированная паста, другие консервированные пищевые продукты, замороженные пищевые продукты, замороженное красное мясо, замороженное куриное мясо, замороженное рыбное филе и морепродукты, замороженные обработанные овощи, замороженные заменители мяса, замороженный картофель, готовые к употреблению замороженные картофельные чипсы, другие готовые к употреблению замороженные картофельные продукты, замороженные картофельные продукты, замороженные кондитерские изделия, замороженные десерты, замороженные блюда, готовые к употреблению, замороженная пицца, замороженный суп, замороженная лапша, другие замороженные пищевые продукты, пищевые концентраты, десертные смеси, концентраты готовых блюд, суповой концентрат, суп быстрого приготовления, сухая паста, обычная лапша, лапша быстрого приготовления, лапша быстрого приготовления в емкости для еды, охлажденные продукты питания, охлажденное мясо, охлажденная рыба и морепродукты, охлажденное рыбное филе, охлажденная рыба, охлажденная копченая рыба, охлажденный набор для второго завтрака, охлажденные готовые к употреблению блюда, охлажденная пицца, охлажденный суп, охлажденная/свежая паста, охлажденная лапша, масла и жиры, оливковое масло, растительное и рапсовое масло, кулинарные жиры, сливочное масло, маргарин, пастообразные растительные масла и жиры, функциональные пастообразные растительные масла и жиры, соусы, дрессинги и заправки, томатная паста и пюре, бульонные кубики, гранулированная подлива, жидкие бульоны и основы, травы и специи, ферментированные соусы, соусы на основе сои, соусы для пасты, жидкие соусы, сухие соусы/порошкообразные смеси, кетчуп, майонез, обычный майонез, горчица, салатные дрессинги, обычные салатные дрессинги, салатные дрессинги с низким содержанием жира, винегреты, подлива, маринованные продукты, другие соусы, дрессинги и заправки, детское питание, молочное детское питание, традиционное молочное детское питание, усовершенствованное молочное детское питание, молочное детское питание для детей ясельного возраста, гипоаллергенное молочное детское питание, готовое детское питание, сухое детское питание, другие виды детского питания, спрэды, консервы и пресервы, мед, шоколадные спреды, спреды на ореховой основе и спреды на дрожжевой основе.
Предпочтительно соединения формулы (I) могут быть использованы для модификации или усиления острого вкусо-аромата одного или более из следующих подклассов пищевых композиций: штучных кондитерских изделий, выпечки, мороженого, молочных продуктов, острых снеков, батончиков для перекусывания, продуктов, заменяющих еду, готовых к употреблению блюд, супов, пасты, лапши, консервированных пищевых продуктов, замороженных пищевых продуктов, сухих пищевых продуктов, охлажденных пищевых продуктов, масел и жиров, детского питания, спрэдов или смесей из них.
Как правило, получают усваиваемую композицию, содержащую достаточное количество, по меньшей мере, одного соединения формулы (I) или различных его подклассов по настоящему изобретению, приведенных в описании выше, для получения композиции с требуемыми вкусо-ароматическими характеристиками, такими как «острые» вкусовые характеристики.
Как правило, по меньшей мере, количество, модулирующее острый вкусо-аромат одного или более соединений формулы (I), вводят в пищевой продукт, таким образом, модифицированный пищевой продукт с острым вкусо-ароматом обладает усиленным острым вкусо-ароматом по сравнению с пищевым продуктом, полученным без соединения формулы (I), согласно предпочтению людей или животных или в случае тестирования рецептур согласно большинству из представителей комиссии, состоящей, по меньшей мере, из 8 человек, оценивающих вкус с использованием описанных здесь процедур.
Концентрация агента, придающего острый вкусо-аромат, необходимая для модулирования или улучшения вкусо-аромата пищевого продукта или композиции, значительно варьирует в зависимости от многих факторов, в том числе от специфичности усваиваемой композиции, от изначально присутствующих соединений, придающих острый вкусо-аромат, и их концентрации, от изначально присутствующего количества MSG и усиливающего эффекта, оказываемого определенным соединением на такие соединения, придающие острый вкусо-аромат. Как было отмечено, важность применения соединений формулы (I) заключается в модулировании (включая усиление и/или ингибирование) острого вкуса и других вкусовых свойств натуральных или синтетических тастантов острого вкусо-аромата, в частности MSG. Для обеспечения усиления острого вкуса соединения формулы (I) могут быть применены в широких пределах, т.е. от около 0,001 частей на миллион до 100 частей на миллион, в более узких альтернативных пределах от около 0,1 частей на миллион до 10 частей на миллион, от около 0,1 частей на миллион до 30 частей на миллион, от около 0,05 частей на миллион до 15 частей на миллион, от около 0,1 частей на миллион до 5 частей на миллион или от около 0,1 частей на миллион до 3 частей на миллион.
Примеры пищевых продуктов и напитков, в которые могут быть введены соединения по настоящему изобретению, включают, но не ограничивают категорию жидких супов, категорию пищевых концентратов и кулинарных продуктов, категорию напитков, категорию замороженных пищевых продуктов, категорию снеков и приправы или их смеси.
«Категория жидких супов» обозначает жидкие/содержащие влагу супы независимо от концентрации или упаковки, включая замороженные супы. Под определением суп(ы) понимается пищевой продукт, полученный из мяса, мяса птицы, рыбы, овощей, зерна, фруктов и других ингредиентов, сваренный в жидкости, которая может включать видимые кусочки некоторых или всех из этих ингредиентов. Он может быть прозрачным (как бульон) или густым (как рыбная похлебка), однородным, пюреобразным, содержащим кусочки, готовым к употреблению, полуфабрикатом или концентратом, может употребляться как горячим, так и холодным, как первое блюдо, так и основное или в качестве закуски (употребляется маленькими глотками как напиток). Суп может быть использован в качестве ингредиента для приготовления других видов блюд и разграничивается от бульона (консоме) до соусов (сливочные или сырные супы).
«Категория пищевых концентратов и кулинарных продуктов» обозначает: (i) полуфабрикаты, такие как порошки, гранулы, пасты, концентрированные жидкие продукты, включая концентрированный бульон, бульон и бульонные продукты, такие как бульонные кубики, таблетированные, порошкообразные или гранулированные формы бульона, которые продаются отдельно как готовый продукт или как ингредиент; соусы и сухие соусы (независимо от технологии); (ii) пищевые концентраты, требующие внесения влаги при приготовлении, такие как: концентрированные и замороженные сухие супы, включая концентрированные суповые смеси, концентрированные супы быстрого приготовления, готовые к употреблению концентрированные супы, концентраты или готовые к употреблению блюда для приготовления на природе, однопорционные блюда и закуски, включая пасту, картофельные и рисовые блюда; и (iii) соусы и заправки, такие как заправки, маринады, салатные дрессинги, салатные топпинги, подливы, панировки, масляные смеси, спрэды с длительным сроком хранения, соусы барбекю, жидкие рецептурные смеси для соусов, концентраты, соусы или соусные смеси, включая рецептурные смеси для салатов, которые продаются отдельно как готовый продукт или как ингредиент без разграничения на концентрированные, жидкие или замороженные.
«Категория напитки» обозначает напитки, смеси и концентраты для напитков, включая, но, не ограничивая алкогольные и безалкогольные, готовые к употреблению напитки и сухие порошкообразные напитки.
Другие примеры пищевых продуктов и напитков, куда могут быть введены соединения по настоящему изобретению, включают, но не ограничивают газированные и негазированные напитки, например, содовую, фруктовые и овощные соки, алкогольные и безалкогольные напитки, кондитерские изделия, пирожные, печенье, пироги, конфеты, жевательные резинки, желе, мороженое, щербеты, пудинги, жевательные конфеты, мармелад, салатные дрессинги и другие заправки, зерновые и другие завтраки, консервированные фрукты и фруктовые соусы и т.п.
Кроме того, соединения по настоящему изобретению могут использоваться в препаратах, придающих вкус и аромат, используемых для введения в пищевые продукты и напитки. В предпочтительных примерах композиция включает другие модификаторы вкуса и аромата, такие как тастанты острого вкусо-аромата.
Таким образом, в некоторых вариантах воплощения настоящее изобретение относится к способам модулирования острого вкуса пищевых продуктов, включающим:
а) обеспечение, по меньшей мере, одного пищевого продукта или его предшественника, и
i. смешивание пищевого продукта или его предшественника, по меньшей мере, с одним соединением формулы (I) или представителем любого из его подклассов или его пищевой приемлемой солью, по меньшей мере, в количестве, модулирующем острый вкусо-аромат, с получением модифицированного пищевого продукта.
Настоящее изобретение относится к модифицированным пищевым продуктам, полученным такими способами и аналогичными способами получения пищевых продуктов, хорошо известными специалисту в данной области техники, а именно когда такие композиции содержат MSG и соединение, используемое в качестве усилителя острого вкуса MSG, присутствующее также в композиции.
Амидные соединения формулы (I) и различные их подклассы могут быть смешаны с пищевыми или медицинскими продуктами или их предшественниками или введены в них любыми известными для производителей пищевых или медицинских продуктов способами. Например, соединения формулы (I) могут быть растворены или диспергированы в одну или более из известных приемлемых жидкостей, твердых веществ или других носителей, таких как вода, при нейтральном, кислом или щелочном рН, фруктовые или овощные соки, уксус, маринады, пиво, вино, природную воду/жировые эмульсии, такие как молоко или сгущенное молоко, пищевые масла и шортенинги, жирные кислоты и их алкильные эфиры, низкомолекулярные олигомеры пропиленгликоля, глицериновые эфиры жирных кислот и дисперсии или эмульсии таких гидрофобных веществ в водной среде, соли, такие как хлорид натрия, растительная мука, растворители, такие как этанол, твердые пищевые наполнители, такие как растительные порошки или мука и т.п., затем смешаны с предшественниками пищевых или медицинских продуктов или внесены непосредственно в пищевые или медицинские продукты.
Получение связанных гетероарильных соединений формулы (I)
Исходные материалы, использованные для получения соединений по настоящему изобретению, т.е. различных структурных подклассов и групп соединений синтетических предшественников связанных гетероарильных соединений формулы (I) представляют собой органические карбоксильные кислоты и бензойные кислоты, изоцианаты и различные амины, анилины, аминокислоты и т.п. и являются хорошо известными соединениями или могут быть синтезированы способами, описанными в литературе, или коммерчески доступны из различных источников, хорошо известных специалисту в данной области, таких как, например, Sigma-Aldrich Corporation of St. Louis, Missouri USA и их дочерние компании Fluka and Riedel-de Haеn, расположенные в различных офисах по всему миру, и другие хорошо известные поставщики, такие как Fisher Scientific, TCI America of Philadelphia, PA, ChemDiv of San Diego, CA, Chembridge of San Diego, CA, Asinex of Moscow, Russia, SPECS/BIOSPECS of the Netherlands, Maybridge of Cornwall, England, Acros, TimTec of Russia, Comgenex of South San Francisco, CA и ASDI Biosciences of Newark, DE.
Очевидно, специалист в данной области органической химии может легко синтезировать большую часть исходного сырья и провести последующие манипуляции самостоятельно, таким образом, он может легко осуществить на практике большинство требуемых манипуляций. Эти манипуляции включают восстановление углеродных соединений до спиртов, окисления, ацилирования, замещения в ароматическом ядре, как электрофильные, так и нуклеофильные, получение простых и сложных эфиров, омыление, нитрование, гидрогенизацию, восстановление аминированием и тому подобное. Эти манипуляции описаны в стандартных текстах, таких как March's Advanced Organic Chemistry (3d Edition, 1985, Wiley-Interscience, New York), Feiser and Feiser's Reagents for Organic Synthesis, и его различные тома и издания от Methoden der Organischen Chemie (Houben-Weyl) и тому подобное. Многие традиционные способы получения исходного сырья включают различные замещения гетероцикла, гетероарила и арильных колец (предшественники Ar, hAr1, и/или hAr2), могут быть найдены в Methoden der Organischen Chemie (Houben-Weyl), различные тома и издания которой доступны от Georg Thieme Verlag, Stuttgart. Полное описание приведенной выше монографии включено посредством полной ссылки, включая технологии способов синтеза органических соединений и их предшественников.
Также специалисту в данной области техники легко понять, что определенные реакции проведены хорошо, если дополнительные функции молекулы замаскированы или защищены, что позволяет избежать нежелательных побочных реакций и/или увеличить выход продукта реакции. Часто специалист в данной области техники использует защищающие группы, чтобы увеличить выход продукта или избежать нежелательных реакций. Эти реакции описаны в литературе и тоже хорошо известны специалисту в данной области техники. Примеры многих из этих манипуляций могут быть найдены, например, в T. Greene and P. Wuts, Protecting Groups in Organic Synthesis, 3rd Ed., John Wiley & Sons (1999).
Следующие сокращения, использованные в примерах и описании, приведены ниже:
CH3CN=ацетонитрил
CHCl3=хлороформ
DIC=N,N'-диизопропилкарбодиимид
DIPEA=диизопропилэтиламин
DMAP=4-(диметиламино)пиридин
DMF=N,N-диметилформамид
EDCI=1-(3-диметиламинопропил)-3-этилкарбодиимид гидрохлорид
DCM=дихлорметан
ESIMS=распылительная электронная масс-спектрометрия
Et3N=триэтиламин
EtOAc=этилацетат
EtOH=этиловый спирт
Fmoc=N-(9-флуоренилметоксикарбонил)
HCl=соляная кислота
H2SO4=серная кислота
HOBt=1-гидроксибензотриазол
MeOH=метиловый спирт
MgSO4=сульфат магния
NaHCO3=бикарбонат натрия
NaOH=гидроксид натрия
Na2SO4=сульфат натрия
Ph=фенил
r.t.= комнатная температура
SPOS=твердофазный органический синтез
THF=тетрагидрофуран
TLC=тонкослойная хроматография
Сокращения для алкильной группы
Me=метил
Et=этил
n-Pr=нормальный пропил
i-Pr=изопропил
n-Bu=нормальный бутил
i-Bu=изобутил
t-Bu=третичный бутил
s-Bu=вторичный бутил
n-Pen=нормальный пентил
i-Pen=изопентил
n-Hex=нормальный гексил
i-Hex=изогексил
Сокращения для реагентов на полимерной подложке
PS-Trisamine=Tris-(2-аминоэтил)амин полистирол
PS-NCO=метилизоцианат полистирол
PS-TsNHNH2=толуолсульфонилгидразон полистирол.
Примеры способов получения гетероарильных соединений формулы (I)
Схема 1А
Способы получения 3,5-двузамещенных 1H-1,2,4-триазолов

Как показано на схеме 1А, производные карбоновой кислоты Ar радикала могут быть активированы превращением хлорангидридов (Способ А) или эфиров карбодиимида (Способ В), которые реагируют с тиосемикарбазидом, обеспечивая взаимодействие триазол-тионов, которые могут реагировать с производными замещенного алкила hAr2, включая подходящие уходящие группы (“LG”, такие как хлориды, бромиды, иодиды, тозилаты и им подобные) с образованием производных триазола, имеющих структуры, которые входят в объем формулы (I).
Схема 1В
Альтернативный способ получения 3,5-двузамещенных 1H-1,2,4-триазолов

Как показано на схеме 1В, производные 1,2,4,-триазола (I) могут быть получены альтернативно в два этапа из амидных предшественников Ar кольца обработкой сильными основаниями, сернистым углеродом и электрофильным предшественником hAr2 радикала в форме промежуточного соединения ацилкарбонодитиоимидата, который в присутствии гидразина превращается в требуемый триазольный продукт. (См.M. Satoet al., Synthesis, 7, 1981, 554-557).
Схема 1С
Способ получения 3,4,5-тризамещенных-4H-1,2,4-триазолов

Как показано на схеме 1С, N-замещенный триазол, который входит в объем формулы (I), может быть получен многоэтапным способом, начиная с обработки аминного предшественника N-замещенного триазола сернистым углеродом и метилиодидом с образованием дитиокарбамата, который может реагировать с гидразином с образованием тиосемикарбазида, который может быть конденсирован с Ar предшественником карбоновой кислоты с образованием циклического меркаптотриазола, который может быть алкилирован с использованием подходящих электрофильных предшественников hAr2, таких как алкилиодид (см. Ashtonet al., J. Med. Chem. 1992, 35, 2103-2112).
Схема 1D
Способ получения 5-амино-1,2,4-триазолов

Как показано на схеме 1D, 5-аминопроизводные 1,2,4-триазолов могут быть получены в два этапа из Ar предшественников метилового эфира реакцией с гуанидином при основных условиях с образованием промежуточного соединения 5-аминотриазола, который реагирует с электрофилами, такими как изотиоцианаты, с образованием соединения N-тиоацилтриазол, которое затем может быть конденсировано с hAr2электрофильным предшественником и гидролизовано. (См.Y. Naitoet al., J. Med. Chem. 39, 15, 1996, 3019-3029).
Схема 1Е
Альтернативный способ получения 2H-1,2,4-триазол-3-аминов

Как показано на схеме 1Е, 5-аминопроизводные 1,2,4-триазолов (I) могут быть получены альтернативно реакцией Ar предшественников ортоэфира с цианоамином и уксусным ангидридом с образованием N-цианомидата, который затем реагирует с гидразином с образованием 3-аминотетразола, который может вступить в реакцию с hAr2электрофильными предшественниками (см.K.R. Husfmann et al., J. Org. Chem. 28, 1963, 1816-1821).
Схема 2А
Способ получения 2,5-двузамещенных-1,3,4-оксадиазолов

Как показано на схеме 2А, 1,3,4-оксадиазолы (I) могут быть получены из Ar предшественников гидразида и hAr2предшественников хлорангидридов (См.B.G. Szczepankiewiczet al., J. Med Chem. 2001, 44, 4416-4430).
Схема 2В
Способ получения N,3-двузамещенных-1-1,2,4-оксадиазол-5-аминов
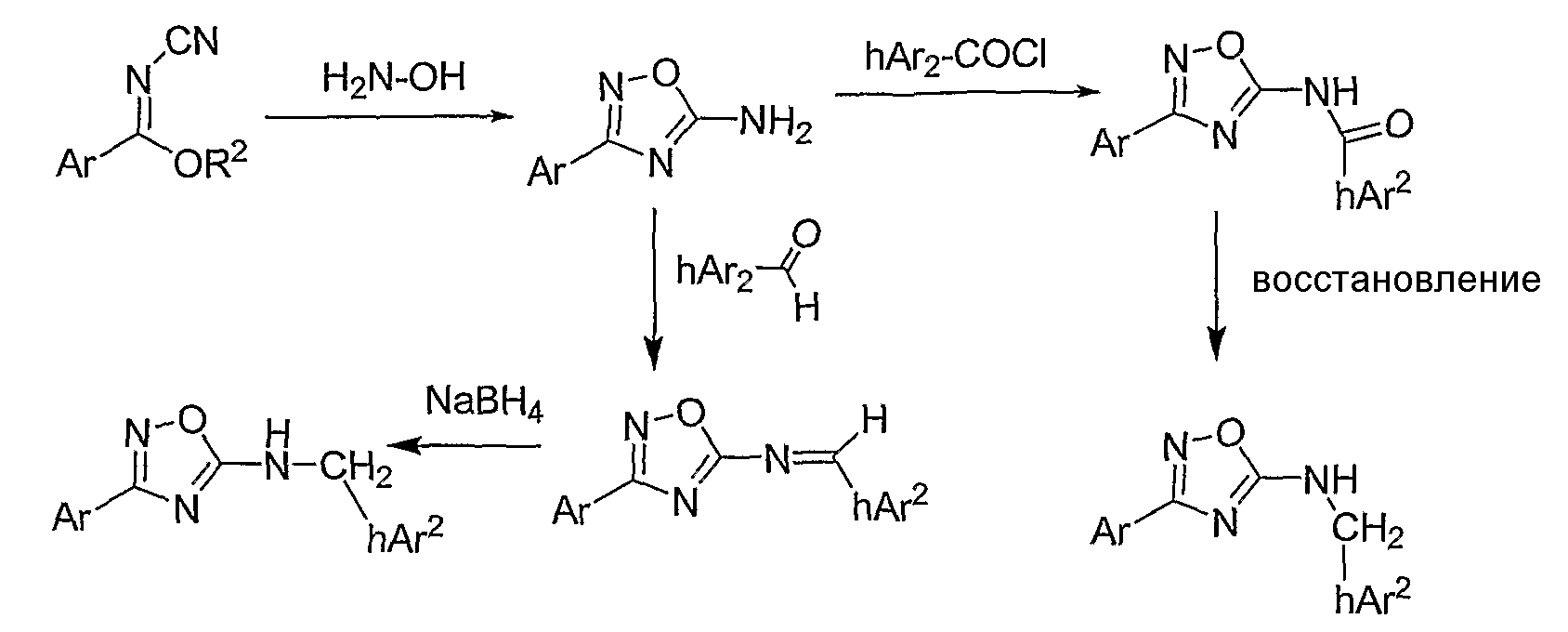
Как показано на схеме 2В, N-цианомидаты (полученные, как показано выше на схеме 1Е) реагируют с гидроксиламином с образованием 5-амино-1,2,4-оксидиазолов (II), которые могут быть алкилированы или ацилированы с образованием N,3-двузамещенных-1-1,2,4-оксадиазол-5-аминов. (См.K.R. Husfmannet al., J. Org. Chem. 28, 1963, 1816-1821).
Схема 2С
Способ получения N,3-двузамещенных-1-1,2,4-оксадиазол-5-аминов

Как показано на схеме 2С, Ar предшественники гидразида могут быть обработаны бромцианом в EtOH с образованием 1,3,4-оксадизолиламинов, которые могут быть превращены в замещенные триазолы или оксадиазолы, которые входят в объем соединений формулы (I). См. РСТ патентную публикацию WO02/078696 Marino et al., стр.14, опубликовано 10 октября 2002.
Схема 3А
Способ получения N,3-двузамещенных-1,2,4-тиадиазол-5-аминов
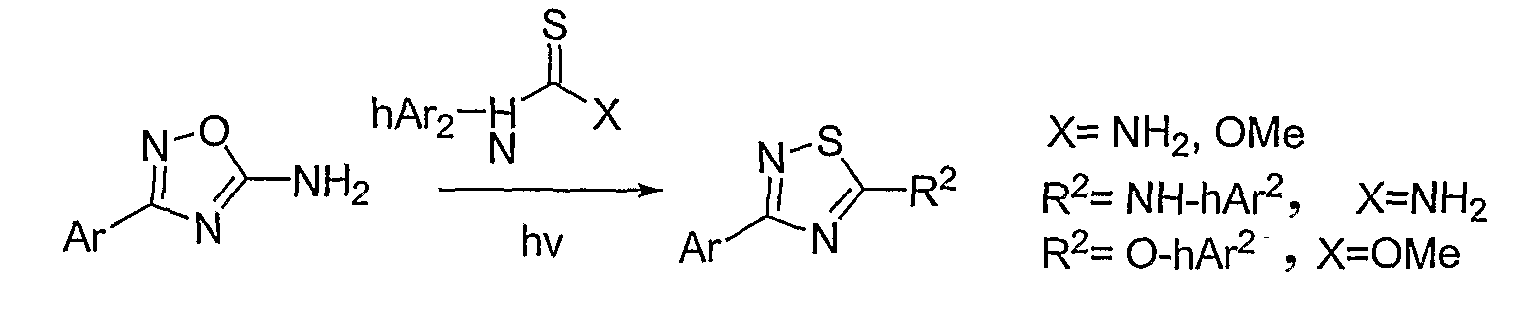
Как показано на схеме 3А, промежуточное соединение оксадиазола (см. получение на схеме 2В) может перестраиваться с участием серных нуклеофилов с УФ-облучением с образованием 1,2,4-тиадиазол-5-аминов (см.N. Vivonaet.al., Tetrahedron 53, 37, 1997, 12629-12636).
Схема 3В
Способ получения 2,5-двузамещенных-1,3,4-тиадиазолов

Как показано на схеме 3В, 1,3,4-тиадиазолы могут быть получены реакцией ВОС защищенных гидразидов с реагентом Лавессона в присутствии трифторуксусной кислоты с образованием тиогидразидов, реагирующих с замещенными альдегидами со спонтанной циклизацией. (См.B.G. Szczepankiewiczet al., J. Med Chem. 2001, 44, 4416-4430).
Схема 4А
Получение соединений формулы (I), содержащих аминопиридин, пиримидин и пиразин hAr1кольца

Многие замещенные и незамещенные бромонитропиридины, такие как соединение (4А1) на схеме 4А, представляют собой соединения, коммерчески доступные или легко синтезируемые по способам, хорошо известными специалисту в данной области. Восстановление нитрогрупп соединений (4А1) может проводиться различными способами, включая обработку SnCl2, которая может обеспечить образование аминопиридинов (4А2). Альтернативно, многие аминопиридины (4А2) также являются коммерчески доступными.
Бромопиридины, такие как (4А2) или (подобные пиридины включают трифлатные заместители), могут быть использованы в катализируемой палладием реакции по Сузуки в сочетаниях предшественников арилбороновой кислоты из Ar кольца соединений формулы (I) для образования сочетаний ароматического пиридина (4А4). Для получения необходимы арилбороновые кислоты и обеспечение способов проведения реакций по Сузуки, хорошо известных из уровня техники и описанных, например, Suzuki, Pure & Applied Chem., 66:213-222 (1994), Miyaura and Suzuki, Chem. Rev. 95:2457-2483 (1995), Watanabe, Miyaura and Suzuki, Synlett. 207-210 (1992), Littke and Fu, Angew. Chem. Int. Ed., 37:3387-3388 (1998), Indolese, Tetrahedron Letters, 38:3513-3516 (1997), Firooznia, et al., Tetrahedron Letters 40:213-216 (1999), и Darses, et al., Bull. Soc. Chim. Fr. 133:1095-1102 (1996); включены посредством ссылки.
Сочетания ароматических пиридинов (4А4) могут быть обработаны основанием и алкилирующим агентом, таким как, например, VI с образованием hAr2 предшественника производного электрофильного пиридина с выходом соединений формулы (I).
Альтернативно, промежуточное соединение амино (4А4) может быть получено, во-первых, по реакции Сузуки сочетанием бромонитропиридина (4А1) с арилбороновой кислотой и затем восстановлением нитрогруппы с образованием аминосоединения (4А3). Аналогичная серия реакций, где NH2 группа соединения (4А2) замещается гидроксильной или сульфгидрильной группой или защищена ее производным, затем проводят реакцию Сузуки и алкилирование или необязательно оксидацию серных аналогов органическими перкислотами, обеспечивая готовые синтетические подходы к соединениям формулы (I), где X представляет собой O, S, SO или SO2.
Подобным образом синтез производных пиримидина и пиразина начинают с коммерчески доступных бромоаминопиримидинов или пиридинов, которые могут быть получены аналогично реакциям, описанными выше или в соответствии со схемой 4В, как показано ниже:
Схема 4В

Исходное сырье бромопиримидин или пиразин, являющееся легко доступным, может быть алкилировано электрофильными hAr2 предшественниками и основанием с образованием синтетических промежуточных соединений со связанными hAr1 и hAr2 радикалами, которые в свою очередь могут быть подвергнуты реакции Сузуки предшественниками арилбороновой кислоты из Ar с образованием требуемых пиримидиновых и пиразиновых соединений формулы (I).
Схема 5
Способ получения 3-(арилтио)-необязательно замещенных пиридазинов

Как показано на схеме 5, 3-(арилтио)пиридазины (5А5) могут быть получены многоэтапным способом посредством конденсирования подходящих предшественников ацетофенона из Ar группы (5A1) с α-кетокислотами с образованием промежуточных соединений ациклической кетокислоты, которые затем конденсируют с гидразином с выходом циклизованного продукта (5А2) - предшественника hAr1. (5A2) может быть обработан POCl3 с выходом промежуточного соединения циклического монохлорида (5А3), который может вступать в реакцию с тиомочевиной с выходом циклических тионов формулы (5А4), которые, таким образом, представляют собой алкилирующие агенты - предшественники hAr2, такие как галиды, тозилаты и им подобные, с образованием требуемых 3-(арилтио)пиридазинов (5А5). См. J. Med. Chem. 2001, 44, 2707-2718 (J.-M. Contreras); и Molecules, 2003, 8, 322-332 (G.H. Sayed).
Схема 6
Способ получения 3-(арилокси) или 3 (ариламино)-необязательно замещенных пиридазинов
Схема 6А: Получение необязательно замещенных пиридазинов

Как показано на схеме 6А, хлоропиридазин (5А3) (см. схему 5) может быть преобразован в необязательно замещенный (6А2а) или (6А2b) посредством реагирования с соответствующим первичным спиртом (6А1а) или амином (6А1b). См. J. Med. Chem. 2001, 44, 2707-2718 (J.-M. Contreras);
Схема 6В: Получение незамещенных пиридазинов

Как показано на схеме 6В, незамещенные пиридазины (6А6а) и (6А6b) могут быть получены, начиная с обработки симметричного дихлоропиридазина (6А3) соответствующим спиртом (6А1а) или амином (6А1b), с последующим проведением реакции Сузуки в присутствии бороновой кислоты (6А5). Альтернативно незамещенные пиридазины (6А6а) и (6А6b) могут быть сначала подвергнуты реакции в присутствии бороновой кислоты (6А5) с образованием хлоропиридазинов (6А7а) и (6А7b), которые могут быть обработаны спиртом (6А1а) или амином (6А1b) с образованием соответствующих пиридазинов (6А6а) и (6А6b).
Схема 7
Способ получения 1,4-двузамещенных-1,2,3-триазолов

Как показано на схеме 7, 1,4-двузамещенные-1,2,3-триазолы (7А3) могут быть получены с использованием микроволнового излучения, способствующего проведению трехкомпонентной реакции алкилгалида (7А1), азида натрия и алкина (7А2), см. P. Appukkuttan et al Org. Lett. 2004, 6, 23, 4223-4225.
Схема 8
Способ получения 2,5-двузамещенных-2Н-тетразолов

Как показано на схеме 8, 2,5-двузамещенные-2Н-тетразолы (8А3) могут быть получены из нитрила (8А1) реакцией с триметилсилильным азидом (TMSiN3) с тетрабутиламмония бромидом (TBAF) (См. D. Amantini J. Org. Chem. 2004, 69,8, 2896-2898), с образованием промежуточного соединения тетразола (8A2), который может быть алкилирован алкилгалидами (8A4). См. J.R. Maxwell, J. Med. Chem. 1984, 2, 1565-1570.
Вышеприведенные примерные схемы и документы из уровня техники обеспечивают руководство для получения представленных здесь соединений формулы (I). Статьи и патенты, цитированные из уровня техники, включены сюда в качестве ссылки для описания релевантных стратегий синтеза и экспериментальных способов. Перечисленные выше способы не ограничивают объем изобретения и понятны специалисту в данной области техники, даже если для получения соединений формулы (I) будут проведены модификации схем и/или изменены стратегии синтеза, приведенные выше. Такие способы, в частности, основаны на твердофазном синтезе комбинаторной химии. Таким образом, специалист в данной области техники вполне способен получить необходимые и/или заявленные соединения способами, описанными в монографиях и литературе и в описании настоящего изобретения. Специалист, имеющий литературу и описание, в достаточной мере вооружен знаниями для того, чтобы получить любое необходимое исходное сырье и/или заявленные соединения. Несмотря на это, в некоторых примерах, приведенных ниже, использованное исходное сырье не относится к легко доступному и по этой причине оно должно быть синтезировано, и синтез исходных материалов приведен в примерах.
Измерение биологической активности соединений по настоящему изобретению
Основные клеточные технологии и анализы, такие, как описанные в WO 02/064631 и WO 03/001876 и патентной публикации США US 2003-0232407 А1, были использованы для начального отбора широко варьирующих классов соединений агонистов или антагонистов активности T1R1/T1R3 рецепторов «острого» вкуса, которые были экспрессированы в подходящих линиях клеток. Как только начальные «хиты» были получены отбором из таких линий клеток, те же анализы и так же определенные на основе анализов клетки и/или основные рецепторы были использованы в качестве аналитических средств для измерения количественной способности соединений формулы (I) усиливать острый вкус MSG и были использованы для получения имперических данных, служащих проводником в интерактивном процессе синтеза и тестирования структурных вариантов начальных соединений, тестирования восприятия вкуса человеком с использованием групп соединений, вызывающих наибольший интерес, таким образом, конструируя, тестируя и выявляя классы соединений и группы, у которых проявляются повышенные или оптимальные уровни требуемой биологической активности.
Многие варианты воплощения настоящего изобретения относятся к идентификации определенных соединений и классов амидных соединений формулы (I), которые модулируют (повышают или понижают) активность T1R1/T1R3 (предпочтительно hT1R1/hT1R3) рецептора острого вкуса (рецептор умами), по отдельности или в комбинации с другими соединениями, которые активируют hT1R1/hT1R3, а именно MSG. В частности, многие варианты воплощения настоящего изобретения относятся к связанным гетероарильным соединениям формулы (I), которые модулируют активность hT1R1/hT1R3 (рецептор умами человека) in vitro и/или in vivo. В другом аспекте настоящее изобретение относится к соединениям формулы (I), которые модулируют восприятие человеком острого (умами) вкуса по отдельности или в комбинации с другим соединением или ароматизатором, таким как MSG, где (1) одно или более соединений формулы (I) и (2) MSG введены в пищевую композицию, в результате чего острый вкусо-аромат MSG усилен или умножен, таким образом, требуется введение меньшего количества MSG в модифицированные пищевые композиции для получения требуемого уровня умами/острого вкуса.
Анализ активации In Vitro рецептора hT1R1/hT1R3 вкуса умами
Для выявления новых агентов, придающих острый вкус и аромат, и усилителей, включая соединения агонисты острого вкусо-аромата и усилители активности (двойная активность), соединения формулы (I) были отобраны в результате первичных и вторичных анализов, включая анализ на доза-эффект соединения и анализ на усиление. В первичном анализе на потенциальную способность модулировать вкус умами были идентифицированы соединения формулы (I), которые могут быть как собственно агентами, придающими острый вкусо-аромат, так и усилителями вкусо-аромата MSG, и подсчитали их активность в процентах от максимальной интенсивности MSG (%). По доза-эффект соединения было высчитано EC50 для отражения эффективности соединения в качестве агониста или усилителя острого вкуса.
Получена НЕК клеточная линия 293 (См.,например, Chandrashekar, et al., Cell (2000) 100: 703-711), которые при использовании индуцибельного промотора стабильно экспрессируют Gα15 и hT1R1/hT1R3 (См. WO 03/001876 A2), которые используют для идентификации соединений со свойствами тастантов острого вкусо-аромата.
Соединения по настоящему изобретению первоначально были выбраны на основе их активности к рецептору hT1R1/hT1R3 клеточной НЕК линии 293-Gα15. Активность была определена с использованием автоматического дисплейного прибора для проведения флуорометрического анализа FLIPR (Fluorometric Intensity Plate Reader, Molecular Devices, Sunnyvale, CA) (обозначенного FLIPR анализ). Клетки из одного клона (обозначенного клон I-17) были высеяны на 384-луночные планшеты (около 48000 клеток на лунку) в среду, содержащую модифицированную по способу Дульбекко среду Игла (DMEM), с добавлением GlutaMAX (Invitrogen, Carlsbad, CA), 10% диализованной эмбриональной бычьей сыворотки (Invitrogen, Carlsbad, CA), 100 единиц/мл пенициллина G, 100 мкг/мл стрептомицина (Invitrogen, Carlsbad, CA) и 60 пM мифепристона (для индуцирования экспрессии hT1R1/hT1R3) (см. WO03/001876 А2). I-17 клетки были выращены в течение 48 часов при температуре 37°С. Затем I-17 клетки наполняли кальциевым сенсором Fluo-3AM (Molecular Probes, Eugene, OR), 4 мкM в фосфатно-буферном солевом растворе (D-PBS) (Invitrogen, Carlsbad, CA), в течение 1,5 часов при комнатной температуре. После замещения 25 мкл D-PBS была проведена стимуляция в приборе FLIPR при комнатной температуре введением 25 мкл D-PBS с добавлением различных стимуляторов в концентрациях, превышающих в два раза требуемый конечный уровень. Активность рецептора определялась в количественном выражении определением максимального повышения флуоресценции (с использованием 480 нм и 535 нм эмиссии) после нормализации до базовой флуоресцентной интенсивности, измеренной перед стимуляцией.
Для анализов доза-эффект стимуляторы были продублированы в 10 различных концентрациях в пределах от 1,5 нM дo 30 мкM. Активность была нормализована до ответа с 60 мМ глютамата натрия, концентрации, при которой выявляется максимальный ответ рецепторов. EC50 (концентрация соединения, при которой происходит 50% активация рецептора) была определена с использованием нелинейного возвратного алгоритма, где коэффициент Хилла нижней и верхней асимптоты варьировал. Идентичные результаты были получены для анализов доза-эффект с использованием коммерчески доступного программного обеспечения для анализа нелинейных возвратных алгоритмов, такого как GraphPad PRISM (San Diego, СА).
Для определения зависимости hT1R1/hT1R3 от клеточного ответа на различные стимуляторы отобранные соединения были проанализированы с использованием анализов, как для I-17 клеток, которые не были индуцированы мифепристоном для экспрессирования рецептора (обозначенные, как неиндуцирующие I-17 клетки). Неиндуцирующие I-17 клетки не показали никакого функционального ответа в FLIPR анализе на глютамат натрия или другие вещества - тастанты острого вкуса. Соединения присутствовали в неиндуцирующих умами клетках при 10 мкM или в количестве в три раза большем, чем в анализах доза-эффект. Соединения по настоящему изобретению не показали никакого функционального ответа при использовании в FLIPR анализе неиндуцирующих умами клеток.
В некоторых аспектах настоящего изобретения соотношение EC50 ниже, чем около 10 мМ, является индикатором соединений, которые индуцируют активность hT1R1/hT1R3 и считаются агонистом острого вкусо-аромата. Предпочтительно агонист острого вкусо-аромата имеет соотношение EC50 ниже, чем около 1 мМ; и более предпочтительно имеет соотношение EC50 ниже, чем около 20 мкM, 15 мкM, 10 мкM, 5 мкM, 3 мкM, 2 мкM, 1 мкM, 0,8 мкM или 0,5 мкM.
В анализах усиления активности вкуса умами также получали «соотношение EC50» в измерениях, показывающих насколько эффективно амидные соединения по настоящему изобретению усиливают ароматизатор острого вкусо-аромата (как правило, MSG) в ранее тестированном растворе. Серии измерений доза-эффект проводили одновременно в растворах, содержащих только один MSG, затем повторно измеряли доза-эффект в растворах, где MSG находился в комбинации с заранее определенными количествами соединения-кандидата формулы (I).
В этом анализе повышали присутствующие концентрации глютамата натрия (в пределах от 12 мкM до 81 мM) с дублированием его в присутствии или отсутствие фиксированной концентрации тестируемого соединения. Как правило, концентрации тестируемого соединения составляли 30 мкM, 10 мкM, 3 мкM, 1 мкM, 0,3 мкM, 0,1 мкM и 0,03 мкM. Относительная эффективность соединений формулы (I) при усилении рецептора была определена вычислением величины сдвига EC50 для глютамата натрия. Усиление было определено как соотношение (EC50R), соответствующее EC50 для глютамата натрия, определенного в отсутствие тестируемого соединения, деленного на EC50 для глютамата натрия, определенного в присутствии тестируемого соединения. Соединения, демонстрирующие EC50R>2,0, считаются усилителями.
Альтернативный вариант расчета «соотношения EC50» в сравнении с MSG был высчитан исходя из следующей формулы:
соотношение EC50для MSG=EC50 (MSG)/EC50 (MSG+[Соединение]),
где «[Соединение]» обозначает концентрацию соединения формулы (I), используемого для выявления (или усиления или потенциирования) доза-эффекта MSG.
Следует отметить, что измеренное соотношение EC50 может зависеть в некоторой степени от концентрации соединения. Предпочтительные усилители острого вкусо-аромата должны иметь высокое соотношение EC50 к MSG при низкой концентрации используемого соединения. Предпочтительно, соотношение EC50 в экспериментах по измерению усиления вкуса умами колеблется в зависимости от концентрации соединения формулы (I) от около 10 мкM до около 0,1 мкM, или предпочтительно от 1,0 мкM или 3,0 мкM.
Соотношение EC50 выше 1 является индикатором соединения, которое модулирует (потенциирует) активность hT1R1/hT1R3 и является усилителем острого вкуса. Более предпочтительно, соединения формулы (I) - усилители острого вкуса имеют соотношение EC50, равное, по меньшей мере, 1,2, 1,5, 2,0, 3,0, 4,0, 5,0, 8,0 или 10,0, или даже выше.
В одном аспекте пределы модуляции острого вкусо-аромата определенного соединения определены на основе его воздействия на MSG активность рецептора T1R1/T1R3 in vitro. Следует понимать, что подобные анализы могут быть проведены для других соединений, известных как активаторы рецепторов T1R1/T1R3.
Определенные соединения и основные классы соединений, которые демонстрируют способность модулировать T1R1/T1R3, основываясь на соотношениях EC50, высчитанных на основе указанной выше формулы, приведены в детальном описании настоящего изобретения, примерах и формуле изобретения.
Процедуры, использованные при проведении вкусовых тестов людьми соединений по настоящему изобретению формулы (I) умами/острого вкуса, описаны здесь ниже. Сравнительные анализы EC50 активности соединений формулы (I) для рецепторов агонистов сладкого вкуса и/или восприятия сладкого вкуса человеком описаны здесь ниже.
ПРИМЕРЫ
Следующие примеры приведены для иллюстрации различных вариантов воплощения настоящего изобретения, но не ограничивают объем настоящего изобретения.
Для целей настоящего изобретения соединения описаны по отдельности в следующих примерах 1-12 и соответствующих таблицах А и В и могут быть введены сокращенно номером примера. Например, как показано здесь ниже, пример 1 описывает синтез определенного соединения 2-((5-(2-метокси-4-метилфенил)-1H-1,2,4-триазол-3-илтио)метил)пиридин и результаты экспериментов по его биологической эффективности, которой обладает соединение, и оно может быть введено сокращением, как соединение 1. Подобным образом первое соединение, показанное в Таблице А, может быть введено сокращением, как соединение А1.
Пример 1
2-((5-(2-Метокси-4-метилфенил)-1H-1,2,4-триазол-3-илтио)метил)пиридин

В раствор 5-(2-метокси-4-метилфенил)-2H-1,2,4-триазол-3(4H)-тиона (пример 1а) (110 мг, 0,5 ммоль) в 2 мл EtOH вводили 2-(бромметил)пиридин гидробромид (152 г, 0,6 ммоль). Суспензию нагревали при 60°C в течение 22 часов. Продукты реакция разбавляли с EtOAc и промывали водой, рассолом, высушивали MgSO4, профильтровали с получением масла. Масло было очищено методом препаративной TLC с получением требуемого продукта (72%).1H ЯМР (500 MГц, CDCl3): δ 2,40 (с, 3H), 3,99 (с, 3H), 4,55 (с, 2H), 6,84 (с, 1H), 6,92-6,93 (д, 1H), 7,16-7,19 (дд, 1H), 7,53-7,55 (д, 1H), 7,62-7,65 (м, 1H), 8,15-8,17 (д, 1H), 8,56-8,57 (д, 1H), MS (M+H, 313).
0,08 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293, и когда соединение присутствовало в концентрации 0,03 мкM, усиливало эффективность глютамата натрия и имело соотношение EC50, равное 5,9.
Пример 1а
5-(2-Метокси-4-метилфенил)-2H-1,2,4-триазол-3(4H)-тиона
В раствор 2-метокси-4-метилбензойной кислоты (1,81 г, 9,22 ммоль) в 9 мл пиридина вводили EDCI (1,9 г, 9,3 ммоль) и суспензию перемешивали при комнатной температуре в течение 1 часа. Затем ввели тиосемикарбазид (800 мг, 8,8 ммоль), реакцию проводили при перемешивании при комнатной температуре в течение 21 часа. Смесь выпаривали досуха и затем разбавляли водой. Твердый остаток белого цвета затем отфильтровали, промыли водой и суспендировали в 20 мл 1М водного NaHCO3и затем нагревали с дефлегматором в течение 2 дней. Суспензию профильтровали в горячем виде, водный раствор охладили на льду и подкислили концентрированной HCl до рН 3. Остаток профильтровали и промыли водой, и высушили с получением порошка белого цвета (47%).
Пример 2
2-((5-(2-Метокси-4-метилфенил)-1H-1,2,4-триазол-3-илтио)метил)-5-метилпиридин

Получают аналогично примеру 1, но с использованием 5-(2-метокси-4-метилфенил)-2H-1,2,4-триазол-3(4H)-тиона (пример 1а) и 2-(хлорметил)-5-метилпиридина (пример 2). Выход 14%.1H ЯМР (500 MГц, CDCl3): δ 2,29 (с, 3H), 2,41 (с, 3H), 4,00 (с, 3H), 4,51 (с, 2H), 6,75 (с, 1H), 6,90 (с, 1H), 7,40 (с, 1H), 8,1 (д, 1H), 8,4 (с, 1H), 11,5-11,7 (шир.с, 1H). MS (M+H, 327,1).
0,49 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293.
Пример 2а
2-(Хлорметил)-5-метилпиридин
2,5-Диметилпиридин (5,18 мл, 44,8 ммоль) смешивали с DCM (100 мл) и охлаждали на ледяной бане. MСРВА (15,5 г, 2 экв.) вводили частями в течение более 30 минут. Раствор перемешивали при комнатной температуре в течение ночи. Затем реакционную смесь промывали водным NaHCO3, рассолом, высушивали и выпаривали с получением N-оксида, который использовали без дополнительной очистки. Раствор N-оксида (22,2 г, 18 ммоль), p-TsCl (5,15 г, 27 ммоль) в DCM (3 мл) нагревали до 40°С в атмосфере аргона в течение 2 часов. Затем раствор по каплям добавили в раствор триэтиламина (3,8 мл, 27 мл) в DCM (18 мл) с последующим нагреванием до 40°С в атмосфере аргона. Раствор оранжевого цвета нагревали при 40°С дополнительно в течение 3 часов. Затем смесь охлаждали, нейтрализовали твердым NaHCO3 (2 г) и выпаривали в вакууме. Неочищенный материал разбавляли MeOH (24 мл) с получением предполагаемого продукта в 0,75 М растворе. Неочищенный раствор 2-(хлорметил)-5-метилпиридина использовали на следующей стадии без дополнительной очистки.
Пример 3
2-((5-(2,4-Диметилфенил)-1H-1,2,4-триазол-3-илтио)метил)пиридин

Получают аналогично примеру 1, но с использованием 5-(2,4-диметилфенил)-2H-1,2,4-триазол-3(4H)-тиона (пример 3а) и 2-(бромметил)пиридин гидробромида. Выход 64%.1H ЯМР (500 MГц, CDCl3): δ 2,34 (с, 3H), 2,57 (с, 3H), 4,37 (с, 2H), 4,51 (с, 2H), 7,04-7,08 (м, 2H), 7,28-7,31 (м, 1H), 7,41-7,43 (д, 1H), 7,74-7.77 (м, 2H), 8,63-8,64 (д, 1H). MS (M+H, 297); т.п.=112-114°C.
0,09 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293, и когда соединение присутствовало в концентрации 0,01 мкM, усиливало эффективность глютамата натрия и имело соотношение EC50, равное 4,3.
Пример 3а
5-(2,4-Диметилфенил)-2H-1,2,4-триазол-3(4H)-тион
Суспензию тиосемикарбазида (800 мг, 8,78 ммоль) в 9 мл пиридина вводили в 2,4-диметилбензоилхлорид (1,68 г, 10 ммоль). Продукты реакции нагревали при 150°C в течение 10 минут с использованием источника микроволнового излучения. Раствор желтого цвета выпаривали досуха и затем разбавляли водой. Затем твердый остаток белого цвета собрали и промывали водой. Твердый остаток суспендировали в 20 мл 1 М водного NaHCO3. Суспензию нагревали до 180°C в течение одного часа с использованием источника волнового излучения. Суспензию профильтровали в горячем виде, водный раствор охлаждали на льду и подкислили до рН 3 концентрированной HCl. Твердый остаток профильтровали и промыли водой, и высушили с получением порошка белого цвета (43%).
Пример 4
2-((5-(4-Этилфенил)-1H-1,2,4-триазол-3-илтио)метил)пиридин

Получают аналогично примеру 1, но с использованием 5-(4-этилфенил)-2H-1,2,4-триазол-3(4H)-тиона (пример 4а) и 2-(бромметил)пиридин гидробромида. Выход 71%.1H ЯМР (500 MГц, ДMСO): δ 1,18-1,22 (т, 3H), 2,64-2,66 (т, 2H), 4,52 (с, 2H), 7,30-7,88 (м, 8H), 14,3 (шир.с, 1H). MS (M+H, 297).
0,14 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293, и когда соединение присутствовало в концентрации 0,03 мкM, усиливало эффективность глютамата натрия и имело соотношение EC50, равное 4,4.
Пример 4а
5-(4-Этилфенил)-2H-1,2,4-триазол-3(4H)-тион
Получено аналогично примеру 3а с использованием 4-этилбензоил хлорида (выход 65%).
Пример 5
2-((5-(4,5-Диметилфуран-2-ил)-1H-1,2,4-триазол-3-илтио)метил)пиридин
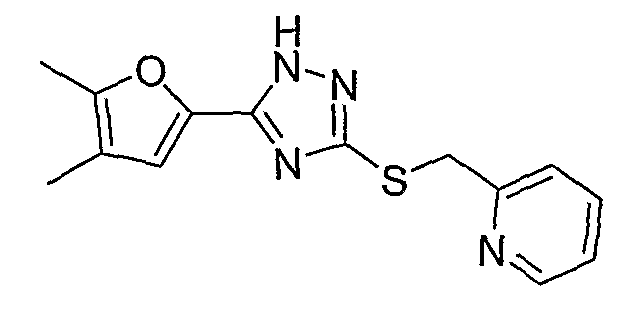
Получают аналогично примеру 1, но с использованием 5-(4,5-диметилфуран-2-ил)-2H-1,2,4-триазол-3(4H)-тиона (пример 5а) и 2-(бромметил)пиридин гидробромида. Выход 27%.1H ЯМР (500 MГц, ДMСO): δ 1,98 (с, 3H), 2,28 (с, 3H), 4,37 (с, 2H), 6,76 (с, 1H), 7,3 (м, 1H), 7,45 (д, 1H), 7,75 (т, 1H), 8,6 (с, 1H). MS (M+H, 287).
0,58 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293, и когда соединение присутствовало в концентрации 0,1 мкM, усиливало эффективность глютамата натрия и имело соотношение EC50, равное 4,4.
Пример 5а
5-(4,5-Диметилфуран-2-ил)-2H-1,2,4-триазол-3(4H)-тион
Получено аналогично примеру 1а с использованием 4,5-диметилфуран-2-карбоновой кислоты (выход 25%).
Пример 6
2-((5-(4,5-Диметилфуран-2-ил)-1H-1,2,4-триазол-3-илтио)метил)пиридин

Получают аналогично примеру 1, но с использованием 5-(бензофуран-2-ил)-2H-1,2,4-триазол-3(4H)-тиона (пример 6а) и 2-(бромметил)пиридин гидробромида. Выход (59%).1H ЯМР (500 MГц, CDCl3): δ 4,37 (с, 2H), 7,26-7,34 (м, 5H), 7,4-7,42 (д, 1H), 7,55-7,57 (д, 1H), 7,65-7,67 (д, 1H), 7,75 (т, 1H), 8,62 (с, 1H). MS (M+H, 309).
2,58 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293, и когда соединение присутствовало в концентрации 0,1 мкM, усиливало эффективность глютамата натрия и имело соотношение EC50, равное 2,88.
Пример 6а
5-(Бензофуран-2-ил)-2H-1,2,4-триазол-3(4H)-тион
Получено аналогично примеру 3а с использованием бензофуран-2-карбонилхлорида (выход 73%).
Пример 7
2-((5-(2,5-Диметилфуран-3-ил)-1H-1,2,4-триазол-3-илтио)метил)пиридин

Получают аналогично примеру 1, но с использованием 5-(2,5-диметилфуран-3-ил)-2H-1,2,4-триазол-3(4H)-тиона (пример 7а) и 2-(бромметил)пиридин гидробромида. Выход (70%)1H ЯМР (500 MГц, CDCl3): δ 2,27 (с, 3H), 2,59 (с, 3H), 4,32 (с, 2H), 6,35 (с, 1H), 7,28-7,29 (д, 1H), 7,35-7,36 (д, 1H), 7,75 (т, 1H), 8,62 (с, 1H). MS (M+H, 287).
2,07 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293, и когда соединение присутствовало в концентрации 0,1 мкM, усиливало эффективность глютамата натрия и имело соотношение EC50, равное 2,1.
Пример 7а
5-(2,5-Диметилфуран-3-ил)-2H-1,2,4-триазол-3(4H)-тион
Получено аналогично примеру 3а с использованием 2,5-диметилфуран-3-карбонилхлорида (выход 72%).
Пример 8
2-(2-(5-(4,5-Диметилфуран-2-ил)-1H-1,2,4-триазол-3-илтио)этил)пиридин
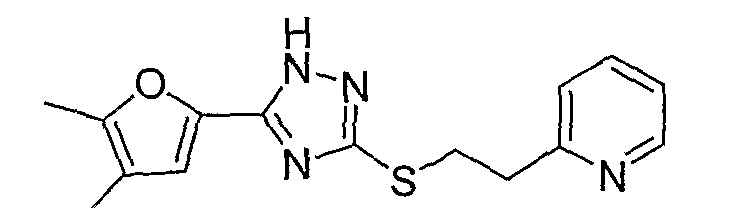
Получают аналогично примеру 1, но с использованием 5-(4,5-диметилфуран-2-ил)-2H-1,2,4-триазол-3(4H)-тиона (пример 5а) и 2-(2-бромэтил)пиридиния бромида (пример 8а). Выход (55%).1H ЯМР (500 MГц, CDCl3): δ 1,96 (с, 3H), 2,24 (с, 3H), 3,28 (т, 2H), 3,49 (т, 2H), 6,77 (с, 1H), 7,13-7,23 (м, 2H), 7,65 (т, 1H) 8,58 (с, 1H). MS (M+H, 301).
1,87 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293, и когда соединение присутствовало в концентрации 0,1 мкM, усиливало эффективность глютамата натрия и имело соотношение EC50, равное 2,66.
Пример 8а
2-(2-Бромэтил)пиридиний бромид
В раствор 2-(2-гидроксиэтил)пиридина (3 мл, 26,6 ммоль) ввели 30 мл 33% HBr в уксусной кислоте. Раствор желтого цвета нагревали в закрытой емкости при температуре 78°C в течение 2 дней. Продукты реакции выпаривали при глубоком вакууме с получением твердого остатка коричневого цвета. Твердый остаток был перекристаллизован из горячего изопропанола с получением твердого остатка светлого желто-коричневого цвета (73%).1H ЯМР (500 MГц, ДMСO): δ 3,62-3,65 (т, 2H), 3,95-3,98 (т, 2H), 7,95 (т, 1H), 8,09-8,10 (д, 1H), 8,58 (т, 1H), 8,90 (д, 1H).
Пример 9
2-((5-(2,4-Диметоксибензил)-1H-1,2,4-триазол-3-илтио)метил)пиридин

Получают аналогично примеру 1, но с использованием 5-(2,4-диметоксибензил)-2H-1,2,4-триазол-3(4H)-тиона (пример 9а) и 2-(бромметил)пиридин гидробромида. Выход (34%).1H ЯМР (500 MГц, CDCl3): δ 3,77 (с, 3H), 3,79 (с, 3H), 4,0 (с, 2H), 4,34 (с, 2H), 6,35-6,45 (м, 2H), 7,1 (д, 1H), 7,15 (т, 1H), 7,3 (д, 1H), 7,7 (т, 1H), 8,5 (с, 1H). MS (M+H, 343).
1,2 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293, и когда соединение присутствовало в концентрации 0,1 мкM, усиливало эффективность глютамата натрия и имело соотношение EC50, равное 2,66.
Пример 9а
5-(2,4-Диметоксибензил)-2H-1,2,4-триазол-3(4H)-тион
Получено аналогично примеру 1а с использованием 2,4-диметоксифенил уксусной кислоты.1H ЯМР (500 MГц, CDCl3): δ 3,80 (с, 3H), 3,90 (с, 3H), 6,4-6,5 (м, 2H), 7,1 (шир.с, 1H), 9,8 (шир.с, 1H), 10,2 (шир.с, 1H).
Пример 10
2-((5-(4-Этил)-2-метилфенил)-1H-1,2,4-триазол-3-илтио)метил)пиридин

Получают аналогично примеру 1, но с использованием 5-(4-этил-2-метилфенил)-2H-1,2,4-триазол-3(4H)-тиона (пример 10а) и 2-(бромметил)пиридин гидробромида. Выход (39%).1H ЯМР (300 MГц, ДMСO): δ 1,17-1,22 (т, 3H), 2,46 (с, 3H), 2,60-2,64 (дд, 2H), 4,50 (с, 2H), 7,14-7,18 (м, 2H), 7,27-7,29 (м, 1H), 7,47-7,49 (д, 1H), 7,58 (шир.д, 1H), 7,72-7,77 (м, 1H), 8,50-8,51 (д, 1H). MS (M+H, 311).
0,02 мкM Соединения имело EC50 для активации рецептора умами hT1R1/hT1R3, экспрессированного клеточной НЕК линией 293.
Пример 10а
5-(4-Этил-2-метилфенил)-2H-1,2,4-триазол-3(4H)-тион
Получено аналогично примеру 1а с использованием 4-этил-2-метилбензойной кислоты (пример 10b). Выход (59%). MS (М+Н, 220).
Пример 10b
4-Этил-2-метилбензойная кислота
Метил-4-этил-2-метилбензоат (пример 10с) (2,37 г) растворяли в водном NaOH (1 М, 40 мл) и раствор нагревали при 60°С в течение ночи. Смесь промывали гексаном, и водный слой подкисляли 6N HCl до pH 2. Продукт получали в виде осадка белого цвета с последующей фильтрацией и сушкой (2,17 г, 80%).
Пример 10с
Метил-4-этил-2-метилбензоат
4-Хлор-2-метилбензойную кислоту (3 г, 17,6 ммоль) суспендировали в 12 мл МеОН с 1 мл концентрированной H2SO4. Смесь нагревали при температуре кипения с обратным холодильником в течение ночи, МеОН выпаривали и осадок экстрагировали EtOAc, высушивали MgSO4, отфильтровали и получили метил-4-хлор-2-метилбензоата в виде бесцветной вязкой жидкости (2,96 г, 92%), которая была использована на следующей стадии без дополнительной очистки. Эфир (2,96 г, 16 ммоль) растворяли в инертной атмосфере в THF (100 мл) и NMP (9 мл) и вводили ацетилацетонат железа (III) (318 мг, 0,9 ммоль) с получением раствора красного цвета. Затем EtMgBr (7 мл 1М раствора в эфире) добавляли по каплям при энергичном перемешивании. Смесь стала темно-коричневой, затем фиолетовой и затем была перемешана в течение более 15 минут. Продукты реакции разбавляли эфиром, и реакцию останавливали введением водного HCl (1M, 10 мл). Неочищенный продукт экстрагировали эфиром. Объединенные органические слои промывали водой и рассолом, высушивали MgSO4 и выпаривали. Осадок очищали на силикагеле (30% EtOAc/гексаны) с получением метил-4-этил-2-метилбензоата в виде масла (2,37 г, 83%). (1H ЯМР (500 MГц, CDCl3): δ 1,26 (т, 3H), 2,63 (дд, 2H), 3,9 (с, 3H), 7,1 (шир., 2H), 7,85 (д, 1H)).
Пример 11
2-((4-п-Толил-1H-1,2,3-триазол-1-ил)метил)пиридин

Смесь tBuOH (1,5 мл), воды (1,5 мл), 2-(бромметил)пиридина (253 мг, 1 ммоль), 1-этинил-4-метилбензена (122 мг, 1,05 ммоль) и NaN3(68 мг, 1,05 ммоль) вводили в емкость для микроволнового облучения. Медную проволоку (50 мг) и CuSO4(200 мкл 1M водного раствора) вводили при перемешивании в суспензию. Сосуд закрыли, и смесь облучали (Microwave, Personnal Chemistry, Biotage from Upsala sweeden) при 125°C в течение 5 пяти минут. Смесь разбавили водой, и продукт экстрагировали EtOAc, промыли 1 М цитратом аммония, 0,25 М водной HCl и рассолом, высушили MgSO4, профильтровали и выпарили. Неочищенный продукт очищали на силикагеле (элюент: 10% MeOH в DCM) с получением 2-((4-п-толил-1H-1,2,3-триазол-1-ил)метил)пиридина (88 мг, 35%).1H ЯМР (300 MГц, ДМСО): δ 2,30 (с, 3H), 5,72 (с, 2H), 7,30-7,45 (м, 4H), 7,77-7,89 (м, 3H), 8,60 (с, 1H); MS (M+H, 251).
4,66 мкM Соединения имело EC50 для активации рецептора умами, экспрессированного клеточной НЕК линией 293.
Пример 12
2-(2-(4-п-Толил-1H-1,2,3-триазол-1-ил)этил)пиридин
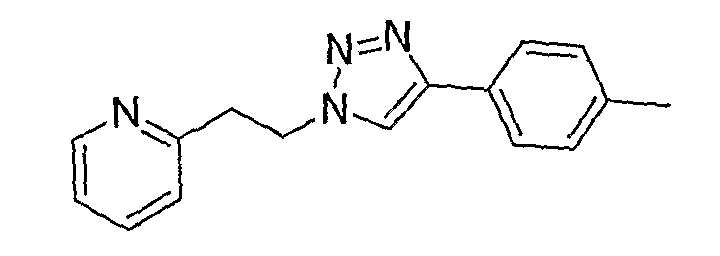
Получают аналогично примеру 11, но с использованием 2-(2-бромэтил)пиридин гидробромида. Выход 74 мг, 28%.1H ЯМР (300 MГц, ДМСО): δ 2,30 (с, 3H), 3,99 (с, 3H), 3,36-3,38 (м, 2H), 4,76-4,79 (м, 2H), 7,21-7,23 (м, 4H), 7,65-7,67 (м, 3H), 7,53-7,55 (д, 1H), 8,46 (с, 1H); MS (M+H, 265).
16,35 мкM Соединения имело EC50 для активации рецептора умами, экспрессированного клеточной НЕК линией 293.
Пример 13
3-(2,4-Диметилфенил)-6-(пиридин-2-илметилтио)пиридазин

В смесь 2-(бромметил)пиридин гидрохлорида (116 мг; 0,46 ммоль) и 6-(2,4-диметилфенил)пиридазин-3-(2Н)-тиона (пример 13а) (100 мг, 0,46 ммоль) в EtOH (3 мл) вводили EtONa (20% в EtOH, 25 мкл), и продукты реакции облучали микроволнами при 140°C в течение 4 минут. Неочищенную смесь высушивали, очищали на силикагеле (элюент: 5% MeOH в DCM) с получением 3-(2,4-диметилфенил)-6-(пиридин-2-илметилтио)пиридазина (49 мг, 35%) в виде твердого остатка белого цвета.1H ЯМР (300 MГц, ДМСО): δ 2,49 (с, 3H), 2,54 (с, 3H), 4,09 (с, 2H), 6,32-6,37 (м, 2H), 6,45-6,52 (м, 2H), 6,75-6,78 (д, 1H), 6,84-6,87 (м, 2H), 6,95-6,98 (т, 1H), 7,67-7,68 (д, 1H); MS (M+H, 308).
1,5 мкM Соединения имело EC50 для активации рецептора умами, экспрессированного клеточной НЕК линией 293.
Пример 13а
6-(2,4-Диметилфенил)пиридазин-3-(2Н)-тион
3-Хлор-6-(2,4-диметилфенил)пиридазин (пример 13b) (1,36 г) нагревали при температуре кипения с обратным холодильником с тиомочевиной (473 мг, 6,2 ммоль) в EtOH (25 мл) в течение 5 часов. Смесь выпаривали и осадок смешивали с водой (45 мл) с последующим введением Na2CO3 (318 мг, 3 ммоль). Полученный осадок собирали фильтрованием, промывали водой с диэтиловым эфиром и высушивали с получением 6-(2,4-диметилфенил)пиридазин-3-(2Н)-тиона (1,12 г, 52%).1H ЯМР (300 MГц, ДМСО): δ 2,29 (с, 3H), 2,32 (с, 3H), 7,12-7,30 (м, 2H), 7,29-7,31 (д, 1H), 7,46-7,49 (д, 1H), 7,65-7,68 (дд, 1H); MS (M+H, 217).
Пример 13b
3-Хлор-6-(2,4-диметилфенил)пиридазин
6-(2,4-Диметилфенил)пиридазин-3(2Н)-он (пример 13с) нагревали с POCl3 (5,15 мл, 55 ммоль) при 85°C в течение 4 часов. Затем проводили охлаждение и обработку ледяной крошкой с получением твердого остатка белого цвета и собирали его, получая 1,36 г 3-хлор-6-(2,4-диметилфенил)пиридазина.1H ЯМР (300 MГц, ДМСО): δ 2,29 (с, 3H), 2,34 (с, 3H), 7,16-7,19 (м, 2H), 7,35-7,37 (д, 1H), 7,93-8,00 (дд, 2H); (M+H, 313).
Пример 13с
6-(2,4-Диметилфенил)пиридазин-3(2Н)-он
Смесь моногидрата глиоксиловой кислоты (920 мг, 10 ммоль) и 2',4'-диметилацетофенона (4,45 мл, 30 ммоль) перемешивали при 150°C в течение 2 часов. Затем смесь охлаждали до комнатной температуры и вводили воду (4 мл) с последующим добавлением концентрированного водного NH4OH (1 мл). Смесь промывали DCM. В аммиачный раствор вводили гидразин (314 мкл, 10 ммоль) и раствор нагревали при температуре кипения с обратным холодильником в течение 3 часов. После охлаждения до комнатной температуры осадок собирали фильтрованием с получением требуемого продукта в виде порошка белого цвета (1,1 г, 55%),1H ЯМР (300 MГц, ДМСО): δ 2,22 (с, 3H), 2,25 (с, 3H), 6,93-6,95 (д, 1H), 7,15 (м, 3H), 7,21-7,23 (д, 1H), 7,57-7,61 (д, 1H), 13,1 (шир.с, 1H); (M+H, 201).
Пример 14
3-(Бензилтио)-6-(2,4-диметилфенил)пиридазин
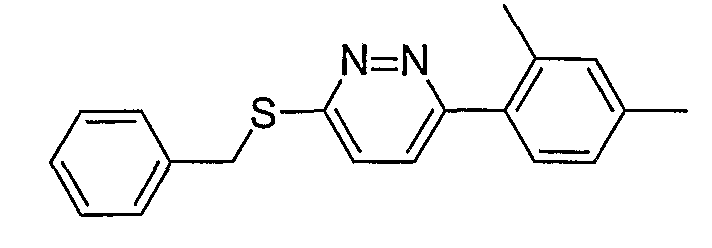
Получают аналогично примеру 13, но с использованием бензилбромида и 6-(2,4-диметилфенил)пиридазин-3(2Н)-тиона (пример 13а). Выход 53,5 мг (38%).1H ЯМР (300 MГц, ДМСО): δ 2,29 (с, 3H), 2,34 (с, 3H), 4,60 (с, 2H), 7,16-7,17 (м, 2H), 7,30-7,34 (м, 4H), 7,47-7,49 (д, 2H), 7,64-7,72 (м, 2H); MS (M+H, 307).
2,7 мкM Соединения имело EC50 для активации рецептора умами, экспрессированного клеточной НЕК линией 293.
Пример 15
3-(2,4-Диметилфенил)-6-(пиридин-2-илметокси)пиридазин

3-Хлор-6-(пиридин-2-илметокси)пиридазин (пример 15а) (221 мг, 1 ммоль) разбавляли толуолом (10 мл), EtOH (2 мл) и водой (1,5 мл). Затем 2,4-диметилфенилбороновую кислоту (150 мг, 1 ммоль) добавляли с последующим введением K2CO3 (276 мг, 2 ммоль) и смесь дегазировали с использованием аргона. Тетракис(трифенилфосфин)палладия (232 мг, 0,2 ммоль) вводили в атмосфере аргона, и смесь нагревали при температуре кипения с обратным холодильником в течение ночи. Растворители удаляли в вакууме и твердый осадок экстрагировали EtOAc и затем промыли водой и рассолом, высушили MgSO4, профильтровали и выпарили. Неочищенный материал очищали на силикагеле (элюент: 50% EtOAc в гексанах) с получением 3-(2,4-диметилфенил)-6-(пиридин-2-илметокси)пиридазина (169 мг, 58%) в виде твердого остатка белого цвета.1H ЯМР (300 MГц, ДМСО): δ 2,26 (с, 3H), 2,32 (с, 3H), 5,62 (с, 2H), 7,13-7,15 (м, 2H), 7,28-7,40 (м, 2H), 7,55-7,56 (д, 1H), 7,78-7,84 (м, 2H), 8,58-8,60 (д, 1H); MS (M+H, 292).
6,9 мкM Соединения имело EC50 для активации рецептора умами, экспрессированного клеточной НЕК линией 293.
Пример 15а
3-Хлор-6-(пиридин-2-илметокси)пиридазин
В раствор NaH (1,44 г, 36 ммоль, 60% в минеральном масле) в THF (15 мл) вводили пиридин-2-илметанол (1,16 мл, 12 ммоль) и смесь перемешивали в течение 30 минут при комнатной температуре. Затем вводили 3,6-дихлорпиридазин (1,79 г, 14 ммоль) и смесь перемешивали при 55°C в течение 4 часов. Реакцию останавливали водой и вводили насыщенный NaHCO3. Продукт экстрагировали EtOAc, высушили MgSO4, профильтровали и выпарили. Осадок очищали на силикагеле (элюент: 80% EtOAc в гексанах) с получением 3-хлор-6-(пиридин-2-илметокси)пиридазина виде твердого остатка белого цвета (1,64 г, 62%).1H ЯМР (300 MГц, ДМСО): δ 5,57 (с, 2H), 7,35-7,38 (м, 1H), 7,48-7,54 (м, 2H), 7,82-7,88 (м, 2H), 8,57-8,59 (дд, 1H); MS (M+H, 222).
Пример 16
5-(2,4-Диметилфенил)-N-(пиридин-2-илметил)-1,3,4-оксадиазол-2-амин

В раствор 5-(2,4-диметилфенил)-1,3,4-оксадиазол-2-амина (пример 16а) (94,5 мг, 0,5 ммоль) в 5 мл сухого ацетонитрила вводили K2CO3 (207 мг, 1,5 ммоль). В суспензию вводили 2-(бромметил)пиридин гидробромид (127 мг,0,5 ммоль), и смесь перемешивали при 90°C в течение ночи. Растворитель удаляли в вакууме, твердый остаток разбавляли EtOAc с последующим промыванием водным NaHCO3 и рассолом, высушили MgSO4, профильтровали и выпарили. Осадок очищали на силикагеле с получением 5-(2,4-диметилфенил)-1,3,4-оксадиазол-2-амина (136 мг 96%) в виде твердого остатка белого цвета.1H ЯМР (300 MГц, CDCl3): δ 2,34 (с, 3H), 2,5 (с, 3H), 5,1 (с, 2H), 7,07-7,08 (м, 2H), 7,21-7,33 (м, 2H), 7,64-7,68 (м, 2H), 8,59-8,60 (д, 1H); MS (M+H, 281).
10,3 мкM Соединения имело EC50 для активации рецептора умами, экспрессированного клеточной НЕК линией 293.
Пример 16а
5-(2,4-Диметилфенил)-1,3,4-оксадиазол-2-амин
В раствор 2,4 -диметилбензогидразида (пример 16b) (2 г) в сухом диоксане (12 мл) вводили цианистый бромид (1,28 г, 12,2 ммоль) с последующим введением раствора NaHCO3 (1,02 г, 12,2 ммоль) в воде (12 мл). Полученную в результате смесь перемешивали в течение 2 часов при комнатной температуре. Раствор концентрировали в вакууме до 1/2 объема и разбавляли водой (20 мл). Полученный в результате твердый остаток собирали и высушивали в вакууме с получением 5-(2,4-диметилфенил)-1,3,4-оксадиазол-2-амина (1,88 г 82 %) в виде твердого остатка белого цвета.1H ЯМР (300 MГц, ДМСО): δ 2,29 (с, 3H), 2,52 (д, 3H), 7,13 (д, 1H), 7,16 (с, 3H), 7,54-7,56 (д, 1H); MS (M+H, 190).
Пример 16b
2,4-Диметилбензогидразид
В раствор метил-2,4-диметилбензоата (2 г, 12,2 ммоль) в MeOH (10 мл) вводили обезвоженный гидразин (1,95 мл, 61 ммоль) и смесь нагревали при температуре кипения с обратным холодильником 40 часов. Затем смесь выпаривали и сушили в вакууме с получением 2,4-диметилбензогидразида в виде твердого остатка белого цвета (2 г, 100%; MS (M+H, 165).
Пример 17
3-(Бензилтио)-6-(2,4-диметилфенил)пиридазин

Получают аналогично примеру 13, но с использованием 3-(бромметил)пиридин гидробромида 6-(2,4-диметилфенил)пиридазин-3-(2Н)-тион (пример 13а). Выход 39,5 мг (28%).1H ЯМР (300 MГц, ДМСО): δ 2,29 (с, 3H), 2,34 (с, 3H), 4,62 (с, 2H), 7,13-7,17 (м, 2H), 7,31-7,37 (м, 2H), 7,65-7,71 (м, 2H), 7,89-7,90 (д, 1H), 8,45-8,46 (м, 1H), 8,69-8,70 (д, 1H); MS (M+H, 308).
15,17 мкM Соединения имело EC50 для активации рецептора умами, экспрессированного клеточной НЕК линией 293.
Пример 18
2-((5-(4-Этил-2-метоксифенил)-1H-1,2,4-триазол-3-илтио)метил)пиридин

В раствор 5-(4-этил-2-метоксифенил)-2H-1,2,4-триазол-3(4Н)-тиона (пример 18а) (100 г, 0,43 ммоль) в EtOH (2 мл) вводили 2-(бромметил)пиридин гидробромид (129 мг, 0,51 ммоль). Суспензию нагревали при 60°C в течение 22 часов. Реакционную смесь разбавляли EtOAc с последующим промыванием водой и рассолом, высушили MgSO4, профильтровали и выпарили. Осадок очищали на силикагеле (элюент: 5% MeOH в DCM) с получением 2-((5-(4-этил-2-метоксифенил)-1H-1,2,4-триазол-3-илтио)метил)пиридина (95 мг) в виде порошка белого цвета (68%).1H ЯМР (300 MГц, ДМСО): δ 1,19-1,22 (т, 3H), 2,63-2,69 (дд, 2H), 3,93 (с, 3H), 4,48 (с, 2H), 6,93-7,03 (м, 2H), 7,25-7,29 (м, 1H), 7,49-7,5 (м, 1H), 7,71-7,75 (м, 1H), 7,93-7,95 (д, 1H), 8,50-8,51 (д, 1H), 13,65 (шир.с, 1H). MS (M+H, 327).
0,05 мкM Соединения имело EC50 для активации рецептора умами, экспрессированного клеточной НЕК линией 293.
Пример 18а
5-(4-Этил-2-метоксифенил)-2H-1,2,4-триазол-3(4Н)-тион
В раствор 4-этил-2-метоксибензойной кислоты (пример 18b) (1 г, 6,1 ммоль) в пиридине (6 мл) вводили EDCI (1,2г, 6,3 ммоль) и суспензию перемешивали при комнатной температуре в течение 2 часов. Затем вводили тиосемикарбазид (547 мг, 6 ммоль), и реагенты перемешивали при комнатной температуре в течение 24 часов. Смесь выпарили досуха и разбавили водой. Твердый остаток белого цвета собирали и промывали водой. Твердый остаток суспендировали в водном NaHCO3 (1M, 20 мл) и нагревали при температуре кипения с обратным холодильником в течение 2 дней. Суспензию профильтровали в горячем виде, и водный раствор охладили на льду и подкислили до рН 3 концентрированной HCl. Твердый остаток собирали, промывали водой и высушили с получением 5-(4-этил-2-метоксифенил)-2H-1,2,4-триазол-3(4Н)-тиона в виде порошка белого цвета (55%). MS (M+H, 236).
Пример 18b
4-Этил-2-метоксибензойная кислота
Метил-4-этил-2-метоксибензоат (пример 18с) (2,01 г, 10,3 ммоль) суспендировали в 1M водном NaOH (40 мл), смесь перемешивали при 60°C в течение ночи. Реакционную смесь охладили до комнатной температуры и промыли гексаном. Затем водный слой отделили и подкислили 6N HCl до pH 2. Осадок белого цвета собирали, промыли водой и высушили с получением 4-этил-2-метоксибензойной кислоты (1,8 г 97%) в виде твердого остатка белого цвета.1H ЯМР (300 MГц, ДМСО): δ 1,16-1,20 (т, 3H), 2,60-2,65 (дд, 2H), 3,80 (с, 3H), 6,82-6,84 (д, 1H), 6,95 (с, 1H), 7,57-7,59 (д, 1H).
Пример 18с
Метил-4-этил-2-метоксибензоат
В раствор метил-4-хлор-2-метоксибензоата (пример 18d) (4,16 г, 20,8 ммоль) в THF (120 мл) и NMP (12 мл) и в инертной атмосфере вводили ацетилацетонат железа (III) (398 мг, 1,17 ммоль) с получением раствора красного цвета. Затем EtMgBr (29 мл 1М раствора в эфире) вводили по каплям при энергичном перемешивании. Смесь стала темно-коричневого цвета, затем фиолетового цвета и затем смесь перемешивали еще более 15 минут. Продукты реакции разбавляли эфиром, и реакция останавливали введением водной HCl (1M, 50 мл). Неочищенный продукт экстрагировали эфиром, и затем объединенные органические слои промывали водой и рассолом, высушивали MgSO4, фильтровали и выпаривали. Осадок очищали на силикагеле (элюент: 30% EtOAc в гексанах) с получением метил-4-этил-2-метоксибензоата в виде масла (2,01 г, 50%).1H ЯМР (300 MГц, ДМСО): δ 1,20-1,22 (т, 3H), 2,65-2,7 (дд, 2H), 3,9 (с, 3H), 6,8 (с, 1H), 6,97 (м, 1H), 7,7 (м, 1H).
Пример 18d
Метил-4-хлор-2-метоксибензонат
Суспензию 4-хлор-2-метоксибензойной кислоты (5 г, 27 ммоль) в MeOH (18 мл) и концентрированной H2SO4 (1,5 мл) нагревали при температуре кипения с обратным холодильником в течение ночи. MeOH выпаривали и осадок экстрагировали EtOAc с последующим промыванием водой и рассолом, высушили MgSO4, профильтровали и выпарили с получением метил-4-хлор-2-метоксибензоата в виде твердого остатка белого цвета (5,17 г, 96%).
Дополнительные соединения «триазол», синтезированные (А1-22) или закупленные (A23-26 у Asinex, Russia; A27 у Maybridge, England), были экспериментально протестированы и были выявлены имеющие относительно высокий уровень эффективности в качестве активатора рецепторов умами hT1R1/hT1R3, экспрессированных в клеточной НЕК линии 293. Результаты тестирования показаны ниже в таблице А.
Дополнительные соединения «пиридазина», закупленные (B1-2 у Asinex of Moscow, Russia; B3 у ICN biomedical research of Irvine, СА; B4 у Life Chemicals of Burlington, Canada), были экспериментально протестированы с выявлением соединений, имеющих хорошую эффективность в качестве активатора рецепторов умами hT1R1/hT1R3, экспрессированных в клеточной НЕК линии 293. Результаты тестирования показаны ниже в таблице В.
Дополнительное соединение «тетразола», закупленное у Ryan Scientific of Isle of Palms, South Carolina, было экспериментально протестировано с выявлением соединения, имеющего хорошую эффективность в качестве активатора рецепторов умами hT1R1/hT1R3, экспрессированного в клеточной НЕК линии 293. Результаты тестирования показаны ниже в таблице С.
Эксперименты с участием дегустационной комиссии умами/острого вкусо-аромата
Главные принципы отбора в дегустационную комиссию: Основы отбора дегустаторов вкуса. Потенциальные участники дегустационной комиссии были протестированы на способность давать оценку и определять интенсивность растворов, представляющих пять основных вкусов. Дегустационная комиссия оценила и определила интенсивность пяти различных концентраций каждого из пяти следующих соединений: сахароза (сладкий), хлорид натрия (соленый), лимонная кислота (кислый), кофеин (горький) и глютамат натрия (острый). Чтобы быть отобранными в дегустационную комиссию, участники должны были правильно оценить и определить интенсивность образцов с приемлемым числом ошибок.
Предварительные тестирования вкуса: дегустаторы, выбранные согласно вышеописанной процедуре, были признаны квалифицированными для проведения процедуры предварительного тестирования вкуса. Предварительные тестирования вкуса были использованы для оценки новых соединений по интенсивности основных вкусов и посторонних привкусов. Небольшая группа дегустаторов вкуса (n=5) оценивали около 5 концентраций соединения (как правило, находящихся в пределах между 1-100 мкM, в половине log цикла, например, 1, 3, 10, 30 и 100 мкM) в воде и в растворе 12 мМ MSG для оценки усиления восприятия его вкусо-аромата. Дегустационная комиссия определяла пять основных вкусов (сладкого, соленого, кислого, горького и острого) так же, как и посторонние привкусы (такие как химический, металлический, серный), по оценочной шкале. Образцы были представлены порциями по 10 мл при комнатной температуре. Целью теста являлось выявление максимальной концентрации, при которой не ощущается посторонний привкус, и определении того, присутствует ли ощущаемый острый вкус или усиление острого вкуса, присутствующие в любой из тестируемых концентраций.
Если соединение было эффективным и не имело ощутимых посторонних привкусов, его тестировали с участием высококвалифицированных (экспертов-дегустаторов) на последующей стадии.
Отбор высококвалифицированных экспертов-дегустаторов: Высококвалифицированные эксперты-дегустаторы провели оценку соединений, протестированных предварительно.
Дегустаторы для высококвалифицированной экспертной дегустационной комиссии отбирались из большей группы квалифицированных дегустаторов вкуса. Дегустаторы прошли дополнительный тест на оценку и определение острого вкуса с использование комбинаций MSG и IMP. Дегустаторы провели серию проб, оценивая, определяя и выявляя различия упомянутых вкусов растворов с острым вкусом. В экспериментах дегустаторы оценивали и определяли каждую из концентраций MSG (0, 6, 18, 36 мМ) и более сложных концентраций MSG в воде (3, 6, 12, 18 мM MSG).
Соединение, тестируемое высококвалифицированной экспертной дегустационной комиссией: Соединения, протестированные высококвалифицированной экспертной дегустационной комиссией, оценивались в различных экспериментах. Дегустаторам выдавали вышеописанный образец в качестве контроля (12 мM MSG + 100 мкM IMP) и предлагали оценить образцы по шкале от -5 до +5 с учетом различий острого вкуса в сравнении с контролем (оценка: -5=самый наименее острый вкус по сравнению с контролем; 0=острый вкус, такой же, как у контроля; +5=вкус более острый, чем у контроля). Тестируемые образцы представляли собой растворы с варьирующими количествами MSG, IMP и соединения. Как правило, в каждой серии контрольный образец сравнивался с множеством тестируемых образцов. Тесты, как правило, включали различные образцы с варьирующими концентрациями MSG и IMP, так же как и один пустой образец для контроля правильности выводов дегустационной комиссии. Результаты вкусовых тестов приведены в таблице D и показывают, что были выявлены соединения по настоящему изобретению, обеспечивающие острый вкус или усиливающие острый вкус при 1 мкM+MSG, по сравнению с 100 мкM IMP+MSG. Соединения тестировали по сравнению с контролем в образцах с и без 12 мM MSG. Все образцы были представлены в объеме 10 мл при комнатной температуре. Для каждого тестируемого соединения проводили по две серии для подтверждения результатов работы дегустационной комиссии.
Вкусовой тест продукта прототипа: может быть проведен, как описано выше.
Пример 19
Приготовление супа с использованием раствора этанола в качестве исходного
Соединение по настоящему изобретению разводили с использованием 200 концентрированного этанола в 1000 раз с получением требуемой для супа концентрации. Соединение может быть обработано ультразвуком и/или нагрето до получения полной растворимости в этаноле. Суп готовили введением 6 г концентрата растительного бульона в 500 мл горячей воды в стеклянной емкости или емкости для нагревания для микроволновой обработки. Воду нагревали до 80°C. Концентрация MSG в разведенном бульоне составила 2,2 г/л, и IMP не вводили. После разведения бульонного концентрата в суповую основу вводили исходный раствор этанола. На 500 мл супа вводили 0,5 мл в 1000 раз разведенного исходного раствора этанола с конечной концентрацией этанола 0,1%. Если этанол ухудшает вкус супа, то может быть получена более высокая концентрация исходного раствора этанола, обеспечивающая лучшую растворимость соединению.
Пример 20
Получение чипсов
Композиция пищевого наполнителя, содержащая соединение формулы (I), получена смешиванием соединения формулы (I) с солевой смесью (как правило, смесь хлорида натрия и глютамата натрия), таким образом, что 1,4% солевой смеси вводят по массе (мас/мас) в чипсы с получением в требуемой концентрации MSG и соединения формулы (I). Для получения 1 части на миллион соединения в чипсах 7 мг соединения смешивают с 10 г соли и/или MSG. Смесь измельчают с использованием ступки и пестика для хорошего измельчения. Чипсы измельчают на одинаковые маленькие кусочки в блендере. Для каждых 98,6 г чипсов отвешивают 1,4 г солевой смеси. Кусочки чипсов сначала нагревают в микроволновой печи в течение 50 секунд или до того момента, когда они станут теплыми. Кусочки раскладывают на большом листе алюминиевой фольги. Солевую смесь распределяют равномерно по всем чипсам. Затем чипсы помещают в пластиковый пакет, убедившись, что вся соль также равномерно распределена в пакете. Солевую смесь и чипсы встряхивают, чтобы гарантировать равномерное распределение соли по чипсам.
Пример 21
Получение сока
Соединение формулы (I) разводили с использованием 200 концентрированного этанола в 1000 раз с получением требуемой для овощного сока концентрации. Спиртовой раствор соединения дополнительно смешивают с натуральными и/или искусственными ароматизаторами (включая MSG) с получением «ключевого ароматизатора». Ключевой ароматизатор смешивали с частью концентрата овощного сока с достижением однородности. Оставшийся концентрат сока разводили водой и смешивали. Могут быть использованы подсластители, такие как HFCS (высокофруктозный кукурузный сироп), аспартам или сукралоза или их смеси. Часть ароматизатора/соединения вводят на конечном этапе с перемешиванием.
Пример 22
Томатный сок со специями или коктейль «Кровавая Мэри»
Соединение формулы (I) вводят в качестве сухого ингредиента в смесь специй, которая может включать MSG, и тщательно перемешивают. Смесь специй диспергируют в часть томатной пасты, перемешивают и перемешанную пасту затем смешивают с оставшейся пастой. Затем пасту разводят водой. Процесс можно проводить при высокой температуре за короткое время.
Для специалиста в данной области должно быть ясно, что в настоящем изобретении могут быть сделаны различные модификации и варианты, которые входят в объем настоящего изобретения. Другие варианты воплощения настоящего изобретения должны быть понятны специалисту в данной области исходя из представленного описания практической части изобретения, описанной здесь. Примеры и описание приведены только для иллюстрации конкретных вариантов воплощения изобретения.
Реферат
Настоящее изобретение относится к соединениям, имеющим формулу ! ! где значения радикалов раскрыты в материалах заявки, а также к пищевым композициям, содержащим такие соединения. Такие соединения полезны в качестве ароматизатора или модификаторов вкуса, в частности модификаторов острого («умами») вкуса, агентов, придающих острый вкусо-аромат, и усилителей острого вкусо-аромата в пищевых продуктах, напитках и других пищевых композициях. Также настоящее изобретение относится к способам модулирования острого вкуса пищевых продуктов и к продуктам, получаемым по таким способам. 13 н. и 98 з.п. ф-лы, 4 табл.
Формула
a) по меньшей мере, один пищевой продукт или один или более его предшественников, и
b) по меньшей мере, количество, модулирующее острый вкус и аромат, по меньшей мере, одного соединения формулы
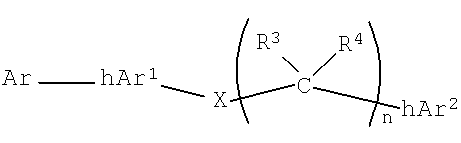
где i) Ar представляет собой моноциклический или бициклический арильный или гетероарильный радикал, включающий одно или два ароматических кольца, независимо выбранных из бензольных колец и пяти- или шестичленных гетероарильных колец, причем каждое гетероарильное кольцо содержит от 1 до 4 гетероатомов, независимо выбранных из кислорода, серы и/или азота, каждое ароматическое кольцо необязательно имеет один, два или три R20 замещающих радикала, где каждый R20 радикал независимо выбран из гидроксила, NH2, SH, галогена, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
ii) hAr1 представляет собой пяти- или шестичленный гетероарильный кольцевой радикал, имеющий от 1 до 4 гетероатомов, независимо выбранных из кислорода, серы и/или азота, где любой из оставшихся членов гетероароматического кольца независимо выбран из CR6, N, NR7;
iii) Х представляет собой О, S, S(O), SO2, CR8R9 или NR10;
iv) n равно 0,1,2 или 3;
v) R3, R4, R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, SH, галогена, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и R7 и R10 независимо выбраны из водорода, гидроксила, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и R6 представляет собой водород, галоген или С1-С4алкил или С1-С4алкоксил;
vi) hAr2 представляет собой пяти- или шестичленное гетероарильное кольцо, имеющее, по меньшей мере, один атом углерода в кольце и, по меньшей мере, один атом азота в кольце, и где оставшиеся члены гетероарильного кольца независимо выбраны из CR30, N, NR31, О и S, где каждый R30 независимо выбран из водорода, гидроксила, NH2, SH, галогена, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и каждый R31 независимо выбран из водорода, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
или его пищевой приемлемой соли.
R30 независимо выбран из водорода, гидрокси, фтора, хлора, NH2, NHCH3, N(CH3)2, СО2СН3, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп.







где R20 и R20' радикалы независимо выбраны из гидрокси, фтора, хлора, NH2, NHCH3, N(СН3)2, СО2СН3, амида, CN, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп.

где R20 и R20' радикалы независимо выбраны из гидрокси, фтора, хлора, NH2, NHCH3, N(СН3)2, СО2СН3, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп.






где R6 и R6' радикалы независимо присутствуют или отсутствуют и независимо выбраны из фтора, хлора, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси групп.






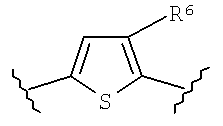









где R6 представляет собой водород или C1-C4 алкильный или алкоксильный радикал и R7 представляет собой водород или C1-C4 алкильный радикал.








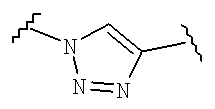
где R7 представляет собой водород, C1-C4 алкил, C1-C4 алкоксил, C1-C4 гидроксиалкил, C1-C4 алкилкарбонил, C1-C4 алкоксикарбонил, C1-C4 алкоксиалкил, СО2Н, CN или амид.

где R7 представляет собой водород или C1-C4 алкильный радикал.



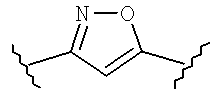


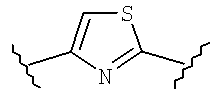




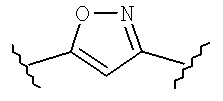



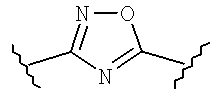

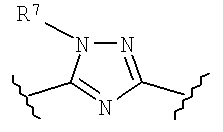



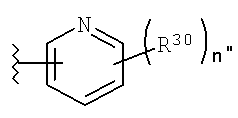
где n'' равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из гидрокси, фтора, хлора, NH2, NHCH3, N(СН3)2, CO2CH3, CN, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси.

где n'' равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из гидрокси, фтора, хлора, NH2, NHCH3, N(СН3)2, СО2СН3, CN, SEt, SCH3, метила, этила, изопропила, трифторметила, метокси, этокси, изопропокси и трифторметокси.
a) обеспечение, по меньшей мере, одного пищевого продукта или одного или более его предшественников, и
b) комбинирование пищевого продукта или одного или более его предшественников, по меньшей мере, с одним соединением формулы (IA) или его употребляемой в пищу приемлемой солью с получением модифицированного пищевого продукта, содержащего, по меньшей мере, около 0,01 млн-1 одного или более соединений формулы (IA);
где соединение формулы (IA) имеет формулу

где i) n' равно 0, 1, 2, или 3 и каждый R20 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, CO2H, CN или амида;
ii) n'' равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
iii) Х представляет собой NH, О, S, S(O), SO2 или CH2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила, пирролила, бензофуранила, бензотиофуранила или бензопирролила;
v) hAr1 имеет структуру


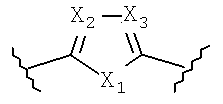
(1) X1 представляет собой NH, О или S,
(2) X2 представляет собой N или CR6, где R6 представляет собой водород, галоген, C1-C4 алкил, C1-C4 алкоксил, C1-C4 гидроксиалкил, C1-C4 алкилкарбонил, C1-C4 алкоксикарбонил, C1-C4 алкоксиалкил, СО2Н, CN или амид,
(3) Х3 представляет собой N или CR6, где R6 представляет собой водород, галоген, C1-C4 алкил, C1-C4 алкоксил, C1-C4 гидроксиалкил, C1-C4 алкилкарбонил, C1-C4 алкоксикарбонил, C1-C4 алкоксиалкил, СО2Н, CN или амид, и
vi) hAr2 представляет собой кольцо пиридила, пиразинила или пиримидинила.


a) по меньшей мере, один пищевой продукт или один или более его предшественников, и
b) по меньшей мере, 0,01 млн-1 одного или более триазольных соединений, имеющих формулу (IB)

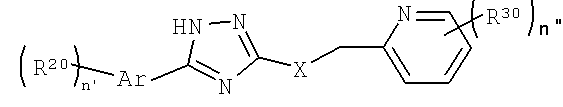

или его пищевой приемлемой соли,
где i) n' равно 0, 1, 2 или 3 и каждый R20 независимо выбран из гидрокси, SH, NH2, галогена и радикала С1-С4, выбранного из алкила, алкоксила, алкокси-алкила, гидроксиалкила, галогеналкила, амида, CN, CO2H, CHO, COR21, CO2R21, NHR21, NR21R21' или SR21 радикала, где R21 и R21' независимо выбраны из алкилов;
ii) n'' равно 0, 1, 2 или 3 и каждый R30 независимо выбран из гидрокси, SH, NH2, галогена и радикала C1-C4, выбранного из алкила, алкоксила, алкокси-алкила, гидроксиалкила, галогеналкила, CN, CO2H, СНО, COR32, CO2R32, NHR32, NR32R32' или SR32 радикала, где R32 и R32' независимо выбраны из алкилов;
iii) Х представляет собой NH, О, S, S(O), SO2 или СН2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила или пирролила.
2-((3-(2,3-диметоксифенил)-1Н-1,2,4-триазол-5-илтио)метил)пиридин;
2-((5-(2-метокси-4-метилфенил)-1Н-1,2,4-триазол-3-илтио)метил)пиридин;
2-((5-(2,4-диметилфенил)-1Н-1,2,4-триазол-3-илтио)метил)пиридин;
2-((5-(4-этилфенил)-1Н-1,2,4-триазол-3-илтио)метил)пиридин;
2-((5-(4,5-диметилфуран-2-ил)-1Н-1,2,4-триазол-3-илтио)метил)пиридин;
2-((5-(4-этил-2-метилфенил)-1Н-1,2,4-триазол-3-илтио)метил)пиридин;
2-((5-(4-этил-2-метоксифенил)-1Н-1,2,4-триазол-3-илтио)метил)пиридин;
или его пищевая приемлемая соль.
a) обеспечение, по меньшей мере, одного пищевого продукта или одного или более его предшественников, и
b) комбинирование пищевого продукта или одного или более его предшественников, по меньшей мере, с одним соединением формулы (IC) или его употребляемой в пищу приемлемой солью в количестве, модулирующем острый вкусо-аромат, по меньшей мере, с получением модифицированного пищевого продукта;
где соединение формулы (IC) имеет формулу



и где
i) n' равно 0, 1, 2 или 3 и каждый R20 независимо выбран из группы, состоящей из гидроксила, SH, NH2, галогена, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, CO2H, CN или амида;
ii) n'' равно 0, 1, 2 или 3 и каждый R30 независимо выбран из группы, состоящей из ОН, SH, NH2, галогена C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
iii) Х представляет собой NH, О, S, S(O), SO2 или CR8R9, где R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, галогена C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
iv) Y представляет собой NH, О, S, S(O), SO2 или CR8R9, где R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, галогена C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
v) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила или пирролила.
a) обеспечение, по меньшей мере, одного пищевого продукта или одного или более его предшественников, и
b) комбинирование пищевого продукта или одного или более его предшественников, по меньшей мере, с одним соединением формулы (ID) или его употребляемой в пищу приемлемой солью с получением модифицированного пищевого продукта, содержащего, по меньшей мере, около 0,01 млн-1 одного или более соединения формулы (ID);
где соединение формулы (ID) имеет формулу

и где
i) n' равно 0, 1, 2 или 3 и каждый R20 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
ii) n'' равно 0, 1, 2 или 3, и каждый R30 независимо выбран из группы, состоящей из гидрокси, SH, NH2, галогена C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
iii) Х представляет собой NH, О, S, S(O), SO2 или СН2;
iv) Ar представляет собой кольцо фенила, пиридила, пиразинила, пиримидинила, фуранила, тиофуранила, пирролила, бензофуранила, бензотиофуранила или бензопирролила;
v) hAr1 имеет структуру




где R6 и R6' независимо выбраны из водорода, галогена C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и
vi) hAr2 представляет собой кольцо пиридила, пиразинила или пиримидинила.
a) обеспечение, по меньшей мере, одного пищевого продукта или одного или более его предшественников, и
b) комбинирование пищевого продукта или одного или более его предшественников, по меньшей мере, с одним соединением формулы (1) или его употребляемой в пищу приемлемой солью в количестве, модулирующем острый вкусо-аромат, по меньшей мере, с получением модифицированного пищевого продукта;
где соединение формулы (I) имеет формулу

где i) Ar представляет собой моноциклический или бициклический арильный или гетероарильный радикал, включающий одно или два ароматических кольца, независимо выбранных из бензольных колец и пяти- или шестичленных гетероарильных колец, причем каждое гетероарильное кольцо содержит от 1 до 4 гетероатомов, независимо выбранных из кислорода, серы и/или азота, каждое ароматическое кольцо необязательно имеет один, два или три R20 замещающих радикалов, где каждый R20 радикал независимо выбран из гидроксила, NH2, SH, галогена, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
ii) Y представляет собой О, S, S(O), SO2, CRlR2 или NR5;
iii) m равно 0 или 1;
iv) hAr1 представляет собой пяти- или шестичленный гетероарильный кольцевой радикал, содержащий, по меньшей мере, два атома углерода в кольце и от одного до трех гетероатомов в кольце, независимо выбранных из О, N или S, где любой из оставшихся членов гетероароматического кольца независимо выбран из CR6, N, NR7;
v) Х представляет собой О, S, S(O), SO2, CR8R9 или NR10;
vi) n равно 0, 1, 2 или 3;
vii) R1, R2, R3, R4, R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, SH, галогена C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и R5, R7 и R10 независимо выбраны из водорода, гидроксила, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и R6 представляет собой водород, галоген или С1-C4алкил или C1-С4алкоксил;
viii) hAr2 представляет собой пяти- или шестичленное гетероарильное кольцо, имеющее, по меньшей мере, один атом углерода в кольце и, по меньшей мере, один атом азота в кольце, и где оставшиеся члены гетероарильного кольца независимо выбраны из CR30, N, NR31, О и S, где каждый R30 независимо выбран из водорода, галогена C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, С1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, CO2H, CN или амида, и каждый R31 независимо выбран из водорода C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и
где соединение формулы (I) имеет ЕС50 для рецептора умами hT1R1/hT1R3 менее чем около 30 мкМ.
a) обеспечение, по меньшей мере, одного пищевого продукта или одного или более его предшественников, и
b) комбинирование пищевого продукта или одного или более его предшественников, по меньшей мере, с одним соединением формулы (I) или его употребляемой в пищу приемлемой солью в количестве, модулирующем острый вкусо-аромат, по меньшей мере, с получением модифицированного пищевого продукта;
где соединение формулы (I) имеет формулу

где i) Ar представляет собой моноциклический или бициклический арильный или гетероарильный радикал, включающий одно или два ароматических кольца, независимо выбранных из бензольных колец и пяти- или шестичленных гетероарильных колец, причем каждое гетероарильное кольцо содержит от 1 до 4 гетероатомов, независимо выбранных из кислорода, серы и/или азота, каждое ароматическое кольцо необязательно имеет один, два или три R20 замещающих радикалов, где каждый R20 радикал независимо выбран из гидроксила, NH2, SH, галогена, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида;
ii) Y представляет собой О, S, S(O), SO2, CR1R2 или NR5;
iii) m равно 0 или 1;
iv) hAr1 представляет собой пяти- или шестичленный гетероарильный кольцевой радикал, содержащий, по меньшей мере, два атома углерода в кольце и от одного до трех гетероатомов в кольце, независимо выбранных из О, N или S, где любой из оставшихся членов гетероароматического кольца независимо выбран из CR6, N, NR7;
v) Х представляет собой О, S, S(O), SO2, CR8R9 или NR10;
vi) n равно 0, 1, 2 или 3;
vii) R1, R2, R3, R4, R8 и R9 независимо выбраны из водорода, кислорода, гидроксила, NH2, SH, галогена C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и R5, R7 и R10 независимо выбраны из водорода, гидроксила, C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и R6 представляет собой водород, галоген или С1-С4алкил или С1-С4алкоксил;
viii) hAr2 представляет собой фенильное кольцо, необязательно замещенное 0, 1, 2 или 3 R30 радикалами, независимо выбранными из водорода, галогена C1-C4 алкила, C1-C4 алкоксила, C1-C4 гидроксиалкила, C1-C4 алкилкарбонила, C1-C4 алкоксикарбонила, C1-C4 алкоксиалкила, СО2Н, CN или амида, и
где соединение формулы (I) имеет ЕС50 для рецептора умами hT1R1/hT1R3 менее чем около 30 мкМ.
Документы, цитированные в отчёте о поиске
Замещенные арилтиоалкилтиопиридины, способ их получения, лекарственное средство на их основе и способ получения лекарственного средства.
















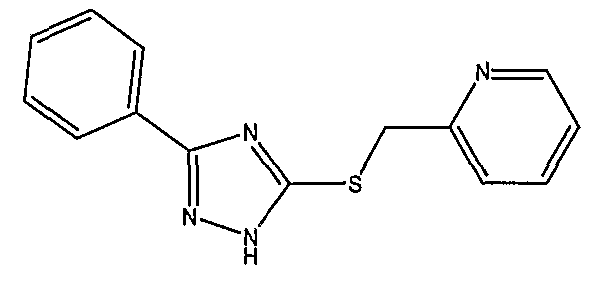



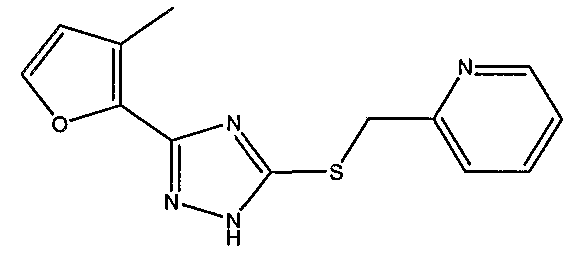

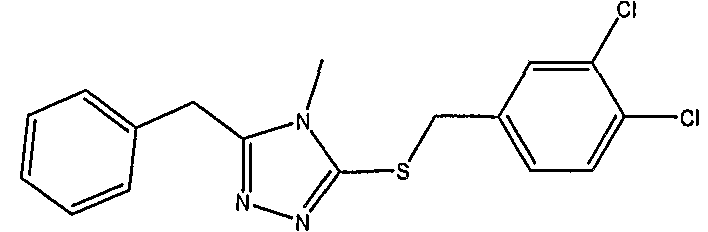
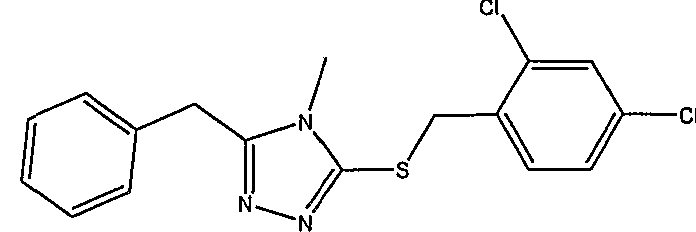

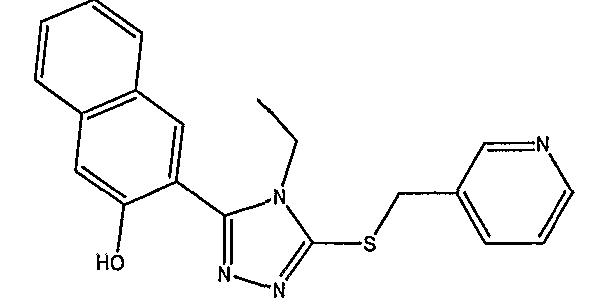







Комментарии