Продукты, содержащие полифенол(ы) и l-аргинин, для стимуляции продукции окиси азота - RU2269268C2
Код документа: RU2269268C2
Описание
Изобретение относится к продуктам, содержащим полифенолы и L-аргинин, которые оказывают положительное воздействие на здоровье млекопитающих.
Полифенольные соединения являются биоактивными веществами, которые происходят из растительных материалов и тесно связаны с сенсорным восприятием и пищевым качеством продуктов, содержащих их.
Проантоцианидины являются классом полифенольных соединений, обнаруженных в нескольких видах растений. Они являются олигомерами мономерных единиц флаван-3-ола, чаще всего связанных либо 4→6, либо 4→8. Наиболее известными классами являются процианидины, которые представляют собой цепи катехина, эпикатехина и их эфиров галловой кислоты, и проделфинидины, которые состоят из галлокатехина, эпигаллокатехина и их эфиров галловой кислоты в качестве мономерных единиц. Могут также иметь место структурные вариации в проантоцианидиновых олигомерах с образованием второго интерфлаваноида, связанного С-O окислительным сочетанием с образованием олигомеров А-типа. Вследствие сложности этого превращения проантоцианидины А-типа встречаются нечасто в природе по сравнению с олигомерами В-типа.
Термин "полифенолы какао" включают полифенольные продукты, включая проантоцианидины, точнее процианидины, экстрагированные из какао-бобов и их производных. Конкретнее термин "полифенол какао" включает мономеры формулы An (где n означает 1) или олигомеры формулы An (где n означает целое число от 2 до 18 и выше), где А имеет формулу
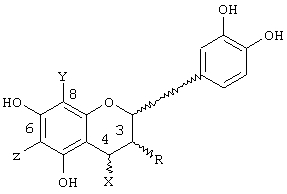
и R является 3-(α)-ОН, 3-(β), 3-(α)-O-сахаридом, 3(β)-O-сахаридом, 3-(α)-O-С(О)-R1 или 3-(β)-ОС(О)-R1;
связывание смежных мономеров имеет место в 4-, 6- или 8-положениях;
связь с мономером в 4-положении имеет альфа или бета стереохимию;
X, Y и Z выбираются из группы, состоящей из А, водорода и сахаридной группы при условии, что, по меньшей мере, к одному конечному мономеру связывание смежного мономера находится в 4-положении и необязательно Y = Z = водороду; и
где сахаридная группа является моно- или дисахаридной группой и может быть необязательно замещена фенильным радикалом, и R' может быть радикалом арилом или гетероарилом, необязательно замещенным, по меньшей мере, одной гидроксильной группой; и
их соли, производные и продукты окисления.
Предпочтительно сахаридная группа является производным группы, состоящей из глюкозы, галактозы, ксилозы, рамнозы и арабинозы. Сахаридная группа и любой или все R, X, Y и Z могут быть необязательно замещены в любом положении фенильным радикалом через эфирную связь. Фенильный радикал выбирается из группы, состоящей из кофейной, коричной, кумаровой, феруловой, галловой, оксибензойной и синапиновой кислоты.
Проантоцианидины привлекают все возрастающее внимание вследствие быстро увеличивающейся совокупности доказательств, связывающих эти соединения с широким рядом потенциальных положительных воздействий на здоровье. Недавно катехины чая были связаны с антиокислительной активностью и с замедлением роста опухолей у лабораторных мышей (Lunder, 1992; Wang et al., 1992; Chung et al., 1992). Кроме того, было показано, что проантоцианидины в экстрактах виноградных семян обладают способностью подавлять свободные радикалы и снижать чувствительность здоровых клеток к токсичным и канцерогенным агентам (Bagchi et al., 1997; Waterhouse and Walzem, 1997; Joshi et al., 1998). Полифенолы, содержащиеся в виноградном соке и красном вине, ассоциируются с потенциальным положительным действием на сердечно-сосудистую систему, включая снижение агрегации тромбоцитов, модуляцию синтеза эйкозаноидов и ингибирование окисления липопротеинов низкой плотности (Waterhouse and Walzem, 1997; Schramm et al., 1998; Frankel et al., 1995). Недавно было высказано предположение, что на любые потенциальные положительные воздействия на здоровье, связанные с этими соединениями, может влиять степень полимеризации (Saito et al., 1998).
Многие растительные полифенолы обладают антиокислительной активностью и могут оказывать ингибирующее действие на мутагенез и канцерогенез. Например, в патенте США №5554645 и патенте США №5712305 раскрываются экстракты полифенолов какао, в частности процианидинов, которые показали, что обладают значительной биологической применимостью. В международном патенте WO 97/36497 (опубликован 24 декабря 1997) раскрывается, что эти экстракты также способствуют ослаблению пародонтоза, артериосклероза и гипертонии; ингибированию окисления LDL и ДНК-топоизомеразы II; модуляции циклооксигеназы, липоксигеназы, окиси азота или NO-синтазы, апоптозу и агрегации тромбоцитов; и обладают противовоспалительной, антигингивитной и антипародонтозной активностью. Кроме того, в WO 97/36497 раскрывается, что олигомеры полифенолов 5-12 обладают повышенной противоопухолевой активностью по сравнению с другими полифенольными соединениями, выделенными из какао. Таким образом, потребление этих высших олигомеров в продуктах какао может обеспечить значительные положительные воздействия на здоровье.
Как отмечалось ранее, использование какао-экстрактов или полифенолов, выделенных из них, в качестве модуляторов NO или NO-синтазы, описывается в публикации международного патента WO 97/36497. Было показано, что окись азота играет роль во многих существенных биологических процессах, таких как передача нервного импульса, свертывание крови, регуляция кровяного давления, регуляция уровней липидов в сыворотке крови, сердечно-сосудистое заболевание, церебральное кровообращение (сосудистая головная боль) и роль в способности иммунной системы уничтожать опухолевые клетки и внутриклеточных паразитов. Р. Clarkson et al., "Oral L-arginine Improves Endothelium dependent Situation in Hypercholesterolemic Young Adults", J. Clin. Innest. 97, No.8: 1989-1994 (April 1996), P.L. Feldman et al., "The Surprising Life of Nitric Oxide", Chem. & Eng. News, pp.26-38 (December 20, 1993); S.H. Snyder et al., "Biological Rules of Nitric Oxide", Scientific American, pp.68-77 (May 1992); P. Chowienczyk et al., "L-arginine: No More Than A Simple Amino Acid?", Lancet, 350: 901-30 (September 27, 1997); M.A. Wheeler et al., "Efforts of Long Term Oral L-Arginine on The Nitric Oxide Synthase Pathway in The Urine from Patients with Interstitial Cystitis", J. Urology 158: 2045-2050 (Dec. 1997); A. Tenenbaum, "L-Arginine: Rediscovery in Progress", Cardiology 90: 153-159 (1998); I.К. Mohan et al., "Effort of L-arginine Nitric Oxide System On Chemical-Induced Diabetes Mellitus", Free Radical Biology & Medicine 25, No. 7: 757-765 (1998); S. Klahr. "The Role of L-Arginine in Hypertension and Nephrotoxicity", Pharmacology and Therapeutics, pp.547-550 (1998); и R.H. Boger et al., "Dietary L-arginine and L-Tocopheral Reduce Vascular Oxidation Stress and Preserve Endothelial Function in some Hypocholesteralemic Rabbits via Different Mechanisms", Arterosclerosis 141: 31-43 (1998).
Например, было высказано предположение о положительных воздействиях на здоровье различных пищевых продуктов. Имелось сообщение о том, что арахис является источником ресвератрола, соединения, обнаруженного в винограде и красном вине, которое связано с облегчением сердечно-сосудистого заболевания. Было установлено, что рацион, включающий грецкие орехи, приводит к снижению сывороточных уровней липидов и кровяного давления. См. Sabate J. et al., "Effects of Walnuts on Serum Lipid Levels And Blood Pressure in Normal Men", New England J. Med. 328: 603-607 (March 4, 1993). Также было высказано предположение, что частое потребление орехов может оказывать защитное действие в отношении коронарного заболевания сердца. См. Sabate J. et al., "Nuts; A New Protective Food Againts Coronary Heart Disease", Lipidology 5: 11-16 (1994). He желая связываться с какой-либо теорией, обоснованный механизм действия, среди прочего, включает наличие относительно высоких концентраций аргинина в орехах, что приводит к продукции окиси азота, тем самым вызывая релаксацию гладкой мускулатуры сосудов. Полагают, что L-аргинин является субстратом для продукции окиси азота с участием синтазы окиси азота.
Следовательно, будут желательны продукты, такие как кондитерские изделия и какаосодержащие продукты (какао-порошок, какао тертое или их экстракты), имеющие высокую концентрацию полифенолов какао, особенно высокую концентрацию олигомеров полифенолов какао 5-12. Также будут очень желательны продукты, содержащие эффективные количества как полифенолов, в частности процианидина(ов) какао, так и L-аргинина для стимуляции продукции окиси азота и проявления положительного воздействия на здоровье, обеспеченного в результате этого.
Изобретение относится к новым пищевым продуктам, включающим, по меньшей мере, один полифенол (т.е. процианидин какао и/или орехов) и L-аргинин в общем количестве, эффективном, чтобы вызвать физиологическое усиление продукции окиси азота у млекопитающего после приема пищевого продукта. Процианидин может быть синтетическим или природным. В предпочтительном воплощении изобретения полифенол какао и L-аргинин обеспечиваются соответственно полифенолсодержащим компонентом (например, ингредиентом какао, и/или какао-порошком, и/или ореховой оболочкой) и L-аргининсодержащим компонентом (например, ореховой массой). Однако это изобретение также включает пищевые продукты, в которых полифенол какао, и/или орехов, и/или L-аргинин, каждый из которых может быть природным или синтетическим, добавляется непосредственно к пищевому продукту.
Пищевые продукты по этому изобретению оказывают положительное воздействие на здоровье млекопитающих, принимающих пищевые продукты. Особенно преимущественным положительным воздействием на здоровье является снижение кровяного давления. Другие положительные воздействия на здоровье могут включать ослабление сердечно-сосудистого заболевания, противоопухолевую активность, антиокислительную активность, лечение почечного заболевания, повышенную функцию иммунной системы и улучшенную познавательную функцию.
Полифенолы какао, содержащиеся в пищевых продуктах согласно изобретению, предпочтительно являются олигомерами полифенолов какао 12-18 и более предпочтительно олигомерами полифенолов какао 5-12.
Полифенолы какао, которые содержат процианидины, присутствуют в какао-бобах. Их получают экстракцией растворителями измельченных в порошок неферментированных бобов, как описано в патенте США 5554645. Они также присутствуют в шоколадных компонентах, приготовленных из какао-бобов.
Пригодные процианидинсодержащие ингредиенты какао включают обжаренные ядра какао-бобов, какао тертое, частично обезжиренное сухое вещество какао, не содержащее жира сухое вещество какао, какао-порошок, полученный размельчением из сухого вещества какао и их смеси. Предпочтительно ингредиенты готовят из недоферментированных бобов, поскольку эти бобы содержат более высокие количества полифенолов какао, включая процианидины какао.
Одним особенно предпочтительным пищевым продуктом согласно настоящему изобретению являются кондитерские изделия, наиболее предпочтительно шоколады, которые включают стандарт подлинности и нестандарт подлинности шоколадов. Пищевые продукты согласно изобретению также могут быть нешоколадными пищевыми продуктами. Предпочтительные нешоколадные пищевые продукты включают продукты на основе орехов, такие как арахисовое масло, арахисовый лом и тому подобное. Другим предпочтительным пищевым продуктом по этому изобретению является пищевой продукт с низким содержанием жира, приготовленный на основе не содержащей жира или частично обезжиренной ореховой массы.
L-аргинин может быть получен из любого доступного источника аргинина, например Arachis hypogaea (арахиса), Juglans regia (грецких орехов), Prunus amygdalus (миндаля), Corylus avellana (фундука), Clycine max (соевых бобов) и тому подобное. Также пригодны Carya illinoensis (орех пекан), Amacardium occidentals (орех кешью) и Macadamia integrifolia, М. tetraphylla (орех макадамия). Известно, что содержание L-аргинина в орехах может колебаться в зависимости от зрелости орехов и, кроме того, некоторые культуры могут иметь более высокие концентрации. Также здесь могут быть полезными родственные виды в каждом роду. Арахисовые орехи обычно содержат примерно 2-3 г L-аргинина на 100 г ореховой массы. Содержание L-аргинина в миндале составляет примерно 2-3 г на 100 г, в грецких орехах - примерно 2-4 г на 100 г, в фундуке - примерно 1,5-2,5 г на 100 г и в орехе пекане и орехе макадамии - примерно 0,5-1,5 г на 100 г. Орех может быть частью ореха, ореховой оболочкой, ореховой пастой и/или ореховой мукой в количествах, которые обеспечивают желаемое количество L-аргинина, которое будет колебаться в зависимости от источника орехов.
L-аргининсодержащий ингредиент может также представлять собой семена, пасту, полученную из семян, и/или муку из семян. Пригодные семена включают Helianthus annuus (семена подсолнечника), Sesamum indicum (семена кунжута), семена пажитника, Cucurbita spp. (семена тыквы) и тому подобное. Семена подсолнечника, семена тыквы и семена кунжута соответственно содержат примерно 1,5-3,0 г, примерно 3,5-6,0 г и примерно 2-3 г L-аргинина на 100 г.
Другим источником с высоким содержанием L-аргинина является желатин, который содержит примерно 5 г L-аргинина на 100 г желатина.
Пищевой продукт содержит примерно 200 мг, предпочтительно 300 мг, процианидинов на 100 г продукта и, по меньшей мере, 0,9 г, предпочтительно 1,2 г, более предпочтительно 1,6 г L-аргинина на 100 г пищевого продукта.
Пищевой продукт может содержать полифенолы из иного источника, чем какао, например полифенолы, обнаруженные в оболочках орехов, таких как описанные выше. Оболочки арахисовых орехов содержат примерно 17% процианидинов и оболочки миндальных орехов содержат до 30% процианидинов. В предпочтительном воплощении ореховые оболочки используются в пищевом продукте, например в нуге шоколадной конфеты. Также для использования здесь пригодны полифенолы, содержащиеся во фруктах и овощах. Известно, что кожура фруктов, таких как яблоки и апельсины, а также виноградные семена имеют высокое содержание полифенолов.
Полагается, что комбинация полифенола(ов) какао и L-аргинина обеспечивает неожиданно повышенные положительные эффекты на здоровье в результате положительной модуляции под воздействием полифенолов NO и/или NO-синтазы в присутствии L-аргинина, субстрата NO-синтазы. Таким образом, продукция окиси азота усиливается под действием комбинации полифенола какао и/или орехов и L-аргинина, которое приводит к улучшенному положительному воздействию на здоровье, осуществляемому посредством окиси азота, например предупреждению сердечно-сосудистого заболевания, пониженному кровяному давлению, противоопухолевой активности и тому подобное.
Настоящее изобретение также относится к фармацевтической композиции, содержащей, по меньшей мере, один полифенол(ы) какао и/или орехов, L-аргинин и фармацевтически приемлемый носитель. Полифенол(ы) и L-аргинин присутствуют в количестве, эффективном для индукции физиологического усиления продукции окиси азота у млекопитающего, принимающего внутрь композицию. Процианидин(ы) из какао и/или орехов присутствуют в количестве от 1 мкг до примерно 10 г на разовую дозу. L-аргинин присутствует в количестве примерно от 1 мкг до примерно 10 г на разовую дозу. Полифенольный ингредиент какао может быть экстрактом какао (бобы, паста или порошок и т.д.), или может быть его синтезированным производным, или может быть синтезированным полифенольным соединением, или смесью полифенольных соединений и их производных. Процианидин, экстрагированный из ореховых оболочек, также пригоден для использования здесь.
Детальное описание изобретения
Пищевой продукт согласно изобретению содержит, по меньшей мере, один полифенол какао и необязательно полифенолы из других источников, как обсуждалось выше. Полифенол какао может быть из любого другого источника, т.е. натуральным (природным) или синтезированным. Наиболее предпочтительно полифенол какао является олигомером.
Термин "полифенол какао" включает процианидины, присутствующие в какао-бобах или какао-ингредиентах, используемых в производстве шоколадных кондитерских изделий, экстрактах какао-бобов или какао-ингредиентах, включающих процианидины, и их синтезированные производные и включает синтезированные полифенольные соединения какао или синтезированные смеси полифенольных соединений какао и их производных. Какао-бобы могут быть полностью ферментированными или недоферментированными.
Термин "ингредиент какао" относится к материалу, содержащему сухое (твердое) вещество какао, происходящему из свободных от какаовеллы ядер какао-бобов, и включает какао тертое, частично или полностью обезжиренное сухое вещество какао (например, жмых или порошок, подвергнутый обработке щелочными агентами, какао-порошок или подвергнутое обработке щелочными агентами какао тертое и тому подобное).
Термин "какао тертое" относится к темно-коричневой жидкости "пасте", полученной при измельчении ядер какао-бобов. Жидкое состояние является результатом разрушения клеточных стенок и высвобождения какао-масла во время обработки, приводящей к образованию суспензии раздробленных частиц сухого вещества какао, суспендированного в какао-масле.
Частично обезжиренное сухое вещество какао, имеющее высокое содержание полифенолов какао (СР), включая высокое содержание процианидинов какао, можно получить при переработке какао-бобов непосредственно в сухое вещество без стадии обжаривания бобов или ядер бобов. Этот способ сохраняет полифенолы какао, поскольку в нем опускается традиционная стадия обжаривания. Способ в основном состоит из стадий а) нагревания какао-бобов до внутренней температуры бобов, достаточной для снижения содержания влаги примерно до 3% по массе и для отделения какаовеллы; b) провеивания ядер какао-бобов с отделением какаовеллы; с) прессования ядер какао-бобов на винтовом прессе и d) извлечения какао-масла и частично обезжиренного сухого вещества, которое содержит полифенолы какао, включая процианидины какао. Необязательно какао-бобы очищают перед стадией нагревания, например, в воздушном сепараторе с отделением по плотности в псевдоожиженном слое. Провеивание можно также проводить в воздушном сепараторе с отделением по плотности в псевдоожиженном слое. Предпочтительно какао-бобы нагревают до внутренней температуры бобов примерно от 100°С до примерно 110°С, более предпочтительно менее, чем примерно 105°С, обычно используя аппарат для нагревания инфракрасными лучами в течение от 3 до 4 мин. Если желательно, сухое вещество какао можно подвергнуть обработке щелочными агентами или измельчить до какао-порошка.
Внутреннюю температуру бобов (IBT) можно замерить при заполнении изолированного контейнера, такого как термос, бобами (примерно 80-100 бобов). Затем изолированный контейнер соответствующим образом герметично закрывают для поддержания в нем температуры пробы. Внутрь изолированного контейнера, заполненного бобами, помещают термометр и уравновешивают температуру термометра для бобов в термосе. Определяемая температура является IBT-температурой бобов. IBT также можно рассматривать, как температуру уравновешенной массы бобов.
Какао-бобы можно разделить на четыре категории, основываясь на их цвете: преимущественно коричневый (полностью ферментированные), пурпурно-коричневые, пурпурные и синевато-серые (неферментированные). Предпочтительно сухое вещество какао готовят из недоферментированных какао-бобов, которые имеют более высокое содержание полифенолов какао, чем в ферментированных бобах. Недоферментированные бобы включают синевато-серые какао-бобы, пурпурные какао-бобы, смеси синевато-серых и пурпурных какао-бобов, смеси пурпурных и коричневых какао-бобов, или смеси синевато-серых, пурпурных и коричневых какао-бобов. Более предпочтительно какао-бобы являются синевато-серыми и/или пурпурными какао-бобами.
Как обсуждалось выше, содержание полифенолов какао (СР), включая содержание процианидинов какао, в жареных ядрах какао-бобов, какао тертом и частично обезжиренном или не содержащем жира сухом веществе выше, когда они приготовлены из какао-бобов или их смесей, которые являются недоферментированными, т.е. бобы, имеющие фактор ферментации 275 или меньше.
"Фактор ферментации" определяется при использовании системы градации для характеристики ферментации какао-бобов. Синевато-серый цвет означает 1, пурпурный 2, пурпурно-коричневый означает 3 и коричневый означает 4. Процент бобов, попадающих в каждую категорию, умножается на их взвешенное число. Таким образом, "фактор ферментации" для пробы из 100% коричневых бобов будет составлять 100×4 или 400, в то время как 100% проба из пурпурных бобов будет составлять 100×2 или 200. Проба из 50% синевато-серых бобов и 50% пурпурных бобов будет иметь фактор ферментации 150[(50×1)+(50×2)].
Какао тертое с высоким содержанием СР и/или сухое вещество какао с высоким содержанием СР можно приготовить а) обжариванием отобранных какао-бобов (фактор ферментации 275 или меньше) до внутренней температуры бобов от 95°С до 160°С; b) провеиванием ядер какао-бобов от обжаренных какао-бобов; с) измельчением ядер какао-бобов в какао тертое и d) необязательно извлечением какао-масла и частично обезжиренного сухого вещества какао из какао тертого. Альтернативно какао тертое и/или сухое вещество какао можно получить а) нагреванием отобранных какао-бобов (фактор ферментации 275 или меньше) до внутренней температуры бобов 95-135°С для снижения содержания влаги примерно до 3% по массе и для отделения какаовеллы от ядер какао-бобов; b) провеиванием ядер какао-бобов от какаовеллы; с) обжариванием ядер какао-бобов до внутренней температуры ядер от 95°С до 160°С; d) измельчением обжаренных ядер в какао тертое и е) необязательно извлечением какао-масла и частично обезжиренного сухого вещества какао из тертого какао. Какао тертое и частично обезжиренное сухое вещество какао, содержащие, по меньшей мере, 50000 мкг общего количества процианидинов какао и/или, по меньшей мере, 5000 мкг пентамера процианидина какао на г не содержащего жира сухого вещества какао, можно получить вышеуказанными способами.
Экстракт, содержащий полифенолы какао, включая процианидины какао, можно получить экстракцией растворителями частично обезжиренного сухого вещества какао или не содержащего жира сухого вещества, полученных из недоферментированных какао-бобов или ядер какао-бобов.
Частично обезжиренное сухое вещество какао и/или полифенольные экстракты какао можно использовать в терапевтических композициях необязательно с носителем или разбавителем. Терапевтические композиции являются пригодными в качестве противоопухолевых композиций, антиоксидантов, антимикробных агентов, модуляторов окиси азота (NO) или NO-синтазы, модуляторов циклооксигеназы, модуляторов липоксигеназы и in vivo модуляторов глюкозы.
Пищевые продукты с высоким содержанием СР можно получить, используя или обжаренные ядра какао-бобов с высоким содержанием СР, какао тертое с высоким содержанием СР и/или частично обезжиренное или не содержащее жира сухое вещество какао с высоким содержанием СР. Пищевые продукты включают корм для домашних животных, сухие смеси для приготовления какао-напитка, пудинги, сиропы, печенье, закусочные соусы, рисовые смеси, рисовые кексы, сухие смеси для приготовления напитков, напитки и тому подобное. Предпочтительно пищевые продукты являются кондитерскими изделиями, например темным шоколадом или молочным шоколадом. Экстракт также можно использовать для приготовления пищевых продуктов, имеющих высокое содержание полифенолов какао.
Здоровье млекопитающего можно улучшить назначением млекопитающему композиции, содержащей процианидины какао и/или орехов, или компонентов какао и/или компонентов орехов с высоким содержанием СР. В этих композициях общее количество олигомера(ов) процианидина составляет, по меньшей мере, 1 мкг или выше, и композицию назначают ежедневно в течение больше 60 дней.
Структуру процианидинов какао можно представить в виде олигомеров мономера А, имеющих формулу An, где n означает 2-18, где А имеет формулу

и R является 3-(α)-ОН, 3-(β)-ОН, 3-(α )-O-сахаридом, 3(β)-O-сахаридом; связывание смежных мономеров имеет место в 4-, 6- или 8-положениях; при условии, что X, Y и Z выбираются из группы, состоящей из А, водорода и сахарида; связь с мономером в 4-положении имеет α или β стереохимию, по меньшей мере, с одним концевым мономером; и связывание к нему смежного мономера находится в 4-положении. Необязательно Y = Z = водороду, и их соли, где сахаридная группа является производным моно- или дисахарида.
Термин "олигомер", использованный здесь, относится к любому соединению, имеющему вышеуказанную формулу, представленную выше, где n равно от 2 до 18, и предпочтительно, где n равно 5-12. Когда n равняется 2, олигомер определяется как "димер"; когда n равняется 3, олигомер определяется как "тример"; когда n равняется 4, олигомер определяется как "тетрамер"; когда n равняется 5, олигомер определяется как "пентамер", и подобные перечисления могут использоваться для обозначения олигомеров, имеющих n до и включая 18 и выше, так, когда n равняется 18, олигомер определяется как "октадекамер".
Синтезированные производные полифенолов какао включают соединения, соответствующие структуре An, где R может быть 3-(α)-O-сахаридом, 3-(β)-O-сахаридом, 3-(α)-О-С(О)-R1 или 3-(β)-O-С(О)-R1, где сахаридная группа может быть производной моно- или дисахарида, выбранного из группы, состоящей из глюкозы, галактозы, ксилозы, рамнозы и арабинозы, где сахаридная группа любого или из всех R, X, Y и Z может быть необязательно замещена в любом положении фенильным радикалом через эфирную связь; где фенильный радикал может быть выбран из группы, состоящей из кофейной, коричной, кумаровой, феруловой, галловой, оксибензойной и синапиновой кислоты; и где R1 является радикалом арилом или гетероарилом, необязательно замещенным, по меньшей мере, одной гидроксильной группой. Замещенный радикал арил или гетероарил R1 может предпочтительно содержать заместитель, соответствующий замещенным фенильным радикалам кофейной, коричной, кумаровой, феруловой, галловой, оксибензойной и синапиновой кислот.
Полифенольные олигомеры можно получить
(a) путем защиты каждой фенольной гидроксильной группы первого и второго полифенольного мономера защитной группой, получая при этом первый и второй защищенный полифенольный мономер;
(b) функционализации 4-положения первого защищенного полифенольного мономера с получением функционализированного защищенного полифенольного мономера, имеющего формулу

где с является целым числом от 1 до 2;
d является целым числом от 1 до 4;
у является целым числом от 2 до 6;
R является защитной группой;
R* является Н или ОН;
(c) сочетанием второго защищенного полифенольного мономера с функционализированным защищенным полифенольным мономером с получением защищенного полифенольного димера в качестве полифенольного олигомера;
(d) необязательно повторением стадий функционализации и сочетания для образования полифенольного олигомера, имеющего n мономерных единиц, где n является целым числом от 3 до 18; предпочтительно 5-12;
(e) удалением защитных групп из фенольных гидроксильных групп.
Предпочтительным защищенным полифенольным мономером является бромированный защищенный эпикатехин или бромированный защищенный катехин, более предпочтительно 8-бром-эпикатехин или 8-бром-катехин.
В вышеуказанном способе 4-положение защищенного полифенольного мономера может быть функционализировано окислением, используя хиноновый окислительный агент в присутствии диола, например этиленгликоля, когда у равняется 2.
Вышеуказанный способ дополнительно включает стадию образования производного полифенольного олигомера путем этерификации полифенольного олигомера в 3-положении, по меньшей мере, одной мономерной единицы с получением этерифицированного полифенольного олигомера. Эфирную группу можно выбрать из группы, состоящей из -ОС(О)-арила, -ОС(O)-замещенного арила, -ОС(О)-стирила и -ОС(О)-замещенного стирила, где замещенный арил или замещенный стирил содержат, по меньшей мере, один заместитель, выбранный из группы, состоящей из галогена, гидроксила, нитро, циано, амино, тиола, метилендиокси, дигалогенметилендиокси, C1-С6алкила, C1-С6алкокси, C1-С6галогеналкила, C1-С6галогеналкокси, С3-C8циклоалкила и С3-С8циклоалкокси. Предпочтительно 3-положение, по меньшей мере, одной мономерной единицы превращается в группу, производную кислоты, выбранной из кофейной, коричной, кумаровой, феруловой, галловой, оксибензойной и синапиновой кислот.
Вышеуказанный способ может дополнительно включать стадию образования производного полифенольного олигомера путем гликозидирования полифенольного олигомера в 3-положении, по меньшей мере, одной мономерной единицы с получением гликозидированного полифенольного олигомера. Предпочтительно 3-положение, по меньшей мере, одной мономерной единицы превращается в производную группу, выбранную из группы, состоящей из -O-гликозида или -O-замещенного гликозида, где замещенный гликозид замещается -С(О)-арилом, -С(О)-замещенным арилом, -С(О)-стирилом или -С(О)-замещенным стирилом. Замещенный арил или замещенный стирил может включать заместители, выбранные из группы, состоящей из галогена, гидроксила, нитро, циано, амино, тиола, метилендиокси, дигалогенметилендиокси, C1-С6алкила, C1-С6алкокси, C1-С6галогеналкила, C1-С6галогеналкокси, С3-С8циклоалкила и С3-С8циклоалкокси. Предпочтительно гликозид выбирается из группы, состоящей из глюкозы, галактозы, ксилозы, рамнозы и арабинозы.
Пищевые продукты согласно изобретению могут включать один или более полифенольных мономеров какао, олигомеров 2-18 или их производные. Предпочтительно пищевые продукты по этому изобретению содержат смеси полифенольных олигомеров 2-18 или их производных; более предпочтительно пищевые продукты содержат смеси олигомеров полифенолов какао 5-12 или их производных.
Пищевые продукты по этому изобретению включают продукты, предназначенные для приема человеком и другими млекопитающими, например собаками, кошками, лошадьми и тому подобное. Пищевые продукты согласно изобретению можно принимать для питания, удовольствия или в медицинских и ветеринарных целях.
Предпочтительным пищевым продуктом является кондитерское изделие, выпечка, приправа, брикет на основе злаковых, брикет, заменяющий пищу, сироп, порошкообразная смесь для приготовления напитка, напиток и тому подобное. Более предпочтительно, если пищевым продуктом по этому изобретению является шоколадное кондитерское изделие, содержащее орехи, например арахис, грецкий орех, миндаль, фундук, семянки и тому подобное. Ореховая масса может быть в любой форме, например цельных орехов, измельченных орехов, молотых орехов, ореховых паст и тому подобное. Предпочтительные нешоколадные пищевые продукты включают арахисовое масло, арахисовый лом и тому подобное. Подобные нешоколадные пищевые продукты могут содержать ингредиенты какао, в частности ингредиенты какао, содержащие полифенолы какао, но они не будут рассматриваться шоколадным продуктом специалистом обычной квалификации в этой области, например это арахисовое масло, содержащее относительно небольшой процент какао-порошка, имеющего высокие концентрации полифенолов какао.
Шоколад, используемый в пищевых продуктах в США, является предметом стандарта подлинности (SOI), установленного Администрацией по контролю за качеством пищевых продуктов и лекарственных препаратов США согласно федеральному закону о пищевых продуктах, лекарственных препаратах и косметических средствах, который устанавливает необходимые ингредиенты и их пропорции в кондитерском изделии для допущения ярлыка на кондитерском изделии "шоколад".
Наиболее популярным шоколадом или шоколадной конфетой, потребляемой в США, являются таковые в виде сладкого шоколада или молочного шоколада. Шоколад в основном представляет собой смесь сухих веществ какао, суспендированных в жире. Молочный шоколад представляет собой кондитерское изделие, которое включает не содержащее жира сухое молоко, молочный жир, какао тертое, пищевой углеводный подсластитель, какао-масло и может включать разнообразные другие ингредиенты, такие как эмульгаторы, ароматизаторы и другие добавки. Сладкий шоколад содержит более высокие количества какао тертого, но более низкие количества сухого молока, чем молочный шоколад. Для полусладкого шоколада необходимо, по меньшей мере, 35% по массе какао тертого, а в противном случае он является по определению сладким шоколадом. Темный шоколад обычно включает только какао тертое, пищевой углеводный подсластитель, какао-масло, иначе по определению он представляет собой либо сладкий шоколад, либо полусладкий шоколад. Сливочный шоколад и шоколад с обезжиренным молоком отличается от молочного шоколада тем, что молочный жир происходит из различных видов свежих сливок, молочного масла и обезжиренного молока соответственно. Для обезжиренного молока требуется ограничить общее количество молочного жира до менее, чем минимум для молочного шоколада. Шоколады из смешанных молочных продуктов отличаются от молочного шоколада тем, что сухое молоко включает один или все виды сухого молока, перечисленные для молочного шоколада, сливочного шоколада или шоколада с обезжиренным молоком. Белый шоколад отличается от молочного шоколада тем, что не включает не содержащего жира сухого вещества какао. Здесь также пригодны стойкие к нагреванию шоколады (термоустойчивые).
Нестандартизированными шоколадами являются такие шоколады, которые имеют композиции, которые не входят в указанные уровни стандартизированных шоколадов. Шоколады классифицируются как "нестандартизированные" шоколады, когда указанный ингредиент замещается частично или полностью, так, когда какао-масло заменяется растительным маслом или жиром. Любые добавки или исключения из рецептуры шоколада, сделанные помимо стандартов подлинности Администрации по контролю за качеством пищевых продуктов и лекарственных препаратов США для шоколада, будут приводить к запрету использовать "шоколад" для описания кондитерского изделия. Однако, как здесь использовано, термин "шоколад" или "шоколадный продукт" относится к любому стандарту подлинности или нестандарту подлинности в отношении шоколадного продукта.
Шоколад может иметь форму твердых кусочков шоколада, таких как брикеты, или новые формы. Шоколад может быть также включен в качестве ингредиента в другие более сложные кондитерские изделия, где шоколад соединяется с и обычно покрывает другие пищевые включения, такие как карамель, арахисовое масло, нуга, кусочки фруктов, орехи, вафли, мороженое или тому подобное. Эти продукты характеризуются как устойчивые к воздействию микробов при хранении 65-85°F (18-29°С) при нормальном атмосферном давлении.
Термин "углевод" относится к пищевым углеводным подсластителям с различными степенями сладости и может быть любым из обычно используемых и включает, но не ограничивается сахарозой (например, из сахарного тростника или свеклы), декстрозой, фруктозой, лактозой, мальтозой, сухим веществом глюкозного сиропа, сухим веществом кукурузной патоки, инвертным сахаром, гидролизированной лактозой, медом, кленовым сахаром, коричневым сахаром, мелассой и тому подобное.
Шоколадные пищевые продукты могут дополнительно включать другие ингредиенты, такие как не содержащее жира сухое молоко, не содержащее жира сухое вещество какао (какао-порошок), заменители сахара, натуральные и искусственные вкусовые вещества (например, специи, кофе, соль и тому подобное, а также их смеси), протеины и тому подобное.
Пищевые продукты по этому изобретению также включают L-аргинин. Можно использовать любой источник L-аргинина, т.е. синтетический или натуральный (природный). Особо предпочтительные источники L-аргинина включают соевые бобы и ореховую массу таких орехов, как арахис, грецкие орехи, миндаль, фундук и тому подобное. Обезжиренную и частично обезжиренную ореховую массу можно также использовать для увеличения концентрации L-аргинина. Частично или полностью обезжиренная молотая ореховая масса относится к ореховой муке.
В дополнение к физиологическим активностям, известным как проявляемые процианидинами какао или композициями, содержащими процианидины, комбинация L-аргинина с процианидинами какао приводит к лучшему эффекту, что было показано усиленной продукцией окиси азота.
Одно воплощение синергического действия на модуляцию NO и/или NO-синтазы, например, заключается в следующем. Многие пищевые продукты содержат значительные количества L-аргинина, но необязательно таковые в отношении полифенолов какао. Установив, что L-аргинин является субстратом для NO-синтазы, и что NO-зависимое расширение сосудов значительно улучшается у животных с гиперхолестеринемией, получающих добавки L-аргинина (см. Cooke et al., Circulation 83: 1057-1062, 1991), и что полифенолы какао могут модулировать концентрацию NO, можно ожидать синергического улучшения эндотелийзависимого расширения сосудов. Сообщалось об уровнях L-аргинина от 1,0 до 1,1 г/100 г в неподслащенном какао-порошке. Исходя из этого, в пищевые продукты включают другие источники L-аргинина для обеспечения максимального положительного эффекта в отношении модуляции NO и NO-синтазы. В особо предпочтительном воплощении полифенолы какао и/или орехов и L-аргинин присутствуют в количествах, эффективных для обеспечения вышеуказанного синергического положительного воздействия, например примерно от 1 мг до примерно 10 г на единичную дозу, предпочтительно примерно от 25 мг до 3 г процианидинов. Продукты по изобретению можно использовать для ингибирования роста опухолевых клеток у млекопитающих, для снижения гипертонии у млекопитающих, для лечения воспалительного заболевания кишечника, для ингибирования роста бактерий у млекопитающих, для предупреждения или снижения атеросклероза или повторного стеноза, для модуляции агрегации тромбоцитов, для модуляции апоптоза, в качестве антиоксиданта, особенно для предотвращения окисления LDL у млекопитающих, для модуляции циклооксигеназы и/или липоксигеназы, для модуляций или стимуляции продукции окиси азота (NO) или синтазы окиси азота (NO) у млекопитающих, для лечения связанной с окисью азота гиперхолестеринемии у млекопитающих, для модуляций глюкозы in vivo, для ингибирования тепоизомеразы II, для индукции INOS в моноцитах и/или макрофагах млекопитающих, а также в качестве антимикробного, противоопухолевого, антигингивитного и антипародонтозного средства.
Можно осуществлять на практике использование пищевых продуктов и фармацевтических композиций по этому изобретению, содержащих полифенолы какао и/или орехов и L-аргинин, новые способы улучшения здоровья млекопитающего, в частности человека.
Предпочтительным воплощением изобретения является способ улучшения здоровья млекопитающего путем назначения млекопитающему эффективного количества пищевого продукта или фармацевтической композиции, содержащих полифенолы какао и/или орехов и L-аргинин, в течение эффективного периода времени. В зависимости от заболевания, которое подлежит лечению, эффективный период времени может колебаться от очень короткого до периода больше 60 дней. В одном аспекте здоровье млекопитающего улучшается при потреблении съедобной композиции, содержащей полифенолы какао и L-аргинин, каждый день в течение периода времени от больше пяти дней до периода времени более 60 дней.
Полифенолы, используемые в этом изобретении, модулируют окись азота (NO) и NO-синтазу. Аргинин действует в качестве субстрата для NO-синтазы. Объединенное количество полифенолов какао и L-аргинина является эффективным для того, чтобы добиться физиологической ответной реакции у млекопитающего, получающего пищевой продукт. Физиологическая ответная реакция заключается в повышенной продукции окиси азота, которая будет получена при введении полифенола какао или одного L-аргинина. Полагается, что эта усиленная продукция окиси азота приведет к вышеуказанным положительным воздействиям на здоровье, связанным с продукцией окиси азота.
Пищевые продукты и фармацевтические композиции по этому изобретению являются полезными, например, для модуляции расширения сосудов и дополнительно полезны в отношении модуляции кровяного давления или при обращении к коронарным заболеваниям и мигрени. Ответные реакции, полученные при назначении композиции по этому изобретению, включают снижение гипертонии и расширение кровеносных сосудов.
Новые пищевые продукты по этому изобретению могут легко приготовить специалисты обычной квалификации в этой области, используя методы, описанные ниже.
Ингредиенты какао можно получить из какао-бобов, имеющих фактор ферментации менее 300, и/или из какао-бобов, имеющих фактор ферментации 300 или выше. Обработанные щелочными агентами ингредиенты шоколада, полученные из какао-бобов, имеющих фактор ферментации 300 или выше, можно использовать в сочетании с ингредиентами какао, полученными из какао-бобов, имеющих фактор ферментации меньше 300.
Содержание процианидинов какао в пищевом продукте на основе шоколада можно сохранять путем защиты углеводного ингредиента(ов) и/или ингредиента(ов) молока во время составления рецептуры пищевого продукта. Ингредиент(ы) защищается до добавления ингредиента(ов) шоколада. По меньшей мере один защищающий ингредиент, выбранный из группы, состоящей из жира, эмульгатора, антиокислителя, вкусового вещества и их смесей, добавляют к углеводному ингредиенту(ам) и/или ингредиенту(ам) молока для образования первой смеси. Первая смесь соединяется с ингредиентом(ами) шоколада для образования второй смеси. Пищевой продукт получают из второй смеси. Пищевой продукт может быть кондитерским изделием или пищевой добавкой. Кондитерское изделие может быть темным или молочным щоколадом. Необязательно углеводный и/или молочный ингредиент(ы) измельчаются для уменьшения размера частиц перед смешением с защитным ингредиентом. Ингредиент(ы) шоколада можно также измельчить перед объединением с первой смесью защищенного углеводного и/или молочных ингредиентов. Предпочтительными жирами для использования в качестве ингредиентов для предварительной обработки являются какао-масло и/или какао тертое, которое содержит какао-масло и которое получают из какао-бобов, имеющих фактор ферментации 300 или выше. Предпочтительные эмульгаторы включают лецитин или фракционированный лецитин. Пригодные антиокислители включают таннины, хиноны, полигидроксильные соединения, фосфолипиды, соединения токола и/или их производные. Пригодные вкусовые вещества включают ванилин, специи и/или выжатые натуральные цитрусовые масла или эфирные масла из пряностей. Можно коншировать первую смесь, ингредиент(ы) шоколада и/или вторую смесь. Шоколад коншируют при примерно от 50 до примерно 65°С. Второй эмульгатор можно добавить во время или после конширования. Этот второй эмульгатор может быть лецитином, полиэруиатом сахарозы, фосфатидом аммония, полиглицерином, полирицинолеатом, фосфатированными моно- и дигликозид/деактил винной кислоты эфирами моноглицеридов и фракционированным лецитином. Пищевые продукты, полученные с защищенным углеводом(ами) и/или ингредиентом(ами) молока, содержат, по меньшей мере, от 10 до 20% по массе процианидинов какао больше, чем пищевой продукт, полученный способом, который не включает предварительную обработку углеводного ингредиента(ов) и/или ингредиента(ов) молока.
Добавление L-аргинина к пищевому продукту можно производить при добавлении ореховой массы, например арахисовой, в количестве, достаточном для обеспечения соответствующей желаемой концентрации L-аргинина.
Как отмечалось выше, особенно предпочтительным пищевым продуктом является шоколадное кондитерское изделие. Шоколад в шоколадном кондитерском изделии содержит относительно высокую концентрацию полифенолов какао. В этом воплощении шоколад включает, по меньшей мере, 3600 мкг, предпочтительно, по меньшей мере, 4000 мкг, более предпочтительно, по меньшей мере, 4500 мкг, еще более предпочтительно, по меньшей мере, 5000 мкг и наиболее предпочтительно, по меньшей мере, 5500 мкг процианидинов какао на г шоколада, основываясь на общем количестве не содержащего жира сухого вещества в продукте. По одному предпочтительному воплощению изобретения шоколад содержит, по меньшей мере, 6000 мкг, предпочтительно, по меньшей мере, 6500 мкг, более предпочтительно, по меньшей мере, 7000 мкг и наиболее предпочтительно, по меньшей мере, 8000 мкг процианидинов какао на г и еще более предпочтительно 10000 мкг, основываясь на не содержащем жира сухом веществе какао в продукте.
Другое воплощение относится к шоколадному пищевому продукту, включающему шоколад, имеющему, по меньшей мере, 200 мкг, предпочтительно, по меньшей мере, 225 мкг, более предпочтительно, по меньшей мере, 275 мкг и наиболее предпочтительно, по меньшей мере, 300 мкг процианидинового пентамера какао на г, основываясь на общем количестве не содержащего жира сухого вещества какао в шоколадном пищевом продукте. Предпочтительно шоколад содержит, по меньшей мере, 325 мкг, предпочтительно, по меньшей мере, 350 мкг, более предпочтительно, по меньшей мере, 400 мкг и наиболее предпочтительно, по меньшей мере, 450 мкг процианидинового пентамера какао на г, основываясь на общем количестве не содержащего жира сухого вещества какао в шоколадном пищевом продукте.
Еще одно воплощение относится к кондитерскому изделию из молочного шоколада, которое имеет, по меньшей мере, 1000 мкг, предпочтительно, по меньшей мере, 1250 мкг, более предпочтительно, по меньшей мере, 1500 мкг и наиболее предпочтительно, по меньшей мере, 2000 мкг полифенолов какао на г, основываясь на общей массе не содержащего жира сухого вещества в продукте из молочного шоколада. В предпочтительном воплощении молочный шоколад содержит, по меньшей мере, 2500 мкг, предпочтительно, по меньшей мере, 3000 мкг, более предпочтительно, по меньшей мере, 4000 мкг и наиболее предпочтительно, по меньшей мере, 5000 мкг процианидинов какао на г, основываясь на общем количестве не содержащего жира сухого вещества в продукте из молочного шоколада.
В другом воплощении пищевой продукт является молочным шоколадом, который имеет, по меньшей мере, 85 мкг, предпочтительно, по меньшей мере, 90 мкг, более предпочтительно, по меньшей мере, 100 мкг и наиболее предпочтительно, по меньшей мере, 125 мкг пентамера процианидина какао на г, основываясь на общем количестве не содержащего жира сухого вещества в продукте из молочного шоколада. В предпочтительном воплощении молочный шоколад включает, по меньшей мере, 150 мкг, предпочтительно, по меньшей мере, 175 мкг, более предпочтительно, по меньшей мере, 200 мкг и наиболее предпочтительно, по меньшей мере, 250 мкг пентамера процианидина какао на г, основываясь на общем количестве не содержащего жира сухого вещества в продукте из молочного шоколада.
Нешоколадные пищевые продукты будут содержать, по меньшей мере, 1 мкг, предпочтительно, по меньшей мере, 5 мкг, более предпочтительно, по меньшей мере, 10 мкг, более предпочтительно, по меньшей мере, 25 мкг, наиболее предпочтительно, по меньшей мере, 50 мкг процианидинов какао. Если желательно, нешоколадные продукты питания могут содержать более высокие уровни процианидинов какао по сравнению с установленными в вышеописанных шоколадных пищевых продуктах.
Количество L-аргинина в пищевых продуктах может варьировать. Обычно какао содержит между 1 и 1,1 г L-аргинина на 100 г частично обезжиренного сухого вещества какао. Оно может находиться в пределах от 0,8 до 1,5 г на 100 г какао. Шоколадные пищевые продукты по этому изобретению содержат L-аргинин в количестве выше, чем обычно имеет место в ингредиентах какао. Зная количество ингредиентов какао и L-аргинина, использованного в пищевом продукте, специалист обычной квалификации в этой области легко определит общее количество L-аргинина в конечном продукте. Пищевой продукт будет обычно включать, по меньшей мере, 1 мкг, предпочтительно, по меньшей мере, 10 мкг или, по меньшей мере, 100 мкг, еще более предпочтительно, по меньшей мере, 1000 мкг, или 5000 мкг, или 10000 мкг и наиболее предпочтительно, по меньшей мере, 20000, 50000 или 100000 мкг L-аргинина на г пищевого продукта.
Как было отмечено ранее, настоящее изобретение также относится к фармацевтической композиции, содержащей, по меньшей мере, один полифенол какао, L-аргинин и фармацевтически приемлемый носитель. Включение L-аргинина в количестве примерно от 1 мкг до примерно 10 г на единичную дозу может легко осуществить специалист обычной квалификации в этой области. Фармацевтические композиции по настоящему изобретению являются полезными для лечения млекопитающих в случае необходимости увеличения продукции окиси азота и получения положительного эффекта, вытекающего отсюда, такого как пониженное кровяное давление.
Экспериментальные способы
Следующие способы можно использовать для количественного определения процианидинов и L-аргинина в различных примерах.
Способ А использовали для количественного определения содержания процианидинов (общего и пентамера), представлен в примерах 1-3.
Способ В следует использовать для количественного определения содержания процианидинов какао и орехов (общего и пентамера) в пищевых продуктах и пищевых ингредиентах в примерах 4-10. Способ В использовали для количественного определения содержания процианидинов какао очищенных процианидиновых олигомеров какао, представленного в примере 14, и использован в примерах 17-19.
Способ С следует использовать для экстракции и идентификации процианидинов орехов.
ОПРЕДЕЛЕНИЕ ПРОЦИАНИДИНА
Способ А
Экстракты полифенолов какао получали при размельчении 6-7 г образца с использованием аналитической мельницы Tekmar A-10 в течение 5 мин или в случае какао тертого из 6-7 г образца какао тертого без дополнительного размельчения. Затем образец переносят в полипропиленовую центрифужную пробирку емкостью 50 мл, добавляют примерно 35 мл гексана и энергично встряхивают в течение 1 мин. Образец центрифугируют при 3000 об/мин в течение 10 мин, используя центрифугу International Equipment Company IECPR-7000. После декантирования гексанового слоя экстракцию жира повторяют еще дважды. Отвешивают примерно 1 г обезжиренного материала в полипропиленовую центрифужную пробирку емкостью 15 мл и добавляют 5 мл раствора 70% ацетона: 29,5% воды: 0,5% уксусной кислоты. Образец перемешивают в течение примерно 30 сек, используя вортекс-аппарат Scientific Industries Vortex Genie 2, и центрифугируют при 300 об/мин в течение 10 мин на центрифуге IECPR-7000. Затем жидкость фильтруют в небольшую пробирку емкостью 1 мл через фильтр 0,45 мкм Millex-HV.
Экстракты полифенолов какао анализируют в системе для ВЭЖХ Hewlett Packard 1090 Series II, снабженной программируемым флуоресцентным детектором HP model 1046A и диодным детектором. Разделение проводят при 37°С на колонке Supeico Supelcosil LC-Si 5 мкм (250×4,6 мм), соединенной с предохранительной колонкой Supelco Supelguard LC-Si 5 мкм (20×2,1 мм). Процианидины элюируют линейным градиентом в следующих условиях: (время, %А, %В, %С); (0, 82, 14, 4), (30, 67,6, 28,4, 4), (60, 46, 50, 4), (65, 10, 86, 4) с последующим повторным пятиминутным уравновешиванием. Состав подвижной фазы: А = дихлорметан, В = метанол и С = уксусная кислота: вода в объемном соотношении 1:1. Используют скорость потока 1 мл/мин. Компоненты детектируют по флуоресценции, где λвозбуждения=276 нм и λэмиссии=316 нм или в УФ при 280 нм. В качестве внешнего стандарта используют эпикатехин.
Условия для ВЭЖХ
Колонка Supelco Supelcosil LC-Si (5 мкм) (250×4,6 мм) с предохранительной колонкой Supelco LC-Si (5 мкм) (20×2,1 мм)
Детекторы: фотодиодный при 280 нм
Флуоресценция: λвозбуждения=276 нм и λэмиссии=316 нм
Скорость потока: 1 мл/мин
Температура колонки: 37°С
(см. табл.1).
Способ В
В этом способе количественно анализируются мономерные и олигомерные процианидины какао и орехов с использованием высокоэффективной жидкостной хроматографии с нормальной фазой (ВЭЖХ) с флуоресцентным детектированием вместо УФ-детектирования при 280 нм.
Способ ВЭЖХ с нормальной фазой, о котором сообщается Hammerstone et al., "Identification of Procyanidins in Cocoa (Theobroma cacao) and Chocolate Using High Performance Liquid Chromatography/Mass Spectrometry", J. Agric. Food Chems. 47, 2: 490-496 (1/14/99), использовали для разделения и количественного анализа олигомеров вплоть до декамера.
Стандарты процианидинов до декамеров получали экстракцией из какао-бобов, обогащением гель-хроматографией на Sephadex LH-20 и конечной очисткой препаративной ВЭЖХ с нормальной фазой. Чистоту каждой олигомерной фракции оценивали, используя ВЭЖХ в сочетании с масс-спектрометрией.
Затем готовили смешанный стандарт и для каждого олигомерного класса строили калибровочные кривые, используя квадратичную обработку зависимости суммарной площади от концентрации.
Какао-бобы поставлялись центром исследований какао Almirante в Itajuipe, Бразилия.
Стандартными соединениями являются (-)-эпикатехин (Sigma Chemical, St. Louis) и очищенные олигомеры из бразильских какао-бобов.
Процианидины какао экстрагируют путем размельчения свежих семян на высокоскоростной лабораторной мельнице с жидким азотом, пока величина частиц не уменьшается до примерно 90 мкм. Липиды удаляют из 220 г размельченных семян трехкратной экстракцией 1000 мл гексана. Обезжиренное сухое вещество высушивают струей воздуха для получения 100 г не содержащего жира материала. Фракцию, содержащую процианидины, получают экстракцией 1000 мл 70% ацетона в воде по объему. Суспензию центрифугируют в течение 10 мин при 1500×g. Ацетоновый слой декантируют через воронку со стекловатой. Затем водный ацетон повторно экстрагируют гексаном (≈75 мл) для удаления остаточных липидов. Гексановый слой отбрасывают и водный ацетон выпаривают на ротационном испарителе при неполном вакууме при 40°С до конечного объема 200 мл. Водный экстракт высушивают сублимацией для получения примерно 19 г экстрагированного ацетоном материала.
Для постановки гель-хроматографии примерно 2 г ацетонового экстракта суспендируют в 10 мл 70% водного метанола и центрифугируют при 1500×g. Супернатант полуочищают на колонке Sephadex LH-20 (70×3 см), которую предварительно уравновешивают метанолом со скоростью потока 3,5 мл/мин. Через 2,5 ч после внесения пробы каждые 20 мин собирают фракции и анализируют ВЭЖХ на теобромин и кофеин (Clapperton et al., "Polyphenols and Cocoa Flavour", Proceedings, 16th International Conference of Group Polyphenols, Lisbon, Portugal, Grouppe Polyphenols, Norbonne France, Tome II: 112-115, 1992). Как только с колонки элюируют теобромин и кофеин (≈3,5 ч), еще в течение дополнительных 4,5 ч собирают оставшийся элюат и выпаривают на ротационном испарителе в неполном вакууме при 40°С для удаления органического растворителя. Затем экстракт суспендируют в воде и высушивают сублимацией.
Олигомеры процианидинов какао очищают препаративной ВЭЖХ с нормальной фазой. Примерно 0,7 г полуочищенного ацетонового экстракта растворяют в 7 мл ацетона: воды: уксусной кислоты в объемном соотношении 70:29,5:0,5 соответственно. Разделение проводят при комнатной температуре с использованием Supelcosil LC-Si 5 мкм 100 Å (50×2 см). Процианидины элюируют линейным градиентом в условиях, представленных в таблице 2. Разделение олигомеров контролируют в УФ при 280 нм и собирают фракции на ровных участках между пиками, соответствующих олигомерам. Объединяют фракции с одинаковым временем удерживания из нескольких препаративных разделений, выпаривают на ротационном испарителе в неполном вакууме и высушивают сублимацией.
Градиентный профиль препаративной ВЭЖХ с нормальной фазой представлен в табл.2.
Для масс-спектрометрического анализа частично очищенных олигомеров процианидинов какао очищенные фракции анализируют ВЭЖХ/масс-спектрометрией (МС), используя параметры, описанные Lazarus et al., "High Performance Liquid Chromatography/Mass Spectrometry Analysis of Proanthocyanidins in Food Stuffs", J. Agric. Food Chem. (сдана в печать в 1998). Чистоту каждой фракции определяют по площади пика, используя УФ-детектирование при 280 нм в комбинации со сравнительным анализом соотношения распространенности ионов между каждым классом олигомеров. Смешанные стандартные маточные растворы готовят, используя имеющийся в продаже (-)-эпикатехин для мономера и очищенные олигомеры для димеров-декамеров.
Профиль олигомеров смешанного стандартного маточного раствора показан в таблице 3.
Маточные растворы готовят в следующих концентрациях: 20 мг/мл, 10 мг/мл, 5 мг/мл, 2 мг/мл, 1 мг/мл и 0,4 мг/мл.
Пробы (образцы) какао тертого и шоколада экстрагируют, как описано выше, используя только (примерно 8 г пробы) 45 мл гексана. Примерно 1 г обезжиренного материала экстрагируют, как описано выше, 5 мл ацетона: воды: уксусной кислоты. Твердое вещество собирают центрифугированием в течение 10 мин при 1500×g. Затем супернатант отфильтровывают через найлоновый фильтр 0,45 ммкм в пробирку для проб ВЭЖХ для инжектирования. Все обезжиренные пробы взвешивают, экстрагируют и впрыскивают в двух параллелях. Состав жира в какао тертом и шоколаде определяют, используя официальный метод 920.177 АОАС. Необходима незначительная модификация размера пробы, которая состоит в том, что используют 1 г для проб шоколада и 0,5 г для проб какао тертого. Высокоэффективную жидкостную хроматографию процианидинов какао проводят, используя хроматограф HP 1100 Series HPLC (Hewlett Packard, Palo Alto, CA), снабженный автоинжектором, насосом на четыре компонента для ВЭЖХ, нагревателем колонки, флуоресцентным детектором и химической станцией HP ChemStation для сбора данных и управления. Детектирование флуоресценции проводят при длине волны возбуждения 276 нм и волне эмиссии 316 нм. Нормально-фазовое разделение олигомеров процианидинов осуществляют при использовании колонки Phenomenex (Torrance, CA) 5 мкм Lichrosphere silica (25×4,6 мм) при 37°С с объемом впрыскивания 5 мкл. Трехкомпонентная подвижная фаза состоит из А) дихлорметана, В) метанола и С) уксусной кислоты и воды (1:1 объем/объем). Разделение проводят линейным градиентом концентрации В в А с постоянным 4% уровнем С при скорости потока 1 мл/мин следующим образом: элюирование начинают с 14% В в А; 14-28,4% В в А, 0-30 мин; 28,4-39,2% В в А, 30-45 мин; 39,2-86% В в А, 45-50 мин. Колонки повторно уравновешивают между впрыскиваниями эквивалента 25 мл (10 объемов колонки) исходной подвижной фазы.
Для количественного определения процианидинов какао в тертом какао и шоколаде строят калибровочные кривые на основе маточных растворов, используя квадратичную обработку зависимости суммарной площади от концентрации для пиков, соответствующих каждому классу олигомеров.
Способ С
Этот способ используется для определения типа процианидинов в орехах. Мономерные и олигомерные процианидины, присутствующие в орехах, разделяют по степени полимеризации и идентифицируют, используя высокоэффективную жидкостную хроматографию с нормальной фазой (ВЭЖХ) в сочетании с масс-спектрометрией с камерой ионизации в электрическом поле при атмосферном давлении (API-ES).
Сырой арахис был поставлен M&M/MARS (Hackettstown, NY). Сырой миндаль поставила Almond Board of California (Modesto, CA).
Используемыми стандартами являлись (-)-эпикатехин и (+)-катехин (Sigma Chemical, St. Louis, МО).
Колонки для твердо-фазной экстракции (SPE), колонки (Supelcosil Envi-18 емкостью 20 мл от Supelco, Inc., Bellafonte, PA) промывают метанолом 3×5 мл и затем кондиционируют водой 3×5 мл перед нанесением пробы. После нанесения соответствующей пробы и промывания колонки высушивают в вакууме в течение 1-2 мин. Затем колонку для SPE пропитывают 10 мл ацетона, воды и уксусной кислоты в объемном соотношении 70:29,5:0,5 соответственно в течение 1 мин перед элюированием процианидинов с колонки. Для экстракции процианидинов из оболочек арахиса примерно 3,5 г оболочек арахиса измельчают на лабораторной мельнице перед экстракцией в 25 мл ацетона, воды и уксусной кислоты в объемном соотношении 70:29,5:0,5 соответственно. Суспензию центрифугируют в течение 10 мин при 1500×g и супернатант декантируют. К супернатанту добавляют 20 мл воды прежде, чем удаляют органический растворитель на ротационном испарителе в неполном вакууме при 45° С для получения примерно 22 мл водного экстракта. Водный экстракт (22 мл) наносят на предварительно кондиционированную колонку для SPE и промывают 40 мл воды. Затем процианидины элюируют, как описано выше. Для экстракции процианидинов из арахисовой ореховой массы ореховую массу замораживают в жидком азоте и затем измельчают в порошок на лабораторной мельнице. Порошок ореховой массы (≈10 г) экстрагируют три раза 45 мл гексана для удаления липидов. Один грамм полученной обезжиренной ореховой массы экстрагируют 5 мл ацетона, воды и уксусной кислоты в объемном соотношении 70:29,5:0,5 соответственно.
Что касается оболочек миндаля, примерно 24 г оболочек снимают с сырых миндальных орехов, используя бритвенный нож. Оболочки затем дважды обезжиривают 135 мл гексана и центрифугируют в течение 10 мин при 1500×g для получения примерно 14,6 г обезжиренного материала. Обезжиренные оболочки экстрагируют 90 мл ацетона, воды и уксусной кислоты в объемном соотношении 70:29,5:0,5 соответственно. К супернатанту добавляют 30 мл воды и полученный подкисленный водный ацетон выпаривают на ротационном испарителе при неполном вакууме при 45°С до конечного объема 50 мл. Водный раствор наносят на предварительно кондиционированную колонку для SPE, промывают примерно 10 мл воды и процианидины элюируют, как описано выше.
Анализ экстрактов ВЭЖХ/МС проводят, используя хроматограф для ВЭЖХ HP 1100 Series HPLC, как описано в способе В выше, подсоединенный к масс-селективному детектору, HP Series 1100 (model G1946A), снабженному ионизационной камерой API-ES. Через тройник в элюент ВЭЖХ добавляют буферный реагент непосредственно перед масс-спектрометром и доставляют насосом для ВЭЖХ HP 1100 Series HPLC при прохождении через дегазатор. Условия анализа в отрицательном ионном режиме включают ≈0,75 М гидроокиси аммония в качестве буферного агента со скоростью потока 0,04 мл/мин, капиллярное напряжение 3 kV, фрагментатор при 75 V, давление распыления 25 фунтов на квадратный дюйм и температура высушивания газа при 350°С. На HP ChemStation собирают данные, используя как сканорный режим, так и мониторинг выбранных ионов. Спектры сканируют в пределах масс m/z 100-3000 при 1,96 сек на цикл.
Данные масс-спектров ионов оболочек миндаля указывают на присутствие связанных простой связью олигомеров процианидинов до гептамеров, в то время как масс-спектры оболочек арахисовых орехов указывают как на связанные простой, так и двойной связью олигомеры до октамеров. Процианидины не обнаруживаются в ореховой массе арахиса.
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ L-АРГИНИНА
L-Аргинин определяют, используя метод, раскрытый в официальном методе 982.30 АОАС Official Methods of Analysis 91995, Vitamins and Other Nutrients, Chapter 45, p.59-61. Пробу гидролизуют кислотой и каждые из 3-х гидролизатов анализируют, используя параметры, оптимальные для аминокислотного анализатора. Для калибровки анализатора, по меньшей мере, каждые 24 ч используют стандартный раствор L-аргинина. Азот определяют по официальному методу АОАС 955.04С, 920.39А, 976.05А или другому соответствующему методу Кьельдаля. Некорректированное количество г/16 г N вычисляют по: г L-аргинина (некорректированная 16-г проба N = (n моль L-аргинина × первоначальный объем пробы (мл) × молекулярную массу L-аргинина)/(объем вводимой пробы (мл) × массу пробы (г) × %N для пробы × 6,25×105).
Кислотный гидролиз проводят при помещении примерно 0,1 г (взвешивать с точностью до 0,1 мг) пробы в пробирку для гидролиза, добавляют 10 мл 6 н HCl и перемешивают. Смесь замораживают на бане со смесью сухой лед-спирт. Смесь вакуумируют при <50u в течение 1 мин и пробирку запаивают в вакууме. Пробу гидролизуют в течение 24 ч при 110+1°С. Пробирку охлаждают и открывают. Гидролизат фильтруют через бумагу Ватман №1. Пробирку промывают три раза водой и каждую промывную фракцию фильтруют. Фильтрат высушивают при 65°С под вакуумом. Сухой гидролизат растворяют в объеме буфера, пригодном для аминокислотного анализатора. Гидролизат не может храниться более одной недели до анализа.
ПРИМЕРЫ
Нижеследующие примеры предназначены для иллюстрации некоторых предпочтительных вариантов изобретения без ограничения изобретения. Выделенные олигомеры процианидинов какао, использованные в этих примерах 17, 18 и 19, выделяли, используя способ, описанный в патенте США 5554645 (выданный 9/10/96 L. Romanczyk et al.), и дополнительно очищали, используя способ В.
Пример 1
Способ получения полифенолов какао сухого вещества какао из какао-бобов
Имеющиеся в продаже какао-бобы с первоначальным содержанием влаги примерно от 7 до 8% по массе предварительно очищали, используя скальператор (изготовлен Carter Day International, Minneapolis, MN, США). Примерно 600 мешков какао-бобов (39000 кг) предварительно очищали в течение 6,5 ч. Бобы подавали в загрузочный бункер, где скорость потока регулировалась роликом положительной подачи. Бобы подавали на внешнюю сторону вращающегося отсеивающего бурата с ситовой поверхностью из проволочной сетки. Бобы проходили через бурат с ситовой поверхностью из проволочной сетки и затем через воздушную аспирационную камеру, где легкая грязь, пыль и волокна отсасывались из потока продукта. Бобы, которые не прошли через отсеивающий бурат, передавались в поток отбракованного материала. Этот поток отбракованного материала состоял из крупных комков бобов, палок, камней и т.д. Количество полученного отбракованного материала составляло примерно 150 кг или 0,38% от исходного материала. Вес полученного предварительно очищенного продукта составил примерно 38850 кг и далее его пропускали на стадию очистки бобов.
Предварительно очищенные бобы из скальператора затем очищали с помощью воздушного сепаратора с отделением по плотности в псевдоожиженном слое Camas International SV4-5 (AFBDS, произведен Camas International, Pocotello, ID, США). Примерно 38850 кг какао-бобов пропускали в AFBDS в течение примерно 6,5 ч. В аппарате у бобов удаляли в основном все тяжелые примеси, такие как камни, металл, стекло и т.д., а также более мелкие неиспользуемые материалы, такие как пораженные плесенью и зараженные какао-бобы, приводя к получению очищенных бобов, которые в основном содержали только используемые какао-бобы. Полученные удаленные тяжелые примеси весили примерно 50 кг и масса легких неиспользуемых материалов составляла примерно 151 кг. В целом было получено примерно 38649 кг очищенных бобов после обеих стадий предварительной и основной очисток, описанных выше (выход 91% после очистки).
Затем очищенные какао-бобы пропускали через аппарат для нагревания инфракрасными лучами. Используемым аппаратом был электрический вибрирующий инфракрасный микронайзер Micro Red 20 (изготовлен Micronizing Company (Великобритания) Limited, Великобритания). Микронайзер работал со скоростью примерно 1701 кг в ч. Глубина бобов в вибрирующем слое микронайзера равнялась примерно 2 дюйма или составляла примерно глубину в 2-3 боба. Температура поверхности микронайзера была установлена примерно на 165°С, приводя к IBT примерно 135°С, в течение периода времени в пределах от 1 до 1,5 мин. Эта обработка приводила к быстрой сушке какаовеллы и ее отделению от ядра какао-боба. Поскольку в основном все какао-бобы, подаваемые в микронайзер, представляли собой цельные бобы и в основном они были свободны от небольших разбитых кусочков боба или какаовеллы, на стадии нагревания инфракрасными лучами не наблюдали искр и пожара. Разбитые кусочки, отсеянные вибрирующим ситом перед микронайзером, вновь возвращали в поток продукта перед стадией провеивания.
Содержание влаги бобов из микронайзера составляло примерно 3,9% по массе. Бобы, вышедшие из микронайзера при IBT примерно 135°С, немедленно охлаждали до температуры примерно 90°С в течение примерно 3 мин, сводя до минимума дополнительные потери влаги. Общее количество бобов после стадии нагревания составляло примерно 36137 кг.
Затем бобы подвергали провеиванию на веялке Jupiter Mitra Seita (изготовлена Jupiter Mitra Seita, Jakarta, Индонезия). Стадия провеивания приводила к растрескиванию бобов с потерей какаовеллы и отделением более легких оболочек от ядер какао-бобов, в то же время сводя до минимума потерю ядер с потоком отбракованных оболочек. Скорость подачи в веялку составляла примерно 1591 кг в час. Полученный продукт включал примерно 31861 кг используемых ядер и 4276 кг отбракованных оболочек. В целом выход используемых ядер из исходного материала составлял примерно 81,7%.
Полученные ядра какао-бобов прессовали, используя пресс Dupps 10-6 (изготовлен The Dupps Company, Germantown, Ohio, США). Для экстракции масла ядра с ровной постоянной скоростью 1402 кг в 1 ч подавали в два винтовых пресса. Пресс производил примерно 16198 кг какао-масла, которое содержало примерно 10% сухого вещества какао и примерно 15663 кг сухого вещества какао, которое содержало примерно 10% масла.
Какао-масло затем обрабатывали на центрифуге с декантацией Sharples P3000 (изготовлена Jenkins Centrifuge Rebuilders, N. Kansas City, МО, США). Центрифугирование снижало содержание сухого вещества в масле примерно до 1-2% сухого вещества и обеспечивало примерно 13606 кг масла и 2592 кг сухого вещества какао, содержащего примерно 40-45% масла. Масло, содержащее 1-2% сухого вещества, затем обрабатывали, используя пластинчатый и рамный фильтр (изготовлен Jupiter Mitra Seita), который удалял оставшиеся сухие вещества из масла и обеспечивал примерно 13271 кг чистого какао-масла и примерно 335 кг сухого вещества какао, содержащего 40-45% масла.
Сухое вещество какао, выгруженное из центрифуги и фильтра-пресса, содержало примерно 40-45% жира и было подвергнуто прессованию в порционном гидравлическом прессе для получения какао-жмыха с 10% жира. Этот материал давал примерно 1186 кг чистого масла и 1742 кг сухого вещества какао.
Общий выход чистого масла из поступивших бобов составлял 14456 кг или 37,1%. Общее количество сухого вещества, полученное из поступивших бобов, равнялось 17405 кг или 44,6%.
Проба частично обезжиренного сухого вещества какао в какао-порошке, полученном вышеописанным способом из недоферментированных какао-бобов (фактор ферментации 100), содержала следующие концентрации процианидинов: общее содержание процианидинов 32743 мкг/г, процианидин 9433 мкг/г, димер процианидина 5929 мкг/г, тример процианидина 5356 мкг/г, тетрамер процианидина 4027 мкг/г, пентамер процианидина 3168 мкг/г, гексамер процианидина 2131 мкг/г, гептамер процианидина 1304 мкг/г, октамер процианидина 739 мкг/г, нонамер процианидина 439 мкг/г.
Пример 2
Продукция какао тертого, содержащего полифенолы какао
Отбирали соответствующее среднее количество (FAQ) какао-бобов Sulawesi, имеющих первоначальное содержание влаги 7,4% по массе и фактор ферментации 233 (31% сине-серые, 29% пурпурные, 22% пурпурно-коричневые и 17% коричневые) в качестве исходного материала. Затем какао-бобы пропускали через аппарат для нагревания инфракрасными лучами. Используемый аппарат был инфракрасным вибрирующим микронайзером (изготовлен Micronizer Company (Великобритания) Limited, Великобритания). Скорость подачи бобов через инфракрасный нагреватель и угол наклона слоя в инфракрасном нагревателе менялись для регуляции количества тепловой обработки, которое получали бобы. Время, которое бобы провели в инфракрасном нагревателе (время нахождения), определяли углом наклона слоя и скоростью подачи. Периоды времени, используемые для приготовления материалов, перечислены в таблице 4 ниже. Замеряли на выходе микронайзера внутреннюю температуру бобов (IBT), эти значения также представлены в таблице 4.
1 кг Пробы бобов, обработанных в инфракрасном нагревателе, выгруженных из инфракрасного нагревателя при различных значениях IBT, дробили на меньшие кусочки. Это делали для облегчения отделения ядра от какаовеллы. Используемым лабораторным оборудованием для удаления оболочки была дробилка для какао-бобов Limiprimita, изготовленная John Gordon Co. LTD, Англия. Затем раздробленные бобы пропускали через веялку лабораторного масштаба, используя Catador СС-1, изготовленную John Gordon Co. LTD, Англия.
Затем ядра какао-бобов измельчали в какао тертое, используя мельницу Melange, изготовленную Pascall Engineering Со. LTD, Англия. Это устройство разбивает и измельчает ядра в какао тертое. Обычная рабочая температура для какао тертого в Melange составляет примерно 50°С. Этот же способ превращения ядер в какао тертое можно проводить в большем промышленном масштабе, используя другие типы мельниц, такие как Carle & Montanari Mill. Ядра какао-бобов измельчали в Melange в течение одного ч. Концентрацию процианидинов какао определяли для проб по отношению к значениям температуры при инфракрасном нагревании. Эти значения представлены в таблице 4.
Пример 3
Шоколадный пищевой продукт
Для совместного перемешивания ингредиентов в пределах концентраций, приведенных ниже, использовали лопастную мешалку Sigma вместимостью 10 фунтов (изготовлена Teledyne Read Co., York, Pennsylvania). Выбор соответствующих ингредиентов и их количеств внутри данных пределов для приготовления шоколада легко осуществляются специалистом в этой области без чрезмерного экспериментирования.
Лецитин и жир объединяли и перемешивали, используя лопастную мешалку Sigma вместимостью 10 фунтов, до гомогенности массы. Полученную смесь жир/лецитин добавляли к гранулированной сахарозе во вторую мешалку Sigma вместимостью 10 фунтов. Сахарозу, жир и лецитин перемешивали при примерно от 35°С до примерно 90°С пока масса не стала гомогенной. Добавляли оставшиеся ингредиенты, включая какао тертое из примера 2, имеющее высокую концентрацию процианидинов какао, и перемешивали до гомогенности. Полученную смесь рафинировали до микрометрового размера частиц примерно 20 мкм, коншировали, стандартизировали. Концентрация пентамера процианидина какао в полученном шоколаде находилась в пределах примерно от 385 до 472 мкг на г шоколада.
Добавляли арахис в количестве примерно 5-30% по массе конечного продукта с получением шоколадсодержащего арахисового продукта с высоким уровнем процианидинов какао и L-аргинина.
Пример 4
Пищевой продукт с арахисовым маслом.
Предварительно обжаренный арахис измельчают с добавлением соли и сахара по желанию для получения арахисового масла. При перемешивании к смеси добавляют какао-порошок из примера 1, который имеет высокое содержание процианидинов какао, в количестве примерно 2-3% по массе всей смеси. Продукт является арахисовым маслом, содержащим полифенолы какао и L-аргинин.
Пример 5
Фармацевтическая композиция
Готовят смесь для таблетирования, которая включает следующие ингредиенты (проценты, выраженные в весовых процентах)
Какао-порошок, ванильный экстракт и L-аргинин смешивают вместе в пищевом процессоре в течение нескольких минут. Сахара и магний стеарат осторожно перемешивают друг с другом, смешивая затем со смесью какао-порошка/ванильного экстракта/L-аргинина. Этот материал помещают в пресс для таблетирования Manesty (B3B) при максимальном давлении и сжатии для получения круглых таблеток (15 мм × 5 мм) с массой от 1,5 до 1/8 г.
Пример 6
Темный шоколад
Темный шоколад готовят способом, в основном аналогичным способу, описанному в примере 3, используя следующую общую рецептуру:
Уровень ингредиента (вес.%)
15-35% сахароза
40-75% какао тертое с высоким содержанием СР из примера 2
1-10% какао тертое с высоким содержанием СР из примера 1
1-10% жир
0,01-0,05% ванилин
0,1-1,0% лецитин.
К темному шоколаду добавляют арахис в количестве примерно от 5 до 30% по массе всего продукта.
Пример 7
Молочный шоколад
Молочный шоколад готовят способом, в основном аналогичным способу, описанному в примере 3, используя следующую общую рецептуру:
Уровень ингредиента (вес.%)
35-55% сахароза
12-25% молочный ингредиент
10-25% какао тертое с высоким содержанием СР из примера 2
15-25% жир
0,1-1,0% эмульгатор
К шоколаду добавляют миндаль в количестве примерно от 5 до 30% по массе всего продукта.
Пример 8
Арахисовое масло - соевое печенье в брикетах, глазированное темным шоколадом с высоким содержанием СР
Арахисовое масло готовят смешением арахиса, сахара, растительного масла и пропилгаллата. Печенье готовят при объединении соевой муки, воды, растительного масла и натрия бикарбоната и выпечке. На выпеченное печенье затем выдавливают арахисовое масло и затем весь брикет глазируют темным шоколадом с высоким содержанием СР.
Ниже приводятся теоретические концентрации процианидина и аргинина, основываясь на содержании процианидинов какао, процианидинов орехов и аргинина в ингредиентах по рецептуре:
Пример 9
Сухая смесь для приготовления напитка с высоким содержанием СР какао и L-аргинина
Сухую смесь для приготовления напитка, содержащую какао-порошок из примера 1, имеющего повышенное содержание полифенолов какао (CPs) и L-аргинина, готовят по следующей рецептуре:
Сухие ингредиенты дозируют согласно вышеуказанной рецептуре и перемешивают в течение 1 ч на кухонной профессиональной мешалке (Model KSM50P), используя проволочную взбивалку на скорости #2. Лецитин агломерируют перед использованием по рецептуре в агломераторе Niro-Aeromatic Agglomerator (Model STREA/1).
Ниже представлены теоретические концентрации процианидинов и L-аргинина, основываясь на содержании процианидина какао, процианидина орехов и аргинина в ингредиентах по рецептуре:
Пример 10
Ореховые и семенные брикеты с экстрактом какао
Миндаль слегка подрумянивают в соленом масле. Добавляют семена тыквы пепо, семена подсолнечника и семена кунжута. Объединяют масло, кукурузную патоку, лецитин и соль и нагревают в микроволновой печи на 1/2 мощности в течение 1 мин. Сахар помещают в кастрюлю из нержавеющей стали и нагревают на индукционном варочном аппарате на полной мощности. Когда сахар почти полностью расплавлен, нагревание уменьшают до средней мощности (290°F) и сахар нагревают, пока он полностью не расплавится и не приобретет цвет меда. Когда сахар полностью расплавится, его медленно добавляют к смеси кукурузной патоки/масла и перемешивают. Ореховую смесь помещают в настольную мешалку. Сироп медленно выливают в ореховую смесь при перемешивании лопастями на небольшой скорости. Смесь орехов/сиропа формируют в брикеты и охлаждают.
Ниже приведены теоретические концентрации процианидинов и аргинина, основываясь на содержании процианидинов какао, процианидинов орехов и аргинина в ингредиентах по рецептуре:
Пример 11
Арахис, карамель, нуга, брикет, глазированный темным шоколадом с высоким содержанием СР
Смесь нуги готовят так, что она содержит 45% арахиса, и раскатывают на охлаждающемся столе и режут на прямоугольные брикеты. Готовят карамельную смесь, которая содержит примерно 38% арахиса, охлаждают и режут на одинаковые кусочки. Нугу покрывают сверху пластом карамели, и брикет целиком глазируют в шоколаде, который содержит примерно 10% арахиса.
Ниже представлены теоретические концентрации процианидинов и L-аргинина, основываясь на содержании процианидинов какао, процианидинов орехов и аргинина в ингредиентах по рецептуре:
Пример 12
Источник какао и способ получения
Получали какао Theobroma, относящихся к нескольким генотипам, которые представляют три общепризнанные садовые расы какао (Enriquez, 1967; Engels, 1981) из трех основных регионов мира, производящих какао. Перечень этих генотипов представлен в таблице 5. Также в данном случае пригодны для использования другие виды какао Theobroma и тесно связанный с ними род Herranina.
Собранные какао-стручки вскрывали и недоферментированные бобы с пульпой извлекали и замораживали. Пульпу удаляли вручную. Бобы лущили вручную и измельчали до мелкой порошкообразной массы на мельнице Tekmar. Полученную массу затем обезжиривали в течение ночи в аппарате Сокслета, используя перегнанный гексан в качестве растворителя. Оставшийся растворитель удаляли из обезжиренной массы в вакууме при комнатной температуре.
Пример 12
Способы экстракции процианидинов
А. Способ 1
Процианидины экстрагировали из обезжиренных, недоферментированных, высушенных сублимацией какао-бобов из примера 11, используя метод, описанный Jalal and Collin (1977) в модификации. Процианидины экстрагировали из 50-г партий обезжиренной какао-массы 2400 мл 70% ацетона/деионизированной воды, затем 400 мл 70% метанола/деионизированной воды. Экстракты объединяли и растворители удаляли отгонкой при 45°С на ротационном испарителе в неполном вакууме. Полученную водную фазу разбавляли до 1 л деионизированной водой и экстрагировали 2 раза 400 мл CHCl3. Растворитель отбрасывали. Водную фазу затем экстрагировали 4 раза 500 мл этилацетата. Любую эмульсию разбивали центрифугированием на центрифуге Sorvall RC 28S при 2000×g в течение 30 мин при 10°С с ротационным испарителем в вакууме. Полученную водную фазу замораживали в жидком азоте, затем сушили сублимацией на установке для сублимационной сушки LABCONCO. Выходы сырых процианидинов, полученные из какао различных генотипов, перечислены в таблице 6.
В. Способ 2
Альтернативно процианидины экстрагировали из обезжиренных, недоферментированных, высушенных сублимацией какао-бобов из примера 1 70%-водным ацетоном. 10 г обезжиренного материала суспендировали в 100 мл растворителя в течение 5-10 мин. Суспензию центрифугировали в течение 15 мин при 4°С при 3000×g и супернатант пропускали через стекловату. Фильтрат подвергали перегонке при неполном вакууме и полученную водную фазу замораживали в жидком N2 с последующим высушиванием сублимацией на установке для сублимационной сушки LABCONCO. Выходы сырых процианидинов находились в пределах 15-20%.
Полагается, что различия в выходах сырых веществ отражают вариации, связанные с различными генотипами, географическим происхождением, садовой расой и способом получения.
Пример 13
Частичная очистка процианидинов какао
А. Гель-хроматография
Процианидины, полученные в примере 12, частично очищали жидкостной хроматографией на Sephadex LH-20 (28×2,5 см). Разделение проводили ступенчатым градиентом от деионизированной воды к метанолу. Исходная градиентная композиция начиналась с 15% метанола в деионизированной воде с последующим ступенчатым возрастанием каждые 30 мин, 25% метанолом в деионизированной воде, 35% метанолом в деионизированной воде, 70% метанолом в деионизированной воде и наконец 100% метанолом. Собирали элюент после элюирования ксантиновых алкалоидов (кофеина и теобромина) в виде одной фракции. Фракция давала свободную от ксантиновых алкалоидов субфракцию, которую подвергали дополнительному субфракционированию для получения пяти субфракций, обозначенных от ММ2А до ММ2Е. Растворитель удаляли из каждой субфракции отгонкой при 45°С на ротационном испарителе, проводимой при неполном вакууме. Полученную водную фазу замораживали в жидком N2 и сушили в течение ночи сублимацией на установке для сублимационной сушки LABCONCO.
Условия хроматографии: колонка Sephadex LH-20 28×2,5 см, подвижная фаза: ступенчатый градиент метанол/вода 15:85, 25:75, 35:65, 70:30, 100:0 при ступенчатом переходе с интервалами в 1/2 ч, скорость потока 1,5 мл/мин, УФ детектор при λ1=254 нм и λ2=365 нм, скорость бумаги: 9,5 мм/мин, нанесение на колонку: 120 мг.
В. Полупрепаративная высокоэффективная жидкостная хроматография (ВЭЖХ)
Способ 1. Разделение на обращенной фазе
Процианидины, полученные в примере 2 и/или 3А, частично очищали полупрепаративной ВЭЖХ. Система для ВЭЖХ Hewlett Packard 1050, снабженная детектором с переменной длиной волны, инжекторным клапаном Rheodyne 7010 с инжекторной петлей емкостью 1 мл соединяли коллектором фракций Pharmacia FRAC-100. Разделение проводили на колонке Phenomenex Ultracarb™ 10 мкм ODS (250×22,5 мм), соединенной с предохранительной колонкой Phenomenex 10 мкм ODS Ultracarb™ (60×10 мм). Состав подвижной фазы: А = вода; В = метанол, использовали в следующих условиях линейного градиента: [время, %А]; (0, 85), (60, 50), (90, 0) и (110, 0) при скорости потока 5 мл/мин. Соединения детектировали в УФ при 254 нм.
Способ 2. Нормально-фазовое разделение
Экстракты процианидинов, полученные в примерах 2 и/или 3а, частично очищали полупрепаративной ВЭЖХ. Систему для ВЭЖХ Hewlett Packard 1050, детектор Millipore-Waters Model 480 LC, установленный на 254 нм, соединяли с коллектором фракций Pharmacia Frac-100, установленным в режиме пиков. Разделение проводили на колонке Supeico Supelcosil LC-Si 5 мкм (250×10 мм), соединенной с предохранительной колонкой Supelco Supelguard LC-Si 5 мкм (20×4,6 мм). Процианидины элюировали линейным градиентом в следующих условиях: (время: %А, %В); (0, 12, 14), (30, 67,6, 28,4), (60, 46, 50), (65, 46, 50), (65, 10, 86), (70, 10, 86) с последующим 10-мин повторным уравновешиванием. Состав подвижной фазы: А = дихлорметан; В = метанол и С = уксусная кислота:вода (1:1). Использовали скорость потока 3 мл/мин. Компоненты детектировали в УФ при 254 нм и записывали самописцем Kipp & Zonan BD41. Объем внесения находился в пределах 100-250 мкл экстракта 10 мг процианидина, растворенного в 0,25 мл 70% водного ацетона.
Отдельные пики или выбранные участки хроматограммы собирали в определенные интервалы времени или вручную при сборе фракций для дополнительной очистки и последующей оценки.
Условия ВЭЖХ: полупрепаративная колонка Supelco
Supelcosil LC-Si (5 мкм) (250×10 мм)
предохранительная колонка Supelco
Supelcosil LC-Si (5 мкм) (20×4,6 мм)
Детектор: Waters LC
Спектрофотометр Model 480@ 254 нм
Скорость потока: 3 мл/мин
Температура колонки: комнатная
Внесение: 250 мкл 70% водного ацетонового экстракта (см. табл.7).
Пример 14
Способы очистки на основе ВЭЖХ
Способ А. Очистка гель-хроматографией
Процианидины, полученные в примере 12, частично очищали жидкостной хроматографией на Sephadex LH 20 (72,5×2,5 см), используя 100% метанол в качестве элюента, со скоростью потока 3,5 мл/мин. Фракции элюента собирали после первых 1,5 ч, и фракции концентрировали на ротационном испарителе, повторно растворяли в воде и сушили сублимацией. Эти фракции относились к фракциям, обогащенным пентамером. Примерно 2,00 г экстракта, полученного в примере 2, субфракционировали этим способом. Результаты представлены в таблице 8.
Способ В. Нормально-фазовое разделение
Процианидины, полученные как в примере 12, разделяли, очищали нормально-фазовой хроматографией на Supelcosil LC-Si, 100 А, 5 мкм (250×4,6 мм) со скоростью потока 1,0 мл/мин или альтернативно на Lichrosphere Silica 100, 100 A, 5 мкм (235×3,2 мм) со скоростью потока 0,5 мл/мин. Разделение проводили ступенчатым градиентом в следующих условиях: (время, %А, %В); (0, 82, 14), (30, 67,6, 28,4), (60, 46, 50), (65, 10, 86), 70, 10, 86). Состав подвижной фазы: А = дихлорметан; В = метанол и С = уксусная кислота: вода (1:1). Компоненты детектировали по флуоресценции, где λвозвуждения=276 нм и λэмиссии=316 нм или в УФ при 280 нм. Объем введения 5,0 мкл (20 мг/мл) процианидинов, полученных в примере 2.
Альтернативно разделение проводили ступенчатым градиентом в следующих условиях: (время, %А, %В); (0, 76, 20), (25, 46, 50), (30, 10, 86). Состав подвижной фазы: А = дихлорметан; В = метанол и С = уксусная кислота: вода (1:1).
Способ С. Разделение на обращенной фазе.
Процианидины, полученные как в примере 12, разделяли и очищали обращенно-фазовой хроматографией на колонке Hewlett Packard Hypersil ODS 5 мкм (200×2,1 мм) и предохранительной колонке Hewlett Packard Hypersil ODS 5 мкм (20×2,1 мм). Процианидины элюировали линейным градиентом 20% В в А в течение 20 мин, затем колонку промывали 100% В со скоростью 0,3 мл/мин. Состав подвижной фазы: дегазированная смесь В = 1,0% уксусной кислоты в метаноле и А = 2,0% уксусной кислоты в воде, очищенной на нанофильтре. Компоненты детектировали в УФ при 280 нм и по флуоресценции, где λвозбуждения=276 нм и λэмиссии=316 нм; объем введения составлял 2,0 мкл (20 мг/мл).
Пример 15
Разделение ВЭЖХ фракций, обогащенных пентамером
Способ А. Полупрепаративная ВЭЖХ с нормальной фазой
Фракции, обогащенные пентамером, дополнительно очищали полупрепаративной ВЭЖХ с нормальной фазой в системе для ВЭЖХ Hewlett Packard 1050, снабженной детектором Millipore - Waters model 480 LC при 254 нм, которая была соединена с коллектором фракций Pharmacia Frac-100, установленным в режиме пиков. Разделение проводили на колонке Supeico Supelcosel LC-Si, 5 мкм 100 А (250×10 мм), соединенной с предохранительной колонкой Supelco Supelguard LC-Si 5 мкм (20×4,6 мм). Процианидины элюировали линейным градиентом в следующих условиях: (время, %А, %В); (0, 82, 14), (30, 67,6, 28,4), (60, 46, 50), (65, 10, 86), (70, 10, 86) с последующим 10-мин повторным уравновешиванием. Состав подвижной фазы: А = дихлорметан; В = метанол и С = уксусная кислота: вода (1:1). Использовали скорость потока 3 мл/мин. Компоненты проектировали в УФ при 254 нм и записывали самописцем Kipp & Zonan BD41. Объемы введения находились в пределах 100-250 мкл экстрактов 10,0 мг процианидинов, растворенных в 0,25 мл 70% водного ацетона. Отдельные пики или выбранные участки хроматограммы были собраны в определенные интервалы времени или вручную при сборе фракций для дальнейшей очистки и последующей оценки.
Условия ВЭЖХ: полупрепаративная колонка Supelco
Supelcosil LC-Si (5 мкм) (250×100 мм)
предохранительная колонка Supelco
Supelcosil LC-Si (5 мкм) (20×4,6 мм)
Детектор: Waters LC
Спектрофотометр Model 480@ 254 нм
Скорость потока: 3 мл/мин
Температура колонки: комнатная
Введение: 250 мкл экстракта, обогащенного пентамером (см. табл.9).
Способ В. Разделение на обращенной фазе
Экстракты процианидинов, полученные как в примере 15, фильтровали через найлоновый фильтр 0,45 мкм и анализировали в трехкомпонентной системе для ВЭЖХ Hewlett Packard 1090, снабженной диодным детектором и программируемым флуоресцентным детектором HP model 1046A. Разделение проводили при 45°С на колонке Hewlett Packard Hypersil ODS 5 мкм (200×2,1 мм). Процианидины элюировали линейным градиентом 60% В в А, затем колонку промывали В со скоростью 0,3 мл/мин. Состав подвижной фазы: дегазированная смесь В = 0,5% уксусной кислоты в метаноле и А = 0,5% уксусной кислоты в воде, пропущенной через нанопоровый фильтр. Содержание уксусной кислоты в подвижных фазах А и В можно повысить до 2%. Компоненты детектировали по флуоресценции, где λвозбуждения=276 нм и λэмиссии=316 нм и в УФ при 280 нм. Концентрации (+)-катехина и (-)-эпикатехина определяли по отношению к растворам стандартов. Концентрации процианидинов определяли, используя поправочный коэффициент для (-)-эпикатехина.
Способ С. Нормально-фазовое разделение
Экстракты процианидинов, обогащенные пентамером, полученные как в примере 15, фильтровали через найлоновый фильтр 9,45 мкм и анализировали в системе для ВЭЖХ Hewlett Packard 1090, Series II, снабженной программируемым флуоресцентным детектором HP Model 1046A и диодным детектором. Разделение проводили при 37°С на колонке Phenomenex Lichrosphere Silica 100 5 мкм (250×3,2 мм), соединенной с предохранительной колонкой Supelco Supelguard LC-Si 5 мкм (20×4,6 мм). Процианидины элюировали линейным градиентом в следующих условиях: (время, %А, %В); (0, 82, 14), (30, 67,6, 28,4), (60, 46, 50), (65, 10, 86), (70, 10, 86) с последующим 8-мин повторным уравновешиванием. Состав подвижной фазы: А = дихлорметан; В = метанол и С = уксусная кислота; вода в объемном соотношении (1:1). Использовали скорость потока 0,5 мл/мин. Компоненты детектировали по флуоресценции, где λвозбуждения=276 нм и λэмиссии=316 нм или в УФ при 280 нм.
Аналогичный профиль ВЭЖХ получали с другими Theobroma, Herrania и/или их меж- или внутривидовыми гибридами.
Условия ВЭЖХ: колонка хеноменекс Lichrosphere Silica
100 (5 мкм) 250×3,2 мм
предохранительная колонка Supelco
Supelguard LC-Si (5 мкм) 20×4,6 мм
Детекторы: фотодиодный @ 280 нм
Флуоресценция λвозбуждения=276 нм и λэмиссии = 316 нм
Скорость потока: 9,5 мл/мин
Температура колонки: 37°С
Динамика подвижной фазы:
(см. табл.10).
Способ D. Препаративное нормально-фазовое разделение
Фракции, обогащенные пентамером, полученные, как в примере 5, дополнительно очищали препаративной нормально-фазовой хроматографией способом Riguad et al. в модификации (J. Chrom. 654: 255-260 (1993)).
Разделение проводили при комнатной температуре на колонке 5 мкм Supelcosil LC-Si 100A (50×2 см) с соответствующей предохранительной колонкой. Процианидины элюировали линейным градиентом в следующих условиях: (время, %А, %В, скорость потока); (0, 92,5, 7,5, 10), (10, 92,5, 7,5, 40), (30, 91,5, 18,5, 40), (145, 88, 22, 40), (150, 24, 86, 40), (155, 24, 86, 50), (180, 0, 100, 50). Перед использованием компоненты подвижной фазы смешивали по следующей прописи:
Приготовление растворителя А (82% CH2Cl2, 14% метанола, 2% уксусной кислоты, 2% воды):
1. Отмерить 80 мл воды и вылить в бутыль емкостью 4 л.
2. Отмерить 80 мл воды и вылить в ту же бутыль емкостью 4 л.
3. Отмерить 560 мл метанола и вылить в ту же бутыль емкостью 4 л.
4. Отмерить 3280 мл метиленхлорида и вылить в ту же бутыль емкостью 4 л.
5. Закрыть бутыль крышкой и хорошо перемешать.
6. Продуть смесь гелием высокой чистоты в течение 5-10 мин для дегазирования.
Повторить стадии 1-6 два раза для получения 8 объемов растворителя А.
Приготовление растворителя В (96% метанола, 2% уксусной кислоты, 2% воды):
1. Отмерить 80 мл воды и вылить в бутыль емкостью 4 л.
2. Отмерить 80 мл уксусной кислоты и вылить в ту же бутыль емкостью 4 л.
3. Отмерить 3840 мл метанола и вылить в ту же бутыль емкостью 4 л.
4. Закрыть бутыль крышкой и хорошо перемешать.
5. Продуть смесь гелием высокой чистоты в течение 5-10 мин для дегазирования.
Повторить стадии 1-5 для получения 4 объемов растворителя В. Состав подвижной фазы: А = метиленхлорид с 2% уксусной кислоты и 2% воды; В = метанол с 2% уксусной кислоты и 2% воды. На колонку вносили 0,7 г в 7 мл. Компоненты детектировали в УФ при 254 нм.
Условия ВЭЖХ:
Колонка 5 мкм Supercosil LC-Si 50×2 см при комнатной температуре
Подвижная фаза: А = метиленхлорид с 2% уксусной кислоты и 2% воды
В = метанол с 2% уксусной кислоты и 2% воды.
Профиль градиента/потока представлен в табл.11.
Пример 16
Очистка олигомерных фракций
Способ А. Очистка полупрепаративной ВЭЖХ на обращенной фазе
Процианидины, полученные в примере 15, способы А, В и С, разделяли дополнительно для получения экспериментальных количеств олигомеров. Систему для ВЭЖХ Hewlett Packard 1050, снабженную детектором с переменной длиной волны, инжекторным клапаном Rheodyne 7010 с инжекторной петлей емкостью 1 мл, соединяли с коллектором фракций Pharmacia Frac-100. Разделение проводили на колонке Phenomenex Ultracarb® 10 мкм ODS (250×22,5 мм), соединенной с предохранительной колонкой Phenomenex 10 мкм ODS Ultracarb® (60×10 мм). Состав подвижной фазы: А = вода; В = метанол, используют в следующих условиях линейного градиента; (время, %А); (0, 85), (60, 50), (90, 0) и (110, 0) при скорости потока 5 мл/мин. Отдельные пики или выбранные участки хроматограммы были собраны в определенные интервалы времени или вручную при сборе фракций для дальнейшей оценки MADLY-OF/MS и NKr. Вводимые количества находились в пределах 25-100 мг материала.
Способ В. Модифицированная полупрепаративная ВЭЖХ
Процианидины, полученные в примере 15, способы А, В и D, дополнительно разделяли для получения экспериментальных количеств олигомеров или дополнительной структурной идентификации и выяснения (например, примеры 15, 18, 19 и 20). Колонка Supelcosil LC-Si 5 мкм (250×10 мм) с предохранительной колонкой Supelcosil LC-Si 5 мкм (20×2 мм). Разделение проводили со скоростью потока 3,0 мл/мин при комнатной температуре. Состав подвижной фазы: А = дихлорметан; В = метанол и С = уксусная кислота: вода (1:1) используют в следующих условиях линейного градиента: (время, %А, %В); (0, 82, 14), (22, 74, 21), (60, 74, 21), (60, 74, 50, 4), (61, 82, 14) с последующим 7-мин повторным уравновешиванием. Объем внесения составил 60 мкл, содержащий 12 мг обогащенного пентамера. Компоненты детектировали в УФ при 280 нм.
Пример 17
Оценка активности синтазы окиси азота
Используемой культуральной средой была среда 200 (Cascade Biologics Inc.) с добавлением ростовой добавки с низким содержанием сыворотки (Cascade Biologics Inc.) и 20% фетальной сыворотки теленка (DAP).
Процианидинами какао для оценки были мономер, димер, тример, тетрамер, пентамер и гептамер эпикатехина. Определяли уровень нитритов в процианидинах какао. При максимальной используемой концентрации (100 мкг/мл) нитриты не были обнаружены.
Приобретали эндотелиальные клетки пупочной вены человека (HUVEC) на первичной стадии культивирования в Cascade Biologics Inc. (Портлэнд). Клетки культивировали в среде с добавлением ростовой добавки с низким содержанием сыворотки и 20% фетальной сыворотки теленка (FCS) в матрасах емкостью 75 см2. Клетки высевали в течение недели после обработки трипсином-ЭДТА (2 мл/матрас) при 37°С в атмосфере CO2. Трипсин нейтрализовали добавлением 3 мл FCS.
Суспензию клеток центрифугировали в течение 10 мин при 1200 об/мин и клеточный осадок повторно суспендировали в культуральной среде, описанной выше.
Активность синтазы окиси азота оценивали по определению концентрации нитритов в культуральной среде. HUVEC использовали между пассажами 2-13. Клетки культивировали в 24-луночных культуральных планшетах в концентрации 5×105 клеток в мл среды 200, содержащей LSGS (300 мкл на лунку) и 20% CS. Через 24-48 ч инкубации при 37°С в атмосфере 5% CO2использовали слившиеся клетки (2,5×106 клеток). Среду удаляли и добавляли свежую.
К культуральной среде добавляли мономер и олигомеры процианидина в концентрации 100 мкг/мл, 10 мкг/мл или 1 мкг/мл (конечная концентрация). Контроли состояли из клеток, культивированных без процианидинов. Стандарты включали ацетилхолин, иономицин (стимулятор NO-синтазы через регуляцию поступления кальция), липополисахарид (индуктор NO-синтазы) и N-метил-L-аргинин ацетат (ингибитор NO-синтазы). Стандарты использовали для того, чтобы показать продукцию нитритов в результате синтеза NO эндотелиальными клетками.
Продукцию NO оценивали путем определения концентрации нитритов (NO2) в культуральных супернатантах по реакции Griess. Кратко, 50 мкл кондиционированной среды инкубировали со 150 мкл реагента Griess (1% сульфаниламид в 30% уксусной кислоте/0,1% N-(1-нафтил)этилендиамин дигидрохлорид в 60% уксусной кислоте) при комнатной температуре в течение 2 мин. Измеряли поглощение при 450 нм в мультискане Labsystems МСС/340. Концентрацию нитритов определяли, используя нитрит натрия в качестве стандарта, и анализировали при использовании программного обеспечения ΔSOFT 2.12. Свободная от клеток среда и 100 мкг/мл процианидинов не содержали детектируемых концентраций нитритов.
Необработанные данные1: демонстрация эффекта процианидинов какао на продукцию окиси азота в HUVEC (13 опытов) представлены в табл.12.
Нестимулированные HUVEC продуцировали 2,6±0,3 мкМ NO в течение 48-часового инкубационного периода. Ацетилхолин в количестве 10 мкМ был неэффективен в индукции образования окиси азота в HUVEC. В противоположность, иономицин (1 мкМ) и липополисахарид (100 нг/мл) приводили к заметной продукции окиси азота. Эта продукция окиси азота в HUVEC блокировалась N-метил-L-аргинином при добавлении к инкубационной среде.
Димер, пентамер и гептамер процианидина какао усиливали в зависимости от дозы продукцию NO в HUVEC. Максимальную выработку наблюдали при самой высокой тестированной концентрации, т.е. 100 мкг/мл. Мономер, тример и тетрамер процианидина также приводили к заметной продукции, но только в концентрации 100 мкг/мл. Эффективность различных процианидинов в самой высокой использованной дозе находилась в следующем порядке: димер > тример > гептамер = пентамер = тетрамер > мономер.
Пример 18
NO-Зависимая гипертония у морских свинок
Морских свинок (с массой примерно 400 г, самцы и самки) анестезировали введением пентобарбитала натрия в дозе 40 мг/кг. На сонную артерию накладывали канюлю для мониторинга артериального кровяного давления с помощью датчика давления Gould (Model P4500). Каждый из шести процианидинов какао вводили внутривенно в яремную вену в концентрации 1, 3, 10 и 25 мг/кг. Изменения кровяного давления записывались на полиграф.
В предварительных опытах (2 животных) установили, что дозу 100 мг/кг использовать невозможно, поскольку носитель, содержащий ДМСО, оказывает прямое действие на среднее артериальное кровяное давление. Не было отмечено заметного эффекта носителя, содержащего ДМСО, когда использовали дозу процианидинов какао 25 мг/кг (15± 5%).
Исследовали влияние введения процианидинов какао в дозах 1, 3, 10 или 25 мг/кг на артериальное давление у анестезированных морских свинок. При внутривенном введении мономер и димер процианидина вызывали снижение кровяного давления примерно на 20%, т.е. этот эффект незначительно отличался от введения одного растворителя (15±5%, n=5). В противоположность тример, пентамер и гексамер процианидина (10 мг/кг) индуцировали заметное снижение артериального кровяного давления, т.е. до 62-85% для тетрамера и гексамера процианидина какао. Порядок расположения различных процианидинов какао по эффективности при введении в самой высокой использованной дозе был следующим: гексамер = тетрамер > пентамер > тример (см. табл.13).
Сравнение результатов опытов in vitro и in vivo показывает следующий порядок расположения процианидинов по эффективности:
Продукция NO (100 мкг/мл): димер > тример > гексамер = пентамер = тетрамер > мономер.
Продукция NO (10 мкг/мл): пентамер, тетрамер и димер (слабая индукция).
Гипотония: гексамер = тетрамер > пентамер > тример > димер = мономер.
За исключением димера гептамер или тетрамер, которые индуцировали продукцию NO в более низкой дозе, были наиболее эффективными в индукции снижения артериального кровяного давления. На основании этих результатов можно высказать предположение, что процианидины какао могут индуцировать in vitro продукцию NO, коррелирующую в условиях in vivo.
Пример 19
Кольца аорты от новозеландских белых кроликов помещали в баню для органов емкостью 20 мл. Зависимая от эндотелия релаксация (EDR) на однократную дозу процианидина какао (10-5М) и ацетилхолина (Ach) была показана на параллельных кольцах, предварительно сокращенных под действием процианидинов какао норепинефина (NE) (10-5 М). Тестируемыми процианидинами какао были мономер, димер, тример, тетрамер, пентамер, гексамер. Из них только пентамер, гексамер и гептамер показали сосудорасширяющую активность. Из двух смесей процианидинов какао только содержащая пентамер-декамер (combo-2) показала значительную EDR, в то время как другая смесь (combo-1), которая включала мономер-тетрамер, не имела эффекта на тонус сосудов.
Как combo-2, так и пентамер затем использовали для демонстрации зависимой от дозы вазорелаксации (10-8-10-5 М). Кольца инкубировали в течение 30' с этими процианидинами какао (10-5 М) и повторно тестировали с Ach и процианидинами какао (10-7-10-4 М). Инкубация ткани с этим(и) процианидином(ами) какао уменьшала EDR, резко вызванную как под действием процианидинов какао, так и Ach. Максимальная релаксация на предварительное инкубирование с Ach составляла 49±5%; после инкубации с пентамером, 2±1,4%; после инкубирования с combo-2, 0,8±0,8%: на предварительное инкубирование с пентамером 46,5±4,5%; после инкубирования - 6,8±3,2%: на предварительное инкубирование с combo-2 54,3±7%; после инкубирования 1,7±1,1%, n=5).
Действие инкубирования с обоими процианидинами (т.е. снятие EDR) частично восстанавливалось при инкубировании тканей с L-аргинином (10-4 М) в течение 30' (максимальная релаксация на Ach: после L-аргинина, 21,5±6%, после combo-2, после L-аргинина, 13,7±2,6%: на пентамер; после инкубирования с пентамером, после L-аргинина, 18,3±5,8%: на combo-2; после инкубирования combo-2, после L-аргинина, 5,5±2,8%, n=5). На основании этих данных можно предположить, что расход субстрата для NO-синтазы может быть ответственным за этот эффект.
Вышеуказанные результаты представлены в таблицах 14-17.
Вышеприведенные обнаруженные данные показывают, что из вышеуказанных процианидинов какао только тример способен вызывать вазорелаксацию и что процианидины какао оказывают дискретное действие на тонус сосудов, которое, вряд ли, связано с антиокислительной активностью.
Другие вариации и модификации, которые будут очевидны для специалистов в этой области, находятся в объеме и положениях этого изобретения. Это изобретение не ограничивается за исключением последующей формулы изобретения.
Реферат
Изобретение относится к продуктам, содержащим полифенолы и L-аргинин, которые оказывают положительное воздействие на здоровье млекопитающих, а также относится к медицине и касается лечения сердечно-сосудистых заболеваний. Пищевой продукт и фармацевтические композиции содержат процианидин(ы) какао и/или орехов в комбинации с L-аргинином. Они являются эффективными для индукции физиологического усиления продукции окиси азота у млекопитающего, получающего продукт. Пищевой продукт в одном варианте может не содержать шоколад, в другом варианте может содержать шоколад, в третьем варианте может содержать процианидин орехов. В качестве шоколада используют темный или молочный шоколад, содержащий орехи. Процианидины используют натуральные или синтетические. L-аргинин используют натуральный или синтетический. В качестве источника L-аргинина могут быть использованы ореховые массы, ореховые пасты и/или ореховая мука, семена, пасты из семян и/или мука из семян или желатин. Указанные композиции используют также в способах лечения сердечно-сосудистых заболеваний при расчете эффективной дозы по содержанию процианидина. Изобретение обеспечивает благоприятное воздействие на организм, в частности вазорелаксацию. 10 н. и 97 з.п. ф-лы, 17 табл.
Формула









Комментарии