Способ производства винилхлорида из этана и этилена (варианты) - RU2259990C2
Код документа: RU2259990C2
Чертежи

Описание
Настоящее изобретение направлено на устройство и способ производства мономера винилхлорида (VCM) из этана и этилена. В особенности, настоящее изобретение направлено на способы производства мономера винилхлорида, где (1) во входных потоках в соответствующий реактор присутствуют значительные количества как этана, так и этилена, (2) хлористый водород в потоке, выходящем из реактора, только частично извлекается из выходного потока при работе первого узла после стадии или ступени реакции превращения этана/этилена в винил и (3) часть остатка хлористого водорода рециклируется в реактор в потоке рециклируемого газа.
Винилхлорид является важнейшим материалом в современной торговле, и в большинстве способов, используемых в настоящее время, получают винилхлорид из 1,2-дихлорэтана (EDC), где EDC сначала получают из этилена; таким образом, согласно известным литературным данным, используется система всего, по меньшей мере, из трех операций (получение этилена из первичных углеводородов, преимущественно путем термического крекинга; превращение этилена в EDC, а затем превращение EDC в винилхлорид). Промышленности присуща долговременная потребность в том, чтобы продвигаться к таким решениям, в которых винилхлорид получают из первичных углеводородов более прямым путем и более экономично, без необходимости в предварительном получении и очистке этилена, и присущая такому подходу экономическая выгода стимулировала значительное количество разработок.
В качестве первой общей области для разработок производство винила из этана представляет интерес для ряда фирм, вовлеченных в производство винилхлорида, и в настоящее время доступным является значительное количество литературы по этой теме. Следующие далее разделы дают обзор основных работ, связанных с воплощениями, представленными в новых разработках по настоящему описанию.
Патент Великобритании 1039369, озаглавленный "CATALYTIC CONVERSION OF ETHANE TO VINYL CHLORIDE", который выдан 17 августа 1966 г., описывает использование многовалентных металлов, включая металлы из ряда лантаноидов, в производстве винилхлорида из этана. Этот патент описывает использование определенных катализаторов при условии, что "пар, доступный хлор и кислород используются в конкретных контролируемых отношениях". Описанная система работает при температурах в пределах между 500 и 750°С. Доступный хлор в описываемой технологии необязательно включает 1,2-дихлорэтан. Однако данный патент не упоминает, что вместе с этаном нужно подавать этилен. В нем также не упоминается, что в процессе должно быть задано определенное мольное отношение этана к этилену, не описывается рециркулирование этилена, а вместо этого указывается лишь, что этилен вступает в реакцию с образованием полимеров либо этилендихлорида, либо этилхлорида.
Патент Великобритании 1492945, озаглавленный "PROCESS FOR PRODUCING VINYL CHLORIDE", который выдан 23 ноября 1977 г. на имя John Lynn Barclay, описывает способ производства винилхлорида с использованием лантана в катализаторе превращения этана в винил на основе меди. Как описывают авторы, лантан присутствует с целью благоприятного изменения летучести меди при повышенной температуре, необходимой для работы. Примеры демонстрируют преимущества избытка хлористого водорода в соответствующей реакции.
Патент Великобритании 2095242, озаглавленный "PREPARATION OF MONOCHLORO-OLEFINS BY OXYCHLORINATION OF ALKANES", который выдан 29 сентября 1982 г. на имя David Roger Pyke и Robert Reid, описывает способ для получения монохлорированных олефинов, который включает приведение во взаимодействие при повышенной температуре газообразной смеси, содержащей алкан, источник хлора и молекулярный кислород, в присутствии катализатора, содержащего металлическое серебро и/или его соединение, и одно или несколько соединений марганца, кобальта или никеля". Как указывают авторы, на катализатор могут подаваться смеси этана и этилена. Никаких примеров не приведено, и конкретные преимущества смесей этан/этилен не описываются.
Патент Великобритании 2101596, озаглавленный "OXYCHLORINATION OF ALKANES TO MONOCHLORINATED OLEFINS", который выдан 19 января 1983 г. на имя Robert Reid и David Pyke, описывает способ для производства монохлорированных олефинов, который включает приведение во взаимодействие при повышенной температуре газообразной смеси, содержащей алкан, источник хлора и молекулярный кислород, в присутствии катализатора, содержащего соединения меди, марганца и титана, и является пригодным для использования в производстве винилхлорида из этана. Кроме того, как описывают авторы, продукты реакции, в одном из воплощений, выделяют и используют, как есть, или, в одном из воплощений, рециклируют в реактор для увеличения выхода монохлорированного олефина. Как указывают авторы, на катализатор могут подавться смеси этана и этилена. Никаких примеров не приведено, и конкретные преимущества смесей этан/этилен не описываются.
Патент США 3629354, озаглавленный "HALOGENATED HYDROCARBONS", который выдан 21 декабря 1971 г. на имя William Q. Beard, Jr. описывает способ производства винилхлорида и совместного с ним производства этилена из этана в присутствии хлористого водорода и кислорода. Предпочтительным катализатором является медь или железо на подложке. Один из примеров в этом патенте демонстрирует избыток хлористого водорода (HCl) по отношению к этану в реакционной смеси. Отношение этана к хлористому водороду один к четырем используется для получения потока, содержащего 38,4% этилена (который не требует HCl для получения) и 27,9% винилхлорида (который требует для получения только 1 моля HCl на 1 моль винилхлорида).
Патент США 3658933, озаглавленный "ETHYLENE FROM ETHANE, HALOGEN AND HYDROGEN HALIDE THROUGH FLUIDIZED CATALYST", который выдан 25 апреля 1972 г. на имя William Q. Beard, Jr., описывает способ производства винилгалогенидов в системе из трех реакторов, объединяющей реактор для оксидегидрирования, реактор для оксигалогенирования и реактор для дегидрогалогенирования. Авторы показывают, что (окси)галогендегидрирование этана, в некоторых случаях, усиливается путем добавления как галогена, так и галогенида водорода. Как и в патенте США 3629354, получаемый этилен дает VCM путем обычного оксигалогенирования (оксихлорирования) и крекинга. HCl, получаемый при операции крекинга, возвращается в реактор галогендегидрирования.
Патент США 3658934, озаглавленный "ETHYLENE FROM ETHANE AND HALOGEN THROUGH FLUIDIZED RARE EARTH CATALYST", который выдан 25 апреля 1972 г. на имя William Q. Beard, Jr., и патент США 3702311, озаглавленный "HALODEHYDROGENATION CATALYST", который выдан 7 ноября 1972 г. на имя William Q. Beard, Jr., описывают оба способа для производства винилгалогенидов в системе из трех реакторов, объединяющей реактор галогендегидрирования, реактор оксигалогенирования и реактор дегидрогалогенирования. Авторы описывают галогендегидрирование этана с получением этилена для последующего превращения в EDC путем оксигалогенирования (оксихлорирования) с последующим получением VCM путем обычного термического крекинга. HCl, получаемый при операции крекинга, возвращают в реактор оксигалогенирования в '934 и в реактор галогендегидрирования в '311. Как показано в последнем патенте, преимущества избытка общего хлора как в виде HCl, так и Cl2, увеличивает выход желаемых продуктов.
Патент США 3644561, озаглавленный "OXYDEHYDROGENATION OF ETHANE", который выдан 22 февраля 1972 г. на имя William Q. Beard, Jr., и патент США 3769362, озаглавленный "OXYDEHYDROGENATION OF ETHANE", который выдан 30 октября 1973 г. на имя William Q. Beard, Jr., тесно связаны с указанными выше патентами и описывают способы оксидегидрирования этана до этилена в присутствии избыточных количеств галогенида водорода. Патент описывает катализатор из галогенида либо меди, либо железа, дополнительно стабилизированный с помощью галогенида редкоземельного элемента, где отношение галогенида редкоземельного элемента к галогениду меди или железа является более высоким чем 1:1. Патент описывает использование значительного избытка HCl по отношению к мольному количеству вводимого этана, причем HCl остается не потребленным в реакции.
Патент США 4046823, озаглавленный "PROCESS FOR PRODUCING 1, 2-DICHLOROETHANE", который выдан 6 сентября 1977 г. на имя Ronnie D. Gordon и Charles M. Starks, описывает способ производства EDC, где этан и хлор взаимодействуют в газовой фазе над катализатором, содержащим медь.
Патент США 4100211, озаглавленный "PROCESS FOR PREPARATION OF ETHYLENE AND VINYL CHLORIDE FROM ETHANE", который выдан 11 июля 1978 г. на имя Angelo Joseph Magistro, описывает регенерацию катализатора на основе железа для способа, где этан превращается как в этилен, так и в VCM в смеси. Этот патент описывает, что источник хлора присутствует в количестве от 0,1 до 10 моль на 1 моль этана. Как правило, при увеличении отношения хлористого водорода к этану выход винилхлорида и других хлорированных продуктов также увеличивается, даже при уменьшении выхода этилена.
Патент США 4300005, озаглавленный "PREPARATION OF VINYL CHLORIDE", который выдан 10 ноября 1981 г. на имя Тао Р. Li, предлагает катализатор на основе меди для производства VCM в присутствии избытка HCl.
Патент США 5097083, озаглавленный "PROCESS FOR THE CHLORINATION OF ETHANE", который выдан 17 марта 1992 г. на имя John E. Stauffer, описывает хлоруглероды в качестве источника хлора для процесса превращения этана в VCM. Этот патент описывает способы, где хлоруглеводороды могут быть использованы для захвата HCl с целью последующего использования при получении винила.
EVC Corporation является очень активной в области технологии превращения этана в винил, и следующие четыре патента являются следствием их усилий по разработке.
Европейский патент ЕР 667845, озаглавленный "OXYCHLORINATION CATALYST", который выдан 14 января 1998 г. на имя Ray Hardman и lan Michael Clegg, описывает катализатор на основе меди со стабилизирующей упаковкой, предназначенный для катализа превращения этана в винил. Этот катализатор, очевидно, относится и к последующей технологии, описанной в следующих трех патентах США.
Патент США 5663465, озаглавленный "BY-PRODUCT RECYCLING IN OXYCHLORINATION PROCESS", который выдан 2 сентября 1997 г. на имя Ian Michael Clegg и Ray Hardman, описывает способ каталитического превращения этана в VCM, в котором объединяют этан и источник хлора в реакторе оксихлорирования с соответствующим катализатором; рециклируют побочные продукты в реактор для оксихлорирования; обрабатывают побочные продукты ненасыщенные хлорированные углеводороды на стадии гидрирования для превращения их в их насыщенные аналоги и направляют их обратно в реактор; хлорируют побочный продукт - этилен до 1,2-дихлорэтана для рециклирования.
Патент США 5728905, озаглавленный "VINYL CHLORIDE PRODUCTION PROCESS", который выдан 17 марта 1998 г. на имя Ian Michael Clegg и Ray Hardman, описывает производство винила из этана в присутствии избытка HCl при использовании катализатора на основе меди. Этот патент описывает способ каталитического оксихлорирования этана в случае присутствия этана, источника кислорода и источника хлора, в присутствии катализатора, содержащего медь и щелочной металл. HCl подают в реактор оксихлорирования в избытке по отношению к стехиометрической потребности в расчете на хлор.
Патент США 5763710, озаглавленный "OXYCHLORINATION PROCESS", который выдан 9 июня 1998 г. на имя Ian Michael Clegg и Ray Hardman, обсуждает каталитическое оксихлорирование этана до VCM путем объединения этана и источника хлора в реакторе для оксихлорирования в присутствии катализатора оксихлорирования (условия реакции выбираются с поддержанием избытка HCl); отделения продуктов VCM и рециклирования побочных продуктов в реактор.
Обращаясь теперь к области получения винилхлорида из этилена, в большинстве коммерческих способов для производства VCM используют этилен и хлор в качестве ключевых исходных веществ. Этилен приводят в контакт с хлором в жидком 1,2-дихлорэтане, содержащем катализатор, в реакторе прямого хлорирования. 1,2-Дихлорэтан затем подвергают крекингу при повышенной температуре с получением VCM и хлористого водорода (HCl). Получаемый HCl, в свою очередь, вводят в реактор оксихлорирования, где он взаимодействует с этиленом и кислородом, для получения дополнительного количества 1,2-дихлорэтана. Этот 1,2-дихлорэтан также подают на термический крекинг с целью получения VCM. Такой способ описывается в патенте США 5210358, озаглавленном "CATALYST COMPOSITION AND PROCESS FOR THE PREPARATION OF ETHYLENE FROM ETHANE", который выдан 11 мая, 1993 г. на имя Angelo J. Magistro.
Три отдельных процесса (прямое хлорирование, оксихлорирование и термический крекинг) в большинстве используемых в настоящее время коммерческих способов часто упоминаются в сочетании как "сбалансированная" установка для получения EDC, хотя дополнительные источники хлора (HCl), в одном из воплощений, также вводятся в эти расширенные системы установок. Общая стехиометрия "сбалансированной" установки следующая:
4C2H4+2Cl2+О2 ->4С2Н3Cl+2Н2О
Стоимость этилена представляет собой значительную долю общей стоимости производства VCM и требует значительных затрат на производство. Этан является менее дорогим, чем этилен, и производство VCM из этана должно, следовательно, значительно понизить стоимость производства VCM по сравнению со стоимостью производства VCM, когда он производится, прежде всего, из очищенного и выделенного этилена.
Общепринято называть превращение этилена, кислорода и хлористого водорода в 1,2-дихлорэтан оксихлорированием. Катализаторы для производства 1,2-дихлорэтана с помощью оксихлорирования этилена имеют многие общие для всех таких катализаторов характеристики. Катализаторы, способные осуществить эту химическую реакцию, классифицируются как модифицированные катализаторы процесса Дикона (Deacon) [Olah, G. A., Molnar, A., Hydrocarbon Chemistry, John Wiley & Sons (New York, 1995), p. 226]. Химический механизм процесса Дикона сводится к реакции Дикона - окислению HCl с получением элементарного хлора и воды. Другими авторами было предложено, чтобы оксихлорирование применялось с целью использования HCl для хлорирования и чтобы HCl окислительно превращали в Cl2 посредством процесса Дикона [Selective Oxychlorination hydrocarbons: A Critical Analysis, Catalytica Associates, Inc., Study 4164A, October 1982, page 1]. Таким образом, катализаторы оксихлорирования определяются их способностью производить свободный хлор (Cl2). В самом деле, оксихлорирование алканов связано с производством свободного хлора в системе [Selective Oxychlorination hydrocarbons: A Critical Analysis, Catalytical Associates, Inc., Study 4164A, October 1982, page 21 и ссылки в нем]. В этих катализаторах используют металлы на носителе, способные принимать более чем одно стабильное состояние окисления, такие как медь и железо. В обычной технологии оксихлорирование представляет собой окислительное добавление двух атомов хлора к этилену от HCl или другого источника восстановленного хлора.
Производство винила из этана может осуществляться путем оксихлорирования при том условии, что присутствуют катализаторы, которые являются способными производить свободный хлор. Такие катализаторы будут превращать этилен в 1,2-дихлорэтан при низких температурах. При более высоких температурах 1,2-дихлорэтан будет подвергаться термическому крекингу с получением HCl и винилхлорида. Катализаторы оксихлорирования хлорируют олефиновые вещества до хлоруглеродов с более высокой степенью хлорирования. Таким образом, подобно тому как этилен превращается в 1,2-дихлорэтан, винилхлорид превращается в 1,1,2-трихлорэтан. Процессам с использованием катализаторов оксихлорирования присуще образование побочных продуктов с более высокой степенью хлорирования. Это исследовано очень подробно в патентах фирмы EVC (Европейский патент ЕР 667845, патент США 5663465, патент США 5728905 и патент США 5763710), в которых показано, что производятся при использовании катализатора оксихлорирования высокие уровни многократно хлорированных побочных продуктов. Рассматривая вышеизложенное, можно подытожить, что многие концепции касающиеся использования этана для производства VCM, были ясно описаны ранее. Используемые катализаторы чаще всего являются модифицированными катализаторами процесса Дикона, работающими при температурах, значительно более высоких (>400°С), чем те, которые требуются для осуществления оксихлорирования этилена (<275° С). Катализаторы, используемые для производства VCM из этана, часто стабилизируют против миграции переходных металлов первого ряда, как описано и рассмотрено в патенте Великобритании 1492945; патенте Великобритании 2101596; патенте США 3644561; патенте США 4300005 и патенте США 5728905.
Использование хлоруглеродов в качестве источников хлора в способах превращения этана в VCM описано в патенте Великобритании 1039369; патенте Великобритании 2101596; патенте США 5097083; патенте США 5663465 и патенте США 5763710. Патент Великобритании 1039369 требует, чтобы в систему реакторов вводилась вода. В патенте Великобритании 2101596 используют специфические катализаторы на основе меди. Патент США 5663465 описывает способ, который использует стадию прямого хлорирования для превращения этилена в EDC перед его введением в реактор VCM.
Источник известного уровня техники ЕР 0162457 описывает способ получения винилхлорида дегидрохлорированием этилендихлорида (EDC->МВХ+HCl). Данный источник относится к иному процессу, отличающемуся от заявляемого здесь химического процесса «оксидегидрохлорирования».
Новые подходы в способах производства винилхлорида могли бы состоять в разработке и использовании катализаторов, пригодных для превращения значительных количеств как этана, так и этилена в мономер винилхлорида. Однако при этом в числе продуктов реакции образуется хлористый водород. В этой связи управление потоками хлористого водорода (и связанной с ним хлористоводородной кислоты) в процессе является главной задачей, которая должна быть решена, когда используется система катализаторов, способная превращать как этан, так и этилен в мономер винилхлорида. При конструировании установки для получения винилхлорида существует также необходимость в том, чтобы дать возможность в максимально возможной степени использовать ранее применявшееся оборудование, при том что некоторая часть имеющегося оборудования может иметь возможность работы с хлористым водородом, а другая часть имеющегося оборудования не имеет возможности работы с хлористым водородом. Настоящее изобретение предусматривает воплощения для удовлетворения этих потребностей за счет того, что предлагаются устройство и способ для работы с хлористым водородом, вырабатываемым реактором для получения винила из этана/этилена, путем его практически полного извлечения из выходного потока реактора в процессе работы первого узла, следующего после стадии или ступени реакции получения винила из этана/этилена.
Настоящее изобретение предусматривает способ производства винилхлорида, использующий следующие стадии:
генерирования выходного потока из первого реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора из числа хлористого водорода, хлора или насыщенного хлоруглеводорода, где мольное отношение этана к этилену находится в пределах от 0,02 до 50;
охлаждения и конденсирования выходного потока из первого реактора для создания потока сырого продукта, содержащего первую часть хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть хлористого водорода;
разделения потока сырого продукта на поток продукта - мономера винилхлорида и на поток легких фракций, содержащий первую часть хлористого водорода, и
рециклирования потока легких фракций для каталитического взаимодействия совместно с этаном, этиленом, кислородом и источником хлора на стадии генерирования.
Настоящее изобретение также предусматривает способ производства винилхлорида, включающий следующие стадии:
генерирования выходного потока из первого реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или насыщенного хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
охлаждения и конденсирования указанного выходного потока из первого реактора для создания потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
разделения указанного потока сырого продукта на поток продукта - мономера винилхлорида и на поток легких фракций, содержащий указанную первую часть хлористого водорода, и
рециклирования указанного потока легких фракций для каталитического взаимодействия совместно с указанным этаном, указанным этиленом, указанным кислородом и указанным источником хлора на стадии генерирования.
Настоящее изобретение дополнительно предусматривает способ производства винилхлорида, включающий следующие стадии:
генерирования выходного потока из первого реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или насыщенного хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
охлаждения и конденсирования указанного выходного потока из первого реактора для создания потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
разделения указанного потока сырого продукта на поток продукта воды и поток продукта мономера винилхлорида, поток этилхлорида, смешанный поток цис-1,2-дихлорэтилена и транс-1, 2-дихлорэтилена, поток 1, 2-дихлорэтана, поток тяжелых фракций и поток легких фракций, содержащий указанную первую часть указанного хлористого водорода;
извлечения потока безводного хлористого водорода из указанного охлажденного потока сырого хлористого водорода;
рециклирования указанного потока безводного хлористого водорода в указанный реактор в виде указанного реагента хлористого водорода и
рециклирования указанного потока легких фракций в указанный реактор.
Настоящее изобретение далее предусматривает способ производства винилхлорида, включающий следующие стадии:
генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и/ по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
охлаждения и конденсирования указанного выходного потока из реактора для создания потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
разделения указанного потока сырого продукта на поток продукта - воды, поток продукта - мономера винилхлорида, поток этилхлорида, смешанный поток цис-1,2-дихлорэтилена и транс-1,2-дихлорэтилена, поток 1,2-дихлорэтана, поток тяжелых фракций и поток легких фракций, содержащий указанную первую часть указанного хлористого водорода;
извлечения потока безводного хлористого водорода из указанного потока сырого охлажденного хлористого водорода;
рециклирования указанного потока безводного хлористого водорода в указанный реактор в виде указанного реагента хлористого водорода;
разделения указанного потока легких фракций на продувочный поток и поток рециклируемого газа;
абсорбции хлористого водорода из указанного продувочного потока для отделения потока водного раствора хлористого водорода;
объединения указанного потока водного раствора хлористого водорода с указанным потоком сырого охлажденного хлористого водорода;
абсорбции и рециклирования в указанный реактор потока С2 из указанного продувочного потока и
рециклирования указанного рециклируемого потока газа в указанный реактор.
Настоящее изобретение далее предусматривает способ производства винилхлорида, включающий стадии:
генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
охлаждения и конденсирования указанного выходного потока из реактора для образования потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
разделения указанного потока сырого продукта на поток продукта - воды, поток продукта - мономера винилхлорида, поток этилхлорида, смешанный поток цис-1,2-дихлорэтилена и транс-1,2-дихлорэтилен, поток 1,2-дихлорэтана, поток тяжелых фракций и поток легких фракций, содержащий указанную первую часть указанного хлористого водорода;
извлечения потока безводного хлористого водорода из указанного потока сырого охлажденного хлористого водорода;
рециклирования указанного потока безводного хлористого водорода в указанный реактор в виде указанного реагента - хлористого водорода;
разделения указанного потока легких фракций на продувочный поток и поток рециклируемого газа;
абсорбции хлористого водорода из указанного продувочного потока для отделения потока водного раствора хлористого водорода;
объединения указанного потока водного раствора хлористого водорода с указанным потоком сырого охлажденного хлористого водорода;
гидрирования указанного смешанного потока цис-1,2-дихлорэтилена и транс-1, 2-дихлорэтилена с образованием рециклируемого потока для ввода в указанный реактор;
абсорбции и рециклирования в указанный реактор потока С2 из указанного продувочного потока и
рециклирования указанного потока рециклируемого газа в указанный реактор.
Настоящее изобретение далее предусматривает устройство для производства винилхлорида, содержащее
реактор для генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
средства для охлаждения и конденсирования указанного выходного потока из реактора, для образования потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
средства для разделения указанного потока сырого продукта на поток продукта - мономера винилхлорида и на поток легких фракций, содержащий указанную первую часть указанного хлористого водорода, и
средства для рециклирования указанного потока легких фракций в указанный реактор.
Настоящее изобретение далее предусматривает устройство для производства винилхлорида, включающее
реактор для генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
средства для охлаждения и конденсирования указанного выходного потока из реактора для образования потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
средства для разделения указанного потока сырого продукта на поток продукта - воды, поток продукта - мономера винилхлорида, поток этилхлорида, смешанный поток цис-1,2-дихлорэтилена и транс-1,2-дихлорэтилена, поток 1,2-дихлорэтана, поток тяжелых фракций и поток легких фракций, содержащий первую часть указанного хлористого водорода;
средства для извлечения потока безводного хлористого водорода из указанного потока сырого охлажденного хлористого водорода;
средства для рециклирования указанного потока безводного хлористого водорода в указанный реактор в виде указанного реагента - хлористого водорода и
средства для рециклирования указанного потока легких фракций в указанный реактор.
Настоящее изобретение далее предусматривает устройство для производства винилхлорида, содержащее
реактор для генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
средства для охлаждения и конденсирования указанного выходного потока из реактора для образования потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
средства для разделения указанного потока сырого продукта на поток продукта - воды, поток продукта - мономера винилхлорида, поток этилхлорида, смешанный поток цис-1,2-дихлорэтилена и транс-1,2-дихлорэтилена, поток 1,2-дихлорэтана, поток тяжелых фракций и поток легких фракций, содержащий указанную первую часть указанного хлористого водорода;
средства для извлечения потока безводного хлористого водорода из указанного потока сырого охлажденного хлористого водорода;
средства для рециклирования указанного потока безводного хлористого водорода в указанный реактор в виде указанного реагента - хлористого водорода;
средства для разделения указанного потока легких фракций на продувочный поток и поток рециклируемого газа;
средства для абсорбции хлористого водорода из указанного продувочного потока для отделения потока водного раствора хлористого водорода;
средства для объединения указанного водного потока хлористого водорода с указанным потоком сырого охлажденного хлористого водорода;
средства для абсорбции и рециклирования в указанный реактор потока С2 из указанного продувочного потока и
средства для рециклирования указанного потока рециклируемого газа в указанный реактор.
Настоящее изобретение далее предусматривает устройство для производства винилхлорида, содержащее
реактор для генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
средства для охлаждения и конденсирования указанного выходного потока из реактора, для образования потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
средства для разделения указанного потока сырого продукта на поток продукта - воды, поток продукта - мономера винилхлорида, поток этилхлорида, смешанный поток цис-1,2-дихлорэтилена и транс-1, 2-дихлорэтилена, поток 1,2-дихлорэтана, поток тяжелых фракций и поток легких фракций, содержащий указанную первую часть указанного хлористого водорода;
средства для извлечения потока безводного хлористого водорода из указанного потока сырого охлажденного хлористого водорода;
средства для рециклирования указанного потока безводного хлористого водорода в указанный реактор в виде указанного реагента - хлористого водорода;
средства для разделения указанного потока легких фракций на продувочный поток и поток рециклируемого газа;
средства для абсорбции хлористого водорода из указанного продувочного потока для отделения потока водного раствора хлористого водорода;
средства для объединения указанного потока водного раствора хлористого водорода с указанным потоком сырого охлажденного хлористого водорода;
средства для гидрирования указанного смешанного потока цис-1,2-дихлорэтилена и транс-1, 2-дихлорэтилена для создания рециклируемого питающего потока в указанный реактор;
средства для абсорбции и рециклирования в указанный реактор потока С2 из указанного продувочного потока и
средства для рециклирования указанного потока рециклируемого газа в указанный реактор.
Настоящее изобретение далее предусматривает винилхлорид, произведенный с использованием способа, включающего следующие стадии:
генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
охлаждения и конденсирования указанного выходного потока из реактора с образованием потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
разделения указанного потока сырого продукта на поток продукта - мономера винилхлорида - и на поток легких фракций, содержащий указанную первую часть указанного хлористого водорода, и
рециклирования указанного потока легких фракций для каталитического взаимодействия совместно с указанным этаном, указанным этиленом, указанным кислородом и указанным источником хлора на указанной стадии генерирования.
Настоящее изобретение далее предусматривает винилхлорид, произведенный с использованием способа, включающего следующие стадии:
генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
охлаждения и конденсирования указанного выходного потока из реактора с образованием потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
разделения указанного потока сырого продукта на поток продукта - воды, поток продукта - мономера винилхлорида, поток этилхлорида, смешанный поток цис-1,2-дихлорэтилена и транс-1,2-дихлорэтилена, поток 1,2-дихлорэтана, поток тяжелых фракций и поток легких фракций, содержащий указанную первую часть указанного хлористого водорода;
извлечения потока безводного хлористого водорода из указанного потока сырого охлажденного хлористого водорода;
рециклирования указанного потока безводного хлористого водорода в указанный реактор в виде указанного реагента - хлористого водорода и
рециклирования указанного потока легких фракций в указанный реактор.
Настоящее изобретение далее предусматривает винилхлорид, произведенный с использованием способа, включающего стадии:
генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
охлаждения и конденсирования указанного выходного потока из реактора с образованием потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
разделения указанного потока сырого продукта на поток продукта - воды, поток продукта - мономера винилхлорида, поток этилхлорида, смешанный поток цис-1,2-дихлорэтилена и транс-1,2-дихлорэтилена, поток 1,2-дихлорэтана, поток тяжелых фракций и поток легких фракций, содержащий указанную первую часть указанного хлористого водорода;
извлечения потока безводного хлористого водорода из указанного потока сырого охлажденного хлористого водорода;
рециклирования указанного потока безводного хлористого водорода в указанный реактор в виде указанного реагента - хлористого водорода;
разделения указанного потока легких фракций на продувочный поток и поток рециклируемого газа;
абсорбции хлористого водорода из указанного продувочного потока для отделения потока водного раствора хлористого водорода;
объединения указанного потока водного раствора хлористого водорода с указанным потоком сырого охлажденного хлористого водорода;
абсорбции и рециклирования в указанный реактор потока С2 из указанного продувочного потока и
рециклирования указанного рециклируемого потока газа в указанный реактор.
Настоящее изобретение далее предусматривает винилхлорид, произведенный с использованием способа, включающего следующие стадии:
генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50;
охлаждения и конденсирования указанного выходного потока из реактора с образованием потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода;
разделения указанного потока сырого продукта на поток продукта - воды, поток продукта - мономера винилхлорида, поток этилхлорида, смешанный поток цис-1,2-дихлорэтилена и транс-1,2-дихлорэтилена, поток 1,2-дихлорэтана, поток тяжелых фракций и поток легких фракций, содержащий указанную первую часть указанного хлористого водорода;
извлечения потока безводного хлористого водорода из указанного потока сырого охлажденного хлористого водорода;
рециклирования указанного потока безводного хлористого водорода в указанный реактор в виде указанного реагента хлористого водорода;
разделения указанного потока легких фракций на продувочный поток и поток рециклируемого газа;
абсорбции хлористого водорода из указанного продувочного потока для отделения потока водного раствора хлористого водорода;
объединения указанного потока водного раствора хлористого водорода с указанным потоком сырого охлажденного хлористого водорода;
гидрирования указанного смешанного потока цис-1,2-дихлорэтилена и транс-1, 2-дихлорэтилена для создания рециклируемого потока в указанный реактор;
абсорбции и рециклирования в указанный реактор потока С2 из указанного продувочного потока и
рециклирования указанного потока рециклируемого газа в указанный реактор.
Дополнительные особенности и преимущества настоящего изобретения становятся более очевидными при чтении подробного описания предпочтительных воплощений и прилагаемых чертежей.
Фиг.1 демонстрирует схематическое описание, в той максимально возможной степени, в какой его можно представить на основе более ранних публикаций, предлагаемого способа превращения этана в винилхлорид с использованием катализатора, способного превращать этан в VCM.
Фиг.2 демонстрирует способ превращения этана/этилена в винилхлорид с использованием катализатора, способного к превращению этана и этилена в VCM путем оксидегидрохлорирования.
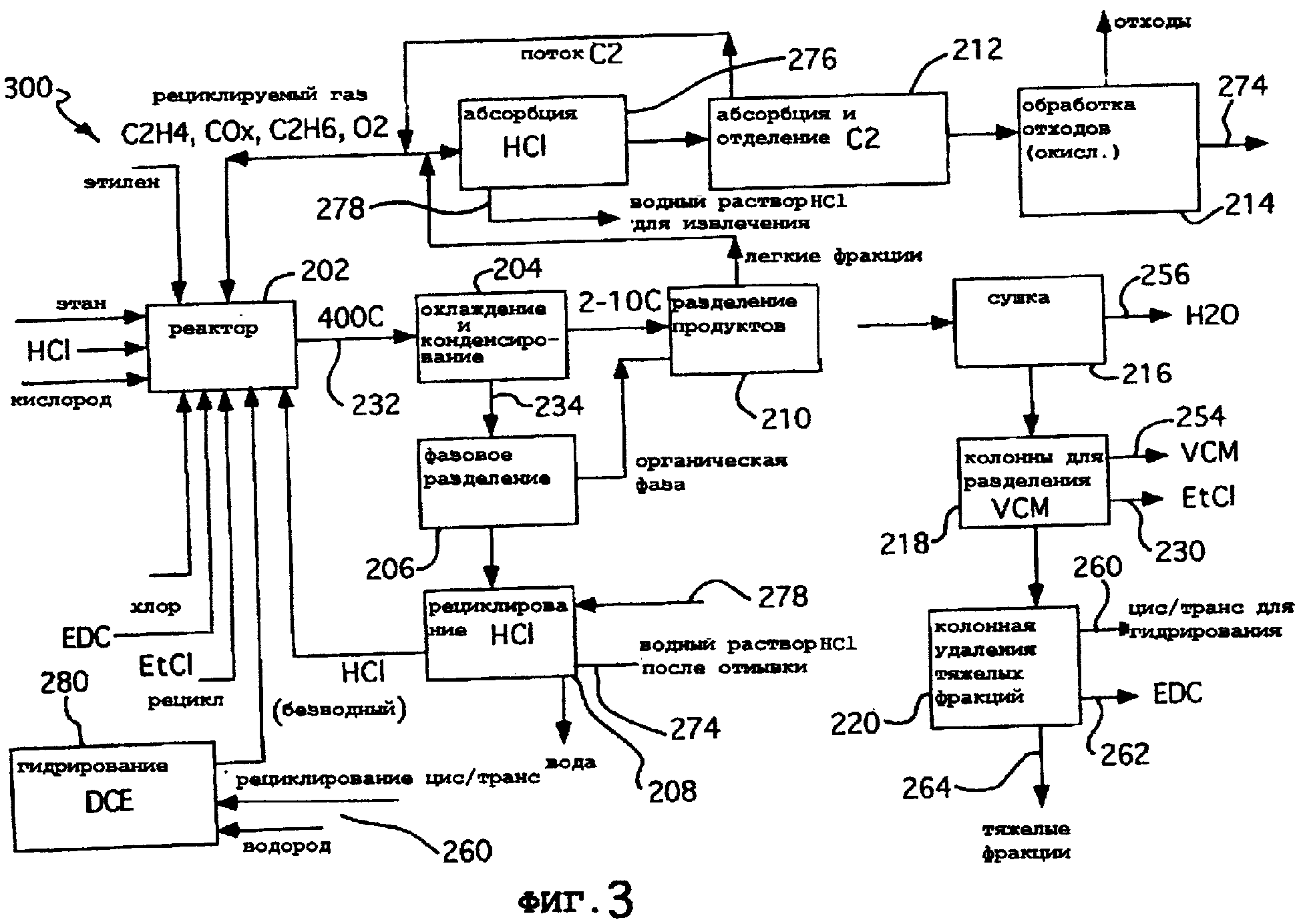
На фиг.3 показан модифицированный процесс оксидегидрохлорирования согласно фиг.2, где продемонстрировано дополнительное гидрирование потоков цис-дихлорэтилена и транс-дихлорэтилена до 1,2-дихлорэтана.
Как отмечено при обсуждении раздела ПРЕДПОСЫЛКИ настоящего описания, оксихлорирование обычно рассматривается как окислительное добавление двух атомов хлора к этилену от HCl или другого источника восстановленного хлора. Катализаторы, способные к осуществлению этого химического процесса, классифицируются как модифицированные катализаторы процесса Дикона [Olah, G. A., Molnar, A., Hydrocarbon Chemistry, John Wiley & Sons (New York, 1995), p. 226]. Химический механизм процесса Дикона связан с реакцией Дикона - окислением HCl с получением элементарного хлора и воды.
В противоположность оксихлорированию в предпочтительном способе, описываемом здесь, предпочтительно используют оксидегидрохлорирование при превращании этансодержащих и этиленсодержащих потоков в VCM с высокой селективностью. Оксидегидрохлорирование представляет собой превращение углеводорода, с использованием кислорода и источника хлора, в хлорированный углеводород, где атомы углерода либо сохраняют их исходную валентность, либо их валентность уменьшается (то есть sp3 атомы углерода остаются sp3 или преобразуются в sp2, a sp2 атомы углерода остаются sp2 или преобразуются в sp). Это отличается от обычного определения оксихлорирования, где этилен превращается в 1,2-дихлорэтан, с использованием кислорода и источника хлора, с общим увеличением валентности атомов углерода (то есть sp2 атомы углерода преобразуются в sp3атомы углерода). При способности катализатора к превращанию этилена в винилхлорид является выгодным рециклировать этилен, производимый в процессе реакции оксидегидрохлорирования, назад в реактор. Побочные продукты, производимые в реакторе оксидегидрохлорирования, включают этилхлорид, 1,2-дихлорэтан, цис-1,2-дихлорэтилен и транс-1,2-дихлорэтилен. Катализатор оксидегидрохлорирования является также активным катализатором для устранения HCl из насыщенных хлоруглеводородов. Рециклирование этилхлорида и 1,2-дихлорэтана в некоторых случаях с выгодой применяется при производстве винилхлорида.
Остальные значимые хлорированные органические побочные продукты представляют собой дихлорэтилены. Эти вещества, в одном из воплощений, гидрируются с получением 1,2-дихлорэтана. 1,2-Дихлорэтан (ЕДС) представляет собой химический реагент, производимый в больших объемах, и либо продается, либо рециклируется. В альтернативном воплощении EDC полностью гидрируют с получением этана и HCl. Гидрирование в условиях промежуточной степени жесткости дает смеси 1,2-дихлорэтана, этана, этилхлорида и HCl; такие смеси являются также пригодными для рециклирования в реактор оксидегидрохлорирования.
Обратимся теперь к фиг.1. В отношении превращения этана в винил, в той степени, в какой возможно наилучшим образом понять из более ранних публикаций, способ 100 превращения этана в VCM показывает схему предполагаемого способа превращения этана в винилхлорид с использованием катализатора, способного к превращанию этана в VCM; в этой связи способ не предусматривает ввода значительных количеств этилена либо из рециклируемых потоков, либо из входных потоков в реактор для превращения этана в VCM (Этановый Реактор 102). Нужно также заметить, что, поскольку система производства винила из этана в соответствующем масштабе нормального производства, насколько известно авторам, еще не сконструирована, предлагаемые решения для способа являются единственными источниками для разработки воплощений, которые ранее были сформулированы в виде концепций. В этой связи, способ 100 представляет собой унифицированное и упрощенное приближение для способов, совместно рассмотренных в нескольких публикациях, относящихся к исследованиям и разработкам EVC Corporation: Vinyl Chloride/Ethylene Bichloride 94/95-5 (August, 1996; Chemical Systems, Inc.; Tarrytown, New York); Европейский патент ЕР 667845; патент США 5663465; патент США 5728905 и патент США 5763710.
При рассмотрении деталей, представленных на фиг.1, можно видеть, что Этановый Реактор 102 дает выходной поток флюида в Колонну Гашения 106, где HCl гасится в выходном потоке из реактора. Колонна Гашения 106 направляет поток сильно концентрированного водного раствора сырого HCl в Подсистему Фазового Разделения 108. Подсистема Фазового Разделения 108 дает выходной поток флюида в Подсистему Извлечения Безводного HCl 110, где водный раствор хлористого водорода (хлористоводородная кислота), безводный HCl и вода выделяются из потока сильно концентрированного водного раствора сырого HCl.
Подсистема Извлечения Безводного HCl 110 дает выходной Поток 130 для рециклирования безводного хлористого водорода в Этановый Реактор 102, а также Подсистема Извлечения Безводного HCl 110 дает на выходе воду (для последующего использования и для удаления в качестве отходов). Подсистема Извлечения Безводного HCl 110 возвращает относительно разбавленный поток водного раствора HCl (хлористоводородной кислоты) с помощью Потока 128 в Колонну Гашения 106. Колонна Гашения 106 также дает выходной поток флюида в Колонну Выделения Легких Фракций 114, где поток легких фракций, содержащий этилен, дополнительно удаляют из потока продукта, выходящего из реактора.
Колонна Выделения Легких Фракций 114 выдает поток легких фракций в Реактор Прямого Хлорирования 112, где хлор (Поток 126) добавляют для прямого хлорирования этилена в потоке легких фракций до EDC (1,2-дихлорэтан). EDC извлекают в Колонне для Извлечения EDC 116 для рециклирования в Этановый Реактор 102 и некоторое количество оставшихся газообразных легких фракций рециклируют в Этановый Реактор 102 в виде Потока 134, причем устройства для определения СО (моноокись углерода) в композиции обеспечивают измерение (не показано) с целью использования при определении системой контроля (не показано) соответствующей части оставшихся газообразных легких фракций для обработки с помощью Узла Окисления Отходов 118, с генерацией потока отходов для удаления СО, CO2 и других примесей из системы.
Выходной поток из Колонны Выделения Легких Фракций 114, который не поступает в Реактор Прямого Хлорирования 112 направляется (а) сначала в Подсистему Сушки 120 для удаления воды; (b) затем в Колонну Очистки VCM 122, для выделения продукта - VCM (мономера винилхлорида), а затем (с) дополнительно в Колонну Удаления Тяжелых Фракций 124, для удаления тяжелых фракций и генерирования Потока 132. Поток 132 представляет собой смешанный флюид цис-1,2-дихлорэтилена и транс-1,2-дихлорэтилена, 1,2-дихлорэтана, этилхлорида и других хлорированных органических веществ. В альтернативном предполагаемом воплощении, основанном на рассмотрении литературы, Подсистема Сушки 120 удаляет воду перед Колонной Выделения Легких Фракций 114, при этом несущий VCM выходной поток из Колонны Выделения Легких Фракций 114 направляют (а) сначала в Колонну для Очистки VCM 122, для выделения продукта - VCM (мономер винилхлорида), а затем (b) дополнительно в Колонну Удаления Тяжелых Фракций 124 для удаления тяжелых фракций и генерирования Потока 132.
Наконец, Поток 132 направляют в Реактор Гидрирования RCl (хлорированных органических веществ) 104, где добавление водорода производит рециклируемый поток для направления в Этановый Реактор 102.
Обратимся теперь к рассмотрению фиг.2, в соответствии с предпочтительными воплощениями по настоящему описанию. Способ 200 Оксидегидрохлорирования этана до VCM демонстрирует способ получения винилхлорида из этана/этилена с использованием катализатора, способного к превращанию этана и этилена в VCM путем оксидегидрохлорирования; в связи с этим способ предусматривает ввод значительных количеств как этана, так и этилена либо из рециклируемых потоков, либо из входных потоков в реактор (Реактор 202 Оксидегидрохлорирования Этана/Этилена до VCM). На вход реактора 202 Оксидегидрохлорирования Этана/Этилена до VCM поступают (а) входные потоки - Входной Поток Этана 222, Входной Поток HCl 224, Входной Поток Кислорода 226 и Входной Поток Хлора 228 и (b) рециклируемые потоки - Поток Этилхлорида 230, Поток Хлористого Водорода (HCl) 266 и Поток рециклируемых Легких Фракций 248, а также часть Потока EDC 262, когда EDC выгодно используется для рециклирования в соответствии с рыночными условиями и условиями работы в конкретный момент производства.
Как отражено в заявке Dow No. 44649 от Mark E. Jones, Michael M. Olken, и Daniel A. Hickman, озаглавленной "А PROCESS FOR CONVERSION OF ETHYLENE TO VINYL CHLORIDE, AND NOVEL CATALYST COMPOSITIONS USEFUL FOR SUCH PROCESS", подано 3 октября 2000 г., United States Receiving Office, Express Mail Mailing Number EL636832801US, катализатор, используемый в Реакторе 202 для Оксидегидрохлорирования Этана/Этилена до VCM, содержит, по меньшей мере, один редкоземельный материал. Редкоземельные элементы представляют собой группу из 17 элементов, состоящую из скандия (атомный номер 21), иттрия (атомный номер 39) и лантаноидов (атомные номера 57-71) [James В. Hedrick, U.S. Geological Survey - Minerals Information - 1997, "Rare-Earth Metals"]. Катализатор может присутствовать либо в виде пористого объемного материала, либо он может быть нанесен на соответствующую подложку. Предпочтительными редкоземельными материалами являются такие, основой которых является лантан, церий, неодим, празеодим, диспрозий, самарий, иттрий, гадолиний, эрбий, иттербий, гольмий, тербий, европий, тулий и лютеций. Наиболее предпочтительными редкоземельными материалами для использования в рассмотренном выше способе получения VCM являются те, которые имеют в качестве основы такие редкоземельные элементы, которые обычно рассматриваются как материалы только с одной постоянной валентностью. Каталитические характеристики материалов с переменной валентностью оказываются менее 0желательными, чем у тех, которые имеют одну постоянную валентность. Например, церий, как известно, является катализатором окисления-восстановления, имеющим возможность находиться как в 3+, так и в 4+ стабильных степенях окисления. Это представляет собой одну из причин того, почему, если редкоземельный материал имеет в качестве основы церий, катализатор дополнительно содержит, по меньшей мере, еще один редкоземельный элемент, иной чем церий. Предпочтительно, если один из редкоземельных элементов, используемых в катализаторе, представляет собой церий, церий присутствует в мольном отношении, которое является меньшим, чем общее количество других редкоземельных материалов, присутствующих в катализаторе. Более предпочтительно, однако, чтобы церия по существу не было в катализаторе. Под выражением «по существу не было церия» подразумевается, что церий находится в количестве, меньшем чем 33 ат.% от редкоземельных компонентов, предпочтительно меньшем чем 20 ат.%, а наиболее предпочтительно меньшем чем 10 ат.%.
Редкоземельный материал для катализатора более предпочтительно имеет в качестве основы лантан, неодим, празеодим или их смеси. Наиболее предпочтительно, по меньшей мере, один из редкоземельных элементов, используемых в катализаторе, представляет собой лантан. Кроме того, для этиленсодержащего входного потока в способе получения VCM по настоящему изобретению катализатор по существу не содержит железа и меди. Как правило, присутствие материалов, которые являются способными к окислению-восстановлению (редокс), является нежелательным для катализатора. Предпочтительным для катализатора является также, чтобы он по существу не содержал других переходных металлов, которые имеют более чем одну стабильную степень окисления. Например, марганец представляет собой другой переходной металл, который предпочтительно исключается из катализатора. Под выражением "по существу не содержал" подразумевается, что атомное отношение редкоземельного элемента к редокс-металлу в катализаторе является более высоким чем 1, предпочтительно более высоким чем 10, более предпочтительно более высоким чем 15, а наиболее предпочтительно более высоким чем 50.
Как указано выше, катализатор может также быть осажден на инертной подложке. Предпочтительные инертные подложки включают окись алюминия, силикагель, окись кремния - окись алюминия, окись кремния - окись магния, боксит, окись магния, карбид кремния, оксид титана, оксид циркония, силикат циркония и их сочетания. Однако в наиболее предпочтительном воплощении подложка не является цеолитом. Когда используется инертная подложка, компонент редкоземельного материала катализатора, как правило, составляет от 3 до 85 мас.% от общей массы катализатора и подложки. Катализатор может наноситься на подложку с использованием способов, уже известных в данной области.
Может также быть выгодным включать другие элементы в катализатор, в формах как пористого объемного материала, так и материала, нанесенного на подложку. Например, предпочтительные добавки элементов включают редкоземельные элементы, бор, фосфор, серу, кремний, германий, титан, цирконий, гафний, алюминий и их сочетания. Эти элементы могут присутствовать для изменения каталитических характеристик композиции или для улучшения механических свойств (например, устойчивости к трению) материала.
Перед объединением этиленсодержащего входного потока, источника кислорода и источника хлора в реакторе для варианта способа получения VCM по настоящему изобретению, для композиции катализатора является желательным, чтобы она содержала соль, по меньшей мере, одного редкоземельного элемента, при условии, что катализатор по существу не содержит железа и меди, и при дополнительном условии, что, когда используется церий, катализатор дополнительно содержит, по меньшей мере, еще один редкоземельный элемент, иной чем церий. Соль, по меньшей мере, одного редкоземельного элемента предпочтительно выбирается из оксихлоридов редкоземельных элементов, хлоридов редкоземельных элементов, оксидов редкоземельных элементов и их сочетаний, при условии, что катализатор по существу не содержит железа и меди, и при дополнительном условии, что, когда используется церий, катализатор дополнительно содержит, по меньшей мере, еще один редкоземельный элемент, иной, чем церий. Более предпочтительно соль включает оксихлорид редкоземельного элемента формулы MOCl, где М представляет собой, по меньшей мере, один редкоземельный элемент, выбранный из лантана, церия, неодима, празеодима, диспрозия, самария, иттрия, гадолиния, эрбия, иттербия, гольмия, тербия, европия, тулия, лютеция или их смесей, при условии, что, когда присутствует церий, то также присутствует, по меньшей мере, еще один редкоземельный элемент, иной, чем церий. Наиболее предпочтительно, соль представляет собой пористый, объемный материал оксихлорида лантана (LaOCl). Как уже упоминалось, этот материал выгоден тем, что не подвергается большим изменениям (например, не разламывается), когда хлорируется in situ в этом способе, и обеспечивает дополнительное выгодное свойство растворимости в воде в контексте этого способа, после периода использования (LaOCl первоначально является нерастворимым в воде), так что при необходимости удаления использованного катализатора из реактора с ожиженным слоем, с фиксированным слоем или из другого оборудования или емкостей в настоящем способе, это может быть сделано без водоструйной очистки или обычных трудоемких механических методик, путем простого слива использованного катализатора из рассматриваемого реактора вместе с водой.
Как правило, когда соль представляет собой оксихлорид редкоземельного элемента (MOCl), она имеет площадь поверхности по БЭТ, по меньшей мере, 12 м2 /г, предпочтительно, по меньшей мере, 15 м2/г, более предпочтительно, по меньшей мере, 20 м2/г и наиболее предпочтительно, по меньшей мере, 30 м2/г. Как правило, площадь поверхности по БЭТ является меньшей чем 200 м2/г. Для этих вышеуказанных измерений изотерму адсорбции азота измеряют при 77 К и площадь поверхности вычисляют по данным изотермы с использованием метода БЭТ (Brunauer, S., Emmett, P.M., и Teller, E., J. Am. Chem. Soc., 60, 309 (1938)). Кроме того, замечено, что фазы MOCl обладают характерными дифрактограммами при рентгеноскопии на порошках (XRD), которые отличаются от фаз MCl3.
Является также возможным, как в некоторых случаях указано ранее, получение смесей редкоземельных элементов (М) в составе композиции MOCl. Например, М может быть смесью, по меньшей мере, двух редкоземельных элементов, выбранных из лантана, церия, неодима, празеодима, диспрозия, самария, иттрия, гадолиния, эрбия, иттербия, гольмия, тербия, европия, тулия и лютеция. Подобным же образом является также возможным получение смесей из различных композиций MOCl, где М является различным для каждой композиции MOCl в смеси.
Как только этиленсодержащий входной поток, источник кислорода и источник хлора объединяются в реакторе, формируется катализатор из соли, по меньшей мере, одного редкоземельного элемента in situ. В этом отношении предполагается, что образующийся in situ катализатор содержит хлорид редкоземельного компонента. Примером такого хлорида является MCl3, где М представляет собой редкоземельный компонент, выбранный из лантана, церия, неодима, празеодима, диспрозия, самария, иттрия, гадолиния, эрбия, иттербия, гольмия, тербия, европия, тулия, лютеция и их смесей, при условии, что, когда присутствует церий, катализатор дополнительно содержит, по меньшей мере, еще один редкоземельный элемент, иной, чем церий. Как правило, когда соль представляет собой хлорид редкоземельного элемента (MCl3), она имеет площадь поверхности по БЭТ, по меньшей мере, 5 м2/г предпочтительно, по меньшей мере, 10 м2/г, более предпочтительно, по меньшей мере, 15 м2/г, более предпочтительно, по меньшей мере, 20 м2/г и наиболее предпочтительно, по меньшей мере, 30 м2/г.
В свете настоящего описания специалист в данной области, несомненно, усмотрит альтернативные способы получения пригодных для использования композиций катализаторов. Способ, который, как полагают авторы, является предпочтительным для формирования композиции, содержащей оксихлорид редкоземельного элемента (MOCl), включает следующие стадии: (а) приготовления раствора хлоридной соли редкоземельного элемента или элементов в растворителе, содержащем либо воду, либо спирт, либо их смеси; (b) добавления азотосодержащего основания для формирования осадка и (с) сбора, сушки и прокаливания осадка для образования материала MOCl. Как правило, азотосодержащее основание выбирают из гидроксида аммония, алкиламина, ариламина, арилалкиламина, гидроксида алкиламмония, гидроксида ариламмония, гидроксида арилалкиламмония и их смесей. Азотосодержащее основание может быть также представлено в виде смеси азотосодержащего основания с другими основаниями, которые не содержат азота. Предпочтительно азотосодержащее основание представляет собой гидроксид тетраалкиламмония. Растворитель на стадии (а) предпочтительно представляет собой воду. Сушка пригодной в качестве катализатора композиции может производиться любым способом, включая сушку распылением, сушку в печи с продувкой и другие известные способы. Для предпочтительного в настоящее время режима работы в ожиженном слое предпочтительным является катализатор, высушенный распылением.
Способ, считающийся в настоящее время предпочтительным для формирования композиции катализатора, содержащей хлорид редкоземельного элемента (MCl3), включает следующие стадии: (а) приготовления раствора хлоридной соли редкоземельного элемента или элементов в растворителе, содержащем либо воду, либо спирт, либо их смеси; (b) добавления азотосодержащего основания для образования осадка; (с) сбора, сушки и прокаливания осадка и (d) приведения в контакт прокаленного осадка с источником хлора. Например, одним из применений настоящего способа (с использованием La для иллюстрации) может быть осаждение LaCl3 из раствора с помощью азотосодержащего основания, его сушка, его добавление в реактор, нагрев его до 400°С в реакторе для осуществления прокаливания, а затем приведение в контакт прокаленного осадка с источником хлора, с формированием композиции катализатора in situ в реакторе. Катализаторы для предпочтительного использования будут дополнительно уточняться при рассмотрении примеров, представленных в следующем разделе настоящего описания.
В Реакторе 202 Оксидегидрохлорирования Этана/Этилена до VCM каталитически взаимодействуют совместно этан, этилен, хлористый водород, кислород и хлор, наряду с, по меньшей мере, одним рециклированным потоком, с получением Выходного Потока 232 из Реактора; необходимо специально заметить, что мольное отношение этана к этилену, вычисленное для всех входных потоков реактора 202 Оксидегидрохлорирования Этана/Этилена до VCM, находится в пределах от 0,02 до 50 (заметим, что конкретное рабочее отношение в любой момент определяется требованиями состояния рабочего процесса) без долговременного ухудшения функциональных свойств катализатора. В зависимости от рыночных условий и условий работы в конкретный момент производства этилен добавляют в Реактор 202 в Потоке Этилена 289. В этом отношении более предпочтительное мольное отношение этана к этилену, вычисленное для всех входных потоков в Реактор 202 Оксидегидрохлорирования Этана/Этилена до VCM, находится в пределах от 0,1 до 10. Когда условия работы и рыночные условия (в конкретный момент производства) позволяют, наиболее предпочтительный режим для Потока Этилена 289 представляет собой нулевой поток, а для мольного отношения этана к этилену, вычисленного для всех входных потоков в Реактор 202 Оксидегидрохлорирования Этана/Этилена до VCM, наиболее предпочтительно, чтобы оно находилось в пределах от 0,3 до 4, при этом разброс зависит от локальных условий процесса и срока службы катализатора. Даже если выходной поток из Реактора 202 (Поток 232) генерируется путем каталитического взаимодействия этана, этилена, кислорода вместе и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или насыщенного хлоруглеводорода, необходимо заметить, что селективность катализатора при превращании этих потоков в VCM выигрывает, прежде всего за счет предварительного кондиционирования катализаторов на основе лантаноидов с помощью элементарного хлора. Селективность катализатора при превращании этих потоков в VCM с использованием катализаторов на основе лантаноидов также улучшается, когда элементарный хлор (Поток 228) включен как часть в состав источника хлора в Реактор 202. Нужно также заметить, что все иные системы катализаторов, которые демонстрируют способность к превращанию как этана, так и этилена в VCM, могут быть также с выгодой использованы в альтернативных воплощениях, вместе с описанными здесь способом и устройством для получения VCM.
Источники хлора (выбранные из хлористого водорода, хлора и хлоруглеводорода), Входной Поток HCl 224, Входной Поток Хлора 228, какая-либо часть ПОТОКА EDC 262, выбранная для рециклирования, и любые другие рециклированные или входные потоки сырья, содержащие, без ограничения, по меньшей мере, одно вещество, выбранное из хлорированного метана или хлорированного этана (например, без ограничения, четыреххлористый углерод, 1,2-дихлорэтан, этилхлорид, 1,1-дихлорэтан и 1,1,2-трихлорэтан) коллективно поставляют хлор в реакцию оксидегидрохлорирования; эти потоки индивидуально изменяются от одного момента времени к другому при работе в режиме реального времени для обеспечения стехиометрического количества хлора, необходимого для превращения с получением VCM. Что касается EDC из Потока EDC 262, рыночные условия, влияющие на возможность непосредственной продажи, определяют соответствующие количества либо для рециклирования в Реактор 202, либо непосредственно для продажи. Дополнительной возможностью для использования части Потока EDC 262, в зависимости от конкретных возможностей, является введение в качестве сырья в печь конверсии в VCM. В этом отношении работа Способа 200 альтернативно осуществляется таким образом, что (а) 1,2-дихлорэтан, генерируемый в Реакторе 202, очищают для продажи, (b) 1, 2-дихлорэтан, генерируемый в Реакторе 202 очищают для рециклирования в Реактор 202, и/или (с) 1,2-дихлорэтан, генерируемый в Реакторе 202, очищают для крекинга в печи для получения винила. Необходимо также заметить, что иногда также выгодно покупать EDC в качестве источника хлора.
Реактор 202 Оксидегидрохлорирования Этана/Этилена до VCM выдает выходной поток из Реактора 232 для ввода в Охлаждающий Конденсор 204. Охлаждающий Конденсор 204 обрабатывает выходной поток из Реактора 232 с получением (а) потока сырого продукта (пара), содержащего первую часть хлористого водорода, и (b) потока сырого охлажденного (водного) хлористого водорода, содержащего оставшуюся часть хлористого водорода, который покидает Реактор 202; поток сырого продукта (пара) представляет собой Поток 240.
Поток 234 переносится в Подсистему 206 Фазового Разделения для удаления оставшихся органических соединений из сырого охлажденного HCl. Подсистема 206 Фазового Разделения представляет собой, в альтернативных воплощениях, отстойник, десорбер или сочетание отстойника и десорбера. Из Подсистемы 206 Фазового Разделения удаленные органические материалы (в основном, в жидкой фазе) переносятся в Колонну 210 Выделения Легких Фракций с помощью Потока 242, и выделенный сырой охлажденный (в основном, жидкий водный раствор) HCl переносится в виде Потока 236 в Подсистему 208 Извлечения Безводного HCl. Подсистема 208 Извлечения Безводного HCl принимает (водный) Поток 274 из Узла 214 Окисления Отходов (узел термического окисления или иного окисления, пригодный для очистки выходного потока до композиций, приемлемых для окружающей среды), Поток 278 (водный) из Узла 276 Адсорбции HCl из Легких Фракций и (водный) Поток 236, и генерирует выходной поток - Поток 266 в виде рецикла безводного HCl в Реактор 202 Оксидегидрохлорирования Этана/Этилена до VCM. Поток 268 выводит воду из Подсистемы Извлечения Безводного HCl 208 для последующего использования или для извлечения отходов. В итоге. Подсистема 208 Извлечения Безводного HCl функционирует с извлечением потока безводного хлористого водорода из потока сырого охлажденного хлористого водорода и других потоков водных растворов HCl Способа 200. Подсистема 208 Извлечения Безводного HCl также рециклирует поток безводного хлористого водорода (пар) в реактор. Как должно быть понятно специалистам в данной области, существуют и другие методики для выделения безводного HCl из смесей воды и HCl.
Охлаждающий Конденсор 204 также выдает Поток 240 (пар) в Колонну 210 Выделения Легких Фракций, где поток легких фракций (паровой Поток 244), содержащий этилен, дополнительно удаляется из выходного потока продукта из реактора. Заметим, что, в противоположность ранее обсуждавшейся системе согласно Фиг.1 этилен из Колонны 210 Выделения Легких Фракций по большей части возвращается в виде рецикла в Реактор 202 Оксидегидрохлорирования Этана/Этилена до VCM без превращения в EDC.
После выделения HCl и потока легких фракций (Поток 244) из выходного потока из реактора Колонна 210 Выделения Легких Фракций направляет Поток 252 для разделения потока продукта - воды, потока продукта - мономера винилхлорида (Поток 254), потока этилхлорида (Поток 230), смешанного потока цис-1,2-дихлорэтилена и транс-1,2-дихлорэтилена (Поток 260), потока 1,2-дихлорэтана (Поток 262) и потока тяжелых фракций (Поток 264). Способ осуществления этих конечных отделений является очевидным для специалиста в данной области, и значительное количество используемых в классических способах узлов может использоваться в различных конфигурациях для достижения этих разделений. Подсистему 216 Сушки, Колонну 218 для Очистки VCM и Колонну 220 Удаления Тяжелых Фракций удобно обозначать, следовательно, как общие системы разделения (и, как таковые, они должны иметь термин "колонна", интерпретируемый как "виртуальная колонна", представляющие собой, по меньшей мере, одну физическую колонну, хотя, в одном из предполагаемых воплощений, каждая колонна может быть отдельной физической колонной) для разделения Потока Воды 256, Потока Продукта VCM 254, Потока Этилхлорида 230, Потока цис/транс-1,2-дихлорэтилена 260 и Потока EDC 262, с Потоком Тяжелых Фракций 264 в качестве органического материала для уничтожения в печи для сжигания органических отходов или для использования в соответствующем продукте, где общие свойства Потока Тяжелых Фракций 264 являются приемлемыми. В альтернативном предполагаемом воплощении Подсистема 216 Сушки удаляет воду перед Колонной 210 Выделения Легких Фракций, при этом выходной поток из Колонны 210 Выделения Легких Фракций направляется в Колонну 218 Очистки VCM. Снова заметим, что по отношению к EDC из Потока EDC 262 рыночные условия влияют на возможность его непосредственной продажи, определяя соответствующее количество либо для рециклирования в Реактор 202, либо для непосредственной продажи. В этом отношении работа Колонны 218 Очистки VCM и Колонны 220 Удаления Тяжелых Фракций производится попеременно, так что (а) 1,2-дихлорэтан очищается для продажи, (b) 1,2-дихлорэтан очищается для рециклирования в Реактор 202 и/или (с) 1, 2-дихлорэтан очищается для крекинга в печи для получения винила.
Обратимся теперь к Потоку 244, в том виде как он выходит из Колонны 210 Выделения Легких Фракций. Поток 244 разделяют на первую часть потока, направляемую непосредственно в Потоке 248 в Реактор 202 Оксидегидрохлорирования Этана/Этилена до VCM, и на второй поток, который направляют сначала в Узел 276 абсорбции HCl из Легких Фракций, а затем в Колонны 212 Абсорбции и Отделения С2. Узел 276 Абсорбции HCl из Легких Фракций дает на выходе водный раствор HCl в виде Потока 278 в Подсистему 208 Извлечения Безводного HCl. Колонны 212 Абсорбции и Отделения С2 абсорбируют и отделяют материалы С2 (этан и этилен) от направляемой второй части потока из Потока 244 и обеспечивают рециклирование материалов С2 в Реактор 202 с помощью Потока 246 Рецикла С2, который, в сочетании с первой частью потока из Потока 244, образует Поток 248. Колонны 212 Абсорбции и Отделения С2 также выдают продувочный поток в УЗЕЛ 214 ОКИСЛЕНИЯ ОТХОДОВ, который выдает ПОТОК 250 ОТХОДОВ в атмосферу, а также (водный) Поток 274 в Подсистему 208 Извлечения Безводного HCl. Устройства для контроля содержания СО (моноокиси углерода) в композиции обеспечивают измерения (не показано) для использования системой контроля (не показано) при определении соответствующей части остаточных газообразных легких фракций для обработки с помощью Колонн 212 Адсорбции и Отделения С2 и Узла 214 Окисления Отходов с целью генерирования Потока 250 Отходов таким образом, чтобы СО не накапливался до уровней, неприемлемых в процессе.
Модельные относительные скорости потоков и составы потоков для Способа 202 Оксидегидрохлорирования ЭТАНА ДО VCM ясны из рассмотрения таблицы 1. Данные таблицы 1 (единица массы/единица времени) используют выполненные в лаборатории измерения рабочих характеристик катализатора для оксихлорида лантана при 400°C и при давлении, по существу, окружающей среды; дополнительные детали по предпочтительному катализатору ясны из исследования "A PROCESS FOR THE CONVERSION OF ETHYLENE TO VINYL CHLORIDE, AND NOVEL CATALYST COMPOSITIONS USEFUL FOR SUCH PROCESS». Таблица 1 показывает некоторые потоки как нулевые, в контексте генерации данных при моделировании, но такое численное значение не предназначено для обозначения полного отсутствия потока или отсутствия необходимости в потоке. Таблица 1 не показывает входного Потока Этилена 289; в этом отношении, и, повторяя предыдущие рассуждения, когда рынок и рабочие условия в конкретный момент производства позволяют, наиболее предпочтительным режимом для Потока Этилена 289 является нулевой поток. Однако при определенных условиях Поток Этилена 289 дает экономически выгодный поток.
Обратимся теперь к фиг.3. Процесс 300 Оксидегидрохлорирования Этана до VCM с цис/транс-Рециклированием является модификацией процесса 200 Оксидегидрохлорирования Этана до VCM за счет включения Узла 280 Гидрирования DCE (дихлорэтилен) для (а) гидрирования цис-1, 2-дихлорэтилена и транс-1,2-дихлорэтилена из потока цис/транс-1,2-дихлорэтилена 260 и (b) рециклирования выходного потока в Реактор 202. В альтернативном воплощении Потоки 230, 260, и 262 отделяют в виде единого смешанного потока в Колонну 220 для Удаления Тяжелых Фракций и этот единый смешанный поток рециклируют в Узел 280 Гидрирования DCE.
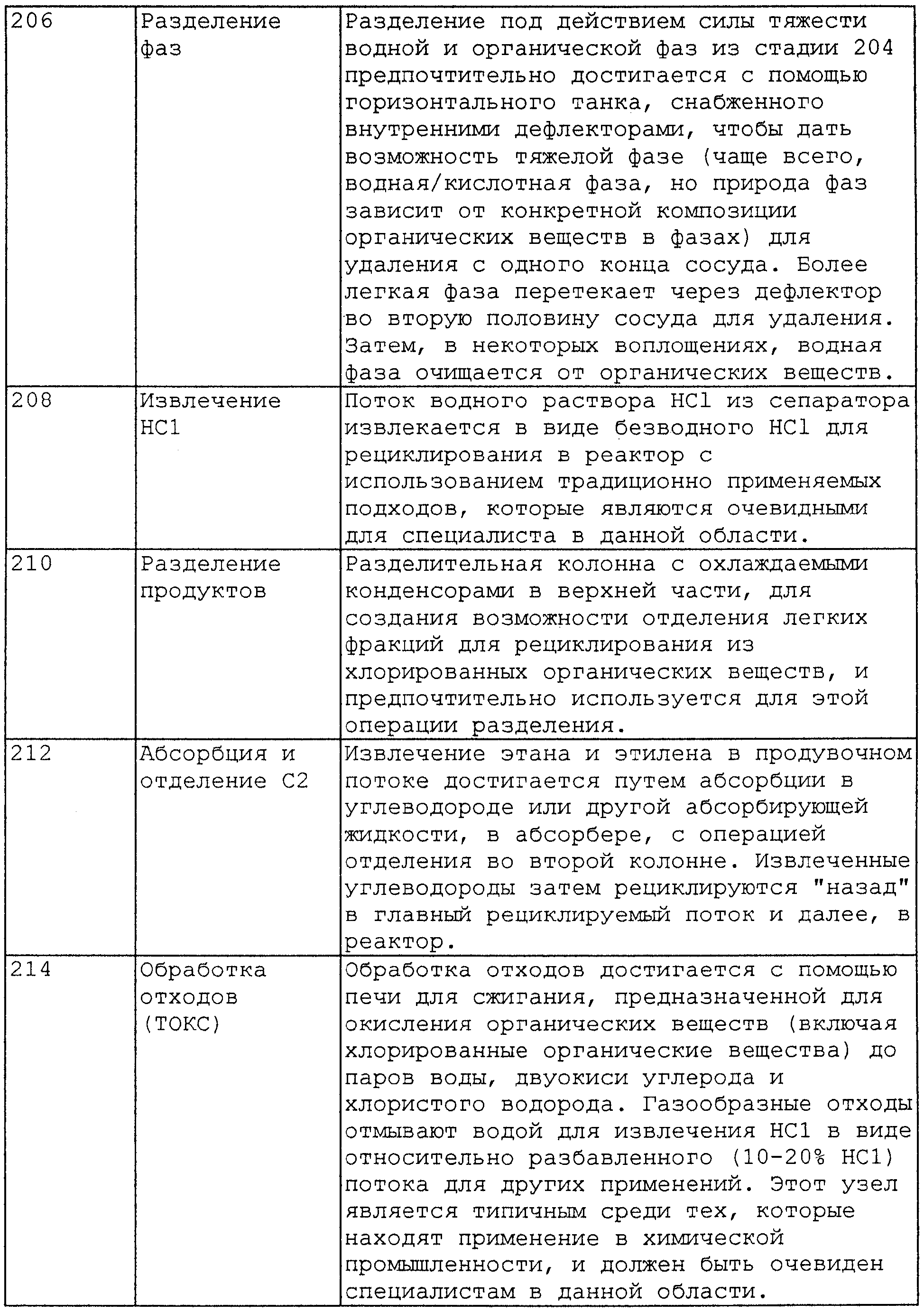
Таблица 2 представляет дополнительные подробности относительно компонентов, указанных на чертежах.




Конкретные особенности катализаторов дополнительно разъясняются с помощью рассмотрения следующих примеров, которые, как предполагается, являются чисто пояснительными.
Пример 1
Для демонстрации производства винилхлорида из потока, содержащего этилен, готовят пористую, огнеупорную композицию, содержащую лантан. Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (получают от J.T. Baker Chemical Company) в 8 частях деионизованной воды. Добавление по каплям при перемешивании гидроксида аммония (получают от Fisher Scientific, сертифицированная спецификация ACS) до получения нейтрального рН (по универсальной индикаторной бумаге) вызывает образование геля. Смесь центрифугируют и раствор декантируют с твердого продукта. Добавляют приблизительно 150 мл деионизованной воды и гель энергично перемешивают для диспергирования твердого продукта. Полученный раствор центрифугируют и раствор декантируют. Эту стадию промывки повторяют дополнительно два раза. Собранный промытый гель сушат в течение двух часов при 120°С, а затем прокаливают при 550°С в течение четырех часов на воздухе. Полученный твердый продукт измельчают и просеивают с получением частиц, пригодных для дополнительного исследования. Эта методика дает твердый продукт с дифрактограммой рентгеноструктурного анализа на порошке, соответствующей LaOCl.
Частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы этилен, этан, HCl, O2 и инертный газ (смесь Не и Ar) можно было вводить в реактор. Функция аргона состоит в том, чтобы служить внутренним стандартом для анализа веществ, входящих в реактор и выходящих из него, с помощью газовой хроматографии. Время контакта (объемное) вычисляется как объем катализатора, деленный на объемную скорость потока при стандартных условиях. Скорости подачи соответствуют мольным отношениям. В систему реактора подается непосредственно этансодержащий поток со стехиометрией один этан, один HCl и один кислород. Это обеспечивает сбалансированную стехиометрию для производства VCM из этилена.
Таблица 3 ниже представляет результаты исследований реактора с использованием этой композиции.
Столбец 1 таблицы 3 демонстрирует высокую селективность по отношению к винилхлориду, когда в систему катализаторов подается этилен при окислительных условиях в присутствии HCl. Композиция содержит гелий с целью моделирования реактора, работающего с воздухом в качестве окисляющего газа.
Столбец 2 таблицы 3 показывает высокую селективность по отношению к винилхлориду, когда в систему катализаторов подается этилен при окислительных условиях в присутствии HCl. Теперь композиция обогащена горючим для устранения ограничений, налагаемых воспламеняемостью, и не содержит гелия.
Столбец 3 таблицы 3 показывает высокую селективность по отношению к винилхлориду и этилену, когда в систему катализаторов подают этан при окислительных условиях в присутствии HCl. Композиция моделирует реактор, работающий с воздухом в качестве окисляющего газа. Этилен во входном потоке не присутствует. Этилен, присутствующий в реакторе, является продуктом частичного окисления этана.
Столбец 4 таблицы 3 показывает результат для случая, когда вводят как этан, так и этилен. Реактор работает таким образом, что количества этилена, вводимого в реактор и покидающего реактор, равны. При работе таким образом этилен выступает в роли инертного разбавителя, и превращается только этан. Результаты показывают высокий выход винилхлорида и 1,2-дихлорэтана. Аргон используется в качестве внутреннего стандарта для обеспечения того, чтобы поток этилена, входящий в реактор, и поток, покидающий реактор, были равны. Отношения площадей под хроматографическими пиками этилена и аргона являются идентичными для входного и выходного потока из реактора. Таким путем рециклирование этилена моделируется внутри реакторного устройства.
Пример 2
Для дальнейшей демонстрации использования композиции этилен окислительно превращают в винилхлорид с использованием разнообразных источников хлора. Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Avocado Research Chemicals Ltd.) в 6,6 частях деионизованной воды. Быстрое добавление при перемешивании 6М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь фильтруют, чтобы собрать твердый продукт. Собранный гель сушат при 120°С перед прокаливанием при 550°С в течение четырех часов на воздухе. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор можно было вводить этилен, HCl, кислород, 1,2-дихлорэтан, четыреххлористый углерод и гелий. Время контакта (объемное) вычисляют как объем катализатора, деленный на объемную скорость потока при стандартной температуре и давлении. Скорости входных потоков соответствуют мольным отношениям. Композицию нагревают до 400°С и обрабатывают смесью 1:1:3 HCl:O2:Не в течение 2 часов перед началом работы.
Работа полученной композиции в производстве винилхлорида происходит путем подачи этилена, источника хлора и кислорода при 400°С. Следующая далее таблица демонстрирует данные по потоку, полученные между 82 и 163 часами с использованием различных источников хлора. Хлор подают в виде HCl, четыреххлористого углерода и 1,2-дихлорэтана. VCM обозначает винилхлорид. Время контакта (объемное) вычисляют как объем катализатора, деленный на объемную скорость потока при стандартной температуре и давлении. Реакторы работают при атмосферном давлении на выходе реактора. Как этилен, так и 1,2-дихлорэтан обозначаются как частицы С2 .
Эти данные показывают, что множество источников хлора может использоваться при окислительном получении винила. При использовании четыреххлористого углерода, 1,2-дихлорэтана и HCl все они дают винилхлорид в качестве доминирующего продукта.
Пример 3
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Avocado Research Chemicals Ltd.) в 6,67 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля и дает конечное значение рН 8,85. Смесь фильтруют, чтобы собрать твердый продукт. Собранный материал прокаливают на воздухе при 550°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ.
Таблица 5 демонстрирует данные, где входные потоки в реактор устанавливаются таким образом, что поток этилена (моль/мин), входящий в реактор, и поток этилена, покидающий реактор, являются по существу одинаковыми. Подобным же образом входные потоки в реактор, аналогично, регулируются таким образом, что потоки HCl, входящие в реактор и покидающие его, являются по существу одинаковыми. Степень превращения кислорода устанавливается несколько меньшей, чем полная конверсия, чтобы сделать возможным мониторинг активности катализатора. При работе в таком режиме потребляемыми вводимыми веществами являются этан, кислород и хлор. Как этилен, так и HCl выступают в роли веществ, которые не производятся и не потребляются. Время контакта вычисляется как объем катализатора, деленный на объемную скорость потока при стандартной температуре и давлении. Настоящий пример дополнительно иллюстрирует использование газообразного хлора в качестве источника хлора при производстве винилхлорида.
Как и во всех примерах, VCM здесь обозначает винилхлорид. С2Н4Cl2 является только 1,2-дихлорэтаном. СОх представляет собой сочетание СО и CO2.
Примеры 4 - 11
Примеры 4 - 11 иллюстрируют получение многочисленных редкоземельных композиций, каждая из которых содержит только один редкоземельный материал. Данные, иллюстрирующие рабочие характеристики этих композиций, представлены в таблице 6.
Пример 4
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Aldrich Chemical Company) в 6,67 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Гель повторно суспендируют в 6,66 части деионизованной воды. Центрифугирование позволяет собрать гель. Собранный гель сушат при 120°С перед прокаливанием при 550°С в течение четырех часов на воздухе. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы этилен, этан, HCl, кислород, и инертный (смесь гелия и аргона) газ могли быть введены в реактор. Рентгеноструктурный анализ на порошке показывает, что материал представляет собой LaOCl. Измеренная площадь поверхности по БЭТ составляет 42,06 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 6.
Пример 5
Раствор NdCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида неодима (Alfa Aesar) в 6,67 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь фильтруют, чтобы собрать твердый продукт. Собранный гель сушат при 120°С перед прокаливанием на воздухе при 550°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Рентгеноструктурный анализ на порошке показывает, что материал представляет собой NdOCl. Измеренная площадь поверхности по БЭТ составляет 22,71 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 6.
Пример 6
Раствор PrCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида празеодима (Alfa Aesar) в 6,67 части деионизованной воды. Повторение добавления при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь фильтруют, чтобы собрать твердый продукт. Собранный гель сушат при 120°С перед прокаливанием на воздухе при 550°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Рентгеноструктурный анализ на порошке показывает, что материал представляет собой PrOCl. Измеренная площадь поверхности по БЭТ составляет 21, 37 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 6.
Пример 7
Раствор SmCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида самария (Alfa Aesar) в 6,67 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь фильтруют, чтобы собрать твердый продукт. Собранный гель сушат при 120°С перед прокаливанием при 500°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Рентгеноструктурный анализ на порошке показывает, что материал представляет собой SmOCl. Измеренная площадь поверхности по БЭТ составляет 30,09 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 6.
Пример 8
Раствор HoCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида гольмия (Alfa Aesar) в 6,67 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь фильтруют, чтобы собрать твердый продукт. Собранный гель сушат при 120°С перед прокаливанием при 500°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 20,92 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 6.
Пример 9
Раствор ErCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида эрбия (Alfa Aesar) в 6,67 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь фильтруют, чтобы собрать твердый продукт. Собранный гель сушат при 120°С перед прокаливанием при 500°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 19,80 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 6.
Пример 10
Раствор VbCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида иттербия (Alfa Aesar) в 6,67 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь фильтруют, чтобы собрать твердый продукт. Собранный гель сушат при 120°С перед прокаливанием при 500°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 2,23 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 6.
Пример 11
Раствор YCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида иттрия (Alfa Aesar) в 6,67 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь фильтруют, чтобы собрать твердый продукт. Собранный гель сушат при 120°С перед прокаливанием при 500°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 29,72 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 6.
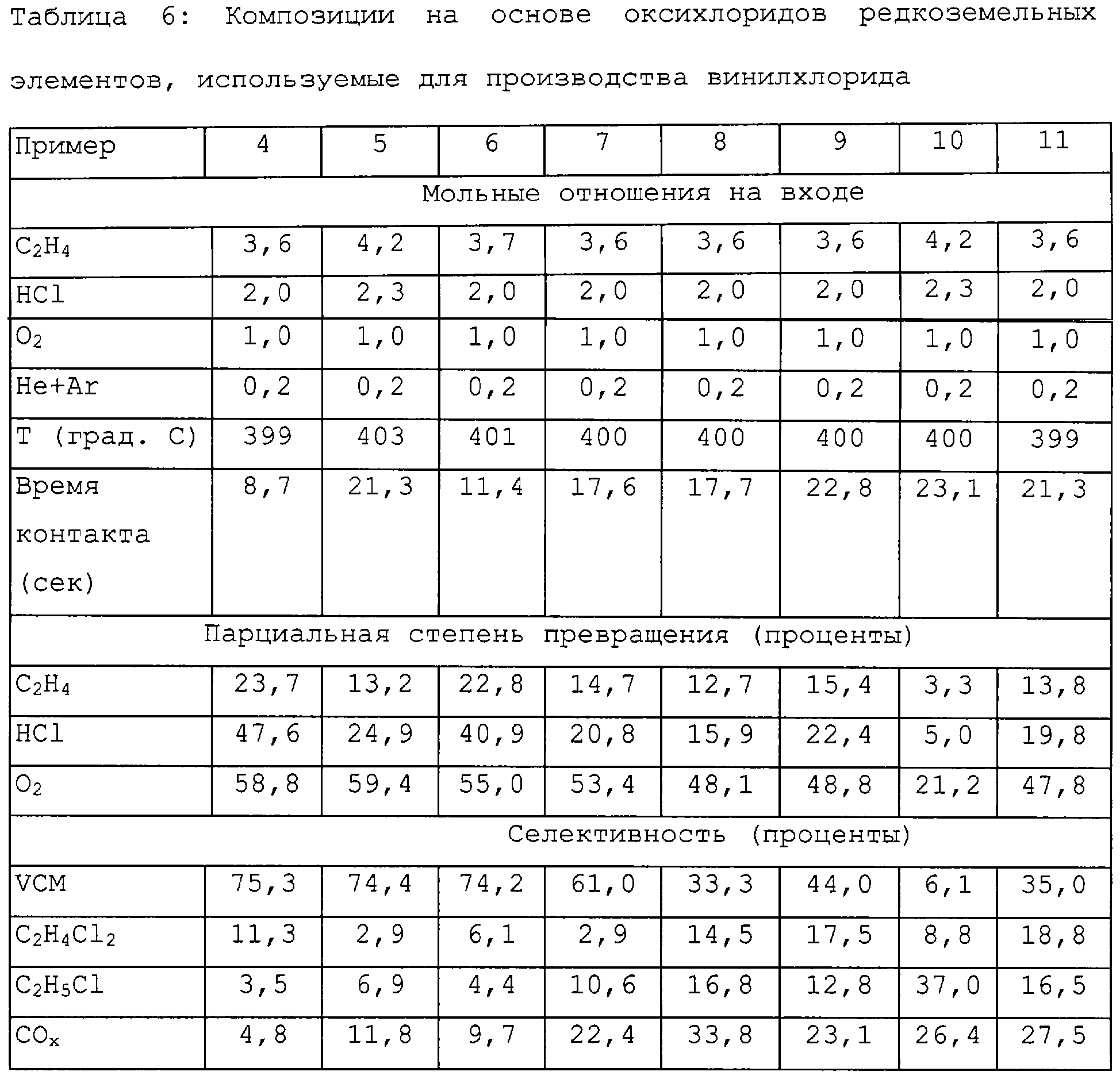
Эти данные демонстрируют пригодность объемных композиций, содержащих редкоземельные элементы, для конверсии этиленсодержащих потоков в винилхлорид.
Примеры 12 - 16
Примеры 12 - 16 иллюстрируют получение различных композиций на основе редкоземельных элементов, каждая из которых содержит смеси редкоземельных материалов. Данные, иллюстрирующие рабочие характеристики этих образцов, представлены в таблице 7.
Пример 12
Раствор LaCl3 и NdCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Spectrum Quality Products) и 0,67 части коммерчески доступного гидратированного хлорида неодима (Alfa Aesar) в 13,33 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Конечное измеренное значение рН составляет 8,96. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Собранный гель сушат при 80°С перед прокаливанием на воздухе при 550°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 21,40 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 7.
Пример 13
Раствор LaCl3 и SmCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Spectrum Quality Products) и 0,67 части коммерчески доступного гидратированного хлорида самария (Alfa Aesar) в 13,33 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Конечное измеренное значение рН составляет 8,96. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Собранный гель сушат при 80°С перед прокаливанием на воздухе при 550°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 21,01 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 7.
Пример 14
Раствор LaCl3 и YCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Spectrum Quality Products) и 0,52 части коммерчески доступного гидратированного хлорида иттрия (Alfa Aesar) в 13,33 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Конечное измеренное значение рН составляет 8,96. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Собранный гель сушат при 80°С перед прокаливанием на воздухе при 550°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 20,98 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 7.
Пример 15
Раствор LaCl3 и HoCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Spectrum Quality Products) и одной части коммерчески доступного гидратированного хлорида гольмия (Alfa Aesar) в 13,33 частях деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Конечное измеренное значение рН составляет 8,64. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют из геля и отбрасывают. Собранный гель сушат при 80°С перед прокаливанием на воздухе при 550°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 19,68 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 7.
Пример 16
Раствор LaCl3 и HoCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Spectrum Quality Products) и 0,75 части коммерчески доступного гидратированного хлорида иттербия (Alfa Aesar) в 13,33 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Конечное измеренное значение рН составляет 9,10. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Собранный гель сушат при 80°С перед прокаливанием на воздухе при 550°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 20,98 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 7.

Эти данные демонстрируют пригодность объемных, содержащих редкоземельные элементы композиций, которые содержат смеси редкоземельных материалов, для превращения этиленсодержащих потоков в винилхлорид.
Примеры 17 - 24
Примеры 17 - 24 представляют собой композиции, содержащие редкоземельные материалы с присутствием других добавок.
Пример 17
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Aldrich Chemical Company) в 6,67 части деионизованной воды. 0,48 части гидроксида аммония (Fisher Scientific) добавляют к 0,35 части порошка CeO2, полученного уже приготовленным из коммерческих источников (Rhone-Poulenc). Содержащие лантан и церий смеси добавляют вместе при перемешивании для образования геля. Полученную в результате, содержащую гель смесь фильтруют и собранный твердый продукт прокаливают на воздухе при 550°С в течение 4 часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 8.
Пример 18
Композицию, содержащую лантан, приготовленную с использованием способа примера 5, измельчают с помощью ступки и пестика с формированием мелкодисперсного порошка. Одну часть измельченного порошка объединяют с 0,43 части порошка BaCl2 и дополнительно измельчают с использованием ступки и пестика для образования однородной смеси. Содержащую лантан и барий смесь прессуют для формирования кусков. Куски прокаливают при 800°С на воздухе в течение 4 часов. Полученный материал помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 8.
Пример 19
Высушенную окись кремния Grace Davison Grade 57 сушат при 120°С в течение 2 часов. Насыщенный раствор LaCl3 в воде образуется с использованием коммерчески доступного гидратированного хлорида лантана. Высушенную окись кремния пропитывают до точки появления влажности с помощью раствора LaCl3. Пропитанную окись кремния оставляют сушиться на воздухе в течение 2 дней при температуре окружающей среды. Ее дополнительно сушат при 120°С в течение 1 часа. Полученный материал помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 8.
Пример 20
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Spectrum Quality Products) в 6,67 части деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Гель повторно суспендируют в 12,5 части ацетона (Fisher Scientific), центрифугируют и жидкость опять декантируют и отбрасывают. Стадия промывки ацетоном дополнительно повторяется 4 раза, с использованием 8,3 части ацетона. Гель повторно суспендируют в 12,5 части ацетона, добавляют 1,15 части гексаметилдисилизана (покупают у Aldrich Chemical Company) и раствор перемешивают в течение одного часа. Смесь центрифугируют, чтобы собрать гель. Собранному гелю дают возможность сушиться на воздухе при температуре окружающей среды перед прокаливанием на воздухе при 550°С в течение четырех часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Измеренная площадь поверхности по БЭТ составляет 58,82 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 8.
Пример 21
Раствор LaCl2 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (Alfa Aesar) и 0,043 части коммерчески доступного HfCl4 (покупают у Acros Organics) в 10 частях деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Собранный гель сушат при 80°С в течение ночи перед прокаливанием при 550°С в течение 4 часов. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 8.
Пример 22
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (Alfa Aesar) и 0,086 части коммерчески доступного HfCl4 (покупают у Acros Organics) в 10 частях деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Собранный гель сушат при 80° С в течение ночи перед прокаливанием при 550°С в течение 4 часов. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 8.
Пример 23
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (Alfa Aesar) и 0,043 части коммерчески доступного ZrOCl2 (покупают у Acros Organics) в 10 частях деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Гель повторно суспендируют в 6,67 части деионизованной воды и впоследствии центрифугируют. Раствор декантируют и отбрасывают. Собранный гель прокаливаютпри 550°С в течение 4 часов. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 8.
Пример 24
Раствор LaCl3 в воде готовят путем растворения коммерчески доступного гидратированного хлорида лантана в деионизованной воде с получением 2,16 М раствора. Коммерчески произведенный оксид циркония (получают от Engelhard) сушат при 350°С в течение ночи. Одну часть оксида циркония пропитывают 0,4 части раствора LaCl3. Образец сушат на воздухе при комнатной температуре, а затем прокаливают на воздухе при 550°С в течение 4 часов. Полученный твердый продукт измельчают и просеивают. Просеянные частицы помещают в реактор из чистого никеля (сплав 200). Реактор конфигурируют таким образом, чтобы в реактор могли быть введены этилен, этан, HCl, кислород и инертный (смесь гелия и аргона) газ. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 8.
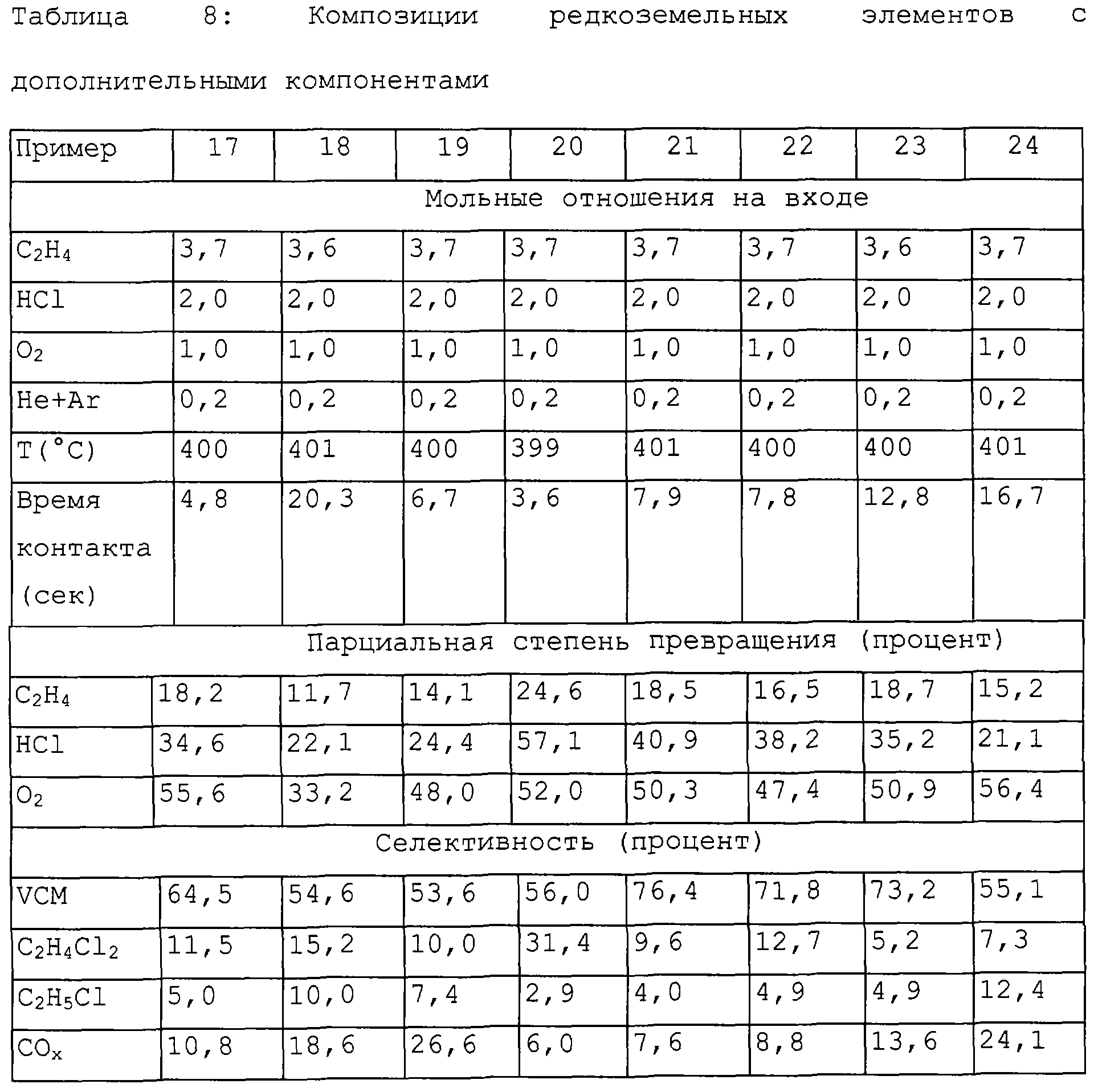
Эти данные демонстрируют получение винилхлорида из этиленсодержащих потоков с использованием катализаторов на основе лантана, которые содержат другие элементы или нанесены на подложку.
Примеры 25 - 30
Примеры 25 - 30 демонстрируют некоторые модификации, которые возможны для изменения приготовления композиций с редкоземельными элементами, пригодных для использования.
Пример 25
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Spectrum Quality Products) в 10 частях деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь центрифугируют, чтобы собрать твердый продукт. Раствор декантируют с геля и отбрасывают. Готовят насыщенный раствор 0,61 части бензилтриэтиламмонийхлорида (покупают у Aldrich Chemical Company) в деионизованной воде. Раствор добавляют к гелю и перемешивают. Собранный гель прокаливают при 550°С в течение 4 часов. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 9. Этот пример иллюстрирует использование добавленных солей аммония для изменения приготовления композиций с редкоземельными элементами.
Пример 26
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Spectrum Quality Products) в 10 частях деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь центрифугируют, чтобы собрать твердый продукт. Добавляют одну часть ледяной уксусной кислоты к гелю, и гель повторно растворяется. Добавление раствора к 26 частям ацетона вызывает образование осадка. Раствор декантируют и твердый продукт прокаливают при 550°С в течение 4 часов. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 9. Этот пример демонстрирует приготовление композиций с лантаном, пригодных для использования путем разложения продуктов добавления хлора к карбоновым кислотам, содержащих соединения редкоземельных элементов.
Пример 27
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Spectrum Quality Products) в 10 частях деионизованной воды. Быстрое добавление при перемешивании 6 М гидроксида аммония в воде (разбавленный сертифицированный реагент ACS, получают от Fisher Scientific) вызывает образование геля. Смесь центрифугируют, чтобы собрать твердый продукт. Собранный гель повторно суспендируют в 3,33 части деионизованной воды. Последующее добавление 0,0311 части реагента фосфорной кислоты (покупают у Fisher Scientific) не производит видимых изменений в суспендированном геле. Смесь снова центрифугируют и раствор декантируют с содержащего фосфор геля. Собранный гель прокаливают при 550°С в течение 4 часов. Прокаленный твердый продукт имеет площадь поверхности по БЭТ 33,05 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 9. Этот пример демонстрирует приготовление композиций с редкоземельными элементами, также содержащих фосфор в виде фосфата.
Пример 28
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Acros Organics) в 6,66 части деионизованной воды. Раствор формируют путем перемешивания 0,95 части коммерчески доступного DABCO, или 1, 4-диазабицикло[2,2,2]октана (покупают у ICN Pharmaceuticals), растворенного в 2,6 части деионизованной воды. Быстрое смешивание двух растворов при перемешивании вызывает образование геля. Смесь центрифугируют, чтобы собрать твердый продукт. Собранный гель повторно суспендируют в 6,67 части деионизованной воды. Смесь снова центрифугируют и раствор декантируют с геля. Собранный гель прокаливают в течение 4 часов при 550°С. Прокаленный твердый продукт имеет площадь поверхности по БЭТ 38,77 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 9. Этот пример демонстрирует пригодность алкиламина при приготовлении композиции с редкоземельными элементами, пригодной для использования.
Пример 29
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Acros Organics) в 10 частях деионизованной воды. К этому раствору быстро добавляют 2,9 части коммерчески доступного тетраметиламмонийгидроксида (покупают у Aldrich Chemical Company) при перемешивании, вызывая образование геля. Смесь центрифугируют и раствор декантируют с геля. Собранный гель повторно суспендируют в 6,67 части деионизованной воды. Смесь снова центрифугируют и раствор декантируют с геля. Собранный гель прокаливают в течение 4 часов при 550°С. Прокаленный твердый продукт имеет площадь поверхности по БЭТ 80,35 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 9. Этот пример демонстрирует пригодность алкиламмонийгидроксида при приготовлении композиции с редкоземельными элементами, пригодной для использования.
Пример 30
Раствор LaCl3 в воде готовят путем растворения одной части коммерчески доступного гидратированного хлорида лантана (покупают у Avocado Research Chemicals Ltd.) в 6,67 части деионизованной воды. К этому раствору быстро и при перемешивании добавляют 1,63 части коммерчески доступного 5 н. раствора NaOH (Fisher Scientific), вызывая формирование геля. Смесь центрифугируют и раствор декантируют с геля. Собранный гель прокаливают в течение 4 часов при 550°С. Прокаленный твердый продукт имеет площадь поверхности по БЭТ 16,23 м2/г. Конкретные данные по рабочим характеристикам для этого примера представлены ниже в таблице 9. Этот пример демонстрирует пригодность не содержащих азота оснований для формирования каталитически интересующих материалов. Хотя они и являются потенциально функциональными, исследуемые материалы, видимо, являются неполноценными по отношению к тем, которые производят с использованием содержащих азот оснований.

Настоящее изобретение описано иллюстративным образом. В этой связи, является очевидным, что специалист в данной области, как только он поймет преимущества согласно предыдущему описанию, сможет производить модификации описанных здесь конкретных воплощений, без отклонений от сути настоящего изобретения. Такие модификации должны рассматриваться в рамках настоящего изобретения, которое ограничивается только объемами и сутью прилагаемой формулы изобретения.
Реферат
Изобретение относится к получению мономера винилхлорида из этана и этилена. Способ осуществляют путем генерирования выходного потока из реактора путем каталитического взаимодействия совместно этана, этилена, кислорода и, по меньшей мере, одного источника хлора, выбранного из хлористого водорода, хлора или хлоруглеводорода, где мольное отношение указанного этана к указанному этилену находится в пределах от 0,02 до 50. На указанной стадии каталитического взаимодействия используют катализатор, содержащий компонент редкоземельного материала, при условии, что катализатор практически не содержит железа и меди, и при дополнительном условии, что когда компонент редкоземельного материала представляет собой церий, катализатор дополнительно содержит, по меньшей мере, еще один компонент редкоземельного материала, иной чем церий. Указанный выходной поток из реактора охлаждают и конденсируют с образованием потока сырого продукта, содержащего первую часть указанного хлористого водорода, и потока сырого охлажденного хлористого водорода, содержащего вторую часть указанного хлористого водорода. Затем разделяют указанный поток сырого продукта на поток продукта - мономера винилхлорида - и на поток легких фракций, содержащий указанную первую часть указанного хлористого водорода. И рециклируют указанный поток легких фракций для каталитического взаимодействия совместно с указанным этаном, указанным этиленом, указанным кислородом и указанным источником хлора на указанной стадии генерирования. Также предложены варианты способа производства винилхлорида из этана и этилена. Технический результат - получение винила из этана/этилена, путем полного извлечения хлористого водорода из выходного потока реактора. 4 н. и 36 з.п. ф-лы, 9 табл., 3 ил.

Формула
Документы, цитированные в отчёте о поиске
Способ каталитического оксихлорирования этана до винилхлорида
Патенты аналоги
Способ каталитического оксихлорирования этана до винилхлорида

Комментарии