Применение lactobacillus paracasei для усиления восстановления разнообразия кишечной микрофлоры после дисбактериоза - RU2704133C2
Код документа: RU2704133C2
Чертежи




Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к области пробиотиков. В частности, изобретение касается применения Lactobacillus paracasei (L. paracasei) для восстановления разнообразия кишечной микрофлоры (микробиоты) у субъекта. В предпочтительном воплощении настоящее изобретение касается применения Lactobacillus paracasei subsp. paracasei для ускорения снижения Enterococcus faecalis в микрофлоре кишечника у субъекта с дисбактериозом (дисбиозом) кишечника.
Уровень техники
Согласно определению, составленному совместно экспертами Продовольственной и сельскохозяйственной организации ООН и Всемирной организации здравоохранения (FAO/WHO) в Рекомендации по вопросам здравоохранения и питательных свойств сухого молока с живыми молочнокислыми бактериями в 2001 г., пробиотиками являются "живые микроорганизмы, которые при введении в достаточных количествах приносят пользу для здоровья хозяина". Пробиотические бактерии были описаны среди видов, относящихся к родам Lactobacillus, Bifidobacterium, Streptococcus и Lactococcus, которые обычно используются в молочной промышленности. Считается, что пробиотики действуют на уровне кишечной микрофлоры, препятствуя развитию патогенных микроорганизмов и/или действуя более непосредственно на иммунную систему.
Оппортунистические бактериальные инфекции, ответственные за связанные со здравоохранением инфекции (HAIs), вносят значительный вклад в смертность и заболеваемость пациентов, а также в расходы на здравоохранение как в развитых, так и в развивающихся странах (WHO, 2008). Желудочно-кишечный тракт (ЖКТ) является резервуаром для условно-патогенных микроорганизмов, которые извлекают выгоду из нарушения баланса кишечной микрофлоры или дисбактериоза, вторгаясь и заражая восприимчивых пациентов. Лечение антибиотиками оказывает вредное воздействие на разнообразие кишечной микрофлоры и способствует распространению условно-патогенных бактерий у человека, включая Enterococcus faecalis, Enterococcus faecium или Clostridium difficile.
Приобретая устойчивость к антибиотикам и другие патогенные признаки, колонизирующие и/или инвазивные изоляты Е. faecalis с множественной лекарственной устойчивостью, которые вызывают серьезные внутрибольничные инфекции, составляют семь адаптированных к больнице комплексов, обозначаемых как клональные комплексы энтерококков высокого риска (High-Risk Enterococcal Clonal Complexes, HiRECCs). Пролиферация и живучесть HiRECCs в GIT является главным фактором риска возникновения устойчивой к ванкомицину энтерококковой (VRE) инфекции, подчеркивая потребность в лучшем понимании биологических и биохимических факторов, задействованных при колонизации GIT Е. faecalis. Изоляты, принадлежащие к HiRECC-2, являются одной из наиболее распространенных причин инфекций Е. faecalis в США и в ряде европейских стран. Некоторые штаммы Е. faecalis приобрели патогенные черты и могут вызывать тяжелые инфекции. Так, они могут колонизировать GIT и/или проходить через барьер кишечного эпителия и попадать в кровоток. Более того, Enterococcus spp. способствуют внебольничным внутрибрюшным инфекциям и входят в число десяти наиболее часто выделяемым микроорганизмов при связанных со здравоохранением инфекциях (HCAI). Поэтому снижение пролиферации и живучести Е. faecalis, особенно HiRECCs, в GIT снижает риск возникновения не только инфекций GIT, но и внутрибрюшных инфекций.
Как видно из вышеизложенного, существует потребность в альтернативах или дополнениях к антибиотикам для лечения или профилактики инфекции Е. faecalis.
"Кишечная микрофлора (микробиота)" означает популяцию микроорганизмов, обитающих в кишечнике любого организма, принадлежащего к царству животных (людей, животных, насекомых и т.д.). Хотя состав микрофлоры у каждого индивида уникален (от 60 до 80 видов бактерий являются общими для более чем 50% выборочной совокупности из общего числа 400-500 различных видов бактерий у индивида), она всегда выполняет аналогичные основные физиологические функции и имеет прямое воздействие на здоровье человека:
- способствует перевариванию некоторых продуктов питания, которые желудок и тонкий кишечник не в состоянии переварить (в основном неусвояемые волокна);
- способствует выработке некоторых витаминов (B и K);
- защищает от агрессии со стороны других микроорганизмов, поддерживая целостность слизистой оболочки кишечника;
- играет важную роль в должном развитии иммунной системы;
- здоровая, разнообразная и сбалансированная микрофлора кишечника играет ключевую роль в обеспечении надлежащего функционирования кишечника.
Принимая во внимание то, что микрофлора кишечника играет важную роль в нормальном функционировании организма и выполняет различные функции, она иногда считается "органом". Однако это "приобретенный" орган, так как младенцы рождаются стерильными; то есть колонизация кишечника начинается с рождения и развивается впоследствии.
Степень нарушения микрофлоры кишечника после таких расстройств, как изменение рациона, лечение антибиотиками и инвазия экзогенных микробов, а также скорость и степень восстановления до состояния перед расстройством, определяется как "устойчивость микрофлоры". Устойчивость микрофлоры варьирует у разных людей и при различных расстройствах у одного индивида.
Из вышеизложенного очевидно, что существует также важная потребность в средствах повышения устойчивости микрофлоры.
Все возрастающая совокупность данных показывает, что пробиотики или трансплантация фекальной микрофлоры предотвращает или лечит целый ряд заболеваний, в том числе кишечные инфекции. Такие подходы также связаны с усилением клиренса VRE из кишечника у мышей.
Сущность изобретения
Вне ожидания, авторы изобретения обнаружили, что бактерии вида Lactobacillus paracasei способны стимулировать восстановление разнообразия кишечной микрофлоры и/или уменьшать нагруженность штаммами Е. faecalis in vivo.
Соответственно, предметом настоящего изобретения является применение Lactobacillus paracasei для повышения устойчивости микрофлоры кишечника. В частности, настоящее изобретение касается применения Lactobacillus paracasei для повышения разнообразия кишечной микрофлоры у субъекта. В предпочтительном воплощении настоящее изобретение касается применения штамма Lactobacillus paracasei для ускорения снижения Enterococcus faecalis в микрофлоре кишечника у субъекта с вызванным антибиотиками дисбактериозом кишечника.
Другие аспекты настоящего изобретения предусматривают применение Lactobacillus paracasei для предотвращения, уменьшения или лечения дисбактериоза кишечника; и/или профилактики заболеваний, вызванных патогенами, присутствующими в желудочно-кишечном тракте; и/или повышения уровня короткоцепочечных жирных кислот у субъекта.
Изобретением также предусмотрены композиции, содержащие Lactobacillus paracasei, для применения в соответствии с настоящим изобретением.
Раскрытие сущности изобретения
В настоящем описании выражение "сохранить разнообразие микрофлоры" применяется для выражения того, что видовое разнообразие (видовое богатство и/или равномерность распределения видов) микрофлоры у индивида не должно существенно изменяться или пострадать, особенно в случае дисбактериоза. В частности, сохранение многообразия микрофлоры могло бы способствовать быстрейшему выздоровлению субъекта в случае риска дисбактериоза или избежать ухудшения дисбактериоза. Выражения "повышение разнообразия микрофлоры", "способствовать восстановлению разнообразия микрофлоры", "лечение/снижение/уменьшение дисбактериоза" и т.д. должны означать повышение видового разнообразия (видового богатства и/или равномерности распределения видов) микрофлоры у индивида. Методы расчета видового разнообразия, видового богатства и равномерности распределения видов известны в данной области и включают, без ограничения, индекс Симпсона, индекс разнообразия Симпсона и обратный индекс Симпсона, индекс Чао и индекс Шеннона.
Кроме того, "ускорить повышение разнообразия кишечной микрофлоры", "способствовать восстановлению разнообразия микрофлоры кишечника", "способствовать возврату к исходному/нормальному/здоровому разнообразию микрофлоры", "ускорить снижение/уменьшение/исчезновение дисбактериоза" и т.д. применяются для выражения того, что разнообразие (богатство и/или равномерность) микрофлоры у лиц с дисбак-териозом кишечника после лечения антибиотиками возрастает статистически быстрее у лиц, принимающих пробиотический штамм, чем у контрольных лиц, не принимающих его, так что структура микрофлоры через три недели после лечения антибиотиками будет статистически ближе к структуре до указанного лечения у тех лиц, которые принимают пробиотический штамм, чем у контрольных лиц, не принимающих его. При этом термин "дисбактериоз" служит для обозначения изменения разнообразия комменсальных видов микрофлоры по сравнению со здоровой или общей популяцией и должен означать уменьшение полезных микроорганизмов и/или увеличение патобионтов (патогенных или потенциально патогенных микроорганизмов) и/или уменьшение общего видового разнообразия микрофлоры. Многие факторы могут нанести вред полезным представителям кишечной микрофлоры, вызывая дисбактериоз, в том числе применение антибиотиков, психологический и физический стресс, радиация и изменения рациона. Применение антибиотиков является наиболее распространенной и значительной причиной крупных изменений нормальной микрофлоры. Так, в настоящем изобретении термин "вызванный антибиотиками дисбиоз" относится к дисбактериозам, вызванным антибиотиками, и включает усиление чрезмерного роста условно-патогенных бактерий, включая Enterococcus faecalis, Enterococcus faecium или Clostridium difficile.
В настоящем изобретении термин "молочная композиция" служит для обозначения композиций на основе молока, пригодных для потребления животными, в частности, для потребления людьми.
В настоящем изобретении термин "молоко" охватывает растительное или животное молоко, как-то, без ограничения, соевое, миндальное молоко, молоко из полбы, овса, конопли, кокосовых орехов, риса, козье, овечье или коровье молоко.
В настоящем изобретении термин "x% (вес/вес)" считается эквивалентным "x г на 100 г".
В настоящем изобретении ссылка на бактериальный штамм или вид должна охватывать и бактерии, происходящие из него, причем данные бактерии сохраняют способность к снижению кишечного дисбактериоза у субъекта, предпочтительно у субъекта с вызванным антибиотиками дисбактериозом. Для оценки этой способности можно использовать ту же модель, что описана в приведенных ниже примерах. Штаммы, происходящие из родительского штамма, которые можно использовать в соответствии с настоящим изобретением, включают мутантные штаммы и генетически трансформированные штаммы. Эти мутанты или генетически трансформированные штаммы могут представлять собой штаммы, у которых один или несколько эндогенных генов исходного штамма подверглись мутации, к примеру, чтобы модифицировать некоторые метаболические свойства (напр., способность сбраживать сахара, кислотоустойчивость, выживание при прохождении через желудочно-кишечный тракт, их свойства после подкисления или выработку ими метаболитов). Они также могут представлять собой штаммы, полученные при генетической трансформации исходного штамма для вставки одного или нескольких нужных генов, например, для того, чтобы придать данным генетически трансформированным штаммам дополнительные физиологические признаки или способность к экспрессии белков, представляющих терапевтический или вакцинный интерес, которые желательно вводить через данные штаммы. Эти мутанты или генетически трансформированные штаммы могут быть получены из исходного штамма стандартными методами случайного или направленного мутагенеза и генетической трансформации бактерий или же с помощью метода, известного как "перетасовка генома". В настоящем описании штаммы, мутанты и варианты, происходящие из исходного вида или штамма и сохраняющие способность к поддержанию или увеличению разнообразия кишечной микрофлоры у субъекта, страдающего вызванным антибиотиками дисбактериозом, должны рассматриваться как охваченные ссылкой на указанный родительский вид или штамм, напр., выражения "Lactobacillusparacasei" и "штамм CNCM I-3689" должны охватывать и происходящие из них штаммы, мутанты и варианты.
В настоящем изобретении термин "пищевая добавка" служит для обозначения продуктов, полученных из таких соединений, которые обычно используются в пищевых продуктах, но имеют вид таблеток, порошков, капсул, микстуры или любой другой формы, которая обычно не связана с питанием, но оказывает благотворное влияние на здоровье.
В настоящем изобретении термин "функциональный продукт" служит для обозначения пищевых продуктов, оказывающих благотворное влияние на здоровье наряду с обеспечением питательными веществами. В частности, пищевые добавки и функциональные продукты могут оказывать физиологическое действие - для профилактики, облегчения или лечения заболевания, к примеру, хронического заболевания.
В настоящем изобретении термин "ферментированная молочная" или "кисломолочная" относится к композиции, полученной из молочного продукта или молочной композиции, соответственно, при подкисляющем действии по меньшей мере одной молочнокислой бактерии, которая может содержаться в закваске, культуре или заквасочной культуре.
В настоящем изобретении термин "можно есть ложкой" служит для обозначения твердых или полутвердых продуктов, которые можно потреблять при помощи ложки или другой утвари.
В настоящем изобретении выражения "ускорить снижение Е. faecalis", "уменьшить нагруженность Е. faecalis", "способствовать уменьшению Е. faecalis" и т.д. применяются для выражения того, что содержание Е. faecalis в микрофлоре у лиц с дисбактериозом кишечника после лечения антибиотиками уменьшается быстрее у тех, кто принимает пробиотический штамм, чем у контрольных лиц, не принимающих его.
Применение Lactobacillus paracasei
Настоящим изобретением предусмотрено применение L. paracasei, предпочтительно подвида paracasei, более предпочтительно штамма CNCM I-3689, для поддержания или увеличения разнообразия кишечной микрофлоры у субъекта, предпочтительно у субъекта, страдающего дисбактериозом кишечника.
Соответственно, в одном воплощении настоящего изобретения предусмотрено применение L. paracasei, предпочтительно подвида paracasei, более предпочтительно штамма CNCM I-3689, для предотвращения или уменьшения дисбактериоза кишечника у субъекта. Штамм CNCM I-3689 L. paracasei subsp. paracasei депонирован, в соответствии с Будапештским договором, в CNCM (Национальная коллекция культур микроорганизмов, 25 rue du Docteur Roux, Париж) 9 ноября 2006 г. Этот штамм описан в международной патентной заявке WO 2009/130423.
В предпочтительном воплощении дисбактериоз кишечника вызван или возник после лечения субъекта антибиотиками. Вызванный антибиотиками дисбактериоз, как правило, характеризуется возрастанием Enterococcus faecalis, Enterococcus faecium и/или Clostridium difficile в желудочно-кишечном тракте. Вне ожидания авторы изобретения обнаружили, что L. paracasei не только способствует разнообразию кишечной микрофлоры у субъекта, но также уменьшает содержание условно-патогенного Enterococcus faecalis в желудочно-кишечном тракте. Соответственно, настоящим изобретением предусмотрено применение L. paracasei, предпочтительно подвида paracasei, более предпочтительно штамма CNCM I-3689, для снижения или ускорения уменьшения Enterococcus faecalis. В альтернативном воплощении настоящим изобретением предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689, для предотвращения транслокации Enterococcus faecalis через кишечный барьер и/или для профилактики внутрибрюшной инфекции, вызванной Enterococcus faecalis. В другом воплощении настоящим изобретением предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689, для снижения или ускорения снижения устойчивых к лекарствам энтерококков, предпочтительно HiRECCs, после лечения антибиотиками. Соответственно, в одном воплощении изобретением предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689, для снижения или ускорения снижения устойчивых к антибиотикам Е. faecalis, как правило, в кишечнике. Обычно данные Е. faecalis устойчивы к одному или нескольким антибиотикам, выбранным из пенициллинов, цефалоспоринов, фторхинолонов, аминогликозидов и гликопептидов.
Предпочтительно субъект страдает дисбактериозом кишечника. В предпочтительном воплощении дисбактериоз кишечника вызван или возник после лечения субъекта антибиотиками. Предпочтительно Enterococcus faecalis находится в желудочно-кишечном тракте, более предпочтительно в кишечнике.
Композиции
В следующем аспекте настоящего изобретения предусмотрены композиции, содержащие L.paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамм CNCM I-3689, для применения в соответствии с настоящим изобретением.
Соответственно, в предпочтительном воплощении настоящего изобретения предусмотрены штаммы L paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамм CNCM I-3689, в виде композиции для перорального введения. В такой композиции данный штамм может применяться в виде целых бактерий, которые могут быть живыми или мертвыми. С другой стороны, данный штамм может применяться в виде бактериального лизата. Предпочтительно бактериальные клетки присутствуют в виде живых и жизнеспособных клеток.
В соответствии с настоящим изобретением, композиция может быть в любой форме, подходящей для перорального введения. Это включает в себя, к примеру, твердые, полутвердые, жидкие формы и порошки. Предпочтительны полутвердые композиции типа йогуртов и жидкие композиции типа напитков.
Композиция предпочтительно содержит по меньшей мере 1⋅106 колониеобразующих единиц (к.о.е.), по меньшей мере 1⋅107 колониеобразующих единиц (к.о.е.) или предпочтительно по меньшей мере 1⋅108 к.о.е. на грамм массы L. paracasei, предпочтительно подвида paracasei, предпочтительно штамма CNCM I-3689. Предпочтительно композиция по изобретению также содержит вплоть до 1011, более предпочтительно по меньшей мере 1010 и наиболее предпочтительно по меньшей мере 109 колониеобразующих единиц (к.о.е.) L. paracasei, предпочтительно подвида paracasei, предпочтительно штамма CNCM I-3689, на грамм (г) композиции по изобретению.
Композиции также могут содержать и другие штаммы Lactobacillus и/или другие штаммы бактерий, чем штаммы, приведенные выше, в частности такие пробиотические штаммы, как штаммы Streptococcus thermophilus, Bifidobacterium и Lactococcus.
Композиции могут представлять собой фармацевтические композиции или пищевые композиции. В соответствии с предпочтительным воплощением композиция представляет собой пищевую композицию типа пищевого продукта (включая и функциональные пищевые продукты) или пищевой добавки.
Пищевые композиции, которые можно использовать в соответствии с изобретением, включают молочные композиции, предпочтительно кисломолочные композиции. Ферментированные композиции могут иметь вид жидкости или же сухого порошка, полученного при высушивании ферментированной жидкости. Примеры молочных композиций включают ферментированное молоко и/или ферментированную сыворотку в застывшем, перемешанном или питьевом виде, сыр и йогурт. Ферментированный продукт также может представлять собой ферментированный растительный продукт типа ферментированной сои, злаков и/или фруктов в застывшем, перемешанном или питьевом виде. Пищевые композиции, которые можно использовать в соответствии с изобретением, также включают детское питание, детские молочные смеси и смеси для продолжающих. В предпочтительном воплощении ферментированный продукт представляет собой свежий продукт. Свежий продукт, который не подвергался сильной термообработке, имеет то преимущество, что бактериальные штаммы присутствуют в живом виде.
Особенно предпочтительно, чтобы композиция по изобретению представляла собой молочную композицию, в частности кисломолочную композицию.
Предпочтительно молочная композиция по изобретению содержит или получена (в частности, путем ферментации) из композиции, содержащей от 30 до 100% (вес/вес) молока, более предпочтительно от 50 до 100% молока и еще более предпочтительно от 70 до 100% молока. Также предпочтительно молочная композиция по изобретению содержит или получена (в частности, путем ферментации) из композиции, в основном состоящей из молока или состоящей только из молока, предпочтительно из коровьего молока.
Предпочтительно молочная композиция по изобретению содержит или получена (в частности, путем ферментации) из композиции, содержащей либо обезжиренное, либо не обезжиренное молоко, либо то и другое. Предпочтительно молоко находится в жидком, порошкообразном и/или концентрированном виде. В одном воплощении данное молоко может быть обогащено или усилено другими компонентами молока или другими питательными веществами, такими, без ограничения, как витамины, минералы, микроэлементы или другие микронутриенты.
Кисломолочные композиции получают из молочной композиции по изобретению при подкисляющем действии по меньшей мере одной молочнокислой бактерии, которая может содержаться в закваске, культуре или заквасочной культуре. Более предпочтительно кисломолочные композиции по изобретению получают при подкисляющем действии по меньшей мере одного, двух, трех, четырех, пяти, шести, семи или больше штаммов молочнокислых бактерий. Соответственно, "кисломолочная композиция" содержит по меньшей мере один, два, три, четыре, пять, шесть, семь или больше штаммов молочнокислых бактерий.
Способы получения кисломолочных продуктов типа йогурта или их эквивалентов хорошо известны в данной области. Как правило, кисломолочные продукты получают путем культивирования прошедшего термообработку (напр., пастеризацию) обезжиренного и/или не обезжиренного молока с подходящими микроорганизмами, обеспечивающими снижение pH. Выбор подходящих микроорганизмов (напр., термофильных молочнокислых бактерий) находится в компетенции специалиста.
Молочные композиции, в частности, кисломолочные композиции по изобретению, необязательно могут дополнительно содержать вторичные ингредиенты, как-то фрукты, овощи, пищевые и некалорийные подсластители, крупы, ароматизаторы, крахмал, загустители, консерванты или стабилизаторы. Предпочтительно молочная композиция, в частности кисломолочная композиция по изобретению, должна содержать вплоть до 30% (вес/вес) таких вторичных ингредиентов, напр., до 10%, 15%, 20%, 25% (вес/вес).
Предпочтительно молочная композиция по изобретению представляет собой кисломолочную композицию, более предпочтительно кисломолочную композицию, которая содержит, в основном содержит или же состоит из молока, которое подвергалось термообработке, по меньшей мере эквивалентной пастеризации, а предпочтительно такая термообработка проводится перед получением молочной композиции или кисломолочной композиции.
Предпочтительно молочная композиция по изобретению представляет собой ферментированную молочную композицию, более предпочтительно кисломолочную композицию, которая содержит более 0,3 г свободной молочной кислоты на 100 г массы, более предпочтительно изобретением предусмотрены кисломолочные композиции, содержащие более 0,7 г или 0,6 г свободной молочной кислоты на 100 г массы. Предпочтительно молочная композиция по изобретению представляет собой ферментированную молочную композицию, более предпочтительно кисломолочную композицию, которая имеет содержание белка, по меньшей мере эквивалентное тому молоку, из которого она получена.
Предпочтительно молочная композиция по изобретению представляет собой ферментированную молочную композицию, более предпочтительно кисломолочную композицию, которая имеет значение pH, равное или меньше 5, более предпочтительно между 3,5 и 4,5.
Предпочтительно молочная композиция по изобретению представляет собой ферментированную молочную композицию, более предпочтительно кисломолочную композицию, которая имеет вязкость менее 200 мПа⋅с, более предпочтительно менее 100 мПа⋅с и наиболее предпочтительно менее 60 мПа⋅с при 10°C, при скорости сдвига в 64 с-1. В одном воплощении молочная композиция по изобретению представляет собой питьевую ферментированную молочную композицию, более предпочтительно кисломолочный напиток, такой, без ограничения, как йогурт, кефир и т.д. В альтернативном воплощении молочная композиция по изобретению представляет собой ферментированную молочную композицию, более предпочтительно кисломолочную композицию, которую можно есть ложкой.
Также предпочтительно молочная композиция, в частности ферментированная молочная композиция по изобретению или продукт по изобретению может храниться при температуре от 1°C до 10°C.
Одна порция молочной композиции, в частности ферментированной молочной композиции по изобретению, более предпочтительно кисломолочной композиции или продукта по изобретению предпочтительно составляет около 50 г, 60 г, 70 г, 75 г, 80 г, 85 г, 90 г, 95 г, 100 г, 105 г, 110 г, 115 г, 120 г, 125 г, 130 г, 135 г, 140 г, 145 г, 150 г, 200 г, 300 г или 320 г или же примерно 1 унцию, 2 унции, 3 унции, 4 унции, 5 унций, 6 унций или 12 унций по весу.
Предпочтительно молочная композиция, в частности ферментированная молочная композиция по изобретению, более предпочтительно кисломолочная композиция по изобретению содержит по меньшей мере 106, более предпочтительно по меньшей мере 107 и наиболее предпочтительно по меньшей мере 108 колониеобразующих единиц (к.о.е.) L. paracasei, предпочтительно подвида paracasei, предпочтительно штамма CNCM I-3689 по изобретению на 1 грамм (г) композиции по изобретению.
Терапевтическое применение
Предметом настоящего изобретения также является применение L. paracasei, предпочтительно подвида paracasei, предпочтительно штамма CNCM I-3689 или композиции, как определено выше, для изготовления лекарственного средства для поддержания или повышения разнообразия кишечной микрофлоры; и/или для профилактики или лечения дисбактериоза кишечника. Настоящим изобретением предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 для изготовления лекарственного средства для уменьшения или снижения или ускорения снижения Enterococcus faecalis. В альтернативном воплощении настоящего изобретения предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 для получения лекарственного средства для предотвращения транслокации Enterococcus faecalis через кишечный барьер и/или для профилактики внутрибрюшных инфекций Enterococcus faecalis. В следующем воплощении настоящего изобретения предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 для изготовления лекарственного средства для уменьшения или ускорения снижения устойчивых к лекарствам энтерококков, предпочтительно HiRECCs, после лечения антибиотиками. Соответственно, в одном воплощении изобретения предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689, для изготовления лекарственного средства для уменьшения или ускорения снижения устойчивых к антибиотикам Е. faecalis, как правило, в кишечнике. Как правило, такие Е. faecalis устойчивы к одному или нескольким антибиотикам, выбранным из пенициллинов, цефалоспоринов, фторхинолонов, аминогликозидов и гликопептидов.
Предметом настоящего изобретения также является применение L. paracasei, предпочтительно подвида paracasei, предпочтительно штамма CNCM I-3689 или же композиции, как определено выше, для профилактики или лечения дисбактериоза кишечника.
Настоящим изобретением предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 для лечения вызванных Enterococcus faecalis инфекций. В альтернативном воплощении настоящего изобретения предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 для лечения или предотвращения транслокации Enterococcus faecalis через кишечный барьер и/или для лечения или профилактики внутрибрюшного заражения Enterococcus faecalis. В следующем воплощении настоящего изобретения предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 для лечения устойчивых к лекарствам энтерококков, предпочтительно HiRECCs, после лечения антибиотиками. Соответственно, в одном воплощении изобретения предусмотрено применение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689, для лечения устойчивых к антибиотикам Е. faecalis, как правило, в кишечнике. Как правило, такие Е. faecalis устойчивы к одному или нескольким антибиотикам, выбранным из пенициллинов, цефалоспоринов, фторхинолонов, аминогликозидов и гликопептидов.
Предметом настоящего изобретения также является способ поддержания или повышения разнообразия кишечной микрофлоры; и/или профилактики или лечения дисбактериоза кишечника, который включает введение данному субъекту терапевтически эффективного количества L. paracasei, предпочтительно подвида paracasei, как определено выше, предпочтительно штамма CNCM I-3689 или композиции, как определено выше.
Определение терапевтически эффективного количества хорошо известно специалистам в данной области, особенно в свете приведенного здесь подробного описания.
Предметом настоящего изобретения также является способ изготовления лекарственного средства для поддержания или повышения разнообразия кишечной микрофлоры; и/или для профилактики или лечения дисбактериоза кишечника, который включает введение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 по меньшей мере в один фармацевтически приемлемый разбавитель, носитель или наполнитель. Настоящим изобретением предусмотрен способ изготовления лекарственного средства для уменьшения или ускорения снижения Enterococcus faecalis, который включает введение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 по меньшей мере в один фармацевтически приемлемый разбавитель, носитель или наполнитель. В альтернативном воплощении настоящего изобретения предусмотрен способ изготовления лекарственного средства для предотвращения транслокации Enterococcus faecalis через кишечный барьер и/или для профилактики внутрибрюшного заражения Enterococcus faecalis, который включает введение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 по меньшей мере в один фармацевтически приемлемый разбавитель, носитель или наполнитель. В следующем воплощении настоящего изобретения предусмотрен способ изготовления лекарственного средства для уменьшения или ускорения снижения устойчивых к лекарствам энтерококков, предпочтительно HiRECCs, после лечения антибиотиками, который включает введение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 по меньшей мере в один фармацевтически приемлемый разбавитель, носитель или наполнитель. Соответственно, в одном воплощении изобретения предусмотрен способ изготовления лекарственного средства для уменьшения или ускорения снижения устойчивых к антибиотикам Е. faecalis, как правило, в кишечнике, который включает введение L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 по меньшей мере в один фармацевтически приемлемый разбавитель, носитель или наполнитель. Как правило, такие Е. faecalis устойчивы к одному или нескольким антибиотикам, выбранным из пенициллинов, цефалоспоринов, фторхинолонов, аминогликозидов и гликопептидов.
Предпочтительно субъект для описанных выше лекарственных средств, применений и/или способов страдает дисбактериозом кишечника, а также предпочтительно дисбактериоз вызван или возник после лечения субъекта антибиотиками. Предпочтительно Enterococcus faecalis при описанных выше лекарственных средствах, применениях и/или способах находится в желудочно-кишечном тракте, более предпочтительно в кишечнике.
Дозировка
В одном воплощении настоящего изобретения предусмотрено потребление или введение дозы от 108 до 1011 колониеобразующих единиц (к.о.е.) L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689; предпочтительно от 108 до 109, более предпочтительно от 109 до 1010 колониеобразующих единиц (к.о.е.), а в альтернативном воплощении от 1010 до 1011 колониеобразующих единиц (к.о.е.) L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 для описанных здесь применений и способов. В другом воплощении предусмотрено по меньшей мере 1, 2, 3 или 4 дозы за период времени в 24 часа. Также предпочтительно, чтобы ежедневная схема дозировки сохранялась по меньшей мере в течение 1, 2, 3, 4, 5, 6 или 7 дней, а в альтернативном воплощении по меньшей мере в течение 1,2, 3, 4, 5, 6 или 7 недель.
Соответственно, в одном воплощении настоящего изобретения предусмотрено ежедневное потребление или введение по меньшей мере 1, 2, 3 или 4 порций молочной композиции, в частности ферментированной молочной композиции по изобретению, более предпочтительно кисломолочной композиции по изобретению. Каждая порция может потребляться или вводиться по отдельности или же может потребляться или вводиться по несколько порций за один раз. Каждая из таких порций может потребляться во время приема пищи или между приемами пищи (напр., в качестве закуски, после спортивных мероприятий и т.д.).
Одна порция молочной композиции, в частности ферментированной молочной композиции по изобретению, более предпочтительно кисломолочной композиции по изобретению предпочтительно составляет около 50 г, 60 г, 70 г, 75 г, 80 г, 85 г, 90 г, 95 г, 100 г, 105 г, 110 г, 115 г, 120 г, 125 г, 130 г, 135 г, 140 г, 145 г, 150 г, 200 г, 300 г или 320 г или же примерно 1 унцию, 2 унции, 3 унции, 4 унции, 5 унций, 6 унций или 12 унций по весу.
Предпочтительно композиция по изобретению содержит по меньшей мере 106, более предпочтительно по меньшей мере 107 и наиболее предпочтительно по меньшей мере 108 колониеобразующих единиц (к.о.е.) L. paracasei, предпочтительно подвида paracasei, еще более предпочтительно штамма CNCM I-3689 по изобретению на 1 грамм (г) композиции по изобретению. Также предпочтительно композиция по изобретению содержит по меньшей мере 1011, более предпочтительно по меньшей мере 1010 и наиболее предпочтительно по меньшей мере 109 колониеобразующих единиц (к.о.е.) бактерий L. paracasei, предпочтительно подвида paracasei, более предпочтительно штамма CNCM I-3689 на 1 грамм (г) композиции по изобретению.
Например, в одном воплощении настоящего изобретения предусмотрено ежедневное потребление по меньшей мере 2 или по меньшей мере 3 порций по 100 г или по 125 г кисломолочного продукта, содержащего по меньшей мере от 107 до 108 колониеобразующих единиц (к.о.е.) L. paracasei, предпочтительно подвида paracasei, более предпочтительно штамма I-3689 на 1 г продукта. В другом воплощении указанный суточный уровень потребления сохраняется на протяжении по меньшей мере 1, 2, 3, 4 и более недель.
Настоящее изобретение станет более понятным из дальнейшего описания, которое следует ниже, в котором приведены примеры, иллюстрирующие способность L. paracasei уменьшать дисбактериоз in vivo.
Краткое описание фигур
На фиг. 1 представлена схема, на которой приведена последовательность экспериментов.
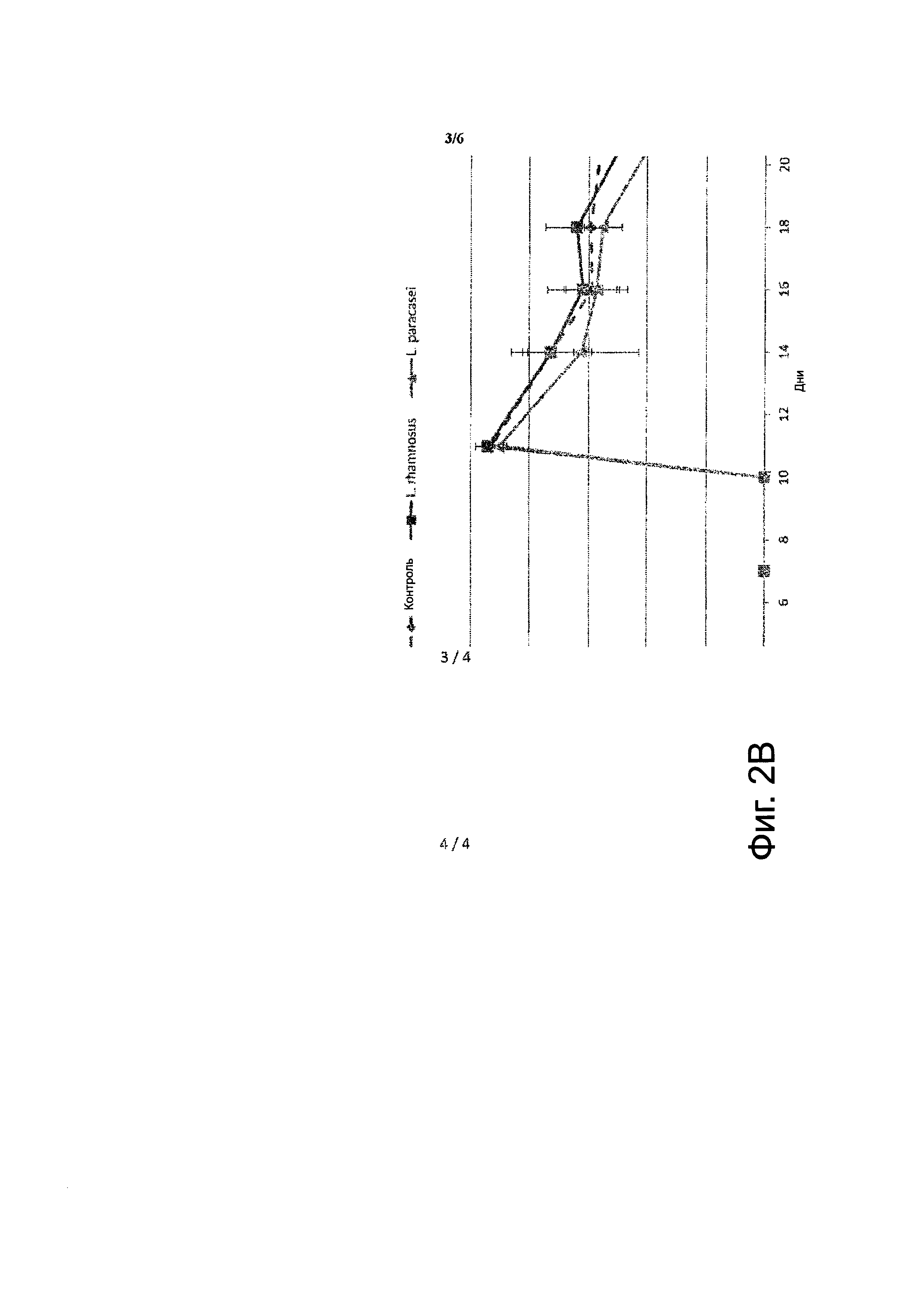
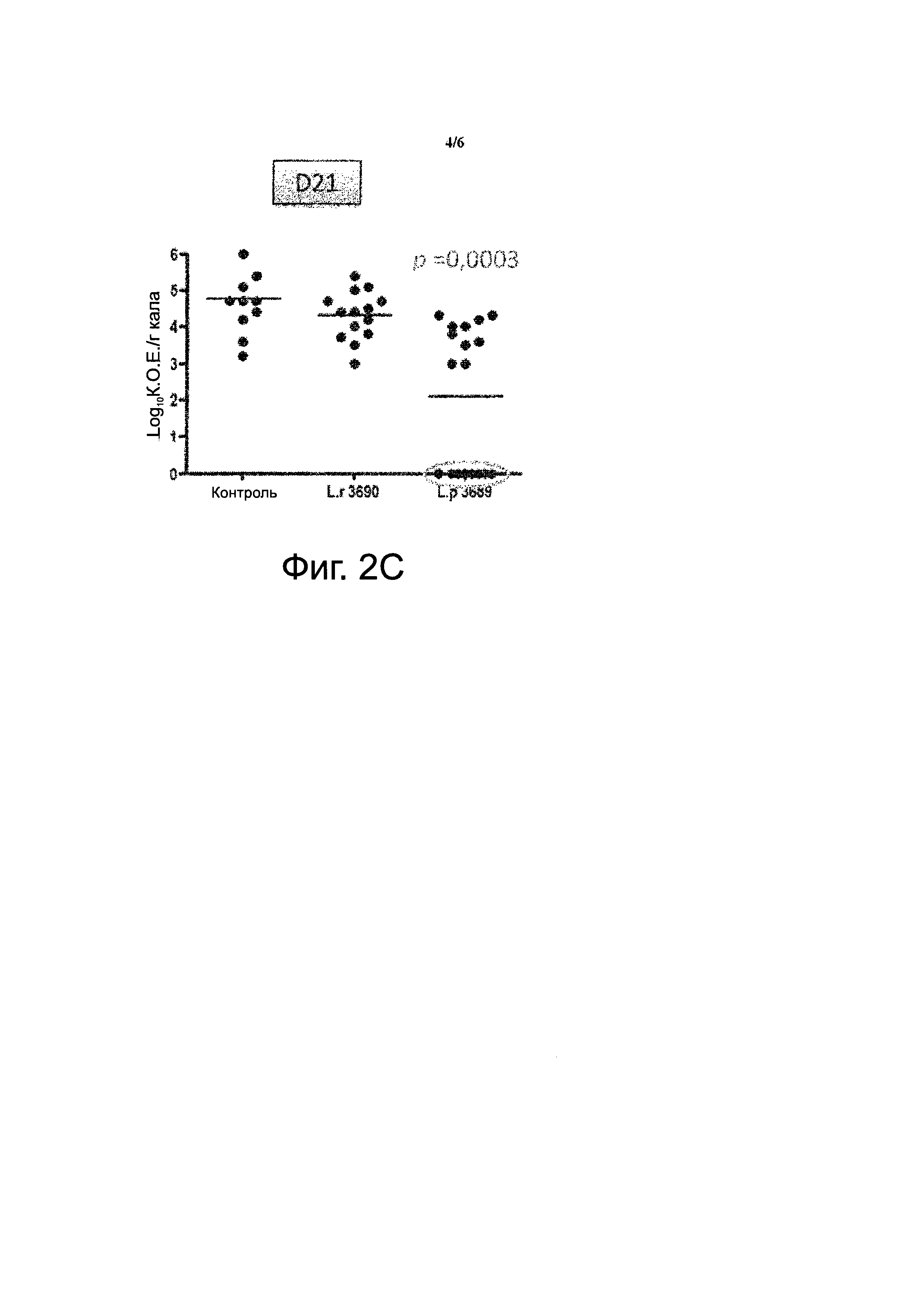
На фиг. 2 представлена кинетика и уровни, определенные путем селективного высева общей популяции энтерококков из мышей, получавших суточную дозу в 0,1 мл 0,9% солевого раствора (контроль) или 109 к.о.е. пробиотического штамма в 0,1 мл 0,9% солевого раствора при введении через желудочный зонд (А); кинетика и уровни Е. faecalis штамма V583 исходно (В) и уровни Е. faecalis штамма V583 через 11 дней после прекращения приема антибиотика, что соответствует D21 (С). Эксперименты проводились в трех повторах.
На фиг. 3 представлена относительная численность представителей Actinobacteria, Bacteroidetes, Firmicutes и Proteobacteria в день 0 ("исходно"; фиг 3А) и в день 21 (забой; фиг 3В) у мышей, получавших суточную дозу в 0,1 мл 0,9% солевого раствора (контроль "C") или 109 к.о.е. пробиотического штамма (L. rhamnosus "L.r" или L. paracasei "L.p") в 0,1 мл 0,9% солевого раствора при введении через желудочный зонд.
ПРИМЕРЫ
Методы
Культивирование бактерий
Е. faecalis штамма V583 культивировали в среде М17 с добавлением 0,5% глюкозы (GM17) и собирали центрифугированием через 1 ч после достижения стационарной фазы. Бактериальные клетки дважды промывали 0,9% солевым раствором и хранили в виде сухого замороженного осадка при -80°C. Этот штамм принадлежит к СС2 и был первым устойчивым к ванкомицину изолятом, о котором сообщалось в США (Sahm et al., 1989).
Пробиотические штаммы культивировали в среде MRS и собирали, как описано выше.
По крайней мере за два дня до введения замороженные бактерии суспендировали в солевом растворе и проводили высев серийных разведений на агаровые чашки с GM17 или MRS для определения количества бактерий в осадке.
Модель колонизации Е. faecalis на мышах
Эксперименты на мышах проводили на лишенных определенных патогенов 6-8-недельных самцах мышей CF-1 (Harlan, USA). В каждой клетке размещали по 5 мышей и давали им автоклавированный корм и воду ad libitum.
Они ежедневно получали дозу в 109 к.о.е. пробиотического штамма в 0,1 мл 0,9% солевого раствора через желудочный зонд с помощью стальной питательной трубки (Ecimed). Группе Lr вводили Lactobacillus rhamnosus CNCM I-3690, а группе Lp - Lactobacillus paracasei CNCM I-3689. Животные из контрольной группы получали 0,1 мл 0,9% солевого раствора таким же способом. Через одну неделю лечения пробиотиками им вводили подкожно клиндамицин в дозе 1,4 мг/день раз в день в течение трех дней. Через день вводили 1010 колониеобразующих единиц (к.о.е.) Е. faecalis (устойчивых к ванкомицину энтерококков, отмеченных "VRE") штамма V583 в 0,1 мл 0,9% солевого раствора через желудочный зонд с помощью стальной питательной трубки (Ecimed).
Статистический анализ
Различия в количества бактерий анализировали с помощью теста Манна-Уитни (GraphPad). Различия считались значимыми при p<0,05.
Анализ микрофлоры
Брали образцы кала в D0 (исходный уровень) и D21 (забой). Экстрагировали ДНК по методике Godon et al. (Godon, 1997). Для пиросеквенирования амплифицировали участок V3-V5 гена 16S рРНК с помощью эубактериальных праймеров с тегами key (Lifesequencing S.L., Valencia, Испания) на основе схемы Sim et al., 2012. Реакции ПЦР проводили при 20 нг метагеномной ДНК, по 200 мкМ каждого из четырех дезоксинуклеозидтрифосфатов, 400 нМ каждого праймера, 2,5 ед. полимеразы FastStart HiFi в соответствующем буфере с MgCl2 от производителя (Roche, Mannheim, Германия), 4% 20 г/мл BSA (Sigma, Dorset, Великобритания) и 0,5 М бетаина (Sigma). Термический цикл состоял из начальной денатурации при 94°C в течение 2 мин с последующими 35 циклами из денатурации при 94°C в течение 20 секунд, отжига при 50°C в течение 30 секунд и наращивания при 72°C в течение 5 минут. Ампликоны объединяли в одной пробирке в эквимолярных концентрациях. Общую смесь ампликонов дважды подвергали очистке (AMPure ХР kit, Agencourt, Takeley, Великобритания), а очищенный пул снова подвергали количественному анализу методом PicoGreen (Quant-iT, PicoGreen DNA assay, Invitrogen). После этого ампликон отправляли на сервис пиросеквенирования фирмы Life Sequencing S.L. (Valencia, Испания), где проводили EmPCR, после чего проводили одностороннее пиросеквенирование на приборе 454 Life Sciences GS FLX+ (Roche) по методике Roche Amplicon Lib-L. Биоинформационный анализ проводили при помощи QIIME v. 1.6 (Caporaso, 2010). Данные относили к 50 образцам после фильтрации в соответствии со следующими критериями качества: размер от 500 до 1000 нт, качество выше 25 в окне из 50 пар оснований, не допускается рассогласования в последовательностях праймеров и штрихкода, а также отсутствие полимеров более чем в 6 нт. Остающиеся прочтения группировали в операционные таксономические единицы (OTU), определяемые по степени идентичности в 97% с помощью cd-hit (Li, 2006), и для каждого OTU проводили совмещение репрезентативных последовательностей и таксономическую привязку по базе данных Greengenes v_13_08.
Результаты
Штамм CNCM I-3689 L. paracasei способствует восстановлению разнообразия состава микрофлоры и очищению кишечника от устойчивых к ванкомицину Е. faecalis V583
Используя модель колонизации Е. faecalis, мышам ежедневно вводили перорально два пробиотических штамма L. paracasei CNCM I-3689 и L. rhamnosus CNCM I-3690, начиная за 1 неделю до лечения антибиотиками и вплоть до 2 недель после прекращения лечения антибиотиками и инокуляции VRE. Определяли общий уровень популяции энтерококков и VRE путем селективного высева. Кинетики и уровни популяции энтерококков, а также кинетики укоренения штамма VRE Е. faecalis были близкими у контрольных и получавших пробиотики мышей (А и В). Напротив, клиренс VRE значительно отличался у мышей, получавших штамм L. paracasei CNCM I-3689, по сравнению с контрольными и получавшими L. rhamnosus CNCM I-3690 мышами (В). У половины мышей, получавших L. paracasei, VRE не обнаруживались через 11 дней после прекращения обработки антибиотиками, что соответствует D21 всего эксперимента, а у другой половины уровень VRE существенно снижался по сравнению с контрольными мышами (С).
В целом эти результаты показывают, что введение L. paracasei CNCM I-3689 значительно уменьшает живучесть патогенных Е. faecalis в кишечнике. Принимая во внимание, что уменьшение колонизации кишечника или носительства после лечения антибиотиками может ограничить риски заражения и распространения VRE, L. paracasei CNCM 1-3689 является перспективным кандидатом для усиления клиренса VRE. L. paracasei CNCM I-3689 может быть частью стратегии усиления кишечного клиренса условно-патогенных микроорганизмов без применения антибиотиков после вызванного антибиотиками дисбактериоза. Чтобы выявить эффекты обработки клиндамицином + инокуляции VRE, а также введения L. paracasei CNCM I-3689 на структуру микрофлоры, проводили 454 пиросеквенирования вариабельных участков V3-V5 бактериального гена 16S рРНК в образцах кала, собранных у мышей в день D0 (исходный уровень) и D21 ("восстановление"). Анализ микрофлоры в образцах кала, взятых в D0 и D21, показал, что обработка клиндамицином приводила к резкому изменению состава микрофлоры, с преобладанием Firmicutes и в меньшей степени Proteobacteria в контрольных образцах.
Напротив, наблюдалось некоторое восстановление Bacteroidetes в группе L. paracasei (фиг. 2), а также в группе L. rhamnosus.
Реферат
Группа изобретений относится к медицине. Предложено применение штамма Lactobacillus paracasei CNCM I-3689 для восстановления численности Bacteroidetes у субъекта с дисбактериозом, вызванным или являющимся следствием лечения антибиотиками, применение его для ускорения снижения Enterococcus faecalis в микрофлоре кишечника у субъекта с дисбактериозом, вызванным или являющимся следствием лечения антибиотиками указанного субъекта, и для предотвращения транслокации E. faecalis через кишечный барьер у субъекта. Технический результат состоит в реализации заявленных назначений и в снижении живучести патогенной E. Faecalis в кишечнике по сравнению с контролем. 3 н. и 4 з.п. ф-лы, 3 ил.
Формула
Документы, цитированные в отчёте о поиске
Штамм lactobacillus paracasei subspecies paracasei, обладающий антимикробными и иммуномодулирующими свойствами, и пищевой продукт на его основе

Комментарии