Устройство для очистки крови на основе мембран в виде полых волокон - RU2648027C1
Код документа: RU2648027C1
Чертежи


Описание
Область техники
[0001] Настоящее изобретение предлагает устройство для очистки крови на основе мембран в виде полых волокон.
Уровень техники
[0002] В традиционной терапии методом очистки крови, которая используется для лечения почечной недостаточности и аналогичных заболеваний, устройства для очистки крови на основе полых мембран, такие как гемодиализатор, гемофильтр и гемодиафильтр, включающие, в качестве разделяющего материала, мембраны в виде полых волокон, содержащих полимеры, такие как целлюлоза, ацетат целлюлозы, полисульфон, простой полиэфирсульфон, полиметилметакрилат или полиакрилонитрил, широко применяют для удаления уремических токсинов и выделений организма из крови.
В качестве этих устройств для очистки крови на основе мембран в виде полых волокон широко используют мембраны в виде полых волокон на основе полисульфонов и мембраны в виде полых волокон на основе простых полиэфирсульфонов, потому что такие мембраны являются превосходными для уменьшения количества крови, которая должна циркулировать вне организма, и отличаются высокой эффективностью удаления уремических токсинов из крови и высокой производительностью модульного производства, а также особой способностью одновременного обеспечения высокой проницаемости и совместимости с кровью (см. патентные документы 1 и 2).
[0003] В последние годы, не только для цели удаления уремических токсинов и выделений организма из крови, но также для снижения окислительного стресса, которому, очевидно, подвергается пациент, находящийся на диализе в течение продолжительного периода времени, делаются попытки, например, использования разделительных мембран для исключения пероксидов, то есть веществ, вызывающих окислительный стресс, или восстановления противоокислительных функций живого организма.
Патентные документы 3 и 4 предлагают устройства для очистки крови на основе мембран в виде полых волокон, в которых растворимый в жирах витамин, такой как витамин E, выполняющий разнообразные физиологические функции в живом организме, включая противоокислительное действие, эффект стабилизации биологических мембран и эффект ингибирования агрегация тромбоцитов, вводят в мембраны в виде полых волокон. Как известно, мембраны в виде полых волокон на основе полисульфонов и мембраны в виде полых волокон на основе простых полиэфирсульфонов имеют высокое сродство к растворимым в жирам витаминам, которые способны эффективно ингибировать окислительный стресс, вызываемый циркуляцией крови вне организма, и, следовательно, растворимый в жирах витамин может быть легко иммобилизован на мембране в виде полых волокон.
[0004] При этом даже в настоящее время постоянно описывают случаи осложнений, которые наблюдаются при терапии методом очистки крови, такие как синдром нарушенного равновесия, который проявляется в виде симптомов головной боли, тошноты или рвоты и возникает вследствие разности осмотического давления между кровью, в которой резко снижается концентрация уремических токсинов, и тканями организма, в которых сохраняется высокая концентрация уремических токсинов, и хотя эти осложнения не вызывают риск немедленной смерти или серьезного физического нарушения, они являются болезненными для пациента.
Список цитируемой литературы
Патентная литература
[0005] Патентный документ 1: японская выложенная патентная заявка № 7-178166
Патентный документ 2: японская выложенная патентная заявка № 2006-296931
Патентный документ 3: японская выложенная патентная заявка № 2013-9761
Патентный документ 4: японская выложенная патентная заявка № 2013-94525
Сущность изобретения
Техническая проблема
[0006] Считается, что осложнения могут быть устранены посредством использования устройства для очистки крови на основе мембран в виде полых волокон, в котором растворимый в жирах витамин вводится в мембрану в виде полых волокон, но в целях дополнительного ослабления воздействия на пациента оказывается желательным устройство для очистки крови на основе мембран в виде полых волокон, которое имеет усиленные противоокислительные характеристики.
В ходе всесторонних исследований, проведенных с учетом вышеупомянутых обстоятельств, было изучено увеличение количества растворимого в жирах витамина, который иммобилизуется в целях дополнительного улучшения противоокислительных характеристик, и в результате их исследований было обнаружено, что количество растворимого в жирах витамина, подлежащего иммобилизации, не может быть увеличено так просто вследствие описанной далее проблемы.
[0007] В качестве способа введения растворимого в жирах витамина в мембрану в виде полых волокон были предложены, в основном, два способа. Один из них представляет собой способ, в котором растворимый в жирах витамин добавляют в прядильный раствор (см., например, патентный документ 4), а другой из них представляет собой способ, согласно которому мембрану в виде полых волокон покрывают растворимым в жирах витамином (см., например, патентный документ 3).
В устройстве для очистки крови на основе мембран в виде полых волокон, изготовленном любым из этих способов, растворимый в жирах витамин распределяют практически равномерно в продольном направлении устройства для очистки крови на основе мембран в виде полых волокон. Было обнаружено, что если в этом устройстве количество растворимого в жирах витамина, подлежащего иммобилизации на всей поверхности мембраны в виде полых волокон устройства для очистки крови на основе мембран в виде полых волокон, увеличивается для улучшения противоокислительных характеристик, возникают недостатки, заключающиеся в том, что ухудшается водопроницаемость всей мембраны в виде полых волокон, снижается совместимость с кровью, и получаемое в результате устройство не является экономичным.
[0008] Соответственно, авторы настоящего изобретения сосредоточили свое внимание на следующем:
По существу, кровообращение, осуществляемое в процессе терапии методом очистки крови, представляет собой впуск крови в имеющую отверстие часть устройства для очистки крови на основе мембран в виде полых волокон, таким образом, что становится наиболее высокой концентрация пероксидного соединения, которое присутствует в крови, проходящей через устройство для очистки крови на основе мембран в виде полых волокон. Другими словами, растворимый в жирах витамин расходуется в наибольшем количестве в имеющей отверстие для впуска крови части устройство для очистки крови на основе мембран в виде полых волокон.
Кроме того, когда кровь проходит через устройство для очистки крови на основе мембран в виде полых волокон, реакционноспособный кислород образуется в процессе взаимодействия между мембраной в виде полых волокон и кровью, и в результате этого растворимый в жирах витамин, вероятно, расходуется в большом количестве также и в имеющей отверстие для впуска крови части устройства для очистки крови на основе мембран в виде полых волокон. В результате этого растворимый в жирах витамин расходуется в относительно больших количествах в обеих концевых частях корпуса устройства для очистки крови на основе мембран в виде полых волокон, и, следовательно, предполагается, что увеличивается количество растворимого в жирах витамина, подлежащего иммобилизации только в этих частях, могут быть обеспечены более высокие противоокислительные характеристики, чем в традиционной технологии, не вызывая ухудшения водопроницаемости, снижения совместимости с кровью и увеличения стоимости.
[0009] Кроме того, когда центральная часть и наружная часть пучка мембран в виде полых волокон сопоставимы друг с другом, было обнаружено, что количество крови, проходящей через центральную часть, составляет более чем количество крови, проходящей через наружную часть. Центральная часть и наружная часть пучка мембран в виде полых волокон будут описаны далее.
В фактическом кровообращении, осуществляемом в терапии методом очистки крови, на центральную часть устройства для очистки крови на основе мембран в виде полых волокон влияет линейная скорость и, следовательно, увеличивается количество крови, проходящей через нее, и, таким образом, в устройстве для очистки крови на основе мембран в виде полых волокон концентрация пероксидного соединения, которое присутствует в крови, оказывается относительно более высоким в центральной части, чем в наружной части. Другими словами, растворимый в жирах витамин расходуется в относительно больших количествах в центральной части устройства для очистки крови на основе мембран в виде полых волокон.
[0010] До настоящего времени в технике отсутствовало устройство для очистки крови на основе мембран в виде полых волокон, сконструированное с учетом вышеупомянутых проблем.
Соответственно, задача настоящего изобретения заключается в том, чтобы предложить устройство для очистки крови на основе мембран в виде полых волокон, имеющее улучшенные противоокислительные характеристики, хорошие характеристики водопроницаемости и характеристики совместимости с кровью, а также экономическую целесообразность.
Решение проблемы
[0011] В результате проведения всесторонних исследований для решения вышеупомянутой проблемы авторы настоящего изобретения обнаружили, что проблема, которую должно решить настоящее изобретение, может быть преодолена посредством регулирования количества растворимого в жирах витамина, которое присутствует в пучке мембран в виде полых волокон в устройстве для очистки крови на основе мембран в виде полых волокон, в котором мембраны в виде полых волокон загружают в резервуар, и, таким образом, было выполнено настоящее изобретение.
[0012] В частности, настоящее изобретение предлагает следующее:
(1) Устройство для очистки крови на основе мембран в виде полых волокон, включающее мембраны в виде полых волокон, загруженные в резервуар,
причем мембраны в виде полых волокон содержат гидрофобный полимер, гидрофильный полимер и растворимый в жирах витамин,
при этом в пучке мембран в виде полых волокон выделяют пять секций в продольном направлении, а разделенные секции, расположенные в самых концевых участках, определяют как концевые части корпуса; количество растворимого в жирах витамина, которое присутствует, по меньшей мере, в одной из концевых частей корпуса, является наибольшим среди количеств растворимого в жирах витамина, которые присутствуют, соответственно, во всех разделенных секциях, и количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, по меньшей мере, одной концевой части корпуса составляет 20 мг/м2 или более и 300 мг/м2 или менее.
(2) Устройство для очистки крови на основе мембран в виде полых волокон по пункту (1), в котором, когда количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в концевой части корпуса, причем количество растворимого в жирах витамина является наибольшим, определяется как A (мг/м2), а количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в разделенной секции, при этом количество растворимого в жирах витамина является наименьшим среди других разделенных секций, определяется как B (мг/м2), соотношение (A/B) между количествами A и B составляет 1,1 или более и 10 или менее.
(3) Устройство для очистки крови на основе мембран в виде полых волокон по пункту (2), в котором соотношение (A/B) между количествами A и B составляет 1,3 или более и 10 или менее.
(4) Устройство для очистки крови на основе мембран в виде полых волокон по любому из пп. (1)-(3), в котором, когда часть в пределах внутренней окружности, имеющей 1/2 радиуса пучка мембран в виде полых волокон, определяют как центральную часть, а часть, не включенную в центральную часть, определяют как наружную часть, количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в центральной части, составляет более чем количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в наружной части.
(5) Устройство для очистки крови на основе мембран в виде полых волокон по п. (4), в котором, когда количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в центральной части, определяют как C (мг/м2), а количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в наружной части определяют как D (мг/м2), соотношение (C/D) между количествами C и D составляет 1,1 или более и 50 или менее.
(6) Устройство для очистки крови на основе мембран в виде полых волокон по любому из пп. (1)-(5), в котором гидрофобный полимер имеет параметр растворимости δ (кал/см3)1/2, составляющий 13,0 или менее.
(7) Устройство для очистки крови на основе мембран в виде полых волокон по любому из пп. (1)-(6), в котором гидрофобный полимер представляет собой любой полимер, выбранный из группы, состоящей из полисульфонов, простых полиэфирсульфонов и ацетатов целлюлозы.
(8) Устройство для очистки крови на основе мембран в виде полых волокон по любому из пп. (1)-(7), в котором гидрофильный полимер представляет собой поливинилпирролидон.
Полезные эффекты изобретения
[0013] Согласно настоящему изобретению, может быть предложено устройство для очистки крови на основе мембран в виде полых волокон, имеющее улучшенные противоокислительные характеристики, хорошие характеристики водопроницаемости и характеристики совместимости с кровью, а также экономическую целесообразность.
Краткое описание чертежей
[0014] [Фиг. 1] Фиг. 1 - случай, в котором устройство для очистки крови на основе мембран в виде полых волокон имеет одну концевую часть корпуса, причем количество растворимого в жирах витамина является наибольшим.
[Фиг. 2] Фиг. 2 - случай, в котором устройство для очистки крови на основе мембран в виде полых волокон имеет две концевые части корпуса, причем количество растворимого в жирах витамина является наибольшим.
[Фиг. 3] Фиг. 3 - типичное устройство для очистки крови на основе мембран в виде полых волокон, а также иллюстрирует примерное расположение пучка мембран в виде полых волокон в устройстве для очистки крови на основе мембран в виде полых волокон.
[Фиг. 4] Фиг. 4 - диаграмма, схематически иллюстрирующая центральную часть и наружную часть пучка мембран в виде полых волокон.
Описание вариантов осуществления
[0015] Далее будет подробно описан вариант практического осуществления настоящего изобретения (далее называется "настоящий вариант осуществления"). Следует отметить, что настоящее изобретение не ограничивается следующим вариантом осуществления, но может модифицироваться разнообразными способами в пределах его объема.
[0016] Устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления представляет собой устройство для очистки крови на основе мембран в виде полых волокон, в котором мембраны в виде полых волокон загружают в резервуар; мембраны в виде полых волокон содержат гидрофобный полимер, гидрофильный полимер и растворимый в жирах витамин; при этом в пучке мембран в виде полых волокон выделяют пять секций в продольном направлении, а разделенные секции, расположенные в самых концевых участках, определяют как концевые части корпуса; количество растворимого в жирах витамина, которое присутствует, по меньшей мере, в одной из концевых частей корпуса, является наибольшим среди количеств растворимого в жирах витамина, которые присутствуют, соответственно, во всех разделенных секциях, а количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, по меньшей мере, одной концевой части корпуса составляет 20 мг/м2 или более и 300 мг/м2 или менее.
Согласно настоящему изобретению, термин "устройство для очистки крови на основе мембран в виде полых волокон" означает оборудование для очистки крови, которое используют в терапии искусственного кровообращения, такое как гемодиализатор, фильтр для гемодиализа, гемофильтр или непрерывный гемо(диа)фильтр.
[0017] <Мембрана в виде полых волокон>
Согласно настоящему варианту осуществления, термин "мембрана в виде полых волокон" означает мембрану, представляющую собой полое волокно для очистки крови, используемое в устройстве для очистки крови на основе мембран в виде полых волокон.
Параметры мембраны в виде полых волокон, такие как внутренний диаметр, толщина и длина, могут регулироваться произвольным образом, а, например, внутренний диаметр может составлять 100 мкм или более и 300 мкм или менее, толщина может составлять 10 мкм или более и 100 мкм или менее, а длина может составлять 10 мкм или более и 40 см или менее.
Может присутствовать так называемая асимметричная мембрана, включающая тонкий плотный слой (активный разделительный слой), который одновременно обеспечивает свойство фракционирования высокомолекулярных веществ и высокую водопроницаемость, и пористый слой (опорный слой), обеспечивающий прочность мембраны в виде полых волокон, или симметричная мембрана, представляющая собой просто тонкий плотный слой (активный разделительный слой), когда имеет значение только молекулярно-массовое фракционирование.
Согласно настоящему варианту осуществления, термин "внутренняя поверхность мембраны в виде полых волокон" означает поверхность на стороне полой части мембраны в виде полых волокон.
Согласно настоящему варианту осуществления, в устройстве для очистки крови на основе мембран в виде полых волокон мембрану в виде полых волокон загружают в резервуар, составляющий устройство для очистки крови на основе мембран в виде полых волокон, и множество мембран в виде полых волокон загружают в форме пучка мембран в виде полых волокон.
[0018] <Гидрофобный полимер>
Согласно настоящему варианту осуществления, гидрофобный полимер означает синтетический полимер или натуральный полимер, который не растворяется в воде и не проявляет сродство к воде.
Гидрофобный полимер не ограничивается определенным образом, и соответствующие примеры представляют собой полимеры на основе полисульфонов, такие как полисульфон, простой полиэфирсульфон, и полимерный сплав типа простой полиэфирсульфон-полиарилат; полимеры на метакрилатной основе, такие как полиметилметакрилат, полигидроксиэтилметакрилат, и сополимеры, содержащий метилметакрилат или гидроксиэтилметакрилат; полиолефины, такой как полиэтилен, полипропилен, поли-3-метилбутен-1 и поли-4-метилпентен-1; ацетаты целлюлозы, такие как триацетат целлюлозы и диацетат целлюлозы; а также полиакрилонитрил, полиамид, полиарилат, поликарбонат, полиэфирэфиркетон и полиаллилэфиркетон.
В качестве гидрофобного полимера они могут использоваться индивидуально или в сочетаниях двух или более веществ.
Среди них синтетические полимеры являются предпочтительными с точки зрения однородности состава полимера, причем полисульфон, полимерный сплав типа простой полиэфирсульфон-полиарилат, полиметилметакрилат и полиэтилен являются более предпочтительными, потому что эти полимеры соответствующим образом использовались для очистки крови в многочисленных клинических исследованиях и являются превосходными в отношении устойчивой поставки в качестве исходных материалов.
[0019] Полимеры на основе полисульфонов включают полифенилсульфон, полиаллилэфирсульфон и т. д., причем они могут представлять собой соединения, в которых часть ароматического кольца является химически модифицированной.
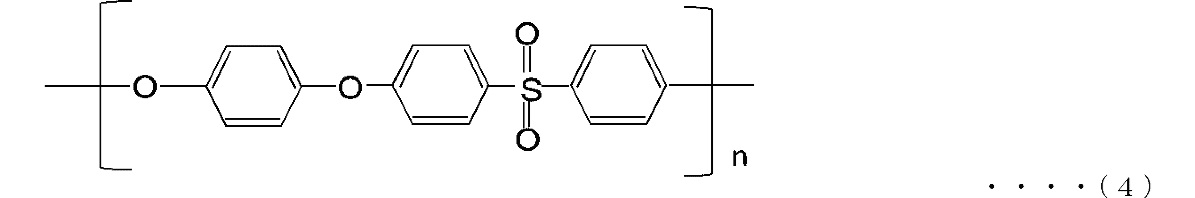
Полимеры на основе полисульфонов не ограничиваются определенным образом, и соответствующие примеры представляют собой полимеры, имеющие повторяющееся звено, которое представляет какая-либо из следующих формул (1)-(5). В этих формулах n представляет собой степень полимеризации и может принимать произвольное значение.
[0020]
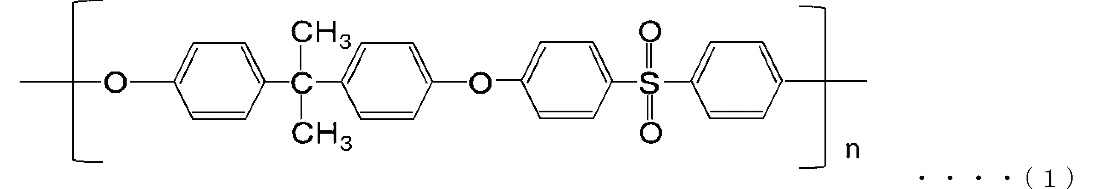



[0021] Полисульфон формулы (1) не ограничивается определенным образом, и соответствующие примеры представляют собой продукт, поставляемый под товарным наименованием "Udel" от компании Solvay Advanced Plolymers (далее называется "Solvay"), и продукт, поставляемый под товарным наименованием "Ultrazone" от компании BASF Japan Ltd., и существуют продукты множества типов, которые различаются по степени полимеризации.
Простой полиэфирсульфон формулы (2) не ограничивается определенным образом, и соответствующие примеры представляют собой продукт, поставляемый под товарным наименованием "Sumika Excel PES" от компании Sumitomo Chemical Co., Ltd, и продукт, поставляемый под товарным наименованием "Ultrazone" от компании BASF Japan Ltd. С точки зрения технологичности и легкодоступности, приведенная вязкость, измеренная с использованием раствора 1 мас./об.% диметилформамида, составляет предпочтительно от 0,30 до 0,60 и предпочтительнее 0,36 до 0,50.
[0022] Полиарилат не ограничивается определенным образом, и соответствующий пример представляет собой полимер, имеющий повторяющееся звено, которое представляет следующая формула (6), причем может использоваться соединение, в котором часть ароматического кольца является химически модифицированной. В данной формуле n представляет собой степень полимеризации и может принимать произвольное значение.
[0023]
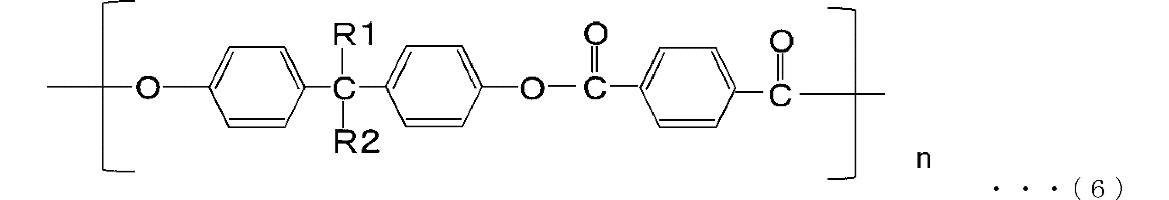
[0024] В формуле (6) R1 и R2 представляют собой низшие алкильные группы, содержащие от 1 до 5 атомов углерода. Группы R1 и R2 могут быть одинаковыми или отличаться друг от друга.
Примеры R1 и R2 представляют собой метильная группа, этильная группа, пропильная группа, бутильная группа и пентильная группа.
[0025] С точки зрения технологичности и легкодоступности, полиарилат имеет молекулярную массу, предпочтительно составляющую приблизительно от 20000 до 50000.
В качестве полиарилата может использоваться полиарилат, соответствующим образом синтезированный посредством поликонденсации двухвалентного фенола и ароматической дикарбоновой кислоты, или может использоваться имеющийся в продаже продукт.
Имеющийся в продаже продукт не ограничивается определенным образом, и соответствующие примеры представляют собой продукты, поставляемые под товарным наименованием "U Polymer" от компании Unitika Ltd., под товарным наименованием "APE" от компании Bayer, под товарным наименованием "DUREL" от компании Celanese Corporation и под товарным наименованием "Arylon" от компании Du Pont.
[0026] Полимеры на метакрилатной основе не ограничиваются определенным образом, и соответствующий пример представляет собой полиметилметакрилат, имеющий повторяющееся звено, которое представляет следующая формула (7). В данной формуле n представляет собой степень полимеризации и может принимать произвольное значение.
Полиметилметакрилат не ограничивается определенным образом, и соответствующий пример представляет собой продукт, поставляемый под товарным наименованием "Dianal BR-80" от компании Mitsubishi Rayon Co., Ltd.
[0027]

[0028] Полиолефины не ограничиваются определенным образом, и соответствующие примеры представляют собой полиэтилен, полипропилен, поли-3-метилбутен-1 и поли-4-метилпентен-1.
Среди них полиэтилен и полипропилен являются предпочтительными, потому что при их использовании может быть получена мембрана в виде полых волокон, имеющая достаточно большой размер пор.
Полиэтилен не ограничивается определенным образом, но имеет повторяющееся звено, которое представляет следующая формула (8), и соответствующие примеры представляют собой продукты, поставляемый под товарным наименованием "HI-ZEX 2208J" от компании Prime Polymer Co., Ltd. и под товарным наименованием "Suntec HdJ240" от компании Asahi Kasei Chemicals Corp.
[0029]

[0030] <Гидрофильный полимер>
Согласно настоящему варианту осуществления, гидрофильный полимер не ограничивается определенным образом, и соответствующие примеры представляют собой поливинилпирролидон, полиэтиленгликоль, поливиниловый спирт, полипропиленгликоль, а также сополимер этилена и винилового спирта.
С точки зрения устойчивости прядения и сродства к полимерам на основе полисульфоновов, предпочтительно используется поливинилпирролидон.
В качестве гидрофильного полимера эти полимеры могут использоваться индивидуально или в сочетаниях двух или более веществ.
Поливинилпирролидон не ограничивается определенным образом, и соответствующий пример представляет собой продукт, поставляемый под товарным наименованием "Plasdone" от компании BASF Japan Ltd., причем существуют продукты, имеющие различные молекулярные массы, такие как K-15, -30 и -90.
сополимер этилена и винилового спирта не ограничивается определенным образом, и соответствующие примеры представляют собой продукты, поставляемые под товарным наименованием "Soarnol E" от компании Nippon Synthetic Chemical Industry Co., Ltd. и под товарным наименованием "Eval" от компании Kuraray Co., Ltd.
[0031] <Растворимый в жирах витамин>
Согласно настоящему варианту осуществления, растворимый в жирах витамин не ограничивается определенным образом, и соответствующие примеры представляют собой витамин A, витамин D, витамин E и витамин K.
Среди них витамин E является предпочтительным с той точки зрения, что он не вызывает расстройства даже в случае передозировки.
В качестве растворимого в жирах витамина эти витамины могут использоваться индивидуально или в сочетаниях двух или более веществ.
Витамин E не ограничивается определенным образом, и соответствующие примеры представляют собой α-токоферол, α-токоферолацетат, α-токоферолникотинат, β-токоферол, γ-токоферол и δ-токоферол.
Среди них предпочтительным является α-токоферол, потому что он является превосходным в отношении разнообразных физиологических функций в живом организме, включая противоокислительное действие, эффект стабилизации биологических мембран и эффект ингибирования агрегации тромбоцитов, а также он проявляет высокую эффективность подавления окислительного стресса.
[0032] <Растворимый в жирах витамин, присутствующий в каждой разделенной секции, полученной посредством деления пучка мембран в виде полых волокон на пять секций в продольном направлении>
Согласно настоящему варианту осуществления, секция, расположенная в самом концевом участке, когда пучок мембран в виде полых волокон разделен на пять секций в продольном направлении, определена как концевая часть корпуса (см. фиг. 1 и 2).
Как проиллюстрировано на фиг. 2, одно устройство для очистки крови на основе мембран в виде полых волокон имеет две концевые части корпуса.
В процессе кровообращения одна из этих концевых частей корпуса соответствует стороне впуска крови, а другая соответствует стороне выпуска крови.
[0033] Согласно настоящему варианту осуществления, пучок мембран в виде полых волокон означает часть, которая выполняет основную функцию очистки крови в устройстве для очистки крови на основе мембран в виде полых волокон и соответствует, например, части, которая присутствует между герметизирующими слоями (каждый из них соответствует границе между содержащей герметизирующее вещество области и не содержащей герметизирующее вещество области), причем они располагаются на обоих концах устройства для очистки крови на основе мембран в виде полых волокон, когда устройство для очистки крови на основе мембран в виде полых волокон разбирается (см. фиг. 3).
[0034] <Растворимый в жирах витамин, присутствующий в центральной части и в наружной части с центральной частью, определенной как часть в пределах внутренней окружности, имеющая 1/2 радиуса пучка мембран в виде полых волокон, причем наружная часть определяется как часть, не включаемая в центральную часть>
Согласно настоящему варианту осуществления, окружность, имеющая 1/2 радиуса в поперечном направлении пучка мембран в виде полых волокон, определяется как внутренняя окружность. Кроме того, часть в пределах внутренней окружности в поперечном направлении пучка мембран в виде полых волокон, определяется как центральная часть, а часть, не включаемая в центральную часть, определяется как наружная часть (см. фиг. 4).
Другими словами, когда часть, соответствующая наружному периметру пучка мембран в виде полых волокон, определяется как наружная окружность, а окружность, имеющая 1/2 радиуса в поперечном направлении, определяется как внутренняя окружность, часть пучка мембран в виде полых волокон, не включаемая во внутреннюю окружность, а именно часть, имеющая радиус, составляющий 1/2 радиуса или более в пределах наружного периметра (соответствующего радиусу) в поперечном направлении, определяется как наружная часть (см. фиг. 4).
[0035] <Распределение растворимого в жирах витамина>
Согласно настоящему варианту осуществления, количество растворимого в жирах витамина, которое присутствует, по меньшей мере, в одной из концевых частей корпуса, является наибольшим среди количеств растворимого в жирах витамина, которые присутствуют, соответственно, во всех разделенных секциях. Кроме того, количество растворимого в жирах витамина, которое присутствует в центральной части, предпочтительно составляет более чем количество растворимого в жирах витамина, которое присутствует в наружной части.
Как описано в представленных ниже примерах, если количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон в концевой части корпуса или центральная часть сопоставимо с количеством растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон в других разделенных секциях или наружной части, можно определить, что количество растворимого в жирах витамина, которое присутствует в концевой части корпуса или центральной части составляет более чем количества растворимого в жирах витамина, которые присутствуют, соответственно, в других разделенных секциях или в наружной части. В частности, мембрана в виде полых волокон, которая присутствует на периметре внутренней окружности пучка мембран в виде полых волокон, считается принадлежащей к центральной части.
При фактическом кровообращении именно в содержащих отверстия для выпуска/впуска крови частях устройства для очистки крови на основе мембран в виде полых волокон наблюдается наиболее высокая концентрация пероксидного соединения, которое присутствует в крови, проходящей через устройство для очистки крови на основе мембран в виде полых волокон. Если количество растворимого в жирах витамина, которое присутствует в концевой части корпуса на стороне впуска крови устройства для очистки крови на основе мембран в виде полых волокон является наибольшим, пероксидное соединение эффективно нейтрализуется растворимым в жирах витамином. Кроме того, если является наибольшим количество растворимого в жирах витамина, которое присутствует в концевой части корпуса на стороне выпуска крови устройства для очистки крови на основе мембран в виде полых волокон, эффективно устраняется реакционноспособный кислород, образующийся в процессе взаимодействия между мембраной в виде полых волокон и кровью. Количества растворимого в жирах витамина в двух концевых частях корпуса можно установить на максимальном уровне, таким образом, чтобы можно было эффективно устранять как пероксидное соединение, так и реакционноспособный кислород.
Кроме того, когда сравниваются между собой центральная часть и наружная часть устройство для очистки крови на основе мембран в виде полых волокон, концентрация пероксидного соединения, которое присутствует в крови, проходящей через устройство для очистки крови на основе мембран в виде полых волокон, оказывается выше в центральной части, где количество крови увеличивается, вследствие воздействия линейной скорости, чем в наружной части. Таким образом, если количество растворимого в жирах витамина в центральной части составляет более чем в наружной части, пероксидное соединение эффективно устраняется растворимым в жирах витамином. Кроме того, может эффективно устраняться реакционноспособный кислород, образующийся в процессе взаимодействия между мембраной в виде полых волокон и кровью.
[0036] Согласно настоящему варианту осуществления, в пересчете на единицу площади внутренней поверхности мембраны в виде полых волокон, количество растворимого в жирах витамина, которое присутствует, по меньшей мере, в одной из концевых частей корпуса, а именно количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон в концевой части корпуса составляет 20 мг/м2 или более и 300 мг/м2 или менее, предпочтительно 20 мг/м2 или более и 250 мг/м2 или менее, и предпочтительнее 20 мг/м2 или более и 200 мг/м2 или менее. Если количество растворимого в жирах витамина составляет 20 мг/м2 или более, может быть достигнут эффект, возникающий в результате использования растворимого в жирах витамина, а если данное количество составляет 300 мг/м2 или менее, могут быть обеспечены превосходные характеристики совместимости с кровью и характеристики водопроницаемости.
[0037] Согласно настоящему варианту осуществления, в пересчете на единицу площади внутренней поверхности мембраны в виде полых волокон, количество растворимого в жирах витамина, которое присутствует в центральной части, а именно количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон в центральной части, составляет предпочтительно 20 мг/м2 или более и 300 мг/м2 или менее, предпочтительнее 20 мг/м2 или более и 250 мг/м2 или менее, и еще предпочтительнее 20 мг/м2 или более и 200 мг/м2 или менее. Если количество растворимого в жирах витамина составляет 20 мг/м2 или более, может быть достигнут эффект, возникающий в результате использования растворимого в жирах витамина, а если данное количество составляет 300 мг/м2 или менее, могут быть обеспечены превосходные характеристики совместимости с кровью и характеристики водопроницаемости.
[0038] Согласно настоящему варианту осуществления, оказывается предпочтительным, что количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, которое присутствует, по меньшей мере, в одной из концевых частей корпуса, является наибольшим среди количеств растворимого в жирах витамина, которые присутствуют, соответственно, во всех разделенных секциях; что количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, которое присутствует, по меньшей мере, в одной концевой части корпуса составляет 20 мг/м2 или более и 300 мг/м2 или менее; и что когда часть в пределах внутренней окружности, имеющей 1/2 радиуса пучка мембран в виде полых волокон, определяется как центральная часть, и часть, не включенная в центральную часть, определяется как наружная часть, количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в центральной части, составляет более чем количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в наружной части.
Количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в центральной части, составляет предпочтительно 20 мг/м2 или более и 300 мг/м2 или менее, предпочтительнее 20 мг/м2 или более и 250 мг/м2 или менее, и еще предпочтительнее 20 мг/м2 или более и 200 мг/м2 или менее. Кроме того, когда количества растворимого в жирах витамина, которые присутствуют в центральной части и наружной части, соответственно, находятся в предпочтительных интервалах, количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, которое присутствует, по меньшей мере, в одной концевой части корпуса, составляет предпочтительно 20 мг/м2 или более и 250 мг/м2 или менее, и предпочтительнее 20 мг/м2 или более и 200 мг/м2 или менее.
[0039] Согласно настоящему изобретению, термин "количество растворимого в жирах витамина, которое присутствует в мембране в виде полых волокон" означает содержание растворимого в жирах витамина, который прикрепляется, адсорбируется или удерживается на поверхности мембраны в виде полых волокон, и количество растворимого в жирах витамина, которое присутствует в мембране в виде полых волокон, можно количественно определять, например, в зависимости от содержания растворимого в жирах витамина, извлекаемого с использованием растворителя без разрушения или растворения мембраны в виде полых волокон.
[0040] Далее будет описан примерный способ измерения количество растворимого в жирах витамина, которое присутствует в мембране в виде полых волокон.
Устройство для очистки крови на основе мембран в виде полых волокон разбирается, и таким образом, мембрана в виде полых волокон извлекается, промывается водой и высушивается. После высушивания и точного взвешивания мембраны в виде полых волокон в нее добавляется поверхностно-активное вещество, способное растворять растворимый в жирах витамин, такое как водный раствор 1 мас.% полиэтиленгликоль-трет-октилфенилового эфира, после чего осуществляется перемешивание и экстрагирование. Для экстрагированной мембраны в виде полых волокон площадь внутренней поверхности мембраны в виде полых волокон вычисляется на основании внутреннего диаметра и длины мембраны в виде полых волокон.
Для измерения количеств растворимого в жирах витамина, которые присутствуют соответственно в центральной части и в наружной части мембран в виде полых волокон, устройство для очистки крови на основе мембран в виде полых волокон разбирается, разделяется на центральную часть и наружную часть, и мембраны в виде полых волокон выбираются из соответствующих частей для измерения.
Операция количественного измерения осуществляется, например, методом жидкостной хроматографии, таким образом, чтобы вычислить концентрацию растворимого в жирах витамина в экстракте с использованием построенной калибровочной кривой, на основании площади пика стандартного раствора растворимого в жирах витамина.
Жидкостная хроматография, которая описывается исключительно в качестве примера, может осуществляться следующим образом: колонка (наполненная колонка ODP-506E для жидкостной хроматографии высокого разрешения, изготовленная компанией Shodex Asahipak) устанавливается в жидкостной хроматограф высокого разрешения (насос: Jasco Corporation PU-1580, детектор: Shimadzu RID-6A, автоматический инжектор: Shimadzu SIL-6B, устройство обработки данных: Tosoh GPC-8020, колоночный термостат: GL Sciences 556), метанол для жидкостной хроматографии высокого разрешения, используемый в качестве подвижной фазы, пропускается через колонку при температуре, составляющей 40°C, и скорости потока, составляющей, например, 1 мл/мин, и концентрация растворимого в жирах витамина определяется на основании площади пика поглощения при длине волны 295 нм с помощью детектора ультрафиолетового излучения.
[0041] Согласно настоящему варианту осуществления, когда количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, которое присутствует, по меньшей мере, в одной концевой части корпуса, где количество растворимого в жирах витамина является наибольшим определяется как A (мг/м2), и количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в разделенной секции, где количество растворимого в жирах витамина является наименьшим среди других разделенных секций, определяется как B (мг/м2), соотношение (A/B) между количествами A и B составляет предпочтительно 1,1 или более и 10 или менее, предпочтительнее 1,3 или более и 10 или менее, и еще предпочтительнее 1,3 или более и 5,0 или менее.
Если соотношение A/B составляет 1,1 или более, устройство для очистки крови на основе мембран в виде полых волокон является превосходным в отношении противоокислительных характеристик, и если соотношение A/B составляет 10 или менее, может обеспечиваться соответствующее количество растворимого в жирах витамина, которое иммобилизуется в разделенных секциях, не представляющих собой концевые части корпуса устройства для очистки крови на основе мембран в виде полых волокон, и, следовательно, устройство для очистки крови на основе мембран в виде полых волокон является превосходным в отношении противоокислительных характеристик в целом.
[0042] Когда количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в центральной части, определяется как C (мг/м2), и количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в наружной части, определяется как D (мг/м2), соотношение (C/D) между количествами C и D составляет предпочтительно 1,1 или более и 50 или менее, предпочтительнее 1,3 или более и 50 или менее, еще предпочтительнее 2,0 или более и 50 или менее, и еще предпочтительнее 4,0 или более и 50 или менее.
Если соотношение C/D составляет 1,1 или более, устройство для очистки крови на основе мембран в виде полых волокон является превосходным в отношении противоокислительных характеристик, и если соотношение C/D составляет 50 или менее, может обеспечиваться соответствующее количество растворимого в жирах витамина, которое иммобилизуется в наружной части устройства для очистки крови на основе мембран в виде полых волокон, и, следовательно, устройство для очистки крови на основе мембран в виде полых волокон является превосходным в отношении противоокислительных характеристик в целом.
[0043] Согласно настоящему варианту осуществления, поскольку таким способом может подавляться изменчивость противоокислительных характеристик, оказывается предпочтительным, что количество растворимого в жирах витамина, которое присутствует, по меньшей мере, в одной концевой части корпуса, является наибольшим среди количеств растворимого в жирах витамина, которые присутствуют, соответственно, во всех разделенных секциях, и что количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в центральной части, составляет более чем количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в наружной части.
Кроме того, когда количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в центральной части, определяется как C (мг/м2), и количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в наружной части определяется как D (мг/м2), соотношение (C/D) составляет предпочтительно 1,1 или более и 50 или менее, и когда количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в концевой части корпуса, где количество растворимого в жирах витамина является наибольшим, определяется как (мг/м2), и количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, присутствующее в разделенной секции, где количество растворимого в жирах витамина является наименьшим среди других разделенных секций, определяется как B (мг/м2), соотношение (A/B) между количествами A и B составляет предпочтительно 1,1 или более и 10 или менее.
Согласно настоящему варианту осуществления, оказывается подходящим, что соотношение A/B составляет 1,1 или более и 10 или менее, и что соотношение C/D составляет 1,1 или более и 50 или менее.
Если оба соотношения A/B и C/D находятся в описанных выше интервалах, а именно, если растворимый в жирах витамин распределяется в продольном направлении, а также в поперечном направлении мембран в виде полых волокон, можно подавляться изменчивость противоокислительных характеристик, таким образом, что устройство для очистки крови на основе мембран в виде полых волокон может проявлять устойчивые противоокислительные характеристики.
[0044] На основании исследований, проведенных до настоящего времени, было обнаружено, что характеристики водопроницаемости устройства для очистки крови на основе мембран в виде полых волокон ухудшаются, если растворимый в жирах витамин иммобилизуется на мембранах в виде полых волокон. Как правило, эта проблема может быть преодолена посредством улучшения общих характеристик водопроницаемости за счет изменения структура мембран в виде полых волокон перед иммобилизацией растворимого в жирах витамина, но степень ухудшения характеристик водопроницаемости изменяется в зависимости от количества растворимого в жирах витамина, подлежащего иммобилизации, и, следовательно, необходимо производить и хранить мембраны в виде полых волокон, имеющие разнообразные характеристики водопроницаемости, что значительно увеличивает нагрузку на производителя.
В устройстве для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления характеристики водопроницаемости могут регулироваться посредством выбора условий для иммобилизации витамина в концевой части корпуса и в других разделенных секциях пучка мембран в виде полых волокон. Кроме того, по сравнению с устройством для очистки крови на основе мембран в виде полых волокон, в котором такое же количество растворимого в жирах витамина, как в концевой части корпуса, практически равномерно распределяется в продольном направлении, улучшенные характеристики водопроницаемости могут быть достигнуты при сохранении практически эквивалентных противоокислительных характеристик.
[0045] <Параметр растворимости δ>
Если гидрофобный полимер согласно настоящему варианту осуществления имеет параметр растворимости (кал/см3)1/2, составляющий 13,0 или менее, сродство к растворимому в жирах витамину предпочтительно является хорошим, таким образом, что растворимый в жирах витамин может легко удерживаться на мембранах в виде полых волокон. Параметр растворимости δ составляет предпочтительно 9,5 или более и 12,0 или менее.
Параметру растворимости δ соответствует показатель, описанный, например, в книге "Информационный справочник полимеров, основное издание" под редакцией Общества наук о полимерах, издательство Baifukan Co., Ltd., первое издание, выпущенное 30 января 1986 г., с. 591-593, причем высокий параметр растворимости означает сильную гидрофильность, а низкий параметр растворимости означает сильную гидрофобность, и если используется гидрофобный полимер, имеющий параметр растворимости в пределах вышеупомянутого интервала, то заданное количество растворимого в жирах витамина удерживается на мембранах в виде полых волокон.
Примеры гидрофобного полимера представляют собой полиэтилен (δ=8,4), полиметилметакрилат (δ=9,10), полиарилат (δ=9,3), полимерный сплав типа простой полиэфирсульфон-полиарилат (δ=9,6), полисульфон (δ=9,9), простой полиэфирсульфон (δ=9,9), полигидроксиэтилметакрилат (δ=10,0), диацетат целлюлозы (δ=11,4), полиакрилонитрил (δ=12,4), триацетат целлюлозы и поликарбонат. Следует отметить, что каждое значение, приведенное выше в качестве δ, упоминается исключительно в качестве примера.
В качестве гидрофобного полимера эти полимеры могут использоваться индивидуально или в сочетаниях двух или более веществ.
[0046] <Способ изготовления мембраны в виде полых волокон>
Согласно настоящему варианту осуществления, мембрана в виде полых волокон может изготавливаться посредством использования известной пленкообразующей технологии.
Гидрофобный полимер и гидрофильный полимер растворяются в обычном растворителе для изготовления прядильного раствора.
Обычный растворитель не ограничивается определенным образом, и соответствующие примеры представляют собой N,N-диметилацетамид, диметилсульфоксид, N-метил-2-пирролидон, диметилформамид, сульфолан, ацетон, диоксан, а также смешанный растворитель, содержащий два или более из этих растворителей.
Прядильный раствор непрерывно экструдируется, приобретая форму полого волокна, и одновременно подвергается коагуляции посредством вступления в контакт с коагулирующее вещество, и, таким образом, получается непрерывная мембрана в виде полых волокон. Коагулирующее вещество содержит смешанный раствор растворителя для гидрофобного полимера и нерастворяющее вещество, в котором концентрация растворителя составляет 0% или более и 70% или менее. В частности, для регулирования пор желательного размера в мембране в виде полых волокон в прядильном растворе может содержаться добавка, такая как вода.
[0047] Концентрация гидрофобного полимера в прядильном растворе не ограничивается определенным образом, при том условии, что может образовываться мембрана, и у получаемой в результате мембрана могут обеспечиваться характеристики проницаемой мембраны, причем эта концентрация составляет предпочтительно 5 мас.% или более и 35 мас.% или менее, и предпочтительнее 10 мас.% или более и 30 мас.% или менее. В целях достижения высоких характеристик водопроницаемости концентрация гидрофобного полимера предпочтительно снижается, и еще предпочтительнее она составляет 10 мас.% или более и 25 мас.% или менее.
[0048] Что касается концентрации гидрофильного полимера по отношению к гидрофобному полимеру в прядильном растворе, содержание в смеси гидрофильного полимера по отношению к 100 мас.% гидрофобного полимера составляет предпочтительно 27 мас.% или менее, предпочтительнее 18 мас.% или более и 27 мас.% или менее, и еще предпочтительнее 20 мас.% или более и 27 мас.% или менее.
Если содержание в смеси гидрофильного полимера по отношению к 100 мас.% гидрофобного полимера составляет 27 мас.% или менее, как правило, количество гидрофильного полимера, подлежащего элюированию, предпочтительно уменьшается. Кроме того, если оно составляет 18 мас.% или более, снижается концентрация гидрофильного полимера на поверхности мембраны в виде полых волокон, и может предпочтительно уменьшаться вероятность возникновения лейкопении за счет резкого снижения концентрации лейкоцитов в крови пациента.
[0049] На стадии изготовления мембраны в виде полых волокон используется двойной кольцевой мундштук, и прядильный раствор выпускается через прядильную фильеру одновременно с полостной внутренней текучей средой, используемый в качестве коагулирующего вещества, из трубки в воздух.
[0050] В качестве полостной внутренней текучей среды может использоваться вода или раствор, в котором содержится, в основном вода, причем его состав и другие параметры могут определяться в соответствии с желательными характеристиками водопроницаемости мембраны в виде полых волокон. Как правило, соответствующим образом используется смешанный раствор, содержащий обычный растворитель, используемый в прядильном растворе, и воду. Чтобы регулировать характеристики проницаемости мембраны по отношению к растворенному веществу, предпочтительно регулируется концентрация обычного растворителя, и, как правило, используется концентрация водного раствора, составляющая 0 мас.% или более и 70 мас.% или менее. Гидрофильный полимер может добавляться в полостную внутреннюю текучую среду до содержания, составляющего 0 мас.% или более и 2 мас.% или менее, таким образом, что может также регулироваться количество гидрофильного полимера, присутствующее на поверхности мембраны в виде полых волокон.
Прядильный раствор, который выходит через прядильную фильеру с полостной внутренней текучей средой, пропускается через секцию выдерживания, вводится и погружается в коагуляционная ванна, которая содержит, в основном, воду и располагается под прядильной фильерой таким образом, чтобы полностью осуществлялась коагуляция, и после стадии промывания и т. д., и полученная таким способом мембрана в виде полых волокон во влажном состоянии наматывается намоточным устройством, и получается пучок мембран в виде полых волокон, и после этого получаемый в результате продукт направляется на стадию высушивания. В качестве альтернативы, после стадии промывания получаемый в результате продукт может высушиваться в сушильном устройстве для получения пучка мембран в виде полых волокон.
[0051] Мембрана в виде полых волокон, содержащая полиолефин в качестве гидрофобного полимера, может изготавливаться любыми известными способами, такими как способ влажного фазового перехода, способ разделения расплавленной фазы и способ, растяжения пор.
Среди эти способов, способ растяжения пор представляет собой способ, согласно которому кристаллический полимер подвергается формованию и превращается в полое волокно или пленку, в процессе холодного растяжения образуется просвет между кристаллическими пластинками, и размер пор увеличивается в процессе горячего растяжения, где получается пористая структура, и в этом способе пористый структура изготавливается физическими средствами растяжения без введения добавки, такой как растворитель, в полимерный материал, и при этом не возникает проблема остаточного растворителя и т. д., и, следовательно, данный способ может соответствующим образом использоваться согласно настоящему варианту осуществления для изготовления мембраны в виде полых волокон, содержащей полиолефин.
В частности, мембрана в виде полых волокон изготавливают, осуществляя прядение полиолефина с использованием двойного кольцевого мундштука при температуре мундштука, составляющей 145°C или более и 155°C или менее, отжиг получаемого таким способом полого волокна при температуре, составляющей 115°C или более и 120°C или менее, в течение одного часа или более и 3 часов или менее и горячее растяжение получаемого в результате продукта при температуре на уровне комнатной температуры или выше и 100°C или ниже на 10% или более и на 30% или менее, а затем при 100°C или более и 120°C или менее на 30% или более и на 350% или менее.
[0052] Если полиолефин используется в качестве гидрофобного полимера, то сополимер этилена и винилового спирта предпочтительно используется в качестве гидрофильного полимера с точки зрения улучшения совместимости с кровью посредством покрытия пористой поверхности мембраны в виде полых волокон.
Содержание этилена в сополимере этилена и винилового спирта составляет предпочтительно 20 мол.% или более и 70 мол.% или менее, и предпочтительнее 25 мол.% или более и 50 мол.% или менее с точки зрения улучшения адгезионной способности для предотвращения отслаивания слоя покрытия с мембраны в виде полых волокон и с точки зрения гидрофильности.
Пористая поверхность мембраны в виде полых волокон, содержащей полиолефин, обрабатывается раствором сополимера этилена и винилового спирта, и, таким образом, может быть получена мембрана в виде полых волокон, содержащая гидрофобный полимер и гидрофильный полимер.
Если раствор сополимера этилена и винилового спирта содержит растворимый в жирах витамин, мембрана в виде полых волокон может быть покрыта сополимером этилена и винилового спирта, и в то же время может быть получена мембрана в виде полых волокон, содержащая растворимый в жирах витамин.
Получается пучок мембран в виде полых волокон, содержащий сополимер этилена и винилового спирта, и после этого получаемый в результате продукт подвергается обработке посредством высушивания.
[0053] Сополимер этилена и винилового спирта растворяется в смешивающемся с водой органическом растворителе.
Смешивающийся с водой органический растворитель не ограничивается определенным образом, и соответствующие примеры представляют собой спирты, такие как метанол, этанол, н-пропанол, изопропанол, н-бутанол, трет-бутанол и циклогексанол, многоатомные спирты, такие как этиленгликоль, пропиленгликоль и глицерин, тетрагидрофуран, диоксан, диметилформамид, диметилсульфоксид, диметилацетамид, формамид и этиленхлоргидрин.
Среди них органический растворитель, имеющий высокую полярность, предпочтительно используется с точки зрения улучшения адгезионной способности по отношению к полиолефину посредством локализации сополимера этилена и винилового спирта, причем этанол и ацетон являются предпочтительными с точки зрения растворимости и низкой токсичности.
Один из этих органических растворителей может использоваться индивидуально, или любой из этих растворителей может использоваться в составе смешанного растворителя. Предпочтительно используется смешанный растворитель, содержащий воду, потому что таким образом повышается полярность.
Относительное содержание воды в смешанном растворителе не ограничивается определенным образом, при том условии, что не уменьшается растворимость сополимера этилена и винилового спирта, причем данное относительное содержание может соответствующим образом устанавливаться в зависимости от содержания этилена в сополимере, температуры раствора и других факторов. Относительное содержание воды предпочтительно составляет, например, 5 мас.% или более и 75 мас.% или менее.
Подходящая концентрация используемого сополимера может произвольным образом выбираться для нанесения покрытия, и она составляет, например, предпочтительно 0,1 мас.% или более и 5 мас.% или менее.
Если используется, раствор, содержащий растворимый в жирах витамин, то концентрация растворимого в жирах витамина составляет предпочтительно 0,01 мас.% или более и 10 мас.% или менее, и предпочтительнее 0,1 мас.% или более и 5 мас.% или менее.
[0054] <Способ изготовления устройства для очистки крови на основе мембран в виде полых волокон>
В предпочтительном способе изготовления устройства для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления, например, пучок мембран в виде полых волокон изготавливается, как описано выше, пучок мембран в виде полых волокон вставляется в цилиндрический резервуар, имеющий отверстие для впуска/выпуска обрабатываемой жидкости в контакте с наружной поверхностью мембран в виде полых волокон, герметизирующее вещество, представляющее собой полиуретан или подобное вещество, вводится в оба конца пучка, образуя герметизирующие слои для герметизации обоих концов, и после этого избыточная часть отвержденного герметизирующего вещества удаляется, открывая торцевые поверхности, торцевые крышки, имеющие отверстия для впуска/выпуска текучей среды, присоединяются к торцевым поверхностям, растворимый в жирах витамин затем иммобилизуется, и, таким образом, изготавливается устройство для очистки крови на основе мембран в виде полых волокон.
[0055] Фиг. 3 иллюстрирует типичное устройство для очистки крови на основе мембран в виде полых волокон, но его конструкция может соответствующим образом изменяться в пределах объема предмета настоящего изобретения. Кроме того, торцевые крышки могут присоединяться после иммобилизации растворимого в жирах витамина.
Предпочтительно осуществляется стадия стерилизационной обработки, которая описана далее. Растворимый в жирах витамин может иммобилизоваться, когда мембраны в виде полых волокон присутствуют в форме пучка, как описано далее.
[0056] <Стадия иммобилизации растворимого в жирах витамина на мембране в виде полых волокон>
Устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления можно изготавливать, сочетая способ непосредственного погружения и способ нанесения покрытия, например, такие способы, которые описаны ниже в подготовительных примерах 1-6, но способ изготовления не ограничивается следующим описанием.
[0057] (Подготовительный пример 1)
Часть пучка мембран в виде полых волокон, соответствующая одной концевой части корпуса пучка мембран в виде полых волокон, непосредственно погружается в раствор растворимого в жирах витамина. После истечения заданного времени мембраны в виде полых волокон извлекаются из раствора. После этого раствор, оставшийся в мембранах в виде полых волокон, выдувается и высушивается потоком воздуха или другого газа, поступающего из одного конца мембран в виде полых волокон, если это необходимо (стадия продувания воздухом). Если продувание воздухом осуществляется со стороны, которая погружается в раствор растворимого в жирах витамина, по направлению к другой стороне, которая не погружается в раствор, небольшое количество растворимого в жирах витамина может наноситься также на сторону, которая не погружается в раствор. Пучок может высушиваться без осуществления стадии продувания воздухом.
Полученный в результате этого пучок мембран в виде полых волокон собирается, и, таким образом, может быть изготовлено устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления.
В пучке мембран в виде полых волокон перед погружением могут использоваться мембраны в виде полых волокон, в которых растворимый в жирах витамин совершенно не иммобилизуется, или могут использоваться мембраны в виде полых волокон, в которых растворимый в жирах витамин в заданном количестве равномерно иммобилизуется в продольном направлении способом нанесения покрытия, и когда эти способы сочетаются, распределение растворимого в жирах витамина в продольном направлении может регулироваться.
Согласно настоящему варианту осуществления, способ нанесения покрытия означает способ получения мембраны в виде полых волокон, в которой содержится растворимый в жирах витамин, иммобилизованный посредством пропускания раствора растворимого в жирах витамина через полую часть полого волокна, и затем высушивания растворителя. В качестве альтернативы, после сборки устройство для очистки крови на основе мембран в виде полых волокон, раствор для нанесения покрытия растворимого в жирах витамина может затем пропускаться через устройство для очистки крови на основе мембран в виде полых волокон.
Распределение растворимого в жирах витамина в продольном направлении устройства для очистки крови на основе мембран в виде полых волокон может регулироваться также в соответствии с концентрацией растворимого в жирах витамина в растворе растворимого в жирах витамина, который используется для погружения, типом растворителя и поверхностно-активным веществом, таким как глицерин. Одно устройство для очистки крови на основе мембран в виде полых волокон имеет две концевые части корпуса, и если оказывается желательным увеличение количества растворимого в жирах витамина, подлежащего иммобилизации, в обеих концевых частях корпуса, то вышеупомянутый способ осуществляется в отношении обеих концевых частей корпуса.
Когда растворимый в жирах витамин иммобилизуется, по меньшей мере, в одной концевой части корпуса, получается пучок мембран в виде полых волокон, который проиллюстрирован на фиг. 1, а когда растворимый в жирах витамин иммобилизуется в двух концевых частях корпуса, может быть получен пучок мембран в виде полых волокон, который проиллюстрирован на фиг. 2. В качестве альтернативы, растворимый в жирах витамин может иммобилизоваться в различных иммобилизованных количествах в двух концевых частях корпуса.
[0058] (Подготовительный пример 2)
Часть пучка мембран в виде полых волокон, соответствующая одной концевой части корпуса пучка мембран в виде полых волокон, непосредственно погружается в раствор растворимого в жирах витамина. После истечения заданного времени мембраны все мембраны в виде полых волокон затем непосредственно погружаются в раствор растворимого в жирах витамина. Мембраны в виде полых волокон извлекаются из растворимого в жирах витамина раствор, и раствор, оставшийся в мембранах в виде полых волокон, выдувается и высушивается потоком воздуха или другого газа, поступающего из одного конца мембран в виде полых волокон, если это необходимо. В этом случае, поскольку только одна из концевых частей корпуса погружается в раствор растворимого в жирах витамина на относительно продолжительный период времени, количество растворимого в жирах витамина, иммобилизованного в этой концевой части корпуса, является наибольшим. Пучок может высушиваться без осуществления стадии продувания воздухом.
Полученный в результате этого пучок мембран в виде полых волокон собирается, и, таким образом, может быть изготовлено устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления.
В пучке мембран в виде полых волокон перед погружением могут использоваться мембраны в виде полых волокон, в которых растворимый в жирах витамин совершенно не иммобилизуется, или могут использоваться мембраны в виде полых волокон, в которых заданное количество растворимого в жирах витамина равномерно иммобилизуется в продольном направлении способом нанесения покрытия, и когда эти способы сочетаются, распределение растворимого в жирах витамина в продольном направлении может регулироваться.
В качестве альтернативы, после сборки устройства для очистки крови на основе мембран в виде полых волокон, раствор для нанесения покрытия растворимого в жирах витамина может затем пропускаться через устройство для очистки крови на основе мембран в виде полых волокон.
Распределение растворимого в жирах витамина в продольном направлении устройства для очистки крови на основе мембран в виде полых волокон может регулироваться также в соответствии с концентрацией растворимого в жирах витамина в растворе растворимого в жирах витамина, который используется для погружения, типом растворителя и поверхностно-активного вещества, такого как глицерин. В подготовительном примере 2 концентрация растворимого в жирах витамина в растворе растворимого в жирах витамина, который используется для погружения, часть, соответствующая концевой части корпуса, и концентрация растворимого в жирах витамина в растворе растворимого в жирах витамина, который используется для погружения всей мембраны в виде полых волокон, могут изменяться, и, таким образом, распределение растворимого в жирах витамина в продольном направлении устройства для очистки крови на основе мембран в виде полых волокон может регулироваться. Аналогичные способы могут использоваться не только в отношении концентрации растворимого в жирах витамина, но также в отношении типа растворителя и концентрации и типа поверхностно-активного вещества. Один устройство для очистки крови на основе мембран в виде полых волокон имеет две концевые части корпуса, и если оказывается желательным увеличение количества растворимого в жирах витамина, подлежащего иммобилизации, в обеих концевых частях корпуса, то вышеупомянутый способ осуществляется в отношении обеих концевых частей корпуса.
Когда растворимый в жирах витамин иммобилизуется, по меньшей мере, в одной концевой части корпуса, получается пучок мембран в виде полых волокон, который проиллюстрирован на фиг. 1, и когда растворимый в жирах витамин иммобилизуется в двух концевых частях корпуса, может получаться пучок мембран в виде полых волокон, который проиллюстрирован на фиг. 2. В качестве альтернативы, растворимый в жирах витамин может иммобилизоваться в различных иммобилизованных количествах в двух концевых частях корпуса.
[0059] (Подготовительный пример 3)
Часть пучка мембран в виде полых волокон, соответствующая одной концевой части корпуса пучка мембран в виде полых волокон, непосредственно погружается в раствор растворимого в жирах витамина. В этом случае, в качестве растворителя, используемого в растворе растворимого в жирах витамина, используется смешанный растворитель, содержащий растворители, которые хорошо и плохо растворяют растворимый в жирах витамин, такие как спирт и вода, и концентрация хорошего растворителя (например, спирта) представляет собой наименьшую концентрацию, при которой может растворяться растворимый в жирах витамин. После истечения заданного времени мембраны в виде полых волокон извлекаются из растворимого в жирах витамина раствор, или все мембраны в виде полых волокон затем непосредственно погружаются в раствор растворимого в жирах витамина на заданное время и после этого извлекаются из раствора витамина. Полученные в результате этого мембраны в виде полых волокон подвергаются продуванию воздухом или аналогичным газом с одного конца мембран в виде полых волокон для выдувания и высушивания раствора, остающегося в мембранах в виде полых волокон, если это необходимо. В этом случае, поскольку только концевая часть корпуса погружается в растворе растворимого в жирах витамина на относительно продолжительный период времени, и концентрация хорошего растворителя (например, спирта) уменьшается до нижней предельной концентрации, при которой может растворяться растворимый в жирах витамин, растворимый в жирах витамин селективно иммобилизуется на гидрофобном полимере, и, таким образом, количество растворимого в жирах витамина, иммобилизованного в концевой части корпуса, является наибольшим. Пучок может высушиваться без осуществления стадии продувания воздухом.
Полученный в результате этого пучок мембран в виде полых волокон собирается, и, таким образом, может быть изготовлено устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления.
В пучке мембран в виде полых волокон перед погружением могут использоваться мембраны в виде полых волокон, в которых растворимый в жирах витамин совершенно не иммобилизуется, или могут использоваться мембраны в виде полых волокон, в которых заданное количество растворимого в жирах витамина равномерно иммобилизуется в продольном направлении способом нанесения покрытия, и когда эти способы сочетаются, может регулироваться распределение растворимого в жирах витамина в продольном направлении.
В качестве альтернативы, после сборки устройства для очистки крови на основе мембран в виде полых волокон раствор для нанесения покрытия растворимого в жирах витамина может затем пропускаться через устройство для очистки крови на основе мембран в виде полых волокон.
Распределение растворимого в жирах витамина в продольном направлении устройства для очистки крови на основе мембран в виде полых волокон может регулироваться также в соответствии с концентрацией растворимого в жирах витамина в растворе растворимого в жирах витамина, который используется для погружения, типами и концентрациями хорошего растворителя и плохого растворителя, а также поверхностно-активного вещества, такого как глицерин. В подготовительном примере 3, поскольку могут изменяться состав раствора растворимого в жирах витамина, который используется для погружения части, соответствующей концевой части корпуса, и состав раствора растворимого в жирах витамина раствора растворимого в жирах витамина, который используется для погружения всех мембран в виде полых волокон, распределение растворимого в жирах витамина в продольном направлении устройства для очистки крови на основе мембран в виде полых волокон может регулироваться с большей точностью.
Одно устройство для очистки крови имеет две концевые части корпуса, и если оказывается желательным увеличение количества растворимого в жирах витамина, подлежащего иммобилизации, в обеих концевых частях корпуса, вышеупомянутый способ осуществляется в отношении обеих концевых частей корпуса. Когда растворимый в жирах витамин иммобилизуется, по меньшей мере, в одной концевой части корпуса, получается пучок мембран в виде полых волокон, который проиллюстрирован на фиг. 1, и когда растворимый в жирах витамин иммобилизуется в двух концевых частях корпуса, может получаться пучок мембран в виде полых волокон, который проиллюстрировано на фиг. 2. В качестве альтернативы, растворимый в жирах витамин может иммобилизоваться в различных иммобилизованных количествах в двух концевых частях корпуса.
[0060] (Подготовительный пример 4)
Пучок мембран в виде полых волокон, на которые растворимый в жирах витамин наносится в концевой части корпуса каждым из способов изготовления согласно подготовительным примерам 1-3, собирается в резервуар, и получаемое в результате изделие устанавливается в устройство для нанесения покрытия раствором растворимого в жирах витамина. Устройство для нанесения покрытия на своем конце включает зажимное приспособление, имеющее устойчивую к давлению часть на своей наружной окружности. Зажимное приспособление имеет конструкцию, образующую тесный контакт с устройством для очистки крови на основе мембран в виде полых волокон, и устойчивая к давлению часть может иметь форму сетки или части, маскирующей всю окружность. Раствор растворимого в жирах витамина поступает из устройства для нанесения покрытия, проходит через устройство для очистки крови на основе мембран в виде полых волокон при скорости потока, составляющей 100 мл/мин или более и 1500 мл/мин или менее, в течение 30 секунд или более и 100 секунд или менее, и после этого устройство для очистки крови на основе мембран в виде полых волокон извлекается. После этого раствор растворимого в жирах витамина, который остается в мембранах в виде полых волокон, выдувается и высушивается, когда осуществляется продувание воздухом или аналогичным газом с одного конца устройства для очистки крови на основе мембран в виде полых волокон, если это необходимо. При этом, если продувание воздухом осуществляется со стороны, покрытой раствором растворимого в жирах витамина, раствор растворимого в жирах витамина может перемещаться также на непокрытую сторону, таким образом, что мембраны в виде полых волокон покрываются равномерно в продольном направлении. В качестве альтернативы, высушивание может осуществляться, если покрытая сторона направлена вверх, без осуществления стадии продувания воздухом. На получаемое в результате изделие надеваются крышки, и, таким образом, может быть изготовлено устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления.
[0061] (Подготовительный пример 5)
Пучок мембран в виде полых волокон, на которые растворимый в жирах витамин наносится в концевой части корпуса каждым из способов изготовления согласно подготовительным примерам 1-3, собирается в резервуар, и получаемое в результате изделие устанавливается в устройство для нанесения покрытия раствором растворимого в жирах витамина. Устройство для нанесения покрытия на своем конце включает зажимное приспособление, имеющее устойчивую к давлению часть на своей наружной окружности. Зажимное приспособление имеет конструкцию, образующую тесный контакт с устройством для очистки крови на основе мембран в виде полых волокон. Из устройства для нанесения покрытия, в котором трубка для введения в зажимное приспособление раствора растворимого в жирах витамина имеет внутренний диаметр, который составляет 1/50 или более и 1/10 или менее по отношению к внутреннему диаметру пучка мембран в виде полых волокон, раствор растворимого в жирах витамина пропускается через устройство для очистки крови на основе мембран в виде полых волокон при скорости потока, составляющей 100 мл/мин или более и 1500 мл/мин или менее, в течение 30 секунд или более и 100 секунд или менее, и после этого устройство для очистки крови на основе мембран в виде полых волокон извлекается. После этого раствор, остающийся в мембранах в виде полых волокон выдувается и высушивается, когда осуществляется продувание воздухом или аналогичным газом с одного конца устройства для очистки крови на основе мембран в виде полых волокон, если это необходимо. При этом, если продувание воздухом осуществляется со стороны, покрытой раствором растворимого в жирах витамина, раствор растворимого в жирах витамина может перемещаться также на непокрытую сторону таким образом, что мембраны в виде полых волокон покрываются равномерно в продольном направлении. В качестве альтернативы, высушивание может осуществляться, если покрытая сторона направлена вверх без осуществления стадии продувания воздухом. На получаемое в результате изделие надеваются крышки, и, таким образом, может быть изготовлено устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления.
[0062] (Подготовительный пример 6)
Пучок мембран в виде полых волокон, на которые растворимый в жирах витамин наносится в концевой части корпуса каждым из способов изготовления согласно подготовительным примерам 1-3, собирается в резервуар, и получаемое в результате изделие устанавливается в устройство для нанесения покрытия раствором растворимого в жирах витамина. Устройство для нанесения покрытия на своем конце включает зажимное приспособление в тесном контакте с устройством для очистки крови на основе мембран в виде полых волокон. Раствор растворимого в жирах витамина поступает из устройства для нанесения покрытия, проходит через устройство для очистки крови на основе мембран в виде полых волокон при скорости потока, составляющей 100 мл/мин или более и 1500 мл/мин или менее, в течение 30 секунд или более и 100 секунд или менее, и после этого устройство для очистки крови на основе мембран в виде полых волокон извлекается. После этого, в случае необходимости, в присутствии маски, покрывающей центральную часть, раствор растворимого в жирах витамина, который остается в наружной части мембран в виде полых волокон, выдувается и высушивается посредством продувания воздухом или аналогичным газом, которое осуществляется с одного конца устройства для очистки крови на основе мембран в виде полых волокон. После этого получаемое в результате изделие выдерживается в состоянии покоя в течение одного часа или более и 12 часов или менее, таким образом, что центральная часть мембран в виде полых волокон может пропитываться раствором растворимого в жирах витамина в направлении толщины, и после этого удаляется маска, покрывающая центральную часть, и раствор, который остается в мембранах в виде полых волокон, выдувается и высушивается посредством продувания воздухом или аналогичным газом. При этом, если продувание воздухом осуществляется со стороны, покрытой раствором, раствор растворимого в жирах витамина может перемещаться также на непокрытую сторону таким образом, что мембраны в виде полых волокон покрываются равномерно в продольном направлении. На получаемое в результате изделие надеваются крышки, и, таким образом, может быть изготовлено устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему варианту осуществления.
[0063] После сборки устройства для очистки крови на основе мембран в виде полых волокон раствор для нанесения покрытия растворимого в жирах витамина может затем пропускаться через устройство для очистки крови на основе мембран в виде полых волокон.
Распределение растворимого в жирах витамина в продольном направлении и в поперечном направлении устройства для очистки крови на основе мембран в виде полых волокон может регулироваться также в соответствии с концентрацией растворимого в жирах витамина в растворе растворимого в жирах витамина, который используется для нанесения покрытия, а также в соответствии с типами растворителя и поверхностно-активного вещества, такого как глицерин.
[0064] В каждом из подготовительных примеров 1-6 согласно настоящему варианту осуществления концентрация растворимого в жирах витамина в растворе растворимого в жирах витамина составляет предпочтительно 0,01 мас.% или более и 10 мас.% или менее, и предпочтительнее 0,1 мас.% или более и 5 мас.% или менее. Кроме того, добавка (такая как поверхностно-активное вещество) для изготовления раствора растворимого в жирах витамина предпочтительно вводится в водный раствор растворимого в жирах витамина в количестве, составляющем 1/10 или более и 2 или менее по отношению к количеству растворимого в жирах витамина.
[0065] В качестве растворителя, используемого в растворе растворимого в жирах витамина, может использоваться любой из разнообразных растворителей, и предпочтительно используется водный раствор спирта, такого как пропанол, в концентрации, составляющей 50 мас.% или более и 80 мас.% или менее.
Продолжительность погружения мембраны в виде полых волокон в раствор растворимого в жирах витамина, в котором растворимый в жирах витамин растворяется в концентрации, составляющей 0,1 мас.% или более и 2,0 мас.% или менее, составляет предпочтительно 30 секунд или более и 60 минут или менее, и предпочтительнее 40 секунд или более и 10 минут или менее.
Раствор растворимого в жирах витамина пропускается в условиях скорости потока, составляющей 100 мл/мин или более и 1500 мл/мин или менее, в течение 30 секунд или более и 60 минут или менее и предпочтительно в условиях скорости потока, составляющей 300 мл/мин или более и 1200 мл/мин или менее, в течение 50 секунд или более и 10 минут или менее.
[0066] В каждом из подготовительных примеров 1-6 согласно настоящему варианту осуществления в качестве пучка мембран в виде полых волокон перед нанесением покрытия могут использоваться, мембраны в виде полых волокон, в которых растворимый в жирах витамин совершенно не иммобилизуется, могут использоваться мембраны в виде полых волокон, в которых растворимый в жирах витамин в заданном количестве равномерно иммобилизуется в поперечном направлении способом нанесения покрытия, или может использоваться пучок мембран в виде полых волокон, имеющих различные характеристики водопроницаемости в центральной части и наружной части. Когда эти способы сочетаются, может регулироваться распределение растворимого в жирах витамина в продольном направлении и поперечное направление.
[0067] <Стадия смачивания мембраны в виде полых волокон>
В устройстве для очистки крови на основе мембран в виде полых волокон, которое собирается после иммобилизации растворимого в жирах витамина, мембраны в виде полых волокон могут смачиваться водным раствором перед стерилизацией. Когда мембраны в виде полых волокон смачиваются водным раствор, мембраны в виде полых волокон стабилизируются, и в меньшей степени изменяются их эксплуатационные характеристики, такие как характеристики водопроницаемости, характеристики диализа и характеристики фильтрации. Примерные способы смачивания мембраны в виде полых волокон водным раствором представляют собой способ, в котором водный раствор заполняет резервуар, в который загружаются мембраны в виде полых волокон, и способ, в котором водный раствор заполняет резервуар и затем выливается. Эта стадия смачивания мембраны в виде полых волокон может осуществляться также как стадия добавления стерилизующего защитного вещества, которая описана ниже.
[0068] <Стадия добавления стерилизующего защитного вещества>
Стерилизующее защитное вещество представляет собой акцептор радикалов, молекула которого содержит множество гидроксильных групп или ароматических колец, и который используется для защиты гидрофильного полимера мембран в виде полых волокон от существенного воздействия энергии излучения, производимого на стадии стерилизационной обработки, описанной ниже.
Примерные стерилизующие защитные вещества представляют собой (многоатомные) спирты, такие как глицерин и пропиленгликоль, растворимые в воде сахара, такие как олигосахариды и полисахариды, а также неорганические соли, имеющие противоокислительные свойства, такие как сульфиты.
В качестве способа пропитывания мембраны в виде полых волокон стерилизующим защитным веществом используются способ, в котором стерилизующее защитное вещество растворяется в соответствующем растворителе, который вводится в устройство для очистки крови на основе мембран в виде полых волокон, способ в котором стерилизующее защитное вещество растворяется, например, в воде или физиологическом солевом растворе, которые заполняют пространство внутри устройства для очистки крови на основе мембран в виде полых волокон или только пропитывают мембраны в виде полых волокон, или аналогичный способ. На стадии смачивания водный раствор, содержащий стерилизующее защитное вещество может использоваться в качестве водного раствора, используемого для смачивания.
Если стерилизующее защитное вещество присутствует в устройстве для очистки крови на основе мембран в виде полых волокон, устройство для очистки крови на основе мембран в виде полых волокон и, в частности, мембраны в виде полых волокон могут защищаться от изменений под действием излучения на стадии стерилизационной обработки, которая описана далее.
Если стерилизующее защитное вещество используется в форме раствора, концентрация стерилизующего защитного вещества может оптимально определяться в соответствии с материалом устройства для очистки крови на основе мембран в виде полых волокон, типом гидрофильного полимера и условиями стерилизации, и она составляет предпочтительно 0,001 мас.% или более и 1 мас.% или менее, и предпочтительнее 0,005 мас.% или более и 0,5 мас.% или менее.
[0069] <Стадия стерилизационной обработки устройства для очистки крови на основе мембран в виде полых волокон>
Устройство для очистки крови на основе мембран в виде полых волокон предпочтительно подвергается стерилизационной обработке. Примерные способы стерилизационной обработки представляют собой радиационная стерилизация и паровая стерилизация.
Поскольку мембрана в виде полых волокон, содержащая большое количество растворимого в жирах витамина, подвергается риску повреждения, когда она чрезмерно нагревается, предпочтительнее осуществляется радиационная стерилизация. Для радиационной стерилизации могут использоваться электронные пучки, гамма-излучение, рентгеновское излучение или другое излучение. Экспозиционная доза излучения при использовании гамма-излучения или электронных пучков составляет предпочтительно 5 кГр или более и 50 кГр или менее, и предпочтительнее 20 кГр или более и 40 кГр или менее.
Примеры
[0070] Далее настоящее изобретение будет описано более подробно с представлением примером, но следует отметить, что настоящее изобретение не ограничивается следующими примерами. В данных примерах используются измерения следующими способами:
[0071] <Измерение количества растворимого в жирах витамина, которое присутствует в мембранах в виде полых волокон в разделенной секции пучка мембран в виде полых волокон>
Устройство для очистки крови на основе мембран в виде полых волокон разбирали для извлечения мембран в виде полых волокон, и мембраны в виде полых волокон разделяли на пять секций для отбора мембраны в виде полых волокон в каждой из разделенных секций. Полученные в результате этого мембраны в виде полых волокон промывали водой и высушивали в вакууме при 40°C. Навеску высушенных мембран в виде полых волокон помещали в стеклянный сосуд таким образом, чтобы получить площадь внутренней поверхности мембран в виде полых волокон, составляющую 0,2 м2, в сосуд добавляли 80 мл водного раствора 1 мас.% химического реагента Triton X-100 (Kishida Chemical Co., Ltd.), и растворимый в жирах витамин экстрагировали при комнатной температуре в течение 60 минут вод действием ультразвуковой вибрации. Операция количественного определения осуществляется методом жидкостной хроматографии, и количество растворимого в жирах витамина в экстракте вычисляли с использованием калибровочной кривой, построенной на основании площади пиков для стандартного раствора растворимого в жирах витамина. В частности, согласно настоящему варианту осуществления, количество растворимого в жирах витамина соответствует значению, которое может быть получено как среднее значение для мембран в виде полых волокон, у которых площадь внутренней поверхности полых волокон составляет 0,2 м2.
Колонку (наполненную колонку Shodex Asahipak ODP-506E для жидкостной хроматографии высокого разрешения) присоединяли к жидкостному хроматографу высокого разрешения (насос: Jasco Corporation PU-1580, детектор: Shimadzu RID-6A, автоматический инжектор: Shimadzu SIL-6B, устройство обработки данных: Tosoh GPC-8020, колоночный термостат: GL Sciences 556), метанол для жидкостной хроматографии высокого разрешения, используемый в качестве подвижной фазы, пропускали через колонку при температуре колонки 40°C и скорости потока 1 мл/мин, и концентрация растворимого в жирах витамина получали на основании площади пика поглощения в ультрафиолетовой области. На основании полученной в результате этого концентрации вычисляли количество (мг/м2) растворимого в жирах витамина, которое присутствует в мембранах в виде полых волокон для каждой разделенной секции мембран в виде полых волокон в предположении того, что эффективность экстракции составляла 100%.
Количество растворимого в жирах витамина, частично окисленного в процессе стерилизационной обработки, также включали в количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон. Для количественного определения количества растворимого в жирах витамина, частично окисленного в процессе стерилизационной обработки, растворимый в жирах витамин, который ранее использовался для построения калибровочной кривой, подвергался воздействию воздуха и облучению дозой 50 кГр для определения пика поглощения частично окисленного растворимого в жирах витамина, и полученный пик поглощения дополнительно включали в пики, используемые для вычисления площади.
[0072] <Измерение количество растворимого в жирах витамина, которые присутствуют в центральной части и в наружной части мембран в виде полых волокон>
Устройство для очистки крови на основе мембран в виде полых волокон разбирали на центральную часть и наружную часть, и мембраны в виде полых волокон отбирали в каждой из этих частей, промывали водой и высушивали в вакууме при 40°C. Навеску высушенных мембран в виде полых волокон помещали в стеклянный сосуд таким образом, чтобы получить площадь внутренней поверхности мембран в виде полых волокон, составляющую 0,2 м2, в сосуд добавляли 80 мл водного раствора 1 мас.% химического реагента Triton X-100 (Kishida Chemical Co., Ltd.), и растворимый в жирах витамин экстрагировали при комнатной температуре в течение 60 минут вод действием ультразвуковой вибрации. Операция количественного определения осуществляется методом жидкостной хроматографии, и количество растворимого в жирах витамина в экстракте вычисляли с использованием калибровочной кривой, построенной на основании площади пиков для стандартного раствора растворимого в жирах витамина. В частности, согласно настоящему варианту осуществления, количество растворимого в жирах витамина соответствует значению, которое может быть получено как среднее значение для мембран в виде полых волокон, у которых площадь внутренней поверхности полых волокон составляет 0,2 м2.
Колонку (наполненную колонку Shodex Asahipak ODP-506E для жидкостной хроматографии высокого разрешения) присоединяли к жидкостному хроматографу высокого разрешения (насос: Jasco Corporation PU-1580, детектор: Shimadzu RID-6A, автоматический инжектор: Shimadzu SIL-6B, устройство обработки данных: Tosoh GPC-8020, колоночный термостат: GL Sciences 556), метанол для жидкостной хроматографии высокого разрешения, используемый в качестве подвижной фазы, пропускали через колонку при температуре колонки 40°C и скорости потока 1 мл/мин, и концентрацию растворимого в жирах витамина получали на основании площади пика поглощения в ультрафиолетовой области. На основании полученной в результате этого концентрации вычисляли количество (мг/м2) растворимого в жирах витамина, которое присутствует в мембранах в виде полых волокон в предположении того, что эффективность экстракции составляла 100%.
Количество растворимого в жирах витамина, частично окисленного в процессе стерилизационной обработки, также включали в количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон. Для количественного определения количества растворимого в жирах витамина, частично окисленного в процессе стерилизационной обработки, растворимый в жирах витамин, который ранее использовался для построения калибровочной кривой, подвергался воздействию воздуха и облучению дозой 50 кГр для определения пика поглощения частично окисленного растворимого в жирах витамина, и полученный пик поглощения дополнительно включали в пики, используемые для вычисления площади.
[0073] <Измерение противоокислительной способности устройства для очистки крови на основе мембран в виде полых волокон>
Гексагидрат хлорида железа(III) растворяли в чистой воде, получая водный раствор 0,3 мас./об.% (количество (г) растворенного вещества на 100 мл раствора). После этого устройство для очистки крови на основе мембран в виде полых волокон разбирали, чтобы отобрать мембраны в виде полых волокон, и эти мембраны в виде полых волокон промывали водой и высушивали в вакууме при 40°C. Навеску 1 г высушенных мембран в виде полых волокон и 20 мл водного раствора хлорида железа(III) помещали в стеклянный сосуд, получаемый в результате раствор дегазировали при 60 мм рт. ст. (8 кПа) в течение 10 минут, а затем инкубировали при 30°C в течение 4 часов в процессе встряхивания (и в результате этого растворимый в жирах витамин, содержащийся в мембранах в виде полых волокон, восстанавливал ионы железа(III), образуя ионы железа(II)). После этого смешивали 2,6 мл инкубированного водного раствора, 0,7 мл этанола и 0,7 мл отдельно изготовленного водно-этанольного раствора 0,5 мас./об.% 2,2'-бипиридила и получаемую в результате смесь инкубировали при 30°C в течение 30 минут в процессе встряхивания (и, таким образом, ионы железа(II) и бипиридил образовывали друг с другом комплекс, который проявлял окраску). Использовали спектрометр для измерения поглощения при 520 нм полученного окрашенного раствора.
Операции инкубирования, реакции проявления цвета и измерения поглощения, аналогичные описанным выше операциям, осуществляли для построения калибровочной кривой, используя, вместо мембран в виде полых волокон, этанольный раствор растворимого в жирах витамина, имеющий известную концентрацию, и противоокислительную способность, проявляемую в расчете на 1 м2 внутренней поверхности мембраны в виде полых волокон, получали как значение эквивалентной массы растворимого в жирах витамина (округленное до первого десятичного знака).
Если значение эквивалентной массы растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон составляло 15 (мг/м2) или более, противоокислительная способность оценивалась как хорошая и определялась знаком O, а если оно составляло менее чем 15 мг/м2, противоокислительная способность как неудовлетворительная и определялась знаком ×.
Кроме того, в целях измерения изменчивости противоокислительных характеристик мембраны в виде полых волокон, содержащиеся в трех устройствах для очистки на основе мембран в виде полых волокон, подвергали измерению в одинаковых условиях, чтобы вычислить среднеквадратическое отклонение. Если среднеквадратическое отклонение составляло менее чем 10, изменчивость оценивали как небольшую и определяли знаком O, а если оно составляло 10 или более, противоокислительные характеристики оценивались как неустойчивые, и их изменчивость определялась знаком ×.
[0074] <Измерение улучшения характеристик водопроницаемости устройства для очистки крови на основе мембран в виде полых волокон>
Используя все устройства, включая устройство для очистки крови на основе мембран в виде полых волокон, изготовленное в каждом из примеров и сравнительных примерах и устройство для очистки крови на основе мембран в виде полых волокон (изготовленное отдельно) в котором растворимый в жирах витамин, в таком же количестве, как, по меньшей мере, в одной концевой части корпуса, где количество растворимого в жирах витамина было наибольшим в предшествующем устройстве для очистки крови на основе мембран в виде полых волокон, практически равномерно иммобилизовался в продольном направлении, чистую воду полностью фильтровали через устройство для очистки крови на основе мембран в виде полых волокон в условиях постоянного давления, составляющего 200 мм рт. ст. (26,7 кПа) и температуры 37°C, и измеряли время, требуемое для фильтрации. На основании полученных результатов вычисляли характеристики водопроницаемости (скорость ультрафильтрации UFR (мл/час⋅мм рт. ст.)).
[0075] После этого, увеличение характеристик водопроницаемости вычисляли в соответствии со следующим уравнением (1):
Увеличение характеристик водопроницаемости (UFR (мл/час⋅мм рт. ст.))=C-D ... (1)
C: характеристики водопроницаемости (UFR (мл/час⋅мм рт. ст.)) устройства для очистки крови на основе мембран в виде полых волокон
D: характеристики водопроницаемости (UFR (мл/час⋅мм рт. ст.)) устройства для очистки крови на основе мембран в виде полых волокон, в котором растворимый в жирах витамин в таком же количестве, как в концевой части корпуса, практически равномерно иммобилизовался в продольном направлении
[0076] Если увеличение характеристик водопроницаемости было большим, характеристики водопроницаемости считались и оценивались как высокие, и целесообразность производства считалась высокой по сравнению с устройством для очистки крови, имеющим противоокислительные характеристики на таком же уровне, а если увеличение характеристик водопроницаемости составляло 10 (UFR (мл/час⋅мм рт. ст.)) или более, характеристики водопроницаемости определялись как хорошие.
[0077] <Измерение активности лактатдегидрогеназы (LDH) устройства для очистки крови на основе мембран в виде полых волокон>
Устройство для очистки крови на основе мембран в виде полых волокон разбирали, разделяя мембраны в виде полых волокон на центральную часть и наружную часть, и мембраны в виде полых волокон случайным образом выбирали из соответствующих частей таким образом, что численное соотношение между мембранами в виде полых волокон центральной части и мембранами в виде полых волокон наружной части могло составлять 1:3. Длины мембран в виде полых волокон концевой части корпуса, где было высоким содержание растворимого в жирах витамина, устанавливали в пределах эффективной длины 15 см. После этого изготавливали мини-модуль, присоединяя оба конца мембран в виде полых волокон друг к другу эпоксидным клеем, таким образом, что площадь внутренней поверхности мембран в виде полых волокон могла составлять 50 мм2. Мини-модуль промывали, пропуская 3 мл солевого раствора (изотонический раствор Otsuka от компании Otsuka Pharmaceutical Co., Ltd.,) через полые части мембран в виде полых волокон при скорости потока, составляющей 0,6 мл/мин.
После этого 15 мл гепаринизированной крови человека термостатировали при температуре 37°C и подвергали циркуляции через мини-модуль при скорости потока, составляющей 1,2 мл/мин, в течение 4 часов. После циркуляции полые части мини-модуля промывали 10 мл солевого раствора, и его наружную поверхность также промывали 10 мл солевого раствора.
Из промытого мини-модуля мембраны в виде полых волокон извлекали, измельчали и помещали в центрифужную пробирку для использования в измерении активности LDH, и получаемый в результате продукт использовали в качестве образца для измерений.
Затем 0,5 мл раствора 0,5 об.% Triton X-100/PBS, полученного посредством растворения Triton X-100 (Nacalai Tesque) в фосфатном буферном растворе (PBS) (Wako Pure Chemical Industries, Ltd.) добавляли в центрифужную пробирку для использования в измерении активности LDH, получаемый в результате продукт центрифугировали (при 2700 об/мин в течение 5 минут), чтобы погрузить в раствор мембраны в виде полых волокон, и получаемый в результате продукт подвергали экстракции в процессе встряхивания в течение 60 минут, чтобы разрушить клетки (главным образом, тромбоциты), прикрепленные к мембранам в виде полых волокон, и, таким образом, экстрагировали LDH, которая присутствовала в клетках. Полученный в результате этого экстракт отбирали в количестве 0,05 мл, и к нему добавляли 2,7 мл раствора 0,6 мМ пирувата натрия и 0,3 мл раствора 1,277 мг/мл никотинамидадениндинуклеотида (NADH), чтобы началась реакция, и после этой реакции при 37°C в течение одного часа измеряли поглощение при 340 нм полученного в результате продукта.
Аналогичным образом, также измеряли поглощение мембран в виде полых волокон, которые не реагировали с кровью (контрольные образцы), и разность поглощения вычисляли, используя следующее уравнение (2). Кроме того, значение, полученное в результате деления значения, полученного из следующего уравнения (2), на площадь внутренней поверхности мембран в виде полых волокон, в соответствии со следующим уравнением (3), получали как активность LDH.
Δ340 нм=поглощение образца, полученного после реакции в течение 60 минут - поглощение контрольного образца, полученного после реакции в течение 60 минут ... (2)
Активность LDH=Δ340 нм/площадь внутренней поверхности мембран в виде полых волокон ... (3)
[0078] Согласно оценке, чем больше значение, вычисленное согласно уравнению (3), тем больше количество тромбоцитов, прикрепленных к внутренней поверхности мембраны в виде полых волокон, и если активность LDH устройства для очистки крови на основе мембран в виде полых волокон составляла 50 или менее, данное устройство оценивали как имеющее хорошую совместимость с кровью.
[0079] [Пример 1]
Для изготовления прядильного раствора 17,5 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,9) и 3,5 мас.% поливинилпирролидона (BASF K90) растворяли в 79,0 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 58,1 мас.% N,N-диметилацетамида и 41,9 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%, внутренний диаметр 185,0 мкм и толщину 45,0 мкм.
Затем часть высушенных мембран, у которых практически 1/5 часть (концевая часть корпуса) в продольном направлении была непосредственно погружена в раствор для нанесения покрытия, полученный посредством растворения 3,2 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. Через 5 минут мембраны в виде полых волокон полностью выдерживали в растворе для нанесения покрытия в течение дополнительных 5 минут. Мембраны в виде полых волокон извлекали из раствора для нанесения покрытия, и растворитель высушивали и удаляли, используя сухой воздух при 24°C, который пропускали через мембраны в течение 30 минут, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
После иммобилизации растворимого в жирах витамина мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты. Торцевую крышку, имеющую наконечник для впуска (выпуска) крови, присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0080] [Пример 2]
Для изготовления прядильного раствора 17,5 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,9) и 3,5 мас.% поливинилпирролидона (BASF K90) растворяли в 79,0 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 58,1 мас.% N,N-диметилацетамида и 41,9 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%, внутренний диаметр 185,0 мкм и толщину 45,0 мкм.
Затем часть высушенных мембран, у которых практически 1/5 часть (концевая часть корпуса) в продольном направлении была непосредственно погружена в раствор для нанесения покрытия, полученный посредством растворения 0,64 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. Через 2 минуты мембраны в виде полых волокон извлекали из раствора для нанесения покрытия и подвергали продуванию воздухом от конца мембран в виде полых волокон на стороне, погруженной в изопропанольный раствор, таким образом, что выдувался раствор для нанесения покрытия, оставшийся в мембранах, и одновременно раствор для нанесения покрытия наносился также на часть, не погруженную в раствор для нанесения покрытия. Растворитель высушивали и удаляли, используя сухой воздух при 24°C, который пропускали через мембраны в течение 30 минут, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
После иммобилизации растворимого в жирах витамина мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты. Торцевую крышку, имеющую наконечник для впуска (выпуска) крови, присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0081] [Пример 3]
Устройство для очистки крови на основе мембран в виде полых волокон получали таким же образом, как в примере 1, за исключением того, что использовали раствор, полученный посредством растворения 0,21 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола.
[0082] [Пример 4]
В мембранах в виде полых волокон, полученных после иммобилизации растворимого в жирах витамина в примере 3, часть мембран в виде полых волокон, включая концевую часть корпуса, дополнительно погружали в раствор для нанесения покрытия, полученный посредством растворения 3,2 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. Через одну минуту мембраны в виде полых волокон извлекали из раствора для нанесения покрытия и подвергали продуванию воздухом от конца на стороне, противоположной стороне, погруженной в раствор для нанесения покрытия, для выдувания раствора для нанесения покрытия, оставшегося в мембранах. Сухой воздух при 24°C пропускали через мембраны в течение 30 минут для удаления растворителя посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
После иммобилизации растворимого в жирах витамина мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты.
Раствор для нанесения покрытия, полученный посредством растворения 1,1 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола изготавливали в устройстве для нанесения покрытия. Мембраны в виде полых волокон, полученные, как описано выше, устанавливали в устройство для нанесения покрытия, оборудованное зажимным приспособлением, имеющим устойчивую к давлению часть на своей наружной окружности, и раствор для нанесения покрытия выпускали из устройства для нанесения покрытия через мембраны в виде полых волокон при скорости потока, составляющей 500 мл/мин в течение 30 секунд, и после этого мембраны в виде полых волокон извлекали. Сухой воздух при 35°C пропускали через мембраны в течение 30 минут от конца мембран в виде полых волокон на стороне, позволяющей проходить раствору для нанесения покрытия, таким образом, чтобы удалять растворитель посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался посредством нанесения покрытия.
Торцевую крышку, имеющую наконечник для впуска (выпуска) крови присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0083] [Пример 5]
Для изготовления прядильного раствора 17,5 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,9) и 3,5 мас.% поливинилпирролидона (BASF K90) растворяли в 79,0 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 58,1 мас.% N,N-диметилацетамида и 41,9 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%, внутренний диаметр 185,0 мкм и толщину 45,0 мкм.
Затем часть высушенных мембран, у которых практически 1/5 часть (концевая часть корпуса) в продольном направлении была непосредственно погружена в раствор для нанесения покрытия, полученный посредством растворения 0,64 мас.% ?-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. Через одну минуту мембраны в виде полых волокон полностью погружали в раствор для нанесения покрытия еще на одну минуту. Мембраны в виде полых волокон извлекали из раствора для нанесения покрытия, и растворитель высушивали и удаляли, используя сухой воздух при 24°C, который пропускали через мембраны в течение 30 минут, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия. После этого, мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты.
Раствор для нанесения покрытия, полученный посредством растворения 1,2 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола изготавливали в устройстве для нанесения покрытия. Мембраны в виде полых волокон, полученные, как описано выше, устанавливали в устройство для нанесения покрытия, и раствор для нанесения покрытия пропускали через мембраны в виде полых волокон при скорости потока, составляющей 1500 мл/мин, в течение 10 секунд, и затем мембраны в виде полых волокон извлекали. Трубка, через которую поступал раствор для нанесения покрытия, имела внутренний диаметр, составляющий 1/40 внутреннего диаметра пучка мембран в виде полых волокон. Сухой воздух при 35°C пропускали через мембраны в течение 30 минут от конца мембран в виде полых волокон на стороне, позволяющей проходить раствору для нанесения покрытия, таким образом, чтобы удалять растворитель посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
Торцевую крышку, имеющую наконечник для впуска (выпуска) крови присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0084] [Пример 6]
Для изготовления прядильного раствора 17,5 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,9) и 3,5 мас.% поливинилпирролидона (BASF K90) растворяли в 79,0 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 58,1 мас.% N,N-диметилацетамида и 41,9 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%, внутренний диаметр 185,0 мкм и толщину 45,0 мкм.
Затем часть высушенных мембран, у которых практически 1/5 часть (концевая часть корпуса) в продольном направлении была непосредственно погружена в раствор для нанесения покрытия, полученный посредством растворения 1,7 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. После 30 секунд, мембраны в виде полых волокон извлекали из раствора для нанесения покрытия и подвергали продуванию воздухом от конца мембран в виде полых волокон на стороне, погруженной в растворе для нанесения покрытия, таким образом, чтобы выдувать раствор для нанесения покрытия оставшийся в мембранах и одновременно наносить раствор для нанесения покрытия на часть, не погруженную в раствор для нанесения покрытия. Сухой воздух при 24°C пропускали через мембраны в течение 30 минут, таким образом, чтобы удалять растворитель посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
После иммобилизации растворимого в жирах витамина мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты.
Раствор для нанесения покрытия, полученный посредством растворения 1,3 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола изготавливали в устройстве для нанесения покрытия. Мембраны в виде полых волокон, полученные, как описано выше, устанавливали в устройство для нанесения покрытия, оборудованное зажимным приспособлением, имеющим устойчивую к давлению часть на своей наружной окружности, и раствор для нанесения покрытия выпускали из устройства для нанесения покрытия через мембраны в виде полых волокон при скорости потока, составляющей 500 мл/мин, в течение 2 минут, и после этого мембраны в виде полых волокон извлекали. Трубка, через которую поступал раствор для нанесения покрытия, имела внутренний диаметр, составляющий 1/10 внутреннего диаметра пучка мембран в виде полых волокон. Сухой воздух при 35°C пропускали через мембраны в течение 30 минут от конца мембран в виде полых волокон на стороне, позволяющей проходить раствору для нанесения покрытия, таким образом, чтобы удалять растворитель посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался посредством нанесения покрытия.
Торцевую крышку, имеющую наконечник для впуска (выпуска) крови присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0085] [Пример 7]
Для изготовления прядильного раствора 17,5 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,9) и 3,5 мас.% поливинилпирролидона (BASF K90) растворяли в 79,0 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 58,1 мас.% N,N-диметилацетамида и 41,9 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%, внутренний диаметр 185,0 мкм и толщину 45,0 мкм.
Затем часть высушенных мембран, у которых практически 1/5 часть (концевая часть корпуса) в продольном направлении была непосредственно погружена в раствор для нанесения покрытия, полученный посредством растворения 2,2 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. Через одну минуту мембраны в виде полых волокон извлекали из раствора для нанесения покрытия и подвергали продуванию воздухом от конца мембран в виде полых волокон на стороне, погруженной в растворе для нанесения покрытия, таким образом, чтобы выдувать раствор для нанесения покрытия оставшийся в мембранах и одновременно наносить раствор для нанесения покрытия на часть, не погруженную в раствор для нанесения покрытия. Сухой воздух при 24°C пропускали через мембраны в течение 30 минут, таким образом, чтобы удалять растворитель посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
После иммобилизации растворимого в жирах витамина мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты. Торцевую крышку, имеющую наконечник для впуска (выпуска) крови, присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0086] [Пример 8]
Для изготовления прядильного раствора 17,5 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,9) и 3,5 мас.% поливинилпирролидона (BASF K90) растворяли в 79,0 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 58,1 мас.% N,N-диметилацетамида и 41,9 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%, внутренний диаметр 185,0 мкм и толщину 45,0 мкм.
Затем часть высушенных мембран, у которых практически 1/5 часть (концевая часть корпуса) в продольном направлении была непосредственно погружена в раствор для нанесения покрытия, полученный посредством растворения 3,2 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. Через 5 минут мембраны в виде полых волокон полностью погружали в раствор для нанесения покрытия еще на 3 минуты. Мембраны в виде полых волокон извлекали из раствора для нанесения покрытия, и растворитель высушивали и удаляли, используя сухой воздух при 24°C, который пропускали через мембраны в течение 30 минут, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия. После этого, мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты.
Раствор для нанесения покрытия, полученный посредством растворения 1,6 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола изготавливали в устройстве для нанесения покрытия. Мембраны в виде полых волокон, полученные, как описано выше, устанавливали в устройство для нанесения покрытия, оборудованное зажимным приспособлением, имеющим устойчивую к давлению часть на своей наружной окружности, и раствор для нанесения покрытия выпускали из устройства для нанесения покрытия через мембраны в виде полых волокон при скорости потока, составляющей 500 мл/мин в течение 30 секунд, и после этого мембраны в виде полых волокон извлекали. Сухой воздух при 35°C пропускали через мембраны в течение 30 минут от конца мембран в виде полых волокон на стороне, позволяющей проходить раствору для нанесения покрытия, таким образом, чтобы удалять растворитель посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
Торцевую крышку, имеющую наконечник для впуска (выпуска) крови присоединяли к каждой из концевых частей корпуса, получаемое в результате изделие подвергали стерилизационной обработке посредством осуществления стадия смачивания таким же способом, как в примере 1, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
[0087] [Пример 9]
Устройство для очистки крови на основе мембран в виде полых волокон получали таким же образом, как в примере 7, за исключением того, что использовали раствор для нанесения покрытия, полученный посредством растворения 3,2 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола.
[0088] [Пример 10]
Устройство для очистки крови на основе мембран в виде полых волокон получали таким же образом, как в примере 3, за исключением того, что продолжительность непосредственного погружения части высушенных мембран, составляющей практически 1/5 часть (концевая часть корпуса) в продольном направлении, в α-токоферол особой чистоты (Wako Pure Chemical Industries, Ltd.) изменялась и составляла 40 секунд, и площадь внутренней поверхности мембран в виде полых волокон изменялась и составляла 2,5 м2.
[0089] [Пример 11]
Для изготовления прядильного раствора 17,5 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,9) и 3,5 мас.% поливинилпирролидона (BASF K90) растворяли в 79,0 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 58,1 мас.% N,N-диметилацетамида и 41,9 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%, внутренний диаметр 185,0 мкм и толщину 45,0 мкм.
Затем часть высушенных мембран, у которых практически 1/5 часть (концевая часть корпуса) в продольном направлении была непосредственно погружена в раствор для нанесения покрытия, полученный посредством растворения 3,2 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. Через 5 минут мембраны в виде полых волокон полностью погружали в раствор для нанесения покрытия еще на одну минуту. Мембраны в виде полых волокон извлекали из раствора для нанесения покрытия, и растворитель высушивали и удаляли, используя сухой воздух при 24°C, который пропускали через мембраны в течение 30 минут, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
После иммобилизации растворимого в жирах витамина мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты.
Раствор для нанесения покрытия, полученный посредством растворения 1,6 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола изготавливали в устройстве для нанесения покрытия. Мембраны в виде полых волокон, полученные, как описано выше, устанавливали в устройство для нанесения покрытия, оборудованное зажимным приспособлением, имеющим устойчивую к давлению часть на своей наружной окружности, и раствор для нанесения покрытия выпускали из устройства для нанесения покрытия через мембраны в виде полых волокон при скорости потока, составляющей 500 мл/мин, в течение 10 секунд, и после этого мембраны в виде полых волокон извлекали. Сухой воздух при 35°C пропускали через мембраны в течение 30 минут от конца мембран в виде полых волокон на стороне, позволяющей проходить раствору для нанесения покрытия, таким образом, чтобы удалять растворитель посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался посредством нанесения покрытия.
Торцевую крышку, имеющую наконечник для впуска (выпуска) крови присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 2,5 м2.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0090] [Пример 12]
Устройство для очистки крови на основе мембран в виде полых волокон получали таким же образом, как в примере 4, за исключением того, что концентрация водного раствора растворимого в жирах витамина для непосредственного погружения части высушенных мембран, составляющей практически 1/5 часть (концевая часть корпуса) в продольном направлении, сначала изменялась до концентрации раствора для нанесения покрытия, полученного посредством растворения 2,5 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола, и что площадь внутренней поверхности мембран в виде полых волокон изменялась и составляла 2,5 м2.
[0091] [Пример 13]
В мембранах в виде полых волокон, полученных после иммобилизации растворимого в жирах витамина в примере 3, часть мембран в виде полых волокон, включая концевую часть корпуса, дополнительно погружали в раствор для нанесения покрытия, полученный посредством растворения 3,0 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. Через одну минуту мембраны в виде полых волокон извлекали из раствора для нанесения покрытия и подвергали продуванию воздухом от конца мембран в виде полых волокон, противоположного стороне, погруженной в растворе для нанесения покрытия, таким образом, чтобы выдувать раствор для нанесения покрытия оставшийся в мембранах, и сухой воздух при 24°C пропускали через мембраны в течение 30 минут, таким образом, чтобы удалять растворитель посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
После иммобилизации растворимого в жирах витамина мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты.
Раствор для нанесения покрытия, полученный посредством растворения 3,2 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола изготавливали в устройстве для нанесения покрытия. Мембраны в виде полых волокон, полученные, как описано выше, устанавливали в устройство для нанесения покрытия, оборудованное зажимным приспособлением, имеющим устойчивую к давлению часть на своей наружной окружности, и раствор для нанесения покрытия выпускали из устройства для нанесения покрытия через мембраны в виде полых волокон при скорости потока, составляющей 500 мл/мин, в течение 25 секунд, и после этого устройство для очистки крови извлекали. Сухой воздух при 35°C пропускали через мембраны в течение 30 минут от конца мембран в виде полых волокон на стороне, позволяющей проходить раствору для нанесения покрытия, таким образом, чтобы удалять растворитель посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
Торцевую крышку, имеющую наконечник для впуска (выпуска) крови присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 2,5 м2.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0092] [Пример 14]
Устройство для очистки крови на основе мембран в виде полых волокон получали таким же образом, как в примере 1, за исключением того, что использовали раствор для нанесения покрытия, полученный посредством растворения 0,7 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола.
[0093] [Пример 15]
Прядильный раствор, содержащий 17,5 мас.% простого полиэфирсульфона (Sumitomo Chemical Co., Ltd., 4800P, параметр растворимости δ=9,9), 3,5 мас.% поливинилпирролидона (BASF K90), 31,2 мас.% триэтиленгликоля (производитель Mitsubishi Chemical Corporation), 1,0 мас.% воды, используемой в качестве нерастворяющего вещества, и 46,8 мас.% диметилацетамида (производитель Mitsui Chemicals Inc.) выдерживали при 45°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой вода, пропускали через воздушный зазор длиной 600 мм и погружали в коагуляционную ванну, содержащую воду, а затем сматывали в пучок волокон при 60 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80?C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%.
После этого получаемые в результате мембраны промывали чистой водой при 45°C в течение одной минуты и чистой водой при 80°C в течение 90 секунд, а затем сматывали, и, таким образом, получали мембраны в виде полых волокон, имеющие внутренний диаметр 199,0 мкм и толщину 29,5 мкм.
Устройство для очистки крови на основе мембран в виде полых волокон получали таким же образом, как в примере 2, за исключением того, что раствор, полученный посредством растворения 0,7 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола, использовали в способе иммобилизации растворимого в жирах витамина, и что площадь внутренней поверхности мембран в виде полых волокон изменялась и составляла 2,5 м2.
[0094] [Пример 16]
Для изготовления прядильного раствора 15 мас.% полиарилата (Unitika U Polymer, параметр растворимости δ=9,3) и 15 мас.% простого полиэфирсульфона (Sumitomo Chemical Co., Ltd., Sumika Excel PES, параметр растворимости δ=9,9) растворяли в 70 мас.% N-метилпирролидона для получения гомогенного раствора.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор, полученный посредством растворения 0,5 мас.% поливинилпирролидона (BASF Kollidon K-90) в 19,5 мас.% N-метилпирролидона и 80,0 мас.% воды, пропускали через воздушный зазор длиной 0,9 м и погружали в коагуляционную ванну при 50°C, содержащую 19,5 мас.% N-метилпирролидона и 80,5 мас.% воды, а затем сматывали в пучок волокон при 700 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали водой, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали сухим воздухом при 35°C для получения высушенных мембран, имеющих внутренний диаметр 210 мкм и толщину 30 мкм.
Устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему изобретению получали таким же образом, как в примере 2, за исключением того, что раствор, полученный посредством растворения 1,0 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола использовали в способе иммобилизации растворимого в жирах витамина, и что площадь внутренней поверхности мембран в виде полых волокон изменялась и составляла 2,1 м2.
[0095] [Пример 17]
Для изготовления прядильного раствора 125 г син-PMMA, имеющего средневзвешенную молекулярную массу 400000, и 25 г изо-PMMA, имеющего средневзвешенную молекулярную массу 500000, растворяли в 150 г глицерина и 1200 г диметилсульфоксида в процессе перемешивания при 125°C в течение 18 часов, и получаемый в результате раствор выдерживали в состоянии покоя для дегазации и получения гомогенного раствора.
Полученный в результате этого прядильный раствор выпускали, используя шестеренчатый насос, из бункера при 120°C со скоростью 5,3 г/мин в воздух через фильеру для полого волокна при температуре фильеры 60°C. Одновременно полостную внутреннюю текучую среду, представляющую собой смешанный раствор, содержащий 70 мас.% диметилсульфоксида и 30 мас.% воды, вводили со скоростью 1,65 мл/мин. После этого получаемый в результате продукт погружали в коагуляционную ванну, имеющую температуру 60°C и содержащую водный раствор 5% диметилсульфоксида, промывали водой, и получаемые в результате мембраны в виде полых волокон пропитывали водным раствором 63 мас.% глицерина, который использовался в качестве увлажняющего вещества. Получаемый в результате продукт подвергали термической обработке в ванне при 85°C для удаления избытка глицерина и сматывали при 60 м/мин разделительное намоточное устройство для нитей. Смотанный таким способом пучок разрезали, получая пучок полых волокон. Полученные в результате этого мембраны в виде полых волокон имели внутренний диаметр 200 мкм и толщину 30 мкм.
Устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему изобретению изготавливали таким же образом, как в примере 2, за исключением того, что раствор, полученный посредством растворения 0,6 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, и 10 мас.% глицерина в водном растворе 57 мас.% изопропанола использовали в способе иммобилизации растворимого в жирах витамина, и что площадь внутренней поверхности мембран в виде полых волокон изменялась и составляла 1,6 м2.
[0096] [Пример 18]
Полиэтилен высокой плотности (имеющий плотность 0,988, значение Mu=5,5, HI-ZEX 2208J, имеющий параметр растворимости δ=8,40) подвергали прядению, используя двойной кольцевой мундштук при температуре мундштука 150°C для получения полого волокна.
Полученное полое волокно подвергали обработке посредством отжига при 120°C в течение 2 часов, а затем горячему растяжению при комнатной температуре на 30% и после этого при 105°C на 350% для получения мембран в виде полых волокон. Мембраны в виде полых волокон имели внутренний диаметр 300 мкм и толщину 45 мкм.
Сополимер этилена и винилового спирта (Nippon Synthetic Chemical Industry Co., Ltd., Soarnol E), имеющий содержание этилена 38 мол.%, растворяли посредством нагревания в водном растворе 75 мас.% ацетона для получения раствора 0,5 мас.%. Часть мембран в виде полых волокон, включая практически 1/5 часть в продольном направлении (концевая часть корпуса), непосредственно погружали на 5 минут в раствор для нанесения покрытия, полученный посредством растворения, в описанный выше раствор 0,9 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина. Затем мембраны в виде полых волокон целиком погружали на 3 минуты в раствор 0,5 мас.%, полученный посредством растворения при нагревании сополимера этилена и винилового спирта (Nippon Synthetic Chemical Industry Co., Ltd., Soarnol E), имеющего содержание этилена 38 мол.%, в водном растворе 75 мас.% ацетона. После удаления избыточной части раствора сополимера получаемый в результате продукт высушивали горячим воздухом при 40°C в течение 3 часов.
После иммобилизации растворимого в жирах витамина мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты. Торцевую крышку, имеющую наконечник для впуска (выпуска) крови, присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, в котором площадь мембран составляла 1,6 м2.
[0097] [Пример 19]
Для изготовления прядильного раствора 17,5 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,9) и 3,5 мас.% поливинилпирролидона (BASF K90) растворяли в 79,0 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 58,1 мас.% N,N-диметилацетамида и 41,9 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%, внутренний диаметр 185,0 мкм и толщину 45,0 мкм.
Затем часть высушенных мембран, у которых практически 1/5 часть (концевая часть корпуса) в продольном направлении была непосредственно погружена в раствор для нанесения покрытия, полученный посредством растворения 0,64 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.), который использовался в качестве растворимого в жирах витамина, в водном растворе 57 мас.% изопропанола. Через 2 минуты мембраны в виде полых волокон извлекали из раствора для нанесения покрытия. После этого часть высушенных мембран, включая другую 1/5 часть (концевая часть корпуса) была непосредственно погружена в раствор для нанесения покрытия. Через 2 минуты мембраны в виде полых волокон подвергали продуванию воздухом от конца на стороне, погруженной последней в раствор для нанесения покрытия, таким образом, чтобы выдувать раствор для нанесения покрытия оставшийся в мембранах и одновременно наносить раствор для нанесения покрытия также на часть, не погруженную в раствор для нанесения покрытия. Сухой воздух при 24°C пропускали через мембраны в течение 30 минут для удаления растворителя посредством высушивания, и в результате этого растворимый в жирах витамин иммобилизовался на мембранах в виде полых волокон в результате нанесения покрытия.
После иммобилизации растворимого в жирах витамина мембраны в виде полых волокон загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты. Торцевую крышку, имеющую наконечник для впуска (выпуска) крови, присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0098] [Сравнительный пример 1]
Для изготовления прядильного раствора 17,5 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,90) и 3,5 мас.% поливинилпирролидона (BASF K90) растворяли в 79,0 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 58,1 мас.% N,N-диметилацетамида и 41,9 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%.
Высушенные мембраны загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты. Торцевую крышку, имеющую наконечник для впуска (выпуска) крови, присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
Затем раствор для нанесения покрытия, полученный посредством растворения 3,5 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.) в водном растворе 57 мас.% изопропанола пропускали через полые части мембран в виде полых волокон при 24°C в течение одной минуты из наконечник для впуска крови устройства для очистки крови на основе мембран в виде полых волокон, чтобы ввести α-токоферол в контакт с мембранами в виде полых волокон. При этом трубка, через которую поступал раствор для нанесения покрытия, имела внутренний диаметр, составляющий 1/5 внутреннего диаметра пучка мембран в виде полых волокон.
После этого раствор, оставшийся в полых частях, удаляли посредством продувания воздухом, сухой воздух при 24°C в атмосфере изопропанола пропускали через мембраны в течение 30 минут для удаления растворителя посредством высушивания, и, таким образом, α-токоферол иммобилизовался на мембранах в виде полых волокон.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0099] [Сравнительный пример 2]
Устройство для очистки крови на основе мембран в виде полых волокон изготавливали таким же образом, как в сравнительном примере 1, за исключением того, что концентрация α-токоферол в растворе для нанесения покрытия изменялась и составляла 0,16 мас.%.
[0100] [Сравнительный пример 3]
Устройство для очистки крови на основе мембран в виде полых волокон изготавливали на основании данных, описанных в примере 1 японской выложенной патентной заявки № 2006-296931, в частности следующим образом.
Для изготовления прядильного раствора 18,0 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,90) и 4,3 мас.% поливинилпирролидона (BASF K90) растворяли в 77,7 мас.% N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 24 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 30 мас.% N,N-диметилацетамида и 70 мас.% воды, пропускали через воздушный зазор длиной 0,96 м и погружали в коагуляционную ванну, содержащую воду при 75°C, а затем сматывали в пучок волокон при 80 м/мин. После разрезания смотанного таким способом пучка волокон этот пучок промывали, используя душ с горячей водой при 80°C, поступающей сверху на поперечное сечение пучка, в течение 2 часов, таким образом, чтобы удалить растворитель, оставшийся в мембранах, и получаемые в результате мембраны высушивали для получения высушенных мембран, имеющих содержание воды менее чем 1%.
Высушенные мембраны загружали в цилиндрический резервуар, имеющий два наконечника для впуска и выпуска жидкости, причем оба эти конца погружали в уретановый полимер, и отвержденную уретановую часть отрезали, чтобы получить концевую часть корпуса, в которой мембраны в виде полых волокон были открыты. Торцевую крышку, имеющую наконечник для впуска (выпуска) крови, присоединяли к каждой из концевых частей корпуса, и, таким образом, мембраны в виде полых волокон собирали, изготавливая устройство для очистки крови на основе мембран в виде полых волокон, у которого площадь внутренней поверхности мембран в виде полых волокон составляла 1,5 м2.
Затем раствор для нанесения покрытия, полученный посредством растворения 0,23 мас.% α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.) в водном растворе 57 мас.% изопропанола пропускали через полые части мембран в виде полых волокон в течение 52 секунд из наконечника для впуска крови мембран в виде полых волокон, чтобы ввести α-токоферол в контакт с мембранами в виде полых волокон. Кроме того, после удаления раствора, оставшегося в полых частях посредством продувания воздухом, сухой воздух при 24°C пропускали через мембраны в течение 30 минут для удаления растворителя посредством высушивания, и, таким образом, на мембраны в виде полых волокон было нанесено покрытие α-токоферола.
Что касается стадии смачивания, водный раствор, содержащий 0,06 мас.% пиросульфита натрия, используемого в качестве стерилизующего защитного вещества, и 0,03 мас.% карбоната натрия, используемого для регулирования pH, загружали в канал на стороне крови и канал на стороне фильтрата устройства для очистки крови на основе мембран в виде полых волокон, и в состоянии плотного закрытия наконечников получаемый в результате продукт облучали для стерилизации, используя гамма-излучение при дозе 25 кГр, и таким способом получали устройство для очистки крови на основе мембран в виде полых волокон.
[0101] [Сравнительный пример 4]
Устройство для очистки крови на основе мембран в виде полых волокон изготавливали на основании данных, описанных в примере 2 японской выложенной патентной заявки № 2013-9761, в частности, следующим образом.
Для изготовления прядильного раствора 17,0 мас.% полисульфона (Solvay P-1700, параметр растворимости δ=9,90), 4,0 мас.% поливинилпирролидона (BASF K90) и 0,5 массовых частей α-токоферола особой чистоты (Wako Pure Chemical Industries, Ltd.) растворяли в 78,5 массовых частей N,N-диметилацетамида для получения гомогенного раствора. Содержание поливинилпирролидона по отношению к полисульфону в смешанном прядильном растворе составляло 20 мас.%.
Полученный прядильный раствор выдерживали при 60°C, выпускали через двойной кольцевой мундштук вместе с полостной внутренней текучей средой, представлявшей собой смешанный раствор 42,0 мас.% N,N-диметилацетамида и 58,0 мас.% воды, пропускали через воздушный зазор длиной 0,5 м и погружали в коагуляционную ванну, содержащую воду при 60°C, осуществляли стадию коагуляции и стадию промывания водой (обработка промыванием водой) при скорости 30 м/мин, а затем вводили в сушильное устройство для высушивания при 120°C в течение 2 минут и после этого подвергали термической обработке при 160°C в течение 0,5 минуты, а затем получаемую в результате мембрану в виде полых волокон на основе полисульфонов, имеющую изгибы, сматывали.
Смотанный пучок из 10000 мембран в виде полых волокон, полученный таким способом, загружали в пластмассовый цилиндрический резервуар, предназначенный для достижения площади внутренней поверхности мембран в виде полых волокон, составляющей 1,5 м2, с обоих концов мембраны фиксировали с помощью клея на основе уретанового полимера и отрезали, чтобы получить концевые части корпуса, в которых мембраны в виде полых волокон были открыты.
Через мембраны в виде полых волокон пропускали 100 мл водного раствора, содержащего 95 массовых частей дистиллированной воды (Otsuka Pharmaceutical Co., Ltd.) и 5 массовых частей глицерина особой чистоты (Wako Pure Chemical Industries, Ltd.), и получаемые в результате изделия продували воздухом при давлении 0,3 МПа в течение 10 секунд. После этого получаемые в результате изделия высушивали сухим воздухом при 40°C в течение одного часа. После высушивания торцевые крышки присоединяли к обоим концам. После закрытия наконечников для впуска/выпуска крови электронные пучки облучали дозой 20 кГр и, таким образом, получали устройство для очистки крови на основе мембран в виде полых волокон.
[0102]
[0103]
[0104] Настоящая заявка составлена на основании японской патентной заявки (японская патентная заявка № 2013-259551), поданной 16 декабря 2013 г., полное содержание которой включается в данный документ посредством ссылки.
Промышленная применимость
[0105] Настоящее изобретение может предложить устройство для очистки крови на основе мембран в виде полых волокон, которое уменьшает осложнения и является превосходным по биосовместимости. Устройство для очистки крови на основе мембран в виде полых волокон согласно настоящему изобретению имеет промышленную применимость в терапии методом очистки крови.
Список условных обозначений
[0106] 1 - мембрана в виде полых волокон
1a - первый канал
2 - цилиндрический резервуар
2a, 2b - отверстие
3a, 3b - герметизирующий полимер
6a, 6b - наконечник
7a, 7b - торцевая крышка
8 - торцевое внутреннее пространство
10 - устройство для очистки крови на основе мембран в виде полых волокон
11 - второй канал
Fa - направление течения обрабатываемой жидкости 1 (такой как диализат или кровь)
Fb - направление течения обрабатываемой жидкости 2 (такой как кровь)
Реферат
Изобретение относится к области медицинской техники. Устройство включает мембраны в виде полых волокон, загруженные в резервуар. Мембраны содержат гидрофобный полимер, гидрофильный полимер и растворимый в жирах витамин. Когда пучок мембран в виде полых волокон разделен на пять секций в продольном направлении и разделенные секции, расположенные в самых концевых участках, определены как концевые части корпуса, количество растворимого в жирах витамина, которое присутствует, по меньшей мере, в одной из концевых частей корпуса, является наибольшим среди количеств растворимого в жирах витамина, которые присутствуют, соответственно, в любой из разделенных секций. Количество растворимого в жирах витамина на единицу площади внутренней поверхности мембраны в виде полых волокон, по меньшей мере, одной концевой части корпуса составляет 20 мг/мили более и 300 мг/мили менее. Технический результат состоит в улучшении противоокислительных характеристик, водопроницаемости и совместимости с кровью. 18 з.п. ф-лы, 4 ил.
Формула
Документы, цитированные в отчёте о поиске
Устройство для очистки крови типа высоководопроницаемых мембран из полых волокон и способ его получения

Комментарии