Способ получения нафтеновых кислот - RU2670966C9
Код документа: RU2670966C9
Чертежи
Описание
Изобретение относится к электромембранной технике, а именно к способам получения растворов кислот и оснований из растворов соответствующих солей способом электродиализа, и может найти применение при получении органических кислот.
Известен способ очистки нефти от нафтеновых кислот путем их обработки раствором щелочи с концентрацией 10-15% с последующим отделением (отстаиванием) водорастворимых солей щелочных металлов нафтеновых кислот от органической фазы и обработкой водного раствора солей минеральными кислотами (серной кислотой) с образованием нерастворимых в воде нафтеновых кислот, которые отделяются от водного раствора солей нафтеновых кислот отстаиванием и утилизируются [Кулиев, A.M. Нафтеновые кислоты. Производство и применение / Кулиев A.M., Кулиев Р.Ш., Антонова К.И. // М.: Химия, 1965. - 119 с.].
К недостаткам способа относится применение высоко концентрированных кислот и щелочей и образование при этом высокоминерализованных стоков (раствора сульфата натрия). Другим недостатком способа является, образование при кислотной обработке смеси нафтеновых кислот с различным значением рК и молекулярной массы.
Известен способ выделения нафтеновых кислот из асидола перегретым водяным паром. Асидол подают в перегоночную емкость и нагревают до 130-150°C, а водяной пар нагревают до 130-180°C, перегонку осуществляют при атмосферном давлении [пат. РФ №2531147, МПК С07С 51 (2006.01), С07С 53/134 (2006.01), С07С 53/136 (2006.01), опубл. 2014.10.20].
К недостаткам способа относятся высокие энергозатраты необходимые для нагрева воды до 130-180°C и образование смеси нафтеновых кислот с различным значением молекулярной массы.
Наиболее близки аналогом к предлагаемому способу является способ разделения смеси нафтеновых кислот, позволяющий разделить смеси нафтеновых кислот с разной молекулярной массой [пат. РФ №2374220, МПК С07С 51/42 (2006.01), С07С 53/132 (2006.01), С07С 61/00 (2006.01), С07С 51/43 (2006.01), опубл. 2009.11.27].
Для этого водный раствор смеси натриевых солей нафтеновых кислот - мылонафта, концентрации 3-5 М обрабатывают серной кислотой концентрации 3-5 М с контролем рН среды, причем при каждом изменении величины рН на единицу из реакционной массы отделяют выпавший в осадок комплекс нафтеновой кислоты и ее натриевой соли, после чего каждую фракцию продукта растворяют в пятикратном количестве воды для разложения образовавшегося комплекса, затем обрабатывают 3-5 М серной кислотой до рН 1-2 и отделяют нафтеновые кислоты от водного раствора для получения фракций нафтеновых кислот с величинами констант диссоциации рКа=8±1.
Недостатком способа необходимость использования высокой концентрации реагентов (серной кислоты) и образование высокоминерализованных стоков.
Техническим результатом предлагаемого изобретения является разработка экологически чистого способа, не требующего использования минеральной кислоты.
Технический результат достигается тем, что водный раствор солей щелочных металлов и нафтеновых, подвергают электродиализу в электродиализаторе-синтезаторе с чередующимися биполярными и катионообменными мембранами. Раствор мылонафта подают в солевую камеру электродиализатора-синтезатора, образованную двумя катионообменными мембранами. В щелочных камерах, образованных катионообменной мембранной и анионообменной стороной биполярной мембраны концентрируют щелочь, которую возвращают на выщелачивание нафтеновых кислот из нефтепродуктов, а в кислотных камерах автоматически поддерживают концентрацию кислоты ионами Н+. Под действием электрического поля в солевой камере происходит замещение ионов натрия на ионы водорода, при этом изменяют рН от 7 до 2 соответствующих рКа кислот.
Возможно осуществление данного способа и с добавлением в раствор мылонафта неорганической соли с катионом одинаковым с катионом щелочи концентрацией равной 0,2 моль/л, подаваемого в электродиализатор-синтезатор, все последующие действия такие же как описано выше, однако следует отметить, что энергозатраты при этом еще меньше.
В солевых камерах электродиализатора-синтезатора, содержащих мылонафт, рН изменяют ступенчато с шагом в одну единицу рН в интервале значений рН от 7 до 2, а образовавшиеся при каждом фиксированном значении рН нафтеновые кислоты с различными значениями рКа отделяют.
Для снижения энергозатрат в солевую камеру, содержащую раствор мылонафта можно добавлять катионообменную смолу.
В кислотной камере происходит генерация биполярной мембранной ионов Н+ и автоматическая компенсация убыли ионов Н+, переносимых в солевую камеру. В щелочной в результате переноса через катионообменную мембрану ионов Na+ и генерации биполярной мембраны ионов гидроксила образуется щелочь. Поскольку анионы нафтеновых кислот не способны мигрировать через катионообменные мембраны в смежные щелочные камеры электродиализатора, в предложенном способе исключаются потери нафтеновых кислот.
При достижении значений рН ≤7 образовавшиеся слабые нерастворимые нафтеновые кислоты отделяют от водного раствора нафтената натрия в виде верхнего более легкого слоя (с плотностью около 0,9 г/см3), при этом рКа выделенных нафтеновых кислот строго соответствует значению рН, при котором их отделяют от раствора мылонафта. Водный раствор солей нафтеновых кислот и водонерастворимый слой нафтеновых кислот образуют гетерогенную двухслойную жидкую систему. Верхний слой состоит из отделившихся нафтеновых кислот с рКа точно соответствующим значениям рН, при котором их отделяют от водного раствора солей нафтеновых кислот. Таким образом достигается высокая степень конверсии (≥98%) нафтеновых кислот и их фракционирование по рКа. Нижний водный слой нафтеновых солей, имеющий более высокую плотность, направляют повторно на электродиализ.
Общими признаками прототипа и предлагаемого способа являются:
- использование водного раствора смеси натриевых солей нафтеновых кислот;
- контроль рН среды;
- отделение нафтеновых кислот от водного раствора для получения фракций нафтеновых кислот с величинами констант диссоциации рКа=8±1.
- рН изменяют ступенчато с шагом в одну единицу рН в интервале значений рН от 7 до 2.
Отличительными признаками предлагаемого способа от прототипа является использование электродиализатора-синтезатора. Кроме того, в раствор мылонафта можно вводить неорганическую соль с катионом одинаковым с катионом щелочи концентрацией равной 0,2 моль/л, подаваемого в электродиализатор-синтезатор, что уменьшит энергозатраты на получение нафтеновых кислот. Добавление катионообменной смолы в солевую камеру, содержащую раствор мылонафта можно обеспечивает снижение энергозатрат.
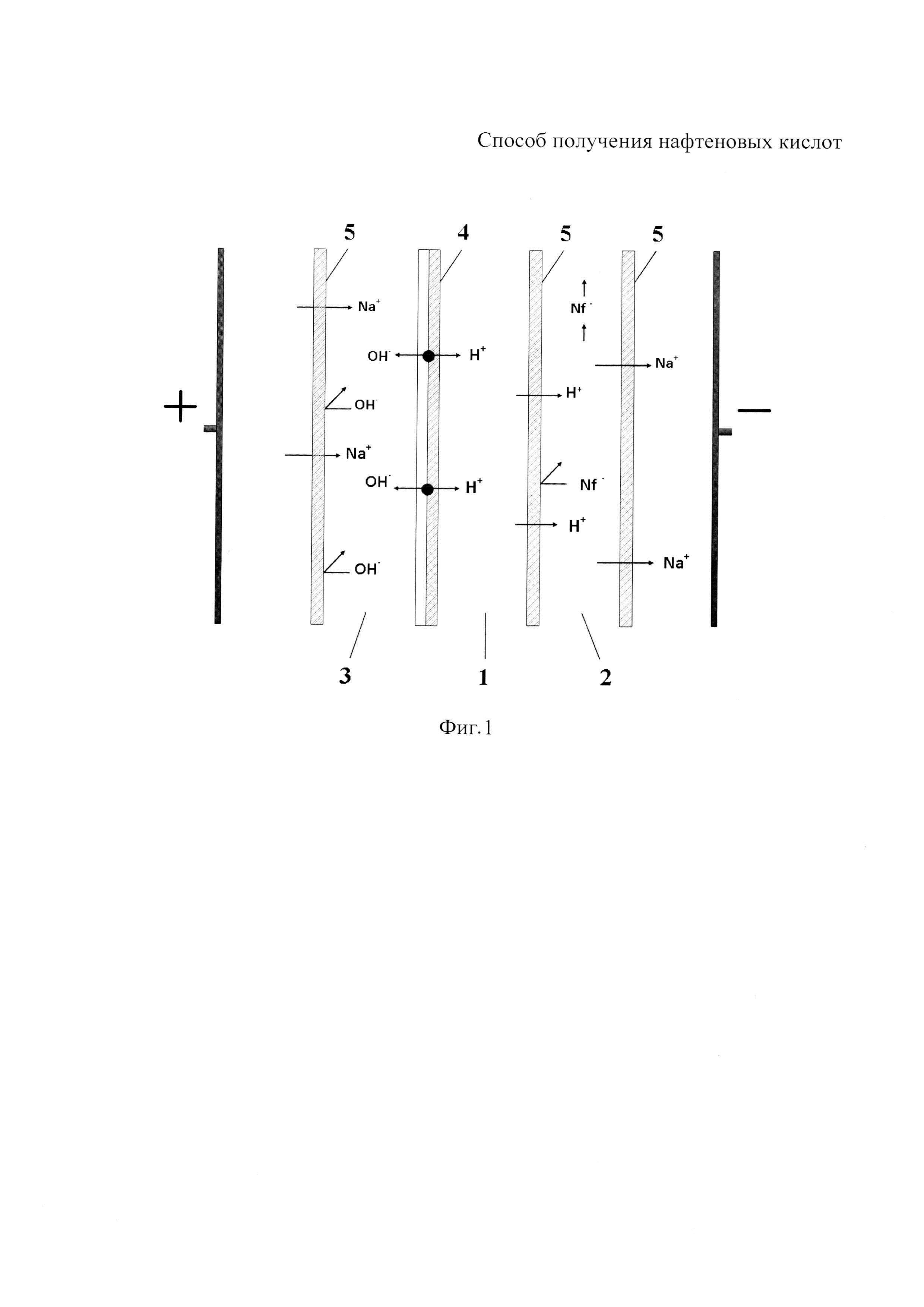
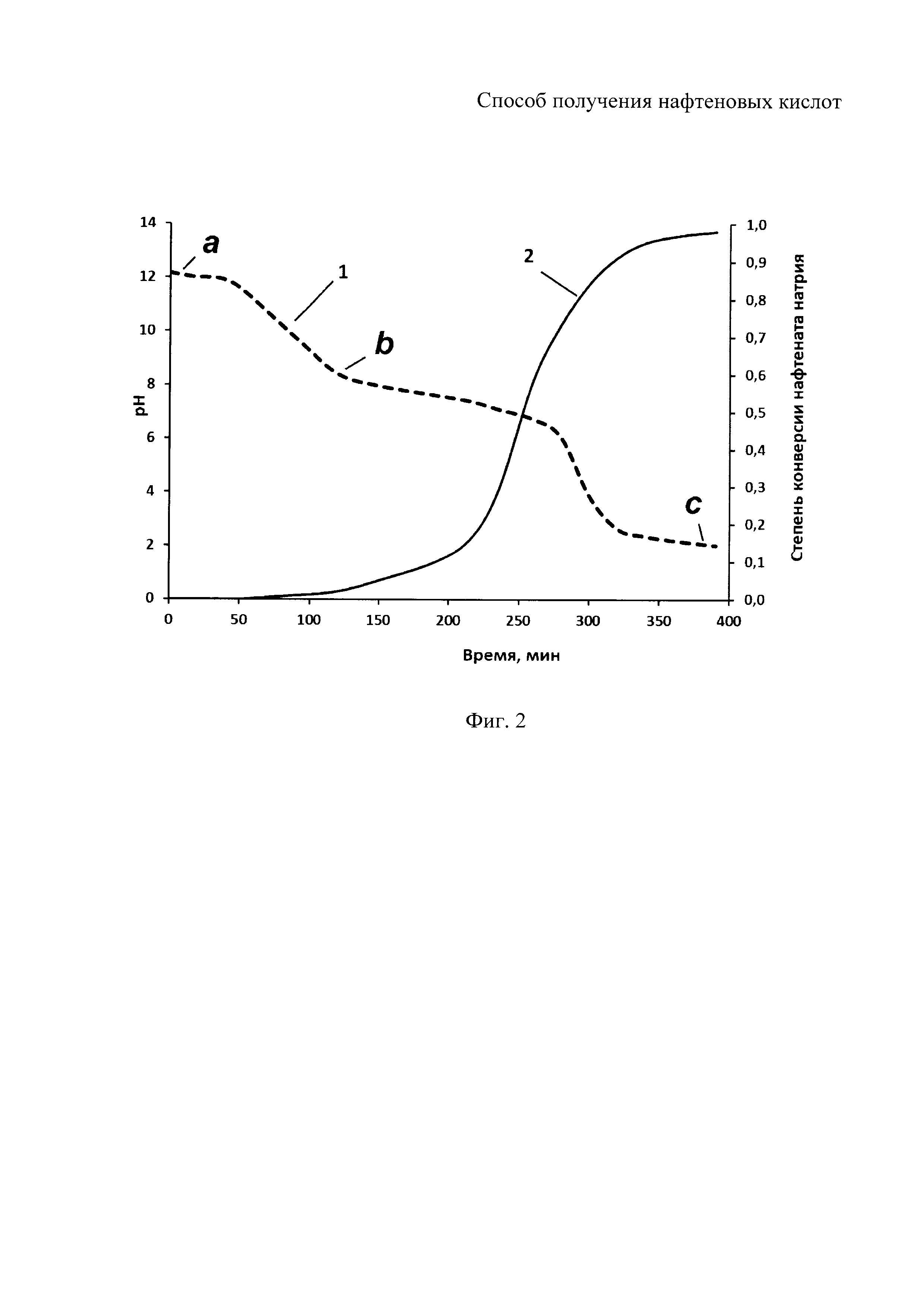
На фигуре 1 показана схема электродиализатора-синтезатора для осуществления процесса получения нафтеновых кислот; на фигуре 2 показана зависимость изменение рН раствора мылонафта в солевой камере 2, при протекании через электродиализатор электрического тока (кривая I) и степень конверсии нафтената натрия в нафтеновую кислоту (кривая II) от времени проведения процесса.
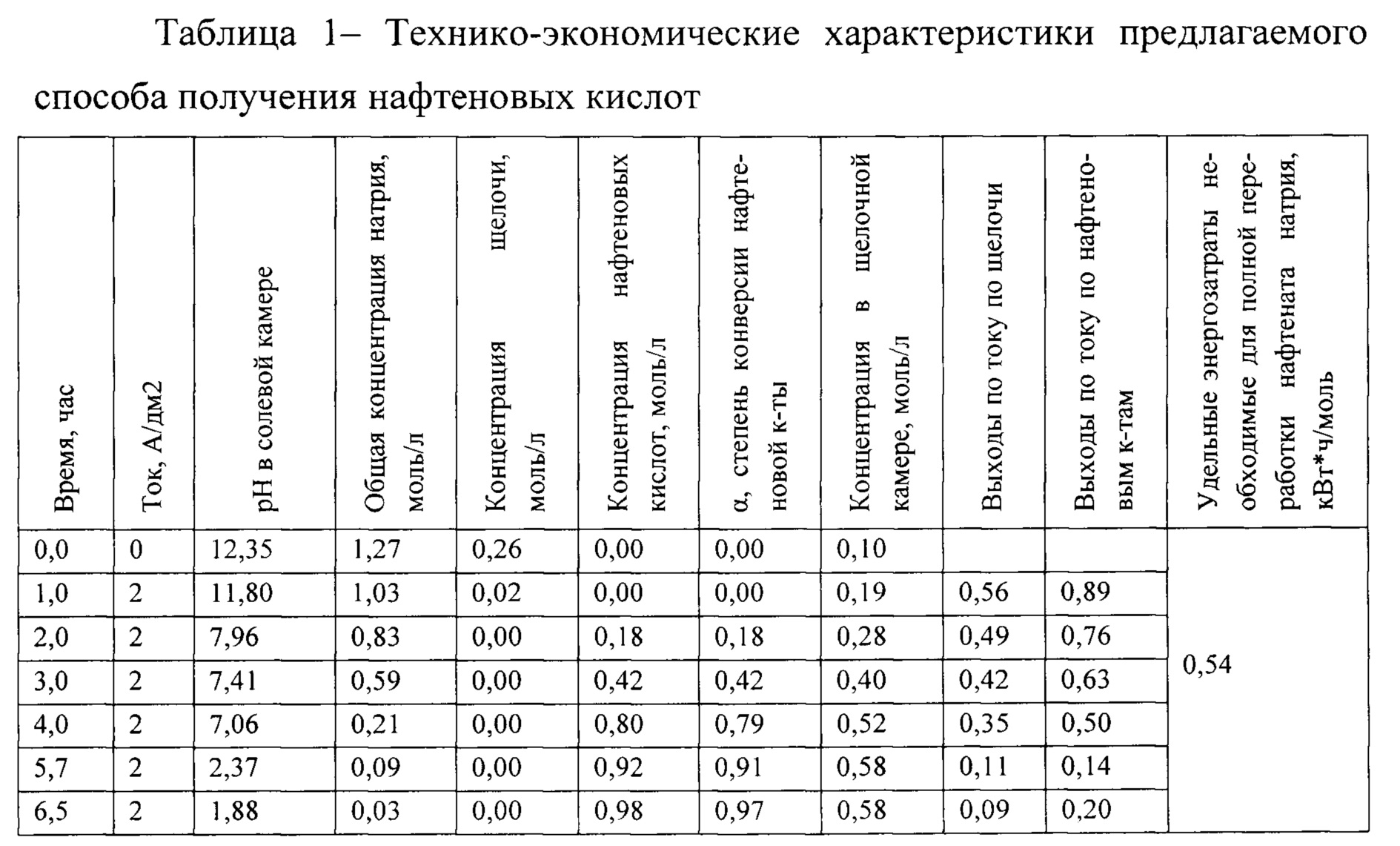
Пример 1. Для осуществления заявляемого способа получения нафтеновых кислот используют электродиализатор-синтезатор, элементарная ячейка которого содержит кислотную камеру 1 через нее циркулирует раствор минеральной кислоты, через солевую камеру 2 - раствор мылонафта (NaNf), через щелочную камеру 3 раствор щелочи (фигура 1). Кислотная камера 1 образованна катионообменной стороной биполярной мембраны 4 и катионообменной мембранной 5; солевая камера 2 - двумя катионообменными мембранами 5; щелочная 3 - анионообменной стороной биполярной мембраны 4 и катионообменной мембранной 5. Площадь каждой мембраны 1 дм2. Межмембранное расстояние 0,9 мм. Электродиализатор состоял из 6 элементарных ячеек, в солевые камеры которого вводили раствор мылонафта объемом 1 литр, содержащий 1 моль/л натриевой соли нафтеновых кислот и 0,26 моль/л гидроксида натрия. Скорость циркуляции растворов по всем камерам одинаковая и составляла 60 л/час, что соответствовало линейной скорости 6,4 см/с. Режим гальваностатический - 2 А/дм2. Технико-экономические характеристики получения нафтеновых кислот представлены в таблице 1.
На фигуре 2 показана зависимость изменение рН раствора мылонафта в солевой камере 2, при протекании через электродиализатор электрического тока (кривая I) и степень конверсии нафтената натрия в нафтеновую кислоту (кривая II) от времени проведения процесса. На начальном участке а-b, кривой I, происходит нейтрализация свободной щелочи. На участке b-с, при достижении рН равного рКа кислоты, начинается конверсия нафтената натрия в нафтеновую кислоту, в точке с процесс конверсии завершается.
Как видно из таблицы 1 при рН=1,88 в солевой камере достигается практически полная конверсия мылонафта в нафтеновую кислоту (97%), и образуется щелочь с концентрацией 0,58 моль/л. Затраты энергии на полную переработку мылонафта при этом составляют 0,54 кВт*ч/моль полученной нафтеновой кислоты, удельная производительность по получению нафтеновой кислоты равна 1,76 моль/час*м2, выходы по току для HNf составили 0,52, для NaOH - 0,30, сопротивление одной элементарной ячейки составило 9,5 Ом/дм2. В отличии от прототипа, в заявляемом способе получение нафтеновых кислот, происходит без использования серной кислоты и образования высокоминерализованных стоков.
Пример 2. Для выделения нафтеновых кислот использовался такой же электродиализатор-синтезатор как в примере 1. В процессе электродиализной переработки раствора мылонафта, в солевом контуре рН изменяют ступенчато с шагом в одну единицу до полного выделения фракций нафтеновых кислот. Указанный процесс проводился при значениях рН 7, 6, 5, 4, 3 и 2. При каждом значении рН отбирают фракции выделившихся нафтеновых кислот, которые, образовывали 2-хслойную гетерогенную систему. Анализ выделенных фракций проводился методом потенциометрического титрования. Молекулярная масса нафтеновых кислот определялась криоскопическим методом, основанный на измерении понижения температуры замерзания растворителя при добавлении к нему исследуемого вещества [Топчиев А.В. Состав и свойства нефтей и бензинокеросиновых фракций / Топчиев А.В., Кизанский Б.А., Кусак М.М., и др. // М.: Изд-во АН СССР, - 1957, - 518 с.]. В таблице 2 приведен фракционный состав по молекулярной массе полученных нафтеновых кислот в зависимости от рН, при котором происходило фракционирование.
Таблица 2 - Значения молекулярной массы различных фракций нафтеновых кислот, отобранных при изменении значения рН на 1.

Полученные фракции нафтеновых кислот имеют различные значения рКа в интервале от 7 до 2 и соответствуют значениям рН, при котором их отбирают.
Контроль рН среды и отделение нафтеновых кислот от водного раствора для получения фракций нафтеновых кислот с величинами констант диссоциации рКа изменяют рН ступенчато с шагом в одну единицу рН в интервале значений рН от 7 до 2, но в отличие от прототипа, в предлагаемом способе не используют серную кислоту и при этом не образуются высокоминерализованные растворы солей.
Пример 3. Для выделения нафтеновых кислот использовался такой же электродиализатор-синтезатор как в примере 1. Дополнительно, в солевую камеру, между катионообменными мембранами вносится гранулы катионообменной смолы (КУ-2). Заполнение солевой камеры гранулами ионита составило не менее 95%. Технико-экономические характеристики предлагаемого способа получения нафтеновых кислот с добавлением катионообменной смолы представлены в таблице 3.

При сравнении с примером 1, ведение катионообменной смолы приводит к снижению энергозатрат с 0,54 кВт⋅ч в расчете на 1 моль полученной нафтеновой кислоты до 0,24 кВт-ч. Удельная производительность по нафтеновой кислоте увеличилась с 1,76 моль/час*м2 до 12,3 моль/час*м2, среднее значение выходов по току для HNf составили 0,63, для NaOH - 0,44. В отличии от прототипа, в заявляемом способе получение нафтеновых кислот, происходит без использования серной кислоты и образования высокоминерализованных стоков.
Пример 4. Для выделения нафтеновых кислот использовался такой же электродиализатор-синтезатор как в примере 1. Дополнительно в раствор мылонафта, циркулирующий через солевую камеру, вводится сульфат натрия с концентрацией 0,05, 0,2 и 0,5 моль/л. Технико-экономические характеристики получения нафтеновых кислот с добавлением минеральной соли с катионом одинаковым катиону солей перерабатываемы нафтеновых кислот, при концентрации фонового электролита сульфата натрия общей концентрацией 0,05, 0,2 и 0,5 моль/л представлены в таблицах 4, 5 и 6 соответственно.
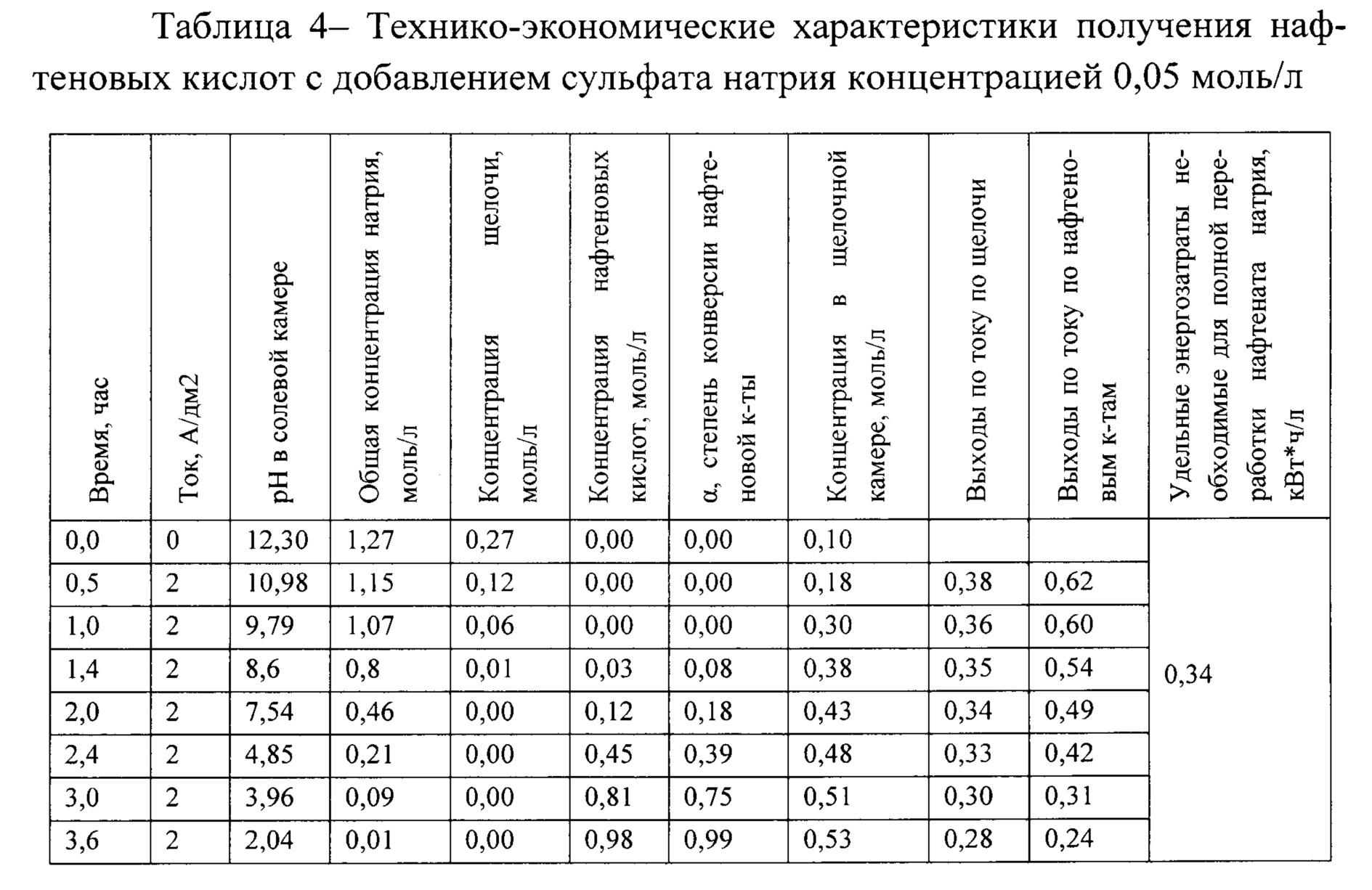

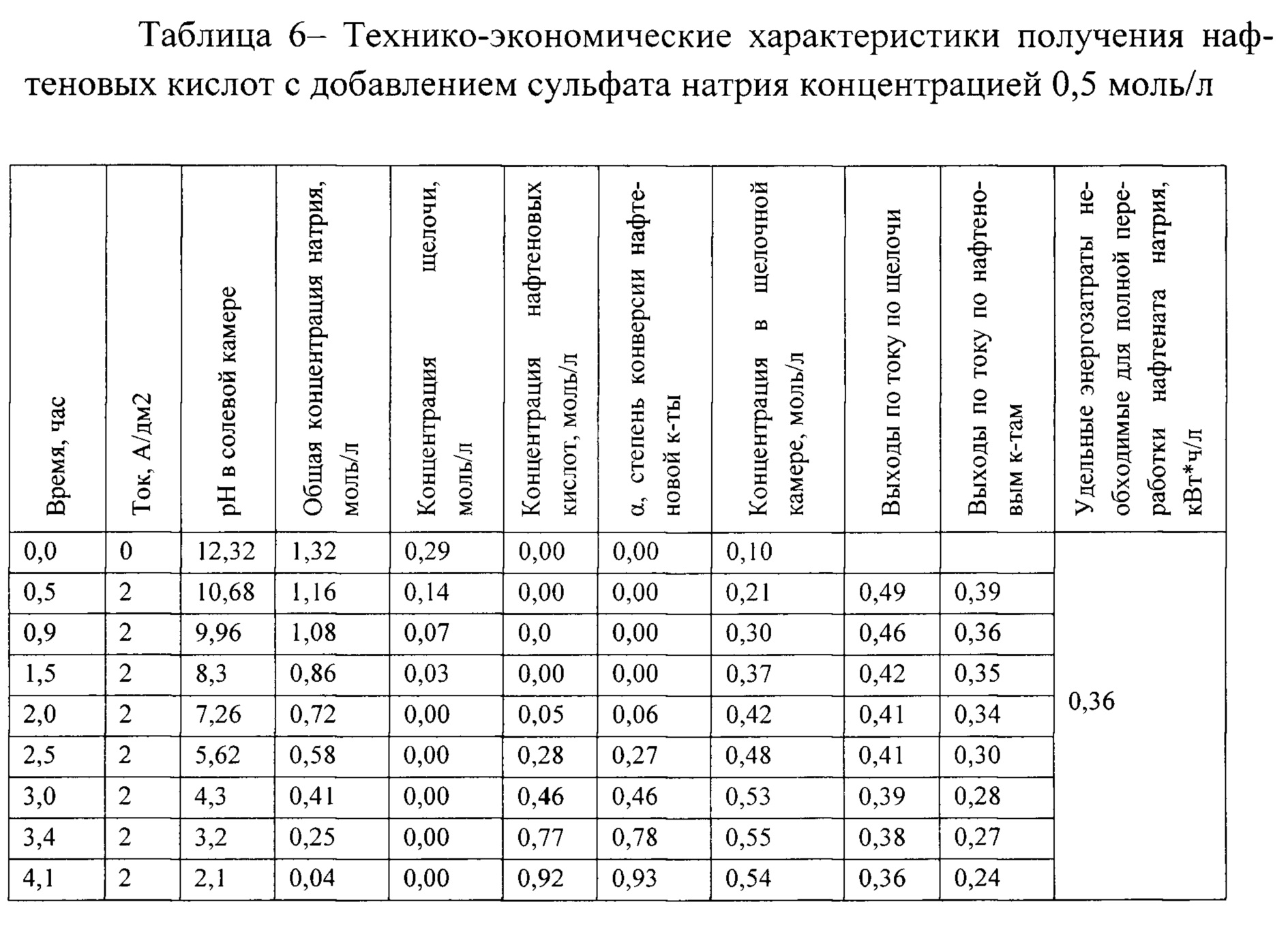
Как видно из таблиц 4-6 наилучший эффект достигается при добавлении сульфата натрия с концентрацией 0,2 моль/л. При этом удельная производительность по нафтеновой кислоте увеличилась с 1,76 моль/час*м2 до 11,1 моль/час*м2, выходы по току для HNf составили 0,6, для NaOH - 0,37, относительно примера 1, а именно: снижение энергозатрат с 0,54 кВт⋅ч в расчете на моль полученной нафтеновой кислот до 0,29 кВт⋅ч и снижению сопротивления на одной парной камере с 9,5 Ом/дм2 до 3,2 Ом/дм2. Изменение концентрации сульфат ионов в результате их неселективного переноса через катионообменные мембраны было незначительным (не более 1%). Добавление сульфата натрия с концентрацией 0,05 моль/л обеспечило снижение энергозатрат до 0,34 кВт⋅ч на моль полученной кислоты, а сопротивление элементарной ячейки составило 4,6 Ом/дм2 (таблица 4). Добавление сульфата натрия с концентрацией 0,5 моль/л обеспечило снижение энергозатрат до 0,36 кВт⋅ч на моль полученной кислоты, при этом сопротивление элементарной ячейки составило 2,9 Ом/дм2, однако из-за высокой концентрации сульфата натрия и диффузии сульфат ионов, выходы по току в солевой камере значительно снизились и составили 0,32 (таблица 6). Присутствие сульфата натрия в растворе мылонафта не повлияло на процесс образования нафтеновых кислот.
Пример 5. Для выделения нафтеновых кислот использовался такой же электродиализатор-синтезатор как в примере 1 и дополнительно в солевую камеру вводится фоновый электролит сульфат натрия с концентрацией 0,2 моль/л. В процессе электродиализной переработки раствора мылонафта, в солевом контуре рН изменяют ступенчато с шагом в одну единицу до полного выделения фракций нафтеновых кислот. Указанный процесс проводили при значениях рН 7, 6, 5, 4, 3 и 2. При каждом значении рН отбирали фракции выделившихся нафтеновых кислот, которые, образовывали 2-хслойную гетерогенную систему. Анализ выделенных фракций проводили методом потенциометрического титрования. Молекулярная масса нафтеновых кислот определялась криоскопическим методом, основанный на измерении понижения температуры замерзания растворителя при добавлении к нему исследуемого вещества. В таблице 7 приведен фракционный состав по молекулярной массе полученных нафтеновых кислот в зависимости от рН, при котором происходит фракционирование.

Полученные фракции нафтеновых кислот имеют различные значения рКа в интервале от 7 до 2 и соответствуют значениям рН, при котором их отбирают.
Пример 6. Для выделения нафтеновых кислот использовался такой же электродиализатор-синтезатор как в примере 1 и дополнительно в солевую камеру вводится фоновый электролит сульфат натрия с концентрацией 0,2 моль/л. Дополнительно, в солевой камере, между мембранами вносились гранулы катионообменной смолы (КУ-2). Технико-экономические характеристики предлагаемого способа получения нафтеновых кислот с добавлением в солевую камеру сульфата натрия концентрацией 0,2 моль/л и добавлением катионита в солевую камеру, представлена в таблице 8.
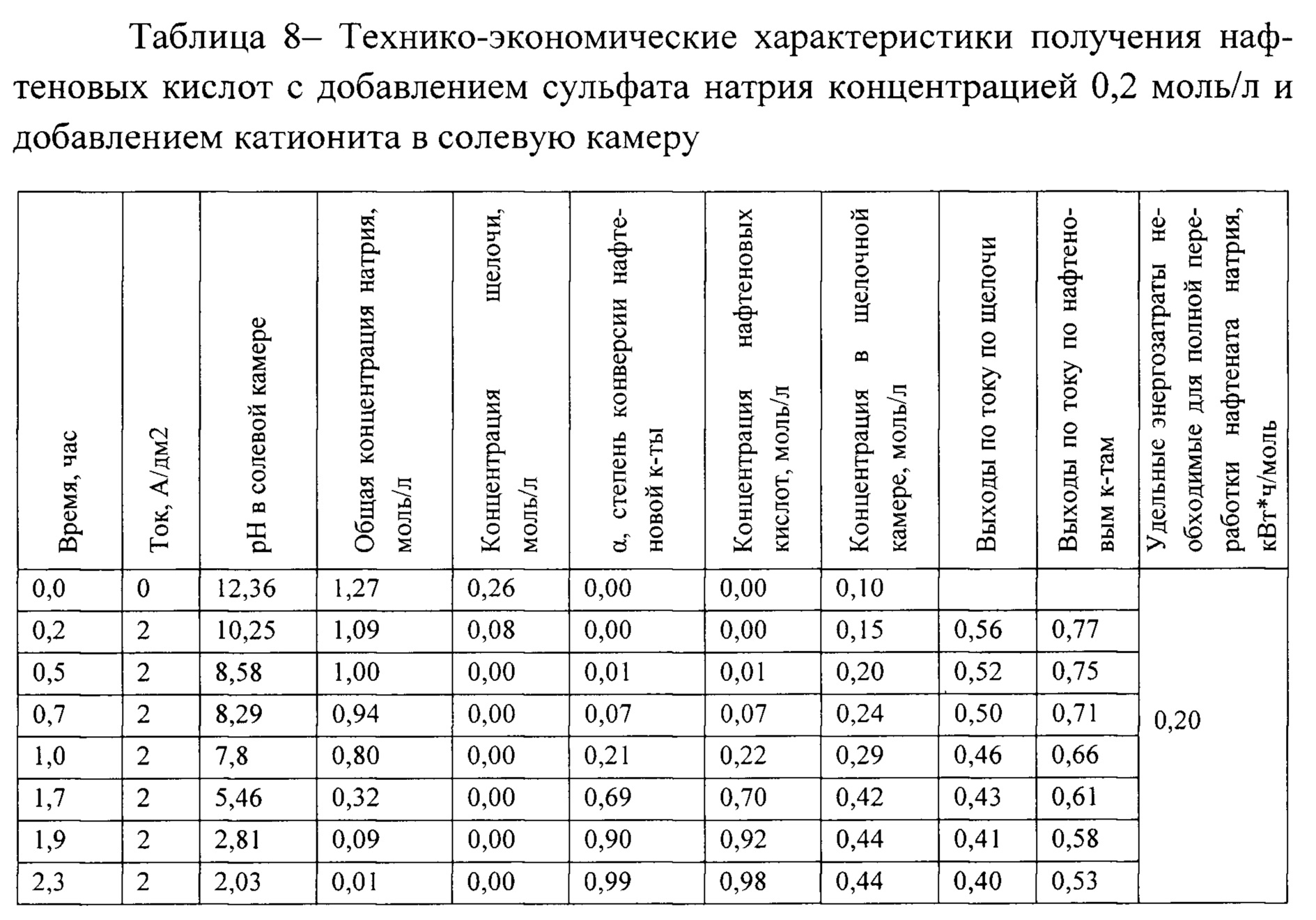
Затраченные для полного извлечения нафтеновой кислоты энергозатраты снизились с 0,54 кВт⋅ч (пример 1) в расчете на моль полученной нафтеновой кислот до 0,20 кВт⋅ч. Удельная производительность по нафтеновой кислоте увеличилась с 1,76 моль/час*м2 до 17,36 моль/час*м2, средние значение выходов по току для HNf составили 0,66, для NaOH - 0,48. В отличии от прототипа, в заявляемом способе получение нафтеновых кислот, происходит без использования серной кислоты и образования высокоминерализованных стоков.
Таким образом, предложенный способ позволяет получать нафтеновые кислоты без использования серной кислоты, а полученная щелочь может повторно использоваться для раскисления нефти и нефтепродуктов. Введение в раствор мылонафта неорганической соли с одинаковым катионом с катионом щелочи позволяет повысить эффективность способа. Наилучший результат достигается при использовании добавок в исходный мылонафт неорганической соли и введения в межмембранное расстояние солевой камеры катионообменной смолы. Ступенчатое изменение рН с шагом в единицу значений рН в интервале значений от 7 до 2, с отделением нафтеновых кислот при каждом значении рКа, позволяет фракционировать нафтеновые кислоты по рКа.
Реферат
Изобретение относится к способу получения нафтеновых кислот путем обработки водного раствора смеси натриевых солей нафтеновых кислот (мылонафта) с контролем рН среды. Способ характеризуется тем, что раствор мылонафта подают в электродиализатор-синтезатор, содержащий биполярные и катионообменные мембраны, причем в кислотных камерах, образованных катионообменной стороной биполярной мембраны и катионообменной мембраной, циркулирует минеральная кислота, в щелочных камерах, образованных катионообменной мембранной и анионообменной стороной биполярной мембраны циркулирует щелочь, в солевых камерах, образованных катионообменными мембранами, циркулирует мылонафт, у которого под действием электрического поля изменяют рН от 7 до 2 соответствующих рКа кислот, и образовавшиеся нафтеновые кислоты отделяют от водного раствора солей нафтеновых кислот, при этом в кислотных камерах автоматически поддерживают концентрацию кислоты ионами Н, а в щелочных камерах концентрируют щелочь, которую возвращают на выщелачивание нафтеновых кислот из нефтепродуктов. Данный способ является экологически чистым и не требует использования минеральной кислоты. 3 з.п. ф-лы, 2 ил., 6 пр., 8 табл.

Комментарии