Композиция для ингибирования вируса, находящегося в оболочке, и в качестве противозачаточного средства - RU2110256C1
Код документа: RU2110256C1
Чертежи







Описание
Изобретение относится к новому способу и новым изделиям для ингибирования активности вирусов в оболочке. Изобретение также относится к лечению вирусных инфекций. Более конкретно, изобретение относится к способу ингибирования развития заболеваний и инфекций, вызванных вирусами в оболочке. Согласно одному аспекту, изобретение, в частности, относится к способу ингибирования активности вирусов, у которых главным путем переноса является половой. Согласно другим аспектам, изобретение также относится к способам ингибирования активности вирусов в оболочке, способ передачи которых не является половым. Заявленные композиции эффективны при ингибировании бактерий и грибков, которые сосуществуют с вирусами или вирусными инфекциями. Изобретение также относится к лечению вирусных заболеваний, в частности заболеваний, связанных со СПИДом, передаваемых половым путем, и заболеваний, относящихся к указанным и другим инфекциям, вызванным условно-патогенными микроорганизмами у носителя с иммунными нарушениями.
Способ согласно изобретению относится к применению смесей бетаинов и аминооксидов при ингибировании вирусов в лечении вирусных инфекций. Бетаин выбирают из группы, состоящей из алкил-N-бетаина, алкил-N-сульфобетаина, анил-N-бетаина, алкил-N-замещенной аминопропионовой кислоты и алкилимидазолиний бетаина, а аминооксид выбирают из группы, состоящей из алкил-N, N-диметиламиноксида, алкил-N, N-диоксиэтиламиноксида и третамидоксида ациламида. Термин "бетаин" при его использовании в данном описании означает N-диметилглицин и его низшие алкильные гомологи. Этот термин включает в себя N-диметиламинопропионовые кислоты и сульфобетаины, которые представляют собой сульфокислотные аналоги таких соединений. Если не указано иное, то подразумевается N-диметиловое соединение. Более конкретно, изобретение относится к способу применения смесей алкил N-ди (низший алкил) бетаинов и алкил N-ди (низший алкил) аминоксидов при ингибировании вирусов в оболочках и использования этих смесей при лечении инфекционных заболеваний, вызванных этими вирусами. Эти смеси также могут использоваться в качестве средств, разрушающих сперматозоиды, без добавок или в сочетании с другими обычными средствами, разрушающими сперматозоиды. Эти смеси могут и применяться в сочетании с противозачаточными устройствами или могут быть введены в противозачаточное устройство.
Известно, что некоторые смеси аминов являются эффективными противомикробными средствами против грамотрицательных и грамположительных бактерий. В частности, известно, что некоторые смеси а) алкил-N-бетаина, алкил-N-сульфобетаина, ацил-N-бетаина, алкил-N-замещенной аминопропионовой кислоты или алкилимидазолинийбетаина и б) алкил-N, N-диметиламиноксида, алкил-N, N-диоксиэтиламиноксила или третаминоксида ациламида могут применяться для дезинфекции, очистки и дезодорации кожи (см. , например, патенты США NN 4183952, 4075350, 4107328). Эти составы также пригодны для долговременного ингибирования запаха тела. Смеси тех же самых активных соединений также известны как улучшающие гигиену полости рта путем уменьшения микрофлоры в полости рта и ингибирования образования зубного налета (патент США 4839158). Составы этого типа также известны как эффективные фунгициды (Corner А.M. и пр. Antimicrobial Agents and Chemotherapy 32(3) : 350 - 353, март 1988; Corner, A. M. The Journal of Clinical Dentistry, vol. 2(2): 34 - 36, 1990, см. также патенты США NN 4075350, 4107328, 4183952 и 4839158).
Также известно, что неионные поверхностно активные вещества, обладающие эфирными или аминными связями между гидрофильными и гидрофобными участками молекулы, быстро инактивируют инфективность вируса I и II герпеса (Asculai, S.S. и пр. Antimicrobial Agents Chemotherapy, Vol. 13:686-690, 1978). B этом документе также указывается, что разрушающая клетки активность была использована в качестве показателя противовирусной активности. Составы, применяемые в изобретении, имеют преимущества по сравнению с описанными в документе Ascular и др., а именно эти составы инактивируют вирусы и бактерии при проявлении низкой активности по разрушению клеток.
Оказалось, что средство, разрушающее сперматозоиды, коноксинол-9 (N-9), обладает бактерицидными и вироцидными свойствами. Например, оказалось, что N-9 инактивирует вирусы, относящиеся к СПИДу (например, ВИЧ, вирус иммунодефицита человека) и к вирусам герпеса (HSV I и II). Было показано, что ин витро N-9 эффективен против организмов, которые вызывают гонорею, хламидию, сифилис, трихомоноз и другие заболевания, передаваемые половым путем (U.S. Pharmacopeial Convention USPDI Update 1990, 755-756), (Договор по фармакопее США, ред. 90).
В настоящее время неожиданным образом было обнаружено, что некоторые описанные ниже смеси бетаинов, таких как а) алкил-N-бетаины, алкил-N-сульфобетаины, ацил-N-бетаины, алкил-N-замещенные аминопропионовые кислоты и алкиламилазолинийбетаины, и аминооксидов, таких как б) алкил-N-диметиламинооксиды, алкил-N, N-диоксиэтиламинооксиды или третамидооксиды ациламида в приемлемых разбавителях, носителях и наполнителях, эффективны при ингибировании активности вирусов в оболочке. Изобретение обеспечивает ингибирование активности вирусов в оболочке, для которых главным путем переноса является половой. Изобретение относится к способу лечения заболеваний и инфекций, вызванных вирусом в оболочке. Заявленные составы также эффективны при ингибировании бактерий и грибков, которые сосуществуют с вирусами или вирусными инфекциями, а также для лечения бактериальных и грибковых инфекций, которые сосуществуют с вирусами или вирусными инфекциями. Изобретение также обеспечивает создание способа дезинфекции воздуха и поверхностей, зараженных вирусами в оболочке.
Изобретение обеспечивает также создание способа предупреждения переноса вируса, содержащего оболочку.
Композиции, применяемые в способе согласно изобретению, также могут применяться в качестве средств, разрушающих сперматозоиды. Эти составы могут применяться без добавок, с другими известными средствами для разрушения сперматозоидов и с включением (или без включения) в противозачаточные устройства так же, как презервативы, тампоны, влагалищные вставки, противозачаточные пленки, мембраны, свечи, противозачаточные бляшки или испытанные устройства или облегчения. Эти составы также могут быть включены в салфетки. Составы могут быть введены в душ. Для применения в качестве вироцидных средств эти составы могут быть использованы без добавок; с другими средствами, разрушающими сперматозоиды; и с введением (или без введения) в вышеописанные противозачаточные устройства. Эти композиции также могут быть применены в виде пены, геля, мази, пасты, желе или лосьона. Этот состав также может быть применен в форме жидкости, аэрозоля или распыления.
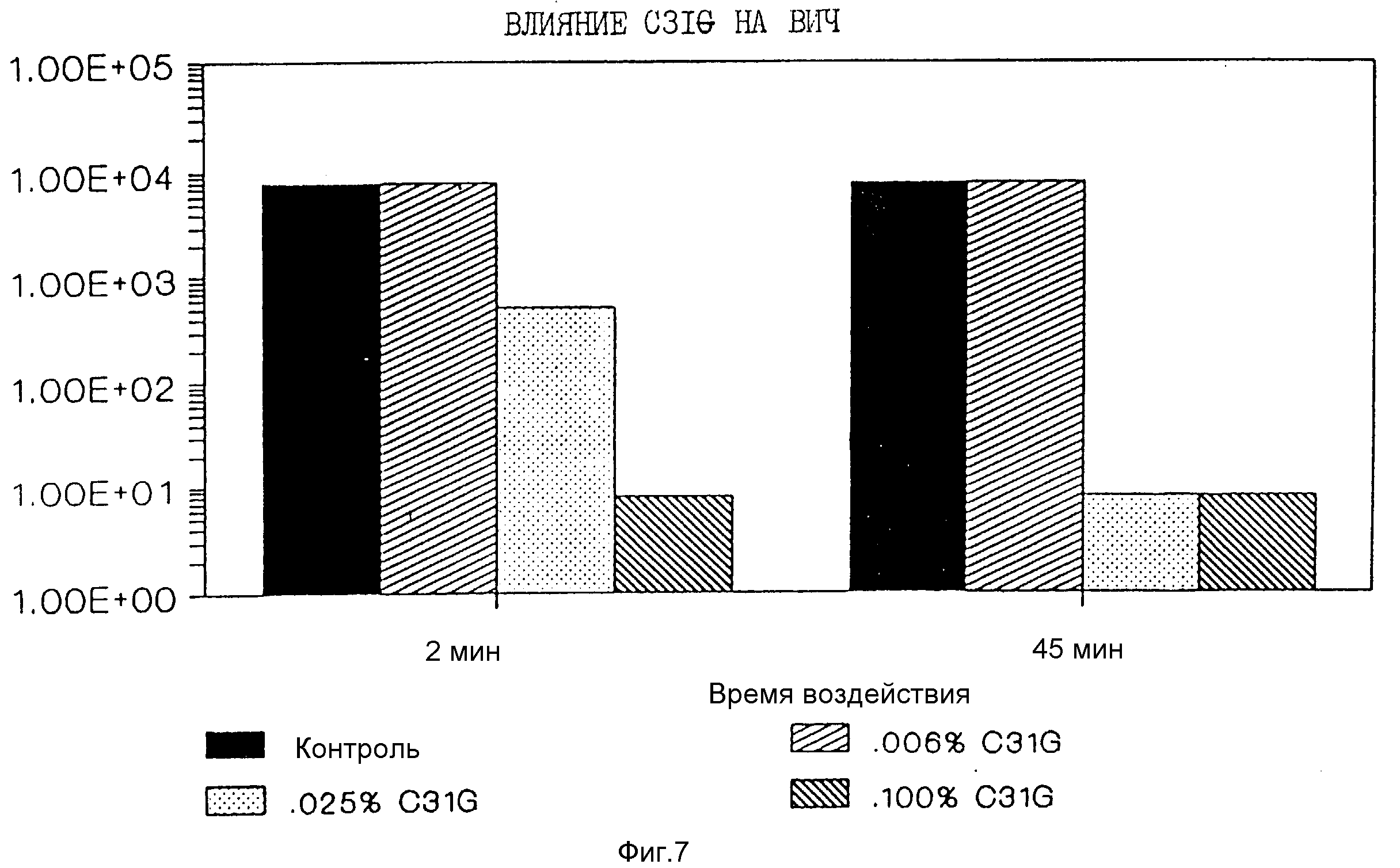
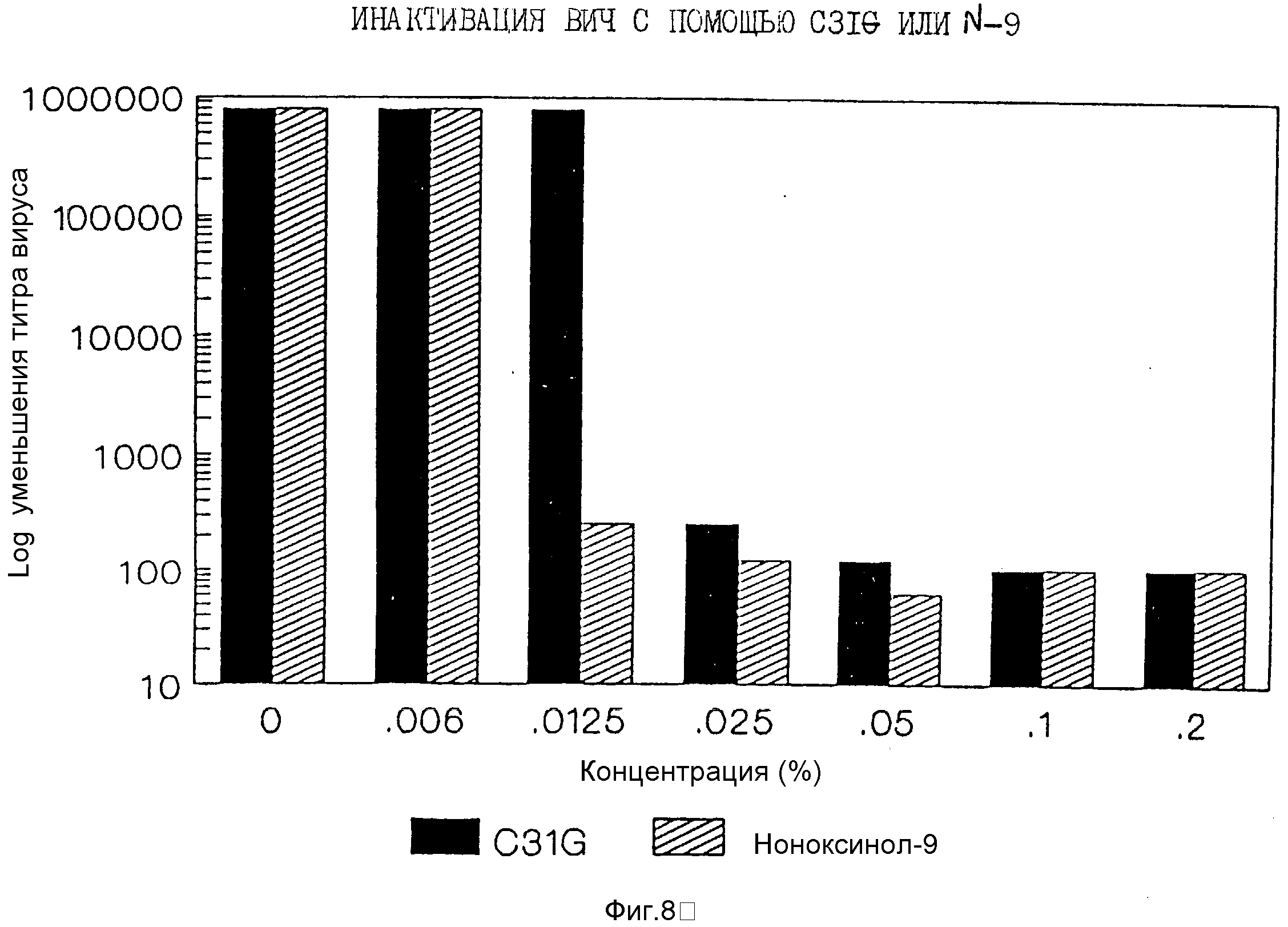
На фиг. 1 представлена диаграмма, на которой показано влияние C31G (состав согласно изобретению) и влияние ноноксинола-9 (N-9) на подвижность сперматозоидов; на фиг. 2 - диаграмма, на которой показано влияние C31G и влияние ноноксинола-9 (N-9) на общее количество сперматозоидов; на фиг. 3 - диаграмма, на которой показана ин витро токсичность C31G по отношению к N-9 на клетки su p-T1; на фиг. 4 - диаграмма, на которой показано влияние C31G и влияние ноноксоинола-9 (N-9) на среднюю прогрессивную скорость сперматозоидов; на фиг. 5 - диаграмма, которая показывает исследование пятидневной токсичности C31G по отношению к N-9 на клетки CEM; на фиг. 6 - диаграмма, на которой показано сравнение влияния C31G по отношению к N-9 на HSV; на фиг. 7 - диаграмма, на которой показано влияние C31G на ВИЧ; на фиг. 8 - диаграмма, на которой сравнивается инактивация ВИЧ с помощью C31G и N-9.
В табл. 1 сравнивается инактивация ВИЧ с помощью C31G и N-9.
Способ согласно изобретению относится к применению смесей бетаинов и аминоксидов при ингибировании вирусов, находящихся в оболочке, и к лечению вирусных инфекций, вызванных вирусами, находящимися в оболочке. Способ согласно изобретению также относится к применению смесей бетаинов и аминооксидов при инактивации вирусов, находящихся в оболочке. Бетаины, которые могут использоваться в данном изобретении, представляют собой алкил-N-бетаины, алкил-N-сульфобетаины, ацил-N-бетаины, алкил-N-замещенные аминопропионовые кислоты или алкилимидазолинийбетаины или их смеси. Аминокислоты, которые могут использоваться в данном изобретении, представляют собой алкил-N, N-диметиламиноксиды, алкил-N, N-диокси-этиламинооксиды или третамидооксиды ациламида или их смеси. Эти композиции также эффективны при лечении вирусных, грибковых и микробных инфекций и заражений. Эти композиции эффективны при ингибировании вирусов, находящихся в оболочке, которые переносятся половым путем или неполовым путем. Эти композиции также эффективны при ингибировании бактерий и грибков, которые сосуществуют с вирусами или вирусными инфекциями. Эти композиции также могут использоваться локально.
Обычно эти композиции применяют на участке, где вирусы переносятся или могут переноситься. Это включает введение во влагалище, на слизистые оболочки и на кожу.
Эти композиции также могут применяться в качестве средств разрушения сперматозоидов, без добавок или в сочетании с другими средствами разрушения сперматозоидов. Эти композиции также могут применяться с противозачаточными устройствами или включенными в них, такими как, например, презервативы, мембраны, губки, противозачаточные пленки, свечи, испытанные устройства для облегчения и противозачаточные бляшки. Например, эта композиция может быть введена в смазочное вещество, наносимое на презерватив, или как часть резервуара в наконечнике презерватива, или вводиться в противозачаточную губку, противозачаточную пленку, в свечу, в испытанное устройство или выделения или в противозачаточную бляшку. Противозачаточная пленка может содержать вышеописанную композицию вместе с желатином типа А, целлюлозной смолой и многоатомным спиртом. Эти композиции также могут применяться в противозачаточных пенах, гелях, желе, мазях. Эти композиции также могут применяться в душах или для предупреждения переноса вирусов эти композиции могут применяться без добавок, с другими средствами разрушения сперматозоидов или включенными в противозачаточное устройство, как описано выше. Данное изобретение также включает способ ингибирования переноса вирусов, которые вызывают передаваемые половым путем заболевания, включающий нанесение этих составов на те части тела, которые оказываются под воздействием вод организма, выделяемых другим в процессе полового акта.
Эти композиции также, как было неожиданным образом установлено, оказались менее токсичными к клеткам млекопитающих, чем ноноксоинол-9 (N-9) (см. фиг. 4 и 5). В табл. 2 показано, что эти композиции имеют эквивалентную N-9 разрушающую сперматозоиды активность, а N-9 является одним из нескольких поверхностно-активных веществ, одобренных Федеральной ассоциацией лекарственных средств для применения в качестве средства разрушения сперматозоидов.
Для локальных случаев применения эта композиция может быть введена в жидкости, кремы, мази, лосьоны, пены и гели.
Изобретение также обеспечивает создание способа дезинфекции воздуха и неживых поверхностей, например в рабочей комнате или в лаборатории. В частности, это изобретение обеспечивает создание способа дезинфекции участков, которые заражены вирусами, находящимися в оболочке. Эти композиции также могут быть включены в разбрызгиваемые среды, аэрозоли, средства для вытирания, распыляемые среды или устройства, которые производят разбрызгиваемые среды, распыляемые среды или аэрозоли. Эти композиции также могут быть применены в виде жидкостей.
Согласно данному изобретению эти композиции могут применяться как вироциды, фунгициды и бактерициды.
Композиции, согласно изобретению, включают смесь бетаинов и аминооксидов. Бетоины,
применяемые по данному изобретению, выбирают из
группы, состоящей из а) алкил-N-бетаинов, алкил-N-сульфобетаинов, ацил-N-бетаинов, алкил-N-замещенной аминопропионовой кислоты,
алкилимидазолинийбетаинов и смесей из двух из них или более. Обычно
бетаины имеют две низшие алкильные группы, связанные с атомом азота. В наиболее эффективном случае они имеют два метильных
заместителя у атома азота. Аминооксиды, согласно данному изобретению,
выбирают из группы, состоящей из б) алкил-N-диметиламинооксидов, алкил-N, N-диоксиэтиламинооксида или третаминооксидов ациламина
и смесей из двух из них или более. Обычно бетаиновый и аминооксидный
компоненты присутствуют в молярном соотношении 1:5 - 5:1, предпочтительно в молярном соотношении 1:1. Алкил-N-бетаин,
алкил-N-сульфобетаин, ацил-N-бетаин, алкил-N-замещенная 2-аминопропионовая кислота
и алкилимидазолинийбетаин (также называемые кокоамфоацетаты), применяемые в качестве компонентов а) состава согласно
изобретению, имеют следующие структуры, соответственно:


где R - высшая алкильная группа, имеющая 10 - 18 атомов углерода, предпочтительно 12 - 16 атомов углерода.
Термин
низший алкил обозначает алкильную группу с 1-3 атомами углерода. Применяют
следующие вещества:
1) коко-N-бетаин, цетил-N-бетаин, стеарил-N-бетаин, изостеарил-N-бетаин, олеил-N-бетаин;
2) коко-N-сульфобетаин, цетил-N-сульфобетаин, стеарил-N-сульфобетаин,
изостеарил-N-сульфобетаин, олеил-N-сульфобетаин;
3) кокоамино-N-бетаин, цетиламидо-N-бетаин, стеариламидо-N-бетаин,
изостеариламидо-N-бетаин, олеин-амино-N-бетаин;
4)
N-коко-2-аминопропионовая кислота, N-цетил-2-аминопропионовая кислота, N-стеарил-2-аминопропионовая кислота,
N-изостеарил-N-аминопропионовая кислота, N-олеил-2-аминопропионовая кислота,
N-стеарил-бис-(2-аминопропионовая кислота), N-олеил-бис-(2-аминопропионовая кислота);
5)
N-оксиэтил-1-карбоксиметил-2-децилимидазолийбетаин-N-лаурил-бис- (2-аминопропионовой кислоты),
1-оксиэтил-1-карбоксиметил-2-додецилимидазолийбетаин, 1-оксиэтил-1-карбоксиметил-2-кокоимидазолийбетаин,
1-оксиэтил-1-карбоксиметил-2-стеарилимидазолийбетаин,
1-оксиэтил-1-карбоксиметил-2-олеилимидазолийбетаин или их смеси.
В данном случае термин "коко", используемый в фирме КТФА (название Ассоциации по косметике, туалетным принадлежностям и благовониям, Вашингтон, округ Колумбия), применяется для обозначения алкильных групп, присутствующих в кокосовом масле, т.е. смесь алкильных групп, содержащих 10 - 18 атомов углерода. Обозначения соединений, приведенных здесь, являются обозначениями КТФА.
1) Алкил-N, N-диэтиламинооксид, 2) алкил-N,
N-диоксиэтиламинооксид или 3) ациламид-трет-аминооксид, используемые в качестве
компонента б) вышеуказанной смеси, соответственно, имеют структуру

где R обозначает высшую алкильную группу, содержащую 10 - 18 атомов углерода, в частности такие радикалы, как децил, ундецил, лаурил, тридецил, мирастил, цетил, стеарил, изостеарил или олеил.
Примерами аминооксидов являются: децил-N, N-диметиламинооксид, лаурил-N, N-диметиламинооксид, стеарил-N, N-диметиламинооксид, олеин-N, N-диметиламинооксид, коко-N, N-диоксиэтиламинооксид, цетил-N, N-диоксиэтиламинооксид, олеил-N, N-диоксиэтиламинооксид,N, N-диоксиэтиламинооксид, олеил-N, N-диоксиэтиламинооксид и их смеси.
Компоненты а) и б) обычно смешивают и затем добавляют кислоту в количестве, необходимом для регулирования pH 0,5%-ного раствора в пределах 4 - 8, предпочтительно до pH 4,5 - 5, 5. pH водного раствора, содержащего вышеуказанные компоненты согласно изобретению, определяют используя водный раствор концентрации 0,5 мас. % общего количества активных компонентов обычно на стеклянном электроде, для точного определения кислотности состава.
В общем кислота, используемая для регулирования общего состава до требуемого pH, является любой органической или неорганической кислотой, которая приемлема для предусмотренного применения состава, например соляной кислотой, фосфорной кислотой, серной кислотой, лимонной кислотой, уксусной кислотой или никотиновой кислотой. Остальная часть композиции до 100% после обеспечения совместимости с кислотой обычно предоставляет приемлемый растворитель, такой как вода или низший (C1-C4 ) одноатомный алифатический спирт, на общее количество в 100 частей или более. Когда используют воду, также можно добавить небольшие количества низшего алкилового спирта, такого как этанол или пропанол, для обеспечения удобства составления рецептуры. Приемлемые разбавители, носители и наполнители - это, например, этиловый или изопропиловый спирты, полиэтиленгликоль, повидон, многоатомные спирты, глицеринцеллюлозные смолы, желатин, красители и ароматизаторы. При необходимости pH композиции затем регулируют до требуемого pH путем добавления к нему подходящей неорганической или органической кислоты.
В результате получают практически однородную гомогенную относительно нетоксичную композицию, имеющую повышенную активность против вирусов, находящихся в оболочке, бактерий и грибков.
Неожиданным образом было обнаружено, что эти композиции проявляют 1) низкую токсичность к клеткам млекопитающих, что представляет собой свойство, которое, как известно, соотносится с низкой раздражаемостью и низкой токсичностью при использовании в контакте со слизистыми оболочками (Journal Clinical Dentistry 2 (2) : 34 - 38, 1990), 2) высокоэффективной инактивацией вирусов, находящихся в оболочке, хотя их активность по разрушению клеток невысока. В прошлом при исследованиях использовали активность по разрушению клеток в качестве показателя активности (Asculai, S.S., Antimicrb. Agents Chemother. 13 : 678 - 690, 1978).
На практике общее количество компонентов а) и б) всего состава может находиться в пределах 0,01 - 40%, в зависимости от предусматриваемого способа применения. Например, применяемые концентрации составляют приблизительно 20 - 30% в противозачаточных пленках и 0,2 - 2% в гелях.
Композиции согласно данному изобретению включают алкил N-ди(низший алкил) глицины и алкил N-ди(низший алкил) аминооксиды, где низший алкил содержит C1-C3 обнаружилось, что один класс бетаинов I практически полезен в данном изобретении, это алкил N-диметилбетаины, такие, как кокобетаины и лаурилбетаины. Особенно полезными аминооксидами для применения в данном изобретении являются алкил N-диметиламинооксиды, такие как кокодиметиламинооксиды и лаурилдиметиламинооксиды.
Один конкретный состав, который может быть использован в данном изобретении, включает кокобетаин, кокаминооксид и моногидрат лимонной кислоты.
Другой состав, который может быть использован в данном изобретении, включает лаурилбетаин, лаураминооксид и моногидрат лимонной кислоты.
В таких составах молярное соотношение бетаинов к аминооксидам обычно составляет 5 : 1 - 1 : 5, предпочтительно при молярном соотношении 2 : 1 - 1 : 2, более предпочтительно примерно 1 : 1.
Другие композиции, которые могут использоваться в данном изобретении, включают смеси бетоинов, аминооксидов, желатина, имеющего прочность по Блуму 100 - 300 и молярную массу примерно 75,000 - 300,000, полиатомных спиртов и целлюлозных смол. Такие составы описаны в рассматриваемой в настоящее время заявке в США, поданной одновременно с настоящей заявкой и имеющей регистрационный номер заявки в США 07/673631.
Композиции, используемые в данном изобретении, могут ингибировать активность вирусов, которые относятся к СПИДу. Также ожидается, что эти составы могут ингибировать активность HSV-1 и HSV-2. Также ожидается, что композиции, используемые в изобретении, могут ингибировать гепатит A, B и C. Ожидается, что эти составы могут использоваться для ингибирования вирусов, бактерий и грибков, которые связаны с заболеваниями, переносимыми половым путем.
Композиции по данному изобретению могут быть полезны в связи со следующим.
1) Передача ВИЧ часто связана с совместной передачей других вирусных и/или микробных возбудителей заболевания. В самом деле, некоторые исследователи предположили, что ВИЧ может быть не единственным агентом, ответственным за СПИД (см. Duesberg Р.Н., 1991, Proc. Nat.Acad.Sci, 88: 1575-1579; Lemaitre M., Guetord D., Henin, Y., Montagnier, L. и Zerial A., 1990, Res. Virol 141: 5 - 16). По этой причине антимикробные агенты, такие как описанные в данной заявке, с широким спектром активности против вирусов, бактерий и дрожжей, таких как Candida, могут иметь особую ценность в предупреждении и лечении синдрома приобретенного иммунодефицита (СПИД).
2) Предполагается, что определенные бактерии, которые, как известно, вызывают заболевания, передаваемые половым путем, могут помогать при передаче ВИЧ. У лиц, которые были подвержены воздействию ВИЧ, определенные бактерии, которые вызывают заболевания, передаваемые половым путем, часто не реагируют на некоторые виды терапевтического лечения, которые в иных случаях высокоэффективны. ВИЧ-инфекция может помогать в распространении бактериального заболевания, передаваемого половым путем, которое в свою очередь помогает распространению ВИЧ. Заболевания, передаваемые половым путем, такие как хламидия, мягкий шанкр, сифилис, герпес половых органов и гонорея, которые вызывают образование язвы верхних слоев половых органов, как кажется, увеличивают опасность приобретения или передачи ВИЧ-инфекции половым путем (Aral, S.O., et al Scientific American 264 (2): 62-69, февраль 1991).
Вышеописанные композиции также могут применяться для инактивизации других вирусов, содержащихся в оболочке, включая коровью оспу, ветряную оспу, опоясывающий герпес, вирус цетомегалии, вирус Општейна-Барра, грипп, эпидемические паротиты, корь, риновирус, бешенство и коревую краснуху. В целях облегчения дальнейшего понимания изобретения следующие примеры представлены главным образом для целей иллюстрации его более конкретных деталей. Изобретение не должно быть ограничено настоящим, исключая то, что определено в формуле изобретения.
Пример 1. Нижеописанная композиция представляет собой концентрат С31С, представляющий собой эквимолярный препарат из кокобетаина и кокодиметиламиноксидов (названия КТФА - Ассоциации по косметике, туалетным принадлежностям и благовониям, Вашингтон, округ Колумбия) (КФТА), который может использоваться в ряде различных конфигураций.
Кокобетаин: 31,5% активного компонента (A1): 183,9 кг (405,5 фунта).
Кокоаминоаксид 31,5% (A1): 147,4 кг (325 фунтов).
Моногидрат лимонной кислоты, фармакопея США: 11,8 кг (26 фунтов).
Очищенная вода, фармакопея США: 11,8 кг (26 фунтов).
Для получения примерно 354,9 кг (782,5 фунта) C31G при 29,6% A1, с разбавлением 1% A1; pH 4,9.
Пример 2. Активность C31G по разрушению сперматозоидов из примера 1 сравнивали с активностью по разрушению сперматозоидов ноноксинола-9 (N-9).
Исследования проводились с использованием анализатора подвижности сперматозоидов Гамильтона-Торна. Пробы отстоянной промытой семенной жидкости инкубировали с разбавленными растворами из обоих соединений в течение 15 с и анализировали (по три раза) для определения минимальной концентрации для инактивации с помощью следующих критериев.
1. Ингибирование подвижности сперматозоидов (фиг. 1).
2. Уменьшение общего подсчитанного количества сперматозоидов (фиг. 2).
3. Ингибирование средней скорости продвижения сперматозоидов (фиг. 3).
Как показано в табл.2, C31G и N-9 давали идентичные результаты.
В табл.2
представлена минимальная концентрация для
активности по разрушению сперматозоидов
Пример 3. Цитотоксические эффекты C31G и N-9 на клетки млекопитающих определяли при нескольких типах
испытаний. Клеточная токсичность представляет
собой показатель относительной безопасности и удобства при использовании поверхностно активных веществ в контрацептивах или в профилактических
средствах.
Как показано на фиг. 4, двухнедельный мониторинг исследования влияния лекарственных средств на клетки SUP-TI (лимфоцитарная клеточная линия человека) показал, что C31G давало минимальную токсичность при 0,001% (10 ч. на 1 млн. ), в то время как N-9 при той же концентрации был исключительно токсичным.
Пример 4. На фиг. 5 показано снижение минимальной и максимальной токсичности для клеток CEM после пятидневного непрерывного воздействия на них. При этих условиях C31G не проявляло токсичности к клеткам млекопитающих при 3 ч. на 1 млн. (0,0003%), в то время как N-9 проявлял токсичность, снижая жизнеспособность клеток млекопитающих на 50% при той же самой концентрации. Неожиданно то, что соединение, имеющее такую же активность по разрушению сперматозоидов, что и N-9, будет менее токсичным к клеткам млекопитающих, чем N-9.
Пример 5. Противовирусную активность C31G испытывали с использованием ВПГ-1 и ВИЧ-1.
Для испытания влияния C31G и N-9 на вирус простого герпеса типа I (штамм KOS) запас вируса готовили в клетках Vero (почка африканской зеленой обезьяны). Вирус выделяли из клеток с помощью одного цикла замораживания-размораживания с последующей ультразвуковой обработкой. Титр вируса составлял 4,5•108 бляшкообразующих единиц (БОЕ/мл), что определяли на клетках Vero. Используемые композиции лекарственных средств были идентичны лекарственным средствам при исследовании активности по разрушению сперматозоидов.
Концентрация каждого лекарственного средства составляла 5%. Были выполнены двухкратные серийные разведения по 0,04% в фосфатно-буферном растворе с pH 7,4 при комнатной температуре, 24 мкл каждого разведения добавляли к 220 мкл вируса (108 БОЕ), с получением конечных концентраций 0,5 - 0,004%. Эти пробы инкубировали при комнатной температуре в течение 10 мин и затем 100 мкл каждого немедленно разбавляли по 1 мл модифицированной по способу Дульбекко средой Игла/5% сыворотки плода коровы. Затем выполняли 10-кратные серийные разведения до 10-7 для титрования оставшегося инфекционного вируса на клетках Vero в 24-ячеечных планшетах. Бляшки подсчитывали спустя 36 ч после инфицирования (табл. 3).
Отметим, что эти титры (т.е. БОЕ/мл) скорее, чем абсолютное количество БОЕ. Титр, определенный для не подвергшегося обработке вируса, составлял 4,7•108 БОЕ/мл в эксперименте с использованием N-9 и 4,5•108 БОЕ/мл в эксперименте с использованием C31G.
Отмечается, что это полное ингибирование образования бляшек с помощью C31G происходит при более чем одном разведении ниже, чем у N-9 (см. фиг. 6).
Пример 6. Инактивацию вируса ВИЧ-1 (СПИД) изучали в ходе двух экспериментов. При первом исследовании сравнивали влияние C31G на ВИЧ-1 с двумя различными сроками воздействия, т.е. 2 мин и 45 мин. При следующем исследовании сравнивали относительную активность C31G и N-9 на ВИЧ при использовании того же штамма вируса и при измерении противовирусной активности по уменьшению титра вируса, что определялось снижением антигена ВИЧ P-24. Протокол и результаты первого исследования приводятся ниже.
Влияние C31G на вирус иммунодефицита человека.
Материалы
Вирус 1:
штамм ВИЧ-1 3B (3•105 единиц средней
инфицирующей дозы/мл).
Клетки: клеточная линия SUP-T I (C 4 + лимфоидные клетки, которые производят характеристическое слияние клеток с гигантскими клетками и синцитиями на инфицировании ВИЧ).
Протокол.
1. Серийное четырехкратное разведение C31G в фосфатно-буферном растворе (4,0 - 0,004% и фосфатно-буферный раствор без добавок в качестве контроля) было получено, pH регулировали до 5,5.
2. Приготовляли отстоянные аликвотные количества вирусного сырья и добавляли C31G при каждой концентрации, при соотношении детергента:вируса 1 : 9 (разбавление детергента 1 : 10). Их инкубировали в течение 2 или 45 мин.
3. Серийное четырехкратное разведение каждой смеси вирус/ детергент по 1 : 4096 было произведено.
4. Добавляли 16,6 мкл каждого разведенного раствора вирус/детергент из каждой серии в четыре лунки реплицирования клеток SUP-TI (104 клеток в объеме 150 мкл; разбавление детергента 1 : 10 с последующими дополнительными четырехкратными разведениями).
5. Лунки проверяли дважды в неделю в течение двух недель и по каждой лунке проводили подсчет - положительно или отрицательно - на присутствие характеристических вирусных синцитиев или образование несинцитиальной тени из-за лизиса детергента.
Примечание: вирус подвергали воздействию C31G при разведении 1 : 10 исходной концентрации в течение 2 или 45 мин, после чего следовало еще одно разведение 1 : 10, а после этого ряд серийных четырехкратных разведений в течение всего периода времени. Клетки подвергали воздействию C31G при разбавлении 1 : 100 и затем при серийных четырехкратных разведениях начальной концентрации в течение всего периода (см. фиг. 7).
Пример 7. Протокол и результаты второго исследования таковы.
Материалы.
Клетки: клеточная линия C M, T-клетка#119, ATCC.
Вирус: ВИЧIIIb
Испытываемые соединения: соединения C31G и N-9, поставляемые в виде 5%-ных растворов, фильтровали через фильтр 0,22 с малым связыванием до
разведения.
Протокол.
1. Серийные 2-кратные разведения соединений N-9 и C31G в фосфатно-буферном растворе с регулированием до pH 5,5 были выполнены. Наивысшая концентрация была 4%, а наинизшая 0,03%. Начальные концентрации составляли 4,2; 1, 0,5, 0,25, 0,125, 0,6 и 0,03%, так же, как и контроль без лекарственного средства. Титрование контроля было проведено дважды.
2. 14 стерильных пластмассовых пробирок 12•75 мм были приготовлены с 0,9 мл в каждой концентрированного вируса (не менее 1•106 средней цитопатогенной дозе/мл). В пробирку переносили 0,1 мл каждого разбавления соединения (разбавление 1 : 10 начальных концентраций лекарственного средства).
3. Инкубирование проводили в течение 10 мин при комнатной температуре, его заканчивали (или замедляли) разбавлением 1 : 10 в полной питательной среде (на льду).
4. Готовили дополнительные серийные 5-кратные разведения (7 разведений, с конечным разведением, равным 1 : 781250) в полной среде на льду.
5. Добавляли 50 мкл разведений вируса в лунки в четырех экземплярах 96-луночного планшета (U-образное дно), содержащих 3•104 клеток CEM в 50 мкл.
6. Давали 60 мин при абсорбции вируса. Клетки дважды промывали путем центрифугирования планшетов на 1500 об/мин в течение 5 мин и осасывания супернатантов. Конечные дебрисы повторно суспендировали в 100 мкл среды и переносили в 96-луночные планшеты с плоским дном. Результаты показаны на фиг. 8 и в табл. 1.
Пример 8. Композиция для противозачаточных/противоинфекционных препаратов.
Концентрат (CCoп) содержит, ч.:
Лаурилбетаин (30% активн. ингред.) - 1000
Лаураминооксид (30% активн. ингред.)
- 870
Моногидрат лимонной кислоты - 69
Вышеуказанное перемешивали до однородного раствора. При разведении 1 ч. до 30 состав должен иметь
pH 4,85 на стеклянном электроде. Предлагаемая
концентрация равна 28,5% активных ингредиентов.
Пример 9. Свечи (вставки) для применения с презервативами или без них, ч.:
CCoп
(из примера 8) - 526
PEG -32 - 4000
PEG -20 - 1000
Повидон - 74
Вышеуказанное перемешивали до раствора при 45oC и вводили под давлением в пресс-формы,
охлаждали и извлекали для упаковки.
Пример 10. Противозачаточная губка (CCoп из примера 8) - 3,5 г.
Добавляли в каждую пресс-форму для отверждения уретана. Загрузку в пресс-форме связывали с полиэфирной петлей для удаления губки после полового акта.
Пример 11. Гели, кремы или желе для разрушения сперматозоидов, применяемые с презервативами, с
цервикальными противозачаточными колпачками,
диафрагмами или без них до полового акта, ч.:
Гель - 1 CCoп (из примера 8) - 7,0
Желатин A200 - 1,5
Глицерин - 10,0
Оксиэтилцеллюлоза (высокая степень вязкости) - 0,
4
Вода - 31,1
Гель-2. Как вышеуказанный, с заменой: 1,0 часть ноноксинола-9 вместо 3,5 частей CCoп (из примера 8).
Процедура - желатин и целлюлозную смолу растирают в глицерине и добавляют в воду при 45oC и перемешивают до получения раствора. В сосуд добавляют поверхностно-активные вещества и теплый раствор удаляют для упаковки. При охлаждении образуется однородный текучий высоковязкий гель.
Желе 1 и 2.
Прозрачные текучие противозачаточные желе готовят при замене желатина и оксиэтилцеллюлозы из вышеуказанных примеров на 1,5 ч. высоковязкой оксипропил- или оксипропилметил-целлюлозы.
Кремы 1 и 2.
Вышеуказанные композиции геля были превращены в крем путем введения 0,5 ч. цетилового спирта в геле (или путем растворения спирта в глицерине при 49oC до растирания желатинирующей и целлюлозной смол.
Пример 12. Противозачаточная пленка.
6,2 фунта желатина типа A100 растирают с 0,5 фунта оксиэтилцеллюлозы. Добавляют 31 фунт глицерина. Раствор тщательно смешивают для образования суспензии. Добавляют 33 фунта CCoп из примера 8 и 15 фунтов воды. Греют при 40oC. Смешивают до полной гидратации смол и желатина. Раствор выливают на лист полиэтилена для отливки пленки толщиной примерно 3 мм, которая должна разрезаться на пленки, предназначенные для применения в качестве противозачаточных пленок после охлаждения.
Реферат
Изобретение относится к медицине. Предложено в качестве средства для ингибирования вируса, находящегося в оболочке, и в качестве противозачаточного средства применять смесь высший алкил N-ди(низший алкил)бетаина и высший алкил N,N-ди(низший алкил)аминооксида, где высший алкил имеет C10 - C18 при молярном соотношении 1:5 - 5:1, а также кислоты для установления pH 4 - 8. В предложенной композиции инактивируют вирусы и бактерии при низкой активности по разрушению клеток. 2 с.п. ф-лы, 8 ил., 3 табл.


Комментарии