Производные 2-арилпропиловых эфиров - RU2045511C1
Код документа: RU2045511C1
Чертежи












































Описание
Изобретение относится к новым соединениям, выбранным из группы, состоящей из
производных 2-арилпропилэфира и производных тиоэфира, которые
представляются общей формулой I
Ar-

R метил или этилгруппа, Y атом кислорода или серы,
В группа формулы




R1 атом водорода или галогена, низший алкил, низшая алкоксигруппа.
Изобретение иллюстрируется следующим образом.
Примеры получения активных веществ, примеры приготовления композиций и их биологическое действие.
Пример синтеза 1 (А способ этерификации).
Получение 3-(4-метоксифенокси)бензил-2-(4-метиленфенил)-2-метилпропилово- го эфира.
К 20 мл сухого ацетонитрила добавляют 0,90 г гидрида натрия (60% в масле), и к смеси по каплям добавляют раствор 2,5 г 2-(4-метилфенил)-2-метилпропилового спирта в 10 мл ацетонитрила при 50оС.
Эту смесь кипятят с обратным холодильником в течение 30 мин и к реакционной смеси в течение 10 мин по каплям добавляют раствор 5,3 г 3-(4-метоксифенокси)бензилбромида. Смесь дополнительно кипятят с обратным холодильником в течение 1 ч, смесь охлаждают до комнатной температуры, выливают ее в воду и экстрагируют смесь толуолом. Толуольный экстракт промывают насыщенным водным раствором хлористого натрия и высушивают над сульфатом натрия и выпаривают при пониженном давлении, полученный неочищенный эфир очищают на хроматографической колонке со 150 г силикагеля (в качестве элюента применяют смешанный растворитель (1:1) из толуола и н-гексана), получая 3,4 г целевого эфира (выход 50% из теории).
nD201,5750: Dмакс см-1 (в пленке): 1590, 1510, 1490, 1245, 1215, 1105, 1040, 815.
δ ССl4, млн.д. 1,30 (с, 6Н), 2,28 (с, 3Н), 3,35 (с, 2Н), 3,75 (с, 3Н), 4,38 (с, 2Н), 6,7-7,3 (м, 12Н), где с синглет, м
мультиплет
Вычислено, C 79,75; H 7,50.
C25 H28O3.
Найдено, C 79,99; H 7,48.
Пример синтеза 2 (Б способ этерификации).
Получение 3-(4-фторфенокси)бензил-2-(3, 4-дихлорфенил)-2-метилпропилового эфира.
К 20 мл толуола добавляют 0,63 г гидрида натрия (60% в масле) и смесь кипятят с обратным холодильником, к этой смеси в течение 15 мин по каплям добавляют раствор 2,3 г 2-(3,4-дихлорфенил)-2-метилпропилового спирта в 10 мл 25% диметилформамида в толуоле. Смесь перемешивают в течение 15 мин и добавляют к ней в течение 20 мин по каплям раствор 3,5 г бромистого 3-(4-фторфенокси)бензила в 10 мл толоула. Затем смесь кипятят в течение 1 ч с обратным холодильником и охлаждают до комнатной температуры и выливают в воду. Органический слой отделяют, промывают водой и высушивают над сульфатом натрия и выпаривают при пониженном давлении, полученный неочищенный эфир очищают на хроматографической колонке со 100 г силикагеля (в качестве элюента применяют смешанный растворитель (1:1) из толуола и н-гексана), получая 3,1 г целевого эфира (выход составил 74% от теории).
nD20 1,5732; Dмакс , см-1 (в пленке): 1590, 1505, 1490, 1265, 1205, 1100, 1035, 695.
δ ССl4, м.д. 1,30 (с, 6Н), 3,34 (с, 2Н), 4,38 (с, 2Н), 5,7-7,4 (м, 11Н).
Вычислено, С 69,09; Н 5,29; Cl 8,87; F 4,75.
C23H21Cl2FO2.
Найдено, С 68,88; Н 5,34; Cl 8,75; F 4,57.
Пример синтеза 3 (В способ этерификации).
Получение 3-(4-метилфенокси)бензил-2-(4-хлорфенил)-2-метилпропилового эфира.
К 15 мл 50% -ного водного раствора NaOH добавляют 6,0 г 2-(4-хлорфенил)-2-метилпропилового спирта, 8,1 г 3-(4-метилфенокси)-бензилхлорида и 1,1 г бромистого тетрабутиламмония и смесь перемешивают 1 ч при 80оС. Смесь охлаждают до комнатной температуры и добавляют воду, смесь экстрагируют толуолом, толуоловый экстракт промывают водой и высушивают над сульфатом натрия, выпаривают при пониженном давлении, полученный неочищенный эфир очищают на хроматографической колонке с 250 г силикагеля (в качестве элюента используют смешанный растворитель (1: 1) толуол н-гексан), получая 9,9 г целевого эфира (выход составляет 80% от теоретического).
nD20 1,5741; Dмакс, см-1 (в пленке): 1595, 1510, 1455, 1260, 1215, 1110, 1015, 830, 695.
δ ССl4, м. д. 1,29 (с, 6Н), 2,31 (с, 3Н), 3,32 (с, 2Н), 4,35 (с, 2Н), 6,7-7,3 (м, 12Н).
Вычислено, С 75,68; Н 6,61; Cl 9,31.
C24 H25ClO2.
Найдено, C 75,85; H 6,42; Cl 9,22.
Пример синтеза 4 (Г способ этерификации).
Получение 3-(4-фторфенокси)бензил-2-(4-фторфенил)-2-метилбутилового эфира.
К 20 мл толуола добавляют 2 мл концентрированной серной кислоты, 2,7 г 3-(4-фторфенокси)бензилового спирта и 2,3 г 2-(4-фторфенил)-2-метилбутилового спирта, смесь кипятят в течение 6 ч с обратным холодильником (образовавшуюся в реакции воду удаляют). Смесь охлаждают до комнатной температуры и к смеси добавляют воду, отделяют толуольный слой, промывают водой, высушивают и выпаривают при пониженном давлении. Полученный неочищенный эфир очищают на хроматографической колонке со 100 г силикагеля (в качестве элюента используют смешанный растворитель (1:1) толуол, н-гексан), получая 2,2 г целевого эфира (выход составляет 46% от теоретического).
nD20 1,5478.
Dмакс, см-1 (в пленке): 1585, 1505, 1230, 1195, 1165; 1110, 830, 780, 690.
δ CCl4, м.д. 0,65 т*) (т триплет). J 7,5 Гц (3Н), 1,28 (с, 3Н), 1,5-1,9 (м, 2Н), 3,37 (с, 2Н), 4,35 (с, 2Н), 6,7-7,3 (м, 12Н).
Вычислено, С 75,37; Н 6,32; F 9,94.
С24Н24F2O2.
Найдено, C 75,54; H 6,21; F 10,01.
Пример синтеза С (Д способ этерификации).
Получение 3-феноксибензил-2-(4-дифторметоксифенил)-2-метилпропилового эфира.
Перемешивают при 50оС в течение 2 ч 2,0 г 2/4-дифторметоксифенил-2-метилпропилового спирта, 2,0 г м-феноксибензилхлорида, 20 г 50%-ного NaOH и 0,3 г триэтилбензил аммоний бромида. Затем в реакционную смесь добавляют воду и бензол, смесь тщательно перемешивают, бензольный слой отделяют, промывают водой, сушат над сульфатом натрия и выпаривают при пониженном давлении. Полученный неочищенный эфир очищают на хроматографической колонке со 130 г силикагеля (в качестве элюента используют смешанный растворителя (2:3) толуол гексан), получая 3,0 г целевого эфира (выход составляет 81% от теоретического).
nD20,5 1,5490.
Dмакс. см-1 (пленка): 1580, 1485, 1380, 1250, 1215, 1130, 1040, 690.
δ ССl4, м. д. 1,32 (с, 6Н), 3,36 (с, 2Н), 4,21 (с, 2Н), 6,38 (с, 1Н, J 7,5 Гц), 6,8-7,4 (м, 13Н).
Пример синтеза 6.
Получение 3-(4-бромфенокси)бензил-2-(4-фторфенил)-2-этилпропилового эфира.
К 20 мл толуола добавляют 060 г гидрида натрия (60% в масле) и смесь кипятят с обратным холодильником, к этой смеси в течение 20 мин по каплям добавляют раствор 2,0 г 2-(4-фторфенил)-2-метилбутилового спирта в 10 мл 40% диметилформамида в толуоле. Смесь перемешивают в течение 10 мин и добавляют к смеси по каплям в течение 10 мин раствор 4,0 г 3-(4-бромфенокси)-бензилбромида и 10 мл толуола. Смесь дополнительно нагревают и кипятят с обратным холодильником в течение 1 ч, охлаждают до комнатной температуры и выливают в воду. Отделяют толуольный слой, промывают водой, высушивают над сульфатом натрия, выпаривают при пониженном давлении и полученный сырой эфир очищают на хроматографической колонке со 100 г силикагеля (в качестве элюента используют смешанный растворитель (1:1) толуол гексан), получая 3,7 г целевого эфира.
nD20,2 1,5778.
νмакс. см-1 (пленка): 16,05, 1580, 1510, 1485, 1250, 1165, 1100, 1070, 1010, 830.
δ CCl4, м.д. 0,67 (т, 3Н, J 7,2 Гц), 1,30 (с, 3Н), 1,5-1,9 (м, 2Н), 3,39 (с, 2Н), 4,39 (с, 2Н), 6,7-7,5 (м, 12Н).
Пример синтеза 7.
3-Феноксибензил 2-(3,4-метилендиоксифенил)-2-метилпропиловый эфир синтезируют по методике, описанной в примере синтеза 2, применяя 0,4 2-(3,4-метилендиоксифенил)-2-метилпропиловый спирт.
nD20,7 1,5839.
Dмакс. см-1 (пленка): 1590, 1490, 1255, 1105, 1045, 940.
δ CCl4, м. д. 1,28 (с, 6Н), 3,32 (с, 2Н), 4,41 (с, 2Н), 5,82 (с, 2Н), 6,5-7,4 (м, 12Н).
Пример синтеза 8 (Е способ этерификации).
Получение 3-(4-метоксифенокси)бензил-2-(3,4-дихлорфенил)-2-метилпропилового эфира.
Смесь 9, 98 г хлористого 3,4-дихлорнеофила, 9,67 г 4-метоксифеноксибензилового спирта, 3,9 г 45% гидроокиси натрия и 48 г диметилсульфоксида нагревают и перемешивают при 140оС в течение 3 ч, дополнительно добавляют 1,8 г (45% ) гидроокиси натрия, выдерживают при той же температуре в течение 4 ч, выливают в воду и экстрагируют бензолом. Бензольный экстракт промывают водой, высушивают над сульфатом натрия, выпаривают при пониженном давлении и полученный сырой эфир очищают на хроматографической колонке с 250 г силикагеля (в качестве элюента променяют смешанный растворитель (1:1) толуол н-гексан), получая 3,34 г целевого эфира (выход составляет 78% от теоретического, в расчете на превращенный хлористый 3,4-дихлорнеофил).
nD201,5830.
Dмакс. см-1 (пленка): 1590, 1510, 1490, 1250, 1220, 1110, 1040, 840.
δ CCl4, м. д. 1,30 (с, 6Н), 3,34 (с, 2Н), 3,76 (с, 3Н), 4,38 (с, 2Н), 6,7-7,5 (м, 11Н).
Пример синтеза 9.
Получение 3-фенолксибензил-2-(4-формилфенил)-2-метилпропилового эфира.
К 30 мл сухого диэтилового эфира добавляют 0,70 г литий-алюминий гидрида, и к этой смеси по каплям добавляют за 15 мин при 0оС 1,63 г этилацетата. Смесь выдерживают в течение 30 мин при 0оС. Затем к этой смеси по каплям добавляют раствор 6,0 г 3-феноксибензил 2-(4-цианфенил)-2-метилпропилового эфира в 10 мл сухого эфира, и полученную смесь перемешивают в течение 1 ч при 0оС. Затем к смеси добавляют 20 мл 4 н. серной кислоты, и образовавшуюся смесь перемешивают в течение 30 мин. Отделяют эфирный слой, промывают его водой, высушивают над сульфатом натрия и выпаривают. Затем 6,4 г остатка очищают на хроматографической колонке со 130 г силикагеля (в качестве элюента используют бензол), получая 2,9 г исходного 3-феноксибензил 2-(4-цианофенил)-2-метилпропилового эфира и 2,3 г целевого 3-феноксибен- зил-2-(4-формилфенил)-2-метилпропилового эфира.
nD20 1,5858.
νмакс., см-1 (пленка): 1720, 1615, 1590, 1500, 1260, 1225, 1105, 835, 700.
δ CCl4 (от ТМС), м.д. 1,37 (с, 6Н), 3,40 (с, 2Н), 4,37 (с, 2Н), 6,7-7,7 (м, 13Н), 9,82 (с, 1Н).
Пример синтеза 10.
3-Феноксибензил 2-(4-этоксиметоксифенил)-2-метилпропиловый эфир синтезирован по следующей методике.
В 20 мл влажного хлороформа растворяют 1,2 г 3-феноксибензил 2-(4-формилфенил)-2-метилпропилового эфира, 0,70 г м-хлорбензойной кислоты добавляют к раствору, смесь выдерживают 4 сут при комнатной температуре. Образовавшийся осадок удаляют, фильтрацией, и хлороформовый слой промывают разбавленной щелочью, затем водой, высушивают над сульфатом натрия и выпаривают при пониженном давлении, получая 1,0 г целевого эфира. Затем 1,0 г эфира растворяют в 30 мл 50%-ного раствора КОН в метаноле,0 и раствор нагревают в течение 3 ч при 50оС, чтобы вызвать гидролиз.
Метанол удаляется перегонкой при пониженном давлении, к остатку добавляют воду и бензол; значение рН смеси понижают ниже 4, добавляя концентрированную хлористоводородную кислоту, смесь перемешивают. Смесь еще выдерживают, отделяют бензольный слой, промывают водой, высушивают над сульфатом натрия и выпаривают при пониженном давлении, получая 0,90 г неочищенного эфира. Сырой эфир очищают на хроматографической колонке с 20 г силикагеля (в качестве элюента используют смешанный растворитель (20:1) бензол-диэтиловый эфир), получая 0,60 г 3-феноксибензил 2-(4-оксифенил)-2-метилпропилового эфира.
δ CCl4 (от ТМС), м.д. 1, 26 (с, 6Н), 3,33 (с, 2Н), 4,34 (с, 2Н), 5,76 (с, 1Н), 6,4-7,4 (м, 13Н).
К 50 мл сухого тетрагидрофурана добавляют 1,0 г гидрида натрия (60% в масле) и затем к этой смеси при кипячении с обратным холодильником по каплям за 30 мин добавляют 5,0 г 3-феноксибензил 2-(4-оксифенил)-2-метилпропилового эфира в 15 мл сухого тетрагидрофурана. Смесь дополнительно кипятят в течение 10 мин и к смеси в течение 30 мин по каплям добавляют 5,0 мл этилхлорметилового эфира. Полученную смесь дополнительно кипятят с обратным холодильником в течение 10 мин, охлаждают до комнатной температуры, выливают в воду и экстрагируют бензолом. Бензольный экстракт промывают водой, высушивают над сульфатом натрия и выпаривают, получая маслянистый остаток, который после очистки на хроматографической колонке со 150 г силикагеля в качестве элюента используют смешанный растворитель (20:1) бензол и диэтиловый эфир, дает 5,0 г 3-феноксибензил 2-(4-этоксиметоксифенил)-2-метилпропилового эфира.
nD20 1,5330.
νмакс. см-1 (пленка), 1580, 1510, 1485, 1230, 1225, 1215, 1105, 1080, 1005, 830, 685.
δ CCl4 (от ТМС), м.д. 1,20 (т. 3Н, J 7,2 Гц), 1,30 (с, 6Н), 3,33 (с, 2Н), 3,65 (к, где К квадруплет, 2Н, J 7,2 Гц), 4,38 (с, 2Н), 5,08 (с, 2Н), 6,5-7,4 (м, 13Н).
Пример синтеза 11.
3-Феноксибензил 2-(4-карбэтоксифенил)-2-метилпропиловый эфир синтезируют по следующей методике.
Смесь 3,5 г 3-феноксибензил 2-(4-цианофенил)-2-метилпропилового эфира, 7,0 г гидроокиси калия, 7,0 г воды и 20 мл этиленгликоля перемешивают при 130оС в течение 4 ч. Смесь охлаждают до комнатной температуры, добавляют в нее воду и подкисляют, добавляя хлористоводородную кислоту. Затем смесь экстрагируют эфиром, и эфирный экстракт промывают водой, высушивают над сульфатом натрия и выпаривают, получая 3,1 г 3-феноксибензил-2-(карбоксифенил)-2-метилпропилового эфира, т.пл. 98,5-102,5оС.
Смесь 1,0 г 3-феноксибензил-2-(4-карбоксифенил)-2-метилпропилового эфира, 0,6 г пятихлористого фосфора и 15 мл бензола нагревают при 70-80оС в течение 30 мин, и растворитель удаляют перегонкой при пониженном давлении. Полученный неочищенный хлорангидрид кислоты растворяют в 10 мл бензола, и этот раствор по каплям добавляют к смешанному раствору 5 мл этанола, 1 мл пиридина и 30 мл бензола, при комнатной температуре. Смесь выдерживают в течение 30 мин, промывают водой, высушивают над сульфатом натрия, и выпаривают при пониженном давлении, получая 1,3 г неочищенного эфира. Полученный неочищенный эфир очищают на хроматографической колонке с 40 г силикагеля (в качестве элюента используют бензол), получая 0,9 г 3-феноксибензил-2-(4-карбэтоксифенил)-2-метилпропиловый эфир.
Dмакс. см-1 (пленка): 1735, 1620, 1595, 1500, 1380, 1285, 1260, 1225, 1120.
δ CCl4 (от ТМС), м.д. 1,24-1,47 (м, 9Н), 3,38 (с, 2Н), 4, 15-4,41 (м, 4Н), 6,7-8,0 (м, 13Н).
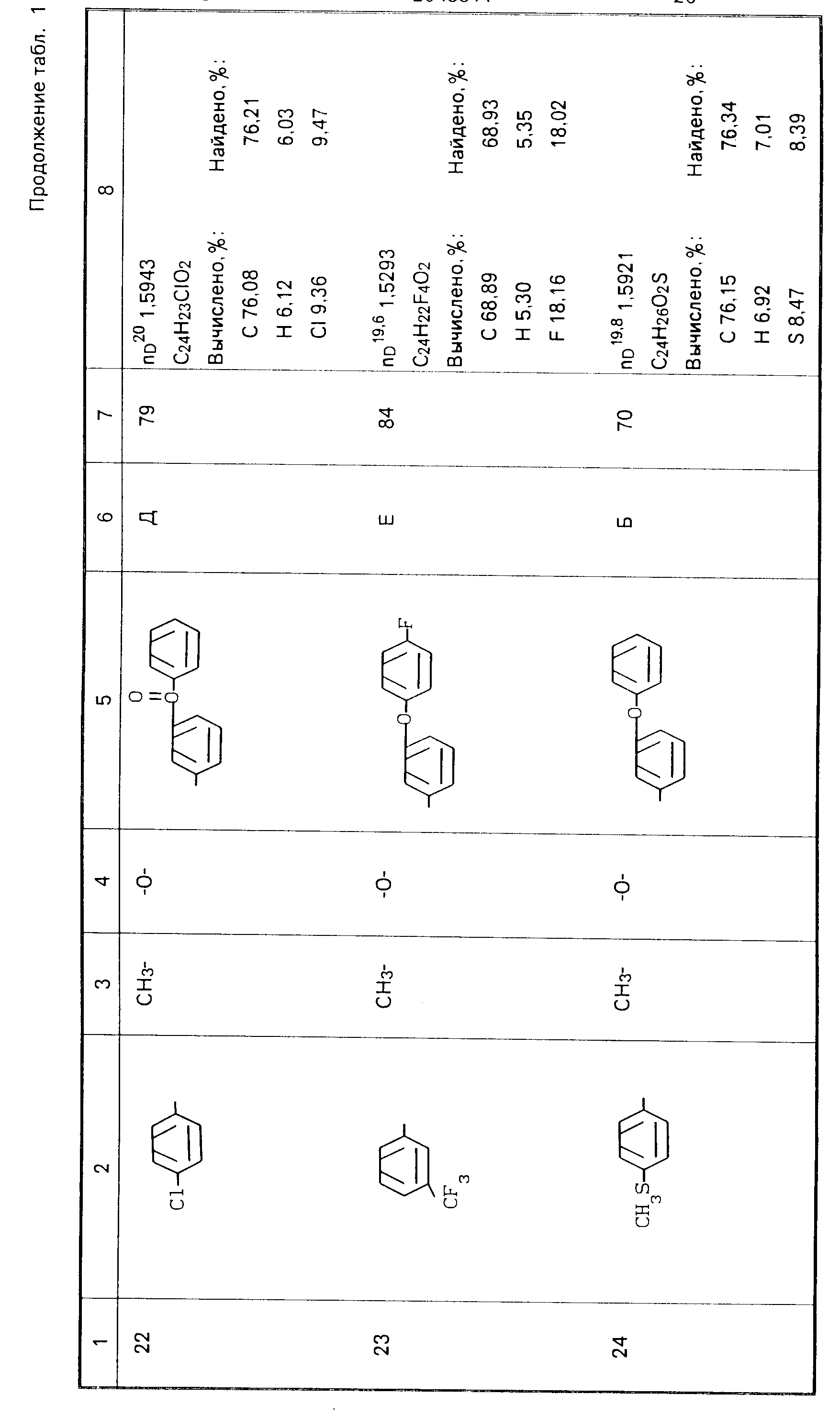
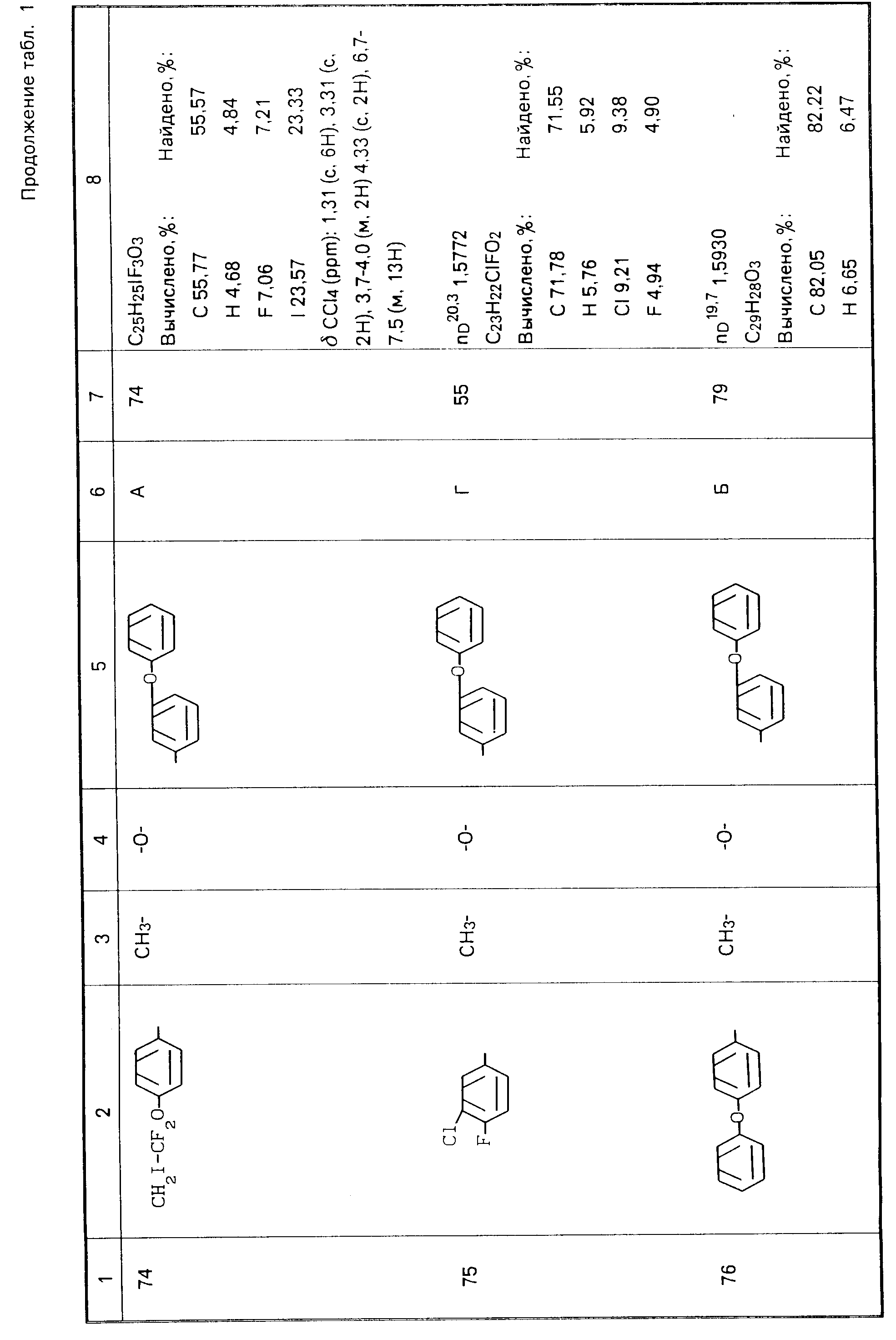
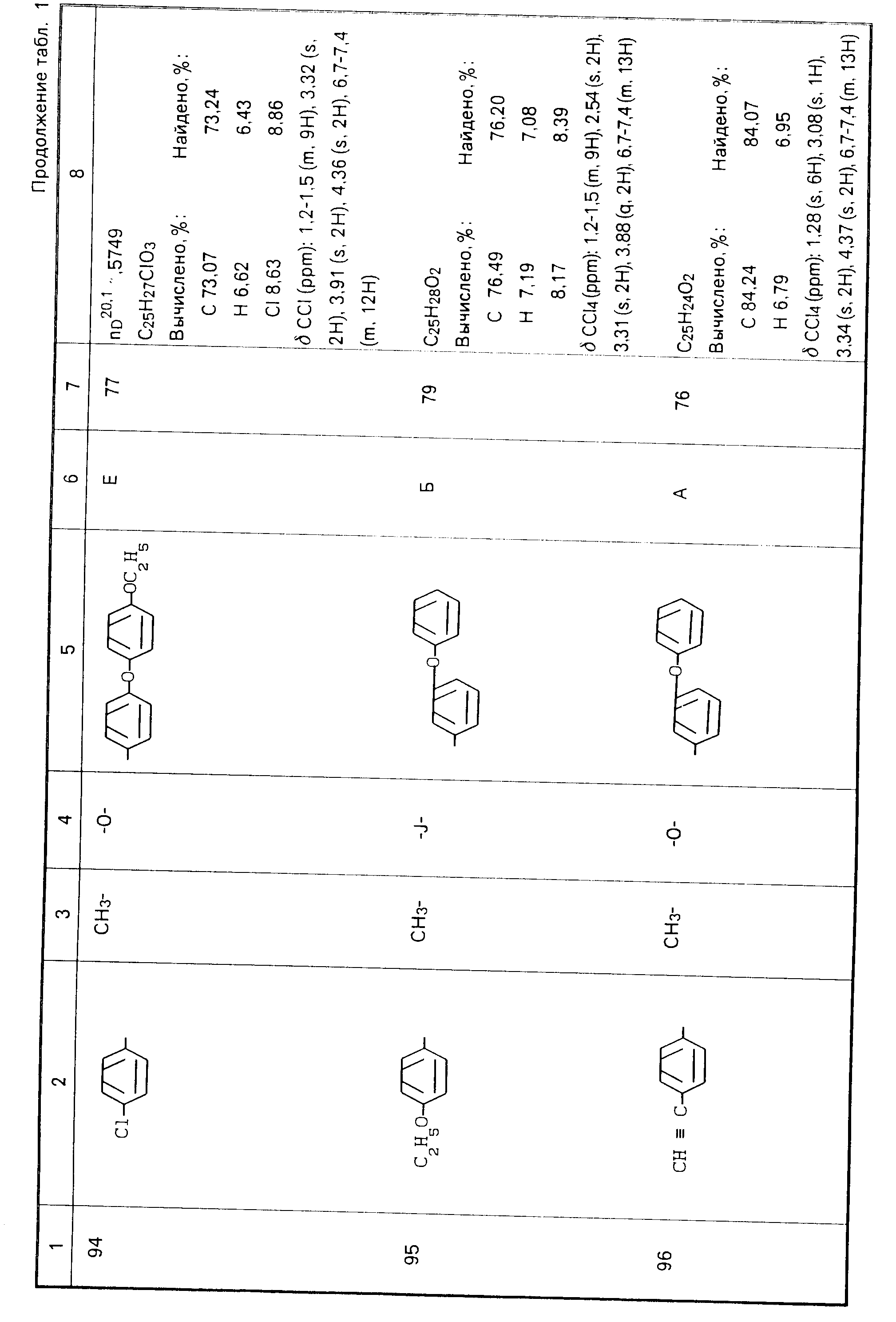
Используемые в композициях активные вещества, полученные по методикам, аналогичным указанным примерам представлены в табл. 1.
Пример композиции 1.
Раствор, образованный смешением 0,4 части соединения настоящего изобретения и 2,0 частей пиперонилбутоксида с 6 частями ксилола и 7,6 частями дезодорированного керосина поместили в аэрозольный баллон и через клапанную часть под давлением ввели 84 части диспергатора (сжиженный нефтяной газ) и получили аэрозоль (А).
Пример композиции 2.
Аэрозоли получили аналогично примеру композиции 1. Данные приведены в табл. 2.
Пример композиции 3.
Аэрозоли получили аналогично примеру композиции 1. Данные приведены в табл. 3.
Пример композиции 4.
Аэрозоли получали аналогично примеру композиции 1. Данные приведены в табл. 4.
Тест 1.
10 женских особой взрослых мух комнатных посадили свободно в чашку Петри (диаметр 9 см, высота 5 см) и затем чашку накрыли металлической сеткой (меш 16). На стеклянную пластину (25х25х0,5 см) поместили стеклянный цилиндр (диаметр 20 см, высота 43 см). Указанную чашку установили вниз стеклянного цилиндра и на этот стеклянный цилиндр поместили стеклянную пластину с отверстием (диаметр 1 см), в середине для покрытия. Аэрозоль, приготовленный по способу, описанному в примере композиции 1, вносили в течение 5 с в каждом случае соединений. После закрытия отверстия аэрозоль не вносился. Через 10 мин упавшие мухи перенесли в полиэтиленовую чашку (диаметр 10 см, высота 5 см). Кусок ваты пропитали 5%-ным водным раствором сахара и питали им мух в чашке. Данную полиэтиленовую чашку закрыли. Через 2 сут подсчитали число погибших и живых мух и вычислили смертность. Полученный результат приведен в табл. 5.
Тест 2.
Все аэрозоли, полученные по способу, описанному в примере композиции 2, провели аналогично тесту 1. Полученный результат показан в табл. 6.
Тест 3.
Все аэрозоли, полученные по способу, описанному в примере композиции 3, проверили аналогично тесту 1. Полученный результат приведен в табл. 7.
Тест 4.
Все аэрозоли, полученные по способу, описанному в примере композиции 4, проверили аналогично тесту 1. Полученный результат приведен в табл. 5.
Реферат
Использование: в сельском хозяйстве, в частности в пестицидах. Сущность изобретения: производные 2-арилпропиловые эфиры ф-лы: Ar-Cr(CH3)-CH2-Y-CH2-B , где Ar фенил не- или замещенный алкилом, алкоксилом, алкилтиогруппой, C5 -C6 -циклоалкилоксигруппой, фенилом, галогеном, алкенилом, галоидалкенилом, галоидалкилом, причем все алкилы низшие. 4 табл.
Формула

где Ar фенил или фенил, замещенный низшей алкилгруппой, низшей алкоксигруппой, низшей алкилтиогруппой, С5 С6 -циклоалкилоксигруппой, фенилом, галогеном, низшим алкенилом, галонизшим алкенилокси, галонизшим алкилом, галонизшим алкокси, низшим алкоксиалкилом, низшим алкенилоксирадикалом, низшим алкинилокси, низшим алкоксиалкилокси, низшим ацилом, низшим алкоксикарбонилом, нитрилом, нитро, фенокси, галонизшим алкоксикарбонилом, метилендиоксигруппой, или незамещенным нафтил или нафтил, замещенный низшим алкилом;
R метил или этилгруппа;
Y кислород или сера;
B группа формулы

или общей формулы

где Z кислород, или сера, или карбонил, или метиленовая группа;
R1 водород или галоген, низший алкил, низшая алкоксигруппа.
02.05.80 Ar фенил, одно- или двузамещенный галогеном, алкилом, содержащим 1,3 или 4 ат. С; Y кислород;

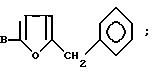

где R1 галоген, низший алкил, низшая алкоксигруппа; R метил, этил.

Комментарии