Способ получения производных бензоилмочевины - SU1402254A3
Код документа: SU1402254A3
Описание
см
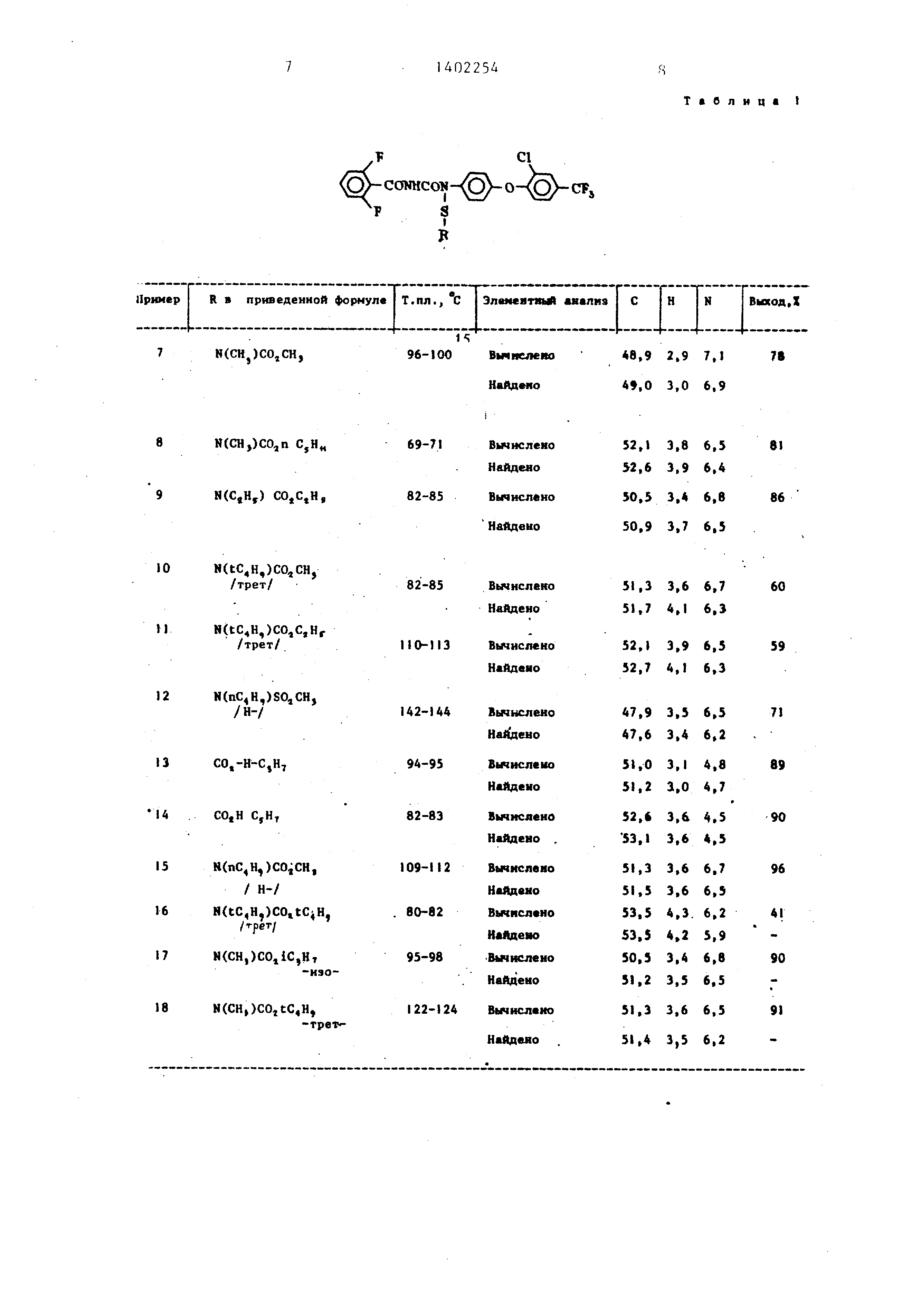
Изобретение относится к способу получения новых производных бензоил- мочевины общей формулы
А-соотсо
I
S К
(
где Y - галоид-низший алкил; Z,A и В - галоид;
R - , ; CO,R,, SOjR,; ; SO NRj-Rg, где R,- Rg- Низший алкил.
Указанные соединения проявляют инсектоакарицидную активность.
Цель изобретения - изыскание новых производных бензоилмочевины, которые по сравнению с известными обладают более высокой активностью.
Пример 1. Получение пропило- вого эфира К-///4-/2-хлор-4-/трифто.р метил/фенокси/фенил/ /амино-тио/-Ы- метилкарбаминовой кислоты.
Раствор пропилового эфира N-хлор- сульфенил-И-метилкарбаминовой кислоты (3,7 г) в сухом хлористом метилене (10 мл) добавляют в течение 20 мин в перемешиваемый раствор 6,3 г 4-/3-хлор-4-/трифторметил/фе- нокси/анилина в том же самом растворителе (25 мл), содержащем 2,5 г триэтиламина. Температуру реакции поддерживают О - 5 С с помощью ледяной бани до тех пор, пока не завершися добавление, и затем дают смеси нагреться до комнатной температуры в течение 2 ч. Растворитель удаляют при пониженном давлении, и остаток суспендируют в 200 мл диэтилового эфира и промьюают три раза водой. Образовавшийся эфирный раствор высушивают над сульфатом магния и вьта- ривают, получая неочищенный продукт который очищают методом экспресс-хрматографии на силикагеле, используя в качестве элюента хлористый метиле После кристаллизации из смеси диэтилового эфира и легкого углеводорда получают чистый продукт в виде светлых, тускло-желтых кристаллов (7,1 г), плавящихся при 61-64 с.
Элементный анализ:
Вычислено,%: С 49,7; Н 4,6; N 6,
Найдено,%: С 49,4; Н 4,2; N 6,3.
0
5
0
30
35
40
45
Приме р 2, Получение N-///4- /2-хлор-4-/трифторметип/-фенокси/фенил /амино/тио/-М-э тилметансульфонами- да.
Раствор 2,6 г двуххлористой серы в 15 мл безводного диэтилового эфира добавляют в течение 10 мин к перемешиваемому раствору N-этилметансуль- фонамида (3,1 г) в 15 мл того же растворителя, поддерживая 10-15 С с помощью внешнего охлаждения. Затем добавляют раствор безводного пиридина (2,0 г) в безводном диэтиловом эфире (13 мл) в течение 15 мин при той же температуре, и реакционной смеси дают нагреться до комнатной температуры в течение 1 ч. Образовавшуюся суспензию переносят в капельную воронку и добавляют ее в течение 5 мин в раствор 7,2 г/4-/2-хлор-4-/трифтор- метил/фенокси/анилина в 75 мл безводного диэтилового эфира, содержащего 2,0 г пиридина, поддерживая темпера- 5 туру 5 - 10°С. После перемешивания при 10-15°С в течение 1 ч реакцион-- ную смесь промывают 3 раза водой, отделяют эфирный слой и высушивают .. его над сульфатом магния. При выпаривании высушенного раствора при пониженном давлении получают неочищен-, ный продукт, который очищают хрома- тографически на силикагеле, используя в качестве элюента диэтиловый эфир. Полученный таким образом чистьй продукт в виде тускло-желтого твердого вещества (6,9 г) плавится при 98-101 с.
Элементный анализ:
Вычислено,%: С 43,6; Н 3,6; N 6,4.
Пайдено,%: С 43,8; Н 3,8; N 6,2.
П р и м е р 3. Получение 0-метил- 3-//4-2-хлор-4-трифторметил/фенокси/ /фенил/амино/тиокарбоната.
Раствор 4,2 г метоксикарбонилсуль- фенилхлорида в 5 мл безводного хлористого метилена добавляют в течение 20 мин в перемешиваемый раствор 8,6 г 4-/2-хлор-4-/трифторметил/фенокси/ анилина в том же растворителе (50 мл) содержащем 6,0 мл триэтиламина, поддерживая температуру ниже 0°С. После завершения добавления перемешиваемой реакционной смеси дают нагреться до комнатной температуры в течение 1 ч. Затем растворитель удаляют при пони- ; женном давлении, остаток суспендируют в Г80 мл диэтилового эфира и промывают водой. При выпаривании
50
55
31
высушенного экстракта получают 11,5 коричневого масла, которое очищают хроматографически на силикагеле, используя в качестве элюента смесь ди- этилового и петролейного эфиров. При перекристаллизации из того же растворителя получают 7,0 г целевого продукта в виде бесцветньпс кристаллов , т.пл.71-72°С.
Элементный анализ:
Вычислено,%: С 47,7; Н 2,9; N 3,7
Найдено,%: С 48,2; Н 3,0; N 3,8.
П р и м е р 4. Получение пропило- вого эфира 4-/4-/2-хлор-4-/трифторме тил/фенокси/фенил/-7-/2,6-дифторфе- нил/-2-метил-5,7-диоксо-3-тиа-2,4, 6-тиазагептановой кислоты.
При перемешивании добавляют раст
перекристаллизации этого материала из смеси диэтшювого эфира и нефтяной фракции получают чистый продукт в виде бесцветных крист яллов (5,8 г) плавящихся при 149-151 С.
Элементный анализ:
Вычислено,%: С 46,2; 1 3,1; N 6,7.
Найдено,%: С 46,7; Н 3,0; N 6,7.
П р и м е р 6. Получение метилового эфира 3-/4-/2-хлор-4-/трифтор- метил/фенокси/фенил/-6-/2,6-дифтор- фенил/-4,6-диоксо-2-тиа-3,5-диаза- гексановой кислоты.
Раствор 2,0 г 2,6-дифторбензоил - изоцианата в безводном толуоле (10 мл) добавляют к перемешиваемому раствору 3,8 г 0-метил-5-//4-/2- хлор-4-/трифторметил/фенокси/фенил/





Реферат
Изобретение касается производных мочевины, в частности способа получения производных бензоилмочевины ДМ1 общей формулы СА СН-СН СН-СВ . -C(0)NHC(0)N(SR)-t CH-CH CX-CH CH, где А и В - галоид, R - C(0)OR, или NRjRj при RI и RI- низший алкил, Rj-C(0)OR или S(0)5R при R - низший алкил или S(0)NRjRg при R у 1 X - О-б - низший алкил; CZ, СН - СИ где Y - галоид-низший алкил; Z - галоид , проявляющих инсектоакарицидную активность, что может быть и пользо- вано в сельском хозяйстве. Цель - создание новых более активных веществ указанного класса. Синтез БМ ведут реакцией соединения формулы NH(SR) - С СН -СН СХ-СН СН и изоцианата формулы СА СН-СН СН -СВ

Формула


Комментарии