Транспортабельный контейнер закрытой системы для хранения биологического материала - RU2079273C1
Код документа: RU2079273C1
Чертежи

Описание
Изобретение касается контейнера для консервации живых биологических тканей и живого клеточного материала и способа хранения таких материалов.
Нарушение метаболических функций ткани млекопетающих может произойти в результате заболеваний, врожденного порока, естественных причин и т.п. Возможность хирургического удаления патологической или биологически погибшей ткани и последующей замены удаленной ткани тканью от донора, известна в медицине давно. Известны также различные способы переливания цельной человеческой крови, взятой у добровольных доноров для реципиентов, кровоснабжение которых естественным или искусственным образом истощено в результате травмы от несчастного случая или заболевания.
Биологические ткани, включающие органы и цельную кровь или ее отдельные компоненты фракции, а далее именуемые биологический материал, не могут жить вне их естественной среды без хранения или консервации.
Биологический распад удаленного биологического материала в ожидании имплантации или введения в реципиента начинается после его попадания в новые среды с меняющимися концентрациями знакомых и незнакомых газов и жидкостей. В попытке сделать такой распад минимальным из-за изменения тонкого метаболического баланса биологического материала было предложено много теорий. Однако ни одна из существующих технологий по этим теориям консервации не давала удовлетворительного решения проблемы долгосрочной консервации биологического материала. Под долгосрочным хранением или консервацией в этой области следует понимать сохранение 1) живой биологической ткани и 2) цельной крови без осуществленного биоразложения или другой потери их естественных функциональных способностей в течение периода времени не менее чем 10 дней и 60 дней соответственно.
В ранних попытках сохранить вырезанную ткань использовалась некоторая форма криогенной обработки, в результате чего биологический материал или орган замораживался, затем оттаивался. Проблемы образования кристаллов и молекулярного расширения, вызывающего разрыв клеток, побудили исследователей сначала откачивать из ткани ее естественные жидкости и заменять их плазмоподобным перфузатом, который выполнял бы функцию антифриза в органе или ткани. Однако возникли существенные проблемы с перфузатом. Многие перфузаты вызывали аллергические реакции у реципиента и часто проводили к отторжению ткани органа иммунной системой реципиента.
Частая необходимость транспортировать биологический материал в консервированной форме привела к дальнейшим осложнениям. Реципиенты, которые сами часто бывают в ослабленном состоянии, вынуждены поспешно отправляться на место, где был вырезан орган, или, как обычно, биологический материал вынуждены отправлять к месту нахождения реципиента.
Существуют портативные устройства транспортировки биологического материала, которые поддерживают метаболическую функцию в транспортировке либо замораживанием органа /ткани, т.е. доведение температуры органа /ткани до 0oC, либо пропусканием имитированной плазмы или перфузата через орган, часто при низкой температуре, но выше точки замерзания. Эти методы транспортировки были довольно успешны. Однако время, необходимое с момента вырезания до трансплантации, остается очень небольшим, обычно орган можно искусственно сохранить ex vivo только 24 72 часа. В результате этого, чтобы получить трансплантат, реципиенты часто вынуждены в срочном порядке переносить утомительные путешествия и нести дополнительные расходы. Во многих случаях из-за отдаленного географического положения потенциальных реципиентов такие операции по трансплантации становятся практически невозможны для многих нуждающихся в таком лечении.
Как указано в патенте США 4473552, существует необходимость консервировать и транспортировать цельную кровь млекопитающих способом, который не требует разрушающей стадии замораживания для такой консервации. Простое охлаждение, которое поддерживает кровь в используемом состоянии только 21 день, также неудовлетворительно. Поэтому существует необходимость подходящего контейнера или опорной системы для сохранения крови при охлажденной температуре в течение срока, превышающего 60 дней.
Известные способы консервации и транспортировки живой биологической ткани требуют либо замораживания ткани после предварительной обработки подходящим перфузатом, чтобы замедлить разрушающие влияния требуемых низких температур, либо непрерывного прокачивания жидкого или газообразного перфузата через день для питания при температурах выше температуры замерзания. Были изобретены различные контейнеры транспортировки для осуществления этих способов консервации ткани.
В патенте США 3810367 описан контейнер, предназначенный для помещения человеческого органа в стерильный физиологический раствор в одно отделение с поддержанием температуры в нем при 0oC с помощью отдельного отделения, содержащего лед. Отделение для органа содержало съемную прокладку, состоящую из материалов, инертных для ткани животных.
В патенте США 4502295 предложена конструкция для хранения гипотермического органа, который снижал метаболическую скорость иссеченных органов поддерживанием окружающей температуры внутри приемников хранения в пределах 0 7o C. Лед раскрывался как охлаждающее средство. Наличие оттока, через который могла стекать растаявшая вода, явилось усовершенствованием в данной области. Еще одно устройство консервации органа, охлаждаемого льдом, было описано в патенте США 4242883. Это устройство также использовало лед для охлаждения контейнера, содержащего орган для трансплантации/печень, а также перфузат, прокачиваемый через орган. В патенте США 4745759 описывают портативную конструкцию для консервации органа, состоящую из термоэлектрической системы охлаждения, предназначенной поддерживать температуру прокачиваемого через орган раствора перфузата при 4oC.
Охлажденные газы также использовались в качестве средства охлаждения в таких устройствах. В патенте США 4471629 предложил использование охлажденного гелия, перфузированного в почку, в то время как орган находился в среде сжатого азота. В этом патенте орган замораживается до температуры между 70 и 140oC. Схема оттаивания предлагается с использованием микроволн. В патенте США 3607646 предлагается использование среды инертного газа, окружающей иссеченный орган в ожидании трансплантации при одновременном снижении количества избыточного кислорода в перфузионной жидкости. При содержании кислорода в перфузионной жидкости более 10% консервации органа ухудшается. В патенте США 4008754 говорится об использовании инертного газа для заполнения консервируемого органа и заморозки органа до температуры ниже -100oC. Как хорошо известно, любое устройство, использующее температуры ниже 0oC, не представляют большой практической ценности для консервации биологического материала, поскольку значительное ухудшение свойств этого материала происходит в результате цикла заморозка/оттаивание.
Настоящее изобретение обладает преимущественном перед устройствами известного уровня и способами сохранения живого биологического материала. Оно применено к консервации органов млекопитающих и других живых биологических тканей, а также и цельной крови или в любому такому компоненту, содержащему или включающему живые клетки. Кроме того, настоящее изобретение использует пневматически работающий микромотор для рециркуляции сжатого воздуха или сжатого инертного охладителя. Это снижает температуру камеры или вогнутой приемной ячейки, содержащей биологический материал, до 1 3oC (или 34 - 37oF), снимая необходимость разработки схемы размораживания, необходимой, если температура достигает или падает ниже точки замерзания. Использование воздуха или рециркулируемого инертного охлаждающего газа предусматривает равномерное охлаждение биологического содержания, устраняя опасность неравных температурных градиентов в консервирующем контейнере. Такая разница температур может повредить консервируемый живой биологический материал. При использовании льда в качестве охлаждающего агента, даже с лучшими термопроводящими материалами для контейнера, существует опасность наличия разницы температур внутри контейнера, что грозит жизнеспособности консервированного биологического материала.
Присутствие и количество кислорода в устройстве четкно контролируется использованием датчика и средством считывания. Предпочтительным консервантом является гидроксиэтиловый крахмал (ГЭК)или любой консервирующий раствор, блокирующий и образующий барьер, окружающий здоровые клетки. Консервант полностью окружает биологический материал и заполняет приемную ячейку, замедляя таким образом лишнее взаимодействие кислорода/биологического материала.
Все устройство транспортабельно. Микромотор питается пневматическими толчками циркулируемого воздуха или инертного газа. Толчки приводятся в движение приборами, питающимися от заряжаемой батарейки. Устройство может использоваться для стационарного хранения и его микромотор снабжается пневматическим давлением от введения дополнительных сжатых инертных газов, таких, как, например, азот, в контейнер через впускные отверстия. Способ использования и работа устройства проста и не влечет больших расходов. Живой биологический материал в этом изобретении можно сохранять при обычных температурах охлаждения в течение продолжительных периодов времени, гораздо дольше, чем по известному уровню. Цельная кровь может храниться неопределенное время, а другая биологическая ткань, включая органы или живые клетки, может сохраняться в трансплантируемом состоянии минимум десять дней. Метаболические процессы в живом биологическом материале существенно замедлены во время консервации и материал хранится в жизнеспособной форме и восстанавливается до температуры тела 98,6oF.
Изобретение раскрывает приемники или камеры для хранения транспортируемого биологического материала. Такой приемник включает конструкцию из двух частей. Нижняя часть состоит из камеры или ячейки содержащей любо стерильный раствор, либо консервирующий гель, в который помещается орган или другой биологический материал, подлежащий консервации. Открывающаяся пластиковая крышка, сформированная и являющаяся верхней частью ячейки, закрывает камеру, и верхняя часть устройства насаживается и закрепляется на нижней части расположенными на окружности креплениями вокруг верхней части и обхватывающими нижнюю часть. Стальной обруч из нержавеющей стали с замком накладывается на верхнюю часть, защелкивая ее с нижней частью.
Две части отформованы таким образом, что они создают пустую воздушную камеру вокруг ячейки с биологическим материалом, и вокруг ячейки создается равномерный однонаправленный воздушный поток. Биологический материал сохраняется в консервирующей среде с поддержанием температур охлаждения от 1 до 3oC. Охлаждающий агент представляет собой сжатый воздух или инертный газ, введенный первоначально через впускные отверстия, расположенные в верхней части основного элемента устройства, и циркулирующий непрерывно по герметичной наружной камере, окружающей внутреннюю вогнутую приемную ячейку, в которую помещается консервируемый биологический материал. Охладитель из инертного газа непрерывно циркулирует в помощью микромотора, выполненного из низкофрикционного с малой массой материала, такого, как кремний, который может работать в стационарном режиме посредством пневматического давления, когда устройство связано с источником сжатого инертного газа. При транспортировке конструкции перезаряжаемая батарейка поддерживает должную концентрацию охладителя подачей пневматического толчка воздуха или инертного газа к микромотору с тем, чтобы поддерживать желаемую скорость мотора. Батарейка также снабжает кислородные датчики и средства считывания, а также любые дополнительные приборы датчиков. Допустимая концентрация кислорода в пустой наружной воздушной камере отграничивается до уровня между 1/4 4% кислорода по объему от общего объема воздушной камеры и четко контролируется применением кислородного датчика и средствами считывания. Такое тщательное регулирование уровня кислорода важно для длительной работы мотора, который чрезвычайно чувствителен к любым изменениям к плотностям в газовой смеси, циркулирующей в воздушной камере. При изменении концентрации кислорода в установленных пределах температура биологического содержимого выйдет за критические пределы 34 37oF. Кроме того, как в любом пластике, со временем кислород будет проникать внутрь через наружную пластиковую стенку конструкции, когда устройство в стационарном использовании. Такое увеличение концентрации кислорода повлияет на плотность охлаждающей смеси, циркулирующей по воздушной камере. Поэтому даже небольшое увеличение содержания кислорода приведет к увеличению оптимального числа оборота микромотора в минуту, и датчик со считыванием насторожит оператора, который подаст дополнительный инертный газ через впускное отверстие, или в другом варианте датчик может автоматически включить пневматический выброс, убирающий ненужный кислород через отверстие но поскольку конструкция может использоваться для хранения крови и другого живого биологического материала в течение неопределенных периодов времени, в конструкции это также учитывается.
В одном предпочтительном варианте в присутствии консервируемого материала добавляется производное крахмала (ГЭК). При необходимости галлирования добавляется геллирующий агент, может использоваться тип акриламида. Как указывалось в патенте США 4473552, биологический материал, содержащий живые клетки, заключается в ГЭК при 38oF на неопределенный период.
Раскрытый здесь контейнер для хранения позволяет набухание, желирование и хранение живого биологического материала в растворе в среде, свободной от кислорода, поскольку весь воздух исключен из ячейки контейнера. В такой среде консервируемый биологический материал можно хранить неопределенное время.
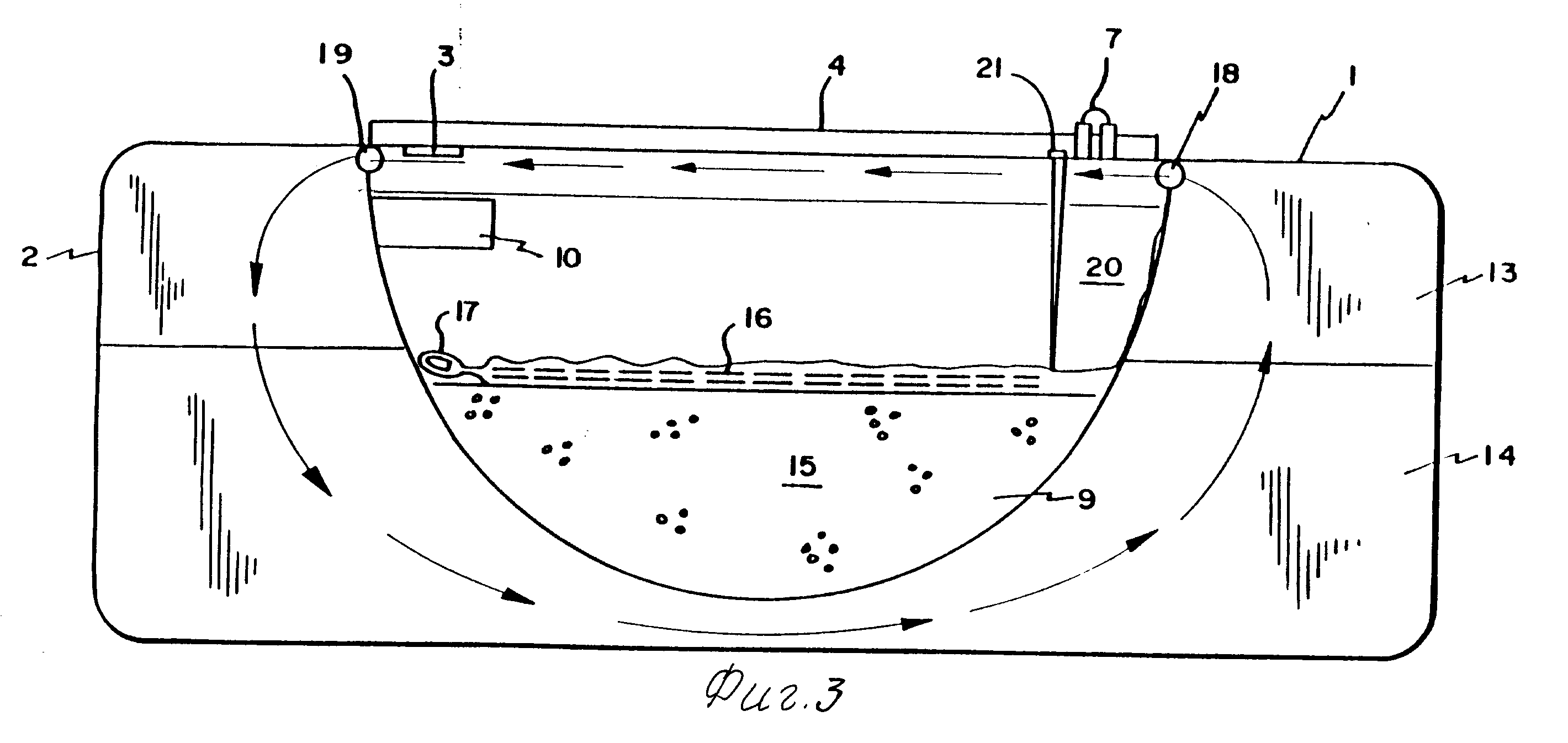
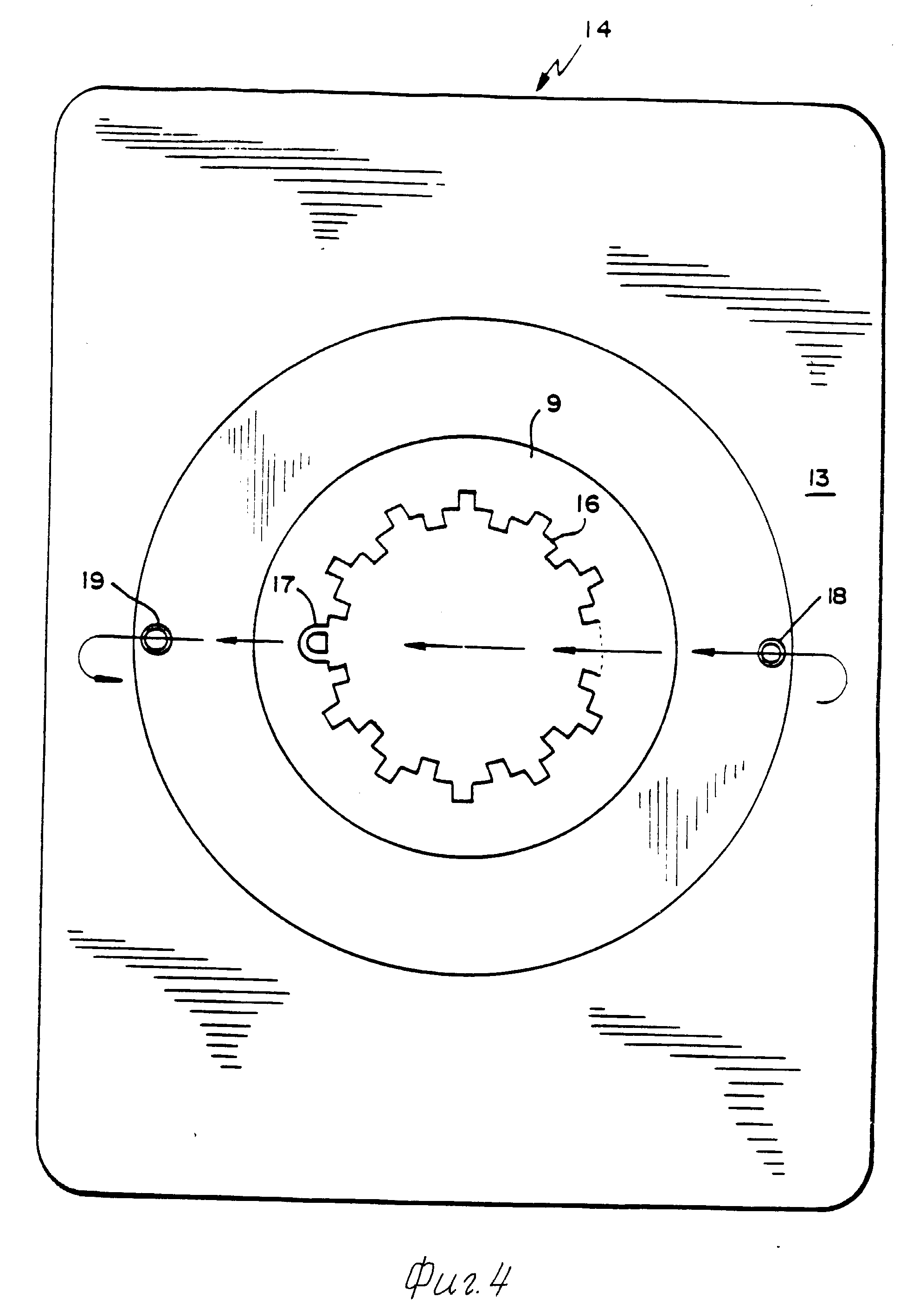
Изобретение поясняется чертежами, где на фиг. 1 показан вид сверху контейнера консервации, на фиг. 2 перспективный вид микромотора, а на фиг. 3 поперечное боковое сечение контейнера с показом направления воздушного потока и ячейки хранения, на фиг. 4 вид сверху нижней части контейнера со снятой верхней латексной частью.
Транспортабельный контейнер 1 выполнен из полиэтилена, полипропилена, полиуретана или другого инертного пластика. Верхняя часть 2 состоит из блока микромотора 3, видимого через прозрачный экран 4. Экран фиброскопического измерителя 5 показывает содержание кислорода в пустой воздушной камере (фиг. 3), которая воспринимается кислородным датчиком 6. Поскольку дополнительный кислород не допускается в систему, единственным присутствующим в системе кислородом является кислород в биологическом материале. Предлагается также введение считывающих средств для датчика веса (не показаны) с целью контроля веса консервируемого биологического содержимого. Вес биологического материала должен оставаться постоянным, если нет биораспада. Съемная верхняя часть 2 имеет двойные отверстия 7 для поступления нужного охлаждающего инертного газа или сжатого воздуха либо иглой, либо другими средствами введения (не показаны). Охладителем может быть азот, фреон, гелий или другой инертный газ. Наружные расположенные по окружности крепления соединяют вместе две части контейнера. Фиксирующий обруч из нержавеющей стали (не показан) окружает структурный выступ 8 в верхней и нижней частей контейнера прижимным замком. Прозрачный экран 4 находится в верхней части контейнера, и перезарядная батарейка 10, которая питает приборы с цифровым считывающим устройством 22, расположена снизу на верхней части 2.
На фиг. 2 блок микромотора 3 показан подробно.
Микромотор 3 выполнен из низкофрикционных небольшой массы соединений, таких, как, кремний, который облегчает способность достижения очень больших оборотов в минуту с минимальной пневматической силой, подаваемой к шестеренкам 11 мотора. Зубья 12 шестеренок 11 также ясно видны. Инертный газ, введенный в систему через впускные отверстия 7, направляется к блоку микромотора 3 с пневматическим давлением, которое первоначально устанавливает мотор 3 в почти безфрикционное самоподдерживающее движение со скоростью 24000 об/мин от одного пневматического выброса воздуха, направленного к мотору 3 с помощью шприца (не показан) через впускные отверстия 7. Микромотор, находящийся в движении, направляет воздушный поток от мотора 3 иследовательно, непрерывно циркулирует воздух или смесь инертного газа вокруг пустой воздушной камеры 13 на фиг. 3, которая окружает ячейку 9 с консервируемым биологическим материалом при температуре 37 34oF.
На фиг. 3 показан поперечный срез сбоку полиэтиленового, полипропиленового, полиуретанового или другого инертного пластика биологического контейнера 1. Нижняя часть 14 содержит оформленный вогнутый приемник, ячейку или камеру 9, включенную опорную систему, содержащую стерильный раствор среды консервации или гельный раствор 15, который помещается орган или другой живой биологический материал, подлежащий консервации. Средой, способствующей консервации, может быть раствор гидроксиэтилового крахмала (ГЭК) или подходящий внеклеточный блокирующий агент, такой как амантадин или подходящий гельакриламид. Предполагается, что к биологическому материалу можно подшить сегмент ткани вилочковой железы, что поможет принятию ткани телом реципиента. Ячейка 9 закрывается съемной пластиковой крышкой 16, которая открепляется и оттягивается назад за язычок 17. После закладки биологического материала крышку 16 можно герметично закрыть. Плотный латекс или другая инертная пластическая структура 20 спускается вниз и укладывается непосредственно на крышку вогнутой приемной ячейки с биологическим материалом. Датчики температуры 21 проходят через твердую латексную часть верхней части устройства и находятся в контакте с пластиковой крышкой 16, закрывающей ячейку 9. Датчики 21 соединены со средствами считывания, которые указывают точную постоянную температуру содержимого ячейки. Часть, расположенная между внутренней вогнутой ячейкой 9 и наружным пластиковым корпусом нижней части 14 и верхней частью 2, выполнена из инертного пластика. При транспортировке такой охладитель,как фреон, вводится в пустую воздушную камеру и циркулирует через микромотор. Когда конструкция подготовлена для стационарного хранения биологического содержимого, фреон можно удалить и заменить другими инертными газами. Воздушный поток направляется под ячейку, вверх через отверстия 18 вверху верхней части блока 2, через верх ячейки 9, через микромотор 3 и в отверстие для воздуха 19 в противоположном конце и вновь вокруг ячейки 9. Воздушный поток должен пройти микромотор 3 и затем направиться назад по указанному стрелкой циклу в одном направлении.
На фиг. 4 показан вид сверху в продольном направлении нижней части 14 блока хранения с биологическим контейнером 9. Предполагается, что нижняя часть 14, которая удерживает живой биологический материал, является одноразовой и удаляется после того, как биологический материал транспортирован. Однако верхняя часть 2 блока со всеми приборами, микромотор 3 и батарейка 10 используются повторно. Когда биологическое содержимое нижней части удаляется из ячейки 9 и используется, вся нижняя часть устройства выбрасывается. Возможность использовать верхнюю часть устройства дает экономию в деньгах и площади, что важно при перевозках на большие расстояния, где учитываются факторы уплаты и занимаемой площади.
Способность замедлить естественный метаболизм живого человеческого материала охлаждением в нужной среде до температуры выше точки замерзания препятствует биологической порче живой ткани, крови, органа или другой группы живых клеток. Поэтому предполагается, что хранение в течение неопределенного времени и транспортировка различного биологического материала послужит облегчению многочисленных медицинских процедур или перевозках на большие расстояния от доноров, и хранение будет жизнеспособным при будущих космических перевозках, поскольку контейнеры можно хранить в течение долгого времени на космических станциях.
Кроме этого, предполагается, что поскольку запасы человеческой крови, которая здорова и свободна от ненужных факторов, таких как HIY I-II и вирусов гепатита, и имеет более короткий срок хранения, изобретение служит для хранения здоровой крови в течение неопределенного времени, уменьшая риск переливания крови от уже истощенного запаса. К ГЭК или гельной консервирующей среде можно добавить производное белых кровяных клеток, такое как молекулу амаитадина, с тем чтобы образовать барьер для проникновения какого-либо необнаруженного HIY вируса к здоровым клеткам и таким образом позволить принять биологический материал в консервирующей среде.
Реферат
Использование: в медицине для облегчения транспортировки и долгосрочного хранения биологического материала. Сущность изобретения: способ обеспечивает стерильную укладку донорского биологического материала в защитных растворах внеклеточных агентов в системе с контролируемой температурой, которая регулируется охлажденным воздухом или инертным газом, пропускаемыми микромотором, обороты которого устанавливают скорость охладителей, регулирующих температуру биологического материала. Контейнер содержит герметическую вогнутую ячейку для размещения в ней живого биологического сохраняемого материала и отверстия для воздуха и инертного газа. Согласно изобретению, введено нижнее основание, в котором размещена вогнутая ячейка, съемная крышка для герметичного закрывания ячейки и микромотор для создания потока охлаждающего средства с температурой 37 - 34oF. Между нижним основанием и ячейкой образована первая воздушная камера. Между закрывающей конструкцией и ячейкой образована вторая воздушная камера, сообщаемая с первой посредством отверстий для воздуха и инертного газа для создания непрерывного циркулирующего потока охлаждающего средства непосредственно вблизи ячейки без контакта с живой биологической материей в ней. 2 с. и 16 з.п. ф-лы, 4 ил.


Комментарии