Репрезентативная диагностика - RU2743169C2
Код документа: RU2743169C2
Чертежи









































































Описание
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка заявляет приоритет по дате подачи предварительной заявки США с серийным №62/418146, поданной 4 ноября 2016 г.; предварительной заявки США с серийным №62/354622, поданной 24 июня 2016 г.; предварительной заявки США с серийным №62/279405, поданной 15 января 2016 г. и предварительной заявки США с серийным №62/252153, поданной 6 ноября 2015 г., описания которых тем самым включены посредством ссылки во всей своей полноте.
ОБЛАСТЬ ТЕХНИКИ
Данное описание в целом относится к разработке методологии создания репрезентативных образцов тканей, например, из целых органов, опухолей, лимфатических узлов, метастазов или их комбинаций, в целях решения проблемы гетерогенности тканей в клинических образцах, в особенности, образцах, предназначенных для применения в клинической онкологии. Более конкретно, данное изобретение относится к применению механических, химических и/или биохимических, например, ферментативных, способов диссоциации к интактным подвергнутым фиксации (или консервации) образцам тканей, например, целым органам, опухолям, лимфатическим узлам, пораженным метастазами тканям или комбинациям любого из вышеперечисленных, с целью создания гомогенного образца, который обеспечивает возможность получения корректного репрезентативного образца несмотря на пространственную гетерогенность в ткани, например, опухоли, увеличивая вероятность обнаружения минорных субклоновых популяций и/или случаев с низкой распространенностью. Репрезентативный образец ткани, например, образец опухолевой ткани, подходит для применения в различных диагностических анализах. В частности, такие репрезентативные опухолевые образцы и их части полезны в методах анализа, применяемых для оценки прогноза развития рака (например, оценки стадии развития опухоли) и для выбора и разработки соответствующих схем лечения. Репрезентативные образцы ткани, например, опухолевые образцы и их части, можно использовать в качестве терапевтических средств или для создания терапевтических средств, например, в виде вакцин, или для изготовления вакцин против рака, или для основанных на использовании иммунных клеток терапий, поскольку репрезентативные образцы содержат набор разнообразных антигенов, экспрессируемых данной опухолью или данными опухолями.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Методы отбора образцов опухолей, используемые для всех диагностических тестирований в медицинской онкологии, основаны на совместном развитии патологической анатомии и хирургической онкологии в конце 1800-х годов. До открытия в 1842 г. анестезии с использованием эфира и изобретения антисептических хирургических методов в 1867 г. образцы для патологоанатомических исследований обычно получали при вскрытиях. До появления этих двух значительных достижений в хирургических методах образцы тканей, полученные патологоанатомами, обычно поступали от пациентов, которые умерли на операционном столе вследствие шока или спустя непродолжительно время вследствие инфекции. Поэтому высокие уровни смертности при хирургическом вмешательстве не позволяли патологоанатомам сопоставить морфологические и полученные с использованием микроскопа характеристики опухолевых структур со статистикой выживаемости пациентов. Влияние анестезии и антисептических методов явилось причиной немедленного и существенного возрастания числа пациентов, выживших при хирургическом вмешательстве, и привело к значительному увеличению числа сложных хирургических процедур.
Описанные выше улучшения в работе хирургического отделения совпали с появлением в 1869 г. методики заливки ткани парафином и повсеместным применением фиксации в формалине, начиная с 1893 года. Благодаря этим двум нововведениям патологоанатомы получили беспрецедентные четкие представления относительно архитектуры тканей и микроскопической морфологии. С начала 1900-х годов были сделаны выводы, которые связали различные картины архитектуры и морфологии тканей со специфическими типами опухолей. Со временем патологоанатомы и хирурги-онкологи смогли связать эти специфические морфологические и полученные с использованием микроскопа признаки одного и того же типа опухоли с различиями в общей выживаемости. Корреляции между гистологическими признаками опухолей и прогнозом для пациента в конечном итоге были сведены в схему определения стадии по системе TNM (опухоль-узлы-метастазы) в начале 1950-х годов.
Цель определения стадии по системе TNM заключается в определении прогноза для ракового пациента путем оценки морфологических аспектов опухоли (Т), степени распространения опухолевых клеток в регионарные лимфатические узлы (N) и того, метастазирует ли или нет опухоль в отдаленные органы (М). Информация, которая необходима для проведения части "Т" анализа определения стадии по системе TNM, требует отбора небольшого количества (обычно 3-5) очень маленьких образцов опухоли на границе раздела опухоли и окружающей нормальной ткани. Образцы должны иметь соответствующий размер (примерно 20×20×3 миллиметра), чтобы обеспечить надлежащую фиксацию в формалине и заливку парафином. С использованием микротома готовят срез фиксированного в формалине и залитого парафином (FFPE) образца толщиной четыре микрона и помещают на предметное стекло для рассмотрения патологоанатомом. Большинство лабораторий патологической анатомии будут иметь основное оборудование, необходимое для определения стадии развития опухолей: пластиковые кассеты для тканей, буфер для фиксации в формалине, гистопроцессор для дегидратации и заливки ткани парафином, микротом для нарезания тонких срезов (обычно толщиной четыре микрона) и предметные стекла, на которых размещаются тканевые срезы.
Определение стадии по системе TNM стало международно признанным методом определения стадии рака в 1987 г. и в настоящее время регулируется Американским объединенным комитетом по изучению рака (AJCC) и Международным союзом по борьбе с раком (UICC). AJCC и UICC, а также Коллегия американских патологоанатомов (САР) обобщают и периодически обновляют руководящие положения, касающиеся критериев принятого во всем мире определения стадии по системе TNM. Определение гистологических и морфологических признаков, которые представляют собой исходную информацию для типичной процедуры оценки TNM, зависят во всем мире от хирургов-патологоанатомов, получающих соответствующие образцы тканей. Поэтому методы отбора образцов, необходимые для определения стадии по системе TNM, основанные на технологии и методах, разработанных в конце 1800-х годов, прочно утвердились в медицинской онкологии.
Получение "корректных" образцов тканей для определения стадии развития опухолей по системе TNM является основной задачей хирургической патологии, о чем свидетельствует тот факт, что в многочисленных руководствах описывается и иллюстрируется то, каким образом хирургам-патологоанатомам следует обращаться с образцом, полученным хирургическим путем. Как правило, готовят срезы, которые наилучшим образом демонстрируют признаки, наблюдаемые при макроскопическом исследовании. Во многих из этих руководств от признанных медицинских институтов излагаются методики, одобренные к применению AJCC, UICC и САР, и содержатся иллюстрации, подробно отображающие точные участки опухоли, подлежащие отбору в качестве образцов (см. ФИГ. 1А-1С). Целью этих руководств является необходимость обучения хирургов-патологоанатомов по всему миру умению отбирать конкретные участки извлеченных резекцией солидных опухолей соответствующим и воспроизводимым образом с тем, чтобы избежать случайного отбора образцов. См., например, утверждение на с. 29 во втором издании иллюстрированного руководства "Препарирование в хирургической патологии": "Ключом к подходу, который является как экономичным, так и всесторонним, является избирательный отбор образцов. Избирательный отбор образцов представляет собой стратегический подход с точки зрения попытки извлечения максимальной информации, которая может быть получена на основании данного среза ткани. В отличие от случайного и неспецифического отбора пробы, в случае отбора образцов ткани, являющегося избирательным, увеличивается количество информации по сравнению с той, которая может быть получена в гистологическом анализе, и для этого необходимо меньшее количество срезов". Эта цитата есть указание на то, что конкретные участки солидных опухолей следует собирать соответствующим и воспроизводимым образом для облегчения определения стадий по системе TNM. Как правило, для всех диагностических тестов используют срез самого высокого качества, а оставшийся образец отбрасывают.
Хирургов-патологоанатомов обучают необходимости воздерживаться от увеличения общего количества образцов, взятых из отобранной хирургическим путем пробы, поскольку увеличение числа отобранных образцов опухоли не дает никакой дополнительной информации. Нет подтверждения того, что можно получить более подробную диагностическую информацию, используя оставшуюся часть опухоли, из которой отбор не производят.
Метастазирование опухоли в локальные дренирующие лимфатические узлы является важным индикатором прогноза (т.е. это "N" для прогностического определения стадии по системе TNM). Присутствие опухолевых клеток в регионарных лимфатических узлах может быть решающим фактором в отношении необходимости получения пациентом адъювантной химиотерапии. Обычно опухолевые клетки обнаруживают в лимфатических узлах после хирургического удаления и исследования с использованием микроскопа одного тонкого среза FFPE ткани. Распространение метастазов в лимфатические узлы может приводить к заполнению целого органа или может быть видимым только под микроскопом с содержанием всего лишь нескольких раковых клеток. Незначительное распространение метастазов в лимфатические узлы может оказаться незамеченным, если в отношении наличия метастазирующей опухоли будет исследован только один тонкий срез иссеченного лимфатического узла. В зависимости от размера лимфатического узла один срез FFPE ткани может содержать только несколько десятых долей процента от общего объема иссеченного узла. Метастазирующая опухоль, растущая в области лимфатического узла, откуда образца не отбирали, не будет идентифицирована, что приведет к ложноотрицательному результату в анализе. Это может привести к тому, что пациент получит менее агрессивный режим терапии, чем необходимо индивиду с регионарно распространенным раком (т.е. с метастазированием в лимфатические узлы, N-положительным).
Описание клинического случая завершается в отделении патологии и отправляется онкологу после того, как образец опухоли вырезан из извлеченного резекцией опухолевого материала и определена стадия по системе TNM. Остальной операционный материал, содержащий оставшуюся опухолевую ткань, которую не использовали для определения стадии по системе TNM, затем уничтожают, обычно путем сжигания, как того требует закон "О передаче данных и ответственности в системе медицинского страхования" (HIPAA) от 1996 года. Однако, САР рекомендует, чтобы все парафиновые блоки и предметные стекла со срезами были сохранены в течение 10 лет. Во всем мире существует система, при которой вся диагностическая информация, полученная из солидных опухолей, основывается на меньшей части самой опухоли. См., например, De Petris, Proteome Science, 8: 9 (2010) ("De Petris"). В работе De Petris для дальнейшего исследования выполняли только "биопсию участка, репрезентативного для данной опухоли", при этом гемолиз и нечеткие требования делали образец неподходящим для последующего гистологического исследования.
Открытие гетерогенности опухолей противоречит традиционным теориям, касающимся развития опухолей. В 1950-х годах в научной среде преобладала теория о том, что конечная, клинически детектируемая опухоль представляла собой продукт последовательного отбора конкретных субпопуляций "линий стволовых опухолевых клеток". Согласно этой теории в основной массе опухоли доминирует одна "линия стволовых клеток", которая превосходит другие "линии стволовых клеток" в результате естественного отбора. Определение стадии по системе TNM было разработано в течение того же периода, что и концепции "линий стволовых опухолевых клеток", согласно которым большая часть опухоли будет состоять из одного "типа" опухоли. См. Peter Nowel, Science (1976) 194: 23-28.
Солидные опухоли фактически являются гетерогенными, а не однородными по составу. Сообщалось, что некоторые солидные опухоли состоят из большого числа генетически различающихся пространственно обособленных популяций раковых клеток. См. Gerlinger et al., NEJM (2012), 366: 883-92; и Yachida et al. Nature (2010), 467(7319): 1114-1117. Как изложено далее в данном описании, авторы изобретения показали, что традиционные методы отбора образцов для гистологического анализа опухолей приводят к получению неадекватного образца опухоли (или ткани, возможно содержащей раковые клетки, такой как лимфатический узел) и могут быть улучшены.
Врачи и ученые, руководствуясь данными современной патологии, обычно не считают информативно важной с медицинской точки зрения опухолевую ткань, оставшуюся после взятия образцов для определения стадии по системе TNM, в результате она подлежит уничтожению. Морфологический анализ и основанный на использовании биомаркеров анализ гистологических срезов также ограничены фенотипической, морфологической и генетической гетерогенностями, демонстрируемыми популяциями злокачественных клеток в опухоли или наблюдаемыми среди опухолей. Небольшая популяция опухолевых клеток может быть основным источником злокачественности и метастазирования и представлять незначительное количество набора генов всей опухоли. Вследствие этого биомаркеры, разработанные в отношении основной массы опухоли, могут не охватывать основных причин, обуславливающих смертность от рака, которая часто вызывается небольшой долей опухоли.
Гетерогенность набора генов отдельно взятой опухоли создает серьезные проблемы для принятия терапевтических решений при диагностировании онкологических заболеваний, когда используется информация, полученная с применением меньшей части опухоли в предположении, что опухоли состоят из клеток, являющихся однородными по своему составу. Например, пространственное расположение генетических подтипов в пределах образца сильно влияет на клинический результат. Используя традиционные методики рутинного приготовления срезов тканей, даже если они базируются на избирательном отборе образцов с опорой на признанные литературные источники, невозможно отобрать всю хирургическую пробу. Кроме того, с использованием существующих в настоящее время методик отбора образцов можно протестировать только меньшую часть опухоли, оставляя тем самым, в подавляющем большинстве случаев, большую часть опухоли никаким образом не исследованной и в конечном итоге подвергаемой уничтожению.
В рамках методик, одобренных AJCC, UICC и САР к применению, патологоанатомы будут использовать только небольшие доли извлеченной хирургической резекцией пробы ткани и отбрасывать оставшийся образец. Поскольку образец опухоли может содержать множество генетически и пространственно различающихся популяций опухолевых клеток, то 3-5 небольших образцов, взятые даже самым опытным патологоанатомом, не могут представлять все генетически разнообразные группы злокачественных новообразований или метастазов, имеющиеся во всей пробе. Кроме того, расположение любых геномно различающихся популяций раковых клеток не может быть известно заранее, поскольку последовательность ДНК опухолевых клеток не становится очевидной в результате макроскопического исследования. Фактически, отбрасывают оставшийся опухолевый материал, который содержит, в подавляющем большинстве случаев, всю информацию о клеточной, геномной и протеомной гетерогенности первичной опухоли, однако до сих пор не существует никакой эффективной по времени и затратам и экономически выгодной методологии или оборудования, которая(ое) позволила(о) бы осуществлять отбор образцов из всей опухоли.
Современная патологоанатомическая практика требует применения способов более тщательного отбора образцов и обработки всей опухоли, которые могут помочь обеспечить захватывание в диагностический образец материала, соответствующего клеточной, геномной и протеомной гетерогенности в пределах всей первичной опухоли.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Согласно данному изобретению предложена композиция обработанного гомогената, приготовленного из образца гетерогенной ткани, содержащего по существу гомогенно распределенные клеточные структуры, при этом соотношение клеточных структур в каждой подгруппе гомогената по существу аналогично соотношению клеточных структур в исходном образце гетерогенной ткани. Композиция на основе гомогената представляет собой новый, уникальный образец ткани, который олицетворяет ключевые характеристики исходного образца гетерогенной ткани. Описанная композиция направлена на ограничения, и в ней преодолены ограничения способов предшествующего уровня техники, которые не учитывают гетерогенности тканей в клинических образцах, в особенности, образцах для применения в клинической онкологии.
Композиция на основе гомогената приготовлена или происходит из различных тканей, органов или их образцов, например, лимфатического узла, метастаза, полипа, кисты, извлеченного резекцией материала, органа или их доли либо пространственно обособленных клеток. Согласно одному из аспектов гомогенат содержит от примерно 25% до примерно 100% клеточных структур образца ткани. Гомогенат может содержать белковую фракцию, липиды, нуклеиновые кислоты или другие группировки, которые присутствуют в исходной ткани, например, в целой опухоли, лимфатических узлах или метастазах, используемых для приготовления на их основе гомогената, при этом относительные пропорции составляющих их компонентов являются репрезентативными характеристиками данной исходной ткани. По существу гомогенные клеточные структуры могут содержать одиночные клетки или множество кластеров клеток, которые выделены из нормальной или аномальной ткани. Согласно некоторым аспектам гомогенат может содержать жидкий или нежидкий образец ткани, приготовленный целым рядом способов, такой как отобранный шприцем аспират для цитологического исследования, образец экссудата или мазок по Папаниколау.
Согласно другим аспектам гомогенат может быть выделен из подвергнутой консервации ткани, например, фиксированной в формалине ткани. Согласно другим аспектам образец ткани не подвергнут консервации или фиксации, и/или он содержит живые клетки. Образец гетерогенной ткани может быть выделен из одной или нескольких тканей, полученных от одного или нескольких пациентов.
Гомогенат подходит для применения в различных диагностических, прогностических и клинических приложениях, включая, но не ограничиваясь этим, получение репрезентативных данных, в том числе относящихся к онкологии репрезентативных данных, определение стадии рака, идентификацию и оценку прогноза заболеваний (например, определение стадии развития опухоли), выбор и разработку соответствующих схем лечения, подбор соответствующего клинического испытания, идентификацию и характеристику маркеров, профилирование тканей и хранение композиции на основе гомогената. Композиция на основе гомогената также полезна для скрининга терапевтических средств или для создания терапевтических средств для лечения пациентов, например, в виде вакцин, или для изготовления вакцин против рака, или для основанных на использовании иммунных клеток терапий, поскольку репрезентативные образцы содержат набор разнообразных антигенов, экспрессируемых данной опухолью или данными опухолями.
Согласно данному изобретению также предложены способы приготовления композиции на основе гомогената, которая является репрезентативным примером образца гетерогенной ткани, например, репрезентативным образцом. Более конкретно, данное изобретение включает применение механических, химических и/или биохимических, например, ферментативных, способов диссоциации к интактным тканесодержащим образцам, например, целым органам, опухолям, лимфатическим узлам, пораженным метастазами тканям или комбинациям любого из вышеперечисленных (от одного и того же пациента или разных пациентов), с целью получения достоверного репрезентативного образца несмотря на пространственную гетерогенность в исходной ткани или исходном органе, например, опухоли, увеличивая тем самым вероятность обнаружения минорных субклоновых популяций и/или случаев с низкой распространенностью.
Согласно одному из аспектов данное изобретение в целом относится к разработке методологии приготовления репрезентативных образцов тканей, например, из целых органов, опухолей, лимфатических узлов, метастазов или их комбинаций, в целях решения проблемы гетерогенности, например, гетерогенности опухолей, в клинических образцах, в особенности, клинических образцах, предназначенных для применения в клинической онкологии, и к применению таких репрезентативных образцов или их частей в различных диагностических и терапевтических методах, а также к композициям, содержащим такие репрезентативные образцы, для применения в диагностике и терапии, в особенности онкологии.
Кроме того, каждый из репрезентативных образцов, полученных от разных пациентов либо приготовленных из разных тканей одного или разных пациентов, может быть помечен уникальными идентифицирующими метками метками, например, гаптеном, и меченые образцы от разных пациентов или тканей объединяли и использовали в желаемых методах анализа.
Репрезентативные образцы, приготовленные согласно типичным воплощениям изобретения, могут найти применение для повышения точности детектирования, диагностики и/или установления стадии развития опухолей разных типов, независимо от типа, локализации, размера или объема опухолевой ткани. Описанные в настоящей заявке способы полезны для приготовления репрезентативного образца нормальной ткани или предположительно предраковых тканей (например, полученных от субъектов с более высоким риском развития рака вследствие генетического риска или предшествующего ракового заболевания) для идентификации немногочисленных клеток.
Согласно одному из аспектов изобретения предложен способ приготовления биологического образца, подходящего для оценки гетерогенности клеток в опухоли, лимфатическом узле или метастазах, и/или для оценки прогноза конкретного ракового заболевания у субъекта, и/или для определения соответствующего терапевтического протокола для субъекта с раковым заболеванием. Этот способ включает (1) получение образца ткани (такой как опухолевая ткань, или лимфатический узел, или метастазы), который содержит пространственно различающиеся участки ткани или который содержит опухоль целиком или существенную ее часть, и (2) гомогенизацию образца этой ткани, в результате чего такие клетки, в отношении гетерогенности, оценивают как "по существу гомогенно распределенные в полученном гомогенате либо его части или доли". Образец или образцы возможно могут быть подвергнуты фиксации и/или консервации, например, фиксации в формалине, фиксации в этаноле, заморозке или сублимационной сушке, хранению в воске (таком как парафиновый) и т.д. до или после гомогенизации всего или по существу всего образца опухоли, лимфатического узла, метастазов или даже целого органа, такого как почка.
Согласно другому аспекту изобретения предложен способ приготовления биологического образца, подходящего для оценки гетерогенности клеток в образце (таком как опухолевый образец, лимфатический узел, метастазы или их комбинация) и/или оценки прогноза конкретного ракового заболевания у субъекта, включающий: (1) получение одного или более интактных образцов из солидной опухоли или лимфатического узла, при этом предпочтительно, чтобы каждый интактный образец содержал по меньшей мере примерно 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 или большее число клеток либо, альтернативно, по меньшей мере 1000, 10000, 100000, 1000000, 5000000, 10000000, 50000000, 100000000, 500000000, 1000000000, 5000000000, 10000000000, 50000000000, 100000000000, 500000000000, 1000000000000, 5000000000000, 10000000000000, 50000000000000, 100000000000000 или большее число клеток, и возможно был подвергнут фиксации или консервации (как например, образец, фиксированный или консервированный в формалине, парафине или этаноле), и (2) по отдельности или в комбинации гомогенизацию одного или нескольких образцов, при этом каждый из одного или более гомогенатов по существу гомогенно отражает гетерогенность соответствующего(их) образца или образцов. В одном из воплощений интактный образец или интактные образцы из солидной опухоли или лимфатического узла содержат часть либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из части солидной опухоли или лимфатического узла. В другом воплощении интактный образец или интактные образцы из солидной опухоли или лимфатического узла содержат части либо, альтернативно, состоят по существу из или, кроме того, в основном состоят по существу из частей солидной опухоли или лимфатического узла. В следующем воплощении интактный образец или интактные образцы из солидной опухоли или лимфатического узла содержат весь объем либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из всей солидной опухоли или всего лимфатического узла.
Репрезентативные образцы возможно могут быть подвергнуты дальнейшей диссоциации и/или обработке для извлечения или выделения молекул конкретных типов, таких как клетки конкретного типа, белки, нуклеиновые кислоты или липиды и тому подобное, и с использованием, например, компьютерного анализа CAVA в отношении данных секвенирования на приборе от Illumina будут применены в диагностических и терапевтических методах.
Согласно еще одному аспекту изобретения предложен способ приготовления биологического образца, подходящего для оценки гетерогенности клеток в опухоли, или лимфатическом узле, или метастазах, или в их комбинации, включающий (1) получение одного или нескольких образцов биопсийного материала из солидной опухоли, или лимфатического узла, или метастазов, при этом предпочтительно, чтобы каждый образец биопсийного материала содержал по меньшей мере примерно 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 либо, альтернативно, по меньшей мере 1000, 10000, 100000, 1000000, 5000000, 10000000, 50000000, 100000000, 500000000, 1000000000, 5000000000, 10000000000, 50000000000, 100000000000, 500000000000, 1000000000000, 5000000000000, 10000000000000, 50000000000000, 100000000000000 или большее число клеток и возможно был подвергнут фиксации или консервации (как например, образец, фиксированный или консервированный в формалине, парафине или этаноле), и (2) по отдельности или в комбинации гомогенизацию одного или нескольких образцов биопсийного материала в условиях, при которых полученный гомогенат или полученные гомогенаты по существу диссоциированы до отдельных клеток и полученный гомогенат или полученные гомогенаты являются по существу гомогенными.
Согласно другому аспекту изобретения предложен способ приготовления биологического образца, подходящего для оценки того, характеризуется ли субъект развитием или имеет риск развития вирулентной формы конкретного рака, и/или имеет ли субъект рак вирулентной формы, включающий (1) получение одного или более интактных образцов биопсийного материала из солидной опухоли, или лимфатического узла, или метастазов, или предраковой кисты, при этом предпочтительно, чтобы каждый образец биопсийного материала содержал по меньшей мере примерно 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 или большее число клеток либо, альтернативно, по меньшей мере 1000, 10000, 100000, 1000000, 5000000, 10000000, 50000000, 100000000, 500000000, 1000000000, 5000000000, 10000000000, 50000000000, 100000000000, 500000000000, 1000000000000, 5000000000000, 10000000000000, 50000000000000, 100000000000000 или большее число клеток и возможно был подвергнут фиксации или консервации (как например, образец, фиксированный или консервированный в формалине, парафине или этаноле), и (2) по отдельности или в комбинации гомогенизацию одного или нескольких образцов биопсийного материала, при этом каждый из полученных одного или более гомогенатов по существу гомогенно отражает гетерогенность соответствующего образца биопсийного материала или соответствующих образцов биопсийного материала, и возможно выделение или детектирование присутствия по меньшей мере одного биомаркера. Согласно этому аспекту присутствие или отсутствие биомаркера является указанием на вирулентную форму рака, или, альтернативно, наличие активации или отрицательной регуляции биомаркера ассоциируется с вирулентной формой конкретного рака.
Согласно еще одному аспекту изобретения предложен способ определения характерных особенностей профиля в гетерогенной опухоли, лимфатических узлах или метастазах либо предраковой кисте, и/или детектирования генетически различающихся субклонов в гетерогенной опухоли, лимфатических узлах или метастазах либо предраковой кисте, и/или идентификации событий с низкой распространенностью в пределах опухоли, лимфатических узлов или метастазов либо предраковой кисты, и/или определения показателя распространенности мишеней в пределах опухоли, лимфатических узлов или метастазов либо предраковой кисты, включающий (1) получение образца или образцов опухоли, лимфатических узлов или метастазов либо предраковой кисты, который(ые) охватывает(ют) пространственно различающиеся участки опухоли, лимфатических узлов или метастазов либо предраковой кисты, который или которые до гомогенизации возможно подвергнуты фиксации или консервации, например, с использованием формалина, парафина и/или этанола, и (2) гомогенизацию образца или образцов опухоли, лимфатических узлов или метастазов либо предраковой кисты по отдельности, тем самым получение набора гомогенатов, который является репрезентативным примером профиля гетерогенности в пределах опухоли, лимфатических узлов, метастазов или предраковой кисты и подходит для определения характерных особенностей профиля опухоли и/или обнаружения генетически различающихся субклонов в гетерогенной опухоли, лимфатических узлах или метастазах либо предраковой кисте, и/или для идентификации событий с низкой распространенностью в пределах опухоли, или лимфатических узлов, или метастазов, или предраковой кисты, и/или для определения показателя распространенности мишеней в пределах опухоли, лимфатических узлов или метастазов либо предраковой кисты. Эти профили связаны с геномным разнообразием (например, числом точечных мутаций, вставок и делеций в пределах опухоли), разнообразием опухолевых фенотипов (например, с количеством опухоли, которая претерпела эпителиально-мезенхимальный переход), разнообразием в иммунном ответе хозяина (например, разнообразием экспрессии регуляторов контрольных точек иммунного ответа в опухолевых и иммунных клетках), разнообразием всевозможных механизмов устойчивости (например, с числом и разнообразием мутаций в опухоли, которые придают устойчивость к направленной терапии), разнообразием гистологических особенностей тканей (например, с количеством опухоли, которая в случае рака легкого представляет собой плоскоклеточную карциному по сравнению с аденокарциномой), разнообразием неоантигенов, экспрессируемых опухолью, и/или с другими, сложными фенотипическими, морфологическими, гистологическими, геномными, протеомными, метаболомными профилями, характерными для всей пораженной или возможно пораженной ткани, которую извлекают путем резекции из субъекта.
Согласно еще одному аспекту изобретения предложен способ обнаружения предраковых клеток или раковых клеток в рассматриваемых нормальных тканях или предположительно предраковых тканях у пациента, например, у пациента с риском развития рака вследствие генетической мутации или предшествующего рака либо у пациента с предраковыми кистами или полипами, включающий (1) получение образца или образцов рассматриваемых нормальных тканей или предположительно предраковых тканей, таких как предраковые кисты или полипы, которые занимают пространственно различающиеся участки рассматриваемых нормальных тканей или предположительно предраковых тканей у пациента, при этом до гомогенизации возможно проводят фиксацию или консервацию образца, и (2) гомогенизацию образца или образцов с получением тем самым гомогената, который является репрезентативным примером рассматриваемых нормальных тканей или предположительно предраковых тканей и который подходит для обнаружения немногочисленных раковых клеток или раковых стволовых клеток, например, еще до манифестации какого-либо признака заболевания у пациента.
Согласно другому аспекту изобретения предложены способы применения репрезентативных образцов и их частей, которые готовят любым из указанных выше способов, в анализах с разным форматом, при этом такие анализы могут быть выполнены с высокой производительностью, проведены одновременно или в разные моменты времени либо с разной локализацией и/или с применением автоматизации (полностью автоматизированным или полуавтоматизированным образом).
Согласно другому аспекту изобретения предложены репрезентативные образцы и их части, приготовленные любым из указанных выше способов, которые хранят для будущего использования, неограничивающие примеры таких образцов включают, например, замороженные, фиксированные в формалине, залитые парафином, обработанные этанолом или высушенные сублимационной сушкой образцы.
Согласно другому аспекту изобретения предложены репрезентативные образцы и их части, приготовленные любым из указанных выше способов, которые используют для получения (и возможно очистки) антигенов или антител, специфичных к конкретному антигену, из раковых клеток или клеток других типов, имеющихся в образце от пациента, при этом антитела или антигены возможно могут быть использованы в персонализированной медицине, т.е. в производстве терапевтических или профилактических вакцин против рака.
Стадия гомогенизации во всех из вышеупомянутых способов может быть проведена с использованием способа, который обеспечивает сохранение целостности клеток в образце, т.е. когда основная масса клеток в гомогенизированном(ых) образце или образцах оказывается не лизированной, и вследствие чего полученный гомогенат и его части являются "репрезентативными примерами" образца или образцов. Таким образом, количества клеток в образце или его части отображают процентные содержания разных клеточных типов в полном объеме образца или образцов тканей, например, солидной опухоли или лимфатического узла. Это может быть осуществлено, например, путем механической диссоциации опухолевого образца или его части (такой как механическая диссоциация, проводимая с добавлением или без добавления жидкости к опухолевому образцу или его части) и/или химической или ферментативной диссоциации опухолевого образца или его части (такой как обработка ферментом, который избирательно, или предпочтительно, или главным образом действует на белки внеклеточного матрикса, а не на мембраноассоциированные белки). Альтернативно, способы гомогенизации могут приводить к диссоциации клеток, тем не менее с одновременным получением образца, который является "репрезентативным примером" данной исходной ткани, такой как целая опухоль. Гомогенизированные репрезентативные образцы возможно могут быть подвергнуты дальнейшей диссоциации и/или обработке для извлечения или выделения молекул конкретных типов, таких как клетки конкретного типа, белки, нуклеиновые кислоты или липиды и тому подобное, с получением тем самым других репрезентативных образцов, которые могут быть использованы в диагностических и терапевтических способах.
Любой из приведенных выше способов может включать детектирование экспрессии по меньшей мере одного биомаркера, например, по меньшей мере одного липидного, белкового или нуклеиновокислотного биомаркера, в гомогенате либо его части или доли. Кроме того, способы могут дополнительно включать определение процентного содержания опухолевых клеток в гомогенате либо его части или доли, которые экспрессируют конкретный биомаркер или комбинацию биомаркеров. Возможно, что осуществляют детектирование и/или выделение опухолевых стволовых клеток и/или определение относительной частоты встречаемости или процентного содержания субклонов опухолевых клеток в гомогенате либо его части или доли. Кроме того, способы также могут включать детектирование генетической мишени (такой как точечная мутация, делеция, вставка, транслокация, слияние генов или амплификация гена).
Любой из приведенных выше методов также можно использовать для обнаружения, выделения и/или измерения числа конкретных иммунных клеток (таких как В-лимфоциты, Т-лимфоциты, макрофаги, природные киллерные (NK) клетки, моноциты или их комбинация), присутствующих в гомогенате либо его части или доли, что предоставляет полезную клиническую информацию, например, иммунный статус и болезненное состояние, а также чтобы выбрать подходящие протоколы лечения, например, с использованием ингибиторов контрольных точек, цитокинов или других иммунных модуляторов.
Полученные гомогенаты или репрезентативные образцы могут содержать, состоять по существу из или, кроме того, в основном состоять примерно из 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 клеток или, альтернативно, по меньшей мере 1000, 10000, 100000, 1000000, 5000000, 10000000, 50000000, 100000000, 500000000, 1000000000, 5000000000, 10000000000, 50000000000, 100000000000, 500000000000, 1000000000000, 5000000000000, 10000000000000, 50000000000000, 100000000000000 или большего числа клеток.
Полученные гомогенаты либо их доля или часть возможно могут быть подвергнуты заморозке или сублимационной сушке, заливке воском (таким как, парафиновый) или, альтернативно, использованы на других стадиях без таких замораживания или сублимационной сушки, или заливки воском. Например, репрезентативный парафиновый блок, т.е. приготовленный из гомогената либо его доли или части после заливки парафином, подходит для применения в современной патологоатономической практике, например, для приготовления срезов, подготовки предметных стекол, окрашивания, микроскопии, демаскирования антигена и т.д.
Гомогенаты могут быть приготовлены из двух или более опухолей, взятых от одного или нескольких субъектов в один и тот же или разные моменты времени (например, от одного и того же субъекта до или после лечения либо от нескольких субъектов до и после одинаковых или отличающихся друг от друга видов лечения), и полученные из каждой опухоли гомогенаты или их доли используют для оценки сходства и/или различия двух или более опухолей либо болезненного состояния у разных пациентов. Согласно другому аспекту гомогенаты от одного или нескольких субъектов могут быть объединены с целью приготовления репрезентативного образца от нескольких субъектов.
Гомогенаты могут быть приготовлены из двух или более предположительно нормальных или предраковых тканей, например, молочной железы, шейки матки, толстой и прямой кишки, либо предраковых кист или полипов, полученных от одного субъекта или нескольких субъектов, например, субъекта с мутацией в BRCA (ген рака молочной железы), и полученные гомогенаты или их доли использовали для оценки того, присутствуют ли какие-либо аномальные клетки или биомаркеры заболевания.
Помимо этого, в гомогенат могут быть добавлены не являющиеся человеческими клетки (такие как клетки насекомых и/или клетки мышей) или другие чужеродные белки, нуклеиновые кислоты или малые молекулы для создания внутреннего контроля с целью положительного детектирования белков или нуклеиновых кислот.
К такому образцу можно добавить малые молекулы (такие как гаптены, пептидные метки, белковые метки, флуоресцентные метки и/или нуклеиновокислотные метки) и использовать для получения пространственной информации, касающейся репрезентативного образца. Например, для создания репрезентативного образца можно приготовить срезы образца (такого как опухоль или лимфатический узел), например, разрезать с получением четырех срезов, и в каждый срез до гомогенизации срезов можно "ввести" другой гаптен (или другую подходящую малую молекулу). Следует понимать, что количество срезов, которые могут быть получены на основе каждого образца, для "введения добавки" до гомогенизации, не ограничивается, а скорее всего, с большой долей вероятности будет выбрано в зависимости от размера образца, т.е. чем больше образец, тем будет получено большее количество срезов, которые могут быть "помечены" малой молекулой до гомогенизации. Таким образом, в полученных гомогенатах или их долях можно сохранять пространственную информацию.
В одном из воплощений малые молекулы также можно добавлять к образцу до объединения данного образца с другим образцом от другого пациента или одного и того же пациента, и это, таким образом, обеспечивает средство для различения образцов при работе в формате мультиплексного анализа.
Гомогенизированные образцы могут быть подвергнуты консервации, например, фиксации в формалине, или могут быть обработаны этанолом до или после гомогенизации. Перед применением в большинстве диагностических методов, из-за проблем безопасности образцы ткани обычно фиксируют в формалине или каким-либо иным образом, после чего секвенируют на приборе от Illumina и данные секвенирования обрабатывают с использованием компьютерного анализа CAVA в патологоанатомической лаборатории. Фиксация в формалине или другие методы фиксации могут быть осуществлены согласно методам, общеизвестным в данной области техники. В таких случаях, фиксированный в формалине опухолевый образец можно выдержать в воде или забуференном физиологическом растворе (таком как PBS (забуференный фосфатом физиологический раствор)) перед гомогенизацией на стадии (2).
Альтернативно или помимо этого, опухолевый образец, используемый в описанных способах, может быть подвергнут консервации в этаноле до гомогенизации. Однако фиксация в формалине, в метаноле или этаноле либо другие методики консервации не являются существенными для способов по изобретению и могут быть исключены без ущерба для пригодности полученного гомогенизированного репрезентативного образца.
Для получения репрезентативного образца живой ткани можно провести гомогенизацию ткани, не подвергнутой фиксации. Чтобы получить репрезентативный образец культивируемой ткани от индивидуальных пациентов, можно провести культивирование репрезентативного образца живой ткани. Такой репрезентативный образец может быть неоднократно разделен на части с получением любого количества репрезентативных культивируемых образцов, которые можно использовать для определения эффективности химиотерапии (как например, определения антитела, нуклеиновой кислоты, малой молекулы или полипептида, который(ая) антагонизирует, ингибирует или блокирует экспрессию или функциональную активность по меньшей мере одного известного или неизвестного биомаркера). Кроме того, с использование анализа FACS (сортировка флуоресцентно-активированных клеток) можно отобрать клетки конкретного типа (такие как иммунные клетки или опухолевые клетки). Например, для определения опухолеспецифических антител, секретируемых иммунной системой, можно провести отбор и культивирование инфильтрующих опухоль иммунных клеток.
Кроме того, как показано в данной заявке, описанные способы приготовления репрезентативных образцов и их применения в диагностических и терапевтических способах подходят как для фиксированных, так и для нефиксированных образцов ткани.
Любой из описанных способов приготовления репрезентативного образца может включать добавление по меньшей мере одной коллагеназы (или другого подходящего фермента, или комбинации ферментов, или другого химического вещества, такого как соль, под действием которого происходит разрушение или который способствует расщеплению внеклеточного матрикса) до, в ходе и после гомогенизации; использование условий повышенной температуры и/или буфера (такого как буфер для выдерживания клеток, например, СС1 или СС2, в котором разрушаются межклеточные сшивки); и/или применение устройства для механического фрагментирования (такого как блендер от IKA, диассоциатор gentleMACS или функциональный эквивалент). И вновь, эти способы могут быть выполнены или могут быть не выполнены в условиях, которые поддерживают жизнеспособность и целостность клеток в образце, например, в некоторых условиях гомогенизации клетки по существу не подвергаются лизису.
Согласно одному из аспектов способы гомогенизации включают применение механического метода, неограничивающие примеры которого включают применение ступки и пестика, гомогенизатора Даунса или измельчителя тканей, ручного электронного гомогенизатора тканей с вращающимися ножами (такого как Omni-TH, поставляемый Thomas Scientific), гомогенизатора по типу шаровой мельницы (такого как блендер серии Bullet, или гомогенизатор тканей Burton Precellys 24, или Bead Ruptor, поставляемый OMNI), возможно со скоростью от примерно 100 до примерно 75000 об./мин для ротационных гомогенизаторов или со скоростью от примерно 0,5 м/с до примерно 2,5 м/с для шаровых мельниц и в течение промежутка времени от примерно 30 секунд до примерно 5 минут, от примерно 5 минут до примерно 10 минут, от примерно 10 минут до примерно 30 минут или от примерно 30 минут до примерно 60 минут. Как указано в данном описании, способ механической гомогенизации можно использовать по отдельности или в сочетании с другими способами.
В другом воплощении гомогенизация включает, по отдельности или в сочетании с другими способами, применение препарата фермента, неограничивающие примеры которого включают, например, интерстициальную коллагеназу, желатиназу-а, стромелизин 1, матрилизин, коллагеназу нейтрофилов, желатиназу-b, стромелизин 2, стромелизин 3, металлоэластазу макрофагов, коллагеназу 3, МТ1-ММР, МТ2-ММР, МТ3-ММР, МТ4-ММР, коллагеназу 4, энамелизин, Х-ММР, СА-ММР, МТ5-ММР, МТ6-ММР, матрилизин-2, ММР-22, эндопротеиназу, трипсин, химотрипсин, эндопротеиназу Asp-N, эндопротеиназу Arg-C, эндопротеиназу Glu-C (V8 протеазу), эндопротеиназу Lys-C, пепсин, термолизин, эластазу, папаин, протеиназу K, субтилизин, клострипаин, экзопептидазу, карбоксипептидазу А, карбоксипептидазу В, карбоксипептидазу Р, карбоксипептидазу Y, катепсин С, высвобождающий ациламинокислоту фермент, пироглутаматаминопептидазу или любую их комбинацию, возможно в концентрации от примерно 0,001 мкг/мл до примерно 1000 мг/мл и в течение промежутка времени от примерно 1 минуты до примерно 120 минут.
Опухолевый или другой образец, использованный в описываемых способах, который охватывает пространственно различающиеся участки опухолевой или другой ткани, может содержать по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, по меньшей мере 85%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или, предпочтительно, полный объем образца опухоли или ткани, изъятого хирургическим путем из пациента. Опухолевый образец может составлять по меньшей мере 1, 5, 10, 20, 50, 100 или более миллиметров (мм) или несколько сантиметров (см) в диаметре.
Образцы, используемые в способах по изобретению, обычно будут приготовлены из любого соответствующего образца ткани, например, солидной опухоли или солидных опухолей (включая первичные опухоли и метастазирующие опухоли), лимфатических узлов, метастазов или предраковых тканей, таких как кисты или полипы. Альтернативно или помимо этого, данные способы также могут быть эффективны в случае несолидных опухолей, например, раковых заболеваний крови. Например, образцы тканей или образцы солидных опухолей, которые являются гомогенизированными, возможно могут быть объединены с образцами жидкостей пациента, например, образцами крови, лимфатической жидкости, проб экссудата, образцами цереброспинальной жидкости, желчи, слизи и/или мочи пациента. Образцы, которые являются гомогенизированными, помимо этого или альтернативно могут представлять собой полные или частичные образцы, например, отобранную посредством биопсии "нормальную" или предраковую ткань, например, чтобы обнаружить пораженные клетки до проявления заболевания.
Такой образец или такие образцы опухолевых либо других тканей, использованный(ые) в описанных способах, может(могут) происходить из любого источника, например, из молочной железы, толстой кишки, легкого, поджелудочной железы, желчного пузыря, кожи, кости, мышцы, печени, почки, шейки матки, яичников, предстательной железы, пищевода, желудка или других органов, например, из раковой опухоли молочной железы, раковой опухоли легкого, опухоли печени, раковой опухоли предстательной железы, раковой опухоли толстой кишки, раковой опухоли мочевого пузыря или раковой опухоли почки. В одном из воплощений опухолевый образец или образец другой ткани, использованный в описанных способах, имеет человеческое происхождение, но может быть получен из любого соответствующего источника ткани.
Образец опухолевой или другой ткани, использованный в описанных способах, может иметь объем, составляющий по меньшей мере 1 см3, по меньшей мере 2 см3, по меньшей мере 3 см3, по меньшей мере 4 см3, по меньшей мере 5 см3, по меньшей мере 6 см3, по меньшей мере 7 см3, по меньшей мере 8 см3, по меньшей мере 9 см3, по меньшей мере 10 см3, по меньшей мере 15 см3, по меньшей мере 20 см3, по меньшей мере 25 см3, по меньшей мере 50 см3, по меньшей мере 100 см3, по меньшей мере 250 см3, по меньшей мере 500 см3, по меньшей мере 1000 см3, по меньшей мере 2500 см3, по меньшей мере 5000 см3, по меньшей мере 7500 см3, по меньшей мере 10000 см3 или больше.
Образец опухолевой или другой ткани, использованный в описанном способе, может иметь ширину в самом широком месте, составляющую по меньшей мере 0,5 см, по меньшей мере 1 см, по меньшей мере 1,5 см, по меньшей мере 2 см, по меньшей мере 2,5 см, по меньшей мере 3 см, по меньшей мере 3,5 см, по меньшей мере 4 см, по меньшей мере 4,5 см, по меньшей мере 5 см, по меньшей мере 6 см, по меньшей мере 7 см, по меньшей мере 10 см, по меньшей мере 25 см, по меньшей мере 50 см или больше.
В дополнительном воплощении можно приготовить репрезентативные образцы ткани, которая предварительно была подвергнута фиксации в формалине и заливке парафиновым воском. В частности, воск можно растопить, ткань извлечь и подвергнуть гидратации и затем применить способы, описанные в данной заявке, т.е. гомогенизацию, к образцу, который подходит для применения в любом количестве анализов. Таким образом, описанные способы можно применять для приготовления репрезентативного образца с использованием образца или образцов, уже полученных для определения стадии по системе TNM, посредством расплавления воска, извлечения образца, регидратации и гомогенизации ткани, соответственно.
Любой из приведенных выше способов может дополнительно включать (3) нанесение гомогената либо его части или доли на одно или несколько предметных стекол либо одну или несколько других твердых подложек и, возможно, окрашивание одного или нескольких предметных стекол либо одной или нескольких других твердых подложек, содержащих гомогенат либо его часть или долю, красящим веществом на основе гематоксилина и эозина; осуществление иммуногистохимического окрашивания на предметном стекле или другой твердой подложке, содержащих гомогенат либо его часть или долю; или осуществление гибридизации in situ на предметном стекле или другой твердой подложке, содержащих гомогенат либо его часть или долю, т.е. любое из перечисленного будет считаться стадией (4) в данных способах. Например, анализ гомогената или его части можно выполнять на автоматизированной платформе для анализа. Такие платформы известны в данной области техники и имеются в продаже у Ventana Medical Systems, Inc. (VMSI) (см. Ventana.com для типичных автоматизированных платформ).
Кроме того, любой из приведенных выше способов может дополнительно включать (3) очистку нуклеиновых кислот (таких как ДНК или мРНК) из гомогената либо его части или доли. Очищенные нуклеиновые кислоты могут быть исследованы с использованием нозерн-блоттинга, секвенирования ДНК, полимеразной цепной реакции (ПЦР), ОТ-ПЦР, профилирования с применением микрочипов, дифференциального дисплея или гибридизации in situ. Альтернативно, очищенная нуклеиновая кислота может быть конъюгирована с наночастицей (такой как квантовые точки, парамагнитные наночастицы, суперпарамагнитные наночастицы и металлические наночастицы, предпочтительно легированные квантовые точки, включая, в качестве примера и без ограничения, CdSe, ZnSSe, ZnSeTe, ZnSTe, CdSSe, CdSeTe, ScSTe, HgSSe, HgSeTe, HgSTe, ZnCdS, ZnCdSe, ZnCdTe, ZnHgS, ZnHgSe, ZnHgTe, CdHgS, CdHgSe, CdHgTe, ZnCdSSe, ZnHgSSe, ZnCdSeTe, ZnHgSeTe, CdHgSSe, CdHgSeTe, InGaAs, GaAIAs и InGaN, в качестве примера).
Также подразумевается, что любой из приведенных выше способов может дополнительно включать очистку липидов или экзосом либо других органелл из гомогената либо его части или доли. Очищенные липиды могут быть исследованы методами масс-спектрометрии или гистохимии.
Кроме того, также подразумевается, что любой из приведенных выше способов может дополнительно включать очистку белков из гомогената либо его части или доли. Очищенные белки могут быть исследованы с использованием вестерн-блоттинга, иммуноферментного твердофазного анализа (ELISA), иммунопреципитации, хроматографии, масс-спектрометрии, профилирования с применением микрочипов, интерферометрии, электрофоретического окрашивания или иммуногистохимического окрашивания. Альтернативно или в дополнение к вышеупомянутому, очищенные белки можно использовать для приготовления образцов антисыворотки, специфичных к образцу опухоли или ткани.
Кроме того, подразумевается, что любой из приведенных выше способов дополнительно включает (3) проведение геномного, эпигеномного, транскриптомного, протеомного и/или метаболомного анализа в отношении гомогената либо его части или доли.
Кроме того, подразумевается, что любой из приведенных выше способов дополнительно включает (3) аффинную очистку клеток конкретного типа из гомогената либо его части или доли. Клетки конкретного типа могут содержать представляющий интерес биомаркер. Типичные представляющие интерес биомаркеры могут включать Her2, bRaf, амплификацию ERBB2, мутацию в PI3KCA, амплификацию FGFR2, мутацию в р53, мутацию в BRCA, амплификацию CCND1, мутацию в MAP2K4, мутацию в ATR или любой другой биомаркер, экспрессия которого коррелирует с конкретным видом рака; по меньшей мере один из AFP, ALK, BCR-ABL, BRCA1/BRCA2, BRAF, V600E, СА-125, СА19.9, EGFR, Her-2, KIT, PSA, S100, KRAS, ER/Pr, UGT1A1, CD30, CD20, F1P1L1-PDGRFa, PDGFR, TMPT и TMPRSS2; или по меньшей мере один биомаркер, выбранный из АВСВ5, AFP-L3, альфа-фетопротеина, альфа-метил-ацил-КоА-рацемазы, BRCA1, BRCA2, СА 15-3, СА 242, СА 27-29, СА-125, СА15-3, СА19-9, кальцитонина, канцероэмбрионального антигена, пептида-1 канцероэмбрионального антигена, дез-гамма-карбоксипротромбина, десмина, раннего антигена-2 рака предстательной железы, рецептора эстрогенов, продукта деградации фибрина, глюкозо-6-фосфат-изомеразы, антигена HPV, такого как vE6, Е7, L1, L2 или p16INK4a, хорионического гонадотропина человека, интерлейкина-6 (IL-6), кератина 19, лактатдегидрогеназы, лейциламинопептидазы, липотропина, метанефринов, неприлизина, NMP22, норметанефрина, РСА3 простатоспецифического антигена, кислой фосфатазы предстательной железы, синаптофизина, тиреоглобулина, фактора некроза опухоли (TNF), транскрипционного фактора, выбранного из ERG, ETV1 (ER81), FLI1, ETS1, ETS2, ELK1, ETV6 (TEL1), ETV7 (TEL2), GABPa, ELF1, ETV4 (E1AF; РЕА3), ETV5 (ERM), ERF, PEA3/E1AF, PU.1, ESE1/ESX, SAP1 (ELK4), ETV3 (METS), EWS/FLI1, ESE1, ESE2 (ELF5), ESE3, PDEF, NET (ELK3; SAP2), NERF (ELF2) или FEV, опухолеассоциированного гликопротеина 72, c-kit, SCF, pAKT, pc-kit и виментина.
Альтернативно или в дополнение к этому представляющим интерес биомаркером может быть ингибитор контрольных точек иммунного ответа, таких как, но не ограничиваясь этим, CTLA-4, PDL1, PDL2, PD1, В7-Н3, В7-Н4, BTLA, HVEM, KIR, TIM3, GAL9, GITR, LAG3, VISTA, KIR, 2В4, TRPO2, CD160, CGEN-15049, CHK 1, CHK2, A2aR, TL1A и лиганды В-7 семейства или их комбинация, либо этот биомаркер представляет собой лиганд белка-контрольной точки, выбранного из группы, состоящей из CTLA-4, PDL1, PDL2, PD1, В7-Н3, В7-Н4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2В4, CD160, CGEN-15049, CHK1, CHK2, A2aR, лигандов В-7 семейства или их комбинации.
Способы по данному изобретению также могут включать или включают детектирование по меньшей мере одного биомаркера, ассоциированного с острым лимфобластным лейкозом (etv6, am11, циклофилина b), В-клеточной лимфомой (Ig-идиотипа), глиомой (Е-кадгерина, альфа-катенина, бета-катенина, гамма-катенина, р120 ctn), раком мочевого пузыря (p21ras), раком желчных протоков (p21ras), раком молочной железы (представителя MUC семейства, HER2/neu, с-erbB-2), карциномой шейки матки (р53, p21ras), раком толстой кишки (p21ras, HER2/neu, c-erbB-2, представителя MUC семейства), колоректальным раком (антигена, ассоциированного с толстой и прямой кишкой (CRC)-C017-1A/GA733, АРС), хориокарциномой (СЕА), плоскоклеточным раком (циклофилина b), раком желудка (HER2/neu, c-erbB-2, гликопротеина ga733), гепатоклеточным раком (α-фетопротеина), лимфомой Ходжкина (Imp-1, EBNA-1), раком легкого (СЕА, MAGE-3, NY-ESO-1), лейкозом, начинающимся в лимфоидных клетках (циклофилина b), меланомой (белка р5, др75, онкофетального антигена, ганглиозидов GM2 и GD2, мелан-A/MART-1, cdc27, MAGE-3, p21ras, gp100.sup.Pmel117), миеломой (представителя MUC семейства, p21ras), немелкоклеточным раком легкого (HER2/neu, c-erbB-2), раком носоглотки (Imp-1, EBNA-1), раком яичников (представителя MUC семейства, HER2/neu, c-erbB-2), раком предстательной железы (простатоспецифического антигена (PSA) и его антигенных эпитопов PSA-1, PSA-2 и PSA-3, PSMA, HER2/neu, c-erbB-2, гликопротеина ga733), почечным раком (HER2/neu, c-erbB-2), случаями плоскоклеточного рака шейки матки и пищевода (продуктов вирусного происхождения, таких как белки папилломавируса человека), раком яичка (NY-ESO-1) и/или Т-клеточным лейкозом (эпитопов HTLV-1).
Способы по данному изобретению дополнительно включают (3) обработку гомогената либо его части или доли коллагеназой или другим ферментом либо химическим путем или их комбинацией, в результате чего внеклеточные матриксы разрушаются, инкубацию гомогената либо его части или доли в условиях высоких температур и/или механическое встряхивание гомогената либо его части или доли с целью осуществления диссоциации клеток в гомогенате либо его части или доли. В общем случае, в результате применения этих способов будет получена популяция отдельных клеток или небольшие кластеры клеток из репрезентативного образца, который может быть использован в описанных аналитических или терапевтических способах либо в случае их сочетания.
Кроме того, любой из вышеупомянутых способов дополнительно включает (3) фильтрование или разделение на основании размера для гомогената либо его части или доли, в результате чего могут быть получены одиночные клетки или небольшие кластеры клеток, такие как дублеты или триплеты.
Разделение клеточных компонентов репрезентативного образца может быть выполнено с использованием одной или нескольких стадий фильтрования. Например, после проведения гомогенизации и диссоциации гомогената с использованием физических и/или биохимических методов подвергнутый диссоциации образец можно пропустить через фильтр с размером пор 1 микрон для удаления всего интактного клеточного материала. Ожидается, что неклеточный репрезентативный образец будет содержать факторы, секретируемые из опухоли и нормальной стромы в пределах опухоли, которые найдут клиническое применение, т.е. антитела, факторы роста, иммуномодуляторы и другие неизвестные факторы. Анализ неклеточного репрезентативного образца может быть выполнен посредством ELISA, масс-спектрометрии, методов секвенирования следующего поколения и других диагностических методов. В тех случаях, когда одиночные клетки, происходящие из репрезентативного образца, получают после фильтрования, анализ таких клеток может быть проведен с использованием сортировки флуоресцентно-активированных клеток (FACS) и анализа посредством проточной цитометрии.
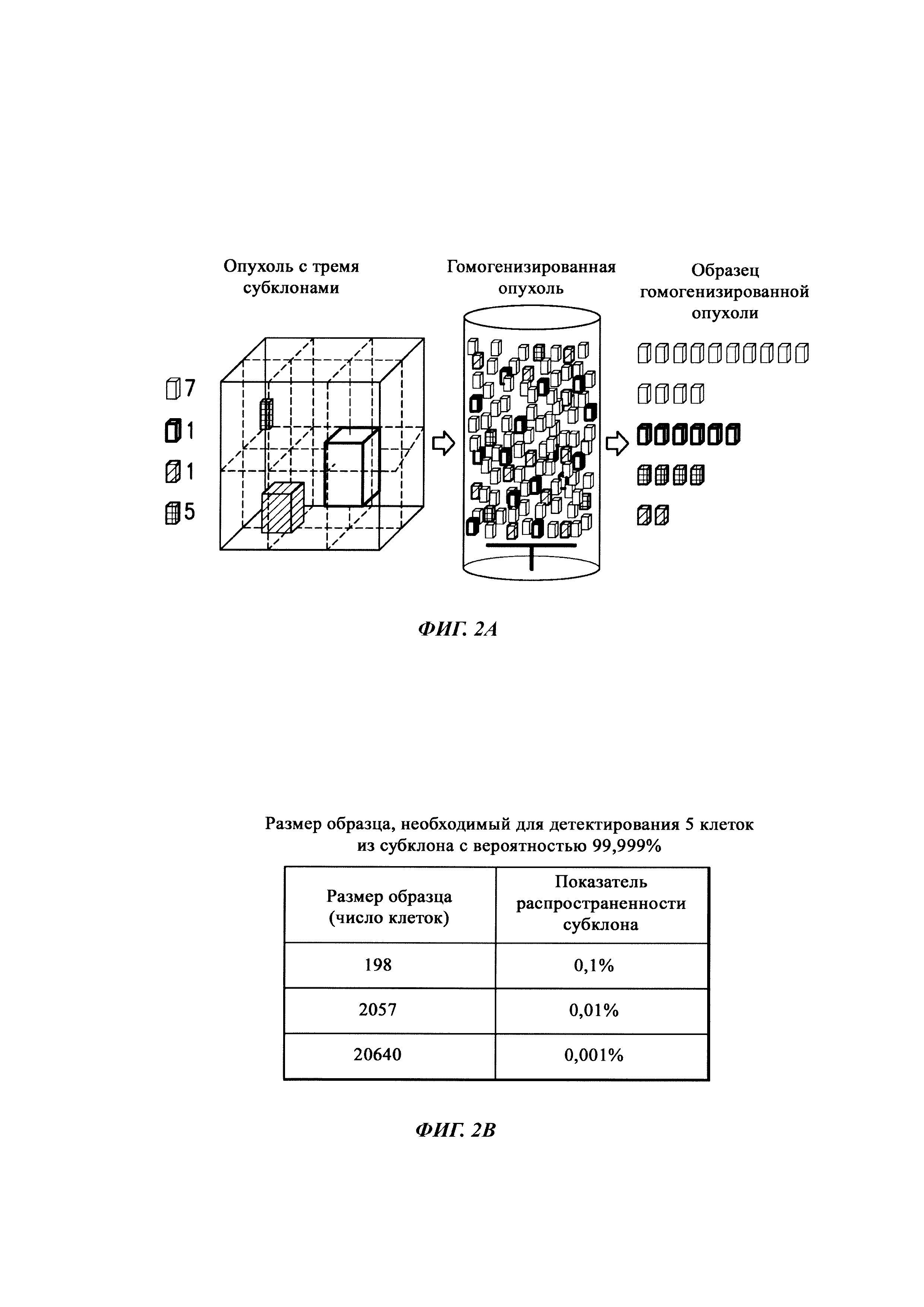
С учетом репрезентативной природы гомогената, полученного описанными способами, гомогенат либо его часть или долю можно использовать для детектирования генетического события с низкой распространенностью (такого как генетическое событие, которое происходит с показателем распространенности 20%, показателем распространенности 15%, показателем распространенности 10%, показателем распространенности 5%, показателем распространенности 2%, показателем распространенности 1%, показателем распространенности 0,5%, показателем распространенности 0,1%, показателем распространенности 0,01%, показателем распространенности 0,001%, показателем распространенности 0,0001%, показателем распространенности 0,00001%, показателем распространенности 0,000001% или меньше). Типичные генетические события включают точечную мутацию, делецию, вставку, транслокацию, слияние генов или амплификацию гена. Аналогичным образом, способы также могут включать детектирование генетической или эпигенетической гетерогенности в опухолевом образце или его части и/или детектирование клеток, содержащих редко встречающиеся генетические или эпигенетические вариации. Такие клетки могут быть представлены в опухолевом образце с частотой встречаемости менее 5%, менее 1%, менее 0,5%, менее 0,1%, менее 0,05% или менее 0,01%.
Детектируемые немногочисленные клетки могут содержать одно или несколько генетических или эпигенетических различий, которые придают устойчивость к терапии, обеспечивают восприимчивость к одной терапии по сравнению с другой, противораковую терапию и/или стимулируют метастазирование. Таким образом, согласно одному из аспектов обнаружение таких клеток будет способствовать прогнозу развития рака, а также выбору соответствующего режима терапии, такого как химиотерапия, комбинированная направленная терапия и/или применение биологических средств.
Указанные выше способы также могут включать применение по меньшей мере одной детектируемой метки, выбранной из флуоресцентных молекул или флуорохромов, таких как 4-ацетамидо-4'-изотиоцианатостильбен-2,2'-дисульфоновая кислота, акридин и такие производные, как акридин и акридина изотиоцианат, 5-(2'-аминоэтил)аминонафталин-1-сульфоновая кислота (EDANS), 4-амино-N-[3-винилсульфонил)фенил]нафталимид-3,5-дисульфонат (люцифер желтый VS), N-(4-анилино-1-нафтил)малеимид, антраниламид, бриллиантовый желтый, кумарин и такие производные, как кумарин, 7-амино-4-метилкумарин (АМС, кумарин 120), 7-амино-4-трифторметилкумарин (кумаран 151); цианозин; 4',6-диаминидино-2-фенилиндол (DAPI); 5',5''-дибромпирогаллол-сульфонфталеин (бромпирогаллол красный); 7-дизтиламино-3-(4'-изотиоцианатофенил)-4-метилкумарин; диэтилентриамина пентаацетат; 4,4'-диизотиоцианатодигидро-стильбен-2,2'-дисульфоновая кислота; 4,4'-диизотиоцианатостильбен-2,2'-дисульфоновая кислота; 5-[диметиламино]нафталин-1-сульфонилхлорид (DNS, данзилхлорид); 4-(4'-диметиламинофенилазо)бензойная кислота (DABCYL); 4-диметиламинофенилазофенил-4'-изотиоцианат (DABITC); эозин и такие производные, как эозин и эозина изотиоцианат; эритрозин и такие производные, как эритрозин В и эритрозина изотиоцианат; этидий; флуоресцеин и такие производные, как 5-карбоксифлуоресцеин (FAM), 5-(4,6-дихлортриазин-2-ил)аминофлуоресцеин (DTAF), 2',7'-диметокси-4',5'-дихлор-6-карбоксифлуоресцеин (JOE), флуоресцеин, флуоресцеина изотиоцианат (FITC) и QFITC (XRITC); 2',7'-дифторфлуоресцеин (OREGON GREEN®); флуорескамин; IR144; IR1446; малахитового зеленого изотиоцианат; 4-метилумбеллиферон; орто-крезолфталеин; нитротирозин; парарозанилин; феноловый красный; В-фикоэритрин; о-фталевый диальдегид; пирен и такие производные, как пирен, пирена бутират и сукцинимидил-1-пирена бутират; реактивный красный 4 (цибакрон R (красный)™, бриллиантовый красный 3В-А); родамин и такие производные, как 6-карбокси-Х-родамин (ROX), 6-карбоксиродамин (R6G), лиссамин, родамина В сульфонилхлорид, родамин (Rhod), родамин В, родамин 123, родамина X изотиоцианат, родамин зеленый, сульфородамин В, сульфородамин 101 и сульфонилхлоридное производное сульфородамина 101 (техасский красный); N,N,N',N'-тетраметил-6-карбоксиродамин (TAMRA); тетраметилродамин; тетраметилродамина изотиоцианат (TRITC); рибофлавин; розоловая кислота и хелатный комплекс производных тербия, тиол-реактивные хелатные комплексы европия, которые излучают на длине волны приблизительно 617 нм.
Описанные способы могут быть автоматизированы, целиком или частично. Например, стадии (1) и (2) могут быть автоматизированы, но любые последующие стадии, например, стадии (3) и (4), выполняются вручную. Альтернативно, в качестве примера, стадии (1) и (2) могут быть выполнены вручную, в то время как последующие стадии, например, стадии (3) и (4), являются автоматизированными. Кроме того, автоматизированными могут быть все стадии, охватываемые данными способами, в этом случае такие способы являются полностью автоматизированными.
Описанные способы можно применять, по отдельности или в сочетании с другими известными способами (такими как TNM), для определения стадии развития опухоли. Согласно одному из аспектов способы дополнительно включают оценку одного или более аспектов репрезентативного образца из опухоли и степени, до которой опухолевые клетки распространяются в регионарные лимфатические узлы, посредством анализа репрезентативного образца из извлеченных резекцией лимфатических узлов для предсказания вероятности рецидива и/или прогрессирования заболевания.
Описанные способы могут дополнительно включать применение алгоритма для расчета процентного содержания отобранных в качестве образца клеток, например, опухолевых клеток со специфическим биомаркером или без него. Относительный риск распространения метастазов (или вирулентного субклона) может быть определен на основании процентного содержания клеток в репрезентативном образце из опухоли и/или репрезентативном образце из лимфатического узла, имеющих конкретные детектируемые биомаркеры или комбинацию биомаркеров.
Описанные способы могут дополнительно включать разработку персональной дозировки или схемы лечения на основании биомаркерного профиля, антигенного профиля, мутационного профиля, липидного профиля, белкового профиля и/или экзосомного профиля, характеризующих репрезентативный образец. Например, на основании информации, характеризующей репрезентативный образец, или в комбинации с информацией, полученной в случае репрезентативного образца из лимфатического узла, может быть изменен выбор одного или более лекарственных средств и/или дозировки (количества, продолжительности введения и т.д.) таких лекарственных средств, вводимых пациенту, с целью разработки персонализированного лечения с учетом индивидуального тканевого или ракового профиля пациента.
Описанные способы могут дополнительно включать сравнение геномного профиля репрезентативного образца с геномным профилем репрезентативного образца ткани от тестируемого пациента или другого пациента, например, образца из лимфатического узла, и возможно дальнейшее сравнение этих профилей с циркулирующей опухолевой ДНК из любых отдаленных метастазов или репрезентативного образца метастазирующей опухоли.
Описанные способы могут дополнительно включать разработку критериев включения для клинического испытания на основании биомаркерного профиля, антигенного профиля, мутационного профиля, липидного профиля, белкового профиля и/или экзосомного профиля, характеризующих репрезентативный образец.
Настоящее изобретение также охватывает репрезентативные композиции на основе гомогената, которые готовят любым из указанных выше способов, по отдельности или в комбинации с другими композициями и носителями.
Кроме того, результаты применения указанных выше способов (таких как детектирование редко встречающихся генетических и/или эпигенетических событий, немногочисленных клеток и т.д.) или композиций, приготовленных любым из указанных выше способов, которые включают гомогенизацию образца, такого как опухолевый образец, для получения репрезентативного образца, подходящего для дальнейшего анализа с использованием любого числа стандартных диагностических анализов, можно использовать в выборе соответствующего режима терапии для ракового пациента. Такой режим терапии может включать генную терапию, химиотерапию, направленную терапию малыми молекулами, другие направленные терапии, введение иммуномодуляторов, облучение, введение цитокинов, хирургическое вмешательство или их сочетание.
Кроме того, описанные способы можно использовать для выбора по меньшей мере одного терапевтического агента (например, агента для генной терапии (например, CRISPR), для Т-клеточной терапии (например, CAR Т-клетки), антитела, нуклеиновой кислоты, малой молекулы или полипептида, которые антагонизируют, ингибируют или блокируют экспрессию или функциональную активность по меньшей мере одного детектируемого биомаркера), подходящего для применения субъектом, образец или опухоль от которого являлись источником для репрезентативного образца, получаемого предложенными способами.
Согласно дополнительному аспекту настоящее изобретение относится к способу приготовления репрезентативного образца для анализа, включающему (1) получение извлеченного хирургической резекцией образца ткани по меньшей мере от одного субъекта; и (2) гомогенизацию извлеченного хирургической резекцией образца ткани для получения гомогенизированного образца. В одном из воплощений по меньшей мере часть извлеченного хирургической резекцией образца ткани подвергают фиксации. В дополнительном воплощении способ также включает обработку первой части извлеченного хирургической резекцией образца и приготовление одного или нескольких блоков подвергнутой фиксации и заливке ткани и последующую гомогенизацию второй части оставшегося извлеченного хирургической резекцией образца. Часть одного или нескольких блоков подвергнутой фиксации и заливке ткани можно обработать посредством микротомии с получением одного или нескольких тонких тканевых срезов для морфологического анализа. Помимо этого, по меньшей мере часть одного или нескольких блоков подвергнутой фиксации и заливке ткани может быть гомогенизирована. Согласно одному из аспектов извлеченный хирургической резекцией образец ткани включает один или несколько отдельных кусочков ткани. В дополнительном воплощении один или несколько отдельных кусочков ткани содержат по меньшей мере часть одной или нескольких масс ткани первичной солидной опухоли, извлеченных резекцией из субъекта для получения извлеченного хирургической резекцией образца. Согласно другому аспекту один или несколько отдельных кусочков ткани содержат по меньшей мере часть одного или нескольких лимфатических узлов, извлеченных резекцией из субъекта.
В дополнительном воплощении способ также включает раздельно проводимую гомогенизацию по меньшей мере части отдельных кусочков ткани с получением отдельных гомогенизированных образцов. В дополнительном воплощении извлеченный хирургической резекцией образец ткани содержит массу одной ткани, которая может быть дополнительно разделена на два или более кусочков массы одной ткани. Кроме того, по меньшей мере один из двух или более кусочков массы одной ткани могут быть подвергнуты гомогенизации и консервации. Согласно одному из аспектов гомогенизация может включать физическое разделение, такое как нарезание, шинкование или измельчение. Согласно другому аспекту гомогенизация может включать механическую диссоциацию, например, путем обработки в блендере или обработки в соковыжималке. Согласно еще одному аспекту гомогенизацию осуществляют посредством биохимической диссоциации, например, с использованием протеазы.
Согласно дополнительному аспекту одна или более биомолекул могут быть очищены по меньшей мере из части гомогената, такие биомолекулы могут включать ДНК, РНК, белки, липиды и метаболиты. Затем можно провести анализ биомолекул, например, посредством ПЦР, масс-спектрометрии, методов секвенирования следующего поколения или ELISA. В результате проведения такого анализа получают по меньшей мере один набор данных.
В дополнительном воплощении по меньшей мере часть гомогенизированного образца может быть залита парафином. Согласно дополнительному аспекту способ также включает приготовление одного или нескольких тонких срезов залитого парафином гомогенизированного образца и проведение гистологического анализа образца. Такой гистологический анализ может включать окрашивание гематоксилином-эозином (Н&Е), иммуногистохимическое (IHC) окрашивание, окрашивание с использованием гибридизация in situ (ISH) и окрашивание с использованием флуоресцентной гибридизации in situ (FISH). Результат гистологического анализа может быть интерпретирован человеком или количественно определен на автоматизированном устройстве. В дополнительном воплощении после такой интерпретации или количественного определения получают по меньшей мере один набор данных.
Согласно одному из аспектов данное изобретение также относится к дальнейшей обработке по меньшей мере части гомогената для получения клеточных фрагментов. Такая обработка может включать физические, механические, химические или ферментативные методы. Такие клеточные фрагменты могут включать ядра, клеточные мембраны и клеточные органеллы. Согласно другому аспекту по меньшей мере часть клеточных фрагментов прикрепляют по меньшей мере к одному предметному стеклу и возможно подвергают гистологическому анализу. Такой гистологический анализ может включать Н&Е окрашивание, IHC окрашивание, ISH окрашивание или FISH окрашивание. Результат такого анализа может быть интерпретирован человеком или количественно определен с применением автоматизированного устройства. В результате выполнения такой интерпретации или количественного определения получают по меньшей мере один набор данных.
Согласно дополнительному аспекту по меньшей мере часть клеточных фрагментов анализируют с применением проточной цитометрии, FACS или анализатора частиц, при этом после проведения такого анализа получают набор данных. Согласно одному из аспектов по меньшей мере один клеточный фрагмент по меньшей мере из части клеточных фрагментов очищают. Такая очистка может быть выполнена, например, посредством FACS, аффинной очистки, дифференциального центрифугирования с разделением на основании размера, фильтрования или электрофореза. В другом воплощении биомолекулы могут быть выделены по меньшей мере из одного клеточного фрагмента, очищенного по меньшей мере из части клеточных фрагментов. Анализ биомолекул может быть проведен посредством ПЦР, масс-спектрометрии, методов секвенирования следующего поколения или ELISA. Согласно одному из аспектов в результате анализа получают по меньшей мере один набор данных.
В еще одном воплощении способ по настоящему изобретению также включает дальнейшую обработку по меньшей мере части гомогената с получением по меньшей мере одной подвергнутой диссоциации клетки, например, физическим, механическим, химическим или ферментативным путем. Подвергнутаая диссоциации клетка представляет собой нормальную клетку, раковую клетку или бактериальную клетку. Согласно одному из аспектов подвергнутую диссоциации клетку прикрепляют по меньшей мере к одному предметному стеклу и подвергают гистологическому анализу. Такой анализ может включать, например, Н&Е окрашивание, IHC окрашивание, ISH окрашивание или FISH окрашивание. В дополнительном воплощении результат такого анализа может быть интерпретирован человеком или количественно определен с применением автоматизированного устройства. В дополнительном воплощении в результате осуществления такой интерпретации или количественного определения получают по меньшей мере один набор данных. Согласно дополнительному аспекту по меньшей мере одну клетку очищают по меньшей мере из одной подвергнутой диссоциации клетки с использованием таких средств, как FACS, аффинная очистка, дифференциальное центрифугирование с разделением на основании размера, фильтрация или электрофорез. В дополнительном воплощении биомолекулы могут быть выделены по меньшей мере из одной клетки, очищенной по меньшей мере из одной подвергнутой диссоциации клетки. Согласно дополнительному аспекту анализ биомолекул может быть проведен, например, посредством ПЦР, масс-спектрометрии, методов секвенирования следующего поколения или ELISA. В дополнительном воплощении после такого анализа получают по меньшей мере один набор данных.
Согласно дополнительному аспекту, по меньшей мере одну клетку, очищенную по меньшей мере из одной подвергнутой диссоциации клетки, прикрепляют по меньшей мере к одному предметному стеклу и возможно проводят гистологический анализ. В дополнительном воплощении гистологический анализ представляет собой Н&Е окрашивание, IHC окрашивание, ISH окрашивание или FISH окрашивание. Результаты такого анализа могут быть интерпретированы человеком или определены количественно с помощью автоматизированного устройства. Согласно дополнительному аспекту в результате? анализа или интерпретации получают по меньшей мере один набор данных.
В дополнительном воплощении наборы данных, полученные описанными выше способами, анализируют далее. Согласно одному из аспектов такой анализ включает определение разнообразия биомаркеров или фенотипического разнообразия. В дополнительном воплощении анализ включает принятие по меньшей мере одного клинического решения. Такое клиническое решение, согласно одному из аспектов, включает в себя определение прогноза заболевания, предсказание рецидива заболевания, предсказание мишеней для лечения заболевания, включение субъектов в клинические испытания или стратегию терапевтического лечения по меньшей мере для одного субъекта.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Относящийся к патенту или заявке файл содержит по меньшей мере один графический материал, выполненный в цвете. Копии публикации этого патента или этой патентной заявки с цветным(ыми) графическим(ими) материалом(ами) будут предоставлены Ведомством по запросу и при оплате необходимой пошлины.
На ФИГ. 1А-1С приведены схематичные представления описанных способов приготовления образцов при патологии. ФИГ. 1А представляет иллюстрацию приготовления образцов толстой кишки; ФИГ. 1В представляет иллюстрацию приготовления образцов ткани легкого; ФИГ. 1С представляет иллюстрацию приготовления образцов ткани почки.
ФИГ. 2А и 2В представляют иллюстрацию схематичного представления гомогената по изобретению. ФИГ. 2А представляет иллюстрацию того, как с использованием описанных способов гомогенизации приготовить репрезентативный образец, содержащий субклоны в той пропорции, в которой они существовали в солидной опухоли. ФИГ. 2В представляет иллюстрацию того, как использование гомогената облегчает обнаружение субклонов с низкой распространенностью.
ФИГ. 3 представляет блок-схему, схематично изображающую описываемый протокол с использованием физических, механических, биохимических способов приготовления репрезентативных опухолевых образцов, которые являются репрезентативным примером гетерогенности в опухоли.
ФИГ. 4 представляет график, показывающий результаты фракционирования репрезентативного образца по размерам.
ФИГ. 5А-С показывают Н&Е окрашивание прошедших и удержанных фракций, собранных после серии фильтрований расщепленного биохимическим путем репрезентативного образца. ФИГ. 5А представляет иллюстрацию результата Н&Е окрашивания фракции, удержанной на сетке (вверху) и прошедшей через микронную сетку (внизу). ФИГ. 5В представляет иллюстрацию результата Н&Е окрашивания фракции, удержанной на сетке (вверху) и прошедшей через микронную сетку (внизу). ФИГ. 5С представляет иллюстрацию результата Н&Е окрашивания фракции, удержанной на сетке (вверху) и прошедшей через микронную сетку (внизу).
ФИГ. 6A-6D показывают детектирование белка в репрезентативном образце, приготовленном из Her2-положительного ксенотрансплантата, происходящего из клеток рака молочной железы человека, смешанного с тканью животного посредством гомогенизации, с последующим расщеплением биохимическим путем в условиях выдерживания при определенных температуре и рН. ФИГ. 6А представляет иллюстрацию результата предварительного выдерживания в СС1 буфере при 85°С. ФИГ. 6В представляет иллюстрацию результата предварительного выдерживания в СС1 буфере при 85°С с последующим расщеплением коллагеназой Н в течение по меньшей мере 30 минут. ФИГ. 6С представляет иллюстрацию образца, подвергнутого механической диссоциации, предварительно выдержанного в СС1 буфере и расщепленного коллагеназой Н. ФИГ. 6D представляет изображение тканей животного, т.е. куриной грудки, рыбного филе и куриной печени, вместе с Her2-положительным ксенотрансплантатом и вид после обработки в блендере для получения репрезентативного образца, проанализированного так, как показано на ФИГ. 6А-6С.
ФИГ. 7А и 7В показывают репрезентативный образец, приготовленный из ткани человека с использованием расщепления биохимическим путем в условиях выдерживания при определенных температуре и рН, после механической диссоциации. ФИГ. 7А представляет иллюстрацию результата предварительного выдерживания в СС1 буфере с последующим расщеплением коллагеназой Н в течение 30 минут. ФИГ. 7В представляет иллюстрацию результата увеличения продолжительности расщепления коллагеназой Н после предварительного выдерживания в СС1.
ФИГ. 8A-8D показывают детектирование белка в репрезентативном образце, приготовленном из образца почки человека. ФИГ. 8А представляет иллюстрацию результата Н&Е окрашивания репрезентативного образца почки человека после механической диссоциации, предварительного выдерживания и ферментативного расщепления. ФИГ. 8В представляет иллюстрацию результата основанного на применении DAB (3,3'-диаминобензидин) IHC анализа репрезентативного образца почки человека в отношении детектирования PD-L1. ФИГ. 8С представляет иллюстрацию результата DAB-IHC анализа репрезентативного образца почки человека в отношении детектирования CD8. ФИГ. 8D представляет иллюстрацию результата DAB-IHC анализа репрезентативного образца почки человека в отношении детектирования Ер-Cam. В левой колонке показаны срезы, содержащие репрезентативный образец, с 10-кратным увеличением, в то время как в правой колонке показаны срезы, содержащие репрезентативный образец, с 20-кратным увеличением.
ФИГ. 9A-9D показывают детектирование белка в репрезентативном образце, приготовленном из образца легкого человека. ФИГ. 9А представляет изображение образца опухоли легкого размером приблизительно 3 см, используемого в качестве исходного материала для приготовления репрезентативного образца; ФИГ. 9В представляет иллюстрацию результата Н&Е окрашивания репрезентативного образца легкого человека после механической диссоциации, предварительного выдерживания и ферментативного расщепления; ФИГ. 9С представляет иллюстрацию результата DAB-IHC анализа репрезентативного образца легкого человека в отношении детектирования PD-L1; ФИГ. 9D представляет иллюстрацию результата DAB-IHC анализа репрезентативного образца легкого человека в отношении детектирования CD8; ФИГ. 9Е представляет иллюстрацию результата DAB-IHC анализа репрезентативного образца легкого человека в отношении детектирования Ер-Cam.
ФИГ. 10 представляет иллюстрацию типичного протокола иммуноцитохимического (ICC) анализа с применением DAB, приведенного для стадий 1-102, для детектирования белков в репрезентативных образцах. В этом конкретном примере протокол использовали для детектирования Her2.
На ФИГ. 11 приведен типичный протокол флуоресцентной ICC (приведенный для стадий 1-38) для детектирования белков в репрезентативных образцах.
На ФИГ. 12 показано детектирование CD20, характерного для В-клеток, с использованием автоматизированного DAB-ICC анализа, в репрезентативном образце, полученном из смеси проб ткани животного и миндалин человека. CD20 детектировали в клетках из ткани миндалин человека, содержащейся в репрезентативном образце.
На ФИГ. 13А и 13В показано обнаружение Her2-положительных клеток Calu-3, присутствующих в репрезентативном образце, приготовленном из ткани миндалин и Her-2-положительного ксенотрансплантата опухоли, с использованием флуоресцентной ICC. ФИГ. 13А представляет иллюстрацию репрезентативного образца, содержащего клетки Calu-3, инкубированные только с вторичным антителом (отрицательный контроль). Фоновый сигнал в клетках Calu-3, генерируемый вторичным антителом, обозначен стрелкой, изображенной пунктирной линией. ФИГ. 13В представляет иллюстрацию репрезентативного образца, содержащего клетки Calu-3, инкубированные с антителом к Her2 (4В5), перед добавлением вторичного антитела.
На ФИГ. 14 представлен типичный протокол мультиплексного хромогенного ICC анализа (приведенный для стадий 1-225) для детектирования нескольких белков в репрезентативном образце.
На ФИГ. 15 показано детектирование Ki-67, CD20 и CD3 с использованием мультиплексного хромогенного IHC анализа в репрезентативном образце, приготовленном из пробы миндалин человека.
На ФИГ. 16 показано обнаружение b-Raf-положительных клеток, присутствующих с показателем распространенности примерно 0,015% в репрезентативном образце миндалин.
На ФИГ. 17 показана гомогенизированная ткань миндалины с 5-кратным увеличением. Обратите внимание на масштабную линейку, показывающую длину 50 микрон.
На ФИГ. 18А и 18В показаны изображения оставшегося операционного материала. ФИГ. 18А представляет иллюстрацию материала после резекции толстой кишки, который все еще содержит аденокарциному толстой кишки размером восемь (8) см; ФИГ. 18В представляет иллюстрацию ткани, оставшейся после частичной нефректомии почки с папиллярной уротелиальной опухолью почки.
На ФИГ. 19А-19С показано Н&Е окрашивание различающихся гистологических срезов, полученных из аденокарциномы толстой кишки. ФИГ. 19А представляет иллюстрацию первого среза, полученного из аденокарциномы толстой кишки; в то время как ФИГ. 19В представляет иллюстрацию второго и отличающегося среза из аденокарциномы толстой кишки. Каждый из срезов, представленных на ФИГ. 19А и 19В, был приготовлен патологоанатомом. Разница в Н&Е окрашивании показывает вариацию в пределах одной и той же опухоли. ФИГ. 19С представляет иллюстрацию Н&Е окрашивания репрезентативного образца, приготовленного из аденокарциномы толстой кишки.
На ФИГ. 20А-20С показано Н&Е окрашивание различающихся гистологических срезов, полученных из папиллярной уротелиальной опухоли почки. ФИГ. 20А представляет иллюстрацию первого среза, взятого из папиллярной уротелиальной опухоли почки; ФИГ. 20В представляет иллюстрацию второго, отличающегося от первого, среза, взятого из папиллярной уротелиальной опухоли почки. Каждый из срезов, проиллюстрированных на ФИГ. 20А и 20В, был приготовлен патологоанатомом. Разница в Н&Е окрашивании показывает вариацию в пределах одной и той же опухоли. ФИГ. 20С представляет иллюстрацию Н&Е окрашивания репрезентативного образца, приготовленного из папиллярной уротелиальной опухоли почки.
На ФИГ. 21А-21С показан результат Alk DAB окрашивания различающихся гистологических срезов, полученных из аденокарциномы толстой кишки. ФИГ. 21А представляет иллюстрацию первого среза, взятого из аденокарциномы толстой кишки; ФИГ. 21В представляет иллюстрацию второго, отличающегося от первого, среза, взятого из аденокарциномы толстой кишки. Каждый из срезов, проиллюстрированных на ФИГ. 21А и 21В был приготовлен патологоанатомом. Разница в Alk DAB окрашивании показывает вариацию в пределах одной и той же опухоли. ФИГ. 21С представляет иллюстрацию выполненного с применением Alk DAB окрашивания репрезентативного образца, приготовленного из аденокарциномы толстой кишки.
На ФИГ. 22А-22С показан результат Alk DAB окрашивания различающихся гистологических срезов, полученных из папиллярной уротелиальной опухоли почки. ФИГ. 22А представляет иллюстрацию первого среза, взятого из папиллярной уротелиальной опухоли почки; ФИГ. 22В представляет иллюстрацию второго, отличающегося от первого, среза, взятого из папиллярной уротелиальной опухоли почки. Каждый из срезов, проиллюстрированных на ФИГ. 22А и 22В был приготовлен патологоанатомом. Разница в Alk DAB окрашивании показывает вариацию в пределах одной и той же опухоли. ФИГ. 22С представляет иллюстрацию выполненного с применением Alk DAB окрашивания репрезентативного образца, приготовленного из папиллярной уротелиальной опухоли почки.
ФИГ. 23 представляет изображение присутствующих в опухоли тромбоцитов и других клеток крови, выделенных посредством центрифугирования из расщепленного биохимическим путем репрезентативного образца. Карциноидную опухоль яичника человека, серозный вариант, подвергали обработке в блендере и расщеплению с использованием AccuMax® и коллагеназы Н, после чего центрифугировали, что приводило к накоплению тромбоцитов и эритроцитов в верхней части подвергнутого центрифугированию образца (красная линия).
На ФИГ. 24 показан результат окрашивания на HPV16 с использованием ISH на клетках Caski в репрезентативном образце, приготовленном из ткани, извлеченной из парафинового блока. Ткань, которая предварительно была залита парафиновым воском, извлекали и гомогенизировали в блендере от IKA с получением репрезентативного образца.
ФИГ. 25A-D показывают изображения Н&Е-окрашенных гистологических срезов, приготовленных из нарезанных и измельченных миндалин. ФИГ. 25А и 25В представляют иллюстрации нарезанной вручную ткани (приблизительно 2 мм2), тогда как ФИГ. 25С и 25D представляют иллюстрации ткани, измельченной с помощью "соковыжималки" (приблизительно 200 мкм2).
На ФИГ. 26A-26D показан подвергнутый механической обработке в блендере и фильтрованию образец опухоли толстой кишки. ФИГ. 26А представляет светлопольное изображение сбора 1; ФИГ. 26В представляет светлопольное изображение сбора 2; ФИГ. 26С представляет светлопольное изображение сбора 3; и ФИГ. 26D представляет светлопольное изображение фильтрата.
На ФИГ. 27А-27С показано распределение по размерам для подвергнутых механической диссоциации и фильтрованию одиночных клеток. На ФИГ. 27А показаны клетки из образца опухоли толстой кишки; на ФИГ. 27В показаны подвергнутые механической диссоциации и фильтрованию иммунные клетки из миндалин; и на ФИГ. 27С показаны ЕрСАМ-положительные клетки (опухолевые клетки), отсортированные из подвергнутых механической диссоциации и фильтрованию клеток из образца опухоли толстой кишки.
На ФИГ. 28 показано флуоресцентное изображение ЕрСАМ-положительных опухолевых клеток, подвергнутых механической диссоциации и фильтрованию из образца опухоли толстой кишки и отсортированных с помощью клеточного сортера SH800 от Sony.
На ФИГ. 29A-29F показаны подвергнутые механической диссоциации и фильтрованию опухолевые клетки из толстой кишки, окрашенные на клеточные маркеры CK8/18 (ФИГ. 29В), CD45 (ФИГ. 29С), CD8 (ФИГ. 29D), PD-L1 (ФИГ. 29Е) и EGFR (ФИГ. 29F), и проанализированные с помощью проточного цитометра с акустической фокусировкой Attune. ФИГ. 29А представляет иллюстрацию того, как для различения дублетов использовали сравнение FSC-A с FSC-H. Красный цвет: положительно окрашенные клетки, и фиолетовый цвет: контроль (окрашенные клетки в отсутствие первичного антитела (Ab)).
На ФИГ. 30А-30С показаны результаты анализа отсортированных с помощью клеточного сортера SH800 от Sony ЕрСАМ-положительных клеток. На ФИГ. 30А использован техасский красный; на ФИГ. 30В использован DAPI; на ФИГ. 30С использован DAPI. ЕрСАМ-положительные клетки соответствуют клеткам с более высоким содержанием ДНК на основании графика зависимости интенсивности DAPI.
На ФИГ. 31А и ФИГ. 31В показан результат сортировки подвергнутых диссоциации клеток миндалины с использованием магнитных гранул. На ФИГ. 31А показано, что для различения дублетов использовали сравнение FSC-A с FSC-H. Для сравнения использовали флуоресцентные клетки выше определенного порога. ФИГ. 31В представляет иллюстрации гистограмм, показывающих процентное содержание флуоресцентных клеток (CD3- или CD8-положительных клеток) во всей популяции клеток до и после истощения.
На ФИГ. 32 показаны результаты ультразвуковой обработки многоклеточных агрегатов. После ультразвуковой обработки многоклеточных агрегатов (размер популяции от 12 до 18 мкм) получаются одиночные клетки (размер популяции от 5,5 до 9,3 мкм). Размер образованных одиночных клеток соответствует размеру опухолевых клеток.
На ФИГ. 33A-33D показаны многоклеточные агрегаты, обработанные коллагеназой, затем обработанные ультразвуком. На ФИГ. 33А показано распределение по размерам обработанных коллагеназой клеточных агрегатов с ультразвуковой обработкой; на ФИГ. 34В показано распределение по размерам обработанных коллагеназой клеточных агрегатов без ультразвуковой обработки. ФИГ. 33С представляет иллюстрации изображений образцов, показанных на ФИГ. 33А; ФИГ. 33D представляет иллюстрации изображений образцов показанных на ФИГ. 33B.
ФИГ. 34 показывает содержание РНК и ДНК, выделенных из гомогенатов, приготовленных из репрезентативных образцов (Rep) и свежеполученной (Trad) ткани миндалин.
На ФИГ. 35A-35D показана стабильность РНК при разных условиях хранения в течение 6 месяцев. ФИГ. 35А представляет иллюстрацию того, что ткань из хорошо дифференцированной нейроэндокринной опухоли поджелудочной железы инкубировали в необходимых стандартных растворах для хранения клеток; ФИГ. 35В представляет иллюстрацию того, что ткань из папиллярной уротелиальной карциномы инкубировали в необходимых стандартных растворах для хранения клеток; ФИГ. 35С представляет иллюстрацию того, что ткань из аденокарциномы толстой кишки инкубировали в указанных стандартных растворах для хранения клеток.
На ФИГ. 36А и В показана стабильность белка при разных условиях хранения в течение 6 месяцев. ФИГ. 36А представляет иллюстрацию того, что белок, по результатам измерений с использованием IHC для C-met, стабилен при папиллярной уротелиальной карциноме при всех условиях хранения и температурах; ФИГ. 36В представляет иллюстрацию того, что белок, по результатам измерений с использованием IHC для C-met, стабилен при аденокарциноме толстой кишки при всех условиях хранения и температурах.
На ФИГ. 37 и 37В показана стабильность клеток и белка на протяжении повторных циклов замораживания-оттаивания для репрезентативного образца, приготовленного из аденокарциномы толстой кишки. ФИГ. 37А представляет иллюстрацию стабильности морфологии клеток, которую исследовали с использованием Н&Е окрашивания; ФИГ. 37В представляет иллюстрацию стабильности белка, которую определяли по окрашиванию клеток на C-met.
На ФИГ. 38 показана стабильность нуклеиновых кислот (ДНК и РНК) на протяжении повторных циклов замораживания-оттаивания для репрезентативного образца, приготовленного из аденокарциномы толстой кишки.
На ФИГ. 39 показана иллюстрация схемы детектирования Her2/Chr17 (хромосома 17).
На ФИГ. 40 показано исследование депарафинизации. Представлены изображения выделенных ядер, полученных из ткани толстой кишки и окрашенных на Her2 (серебро) и хромосому 17 (красный) (40х). В качестве вариантов депарафинизации рассматривали А: депарафинизацию с использованием технологии жидких покровных стекол (LCS), В: депарафинизацию с использованием раствора EZ prep и С: вариант с загрузкой влажного растворителя вместо депарафинизации.
На ФИГ. 41 показано исследование гибридизации в зависимости от времени инкубации. Представлены изображения выделенных ядер, полученных из ткани толстой кишки и окрашенных на Her2 (серебро) и хромосому 17 (красный) (40х). В качестве вариантов гибридизации рассматривали А: гибридизацию в течение 1 часа, В: гибридизацию в течение 2 часов и С: гибридизацию в течение 4 часов.
На ФИГ. 42А и 42В показаны репрезентативные образцы из ткани миндалин, подвергнутой диссоциации ферментативными методами. ФИГ. 42А представляет иллюстрацию Н&Е-окрашенных срезов ткани после расщепления пепсином, 5 мг/мл, при 37 градусах С, в течение 30 мин (левая панель) или 24 часов (правая панель). ФИГ. 42В представляет иллюстрацию Н&Е-окрашенных срезов ткани после расщепления трипсином, 0,25%-ным, при 37 градусах С в течение 30 мин (левая панель) или 24 часов (правая панель).
ФИГ. 43 представляет график для частиц размером ниже 100 микрон, выделенных из параллельных репрезентативных образцов миндалин с использованием различных ферментативных методов, проиллюстрированных в Таблице 6.
На ФИГ. 44А показан график, иллюстрирующий частицы размером ниже 100 микрон, выделенные из репрезентативных образцов миндалин, подвергнутых диссоциации механическими методами или методами с использованием протеиназы K-пепсина. Величина ошибок представляет собой стандартное отклонение (S.D.) для трех независимых экспериментов: **р = 0,0037 с использованием непарного Т-критерия. На ФИГ. 44В показаны светлопольные изображения Н&Е-окрашенных срезов для частиц, выделенных с использованием механической диссоциации; на ФИГ. 44С показаны светлопольные изображения Н&Е-окрашенных срезов для частиц, выделенных с использованием методов с применением протеиназы K-пепсина.
На ФИГ. 45А и 45В показана воспроизводимость способа выделения ядер. ФИГ. 45А представляет гистограмму, показывающую средний выход ядерных частиц, выделенных из аликвот репрезентативных образцов, приготовленных из опухоли толстой кишки (N = 3) и легкого (N = 4). ФИГ. 45В представляет график, показывающий распределение ядерных частиц, полученных из аликвот репрезентативного образца опухоли толстой кишки, с шагами разбиения в соответствии с размером частиц.
На ФИГ. 46А и 46В показана оценка клеточного повреждения, ассоциированного с механической и ферментативной обработкой. ФИГ. 46А представляет собой гистограмму, показывающую среднее процентное содержание ДНК, высвободившейся в результате диссоциации репрезентативных образцов миндалин с использованием механического (mech) способа или способа с применением протеиназы K (ProtK) и пепсина (Pep). ФИГ. 46В представляет собой гистограмму, показывающую процентное содержание ДНК, высвободившейся в результате диссоциации репрезентативных опухолевых образцов.
На ФИГ. 47А и 47В показаны результаты проточного цитометрического анализа в отношении агрегации частиц, выделенных из фиксированной в формалине ткани миндалины способом с применением протеиназы K-пепсина. На ФИГ. 47А показаны образцы, полученные с использованием autoMACS буфера; на ФИГ. 47В показаны образцы, полученные с использованием autoMACS буфера с 1% твина 20.
На ФИГ. 48A-48D показана аденокарцинома толстой кишки (ADC), окрашенная на цитокератин 8/18 (CK-8/18). ФИГ. 48А представляет иллюстрацию светлопольного изображения среза ткани, окрашенного на CK-8/18 в иммуногистохимическом (IHC) анализе. Пораженные ADC ткани, подвергнутые визуализации с использованием CK-8/18, окрашены коричневым цветом; ФИГ. 48В представляет иллюстрацию светлопольного изображения репрезентативного образца, который подвергали механической диссоциации, заливали парафиновым воском с последующим приготовлением срезов и окрашивания на CK-8/18 в IHC анализе. CK-8/18-положительные ткани окрашены коричневым цветом; ФИГ. 48С представляет иллюстрацию флуоресцентного изображения репрезентативного образца, подвергнутого диссоциации с использованием способа с применением протеиназы K-пепсина и окрашенного в растворе на DAPI и CK-8/18, визуализированного с использованием Alexa 488. Псевдоокрашенные изображения отражают окрашивание на CK-8/18 (зеленый) и DAPI (синий). ФИГ. 48D представляет иллюстрацию отрицательных контрольных образцов тканей, показанных на ФИГ. 48С, которые инкубировали без антитела к CK-8/18. Все образцы готовили из одной и той же опухоли ADC толстой кишки.
На ФИГ. 49А и 49В показано, что тирамидная амплификация сигнала_(TSA) улучшает окрашивание материала, выделенного из репрезентативных образцов. ФИГ. 49А представляет иллюстрацию изображений (20х) выделенных механическим путем клеток из фиксированной ткани миндалин, окрашенной на CD45 (красный) стандартным методом с применением иммунофлуоресценции (IF, верхняя левая панель) или методом с применением TSA (верхняя правая панель). Окрашивание с использованием DAPI (синий) помечает ядра. Для обоих изображений использовали продолжительность экспонирования 100 мс. ФИГ. 49В представляет иллюстрацию изображений (40х) ядер, выделенных из фиксированной опухолевой ткани, окрашенной с применением TSA. На левых панелях показаны изображения клеток, окрашенных с использованием первичного антитела (отрицательный контроль), а на правых панелях показано окрашивание с использованием первичных антител к цитокератину (красный). Окрашивание с использованием DAPI (синий) помечает ядра. Для всех изображений использовали продолжительность экспонирования 2 мс.
На ФИГ. 50 показано, что положительное окрашивание на цитокератин (CK) позволяет отличить ядра опухолевых клеток от ядер нормальных клеток. Представлены гистограммы данных проточной цитометрии для ядер, выделенных из репрезентативных образцов опухоли толстой кишки (верхняя панель) или опухоли легкого (нижняя панель).
На ФИГ. 51А-51С показан клеточный состав опухолей. ФИГ. 51А представляет иллюстрацию, с использованием проточной цитометрии, фракции ядер, выделенных из аденокарциномы толстой кишки (389); ФИГ. 51В представляет иллюстрацию фракции ядер, выделенных из плоскоклеточной карциномы легкого (528); во всех случаях использовали обозначение "нормальные клетки" в сравнении с "опухолевыми клетками".
ФИГ. 52 представляет иллюстрацию графика, показывающего результат количественного определения выхода ДНК из ядер, выделенных из репрезентативных образцов.
На ФИГ. 53А и 53В представлены полученные для целого предметного стекла изображения гистологического среза, отобранного из интактной миндалины, окрашенной с использованием антитела к пан-кератину. ФИГ. 53А представляет иллюстрацию традиционного гистологического среза нормальной миндалины после детектирования с использованием DAB на пан-кератин. ФИГ. 53В представляет иллюстрацию среза из репрезентативного образца миндалины после детектирования с использованием DAB на пан-кератин.
На ФИГ. 54А и 54В представлены изображения образцов гомогенизированной миндалины после заливки парафином и приготовления из нее срезов. На ФИГ. 54А представлен традиционный гистологический срез нормальной миндалины после детектирования с использованием DAB на CD8. На ФИГ. 54В представлен срез из репрезентативного образца миндалины после детектирования с использованием DAB на CD8.
ФИГ. 55 представляет диаграмму организации рабочего процесса по настоящему изобретению.
ПОДРОБНОЕ ОПИСАНИЕ
Следует понимать, что настоящее изобретение не ограничивается конкретными описанными аспектами, поскольку таковые, несомненно, могут варьировать. Также следует понимать, что терминология, использованная в данном описании, приводится только с целью описания конкретных аспектов и не предназначена для ограничения ввиду того, что объем настоящего изобретения будет ограничен только прилагаемой формулой изобретения.
Если не определено иным образом, то все технические и научные термины, использованные в данном описании, имеют те же значения, которые обычно понимаются специалистом средней квалификации в области техники, к которой эта технология относится. Несмотря на то, что при практическом применении или испытании технологии по настоящему изобретению могут быть использованы способы и материалы, аналогичные или эквивалентные описанным в данной заявке, теперь будут описаны предпочтительные способы, устройства и материалы. Все технические и патентные публикации, упоминаемые в данной заявке, включены в данное описание посредством ссылки во всей своей полноте. Ничто в данном описании не должно истолковываться как признание того, что технология по настоящему изобретению не имеет права предвосхищать такое описание исходя из предшествующего изобретения.
При практическом применении технологии по настоящему изобретению будут применены, если не указано иное, традиционные методы культивирования тканей, иммунологии, молекулярной биологии, микробиологии, клеточной биологии и рекомбинантной ДНК, которые известны специалисту в данной области техники. См., например, Sambrook and Russell eds. (2001) Molecular Cloning: A Laboratory Manual, 3-е издание; серию Ausubel et al. eds. (2007) Current Protocols in Molecular Biology; серию Methods in Enzymology (Academic Press, Inc., N.Y.); MacPherson et al. (1991) PCR 1: A Practical Approach (IRL Press at Oxford University Press); MacPherson et al. (1995) PCR 2: A Practical Approach; Harlow and Lane eds. (1999) Antibodies, A Laboratory Manual; Freshney (2005) Culture of Animal Cells: A Manual of Basic Technique, 5-е. издание; Gait ed. (1984) Oligonucleotide Synthesis; патент США №4683195; Hames and Higgins eds. (1984) Nucleic Acid Hybridization; Anderson (1999) Nucleic Acid Hybridization; Hames and Higgins eds. (1984) Transcription and Translation; Immobilized Cells and Enzymes (IRL Press (1986)); Perbal (1984) A Practical Guide to Molecular Cloning; Miller and Calos eds. (1987) Gene Transfer Vectors for Mammalian Cells (Cold Spring Harbor Laboratory); Makrides ed. (2003) Gene Transfer and Expression in Mammalian Cells; Mayer and Walker eds. (1987) Immunochemical Methods in Cell and Molecular Biology (Academic Press, London); и Herzenberg et al. eds (1996) Weir's Handbook of Experimental Immunology.
Все цифровые обозначения, например, для рН, температуры, времени, концентрации и молекулярной массы, включая их диапазоны, представляют собой приблизительныеи величины, которые варьируют (+) или (-) с приращениями 1,0 или 0,1, при необходимости, или альтернативно с вариацией +/- 15%, или альтернативно 10%, или альтернативно 5%, или альтернативно 2%. Следует понимать, хотя не всегда имеется четкое указание, что все цифровые обозначения предваряются термином "примерно". Также следует понимать, хотя не всегда имеется четкое указание, что реагенты, описанные в данной заявке, являются всего лишь типичными и что в данной области техники известны эквиваленты таких реагентов.
Необходимо предположить, без явного описания и если не предусмотрено иное, что когда технология по настоящему изобретению относится к полипептиду, белку, полинуклеотиду или антителу, тогда в рамках технологии по настоящему изобретению предусмотрен эквивалент или биологический эквивалент только что упомянутого выше.
Как использовано в описании и формуле изобретения, артикли "a", "an" и "the", определяющие форму единственного числа, включают в себя ссылки на множественное число, если контекст ясно не предусматривает иное. Например, термин "клетка" включает множество клеток, в том числе их смеси.
Использованный в данном описании термин "животное" относится к живым многоклеточным организмам позвоночных, категория которых включает, например, млекопитающих и птиц. Термин "млекопитающее" включает в себя и являющихся человеком, и не являющихся человеком млекопитающих.
Термины "субъект", "реципиент", "индивидуум" и "пациент", как использованные взаимозаменяемо в данном описании, относятся к участникам медицинских и ветеринарных исследований, например, людям, животным, не являющимся человеком приматам, собакам, кошкам, овцам, мышам, лошадям и крупному рогатому скоту. В некоторых воплощениях, субъектом является человек.
"Композиция" обычно подразумевает комбинацию активного агента, например, соединения или композиции, и природного или неприродного носителя, инертного (например, детектируемый агент или метка) или активного, такого как адъювант, разбавитель, связующее вещество, стабилизатор, буферы, соли, липофильные растворители, консервант, адъювант или тому подобное, и включает фармацевтически приемлемые носители. Носители также включают фармацевтические эксципиенты и вспомогательные белки, пептиды, аминокислоты, липиды и углеводы (например, сахара, в том числе моносахариды, ди-, три-, тетра-олигосахариды и олигосахариды; производные сахаров, такие как альдиты, альдоновые кислоты, этерифицированные сахара и тому подобное; и полисахариды или полимеры сахаров), которые могут быть представлены в одиночку или в комбинации, с содержанием по отдельности или в комбинации, составляющим 1-99,99% по массе или объему. Типичные белковые эксципиенты включают сывороточный альбумин, такой как сывороточный альбумин человека (HSA), рекомбинантный альбумин человека (rHA), желатин, казеин и тому подобное. Репрезентативные компоненты, такие как аминокислоты/антитела, которые также могут вносить вклад в буферную емкость, включают аланин, аргинин, глицин, аргинин, бетаин, гистидин, глутаминовую кислоту, аспарагиновую кислоту, цистеин, лизин, лейцин, изолейцин, валин, метионин, фенилаланин, аспартам и тому подобное. В объеме этой технологии также подразумевается использование углеводных эксципиентов, примеры которых включают, но не ограничиваются этим, моносахариды, такие как фруктоза, мальтоза, галактоза, глюкоза, D-манноза, сорбоза и тому подобное; дисахариды, такие как лактоза, сахароза, трегалоза, целлобиоза и тому подобное; полисахариды, такие как раффиноза, мелицитоза, мальтодекстрины, декстраны, крахмалы и тому подобное; и альдиты, такие как маннит, ксилит, мальтит, лактит, ксилит, сорбит (глюцит) и миоинозит.
Если не указано иное, то все технические и научные термины, использованные в данном описании, имеют то же значение, которое обычно понимается специалистом средней квалификации в области техники, к которой это изобретение относится.
Термин "репрезентативный образец" в данном изобретении относится к образцу (или подгруппе образцов), который достоверно отражает компоненты целого, и поэтому такой образец определяет объективное показание всей совокупности. Образцы происходят из солидных органов, тканей и опухолей ("ОТТ"), которые изначально составлены из пространственно обособленных клеточных структур и далее организуются в пространственно обособленные типы клеток. Методы и способы отбора репрезентативных образцов являются такими, при применении которых гомогенизация, перемешивание или иное разрушение пространственно неоднородной трехмерной структуры ОТТ осуществляется в достаточной степени, в результате чего компоненты (клеточные структуры, клетки, пептиды, нуклеиновые кислоты, липиды, метаболиты и т.д.) исходных пространственно неоднородных ОТТ представлены в субобразце (также известном как аналитический образец) в пропорции, в которой они существуют в исходных органе, ткани или опухоли. В некоторых воплощениях репрезентативный образец относится к образцу ОТТ, который составляет как можно большую часть ОТТ, приближаясь ко всей массе ОТТ или охватывая достаточно значительную часть ОТТ для приближения к цели представления разнообразия ОТТ на уровне кластеров соединенных друг с другом клеток, отдельных клеток, фрагментов клеток, органелл, пептидов, нуклеиновых кислот, липидов, метаболитов и т.д. Репрезентативный образец может содержать минимальное количество интактных ОТТ, необходимое, чтобы охватить разнообразие ОТТ. В дополнительном воплощении репрезентативный образец может содержать множество сегментов или частиц, при этом по меньшей мере часть этих частиц залита парафином и по меньшей мере часть остальных частиц подвергнута гомогенизации.
Из одиночных ОТТ можно приготовить много репрезентативных образцов. В таком воплощении сначала выполняют обработку удаленных или иссеченных хирургическим путем ОТТ или иную манипуляцию с ними с получением отдельных субъединиц, в результате чего каждая субъединица будет составлена из пространственно неоднородных клеточных структур, клеток, пептидов, нуклеиновых кислот и т.д. Затем выполняют гомогенизацию, перемешивание или иное разрушение каждой субъединицы в достаточной степени для получения репрезентативного образца из субъединицы ОТТ.
Гомогенизацию или иное перемешивание либо разрушение репрезентативного образца можно выполнить до такой степени, чтобы любой аналитический образец или часть репрезентативного образца содержал(а) случайную выборку образцов из материала, присутствующего в репрезентативном образце. Аналитический образец представляет собой довольно большую долю репрезентативного образца, вследствие чего он охватывает разнообразие репрезентативного образца применительно к предполагаемому результату используемого аналитического теста (т.е. с точки зрения клеток по сравнению с кластерами соединенных друг с другом клеток). В случае любого аналитического образца, используемого для конкретного анализа, будут получены данные, согласующиеся с другим аналитическим образцом, используемым для одного и того же анализа, в пределах экспериментальной ошибки. Помимо этого, любой аналитический образец, выбранный для конкретного анализа, будет предоставлять информацию, которая может быть перекрестно привязана к данным, полученным с помощью разных анализов при использовании аналитических образцов, взятых из одного и того же репрезентативного образца или из других репрезентативных образцов, приготовленных из ОТТ от одного и того же пациента, другого пациента или комбинации пациентов либо субъектов. Поскольку в каждом аналитическом образце, взятом из репрезентативного образца, присутствуют доли исходных биологических компонентов, данные, полученные на основании аналитических образцов, относящиеся к пропорциям биологических компонентов ОТТ, можно сравнивать между пациентами или комбинациями пациентов.
Из репрезентативного образца для анализа могут быть взяты другие образцы с меньшим разнообразием, чем у аналитического образца, например, одиночная клетка. Тем не менее, миллионы одиночных клеток, взятых из репрезентативного образца ОТТ, будут предоставлять "репрезентативный набор данных", который включает в себя "репрезентативные онкологические данные".
В одном из воплощений клетки или клеточные компоненты подвергнуты диссоциации в репрезентативном образце, в результате чего их относительная пропорция или процентное содержание в репрезентативном образце либо его части достоверно отражает или имитирует относительную пропорцию или процентное содержание клеток этих типов или клеточных компонентов во всей пробе интактной ткани. В одном из воплощений пробой может быть солидная опухоль, лимфатический узел, метастазы, полип, киста или их часть либо комбинация любого из вышеперечисленных.
В одном из воплощений репрезентативные образцы, описанные в данной заявке, получают путем гомогенизации больших объемов интактной ткани или образца опухоли (такого как клинический образец опухоли), или лимфатического узла, или метастаза, или их комбинации, полученных от субъекта. Например, целая опухоль или значительная ее часть может быть использована в качестве исходного материала, из которого готовят репрезентативный образец, например, по меньшей мере из 50%, по меньшей мере из 75%, или по меньшей мере из 95%, или предпочтительно из всей опухоли либо всего лимфатического узла. Репрезентативный образец может быть приготовлен на основе образца интактного опухолевого биопсийного материала из солидной опухоли. В одном из воплощений образец содержит по меньшей мере примерно 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 или большее число клеток, возможно из пространственно различающихся участов опухоли. Как правило, в опухоли или ее части, имеющей примерно 1 см в диаметре, содержится примерно 1 миллиард клеток, и в большинстве случаев это соотношение выполняется в линейном масштабе. Например, иссеченный образец, такой как биопсийный материал, имеющий примерно 2 см в диаметре, может содержать 3-5 миллиардов клеток. В другом воплощении репрезентативные образцы, описанные в данной заявке, готовят путем гомогенизации одной или нескольких проб предположительно нормальной ткани, например, происходящей от субъекта с риском развития рака по причине генетической мутации или предыдущего случая рака, или расположенной вблизи нормальной ткани из извлеченного хирургической резекцией материала для применения в качестве контрольного образца.
В дополнительном воплощении термин "репрезентативный опухолевый образец" относится к репрезентативному образцу, приготовленному из опухоли, например, извлеченной резекцией опухоли, или из образца, возможно содержащего раковые клетки, или из образца, подлежащего тестированию в отношении возможного присутствия раковых клеток, такого как лимфатический узел. Аналогичным образом, фраза "опухолевый образец" охватывает образцы, приготовленные из опухоли, или образца, возможно содержащего раковые клетки, или из образца, подлежащего тестированию в отношении возможного присутствия раковых клеток, такого как лимфатический узел.
В дополнительном воплощении термин "репрезентативный нормальный образец" относится к репрезентативному образцу, полученному из предположительно нормальной ткани, например, к биопсийному материалу, полипу или кисте, полученному(ой) от пациента, или к образцу, подлежащему тестированию в отношении возможного присутствия раковых или предраковых клеток или иммунных клеток, указывающих на нарушение в работе иммунной системы. Аналогичным образом, фраза "нормальный образец" охватывает образцы, полученные из предположительно нормальной ткани, например, из биопсийного материала, полипа или кисты, возможно содержащих раковые клетки или подлежащих тестированию в отношении возможного присутствия раковых клеток, например, из лимфатического узла. В дополнительном воплощении "нормальный образец" также может относиться к ткани, которая по всей вероятности не несет признаков заболевания, с которой можно сравнивать опухолевый образец, чтобы идентифицировать фенотипические изменения, обусловленные данным болезненным состоянием.
Термин "репрезентативные данные", использованный в данном описании, относится к любому набору данных (например, в отношении экспрессии гена, процентного содержания клеток определенного типа (например, иммунных клеток), экспрессии белков, экспрессии при SNP (однонуклеотидный полиморфизм) или ее отсутствия, уровня, степени экспрессии микроРНК или числа гистологических подтипов) или относительно небольшому количеству данных, достоверно отражающих полный набор данных, источником которого является репрезентативный образец ткани, органа или опухоли. В одном из воплощений репрезентативные данные представляют собой объективные данные, показывающие разнообразие взятых целиком ткани, органа или опухоли. Как использовано в данном описании, "набор данных" представляет собой совокупность объединенных данных. В одном из воплощений набор данных составлен из отдельных элементов, но с ними можно работать как с единым целым. В одном из воплощений набор данных может включать информацию, касающуюся разнообразия биомаркеров или фенотипического разнообразия.
Использованный в данном описании термин "гистологический анализ" относится к изучению под микроскопом анатомического строения клеток и тканей растений и животных. Этот анализ полезен для сбора информации касательно биологических компонентов образца, например, нуклеиновых кислот (РНК, ДНК), белков, липидов или метаболитов. Гистологические методы включают методы, известные специалисту в данной области техники, при этом некоторые неограничивающие примеры включают ПЦР, масс-спектрометрию, методы секвенирования следующего поколения и ELISA. Помимо этого, гистологический анализ может включать одновременное детектирование более одного биологического компонента, т.е. мультиплексирование.
Как использовано в данном описании, "принятие клинического решения" относится к сбору информации и объединению этой информации с целью представления диагностических заключений и определения, какой из видов лечения будет получать пациент. Такие диагностические заключения могут включать в себя констатацию заболевания, от которого страдает пациент, и какое тестирование следует выполнить пациенту. В одном из воплощений клиническое решение также может включать в себя определение прогноза заболевания, предсказание рецидива заболевания, предсказание мишеней для лечения заболевания, включение субъектов в клинические испытания или определение стратегии терапевтического лечения по меньшей мере для одного субъекта.
Использованный в данном описании термин "гомогенат" относится к биомассе, полученной после подвергания ткани гомогенизации или обработке. Гомогенат может содержать любые клеточные компоненты из ткани, включая, но не ограничиваясь этим, клетки, пептиды, нуклеиновые кислоты, липиды, метаболиты и т.д. Согласно одному из аспектов гомогенат представляет собой репрезентативный образец, который достоверно отражает долю, соотношение или относительное содержание компонентов ткани, из которой он приготовлен. В некоторых воплощениях соотношение клеточных структур, клеточных компонентов или любых составляющих (клеток, пептидов, нуклеиновых кислот, липидов, метаболитов и т.д.) гомогената (либо некоторой или каждой подгруппы гомогената) является одним и тем же, аналогичным или по существу аналогичным соотношению клеточных структур, клеточных компонентов или любых составляющих в исходной интактной ткани. Подобно репрезентативному образцу, гомогенат может содержать минимальное количество интактного органа, интактной ткани или опухоли, необходимое, чтобы охватить разнообразие органа, ткани или опухоли.
Ткань(и), из которой(ых) готовят гомогенат, может(гут) происходить из одной ткани, двух тканей или нескольких тканей. В некоторых воплощениях гомогенат происходит от одного субъекта, двух субъектов или более двух субъектов. Согласно одному из аспектов, два или более субъектов являются генетически гомогенными субъектами. Согласно другому аспекту, два или более субъектов являются фенотипически гомогенными субъектами. Согласно некоторым аспектам, два или более субъектов являются генетически различными субъектами. Согласно одному из аспектов, два или более субъектов являются фенотипически различными субъектами. Согласно другому аспекту, два или более субъектов являются субъектами одного и того же пола. Согласно другому аспекту, два или более субъектов являются субъектами разного пола. Согласно еще одному аспекту, два или более субъектов являются субъектами из групп разной этнической принадлежности. Согласно одному из аспектов, два или более субъектов являются субъектами из группы одной и той же этнической принадлежности. Согласно другому аспекту, субъект выбран из группы, состоящей из животного или человека.
Использованный в данном описании термин "по существу" означает высокую степень идентичности в отношении качества или количества, например, по меньшей мере примерно 60%, либо, альтернативно, по меньшей мере примерно 70%, или альтернативно примерно 80%, или альтернативно примерно 85%, или альтернативно примерно 90%, или альтернативно примерно 95%, или альтернативно примерно 98%.
"Аналогичный" означает "идентичный менее чем на 100%", или альтернативно "идентичный более чем 98%", или альтернативно "идентичный более чем 95%", или альтернативно "идентичный более чем 90%", или альтернативно "идентичный более чем 85%", или альтернативно "идентичный более чем 80%", или альтернативно "идентичный более чем 75%". Термин "однородный" подразумевает идентичность, составляющую по меньшей мере 80%, или альтернативно "идентичный по меньшей мере на" 85%, или альтернативно по меньшей мере на 90%, или альтернативно по меньшей мере на 95%, или альтернативно по меньшей мере на 98%, или альтернативно по меньшей мере на 100%. "Неоднородный" подразумевает "идентичный менее чем на 80%".
Использованный в данном описании термин "подвергнутый обработке" означает, что композиция на основе гомогената подвергнута как минимум физической, механической или химической обработке. Согласно одному из аспектов, полученную композицию на основе гомогената подвергают более чем двум типам обработки. Согласно другим аспектам композицию на основе гомогената подвергают трем типам обработки. Согласно еще одному аспекту гомогенат подвергают четырем более чем четырем типам обработки.
Термин "происходящий из" означает, что образец был приготовлен или получен из некоторого источника.
Термин "подгруппа" означает часть или компонент более многочисленной группы. "Соотношение" представляет собой относительное количественное значение содержания какой-либо части по отношению к более многочисленной группе компонентов или частей.
Использованные в данном описании термины "клеточная структура", "клеточный компонент" или "компонент" можно использовать взаимозаменяемо в отношении любых веществ или материалов, присутствующих в клетках, тканях или организмах, или любых веществ или материалов, которые образуются в процессе и после обработки клеток, тканей или организмов. Вещества или материалы могут быть нативными или чужеродными для клеток, тканей или организмов. Согласно некоторым аспектам, "клеточная структура" и "клеточный компонент" также могут включать любые вещества или материалы, которые являются модифицированными или обработанными, например, клетки или нуклеиновые кислоты, обработанные красителем или радиоактивными материалами. Клеточные структуры или клеточные компоненты включают, но не ограничиваются этим клетки, рецепторы, белки, липиды, клеточные органеллы, мембраны, химические вещества, нуклеиновые кислоты, малые молекулы, бактерии, простейшие, вирусы, паразиты и/или их части или доли. Как использовано в данном описании, термин "фрагменты клетки" включает в себя части целой клетки, такие как ядра, клеточные мембраны и клеточные органеллы.
Использованный в данном описании термин "пространственно различающиеся" или "пространственно обособленные" относится к элементам, которые распределены в разных участках трехмерного пространства. В одном из воплощений репрезентативный образец охватывает все из пространственно различающихся субпопуляций раковых клеток в пределах опухоли. В другом воплощении опухолевые образцы, используемые для приготовления репрезентативного образца, отбирают из разных участков опухолевого образца. Например, из проксимальных участков опухоли в сопоставлении с дистальными, разных краев опухоли, разных слоев опухоли и т.д., чтобы охватить разнообразие всей опухоли.
Термины "гомогенизирование" или "гомогенизация" относятся к процессу (такому как механический процесс и/или биохимический процесс), посредством которого биологический образец приводят в такое состояние, что все части образца в композиции становятся одинаковыми. Репрезентативные аналитические образцы могут быть приготовлены путем отбора части подвергнутого гомогенизации образца. Обычно понимают, что опухоль, лимфатический узел или другой образец, упоминаемый в контексте настоящего изобретения как "превращенный в жидкость", подвергнут перемешиванию или обработке в блендере в достаточной степени, чтобы быть гомогенизированным. Гомогенизированный образец перемешивают таким образом, что удаление некоторой части образца (аликвоты) по существу не изменяет общего компонентного состава остального образца, и компоненты удаленной аликвоты по существу идентичны компонентам остального образца. В настоящем изобретении "гомогенизация" обычно будет обеспечивать сохранение целостности большей части клеток в образце, например, по меньшей мере 50, 80, 85, 90, 95, 96, 97, 98, 99, 99,9% или большая процентная доля клеток в образце не будет разрушена или подвергнута лизису в результате применения метода гомогенизации. Гомогенаты могут быть по существу диссоциированы на отдельные клетки (или кластеры клеток), и полученный гомогенат или полученные гомогенаты являются по существу гомогенными (состоящими из или составленными из аналогичных элементов или однородными по всему объему). В одном из воплощений термин "гомогенизация" относится к процессу, согласно которому обрабатывают ткань или биологический образец до такой степени, что любые подгруппы, части или доли ткани являются аналогичными, по существу аналогичными или идентичными в некоторых аспектах.
В одном из воплощений термин "механическая гомогенизация" относится к гомогенизации, осуществляемой механическими средствами.
Использованный в данном описании термин "биохимическая диссоциация" означает диссоциацию с использованием фермента, такого как протеаза. На биохимическую диссоциацию могут влиять концентрация протеазы, продолжительность и температура инкубации.
Использованный в данном описании термин "физическое разделение" или "физическая диссоциация" образца ткани относится к гомогенизации или диссоциации образца с использованием острого предмета механическим способом, например, путем нарезания, измельчения или шинкования. В результате "нарезания" обычно получают тканевые срезы размером приблизительно от 1,0 мм до 5,0 мм. В результате измельчения обычно получают тканевые срезы размером приблизительно 0,5-2,0 мм. В результате шинкования обычно получают тканевые срезы размером приблизительно 0,1-1,0 мм.
Использованный в данном описании термин "механическое разделение" или "механическая диссоциация" образца ткани относится к гомогенизации или диссоциации образца с использованием механического источника, такого как традиционный блендер, соковыжималка или шаровая мельница, который известен специалисту в данной области техники.
Использованный в данном описании термин "подвергнутая диссоциации клетка" означает клетку, которая некогда представляла собой часть ткани или органа, но которая не отделена от этой ткани или органа.
В зависимости от применяемого к образцу способа механической и/или биохимической диссоциации для получения гомогената, кластеры клеток могут содержать более одной (1) клетки и до нескольких тысяч клеток. Эти кластеры могут быть подвергнуты диссоциации (уменьшению в размере и/или в количестве клеток, содержащихся в них) в результате применения методов дальнейшей обработки, например, в результате дальнейшей механической и/или биохимической диссоциации и/или разделения на основании размера, в зависимости от последующего анализа, выполняемого с использованием репрезентативного образца (например, IHC анализа, для которого необходимы кластеры клеток, содержащие от нескольких десятков до нескольких тысяч клеток, либо FACS или проточной цитометрии, для которых необходимы одиночные клетки или фрагменты клеток).
Описанные в настоящей заявке способы являются адаптируемыми с точки зрения уровня диссоциации образца. Целевой размер агрегатов клеток можно регулировать посредством дальнейшей обработки кластеров клеток, полученных после применения первого механического способа (такого как обработка в блендере или эквивалентная ей обработка), в результате чего эти кластеры соответствуют цели диссоциации метода отбора образцов. Согласно одному из аспектов механическое фрагментирование и разделение на основании размера, например, разделение на сетках с использованием серии сеток, можно использовать для извлечения кластеров клеток, соответствующих определенному размеру или имеющих размер ниже такового, при одновременном сохранении более крупных кластеров клеток для дальнейшей обработки с целью достижения целевого размера частиц. Полученное распределение размеров частиц кластеров клеток оценивают методами разделения на основании размера с целью удаления определенных частиц из процесса диссоциации, скорее для достижения плато разделения на основании размера, чем распределения.
После гомогенизации полученные кластеры могут содержать по меньшей мере 1-2, 2-100, 100-500, 500-1000, 1000-10000, 10000-50000 или большее число клеток. Согласно одному из аспектов кластеры содержат одиночные клетки, примерно 2-10 клеток, примерно 10-20 клеток или примерно 20-40 клеток. Размер полученных кластеров будет варьировать. См., например, ФИГ. 20.
В результате гомогенизации образца распределение клеток в образце соответствует по существу гомогенному распределению в полученном гомогенате либо его части или доли, вследствие чего гомогенат или любая его доля отражает гетерогенность исходного образца. Гомогенизированный образец может быть обозначен как жидкий или превращенный в жидкость образец на основании его способности к растеканию, несмотря на то, что многие клетки или большинство клеток остаются интактными.
В эти гомогенаты или репрезентативные образцы могут быть добавлены другие группировки, например другие клетки, гаптены или метки.
Термин "гетерогенность" относится к разнообразию или неконгруэнтности, например, к сочетанию разных или разнородных частей или к вариантам формы, функции и поведения. Термин "образец гетерогенной ткани" подразумевает образец, который не является однородным по составу или характеристикам, например, является разнообразным по форме, функции или поведению. В контексте рака термин "гетерогенность опухоли" описывает то наблюдение, что разные опухолевые клетки могут проявлять различающиеся морфологические, фенотипические и генетические профили, в том числе клеточную морфологию, экспрессию генов, мутации генов, метаболизм, подвижность, пролиферацию и метастатический потенциал. Гетерогенность может возникать среди опухолей (межопухолевая гетерогенность) и внутри опухолей (внутриопухолевая гетерогенность). Гетерогенность опухолей наблюдалась при различных раковых заболеваниях, включая, но не ограничиваясь этим, рак легкого, лейкозы, рак молочной железы, рак почки, рак предстательной железы, рак толстой кишки, рак головного мозга, рак пищевода, виды рака головы и шеи, рак мочевого пузыря, гинекологические виды карциномы, липосаркомы и множественную миелому. Для объяснения гетерогенности в опухолевых клетках предложены две модели: модель раковых стволовых клеток и модель клональной эволюции. Согласно модели раковых стволовых клеток гетерогенность, наблюдаемая между опухолевыми клетками, обусловлена различиями в раковых стволовых клетках, из которых происходят опухолевые клетки. Согласно модели клональной эволюции опухоли возникают из одной подвергнутой мутации клетки, но накапливают дополнительные мутации (приводящие к появлению дополнительных субпопуляций, каждая из которых обладает способностью делиться и мутировать дальше), что объясняет наблюдаемое разнообразие в раковых клетках из одной и той же опухоли. Считается, что эти модели не являются взаимоисключающими и, таким образом, они обе вероятно, в различном соотношении, вносят вклад в гетерогенность среди опухолей разных типов. Гетерогенность опухолей включает глобальную дисперсию (дисперсию генеральной совокупности) и пространственную структуру этой вариации (пространственную стратификацию генеральной совокупности), и, таким образом, оба элемента вариации следует учитывать в схемах приготовления образцов. Причиной гетерогенности опухолей может быть генетическая гетерогенность (например, в результате воздействия экзогенных факторов, геномной нестабильности, терапии и т.д.), другая гетерогенность (например, эпигенетическая) и/или микроокружение опухоли (например, региональное различие в опухоли, например, в отношении доступности кислорода или иммунного контроля, накладывает различные селективные давления на опухолевые клетки).
Разные популяции опухолевых клеток, которые возникают как результат гетерогенности опухолей, называются "субклонами", потомством мутантной клетки, возникающей в клоне.
Показатель распространенности субклонов в опухоли может варьировать. Некоторые субклоны составляют большую часть опухоли, но со временем и/или после определенных видов лечения их размер уменьшается. Другие субклоны изначально не обнаруживаются, но позже становятся самыми многочисленными. Несколько субклонов могут существовать одновременно и отличаться в показателе своей распространенности с течением времени, которое требуется для того, чтобы опухоль стала настолько большой, чтобы ее можно было обнаружить. Термин "события с низкой распространенностью" или "генетические события с низкой распространенностью" применительно к опухоли относится к редко встречающимся событиям или редко встречающимся генетическим событиям (таким как мутации), которые происходят с частотой 10-1%, 1-0,1%, 0,1-0,01%, 0,01-0,001%, 0,001-0,0001%, 0,0001-0,00001%, 0,00001-0,000001% или ниже 0,000001%. Поскольку образец, приготовленный описываемыми способами, является репрезентативным (или по существу репрезентативным) для опухоли в целом, то можно обнаружить субклоны даже с низкой распространенностью (например, ниже по меньшей мере 0,000001%) в опухоли или биологическом образце, помимо всех других субклонов, которые встречаются с более высокими показателями распространенности.
Термин "биологический образец" или "образец ткани" относится к любому образцу, включающему биомолекулу (такую как белок, пептид, нуклеиновая кислота, липид, углевод или их комбинация), который получают из любого организма, в том числе из вирусов. Другие примеры организмов включают млекопитающих (таких как люди; ветеринарные животные типа кошек, собак, лошадей, крупного рогатого скота и свиней; и лабораторные животные типа мышей, крыс и приматов), насекомых, аннелидов, паукообразных, сумчатых, рептилий, амфибий, бактерии и грибы. Биологические образцы включают образцы ткани (как например, тканевые срезы и образцы ткани, полученные путем пункционной биопсии), образцы клеток (как например, цитологические мазки, такие как мазки по Папаниколау или мазки крови, либо образцы клеток, полученные путем препаровки под микроскопом), или части клеток, клеточные фрагменты или органеллы (как например, полученные в результате разрушения клеток и разделения их компонентов посредством центрифугирования или иным образом). Другие примеры биологических образцов включают кровь, сыворотку крови, мочу, семенную жидкость, фекалии, цереброспинальную жидкость, интерстициальную жидкость, слизь, слезы, пот, гной, отобранную биопсией ткань (например, полученную путем хирургической биопсии или пункционной биопсии), аспираты, отобранные с использованием штуцера, серную пробку, молоко, вагинальную жидкость, слюну, мазки (такие как мазки из ротовой полости) или любой материал, содержащий биомолекулы, происходящие из первого биологического образца. В некоторых воплощениях термин "биологический образец", использованный в данном описании, относится к образцу (например, гомогенизированному или превращенному в жидкость образцу), приготовленному из опухоли или ее части, полученной от субъекта.
Использованный в данном описании термин "нормальная ткань" относится к ткани, не имеющей никакого обнаруживаемого повреждения или нарушения, которое предположительно коррелирует с увеличением числа случаев заболевания или, в контексте рака, числа случаев злокачественных новообразований. Эти нормальные образцы могут быть получены от пациентов, имеющих генетические мутации или состояния, которые коррелируют с увеличением числа случаев заболевания (генетическим или иным образом), рака или злокачественных новообразований. Тип нормальной ткани может быть таким же, что и тип ткани, соответствующей патологической ткани от одного и того же индивида или другого индивида; или нормальной ткани, которая не связана (например, отобрана из другого места в организме или имеет другой гистологический тип) с патологической тканью либо от одного и того же индивида, либо от других индивидов.
Использованный в данном описании термин "предраковая ткань" относится к ткани, имеющей некоторое повреждение или нарушение, которое предположительно коррелирует с увеличением заболеваемости раком или злокачественности.
Термин "опухоль" относится к опухолевому разрастанию или новообразованию, что само по себе определяется как аномальный новый рост клеток, которые обычно растут быстрее, чем нормальные клетки, и будут продолжать расти, если не проводить их лечение, что иногда вызывает повреждение расположенных вблизи структур. Размеры опухолей могут варьировать в широких пределах. Опухоль может быть солидной или заполненной жидкостью. Опухоль может относиться к доброкачественному (не злокачественному, обычно безопасному) или злокачественному (со способностью к метастазированию) росту. Некоторые опухоли могут содержать неопластические клетки, которые являются доброкачественными (как например, в случае карциномы in situ), и одновременно содержать злокачественные раковые клетки (как например, в случае аденокарциномы). Следует понимать, что они включают новообразования, локализованные в нескольких местах по всему организму. Таким образом, применительно к задачам данного изобретения, опухоли включают первичные опухоли, лимфатические узлы, лимфатическую ткань и метастазирующие опухоли. Грань между раковыми, предраковыми и раковыми опухолями не всегда ясна, но есть общие свойства для роста каждого типа. Доброкачественные опухоли представляют собой незлокачественные опухоли. Доброкачественная опухоль обычно локализована и не распространяется (не метастазирует) в другие части организма. Большинство доброкачественных опухолей хорошо восприимчивы к лечению. Однако, если их не лечить, некоторые доброкачественные опухоли могут вырасти большими и привести к серьезной травме или повреждению из-за их размера. Таким образом, доброкачественные опухоли могут имитировать злокачественные опухоли и, таким образом, иногда их подвергают лечению. Злокачественные опухоли представляют собой раковые опухоли, которые часто устойчивы к лечению, могут распространяться в другие части организма и иногда возникать вновь после удаления. "Рак" представляет собой другой термин для определения злокачественного роста (злокачественной опухоли или новообразования).
Вирулентность опухолей может варьировать. Некоторые виды рака могут относительно легко поддаваться лечению и/или исцелению, в то время как другие виды рака являются более агрессивными. Вирулентность опухолей можно определить, по меньшей мере частично, посредством дифференциальной экспрессии генов или посредством определения характеристик геномных изменений. В раковых клетках повреждаются механизмы, которые позволяют клетке активировать или выключать гены. В результате часто наблюдается аберрантная активация генов, специфичная для других тканей и/или для других стадий развития. Например, в случаях рака легкого опухолевые клетки, экспрессирующие гены, специфичные для образования сперматозоидов, которые должны быть молчащими, являются чрезвычайно вирулентными (это рак с высоким риском развития, который проявляет повышенные пролиферативные способности и возможность "укрыться" от иммунной системы организма). Также показано, что почти во всех случаях рака аберрантно активированы десятки специфических генов зародышевой линии. См., например, Rousseaux et al., Ectopic Activation of Germline and Placental Genes Identifies Aggressive Metastasis-Prone Lung Cancers. Science Translational Medicine (2013) 5(186): 186. Соответственно, поскольку активация или отрицательная регуляция генов может быть ассоциирована с вирулентной формой конкретного рака, то можно суметь предсказать, после диагностических тестирований, какие раковые заболевания характеризуются высоким риском рецидива и фатальным прогнозом, даже в случаях, когда опухоль подвергают адекватному лечению на ранней стадии ее развития.
Термин "лимфатический узел" относится к органу лимфатической системы, имеющему форму овала или почки, представленному в различных местах по всему организму, включая подмышечную впадину и желудок, и соединенному лимфатическими сосудами. Лимфатические узлы содержат различное количество иммунных клеток, в том числе, но не ограничиваясь этим, В-клеток и Т-клеток. Лимфатические узлы играют важную роль в надлежащем функционировании иммунной системы и могут действовать в качестве фильтров для чужеродных частиц и раковых клеток.
Термин "полип" или "полипы" относится к аномальной биологической опухоли, которая выступает из слизистой оболочки. Полипы можно обнаружить в ряде тканей, включая, но не ограничиваясь этим, ткань толстой кишки, желудка, носа, глаза, синуса(ов), мочевого пузыря и матки.
Термин "метастазирование" или "метастазирующая опухоль" относится к опухоли и/или к ассоциированным с ней компонентам, включая, но не ограничиваясь, этим кровеносные сосуды, кости, мозговые оболочки, которые развились или распространились от одного органа или части тела к другому.
Термин "киста" относится к закрытой капсуле круглой или овальной формы, которая имеет отчетливую мембрану и перегородку, отделяющие ее от близлежащей ткани. Согласно некоторым аспектам кистой является кластер клеток, которые сгруппированы вместе с образованием капсулы (весьма возможным образом подобно тому, как молекулы воды группируются вместе, образуя пузырек). Согласно некоторым аспектам, клетки, образующие "оболочку" такой капсулы или кисты, являются по-разному аномальными при сравнении со всеми окружающими клетками для этого заданного местоположения. Киста может включать в себя, но не ограничивается этим, воздух, жидкости или любые полутвердые вещества. Некоторые опухоли могут содержать кисты или быть описаны как "кистозные".
Термин "извлеченный резекцией материал" относится ко всему органу или части органа либо другой структуры организма, которую извлекают из субъекта.
Термин "орган" или "органы", использованный в данном описании, относится к любой анатомически обособленной части или ткани, имеющей у животного конкретную функцию. Термин включает в себя долю анатомически обособленной части или ткани либо всю анатомически обособленную часть или ткань, например, долю легкого. Такие органы включают, но не ограничиваются этим, надпочечник, аппендикс, мочевой пузырь, головной мозг, ухо, пищевод, глаз, желчный пузырь, сердце, почку, кишечник (например, толстый или тонкий кишечник), печень, легкое, полость рта, мышцу, нос, поджелудочную железу, паращитовидную железу, эпифиз, гипофиз, кожу, селезенку, желудок, тимус, щитовидную железу, трахею, матку, червеобразный отросток или их часть.
Термин "кластер клеток" (или "кластеры клеток") относится к агрегату или агрегатам клеток, например, озлокачествленных клеток, фибробластов, иммунных клеток, стволовых клеток или эндотелиальных клеток. Согласно одному из аспектов, кластеры клеток содержат 1-10, 10-100, 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 или большее число клеток. Термин "множество кластеров клеток" относится более чем к одному кластеру клеток. Кластеры клеток агрегируют или существуют по отдельности. Клетки в кластерах клеток прикреплены друг к другу посредством белков, таких как кадгерины, и прикреплены к окружающему внеклеточному матриксу посредством интегринов. Таким образом, клетки в кластере клеток с наибольшей вероятностью связаны друг с другом и могут считаться субклоном или происходящими из субклона.
Использованный в данном описании термин "органелла" относится к связанным с клеточной мембраной структурам, таким как хлоропласт, митохондрия и ядро. Термин "органелла" включает в себя природные и синтетические органеллы.
Термин "пептид", использованный в данном описании, означает короткий полимер из аминокислот, соединенных пептидными связями. Каждая из аминокислот может иметь L- или D-конфигурацию.
Термин "нуклеиновая кислота", использованный в данном описании, относится к полимерной форме нуклеотидов любой длины, рибонуклеотидов, либо дезоксирибонуклеотидов, или пептидо-нуклеиновых кислот (PNA), которые содержат пуриновые и пиримидиновые основания или другие природные, химически или биохимически модифицированные, неприродные или дериватизированные нуклеотидные основания. Остов полинуклеотида может содержать сахара и фосфатные группы, которые обычно могут быть обнаружены в РНК или ДНК, либо модифицированные или замещенные сахара или фосфатные группы. Согласно одному из аспектов полинуклеотид содержит модифицированные нуклеотиды, такие как метилированные нуклеотиды и нуклеотидные аналоги.
Термин "липид" используется в своем традиционном смысле как общий термин, охватывающий жиры, липиды, растворимые в смеси спирта с эфиром компоненты протоплазмы, которые не растворяются в воде. Липиды входят в состав жиров, нелетучих жидких масел, эфирных масел, восков, стероидов, стеринов, фосфолипидов, гликолипидов, сульфолипидов, аминолипидов, хромолипидов (липохромов) и содержат жирные кислоты. Термин охватывает как природные, так и полученные в результате синтеза липиды. Предпочтительными липидами применительно к настоящему изобретению являются: фосфолипиды, в том числе фосфатидилхолины и фосфатидилэтаноламины, и сфингомиелины.
Термин "метаболит" относится к соединению, белку или любому веществу, промежуточному продукту или материалу, образующемуся в результате ферментативных реакций, т.е. соединению, синтезированному в процессе, в котором участвует фермент.
Термин "жидкая ткань" относится к любой ткани, которая существует или может существовать в форме жидкости, который включает в себя, но не ограничивается этим, кровь, плазму крови, сыворотку крови, слюну, семенную жидкость, секреты из шейки матки, слюну, мочу, слезы, пот, молоко из молочной железы и амниотические жидкости. Термин "нежидкая ткань" относится к любой ткани, которая не является жидкой тканью.
Термин "отобранный шприцем аспират для цитологического исследования" относится к процедуре тонкоигольной пункционной аспирационной биопсии (FNAB, FNA или NAB) или тонкоигольной пункционной аспирации с последующим цитологическим исследованием (FNAC).
Термин "экссудирование" относится к процедуре отбора жидкости у субъекта. В некоторых аспектах жидкость, отобранную путем экссудирования, можно описать как характеризующую патологическое состояние, расстройство, признак или симптом аномальности. Согласно другому аспекту жидкость из экссудата может быть результатом чрезмерного накопления жидкостей в полостях тела или перитонеальном пространстве.
Термин "мазок по Папаниколау" относится к методике скрининга рака шейки матки. С его помощью тестируют присутствие предраковых или раковых клеток на шейке, входном отверстии матки.
Использованный в данном описании термин "аномальная ткань" подразумевает ткань, которая проявляет определенную характеристику, отличающуюся от этой характеристики в нормальной ткани. Например, раковая ткань молочной железы может, согласно одному из аспектов, быть "аномальной" по сравнению с тканью молочной железы, которая фенотипически не является раковой, но может, тем не менее, быть "нормальной" с точки зрения другой характеристики, такой как генная экспрессия конкретного биомаркера.
Термин "фенотипически нормальная ткань" относится к ткани, которая имеет физические характеристики, например, гистологическое проявление, точно такие же, аналогичные или по существу аналогичные характеристикам, которые считаются нормальными. Термин "фенотипически аномальная ткань" относится к ткани, которая имеет физические характеристики, точно такие же, аналогичные или по существу аналогичные характеристикам, которые считаются аномальными.
Термин "фенотипически гомогенный" подразумевает, что по меньшей мере одна или более чем одна физическая характеристика, например, гистологическое проявление, является точно такой же либо аналогичной или по существу аналогичной идентифицированной(ым) характеристике(ам), что и у других членов группы или типа ткани, например, молочной железы, толстой кишки, легкого.
Термин "генотипически нормальная ткань" относится к ткани, которая имеет геномные, например, на уровне хромосом, митохондрий, РНК, микроРНК и/или некодирующей РНК, характеристики, например, последовательность генов, точно такие же, аналогичные или по существу аналогичные характеристикам, которые считаются нормальными. Термин "генотипически аномальная ткань" относится к ткани, которая имеет генетические характеристики, например, последовательность генов, точно такие же, аналогичные или по существу аналогичные характеристикам, которые считаются аномальными.
Термин "генетически различный" применительно к клеткам, тканям или субъектам, относится к популяции субъектов, тканей или клеток, при этом по меньшей мере два члена группы отличаются друг от друга или по меньшей мере от другого индивида, клетки или ткани на геномном уровне, например, на уровне хромосом, митохондрий, РНКА, микроРНК и/или некодирующей РНК. Термин "генетически гомогенный субъект" применительно к двум или более индивидам, относится к индивидам, которые демонстрируют по существу идентичный конкретный маркер или по существу идентичную характеристику на геномном уровне, например, на уровне хромосом, митохондрий, РНК, микроРНК и/или некодирующей РНК.
Термин "группа этнической принадлежности" относится к социальной группе, которая имеет общую национальную или культурную традицию. Согласно одному из аспектов этот термин подразумевает членов группы, которые имеют общее или близкородственное генетическое происхождение.
Термин "малая молекула" относится к низкомолекулярному органическому веществу, которое можно использовать для регулирования биологического процесса. Согласно одному из аспектов молекулярная масса изменяется в диапазоне 0-100 дальтон, 100-200 дальтон, 200-300 дальтон, 300-400 дальтон, 400-500 дальтон, 500-600 дальтон, 600-700 дальтон, 700-800 дальтон, 800-900 дальтон или 900-1000 дальтон. Согласно другому аспекту значение молекулярной массы составляет меньше 1000 дальтон. Малые молекулы включают, но не ограничиваются этим, органические соединения, пептиды, метаболиты и липиды.
Термин "краситель" относится к веществу, которое может придавать цвет субъекту благодаря избирательному поглощению света. В некотором воплощении краситель является растворимым или представляет собой твердое вещество. В другом воплощении краситель удерживается на подложке в результате абсорбции, растворения и механического удерживания либо посредством ионных или ковалентных химических связей. В следующем воплощении краситель представляет собой любую органическую или неорганическую молекулу или группировку, которая поглощает электромагнитное излучение, например, на выбранной длине волны.
Использованный в данном описании термин "количественные данные" означает данные, отражающие некоторое количество, уровень или диапазон, которые ассоциированы с единицами измерения. Например, количественные данные для опухолей включают, но не ограничиваются этим, размеры опухолей или уровни экспрессии биомаркеров.
Использованный в данном описании термин "качественные данные" относится к информации, которая описывает признаки, характеристики или другие особенности объекта. Например, качественные данные для рака включают, но не ограничиваются этим, стадии, внешний вид и другие физические характеристики опухоли.
Использованный в данном описании термин "норммированный" применительно к измеренному значению, подразумевает корректировку значения, измеренного в разных масштабах, к условному общепринятому масштабу.
Гены представляют собой всего лишь один тип биомаркеров рака. Использованный в данном описании термин "биомаркер" или "маркер" относится к биологической молекуле, обнаруживаемой в крови, других жидкостях организма или тканях, которая является признаком нормального или аномального процесса, либо состояния, либо заболевания (такого как рак). Биомаркер можно использовать для определения того, в какой степени организм восприимчив к лечению заболевания или состояния либо предрасположен ли данный субъект к заболеванию или состоянию. В контексте рака биомаркер относится к биологическому веществу, которое является указанием на наличие ракового заболевания в организме. Биомаркер может представлять собой молекулу, секретируемую опухолью, или специфический ответ организма на наличие ракового заболевания. Генетические, эпигенетические, протеомные, гликомные и визуализируемые биомаркеры можно использовать для диагностики, прогноза и эпидемиологии рака. Анализ таких биомаркеров может быть проведен в неинвазивно отобранных биологических жидкостях типа крови или сыворотки крови. При лечении пациентов уже были применены несколько биомаркеров на основе генов и белков, включая, но не ограничиваясь этим, AFP (рак печени), BCR-ABL (хронический миелоидный лейкоз), BRCA1/BRCA2 (рак молочной железы/яичников), BRAF V600E (меланома/колоректальный рак), СА-125 (рак яичников), СА19.9 (рак поджелудочной железы), СЕА (колоректальный рак), EGFR (немелкоклеточный рак легкого), HER-2 (рак молочной железы), KIT (гастроинтестинальная стромальная опухоль), PSA (простатоспецифический антиген), S100 (меланома) и многие другие. Биомаркеры могут быть полезны в качестве диагностических (для выявления раковых заболеваний на ранней стадии) и/или прогностических средств (для предсказания того, насколько агрессивным является рак, и/или для прогнозирования того, в какой степени субъект будет восприимчив к конкретному лечению, и/или того, насколько вероятен рецидив рака).
Использованный в данном описании термин "клинически релевантный маркер" подразумевает маркер или биомаркер, который соотносится с клиническим результатом или состоянием, например, присутствием или отсутствием заболевания или состояния, например, рака.
Использованный в данном описании термин "раковая ткань" относится к любой ткани, несущей опухолевые клетки. Раковые ткани включают, но не ограничиваются этим, мышечную ткань, ткань кожи, головного мозга, легкого, печени, селезенки, костного мозга, тимуса, сердца, лимфы, крови, кости, хряща, поджелудочной железы, почки, желчного пузыря, желудка, кишечника, яичка, яичника, матки, прямой кишки, нервной системы, глаз, желез или соединительную ткань.
"Прогноз" подразумевает предсказание или вероятный исход текущего состояния субъекта, включая возможность рецидива рака и/или метастазирования рака у пациента.
Использованный в данном описании термин "подвергать консервации" или "подвергать фиксации" относится к стадии приготовления биологических образцов, например, гистологических срезов. Методы консервации или фиксации включают, но не ограничиваются, химическую фиксацию, термическую фиксацию, погружение, перфузию и/или лиофилизацию. Соответственно, "подвергнутым фиксации образцом" является образец, который обработан так, как указано выше.
Термин "живые клетки" относится к любым клеткам, которые не были подвергнуты фиксации или консервации. В некоторых воплощениях термин "живая клетка" включает в себя функционирующую клетку. Специалисты в данной области техники могут легко найти различия между живой клеткой и фиксированной клеткой для решения задач настоящего изобретения.
Использованный в данном описании термин "заливка воском" или "заливка парафином" используется для описания процесса, при котором тканевую пробу инфузируют в парафиновый воск с целью консервации ее клеточных структур при приготовлении срезов с использованием микротома и который имеет дополнительное преимущество, выражающееся в пригодности срезов для долгосрочного хранения.
Использованный в данном описании термин "одна или несколько тканей" относится к тканям, полученным от одного или более чем одного субъекта, или к одной или более чем одной ткани, полученной от одного и того же субъекта. Термин "две или более тканей" используется для ткани, полученной от двух или более субъектов, или для двух или более тканей, полученных от одного и того же субъекта или пациента.
Использованный в данном описании термин "клетка в состоянии, предшествующем злокачественному перерождению, или озлокачествленная клетка" применяется для описания любых клеток, которые подверглись злокачественной трансформации или готовы подвергнуться злокачественной трансформации. Характеристики клеток в состоянии, предшествующем злокачественному перерождению, или озлокачествленных клеток включают, но не ограничиваются этим, неконтролируемую пролиферацию, метастазирование, аномальный клеточный метаболизм, уклонение от апоптоза, самообеспеченность ростовыми сигналами и устойчивый ангиогенез. Например, полип в толстой кишке может быть в состоянии, предшествующем злокачественному перерождению в рак толстой кишки.
Использованный в данном описании термин "циркулирующие опухолевые клетки" относится к опухолевым или раковым клеткам, которые циркулируют в сосудистой системе, лимфатической системе или другой жидкости. Циркулирующие опухолевые клетки включают, но не ограничиваются этим, лейкозные клетки.
Использованный в данном описании термин "нормальная близко расположенная ткань" относится к нормальной ткани, расположенной вблизи опухолевой клетки или опухолевой ткани.
Термин "реконструирование" применительно к реконструированию гомогенизированного образца подразумевает смешивание или объединение.
Термин "экстрагирование содержимого" применительно к гомогенату подразумевает выделение или очистку компонента клеточной структуры.
Использованный в данном описании термин "FFPE образец" относится к фиксированному в формалине залитому парафином образцу. FFPE образец может быть использован для ряда медицинских исследований, включая, но не ограничиваясь этим, диагностику, IHC анализ и профилирование генной экспрессии или источников заболеваний.
Использованный в данном документе термин "предварительно заданное значение" обычно представляет собой значение, которое используют для вычисления изменения данных. Согласно одному из аспектов предварительно заданное значение рассчитывают на основании данных за прошедшие периоды либо на основании данных для другой группы образцов или группы образцов, данные для которых аналогичны исследуемым данным.
Термин "показатель риска" относится к количественной или качественной величине, связанной с риском. Например, показатель риска рака представляет собой величину, которая количественно или качественно оценивает риск возникновения рака.
Термин "хромосомная транслокация" относится к аномалии хромосом, вызванной перестройкой частей между негомологичными хромосомами.
Термин "внутрихромосомная инверсия" относится к хромосомной перестройке, при которой сегмент хромосомы реверсирован по типу "конец-в-конец". Согласно одному из аспектов инверсия имеет место тогда, когда одна хромосома подвергается разрыву и перестройке внутри себя.
Термин "режим терапии" используется в соответствии со значением, хорошо известным в данной области техники. Например, термин относится к плану лечения для индивида, страдающего от патологического состояния (например, от хронической инфекции вирусом гепатита С или рака), в котором подробно описываются факторы, включая, но не ограничиваясь этим, агент или агенты, подлежащий(ие) введению пациенту, дозировки такого(их) агента(ов) и график и продолжительность лечения. Персональная дозировка или схема лечения представляет собой режим терапии или введения, основанный на концепциях индивидуализированной медицины с учетом индивидуальных характеристик пациента или субъекта, например, данных о наборе генов, фармакогенетике, этнической принадлежности, истории лечения, семейной истории, клинической химии, либо других релевантных характеристик или измерений.
Термин "химиотерапия" относится к лечению химическим агентом. Химиотерапию можно определить как применение фармацевтических средств, специально разработанных для направленного воздействия на пораженные клетки, их лечения и/или уничтожения. Неограничивающие примеры заболеваний, которые можно лечить химиотерапией, включают раковые заболевания, аутоиммунные заболевания, такие как системный склероз, красная волчанка, ревматоидный артрит, васкулит, и вирусные инфекции. Согласно одному из аспектов химиотерапевтический агент разрушает раковые клетки посредством направленного воздействия на быстро делящиеся клетки в организме. Из-за отсутствия специфичности к раковым клеткам токсические эффекты химиотерапии также наблюдаются для других быстро делящихся нераковых клеток. Некоторыми из быстро делящихся клеток в организме являются клетки крови, клетки в полости рта, кишечном тракте, носу, ногтях и волосах. Разрушение нормальных клеток в организме вызывает такие побочные эффекты, как алопеция, кахексия, анемия, лейкопения и нейтропения. Эти побочные эффекты ограничивают эффективность химиотерапии и повышают риск, обусловленный снижением дозы, напрямую влияя на выживаемость пациентов.
Термин "иммунотерапия" относится к лечению, включающему активацию или инактивацию специфического иммунного ответа и/или иммунной(ых) эффекторной(ых) функции(ий).
Термин "облучение" или "лучевая терапия" относится к лечению, включающему применение высокоэнергетических частиц или волн, в том числе, но не ограничиваясь этим, рентгеновских лучей, гамма-лучей, электронных пучков или протонов, для лечения заболеваний (например, рака) или патологического состояния.
Термин "хирургическое вмешательство" относится к любому методическому действию, либо с использованием инструментов, либо без них, по отношению к пациенту для получения целебного или лечебного эффекта.
Термин "генная терапия" относится к использованию процесса переноса генов или процесса редактирования генов (например, CRISPR), предпочтительно с целью получения терапевтического эффекта у субъекта или пациента.
Термин "гормональная терапия", использованный в данном описании, определяется как лечение, связанное с модулированием гормонов. Гормональная терапия может включать, но не ограничивается этим, удаление железы, которая синтезирует данный гормон или прогормон, блокирование или ингибирование синтеза гормона, либо препятствование связыванию гормона с его рецептором, либо отрицательную регуляцию или деградацию рецептора гормона.
Термин "терапия стволовыми клетками", использованный в данном описании, относится к лечению посредством использования стволовых клеток для лечения или предотвращения заболевания или патологического состояния.
Термин "переливание крови" относится к процедуре получения крови через внутривенный катетер.
Использованный в данном описании термин "физиотерапия" относится к лечению физической дисфункции или физического повреждения с использованием лечебной физкультуры и применения способов воздействия, предназначенных для восстановления или облегчения нормальной функции или нормального развития.
Использованный в данном описании термин "фотодинамическая терапия" относится к способу, при котором свет определенной длины волны направляется на подлежащие лечению либо исследованию ткани или клетки, сделанные чувствительными к свету путем введении фотореактивного или фотосенсибилизирующего агента. В одном из воплощений может решаться диагностическая задача, при этом длину волны света выбирают такой, чтобы фотореактивный агент флуоресцировал, тем самым давая информацию о ткани без повреждения ткани. Также можно решать терапевтическую задачу, при этом длина волны света, передаваемого в подвергаемую лечению ткань-мишень, обуславливает фотохимическое взаимодействие фотореактивного агента с кислородом, в результате чего наблюдается образование высокоэнергетической разновидности, такой как синглетный кислород, вызывающий локальное разрушение или локальную деструкцию ткани либо инициацию иммунного ответа фотосенсибилизированной ткани или клетки.
Использованный в данном описании термин "дифференциальная экспрессия" относится к различиям в уровнях экспрессии генов или белков для двух или более образцов. Согласно одному из аспектов результаты дифференциальной экспрессии могут быть использованы для идентификации заболевания, биомаркера или любых образцов, которые можно ассоциировать с патологическими состояниями.
Использованный в данном описании термин "первый профиль" относится к набору данных, полученных от субъекта или группы субъектов. Согласно одному из аспектов первый профиль можно использовать в качестве исходного уровня с целью определения изменений в последующем(их) профиле(ях). Согласно другому аспекту данные, приведенные в первом профиле, можно включать в последующий анализ или в процесс получения последующих профилей.
Использованный в данном описании термин "предварительно заданный профиль" относится к набору данных или панелям наборов данных, которые ассоциируются с физиологическими условиями. Предварительно заданный профиль может быть получен от субъекта или группы субъектов. Согласно одному из аспектов, предварительно заданный профиль может включать гистологический или известный набор данных для физиологических состояний. Согласно другому аспекту, предварительно заданный профиль используют в качестве исходного уровня с целью определения изменений физиологических состояний (например, прогрессирования опухоли).
Использованный в данном описании термин "количественная оценка в баллах" относится к численному представлению физиологических состояний (например, показателю риска заболевания).
Использованный в данном описании термин "пролиферация" означает рост и деление клеток. В некоторых воплощениях термин "пролиферация", использованный в данном описании применительно к клеткам, относится к группе клеток, которая может увеличиваться по численности в течение какого-либо периода времени.
Термин "апоптоз" относится к процессу программируемой клеточной смерти. Согласно некоторому аспекту апоптоз сопровождается клеточными морфологическими изменениями и утратой жизнеспособности клеток.
Термин "некроз" охватывает состояния некротической гибели клеток, а также промежуточные состояния, демонстрирующие некротические и апоптотические характеристики.
Термин "клеточная миграция", использованный в данном описании, означает миграцию клеток, которая индуцируется физиологически активными веществами или которая вызывается физиологическими изменениями (например, трансформацией).
Термин "эпителиально-мезенхимальный переход" или "ЕМТ" относится к процессу, при котором эпителиальные клетки, которые обычно являются непролиферирующими и неподвижными, претерпевают переход в мезенхимальные клетки, характеризующиеся пролиферативным и подвижным фенотипом. ЕМТ является центральным механизмом диверсификации клеток, обнаруженных в ткани, состоящей их нескольких видов клеток, поэтому представляет собой процесс, вовлеченный в организацию формирования общего строения организма (Kalluri and Nelson, J. Clin. Invest., 112(12): 1776-1784, 2003). Хотя эпителиальные клетки когда-то считались окончательно дифференцированными, признано, что эпителий обладает элементом пластичности, что позволяет осуществиться переходу в подвижные мезенхимальные клетки (Boyer et al. Biochem. Pharmacol., 60: 1099, 2000; Nieto, Nat. Rev. Mol. Cell Biol., 3: 155-166, 2002). Таким образом, EMT необходим в дефинитивной ткани (adult tissue) для образования фибробластов в пораженных тканях (Strutz et al. J. Cell Biol.. 130: 393-405, 1995; Iwano et al. J. Clin. Invest., 110: 341-350, 2002) и в начале метастазирования при эпителиальном раке (Kiermer et al. Oncogene, 20: 6679-6688, 2001; Janda et al. J. Cell Biol., 156: 299-313, 2002; Xue et al. Cancer Res., 63: 3386-3394, 2003).
Согласно одному из аспектов EMT представляет собой процесс дезагрегации эпителиальных единиц и реконструирования эпителия в сторону образования мезенхимальных клеток. Для такого перехода требуется молекулярное перепрограммирование эпителия, обычно считается, что это происходит с участием ряда цитокинов, металлопротеиназ и ингибиторов сборки мембран (Kalluri and Neilson, 2003, выше; Yang and Liu, Am. J. Pathol., 159: 1465-1475, 2001; Zeisberg et al. Am. J. Pathol., 159: 1313-1321, 2001; Fan, Kindney Int. 56: 1455-1467, 1999).
Использованный в данном описании термин "митоз" можно применять взаимозаменяемо с термином "деление клеток". В некоторых воплощениях митоз относят только к одной фазе процесса деления клеток: процессу, при котором сестринские хроматиды равномерно распределяются между двумя дочерними клетками. В эукариотических клетках за митозом следует цитокинез, представляющий собой процесс, в результате которого цитоплазма клетки разделяется на две различающиеся, но генетически идентичные дочерние клетки.
В начале митоза небольшие внутриклеточные нитчатые структуры, известные как цитоплазматические микротрубочки, основным компонентом которых является белок, называемый тубулином, разбираются на молекулы тубулина. Затем тубулин вновь собирается в микротрубочки, образуя внутриклеточную структуру, известную как "митотическое веретено". Митотическое веретено играет критическую роль в распределении хромосом в делящейся клетке точно между двумя дочерними ядрами. Раковые клетки характеризуются более быстрым делением и пролиферацией клеток, чем это наблюдается у большинства здоровых клеток, и действие многих противораковых средств осуществляется путем ингибирования деления клеток. Поскольку раковые клетки делятся более быстро, чем это делают здоровые клетки, раковые клетки предпочтительно уничтожают, используя противораковые средства, которые ингибируют митоз. Такие соединения называют "антимитотическими".
Термин "арест клеточного цикла" относится к точке остановки в клеточном цикле, в которой клетки не участвуют в процессах, связанных с удвоением и делением. Природный клеточный цикл включает в себя несколько контрольных точек, которые позволяют клетке определять, следует ли продолжать деление или необходимо остановиться. Эти остановки также могут быть вызваны внешними факторами, такими как радиоактивное облучение или лекарственные препараты, используемые для регулирования клеточного роста.
Первой фазой клеточного цикла является G1-фаза, в которой клетка готовится к удвоению. Генетический материал клетки удваивается во время S-фазы. Репарация клеточного повреждения происходит во время G2-фазы, после чего следует переход в М-фазу, фазу митоза. После митоза клетка снова может войти в G1-фазу или перейти в G0-фазу, стадию покоя. Контрольная точка на время приостанавливает клеточный цикл в каждой фазе, чтобы позволить клетке решить, следует ли продолжить цикл. Некоторые клетки запрограммированы на то, чтобы удвоение происходило не часто, вместе с тем поврежденным клеткам может потребоваться время для репарации или разрушения.
В некоторых воплощениях арест клеточного цикла предшествует апоптозу или гибели клеток. Это происходит тогда, когда клетка больше не функционирует вследствие повреждения ДНК. Такая клетка подлежит уничтожению. Арест клеточного цикла позволяет клеткам периодически проводить проверку признаков разрушения ДНК, которые могут вызвать функциональные проблемы или привести к развитию опухоли.
Термин "S-фаза" относится к периоду во время клеточного цикла, в котором происходит репликация ДНК. Обычно S-фаза протекает между G1-фазой и G2-фазой. Точное и безошибочное выполнение репликации ДНК во время S-фазы необходимо для предотвращения генетических аномалий.
Термин "старение", использованный в данном описании, относится к необратимому прекращению репликации ДНК и клеточного роста, которое невозможно сделать обратимым под действием факторов роста. Это явление может наблюдаться в конце этапа пролиферации нормальных клеток либо в нормальных или опухолевых клетках в ответ на цитотоксические лекарственные средства, повреждение ДНК. Старение характеризуется определенными морфологическими признаками, включая, но не ограничиваясь этим, увеличение размера клеток, сглаженную морфологию клеток, увеличение гранулярности и наличие ассоциированной со старением β-галактозидазной (SA-β-gal) активности.
Использованный в данном описании термин "дифференцировка" относится к процессу, при котором структура или функция клеток подвергается биологической специализации в ходе их деления, пролиферации и роста. Как правило, дифференцировка относится к явлению, при котором относительно простая система разделяется на две или более качественно разных "частичных" систем.
Использованный в данном описании термин "детектирование" относится к действию или процессу идентификации присутствия конкретной молекулы. В одном из воплощений детектирование биомаркера может означать идентификацию экспрессии биомаркера.
Использованный в данном описании термин "фиксирующий агент" относится к агенту, используемому для фиксации ткани в случае решения ряда задач, включая, но не ограничиваясь этим, доставку, хранение, гистологическое исследование и обработку.
Использованные в данном описании термины "нуклеиновокислотная последовательность" и "полинуклеотид" применяются взаимозаменяемо для обозначения полимерной формы нуклеотидов любой длины, или рибонуклеотидов, или дезоксирибонуклеотидов. Таким образом, этот термин включает в себя, но не ограничивается этим, одно-, двух- или многоцепочечную ДНК или РНК, геномную ДНК, кДНК, гибриды ДНК-РНК или полимер, содержащий пуриновые и пиримидиновые основания или другие природные, химически или биохимически модифицированные, неприродные или измененные нуклеотидные основания.
Термин "кодировать" в том смысле, в каком его применяют к нуклеиновокислотным последовательностям, относится к полинуклеотиду, который при нахождении в своем нативном состоянии или при манипулировании с ним методами, хорошо известными специалистам в данной области техники, может транскрибироваться и/или транслироваться с получением мРНК. Антисмысловая нить представляет собой комплементарную последовательность для такой нуклеиновой кислоты, и из нее можно вывести кодирующую последовательность.
Использованный в данном описании термин "вектор" относится к конструкции на основе нуклеиновой кислоты, созданной для перенесения материала между разными хозяевами, включая, но не ограничиваясь этим, плазмиду, вирус, космиду, фаг, бактериальную искусственную хромосому (ВАС), искусственную хромосому дрожжей (YAC) и т.д. В некоторых воплощениях плазмидные векторы могут быть получены из имеющихся в продаже векторов. В других воплощениях вирусные векторы могут быть получены из бакуловирусов, ретровирусов, аденовирусов, аденоассоциированного вируса (AAV) и т.д. в соответствии с методами, известными в данной области техники. В одном из воплощений вирусным вектором является лентивирусный вектор.
Термин "промотор", использованный в данном описании, относится к любой последовательности, которая регулирует экспрессию кодирующей последовательности, такой как ген. Промоторы могут быть, например, конститутивными, индуцибельными, репрессируемыми или тканеспецифичными. "Промотором" является контрольная последовательность, представляющая собой участок полинуклеотидной последовательности, в котором осуществляется регулирование инициации и скорости транскрипции. Он может содержать генетические элементы, с которыми могут связываться регуляторные белки и молекулы, такие как РНК-полимераза и другие транскрипционные факторы.
Использованный в данном описании термин "выделенная клетка" обычно относится к клетке, которая по существу отделена от других клеток ткани.
Термин "эффективное количество" или "дающее нужный эффект количество" относится к количеству агента или к объединенным количествам двух или более агентов, которого(ых), при введении для лечения пациента, млекопитающего или другого субъекта, достаточно для осуществления такого лечения заболевания. "Эффективное количество" будет варьировать в зависимости от агента(ов), заболевания и его тяжести и возраста, массы и т.д. подлежащего лечению субъекта.
Использованный в данном описании термин "детектируемый(ая) маркер или метка" относится по меньшей мере к одному маркеру, способному непосредственно или опосредованно генерировать детектируемый сигнал. Неисчерпывающий список маркеров включает ферменты, которые генерируют сигнал, детектируемый, например, с использованием колориметрии, флуоресценции, люминесценции, такие как пероксидаза хрена, щелочная фосфатаза, β-галактозидаза, глюкоза-6-фосфат-дегидрогеназа, хромофоры, такие как флуоресцентные, люминесцентные красители, группы с электронной плотностью, детектируемые посредством электронной микроскопии или на основании своего электрического свойства, такого как проводимость, с использованием амперометрии, вольтамперометрии, импедансного анализа, детектируемые группы, например, молекулы которых имеют достаточный размер, чтобы индуцировать детектируемые изменения своих физических и/или химических свойств, при этом такое детектирование может быть выполнено оптическими методами, как например, с использованием дифракции, поверхностного плазмонного резонанса, изменения поверхности, изменения контактного угла, или физическими методами, такими как атомно-силовая спектроскопия, применение туннельного эффекта или молекул, содержащих радиоактивные изотопы, такие как32Р,35S или125I.
Использованный в данном описании термин "маркер для очистки" относится по меньшей мере к одному маркеру, полезному для очистки или идентификации. Неисчерпывающий список маркеров включает His, lacZ, GST (глутатион-S-трансфераза), мальтоза-связывающий белок, NusA, ВССР, c-myc, СаМ, FLAG, GFP (зеленый флуоресцентный белок), YFP (желтый флуоресцентный белок), краситель вишневый, тиоредоксин, поли(NANP), V5, Snap, НА (гемагглютинин), хитин-связывающий белок, Softag 1, Softag 3, Strep или S-белок. Флуоресцентный маркер, подходящий для прямого и опосредованного детектирования, содержит FLAG, GFP, YFP, RFP (красный флуоресцентный белок), краситель dTomato, краситель вишневый, Су3, Су 5, Су 5.5, Су 7, DNP (динитрофенол), АМСА (аминометилкумарина ацетат), биотин, дигоксигенин, TAMRA, техасский красный, родамин, красители серии Alexa fluor, FITC, TRITC или любой другой флуоресцентный краситель или гаптен.
Использованный в данном описании термин "экспрессия" относится к процессу, в результате которого полинуклеотиды транскрибируются в мРНК, и/или процессу, в результате которого транскрибированная мРНК впоследствии транслируется в пептиды, полипептиды или белки. Если полинуклеотид происходит из геномной ДНК, то экспрессия может включать сплайсинг мРНК в эукариотической клетке. Уровень экспрессии гена может быть определен путем измерения количества мРНК или белка в клетке или тканевом образце. Согласно одному из аспектов уровень экспрессии гена из одного образца можно непосредственно сравнивать с уровнем экспрессии этого гена из контрольного образца или образца сравнения. Согласно другому аспекту уровень экспрессии гена из одного образца можно непосредственно сравнивать с уровнем экспрессии этого гена из того же самого образца после введения соединения.
Использованный в данном описании термин "гомология" или "идентичный", "процент идентичности" или "сходство", в случае применения в контексте двух или более нуклеиновых кислот или полипептидных последовательностей, относится к двум или более последовательностям или подпоследовательностям, которые являются одинаковыми или имеют конкретное процентное содержание нуклеотидов или аминокислотных остатков, которые являются одинаковыми, например, имеют по меньшей мере 60% идентичности, предпочтительно, по меньшей мере 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более высокий процент идентичности в конкретном участке (например, нуклеотидной последовательности, кодирующей антитело, описанное в данной заявке, или аминокислотной последовательности антитела, описанного в данной заявке). Гомологию можно определить, сравнивая какое-либо положение в каждой последовательности, которая может быть подвергнута выравниванию с целью сравнения. Если какое-либо положение в сравниваемой последовательности занято тем же основанием или той же аминокислотой, то молекулы считаются гомологичными по такому положению. Степень гомологии последовательностей является функций от числа совпадений или гомологичных положений, являющихся общими для этих последовательностей. Выравнивание и процент гомологии или идентичность последовательности можно определить, используя программы системы программного обеспечения, известные в данной области техники, например, программы, описанные в Current Protocols in Molecular Biology (Ausubel et a/., eds. 1987) Supplement 30, section 7.7.18, Table 7.7.1. Предпочтительно, чтобы для выравнивания были использованы параметры по умолчанию. Предпочтительной программой для выравнивания является BLAST, в которой используются параметры по умолчанию. В частности, предпочтительными программами являются BLASTN и BLASTP, в которых используются следующие параметры по умолчанию: генетический код = стандартный; фильтр = отсутствует; цепь = обе; предельное значение = 60; ожидаемое значение = 10; матрица = BLOSUM62; описания = 50 последовательностей; сортировка по = HIGH SCORE; базы данных = неизбыточные, GenBank + EMBL + DDBJ + PDB + GenBank CDS translations + SwissProtein + SPupdate + PIR. Подробные описания этих программ можно найти в интернете по следующему адресу: ncbi.nlm.nih.gov/cgi-bin/BLAST. Термины "гомология" или "идентичный", "процент идентичности" или "сходство" также относятся или могут быть применены к последовательности, комплементарной тестируемой. Термины также включают в себя последовательности, которые имеют делеции и/или вставки, а также последовательности, которые имеют замены. Как изложено в данном описании, предпочтительные алгоритмы могут учитывать разрывы и тому подобное. Предпочтительно, идентичность наблюдается в участке протяженностью по меньшей мере примерно 25 аминокислот или нуклеотидов либо, более предпочтительно, в участке протяженностью по меньшей мере 50-100 аминокислот или нуклеотидов. "Несоответствующая" или "негомологичная" последовательность имеет менее 40% идентичности или, альтернативно, менее 25% идентичности, с одной из последовательностей, описанных в данной заявке.
Согласно одному из аспектов, термин "эквивалент" или "биологический эквивалент" антитела относится к способности антитела избирательно связываться со специфичным для него эпитопом белка или его фрагмента, выявленной по результатам измерений посредством ELISA или других подходящих методов. Биологически эквивалентные антитела включают, но не ограничиваются этим, эти антитела, пептиды, фрагменты антител, варианты антител, производные антител и миметики антител, которые связываются с тем же эпитопом, что и референсное антитело.
Необходимо оговорить, без явного описания и если не подразумевается иное, что когда настоящее изобретение относится к полипептиду, белку, полинуклеотиду или антителу, тогда в рамках этого описания подразумевается эквивалент или биологический эквивалент только что упомянутого выше. Подразумевается, что использованный в данном описании термин "их биологический эквивалент" является синонимом термину "их эквивалент" при ссылке на референсные белок, антитело, полипептид или нуклеиновую кислоту, и предусматривает таковые, имеющие минимальную гомологию, однако же при сохранении желаемой структуры или функциональности. Если в данном описании конкретно не указано, то подразумевается, что любой полинуклеотид, полипептид или белок, упомянутый в данном описании, также включает свои эквиваленты. Например, эквивалент предусматривает по меньшей мере примерно 70% гомологии или идентичности, либо по меньшей мере 80% гомологии или идентичности, и, альтернативно, либо по меньшей мере примерно 85%, либо, альтернативно, по меньшей мере примерно 90%, либо, альтернативно, по меньшей мере примерно 95%, либо, альтернативно, 98% гомологии или идентичности, и проявляет по существу эквивалентную биологическую активность по сравнению с референсными белком, полипептидом или нуклеиновой кислотой. Альтернативно, при ссылке на полинуклеотиды, их эквивалент представляет собой полинуклеотид, который гибридизуется в жестких условиях с референсным полинуклеотидом или комплементарным ему.
Если говорят, что полинуклеотид или участок полинуклеотида (либо полипептид или участок полипептида) имеет определенный процент (например, 80%, 85%, 90% или 95%) "идентичности последовательности" относительно другой последовательности, то это означает, что при выравнивании этот процент оснований (или аминокислот) оказывается одинаковым в случае сравнения двух последовательностей. Выравнивание и процент гомологии или идентичность последовательности можно определить, используя программы из программного обеспечения, известные в данной области техники, например, описанные в Current Protocols in Molecular Biology (Ausubel et al., eds. 1987) Supplement 30, section 7.7.18, Table 7.7.1. Предпочтительно, чтобы для выравнивания были использованы параметры по умолчанию. Предпочтительной программой для выравнивания является BLAST, в которой используются параметры по умолчанию. В частности, предпочтительными программами являются BLASTN и BLASTP, в которых используются следующие параметры по умолчанию: генетический код = стандартный; фильтр = отсутствует; цепь = обе; предельное значение = 60; ожидаемое значение = 10; матрица = BLOSUM62; описания = 50 последовательностей; сортировка по = HIGH SCORE; база данных = неизбыточная, GenBank + EMBL + DDBJ + PDB + GenBank CDS translations + SwissProtein + SPupdate + PIR. Подробные описания этих программ можно найти по следующему Интернет-адресу: ncbi.nlm.nih.gov/cgi-bin/BLAST.
"Гибридизация" относится к реакции, при протекании которой один или несколько полинуклеотидов взаимодействуют с образованием комплекса, который стабилизируется посредством образования водородных связей между основаниями нуклеотидных остатков. Образование водородных связей может происходить в результате образования пар оснований по Уотсону-Крику, связывания по Хугстину или любым другим специфичным для последовательностей образом. Данный комплекс может содержать две цепи, образующие дуплексную структуру, три цепи или большее число цепей, образующих многоцепочечный комплекс, одну само-гибридизующуюся цепь или любую комбинацию из них. Реакция гибридизации может составлять стадию в более длительном процессе, таком как инициация ПЦР реакции или ферментативное расщепление полинуклеотида под действием рибозима.
Примеры жестких условий гибридизации включают: температуры инкубации от примерно 25°С до примерно 37°С; концентрации буфера для гибридизации от примерно 6х SSC до примерно 10х SSC; концентрации формамида от примерно 0% до примерно 25%; и отмывающих растворов от примерно 4х SSC до примерно 8х SSC. Примеры умеренных условий гибридизации включают: температуры инкубации примерно 40°С до примерно 50°С; концентрации буфера от примерно 9х SSC до примерно 2х SSC; концентрации формамида от примерно 30% до примерно 50%; и отмывающих растворов от примерно 5х SSC до примерно 2х SSC. Примеры очень жестких условий включают: температуры инкубации от примерно 55°С до примерно 68°С; концентрации буфера от примерно 1х SSC до примерно 0,1х SSC; концентрации формамида от примерно 55% до примерно 75%; и отмывающие растворы, представляющие собой примерно 1х SSC, 0,1х SSC или деионизованную воду. В общем случае продолжительности инкубирования при гибридизации составляют от 5 минут до 24 часов, с 1, 2 или более стадиями промывки, и продолжительности инкубирования при промывке составляют примерно 1, 2 или 15 минут. SSC представляет собой буфер на основе 0,15 М NaCl и 15 мМ цитрата. Очевидно, что можно применять эквиваленты SSC, в которых используются другие буферные системы.
Термин "выделенный", использованный в данном описании, относится к молекулам, клеткам или биологическим веществам либо клеточным материалам, по существу не содержащим другие материалы. Согласно одному из аспектов термин "выделенный" относится к нуклеиновой кислоте, такой как ДНК или РНК, либо к белку или полипептиду (например, к антителу или его производному), либо к клетке или клеточной органелле, либо к ткани или органу, отделенных от других ДНК или РНК, либо белков или полипептидов, либо клеток или клеточных органелл, либо тканей или органов, соответственно, которые присутствуют в природном источнике. Термин "выделенная(ый)" также относится к нуклеиновой кислоте или пептиду, которая(ый) по существу не содержит клеточного материала, вирусного материала или культуральной среды, в случае получения методами рекомбинантной ДНК, либо химических предшественников или других химических реагентов, в случае получения химическим синтезом. Кроме того, подразумевается, что термин "выделенная нуклеиновая кислота" включает в себя фрагменты нуклеиновой кислоты, которые не являются природными фрагментами и не могут быть обнаружены в природном состоянии. Термин "выделенный" также используется в данном описании в смысле отнесения к полипептидам, которые получают из других клеточных белков, и подразумевается, что он охватывает как очищенные, так и рекомбинантные полипептиды. Термин "выделенный" также используется в данном описании в смысле отнесения к клеткам или тканям, которые выделяют из других клеток или тканей, и подразумевается, что он охватывает как культивированные, так и созданные методами инженерии разновидности.
Термин "отдельная клетка" или "одиночная клетка" означает структурную и/или функциональную единицу организма. Согласно некоторому аспекту отдельная клетка содержит, но не ограничивается этим, цитоплазму, ядро или клеточную мембрану.
Использованный в данном описании термин "моноклональное антитело" относится к антителу, продуцируемому одним клоном В-лимфоцитов или клеткой, в которую были трансфицированы гены легкой и тяжелой цепи одного антитела. Моноклональные антитела получают методами, известными специалистам в данной области техники, например, путем создания гибридных антителообразующих клеток в результате слияния миеломных клеток с иммунными клетками селезенки. Моноклональные антитела включают гуманизированные моноклональные антитела.
Термины "белок", "пептид" и "полипептид" используются взаимозаменяемо и в своем самом широком толковании относятся к соединению, составленному из двух или более субъединиц, таких как аминокислоты, аминокислотные аналоги или пептидомиметики. Субъединицы могут быть соединены пептидными связями. Согласно другому аспекту такие субъединицы могут быть соединены посредством других связей, например, сложноэфирных, простых эфирных и т.д. Белок или пептид должны содержать по меньшей мере две аминокислоты, и никакого ограничения на максимальное число аминокислот, которые могут содержаться в последовательности белка или пептида, не накладывается. Использованный в данном описании термин "аминокислота" относится или к природным, и/или к неприродным либо синтетическим аминокислотам, включая глицин, и оптическим как D-, так и L-изомерам, аминокислотным аналогам и пептидомиметикам.
Использованный в данном описании термин "очищенный" не требует абсолютной чистоты; скорее всего подразумевается, что он является относительным термином. Таким образом, например, очищенные нуклеиновая кислота, пептид, белок, биологические комплексы или другое активное соединение представляют собой что-либо, что отделяют целиком или частично от белков или других примесей. В общем случае, по существу очищенные пептиды, белки, биологические комплексы или другие активные соединения для применения в соответствии с данным изобретением составляют более 80% от всех макромолекулярных разновидностей, присутствующих в препарате, перед смешиванием или приготовлением композиции на основе такого пептида, белка, биологического комплекса или другого активного соединения вместе с фармацевтическим носителем, эксципиентом, буфером, усиливающим всасывание агентом, стабилизатором, консервантом, адъювантом или другим совместно вводимым ингредиентом в окончательной фармацевтической композиции для терапевтического введения. В более типичном случае, пептид, белок, биологический комплекс или другое активное соединение очищают так, чтобы его содержание составляло более 90%, часто более 95% от всех макромолекулярных разновидностей, присутствующих в очищенном препарате, перед смешиванием с другими ингредиентами композиции. В других случаях очищенный препарат может быть по существу гомогенным, при этом другие макромолекулярные разновидности невозможно обнаружить традиционными методами.
Использованный в данном описании термин "рекомбинантный белок" относится к полипептиду, получаемому методами рекомбинантной ДНК, при этом, как правило, ДНК, кодирующая данный полипептид, встроена в подходящий экспрессирующий вектор, который в свою очередь используют для трансфекции клетки хозяина с целью получения гетерологичного белка.
Использованный в данном описании термин "ультразвуковая обработка" относится к применению звуковых волн (акустической энергии), проходящих через жидкую среду. Звуковые волны могут вызывать колебания частиц (например, клеток или кластеров клеток) относительно их среднего положения. Согласно одному из аспектов ультразвуковая обработка приводит к диссоциации кластеров клеток до суспензии одиночных клеток.
Использованный в данном описании термин "лечение" или "подвергание лечению" заболевания у субъекта относится (1) к предупреждению появления симптомов или заболевания у субъекта, который имеет предрасположенность или еще не проявляет симптомов заболевания; и/или (2) к ингибированию заболевания или подавлению его развития; и/или (3) к уменьшению интенсивности симптомов или вызыванию регрессии заболевания или симптомов данного заболевания. В данной области техники очевидно, что "подвергание лечению" представляет собой подход к получению полезного или желаемого результата, включая клинические результаты. Для задач настоящей технологии полезные или желаемые результаты могут включать, но не ограничиваются этим, одно или более чем одно из следующего: ослабление или уменьшение интенсивности одного или нескольких симптомов, снижение степени состояния (в том числе заболевания), стабильное (т.е. без ухудшения) состояние расстройства (в том числе заболевания), задержку или замедление прогрессирования состояния (в том числе заболевания), улучшение или временное облегчение состояния (в том числе заболевания), состояний и ремиссию (будь то частичную или полную), как детектируемую, так и недетектируемую.
По существу гомогенные репрезентативные образцы
В данном изобретении рассматриваются ограничения способов отбора клинических образцов предшествующего уровня техники, из-за которых нет возможности приготовить репрезентативный образец. Характеристики репрезентативного образца соответствуют ключевым переменным и характеристикам более крупного объекта или образца. Современная практика избирательного отбора образцов ориентирована на сбор образцов ткани с целью соответствия требованиям определения стадии по системе TNM. Образцы для определения стадии по системе TNM специально отбирают таким образом, чтобы они отражали нормальные анатомические особенности удаленного органа, содержащего опухоль. Несмотря на то, что этот метод избирательного отбора образцов имеет важное значение для прогностического определения стадии по системе TNM, в результате его применения получаются "необъективные" опухолевые образцы или образцы, которые не отражают генетического и фенотипического разнообразия, обнаруженного во всей массе опухоли.
Согласно настоящему изобретению предложена композиция на основе обработанного гомогената, приготовленная из образца гетерогенной ткани, содержащая по существу гомогенно распределенные клеточные структуры, при этом соотношение клеточных структур в каждой и/или какой-либо подгруппе репрезентативного образца по существу аналогично соотношению клеточных структур в предоставляемом из источника образце гетерогенной ткани. Композиция на основе гомогената представляет собой новый, уникальный образец ткани, который также олицетворяет ключевые характеристики исходного, предоставляемого образца гетерогенной ткани. В композициях и способах приготовления таких композиций, которые изложены в данном описании, преодолен недостаток способов предшествующего уровня техники путем учета проблемы гетерогенности тканей в клинических образцах, в особенности, образцах, предназначенных для применения в областях клинических исследований, например, в клинической онкологии.
Репрезентативный образец по настоящему изобретению проиллюстрирован на ФИГ. 2А и 2В, на которых показано схематичное представление гомогената по изобретению. На ФИГ. 2А показана опухоль с тремя субклонами, присутствующими в разных пропорциях. С использованием описанных способов гомогенизации готовят репрезентативный образец, содержащий субклоны в той пропорции, в которой они существовали в солидной опухоли. Любой образец, отобранный из гомогената, будет содержать каждый субклон в той же самой пропорции, которая имеется в исходной опухоли. ФИГ. 2В представляет иллюстрацию того, как использование гомогената облегчает обнаружение субклонов с низкой распространенностью.
Репрезентативные образцы по настоящему изобретению преодолевают проблемы отбора образцов, налагаемые пространственно неоднородной трехмерной структурой ткани. В репрезентативном образце компоненты (клеточные структуры, клетки, пептиды, нуклеиновые кислоты, липиды, метаболиты и т.д.) исходных пространственно неоднородных органа, опухоли или ткани ("ОТТ") присутствуют в субобразце или подгруппе образца в пропорции, в которой они существуют в исходных ОТТ. В некоторых воплощениях репрезентативный образец относится к образцу ОТТ, который составляет как можно большую часть ОТТ, приближаясь ко всей массе ОТТ или охватывая достаточно значительную часть ОТТ для приближения к цели представления разнообразия ОТТ на уровне кластеров присоединенных друг к другу клеток, отдельных клеток, фрагментов клеток, органелл, пептидов, нуклеиновых кислот, липидов, метаболитов и т.д. Репрезентативный образец может содержать минимальное количество интактных ОТТ, необходимое, чтобы охватить разнообразие ОТТ.
Из взятых в одном экземпляре ОТТ можно приготовить много репрезентативных образцов. В таком воплощении сначала выполняют обработку удаленных хирургическим путем ОТТ или иную манипуляцию с ними с получением отдельных субъединиц, в результате чего каждая субъединица будет составлена из пространственно неоднородных клеточных структур, клеток, пептидов, нуклеиновых кислот и т.д. Затем в достаточной степени выполняют гомогенизацию, перемешивание или иное разрушение каждой субъединицы с получением репрезентативного образца из субъединицы ОТТ.
Гомогенизацию или иное перемешивание либо разрушение репрезентативного образца можно выполнить до такой степени, чтобы любой аналитический образец или часть репрезентативного образца содержал(а) случайную выборку образцов из материала, присутствующего в репрезентативном образце. Характеристикой аналитического образца является то, что он представляет собой довольно большую долю репрезентативного образца, вследствие чего он сосредоточивает в себе разнообразие репрезентативного образца применительно к предполагаемому результату используемого аналитического теста (т.е. с точки зрения клеток по сравнению с кластерами клеток). В случае любого, используемого для конкретного анализа, аналитического образца, приготовленного на основе репрезентативного образца, будут получены данные, согласующиеся с другим аналитическим образцом, используемым для одного и того же анализа, в пределах экспериментальной ошибки. Кроме того, подразумевается, что любая подгруппа репрезентативного образца, выбранного для конкретного анализа, будет предоставлять информацию, которая может быть перекрестно привязана к данным, полученным с помощью разных анализов при использовании аналитических образцов, взятых из одного и того же репрезентативного образца или из других репрезентативных образцов, приготовленных из ОТТ от одного и того же пациента. Также предполагается, что поскольку в каждом аналитическом субобразце присутствуют исходные биологические компоненты в исходных пропорциях, то данные, полученные на основании аналитических субобразцов, относящиеся к частям биологических компонентов ОТТ, можно сравнивать между пациентами.
В одном из воплощений репрезентативный образец представляет собой композицию на основе обработанного гомогената, приготовленную из образца гетерогенной ткани. Композиция на основе гомогената содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из по существу гомогенно распределенных клеточных структур, при этом соотношение клеточных структур в каждой подгруппе гомогената по существу аналогично соотношению клеточных структур в образце ткани. В одном из воплощений образец ткани выбран из группы, состоящей из: опухоли, лимфатического узла, метастаза, полипа, кисты, извлеченного резекцией материала, органа или их доли. В другом воплощении, образец ткани содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из пространственно обособленных клеточных структур. Согласно другому аспекту клеточные структуры содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из кластера клеток, отдельной клетки, фрагмента клетки, органеллы, пептида, нуклеиновой кислоты, липида, метаболита или их комбинации. Согласно одному из аспектов гомогенат содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из клеточных структур из образца ткани в количестве до 25% включительно. Согласно одному из аспектов гомогенат содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из клеточных структур из образца ткани в количестве до 50% включительно. Согласно другому аспекту гомогенат содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из клеточных структур из образца ткани в количестве до 75% включительно. Согласно другому аспекту гомогенат содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из клеточных структур из образца ткани в количестве до 100% включительно. Согласно другому аспекту гомогенат содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит на 100% из клеточных структур из образца ткани.
В другом воплощении гомогенат содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит на 100% из клеточных структур из образца ткани. Согласно одному из аспектов образец ткани содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из нежидкого образца ткани. Согласно другому аспекту образец ткани содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из жидкого образца ткани. Согласно одному из аспектов жидкий образец ткани содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из ткани, выделенной из одного или более чем одного из следующего: извлеченного хирургической резекцией материала, отобранного шприцем аспирата для цитологического исследования, образца экссудата или мазка по Папаниколау.
В еще одном воплощении по существу гомогенные клеточные структуры содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из множества одиночных клеток или множества кластеров клеток. Согласно одному из аспектов клеточные структуры выделены из нормальной ткани. Согласно другому аспекту клеточные структуры выделены из фенотипически или генотипически нормальной ткани. Согласно еще одному аспекту клеточные структуры выделены из аномальной ткани. Согласно одному из аспектов клеточные структуры выделены из фенотипически или генотипически аномальной ткани.
В одном из воплощений образец ткани содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из стволовой клетки, эпителиальной клетки, клетки крови, жировой клетки, клетки кожи, эндотелиальной клетки, опухолевой клетки или иммунной клетки. Согласно одному из аспектов опухолевая клетка происходит из раковой ткани, выбранной из группы, состоящей из: рака легкого, лейкоза, рака молочной железы, рака предстательной железы, рака толстой кишки, рака головного мозга, рака пищевода, случаев рака головы и шеи, рака мочевого пузыря, гинекологических видов карцином, рака яичника, рака шейки матки, липосаркомы, меланомы, лимфомы, плазмоцитомы, саркомы, глиомы, тимомы, гепатомы и миеломы. Согласно другому аспекту иммунные клетки представляют собой клетки, выбранные из группы, состоящей из: нейтрофилов, моноцитов, дендритных клеток, макрофагов, лимфоцитов, Т-клеток, В-клеток или природных киллерных клеток.
В другом воплощении образец ткани не подвергнут консервации или фиксации. Согласно одному из аспектов образец ткани содержит живую клетку или клетку, недавно выделенную из субъекта. В другом воплощении образец ткани подвергнут консервации или фиксации. Согласно одному из аспектов, подвергнутый консервации или фиксации образец ткани содержит образец, который был подвергнут заморозке или фиксации методом, выбранным из группы, состоящей из замораживания, сублимационной сушки и заливки воском.
В одном из воплощений образец гетерогенной ткани выделен из одной или несколько тканей от одного и того же субъекта или разных субъектов. Согласно одному из аспектов образец ткани выделен от одного субъекта. Согласно другому аспекту, образец ткани содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из ткани, выделенной от двух или более субъектов, и из тканей одних и тех же или похожих типов либо тканей разных типов. Согласно другому аспекту, два или более субъектов являются генетически гомогенными субъектами. Согласно другому аспекту, два или более субъектов являются фенотипически гомогенными субъектами. Согласно другому аспекту, два или более субъектов являются генетически различными субъектами. Согласно одному из аспектов, два или более субъектов являются фенотипически различными субъектами. Согласно другому аспекту, два или более субъектов относятся к одному и тому же полу или к разным полам.
Согласно другому аспекту, два или более субъектов относятся к разным полам. Согласно еще одному аспекту, два или более субъектов состоят в группах разной этнической принадлежности. Согласно одному из аспектов, два или более субъектов состоят в группе одной и той же этнической принадлежности. Согласно другому аспекту, субъект выбран из группы, состоящей из животного, сельскохозяйственного животного, домашнего животного, человека.
В одном из воплощений гомогенат дополнительно содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из одного или более чем одного материала, выбранного из клетки, не являющейся клеткой человека, человеческой клетки, детектируемой метки, используемой для очистки метки, ненативного(ой) белка, нуклеиновой кислоты или полинуклеотида, малой молекулы, красителя, вируса, бактерии, паразита, представителя простейших или химического вещества. Согласно одному из аспектов малая молекула содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из гаптена, пептидной метки, белковой метки, флуоресцентной метки, нуклеиновокислотной метки и их комбинации.
Способ получения репрезентативных данных
Данное изобретение также относится к получению репрезентативных данных на основе репрезентативного образца или композиции на основе гомогената, описанных в данной заявке. Согласно одному из аспектов способ получения репрезентативных данных включает анализ композиции на основе гомогената, которая описана в данной заявке. Согласно другому аспекту такой анализ включает получение количественных и/или качественных данных для маркера в композиции на основе гомогената. Для получения данных, относящихся к маркеру, можно использовать любой соответствующий метод, неограничивающие примеры которого включают измерение с использованием секвенирования из одной клетки, секвенирования из одного ядра, проточной цитометрии, иммуногистохимического окрашивания, окрашивания гематоксилином и эозином, секвенирования полного генома, высокопроизводительного секвенирования, масс-спектрометрии, ДНК микрочипа или их комбинации.
Описанный в настоящей заявке способ представляет собой мощное средство для создания наборов данных, отчасти вследствие применения уникальных методов отбора образцов и композиции по изобретению. Клеточные структуры и/или отдельные компоненты репрезентативного образца по существу достоверно отражают или имитируют относительную пропорцию или процентные содержания этих клеточных структур (включая, но не ограничиваясь этим, типы, состав и вариации) во всей пробе ткани, как правило, в солидной опухоли, лимфатическом узле, метастазах, полипе, кисте или их части либо в комбинации любого из вышеперечисленных. Таким образом, набор данных, полученных в результате анализа репрезентативного образца (или композиции на основе гомогената) или его подгруппы, будет достоверно отражать соответствующую информацию от целой ткани или целого биологического образца, из которых приготовлен репрезентативный образец. В некоторых воплощениях репрезентативные данные являются указанием на все признаки всей совокупности исходных органа, ткани или опухоли, из которых был приготовлен репрезентативный образец.
Как указано выше, способ получения репрезентативных данных включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в получении количественных и/или качественных данных для маркера в композиции на основе гомогената.
В контексте этого способа и композиции маркер содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из полинуклеотида, ДНК, белка, РНК, липида, клеточной органеллы, метаболита или клетки. Согласно одному из аспектов, белок содержит модификацию, при этом указанная модификация выбрана из группы, состоящей из ацетилирования, АДФ-рибозилирования, ацилирования, АДФ-рибозилирования, амидирования, ковалентного присоединения флавина, ковалентного присоединения тема, ковалентного присоединения нуклеотида или нуклеотидного производного, ковалентного присоединения липида или липидного производного, ковалентного присоединения фосфатидилинозита, перекрестного сшивания, циклизации, образования дисульфидных связей, дезметилирования, образования ковалентных сшивок, образования цистина, образования пироглутамата, формилирования, гамма-карбоксилирования, гликозилирования, образования GPI якоря, гидроксилирования, иодинирования, метилирования, миристоилирования, окисления, протеолитического процессинга, фосфорилирования, пренилирования, рацемизации, селеноилирования, сульфатирования, аргинилирования и убиквитинилирования. Согласно другому аспекту маркер содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из геномного полиморфизма, обуславливающего фармакогеномику однонуклеотидного полиморфизма (SNP), геномного SNP, соматического полиморфизма и дифференциальной экспрессии белка, липида и/или клеточной органеллы.
Согласно другому аспекту маркер содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из однонуклеотидного положения; внутригенного участка или межгенного участка; экзона или интрона либо их фрагмента; кодирующего участка или некодирующего участка; промотора, энхансера, 5'-нетранслируемого участка (5-UTR) или 3'-нетранслируемого участка (3'-UTR) либо их фрагмента; кДНК или ее фрагмента; SNP; соматической мутации, мутации в зародышевой линии или их обеих; точечной мутации или мутации в одном сайте; делеционной мутации; делеции внутри рамки считывания, внутригенной делеции, полной делеции гена; инсерционной мутации; внутригенной вставки; инверсионной мутации; внутрихромосомной инверсии; мутации с нарушением связывания (linking mutation); сопряженной инсерционной мутации; мутации типа инвертированной дупликации; тандемной дупликации; внутрихромосомной тандемной дупликации; транслокации; хромосомной транслокации, нереципрокной транслокации; перестройки; геномной перестройки; перестройки одного или более интронов или их фрагментов; интрона с перестроенной структурой; 5'- или 3'-UTR или их комбинации. Согласно другому аспекту маркер содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из измененной нуклеотидной последовательности, которая кодирует измененную аминокислотную последовательность, хромосомной транслокации, внутрихромосомной инверсии, изменения числа копий, изменения уровня экспрессии, изменения уровня белка, изменения активности белка или изменения статуса метилирования в раковой ткани или раковой клетке по сравнению с нормальной, здоровой тканью или клеткой.
Согласно другому аспекту маркер представляет собой опухолевый маркер, выбранный из группы, состоящей из: белка, антигена, фермента, гормона, ДНК, РНК, микроРНК или углевода. Согласно другому аспекту маркер представляет собой опухолевый маркер, выбранный из группы, состоящей из: Her2, bRaf, ERBB2, PI3KCA, FGFR2, р53, BRCA, CCND1, MAP2K4, ATR, AFP, ALK, BCR-ABL, BRCA1/BRCA2, BRAF, V600E, Са-125, СА19.9, EGFR, Her-2, KIT, PSA, S100, KRAS, ER/Pr, UGT1A1, CD30, CD20, F1P1L1-PDGRFα, PDGFR, TMPT, TMPRSS2; ABCB5, AFP-L3, альфа-фетопротеина, альфа-метил-ацил-КоА-рацемазаа, BRCA1, BRCA2, СА 15-3, СА 242, Са 27-29, СА-125, СА15-3, СА19-9, кальцитонина, канцероэмбрионального антигена, пептида-1 канцероэмбрионального антигена, дез-гамма-карбоксипротромбина, десмина, раннего антигена-2 рака предстательной железы, рецептора эстрогенов, продукта деградации фибрина, глюкозо-6-фосфат-изомеразы, vE6, Е7, L1, L2 или p1611NK4a, хорионического гонадотропина человека, IL-6, кератина 19, лактатдегидрогеназы, лейциламинопептидазы, липотропина, метанефринов, неприлизина, NMP22, норметанефрина, РСА3, простатоспецифического антигена, кислой фосфатазы предстательной железы, синаптофизина, тиреоглобулина, TNF, транскрипционного фактора, выбранного из ERG, ETV1 (ER81), FLI1, EST1, EST2, ELK1, ETV6, ETV7, GABPα, ELF1, ETV4, ETV5, ERF, PEA3/E1AF, PU.1, ESE1/ESX, SAP1 (ELK4), ETV3 (METS), EWS/FLI1, ESE1, ESE2 (ELF5), ESE3, PDEF, NET (ELK3; SAP2), NERF (ELF2) или FEV. XXX; опухолеассоциированного гликопротеина 72, c-kit, SCF, pAKT, pc-kit, виментина, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, KIR, TIM3, GAL9, GITR, LAG3, VISTA, KIR, 2B4, TRP02, CD160, CGEN-15049, CHK 1, CHK2, A2aR, TL1A, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2B4, CD160, CGEN-15049, CHK1, CHK2, A2aR, семейства B-7 или их комбинации. Согласно одному из аспектов маркером является опухолевый маркер, который содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из одного или более чем одного маркера, выбранного из группы: геномного полиморфизма, обуславливающего фармакогеномику однонуклеотидного полиморфизма (SNP), геномного SNP, соматического полиморфизма и дифференциальной экспрессии белка, липида и/или клеточной органеллы. Согласно другому аспекту опухолевый маркер выбран из группы, состоящей из: однонуклеотидного положения; внутригенного участка или межгенного участка; экзона или интрона либо их фрагмента; кодирующего участка или некодирующего участка; промотора, энхансера, 5'-нетранслируемого участка (5'-UTR) или 3'-нетранслируемого участка (3'-UTR) либо их фрагмента; кДНК или ее фрагмента SNP; соматической мутации, мутации в зародышевой линии или их обеих; точечной мутации или мутации в одном сайте; делеционной мутации; делеции внутри рамки считывания, внутригенной делеции, полной делеции гена; инсерционной мутации; внутригенной вставки; инверсионной мутации; внутрихромосомной инверсии; мутации с нарушением связывания; сопряженной инсерционной мутации; мутации типа инвертированной дупликации; тандемной дупликации; внутрихромосомной тандемной дупликации; транслокации; хромосомной транслокации, нереципрокной транслокации; перестройки; геномной перестройки; перестройки одного или более интронов либо их фрагментов; интрона с перестроенной структурой; 5'- или 3'-UTR или их комбинации. Согласно другому аспекту маркер представляет собой опухолевый маркер, который содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из маркера, выбранного из группы: измененной нуклеотидной последовательности, которая кодирует измененную аминокислотную последовательность, хромосомной транслокации, внутрихромосомной инверсии, изменения числа копий, изменения уровня экспрессии, изменения уровня белка, изменения активности белка и изменения статуса метилирования в раковой ткани или раковой клетке, каждый раз "изменение" по сравнению с нормальной, здоровой тканью или клеткой.
Эти данные получают по результатам анализа композиции на основе гомогената, которая описана в данной заявке. Неограничивающими примерами ткани для анализа являются образцы, выбранные из группы, состоящей из: одной или нескольких клеток в состоянии, предшествующем злокачественному перерождению, или озлокачествленных клеток, клеток из солидной опухоли, опухоли мягких тканей или метастатического поражения, ткани или клеток из хирургического края (опухоли), гистологически нормальной ткани, одной или нескольких циркулирующих опухолевых клеток (СТС), нормальной близко расположенной ткани (NAT), образца крови от одного и того же субъекта, имеющего опухоль или имеющего риск наличия опухоли, или FFPE образца.
В одном из воплощений репрезентативные данные содержат качественные и количественные данные, полученные для одного маркера. Согласно одному из аспектов репрезентативные данные содержат качественные и/или количественные данные, полученные из двух или более разных маркеров. Согласно другому аспекту репрезентативные данные получают путем измерения уровня одного и того же или нескольких маркеров в разные моменты времени, например, до и после терапии, и согласно одному из аспектов их можно использовать для мониторинга терапии или состояния пациента при прохождении курса лечения.
В одном из воплощений способ получения репрезентативных данных дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в установлении внутреннего значения для качественных и/или количественных данных. В другом воплощении способ получения репрезентативных данных дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в сравнении репрезентативных данных с предварительно заданным значением для этих данных. Согласно другому аспекту измеренные значения для маркера нормируют и на основе этого нормированного измеренного значения для маркера получают суммарную оценку в баллах. Далее суммарную оценку в баллах можно сравнивать с предварительно заданной оценкой в баллах. В контексте рака, в еще одном воплощении, способ получения репрезентативных данных дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в (а) измерении уровня опухолевого маркера в первом биологическом образце, при этом измеренное значение для опухолевого маркера является нормированным; (b) получении суммарной оценки в баллах на основании этого нормированного измеренного значения; и (с) сравнении суммарной оценки в баллах с предварительно заданной оценкой в баллах с целью определения показателя риска рака у субъекта.
В другом воплощении предварительно заданное значение выбрано из данных клинических испытаний, данных для субъекта, данных из научной литературы и данных для находящейся в клинической разработке биологической или малой молекулы. Согласно одному из аспектов репрезентативные данные содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из репрезентативных онкологических данных, при этом репрезентативные онкологические данные содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из количественных и/или качественных данных по меньшей мере для одного опухолевого маркера из первого биологического образца, при этом указанный опухолевый маркер ассоциирован с наличием опухоли.
В одном из воплощений предварительно заданная оценка в баллах выбрана из группы, состоящей из: данных клинических испытаний, репрезентативных онкологических данных, полученных для второго биологического образца, репрезентативных онкологических данных, полученных для группы биологических образцов, данных для находящейся в клинической разработке биологической или малой молекулы.
Способы определения фенотипических профилей
В одном из воплощений данное изобретение относится к способу определения фенотипического профиля образца ткани, при этом данный способ включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в анализе клеточных структур в композиции на основе гомогената. Согласно одному из аспектов клеточные структуры, которые могут быть проанализированы в отношении фенотипического профиля, содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из кластера клеток, отдельной клетки, фрагмента клетки, из органеллы, пептида, нуклеиновой кислоты, липида, метаболита или их комбинации. Согласно другому аспекту клеточные структуры содержат одиночную клетку или одиночное ядро, при этом одиночная клетка или одиночное ядро является интактной(ым). В некоторых воплощениях анализ включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в анализе количеств, типов, статусов, процентных содержаний и/или процессов экспрессии клеточных структур. Согласно другому аспекту анализ включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в анализе одиночных клеток, анализе одиночных ядер, анализе одиночных органелл или их сочетании. Согласно одному из аспектов, статус клеточных структур содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из пролиферации, апоптоза, некроза, миграции, эпителиально-мезенхимального перехода ("ЕМТ"), митоза, ареста клеточного цикла, S-фазы, старения и/или дифференцировки. Согласно другому аспекту анализ включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в анализе маркера из гомогената.
В одном из воплощений маркер выбран из группы, состоящей из ДНК, белка, РНК, липида, клеточной органеллы, метаболита или клетки. Согласно одному из аспектов, анализ маркера включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в детектировании данного маркера. Согласно другому аспекту анализ маркера включает анализ маркера из одиночной клетки или одиночного ядра.
Способ лечения заболевания
Данное изобретение, согласно другому аспекту, относится к способу лечения заболевания путем выбора эффективного режима терапии на основе репрезентативных данных, полученных с использованием способов по изобретению. При правильном количестве или типе информации, поступающей от пациента, режим терапии может быть адаптирован с целью достижения пациентом результата лечения с наилучшим ответом и максимальным пределом безопасности. Кроме того, эта информация также может обеспечить пациенту получение многих других преимуществ, например, ранних диагнозов, оценок риска и эффективных методов лечения, что тем самым значительно улучшит качество медицинского обслуживания.
Выбор эффективного режима терапии зависит от нескольких факторов. Во-первых, необходимо обеспечить надежную диагностику заболевания или состояния здоровья. В случае инфекционных заболеваний, рака или других острых опасных для жизни заболеваний эта диагностика должна быть выполнена быстро и эффективно, поскольку время играет решающую роль в выживаемости пациентов, страдающих этими заболеваниями. Во-вторых, терапевтическое лечение отдельного пациента становится более эффективным, если поставлен точный диагноз. Например, когда рак иногда лечат стандартным "коктейлем" противораковых лекарственных средств, зачастую этот "коктейль" вызывает серьезные побочные эффекты у пациента. Если тип рака (или другого заболевания) точно не определен, то индивидуальная схема лечения этого типа заболевания не будет в высшей степени эффективной по сравнению с любой другой схемой лечения. Таким образом, эффективность напрямую зависит от данных или информации, полученных от подлежащего лечению пациента. Более эффективное лечение было бы возможным, если бы данная схема лечения была перепроверена путем сравнения со схемами, уже успешно примененными к этому пациенту или другим пациентам с учетом физиологической реакции на ранее применяемую схему. Кроме того, точная диагностика заболевания приведет к снижению затрат на разработку индивидуальной схемы лечения, поскольку позволит избежать приема ненужного и неэффективного лекарственного средства. Тем не менее, даже тем, кто владеет информацией о самых современных методах лечения, необходимо время для усвоения этой информации и понимания того, как она соотносится к информацией о другом методе лечения, чтобы обеспечить наилучшее доступное лечение для пациента.
Таким образом, согласно данному изобретению предложен способ лечения заболевания у субъекта, включающий или, альтернативно, заключающийся по существу в или, кроме того, в основном заключающийся в выборе соответствующей схемы лечения на основании репрезентативных данных, при этом репрезентативные данные содержат первый профиль от субъекта.
Согласно одному из аспектов неограничивающие примеры первого профиля содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из профиля, выбранного из группы: биомаркерного профиля, антигенного профиля, белкового профиля, мутационного профиля, липидного профиля, экзосомного профиль или их комбинации. Согласно другому аспекту маркер содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из одного или более маркеров из группы, состоящей из: Her2, bRaf, ERBB2, PI3KCA, FGFR2, р53, BRCA, CCND1, MAP2K4, ATR, AFP, ALK, BCR-ABL, BRCA1/BRCA2, BRAF, V600E, Са-125, СА19.9, EGFR, Her-2, KIT, PSA, S100, KRAS, ER/Pr, UGT1A1, CD30, CD20, F1P1L1-PDGRFα, PDGFR, TMPT, TMPRSS2; ABCB5, AFP-L3, альфа-фетопротеина, альфа-метил-ацил-КоА-рацемазы, BRCA1, BRCA2, CA 15-3, CA 242, Ca 27-29, СА-125, CA15-3, CA19-9, кальцитонина, канцероэмбрионального антигена, пептида-1 канцероэмбрионального антигена, дез-гамма-карбоксипротромбина, десмина, раннего антигена-2 рака предстательной железы, рецептора эстрогенов, продукта деградации фибрина, глюкозо-6-фосфат-изомеразы, vE6, Е7, L1, L2 или p16INK4a, хорионического гонадотропина человека, IL-6, кератина 19, лактатдегидрогеназы, лейциламинопептидазы, липотропина, метанефринов, неприлизина, NMP22, норметанефрина, РСА3, простатоспецифического антигена, кислой фосфатазы предстательной железы, синаптофизина, тиреоглобулина, TNF, транскрипционного фактора, выбранного из ERG, ETV1 (ER81), FLI1, EST1, EST2, ELK1, ETV6, ETV7, GABPα, ELF1, ETV4, ETV5, ERF, PEA3/E1AF, PU.1, ESE1/ESX, SAP1 (ELK4), ETV3 (METS), EWS/FLI1, ESE1, ESE2 (ELF5), ESE3, PDEF, NET (ELK3; SAP2), NERF (ELF2) или FEV. XXX, опухолеассоциированного гликопротеина 72, c-kit, SCF, pAKT, pc-kit, виментина, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, KIR, TIM3, GAL9, GITR, LAG3, VISTA, KIR, 2B4, TRPO2, CD160, CGEN-15049, CHK 1, CHK2, A2aR, TL1A, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2B4, CD160, CGEN-15049, CHK1, CHK2, A2aR, семейства B-7 и их комбинации. Согласно некоторому аспекту первый профиль содержит профиль, полученный из группы, состоящей из: одного или нескольких маркеров, одного или нескольких антигенов, одного или нескольких белков, одной или нескольких мутаций, одного или нескольких липидов, одной или нескольких экзосом или их комбинации.
В некоторых воплощениях используемый в способе маркер выбран из группы, состоящей из: геномного полиморфизма, обуславливающего фармакогеномику однонуклеотидного полиморфизма (SNP), геномного SNP, соматического полиморфизма и дифференциальной экспрессии белка, липида и/или клеточной органеллы. Согласно одному из аспектов маркер выбран из группы, состоящей из: однонуклеотидного положения; внутригенного участка или межгенного участка; экзона или интрона либо их фрагмента; кодирующего участка или некодирующего участка; промотора, энхансера, 5'-нетранслируемого участка (5'-UTR) или 3'-нетранслируемого участка (3'-UTR) либо их фрагмента; кДНК или ее фрагмента; SNP; соматической мутации, мутации в зародышевой линии или их обеих; точечной мутации или мутации в одном сайте; делеционной мутации; делеции внутри рамки считывания, внутригенной делеции, полной делеции гена; инсерционной мутации; внутригенной вставки; инверсионной мутации; внутрихромосомной инверсии; мутации с нарушением связывания; сопряженной инсерционной мутации; мутации типа инвертированной дупликации; тандемной дупликации; внутрихромосомной тандемной дупликации; транслокации; хромосомной транслокации, нереципрокной транслокации; перестройки; геномной перестройки; перестройки одного или более интронов либо их фрагментов; интрона с перестроенной структурой; 5'- или 3'-UTR и их комбинации.
Данный способ можно использовать для определения возможности применения схемы лечения, которая содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из персонального режима введения. Согласно одному из аспектов схема лечения выбрана из группы, состоящей из: химиотерапии, иммунотерапии, облучения, хирургического вмешательства, генной терапии, гормональной терапии, терапии стволовыми клетками, переливания крови, физиотерапии, фотодинамической терапии и их комбинации.
В другом воплощении способ лечения заболевания у субъекта дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в сравнении первого профиля от субъекта с предварительно заданным профилем для определения соответствия данной схемы лечения субъекту. Согласно одному из аспектов предварительно заданный профиль определен на основании данных, выбранных из группы, состоящей из: данных клинических испытаний, второго профиля от субъекта, профиля другого биологического образца или группы биологических образцов, профиля от другого субъекта или группы субъектов, данных для биологической или малой молекулы и их комбинации.
Согласно другому аспекту такое лечение включает выбор одного или более лекарственных средств и/или дозировки (количества, продолжительности введения и т.д.) таких лекарственных средств, вводимых пациенту, с целью разработки персонализированного лечения с учетом индивидуального тканевого или ракового профиля пациента. Например, если в одном репрезентативном образце обнаруживаются два биомаркера в репрезентативном образце, указывающие на возможность ответной реакции на конкретное лекарственное средство X и другое лекарственное средство Y, то пациенту могут быть назначены оба лекарственных средства. Если присутствие биомаркера для лекарственного средства X определяется в пределах 75%, а присутствие биомаркера для лекарственного средства Y определяется на уровне 25%, то тогда лекарственному средству X может быть отдано предпочтение, и его доставляют первым, а затем лекарственное средство Y. Альтернативно, лекарственное средство Y может превосходить по важности лекарственное средство X.
Данный способ может быть повторен в разные периоды приема курса терапии и модифицирован с учетом изменения экспрессии маркера в профиле. Согласно этому аспекту данный способ полезен для мониторинга терапии и прогрессирования заболевания у пациента или у разных пациентов с одинаковым или похожим заболеванием, получающего(их) одинаковые или разные методы терапии.
Способ идентификации клинически релевантного маркера
Данные или информация о клинически релевантных маркерах или биомаркерах могут давать представление о вероятности патологических состояний. Репрезентативные данные, приведенные в описаниях, могут быть использованы для идентификации клинически релевантных маркеров, в особенности тех, которые ранее не были ассоциированы с какими-либо патологическими состояниями.
Таким образом, другой аспект данного изобретения относится к способу идентификации клинически релевантного маркера, включающему сравнение репрезентативных данных с предварительно заданными данными. Неограничивающие примеры маркеров указаны выше. Согласно одному из аспектов маркер выбран из группы, состоящей из белка, антигена, фермента, гормона, ДНК, РНК, микроРНК или углевода. Согласно другому аспекту маркер содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из геномного полиморфизма, обуславливающего фармакогеномику однонуклеотидного полиморфизма (SNP), геномного SNP, соматического полиморфизма и дифференциальной экспрессии белка, липида, модификации белка и клеточной органеллы. Согласно некоторому аспекту маркер выбран из группы, состоящей из: однонуклеотидного положения; внутригенного участка или межгенного участка; экзона или интрона либо их фрагмента; кодирующего участка или некодирующего участка; промотора, энхансера, 5'-нетранслируемого участка (5'-UTR) или 3'-нетранслируемого участка (3'-UTR) либо их фрагмента; кДНК или ее фрагмента; SNP; соматической мутации, мутации в зародышевой линии или их обеих; точечной мутации или мутации в одном сайте; делеционной мутации; делеции внутри рамки считывания, внутригенной делеции, полной делеции гена; инсерционной мутации; внутригенной вставки; инверсионной мутации; внутрихромосомной инверсии; мутации с нарушением связывания; сопряженной инсерционной мутации; мутации типа инвертированной дупликации; тандемной дупликации; внутрихромосомной тандемной дупликации; транслокации; хромосомной транслокации, нереципрокной транслокации; перестройки; геномной перестройки; перестройки одного или более интронов либо их фрагментов; интрона с перестроенной структурой; 5'- или 3'-UTR и их комбинации. Согласно одному из аспектов маркер выбран из группы, состоящей из: измененной нуклеотидной последовательности, которая кодирует измененную аминокислотную последовательность, хромосомной транслокации, внутрихромосомной инверсии, изменения числа копий, изменения уровня экспрессии, изменения уровня белка, изменения активности белка и изменения статуса метилирования в раковой ткани или раковой клетке, каждый раз по сравнению с нормальной, здоровой тканью или клеткой.
В одном из воплощений предварительно заданные данные получены на основании данных, выбранных из группы, состоящей из: данных клинических испытаний, данных для субъекта или группы субъектов, данных для образца ткани или группы образцов ткани, данных для находящейся в клинической разработке биологической или малой молекулы либо их комбинации.
Согласно некоторому аспекту предложен способ определения прогноза рака у субъекта, включающий оценку репрезентативных данных, полученных от субъекта. В одном из воплощений способ определения прогноза рака дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в расчете количественной оценки в баллах в отношении прогноза рака, при этом такой прогноз устанавливают на основании количественной оценки в баллах.
В одном из воплощений репрезентативные данные содержат информацию о количестве, типах, статусах и/или процентном содержании клеточных структур в гомогенате. В другом воплощении клеточные структуры содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из стволовых клеток, эпителиальных клеток, клеток крови, жировых клеток клеток, клеток кожи, эндотелиальных клеток, раковых клеток или иммунных клеток. В одном из воплощений иммунные клетки содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из нейтрофилов, моноцитов, макрофагов, дендритных клеток, природных киллерных клеток, Т-клеток и/или В-клеток. В некотором воплощении Т-клетки содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из киллерных Т-клеток, хелперных Т-клеток, регуляторных Т-клеток, пан-Т-клеток, наивных Т-клеток, активированных Т-клеток и/или гамма-дельта-Т-клеток.
В одном из воплощений статус клеточных структур содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из пролиферации, апоптоза, некроза, миграции, эпителиально-мезенхимального перехода ("ЕМТ"), митоза, ареста клеточного цикла, S-фазы, старения и/или дифференцировки. В одном из воплощений репрезентативные данные содержат информацию о маркере в гомогенате. В другом воплощении маркер выбран из группы, состоящей из ДНК, белка, РНК, липида, клеточной органеллы, метаболита или клетки. В некотором воплощении маркер содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из одного или более маркеров из Her2, bRaf, ERBB2, PI3KCA, FGFR2, р53, BRCA, CCND1, MAP2K4, ATR, AFP, ALK, BCR-ABL, BRCA1/BRCA2, BRAF, V600E, Са-125, СА19.9, EGFR, Her-2, KIT, PSA, S100, KRAS, ER/Pr, UGT1A1, CD30, CD20, F1P1L1-PDGRFα, PDGFR, TMPT, TMPRSS2; ABCB5, AFP-L3, альфа-фетопротеина, альфа-метил-ацил-КоА-рацемазы, BRCA1, BRCA2, CA 15-3, CA 242, Са 27-29, СА-125, CA15-3, CA19-9, кальцитонина, канцероэмбрионального антигена, пептида-1 канцероэмбрионального антигена, дез-гамма-карбоксипротромбина, десмина, раннего антигена-2 рака предстательной железы, рецептора эстрогенов, продукта деградации фибрина, глюкозо-6-фосфат-изомеразы, vE6, Е7, L1, L2 или p16INK4a, хорионического гонадотропина человека, IL-6, кератина 19, лактатдегидрогеназы, лейциламинопептидазы, липотропина, метанефринов, неприлизина, NMP22, норметанефрина, РСА3, простатоспецифического антигена, кислой фосфатазы предстательной железы, синаптофизина, тиреоглобулина, TNF, транскрипционного фактора, выбранного из ERG, ETV1 (ER81), FLI1, EST1, EST2, ELK1, ETV6, ETV7, GABPα, ELF1, ETV4, ETV5, ERF, PEA3/E1AF, PU.1, ESE1/ESX, SAP1 (ELK4), ETV3 (METS), EWS/FLI1, ESE1, ESE2 (ELF5), ESE3, PDEF, NET (ELK3; SAP2), NERF (ELF2) или FEV. XXX, опухолеассоциированного гликопротеина 72, c-kit, SCF, pAKT, pc-kit, виментина, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, KIR, TIM3, GAL9, GITR, LAG3, VISTA, KIR, 2B4, TRPO2, CD160, CGEN-15049, CHK 1, CHK2, A2aR, TL1A, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2B4, CD160, CGEN-15049, CHK1, CHK2, A2aR, семейства B-7 и их комбинации. В другом воплощении маркер выбран из группы, состоящей из: модификации белка, при этом указанная модификация выбрана из группы, состоящей из ацетилирования, АДФ-рибозилирования, ацилирования, АДФ-рибозилирования, амидирования, ковалентного присоединения флавина, ковалентного присоединения тема, ковалентного присоединения нуклеотида или нуклеотидного производного, ковалентного присоединения липида или липидного производного, ковалентного присоединения фосфатидилинозита, перекрестного сшивания, циклизации, образования дисульфидных связей, дезметилирования, образования ковалентных сшивок, образования цистина, образования пироглутамата, формилирования, гамма-карбоксилирования, гликозилирования, образования GPI якоря, гидроксилирования, иодинирования, метилирования, миристоилирования, окисления, протеолитического процессинга, фосфорилирования, пренилирования, рацемизации, селеноилирования, сульфатирования, аргинилирования и убиквитинилирования. Согласно некоторому аспекту маркер выбран из группы, состоящей из: геномного полиморфизма, обуславливающего фармакогеномику однонуклеотидного полиморфизма (SNP), геномного SNP, соматического полиморфизма и дифференциальной экспрессии белка, липида и/или клеточной органеллы, однонуклеотидного положения; внутригенного участка или межгенного участка; экзона или интрона либо их фрагмента; кодирующего участка или некодирующего участка; промотора, энхансера, 5'-нетранслируемого участка (5'-UTR) или 3'-нетранслируемого участка (3'-UTR) либо их фрагмента; кДНК или ее фрагмента; SNP; соматической мутации, мутации в зародышевой линии или их обеих; точечной мутации или мутации в одном сайте; делеционной мутации; делеции внутри рамки считывания, внутригенной делеции, полной делеции гена; инсерционной мутации; внутригенной вставки; инверсионной мутации; внутрихромосомной инверсии; мутации с нарушением связывания; сопряженной инсерционной мутации; мутации типа инвертированной дупликации; тандемной дупликации; внутрихромосомной тандемной дупликации; транслокации; хромосомной транслокации, нереципрокной транслокации; перестройки; геномной перестройки; перестройки одного или более интронов либо их фрагментов; интрона с перестроенной структурой; 5'- или 3'-UTR, измененной нуклеотидной последовательности, которая кодирует измененную аминокислотную последовательность, хромосомной транслокации, внутрихромосомной инверсии, изменения числа копий, изменения уровня экспрессии, изменения уровня белка, изменения активности белка или изменения статуса метилирования в раковой ткани или раковой клетке по сравнению с нормальной, здоровой тканью или клеткой.
Согласно другому аспекту данное изобретение относится к способу мониторинга заболевания у пациента, включающему или, альтернативно, заключающемуся по существу в или, кроме того, в основном заключающемуся в анализе клинически релевантного маркера, при этом клинически релевантный маркер идентифицирован на основе репрезентативных данных. Согласно одному из аспектов маркер выбран из группы, состоящей из: белка, антигена, фермента, гормона, ДНК, РНК, микроРНК или углевода. Согласно другому аспекту маркер представляет собой ДНК или РНК, выделенную из образца, выбранного из группы, состоящей из: одной или нескольких клеток в состоянии, предшествующем злокачественному перерождению, или озлокачествленных клеток, клеток из солидной опухоли, опухоли мягких тканей или метастатического поражения, ткани или клеток из хирургического края (опухоли), гистологически нормальной ткани, одной или нескольких циркулирующих опухолевых клеток (СТС), нормальной близко расположенной ткани (NAT), образца крови от одного и того же субъекта, имеющего опухоль или имеющего риск наличия опухоли, или FFPE образца. Согласно одному из аспектов заболевание представляет собой рак.
Способы хранения репрезентативного образца (или композиции на основе гомогената)
После приготовления репрезентативного образца этот образец может быть передан для проведения дальнейшей обработки и/или анализа. Таким образом, данное изобретение, в некоторых воплощениях, также относится к способу хранения композиции на основе гомогената, включающему либо, альтернативно, заключающемуся по существу в или, кроме того, в основном заключающемуся в смешивании композиции с эффективным количеством способствующего хранению реагента, неограничивающие примеры которого приведены в данном описании.
В одном из воплощений способствующий хранению реагент содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из консерванта, хаотропа, детергента, восстанавливающего агента, хелатора, буфера или их комбинации. Согласно одному из аспектов смешанная композиция сохраняет фенотипические и генотипические характеристики композиции до смешивания со способствующим хранению реагентом. Согласно другому аспекту смешанная композиция содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из денатурированных белков, инактивированной нуклеазы, инактивированной протеазы, инактивированного патогена, нерасщепленной нуклеиновой кислоты или их комбинации. Согласно некоторому аспекту хаотроп содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из гуанидина тиоцианата, гуанидина изоцианата, гуанидина гидрохлорида или их комбинации. Согласно одному из аспектов детергент содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из натрия додецилсульфата, лития додецилсульфата, натрия тауродезоксихолата, натрия таурохолата, натрия гликохолата, натрия дезоксихолата, натрия холата, натрия алкилбензолсульфоната, N-лауроилсаркозина или их комбинации. Согласно другому аспекту восстанавливающий реагент содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из меркаптоэтанола, трис(2-карбоксиэтил)фосфина, дитиотреита, диметилсульфоксида, трис(2-карбоксиэтил)фосфина или их комбинации. Согласно другому аспекту хелатор содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из этиленгликольтетрауксусной кислоты, гидроксиэтилэтилендиаминтриуксусной кислоты, диэтилентриаминпентауксусной кислоты, N,N-бис(карбоксиметил)глицина, этилендиаминтетрауксусной кислоты, цитрата безводного, цитрата натрия, цитрата кальция, цитрата аммония, бицитрата аммония, лимонной кислоты, цитрата диаммония, цитрата аммония-трехвалентного железа, цитрата лития или их комбинации. Согласно другому аспекту буфер содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из трис(гидроксиметил)аминометана, цитрата, 2-(N-морфолино)этансульфоновой кислоты, N,N-бис(2-гидроксиэтил)-2-аминоэтансульфоновой кислоты, 1,3-бис(трис(гидроксиметил)метиламино)пропана, 4-(2-гидроксиэтил)-1-пиперазин этансульфоновой кислоты, 3-(N-морфолин)пропансульфоновой кислоты, бикарбоната, фосфата или их комбинации.
Способ приготовления репрезентативного образца
Данное описание в целом относится к разработке методологии создания репрезентативных образцов тканей, например, из целых органов, опухолей, лимфатических узлов, метастазов или их комбинаций для решения проблемы гетерогенности, например, гетерогенности опухолей, в клинических пробах, в особенности, клинических пробах для применения в клинической онкологии, и к применению таких репрезентативных образцов или их частей в различных диагностических и терапевтических методах, а также к композициям, содержащим такие репрезентативные образцы для применения в диагностике и терапии, в особенности, онкологии.
В настоящей заявке показано, что методы отбора образцов, обычно применяемые для диагностики рака, в которых для диагностического тестирования используются небольшие образцы опухолей, могут приводить к серьезной систематической ошибке при отборе образцов для диагностической патологии и онкологии. Решения, касающиеся лечения пациента, как прогностического (например, ожидания времени выживания пациента), так и предиктивного (например, будет ли пациент восприимчив к конкретной терапии) характера, зачастую принимаются при применении одного из срезов FFPE тканей в опухолях, которые считаются "небольшими", т.е. в опухоли размером два сантиметра; с использованием традиционных методов все диагностические данные обычно получают на основании менее чем 0,03% объема опухоли (т.е. одного среза из FFPE блока). Кроме того, такие образцы ткани из опухолей традиционно берутся из очень неоднородных участков опухолей, что делает диагностическую онкологию "слепой" в отношении гетерогенности, присутствующей в остальной части опухоли. В результате набор данных оказывается незначительным (по отношению к популяции) и в связи с этим "необъективным".
Аналогичным образом, как и в случае с низкой вероятностью детектирования небольших субпопуляций генетически различающихся раковых клеток в солидных опухолях, небольшие метастазирующие опухоли в лимфатических узлах, окружающих место локализации первичной опухоли, невозможно обнаружить с использованием традиционного гистологического метода исследования. Лимфатические узлы изменяются в размере от одного миллиметра до нескольких сантиметров в диаметре. Присутствие опухолевых клеток в лимфатическом узле зависит от мутаций в ДНК, наличие которых выражается в подвижности и инвазии опухолевых клеток, а также мутаций, наличие которых придает способность выживать в новом окружении (т.е. в молочной железе в противоположность лимфатическому узлу). Размер метастазирующей опухоли в лимфатическом узле зависит от скорости пролиферации опухоли и продолжительности периода времени, в течение которого метастазирующая опухоль росла в лимфатическом узле. Для диагностического теста присутствия опухолевых клеток в лимфатических узлах применяют один или два тонких среза ткани (обычно толщиной четыре микрона) из FFPE блока. С использованием таких методов решающим фактором для обнаружения является размер опухоли относительно размера лимфатического узла. В то время как метастазирующая опухоль диаметром 0,1 мм может заполнить 10% объема небольшого лимфатического узла и иметь разумную вероятность обнаружения, опухоль того же размера будет содержать только 0,005% лимфатического узла, диаметр которого составляет два сантиметра, и иметь очень низкую вероятность обнаружения с использованием существующих в настоящее время гистологических методов. Значительное число пациентов, которые с использованием традиционных методов могут быть ложно отнесены к категории "без поражения лимфатических узлов", могли бы быть выявлены и получить более надлежащее лечение с использованием способов, описанных в данной заявке. Например, характеризующееся большей чувствительностью обнаружение пациентов "с поражением лимфатических узлов" может давать лучшую информацию для принятия решения относительно того, следует ли применять адъювантную химиотерапию.
С использованием IHC анализа репрезентативных образцов из ткани лимфатических узлов (например, приготовленных из удаленных хирургическим путем лимфатических узлов) можно детектировать микрометастазы чрезвычайно мелких опухолей путем окрашивания на эпителиальные маркеры в сочетании с маркерами пролиферации (например, используя двойное IHC окрашивание на цитокератин 8/18 вместе с Ki67). Этого можно достичь путем применения маркеров, для которых был получен положительный результат в первичной опухоли, используя другие маркеры метастазирующих клеток или другие диагностические маркеры. Обнаружение клеток метастазирующих опухолей также может быть осуществлено посредством идентификации нуклеиновых кислот, например, с использованием панели методов секвенирования следующего поколения, для идентификации ассоциированных с раком мутаций, в том числе мутаций, присутствующих в первичной опухоли. С использованием этих методов будут идентифицированы клетки метастазирующих опухолей. Помимо этого, естественный ход развития заболевания для каждого пациента можно определить и соотнести с конкретными мутациями, которые могут представлять собой мишени для терапии.
Современная клиническая практика для оценки опухолей включает в себя получение лишь небольшой части опухолевой ткани для заливки и приготовления срезов. В основном плане действий определение места нахождения участка в опухоли, содержащей представляющий интерес субклон, считается случайным событием. Поэтому, поскольку существующая в настоящее время практика дает осторожные инструкции относительно того, в каком участке следует отобрать образец и получить наиболее адекватную информацию для определения стадии по системе TNM, это не обязательно является информативным с точки зрения определения места нахождения субклональных участков опухоли. Также невозможно на основе макроскопического исследования определить, присутствует ли субклон.
Воплощения способов по настоящему изобретению могут учитывать гетерогенность опухолей в условиях онкологических клиник путем предоставления способов эффективного и воспроизводимого приготовления образцов клеток, которые являются репрезентативными для взятых целиком лимфатического узла, опухоли или опухолей пациента. Как показано на ФИГ. 2А, "репрезентативный" образец по изобретению содержит разные субпопуляции раковых клеток, содержащихся в опухоли, независимо ее размера. "Репрезентативный" образец по изобретению, альтернативно, может содержать разные субпопуляции из нормальных или контрольных популяций или может содержать образец, приготовленный смешиванием опухолевых клеток и нормальных клеток.
Все также альтернативно, репрезентативный образец по изобретению может содержать репрезентативные или гомогенные биомолекулы, происходящие из целой опухоли, лимфатических узлов или метастазов, фракции, содержащей белок, липиды, нуклеиновые кислоты или другие группировки, которые присутствуют в исходной ткани, например, во взятых целиком опухоли, лимфатических узлах или метастазах, используемых для приготовления образца или его фракции, при этом относительные пропорции таких составляющих снова являются репрезентативными характеристиками для данной исходной ткани. Например, такие биомолекулы могут быть выделены в результате дальнейшей диссоциации либо химической или ферментативной обработки образца и/или посредством применения методов, с использованием которых выделяют или извлекают конкретные части образца, например, посредством применения разделения на основании размера, например, фильтрования, для выделения или извлечения молекул конкретного размера или конкретной молекулярной массы, методов аффинной очистки, с использованием которых выделяют или извлекают конкретные типы молекул из репрезентативного образца, и тому подобного. Соответственно, такие способы по существу приводят к получению других типов репрезентативных образцов по изобретению, например, гомогенных, или репрезентативных образцов, содержащих все белки, нуклеиновые кислоты или липиды исходного образца, например, целой опухоли, целых лимфатических узлов, метастазов или целого органа, при этом такой репрезентативный образец можно использовать для методов анализа содержания белков, нуклеиновых кислот и/или липидов и при этом он отражает образец целой опухоли.
Поэтому в случае таких репрезентативных образцов, независимо от происхождения, в образце достоверно отражены относительные процентные содержания субпопуляций клеток в опухоли или опухолях либо других специфических группировок, присутствующих в исходной ткани, например, в опухоли или лимфатическом узле, метастазах или органе. Кроме того, эти репрезентативные образцы, в отличие от образцов, приготовленных традиционными диагностическими методами, могут быть использованы во многих методах анализа без ущерба в отношении возможности использования этой пробы в традиционных диагностических анализах. Более того, репрезентативные образцы, приготовленные в соответствии с изобретением, можно использовать (и возможно повторно использовать) в нескольких разных форматах проведения анализа по отдельности или одновременно для обнаружения присутствия даже небольших популяций субклонов или других группировок, таких как опухолевые антигены или нуклеиновые кислоты, в образце, например, опухоли, лимфатическом узле или метастазах.
Кроме того, как обсуждалось выше, каждый из репрезентативных образцов, полученных от разных пациентов либо приготовленных из разных тканей одного или разных пациентов, может быть помечен уникальными идентифицирующими метками метками, например, гаптеном, и меченые образцы от разных пациентов или из разных тканей комбинировали и использовали в желаемых способах анализа. По существу, это обеспечивает мультиплексирование различных образцов от пациентов.
На этом основании применение репрезентативных образцов, приготовленных в соответствии с типичными воплощениями описанных в настоящей заявке способов, будут способствовать повышению точности и по существу повышать точность детектирования, диагностики и/или установления стадии развития опухолей разных типов, т.е. разных солидных опухолей, независимо от типа, локализации, размера или объема опухолевой ткани. Кроме того, способы по настоящему изобретению можно использовать для приготовления репрезентативных образцов из рассматриваемых образцов нормальной ткани или предположительно предраковых тканей (например, полученных от субъектов с более высоким риском развития рака вследствие генетического риска или предшествующего ракового заболевания) с целью идентификации типов немногочисленных клеток, таких как линии раковых стволовых клеток, которые могут присутствовать в них еще до манифестации какого-либо признака заболевания.
В следующем воплощении данное изобретение относится к способу приготовления тканевых или биологических образцов, содержащих гетерогенные клеточные структуры, включающему: (а) гомогенизацию образца; (b) реконструирование гомогенизированного образца с получением гомогената, причем указанный гомогенат содержит по существу гомогенные клеточные структуры, и соотношение клеточных структур в подгруппе гомогената по существу аналогично соотношению клеточных структур в образце ткани. Согласно одному из аспектов, гомогенат содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из множества одиночных клеток или множества кластеров клеток.
В одном из воплощений способ приготовления образца ткани дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в фиксации гомогената с использованием фиксирующего агента. Согласно другому аспекту фиксирующий агент содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из формалина, кальция, уксусной кислоты, физиологического раствора, спирта, мочевины, бронопола, воды или их комбинации. Согласно другому аспекту подвергнутый фиксации гомогенат размещают на предметном стекле.
В некоторых воплощениях способ приготовления образца ткани дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в экстрагировании компонента из гомогената. Согласно одному из аспектов компонент представляет собой ДНК, РНК, белок, липид, клеточную органеллу, экзосому, клетку или их комбинацию. В другом воплощении способ приготовления образца ткани дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в выделении клеточной структуры или компонента из гомогената. Согласно одному из аспектов клеточная структура или компонент содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из одиночной клетки или одиночного ядра. Согласно одному из аспектов выделение включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в выделении одной клетки или выделении одного ядра. Согласно другому аспекту выделение одной клетки выполняют с использованием проточной цитометрии, препаровки под лазерным микроскопом, ручной сортировки клеток, случайного посева и разведения, микрофлюидного устройства, устройства типа "лаборатории на чипе" или их комбинации. Согласно одному из аспектов выделение одного ядра выполняют с использованием проточной цитометрии.
В одном из воплощений гомогенизация включает или, альтернативно, заключается по существу в или, кроме того, в основном заключается в химической и/или биохимической диссоциации и/или возможно механической гомогенизации. Согласно одному из аспектов способ гомогенизации не вызывает лизиса клеток. Согласно другому аспекту химическая обработка образца включает или, альтернативно, заключается по существу в или, кроме того, в основном заключается в ферментативного расщепления образца, при этом указанное ферментативное расщепление включает применение фермента, выбранного из группы, состоящей из интерстициальной коллагеназы, желатиназы-а, стромелизина 1, матрилизина, коллагеназы нейтрофилов, желатиназы-b, стромелизина 2, стромелизина 3, металлоэластазы макрофагов, коллагеназы 3, МТ1-ММР, МТ2-ММР, МТ3-ММР, МТ4-ММР, коллагеназы 4, энамелизина, Х-ММР, СА-ММР, МТ5-ММР, МТ6-ММР, матрилизина-2, ММР-22, эндопротеиназы, трипсина, химотрипсина, эндопротеиназы Asp-N, эндопротеиназы Arg-C, эндопротеиназы Glu-C (V8 протеазы), эндопротеиназы Lys-C, пепсина, термолизина, эластазы, папаина, протеиназы K, субтилизина, клострипаина, экзопептидазы, карбоксипептидазы А, карбоксипептидазы В, карбоксипептидазы Р, карбоксипептидазы Y, катепсина С, высвобождающего ациламинокислоту фермента и пироглутаматаминопептидазы. Согласно одному из аспектов механическую гомогенизацию выполняют с использованием устройства, выбранного из группы, состоящей из блендера, диассоциатора, экстрактора, ступки, пестика, гомогенизатора Даунса, измельчителя тканей, гомогенизатора тканей с вращающимися ножами и гомогенизатора по типу шаровой мельницы. Согласно другому аспекту гомогенат готовят путем шинкования вручную с использованием скальпеля или ножа. В одном из воплощений гомогенизация дополнительно включает или, альтернативно, заключается по существу в или, кроме того, в основном заключается в выдерживании клеток, при этом указанное выдерживание клеток включает подведение рН и/или температуры либо обработку образца буфером для выдерживания клеток.
Согласно некоторым аспектам, до или после гомогенизации образца, образец обрабатывают гормонами, белками, ферментами, липидами, детергентами, ультразвуком, посредством физического встряхивания или их комбинации, до или после гомогенизации.
Согласно другому аспекту гомогенизированный образец содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из клеток и/или кластеров клеток. Согласно некоторому аспекту гомогенизированный образец содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из кластеров клеток одинаковых размеров. Согласно другому аспекту гомогенизированный образец содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из кластеров клеток неодинаковых размеров. Согласно некоторому аспекту кластеры клеток содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из 1-100 клеток или 100-1000 клеток, 1000-10000 клеток или 10000-100000 клеток. Согласно дополнительному аспекту кластеры клеток содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят более чем из 100000 клеток.
В одном из воплощений способ приготовления образца ткани дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в пропускания гомогенизированного образца через сетку, фильтр либо ряд сеток или фильтров. Согласно одному из аспектов сетка или фильтр имеет размер пор, изменяющийся в диапазоне от примерно 1 микрона до примерно 500 микрон. Согласно другому аспекту сетка или фильтр имеет размер пор меньше 1 микрона. Согласно некоторому аспекту сетка или фильтр имеет размер пор, изменяющийся в диапазоне от примерно 1 микрона до примерно 100 микрон, от примерно 100 микрон до примерно 200 микрон, от примерно 200 микрон до примерно 300 микрон, от примерно 300 микрон до примерно 400 микрон или от примерно 400 микрон до примерно 500 микрон. Согласно дополнительному аспекту сетка или фильтр имеет размер пор больше 500 микрон.
В дополнительном воплощении образец ткани отбирают из ткани, выбранной из группы, состоящей из опухоли, лимфатического узла, метастаза, полипа, кисты, биопсийного материала, целого органа и их комбинации. Согласно одному из аспектов образец ткани представляет собой твердый образец или жидкий образец. Согласно другому аспекту жидкий образец содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из отобранного шприцем аспирата для цитологического исследования, образца экссудата или мазка по Папаниколау. Согласно одному из аспектов клеточные структуры гомогената содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят по меньшей мере из одной клетки. Согласно другому аспекту клеточные структуры гомогената содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят по меньшей мере из 100 клеток. Согласно другому аспекту клеточные структуры гомогената содержат от примерно 100 до примерно 200 клеток, от примерно 200 до примерно 1000 клеток, от примерно 1000 до примерно 5000 клеток или от примерно 10000 до примерно 100000 клеток. Согласно другому аспекту клеточные структуры гомогената содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят из от примерно 100000 до примерно 1000000 клеток; от примерно 1000000 до примерно 5000000 клеток, от примерно 5000000 до примерно 1000000000 клеток или от примерно 1000000000 до примерно 5000000000 клеток. Согласно другому аспекту клеточные структуры гомогената содержат либо, альтернативно, состоят по существу из или, кроме того, в основном состоят более чем из примерно 5000000000 клеток.
В одном из воплощений гомогенат не подвергнут консервации или фиксации. Согласно одному из аспектов гомогенат содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из живой клетки. Согласно другому аспекту гомогенат подвергнут консервации или фиксации. Согласно одному из аспектов гомогенат замораживают, подвергают сублимационной сушке или заливают средой для заливки. Согласно другому аспекту гомогенат содержит клетки из одной или нескольких тканей и/или от одного или более чем одного субъекта.
В одном из воплощений образец ткани выделен из опухоли, лимфатического узла, метастазов, полипа, кисты, извлеченного резекцией материала, целого органа или их комбинации. Согласно одному из аспектов, гомогенат дополнительно содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из клетки, не являющейся клеткой человека, человеческой клетки, ненативного(ой) белка, нуклеиновой кислоты или малой молекулы. В одном из воплощений малая молекула выбрана из группы, состоящей из гаптена, пептидной метки, белковой метки, флуоресцентной метки, нуклеиновокислотной метки и их комбинации. Согласно дополнительному аспекту малая молекула содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из гаптена, пептидной метки, белковой метки, флуоресцентной метки, нуклеиновокислотной метки, люминесцентной метки, биотина и их комбинации.
В дополнительном воплощении способ приготовления образца ткани дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в оценке по существу гомогенных клеточных структур в гомогенате. Согласно одному из аспектов по существу гомогенные клеточные структуры оценивают путем измерения распределения внутреннего контроля в гомогенате. Согласно другому аспекту внутренний контроль выбран из группы, состоящей из клетки, не являющейся клеткой человека, человеческой клетки, ненативного белка, нуклеиновой кислоты, малой молекулы, красителя, химического вещества и их комбинации.
Согласно другому аспекту изобретения предложен способ приготовления биологического образца, подходящего для оценки гетерогенности клеток в образце (таком как опухолевый образец, или лимфатический узел, или метастазы, или их комбинация) и/или для оценки прогноза конкретного ракового заболевания у субъекта, включающий (1) получение одного или более интактных образцов биопсийного материала из солидной опухоли или лимфатического узла, при этом предпочтительно, чтобы каждый образец биопсийного материала содержал по меньшей мере примерно 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 или большее число клеток и возможно был подвергнут фиксации или консервации (как например, образец, фиксированный или консервированный в формалине, парафине или этаноле), и (2) по отдельности или в комбинации гомогенизацию одного или нескольких образцов биопсийного материала, при этом каждый из одного или более гомогенатов по существу гомогенно выражает гетерогенность соответствующего образца биопсийного материала или соответствующих образцов биопсийного материала.
Как уже упомянуто, такие репрезентативные образцы возможно могут быть подвергнуты дальнейшей диссоциации и/или обработке для извлечения или выделения молекул конкретных типов, таких как клетки конкретного типа, белки, нуклеиновые кислоты или липиды и тому подобное, с получением тем самым других репрезентативных образцов, которые могут быть использованы в диагностических и терапевтических способах.
Согласно еще одному аспекту изобретения предложен способ приготовления биологического образца, подходящего для оценки гетерогенности клеток в опухоли, или лимфатическом узле, или метастазах, или их комбинации, включающий (1) получение одного или более образцов биопсийного материала из солидной опухоли, или лимфатического узла, или метастазов, при этом предпочтительно, чтобы каждый образец биопсийного материала содержал по меньшей мере примерно 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 или большее число клеток и возможно был подвергнут фиксации или консервации (как например, образец, фиксированный или консервированный в формалине, парафине или этаноле) и (2) по отдельности или в комбинации гомогенизацию одного или нескольких образцов биопсийного материала в условиях, при которых полученный гомогенат или полученные гомогенаты по существу диссоциированы до отдельных клеток и полученный гомогенат или полученные гомогенаты являются по существу гомогенными.
И вновь, эти репрезентативные образцы возможно могут быть подвергнуты дальнейшей диссоциации и/или обработке для извлечения или выделения молекул конкретных типов, таких как клетки конкретного типа, белки, нуклеиновые кислоты или липиды и тому подобное, с получением тем самым других репрезентативных образцов, которые могут быть использованы в диагностических и терапевтических способах.
Согласно другому аспекту изобретения предложен способ приготовления биологического образца, подходящего для оценки того, характеризуется ли субъект развитием или имеет риск развития вирулентной формы конкретного рака, и/или имеет ли субъект с диагнозом рак вирулентной формы конкретного рака, включающий (1) получение одного или более интактных образцов биопсийного материала из солидной опухоли, или лимфатического узла, или метастазов, или предраковой кисты, при этом предпочтительно, чтобы каждый образец биопсийного материала содержал по меньшей мере примерно 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 или большее число клеток и возможно был подвергнут фиксации или консервации (как например, образец, фиксированный или консервированный в формалине, парафине или этаноле), и (2) по отдельности или в комбинации гомогенизацию одного или нескольких образцов биопсийного материала, при этом каждый из полученных одного или более гомогенатов по существу отражает гетерогенность соответствующего образца биопсийного материала или соответствующих образцов биопсийного материала, и возможно выделение по меньшей мере одного биомаркера или детектирование его экспрессии. Активация или отрицательная регуляция биомаркера ассоциируется с вирулентной формой конкретного рака.
Согласно еще одному аспекту изобретения предложен способ определения характерных особенностей фенотипического разнообразия в гетерогенной опухоли, лимфатических узлах или метастазах либо предраковой кисте, и/или детектирования генетически различающихся субклонов в гетерогенной опухоли, лимфатических узлах или метастазах либо предраковой кисте, и/или идентификации событий с низкой распространенностью в пределах опухоли, лимфатических узлов или метастазов либо предраковой кисты, и/или определения показателя распространенности мишеней в пределах опухоли, лимфатических узлов или метастазов либо предраковой кисты, включающий (1) получение образца или образцов опухоли, лимфатических узлов или метастазов либо предраковой кисты, который(ые) охватывает(ют) пространственно различающиеся участки опухоли, лимфатических узлов или метастазов либо предраковой кисты, который или которые до гомогенизации возможно подвергнуты фиксации или консервации, например, с использованием формалина, парафина и/или этанола, и (2) гомогенизацию образца или образцов опухоли, лимфатических узлов или метастазов либо предраковой кисты, тем самым получение гомогената, который представляет собой репрезентативный пример фенотипического разнообразия гетерогенной опухоли, лимфатических узлов, метастазов или предраковой кисты и подходит для определения характерных особенностей профиля опухоли, и/или обнаружения генетически различающихся субклонов в гетерогенной опухоли, лимфатических узлах или метастазах либо предраковой кисте, и/или для идентификации событий с низкой распространенностью в пределах опухоли, или лимфатических узлов, или метастазов, либо предраковой кисты, и/или для определения показателя распространенности мишеней в пределах опухоли, лимфатических узлов или метастазов либо предраковой кисты.
Согласно еще одному аспекту изобретения предложен способ обнаружения предраковых клеток или раковых клеток в рассматриваемых нормальных тканях или предположительно предраковых тканях у пациента, например, у пациента с риском развития рака вследствие генетической мутации или предшествующего рака либо у пациента с предраковыми кистами или полипами, включающий (1) получение образца или образцов рассматриваемых нормальных тканей или предположительно предраковых тканей, таких как предраковые кисты или полипы, которые занимают пространственно различающиеся участки рассматриваемых нормальных тканей или предположительно предраковых тканей пациента, при этом до гомогенизации возможно проводят фиксацию или консервацию образца, например, с использованием формалина, парафина и/или этанола, и (2) гомогенизацию образца или образцов с получением тем самым гомогената, который представляет собой репрезентативный пример рассматриваемых нормальных тканей или предположительно предраковых тканей и который подходит для обнаружения немногочисленных раковых клеток или раковых стволовых клеток, например, еще до манифестации какого-либо признака заболевания у пациента.
Согласно другому аспекту изобретения предложены способы применения репрезентативных образцов и их частей, которые готовят любым из указанных выше способов, в анализах с разным форматом, при этом такие анализы могут быть выполнены с высокой производительностью, проведены одновременно или в разные моменты времени либо с разной локализацией и/или с применением автоматизации (полностью автоматизированным или полуавтоматизированным образом).
Согласно другому аспекту, репрезентативные образцы по изобретению и их части, которые готовят любым из указанных выше способов, хранят для будущего использования, например, в замороженном или подвергнутом сублимационной сушке виде.
Согласно другому аспекту, репрезентативные образцы по изобретению и их части, приготовленные любым из указанных выше способов, используют для получения (и возможно очистки) антигенов или антител, специфичных к конкретному антигену из раковых клеток или клеток других типов, имеющихся в образце от пациента, при этом антитела или антигены возможно могут быть использованы в персонализированной медицине, т.е. в производстве терапевтических или профилактических вакцин против рака.
Стадия гомогенизации во всех из вышеупомянутых способов может быть проведена с использованием способа, который обеспечивает сохранение целостности клеток в образце, т.е. когда основная масса клеток в гомогенизированном(ых) образце или образцах оказывается не лизированной, и вследствие чего полученный гомогенат и его части являются "репрезентативными примерами" образца или образцов. И вновь это означает, что количества клеток в образце или его части отображают процентные содержания разных клеточных типов в полном объеме образца или образцов тканей, например, солидной опухоли или лимфатического узла. Это может быть проведено, например, путем механической диссоциации опухолевого образца или его части (такой как механическая диссоциация, проводимая с добавлением или без добавления жидкости к опухолевому образцу или его части) и/или химической или ферментативной диссоциации опухолевого образца или его части (такой как обработка ферментом, который избирательно, или предпочтительно, или главным образом действует на белки внеклеточного матрикса, а не на мембраноассоциированные белки). Альтернативно, способы гомогенизации могут приводить к диссоциации клеток, тем не менее с одновременным получением образца, который является "репрезентативным примером" данной исходной ткани, например, целой опухоли. Кроме того, гомогенизированные репрезентативные образцы возможно могут быть подвергнуты дальнейшей диссоциации и/или обработке для извлечения или выделения молекул конкретных типов, таких как клетки конкретного типа, белки, нуклеиновые кислоты или липиды и тому подобное, с получением тем самым других репрезентативных образцов, которые могут быть использованы в диагностических и терапевтических способах.
Любой из приведенных выше способов может включать детектирование экспрессии по меньшей мере одного биомаркера, например, по меньшей мере одного липидного, белкового или нуклеиновокислотного биомаркера, в гомогенате либо его части или доли. Кроме того, способы могут дополнительно включать определение процентного содержания опухолевых клеток в гомогенате либо его части или доли, которые экспрессируют конкретный биомаркер или комбинацию биомаркеров. Возможно, что осуществляют детектирование и/или выделение опухолевых стволовых клеток и/или определение относительной частоты встречаемости или процентного содержания субклонов опухолевых клеток в гомогенате либо его части или доли. Кроме того, способы также могут включать детектирование генетической мишени (такой как точечная мутация, делеция, вставка, транслокация, слияние генов или амплификация гена).
Любой из приведенных выше методов также можно использовать для обнаружения, выделения и/или измерения числа конкретных иммунных клеток (таких как В-лимфоциты, Т-лимфоциты, макрофаги, NK клетки, моноциты или их комбинация), присутствующих в гомогенате либо его части или доли, что предоставляет полезную клиническую информацию, например, иммунный статус и болезненное состояние, а также чтобы выбрать подходящие протоколы лечения, например, с использованием ингибиторов контрольных точек, цитокинов или других иммунных модуляторов.
Полученные гомогенаты или репрезентативные образцы могут содержать по меньшей мере 1000, 10000, 100000, 1000000, 5000000, 10000000, 50000000, 100000000, 500000000, 1000000000, 5000000000, 10000000000, 50000000000, 100000000000, 1000000000000 или большее число клеток.
Полученные гомогенаты либо их доля или часть возможно могут быть подвергнуты заморозке, или сублимационной сушке, или заливке воском (таким как, парафиновый) либо, альтернативно, использованы на других стадиях (некоторые из них обсуждаются ниже) без таких замораживания, или сублимационной сушки, или заливки воском. Например, репрезентативный парафиновый блок, т.е. приготовленный из гомогената либо его доли или части после заливки парафином, подходит для применения в современной патологоатономической практике, например, для приготовления срезов, приготовления микроскопических препаратов, окрашивания, микроскопии, демаскирования антигена и т.д.
Гомогенаты могут быть приготовлены из двух или более опухолей, взятых от одного или нескольких субъектов, и полученные из каждой опухоли гомогенаты или их доли используют для оценки сходства и/или различия двух или более опухолей или болезненного состояния у разных пациентов.
Помимо этого гомогенаты могут быть приготовлены из двух или более предположительно нормальных или предраковых тканей, например, молочной железы, шейки матки, толстой и прямой кишки, либо предраковых кист или полипов, полученных от субъекта, например, субъекта с мутацией в BRCA, и полученные гомогенаты или их доли использовали для оценки того, присутствуют ли какие-либо аномальные клетки или биомаркеры заболевания.
Помимо этого, в гомогенат могут быть добавлены не являющиеся человеческими клетки (такие как клетки насекомых и/или клетки мышей) или другие чужеродные белки, нуклеиновые кислоты или малые молекулы для создания внутреннего контроля с целью положительного детектирования белков или нуклеиновых кислот.
Кроме того, к такому образцу можно добавить малые молекулы (такие как гаптены, пептидные метки, белковые метки, флуоресцентные метки и/или нуклеиновокислотные метки) и использовать для получения пространственной информации, касающейся репрезентативного образца. Например, для создания репрезентативного образца можно приготовить срезы образца (такого как опухоль или лимфатический узел), например, разрезать с получением четырех срезов, и в каждый срез до гомогенизации срезов можно "ввести другой гаптен (или другую подходящую малую молекулу). Следует понимать, что количество срезов, которые могут быть получены на основе каждого образца, для "введения добавки" до гомогенизации, не ограничивается, а скорее всего, с большой долей вероятности будет выбрано в зависимости от размера образца, т.е. чем больше образец, тем будет получено большее количество срезов, которые могут быть "помечены малой молекулой до гомогенизации. Таким образом, в полученных гомогенатах или их фракциях можно сохранять пространственную информацию.
Малые молекулы также можно добавлять к образцу до объединения данного образца с другим образцом от другого пациента или одного и того же пациента и это, таким образом, обеспечивает средство для различения образцов при работе в формате мультиплексного анализа.
Гомогенизированные образцы могут быть подвергнуты фиксации в формалине или могут быть подвергнуты консервации в этаноле до или после гомогенизации. Перед применением в патологоанатомических или диагностических методах, из-за проблем безопасности образцы ткани обычно фиксируют в формалине или каким-либо иным образом. Фиксация в формалине или другие методы фиксации являются общеизвестными в данной области техники. Типичные методы описаны ниже. В таком случае, фиксированный в формалине опухолевый образец можно выдержать в воде или забуференном физиологическом растворе (таком как PBS) перед гомогенизацией на стадии (2).
Альтернативно или помимо этого, опухолевый образец, используемый в описанных способах, может быть подвергнут консервации в этаноле до гомогенизации. Однако, фиксация в формалине или этаноле либо другие методики консервации не являются существенными для способов по изобретению и могут быть исключены без ущерба для пригодности полученного гомогенизированного репрезентативного образца.
Для получения репрезентативного образца живой ткани можно провести гомогенизацию ткани, не подвергнутой фиксации. Чтобы получить репрезентативный образец культивируемой ткани от индивидуальных пациентов, можно провести культивирование репрезентативного образца живой ткани. Такой репрезентативный образец может быть неоднократно разделен на части с получением любого количества репрезентативных культивируемых образцов, которые можно использовать для определения эффективности химиотерапии (как например, определения антитела, нуклеиновой кислоты, малой молекулы или полипептида, который(ая) антагонизирует, ингибирует или блокирует экспрессию или функциональную активность по меньшей мере одного известного или неизвестного биомаркера). Кроме того, с использование анализа FACS можно отобрать клетки конкретного типа (такие как иммунные клетки или опухолевые клетки). Например, для определения опухолеспецифичных антител, секретируемых иммунной системой, можно провести отбор и культивирование инфильтрующих опухоль иммунных клеток.
Кроме того, как показано в данном описании, описанные способы приготовления репрезентативных образцов и их применения в диагностических и терапевтических способах подходят как для фиксированных, так и для нефиксированных образцов ткани.
Любой из описанных способов приготовления репрезентативного образца (такого как гомогенат, полученный из образца опухолевого биопсийного материала) может включать добавление по меньшей мере одной коллагеназы, или другого подходящего фермента, или комбинации ферментов, или другого химического вещества, такого как соль, под действием которого происходит разрушение или который способствует расщеплению внеклеточного матрикса до, в ходе и после гомогенизации; использование условий повышенной температуры и/или буфера, такого как буфер для выдерживания клеток, например, СС1 или СС2, в котором разрушаются межклеточные сшивки); и/или применение устройства для механического фрагментирования (такого как блендер от IKA, диассоциатор gentleMACS или функциональный эквивалент). Эти способы могут быть выполнены или могут быть не выполнены в условиях, которые поддерживают жизнеспособность и целостность клеток в образце, например, в некоторых условиях гомогенизации клетки по существу не подвергаются лизису.
Согласно одному из аспектов гомогенизация включает применение ступки и пестика, гомогенизатора Даунса или измельчителя тканей, ручного электронного гомогенизатора тканей с вращающимися ножами (такого как Omni-TH, поставляемый Thomas Scientific), гомогенизатора по типу шаровой мельницы (такого как блендер серии Bullet, или гомогенизатор тканей Burton Precellys 24, или Bead Ruptor, поставляемый OMNI), возможно со скоростью от примерно 100 до примерно 75000 об./мин для ротационных гомогенизаторов или со скоростью от примерно 0,5 м/с до примерно 2,5 м/с для шаровых мельниц и в течение промежутка времени от примерно 30 секунд до примерно 5 минут, от примерно 5 инут до примерно 10 минут, от примерно 10 минут до примерно 30 минут или от примерно 30 минут до примерно 60 минут.
В другом воплощении гомогенизация включает применение интерстициальной коллагеназы, желатиназы-а, стромелизина 1, матрилизина, коллагеназы нейтрофилов, желатиназы-b, стромелизина 2, стромелизина 3, металлоэластазы макрофагов, коллагеназы 3, МТ1-ММР, МТ2-ММР, МТ3-ММР, МТ4-ММР, коллагеназы 4, энамелизина, Х-ММР, СА-ММР, МТ5-ММР, МТ6-ММР, матрилизина-2, ММР-22, эндопротеиназы, трипсина, химотрипсина, эндопротеиназы Asp-N, эндопротеиназы Arg-C, эндопротеиназы Glu-C (протеазы V8), эндопротеиназы Lys-C, пепсина, термолизина, эластазы, папаина, протеиназы K, субтилизина, клострипаина, экзопептидазы, карбоксипептидазы А, карбоксипептидазы В, карбоксипептидазы Р, карбоксипептидазы Y, катепсина С, высвобождающего ациламинокислоту фермента, пироглутаматаминопептидазы или любой их комбинации, возможно в концентрации от примерно 0,001 мкг/мл до примерно 1000 мг/мл и в течение промежутка времени от примерно 1 минуты до примерно 120 минут.
Опухолевый образец, использованный в описанных способах, который охватывает пространственно различающиеся участки опухолевой или другой ткани, может содержать по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, по меньшей мере 85%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или, предпочтительно, полный объем опухоли, изъятой хирургическим путем из пациента. Опухолевый образец может составлять по меньшей мере 1, 5, 10, 20, 50, 100 или более миллиметров (мм) или сантиметров (см) в диаметре.
Образцы, используемые в способах по изобретению, обычно будут приготовлены из солидной опухоли или солидных опухолей (включая первичные опухоли и метастазирующие опухоли), лимфатических узлов, метастазов или предраковых тканей, таких как кисты или полипы. Альтернативно или помимо этого, данные способы также возможно могут быть эффективны в случае несолидных опухолей, например, раковых заболеваний крови. Например, образцы солидных опухолей, которые являются гомогенизированными, возможно могут быть объединены с образцами жидкостей пациента, например, образцами крови, лимфатической жидкости, проб экссудата, образцами цереброспинальной жидкости, желчи, слизи и/или мочи пациента. Образцы, которые являются гомогенизированными, помимо этого или альтернативно могут представлять собой отобранную посредством биопсии "нормальную" или предраковую ткань, например, чтобы обнаружить пораженные клетки до проявления заболевания.
Такой образец или такие образцы опухолевых либо других тканей, использованный(ые) в описанных способах, может(могут) происходить из любого источника, например, из молочной железы, толстой кишки, легкого, поджелудочной железы, желчного пузыря, кожи, кости, мышцы, печени, почки, шейки матки, яичников, предстательной железы, пищевода, желудка или других органов, например, из раковой опухоли молочной железы, раковой опухоли легкого, опухоли печени, раковой опухоли предстательной железы, раковой опухоли толстой кишки, раковой опухоли мочевого пузыря или раковой опухоли почки. Как правило, опухолевый образец или образец другой ткани, использованный в описанных способах, имеет человеческое происхождение.
Образец опухолевой или другой ткани, использованный в описанных способах, может иметь объем, составляющий по меньшей мере 1 см3, по меньшей мере 2 см3, по меньшей мере 3 см3, по меньшей мере 4 см3, по меньшей мере 5 см3, по меньшей мере 6 см3, по меньшей мере 7 см3, по меньшей мере 8 см3, по меньшей мере 9 см3, по меньшей мере 10 см3, по меньшей мере 15 см3, по меньшей мере 20 см3, по меньшей мере 25 см3, по меньшей мере 50 см3, по меньшей мере 100 см3, по меньшей мере 250 см3, по меньшей мере 500 см3, по меньшей мере 1000 см3, по меньшей мере 2500 см3, по меньшей мере 5000 см3, по меньшей мере 7500 см3, по меньшей мере 10000 см3 или больше.
Образец опухолевой или другой ткани, использованный в описанном способе, может иметь ширину в самом широком месте, составляющую по меньшей мере 0,5 см, по меньшей мере 1 см, по меньшей мере 1,5 см, по меньшей мере 2 см, по меньшей мере 2,5 см, по меньшей мере 3 см, по меньшей мере 3,5 см, по меньшей мере 4 см, по меньшей мере 4,5 см, по меньшей мере 5 см, по меньшей мере 6 см, по меньшей мере 7 см, по меньшей мере 10 см, по меньшей мере 25 см, по меньшей мере 50 см или больше.
Кроме того, в некоторых воплощениях можно приготовить репрезентативные образцы ткани, которая предварительно была подвергнута фиксации в формалине и заливке парафиновым воском. В частности, воск можно растопить, ткань извлечь и подвергнуть гидратации и затем применить способы, описанные в данной заявке, т.е. гомогенизацию, к образцу, который подходит для применения в любом количестве анализов (см., например, ФИГ. 24). На ФИГ. 24 показан результат окрашивания HPV16 ISH на клетках Caski в репрезентативном образце, приготовленном из ткани, извлеченной из парафинового блока. Ткань, которая предварительно была залита парафиновым воском, извлекали и гомогенизировали в блендере от IKA с получением репрезентативного образца.
Таким образом, описанные способы можно применять для приготовления репрезентативного образца с использованием образца или образцов, уже полученных для определения стадии по системе TNM, посредством расплавления воска, извлечения образца, регидратации и гомогенизации ткани, соответственно.
Любой из приведенных выше способов может дополнительно включать (3) нанесение гомогената либо его части или доли на одно или несколько предметных стекол или одну или несколько других твердых подложек и, возможно, окрашивание одного или нескольких предметных стекол или одной или нескольких других твердых подложек, содержащих гомогенат либо его часть или долю, красящим веществом на основе гематоксилина и эозина; осуществление иммуногистохимического окрашивания на предметном стекле или другой твердой подложке, содержащей гомогенат либо его часть или долю; или осуществление гибридизации in situ на предметном стекле или другой твердой подложке, содержащей гомогенат либо его часть или долю, т.е. любое из перечисленного будет считаться стадией (4) в данных способах.
Кроме того, любой из приведенных выше способов может дополнительно включать (3) очистку нуклеиновых кислот (таких как ДНК или мРНК) из гомогената либо его части или доли. Очищенные нуклеиновые кислоты могут быть исследованы с использованием нозерн-блоттинга, секвенирования ДНК, ПЦР, RT-ПЦР, профилирования с применением микрочипов, дифференциального дисплея или гибридизации in situ. Альтернативно, очищенная нуклеиновая кислота может быть конъюгирована с наночастицей (такой как квантовые точки, парамагнитные наночастицы, суперпарамагнитные наночастицы и металлические наночастицы, предпочтительно легированные квантовые точки, включая, в качестве примера и без ограничения, CdSe, ZnSSe, ZnSeTe, ZnSTe, CdSSe, CdSeTe, ScSTe, HgSSe, HgSeTe, HgSTe, ZnCdS, ZnCdSe, ZnCdTe, ZnHgS, ZnHgSe, ZnHgTe, CdHgS, CdHgSe, CdHgTe, ZnCdSSe, ZnHgSSe, ZnCdSeTe, ZnHgSeTe, CdHgSSe, CdHgSeTe, InGaAs, GaAlAs и InGaN, в качестве примера).
Также подразумевается, что любой из приведенных выше способов может дополнительно включать очистку липидов или экзосом либо других органелл из гомогената либо его части или доли. Очищенные липиды могут быть исследованы методами масс-спектрометрии или гистохимии.
Кроме того, также подразумевается, что любой из приведенных выше способов может дополнительно включать очистку белков из гомогената либо его части или доли. Очищенные белки могут быть исследованы с использованием вестерн-блоттинга, ELISA, иммунопреципитации, хроматографии, масс спектрометрии, профилирования с применением микрочипов, интерферометрии, электрофоретического окрашивания или иммуногистохимического окрашивания. Альтернативно или в дополнение к вышеупомянутому, очищенные белки можно использовать для приготовления образцов антисыворотки, специфичной для данной опухоли.
Кроме того, подразумевается, что любой из приведенных выше способов дополнительно включает (3) проведение геномного, транскриптомного, протеомного и/или метаболомного анализа в отношении гомогената либо его части или доли.
Кроме того, подразумевается, что любой из приведенных выше способов дополнительно включает (3) аффинную очистку клеток конкретного типа из гомогената либо его части или доли. Клетки конкретного типа могут содержать представляющий интерес биомаркер. Типичные представляющие интерес биомаркеры могут включать Her2, bRaf, амплификацию ERBB2, мутацию в PI3KCA, амплификацию FGFR2, мутацию в р53, мутацию в BRCA, амплификацию CCND1, мутацию в MAP2K4, мутацию в ATR или любой другой биомаркер, экспрессия которого коррелирует с конкретным видом рака; по меньшей мере один из AFP, ALK, BCR-ABL, BRCA1/BRCA2, BRAF, V600E, СА-125, СА19.9, EGFR, Her-2, KIT, PSA, S100, KRAS, ER/Pr, UGT1A1, CD30, CD20, F1P1L1-PDGRFa, PDGFR, TMPT и TMPRSS2; или по меньшей мере один биомаркер, выбранный из АВСВ5, AFP-L3, альфа-фетопротеина, альфа-метил-ацил-КоА-рацемазы, BRCA1, BRCA2, СА 15-3, СА 242, СА 27-29, СА-125, СА15-3, СА19-9, кальцитонина, канцероэмбрионального антигена, пептида-1 канцероэмбрионального антигена, дез-гамма-карбоксипротромбина, десмина, раннего антигена-2 рака предстательной железы, рецептора эстрогенов, продукта деградации фибрина, глюкозо-6-фосфат-изомеразы, антигена HPV, такого как vE6, Е7, L1, L2 или p16INK4a, хорионического гонадотропина человека, IL-6, кератина 19, лактатдегидрогеназы, лейциламинопептидазы, липотропина, метанефринов, неприлизина, nmp22, норметанефрина, РСА3, простатоспецифического антигена, кислой фосфатазы предстательной железы, синаптофизина, тиреоглобулина, TNF, транскрипционного фактора, выбранного из ERG, ETV1 (ER81), FLI1, ETS1, ETS2, ELK1, ETV6 (TEL1), ETV7 (TEL2), GABPa, ELF1, ETV4 (E1AF; РЕА3), ETV5 (ERM), ERF, PEA3/E1AF, PU.1, ESE1/ESX, SAP1 (ELK4), ETV3 (METS), EWS/FLI1, ESE1, ESE2 (ELF5), ESE3, PDEF, NET (ELK3; SAP2), NERF (ELF2) или опухолеассоциированного гликопротеина 72, c-kit, SCF, pAKT, pc-kit и виментина.
Альтернативно или в дополнение к этому представляющим интерес биомаркером может быть ингибитор контрольных точек иммунного ответа, таких как, но не ограничиваясь этим, CTLA-4, PDL1, PDL2, PD1, В7-Н3, В7-Н4, BTLA, HVEM, KIR, TIM3, GAL9, GITR, LAG3, VISTA, KIR, 2В4, TRPO2, CD160, CGEN-15049, CHK 1, CHK2, A2aR, TL1A и лиганды В-7 семейства или их комбинация, либо такой биомаркер представляет собой лиганд белка-контрольной точки, выбранного из группы, состоящей из CTLA-4, PDL1, PDL2, PD1, В7-Н3, В7-Н4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2В4, CD160, CGEN-15049, CHK1, CHK2, A2aR, лигандов В-7 семейства или их комбинации.
Способ по любому из упомянутых выше пунктов формулы изобретения, который включает детектирование по меньшей мере одного биомаркера, ассоциированного с острым лимфобластным лейкозом (etv6, am11, циклофилина b), В-клеточной лимфомой (Ig-идиотипа), глиомой (Е-кадгерина, альфа-катенина, бета-катенина, гамма-катенина, р120 ctn), раком мочевого пузыря (p21ras), раком желчных протоков (p21ras), раком молочной железы (представителя MUC семейства, HER2/neu, c-erbB-2), карциномой шейки матки (р53, p21ras), раком толстой кишки (p21ras, HER2/neu, с-erbB-2, представителя MUC семейства), колоректальным раком (антигена, ассоциированного с толстой и прямой кишкой (CRC)-C017-1A/GA733, АРС), хориокарциномой (СЕА), плоскоклеточным раком (циклофилина b), раком желудка (HER2/neu, c-erbB-2, гликопротеина ga733), гепатоклеточным раком (альфа-фетопротеина), лимфомой Ходжкина (Imp-1, EBNA-1), раком легкого (СЕА, MAGE-3, NY-ESO-1), лейкозом, начинающимся в лимфоидных клетках (циклофилина b), меланомой (белка р5, gp75, онкофетального антигена ганглиозидов GM2 и GD2, мелан-A/MART-1, cdc27, MAGE-3, p21ras, gp100.sup.Pmel117), миеломой (представителя MUC семейства, p21ras), немелкоклеточным раком легкого (HER2/neu, c-erbB-2), раком носоглотки (Imp-1, EBNA-1), раком яичников (представителя MUC семейства, HER2/neu, с-erbB-2), раком предстательной железы (простатоспецифического антигена (PSA) и его антигенных эпитопов PSA-1, PSA-2 и PSA-3, PSMA, HER2/neu, c-erbB-2, гликопротеина ga733), почечным раком (HER2/neu, c-erbB-2), случаями плоскоклеточного рака шейки матки и пищевода (продуктов вирусного происхождения, таких как белки папилломавируса человека), раком яичка (NY-ESO-1) и/или Т-клеточным лейкозом (эпитопов HTLV-1).
Также подразумевается, что любой из вышеупомянутых способов дополнительно включает (3) обработку гомогената либо его части или доли коллагеназой или другим ферментом либо химическим путем или их комбинацией, в результате чего внеклеточные матриксы разрушаются, инкубацию гомогената либо его части или доли в условиях высоких температур и/или механическое встряхивание гомогената либо его части или доли с целью осуществления диссоциации клеток в гомогенате либо его части или доли. В общем случае, в результате применения этих способов будет получен другой репрезентативный образец, который может быть использован в описанных аналитических или терапевтических способах либо в случае их сочетания.
Кроме того, подразумевается, что любой из описанных выше способов дополнительно включает (3) фильтрование или разделение на основании размера для либо его части или доли, в результате чего могут быть получены одиночные клетки или небольшие кластеры клеток, такие как дублеты или триплеты.
Разделение клеточных компонентов репрезентативного образца может быть выполнено с использованием одной или нескольких стадий фильтрования. Например, после проведения гомогенизации и диссоциации гомогената с использованием физических и/или биохимических методов подвергнутый диссоциации образец можно пропустить через фильтр с размером пор 1 микрон для удаления всего интактного клеточного материала. Ожидается, что неклеточный репрезентативный образец будет содержать факторы, секретируемые из опухоли и нормальной стромы в пределах опухоли, которые найдут клиническое применение, т.е. антитела, факторы роста, иммуномодуляторы и другие неизвестные факторы. Анализ неклеточного репрезентативного образца может быть выполнен посредством ELISA, масс-спектрометрии, методов секвенирования следующего поколения и других диагностических методов. В тех случаях, когда одиночные клетки, происходящие из репрезентативного образца, получают после фильтрации, анализ таких клеток может быть проведен с использованием (метода) сортировки флуоресцентно-активированных клеток (FACS) и анализа посредством проточной цитометрии.
С учетом репрезентативной природы гомогената, полученного описанными способами, гомогенат либо его часть или долю можно использовать для детектирования генетического события с низкой распространенностью (такого как генетическое событие, которое происходит с показателем распространенности 20%, показателем распространенности 15%, показателем распространенности 10%, показателем распространенности 5%, показателем распространенности 2%, показателем распространенности 1%, показателем распространенности 0,5%, показателем распространенности 0,1%, показателем распространенности 0,001%, показателем распространенности 0,0001%, показателем распространенности 0,00001%, показателем распространенности 0,000001% или меньше). Типичные генетические события включают точечную мутацию, делецию, вставку, транслокацию, слияние генов или амплификацию гена. Аналогичным образом, способы также могут включать детектирование генетической или эпигенетической гетерогенности в опухолевом образце или его части и/или детектирование клеток, содержащих редко встречающиеся генетические или эпигенетические вариации. Такие клетки могут быть представлены в опухолевом образце с частотой встречаемости менее 5%, менее 1%, менее 0,5%, менее 0,1%, менее 0,05% или менее 0,01%.
Детектируемые немногочисленные клетки могут содержать одно или несколько генетических или эпигенетических различий, которые придают устойчивость к противораковой терапии и/или стимулируют метастазирование. Таким образом, обнаружение таких клеток будет способствовать прогнозу развития рака, а также выбору соответствующего режима терапии, такого как хирургическое вмешательство, химиотерапия и/или применение биологических средств.
Указанные выше способы также могут включать применение по меньшей мере одной детектируемой метки, выбранной из флуоресцентных молекул или флуорохромов (как например, поставляемые Invitrogen, например, см. The Handbook: A Guide to Fluorescent Probes and Labeling Technologies, Invitrogen Detection Technologies, Molecular Probes, Eugene, Oreg., или описанные в патенте США №5866366 авторами Nazarenko и др.), таких как 4-ацетамидо-4'-изотиоцианатостильбен-2,2'-дисульфоновая кислота, акридин и такие производные, как акридин и акридина изотиоцианат, 5-(2'-аминоэтил)аминонафталин-1-сульфоновая кислота (EDANS), 4-амино-N-[3-винилсульфонил)фенил]нафталимид-3,5-дисульфонат (люцифер желтый VS), N-(4-анилино-1-нафтил)малеимид, антраниламид, бриллиантовый желтый, кумарин и такие производные, как кумарин, 7-амино-4-метилкумарин (АМС, кумарин 120), 7-амино-4-трифторметилкумарин (кумаран 151); цианозин; 4',6-диаминидино-2-фенилиндол (DAPI); 5',5''-дибромпирогаллол-сульфонфталеин (бромпирогаллол красный); 7-диэтиламино-3-(4'-изотиоцианатофенил)-4-метилкумарин; диэтилентриамина пентаацетат; 4,4'-диизотиоцианатодигидро-стильбен-2,2'-дисульфоновая кислота; 4,4'-диизотиоцианатостильбен-2,2'-дисульфоновая кислота; 5-[диметиламино]нафталин-1-сульфонилхлорид (DNS, данзилхлорид); 4-(4'-диметиламинофенилазо)бензойная кислота (DABCYL); 4-диметиламинофенилазофенил-4'-изотиоцианат (DABITC); эозин и такие производные, как эозин и эозина изотиоцианат; эритрозин и такие производные, как эритрозин В и эритрозина изотиоцианат; этидий; флуоресцеин и такие производные, как 5-карбоксифлуоресцеин (FAM), 5-(4,6-дихлортриазин-2-ил)аминофлуоресцеин (DTAF), 2',7'-диметокси-4',5'-дихлор-6-карбоксифлуоресцеин (JOE), флуоресцеин, флуоресцеина изотиоцианат (FITC) и QFITC (XRITC); 2',7'-дифторфлуоресцеин (OREGON GREEN®); флуорескамин; IR144; IR1446; малахитовый зеленый изотиоцианат; 4-метилумбеллиферон; орто-крезолфталеин; нитротирозин; парарозанилин; феноловый красный; В-фикоэритрин; о-фталевый диальдегид; пирен и такие производные, как пирен, пирена бутират и сукцинимидил-1-пирена бутират; реактивный красный 4 (Cibacron®™, бриллиантовый красный 3В-А); родамин и такие производные, как 6-карбокси-Х-родамин (ROX), 6-карбоксиродамин (R6G), лиссамин, родамина В сульфонилхлорид, родамин (Rhod), родамин В, родамин 123, родамина X изотиоцианат, родамин зеленый, сульфородамин В, сульфородамин 101 и сульфонилхлоридное производное сульфородамина 101 (техасский красный); N,N,N',N'-тетраметил-6-карбоксиродамин (TAMRA); тетраметилродамин; тетраметилродамина изотиоцианат (TRITC); рибофлавин; розоловая кислота и хелатный комплекс производных тербия, тиол-реактивные хелатные комплексы европия, которые излучают на длине волны приблизительно 617 нм (Heyduk and Heyduk, Analyt. Biochem., 248: 216-27, 1997; J. Biol. Chem., 274: 3315-22, 1999), a также GFP, Lissamine™, диэтиламинокумарин, флуоресцеина хлортриазинил, нафтофлуоресцеин, 4,7-дихлорродамин и ксантен (как описано в патенте США №5800996 авторами Lee и др.) и их производные. Также могут быть использованы другие флуорофоры, известные специалистам в данной области техники, например, флуорофоры, поставляемые Invitrogen, Detection Technologies, Molecular Probes (Eugene, Oreg) и включающие серию красителей ALEXA FLUOR™ (например, которые описаны в патентах США №№5696157, 6130101 и 6716979), серию красителей BODIPY (дипиррометенбордифторидные красители, например, которые описаны в патентах США №№4774339, 5187288, 5248782, 5274113, 5338854, 5451663 и 5433896), Cascade Blue® (реакционноспособное в отношении аминов производное сульфонированного пирена, описанное в патенте США №5132432) и Marina Blue® (патент США №5830912), флуоресцентная наночастица, такая как полупроводниковый нанокристалл, например, QUANTUM DOT™ (полученный, например, от QuantumDot Corp., Invitrogen Nanocrystal Technologies, Eugene, Oreg.; также см. патенты США №№6815064, 6682596 и 6649138), полупроводниковые нанокристаллы, описанные, например, в патенте США №6602671, Bruchez et. al. (1998) Science, 281: 2013-6, Chan et al. (1998) Science, 281: 2016-8 и в патенте США №6274323, патентах США №№6927069, 6914256, 6855202, 6709929, 6689338, 6500622, 6306736, 6225198, 6207392, 6114038, 6048616, 5990479, 5690807, 5571018, 5505928, 5262357 и в публикации на патент США №2003/0165951, а также в публикации РСТ №99/26299 (опубликованной 27 мая 1999 г.), радиоактивные изотопы (такие как3Н), хелаты металлов, такие как хелаты ионов радиоактивных или парамагнитных металлов, подобных Gd3+, DOTA и DPTA, и липосомы, ферменты, например, пероксидаза хрена, щелочная фосфатаза, кислая фосфатаза, глюкозооксидаза, β-галактозидаза, β-глюкуронидаза или β-лактамаза, фермент в комбинации с хромогенным, флуорогенным или люминогенным соединением, которое генерирует детектируемый сигнал, например, поставляемым фирмой Invitrogen Corporation, Eugene Oreg.). Конкретные примеры хромогенных соединений включают диаминобензидин (DAB), 4-нитрофенилфосфат (pNPP), прочный красный, бромхлориндолилфосфат (BCIP), нитросиний тетразолий (NBT), BCIP/NBT, прочный красный, АР оранжевый, АР голубой, тетраметилбензидин (ТМВ), 2,2'-азино-ди-[3-этилбензотиазолинсульфонат] (ABTS), о-дианизидин, 4-хлорнафтол (4-CN), нитрофенил-бета-D-галактопиранозид (ONPG), о-фенилендиамин (OPD), 5-бром-4-хлор-3-индолил-бета-галактопиранозид (X-Gal), метилумбеллиферил-бета-D-галактопиранозид (MU-Gal), пара-нитрофенил-альфа-D-галактопиранозид (PNP), 5-бром-4-хлор-3-индолил-бета-D-глюкуронид (X-Gluc), 3-амино-9-этилкарбазол (АЕС), фуксин, иоднитротетразолий (INT), тетразолий голубой и тетразолий фиолетовый, среди прочих.
Описанные способы могут быть автоматизированы, целиком или частично. Например, стадии (1) и (2) могут быть автоматизированы, но любые последующие стадии, например, стадии (3) и (4), выполняются вручную. Альтернативно, в качестве примера, стадии (1) и (2) могут быть выполнены вручную, в то время как последующие стадии, например, стадии (3) и (4), являются автоматизированными. Кроме того, автоматизированными могут быть все стадии, охватываемые данными способами.
Описанные способы можно применять, по отдельности или в сочетании с другими известными способами (такими как TNM), для определения стадии развития опухоли. Согласно одному из аспектов способы дополнительно включают оценку одного или более морфологических аспектов опухоли, степени, до которой опухолевые клетки распространяются в регионарные лимфатические узлы и/или лимфатическую систему, и того, метастазировала ли или не метастазировала опухоль в отдаленные органы, на основании геномной, протеомной и/или липидомной информации, содержащейся в репрезентативном образце.
Описанные способы могут дополнительно включать применение алгоритма для расчета процентного содержания опухолевых клеток со специфическим биомаркером или без него. Относительный риск распространения метастазов (или вирулентного субклона) может быть определен на основании процентного содержания клеток в репрезентативном образце из опухоли и/или репрезентативном образце из лимфатического узла, имеющих конкретные детектируемые биомаркеры или комбинацию этих биомаркеров.
Описанные способы могут дополнительно включать разработку персонального режима введения на основании биомаркерного профиля, антигенного профиля, мутационного профиля, липидного профиля, белкового профиля и/или экзосомного профиля, характеризующих репрезентативный образец. Например, на основании информации, характеризующей репрезентативный образец (или подобной информации в сравнении с репрезентативным образцом из лимфатического узла и/или профилем циркулирующей ДНК), может быть изменен выбор лекарственных средств и/или дозировки (количества, продолжительности введения и т.д.) таких лекарственных средств, вводимых пациенту, с целью разработки персонализированного лечения с учетом индивидуального ракового профиля пациента.
Описанные способы могут дополнительно включать сравнение геномного профиля репрезентативного образца с геномным профилем репрезентативного образца из лимфатического узла, и возможно дальнейшее сравнение этих профилей с циркулирующей опухолевой ДНК из любых отдаленных метастазов или репрезентативного образца метастазирующей опухоли.
Настоящее изобретение также охватывает композиции, приготовленные любым из способов по данному изобретению.
Анализ репрезентативного образца
Кроме того, в данном изобретении предлагается использование результатов указанных выше способов (таких как детектирование редко встречающихся генетических и/или эпигенетических событий, немногочисленных клеток и т.д.) или композиций, приготовленных любым из указанных выше способов, которые включают гомогенизацию опухолевого образца для получения репрезентативного образца, подходящего для дальнейшего анализа с использованием любого числа стандартных диагностических анализов при выборе соответствующего режима терапии для лечения субъекта. Такой режим терапии может включать любое, выбранное из химиотерапии, введения иммуномодуляторов, облучения, введения цитокинов, хирургического вмешательства или их сочетания.
Кроме того, описанный способ можно использовать для выбора по меньшей мере одного терапевтического агента (такого как антитело, нуклеиновая кислота, малая молекула или полипептид, которые антагонизируют, ингибируют или блокируют экспрессию или функциональную активность по меньшей мере одного детектируемого биомаркера), подходящего для применения субъектом, опухоль от которого являлась источником для репрезентативного образца, получаемого предложенными способами.
Недавние достижения в области биологии рака подорвали устоявшиеся представления в отношении физиологии опухолей. Ранее преобладающая мысль заключалась в том, что все клетки в опухоли походили друг на друга, независимо от стадии рака. Однако с внедрением новых технологий, таких как секвенирование из одной клетки, теперь понятно, что клетки в опухоли могут быть очень разнообразными. См. Campbell et al. Subclonal phylogenetic structures in cancer revealed by ultra-deep sequencing. PNAS, 2008, 105: 13081-13086; и Navin et al. Tumor evolution inferred by single-cell sequencing. Nature, 2011, 472: 90-94. Открытие внутриопухолевой гетерогенности выявляет новые сложности, которые необходимо будет решать в клинической онкологии, в том числе в диагностике рака.
Существующие в настоящее время методы патологии основаны на вырезании только незначительно малых участков из опухоли, помещения их в парафиновые блоки и нарезании небольших срезов из этих блоков, подлежащих тестированию на биомаркеры рака. См. Westra et al. Surgical Pathology Dissection: An Illustrated Guide. New York: Springer. 2003. Этот метод может быть полезен при определении стадии развития рака, однако расчет на отбор образцов лишь из небольшой доли всей опухоли делает маловероятным, чтобы результаты диагностики были репрезентативными для всей опухоли. В итоге, с использованием существующих в настоящее время методов: 1) не удается идентифицировать важные характеристики заболевания и 2) делается избыточный отбор, связанный с минорым признаком заболевания, что зачастую не определяет или не влияет на прогрессирование и/или результат заболевания.
Эти проблемы усиливаются по мере увеличения размера опухоли, и в результате, зачастую негативно влияют на показатели долгосрочной выживаемости раковых пациентов. Например, независимо от стадии рака, по мере увеличения размера опухоли, средние показатели выживаемости снижаются до 5 лет. См. Lopez-Encuentra et al. Staging in lung cancer: is 3 cm a prognostic threshold in pathological stage 1 non-small cell lung cancer? A multicenter study of 1,020 patients. Chest., 2002, 121(5): 1515-1520; Miller and Grigsby. Measurement of tumor volume by PET to evaluate prognosis in patients with advanced cervical cancer treated by radiation therapy. Int. J. Radiat. Oncol. Biol. Phys., 2002, 53(2): 353-359; Elkin et al. The effect of changes in tumor size on breast carcinoma survival in the U.S.: 1975-1999. Cancer, 2005, 104(6): 1149-1157; Brookman-May et al. Difference between clinical and pathological renal tumor size, correlation with survival, and implications for patient counseling regarding nephron-sparing хирургическое вмешательство. AJR, 2011, 197(5): 1137-1145; и Kornprat et al. Value of tumor size as a prognostic variable in colorectal cancer: a critical reappraisal. Am. J. Clin. Oncol., 2011, 34(1): 43-49.
Соответственно, чтобы решить проблему гетерогенности опухолей в клинической онкологии, особенно в случае таких пациентов с большими солидными опухолями, необходимы новые технологии. Кроме того, улучшенные способы необходимы для идентификации образцов пациента, содержащих аномальные клетки, до проявления заболевания с целью повышения вероятности хорошего терапевтического эффекта.
Чтобы решить проблему гетерогенности опухолей некоторые эксперты в области онкологии предложили протестировать несколько регионов, тем самым увеличив количество опухолевых образцов, отобранных за один раз. См., например, Alizadeh et al. Toward understanding and exploiting tumor heterogeneity. Nature Medicine. 2015; 21: 846-853. Как продемонстрировано с использованием вышеупомянутой вероятностной модели, этот метод не может полностью решить проблемы гетерогенности опухолей. Увеличение рабочей нагрузки для лаборатории патологической анатомии, которой поручено обрабатывать такое количество образцов в расчете на одного пациента, делает этот предложенный способ невозможным в исполнении.
Чтобы образец был репрезентативным, все разнообразные фрагменты исходного материала должны иметь равный шанс попасть в образец, и это условие должно быть четко выдержано во всех образцах. См. Petersen и др., 2005. Однако, при выполнении существующих методик приготовления срезов большая часть опухоли сжигается после получения парафиновых блоков. См. Westra и др., 2003. Таким образом, на сегодняшний день не только не налажено приготовление репрезентативных образцов опухолей, но и существующие патологоанатомические практики не поощряют и даже запрещают их приготовление.
Согласно дополнительному аспекту, для приготовления репрезентативного образца из опухоли можно применять механические методы, например, фрагментирование, и/или биохимические методы, например, выдерживание при определенных температуре и рН и ферментативное расщепление внеклеточного матрикса. Сочетание этих подходов приводит к получению репрезентативного образца на основе образца или образцов тканей, например, целой опухоли или значительной ее части, без ущерба в отношении возможности использования этой пробы в традиционных основанных на использовании тканей анализах, например, при окрашивании гематоксилином и эозином, иммуногистохимическом анализе и выделении нуклеиновых кислот. Действительно, каждый репрезентативный образец можно одновременно использовать в нескольких разных анализах. Помимо этого, гомогенизация органа, ткани или опухоли делает их пригодными для применения в дополнительных диагностических тестах, таких как секвенирование полного генома, что может иметь важное значение для будущих фармакологических и диагностических открытий и для персонализированной медицины. Кроме того, гомогенат пригоден для применения в автоматизированных методах, аналогичных тем, которые используются для диагностических тестирований крови. Таким образом, репрезентативный образец можно использовать для ряда диагностических протоколов, применяемых для идентификации субклонов немногочисленных опухолевых клеток, и, если брать более широко, для усовершенствования клинической диагностики и персонализированного лечения рака. Кроме того, приготовленные репрезентативные образцы можно использовать для получения антител или антигенов, полезных при разработке терапевтических или профилактических противоопухолевых вакцин.
Как проиллюстрировано в данном описании, авторы изобретения продемонстрировали способность приготовления репрезентативного образца из клинических проб, например, клинических проб опухоли человека, а также показали, что редко встречающиеся фенотипы, которые по всей вероятности будут оставаться неопознанными при использовании традиционного приготовления срезов опухоли, могут быть обнаружены в репрезентативном образце, приготовленном способами, описанными в данной заявке. Кроме того, авторы изобретения показали, что описанные способы можно использовать для приготовления репрезентативного образца из целого ряда тканей различных типов, подвергнутых или не подвергнутых фиксации тканей, и полученный репрезентативный образец можно использовать для разнообразных диагностических тестов, включая IHC и выделение нуклеиновой кислоты.
В зависимости от применяемого к образцу способа механической и/или биохимической диссоциации для получения гомогената, кластеры клеток могут содержать больше, чем от одной (1) клетки до нескольких тысяч клеток. Эти скопления клеток могут быть подвергнуты диссоциации (уменьшению в размере и/или в количестве клеток, содержащихся в них) в результате применения других методов, например, в результате дальнейшей механической и/или биохимической диссоциации и/или разделения на основании размера, в зависимости от последующего анализа, выполняемого с использованием репрезентативного образца (например, FACS и проточной цитометрии, для которых необходимы одиночные клетки).
Данный способ является адаптируемым с точки зрения уровня диссоциации образца. Таким образом, существует возможность регулирования механического(их) способа(ов) для получения целевого размера агрегатов клеток, например, посредством дальнейшей обработки кластеров клеток, полученных после применения первого механического способа (такого как обработка в блендере или эквивалентная ей обработка), до тех пор, пока эти кластеры не будут соответствовать цели диссоциации метода отбора образцов (таких как одиночные клетки). Согласно одному из аспектов механическое фрагментирование и разделение на основании размера, например, разделение на сетках с использованием серии сеток, используют для извлечения кластеров клеток, соответствующих определенному размеру или имеющих размер ниже такового, при при одновременном сохранении более крупных кластеров клеток для дальнейшей обработки с целью достижения целевого размера частиц. Таким образом, наряду с тем, что диапазон размеров может выглядеть как нормальное распределение, полученное распределение размера частиц кластеров клеток регулируется путем применения разделения на основании размера, например, размера ячеек сеток, с целью удаления определенных частиц из процесса диссоциации и, таким образом, скорее для достижения плато разделения по размерам, чем распределения.
После гомогенизации полученные кластеры могут содержать по меньшей мере 1-2, 2-100, 100-500, 500-1000, 1000-10000, 10000-50000 или большее число клеток. Согласно одному из аспектов кластеры содержат одиночные клетки, примерно 2-10 клеток, примерно 10-20 клеток или примерно 20-40 клеток. Размер полученных кластеров будет варьировать. См., например, ФИГ. 17.
В результате гомогенизации образца опухоли и/или лимфатического узла (или гомогенизации опухолевого образца) любая гетерогенность клеток в образце, например, опухоли или лимфатическом узле, соответствует по существу гомогенному (равномерному) распределению в полученном гомогенате либо его части или доли, вследствие чего гомогенат (или любая его доля) по существу гомогенно отражает гетерогенность образца опухолевого биопсийного материала, который являлся исходным материалом. Путем гомогенизации опухолей для приготовления образца (или гомогената), который является репрезентативным для всей опухоли, можно охарактеризовать фенотипическое разнообразие (как например, процентное содержание клеток с мутацией в конкретном гене) опухоли. Гомогенизированный образец может быть обозначен как жидкий или превращенный в жидкость образец на основании его способности к растеканию или выливанию, несмотря на то, что многие клетки или большинство клеток остаются интактными. В некоторых случаях репрезентативный образец может представлять собой жидкий образец (как например, отобранный шприцем аспират для цитологического исследования, образец экссудата или мазок по Папаниколау).
Как уже упомянуто, в эти гомогенаты или репрезентативные образцы могут быть добавлены другие группировки, как например, другие клетки, гаптены или метки.
Секвенирование репрезентативных образцов
Чтобы достичь конечной цели персонализированной медицины, онкологи прибегают к помощи диагностов для обнаружения ключевых мутаций, характерных для опухолей, чтобы можно было увязать целевые терапии с конкретными изменениями в опухоли. Сбор информации о последовательностях из солидных опухолей с использованием методов секвенирования следующего поколения (NGS) является критическим звеном технологического процесса в области клинической онкологии, поскольку с течением времени опухолевые клетки неизменно могут становиться устойчивыми к терапии. Одним из наиболее значительных препятствий, присущих всем существующим клиническим рабочим процессам NGS, является то, что клиницисты не могут обнаружить мутации, которые провоцируют опухолевый рост во всех частях опухоли, а также клиницисты не могут обнаружить мутации, которые придают устойчивость к получаемой ранее терапии. Кроме того, несмотря на то, что некоторые из мутаций могут иметь высокий показатель распространенности в опухоли, другие мутации (в том числе драйверные мутации и мутации резистентности) могут присутствовать, но только в небольшой части опухоли. Как правило, корнем этой проблемы является тот факт, что клиницисты используют фиксированные в формалине, залитые парафином (FFPE) срезы тканей, приготовленные из образцов, взятых из первичной опухоли. Несмотря на то, что проблема отбора образцов может быть полностью решена посредством применения способа отбора репрезентативных образцов, все еще имеются некоторые существенные проблемы, которые необходимо решить в клинических рабочих процессах NGS, чтобы полностью реализовать возможности персонализированной медицины.
На сегодняшний день NGS в клинике можно использовать только для обнаружения мутации, подверженной направленному воздействию (т.е. мутации, связанной с направленной терапией), которая присутствует в большей части опухоли. Клиницисты и исследователи сосредоточились на мутациях, подверженных направленному воздействию, в первую очередь из-за объема данных, получаемых при использовании технологий NGS. Например, при полноэкзомном анализе образца ткани будут исследованы десятки тысяч генов, при этом каждый ген секвенируется в виде небольших сегментов в количестве от нескольких десятков до нескольких сотен. Вместо того, чтобы для принятия клинических решений использовать все данные, многие группы скрывают подавляющее большинство данных и сообщают только о мутациях, которые, как известно, связаны с терапией.
Однако, неудовлетворенная техническая и клиническая потребность заключается в обнаружении всех мутаций, присутствующих в солидной опухоли, независимо от того, "подвержены ли они направленному воздействию" или нет. Кроме того, клиницистам крайне важно определить процентное содержание опухолевых клеток, которые содержат специфическую мутацию. Только с использованием данных, которые охватывают геномное разнообразие значительной части опухоли, клиницисты могут понять, как лечить пациента с несколькими "подверженными направленному воздействию или восприимчивыми к лекарственным средствам" мутациями. Например, если солидная опухоль содержит мутацию в гене EGFR с показателем распространенности 55%, мутацию в гене bRaf с показателем распространенности 20% и мутацию в гене KIT с показателем распространенности 5%, то клиницист хотел бы направленно воздействовать на основную массу опухоли ингибитором EGFR (например, цетуксимабом, панитумумабом) до тех пор, пока клинический ответ не будет обнаружен посредством визуализации или в течение определенного периода времени. Затем прием ингибитора EGFR будет прекращен и будет вводиться следующая наиболее распространенная направленная терапия, в этом случае ингибитор bRaf (например, вемурафениб). В данный момент клиницист может отследить или не может отследить клинический ответ посредством визуализации. Прием ингибитора bRaf будет прекращен, и будет назначена наименее часто применяемая направленая терапия, а именно ингибитор KIT (например, иматиниб, сунитиниб). Затем этот режим лечения тремя лекарственными средствами можно повторить. Если эти лекарственные средства могут переноситься вместе, то другой возможностью будет комбинированная терапия. Альтернативно, данные лекарственные средства можно вводить в обратном порядке: ингибитор KIT, ингибитор bRaf, затем ингибитор EGFR.
Критический компонент этого режима приема лекарственных средств заключается не в технологии или ингибиторах NGS, а скорее в определении как присутствия всех перспективных мишеней, так и относительного показателя их распространенности в опухоли с использованием методов отбора репрезентативных образцов. В приведенном выше примере и мутация в гене KIT, и мутация в гене bRaf были бы пропущены, поскольку они присутствуют с низким показателем распространенности. Если бы область опухоли в отобранном образце характеризовалась высоким процентным содержанием bRaf-мутантных клеток, это выглядело бы так, как если бы мутация в гене bRaf являлась причиной большей части опухоли и ингибитор bRaf был бы дан в качестве единственного агента. Воздействие только на одну из этих трех мутаций в приведенном выше примере приводило бы к появлению устойчивости к терапии, поскольку опухолевые клетки, которые содержали другие две мутации, не отвечали бы на этот единственный агент.
При других использованиях данных NGS о первичных опухолях делаются попытки определить, могут ли опухолевые клетки быть мишенью для иммунной системы, т.е. возможно ли применение иммунотерапии. Это включает предсказание наличия неоантигенов, которые могут быть мишенью для иммунной системы. С использованием секвенирования экзома опухолей можно выявить мутации, которые, как предполагается, приводят к изменениям в экспрессированном белке.
Критическим фактором в определении показателя распространенности мутации в солидной опухоли является обогащение/очистка опухолевых клеток из смешанной популяции опухолевых и нормальных клеток. Одним из методов, который можно использовать для захвата высокой процентной доли опухолевых клеток, является сортировка флуоресцентно-активированных клеток (FACS). Для применения этого метода в отношении репрезентативных образцов сначала необходимо провести диссоциацию гомогенизированной солидной опухоли до одиночных клеток или небольших состоящих из многих клеток фрагментов ткани. Одиночные клетки могут быть отсортированы с учетом размера клеток и ядер в дополнение к детектированию сигнала флуоресценции от опухолевого маркера. Результатом негативного отбора нормальных клеток с отделением от опухолевых клеток также будет получение образца, преимущественно состоящего из опухолевых клеток. Сортировка фрагментов ткани, состоящих из многих клеток, (MTFS) может быть улучшена посредством детектирования сигнала флуоресценции от опухолевого маркера или, в случае негативного отбора, маркера нормальных клеток. Этот метод не только упрощает интерпретацию NGS данных, но предоставляет возможность обнаруживать мутации в опухоли с крайне низкой распространенностью.
Кроме того, FACS или MTFS можно использовать для различения многочисленных разнообразных популяций клеток из опухолей, каждую из которых можно обрабатывать в качестве единичного образца и анализировать независимо друг от друга. Примеры этого могут относиться к дифференцировке опухолевых клеток, нормальных эпителиальных клеток, эндотелиальных клеток и иммунных клеток.
Еще одним применением NGS для репрезентативного образца является детектирование неоантигенов, которые могут быть обнаружены иммунной системой. Чтобы эффективного использовать неоантигены в схеме противоопухолевого лечения, клиницисты должны обнаружить всевозможные антигенные мутации из опухоли. Как и в случае с направленной терапией, для осуществления терапии с использованием химерного антигенного рецептора (CAR-Т) важно выявить большинство неоантигенов.
Кроме того, проточная цитометрия представляет собой важный компонент организации диагностического этапа рабочего процесса, когда клиницисты могут использовать данные проточной цитометрии для определения состава репрезентативного образца, касающиеся процентного содержания в образце опухолевых клеток, нормальных клеток, клеток диплоидной опухоли или различных популяций опухолевых клеток, которые являются положительными в отношении специфического биомаркера. Примером такой организации рабочего процесса будет расчет минимального числа клеток, необходимого для проведения статистически эффективного IHC анализа, для которого требуется 1000 положительных клеток, в результате вычисления процентного содержания клеток опухоли в репрезентативном образце.
Гомогенизация опухолей или их частей
Настоящее изобретение относится к способам гомогенизации образца опухолевой или другой ткани, например, предраковых или предположительно нормальных тканей, которые возможно могут быть подвергнуты консервации или фиксации до или после гомогенизации, например, с использованием формалина, парафина и/или этанола, для приготовления "репрезентативного образца", который определяет объективное показание ткани целиком, например, опухоли, лимфатического узла, метастазов, полипа, кисты, биопсийного материала, целого органа или комбинации любого из вышеперечисленных. И вновь применение этих способов может сохранить целостность и/или жизнеспособность клеток в образце. Такие репрезентативные образцы могут содержать основные клоны (имеющие показатель распространенности более чем 50%), первичные субклоны (имеющие показатель распространенности от примерно 20% до примерно 50%), вторичные субклоны (имеющие показатель распространенности от примерно 10% до примерно 20%) и минорные субклоны (имеющие показатель распространенности менее 10%, предпочтительно показатель распространенности менее 5%, более предпочтительно показатель распространенности менее 1% и наиболее предпочтительно показатель распространенности менее 0,1%). Как обсуждалось выше, использование репрезентативных образцов способствует обнаружению событий с низкой распространенностью, т.е. с распространенностью выше или ниже 0,000001%. Репрезентативные образцы, поскольку они отражают полноту образца ткани, например, солидной опухоли или лимфатического узла, позволяют осуществлять обнаружение мутаций пропорционально их наличию в ткани, обычно в опухолевой ткани или ткани лимфатического узла/лимфатической ткани, что нельзя гарантированно выполнить с использованием существующих в настоящее время методов (таких как окрашивание FFPE срезов).
Концепция гомогенизации клинических проб, например, опухолей человека, противоречит исторически сложившимся методам отбора образцов в патологоанатомических и онкологических исследованиях. Не существует исторического прецедента для гомогенизации целых опухолей человека или даже больших частей опухолей человека. Действительно, после отбора образцов для определения стадии по системе TNM оставшийся материал опухоли уничтожают (поскольку считается, что вся с медицинской точки зрения релевантная информация находится в срезах, собранных для определения стадии по системе TNM).
Однако, авторы изобретения установили, что вместо уничтожения оставшегося опухолевого материала, если весь материал (или по существу весь материал) из имеющейся в распоряжении опухоли подвергнут консервации и гомогенизирован в виде одного образца, можно провести детектирование и анализ информации от небольших субпопуляций раковых клеток.
Во многих случаях, образец (такой как опухоль, лимфатический узел или метастазы) представляют на рассмотрение целиком, либо в виде одного блока, либо в виде нескольких блоков в зависимости от размера опухоли. Например, многие опухоли молочной железы менее 2 см в диаметре представляют на рассмотрение целиком как и большинство меланом. Среди ориентировочно 935000 установленных случаев рака в 2015 г., по оценкам, по меньшей мере одна треть опухолевых образцов оказываются пригодными для гомогенизации. Опухоли, особенно пригодные для гомогенизации, включают опухоли толстой кишки и опухоли почки.
Жидкая природа гомогенизированной опухоли способствует проведению статистического анализа клеточной популяции опухоли. Например, эффективный анализ предполагает, что вероятность детектирования субклона с низким показателем распространенности повышается при использовании в таком анализе образца с более высоким процентным содержанием. Например, использование образца размером примерно 95 клеток позволяет обнаружить субклон с показателем распространенности примерно 20%, использование образца размером примерно 200 клеток позволяет обнаружить субклон с показателем распространенности примерно 0,1%, использование образца размером примерно 2000 клеток позволяет обнаружить субклон с показателем распространенности примерно 0,01% и использование образца размером примерно 20000 клеток позволяет обнаружить субклон с показателем распространенности примерно 0,001%. Разумно предположить, что опухолевый образец из клиники содержит по меньшей мере примерно 100-200, 200-1000, 1000-5000, 10000-100000, 100000-1000000, 1000000-5000000, 5000000-1000000000, 1000000000-50000000000 или большее число клеток (т.е. несколько триллионов клеток), вероятно из пространственно различающихся участков опухоли, и репрезентативные образцы, приготовленные из этих опухолей, будут содержать достаточные количества клеток, чтобы обеспечить адекватное обнаружение субклонов. Таким образом, "усиление" каждого диагностического анализа достаточным количеством клеток из репрезентативных опухолевых образцов, приготовленных в соответствии с описанными способами, способствует обнаружению немногочисленных субклонов в опухоли и, таким образом, способствует объективному определению мутационного профиля раковых заболеваний.
В описанных способах приготовления репрезентативного образца нет необходимости в лизисе клеток, и в некоторых воплощениях сохраняется структура клеток. В результате, репрезентативные образцы, приготовленные в соответствии с описанными способами при сохранении целостности клеток, можно использовать, например, в ICC, IHC и проточной цитометрии. Альтернативно или помимо этого, образец или репрезентативный образец либо их части возможно могут быть обработаны с целью разрушения (лизиса) клеток и, таким образом, позволяют провести анализ клеточных компонентов с использованием, например, ПЦР, секвенирования следующего поколения (NGS) и масс-спектрометрии.
На начальной стадии в процессе отбора образца в виде целой опухоли или идентификации типов немногочисленных клеток в предположительно нормальных или предраковых тканях получают достаточное количество ткани, например, опухолевой ткани. Обычно, чем большее количество опухолевой ткани доступно для гомогенизации, тем больше вероятность обнаружения субпопуляций немногочисленных опухолевых клеток. Реально, суммарное количество опухолевого материала, доступного для приготовления репрезентативного образца, будет составлять менее 100% (по причине того, что образцы для определения стадии по системе TNM уже изъяты из опухоли). Однако, заглядывая в будущее, т.е. как только способы по настоящему изобретению станут стандартом клинической практики, целые опухоли (или по меньшей мере большая часть оставшейся опухоли) будут доступны для гомогенизации в клинике. Существующая в настоящее время практика заключается в фиксации в формалине извлеченного хирургической резекцией материала целиком перед макроскопическим исследованием и отбором образцов хирургом-патологоанатомом; при этом как фиксированная, так и нефиксированная ткань пригодны для отбора репрезентативных образцов. Однако, предполагается, что фиксация в формалине может быть устранена или прекращена, например, как только способы по настоящему изобретению станут стандартом клинической практики. Несмотря на это, также существует возможность применения существующих методов определения стадии по системе TNM в комбинации со способами отбора репрезентативных образцов, описанными в данной заявке.
С того момента, когда получена опухолевая или другая ткань, как можно большее количество опухоли или другой ткани помещают в блендер (или другое подходящее устройство) и гомогенизируют, как правило, посредством механического фрагментирования (хотя гомогенизации также может способствовать химическая и/или биохимическая, например, ферментативная, диссоциация).
Гомогенизация чисто механическими способами, например, обработка в блендере, приводит к получению диапазона фрагментов ткани, каждый раз от нескольких тысяч до нескольких сотен клеток, что вероятно соответствует нормальному распределению. Однако, применение других методов гомогенизации, по отдельности или в сочетании с механическими способами, например, методов биохимической/химической диссоциации, по отдельности или в сочетании с механическими способами, может изменять распределение фрагментов ткани в сторону от нормального распределения.
Помимо этого, сочетание используемых параллельно или последовательно механических способов, в результате применения которых осуществляется диссоциация и гомогенизация образца, например, опухоли или лимфатического узла, на фрагменты ткани (как например, отдельные клетки и клеточные кластеры), можно использовать для приготовления образца для анализа на биомаркеры во время или после получения клеточного образца. Например, репрезентативный образец, содержащий интактные клетки, может быть приготовлен путем обработки образца в блендере, как рассмотрено выше, и полученный "образец клеток" можно использовать для анализа интактных клеток; однако, образец клеток можно подвергнуть дальнейшей обработке с применением других механических способов, например, ультразвуковой обработки, с получением образца для анализа на биомаркеры, т.е. разрушение (лизис) интактных клеток позволяет провести анализ белковых и/или ДНК биомаркеров в образце.
Средняя величина размера фрагментов ткани обратно пропорциональна мощности блендера (или другого подходящего устройства), поэтому при высокой мощности фрагменты ткани очень малы. Характеристикой ткани, наиболее подходящей для мощности блендера, является содержание коллагена, поскольку для полной диссоциации дермы необходима значительная мощность. Время обработки в блендере также является важной характеристикой; однако, для наиболее эффективного клинического применения необходимо, чтобы диссоциация всей опухоли была проведена за считанные минуты. Если время обработки в блендере установлено, то можно легко определить мощность, необходимую для достижения диссоциации опухоли в течение заданного временного предела.
После надлежащего механического фрагментирования (путем обработки в блендере или применения другого подходящего усилия) с целью диссоциации целой опухоли все субпопуляции опухолевых клеток, которые изначально были пространственно обособлены, оказываются распределенными по всему только что превращенному в жидкость опухолевому образцу. Тестируемые образцы могут быть взяты из гомогенизированного образца, и с использованием различных методов тестирования можно обнаружить субпопуляции опухолевых клеток (в том числе немногочисленные, или имеющие низкий показатель распространенности, или минорные субпопуляции).
Например, можно отобрать аликвоты превращенного в жидкость образца целой опухоли, провести лизирование для высвобождения клеточных компонентов и очистить нуклеиновые кислоты для анализа посредством ПЦР или NGS. Например, клетки можно разрушить, используя микрофлюидизатор, и/или путем шинкования, измельчения, химического или ферментативного разрушения и/или других методов, известных в данной области техники. Альтернативно или помимо этого, белковые компоненты опухолевых клеток можно очистить для применения в таких методах протеомного анализа способы, как масс-спектрометрия (MS). Кроме того, можно выполнить заливку тканевых фрагментов парафиновым воском и отобрать образец, используя современную патологоанатомическую практику. Для долговременного хранения репрезентативных образцов, содержащих превращенную в жидкость опухоль, их можно хранить в подходящем буфере и в холодильнике, или заморозить, или залить воском (например, парафиновым) для хранения.
Как правило, такие упомянутые выше анализы (например, ПЦР, NGS, MS, IHC, ICC и т.д.), в которых может быть эффективно использован образец изначально обработанной в блендере целой опухоли (который содержит кластеры клеток), можно выполнить после приложения механического усилия (с использованием блендера или ультразвукового диспергатора либо другого устройства, подходящего для индуцирования механического фрагментирования) и без биохимической (ферментативной) обработки. Однако, при исследовании репрезентативного образца также можно использовать анализы, для проведения которых необходимы более мелкие группы клеток (как например, по 2-20 клеток или даже одиночные клетки), однако чтобы устранить перекрестные связи между белками, образованные в процессе фиксации в формалине удаленной хирургическим путем ткани, необходимо провести дополнительную обработку образца. В частности, для приготовления репрезентативного образца, состоящего из одиночных клеток и небольших кластеров клеток, подходящего для применения в определенных анализах, например, в методе сортировке клеток, необходимо провести ферментативное расщепление обработанной в блендере опухолевой ткани.
Как рассмотрено выше, гомогенизация может быть осуществлена с применением только механических способов (таких как обработка в блендере, которую используют в одиночку либо последовательно или параллельно с другими механическими способами), только биохимических/химических способов (таких как ферментативное расщепление) или их сочетания. Путем сочетания как физического, так и биохимического (ферментативного) способа разрушения тканевых фрагментов можно приготовить образец, подходящий для диагностического анализа, для которого необходимы интактные клетки. Первый физический способ, который инициирует расщепление перекрестных связей между белками, заключается в инкубации тканевых фрагментов в буфере с низким значением рН при температуре от примерно 80 до примерно 85 градусов по Цельсию. В ходе стадии инкубации, которая представляет собой биохимическое расщепление связей клетка-внеклеточный матрикс, удерживающих вместе фрагменты ткани, начинает неспецифически "открываться доступ" к фрагментам ткани, что готовит их к следующим стадиям способа. Чтобы расщепить эти связи, можно провести, в подходящих условиях, инкубацию с ферментом, таким как не обладающие специфичностью к белкам протеазы, например, пепсин, трипсин, протеиназа K, фурин, эндопротеиназы (такие как Asp-N и Glu-C, поставляемые NEB, Sigma-Aldrich, Thermo Fisher, Promega и тому подобными фирмами), энтерокиназа и субтилизины; обладающие специфичностью к белкам протеазы, например, коллагеназы (такие как коллагеназы типов I-S, I-A, IA-S, II, II-S, IV, IV-S, VIII, V, V-S, XI, XI-S, III, VII, VII-S, S, F, Н и L, поставляемые NEB, Sigma-Aldrich, Thermo Fisher, Promega и тому подобными фирмами), желатиназы, стромелизины, матрилизин, энамелизин и ADMATS (как например, разрушающие протеогликан ферменты); и/или заменители ферментов, не происходящие из млекопитающих/бактерий, например, ферменты грибов, например, Accutase® и AccuMax® (Innovative Cell Technologies, Сан-Диего, СА), или комбинация любого из вышеперечисленных. Типичные ферменты включают, но не ограничиваются этим, интерстициальную коллагеназу, желатиназу-а, стромелизин 1, матрилизин, коллагеназу нейтрофилов, желатиназу-b, стромелизин 2, стромелизин 3, металлоэластазу макрофагов, коллагеназу 3, МТ1-ММР, МТ2-ММР, МТ3-ММР, МТ4-ММР, коллагеназу 4, энамелизин, Х-ММР, СА-ММР, МТ5-ММР, МТ6-ММР, матрилизин-2, ММР-22, эндопротеиназу, трипсин, химотрипсин, эндопротеиназу Asp-N, эндопротеиназу Arg-C, эндопротеиназу Glu-C (V8 протеазу), эндопротеиназу Lys-C, пепсин, термолизин, эластазу, папаин, протеиназу K, субтилизин, клострипаин, экзопептидазу, карбоксипептидазу А, карбоксипептидазу В, карбоксипептидазу Р, карбоксипептидазу Y, катепсин С, высвобождающий ациламинокислоту фермент, пироглутаматаминопептидазу; инкубацию с ними в подходящих условиях можно провести, чтобы расщепить эти связи. Ферменты можно использовать по отдельности или в комбинации, например, коллагеназу (такую как коллагеназа Н) и другой фермент (такой как АссиМах®), несколько коллагеназ, несколько других ферментов и т.д.
Альтернативно или помимо этого, фрагменты ткани подвергают фрагментированию путем прикладывания механического усилия (например, с применением ступки и пестика, прибора для измельчения, аналогичного мясорубке, используемой в колбасном производстве, или ультразвуковой обработки), как до, так и, альтернативно или в дополнение к этому, после расщепления репрезентативного образца биохимическим путем.
Аналогичным образом, расщепленный биохимическим путем репрезентативный образец можно подвергнуть дальнейшей обработке посредством выполнения центрифугирования, что можно использовать с целью выделения определенных клеток или другого материала из образца для дополнительного анализа. Например, центрифугирование репрезентативного образца, приготовленного из карциноидной опухоли яичника человека, серозного варианта, который подвергали обработке в блендере и расщеплению с использованием AccuMax® и коллагеназы Н, приводит к выделению присутствующих в опухоли тромбоцитов и других клеток крови (ФИГ. 23). ФИГ. 23 представляет изображение присутствующих в опухоли тромбоцитов и других клеток крови, выделенных посредством центрифугирования из расщепленного биохимическим путем репрезентативного образца. Карциноидную опухоль яичника человека, серозный вариант, подвергали обработке в блендере и расщеплению с использованием AccuMax® и коллагеназы Н, после чего центрифугировали, что приводило к накоплениютромбоцитов и эритроцитов в верхней части подвергнутого центрифугированию образца (красная линия).
В данном описании авторы изобретения показывают, что сочетание выдерживания клеток при определенных рН и температуре с ферментативным расщеплением обеспечивает получение эффективно диссоциированных репрезентативных образцов. Процесс улучшения возможности доступа красящего вещества (биологического или химического) к молекулярной мишени обозначается в данном описании как "выдерживание клеток". Например, выдерживание клеток в СС1 буфере или СС2 буфере (Ventana) при высокой температуре (70-100 градусов по Цельсию) способствует ферментативному расщеплению опухолевой ткани. В качестве раствора для выдерживания клеток можно использовать многие альтернативные варианты цитратному буферу.
Одна эффективная мера размера фрагментов ткани после дополнительной обработки включает в себя оценку того, насколько хорошо пробы жидкости проходят через сетку или фильтр
Один из эффективных критериев размера фрагментов ткани после дополнительной обработки включает оценку того, насколько хорошо проходит жидкий образец через сетку или фильтр (или серию таких сеток или фильтров) с известным размером пор, например, меньше 1 микрона (например, примерно 0,5 микрона), примерно 1-6 микрон, примерно 6-10 микрон, примерно 10-20 микрон, примерно 20-30 микрон, примерно 30-40 микрон, примерно 40-100 микрон, примерно 100-300 микрон, примерно 300-500 микрон или более 500 микрон. Согласно одному из аспектов, для разделения клеток, присутствующих в гомогенате, используют серию фильтров с изменением размера пор от примерно 1 микрона до примерно 500 микрон. Также можно применять фильтр с меньшим размером пор, например, меньше 1 микрона, например, приблизительно 0,45 мкм, для отделения субклеточной части образца для анализа на биомаркеры от клеточной части образца после получения репрезентативной клеточной фракции. Таким образом, после осуществления методов механической диссоциации (таких как обработка в блендере или эквивалентная ей обработка), могут быть использованы методы разделения на основании размера, например, разделение на ситах, как быстрый метод отделения образца для анализа на биомаркеры от образца для анализа на клетки.
Анализ репрезентативного образца или композиции на основе гомогената
Репрезентативные образцы, например, опухолевые образцы, приготовленные описанными способами, предоставляют некоторые преимущества по сравнению с традиционными опухолевыми образцами, используемыми в патологоанатомической практике и диагностике, включая (1) возможность применения репрезентативного образца в нескольких различных диагностических анализах, при этом некоторые из них могут быть несовместимы с солидной тканью; (2) повышенную возможность обнаружения субклонов с низкой распространенностью, т.е. приготовление репрезентативного образца из опухоли целиком устраняет систематические ошибки при отборе образца, которые препятствуют обнаружению субклонов с низкой распространенностью; и (3) устранение увеличения количества образцов в диагностической лаборатории онкологического центра, что тем самым способствует более эффективной организации рабочего процесса в лаборатории, т.е. современная практика диктует, чтобы из расчета на одну опухоль было сделано примерно 3-10 блоков, хотя тестируется только 1 блок.
Таким образом, данное изобретение также относится к способам анализа репрезентативного образца или композиции на основе гомогената. Согласно одному из аспектов анализ содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из анализа нуклеиновых кислот, анализа белков, анализа липидов, анализа клеток, анализа метаболитов, геномного анализа, транскриптомного анализа, протеомного анализа, метаболомного анализа, липидомного анализа, иммунологического анализа, цитохимического анализа, генотипического анализа, фенотипического анализа или их комбинации. Согласно одному из аспектов анализ нуклеиновых кислот содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из анализа ДНК или анализа РНК. Согласно другому аспекту анализ РНК содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из анализа микроРНК. Согласно другому аспекту анализ гомогената включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в очистке нуклеиновой кислоты, белка, органеллы, метаболита, химического вещества, неклеточного компонента или их комбинации.
В другом воплощении анализ гомогената включает либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из связывания связывающегося агента с компонентом гомогената. Согласно некоторому аспекту связывающийся агент содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из антитела, радиоактивной метки, флуорохрома, гаптена, фермента, нуклеиновой кислоты, белка, химического вещества, праймера, лиганда, клетки, пептида, зонда, флуоресцентного красителя, нефлуоресцентного красителя, фермента, биотина или их комбинации. В одном из воплощений компонент гомогената содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из нуклеиновой кислоты, белка, органеллы, метаболита, химического вещества, неклеточного компонента или их комбинации.
В одном из воплощений анализ гомогената дополнительно включает либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из детектирования сигнала от связывающегося агента или компонента. Согласно одному из аспектов, такой сигнал содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из радиоактивного сигнала или нерадиоактивного сигнала. Согласно другому аспекту нерадиоактивный сигнал содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из флуоресцентного сигнала, хемифлуоресцентного сигнала или люминесцентного сигнала. Согласно другому аспекту анализ гомогената включает либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из анализа с использованием секвенирования, гистологического анализа или анализа изображений. Согласно одному из аспектов анализ с использованием секвенирования включает либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из анализа с использованием секвенирования следующего поколения, анализа с использованием секвенирования из одной клетки и/или секвенирования из одного ядра. Согласно другому аспекту гистологический анализ включает либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из гистологического анализа следующего поколения. Согласно одному из аспектов анализ изображений включает либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из анализа следующего поколения.
В одном из воплощений способ приготовления образца ткани дополнительно включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в детектирования или количественного определения компонента гомогената, при этом компонент содержит клетку, нуклеиновую кислоту, белок, органеллу, метаболит, химическое вещество, неклеточный компонент или их комбинацию. Согласно одному из аспектов, клетка содержит либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из иммунной клетки, опухолевой клетки, стволовой клетки, клетки-предшественника, клетки крови, зародышевой клетки и соматической клетки. Согласно другому аспекту анализ гомогената включает либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из анализа поляризованного света, отраженного от гомогената. Согласно одному из аспектов, анализ гомогената включает либо, альтернативно, состоит по существу из или, кроме того, в основном состоит из анализа акустического свойства, механического свойства или оптического свойства гомогената. Согласно другому аспекту анализ гомогенат выполняют с проточной цитометрии, окрашивания гематоксилином и эозином или иммуногистохимии.
В одном из воплощений, когда клетки из всей опухоли были диссоциированы до желаемой степени, репрезентативный образец может быть нанесен на предметное стекло при подготовке к окрашиванию, например, ISH или ICC или IHC окрашиванию.
Существует множество способов нанесения клеток на предметные стекла, и все из них включают сушку клеток на предметных стеклах. Буферы, которые способствуют нанесению клеток на предметные стекла, изменяются от органических растворителей (таких как этанол, метанол, лимонен, формалин и ацетон), неводных растворителей (пропиленгликоля, полиэтиленгликоля, глицерина, растительных маслел, таких как оливковое масло, и вводимых инъекцией органических сложных эфиров, таких как этилолеат), неорганических неводных растворителей (таких как жидкий аммиак, жидкий диоксид серы, сульфурилхлорид и сульфурилхлорида фторид, фосфорилхлорид, динитротетроксид, сурьмы трихлорид, брома пентафторид, фтористый водород, чистая серная кислота и другие неорганические кислоты), обычных буферов (например, на основе PBS, HEPES, MES, PIPES, лимонной кислоты, TAPS, бицина, триса, трицина, TAPSO, TES, MOPS, PIPES, CHES, какодилата, угольной кислоты, бикарбоната или ТЕ) до воды. Например, клетки могут быть разведены в метаноле, который способствует равномерному распределению по предметному стеклу и быстро испаряется.
Кроме того, чтобы получить клеточные репрезентативные образцы на предметных стеклах без воздействия спиртовых растворителей, можно использовать другие сильно летучие растворители (такие как ацетонитрил, октанол, хлорбутан или другие растворители для высокоэффективной жидкостной хроматографии (HPLC)) и охлаждающие жидкости (такие как четыреххлористый углерод, трихлорфторметан, дибромдифторметан и другие жидкости, которые имеют значения точки кипения, близкие комнатной температуре (например, 25°С)).
Типичные методы Н&Е окрашивания, ISH, in situ ПЦР, иммуногистохимические (IHC), гистохимические (НС) методы или гистохимические методы с использованием ферментов (ЕНС) могут быть осуществлены с использованием стандартных методов и, предпочтительно, методов, приведенных в данном описании (см. ФИГ. 10, ФИГ. 11 и ФИГ. 14). Пригодными форматами для реакции детектирования по настоящему изобретению могут быть методы с использованием блоттинга, такие как вестерн-блоттинг, саузерн-блоттинг, нозерн блоттинг, иммуноцитохимические или иммуногистохимические методики. Методы с использованием блоттинга известны специалистам средней квалификации в данной области техники и могут быть выполнены, например, в виде процедур электроблоттинга, "полусухого" блоттинга, вакуум-блоттинга или дот-блоттинга. Методики иммуноцитохимического/гистохимического окрашивания известны специалистам в данной области техники и могут включать опосредуемое связывающимся агентом детектирование полипептидов, а также методы гибридизации in situ. Оба эти разных метода можно применять даже одновременно. В определенном воплощении для детектирования нуклеиновых кислот можно использовать метод гибридного захвата. Реакция амплификации также может быть применима для детектирования, например, молекул нуклеиновых кислот.
Гибридизация in situ (ISH) представляет собой метод, который может быть предпочтительно применен в соответствии с настоящим изобретением, либо по отдельности, либо в комбинации с другими методами, поскольку многие стадии в ISH должны быть проведены при строгом контроле температуры в течение точно выверенного периода времени. Для денатурации ДНК в достаточной степени необходимо точное количество тепла в течение конкретного периода времени, чтобы могла произойти последующая гибридизация без перегрева до того момента, когда морфология клеток разрушается. Различные пробы можно подвергать денатурации путем использования разных температур в зависимости от того, каким образом готовили и фиксировали эту ткань. Стадии денатурации, гибридизации и постгибридизационных промывок могут быть проведены при разных температурах, которые могут зависеть от особенностей зонда и подлежащей тестированию ткани. Эти температуры можно регулировать посредством индивидуального управления нагревательными устройствами, как обсуждалось ранее. Обычно ДНК зонды гибридизуются при температуре от 30 градусов до 55 градусов по Цельсию, в то время как РНК зонды обычно гибридизуются при более высоких температурах, при этом продолжительность гибридизации варьирует от 30 мин до 24 часов в зависимости от числа копий мишени, размера зонда и типа пробы. Стандартную денатурацию для цитогенетических препаратов осуществляют при температуре примерно 72 градуса по Цельсию в течение 2 мин, в то время как для срезов тканей такие условия могут варьировать от 55 градусов по Цельсию до 95 градусов по Цельсию в течение от 2 до 30 мин. Температуры при проведении постгибридизационных промывок могут варьировать от примерно 37 градусов по Цельсию до 72 градусов по Цельсию в течение от 2 мин до 15 мин. Концентрация соли может варьировать от 0,1x до 2х SSC. Температуры детектирования зондов могут варьировать от температуры окружающей среды до 42 градусов по Цельсию в течение от 2 мин до 30 мин.
ISH можно применять для обнаружения ДНК, кДНК и высококопийной мРНК. Ее можно применять в случае мазков, ткани, клеточных линий и замороженных срезов и, в контексте настоящего изобретения, для репрезентативных образцов, приготовленных в соответствии с описанными способами, а также композиций, содержащих репрезентативные образцы. В типичном случае пробу размещают на предметном стекле размером 1'' × 3''.
Одним из преимуществ основанного на IHC детектирования биомаркеров является чувствительность детектирования DAB. С применением этого способа можно обнаружить очень редко встречающиеся события в смешанной популяции клеток. Например, авторы изобретения показали, что минорный субклон, который представляет собой пространственно различающийся компонент целого образца (т.е. Her-2-положительная клетка, присутствующая в количестве немногим более 0,1% от всего объема ткани), был отчетливо различим в репрезентативном образце, приготовленном в соответствии с описанными способами, при визуализации с 20-кратным увеличением. См. пример 1 и ФИГ. 6A-6D. Кроме того, авторы изобретения показали, что минорный субклон (экспрессирующий мутантный bRaf ксенотрансплантат опухоли, присутствующий в основной массе образца подвергнутой диссоциации ткани миндалин на уровне 0,015% от всего образца), также четко детектировался. См. пример 4 и ФИГ. 16.
В дополнение к основанному на применении DAB IHC окрашиванию все анализы, основанные на использовании стандартных предметных стекол, подходят для применения в случае гомогенизированного опухолевого образца. Например, авторы изобретения показали, что для анализа репрезентативных образцов, приготовленных в соответствии с описанными способами, можно использовать мультиплексное IHC окрашивание (с применением трех антител, детектируемых в отдельных процедурах окрашивания), основанную на применении РНК ISH и основанную на применении ДНК ISH. См. пример 3 и ФИГ. 11 и 12.
Методики детектирования по настоящему изобретению помимо всего прочего могут включать методику цитохимического окрашивания, обеспечивающую хромогенное или флуоресцентное окрашивание клеток или клеточных компартментов. Такие методики окрашивания известны специалистам в данной области техники и могут, например, включать, например, окрашивание окрашивающихся кислотными или основными красителями структур, субклеточных участков (например, ядра, митохондрий, аппарата Гольджи, цитоплазмы и т.д.), конкретных молекул (хромосом, липидов, гликопротеинов, полисахаридов и т.д.) в цитологических пробах. Можно использовать флуоресцентные красители, такие как DAPI, хинакрин, хромомицин и т.д. Кроме того, можно применять хромогенные красители, такие как азан, акридиновый оранжевый, гематоксилин, эозин, судановый красный, тиазиновые красящие вещества (толуидиновый синий, тионин). В других воплощениях такие методики окрашивания, как окрашивание по Папаниколау (Рар), окрашивание по Гимзе, окрашивание гематоксилином-эозином, окрашивание по Ван-Гизону, окрашивание по методу Шиффа (с использованием реактива Шиффа), методики окрашивания с использованием осаждения металлов (в частности, например, серебра, в методиках окрашивания с использованием нитрата серебра) или нерастворимых красящих веществ, в частности, например, турнбуллевой сини (или других нерастворимых цианидов металлов) и т.д., могут быть применены при выполнении способа, описанного в данной заявке. Следует понимать, что упомянутые красители и методы окрашивания будут представлять собой примеры пригодных методов, и любой другой метод, известный в данной области техники, может быть использован в приложении к способу, описанному в данной заявке.
В методиках окрашивания могут быть использованы хромогенные красящие вещества для исследования с использованием светового микроскопа или флуоресцентные красящие вещества для исследования в условиях флуоресценцентной микроскопии. В другом воплощении настоящего изобретения в способе по настоящему изобретению могут быть применены методики с испусканием излучения, методики с использованием веществ, ослабляющих передачу излучения, или других контрастных сред для визуализации цитологических состояний в образце (например, генерирование оптического импринта с помощью таких средств, как получение (микро)авторадиографической или (микро-) рентгенографической картины).
Все процедуры окрашивания и визуализации можно использовать для анализа не только в методиках с применением микроскопа, но также в методиках автоматизированного анализа, таких как проточная цитометрия, автоматизированный микроскопический (компьютеризированный или компьютерный, например, с использованием сканирующего устройства для сканирования всего предметного стекла) анализ или любой другой метод для анализа окрашенных цитологических проб. Термин "автоматизированный" или "автоматический" относится к процессу, управляемому по существу компьютером или машиной и осуществляемому практически без участия человека.
К репрезентативным образцам и композициям, содержащим репрезентативный образец, могут быть применены дополнительные диагностические методы, включая, но не ограничиваясь этим, основанное на ELISA детектирование белков, аффинную очистку клеток конкретного типа и т.д. С целью дальнейшей иллюстрации многочисленных диагностических и терапевтических применений настоящего изобретения в данном описании ниже приведен дополнительный обзор различных методов, которые могут быть осуществлены в отношении репрезентативных образцов по изобретению и субобразцов или компонентов, выделенные из них, например, клеток, нуклеиновых кислот, белков, липидов и др.
Подходы, связанные с мультиплексированием и работой со смесями, применяемые к репрезентативным образцам или композиции на основе гомогената
Согласно одному из аспектов репрезентативный образец, приготовленный из одного образца, полученного от одного пациента, можно применять для последующего диагностического анализа с использованием любого из способов, описанных в данной заявке, и/или других сопоставимых способов, известных в данной области техники. Образец, полученный от пациента, можно "пометить" малой молекулой перед гомогенизацией и возможной дальнейшей обработкой, например, фильтрованием (разделением на сетках). В результате введения в образец низкомолекулярной метки этот образец теперь можно отличить от других образцов (в том числе других образцов ткани и/или опухоли от того же пациента, а также образцов ткани и/или опухоли, полученных от разных пациентов и, таким образом, применяя для мечения этот подход, можно использовать разные репрезентативные образцы в формате мультиплексного анализа.
Например, первая опухоль, вторая опухоль и третья опухоль могут быть получены от первого пациента. Первая опухоль может быть помечена первой малой молекулой, вторая опухоль помечена второй малой молекулой, а третья опухоль помечена третьей малой молекулой, при этом каждую малую молекулу можно отличить от других. Затем меченые первая опухоль, вторая опухоль и третья опухоль могут быть подвергнуты гомогенизации, по отдельности или в комбинации, и полученный "смешанный" гомогенат будет содержать репрезентативный образец каждой опухоли.
Тот же самый подход, "связанный с работой со смесями" можно использовать для проведения мультиплексного анализа с использованием нескольких образцов из лимфатического узла от одного и того же пациента и/или комбинации образцов из опухоли и лимфатического узла от одного и того же пациента.
Согласно другому аспекту готовят срезы образца, например, опухоли или лимфатического узла, полученного от пациента, и каждый срез "помечают" малой молекулой до объединения и совместной гомогенизации этих срезов с целью создания репрезентативного образца с пространственной информацией. Например, для создания репрезентативного образца с пространственной информацией можно разрезать образец (такую опухоль или такой лимфатический узел) с получением четырех срезов, и в каждый срез до совместной гомогенизации срезов можно "ввести" другой гаптен (или другую подходящую малую молекулу), например, каждый меченый срез помещают в блендер и гомогенизируют. Следует понимать, что количество срезов, которые могут быть получены на основе каждого образца, для "введения добавки" до гомогенизации, не ограничивается, а скорее всего, с большой долей вероятности будет выбрано в зависимости от размера образца, т.е. чем больше образец, тем будет получено большее количество срезов, которые могут быть "помечены" малой молекулой до гомогенизации. Например, образец опухоли и/или лимфатического узла может быть разрезан с образованием 2 срезов, 3 срезов, 4 срезов, 5 срезов, 6 срезов, 7 срезов, 8 срезов, 10 срезов, 15 срезов, 20 срезов, 25 срезов, 30 срезов, 35 срезов, 40 срезов, 45 срезов, 50 срезов, 55 срезов, 60 срезов, 65 срезов, 70 срезов, 75 срезов, 80 срезов, 85 срезов, 90 срезов, 95 срезов, 100 срезов или больше. И вновь, количество срезов, полученных от каждого образца, будет варьировать в зависимости от размера образца. Например, ориентировочно, из образца опухоли размером 2 см путем разрезания можно получить четыре среза, каждый из которых будет помечен различной малой молекулой, в то время как опухоль размером 50 см (такая как опухоль желудка) может быть разрезана на 100 срезов, каждый из которых будет помечен различной малой молекулой.
Следует отметить, что взятые в любом количестве разные образцы от одного и того же пациента или от разных пациентов могут быть объединены и мультиплексированы, при этом разрешено, чтобы каждый образец был "помечен" различными метками, например, по меньшей мере 2 метками, по меньшей мере 3 метками, по меньшей мере 4 метками, по меньшей мере 5 метками, по меньшей мере 6 метками, по меньшей мере 7 метками, по меньшей мере 8 метками, по меньшей мере 10 метками, по меньшей мере 15 метками, по меньшей мере 20 метками, по меньшей мере 25 метками, по меньшей мере 50 метками, по меньшей мере 75 метками, по меньшей мере 100 метками и т.д.
Образцы, например, опухолевый образец, приготовленный на основе целых опухолей, происходящих или от одного, или от нескольких субъектов, либо приготовленный путем получения срезов опухолей, происходящих или от одного, или от нескольких субъектов, могут быть конъюгированы с малой(ыми) молекулой(ами) (такой(ими) как, но не ограничиваясь этим, гаптены, пептидные метки, белковые метки, флуоресцентные метки или нуклеиновокислотные метки, например) с целью определения происхождения исследуемого опухолевого образца.
Конъюгирование может быть осуществлено посредством применения различных механизмов, как подробно описано в работе Lemus and Karol, Methods Mol. Med., 2008, 138: 167-82 (которая тем самым включена посредством ссылки во всей своей полноте). Такие методы конъюгирования могут включать, но не ограничиваются этим, самопроизвольные химические реакции с участием гаптенов, характеризуемых как изоцианаты или ангидриды, активированные химические реакции с участием гаптенов, несущих карбоксильную группу, реакции перекрестного сшивания с участием гаптенов и карбодиимидов или гаптенов и глутарового альдегида. Дополнительные способы конъюгирования могут осуществляться посредством применения диизоцианата и любой из следующих реакционноспособных групп: α-NH2, ε-NH2Lys, α-COOH, SH-Cys; ангидрида кислоты и любой из следующих реакционноспособных групп: α-NH2, ε-NH2Lys, α-COOH, SH-Cys; 2,4,6-тринитробензолсульфоновой кислоты (TNBS) и любой из следующих реакционноспособных групп: α-NH2 и ε-NH2Lys; ароматической аминокислоты и тирозина (при этом ароматическая аминокислота превращается в диазониевую группу); углевода и α-NH2 или ε-NH2Lys (при этом сочетание может осуществляться либо через редуцирующий конец, либо через карбоксильные группы углеводов с кислотной функциональностью, либо через гидроксильные группы); бромциана и α-NH2 или ε-NH2Lys (при этом углеводы, активированные бромцианом, самопроизвольно соединяются с аминогруппами); или смешанного ангидрида и α-NH2 или ε-NH2Lys (при этом R-COOH превращается в ангидрид с использованием изобутилхлоркарбоната).
Дополнительные формы конъюгирования малой молекулы с опухолевым образцом или образцом в виде среза опухоли могут осуществляться, но не ограничиваться этим, в результате таких химических реакций, как реакция образования эфира с использованием NHS (с образованием связи с аминогруппой), малеимидная реакция (с образованием простой тиоэфирной связи), реакция с использованием гидразидов (с образованием гидразоновой связи) или реакция сочетания с использованием EDC (с образованием амидной связи). Кроме того, конъюгирование малой молекулы с опухолевым образцом или образцом в виде среза опухоли либо лимфатическим узлом или срезом лимфатического узла может осуществляться путем применения гомобифункциональных или гетеробифункциональных сшивающих агентов (примеры которых включают, но не ограничиваются этим, сульфо-SMCC, DSS или сульфо-SBED).
Примером малых молекул, которые можно использовать в качестве идентификаторов, могут быть гаптены. Примерами гаптенов, которые используются в типичном случае, являются дигоксигенин, 2,4-динитрофенил, биотин или авидин, либо гаптены, выбранные из азолов, нитроарильных соединений, бензофуразанов, тритерпенов, производных мочевины, производных тиомочевины, ротенонов, оксазолов, тиазолов, кумаринов, циклолигнанов, гетеробиарильных соединений, азоарильных соединений или бензодиазепинов. Другие примеры гаптенов могут включать, но не ограничиваются этим, 2,4-динитрофенил, нитропиразол и тиазолсульфонамид. См. заявку WO 2014139979, которая тем самым включена посредством ссылки во всей своей полноте. Дополнительные примеры гаптенов, которые могут быть использованы, включают, но не ограничиваются этим, гаптены, выбранные из азола (например, оксазола, пиразола, тиазола), бензофуразана, тритерпена, мочевины, тиомочевины, отличной от родамин-тиомочевины, нитроарила, отличного от динитрофенила или тринитрофенила, ротеноида, циклолигнана, гетеробиарила, азоарила, бензодиазепина или кумарина (например, 2,3,6,7-тетрагидро-11-оксо-1Н,5Н,11Н-[1]бензопирано[6,7,8-ij]хинолизин-10-карбоновой кислоты или 7-диэтиламино-3-карбоксикумарина). См. заявки WO 2012003476 и WO 2008063378, обе из которых тем самым включены посредством ссылки во всей своей полноте. Другие примеры гаптенов, которые могли бы быть использованы, включают, но не ограничиваются этим, биотин, урушиол, гидралазин, флуоресцеин, дигоксигенин, динитрофенол, 2,4-дихлорфеноксиуксусную кислоту, 2-хлор-4-(этиламино)-6-(изопропиламино)-s-триазин, никотин, морфин, структурно родственные s-триазины, сулкофурон, флукофурон, агазарезинол, секуирин С, суджирезинол, гидроксисуджирезинол, хинокирезинол, конифериловый спирт, лара-кумаровая кислота, хинокинин, гваяцилглицерин-бета-гваяциловый простой эфир, морфин-3-глюкуронид (M3G), кодеин, норкодеин, 6-моноацетилморфин, (+)-метамфетамин, цефтазидим, фенобарбитал, пара-гид роксифенобарбитал, пара-аминофенобарбитал, гексаметилендиизоцианат, циклобарбитал, 3'-кетоциклобарбитал, 3'-гидроксициклобарбитал, секобарбитал, барбитал, метарбитал, барбитуровую кислоту, тиопентал, тиобарбитуровую кислоту, примидон, глутетимид, пентобарбитал, диацетилморфин, морфин-6-глюкуронид (M6G), L-11-аллил-1,2,3,9,10,10а-гексагидро-4Н-10,4а-иминоэтанофенантрен-6-ол, налоксон, петидин, бензоилэкгонин, 5-бензимидазолкарбоновую кислоту, дексаметазон, флуметазон, бетаметазон, 9-альфа-фторпреднизолон, дезоксиметазон, триамцинолон, преднизолон, флуокортолон, кортизол, преднизон, кортизон, метилпреднизолон, триамцинолон гексацетонид, карбофуран, BFNP (3-[[(2,3-дигидро-2,2-диметил-7-бензофуранилокси)карбонил]амино]пропановую кислоту), 2,3-дигидро-2,2-диметил-7-бензофуранол, бендиокарб, карбарил, метиокарб, пропоксур, алдикарб, метомил, беналаксил, Bn-Ва (4-[2-(N-фенилацетил-N-2,6-ксилиламино)пропионамидо]-масляную кислоту), Bn-СООН (4-[2-(N-фенилацетил-N-2,6-ксилил-DL-аланин), Bn-HG, фуралаксил, металаксил, ацетохлор, диметахлор, метолахлор, диэтатил-этил, бензоилпроп-этил, пропахлор, 2,4,5-трихлорфеноксиуксусную кислоту, 2,4-дихлорфеноксимасляную кислоту (2,4-DB), МСРА, дихлорпроп (2,4-DP), 1-[(2-хлор)фенилсульфонил]моноамидоянтарную кислоту, хлорсульфурон, хлорбромурон, амидосульфурон, хлортолурон, изопротурон, диурон, линурон, О-метил-O-(4-нитрофенил)-N-(4-карбоксибутил)-фосфорамидотиоат, паратион-метил, паратион-этил, фенитротион, фентион, бромофос, хлорпирифос-метил окисленный паратион-метил, параоксон, диазинон, азинфос-метил, пиримифос-метил, метидатион, диметилхлортиофосфат, 4-нитрофенол, 2-нитрофенол, 2-хлорфенол, 4-хлор-3-метилфенол, фенитроксон, 3-метил-4-нитрофенол, нонилфенол, НОМ (3-[2-гидрокси-5нитро-бензилтио]-пропионовую кислоту), делор 103, 2,4,4'-трихлорбифенил, 2-(5-карбоксипентаноиламино)-4,4'-дихлорбифенил, 4-хлорфеноксиуксусную кислоту, 2-хлорфеноксиуксусную кислоту, 1,1,1-трихлор-2,2-бис-(пара-хлорфенил)этан, 1,1-дихлор-2,2-бис(пара-хлорфенил)этилен, витамин D2, витамин D3, деэтилгидроксиатразин (DEHA), флуоресцеинизотиоцианат, метанефрин, пропазин, тербутилазин, аметрин (2-этиламино-4-изопропиламино-6-метилтио-1,3,5-триазин), цианазин, ОН-тербутилазин, гидрокситриазин (EQ-0027), атратон, атразин-меркаптуровую кислоту (AM), N4-ацетил-сульфаметазин, 2,4-дихлорфенол, 4-бромфенол, амоксициллин, 6-амино-пенициллановую кислоту (6-АРА), азлоциллин, бакампициллин, карбенициллин, пенициллин, 1-бензил-3-(4-нитрофенил)мочевину, 1-(3-хлорфенил)-3-(2-метокси-5-нитрофенил)мочевину, 1-(3-хлорфенил)-3-(4-метокси-3-нитрофенил)мочевину, 1-(4-хлорфенил)-3-(4-нитрофенил)мочевину, карбофуран-фенол, карбосульфан, бенфуракарб, эндрин, нендрин, гептахлор, хлордан, эндосульфан, альдрин, дильдрин, изомеры фенвалерата, тиабендазол, производные тиабендазола, альбендазол, мебендазол, фенбендазол, камбендазол, гаптены фенвалерата, пиримифос-этил, 4-(метилтио)-мета-крезол, хлорпирифос-оксон, фенхлорфос, трихлоронат, дихлофентион, паратион, триадимефон, дифлубензурон, метолазон, фурфурил-бензоат, паракват, диэтилкарбамазин, 2,4,6-трифенил-N-(4-гидроксифенил)-пиридиний, o-DNCP, аналоги РСВ, 1-2-дихлорбензол, ретронецин, дикофол, тетраконазол, 2-(2,4-дихлорфенил)-3-(1Н-1,2,4-триазол-1-ил)пропанол, имазалил, фенаримол и метаболиты лупанина. Другие примеры см. в работах Singh М.K., Srivastava S., Raghava G.P.S. and Varsheny G.C. (2004): Hapten DB, Nucleic Acids Research и Singh M. et. al. Hapten DB: a comprehensive database of haptens, carrier proteins and anti-hapten antibodies. Bioinformatics, 2006, 22: 253-255, обе из которых включены тем самым посредством ссылки во всей своей полноте.
Дополнительные низкомолекулярные идентификаторы могут включать, но не ограничиваются этим, флуоресцентные молекулы или флуорохромы (как например, (как например, поставляемые Invitrogen, например, см. The Handbook: А Guide to Fluorescent Probes and Labeling Technologies, Invitrogen Detection Technologies, Molecular Probes, Eugene, Oreg., или описанные в патенте США №5866366 авторами Nazarenko и др.), такие как как 4-ацетамидо-4'-изотиоцианатостильбен-2,2'-дисульфоновая кислота, акридин и такие производные, как акридин и акридина изотиоцианат, 5-(2'-аминоэтил)аминонафталин-1-сульфоновая кислота (EDANS), 4-амино-N-[3-винилсульфонил)фенил]нафталимид-3,5-дисульфонат (люцифер желтый VS), N-(4-анилино-1-нафтил)малеимид, антраниламид, бриллиантовый желтый, кумарин и такие производные, как кумарин, 7-амино-4-метилкумарин (АМС, кумарин 120), 7-амино-4-трифторметилкумарин (кумаран 151); цианозин; 4',6-диаминидино-2-фенилиндол (DAPI); 5',5''-дибромпирогаллол-сульфонфталеин (бромпирогаллол красный); 7-диэтиламино-3-(4'-изотиоцианатофенил)-4-метилкумарин; диэтилентриамина пентаацетат; 4,4'-диизотиоцианатодигидро-стильбен-2,2'-дисульфоновая кислота; 4,4'-диизотиоцианатостильбен-2,2'-дисульфоновая кислота; 5-[диметиламино]нафталин-1-сульфонилхлорид (DNS, данзилхлорид); 4-(4'-диметиламинофенилазо)бензойная кислота (DABCYL); 4-диметиламинофенилазофенил-4'-изотиоцианат (DABITC); эозин и такие производные, как эозин и эозина изотиоцианат; эритрозин и такие производные, как эритрозин В и эритрозина изотиоцианат; этидий; флуоресцеин и такие производные, как 5-карбоксифлуоресцеин (FAM), 5-(4,6-дихлортриазин-2-ил)аминофлуоресцеин (DTAF), 2',7'-диметокси-4',5'-дихлор-6-карбоксифлуоресцеин (JOE), флуоресцеин, флуоресцеина изотиоцианат (FITC) и QFITC (XRITC); 2',7'-дифторфлуоресцеин (OREGON GREEN®); флуорескамин; IR144; IR1446; малахитовый зеленый изотиоцианат; 4-метилумбеллиферон; орто-крезолфталеин; нитротирозин; парарозанилин; феноловый красный; В-фикоэритрин; о-фталевый диальдегид; пирен и такие производные, как пирен, пирена бутират и сукцинимидил-1-пирена бутират; реактивный красный 4 (Cibacron®, бриллиантовый красный 3В-А); родамин и такие производные, как 6-карбокси-Х-родамин (ROX), 6-карбоксиродамин (R6G), лиссамин, родамина В сульфонилхлорид, родамин (Rhod), родамин В, родамин 123, родамина X изотиоцианат, родамин зеленый, сульфородамин В, сульфородамин 101 и сульфонилхлоридное производное сульфородамина 101 (техасский красный); N,N,N',N'-тетраметил-6-карбоксиродамин (TAMRA); тетраметилродамин; тетраметилродамина изотиоцианат (TRITC); рибофлавин; розоловая кислота и хелатный комплекс производных тербия, тиол-реактивные хелатные комплексы европия, которые излучают на длине волны приблизительно 617 нм (Heyduk and Heyduk, Analyt. Biochem., 248: 216-27, 1997; J. Biol. Chem., 274: 3315-22, 1999), a также GFP, Lissamine™, диэтиламинокумарин, флуоресцеина хлортриазинил, нафтофлуоресцеин, 4,7-дихлорродамин и ксантен (как описано в патенте США №5800996 авторами Lee и др.) и его производные, серия красителей ALEXA FLUOR™ (например, которые описаны в патентах США №№5696157, 6130101 и 6716979), серия красителей BODIPY (дипиррометенбордифторидные красители, например, которые описаны в патентах США №№4774339, 5187288, 5248782, 5274113, 5338854, 5451663 и 5433896), Cascade Blue® (реакционноспособное в отношении аминов производное сульфонированного пирена, описанное в патенте США №5132432) и Marina Blue® (патент США №5830912)), флуоресцентная наночастица (такая как полупроводниковый нанокристалл, например, QUANTUM DOT™ (полученный, например, от QuantumDot Corp., Invitrogen Nanocrystal Technologies, Eugene, Oreg.; также см. патенты США №№6815064, 6682596 и 6649138)), наночастица (такая как квантовые точки, парамагнитные наночастицы, суперпарамагнитные наночастицы и металлические наночастицы, предпочтительно легированные квантовые точки, включая, в качестве примера и без ограничения, CdSe, ZnSSe, ZnSeTe, ZnSTe, CdSSe, CdSeTe, ScSTe, HgSSe, HgSeTe, HgSTe, ZnCdS, ZnCdSe, ZnCdTe, ZnHgS, ZnHgSe, ZnHgTe, CdHgS, CdHgSe, CdHgTe, ZnCdSSe, ZnHgSSe, ZnCdSeTe, ZnHgSeTe, CdHgSSe, CdHgSeTe, InGaAs, GaAlAs и InGaN, в качестве примера), полупроводниковые нанокристаллы, описанные, например, в патенте США №6602671, Bruchez et. al. (1998) Science, 281: 2013-6, Chan et al. (1998) Science, 281: 2016-8 и в патенте США №6274323, патентах США №№6927069, 6914256, 6855202, 6709929, 6689338, 6500622, 6306736, 6225198, 6207392, 6114038, 6048616, 5990479, 5690807, 5571018, 5505928, 5262357 и в публикации на патент США №2003/0165951, а также в публикации РСТ №99/26299 (опубликованной 27 мая 1999 г.), радиоактивные изотопы (такие как3Н), хелаты металлов, такие как хелаты ионов радиоактивных или парамагнитных металлов, подобных Gd3+, DOTA и DPTA, и липосомы, ферменты, например пероксидаза хрена, щелочная фосфатаза, кислая фосфатаза, глюкозооксидаза, β-галактозидаза, β-глюкуронидаза или β-лактамаза, фермент в комбинации с хромогенным, флуорогенным или люминогенным соединением, которое генерирует детектируемый сигнал, например, поставляемым Invitrogen Corporation, Eugene Oreg.), хромогенные соединения (включая диаминобензидин (DAB), 4-нитрофенилфосфат (pNPP), прочный красный, бромхлориндолилфосфат (BCIP), нитросиний тетразолий (NBT), BCIP/NBT, прочный красный, АР оранжевый, АР голубой, тетраметилбензидин (ТМВ), 2,2'-азино-ди-[3-этилбензотиазолинсульфонат] (ABTS), о-дианизидин, 4-хлорнафтол (4-CN), нитрофенил-бета-D-галактопиранозид (ONPG), о-фенилендиамин (OPD), 5-бром-4-хлор-3-индолил-бета-галактопиранозид (X-Gal), метилумбеллиферил-бета-D-галактопиранозид (MU-Gal), пара-нитрофенил-альфа-D-галактопиранозид (PNP), 5-бром-4-хлор-3-индолил-бета-D-глюкуронид (X-Gluc), 3-амино-9-этилкарбазол (АЕС), фуксин, иоднитротетразолий (INT), тетразолий голубой и тетразолий фиолетовый, среди прочих).
Малые молекулы обнаружены напрямую или обнаружены в сочетании друг с другом. Например, если гаптен конъюгирован с квантовой точкой, то квантовая точка может быть обнаружена по его сигналу флуоресценции на характерной длине волны. В других случаях детектирование гаптена включает приведение образца в контакт с антителом к гаптену и детектируемой меткой и детектирование метки. В некоторых воплощениях детектируемая метка конъюгирована с антителом к гаптену для образования конъюгата (антитело к гаптену)-метка, и с гаптеном связывается конъюгат. В других случаях образец приводят в контакт с антителом к гаптену, которое связывается с гаптеном. Затем образец приводят в контакт с конъюгатом на основе антитела, способным связываться с антителом к гаптену, при этом конъюгат на основе антитела включает детектируемую метку или компонент системы детектируемых меток. В некоторых случаях компонентом системы детектируемых меток является фермент, такой как пероксидаза хрена или щелочная фосфатаза, который взаимодействует с хромогенным субстратом или комплексом субстрат/хромоген с образованием тем самым детектируемого хромогенного покрытия. В других примерах меткой является флуоресцентная метка, такая как квантовая точка. См. заявку WO 2012003476, которая тем самым включена во всей своей полноте.
Дополнительные средства для определения происхождения опухолевых образцов в смешанном гомогенате, который содержит образцы опухолей, полученные от разных субъектов, могут включать применение ДНК-штрихкодирования. ДНК-штрихкодирование является таксономическим методом, согласно которому в ДНК организма для его идентификации используют короткий генетический маркер. В сочетании с методами секвенирования ДНК следующего поколения существует возможность определения идентичности образца с точки зрения субъекта, из которого он происходит, путем обнаружения последовательности ДНК, которая является специфической для субъекта, из которого он происходит. Кроме того, возможно, что уникальная искусственная последовательность ДНК, не полученная непосредственно от субъекта, может быть конъюгирована с образцом, полученным от субъекта, перед объединением с другими опухолевыми образцами, имеющими другое происхождение, и что штрих-код этой уникальной искусственной ДНК можно прочитать позже путем анализа последовательности ДНК для определения происхождения исследуемого образца.
Аналогичным образом, дополнительный способ для идентификации субъекта с использованием смешанного гомогената, который содержит опухолевые образцы, происходящие от разных субъектов, или содержит другой образец, происходящий от того же субъекта, может включать применение аффинных меток (таких как метки, обычно используемые при выполнении лабораторных методик очистки белков, которые могут включать, но не ограничиваются этим, пептидные метки и белковые метки), которые конъюгированы с образцом среза опухоли. Аффинную метку можно идентифицировать в желаемый момент проведения анализов образцов для определения происхождения исследуемого образца аналогично принципу ДНК-штрихкодирования. Такие аффинные метки включают, но не ограничиваются этим, пептидные метки или белковые метки, такие как пента-гистидин, тетра-гистидин, глутатион-S-трансфераза, СВР, CYD (ковалентно присоединенный, но еще диссоциируемый пептид от NorpD), Strep II, FLAG, НРС (тяжелая цепь белка С), SUMO, AviTag, кальмодулиновая метка, полиглутаматная метка, E-tag, HA-tag, Мус-tag, S-tag, SBP-tag, Softag 1, Softag 3, TC tag, V5 tag, VSV-tag, Xpress tag, Isopeptag, MBP, SpyTag, BCCP, метка на основе зеленого флуоресцентного белка, halo-tag, Nus-tag, тиоредоксиновая метка, Fc-tag и Ту tag.
С использованием "смешанного" гомогената может быть выполнено любое число аналитических анализов, включая, но не ограничиваясь этим, окрашивание, иммуногистохимическое окрашивание, проточную цитометрию, FACS, сортировку флуоресцентно активированных капель, анализ изображений, гибридизацию, DASH, метод молекулярных маячков, удлинение праймеров, применение микрочипов, CISH, FISH, волоконную FISH, количественную FISH, проточную FISH, сравнительную геномную гибридизацию, блоттинг, вестерн-блоттинг, саузерн-блоттинг, истерн-блоттинг, фар-вестерн-блоттинг, сауз-вестерн-блоттинг, норз-вестерн-блоттинг и нозерн-блоттинг, ферментативные анализы, ELISA, анализы связывания лигандов, иммунопреципитацию, иммунопреципитацию хроматина (ChIP), ChIP-секв. (ChIP-секвенирование), технологию ChIP-чип, радиоиммуноанализы, поляризацию флуоресценции, резонансный перенос энергии флуоресценции (FRET), поверхностный плазмонный резонанс, анализы связывания на фильтрах, аффинную хроматографию, иммуноцитохимию, электрофоретические анализы, электрофорез нуклеиновых кислот, электрофорез в полиакриламидном геле, методы гель-электрофореза в нативных условиях, электрофорез со свободным потоком, изоэлектрическое фокусирование, иммуноэлектрофорез, анализы изменения электрофоретической подвижности, анализ полиморфизма длин рестрикционных фрагментов, зимографию, профилирование экспрессии генов, профилирование ДНК с использованием ПЦР, применение ДНК микрочипов, серийный анализ генной экспрессии, полимеразную цепную реакцию в режиме реального времени, дифференциальный дисплей с применением ПЦР, РНК-секв. (секвенирование РНК), масс-спектрометрию, детектирование метилирования ДНК, применение акустической энергии, основанные на изучении липидов анализы, определение количества иммунных клеток, детектирование ассоциированных с раком маркеров, аффинную очистку клеток конкретного типа, секвенирование ДНК, секвенирование следующего поколения, детектирование ассоциированных с раком слитых белков и детектирование маркеров устойчивости к химиотерапии.
Мультиплексные анализы часто, но не обязательно, используются в высокопроизводительных скрининговых исследованиях. Типичные методы мультиплексных анализов включают мультиплексные методы на основе нуклеиновых кислот (такие как применение ДНК микрочипов для изучения генной экспрессии или детектирования SNP; SAGE для генной экспрессии; высокопроизводительное секвенирование (такое как NGS); множественная ПЦР; мультиплексная зависящая от лигирования амплификация зондов (MLPA); секвенирование ДНК лигированием; основанное на использовании гранул мультиплексирование (например, технологию Luminex/LAMP)) и мультиплексные методы на основе белков (такие как применение белковых микрочипов, микрочипов для антител, микрочипов для антигенов, профилирование антител и основанное на использовании гранул мультиплексирование (например, технологию Luminex/LAMP)), а также другие мультиплексные методы (например, с применением тканевого микрочипа, клеточного микрочипа, микрочипа для химических соединений, анализ биомаркеров и ELISA).
Обзор других аналитических методов
Образец по настоящему изобретению, например, приготовленный любым из способов, описанных в данной заявке, может быть подвергнут стадиям дальнейшей обработки. Такие стадии включают, но не ограничиваются этим, применение других аналитических методов, таких как подробно изложенные в настоящей заявке, в том числе дополнительных диагностических анализов, подходящих для анализов гетерогенных материалов, содержащихся в репрезентативном образце опухоли. Вместе с образцами по изобретению можно применять следующие методологии, которые могут приводить к получению информации касательно идентичности и биологических свойств клеток, содержащихся в гетерогенной популяции опухолевых клеток. Применение объединенных анализов, приведенных в описании, и методов, описанных ниже, может позволить осуществить идентификацию, детектирование или определение характеристик даже минорных субклоновых популяций в опухоли. Эти результаты могут нести информацию, необходимую для диагностики, выбора способов лечения и ведения пациентов.
В типичных воплощениях репрезентативный образец по настоящему изобретению может быть подвергнут одному или более чем одному из следующих способов или стадий: окрашиванию, иммуногистохимическому окрашиванию, проточной цитометрии, FACS, сортировке флуоресцентно активированных капель, анализу изображений, гибридизации, DASH, методу молекулярных маячков, удлинению праймеров, применению микрочипов, CISH, FISH, волоконной FISH, количественной FISH, проточной FISH, сравнительной геномной гибридизации, блоттингу, вестерн-блоттингу, саузерн-блоттингу, истерн-блоттингу, фар-вестерн-блоттингу, сауз-вестерн-блоттингу, норз-вестерн-блоттингу и нозерн-блоттингу, ферментативным анализам, ELISA, анализам связывания лигандов, иммунопреципитации, ChIP, ChIP-секв., технологии ChIP-чип, радиоиммуноанализам, поляризации флуоресценции, FRET, поверхностному плазмонному резонансу, анализам связывания на фильтрах, аффинной хроматографии, иммуноцитохимии, электрофоретическим анализам, электрофорезу нуклеиновых кислот, электрофорезу в полиакриламидном геле, методам гель-электрофореза в нативных условиях, электрофорезу со свободным потоком, изоэлектрическому фокусированию, иммуноэлектрофорезу, анализам изменения электрофоретической подвижности, анализу полиморфизма длин рестрикционных фрагментов, зимографии, профилированию экспрессии генов, профилированиюе ДНК с использованием ПЦР, применению ДНК микрочипов, серийному анализу генной экспрессии, полимеразной цепной реакции в режиме реального времени, дифференциальному дисплею с применением ПЦР, РНК-секв., масс-спектрометрии, детектированию метилирования ДНК, применению акустической энергии, основанным на изучении липидов анализам, определению количества иммунных клеток, детектированию ассоциированных с раком маркеров, аффинной очистке клеток конкретного типа, секвенированию ДНК, секвенированию следующего поколения, детектированию ассоциированных с раком слитых белков и детектированию маркеров устойчивости к химиотерапии и Ki67, ДНК-плоидии или другому генотипическому или фенотипическому анализу. Ниже описаны типичные воплощения этих способов, которые предназначены для иллюстрации этих методов. Однако следует понимать, что могут быть применены варианты и альтернативы этих методологий и другие методологий.
Методы окрашивания
Жидкости можно применять для предварительной обработки (например, перекрестного сшивания белков, воздействия на нуклеиновые кислоты и т.д.), денатурации, гибридизации, промывки (например, промывки в жестких условиях), детектирования (например, для присоединения видимой или маркерной молекулы к зонду), амплификации (например, амплификации белков, генов и т.д.), контрастирующего окрашивания или тому подобного. В различных воплощениях такие вещества включают, без ограничения, растворы красящих веществ (например, растворы гематоксилина, растворы эозина или тому подобное), увлажняющие агенты, зонды, антитела (например, моноклональные антитела, поликлональные антитела и т.д.), жидкости для восстановления антигенов (например, водные или неводные растворы для демаскирования антигенов, буферы для восстановления антигенов и т.д.), растворители (например, спирт, лимонен или тому подобное) или тому подобное. Красящие вещества включают, без ограничения, красители, красящие вещества на основе гематоксилина, красящие вещества на основе эозина, конъюгаты антител или нуклеиновых кислот с детектируемыми метками, такими как гаптены, ферменты или флуоресцентные группировки, или другие типы веществ для придания окраски и/или для усиления контраста. См. заявки WO 2015197742 и WO 2015150278, каждая из которых тем самым включена посредством ссылки во всей своей полноте.
В методах окрашивания могут применяться системы и способы для получения в результате анализа большого количества информации наряду с запросом на предмет одного или более чем одного представляющего интерес признака, и перенесения касающейся морфологии информации из анатомического анализа на изображение, полученное из анализа с использованием окрашивания, например, иммуногистохимического (IHC) анализа, результаты которого обычно регистрируются вместе с результатами анатомического анализа, с целью локализации или определения соответствующих анализу признаков. Касающуюся морфологии информацию из анатомического анализа можно использовать для получения шаблона, который переносится на один или более чем один анализ с использованием обычного регистрируемого окрашивания или IHC анализ. Локализация представляющего интерес признака в IHC анализе может быть сопоставлена с анатомическим контекстом, обеспечиваемым данным шаблоном, с любыми представляющими интерес признаками, которые соответствуют выбранному анатомическому шаблону или обозначены как соответствующие для анализа. Кроме того, анатомический шаблон может быть распределен на несколько участков, и многие представляющие интерес признаки из многих IHC анализов могут быть сопоставлены с каждым из этих участков по отдельности. Следовательно, описанные системы и способы обеспечивают систематические, количественные и удобные подходы для проведения всестороннего мультиплексного анализа, преодолевая тем самым ограничения, присущие стадиям узкоспециализированного или субъективного визуального анализа в данной области техники. См. заявку WO 2015052128, которая тем самым включена посредством ссылки во всей своей полноте.
Обычно, образцы из раковых опухолей подвергают патологоанатомическому исследованию путем фиксации клеток на предметных стеклах для микроскопа и окрашивания их с использованием ряда методов окрашивания (например, с применением красящих веществ для морфологических или цитогенетических анализов). Затем окрашенные пробы оценивают на предмет присутствия или отсутствия аномальных или раковых клеток и исследуют морфологические особенности клеток. Несмотря на получение только общей информации, методы гистологического окрашивания являются самыми общепринятыми в настоящее время методами, применяемыми на практике для обнаружения раковых клеток в биологических образцах. Другие методы окрашивания, часто используемые для обнаружения рака, включают иммуногистохимическое окрашивание и окрашивание по активности. Эти способы основаны на детектировании присутствия или отсутствия конкретных антигенов или ферментативных активностей в раковых клетках. См. заявку WO 2012152747, которая тем самым включен посредством ссылки во всей своей полноте.
Описаны способы, наборы и системы для обработки образцов, содержащих затемняющие пигменты. Способ включает внесение осветляющего реагента в образец, в результате чего затемняющие пигменты в образце обесцвечиваются. Обесцвечивание затемняющих пигментов повышает возможности патологоанатомов при изучении образца. В иллюстративных воплощениях описан автоматизированный способ обработки образца, размещенного на подложке, применяемый для ослабления окрашивания затемнений, ассоциированных с пигментами в образце. Способ включает размещение подложки, на которую помещен образец, на автоматизированном приборе и внесение осветляющего реагента, в результате чего осветляющий реагент контактирует с образцом и пигменты в образце обесцвечиваются. Способ также включает внесение отмывающего реагента, в результате чего осветляющий реагент по существу удаляется из образца, и внесение хромогенного реагента, в результате чего образец приобретает специфическую окраску. Пигменты в образце обесцвечиваются под действием осветляющего реагента, в результате чего у квалифицированного специалиста появляется возможность интерпретировать специфически окрашенный образец. В других иллюстративных воплощениях описан набор для обесцвечивания затемняющих пигментов в образце. Набор включает флакон для реагентов и осветляющий реагент, хранящийся во флаконе для реагентов. Осветляющий реагент содержит водный раствор перекиси водорода, а конфигурация флакона для реагентов позволяет осуществлять оперативное подсоединение к автоматизированному устройству для окрашивания срезов таким образом, что автоматизированное устройство для окрашивания срезов будет осуществлять регулировку нанесения осветляющего реагента, вследствие чего осветляющий реагент будет контактировать с образцом. В следующих иллюстративных воплощениях описана система для ослабления специфического затемнения сигнала для гистопатологического образца, содержащего пигменты. Система включает автоматизированный прибор, осветляющий реагент и хромогенный реагент. Автоматизированный прибор выполнен с возможностью размещения гистопатологического образца, прикрепленного к подложке, доставки осветляющего реагента и хромогенного реагента к образцу и обеспечения нагревания и смешивания с осветляющим реагентом и хромогенным реагентом, доставляемыми к образцу. Осветляющий реагент выполнен с возможностью контактирования с гистопатологическим образцом и обесцвечивания затемняющих пигментов. Хромогенный реагент выполнен с возможностью контактирования с гистопатологическим образцом и выдачи специфического сигнала. См. заявку WO 2014056812, которая тем самым включена посредством ссылки во всей своей полноте.
Иммуноокрашивание и анализ ДНК in situ могут быть полезными инструментами в гистологической диагностике. Иммуноокрашивание может опираться на аффинность специфического связывания антител с эпитопами в образцах и возрастание доступности антител, специфически связывающихся с уникальными эпитопами, которые иногда присутствуют только в определенных типах пораженных клеток. Иммуноокрашивание может включать ряд стадий обработки, выполненных в отношении образца, размещенного на предметном стекле, для избирательного выявления определенных морфологических индикаторов болезненных состояний. В некоторых случаях стадии обработки могут включать предварительную обработку образца для ослабления неспецифического связывания, обработку антителом и инкубацию с ним, обработку вторичным антителом, меченным ферментом, и инкубацию с ним, осуществление взаимодействия субстрата с ферментом и контрастирующее окрашивание. В результате этого могут быть получены подсвеченные флуоресцентной или хромогенной меткой области образца, имеющего эпитопы, связывающиеся с антителом. В некоторых случаях анализ ДНК in situ опирается на аффинность специфического связывания зондов с нуклеотидными последовательностями в клетке или образцах. Иммуногистохимический (IHC) или иммуноцитохимический (ICC) анализ может включать визуализацию клеточного компонента in situ путем детектирования специфических взаимодействий антитело-антиген, при этом антитело мечено видимым маркером. IHC иногда называют детектированием антигенов в тканях, в то время как ICC иногда называют детектированием антигенов в или на культивируемых клетках (издание JAVOIS, Methods in Molecular Medicine, V. 115: Immunocytochemical Methods and Protocols, 2nd edition, (1999) Humana Press, Totowa, New Jersey, которое тем самым включено посредством ссылки во всей своей полноте), однако, методы, описанные как IHC или IIC, в равной степени могут быть пригодны для настоящего изобретения. Видимым маркером может быть флуоресцентный краситель, коллоидный металл, гаптен, радиоактивный маркер или фермент. Независимо от способа получения максимальный уровень сигнала с минимальным фоном или неспецифическим окрашиванием может быть желательными для обеспечения визуализации антигена. См. заявку WO 2013139555, которая тем самым включена посредством ссылки во всей своей полноте.
На основании проведенных ранее исследований можно полагать, что микроРНК играют роль в развитии регуляции и клеточной дифференцировки у млекопитающих, а также кардиогенезе и развитии лимфоцитов. Помимо этого, микроРНК вовлечены в другие биологические процессы, такие как гипоксия, апоптоз, дифференцировка стволовых клеток, пролиферация, воспаление и ответ на инфекцию. МикроРНК можно использовать для одновременного направленного воздействия на многочисленные эффекторы путей, вовлеченных в дифференцировку, пролиферацию и выживаемость клеток, ключевые характеристики онкогенеза. Некоторые микроРНК связаны с раком. Ввиду этого, проводимый in situ анализ микроРНК может быть полезен для диагностики рака и выбора терапевтических средств, поскольку микроРНК, по-видимому, действуют в качестве репрессоров онкогенов или опухолей. Например, многие опухолевые клетки имеют различающиеся картины экспрессии микроРНК при сравнении с нормальными тканями. В исследованиях с использованием мышей, генетически измененных с целью продуцирования избытка с-Мус, - белка, мутированные формы которого имеют отношение к нескольким раковым заболеваниям, - установили, что микроРНК влияет на развитие рака. Методы детектирования микроРНК, а также белка, транслируемого или иным образом регулируемого с участием микроРНК, являются востребованными, в частности, в автоматизированных методах для эффективного и быстрого детектирования. В применяемых ранее методах детектирования микроРНК не имеется одновременного детектирования микроРНК и ее экспрессируемых белков-мишеней (возможно регулируемых микроРНК) в одном и том же образце. В типичных методах обычно применяется основанное на использовании протеаз выдерживание клеток с целью расщепления клеточных компонентов для выявления нуклеиновых кислот-мишеней. Кроме того, в типичных методах для корреляции уровней микроРНК и уровней белка используют нозерн- и вестерн-блоттинг. Кроме того, можно применять молекулярные подходы, в которых образец "шинкуют и связывают" (grind and bind). Ранее были продемонстрированы подходы, основанные на использовании тканей. Как правило, эти способы включают стадию с применением ферментов. См. заявку WO 2013079606, которая тем самым включена посредством ссылки во всей своей полноте.
В описанных воплощениях может использоваться автоматизированный метод, в частности, подходящий для мультиплексного детектирования микроРНК и белков. В иллюстративных воплощениях экспрессия одного или более белков может регулироваться микроРНК. В другом воплощении способ позволяет идентифицировать клеточное окружение между микроРНК и белком. Способ может включать, например, использование автоматизированной системы для внесения в образец (а) реагентов, подходящих для детектирования микроРНК-мишени, (b) реагентов, подходящих для детектирования белковой мишени, и (с) реагентов, подходящих для окрашивания микроРНК-мишени и белковой мишени. Один из аспектов воплощений по настоящему изобретению относится к использованию выдерживания клеток без участия ферментов, т.е. к избеганию основанного на применении протеаз выдерживания клеток с целью сохранения белковых мишеней. Стадия выдерживания клеток может включать обработку образца раствором для выдерживания клеток, таким как буфер, имеющий слегка щелочное значение рН, включая буфер на основе триса, имеющий рН от примерно 7,7 до примерно 9, при температуре, превышающей температуру окружающей среды, в частности, от примерно 80°С до примерно 95°С. С использованием автоматизированного способа можно детектировать микроРНК- и белковые мишени одновременно или последовательно, хотя более удовлетворительные результаты окрашивания обычно получают, сначала выполняя детектирование и окрашивание на микроРНК, а затем выполняя детектирование и окрашивание на белковую мишень. Более конкретное описываемое воплощение сначала включает осуществление в отношении образца выдерживания клеток без участия ферментов. Затем образец приводят в контакт со специфически связывающейся с нуклеиновыми кислотами группировкой, выбранной для конкретной микроРНК-мишени, после чего осуществляют детектирование группировки, специфически связывающейся с микроРНК. Затем образец приводят в контакт со специфически связывающейся с белками группировкой, выбранной для белковой мишени, после чего осуществляют детектирование группировки, специфически связывающейся с данным белком. В некоторых воплощениях группировкой, специфически связывающейся с нуклеиновыми кислотами, является зонд на основе "закрытой" нуклеиновой кислоты (LNA), конъюгированной с детектируемой группировкой, такой как фермент, флуорофор, люминофор, гаптен, флуоресцентная наночастица или их комбинации. Некоторые подходящие гаптены являются общими в данной области техники, как например, дигоксигенин, динитрофенил, биотин, флуоресцеин, родамин, бромдезоксиуридин, мышиный иммуноглобулин или их комбинации. Другие подходящие гаптены были специально разработаны Ventana Medical Systems, Inc., включая гаптены, выбранные из оксазолов, пиразолов, тиазолов, бензофуразанов, тритерпенов, производных мочевины, производных тиомочевины, ротеноидов, кумаринов, циклолигнанов, гетеробиарилов, азоарилов, бензодиазепинов и их комбинаций. Детектирование гаптенов можно осуществлять, используя антитело к гаптену. В некоторых описанных воплощениях детектирование антитела к гаптену осуществляют посредством использования конъюгата антивидовое антитело-фермент, при этом фермент представляет собой любой подходящий фермент, такой как щелочная фосфатаза или пероксидаза хрена. См. заявку WO 2013079606, которая тем самым включена посредством ссылки во всей своей полноте.
Контрастирующее окрашивание представляет собой способ последующей обработки образцов после того, как они уже были окрашены с использованием агентов для детектирования одной или более мишеней, благодаря чему их структуры можно более легко визуализировать под микроскопом. Например, контрастирующее окрашивание возможно используют перед наложением покровного стекла, чтобы сделать иммуногистохимическое окрашивание отчетливым. Контрастирующее окрашивание отличается по цвету от первичного окрашивания. Хорошо известны многочисленные виды контрастирующего окрашивания, такие как окрашивание с использованием гематоксилина, эозина, метилового зеленого, метиленового синего, красителя Гимзы, альцианового синего, DAPI и ядерного быстрого красного. В некоторых примерах, для получения контрастирующего окрашивания можно смешать вместе красящие вещества в количестве более одного. Это обеспечивает гибкость применения и дает возможность выбирать красящие вещества. Например, первое красящее вещество может быть выбрано из смеси, которая обладает определенным свойством, но при этом не обладает другим желаемым свойством. Второе красящее вещество может быть добавлено к смеси, которая проявляет недостающее желаемое свойство. Например, для контрастирующего окрашивания могут быть смешаны вместе толуидиновый синий, DAPI и понтамин небесно-голубой. См. заявку WO 2012116949, которая тем самым включена посредством ссылки во всей своей полноте.
Гематоксилин представляет собой природное соединение, обнаруженное в красном ядре деревьев рода Hematoxylon. Сам гематоксилин в водном растворе является бесцветным и не является активным ингредиентом, который окрашивает компоненты тканей. Скорее, продукт окисления гематоксилина, гематеин, становится активным окрашивающим компонентом красящего раствора гематоксилина, в частности, после образования комплекса с закрепителем краски (mordant). Гематеин образуется естественным путем в результате воздействия воздуха и солнечного света. Естественный процесс называется "созреванием" и для получения раствора, подходящего для окрашивания клеток, может пройти 3 или более месяцев. В автоматизированных методиках и системах окрашивания применяются механические системы для доставки окрашивающих растворов к биологическому образцу. В стандартных методиках окрашивания гематеином применяли смешанный заранее концентрированный раствор, содержащий как гематоксилин/гематеин, так и закрепитель краски. См. заявку WO 2012096842, которая тем самым включена посредством ссылки во всей своей полноте.
Обычно при иммуноокрашивании выполняют ряд стадий обработки, проводимых на образце, размещенным на предметном стекле, для избирательного выявления определенных морфологических индикаторов болезненных состояний. Типичные стадии включают предварительную обработку образца с целью ослабления неспецифического связывания, обработку антителом и инкубацию с ним, обработку вторичным антителом, меченным ферментом, и инкубацию с ним, проведение взаимодействия субстрата с ферментом с получением флуорофора или хромофора, выявляющих области в образце, имеющие эпитопы, связывающиеся с антителом, контрастирующее окрашивание и тому подобное. Между каждыми из этих стадий проводят несколько стадий промывки для удаления непрореагировавшего остаточного реагента с предыдущей стадии. Процедуры инкубации выполняют при повышенных температурах, обычно при примерно 40°С, и образцы в типичном случае постоянно защищают от дегидратация. При проведении анализа ДНК in situ используют аффинность специфического связывания зондов с уникальными нуклеотидными последовательностями в образцах, и аналогичным образом он включает в себя ряд стадий процесса с применением различных реагентов и температуры. См. заявку WO 2011139976, которая тем самым включена посредством ссылки во всей своей полноте.
Иммуногистохимическое (IHC) окрашивание
Иммуногистохимическое или IHC окрашивание образца (или иммуноцитохимия, которая представляет собой окрашивание клеток), возможно является чаще всего применяемым методом иммуноокрашивания. В то время как в первых случаях применения IHC окрашивания использовали флуоресцентные красители (раздел Иммунофлуоресценция), в настоящее время применяют другие, нефлуоресцентные методы с использованием ферментов, таких как пероксидаза (см. раздел Иммунопероксидазное окрашивание) и щелочная фосфатаза. Эти ферменты способны катализировать реакции, в результате которых образуется окрашенный продукт, который легко детектировать с использованием световой микроскопии. Альтернативно, в качестве меток можно использовать радиоактивные элементы, а иммунную реакцию можно визуализировать с использованием авторадиографии. Подготовка или фиксация могут оказывать воздействие на сохранение морфологии и архитектуры клеток. Несоответствующая или длительная фиксация может значительно снижать связывающую способность антитела. Многие антигены могут быть успешно продемонстрированы в фиксированном в формалине образце. Детектирование многих антигенов можно улучшить посредством использования методов демаскирования антигенов, которые действуют путем разрушения некоторых перекрестных сшивок между белками, образуемых в результате фиксации, с выявлением скрытых антигенных сайтов. Это может быть достигнуто посредством нагревания в течение различных периодов времени (в случае индуцированной теплом демаскировки эпитопа или HIER) или с использованием ферментативного расщепления (в случае протеолитически индуцированной демаскировки эпитопа или PIER).
Иммуногистохимия (IHC) относится к методу определения присутствия или распределения антигена (такого как белок) в образце (таком как образец из раковой опухоли поджелудочной железы) посредством детектирования взаимодействия антигена со специфическим связывающимся агентом, таким как антитело. Образец, содержащий антиген (такой как целевой антиген), инкубируют с антителом в условиях, допускающих связывание антитела с антигеном. Детектирование связывания антитела с антигеном можно осуществить с использованием детектируемой метки, конъюгированной с антителом (непосредственное детектирование) или с использованием детектируемой метки, конъюгированной с вторичным антителом, которое вырабатывается в ответ на первичное антитело (например, с использованием опосредованного детектирования). Типичные детектируемые метки, которые можно использовать для IHC, включают, но не ограничиваются этим, радиоактивные изотопы, флуорохромы (такие как флуоресцеин, флуоресцеина изотиоцианат и родамин), гаптены, ферменты (такие как пероксидаза хрена или щелочная фосфатаза) и хромогены (такие как 3,3'-диаминобензидин или быстрый красный). В некоторых примерах IHC используют для детектирования присутствия или определения количества одного или более белков в образце, например, в образце из раковой опухоли поджелудочной железы. См. заявку WO 2013019945, которая тем самым включена посредством ссылки во всей своей полноте.
Иммуногистохимия или IHC, относится к методу локализации антигенов, таких как белок, в клетках образца и использованию антигенов для стимулирования специфического связывания антител с конкретными антигенами. Этот метод детектирования имеет то преимущество, что он позволяет точно показать, где заданный белок локализован в образце. Он также является эффективным методом исследования самих образцов. Применение малых молекул, таких как гаптены, для детектирования антигенов и нуклеиновых кислот стало значительным методом в IHC. Гаптены, в комбинации с антителами к гаптену, полезны для детектирования конкретных молекулярных мишеней. Например, специфически связывающиеся группировки, такие как первичные антитела и нуклеиновокислотные зонды, могут быть помечены одной или несколькими молекулами гаптена, и как только эти специфически связывающиеся группировки связываются со своими молекулярными мишенями, можно осуществить их детектирование с использованием конъюгата на основе антитела к гаптену, который включает фермент как часть основанной на использовании хромогена системы детектирования, или детектируемую метку, такую как флуоресцентная метка. Связывание конъюгата на основе детектируемого антитела к гаптену с образцом указывает на присутствие мишени в образце. Дигоксигенин, присутствующий исключительно в растениях наперстянка (Digitalis plants) в качестве вторичного метаболита, представляет собой пример гаптена, используемого в целом ряде молекулярных анализов. В патенте США №4469797 описывается применение иммуноанализов для определения концентраций дигоксина в образцах крови на основании специфического связывания антител к дигоксину с этим лекарственным средством в тестируемом образце. В патенте США №5198537 описывается ряд дополнительных производных дигоксигенина, которые были использованы в иммунологических тестах, таких как иммуноанализы. Для анализов образцов in situ, таких как иммуногистохимические (IHC) анализы и анализы гибридизации in situ (ISH), в особенности для мультиплексных анализов таких образцов, крайне желательно идентифицировать и разработать способы, которые обеспечивают получение желаемых результатов без помех от фона. Один такой способ включает применение тирамидной амплификации сигнала (TSA), в основе которой лежит запатентованное катализируемое осаждение репортера (CARD). В патенте США №6593100, который тем самым включен посредством ссылки во всей своей полноте, описывается усиление катализа фермента в способе с применением CARD или тирамидной амплификации сигнала (TSA) в результате взаимодействия меченого фенольного конъюгата с ферментом, при этом данное взаимодействие осуществляют в присутствии усиливающего реагента. См. заявку WO 2012003476, которая тем самым включена посредством ссылки во всей своей полноте, как и предшествующие публикации.
Можно использовать воплощения способов с применением конъюгатов на основе гаптена. В общем случае, способ может включать стадии а) иммобилизации пероксидазы на мишени в образце, при этом пероксидаза способна к взаимодействию с активирующей пероксидазу арильной группировкой, например, тирамином или производным тирамина, b) приведение в контакт образца с раствором, содержащим конъюгат на основе гаптена, при этом конъюгат на основе гаптена содержит гаптен, связанный с активирующей пероксидазу арильной группировкой, которая описана выше, и с) приведение в контакт образца с раствором, содержащим перекись, посредством чего конъюгат на основе гаптена взаимодействует с пероксидазой и перекисью с образованием ковалентной связи с иммобилизованной пероксидазой или в непосредственной близости от иммобилизованной пероксидазы; и d) определение места нахождения мишени в образце посредством детектирования гаптена. См. заявку WO 2012003476, которая тем самым включена посредством ссылки во всей своей полноте.
Расширительная микроскопия
Расширительная микроскопия (ЕхМ) дает возможность осуществлять метод оптической визуализации представляющих интерес биологических образцов, включая, но не ограничиваясь этим, клетки, ткани, ДНК, РНК или липиды, с более высоким разрешением по сравнению с дифракционным пределом классической микроскопии. ЕхМ позволяет выполнять физическое увеличение подвергнутых консервации биологических образцов, при этом в представляющие интерес биологические образцы посредством инфузии вводят состав (например, полимерный гель или гидрогель) в том объеме, в котором состав может быть введен в представляющие интерес образцы. Когда происходит изотропное расширение данного состава, биологические образцы или краситель (или флуорофор), присоединенный к образцам, будут увеличиваться в размере, позволяя тем самым осуществлять оптическую визуализацию биологических образцов или флуорофора с более высоким разрешением. В случае ЕхМ биологический образец сначала "окрашивают" меткой, используя стандартные методы, известные специалисту в данной области техники, например, FISH, иммуногистохимическое окрашивание. Затем образцы подвергают перфузии с использованием одного или более растворов желатина, например, растворов мономера, сшивающего агента или инициатора. В одном из воплощений растворы желатина содержат поддающиеся набуханию материалы. Как только завершается процесс гелеобразования, далее биологические образцы возможно подвергают расщеплению протеазами или другим химическим обработкам. Гель при набухании расширяется, что может быть достигнуто путем контакта с внешними факторами, такими как вода или тепло. Расширение геля приводит к физическому увеличению или расширению образцов или меток, встроенных в гель. Увеличение в размерах и/или расширение образцов или меток позволяет осуществлять оптическую визуализацию с гораздо более высокими разрешениями (например, в наномасштабе). ЕхМ применима к большому количеству биологических образцов, включая, но не ограничиваясь этим, белки, РНК, ДНК, липиды и те образцы, которые невозможно идентифицировать и определить место их нахождения с высоким разрешением с применением классической микроскопии. См. заявку США №14/627310, которая включена посредством ссылки во всей своей полноте.
Согласно настоящему изобретению предложен способ приготовления репрезентативного образца для микроскопии, включающий или, альтернативно, заключающийся по существу в или, кроме того, в основном заключающийся в заливке репрезентативного образца (например, композиции на основе гомогената) или его части поддающимся набуханию материалом. Термин "поддающийся набуханию материал", использованный в данном описании, относится к материалу, который расширяется при физическом воздействии, включая, но не ограничиваясь этим, контакт с водой, температуру (например, тепло), физическое растяжение и влажность. Поддающийся набуханию материал может расширяться в одном измерении, или в двух измерениях или в трех измерениях. В одном из воплощений поддающийся набуханию материал является прозрачным, вследствие чего после расширения через образец может проходить свет. В одном из воплощений поддающийся набуханию материал представляет собой поддающийся набуханию полимер или гидрогель. В одном из воплощений поддающийся набуханию материал образуется in situ из своих предшественников. Например, можно использовать один или несколько полимеризуемых материалов, мономеров или олигомеров, таких как мономеры, выбранные из группы, состоящей из водорастворимых групп, содержащих полимеризуемую группу с этиленовыми двойными связями. В предпочтительном воплощении поддающимся набуханию полимером является полиакрилат и сополимеры или их перекрестно сшитые сополимеры. Альтернативно или помимо этого, поддающийся набуханию материал может образовываться in situ путем перекрестного сшивания химическим путем водорастворимых олигомеров или полимеров.
Термин "полимеризуемый материал" относится к материалу, обладающему способностью к полимеризации, включая, но не ограничиваясь этим, мономер и олигомер. Термин "сшивающий агент" относится к молекуле, которая содержит два или более реакционно-способных конца, которые могут присоединяться химическим путем к конкретным функциональным группам (первичным аминам, сульфгидрильным группам и т.д.) на белках или других молекулах. В одном из воплощений полимеризацию олигомеров или мономеров вызывает сшивающий агент. Термин "инициатор полимеризации" относится к соединению или его аниону, которое(ый) взаимодействует с этиленоксидом способом, приводящим к его полимеризации. В некоторых воплощениях инициатором полимеризации является анион функциональной группы, которая инициирует полимеризацию этиленоксида.
В одном из воплощений способ также включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в увеличении в размере композиции на основе гомогената, посредством разбухания поддающегося набуханию материала. В другом воплощении способ заливки включает либо, альтернативно, заключается по существу в или, кроме того, в основном заключается в пропитывании гомогената составом, содержащим предшественники поддающегося набуханию материала, образовании поддающегося набуханию материала in situ и закреплении композиции на основе гомогената в поддающемся набуханию материале. Согласно одному из аспектов поддающийся набуханию материал образуется из предшественника поддающегося набуханию материала, при этом предшественник содержит полимеризуемый материал, инициатор полимеризации или сшивающий агент. Согласно другому аспекту полимеризуемым материалом является мономер или олигомер. В следующем воплощении мономер или олигомер содержит замещенный или незамещенный метакрилат, акрилат, акриламид, метакриламид, виниловый спирт, виниламин, аллиламин, аллиловый спирт или сшивающие их дивиниловые агенты (например, N,N-алкилена бисакриламиды).
Проточная цитометрия
Проточная цитометрия представляет собой основанную на использовании лазера биофизическую технологию, применяемую для подсчета клеток, сортировки клеток, детектирования биомаркеров и белковой инженерии, путем суспендирования клеток в потоке жидкости и пропускания их через электронное средство обнаружения. Она позволяет осуществлять одновременный мультипараметрический анализ физических и химических характеристик до нескольких тысяч частиц в секунду. Проточную цитометрию обычно используют в диагностике расстройств здоровья, в особенности в случаях рака крови, однако она имеет много других применений в фундаментальных исследованиях, клинической практике и клинических испытаниях. Общей составляющей является физическая сортировка частиц на основании их свойств с целью проведения очистки представляющих интерес популяций.
Сортировка флуоресцентно-активированных клеток (FACS)
Сортировка флуоресцентно-активированных клеток (FACS) представляет собой специальный тип проточной цитометрии. Она дает возможность осуществлять процесс сортировки гетерогенной смеси клеток в два или несколько контейнеров, по одной клетке за один раз, на основании специфического рассеяния света и флуоресцентных характеристик для каждой клетки. Она является полезным научным инструментом, поскольку обеспечивает быструю, объективную и количественную регистрацию флуоресцентных сигналов от отдельных клеток, а также физическое разделение представляющих особый интерес клеток. Суспензию клеток загружают в центр узкой, быстро текущей струи жидкости. Поток устроен таким образом, что между клетками образуется большое расстояние, зависящее от их диаметра. Вибрационный механизм заставляет струю с клетками разбиваться на отдельные капли. Систему настраивают таким образом, что вероятность нахождения в капле более одной клетки оказывается низкой. Прямо перед разбиванием струи на капли поток проходит через точку измерения флуоресценции, где выполняют измерения представляющих интерес характеристик флуоресценции для каждой клетки. Заряжающее кольцо помещают точно в ту точку, где струя разбивается на капли. Заряд наводят на кольцо непосредственно перед измерением интенсивности флуоресценции, и на капле, когда она выходит из струи, захватывается заряд противоположного знака. Затем заряженные капли попадают в систему электростатического отклонения, в которой происходит распределение капель по контейнерам на основании их заряда. В некоторых системах заряд прикладывают непосредственно к струе, и оторванная капля сохраняет заряд того же знака, что и струя. Затем, после отрыва капли, струю возвращают в нейтральное состояние.
Метод сортировки флуоресцентно активированных капель применительно к одиночным клеткам
Распределение одиночных клеток по каплям дает возможность проводить анализ белков, высвободившихся из клеток или секретируемых клетками, тем самым преодолевается одно из главных ограничений традиционной проточной цитометрии и сортировки флуоресцентно-активированных клеток. Примером этого подхода является анализ связывания для детектирования антител, секретированных из одиночных клеток мышиных гибридом. Секретированные антитела детектируют всего через 15 мин после совместного обособления одиночных клеток мышиных гибридом, флуоресцентного зонда и одиночных гранул, покрытых антителами к мышиному IgG, в каплях объемом 50 пл. Гранулы захватывают секретированные антитела, и когда захваченные антитела связываются с зондом, флуоресцентный зонд оказывается локализованным на этих гранулах, генерируя четко различимый сигнал флуоресценции при приблизительно 200 Гц, позволяющий осуществить сортировку капель, а также обогащение клеток. Описанная микрофлюидная система легко адаптируется для скрининга других внутриклеточных, находящихся на клеточной поверхности или секретируемых белков и для количественного определения каталитической или регуляторной активностей. В случае проведения скрининга примерно 1 миллиона клеток, микрофлюидные операции могут быть завершены за 2-6 ч; процесс целиком, включая подготовку микрофлюидных устройств и клеток млекопитающих, может быть завершен за 5-7 сут. См. работу Mazutis et al. (2013). "Single-cell analysis and sorting using droplet-based microfluidics". Nat. Protoc, 8: 870-891, которая тем самым включена посредством ссылки во всей своей полноте.
Анализ изображений
Анализ образцов может быть проведен с использованием систем и компьютеризованных методов автоматического обнаружения иммунных клеток, которые помогают в исследованиях клинического иммунного профиля. Автоматический метод обнаружения иммунных клеток включает в себя извлечение нескольких каналов изображения из многоканального изображения, такого как RGB (красный, зеленый, синий) изображение, или биологически значимого несмешанного изображения (biologically meaningful unmixed image). См. заявку WO 2015177268, которая тем самым включена посредством ссылки во всей своей полноте.
Можно использовать алгоритм и/или систему анализа изображений, который(ая) автоматически выдает иммунную оценку в баллах, исходя из набора изображений, полученных для предметных стекол в мультиплексном IHC анализе и/или на флуоресцентно окрашенных предметных стеклах. Алгоритм анализа изображений включает в себя компьютеризованный метод подсчета количества типов клеток в отдельном образце, который был окрашен в мультиплексном анализе, при этом алгоритм включает в себя: визуализацию образца, который был окрашен в мультиплексном анализе, в том числе детектирование маркеров лимфоцитов CD3, CD8, CD20, FoxP3 и опухолевых маркеров; не-смешивание (unmixing) изображения отдельного образца, который был окрашен в мультиплексном анализе в отдельных каналах изображения, для каждого маркера в мультиплексном анализе; идентификацию представляющих интерес участков в каждом канале изображения на основании информации об интенсивности (окрашивания) в каждом канале, при этом участки с низкой интенсивностью в каждом канале удаляют, а участки с высокой интенсивностью представляют собой сигналы от клеток; получение отдельного свернутого изображения (surrogated image), при этом данное свернутое изображение представляет собой комбинацию информации, содержащейся в каналах изображения, обо всех маркерах лимфоцитов; применение алгоритма обнаружения клеток, при этом алгоритм обнаружения клеток представляет собой алгоритм поиска мембран или алгоритм поиска ядер; идентификацию признаков лимфоцитов и комбинаций лимфоцитов в каждом канале изображения, или в изображении в объединенных канала, или в преобразованном изображении, таком как изображение в серых тонах, или изображение в поглощенном свете, или свернутое изображение; подготовку классификационного алгоритма на основании признаков известных лимфоцитов и комбинаций лимфоцитов; применение подготовленного алгоритма для характеристики лимфоцитов и комбинаций лимфоцитов в каждом канале изображения, или в каждом изображении объединенных каналов, или в преобразованном изображении, таком как изображение в серых тонах, или изображение в поглощенном свете, или свернутое изображение, которые были идентифицированы для классификации обнаруженных клеток, как например, по меньшей мере для одной из дающих ложноположительный сигнал клеток, Т-клеток только с CD3, Т-клеток с CD3 и CD8, Т-клеток с FP3, и В-клеток с CD20; подсчет количества разных классифицированных типов клеток; получение оценки в баллах для образца, при этом данная оценка в баллах основывается на подсчитанном количестве клеток каждого типа. См. заявку WO 2015124737, которая тем самым включена посредством ссылки во всей своей полноте.
Типичные воплощения настоящего изобретения могут включать применение систем и методов, которые включают в себя двухстадийный метод классификации. Действия, описанные в данной заявке, включают разделение WS изображения на множество участков и проведение первой классификации каждого участка с использованием "мягкой" классификации, такой как SVM, и формирование доверительной оценки в баллах (confidence score) и метки для каждого участка. Место нахождения каждого участка, его признаки и его тип, полученные в виде результата классификации, его доверительная оценка в баллах могут быть сохранены в базе данных. Вторая стадия классификации включает в себя сравнение участков с низкой доверительной оценкой с участками с высокой доверительной оценкой из базы данных и использование схожих участков для увеличения пространственной согласованности участков из базы данных. Другими словами, что касается каждого участка с низкой доверительной оценкой, то соседние участки с высокой доверительной оценкой вносят большие вклады в уточнение меток для каждого участка, что улучшает точность сегментации для участков с низкой доверительной оценкой. В противоположность существующим адаптивным/активным методам обучения для развития обучающихся баз данных, описанные действия меньше связаны с развитием одиночной обучающейся базы данных, а вместо этого сосредоточены на обработке каждого тестируемого изображения независимо, при одновременном адаптивном улучшении точности классификации на основании мечения доверительной информации (confidence information) для анализируемого изображения. Другими словами, для каждого изображения создается база данных надежно меченых участков, и для уточнения результатов классификации для участков с низкой доверительной оценкой выполняются операции поиска подобия в пределах изображения. См. заявку WO 2015113895, которая тем самым включена посредством ссылки во всей своей полноте.
Типичные воплощения настоящего изобретения могут включать применение способов детектирования и выставления оценки в баллах для экспрессии мезотелина (MSLN), как например, экспрессии белка MSLN. В конкретных примерах способы включают приведение в контакт образца, который содержит опухолевые клетки, с агентом, специфически связывающимся с белком MSLN (таким, как антитело). Типичные опухоли, которые экспрессируют MSLN, включают, но не ограничиваются этим, рак яичников, рак легкого (например, случаи немелкоклеточного рака легкого, NSCLC), рак поджелудочной железы и мезотелиому. Детектирование или оценку экспрессии белка MSLN в опухолевых клетках проводят, например, с использованием микроскопии и иммуногистохимии (IHC). Для оценки образца в отношении экспрессии белка MSLN используют шкалу от 0 до 3+. Например, определяют, окрашено ли по меньшей мере 10% опухолевых клеток (в частности, по меньшей мере примерно 10% опухолевых клеток) в образце специфичным к этому белку связывающимся агентом (например, обнаруживают детектируемую экспрессию белка MSLN). Образец оценивают баллом "нуль" в отношении экспрессии белка MSLN, если менее чем 10%> (как например, менее чем примерно 10%>) опухолевых клеток окрашивается этим специфически связывающимся агентом. Образец оценивают баллом 1+ в отношении экспрессии белка MSLN, если по меньшей мере 10% опухолевых клеток (как например, по меньшей мере примерно 10% опухолевых клеток) в образце окрашивается специфичным к этому белку связывающимся агентом (например, обнаруживают детектируемую экспрессию белка MSLN), но менее чем 10%> опухолевых клеток (как например, менее чем примерно 10%) окрашивается этим специфически связывающимся агентом с интенсивностью 2+ или выше. Образец оценивают баллом 2+ в отношении экспрессии белка MSLN, если по меньшей мере 10% опухолевых клеток (как например, по меньшей мере примерно 10% опухолевых клеток) в образце окрашивается специфичным к этому белку связывающимся агентом (например, обнаруживают детектируемую экспрессию белка MSLN) с интенсивностью 2+ или выше, а большинство окрашенных опухолевых клеток окрашивается с интенсивностью 2+. Образец оценивают баллом 3+ в отношении экспрессии белка MSLN, если по меньшей мере 10% опухолевых клеток (как например, по меньшей мере примерно 10% опухолевых клеток) в образце окрашивается специфичным к этому белку связывающимся агентом (например, обнаруживают детектируемую экспрессию белка MSLN) с интенсивностью 2+ или выше, а большинство окрашенных опухолевых клеток окрашивается с интенсивностью 3+, и по меньшей мере 10% опухолевых клеток (как например, по меньшей мере примерно 10% опухолевых клеток) в образце окрашивается специфичным к этому белку связывающимся агентом (например, обнаруживают детектируемую экспрессию белка MSLN) с интенсивностью 3+. Обзор приведен в Таблице 13 и на ФИГ. 20 в заявке WO 2015032695, которая тем самым включена посредством ссылки во всей своей полноте.
Гибридизация
Гибридизация in situ (ISH) включает приведение в контакт образца, содержащего нуклеиновую кислоту-мишень (геномную нуклеиновую кислоту-мишень в случае препарата хромосом в метафазе или интерфазе (такого как образец, размещенный на предметном стекле), с меченым зондом, например, способным к гибридизации или обладающим специфичностью к данной нуклеиновой кислоте-мишени (например, с одним или несколькими зондами, описанными в данной заявке). Предметные стекла возможно предварительно обрабатывают, например, для удаления материалов, которые могут мешать однородной гибридизации. И образец хромосомы, и зонд оба обрабатывают, например, путем нагревания с целью денатурации двухцепочечных нуклеиновых кислот. Зонд (приготовленный в подходящем для гибридизации буфере) и образец объединяют в условиях и в течение промежутка времени, достаточных для осуществления гибридизации (обычно до момента достижения равновесия). Препарат хромосом промывают для удаления избытка зонда и выполняют детектирование специфического мечения мишени, используя стандартные методы. См. заявку WO 2015124702, которая тем самым включена посредством ссылки во всей своей полноте.
В других методах детектирования раковых клеток используется наличие хромосомных аберраций в раковых клетках. В частности, делеция или увеличение числа копий целых хромосом или хромосомных сегментов и более высокие уровни амплификации определенных участков генома являются общими событиями при раке. Детектирование хромосомных аберраций часто выполняют с использованием цитогенетических способов, таких как окрашивание хромосом красителем Гимзы (дифференциальное G-окрашивание) или флуоресцентная гибридизация in situ (FISH). См. заявку WO 2012152747, которая тем самым включена посредством ссылки во всей своей полноте.
Описанная в настоящей заявке технология предоставляет улучшенные способы для повышения специфичности анализа молекулярных механизмов рака. Так, в некоторых воплощениях технология относится к многопараметрическому способу диагностики рака, при этом в результате применения указанного способа определяют наличие как молекулярных маркеров, так и фенотипических морфометрических маркеров на клеточном уровне в одиночной клетке или отдельном образце, содержащем клетки, причем указанный способ включает: а) получение данных о молекулярных маркерах из отдельного образца от субъекта, образца, содержащего одиночную клетку или одиночные клетки; b) получение количественных данных о морфологии клеток из той же одиночной клетки или тех же одиночных клеток, которые использованы на стадии (а), для проведения многопараметрического анализа указанного отдельного образца, для получения многопараметрического набора данных, содержащего как количественные данные о морфологии клеток со стадии (b), так и данные о молекулярных маркерах со стадии (а); и с) сравнение набора данных многопараметрического анализа, полученных на стадии (b), с набором данных референсного многопараметрического анализа, созданным посредством получения как данных о молекулярных маркерах, так и количественных данных о морфологии клеток из образцов раковой и нераковой клеток, взятых от индивидов с известным клиническим исходом.
Сравнение результатов стадии (с) обеспечивает получение предсказания клинического исхода для субъекта, определенного по специфической комбинации признаков и маркеров, статистически связанных с прогрессированием рака, частотой встречаемости, наличием метастазов или другим признаком клинического исхода, который можно найти в наборе данных референсного многопараметрического анализа. См. заявку WO 2012152747, которая тем самым включена посредством ссылки во всей своей полноте.
Типичные воплощения настоящего изобретения могут включать в себя применение технологии, обеспечивающей получение информации для определения прогноза патологических состояний при раке путем использования флуоресцентного мечения молекулярных маркеров, в сочетании со специализированными подходами к визуализации, включающими детектирование со спектральным разрешением и предварительную обработку данных. Данная технология предоставляет подход к визуализации, с использованием которого можно получить и проанализировать морфологию ядер в образце, который разработан для детектирования молекулярно специфичных зондов в образце, в течение одного цикла сбора данных. В этом подходе к визуализации используется сочетание технологий мечения, сбора, предварительной обработки и анализа. Многомерное изображение собирают и анализируют для разделения и различения разных представляющих интерес каналов обнаружения аналитов по длине волны излучения. Полученные в результате этого каналы обнаружения аналитов представляют различные аспекты данных, которые количественно характеризуют морфологическую и генетическую перестройку, экспрессию генов и/или экспрессию белков в клетке. См. заявку WO 2012152747, которая тем самым включена посредством ссылки во всей своей полноте.
Типичные воплощения настоящего изобретения могут включать в себя использование системы, способа и набора для визуализации ядра. Образец может быть предварительно обработан протеазой для пермеабилизации ядра и затем проинкубирован с конъюгатом наночастица/ДНК-связывающая группировка. ДНК-связывающая группировка включает по меньшей мере одну ДНК-связывающую молекулу. Конъюгат связывается с ДНК в ядре, и наночастицу визуализируют, визуализируя тем самым ядро. Для оценки характеристик ядра, таких как распределение хромосом, плоидность, форма, размер, характеристики структуры и/или зависящие от условий характеристики, используют компьютерные методы и методы анализа изображений. Применительно к образцу данный способ можно использовать в сочетании с другими мультиплексными тестами, включая флуоресцентную гибридизацию in situ. См. заявку WO 2012116949, которая тем самым включена посредством ссылки во всей своей полноте.
Флуоресцентная гибридизация in situ (FISH) представляет собой метод, который можно использовать для детектирования и локализации присутствия или отсутствия конкретных последовательностей ДНК в хромосомах. В случае FISH используются флуоресцентные зонды, которые связываются только с теми частями хромосомы, с которыми они демонстрируют высокую степень сходства последовательностей. FISH также можно использовать для детектирования конкретных последовательностей мРНК в образце. См. заявку WO 2012116949, которая тем самым включена посредством ссылки во всей своей полноте.
В данной области техники известны многочисленные методики для FISH, CISH и SISH. Например, методики осуществления FISH описаны в патентах США №№5447841, 5472842 и 5427932; метод CISH описан в патенте США №6942970, и дополнительные способы детектирования предложены в патенте США №6280929, описания которых включены в данное описание посредством ссылки во всей своей полноте. Чтобы улучшить чувствительность, разрешение или другие желательные свойства, вместе с методиками FISH, CISH и SISH можно применять многочисленные реагенты и схемы детектирования. Как обсуждалось выше, при проведении FISH можно выполнить непосредственное детектирование оптическими методами зондов, меченных флуорофорами (в том числе флуоресцентными красителями и квантовыми точками). Альтернативно, зонд может быть помечен нефлуоресцентной молекулой, такой как гаптен (как например, следующие неограничивающие примеры: биотин, дигоксигенин, DNP и различные оксазолы, пиразолы, тиазолы, нитроарилы, бензофуразаны, тритерпены, производные мочевины, производные тиомочевины, ротеноны, кумарин, соединения на основе кумарина, подофиллотоксин, соединения на основе подофиллотоксина и их комбинации), лиганд или другая опосредованно детектируемая группировка. Зонды, меченые такими нефлуоресцентными молекулами (и нуклеиновокислотные последовательности-мишени, с которыми они связываются), затем могут быть обнаружены путем приведения в контакт образца (например, образца клетки, с которым связывается зонд) с меченым детектирующим реагентом, таким как антитело (или рецептор либо другой специфически связывающийся партнер), специфичное к выбранному гаптену или лиганду. Детектирующий реагент может быть помечен флуорофором (например, квантовой точкой) или другой опосредованно детектируемой группировкой, либо может быть приведен в контакт с одним или несколькими дополнительными специфически связывающимися веществами (например, вторичными или специфичными антителами), которые в свою очередь могут быть помечены флуорофором. Возможно, детектируемую метку присоединяют непосредственно к антителу, рецептору (или другому специфически связывающемуся агенту). Альтернативно, детектируемую метку присоединяют к связывающемуся агенту через линкер, такой как гид рази д-тиоловый линкер, полиэтиленгликолевый линкер или любая другая гибкая соединительная группировка с сопоставимой реакционной способностью. Например, специфически связывающееся вещество, такое как антитело, рецептор (или другой антилиганд (anti-ligand)), авидин или тому подобное, может быть ковалентно модифицировано флуорофором (или другой меткой) с использованием гетеробифункционального полиалкиленгликолевого линкера, такого как гетеробифункциональный полиэтиленгликолевый (PEG) линкер. Гетеробифункциональный линкер объединяет две разные реакционноспособные группы, выбранные, например, из реакционноспособной в отношении карбонила группы, реакционноспособной в отношении амина группы, реакционноспособной в отношении тиола группы и фотореакционноспособной группы, при этом первая из них присоединяется к метке, а вторая из них присоединяется к специфически связывающемуся агенту. В других примерах зонд или специфически связывающийся агент (такой как антитело, например, первичное антитело, рецептор или другое связывающееся вещество) помечено ферментом, который способен к превращению флуорогенного или хромогенного соединения в детектируемый флуоресцентный, цветной или иным образом детектируемый сигнал (например, как при осаждении детектируемых металлических частиц при проведении SISH). Как указано выше, фермент может быть присоединен непосредственно или опосредованно через линкер к релевантному зонду или детектирующему реагенту. Примеры подходящих реагентов (например, связывающихся реагентов) и химических структур (например, линкеров и соединительных химических структур) описаны в публикации заявок на патент США №№2006/0246524, 2006/0246523 и 2007/0117153, описания которых включены в данное описание во всей своей полноте посредством ссылки. См. заявку WO 2015124702, которая тем самым включена посредством ссылки во всей своей полноте.
Способы по настоящему изобретению могут позволить осуществлять детектирование разных мишеней в количестве больше одной (например, 2, 3, 4 и т. д.). В некоторых воплощениях для каждой из мишеней могут быть использованы разные детектируемые метки и/или системы детектирования, благодаря чему каждую мишень можно детектировать по отдельности в одном образце. Можно использовать любую соответствующую детектируемую метку и/или систему детектирования. Более конкретно, в настоящем изобретении описываются системы для гибридизации in situ методом светлого поля. В некоторых воплощениях система содержит набор зондов, содержащий X уникальных 2'-O-метил-РНК зондов, специфичных к РНК-мишени, при этом X составляет число больше 2 (например, X равно 2, X равно 3, X равно 4, X равно 5 и т.д.), зонды направленно взаимодействуют с X различными участками в пределах данной РНК-мишени. Каждый 2'-O-метил-РНК зонд может быть конъюгирован по меньшей мере с одной детектируемой группировкой. Детектируемая группировка может быть адаптирована для связывания с реакционноспособной системой для конъюгирования с хромогеном (например, тирамидной системой для конъюгирования с хромогеном) с целью амплификации сигнала. В некоторых воплощениях каждый из 2'-O-метил-РНК зондов содержит от 15 до 30 нуклеотидов, от 20 до 50 нуклеотидов, от 40 до 80 нуклеотидов, от 20 до 100 нуклеотидов или от 20 до 200 нуклеотидов. См. заявку WO 2015124738, которая тем самым включена посредством ссылки во всей своей полноте.
Проба может представлять собой образец клеток молочной железы, обработанный в соответствии с протоколом гибридизации in situ (ISH). Протокол ISH может обеспечить осуществление визуализации специфических нуклеиновокислотных последовательностей (например, ДНК, мРНК и т.д.) в препаратах клеток посредством гибридизации комплементарных нитей нуклеотидов (например, зондов) с представляющей интерес последовательностью. Протокол ISH может включать, без ограничения, протокол двойной SISH и протокол красной ISH, протокол одиночной красной ISH, протокол одиночной SISH или тому подобное. См. заявку WO 2013113707, которая тем самым включена посредством ссылки во всей своей полноте.
Динамическая аллель-специфическая гибридизация (DASH)
При проведении генотипирования с использованием динамической аллель-специфической гибридизации (DASH) используют преимущества различий в температуре плавления ДНК, являющихся результатом нестабильности ошибочно спаренных пар оснований. Способ может быть в значительной степени автоматизирован и охватывает несколько простых принципов. На первой стадии, геномный сегмент амплифицируют и присоединяют к грануле с использованием ПЦР реакции с биотинилированным праймером. На второй стадии, амплифицированный продукт присоединяют к колонке с иммобилизованным стрептавидином и промывают раствором NaOH для удаления небиотинилированной нити. Затем добавляют аллель-специфические олигонуклеотиды в присутствии молекулы, которая флуоресцирует при связывании с двухцепочечной ДНК. Затем измеряют интенсивность флуоресценции по мере увеличения температуры до температуры плавления (Тпл). Наличие SNP приведет к получению более низкой Тпл, чем ожидалось. Поскольку генотипирование с использованием DASH представляет собой количественное измерение изменения Тпл, при его проведении можно определить наличие всех типов мутаций, а не только SNP. Другие преимущества DASH включают в себя возможность при ее проведении работать с немечеными зондами, простой дизайн и простые условия работы.
Метод молекулярных маячков
В методе молекулярных маячков используют специально сконструированный одноцепочечный олигонуклеотидный зонд. Олигонуклеотид сконструирован так, что имеются комплементарные участки на каждом конце и расположенная между ними последовательность зонда. Такой дизайн позволяет зонду принимать форму шпильки или петли-на-стебле, структуру в его естественном, выделенном состоянии. К одному из концов зонда присоединен флуорофор, а к другому концу - гаситель флуоресценции. Из-за наличия у зонда структуры "петля-на-стебле", флуорофор находится в непосредственной близости от гасителя, тем самым предотвращая испускание молекулой какой-либо флуоресценции. Молекула также сконструирована таким образом, что только последовательность зонда комплементарна геномной ДНК, которая будет использована в анализе (Abravaya et al. (April 2003). "Molecular beacons as diagnostic tools: technology and applications". Clin. Chem. Lab. Med., 41 (4): 468-74). Если последовательность зонда молекулярного маячка встречается во время анализа со своей целевой геномной ДНК, она будет отжигаться и гибридизоваться. Из-за определенной длины последовательности зонда, шпилечный сегмент зонда будет подвергаться денатурации с приоритетным образованием более длинного, более стабильного гибрида зонд-мишень. Это конформационное изменение позволяет флуорофору и гасителю освободиться от тесного соседства, обусловленного объединением в шпильку, давая возможность молекуле флуоресцировать. Если, с другой стороны, последовательность зонда встречает последовательность-мишень всего с одним некомплементарным нуклеотидом, молекулярный маячок будет предпочтительно оставаться в его природном состоянии в виде шпильки, и никакой флуоресценции не будет наблюдаться, поскольку флуорофор остается гашеным.
Удлинение праймеров
Удлинение праймеров представляет собой двухстадийный процесс, который сначала включает гибридизацию зонда с основаниями непосредственно вверх по течению от SNP-нуклеотида, за которой следует реакция "минисеквенирования", в которой ДНК-полимераза удлиняет гибридизованный праймер, добавляя основание, комплементарное SNP-нуклеотиду. Это встроенное основание детектируют и определяют SNP аллель (Syvanen, Nat. Rev. Genet., 2001 Dec, 2 (12): 930-42). Поскольку удлинение праймера основано на действии очень точного фермента ДНК-полимеразы, этот способ, как правило, является очень надежным. Методом удлинения праймеров можно генотипировать большинство SNP в очень схожих реакционных условиях, что делает его тоже очень гибким. Метод удлинения праймеров используют в ряде форматов анализа. В этих форматах применяется широкий диапазон методов детектирования, которые включают времяпролетную масс-спектрометрию с ионизацией посредством лазерной десорбции ионов из матрицы (MALDI-TOF масс-спектрометрию) (см. Sequenom) и ELISA-подобные методы. Как правило, имеется два основных подхода, в которых применяется встраивание либо флуоресцентно меченных дидезоксинуклеотидов (ddNTP), либо флуоресцентно меченных дезоксинуклеотидов (dNTP). При использовании ddNTP, зонды гибридизуются с ДНК-мишенью непосредственно вверх по течению от SNP нуклеотида и одиночный ddNTP, комплементарный SNP аллели, добавляют к 3'-концу зонда (отсутствие 3'-гидроксила в дидезоксинуклеотиде предотвращает дальнейшее добавление нуклеотидов). В каждый ddNTP вводят метку со своим флуоресцентным сигналом, что дает возможность детекции всех четырех аллелей в одной и той же реакции. В случае использования dNTP аллель-специфические зонды содержат на 3'-конце основания, которые комплементарны каждому из детально изученных SNP аллелей. Если ДНК-мишень содержит аллель, комплементарную основанию на 3'-конце зонда, то ДНК-мишень будет полностью гибридизоваться с зондом, давая возможность ДНК-полимеразе удлинять зонд с 3'-конца. Это детектируют посредством встраивания флуоресцентно-меченых dNTP на конец зонда. Если ДНК-мишень не содержит аллель, комплементарную основанию на 3'-конце зонда, то ДНК-мишень будет образовывать ошибочное спаривание на 3'-конце зонда и ДНК-полимераза будет не способна удлинять зонд с 3'-конца. Преимущество второго подхода заключается в то, что в растущую нить могут быть встроены несколько меченных dNTP, что позволяет усилить сигнал.
Микрочипы
Основным принципом, лежащим в основе применения микрочипов, является гибридизация между двумя нитями ДНК, свойство комплементарных нуклеиновокислотных последовательностей специфически формировать пары друг с другом посредством образования водородных связей между комплементарными парами нуклеотидных оснований. Наличие большого числа комплементарных пар оснований в нуклеотидной последовательности приводит к прочному нековалентному связыванию между этими двумя нитями. После отмывки неспецифически связанных последовательностей, только сильно спаренные нити будут оставаться гибридизованными. Флуоресцентно-меченные последовательности-мишени, которые связываются с последовательностью зонда, генерируют сигнал, который зависит от условий гибридизации (таких как температура) и промывки после гибридизации. Общая интенсивность сигнала, от пятна (признака), зависит от количества присутствующего в пятне целевого образца, связанного с зондами. Применение микрочипов позволяет произвести относительное количественное определение, при котором интенсивность признака сравнивают с интенсивностью того же самого признака в разных условиях, а идентичность признака узнают по его положению.
Массивы нуклеиновых кислот (также известные как олигонуклеотидные массивы, ДНК микрочипы, ДНК чипы, генные чипы или биочипы) стали мощным аналитическим инструментом. Массив нуклеиновых кислот по существу представляет собой системное распределение олигонуклеотидов на поверхности, например, по рядам и колонкам. Олигонуклеотиды могут быть либо физически, либо ковалентно прикреплены к поверхности. Один подход для физического прикрепления олигонуклеотидов к поверхности включает в себя сушку растворов олигонуклеотидов при их контакте с поверхностью. После сушки или фиксации иным образом, олигонуклеотиды удерживаются в "пятне" на поверхности. С использования подхода с сушкой началось получение массивов с очень низкой плотностью, получивших название "точечных блотов". Точечные блоты могут быть приготовлены посредством нанесения вручную капель растворов олигонуклеотидов на твердую поверхность и сушки. Большинство точечных блотов содержат менее 20 разных олигонуклеотидных пятен, расположенных в рядах и колонках. Продвигаясь дальше точечных блотов, в подходах с нанесением микроскопических пятен использовали механические или автоматизированные системы для создания множества микроскопических пятен. Небольшой размер пятен позволил значительно увеличить плотность нанесения пятен. Например, для нанесения от нескольких десятков до нескольких тысяч пятен на предметное стекло для микроскопа использовали нанесение микроскопических пятен. В соответствии с другим подходом, олигонуклеотиды напрямую синтезировали на носителе или подложке. Методы безмасочной фотолитографии и цифровой оптической химии (digital optical chemistry) представляют собой методы прямого синтеза нуклеиновых кислот на подложке; эти подходы были использованы для создания массивов очень высокой плотности (например, в патенте США №7785863, который тем самым включен посредством ссылки во всей своей полноте). Аналогичным образом, безмасочную фотолитографию использовали для производства пептидных массивов (см., например, работу Singh-Gasson et al. Maskless fabrication of light-directed oligonucleotide microarrays using a digital micromirror array. Nat. Biotechnol., 1999, 17: 974-978, которая тем самым включена посредством ссылки во всей своей полноте). Была использована цифровая оптическая химия, с помощью которой создают массивы с миллионами отдельных областей, каждая из которых содержит популяцию уникальных олигонуклеотидов. Нуклеиновокислотные и пептидные массивы включают в себя массив областей (называемых в настоящем описании "точками") на поверхности носителя, при этом каждая область разработана для конкретного олигонуклеотида или пептида. "Плотность массива" представляет собой по существу количество рядов и колонок точек, распределенных в данной области. Массив высокой плотности содержит большее количество рядов и колонок в заданной области. По мере развития индустрии массивов нуклеиновых кислот и пептидов, доступность массивов высокой плотности также возросла. По мере увеличения количества точек в заданной области, размер каждой точки уменьшается. Например, одна точка в массиве, содержащем миллионы уникальных олигонуклеотидов или пептидов, распределенных по площади предметного стекла микроскопа, будет составлять приблизительно 100 пм2. Небольшой размер этого точки создает технические проблемы при считывании и понимании результатов использования такого массива. Например, хотя точку размером 100 пм2 можно визуально наблюдать в отдельности, люди не могут без увеличения визуально различать две или более точек размером 100 пм2, расположенных в непосредственной близости друг от друга. Таким образом, производство и применение массивов высокой плотности продвинулось до такой степени, что пользователи уже не могут больше считывать данные с массива визуально. Поскольку массивы содержат огромное количество (несколько миллионов) близко расположенных точек на небольшой площади, сложные визуализирующие устройства детектируют сигналы от массива и для интерпретации данных используют программное обеспечение. Кроме того, могут быть использованы высоко чувствительные способы детектирования. Визуализация флуоресценции, являющаяся высоко чувствительным методом, стала стандартным подходом для детектирования связанных с гибридизацией событий. Для визуализации флуоресценции этих массивов, как правило, используются микроскопы, оборудованные фильтрами и камерами. Флуоресценцию обычно невозможно визуально разрешить без помощи этих приборов. Очень сложные полученные с использованием флуоресценции изображения обрабатывают с применением программного обеспечения, поскольку объем данных очень большой и его представление не является понятным. Например, в патенте США №6090555 авторов Fiekowsky и др. описывается сложный способ, включающий компьютерное выравнивание и устранение искажений, полученных с использованием флуоресценции изображений, полученных из массива нуклеиновых кислот. Несмотря на то, что способность проводить широкомасштабные параллельные геномные или протеомные исследования имеет большое значение, применимость массивов нуклеиновых кислот и пептидов была ограничена ввиду трудности детектирования и расшифровки касающихся связывания событий. Кроме того, применение флуоресценции создает множество препятствий в плане общей применимости массивов из-за ухудшения сигналов флуоресценции со временем и сложности сопутствующего оборудования для детектирования флуоресценции. Настоящее изобретение относится к устройству и способу использования данного устройства для детектирования молекул-мишеней, устройства, включающего в себя олигонуклеотидный или пептидный массив. Данное устройство включает множество связывающих молекул, соединенных с поверхностью носителя. Связывающие молекулы разработаны так, что они связываются с молекулой-мишенью. Связывание мишени и связывающих молекул может быть идентифицировано посредством изучения с использованием устройства. В некоторых воплощениях устройство позволяет осуществлять детектирование события гибридизации между нуклеиновой кислотой-мишенью и иммобилизованным олигонуклеотидом. В других воплощениях данное устройство позволяет осуществлять детектирование события связывания между полипептидом-мишенью и иммобилизованным пептидом. В иллюстративных воплощениях устройство содержит носитель по меньшей мере с одной поверхностью и множество иммобилизованных олигонуклеотидов или пептидов, связанных с данной поверхностью носителя, при этом множество иммобилизованных олигонуклеотидов или пептидов структурировано на поверхности носителя с образованием по меньшей мере одного оптически дешифруемого образца. См. заявку WO 2013110574, которая тем самым включена посредством ссылки во всей своей полноте.
Типичные воплощения настоящего изобретения могут включать использование устройства для детектирования одного или более соединений-мишеней. Один тип представляющего особый интерес соединения-мишени представляют собой нуклеиновые кислоты-мишени или олигонуклеотиды-мишени. Другой тип представляющего особый интерес соединения-мишени представляют собой полипептиды-мишени. Для воплощений настоящего изобретения, включая иммобилизованные олигонуклеотиды, нуклеиновые кислоты-мишени обычно понимают как типичные молекулы-мишени. Однако, среднему специалисту в данной области техники известно, что иммобилизованные олигонуклеотиды обеспечивают получение связывающего партнера для олигонуклеотид-связывающейся группировки конъюгатов, которые дают возможность детектировать множество других соединений-мишеней. Например, используя иммобилизованный олигонуклеотид, конъюгат антитело-олигонуклеотид можно иммобилизовать в устройстве для превращения данного устройства в микрочип для антител. Микрочип для антител может быть использован для детектирования представляющей интерес белковой мишени. Аналогичным образом, для воплощений, которые включают иммобилизованные пептиды, типичные молекулы-мишени могут включать антитела, белки или ферменты. Однако, соответствующие пептиды также могут быть модифицированы с использованием конъюгатов с пептид-связывающейся группировкой и молекулярной направляющей группировкой. Кроме того, хотя в настоящем изобретении конкретно раскрываются иммобилизованные олигонуклеотиды и пептиды, это всего лишь типичные иммобилизованные детектирующие группировки. Имеется много других полезных иммобилизованных детектирующих группировок, которые могут быть введены в устройство, как изложено в данном описании, без отклонения от изложенной в данном описании концепции. Например, детектирующие группировки могут включать аптамеры, лиганды, хелаторы, углеводы и их созданные человеком эквиваленты. См. заявку WO 2013110574, которая тем самым включена посредством ссылки во всей своей полноте.
Методы выделения СТС могут включать применение антител, специфичных к ЕрСАМ, ERG, PSMA или их комбинации. Выделенные СТС наносят на предметное стекло или другую подложку и проводят фиксацию (например, используя методы, известные в данной области техники). Новые способы распределения с использованием специфичных к антигенам предстательной железы антителам, которые обсуждаются в данном описании, также можно использовать для выделения СТС и нанесения их на подложку, такую как предметное стекло, до осуществления фиксации. Размещенные и фиксированные СТС затем приводят в контакт с одним или несколькими нуклеиновокислотными зондами, специфичными к ERG, PTEN и CEN-10, например в условиях, достаточных для того, чтобы нуклеиновокислотные зонды гибридизовались с комплементарной им последовательностью в СТС. Нуклеиновокислотные зонды помечены, например, одной или более квантовыми точками. Например, нуклеиновокислотный(е) зонд(ы), специфичный(ые) к ERG, PTEN и CEN-10, может(гут) быть помечен(ы) разными квантовыми точками, чтобы можно было отличить зонды друг от друга. После гибридизации нуклеиновокислотных зондов с ERG, PTEN и CEN-10 сигналы от одной или более квантовых точек на одном или более нуклеиновокислотных зондах детектируют, например, с использованием спектральной визуализации. Затем сигналы анализируют, чтобы определить, были ли в выделенных СТС один или более ERG перегруппированы, были ли делетированы один или более генов PTEN и детектируется ли CEN-10. Исходя из того, перегруппированы ли один или более ERG, делетированы ли один или более генов PTEN и детектируется ли CEN-10, характеризуют рак предстательной железы. См. заявку WO 2013101989, которая тем самым включена посредством ссылки во всей своей полноте.
Хромогенная гибридизация in situ (CISH)
Хромогенная гибридизация in situ (CISH) представляет собой цитогенетический метод, который объединяет метод детектирования хромогенного сигнала иммуногистохимических (IHC) методов с гибридизацией in situ. Он был разработан приблизительно в 2000 году в качестве альтернативы флуоресцентной гибридизации in situ (FISH) для детектирования амплификации онкогена HER-2/neu. Метод CISH похож на FISH тем, что оба этих метода представляют собой методы гибридизации in situ, применяемые для детектирования присутствия или отсутствия конкретных участков ДНК. Однако, применение CISH в диагностических лабораториях является гораздо более практичным, потому что в этом методе используются светлопольные микроскопы, а не более дорогие и сложные флуоресцентные микроскопы, используемые в FISH.
Конструкция зондов для CISH может быть очень похожа на таковую для FISH с различиями в используемых метках и способах детектирования. FISH зонды, как правило, метят разными флуоресцентными метками и их можно детектирвать только под флуоресцентным микроскопом, в то время как CISH зонды метят биотином или дигоксигенином и их можно детектировать с использованием светлопольного микроскопа после применения других стадий обработки. Длина CISH зондов составляет приблизительно 20 нуклеотидов и они разрабатываются для ДНК-мишеней. Они комплементарны последовательности-мишени и связываются с ней после стадии денатурации и гибридизации. Только незначительное количество CISH зондов имеется в продаже, поэтому для большинства применений их необходимо выделять, амплифицировать, секвенировать, метить и картировать из бактериальных искусственных хромосом (ВАС). ВАС были разработаны во время выполнения проекта Геном человека, поскольку было необходимо в целях секвенирования выделить и амплифицировать короткие фрагменты человеческой ДНК. В настоящее время ВАС могут быть отобраны и расположены в геноме человека с использованием общедоступных баз данных, таких как UCSC Genome Browser. Это обеспечивает комплементарность и специфичность последовательностей. ДНК выделяют из клонов ВАС и амплифицируют с использованием метода, основанного на применении полимеразы, такого как праймированная вырожденными олигонуклеотидами ПЦР ((DOP)-ПЦР). Далее последовательности из клонов секвенируют и их положение в геноме определяют. Введение метки в зонды может быть осуществлено с использованием либо случайного праймирования, либо ник-трансляции для встраивания биотина или дигоксигенина.
Приготовление образцов, гибридизация зондов и детектирование: образец может включать хромосомы в интерфазе или метафазе. Образцы надежно прикрепляют к поверхности, такой как поверхность предметного стекла. Образец можно подвергнуть расщеплению пепсином для обеспечения доступа к мишени. Добавляют 10-20 мкл раствора зонда, образец покрывают покровным стеклом, которое герметично закрывают резиновым клеем и предметное стекло нагревают до 97°С в течение 5-10 минут для денатурации ДНК. Затем предметное стекло помещают на ночь в сушильный шкаф на 37°С, чтобы зонд мог гибридизоваться. На следующий день образец промывают и применяют блокатор неспецифических сайтов связывания белка. Если будет использоваться пероксидаза хрена (HRP), образец должен быть проинкубирован в перекиси водорода для подавления эндогенной пероксидазной активности. Если в качестве зондовой метки использовали дигоксигенин, то далее применяют конъюгированное с флуоресцеином первичное антитело к дигоксигенину, после чего применяют конъюгированное с HRP вторичное антитело к флуоресцеину. Если в качестве зондовой метки использовали биотин, то сначала сайты неспецифического связывания должны быть блокированы с использованием бычьего сывороточного альбумина (BSA). Затем, для детектирования используют конъюгированный с HRP стрептавидин. HRP затем превращает диаминобензидин (DAB) в нерастворимый коричневый продукт, который может детектировать на светлопольном микроскопе при 40-60-кратном увеличеним. Чтобы сделать продукт более заметным, можно использовать контрастирующее окрашивание, как, например, с применением гематоксилина и эозина.
Молекулярные цитогенетические методы, такие как хромогенная гибридизация in situ (CISH), объединяют визуальную оценку хромосом (кариотипический анализ) с молекулярными методами. Молекулярные цитогенетические методы основаны на гибридизации нуклеиновокислотного зонда с комплементарной ему нуклеиновой кислотой в клетке. Зонд для конкретного хромосомного участка будет распознавать комплементарную ему последовательность и гибридизоваться с ней в метафазной хромосоме или в интерфазном ядре (например, в образце). Были разработаны зонды для различных диагностических и исследовательских целей. Специфичные к последовательностям зондов (sequence probes) гибридизуются с последовательностями единичной копии ДНК в конкретном участке хромосомы или гене. Эти зонды используются для идентификации критического участка хромосомы или гена, связанных с представляющим интерес синдромом или состоянием. На метафазных хромосомах такие зонды гибридизуются с каждой хроматидой, обычно давая два небольших, дискретных сигнала на одну хромосому. Гибридизация специфичных к последовательностям зондов, таких как истощенные по повторам зонды (repeat depleted probes) или зонды с уникальной последовательностью, позволяет выявить нарушения в хромосомах, связанные со многими заболеваниями и синдромами, включая конститутивные генетические аномалии, такие как синдромы с потерей части хромосомы, транслокации хромосом, амплификация генов, и связанные с анеуплоидией синдромами, неопластическими заболеваниями, а также инфекциями, вызываемыми патогенами. Чаще всего эти методы применимы к стандартным цитогенетическим препаратам на предметных стеклах для микроскопа. В дополнение к этому, эти методики можно использовать на предметных стеклах с фиксированными клетками или другими ядерными изолятами. Например, эти методы часто используют для того, чтобы охарактеризовать опухолевые клетки в плане как диагностики, так и прогноза рака. Многочисленные хромосомные нарушения были связаны с развитием рака (например, анеуплоидии, как, например, трисомия 8, ассоциированная с определенными миелоидными расстройствами; транслокации, как, например, перегруппировка BCR/ABL при хроническом миелогенном лейкозе; и амплификации конкретных нуклеиновокислотных последовательностей, ассоциированные с неопластической трансформацией). Молекулярные методы могут дополнять стандартное цитогенетическое тестирование, связанное с детектированием и определением характеристик таких приобретенных хромосомных нарушений. Внедрены системы для двойной окраски при проведении CISH. Они включают систему DuoCISH™ Dako и систему ZytoDot® 2С Zyto Vision. В обеих этих системах применяются отдельные ферменты (щелочная фосфатаза и пероксидаза хрена) для этих двух стадий детектирования окраски.
Настоящее изобретение относится к системам и способам хромогенной гибридизации in situ (CISH) и, в частности, к способам, которые предотвращают перекрестное взаимодействие между двумя или более системами детектирования окраски в одном анализе, и также относится к способам оценки результатов анализов, в которых применяются разделенные на части зонды (break-apart probes). См. заявку WO 2011133625, которая тем самым включена во всей своей полноте.
Флуоресцентная гибридизация in situ (FISH)
Флуоресцентная гибридизация in situ (FISH) представляет собой цитогенетический метод, в котором используются флуоресцентные зонды, связывающиеся только с теми частями хромосомы, которые имеют высокую степень комплементарности последовательности. Он был разработан исследователями в области биомедицины в начале 1980-х годов и используется для детектирования и определения присутствия или отсутствия конкретных последовательностей ДНК в хромосомах. Для выяснения того, где флуоресцентный зонд связан с хромосомами, можно использовать флуоресцентную микроскопию. FISH часто используют для обнаружения специфических особенностей ДНК при генетических консультациях, в медицине и идентификации видов. FISH также можно использовать для детектирования и определения местонахождения конкретных РНК-мишеней (такие как мРНК, длинные некодирующие РНК (IncRNA) и микроРНК) в клетках, циркулирующих опухолевые клетках и образцах. В этом контексте, данный метод может помочь в определении пространственно-временных закономерностей генной экспрессии в клетках.
Зонды: РНК и ДНК. РНК зонды могут быть разработаны для любого гена или любой последовательности в гене для визуализации мРНК, IncRNA и микроРНК в клетках. FISH используют для исследования репродуктивного клеточного цикла, в частности интерфазы ядра, связанного с любыми хромосомными нарушениями. Этот метод (FISH) позволяет намного легче осуществлять анализ большой серии архивных случаев с целью идентификации точно указанной хромосомы путем создания зонда на основе искусственной хромосомы, который будет "привлекать" аналогичные хромосомы. Детектируют сигналы гибридизации для каждого зонда в случае нарушений в ядре. Каждый зонд для детектирования мРНК и IncRNA состоит из 20 олигонуклеотидных пар, каждая пара перекрывает пространство 40-50 п.о. Для детектирования микроРНК используют зонды, полученные с применением запатентованных химических операций для специфического детектирования микроРНК, и они перекрывают всю последовательность микроРНК. Зонды часто происходят из фрагментов ДНК, которые выделяли, очищали и амплифицировали для применения в проекте Геном человека. Размер генома человека настолько велик в сравнении с длиной, которая может быть секвенирована непосредственно, что было необходимо разделять геном на фрагменты. (В конечном анализе, порядок следования этих фрагментов определяли посредством расщепления копии каждого фрагмента на более мелкие фрагменты с использованием специфичных к последовательности эндонуклеаз, измерения размера каждого небольшого фрагмента с использованием гель-проникающей хроматографии и использования этой информация для определения того, где большие фрагменты перекрывались друг с другом). Чтобы сохранить фрагменты с их индивидуальными последовательностями ДНК, эти фрагменты добавляли в систему постоянно реплицирующихся популяций бактерий. Клоны бактерий, где каждая популяция поддерживает единственную искусственную хромосому, сохраняют в различных лабораториях по всему миру. Искусственные хромосомы (ВАС) могут быть "выращены", выделены и помечены в любой лаборатории. Размер этих фрагментов составляет примерно 100 тысяч пар оснований, и они являются основой для большинства FISH зондов.
Способ получения и гибридизации для РНК. Чтобы обеспечить доступ к мишени, клетки можно подвергнуть пермеабилизации. FISH также успешно выполняется на нефиксированных клетках. Специфичный к мишени зонд, состоящий из 20 пар олигонуклеотидов, гибридизуется с РНК-мишенью(ями). Отдельные, но совместимые системы амплификации сигнала позволяют проводить мультиплексный анализ (до двух мишеней в одном анализе). Амплификации сигнала достигают в результате серии последовательных стадий гибридизации. По окончании анализа образцы визуализируют под флуоресцентным микроскопом.
Способ получения и гибридизации для ДНК. Сначала конструируют зонд. Зонд должен быть достаточно большим, чтобы специфически гибридизоваться со своей мишенью, но не настолько большим, чтобы затруднять процесс гибридизации. Зонд помечен непосредственно флуорофорами, мишенями для антител или биотином. Мечение может быть выполнено различными путями, такими как ник-трансляция или ПЦР с использованием меченых нуклеотидов. Затем получают препарат интерфазных или метафазных хромосом. Хромосомы прочно прикрепляют к подложке, обычно к стеклу. Повторяющиеся последовательности ДНК должны быть блокированы посредством добавления коротких фрагментов ДНК к образцу. Затем зонд добавляют к хромосомной ДНК и инкубируют в течение приблизительно 12 часов для прохождения гибридизации. За несколько стадий промывки удаляются все негибридизованные или частично гибридизованные зонды. Затем результаты визуализируют и выполняют количественное определение с использованием микроскопа, с помощью которого можно возбуждать краситель и регистрировать изображения. Если сигнал флуоресценции является слабым, может быть необходима амплификация сигнала, чтобы превысить порог детектирования для микроскопа. Интенсивность сигнала флуоресценции зависит от многих факторов, таких как эффективность мечения зонда, тип зонда и тип красителя. Флуоресцентно меченые антитела или стрептавидин связывают с молекулой красителя. Эти вторичные компоненты выбирают такими, чтобы они имели сильный сигнал.
Волоконная FISH
В альтернативном методе изучения препаратов интерфазных или метафазных хромосом, волоконной FISH, интерфазные хромосомы присоединяют к предметному стеклу таким образом, что они растягиваются по прямой линии, а не являются плотно свернутыми, как в традиционной FISH, или не принимают занимаемую хромосомами конформацию, как при интерфазной FISH. Это достигается посредством приложения механического воздействия (shear) вдоль предметного стекла или к клеткам, которые были фиксированы на предметном стекле и затем лизированы, или к раствору очищенной ДНК. Для этой цели все чаще используют метод, известный как растягивание хромосом. Вытянутая конформация хромосом позволяет получить значительно более высокое разрешение, вплоть до нескольких тысяч пар нуклеотидов.
Количественная FISH (Q-FISH)
Количественная флуоресцентная гибридизация in situ (Q-FISH) представляет собой цитогенетический метод, в основе которого лежит традиционная методология FISH. В методе Q-FISH используются меченные (с использованием Су3 или FITC) имитаторы синтетической ДНК, называемые олигонуклеотидами пептидо-нуклеиновой кислоты (PNA), для количественного определения последовательностей-мишеней в хромосомной ДНК с использованием флуоресцентной микроскопии и аналитического программного обеспечения.
Проточная FISH
Проточная FISH представляет собой цитогенетический метод количественного определения числа копий конкретных повторяющихся элементов в геномной ДНК в целой клеточной популяции посредством сочетания протоколов проточной цитометрии с протоколами цитогенетического окрашивания при флуоресцентной гибридизации in situ. Метод проточной FISH впервые был опубликован Rufer и др. в 1998 г. как модификация другого метода - метода анализа длины теломеров, Q-FISH, в котором используется пептидо-нуклеиновокислотные зонды с последовательностью 3'-СССТААСССТААСССТАА-5', меченые флуорофором флуоресцеином, для окрашивания теломерных повторов на приготовленных метафазных распределенных по поверхности клеток, которые были обработаны колцемидом, подвергнуты гипотоническому шоку и фиксированы на предметных стеклах посредством обработки метанолом/уксусной кислотой (протокол доступен в режиме онлайн). Изображения полученных флуоресцентных пятен затем могут быть проанализированы с использованием специализированной компьютерной программы (способ и программное обеспечение, поставляемые Flintbox Network), с получение количественных данных, касающихся флуоресценции, которые затем могут быть использованы для оценки фактической длины теломер. Флуоресценцию, полученную в результате окрашивания зондом, считают количественной, потому что PNA связывается преимущественно с ДНК при низких концентрациях ионов соли и в присутствии формамида, поэтому ДНК-дуплекс может не восстанавливаться после того, как он был расплавлен и отожжен с зондом PNA, что позволяет зонду насыщать свою повторяющуюся последовательность-мишень (поскольку он не вытесняется из целевой ДНК-мишени конкурирующей антисмысловой ДНК на комплементарной нити), тем самым, обеспечивая надежные и поддающиеся количественному измерению данные о частоте нахождения PNA зонда-мишени в заданном сайте хромосомы после отмывки несвязанного зонда.
Сравнительная геномная гибридизация
Сравнительная геномная гибридизация представляет собой молекулярный цитогенетический метод анализа числа вариантов копий (CNV), связанных с уровнем плоидии ДНК тестируемого образца в сравнении с образцом сравнения, без необходимости в культивировании клеток. Цель этого метода заключается в быстром и эффективном сравнении двух образцов геномной ДНК, происходящих из двух источников, которые чаще всего являются близкородственными, поскольку предполагается, что они содержат различия в терминах либо увеличения количества, либо потери целых хромосом или субхромосомных участков (части целой хромосомы). Этот метод первоначально был разработан для оценки различия между хромосомными наборами солидной опухоли и образцами нормальной ткани и характеризуется улучшенным разрешением, составляющим 5-10 миллионов пар оснований, в сравнении с более традиционными методами цитогенетического анализа результатов окрашивания с использованием красителя Гимзы (G-окрашивания) и флуоресцентной гибридизации in situ (FISH), которые ограничены разрешением применяемого микроскопа.
Блоттинг
Типичные методы блоттинга, которые могут быть использованы, включают вестерн-, саузерн-, истерн-, фар-вестерн-, сауз-вестерн-, норз-вестерн- и нозерн-блоттинг, как далее описано в последующих разделах и как известно в данной области техники.
Вестерн-блоттинг
Вестерн-блоттинг (иногда называемый иммуноблоттингом белков) представляет собой широко используемый аналитический метод, применяемый для детектирования конкретных белков в образце гомогената или экстракта. В нем используется гель-электрофорез для разделения нативных белков на основании 3-D структуры или денатурированных белков на основании длины полипептида. Затем белки переносят на мембрану (обычно из нитроцеллюлозы или PVDF), где их окрашивают антителами, специфичными к белку-мишени. Стадию гель-электрофореза включают в анализ с использованием вестерн-блоттинга для решения проблемы перекрестной реактивности антител.
Саузерн-блоттинг
В саузерн-блоттинге объединяется перенос разделенных электрофорезом фрагментов ДНК на мембранный фильтр и последующая детекция фрагментов посредством гибридизации с зондом. Гибридизация зонда со специфическим фрагментом ДНК на мембранном фильтре указывает на то, что этот фрагмент содержит последовательность ДНК, которая комплементарна зонду. Стадия переноса ДНК с геля для электрофореза на мембрану позволяет легко осуществлять связывание меченного гибридизационного зонда с фракционированной по размеру ДНК. Это также позволяет фиксировать гибриды мишень-зонд, которые могут быть использованы для анализа с применением авторадиографии или других способов детекции. Саузерн-блоты, выполненные с расщепленной ферментами рестрикции геномной ДНК, можно использовать для определения количества последовательностей (например, числа копий) в геноме. Зонд, гибридизующийся только с единичным сегментом ДНК, который не был разрезан ферментом рестрикции, будет давать одну зону на саузерн-блоте, в то время как множественные зоны, вероятно, будут наблюдаться, когда зонд гибридизуется с несколькими очень схожими последовательностями (например, теми, которые могут происходить в результате дубликации последовательностей). Модификацию условий гибридизации (например, повышение температуры гибридизации или уменьшение концентрации соли) можно использовать для повышения специфичности и ослабления гибридизации зонда с последовательностями, которые отличаются более, чем на 100%.
Истерн-блоттинг
Истерн-блоттинг представляет собой биохимический метод, используемый для анализа посттрансляционных модификаций белков (РТМ), таких как образование комплексов с липидами, присоединение фосфо-группировок и образование гликоконъюгатов. Его наиболее часто используют для детекции углеводных эпитопов. Таким образом, истерн-блоттинг можно рассматривать как расширение биохимического метода вестерн-блоттинга. Под термином истерн-блоттинг были описаны многочисленные методы, в большинстве из которых применяются белки, перенесенные с геля после SDS-PAGE (электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия) на PVDF или нитроцеллюлозную мембрану. Перенесенные белки анализируют на посттрансляционные модификации с использованием зондов, с помощью которых можно детектировать липиды, углеводы, фосфорилирование или любую другую модификацию белков. Термин "истерн-блоттинг" следует использовать для обозначения методов, в которых детектируют мишени посредством специфического взаимодействия белков, имеющих РТМ, и зонда, что отличает его от стандартного фар-вестерн-блоттинга. В принципе, истерн-блоттинг похож на лектиновый блоттинг (т. е. на детектирование углеводных эпитопов на белках или липидах).
Фар-вестерн-блоттинг
В фар-вестерн-блоттинге для зондирования представляющего(их) интерес белка(ов) используются белки, не являющиеся антителами. Благодаря этому, могут быть идентифицированы связывающие партнеры зондирующего (или переносимого) белка. Зондирующий белок часто продуцируют в Е. coli с использованием экспрессионного вектора. Белки в клеточном лизате, содержащем белки-добычу (prey protein), сначала разделяют с использованием SDS PAGE или PAGE в нативных условиях и переносят на мембрану, как в стандартном вестерн-блоттинге (WB). Затем белки на мембране подвергают денатурации и ренатурации. Далее мембрану блокируют и зондируют, обычно с использованием очищенного(ых) белка(ов)-приманки (bait protein). Белки-приманки детектируют в пятнах на мембране, где локализован белок-добыча, если белки-приманки и белок-добыча совместно образуют комплекс. Далее зондирующий белок может быть визуализирован обычными способами: он может быть помечен радиоактивной меткой; он может нести специфическую аффинную метку, подобную His или FLAG, для которой существуют антитела; или может существовать специфичное к белку антитело (к зондирующему белку).
Сауз-вестерн-блоттинг
Сауз-вестерн-блоттинг, основанный по образцу саузерн-блоттинга (который был разработан Edwin Southern) и впервые описанный В. Bowen, J. Steinberg и коллегами в 1980 г., представляет собой лабораторный метод, который включает идентификацию и определение характеристик ДНК-связывающих белков (белков, которые связываются с ДНК) по их способности связываться со специфическими олигонуклеотидными зондами. Белки разделяют с помощью гель-электрофореза и затем переносят на нитроцеллюлозные мембраны аналогично другим видам блоттинга. "Картирование с использованием сауз-вестерн-блоттинга" проводят для быстрого определения характеристик как ДНК-связывающих белков, так и их специфических сайтов на геномной ДНК. Белки разделяют в полиакриламидном геле (PAGE), содержащем додецилсульфат натрия (SDS), ренатурируют после удаления SDS в присутствии мочевины и переносят на нитроцеллюлозу посредством диффузии. Представляющий интерес участок геномной ДНК расщепляют с использованием ферментов рестрикции, выбранных для получения фрагментов соответствующих, но разных размеров, которые далее метят по концам и которым предоставляют возможность связаться с разделенными белками. Специфически связавшуюся ДНК элюируют из каждого индивидуального комплекса белок-ДНК и анализируют с помощью электрофореза в полиакриламидом геле. Представлено доказательство, что этим методом могут быть обнаружены специфически связывающиеся с ДНК белки. Кроме того, их специфическое связывание с последовательностью позволяет осуществлять очистку соответствующих избирательно связанных фрагментов ДНК и может улучшить белок-опосредуемое клонирование регуляторных последовательностей ДНК.
Норз-вестерн-блоттинг
Проведение норз-вестерн-блоттинга включает разделение РНК-связывающих белков с помощью гель-электрофореза, в котором РНК-связывающие белки будут разделяться на основе их размера и заряда. Для того, чтобы проанализировать несколько образцов одновременно, отдельные образцы могут быть загружены на агарозный или полиакриламидный гель (обычно SDS-PAGE). По завершении гель-электрофореза гель и связанные с ним РНК-связывающие белки переносят на сэндвичи из нитроцеллюлозной мембраны и фильтровальной бумаги для переноса белков. Затем, сразу после перенесения, блоты вымачивают в блокирующем растворе; обычные блокирующие буферы имеют в своем составе обезжиренное молоко и бычий сывороточный альбумин. Этот блокирующий раствор помогает предотвращать неспецифическое связывание первичных и/или вторичных антител с нитроцеллюлозной мембраной. После достаточного времени контактирования блокирующего раствора с блотом применяют специфически конкурирующее с РНК соединение и оставляют инкубироваться при комнатной температуре. В течение этого промежутка времени конкурирующее с РНК соединение связывается с РНК-связывающими белками в образцах, которые находятся на блоте. Продолжительность инкубации при применении этого метода может варьировать в зависимости от концентрации примененного конкурирующего с РНК соединения, хотя обычно продолжительность инкубации составляет один час. По завершении инкубации блот обычно промывают по меньшей мере 3 раза в течение 5 минут для каждой промывки, чтобы перевести РНК в раствор. Обычные буферы для промывок включают забуференный фосфатом физиологический раствор (PBS) или 10%-ный раствор твина 20. Неправильная или неадекватная промывка будет влиять на четкость проявления блота. По завершении промывки блот обычно проявляют с использованием рентгеновского излучения или аналогичных авторадиографических методов.
Нозерн-блоттинг
Общая методика нозерн-блоттинга начинается с экстракции суммарной РНК из гомогенизированного образца или из клеток. Эукариотическая мРНК может быть выделена с применением хроматографии на олиго-(dT)-целлюлозе для выделения только тех РНК, которые содержат поли(А)-хвост. Затем образцы РНК разделяют с помощью гель-электрофореза. Поскольку гели являются непрочными и поскольку зонды не могут проникнуть в эту матрицу, разделенные теперь по размеру образцы РНК переносят на найлоновую мембрану, используя капиллярную или вакуумную блоттинговую систему. Найлоновая мембрана с положительным зарядом является наиболее эффективной для применения в нозерн-блоттинге, поскольку отрицательно заряженные нуклеиновые кислоты обладают к ней высокой аффинностью. Используемый для блоттинга буфер для переноса обычно содержит формамид, поскольку он снижает температуру отжига при взаимодействии зонда с РНК, тем самым устраняя необходимость применения высоких температур, которые могут вызвать разрушение РНК. После переноса РНК на мембрану, ее иммобилизуют в результате образования ковалентной связи с мембраной под действием УФ-излучения или нагревания. После того, как зонд помечен, его гибридизуют с РНК на мембране. Экспериментальные условия, которые могут влиять на эффективность и специфичность гибридизации, включают ионную силу, вязкость, длину дуплекса, ошибочное спаривание пар оснований и состав оснований. Мембрану промывают для того, чтобы убедиться, что зонд связан специфически и предотвратить возникновение фоновых сигналов. Сигналы от гибридов затем детектируют с использованием рентгеновской пленки, а количественное определение может быть выполнено с использованием денситометрии. Для создания контролей сравнения, в образце при проведении нозерн-блоттинга можно использовать не проявляющий представляющий интерес генный продукт после определения с применением микрочипов или RT-ПЦР.
Ферментативные анализы
Описан метод детектирования близкого расположения (proximity detection method), в котором используется ферментативное биотинилирование для детекции мишеней в образце с возможным применением автоматизированных платформ для окрашивания. Одно из раскрытых воплощений содержит приведение в контакт образца с первым конъюгатом, содержащим биотин-лигазу и первую специфически связывающуюся группировку, которая связывается рядом с первой мишенью; приведение в контакт образца со вторым конъюгатом, содержащим субстрат биотин-лигазы и вторую специфически связывающуюся группировку, которая связывается рядом со второй мишенью; приведение образца в условия, которые позволяют осуществить биотинилирование субстрата биотин-лигазы, катализируемое биотин-лигазой, когда первая мишень и вторая мишень расположены рядом друг с другом; и детекцию биотинилирования субстрата биотин-лигазы. Условия, которые позволяют осуществить биотинилирование субстрата, включают добавление биотина и АТФ. Способ также может содержать приведение в контакт образца с конъюгатом стрептавидин-фермент. Кроме этого можно использовать амплификацию сигнала. См. заявку WO 2014139980, которая тем самым включена посредством ссылки во всей своей полноте.
Иммуноферментный твердофазный анализ (ELISA)
При проведении ELISA используют по меньшей мере одно антитело со специфичностью к конкретному антигену. Образец с неизвестным количеством антигена иммобилизуют на твердой подложке (обычно в полистирольном титрационном микропланшете), либо с применением неспецифического связывания (посредством адсорбции на поверхности), либо с применением специфического связывания (посредством захвата другим антителом, специфичным по отношению к этому же антигену в "сэндвич" ELISA). После того, как антиген иммобилизован, добавляют детектирующее антитело, формируя комплекс с антигеном. Детектирующее антитело может быть ковалентно связано с ферментом или его само можно детектировать с использованием вторичного антитела, которое связано с ферментом посредством био-конъюгирования. Между стадиями, планшет обычно промывают раствором умеренного детергента для удаления всех неспецифически связанных белков или антител. После стадии заключительной промывки, планшет обрабатывают, добавляя субстрат для фермента, с целью получения видимого сигнала, который указывает на количество антигена в образце.
Анализы связывания лигандов
Метод анализа образца, который, как известно, содержит или предположительно содержит циркулирующие СТС, может включать стадию визуализации. В одном из примеров визуализация включает визуализацию иммунофлуоресценции от идентифицирующих СТС реагентов (например, путем детектирования метки, связанной с каждым используемым антителом). В другом примере визуализация включает использование многоспектральных полосовых фильтров. Сигнал иммунофлуоресценции может исходить из антител, меченных непосредственно или опосредованно флуорофорами, либо иммунофлуоресценция может быть результатом возбуждения флуорофоров спектрально фильтрованным видимым светом. В одном из воплощений спектрально фильтрованный видимый свет включает в себя свет в первом выбранном диапазоне для возбуждения первого флуорофора и во втором выбранном диапазоне для возбуждения второго флуорофора, при этом свет в первом выбранном диапазоне не вызывает значительного возбуждения второго флуорофора, а во втором выбранном диапазоне не вызывает значительного возбуждения первого флуорофора. Визуализация образца может включать получение первого иммунофлуоресцентного изображения образца, возбуждаемого светом в первом выбранном диапазоне, и получение второго иммунофлуоресцентного изображения образца, возбуждаемого светом во втором выбранном диапазоне (и получение дополнительных иммунофлуоресцентных изображений для каждой метки, если использованы более двух реагентов для идентификации СТС), и определение местоположения, либо идентификацию СТС по местоположению или посредством визуализации идентифицирующих СТС реагентов, что может включать в себя сравнение или наложение первого иммунофлуоресцентного изображения и второго иммунофлуоресцентного изображения (и дополнительных изображений, если они получены). Например, посредством визуализации первого иммунофлуоресцентного изображения можно идентифицировать CK+-клетки, а второго иммунофлуоресцентного изображения можно идентифицировать CD45+-клетки, при этом сравнение или наложение включает в себя идентификацию клеток, которые являются CK+ и CD45-. В другом воплощении определение местоположения СТС посредством определения местоположения идентифицирующих СТС реагентов включает в себя проведение алгоритмического анализа (algorithmically analyzing) первого иммунофлуоресцентного изображения и второго иммунофлуоресцентного изображения (и дополнительных иммунофлуоресцентных изображений, если они получены) с использованием компьютера. В одном из воплощений алгоритмический анализ включает в себя детальное исследованиев цифровом формате изображения для измерения размера клетки, местоположения маркеров в клеточных компартментах и/или интенсивности экспрессии маркеров. См. заявку WO 2013101989, которая тем самым включена посредством ссылки во всей своей полноте.
Иммунопреципитация (IP)
Анализ связывания лигандов из жидкой фазы посредством иммунопреципитации (IP) представляет собой метод с использованием антитела, который применяют для очистки или обогащения конкретного белка или группы белков из сложной смеси. Экстракт разрушенных клеток или образцов можно смешать с антителом к представляющему интерес антигену с получением комплекса антиген-антитело. Когда концентрация антигена является низкой, выпадение в осадок комплекса антиген-антитело может занять несколько часов или даже суток, и становится трудно выделить небольшое количество образованного осадка. Иммуноферментный твердофазный анализ (ELISA) или вестерн-блоттинг представляют собой два разных метода получения и анализа очищенного антигена (или нескольких антигенов). Этот метод включает очистку антигена с использованием антитела, присоединенного к твердой (в виде гранул) подложке, такой как носитель на основе агарозы. Иммобилизованный белковый комплекс может быть приготовлен либо за одну стадию, либо за несколько последовательных стадий. IP также можно использовать вместне с мечением биосинтетическим радиоактивным изотопом. Используя сочетание этих методов, можно определить синтезируется специфический антиген в образце или в клетке.
Иммунопреципитация хроматина (ChIP)
Иммунопреципитация хроматина (ChIP) представляет собой тип экспериментального метода иммунопреципитации, используемого для исследования взаимодействия между белками и ДНК в клетке. Его цели состоят в определении того, ассоциированы ли специфические белки со специфическими геномными участками, например, транскрипционные факторы с промоторами или с другими сайтами связывания на ДНК, и, возможно, в определении цистромов. ChIP также направлена на определение конкретного места в геноме, с которым связаны различные модификации гистонов, указывающие на мишень модификаторов гистонов.
Иммунопреципитационное секвенирование хроматина (ChIP-секв.)
ChIP-секвенирование, также известное как ChIP-секв., представляет собой метод, используемый для анализа взаимодействий белков с ДНК. ChIP-секв. объединяет иммунопреципитацию хроматина (ChIP) с широкомасштабным параллельным секвенированием ДНК для идентификации сайтов связывания ДНК-ассоциированных белков. Этот метод можно использовать с целью точного картирования глобальных сайтов связывания для любого представляющего интерес белка. ChIP-секв. используют преимущественно для определения того, каким образом транскрипционные факторы и другие хроматин-ассоциированные белки влияют на воздействующие на фенотип механизмы. Определение того, как взаимодействующие с ДНК белки регулируют генную экспрессию, является важным для полного понимания многих биологических процессов и болезненных состояний. Эта эпигенетическая информация дополняет генотипический и экспрессионный анализ. В настоящее время технология ChIP-секв. рассматривается преимущественно в качестве альтернативы технологии ChIP-чип, в которой может использоваться гибридизационный массив. Его использование в обязательном порядке приводит к получению некоторых систематических ошибок, поскольку массив ограничен фиксированным количеством зондов. Считается, что секвенирование, в противоположность этому, связано с получением меньших систематических ошибок, хотя связанные с различными технологиями секвенирования систематические ошибки до конца еще не поняты. Специфические сайты ДНК, участвующие в непосредственном физическом взаимодействии с транскрипционными факторами и другими белками, могут быть выделены с использованием иммунопреципитации хроматина. С применением ChIP создают библиотеку целевых сайтов ДНК, связанных с представляющим интерес белком in vivo. Широкомасштабные параллельные анализы последовательностей используют вместе с полногеномными базами данных для последовательностей с целью анализа характера взаимодействия любого белка с ДНК или характера любой эпигенетической модификации хроматина. Это может быть применено к набору белков и модификациям, которые можно исследовать с использованием ChIP, таким как транскрипционные факторы, полимеразы и транскрипционный комплекс, структурные белки, модификации белков и модификации ДНК. В качестве альтернативы зависимости от специфических антител были разработаны разные методы нахождения расширенного множества всех нуклеосомно-истощенных или нуклеосомно-разрушенных активных регуляторных участков в геноме, такие методы как ДНК-секв. и FAIRE-секв.
ChIP-на-чипе (ChIP-чип)
Метод ChIP-на-чипе (также известный как ChIP-чип) представляет собой технологию, в которой объединена иммунопреципитация хроматина ("ChIP") с использованием микрочипа ДНК ("чип"). Подобно обычной ChIP, ChIP-на-чипе используют для иссследования взаимодействий между белками и ДНК in vivo. Конкретно, этот метод позволяет осуществлять идентификацию цистрома, совокупности сайтов связывания, для ДНК-связывающих белков на основе всего генома. Полногеномный анализ может быть проведен с целью определения расположения сайтов связывания практически для любого представляющего интерес белка. Как следует из названия метода, такие белки, как правило, представляют собой белки, действующие применительно к хроматину. Наиболее видными представителями этого класса являются транскрипционные факторы, связанные с репликацией белки, подобные белку предрепликационного комплекса (ORC), гистоны, их варианты и модифицированные формы гистонов. Целью метода ChIP-на-чипе является определение места положения сайтов связывания белков, что может помочь в идентификации функциональных элементов в геноме. Например, в случае транскрипционного фактора как представляющего интерес белка, можно определить сайты связывания этого транскрипционного фактора по всему геному. Другие белки позволяют осуществить идентификацию участков промоторов, энхансеров, репрессоров и сайленсирующих элементов, инсуляторов, граничных элементов и последовательностей, которые регулируют репликацию ДНК. Если объектом, представляющим интерес, являются гистоны, считается, что распределение модификаций и мест их положений может дать новые представления о механизмах регуляции. Одной из перспективных целей метода ChIP-на-чипе было создание каталога (отобранных) микроорганизмов, в котором перечислены все взаимодействия белок-ДНК в различных физиологических условиях. Эта информация в конечном итоге поможет в понимании механизмов, лежащих в основе регуляции генов, пролиферации клеток и прогрессирования заболеваний. Таким образом, метод ChIP-на-чипе обладает не только огромным потенциалом в плане пополнения наших знаний о механизме управления геномом на уровне нуклеотидов, но также и на более высоких уровнях информации и регуляции, поскольку он распространяется и на исследования по эпигенетике.
Радиоиммуноанализ
Радиоиммуноанализ (RIA) представляет собой очень чувствительный метод анализа in vitro, используемый для измерения концентраций антигенов (например, уровней гормонов в крови) с применением антител. В связи с этим его можно рассматривать как метод, обратный анализу связывания радиоактивной метки, в котором осуществляют количественное определение концентрации антитела посредством применения соответствующих антигенов. В классическом варианте, для проведения радиоиммуноанализа известное количество антигена делают радиоактивным, часто посредством его мечения гамма-радиоактивными изотопами йода, такими как125I, присоединенными к тирозину. Этот меченный радиоактивной меткой антиген затем смешивают с известным количеством антитела к этому антигену и, в результате, эти два соединения специфически связываются одно с другим. Затем добавляют образец сыворотки крови пациента, содержащий неизвестное количество того же самого антигена. Это приводит к тому, что немеченый (или "холодный") антиген из сыворотки крови конкурирует с меченным радиоактивной меткой антигеном ("горячим") за сайты связывания антитела. По мере увеличения концентрации "холодного" антигена, все большее его количество связывается с антителом, вытесняя меченный радиоактивной меткой вариант и уменьшая соотношение между связанным с антителом меченным радиоактивной меткой антигеном и свободным меченным радиоактивной меткой антигеном. Связавшиеся антигены затем отделяют от несвязавшихся и радиоактивность связанного антигена, оставшегося в супернатанте, измеряют, используя гамма-счетчик.
Этот метод в принципе можно использовать применительно к любой биологической молекуле, и он не ограничен ни антигенами сыворотки крови, ни необходимостью применения непрямого метода измерения свободного антигена вместо непосредственного измерения захваченного антигена. Например, если нежелательно или невозможно получить меченный радиоактивной меткой антиген или представляющую интерес молекулу-мишень, RIA может быть осуществлен, если имеются два разных антитела, которые распознают мишень, и мишень достаточно больших размеров (например, белок), чтобы презентовать данным антителам множественные эпитопы. Одно антитело может быть меченным радиоактивной меткой, как описано выше, в то время как другое будет оставаться немодифицированным. RIA будет начинаться с того, что "холодное" немеченое антитело оставляют для осуществления взаимодействия и связывания с молекулой-мишенью в растворе. Предпочтительно, это немеченое антитело должно быть каким-либо образом иммобилизовано, например, присоединено к агарозной грануле агарозы, сенсибилизировано на поверхности и так далее. Затем, "горячее" меченное радиоактивной меткой антителе оставляют взаимодействовать с первым комплексом антитело-(молекула-мишень). После интенсивной промывки непосредственно измеряют количество связанного радиоактивного антитела и выполняют количественное определение содержания молекулы-мишени, сравнивая его с референсным количеством, измеренным в то же самое время. Этот метод, в принципе, аналогичен нерадиоактивному метод сэндвич-ELISA.
Поляризация флуоресценции
Термин "поляризация флуоресценции" является синонимом "анизотропии флуоресценции". В этом методе измеряют изменение скорости вращения меченного флуоресцентной меткой лиганда, когда он связан с рецептором. Для возбуждения лиганда используют поляризованный свет и измеряют характеристики испускаемого света. Деполяризация испускаемого света зависит от размера присутствующего лиганда. Если используют небольшой лиганд, он будет характеризоваться большой деполяризацией, в результате чего будет происходить быстрое вращение плоскости поляризации света. Если используемый лиганд представляет собой лиганд большего размера, полученная деполяризация будет ослаблена. Преимущество этого метода заключается в том, что он может включать только одну стадию введения метки. Однако, если этот метод используют при низких наномолярных концентрациях, результаты могут быть точными.
Ферстеровский резонансный перенос энергии (FRET)
В Ферстеровском резонансном переносе энергии (также называемом как резонансный перенос энергии флуоресценции) используется энергия, переносимая между донорной и акцепторной молекулами, которые находятся в непосредственной близости, например, между донором-флуорофором и акцептором-флуорофором или флуорофором и гасителем. В FRET используется флуоресценция меченого лиганда, такого как флуоресцентный белок (FP). Перенос энергии при FRET начинается с возбуждения донора. В результате диполь-дипольного взаимодействия между донорной и акцепторной молекулами происходит перенос энергия с донорной на акцепторную молекулу. Взаимодействия между молекулами или среди молекул, к которым присоединены доноры и акцепторы, можно регистрировать посредством детектирования спектров флуоресценции, ассоциированных с наличием переноса или его отсутствием. Например, если лиганд связан с комплексом рецептор-антитело, то акцептор будет излучать свет. Перенос энергии зависит от расстояния между донором и акцептором, так что наличие или отсутствие переноса указывает на межмолекулярное расстояние. Обычно расстояние меньше 10 нм позволяет осуществлять эффективный перенос энергии между акцептором и донором, хотя в зависимости от конфетных участвующих в переносе молекул могут быть использованы большие или меньшие расстояния.
Поверхностный плазмонный резонанс (SPR)
Поверхностный плазмонный резонанс (SPR) не требует мечения лиганда. Вместо этого он работает посредством измерения изменения угла, под которым поляризованный свет отражается от поверхности (показателя преломления). Данный угол связан с изменением массы или толщины слоя, как например, в результате иммобилизации лиганда, изменяющей резонансный угол, что усиливает отраженный свет. Прибор, для которого разработан SPR, включает сенсорный чип, проточную ячейку, источник света, призму и позиционный детектор с фиксированным углом.
Анализы связывания на фильтрах
Анализы на фильтрах представляют собой анализы связывания лигандов на твердой фазе, в которых применяют фильтры для измерения аффинности между двумя молекулами. В анализе связывания на фильтрах фильтры используют для захвата клеточных мембран посредством пропускания через них среды. Этот быстрый метод осуществляется с большой скоростью, при которой для отыскиваемой фракции может быть осуществлены фильтрация и извлечение. В результате промывки фильтров буфером удаляются оставшиеся несвязанные лиганды и любые другие присутствующие лиганды, которые могут быть отмыты из сайтов связывания. Комплексы рецептор-лиганд, присутствующие на фильтре во время промывки, не будут в значительной степени диссоциировать, потому что они будут полностью захвачены фильтрами. Характеристики фильтра являются важными для каждого выполняемого вида работы. Более толстый фильтр полезен для более полного извлечения мелких частей мембраны, но может требовать более продолжительного времени промывки. Рекомендуется предварительно обработать фильтры, чтобы помочь захвату отрицательно заряженных частей мембраны. Вымачивание фильтра в растворе, который будет придавать поверхности фильтра положительный заряд, будет вызывать притяжение отрицательно заряженных фрагментов мембраны.
Аффинная хроматография
Аффинная хроматография представляет собой метод разделения биохимических смесей, основанный на высокоспецифичном взаимодействии, таком как взаимодействие между антигеном и антителом, ферментом и субстратом или рецептором и лигандом. Неподвижная фаза обычно представляет собой гелевую матрицу, зачастую на основе агарозы, линейной молекулы сахара, происходящего из водорослей. Обычно, исходная смесь представляет собой гетерогенную группу неизвестных молекул в растворе, таком как клеточный лизат, ростовая среда или сыворотка крови. Представляющая интерес молекула будет обладать хорошо известным и определенным свойством и оно может быть использовано в процессе аффинной очистки. Сам процесс можно рассматривать как улавливание молекулы-мишени, которая захватывается на твердой или неподвижной фазе или среде. Другие молекулы в подвижной фазе не будут захватываться, поскольку они не обладают этим свойством. Затем неподвижную фазу можно отделить от смеси, промыть, и молекула-мишень может быть высвобождена из захваченного состояния в процессе, известном как элюирование. Возможно, наиболее общим применением аффинной хроматографии является очистка рекомбинантных белков.
Иммуноаффинность: другим применением данной методики является аффинная очистка антител из сыворотки крови. Если известно, что сыворотка крови содержит антитела к конкретному антигену (например, если сыворотка крови происходит из организма, иммунизированного с использованием рассматриваемого антигена), то ее можно использовать для аффинной очистки этого антигена. Этот метод также известен как иммуноаффинная хроматография. Например, если организм иммунизирован с использованием слитого с GST белка, он будет вырабатывать антитела к этому слитому белку и, возможно, также антитела к GST метке. Затем данный белок можно ковалентно присоединить к твердой подложке, такой как агароза, и использовать в качестве аффинного лиганда при очистке антител из иммунной сыворотки. Для полноты, каждый из белков, белок GST и слитый с GST белок, могут быть присоединены по отдельности. Изначально сыворотку оставляют связываться с матрицей, обладающей аффинностью к GST. Посредством этого будут извлекаться антитела к GST-части слитого белка. Затем сыворотку крови отделяют от твердой подложки и оставляют связываться с матрицей, содержащей GST-слитый белок. Это позволяет захватить на твердой подложке все антитела, которые распознают антиген. Элюирование представляющих интерес антител наиболее часто достигается с использованием буфера с низким значением рН, такого как глициновый буфер с рН 2,8. Элюат собирают в буфер на основе триса или фосфата с нейтральным значением рН для нейтрализации элюирующего буфера с низким значением рН и остановки любой потери активности антитела. Это представляет собой наглядный пример того, как аффинную очистку используют для очистки исходного слитого с GST белка, для удаления нежелательных антител к GST из сыворотки крови и для очистки целевого антитела. Для очистки антител, созданных к пептидным антигенам, часто применяю у прощенную стратегию. Когда пептидные антигены получают синтетическим путем, на N- или С-конец пептида добавляют концевой остаток цистеина. Этот остаток цистеина содержит сульфгидрильную функциональную группу, которая позволяет легко конъюгировать пептид с белком-носителем (например, гемоцианином лимфы улитки (KLH)). Такой же цистеинсодержащий пептид также иммобилизуют на агарозной смоле через остаток цистеина и затем используют для очистки антитела. Большинство моноклональных антител было очищено с использованием аффинной хроматографии на основе иммуноглобулин-специфичного белка А или белка G, происходящих из бактерий.
Иммуноцитохимия (ICC)
Иммуноцитохимия (ICC) представляет собой общеизвестный лабораторный метод, который используется для анатомической визуализации локализации конкретного белка или антигена в клетках посредством применения специфического первичного антитела, которое связывается с ним. Применение первичного антитела позволяет осуществить визуализацию белка под флуоресцентным микроскопом в том случае, когда оно связано с вторичным антителом, имеющим конъюгированный флуорофор. ICC позволяет исследователям оценить, экспрессируют или нет клетки рассматриваемый антиген в конкретном образце. В тех случаях, когда иммуноположительный сигнал обнаружен, ICC также позволяет исследователям определить, какие субклеточные компартменты экспрессируют антиген. Существует много методов иммунологического детектирования в образцах, в том числе связанных непосредственно с использованием первичных антител или антисыворотки. Прямой метод включает применение детектируемой метки (например, флуоресцентной молекулы, частиц золота и т. д.) непосредственно в составе антитела, которому затем дают возможность связаться с антигеном (например, белком) в клетке. Альтернативно, существует много опосредованных методов. В одном из таких методов антиген связывается с первичным антителом, которое затем амплифицируют посредством применения вторичного антитела, связывающегося с первичным антителом. Далее применяют третичный реагент, содержащий ферментативную группировку, и выполняют его связывание с вторичным антителом. Когда применяют четвертичный реагент или субстрат, то при участии ферментативного "конца" третичного реагента субстрат превращается в окрашенный продукт реакции, дающий окраску (возможно появление нескольких цветов: коричневого, черного, красного и т.д.) в том же самом месте, где произошло распознавание представляющего интерес антигена исходным первичным антителом. Некоторыми примерами использованных субстратов (также известных как хромогены) являются АЕС (3-амино-9-этилкарбазол) или DAB (3,3'-диаминобензидин). В результате применения одного из этих реагентов после воздействия необходимого фермента (например, пероксидазы хрена, конъюгированной с реагентом на основе антитела) получается положительно "окрашенный" продукт иммунной реакции. Иммуноцитохимическую визуализацию специфических представляющих интерес антигенов можно использовать, когда для получения диагноза не может быть использовано менее специфичное окрашивание, типа Н&Е (гематоксилином и эозином), или для получения дополнительной предсказательной информации относительно лечения (например, при некоторых видах рака). Альтернативно, вторичное антитело может быть ковалентно связано с флуорофором (FITC и родамин являются наиболее типичными), который детектируют по флуоресценции или с использованием конфокального микроскопа. Расположение флуоресцентной метки будет варьировать в соответствии с расположением молекулы-мишени, то есть снаружи клетки в случае мембранных белков и внутри клетки в случае цитоплазматических белков. Таким образом, иммунофлуоресценция при объединении с конфокальной микроскопией представляет собой мощный метод изучения расположения белков и динамических процессов (экзоцитоза, эндоцитоза и т.д.).
Электрофоретические анализы
Типичные электрофоретические анализы, которые могут быть использованы, включают электрофорез нуклеиновых кислот, PAGE, методы с использованием гелей в нативных условиях, электрофорез со свободным потоком, IEF, EMSA, RFLP анализ и зимографию, которые известны в данной области техники и которые также описаны ниже.
Электрофорез нуклеиновых кислот
Электрофорез нуклеиновых кислот представляет собой аналитический метод, используемый для разделения фрагментов ДНК или РНК по размеру и реакционной способности. Подлежащие анализу молекулы нуклеиновой кислоты помещают в вязкую среду, гель, где электрическое поле вызывает миграцию нуклеиновых кислот по направлению к аноду ввиду наличия общего отрицательного заряда сахарофосфатного остова цепи нуклеиновой кислоты. Разделение этих фрагментов осуществляется в результате использования подвижностей, с которыми молекулы разного размера способны проходить через гель. Более длинные молекулы мигрируют более медленно, потому что испытывают большее сопротивление со стороны геля. Поскольку размер молекулы влияет на ее подвижность, за определенный период времени более мелкие фрагменты оказываются более близко к аноду, чем более длинные. По прошествии некоторого промежутка времени, источник напряжения отключают и проводят анализ разделения на фрагменты. Для улучшения разделения между фрагментами близких размеров могут быть изменены либо разность потенциалов, либо время проведения разделения. Наиболее точное разделение дает проведение электрофореза с увеличенным временем при приложении к гелю низкой разности потенциалов. Разность потенциалов, однако, является не единственным фактором, влияющим на электрофорез нуклеиновых кислот.
Электрофорез в полиакриламидом геле (PAGE)
Электрофорез в полиакриламидом геле (PAGE) описывает метод, широко используемый в биохимии, криминалистике, генетике, молекулярной биологии и биотехнологии для разделения биологических макромолекул, обычно белков или нуклеиновых кислот, в соответствии с их электрофоретической подвижностью. Подвижность зависит от длины, конформации и заряда молекулы.
SDS-PAGE: додецилсульфат натрия (SDS) представляет собой анионный детергент, применяемый для образцов белков с целью перевода белков в линейную форму и придания отрицательного заряд белкам в линейной форме. Эту методику называют SDS-PAGE. Для большинства белков связывание SDS с полипептидной цепью приводит к равномерному распределению заряда на единицу массы, в результате чего в процессе электрофореза происходит разделение приблизительно в соответствии с размером. Белки, которые содержат больше гидрофобных участков, например, многие мембранные белки, и белки, которые взаимодействуют с поверхностно-активными веществами в их нативном окружении, принципиально труднее анализировать с использованием этого способа из-за большей вариабельности в отношении связавшегося SDS.
Двумерный гель-электрофорез: 2-D электрофорез начинается с проведения 1-D электрофореза, но затем проводят разделение молекул на основании второго свойства в направлении 90 градусов относительно первого направления. При проведении 1-D электрофореза белки (или другие молекулы) разделяют в одном направлении, так что все белки/молекулы будут располагаться вдоль линии, но таким образом, чтобы данные молекулы разделялись в геле при проведении 2-D варианта. Поскольку маловероятно, чтобы две молекулы были одинаковыми в отношении двух различных свойств, то такие молекулы более эффективно будут разделяться в случае 2-D электрофореза, чем в случае 1-D электрофореза. Двумя факторами, в соответствии с которыми происходит разделение белков при использовании этого метода, могут быть изоэлектрическая точка, в случае сложной смеси белков в нативном состоянии, и масса белка. Результатом этого является получение геля с белками, распределенными по его поверхности. Затем эти белки можно регистрировать различными способами, но наиболее часто используется окрашивание с применением серебра и кумасси бриллиантового голубого.
Методы гель-электрофореза в нативных условиях
В гелях в нативных условиях, также известных как неденатурирующие гели, анализируют белки, которые находятся в своем свернутом состоянии. В этих условиях электрофоретическая подвижность зависит не только от отношения заряда к массе, но также от физической формы и размера белка. Ниже приводятся примеры различных видов метода гель-электрофореза в нативных условиях.
Гель-электрофорез в чисто нативных условиях: в CN-PAGE (обычно называемом как PAGE в нативных условиях) разделяют кислые водорастворимые и мембранные белки в градиентном полиакриламидном геле. В этом методе не используется заряженный краситель, поэтому электрофоретическая подвижность белков в CN-PAGE (в противоположность методу BN-PAGE со сдвигом заряда) связана с собственным зарядом белков. Пробег в геле зависит от заряда белка, его размера и размера пор геля. Во многих случаях этот метод дает более низкое разрешение, чем BN-PAGE, но преимущества CN-PAGE проявляются в том случае, когда краситель кумасси будет мешать выполнению других аналитических методов, например, данный метод описан как очень эффективный метод микромасштабного разделения для FRET-анализов. Также метод CN-PAGE является более мягким, чем метод BN-PAGE, поэтому при его выполнении могут сохраняться лабильные надмолекулярные ансамбли мембранных белковых комплексов, которые диссоциируют в условиях BN-PAGE.
Голубой PAGE в нативных условиях: BN-PAGE представляет собой метод PAGE в нативных условиях, когда краситель кумасси голубой обеспечивает необходимые заряды белковым комплексам для электрофоретического разделения. Недостаток использования кумасси состоит в том, что при связывании с белками он может действовать как детергент, вызывая диссоциацию комплексов. Другой недостаток состоит в возможном гашении хемилюминесценции (например, при последующей детекции с использованием вестерн-блоттинга или в анализах активности) или флуоресценции белков с простетическими группами (например, флуоресценции тема или хлорофилла) или меченных флуоресцентными красителями белков.
Количественный препаративный непрерывный электрофорез в полиакриламидном геле в нативных условиях: QPNC-PAGE или количественный препаративный непрерывный электрофорез в полиакриламидом геле в нативных условиях представляет собой метод с высоким разрешением, применяемый в биохимии и бионеорганической химии для разделения белков в соответствии с изоэлектрической точкой. Этот стандартный вариант гель-электрофореза в нативных условиях используется биологами для выделения активных или нативных металлопротеинов в биологических образцах и для разделения правильно и неправильно свернутых белков или изоформ белков, содержащих металл в качестве кофактора, из сложной белковой смеси. В качестве платформы омиков для биомедицинских подходов QPNC-PAGE вносит вклад в разработку лекарственных средств на основе металлов для заболеваний, обусловленных неправильным фолдингом белков, и ввиду этого в биоэкономику.
Электрофорез со свободным потоком
Электрофорез со свободным потоком (FFE), также известный как электрофорез без носителя, представляет собой метод непрерывного электрофоретического разделения, основанного на использовании жидкой фазы. Его обычно применяют для количественного и полуколичественного разделения белков, пептидов, органелл, клеток, ДНК-оригами и частиц. Преимущество FFE состоит в том, что разделение проводят быстрым и мягким способом, основанным на использовании жидкой фазы, без какого-либо взаимодействия с твердой матрицей, подобной полиакриламиду в гель-электрофорезе. Это обеспечивает очень высокую степень извлечения, поскольку нет никаких потерь аналитов. Разделения при проведении FFE являются непрерывными, что обеспечивает высокую производительность при разделении аналитов в случае препаративных применений. Кроме того, разделения могут быть проведены в нативных или денатурирующих условиях. Однородную и ламинарную пленку из жидкости пропускают между двумя пластинами, распределяют между параллельными пробирками для фракционирования и собирают в титрационные микропланшеты. Перпендикулярно ламинарному потоку прикладывают электрическое поле высокого напряжения. Аналиты в ламинарном потоке разделяются в соответствии с плотностью заряда и изоэлектрической точкой.
Изоэлектрическое фокусирование
Изоэлектрическое фокусирование (IEF), также известное как электрофокусирование, представляет собой метод разделения разных молекул, основанный на различиях в их изоэлектрических точках (pi). IEF включает в себя добавление раствора амфолитов в гели с иммобилизованным градиентом рН (IPG). IPG представляют собой акрил амидную гелевую матрицу, полимеризованную при одновременном создании градиента рН, в результате чего образуются полностью стабильные градиенты, за исключением области с наиболее щелочными (>12) значениями рН. Иммобилизованный градиент рН получают в результате непрерывного изменения в соотношении иммобилинов. Иммобилин представляет собой слабую кислоту или основание, определяемую(ый) своим значением pH. Белок, находящийся в области рН ниже своей изоэлектрической точки (pI), будет положительно заряженным и поэтому будет двигаться по направлению к катоду (отрицательно заряженному электроду). Однако, по мере его продвижения через градиент в сторону увеличения рН, общий заряд белка будет уменьшаться до тех пор, пока белок не достигнет области рН, которая соответствует его pI. В этой точке у него отсутствует суммарный заряд, и поэтому движение прекращается (поскольку нет никакого электрического притяжения к какому-либо из электродов). В результате этого белки фокусируются в узкие стационарные зоны с расположением каждого белка в точке рН градиента, соответствующей его pI. С помощью этого метода можно добиться чрезвычайно высокого разрешения для белков, различающихся на единицу заряда, которые будут расфракционированы на отдельные зоны. Молекулы, подлежащие фокусированию, распределяют в среде с градиентом рН (обычно создаваемым алифатическими амфолитами). Через среду пропускают электрический ток, создавая "положительный" анодный и "отрицательный" катодный край. Отрицательно заряженные молекулы мигрируют через градиент рН в среде по направлению к "положительному" краю, в то время как положительно заряженные молекулы двигаются по направлению к "отрицательному" краю. По мере того, как частица движется по направлению к полюсу, противоположному ее заряду, она движется через изменяющийся градиент рН, пока не достигнет точки, в которой рН молекулы станет равным изоэлектрической точке. В этой точке молекула больше не имеет суммарного электрического заряда (обусловленного протонированием или депротонированием соответствующих функциональных групп) и поэтому не будет продолжать дальнейшее движение в геле. Градиент устанавливается перед добавлением представляющих интерес частиц посредством первоначального электрофореза раствора молекул небольших размеров, таких как полиамфолиты, с различными значениями pI.
Иммуноэлектрофорез
Иммуноэлектрофорез - это общее название ряда биохимических методов разделения и определения характеристик белков, основанных на электрофорезе и реакции с антителами. В вариантах иммуноэлектрофореза обычно используют иммуноглобулины, также известные как антитела, взаимодействующие с белками, подлежащими разделению и характеристике. Агароза в виде пластинок 1%-ого геля толщиной примерно 1 мм в буфере с высоком значении рН (около 8,6) традиционно является предпочтительной для проведения электрофореза, а также взаимодействия с антителами. Агарозу выбирают в качестве гелевой матрицы ввиду того, что она имеет поры большого размера, дающие возможность для свободного прохождения и разделения белков, но обеспечивает "заякоривание" иммунопреципитатов белка и специфических антител. Высокое значение рН выбирают ввиду того, что антитела практически неподвижны при высоком значении рН. Для проведения электрофореза обычно рекомендуется электрофоретическое оборудование с горизонтальной охлаждаемой пластиной. Иммунопреципитаты можно разглядеть во влажном агарозном геле, но их окрашивают красителями для белков, подобными кумасси бриллиантовому голубому, в высушенном геле. В противоположность SDS-гель-электрофорезу, электрофорез в агарозе дает возможность использовать нативные условия, сохраняя нативные структуру и активности исследуемых белков, поэтому иммуноэлектрофорез позволяет характеризовать активности ферментов, связывание лигандов и т. д. в дополнение к электрофоретическому разделению.
Аффинный иммуноэлектрофорез основан на изменениях в электрофоретическом поведении белков в результате специфического взаимодействия или образования комплексов с другими макромолекулами или лигандами. Аффинный иммуноэлектрофорез был использован для оценки констант связывания, как например, в случае с пектинами, или для характеристики белков с определенными признаками, такими как содержание в них гликанов или связывание с лигандами. Некоторые варианты аффинного иммуноэлектрофореза аналогичны аффинной хроматографии с использованием иммобилизованных лигандов. Открытая структура иммунопреципитата в агарозном геле будет давать возможность для дополнительного связывания меченных радиоактивной меткой антител с целью выявления конкретных белков. Эта разновидность метода была использована для идентификации аллергенов посредством взаимодействия с IgE.
Анализ изменения электрофоретической подвижности (EMSA)
Анализ изменения электрофоретической подвижности (EMSA) или электрофорез со сдвигом подвижности, также называемый как анализ сдвига в геле, анализ изменения подвижности в геле, анализ сдвига зон в геле или ретардационный анализ в геле, представляет собой стандартный метод аффинного электрофореза, используемый для изучения взаимодействий белок-ДНК или белок-РНК. Эта методика позволяет определить, способен ли белок или способна ли смесь белков связываться с заданной последовательностью ДНК или РНК, и может в некоторых случаях указать на участие в комплексе более одной молекулы белка. Анализы сдвига в геле часто проводят in vitro одновременно с футпринтингом ДНКаз, удлинением праймеров и экспериментами с зондами для промоторов, когда изучают инициацию транскрипции, репликацию ДНК, репарацию ДНК или процессинг и созревание РНК. Хотя предшественники могут быть найдены в более ранней литературе, большинство современных видов анализа основаны на методах, описанных авторами Garner и Revzin и Fried и Crothers.
Анализ полиморфизма длин рестрикционных фрагментов
RFLP анализ. ДНК собирают из клеток, например, из образца крови, и разрезают на небольшие кусочки, используя фермент рестрикции. В результате этого образуются тысячи фрагментов ДНК различных размеров вследствие вариаций между последовательностями ДНК у разных индивидов. Затем проводят разделение фрагментов на основании размера, используя гель-электрофорез. Разделенные фрагменты далее переносят на нитроцеллюлозный или найлоновый фильтр; эта методика называется саузерн-блоттингом. Фрагменты ДНК на блоте необратимо фиксируют на фильтре и нити ДНК подвергают денатурации. Затем добавляют молекулы меченных радиоактивной меткой зондов, комплементарных последовательностям в геноме, которые содержат повторяющиеся последовательности. Эти повторяющиеся последовательности имеют тенденцию варьировать по длине среди разных индивидов и называются варьирующими по числу звеньев тандемными повторами или VNTR. Молекулы зондов гибридизуются с фрагментами ДНК, содержащими последовательности повторов, и избыток молекул зондов отмывают. Затем блот приводят в контакт с рентгеновской пленкой. Фрагменты ДНК, которые связаны с молекулами зондов, появляются как темные зоны на пленке.
Зимография
Зимография представляет собой электрофоретический метод детекции гидролитических ферментов, основанный на использовании репертуара субстратов для фермента. Для проведения зимографии в геле образцы готовят в стандартном загрузочном буфере в невосстанавливающих условиях для SDS-PAGE. Нет необходимости ни в каком восстанавливающем агенте или кипячении, поскольку это будет препятствовать рефолдингу фермента. Подходящий субстрат (обычно желатин или казеин) вводят в разделяющий гель во время приготовления полиакриламидного геля. После проведения электрофореза SDS удаляют из геля (или зимограммы) посредством инкубации в незабуференном тритоне Х-100, после чего инкубируют в соответствующем буфере для расщепления в течение продолжительного промежутка времени при 37°С. Потом зимограмму окрашивают (обычно амидо-черным или кумасси бриллиантовым голубым), и там, где субстрат был расщеплен под действием фермента, зоны расщепления появляются как прозрачные зоны на фоне темного окрашенного фона.
Профилирование экспрессии генов
Типичные методы профилирования экспрессии генов, которые могут быть использованы, включают профилирование ДНК с использованием ПЦР, ДНК микрочипов, SAGE, ПЦР в режиме реального времени, дифференциального дисплея с применением ПЦР и РНК-секв., как описано далее в следующих разделах и как известно в данной области техники.
Профилирование ДНК с использованием ПЦР
Метод полимеразной цепной реакции (ПЦР) имитирует биологический процесс репликации ДНК, но ограничивает его специфическими представляющими интерес последовательностями ДНК. С открытием метода ПЦР профилирование ДНК сделало огромный шаг вперед как в разрешающей способности, так и в способности извлекать информацию с использованием очень небольших (или разрушенных) исходных образцов. Применение ПЦР позволяет увеличить в значительной степени количества конкретного участка ДНК. В процессе ПЦР образец ДНК посредством нагревания подвергают денатурации до отделенных друг от друга индивидуальных полинуклеотидных нитей. Для гибридизации с двумя соответствующими близлежащими сайтами на противоположных нитях ДНК используют два олигонуклеотидных ДНК праймера таким образом, что обычное ферментативное удлинение активного конца каждого праймера (то есть, 3'-конца) происходит по направлению к другому праймеру. При проведении ПЦР используют ферменты репликации, которые устойчивы к высоким температурам, такие как термостабильная Taq полимераза. Таким путем образуются две новых копии представляющей интерес последовательности. В результате повторной денатурации, гибридизации и удлинения этим же способом образуется растущее по экспоненте количество копий представляющей интерес ДНК. Приборы, с помощью которых выполняют периодическое изменение температуры, в настоящее время легко доступны из коммерческих источников. В результате этого процесса можно провести амплификацию желаемого участка в миллион или более раз за 2 часа или меньше.
ДНК микрочип
Основным принципом, лежащим в основе работы микрочипов, является гибридизация между двумя нитями ДНК, свойство комплементарных нуклеиновокислотных последовательностей специфически образовывать пары друг с другом посредством образования водородных связей между комплементарными парами нуклеотидных оснований. Наличие большого числа комплементарных пар оснований в нуклеотидной последовательности означает более сильное нековалентное связывание между двумя нитями. После отмывки неспецифически связавшихся последовательностей только прочно спаренные нити будут оставаться гибридизованными. Флуоресцентно меченные последовательности-мишени, которые связываются с последовательностью зондов, генерируют сигнал, зависящий от условий гибридизации (таких как температура) и промывки после гибридизации. Суммарная интенсивность сигнала, исходящего из пятна, зависит от количества образца-мишени, связавшегося с зондами, присутствующими в данном пятне. Микрочипы используют для относительного количественного определения, при котором интенсивность, обусловленную каким-либо признаком, сравнивают с интенсивностью, обусловленной этим же признаком, в других условиях, а идентичность, обусловленная этим признаком, известна на основании его положения.
Серийный анализ экспрессии генов (SAGE)
Серийный анализ экспрессии генов (SAGE) представляет собой метод, используемый молекулярными биологами для получения мгновенного "снимка" популяции информационной РНК в представляющем интерес образце в форме небольших меток, которые соответствуют фрагментам этих транскриптов. Кратко, эксперименты при проведении SAGE выполняют так, как представлено ниже.
Из исходного образца (например, опухоли) выделяют мРНК и для синтеза кДНК на основе этой мРНК используют обратную транскриптазу и биотинилированные праймеры.
Проводят связывание кДНК со стрептавидиновыми гранулами посредством взаимодействия с биотином, присоединенным к праймерам, и затем расщепление с использованием эндонуклеазы рестрикции, называемой заякоривающим ферментом (АЕ). Расположение сайта расщепления и, следовательно, длина оставшейся кДНК, связанной с гранулой, будут варьировать для каждой индивидуальной кДНК (мРНК).
Отщепленную вниз по течению от сайтов расщепления кДНК затем отбрасывают и фрагменты кДНК, оставшиеся закрепленными вверх по течению от сайтов расщепления, делят пополам и подвергают воздействию одного из двух адаптерных олигонуклеотидов (А или В), содержащих разные компоненты в следующем порядке вверх по течению от сайта присоединения: 1) липкие концы с сайтом разрезания АЕ, чтобы обеспечить возможность прикрепления к расщепленной кДНК; 2) сайт распознавания для эндонуклеазы рестрикции, известной как метящий фермент (ТЕ, tagging enzyme), которая делает разрез в положении примерно 15 нуклеотидов вниз по течению относительно своего сайта распознавания (в исходной последовательности кДНК/мРНК); 3) короткий праймер с последовательностью, уникальной для любого из адапторов А или В, который позже будет использован для дальнейшей амплификации посредством ПЦР.
После лигирования адаптеров кДНК расщепляют с использованием ТЕ, чтобы удалить ее из гранул, оставляя только короткую "метку" примерно из 11 нуклеотидов из исходной кДНК (15 нуклеотидов минус 4, соответствующие сайту распознавания АЕ).
Отщепленные кДНК метки затем восстанавливают с использованием ДНК-полимеразы для получения фрагментов кДНК с тупыми концами.
Эти фрагменты на основе меток кДНК (с адаптерными праймерами и присоединенными сайтами распознавания АЕ и ТЕ) лигируют, формируя структуру типа сэндвич, состоящую из двух последовательностей меток вместе и фланкирующими адапторами А и В на каждом конце. Затем эти новые конструкции, называемые двойными метками (ditags), подвергают ПЦР амплифиции, используя специфические праймеры к А и В с заякоривающей частью.
Затем двойные метки расщепляют, используя исходный АЕ, и дают возможность соединиться вместе с другими двойными метками, которые будут лигированы для создания конкатемера кДНК с каждой двойной меткой, разделенной сайтом распознавания АЕ.
Этими конкатемерами затем трансформируют бактерии для амплификации в ходе бактериальный репликации.
Затем конкатемеры кДНК могут быть выделены и секвенированы с использованием современных высокопроизводительных ДНК секвенаторов, и эти последовательности могут быть проанализированы с применением компьютерных программ, которые количественно определяют повторяемость отдельных меток.
Полимеразная цепная реакция в режиме реального времени
Полимеразная цепная реакция в режиме реального времени представляет собой лабораторный метод молекулярной биологии, основанный на использовании полимеразной цепной реакции (ПЦР). В нем регистрируют амплификацию целевой молекулы ДНК в ходе ПЦР, т.е. в режиме реального времени, а не по ее окончании, как при проведении традиционной ПЦР. ПЦР в режиме реального времени можно использовать количественно (количественная ПЦР в режиме реального времени), полуколичественно, т.е. для определения количества молекул ДНК выше/ниже определенного значения (полуколичественная ПЦР в режиме реального времени) или качественно (качественная ПЦР в режиме реального времени). Двумя общими способами детектирования продуктов ПЦР при проведении ПЦР в режиме реального времени являются: (1) применение неспецифических флуоресцентных красителей, которые интеркалируют между цепями любой двухцепочечной ДНК и (2) применение специфичных к последовательности зондов ДНК, состоящих из олигонуклеотидов, меченных флуоресцентным репортером, позволяющим осуществлять детектирование только после гибридизации зонда с комплементарной ему последовательностью. ПЦР в режиме реального времени осуществляют в термоциклере с возможностью подвергать каждый образец воздействию луча света по меньшей мере одной конкретной длины волны и детектировать флуоресценцию, излучаемую возбужденным флуорофором. В термоциклере также можно быстро нагревать и охлаждать образцы, используя тем самым преимущества физико-химических свойств нуклеиновых кислот и ДНК-полимеразы. Процесс проведения ПЦР обычно состоит из серий изменений температуры, которые повторяются 25-50 раз. Эти циклы обычно состоят из трех стадий: первой, приблизительно при 95°С, позволяющей разделить двойную цепь; второй, при температуре приблизительно 50-60°С, позволяющей осуществить связывание праймеров с матрицей ДНК; третьей, при температуре от 68 до 72°С, облегчающей полимеризацию, осуществляемую ДНК-полимеразой. Ввиду небольшого размера фрагментов последняя стадия обычно опускается для этого типа ПЦР, так как фермент способен увеличить их количество во время изменения между стадией выравнивания и стадией денатурации. Помимо этого, для четырехстадийной ПЦР измеряют флуоресценцию во время короткой температурной фазы, длящейся только несколько секунд в каждом цикле, при температуре, например, 80°С, чтобы уменьшить сигнал, вызываемый присутствием димеров праймеров, когда используют неспецифический краситель. Температуры и временные рамки, применяемые для каждого цикла, зависят от широкого спектра параметров, таких как: фермент, используемый для синтеза ДНК, концентрация двухвалентных ионов и дезоксирибонуклеотидов (dNTP) в реакционной смеси и температура связывания праймеров.
Дифференциальный дисплей с применением ПЦР
Дифференциальный дисплей (также называемый DDRT-ПЦР (дифференциальный дисплей с применением ПЦР с обратной транскриптазой) или DD-ПЦР) представляет собой метод, с использованием которого исследователь может сравнивать и идентифицировать изменения в генной экспрессии на уровне мРНК между любой парой образцов эукариотических клеток. Данный анализ при необходимости может быть распространен более чем на одну пару. Образцы в парах должны иметь морфологические, генетические или другие определяемые экспериментально различия, с учетом которых исследователь хочет изучать картины генной экспрессии, надеясь выяснить основную причину конкретного различия или конкретные гены, на которые оказывает воздействие эксперимент. Концепция дифференциального дисплея заключается в применении ограниченного числа коротких произвольных праймеров в комбинации с заякоренными олиго-dT праймерами для систематической амплификации и визуализации большей части мРНК в клетке. После того, как этот метод был описан в начале 1990-х годов, дифференциальный дисплей стал общепринятым методом для идентификации дифференциально экспрессированных генов на уровне мРНК. Были предложены разные усовершенствованные протоколы DD-ПЦР, включая флуоресцентный способ DD, а также радиоактивное мечение, которые обеспечивают высокую точность и считывание показаний.
Секвенирование РНК (РНК-секв.)
Секвенирование РНК (РНК-секв.), также называемое шотган-секвенированием целого транскриптома (WTSS), представляет собой технологию, в которой используются возможности секвенирования следующего поколения для выявления мгновенного "снимка" присутствия и количества РНК из генома на данный момент времени.
РНК-секв. для РНК "поли(А)"-библиотеки: создание библиотеки последовательностей может претерпевать изменения от платформы к платформе при высокопроизводительном секвенировании, поскольку каждая из них имеет несколько наборов, предназначенных для создания библиотек разных типов и адаптирования полученных последовательностей к конкретным требованиям для используемых в них приборов. Однако, в силу природы матрицы, предназначенной для анализа, имеются общие черты для каждой из технологий. Часто при проведении анализа мРНК в качестве мишени используется 3'-полиаденилированный (поли(А)) хвост для обеспечения того, чтобы кодирующая РНК была отделена от некодирующей РНК. Это можно осуществить посредством простого ковалентного присоединения поли(Т)-олигонуклеотидов к заданному носителю. В настоящее время во многих исследованиях на этой стадии используются магнитные гранулы. Исследования частей транскриптома, не содержащих поли(А)-РНК, показали, что при использовании поли(Т)-магнитных гранул, изучение проходящей без задержки РНК (РНК, не содержащей поли(А)) может обеспечить открытие генов, соответствующих некодирующей РНК, которые в противном случае были бы незамеченными. Кроме того, поскольку рибосомная РНК представляет собой более 90% РНК в заданной клетке, ее удаление с помощью гибридизации зонда, как показали исследования, увеличивает возможность получения данных от остальной части транскриптома. Следующая стадия представляет собой стадию обратной транскрипции. Из-за систематических ошибок при 5'-конце праймированной случайным образом обратной транскрипции, а также наличия вторичных структур, влияющих на сайты связывания праймеров, перед проведением обратной транскрипции применяют гидролиз РНК до 200-300 нуклеотидов, который приводит к устранению обеих проблем одновременно. Однако, у этого метода имеются преимущества и недостатки, когда, несмотря на то, что общее количество транскриптов эффективно преобразуется в ДНК, 5'- и 3'-концы преобразуются с меньшей эффективностью. В зависимости от цели исследований исследователи могут либо выбрать применение этой стадии, либо проигнорировать ее.
Секвенирование малых РНК/некодирующих РНК: при секвенировании РНК, отличной от мРНК, метод получения библиотеки претерпевает модификации. Проводят разделение клеточной РНК на основании желаемого диапазона размеров. Для РНК-мишеней малых размеров, таких как микроРНК, РНК выделяют на основании размера. Это может быть осуществлено с использованием матрицы для гель-фильтрации, магнитных гранул для отбора по размеру или с использованием коммерческого набора. После выделения к 3'- и 5'-концу добавляют линкеры и затем проводят очистку. Конечная стадия заключается в получении кДНК методом обратной транскрипции.
Прямое секвенирование РНК: поскольку было показано, что превращение РНК в кДНК с использованием обратной транскриптазы приводит к получению систематических ошибок и артефактов, которые могут оказывать влияние как на надлежащее определение характеристик, так и на количественное определение транскриптов, компанией Helicos (теперь банкротом) разрабатывалась технология мономолекулярного прямого секвенирование РНК (DRSTM). При проведении DRSTM молекулы РНК секвенируют непосредственно в массовом параллельном режиме без превращения РНК в кДНК или без других дающих систематическую ошибку манипуляций с образцом, таких как лигирование и амплификация. В случае синтеза кДНК ее можно далее фрагментировать до фрагментов желаемой для системы секвенирования длины.
Масс-спектрометрия (белков)
Масс-спектрометрия белков относится к применению масс-спектрометрии для исследования белков. Масс-спектрометрия представляет собой важный перспективный метод определения характеристик белков. Двумя основными способами ионизации целых белков являются ионизация электрораспылением (ESI) и ионизация посредством лазерной десорбции ионов из матрицы (MALDI). Для определения характеристик белков используют два подхода в соответствии с характеристиками и диапазоном масс доступных масс-спектрометров. В первом, интактные белки ионизуют одним из двух описанных выше методов и затем вводят в масс-анализатор. Этот подход называется стратегией анализа белков "сверху-вниз". Во втором, белки расщепляют ферментативным путем на пептиды меньших размеров, используя протеазу, такую как трипсин. Потом эти пептиды вводят в масс-спектрометр и идентифицируют "по отпечаткам пептидных масс" или с применением тандемной масс-спектрометрии. Таким образом, в этом последнем подходе (также называемом протеомикой "снизу-вверх") для выявления присутствия белков используется идентификация на уровне пептидов. Анализ масс для целого белка в основном проводят с использованием либо времяпролетной (TOF) MS, либо ионного циклотронного резонанса с преобразованием Фурье (FT-ICR). Эти два типа прибора в данной ситуации являются предпочтительными ввиду возможности работы на них в широком диапазоне масс и, в случае FT-ICR, высокой точности определения массы. Анализ масс пептидов, подвергнутых протеолизу, является намного более популярным методом определения характеристик белков, поскольку для определения характеристик можно использовать более дешевые конструкции приборов. Кроме того, приготовление образцов упрощается, если целые белки расщеплены на более мелкие пептидные фрагменты. Наиболее часто используемым прибором для масс-спектрометического анализа пептидов являются времяпролетные приборы с использованием MALDI, поскольку они позволяют получать отпечатки пептидных масс (PMF) с высокой скоростью (1 PMF можно проанализировать приблизительно за 10 сек). Многокаскадный квадрупольный времяпролетный прибор и квадрупольная ионная ловушка также находят применение в этом приложении.
В биоаналитических анализах все чаще используют CMS вариант масс-спектрометрии (сочетание хроматографии с масс-спектрометрией). Масс-спектрометрия хорошо подходит для мультиплексирования, поскольку для установление различия между массами можно использовать много каналов для одновременного детектирования. Однако, сложные биомолекулы, такие как ДНК, характеризуются сложными масс-спектрами, и их детектирование в матрице бывает затруднительным ввиду относительно низкой чувствительности. MS представляет собой аналитический метод, в котором измеряют отношение массы к заряду заряженных частиц. Этот метод можно использовать для определения химического состава образца или молекулы. Образцы, анализируемые с применением масс-спектрометрии, ионизуют для получения заряженных молекул или атомов, разделяют в соответствии с отношением их массы к заряду и детектируют. Метод используют как качественно, так и количественно, в соответствии различными приложениями. Источник индуктивно-связанной плазмы (ICP) представляет собой тип источника плазмы, в котором энергия поставляется электрическими токами, которые генерируются в результате электромагнитной индукции, то есть, изменяющимися во времени магнитными полями. В качестве источника ионизации для масс-спектрометрии можно использовать ICP. Комбинацию индуктивно-связанной плазмы и масс-спектрометрии называют ICP-MS. Масс-спектральная визуализация (MSI) представляет собой применение масс-спектрометрии, которое включает в себя анализ химической информации совместно с пространственной информацией, вследствие чего химическая информация может быть визуализирована в виде химического изображения или карты. В результате получения химической карты могут быть выяснены различия состава в пределах поверхности образца. Лазерная абляция представляет собой способ извлечения вещества с твердой поверхности путем облучения его лазерным лучом. Лазерную абляцию использовали в качестве средства отбора образцов для масс-спектрометрии, в частности, для масс-спектральной визуализации. Согласно одному из воплощений система для масс-спектральной визуализаци образца включает пробоотборник для лазерной абляции, ионизатор индуктивно-связанной плазмы, масс-спектрометр и компьютер. Как иллюстрация, пробоотборник для лазерной абляции содержит лазер, камеру для лазерной абляции и платформу для образца, сконфигурированную таким образом, чтобы лазером можно было облучать образец, расположенный на платформе для образцов, с получением подвергнутого абляции образца, при этом лазер и платформа для образцов координируются компьютером. Пробоотборник для лазерной абляции и ионизатор индуктивно-связанной плазмы функционально связаны таким образом, чтобы подвергнутый абляции образец мог быть перенесен из пробоотборника для лазерной абляции в ионизатор индуктивно-связанной плазмы, тем самым происходит испарение, превращение в пар, распыление и ионизация подвергнутого абляции образца с образованием совокупности ионизированных атомов, характеризующихся распределением отношения массы к заряду. Масс-спектрометр функционально связан с ионизатором индуктивно-связанной плазмы таким образом, что совокупность ионов может быть перенесена из ионизатора индуктивно-связанной плазмы в масс-спектрометр, при этом в масс-спектрометре происходит разделение совокупности ионов в соответствии с распределением отношения массы к заряду с получением в результате этого данных об отношении массы к заряду. Компьютер сконфигурирован с возможностью приема входных координат (location inputs) и связывания их с пробоотборником для лазерной абляции, чтобы способствовать абляции образца в соответствии с входными координатами, и он сконфигурирован с возможностью связывания данных об отношении массы к заряду с местом на образце в соответствии с входными координатами. В других иллюстративных воплощениях система дополнительно содержит систему регистрации, сконфигурированную с возможностью определения положения образца, тем самым обеспечивая возможность автоматического соотнесения входных координат с местом на образце, на облучения которого настроен лазер. В иллюстративных воплощениях композиция для мультиплексных LA-ICP-MS анализов образцов включает в себя метку массы (mass tag) и специфически связывающуюся группировку, конъюгированную с этой меткой массы. Метка массы включает совокупность атомов первого вида, которая детектируемо отличается от элементов, эндогенных по отношению к образцу. В одном из воплощений совокупность атомов первого вида представляет собой неэндогенный стабильный изотоп элемента. В другом воплощении совокупность атомов имеет конфигурацию коллоидной частицы. См. заявку WO 2014079802, которая тем самым включена посредством ссылки во всей своей полноте.
Способ детектирования мишени в образце касается приведения в контакт образца с конъюгатом, содержащим специфически связывающуюся с ферментом группировку, выбранным для распознавания мишени. Затем образец приводят в контакт с конъюгатом предшественника метки массы, содержащим предшественник метки массы и субстрат фермента, тираминовую группировку или производное тирамина и возможный линкер. Конъюгат предшественника метки массы претерпевает взаимодействие с ферментом или с продуктом ферментативной реакции с получением выпавших в осадок меток массы, ковалентно связанных меток массы или нековалентно связанных меток массы. Образец подвергают воздействию источника энергии, который обеспечивает получение достаточной энергии для получения стандарта массы (mass code) из метки массы. После ионизации можно осуществить детекирование стандарта, используя такой метод детекции, как масс-спектрометрия. В некоторых воплощениях на образец воздействуют первым раствором, содержащим конъюгат со специфически связывающейся с ферментом группировкой, и вторым раствором, содержащим конъюгат на основе предшественника метки массы. Ферменты, с которыми связываются специфически связывающиеся с ферментом группировки, могут быть выбраны из ферментов оксидоредуктаз (например, пероксидаз), фосфатаз (например, щелочной фосфатазы), лактамаз (например, (β-лактамазы) и галактозидаз (например, β-D-галактозидазы, β-галактозидазы). Специфически связывающиеся группировки могут быть выбраны из белка, полипептида, олигопептида, пептида, нуклеиновой кислоты, ДНК, РНК, олигосахарида, полисахарида и их мономеров. Конкретные описанные воплощения касаются использования конъюгатов (щелочная фосфатаза)-антитело и конъюгатов (пероксидаза хрена)-антитело. В некоторых описанных воплощениях специфически связывающаяся группировка распознает мишень. В других описанных воплощениях специфически связывающаяся группировка распознает первичное антитело, связанное с мишенью. В некоторых воплощениях осаждение метки массы включает иммобилизацию фермента на мишени и приведение в контакт образца с группировкой субстрата фермента и предшественником метки массы. Группировка субстрата фермента взаимодействует с ферментом и предшественником метки массы с получением и осаждением метки массы на мишени. Когда две или более мишеней присутствуют в образце, метки массы осаждаются последовательно на каждой мишени, как описано выше. После осаждения метки массы, соответствующий фермент дезактивируют перед осаждением следующей метки массы на следующей мишени. В других описанных воплощениях фермент взаимодействует с предшественником метки массы -конъюгатом тирамина, или с предшественником метки массы - конъюгатом производного тирамина, с целью осаждения, обычно ковалентного, ближайшей к мишени метки массы. В некоторых воплощениях иммобилизация фермента на мишени включает приведение в контакт образца с конъюгатом, содержащим специфически связывающуюся группировку и фермент. В некоторых воплощениях специфически связывающаяся группировка представляет собой антитело. Специфически связывающаяся группировка способна распознавать и связываться непосредственно с мишенью или с другой специфически связывающейся группировкой, ранее связавшейся с мишенью. В конкретных воплощениях первый фермент, второй фермент и любой дополнительный фермент являются одинаковыми. См. заявку WO 2012003478, которая тем самым включена посредством ссылки во всей своей полноте.
Детектирование метилирования ДНК
Недавно были предложены способы диагностики рака с использованием измерения метилирования ДНК. Метилирование ДНК происходит главным образом по цитозинам CpG-островков в промоторном участке конкретного гена, чтобы препятствовать связыванию транскрипционных факторов, тем самым осуществляется подавление экспрессии данного гена. Таким образом, детектирование метилирования CpG-островков в промоторе ингибирующих образование опухолей генов значительно помогает в исследованиях рака. Недавно для диагностики и скрининга рака была предпринята активная попытка определения метилирования промотора такими способами, как специфичная к метилированию ПЦР (далее упоминаемая как MSP) или автоматическое секвенирование ДНК. См. заявку WO 2009069984 A2, которая тем самым включена посредством ссылки во всей своей полноте.
Акустическая энергия
По меньшей мере некоторые воплощения направлены на способы и системы для анализа пробы. Пробу можно анализировать на основании ее характеристик. Эти характеристики включают акустические характеристики, механические характеристики, оптические характеристики или тому подобные, которые могут быть статическими или динамическими во время обработки. В некоторых воплощениях характеристики пробы постоянно или периодически контролируют во время обработки для оценки качества и состояния пробы. На основе полученной информации можно регулировать обработку, чтобы повысить стабильность обработки, сократить время обработки, улучшить качество обработки или тому подобное. Для анализа мягких объектов, таких как образцы, можно использовать акустические характеристики. Когда акустический сигнал взаимодействует с образцом, прошедший сигнал зависит от различных механических свойств образца, таких как эластичность и твердость. Поскольку образцы, которые были помещены в фиксирующий агент (например, формалин), становятся более сильно перекрестно сшитыми, скорость прохождения будет изменяться в зависимости от характеристик образца. В некоторых воплощениях статус биологического образца можно контролировать, основываясь на времени прохождения звуковых волн. Статус может характеризоваться состоянием плотности, состоянием фиксации, состоянием окрашивания или тому подобным. Контроль может включать, без ограничения, измерение изменения плотности образца, степени перекрестного сшивания, декальцификации, окраски пятен или тому подобное. Биологический образец может представлять собой не жидкий образец, как например, кость или другой тип образца. В некоторых воплощениях способы и системы направлены на использование акустической энергии для контроля пробы. Информация о пробе может быть получена на основе взаимодействия между акустической энергией в отраженной и/или прошедшей модах. Могут быть выполнены связанные с акустикой измерения. Примеры измерений включают измерение амплитуды звукового сигнала, затухания, рассеяния, поглощения, времени прохождения (TOF) для пробы, сдвига фазы звуковых волн или их комбинаций. Проба в некоторых воплощениях обладает свойствами, которые изменяются во время обработки. В некоторых воплощениях для пробы применяется фиксация. Поскольку проба становится более фиксированной, механические свойства (например, эластичность, жесткость и т.д.) изменяются из-за молекулярного перекрестного сшивания. Эти изменения можно контролировать с использованием измерений скорости распространения звука посредством измерения TOF. На основании этих измерений могут быть определены связанные с фиксацией характеристики или другие гистологические характеристики пробы. Чтобы избежать недостаточной фиксации или чрезмерной фиксации, можно контролировать статические характеристики образца, динамические характеристики образца или и те и другие. Характеристики образца включают связанные с прохождением характеристики, связанные с отражением характеристики, связанные с поглощением характеристики, связанные с ослаблением сигнала характеристики или тому подобное. В некоторых воплощениях метод оценки образца включает анализ скорости звуковой волны до, во время и/или после обработки образца. Это достигается путем проведения первоначального исходного измерения для свежеполученного, нефиксированного образца путем подачи звуковой волны из передатчика на образец, взятый от субъекта. Исходное значение TOF звуковой волны регистрируют с использованием приемника. После проведения или во время проведения обработки образца, из передатчика на образец доставляют вторую звуковую волну. Второе измерение TOF звуковой волны проводят с использованием приемника после прохождения через образец второй звуковой волны. Для определения изменения скорости осуществляют сравнение скоростей звуковых волн в образце, основываясь на значениях первого TOF и второго TOF. Эти измерения могут быть уникальными для каждого анализируемого образца и, следовательно, могут быть использованы для установления исходного значения для каждого образца. Дополнительные измерения TOF можно использовать для определения вкладов в TOF, относящихся к среде, каналу измерения или тому подобному. В некоторых воплощениях, чтобы определить исходное значение TOF в средах, проводят измерение TOF в средах в отсутствие пробы. См. заявку WO 2011109769, которая тем самым включена посредством ссылки во всей своей полноте.
Липидомика
Исследования в области липидомики включают идентификацию и количественное определение тысяч молекулярных разновидностей клеточных липидов и их взаимодействий с другими липидами, белками и другими метаболитами. Исследователи в области липидомики изучают структуры, функции, взаимодействия и динамику клеточных липидов и изменения, которые происходят во время возмущения системы. Методы липидомного анализа могут включать масс-спектрометрию (MS), спектроскопию ядерного магнитного резонанса (ЯМР), флуоресцентную спектроскопию, интерферометрию двойной поляризации и компьютерные методы. В исследованиях в области липидомики, данные, количественно описывающие пространственные и временные изменения содержания и состава разных молекулярных разновидностей липидов, собирают после возмущения клеток посредством изменения их физиологического или патологического состояния. Информация, полученная из этих исследований, облегчает механистическое понимание изменений функции клеток.
Количественное определение иммунных клеток
Количественное определение иммунных клеток в образцах можно осуществлять с использованием подсчета клеток с применением основанной на эпигенетических особенностях количественной ПЦР в режиме реального времени (qPACC). Статус метилирования структуры хроматина либо активно экспрессируемых, либо молчащих генов является фундаментальным принципом основанной на эпигенетических особенностях технологии идентификации и количественного определения клеток. Открытие специфического для разных типов клеток удаления метальных групп (дезметилирования) с 5'-углерода основания цитозина в динуклеотиде цитозинфосфат-гуанин позволяет точно и достоверно провести количественное определение иммунных клеток исходя из очень небольшого количества образцов крови или ткани человека. Эти эпигенетические биомаркеры, расположенные на геномной ДНК, стабильно связаны с представляющими интерес клетками. Kleen and Yuan (November 2015), "Quantitative real-time PCR assisted cell counting (qPACC) for epigenetic - based immune cell quantification in blood and tissue", J. Immunother. Cancer, 46 (3).
Детектирование ассоциированных с раком маркеров
Детектирование "опухолевых маркеров", включая, но не ограничиваясь этим, белки, антигены, ферменты, гормоны, мутации ДНК и углеводы, ассоциированные с наличием рака, с использованием, но не ограничиваясь этим, таких методов, как секвенирование РНК, ДНК или белков, имеет важное значение для правильной диагностики типов рака и для выбора соответствующего способа лечения. Такие маркеры включают, но не ограничиваются этим, альфа-фетопротеин (часто ассоциируемый, но не ограничиваясь этим, с эмбрионально-клеточными опухолями и гепатоклеточными карциномами), СА15-3 (часто ассоциируемый, но не ограничиваясь этим, с раком молочной железы), СА27-29 (часто ассоциируемый, но не ограничиваясь этим, с раком молочной железы), СА19-9 (часто ассоциируемый, но не ограничиваясь этим, с раком поджелудочной железы, колоректальным раком и другими типами рака желудочно-кишечного тракта), СА-125 (часто ассоциируемый, но не ограничиваясь этим, с раком яичников, раком эндометрия, раком фаллопиевых труб, раком легкого, раком молочной железы и раком желудочно-кишечного тракта), кальцитонин (часто ассоциируемый, но не ограничиваясь этим, с медуллярным раком щитовидной железы), кальретинин (часто ассоциируемый, но не ограничиваясь этим, с мезотелиомой, опухолью стромы полового тяжа яичников, адренокортикальной карциномой, синовиальной саркомой), канцероэмбриональный антиген (часто ассоциируемый, но не ограничиваясь этим, с раком желудочно-кишечного тракта, раком шейки матки, раком легкого, раком яичников, раком молочной железы, раком мочевыводящих путей), CD34 (часто ассоциируемый, но не ограничиваясь этим, с гемангиоперицитомой/солитарной фиброзной опухолью, плейоморфной липомой, гастроинтестинальной стромальной опухолью, выбухающей дерматофибросаркомой), CD99MIC 2 (часто ассоциируемый, но не ограничиваясь этим, с саркомой Юинга, примитивной нейроэктодермальной опухолью, гемангиоперицитомой/солитарной фиброзной опухолью, синовиальной саркомой, лимфомой, лейкозом, опухолью стромы полового тяжа яичников), CD117 (часто ассоциируемый, но не ограничиваясь этим, с гастроинтестинальной стромальной опухолью, мастоцитозом, семиномой), хромогранин (часто ассоциируемый, но не ограничиваясь этим, с нейроэндокринной опухолью), хромосомы 3, 7, 17 и 9р21 (часто ассоциируемые, но не ограничиваясь этим, с раком мочевого пузыря), различные типы цитокератина (часто ассоциируемые, но не ограничиваясь этим, с многими типами карциномы и некоторыми типами саркомы), десмин (часто ассоциируемый, но не ограничиваясь этим, с саркомой гладких мышц, саркомой скелетных мышц и эндометриальной стромальной саркомой), поверхностный антиген эпителеоцитов (часто ассоциируемый, но не ограничиваясь этим, с различными типами карциномы, менингиомы и некоторыми типами саркомы), фактор VIII/CD31 FL1 (часто ассоциируемый, но не ограничиваясь этим, с сосудистой саркомой), глиофибрилярный кислый белок (часто ассоциируемый, но не ограничиваясь этим, с глиомой (астроцитомой, эпендимомой)), белковую жидкость при обширных кистозных болезнях (часто ассоциируемую, но не ограничиваясь этим, с раком молочной железы, раком яичников и раком слюнных желез), НМВ-45 (часто ассоциируемый, но не ограничиваясь этим, с меланомой, околососудистой опухолью из эпителиоидных клеток (PEComa) (например, ангиомиолипомой), светлоклеточной карциномой, адренокортикальной карциномой), хорионический гонадотропин человека (часто ассоциируемый, но не ограничиваясь этим, с гестанционной трофобластической болезнью, эмбрионально-клеточной опухолью и хориокарциномой), иммуноглобулин (часто ассоциируемый, но не ограничиваясь этим, с лимфомой, лейкозом), ингибин (часто ассоциируемый, но не ограничиваясь этим, с опухолью стромы полового тяжа яичников, адренокортикальной карциномой, гемангиобластомой), различные типы кератина (часто ассоциируемые, но не ограничиваясь этим, с карциномой, некоторыми типами саркомы), различные типы маркеров лимфоцитов (часто ассоциируемые, но не ограничиваясь этим, с лимфомой, лейкозом), MART-1 (мелан-А) (часто ассоциируемый, но не ограничиваясь этим, с меланомой, стероид-продуцирующими опухолями (адренокортикальной карциномой, относящейся к половым железам опухолью)), MyoD1 (часто ассоциируемый, но не ограничиваясь этим, с рабдомиосаркомой, мелкокруглоклеточной опухолью синих клеток), мышечно-специфический актин (MSA) (часто ассоциируемый, но не ограничиваясь этим, с миосаркомой (лейомиосаркомой, рабдомиосаркомой)), нейрофиламент (часто ассоциируемый, но не ограничиваясь этим, с нейроэндокринной опухолью, мелкоклеточной карциномой легкого), нейрон-специфическую енолазу (часто ассоциируемую, но не ограничиваясь этим, с нейроэндокринной опухолью, мелкоклеточной карциномой легкого, раком молочной железы), плацентарную щелочную фосфатазу (PLAP) (часто ассоциируемую, но не ограничиваясь этим, с семиномом, дисгерминомом, эмбриональной карциномой), простатоспецифический антиген (часто ассоциируемый, но не ограничиваясь этим, с раком предстательной железы), PTPRC (CD45) (часто ассоциируемый, но не ограничиваясь этим, с лимфомой, лейкозом, гистиоцитарной опухолью), белок S100 (часто ассоциируемый, но не ограничиваясь этим, с меланомой, саркомой (нейросаркомой, липомой, хондросаркомой), астроцитомой, гастроинтестинальной стромальной опухолью, раком слюнных желез, некоторыми типами аденокарциномы, гистиоцитарной опухолью (дендритная клетка, макрофаг)), актин гладких мышц (SMA) (часто ассоциируемый, но не ограничиваясь этим, с гастроинтестинальной стромальной опухолью, лейомиосаркомой, РЕСомой), синаптофизин (часто ассоциируемый, но не ограничиваясь этим, с нейроэндокринной опухолью), тиреоглобулин (часто ассоциируемый, но не ограничиваясь этим, с послеоперационным маркером рака щитовидной железы), транскрипционный фактор-1 щитовидной железы (часто ассоциируемый, но не ограничиваясь этим, со всеми типами рака щитовидной железы, рака легкого), опухолевую М2-пируваткиназу (часто ассоциируемую, но не ограничиваясь этим, с колоректальным раком, раком молочной железы, почечноклеточной карциномой, раком легкого, раком поджелудочной железы, раком пищевода, раком желудка, раком шейки матки, раком яичников), виментин (часто ассоциируемый, но не ограничиваясь этим, с саркомой, почечноклеточной карциномой, раком эндометрия, раком легкого, лимфомой, лейкозом, меланомой), перестройки гена ALK (часто ассоциируемые, но не ограничиваясь этим, с немелкоклеточным раком легкого и анапластической крупноклеточной лимфомой), бета-2-микроглобулин (В2М) (часто ассоциируемый, но не ограничиваясь этим, с множественной миеломой, хроническим лимфоцитарным лейкозом и некоторыми лимфомами), бета-хорионический гонадотропин человека (бета-hCG) (часто ассоциируемый, но не ограничиваясь этим, с хориокарциномой и эмбрионально-клеточными опухолями), мутации в генах BRCA1 и BRCA2 (часто ассоциируемые, но не ограничиваясь этим, с раком яичников), слитый ген BCR-ABL (филадельфийская хромосома) (часто ассоциируемый, но не ограничиваясь этим, с хроническим миелоидным лейкозом, острым лимфобластным лейкозом и острым миелогенным лейкозом), мутации в BRAF V600 (часто ассоциируемые, но не ограничиваясь этим, с меланомой кожи и колоректальным раком), CD20 (часто ассоциируемый, но не ограничиваясь этим, с неходжкинской лимфомой), хромогранин А (CgA) (часто ассоциируемый, но не ограничиваясь этим, с нейроэндокринными опухолями), циркулирующие опухолевые клетки эпителиального происхождения (CELLSEARCH®) (часто ассоциируемые, но не ограничиваясь этим, с метастатическими видами рака молочной железы, предстательной железы и колоректального рака), фрагмент 21-1 цитокератина (часто ассоциируемый, но не ограничиваясь этим, с раком легких), мутации в гене EGFR (часто ассоциируемые, но не ограничиваясь этим, с немелкоклеточным раком легкого), эстрогеновый рецептор (ER)/прогестероновый рецептор (PR) (часто ассоциируемые, но не ограничиваясь этим, с раком молочной железы), НЕ4 (часто ассоциируемый, но не ограничиваясь этим, с раком яичников), мутации в гене KRAS (часто ассоциируемые, но не ограничиваясь этим, с колоректальным раком и немелкоклеточным раком легкого), лактатдегидрогеназу (часто ассоциируемую, но не ограничиваясь этим, с эмбрионально-клеточными опухолями, лимфомой, лейкозом, меланомой и нейробластомой), нейрон-специфичную енолазу (NSE) (часто ассоциируемую, но не ограничиваясь этим, с мелкоклеточным раком легкого и нейробластомой), белок ядерного матрикса 22 (часто ассоциируемый, но не ограничиваясь этим, с раком мочевого пузыря), лиганд 1 белка программируемой смерти (PD-L1) (часто ассоциируемый, но не ограничиваясь этим, с немелкоклеточным рак легкого), активатор плазминогена урокиназного типа (uPA) и ингибитор активатора плазминоген (РАМ) (часто ассоциируемые, но не ограничиваясь этим, с раком молочной железы), показатели 5 белков (OVA1®) (часто ассоциируемые, но не ограничиваясь этим, с раком яичников), показатели 21 гена (Oncotype DX®) (часто ассоциируемые с раком молочной железы), показатели 70 генов (Mammaprint®) (часто ассоциируемые, но не ограничиваясь этим, с раком молочной железы) и амплификацию или сверхэкспрессию гена HER2/neu (часто ассоциируемую, но не ограничиваясь этим, с раком молочной железы, раком яичников, аденокарциномой желудочно-пищеводного соединения, раком желудка, немелкоклеточным раком легкого и раком матки). Дополнительные биомаркеры, ассоциированные с опухолями, могут включать, но не ограничиваются этим, мутацию в PI3KCA, амплификацию FGFR2, мутацию в р53, мутацию в BRCA, амплификацию CCND1, мутацию в MAP2K4, мутацию в ATR или любой другой биомаркер, экспрессия которого коррелирует с конкретным видом рака; по меньшей мере один из AFP, ALK, BCR-ABL, BRCA1/BRCA2, BRAF, V600E, Са-125, СА19.9, EGFR, Her-2, KIT, PSA, S100, KRAS, ER/Pr, UGT1A1, CD30, CD20, F1P1L1-PDGRFa, PDGFR, TMPT и TMPRSS2; или по меньшей мере один биомаркер, выбранный из АВСВ5, AFP-L3, альфа-фетопротеина, альфа-метил-ацил-КоА-рацемазы, BRCA1, BRCA2, СА 15-3, СА 242, СА 27-29, СА-125, СА15-3, СА19-9, кальцитонина, канцероэмбрионального антигена, пептида-1 канцероэмбрионального антигена, дез-гамма-карбоксипротромбина, десмина, раннего антигена-2 рака предстательной железы, рецептора эстрогенов, продукта деградации фибрина, глюкозо-6-фосфат-изомеразы, антигена HPV, такого как vE6, Е7, L1, L2 или p16INK4a, хорионического гонадотропина человека, IL-6, кератина 19, лактатдегидрогеназы, лейциламинопептидазы, липотропина, метанефринов, неприлизина, nmp22, норметанефрина, РСА3, простатоспецифического антигена, кислой фосфатазы предстательной железы, синаптофизина, тиреоглобулина, TNF, транскрипционного фактора, выбранного из ERG, ETV1 (ER81), FLU, ETS1, ETS2, ELK1, ETV6 (TEL1), ETV7 (TEL2), GABPa, ELF1, ETV4 (E1AF; РЕА3), ETV5 (ERM), ERF, PEA3/E1AF, PU.1, ESE1/ESX, SAP1 (ELK4), ETV3 (METS), EWS/FLI1, ESE1, ESE2 (ELF5), ESE3, PDEF, NET (ELK3; SAP2), NERF (ELF2) или FEV, опухолеассоциированного гликопротеина 72, c-kit, SCF, pAKT, pc-kit и виментина. Альтернативно или в дополнение к этому представляющим интерес биомаркером может быть ингибитор контрольных точек иммунного ответа, таких как, но не ограничиваясь этим, CTLA-4, PDL1, PDL2, PD1, В7-Н3, В7-Н4, BTLA, HVEM, KIR, TIM3, GAL9, GITR, LAG3, VISTA, KIR, 2В4, TRPO2, CD160, CGEN-15049, CHK1, CHK2, A2aR, TL1A и лиганды В-7 семейства или их комбинация, либо может быть лиганд белков - контрольных точек, выбранных из группы, состоящей из CTLA-4, PDL1, PDL2, PD1, В7-Н3, В7-Н4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2В4, CD160, CGEN-15049, CHK1, CHK2, A2aR, лигандов В-7 семейства или их комбинации. Способ с применением дополнительных маркеров может включать, но не ограничивается этим, детектирование по меньшей мере одного биомаркера, ассоциированного с острым лимфобластным лейкозом (etv6, am11, циклофилина b), В-клеточной лимфомой (lg-идиотипа), глиомой (Е-кадгерина, альфа-катенина, бета-катенина, галша-катенина, р120 ctn), раком мочевого пузыря (p21ras), раком желчных протоков (p21ras), раком молочной железы (представителя MUC семейства, HER2/neu, c-erbB-2), карциномой шейки матки (р53, p21ras), раком толстой кишки (p21ras, HER2/neu, c-erbB-2, представителя MUC семейства), колоректальным раком (антигена, ассоциированного с толстой и прямой кишкой (CRC)-C017-1A/GA733, АРС), хориокарциномой (СЕА), плоскоклеточным раком (циклофилина b), раком желудка (HER2/neu, c-erbB-2, гликопротеина ga733), гепатоклеточным раком (зльфа-фетопротеина), лимфомой Ходжкина (Imp-1, EBNA-1), раком легкого (СЕА, MAGE-3, NY-ESO-1), лейкозом, начинающимся в лимфоидных клетках (циклофилина b), меланомой (белка p5, gp75, онкофетального антигена ганглиозидов GM2 и GD2, мелан-A/MART-1, cdc27, MAGE-3, p21ras, gp100.sup.PmeI117), миеломой (представителя MUC семейства, p21ras), немелкокпеточным раком легкого (HER2/neu, c-erbB-2), раком носоглотки (Imp-1, EBNA-1), раком яичников (представителя MUC семейства, HER2/neu, с-erbB-2), раком предстательной железы (простатоспецифического антигена (PSA) и его антигенных эпитопов PSA-1, PSA-2 и PSA-3, PSMA, HER2/neu, c-erbB-2, гликопротеина ga733), почечным раком (HER2/neu, c-erbB-2), случаями плоскоклеточного рака шейки матки и пищевода (продуктов вирусного происхождения, таких как белки папилломавируса человека), раком яичка (NY-ESO-1) и/или Т-клеточным лейкозом (эпитопов HTLV-1).
В настоящее время известно, что точное направленное воздействие на конкретные особенности киназных каскадов обеспечивает ранее недостижимые прорывы в терапии заболеваний. Важность протеинкиназного семейства подчеркивается многочисленными болезненными состояниями, которые возникают в результате дисрегуляции активности киназ. Аберрантная передача сигнала в клетках многими из этих протеинкиназ и липидных киназ может приводить к таким заболеваниям, как рак. Известно, что некоторые сериновые/треониновые и тирозиновые протеинкиназы активируются в раковых клетках и способствуют росту и прогрессированию опухолей. Технология, описанная в данной заявке, предусматривает способы обогащения (или выделения) киназ, например АТФ-зависимых киназ, с использованием одного или более захватывающих киназы агентов. Примеры захватывающих киназы агентов включают, но не ограничиваются этим, относительно неселективные ингибиторы протеинкиназ, субстраты или псевдосубстраты. Данные способы полезны, например, для профилирования киномов с использованием тандемной масс-спектрометрии. Хотя ранее были идентифицированы многие высокоселективные и сильнодействующие низкомолекулярные ингибиторы киназ, которые описаны в данной заявке выше, также было идентифицировано большое число относительно неселективных низкомолекулярных ингибиторов киназ. Для способов, описанных в данной заявке, применение относительно неселективных низкомолекулярных ингибиторов киназ снижает потребность в оптимизации методик очистки для индивидуальных киназ и усиливает аналитический сигнал, генерируемый образцами обогащенных ферментов, в норме присутствующих в клетках, тканях и жидкостях организма только в каталитических концентрациях. Однако, следует признать, что селективные низкомолекулярные ингибиторы киназ также могут быть полезны в этих методах анализа киназ. Помимо этого, в таких методах может быть полезна комбинация неселективных и селективных низкомолекулярных ингибиторов киназ. Кроме того, захватывающий киназу агент (или более чем один захватывающий киназу агент) также может быть объединен с захватывающим фосфатазу агентом для одновременного обогащения (или выделения) киназ и фосфатаз. Способы, описанные в даннойзаявке, также могут быть применены для мультиплексного анализа протеинкиназ и/или фосфатаз с использованием тандемной масс-спектрометрии для одной или нескольких проб. Технология, описанная в данной заявке, предусматривает способ анализа популяции киназ, такой как кином. Способ включает выделение киназ из образца с использованием одного или более чем одного захватывающего киназу агента, протеолитического расщепления белка в образце до составляющих его пептидов (например, протеазой, такой как трипсин), добавление к полученным пептидам рационально сконструированных калибровочных пептидов, родственных конкретным пептидным последовательностям протеинкиназ, которые содержат поддающиеся расщеплению связи аспартат-пролин (DP), и количественное определение нативных пептидов, происходящих из популяции киназ, тандемной масс-спектрометрией. Также описаны стратегии профилирования относительного содержания протеинкиназ и липидных киназ в многочисленных образцах с использованием изобарных пептидных меток, содержащих поддающиеся расщеплению связи DP. Специалисту в данной области техники будет известно, что аналогичная методология может быть применена для анализа фосфатаз или комбинации киназ и фосфатаз. См. заявку WO 2007131191, которая тем самым включена посредством ссылки во всей своей полноте.
Аффинная очистка клеток конкретного типа
Сообщается, что циркулирующие опухолевые клетки предположительно обнаружены во многих опухолях человека, включая AML, CML, множественную миелому, опухоли головного мозга, опухоли молочной железы, меланому и рак предстательной железы, рак толстой кишки и рак желудка. В принципе, циркулирующие опухолевые клетки могут быть идентифицированы с использованием различных экспериментальных стратегий. Многие циркулирующие опухолевые клетки, по-видимому, экспрессируют маркеры клеточной поверхности, которые отождествляются со своими существующими в норме аналогами. Это наблюдение обеспечивает относительно простую методику обогащения с использованием либо основанной на проточной цитометрии сортировки клеток, либо основанной на применении микрогранул аффинной очистки клеток. См. Schawb, М. Encyclopedia of Cancer, 3rd edition, Springer-Verlag, Berlin Heidelberg, 2011.
Секвенирование ДНК
В следующих типичных воплощениях ДНК в образце или в одной или большем числе клеток в нем может быть подвергнута секвенированию. Секвенирование ДНК может быть направленным, например, на конкретные гены, участки, регуляторные последовательности, интроны, экзоны, SNP, возможные слитые молекулы и т. д., например, с целью детектирования последовательностей, ассоциированных с раком или имеющих отношение к его диагностике. Секвенирование ДНК может также быть проведено на целом геноме или значительной его части. Типичные методы секвенирования, которые могут быть использованы, включают, без ограничения, секвенирование по Сэнгеру и секвенирование с использованием технологии красителя-терминатора, а также технологии секвенирование следующего поколения (NGS), такие как пиросеквенирование, нанопоровое секвенирование, секвенирование с использованием микропор (micropore-based sequencing), секвенирование на наносферах, MPSS, технологии SOLiD™, Solexa, Ion Toppent, Starlite, SMRT, tSMS, секвенирование путем синтеза, секвенирование через лигирование, масс-спектрометрическое секвенирование, секвенирование с использованием полимеразы, секвенирование с использованием РНК-полимеразы (RNAP), секвенирование на основе микроскопии (microscopy-based sequencing), микрожидкостное секвенирование по Сэнгеру, секвенирование на основе микроскопии, RNAP-секвенирование, секвенирование ДНК с использованием туннельных токов и секвенирование с использованием вируса in vitro (in vitro virus sequencing). См. заявки WO 2014144478, WO 2015058093, WO 2014106076 и WO 2013068528, каждая из которых тем самым включена посредством ссылки во всей своей полноте.
Технологии секвенирования ДНК развиваются экспоненциально. С недавнего времени с использованием технологий высокопроизводительного секвенирования (или секвенирования следующего поколения) распараллеливают процесс секвенирования, осуществляя за один раз секвенирование сразу тысяч или миллионов последовательностей. В режиме сверхвысокой производительности секвенирования параллельно могут быть проведены порядка 500000 операций секвенирования путем синтеза. Секвенирование следующего поколения снижает затраты и значительно увеличивает скорость по сравнению со стандартными рабочими методами секвенирования с использованием технологии красителя-терминатора.
При проведении пиросеквенирования ДНК амплифицируется внутри капель воды в масляном растворе (эмульсионная ПЦР), при этом каждая капля содержит единственную матрицу ДНК, присоединенную к одной покрытой праймером грануле, которая затем образует клональную колонию (clonal colony). Секвенатор содержит много лунок пиколитрового объема, каждая из которых содержит одну гранулу и ферменты для секвенирования. При проведении пиросеквенирования используют люциферазу для генерации света с целью детекции индивидуальных нуклеотидов, добавленных к растущей ДНК, и объединенные данные используют для получения сведений о последовательности. См. работу Margulies, М et al. 2005, Nature, 437, 376-380, которая тем самым включена посредством ссылки во всей своей полноте. Пиросеквенирование представляет собой технологию секвенирования путем синтеза, в которой также используется пиросеквенирование. Пиросеквенирование ДНК включает в себя две стадии. На первой стадии ДНК нарезают на фрагменты приблизительно 300-800 пар оснований, фрагменты, имеющие тупые концы. По концами этих фрагментов затем лигируют олигонуклеотидные адаптеры. Адаптеры служат в качестве праймеров для амплификации и секвенирования данных фрагментов. Фрагменты могут быть присоединены к захватывающим ДНК гранулам, например, покрытым стрептавидином гранулам, с использованием, например, адаптора В, который содержит 5'-биотиновую метку. Фрагменты, присоединенные к гранулам, амплифицируют посредством ПЦР внутри капель в эмульсии типа масло в воде. Результатом является получение множественных копий клонально амплифицированных фрагментов ДНК на каждой грануле. На второй стадии, гранулы захватывают в лунки (пиколитрового размера). Пиросеквенирование проводят параллельно для каждого из фрагментов ДНК. В результате добавления одного или более нуклеотидов генерируется световой сигнал, который регистрируют в секвенаторе с использованием CCD камеры. Интенсивность сигнала пропорциональна количеству встроенных нуклеотидов. В пиросеквенировании используется пирофосфат (PPi), который высвобождается при добавлении нуклеотида. PPi превращают в АТФ с использованием АТР-сульфурилазы в присутствии аденозин-5'-фосфосульфата. Люцифераза использует АТФ для превращения люциферина в оксилюциферин, и в результате этой реакции генерируется свет, который детектируют и анализируют. В другом воплощении пиросеквенирование используют для измерения генной экспрессии. Пиросеквенирование РНК применяется аналогично пиросеквенированию ДНК и выполняется посредством присоединения частичных последовательностей генов рРНК к микроскопическим гранулам и затем помещения присоединенных последовательностей в отдельные лунки. Эту присоединенную частичную последовательности рРНК далее амплифицируют, чтобы определить профиль генной экспрессии. Sharon Marsh, Pyrosequencing® Protocols in Methods in Molecular Biology, Vol. 373, 15-23 (2007).
Другим примером метода секвенирования, который можно использовать в способах по предложенному изобретению, является нанопоровое секвенирование (работа Soni G.V. and Meller., Clin. Chem., 53: 1996-2001, 2007, которая тем самым включена посредством ссылки во всей своей полноте). Нанопора представляет собой небольшое отверстие, примерно 1 нанометр в диаметре. Погружение нанопоры в проводящую жидкость и приложение к ней разности потенциалов приводит к получению слабого электрического тока, обусловленного прохождение через нанопору ионов. Вличина проходящего тока зависит от размера нанопоры. По мере прохождения молекулы ДНК через нанопору, каждый нуклеотид на молекуле ДНК перекрывает нанопору в разной степени. Таким образом, изменение тока, протекающего через нанопору, по мере прохождения через нанопору молекулы ДНК, имитирует считывание последовательности ДНК. См. работу Bayley, Clin. Chem., 2015 Jan, 61 (1): 25-31, которая тем самым включена посредством ссылки во всей своей полноте.
Другим примером методов детектирования ДНК и РНК, который можно использовать в способах по предложенному изобретению, является технология SOLiD™ (Applied Biosystems). Системы технологии SOLD™ представляют собой технологию секвенирования через лигирование, которая может быть использована для проведения массового параллельного секвенирования следующего поколения, как для ДНК, так и РНК. При секвенировании ДНК с использованием технологии SOLiD™ геномную ДНК нарезают на фрагменты и к 5'- и 3'-концам фрагментов присоединяют адапторы для создания библиотеки фрагментов. Альтернативно, внутренние адаптеры могут быть введены посредством лигирования адаптеров по 5'- и 3'-концам фрагментов, циклизации фрагментов, расщепления циклизованных фрагментов с образованием внутреннего адаптера и присоединения адаптеров к 5'- и 3'-концам полученных фрагментов для создания библиотеки с длинной вставкой. Далее получают клональные популяции гранул в микрореакторах, содержащих гранулы, праймеры, матрицу и компоненты ПЦР. После проведения ПЦР, матрицы подвергают денатурации и производят обогащение гранул для отделения гранул с удлиненными матрицами. Матрицы на отобранных гранулах подвергают модификации по 3'-концу, которая позволяет осуществить связывание с предметным стеклом. Последовательность может быть определена посредством последовательной гибридизации и лигирования частично случайных олигонуклеотидов с определенным центральным основанием (или парой оснований), которое идентифицируют с использованием специфического флуорофора. После регистрации излучения лигированный олигонуклеотид отщепляют и удаляют, и затем процесс овторяют.
В других воплощениях SOLD™, для измерения экспрессии генов используют серийный анализ экспрессии генов (SAGE). Серийный анализ экспрессии генов (SAGE) представляет собой способ, который позволяет провести одновременный и количественный анализ большого числа генных транскриптов, без необходимости предоставления отдельного гибридизационного зонда для каждого транскрипта. Сначала получают метку с короткой последовательностью (примерно 10-14 п.о.), которая содержит достаточную информацию для однозначной идентификации транскрипта, при условии, что данную метку получают для уникального положения в каждом транскрипте. Затем множество транскриптов соединяют друг с другом с образованием длинных последовательных молекул, которые можно секвенировать, одновременно выявляя идентичность многочисленных меток. Картину экспрессии любой популяции транскриптов можно оценить количественно, определив относительное содержание индивидуальных меток и идентифицировав ген, соответствующий каждой метке. Более подробно см., например, работу Velculescu et al., Science, 270: 484 487 (1995) и Velculescu et al., Cell, 88: 243 51 (1997), содержание которой включено посредством ссылки в данное описание во всей своей полноте).
Другой метод секвенирования, который можно использовать в способах по предложенному изобретению, включает, например, технологию фирмы Helicos точного одномолекулярного секвенирования (tSMS) (Harris T.D. et al. (2008) Science, 320: 106-109). В методе tSMS, образец ДНК расщепляют на нити размером приблизительно от 100 до 200 нуклеотидов и к 3'-концу каждой нити ДНК добавляют поли(А)-последовательность. Каждую нить метят, добавляя флуоресцентно меченный содержащий аденозин нуклеотид. Нити ДНК затем гибридизуют в проточной ячейке, которая содержит миллионы захватывающих сайтов с олиго(Т), иммобилизованными на поверхности проточной ячейки. Плотность данных матриц может составлять примерно 100 матриц/см. Проточную ячейку далее помещают в прибор, например, секвенатор HeliScope, и с использованием лазера освещают поверхность проточной ячейки, выявляя положение каждой матрицы. CCD-камера может отражать положение матриц на поверхности проточной ячейки. Затем производят отщепление и отмывание флуоресцентной метки матрицы. Реакцию секвенирования начинают с введения ДНК-полимеразы и флуоресцентно меченого нуклеотида. Олиго(Т)-нуклеиновая кислота служит в качестве праймера. Полимераза катализирует включение меченых нуклеотидов в праймер в соответствии с матрицей. Полимеразу и невключившиеся нуклеотиды удаляют. Матрицы, в которые целенаправленно включен флуоресцентно меченый нуклеотид, детектируют посредством визуализации на поверхности проточной ячейки. После проведения визуализации, на стадии отщепления производят удаление флуоресцентной метки и процесс повторяют с другими флуоресцентно меченными нуклеотидами до получения желаемой длины считывания. Информацию о последовательности собирают на каждой стадии присоединения нуклеотида. Дальнейшее описание tSMS показано, например, в Lapidus и др. (патент США с номером 7169560), Lapidus и др. (заявка на патент США с номером 2009/0191565), Quake и др. (патент США с номером 6818395), Harris (патент США с номером 7282337), Quake и др. (заявка на патент США с номером 2002/0164629) и Braslavsky, et al., PNAS (USA), 100: 3960-3964 (2003), все это включено в данное описание посредством ссылки во всей своей полноте.
Другой пример технологии секвенирования, который можно использовать в способах по предложенному изобретению, включает одномолекулярную, в режиме реального времени, технологию (SMRT) секвенирования последовательности как ДНК, так и РНК от Pacific Biosciences. В технологии SMRT каждое из четырех оснований ДНК присоединяют к одному из четырех различных флуоресцентных красителей. Эти красители присоединены к фосфатной цепи. Одну молекулу ДНК-полимеразы иммобилизуют с одной молекулой матрицы одноцепочечной ДНК на дне волновода с нулевой модой (ZMW). ZMW представляет собой изолированную структуру, которая дает возможность наблюдать включение единичного нуклеотида, катализируемое ДНК-полимеразой, на фоне флуоресцирующих нуклеотидов, которые быстро диффундируют из ZMW (за микросекунды). Для включения нуклеотида в растущую цепь требуется несколько миллисекунд. За этот промежуток времени флуоресцентная метка возбуждается и генерирует флуоресцентный сигнал, и флуоресцентная метка отщепляется. Детектирование соответствующей флуоресценции красителя указывает на то, какое основание было включено. Процесс повторяют. Чтобы секвенировать последовательность РНК, ДНК-полимеразу в ZMW заменяют на обратную транскриптазу и процесс проводят соответствующим образом.
Другой пример метода секвенирования, который можно использовать в способах по предложенному изобретению, включает применение массива с химически-чувствительным полевым транзистором (chemFET) для секвенирования ДНК (например, как описано в публикации патентной заявки США №20090026082). В одном из примеров данного метода молекулы ДНК могут быть помещены в реакционные камеры и молекулы матрицы могут быть гибридизованы с праймером для секвенирования, связанным с полимеразой. Включение одного или более трифосфатов в новую ветвь нуклеиновой кислоты при 3'-конце праймера для секвенирования можно детектировать по изменению тока chemFET. Массив может содержать много chemFET сенсоров. В другом примере одиночные молекулы нуклеиновой кислоты могут быть присоединены к гранулам и молекулы нуклеиновой кислоты могут быть амплифицированы на грануле, отдельные гранулы могут быть перенесены в отдельные реакционные камеры массива chemFET, где каждая камера имеет chemFET сенсор, и нуклеиновые кислоты могут быть секвенированы.
Другой пример метода секвенирования, который можно использовать в способах по предложенному изобретению, включает применение электронного микроскопа (Moudrianakis E.N. and Beer M. Proc. Natl. Acad. Sci. USA, 1965, March, 53: 564-71). В одном из примеров данного метода отдельные молекулы ДНК метят с использованием металлических меток, которые можно различить с использованием электронного микроскопа. Затем эти молекулы растягивают на плоской поверхности и подвергают визуализации с использованием электронного микроскопа для определения последовательностей.
Секвенирование ДНК на наносферах представляет собой тип высокопроизводительной технологии секвенирования, используемой для определения всей геномной последовательности организма. В способе используется репликация по типу катящегося кольца для амплификации небольших фрагментов геномной ДНК с образованием наносфер ДНК. Затем, для определения нуклеотидной последовательности используется свободное (unchained) секвенирование через лигирование. Этот метод секвенирования ДНК позволяет за один прием секвенировать большое количество наносфер ДНК. См. WO 2014122548 и Drmanac et al., Science, 2010 Jan, 1, 327 (5961): 78-81; Porreca, Nat. Biotechnol., 2010 Jan, 28 (1): 43-4; все они тем самым включены посредством ссылки во всей своей полноте.
Массивно-параллельное опознавательное секвенирование (MPSS) было одной из ранних технологий секвенирования следующего поколения. В MPSS используется комплексный подход лигирования адаптеров с последующим декодированием адаптеров, прочтением последовательности с шагом в четыре нуклеотида.
Полони-секвенирование объединяет in vitro библиотеку парных меток (paired-tag) с эмульсионной ПЦР, применением автоматизированного микроскопа и химическими методиками секвенирования через лигирование для секвенирования генома Е. coli. Эта технология также включена в платформу SOLiD™ от Applied Biosystems.
В методе секвенирования, разработанном Solexa, молекулы ДНК и праймеры первоначально прикрепляют к предметному стеклу и амплифицируют с использованием полимеразы, таким образом, чтобы образовались локальные клональные колонии, т.е. первоначально созданные "колонии ДНК". Для определения последовательности добавляют четыре типа обратимых оснований-терминаторов (RT-оснований) и проводят отмывку невключившихся нуклеотидов. В отличие от пиросеквенирования цепи ДНК удлиняются за один раз на один нуклеотид, и получение изображения может выполняться с задержкой по времени, позволяя захватывать большие массивы колоний ДНК посредством последовательных изображений, сделанных из одной камеры. В технологии SOLiD применяется секвенирование через лигирование. Здесь, пул всех возможных олигонуклеотидов фиксированной длины метят в соответствии секвенированным положением.
Олигонуклеотиды отжигают и лигируют; предпочтительное лигирование с использованием ДНК-лигазы согласующихся последовательностей приводит к получению сигнала, несущего информацию о нуклеотиде по этому положению. Перед проведением секвенирования, ДНК амплифицируют, используя эмульсионную ПЦР. Полученные гранулы, каждая из которых содержит одну копию одной и той же молекулы ДНК, осаждают на предметное стекло. Результатом является получение последовательностей, по количеству и длине сопоставимых с секвенированием от Solexa.
В случае секвенирования по технологии Ion Toppent™ ДНК разрезают на фрагменты длиной приблизительно 300-800 пар оснований, имеющие тупые концы. Затем по концам фрагментов лигируют олигонуклеотидные адаптеры. Адаптеры служат в качестве праймеров для амплификации и секвенирования фрагментов. Фрагменты могут быть присоединены к поверхности, и их присоединяют на таком расстоянии, чтобы фрагменты были отделены друг от друга. Добавление одного или более нуклеотидов приводит к высвобождению протона (Н+), сигнал от которого детектируют и регистрируют с использованием секвенатора. Интенсивность сигнала пропорциональна числу встроенных нуклеотидов. Данные по Ion Toppent также могут выводиться как файл FASTQ. См. публикации заявок США с номерами 2009/0026082, 2009/0127589, 2010/0035252, 2010/0137143, 2010/0188073, 2010/0197507, 2010/0282617, 2010/0300559, 2010/0300895, 2010/0301398 и 2010/0304982, каждая из которых тем самым включена посредством ссылки во всей своей полноте.
Детектирование ассоциированных с раком слитых белков
Слитые гены могут вносить вклад в образование опухолей, поскольку слитые гены могут продуцировать гораздо более активный аномальный белок, чем неслитые гены. Часто, слитые гены являются онкогенами, которые вызывают рак; они включают BCR-ABL, TEL-AML1 (ALL с t(12; 21)), AML1-ETO (М2 AML с t(8; 21)) и TMPRSS2-ERG с интерстициальной делецией в хромосоме 21, часто встречающейся при раке предстательной железы. В случае TMPRSS2-ERG, нарушая передачу сигнала с андрогенного рецептора (AR) и ингибируя экспрессию AR посредством онкогенного транскрипционного фактора ETS, слитый продукт регулирует рак предстательной железы. Большинство слитых генов обнаруживают при гематологических онкологических заболеваниях, саркомах и раке предстательной железы. Онкогенные слитые гены могут приводить к образованию генного продукта с новой функцией или функцией, отличающейся от функции двух партнеров по слиянию. Альтернативно, протоонкоген сливается с сильным промотором, и поэтому онкогенная функция настроена на активацию, обуславливаемую этим сильным промотором расположенного вверх по течению партнера по слиянию. Последний случай является общим для лимфом, где онкогены располагаются рядом с промоторами генов иммуноглобулинов. Образование онкогенных слитых транскриптов также может быть вызвано транссплайсингом или событиями, связанными со сквозным прохождением. Наличие определенных хромосомных аберраций и образующихся в результате них слитых генов обычно используют для диагностики рака с целью установления точного диагноза. Дифференциальное окрашивание хромосом, флуоресцентная гибридизация in situ (FISH), полимеразная цепная реакция с обратной транскрипцией (RT-ПЦР) и методы секвенирования следующего поколения (экзом и/или транскриптом) являются распространенными методами, применяемыми в диагностических лабораториях для идентификации ассоциированных с раком слитых белков.
Детектирование маркеров устойчивости к химиотерапии
Лекарственная устойчивость представляет собой случай неэффективности химиотерапии злокачественных опухолей, при этом такая устойчивость либо является существовавшей ранее (собственной устойчивостью), либо индуцированной лекарственными средствами (приобретенной устойчивостью). Детектирование маркеров устойчивости основано, но не ограничивается этим, на идентификации карцинома-ассоциированных фибробластов посредством иммуногистохимии и проточной цитометрии, альдегид-дегидрогеназы 1, расщепляющей каспазы 3, циклооксигеназы 2, фосфорилированных белков Akt, Ki-67 и Н2АХ с использованием иммуногистохимического окрашивания, экспрессии Р-гликопротеина, гиалуронана (основного гликозаминогликанового компонента внеклеточного матрикса), на увеличении в 3q26.2 и потерях в 6q11.2-12, 9р22.3, 9р22.2-22.1, 9р22.1-21.3, Хр22.2-22.12, Хр22. 11-11.3 и Хр11.23-11.1, как идентифицировано с использованием сравнительной геномной гибридизации целого генома, сверхэкспрессии LRP, которую идентифицируют посредством иммуноокрашивания, HGF и с-МЕТ, которые представляют собой генные продукты, связанные с микроРНК MiR-193a-5p, как установлено с использованием секвенирования РНК, сверхэкспрессии CD44, идентифицированной посредством сортировки клеток, и трихостатина А, сильнодействующего ингибитора гистондеацетилаз. Маркеры устойчивости к химиотерапии часто могут принимать форму сверхэкспрессии белка, идентификацию такой сверхэкспрессии на уровне ДНК, РНК или белка (или того и другого) осуществляют, используя такие методы, как, но не ограничиваясь этим, секвенирование ДНК, секвенирование РНК и секвенирование белка. Некоторые маркеры устойчивости к химиотерапии принимают форму эпигенетических изменений, и идентификация этих изменений посредством пиросеквенирования ДНК может быть особенно полезной для идентификации маркеров устойчивости к химиотерапии. Кроме того, мутации в генах могут непосредственно влиять на экспрессию генного продукта, что может приводить к образованию раковых клеток, и идентификация мутаций в генах посредством секвенирования ДНК является очень полезной. В настоящее время, устойчивость обычно диагностируют в ходе лечения после продолжительного периода введения лекарственных средств. В течение некоторого периода времени могут быть обнаружены специфические мутации, которые придают устойчивость к ингибиторам тирозинкиназ, например, ингибиторам рецептора эпителиального фактора роста (EGFR). Детектирование таких мутаций, как Т790М, в гене EGFR с использованием ПЦР или секвенирования ДНК указывает на устойчивость к ингибированию тирозинкиназы EGFR и исключает возможность лечения пациентов такими ингибиторами, в особенности в случае немелкоклеточного рака легкого. В настоящее время существуют методы быстрой оценки лекарственной устойчивости. Обычно используют три класса методик тестирования: тесты на свежих культурах опухолевых клеток, тесты на биомаркеры рака и тесты с использованием позитронно-эмиссионной томографии (PET). Лекарственную устойчивость можно диагностировать до лечения, используя тестирование in vitro на свежих культурах опухолевых клеток, и по истечению короткого периода лечения, используя тестирование in vivo с применением PET. См. Lippert Т. et al. (2011). "Current status of methods to assess cancer drug resistance". Int. J. Med. Sci., 8 (3): 245-253.
Кроме того, поскольку присутствие опухолевых клеток в дринирующих лимфатических узлах является указанием на метастатический потенциал рака, определение профиля устойчивости опухолевых клеток, которые уже покинули первичную опухоль, имеет первостепенное значение. Отбор репрезентативных образцов из иссеченных лимфатических узлов (или других лимфатических тканей) в соответствии с описанными выше способами для оценки терапевтической устойчивости будет очень полезным. Лимфатическая система включает в себя лимфатические узлы (такие как лимфатические узлы шейки матки, поясничные лимфатические узлы, лимфатические узлы таза, паховые лимфатические узлы и аксиллярные лимфатические узлы), а также другие органы, состоящие из лимфатической ткани (такие как селезенка и тимус), и следует понимать, что она также включает лимфатические сосуды молочной железы, расширение грудного протока, лимфатические сосуды нижних конечностей, грудной проток и лимфатические сосуды верхних конечностей). В настоящее время, анализ маркеров устойчивости в лимфатических узлах и лимфатической ткани не практикуется вследствие ограниченного количества образца. Однако, способы отбора репрезентативных образцов, описанные в данной заявке, предусматривают метод характеристики геномного профиля этой ткани.
Использование репрезентативных образцов для получения опухолеспецифичных антигенов или опухолеспецифичных антител и приготовления противоопухолевых вакцины
Как уже упомянуто выше, другое применение образцов по изобретению предназначено для выделения опухолевых клеток и антигенов, происходящих из них, которые можно использовать для получения опухолеспецифичных антител или для изготовления противораковых или противоопухолевых вакцин.
Одним из подходов к вакцинации против рака является отделение белков от раковых клеток и иммунизация раковых пациентов этими белками в надежде на стимулирующую иммунную реакцию, которая может убить раковые клетки. Терапевтические вакцины против рака разрабатываются для лечения рака молочной железы, легкого, толстой кишки, кожи, почки, предстательной железы и других видов рака. Фактически, одна такая вакцина, разработанная Dendreon Corporation для лечения рака предстательной железы, 29 апреля 2010 года получила одобрение Управления по контролю качества пищевых продуктов и лекарственных средств США (FDA) для применения в лечении пациентов с диагнозом распространенного рака предстательной железы. Одобрение этой вакцины Provenge® стимулировало возобновление интереса к этому типу терапии.
Например, опухолевые клетки или расщепленные протеолитическим путем антигены клеточной поверхности, происходящие из опухолевых клеток, идентифицированных в гомогенизированных опухолевых образцах по изобретению, могут быть использованы в разработке эффективных терапевтических или профилактических противоопухолевых вакцин. Эти антигены могут быть немодифицированы или мультимеризованы либо конъюгированы с другими группировками, например, другими белками, адъювантами, или введены в клетки, например, дендритные клетки. Показано, что в результате протеолитической обработки живых раковых клеток может происходить высвобождение антигенных мишеней, достаточное для индуцирования противоракового иммунного ответа, который превышает таковой в необработанных раковых клетках in vitro. (Lokhov et al., J. Cancer, 2010, 1: 230-241).
В конкретном воплощении изобретения предложены противоопухолевые вакцины, содержащие один антиген или смесь разных антигенов, происходящих из опухолевых клеток, выделенных из образца от конкретного пациента, по существу предложено приготовление "персонализированной вакцины против рака", благодаря чему пациент может получать лечение иммунностимулирующими группировками, специфичными к конкретному для них типу опухоли. В общем случае эти вакцины будут содержать эффективное количество таких антигенов для получения эффективного иммунного ответа, например, антиген-специфического CTL ответа на опухолевые клетки, экспрессирующие данные конкретные антигены. Как уже упомянуто, в некоторых случаях эти антигены могут быть введены в другие группировки, например, дендритные клетки. Как правило, такие вакцины также будут содержать другие иммунные адъюванты, например, цитокины, агонисты толл-подобного рецептора (TLR), агонисты или антагонисты фактора/рецептора фактора некроза опухоли (TNF/R), агенты, которые модулируют ингибиторы контрольных точек, и тому подобное. Хотя на самом основном уровне, сам репрезентативный образец может быть использован непосредственно в качестве терапевтического средства. Например, первичную опухоль, удаленную у пациента, можно гомогенизировать согласно способам, описанным в данной заявке, и репрезентативный образец снова ввести инъекцией пациенту для получения иммунного ответа на опухолевые антигены, содержащиеся в образце. Ожидается, что сам репрезентативный образец будет иметь наиболее разнообразный связанный с опухолью антигенный профиль, поскольку он содержит все субклоны (например, преобладающие, первичные, вторичные, с низким показателем распространенности и т. д.).
Кроме того, согласно изобретению также предложено применение таких антигенов для приготовления образцов антисыворотки и моноклональных антител. Эти антитела можно использовать в диагностических целях, т. е. для обнаружения опухолевых клеток или антигенов в образцах. Альтернативно такие антитела, в частности, человеческие или гуманизированные антитела, обладающие специфичностью к таким опухолевым антигенам, можно использовать для терапевтического лечения злокачественных новообразований, которые экспрессируют эти антигены. Способы получения антител для возможного применения в терапии хорошо известны в данной области техники.
Кроме того, согласно изобретению также предложено применение репрезентативных образцов от субъекта для идентификации популяции В-клеточных рецепторов и/или Т-клеточных рецепторов, информацию о которой, в свою очередь, можно использовать для создания стратегически важной вакцины.
Кроме того, репрезентативные образцы, приготовленные способами по изобретению, также можно использовать для разработки CAR-T систем.
Применение репрезентативных образцов для детектирования неоантигенов
Идентификация неоантигенов из выделенных опухолевых клеток имеет первостепенное значение для лечения субъекта с диагнозом ракового(ых) заболевания(ий). Таким образом, образцы, приготовленные с использованием данного описания, могут быть объектом для любых релевантных диагностических методов, таких как, но не ограничиваясь этим, методы, рассмотренные в настоящей заявке, для идентификации биомаркера-неоантигена в образце опухоли.
Неоантигены получаются в результате мутаций, происходящих во время роста опухоли, и отличаются от нативных антигенов, к которым иммунная система толерантна. Растущее количество данных свидетельствует о том, что иммунное отторжение опухолей, например то, что наблюдается с модуляторами контрольных точек, может быть опосредовано распознаванием неоантигенов. Неоантигены обладают возможностью: (1) однозначно маркировать опухоль (по сравнению с неопухолевыми клетками) для распознавания и разрушения, например, под действием иммунной системы (см. работу Lennerz et al., 2005, Ргос. Natl. Acad. Sci. USA, 102 (44): 16013-8, которая тем самым включена посредством ссылки во всей своей полноте); и (2) избегать центральной и иногда периферической толерантности и, ввиду этого, быть распознаваемыми при направленном лечении рака (см. работу Gotter et al. "Medullary Epithelial Cells of the Human Thymus Express a Highly Diverse Selection of Tissue-specific Genes Colocalized in Chromosomal Clusters". J. Exp. Med., 199.2 (2004): 155-166, которая тем самым включена посредством ссылки во всей своей полноте). См. заявку US 20110293637 А1, которая тем самым включена посредством ссылки во всей своей полноте.
Недавние технологические новшества предоставили возможность для анализа иммунного ответа на специфические для пациента неоантигены, которые возникают вследствие опухолеспецифических мутаций, и новые данные свидетельствуют о том, что распознавание таких неоантигенов является основным фактором деятельности в областях клинической иммунотерапии. Эти наблюдения указывают на то, что неоантигенная нагрузка может приводить к образованию биомаркера в иммунотерапии рака и служить стимулом для развития новых терапевтических подходов. См. работу Schumacher, T.N. and Schreiber, R.D. (2015) Neoantigens in cancer immunotherapy. Science, 348: 6230, 69-74, которая тем самым включена посредством ссылки во всей своей полноте.
На основании данных, полученных за последние несколько лет, представляется правдоподобным, что неоантиген-специфическая реакционная способность является основным "активный ингредиентом" успешных противораковых иммунотерапии. Другими словами, генетическое повреждение, которое, с одной стороны, приводит к онкогенному росту, может также быть мишенью для иммунной системы для борьбы со злокачественными новообразованиями. Основываясь на этом наблюдении, важно будет разработать терапевтические вмешательства, при которых неоантиген-специфическая реакционная способность избирательно повышается. Из-за ограниченной экспрессии опухолью антигенов, которые предполагаются в качестве мишеней, эти персонализированные противораковые иммунотерапии дают надежду на получение высокой специфичности и безопасности. По-видимому, повышение неоантиген-специфической реакционной способности, которое может быть достигнуто с использованием такой персонализированной иммунотерапии, еще больше расширит спектр злокачественных новообразований у людей, поддающихся лечению при осуществлении иммунотерапии рака. См. работу Schumacher, T.N. and Schreiber, R.D. (2015) Neoantigens in cancer immunotherapy. Science, 348: 6230, 69-74, которая тем самым включена посредством ссылки во всей своей полноте.
Неоантигены могут образовываться в результате индивидуальных мутаций, уникальных для каждого пациента, которые численно значительно превосходят мутации, приводящие к образованию онкогенов. Подмножество таких мутаций, которые изменяют кодирующие белок последовательности, также приводит к образованию индивидуальных новых антигенов - неоантигенов, которые могут предоставлять "чужеродный" сигнал, необходимый для осуществления иммунотерапии рака. См. Hacohen et al. Getting Personal with Neoantigen-based Therapeutic Cancer Vaccines. Cancer Immunol. Res., 1 (1), 11-15. ©2013 AACR.
Как обсуждалось выше, пептидные вакцины против рака представляют собой другой подход для вызывания и усиления противоопухолевых иммунных ответов. Подход, который нацелен на опухолеспецифические антигены, образованные в результате мутаций генов, происходящих в опухолевых клетках во время опухолевой трансформации, будет полезен при персонализированном лечении пациентов. Иммунные ответы на такие, так называемые "раковые неоантигены" не могут быть ослаблены под действием центральной толерантности хозяина в тимусе и не вызывают аутоиммунных реакций. Недавние разработки в области геномики и биоинформатики, включая массовое параллельное секвенирование (MPS) и алгоритмы предсказания эпитопов, обеспечили значительный прорыв, позволяющий более полно и эффективно идентифицировать антигены-мишени. См. работу Kitano, I.A. et al. (2015) Cancer Neoantigens: A Promising Source of Immunogens for Cancer Immunotherapy. J. Clin. Cell Immunol., 6: 322, которая тем самым включена посредством ссылки во всей своей полноте.
Растет интерес к методам лечения рака, которые направлены на то, чтобы нацелить на раковые клетки собственную иммунную систему пациента (например, используя вакцины против рака), поскольку такие терапии могут сглаживать/устранять некоторые из описанных в данной заявке недостатков. В состав вакцин против рака обычно входят опухолевые антигены и иммуностимулирующие молекулы (например, цитокины или лиганды TLR), которые действуют совместно в отношении индуцирования антиген-специфических цитотоксических Т-клеток, направленных на опухолевые клетки и разрушающих их. Современные вакцины против рака обычно содержат перекрестно-реагирующие опухолевые антигены, которые представляют собой нативные белки (т. е. белки, кодируемые посредством ДНК всех нормальных клеток у индивида), которые избирательно экспрессируются или сверхэкспрессируются в опухолях, обнаруживаемых у многих индивидов. Вакцины, содержащие опухолеспецифические и пациентоспецифические неоантигены, являются возможно полезным терапевтическим средством для лечения субъекта, страдающего от рака. См. заявку WO 2015095811 А2, которая тем самым включена посредством ссылки во всей своей полноте.
Соответственно, репрезентативные образцы, приготовленные из ткани, например, опухолей или лимфатических узлов, полученных от раковых пациентов, можно использовать для идентификации неоантигенной нагрузки, которая может приводить к образованию биомаркера в иммунотерапии и, таким образом, обеспечивать разработку новых терапевтических подходов, при которых избирательно повышается реакционная способность Т-клеток в отношении идентифицированного класса или идентифицированных классов антигенов.
Современные методы отбора образцов в лаборатории диагностической патологии сфокусированы на взятии предписанных образцов из конкретных анатомических положений в извлеченных хирургической резекцией тканях. Как указано в выделенных пунктирной линией вкладках на ФИГ. 56, историческая общепринятая практика заключается в отборе 5-7 небольших участков извлеченной хирургической резекцией опухоли для выполнения требований метода определения стадии по системе TNM. Иссеченные образцы далее обрабатывают, превращая их в залитые парафином блоки тканей, выбирают гистологические срезы и определяют стадию развития опухоли и возможно анализируют на биомаркеры с использованием общепринятых методов окрашивания. После того, как вся диагностическая информация собрана и проанализирована патологоанатомом, оставшуюся извлеченную хирургическим путем ткань, включая всю оставшуюся опухолевую ткань, уничтожают посредством сжигания.
Изобретательский аспект этой работы включает использование оставшегося извлеченного хирургической резекцией материала, источника ткани, которую повсеместно уничтожали после мирового признания метода определения стадии по системе TNM в середине 1950-х годов. Во многие моменты в рамках текущего рабочего процесса извлеченная хирургической резекцией ткань может быть обработана с целью ее фрагментирования путем использования многочисленных методов диссоциации ткани (включая, но не ограничиваясь этим, обработку в блендере, измельчение/шинкование и обработку в соковыжималке). Как показано на ФИГ. Z, диссоциации можно подвергнуть ткань сразу после хирургического удаления (свежевыделенную ткань), ткань после фиксации, после приготовления TNM образцов или после заливки образцов ткани парафиновым воском. После проведения гомогенизации в достаточной степени подвергнутую диссоциации ткань обозначают как "репрезентативный образец". Уникальное и непредвиденное свойство репрезентативного образца заключается в том, что он содержит все из того разнообразия, которое существовало в изначальной извлеченной хирургической резекцией ткани ткани, например, разнообразия, обусловленного тканью, клетками и всеми биомолекулами.
Другие изобретательские аспекты этой заявки включают всю дальнейшую обработку свежевыделенных и подвергнутых фиксации репрезентативных образцов, в связи с тем, что, начиная с 1950-х годов, такие большие количества образца оставшегося операционного материала человека никогда не отбирали в диагностической онкологии, поскольку этот материал подвергался уничтожению. Как указано на ФИГ. 56, в некоторых воплощениях биомолекулы можно выделять непосредственно из репрезентативного образца, используя новые методы, и далее анализировать, используя существующие в настоящее время аналитические средства и те, которые будут разработаны в будущем. Такие биомолекулы, как ДНК, можно выделять и секвенировать, используя NGS, и полученные данные можно использовать для расчета процентного содержания опухоли, которая содержит конкретную целевую мутацию. Кроме того, частоту появления мутаций также можно использовать для определения разнообразия опухолевых субклонов, содержащихся в извлеченной резекцией опухоли. Анализ белка с применением ELISA, иммунопреципитации или масс-спектрометрии можно использовать для определения присутствия являющегося мишенью белкового комплекса или состояний активации тирозинкиназ в опухоли.
В другом воплощении часть репрезентативного образца в форме гомогената может быть только обработана и залита парафиновым воском для анализа с использованием существующей в настоящее время гистологической методологии. Результат окрашивания подвергнутых заливке репрезентативных образцов может быть прочитан и интерпретирован патологоанатомом, или они могут быть подвергнуты визуализации с использованием системы цифровой визуализации. После подвергания цифровой визуализации можно выполнить количественное оценку результатов гетерогенности после окрашивания и использовать для математического представления пространственной гетерогенности с точки зрения экспрессии белка, изменений числа копий гена или экспрессии мРНК.
В другом воплощении часть репрезентативного образца может быть обработана далее с использованием новых методов механической и ферментативной диссоциации для приготовления суспензии отдельных ядер. Ядра, выделенные из репрезентативных образцов, можно окрасить, используя новые методы окрашивания, для проведения дальнейшего анализа с применением проточной цитометрии с целью определения процентного содержания клеток, экспрессирующих определенные ядерные транскрипционные факторы и другие индикаторы фенотипических изменений. Альтернативно, окрашенные ядра могут быть выделены с использованием FACS (сортировка флуоресцентно-активированных клеток) или изъятия на основании аффинности к магнитным гранулам, с последующим выделением ДНК и проведением NGS или ПЦР анализа. Альтернативно, выделенные ядра можно поместить на предметные стекла и проанализировать гистологическими методами, такими как IHC и ISH.
В еще одном воплощении часть репрезентативного образца может быть обработана далее с использованием новых методов механической и ферментативной диссоциации для получения популяции отдельных клеток. Клетки, полученные из репрезентативных образцов извлеченных резекцией тканей, можно подвергнуть дальнейшему анализу посредством проточной цитометрии для детального исследования разнообразия клеточных типов, фенотипов и других биомаркеров, таких как являющиеся мишенью онкогены и иммуномодуляторы в опухолевых клетках, и иммунофенотипирования иммунных клеток, извлеченных из опухоли. Клетки можно подготовить для FACS, чтобы выделить клетки, экспрессирующие конкретные биомаркеры. Биомолекулы из FACS-отсортированных клеток можно выделить для дальнейшего аналитического тестирования или клетки можно поместить на предметные стекла для выполнения методов гистологического детектирования, включая IHC и ISH.
Поскольку оставшуюся извлеченную хирургическим путем ткань, в особенности в области онкологии солидных опухолей, подвергали уничтожению в течение последних примерно 50 лет, данные, получаемые благодаря новому способу отбора репрезентативных образцов и новым аналитическим методам, будут являться беспрецедентными данными для клинической онкологии. Такие "репрезентативные онкологические данные" (ФИГ. 56) впервые позволят оценить мутационное и фенотипическое разнообразие среди опухолевых клеток, а также статус противоопухолевого иммунного ответа и других нормальных тканей. Новые "репрезентативные онкологические данные" будут использованы для уточнения прогноза раковых пациентов, предсказания рецидива в месте хирургического вмешательства или отдаленных метастазов, выявления всех возможных "являющихся мишенью" изменений, отбора с целью включения в клиническое испытание и определения мишеней, дозировки и режима хронометрирования для комбинированной терапии.
Настоящее изобретение описано подробно. Чтобы проиллюстрировать далее настоящее изобретение и присущие ему преимущества, авторы изобретения приводят следующие примеры с обсуждением проведенных экспериментов.
Приведенные ниже примеры предназначены для иллюстрации, а не для ограничения, заявляемого изобретения.
ПРИМЕРЫ
Пример 1. Приготовление репрезентативных образцов тканей
Репрезентативные образцы тканей готовили из фиксированных в формалине опухолевых образцов, используя методологию гомогенизации, изложенную в данном описании и схематично представленную на ФИГ. 3. В общем случае, опухолевые образцы, т.е. образцы фиксированной в формалине опухоли, по возможности отделяли от окружающей их расположенной вблизи нормальной ткани и выполняли механическую диссоциацию, получая репрезентативный образец, содержащий все компоненты исходной извлеченной резекцией опухоли. Затем репрезентативный образец может быть дополнительно обработан для проведения последующего анализа. Такая обработка включала предварительное выдерживание в СС1 буфере при 85°С, после чего все переносили в буфер (например, PBS), содержащий коллагеназу Н в концентрации 60 мг/мл и 1 мМ CaCl2. Затем полученную гомогенизированную ткань с добавленным ферментом инкубировали с коллагеназой Н в течение по меньшей мере 30 минут при 40°С, после чего возвращали в СС1 буфер и нагревали при 85°С в течение примерно 10 минут, чтобы инактивировать любой оставшийся фермент коллагеназу. Затем репрезентативный образец использовали для приготовления подгрупп образцов, которые далее использовали в различных диагностических анализах.
Методы
Материалы: механическое фрагментирование тканей проводили, используя блендер на одну порцию Hamilton Beach® (Walmart, Тусон, AZ) или шаровую барабанную мельницу с системой управления IKA Works (0004180001) от IKA-Works (Штауфен-им-Брайсгау, Германия) и применяя диссоциатор gentleMACS от Miltenyi Biotec (Тетеров, Германия). Следует обратить внимание на различный размер фрагментов ткани после гомогенизации, изменяющийся в диапазоне от нескольких клеток до кластеров, содержащих десятки тысяч клеток (ФИГ. 15). Выдерживание клеток при определенных температуре и рН проводили в буфере 1 для выдерживания клеток (СС1) от Ventana Medical Systems (Тусон, AZ; № по каталогу 950-124). AccuMax® получали от Innovative Cell Technologies (Сан-Диего, СА). Коллагеназу Н (11074032001) получали от Roche (Базель, Швейцария). Использовали следующие антитела от Ventana Medical Systems (Тусон, AZ): антитело кролика к PD-L1 (SP263), моноклональное первичное антитело (790-4905); антитело мыши к Ber-EP4, моноклональное антитело (760-4383); антитело кролика к CD8 (SP57), моноклональное первичное антитело (790-4460); антитело кролика к HER-2/neu (4В5), моноклональное первичное антитело (790-2991).
Образцы тканей: все образцы тканей и мяса фиксировали в 10%-ном забуференном до нейтрального значения рН формалине в течение 24 часов в Ventana Medical Systems. Her2-положительный ксенотрансплантат готовили в Ventana Medical Systems. Куриное мясо и рыбу получали от Walmart (Тусон, AZ). Миндалины человека получали из Северо-западного медицинского центра (Тусон, AZ).
Расщепление и анализ: образец предварительно выдерживали в СС1 буфере при 85°С и после этого обрабатывали реагентом AccuMax®, содержащим коллагеназу Н в концентрации 1 мг/мл, в течение 1 часа при комнатной температуре, затем инкубировали в течение 1 часа при 40°С. Расщепление тканей биохимическим путем анализировали, пропуская расщепленный образец через микронные сетки в следующем порядке: 500, 300, 100, 40, 20, 10, 6 и 1 микрон. Прошедшие и удержанные фракции взвешивали для каждой сетки.
Окрашивание гематоксилином и эозином: репрезентативные образцы помещали в 70 мкл метанола на предметные стекла VWR plus. Окрашивание гематоксилином и эозином (Н&Е) проводили, используя платформу Symphony от Ventana Medical Systems (Ventana Medical Systems, Тусон, AZ) и соответствующие реагенты Н&Е серии Symphony (Ventana Medical Systems, Тусон, AZ).
Иммуногистохимия: репрезентативные образцы помещали в 70 мкл метанола на предметные стекла VWR plus. Основанный на измерении DAB иммуногистохимический (IHC) анализ методом светлого поля проводили, используя платформу BenchmarkXT от Ventana Medical Systems (Ventana Medical Systems, Тусон, AZ). Визуализацию биомаркеров осуществляли, используя набор для детекции DAB OptiView от Ventana (760-700). Антитела инкубировали в течение 4 минут.
Выделение РНК: РНК выделяли из репрезентативных образцов миндалин человека, используя кислый фенольный метод, описанный ранее в работе Chen и др., 2007.
Результаты и обсуждение
Используя описанные выше способы, готовили репрезентативные образцы из образцов различных типов, включая клинические пробы тканей из опухолей человека и подвергнутые фиксации ткани животных.
После предварительного выдерживания клеток в СС1 буфере при 85°С проводили ферментативное расщепление внеклеточного матрикса для получения образца с размером, изменяющимся в диапазоне от одиночных клеток до небольших скоплений клеток.
Чтобы минимизировать потерю мембраноассоциированных биомаркеров в процессе расщепления ткани биохимическим путем, вместо общеизвестной протеазы, например, трипсина, использовали фермент, специфичный к белкам внеклеточного матрикса, т.е. коллагеназу Н.
Большую часть образца расщепляли на фрагменты размером 100 микрон и меньше (ФИГ. 4). При этом, выраженное в процентах значение массы расщепленного образца использовали для того, чтобы охарактеризовать фрагменты разных размеров в расщепленном биохимическим путем репрезентативном образце после фильтрования через серию микронных сеток. Неопухолевые клетки фильтровали путем пропускания образца через сетчатые фильтры с размером ячеек 6 микрон и меньше, что видно при Н&Е окрашивании. На ФИГ. 5А-С показан результат Н&Е окрашивания прошедших и удержанных фракций, собранных после серийного фильтрования расщепленного биохимическим путем репрезентативного образца. ФИГ. 7А представляет иллюстрацию Н&Е окрашивания фракции, удержанной на сетке (вверху) и прошедшей через сетку с ячейками 500, 300, 100 и 40 микрон (внизу). ФИГ. 7В представляет иллюстрацию Н&Е окрашивания фракции, удержанной на сетке (вверху) и прошедшей через сетку с ячейками 30, 20 и 10 микрон (внизу). ФИГ. 7С представляет иллюстрацию Н&Е окрашивания фракции, удержанной на сетке (вверху) и прошедшей через сетку с ячейками 6 и 1 микрон (внизу).
Н&Е окрашивание фракций, прошедших через фильтры с размером пор 6 микрон и 1 микрон (в частности, ФИГ. 5С), показало отсутствие в клетках увеличенных ядер, характерных для опухолевых клеток. Соответственно, этот подход может быть использован для обогащения опухолевых клеток в репрезентативном образце, а также выделения из образца присутствующих в опухоли тромбоцитов и других клеток крови.
Описанный выше способ сначала опробовали на образце ткани, содержащем 300 граммов различных подвергнутых фиксации тканей животных, включая куриную грудку, куриную печень и рыбное филе. Для моделирования субклона немногочисленных опухолевых клеток в образец ткани добавляли небольшое количество (0,4 грамма) HER2-положительного ксенотрансплантата. Перед применением в этом эксперименте ткань подвергали механической диссоциации и фильтровали, используя френч-пресс. Затем образец ткани предварительно выдерживали в СС1 буфере в течение 15 минут при 85°С. Этот предварительно выдержанный образец ткани гомогенизировали, используя диссоциатор gentleMACS (ФИГ. 6D), и каждые 5 минут отбирали образец объемом 1 мл. Каждый отобранный образец пропускали через сетку 600pcs для измерения уровня диссоциации ткани. Одно только предварительное выдерживание могло способствовать некоторому расщеплению, однако реакция достигала плато через 10 минут (ФИГ. 6А). Сравнивая способность к диссоциации образца под действием только коллагеназы Н, а также коллагеназы Н в комбинации с предварительным выдерживанием в СС1, определяли, что предварительное выдерживание в СС1 способствовало стимулированию расщепления коллагеназой Н. В частности, предварительное выдерживание в СС1 с последующим расщеплением коллагеназой Н в течение по меньшей мере 30 минут приводило к наилучшему уменьшению размера частиц по результатам измерений с использованием сетки 600pcs (ФИГ. 6В). Репрезентативность образца тестировали путем нанесения нескольких аликвот и анализа каждой из них на HER-2-положительные клетки с использованием DAB-IHC. В каждом приготовленном срезе обнаруживали HER-2-положительные клетки (ФИГ. 6С). С учетом соотношений по массе (0,4 грамма HER-2-положительного ксенотрансплантата на 300 граммов мяса) описанным выше способом получали репрезентативный образец, в котором оказалось возможным обнаружить субклоны с показателем распространенности по меньшей мере 0,1%.
Далее, данный протокол тестировали на тканях лимфатического узла (миндалины) человека. Для приготовления репрезентативного образца из лимфатического узла извлеченную резекцией миндалину подвергали механической диссоциации в шаровой барабанной мельнице от IKA. Предварительное выдерживание ткани миндалины в СС1 с последующим расщеплением коллагеназой Н в течение 30 минут приводило к ее диссоциации (ФИГ. 7А). Временной интервал для расщепления под действием коллагеназы Н увеличивали до 90 минут, и было установлено, что ферментативная реакция выходила на плато примерно через 60 минут (ФИГ. 7В). Соответственно, ожидается, что только для расщепления большей части ткани человека под действием коллагеназы Н необходимо от примерно 30 до примерно 60 минут, но не более чем примерно 90 минут.
Далее для выделения нуклеиновых кислот использовали четыре аликвоты по 500 мкл образца подвергнутой диссоциации ткани миндалины человека. Две аликвоты по 500 мкл хранили при -20°С в виде клеточных осадков после центрифугирования, в то время как другие две аликвоты по 500 мкл заливали парафином. РНК выделяли из всех аликвот, но выход был гораздо больше из не залитых парафином аликвот (Таблица 1).
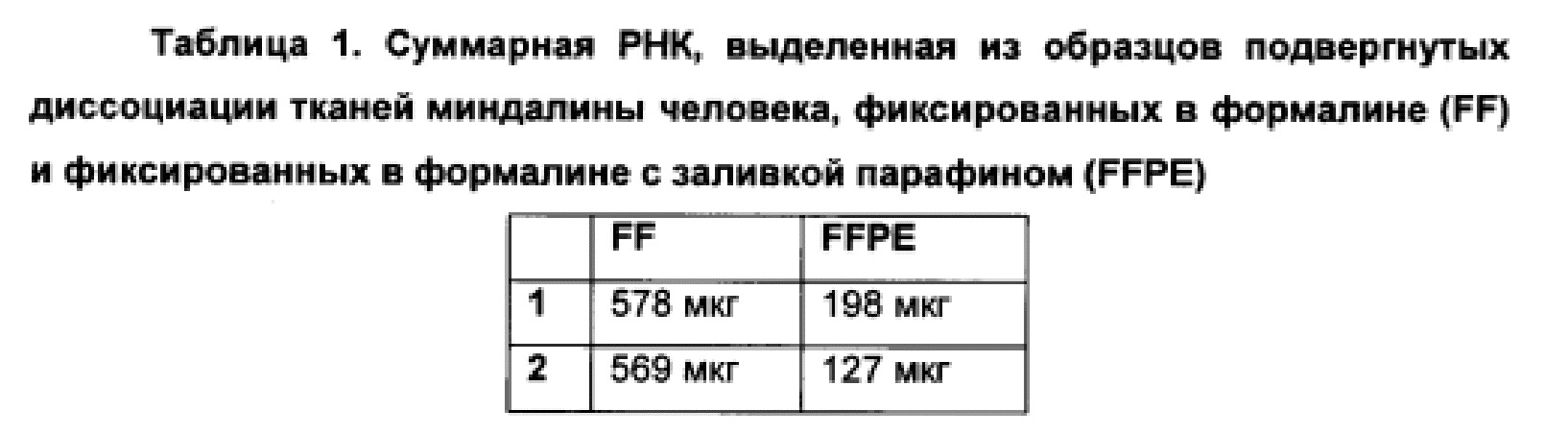
Эти результаты указывают на то, что данные репрезентативные образцы подходят для диагностических тестов, таких как геномное и транскриптомное го секвенирование, и, кроме того, что репрезентативные образцы, приготовленные с применением описанных в данной заявке способов, являются лучшим источником материала, чем традиционные залитые парафином образцы тканей.
Пример 2. Приготовление репрезентативных опухолевых образцов Репрезентативные опухолевые образцы готовили из образца почки и 25 образца легкого.
Методы
Материалы: механическое фрагментирование тканей проводили, используя шаровую барабанную мельницу с системой управления IKA Works (0004180001) от IKA-Works (Штауфен-им-Брайсгау, Германия) и применяя диссоциатор gentleMACS от Miltenyi Biotec (Тетеров, Германия). Выдерживание клеток при определенных температуре и рН проводили в буфере 1 для выдерживания клеток (СС1) от Ventana Medical Systems (Тусон, AZ; № по каталогу 950-124). Коллагеназу Н (11074032001) получали от Roche (Базель, Швейцария). Использовали следующие антитела от Ventana Medical Systems (Тусон, AZ): антитело кролика к PD-L1 (SP263), моноклональное первичное антитело (790-4905); антитело мыши к Ber-EP4, моноклональное антитело (760-4383); антитело кролика к CD8 (SP57), моноклональное первичное антитело (790-4460); антитело кролика к HER-2/neu (4В5), моноклональное первичное антитело (790-2991).
Клинические образцы: образцы тканей фиксировали в 10%-ном забуференном до нейтрального значения рН формалине в течение от 24 до 72 часов в Медицинском центре в Тусоне и Медицинском центре Университета Вандербильта. Биопсийный материал опухоли легкого получали из Медицинского центра в Тусоне (Тусон, AZ). Фрагменты биопсийного материала опухоли почки получали из Университета Вандербильта (Нэшвилл, TN).
Анализ расщепления: расщепление тканей биохимическим путем анализировали, пропуская образец объемом 1 мл через сетку 600pcs и взвешивая материал, собранный на сетке.
Окрашивание гематоксилином и эозином: репрезентативные образцы помещали в 70 мкл метанола на предметные стекла VWR plus. Окрашивание гематоксилином и эозином (Н&Е) проводили, используя платформу Symphony от Ventana Medical Systems (Ventana Medical Systems, Тусон, AZ) и соответствующие реагенты Н&Е серии Symphony (Ventana Medical Systems, Тусон, AZ).
Иммуногистохимия: репрезентативные образцы помещали в 70 мкл метанола на предметные стекла VWR plus. Основанный на измерении DAB иммуногистохимический (IHC) анализ методом светлого поля проводили, используя платформу BenchmarkXT от Ventana Medical Systems (Ventana Medical Systems, Тусон, AZ). Визуализацию биомаркеров осуществляли, используя набор для детекции DAB OptiView от Ventana (760-700). Антитела инкубировали в течение 4 минут.
Выделение РНК: РНК выделяли из репрезентативных образцов миндалины человека, используя кислый фенольный метод, описанный ранее в работе Chen и др., 2007.
Результаты и обсуждение
В частности, репрезентативный образец готовили из опухоли почки размером с бейсбольный мяч, полученной от мужчины в возрасте 61 года в соответствии с методологией, изложенной в данном описании и представленной на ФИГ. 3. Для визуализации размеров фрагментов ткани в образце почки после механической диссоциации, предварительного выдерживания и ферментативного расщепления использовали стандартное Н&Е окрашивание (ФИГ. 8А). Затем образец подвергали DAB-IHC анализу на предмет трех разных биомаркеров: PD-L1 (ФИГ. 8В), CD8 (ФИГ. 8С) и Ер-Cam (ФИГ. 8D). В репрезентативном клиническом образце опухоли почки детектировали все три белка.
Кроме того, репрезентативный образец готовили из части опухоли легкого размером с монету в 50 центов, полученной от женщины в возрасте 87 лет (ФИГ. 9А). Готовили небольшой срез, используя клинический образец ткани (ФИГ. 9А), и обрабатывали в соответствии со стандартными патологоанатомическими практиками. Остальную ткань использовали для приготовления репрезентативного образца в соответствии с методологией, изложенной в данном описании и представленной на ФИГ. 1. Для визуализации размеров фрагментов ткани в образце легкого после механической диссоциации, предварительного выдерживания и ферментативного расщепления использовали стандартное Н&Е окрашивание (ФИГ. 9В).
Репрезентативный образец и приготовленные традиционным способом срезы ткани (из "тканевого блока") затем подвергали DAB-IHC анализу на предмет трех разных биомаркеров: PD-L1 (ФИГ. 9С), CD8 (ФИГ. 9D) и Ер-Cam (ФИГ. 9Е). Сходные уровни окрашивания наблюдали для репрезентативного образца и приготовленных традиционным способом срезов ткани, что указывает на отсутствие каких-либо потерь сигнала, связанных с большой распространенностью субклонов, при использовании способов по изобретению.
Эти результаты демонстрируют, что посредством сочетания механического воздействия на ткань с расщеплением биохимическим путем можно приготовить образец, репрезентативный с точки зрения гетерогенности и разнообразия в опухолях различных типов. Кроме того, эти репрезентативные образцы подходят для применения в различных диагностических тестах, таких как окрашивание гематоксилином и эозином, иммуногистохимический анализ, выделение и секвенирование нуклеиновых кислот, и облегчают детектирование субклонов немногочисленных опухолевых клеток, улучшая тем самым клиническую диагностику и персонализированное лечение рака.
Пример 3. Иммуноцитохимическое детектирование белков в репрезентативных образцах, приготовленных из интактных фиксированных в формалине проб
Репрезентативные образцы тканей и опухолей готовили из фиксированных проб тканей или опухолей, используя методологию гомогенизации, изложенную в данном описании и схематично представленную на ФИГ. 3, и детектирование представляющих интерес белков, например, как прогностических или предсказательных, с биологической и/или медицинской точки зрения, маркеров, в репрезентативном образце выполняли с использованием иммуноцитохимии (ICC).
Иммуногистохимическое (IHC) детектирование белков из гистологических срезов фиксированных биологических образцов является общепринятой практикой в патологической анатомии, что оказывает влияние на вынесение медицинских заключений, в частности, в контексте онкологии солидных опухолей. Иммуноцитоохимическое (ICC) детектирование белков из фиксированных проб также оказывает влияние на вынесение медицинских заключений, например, при цитологическом исследовании плевральных выпотов в случае метастазирующей карциномы, и отличается от IHC тем, что образец первоначально не имеет гистологической архитектуры. ICC ограничивается цитологическими пробами, например, в виде мазка по Папаниколау или тонкослойного препарата для онкоцитологии шейки матки. Гистологические срезы, сохраняя при этом многие признаки, важные для современной практики в области патологии солидных опухолей, такие как архитектура стромальной ткани по сравнению с опухолевой, дают представление о части клеточного содержимого опухоли и расширяют биоинформационное содержание касательно целой фиксированной биологической пробы. Изменение формата интактных фиксированных опухолевых проб с получением образца, являющегося репрезентативным для опухоли в целом, и образца, который может обеспечить получение статистически значимой информации, имеющей возможное значение для медицины, является решающим для будущего приоритетной персонализированной медицины.
Методы
Антитела: в Таблице 2 перечислены антитела и подвергнутые фиксации пробы, использованные в этом исследовании. Антитела поставляются Ventana Medical Systems, Inc.

Образцы тканей: все образцы тканей фиксировали в 10%-ном забуференном до нейтрального значения рН формалине в течение 24 часов в Ventana Medical Systems. Миндалины человека получали из Северо-западного медицинского центра (Тусон, AZ). Ткани животных закупали в коммерческих источниках, например, куриную печень приобретали в магазине.
Материалы: механическое фрагментирование тканей проводили, используя шаровую барабанную мельницу с системой управления IKA Works (0004180001) от IKA-Works (Штауфен-им-Брайсгау, Германия) и применяя диссоциатор gentleMACS от Miltenyi Biotec (Тетеров, Германия). Выдерживание клеток при определенных температуре и рН проводили в буфере 1 для выдерживания клеток (СС1) от Ventana Medical Systems (Тусон, AZ; № по каталогу 950-124).
Измельчение: 200 мкл минерального масла добавляли в сальник смесителя шаровой барабанной мельницы от IKA (№ изд. МТ 40.100) для предотвращения утечки при выполнении гомогенизации. В мельницу помещали 5 граммов ткани вместе с PBS в объеме, равном 1 объему ткани. Образец обрабатывали при 15000 об. /мин в течение 2 минут (обработка в течение 10 секунд, пауза между обработками 2 секунды). Гомогенизированный образец извлекали из мельницы и помещали в диссоциатор GentleMACS (№ изд. 30-093-237) вместе с двойным объемом PBS. Образец измельчали, используя программу h_tumor_01 (вращение в течение 36 секунд), что повторяли в общей сложности три раза, после чего образец переливали в коническую пробирку емкостью 50 мл и центрифугировали при 300 × g в течение 3 минут. PBS-содержащий водный слой извлекали для осуществления этапа выдерживания.
Выдерживание клеток: добавляли 1 объем предварительно нагретого раствора для выдерживания клеток (СС1). Затем образец помещали на 5 минут в термоблок, установленный на 85 градусов С. После этого образец подвергали измельчению, применяя диссоциатор GentleMACS (3× программа h_tumor_02). Стадию нагревания и стадию измельчения проводили еще два раза каждую, после чего образец центрифугировали при 300 × g в течение 3 минут.
Нанесение: аликвоту образца объемом 100 мкл переносили в пробирку Эппендорфа и добавляли 1 объемный эквивалент 100%-ного метанола. Для нанесения и запивки парафином использовали 70 мкл метанола/образец из расчета на одно предметное стекло с суперматовым полем от VWR.
Автоматизированная иммуноцитохимия: основанный на применении DAB иммуноцитохимический (ICC) анализ методом светлого поля проводили на репрезентативных образцах, нанесенных на положительно заряженные предметные стекла, используя платформу Benchmark XT от Ventana Medical Systems, Inc. (Ventana Medical Systems, Inc, Тусон, AZ) с программным обеспечением для научных исследований. Детектирование каждого антитела с применением DAB проводили, используя набор для детекции DAB OptiView (VMSI, № по каталогу 760-700) вместе с набором OptiView AMP (VMSI, № по каталогу 760-099) и без него. Чтобы получить низкий уровень фонового сигнала для проб и уменьшить времена инкубации с первичными антителами, использовали амплификацию. Все процедуры детектирования были полностью автоматизированы, и их проводили с использованием устройства для автоматического окрашивания Benchmark XT (VMSI) после осуществления выдерживания содержащихся в пробах клеток в СС1 буфере (VMSI, № по каталогу 950-124) в течение двух раундов по 4 минуты. Все процедуры инкубации с первичными антителами проводили при 37°С в течение 4 минут (см. Результаты и обсуждение), что позволяло сохранить общее время обработки меньше 2 часов и 20 минут. Проводили один DAB-ICC анализ, используя протокол, показанный на ФИГ. 10. На ФИГ. 10 предложен типичный протокол для DAB ICC, изложенный для стадий 1-102, для детектирования белков в репрезентативных образцах. В этом конкретном примере данный протокол использовали для детектирования Her2.
Хромогенное мультиплексное детектирование осуществляли так, как описано на ФИГ. 11, в следующем порядке: Ki-67→CD20→CD3. Чтобы предотвратить перекрестную реактивность, тепловую денатурацию ферментов и плавление первичных антител проводили между Ki-67 и CD20, и CD20 и CD3 путем инкубирования в течение 12 минут при 90°С в буфере 2 для выдерживания клеток (СС2) (VMSI, № по каталогу 950-123).
Результаты й обсуждение
Чтобы определить, могут ли репрезентативные образцы, нанесенные на предметные стекла, окрашиваться с использованием автоматизированного ICC анализа, образцы, приготовленные из смеси проб ткани животного и миндалины, окрашивали на один биомаркер с использованием DAB ICC (ФИГ. 12). На ФИГ. 12 показано детектирование CD20, характерного для В-клеток, с использованием автоматизированного DAB-ICC анализа, в репрезентативном образце, полученном из смеси проб ткани животного и миндалины человека. CD20 детектировали в клетках из ткани миндалины человека, содержащейся в репрезентативном образце.
Для сведения к минимуму фонового сигнала и времени обработки выбирали четырехминутную инкубацию с первичными антителами с амплификацией (например, протокол Rep Dia-DAB-Her2, ФИГ. 10). Было установлено, что все протестированные антитела (см. Таблицу 2) совместимы с этим протоколом.
Помимо этого был разработан протокол для тестирования возможности детектирования одиночных маркеров с использованием флуоресцентной ICC (см. ФИГ. 11). Например, детектирование Her2 осуществляли с использованием флуоресцентной ICC (ФИГ. 13А и 13В). Здесь, на ФИГ. 13А и 13В, показано обнаружение Her2-положительных клеток Calu-3, присутствующих в репрезентативном образце, приготовленном из ткани миндалины и Her-2-положительного ксенотрансплантата опухоли, с использованием флуоресцентной ICC. ФИГ. 13А представляет иллюстрацию репрезентативного образца, содержащего клетки Calu-3, инкубированные только с вторичным антителом (отрицательный контроль). Фоновый сигнал в клетках Calu-3, генерируемый вторичным антителом, обозначен стрелкой, изображенной пунктирной линией. ФИГ. 13В представляет иллюстрацию репрезентативного образца, содержащего клетки Calu-3, инкубированные с антителом к Her2 (4В5), перед добавлением вторичного антитела. Сигнал от Her-2 в клетках Calu-3 обозначен стрелкой, изображенной сплошной линией. Сигнал от более мелких неспецифических клеток, происходящих из миндалины, наблюдается в случаях без добавления антитела к Her2 (4 В5) (ФИГ. 13А) и с добавлением антитела к Her2 (4B5) (ФИГ. 13В).
Далее, готовили репрезентативный образец, полученный из пробы миндалины, и помещали на предметное стекло для проведения тест-анализа с использованием мультиплексной хромогенной ICC. Репрезентативные пробы миндалины окрашивали на предмет трех иммунных маркеров, при этом при детектировании каждого из них наблюдали различную окраску в соответствии с протоколом, показанным на ФИГ. 14. На ФИГ. 14 приведен типичный протокол мультиплексного хромогенного ICC анализа (приведенный для стадий 1-225) для детектирования нескольких белков в репрезентативном образце. В этом конкретном примере для детектирования трех иммунных маркеров использовали видоспецифичные антитела к Ki-67, CD20 и CD3 и осаждение хромогена, обусловленное конъюгатом (антивидовое антитело)-фермент.
Например, на репрезентативных пробах миндалины проводили хромогенный мультиплексный анализ для детектирования Ki-67, CD20 и CD3 с использованием видоспецифичных вторичных антител с последующим осаждением, обусловленным конъюгатом (антивидовое антитело)-фермент, в сочетании со стадией тепловой денатурации для устранения ферментативной активности, как описано ранее в Wenjun Zang et al., "Quantum dot in situ hybridization", WO 2014139979. В репрезентативных пробах миндалины, подвергнутых хромогенному мультиплексному анализу, наблюдали биологически приемлемое детектирование и наложение цветов (ФИГ. 15).
Далее, на репрезентативных образцах, приготовленных из клинических проб, проводили ICC анализ. В частности, готовили репрезентативные образцы, полученные из фиксированной в формалине опухоли легкого или фиксированной в формалине опухоли почки, и тестировали на предмет PDL-1 (маркера, продуцируемого опухолями для блокирования противоопухолевого иммунитета, и мишени для предписанной иммунотерапии), CD8 (важнейшего маркера Т-клеток для выяснения уровня противоопухолевого иммунитета) и Ер-Cam (маркера, указывающего виды эпителиального рака). В репрезентативных образцах, приготовленных из клинических опухолевых проб, детектировали, с разными уровнями, каждый из тестируемых биомаркеров (PDL-1, CD8 и Ер-Cam) (см. ФИГ. 8A-8D и ФИГ. 9A-9D).
Эти результаты демонстрируют возможность использования полностью автоматизированного одиночного и мультиплексного ICC анализа для детектирования маркеров в репрезентативных образцах, приготовленных из интактных проб фиксированных в формалине тканей и, кроме того, показывают, что применение образца, являющегося репрезентативным для пробы интактной подвергнутой фиксации ткани, дает возможность детектировать в данном образце немногочисленные субпопуляции клеток.
Пример 4. Приготовление репрезентативных образцов из лимфатических узлов и их применение для детектирования немногочисленных субклонов
В этом примере описывается приготовление репрезентативного образца из ткани лимфатического узла, что позволяет осуществить с высокой чувствительностью обнаружение раковых клеток, которые могут появиться в результате метастазирования опухоли. Репрезентативные образцы тканей готовили из фиксированных в формалине опухолевых образцов, используя методологию гомогенизации, изложенную в данном описании и схематично представленную на ФИГ. 3. В общем случае, опухолевые образцы, т.е. фиксированные в формалине опухолевые образцы, сначала подвергали механической диссоциации и затем предварительно выдерживали в СС1 буфере при 85°С, после чего переносили в буфер, представляющий собой 1× PBS буфер.
Методы
Антитела: для детектирования b-Raf использовали мышиное моноклональное антитело к BRAFV600E (№ по каталогу 790-4855, Ventana Medical Systems, Inc.).
Образцы тканей: все образцы тканей фиксировали в 10%-ном забуференном до нейтрального значения рН формалине в течение 24 часов в Ventana Medical Systems. Her2-положительный или BRAF ксенотрансплантат готовили в Ventana Medical Systems. Миндалины человека получали из Северозападного медицинского центра (Тусон, AZ).
Материалы: механическое фрагментирование тканей проводили, используя шаровую барабанную мельницу с системой управления IKA Works (0004180001) от IKA-Works (Штауфен-им-Брайсгау, Германия) и применяя диссоциатор gentleMACS от Miltenyi Biotec (Тетеров, Германия). Выдерживание клеток при определенных температуре и рН проводили в буфере 1 для выдерживания клеток (СС1) от Ventana Medical Systems (Тусон, AZ; № по каталогу 950-124).
Измельчение: 200 мкл минерального масла добавляли в сальник смесителя шаровой барабанной мельницы от IKA (№ изд. МТ 40.100) для предотвращения утечки при выполнении гомогенизации. В мельницу помещали 5 граммов ткани вместе с PBS в объеме, равном 1 объему ткани. Образец обрабатывали при 15000 об./мин в течение 2 минут (обработка в течение 10 секунд, пауза между обработками 2 секунды). Гомогенизированный образец извлекали из мельницы и помещали в диссоциатор GentleMACS (№ изд. 30-093-237) вместе с двойным объемом PBS. Образец измельчали, используя программу h_tumor_01 (вращение в течение 36 секунд), что повторяли в общей сложности три раза, после чего образец переливали в коническую пробирку емкостью 50 мл и центрифугировали при 300 × g в течение 3 минут. PBS-содержащий водный слой извлекали для осуществления этапа выдерживания.
Выдерживание клеток: добавляли 1 объем предварительно нагретого раствора для выдерживания клеток (СС1). Затем образец помещали на 5 минут в термоблок, установленный на 85 градусов С. После этого образец подвергали измельчению, применяя диссоциатор GentleMACS (3× программа h_tumor_02). Стадию нагревания и стадию измельчения проводили еще два раза каждую, после чего образец центрифугировали при 300 × g в течение 3 минут.
Нанесение: аликвоту образца объемом 100 мкл переносили в пробирку Эппендорфа и добавляли 1 объемный эквивалент 100%-ного метанола. Для нанесения использовали 70 мкл метанола/образец из расчета на одно предметное стекло с суперматовым полем от VWR.
Автоматизированная иммуноцитохимия: основанный на применении DAB иммуноцитохимический (ICC) анализ методом светлого поля проводили на репрезентативных образцах, нанесенных на положительно заряженные предметные стекла, используя платформу Benchmark XT от Ventana Medical Systems, Inc. (Ventana Medical Systems, Inc, Тусон, AZ) с программным обеспечением для научных исследований. Детектирование антитела с применением DAB проводили, используя набор для детекции DAB OptiView (VMSI, № по каталогу 760-700) вместе с набором OptiView AMP (VMSI, № по каталогу 760-099) и без него. Чтобы получить низкий уровень фонового сигнала для проб и уменьшить времена инкубации с первичными антителами, использовали амплификацию. Все процедуры детектирования были полностью автоматизированы, и их проводили с использованием устройства для автоматического окрашивания Benchmark XT (VMSI) после осуществления выдерживания содержащихся в пробах клеток в СС1 буфере (VMSI, № по каталогу 950-124) в течение двух раундов по 4 минуты.
Результаты и обсуждение
Чтобы определить, могут ли быть обнаружены события с низкой распространенностью в репрезентативных образцах из лимфатического узла (например, миндалины), репрезентативный образец из лимфатического узла наносили на предметные стекла и окрашивали с использованием автоматизированной ICC так, как показано на ФИГ. 10.
Чтобы протестировать чувствительность обнаружения опухолевых клеток в репрезентативном образце из лимфатического узла, в гомогенат лимфатического узла добавляли репрезентативный образец bRaf V600E-положительного ксенотрансплантата человека, снижая его количества. Использовали следующие значения процентного содержания клеток (показателя распространенности BRAFV600E-положительных клеток в общем объеме образца): 50%, 25%, 12,5%, 6,25%, 3,12%, 1,5%, 0,15%, 0,015%, 0,0015% и 0,00015%. Детектировали bRaf-положительные клетки с распространенностью до 0,015% (ФИГ. 16), и это демонстрировало, что ICC анализ можно применять в отношении репрезентативных образцов тканей, приготовленных из лимфатических узлов, для нахождения субпопуляций крайне немногочисленных клеток, что может дать основание для терапевтического воздействия (например, применения вемурафениба в случае BRAFV600E+).
Аналогичный эксперимент с серией разведений также выполняли с Her2-положительными клетками, которые добавляли, при уменьшении соотношений, к репрезентативному образцу миндалины, получая следующие значения процентного содержания: 50%, 25%, 12,5%, 6,25%, 3,12%, 1,5%, 0,15%, 0,015%, 0,0015% и 0,00015%. Как в случае с b-Raf-положительными клетками, Her2-положительные клетки также могут быть обнаружены с очень низкими уровнями, т.е. примерно 0,015% (данные не показаны), и это снова указывает на то, что ICC анализ репрезентативных образцов можно использовать для нахождения субпопуляций крайне немногочисленных клеток, что может дать основание для терапевтического воздействия (например, применения герсептина случае Her2+).
Пример 5. Приготовление репрезентативных образцов из целых опухолей
В этом примере описываются репрезентативные образцы, приготовленные из извлеченных хирургической резекцией первичных опухолей.
Методы
Репрезентативные образцы тканей готовили из фиксированной в формалине извлеченной хирургической резекцией толстой кишки приблизительно восьми см в диаметре и извлеченной резекцией части почки (полученных от GLAS Tissue Consultants, Уинстон-Сейлем, NC) (ФИГ. 18А и 18В). Здесь, на ФИГ. 18А проиллюстрирован материал, полученный в результате резекции толстой кишки, который все еще содержит аденокарциному толстой кишки диаметром восемь (8) см, в то время как на ФИГ. 18В проиллюстрирована остальная ткань после частичной нефректомии почки, содержащая папиллярную уротелиальную опухоль почки.
Получали образцы опухоли и проводили их обработку для гистологического исследования (т.е. осуществляли заливку парафином, нарезание гистологических срезов) с целью имитации процесса отбора TNM образцов. Оставшаяся часть опухолевой ткани была иссечена патологоанатомом с использованием скальпеля, и опухолевую ткань подвергали гомогенизации с применением шаровой барабанной мельницы с системой управления IKA Works (0004180001) от IKA-Works (Штауфен-им-Брайсгау, Германия) или блендера на одну порцию Hamilton Beach®. Затем образцы гомогенатов подвергали механической диссоциации и далее выполняли предварительное выдерживание в СС1 буфере при 85°С, после чего переносили в буфер (например, PBS), содержащий АссиМах® с коллагеназой Н (1 мг/мл) в AccuMax® буфере. Затем полученную гомогенизированную ткань с добавленным ферментом инкубировали с коллагеназой Н в течение по меньшей мере 30 минут при 40°С, после чего возвращали в СС1 буфер и нагревали при 85°С в течение примерно 10 минут, чтобы инактивировать любой оставшийся фермент коллагеназу. Затем репрезентативный образец использовали для приготовления подгрупп образцов, которые далее использовали в различных диагностических анализах.
Образцы окрашивали с использованием Н&Е, а также ALK IHC, применяя платформу для окрашивания от Ventana.
Результаты и обсуждение
Чтобы определить, имеется ли разнообразие типов клеток, содержащихся в исходном образце, проводили окрашивание с использованием Н&Е и гистологических срезов, и репрезентативных образцов (ФИГ. 19 и 20 и 23). Здесь, ФИГ. 19А представляет иллюстрацию первого среза, полученного из аденокарциномы толстой кишки; в то время как ФИГ. 19В представляет иллюстрацию второго и отличающегося среза из аденокарциномы толстой кишки. Каждый из срезов, показанных на ФИГ. 19А и 19В, был приготовлен патологоанатомом. Разница в Н&Е окрашивании показывает вариацию в пределах одной и той же опухоли. ФИГ. 19С представляет иллюстрацию Н&Е окрашивания репрезентативного образца, приготовленного из аденокарциномы толстой кишки. На ФИГ. 20А-20С показано Н&Е окрашивание различающихся гистологических срезов, полученных из папиллярной уротелиальной опухоли почки. ФИГ. 20А представляет иллюстрацию первого среза, взятого из папиллярной уротелиальной опухоли почки; ФИГ. 20В представляет иллюстрацию второго, отличающегося от первого, среза, взятого из папиллярной уротелиальной опухоли почки. Каждый из срезов, проиллюстрированных на ФИГ. 10А и 20В, был приготовлен патологоанатомом. Разница в Н&Е окрашивании показывает вариацию в пределах одной и той же опухоли. ФИГ. 20С представляет иллюстрацию Н&Е окрашивания репрезентативного образца, приготовленного из папиллярной уротелиальной опухоли почки.
Как видно из Фиг. 19 и 20, хотя структуры гистологических срезов, взятых из разных участков извлеченной резекцией опухоли, имеют разные гистологические проявления (А, В), репрезентативные образцы (С) воспроизводят гетерогенность в клетках, которые составляют каждый тип опухоли (т.е. опухолевых, нормальных, иммунных).
Чтобы определить, имеется ли какая-либо гетерогенность в экспрессии биомаркеров в гистологических тканях, которые были воспроизведены в репрезентативном образце, все образцы анализировали на предмет экспрессии Alk, вероятно являющейся результатом геномной перестройки с EML4. Все предметные стекла подвергались повторному рассмотрению патологоанатомом, который определял положительную, или наоборот, отрицательную экспрессию Alk при окрашивании с использованием DAB. На ФИГ. 21А-21С и ФИГ. 22А-22С показано, что и для почки, и для толстой кишки один гистологический срез демонстрировал точечное и редкое положительное окрашивание на Alk, в то время как для одного среза получали отрицательный результат. Такое несоответствие в окрашивании среди блоков хоть и является удивительным, является указанием на системную ошибку при отборе образцов, присущую проведению определения стадии по системе TNM. Гетерогенность в отношении положительного окрашивания на Alk (т.е. низкая распространенность относительно размера целой опухоли) была очевидной в репрезентативных образцах, окрашенных с использованием Alk IHC, поскольку существовали небольшие кластеры или одиночные клетки, для которых получали положительный результат в случае Alk DAB окрашивания. На ФИГ. 21А-21С показан результат Alk DAB окрашивания различающихся гистологических срезов, полученных из аденокарциномы толстой кишки. ФИГ. 21А представляет иллюстрацию первого среза, взятого из папиллярной уротелиальной опухоли почки; ФИГ. 21В представляет иллюстрацию второго, отличающегося от первого, среза, взятого из папиллярной уротелиальной опухоли почки. Каждый из срезов, проиллюстрированных на ФИГ. 21А и 21В, был приготовлен патологоанатомом. Разница в Alk DAB окрашивании показывает вариацию в пределах одной и той же опухоли. ФИГ. 21С представляет иллюстрацию Alk DAB окрашивания репрезентативного образца, приготовленного из аденокарциномы толстой кишки.
На ФИГ. 21С показан небольшой кластер из трех клеток аденокарциномы толстой кишки, которые являются положительными в отношении Alk (стрелка), а на ФИГ. 25С показан небольшой кластер из шести клеток папиллярного уротелиального рака почки (стрелка) и лимфоцит в качестве контроля, для которого получен положительный результат (стрелка-указатель). На ФИГ. 22А-22С показан результат Alk DAB окрашивания различающихся гистологических срезов, полученных из папиллярной уротелиальной опухоли почки. ФИГ. 22А представляет иллюстрацию первого среза, взятого из папиллярной уротелиальной опухоли почки, ФИГ. 22В представляет иллюстрацию второго, отличающегося от первого, среза, взятого из папиллярной уротелиальной опухоли почки. Каждый из срезов, проиллюстрированных на ФИГ. 22А и 22В, был приготовлен патологоанатомом. Разница в Alk DAB окрашивании показывает вариацию в пределах одной и той же опухоли. ФИГ. 22С представляет иллюстрацию Alk DAB окрашивания репрезентативного образца, приготовленного из папиллярной уротелиальной опухоли почки.
Пример 6. Механическая диссоциация и гомогенизация образцов ткани
В этом примере описывается стадия механической диссоциации и гомогенизации образцов ткани для приготовления репрезентативного образца. Методы включают нарезание и измельчение образца ткани и диссоциацию до одиночных клеток.
Методы
Ткани нарезали вручную (ФИГ. 25А) или измельчали, используя соответствующий прибор для переработки пищевых продуктов, такой как "соковыжималка" (ФИГ. 25В). Несмотря на то, что в этих методах применяется фиксированная в формалине ткань миндалин (показанная на ФИГ. 25A-25B), также можно использовать другие типы тканей. Миндалины заказывали свежполученными, фиксировали в 10%-ном забуференном до нейтрального значения формалине в течение 24 часов, и затем хранили в чистом этаноле. Миндалину шинковали вручную, используя скальпель, или подвергали механической диссоциации в соковыжималке. Затем проводили дегидратацию полученных гомогенатов и перфузировали парафиновым воском в гистопроцессоре (НАЗВАНИЕ ПРОЦЕССОРА). Готовили срезы образцов толщиной четыре микрона и для визуализации распределения тканевых фрагментов по размерам использовали Н&Е окрашивание.
Результаты и обсуждение
Чтобы определить, привели ли процедуры измельчения, нарезания и обработки в соковыжималке к получению равномерного распределения фрагментов ткани, лимфатический узел (миндалину) шинковали вручную или подвергали механической диссоциации, используя соковыжималку. Как видно из ФИГ. 25А и ФИГ. 25В, шинкование вручную подвергнутой фиксации миндалины приводит к получению смеси фрагментов ткани с очень равномерным распределением по размерам. Фрагменты ткани содержат от десятков тысяч до сотен тысяч клеток и сохраняют структуру органа гистологически распознаваемым образом.
Подвергание лимфатического узла диссоциации с использованием соковыжималки приводит к образованию более мелких фрагментов ткани, содержащих от нескольких сотен до нескольких тысяч клеток (ФИГ. 25С и ФИГ. 25D). Фрагменты ткани, образующиеся с помощью соковыжималки, представляют собой такой гомогенат ткани, межклеточные взаимодействия в котором могут быть оценены патологоанатомом.
Подразумевается, что измельчение, обработку в соковыжималке и обработку в блендере можно применять независимо или в сочетании. Например, извлеченную резекцией опухоль сначала можно измельчить с получением однородной популяции фрагментов ткани для заливки парафином и гистологического исследования. Образец измельченного гомогената затем можно обработать в соковыжималке или блендере с целью проведения дальнейшей диссоциации ткани в процессе подготовки к дальнейшей ферментативной диссоциации, предназначенной для выделения одиночной клетки или одиночных ядер.
Пример 7. Диссоциация гомогенатов (или репрезентативных образцов) до одиночных клеток
В этом примере описывается дальнейшая обработка репрезентативных образцов, происходящих из органов, тканей или опухолей (путем обработки в блендере, обработки в соковыжималке или измельчения), до получения одиночных клеток для количественного определения, выделения и анализа биомаркеров. Способы включают механическую диссоциацию, фильтрование, ферментативную диссоциацию и ультразвуковую обработку.
Способы механической диссоциации и фильтрации
Клинический опухолевый образец, использованный в этом примере, представляет собой образец вышеупомянутой аденокарциномы толстой кишки, полученный от GLAS Tissue Consultants. Гомогенаты лимфатического узла (миндалины) и аденокарциномы толстой кишки готовили так, как описано выше. Образец гомогената фильтровали, используя сито с размером ячеек 1 мм (Advantech Manufacturing, New Berlin, WI), и собирали материал, который не мог пройти через сито. Образец гомогената, который проходил через сито с размером ячеек 1 мм, далее фильтровали, используя фильтр с размером пор 20 микрон (Pluriselect, Сан-Диего, СА). Собирали материал, который не мог пройти через фильтр с размером пор 20 микрон. Гомогенат, который мог пройти через фильтр с размером пор 20 микрон, далее пропускали через фильтр с размером пор 10 микрон и собирали одиночные клетки, прошедшие через него. Одиночные клетки, прошедшие через фильтр с размером пор 10 микрон, центрифугировали в течение 5 минут при 800 g, ресуспендировали в PBS с 3% BSA и 0,09% азида натрия, повторяя это три раза, и супернатант отбрасывали. Теперь одиночные клетки готовы для хранения при 4°С.
Чтобы охарактеризовать распределение по размерам для одиночных клеток, собранных на стадиях фильтрования, использовали счетчик Коултера Multisizer 4е (Beckman Coulter, Indianapolis, IN). Для определения характеристик одиночных клеток, а также для сортировки и сбора одиночных клеток использовали проточный цитометр с акустической фокусировкой Attune (ThermoFisher Scientific). Чтобы осуществить механическую диссоциацию многоклеточных кластеров до одиночных клеток, использовали ультразвуковой диспергатор. В некоторых случаях использовали 250 единиц коллагеназы (ТИП & КОМПАНИЯ) для осуществления биохимической диссоциации многоклеточных кластеров путем инкубации при 37°С в течение 1 часа в сбалансированном солевом буферном растворе Хенкса. После инкубации смесь центрифугировали при 800 g в течение 1 мин и ресуспендировали в PBS.
Для окрашивания эпителиальных клеток из фильтрата использовали антитело к EpCam (Ventana Medical Systems, Inc., Тусон, AZ). Первичное антитело инкубировали с ядрами из образца в течение 1 ч при 37°С или в течение 24 ч при 4°С. В контрольные образцы не вносили первичного антитела. После инкубации образцы промывали 6 раз буфером EZ prep и затем ресуспендировали в растворе конъюгированного с Alexa-488 антимышиного антитела козы (1:500) в MACS буфере в течение 0,5-1 ч при 37°С. Некоторые образцы также окрашивали, используя 3 мкМ DAPI в течение 10 мин. Окрашенные образцы промывали 4 раза реакционным буфером при 4°С. Образец объемом 50 мкл наносили на предметные стекла VWR plus и незамедлительно подвергали визуализации через покровное стекло. Изображения окрашенных клеток получали с использованием эпифлуоресцентного микроскопа Axio от Zeiss, управляемого программным обеспечением собственной разработки, и изображения анализировали с использованием ImageJ. Окрашенные ядра хранили при 4°С в MACS-T-STC.
Результаты и обсуждение
Цель последовательно проводимых стадий фильтрации заключалась в определении состава частиц различного размера, которые содержатся в гомогенате. На каждой стадии ткань, которая не могла пройти через фильтр, тщательно анализировали с использованием световой микроскопии (Фиг. 29). Как показано на ФИГ. 26А, материал, который не мог пройти через сито с размером ячеек 1 мм, состоял в основном из соединительной ткани и мышечных волокон. Этот материал не обладал клеточностью, и поэтому его отбрасывали. Материал, который не мог пройти через фильтр с размером пор 20 микрон, в основном состоял из больших многоклеточных кластеров (ФИГ. 26В). Материал, который не мог пройти через через фильтр с размером пор 10 микрон, в основном состоял из небольших многоклеточных кластеров опухолевых клеток (ФИГ. 26С), в то время как материал, прошедший через фильтр с размером пор 10 микрон, представлял собой одиночные клетки, которые высвобождались во время процесса гомогенизации (ФИГ. 26D). Таким образом, в результате гомогенизации опухолей человека с целью приготовления репрезентативных образцов получаются фрагменты тканей с распределением по размерам в диапазоне от больших многоклеточных кластеров до отдельных клеток.
Для измерения выхода (количества одиночных клеток на один грамм гомогенизированной ткани), а также размера подвергнутых диссоциации одиночных клеток, выделенных из аденокарциномы толстой кишки, использовали счетчик Коултера Multisizer 4е (Beckman Coulter, Indianapolis IN). Подсчитывали число частиц размером от 4 до 10 мкм и их рассматривали как одиночные клетки. Выход на один грамм гомогената опухоли с использованием способа с применением фильтрации составлял приблизительно 320106 клеток/грамм. Клетки, выделенные из гомогената опухоли, распределяли на две различающиеся популяции: клетки с размером в диапазоне 4-5,5 микрон в диаметре и клетки с размером в диапазоне 5,5-9,3 микрон в диаметре (ФИГ. 27А). Такой же анализ проводили для клеток, очищенных из гомогенизированной миндалины, и большинство клеток, выделенных из миндалины, составляли от 4 до 5,5 микрон в диаметре (ФИГ. 27В).
Распределения по размерам для одиночных клеток, выделенных из опухоли толстой кишки и миндалины, свидетельствует о том, что клетки с размером в диапазоне от 4 до 5,5 микрон в диаметре, представляют собой иммунные клетки, в то время как клетки с размером в диапазоне от 5,5 до 9,3 микрон представляют собой опухолевые клетки. Чтобы подтвердить этот вывод, отдельные опухолевые клетки, выделенные из опухоли толстой кишки, флуоресцентно окрашивали на EpCam с целью определения размера компонента - опухолевой клетки. Флуоресцентно окрашенные клетки сначала наносили на предметное стекло для микроскопа и подвергали визуализации с использованием флуоресцентного микроскопа для оценки процедуры окрашивания (ФИГ. 28). После сортировки на устройстве для проточной сортировки Attune проводили повторную оценку размера отсортированных ЕрСАМ-положительных клеток, используя счетчик Коултера. Соответственно, распределение по размерам для ЕрСАМ-положительных опухолевых клеток коррелирует с клеточной популяцией, чего не наблюдается для не содержащей опухоли миндалины, но имеет место для одиночных клеток из гомогенизированной опухоли толстой кишки.
Эти данные свидетельствовали о том, что подвергнутые механической диссоциации и фильтрованию клетки из гомогенизированной опухоли толстой кишки представлены двумя различающимися популяциями: нормальными иммунными клетками и опухолевыми клетками. Эти две популяции можно легко различить, используя анализатор размера частиц, и выделенные клетки можно анализировать далее с применением проточной цитометрии и сортировки. Кроме того, эти данные позволяют высказать предположение, что методы разделения на основании размера (с применением колонок для гель-фильтрации, микрофлюидного устройства, центрифугирования в градиенте плотности и т.д.) могут быть адаптированы для разделения данных двух популяций с получением обогащенных образцов опухолевых или иммунных клеток.
Диссоциация многоклеточных фрагментов
Многоклеточные фрагменты (или кластеры), которые не проходили через фильтры с размером пор 20 и 10 микрон, подвергали дальнейшей обработке с целью получения одиночных клеток. В попытках осуществления физической диссоциации многоклеточных фрагментов до одиночных клеток применяли ультразвуковую обработку с использованием снабженного зондом ультразвукового диспергатора. Многоклеточные фрагменты подвергали воздействию возрастающих количеств энергии звуковой волны и высвобождение опухолевых клеток оценивали, анализируя размер частиц с использованием счетчика Коултера. Как показано на ФИГ. 35, возрастание количества энергии звуковой волны приводит к высвобождению частиц диаметром от 5,5 до 9,3 микрон (стрелка на панели 245J). Высвобожденные физическим путем клетки коррелируют с опухолевыми клетками, выделенными из гомогената в приведенном выше примере, что свидетельствует о том, что многоклеточные фрагменты состоят преимущественно из опухолевых клеток.
Для дальнейшего усиления диссоциации многоклеточных фрагментов до одиночных клеток образец многоклеточных фрагментов инкубировали с коллагеназой. После 72 часов инкубирования с коллагеназой 1 типа проводили анализ распределения по размерам обработанных коллагеназой многоклеточных фрагментов. Как показано на ФИГ. 33А и 33С, действие одной только коллагеназы не приводит к высвобождению одиночных клеток из многоклеточных фрагментов. Когда после обработки коллагеназой добавляли ультразвуковую обработку, большая часть многоклеточных фрагментов диссоциировала до одиночных частиц с размерами в диапазоне от размера нормальных иммунных клеток (4-5,5 микрон в диаметре) до размера опухолевых клеток (5,5-9,3 микрон в диаметре). Эти данные демонстрируют, что репрезентативные образцы, происходящие из органов, тканей и опухолей человека, можно подвергнуть дополнительной обработке для получения одиночных клеток с использованием механических, физических и биохимических методов.
Определение характеристик биомаркеров в случае одиночных клеток из репрезентативных образцов
Одиночные клетки из репрезентативного образца опухоли толстой кишки далее характеризовали в отношении экспрессии биомаркеров в анализе с применением флуоресцентного окрашивания и проточной цитометрии. Проточная цитометрия представляет собой общепринятый диагностический метод анализа живых клеток, взятых из образцов-биоптатов. От нескольких тысяч до нескольких сотен тысяч клеток можно детально исследовать на предмет присутствия или отсутствия биомаркеров с одновременным количественным определением числа клеток и уровня экспрессии биомаркеров для каждой клетки. Специалисту в данной области техники известно, что фиксированные в формалине образцы тканей, приготовленные из извлеченных резекцией органов, тканей или опухолей, не поддаются исследованию с применением проточной цитометрии, поскольку имеющиеся в настоящее время методы анализа для фиксированных в формалине образцов включают заливку парафином и приготовление гистологических срезов, а не диссоциацию до одиночных клеток. Целью приведенного далее примера является определение того, можно ли обработанные клетки, полученные из опухоли толстой кишки, анализировать с использованием проточной цитометрии.
Методы
Клетки окрашивали антителами к CD3, CD8, CD45, CK8/18, EGFR и PD-L1 от Ventana Medical Systems, Inc. В некоторых случаях для улучшения флуоресцентного окрашивания использовали тирамидную амплификацию сигнала. Клетки (приблизительно 3×107 клеток на одну пробирку) центрифугировали при 300 × g в течение 2 мин, после чего ресуспендировали в 0,3 мл 3%-ного раствора H2O2. После инкубации в течение 15 мин клетки промывали 3 раза PBS, содержащим 0,1% твина 20, 0,1% BSA. На 5 мин добавляли TSA-блокирующий буфер (0,3 мл), затем инкубировали в 0,2 мл раствора первичного антитела в течение 30 мин при 37°С. Затем клетки 3 раза промывали PBS, содержащим 0,1% твина 20, 0,1% BSA, и далее ресуспендировали в 0,2 мл раствора антивидового антитела козы, конъюгированного с пероксидазой хрена, в течение 30 мин при 37°С. После этого клетки разбавляли, используя 1,2 мл 20 мкМ тирамида-родамина 101, и инкубировали в течение 5 мин, затем добавляли 1,2 мл TSA H2O2 в течение 30 мин. Клетки 3 раза промывали PBS, содержащим 0,5% декстрана, 0,1% твина 20, 0,1% BSA, и ресуспендировали в MACS-T-STC для хранения. Перед проведением визуализации или проточной цитометрии клетки окрашивали, используя 3 мкМ DAPI, в течение 10 мин.
Анализ биомаркеров с применением проточной цитометрии
Систему проточной цитометрии Attune (ThermoFisher Scientific) использовали для количественного определения процентных содержаний клеток, экспрессирующих различные биомаркеры. Разница в интенсивности флуоресценции между контролем (клеткой, окрашенной без использования первичного Ab) и образцами (клеткой, окрашенной с использованием первичного Ab) пропорциональна численности клеток-мишеней в целой клеточной популяции, и ее использовали для расчета процентного содержания положительно окрашенных клеток в данной популяции. Как показано на ФИГ. 29А-29Е, для всех протестированных биомаркеров детектировали сигналы флуоресценции, превышающие фон. Для одного и того же образца детектировали компоненты иммунных систем и опухоли: CD45 и CD8, в сравнении с CK8/18 и EGFR (ФИГ. 29А-29С). В некоторых случаях одновременно могут окрашиваться как иммунные клетки, так и опухолевые клетки (PD-L1 на ФИГ. 29Е). Кроме того, процентное содержание клеток, окрашенных положительно в анализе с применением проточной цитометрии, аналогично таковому в случае IHC окрашивания подвергнутого заливке репрезентативного образца, соответствующего тому же клиническому случаю (ФИГ. 29А-29Е).
Опираясь на эти данные, авторы изобретения демонстрируют способы и последовательность действий, необходимые для подвергания гомогенатов, приготовленных из органов, тканей и опухолей, дальнейшей диссоциации до одиночных клеток с целью анализа биомаркеров с использованием проточной цитометрии. Специалисту в данной области техники будет известен количественный характер данных, полученных с использованием проточной цитометрии. Теперь, опираясь на эти данные, можно рассчитать процентные содержания клеточных компонентов из извлеченных резекцией опухолей, оценив относительное содержание каждого типа клеток. Например, согласно приведенным выше данным 33% клеток опухоли толстой кишки, анализируемой в этом примере, представляют собой опухолевые клетки. Кроме того, приблизительно 33% опухолевых клеток являются PD-L1-положительными (см. разницу в измерении DAPI в анализе PD-L1 проточной цитометрией, ФИГ. 29Е), и обнаружено еще меньшее процентное содержание для клеток, являющихся EGFR-положительными (EGFR-положительными клетками, ФИГ. 29F). Для опухоли толстой кишки 20% клеток представляют собой иммунные клетки (CD45-положительные клетки, ФИГ. 29С) и только часть этих клеток является CD8-положительными (ФИГ. 29D).
Выделение и захват одиночных клеток
Чтобы обеспечить возможность выполнения анализа биомолекул специфических клеточных популяций, проводили выделение и захват одиночных клеток из репрезентативного образца опухоли толстой кишки. В этом примере использовали два типа выделения и захвата, проточную сортировку и сортировку на основе аффинности с применением магнитных гранул.
Для идентификации и захвата опухолевых клеток из одиночных клеток, полученных посредством диссоциации репрезентативного образца аденокарциномы толстой кишки, клетки окрашивали на ЕрСАМ (молекулы адгезии эпителиальных клеток), используя предварительно описанный метод окрашивания с применением тирамида для осаждения родамина 101 и окрашивания ДНК с использованием DAPI. В анализе с использованием клеточного сортера SH800 от Sony, ЕрСАМ-положительные опухолевые клетки (зеленая популяция на ФИГ. 30А) демонстрируют более высокое содержание ДНК при обратном гейтировании на на графике зависимости интенсивности DAPI (ФИГ. 30В). ЕрСАМ-отрицательные клетки с характеризующей диплоидную ДНК интенсивностью DAPI представляют собой нормальные клетки. В этом примере отсортировывали клетки, которые одновременно являются ЕрСАМ-положительными и характеризуются высокими уровнями окрашивания DAPI. При последующем анализе размера отсортированных клеток с использованием счетчика Коултера диапазон размеров составляет от 5,5 до 9,3 микрон в диаметре (ФИГ. 27С). Специалисту в данной области техники будет известно, что также могут быть отсортированы ЕрСАМ-отрицательные клетки с характеризующей диплоидную ДНК окрашиванием DAPI. Эти данные демонстрируют способность к выделению и захвату различающихся популяций клеток из репрезентативных образцов, приготовленных из органов, тканей и опухолей, с использованием устройства для проточной сортировки.
Отдельным способом выделения и захвата специфических клеточных популяций является извлечение популяций клеток, экспрессирующих специфические маркеры клеточной поверхности, посредством отбора на основании аффинности с применением магнитных гранул. В этом примере одиночные клетки из лимфатического узла инкубировали с магнитными гранулами (Dynabeads, ThermoFisher Scientific), соединенными с первичными антителами к CD3 или CD8. Клетки инкубируют с магнитными гранулами, конъюгированными с антителами, в соответствии с протоколом производителя. По окончании инкубации магнитные гранулы благодаря магнитным свойствам осаждаются на дне, и жидкость, содержащую несвязавшиеся клетки, удаляют из пробирки. Проточную цитометрию использовали для того, чтобы продемонстрировать истощение CD3-или CD8-положительных клеток в образце, аналогично анализу на ФИГ. 31А. На Фиг. 34В можно видеть истощение клеток конкретного типа, при этом процентное содержание клеток, экспрессирующих CD3 или CD8, уменьшается после инкубации с магнитными гранулами, конъюгированными с соответствующими антителами.
Опираясь на эти данные, авторы изобретения демонстрируют, что одиночные клетки, полученные из репрезентативных образцов, приготовленных из органов, тканей и опухолей, могут быть выделены и захвачены для дальнейшего диагностического исследования. Специалисту в данной области техники будет очевидно, что для анализа очищенных клеточных популяций может быть использовано любое количество диагностических методов, таких как ПЦР, NGS, проточная цитометрия, секвенирование из одной клетки или транскриптомика, основанный на масс-спектрометрии протеомный анализ и другие диагностические методы.
Пример 8. Исследования жизнеспособности и стабильности образца ткани
Жизнеспособность свежеполученной ткани
Свежеполученную миндалину обрабатывали в блендере IKA в DPBS без магния и без кальция в соотношении 1:1 (масс.:об.) при 3000 об./мин в течение двух минут (Rep) и сравнивали с миндалиной, приготовленной традиционным методом измельчения ткани скальпелем с последующим расщеплением коллагеназой для первичной клеточной культуры (Trad) (Donnenberg, et al., Methods Mol. Biol., 568: 261-279, 2009).
Повреждение ткани оценивали, измеряя высвобождение РНК (цитоплазматическое повреждение) и ДНК (повреждение ядер) в супернатант (ФИГ. 34). Гомогенизация ткани миндалины является намного более быстрым процессом, чем традиционный способ измельчения с последующим расщеплением под действием коллагеназы, поскольку для гомогенизации не требуется какой-либо ферментативной обработки. Как указано на Фиг. 37, по результатам измерений высвобождения ДНК и РНК в супернатант после гомогенизации свежеполученной миндалины образуется меньше повреждений, чем при традиционном способе. Величина ошибок представляет собой стандартную ошибку для двух экспериментов.
Исследования стабильности нуклеиновых кислот, белков и клеток из фиксированных в формалине тканей
Ткань из хорошо дифференцированной нейроэндокринной опухоли поджелудочной железы, папиллярной уротелиальной карциномы и аденокарциномы толстой кишки (ФИГ. 35А, 35В и 35С, соответственно) инкубировали в стандартных растворах для хранения клеток (20%-ном глицерине, 10%-ном диметилсульфоксиде (DMSO), 5%-ном МеОН и 100%-ном МеОН) при указанных температурах в течение 6 месяцев. РНК выделяли и анализировали на биоанализаторе от Agilent. Как показано на ФИГ. 35А, 35В и 35С, при всех способах хранения сохранялась целостность РНК, хотя и на разных уровнях, на что указывают незначительные различия в интенсивностях пиков 18S РНК в кривых записи биоанализатора (см. образец в 20%-ном глицерине на ФИГ. 38А). Эти данные указывают на то, что при многочисленных способах хранения фиксированных в формалине репрезентативных образцов сохраняется целостность РНК в течение некоторого периода времени.
Белок, по результатам измерений с использованием IHC окрашивания на с-Met, довольно стабилен как в случае папиллярной уротелиальной карциномы, так и в случае аденокарциномы толстой кишки (ФИГ. 36А и 36В, соответственно) при всех условиях хранения и всех температурах на протяжении всего периода тестирования 6 месяцев. По окончании шестимесячного периода хранения образцы наносили на предметные стекла, окрашивали на c-Met и подвергали визуализации, используя светлопольный микроскоп. Поскольку имеет место некоторая агрегация образца и морфология клеток со временем может ухудшаться, то на протяжении всего исследования зависимости стабильности от времени для всех составов буфера можно обнаружить как положительное, так и отрицательное окрашивание клеток.
Возможность хранения репрезентативных образцов далее исследовали путем оценки "сверхбыстрого замораживания" в PBS. Тридцать миллилитров репрезентативного образца аденокарциномы толстой кишки подвергали сверхбыстрому замораживанию в PBS в бане со смесью сухой лед/спирт и хранили при -80°С. Затем их размораживали при 37°С и отбирали аликвоту для 10 последовательных циклов замораживания-оттаивания. Все образцы, взятые после проведения цикла замораживания-оттаивания, наносили на предметные стекла, при этом для оценки стабильности морфологии клеток использовали Н&Е окрашивание, а для оценки стабильности белка использовали с-Met IHC. Как показано на ФИГ. 37А, морфология клеток оказалась очень стабильной на протяжении всех циклов замораживания-оттаивания, в случае подвергания образцов сверхбыстрому замораживанию и хранения при -80°С, также как и белок, по данным на основе биомаркеров (ФИГ. 37В).
Стабильность РНК и ДНК оценивали в этих же образцах на протяжении 10 циклов замораживания-оттаивания. Суммарную ДНК и РНК экстрагировали из образцов, используя стандартные методы с применением смеси фенол/хлороформ, и анализировали на биоанализаторе от Agilent. Как ДНК, так и РНК были стабильны на протяжении курса, состоящего из циклов замораживания-оттаивания, при этом ДНК была более стабильна, чем РНК (ФИГ. 38).
Опираясь на эти данные, авторы изобретения продемонстрировали многочисленные способы для хранения репрезентативных образцов, приготовленных из органов, тканей и опухолей.
Пример 9. Обогащение ядер опухолевых клеток из репрезентативного образца
В этом примере описывается дальнейшая обработка фиксированных в формалине репрезентативных образцов, приготовленных из органов, тканей или опухолей (путем обработки в блендере, обработки в соковыжималке или измельчения), до получения отдельных ядер для количественного определения, выделения и анализа биомаркеров. Способы включают механическую диссоциацию, фильтрование и ферментативную диссоциацию. Уникальные аспекты способов включают: 1) установление способа экстракции и дезагрегирования одиночных частиц, содержащих ядра, из фиксированных в формалине репрезентативных образцов; 2) оценку воспроизводимости выделения частиц из разных аликвот одного и того же репрезентативного образца; 3) установление подхода для контроля степени разрушения клеток, нанесенного образцу в результате применения способов механической диссоциации и экстракции ядер; 4) идентификацию маркеров, остающихся в ассоциации с ядрами, экстрагированными из репрезентативных образцов, которые будут служить для различения опухолевых и нормальных субпопуляций; 5) установление методологии анализа экстрагированного, окрашенного материала из подвергнутых фиксации репрезентативных образцов посредством проточной цитометрии; 6) установление количества опухолевых частиц, которое потребуется для: а) получения достаточного для секвенирования количества ДНК и b) сохранения аналитической чувствительности в отношении субклонов с низкой распространенностью.
Методы и материалы
Механическую диссоциацию проводили, используя шаровую барабанную мельницу с системой управления от IKA-Works (0004180001; Штауфен-им-Брайсгау, Германия) и диссоциатор gentleMACS от Miltenyi Biotech (Тетеров, Германия). Все применяемые фильтры поступали от Pluriselect (Сан-Диего, СА). Использовали буферы следующих компаний: СС1 (950-124; Ventana Medical Systems, Тусон, AZ), EZ prep (950-102; Ventana Medical Systems), реакционный буфер (950-300; Ventana Medical Systems), autoMACS буфер (130-091-221, Miltenyi Biotech), DPBS (14190, Fisher Scientific, USA). Твин 20 приобретали у Fisher Scientific, USA (AC233362500). У Sigma, США, приобретали следующие реагенты: NP40 (74385), ДНКазу (AMPD1), тетрахлорид спермина (S2876), DAPI (D9542), трипсин (59427 с), пепсин (р7012), проназу (Р5147). Другие ферменты поступали от следующих компаний: протеиназа К (0706, VWR, USA), AccuMax® (АМ105, Innovative Cell Technologies, Сан-Диего, СА), коллагеназа Н (11074032001, Roche, Базель, Швейцария). Тирамид-родамин 101 синтезировали своими силами, используя химические реагенты, приобретенные у Sigma. Мышиное антитело к цитокератину 8/18 (760-4344), мышиное антитело к CD45 (760-2505) и HRP-конъюгированное антимышиное антитело козы (760-4310) поступали от Ventana Medical Systems. Конъюгированное с Alexa 488 антимышиное антитело козы приобретали у Invitrogen (А-11001).
Модели тканей и клинические образцы
Миндалины человека получали из Северо-западного медицинского центра (Тусон, AZ) и фиксировали в 10%-ном забуференном до нейтрального значения рН формалине в течение 24 часов в Ventana Medical Systems. Опухолевые образцы получали от GLAS/(Уинстон-Сейлем, NC http://glaswpcopy.wpengine.com/). и они предварительно были фиксированы в формалине.
Окрашивание гематоксилином и эозином
Репрезентативные образцы в autoMACS буфере помещали на предметные стекла VWR plus. Окрашивание гематоксилином и эозином (Н&Е) проводили, используя платформу Symphony от Ventana Medical Systems (Ventana Medical Systems, Тусон, AZ) и соответствующие реагенты Н&Е серии Symphony (Ventana Medical Systems, Тусон, AZ).
Иммуногистохимия
Срезы тканей или залитые парафином репрезентативные образцы подвергали основанному на измерении DAB иммуногистохимическому (IHC) анализу методом светлого поля, используя платформу BenchmarkXT от Ventana Medical Systems (Ventana Medical Systems, Тусон, AZ). Визуализацию биомаркеров осуществляли, используя набор для детекции DAB OptiView от Ventana (760-700). Антитела инкубировали в течение 4 минут. Изображения получали на светлопольном микроскопе Axio от Zeiss.
Проточная цитометрия
Что касается анализа агрегации, то перед проведением анализа на проточном цитометре с акустической фокусировкой Attune (Thermo Fisher Scientific, USA) образцы пропускали через фильтр с размером пор 40 мкм. Перед фильтрованием частицы инкубировали с DAPI (3 мкМ) в течение 10 мин. Если скорость потока была более 4000 событий в минуту, образец разбавляли.
Для проведения проточной сортировки образцы пропускали через фильтр с размером пор 40 мкм, после чего окрашивали (см. ниже) и анализировали на клеточном сортере SH800 от Sony. Для различения дублетов использовали длительность и интенсивность обусловленного DAPI импульса.
Способ экстрагирования частиц, содержащих одиночные ядра, из репрезентативного образца
Используя фиксированную в формалине миндалину в качестве модельной системы, исследовали различные ферментативные методы для диссоциации аликвот репрезентативного образца до одиночных частиц. Сначала, до проведения ферментативных стадий, материал миндалины подвергали механической диссоциации в блендере IKA в auto MACS буфере, разбавленном в соотношении 1:1 в СС1 буфере, который был нагрет до 85°С, и далее измельчали в пробирках gentleMACS, используя диссоциатор gentleMACS. Образец подвергали двум раундам нагревания при 85°С в течение 5 мин с последующей обработкой в блендере. По завершении механической диссоциации проводили качественную оценку разных условий ферментативной обработки посредством визуального контроля окрашенного Н&Е материала после его расщепления и пропускания через фильтр с размером пор 100 мкм. Инактивацию ферментов исследовали, инкубируя материал при 4°С в течение 24 ч после каждой стадии инактивации, нанося материал на предметные стекла VWR plus, окрашивая с использованием Н&Е и регистрируя морфологию клеток или целостность ядра. Протестированные условия суммированы в Таблице 3.

Сравнение выхода частиц при каждом способе диссоциации
Проводили параллельное сравнение разных способов ферментативной и механической диссоциации, используя последовательно отобранные аликвоты репрезентативного образца миндалины. Результаты сравнения этих способов суммированы в Таблице 6. Эффективность каждого способа оценивали путем подсчета, с использованием гемоцитометра, числа частиц, высвобождающихся при применении каждого способа, на один грамм исходного вещества. Там где это указано, биологические образцы анализировали в трех повторах.
Оценка разрушения клеток
На каждой стадии в ходе проведения диссоциации отбирали супернатанты и анализировали на предмет высвободившейся в раствор ДНК, как индикатора разрушения ядер. Супернатанты разделяли на три части для проведения технических повторов. Там, где необходимо, образцы концентрировали, используя geneVac (SP Scientific). Из остатка экстрагировали ДНК, используя набор High Pure FFPE от Roche в соответствии с инструкциями производителя. Кроме того, ДНК экстрагировали из ал и квоты массой 0,1 г, вместе с сохраненными при обработке жидкостями, отобранной из основной массы гомогената, для получения образца сравнения. Выходы ДНК оценивали с использованием спектрофотометра Nanodrop-1000 (Thermo Scientific). ДНК, экстрагированную из прошедших обработку жидкостей, выражали в процентах от ДНК, экстрагированной из образца сравнения, выполняющей функцию биомаркера повреждения клеточных ядер, при том предположении, что процентное содержание высвободившейся ДНК пропорционально процентному содержанию поврежденных ядер.
Сведение агрегации частиц к минимуму
Частицы, выделенные из репрезентативных образцов миндалины способом с применением протеиназы K-пепсина, окрашивали с использованием DAPI (3 мкМ, 10 мин) с целью визуализации содержания ДНК и анализировали с использованием проточной цитометрии. Об агрегации свидетельствует наличие частиц, содержащих двойные, тройные и более, чем тройные уровни ДНК. Для определения вспомогательных веществ, которые могут способствовать дезагрегации частиц, тестировали следующие условия: 1% твина 20, 1% NP40, ДНКаза, 1,5 мМ тетрахлорид спермидина, 5 мМ CaCl2. Для оценки процента двойных, тройных и более, чем тройных уровней ДНК из препаратов нормальной миндалины в присутствии каждого из вспомогательных веществ использовали проточную цитометрию с применением гистограмм для DAPI.
Выделение ядер из репрезентативных образцов с использованием способа расщепления с применением протеиназы K-пепсина
Репрезентативные образцы, приготовленные из ткани миндалины, подвергали механической диссоциации, используя СС1 буфер, как описано выше. Что касается опухолевой ткани, то сначала проводили механическую диссоциацию основной массы в MACS буфере в блендере IKA при соотношении опухоль:MACS, равном 1:1, затем отбирали аликвоты из суммарного гомогената и проводили дальнейшую обработку в блендере ЖА, используя соотношение 1 г опухолевой ткани: 5 мл раствора. Разбавленный обработанный в блендере материал фильтровали через металлическое сито с размером ячеек 1 мм × 1 мм и профильтрованный материал подвергали выдерживанию в СС1 буфере, используя соотношение 1 г опухолевой ткани: 5 мл СС1 буфера, как описано выше. Как для образцов миндалины, так и опухоли СС1 буфер заменяли на DPBS (1:1), используя центрифугирование при 300 × g в течение 1 мин в настольной микроцентрифуге (Eppendorf); все последующие замены жидкостей осуществляли аналогичным образом. После центрифугирования осадок ресуспендировали как 1:1 в DPBS, содержащем протеиназу K в концентрации 1 мг/мл, и инкубировали при 50°С в течение 10 мин. Для инактивации протеиназы K и для дальнейшей диссоциации образец переносили в раствор, содержащий пепсин (5 мг/мл) в 150 мМ NaCl, рН 1,5. Значение рН раствора тестировали с применением рН-полосок и при необходимости повторно подводили до 1,5-2, используя 5 М раствор HCl. Образец инкубировали в течение 30 мин при 37°С при осторожном перемешивании каждые 10 мин.
В случае опухолевой ткани для повышения выходов пробирку встряхивали при 600 об./мин в ThermoMixer F1.5 (Eppendorf) при прохождении обеих стадий ферментативного расщепления. Пепсин инактивировали путем подведения рН до значения выше 8, используя 5 М раствор NaOH, и затем раствор, содержащий пепсин, заменяли на autoMACS буфер с 1% твина 20 и 1,5 мМ тетрахлоридом спермидина (MACS-T-STC). Расщепленный образец пропускали через фильтр с размером пор 40 микрон, используя 10 мл MACS-T-STC, собирали центрифугированием и ресуспендировали в 500 мкл MACS-T-STC для хранения перед последующими применениями. Воспроизводимость получения ядер из опухолевых клеток оценивали путем регистрации выходов частиц с размером в диапазоне 3-30 микрон, измеренных на Multisizer 4е (Beckman Coulter), с нормировкой на исходный "сухой" вес опухолевой ткани среди всех многочисленных процедур получения для одной и той же опухоли. Воспроизводимость далее оценивали путем регистрации распределения по размерам для частиц из разных процедур получения для одной и той же опухоли.
Окрашивание материала, выделенного из репрезентативных образцов
Стандартная иммунофлуоресценция
Ядра, полученные из 1 г репрезентативного образца опухоли способом с применением протеиназы K-пепсина, собирали центрифугированием при 300 × g в течение 1 мин, после чего ресуспендировали в 200 мкл раствора первичного мышиного антитела к цитокератину 8/18. Первичное антитело инкубировали с ядрами образца в течение 1 ч при 37°С или в течение 24 ч при 4°С. В контрольные образцы не вносили первичного антитела. После инкубации образцы промывали 6 раз буфером EZ prep и затем ресуспендировали в растворе конъюгированного с Alexa-488 антимышиного антитела козы (1:500) в MACS буфере в течение 0,5-1 ч при 37°С. Некоторые образцы также окрашивали, используя 3 мкМ DAPI в течение 10 мин. Окрашенные образцы промывали 4 раза реакционным буфером при 4°С. Образец объемом 50 мкл наносили на предметные стекла VWR plus и незамедлительно подвергали визуализации через покровное стекло. Изображения окрашенных клеток получали с использованием эпифлуоресцентного микроскопа Axio от Zeiss, управляемого программным обеспечением собственной разработки, и изображения анализировали с использованием ImageJ. Окрашенные ядра хранили при 4°С в MACS-T-STC.
Окрашивание с использованием тирамидной амплификации сигнала (TSA)
Ядерные частицы, выделенные посредством механической гомогенизации или способом с применением протеиназы K-пепсина (3×107 частиц на одну пробирку), центрифугировали при 300 × g в течение 2 мин, после чего ресуспендировали в 0,3 мл 3%-ного раствора H2O2. После инкубации в течение 15 мин ядра промывали три раза PBS, содержащим 0,1% твина 20, 0,1% BSA. На пять мин добавляли TSA-блокирующий буфер (0,3 мл), затем инкубировали в 0,2 мл раствора первичного антитела в течение 30 минут при 37°С. Ядра 3 раза промывали PBS, содержащим 0,1% твина 20, 0,1% BSA, и далее ресуспендировали в 0,2 мл раствора антивидового антитела козы, конъюгированного с пероксидазой хрена, в течение 30 мин при 37°С. Ядра разбавляли, используя 1,2 мл 20 мкМ тирамида-родамина 101, и инкубировали в течение 5 мин, затем добавляли 1,2 мл TSA H2O2 в течение 30 мин. Ядра 3 раза промывали PBS, содержащим 0,5% декстрана, 0,1% твина 20, 0,1% BSA, и ресуспендировали в MACS-T-STC для хранения. Перед проведением визуализации или проточной цитометрии ядра окрашивали, используя 3 мкМ раствор DAPI в течение 10 мин. Изображения окрашенных ядер получали с использованием эпифлуоресцентного микроскопа ВХ63 от Olympus и анализировали с использованием ImageJ.
Калибровка выхода ДНК из расчета на число частиц, выделенных механическим и ферментативным способами
Ядра выделяли из миндалины способом с применением протеиназы K-пепсина, как описано выше. Число частиц подсчитывали с использованием гемоцитометра. ДНК получали из 105, 106 и 107 частиц, используя набор High Pure FFPE от Roche в соответствии с инструкциями производителя. Выходы ДНК оценивали с использованием спектрофотометра Nanodrop-1000 (Thermo Scientific).
Результаты
Дальнейшая обработка репрезентативных образцов с целью получения отдельных ядер
Для дальнейшей обработки репрезентативных образцов с целью получения отдельных ядер необходимо удалить клеточную мембрану. Существующие в настоящее время способы выделения ядер из свежеполученных клеток не требуют применения ферментов для высвобождения ядер, а выделение ядер из фиксированного в формалине образца не является общепринятым способом. Для эффективного выделения отдельных ядер с сохранением маркеров цитоскелета, которые позволили бы различить ядра нормальных и опухолевых клеток, был разработан ферментативный способ для высвобождения ядер без чрезмерного повреждения, при котором ДНК будет высвобождаться из обработанных ядер.
Способность отщеплять клеточную мембрану от ядер оценивали для нескольких ферментов, включая проназу, протеиназу K, пепсин, трипсин, Accumax, коллагеназу Н. На ФИГ. 42 показаны примеры образцов, расщепленных под действием пепсина или трипсина в разных условиях. Набухшие, подвергнутые фрагментированию ядра, присутствующие на нижней правой панели, свидетельствуют о чрезмерном расщеплении.
После определения условий применения и инактивации для каждого фермента проводили прямое сравнение каждого способа на параллельных аликвотах из репрезентативного образца, приготовленного из фиксированной в формалине ткани миндалины. См. Таблицу 3. Помимо этого каждый способ отдельно сравнивали со способом механической гомогенизации, как описано в разделе "Методы". На ФИГ. 43 показано, что в результате обработки протеиназой K с последующим расщеплением под действием пепсина из репрезентативного образца высвобождается большая часть частиц. Несмотря на то, что в этом эксперименте показано незначительное различие в случаях использования протеиназы K в концентрации 0,1 мг/мл и 1 мг/мл, дальнейшие эксперименты с образцами опухоли продемонстрировали, что использование протеиназы K в концентрации 1 мг/мл приводит к получению наиболее согласованных результатов (не показано).
Ферментативная диссоциация увеличивает выход частиц по сравнению с механической диссоциацией
Способ диссоциации с применением протеиназы K-пепсина сравнивали с одной только механической диссоциацией для трех независимых образцов миндалины. На ФИГ. 44А-44С показано, что способ с применением протеиназы K-пепсина позволяет значительно увеличить число частиц, высвобождаемых из репрезентативного образца. Интересно, что результаты Н&Е окрашивания показывают, что многие частицы, высвободившиеся способом с применением протеиназы K-пепсина, состоят из ядер с присоединенными цитоплазматическими фрагментами или без них, в то время как подвергнутый механической диссоциации образец содержит более интактный клеточный материал (ФИГ. 48, нижние панели).
Процедуры получения ядер из опухолей являются воспроизводимыми в отношении выхода и распределения по размерам
Чтобы определить воспроизводимость получения ядер из одного и того же репрезентативного образца опухоли, оценивали стабильность выполнения способов и стабильность состава популяций, присутствующих в отдельных аликвотах. Из разных аликвот (приблизительно по 1 грамму), взятых из суммарного гомогената, получали ядра, используя способ с применением протеиназы K-пепсина, как описано выше. На Фиг. 45А показано, что выход ядер, полученных из двух разных опухолей (толстой кишки и легкого) является очень стабильным среди нескольких аликвот, взятых из одного и того же репрезентативного образца. Распределение по размерам для частиц, выделенных из опухоли толстой кишки, далее анализировали на предмет идентификации очень воспроизводимого и характерного распределения по размерам среди трех разных процедур получения (ФИГ. 45В). Примечательно, что ядра распределяются на две популяции с характерными размерами (ФИГ. 45В). Эти данные подтверждают, что разные аликвоты одного и того же репрезентативного образца имеют стабильный клеточный состав и что разработанные способы экстракции ядер дают стабильные выходы для двух разных популяций ядер.
Оценка повреждения клеток в результате диссоциации
Дальнейшая обработка репрезентативных образцов до отдельных ядер может привести к высвобождению ДНК из ядерного компартмента. Высвобождение ДНК в супернатант представляет собой возможное указание на повреждение ядер. На ФИГ. 46 показано, что примерно 4% суммарной ДНК высвобождается в ходе обработки материала миндалины механическим способом или способом с применением протеиназы K-пепсина. Обработка трех разных опухолей приводит к высвобождению менее 10% ДНК (ФИГ. 46). Интересно, что аналогичное выраженное в процентах повреждение ядер имеет место как для механического, так и для ферментативного способов, и это подтверждает, что использование способа с применением протеиназы K-пепсина позволяет выделить интактные ядра без их значительного повреждения.
Уменьшение агрегации ядер
Первоначальные эксперименты с использованием проточной цитометрии выявили, что ~35% частиц существовали в агрегированном состоянии, о чем свидетельствует присутствие частиц в пиках с более высокой интенсивностью окрашивания с применением DAPI (ФИГ. 47, панель (ii), R2 (зеленый) и R3 (розовый)). При обратном гейтировании на точечной диаграмме бокового светорассеяния против прямого светорассеяния (панель (i), зеленая и розовая популяции), эти частицы, попадающие в пики с более высокой интенсивностью DAPI, переходят в области с более высоким прямым и боковым светорассеянием, что указывает на больший размер. Несмотря на то, что общепринятое различение дублетов может позволить специфически анализировать синглетные ядра (R1, красный), число синглетных ядер, присутствующих в образце, было увеличено. Для уменьшения агрегации выделенных ядер добавляли несколько вспомогательных веществ (см. раздел Методы). Было обнаружено, что добавление 1% твина 20 снижало число агрегированных частиц с ~35% до ~23% (сравните R2+R3 графиков для В с теми же участками графиков для А). Другие вспомогательные вещества оказались неэффективными в плане снижения числа агрегированных частиц; тем не менее, добавление 1,5 мМ тетрахлорида спермина поддерживало целостность ядер в течение некоторого периода времени (не показано). Примечательно, что в отличие от свежеполученной ткани, для дезагрегации подвергнутой фиксации ткани ДНКаза не может быть использована, поскольку нет никаких функциональных клеточных или ядерных мембран, препятствующих ДНКазе в получении доступа к ядерной ДНК в клетке и ее разрушению (данные не показаны).
Цитокератины остаются в ассоциации с ядрами, выделенными из репрезентативных опухолевых образцов
Чтобы осуществить сортировку выделенных из репрезентативного образца ядер с целью отличения опухолевого варианта от нормального, были идентифицированы маркеры, которые остаются в ассоциации с ядрами. Промежуточные фнламенты (цитокератины, виментин) зачастую находятся в тесной ассоциации с ядром, и их также часто используют для распознавания карцином среди окружающей нормальной стромы. Была высказана гипотеза, что такими маркерами могут быть линиеспецифические маркеры, которые могут быть окрашены в выделенных ядерных частицах, собранных способом с применением протеиназы K-пепсина. На ФИГ. 48А показан срез из аденокарциномы толстой кишки с характерным сильным иммуногистохимическим окрашиванием на цитокератин 8/18; и срез, взятый из репрезентативного образца из той же подвергнутой фиксации опухоли, залитой парафиновым воском, показывает аналогичное окрашивание (ФИГ. 52В). На ФИГ. 48С показан материал, выделенный из репрезентативного образца этой опухоли способом с применением протеиназы K-пепсина, окрашенный на CK8/18 и визуализированный с использованием конъюгированного с флуоресцентным красителем вторичного антитела. Примечательно, что этот маркер сохраняется, когда образец подвергают диссоциации способом с применением протеиназы K-пепсина, а отрицательный контрольный образец, инкубированный без первичного антитела, показывает небольшое фоновое окрашивание (ФИГ. 48D). Виментин остается в ассоциации со многими ядрами, выделенными из миндалины. Однако, поверхностный маркер CD45, который окрашивается положительно в подвергнутом механической диссоциации образце, утрачивается при обработке протеиназой K-пепсином (не показано). Таким образом, цитокератины и виментин будут выполнять функцию линиеспецифических ассоциированных с ядрами маркеров для анализа с использованием проточной цитометрии и сортировки клеток, даже в случае разрушения поверхностных маркеров. Другие маркеры для ядер, такие как линиеспецифические транскрипционные факторы, также могут окрашиваться в случае опухолей определенных типов. Это является уникальной особенностью выделения ядер из фиксированных в формалине образцов.
Улучшение окрашивания маркеров с использованием тирамидной амплификации сигнала
Традиционное иммунофлуоресцентное (IF) окрашивание (ФИГ. 48С) не обеспечивало получения яркого и достаточно стабильного сигнала для стабильного разрешения положительно окрашенных популяций с использованием проточной цитометрии (не показано). Для анализа окрашенных образцов с использованием проточной цитометрии зачастую необходимо применение антител, которые напрямую конъюгированы с флуорофорами, чтобы получить более стабильный сигнал. В случае материала, выделенного из репрезентативных образцов, проблема состоит в том, что этот материал происходит из опухолей, которые зачастую прочно фиксированы формалином. Чтобы иметь возможность проведения общепринятого анализа подвергнутых фиксации репрезентативных образцов проточной цитометрией, использовали тирамидную амплификацию сигнала (TSA) для окрашивания антителами с использованием антител, применяемых для фиксированных формалином тканей. В случае TSA, тирамид-конъюгированные флуорофоры активируются HRP, конъюгированной с вторичным антителом, которое связывается с маркер-специфичным первичным антителом. Активированные флуоресцентные красители ковалентно связываются с белками рядом с маркером, распознаваемым первичным антителом, что дает яркий и стабильный сигнал. На Фиг. 53А показано сравнение подвергнутой механической диссоциации миндалины, окрашенной на CD45 с использованием традиционной иммунофлуоресценции, в сравнении с TSA. На Фиг. 53В показано окрашивание на цитокератин для двух опухолей разных типов, усиленное с использованием TSA. Обратите внимание на присутствие окрашенных DAPI цитокератин-отрицательных клеток в окрашенном на цитокератин образце, что указывает на специфичность TSA в растворе.
Окрашивание на цитокератин позволяет различать ядра опухолевых и нормальных клеток с использованием проточной цитометрии
Далее, проводили анализ окрашенных цитокератином (CK) и DAPI ядер из репрезентативных образцов опухолей толстой кишки и легкого с использованием проточной цитометрии (ФИГ. 50). В обоих случаях наблюдали CK-положительные (сине-зеленые) и CK-отрицательные (розовые) популяции (ФИГ. 50, панель i). CK-отрицательные популяции ассоциированы с содержанием диплоидной ДНК (ФИГ. 50, панель N), и это подтверждает, что данные ядра происходят из популяции нормальных клеток (по всей вероятности, иммунных клеток), присутствующих в опухоли. Что касается CK-положительной популяции, то окрашивание с применением DAPI выявило фракцию ядер с анеуплоидной ДНК (ФИГ. 50, панель iii), и это подтверждает, что они по всей вероятности происходят из опухолевых клеток. Для каждого образца была выполнена успешная сортировка ядер во фракции, которые были обогащены ядрами нормальных клеток (ФИГ. 50, панель iv) или ядрами опухолевых клеток (панель v). Из этих собранных популяций было проведено успешное экстрагирование ДНК, которая может быть проанализирована с использованием секвенирования следующего поколения (NGS), ПЦР, гибридизации in situ или другого последующего анализа.
В дополнение к этому, на ФИГ. 51А и 51В показано, что процентное содержание ядер опухолевых и нормальных клеток из различных опухолей варьирует. В случае образца опухоли толстой кишки данные для всей опухоли были разделены на разные сегменты гистограммы. Неидентифицированная фракция (серый цвет) соответствует материалу (в процентах по массе), который извлекали фильтрованием (см. раздел Методы). Процентное содержание эритроцитов оценивали путем вычитания общего числа частиц после ферментативного расщепления, в результате которого эритроциты разрушаются, из общего числа частиц до ферментативного расщепления. Оставшуюся фракцию относили к опухолевой и нормальной ткани в соответствии с проточным цитометрическим анализом ядер опухолевых клеток. Анализ состава опухоли на клеточном уровне может быть диагностически релевантным, в частности, когда пытаются идентифицировать популяции иммунных клеток, присутствующих в гомогенате опухоли.
Установление выхода ДНК из частиц, выделенных из репрезентативного образца
С использованием проточной сортировки собирали определенное количество частиц, имеющих специфические характеристики. Калибровка выхода ДНК из взятых в разных количествах частиц будет определять, сколько материала необходимо собрать из репрезентативных образцов для конкретного последующего анализа, такого как NGS. На ФИГ. 52 показан выход ДНК из частиц, подвергнутых механической диссоциации и диссоциации с применением протеиназы K-пепсина, из репрезентативных образцов миндалины. Важно отметить, что эти данные показывают, что частицы, выделенные способом с применением протеиназы K-пепсина, обеспечивают получение аналогичного выхода ДНК, как и частицы, выделенные с использованием одной только механической диссоциации, что указывает на то, что при ферментативном способе сохраняется целостность ДНК. Помимо этого рассчитывали количество частиц с целью определения количества, необходимого для обнаружения клона, присутствующего с показателем распространенности 5% (Таблица 8). Эти результаты будут направлять усилия на сбор достаточного количества частиц из конкретных популяций из репрезентативного образца для обеспечения варианта обнаружения в последующих приложениях с применением секвенирования.
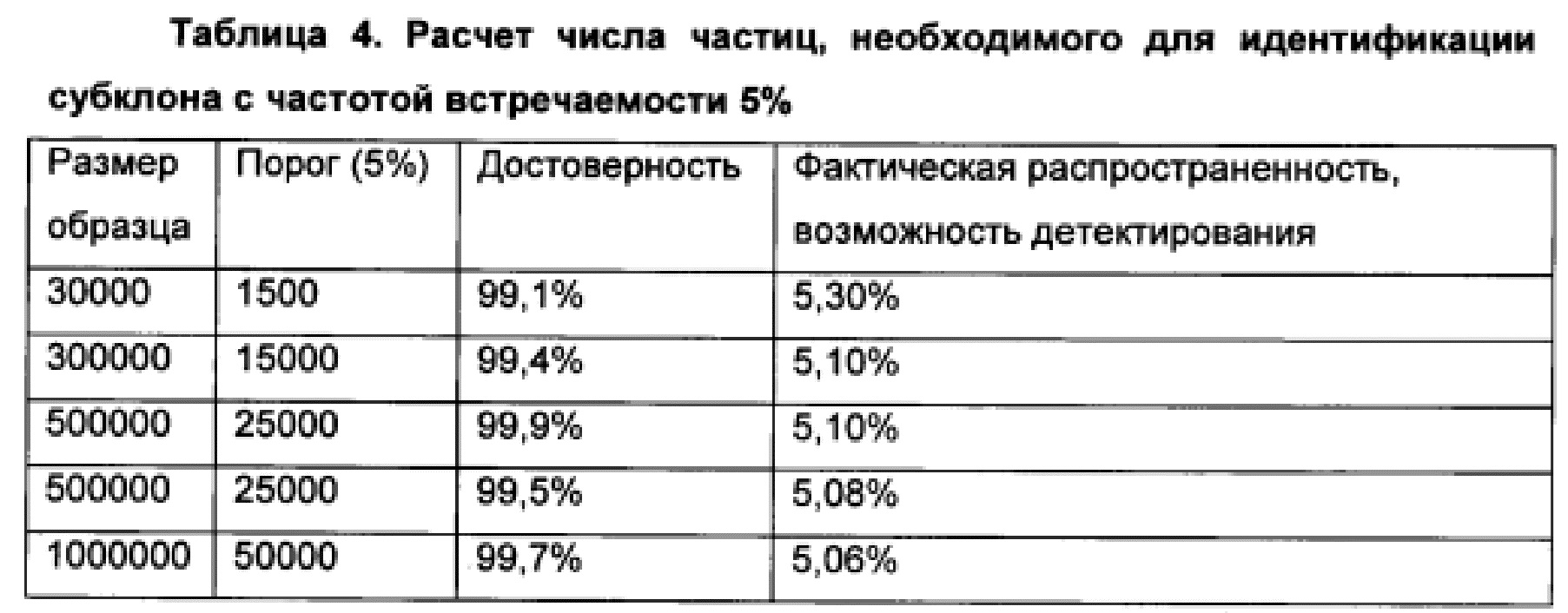
Пример 10. Гибридизация in situ на выделенных ядрах
Предшествующий уровень техники
Выделение ядер из репрезентативного образца дает возможность провести гибридизацию in situ (ISH) для образца опухоли, который является репрезентативным с точки зрения разнообразия целой опухоли, в автоматизированном режиме на автоматизированной платформе для окрашивания BenchMark от VENTANA. Интерпретация результата ISH окрашивания выделенных ядер, по всей вероятности, будет более легкой, с меньшим неспецифическим фоновым окрашиванием ввиду отсутствия залитой парафином ткани.
Материалы
Механическую диссоциацию проводили так, как описано в примере 9.
Клинические образцы
Клинические образцы описывали в примере 9.
Окрашивание гематоксилином и эозином
Репрезентативные образцы в autoMACS буфере помещали на предметные стекла VWR plus. Окрашивание гематоксилином и эозином (Н&Е) проводили, используя платформу Symphony от Ventana Medical Systems (Ventana Medical Systems, Тусон, AZ) и соответствующие реагенты Н&Е серии Symphony (Ventana Medical Systems, Тусон, AZ).
Гибридизация in situ
Выделенные ядра получали так, как в примере 8, помещали на предметные стекла в количестве 2×107 частиц на мл и оставляли высыхать на воздухе в течение ночи. Анализ образцов проводили с использованием протокола для двойной Her2/Chr17 гибридизации in situ (ISH), применяя платформу Benchmark XT от Ventana Medical Systems (Ventana Medical Systems, Тусон, AZ). Визуализацию биомаркеров осуществляли, используя детектирование с применением серебра в сочетании с HRP и детектирование с применением щелочной фосфатазы (АР) и красного красителя, соответственно. Смесь антител инкубировали в течение 8 минут. Изображения получали с использованием светлопольного микроскопа Axio от Zeiss.
Результаты
В результате выделения ядер из опухоли толстой кишки и легкого получается новый образец для ISH анализа фиксированных в формалине образцов тканей. Выделение ядер позволяет быстро оценить число копий генов, поскольку окружающая ткань не усложняет получения и интерпретации сигнала; схема детектирования показана на ФИГ. 39. Как показано на ФИГ. 39, когда олигоДНК зонды на Her2/Chr17 гибридизуются с ядрами, выделенными из репрезентативного образца, происходящего из опухоли толстой кишки, легко детектируются два гена Her2 и две альфа-сателлитные области хромосомы 17 (черный сигнал от SISH для Her2 и красный сигнал от щелочной фосфатазы для Chr17, пунктирная стрелка и стрелка, соответственно). Интересно, что фракция ядер, выделенных из репрезентативного образца, приготовленного из опухоли легкого, имеет амплификацию локуса Her2, о чем свидетельствует значительный в процентном отношении к количеству ядер сигнал SISH (ФИГ. 40, сигнал SISH для Her2, пунктирная стрелка).
Опираясь на эти данные, авторы изобретения демонстрируют возможность детального исследования отдельных ядер, происходящих из репрезентативных образцов фиксированных в формалине опухолей человека, с использованием ISH. Выделенные ядра обеспечивают получение улучшенного субстрата для ISH, поскольку в ткани нет остаточного парафинового воска, который является общей причиной фонового окрашивания в методиках ISH.
Пример 11. Анализ репрезентативных образцов с применением методов секвенирования следующего поколения
Предшествующий уровень техники
Секвенирование следующего поколения (NGS) представляет собой высокопроизводительную технологию секвенирования ДНК, которая позволяет осуществлять одновременный анализ от нескольких миллионов до нескольких миллиардов фрагментов ДНК. За последнее десятилетие значительные успехи в технологии NGS позволили исследователям и клиницистам связать мутации ДНК с гетерогенностью опухолей, устойчивостью в отношении направленной терапии и эффективностью иммунотерапии рака. Однако, опухолевые образцы, используемые для NGS в клинике, представляют собой исключительно FFPE ткани, что вносит систематическую ошибку, как описано выше. Анализ с применением NGS репрезентативных образцов из опухолей значительно улучшит клиническую значимость данных NGS.
Материалы и методы
Механическую диссоциацию опухолей проводили, используя блендер на одну порцию Hamilton Beach®, приобретенный у Walmart (Тусон, AZ) или используя шаровую барабанную мельницу с системой управления IKA Works (0004180001) от IKA-Works (Штауфен-им-Брайсгау, Германия). Все, необходимое для получения библиотек (панель онкомаркеров TruSeq Amplicon), и наборы реагентов MiSeq (наборы реагентов V2 MiSeq) приобретали у (Illumina Inc. (Сан-Диего, СА). Секвенирование проводили на секвенаторе MiSeq (Illumina, Сан-Диего, СА).
Образцы тканей толстой кишки, легкого и папиллярной уротелиальной карциномы получали от GLAS (Уинстон-Сейлем, NC), образец светлоклеточного рака почки получали из Северо-западного госпиталя (Тусон, AZ), а образец транслокационной карциномы почки получали из Регионального госпиталя города Чендлер (Чендлер, AZ). Все ткани поступали в Ventana Medical Systems в 10%-ном забуференном до нейтрального значения рН формалине.
Все ткани извлекали из упаковочного материала и направляли для изучения патологоанатомом. Ткань иссекали для отделения опухолевой ткани от нормальной и отбирали блоки для традиционных гистологических исследований. Пробы опухолевых и нормальных тканей для каждого клинического образца подвергали механической диссоциации, сначала взвешивая ткань и затем измельчая в растворе MACS PBS (Miltenyi Biotec; Тетеров, Германия) в соотношении 1:1 или 1:1,25 (масса:объем). Репрезентативные образцы хранили в MACS PBS при 4°С.
Для выделения ДНК из репрезентативных образцов использовали реагент TRIzol™ (Thermo-Fisher; Уолтем, MA) в соответствии со стандартным протоколом с одной модификацией. Образцы инкубировали в течение ночи при 60°С в TRIzol™ с протеиназой K в концентрации 2 мг/мл (VWR; Раднор, РА). В некоторых случаях гистологические срезы, взятые из FFPE блоков, использовали для сравнения общепринятой методологии отбора образцов с методологией отбора репрезентативных образцов. Для случаев, когда готовили FFPE блоки тканей, из блоков проб толстой кишки, легкого и почки с транслокационной карциномой нарезали пять срезов толщиной 10 мкм, а также один срез толщиной 4 мкм, который окрашивали гематоксилином и эозином (Н&Е). Н&Е окрашенный срез поступал на рассмотрение патологоанатомом, который идентифицировал содержащие опухоль участки. Для остальных срезов содержащие опухоль участки выделяли с использованием устройства для мезодиссекции (Roche; Базель, Швейцария). Затем выделяли ДНК, используя набор для выделения ДНК High Pure FFPET (Roche; Базель, Швейцария).
Концентрацию ДНК определяли, используя набор для dsDNA Quant-iT PicoGreen (Thermo-Fisher; Уолтем, MA). Качество ДНК оценивали, используя набор TruSeq FFPE DNA Library Prep QC от (Illumina (Сан-Диего, CA).
Для каждого образца использовали по 400 нг ДНК в качестве матрицы для набора, используемого для получения библиотек панелей онкомаркеров TruSeq Amplicon в соответствии с протоколом производителя ((Illumina; Сан-Диего, СА). После проведения амплификации реакционные смеси для ПЦР очищали, используя набор для очистки Qiaquick PCR (Qiagen; Дюссельдорф, Германия). Затем измеряли концентрации ДНК, используя набор для определения dsDNA Quant-iT PicoGreen (Thermo-Fisher; Уолтем, MA). Библиотеки смешивали в равных количествах для создания объединенной 4 нМ библиотеки. Затем библиотеки подвергали денатурации, используя равное количество 0,2 н. раствора NaOH и далее разбавляли до концентрации 20 пМ в НТ1 буфере ((Illumina; Сан-Диего, СА). Затем каждую библиотеку дополнительно разбавляли до концентрации 15 пМ в НТ1 буфере перед внесением в картридж для секвенирования.
Секвенирование выполняли на приборе MiSeq, используя наборы реагентов MiSeq V2 ((Illumina; Сан-Диего, СА) и нанося 600 мкл 15 пМ объединенной библиотеки. Секвенирование спаренных концов выполняли в соответствии с протоколом производителя.
Необработанные данные секвенирования анализировали с использованием TruSeq Amplicon Арр от (Illumina (Сан-Диего, СА) и с помощью модифицированной базы данных CAVA (клиническая аннотация вариантов) (The Wellcome Trust Center for Human Genetics; Oxford, UK). В набор данных включали только варианты с показателем распространенности выше 5%, поскольку частота встречаемости мутантного аллеля 5% является общим порогом отсечения для представления данных NGS.
Результаты и обсуждение
Для проведения глубокого секвенирования репрезентативных образцов, приготовленных из фиксированных в формалине опухолей человека, использовали небольшую панель целевых генов, состоящую из 48 известных ассоциированных с раком генов. Чтобы продемонстрировать значительное улучшение в обнаружении мутаций в раковых тканях, репрезентативные образцы сравнивали с гистологическими срезами, приготовленными из этих же опухолей. Во всех случаях, при использовании репрезентативных образцов получали значительно большее число ассоциированных с опухолями мутаций, чем это наблюдали для существующего в настоящее время и исторического метода отбора образцов с получением небольших FFPE блоков.

В Таблице 5 суммированы клинические образцы, которые использовали в этом примере для приготовления репрезентативных образцов для NGS анализа. Анализ данных NGS сначала выполняли, используя приложение TRUSeq Amplicon от (Illumina, с целью идентификации вариантов. Посредством этой программы выравнивают показания секвенирования с homo sapiens hg19 (19-я редакция генома человека) в качестве референсного генома с целью идентификации точечных мутаций и делеций, которые присутствуют с порогом распространенности 5% или выше. По результатам этого начального анализа данных все мутации, идентифицированные в репрезентативных образцах, которые не были обнаружены ни в одном из FFPE блоков, взятых из той же самой опухоли, аннотировали как уникальные для репрезентативного образца, и они приведены в таблицах 6-11 для каждой протестированной опухоли. Репрезентативные образцы для каждой протестированной опухоли содержали гораздо больше мутаций, чем FFPE блоки, взятые из тех же опухолей.






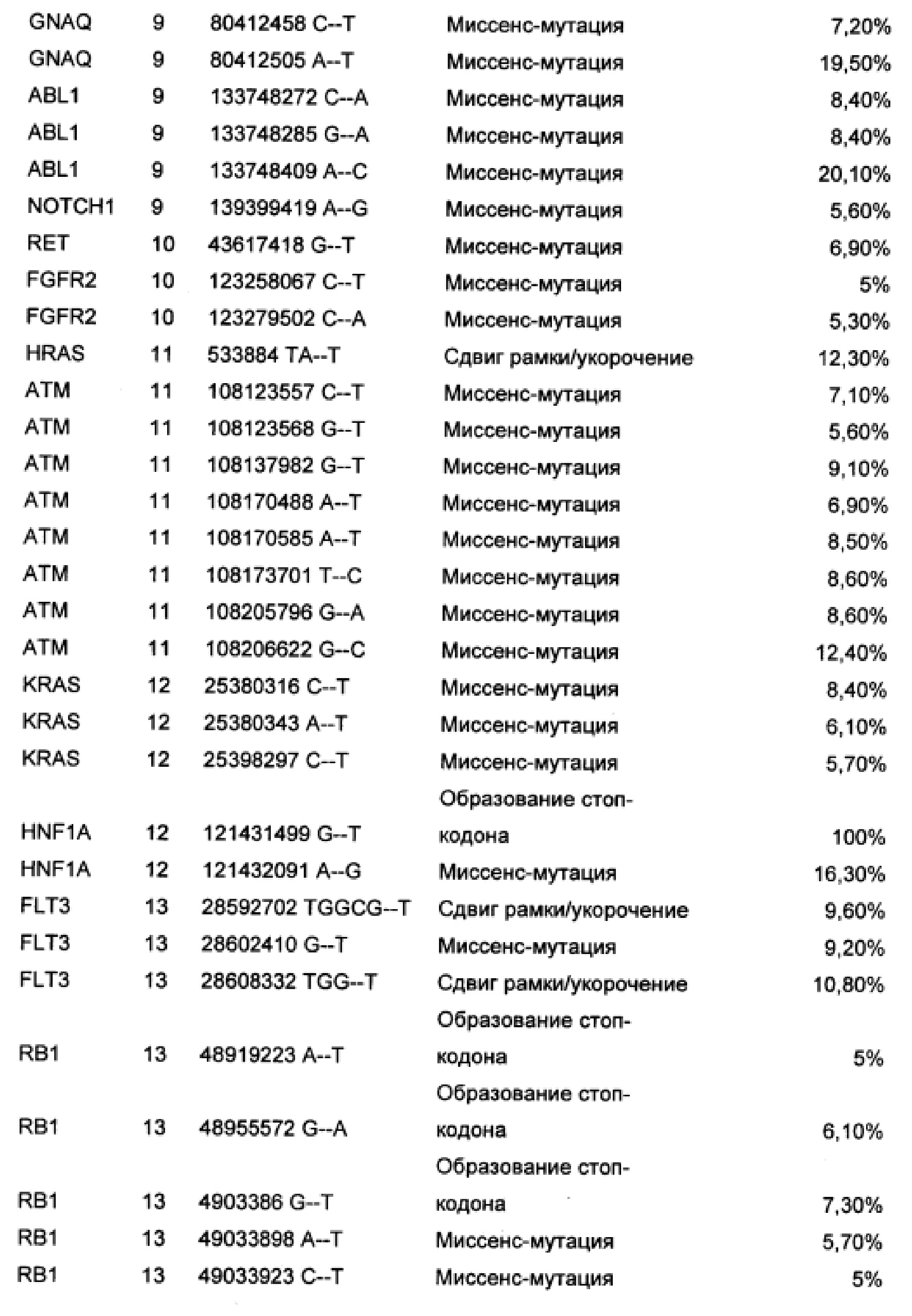



Были обнаружены мутации в FFPE блоках, которые не были обнаружены в репрезентативных образцах, однако это были значительно более редкие уникальные для блоков мутации по сравнению с репрезентативными образцами (Таблицы 9-12).




Далее проводили анализ данных NGS для аденокарциномы толстой кишки, транслокационной почечноклеточной карциномы и плоскоклеточной карциномы легкого, используя базу данных CAVA для определения количества мутаций, приводящих к изменениям в кодирующей области (например, миссенс-мутации, приводящей к аминокислотной замене). В Таблицах 13-15 показаны мутации, приводящие к изменениям в кодирующей области, и это свидетельствует о том, что данные мутации могут иметь научное и/или клиническое значение.





Опираясь на эти данные, авторы изобретения продемонстрировали, что репрезентативные образцы превосходят принятые в настоящее время методы отбора образцов в клинической патологии и онкологии. Более того, тот факт, что показатели распространенности мутаций отличаются, демонстрирует, что NGS анализ репрезентативных образцов опухолей позволяет обнаруживать клональные и субклональные мутации в опухолях человека. Все вместе эти данные демонстрируют, что репрезентативные образцы из извлеченных резекцией опухолей человека можно использовать для детального исследования геномного разнообразия в случаях рака.
Пример 12. Заливка репрезентативных образцов парафиновым воском и гистологический анализ
Предшествующий уровень техники
Репрезентативные образцы, приготовленные из органов, тканей или опухолей, можно залить парафиновым воском для получения типа образца, который содержит клеточные фрагменты ткани, тем самым сохраняя морфологические взаимосвязи между структурами, содержащимися в исходных органе, ткани или опухоли. Гистологические срезы, приготовленные из подвергнутых заливке репрезентативных образцов, могут быть проанализированы патологоанатомом или посредством использования сканирующей системы цифрового микроскопа. Данные, полученные с использованием цифровых сканирующих систем, могут быть дополнительно детально исследованы на предмет количественной оценки уровня гетерогенности между биомаркерами или между пациентами. Кроме того, выходные данные сканирующих систем можно использовать в качестве входных данных для математического анализа гетерогенности, как показано ниже.
Материалы и методы
Свежевыделенные миндалины получали из Северо-западного госпиталя (Оро Вэлли, AZ) и по прибытии фиксировали в 10%-ном забуференном до нейтрального значения формалине. Некоторые образцы миндалин обрабатывали для получения FFPE блоков, помещая миндалину целиком в кассету для тканей с последующей дегидратацией и перфузированием парафином. Репрезентативные образцы миндалин готовили так, как описано в предыдущих примерах. Репрезентативные образцы, приготовленные из опухолей легкого и толстой кишки человека, представляли собой точно такие же образцы, которые описаны в примере 11. Пробу репрезентативных образцов из миндалины, опухоли толстой кишки и опухоли легкого заворачивали в оберточную бумагу для оптических стекол микроскопа и помещали в кассету для тканей. Кассету для тканей помещали в ксилол, дегидратировали в гистопроцессоре (Leica Biosystems, Вецлар, Германия) и затем заливали воском. Из всех анализируемых блоков брали срезы толщиной четыре микрона.
Для проведения IHC, срезы окрашивали с использованием протокола для DAB IHC OptiView, примененяя платформу Benchmark XT от Ventana Medical Systems (Ventana Medical Systems, Тусон, AZ). Визуализацию антител проводили, используя набор для детекции DAB OptiView. Антитела инкубировали в соответствии с инструкциями по применению.
Для анализа цифровых изображений получали полные сканограммы срезов, используя сканирующее устройство АТ2 от Aperio, а анализ изображений проводили, используя алгоритм ImageScope "Positive Pixel Count v9" от Aperio.
Результаты и обсуждение
Для интерпретации результатов многих гистологических окрашиваний требуется сохранение архитектуры тканей, например, ориентировки иммунных клеток относительно опухолевых клеток. Таким образом, диссоциация опухолей до отдельных клеток может не подходить для проведения всех гистологических анализов. Чтобы определить, можно ли подвергнутые механической диссоциации репрезентативные образцы, приготовленные из интактного органа, залить воском, разделить на гистологические срезы и оценить в соответствии с конкретными архитектурными признаками, миндалины целиком подвергали механической диссоциации в шаровой барабанной мельнице от IKA. Образец гомогената миндалины подвергали дегидратации и заливке воском, готовили срезы толщиной четыре микрона, помещали на предметные стекла и окрашивали на различные биомаркеры на устройстве BenchMark XT от Ventana.
На ФИГ. 53А и 53В представлены полученные для целого предметного стекла изображения гистологического среза, отобранного из интактной миндалины, окрашенной с использованием антитела к пан-кератину. ФИГ. 53А представляет собой традиционный срез нормальной миндалины после детектирования с использованием DAB на пан-кератин. ФИГ. 53В представляет собой срез из репрезентативного образца миндалины после детектирования с использованием DAB на пан-кератин. Организация и структура миндалины дополнительно выделены в рамке на ФИГ. 53А, при этом эпителиальная ткань коричневого цвета расположена вблизи нескольких зародышевых центров, содержащих много разных типов лимфоцитов. Такая организация ткани сохраняется при заливке образца гомогенизированной миндалины парафином и приготовления из нее срезов (ФИГ. 54А и 54В). На ФИГ. 54А представлен традиционный гистологический срез нормальной миндалины после детектирования с использованием DAB на CD8. На ФИГ. 54В представлен срез из репрезентативного образца миндалины после детектирования с использованием DAB на CD8. При окрашивании на присутствие CD8-положительных клеток продемонстрировано наличие CD8-положительных клеток, окружающих округлые зародышевые центры, как для среза из целой миндалины, так и для гомогенизированной миндалины. Эти данные демонстрируют пригодность залитых парафином репрезентативных образцов, происходящих из органов, тканей и опухолей, для приготовления гистологического образца, в котором сохраняется морфологическая и тканевая архитектура, для проведения дальнейшего анализа.
Два репрезентативных образца, приготовленные из опухолей толстой кишки и легкого из примера 9, заливали парафиновым воском для проведения гистологического анализа. Из них нарезали тонкие срезы толщиной четыре микрона и окрашивали на многочисленные опухолевые и иммунные специфические биомаркеры (Met, Alk, bRaf, EGFR, PD-L1, CD8 и CK 8/18). Анализ прочтения срезов и оценок интенсивности в баллах проводился патологоанатомом. В этот анализ включали стандартные FFPE блоки, приготовленные из образцов, взятых для имитации существующего в настоящее время определения стадии по системе TNM (блоки из Таблицы 16). Как показано в Таблице 16, патологоанатом мог прочитать и интерпретировать окрашивание как FFPE блоков, так и репрезентативных образцов.

Интерпретация репрезентативного образца патологоанатомом, по всей видимости не затрагивала гетерогенности в отношении интенсивности сигнала и окрашивания по всему срезу. Для получения математического представления в отношении гетерогенности при IHC окрашивании репрезентативных образцов, iHC окрашенные срезы анализировали с использованием цифрового сканирующего устройства для срезов. После сканирования среза целиком проводили количественное определение интенсивности DAB, используя алгоритм ImageScope "Positive Pixel Count v9" от Aperio. Для математического выражения зависимости гетерогенности обусловленного биомаркером сигнала от содержания опухоли интенсивность сигнала для CD8, PD-L1, EGFR и МЕТ делили на интенсивность сигнала для CK 8/18 для всех блоков и репрезентативных образцов. Как показано в Таблицах 16-23, в то время как средние значения для CD8 относительно CK 8/18 в случае гистологических блоков из опухоли толстой кишки и легкого равны таковым для репрезентативного образца, имеется значимая разница в средних значениях относительных интенсивностей сигнала между образцами, окрашенными на PD-L1, EGFR и МЕТ. Эти данные свидетельствуют о том, что IHC окрашивание гистологических срезов, приготовленных из проб репрезентативных образцов, дает лучшее представление о гетерогенности обусловленных биомаркером сигналов и уменьшает разброс результатов IHC, поскольку блоки значительно отличаются между собой.



Все ссылки на патенты и не относящиеся к патентам документы, цитированные в данном описании, включены посредством ссылки во всей своей полноте.
Следует понимать, что хотя данное изобретение описано вместе с указанными выше воплощениями, изложенные выше описание и примеры предназначены для иллюстрации и не ограничивают объема данного изобретения. Другие аспекты, преимущества и модификации в объеме данного изобретения будут очевидны специалистам в данной области техники, к которой данное изобретение относится.
Изобретения, иллюстративно изложенные в данном описании, могут быть соответствующим образом реализованы на практике в отсутствие какого-либо элемента или каких-либо элементов, ограничения или ограничений, конкретно не описанных в данной заявке. Так, например, термины "содержащий", "включающий", "имеющий в своем составе" и т.д. должны читаться в широком смысле и без ограничения. Кроме того, термины и выражения, использованные в данном описании, применены как термины для описания, а не для ограничения, и нет намерения использовать такие термины и выражения для исключения каких-либо эквивалентов показанных и описанных признаков или их частей, но признается, что возможны различные модификации в объеме заявленного изобретения.
Таким образом, следует понимать, что несмотря на то, что настоящее изобретение конкретно описано посредством предпочтительных воплощений и возможных признаков, модификация, улучшение и изменение предметов изобретения, описанных в данной заявке посредством воплощений, могут быть пересортированы специалистами в данной области техники, и считается, что такие модификации, улучшения и изменения включены в объем этого описания. Материалы, способы и примеры, приведенные в данной заявке, являются репрезентативными примерами предпочтительных воплощений, являются типичными и не предназначены для ограничения объема данного изобретения.
Изобретение описано в данной заявке широко и в общем виде. Каждая из более узких разновидностей и субродовых группировок, подпадающих под общее описание, также составляет часть изобретения. Это включает в себя общее описание изобретения, при условии или отрицательном ограничении, удаляющем какой-либо объект изобретения из рода, независимо от того, является ли исключенный материал конкретно изложенным в данном описании или нет.
В дополнение к этому, если признаки или аспекты изобретения описаны в терминах групп Маркуша, то специалистам в данной области техники будет известно, что данное изобретение тем самым также описано в терминах любого отдельного члена или подгруппы членов группы Маркуша.
Другие воплощения
1. Способ приготовления репрезентативного образца для анализа, включающий:
a) получение извлеченного хирургической резекцией образца ткани по меньшей мере от одного субъекта; и
b) гомогенизацию извлеченного хирургической резекцией образца ткани с получением гомогенизированного образца.
2. Способ по воплощению 1, дополнительно включающий фиксацию по меньшей мере части извлеченного хирургической резекцией образца ткани.
3. Способ по воплощению 1, дополнительно включающий обработку первой части извлеченного хирургической резекцией образца и приготовление одного или нескольких блоков подвергнутой фиксации и заливке ткани.
4. Способ по воплощению 3, дополнительно включающий гомогенизацию второй части оставшегося извлеченного хирургической резекцией образца ткани.
5. Способ по воплощению 3 или 4, дополнительно включающий обработку по меньшей мере части одного или нескольких блоков подвергнутой фиксации и заливке ткани посредством микротомии с получением одного или нескольких тонких тканевых срезов для морфологического анализа.
6. Способ по воплощению 5, дополнительно включающий депарафинизацию по меньшей мере одного или нескольких блоков подвергнутой фиксации и заливке ткани и гомогенизацию ткани из одного или нескольких депарафинизированных блоков подвергнутой фиксации и заливке ткани.
7. Способ по воплощению 1, где извлеченный хирургической резекцией образец ткани включает один или несколько отдельных кусочков ткани.
8. Способ по воплощению 7, где один или несколько отдельных кусочков ткани содержат по меньшей мере часть одной или нескольких масс ткани первичной солидной опухоли, извлеченных резекцией из субъекта для получения извлеченного хирургической резекцией образца.
9. Способ по воплощению 8, где один или несколько отдельных кусочков ткани содержат по меньшей мере часть одного или нескольких лимфатических узлов, извлеченных резекцией из субъекта.
10. Способ по воплощению 7, 8 или 9, дополнительно включающий гомогенизацию по отдельности по меньшей мере части отдельных кусочков ткани с получением отдельных гомогенизированных образцов.
11. Способ по воплощению 1, где извлеченный хирургической резекцией образец ткани содержит массу одной ткани.
12. Способ по воплощению 11, где масса одной ткани дополнительно разделена на два или более кусочков массы одной ткани.
13. Способ по воплощению 12, дополнительно включающий гомогенизацию по меньшей мере одного из двух или более кусочков массы одной ткани и консервацию по меньшей мере одного из оставшихся двух или более кусочков массы одной ткани.
14. Способ по воплощению 1, где гомогенизация включает физическое разделение.
15. Способ по воплощению 14, где физическое разделение осуществляют посредством нарезания, шинкования или измельчения.
16. Способ по воплощению 1, где гомогенизация включает механическую диссоциацию.
17. Способ по воплощению 16, где механическую диссоциацию осуществляют путем обработки в блендере или обработки в соковыжималке.
18. Способ по воплощению 1, где гомогенизацию осуществляют посредством биохимической диссоциации.
19. Способ по воплощению 18, где биохимическую диссоциацию осуществляют с использованием протеазы.
20. Способ по воплощению 1, дополнительно включающий очистку одной или более биомолекул по меньшей мере из части гомогената.
21. Способ по воплощению 20, где одна или более биомолекул выбраны из группы, состоящей из ДНК, РНК, белков, липидов и метаболитов.
22. Способ по воплощению 21, дополнительно включающий анализ одной или более биомолекул.
23. Способ по воплощению 22, где анализ одной или более биомолекул выполняют посредством ПЦР, масс-спектрометрии, методов секвенирования следующего поколения или ELISA.
24. Способ по воплощению 22, где в результате анализа получают по меньшей мере один набор данных.
25. Способ по воплощению 1, дополнительно включающий заливку парафином по меньшей мере части гомогенизированного образца.
26. Способ по воплощению 25, дополнительно включающий приготовление одного или более тонких срезов залитого парафином гомогенизированного образца.
27. Способ по воплощению 26, дополнительно включающий проведение гистологического анализа на тонких срезах залитого парафином гомогенизированного образца.
28. Способ по воплощению 27, где гистологический анализ осуществляют посредством Н&Е окрашивания, IHC окрашивания, ISH окрашивания и FISH окрашивания.
29. Способ по воплощению 27, где результат гистологического анализа на тонких срезах залитого парафином гомогенизированного образца интерпретируется человеком.
30. Способ по воплощению 27, где количественную оценку результата гистологического анализа на тонких срезах залитого парафином гомогенизированного образца выполняют с использованием автоматизированного устройства.
31. Способ по воплощению 29, где в результате интерпретации получают по меньшей мере один набор данных.
32. Способ по воплощению 30, где в результате количественного определения получают по меньшей мере один набор данных.
33. Способ по воплощению 1, дополнительно включающий дальнейшую обработку по меньшей мере части гомогената для получения клеточных фрагментов.
34. Способ по воплощению 32, где обработку по меньшей мере части гомогената осуществляют с использованием физических, механических, химических или ферментативных методов.
35. Способ по воплощению 33, где клеточные фрагменты выбраны из группы, состоящей из ядер, клеточных мембран и клеточных органелл.
36. Способ по воплощению 33, где по меньшей мере часть клеточных фрагментов прикрепляют по меньшей мере к одному предметному стеклу.
37. Способ по воплощению 36, где по меньшей мере часть клеточных фрагментов, прикрепленных по меньшей мере к одному предметному стеклу, подвергают гистологическому анализу.
38. Способ по воплощению 37, где гистологический анализ осуществляют посредством Н&Е окрашивания, IHC окрашивания, ISH окрашивания или FISH окрашивания.
39. Способ по воплощению 36, где результат гистологического анализа в отношении по меньшей мере части клеточных фрагментов, прикрепленных по меньшей мере к одному предметному стеклу, интерпретируется человеком.
40. Способ по воплощению 36, где результат гистологического анализа в отношении по меньшей мере части клеточных фрагментов, прикрепленных по меньшей мере к одному предметному стеклу, количественно определяется с помощью автоматизированного устройства.
41. Способ по воплощению 39, где в результате интерпретации получают по меньшей мере один набор данных.
42. Способ по воплощению 40, где в результате количественного определения получают по меньшей мере один набор данных.
43. Способ по воплощению 33, где по меньшей мере часть клеточных фрагментов анализируют с применением проточной цитометрии, FACS или анализатора частиц.
44. Способ по воплощению 43, где в результате анализа получают набор данных.
45. Способ по воплощению 33, дополнительно включающий очистку по меньшей мере одного клеточного фрагмента по меньшей мере из части клеточных фрагментов.
46. Способ по воплощению 45, где очистку осуществляют посредством FACS, аффинной очистки, дифференциального центрифугирования с разделением на основании размера, фильтрации или электрофореза.
47. Способ по воплощению 45, дополнительно включающий выделение биомолекул из очищенного по меньшей мере одного клеточного фрагмента по меньшей мере из части клеточных фрагментов.
48. Способ по воплощению 47, дополнительно включающий анализ биомолекул из очищенного по меньшей мере одного клеточного фрагмента по меньшей мере из части клеточных фрагментов.
49. Способ по воплощению 48, где анализ представляет собой ПЦР, масс-спектрометрию, методы секвенирования следующего поколения или ELISA.
50. Способ по воплощению 49, где в результате анализа получают по меньшей мере один набор данных.
51. Способ по воплощению 1, дополнительно включающий дальнейшую обработку по меньшей мере части гомогената с получением по меньшей мере одной подвергнутой диссоциации клетки.
52. Способ по воплощению 51, где обработку по меньшей мере части гомогената осуществляют физическим, механическим, химическим или ферментативным путем.
53. Способ по воплощению 51, где по меньшей мере одна подвергнутая диссоциации клетка представляет собой нормальную клетку, раковую клетку или бактериальную клетку.
54. Способ по воплощению 51, где по меньшей мере одну подвергнутую диссоциации клетку прикрепляют по меньшей мере к одному предметному стеклу.
55. Способ по воплощению 54, где по меньшей мере одну подвергнутую диссоциации клетку, прикрепленную по меньшей мере к одному предметному стеклу, подвергают гистологическому анализу.
56. Способ по воплощению 55, где гистологический анализ представляет собой Н&Е окрашивание, IHC окрашивание, ISH окрашивание или FISH окрашивание.
57. Способ по воплощению 55, где результат гистологического анализа в отношении по меньшей мере одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, интерпретируется человеком.
58. Способ по воплощению 55, где результат гистологического анализа в отношении по меньшей мере одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, количественно определяется с помощью автоматизированного устройства.
59. Способ по воплощению 57, где в результате интерпретации получают по меньшей мере один набор данных.
60. Способ по воплощению 58, где в результате количественного определения получают по меньшей мере один набор данных.
61. Способ по воплощению 51, где по меньшей мере одну подвергнутую диссоциации клетку анализируют с применением проточной цитометрии, FACS или анализатора частиц.
62. Способ по воплощению 61, где в результате анализа получают набор данных.
63. Способ по воплощению 51, дополнительно включающий очистку по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки.
64. Способ по воплощению 63, где очистку осуществляют посредством FACS, аффинной очистки, дифференциального центрифугирования с разделением на основании размера, фильтрации или электрофореза.
65. Способ по воплощению 63, дополнительно включающий выделение биомолекул из очищенной по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки.
66. Способ по воплощению 65, дополнительно включающий анализ биомолекул из очищенной по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки.
67. Способ по воплощению 66, где анализ представляет собой ПЦР, масс-спектрометрию, методы секвенирования следующего поколения или ELISA.
68. Способ по воплощению 67, где в результате анализа получают по меньшей мере один набор данных.
69. Способ по воплощению 63, где очищенную по меньшей мере одну клетку по меньшей мере из одной подвергнутой диссоциации клетки прикрепляют по меньшей мере к одному предметному стеклу.
70. Способ по воплощению 69, где очищенную по меньшей мере одну клетку по меньшей мере из одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, подвергают гистологическому анализу.
71. Способ по воплощению 70, где гистологический анализ представляет собой Н&Е окрашивание, IHC окрашивание, ISH окрашивание или FISH окрашивание.
72. Способ по воплощению 70, где результат гистологического анализа в отношении очищенной по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, интерпретируется человеком.
73. Способ по воплощению 70, где результат гистологического анализа в отношении очищенной по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, количественно определяется с помощью автоматизированного устройства.
74. Способ по воплощению 72, где в результате интерпретации получают по меньшей мере один набор данных.
75. Способ по воплощению 73, где в результате количественного определения получают по меньшей мере один набор данных.
76. Способ по любому из воплощений 24, 31, 32, 41, 42, 44, 50, 59, 60, 62, 68, 74 и 75, дополнительно включающий анализ по меньшей мере одного набора данных по меньшей мере от одного субъекта.
77. Способ по воплощению 76, где анализ включает определение набора данных для разнообразия биомаркеров или фенотипического разнообразия.
78. Способ по воплощению 76, где анализ включает определение показателя распространенности по меньшей мере для одного различающегося биомаркера или фенотипа.
79. Способ по воплощению 76, где анализ включает принятие по меньшей мере одного клинического решения.
80. Способ по воплощению 79, где клиническое решение представляет собой определение прогноза заболевания, предсказание рецидива заболевания, предсказание мишеней для лечения заболевания, включение субъектов в клинические испытания или стратегию терапевтического лечения по меньшей мере для одного субъекта.
ФОРМУЛА ИЗОБРЕТЕНИЯ
1. Способ приготовления репрезентативного образца для анализа, включающий:
a) получение извлеченного хирургической резекцией образца ткани по меньшей мере от одного субъекта; и
b) гомогенизацию извлеченного хирургической резекцией образца ткани с получением гомогенизированного образца.
2. Способ по п. 1, дополнительно включающий фиксацию по меньшей мере части извлеченного хирургической резекцией образца ткани.
3. Способ по п. 1, дополнительно включающий обработку первой части извлеченного хирургической резекцией образца и приготовление одного или нескольких блоков подвергнутой фиксации и заливке ткани.
4. Способ по п. 3, дополнительно включающий гомогенизацию второй части оставшегося извлеченного хирургической резекцией образца ткани.
5. Способ по п. 3 или 4, дополнительно включающий обработку по меньшей мере части одного или нескольких блоков подвергнутой фиксации и заливке ткани посредством микротомии с получением одного или нескольких тонких тканевых срезов для морфологического анализа.
6. Способ по п. 5, дополнительно включающий депарафинизацию по меньшей мере одного из одного или нескольких блоков подвергнутой фиксации и заливке ткани и гомогенизацию ткани из одного или нескольких депарафинизированных блоков подвергнутой фиксации и заливке ткани.
7. Способ по п. 1, где извлеченный хирургической резекцией образец ткани включает один или несколько отдельных кусочков ткани.
8. Способ по п. 7, где один или несколько отдельных кусочков ткани содержат по меньшей мере часть одной или нескольких масс ткани первичной солидной опухоли, извлеченных резекцией из субъекта для получения извлеченного хирургической резекцией образца.
9. Способ по п. 8, где один или несколько отдельных кусочков ткани содержат по меньшей мере часть одного или нескольких лимфатических узлов, извлеченных резекцией из субъекта.
10. Способ по п. 7, 8 или 9, дополнительно включающий гомогенизацию по отдельности по меньшей мере части отдельных кусочков ткани с получением отдельных гомогенизированных образцов.
11. Способ по п. 1, где извлеченный хирургической резекцией образец ткани содержит массу одной ткани.
12. Способ по п. 11, где масса одной ткани дополнительно разделена на два или более кусочков массы одной ткани.
13. Способ по п. 12, дополнительно включающий гомогенизацию по меньшей мере одного из двух или более кусочков массы одной ткани и консервацию по меньшей мере одного из оставшихся двух или более кусочков массы одной ткани.
14. Способ по п. 1, где гомогенизация включает физическое разделение.
15. Способ по п. 14, где физическое разделение осуществляют посредством нарезания, шинкования или измельчения.
16. Способ по п. 1, где гомогенизация включает механическую диссоциацию.
17. Способ по п. 16, где механическую диссоциацию осуществляют путем обработки в блендере или обработки в соковыжималке.
18 Способ по п. 1, где гомогенизацию осуществляют посредством биохимической диссоциации.
19. Способ по п. 18, где биохимическую диссоциацию осуществляют с использованием протеазы.
20. Способ по п. 1, дополнительно включающий очистку одной или более биомолекул по меньшей мере из части гомогената.
21. Способ по п. 20, где одна или более биомолекул выбраны из группы, состоящей из ДНК, РНК, белков, липидов и метаболитов.
22. Способ по п. 21, дополнительно включающий анализ одной или более биомолекул.
23. Способ по п. 22, где анализ одной или более биомолекул выполняют посредством ПЦР, масс-спектрометрии, методов секвенирования следующего поколения или ELISA.
24. Способ по п. 22, где в результате анализа получают по меньшей мере один набор данных.
25. Способ по п. 1, дополнительно включающий заливку парафином по меньшей мере части гомогенизированного образца.
26. Способ по п. 25, дополнительно включающий приготовление одного или более тонких срезов залитого парафином гомогенизированного образца.
27. Способ по п. 26, дополнительно включающий проведение гистологического анализа на тонких срезах залитого парафином гомогенизированного образца.
28. Способ по п. 27, где гистологический анализ осуществляют посредством Н&Е окрашивания, IHC окрашивания, ISH окрашивания и FISH окрашивания.
29. Способ по п. 27, где результат гистологического анализа на тонких срезах залитого парафином гомогенизированного образца интерпретируется человеком.
30. Способ по п. 27, где количественную оценку результата гистологического анализа на тонких срезах залитого парафином гомогенизированного образца выполняют с использованием автоматизированного устройства.
31. Способ по п. 29, где в результате интерпретации получают по меньшей мере один набор данных.
32. Способ по п. 30, где в результате количественного определения получают по меньшей мере один набор данных.
33. Способ по п. 1, дополнительно включающий дальнейшую обработку по меньшей мере части гомогената для получения клеточных фрагментов.
34. Способ по п. 32, где обработку по меньшей мере части гомогената осуществляют с использованием физических, механических, химических или ферментативных методов.
35. Способ по п. 33, где клеточные фрагменты выбраны из группы, состоящей из ядер, клеточных мембран и клеточных органелл.
36. Способ по п. 33, где по меньшей мере часть клеточных фрагментов прикрепляют по меньшей мере к одному предметному стеклу.
37. Способ по п. 36, где по меньшей мере часть клеточных фрагментов, прикрепленных по меньшей мере к одному предметному стеклу, подвергают гистологическому анализу.
38. Способ по п. 37, где гистологический анализ осуществляют посредством Н&Е окрашивания, IHC окрашивания, ISH окрашивания или FISH окрашивания.
39. Способ по п. 36, где результат гистологического анализа в отношении по меньшей мере части клеточных фрагментов, прикрепленных по меньшей мере к одному предметному стеклу, интерпретируется человеком.
40. Способ по п. 36, где результат гистологического анализа в отношении по меньшей мере части клеточных фрагментов, прикрепленных по меньшей мере к одному предметному стеклу, количественно определяется с помощью автоматизированного устройства.
41. Способ по п. 39, где в результате интерпретации получают по меньшей мере один набор данных.
42. Способ по п. 40, где в результате количественного определения получают по меньшей мере один набор данных.
43. Способ по п. 33, где по меньшей мере часть клеточных фрагментов анализируют с применением проточной цитометрии, FACS или анализатора частиц.
44. Способ по п. 43, где в результате анализа получают набор данных.
45. Способ по п. 33, дополнительно включающий очистку по меньшей мере одного клеточного фрагмента по меньшей мере из части клеточных фрагментов.
46. Способ по п. 45, где очистку осуществляют посредством FACS, аффинной очистки, дифференциального центрифугирования с разделением на основании размера, фильтрации или электрофореза.
47. Способ по п. 45, дополнительно включающий выделение биомолекул из очищенного по меньшей мере одного клеточного фрагмента по меньшей мере из части клеточных фрагментов.
48. Способ по п. 47, дополнительно включающий анализ биомолекул из очищенного по меньшей мере одного клеточного фрагмента по меньшей мере из части клеточных фрагментов.
49. Способ по п. 48, где анализ представляет собой ПЦР, масс-спектрометрию, методы секвенирования следующего поколения или ELISA.
50. Способ по п. 49, где в результате анализа получают по меньшей мере один набор данных.
51. Способ по п. 1, дополнительно включающий дальнейшую обработку по меньшей мере части гомогената с получением по меньшей мере одной подвергнутой диссоциации клетки.
52. Способ по п. 51, где обработку по меньшей мере части гомогената осуществляют физическим, механическим, химическим или ферментативным путем.
53. Способ по п. 51, где по меньшей мере одна подвергнутая диссоциации клетка представляет собой нормальную клетку, раковую клетку или бактериальную клетку.
54. Способ по п. 51, где по меньшей мере одну подвергнутую диссоциации клетку прикрепляют по меньшей мере к одному предметному стеклу.
55. Способ по п. 54, где по меньшей мере одну подвергнутую диссоциации клетку, прикрепленную по меньшей мере к одному предметному стеклу, подвергают гистологическому анализу.
56. Способ по п. 55, где гистологический анализ представляет собой Н&Е окрашивание, IHC окрашивание, ISH окрашивание или FISH окрашивание.
57. Способ по п. 55, где результат гистологического анализа в отношении по меньшей мере одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, интерпретируется человеком.
58. Способ по п. 55, где результат гистологического анализа в отношении по меньшей мере одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, количественно определяется с помощью автоматизированного устройства.
59. Способ по п. 57, где в результате интерпретации получают по меньшей мере один набор данных.
60. Способ по п. 58, где в результате количественного определения получают по меньшей мере один набор данных.
61. Способ по п. 51, где по меньшей мере одну подвергнутую диссоциации клетку анализируют с применением проточной цитометрии, FACS или анализатора частиц.
62. Способ по п. 61, где в результате анализа получают набор данных.
63. Способ по п. 51, дополнительно включающий очистку по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки.
64. Способ по п. 63, где очистку осуществляют посредством FACS, аффинной очистки, дифференциального центрифугирования с разделением на основании размера, фильтрации или электрофореза.
65. Способ по п. 63, дополнительно включающий выделение биомолекул из очищенной по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки.
66. Способ по п. 65, дополнительно включающий анализ биомолекул из очищенной по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки.
67. Способ по п. 66, где анализ представляет собой ПЦР, масс-спектрометрию, методы секвенирования следующего поколения или ELISA.
68. Способ по п. 67, где в результате анализа получают по меньшей мере один набор данных.
69. Способ по п. 63, где очищенную по меньшей мере одну клетку по меньшей мере из одной подвергнутой диссоциации клетки прикрепляют по меньшей мере к одному предметному стеклу.
70. Способ по п. 69, где очищенную по меньшей мере одну клетку по меньшей мере из одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, подвергают гистологическому анализу.
71. Способ по п. 70, где гистологический анализ представляет собой Н&Е окрашивание, IHC окрашивание, ISH окрашивание или FISH окрашивание.
72. Способ по п. 70, где результат гистологического анализа в отношении очищенной по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, интерпретируется человеком.
73. Способ по п. 70, где результат гистологического анализа в отношении очищенной по меньшей мере одной клетки по меньшей мере из одной подвергнутой диссоциации клетки, прикрепленной по меньшей мере к одному предметному стеклу, количественно определяется с помощью автоматизированного устройства.
74. Способ по п. 72, где в результате интерпретации получают по меньшей мере один набор данных.
75. Способ по п. 73, где в результате количественного определения получают по меньшей мере один набор данных.
76. Способ по любому из п.п. 24, 31, 32, 41, 42, 44, 50, 59, 60, 62, 68, 74 и 75, дополнительно включающий анализ по меньшей мере одного набора данных по меньшей мере от одного субъекта.
77. Способ по п. 76, где анализ включает определение набора данных для разнообразия биомаркеров или фенотипического разнообразия.
78. Способ по п. 76, где анализ включает определение показателя распространенности по меньшей мере для одного различающегося биомаркера или фенотипа.
79. Способ по п. 76, где анализ включает принятие по меньшей мере одного клинического решения.
80. Способ по п. 79, где клиническое решение представляет собой определение прогноза заболевания, предсказание рецидива заболевания, предсказание мишеней для лечения заболевания, включение субъектов в клинические испытания или стратегию терапевтического лечения по меньшей мере для одного субъекта.
81. Композиция обработанного гомогената, приготовленного из образца гетерогенной ткани, содержащего по существу гомогенно распределенные клеточные структуры, где соотношение клеточных структур в каждой подгруппе гомогената по существу аналогично соотношению клеточных структур в образце ткани.
81. Гомогенат по п. 81, где образец ткани выбран из группы, состоящей из: опухоли, лимфатического узла, метастаза, полипа, кисты, извлеченного резекцией материала, органа или их доли.
82. Гомогенат по п. 81 или 82, где образец ткани содержит пространственно обособленные клеточные структуры.
83. Гомогенат по любому из п.п. 81-83, где клеточные структуры содержат кластер клеток, отдельную клетку, фрагмент клетки, органеллу, пептид, нуклеиновую кислоту, липид, метаболит или их комбинацию.
84. Гомогенат по любому из п.п. 81-84, где гомогенат содержит до 25% включительно клеточных структур из образца ткани.
85. Гомогенат по любому из п.п. 81-84, где гомогенат содержит до 50% включительно клеточных структур из образца ткани.
86. Гомогенат по любому из п.п. 81-84, где гомогенат содержит до 75% включительно клеточных структур из образца ткани.
87. Гомогенат по любому из п.п. 81-84, где гомогенат содержит до 100% включительно клеточных структур из образца ткани.
88. Гомогенат по любому из п.п. 81-84, где гомогенат содержит 100% клеточных структур из образца ткани.
89. Гомогенат по п. 81, где образец ткани содержит нежидкий образец ткани.
90. Гомогенат по п. 81, где образец ткани содержит жидкий образец ткани.
91. Гомогенат по п. 91, где жидкий образец ткани содержит ткань, выделенную из одного или более чем одного из следующего: отобранного шприцем аспирата для цитологического исследования, образца экссудата или мазка по Папаниколау.
92. Гомогенат по п. 81, где по существу гомогенные клеточные структуры содержат множество одиночных клеток или множество кластеров клеток.
93. Гомогенат по любому из п.п. 81-93, где клеточные структуры выделены из нормальной ткани.
95. Гомогенат по любому из п.п. 81-93, где клеточные структуры выделены из фенотипически или генотипически нормальной ткани.
96. Гомогенат по любому из п.п. 81-93, где клеточные структуры выделены из аномальной ткани.
97. Гомогенат по любому из п.п. 81-93, где клеточные структуры выделены из фенотипически или генотипически аномальной ткани.
98. Гомогенат по любому из п.п. 81-97, где образец ткани содержит стволовую клетку, эпителиальную клетку, клетку крови, жировую клетку, клетку кожи, эндотелиальную клетку, опухолевую клетку или иммунную клетку.
99. Гомогенат по п. 98, где опухолевая клетка происходит из раковой ткани, выбранной из группы, состоящей из: рака легкого, лейкоза, рака молочной железы, рака предстательной железы, рака толстой кишки, рака головного мозга, рака пищевода, случаев рака головы и шеи, рака мочевого пузыря, гинекологических видов карцином, рака яичника, рака шейки матки, липосаркомы, меланомы, лимфомы, плазмоцитомы, саркомы, глиомы, тимомы, гепатомы и миеломы.
100. Гомогенат по п. 98, где иммунные клетки представляют собой клетки, выбранные из группы, состоящей из: нейтрофилов, моноцитов, дендритных клеток, макрофагов, лимфоцитов, Т-клеток, В-клеток или природных киллерных клеток.
101. Гомогенат по любому из п.п. 81-100, где образец ткани не подвергнут консервации или фиксации.
102. Гомогенат по любому из п.п. 81-100, где образец ткани содержит живую клетку.
103. Гомогенат по любому из п.п. 81-100, где образец ткани подвергнут консервации или фиксации.
104. Гомогенат по п. 103, где подвергнутый консервации или фиксации образец ткани содержит образец, который был подвергнут заморозке или фиксации методом, выбранным из группы: замораживания, сублимационной сушки и заливки воском.
105. Гомогенат по любому из п.п. 81-104, где образец гетерогенной ткани выделен из одной или несколько тканей.
106. Гомогенат по любому из п.п. 81-104, где образец ткани выделен от одного субъекта.
107. Гомогенат по любому из п.п. 81-106, где образец ткани содержит ткань, выделенную от двух или более субъектов.
108. Гомогенат по п. 107, где два или более субъектов представляют собой генетически гомогенные субъекты.
109. Гомогенат по п. 107, где два или более субъектов представляют собой фенотипически гомогенные субъекты.
110. Гомогенат по п. 107, где два или более субъектов являются генетически различными субъектами.
111. Гомогенат по п. 107, где два или более субъектов являются фенотипически различными субъектами.
112. Гомогенат по п. 107, где два или более субъектов являются субъектами одного и того же пола.
113. Гомогенат по п. 107, где два или более субъектов относятся к разным полам.
114. Гомогенат по п. 107, где два или более субъектов состоят в группах разной этнической принадлежности.
115. Гомогенат по п. 107, где два или более субъектов состоят в группе одной и той же этнической принадлежности.
116. Гомогенат по любому из п.п. 106-115, где субъект выбран из группы, состоящей из животного, сельскохозяйственного животного, домашнего животного, человека.
117. Гомогенат по любому из п.п. 81-116, где гомогенат дополнительно содержит один или более чем один материал, выбранный из клетки, не являющейся клеткой человека, человеческой клетки, ненативного белка, нуклеиновых кислот или малой молекулы, красителя, вируса, бактерии, паразита, представителя простейших или химического вещества.
118. Композиция по п. 117, где малая молекула содержит гаптен, пептидную метку, белковую метку, флуоресцентную метку, нуклеиновокислотную метку и их комбинацию.
119. Способ получения репрезентативных данных, включающий анализ композиции гомогената по любому из п.п. 81-118.
120. Способ по п. 119, где анализ включает получение количественных и/или качественных данных для маркера в композиции гомогената.
121. Способ по п. 120, где маркер содержит ДНК, белок, РНК, липид, клеточную органеллу, метаболит или клетку.
122. Способ по п. 121, где белок содержит модификацию, при этом указанная модификация выбрана из группы, состоящей из ацетилирования, АДФ-рибозилирования, ацилирования, АДФ-рибозилирования, амидирования, ковалентного присоединения флавина, ковалентного присоединения гема, ковалентного присоединения нуклеотида или нуклеотидного производного, ковалентного присоединения липида или липидного производного, ковалентного присоединения фосфатидилинозита, перекрестного сшивания, циклизации, образования дисульфидных связей, дезметилирования, образования ковалентных сшивок, образования цистина, образования пироглутамата, формилирования, гамма-карбоксилирования, гликозилирования, образования GPI якоря, гидроксилирования, иодинирования, метилирования, миристоилирования, окисления, протеолитического процессинга, фосфорилирования, пренилирования, рацемизации, селеноилирования, сульфатирования, аргинилирования и убиквитинилирования.
123. Способ по п. 120, где маркер содержит геномный полиморфизм, обуславливающий фармакогеномику однонуклеотидный полиморфизм (SNP), геномный SNP, соматический полиморфизм и дифференциальную экспрессию белка, липида и/или клеточной органеллы.
124. Способ по п. 120, где маркер содержит однонуклеотидное положение; внутригенный участок или межгенный участок; экзон или интрон либо их фрагмент; кодирующий участок или некодирующий участок; промотор, энхансер, 5'-нетранслируемый участок (5'-UTR) или 3'-нетранслируемый участок (3'-UTR) либо их фрагмент; кДНК или ее фрагмент; SNP; соматическую мутацию, мутацию в зародышевой линии или обе из них; точечную мутацию или мутацию в одном сайте; делеционную мутацию; делецию внутри рамки считывания, внутригенную делецию, полную делецию гена; инсерционную мутацию; внутригенную вставку; инверсионную мутацию; внутрихромосомную инверсию; мутацию с нарушением связывания; сопряженную инсерционную мутацию; мутацию типа инвертированной дупликации; тандемную дупликацию; внутрихромосомную тандемную дупликацию; транслокацию; хромосомную транслокацию, нереципрокную транслокацию; перестройку; геномную перестройку; перестройку одного или более интронов либо их фрагментов; интрон с перестроенной структурой; 5'- или 3'-UTR или их комбинацию.
125. Способ по п. 120, где маркер содержит измененную нуклеотидную последовательность, которая кодирует измененную аминокислотную последовательность, содержит хромосомную транслокацию, внутрихромосомную инверсию, изменение числа копий, изменение уровня экспрессии, изменение уровня белка, изменение активности белка или изменение статуса метилирования в раковой ткани или раковой клетке по сравнению с нормальной, здоровой тканью или клеткой.
126. Способ по любому из п.п. 120-125, где маркер измеряют посредством секвенирования из одной клетки, секвенирования из одного ядра, проточной цитометрии, иммуногистохимического окрашивания, окрашивания гематоксилином и эозином, секвенирования полного генома, высокопроизводительного секвенирования, масс-спектрометрии, ДНК микрочипа или их комбинации.
127. Способ по п. 119, где образец ткани содержит образец, выбранный из группы, состоящей из: одной или нескольких клеток в состоянии, предшествующем злокачественному перерождению, или озлокачествленных клеток, клеток из солидной опухоли, опухоли мягких тканей или метастатического поражения, ткани или клеток из хирургического края (опухоли), гистологически нормальной ткани, одной или нескольких циркулирующих опухолевых клеток (СТС), нормальной близко расположенной ткани (NAT), образца крови от одного и того же субъекта, имеющего опухоль или имеющего риск наличия опухоли, или FFPE образца.
128. Способ по п. 119, где репрезентативные данные содержат качественные и количественные данные, полученные от одного маркера.
129. Способ по п. 119, где репрезентативные данные содержат качественные и/или количественные данные, полученные от двух или более разных маркеров.
130. Способ по любому из п.п. 39-49, дополнительно включающий установление внутреннего значения для качественных и/или количественных данных.
131. Способ по п. 119, дополнительно включающий сравнение репрезентативных данных с предварительно заданным значением для этих данных.
132. Способ по п. 131, где предварительно заданное значение выбрано из данных клинических испытаний, данных для субъекта, данных из научной литературы, данных для находящейся в клинической разработке биологической или малой молекулы.
133. Способ по п. 119, где репрезентативные данные содержат репрезентативные онкологические данные, при этом репрезентативные онкологические данные содержат количественные и/или качественные данные по меньшей мере для одного опухолевого маркера из первого биологического образца, при этом указанный опухолевый маркер ассоциирован с наличием опухоли.
134. Способ по п. 133, дополнительно включающий:
(a) измерение опухолевого маркера в первом биологическом образце, при этом измеренное значение для опухолевого маркера является нормированным;
(b) получение суммарной оценки в баллах на основании этого нормированного измеренного значения; и
(c) сравнение суммарной оценки в баллах с предварительно заданной оценкой в баллах с целью определения показателя риска рака у субъекта.
135. Способ по п. 134, где опухолевый маркер выбран из группы, состоящей из: белка, антигена, фермента, гормона, ДНК, РНК, микроРНК или углевода.
136. Способ по п. 134, где опухолевый маркер выбран из группы, состоящей из: Her2, bRaf, ERBB2, PI3KCA, FGFR2, р53, BRCA, CCND1, MAP2K4, ATR, AFP, ALK, BCR-ABL, BRCA1/BRCA2, BRAF, V600E, Са-125, СА19.9, EGFR, Her-2, KIT, PSA, S100, KRAS, ER/Pr, UGT1A1, CD30, CD20, F1P1L1-PDGRFα, PDGFR, TMPT, TMPRSS2; ABCB5, AFP-L3, альфа-фетопротеина, альфа-метил-ацил-КоА-рацемазы, BRCA1, BRCA2, СА 15-3, СА 242, Са 27-29, СА-125, СА15-3, СА19-9, кальцитонина, канцероэмбрионального антигена, пептида-1 канцероэмбрионального антигена, дез-гамма-карбоксипротромбина, десмина, раннего антигена-2 рака предстательной железы, рецептора эстрогенов, продукта деградации фибрина, глюкозо-6-фосфат-изомеразы, vE6, Е7, L1, L2 или p16INK4a, хорионического гонадотропина человека, IL-6, кератина 19, лактатдегидрогеназы, лейциламинопептидазы, липотропина, метанефринов, неприлизина, NMP22, норметанефрина, РСА3, простатоспецифического антигена, кислой фосфатазы предстательной железы, синаптофизина, тиреоглобулина, TNF, транскрипционного фактора, выбранного из ERG, ETV1 (ER81), FLU, EST1, EST2, ELK1, ETV6, ETV7, GABPα, ELF1, ETV4, ETV5, ERF, PEA3/E1AF, PU.1, ESE1/ESX, SAP1 (ELK4), ETV3 (METS), EWS/FLI1, ESE1, ESE2 (ELF5), ESE3, PDEF, NET (ELK3; SAP2), NERF (ELF2) или FEV.XXX, опухолеассоциированного гликопротеина 72, c-kit, SCF, pAKT, pc-kit, виментина, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, KIR, TIM3, GAL9, GITR, LAG3, VISTA, KIR, 2B4, TRP02, CD160, CGEN-15049, CHK 1, CHK2, A2aR, TL1A, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2B4, CD160, CGEN-15049, CHK1, CHK2, A2aR, B-7 семейства и их комбинации.
137. Способ по п. 133, где опухолевый маркер содержит один или более маркер, выбранный из группы, состоящей из: геномного полиморфизма, обуславливающего фармакогеномику однонуклеотидного полиморфизма (SNP), геномного SNP, соматического полиморфизма и дифференциальной экспрессии белка, липида и/или клеточной органеллы.
138. Способ по п. 133, где опухолевый маркер выбран из группы, состоящей из: однонуклеотидного положения; внутригенного участка или межгенного участка; экзона или интрона либо их фрагмента; кодирующего участка или некодирующего участка; промотора, энхансера, 5'-нетранслируемого участка (5'-UTR) или 3'-нетранслируемого участка (3'-UTR) либо их фрагмента; кДНК или ее фрагмента; SNP; соматической мутации, мутации в зародышевой линии или их обеих; точечной мутации или мутации в одном сайте; делеционной мутации; делеции внутри рамки считывания, внутригенной делеции, полной делеции гена; инсерционной мутации; внутригенной вставки; инверсионной мутации; внутрихромосомной инверсии; мутации с нарушением связывания; сопряженной инсерционной мутации; мутации типа инвертированной дупликации; тандемной дупликации; внутрихромосомной тандемной дупликации; транслокации; хромосомной транслокации, нереципрокной транслокации; перестройки; геномной перестройки; перестройки одного или более интронов либо их фрагментов; интрона с перестроенной структурой; 5'- или 3'-UTR и их комбинации.
139. Способ по п. 133, где опухолевый маркер содержит маркер из группы, состоящей из: измененной нуклеотидной последовательности, которая кодирует измененную аминокислотную последовательность, хромосомной транслокации, внутрихромосомной инверсии, изменения числа копий, изменения уровня экспрессии, изменения уровня белка, изменения активности белка и изменения статуса метилирования в раковой ткани или раковой клетке, каждый раз по сравнению с нормальной, здоровой тканью или клеткой.
140. Способ по п. 134, где предварительно заданная оценка в баллах выбрана из группы, состоящей из: данных клинических испытаний, репрезентативных онкологических данных, полученных для второго биологического образца, репрезентативных онкологических данных, полученных для группы биологических образцов, данных для находящейся в клинической разработке биологической или малой молекулы.
141. Способ лечения заболевания у субъекта, включающий выбор соответствующей схемы лечения на основании репрезентативных данных по п. 119, при этом репрезентативные данные содержат первый профиль от субъекта.
142. Способ по п. 141, где первый профиль содержит профиль из группы, состоящей из: маркерного профиля, антигенного профиля, белкового профиля, мутационного профиля, липидного профиля, экзосомного профиля или их комбинации.
143. Способ по п. 142, где маркер содержит один или более маркеров из группы, состоящей из: Her2, bRaf, ERBB2, PI3KCA, FGFR2, р53, BRCA, CCND1, MAP2K4, ATR, AFP, ALK, BCR-ABL, BRCA1/BRCA2, BRAF, V600E, Са-125, СА19.9, EGFR, Her-2, KIT, PSA, S100, KRAS, ER/Pr, UGT1A1, CD30, CD20, F1P1L1-PDGRFα, PDGFR, TMPT, TMPRSS2; ABCB5, AFP-L3, альфа-фетопротеина, альфа-метил-ацил-КоА-рацемазы, BRCA1, BRCA2, CA 15-3, CA 242, Са 27-29, СА-125, CA15-3, CA19-9, кальцитонина, канцероэмбрионального антигена, пептида-1 канцероэмбрионального антигена, дез-гамма-карбоксипротромбина, десмина, раннего антигена-2 рака предстательной железы, рецептора эстрогенов, продукта деградации фибрина, глюкозо-6-фосфат-изомеразы, vE6, Е7, L1, L2 или p16INK4a, хорионического гонадотропина человека, IL-6, кератина 19, лактатдегидрогеназы, лейциламинопептидазы, липотропина, метанефринов, неприлизина, nmp22, норметанефрина, РСА3, простатоспецифического антигена, кислой фосфатазы предстательной железы, синаптофизина, тиреоглобулина, TNF, транскрипционного фактора, выбранного из ERG, ETV1 (ER81), FLU, EST1, EST2, ELK1, ETV6, ETV7, GABPα, ELF1, ETV4, ETV5, ERF, PEA3/E1AF, PU.1, ESE1/ESX, SAP1 (ELK4), ETV3 (METS), EWS/FLI1, ESE1, ESE2 (ELF5), ESE3, PDEF, NET (ELK3; SAP2), NERF (ELF2) или FEV.XXX, опухолеассоциированного гликопротеина 72, c-kit, SCF, pAKT, pc-kit, виментина, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, KIR, TIM3, GAL9, GITR, LAG3, VISTA, KIR, 2B4, TRP02, CD160, CGEN-15049, CHK 1, CHK2, A2aR, TL1A, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2B4, CD160, CGEN-15049, CHK1, CHK2, A2aR, B-7 семейства и их комбинации.
144. Способ по п. 141, где первый профиль содержит профиль, полученный из группы, состоящей из: одного или нескольких маркеров, одного или нескольких антигенов, одного или нескольких белков, одной или нескольких мутаций, одного или нескольких липидов, одной или нескольких экзосом или их комбинации.
145. Способ по п. 142, где маркер выбран из группы, состоящей из: геномного полиморфизма, обуславливающего фармакогеномику однонуклеотидного полиморфизма (SNP), геномного SNP, соматического полиморфизма и дифференциальной экспрессии белка, липида и/или клеточной органеллы.
146. Способ по п. 142, где маркер выбран из группы, состоящей из: однонуклеотидного положения; внутригенного участка или межгенного участка; экзона или интрона либо их фрагмента; кодирующего участка или некодирующего участка; промотора, энхансера, 5'-нетранслируемого участка (5'-UTR) или 3'-нетранслируемого участка (3'-UTR) либо их фрагмента; кДНК или ее фрагмента; SNP; соматической мутации, мутации в зародышевой линии или их обеих; точечной мутации или мутации в одном сайте; делеционной мутации; делеции внутри рамки считывания, внутригенной делеции, полной делеции гена; инсерционной мутации; внутригенной вставки; инверсионной мутации; внутрихромосомной инверсии; мутации с нарушением связывания; сопряженной инсерционной мутации; мутации типа инвертированной дупликации; тандемной дупликации; внутрихромосомной тандемной дупликации; транслокации; хромосомной транслокации, нереципрокной транслокации; перестройки; геномной перестройки; перестройки одного или более интронов либо их фрагментов; интрона с перестроенной структурой; 5'- или 3'-UTR и их комбинации.
147. Способ по п. 141, где схема лечения содержит персональный режим введения.
148. Способ по п. 141, где схема лечения выбрана из группы, состоящей из: химиотерапии, иммунотерапии, облучения, хирургического вмешательства, генной терапии, гормональной терапии, терапии стволовыми клетками, переливания крови, физиотерапии, фотодинамической терапии и их комбинации.
149. Способ по любому из п.п. 141-148, дополнительно включающий сравнение первого профиля от субъекта с предварительно заданным профилем для определения соответствия данной схемы лечения субъекту.
150. Способ по п. 149, где предварительно заданный профиль определен на основании данных, выбранных из группы, состоящей из: данных клинических испытаний, второго профиля от субъекта, профиля другого биологического образца или группы биологических образцов, профиля от другого субъекта или группы субъектов, данных для биологической или малой молекулы и их комбинации.
151. Способ идентификации клинически релевантного маркера, включающий сравнение репрезентативных данных по п. 19 с предварительно заданными данными.
152. Способ по п. 151, где маркер выбран из группы, состоящей из: белка, антигена, фермента, гормона, ДНК, РНК, микроРНК или углевода.
153. Способ по п. 151, где маркер содержит геномный полиморфизм, обуславливающий фармакогеномику однонуклеотидный полиморфизм (SNP), геномный SNP, соматический полиморфизм и дифференциальную экспрессию белка, липида, белковую модификацию и клеточную органеллу.
154. Способ по п. 151, где маркер выбран из группы, состоящей из: однонуклеотидного положения; внутригенного участка или межгенного участка; экзона или интрона либо их фрагмента; кодирующего участка или некодирующего участка; промотора, энхансера, 5'-нетранслируемого участка (5'-UTR) или 3'-нетранслируемого участка (3'-UTR) либо их фрагмента; кДНК или ее фрагмента; SNP; соматической мутации, мутации в зародышевой линии или их обеих; точечной мутации или мутации в одном сайте; делеционной мутации; делеции внутри рамки считывания, внутригенной делеции, полной делеции гена; инсерционной мутации; внутригенной вставки; инверсионной мутации; внутрихромосомной инверсии; мутации с нарушением связывания; сопряженной инсерционной мутации; мутации типа инвертированной дупликации; тандемной дупликации; внутрихромосомной тандемной дупликации; транслокации; хромосомной транслокации, нереципрокной транслокации; перестройки; геномной перестройки; перестройки одного или более интронов либо их фрагментов; интрона с перестроенной структурой; 5'- или 3'-UTR и их комбинации.
155. Способ по п. 151, где маркер выбран из группы, состоящей из: измененной нуклеотидной последовательности, которая кодирует измененную аминокислотную последовательность, хромосомной транслокации, внутрихромосомной инверсии, изменения числа копий, изменения уровня экспрессии, изменения уровня белка, изменения активности белка и изменения статуса метилирования в раковой ткани или раковой клетке, каждый раз по сравнению с нормальной, здоровой тканью или клеткой.
156. Способ по п. 151, где предварительно заданные данные получены на основании данных, выбранных из группы, состоящей из: данных, определенных на основании данных клинических испытаний, данных для субъекта или группы субъектов, данных для образца ткани или группы образцов ткани, данных для находящейся в клинической разработке биологической или малой молекулы либо их комбинации.
157. Способ определения прогноза рака у субъекта, включающий оценку репрезентативных данных по п. 119 от субъекта.
158. Способ по п. 157, дополнительно включающий расчет количественной оценки в баллах в отношении прогноза рака, при этом такой прогноз устанавливают на основании количественной оценки в баллах.
159. Способ по п. 157, где репрезентативные данные содержат информацию о количестве, типах, статусах и/или процентном содержании клеточных структур в гомогенате.
160. Способ по п. 159, где клеточные структуры содержат стволовые клетки, эпителиальные клетки, клетки крови, жировые клетки, клетки кожи, эндотелиальные клетки, раковые клетки или иммунные клетки.
161. Способ по п. 160, где иммунные клетки содержат нейтрофилы, моноциты, макрофаги, дендритные клетки, природные киллерные клетки, Т-клетки и/или В-клетки.
162. Способ по п. 161, где Т-клетки содержат киллерные Т-клетки, хелперные Т-клетки, регуляторные Т-клетки, пан-Т-клетки, наивные Т-клетки, активированные Т-клетки и/или гамма-дельта Т-клетки.
163. Способ по п. 159, где статусы клеточных структур включают пролиферацию, апоптоз, некроз, миграцию, эпителиально-мезенхимальный переход ("ЕМТ"), митоз, арест клеточного цикла, S-фазу, старение и/или дифференцировку.
164. Способ по п. 157, где репрезентативные данные содержат информацию о маркере в гомогенате.
165. Способ по п. 164, где маркер выбран из группы, состоящей из ДНК, белка, РНК, липида, клеточной органеллы, метаболита или клетки.
166. Способ по п. 164, где маркер содержит один или более маркеров из Her2, bRaf, ERBB2, PI3KCA, FGFR2, р53, BRCA, CCND1, MAP2K4, ATR, AFP, ALK, BCR-ABL, BRCA1/BRCA2, BRAF, V600E, Са-125, СА19.9, EGFR, Her-2, KIT, PSA, S100, KRAS, ER/Pr, UGT1A1, CD30, CD20, F1P1L1-PDGRFα, PDGFR, TMPT, TMPRSS2; ABCB5, AFP-L3, альфа-фетопротеина, альфа-метил-ацил-КоА-рацемазы, BRCA1, BRCA2, СА 15-3, СА 242, Са 27-29, СА-125, СА15-3, СА19-9, кальцитонина, канцероэмбрионального антигена, пептида-1 канцероэмбрионального антигена, дез-гамма-карбоксипротромбина, десмина, раннего антигена-2 рака предстательной железы, рецептора эстрогенов, продукта деградации фибрина, глюкозо-6-фосфат-изомеразы, vE6, Е7, L1, L2 или p16INK4a, хорионического гонадотропина человека, IL-6, кератина 19, лактатдегидрогеназы, лейциламинопептидазы, липотропина, метанефринов, неприлизина, NMP22, норметанефрина, РСА3, простатоспецифического антигена, кислой фосфатазы предстательной железы, синаптофизина, тиреоглобулина, TNF, транскрипционного фактора, выбранного из ERG, ETV1 (ER81), FLU, EST1, EST2, ELK1, ETV6, ETV7, GABPα, ELF1, ETV4, ETV5, ERF, PEA3/E1AF, PU.1, ESE1/ESX, SAP1 (ELK4), ETV3 (METS), EWS/FL11, ESE1, ESE2 (ELF5), ESE3, PDEF, NET (ELK3; SAP2), NERF (ELF2) или FEV.XXX, опухолеассоциированного гликопротеина 72, c-kit, SCF, pAKT, pc-kit, виментина, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, KIR, TIM3, GAL9, GITR, LAG3, VISTA, KIR, 2B4, TRP02, CD160, CGEN-15049, CHK 1, CHK2, A2aR, TL1A, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2B4, CD160, CGEN-15049, CHK1, CHK2, A2aR, семейства B-7 и их комбинации.
167. Способ по п. 164, где маркер выбран из группы, состоящей из: модификации белка, при этом указанная модификация выбрана из группы, состоящей из ацетилирования, АДФ-рибозилирования, ацилирования, АДФ-рибозилирования, амидирования, ковалентного присоединения флавина, ковалентного присоединения гема, ковалентного присоединения нуклеотида или нуклеотидного производного, ковалентного присоединения липида или липидного производного, ковалентного присоединения фосфатидилинозита, перекрестного сшивания, циклизации, образования дисульфидных связей, дезметилирования, образования ковалентных сшивок, образования цистина, образования пироглутамата, формилирования, гамма-карбоксилирования, гликозилирования, образования GPI якоря, гидроксилирования, иодинирования, метилирования, миристоилирования, окисления, протеолитического процессинга, фосфорилирования, пренилирования, рацемизации, селеноилирования, сульфатирования, аргинилирования и убиквитинилирования.
168. Способ по п. 164, где маркер выбран из группы, состоящей из: геномного полиморфизма, обуславливающего фармакогеномику однонуклеотидного полиморфизма (SNP), геномного SNP, соматического полиморфизма и дифференциальной экспрессии белка, липида и/или клеточной органеллы, однонуклеотидного положения; внутригенного участка или межгенного участка; экзона или интрона либо их фрагмента; кодирующего участка или некодирующего участка; промотора, энхансера, 5-нетранслируемого участка (5'-UTR) или 3'-нетранслируемого участка (3'-UTR) либо их фрагмента; кДНК или ее фрагмента; SNP; соматической мутации, мутации в зародышевой линии или их обеих; точечной мутации или мутации в одном сайте; делеционной мутации; делеции внутри рамки считывания, внутригенной делеции, полной делеции гена; инсерционной мутации; внутригенной вставки; инверсионной мутации; внутрихромосомной инверсии; мутации с нарушением связывания; сопряженной инсерционной мутации; мутации типа инвертированной дупликации; тандемной дупликации; внутрихромосомной тандемной дупликации; транслокации; хромосомной транслокации, нереципрокной транслокации; перестройки; геномной перестройки; перестройки одного или более интронов либо их фрагментов; интрона с перестроенной структурой; 5'- или 3'-UTR, измененной нуклеотидной последовательности, которая кодирует измененную аминокислотную последовательность, хромосомной транслокации, внутрихромосомной инверсии, изменения числа копий, изменения уровня экспрессии, изменения уровня белка, изменения активности белка или изменения статуса метилирования в раковой ткани или раковой клетке по сравнению с нормальной, здоровой тканью или клеткой.
169. Способ определения фенотипического профиля образца ткани, который включает анализ клеточных структур гомогената по п. 81.
170. Способ по п. 169, где клеточные структуры содержат кластер клеток, отдельную клетку, фрагмент клетки, органеллу, пептид, нуклеиновую кислоту, липид, метаболит или их комбинацию.
171. Способ по п. 169, где клеточные структуры содержат одиночную клетку или одиночное ядро, при этом одиночная клетка или одиночное ядро является интактной(ым).
172. Способ по п. 169, где анализ включает анализ количеств, типов, статусов, процентных содержаний и/или процессов экспрессии клеточных структур.
173. Способ по п. 169, где анализ включает анализ одиночных клеток, анализ одиночных ядер, анализ одиночных органелл или их комбинацию.
174. Способ по п. 162, где статус клеточных структур включает пролиферацию, апоптоз, некроз, миграцию, эпителиально-мезенхимальный переход ("ЕМТ"), митоз, арест клеточного цикла, S-фазу, старение и/или дифференцировку.
175. Способ по п. 169, где анализ включает анализ маркера из гомогената.
176. Способ по п. 175, где маркер выбран из группы, состоящей из ДНК, белка, РНК, липида, клеточной органеллы, метаболита или клетки.
177. Способ по п. 175, где анализ маркера включает детектирование маркера.
178. Способ по п. 175, где анализ маркера включает анализ маркера из одиночной клетки или одиночного ядра.
179. Способ хранения композиции на основе гомогената по п. 1, включающий смешивание композиции с эффективным количеством способствующего хранению реагента.
180. Способ по п. 179, где способствующий хранению реагент содержит что-либо одно или более из: консерванта, хаотропа, детергента, восстанавливающего агента, хелатора, буфера или их комбинации.
181. Способ по п. 179, где смешанная композиция сохраняет фенотипические и генотипические характеристики композиции до смешивания со способствующим хранению реагентом.
182. Способ по п. 189, где смешанная композиция содержит денатурированные белки, инактивированную нуклеазу, инактивированную протеазу, инактивированный патоген, нерасщепленную нуклеиновую кислоту или их комбинацию.
183. Способ по п. 180, где хаотроп содержит гуанидина тиоцианат, гуанидина изоцианат, гуанидина гидрохлорид или их комбинацию.
184. Способ по п. 180, где детергент содержит натрия додецилсульфат, лития додецилсульфат, натрия тауродезоксихолат, натрия таурохолат, натрия гликохолат, натрия дезоксихолат, натрия холат, натрия алкилбензолсульфонат, N-лауроилсаркозин или их комбинацию.
185. Способ по п. 180, где восстанавливающий реагент содержит меркаптоэтанол, трис(2-карбоксиэтил)фосфин, дитиотреит, диметилсульфоксид, трис(2-карбоксиэтил)фосфин или их комбинацию.
186. Способ по п. 180, где хелатор содержит этиленгликольтетрауксусную кислоту, гидроксиэтилэтилендиаминтриуксусную кислоту, диэтилентриаминпента-уксусную кислоту, N,N-бис(карбоксиметил)глицин, этилендиаминтетрауксусную кислоту, цитрат безводный, цитрат натрия, цитрат кальция, цитрат аммония, бицитрат аммония, лимонную кислоту, цитрат диаммония, цитрат аммония-трехвалентного железа, цитрат лития или их комбинацию.
187. Способ по п. 180, где буфер содержит трис(гидроксиметил)аминометан, цитрат, 2-(N-морфолино)зтансульфоновую кислоту, N,N-бис(2-гидроксиэтил)-2-аминоэтансульфоновую кислоту, 1,3-бис(трис(гидроксиметил)метиламино)пропан, 4-(2-гидроксиэтил)-1-пиперазин-этансульфоновую кислоту, 3-(N-морфолин)пропансульфоновую кислоту, бикарбонат, фосфат или их комбинацию.
188. Способ приготовления образца ткани, содержащего гетерогенные клеточные структуры, включающий:
a) гомогенизацию образца;
b) реконструирование гомогенизированного образца с получением гомогената, причем указанный гомогенат содержит по существу гомогенные клеточные структуры,
при этом соотношение клеточных структур в подгруппе гомогената по существу аналогично или равно соотношению клеточных структур в образце ткани.
189. Способ по п. 188, где гомогенат содержит множество одиночных клеток или множество кластеров клеток.
190. Способ по п. 188, дополнительно включающий фиксацию гомогената с использованием фиксирующего агента.
191. Способ по п. 190, где фиксирующий агент содержит формалин, кальций, уксусную кислоту, физиологический раствор, спирт, мочевину, бронопол, воду или их комбинацию.
192. Способ по п. 190, где подвергнутый фиксации гомогенат размещают на предметном стекле.
193. Способ по любому из п.п. 108-112, дополнительно включающий экстрагирование компонента из гомогената.
194. Способ по п. 193, где указанный компонент представляет собой ДНК, РНК, белок, липид, клеточную органеллу, экзосому, клетку или их комбинацию.
195. Способ по любому из п.п. 108-114, дополнительно включающий выделение клеточной структуры или компонента из гомогената.
196. Способ по п. 195, где клеточная структура или компонент содержит одиночную клетку или одиночное ядро.
197. Способ по п. 195, где выделение включает выделение одной клетки или выделение одного ядра.
198. Способ по п. 197, где выделение одной клетки выполняют с использованием проточной цитометрии, препаровки под лазерным микроскопом, ручной сортировки клеток, случайного посева и разведения, микрофлюидного устройства, устройства типа "лаборатории на чипе" или их комбинации.
199. Способ по п. 197, где выделение одного ядра выполняют с использованием проточной цитометрии.
200. Способ по п. 188, где гомогенизация включает химическую и/или биохимическую диссоциацию и/или, возможно, механическую гомогенизацию.
201. Способ по п. 188, где гомогенизация не вызывает лизиса клеток.
202. Способ по п. 200, где химическая обработка образца включает ферментативное расщепление образца, причем указанное ферментативное расщепление включает применение фермента, выбранного из группы, состоящей из интерстициальной коллагеназы, желатиназы-а, стромелизина 1, матрилизина, коллагеназы нейтрофилов, желатиназы-b, стромелизина 2, стромелизина 3, металлоэластазы макрофагов, коллагеназы 3, МТ1-ММР, МТ2-ММР, МТ3-ММР, МТ4-ММР, коллагеназы 4, энамелизина, Х-ММР, СА-ММР, МТ5-ММР, МТ6-ММР, матрилизина-2, ММР-22, эндопротеиназы, трипсина, химотрипсина, эндопротеиназы Asp-N, эндопротеиназы Arg-C, эндопротеиназы Glu-C (протеазы V8), эндопротеиназы Lys-C, пепсина, термолизина, эластазы, папаина, протеиназы K, субтилизина, клострипаина, экзопептидазы, карбоксипептидазы А, карбоксипептидазы В, карбоксипептидазы Р, карбоксипептидазы Y, катепсина С, высвобождающего ациламинокислоту фермента и пироглутаматаминопептидазы.
203. Способ по п. 200, где механическую гомогенизацию выполняют с использованием устройства, выбранного из группы, состоящей из блендера, соковыжималки, диассоциатора, экстрактора, ступки, пестика, гомогенизатора Даунса, измельчителя тканей, гомогенизатора тканей с вращающимися ножами и гомогенизатора по типу шаровой мельницы.
204. Способ по п. 188, где образец обрабатывают гормонами, белками, ферментами, липидами, детергентами, ультразвуком, их комбинацией до или после гомогенизации.
205. Способ по п. 200, где гомогенизация дополнительно включает выдерживание клеток, при этом указанное выдерживание клеток включает подведение рН и/или температуры либо обработку образца буфером для выдерживания клеток.
206. Способ по п. 188, где гомогенизированный образец содержит клетки и/или кластеры клеток.
207. Способ по п. 200, где гомогенизированный образец содержит кластеры клеток одинаковых размеров.
208. Способ по п. 200, где гомогенизированный образец содержит кластеры клеток неодинаковых размеров.
209. Способ по п. 120, где кластеры клеток содержат 1-100 клеток или 100-1000 клеток, 1000-10000 клеток или 10000-100000 клеток.
210. Способ по п. 120, где кластеры клеток содержат более 100000 клеток.
211. Способ по п. 108, дополнительно включающий пропускание гомогенизированного образца через сетку, фильтр либо серию сеток или фильтров.
212. Способ по п. 211, где сетка или фильтр имеет размер пор, изменяющийся в диапазоне от примерно 1 микрона до примерно 500 микрон.
213. Способ по п. 211, где сетка или фильтр имеет размер пор меньше 1 микрона.
214. Способ по п. 211, где сетка или фильтр имеет размер пор, изменяющийся в диапазоне от примерно 1 микрона до примерно 100 микрон, от примерно 100 микрон до примерно 200 микрон, от примерно 200 микрон до примерно 300 микрон, от примерно 300 микрон до примерно 400 микрон или от примерно 400 микрон до примерно 500 микрон.
215. Способ по п. 211, где сетка или фильтр имеет размер пор больше 500 микрон.
216. Способ по п. 188, где образец ткани происходит из ткани, выбранной из группы, состоящей из опухоли, лимфатического узла, метастаза, полипа, кисты, биопсийного материала, целого органа и их комбинации.
217. Способ по п. 188, где образец ткани представляет собой твердый образец или жидкий образец.
218. Способ по п. 217, где жидкий образец содержит отобранный шприцем аспират для цитологического исследования, образец экссудата или мазок по Папаниколау.
219. Способ по п. 188, где клеточные структуры гомогената содержат по меньшей мере одну клетку.
220. Способ по п. 188, где клеточные структуры гомогената содержат по меньшей мере 100 клеток.
221. Способ по п. 188, где клеточные структуры гомогената содержат от примерно 100 до примерно 200 клеток, от примерно 200 до примерно 1000 клеток, от примерно 1000 до примерно 5000 клеток или от примерно 10000 до примерно 100000 клеток.
222. Способ по п. 108, где клеточные структуры гомогената содержат от примерно 100000 до примерно 1000000 клеток; от примерно 1000000 до примерно 5000000 клеток, от примерно 5000000 до примерно 1000000000 клеток или от примерно 1000000000 до примерно 5000000000 клеток.
223. Способ по п. 188, где клеточные структуры гомогената содержат более чем примерно 5000000000 клеток.
224. Способ по п. 188, где гомогенат не подвергают консервированию или фиксации.
225. Способ по п. 188, где гомогенат содержит живую клетку.
226. Способ по п. 188, где гомогенат подвергают консервированию или фиксации.
227. Способ по п. 188, где гомогенат замораживают, подвергают сублимационной сушке или заливают средой для заливки.
228. Способ по п. 188, где гомогенат содержит клетки из одной или нескольких тканей и/или от одного или более чем одного субъекта.
229. Способ по п. 188, где образец ткани выделяют из опухоли, лимфатического узла, метастазов, полипа, кисты, извлеченного резекцией материала, целогой органа или их комбинации.
230. Способ по п. 188, где гомогенат дополнительно содержит клетку, не являющуюся клеткой человека, человеческую клетку, ненативный белок, нуклеиновую кислоту или малую молекулу.
231. Способ по п. 230, где малая молекула выбрана из группы, состоящей из гаптена, пептидной метки, белковой метки, флуоресцентной метки, нуклеиновокислотной метки и их комбинации.
232. Способ по п. 188, дополнительно включающий оценку по существу гомогенных клеточных структур в гомогенате.
233. Способ по п. 232, где по существу гомогенные клеточные структуры оценивают путем измерения распределения внутреннего контроля в гомогенате.
234. Способ по п. 233, где внутренний контроль выбран из группы, состоящей из клетки, не являющейся клеткой человека, человеческой клетки, ненативного белка, нуклеиновой кислоты, малой молекулы, красителя, химического вещества и их комбинации.
235. Способ по п. 234, где малая молекула содержит гаптен, пептидную метку, белковую метку, флуоресцентную метку, нуклеиновокислотную метку, люминесцентную метку, биотин и их комбинацию.
236. Способ по п. 188, дополнительно включающий анализ гомогената.
237. Способ по п. 236, где анализ включает анализ нуклеиновых кислот, анализ белков, анализ липидов, анализ клеток, анализ метаболитов, геномный анализ, транскриптомный анализ, протеомный анализ, метаболомный анализ, липидомный анализ, иммунологический анализ, цитохимический анализ, генотипический анализ, фенотипический анализ или их комбинацию.
238. Способ по п. 237, где анализ нуклеиновых кислот включает анализ ДНК или анализ РНК.
239. Способ по п. 238, где анализ РНК включает анализ микроРНК.
240. Способ по п. 236, где анализ гомогената включает очистку нуклеиновой кислоты, белка, органеллы, метаболита, химического вещества, неклеточного компонента или их комбинации.
241. Способ по п. 236, где анализ гомогената включает связывание связывающегося агента с компонентом гомогената.
242. Способ по п. 241, где связывающийся агент содержит антитело, радиоактивную метку, флуорохром, гаптен, фермент, нуклеиновую кислоту, белок, химическое вещество, праймер, лиганд, клетку, пептид, зонд, флуоресцентный краситель, нефлуоресцентный краситель, фермент, биотин или их комбинацию.
243. Способ по п. 241, где компонент гомогената содержит нуклеиновую кислоту, белок, органеллу, метаболит, химическое вещество, неклеточный компонент или их комбинацию.
244. Способ по п. 236, где анализ гомогената дополнительно включает детектирование сигнала от связывающегося агента или компонента.
245. Способ по п. 244, где сигнал содержит радиоактивный сигнал или нерадиоактивный сигнал.
246. Способ по п. 245, где нерадиоактивный сигнал содержит флуоресцентный сигнал, хемифлуоресцентный сигнал или люминесцентный сигнал.
247. Способ по п. 236, где анализ гомогената включает анализ с использованием секвенирования, гистологический анализ или анализ изображений.
248. Способ по п. 247, где анализ с использованием секвенирования включает анализ с использованием секвенирования следующего поколения, анализ с использованием секвенирования из одной клетки и/или секвенирование из одного ядра.
249. Способ по п. 247, где гистологический анализ включает гистологический анализ следующего поколения.
250. Способ по п. 247, где анализ изображений включает анализ следующего поколения.
251. Способ по п. 188, дополнительно включающий детектирование или количественное определение компонента гомогената, при этом компонент содержит клетку, нуклеиновую кислоту, белок, органеллу, метаболит, химическое вещество, неклеточный компонент или их комбинацию.
252. Способ по п. 251, где клетка включает иммунную клетку, опухолевую клетку, стволовую клетку, клетку-предшественник, клетку крови, зародышевую клетку и соматическую клетку.
253. Способ по п. 236, где анализ гомогената включает анализ поляризованного света, отраженного от гомогената.
254. Способ по п. 236, где анализ гомогената включает анализ акустического свойства, механического свойства или оптического свойства гомогената.
255. Способ по п. 236, где гомогенат анализируют с использованием проточной цитометрии, окрашивания гематоксилином и эозином или иммуногистохимического анализа.
256. Способ мониторинга заболевания у пациента, включающий анализ маркера по п. 151, при этом клинически релевантный маркер идентифицируют на основании репрезентативных данных по п. 119.
257. Способ по п. 256, где маркер выбран из группы, состоящей из: белка, антигена, фермента, гормона, ДНК, РНК, микроРНК или углевода.
258. Способ по п. 256, где маркер представляет собой ДНК или РНК, выделенную из образца, выбранного из группы, состоящей из: одной или нескольких клеток в состоянии, предшествующем злокачественному перерождению, или озлокачествленных клеток, клеток из солидной опухоли, опухоли мягких тканей или метастатического поражения, ткани или клеток из хирургического края (опухоли), гистологически нормальной ткани, одной или нескольких циркулирующих опухолевых клеток (СТС), нормальной близко расположенной ткани (NAT), образца крови от одного и того же субъекта, имеющего опухоль или имеющего риск наличия опухоли, или FFPE образца.
259. Способ по п. 256, где заболевание представляет собой рак.
260. Способ приготовления композиции на основе гомогената по любому из п.п. 1-38 для микроскопии, включающий заливку композиции на основе гомогената или ее части поддающимся набуханию материалом.
261. Способ по п. 260, дополнительно включающий увеличение в размере композиции на основе гомогената посредством разбухания поддающегося набуханию материала.
262. Способ по п. 260, где способ заливки включает пропитывание гомогената составом, содержащим предшественники поддающегося набуханию материала, образование поддающегося набуханию материала in situ и закрепление композиции на основе гомогената в поддающемся набуханию материале.
263. Способ по п. 260, где поддающийся набуханию материал образуется из предшественника поддающегося набуханию материала, причем предшественник содержит полимеризуемый материал, инициаторы полимеризации или сшивающий агент.
264. Способ по п. 263, где полимеризуемый материал представляет собой мономер или олигомер.
265. Способ по п. 264, где мономер или олигомер содержит замещенный или незамещенный метакрилат, акрилат, акриламид, метакриламид, виниловый спирт, виниламин, аллиламин, аллиловый спирт или сшивающие их дивиниловые агенты.
Реферат
Изобретение относится к диагностике, а именно к способу приготовления образца опухолевой ткани. Способ приготовления образца опухолевой ткани для определения фенотипического профиля образца опухолевой ткани, который включает: гомогенизацию образца опухолевой ткани; реконструирование гомогенизированного образца с получением гомогената, причем указанный гомогенат содержит по существу гомогенные клеточные структуры, где соотношение клеточных структур в подгруппе гомогената по существу аналогично или равно соотношению клеточных структур в образце ткани; анализ клеточных структур гомогената; определение фенотипического профиля опухолевой ткани. Вышеописанный способ позволяет повысить обнаружение мутаций из раковых тканей по сравнению с гистологическими срезами, взятыми из FFPE блоков той же самой ткани. 55 ил., 24 табл., 12 пр.

Комментарии