Способ получения scr-активного цеолитного катализатора и scr-активный цеолитный катализатор - RU2506999C2
Код документа: RU2506999C2
Чертежи
Описание
Данное изобретение касается способа получения SCR-активного цеолитного катализатора. Кроме того, данное изобретение касается SCR-активного цеолитного катализатора. Данное изобретение связано с проблемой относительно низкой SCR активности цеолитного катализатора в низкотемпературном диапазоне ниже 300°C, если только небольшое количество NO2, если имеется, присутствует в отработанном газе.
Для удаления оксидов азота из содержащего кислород отработанного газа, такого как газ из двигателя внутреннего сгорания, работающего с избытком воздуха, особенно из дизельного двигателя, известны катализаторы на основе диоксида титана, на которых оксиды азота восстанавливаются в присутствии кислорода посредством добавленного восстанавливающего средства, такого как аммиак, в частности, с получением молекулярного азота и воды. В этом отношении сделана ссылка в качестве примера на патентный документ Германии 2458888 A1. В этом способе селективного каталитического восстановления, для краткости SCR способ, восстанавливающее средство или вещество-предшественник, которое превращается в восстанавливающее средство в отработанном газе, добавляется в отработанный газ перед попаданием в каталитический преобразователь. Например, известным веществом-предшественником для восстанавливающего средства аммиака является мочевина, которая подается в отработанный газ, особенно в форме водного раствора мочевины. Также известны в качестве альтернативных восстанавливающих средств углеводороды, которые, особенно в случае неполного сгорания в двигателе внутреннего сгорания, уже могут присутствовать как продукты сгорания в отработанном газе.
SCR-активные катализаторы, известные из патентного документа Германии 2458888 A1, включают керамическую катализаторную композицию, включающую диоксид титана в качестве основной составляющей, с добавками оксидов вольфрама и/или ванадия. Тела катализаторов, используемые там, могут быть покрытыми катализаторами или катализаторами без подложки. В покрытых катализаторах катализаторная композиция нанесена на материал подложки, такой как, более конкретно, кордиерит (магния алюмосиликат композиции Mg2Al4Si5O18 с ромбической дипирамидальной структурой), который сам по себе каталитически не активен. Катализатор без подложки, в отличие от него, полностью изготавливается из каталитически активной катализаторной композиции. С этой целью исходные материалы обычно обрабатываются с получением перемешанной взвеси, которая экструдируется с получением ячеистого материала, пронизанного каналами. Затем экструдированный ячеистый материал обжигается с затвердением термической обработкой с получением окончательного катализатора без подложки.
Следующими известными составляющими SCR-активных катализаторов также являются цеолиты. Цеолиты, т.е. каркасные алюмосиликаты, в некоторых случаях формируют структуру, пронизанную каналами с диаметром порядка размера молекул газа, и благодаря их высокой удельной площади поверхности особенно пригодны для селективного каталитического восстановления.
Например, патентный документ Германии 198545502 A1 раскрывает SCR-активный катализатор для разложения оксидов азота в присутствии восстанавливающего средства, имеющего активную композицию, включающую диоксид титана и цеолит, причем указанный цеолит является водородным ионообменным, кислым цеолитом.
Патентный документ Великобритании 2193655 A также раскрывает катализатор для разложения оксидов азота SCR способом. Катализаторная композиция катализатора, определенного там, включает диоксид титана с низкой удельной площадью поверхности и содержащий медь цеолит, полученный ионным обменом. Определенными предпочтительными цеолитами являются морденит, ZSM-5 и ферриерит.
Также из европейского патентного документа 0393917 А2 известен катализатор для разложения оксидов азота, катализаторная композиция которого включает цеолит, который после ионного обмена содержит медь и/или железо. Определенными предпочтительными цеолитами являются USY (Ultra Stabilized Y), бета и ZSM-20.
Кроме того, европейский патентный документ 0219854 A2 раскрывает катализатор, который включает диоксид титана в анатазном полиморфе и кислотно-стабилизированный цеолит в водородной форме или в аммонийной форме.
Наконец, патентный документ США 5271913 A раскрывает катализатор для разложения оксидов азота SCR способом, катализаторная композиция которого включает цеолит. Указанный цеолит пропитан оксидом церия или оксидом железа. Определенный катализатор, как указано, имеет высокую стабильность по отношению к содержащим серу компонентам. Определенным предпочтительным цеолитом является цеолит типа ZSM-5.
Цеолитные катализаторы могут быть получены или в форме покрытых катализаторов, или в форме катализаторов без подложки. Конфигурация цеолитного катализатора как катализатора из насыпного материала, особенно в форме пеллет, также, по сути, известна.
В литературе упоминается Fe-ионообменный цеолит, в частности, в отношении его хорошей SCR активности. Например, в публикации “Ultra-Active Fe/ZSM-5 Catalyst For Selective Catalytic Reduction Of Nitric Oxide With Ammonia”, Gongshin Qi, Ralph T. Yang, Apple. Cat. B: Environmental 60 (2005) 13-22, рассматривается SCR активность Fe-ионообменного ZSM-5 цеолита по N0, и скорости преобразования N0 близко к 90% достигаются при температурах выше 350°C в присутствии аммиака. Ионный обмен цеолита рассматриваемого типа ZSM-5 выполняется пропитыванием посредством FrCl3. Обжиг катализаторной композиции происходит в окислительной атмосфере на воздухе. Посредством измерений дифракции рентгеновских лучей и электронного спинового резонанса степень окисления иона железа, включенного в цеолитную структуру, определяется как +2 и/или +3. Есть предположение, что железо со степенью окисления+2, в частности, отвечает за высокую каталитическую активность. В ходе рассматриваемой реакции SCR железо со степенью окисления +2 постепенно окисляется.
В предыдущей публикации “Structure/Reactivity Correlation In Fe/ZSM5 For DENOx Applications. In-situ XAFS Characterization And Catalysis”, A.A. Battiston, J.H. Bitter, D.C. Koningsberger, Elsevier, Fe-ионообменный цеолит типа ZSM-5 также рассматривается в отношении его SCR активности. В этом случае особенно координационный узел иона железа, включенный в цеолитную структуру, анализируется посредством методов рентгеновской спектроскопии. Рассматриваемый ZSM-5 цеолит является ионообменным посредством сублимации FeCl3. SCR активность обожженной катализаторной композиции анализируется с использованием бутана и иэобутана в качестве восстанавливающих средств. Катализаторная композиция изучается рентгеновской спектроскопией в каждом случае после обработки кислородом, монооксидом углерода и изобутаном. Как сообщается, в ходе реакции SCR степень окисления включенного иона железа снижается.
Целью данного изобретения является определение способа получения SCR-активного цеолитного катализатора, который, особенно в низком температурном диапазоне, имеет сравнительно высокую и длительную SCR активность, даже если только небольшое количество NO2, если такое имеется, присутствует в отработанном газе. Следующей целью данного изобретения является определение цеолитного катализатора, обеспеченного упомянутыми свойствами.
Цель в отношении способа получения достигается согласно данному изобретению путем воздействия сначала на Fe-ионообменный цеолит восстановительной углеводородной атмосферой для первой термической обработки в диапазоне от 300°C до 600°C, что снижает степень окисления ионов Fe и/или повышает дисперсность ионов Fe в цеолите, затем путем воздействия на восстановленный цеолит окислительной атмосферой для второй термической обработки от 300°C до 600°C, которая окислительно удаляет углеводородные остатки и/или углеродные остатки, и обжига цеолита в ходе первой и второй термических обработок с получением катализатора.
Обширные исследования в лабораторных условиях подтвердили гипотезу о том, что Fe-ионообменный цеолит обладает повышенной SCR активностью, когда степень окисления включенных ионов железа составляет менее чем +3 и/или дисперсность ионов Fe в цеолите повышается. Под дисперсностью в данном документе подразумевается средняя степень распределения ионов Fe в цеолите. Высокая дисперсность указывает на тонкое распределение. Низкая дисперсность предполагает присутствие кластеров Fe в цеолите.
Такой цеолитный катализатор, в принципе, после ионного обмена и обжига может быть получен, например, путем восстановления его в формир-газе или посредством СО, что снижает степень окисления встроенных ионов железа в направлении +2 или изменяет дисперсность.
В условиях SCR, т.е в присутствии кислорода, однако, каталитическая активность постепенно снижается. Это происходит совместно с изменением основного цвета от бледно-желтого - бежевого в восстановленном Fe-ионообменном цеолитном катализаторе до ржаво-красного оттенка. Это говорит о том, что железо со степенью окисления +2, связанное с цеолитом, окисляется до железа со степенью окисления +3, что соответствует FeCO3. Изменение цвета на ржаво-красный оттенок также может быть связано с уменьшением дисперсности железа, т.е. с образованием кластеров Fe, в цеолите.
Целью данного изобретения, таким образом, является получение Fe-ионообменного цеолитного катализатора с высокой SCR активностью постоянным способом. После чрезвычайно обширных эмпирических исследований было установлено, что такой Fe-ионообменный цеолитный катализатор, где железо присутствует преимущественно со степенью окисления менее чем +3, и/или ионы Fe связаны с цеолитом с высокой дисперсностью, может быть получен постоянным способом путем выполнения обжига не как обычно в окислительной атмосфере, а скорее в восстановительной углеводородной атмосфере.
Из-за пока неопределенной реакции с углеводородами или с продуктами разложения углеводородов во время операции обжига в температурном диапазоне от 300°C до 600°C железо связывается с цеолитом и восстанавливается до более низкой степени окисления, особенно +2, и/или тонкое распределение железа на поверхности цеолита стабилизируется. Повторное окисление в окислительной атмосфере или преобразование кластеров Fe на поверхности, особенно в условиях SCR и при высоких температурах, блокируется. Координационный узел связанного катиона железа в цеолите является высоко сложным. Ни точная структура решетки, ни химическое окружение железа не могут быть точно определены. Более конкретно, степень окисления в этих условиях, в анионном каркасе цеолита, уже не может рассматриваться как целое число; вместо этого обсуждаются дробные степени окисления. Исходя из основного цвета, определенного от бледно-желтого до бежевого, в катализаторной композиции, обожженной при восстановительных условиях, средняя степень окисления, однако, может быть представлена со значением менее чем +3. Другими словами, подавляющее число включенных ионов железа должно присутствовать со степенью окисления +2, если определяются целые степени окисления.
Альтернативно, тонкое распределение железа, в отличие от агломерации кластеров, также может быть ключевым для наблюдаемого цвета. Вот почему было обнаружено путем измерений UV-VIS на полученных соответствующим образом образцах цеолита, т.е. на основе спектра поглощения в ультрафиолетовой и видимой области спектра, что определенная обработка устанавливает постоянно высокую дисперсность железа в цеолите. Тогда как широкий пик поглощения от около 250 до 600 нм наблюдается в UV-VIS спектре в случае образцов, полученных традиционно без этапа способа восстановительного обжига, пик, сдвинутый в сторону более коротких длин волн с максимумом около 250 нм, который снижается при около 400 нм и подрезает кривую поглощения сравнительного образца, наблюдается в случае катализаторов, полученных способом, определенным в данном случае. Поскольку, 6 данном случае поглощение при более чем 400 нм предполагает крупные частицы железа (оксид железа, кластеры), поглощение при 300-400 нм предполагает олигомерные Кластеры Fe, и поглощение при 200-300 нм предполагает железо в тетра- или октаэдрической координации, результат анализа свидетельствуют о повышении дисперсности железа в цеолите. Эта дисперсность постоянно дополнительно поддерживается. Новое формирование кластеров Fe блокируется.
Цеолит, восстановленный в углеводородной атмосфере, затем обжигается дополнительно при второй термической обработке от 300°C до 600°C в окислительной атмосфере, которая удаляет остатки или продукты разложения углеводородов путем окисления. Другими словами, углеводороды или углерод сжигаются. В то же время, происходит дальнейшее затвердение катализаторной композиции, что является ключевым для операции обжига.
В общем, цеолит или катализаторная композиция, включающая цеолит, таким образом, обжигается в два этапа, цеолит сначала восстанавливается в углеводородной атмосфере, а затем окисляется в окислительной атмосфере, главным образом, для удаления органических остатков. В то время как готовая катализаторная композиция имеет основной цвет от бледно-желтого до бежевого, было показано, в то же время, что восстановление в углеводородной атмосфере блокирует окисление железа со степенью окисления +2 до железа со степенью окисления +3 и/или снижение дисперсности железа. Окончательный окислительный обжиг не ведет к возобновленному окислению восстановленного железа и/или к возобновленному снижению дисперсности. Дальнейшие исследования подтверждают, что катализаторная композиция, полученная согласно данному изобретению, обладает желаемой постоянно высокой SCR активностью.
Данное изобретение не имеет никаких ограничений в отношении специфической конфигурации тела катализатора. Описанный обжиг в восстановительной и окислительной атмосфере может быть выполнен или на цеолитном порошке, или на содержащем цеолит катализаторе без подложки, или особенным образом на теле подложки, которое было покрыто или пропитано содержащей цеолит композицией.
Было установлено,, что в катализаторе без подложки, который был обожжен при восстанавливающих условиях и нагревается до температур вплоть до 900°C, а также подвергается потоку воздуха при объемной скорости 10000 л/час, даже через несколько часов не происходит какое-либо изменение цвета, что могло бы говорить об окислении включенного железа в восстановленной форме и/или о снижении дисперсности. При тех же условиях эксперимента Fe-ионообменные традиционные цеолиты, которые были восстановлены после обжига, показывают явное изменение цвета уже через несколько минут.
Дальнейшие исследования показали, что присутствующая доля железа со степенью окисления +2 и/или высокая дисперсность железа могут быть еще более стабилизированы, когда температура превышает 500°C в течение периода более чем 50 минут в ходе первой термической обработки. Возможно, что энергия активации требуется для постоянной конфигурации или сохранения координационного узла железа, а именно окружения анионного каркаса цеолита. Было выявлено, что в данном случае полезна продолжительность более чем 50 минут.
Кроме того, было установлено, что для стабилизации или восстановления связанного железа полезно охладить цеолит в конце первой термической обработки до температуры ниже 400°C. Эмпирически было показано в данном контексте путем серий обширных измерений, что SCR активность повышается, когда этап охлаждения добавляется к восстановительной термической обработке перед окислением в ходе второй термической обработки. Наилучшие результаты могут быть достигнуты в данном документе, когда температура опускается ниже 400°C во время охлаждения.
В следующем предпочтительном варианте конфигурации данного изобретения углеводородная атмосфера содержит менее 1 объемного % кислорода. Более высокое содержание кислорода затрудняет восстановление включенного железа.
В отношении углеводородов особенно пригодными являются продукты разложения, углеводородов с длинной цепью, которые образуются путем пиролиза в определенном температурном диапазоне. Особенно пригодными исходными материалами, как было обнаружено, являются главным образом органические полимеры и/или биополимеры. Эти полимеры также вводятся в печь в ходе первой термической обработки. Они разлагаются в ней при соответствующих температурах с выделением кислорода в газообразные продукты разложения, которые затем вносятся в углеводородную атмосферу. Особенно пригодными органическими полимерами являются полиэтилены, полигликоли или полипропилены. Как было выявлено, выгодными биополимерами являются полисахариды, а в этом контексте особенно целлюлоза. Однако, соответственно, также могут быть применены полиглюкозамины и липиды.
Специфический вариант образования необходимой углеводородной атмосферы заключается в выполнении первой термической обработки в атмосфере инертного газа, в этом случае желаемые углеводороды подаются или непосредственно в газообразной форме, или путем разложения, как описано. Особенно используемым инертным газом может быть азот. Однако, также возможны благородные газы.
В особенно предпочтительную конфигурацию по данному изобретению углеводороды добавляются в цеолитную композицию перед обжигом в форме реакционноспособного предшественника. В ходе первой термической обработки реакционноспособный предшественник разлагается до желаемых продуктов разложения, которые затем образуют углеводородную атмосферу. В этой конфигурации нет необходимости подавать какие-либо дополнительные углеводороды в ходе первой термической обработки. Углеводородная атмосфера образуется в ходе термической обработки путем пиролиза молекул предшественника, присутствующих в цеолитной композиции.
В особенно предпочтительном варианте данного изобретения цеолит предварительно обрабатывается с добавкой органического пластификатора для получения свободнотекучей композиции, особенно экструдируемой композиции, при этом первая термическая обработка выполняется в атмосфере инертного газа таким путем, что органический пластификатор высвобождает углеводороды в атмосферу инертного газа в результате пиролиза. Таким образом, органический пластификатор, который в любом случае необходим для получения экструдируемой композиции, может быть использован одновременно для восстановления и стабилизации восстановленного железа. Никаких дополнительных добавок не требуется.
Тогда как органический пластификатор в традиционных способах окисляется в ходе этапа обжига в воздухе, а именно в окислительной атмосфере, и, таким образом, удаляется, при пиролизе пластификатора в атмосфере инертного газа в это время образуются продукты разложения, которые желательны для восстановления и участия в углеводородной атмосфере или для образования углеводородной атмосферы. Типично, применяемым пластификатором является целлюлоза и полиэтиленгликоль или полиэтиленоксид, отдельно или в комбинации.
Порошкообразный цеолит сначала обрабатывается вместе с пластификатором и необязательно с дополнительными вспомогательными средствами и наполнителями, с добавлением воды, для получения экструдируемой композиции.
В первом варианте эта композиция затем экструдируется с получением ячеистого материала, пронизанного каналами. Затем за сушкой ячеистого материала следует вышеописанная операция обжига. За восстановительным обжигом следует окислительный обжиг, при этом органические остатки пластификатора и образованные продукты разложения удаляются путем окисления. Удаление пластификатора посредством окисления образует поры в теле катализатора в ходе операции обжига, что повышает удельную площадь поверхности.
Во втором варианте полученная композиция наносится как покрытие на инертное тело подложки, например, кордиерит. Затем покрытое тело подложки подвергается восстановительному и окислительному обжигу. Инертное тело подложки также может присутствовать, более конкретно, как пористый материал, пронизанный каналами.
Также можно подвергнуть полученную композицию восстановительному обжигу перед ее дальнейшей обработкой.
Обжиг может быть выполнен двумя последовательными этапами. В этом случае цеолит сначала термически обрабатывается в первой печи в восстановительной углеводородной атмосфере и в результате восстанавливается. Затем цеолит извлекается из первой печи, в это время охлаждается и подается во вторую печь. Во второй печи окислительный обжиг выполняется s окислительной атмосфере, особенно в воздухе, что удаляет органические остаточные составляющие.
В предпочтительной конфигурации полная операция обжига, однако, также может быть выполнена в одной печи. В этом случае при завершении первой термической обработки атмосфера в печи меняется отводом восстановительной углеводородной атмосферы и замещением ее воздухом или содержащей кислород атмосферой. В такой печи должны быть обеспечены соответствующие входы, газовые соединения, клапаны и соответствующие системы управления. Выполнение обжига в одной печи особенно выгодно с точки зрения технологического процесса, поскольку нет операционного этапа транспортировки восстановленного цеолита в следующую печь.
Выяснили, что особенно выгодным цеолитом является цеолит бета типа (обозначение каркасной структуры: ВЕА) или ZSM-5 типа (обозначение каркасной структуры: MFI). Следующими пригодными цеолитами, как выяснили, являются фоязит, ферриерит, Y, ZSM-20, МСМ-41, хабазит и SABO. В отношении общей номенклатуры цеолитов ссылка в данном документе сделана на Kirk-Othmer, “Encyclopedia of Chemical Technology”, 3rd ed., Vol.15, John Wiley & Sons, New York, 1981, p.640-669. Для классификации цеолитов ссылка также сделана на статью “Chemical Nomenclature and Formulation of Compositions of Synthetic And Natural Zeolites”, R.M.Barrer, Pure Appl. Chem. 51 (1979), p.1091-1100. Структура отдельных цеолитов также может быть взята, более конкретно, из “Zeolite Atlas: Atlas of Zeolite Framework Types”, 5th ed., Ch. Baerlocher, W.M. Meier and D.H. Olson, Amsterdam, Elsevier (2001).
Для ионного обмена цеолита существуют принципиально различные способы. Они включают обмен катионов калия, натрия или кальция, каузально включенных в цеолит с желательными катионами, например, железа. В принципе это легко осуществимо, поскольку катионы в цеолите удерживаются исключительно ионным взаимодействием с анионной структурой. Ионный обмен железа может быть осуществлен, например, посредством сублимации из хлорида железа, посредством пропитывания твердого вещества или посредством жидкостного ионного обмена из соответствующего раствора.
Для Fe-ионообменного цеолита, как показано в литературе, SCR активность будет зависеть от операции получения или от операции синтеза. Лабораторные исследования показывают, что SCR активность полученного цеолитного катализатора, как описано в данном случае, постоянно высокая, вне зависимости от того, как Fe-ионообменный цеолит был синтезирован. Очевидно, что восстановление в углеводородной атмосфере, независимо от того, является ли операцией синтеза, или операцией ионного обмена, всегда приводит к соизмеримым восстановлению и стабилизации железа со степенью окисления +2 и/или к стабильно высокой дисперсности, при этом формирование кластеров Fe блокируется.
Цеолит предпочтительно содержит железо с долей от 3 до 7 весовых %. В этом диапазоне достигается желаемая каталитическая активность.
Цель, направленная на катализатор, достигается согласно данному изобретению SCR-активным цеолитным катализатором, который был получен вышеупомянутым способом. Такой цеолитный катализатор с соответственно обожженной катализаторной композицией содержит Fe-ионообменным цеолит, где ионы Fe присутствуют преимущественно со степенью окисления менее чем +3 и/или с высокой дисперсностью. Как упоминалось, последнее может быть продемонстрировано экспериментально посредством UV-VIS спектроскопии. Было установлено, что UV-VIS поглощение соответствующего образца заявляемого катализатора в диапазоне длин волн от 400 нм до 600 нм постоянно понижалось по сравнению с сопоставимо полученными образцами без восстановления в углеводородной атмосфере. Дисперсность железа, следовательно, снижается соответственно. Большие кластеры Fe явно уменьшаются. Цеолитный катализатор, полученный таким путем, отличается в этом отношении от известных в уровне техники тем, что превращение ионов Fe в ионы с более высокой степенью окисления +3 и/или формирование кластеров Fe блокируется.
На момент подачи заявки не возможно предусмотреть, какие способы получения, кроме заявленного способа, могут производить SCR-активный цеолитный катализатор, обладающий упомянутым свойством. SCR-активный цеолитный катализатор с обожженной катализаторной композицией, включающей Fe-ионообменный цеолит, где ионы Fe присутствуют преимущественно со степенью окисления менее чем +3 и/или с высокой дисперсностью согласно UV-VIS спектру, и где превращение ионов Fe в ионы с более высокой степенью окисления +3 и/или формирование кластеров Fe блокируется, поэтому считается патентоспособным сам по себе.
Выбранная формулировка “блокирование превращения ионов Fe в ионы с более высокой степенью окисления +3 и/или формирования кластеров Fe” в этом контексте охватывает замедленную кинетику, а также увеличение энергии активации. Выражение “блокирование” также охватывает необратимое восстановление железа до степени окисления +2 или менее чем +3. Наблюдаемое свойство только что определенного катализатора также может быть описано в том отношении, что центр адсорбции железа в цеолите постоянно стабилизируется так, что дисперсность сохраняется. Каждое отдельное из упомянутых свойств может быть использовано полностью самостоятельно или в комбинации для описания катализатора.
Свойство, которое отличает указанный цеолитный катализатор от такового из уровня техники, в конечном счете, также может наблюдаться и излагаться с точки зрения того факта, что обожженная катализаторная композиция, имеющая основной цвет от бледно-желтого до бежевого, что соответствует наличию низкой степени окисления ионов Fe, при нагревании до температуры до 900°C с одновременным потоком воздуха при объемной скорости 10000 л/час не проявляет какого-либо изменения цвета даже через один час. Сопоставимая катализаторная композиция, которая восстанавливается традиционно посредством формир-газа или СО при тех же экспериментальных условиях, уже через несколько минут демонстрирует изменение цвета до ржаво-красного основного цвета, что соответствует более высокой степени окисления ионов Fe +3 или пониженной дисперсности.
Цеолит, применяемый для SCR-активного цеолитного катализатора, предпочтительно может быть одним из вышеупомянутых цеолитов. Более конкретно, цеолит является цеолитом бета типа или MFI типа.
В предпочтительной конфигурации цеолитный катализатор присутствует в форме экструдированного катализатора без подложки.
Дальнейшие исследования показали, что данное изобретение также может охватывать дополнительные ионообменные цеолиты. Соответственно, на ионообменный цеолит характерного типа сначала воздействуют восстановительной углеводородной атмосферой для первой термической обработки в диапазоне от 300°C до 600°C, которая снижает степень окисления введенных ионов и/или повышает дисперсность этих ионов в цеолите, затем на восстановленный цеолит воздействуют окислительной атмосферой для второй термической обработки от 300°C до 600°C, которая окислительно удаляет углеводородные остатки и/или остатки углерода, и цеолит обжигается в ходе первой и второй термических обработок с получением катализатора.
Было выявлено, что для ионного обмена, как и предпочтительное железо, подходящими металлами в отношении вышеупомянутой каталитической активности являются металлы из группы, включающей Cu, Hf, La, Au, In, V, лантаноиды и переходные металлы VIII группы периодической таблицы. Более конкретно, предпочтение отдается не только железу, а также меди, церию, гафнию, лантану, платине, серебру, индию, ванадию, рутению и осмию. Тогда как эти металлы присутствуют как катионы металлов в цеолите, в этом случае утверждения, сделанные для железа, могут быть применены, соответственно, для этих катионов.
Следовательно, степень окисления ионов металла будет снижена и/или дисперсность их в цеолите будет повышена в ходе первой термической обработки.
Как уже отмечено, из-за пока еще неустановленной реакции с углеводородами или с продуктами разложения углеводородов в ходе операции обжига в температурном диапазоне от 300°C до 600° вышеупомянутые ионы металла, связанные с цеолитом, стабилизируются в пониженной степени окисления и/или их тонком распределении, достигнутом на поверхности цеолита. Повторное окисление в окислительной атмосфере или возобновленное формирование кластеров на поверхности, более конкретно, даже в условиях SCR и высоких температур, блокируется. Координационный узел связанного катиона металла в цеолите является высококомплексным. Ни точная структура решетки, ни химическое окружение связанных ионов металла не могут быть точно определены. Более конкретно, степень окисления в этих условиях уже не может рассматриваться как целое число в анионной структуре цеолита; вместо этого обсуждаются дробные степени окисления.
Следовательно, данное изобретение также охватывает SCR-активный цеолитный катализатор с обожженной катализаторной композицией, включающей ионообменный цеолит, где ионы присутствуют преимущественно со степенью окисления, сниженной восстановлением, и/или цеолит с высокой дисперсностью, при этом превращение ионов в таковые с более высокой степенью окисления и/или снижение дисперсности блокируется. Применяемыми ионами металлов предпочтительно являются металлы из группы, включающей Cu, Hf, La, Au, In, V, лантаноиды и переходные металлы из VIII группы периодической таблицы. Более конкретно, ссылка делается не только на железо, а также на медь, церий, гафний, лантан, платину, серебро, индий, ванадий, рутений и осмий. Такой катализатор, более конкретно, не показывает какое-либо изменение цвета, которое могло бы быть связано с изменением степени окисления или дисперсности, даже когда подвергнут потоку воздуха при относительно высоких температурах (выше 700°C).
Варианты осуществления данного изобретения проиллюстрированы в деталях со ссылкой на следующие графические материалы и примеры. Графические материалы показывают:
фиг.1 схематическую блок-схему получения SCR-активного цеолитного катализатора и
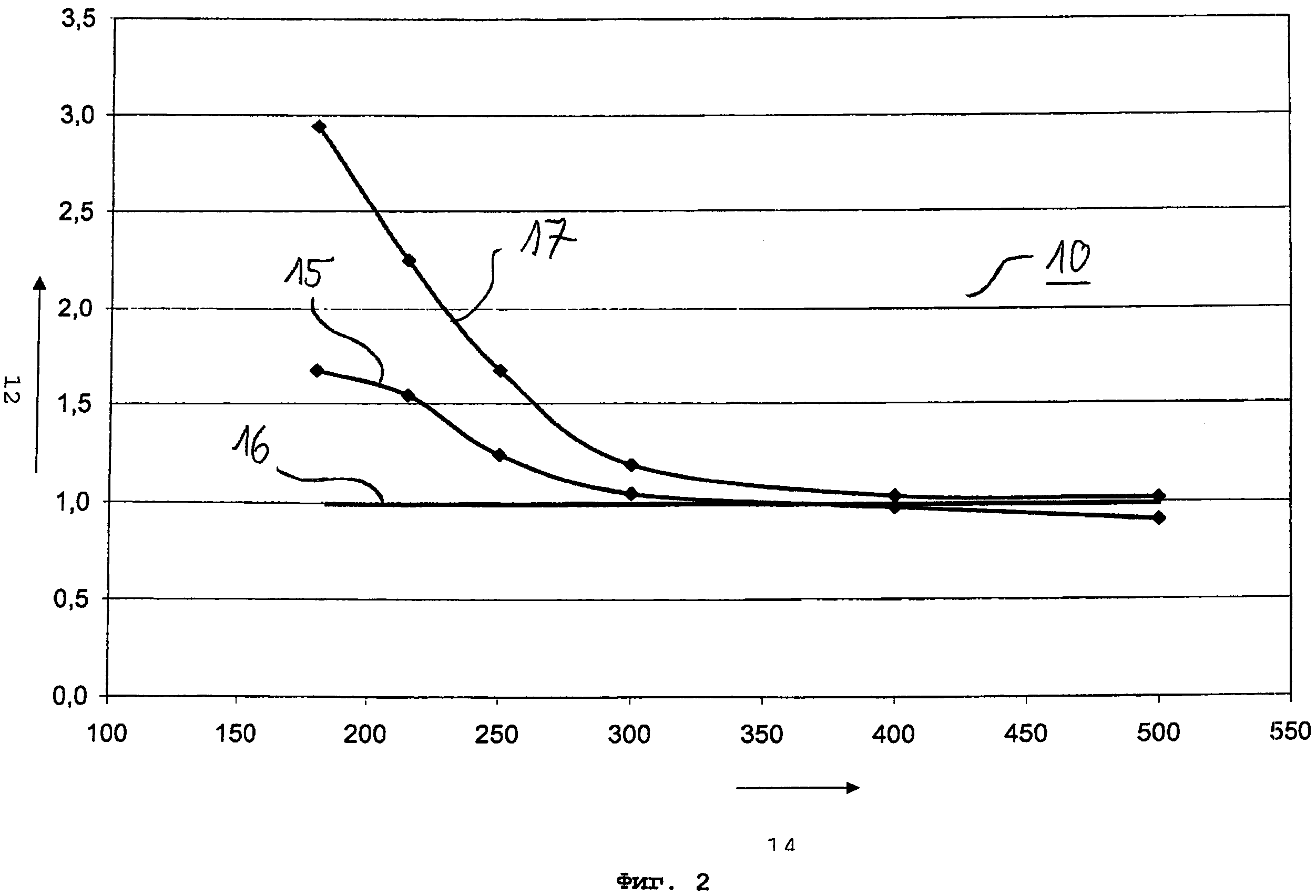
фиг.2 график для различных катализаторов, сравнение зависимой от температуры скорости преобразования для NO в присутствии аммиака.
Пример 1а
Фиг.1 показывает с помощью графической блок-схемы получение SCR-активного цеолитного катализатора согласно иллюстративному варианту осуществления. На первом этапе, 1, порошкообразный Fe-ионообменный синтетический MFI цеолит с долей 3 весовых % железа обрабатывают с получением пластической и свободнотекучей композиции. С этой целью порошкообразный MFI цеолит смешивают со стекловолокном, а также с порошкообразным бомитом, с добавкой целлюлозы, коммерческим пластификатором и полиэтиленоксидом в качестве органического вспомогательного средства, обрабатывают в водном кислом растворе с pH<5 с получением пластической и свободнотекучей смеси. Затем пластическую смесь экструдируют с получением ячеистого тела катализатора, пронизанного каналами и имеющего круглое поперечное сечение с плотностью ячеек 300 cpsi (ячеек на квадратный дюйм). Затем тело катализатора сушат. Катализатор без подложки имеет площадь контакта диаметром около 2,5 см (1 дюйм) и длину растекания около 7 см.
Затем катализатор без подложки, полученный таким путем, подвергают этапу обжига 2. С этой целью тело катализатора помещают в печь в атмосфере N2 для первой термической обработки 3. Тело катализатора нагревают до температуры 600°C и держат там в течение 1,5 часа. Затем тело катализатора охлаждают и извлекают из печи при комнатной температуре.
В ходе первой термической обработки 3 в атмосфере инертного газа целлюлоза и полиэтиленоксид, введенные в качестве органического пластификатора, разлагаются в результате пиролиза до газообразных углеводородов, в результате чего в печи образуется восстановительная углеводородная атмосфера. В этих условиях железо, присутствующее в MFI цеолите, постепенно восстанавливается до железа со степенью окисления +2 или по меньшей мере до дробной степени окисления менее чем +3, и/или дисперсность железа в цеолите повышается. Выбранный температурный профиль достигает такого эффекта, при котором железо в восстановленной форме или высокая дисперсность железа стабилизируется, что осуществляется решающим образом путем влияния углеводородов, присутствующих в атмосфере. Кроме того, термическая обработка выгоняет воду из тела катализатора и обеспечивает затвердение катализаторной композиции. В ходе восстановительного обжига катализаторная композиция в то же время приобретает основной цвет от бледно-желтого до бежевого, что указывает на присутствие железа со степенью окисления +2 и/или повышение дисперсности. Этот цвет может быть замаскирован продуктами разложения органических полимеров, так что тело катализатора выглядит в целом черным.
Затем восстановленный цеолитный катализатор для выполнения второй термической обработки 4 вводят во вторую печь, в которой используемой атмосферой является воздух. Тело катализатора снова доводят там до температуры около 600°C и выдерживают там в течение около 50 минут. В это время продукты разложения, присутствующие в катализаторе, и исходные органические полимеры целлюлозы и пластификатора, все еще присутствующие, окисляются и окончательно удаляются. Катализаторная композиция далее затвердевает. В конце второй термической обработки 4 цеолитный катализатор теперь явно имеет упомянутый основной цвет от бледно-желтого до бежевого.
Затем цеолитный катализатор охлаждают и извлекают из второй печи. Результатом является окончательный цеолитный катализатор, который имеет форму ячеистого катализатора без подложки 5 и получен для применения его в разложении оксидов азота способом SCR.
Пример 1b
В альтернативном варианте термические обработки 3 и 4 выполняют в общей печи. В этом случае при завершении первой термической обработки 3 тело катализатора охлаждают до температуры ниже 400°C, затем восстановительную углеводородную атмосферу откачивают, а в печь вводят воздух. Затем сразу же следует вторая термическая обработка 4, которую проводят аналогично примеру 1а.
Пример 1с
Согласно примеру 1а получают пластическую и свободнотекучую композицию. Тело катализатора, состоящее из кордиерита тех же размеров и той же плотности ячеек, что и инертное тело подложки, покрывают пластической композицией. Затем покрытое тело подложки подвергают следующим этапам 3 и 4 способа согласно примеру 1а. Результатом является покрытое тело катализатора 5'.
В эксперименте катализаторы без подложки 5 и 5', полученные согласно примерам 1а, 1b и 1с, нагревают до 900°C и подвергают потоку воздуха при объемной скорости 10000 л/час в течение 2 часов. Катализаторы без подложки 5 и 5' не проявляют какого-либо изменения цвета в ходе этого. Они сохраняют присущий основной цвет от бледно-желтого до бежевого. Другими словами, железо со степенью окисления +2 и/или высокая дисперсность железа постоянно стабилизируются путем восстановительного обжига согласно первой термической обработке 3. Даже в окислительной атмосфере, такой как воздух, не происходит окисление железа степени окисления +2 до железа степени окисления +3 и не образуются большие кластеры Fe. Любое окисление немедленно привело бы к изменению цвета до ржаво-красного основного цвета, который типичен для железа в степени окисления +3. Этот цвет является типичным для ржавчины, где железо присутствует в основном в форме Fe2O3. То же самое касается присутствующих кластеров оксида железа.
Пример 2
Для сравнения изготавливают цеолитный катализатор, полученный идентично этапу 1 способа примера 1а. Затем его обжигают по традиционной технологии в воздухе при температурах выше 500°C.
Пример 3
Согласно примеру 1а тело катализатора снова экструдируют с круглым поперечным сечением, плотностью ячеек 300 cpsi, с площадью контакта, имеющей диаметр 2,5 см, и длиной растекания около 7 см. Вместо цеолита MFI типа, однако, используемым цеолитом является Fe-ионообменный синтетический цеолит бета типа. Цеолит бета типа отличается от цеолита MFI типа другой характерной трехмерной структурой.
Затем для катализаторов 1а, 2 и 3 определяют каталитическую активность превращения NO в присутствии аммиака. С этой целью каждый из катализаторов 1а, 2 и 3 подвергают потоку стандартного газа, состоящего из азота с долей 600 частей на миллион NO при стандартизированной объемной скорости 25000 л/час. В каждом случае определяют долю NO до и после потока через тело катализатора и используют ее для определения превращения на основе доли NO выше по потоку от катализатора. Аммиак NH4 подают в стандартный газ как восстанавливающее средство со стехиометрическим фактором α=0,9, а именно в незначительном субстехиометрическом количестве по отношению к доле NO. Затем соответствующее превращение определяют для различных температур ниже 300°C.
Тот же эксперимент повторяют для катализатора без подложки с той же геометрией, который включает катализаторную композицию, состоящую из диоксида титана с добавками оксидов вольфрама и ванадия. Этот катализатор далее называют TiMoV катализатором.
Результат исследований показан на фиг.2. График 10 показывает кривые каждого из превращений NO, нормализованных для сравнительного катализатора 2 против температуры 14. График 10 показывает измерения для катализатора 1a (MFI) согласно кривой 15, для катализатора 3 (бета) согласно кривой измерений 17 и для сравнительного катализатора 2 согласно кривой измерений 16. В результате нормализации последняя рассчитывается как прямая линия значения 1.
Согласно графику 10 на фиг.2 очевидно, что катализатор без подложки 1а, полученный восстановительным обжигом, цеолит MFI (кривая измерений 15), в низкотемпературном диапазоне ниже 300°C показывает явное улучшение каталитической активности в отношении селективного каталитического восстановления NO по сравнению с традиционно полученным катализатором из той же композиции. Превращение в этом случае усиливается. Окисленный катализатор без подложки 3, цеолит бета (кривая измерений 17), показывает еще более улучшенную каталитическую активность.
В температурном диапазоне выше 300°C достигнутые превращения NO и каталитические активности катализаторов 1а и 3 приближаются к таковым сравнительного катализатора 2.
Фиг.2 показывает, что катализатор без подложки, полученный согласно вариантам осуществления способа по данному изобретению, обладает превосходной каталитической активностью в отношении селективного каталитического восстановления оксидов азота в низкотемпературном диапазоне ниже 300°C. Постоянная стабилизация железа в степени окисления +2 или в дробной степени окисления менее чем +3 и/или постоянно высокая дисперсность железа в цеолите делает SCR-активный цеолитный катализатор, полученный таким путем, исключительно пригодным в этом отношении для применения при восстановлении оксида азота в отработанных газах двигателей внутреннего сгорания, работающих с избытком воздуха, особенно в случае с дизельным двигателем. Тогда как каталитическая активность в низкотемпературном диапазоне в случае традиционных цеолитных катализаторов принципиально зависит от доли NO2, это не относится к цеолитному катализатору, определенному в данном документе. Фиг.2 показывает исключительную каталитическую активность катализаторов по разложению NO, в частности, при отсутствии NO2. Катализатор окисления, который обычно соединен выше по потоку с традиционными цеолитными катализаторами, более конкретно, также с Fe-ионообменными цеолитными катализаторами, и повышает долю NO2 в выделенных оксидах азота в низкотемпературном диапазоне, таким образом, может полностью обойтись цеолитным катализатором, определенным в данном документе. Это означает не только сохранение конструктивного пространства. Фактически, данное изобретение дает значительное преимущество по себестоимости, поскольку катализаторы окисления обычно должны содержать драгоценные металлы и, следовательно, являются дорогими.
Перечень позиционных обозначений
Реферат
Настоящее изобретение относится к способу получения SCR-активного цеолитного катализатора и к катализатору, полученному этим способом. Описан способ получения указанного катализатора, характеризующийся тем, что на Fe-ионообменный цеолит сначала воздействуют восстановительной углеводородной атмосферой для первой термической обработки (3) в диапазоне от 300 до 600°С, которая снижает степень окисления ионов Fe и/или повышает дисперсность ионов Fe в цеолите, затем на восстановленный цеолит воздействуют окислительной атмосферой для второй термической обработки (4) в диапазоне от 300 до 600°С, которая окислительно удаляет углеводородные остатки и/или остатки углерода, и цеолит обжигают (2) в ходе первой и второй термических обработок (3 и 4) с получением катализатора. Описан SCR-активный катализатор с обожженной катализаторной композицией, включающей Fe-ионообменный цеолит, где ионы Fe присутствуют преимущественно со степенью окисления менее чем +3 и/или с высокой дисперсностью в цеолите, характеризующийся тем, что превращение ионов Fe в ионы с более высокой степенью окисления +3 и/или снижение их дисперсности блокируется. Технический эффект - повышение каталитической активности в отношении селективного восстановления оксидов азота в низкотемпературном диапазоне менее чем 300°С. 3 н. и 16 з.п. ф-лы, 2 ил., 3 пр.
Формула
характеризующийся тем, что
на Fe-ионообменный цеолит сначала воздействуют восстановительной углеводородной атмосферой для первой термической обработки (3) в диапазоне от 300°С до 600°С, которая снижает степень окисления ионов Fe и/или повышает дисперсность ионов Fe в цеолите, затем на восстановленный цеолит воздействуют окислительной атмосферой для второй термической обработки (4) от 300°С до 600°С, которая окислительно удаляет углеводородные остатки и/или остатки углерода, и цеолит обжигают (2) в ходе первой и второй термических обработок (3 и 4) с получением катализатора.
характеризующийся тем, что
температура превышает 500°С в течение периода более чем 50 мин в ходе первой термической обработки (3).
характеризующийся тем, что
цеолит в конце первой термической обработки (3) охлаждают до температуры ниже 400°С.
характеризующийся тем, что
углеводородная атмосфера содержит менее 1 об.% кислорода.
характеризующийся тем, что
первую термическую обработку (3) выполняют в атмосфере инертного газа, в которую подают углеводороды для восстановления.
характеризующийся тем, что
подаваемыми углеводородами являются органические полимеры и/или
биополимеры, которые превращают в газообразные продукты разложения в ходе первой термической обработки (3).
характеризующийся тем, что
подаваемыми углеводородами являются полиэтилены, полигликоли и/или целлюлоза.
характеризующийся тем, что
цеолит предварительно обрабатывают добавками из органического пластификатора с получением свободнотекучей композиции, особенно экструдируемой композиции, и первую термическую обработку (3) выполняют в атмосфере инертного газа, причем органический пластификатор высвобождает углеводороды в атмосферу инертного газа в результате пиролиза.
характеризующийся тем, что
применяемым пластификатором является полиэтиленгликоль, полиэтиленоксид и/или целлюлоза.
характеризующийся тем, что
экструдируемую композицию экструдируют с получением катализатора без подложки (5), а катализатор без подложки (5) подвергают этапам способа.
характеризующийся тем, что
тело подложки (5') покрывают свободнотекучей композицией и покрытое тело подложки (5') подвергают этапам способа.
характеризующийся тем, что
вторую термическую обработку (4) выполняют в воздухе.
характеризующийся тем, что
первую и вторую термические обработки (3 и 4) выполняют в прямой последовательности с обменом газа.
характеризующийся тем, что
применяемым цеолитом является цеолит бета или MFI типа.
характеризующийся тем, что
цеолит содержит от 3 до 7 вес.% железа.
характеризующийся тем, что
превращение ионов Fe в ионы с более высокой степенью окисления +3 и/или снижение их дисперсности блокируется.
характеризующийся тем, что
катализаторная композиция, исходя из бледно-желтого основного цвета, соответствующего низкой степени окисления присутствующих ионов Fe и/или высокой дисперсности, не проявляет какого-либо изменения цвета в ходе термической обработки от 700°С до 900°С с потоком воздуха в течение двухчасового периода.
имеет форму экструдированного катализатора без подложки (5) или форму покрытого тела подложки (5').
Документы, цитированные в отчёте о поиске
Способ и катализатор для восстановления оксидов азота
Способ каталитического восстановления оксидов азота в топочных газах и композиция восстановителя

Комментарии