Улучшенная клеточная композиция и способы ее получения - RU2563518C2
Код документа: RU2563518C2
Чертежи

























Описание
2420-175464RU/052
УЛУЧШЕННАЯ КЛЕТОЧНАЯ КОМПОЗИЦИЯ И СПОСОБЫ ЕЕ ПОЛУЧЕНИЯ
ОПИСАНИЕ
По этой заявке согласно 35 U.S.C. § 119(e) испрашивается приоритет временной заявки на патент США № 61/090577, поданной 20 августа 2008 года, которая таким образом полностью включена в настоящее описание путем ссылки.
1. ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к улучшенным композициям, например, фармацевтическим композициям, включающим клетки, например, стволовые или плацентарные клетки, такие как изолированные адгезивные плацентарные мультипотентные клетки человека, например, плацентарные мультипотентные клетки, описанные в разделе 5.3, или клетки, изолированные из плацентарного перфузата, например, изолированные из плацентарного перфузата клетки, содержащие цельные ядра, и к усовершенствованным способам получения указанных композиций.
2. УРОВЕНЬ ТЕХНИКИ
Клеточные композиции, например, композиции стволовых клеток, стали альтернативной терапией ряда физиологических недостаточностей, например, замены костного мозга. Поэтому существует потребность в улучшенных составах клеток, например, стволовых клеток, которые предназначены для введения индивидуумам, нуждающимся в таких композициях.
3. СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к усовершенствованным способам получения композиций, включающих клетки, например, изолированные плацентарные клетки, такие как плацентарные стволовые клетки, плацентарные мультипотентные клетки, плацентарные клетки, способные разрастаться и дифференцироваться в клетки по меньшей мере двух разных типов, например, в клетки остеогенных и хондрогенных типов, или клетки, выделенные из плацентарного перфузата, например, изолированные из плацентарного перфузата клетки, содержащие цельные ядра, и к композициям, содержащим такие клетки, например, композициям, которые подходят для введения индивидууму. В усовершенствованных способах используются специфические стадии и специфические композиции до-криоконсервационной обработки, криоконсервации и оттаивания клеток. В некоторых вариантах осуществления изобретения усовершенствованные способы снижают или исключают образование скоплений клеток после оттаивания криоконсервированных клеток. В предпочтительных вариантах осуществления изобретения улучшенные композиции включают плацентарные мультипотентные клетки.
В одном варианте осуществления изобретение относится к способу получения композиции, включающему (а) контактирование клеток с раствором, включающим декстран и сывороточный альбумин человека (human serum albumin - HSA), для получения раствора, содержащего клетки; (b) фильтрацию раствора, содержащего клетки, для получения отфильтрованного раствора, содержащего клетки; (с) необязательно разбавление отфильтрованного раствора, содержащего клетки, до примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр раствором первого разбавления, содержащим декстран; и (d) необязательно разбавление отфильтрованного раствора, содержащего клетки, раствором второго разбавления, содержащим декстран. В некоторых вариантах осуществления изобретения стадия (с) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (b) включает более примерно 15×106 клеток на миллилитр, где указанное разбавление на стадии (с) поводится до получения содержания примерно 15×106 клеток на миллилитр. В конкретных вариантах осуществления изобретения стадия (с) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (b) включает более примерно 10±3×106 клеток на миллилитр, где указанное разбавление на стадии (с) проводится до содержания примерно 10±3×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения стадия (с) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (b) включает более примерно 7,5×106 клеток на миллилитр, где указанное разбавление на стадии (с) проводится до достижения содержания примерно 7,5×106 клеток на миллилитр. В специфическом варианте осуществления изобретения раствор стадии (d), включающий декстран, не содержит сывороточный альбумин человека. В специфическом варианте осуществления изобретения отфильтрованная композиция, содержащая клетки, подвергается криоконсервации перед стадией (d). В некоторых вариантах осуществления изобретения, если количество клеток составляет менее примерно 10±3×106 клеток на миллилитр после стадии (а), фильтрация является необязательной. В некоторых вариантах осуществления изобретения, если количество клеток составляет менее примерно 7,5×106 клеток на миллилитр после стадии (а), фильтрация является необязательной.
В некоторых вариантах осуществления изобретения указанный декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% декстрана. В некоторых вариантах осуществления изобретения указанный декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой примерно 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19% или 20% декстрана. Декстран в растворе первого разбавления или растворе второго разбавления может представлять собой декстран любой молекулярной массы, например, декстран молекулярной массы от примерно 1 кДа до примерно 150 кДа, от примерно 1 кДа до примерно 125 кДа, от примерно 1 кДа до примерно 100 кДа, от примерно 1 кДа до примерно 75 кДа, от примерно 1 кДа до примерно 50 кДа или от примерно 1 кДа до примерно 25 кДа. В некоторых вариантах осуществления изобретения молекулярная масса декстрана в растворе первого разбавления или растворе второго разбавления находится в интервале от примерно 1 кДа до примерно 10 кДа, от примерно 30 кДа до примерно 50 кДа или от примерно 60 кДа до примерно 80 кДа. В другом специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой декстран 1. В еще одном специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления и указанном растворе второго разбавления представляет собой декстран 1. В еще одном специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой декстран 70. В еще одном специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления и указанном растворе второго разбавления представляет собой декстран 70. В еще одном специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой декстран 40. В еще одном специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления и указанном растворе второго разбавления представляет собой декстран 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой от 2,5% до 10% декстрана 40. В некоторых вариантах осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% декстрана 40. В некоторых вариантах осуществления изобретения указанный декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой примерно 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19% или 20% декстрана 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления представляет собой 5,0% декстрана 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления представляет собой 5,5% декстрана 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе второго разбавления представляет собой 10% декстрана 40.
В других вариантах осуществления изобретения указанный раствор первого и/или второго разбавления помимо декстрана или вместо него может включать полисахарид. Например, в некоторых вариантах осуществления изобретения указанные растворы первого и/или второго разбавления включают мальтодекстран (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% мальтодекстрина), трегалозу (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% трегалозы) или гетакрахмал (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% гетакрахмала). В других вариантах осуществления изобретения указанные растворы первого и/или второго разбавления включают сахарозу (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% сахарозы), гепарин (например, 55 USP единиц/мл гепарина) или гликоген (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% гликогена). В конкретном варианте осуществления изобретения указанные растворы первого и/или второго разбавления в добавление к декстрану или вместо него включают мальтодекстран. В еще одном конкретном варианте осуществления изобретения указанные растворы первого и/или второго разбавления в добавление к декстрану или вместо него включают трегалозу. В еще одном конкретном варианте осуществления изобретения указанный раствор первого и/или второго разбавления в добавление к декстрану или вместо него включает гетакрахмал.
В другом специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно от 1 до 17% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16% или 17% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно от 4 до 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно 3,125% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно 5% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно 16,875% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, содержащем HSA, представляет собой примерно от 1 до 17% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16% или 17% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно от 4 до 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 3,125% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 5% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 16,875% HSA.
В других вариантах осуществления изобретения бычий сывороточный альбумин (BSA) (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% BSA) или зародышевая телячья сыворотка (FBS) (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% FBS) могут использоваться в дополнение или вместо HSA в указанном растворе.
В некоторых вариантах осуществления изобретение соотношение HSA и декстрана, например, декстрана 1, декстрана 40 или декстрана 70, в первом растворе находится в интервале от примерно 6:1 HSA:декстран до примерно 1:2,6 HSA:декстран. В некоторых вариантах осуществления изобретение соотношение HSA и декстрана составляет примерно 6:1, 5,5:1, 5:1, 4,5:1, 4:1, 3,5:1, 3:1, 2,5:1, 2,0:1, 1,5:1, 1:1, 1:1,5, 1:2 или 1:2,6 HSA:декстран. В некоторых вариантах осуществления изобретения соотношение HSA и декстрана, например, декстрана 1, декстрана 40 или декстрана 70, в первом растворе составляет примерно 3,13% HSA/8,25% декстрана. В некоторых вариантах осуществления изобретения соотношение HSA и декстрана, например, декстрана 1, декстрана 40 или декстрана 70, в первом растворе составляет примерно 16,88% HSA/2,75% декстрана. В конкретных вариантах осуществления изобретения соотношение HSA и декстрана, например, декстрана 1, декстрана 40 или декстрана 70, в первом растворе составляет примерно 10% HSA/5,5% декстран, например, декстрана 1, декстрана 40 или декстрана 70.
В еще одном специфическом варианте осуществления изобретения указанный раствор на стадии (а) или раствор, содержащий клетки, включает криопротектор. В более специфическом варианте осуществления изобретения указанный криопротектор представляет собой диметилсульфоксид (ДМСО). В конкретном варианте осуществления изобретения раствор, указанный в стадии (а), включает от примерно 1% до примерно 15%, от примерно 2,5% до примерно 15%, от примерно 2,5% до примерно 10%, от примерно 5% до примерно 15%, от примерно 5% до примерно 10% или от примерно 10% до примерно 15% ДМСО. В конкретном варианте осуществления изобретения раствор, упомянутый в стадии (а), включает примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% ДМСО. В еще одном конкретном варианте осуществления изобретения раствор, упомянутый в стадии (а), включает примерно 5% ДМСО. В другом специфическом варианте осуществления изобретения указанный раствор первого разбавления дополнительно включает криопротектор. В более специфическом варианте осуществления изобретения указанный криопротектор представляет собой диметилсульфоксид (ДМСО). В конкретном варианте осуществления изобретения указанный раствор первого разбавления дополнительно включает от примерно 1% до примерно 15%, от примерно 2,5% до примерно 15%, от примерно 2,5% до примерно 10%, от примерно 5% до примерно 15%, от примерно 5% до примерно 10% или от примерно 10% до примерно 15% ДМСО. В конкретном варианте осуществления изобретения указанный раствор первого разбавления дополнительно включает примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% ДМСО. В конкретном варианте осуществления изобретения указанный раствор первого разбавления дополнительно включает примерно 5% ДМСО.
В специфическом варианте осуществления изобретения указанный раствор первого разбавления включает примерно 5,5% декстрана 40, примерно 10% HSA и примерно 5% ДМСО.
В конкретном варианте осуществления изобретения указанный способ приводит к получению композиции, содержащей клетки и примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75%, или 10% декстрана, например, декстрана 1, декстрана 40 или декстрана 70. В другом конкретном варианте осуществления изобретения указанные способ приводит к получению композиции, содержащей клетки и примерно 7,5% до примерно 9% декстрана, например, декстрана 40. В другом, специфическом варианте осуществления изобретения указанный способ приводит к получению композиции, содержащей от примерно 1,5×106 клеток на миллилитр до примерно 3,75×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения указанный способ приводит к получению композиции, содержащей от примерно 1,0±0,3×106 клеток на миллилитр до примерно 5,0±1,5×106 клеток на миллилитр. В других специфических вариантах осуществления изобретения указанный способ приводит к получению композиции, содержащей от примерно 1,0×106 клеток на миллилитр до 15×106 клеток на миллилитр, например, в интервале от примерно 7,5×106 клеток на миллилитр до примерно 15×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения указанный способ приводит к получению композиции, содержащей от примерно 1% HSA до примерно 10% HSA.
Настоящее изобретение дополнительно относится к способу получения композиции, включающему (а) фильтрацию множества клеток в растворе, включающем 5,5% декстрана 40 и 10% HSA, через 70 мкм - 150 кМ фильтр для получения отфильтрованного раствора, содержащего клетки; (b) необязательно разбавление отфильтрованного раствора, содержащего клетки, 5,5% декстраном 40, 10% HSA и 5% ДМСО, до примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр; (с) криоконсервацию клеток; (d) оттаивание клеток; (e) разбавление отфильтрованного раствора, содержащего клетки, 10% декстраном 40 для получения указанной композиции. В некоторых вариантах осуществления изобретения стадия (b) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (а) включает более примерно 15×106 клеток на миллилитр, где указанное разбавлении на стадии (b) проводится до достижения содержания 15×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения, если отфильтрованный раствор, содержащий клетки, на стадии (а) включает менее примерно 15×106 клеток на миллилитр, фильтрация является необязательной. В некоторых вариантах осуществления изобретения стадия (b) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (а) включает более примерно 10±3×106 клеток на миллилитр, где указанное разбавление на стадии (b) проводится до содержания примерно до 10±3×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения, если отфильтрованный раствор, содержащий клетки, на стадии (а) включает менее примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной. В некоторых вариантах осуществления изобретения стадия (b) выполняется, когда отфильтрованный раствор, содержащий клетки, на стадии (а) включает более примерно 7,5×106 клеток на миллилитр, где указанное разбавление на стадии (b) проводится до достижения содержания примерно 7,5×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения, если отфильтрованный раствор, содержащий клетки, на стадии (а) включает менее примерно 7,5×106 клеток на миллилитр, фильтрация является необязательной. В некоторых вариантах осуществления изобретения стадия (е) включает разбавление отфильтрованного раствора содержащего клетки, в соотношении от 1:1 до 1:5 (об./об.) 10% декстраном 40. В некоторых вариантах осуществления изобретения стадия (е) включает разбавление отфильтрованного раствора, содержащего клетки, в соотношении от 1:1 до 1:11 (об./об.) 10% декстраном 40. В более специфическом варианте осуществления изобретения раствор стадии (а), содержащий клетки, дополнительно включает криопротектор, например, ДМСО, например, от примерно 2% до примерно 15% ДМСО. В конкретном варианте осуществления изобретения указанный раствор стадии (а) дополнительно включает примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% ДМСО. В конкретном варианте осуществления изобретения указанный раствор на стадии (а) дополнительно включает примерно 5% ДМСО. В предпочтительном варианте осуществления изобретения фильтр на стадии (а) представляет собой от 70 до 100 мкм фильтр.
В еще одном варианте осуществления изобретение относится к способу получения композиции, включающему (а) центрифугирование множества клеток для сбора клеток; (b) повторное суспендирование клеток в 5,5% декстране 40; (с) центрифугирование клеток для сбора клеток; (d) повторное суспендирование клеток в 5,5% растворе декстрана 40, который включает 10% HSA, для получения раствора, содержащего клетки; (е) фильтрацию раствора, содержащего клетки, через 40 мкм - 150 мкм фильтр для получения раствора, содержащего клетки; (f) необязательно разбавление отфильтрованного раствора, содержащего клетки, 5,5% раствором декстрана 40, содержащим 10% HSA и криопротектор, например, ДМСО, например, 5% ДМСО, до примерно от 1 до 50×106, 1 до 40×106, 1 до 30×106, 1 до 20×106, 1 до 15×106 или 1 до 10×106 клеток на миллилитр; (g) криоконсервацию клеток; (h) оттаивание клеток; (i) разбавление раствора, содержащего клетки, в соотношении от 1:1 до 1:11 (об./об.) 10% раствором декстрана 40 для получения указанной композиции. В некоторых вариантах осуществления изобретения стадия (f) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (е) включает более чем примерно 15×106 клеток на миллилитр, где указанное разбавление на стадии (f) проводится до содержания примерно 15×106 клеток на миллилитр. В конкретных вариантах осуществления изобретения стадия (f) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (е) содержит более примерно 10±3×106 клеток на миллилитр, где указанное разбавление на стадии (f) проводится до достижения содержания примерно 10±3×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения стадия (е) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (е) включает более 7,5×106 клеток на миллилитр, где указанное разбавление на стадии (f) проводится до достижения содержания примерно 7,5×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения, если количество клеток составляет менее примерно 10±3×106 клеток на миллилитр после стадии (d), фильтрация является необязательной. В некоторых вариантах осуществления изобретения, если количество клеток составляет менее примерно 7,5×106 клеток на миллилитр после стадии (d), фильтрация является необязательной. В конкретном варианте осуществления изобретения, если указанное повторное суспендирование на стадии (d) должно привести к получению раствора, содержащего менее примерно 10±3×106 клеток на миллилитр, упомянутый в стадии (d) раствор включает криопротектор, например, ДМСО, например, от примерно 2% до примерно 15% ДМСО, и стадия (f) не проводится. В предпочтительном варианте осуществления изобретения фильтр на стадии (е) представляет собой 70 мкм - 100 мкм фильтр.
Настоящее изобретение также относится к способу получения композиции, включающему (а) фильтрацию раствора, включающему изолированные плацентарные клетки, 5,5% декстрана 40 и 10 сывороточного альбумина человека (HSA) с помощью фильтра, который удаляет видимые клеточные сгустки для получения отфильтрованного раствора, содержащего изолированные плацентарные клетки; (b) необязательно разбавление указанного отфильтрованного раствора, содержащего изолированные плацентарные клетки, количеством раствора, включающего 5,5% декстрана 40, 10% HSA и 5% диметилсульфоксида (ДМСО), достаточным для получения отфильтрованного раствора, содержащего изолированные плацентарные клетки, примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр; и (с) разбавление указанного отфильтрованного раствора, содержащего изолированные плацентарные клетки, 10% раствором декстрана 40 для получения указанной композиции. В некоторых вариантах осуществления изобретения стадия (b) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (а) включает более чем примерно 15×106 клеток на миллилитр. В конкретных вариантах осуществления изобретения стадия (b) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (а) включает более чем примерно 10±3×106 клеток на миллилитр, где указанное разбавление на стадии (b) проводится до достижения содержания примерно 3×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения стадия (b) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (а) включает более чем примерно 7,5×106 клеток на миллилитр, где указанное разбавление на стадии (b) проводится до получения содержания примерно 7,5×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения стадия (с) включает разбавление указанного отфильтрованного раствора, содержащего изолированные плацентарные клетки, 10% раствором декстрана 40 в соотношении от примерно 1:1 до примерно 1:11 раствор изолированных клеток:декстран 40 (об./об.). В некоторых вариантах осуществления изобретения стадия (с) включает разбавление указанного отфильтрованного раствора, содержащего изолированные плацентарные клетки, 10% раствором декстрана 40 в соотношении от примерно 1:1 до примерно 1:5 раствор, содержащий изолированные плацентарные клетки:декстран 40 (об./об.). В некоторых вариантах осуществления изобретения, если количество клеток составляет менее чем примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной. В некоторых вариантах осуществления изобретения, если количество клеток после стадии (а) составляет менее чем примерно 7,5×106 клеток на миллилитр, фильтрация является необязательной. В специфическом варианте осуществления изобретения указанный фильтр представляет собой 70 мкм фильтр. В другом специфическом варианте осуществления изобретения указанный фильтр представляет собой 100 мкм фильтр. В еще одном специфическом варианте осуществления изобретения фильтр на стадии (а) представляет собой 70 мкм - 100 мкм фильтр.
В специфическом варианте осуществления любого из указанных способов композиция представляет собой фармацевтическую композицию.
В другом специфическом варианте осуществления любого из указанных выше способов способ дополнительно включает концентрирование полученной клеточной композиции от примерно 5×106 клеток на миллилитр до 1×108 клеток на миллилитр. Такая композиция применяется, например, для подкожного введения композиции индивидууму, нуждающемуся в таком введении.
В соответствии с другим аспектом, настоящее изобретение относится к композициям, например, фармацевтическим композициям, включающим клетки, например, стволовые клетки, изолированные плацентарные клетки, например, плацентарные стволовые клетки или плацентарные мультипотентные клетки. В некоторых вариантах осуществления изобретения композиции получены любым из способов, описанных в изобретении. В одном варианте осуществления изобретение относится к композиции, например, раствору, включающей множество клеток, например, стволовых клеток, изолированных плацентарных клеток, например, плацентарных стволовых клеток или плацентарных мультипотентных клеток, где указанная композиция включает от примерно 1,0±0,3×106 клеток на миллилитр до примерно 5,0±1,5×106 клеток на миллилитр, где указанная композиция не содержит видимых скопления клеток (т.е. не содержит клеточных макроскоплений) или по существу не содержит видимых скоплений клеток. В некоторых других вариантах осуществления изобретения композиция включает от примерно 1,0×106 клеток на миллилитр до 15×106 клеток на миллилитр, например, от примерно 7,5×106 клеток на миллилитр до примерно 15×106 клеток на миллилитр. В некоторых других вариантах осуществления изобретения композиция включает менее примерно 20×106 клеток на миллилитр.
В некоторых вариантах осуществления изобретения указанная композиция включает примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% декстрана, например, декстрана 1, декстрана 40 или декстрана 70. В специфическом варианте осуществления изобретения указанная композиция включает от примерно 7,5% до примерно 9% декстрана 40. В специфическом варианте осуществления изобретения указанная композиция включает примерно 5,5% декстрана 40.
В других вариантах осуществления изобретения указанная композиция, помимо декстрана или вместо него, включает полисахариды. В некоторых вариантах осуществления изобретения полисахарид представляет собой полимер глюкозы, который не содержит неглюкозных сахаридных фрагментов. В других вариантах осуществления изобретения указанная композиция включает мальтодекстрин (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% мальтодекстрина), трегалозу (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% трегалозы) или гетакрахмал (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% гетакрахмала). В других вариантах осуществления изобретения указанная композиция включает сахарозу (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% сахарозы), гепарин (например, 55 USP/мл гепарина) или гликоген (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75%, или 10% гликогена). В конкретном варианте осуществления изобретения указанная композиция, в дополнение к декстрану или вместо него, включает мальтодекстран. В другом конкретном варианте осуществления изобретения указанная композиция, в дополнение к декстрану или вместо, него включает трегалозу. В еще одном конкретном варианте осуществления изобретения указанная композиция включает, в дополнение к декстрану или вместо него, гетакрахмал.
В еще одном специфическом варианте осуществления изобретения указанная композиция включает от примерно 1% до примерно 17% HSA. В некоторых вариантах осуществления изобретения указанная композиция включает примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16% или примерно 17% HSA. В некоторых вариантах осуществления изобретения указанная композиция включает примерно 3,125% HSA. В некоторых вариантах осуществления изобретения указанная композиция включает примерно 5% HSA. В некоторых вариантах осуществления изобретения указанная композиция включает примерно 10% HSA. В некоторых вариантах осуществления изобретения указанная композиция включает примерно 16,875% HSA.
В других вариантах осуществления изобретения указанные композиции, помимо HSA или вместо него, включают бычий сывороточный альбумин (BSA) (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% BSA) или зародышевую телячью сыворотку (FBS) (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% FBS).
В некоторых вариантах осуществления изобретения указанная композиция включает криопротектор, например, ДМСО, например, от примерно 1% до примерно 15% ДМСО. В некоторых вариантах осуществления изобретения указанная композиция включает от примерно 1% до примерно 5% ДМСО. В некоторых вариантах осуществления изобретения указанная композиция включает от примерно 1% до примерно 15%, от примерно 2,5% до примерно 15%, от примерно 2,5% до примерно 10%, от примерно 5% до примерно 15%, от примерно 5% до примерно 10% или от примерно 10% до примерно 15% ДМСО. В некоторых вариантах осуществления изобретения указанная композиция включает примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% ДМСО. В конкретном варианте осуществления изобретения композиция включает примерно 5% ДМСО.
В специфическом варианте осуществления изобретения указанные клетки были подвергнуты криозащите и затем оттаиванию. В другом специфическом варианте осуществления изобретения указанные клетки были отфильтрованы через 70 мкм - 100 мкм фильтр. В еще одном специфическом варианте осуществления изобретения указанная композиция не содержит видимых скоплений клеток. В еще одном специфическом варианте осуществления изобретения указанная композиция включает скопления клеток в количестве менее примерно 200 скоплений на 106 клеток, где указанные скопления клеток видны только под микроскопом, например, под световым микроскопом. В еще одном специфическом варианте осуществления изобретения указанная композиция включает скопления клеток в количестве менее примерно 150 скоплений на 106 клеток, где указанные клеточные скопления различимы только под микроскопом, например, под световым микроскопом. В другом специфическом варианте осуществления изобретения указанная композиция включает скопления клеток в количестве менее примерно 100 скоплений на 106 клеток, где указанные клеточные скопления видны только под микроскопом, например, под световым микроскопом.
В специфическом варианте любого способа или композиций, описанных в изобретении, клетки представляют собой стволовые клетки, например, стволовые клетки, изолированные из послеродовой плаценты человека, которая была дренирована от крови. В некоторых вариантах осуществления изобретения такие клетки были культивированы. В другом специфическом варианте осуществления любого из описанного выше вариантов клетки представляют собой адгезивные клетки, то есть клетки, которые прикреплены к поверхности культуры ткани, например, культуры ткани пластика (без покрытия или с покрытием, например, из фибронектина, ламинина или т.п.). Примеры адгезивных клеток включают, например, адгезивные плацентарные стволовые клетки, как описано в настоящем изобретении; мезенхимальные стволовые клетки, полученные из костного мозга, фибробласты или т.п. В еще одном варианте осуществления изобретения клетки представляют собой клетки человека.
В еще одном варианте осуществления изобретения указанные клетки представляют собой клетки, полученные (например, изолированные) из плацентарного перфузата. В более специфическом варианте осуществления изобретения указанные клетки представляют собой ядросодержащие клетки, например, клетки, содержащие цельные ядра и полученные из плацентарного перфузата. В некоторых вариантах осуществления изобретения плацента, из которой клетки, содержащие цельные ядра, получены перфузией, дренирована от крови и подвергнута перфузии для удаления остаточной крови перед перфузией для сбора плацентарных клеток, содержащих цельные ядра. В определенных других вариантах осуществления изобретения плацента, из которой перфузией получены клетки, содержащие цельные ядра, дренирована от крови, но не подвергалась перфузии для удаления остаточной крови перед перфузией для сбора плацентарных клеток, содержащих цельные ядра. В некоторых других вариантах осуществления изобретения плацента, из которой перфузией получены плацентарные клетки с цельным ядром, не дренировалась от крови и не подвергалась перфузии для удаления остаточной крови перед перфузией для сбора плацентарных клеток, содержащих цельные ядра.
В другом специфическом варианте осуществления способа указанные клетки представляют собой стволовые клетки. В более специфических вариантах осуществления изобретения стволовые клетки представляют собой дифференцированные стволовые клетки, соматические стволовые клетки, эмбриональные стволовые клетки, эмбриональные зародышевые клетки, стволовые клетки пуповины, стволовые клетки амниотической жидкости, стволовые клетки, полученные из костного мозга, мезенхимные стволовые клетки, полученные из пуповинной крови, мезенхимальные стволовые клетки, полученные из периферической крови, мезенхимальные стволовые клетки, полученные из жировой ткани, или мезенхимальные стволовые клетки, полученные из надкостницы. В еще одном варианте осуществления изобретения указанные клетки представляют собой природные клетки-киллеры.
В еще одном специфическом варианте осуществления изобретения указанные клетки представляют собой изолированные плацентарные клетки. В некоторых вариантах осуществления изобретения изолированные плацентарные клетки представляют собой изолированные плацентарные стволовые клетки. В определенных других вариантах осуществления изобретения изолированные плацентарные клетки представляют собой изолированные плацентарные мультипотентные клетки.
В некоторых вариантах осуществления изобретения изолированные плацентарные клетки представляют собой изолированные плацентарные стволовые клетки. В определенных других вариантах осуществления изобретения изолированные плацентарные клетки представляют собой изолированные плацентарные мультипотентные клетки. В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD34-, CD10+ и CD105+ клетки, как определено проточной цитометрией. В более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки представляют собой плацентарные стволовые клетки. В еще одном более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки представляют собой мультипотентные плацентарные клетки. В еще одном специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки обладают потенциалом дифференцироваться в клетки неврального фенотипа, клетки остеогенного фенотипа или клетки хондрогенного фенотипа. В более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой CD200+. В еще одном более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой CD90+ или CD45-, как определено проточной цитометрией. В другом более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой CD90+ или CD45-, как определено проточной цитометрией. В еще более специфическом варианте осуществления изобретения CD34-, CD10+, CD105+, CD200+, плацентарные клетки дополнительно представляют собой CD90+ или CD45- плацентарные клетки. В еще одном более специфическом варианте осуществления изобретения CD34-, CD10+, CD105+, CD200+, CD90+, CD45- дополнительно представляют собой CD80- и CD86-, как определено проточной цитометрией.
В более специфическом варианте осуществления изобретения CD34-, CD10+, CD105+ клетки дополнительно представляют собой клетки одного или нескольких фенотипов из CD29+, CD38-, CD44+, CD54+, CD80-, CD86-, SH3+ или SH4+. В еще одном более специфическом варианте осуществления изобретения клетки дополнительно представляют собой CD44+. В специфическом варианте любых из выделенных CD34-, CD10+, CD105+ плацентарных клеток, указанных выше, клетки дополнительно представляют собой клетки одного или несколько фенотипов из CD117-, CD133-, KDR- (VEGFR2-), HLA-A,B,C+, HLA-DP,DQ,DR- и/или лиганда-1 запрограммированной гибели (Programmed Death-1 Ligand - (PDL1)+).
В более специфических вариантах осуществления изобретения изолированные плацентарные клетки представляют собой CD200+ и HLA-G+; CD73+, CD105+ и CD200+; CD200+ и OCT-4+; CD73+, CD105+ и HLA-G+; CD73+ и CD105+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции плацентарных клеток, включающей указанные изолированные плацентарные клетки, когда указанная популяция культивирована в условиях, дающих возможность образованию эмбриоидоподобного тельца; или OCT-4+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции плацентарных клеток, включающей изолированные плацентарные клетки, когда указанная популяция культивируется в условиях, дающих возможность образованию эмбриоидоподобных телец; или любые их сочетания. В специфическом варианте осуществления изобретения указанные CD200+, HLA-G+ плацентарные клетки представляют собой CD34-, CD38-, CD45-, CD73+ и CD105+. В другом специфическом варианте осуществления изобретения указанные CD73+, CD105+и CD200+ плацентарные клетки представляют собой CD34-, CD38-, CD45- и HLA-G+. В другом специфическом варианте осуществления изобретения указанные CD200+, OCT-4+ плацентарные клетки представляют собой CD34-, CD38-, CD45-, CD73+, CD105+ и HLA-G+. В еще одном специфическом варианте осуществления изобретения указанные CD73+, CD105+ и HLA-G+плацентарные клетки представляют собой CD34-, CD45-, OCT-4+ и CD200+. В еще одном специфическом варианте осуществления изобретения указанные CD73+ и CD105+ плацентарные клетки представляют собой OCT-4+, CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки представляют собой CD73+, CD105+, CD200+, CD34-, CD38- и CD45-.
В некоторых вариантах осуществления изобретения изолированные плацентарные клетки представляют собой клетки одного или нескольких фенотипов, выбранных из CD10+, CD29+, CD34-, CD38-, CD44+, CD45+, CD54+, CD80-, CD86-, CD90+, CD117-, CD133-, CD200+, SH2+, SH3+, SH4+, SSEA3-, SSEA4-, OCT-4+, MHC-I+, KDR- (VEGFR2-), HLA-A,B,C+, HLA-DP,DQ,DR-, PDL1+или ABC-p+, где АВС-р представляет собой плацента-специфический АВС белок-переносчик (известный также как белок устойчивости рака молочной железы (breast cancer resistance protein - BCRP) и как белок устойчивости к митоксантрону (mitoxantrone resistance protein - MXR)). В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD10+, CD29+, CD34-, CD38-, CD44+, CD45-, CD54+, CD90+, SH2+, SH3+, SH4+, SSEA3-, SSEA4-и OCT-4+. В другом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD10+, CD29+, CD34-, CD38-, CD45-, CD54+, SH2+, SH3+ и SH4+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD10+, CD29+, CD34-, CD38-, CD45-, CD54+, SH2+, SH3+, SH4+ и OCT-4+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD10+, CD29+, CD34-, CD38-, CD44+, CD45-, CD54+, CD90+, HLA-1+, SH2+, SH3+, SH4+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой ОСТ-4+ и АВС-р+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой SH2+, SH3+, SH4+ и OCT-4+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+, CD34-, SSEA3- и SSEA4-. В специфическом варианте осуществления изобретения указанные OCT-4+, CD34-, SSEA3- и SSEA4- клетки дополнительно представляют собой CD10+, CD29+, CD34-, CD44+, CD45-, CD54+, CD90+, SH2+, SH3+ и SH4+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой ОСТ-4+ и CD34- и либо SH3+ либо SH4+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD34- и либо CD10+, CD29+, CD44+, CD54+, CD90+, либо OCT-4+. В некоторых вариантах осуществления изобретения изолированные плацентарные клетки представляют собой CD10+, CD34-, CD105+ и CD200+.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в способах обработки, описанных в изобретении, представляют собой клетки одного или несколько фенотипов, выбранных из CD10+, CD29-, CD44+, CD45-, CD54/ICAM-, CD62-E-, CD62-L-, CD62-P-, CD80-, CD86-, CD103-, CD104-, CD105+, CD106/VCAM+, CD144/VE-кадгеринlow, CD184/CXCR4-, β2-микроглобулинlow, MHC-Ilow, MHC-II-, HLA-Glow и/или PDL1low. В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой по меньшей мере CD29- и CD54-. В другом специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой по меньшей мере CD44+ и CD106+. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой по меньшей мере CD29+.
В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки экспрессируют один или несколько генов при обнаружимо более высоком уровне, чем эквивалентное количество мезенхимальных стволовых клеток, полученных из костного мозга, где указанный один или несколько генов представляют собой один или несколько генов, выбранных из ACTG2, ADARB1, AMIGО2, ARTS-1, B4GALT6, BCHE, C11orf9, CD200, COL4A1, COL4A2, CPA4, DMD, DSC3, DSG2, ELOVL2, F2RL1, FLJ10781, GATA6, GPR126, GPRC5B, ICAM1, IER3, IGFBP7, IL1A, IL6, IL18, KRT18, KRT8, LIPG, LRAP, MATN2, MEST, NFE2L3, NUAK1, PCDH7, PDLIM3, PKP2, RTN1, SERPINB9, ST3GAL6, ST6GALNAC5, SLC12A8, TCF21, TGFB2, VTN и ZC3H12A, и где указанные мезенхимальные стволовые клетки, полученные из костного мозга, подвергались количеству пассажей в культуре, эквивалентному количеству пассажей, которому подвергались указанные изолированные плацентарные клетки. В более специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки экспрессируют указанные один или несколько генов, когда культивируются с получением от примерно 3 до примерно 35 удвоений популяций в среде, включающей 60% среду Игла, модифицированную по Дульбекко (DMEM)-LG (предпочтительно от Gibco), и 40% MCDB-201 (предпочтительно от Sigma); 2% зародышевую телячью сыворотку (предпочтительно от Hycline Labs.); 1× инсулин-трансферрин-селен (ITS); 1× линолевую кислоту - бычий сывороточный альбумин (LA-BSA); 10-9М дексаметасона (предпочтительно от Sigma); 10-4 М 2-фосфата сорбиновой кислоты (предпочтительно от Sigma); 10 нг/мл эпидермального фактора роста (предпочтительно от R&D Systems); и 10 нг/мл тромбоцитарного фактора роста (platelet-derived growth factor - PDGF-BB) (предпочтительно от R&D Systems). В более специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки экспрессируют указанные один или несколько генов, когда культивируются с получением от примерно 3 до примерно 35 удвоений популяции в среде, включающей 60% DMEM-LG (предпочтительно от Gibco) и 40% MCDB-201 (предпочтительно от Sigma); 2% зародышевой телячьей сыворотки (предпочтительно от Hycline Labs.); 1× инсулин-трансферрин-селен (ITS); 1× линолевую кислоту - бычий сывороточный альбумин (LA-BSA); 10-9М дексаметасона (предпочтительно от Sigma); 10-4 М 2-фосфата аскорбиновой кислоты (предпочтительно от Sigma); 10 нг/мл эпидермального фактора роста (предпочтительно от R&D Systems); и 10 нг/мл тромбоцитарного фактора роста (PDGF-BB) (предпочтительно от R&D Systems).
В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки экспрессируют нейротрофический фактор роста, полученный из глиальных клеток нейротрофических факторов роста (glial cell derived neurotrophic factor - GDNF), нейтротрофический фактор роста, полученный из мозга (brain-derived neurotrophic factor - BDNF), гепатоцитный фактор роста (hepatocyte growth factor - HGF), плацентарный фактор роста (placental growth factor - PGF) и эндотелиальный фактор роста сосудов (vascular endothelial growth factor - VEGF).
В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки находятся в популяции клеток, в которой по меньшей мере 50% клеток составляют указанные изолированные плацентарные клетки. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки находятся в популяции клеток, в которой по меньшей мере 70% клеток составляют указанные изолированные плацентарные клетки. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки находятся в популяции клеток, в которой по меньшей мере 80% клеток составляют указанные изолированные плацентарные клетки. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки находятся в популяции клеток, в которой по меньшей мере 90% клеток составляют указанные изолированные плацентарные клетки. В некоторых других вариантах осуществления изобретения плацентарные клетки в указанной популяции клеток по существу свободны от клеток, имеющих материнских генотип; например, по меньшей мере 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98% или 99% плацентарных клеток в указанной популяции имеет фетальный генотип, т.е. являются фетальными по происхождению. В некоторых других вариантах осуществления изобретения популяция клеток, включающая указанные плацентарные клетки, по существу свободна от клеток, имеющих материнский генотип; например, по меньшей мере 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98% или 99% клеток в указанной популяции имеют фетальный генотип, то есть являются фетальными по происхождению.
В некоторых вариантах осуществления изобретения изолированные плацентарные клетки представляют собой CD34+ плацентарные клетки, например, гемопоэтические стволовые клетки. Такие клетки могут быть получены из плацентарной ткани, например, из плаценты, которая была дренирована от пуповинной крови и подвергнута перфузии для удаления остаточной крови. В некоторых вариантах осуществления изобретения CD34+ плацентарные клетки представляют собой CD38+. В некоторых других вариантах осуществления изобретения CD34+ плацентарные клетки представляют собой CD38-. В некоторых других вариантах осуществления изобретения CD34+ плацентарные клетки представляют собой CD45+. В специфическом варианте осуществления изобретения плацентарные клетки представляют собой CD34+, CD38- и CD45+.
В любом из описанных выше вариантов изолированных плацентарных клеток изолированные плацентарные клетки обычно не дифференцируются в процессе культивирования в ростовой среде, то есть в среде, приготовленной для способствования пролиферации, например, в процессе пролиферации в ростовой среде. В специфическом варианте осуществления изобретения указанным изолированным плацентарным клеткам не требуется питающий подслой для пролиферации. В другом специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки не дифференцируются в культуре в результате отсутствия в культуре питающего подслоя.
В еще одном более специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки получены перфузией послеродовой плаценты, которая была дренирована от крови и подвергнута перфузии для удаления остаточной крови; дренирована от крови, но не подвергнута перфузии для удаления остаточной крови; или не подвергалась ни дренированию от крови, ни перфузии для удаления остаточной крови. В другом более специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки получены физическим и/или ферментативным разрушением плацентарной ткани.
В некоторых вариантах осуществления указанного выше способа изолированные плацентарные клетки являются отфильтрованными и криозащищенными, как часть структуры банка плацентарных клеток. Например, изолированные плацентарные клетки являются выделенными из плаценты или плацентарной ткани и после культивирования снова суспендированы в растворе, включающем, например, декстран, например, декстран 40, например, 5,5% декстрана 40. В более специфических вариантах осуществления раствор дополнительно включает HSA и/или ДМСО в препарате для криоконсервации. Криоконсервированные изолированные плацентарные клетки в банке клеток, при необходимости, оттаиваются и разбавляются, например, раствором, включающем 10% декстрана 40, как описано в настоящем изобретении. В некоторых вариантах осуществления изобретения способ фильтрации и разбавления, описанный в настоящем изобретении, не является частью первичного выделения изолированных плацентарных клеток.
В некоторых вариантах осуществления указанные изолированные плацентарные клетки получены перфузией послеродовой плаценты, которая была дренирована от крови и подвергнута перфузии для удаления остаточной крови. В другом более специфическом варианте указанные изолированные плацентарные клетки получены физической и/или ферментативной деструкцией плацентарной ткани.
4. КРАТКОЕ ОПИСАНИЕ ФИГУР
Фиг.1 представляет диаграмму трехкомпонентной системы, показывающую состав разбавителя, включающего HSA, Dextran 40 и ДМСО, и план эксперимента оценки влияния изменения концентрации компонента на жизнеспособность и пролиферацию клеток.
Фиг.2 представляет данные анализа фильтрационного удерживания (Filter Retention Assay - FRA) для составов, включающих различное количество ДМСО, выраженное в процентах. Данные представлены в пикселях на миллион загруженных клеток (пикселей/ММ) и получены с помощью анализатора жизнеспособности клеток Vi-Cell. Аналитический контроль = 100% раствор декстрана 40 с красителем для клеток без клеток.
Фиг.3 представляет FRA данные для клеточных составов, включающих различные объемные фракции HSA. Данные выражены в пикселях на миллион загруженных клеток (пикселей/ММ) и получены с помощью анализатора жизнеспособности клеток Vi-Cell. Аналитический контроль = 100% раствор декстрана 40 с красителем для клеток без клеток.
Фиг.4 представляет жизнеспособность клеток после оттаивания с трипановым синим для клеточных составов с различным содержанием ДМСО, выраженным в процентах (0-20%).
Фиг.5 представляет процент регенерированных клеток после оттаивания как функцию изменения концентраций ДМСО (0-20%).
Фиг.6: Восстановление культуры как функция изменения составов с различным содержанием ДМСО, выраженным в процентах, как определено в опыте MTS (см. Раздел 6.3.1 ниже).
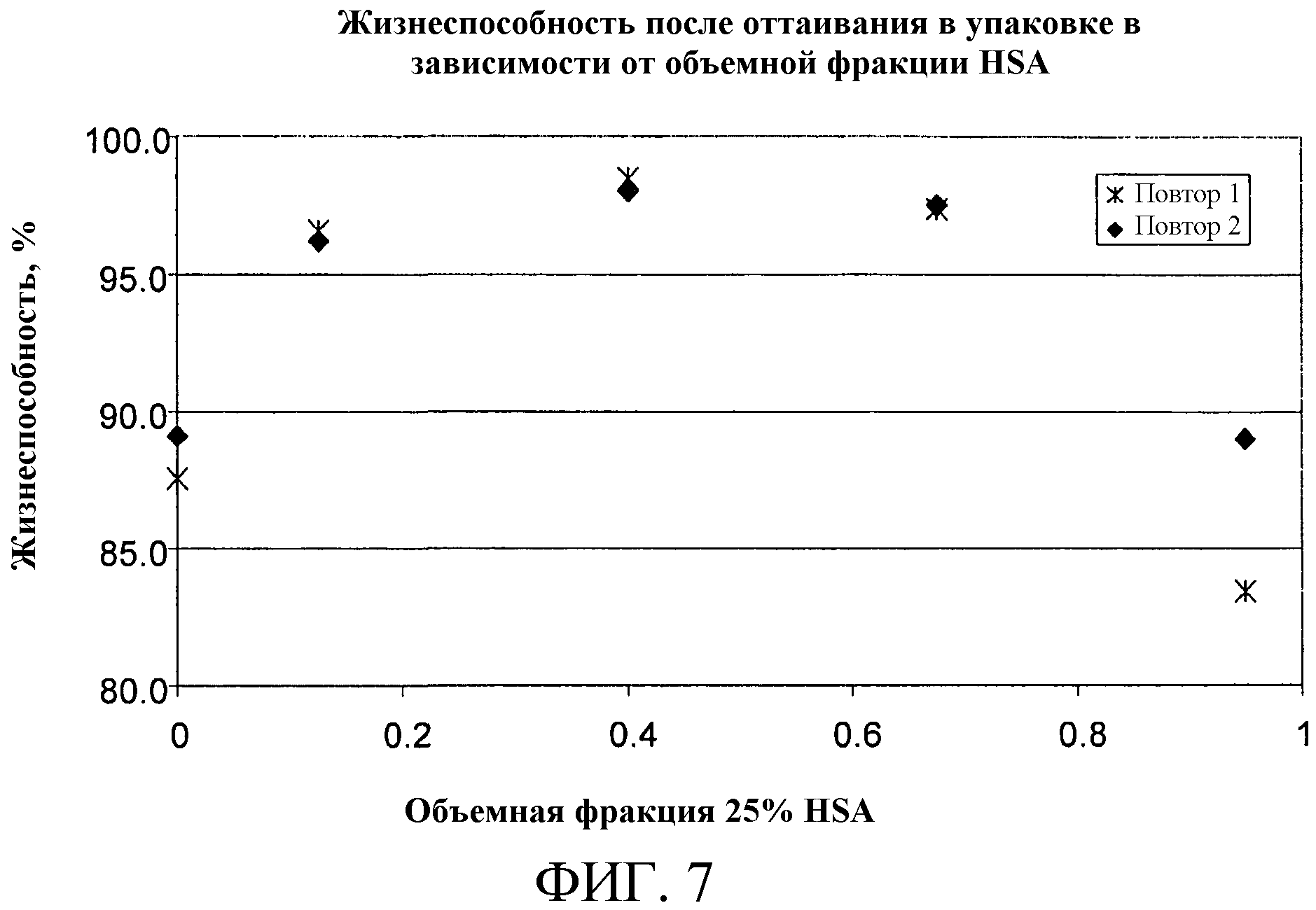
Фиг.7 представляет жизнеспособность клеток после оттаивания клеточных составов, включающих различные объемные фракции 25% HSA.
Фиг.8 представляет восстановление клеток после оттаивания как функцию объемной фракции HSA.
Фиг.9 представляет данные анализа восстановления культуры в зависимости от изменения содержания HSA, полученные при применении водной нерадиоактивной оценки пролиферации клеток с использованием Cell Titer 96® (Aqueous Non-Radioactive Cell Proliferation Assay - Promega, Madison, Wisconsin).
Фиг.10: Уровни подавления иммунного ответа, определенные в опыте реакции Т-лимфоцитов на антигенные гранулы (Bead T-cell Reaction Assay), для составов с различным содержанием компонентов.
Фиг.11: Агрегация клеток как функция изменения плотности замороженных клеток (1-40 × 106 клеток/мл), определенная с помощью FRA анализа. Данные представлены в пикселях на миллион оставшихся на фильтре клеток (пикселей/ММ) и получены c помощью анализатора клеточной жизнеспособности Vi-Cell.
Фиг.12: Клеточная агрегация как функция плотностей замораживающихся клеток (1-40 миллионов клеток/мл). Данные выражены в пикселях на миллион загруженных клеток (микселей/ММ) и получены на анализаторе клеточной жизнеспособности Vi-Cell.
Фиг.13: Агрегация клеток как функция изменения молекулярных масс декстрана, определенная в опыте фильтрационного удерживания (FRA). FRA сигнал получен для декстрана 1000, 40000 и 70000 (т.е. декстрана 1, декстрана 40 и декстрана 70, соответственно). Данные выражены в пикселях на миллион загруженных клеток (пикселей/ММ). Аналитический контроль = 100% раствор декстрана 40 с красителем для клеток без клеток.
Фиг.14 представляет жизнеспособность клеток после оттаивания составов, содержащих декстран различных молекулярных масс.
Фиг.15 представляет восстановление клеток составов, содержащих декстран различных молекулярных масс.
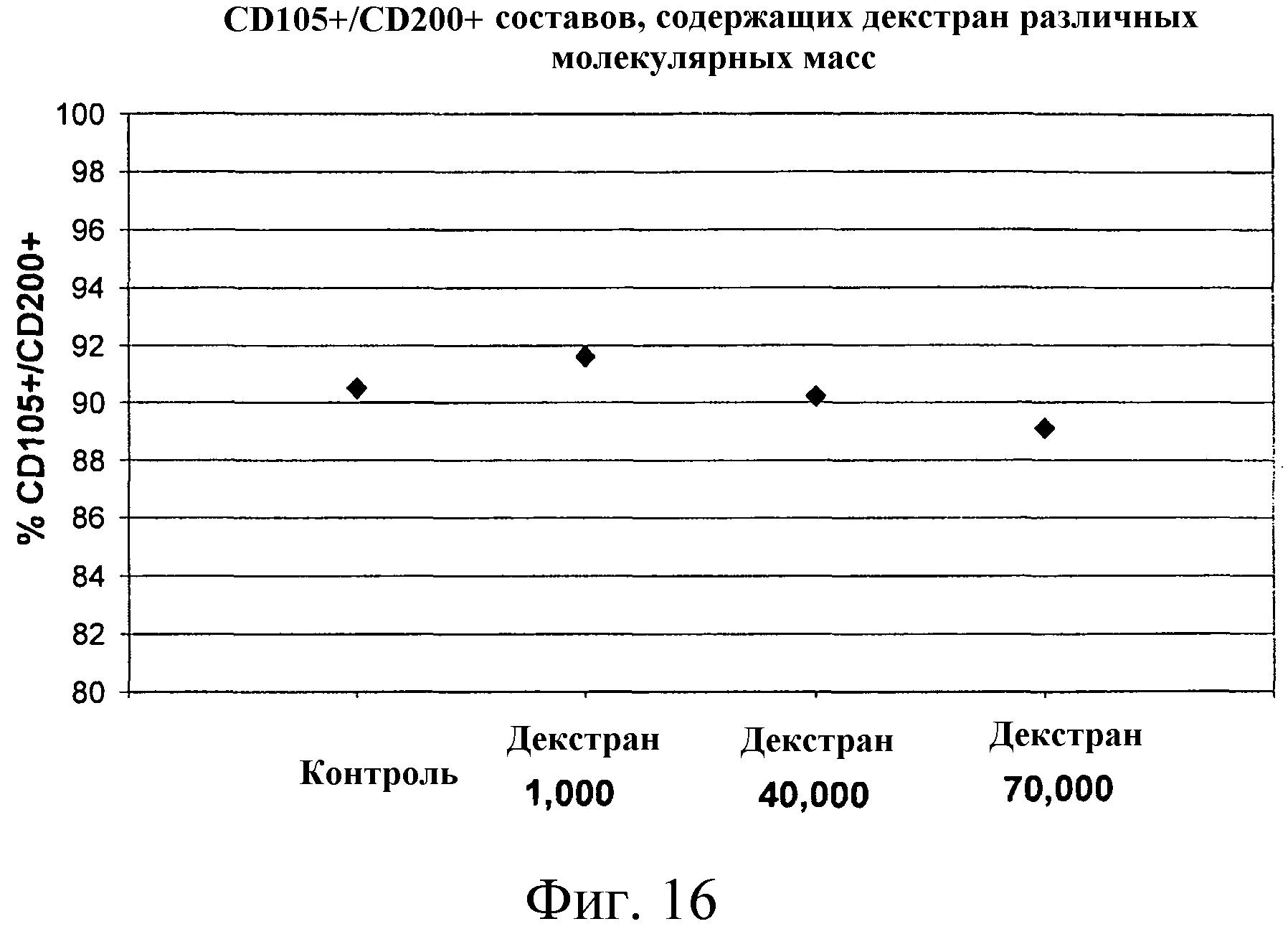
Фиг.16 представляет CD105+/CD200+ составов, содержащих декстран различных молекулярных масс.
Фиг.17 представляет данные реакции Т-лимфоцитов на антигенные гранулы (BTR) для составов, содержащих декстран различных молекулярных масс.
Фиг.18 представляет данные клеточной агрегации, полученные с помощью FRA, для составов, содержащих различные полисахариды. Аналитический контроль = 100% раствор декстрана 40 с красителем для клеток без клеток.
Фиг.19 представляет данные жизнеспособности клеток после оттаивания составов, включающих полисахариды, которые не являются декстраном 40. Данные выражены в пикселях на миллион клеток (пикселей/ММ).
Фиг.20: Восстановление жизнеспособности клеток составов, содержащих различные полисахариды.
Фиг.21 представляет данные экспрессии CD105+/CD200+ в клеточных составах, включающих декстран 40 или мальтодекстран, сахарозу, трегалозу, гепарин, гетакрахмал или гликоген вместо декстрана 40.
Фиг.22 представляет данные BTR для состава, содержащего декстран 40, и шести составов, содержащих другие сахара/полисахариды.
Фиг.23 представляет данные определения агрегации клеток, полученные с помощью FRA для составов, включающих 10% сывороточный альбумин человека (HSA), 10% бычий сывороточный альбумин или 10% зародышевую телячью сыворотку (FBS). Аналитический контроль = 100% раствор декстрана 40 с красителем для клеток без клеток.
Фиг.24: Жизнеспособность клеток после оттаивания для составов, включающих 10% HSA, 10% BSA или 10% FBS.
Фиг.25 представляет данные восстановления клеток после оттаивания для составов, включающих 10% HSA, 4% HSA, 10% BSA или 10% FBS.
Фиг.26 представляет данные идентичности клеток, определенные посредством экспрессии CD105+/CD200+, для составов, включающих 10% HSA, 4% HSA, 10% BSA или 10% FBS.
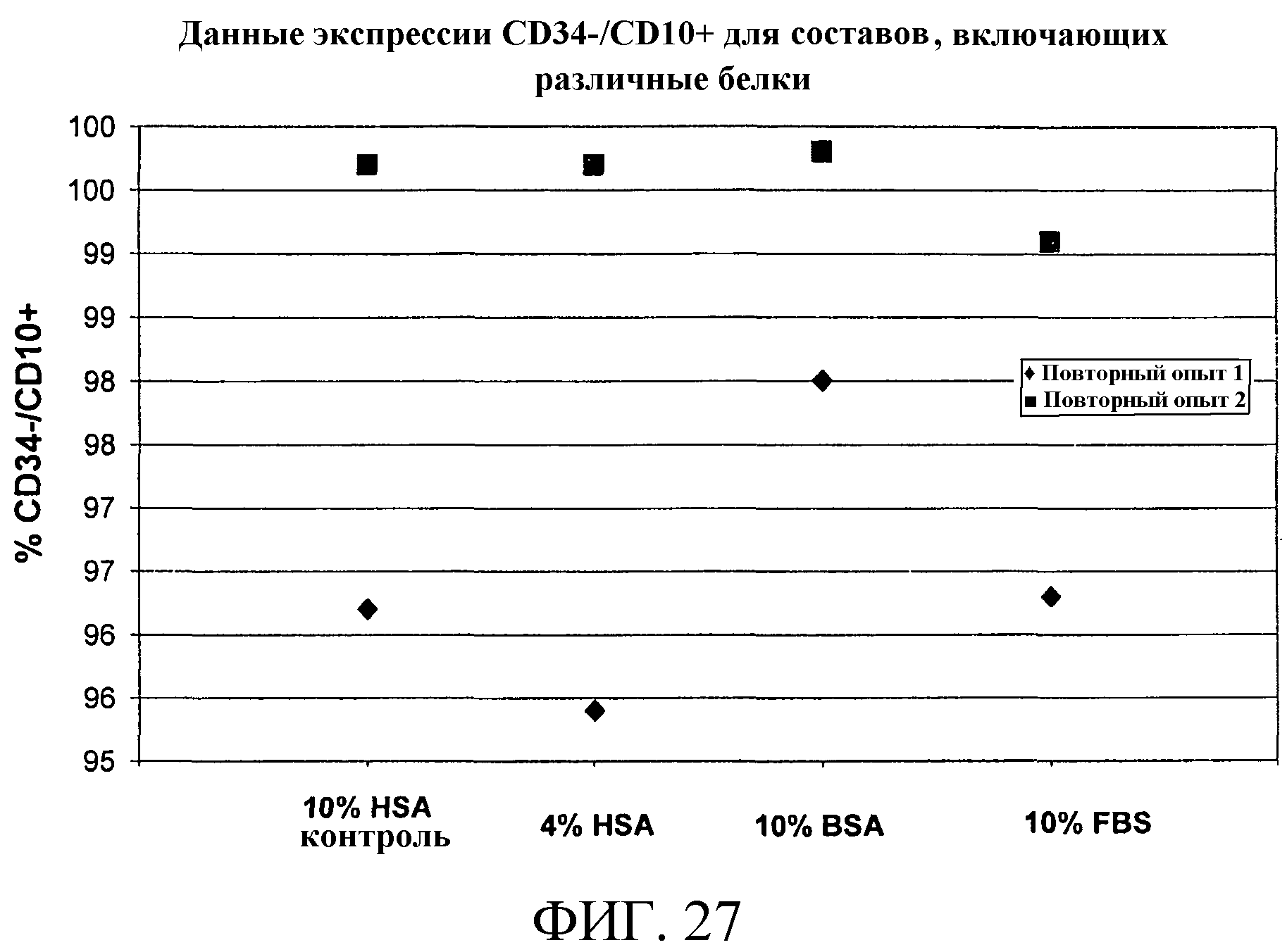
Фиг.27 представляет экспрессию CD34-/CD10+ составами, включающими 10% HSA, 4% HSA, 10% BSA или 10% FBS.
Фиг.28 представляет данные клеточной функциональности, полученные с помощью BTR, для составов, включающих 10% HSA, 4% HSA, 10% BSA или 10% FBS.
Фиг.29 представляет данные клеточной агрегации опыта FRA для мезенхимальных стволовых клеток, полученных из костного мозга (BMMSC), и природных клеток-киллеров (natural killer - NK). Данные выражены в пикселях на миллион клеток (пикселей/ММ).
5. ПОДРОБНОЕ ОПИСАНИЕ
5.1. ОПРЕДЕЛЕНИЯ
Термин «примерно», в рамках изобретения, означает возможное отклонение в пределах 10% от заявленного значения или заявленной величины.
Термин «макроскопление клеток», в рамках изобретения, относится к скоплению клеток, которое можно видеть без увеличения, например, невооруженным глазом, и обычно относится к скоплению клеток размером более чем примерно 150 микрон.
Термин «микроскопление клеток», в рамках изобретения, относится к скоплению клеток, которое можно видеть только при оптическом увеличении, и обычно относится к скоплению клеток размером менее чем примерно 150 микрон.
Термин «SH2», в рамках изобретения, относится к антителу, которое связывает эпитоп на маркере CD105. Таким образом, клетки, которые обозначены как SH2+, представляют собой CD105+.
Термины «SH3» и «SH4», в рамках изобретения, относятся к антителам, которые связывают эпитопы, присутствующие на маркере CD73. Таким образом, клетки, обозначенные как SH3+ и/или SH4+ представляют собой CD73+.
Термин «изолированная клетка», например, «изолированная стволовая клетка», в рамках изобретения, означает клетку, которая по существу отделена от других клеток ткани, например, плаценты, из которой данная клетка получена. Клетка является «изолированной», если по меньшей мере 50%, 60%, 70%, 80%, 90%, 95% или по меньшей мере 99% клеток, с которыми клетка ассоциирована в природной среде, удалены от клетки, например, в процессе сбора и/или культивирования клетки.
Термин «мультипотентная», относящийся к клетке, в рамках изобретения, означает, что клетка обладает способностью дифференцироваться в некоторые, но не обязательно все, типы клеток организма или в клетки, обладающие характеристиками некоторых, но не всех типов клеток организма. В некоторых вариантах осуществления изобретения, например, выделенная мультипотентная клетка, которая обладает способностью дифференцироваться в клетки с характеристиками хондрогенных или остеогенных клеток, является мультипотентной клеткой.
Термин «популяция изолированных клеток», в рамках изобретения, относится к популяции клеток, которая по существу отделена от других клеток ткани, например, плаценты, из которой данная популяция клеток получена.
Термин «плацентарная стволовая клетка», в рамках изобретения, относится к стволовой клетке или клетке-предшественнику, которая получена из плаценты млекопитающего, независимо от морфологии, поверхностных маркеров клеток или количества пассажей после получения первичной культуры. Плацентарная стволовая клетка не получена и не может быть получена из крови, например, из пуповинной или плацентарной крови. Тем не менее, термины «плацентарная стволовая клетка» и «плацентарная мультипотентная клетка», когда используются в данном описании, не относятся к трофобластам, ангиобластам, гемангиобластам, эмбриональным зародышевым клеткам, эмбриональным стволовым клеткам или клеткам, полученным из внутренней клеточной массы бластоциста, клетке, полученной из эмбриональной гонадной складки, например, эмбриональной зародышевой клетке. Клетка считается «стволовой клеткой», если проявляет характеристические признаки стволовой клетки, например, экспрессию маркеров или профиль генной экспрессии, ассоциированные с одним или несколькими типами стволовых клеток; способность воспроизводиться в культуре по меньшей мере 10-40 раз, способность дифференцироваться в клетки одного или нескольким из трех зародышевых слоев; отсутствие характеристик взрослых (т.е. дифференцированных) клеток или т.п. Термины «плацентарная стволовая клетка» и «стволовая клетка, полученная из плаценты» могут использоваться взаимозаменяемым образом. За исключением особо оговоренных случаев, термин «плацентарная» включает пуповину. Плацентарные стволовые клетки, описанные в настоящем изобретении, в некоторых вариантах осуществления изобретения дифференцируются in vitro (в условиях дифференциации), дифференцируются in vivo или и в тех и других условиях.
В рамках изобретения клетка, например, стволовая клетка, является «позитивной» для конкретного маркера, когда указанный маркер может быть обнаружен помимо неспецифических маркеров. Например, плацентарная стволовая клетка является позитивной, например, для CD73, поскольку CD73 может обнаруживаться на плацентарных стволовых клетках в количестве, обнаружимо большем, чем неспецифические маркеры (в сравнении, например, с контрольным изотипом). Клетка также является позитивной для маркера, когда указанный маркер может использоваться для отличия этой клетки от клетки по меньшей мере одного иного типа, или может использоваться для выбора или выделения клетки, когда присутствует в клетке или экспрессируется ею. В контексте, например, обнаружения, опосредуемого антителом, термин «позитивный», как показатель присутствия конкретного маркера клеточной поверхности, означает, что маркер может быть обнаружен с использованием антитела, например, флуоресцентно меченного антитела, специфического для данного маркера; термин «позитивная» относится также к клетке, обнаруживающей этот маркер в количестве, которое дает сигнал, например, в цитометре, который является обнаружимо выше фонового уровня. Например, клетка представляет собой «CD200», когда клетка обнаружимо мечена анителом, специфическим к CD200, и сигнал от антитела обнаружимо выше, чем сигнал контроля (например, фонового или контрольного изотипа). И наоборот, термин «негативная» в этом же контексте означает, что маркер поверхности клетки не может быть обнаружен с использованием антитела, специфического для этого маркера, по сравнению с фоном. Например, клетка представляет собой «CD34-», когда клетка воспроизводимо не может быть обнаружена посредством метки антитела, специфического к CD34, в большей степени, чем контроль (например, фон или контрольный изотип). Маркеры, не обнаруженные или не обнаружимые с использованием антител, определяются как позитивные или негативные аналогичным образом с использованием подходящего контроля. Например, клетка или популяция клеток может определяться как OCT-4+, если количество OCT-4 РНК, обнаруженное в РНК клетки или популяции клеток обнаружимо превосходит фон, как определено, например, способом обнаружения РНК, таким как метод полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР), слот-блот анализы и т.д. За исключением особо оговоренных случаев, маркеры кластера дифференциации («CD») обнаруживаются с использованием антител. ОСТ-4 может определяться как присутствующий, и клетка представляет собой «OCT-4+», если OCT-4 РНК может обнаруживаться с использованием ОТ-ПЦР.
5.2. УЛУЧШЕННЫЕ КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ КЛЕТКИ, И СПОСОБЫ ПОЛУЧЕНИЯ УКАЗАННЫХ КОМПОЗИЦИЙ
Изобретение относится к усовершенствованным способам получения композиций, содержащих клетки, например, стволовые клетки, например, плацентарные стволовые клетки, и к улучшенным композициям, например, фармацевтическим композициям, полученным такими способами. Композиции, например, композиции, включающие клетки, которые могут вводиться в жидкой форме, обычно легче переносятся пациентом, когда, например, клеточные скопления, в особенности клеточные скопления, видимые невооруженным глазом (т.е. макроскопления), удалены перед введением фармацевтической композиции индивидууму. Способы получения композиций, включающих клетки, например, стволовые клетки, такие как стволовые клетки из неонатальной плаценты человека, которая была дренирована от крови, плацентарные клетки, которые были описаны в настоящем изобретении, приводят к получению композиций, которые по существу лучше переносятся при ведении индивидууму.
В одном варианте изобретение относится к способу получения композиции, включающему фильтрацию раствора, содержащего клетки, для получения отфильтрованного раствора, содержащего клетки; разбавление отфильтрованного раствора, содержащего клетки, раствором первого разбавления до концентрации не более примерно 10±3×106 клеток на миллилитр, например, перед криоконсервацией; и необязательно разбавление полученного отфильтрованного раствора, содержащего клетки, раствором второго разбавления, включающим декстран, для получения указанной композиции. В другом варианте осуществления изобретение относится к способу получения композиции, включающему фильтрацию раствора, содержащего клетки, для получения отфильтрованного раствора, содержащего клетки; разбавление отфильтрованного раствора, содержащего клетки, раствором первого разбавления до достижения содержания не более чем примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр, например, перед криоконсервацией; и необязательно разбавление полученного отфильтрованного раствора, содержащего клетки, раствором второго разбавления, включающим декстран, для получения указанной композиции. В некоторых вариантах осуществления изобретения, если количество клеток составляет меньше чем примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной.
В специфическом варианте осуществления изобретения клетки представляют собой стволовые клетки. В более специфическом варианте осуществления изобретения стволовые клетки представляют собой мезенхимальные стволовые клетки, полученные из костного мозга, или дифференцированные (зрелые) стволовые клетки. В специфическом варианте осуществления клетки представляют собой изолированные плацентарные клетки. В еще более специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой плацентарные стволовые клетки или плацентарные мультипотентные клетки. В другом специфическом варианте осуществления изобретения клетки представляют собой клетки, полученные из плацентарного перфузата, например, клетки, содержащие цельные ядра и полученные из плацентарного перфузата. Способы получения клеток плацентарного перфузата описаны в Разделе 5.3.4, ниже.
В специфическом варианте осуществления изобретения клетки криоконсервируют между указанным разбавлением раствором первого разбавления и указанным разбавлением раствором второго разбавления. В другом специфическом варианте осуществления изобретения раствор первого разбавления включает декстран и HSA. В еще одном специфическом варианте осуществления изобретения указанный декстран в растворе первого разбавления представляет собой примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% декстрана. В еще одном специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой декстран 1. В еще одном специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления и указанном растворе второго разбавления представляет собой декстран 1. В еще одном специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой декстран 70. В еще одном специфическом варианте осуществления изобретения указанный декстран в указанном растворе первого разбавления и указанном растворе второго разбавления представляет собой декстран 70. В еще одном специфическом варианте осуществления изобретения декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой декстран 40. В еще одном специфическом варианте осуществления изобретения декстран в указанном растворе первого разбавления и указанном растворе второго разбавления представляет собой декстран 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления представляет собой от примерно 2,5% декстрана 40 до примерно 10% декстрана 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления представляет собой примерно 2,5%, 3,0%, 3,5%, 4,0%, 4,5%, 5,0%, 5,5%, 5,75%, 6,0%, 6,5%, 7,0%, 7,5% 8,0%, 8,5%, 9,0%, 9,5% или 10% декстрана 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления представляет собой примерно 5,5% декстрана 40.
В других вариантах осуществления изобретения указанный(е) раствор(ы) первого и/или второго разбавления может(гут) включать полисахарид в добавление к декстрану или, например, вместо него. В некоторых вариантах осуществления изобретения полисахарид представляет собой полимер (из 2 или нескольких подгрупп) глюкозы и не включает подгрупп сахаридов, которые не являются глюкозой. В других вариантах осуществления изобретения указанный(е) раствор(ы) первого и/или второго разбавления включает(ют) один или несколько компонентов, выбранных из мальтодекстрина (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% мальтодекстрина), трегалозы (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% трегалозы) или гетакрахмала (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% гетакрахмала). В других вариантах осуществления изобретения раствор(ы) первого и/или второго разбавления включает(ют) один или несколько компонентов, выбранных из сахарозы (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% сахарозы), гепарина (например, примерно 55 USP единиц/мл гепарина) или гликогена (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% гликогена). В конкретном варианте осуществления изобретения указанный(ые) раствор(ы) первого и/или второго разбавления включает(ют) мальтодекстран в добавление к декстрану или вместо него. В другом конкретном варианте осуществления изобретения указанный(ые) раствор(ы) первого и/или второго разбавления включает(ют) трегалозу в добавление к декстрану или вместо него. В другом конкретном варианте осуществления изобретения указанный(ые) раствор(ы) первого и/или второго разбавления включает(ют) гетакрахмал в добавление к декстрану или вместо него.
В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно от 1% до 17% HSA. В другом специфическом варианте осуществления изобретения указанный HSA представляет собой примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16% или примерно 17% HSA. В другом специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно от 4 до 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно 3,125% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой 5% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой примерно 16,875% HSA. В еще одном специфическом варианте осуществления изобретения указанный раствор первого разбавления включает HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно от 1 до 17% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16% или 17% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно от 4 до 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 3,125% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 5% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой примерно 16,875%.
В других вариантах осуществления изобретения в указанном растворе в дополнение к HSA или вместо него могут использоваться бычий сывороточный альбумин (BSA) (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% BSA) или зародышевая телячья сыворотка (FBS) (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% FBS).
В некоторых вариантах осуществления изобретения соотношение HSA и декстрана, например, декстрана 1, декстрана 40 или декстрана 70, в первом растворе находится в интервале от примерно 6:1 HSA:декстран до примерно 1:2,6 HSA:декстран. В некоторых вариантах осуществления изобретения соотношение HSA и декстрана составляет примерно 6:1, 5,5:1, 5:1, 4,5:1, 4:1, 3,5:1, 3:1, 2,5:1, 2,0:1, 1,5:1, 1:1, 1:1,5, 1:2 или 1:2,6 HSA:декстран. В некоторых вариантах осуществления изобретения соотношение HSA и декстрана, например, декстрана 1, декстрана 40 или декстрана 70, в первом растворе составляет примерно 3,13% HSA/8,25% декстрана. В некоторых вариантах осуществления изобретения соотношение HSA и декстрана, например, декстрана 1, декстрана 40 и декстрана 70, в первом растворе составляет примерно 16,88% HSA/2,75% декстрана. В конкретных вариантах осуществления изобретения соотношение HSA и декстрана, например, декстрана 1, декстрана 40 или декстрана 70, в первом растворе составляет примерно 10% HSA/5,5% декстрана, например, декстрана 1, декстрана 40 или декстрана 70.
В еще одном специфическом варианте осуществления изобретения указанный раствор первого разбавления дополнительно включает криопротектор. В более специфическом варианте осуществления изобретения указанный криопротектор представляет собой диметилсульфоксид (ДМСО). В отдельном варианте осуществления изобретения указанный раствор первого разбавления дополнительно включает от примерно 1% до примерно 15%, от примерно 2,5% до примерно 15%, от примерно 2,5% до примерно 10%, от примерно 5% до примерно 15%, от примерно 5% до примерно 10% или от примерно 10% до примерно 15% ДМСО. В конкретном варианте осуществления изобретения указанный раствор первого разбавления дополнительно включает примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% ДМСО. В конкретном варианте осуществления изобретения указанный раствор первого разбавления дополнительно включает примерно 5% ДМСО.
В специфическом варианте осуществления изобретения указанный раствор первого разбавления включает примерно 5,5% декстрана 40, примерно 10% HSA и примерно 5% ДМСО.
В другом специфическом варианте осуществления изобретения указанный декстран в указанном растворе второго разбавления представляет собой примерно 10% декстрана 40. В другом специфическом варианте осуществления изобретения указанная композиция, содержащая клетки, включает примерно 2,5%, 3,0%, 3,5%, 4,0%, 4,5%, 5,0%, 5,5%, 5,75%, 6,0%, 6,5%, 7,0%, 7,5% 8,0%, 8,5%, 9,0%, 9,5% или 10% декстрана. В еще одном специфическом варианте осуществления изобретения указанная композиция, содержащая клетки, включает от примерно 7,5% до примерно 9% декстрана. В еще одном специфическом варианте осуществлении изобретения указанная композиция включает от примерно 1,5×106 клеток на миллилитр до примерно 5,0×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения указанная композиция включает от примерно 1,0±0,3×106 клеток на миллилитр до примерно 5,0±1,5×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения указанный раствор второго разбавления не включает HSA.
Декстран, который может использоваться в способах согласно изобретению, может представлять собой декстран молекулярной массы в интервале от примерно 1 кДа до примерно 150 кДа, например, 1 кДа (декстран 1), примерно 40 кДа (декстран 40) или примерно 70 кДа (декстран 70).
В другом специфическом варианте осуществления изобретения раствор, включающий клетки, включает криопротектор. Если раствор, включающий клетки, содержит менее чем примерно 10±3×106 клеток на миллилитр, стадия первого разбавления может быть опущена, и в некоторых вариантах осуществления изобретения раствор, в котором клетки суспендируются, может включать криопротектор, например, ДМСО, например, от примерно 2% до примерно 15% ДМСО, например, примерно 5% ДМСО.
В еще одном варианте осуществления изобретение относится к способу получения композиции, включающему: (а) фильтрацию раствора, содержащего клетки, например, изолированные плацентарные клетки, точнее плацентарные стволовые клетки или плацентарные мультипотентные клетки, или клетки, выделенные из плацентарного перфузата, например, выделенные из плацентарного перфузата клетки, содержащие цельные ядра, декстран и сывороточный альбумин человека (HSA) для получения отфильтрованного раствора, содержащего клетки; (b) необязательно разбавление указанного отфильтрованного раствора, содержащего клетки, до концентрации примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр раствором первого разбавления, включающим декстран; и (с) необязательно разбавление отфильтрованного раствора, содержащего клетки, раствором второго разбавления, включающим декстран, но не включающим HSA, с получением таким образом композиции. В некоторых вариантах осуществления изобретения стадия (b) проводится, когда содержащий клетки отфильтрованный раствор на стадии (а) включает более чем примерно 15×106 клеток на миллилитр, где указанное разбавление на стадии (b) проводится для достижения концентрации примерно 15×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения стадия (b) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (а) включает более чем примерно 10±3×106 клеток на миллилитр, где указанное разбавление на стадии (b) проводится для достижения концентрации примерно 10±3×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения, где указанный отфильтрованный раствор, содержащий клетки, включает менее чем примерно 10±3×106 клеток на миллилитр, разбавление на стадии (b) опускается, и раствор на стадии (а) включает криопротектор, например, ДМСО, в частности, от примерно 2% до примерно 15% ДМСО. В некоторых вариантах осуществления изобретения стадия (b) проводится, когда отфильтрованный раствор, содержащий клетки, на стадии (а) включает более чем примерно 7,5×106 клеток на миллилитр, где указанное разбавление на стадии (b) проводится для достижения концентрации примерно 7,5×106 клеток на миллилитр. В специфическом варианте осуществления способа, указанные клетки перед стадией (с) являются криоконсервированными. В некоторых вариантах осуществления изобретения, если содержание клеток составляет менее чем примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной. В специфическом варианте осуществления способа указанные клетки криоконсервированы перед стадией (с). В другом специфическом варианте осуществления указанный декстран в указанном растворе первого разбавления или указанном растворе второго разбавления представляет собой декстран 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления представляет собой 5,0% декстрана 40. В другом специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления представляет собой 5,5% декстрана 40. В еще одном специфическом варианте осуществления изобретения указанный раствор первого разбавления включает HSA. В более специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой 5% HSA. В более специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный раствор первого разбавления дополнительно включает криопротектор. В более специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе второго разбавления представляет собой 10% декстрана 40. В другом специфическом варианте осуществления изобретения указанный раствор на стадии (а) включает криопротектор.
В одном аспекте способа количество клеточных скоплений в конечной композиции, включающей клетки, снижено, или скопления удалены с использованием фильтрации, предпочтительно перед криоконсервацией. В некоторых вариантах осуществления, где указанные клетки в растворе, содержащем клетки, подвергаются криоконсервации, раствор, содержащий клетки, фильтруется перед криоконсервацией. Например, клетки, точнее плацентарные стволовые клетки, в растворе могут пропускаться через фильтр перед криоконсервацией для удаления различимых клеточных скоплений (агрегаций клеток, т.е. макроскоплений клеток). В одном варианте осуществления изобретения фильтрация включает фильтрацию раствора, содержащего клетки, через фильтр перед криоконсервацией указанных клеток, где диаметры указанного фильтра находятся в интервале от примерно 50 мкм до примерно 150 мкм (т.е. фильтр с диаметром пор от примерно 50 мкм до примерно 150 мкм), где фильтр подходит для фильтрации растворов, содержащих клетки. Например, фильтр может представлять собой фильтр с порами в интервале от примерно 50 мкм до примерно 80 мкм, от примерно 60 мкм до примерно 90 мкм, от примерно 70 мкм до примерно 100 мкм, от примерно 80 мкм до примерно 110 мкм, от примерно 90 мкм до примерно 120 мкм, от примерно 100 мкм до примерно 130 мкм, от примерно 110 мкм до примерно 140 мкм или в интервале от примерно 120 до примерно 150 мкм, либо может представлять собой фильтр с диаметром пор 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 105, 110, 115, 120, 125, 130, 135, 140, 145 или 150 мкм. В одном специфическом варианте осуществления изобретения указанный фильтр представляет собой фильтр с диаметром пор 70 мкм. В другом специфическом варианте осуществления изобретения указанный фильтр представляет собой фильтр с диаметром пор 100 мкм. В еще одном специфическом варианте осуществления изобретения указанный фильтр представляет собой фильтр с диаметром пор от 70 мкм до 100 мкм. В еще одном специфическом варианте осуществления изобретения указанный раствор, содержащий клетки, фильтруется после оттаивания, помимо того, что фильтруется перед замораживанием.
В некоторых других вариантах осуществления изобретения, если количество клеток составляет менее примерно 10±3×106 клеток на миллилитр, фильтрация является необязательно.
В различных вариантах осуществления изобретения способ получения композиции, включающей клетки, например, изолированные плацентарные клетки, включает криоконсервацию клеток при содержании клеток не более чем примерно 50×106, 40×106, 30×106, 20×106, 15×106, 10×106, 9,5×106, 9×106, 8,5×106, 8×106, 7,5×106, 7×106, 6,5×106, 6×106, 5,5×106, 5×106, 4,5×106, 4×106, 3,5×106, 3×106 или 2,5×106 клеток на миллилитр. В одном специфическом варианте осуществления изобретения клетки подвергаются криоконсервации при содержании не более чем примерно 10±3×106 клеток на миллилитр. В другом специфическом варианте осуществления изобретения клетки криоконсервируются при содержании не более чем примерно 15×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения клетки криоконсервируются при содержании не более чем примерно 5×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения клетки криконсервируются при содержании от примерно 5,0×106 клеток на миллилитр до примерно 7,5×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения клетки криоконсервируются при содержании примерно 5×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения клетки криконсервируются при содержании примерно 7,5×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения клетки криконсервируются при содержании примерно 10±3×106 клеток на миллилитр. В другом специфическом варианте осуществления изобретения указанные клетки криоконсервируются при таком содержании, что при оттаивании и разбавлении указанных клеток в соотношении в интервале от 1:1 до 1:11 (об./об.), например, от 1:1 до 1:5, декстраном, например, 10% декстраном 40, образуются 2 или менее различимых клеточных скопления (то есть макроскопления) на 106 клеток. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки криконсервируются при таком содержании клеток, что после оттаивания и разбавлении указанных клеток в соотношении от 1:1 до 1:11, например, от 1:1 до 1:5 (об./об.) декстраном 40, например, 10% декстраном 40, происходит образование не различимых невооруженным глазом клеточных скоплений. В еще одном специфическом варианте осуществления изобретения указанные клетки криоконсервируются при таком содержании, что оттаивание и разбавление указанных клеток в соотношении от 1:1 до 1:11 (об./об.), например, от 1:1 до 1:5 (об./об.), 10% декстраном 40 приводит к образованию менее чем примерно 150, 140, 130, 120, 110 или 100 клеточных микроскоплений на 106 клеток.
В еще одном варианте осуществления изобретение относится к способу получения композиции, например, включающему контактирование клеток, например, изолированных плацентарных клеток, после криоконсервации с раствором, включающим декстран 40, например, повторным суспендированием в растворе, включающем декстран 40, или разбавлением раствором, включающим декстран 40. В специфическом варианте осуществления изобретения раствор включает от примерно 2,5% декстрана 40 до примерно 10% декстрана 40 (масс./об.). В еще одном специфическом варианте осуществления изобретения раствор включает от примерно 5% декстрана 40 до примерно 10% декстрана 40 (масс./об.). В еще одном специфическом варианте осуществления изобретения раствор представляет собой 5,0% раствор декстрана или 10% раствор декстрана. В еще одном специфическом варианте осуществления изобретения раствор представляет собой 5,5% раствор декстрана или 10% раствор декстрана. В других вариантах осуществления изобретения молекулярная масса декстрана, например, среднемассовая молекулярная масса, находится в интервале от примерно 1 килодальтон до примерно 150 килодальтон. В других вариантах осуществления изобретения молекулярная масса декстрана, например, среднемассовая молекулярная масса, находится в интервале от примерно 1 кДа до примерно 150 кДа, от примерно 1 кДа до примерно 125 кДа, от примерно 1 кДа до примерно 100 кДа, от примерно 1 кДа до примерно 75 кДа, от примерно 1 кДа до примерно 50 кДа, от примерно 1 кДа до примерно 25 кДа. В других вариантах осуществления изобретения молекулярная масса декстрана, например, среднемассовая молекулярная масса, находится в интервале от примерно 1 кДа до примерно 10 кДа, от примерно 30 кДа до примерно 50 кДа или от примерно 60 кДа до примерно 80 кДа. В других вариантах осуществления изобретения раствор включает от примерно 2% декстрана до примерно 25% декстрана. В специфическом варианте осуществления изобретения указанный раствор не включает HSA. В другом специфическом варианте осуществления изобретения указанный раствор приготавливается с учетом плотности указанных клеток, например, указанных плацентарных стволовых клеток, например, раствор представляет собой раствор 5%, 2%, 1%, 0,5%, 0,2% или 0,1% плотности изолированных плацентарных клеток. В другом специфическом варианте осуществления изобретения раствор приготавливается без учета плотности указанных клеток.
В еще одном варианте осуществления изобретения способ получения композиции, включающей клетки, например, изолированные плацентарные клетки, включает (а) фильтрацию раствора, содержащего клетки, перед криоконсервацией; (b) криоконсервацию клеток при содержании примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр; (c) оттаивание клеток; и (d) разбавление раствора, содержащего клетки, раствором декстрана 40 в соотношении в интервале от примерно 1:1 (об./об.) до примерно 1:11. В некоторых вариантах осуществления изобретения криоконсервация на стадии (b) проводится при содержании примерно 15×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения клетки криоконсервируются на стадии (b) при содержании не более чем 15×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения на стадии (b) криоконсервация проводится при содержании не более чем примерно 10±3×106 клеток на миллилитр. В некоторых других вариантах осуществления изобретения, если количество клеток составляет менее чем примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной. В более специфическом варианте осуществления изобретения клетки на стадии (b) подвергаются криокорсервации в растворе, включающем от примерно 5% до примерно 10% декстрана 40 и HSA.
В еще одном варианте осуществления изобретения способ получения композиции включает следующие стадии:
(a) фильтрация раствора, включающего клетки, 5,5% декстрана 40 и 10% HSA, через 70 мкм фильтр для получения отфильтрованного раствора, содержащего клетки;
(b) разбавление отфильтрованного раствора, содержащего клетки, раствором, включающим 5,5% декстрана 40, 10% HSA и 5% ДМСО до содержания примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр;
(d) криоконсервация клеток в указанном отфильтрованном растворе, содержащем клетки;
(e) оттаивание клеток;
(f) необязательно разбавление отфильтрованного раствора, содержащего клетки, 10% раствором декстрана 40.
В некоторых вариантах осуществления изобретения указанное разбавление на стадии (b) проводится до содержания не более чем примерно 15×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения указанное разбавление на стадии (b) проводится до содержания не более чем примерно 10±3×106 клеток/мл. В вариантах осуществления изобретения, где отфильтрованный раствор, содержащий клетки, содержит менее чем примерно 10±3×106 клеток/мл, раствор на стадии (а) включает криопротектор, например, ДМСО, точнее от примерно 1% до примерно 5% ДМСО, и стадия (b) опускается. В некоторых других вариантах осуществления изобретения, если количество клеток составляет менее чем примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной. В некоторых вариантах осуществления изобретения стадия (f) включает разбавление отфильтрованного раствора, содержащего клетки, в соотношении в интервале от 1:1 до 1:11 (об./об.) 10% раствором декстрана 40. В других вариантах осуществления изобретения стадия (f) включает разбавление отфильтрованного раствора, содержащего клетки, в соотношении в интервале от 1:1 до 1:5 (об./об.) 10% раствором декстрана 40.
В еще одном варианте осуществления изобретения способ получения композиции согласно изобретению включает следующие стадии:
(a) центрифугирование множества клеток для сбора клеток;
(b) повторное суспендирование клеток в 5,5% растворе декстрана 40;
(с) центрифугирование клеток для сбора клеток;
(d) еще одно суспендирование клеток в 5,5% растворе декстрана 40, который включает 10% HSA, для получения раствора, содержащего клетки;
(e) фильтрация раствора, содержащего клетки, через 70 мкм фильтр для получения отфильтрованного раствора, содержащего клетки;
(f) разбавление отфильтрованного раствора, содержащего клетки, раствором, содержащим 5,5% декстрана 40, 10% HSA и 5% ДМСО, до концентрации примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр;
(g) криоконсервация клеток в указанном отфильтрованном растворе, содержащем клетки;
(h) оттаивание клеток; и
(i) необязательно разбавление отфильтрованного раствора, содержащего клетки, 10% раствором декстрана 40.
В некоторых вариантах осуществления изобретения указанное разбавление на стадии (f) проводится до достижения содержания не более чем примерно 15×106 клеток/мл. В некоторых вариантах осуществления изобретения указанное разбавление на стадии (f) проводится до достижения содержания не более примерно 10±3×106 клеток/мл. В другие вариантах осуществления изобретения, если содержание клеток составляет менее чем примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной. В вариантах осуществления изобретения, где указанное повторное суспендирование на стадии (d) приводит к получению раствора, содержащего менее примерно 10±3×106 клеток/мл, раствор на стадии (d) включает криопротектор, например, ДМСО, в частности от примерно 1% до примерно 5% ДМСО, и стадия (f) опускается. В некоторых вариантах осуществления изобретения стадия (i) включает разбавление отфильтрованного раствора, содержащего клетки, в соотношении от 1:1 до 1:5 (об./об.) 10% раствором декстрана 40. В некоторых вариантах осуществления изобретения стадия (i) включает разбавление отфильтрованного раствора, содержащего клетки, в соотношении от 1:1 до 1:11 (об./об.) 10% раствором декстрана 40.
В специфическом варианте осуществления любого из описанных выше способов ДМСО по существу удаляется из композиции, содержащей клетки, так что конечная концентрация ДМСО в композиции составляет менее чем примерно 2,5%, 2,0%, 1,5%, 1,0%, 0,9%, 0,8%, 0,7%, 0,6%, 0,5%, 0,4%, 0,3%, 0,2% или примерно 0,1%. Удаление ДМСО может выполняться, например, центрифугированием клеток и повторным суспендированием клеток в 10% декстране 40. Такая стадия центрифугирования и суспендирования может повторяться один или несколько раз.
В еще одном специфическом варианте осуществления любого из описанных выше способов способ дополнительно включает концентрирование полученной клеточной композиции до содержания примерно от 5×106 клеток на миллилитр до 1×108 клеток на миллилитр. Такая композиция может использоваться, например, для подкожного введения индивидууму, нуждающемуся в таком введении.
В еще одном специфическом варианте осуществления любого из описанных выше способов клетка представляют собой клетку, отличную от плацентарной стволовой клетки. В более специфических вариантах осуществления изобретения клетки, например, могут представлять собой стволовые клетки или не являться стволовыми клетками. В специфических вариантах осуществления изобретения, где клетки являются стволовыми клетками, стволовые клетки могут представлять собой дифференцированные стволовые клетки, соматические стволовые клетки, эмбриональные стволовые клетки, эмбриональные зародышевые клетки, пуповинные стволовые клетки, стволовые клетки амниотической жидкости, мезенхимальные стволовые клетки, полученные из костного мозга, мезенхимальные стволовые клетки, полученные из пуповинной крови, мезенхимальные стволовые клетки, полученные из периферической крови, мезенхимальные стволовые клетки, полученные из жировой ткани, или стволовые клетки, полученные из периоста. В еще одном специфическом варианте осуществления изобретения клетки представляют собой природные клетки-киллеры, например, CD3-, CD56+ природные клетки-киллеры.
В соответствии с другим аспектом, изобретение относится к композициям, например, фармацевтическим композициям. В некоторых вариантах осуществления изобретения композиции получены описанными выше способами. В некоторых вариантах осуществления изобретения композиции не содержат различимых невооруженным глазом скоплений клеток, т.е. макроскоплений клеток. В некоторых других вариантах осуществления изобретения композиции включают по существу сниженное количество микроскоплений клеток (которые видны только под микроскопом, например, под оптическим микроскопом) по сравнению с композициями, которые не были отфильтрованы, например, меньше на примерно 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99% микроскоплений клеток.
В одном варианте осуществления изобретение относится к композиции, например, фармацевтической композиции, включающей множество клеток, например, множество изолированных плацентарных клеток или клеток, изолированных из плацентарного перфузата, например, выделенных из плацентарного перфузата клеток, содержащих цельные ядра, в растворе, включающем 10% декстрана 40, где указанная композиция включает от примерно 1,0±0,3×106 клеток на миллилитр до примерно 5,0±1,5×106 клеток на миллилитр, и где указанная композиция не содержит различимых невооруженным глазом скоплений клеток (то есть не включает макроскоплений клеток). В некоторых вариантах осуществления изобретения указанная композиция включает от примерно 1,5×106 клеток на миллилитр до примерно 3,75×106 клеток на миллилитр. В определенных других вариантах осуществления изобретения композиция включает от примерно 1,0×106 клеток на миллилитр до примерно 15×106 клеток на миллилитр, например, от примерно 7,5×106 клеток на миллилитр до примерно 15×106 клеток на миллилитр. В некоторых других вариантах осуществления изобретения композиция включает менее примерно 20×106 клеток на миллилитр. В специфическом варианте осуществления изобретения указанные клетки были криоконсервированы и оттаяны. В другом специфическом варианте осуществления изобретения клетки были отфильтрованы через фильтр с размерами пор от 70 мкм до 100 мкм. В еще одном специфическом варианте осуществления указанная композиция не включает макроскоплений клеток. В еще одном специфическом варианте осуществления изобретения указанная композиция включает менее примерно 200 микроскоплений клеток на 106 клеток. В еще одном специфическом варианте осуществления изобретения указанная композиция включает менее примерно 150 микроскоплений клеток на 106 клеток. В еще одном специфическом варианте осуществления изобретения указанная композиция включает менее примерно 100 микроскоплений клеток на 106 клеток. В еще одном специфическом варианте осуществления изобретения указанная композиция включает менее примерно 1%, 0,9%, 0,8%, 0,7%, 0,6%, 0,5%, 0,4%, 0,3%, 0,2% или 0,1% ДМСО.
В некоторых вариантах осуществления изобретения композиция включает примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% декстрана, например, декстрана 1, декстрана 40 или декстрана 70. В специфическом варианте осуществления изобретения указанная композиция включает от примерно 7,5% до примерно 9% декстрана 40. В специфическом варианте осуществления изобретения указанная композиция включает примерно 5,5% декстрана 40.
В других вариантах осуществления изобретения указанная композиция, в дополнение к декстрану или вместо него, включает полисахарид. В некоторых вариантах осуществления изобретения полисахарид представляет собой полимер глюкозы, который не включает в себя подгрупп неглюкозного сахарида. В других вариантах осуществления изобретения указанная композиция включает мальтодекстрин (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% мальтодекстрина), трегалозу (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% трегалозы) или гетакрахмал (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75%, или 10% гетакрахмала). В других вариантах осуществления изобретения указанная композиция включает сахарозу (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% сахарозы), гепарин (например, 55 USP единиц/мл гепарина) или гликоген (например, примерно 2,5%, 2,75%, 3,0%, 3,25%, 3,5%, 3,75%, 4,0%, 4,25%, 4,5%, 4,75%, 5,0%, 5,25%, 5,5%, 5,75%, 6,0%, 6,25%, 6,5%, 6,75%, 7,0%, 7,25%, 7,5%, 7,75%, 8,0%, 8,25%, 8,5%, 8,75%, 9,0%, 9,25%, 9,5%, 9,75% или 10% гликогена). В конкретном варианте осуществления изобретения указанная композиция, в дополнение к декстрану или вместо него, включает мальтодекстран. В другом конкретном варианте осуществления изобретения указанная композиция, в дополнение к декстрану или вместо него, включает трегалозу. В еще одном отдельном варианте осуществления изобретения указанная композиция, в дополнение к декстрану или вместо него, включает гетакрахмал.
В еще одном специфическом варианте осуществления изобретения указанная композиция включает от примерно 1% до примерно 17% HSA. В некоторых других вариантах осуществления изобретения указанная композиция включает примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16% или примерно 17% HSA. В некоторых других вариантах осуществления изобретения указанная композиция включает примерно 3,125% HSA. В некоторых других вариантах осуществления изобретения указанная композиция включает примерно 5% HSA. В некоторые других вариантах осуществления изобретения указанная композиция включает примерно 10% HSA. В некоторых других вариантах осуществления изобретения указанная композиция включает примерно 16,875% HSA.
В других вариантах осуществления изобретения указанная композиция включает бычий сывороточный альбумин (BSA) (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% BSA) или зародышевую телячью сыворотку (FBS) (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% FBS) в дополнение к HSA или вместо него.
В некоторых вариантах осуществления изобретения композиция включает в себя криопротектор, например, ДМСО, например, от примерно 1% до примерно 15% ДМСО. В некоторых вариантах осуществления изобретения указанная композиция включает от примерно 1% до примерно 15%, от примерно 2,5% до примерно 15%, от примерно 2,5% до примерно 10%, от примерно 5% до примерно 15%, от примерно 5% до примерно 10% или от примерно 10% до примерно 15% ДМСО. В некоторых вариантах осуществления изобретения указанная композиция включает примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% ДМСО. В отдельном варианте осуществления изобретения композиция включает примерно 5% ДМСО.
Изобретение дополнительно относится к композициям, включающим клетки, где указанные композиции получены одним из способов, описанных в изобретении. Например, в одном варианте осуществления изобретение относится к композиции, включающей клетки, где указанная композиция получена способом, включающим фильтрацию раствора, содержащего клетки, с получением отфильтрованного раствора, содержащего клетки; разбавление отфильтрованного раствора, содержащего клетки, первым раствором до содержания примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр, например, перед криоконсервацией; и разбавление полученного отфильтрованного раствора, содержащего клетки, вторым раствором, включающим декстран, но не включающим HSA, для получения указанной композиции. В некоторых вариантах осуществления изобретения указанное разбавление проводится до достижения содержания не более примерно 15×106 клеток на миллилитр. В некоторых других вариантах осуществления изобретения указанное разбавление проводится до содержания не более примерно 10±3×106 клеток на миллилитр. В некоторых других вариантах осуществления изобретения указанное разбавление проводится до содержания не более чем примерно 7,5×106 клеток на миллилитр. В некоторых других вариантах осуществления изобретения, если количество клеток составляет менее примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной. В специфическом варианте осуществления изобретения клетки подвергаются криоконсервации между указанным разбавлением раствором первого разбавления и указанным разбавлением раствором второго разбавления. В другом специфическом варианте осуществления изобретения раствор первого разбавления включает декстран и HSA. В еще одном специфическом варианте осуществления изобретения декстран в указанном растворе первого разбавления или указанном раствором второго разбавления представляет собой декстран 40. В еще одном специфическом варианте осуществления изобретения декстран в указанном растворе первого разбавления и указанном раствором второго разбавления представляет собой декстран 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления представляет собой 5,0% декстрана 40. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе первого разбавления представляет собой 5,5% декстрана 40. В еще одном специфическом варианте осуществления изобретения указанный HSA в указанном растворе, включающем HSA, представляет собой 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный раствор первого разбавления включает HSA. В более специфическом варианте осуществления изобретения указанный HSA в указанном растворе первого разбавления представляет собой 10% HSA. В еще одном специфическом варианте осуществления изобретения указанный раствор первого разбавления включает криопротектор. В более специфическом варианте осуществления изобретения указанный криопротектор представляет собой ДМСО. В еще одном специфическом варианте осуществления изобретения указанный декстран 40 в указанном растворе второго разбавления представляет собой примерно 10% декстрана 40. В еще одном специфическом варианте осуществления изобретения указанная композиция, включающая клетки, включает от примерно 7,5% до примерно 9% декстрана. В еще одном специфическом варианте осуществления изобретения указанная композиции, включающая клетки, включает от примерно 1,0±3,0×106 клеток на миллилитр до примерно 5,0±1,5×106 клеток на миллилитр. В еще одном специфическом варианте осуществления изобретения указанная композиция, включающая клетки, включает от примерно 1,5×106 клеток на миллилитр до примерно 3,75×106 клеток на миллилитр.
В еще одном варианте осуществления изобретения композиция, содержащая клетки, получена способом, включающим (а) фильтрацию раствора, содержащего клетки, перед криоконсервацией для получения отфильтрованного раствора, содержащего клетки; (b) криоконсервацию клеток в отфильтрованном растворе, содержащем клетки, при содержании примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр; (с) оттаивание клеток; и (d) разбавление отфильтрованного раствора, содержащего клетки в соотношение от примерно 1:1 до примерно 1:11 (об./об.) раствором декстрана 40. В некоторых вариантах осуществления изобретения, если содержание клеток составляет менее примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной. В более специфическом варианте осуществления изобретения клетки на стадии (b) подвергаются криоконсервации при содержании примерно 10±3×106 клеток на миллилитр. В более специфическом варианте осуществления изобретения клетки на стадии (b) подвергаются криоконсервации в растворе, включающем от примерно 5% до примерно 10% декстрана 40 и HSA. В некоторых вариантах осуществления изобретения указанное разбавление на стадии (d) осуществляется до содержания не более примерно 15×106 клеток на миллилитр.
В еще одном варианте осуществления изобретения композиция, включающая клетки, получена способом, включающим: (а) суспендирование клеток в 5,5% растворе декстрана 40, который включает 10% HSA, с получением раствора, содержащего клетки; (b) фильтрацию раствора, содержащего клетки, через 70 мкм фильтр; (с) разбавление раствора, содержащего клетки, раствором, включающим 5,5% декстрана 40, 10% HSA и 5% ДМСО, до содержания примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, 1 до 15×106 или от 1 до 10×106 клеток на миллилитр; (d) криоконсервацию клеток; (е) оттаивание клеток; и (f) разбавление раствора, содержащего клетки, в соотношении от 1:1 до 1:11 (об./об.) 10% декстраном 40. В некоторых вариантах осуществления изобретения указанное разбавление на стадии (b) осуществляется до содержания не более примерно 15×106 клеток/мл. В некоторых других вариантах осуществления изобретения указанное разбавление на стадии (b) осуществляется до содержания не более примерно 10±3×106 клеток/мл. В еще одном варианте осуществления изобретения композиция, включающая клетки, получена способом, включающим: (а) центрифугирование множества клеток для сбора клеток; (b) повторное суспендирование клеток в 5,5% декстране 40; (с) центрифугирование клеток для сбора клеток; (d) еще одно суспендирование клеток в 5,5% растворе декстрана 40, который включает 10% HSA; (e) фильтрацию клеток через 70 мкм фильтр; (f) разбавление клеток в 5,5% декстране 40, 10% HSA и 5% ДМСО до содержания примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр; (g) криоконсервацию клеток; (h) оттаивание клеток; (i) разбавление клеток в соотношении от 1:1 до 1:11 (об./об.) в 10% растворе декстрана 40. В некоторых вариантах осуществления изобретения указанное разбавление на стадии (f) проводится до содержания клеток не более примерно 15×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения указанное разбавление на стадии (f) проводится до содержания не более примерно 10±3×106 клеток/мл. В определенных других вариантах осуществления изобретения, если содержание клеток составляет менее примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной.
Композиции, например, фармацевтические композиции, содержащие клетки согласно изобретению, могут включать любую клетку млекопитающих, включая стволовые клетки млекопитающих и нестволовые клетки млекопитающих. В некоторых вариантах осуществления изобретения композиции согласно изобретению, например, фармацевтические композиции, включающие клетки, могут включать изолированные плацентарные клетки, например, любые изолированные плацентарные клетки, описанные в настоящем изобретении (см., например, Раздел 5.3, ниже). В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD34-, CD10+ и CD105+, как определено проточной цитометрией. В более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки представляют собой плацентарные стволовые клетки. В еще одном более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки представляют собой мультипотентные плацентарные клетки. В еще одном специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки обладают потенциалом дифференцироваться в клетки неврального фенотипа, клетки остеогенного фенотипа или клетки хондрогенного фенотипа. В более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой CD200+. В еще одном более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+плацентарные клетки дополнительно представляют собой CD90+ или CD45-, как определено проточной цитометрией. В еще одном более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой CD90+ или CD45-, как определено проточной цитометрией. В более специфическом варианте осуществления CD34-, CD10+, CD105+, CD200+ плацентарные клетки дополнительно представляют собой CD90+ или CD45-, как определено проточной цитометрией. В еще одном более специфическом варианте осуществления CD34-, CD10+, CD105+, CD200+ плацентарные клетки дополнительно представляют собой CD90+ и CD45-, как определено проточной цитометрией. В еще одном более специфическом варианте осуществления изобретения CD34-, CD10+, CD105+, CD200+, CD90+, CD45- клетки дополнительно представляют собой CD80- и CD86-, как определено проточной цитометрией.
В более специфическом варианте осуществления изобретения CD34-, CD10+, CD105+ клетки дополнительно представляют собой клетки одного или нескольких фенотипов из CD29+, CD38-, CD44+, CD54+, CD80-, CD86-, SH3+ или SH4+. В другом более специфическом варианте осуществления изобретения клетки дополнительно представляют собой CD44+. В специфическом варианте осуществления любых из изолированных CD34-, CD10+, CD105+ плацентарных клеток, упомянутых выше, клетки дополнительно представляют собой клетки одного или нескольких фенотипов из CD117-, CD133-, KDR- (VEGFR2-), HLA-A,B,C+, HLA-DP,DQ,DR- и/или лиганда-1 запрограммированной гибели (Programmed Death-1 Ligand - (PDL1)+).
В некоторых других вариантах осуществления композиций указанные изолированные плацентарные клетки представляют собой CD200+ и HLA-G+; CD73+, CD105+ и CD200+; CD200+ и OCT-4+; CD73+, CD105+ и HLA-G+; CD73+ и CD105+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции плацентарных клеток, включающей указанные изолированные плацентарные клетки, когда указанная популяция культивируется в условиях, дающих возможность образованию эмбриоидоподобного тельца; или OCT-4+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции плацентарных клеток, включающей изолированные клетки, когда указанная популяция культивируется в условиях, дающих возможность образованию эмбриоидоподобных телец; или любые их сочетания. В специфическом варианте осуществления изобретения указанные CD200+, HLA-G+ клетки представляют собой CD34-, CD38-, CD45-, CD73+ и CD105+. В другом специфическом варианте осуществления изобретения указанные CD73+, CD105+и CD200+ клетки представляют собой CD34-, CD38-, CD45- и HLA-G+. В еще одном специфическом варианте осуществления изобретения указанные CD200+, OCT-4+ клетки представляют собой CD34-, CD38-, CD45-, CD73+, CD105+ и HLA-G+. В еще одном специфическом варианте осуществления изобретения указанные CD73+, CD105+ и HLA-G+клетки представляют собой CD34-, CD45-, OCT-4+ и CD200+. В еще одном специфическом варианте осуществления изобретения указанные CD73+ и CD105+ клетки представляют собой OCT-4+, CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанные OCT-4+ клетки представляют собой CD73+, CD105+, CD200+, CD34-, CD38- и CD45-. Изолированные плацентарные клетки, которые могут содержаться в композициях согласно изобретению, включающих клетки, более подробно описаны в Разделе 5.3, ниже.
В других специфических вариантах осуществления композиций согласно изобретению клетка представляют собой клетку, которая не является плацентарной клеткой. Например, в более специфических вариантах осуществления изобретения клетки могут представлять собой стволовые клетки или нестволовые клетки. В специфических вариантах осуществления изобретения, когда клетки представляют собой стволовые клетки, они могут представлять собой, например, зрелые стволовые клетки, соматические стволовые клетки, эмбриональные стволовые клетки, эмбриональные зародышевые клетки, пуповинные стволовые клетки, стволовые клетки амниотической жидкости, мезенхимальные стволовые клетки, полученные из костного мозга, мезенхимальные стволовые клетки, полученные из пуповинной крови, мезенхимальные стволовые клетки, полученные из периферической крови, мезенхимальные стволовые клетки, полученные из жировой ткани, или стволовые клетки, полученные из периоста. В еще одном специфическом варианте осуществления изобретения клетки представляют собой природные клетки-киллеры, например, CD3-, CD56+ природные клетки-киллеры.
5.3. ИЗОЛИРОВАННЫЕ ПЛАЦЕНТАРНЫЕ КЛЕТКИ И ПОПУЛЯЦИИ ИЗОЛИРОВАННЫХ ПЛАЦЕНТАРНЫХ КЛЕТОК
Изолированные плацентарные мультипотентные клетки, которые могут использоваться в композициях согласно изобретению, например, фармацевтических композициях, могут быть получены из плаценты или ее части, прикреплены к подложке культуры ткани и обладают характеристиками мультипотентных клеток или стволовых клеток. В некоторых вариантах осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в способах согласно изобретению, обладают способностью дифференцироваться в клетки неплацентарных типов. Изолированные плацентарные клетки, которые могут использоваться в способах согласно настоящему изобретению, могут быть фетальными или материнскими по происхождение (то есть могут иметь генотип плода или матери, соответственно). Предпочтительно, изолированные плацентарные клетки и популяции изолированных плацентарных клеток являются фетальными по происхождению. Термин «фетальные по происхождению» или «нематеринские по происхождению», в рамках изобретения, означает, что изолированные плацентарные клетки или популяции изолированных плацентарных клеток получены из пуповинных или плацентарных структур, связанных с плодом, то есть имеют фетальный генотип. Термин «материнские по происхождению», в рамках изобретения, означает, что клетки или популяции клеток получены из плацентарных структур, связанных с матерью, то есть имеют материнский генотип. Изолированные плацентарные клетки или популяции клеток, включающие изолированные плацентарные клетки могут включать изолированные плацентарные клетки, которые являются исключительно фетальными или исключительно материнскими по происхождению или могут включать смешанные популяции изолированных плацентарных клеток фетального и материнского происхождения. Изолированные плацентарные клетки и популяции клеток, включающие изолированные плацентарные клетки, могут идентифицироваться и выбираться с помощью морфологических признаков, маркерных характеристик и характеристик культуры, описанных ниже. Изолированные плацентарные клетки, подходящие для применения в способах и композициях согласно изобретению, могут включать, например, плацентарные клетки, описанные в Публикации заявки на патент США № 2007/0275362 и патенте США № 7468276, содержание которых таким образом полностью включено в настоящее описание путем ссылки.
5.3.1. Физические и морфологические характеристики
Изолированные плацентарные клетки, описанные в настоящем изобретении, при культивировании в первичных культурах или в культуре клеток прикрепляются к субстрату культуры ткани, например, поверхности контейнера культуры ткани (например, пластиковой поверхности контейнера с культурой ткани) или к поверхности культуры ткани, покрытой экстрацеллюлярной матрицей или лигандами, такими как ламинин, коллаген (например, природный или денатурированный), желатин, фибронектин, орнитин, витронектин и экстрацеллюлярный мембранный белок (например, MATRIGEL®). (BD Discovery Labware, Bedford, Mass.). Изолированные плацентарные клетки в культуре обычно принимают фибробластоидный звездчатый вид с рядом цитопласмических процессов, исходящих из центрального клеточного тела. Однако клетки морфологически могут отличаться от фибробластов, выращенных в таких же условиях, поскольку изолированные плацентарные клетки проявляют большее количество таких процессов, чем фибробласты. Морфологически изолированные плацентарные клетки также могут отличаться от гематопоэтических стволовых клеток, которые обычно в культуре принимают более округлую или напоминающую гальку морфологию.
5.3.2. Маркеры клеточной поверхности, молекулярные и генетические маркеры
Изолированные плацентарные клетки, например, мультипотентные клетки или стволовые клетки, и популяции изолированных плацентарных клеток экспрессируют множество маркеров, которые могут использоваться для идентификации и/или выделения стволовых клеток или популяций клеток, которые включают стволовые клетки. Изолированные плацентарные клетки и популяции плацентарных клеток, описанные в настоящем изобретении (то есть двух или более типов плацентарных клеток), включают плацентарные клетки и популяции, содержащие плацентарные клетки, полученные непосредственно из плаценты или любой ее части (например, амниона, хориона, плацентарных котиледонов и т.п.). Популяции изолированных плацентарных клеток включают также популяции (то есть две или более) изолированных плацентарных клеток в культуре и популяцию в контейнере, например, в пакете (пластиковом мешке). Изолированные плацентарные клетки согласно настоящему изобретению не являются трофобластами, цитотрофобластами, гемангиобластами, эмбриональными зародышевыми клетками или эмбриональными стволовыми клетками. Плацентарные мультипотентные клетки, которые могут использоваться в способах и композициях согласно настоящему изобретению, описаны в Публикации заявки на патент США № 2007/0275362 и патентах США №№ 7045148 и 7468276, содержание которых таким образом включено в настоящее описание путем ссылки, как описано ниже.
Изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно настоящему изобретению, обычно экспрессируют маркеры CD73, CD 105, CD200, HLA-G и/или OCT-4, не экспрессируют CD34, CD38 или CD45 и представляют собой HLA-DP, DQ, и DR-. Изолированные мультипотентные клетки обычно также представляют собой CD10+, CD29+, CD54+, CD90+, CD44+ и CD38+. В некоторых вариантах осуществления изобретения клетки представляют собой клетки одного или нескольких видов из SSEA3-, SSEA4- или ABC-p+. Изолированные плацентарные клетки могут также экспрессировать HLA-ABC (MHC-1). Маркеры могут использоваться в любой комбинации для идентификации изолированных плацентарных клеток, например, изолированных плацентарных стволовых клеток или изолированных мультипотентных клеток, и для отличия изолированных плацентарных клеток от клеток других типов. Поскольку изолированные плацентарные клетки могут экспрессировать CD73 и CD 105, они могут обладать характеристиками, подобными характеристикам мезенхимальных стволовых клеток. Отсутствие экспрессии CD34, CD38 и/или CD45, например, идентифицирует изолированные плацентарные клетки как негемопоэтические стволовые клетки.
В некоторых вариантах осуществления изобретения изолированные плацентарные клетки представляют собой изолированные плацентарные стволовые клетки. В некоторых других вариантах осуществления изобретения изолированные плацентарные клетки представляют собой изолированные плацентарные мультипотентные клетки. В одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD34-, CD10+, CD105+, как определено проточной цитометрией. В специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки представляют собой плацентарные стволовые клетки. В другом специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки представляют собой мультипотентные плацентарные клетки. В еще одном специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки обладают потенциалом дифференцироваться в клетки неврального фенотипа, клетки остеогенного фенотипа или клетки хондрогенного фенотипа. В еще одном специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой CD200+. В еще одном специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой CD45- или CD90+. В еще одном специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой CD45- и CD90+, как определено проточной цитометрией. В более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+, CD200+ плацентарные клетки дополнительно представляют собой CD90+ или CD45-, как определено проточной цитометрией. В еще одном более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+, CD200+ плацентарные клетки дополнительно представляют собой CD90+ и CD45-, как определено проточной цитометрией, то есть клетки представляют собой CD34-, CD10+, CD45-, CD90+, CD105+ и CD200+. В более специфическом варианте осуществления изобретения указанные CD34-, CD10+, CD45-, CD90+, CD105+, CD200+ клетки дополнительно представляют собой CD80- и CD86-.
В специфическом варианте осуществления любые из CD34-, CD10+, CD105+ клеток, описанных выше, дополнительно представляют собой клетки одного или нескольких фенотипов из CD29+, CD38-, CD44+, CD54+, SH3+ или SH4+. В еще одном более специфическом варианте осуществления изобретения клетки дополнительно представляют собой CD44+. В еще одном специфическом варианте осуществления изобретения любые клетки из изолированных CD34-, CD10+, CD105+плацентарных клеток, описанных выше, дополнительно представляют собой клетки одного или нескольких фенотипов из CD117-, CD133-, KDR- (VEGFR2-), HLA-A,B,C+, HLA-DP,DQ,DR- и/или PDL1+. В еще одном специфическом варианте осуществления изобретения CD34-, CD10+, CD105+ плацентарные клетки, описанные выше, дополнительно представляют собой клетки одного или нескольких фенотипов из CD13+, CD29+, CD33+, CD38-, CD44+, CD45-, CD54+, CD62E-, CD62L-, CD62P-, SH3+ (CD73+), SH4+ (CD73+), CD80-, CD86-, CD90+, SH2+ (CD105+), CD106/VCAM+, CD117-, CD144/VE-кадгеринlow, CD184/CXCR4-, CD200+, CD133-, OCT-4+, SSEA3-, SSEA4-, ABC-p+, KDR- (VEGFR2-), HLA-A,B,C+, HLA-DP,DQ,DR-, HLA-G+, лиганда-1 запрограммированной гибели (PDL1)+или любой их комбинации. В еще одном более специфическом варианте осуществления изобретения CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой клетки одного или нескольких фенотипов из CD13+, CD29+, CD33+, CD38-, CD44+, CD45-, CD54/ICAM+, CD62E-, CD62L-, CD62P-, SH3+ (CD73+), SH4+ (CD73+), CD80-, CD86-, CD90+, SH2+ (CD105+), CD106/VCAM+, CD117-, CD144/VE-кадгеринlow, CD184/CXCR4-, CD200+, CD133-, OCT-4+, SSEA3-, SSEA4-, ABC-p+, KDR- (VEGFR2-), HLA-A,B,C+, HLA-DP,DQ,DR-, HLA-G+ и лиганда-1 запрограммированной гибели (PDL1)+.
В еще одном варианте осуществления изобретения популяция клеток, которая может использоваться в композициях и способах согласно изобретению, представляет собой популяцию клеток, включающую, CD34-, CD10+ и CD105+ плацентарные клетки, например, обогащенную ими. В различных вариантах осуществления изобретения по меньшей мере примерно 10%, по меньшей мере примерно 20%, по меньшей мере примерно 30%, по меньшей мере примерно 40%, по меньшей мере примерно 50% или по меньшей мере примерно 60% клеток в указанной клеточной популяции представляют собой CD34-, CD10+ и CD105+ плацентарные клетки. Предпочтительно по меньшей мере примерно 70% клеток в указанной клеточной популяции представляют собой CD34-, CD10+, CD105+ плацентарные клетки. Более предпочтительно по меньшей мере примерно 90%, 95% или 99% указанных клеток представляют собой CD34-, CD10+ и CD105+. В специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки дополнительно представляют собой CD200+. В более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+, CD200+ плацентарные клетки дополнительно представляют собой CD90+ или CD45-, как определено проточной цитометрией. В еще одном более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+, CD200+ плацентарные клетки дополнительно представляют собой CD90+ и CD45-, как определено проточной цитометрией. В более специфическом варианте осуществления изобретения любые из изолированных CD34-, CD10+, CD105+ плацентарных клеток, описанных выше, дополнительно представляют собой клетки одного или нескольких фенотипов из CD29+, CD38-, CD44+, CD54+, SH3+ или SH4+. В еще одном более специфическом варианте осуществления изобретения изолированные CD34-, CD10+, CD105+ плацентарные клетки или изолированные CD34-, CD10+, CD105+, CD200+ плацентарные клетки дополнительно представляют собой CD44+. В специфическом варианте осуществления любой из популяций клеток, включающих изолированные CD34-, CD10+, CD105+ плацентарные клетки, указанные выше, изолированные плацентарные клетки дополнительно представляют собой клетки одного или нескольких видов из CD13+, CD29+, CD33+, CD38-, CD44+, CD45-, CD54+, CD62E-, CD62L-, CD62P-, SH3+(CD73+), SH4+ (CD73+), CD80-, CD86-, CD90+, SH2+ (CD105+), CD106/VCAM+, CD117-, CD144/VE-кадгеринlow, CD184/CXCR4-, CD200+, CD133-, OCT-4+, SSEA3-, SSEA4-, ABC-p+, KDR- (VEGFR2-), HLA-A,B,C+, HLA-DP,DQ,DR-, HLA-G+, лиганда-1 запрограмированной гибели клеток (PDL1)+ или любой их комбинации. В более специфическом варианте осуществления изобретения CD34-, CD10+, CD105+ клетки дополнительно представляют собой CD13+, CD29+, CD33+, CD38-, CD44+, CD45-, CD54/ICAM+, CD62E-, CD62L-, CD62P-, SH3+ (CD73+), SH4+ (CD73+), CD80-, CD86-, CD90+, SH2+ (CD105+), CD 106/VCAM+, CD117-, CD 144/VE-кадгеринlow, CD184/CXCR4-, CD200+, CD133-, OCT-4+, SSEA3-, SSEA4-, ABC-p+, KDR- (VEGFR2-), HLA-A,B,C+, HLA-DP,DQ,DR-, HLA-G+ и лиганд-1 программированной гибели (PDL1)+.
В некоторых вариантах осуществления изобретения изолированные плацентарные клетки представляют собой клетки одного или нескольких фенотипов из CD10+, CD29+, CD34-, CD38-, CD44+, CD45-, CD54+, CD90+, SH2+, SH3+, SH4+, SSEA3-, SSEA4-, OCT-4+ и ABC-p+, где указанные изолированные плацентарные клетки, получены физической и/или ферментативной деструкцией плацентарной ткани. В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+ и ABC-p+. В другом специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+ и CD34-, где указанные изолированные плацентарные клетки обладают по меньшей мере одной из следующих характеристик: CD10+, CD29+, CD44+, CD45-, CD54+, CD90+, SH3+, SH4+, SSEA3- и SSEA4-. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+, CD34-, CD10+, CD29+, CD44+, CD45-, CD54+, CD90+, SH3+, SH4+, SSEA3- и SSEA4-. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+, CD34-, SSEA3- и SSEA4-. В более специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+ и CD34-, и либо SH2+, либо SH3+. В еще более специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+, CD34-, SH2+ и SH3+. В другом более специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+, CD34-, SSEA3- и SSEA4-, и либо SH2+, либо SH3+. В еще одном более специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+ и CD34-, и либо SH2+, либо SH3+, и клетки по меньшей мере одного из фенотипов из CD10+, CD29+, CD44+, CD45-, CD54+, CD90+, SSEA3- или SSEA4-. Еще одном более специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+, CD34-, CD10+, CD29+, CD44+, CD45-, CD54+, CD90+, SSEA3- и SSEA4-, и либо SH2+, либо SH3+.
В одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой CD200+ или HLA-G+. В одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD200+ и HLA-G+. В другом специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD73+ и CD105+. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD34-, CD38-, CD45-, CD73+ и CD105+. В еще одном специфическом варианте осуществления изобретения указанные CD200+ или HLA-G+ изолированные плацентарные клетки способствуют образованию эмбриоидопободных телец в популяции плацентарных клеток, включающей изолированные плацентарные клетки, в условиях, которые дают возможность образованию эмбриоидоподобных телец. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки изолированы от плацентарных клеток, которые не являются стволовыми или мультипотентными клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки изолированы от плацентарных стволовых клеток, которые не проявляют эти маркеры.
В другом варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно изобретению, представляет собой популяцию клеток, включающую, CD200+, HLA-G+ плацентарные клетки, например, обогащенную указанными клетками. В различных вариантах осуществления изобретения по меньшей мере примерно 10%, по меньшей мере примерно 20%, по меньшей мере примерно 30%, по меньшей мере примерно 40%, по меньшей мере примерно 50% или по меньшей мере примерно 60% клеток в указанной клеточной популяции представляют собой CD200+, HLA-G+ плацентарные клетки. Предпочтительно по меньшей мере примерно 70% клеток в указанной клеточной популяции представляют собой CD200+, HLA-G+ плацентарные клетки. Более предпочтительно по меньшей мере примерно 90%, 95% или 99% указанных клеток представляют собой CD200+, HLA-G+ плацентарные клетки. В одном специфическом варианте изолированных популяций указанные плацентарные клетки также представляют собой CD73+ и CD105+. В другом специфическом варианте указанные плацентарные клетки представляют собой также CD34-, CD38- или CD45-. В более специфическом варианте указанные плацентарные клетки представляют собой также CD34-, CD38-, CD45-, CD73+ и CD105+. В еще одном варианте указанные изолированная популяция клеток продуцирует одно или несколько эмбриоидоподобных телец, когда культивируется в условиях, которые дают возможность образованию эмбриоидоподобных телец. В еще одном специфическом варианте осуществления изобретения указанная популяция плацентарных клеток изолирована от плацентарных клеток, которые не являются стволовыми клетками. В еще одном специфическом варианте осуществления изобретения указанная популяция плацентарных клеток изолирована от плацентарных клеток, которые не проявляют указанных маркеров.
В еще одном варианте осуществления изобретения плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой CD73+, CD105+ и CD200+. В другом специфическом варианте осуществления изобретения указанные плацентарная клетка представляет собой HLA-G+. В еще одном специфическом варианте указанные плацентарные клетки представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте указанные плацентарные клетки представляют собой CD34-, CD38- и CD45-. В более специфическом варианте осуществления указанные плацентарные клетки представляют собой CD34-, CD38-, CD45- и HLA-G+. В еще одном специфическом варианте изобретения изолированные CD73+, CD105+и CD200+ плацентарные клетки способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции указанных плацентарных клеток, когда популяция культивируется в условиях, которые дают возможность образованию эмбриоидоподобных телец. В еще одном специфическом варианте указанные плацентарные клетки изолированы от плацентарных клеток, которые не являются стволовыми клетками. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки изолированы от плацентарных клеток, которые не проявляют этих маркеров.
В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно изобретению, представляет собой популяцию клеток, включающую изолированные CD73+, CD105+, CD200+ плацентарные клетки. В различных вариантах осуществления изобретения по меньшей мере примерно 10%, по меньшей мере примерно 20%, по меньшей мере примерно 30%, по меньшей мере примерно 40%, по меньшей мере примерно 50% или по меньшей мере примерно 60% клеток в указанном клеточной популяции представляют собой изолированные CD73+, CD105+, CD200+ плацентарные клетки. В еще одном варианте осуществления изобретения по меньшей мере примерно 70% указанных клеток в указанной популяции клеток являются изолированными CD73+, CD105+, CD200+ плацентарными клетками. В другом варианте осуществления изобретения по меньшей мере примерно 90%, 95% или 99% клеток в указанной популяции являются изолированными CD73+, CD105+, CD200+ плацентарными клетками. В специфическом варианте осуществления указанных популяций изолированные плацентарные клетки представляют собой HLA-G+. В другом специфическом варианте изолированные плацентарные клетки дополнительно представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте изолированные плацентарные клетки дополнительно представляют собой CD34-, CD38- и CD45-. В более специфическом варианте осуществления изобретения изолированные плацентарные клетки дополнительно представляют собой CD34-, CD38-, CD45- и HLA-G+. В еще одном специфическом варианте указанная популяция клеток продуцирует одно или несколько эмбриоидоподобных телец, когда выращивается в условиях, которые дают возможность образованию эмбриоидоподобных телец. В еще одном специфическом варианте осуществления изобретения указанная популяция плацентарных клеток изолирована от плацентарных клеток, которые не являются стволовыми клетками. В еще одном специфическом варианте осуществления изобретения указанная популяция плацентарных стволовых клеток отделена от плацентарных клеток, которые не проявляют этих характеристик.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой CD200+ и OCT-4+. В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD73+ и CD105+. В другом специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки представляют собой HLA-G+. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD200+, OCT-4+ плацентарные клетки представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте осуществления изобретения указанные CD200+, OCT-4+ плацентарные клетки представляют собой CD34-, CD38- и CD45-. В более специфическом варианте осуществления изобретения указанные изолированные CD200+, OCT-4+ плацентарные клетки представляют собой CD34-, CD38-, CD45-, CD73+, CD105+ и HLA-G+. В еще одном специфическом варианте осуществления изобретения изолированные CD200+, OCT-4+ плацентарные клетки способствуют образованию одного или нескольких эмбриоидоподобных телец популяцией плацентарных клеток, которая выключает изолированные клетки, когда популяция культивируется в условиях, которые дают возможность образованию эмбриоидоподобных телец. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD200+, OCT-4+ плацентарные клетки изолированы от плацентарных клеток, которые не являются стволовыми клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD200+, OCT-4+ плацентарные клетки изолированы от плацентарных клеток, которые не проявляют этих характеристик.
В еще одном варианте осуществления изобретения клеточная популяции, которая может использоваться в композициях и способах согласно изобретению, представляет собой популяцию клеток, включающую CD200+, OCT-4+ плацентарные клетки, например, обогащенную CD200+, OCT-4+ плацентарными клетками. В различных вариантах осуществления изобретения по меньшей мере примерно 10%, по меньшей мере примерно 20%, по меньшей мере примерно 30%, по меньшей мере примерно 40%, по меньшей мере примерно 50% или по меньшей мере примерно 60% клеток в указанной клеточной популяции являются изолированными CD200+, OCT-4+ плацентарными клетками. В еще одном варианте осуществления изобретения по меньшей мере примерно 70% указанных клеток представляют собой изолированные CD200+, OCT-4+ плацентарные клетки. В еще одном варианте осуществления изобретения по меньшей мере примерно 80%, 90%, 95% или 99% клеток в указанной клеточной популяции представляют собой указанные CD200+, OCT-4+ плацентарные клетки. В специфическом варианте осуществления изолированных популяций, указанные изолированные CD200+, OCT-4+ плацентарные клетки дополнительно представляют собой CD73+ и CD105+. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD200+, OCT-4+ плацентарные клетки дополнительно представляют собой HLA-G+. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD200+, OCT-4+ плацентарные клетки дополнительно представляют собой CD34-, CD38- и CD45-. В более специфическом варианте осуществления изобретения указанные изолированные CD200+, OCT-4+ плацентарные клетки дополнительно представляют собой CD34-, CD38-, CD45-, CD73+, CD105+ и HLA-G+. В еще одном специфическом варианте осуществления изобретения клеточная популяция продуцирует одно или несколько эмбриоидоподобных телец, когда культивируется в условиях, которые дают возможность образованию эмбриоидоподобные телец. В еще одном специфическом варианте осуществления изобретения указанная клеточная популяция изолирована от плацентарных клеток, которые не являются изолированными CD200+, OCT-4+ плацентарными клетками. В еще одном специфическом варианте осуществления изобретения указанная клеточная популяция изолирована от плацентарных клеток, которые не проявляют этих маркеров.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой CD73+, CD105+ и HLA-G+. В еще одном специфическом варианте осуществления изобретения изолированные CD73+, CD105+, HLA-G+ плацентарные клетки дополнительно представляет собой CD34-, CD38- или CD45-. В еще одном специфическом варианте осуществления изобретения изолированные CD73+, CD105+, HLA-G+ плацентарные клетки дополнительно представляют собой CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения изолированные CD73+, CD105+, HLA-G+ плацентарные клетки дополнительно представляют собой OCT-4+. В еще одном специфическом варианте осуществления изобретения изолированные CD73+, CD105+, HLA-G+ плацентарные клетки дополнительно представляют собой CD200+. В более специфическом варианте осуществления изобретения изолированные CD73+, CD105+, HLA-G+ плацентарные клетки дополнительно представляют собой CD34-, CD38-, CD45-, OCT-4+ и CD200+. В еще одном специфическом варианте осуществления изобретения изолированные CD73+, CD105+, HLA-G+ плацентарные клетки способствуют образованию эмбриоидоподобных телец в популяции плацентарных клеток, включающей указанные клетки, когда популяция культивируется в условиях, которые дают возможность образованию эмбриоидоподобных телец. В другом специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+, HLA-G+ плацентарные клетки изолированы от плацентарных клеток, которые не являются изолированными CD73+, CD105+ и HLA-G+ плацентарными клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+, HLA-G+ плацентарные клетки изолированы от плацентарных клеток, которых не проявляют этих маркеров.
В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно изобретению, представляет собой популяцию клеток, включающую изолированные CD73+, CD105+ и HLA-G+ плацентарные клетки, например, обогащена изолированными CD73+, CD105+ и HLA-G+ плацентарными клетками. В различных вариантах осуществления изобретения по меньшей мере примерно 10%, по меньшей мере примерно 20%, по меньшей мере примерно 30%, по меньшей мере примерно 40%, по меньшей мере примерно 50% или по меньшей мере, примерно 60% клеток в указанной популяции клеток представляют собой изолированные CD73+, CD105+, HLA-G+ плацентарные клетки. В еще одном варианте осуществления изобретения по меньшей мере примерно 70% клеток в указанной популяции клеток представляют собой изолированные CD73+, CD105+, HLA-G+плацентарные клетки. В еще одном варианте осуществления изобретения по меньшей мере примерно 90%, 95% или 99% клеток в указанной популяции клеток представляют собой изолированные CD73+, CD105+, HLA-G+плацентарные клетки. В специфическом варианте осуществления указанных популяций указанные изолированные CD73+, CD105+, HLA-G+плацентарные клетки дополнительно представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+, HLA-G+плацентарные клетки дополнительно представляют собой CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+, HLA-G+плацентарные клетки дополнительно представляют собой OCT-4+. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+, HLA-G+плацентарные клетки дополнительно представляют собой CD200+. В более специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+, HLA-G+плацентарные клетки дополнительно представляют собой CD34-, CD38-, CD45-, OCT-4+ и CD200+. В еще одном специфическом варианте осуществления изобретения указанная клеточная популяция отделена от плацентарных клеток, которые не являются CD73+, CD105+, HLA-G+плацентарными клетками. В еще одном специфическом варианте осуществления изобретения указанная клеточная популяция отделена от плацентарных клеток, которые не проявляют этих маркеров.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой CD73+ и CD105+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции изолированных плацентарных клеток, включающей указанные CD73+, CD105+ клетки, когда указанная популяция культивируется в условиях, которые дают возможность образованию эмбриоидоподобных телец. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки дополнительно представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки дополнительно представляют собой CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки дополнительно представляют собой OCT-4+. В более специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки дополнительно представляют собой OCT-4+, CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки изолированы от плацентарных клеток, которые не являются указанными клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки изолированы от плацентарных клеток, которые не проявляют этих характеристик.
В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно настоящему изобретению, представляет собой популяцию клеток, включающую изолированные плацентарные клетки, которые представляют собой CD73+, CD105+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции изолированных плацентарных клеток, включающей указанные клетки, когда указанная популяция культивируется в условиях, которые дают возможность образованию эмбриоидоподобных телец. В различных вариантах осуществления изобретения по меньшей мере примерно 10%, по меньшей мере примерно 20%, по меньшей мере примерно 30%, по меньшей мере примерно 40%, по меньшей мере примерно 50% или по меньшей мере примерно 60% клеток в указанной популяции клеток представляют собой указанные изолированные CD73+, CD105+плацентарные клетки. В еще одном варианте осуществления изобретения по меньшей мере примерно 70% клеток в указанной популяции клеток представляют собой указанные изолированные CD73+, CD105+плацентарные клетки. В еще одном варианте осуществления изобретения по меньшей мере примерно 90%, 95% или 99% клеток в указанной популяции клеток представляют собой указанные изолированные CD73+, CD105+плацентарные клетки. В специфическом варианте осуществления указанных популяций указанные изолированные CD73+, CD105+плацентарные клетки дополнительно представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки дополнительно представляют собой CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки дополнительно представляют собой OCT-4+. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки дополнительно представляют собой CD200+. В более специфическом варианте осуществления изобретения указанные изолированные CD73+, CD105+плацентарные клетки дополнительно представляют собой CD34-, CD38-, CD45-, OCT-4+ и CD200+. В еще одном специфическом варианте осуществления изобретения, указанная клеточная популяция изолирована от плацентарных клеток, которые не являются указанными изолированными CD73+, CD105+плацентарными клетками. В еще одном специфическом варианте осуществления изобретения указанная клеточная популяция отделена от плацентарных клеток, которые не проявляют этих маркеров.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой OCT-4+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции изолированных плацентарных клеток, включающей указанные клетки, когда выращиваются в условиях, которые дают возможность образованию эмбриоидоподобных телец. В специфическом варианте осуществления изобретения указанные изолированные OCT-4+плацентарные клетки дополнительно представляют собой CD73+ и CD105+. В еще одном специфическом варианте осуществления изобретения указанные изолированные OCT-4+плацентарные клетки дополнительно представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные OCT-4+плацентарные клетки дополнительно представляют собой CD200+. В более специфическом варианте осуществления изобретения указанные изолированные OCT-4+плацентарные клетки дополнительно представляют собой CD73+, CD105+, CD200+, CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные OCT-4+ плацентарные клетки изолированы от плацентарных клеток, которые не являются OCT-4+плацентарными клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные OCT-4+плацентарные клетки изолированы от плацентарных клеток, которые не проявляют этих характеристик.
В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно настоящему изобретению, представляет собой популяцию клеток, включающую изолированные плацентарные клетки, например, обогащена указанными клетками, которые представляют собой OCT-4+, и способствует образованию одного или нескольких эмбриоидоподобных телец в популяции изолированных плацентарных клеток, включающей указанные клетки, когда указанная популяция культивируется в условиях, которые дают возможность образованию эмбриоидоподобных телец. В различных вариантах осуществления изобретения по меньшей мере примерно 10%, по меньшей мере примерно 20%, по меньшей мере примерно 30%, по меньшей мере примерно 40%, по меньшей мере примерно 50% или по меньшей мере примерно 60% клеток в указанной популяции клеток представляют собой указанные изолированные OCT-4+плацентарные клетки. В еще одном варианте осуществления изобретения по меньшей мере примерно 70% клеток в указанной популяции клеток представляют собой указанные изолированные OCT-4+плацентарные клетки. В еще одном варианте осуществления изобретения по меньшей мере примерно 80%, 90%, 95% или 99% клеток в указанной популяции клеток представляют собой указанные изолированные OCT-4+плацентарные клетки. В специфическом варианте осуществления указанных популяций указанные изолированные OCT-4+плацентарные клетки дополнительно представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные OCT-4+плацентарные клетки дополнительно представляют собой CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанные изолированные OCT-4+плацентарные клетки дополнительно представляют собой CD73+ и CD105+. В еще одном специфическом варианте осуществления изобретения указанные изолированные OCT-4+плацентарные клетки дополнительно представляют собой CD200+. В более специфическом варианте осуществления изобретения указанные изолированные OCT-4+плацентарные клетки дополнительно представляют собой CD73+, CD105+, CD200+, CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанная клеточная популяция изолирована от плацентарных клеток, которые не являются указанными клетками. В еще одном специфическом варианте осуществления изобретения указанная клеточная популяция отделена от плацентарных клеток, которые не проявляют этих маркеров.
В некоторых других вариантах осуществления изобретения изолированные плацентарные клетки представляют собой клетки одного или нескольких видов из CD10+, CD29+, CD34-, CD38-, CD44+, CD45-, CD54+, CD90+, SH2+, SH3+, SH4+, SSEA3-, SSEA4-, OCT-4+, MHC-I+ или ABC-p+. В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD10+, CD29+, CD34-, CD38-, CD44+, CD45-, CD54+, CD90+, SH2+, SH3+, SH4+, SSEA3-, SSEA4- и OCT-4+. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD10+, CD29+, CD34-, CD38-, CD45-, CD54+, SH2+, SH3+ и SH4+. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD10+, CD29+, CD34-, CD38-, CD45-, CD54+, SH2+, SH3+, SH4+ и OCT-4+. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD10+, CD29+, CD34-, CD38-, CD44+, CD45-, CD54+, CD90+, HLA-1+, SH2+, SH3+ и SH4+. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+ и ABC-p+. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой SH2+, SH3+, SH4+ и OCT-4+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+, CD34-, SSEA3- и SSEA4-. В специфическом варианте осуществления изобретения указанные изолированные OCT-4+, CD34-, SSEA3- и SSEA4- плацентарные клетки дополнительно представляют собой CD10+, CD29+, CD34-, CD44+, CD45-, CD54+, CD90+, SH2+, SH3+, и SH4+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+ и CD34-, а также либо SH3+, либо SH4+. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD34-, а также либо CD10+, CD29+, CD44+, CD54+, CD90+ или OCT-4+.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой изолированные CD10+, CD34-, CD105+ и CD200+плацентарные клетки. В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно настоящему изобретению, представляет собой популяцию клеток, включающую плацентарные клетки, в которой по меньшей мере примерно 70%, по меньшей мере примерно 80%, по меньшей мере примерно 90%, по меньшей мере примерно 95% или по меньшей мере примерно 99% указанной популяции клеток представляют собой CD10+, CD34-, CD105+, CD200+плацентарные клетки. В специфическом варианте осуществления указанных выше вариантов указанные плацентарные клетки дополнительно представляют собой CD90+ и CD45-. В специфическом варианте осуществления изобретения указанная плацентарная клетка или популяция плацентарных клеток отделена от плацентарных клеток, которые не являются стволовыми клетками. В еще одном специфическом варианте осуществления изобретения указанная плацентарная клетка или популяция плацентарных клеток отделена от плацентарных клеток, которые не проявляют этих характеристик. В еще одном специфическом варианте осуществления изобретения указанная изолированная плацентарная клетка является нематеринской по происхождению. В еще одном специфическом варианте осуществления изобретения по меньшей мере примерно 90%, по меньшей мере примерно 95% или по меньшей мере примерно 99% указанных клеток в указанной популяции изолированных плацентарных клеток является нематеринской по происхождению.
В еще одном специфическом варианте осуществления указанных плацентарных клеток или популяций клеток, включающих изолированные плацентарные клетки, количество указанных клеток увеличивалось или численность клеточной популяции увеличивалась, например, пересевом по меньшей мере примерно или не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 раз, или пролиферацией по меньшей мере примерно или не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38 или 40 удвоений популяции. В еще одном специфическом варианте осуществления изолированных плацентарных клеток или популяций клеток, включающих изолированные плацентарные клетки, которые описаны в настоящем изобретении, указанные изолированные плацентарные клетки являются фетальными по происхождению (то есть имеют фетальный генотип).
В еще одном варианте осуществления изобретения плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой OCT-4+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции указанных изолированных плацентарных клеток, когда выращиваются в условиях, которые дают возможность образованию эмбриоидоподобных телец. В специфическом варианте осуществления изобретения указанные плацентарные клетки представляют собой CD73+ и CD105+. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки представляют собой CD34-, CD38- или CD45-. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки представляют собой CD200+. В более специфическом варианте осуществления изобретения указанные плацентарные клетки представляют собой CD73+, CD105+, CD200+, CD34-, CD38- и CD45-. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки изолированы от плацентарных клеток, которые не являются стволовыми клетками. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки изолированы от плацентарных клеток, которые не проявляют этих характеристик.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой изолированные HLA-A,B,C-, CD45-, CD133- и CD34- плацентарные клетки. В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно настоящему изобретению, представляет собой популяцию клеток, включающую изолированные плацентарные клетки, в которой по меньшей мере примерно 70%, по меньшей мере примерно 80%, по меньшей мере примерно 90%, по меньшей мере примерно 95% или по меньшей мере примерно 99% клеток в указанной популяции изолированных клеток представляют собой изолированные HLA-A,B,C-, CD45-, CD133- и CD34- плацентарные клетки. В специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки или популяция изолированных плацентарных клеток изолирована от плацентарных клеток, которые не являются HLA-A,B,C-, CD45-, CD133- и CD34- плацентарными клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки являются нематеринскими по происхождению. В еще одном специфическом варианте осуществления изобретения указанные изолированные популяция плацентарных клеток по существу свободны от материнских компонентов; например, по меньшей мере примерно 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 90%, 85%, 90%, 95%, 98% или 99% указанных клеток в указанной популяции изолированных плацентарных клеток являются нематеринскими по происхождения.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой изолированные CD10+, CD13+, CD33+, CD45-, CD117- и CD133- плацентарные клетки. В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно изобретению, представляет собой популяцию клеток, включающую изолированные плацентарные клетки, в которой по меньшей мере примерно 70%, по меньшей мере примерно 80%, по меньшей мере примерно 90%, по меньшей мере примерно 95% или по меньшей мере примерно 99% клеток в указанной популяции клеток представляют собой изолированные CD10+, CD13+, CD33+, CD45-, CD117- и CD133- плацентарные клетки. В специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки или популяция изолированных плацентарных клеток изолированы(а) от плацентарных клеток, которые не являются указанными изолированными плацентарными клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные CD10+, CD13+, CD33+, CD45-, CD117- и CD133- плацентарные клетки являются нематеринскими по происхождению, т.е. имеют фетальный генотип. В еще одном специфическом варианте осуществления изобретения по меньшей мере примерно 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 90%, 85%, 90%, 95%, 98% или 99% указанных клеток в указанных изолированной популяции плацентарных клеток являются нематеринскими по происхождению. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки или популяция изолированных плацентарных клеток изолированы от плацентарных клеток, которые не проявляют этих характеристик.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой изолированные CD10-, CD33-, CD44+, CD45- и CD117- плацентарные клетки. В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно настоящему изобретению, представляет собой популяцию клеток, включающую изолированные плацентарные клетки, например, обогащена ими, где по меньшей мере примерно 70%, по меньшей мере примерно 80%, по меньшей мере примерно 90%, по меньшей мере примерно 95% или по меньшей мере примерно 99% клеток в указанной популяции клеток представляют собой изолированные CD10-, CD33-, CD44+, CD45- и CD117- плацентарные клетки. В специфическом варианте осуществления изобретения указанная изолированная плацентарная клетка или популяция изолированных плацентарных клеток отделена от плацентарных клеток, которые не являются указанными клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки являются нематеринскими по происхождению. В еще одном специфическом варианте осуществления изобретения по меньшей мере примерно 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 90%, 85%, 90%, 95%, 98% или 99% указанных клеток в указанной популяции являются нематеринскими по происхождению. В еще одном специфическом варианте осуществления изобретения указанная изолированная плацентарная клетка или популяция изолированных плацентарных клеток отделена от плацентарных клеток, которые не проявляют указанных маркеров.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой изолированные CD10-, CD13-, CD33-, CD45- и CD117- плацентарные клетки. В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно изобретению, представляет собой популяцию клеток, включающую изолированные CD10-, CD13-, CD33-, CD45- и CD117- плацентарные клетки, например, обогащена указанными клетками, где по меньшей мере примерно 70%, по меньшей мере примерно 80%, по меньшей мере примерно 90%, по меньшей мере примерно 95% или по меньшей мере примерно 99% клеток в указанной популяции представляют собой CD10-, CD13-, CD33-, CD45- и CD117- плацентарные клетки. В специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки или популяция изолированных плацентарных клеток изолированы от плацентарных клеток, которые не являются указанными клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки являются нематеринскими по происхождению. В еще одном специфическом варианте осуществления изобретения по меньшей мере примерно 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 90%, 85%, 90%, 95%, 98% или 99% указанных клеток в указанной клеточной популяции являются нематеринскими по происхождению. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки или популяция изолированных плацентарных клеток изолированы от плацентарных клеток, которые не проявляют этих характеристик.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой HLA A,B,C+, CD45-, CD34- и CD133- и дополнительно представляют собой CD10+, CD13+, CD38+, CD44+, CD90+, CD105+, CD200+ и/или HLA-G+, и/или являются отрицательными для CD117. В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно настоящему изобретению, представляет собой популяцию клеток, включающую изолированные плацентарные клетки, где по меньшей мере примерно 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98% или примерно 99% клеток в указанной популяции являются изолированными плацентарными клетками HLA A,B,C-, CD45-, CD34-, CD133- и дополнительно являются позитивными для CD10, CD13, CD38, CD44, CD90, CD105, CD200 и/или HLA-G и/или негативными для CD117. В специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки или популяция изолированных плацентарных клеток изолированы от плацентарных клеток, которые не являются указанными клетками. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки являются нематеринскими по происхождению. В еще одном специфическом варианте осуществления изобретения по меньшей мере примерно 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 90%, 85%, 90%, 95%, 98% или 99% указанных клеток в указанной клеточной популяции являются нематеринскими по происхождению. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки или популяция изолированных плацентарных клеток изолированы от плацентарных клеток, которые не проявляют этих маркеров.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой изолированные плацентарные клетки CD200+ и CD10+, как определено связыванием антитела, и CD117-, как определено связыванием антитела и ОТ-ПЦР. В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой изолированные плацентарные клетки, например, плацентарные стволовые клетки или плацентарные мультипотентные клетки, которые представляют собой CD10+, CD29-, CD54+, CD200+, HLA-G+, HLA класса I- и β-2-микроглобулин-. В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой плацентарные клетки, где экспрессия по меньшей мере одного клеточного маркера по меньшей мере в два раза больше, чем мезенхимальной стволовой клеткой (например, мезенхимальной стволовой клеткой, полученной из костного мозга). В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки являются нематеринскими по происхождению. В еще одном специфическом варианте осуществления изобретения по меньшей мере примерно 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 90%, 85%, 90%, 95%, 98% или 99% указанных клеток в указанной клеточной популяции являются нематеринскими по происхождению.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой изолированные плацентарные клетки, например, плацентарные стволовые клетки или плацентарные мультипотентные клетки, которые представляют собой клетки одного или нескольких фенотипов из CD10+, CD29+, CD44+, CD45-, CD54/ICAM+, CD62-E-, CD62-L-, CD62-P-, CD80-, CD86-, CD103-, CD104-, CD105+, CD 106/VCAM+, CD144/VE-кадгеринlow, CD184/CXCR4-, β2-микроглобулинlow, MHC-Ilow, MHC-II-, HLA-Glow, и/или PDL1low. В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой по меньшей мере CD29+ и CD54+. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой по меньшей мере CD44+ и CD106+. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой по меньшей мере CD29+.
В еще одном варианте осуществления изобретения клеточная популяция, которая может использоваться в композициях и способах согласно изобретению, включает изолированные плацентарные клетки, и по меньшей мере 50%, 60%, 70%, 80%, 90%, 95%, 98% или 99% клеток в указанной клеточной популяции представляют собой изолированные плацентарные клетки, которые представляют собой клетки одного или нескольких фенотипов из CD10+, CD29+, CD44+, CD45-, CD54/ICAM+, CD62-E-, CD62-L-, CD62-P-, CD80-, CD86-, CD103-, CD104-, CD105+, CD106/VCAM+, CD144/VE-кадгеринlow, CD184/CXCR4-, β2-микроглобулинlow, MHC-Ilow, MHC-II-, HLA-Glow и/или PDLllow. В более специфическом варианте осуществления изобретения по меньшей мере 50%, 60%, 70%, 80%, 90%, 95%, 98% или 99% клеток в указанной клеточной популяции представляют собой CD10+, CD29+, CD44+, CD45-, CD54/ICAM+, CD62-E-, CD62-L-, CD62-P-, CD80-, CD86-, CD103-, CD104-, CD105+, CD106/VCAM+, CD144/VE-кадгеринlow, CD184/CXCR4-, β2-микроглобулинlow, MHC-Ilow, MHC-II-, HLA-Glow и/или PDL1low.
В некоторых вариантах осуществления изолированных плацентарных клеток, указанные изолированные плацентарные клетки не дифференцируются в процессе культивирования в ростовой среде, т.е., в среде, приготовленной для способствования пролиферации, например, во время пролиферации в ростовой среде. В еще одном специфическом варианте осуществления изобретения указанным изолированным плацентарным клеткам не требуется питающий слой для пролиферации. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки не дифференцируются в культуре в отсутствие питающего слоя исключительно вследствие отсутствия питающего слоя.
В еще одном варианте осуществления изобретения клетки, которые могут использоваться в композициях и способах согласно изобретению, представляют собой изолированные плацентарные клетки, где множество указанных изолированных плацентарных клеток являются позитивными для альдегиддегидрогеназы (aldehyde dehydrogenase - ALDH), как установлено в опыте количественного определения альдегиддегидрогеназной активности. Такие тесты определения биологической активности известны в данном области техники (см., например, Bostian and Betts, Biochem. J., 173, 787, (1978)). В специфическом варианте осуществления изобретения в указанном тесте определения биологической активности ALDH в качестве маркера альдегиддегидрогеназной активности используется ALDEFLUOR® (Aldagen, Inc., Ashland, Oregon). В специфическом варианте осуществления изобретения указанное множество составляет от примерно 3% до примерно 25% клеток в указанное популяции клеток. В еще одном варианте осуществления изобретения предоставлена популяция изолированных клеток пуповины, например, мультипотентных изолированных клеток пуповины, где множество указанных изолированных клеток пуповины являются положительными для альдегиддегидрогеназы, как установлено опытом определения активности альдегиддегидрогеназы, в котором в качестве индикатора альдегиддегидрогеназной активности используется ALDEFLUOR®. В специфическом варианте осуществления изобретения указанное множество составляет от примерно 3% до примерно 25% клеток в указанной популяции клеток. В еще одном варианте осуществления изобретения указанная популяция изолированных плацентарных клеток или изолированных клеток пуповины показывает по меньшей мере в три раза или по меньшей мере в пять раз более высокую ALDH активность, чем популяция мезенхимальных стволовых клеток, полученных из костного мозга, включающая примерно такое же количество клеток и выращенная в таких же условиях.
В еще одном специфическом варианте осуществления указанных плацентарных клеток или популяций клеток, включающих изолированные плацентарные клетки, количество указанных клеток увеличивалось или численность клеточной популяции увеличивалась, например, пассированием по меньшей мере примерно или не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 раз, или пролиферацией по меньшей мере с примерно или не более чем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38 или 40 удвоениями популяции. В еще одном специфическом варианте осуществления изобретения изолированных плацентарных клеток или популяций клеток, включающих изолированные плацентарные клетки, которые описаны в настоящем изобретении, указанные изолированные плацентарные клетки являются фетальными по происхождению (то есть имеют фетальный генотип).
В специфическом варианте любой из указанных выше изолированных плацентарных клеток или популяций изолированных плацентарных клеток, кариотип клеток или по меньшей мере примерно 95% или примерно 99% клеток в указанной популяции является нормальным. В еще одном специфическом варианте любой из описанных выше плацентарных клеток или описанных выше клеточных популяций, клетки или клетки в популяциях клеток являются нематеринскими по происхождению.
Изолированные плацентарные клетки или популяции изолированных плацентарных клеток, несущие любые из указанных выше комбинаций маркеров, могут объединяться в любом соотношении. Любые две или несколько из упомянутых выше популяций изолированных плацентарных клеток могут объединяться для получения популяции изолированных плацентарных клеток. Например, популяция изолированных плацентарных клеток может включать первую популяцию изолированных плацентарных клеток, определенную одной из комбинаций маркеров, описанных выше, и вторую популяцию изолированных плацентарных клеток, определенную другими комбинациями маркеров, описанных выше, в соотношении примерно 1:99, 2:98, 3:97, 4:96, 5:95, 10:90, 20:80, 30:70, 40:60, 50:50, 60:40, 70:30, 80:20, 90:10, 95:5, 96:4, 97:3, 98:2 или примерно 99:1. Подобным образом могут комбинироваться любые три, четыре, пять или более описанных выше изолированных плацентарных клеток или популяций изолированных плацентарных клеток.
Изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно изобретению, могут быть получены, например, деструкцией плацентарной ткани с применением ферментативного расщепления или без него (см. Раздел 5.4.3) или перфузией (см. Раздел 5.4.4). Например, популяции изолированных плацентарных клеток могут быть получены в соответствии со способом, включающим перфузию плаценты млекопитающего, которая была дренирована от пуповинной крови и подвергнута перфузии для удаления остаточной крови; перфузию указанной плаценты перфузионным раствором; и сбор указанного перфузионного раствора, где указанный перфузионный раствор после перфузии включает популяцию плацентарных клеток, которая включает изолированные плацентарные клетки; и выделение множества указанных изолированных плацентарных клеток из указанной популяции клеток. В специфическом варианте осуществления изобретения перфузионный раствор пропускается через пуповинную вену и пуповинные артерии и собирается после выведения из плаценты. В другом специфическом варианте осуществления изобретения перфузионный раствор пропускается через пуповинную вену и собирается из пуповинных артерий, или пропускается через пуповинные артерии и собирается из пуповинной вены.
В различных вариантах осуществления изобретения изолированные плацентарные клетки, которые содержатся в популяции клеток, полученной в результате перфузии плаценты, составляют по меньшей мере 50%, 60%, 70%, 80%, 90%, 95%, 99% или по меньшей мере 99,5% указанной популяции плацентарных клеток. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки, собранные перфузией, включают фетальные клетки и материнские клетки. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки, собранные перфузией, являются по меньшей мере на 50%, 60%, 70%, 80%, 90%, 95%, 99% или по меньшей мере на 99,5% фетальными клетками.
В еще одном специфическом варианте изобретение относится к композиции, включающей популяцию изолированных плацентарных клеток, как описано в изобретении, собранную перфузией, где указанная композиция включает по меньшей мере часть перфузионного раствора, используемого для сбора изолированных плацентарных клеток.
Изолированные популяции изолированных плацентарных клеток, описанные в настоящем изобретении, могут быть получены расщеплением плацентарной ткани ферментом, расщепляющим ткань, для получения популяции плацентарных клеток, включающих клетки, и изолированием или по существу изолированием множества плацентарных клеток из остатка указанных плацентарных клеток. Плацента в целом или любая ее часть может подвергаться расщеплению для получения изолированных плацентарных клеток, описанных в настоящем изобретении. В специфических вариантах осуществления изобретения, например, указанная плацентарная ткань может быть цельной плацентой, амниотической мембраной, хорионом, комбинацией амниона и хориона или комбинацией любых их указанных выше тканей. В другом специфическом варианте осуществления изобретения фермент, расщепляющий ткань, представляет собой трипсин или коллагеназу. В различных вариантах осуществления изобретения изолированные плацентарные клетки, которые содержатся в популяции клеток, полученной в результате расщепления плаценты, составляют по меньшей мере 50%, 60%, 70%, 80%, 90%, 95%, 99% или по меньшей мере 99,5% указанной популяция плацентарных клеток.
Генная характеристика подтверждает, что изолированные плацентарные клетки и популяции изолированных плацентарных клеток могут отличаться от других клеток, например, мезенхимальных стволовых клеток, например, мезенхимальных клеток, полученных из костного мозга. Изолированные плацентарные клетки, описанные в настоящем изобретении, могут отличаться, например, от мезенхимальных стволовых клеток по экспрессии одного или нескольких генов, экспрессия которых значительно выше в изолированных плацентарных клетках или в определенных изолированных пуповинных стволовых клетках, чем в мезенхимальных стволовых клетках, полученных из костного мозга. В частности, изолированные плацентарные клетки, которые могут использоваться в композициях и способах согласно настоящему изобретению, могут отличаться от мезенхимальных стволовых клеток, исходя из экспрессии одного или нескольких генов, экспрессия которого значительно выше (то есть, по меньшей мере в два раза выше) в изолированных плацентарных клетках по сравнению с эквивалентным количеством мехенхимальных стволовых клеток, полученных из костного мозга, где один или несколько генов представляют собой ACTG2, ADARB1, AMIGO2, ARTS-1, B4GALT6, BCHE, C11orf9, CD200, COL4A1, COL4A2, CPA4, DMD, DSC3, DSG2, ELOVL2, F2RL1, FLJ10781, GATA6, GPR126, GPRC5B, HLA-G, ICAM1, IER3, IGFBP7, IL1A, IL6, IL18, KRT18, KRT8, LIPG, LRAP, MATN2, MEST, NFE2L3, NUAK1, PCDH7, PDLIM3, PKP2, RTN1, SERPINB9, ST3GAL6, ST6GALNAC5, SLC12A8, TCF21, TGFB2, VTN, ZC3H12A или комбинацию любых из вышеуказанных генов, когда клетки культивируются в эквивалентных условиях (см., например, Публикацию заявки на патент США № 2007/0275362, содержание которой таким образом полностью включено в настоящее описание путем ссылки). В более специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки экспрессируют указанные один или несколько генов, когда культивируются для от примерно 3 до примерно 35 удвоений популяции в среде, включающей DMEM-LG (Gibco); 2% зародышевую телячью сыворотку (Hyclone Labs.); 1× инсулин-трансферрин-селен (ITS); 1× линолевая кислота-бычий сывороточный альбумин (LA-BSA); 10-9 M дексаметазона (Sigma); 10-4 M 2-фосфата аскорбиновой кислоты (Sigma); 10 нг/мл эпидермального фактора роста (R&D Systems); и 10 нг/мл тромбоцитарного фактора роста (PDGF-BB) (R&D Systems). В специфическом варианте осуществления изобретения специфическим геном изолированных плацентарных клеток или изолированных пуповинных клеток является CD200.
Специфические последовательности для этих генов можно найти в GenBank под номерами доступа NM_001615 (ACTG2), BC065545 (ADARB1), (NM_181847 (AMIGO2), AY358590 (ARTS-1), BC074884 (B4GALT6), BC008396 (BCHE), BC020196 (C11orf9), BC031103 (CD200), NM_001845 (COL4A1), NM_001846 (COL4A2), BC052289 (CPA4), BC094758 (DMD), AF293359 (DSC3), NM_001943 (DSG2), AF338241 (ELOVL2), AY336105 (F2RL1), NM_018215 (FLJ10781), AY416799 (GATA6), BC075798 (GPR126), NM_016235 (GPRC5B), AF340038 (ICAM1), BC000844 (IER3), BC066339 (IGFBP7), BC013142 (IL1A), BT019749 (IL6), BC007461 (IL18), (BC072017) KRT18, BC075839 (KRT8), BC060825 (LIPG), BC065240 (LRAP), BC010444 (MATN2), BC011908 (MEST), BC068455 (NFE2L3), NM_014840 (NUAK1), AB006755 (PCDH7), NM_014476 (PDLIM3), BC126199 (PKP-2), BC090862 (RTN1), BC002538 (SERPINB9), BC023312 (ST3GAL6), BC001201 (ST6GALNAC5), BC126160 или BC065328 (SLC12A8), BC025697 (TCF21), BC096235 (TGFB2), BC005046 (VTN) и BC005001 (ZC3H12A) с марта 2008 года.
В более специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки экспрессируют каждый из ACTG2, ADARB1, AMIGO2, ARTS-1, B4GALT6, BCHE, C11orf9, CD200, COL4A1, COL4A2, CPA4, DMD, DSC3, DSG2, ELOVL2, F2RL1, FLJ10781, GATA6, GPR126, GPRC5B, HLA-G, ICAM1, IER3, IGFBP7, IL1A, IL6, IL18, KRT18, KRT8, LIPG, LRAP, MATN2, MEST, NFE2L3, NUAK1, PCDH7, PDLIM3, PKP2, RTN1, SERPINB9, ST3GAL6, ST6GALNAC5, SLC12A8, TCF21, TGFB2, VTN и ZC3H12A со значительно более высоким уровне, чем эквивалентное количество мезенхимальных стволовых клеток, полученных из костного мозга, когда клетки выращиваются в эквивалентных условиях.
В более специфических вариантах осуществления изобретения популяции плацентарных клеток могут выбираться отбором плацентарных клеток, которые экспрессируют один или несколько генов с обнаружимо более высоким уровнем, чем мезенхимальные стволовые клетки, полученные из костного мозга, где указанные один или несколько генов выбраны из группы, включающей ACTG2, ADARB1, AMIGO2, ARTS-1, B4GALT6, BCHE, C11orf9, CD200, COL4A1, COL4A2, CPA4, DMD, DSC3, DSG2, ELOVL2, F2RL1, FLJ10781, GATA6, GPR126, GPRC5B, HLA-G, ICAM1, IER3, IGFBP7, IL1A, IL6, IL18, KRT18, KRT8, LIPG, LRAP, MATN2, MEST, NFE2L3, NUAK1, PCDH7, PDLIM3, PKP2, RTN1, SERPINB9, ST3GAL6, ST6GALNAC5, SLC12A8, TCF21, TGFB2, VTN и ZC3H12A, и где указанные стволовые клетки, полученные из костного мозга, подверглись количеству пассажей в культуре, эквивалентому количеству пассажей, которому подвергалась указанная плацентарная клетка. В более специфическом варианте осуществления изобретения указанный отбор включает отбор клеток, которые экспрессируют ACTG2, ADARB1, AMIGO2, ARTS-1, B4GALT6, BCHE, C11orf9, CD200, COL4A1, COL4A2, CPA4, DMD, DSC3, DSG2, ELOVL2, F2RL1, FLJ10781, GATA6, GPR126, GPRC5B, HLA-G, ICAM1, IER3, IGFBP7, IL1A, IL6, IL18, KRT18, KRT8, LIPG, LRAP, MATN2, MEST, NFE2L3, NUAK1, PCDH7, PDLIM3, PKP2, RTN1, SERPINB9, ST3GAL6, ST6GALNAC5, SLC12A8, TCF21, TGFB2, VTN и ZC3H12A с обнаружимо более высоким уровнем, чем мезенхимальные стволовые клетки, полученные из костного мозга.
Экспрессия указанных выше генов может оцениваться стандартными методами. Например, исходя из последовательности(ей) гена(ов), могут индивидуально подбираться и стандартными методами конструироваться зонды. Экспрессия генов может оцениваться, например, на микропоследовательности, включающей зонд к одному или нескольким генам, например, Affymetrix GENECHIP® Human Genome U133A 2.0 ряда или Affymetrix GENECHIP® Human Genome U133 Plus 2.0 (Santa Clara, California). Экспрессия этих генов может оцениваться даже тогда, когда последовательность для конкретного инвентарного номера GenBank изменена, поскольку зонды, специфические для такой измененной последовательности, могут легко генерироваться с использованием широко известных стандартных методик.
Уровень экспрессии указанных генов может использоваться для подтверждения идентичности популяции изолированных плацентарных клеток, для идентификации популяции клеток как включающей по меньшей мере множество изолированных плацентарных клеток или т.п. Популяции изолированных плацентарных клеток, идентичность которых подтверждена, могут клонироваться, например, популяциями изолированных плацентарных клеток, выращенными из единственной изолированной плацентарной клетки или смешанной популяции стволовых клеток, например, популяции клеток, включающей только изолированные плацентарные клетки, которые выращены из множества изолированных плацентарных клеток, или популяции клеток, включающей изолированные плацентарные клетки, как описано в изобретении, и клетки по меньшей мере одного иного типа.
Уровень экспрессии указанных генов может использоваться для выбора популяции изолированных плацентарных клеток. Например, популяция клеток, например, клонально выращенных клеток, может отбираться, если экспрессия одного или нескольких генов, перечень которых представлен выше, значительно выше в образце популяции клеток, чем в образце эквивалентной популяции мезенхимальных стволовых клеток. Таким выбором может быть популяция из множества популяций изолированных плацентарных клеток, из множества клеточных популяций, идентичность которых не известна и т.д.
Изолированные плацентарные клетки могут выбираться на основе уровня экспрессии одного или нескольких таких генов по сравнению с уровнем экспрессии одного или нескольких генов, например, в контрольных мезенхимальных стволовых клетках, например, с уровнем экспрессии указанного одного или нескольких генов эквивалентным количеством мезенхимальных стволовых клеток, полученных из костного мозга. В одном варианте осуществления изобретения уровень экспрессии указанного одного или нескольких генов в образце, включающем эквивалентное число мезенхимальных стволовых клеток, используется в качестве контроля. В другом варианте осуществления изобретения контролем для изолированных плацентарных клеток, тестируемых в определенных условиях, является численное значение, представляющее уровень экспрессии указанного одного или нескольких генов в мезенхимальных стволовых клетках в указанных условиях.
Изолированные плацентарные клетки, описанные в настоящем изобретении, проявляют описанные выше характеристики (например, комбинирование маркеров клеточной поверхности и/или профилей генной экспрессии) в первичной культуре или в процессе пролиферации в среде, включающей, например, DMEM-LG (Gibco); 2% зародышевую телячью сыворотку (Hyclone Labs.); 1× инсулин-трансферрин-селен (ITS); 1× линолевая кислота-бычий сывороточный альбумин (LA-BSA); 10-9 M дексаметазона (Sigma); 10-4 M 2-фосфата аскорбиновой кислоты (Sigma); 10 нг/мл эпидермального фактора роста (FGR) (R&D Systems); и 10 нг/мл тромбоцитарного фактора роста (PDGF-BB) (R&D Systems) и 100 единиц пенициллина/100 единиц стрептомицина.
Изолированные популяции плацентарных клеток, описанные выше, и популяции изолированных плацентарных клеток обычно могут включать примерно по меньшей мере или не более чем 1×105, 5×105, 1×106, 5×106, 1×107, 5×107, 1×108, 5×108, 1×109, 5×109, 1×1010, 5×1010, 1×1011 или более изолированных плацентарных клеток. Популяции изолированных плацентарных клеток, которые могут использоваться в композициях и способах согласно изобретению, включают по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98% или 99% жизнеспособных изолированных плацентарных клеток, как определено, например, тестом с применением трипанового синего.
5.3.3 Рост в культуре
Рост изолированных плацентарных клеток, описанных в настоящем изобретения, как и для любой клетки млекопитающего, в некоторой степени зависит от конкретной среды, выбранной для роста. В оптимальных условиях изолированные число плацентарных клеток обычно удваивается в течение 3-5 дней. Изолированные плацентарные клетки, описанные в настоящем изобретении, прикрепляются к подложке в культуре, например, к поверхности материала контейнера культуры (например, пластиковому материалу диска, пластику, покрытому фибронектином и т.п.) и образуют монослой.
Популяции изолированных плацентарных клеток, описанные в настоящем изобретении, при выращивании в подходящих условиях образуют эмбриоидоподобные тельца, то есть, трехмерные кластеры клеток растут поверх слоя адгезивных стволовых клеток. Клетки внутри эмбриоидоподобных телец экспрессируют маркеры, ассоциированные с очень быстро созревающими стволовыми клетками, например, OCT-4, Nanog, SSEA3 и SSEA4. Клетки внутри эмбриоидоподобных телец обычно не прикрепляются к подложке культуры, поскольку представляют собой изолированные плацентарные клетки, описанные в настоящем изобретении, но остаются присоединенными к адгезивным клеткам в культуре. Клетки эмбриоидоподобных телец зависят от адгезивных изолированных плацентарных клеток, которые необходимы для их жизнеспособности, поскольку эмбриоидоподобные тельца не образуются в отсутствии адгезивных изолированных плацентарных клеток. Следовательно, адгезивные изолированные плацентарные клетки способствуют росту одного или нескольких эмбриоидоподобных телец в популяции плацентарных клеток, которые включают адгезивные изолированные плацентарные клетки. Без теоретического обоснования считается, что клетки эмбриоидоподобных телец быстро растут на адгезивных изолированных плацентарных клетках, поскольку эмбриональные стволовые клетки растут на питающем слое клеток. Мезенхимальные стволовые клетки, например, мезенхимальные стволовые клетки, полученные из костного мозга, не приводят к образованию эмбриоидоподобных телец в культуре.
5.3.4 Гемопоэтические плацентарные стволовые клетки
В некоторых вариантах осуществления изобретения изолированные плацентарные клетки представляют собой CD34+плацентарные клетки, например, гемопоэтические плацентарные клетки. Однако термин «мультипотентные» не относится к CD34+ клеткам, в рамках изобретения. Такие клетки могут быть получены из плацента, например, из плаценты, которая была дренирована от пуповинной крови и подвергнута перфузии для удаления остаточной крови. В некоторых вариантах осуществления изобретения CD34+ изолированные плацентарные клетки представляют собой CD38+. В некоторых других вариантах осуществления изобретения CD34+ изолированные плацентарные клетки представляют собой CD38-. В некоторых других вариантах осуществления изобретения CD34+ изолированные плацентарные клетки представляют собой CD45+. В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD34+, CD38- и CD45+.
5.3.5 Клетки, полученные из плацентарного перфузата
В некоторых вариантах осуществления изобретения клетки композиций согласно изобретению, полученных способами согласно изобретению, представляют собой клетки, полученные из плацентарного перфузата. Термин «клетки, полученные из плацентарного перфузата», в рамках изобретения, включает клетки, содержащие цельные ядра и полученные, например, изолированные, из плацентарного перфузата, субпопуляцию ядросодержащих клеток, полученных из плацентарного перфузата, или клетки, культивированные или пролиферированные из клеток, полученных непосредственно из плацентарного перфузата. Плацентарный перфузат может быть получен из плаценты, которая была дренирована от пуповинной крови и подвернута перфузии для удаления остаточной крови перед перфузией для получения плацентарных клеток. Плацентарный перфузат может быть получен из плаценты, которая была дренирована от пуповинной крови, но не подверглась перфузии для удаления остаточной крови. Плацентарный перфузат может быть получен из плаценты, которая не подвергалась ни дренированию от пуповинной крови, ни перфузии для удаления остаточной крови. В двух последних вариантах осуществления изобретения плацентарные клетки, например, ядросодержащие клетки из плацентарного перфузата, в частности, клетки из плацентарного перфузата, содержащие цельные ядра, включают ядросодержащие клетки из плацентарной крови и/или пуповинной крови. Способы получения плацентарного перфузата и клеток из плацентарного перфузата описаны в Разделе 5.4.4, ниже.
5.4. СПОСОБЫ ПОЛУЧЕНИЯ ИЗОЛИРОВАННЫХ ПЛАЦЕНТАРНЫХ КЛЕТОК
5.4.1 Композиция сбора стволовых клеток
Настоящее изобретение дополнительно относится к способам сбора и выделения (изоляции) плацентарных клеток, например, изолированных плацентарных клеток, описанных выше в Разделе 5.2. Обычно такие клетки получают из плаценты млекопитающего с использованием физиологически приемлемого раствора, например, композиции сбора стволовых клеток. Композиция клеточного сбора подробно описана в Публикации родственной заявки на патент США № 2007/0190042, озаглавленной «Улучшенная среда для сбора плацентарных стволовых клеток и консервации органов».
Композиция клеточного сбора может включать любой физиологически приемлемый раствор, подходящий для сбора и/или культивирования клеток, например, изолированных плацентарных клеток, описанных в настоящем изобретении, например, раствор соли (например, форсфатно-буферный раствор, раствор Креба, модифицированный раствор Креба, раствор Игла, 0,9% NaCl и т.д.), культуральную среду (например, DMEM, H.DMEM и т.д.) и т.п.
Композиция клеточного сбора может включать один или несколько компонентов, которые могут служить для консервации изолированных плацентарных клеток, то есть, предохраняют изолированные плацентарные клетки от гибели или замедляют гибель изолированных плацентарных клеток, снижают количество погибших изолированных плацентарных клеток в популяции или т.п. от момента сбора до момента культивирования. Такими компонентами могут быть, например, ингибитор апоптоза (например, ингибитор каспаз или JNK ингибитор); вазодилататор (например, сульфат магния, гипотензивное лекарственное средство, предсердный натрийуретический пептид (atrial natriuretic peptide - ANP), аденокортикотропин, гормон, высвобождающий кортикотропин, нитропруссид натрия, гидралазин, аденозинтрифосфат, аденозин, индометацин или сульфат магния, ингибитор фосфодиэстеразы и т.п.); ингибитор некроза (например, 2-(1H-индол-3-ил)-3-пентиламиномалеимид, пирролидиндитиокарбамат или клоназепам); TNF-α ингибитор; и/или перфторуглерод, способный переносить кислород (например, перфтороктилбромид, перфтордецилбромид и т.д.).
Композиция клеточного сбора может включать один или несколько ферментов, разлагающих ткань, например, металлопротеазу, серинпротеазу, нейтральную протеазу, рибонуклеазу (RNase), ДНазу (DNase) или т.п. Такие ферменты включают, но без ограничения коллагеназы (например, коллагеназу I, II, III или IV, коллагеназу из Clostridium histolyticum и т.д.), диспазу, термолизин, эластазу, трипсин, LIBERASE, гуалуронидазу и т.п.
Композиция клеточного сбора может включать бактерицидно или бактериостатически эффективное количество антибиотика. В некоторых вариантах осуществления изобретения антибиотик представляет собой, но без ограничения, макролид (например, тобрамицин), цефалоспорин (например, цефалексин, цефрадин, цефуроксим, сефпрозил, цефаклор, цефиксим или цефадроксил), кларитромицин, эритромицин, пенициллин (например, пенициллин V) или хинолон (например, офлоксацин, ципрофлоксацин или норфлоксацин), тетрациклин, стрептомицин и т.д. В конкретном варианте осуществления изобретения антибиотик является активным в отношении грамположительных и/или грамотрицательных бактерий, например, Pseudomonas aeruginosa, Staphylococcus aureus и т.п.
Композиция клеточного сбора может также включать одно или несколько из следующих соединений: аденозин (от примерно 1 мМ до примерно 50 мМ); D-глюкозу (от примерно 20 мМ до примерно 100 мМ), ионы магния (от примерно 1 мМ до примерно 50 мМ); макромолекулу с молекулярной массой свыше 20000 дальтон - в одном варианте осуществления изобретения присутствует в количестве, достаточном для поддержания эндотелиальной целостности и жизнеспособности клеток (например, синтетический или природный коллоид, полисахарид, такой как декстран или полиэтиленгликоль, в количестве от примерно 25 г/л до примерно 100 г/л или от примерно 40 г/л до примерно 60 г/л); антиоксидант (например, бутилированный гидроксианизол, бутилированный гидрокситолуол, глутатион, витамин С или витамин Е в количестве от примерно 25 мкм до примерно 100 мкм); восстановитель (например, N-ацетилцистеин в количестве от примерно 0,1 мМ до примерно 5 мМ); добавка, которая предотвращает поступление кальция в клетки (например, верапамил в количестве от примерно 2 мкм до примерно 25 мкм); нитроглицерин (например, от примерно 0,05 г/л до примерно 0,2 г/л); антикоагулянт - в одном варианте осуществления изобретения присутствует в количестве, достаточном для способствования предотвращению свертывания остаточной крови (например, гепарин или гирудин в концентрации от примерно 1000 единиц/л до примерно 100000 единиц/л); амилорид-содержащее соединение (например, амилорид, этилизопропиламилорид, гексаметиленамилорид, диметиламилорид или изобутиламилорид в количестве от примерно 1,0 мкм до примерно 5 мкм).
5.4.2. Сбор плаценты и работа с плацентой
Обычно плаценту человека получают сразу после ее изгнания после родов. В предпочтительном варианте осуществления изобретения плацента получена от пациента после его информированного согласия, а также после получения медицинской карты пациента и соотнесения ее с плацентой. Предпочтительно, ведение медицинской карты продолжается и после получения плаценты. Указанная история болезни может использоваться для координации последующего использования плаценты или стволовых клеток, собранных из нее. Например, плацентарные стволовые клетки человека могут использоваться, в свете истории болезни, для персонифицированного лечения новорожденного, который был ассоциирован с указанной плацентой, или для родителей, братьев, сестер или других родственников новорожденного.
Перед выделением изолированных плацентарных клеток удаляется пуповинная кровь и плацентарная кровь. В некоторых вариантах осуществления изобретения после родов пуповинная кровь извлекается из плаценты. Плацента может подвергаться стандартному процессу извлечения пуповинной крови. Обычно для способствования обескровливанию плаценты под действием силы тяжести используют иглу или канюлю (см., например, Anderson, патент США № 5372581; Hessel et al. патент США № 5415665). Иглу или канюлю обычно помещают в пупочную вену, и плаценту можно осторожно массировать для способствования истечению пуповинной крови из плаценты. Такое извлечение пуповинной крови может проводиться в промышленном масштабе, например, LifeBank USA, Cedar Knolls, N.J., ViaCord, Cord Blood Registry, Cryocell. Предпочтительно, плацента дренируется под действием силы тяжести без дополнительной манипуляции, чтобы свести к минимуму разрушение ткани в процессе выделения пуповинной крови.
Обычно плацента транспортируется из родовой палаты или родильной комнаты в другое место, например, лабораторию, для выпуска пупочной крови и сбора стволовых клеток, например, посредством перфузии или расщеплением ткани. Плацента предпочтительно транспортируется в стерильном термически изолированном устройстве для транспортировки (поддерживающем температуру плаценты в интервале 20-28°С), например, плаценту с зажатой проксимальной пуповиной помещают в герметично закрывающийся стерильный пластиковый пакет, который после этого помещается в изолированный контейнер. В другом варианте осуществления изобретения плацента транспортируется в наборе сбора пуповинной крови, как по существу описано патенте США № 7147626. Предпочтительно плацента доставляется в лабораторию в течение от четырех до двадцати четырех часов после родов. В некоторых вариантах осуществления изобретения перед выделением пуповинной крови проксимальная пуповина зажимается, предпочтительно на расстоянии 4-5 см (сантиметров) от точки ее вставки в плацентарный диск. В других вариантах осуществления проксимальная пуповина зажимается после выделения пуповинной крови, но перед дальнейшей обработкой плаценты.
Плацента перед сбором клеток может храниться в стерильных условиях при комнатной температуре или при температуре в интервале от 5 до 25°С (градусов Цельсия). Плацента может храниться в течение от четырех до двадцати четырех часов до сорока восьми часов или в течение периода, превышающего сорок восемь часов перед перфузией плаценты для удаления любой остаточной пуповинной крови. В одном варианте осуществления изобретения плацента собирается в течение периода от нуля часов до примерно двадцати четырех часов после ее изгнания. Плацента предпочтительно хранится в антикоагулянтном растворе при температуре в интервале от 5 до 25°С. Подходящие антикоагулянтные растворы хорошо известны в данной области техники. Например, можно использовать раствор гепарина или варфарина натрия. В предпочтительном варианте осуществления антикоагулянтный раствор включает раствор гепарина (например, 1% (масс./масс.) в 1:1000 растворе). Обескровленная плацента предпочтительно хранится в течение не более 36 часов до сбора плацентарных клеток.
Плацента млекопитающего или ее часть, собранная и подготовленная, как описано выше, может обрабатываться любым известным образом, например, может подвергаться перфузии или деструкции, например, расщепляться одним или несколькими ферментами, способными расщеплять ткань плаценты, для получения изолированных плацентарных клеток.
5.4.3. Физическая деструкция и ферментативное расщепление плацентарной ткани
В одном варианте осуществления изобретения стволовые клетки собраны из плаценты млекопитающего физической деструкцией части всего органа. Например, плацента или ее часть может измельчаться, нарезаться мелкими кусочками, превращаться в массу, подобную фаршу, нарезаться кубиками, раскалываться, мацерироваться или т.п. После этого ткань может подвергаться культивированию для получения популяции изолированных плацентарных клеток. Обычно плацентарная ткань разрушается с использованием, например, в композиции сбора плацентарных клеток (см. Раздел 5.2 и далее).
Плацента может рассекаться на компоненты перед физической деструкцией и/или ферментативным расщеплением и выделением стволовых клеток. Плацентарные стволовые клетки могут быть получены из всей или части амниотической мембраны, из всего или части хориона, всей или части пуповины, всех или части плацентарных котиледонов или любого их сочетания, в том числе из всей плаценты. Предпочтительно изолированные плацентарные клетки получают из плацентарной ткани, включая амнион и хорион. Обычно изолированные плацентарные клетки могут быть получены деструкцией небольшого блока плацентарной ткани, например, блока плацентарной ткани объемом примерно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500, 600, 700, 800, 900 или примерно 1000 кубических миллиметров. Может использоваться любой метод физической деструкции при условии, что метод оставляет множество клеток, более предпочтительно большинство клеток, еще более предпочтительно по меньшей мере 60%, 70%, 80%, 90%, 95%, 98% или 99% клеток в указанном органе жизнеспособными, как определено, например, анализом с применением трипанового синего.
Стволовые клетки могут обычно собираться из плаценты или ее части в любое время в интервале примерно первых трех дней после изгнания плаценты, но предпочтительно в интервале от примерно 8 часов до примерно 18 часов после изгнания плаценты.
В специфическом варианте осуществления изобретения разрушенная ткань культивируется в среде культуры ткани, подходящей для пролиферации изолированных плацентарных клеток (см., например, Раздел 5.5., ниже, в котором описана культура изолированных плацентарных клеток).
В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки собирают посредством физической деструкции плацентарной ткани, где физическая деструкция включает ферментативное расщепление, которое может достигаться при применении одного или несколько ферментов, расщепляющих ткань. Плацента или ее часть может также физически разрушаться и расщепляться одним или несколькими ферментами, и полученный материал затем погружается в композицию клеточного сбора или смешивается с композицией клеточного сбора.
Предпочтительная композиция клеточного сбора включает один или несколько ферментов, разрушающих ткань. При ферментативном расщеплении предпочтительно используется комбинация ферментов, например, комбинация матриксной металлопротеазы и нейтральной протеазы, например, комбинация коллагеназы и диспазы. В одном варианте осуществления изобретения в ферментативном расщеплении плацентарной ткани используется комбинация матриксной металлопротеазы, нейтральной протеазы и муколитического фермента для расщепления гиалуроновой кислоты, такая как комбинация коллагеназы, диспазы и гиалуронидазы или комбинация LIBERASE (Boehringer Mannheim Corp., Indianapolis, Ind.) и гуалуронидазы. Другие ферменты, которые могут использоваться для расщепления плацентарной ткани, включают папаин, дезоксирибонуклеазы, серинпротеазы, такие как трипсин, химотрипсин или эластаза. Серинпротеазы могут ингибироваться альфа-2-микроглобулином в сыворотке, и, следовательно, среда, используемая для расщепления, обычно свободна от сыворотки. EDTA и ДНаза обычно используются в методиках ферментативного расщепления для повышения эффективности выделения клеток. Фермент, стимулирующий расщепление, обычно разбавляется для предотвращения захвата клеток вязкими продуктами расщепления.
Может использоваться любая комбинация ферментов расщепления ткани. Типичные концентрации для ферментов расщепления ткани включают, например, 50-200 единиц/мл коллагеназы I и коллагеназы IV, 1-10 единиц/мл диспазы и 10-100 единиц/мл эластазы. Протеазы могут использоваться в комбинации, то есть две или несколько протеаз в одной реакции расщепления, или могут использоваться последовательно для высвобождения плацентарных клеток, например, плацентарных стволовых клеток и плацентарных мультипотентных клеток. Например, в одном варианте осуществления изобретения плацента или ее часть расщепляется сначала подходящим количеством коллагеназы I в концентрации от примерно 1 до примерно 2 мг/мл, например, в течение 30 минут, затем подвергается расщеплению трипсином в концентрации примерно 0,25%, например, в течение 10 минут при 37°С. Серинпротеазы предпочтительно используются после применения других ферментов.
В еще одном варианте осуществления изобретения ткань может дополнительно подвергаться расщеплению добавлением комплексона, например, этиленгликоль-бис(2-аминоэфирэфир)-N,N,N'N'-тетрауксусной кислоты (EGTA) или этилендиаминтетрауксусной кислоты (EDTA) к композиции сбора плацентарных клеток или к раствору, в котором ткань разрушается и/или расщепляется перед выделением плацентарных клеток с композицией сбора плацентарных клеток.
После расщепления дигестат промывается, например, три раза, средой культуры, и промытые клетки высеваются в колбы с культурой. После этого клетки изолируют посредством дифференциального прикрепления и характеризуют, например, на жизнеспособность, маркеры клеточной поверхности, дифференциацию и т.п.
Следует представлять, что, когда вся плацента или часть плаценты включает фетальные и материнские клетки (например, когда часть плаценты включает хорион или семядоли), собранные плацентарные клетки будут включать смесь плацентарных клеток, например, плацентарных стволовых клеток или плацентарных мультипотентных клеток, полученных из фетальных и материнских источников. Когда часть плаценты не включает даже самого незначительного количества материнских клеток (например, амнион), собранные плацентарные клетки будут включать почти исключительно фетальные плацентарные клетки, например, эмбриональные плацентарные стволовые клетки или эмбриональные плацентарные мультипотентные клетки.
Плацентарные клетки могут выделяться из расщепленной ткани дифференциальной трипсинизацией (см. Раздел 5.4.5., ниже) с последующей культивацией в одном или нескольких контейнерах с культурой со свежей средой пролиферации, необязательно с последующей стадией дефферениальной трипсинизации.
5.4.4. Плацентарная перфузия
Плацентарные клетки, например, плацентарные стволовые клетки или плацентарные мультипотентные клетки, также могут быть получены перфузией плаценты млекопитающих. Методики перфузии плаценты млекопитающих для получения плацентарных клеток описаны в научной литературе, например, в патентах США №№ 7045148 и 7255729 (Hariri) и в родственной заявке на патент США №№ 2007/0190042, содержание которых таким образом во всех полноте включено в данное изобретение.
Плацентарные клетки могут быть собраны перфузией, например, через плацентарную сосудистую сеть, с использованием, например, композиции сбора клеток в качестве перфузионного раствора. В одном варианте осуществления изобретения перфузия плаценты млекопитающего проводится пропусканием перфузионного раствора через пупочную артерию или пупочную вену, либо через пупочную артерию и пупочную вену. Проток перфузионного раствора через плаценту достигается с использованием, например, ввода потока в плаценту под действием силы тяжести. Предпочтительно, перфузионный раствор пропускается через плаценту с помощью наноса, например, перистальтического насоса. В пупочную вену может вводиться канюля, например, из материала TEFLON® или пластика, которая соединена со стерильным связующим устройством, таким как стерильная система трубок. Стерильное связующее устройство соединено с коллектором перфузата.
При подготовке к перфузии плацента предпочтительно ориентируется (например, подвешивается) таким образом, что пупочная артерия и пупочная вена располагаются в верхней точке плаценты. Перфузия может осуществляться пропуском перфузионного потока через плацентарную сосудистую сеть и окружающую ткань. Перфузия плаценты также может осуществляться вводом перфузионного раствора в пупочную вену и сбором его из пупочных артерий или вводом перфузионного раствора в пупочные артерии и сбором его из пупочной вены.
Например, в одном варианте осуществления изобретения пупочная артерия и пупочная вена присоединены одновременно, например, к пипетке, которая связана через гибкую соединительную трубку с резервуаром для перфузионного раствора. Перфузионный раствор вводится в пупочную вену и артерию. Перфузионный раствор выводится из кровеносных сосудов и/или проходит через стенки кровеносных сосудов в окружающие ткани плаценты и собирается в подходящем открытом сосуде с поверхности плаценты, которая была прикреплена к матке матери во время беременности. Перфузионный раствор также может вводиться посредством открытия пуповины и предоставления ему возможности течь или просачиваться из отверстий в стенке плаценты, которая соединялась со стенкой материнской матки. Плацентарные клетки, собранные этим способом, который может называться методом «ванночки», как правило представляют собой смесь плодных и материнских клеток.
В еще одном варианте осуществления изобретения перфузионный раствор вводится через пупочные вены и собирается из пупочной артерии или вводится через пупочную артерию и собирается из пупочных вен. Плацентарные клетки, собранные таким методом, который может быть назван методом «замкнутой цепи», являются почти исключительно плодными.
Следует понимать, что перфузия с использованием метода ванночки, то есть посредством которого перфузат собирается после его выделения с материнской стороны плаценты, приводит к получению смеси плодных и материнских клеток. В результате клетки, собранные этим способом, включают смешанную популяцию плацентарных клеток, например, плацентарных стволовых клеток или плацентарных мультипотентных клеток фетального или материнского происхождения, либо фетального и материнского происхождения. В отличие от этого способа, перфузия, проводимая только через плацентарную сосудистую сеть в методе замкнутой цепи, посредством которой перфузионный раствор пропускается через один или два плацентарных сосуда и собирается только через остальной(ые) сосуды, приводит к сбору популяции плацентарных клеток почти исключительно фетального происхождения.
В одном варианте осуществления изобретения метод замкнутой цепи может осуществляться следующим образом. Послеродовую плаценту получают в течение приблизительно 48 часов после родов. Пуповину зажимают и отсекают выше зажима. Пуповину можно утилизировать или ее можно подвергнуть дальнейшей обработке для получения, например, из пуповины стволовых клеток и/или для обработки мембраны пуповины и получения биоматериала. Амниотическая мембрана может сохраняться во время перфузии или может отделяться от хориона, например, отслаиванием пальцами. Если амниотическая мембрана отделена от хориона до перфузии, ее можно, например, утилизировать или обработать, например, для получения плацентарных клеток ферментативным расщеплением, или для получения, например, амниотического мембранного биоматериала, например, биоматериала, описанного в Публикации заявки на патент США № 2004/0048796. После очистки плаценты всех видимых кровяных сгустков и остаточной крови, например, с использованием стерильной марли, обнажают сосуды пуповины, например, частично разрезая мембрану пуповины, для открытия поперечного сечения пуповины. Сосуды идентифицируют и открывают, например, продвигая закрытый зажим «крокодильчик» через срезанный кончик сосуда. После этого соединительное устройство, например, пластиковую трубку, связанную с устройством перфузии или перистальтическим насосом, вставляют в каждую из плацентарных артерий. В качестве наноса может использоваться любой насос, подходящий для этой цели, например, перистальтический насос. Затем пластиковую трубку, соединенную со стерильным резервуаром сбора, например, пластиковым мешком для сбора крови, таким как мешок для сбора крови объемом 250 мл, вводят в плацентарную вену. Альтернативно, трубку, соединенную с насосом, вставляют в плацентарную вену, а трубки, соединенные с резервуаром(ами) для сбора крови вставляют в одну или обе плацентарных артерии. Далее, плаценту подвергают перфузии перфузионным раствором, например, перфузионной раствором объемом примерно 750 мл. После этого клетки из перфузата собирают, например, центрифугированием.
В другом варианте осуществления изобретения перфузия, например, для сбора плацентарных клеток перфузата, проводится следующим образом. Плацента, содержащая плацентарную кровь, подвергается перфузии только через плацентарную сосудистую сеть введением с помощью насоса стерильного 0,9% раствора NaCl (например, приблизительно 750 мл), например, с помощью перистальтического насоса, со сбором перфузата в мешке сбора. Клетки из перфузата собирают центрифугированием, например, приблизительно с 420 g, с удалением супернатанта (NaCl, плазма, антигоагулянт). После этого к клеткам, полученным из перфузата, добавляют гетакрахмал для получения 30%-ого разбавления. Затем плетки, полученные из перфузата, помещают в экстрактор плазмы, например, приблизительно на час, для отделения эритроцитов. Полученную плазму и ядросодержащие клетки из мешка сбора снова помещают в экстрактор плазмы. Оставшиеся клетки снова суспендируют в 5%-ом сывороточном альбумине человека с конечным объемом приблизительно 20 мл. Добавляют предварительно полученную смесь ДМСО/PLASMALYTE A® (1:1 об./об.) для получения конечного объема примерно 24 мл. Полученные клетки подвергают криоконсервации. В специфических вариантах осуществления этого способа плацента, из которой получен перфузат, подвергается дренированию от пуповинной крови, но не подвергается перфузии, перед перфузией для сбора плацентарных клеток. В одном специфическом варианте осуществления изобретения плацента, из которой получен перфузат, дренируется от пуповинной крови и подвергается перфузии для удаления остаточной крови перед перфузией для сбора плацентарных клеток.
В одном варианте осуществления изобретения проксимальную пуповину зажимают в процессе перфузии, более предпочтительно зажимают на расстоянии 4-5 см от точки вставки пуповины в плацентарный диск.
Объем пурфузионной жидкости, используемой для сбора плацентарных клеток, может изменяться в зависимости от количества клеток, которое необходимо собрать, размера плаценты, числа сборов, которые должны производиться из одной плаценты, и т.д. В различных вариантах осуществления изобретения объем жидкости может составлять от 50 мл до 5000 мл, от 50 мл до 4000 мл, от 50 мл до 3000 мл, от 100 мл до 2000 мл, от 250 мл до 2000 мл, от 500 мл до 2000 мл или от 750 мл до 2000 мл. Обычно для перфузии плаценты используется 700-800 мл перфузионной жидкости после удаления крови.
Плацента может подвергаться перзуфии множество раз в течение нескольких часов или нескольких дней. Когда плацента предназначена для перфузии множество раз, она может храниться или содержаться в культуре в асептических условиях в контейнере или другой подходящей емкости и подвергаться перфузии композицией сбора клеток или стандартным перфузионным раствором (например, нормальным солевым раствором, таким как фосфатно-буферный раствор (PBS) с добавлением или без добавления антикоагулянта (например, гепарина, варфарина натрия, кумарина, бисгидроксикумарина) и/или с добавлением или без добавления микробиоцидной добавки (например, β-меркаптоэтанола (0,1 мМ)); антибиотиков, таких как стрептомицин (например, 40-100 мкг/мл), пенициллин (например, 40 ед./мл), амфотрецин (например, 0,5 мкг/мл). В одном варианте осуществления изобретения изолированная плацента хранится или содержится в культуре в течение некоторого периода времени без сбора перфузата, так что плацента хранится или выдерживается в культуре в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 или 24 часов либо в течение 2 или 3 или более дней до перфузии и сбора перфузата. После проведения перфузии плацента может храниться в течение одного или нескольких дополнительных периодов времени, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или более часов и подвергаться перфузии второй раз, например, с использованием 700-800 мл перфузионной жидкости. Плацента может подвергаться перфузии 1, 2, 3, 4, 5 или более раз, например, каждые 1, 2, 3, 4, 5 или 6 часов. В предпочтительном варианте осуществления изобретения перфузию плаценты и сбор перфузионного раствора, например, композиции сбора клеток, повторяют до тех пор, пока количество выделяемых ядросодержащих клеток не снизится до менее 100 клеток/мл. Перфузаты, полученные в различные точки времени, могут отдельно подвергаться дополнительной обработке для выделения популяций клеток, которые зависят от времени, например, стволовых клеток. Перфузаты, полученные в различные периоды времени, также могут объединяться. В предпочтительном варианте осуществления изобретения стволовые клетки собирают в период времени или периоды времени в интервале от примерно 8 часов до примерно 18 часов после изгнания плаценты.
Перфузия предпочтительно приводит к сбору значительно большего количества плацентарных клеток, чем количество, которое может быть получено из плаценты млекопитающего без перфузии указанным раствором или без обработки иным образом для получения плацентарных клеток (например, декструкцией ткани, в частности, ферментативным расщеплением). В данном контексте термин «значительно больше» означает больше по меньшей мере на 10%. Перфузия приводит к получению значительно большего количества плацентарных клеток, чем, например, можно получить из культуральной среды, в которой выдерживается плацента или ее часть.
Плацентарные клетки могут выделяться из плаценты перфузией раствором, включающим одну или несколько протеаз или другие ферменты, расщепляющие ткани. В специфическом варианте осуществления изобретения плацента или ее часть (например, амниотическая мембрана, амнион и хорион, плацентарная доля или котиледон, пуповина или их любая комбинация) нагревается до температуры 25-37°С и выдерживается с одним или несколькими ферментами, расщепляющими ткань, в 200 мл культуральной среды в течение 30 минут. Клетки из перфузата охлаждаются до 4°С и промываются охлажденной ингибиторной смесью, включающей 5 мМ EDTA, 2 мМ дитиотреитола и 2 мМ бэта-меркаптоэтанола. Спустя несколько минут плацентарные клетки промываются охлажденной (например, до 4°С) композицией сбора стволовых клеток.
5.4.5. Выделение, сортировка и определение характеристик плацентарных стволовых клеток
Изолированные плацентарные клетки, например, клетки, описанные в Разделе 5.3. ниже, полученные перфузией или физической деструкцией, например, ферментативным расщеплением, могут сначала подвергаться очистке (то есть, изолироваться) от других клеток посредством градиентного центрифугирования по Фиколлу (Ficoll). Такое центрифугирование может проводиться в соответствии с любой стандартной методикой скоростного центрифугирования и т.д. Например, в одном варианте осуществления изобретения клетки, собираемые из плаценты, выделяют из перфузата центрифугированием при 5000 × g в течение 15 минут при комнатной температуре, при которой происходит отделение клеток от, например, загрязняющих остатков органических веществ и тромбоцитов. В другом варианте осуществления изобретения плацентарный перфузат концентрируют до примерно 20 мл, осторожно расслаивают по Фиколлу, центрифугируют с примерно 1100 × g в течение 20 минут при 22°С, и промежуточный слой клеток с низкой плотностью собирают для дальнейшей обработки.
Клеточные пеллеты могут повторно суспендироваться в свежей композиции сбора стволовых клеток или среде, подходящей для хранения стволовых клеток, например, в свободной от сыворотки IMDM, содержащей 2 ед./мл гепарина и 2 мМ EDTA (GibcoBRL, NY). Фракция клеток, содержащих цельные ядра, может выделяться, например, с использованием Lymphoprep (Nycomed Pharma, Oslo, Norway) в соответствии с методикой, рекомендованной производителем.
Плацентарные клетки, полученные перфузией или расщеплением, могут, например, дополнительно или вначале выделяться дифференциальной трипсинизацией с использованием, например, 0,05% раствора трипсина с 0,2% EDTA (Sigma, St. Louis MO). Дифференциальная трипсинизация возможна вследствие того, что изолированные плацентарные клетки обычно открепляются от пластиковых поверхностей в течение примерно пяти минут, в то время как другим адгезивным популяциям необходимо инкубирование в течение свыше 20-30 минут. Открепленные плацентарные клетки могут собираться после трипсинизации и нейтрализации трипсина с использованием трипсин-нейтрализирующего раствора Trypsin Neutralizing Solution (TNS, Cambrex). В одном варианте осуществления выделения адгезивных клеток, аликвоты, например, примерно 5-10×106 клеток, помещают в каждую из нескольких Т-75 колб, предпочтительно с фибронектиновым покрытием. В таком варианте осуществления изобретения клетки могут культивироваться в коммерчески доступной ростовой среде Mesenchymal Stem Cell Growth Medium (MSCGM) (Cambrex) в инкубаторе тканевой среды (37°C, 5% CO2). Спустя 10-15 дней неадгезивные клетки удаляются из колб промывкой PBS. Затем PBS заменяют MSCGM. Колбы предпочтительно проверяют ежедневно на присутствие адгезивных клеток различных типов, в частности, для обнаружения и выявления разрастания кластеров фибробластоидных клеток.
Количество и тип клеток, собранных из плаценты млекопитающего, могут контролироваться, например, измерением изменений в морфологии и маркерах клеточной поверхности с использованием стандартных методик обнаружения клеток, таких как проточная цитометрия, клеточный сортинг, иммуноцитометрия (например, окрашивание с применением антител, специфических к тканям или клеточным маркерам), клеточный сортинг с активацией флуоресценции (fluorescence activated cell sorting - FACS), клеточный сортинг с магнитной активацией (magnetic activated cell sorting - MACS), посредством исследования морфологии клеток с использованием оптического или конфокального микроскопа и/или количественным определением изменений генной экспрессии в соответствии с методиками, хорошо известными в данной области техники, такими как ПЦР и анализ профиля генной экспрессии. Эти методики могут использоваться также для идентификации клеток, которые являются позитивными для одного или нескольких конкретных маркеров. Например, используя антитела к CD34, с помощью описанных выше методик можно определить, включает ли клетка обнаружимое количество CD34; если да, клетка представляет собой CD34+. Аналогично, если клетка вырабатывает достаточно OCT-4 РНК, чтобы обнаруживаться с помощью ОТ-ПЦР, или значительно больше, чем взрослая клетка, то клетка представляет собой ОСТ-4+. Антитела к маркерам клеточных поверхностей (например, CD маркеры, такие как CD34) и последовательности генов, специфических к стволовым клеткам, таким как ОСТ-4, хорошо известны в данной области техники.
Плацентарные клетки, в особенности плацентарные клетки, которые были изолированы с помощью разделения по Фиколлу, дифференциальной адгезией или сочетанием этих способов, могут сортироваться с использованием клеточного сортировщика с активацией флуоресценции (FACS). Клеточный сортинг с активацией флуоресценции является хорошо известным методом разделения частиц, в том числе клеток, на основе флуоресцентных свойств частиц (Kamarch, 1987, Methods Enzymol, 151:150-165). Лазерное возбуждение флуоресцентных фрагментов в отдельных частицах приводит к небольшим электрическим изменениям, позволяющим провести электромагнитное выделение положительных и отрицательных частиц из смеси. В одном варианте осуществления изобретения антитела, специфические к маркерам клеточных поверхностей, или лиганды помечаются различными флуоресцентрыми метками. Клетки обрабатываются сортировщиком клеток, что дает возможность разделить клетки по их способности связываться с используемыми антителами. FACS-сортированные частицы могут быть непосредственно депонированы в отдельные лунки 96-луночнвх или 384-луночных микропланшетов для облегчения разделения и клонирования.
В соответствии с одной схемой сортинга, клетки из плаценты, например, плацентарные стволовые клетки и плацентарные мультипотентные клетки, сортируют на основе экспрессии маркеров CD34, CD38, CD44, CD45, CD73, CD105, OCT-4 и/или HLA-G. Это можно осуществить в соответствии с методиками отбора стволовых клеток на основе их свойств в культуре. Например, отбор адгезивных стволовых клеток может выполняться до или после сортировки на основе экспрессии маркеров. В одном варианте осуществления изобретения, например, клетки сортируются сначала на основе их экспрессии CD34; CD34- остаются, а клетки, которые представляют собой CD200+HLA-G+, отделяются от других CD34- клеток. В другом варианте осуществления изобретения клетки из плаценты сортируются на основе их экспрессии маркеров CD200 и/или HLA-G; например, клетки, экспрессирующие любой из указанных маркеров, выделяются для дальнейшего применения. Клетки, которые экспрессируют, например, CD200 и/или HLA-G, могут в специфическом варианте осуществления изобретения дополнительно разделяться на основе их экспрессии CD73 и/или CD105 или эпитопов, распознаваемых антителами SH2, SH3 или SH4, или отсутствии экспрессии CD34, CD38 или CD45. Например, в одном варианте осуществления изобретения плацентарные клетки сортируются посредством экспрессии или отсутствия экспрессии CD200, HLA-G, CD73, CD105, CD34, CD38 и CD45, и плацентарные клетки, которые представляют собой CD200+, HLA-G+, CD73+, CD105+, CD34-, CD38- и CD45-, изолируются от других плацентарных клеток для дальнейшего применения.
Что касается антитело-опосредуемого обнаружения и сортировки плацентарных клеток, например, плацентарных стволовых клеток или плацентарных мультипотентных клеток, любое антитело, специфическое в отношении конкретного маркера, может использоваться в сочетании с любым люминофором или другой меткой, подходящей для обнаружения и сортировки клеток (например, сортировка клеток с активацией флуоресценции). Комбинации антитело/флуофор к специфическим маркерам включает, но без ограничения, флуоресцеинизотиоцианат-конъюгированные (FITC) моноклональные антитела против HLA-G (доступные от Serotec, Raleigh, North Carolina), CD10 (доступные от BD Immunocytometry Systems, San Jose, California), CD44 (доступные от BD Biosciences Pharmingen, San Jose, California) и CD105 (доступные от R&D Systems Inc., Minneapolis, Minnesota); фикоэретрин-конъюгированные (PE) моноклональные антитела против CD44, CD200, CD117 и CD13 (BD Biosciences Pharmingen); фикоэритрин-Cy7-конъюгированные (PE Cy7) моноклональные антитела против CD33 и CD10 (BD Biosciences Pharmingen); аллофикоцианин-конъюгированный (APC) стрептавидин и моноклональные антитела против CD38 (BD Biosciences Pharmingen); и биотинилированный CD90 (BD Biosciences Pharmingen). Другие антитела, которые могут использоваться, включают, но без ограничения, CD133-APC (Miltenyi), KDR-Biotin (CD309, Abeam), Cytokeratin K-FITC (Sigma или Dako), HLA ABC-FITC (BD), HLA DR,DQ,DP-PE (BD), β-2-микроглобулин-PE (BD), CD80-PE (BD) и CD86-APC (BD).
Другие комбинации антитело/метка, которые могут использоваться, включают, но без ограничения, CD45-PerCP (перидин-хлорофилл-протеин); CD44-PE; CD19-PE; CD10-F (флуоресцеин); HLA-G-F и 7-аминоактиномицин-D (7-AAD); HLA-ABC-F; и т.п.
Изолированные плацентарные клетки согласно настоящему изобретению могут анализироваться на CD117 или CD133 с использованием, например, фикоэритрин-Cy5-конъюгированного (PE Cy5) стрептавидина и биотин-конъюгированных антител против CD117 или CD133; однако при применении этой системы клетки, как оказалось, могут быть положительными для CD117 или CD133, соответственно, ввиду относительно высокого фона.
Изолированные плацентарные клетки, описанные в настоящем изобретении, могут быть мечены антителом к единственному маркеру и обнаружены и/или отсортированы. Плацентарные клетки могут также одновременно быть мечены множеством антител к различным маркерам.
В еще одном варианте осуществления изобретения для разделения клеток могут использоваться магнитные гранулы. Клетки могут сортироваться с использованием метода клеточной сортировки с магнитной активацией (magnetic activated cell sorting - MACS), метода, основанного на их способности связывать магнитные гранулы (диаметром 0,5-100 мкм). Различие применимых модификаций может осуществляться по магнитным микросферам, включая ковалентное добавление антитела, которое специфически распознает конкретную молекулу с конкретной клеточной поверхностью или гаптен. Гранулы затем смешиваются с клетками для обеспечения возможности связывания. После этого клетки пропускают через магнитное поле для отделения клеток, обладающих специфическим маркером клеточной поверхности. В одном варианте осуществления изобретения эти клетки затем выделяют и снова смешивают с магнитными гранулами, связанными с антителом против дополнительных маркеров клеточных поверхностей. Затем клетки снова пропускают через магнитное поле, выделяя клетки, которые связывают оба антитела. Такие клетки после этого разбавляют в отдельных чашках, таких как микротитровальные чашки для клонального изолирования.
Изолированные плацентарные клетки также могут характеризоваться и/или сортироваться на основе клеточной морфологии и характеристик роста. Например, изолированные плацентарные клетки могут характеризоваться как обладающие фибробластоидным признаком и/или выбираться на основе такого признака. Изолированные плацентарные клетки также могут характеризоваться как обладающие способностью образовывать эмбриоидоподобные тельца и/или могут выбираться на основе этой способности. В одном варианте осуществления изобретения, например, изолированные плацентарные клетки, которые являются фибробластоидными по форме, экспрессируют CD73 и CE105 и продуцируют одно или несколько эмбриоидоподобных телец в культуре, изолируют от других плацентарных клеток. В другом варианте осуществления изобретения OCT-4+ плацентарные клетки, которые продуцируют одно или несколько эмбриоидоподобных телец в культуре, изолируют от других плацентарных клеток.
В еще одном варианте осуществления изобретения изолированные плацентарные клетки могут идентифицироваться и характеризоваться посредством анализа колониеобразующих единиц. Методы анализа колониеобразующих единиц, такие как MESENCULT™ medium (Stem Cell Technologies, Inc., Vancouver British Columbia), хорошо известны в данной области техники.
Изолированные плацентарные клетки могут оцениваться на жизнеспособность, потенциал пролиферации и продолжительность жизни с использованием стандартных методик, известных в данной области техники, таких как анализ с использованием трипанового синего, анализа поглощения флуоресцеиндиацетата, анализ поглощения йодида пропидия (для оценки жизнеспособности) и анализ поглощения тимидина, анализ МТТ клеточной пролиферации (для оценки пролиферации). Продолжительность жизни может определяться способами, хорошо известными в данной области техники, такими как определение максимального числа удвоений популяции в продленной культуре.
Изолированные плацентарные клетки также могут отделяться от других плацентарных клеток с использованием других методик, известных в данной области техники, например, селективным выращиванием желательных клеток (положительный отбор), селективным разрушением нежелательных клеток (отрицательный отбор); разделение, основанное на способности к агглютинированию дифферециальных клеток в смешанной популяции, например, с соевым агглютинином; методика замораживания-оттаивания; фильтрация; стандартное и зональное центрифугирование; центробежное сцеживание (противоточное центрифугирование); разделение по плотности; противоточное распределение; электрофорез; и т.п.
5.5. КУЛЬТУРА ИЗОЛИРОВАННЫХ ПЛАЦЕНТАРНЫХ КЛЕТОК
5.5.1. Питательная среда
Изолированные плацентарные клетки или популяции изолированных плацентарных клеток или клетки или плацентарная ткань, из которой они произрастают, могут использоваться для инициирования или высевания клеточных культур. Клетки обычно переносятся в стерильные емкости культуры ткани без покрытия или с покрытием из экстрацеллюлярной матрицы или лигандов, таких как ламинин, коллаген (например, природный или денатурированный), желатин, фибронектин, орнитин, витронектин и экстрацеллюлярный мембранный белок (например, MATRIGEL® (BD Discovery Labware, Bedford, Mass.)).
Изолированные плацентарные клетки могут культивироваться в любой среде и в любых условиях, которые определены в данной области техники как приемлемые для культуры клеток, например, стволовых клеток. Предпочтительно, среда культтивирования включает сыворотку. Изолированные плацентарные клетки могут культивироваться, например, в DMEM-LG (модифицированная эссенциальная среда Дульбекко с низким содержанием глюкозы - Dulbecco's Modified Essential Medium, low glucose)/MCDB 201 (базальная среда куриных фибробластов - chick fibroblast basal medium), содержащей ITS (инсулин-трансферрин-селен), LA+BSA (линолевая кислота-бычий сывороточный альбумин), декстрозу, L-аскорбиновую кислоту, PDGF, EGF, IGF-I и пенициллин/стрептомицин; в DMEM-HG (модифицированная эссенциальная среда Дульбекко с высоким содержанием глюкозы), включающей от 1% до 20% зародышевой телячьей сыворотки (FBS); в DMEM-HG, включающей 15% FBS; IMDM (среда Дульбекко в модификации Искова - Iscove's modified Dulbecco's medium), включающей 10% FBS, 10% сыворотки крови лошади и гидрокортизон; M199, включающей 10% FBS, EGF и гепарин; α-MEM (минимальной эссенциальной среде), включающей 10% FBS, GLUTAMAX™ и гентамицин; DMEM, включающей 10% FBS, GLUTAMAX™ и гентамицин и т.д.
Другие среды, которые могут использоваться для культивирования плацентарных клеток, включают DMEM (с высоким и с низким содержанием глюкозы), базальную среду Игла, среду Хама F10 (F10), среду Хама F12 (F12), модифицированную по Искову среду Дульбекко, среду роста мезенхимальных стволовых клеток (Mesenchymal Stem Cell Growth Medium - MSCGM), среду Лейбовитца L-15 (Liebovitz's L-15 medium), MCDB, DMEM/F12, RPMI 1640, усовершенствованную DMEM (Gibco), DMEM/MCDB201 (Sigma) и CELL-GRO FREE.
В питательную среду культур клеток может добавляться один или несколько компонентов, включая, например, сыворотку крови (например, зародышевую телячью сыворотку (FBS), предпочтительно примерно 2-15% (об./об.); сыворотку крови лошади (ES); сыворотку крови человека (HS)); бэта-меркаптоэтанол (ВМЕ), предпочтительно примерно 0,001% (об./об.); один или несколько факторов роста, например, тромбоцитарный фактор роста (platelet-derived growth factor - PDGF), эпидермальный фактор роста (EGF), основной фактор роста фибробластов (bFGF), инсулиноподобный гормон роста-1 (insulin-like growth factor-1 - IGF-1), фактор, ингибирующий активность лейкозных клеток (leukemia inhibitory factor - LIF), эндотелиальный фактор роста сосудов (vascular endothelial growth factor - VEGF) и эритропоэтин (erythropoietin - EPO); аминокислоты, включая L-валин; и один или несколько антибиотиков и/или микостатических средств для контроля бактериального заражения, таких как, например, пенициллин G, стрептомицин-сульфат, амфотерицин В, гентамицин и нистатин или их сочетания.
Изолированные плацентарные клетки могут выращиваться в стандартных условиях культивирования ткани, например, в чашках с культурой ткани или многолуночных планшетах. Изолированные плацентарные клетки также могут выращиваться с использованием «метода падающей капли». В этом методе изолированные плацентарные клетки суспендируются в концентрации примерно 1×104 клеток на мл в примерно 5 мл среды, и одна или несколько капель среды помещается на внутреннюю сторону крышки контейнера культуры ткани, например, 100 мл чашки Петри. Капли могут быть, например, одиночными каплями или множеством каплей, например, из многоканальной пипетки. Крышку осторожно переворачивают и помещают сверху над донышком чашки, которая содержит объем жидкости, например, стерильного PBS, достаточный для сохранения влажного содержимого в атмосфере чашки, и стволовые клетки выращивают в этих условиях.
В одном варианте осуществления изобретения изолированные плацентарные клетки выращиваются в культуре в присутствии соединения, которые служат для поддержания недифференцированного фенотипа в изолированной плацетарной клетке. В специфическом варианте осуществления изобретения соединение представляет собой 3,4-дигидропиридимол[4,5-d]пиримидин. В более специфическом варианте осуществления изобретения соединение имеет следующую химическую структуру:

Указанное соединение может контактировать с изолированными плацентарными клетками или популяцией изолированных плацентарных клеток в концентрации, например, от примерно 1 мкМ до примерно 10 мкМ.
5.5.2. Рост и пролиферация плацентарных клеток
Изолированная плацентарная клетка или популяция изолированной плацентарной клетки (например, плацентарная клетка или популяция плацентарных клеток, изолированных по меньшей мере от 50% плацентарных клеток, с которыми стволовая клетка или популяция стволовых клеток обычно связана в условиях in vivo), клетка или популяция клеток может пролиферироваться и увеличивать свою численность in vitro. Например, популяция изолированных плацентарных клеток может выращиваться в контейнерах культуры тканей, например, в чашках, колбах, многолуночных планшетах и т.п., в течение периода времени, достаточного для того, чтобы клетки пролиферировали до 70-90% слияния, то есть до тех пор, пока клетки и их потомство не займут 70-90% площади культивирования поверхности контейнера культуры ткани.
Изолированные плацентарные клетки могут высеваться в сосуды для культивирования при плотности, которая дает возможность выращивать клетки. Например, клетки могут высеваться с плотностью от низкой (например, от примерно 1000 до примерно 5000 клеток/см2) до высокой (например, примерно 50000 или более клеток/см2). В предпочтительном варианте осуществления изобретения клетки выращиваются в присутствии от примерно 0 до примерно 5 процентов (об.) СО2 в воздухе. В более предпочтительных вариантах осуществления изобретения клетки выращиваются в присутствии от примерно 2 до примерно 25 процентов О2 в воздухе, предпочтительно от примерно 5 до примерно 20 процентов О2 в воздухе. Клетки предпочтительно выращиваются при температуре от примерно 25°С до примерно 40°С, предпочтительно 37°С. Клетки предпочтительно выращиваются в инкубаторе (термостате). Питательная среда культуры клеток может быть статической или перемешиваться, например, с использованием биореактора. Плацентарные клетки, например, плацентарные стволовые клетки или плацентарные мультипотентные клетки, предпочтительно выращиваются в условиях с незначительным окислительным стрессом (например, с добавлением глютатиона, аскорбиновой кислоты, каталазы, токоферола, N-ацетилцистеина и т.п.).
Как только достигается слияние на уровне менее примерно 100%, например, 70%-90%, клетки могут быть пассированы. Например, клетки могут быть обработаны ферментами, например, подвергаться трипсинизации, с использованием методов, известных в данной области техники, для отделения их от поверхности культуры тканей. После удаления клеток пипетированием и подсчета клеток, приблизительно 10000-100000 клеток/мл2, предпочтительно приблизительно 50000 клеток/мл2, они пересеваются в новый контейнер культуры, содержащий свежую питательную среду. Как правило, свежая питательная среда представляет собой тот же самый тип питательной среды, что и тип среды, из которой были удалены изолированные плацентарные клетки. Изолированные плацентарные клетки могут быть пересеяны по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 16, 18 или 20 раз или более.
ПОЛУЧЕНИЕ БАНКА ПЛАЦЕНТАРНЫХ КЛЕТОК
Изолированные плацентарные клетки из послеродовой плаценты, например, описанные в Разделе 5.3. выше, могут культивироваться различными способами для получения ряда партий, например, набора доз, которые могут вводиться индивидуально, изолированных плацентарных клеток. Такие партии могут быть получены, например, из клеток плацентарного перфузата или из клеток плацентарной ткани, а также плацентарной ткани, подвергнутой ферментативному расщеплению. Ряды партий плацентарных клеток, полученных из множества плацент, могут помещаться в банк изолированных плацентарных клеток, например, для длительного хранения. Обычно плацентарные клетки, прикрепленные к пластику контейнера культуры ткани, получают из исходной культуры плацентарного материала для получения высеянной культуры, которая выращивается в контролируемых условиях для получения популяций клеток из примерно эквивалентного числа удвоений численности популяций. Партии предпочтительно подразделяют на полученные из ткани одной плаценты, но могут быть получены из ткани множества плацент.
В одном варианте осуществления изобретения партии плацентарных клеток получают следующим образом. Плацентарную ткань деструктируют, например, измельчением, подвергают расщеплению подходящим ферментом, например, коллагеназой, (см. Раздел 5.4.3., выше). Плацентарная ткань предпочтительно включает, например, цельный амнион, цельный хорион, либо цельные амнион и хорион из одной плаценты, но может включать только часть амниона или хориона. Расщепленная ткань культивируется, например, в течение примерно 1-3 недель, предпочтительно примерно 2 недели. После удаления неадгезивных клеток собирают образованные колонии высокой плотности, например, трипсинизацией. Указанные клетки собирают, снова суспендируют в подходящем объеме питательной среды культуры клеток и затем используют для пересева культуры для ее выращивания. Питательные культуры для выращивания клеток могут представлять аппараты культуры отдельных клеток любой конфигурации, например, Cell Factory (от NUNC™). Клетки могут подразделяться до любой степени, в которой происходит рост культур, например, 1×103, 2×103, 3×103, 4×103, 5×103, 6×103, 7×103, 8×103, 9×103, 1×104, 1×104, 2×104, 3×104, 4×104, 5×104, 6×104, 7×104, 8×104, 9×104 или 10×104 стволовых клеток. Предпочтительно от примерно 1×103 до примерно 1×104 клеток/см2 используется для высева каждой выращиваемой культуры. Количество клеток в выращиваемых культурах может быть больше или меньше в зависимости от конкретной(ных) плаценты (плацент), из которых получают клетки.
Культуры, выращиваемые с увеличением количества клеток, выращиваются до тех пор, пока плотность клеток в культуре не достигнет определенного значения, например, примерно 1×105 клеток/см2. Клетки могут либо собираться и криоконсервироваться в этой точке либо высеваться в новую питательную среду для выращивания клеток, как описано выше. Клетки могут пересеваться, например, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 раз перед применением. Запись кумулятивного числа удвоений популяций предпочтительно сохраняется в процессе выращивания культуры(культур). Клетки могут выращиваться до 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40 или до 60 удвоений количества клеток. Однако предпочтительно количество удвоений популяции перед разделением популяции клеток на отдельные дозы составляет от примерно 15 до примерно 30. Клетки могут выращиваться непрерывно через процесс экспансии или могут замораживаться в одной или нескольких точках процесса экспансии.
Клетки, предназначенные для применения в индивидуальных дозах, могут замораживаться, например, подвергаться криоконсервации, для последующего применения. Индивидуальные дозы могут включать, например, от примерно 1 миллиона до примерно 50 миллионов клеток на мл и могут в сумме включать от примерно 106 до примерно 1010 клеток.
Таким образом, в одном варианте осуществления изобретения бланк плацентарных клеток может быть изготовлен способом, включающим рост плацентарных клеток первичной культуры из послеродовой плаценты человека для первого множества удвоений популяции; криоконсервацию указанных плацентарных клеток для формирования Master Cell Bank; выращивание множества плацентарных клеток из Master Cell Bank для второго множества удвоений популяции; криоконсервацию указанных плацентарных клеток для формирования Working Cell Bank; рост (экспансию) множества плацентарных клеток из Working Cell Bank для третьего множества удвоений популяции; и криоконсервацию указанных плацентарных клеток в индивидуальных дозах, где указанные индивидуальные дозы вместе составляют банк плацентарных клеток. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки первичной культуры включают плацентарные клетки из плацентарного перфузата. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки первичной культуры включают плацентарные клетки из расщепленной плацентарной ткани. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки первичной культуры включают плацентарные клетки из плацентарного перфузата и расщепленной плацентарной ткани. В еще одном специфическом варианте осуществления изобретения все указанные плацентарные клетки в указанной первичной культуре плацентарных клеток получены из одной и той же плаценты. В еще одном специфическом варианте осуществления изобретения способ дополнительно включает стадию отбора CD200+ или HLA-G+ плацентарных клеток или CD10+, CD34-, CD105+, CD200+ плацентарных клеток из указанного множества указанных плацентарных клеток из указанного Working Cell Bank для формирования индивидуальных доз. В еще одном специфическом варианте осуществления изобретения указанные индивидуальные дозы включают от примерно 104 до примерно 105 плацентарных клеток. В еще одом специфическом варианте осуществления изобретения указанные индивидуальные дозы включают от примерно 105 до примерно 106 плацентарных клеток. В еще одном специфическом варианте осуществления изобретения указанные индивидуальные дозы включают от примерно 106 до примерно 107 плацентарных клеток. В еще одном специфическом варианте осуществления изобретения указанные индивидуальные дозы включают от примерно 107 до примерно 108 плацентарных клеток. В еще одном специфическом варианте осуществления изобретения указанные индивидуальные дозы включают от 108 до примерно 109 плацентарных клеток. В еще одном специфическом варианте осуществления изобретения указанные индивидуальные дозы включают от примерно 109 до примерно 1010 плацентарных клеток.
Способы получения композиций, включающих плацентарные клетки, например, плацентарные стволовые клетки или плацентарные мультипотентные клетки, предоставленные согласно настоящему изобретению, могут объединяться при создании банка плацентарных клеток на любой стадии, как описано выше. В одном варианте осуществления изобретения фармацевтическую композицию получают после создания банка базовых клеток (Master Cell Bank), во время создания одного или нескольких банков рабочих клеток (Working Cell Bank) из указанного банка базовых клеток или в процессе культивации роста (экспансии) плацентарных клеток из указанных банков рабочих клеток. Например, плацентарные клетки из банка рабочих клеток могут подвергаться оттаиванию и культивироваться для множества удвоений популяции. В одном варианте осуществления изобретения, когда произведено желаемое число клеток или имело место желаемое удвоение популяций, плацентарные клетки могут быть собраны, например, центрифугированием и снова суспендированы в растворе, включающем, например, декстран 40, например, 5,5% декстрана 40. В некоторых вариантах осуществления изобретения плацентарные стволовые клетки собирают второй раз и снова суспендируют в растворе, включающем декстран и криоконсервант, например, в 5,5% растворе декстрана 40, включающем 10% HSA, 5% ДМСО и криоконсервант. Криоконсервированные плацентарные клетки подвергаются оттаиванию, например, непосредственно перед применением, например, непосредственно перед конечным получением композиции, как описано в Разделе 5.2., выше.
Описанные выше способы получения композиции, включающей плацентарные клетки, например, плацентарные стволовые клетки или плацентарные мультипотентные клетки, могут использоваться сразу после получения и/или при применении банка плацентарных клеток, например, в каждой точке, где плацентарные клетки должны подвергаться криоконсервированию или, например, в точке, когда плацентарные клетки приготавливают для индивидуального введения перед конечным криоконсервированием и после оттаивания перед введением индивидууму.
В предпочтительном варианте осуществления изобретения донор, от которого получена плацента (например, мать), тестируется на выявление по меньшей мере одного патогена. Если тесты матери положительны на тестируемый патоген, вся партия от данной плаценты бракуется. Такое тестирование может проводиться в любое время в процессе получения партий плацентарных клеток, в том числе перед или после создания исходной культуры клеток или в процессе выращивания (экспансии) культуры. Патогены, присутствие которых тестируется, могут включать, но без ограничения, гепатит А, гепатит В, гепатит С, гепатит D, гепатит Е, вирус иммунодефицита человека (питы I и II), цитомегаловирус, вирус герпеса и т.п.
5.6. КОНСЕРВАЦИЯ ПЛАЦЕНТАРНЫХ КЛЕТОК
Изолированные плацентарные клетки, например, изолированные плацентарные мультипотентные клетки, описанные в Разделе 5.2. выше, могут консервироваться, например, во время сбора, то есть помещаться в условия, позволяющие осуществлять длительное хранения, или условия, которые ингибируют гибель клеток, например, апоптоз или некроз, например, в процессе сбора или перед получением композиций, описанных в настоящем изобретении, например, с использованием способов, описанных в изобретении.
Плацентарные клетки могут подвергаться консервированию с использованием, например, композиции, включающей ингибитор апоптоза, ингибитор некроза и/или перфторуглерод, способный переносить кислород, как описано в родственной Публикации заявки на патент США № 2007/0190042, содержание которой таким образом полностью включено в настоящее описание путем ссылки. В одном варианте осуществления изобретения способ консервации популяции клеток, предназначенных для применения в композициях, включающих клетки, описанные в настоящем изобретении, включает контактирование указанной популяции клеток с композицией клеточного сбора, включающей ингибитор апоптоза и перфторуглерод, способный переносить кислород, где указанный ингибитор апоптоза присутствует в количестве и в течение времени, достаточного для снижения апоптоза в популяции клеток по сравнению с популяцией клеток, не содержащей ингибитор апоптоза. В специфическом варианте осуществления изобретения указанный ингибитор апоптоза представляет собой ингибитор каспазы. В специфическом варианте осуществления изобретения указанный ингибитор апоптоза представляет собой ингибитор JNK. В более специфическом варианте осуществления изобретения указанный JNK ингибитор не модулирует дифференциацию или пролиферацию указанных клеток. В еще одном варианте осуществления изобретения указанная композиция клеточного сбора включает указанный ингибитор апоптоза и указанный перфторуглерод, способный переносить кислород в раздельных фазах. В еще одном варианте осуществления изобретения указанная композиция клеточного сбора включает указанный ингибитор апоптоза и указанный перфторуглерод, способный переносить кислород, в эмульсии. В еще одном варианте осуществления изобретения композиция клеточного сбора дополнительно включает эмульгатор, например, лецитин. В еще одном варианте осуществления изобретения указанный ингибитор апоптоза и указанный перфторуглерод имеют температуру в интервале от примерно 0°С до примерно 25°С во время контактирования клеток. В еще одном более специфическом варианте осуществления изобретения указанные ингибитор апоптоза и указанный перфторуглерод имеют температуру в интервале примерно от 2°С до 10°С или в интервале от примерно 2°С до примерно 5°С во время контактирования клеток. В еще одном более специфическом варианте осуществления изобретения указанное контактирование проводится во время транспортировки указанной популяции клеток. В еще одном более специфическом варианте осуществления изобретения указанное контактирование проводится во время замораживания и оттаивания указанной популяции клеток.
Популяции плацентарных клеток могут консервироваться, например, способом, включающим контактирование указанной популяции клеток с ингибитором апоптоза и орган-консервирующим соединением, где указанный ингибитор апоптоза присутствует в количестве и в течение периода времени, достаточных для снижения или предотвращения апоптоза в популяции клеток по сравнению с популяцией клеток, не контактируемой с ингибитором апоптоза. В специфическом варианте осуществления изобретения орган-консервирующее соединение представляет собой UW раствор (описанный в патенте США № 4798824; также известный как ViaSpan; см. также Southard et al., Transplantation 49(2):251-257 (1990)) или раствор, описанный в патенте США № 5552267 (Stern et al.). В еще одном варианте осуществления изобретения указанно орган-консервирующее соединение представляет собой гидроксиэтилкрахмал, лактобионовую кислоту, раффинозу или их сочетание. В еще одном варианте осуществления изобретения композиция клеточного сбора дополнительно включает перфторуглерод, способный переносить кислород, в виде двух фаз или в виде эмульсии.
В еще одном варианте осуществления способа плацентарные стволовые клетки подвергаются контактированию с композицией клеточного сбора, включающей ингибитор апоптоза и перфторуглерод, способный переносить кислород, орган-консервирующее соединение или их сочетание, в процессе перфузии. В еще одном варианте осуществления указанного способа указанные клетки подвергаются контактированию в процессе деструкции ткани, например, ферментативного расщепления. В еще одном варианте осуществления указанного способа плацентарные клетки подвергаются контактированию с указанной композицией клеточного сбора после перфузии или после сбора клеток посредством деструкции ткани, например, ферментативным расщеплением.
Обычно в процессе сбора плацентарных клеток, обогащения и выделения предпочтительно снижать до минимума или исключить стресс клеток вследствие гипоксии и механического стресса. Поэтому в еще одно варианте осуществления способа клеку или популяцию клеток выдерживают в гипоксических условиях в процессе сбора, обогащения или выделения в течение менее чем шести часов в процессе указанной консервации, где гипоксические условия представляют собой концентрацию кислорода, которая составляет менее нормальной концентрации кислорода в крови. В более специфическом варианте осуществления изобретения указанная популяция клеток выдерживается в указанных гипоксических условиях в течение менее двух часов в процессе указанной консервации. В еще одном более специфическом варианте осуществления изобретения указанная популяция клеток выдерживается в указанных гипоксических условиях в течение менее одного часа или менее тридцати минут или не выдерживается в гипоксических условиях в процессе сбора, обогащения или выделения. В еще одном специфическом варианте осуществления изобретения указанная популяция клеток не подвергается напряжению сдвига в процессе сбора, обогащения или выделения.
Плацентарные клетки могут подвергаться криоконсервации обычно или специфическими способами, описанными в настоящем изобретении. В одном варианте осуществления изобретения криоконсервантом, используемым для криоконсервации плацентарных клеток, является ДМСО. В еще одном варианте осуществления изобретения криоконсервант представляет собой пропиленгликоль, например, примерно 1,5 М пропиленгликоль. Криоконсервантом также может являться глицерин, этиленгликоль, полифенол (например, в концентрации от примерно 30 до примерно 120 м.д.) и т.п. В других вариантах осуществления указанных способов криоконсервант представляет собой зародышевую телячью сыворотку, сыворотку крови человека или альбумин сыворотки крови человека в сочетании с одним или несколькими добавками, выбранными из группы, включающей ДМСО, трегалозу и декстран. В специфическом варианте осуществления изобретения криоконсервант представляет собой сыворотку крови человека, ДМСО и трегалозу или представляет собой зародышевую телячью сыворотку и ДМСО. В некоторых вариантах осуществления изобретения плацентарные клетки подвергаются криоконсервации в криоконсервационной среде в небольших контейнерах, например, ампулах. Плацентарные клетки в процессе криоконсервации предпочтительно охлаждаются со скоростью 1°С/мин. Предпочтительная температура криоконсервации находится в интервале от примерно -80°С до примерно -180°С, предпочтительно от примерно -125°С до примерно -140°С. Криоконсервированные клетки могут переноситься в жидкий азот перед оттаиванием для применения. В некоторых вариантах, например, после того как ампулы достигают температуры примерно -90°С, они переносятся в атмосферу жидкого азота в емкость для хранения. Криоконсервация может также осуществляться с использованием морозильного аппарата с контролируемой скоростью замораживания. Криоконсервированные клетки предпочтительно оттаиваются при температуре в интервале от примерно 25°С до примерно 40°С, предпочтительно при температуре примерно 37°С.
5.7. КОМПОЗИЦИИ, СОДЕРЖАЩИЕ КЛЕТКИ
5.7.1. Композиции, включающие плацентарные клетки
Плацентарные стволовые клетки, описанные в настоящем изобретении, например, в Разделе 5.3., могут включать клетки одного или нескольких видов, например, плацентарные стволовые клетки или плацентарные мультипотентные клетки, описанные в настоящем изобретении, где клетки выделены из плаценты, например, плаценты человека. В специфическом варианте осуществления изобретения любая их указанных выше композиций включает матрицу. В более специфическом варианте осуществления изобретения в любой из описанных выше композиций указанная матрица представляет собой трехмерный каркас. В другом более специфическом варианте осуществления изобретения указанная матрица включает коллаген, желатин, ламинин, фибронектин, пектин, орнитин или витронектин. В еще одном более специфическом варианте осуществления изобретения матрица представляет собой амниотическую мембрану или биоматериал, полученный из амниотической мембраны. В еще одном более специфическом варианте осуществления изобретения указанная матрица включает внеклеточный мембранный белок. В еще одном более специфическом варианте осуществления изобретения указанная матрица включает биоактивное соединение. В еще одном более специфическом варианте осуществления изобретения указанное биоактивное соединение представляет собой фактор роста, цитокин, антитела или органическое соединение с молекулярной массой менее 5000 дальтон.
В еще одном варианте осуществления изобретения композиция, используемая в композициях, например, фармацевтических композициях, согласно настоящему изобретению, включает среду, кондиционированную любыми из описанных выше плацентарных клеток или любой из описанных выше популяций плацентарных клеток. В специфическом варианте осуществления изобретения любая такая композиция включает стволовые клетки, которые не получены из плаценты. В более специфическом варианте осуществления изобретения указанная стволовая клетка представляет собой эмбриональную стволовую клетку. В другом более специфическом варианте осуществления изобретения указанная стволовая клетка является мезенхимальной стволовой клеткой. В еще одном более специфическом варианте осуществления изобретения указанная стволовая клетки представляет собой стволовую клетку, полученную из костного мозга. В еще одном более специфическом варианте осуществления изобретения указанная стволовая клетка представляет собой гемопоэтическую клетку-предшественник. В еще одном более специфическом варианте осуществления изобретения указанная стволовая клетка представляет собой соматическую стволовую клетку. В еще более специфическом варианте осуществления изобретения указанная соматическая клетка представляет собой невральную стволовую клетку, гепатическую стволовую клетку, панкреатическую стволовую клетку, эндотелиальную стволовую клетку, кардиальную стволовую клетку или мышечную стволовую клетку.
5.7.1.1. Фармацевтические композиции
Популяции изолированных плацентарных клеток или популяции клеток, включающие изолированные плацентарные клетки, включены в фармацевтические композиции или являются их компонентами. Изолированные плацентарные клетки могут быть получены в форме, которая может легко вводиться индивидууму, например, в форме плацентарных клеток перфузата или изолированных плацентарных клеток, которые находятся в контейнере, подходящем для медицинского применения. Таким контейнером может быть, например, шприц, стерильный пластиковый пакет (мешок), колба, банка или другой контейнер, из которого популяция плацентарных клеток может легко доставляться потребителю. Например, контейнер может представлять собой ампулу с кровью или другой пластиковый мешок, подходящий для медицинского назначения и для внутривенного введения содержащейся в нем жидкости пациенту. В некоторых вариантах осуществления изобретения контейнер может представлять собой контейнер, который позволяет криоконсервировать популяцию изолированных плацентарных клеток.
В одном варианте осуществления изобретения контейнер представляет собой контейнер, который способствует осуществлению или дает возможность осуществлять одну или несколько стадий способов, описанных в настоящем изобретении. Например, когда способ получения композиции, содержащей клетки, включает, например, стадии (а) контактирования указанных клеток с раствором, включающим декстран и сывороточный альбумин человека (HSA) для получения раствора, содержащего клетки; (b) фильтрации раствора; (с) разбавления указанных клеток до содержания примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр раствором первого разбавления, включающим декстран; и (d) разбавления указанных клеток раствором второго разбавления, включающим декстран, но не включающим HSA; клетки, например, изолированные плацентарные клетки или плацентарные клетки перфузата, могут помещаться в контейнер, например, в промежутке между стадиями (с) и (d), где контейнер представляет собой контейнер, который, например, облегчает процесс криоконсервации и/или способствует доставке клеток индивидууму, нуждающемуся в таких клетках, и т.п. В некоторых вариантах осуществления изобретения указанное разбавление проводится до содержания не более примерно 15×106 клеток на миллилитр. В некоторых других вариантах указанное разбавление проводится до содержания не более примерно 10±3×106 клеток на миллилитр. В некоторых других вариантах, если количество клеток составляет менее примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной.
Например, изолированные плацентарные клетки могут подвергаться криоконсервированию, например, в пакете (мешке), например, в пластиковом пакете для крови или аналогичном мешке, далее подвергаться оттаиванию и, наконец, разбавляться в этом же мешке. В другом варианте осуществления изобретения, где способ получения композиции, включающей клетки, включает, например, (а) центрифугирование множества клеток, например, плацентарных клеток перфузата или изолированных плацентарных клеток для сбора клеток; (b) суспендирование клеток в 5,5% декстране 40; (с) центрифугирование клеток для сбора клеток; (d) повторное суспендирование клеток в 5,5% растворе декстрана 40, который включает 10% HSA; (е) фильтрацию клеток через 70 мкм - 100 мкм фильтр; (f) разбавление клеток в растворе, включающем 5,5% декстрана 40, 10% HSA и 5% ДМСО, до содержания не более чем примерно 10±3×106 клеток/мл; (g) криоконсервацию клеток; (h) оттаивание клеток; (i) разбавление клеток в соотношении от 1:1 до 1:11 раствором, содержащим 10% декстрана 40, для получения указанной фармацевтической композиции; тогда помещение клеток в контейнер, который, например, упрощает криоконсервацию и/или введение клеток индивидууму, нуждающемуся в таком введении, может проводиться, например, на любой стадии после стадии (е). В некоторых вариантах осуществления изобретения указанное разбавление на стадии (f) проводится до содержания примерно от 1 до 50×106, от 1 до 40×106, от 1 до 30×106, от 1 до 20×106, от 1 до 15×106 или от 1 до 10×106 клеток на миллилитр. В некоторых вариантах осуществления изобретения указанное разбавление на стадии (f) проводится до не более чем примерно 15×106 клеток на миллилитр. В других определенных вариантах осуществления изобретения, если количество клеток составляет менее примерно 10±3×106 клеток на миллилитр, фильтрация является необязательной. В специфическом варианте осуществления изобретения клетки, например, изолированные плацентарные клетки или плацентарные клетки перфузата, могут помещаться в контейнер после фильтрации, затем в контейнере подвергаться разбавлению, криоконсервации, оттаиванию и, наконец, разбавлению перед введением индивидууму.
Изолированные плацентарные клетки в композициях, например, в фармацевтических композициях, представленных в настоящем изобретении, могут включать плацентарные клетки, полученные от единственного донора или от множества доноров. Изолированные плацентарные клетки могут быть полностью HLA-совместимыми с предполагаемым реципиентом или частично или полностью HLA-несовместимыми.
Таким образом, в одном варианте осуществления изобретения изолированные плацентарные клетки в композициях согласно настоящему изобретению вводятся индивидууму, нуждающемуся в таком введении. В специфическом варианте указанные изолированные плацентарные клетки вводятся внутримышечно, внутрикожно, интраперитонеально, внутриартериально, подкожно, внутривенно или внутриглазным способом. В одном варианте осуществления изобретения изолированные плацентарные клетки в композициях согласно изобретению вводятся индивидууму, нуждающемуся в таком введении, в форме композиции, включающей изолированные плацентарные клетки в контейнере. В другом специфическом варианте осуществления изобретения контейнер представляет собой мешок, колбу или банку. В более специфическом варианте осуществления изобретения указанный мешок представляет собой стерильный пластиковый мешок. В более специфическом варианте осуществления изобретения указанный мешок облегчает внутривенное введение или дает возможность осуществлять такое введение указанных изолированных плацентарных клеток, например, внутривенным вливанием, инъекцией болюсов или т.п. Мешок может включать множество просветов или отсеков, которые взаимосвязаны, чтобы позволить смешиваться изолированным плацентарных клеткам с одним или несколькими другими растворами, например, лекарственных средств, до или в процессе введения. В еще одном специфическом варианте осуществления изобретения перед криоконсерваций раствор, включающий изолированные плацентарные клетки, включает одно или несколько соединений, которые способствуют криоконсервации объединенных клеток. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки помещены в физиологически приемлемый водный раствор. В более специфическом варианте осуществления изобретения указанный физиологически приемлемый водный раствор представляет собой 0,9% раствор NaCl. В еще одном специфическом варианте осуществления изобретения указанные изолированные плацентарные клетки включают плацентарные клетки, которые являются HLA-совместимыми с реципиентом указанной клеточной популяции. В еще одном специфическом варианте осуществления изобретения указанные объединенные клетки включают плацентарные клетки, которые являются по меньшей мере частично HLA-несовместимыми с реципиентом указанной клеточной популяции. В еще одном специфическом варианте осуществления изобретения указанные плацентарные клетки получены от множества доноров.
Изолированные плацентарные клетки в фармацевтической композиции могут представлять собой любые из изолированных плацентарных клеток, описанных в настоящем изобретении. В специфическом варианте осуществления изобретения изолированные плацентарные клетки, описанные в настоящем изобретении, представляют собой CD10+, CD34-, CD105+, CD200+ клетки, которые находятся в контейнере. В специфическом варианте осуществления изобретения изолированные плацентарные клетки, описанные в настоящем изобретении, представляют собой CD200+, HLA-G+ клетки, которые помещены в контейнер. В еще одном варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD200+, HLA-G+ клетки, которые находятся в контейнере. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD73+, CD105+, CD200+ клетки, которые находятся в контейнере. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD200+, OCT-4+ клетки, которые находятся в контейнере. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD73+, CD105+ клетки, которые находятся в контейнере, где указанные клетки способствуют образованию одного или нескольких эмбриоидоподобных телец, когда культивируются с популяцией плацентарных клеток в условиях, которые дают возможность образованию эмбриоидоподобных телец. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD73+, CD105+, HLA-G+ клетки, которые были подвергнуты криоконсервации и находятся в контейнере. В еще одном специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой OCT-4+ клетки, которые находятся в контейнере, где указанные клетки способствуют образованию одного или нескольких эмбриоидоподобных телец, когда культивируются с популяцией плацентарных клеток в условиях, которые дают возможность образованию эмбриоидоподобных телец. В специфическом варианте осуществления изобретения любых из плацентарных клеток указанный контейнер представляет собой мешок.
В различных специфических вариантах осуществления изобретения указанный контейнер включает примерно по меньшей мере или самое большее 1×106 изолированных плацентарных клеток или плацентарных клеток перфузата, 5×106 изолированных плацентарных клеток или плацентарных клеток перфузата, 1×107 изолированных плацентарных клеток или плацентарных клеток перфузата, 5×107 изолированных плацентарных клеток или плацентарных клеток перфузата, 1×108 изолированных плацентарных клеток или плацентарных клеток перфузата, 5×108 изолированных плацентарных клеток или плацентарных клеток перфузата, 1×109 изолированных плацентарных клеток или плацентарных клеток перфузата, 5×109 изолированных плацентарных клеток или плацентарных клеток перфузата или 1×1010 изолированных плацентарных клеток или плацентарных клеток перфузата. В других вариантах осуществления изобретения стандартная доза изолированных плацентарных клеток или плацентарных клеток перфузата может включать в различных вариантах осуществления изобретения примерно по меньшей мере или самое большее 1×105, 5×105, 1×106, 5×106, 1×107, 5×107, 1×108, 5×108, 1×109, 5×109, 1×1010, 5×1010, 1×1011или более изолированных плацентарных клеток или плацентарных клеток перфузата. В других вариантах осуществления изобретения контейнер или доза изолированных плацентарных клеток или плацентарных клеток перфузата включает от 1×105 до 5×105 изолированных плацентарных клеток или плацентарных клеток перфузата, от 5×105 до 1×106 изолированных плацентарных клеток или плацентарных клеток перфузата, от 1×106 до 5×106 изолированных плацентарных клеток или плацентарных клеток перфузата, от 5×106 до 1×107 изолированных плацентарных клеток или плацентарных клеток перфузата, от 1×107 до 5×107 изолированных плацентарных клеток или плацентарных клеток перфузата, от 5×107 до 1×108 изолированных плацентарных клеток или плацентарных клеток перфузата, от 1×108 до 5×108 изолированных плацентарных клеток или плацентарных клеток перфузата, от 5×108 до 1×109 изолированных плацентарных клеток или плацентарных клеток перфузата, от 1×109 до 5×109 изолированных плацентарных клеток или плацентарных клеток перфузата, от 5×109 до 1×1010 изолированных плацентарных клеток или плацентарных клеток перфузата, от 1×1010 до 5×1010 изолированных плацентарных клеток или плацентарных клеток перфузата, от 5×1010 до 1×1011 изолированных плацентарных клеток или плацентарных клеток перфузата или более изолированных плацентарных клеток или плацентарных клеток перфузата. В предпочтительном варианте осуществления изобретения фармацевтическая композиция включает количество изолированных плацентарных клеток или плацентарных клеток перфузата, достаточное для введения примерно 2×107 до примерно 10×107 клеток на килограмм реципиента.
В других вариантах осуществления любой из описанных выше криоконсервированных популяций указанные клетки пересеваются примерно по меньшей мере или не более 5 раз, не более 10 раз, не более 15 раз или не более 20 раз. В еще одном специфическом варианте осуществления любых из описанных выше криоконсервированных клеток указанные клетки культивируются в указанном контейнере.
Фармацевтические композиции, включающие плацентарные стволовые клетки, описанные в настоящем изобретении, могут включать любые из изолированных плацентарных клеточных популяций или изолированных плацентарных клеточных типов, описанных в настоящем изобретении, или их комбинации. Фармацевтические композиции могут включать плодные, материнские либо плодные и материнские плацентарные клетки, например, плацентарные стволовые клетки или плацентарные мультипотентные клетки. Фармацевтические композиции согласно настоящему изобретению могут дополнительно включать изолированные плацентарные клетки, полученные от единственного индивидуума или плаценты либо от множества индивидуумом или плацент.
Фармацевтические композиции согласно изобретению включают популяции клеток, которые содержат 50% жизнеспособных клеток или более (то есть по меньшей мере 50% клеток в популяции являются функциональными или живыми). Предпочтительно по меньшей мере 60% клеток в популяции являются жизнеспособными. Более предпочтительно по меньшей мере 70%, 80%, 90%, 95% или 99% клеток в популяции в фармацевтической композиции являются жизнеспособными.
В одном варианте осуществления изобретения фармацевтическая композиция включает изолированные плацентарные клетки, которые представляют собой по существу или полностью нематеринскими по происхождению, то есть имеют плодный генотип; например, по меньшей мере примерно 90%, 95%, 98%, 99% или примерно 100% являются нематеринскими по происхождению. Например, в одном варианте осуществления изобретения фармацевтическая композиция включает популяцию изолированных плацентарных клеток, которые представляют собой CD200+ и HLA-G+; CD73+, CD105+ и CD200+; CD200+ и OCT-4+; CD73+, CD105+ и HLA-G+; CD73+ и CD105+, и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции плацентарных клеток, включающей указанную популяцию изолированной плацентарной клетки, когда указанная популяция плацентарных клеток культивируется в условиях, которые дают возможность образованию эмбриоидоподобного тельца; или OCT-4+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции плацентарных клеток, включающей указанную популяцию изолированной плацентарной клетки, когда указанная популяция плацентарных клеток культивируются в условиях, которые дают возможность образованию эмбриоидоподобного тельца; или их сочетание, где по меньшей мере 70%, 80%, 90%, 95% или 99% указанных изолированных плацентарных клеток являются нематеринскими по происхождению. В еще одном варианте осуществления изобретения фармацевтическая композиция включает популяцию изолированных плацентарных клеток, которые представляют собой CD10+, CD105+ и CD34-; CD10+, CD105+, CD200+ и CD34-; CD10+, CD105+, CD200+, CD34- и по меньшей мере CD90+ или CD45-; CD10+, CD90+, CD105+, CD200+, CD34- и CD45-; CD10+, CD90+, CD105+, CD200+, CD34- и CD45-; CD200+ и HLA-G+; CD73+, CD105+ и CD200+; CD200+ и OCT-4+; CD73+, CD105+ и HLA-G+; CD73+ и CD105+, и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяции плацентарных клеток, включающей указанные изолированные плацентарные клетки, когда указанная популяция плацентарных клеток культивируется в условиях, которые делают возможным образование эмбриоидоподобного тельца; OCT-4+ и способствуют образованию одного или нескольких эмбриоидоподобных телец в популяция плацентарных клеток, включающей указанные изолированные плацентарные клетки, когда указанная популяция плацентарных клеток культивируется в условиях, которые делают возможным образование эмбриоидоподобного тельца; или клетки одного или нескольких видов из CD117-, CD133-, KDR-, CD80-, CD86-, HLA-A,B,C+, HLA-DP,DQ,DR- и/или PDL1+; или сочетание клеток указанных видов, где по меньшей мере 70%, 80%, 90%, 95% или 99% указанных изолированных плацентарных клеток являются нематеринскими по происхождению. В специфическом варианте осуществления изобретения фармацевтическая композиция дополнительно включает стволовую клетку, которая получена не из плаценты.
Фармацевтические композиции согласно изобретению могут включать одно или несколько соединений, которые, например, способствуют вживлению трансплантата (например, антитела против рецептора T-клеток, иммуносупрессор или т.п.); стабилизаторы, такие как альбумин, декстран 40, желатин, гидроксиэтилкрахмал, плазмалит (Plasmalyte) и т.п.).
5.7.2 Композиции, включающие гемопоэтические плацентарные клетки или плацентарные клетки перфузата
В некоторых вариантах осуществления композиций согласно изобретению изолированные плацентарные клетки представляют собой CD34+ плацентарные стволовые клетки, например, гемопоэтические плацентарные клетки или клетки-предшественники. Такие клетки могут быть получены из плацентарной ткани, например, из плаценты, которая дренировалась от пуповинной крови и подвергалась перфузии для удаления остаточной крови. В некоторых вариантах осуществления изобретения CD34+ плацентарные стволовые клетки представляют собой CD38+. В некоторых вариантах осуществления изобретения CD34+ изолированные плацентарные клетки представляют собой CD38-. В некоторых других вариантах осуществления изобретения CD34+ изолированные плацентарные клетки представляют собой CD45+. В специфическом варианте осуществления изобретения изолированные плацентарные клетки представляют собой CD34+, CD38- и CD45+. В некоторых вариантах осуществления изобретения клетки представляют собой гемопоэтические клетки. В более специфическом варианте осуществления изобретения плацентарные CD34+ клетки представляют собой гемопоэтические клетки. В некоторых вариантах осуществления CD34+ клетки или гемопоэтические клетки представляют собой клетки, полученные из плацентарного перфузата. В некоторых вариантах осуществления, CD34+ клетки или гемопоэтические клетки представляют собой клетки, полученные ферментативным расщеплением и физической деструкцией плацентарной ткани. CD34+ клетки и гемопоэтические клетки могут быть получены из единственной плаценты или из нескольких плацент.
В некоторых вариантах осуществления клетки композиций согласно изобретению, полученных способами согласно изобретению, представляют собой клетки, полученные из плацентарного перфузата. Термин «клетки, полученные из плацентарного перфузата», в рамках изобретения, включает клетки, содержащие цельные ядра и полученные, например, изолированные, из плацентарного перфузата, подмножество ядросодержащих клеток, полученных из плацентарного перфузата, или клетки, культивированные или пролиферированные из клетки, полученной непосредственно из плацентарного перфузата. Плацентарный перфузат может быть получен из плаценты, которая была дренирована от пуповинной крови и подвергнута перфузии для удаления остаточной крови перед перфузий для получения плацентарных клеток. Плацентарный перфузат может быть получен из плаценты, которая была дренирована от пуповинной крови, но не подвергалась перфузии для удаления остаточной крови. Плацентарный перфузат может быть получен из плаценты, которая не подвергалась ни дренированию от пуповинной крови, ни перфузии для удаления остаточной крови. В двух последний вариантах осуществления изобретения плацентарные клетки, например, ядросодержащие клетки из плацентарного перфузата, например, клетки из плацентарного перфузата, содержащие цельные ядра, включают ядросодержащие клетки из плацентарной крови и/или пуповинной крови. Плацентарные клетки перфузата могут быть получены из одной плаценты или из нескольких плацент.
5.7.3 Иммортализованные линии плацентарных клеток
Плацентарные клетки млекопитающих могут быть условно иммортализированы трансфекцией любым вектором, содержащим ген ускорения роста, то есть белком, кодирующим ген, который в подходящих условиях ускоряет рост трансфицированной клетки, так что продуцирование и/или активность белка, ускоряющего рост, может регулироваться внешним фактором. В предпочтительном варианте осуществления изобретения ген, ускоряющий рост, представляет собой онкоген, такой как, но без ограничения, v-myc, N-myc, c-myc, p53, супер Т-антиген вируса SV40, Т-антиген вируса полиомы, E1a аденовирус или E7 белок папилловируса человека.
Внешняя регуляция ускоряющего рост белка может достигаться при помещении гена, ускоряющего рост, под контроль регулируемого извне промотора, например, промотора, активностью которого можно управлять, например, изменяя температуру инфицированных вирусом клеток или состав питательной среды, которая находится в контакте с клетками. В одном варианте осуществления изобретения может использоваться система тетрациклин(tet)-контролируемой экспрессии гена (см. Gossen et al., Proc. Natl. Acad. Sci. USA 89:5547-5551, 1992; Hoshimaru et al., Proc. Natl. Acad Sci. USA 93:1518-1523, 1996). В отсутствии тетрациклина tet-контролируемый трансактиватор (tTA) внутри данного вектора значительно активирует транскрипцию из phCMV*-1, минимального промотора из цитомегаловируса человека, слитого с tet-операторными последовательностями. tTA является слитым белком репрессора (tetR) транспозон-10-производного tet-резистентного оперона Escherichia coli и кислотного домена VP16 вируса простого герпеса. Низкие нетоксичные концентрации tet (например, 0,01-1,0 мкг/мл) почти полностью аннулируют трансактивацию посредством tTa.
В одном варианте осуществления изобретения вектор дополнительно содержит ген-кодирующий селектируемый маркер, например, белок, который привносит резистентность к лекарственному средству. Ген (neoR) бактериальной резистентности к неомицину представляет собой один такой маркер, который может использоваться в этих способах. Клетки, переносящие neoR, могут выбираться способами, известными специалисту данной области техники, такими как, например, добавление 100-200 мкг/мл G418 в питательную среду, используемую для культивирования.
Трансфицирование может достигаться любым методом, известным специалисту данной области техники, включая, но без ограничения, ретровирусную инфекцию. Обычно культура клеток может быть трансфицирована инкубированием со смесью кондиционированной среды, собранной от продуцентной клеточной линии для вектора и DMEM/F12, содержащего N2 добавки. Например, плацентарная клеточная культура, полученная, как описано выше, может инфицироваться, например, после пяти дней in vitro инкубированием в течение примерно 20 часов в одном объеме кондиционированной среды и двух объемах DMEM/F12, содержащих N2 добавки. Трансфицированные клетки, несущие селектируемый маркер, затем могут отбираться, как описано выше.
После трансфицирования культуры пересевают на поверхность, которая обеспечивает пролиферацию, например, позволяет осуществить удвоение численности по меньшей мере 30% клеток в течение периода продолжительностью 24 часа. Предпочтительно, субстрат представляет собой субстрат полиорнитин/ламинин, состоящий из пластика культуры ткани, покрытого полиорнитином (10 мкг/мл) и/или ламинином (10 мкг/мл), субстрат полилизин/ламинин или поверхность, обработанную фибронектином. Затем культуры вскармливаются каждые 3-4 дня питательной средой, которая может содержать или не содержать в качестве добавок один или несколько факторов, повышающих пролиферацию. Факторы, повышающие пролиферацию, могут добавляться в питательную среду, когда культуры слиты менее чем на 50%.
Условно иммортализованные линии плацентарных клеток могут пересеваться с использованием стандартных методик, таких как трипсинизация, при 80-95% слияния. В некоторых вариантах осуществления изобретения для сохранения отбора успешно проводятся до приблизительно двенадцати пассирований для сохранения селекции (например, добавление G418 для клеток, содержащих ген резистентности к неомицину). Клетки могут также замораживаться в жидком азоте для длительного хранения.
Клональные клеточные линии могут изолироваться от условно иммортализованных плацентарных клеточных линий человека, полученных, как описано выше. Обычно такие клональные клеточные линии могут выделяться с использованием стандартных методик, таких как предельное разбавление или использование циклов клонирования, и увеличиваться в численности. Клональные клеточные линии могут снабжаться питательной средой и подвергаться пересеву, как описано выше.
Условно иммортализованные линии плацентарных клеток человека, которые могут, но не обязательно, клонироваться, обычно могут стимулироваться к дифференциации посредством подавления продуцирования и/или активности белка, ускоряющего рост в условиях культивирования, которые способствуют дифференциации. Например, если ген, кодирующий белок, ускоряющий рост, контролируется промотором, который регулируется извне, условия, например, температура или состав питательной среды, могут модифицироваться для подавления транскрипции гена, стимулирующего рост. Для системы экспрессии тетрациклин-контролируемого гена, описанной выше, дифференциация может достигаться добавлением тетрациклина для подавления транскрипции гена, стимулирующего рост. Обычно для инициирования дифференциации достаточно добавление 1 мкг/мл тетрациклина в течение 4-5 дней. Для ускорения дополнительной дифференциации в ростовую среду могут добавляться другие добавки.
5.6.4. Наборы
В соответствии с другим аспектом, настоящее изобретение дополнительно относится к наборам для получения и/или введения композиций, содержащих изолированные плацентарные клетки согласно настоящему изобретению.
В одном варианте осуществления изобретение относится к набору, включающему в отдельных контейнерах один или несколько растворов, включающих декстран, например, декстран 40, раствор, включающий сывороточный альбумин человека (HSA) и криоконсервант. В специфическом варианте осуществления изобретения набор включает множество изолированных плацентарных клеток, например, криоконсервированных изолированных плацентарных клеток. В специфическом варианте осуществления изобретения набор включает контейнер, содержащий раствор, включающий 5,5% декстрана 40 (масс./об.) и 10% HSA (масс./об.). В еще одном специфическом варианте осуществления изобретения набор включает контейнер, содержащий раствор, включающий 5,5% декстрана 40, 10% HSA и 5% ДМСО. В еще одном специфическом варианте осуществления изобретения набор включает контейнер, содержащий раствор 10% декстрана 40.
В еще одном варианте осуществления изобретения набор включает фильтр или множество фильтров, подходящих для фильтрования клеточных суспензий. В специфических вариантах осуществления изобретения один или несколько фильтров в наборе включают поры диаметром от примерно 50 мкм до примерно 150 мкм. В более специфическом варианте осуществления изобретения размер пор фильтра составляет 70 мкм. В другом специфическом варианте осуществления изобретения размер пор фильтра равен 100 мкм.
В еще одном варианте осуществления изобретения набор включает одну или несколько стеклянных или пластиковых емкостей, подходящих для получения или применения одной из композиций, описанных в настоящем изобретении. Например, набор может включать пластиковый пакет (мешок), подходящий для криоконсервации, разбавления или доставки клеточной суспензии, например, суспензии изолированных плацентарных клеток. В другом варианте осуществления изобретения набор включает (1) множество изолированных плацентарных клеток, например, плацентарных стволовых клеток или плацентарных мультипотентных клеток, например, в одной или нескольких ампулах; (2) пластиковую емкость, достаточную для культивирования указанных изолированных плацентарных клеток, например, 2-3 пассиваций; (3) контейнер, содержащий раствор, включающий 5,5% декстрана 40 (масс./об.) и 10% HSA (масс./об.); (4) контейнер, содержащий раствор, включающий 5,5% декстрана 40, 10% HSA и 5% ДМСО; (5) контейнер, содержащий 10% раствор декстрана 40; и (6) один или несколько фильтров с диаметром пор от примерно 50 мкм до примерно 150 мкм, где фильтры подходят для фильтрации растворов, содержащих клетки.
6. ПРИМЕРЫ
6.1. ПРИМЕР 1: УСОВЕРШЕНСТВОВАННЫЙ СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ВВЕДЕНИЯ И СОДЕРЖАЩИХ ИЗОЛИРОВАННЫЕ ПЛАЦЕНТАРНЫЕ КЛЕТКИ
Этот пример иллюстрирует состав CD34-, CD10+, CD105+, CD200+ изолированных плацентарных клеток человека до криоконсервации и после нее для получения гомогенных изолированных плацентарных клеток человека с высокой жизнеспособностью для введения людям или животным. Полученная композиция включает изолированные плацентарные клетки, которые проявляют высокую жизнеспособность и не содержат макроскоплений клеток в течение по меньшей мере 4 часов после оттаивания. Изучение на мыши действующей дозы конечного состава, описанного ниже, показало, что максимальная толерантная доза NOD/SCID мышей составляет от по меньшей мере 1,5 миллионов клеток на мышь (приблизительно 75 миллионов клеток на кг при предполагаемой средней массе одного животного 20 граммов) при введении внутривенным вливанием - без какой-либо сердечной или легочной токсичности (подтвержденной одышкой, бегом по кругу и атаксией) и до 250 миллионов клеток на кг при подкожном введении, а также показало превосходство данного состава над составами предшествующего уровня. Несмотря на то, что приведенный далее пример описывает состав изолированных плацентарных клеток, экспрессирующих конкретные поверхностные маркеры, представленные результаты показывают, что описанные способы и составы могут использоваться и совместимы с другими клетками, например, клетками млекопитающих, экспрессирующими другие поверхностные маркеры.
Анализ наличия клеточных скоплений
Клеточные скопления (агрегаты) подразделяются на клеточные макроскопления и клеточные микроскопления. Клеточные макроскопления и микроскопления, если таковые присутствуют, идентифицируют в соответствии с представленными ниже методиками.
Анализ наличия клеточных макроскоплений
Клетки оттаивают в контейнере на водяной бане при 37°С до тех пор, пока в контейнере не останется очень маленький кусочек льда. Клетки извлекают из контейнера с помощью шприца, снабженного иглой 16 калибра, и переносят в коническую колбочку объемом 50 мл. Наличие или отсутствие клеточных макроскоплений определяют визуальным осмотром.
Анализ наличия клеточных микроскоплений
Клетки подсчитывают для определения клеточной концентрации. После этого клетки разбавляют до концентрации до 4×106 клеток/мл 10% декстраном 40, затем 50 мкл клеток, 40 мкл 10% декстрана 40 и 10 мкл 40 мкм измерительного раствора гранул добавляют в микроцентрифужную пробирку объемом 1,7 мл. Содержимое пробирки осторожно смешивают. Десять мкл образца переносят на предметное стекло и накрывают покровным стеклом. Подсчитывают число всех микроскоплений клеток, включающих три или более клеток.
Используемые плацентарные клетки сначала получают из банка клеток, который содержит популяции адгезивных плацентарных клеток, как описано в изобретении, подвергались 4-6 пассажам перед криоконсервацией.
Данные, полученные при сравнении инъекций in vivo совместимых буферных растворов с использованием двух различных линий изолированных плацентарных клеток, показывают, что фосфатно-буферный раствор (PBS), Plasmalyte A и модифицированная по Дульбекко среда Игла (DMEM), снабженная 1% сывороточным альбумином человека (HSA), способны поддерживать высокую жизнеспособность клеток по истечении 5 часов после оттаивания. Конечная концентрация клеток в буферном растворе составляет 25×106 клеток/мл. Plasmalyte A выбирают в качестве промотора наивысшей жизнеспособности клеток для тестируемых буферных растворов. Как показано в таблице 10а и таблице 10b, высокая жизнеспособность поддерживается в течение нескольких часов после оттаивания, следовательно, номинальные фенотипы не изменяются в течение 3 часов после оттаивания. Жизнеспособность клеток в составе после оттаивания незначительно ухудшается после пересева клеток через иглу 26 калибра. Определение клеточных скоплений в этих двух экспериментах невозможно вследствие небольшого объема используемых образцов.
На основании данных таблицы 1а и таблицы 1b, методику получения состава после оттаивания оформляют следующим образом: клетки оттаивают при 37°С на водяной бане и сразу же разбавляют в соотношении 1:1 (об./об.) буферным раствором оттаивания (2,5% HSA + 5% Dextran 40). После этого клетки центрифугируют при 400×g в течение 5 минут и снова суспендируют в смеси Plasmalyte A + 1% HSA.


Определение ткани-мишени в организме мыши
Описанный выше состав после оттаивания применяют в предварительном исследовании с целью определения ткани-мишени в организме мыши. Клеточные макроскопления наблюдают после оттаивания при приготовлении клеток, особенно после добавления Plasmalyte. Острая легочная токсичность данного состава наблюдается в дозе 1 миллион клеток на мышь (примерно 20 г) при двух повторных внутривенных вливаниях по 0,5 миллион клеток в каждом. Эти два наблюдения указывают на необходимость дальнейшего исследования состава плацентарных клеток.
Исходя из результатов предварительных исследований поиска ткани-мишени в организме мыши, показывающих, что добавление Plasmalyte, но не Dextran 40, вызывает значительное образование клеточных скоплений, в данном исследовании, наряду с Plasmalyte, HSA и PBS, используют Dextran 40.

Клетки, предварительно замороженные в Plasmalyte A + 10% HSA + 5% ДМСО, оттаивают на водяной бане при 37°С и разбавляют соответствующими буферами в соотношении 1:7. Данные, представленные в таблице 2, показывают, что из всех испытанных сред Dextran 40 и HSA вызывают наименьшее образование скоплений клеток.
Клеточные скопления наблюдают сразу после оттаивания в различных составах. Добавление стадии фильтрации, где клетки после оттаивания фильтруются через 100 мкм фильтр, приводит к удалению клеточных скоплений. Две партии плацентарных клеток тестируют для оценки влияния фильтрации в сочетании со специфическими разбавителями. После фильтрации образование клеточных скоплений не выявляют в течение 4 часов после оттаивания при разбавлении клеток в соотношении 1:1 с использованием 10% Dextran 40 (см. таблицы 3а-3с). Кроме того, жизнеспособность клеток остается высокой. Аналогичные результаты наблюдают с некоторыми другими партиями плацентарных клеток.



На основании данных описанных выше исследований получение плацентарных клеток после оттаивания упрощают до следующей методики: клетки оттаивают при 37°С на водяной бане в течение вплоть до 3 минут, затем отфильтровывают через 100 мкм фильтр. Отфильтрованные клетки затем разбавляют в соотношении 1:1 (об./об.) 10% декстраном 40.
Предварительно замороженный состав
Клеточные скопления также наблюдают в предварительно замороженной фазе клеточной модификации. Для снижения и/или устранения скоплений клеток перед замораживанием исследуют замораживающую среду, плотность замораживаемых клеток и стадию фильтрации суспензии.
Замораживающая среда
Исходя из успешного применения Dextran 40 в составе после оттаивания, как описано выше, Dextran 40 сравнивают с Plasmalyte в качестве замораживающей среды. Клетки из партии 3 замораживают в концентрации 17 миллионов клеток на мл в Plasmalyte A + 10% HSA + 5% ДМСО или в 5% Dextran 40 + 10% HSA + 5% ДМСО. Наличие клеточных скоплений оценивают следующим образом:



Применение Dextran 40 в этих экспериментах приводит к меньшему образованию клеточных макроскоплений, меньшему образованию клеточных микроскоплений и более высокой жизнеспособности клеток, чем применение Plasmalyte A. На основании этих результатов Dextran 40 выбирают в качестве замораживающей среды.
Плотность замораживаемых клеток и фильтрация перед замораживанием
Для исключения образования макроскоплений и снижения до минимума образования клеточных микроскоплений исследуют клеточную плотность и фильтрацию перед замораживанием следующим образом:



Результаты, представленные в таблицах 5b и 5с, четко показывают, что фильтрация до замораживания исключает образование клеточных макроскоплений после оттаивания. Данные также показывают, что образцы с высокой клеточной концентрацией, например, 20×106 клеток/мл, обладают большим потенциалом образовывать клеточные микроскопления после оттаивания. Поэтому влияние плотности замораживаемых клеток на образование клеточных сгустков изучают дополнительно.



Результаты, представленные в таблицах 6b и 6с, показывают, что замораживание клеток с плотностью 7,5×106/мл или менее не вызывает образования клеточных скоплений после оттаивания. Кроме того, при концентрации вплоть до 10×106клеток/мл количество клеточных микроскоплений является достаточно низким: менее 200 микроскоплений/миллион клеток.
Исходя из представленных выше результатов, составы с фильтрацией перед замораживанием и после оттаивания получают следующим образом. Составы с фильтрацией перед замораживанием: плацентарные клетки из жидкой культуры цинтрифугируют при 220×g в течение 5 минут и повторно суспендируют в 5% Dextran 40 до концентрации примерно 7,5×106 клеток/мл. Клетки центрифугируют при 400×g в течение 10 минут, затем снова суспендируют в 6% Dextran 40 и 10% HSA до концентрации примерно 7,5×106 клеток/мл. Повторно суспендированные клетки затем фильтруют через 70 мкм фильтр под действием силы тяжести. Отфильтрованные клетки разбавляют в 5% Dextran 40, 10% HSA и 5% ДМСО до концентрации примерно 7,5×106 клеток на мл. Разбавленные клетки помещают в крио-мешок, замораживают и хранят в паровой фазе азота. Для составов с фильтрацией после оттаивания: замороженные клетки оттаивают на водяной бане при 37°С, затем разбавляют 10% декстраном 40 при различных объемных соотношениях от 1:1 до 1:5 буфер, содержащий клетки:декстран 40.
Оценка состава плацентарных клеток
1. Отсутствие образования клеточных макроскоплений после оттаивания
Пять партий плацентарных клеток получают с использованием описанного выше способа получения составов (включая ПАРТИЮ 11 и ПАРТИЮ 12, описанные ниже). Клеточные макроскопления не обнаруживают в любой из пяти партий, и количество клеточных микроскоплений сохраняется низким.
2. Отсутствие влияния на фенотип
В улучшенном составе фенотип плацентарных клеток не подвергается неблагоприятному воздействию. Более 90% клеток в составе сохраняют фенотипы CD10+, CD34-, CD105+ и CD200+.
3. Исследование на GLP мыши
ПАРТИЮ 12 используют для поиска тканей-мишеней в организме мыши. Плацентарные клетки вводят в описанном выше составе в форме разовой и/или повторных инъекций в хвостовую вену самцам и самкам ΝOD-SCID или самцам C57BL/10SgSnAi-Rag2(tmi)γc(tmi) мышей. Мышей умерщвляют на 4, 14, 28 или 47 день после инъекции, забирают образцы легкого, печени, сердца, почек, селезенки, надпочечников, костного мозга и мозга и анализируют их с помощью Q-PCR для определения наличия ДНК последовательности hTERT; hTERT представляет собой ген теломеразной обратной транскриптазы человека. После i.v. введения определяют ДНК человека в изолированной цельной ДНК из образцов легкого, печени, сердца и/или печени в организмах мышей, которых умерщвляют на 4 день после дозированного введения. Самые высокие уровни ДНК обнаруживают в легком. Мыши способны переносить 25-100 миллионов клеток на кг при введении внутривенным вливанием без какой бы то ни было сердечной или легочной токсичности. Клетки ПАРТИИ 11 используют для изучения на мыши онкогенного потенциала. Мышам вводят до 250 миллионов клеток на кг подкожно (SC) без неблагоприятного действия.
6.2. ПРИМЕР 2: УЛУЧШЕННЫЕ КОМПОЗИЦИИ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ВВЕДЕНИЯ
Этот пример иллюстрирует состав прикрепленных к пластиковой культуре ткани мультипотентных CD34-, CD10+, CD105+, CD200+плацентарных клеток, которые даже после криоконсервации проявляют гомогенность, высокую жизнеспособность клеток, подходящую для введения людям или животным. Клетки данного состава показывают в среднем 400-кратное снижение количества образованных скоплений и повышенную максимальную толерантную дозу (Maximum Tolerated Dose - MTD), которая примерно в 3 раза выше по сравнению с составом предшествующего уровня при внутривенном введении на модели мыши (данные не представлены в описании). Хотя представленный пример описывает состав изолированных плацентарных клеток, экспрессирующих конкретные поверхностные маркеры, результаты, представленные в описании, показывают, что способы и составы могут использоваться и совместимы с другими клетками, например, клетками млекопитающих, экспрессирующими различные поверхностные маркеры.
Состав (обозначенный как «Состав В») включает плацентарные клетки описанного выше клеточного фенотипа в концентрации 10±3×106 клеток/мл в растворе, содержащем 5,5% (масс./об.) Dextran 40, 10% сывороточного альбумина человека (HSA) и 5% диметилсульфоксида (ДМСО). HSA и Dextran 40, используемые в данном примере, являются растворителями клинического качества.
Состав на основе Plasmalyte, обозначенный как «Состав А» описывается и сравнивается в таблице 7 с Составом В, составом на основе Dextran 40. Клетки фильтруют в суспензии через 70 мкм фильтр при получении Состава В, но не фильтруют при получении Состава А.

При оттаивании Состава А наблюдается значительная агрегация клеток. Последующее исследование показало, что ряд параметров, включая композицию среды состава и концентрацию клеток при заморозке, являются ключевым факторами для агрегации клеток. Проводят исследования для оптимизации состава, и композицию состава В разрабатывают специально для снижения или устранения эффектов агрегации клеток. Кроме того, вводят фильтрацию клеточной суспензии через 70 мкм фильтр как часть способа получения для обеспечения лучшего контроля клеточных суспензий в процессе получения состава.
Для определения количества клеточных скоплений клетки в составах разрабатывают в качестве инструментального средства анализа анализ фильтрационного удерживания и используют для сравнения серию плацентарных клеточных композиций, полученных с использованием Состава А и Состава В. Это особенно важно, поскольку агрегация клеток в Составе B была снижена до значения, при котором она больше не обнаруживалась невооруженным глазом. Сравнение результатов анализа множества образцов Состава A и Состава B представлено таблице 8. В соответствии с данным способом, посредством формирования цифрового изображения фильтра определяется количество предварительно окрашенных скоплений клеток, остающихся на фильтре после фильтрации различных образцов, и записывается площадь фильтра («Средняя площадь»), покрытая скоплениями. Как показано в таблице 8, площадь, покрытая скоплениями (площадь агрегатов), для Состава B значительно меньше площади, покрытой скоплениями после фильтрации Состава A, причем в среднем отличие составляет 400 раз. Данные также показывают хороший технологический контроль и воспроизводимость для Состава B. Композиция партий изолированных плацентарных клеток этих двух составов, использованных для исследования в условиях in vivo, представлены в таблице 16. Максимальная толерантная доза (МТД) состава В по сравнению с максимальной толерантной дозой состава А при внутривенном введением в условиях in vivo улучшается примерно в 3 раза (данные не представлены).
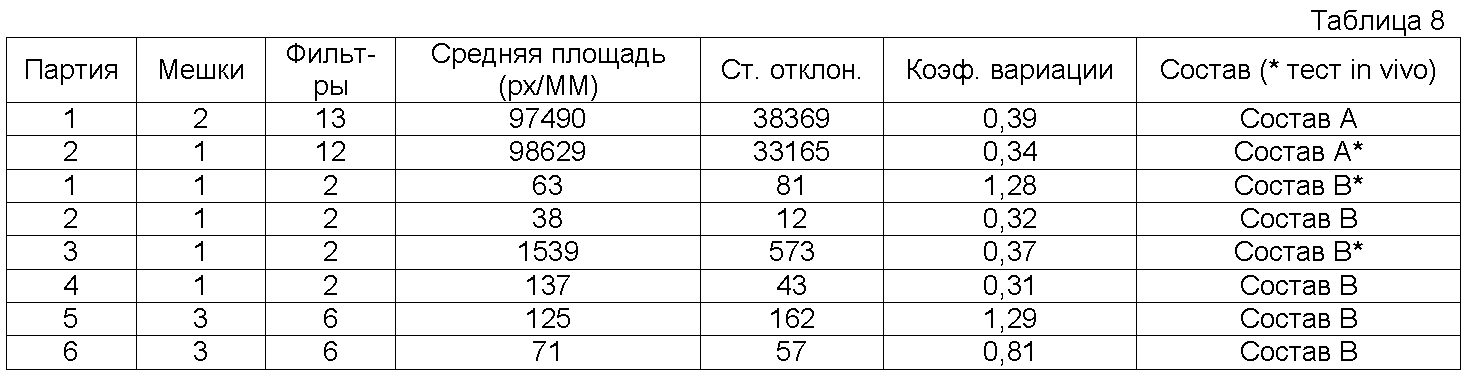
В столбце «Мешки» показано количество мешков композиции изолированных клеток, которые оттаивают и тестируют для данной Партии; в столбце «Фильтры» показано общее количество репликаций для данной Партии; в столбце «Средняя площадь» представлены средние величины площади фильтра, покрытой скоплениями, для данной Партии в «пикселях/миллион клеток»; в столбце «Ст. отклон.» представлены значения стандартных отклонений; «Коэф. Вариации» = коэффициент вариации.
6.3. ПРИМЕР 3: ОПРЕДЕЛЕНИЕ ХАРАКТЕРИСТИК УЛУЧШЕННЫХ КОМПОЗИЦИЙ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ВВЕДЕНИЯ
Этот пример дополнительно характеризует фармацевтические составы, включающие HSA, декстран 40 и ДМСО. В одном или нескольких представленных ниже экспериментах используют следующие методы.
Определение жизнеспособности клеток: Жизнеспособность клеток оценивают посредством анализа с использованием трипанового синего и гемоцитометра или анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California). Жизнеспособность клеток выражают как процент жизнеспособных клеток от общего количества клеток.
Подсчет клеток: Клетки подсчитывают с использованием гемоцитометра или с использованием анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California). Результат подсчета клеток представляют как количество миллионов клеток на миллилитр (ММ/мл).
Клеточная агрегация (скопление клеток): Агрегацию клеток количественно определяют с использованием опыта фильтрационного удерживания (Filter Retention Assay), с помощью которого клеточная агрегация определяется посредством окрашивания клеток и фильтрацией раствора через 70 мкм фильтр. Клеточные скопления размером в диаметре более 70 мкм, которые не могут пройти через фильтр, количественно определяют посредством анализа изображения площади поверхности фильтра с использованием анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California). Данные представляют в пикселях на миллион загруженных клеток (пикселей/ММ).
Проточная цитометрия: Анализ клеток на уровни экспрессии клеточных маркеров CD10, CD34, CD105 и CD200 проводят с помощью проточной цитометрии. Полученные значения выражают в процентах клеток положительных и/или отрицательных по отношению к конкретному маркеру или сочетанию маркеров.
Иммуносуппрессия: Иммуносупрессорную активность клеток в составах, описанных ниже, оценивают с использованием реакции Т-лимфоцитов на антигенные гранулы (Bead T-cell Reaction - BTR), с помощью которой определяют способность клеток подавлять ответ Т-лимфоцитов на антигенные гранулы.
Хотя в следующем в примере описывается состав изолированных плацентарных клеток, экспрессирующих конкретные поверхностные маркеры, результаты, представленные в данном описании, показывают, что способы и составы могут использоваться и совместимы с другими клетками, например, клетками млекопитающих, экспрессирующими другие поверхностные маркеры.
6.3.1. Определение характеристик соотношений ДМСО и Dextran:HSA
Этот пример описывает влияние изменения концентраций HSA, Dextran и ДМСО и изменения соотношения декстрана и HSA на клеточную агрегацию, клеточную жизнеспособность и выход клеток, а также клеточный фенотип и функциональность.
Условия эксперимента
Трехкомпонентый раствор (HSA, декстран и ДМСО) для клеточного состава исследуют в условиях, показанных на диаграмме трехкомпонентной системы, представленной на фиг.1. Условия эксперимента выбирают по двум осям: по одной тестирование проводят при различном процентном содержании ДМСО при постоянном соотношении Dextran:HSA (см. составы 1-4, ниже), по другой тестирование проводят при изменении соотношения Dextran:HSA, оставляя процентное содержание ДМСО постоянным (см. составы 3, 5-8, ниже).
Методы и материалы
Приблизительно двенадцать миллионов криоконсервированных CD10+, CD34-, CD105+, CD200+ плацентарных мультипотентных клеток выращивают до приблизительно 1,2×108 в Nunc™ 10-tray Cell Factories для каждого из составов, представленных ниже. Клетки собирают инкубированием в течение 10 минут при комнатной температуре с 0,25% трипсин/EDTA. Диссоциированные клетки переносят в 50 мл центрифужную пробирку, содержащую 250 мл 2% зародышевой телячьей сыворотки (FBS) в модифицированной по Дульбекко среде Игла (DMEM). Клетки центрифугируют со скоростью 1040 об/мин в 500 пробирках в центрифуге Sorvall RC3BP. Клетки снова суспендируют в растворе, содержащем смесь 0,9% физиологический раствор/5% декстрана 40. После этого клетки снова центрифугируют со скоростью 1420 об/мин. В течение 10 минут и снова суспендируют в 10 мл одного из следующих восьми составов (соотношения декстран:HSA показывают в единицах «объемная фракция 25% HSA» (VF HSA) для составов 3, 5-8):
Состав 1: 20% ДМСО, 8,5% HSA, 4,6% декстрана 40.
Состав 2: 10% ДМСО, 9,5% HSA, 5,2% декстрана 40.
Состав 3: 5% ДМСО, 10% HSA, 5,5% декстрана 40 (VF HSA = 0,4) (контрольный состав).
Состав 4: 0% ДМСО, 10,5% HSA, 5,8% декстрана 40
Состав 5: 5% ДМСО, 0% HSA, 9,5% декстрана 40 (VF HSA = 0).
Состав 6: 5% ДМСО, 3,125% HSA, 8,25% декстрана 40 (VF HSA = 0,125)
Состав 7: 5% ДМСО, 16,88% HSA, 2,75% декстрана 40 (VF HSA = 0,675).
Состав 8: 5% ДМСО, 23,75% HSA, 0% декстрана 40 (VF HSA = 0,95).
Составы получают из следующих исходных растворов: 100% ДМСО (Bioniche Pharma, Belleville, Ontario), 25% HSA (Octapharma, Hoboken, New Jersey) и 10% декстрана 40 в 0,9% растворе соли (Hospira, Lake Forest, Illinois).
Опыт фильтрационного удерживания: клеточную агрегацию оценивают посредством применения опыта фильтрационного удерживания. Концентрацию клеток перед фильтрацией доводят приблизительно до 1,2×107 клеток/мл. Загрузку фильтра (количество клеток на единицу площади фильтра) сохраняются постоянной при приблизительно 2,4×108клеток/мл. Клетки криоконсервируют в морозильной камере с контролируемой скоростью заморозки Thermo до -70°C при концентрации 7,5×106 клеток/мл. Клетки оттаивают перед применением, и образцы подвергают обработке сразу после оттаивания. Образец неразбавленной клеточной суспензии объемом 100 мкл отбирают после оттаивания, разводят 900 мкл фосфатно-буферного раствора (PBS), клетки подсчитывают, выполняя подсчет дважды, с использованием анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California) и результаты представляют в пикселях на миллион клеток (большее число пикселей показывает большее число клеточных скоплений).
Определение жизнеспособности клеток (MTS): Жизнеспособность клеток определяют с использование метода нерадиоактивной пролиферации клеток в микротитровальном планшете (CellTiter 96® Non-Radioactive Cell Proliferation Assay, Promega, Madison, Wisconsin). Клетки в 96-луночных микропланшетах объединяют с 3-(4,5-диметилтиазол-2-ил)-5-(3-карбоксиметоксифенил)-2-(4-сульфофенил)-2Н-тетразолием (MTS) и феназинметосульфатом (PMS) (реагент образования электронной связи) в соответствии с инструкциями производителя. После этого определяют спектральную поглощательную способность при 490 нм полученного формазанового продукта, полученного биологическим клеточным восстановлением MTS.
Анализ на микропланшете с использованием аннексина: Клетки после оттаивания разбавляют до концентрации 1×105 клеток/мл раствором в растворе меченого аннексина-V (Annexin-V Labeling solution, Roche, Cat. No. 11 828 681 001). 100 мкл клеточной суспензии добавляют в 96-луночный микропланшет в троекратно повторенном опыте и инкубируют в течение 15 минут при комнатной температуре, но без экспозиции светом. Спустя 15 минут получают изображение каждой лунки в трех положениях - при освещении ярким светом и люминесцентной лампой (длина волны возбуждения 488 нм, длина волны обнаружения 528 нм). Для подсчета общего числа клеток в каждом изображении используют автоматизированное программное обеспечение подсчета клеток (Axiovision). Популяции апоптотических/некротических клеток определяют подсчетом аннексин-положительных клеток в каждом положении (флуоресцентное изображение) и делением на общее количество клеток в каждом положении (изображение в ярком свете). Популяции апоптотических/некротических клеток на состояние определяют вычислением среднего значения количества клеток в трех различных положениях 3 лунок.
Клеточная агрегация
При изменении процентного содержания ДМСО, например, от 0 до 20 процентов (составы 1-4), влияния ДМСО на клеточную агрегацию не наблюдается, как показано на фиг.2. Все состояния с ДМСО проявляют уровни агрегации в интервале, наблюдаемом для контрольного состава, включающего 5% ДМСО, 5,5% декстрана 40 и 10% HSA. Концентрации HSA и декстрана также изменяют при постоянной концентрации ДМСО, равной 5% (фиг.3) при условии изменения содержания HSA в интервале от нуля (объемная фракция HSA = 0) до снижения до нуля содержания декстрана (объемная фракция HSA = 0,95). Значения, полученные в FRA анализе при изменении объемных фракций от 0,125 до 0,95 25% HSA (конечная концентрация от 3,125% до 23,75 HSA, соответственно) показывает минимальную агрегацию. Наблюдаемые уровни агрегации в присутствии HSA равны или ниже уровней агрегации в контрольном составе, включающем 5% ДМСО, 5,5% декстрана 40 и 10% HSA.
Жизнеспособность и регенерация клеток после оттаивания
Жизнеспособность клеток после оттаивания (фиг.4) и регенерацию клеток после оттаивания (фиг.5) при различном процентном содержании ДМСО (0, 5, 10 и 20%) определяют посредством исключения трипанового синего с использованием автоматического счетчика клеток Vi-Cell для оценки криозащитной способности каждого состава. Жизнеспособность клеток после оттаивания составляет более 90% в составах, включающих 05, 5% и 10% ДМСО, соответственно, причем максимальное значение наблюдается при 5% ДМСО, в то время как жизнеспособность становится ниже 75% в составе, включающем 20% ДМСО. Восстановление культуры определяют посредством MTS анализа. Максимальное восстановление культуры наблюдается при 5% ДМСО (фиг.6).
Профиль жизнеспособности при различных объемных фракциях 25% HSA, то есть при изменении соотношения декстран:HSA, показан на фиг.7-9. Жизнеспособность клеток после оттаивания, определенная с помощью анализа с применением трипанового синего, достигает значений в интервале от 83,5% до 98,5% при изменении объемных фракций HSA (фиг.7). Максимальное значение достигается при 0,40 фракции 25% HSA, т.е. 10% HSA:5,5% Dextran 40. Вычисляют также регенерацию клеток после оттаивания, и полученные значения находятся в интервале от 80% до 120%, хотя образцы, включающие по меньшей мере 0,2 объемную фракцию 25%-ого HSA, показывают значения в интервале от 100% до 120% (фиг.8). Данные восстановления, полученные MTS анализом, показывают профиль, аналогичный профилю жизнеспособности после оттаивания, причем максимальное значение получено для 0,125 фракции 25%-ого HSA, то есть, 3,13 HSA:8,25% % Dextran 40 (фиг.9).
Анализ жизнеспособности с использованием трипанового синего не способен обнаружить апоптозные клетки. Однако анализ распределения клеток по размерам может показать изменения в состоянии здоровья клеток. Для определения содержания апоптозных клеток (в процентах) в популяциях клеток после их оттаивания из замороженного состояния в отсутствии ДМСО проводят анализ на микропланшете с использованием аннексина. Анализ показывает, что 51% клеток, замороженных при 0% ДМСО являются апоптозными, в то время как при 5% ДМСО содержание апоптозных клеток равно 15% (данные не показаны).
Фенотип и функциональность
Способность в зависимости от различного содержания компонентов сохранять клеточный CD10+, CD34-, CD105+, CD200+ фенотип определяют проточной цитометрией. Клетки в составе 2 (10% ДМСО, 9,5% HSA, 5,2% декстрана 40), составе 5 (5% ДМСО, 0% HSA, 9,5% декстрана 40), составе 6 (5% ДМСО, 3,13% HSA, 8,25% декстрана 40) и составе 7 (5% ДМСО, 16,88% HSA, 2,75% декстрана 40) сохраняют данный фенотип примерно также хорошо, как и контрольный состав 3, и значения CD105+/CD200+ находятся в интервале от 80,3% до 84,5%. Состояния 1, 4 и 8 показывают изменения в физических характеристиках клеток, возможно вследствие загрязнений, влияющих на результаты проточной цитометрии.
Функциональность клеток оценивают посредством реакции гранулированных Т-лимфоцитов (BTR анализ), которая определяет способность клеток подавлять реакцию Т-лимфоцитов на антигенные гранулы (фиг.10). Состав 6 (5% ДМСО, 3,13% HSA, 8,25% декстрана 40) и состав 7 (5% ДМСО, 16,88% HSA, 2,75% декстрана 40) проявили супрессорную активность в пределах 1 стандартного отклонения от супрессорной активности контрольного состава 3, включающего 5% ДМСО/10% HSA и 5,5% декстрана 40. Эти три образа проявляют в опыте с применением трипанового синего наивысшие показатели жизнеспособности и регенерации культуры. Другие образцы имеют более низкие уровни подавления со снижением, которое обычно коррелирует со снижением MTS.
Выводы:
Составы, включающие ДМСО в концентрациях в интервале от 0 до 20%, проявляют уровни клеточной агрегации, сравнимые с уровнями, наблюдаемыми в контрольном составе, включающем 5% ДМСО, 10% HSA и 5,5% декстрана 40. Однако жизнеспособность клеток снижается, когда клетки подвергаются криоконсервации в составе, включающем 20% ДМСО, а клетки, замороженные при 0% ДМСО, проявляют в значительно степени повешенный апоптоз по сравнению с клетками, замороженными в 5% ДМСО. Ощутимая деградация CD10+, CD34-, CD105+, CD200+ фенотипа не наблюдается в составах, включающих 5% и 10% ДМСО. Таким образом, результаты, представленные выше, показывают, что применение составов, включающих 5-10% ДМСО, является предпочтительным для поддержания жизнеспособности клеток после оттаивания.
Что касается изменения соотношения HSA:декстран, составы, включающие 23,74% HSA, 0% декстрана, показали некоторое снижение жизнеспособности и регенерации культуры после оттаивания, в то время как наивысшие значения жизнеспособности, подавления иммунной активности и регенерации после оттаивания проявили составы, включающие следующие соотношения декстран:HSA: (i) 3,13% HSA к 8,25% декстрана; (ii) 10% HSA к 5,5% декстрана; и (iii) 16,88% HSA к 2,75% декстрана. Следовательно, эти результаты показывают, что соотношение HSA:декстран составов согласно изобретению может изменяться в пределах определенной области без заметной потери жизнеспособности, регенерации клеток после оттаивания, деградации CD10+, CD34-, CD105+, CD200+ фенотипа или иммуносупрессорной активности по сравнению с составами, включающими HSA и декстран в соотношении 10% HSA к 5,5% Dextran 40. Представленные данные подтверждают, что рабочий интервал соотношений HSA:декстран находится в пределах от по меньшей мере примерно 6:1 HSA:декстран до примерно 1:2,6 HSA:декстран.
6.3.2. ВЛИЯНИЕ ПЛОТНОСТИ ЗАМОРАЖИВАЕМЫХ КЛЕТОК
Этот пример описывает влияние клеточной концентрации, например, плотностей замораживаемых клеток в интервале от 1-40×106 клеток/мл, на жизнеспособность клеток; CD10+, CD34-, CD105+, CD200+ фенотип; клеточную агрегацию; и иммуносупрессивную функциональность клеток.
Методы и материалы
CD10+, CD34-, CD105+, CD200+ плацентарные стволовые клетки культивируют в течение 3 дней, собирают, центрифугируют и снова суспендируют в составе, включающем 5% ДМСО, 5,5% декстрана 40, 10% HSA, до концентрации примерно 3,5×l07 клеток/мл и фильтруют через 70 мкм фильтр. Отфильтрованные клетки последовательно разбавляют в указанном выше составе разбавителя для получения образцов клеток в стерильных мешках с плотностями 1×106 клеток/мл, 7,5×106 клеток/мл, 15×106 клеток/мл и 20×106 клеток/мл. Отдельно собирают клетки для получения клеточного образца, включающего 4,0×107 клеток/мл. Клетки 4,0×107 клеток/мл образца снова суспендируют в 7 мл состава разбавителя, включающего 5% ДМСО, 5,5% декстрана 40, 10% HSA, до концентрации примерно 4,6×107 клеток/мл, фильтруют через 70 мкм фильтр и разбавляют до 4,0×107 клеток/мл в мешке объемом 20 мл с использованием описанного выше состава разбавителя. Один мешок объемом 20 мл с плотностью 4,0×107 клеток/мл, по два образца мешков объемом 20 мл с плотностью 1×106 клеток/мл, 7,5×106 клеток/мл, 15×106 клеток/мл и 20×106 клеток/мл, и пять ампул объемом 280 мкл каждого образца замораживают до -70°C с использованием морозильной камеры с контролируемой скоростью заморозки. Эти образца затем оттаивают и анализируют для определения влияния концентрации клеток на различные характеристики, включая (1) число клеток; (2) жизнеспособность; (3) феотип; (4) скопление клеток; и (5) активность.
Анализ методом фильтрационного удерживания: Агрегацию клеток оценивают методом фильтрационного удерживания. Концентрацию клеток доводят до приблизительно 1,2×107 клеток/мл перед фильтрацией. Нагрузка фильтра (количество клеток на единицу площади фильтра) сохраняется постоянно, равной приблизительно 2,4×108 клеток/фильтр. Клетки криоконсервируют в морозильной камере с контролируемой скоростью заморозки Thermo до -70°С при концентрации 7,5×106 клеток/мл. Клетки оттаивают перед применением, и образцы подвергают дальнейшей обработке сразу после оттаивания. 100 мкл образца неразбавленной суспензии клеток отбирают после оттаивания, разбавляют 900 мкл фосфатно-буферного раствора (PBS), подсчитывают количество клеток с использованием анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California), и данные представляют в пикселях на миллион клеток (более высокое число пикселей показывает более высокое число клеточных агрегатов).
Результаты:
Количество клеток/жизнеспособность
Один или два образца объемом 1 мл из каждого оттаянного мешка отбирают для подсчета жизнеспособных клеток и определения жизнеспособности с использованием анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California) в соответствии с указаниями производителя. Средняя жизнеспособность клеток остается постоянной для всех условий и составляет примерно 97%. Количество жизнеспособных клеток соответствует исходной концентрации до заморозки (см. таблицу 9, ниже).

Фенотип
Способность сохранять клеточный CD10+, CD34-, CD105+, CD200+ фенотип определяют при различных плотностях проточной цитометрией. Как представлено в таблице 10, фенотип не изменяется при замораживании образцов различных концентраций. CD200+/CD105+ экспрессия сохраняется в пределах 86%, и CD34-/CD10+ экспрессия сохраняется примерно на 99% для всех условий.

Клеточная агрегация
Повторы каждого условия анализируют в опыте фильтрационного удерживания для определения степени клеточной агрегации при различных концентрациях замораживания (фиг.11). Двойной анализ проводят на образцах 1×106 клеток/мл, 7,5×106 клеток/мл, 15×106 клеток/мл и 20×106клеток/мл. Один клеточный образец анализируют сдвоенным образом при содержании 40×106 клеток/мл. Образец 40×106 клеток/мл показывает наивысшую клеточную агрегацию относительно всех испытываемых плотностей. Все другие образцы проявляют агрегацию на уровне или ниже агрегации, наблюдаемой в контрольном образце, предварительно криоконсервированном при 7,5×106/мл в 5% ДМСО, 5,5% декстрана 40, 10% HSA.
Дополнительная отдельная клеточная агрегация может проводиться с тестируемыми клетками, криоконсервированными в составе разбавителя, включающем 5% ДМСО, 5,5% декстрана 40, 10% HSA, при 7,5×106/мл и 20×106/мл (фиг.12). Дополнительные данные показывают повышенный сигнал при 20×106/мл, показывая, что клетки, замороженные при 20×106/мл, дают непостоянные результаты агрегации. В результате, клетки, замороженные при данной концентрации или выше, обладают повышенным потенциалом к агрегации. Указанные данные показывают, что агрегация повышается с возрастанием концентрации клеток, и плотность клеток при замораживании, равная 20×106/мл, может приводить к повышению клеточной агрегации относительно плотности клеток при замораживании, равной 7,5×106/мл.
Функциональность
Ампулу с образцом каждого состояния используют для проведения анализа посредством реакции смешанной культуры лейкоцитов (mixed leukocyte reaction - MLR) и реакции гранулированных Т-лимфоцитов (BTR) для оценки иммуномодулирующих свойств клеток при изменении плотности замораживаемых клеток, как определено супрессией пролиферации CD4+ Т-лимфоцитов и CD8+ Т-лимфоцитов. Результаты MLR показывают снижение в CD4 и CD8 супрессии при плотности 15×106 клеток/мл и 40×106 клеток/мл, в то время как супрессия при 20×106 клеток/мл сопоставима с супрессией, наблюдаемой при 1×106 клеток/мл и 7,5×106 клеток/мл. Однако результаты BTR показывают снижение CD4 и CD8 супрессии при плотности 20×106 клеток/мл и 40×106 клеток/мл.

Выводы:
Результаты, представленные выше, показывают, что клеточная жизнеспособность и CD10+, CD34-, CD105+, CD200+ феотип не зависят от плотности клеток при замораживании. Однако клетки, криоконсервированные при плотности 20×106клеток/мл, показывают непостоянное повышения клеточной агрегации и непостоянное снижение иммуносупрессорной активности, в то время как клетки, криоконсериварованные при плотности 40×106клеток/мл проявляют стойкое повышение агрегации клеток и стойкое снижение иммуносупрессорной активности. По существу, хотя клетки могут вводиться в составы согласно изобретению с плотностью, например, вплоть до 40×106 клеток/мл, без заметного снижения клеточной жизнеспособности или в числе клеток, проявляющих CD10+, CD34-, CD105+, CD200+ фенотип, плотность клеток при заморозке в интервале 1,0-15×106 клеток/мл является предпочтительной для снижения до минимума клеточной агрегации после оттаивания.
6.3.3. ВЛИЯНИЕ МОЛЕКУЛЯРНОЙ МАССЫ ДЕКСТРАНА
Этот пример описывает влияние изменения молекулярной массы декстрана и применения, например, декстрана 1 (ММ=1000), декстрана 40 (ММ=40000) и декстрана 70 (ММ=70000) на клеточную агрегацию, жизнеспособность, регенерацию, CD10+, CD34-, CD105+, CD200+ феотип и функциональноть.
Материалы и методы
Двенадцать миллионов криоконсервированных CD10+, CD34-, CD105+, CD200+ плацентарных мульпотентных клеток культивируют в установке Nunc™ 10-tray Cell Factories для составов, описанных ниже, до приблизительно 1,2×108 клеток. Клетки собирают, выдерживая их в течение 10 минут при комнатной температуре в 0,25% трипсин/EDTA на 0,25%. Отделенные клетки переносят в центрифужную пробирку объемом 500 мл, содержащую 250 мл 2% зародышевой телячьей сыворотки (FBS) в модифицированной до Дульбекко питательной среде Игла (DMEM). После этого клетки центрифугируют со скоростью 1040 об/мин в центрифужных пробирках объемом 500 мл в Sorvall RC3BP центрифуге. Клетки снова суспендируют в растворе, содержащем 0,9% соли и 5% декстрана 40. После этого клетки центрифугируют со скоростью 1420 об/мин в течение 10 минут и снова суспендируют в 10 мл следующих составов:
Состав 1: 5% ДМСО, 5,5% декстрана 40 (Hospira, Lake Forest, Illinois), 10% HSA (контроль).
Состав 2: 5% ДМСО, 5,5% Dextran 1 (Pharmacosmos), 10% HSA.
Состав 3: 5% ДМСО, 5,5% Dextran 40 (Pharmacosmos), 10% HSA.
Состав 4: 5% ДМСО, 5,5% Dextran 70 (Pharmacosmos), 10% HSA.
Опыт фильтрационного удерживания: Клеточную агрегацию определяют с использованием опыта фильтрационного удерживания. Перед фильтрацией концентрацию клеток доводят до приблизительно 1,2×107 клеток/мл. Нагрузка фильтра (количество клеток на единицу площади фильтра) сохраняется постоянной, равной приблизительно 2,4×108 клеток/фильтр. Клетки криоконсервируют в морозильной камере с контролируемой скоростью заморозки Thermo до -70°С при концентрации 7,5×106 клеток/мл. Клетки оттаивают перед применением, и образцы подвергают дальнейшей обработке сразу после оттаивания. 100 мкл образца неразбавленной суспензии клеток отбирают после оттаивания, разбавляют 900 мкл фосфатно-буферного раствора (PBS) и дважды проводят подсчет количества клеток с использованием анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California).
Результаты:
Клеточная агрегация
Клеточную агрегацию в каждом составе оценивают в использованием опыта фильтрационного удерживания. Состав 2 (декстран 1), состав 3 (декстран 40) и состав 4 (декстран 70) показывают скорости образования скоплений клеток, эквивалентные или ниже скорости образования скоплений в контрольном составе, включающем 5% ДМСО, 5,5% декстрана 40 и 10% HSA (фиг. 13).
Жизнеспособность и регенерация
Жизнеспособность клеток после оттаивания для образцов, включающих декстран 1, декстран 40 или декстран 70, находится в интервале от 96,0% до 97,7% (фиг.14). Аналогично, регенерация клеток после оттаивания сопоставима с регенерацией клеток после оттаивания в контрольном составе и находится в интервале от 92% до 109% относительно контрольного состава (фиг.15).
Фенотип и функциональность
Способность составов сохранять клеточный CD10+, CD34-, CD105+, CD200+ фенотип для составов, содержащих декстран различной молекулярной массы, тестируют с помощью проточной цитометрии, иммуносупрессорную активность клеток тестируют в BTR анализе. CD200+/CD105+ экспрессия во всех испытанных составах находится в интервале от 89,1% до 91,6%, и экспрессия CD34-/CD10+ составляет >95% для всех составов (фиг.16). Кроме того, Т-лимфоцитарная супрессорная активность CD4+ и CD8+ находится в пределах 1 стандартного отклонения от ожидаемого значения суппрессорной активности, полученной от 4 различных экспериментальных повторов испытаний стандартного контрольного состава, включающего декстран 40 (фиг.17).
Выводы:
Результаты, представленные выше, показывают, что дектран 1 или дестран 70 могут замещаться на декстран 40 в составах, описанных в изобретении, без влияния на клеточную агрегации, жизнеспособность, регенерацию, Фенотип или иммуносупрессорную активность.
6.3.4. ВЛИЯНИЕ РАЗЛИЧНЫХ ПОЛИСАХАРИДОВ
Этот пример описывает влияние полисахаридов, отличных от декстрана 40, в клеточном составе на жизнеспособность и пролиферацию клеток.
Материалы и методы
Двенадцать миллионов криоконсервированных CD10+, CD34-, CD105+, CD200+ плацентарных мульпотентных клеток культивируют в установке Nunc™ 10-tray Cell Factories для каждого из составов, описанных ниже, до приблизительно 1,2×108 клеток. Клетки собирают, выдерживая их в течение 10 минут при комнатной температуре в 0,25% трипсин/EDTA на 0,25%. Отделенные клетки переносят в центрифужную пробирку объемом 500 мл, содержащую 250 мл 2% зародышевой телячьей сыворотки (FBS) в модифицированной по Дульбекко питательной среде Игла (DMEM). После этого клетки центрифугируют со скоростью 1040 об/мин в центрифужных пробирках объемом 500 мл в Sorvall RC3BP центрифуге. Клетки снова суспендируют растворе, содержащем 0,9% соли и 5% декстрана 40. После этого клетки центрифугируют со скоростью 1420 об/мин в течение 10 минут и снова суспендируют в 10 мл следующих составов:
Состав 1: 5% ДМСО, 5,5% декстрана 40, 10% HSA (контроль).
Состав 2: 5% ДМСО, 5,5% мальтодекстрина, 10% HSA.
Состав 3: 5% ДМСО, 5,5% сахарозы, 10% HSA.
Состав 4: 5% ДМСО, 5,5% трегалозы, 10% HSA.
Состав 5: 5% ДМСО, 55 USP/мл гепарина, 10% HSA.
Состав 6: 5% ДМСО, 3,3% гетакрахмала, 10% HSA.
Состав 7: 5% ДМСО, 5,5% гликогена, 10% HSA.
Опыт фильтрационного удерживания: Клеточную агрегацию определяют с использованием опыта фильтрационного удерживания. Перед фильтрацией концентрацию клеток доводят приблизительно до 1,2×107 клеток/мл. Нагрузка фильтра (количество клеток на единицу площади фильтра) сохраняется постоянной, равной приблизительно 2,4×108 клеток/фильтр. Клетки криоконсервируют в морозильной камере с контролируемой скоростью заморозки Thermo до -70°С. Клетки оттаивают перед применением, и образцы подвергают дальнейшей обработке сразу после оттаивания. 100 мкл образца неразбавленной суспензии клеток отбирают после оттаивания, разбавляют 900 мкл фосфатно-буферного раствора (PBS) и дважды проводят подсчет количества клеток с использованием анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California).
Результаты
Клеточная агрегация
Клеточную агрегацию в каждом составе оценивают с использованием опыта фильтрационного удерживания. В составах 2-7 агрегация клеток эквивалентна агрегации или ниже агрегации клеток в контрольном составе, включающем 5% ДМСО, 5,5% декстрана 40 и 10% HSA (фиг.18). Состав 4, включающий трегалозу, состав 5, включающий гепарин, и состав 7, включающий гликоген, показывают скорости агрегации клеток по существу ниже скорости агрегации клеток в контрольном составе.
Жизнеспособность и регенерация клеток после оттаивания
Жизнеспособность после оттаивания, регенерация жизнеспособных клеток и данные размера клеток определяют для каждого из составов 1-7 для оценки криозащитной способности составов. Жизнеспособности после оттаивания оценивают методом окрашивания трипановым синим с использованием анализатора клеточной жизнеспособности Vi-Cell (Beckman Coulter, Fullerton, California). Минимальная жизнеспособность клеток после оттаивания находится в интервале от 95,2% до 98,6% при использовании сахарозы и гликогена (см. фиг.19). Контрольный состав с декстраном проявляет 98% жизнеспособность клеток. Регенерация жизнеспособных клеток после оттаивания вычисляется для оценки потерь клеток в процессе заморозки/оттаивания, и ее значение находится в интервале от 84% до 115% при применении различных полисахаридов (фиг.20).
Фенотип и функциональность
Способность сохранять клеточный CD10+, CD34-, CD105+, CD200+ фенотип для составов, содержащих различные полисахариды, тестируют с помощью проточной цитометрии. Клетки в составах 2-4 и 6 сохраняют данный фенотип примерно также, как и контрольный состав 1, и сохранение фенотипа CD105+/CD200+ составляет от 89,4% до 92,9%. CD10+/CD34- экспрессия составляет >95% для каждого состава. Клетки, замороженные в гепарине, сохраняют 85,4% CD105+/CD200+ фенотипа (фиг.21).
Функциональность клеток оценивают с использованием реакции Т-лимфоцитов на антигенные гранулы (Bead T-cell Reaction - BTR), с помощью которой определяют способность клеток подавлять ответ Т-лимфоцитов на антигенные гранулы. Клетки в составе с сахарозой проявляют сниженную Т-лимфоцитную супрессию по сравнению с супрессией в пределах 1 стандартного отклонения ожидаемого значения, полученного от 4 различных репликатов испытаний контрольного состава, включающего декстран 40 (фиг.22). Составы с другими полисахаридами, Т-лимфоцитная супрессия CD4 и CD8 находится в пределах 1 стандартного отклонения ожидаемого значения.
Выводы:
Что касается клеточной агрегации, жизнеспособности после оттаивания. Регенерации клеток после оттаивания и сохранения фенотипа, применения составов, включающих мальтодекстран, трегалозу и гетекрахмал, приводит к плацентарным клеточным популяциям, обладающим примерно такими же характеристиками, что и состав, включающий декстран 40. Как таковые, хотя составы разбавителей, включающие сахарозу, гепарин или гликоген, могут использоваться для получения составов CD10+, CD34-, CD105+, CD200+ плацентарных стволовых клеток, применение составов, включающих декстран 40, мальтодекстран, трегалозу или гетакрахмал, является предпочтительным.
6.3.5. ВЛИЯНИЕ БЕЛКОВ, АЛЬТЕРНАТИВНЫХ HSA
Этот пример показывает, что в составе, включающем 5,5% декстрана 40, 10% HSA и 5% ДМСО, концентрация альбумина сыворотки крови человека может снижаться, и что HSA может заменяться бычьим сывороточным альбумином и зародышевой телячьей сывороткой.
Состав 1 (F1) включает 5,5% декстрана 40, 10% HSA и 5% ДМСО. Для того чтобы понять роль HSA в составе F1 и понять его влияние на клеточные композиции, тестируют альтернативные составы с белками, аналогичными сывороточному альбумину человека, т.е. бычьим сывороточным альбумином (BSA) и зародышевой телячьей сывороткой.
Материалы и методы
Двенадцать миллионов криоконсервированных CD10+, CD34-, CD105+, CD200+ плацентарных мульпотентных клеток культивируют в установке Nunc™ 10-tray Cell Factories для применения в каждом из составов разбавителей, описанных ниже, до приблизительно 1,2×108 клеток. Клетки собирают, выдерживая их в течение 10 минут при комнатной температуре в 0,25% трипсин/EDTA. Отделенные клетки переносят в центрифужную пробирку объемом 500 мл, содержащую 250 мл 2% зародышевой телячьей сыворотки (FBS) в модифицированной по Дульбекко питательной среде Игла (DMEM). После этого клетки центрифугируют со скоростью 1040 об/мин в центрифужных пробирках объемом 500 мл в Sorvall RC3BP центрифуге. Клетки снова суспендируют в растворе, содержащем 0,9% соли и 5% декстрана 40. После этого клетки центрифугируют со скоростью 1420 об/мин в течение 10 минут и снова суспендируют в 10 мл следующих составах:
Состав 1: 5% ДМСО, 5,5% декстрана 40, 10% HSA (контроль).
Состав 2: 5% ДМСО, 5,5% декстрана 40, 4% HSA.
Состав 3: 5% ДМСО, 5,5% декстрана 40, 10% BSA.
Состав 4: 5% ДМСО, 5,5% декстрана 40, 10% FBS.
Анализ фильтрационного удерживания: Клеточную агрегацию оценивают с использованием анализа фильтрационного удерживания. Перед фильтрацией концентрацию клеток доводят приблизительно до 1,2×107 клеток/мл. Нагрузка фильтра (количество клеток на единицу площади фильтра) сохраняется постоянной, равной приблизительно 2,4×108 клеток/фильтр. Клетки криоконсервируют в морозильной камере с контролируемой скоростью заморозки Thermo до -70°С. Клетки оттаивают перед применением, и образцы подвергают дальнейшей обработке сразу после оттаивания. 100 мкл образец неразбавленной суспензии клеток отбирают после оттаивания, разбавляют 900 мкл фосфатно-буферного раствора (PBS) и дважды проводят подсчет количества клеток с использованием анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California).
Результаты
Клеточная агрегация
Клеточная агрегация, определенная с использованием анализа фильтрационного удерживания, составляет около или менее 100 пикселей на квадратный миллиметр для всех составов (фиг.23). Однако 10% HSA и 10% BSA, как оказалось, приводят к значительно меньшей агрегации, чем 4% HSA и 10% FBS.
Для оценки криозащитной способности каждого раствора, жизнеспособность клеток после оттаивания, регенерацию и размер клеток оценивают с помощью метода триптанового синего с применением анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California). Жизнеспособность клеток для каждого состава находится в пределах показателя изменчивости опыта и составляет от 95% до 98% (фиг.24). Аналогично, регенерация клеток после оттаивания сравнима с регенерацией клеток в контрольном составе, содержащем 10% HSA, и находится в интервале от 100% до 127% (фиг.25).
Фенотип и функциональность
Способность сохранять клеточный CD10+, CD34-, CD105+, CD200+ фенотип различных составов тестируют с помощью проточной цитометрии (фиг.26 и 27). Клетки в составах 2-4 сохраняют данный фенотип примерно также, как и контрольный состав, содержащий 10% HSA, в пределах от 88,2% до 93,5% тестированных клеток. CD10+/CD34- экспрессия составляет >95% для каждого состава.
Функциональность клеток оценивают с помощью анализа реакции Т-лимфоцитов на гранулированные антигены. По сравнению с другими условиями, супрессия CD4 и CD8 Т-лимфоцитами повышается в составах с FBS со значениями в 1,5 стандратных отклонений от ожидаемого значения, полученного из 4 различных экспериментов стандартного контрольного состава, включающего 10% HSA (фиг.28). Для других составов супрессия находится в пределах 1 стандартного отклонения от ожидаемого значения.
Выводы:
Результаты, представленные выше, показывают, что 4% HSA, 10% BSA или 10% FBS могут быть заменены 10% HSA без заметной потери клеточной жизнеспособности, регенерации клеток после оттаивания, деградации CD10+, CD34-, CD105+, CD200+ феотипа или иммуносупрессивной активности. Таким образом, область значений от по меньшей мере примерно 4% до примерно 10% для содержания HSA, BSA и/или FBS особенно подходит для составов, описанных в настоящем изобретении.
6.3.6. СОВМЕСТИМОСТЬ С КЛЕТКАМИ РАЗЛИЧНЫХ ТИПОВ
Этот пример показывает, что мезенхимальные стволовые клетки, полученные из костного мозга, и природные клетки-киллеры, могут вводиться в состав таким же образом, как и плацентарные мультипотентные клетки. Таким образом, данный пример показывает, что другие клетки, отличные от плацентарных мультипотентных клеток, могут вводиться в состав способом, описанным в настоящем изобретении.
Методы и материалы
Мезенхимальные стволовые клетки, полученные из костного мозга (bone marrow-derived mesenchymal stem cell - BMMSC) и природные клетки-киллеры (natural killer - NK) используют в следующих составах:
F1: Культуру клеток выращивают в течение 3 дней, затем собирают и снова суспендируют в 5% ДМСО, 5,5% декстрана 40, 10% HSA, фильтруют через 70 мкм фильтр и криоконсервируют при плотности приблизительно 7,5×106 клеток/мл;
F2: Культуру клеток выращивают в течение четырех дней, затем собирают и снова суспендируют в Plasmalyte A, включающем 5% ДМСО и 10% HSA.
Клетки замораживают при -70°С с помощью морозильного аппарата с контролируемой скоростью заморозки. BMMSC криоконсервируют в 20 мл мешке в составе F2 и в 10 мл состава F1; и CD3-, CD56+ NK клетки криоконсервируют в 10 мл мешках в составе F2 и в 1,5 мл ампулах в составе F1. Указанные образцы позднее оттаивают и анализируют для определения влияния замораживаемого состава на характеристики клеток.
Анализ фильтрационного удерживания: Клеточную агрегацию оценивают посредством анализа фильтрационного удерживания. Перед фильтрацией концентрацию клеток доводят до приблизительно 1,2×107 клеток/мл. Загрузку фильтра (количество клеток на единицу площади фильтра) сохраняют постоянной на уровне приблизительно 2,4×108клеток/фильтр. Клетки криоконсервируют в морозильной камере с контролируемой скоростью заморозки Thermo до -70°С. Клетки оттаивают перед применением, и образцы подвергают дальнейшей обработки непосредственно после оттаивания. 100 мкл образец неразбавленной суспензии клеток отбирают после оттаивания, разбавляют 900 мкл фосфатно-буферного раствора (PBS) и дважды проводят подсчет количества клеток с использованием анализатора жизнеспособности клеток Vi-Cell (Beckman Coulter, Fullerton, California).
Результаты
Жизнеспособность
После оттаивания образцы используют для определения жизнеспособности клеток, замороженных в различных условиях. На жизнеспособность BMMSC и NK клеток условия замораживания значительного влияния не оказывают.
Фенотип
Маркеры NK анализировали для определения влияния составов F1 и F2 на NK фенотип (CD3-, CD56+). Эти два состава не оказывают значительного влияния на процент NK клеток, проявляющих NK фенотип. BMMSC также анализируют на экспрессию CD10, CD34, CD44, CD45, CD90, CD98, CD105, CD117, CD166, CD200, Pan-цитокератина и KDR. Экспрессия или потеря экспрессии этих маркеров в BMMSC не значительно различается между составами F1 или F2.
Клеточная агрегация
В анализе фильтрационного удерживания проводят два испытания для каждого из BMMSC составов и одно испытание с NK составами. F1 состав дает в значительной степени меньше агрегатов, чем F2 состав как для BMMSC, так и для NK клеток; влияние состава F1, однако, более ярко выражено для BMMSC, чем для клеток NK (фиг.29).
Выводы:
Результаты, представленные выше, показывают, что мезенхимальные стволовые клетки, полученные из костного мозга, и природные клетки-киллеры могут успешно вводиться в состав, содержащий 5% ДМСО, 5,5% декстрана 40 и 10% HSA с клеточной агрегацией, жизнеспособностью и сохранением фенотипа, аналогично CD10+, CD34-, CD105+, CD200+ плацентарным мультипотентным клеткам. Кроме того, по сравнению с плацентарными мультипотентными клетками Plasmalyte-содержащие составы BMMSC и NK клетки проявляют в значительно степени более высокие скорости клеточной агрегации; как таковые, предпочтительны декстран-содержащие составы.
Эквиваленты:
Композиции и способы, описанные в настоящем изобретении, не ограничиваются специфическими вариантами осуществления, описанными в настоящем изобретении. В самом деле, различные модификации композиций и способов в дополнение к описанным в настоящем изобретении будут для специалиста данной области техники очевидными из представленного выше описания и приложенных фигур. Подразумевается, что указанные модификации включены в объем прилагаемой формулы изобретения.
Содержание различных публикаций, патентов и заявок на патент, цитированных в описании, полностью включено в описание путем ссылок.
Реферат
Изобретение относится к области биотехнологии и может быть использовано для получения композиций, содержащих стволовые плацентарные клетки. Способ включает: (a) получение адгезивных плацентарных клеток в растворе, включающем от 2% до 10% декстрана, от 2,5% до 10% ДМСО и от 4% до 10% HSA, (b) фильтрацию полученного раствора через 70 мкм - 100 мкм фильтр; (c) разбавление указанных клеток до содержания не более 10±3·10клеток на миллилитр раствором, включающим от 2% до 5% декстрана, от 2,5% до 10% ДМСО и от 4% до 10% HSA, и (d) криоконсервацию раствора, содержащего клетки. После оттаивания раствор с клетками может быть разбавлен в соотношении от 1:1 до 1:11 вторым раствором, содержащим от 2% до 10% декстрана 40 и от 4% до 10% HSA. Изобретение позволяет повысить жизнеспособность адгезивных плацентарных клеток при криоконсервации. 3 н. и 17 з.п. ф-лы, 29 ил., 11 табл., 3 пр.
Формула
(a) контактирование указанных клеток с раствором, включающим от 2% до 10% декстрана, от 2,5% до 10% диметилсульфоксида (ДМСО) и от 4% до 10% сывороточного альбумин человека (HSA), для получения раствора, содержащего клетки;
(b) фильтрацию раствора, содержащего клетки, через 70 мкм - 100 мкм фильтр;
(c) если указанный раствор, содержащий клетки, включает более 10±3·106 клеток на миллилитр, разбавление указанных клеток до содержания не более 10±3·106 клеток на миллилитр раствором для разбавления, включающим от 2% до 5% декстрана, от 2,5% до 10% ДМСО и от 4% до 10% сывороточного альбумин человека (HSA); и
(d) криоконсервацию раствора, содержащего клетки.
(a) суспендирование множества изолированных адгезивных плацентарных клеток человека в первом растворе, включающем от 2% до 10% декстрана 40, от 2,5% до 10% диметилсульфоксида (ДМСО) и от 4% до 10% HSA, для получения раствора, содержащего клетки;
(b) фильтрацию раствора, содержащего клетки, через 70 мкм - 100 мкм фильтр;
(c) разбавление раствора, содержащего клетки, раствором, содержащим от 2% до 10% декстрана 40, от 4% до 10% HSA и от 2,5% до 10% ДМСО, до содержания не более 10±3·106 клеток/мл;
(d) криоконсервацию клеток;
(e) оттаивание клеток; и
(f) разбавление раствора, содержащего клетки, в соотношении от 1:1 до 1:11 вторым раствором, содержащим от 2% до 10% декстрана 40 и от 4% до 10% HSA для получения указанной композиции, включающей клетки.

Комментарии