Способы и композиции для направленной модификации генома - RU2685914C1
Код документа: RU2685914C1
Чертежи



























































Описание
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка заявляет приоритет предварительной заявки на патент США №61/914768, поданной 11 декабря 2013 г., предварительной заявки на патент США №62/017416, поданной 26 июня 2014 г., предварительной заявки на патент США №62/029261, поданной 25 июля 2014 г. предварительной заявки на патент США №62/052906, поданной 19 сентября 2014 г., предварительной заявки на патент США №62/059527, поданной 03 октября 2014 г., и предварительной заявки на патент США №62/064384, поданной 15 октября 2014 г., каждая из которых в полном объеме и во всех смыслах включена в данный документ посредством ссылки.
ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ, ПОДАННЫЙ В ВИДЕ ТЕКСТОВОГО ФАЙЛА ЧЕРЕЗ EFS WEB
[0002] Официальная копия перечня последовательностей подана в электронной форме через EFS-Web в виде файла с перечнем последовательностей в кодировке ASCII под названием 453460SEQLIST.TXT, созданного 15 октября 2014 г. и имеющего размер 27,5 килобайт, и подана одновременно с описанием изобретения. Перечень последовательностей, находящийся в данном документе в кодировке ASCII, является частью описания изобретения и в полном объеме включен в данный документ посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
[0003] Хотя крысы признаны важной животной модельной системой, которая может воспроизводить патологию многих человеческих заболеваний, включая, но не ограничиваясь этим, сердечнососудистые (например, повышенное кровяное давление), метаболические (например, ожирение, диабет), неврологические (например, болевые патологии) заболевания и различные виды рака, применение крыс в моделировании человеческих заболеваний было ограничено по сравнению с мышами, частично вследствие недоступности плюрипотентных крысиных клеток с трансмиссией зародышевой линии, которые могут сохранять свою плюрипотентность после серии генетических модификаций in vitro, например, одной или более серийных электропораций, а частично вследствие отсутствия эффективных методов таргетирования, которые позволяют осуществлять внесение или удаление крупных последовательностей геномной ДНК или замещение крупных последовательностей геномной ДНК экзогенными нуклеотидными последовательностями в плюрипотентных крысиных клетках.
[0004] В данной области техники существует потребность в композициях и способах, которые позволяют осуществлять точные направленные изменения в геноме организма, что может открыть или расширить существующие на данный момент области целевого выявления и позволить быстрее и легче проводить утверждение терапевтических агентов.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0005] Предложены способы модификации представляющего интерес геномного локуса в эукариотической клетке путем направленной генетической модификации. Такой способ включает (а) внесение в эукариотическую клетку: (i) крупного направляющего вектора (LTVEC), содержащего первую нуклеиновую кислоту, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом LTVEC содержит по меньшей мере 10 т.п.о.; (ii) первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas, (iii) второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей направляющую РНК (нРНК), содержащую нуклеотидную последовательность, которая гибридизируется с целевой последовательностью, и транс-активирующую РНК CRISPR (tracrРНК), при этом первый и второй промоторы активны в эукариотической клетке; и (b) выявление модифицированной эукариотической клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе.
[0006] В одном варианте реализации изобретения направленная генетическая модификация представляет собой биаллельную генетическую модификацию.
[0007] В одном варианте реализации изобретения LTVEC составляет по меньшей мере 15 т.п.о., по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о. или по меньшей мере 90 т.п.о. В другом варианте реализации изобретения LTVEC составляет по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
[0008] В одном варианте реализации изобретения эукариотическая клетка является клеткой млекопитающего. В одном варианте реализации изобретения клетка млекопитающего является фибробластом.
[0009] В одном варианте реализации изобретения эукариотическая клетка является плюрипотентной клеткой. В одном варианте реализации изобретения плюрипотентная клетка является человеческой плюрипотентной клеткой. В одном варианте реализации изобретения человеческая плюрипотентная клетка является человеческой эмбриональной стволовой (ЭС) клеткой или человеческой взрослой стволовой клеткой. В другом варианте реализации изобретения человеческая плюрипотентная клетка является человеческой клеткой-предшественником с ограниченным развитием. В другом варианте реализации изобретения человеческая плюрипотентная клетка является человеческой индуцированной плюрипотентной стволовой (иПС) клеткой.
[0010] В одном варианте реализации изобретения белок Cas представляет собой Cas9.
[0011] В одном варианте реализации изобретения целевая последовательность фланкируется последовательностью мотива, прилегающего к протоспейсеру (РАМ). В одном варианте реализации изобретения целевая последовательность непосредственно фланкируется в 3' конце последовательностью мотива, прилегающего к протоспейсеру (РАМ).
[0012] В некоторых вариантах реализации изобретения 5' и 3' плечи гомологии в общей сумме составляют от около 10 т.п.н. до около 150 т.п.н. В некоторых вариантах реализации изобретения 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до 150 т.п.о.
[0013] Дополнительно предложены способы, в которых направленная генетическая модификация включает: (а) замещение эндогенной нуклеотидной последовательности гомологичной или ортологичной нуклеотидной последовательностью; (b) удаление эндогенной нуклеотидной последовательности; (с) удаление эндогенной нуклеотидной последовательности, при этом диапазон удаления составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1.5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.; (d) вставку экзогенной нуклеотидной последовательности; (е) вставку экзогенной нуклеотидной последовательности в диапазоне от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о, до около 400 т.п.о.; (f) вставку экзогенной нуклеотидной последовательности, содержащей гомологичную или ортологичную нуклеотидную последовательность; (g) вставку химерной нуклеотидной последовательности, содержащей человеческую и нечеловеческую нуклеотидную последовательность; (h) вставку кондиционального аллеля, фланкируемого целевыми последовательностями сайт-специфической рекомбиназы; (i) вставку селективного маркера или репортерного гена, функционально связанного с третьим промотором, активным в плюрипотентной клетке; или (j) их комбинацию.
[0014] В одном варианте реализации изобретения представляющий интерес геномный локус содержит (i) 5' целевую последовательность, которая гомологична 5' плечу гомологии; и (ii) 3' целевую последовательность, которая гомологична 3' плечу гомологии.
[0015] В некоторых вариантах реализации изобретения 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 3 м.п.о. В некоторых вариантах реализации изобретения 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 10 т.п.о., по меньшей мере 10 т.п.о., но менее чем 20 т.п.о., по меньшей мере 20 т.п.о., но менее чем 40 т.п.о., по меньшей мере 40 т.п.о., но менее чем 60 т.п.о., по меньшей мере 60 т.п.о., но менее чем 80 т.п.о., по меньшей мере около 80 т.п.о., но менее чем 100 т.п.о., по меньшей мере 100 т.п.о., но менее чем 150 т.п.о., или по меньшей мере 150 т.п.о., но менее чем 200 т.п.о., по меньшей мере около 200 т.п.о., но менее чем около 300 т.п.о., по меньшей мере около 300 т.п.о., но менее чем около 400 т.п.о., по меньшей мере около 400 т.п.о., но менее чем около 500 т.п.о., по меньшей мере около 500 т.п.о., но менее чем около 1 м.п.о., по меньшей мере около 1 м.п.о., но менее чем около 1,5 м.п.о., по меньшей мере около 1,5 м.п.о., но менее чем около 2 м.п.о., по меньшей мере около 2 м.п.о., но менее чем около 2,5 м.п.о., или по меньшей мере около 2,5 м.п.о., но менее чем около 3 м.п.о.
[0016] В одном варианте реализации изобретения представляющий интерес геномный локус содержит локус рецептора интерлейкина-2 гамма, локус АроЕ, локус Rag1, локус Rag2 или оба локуса Rag1 и Rag2.
[0017] В одном варианте реализации изобретения первая и вторая экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[0018] Дополнительно предложен способ модификации генома, включающий воздействие на геном белком Cas и РНК CRISPR в присутствии крупного направляющего вектора (LTVEC), содержащего нуклеотидную последовательность по меньшей мере из 10 т.п.о., при этом после воздействия белком Cas, РНК CRISPR и LTVEC происходит модификация генома так, чтобы он содержал нуклеотидную последовательность по меньшей мере из 10 т.п.о.
[0019] В некоторых таких способах LTVEC содержит нуклеотидную последовательность по меньшей мере из 20 т.п.о., по меньшей мере из 30 т.п.о., по меньшей мере из 40 т.п.о., по меньшей мере из 50 т.п.о., по меньшей мере из 60 т.п.о., по меньшей мере из 70 т.п.о., по меньшей мере из 80 т.п.о. или по меньшей мере из 90 т.п.о. В некоторых таких способах LTVEC содержит нуклеотидную последовательность по меньшей мере из 100 т.п.о., по меньшей мере из 150 т.п.о. или по меньшей мере из 200 т.п.о.
[0020] Дополнительно предложен способ модификации генома, включающий приведение генома в контакт с белком Cas, РНК CRISPR, которая гибридизируется с целевой последовательностью, и tracrРНК в присутствии крупного направляющего вектора (LTVEC), при этом LTVEC состоит по меньшей мере из 10 т.п.о. и содержит первую нуклеиновую кислоту, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом после контакта с белком Cas, РНК CRISPR и tracrРНК в присутствии LTVEC происходит модификация генома в представляющем интерес геномном локусе так, чтобы он содержал первую нуклеиновую кислоту. Целевая последовательность может находиться внутри или вблизи представляющего интерес геномного локуса.
[0021] В некоторых таких способах геном находится в эукариотической клетке, а белок Cas, РНК CRISPR и tracrРНК и LTVEC вносят в эукариотическую клетку. Некоторые такие способы дополнительно включают выявление модифицированной эукариотической клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе.
[0022] В некоторых таких способах РНК CRISPR и tracrРНК вносят вместе в форме одной направляющей РНК (нРНК). В других способах РНК CRISPR и tracrРНК вносят отдельно.
[0023] В некоторых таких способах (а) белок Cas вносят в эукариотическую клетку в форме белка, матричной РНК (мРНК), кодирующей белок Cas, или ДНК, кодирующей белок Cas; (b) РНК CRISPR вносят в эукариотическую клетку в форме РНК или ДНК, кодирующей РНК CRISPR; и (с) tracrРНК вносят в эукариотическую клетку в форме РНК или ДНК, кодирующей tracrРНК.
[0024] В некоторых способах (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; (b) ДНК, кодирующая РНК CRISPR, находится в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей РНК CRISPR; и (с) ДНК, кодирующая tracrРНК, находится в форме третьей экспрессионной конструкции, содержащей третий промотор, функционально связанный с четвертой нуклеиновой кислотой, кодирующей tracrРНК, при этом первый, второй и третий промоторы активны в эукариотической клетке. Необязательно, первая, вторая и/или третья экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[0025] В некоторых способах (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; a (b) ДНК, кодирующая РНК CRISPR, и ДНК, кодирующая tracrРНК, находятся в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей нРНК, содержащую РНК CRISPR и tracrРНК; при этом первый и второй промоторы активны в эукариотической клетке. Необязательно, первая и вторая экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[0026] В некоторых способах белок Cas, РНК CRISPR и tracrРНК вносят в эукариотическую клетку в виде комплекса белок-РНК.
[0027] В некоторых способах направленная генетическая модификация включает одновременное удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус. В некоторых способах удаленная эндогенная нуклеотидная последовательность составляет от около 30 т.п.о. до около 110 т.п.о., а вставленная первая нуклеиновая кислота составляет от около 40 т.п.о. до около 140 т.п.о. В некоторых способах удаленная эндогенная нуклеотидная последовательность составляет от около 38 т.п.о. до около 110 т.п.о., а вставленная первая нуклеиновая кислота составляет от около 43 т.п.о. до около 134 т.п.о.
[0028] В некоторых способах направленная генетическая модификация представляет собой биаллельную генетическую модификацию. Необязательно, биаллельная генетическая модификация включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в двух гомологичных хромосомах.
[0029] В некоторых способах модифицированная эукариотическая клетка является компаунд-гетерозиготной в представляющем интерес геномном локусе. В некоторых способах модифицированная эукариотическая клетка является гемизиготной в представляющем интерес геномном локусе. Необязательно, направленная генетическая модификация в представляющем интерес геномном локусе в одной хромосоме включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты. Необязательно, направленная генетическая модификация включает: (1) удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе в двух гомологичных хромосомах; и (2) вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в первой хромосоме и разрушение представляющего интерес геномного локуса во второй хромосоме. Первая хромосома может быть одной из двух гомологичных хромосом, а вторая хромосома может быть другой гомологичной хромосомой.
[0030] В некоторых способах LTVEC составляет по меньшей мере 15 т.п.о., по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о. или по меньшей мере 90 т.п.о. Необязательно, LTVEC составляет по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
[0031] В некоторых способах первая нуклеиновая кислота составляет по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о., по меньшей мере 200 т.п.о., по меньшей мере 250 т.п.о., или по меньшей мере 300 т.п.о. В некоторых способах первая нуклеиновая кислота составляет от около 40 т.п.о. до около 140 т.п.о. В некоторых способах первая нуклеиновая кислота содержит от около 43 т.п.о. до около 134 т.п.о.
[0032] В некоторых способах эукариотическая клетка является клеткой млекопитающего, фибробластом, плюрипотентной клеткой, нечеловеческой плюрипотентной клеткой, плюрипотентной клеткой грызуна, мышиной или крысиной эмбриональной стволовой (ЭС) клеткой, человеческой плюрипотентной клеткой, человеческой эмбриональной стволовой (ЭС) клеткой, человеческой взрослой стволовой клеткой, человеческой клеткой-предшественником с ограниченным развитием или человеческой индуцированной плюрипотентной стволовой (иПС) клеткой.
[0033] В некоторых способах белок Cas представляет собой Cas9. В некоторых способах целевая последовательность непосредственно фланкируется последовательностью мотива, прилегающего к протоспейсеру (РАМ).
[0034] В некоторых способах 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.н. до около 150 т.п.н. Необязательно, 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до 150 т.п.о.
[0035] В некоторых способах направленная генетическая модификация включает: (а) замещение эндогенной нуклеотидной последовательности гомологичной или ортологичной нуклеотидной последовательностью; (b) удаление эндогенной нуклеотидной последовательности; (с) удаление эндогенной нуклеотидной последовательности, при этом диапазон удаления составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.; (d) вставку экзогенной нуклеотидной последовательности; (е) вставку экзогенной нуклеотидной последовательности в диапазоне от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.; (f) вставку экзогенной нуклеотидной последовательности, содержащей гомологичную или ортологичную нуклеотидную последовательность; (g) вставку химерной нуклеотидной последовательности, содержащей человеческую и нечеловеческую нуклеотидную последовательность; (h) вставку кондиционального аллеля, фланкируемого целевыми последовательностями сайт-специфической рекомбиназы; (i) вставку селективного маркера или репортерного гена, функционально связанного с третьим промотором, активным в плюрипотентной клетке; или (j) их комбинацию.
[0036] В некоторых способах представляющий интерес геномный локус содержит (i) 5' целевую последовательность, которая гомологична 5' плечу гомологии; и (ii) 3' целевую последовательность, которая гомологична 3' плечу гомологии. Необязательно, 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 3 м.п.о. Необязательно, 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 10 т.п.о., по меньшей мере 10 т.п.о., но менее чем 20 т.п.о., по меньшей мере 20 т.п.о., но менее чем 40 т.п.о., по меньшей мере 40 т.п.о., но менее чем 60 т.п.о., по меньшей мере 60 т.п.о., но менее чем 80 т.п.о., по меньшей мере около 80 т.п.о., но менее чем 100 т.п.о., по меньшей мере 100 т.п.о., но менее чем 150 т.п.о., или по меньшей мере 150 т.п.о., но менее чем 200 т.п.о., по меньшей мере около 200 т.п.о., но менее чем около 300 т.п.о., по меньшей мере около 300 т.п.о., но менее чем около 400 т.п.о., по меньшей мере около 400 т.п.о., но менее чем около 500 т.п.о., по меньшей мере около 500 т.п.о., но менее чем около 1 м.п.о., по меньшей мере около 1 м.п.о., но менее чем около 1,5 м.п.о., по меньшей мере около 1,5 м.п.о., но менее чем около 2 м.п.о., по меньшей мере около 2 м.п.о., но менее чем около 2,5 м.п.о., или по меньшей мере около 2,5 м.п.о., но менее чем около 3 м.п.о. Необязательно, 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 110 т.п.о., по меньшей мере 120 т.п.о., по меньшей мере 130 т.п.о., по меньшей мере 140 т.п.о., по меньшей мере 150 т.п.о., по меньшей мере 160 т.п.о., по меньшей мере 170 т.п.о., по меньшей мере 180 т.п.о., по меньшей мере 190 т.п.о. или по меньшей мере 200 т.п.о. В некоторых способах 5' и 3' целевые последовательности разделяют от около 30 т.п.о. до около 110 т.п.о. В некоторых способах 5' и 3' целевые последовательности разделяют от около 38 т.п.о. до около 110 т.п.о.
[0037] В некоторых способах представляющий интерес геномный локус содержит локус рецептора интерлейкина-2 гамма, локус АроЕ, локус Rag1, локус Rag2 или оба локуса Rag1 и Rag2. В других способах представляющий интерес геномный локус содержит локус Adamts5, локус Trpa1, локус Folh1 или локус Erbb4. В других способах представляющий интерес геномный локус содержит локус Lrp5. В других способах представляющий интерес геномный локус содержит локус С5 (Hc), локус Ror1 или локус Dpp4.
[0038] Дополнительно предложен способ получения отличного от человека животного поколения F0, которое содержит направленную генетическую модификацию в представляющем интерес геномном локусе, включающий: (а) приведение в контакт генома в нечеловеческой ЭС клетке с белком Cas, РНК CRISPR и tracrРНК в присутствии крупного направляющего вектора (LTVEC) для формирования модифицированной нечеловеческой ЭС клетки, при этом LTVEC состоит по меньшей мере из 10 т.п.о. и содержит первую нуклеиновую кислоту, фланкируемую 5' плечом гомологии и 3' плечом гомологии; (b) выявление модифицированной нечеловеческой ЭС клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе; (с) внесение модифицированной нечеловеческой ЭС клетки в нечеловеческий эмбрион-хозяина; и (d) вынашивание нечеловеческого эмбриона-хозяина суррогатной матерью, при этом суррогатная мать производит отличное от человека животное поколения F0, которое содержит направленную генетическую модификацию в представляющем интерес геномном локусе.
[0039] В некоторых таких способах РНК CRISPR и tracrРНК вносят вместе в форме одной направляющей РНК (нРНК). В других таких способах РНК CRISPR и tracrРНК вносят отдельно.
[0040] В некоторых таких способах (а) белок Cas вносят в нечеловеческую ЭС клетку в форме белка, матричной РНК (мРНК), кодирующей белок Cas, или ДНК, кодирующей белок Cas; (b) РНК CRISPR вносят в нечеловеческую ЭС клетку в форме РНК или ДНК, кодирующей РНК CRISPR; и (с) tracrРНК вносят в нечеловеческую ЭС клетку в форме РНК или ДНК, кодирующей tracrРНК.
[0041] В некоторых таких способах (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; (b) ДНК, кодирующая РНК CRISPR, находится в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей РНК CRISPR; и (с) ДНК, кодирующая tracrРНК, находится в форме третьей экспрессионной конструкции, содержащей третий промотор, функционально связанный с четвертой нуклеиновой кислотой, кодирующей tracrРНК, при этом первый, второй и третий промоторы активны в нечеловеческой ЭС клетке. Необязательно, первая, вторая и третья экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[0042] В некоторых таких способах (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; a (b) ДНК, кодирующая РНК CRISPR, и ДНК, кодирующая tracrРНК, находятся в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей нРНК, содержащую РНК CRISPR и tracrРНК; при этом первый и второй промоторы активны в нечеловеческой ЭС клетке. Необязательно, первая и вторая экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[0043] В некоторых таких способах белок Cas, РНК CRISPR и tracrРНК вносят в нечеловеческую ЭС клетку в виде комплекса белок-РНК.
[0044] В некоторых таких способах направленная генетическая модификация включает одновременное удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус.
[0045] В некоторых таких способах направленная генетическая модификация представляет собой биаллельную генетическую модификацию. Необязательно, биаллельная генетическая модификация включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в двух гомологичных хромосомах.
[0046] В некоторых таких способах модифицированная нечеловеческая ЭС клетка является компаунд-гетерозиготной в представляющем интерес геномном локусе. В некоторых таких способах модифицированная нечеловеческая ЭС клетка является гемизиготной в представляющем интерес геномном локусе. Необязательно, направленная генетическая модификация в представляющем интерес геномном локусе в одной хромосоме включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты. Необязательно, направленная генетическая модификация включает: (1) удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе в двух гомологичных хромосомах; и (2) вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в первой хромосоме и разрушение представляющего интерес геномного локуса во второй хромосоме. Первая хромосома может быть одной из двух гомологичных хромосом, а вторая хромосома может быть другой гомологичной хромосомой.
[0047] В некоторых таких способах белок Cas представляет собой Cas9.
[0048] Дополнительно предложены способы модификации генома в представляющем интерес геномном локусе в эукариотической клетке, мышиной клетке или человеческой клетке, включающие приведение генома в контакт с белком Cas, РНК CRISPR, которая гибридизируется с целевой последовательностью в представляющем интерес геномном локусе, и tracrРНК в присутствии крупного направляющего вектора (LTVEC), при этом LTVEC составляет по меньшей мере 10 т.п.о. и содержит первую нуклеиновую кислоту, фланкируемую 5' плечом гомологии, которое гомологично 5' целевой последовательности в представляющем интерес геномном локусе, и 3' плечом гомологии, которое гомологично 3' целевой последовательности в представляющем интерес геномном локусе, при этом первая нуклеиновая кислота состоит по меньшей мере из 30 т.п.о. и/или 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 30 т.п.о., при этом после контакта с белком Cas, РНК CRISPR и tracrРНК в присутствии LTVEC, происходит модификация генома так, чтобы он содержал направленную генетическую модификацию, включающую вставку первой нуклеиновой кислоты в представляющем интерес геномном локусе.
[0049] Любой из вышеприведенных способов может дополнительно включать внесение белка Cas, РНК CRISPR, tracrРНК и LTVEC в эукариотическую клетку, мышиную клетку или человеческую клетку. Любой из вышеприведенных способов может дополнительно включать выявление модифицированной эукариотической клетки, модифицированной мышиной клетки или модифицированной человеческой клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе.
[0050] В некоторых из вышеприведенных способов РНК CRISPR и tracrРНК вносят вместе в форме одного транскрипта. В некоторых из вышеприведенных способов РНК CRISPR и tracrРНК вносят отдельно.
[0051] В некоторых из вышеприведенных способов (а) белок Cas вносят в эукариотическую клетку, мышиную клетку или человеческую клетку в форме белка, матричной РНК (мРНК), кодирующей белок Cas, или ДНК, кодирующей белок Cas; (b) РНК CRISPR вносят в эукариотическую клетку, мышиную клетку или человеческую клетку в форме РНК или ДНК, кодирующей РНК CRISPR; и (с) tracrРНК вносят в эукариотическую клетку, мышиную клетку или человеческую клетку в форме РНК или ДНК, кодирующей tracrРНК. В некоторых из вышеприведенных способов белок Cas, РНК CRISPR и tracrРНК вносят в эукариотическую клетку, мышиную клетку или человеческую клетку в виде комплекса белок-РНК.
[0052] В некоторых из вышеприведенных способов (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; (b) ДНК, кодирующая РНК CRISPR, находится в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей РНК CRISPR; и (с) ДНК, кодирующая tracrРНК, находится в форме третьей экспрессионной конструкции, содержащей третий промотор, функционально связанный с четвертой нуклеиновой кислотой, кодирующей tracrРНК, при этом первый, второй и третий промоторы активны в эукариотической клетке, мышиной клетке или человеческой клетке. В некоторых из вышеприведенных способов первая, вторая и третья экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[0053] В некоторых из вышеприведенных способов (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; a (b) ДНК, кодирующая РНК CRISPR, и ДНК, кодирующая tracrРНК, находятся в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей нРНК, содержащую РНК CRISPR и tracrРНК; при этом первый и второй промоторы активны в эукариотической клетке, мышиной клетке или человеческой клетке. В некоторых из вышеприведенных способов первая и вторая экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[0054] В некоторых из вышеприведенных способов LTVEC составляет по меньшей мере 15 т.п.о., по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о. или по меньшей мере 90 т.п.о. В некоторых из вышеприведенных способов LTVEC составляет по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
[0055] В некоторых из вышеприведенных способов первая нуклеиновая кислота составляет по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о., по меньшей мере 200 т.п.о., по меньшей мере 250 т.п.о. или по меньшей мере 300 т.п.о. В некоторых из вышеприведенных способов первая нуклеиновая кислота составляет от около 40 т.п.о. до около 140 т.п.о.
[0056] В некоторых из вышеприведенных способов 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.н. до около 150 т.п.н. В некоторых из вышеприведенных способов 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до 150 т.п.о.
[0057] В некоторых из вышеприведенных способов 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 3 м.п.о. В некоторых из вышеприведенных способов 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 10 т.п.о., по меньшей мере 10 т.п.о., но менее чем 20 т.п.о., по меньшей мере 20 т.п.о., но менее чем 40 т.п.о., по меньшей мере 40 т.п.о., но менее чем 60 т.п.о., по меньшей мере 60 т.п.о., но менее чем 80 т.п.о., по меньшей мере около 80 т.п.о., но менее чем 100 т.п.о., по меньшей мере 100 т.п.о., но менее чем 150 т.п.о., или по меньшей мере 150 т.п.о., но менее чем 200 т.п.о., по меньшей мере около 200 т.п.о., но менее чем около 300 т.п.о., по меньшей мере около 300 т.п.о., но менее чем около 400 т.п.о., по меньшей мере около 400 т.п.о., но менее чем около 500 т.п.о., по меньшей мере около 500 т.п.о., но менее чем около 1 м.п.о., по меньшей мере около 1 м.п.о., но менее чем около 1,5 м.п.о., по меньшей мере около 1,5 м.п.о., но менее чем около 2 м.п.о., по меньшей мере около 2 м.п.о., но менее чем около 2,5 м.п.о., или по меньшей мере около 2,5 м.п.о., но менее чем около 3 м.п.о. В некоторых из вышеприведенных способов 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 110 т.п.о., по меньшей мере 120 т.п.о., по меньшей мере 130 т.п.о., по меньшей мере 140 т.п.о., по меньшей мере 150 т.п.о., по меньшей мере 160 т.п.о., по меньшей мере 170 т.п.о., по меньшей мере 180 т.п.о., по меньшей мере 190 т.п.о. или по меньшей мере 200 т.п.о. В некоторых из вышеприведенных способов 5' и 3' целевые последовательности разделяют от около 30 т.п.о. до около 110 т.п.о.
[0058] В некоторых из вышеприведенных способов эукариотическая клетка не является крысиной клеткой. В некоторых из вышеприведенных способов эукариотическая клетка является плюрипотентной клеткой, неплюрипотентной клеткой, клеткой млекопитающего, человеческой клеткой, клеткой отличного от человека млекопитающего, клеткой грызуна, мышиной клеткой, клеткой хомяка, нечеловеческой плюрипотентной клеткой, человеческой плюрипотентной клеткой, плюрипотентной клеткой грызуна или фибробластом. В некоторых из вышеприведенных способов эукариотическая клетка является первичной клеткой или иммортализованной клеткой. В некоторых из вышеприведенных способов плюрипотентная клетка грызуна является мышиной или крысиной эмбриональной стволовой (ЭС) клеткой.
[0059] В некоторых из вышеприведенных способов мышиная клетка или человеческая клетка является первичной клеткой или иммортализованной клеткой. В некоторых из вышеприведенных способов мышиная клетка или человеческая клетка является плюрипотентной клеткой. В некоторых из вышеприведенных способов мышиная плюрипотентная клетка является мышиной эмбриональной стволовой (ЭС) клеткой. В некоторых из вышеприведенных способов человеческая плюрипотентная клетка является человеческой эмбриональной стволовой (ЭС) клеткой, взрослой человеческой стволовой клеткой, человеческой клеткой-предшественником с ограниченным развитием или человеческой индуцированной плюрипотентной стволовой (иПС) клеткой. В некоторых из вышеприведенных способов человеческие иПС клетки поддерживают в среде, содержащей основную среду и добавки, при этом среда содержит: (а) полипептид фактора, ингибирующего лейкемию (LIF) е; (b) ингибитор киназы гликогенсинтазы (GSK3); и (с) ингибитор MEK; при этом осмолярность среды составляет от около 175 мОсм/кг до около 280 мОсм/кг.
[0060] В некоторых из вышеприведенных способов белок Cas представляет собой Cas9. В некоторых из вышеприведенных способов целевая последовательность непосредственно фланкируется последовательностью мотива, прилегающего к протоспейсеру (РАМ).
[0061] В некоторых из вышеприведенных способов направленная генетическая модификация включает одновременное удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус на одном этапе. В некоторых из вышеприведенных способов удаленная эндогенная нуклеотидная последовательность составляет от около 30 т.п.о. до около 110 т.п.о., а вставленная первая нуклеиновая кислота составляет от около 40 т.п.о. до около 140 т.п.о.
[0062] В некоторых из вышеприведенных способов направленная генетическая модификация представляет собой биаллельную генетическую модификацию. В некоторых из вышеприведенных способов биаллельная генетическая модификация включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в двух гомологичных хромосомах. В некоторых из вышеприведенных способов модифицированная эукариотическая клетка, модифицированная мышиная клетка или модифицированная человеческая клетка является компаунд-гетерозиготной в представляющем интерес геномном локусе. В некоторых из вышеприведенных способов модифицированная мышиная клетка или модифицированная человеческая клетка является гемизиготной в представляющем интерес геномном локусе. В некоторых из вышеприведенных способов направленная генетическая модификация в представляющем интерес геномном локусе в одной хромосоме включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты. В некоторых из вышеприведенных способов направленная генетическая модификация включает: (1) удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе в первой и второй гомологичных хромосомах; и (2) вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в первой хромосоме и разрушение представляющего интерес геномного локуса во второй хромосоме.
[0063] В некоторых из вышеприведенных способов направленная генетическая модификация включает: (а) замещение эндогенной нуклеотидной последовательности гомологичной или ортологичной нуклеотидной последовательностью; (b) удаление эндогенной нуклеотидной последовательности; (с) удаление эндогенной нуклеотидной последовательности, при этом диапазон удаления составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.; (d) вставку экзогенной нуклеотидной последовательности; (е) вставку экзогенной нуклеотидной последовательности в диапазоне от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.; (f) вставку экзогенной нуклеотидной последовательности, содержащей гомологичную или ортологичную нуклеотидную последовательность; (g) вставку химерной нуклеотидной последовательности, содержащей человеческую и нечеловеческую нуклеотидную последовательность; (h) вставку кондиционального аллеля, фланкируемого целевыми последовательностями сайт-специфической рекомбиназы; (i) вставку селективного маркера или репортерного гена, функционально связанного с третьим промотором, активным в плюрипотентной клетке; или (j) их комбинацию.
[0064] В некоторых из вышеприведенных способов представляющий интерес геномный локус содержит локус рецептора интерлейкина-2 гамма, локус АроЕ, локус Rag1, локус Rag2, оба локуса Rag1 и Rag2, локус Adamts5, локус Trpa1, локус Folh1, локус Erbb4, локус Lrp5, локус С5 (Hc), локус Ror1 или локус Dpp4. В некоторых из вышеприведенных способов представляющий интерес геномный локус содержит внехромосомную ДНК.
[0065] Также предложены способы получения отличного от человека животного или мыши поколения F0, которое содержит направленную генетическую модификацию в представляющем интерес геномном локусе, включающие: (а) модификацию нечеловеческой или мышиной ЭС клетки любым из вышеприведенных способов; (b) выявление модифицированной нечеловеческой или мышиной ЭС клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе; (с) внесение модифицированной нечеловеческой или мышиной ЭС клетки в нечеловеческий или мышиный эмбрион-хозяина; и (d) вынашивание нечеловеческого или мышиного эмбриона-хозяина суррогатной матерью, при этом суррогатная мать производит отличное от человека животное или мышь поколения F0, которое содержит направленную генетическую модификацию в представляющем интерес геномном локусе.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0066] Фигура 1 иллюстрирует крысиные ЭСК, которые растут в виде компактных сферических колоний, которые обычно отделяются и плавают в чашке.
[0067] Фигуры 2A-D иллюстрируют различные маркеры плюрипотентности, экспрессируемые крысиными ЭСК: А иллюстрирует Oct-4 (зеленый); В иллюстрирует Sox-2 (красный); С иллюстрирует DAPI (синий); D иллюстрирует наслоение маркеров плюрипотентности, экспрессируемых кЭСК.
[0068] Фигура 3 иллюстрирует, что крысиные ЭСК экспрессируют невысокие уровни щелочной фосфатазы (маркера плюрипотентности).
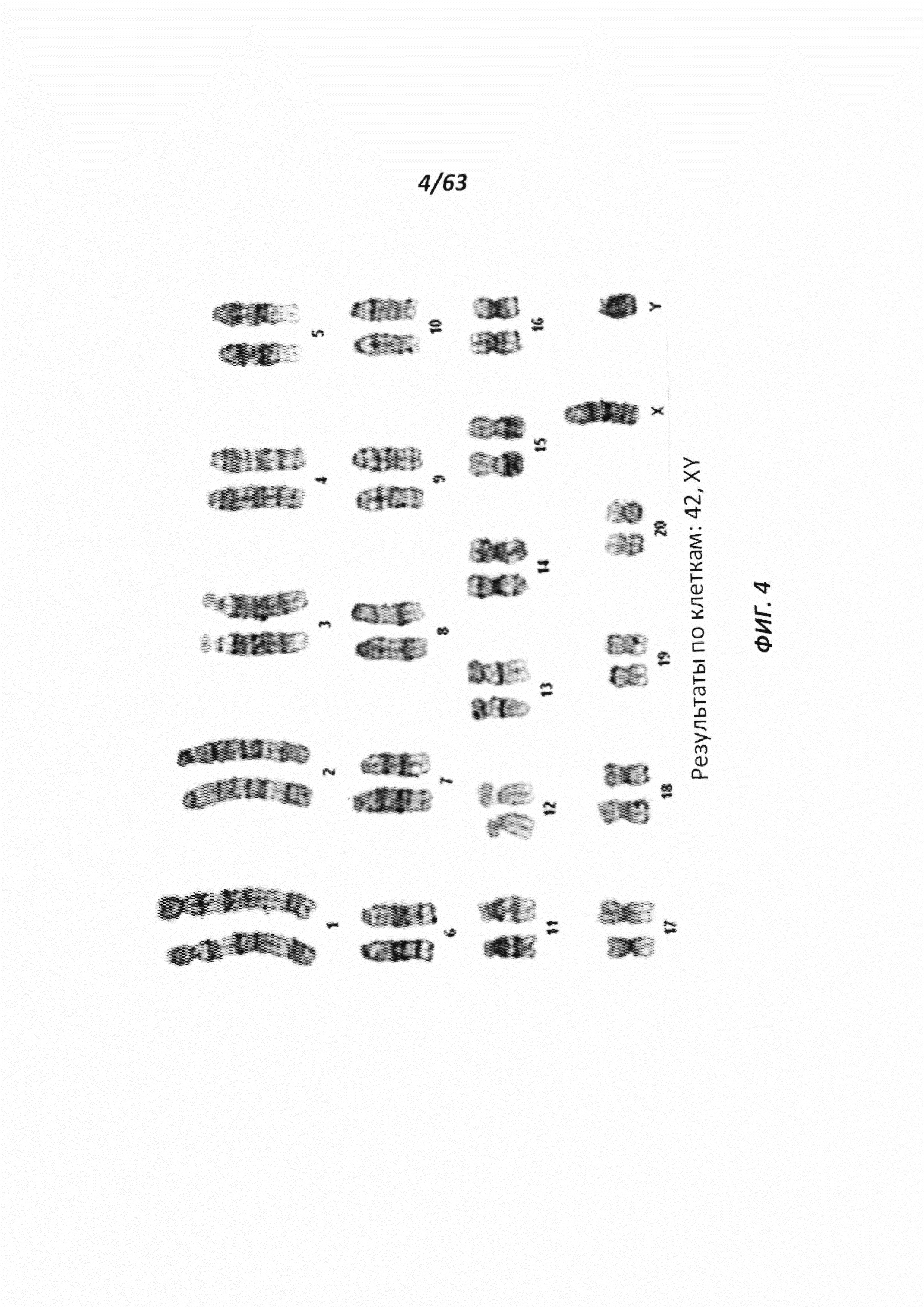
[0069] Фигура 4 иллюстрирует кариотип линии DA.2B, которая является 42X,Y. Кариотипирование проводили, так как крысиные ЭСК часто становятся тетрагаплоидными; поэтому проводили предварительный скрининг линий путем подсчета метафазных хромосомных препаратов, а затем линии с большинством нормальных результатов формально кариотипировали.
[0070] На Фигуре 5А-В приведены фотографии, иллюстрирующие анализ числа хромосом линии крысиных ЭС клеток ACI.G1.
[0071] На Фигуре 6А-В приведены фотографии, иллюстрирующие анализ числа хромосом линии крысиных ЭС клеток DA.2B.
[0072] На Фигуре 7А-В приведены фотографии, иллюстрирующие анализ числа хромосом линии крысиных ЭС клеток DA.2C.
[0073] На Фигуре 8 приведен крупный план крысиных ЭСК с Фигуры 1.
[0074] Фигура 9 иллюстрирует получение химер путем инъекции в бластоцисты и передачу генома крысиных ЭСК через зародышевую линию. Химеры получали путем инъекции в бластоцисты с применением родительских крысиных ЭСК ACI.G1. Химеры с высоким процентным содержанием обычно имеют белые морды.
[0075] Фигура 10 иллюстрирует детенышей агути F1 с однопометными детенышами-альбиносами, полученных от химеры ACI/SD, помеченной звездочкой (*) на Фигуре 9.
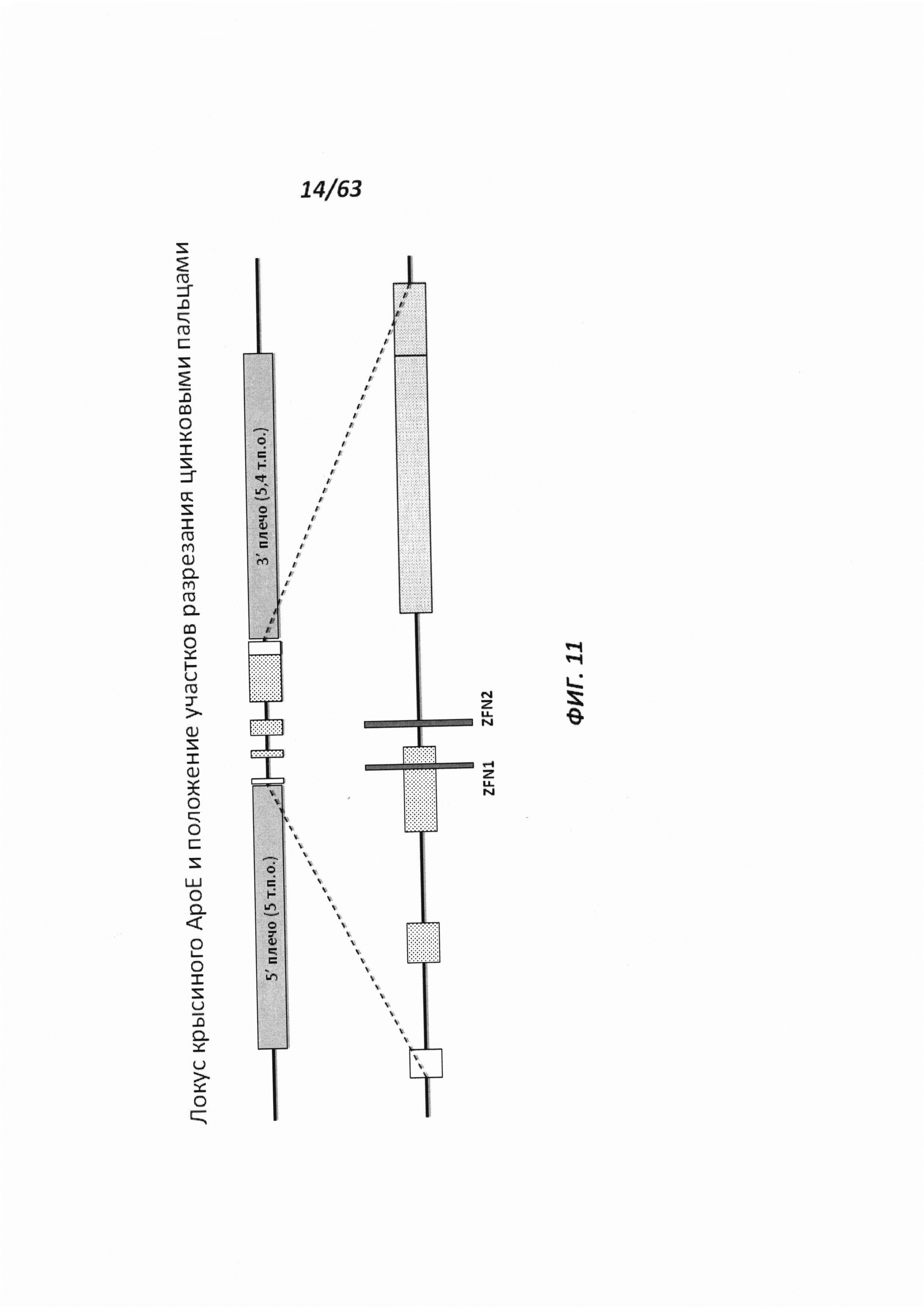
[0076] На Фигуре 11 приведено схематическое изображение локуса крысиного АроЕ, а серыми прямоугольниками обозначены места разрезания цинк-пальцевыми нуклеазами (ZFN1 и ZFN2). Геномные области, соответствующие 5' и 3' плечам гомологии (5 т.п.о. и 5,4 т.п.о., соответственно), обозначены темно-серыми прямоугольниками. Экзон 1 в гене АроЕ является некодирующим и показан в виде неокрашенного прямоугольника, расположенного наиболее близко к 5' плечу гомологии. Три интрона в гене АроЕ обозначены в виде линий. Экзоны 2 и 3 содержат кодирующие области и показаны в виде заштрихованных пунктиром серых прямоугольников. Экзон 4 содержит как кодирующие, так и некодирующие последовательности, обозначенные серым пунктиром и неокрашенным прямоугольником.
[0077] Фигура 12 иллюстрирует таргетирование локуса крысиного Rosa26, который расположен между генами Setd5 и Thumpd3, как и у мыши, с одинаковыми промежутками. Панель А иллюстрирует структуру локуса мышиного Rosa26. Мышиные транскрипты Rosa26 состоят из 2 или 3 экзонов. Панель В иллюстрирует структуру локуса крысиного Rosa26; крысиный локус содержит второй экзон 1 (Ex1b) вдобавок к экзону, гомологичному мышиному экзону 1 (Ех1а); третий экзон у крыс выявлен не был. Панель С иллюстрирует таргетированный крысиный аллель Rosa26; плечи гомологии из 5 т.п.о. каждое были клонированы посредством ПЦР с использованием геномной ДНК из DA кЭСК; таргетированный аллель содержит кассету с акцепторным участком сплайсинга (SA)-lacZ-hUB-neo, замещающую делецию в 117 п.о. в интроне крысиного Rosa26.
[0078] Фигура 13А иллюстрирует контрольный головной мозг 14-недельной крысы дикого типа, который был окрашен X-gal. Для контрольного головного мозга наблюдали низкий уровень фонового окрашивания LacZ (вид сверху).
[0079] Фигура 13В иллюстрирует экспрессию LacZ в головном мозге гетерозиготной крысы rRosa26 (14-недельной). Репортер lacZ экспрессировался по всему объему мозга геторозиготы rRosa26.
[0080] Фигура 13С иллюстрирует контрольные сердце и вилочковую железу (вставка) 14-недельной крысы дикого типа, которые были обработаны X-gal. В контрольном сердце и вилочковой железе наблюдали низкий уровень фонового окрашивания LacZ.
[0081] Фигура 13D иллюстрирует экспрессию LacZ в сердце и вилочковой железе (вставка) 14-недельной гетерозиготной крысы rRosa26. Репортер lacZ экспрессировался по всему объему сердца и вилочковой железы гетерозиготы rROSA26.
[0082] Фигура 13Е иллюстрирует контрольные легкие 14-недельной крысы дикого типа, которые были обработаны X-gal. В контрольных легких наблюдали низкий уровень фонового окрашивания LacZ.
[0083] Фигура 13F иллюстрирует экспрессию LacZ в легких 14-недельной гетерозиготной крысы rRosa26. Репортер lacZ экспрессировался по всему объему легких гетерозиготы rRosa26.
[0084] Фигуры 13G и Н иллюстрируют экспрессию LacZ в крысиных эмбрионах Е12.5. В отличие от контрольного эмбриона дикого типа (Н), в котором наблюдали низкий уровень фонового окрашивания LacZ, гетерозиготный эмбрион rRosa26 демонстрировал экспрессию репортера LacZ по всему объему эмбриона.
[0085] Фигуры 13I и J иллюстрируют экспрессию LacZ в эмбрионах крыс Е14.5. В отличие от контрольного эмбриона дикого типа (J), в котором наблюдали низкий уровень фонового окрашивания LacZ, гетерозиготный эмбрион rRosa26 демонстрировал экспрессию репортера LacZ по всему объему эмбриона.
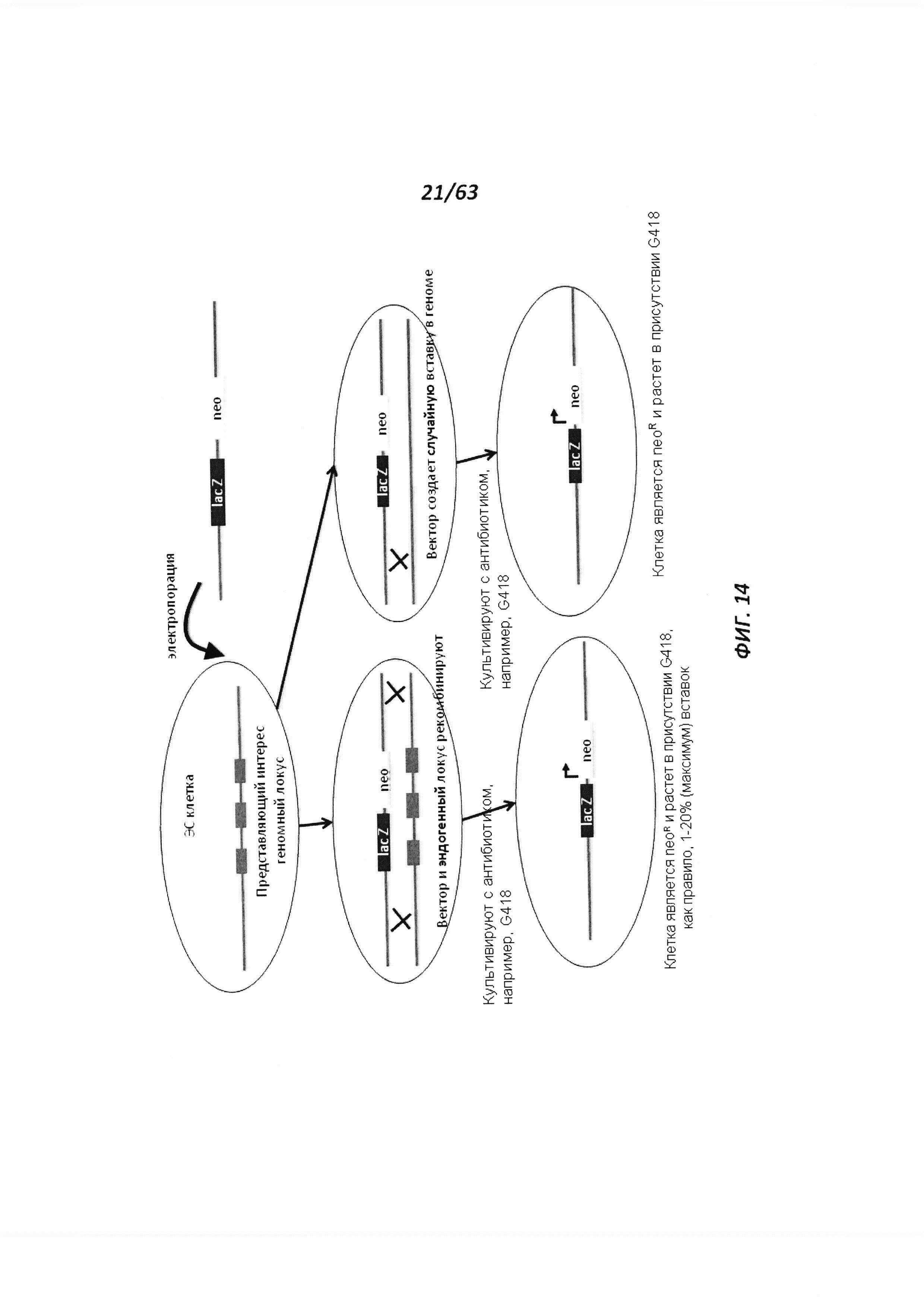
[0086] Фигура 14 иллюстрирует гомологичную или негомологичную рекомбинацию, которая происходит внутри крысиной ЭС клетки после электропорации направляющего вектора, содержащего селекционную кассету (кассету lacZ-neo).
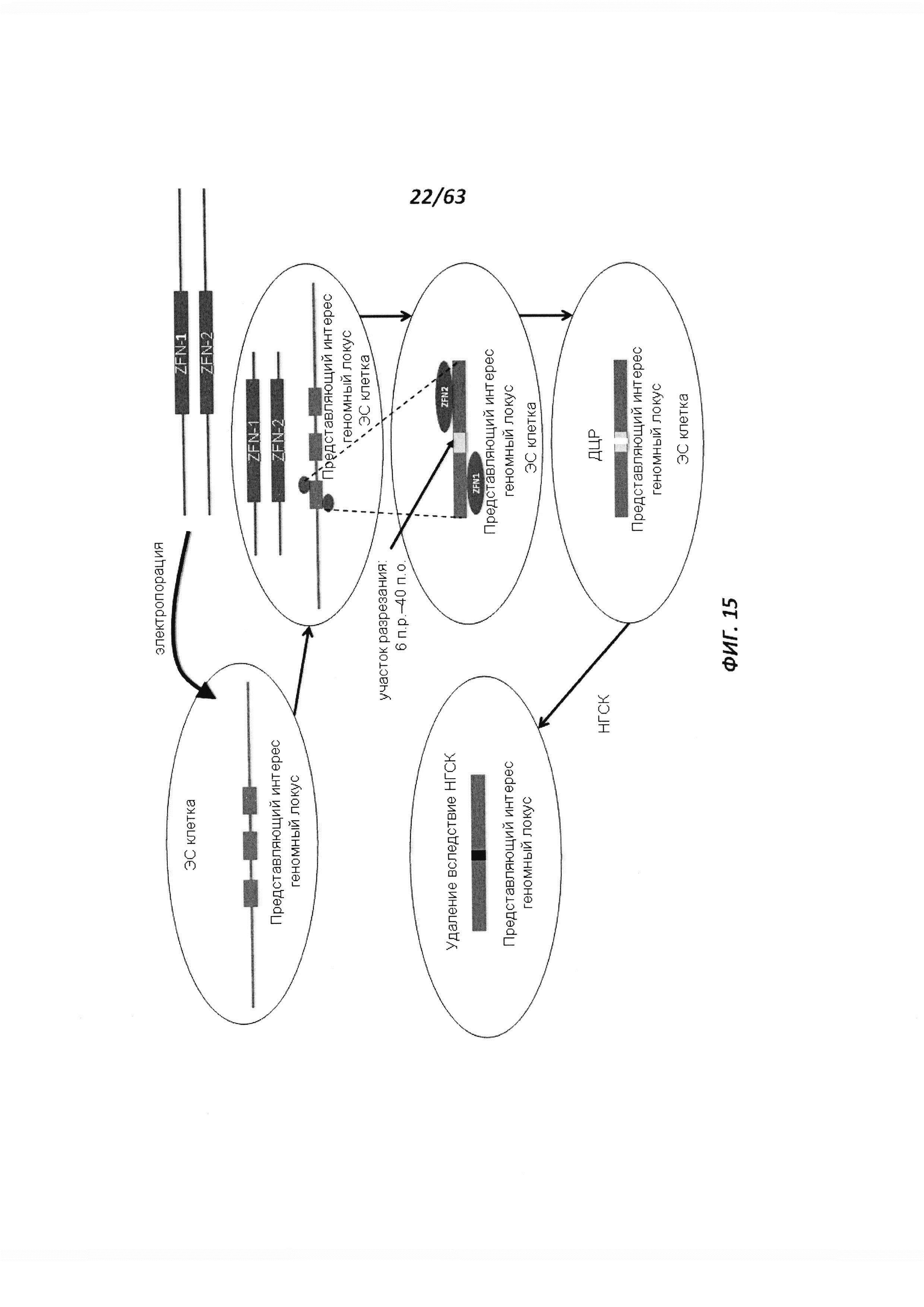
[0087] Фигура 15 иллюстрирует механизм, при помощи которого редактирующие геном эндонуклеазы (например, ZFN и TALEN) создают двухцепочечный разрыв (ДЦР) в геномной целевой последовательности и активируют негомологичное соединение концов (НГСК) в ЭС клетке.
[0088] Фигура 16 иллюстрирует способ таргетирования генов, в котором используются ZFN/TALEN, для улучшения эффективности гомологичной рекомбинации направляющего вектора. ДЦР обозначает двухцепочечный разрыв.
[0089] Фигура 17 иллюстрирует химеры ApoE-ZFN-AB5, полученные методом получения химер и трансмиссии зародышевой линии модифицированного локуса крысиного АроЕ. Направленная модификация была осуществлена при помощи цинк-пальцевых нуклеаз.
[0090] На Фигуре 18 приведено схематическое изображение таргетирования IL2r-γ в комбинации с цинк-пальцевыми нуклеазами, которые нацеливают ZFN U и ZFN D. Показана область крысиного локуса IL2r-γ, который является объектом нацеливания ZFN U и ZFN D (SEQ ID №93). На фигуре обозначены участки разрезания ZFN.
[0091] На Фигуре 19 приведено схематическое изображение таргетирования IL2r-γ в комбинации с цинк-пальцевыми нуклеазами, которые нацеливают ZFN U и ZFN D, или в комбинации с нРНК (нРНК1, нРНК2, нРНК3, нРНК4). Показаны области крысиного локуса IL2r-γ, который является объектом нацеливания ZFN U и ZFN D или нРНК1-4, и обозначены участки разрезания ZFN.
[0092] На Фигуре 20 приведено схематическое изображение локуса крысиного АроЕ и направляющей плазмиды. На верхней схеме показана геномная структура локуса крысиного АроЕ и геномные локусы, соответствующие 5' и 3' плечам гомологии (5 т.п.о. и 5,4 т.п.о., соответственно; темно-серые прямоугольники). Экзон 1 в гене АроЕ является некодирующим и показан в виде неокрашенного прямоугольника, расположенного наиболее близко к 5' плечу гомологии. Три интрона в гене АроЕ обозначены в виде линий. Экзоны 2 и 3 содержат кодирующие области и показаны в виде заштрихованных пунктиром серых прямоугольников. Экзон 4 содержит как кодирующие, так и некодирующие последовательности, обозначенные серым пунктиром и неокрашенным прямоугольником. Нижняя панель иллюстрирует направляющую плазмиду. 5' и 3' плечи гомологии (5 т.п.о. и 5,4 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. Направляющий вектор содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки). Самоуничтожающаяся кассета содержит промотор мышиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
[0093] На Фигуре 21А приведено схематическое изображение таргетирования локуса АроЕ в крысиных ЭС клетках с использованием цинк-пальцевых нуклеаз и направляющего вектора, содержащего репортерный ген (LacZ) и самоуничтожающуюся кассету, содержащую промотор мышиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину. Фигура 21В иллюстрирует гомозиготный таргетированный локус АроЕ.
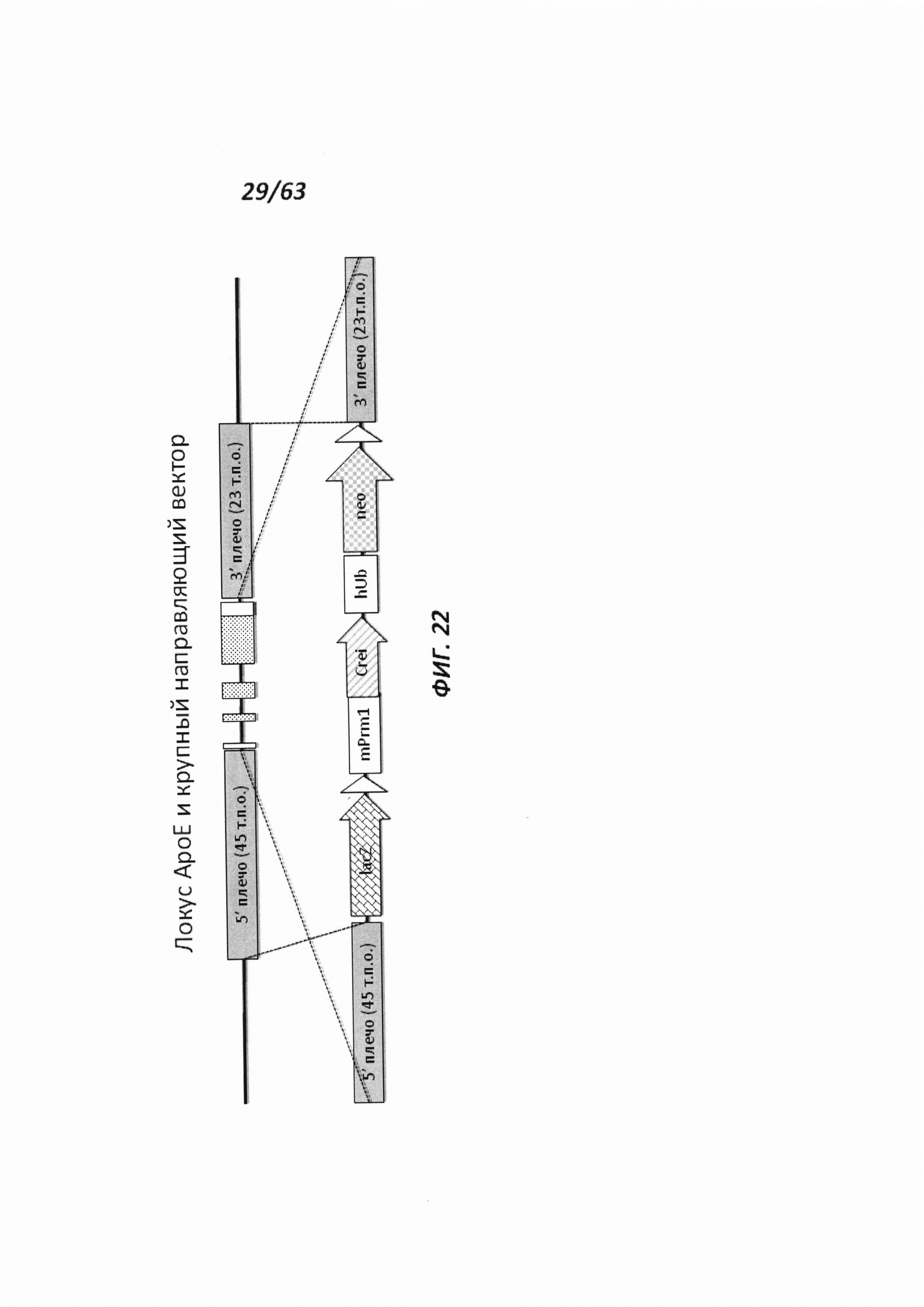
[0094] На Фигуре 22 приведено схематическое изображение локуса крысиного АроЕ и крупного направляющего вектора (LTVEC). На верхней панели показана геномная структура локуса крысиного АроЕ и геномные области, соответствующие 5' и 3' плечам гомологии (45 т.п.о. и 23 т.п.о., соответственно; темно-серые прямоугольники). Экзон 1 АроЕ является некодирующим и показан в виде неокрашенного прямоугольника, расположенного наиболее близко к 5' плечу гомологии. Три интрона в гене АроЕ обозначены в виде линий, а экзоны 2 и 3 содержат кодирующие области и показаны в виде заштрихованных пунктиром серых прямоугольников. Экзон 4 содержит как кодирующие, так и некодирующие последовательности, обозначенные серым пунктиром и неокрашенным прямоугольником. На нижней панели показан LTVEC для модификации локуса крысиного АроЕ. 5' и 3' плечи гомологии (45 т.п.о. и 23 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. LTVEC содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит промотор мышиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
[0095] На Фигуре 23 приведено схематическое изображение локуса крысиного АроЕ и серыми прямоугольниками обозначены места разрезания цинк-пальцевыми нуклеазами (ZFN1 и ZFN2), применяемыми вместе с крупным направляющим вектором (LTVEC), чтобы повысить гомологичную рекомбинацию между направляющим вектором и целевой когнатной областью хромосомы.
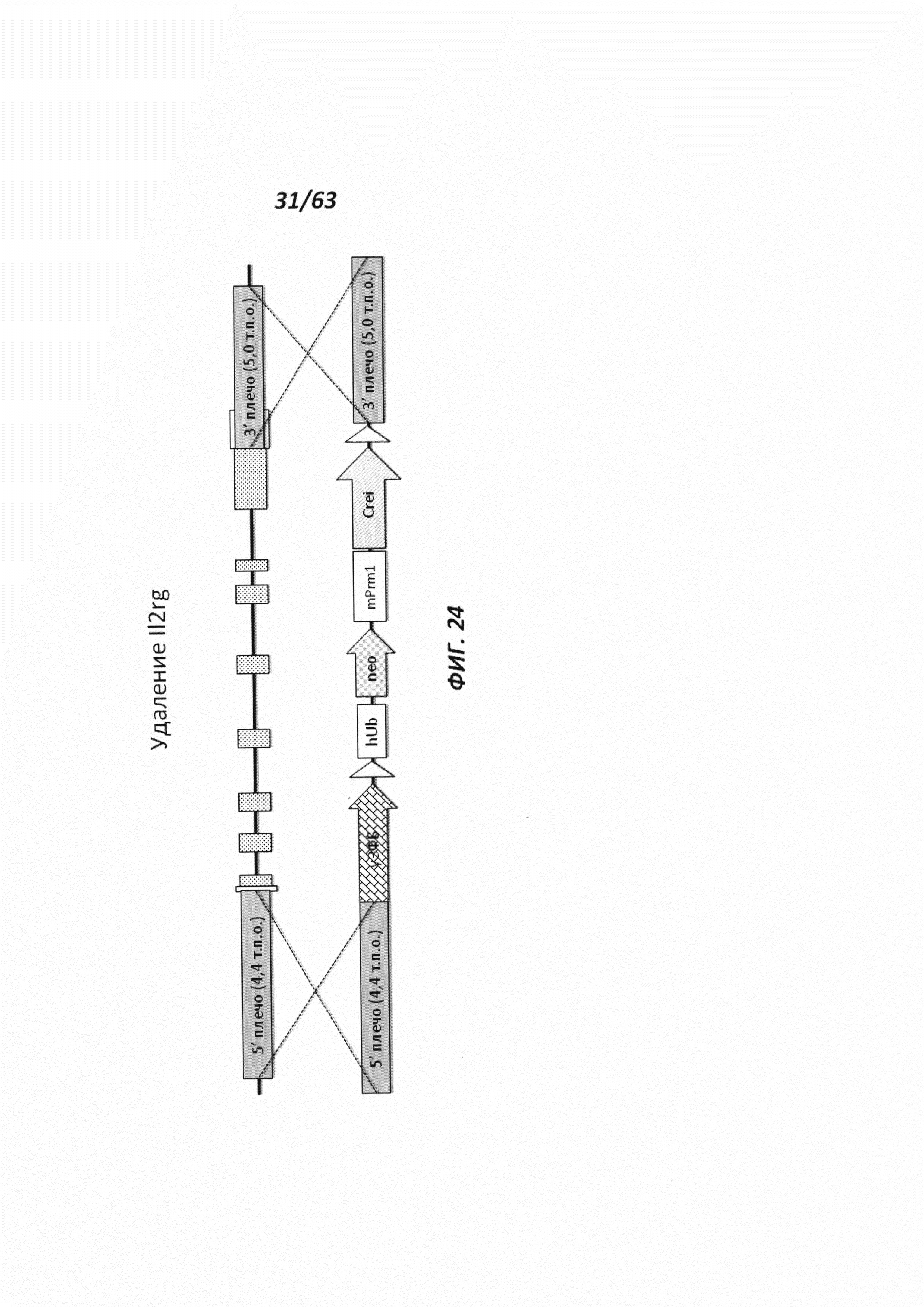
[0096] Фигура 24 иллюстрирует локус крысиного IL2r-γ, в котором была сделана делеция в 3,2 т.п.о. и внесена вставка репортерного гена (уЗФБ) и самоуничтожающейся кассеты, содержащей кассету отбора по чувствительности к лекарственному препарату (hUb-neo) и ген Crei, функционально связанный с промотором мышиного Prm1.
[0097] На Фигуре 25 приведено другое изображение локуса крысиного IL2r-γ, в котором была сделана делеция в 3,2 т.п.о. и внесена вставка репортерного гена (уЗФБ) и самоуничтожающейся кассеты, содержащей ген Crei, функционально связанный с промотором мышиного Prm1, и кассету отбора по чувствительности к лекарственному препарату (hUb-Neo).
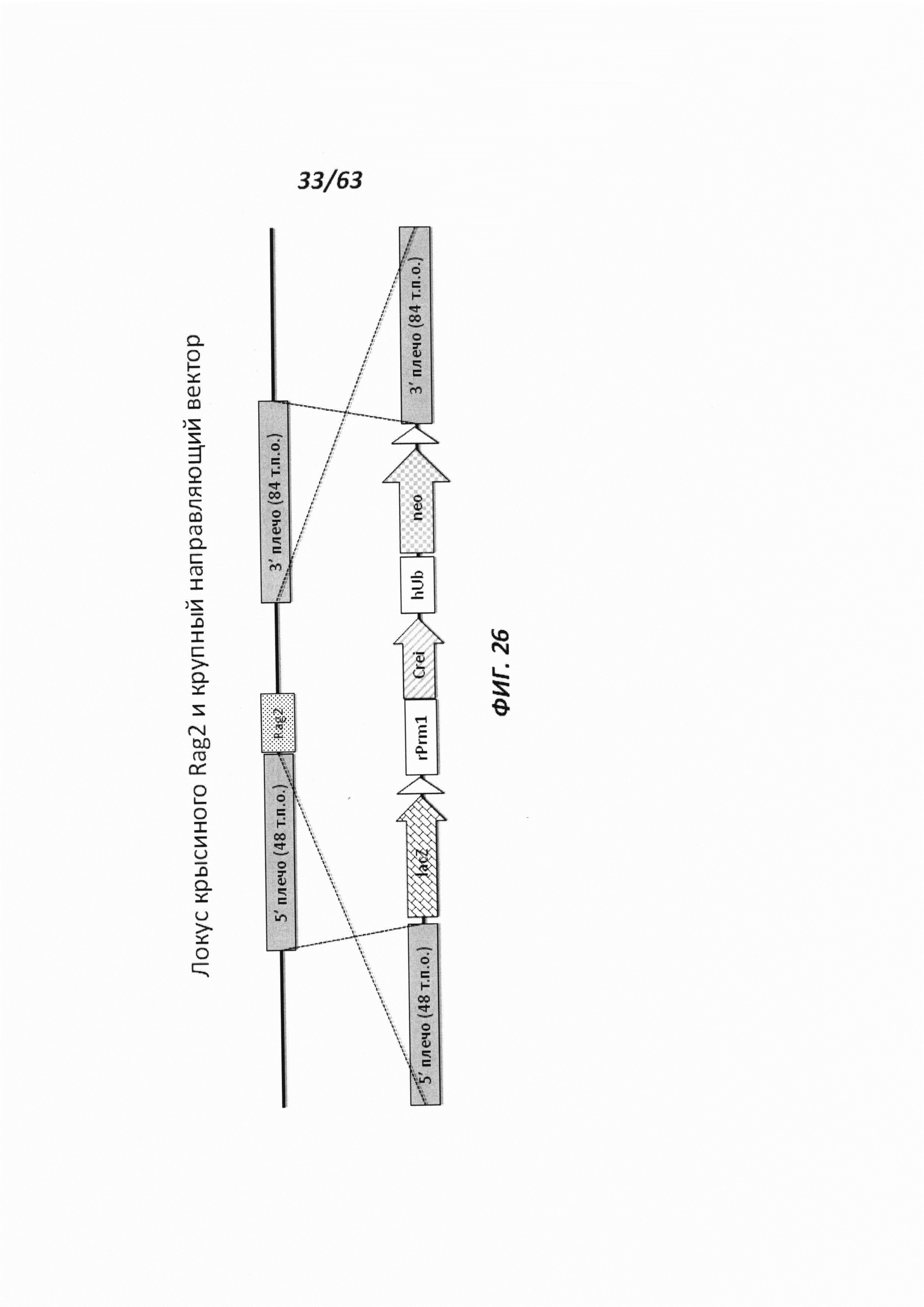
[0098] На Фигуре 26 приведено схематическое изображение локуса крысиного Rag2 и крупного направляющего вектора (LTVEC) для модификации локуса крысиного Rag2. На верхней панели показана геномная структура локуса крысиного Rag2 и когнатных геномных областей, соответствующих 5' и 3' плечам гомологии (48 т.п.о. и 84 т.п.о., соответственно; темно-серые прямоугольники). Rag2 содержит один экзон, обозначенный пунктирной серой штриховкой. Нижняя панель представляет собой LTVEC. 5' и 3' плечи гомологии (48 т.п.о. и 84 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. LTVEC содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит промотор крысиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
[0099] На Фигуре 27 приведена геномная структура локуса крысиного Rag1/Rag2 и геномные области, удаляемые путем таргетирования Rag2 (удаление Rag2) или Rag2/Rag1 двойного таргетирования (удаление Rag2/Rag1).
[00100] На Фигуре 28 приведено схематическое изображение локусов крысиного Rag2 и Rag1 и крупного направляющего вектора (LTVEC), применяемого для модификации локусов. На верхней панели показана геномная структура локусов Rag1 и Rag2 и когнатных геномных областей, соответствующих 5' и 3' плечам гомологии (48 т.п.о. и 15 т.п.о., соответственно; темно-серые прямоугольники). Каждый из Rag2 и Rag1 содержит один экзон, обозначенный пунктирной серой штриховкой. Нижняя панель представляет собой LTVEC. 5' и 3' плечи гомологии (48 т.п.о. и 15 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. LTVEC содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит промотор крысиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
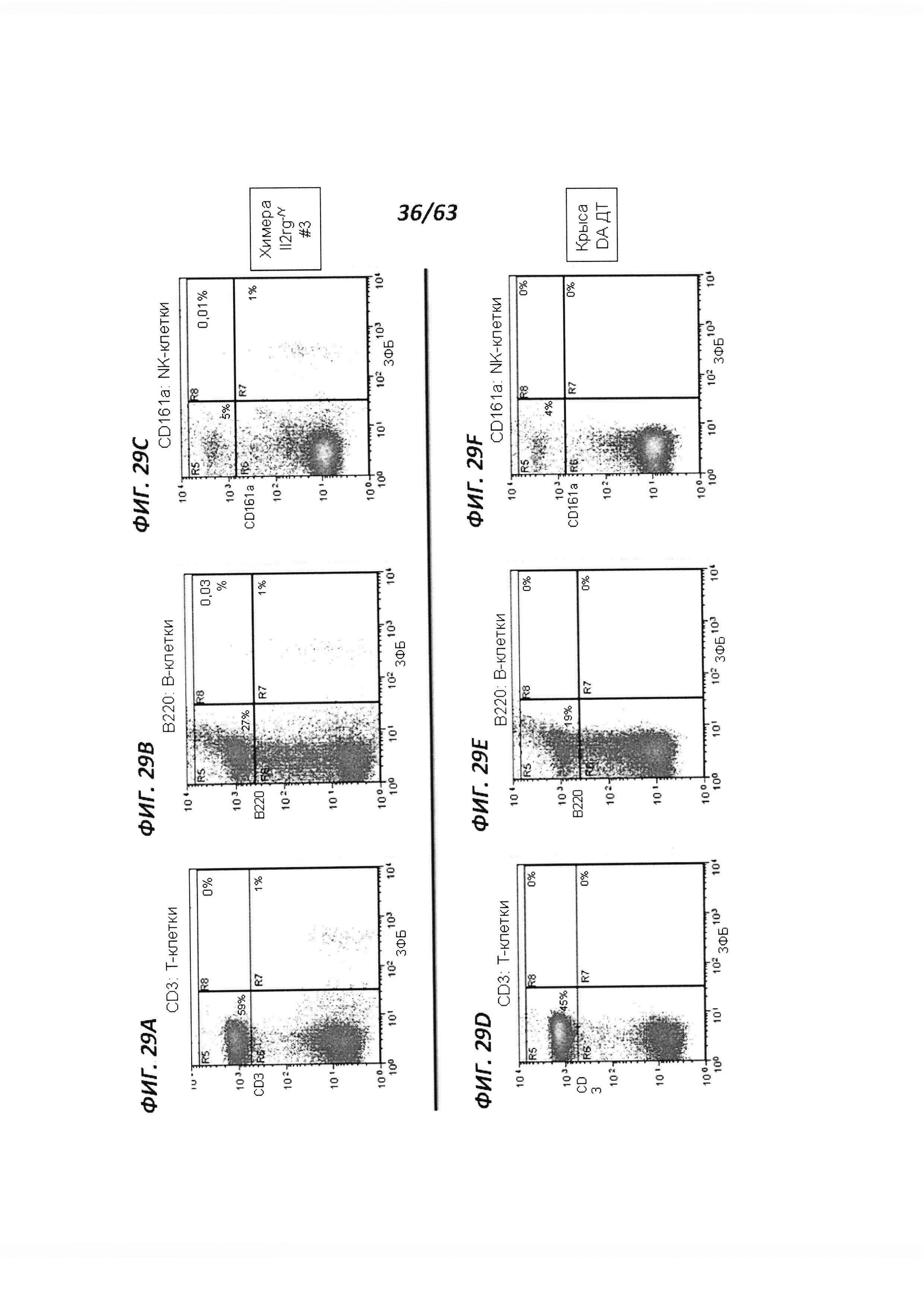
[00101] Фигура 29 иллюстрирует анализ методом проточной цитометрии для экспрессии ЗФБ и для маркера Т-клеток CD3 (панели А и D), маркера В-клеток В220 (панели В и Е), и маркера NK-клеток CD161a (панели С и F) в мононуклеарных клетках периферической крови (МКПК), полученных от химерной II2rg-/y крысы (панели А-С) и крысы DA ДТ (панели D-F). Двойные положительные клетки показаны в квадранте R8. Фигура 29 иллюстрирует, что II2rg-/y МКПК не экспрессируют зрелые маркеры лимфоцитов.
[00102] Фигура 30 иллюстрирует, что ЗФБ-положительные лимфоциты были выявлены в периферической крови 2 из 3 химер II2rg-/y.
[00103] На Фигуре 31 приведено схематическое изображение локуса крысиного Il2rg и направляющей плазмиды для полной гуманизации локуса крысиного Il2rg. На верхней панели показана геномная структура локуса крысиного Il2rg и когнатных геномных областей, соответствующих 5' и 3' плечам гомологии (4,3 т.п.о. и 4,0 т.п.о., соответственно; темно-серые прямоугольники). Нижняя панель представляет собой направляющую плазмиду. 5' и 3' плечи гомологии (4,3 т.п.о. и 4,0 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. Направляющая плазмида содержит человеческую геномную область IL-2rg и делеционную кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
[00104] На Фигуре 32 приведено схематическое изображение локуса крысиного Il2rg и направляющей плазмиды для гуманизации эктодомена локуса крысиного Il2rg. На верхней панели показана геномная структура локуса крысиного Il2rg и когнатных геномных областей, соответствующих 5' и 3' плечам гомологии (4,3 т.п.о. и 4,0 т.п.о., соответственно; темно-серые прямоугольники). Нижняя панель представляет собой направляющую плазмиду. 5' и 3' плечи гомологии (4,3 т.п.о. и 4,0 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. Направляющая плазмида содержит человеческую эктодоменную геномную область IL-2rg и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит промотор крысиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
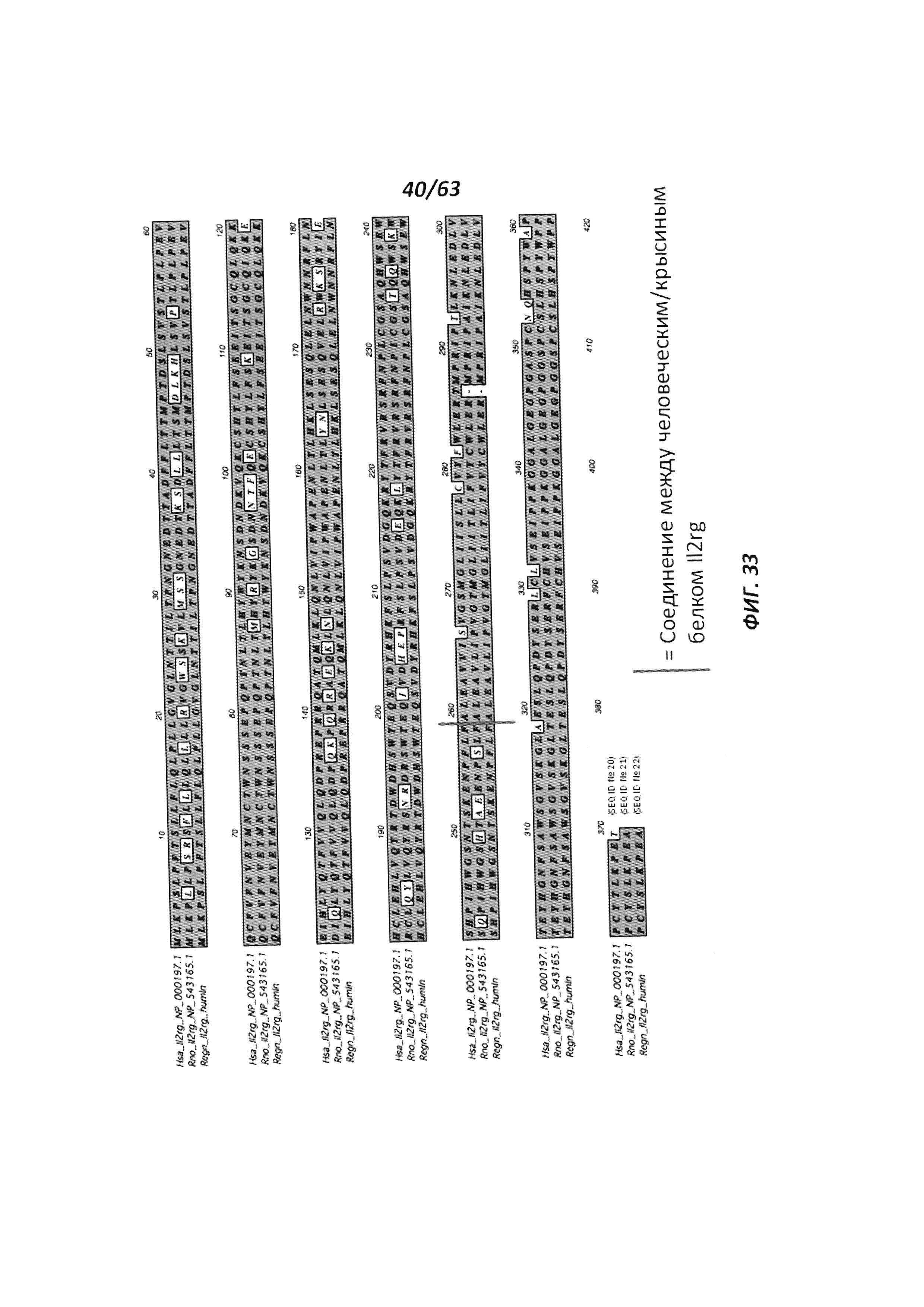
[00105] На Фигуре 33 приведено выравнивание последовательностей белка человеческого IL-2rg (SEQ ID №20; NP_000197.1); белка крысиного IL-2rg (SEQ ID №21; NP_543165.1); и химерного белка IL-2rg (SEQ ID №22), содержащего эктодомен человеческого IL-2rg, слитый с остатком белка крысиного IL-2rg. Место соединения человеческого и крысиного IL-2rg обозначено вертикальной линией.
[00106] На Фигуре 34 приведено схематическое изображение осуществляемой при помощи CRISPR/Cas9 гуманизации гена мышиного Lrp5; LTVEC показан на верхней панели, а локус мышиного Lrp5 показан на нижней панели. Гуманизированная область является эктодоменом. Стрелками указаны целевые сайты для каждой нРНК (gA, gB, gB2, gC, gD, gE2, gE, gF) и ZFN (a-d).
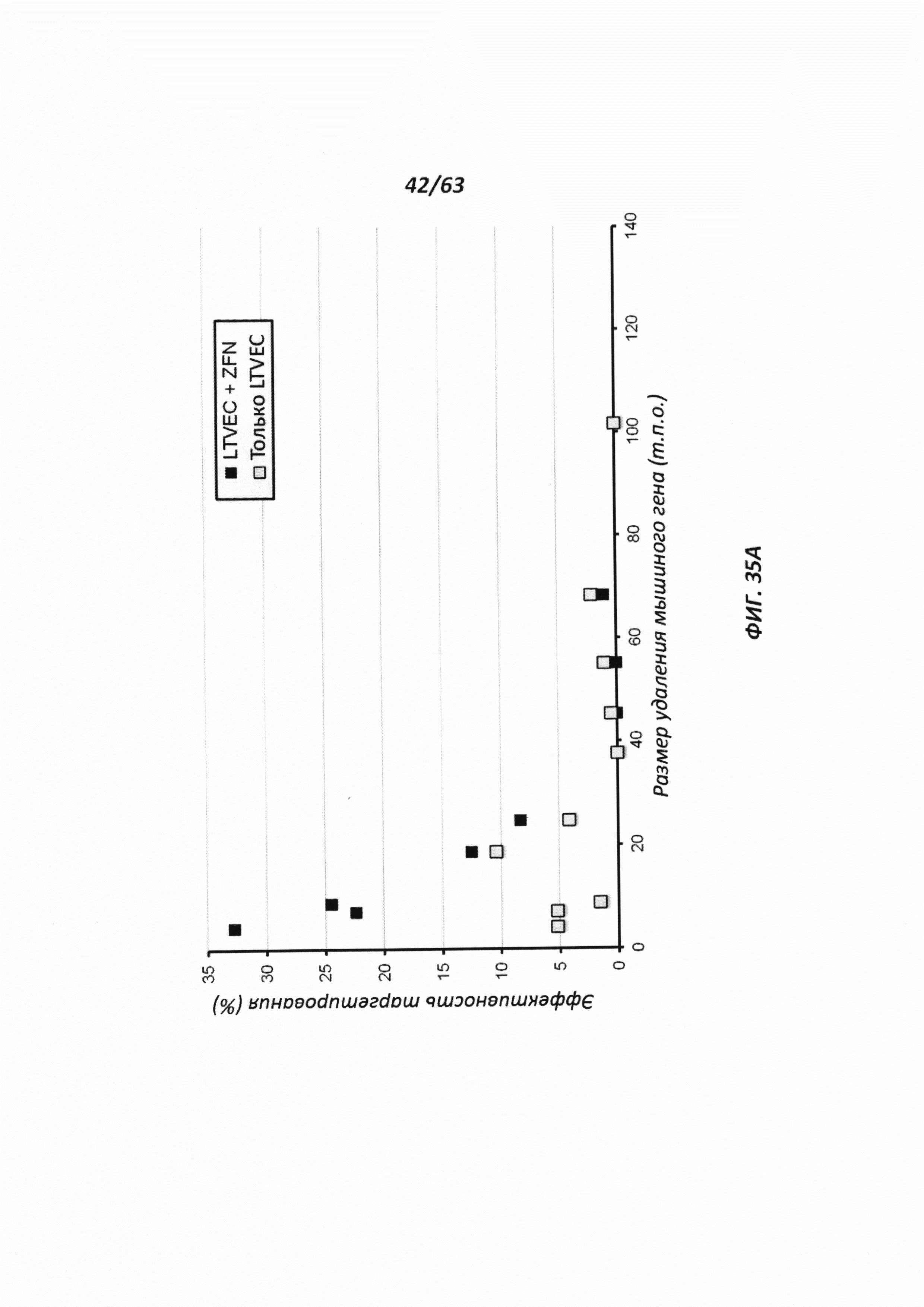
[00107] Фигура 35 иллюстрирует процентную эффективность нацеливания LTVEC, нацеленных на гены с возрастающим размером делеции (Фигура 35А), и LTVEC со вставками человеческих генов возрастающего размера (Фигура 35В). LTVEC применяли одни (серые квадраты или треугольники) или в комбинации с ZFN (черные квадраты или треугольники).
[00108] На Фигуре 36 приведено схематическое изображение осуществляемой при помощи CRISPR/Cas9 гуманизации полной кодирующей области гена мышиного Trpa1, LTVEC показан на верхней панели, а локус мышиного Trpa1 показан на нижней панели. Стрелками указаны целевые сайты для каждой нРНК (gA, gA2, gB, gC, gD, gE2, gE, gF).
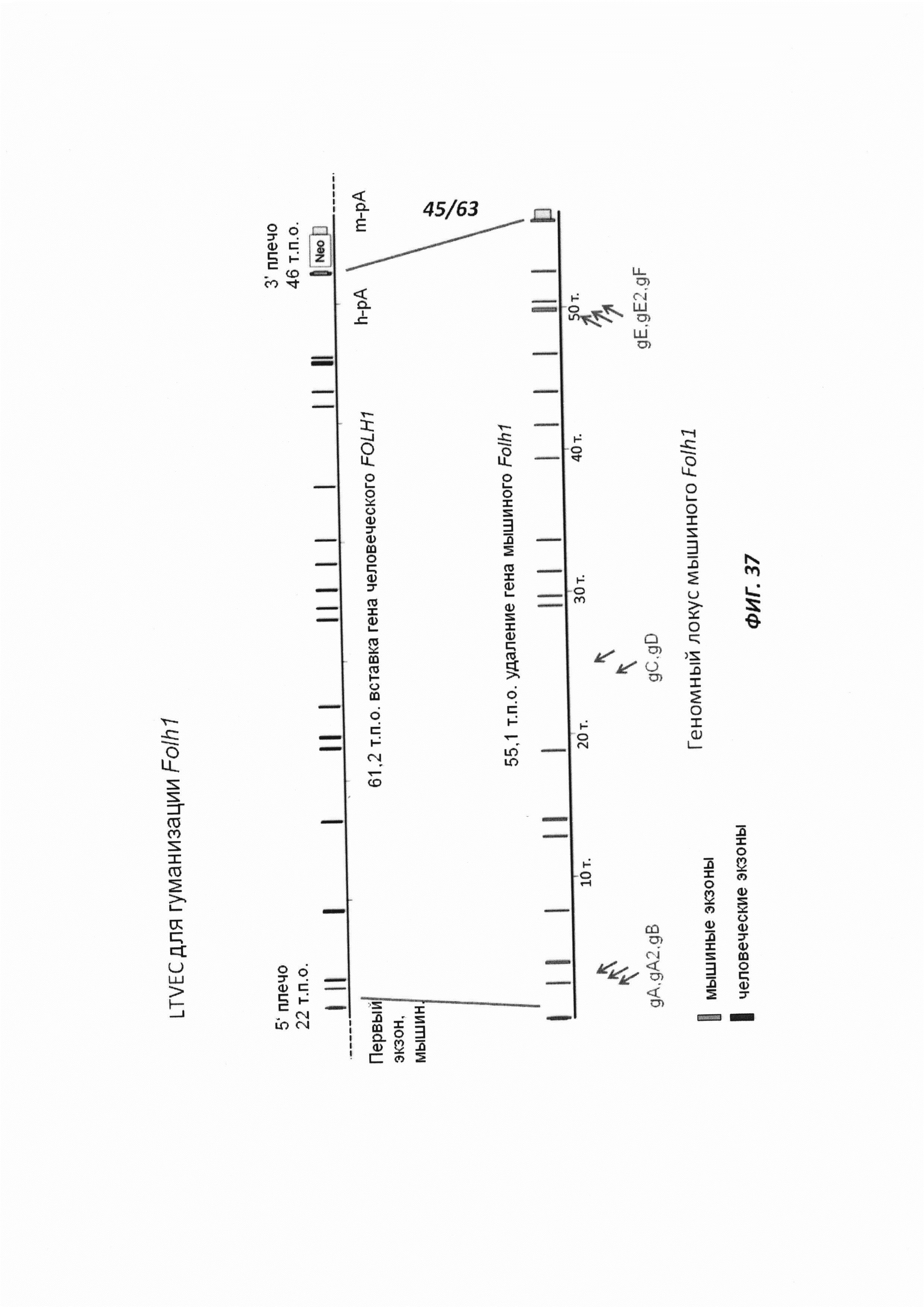
[00109] На Фигуре 37 приведено схематическое изображение осуществляемой при помощи CRISPR/Cas9 гуманизации эктодомена (от экзона 2 до стоп-кодона) гена мышиного Folh1; LTVEC показан на верхней панели, а локус мышиного Folh1 показан на нижней панели. Стрелками указаны целевые сайты для каждой нРНК (gA, gA2, gB, gC, gD, gE, gE2, gF).
[00110] На Фигуре 38 приведено схематическое изображение осуществляемой при помощи CRISPR/Cas9 гуманизации области от экзона 2 до стоп-кодона гена мышиного С5 (Hc); LTVEC показан на верхней панели, а локус мышиного С5 (Hc) показан на нижней панели. Стрелками указаны целевые сайты для каждой нРНК (gA, gB, gB2, gC, gD, gE2, gE, gF).
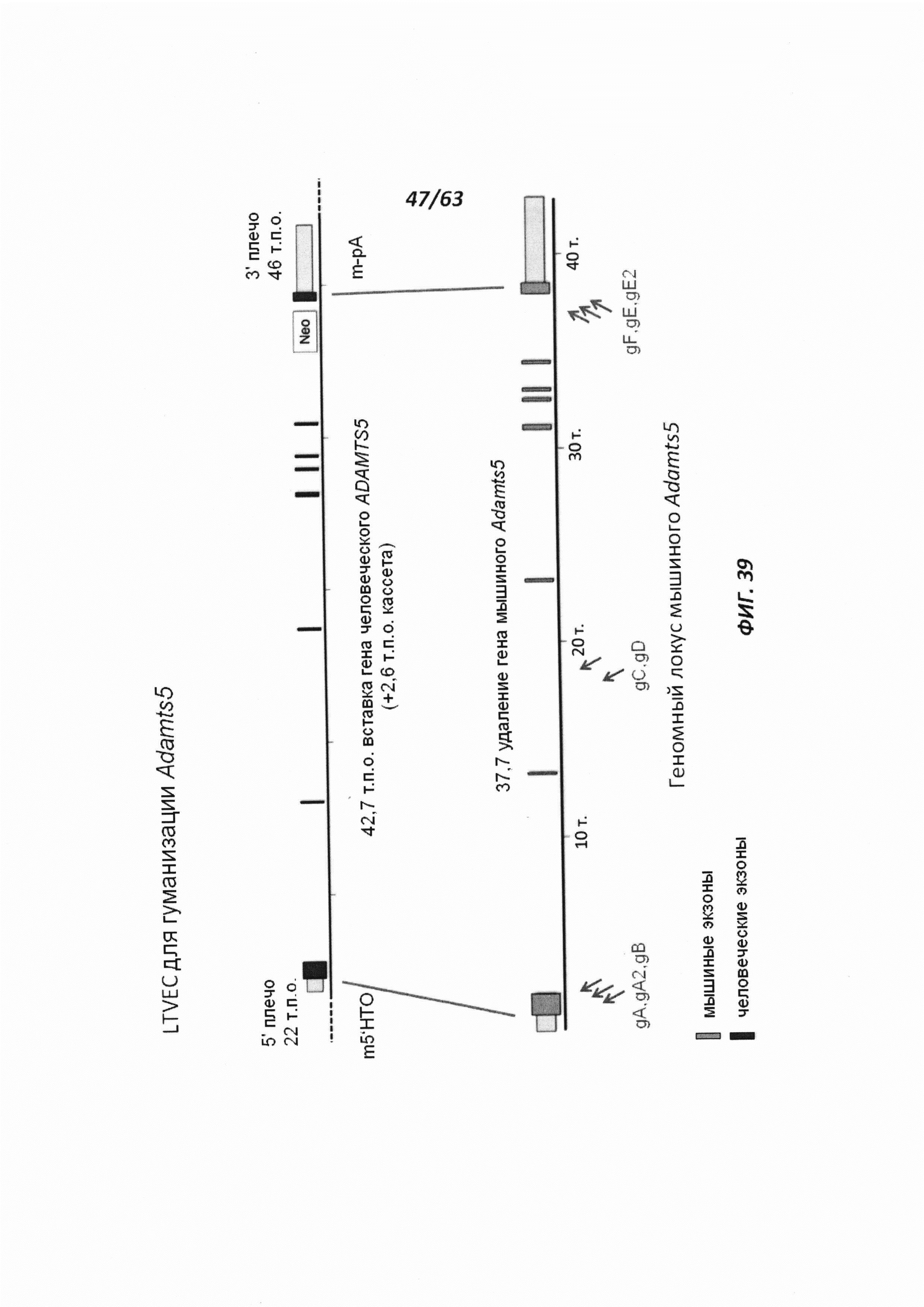
[00111] На Фигуре 39 приведено схематическое изображение осуществляемой при помощи CRISPR/Cas9 гуманизации полной кодирующей области гена мышиного Adamts5; LTVEC показан на верхней панели, а локус мышиного Adamts5 показан на нижней панели. Стрелками указаны целевые сайты для каждой нРНК (gA, gA2, gB, gC, gD, gE2, gE, gF).
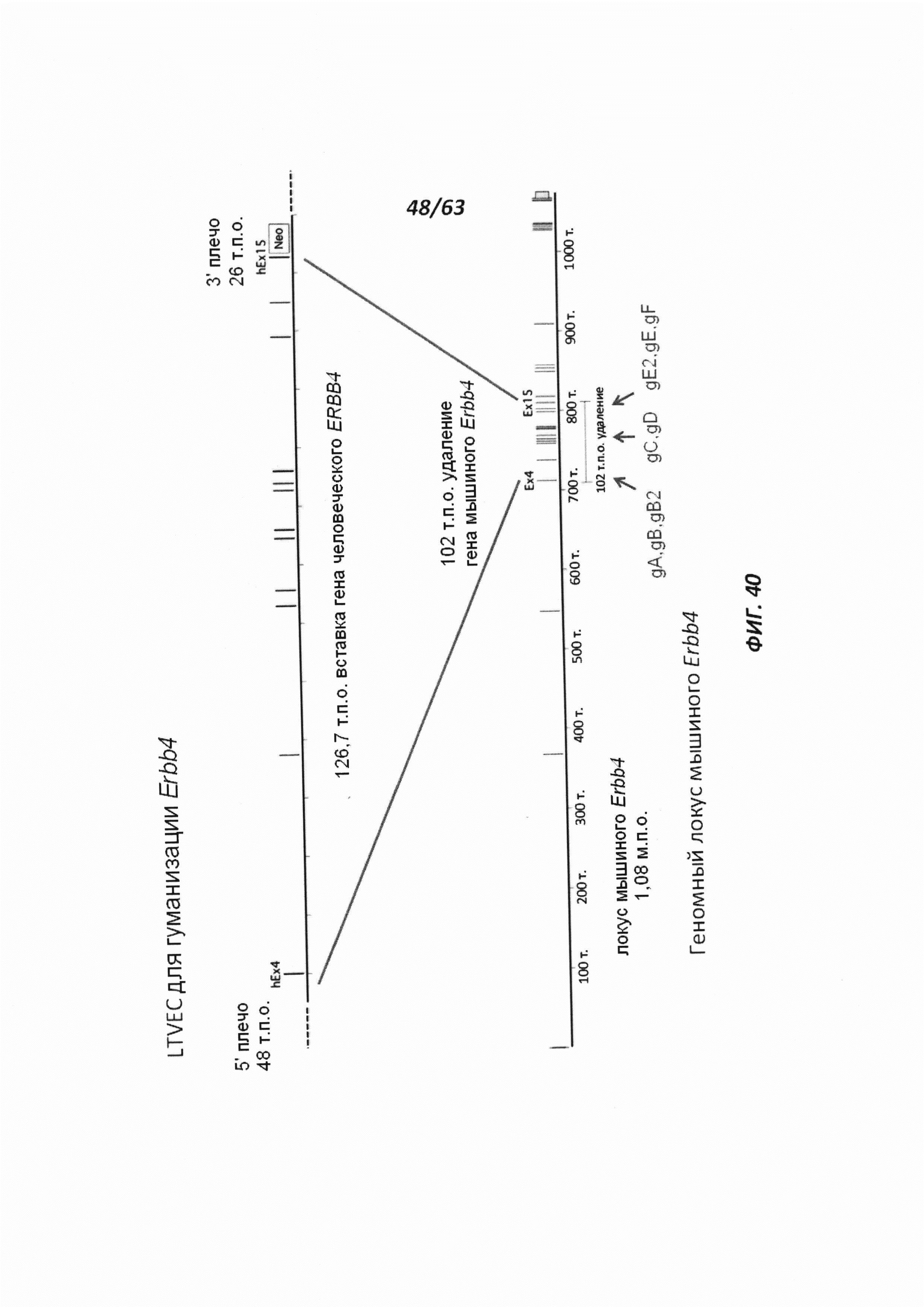
[00112] На Фигуре 40 приведено схематическое изображение осуществляемой при помощи CRISPR/Cas9 гуманизации экзонов 4-15 гена мышиного Erbb4; LTVEC показан на верхней панели, а локус мышиного Erbb4 показан на нижней панели. Стрелками указаны целевые сайты для каждой нРНК (gA, gB, gB2, gC, gD, gE2, gE, gF).
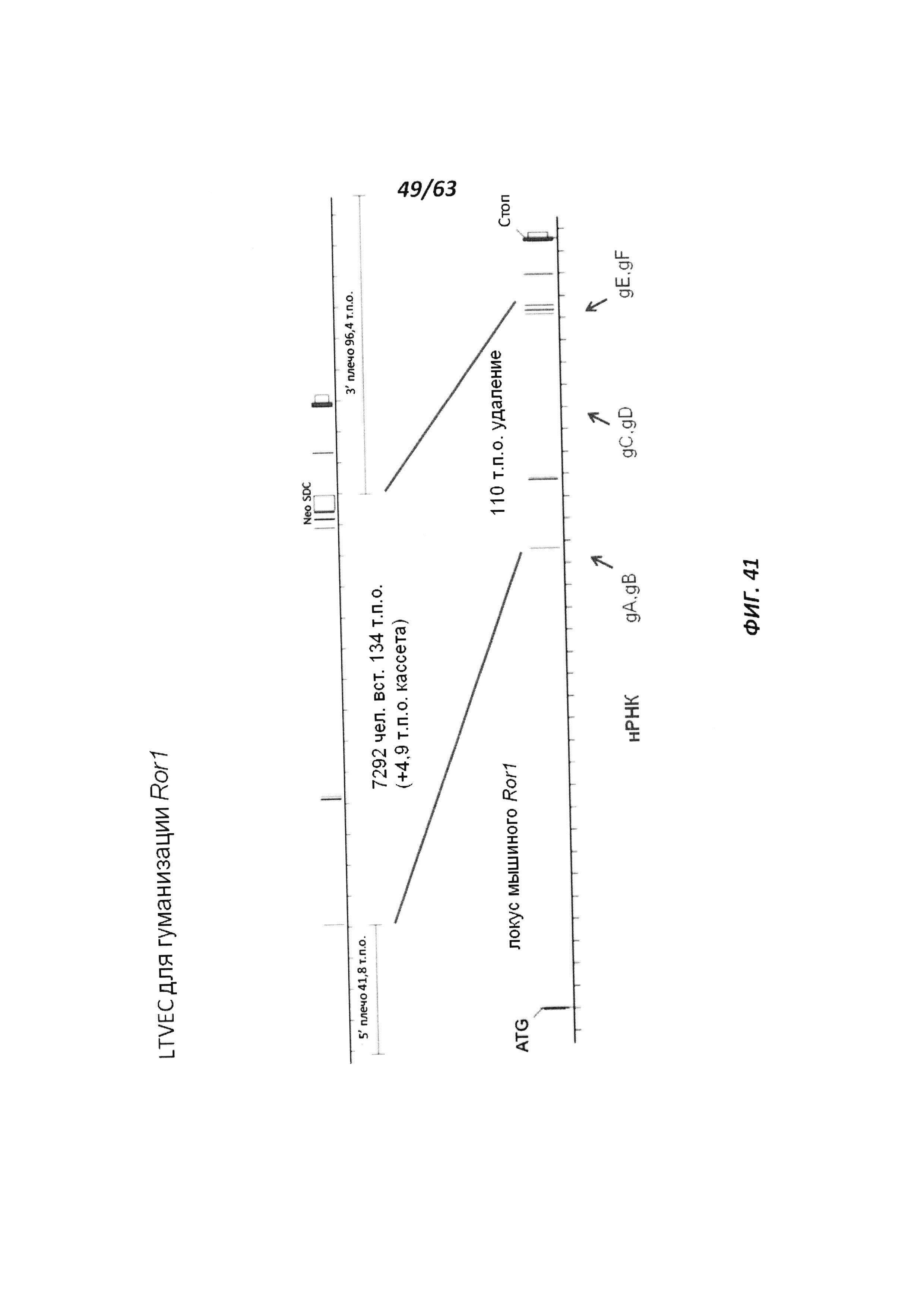
[00113] На Фигуре 41 приведено схематическое изображение осуществляемой при помощи CRISPR/Cas9 гуманизации экзонов 2-7 гена мышиного Ror1; LTVEC показан на верхней панели, а локус мышиного Ror1 показан на нижней панели. Стрелками указаны целевые сайты для каждой нРНК (gA, gB, gC, gD, gE, gF).
[00114] На Фигуре 42 приведено схематическое изображение осуществляемой при помощи CRISPR/Cas9 гуманизации области от экзона 2 до стоп-кодона гена мышиного Dpp4; LTVEC показан на верхней панели, а локус мышиного Dpp4 показан на нижней панели. Стрелками указаны целевые сайты для каждой нРНК (gA, gB, gB2, gC, gD, gE2, gE, gF).
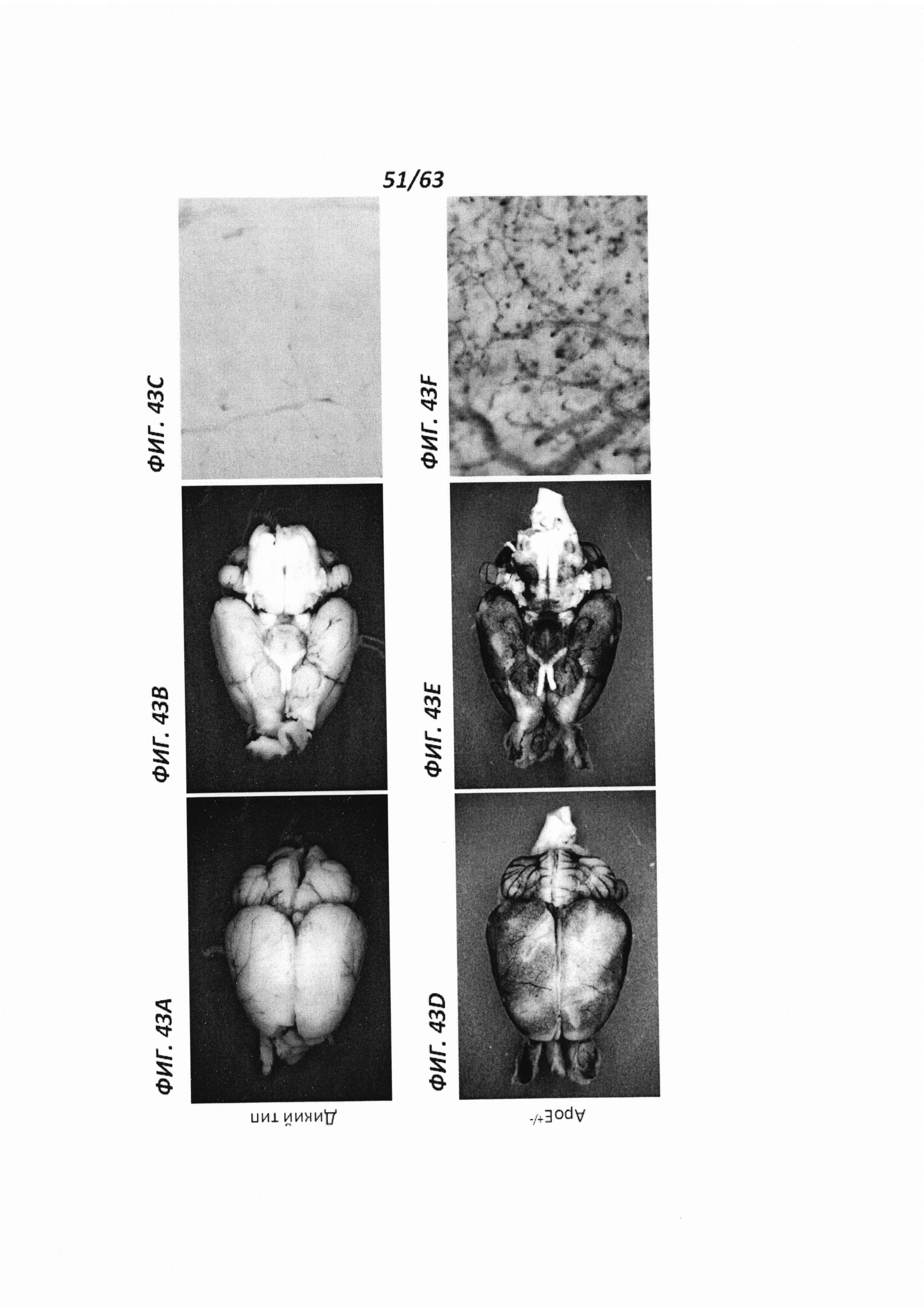
[00115] Фигура 43 иллюстрирует головной мозг 12-месячных самок крыс, окрашенный X-gal. Фигуры 43А-С иллюстрируют мозг крысы дикого типа, а Фигуры 43D-F иллюстрируют мозг крысы АроЕ+/-. Фигуры 43А и D иллюстрируют вид сверху, Фигуры 43В и Е иллюстрируют вид снизу, а Фигуры 43С и F иллюстрируют вид крупным планом.
[00116] Фигура 44 иллюстрирует сердце 12-месячных самок крыс (А и С) и соответствующие кровеносные сосуды крупным планом (В и D), окрашенные X-gal. Фигуры 44А и В иллюстрируют сердце и кровеносные сосуды, соответственно, полученные от крысы дикого типа, и Фигуры 44С и D иллюстрируют сердце и кровеносные сосуды, соответственно, полученные от крысы АроЕ+/-. Окрашивание наблюдали в полости сердца и некоторых сосудах (например, полой вене).
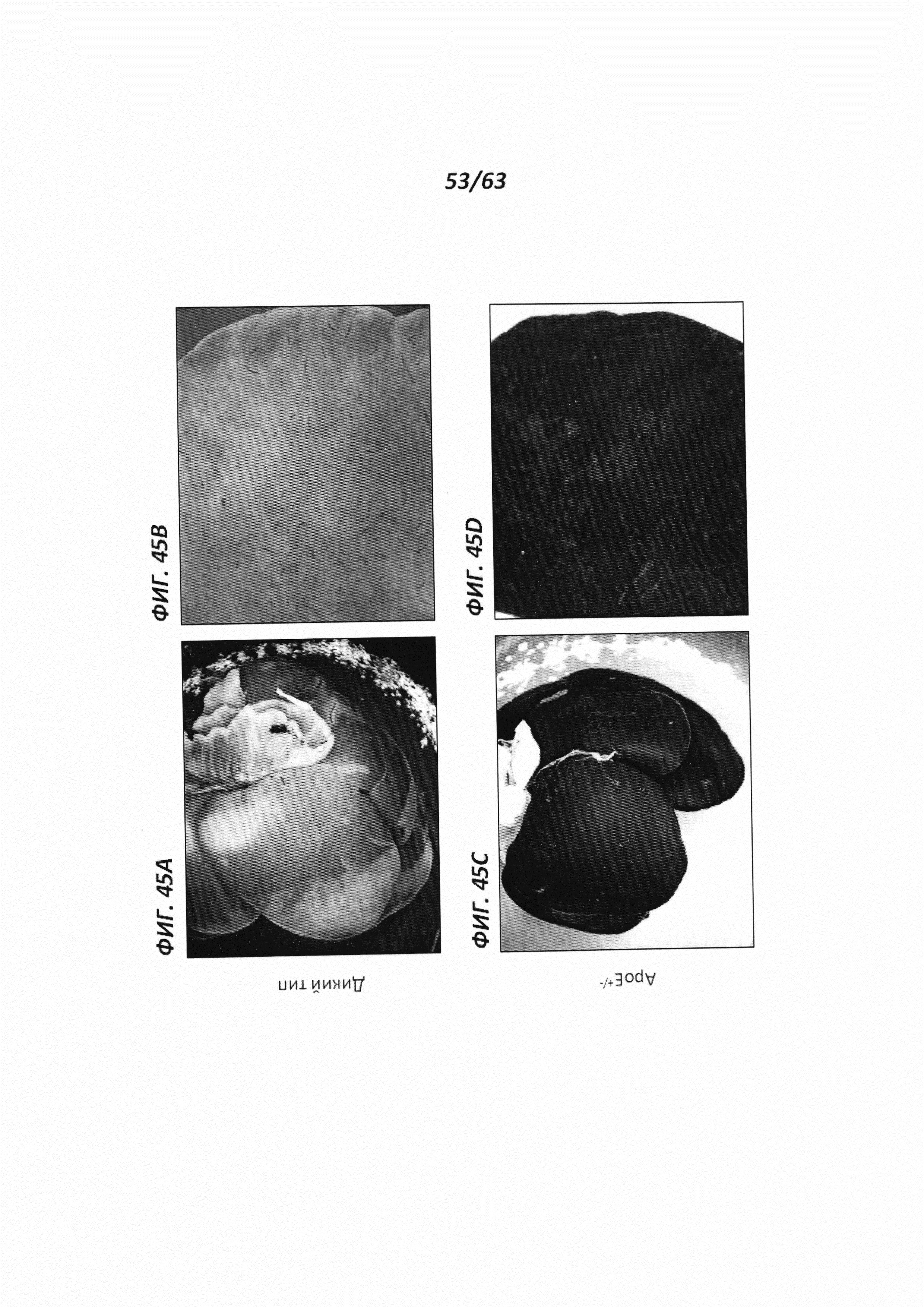
[00117] Фигура 45 иллюстрирует печень 12-месячных самок крыс, окрашенную X-gal. Фигуры 45А и В иллюстрируют печень, полученную от крысы дикого типа, а Фигуры 45С и D иллюстрируют печень крысы АроЕ+/-. На Фигурах 45В и D представлен вид печени крупным планом.
[00118] Фигура 46 иллюстрирует определение уровней холестерина, ЛПНП, ЛПВП и триглицеридов (Фигуры 46A-D, соответственно) у гомозиготных АроЕ-таргетированных крыс, гетерозиготных АроЕ-таргетированных крыс и крыс дикого типа в возрасте 6 недель, 9 недель, 12 недель и 15 недель.
[00119] На Фигуре 47 приведено схематическое изображение локуса крысиного АроЕ (верхняя панель) и крупного направляющего вектора (LTVEC), который нацелен на локус крысиного АроЕ (нижняя панель). На верхней панели показана геномная структура локуса крысиного АроЕ и геномные области, соответствующие 5' и 3' плечам гомологии (45 т.п.о. и 23 т.п.о., соответственно; темно-серые прямоугольники). Экзон 1 АроЕ является некодирующим и показан в виде неокрашенного прямоугольника, расположенного наиболее близко к 5' плечу гомологии. Три интрона в гене АроЕ обозначены в виде линий, а экзоны 2 и 3 содержат кодирующие области и показаны в виде заштрихованных пунктиром серых прямоугольников. Экзон 4 содержит как кодирующие, так и некодирующие последовательности, обозначенные серым пунктиром и неокрашенным прямоугольником. Указаны целевые участки для нРНК2 (SEQ ID №87) и нРНК3 (SEQ ID №88) АроЕ. На нижней панели показан LTVEC для модификации локуса крысиного АроЕ. 5' и 3' плечи гомологии (45 т.п.о, и 23 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. LTVEC содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит промотор мышиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
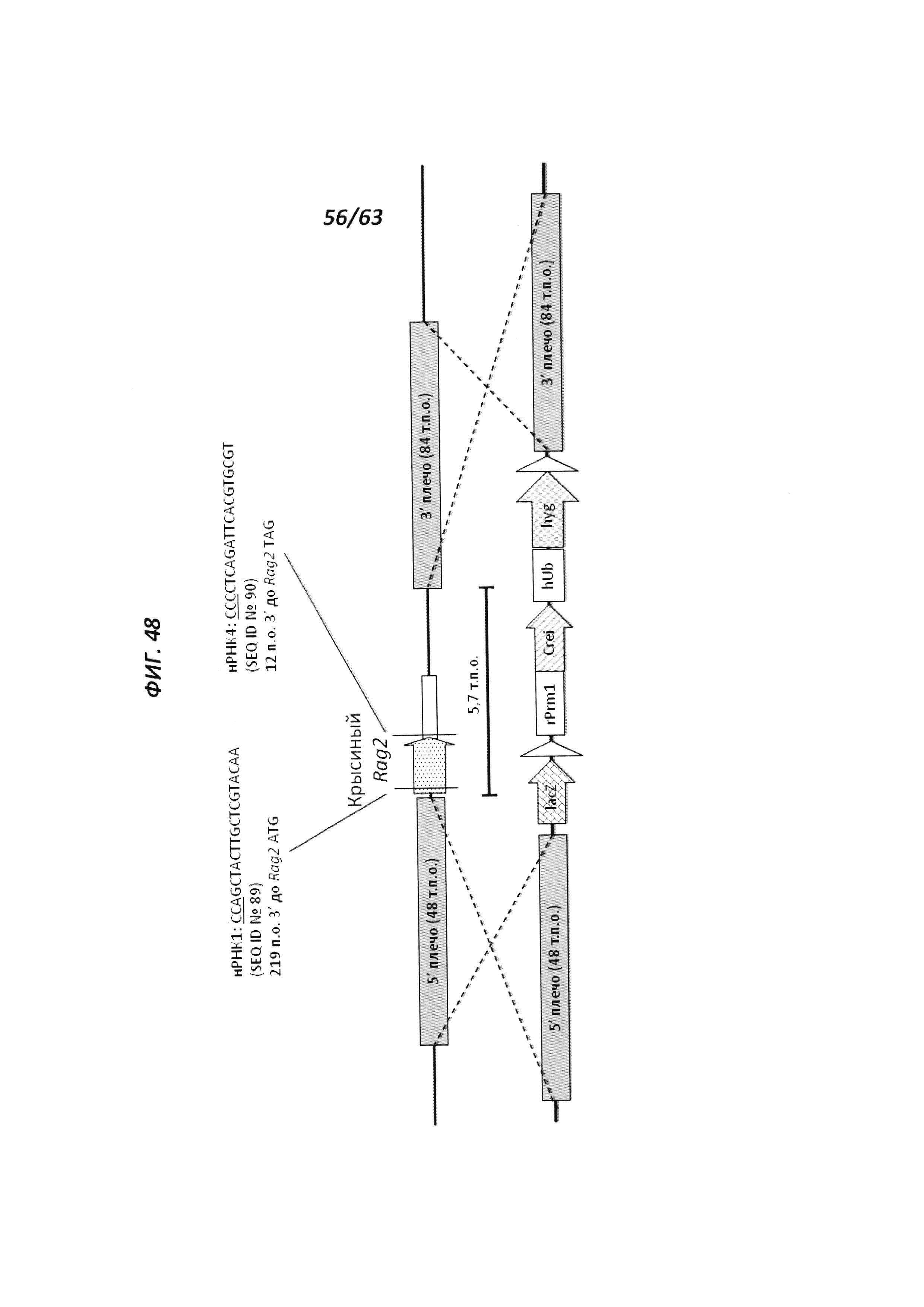
[00120] На Фигуре 48 приведено схематическое изображение локуса крысиного Rag2 (верхняя панель) и крупного направляющего вектора (LTVEC), который нацелен на локус крысиного Rag2 (нижняя панель). На верхней панели показана геномная структура локуса крысиного Rag2 и когнатных геномных областей, соответствующих 5' и 3' плечам гомологии (48 т.п.о. и 84 т.п.о., соответственно; темно-серые прямоугольники). Rag2 содержит один экзон, обозначенный пунктирной серой штриховкой. Rag2 содержит один экзон, обозначенный серым пунктиром. Указаны целевые участки для нРНК1 (SEQ ID №89) и нРНК4 (SEQ ID №90) Rag2. Нижняя панель представляет собой LTVEC. 5' и 3' плечи гомологии (48 т.п.о. и 84 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. LTVEC содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит промотор крысиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
[00121] На Фигуре 49 приведено схематическое изображение локуса крысиного Il2rg (верхняя панель) и направляющей плазмиды для гуманизации эктодомена локуса крысиного Il2rg (нижняя панель). На верхней панели показана геномная структура локуса крысиного Il2rg и когнатных геномных областей, соответствующих 5' и 3' плечам гомологии (4,3 т.п.о. и 4,0 т.п.о., соответственно; темно-серые прямоугольники). Указаны целевые участки для нРНК2 (SEQ ID №891) и нРНК4 (SEQ ID №92) Il2rg. Нижняя панель представляет собой направляющую плазмиду. 5' и 3' плечи гомологии (4,3 т.п.о. и 4,0 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. Направляющая плазмида содержит человеческую эктодоменную геномную область IL-2rg и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит промотор крысиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
[00122] На Фигуре 50 приведено схематическое изображение локусов крысиного Rag2 и Rag1 и крупного направляющего вектора (LTVEC), применяемого для модификации локусов в Il2rg-таргетированных крысиных ЭС клетках (клон Il2rg-CG12). На верхней панели показана геномная структура локусов Rag1 и Rag2 и когнатных геномных областей, соответствующих 5' и 3' плечам гомологии (48 т.п.о. и 15 т.п.о., соответственно; серые прямоугольники). Каждый из Rag2 и Rag1 содержит один экзон, обозначенный неокрашенными стрелками. Нижняя панель представляет собой LTVEC. 5' и 3' плечи гомологии (48 т.п.о. и 15 т.п.о., соответственно) обозначены серыми прямоугольниками. LTVEC содержит репортерный ген (уЗФБ) и ген устойчивости к пуромициру, разделенные участком внутренней посадки рибосомы (IRES) и функционально связанные с промотором актина. LTVEC дополнительно содержит самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит промотор крысиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину.
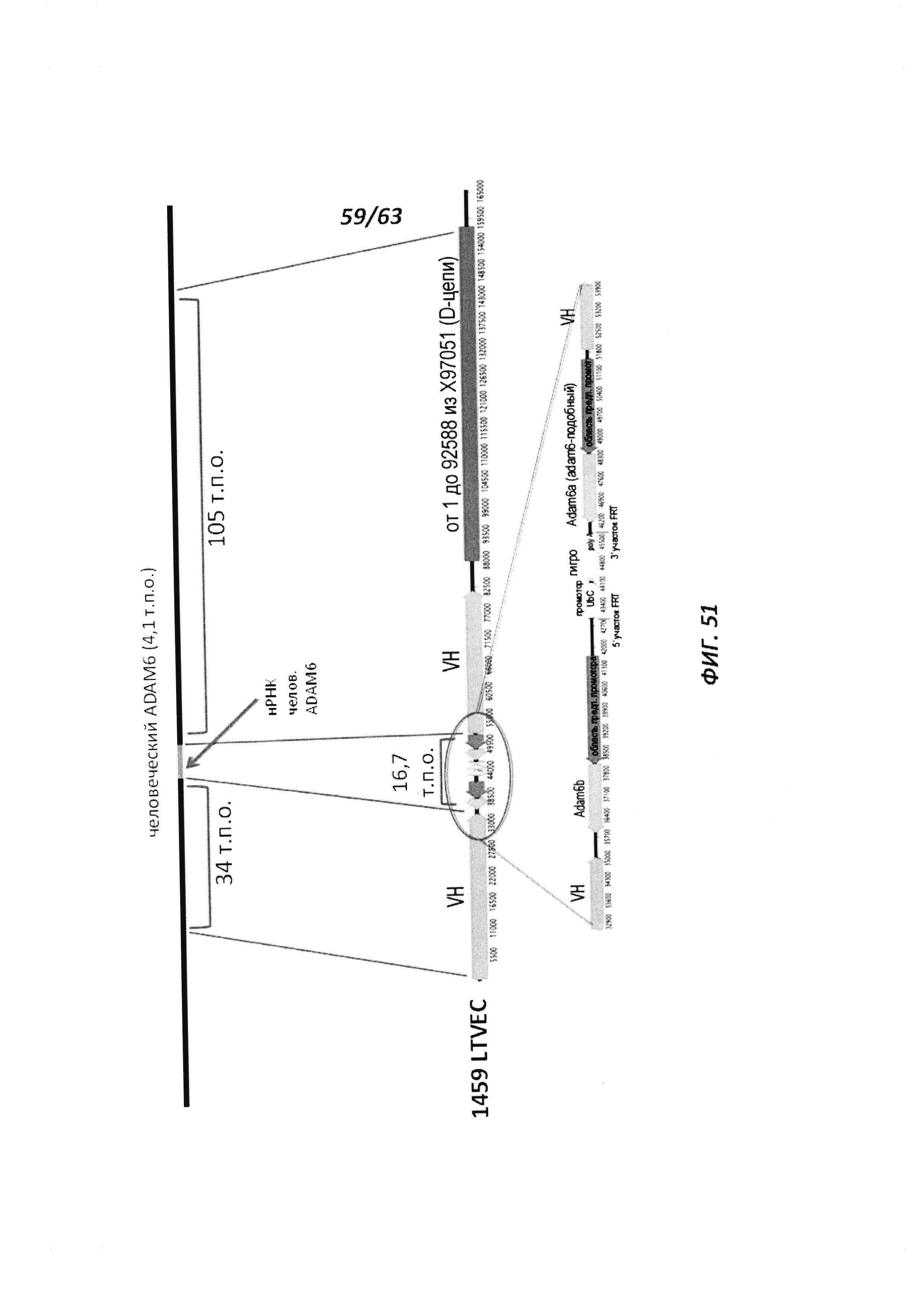
[00123] Фигура 51 иллюстрирует схему замещения части локуса человеческого ADAM6 нуклеиновой кислотой, содержащей локусы мышиных Adam6a и Adam6b, при помощи LTVEC и направляющей РНК в человеческих иПС клетках. Участок-мишень для направляющей РНК обозначен стрелкой.
[00124] Фигура 52А иллюстрирует морфологию, наблюдаемую для человеческих иПС клеток, культивируемых на протяжении 8 дней в среде 2i. Фигура 52В иллюстрирует морфологию, наблюдаемую для человеческих иПС клеток, культивируемых на протяжении 12 дней в среде 2i.
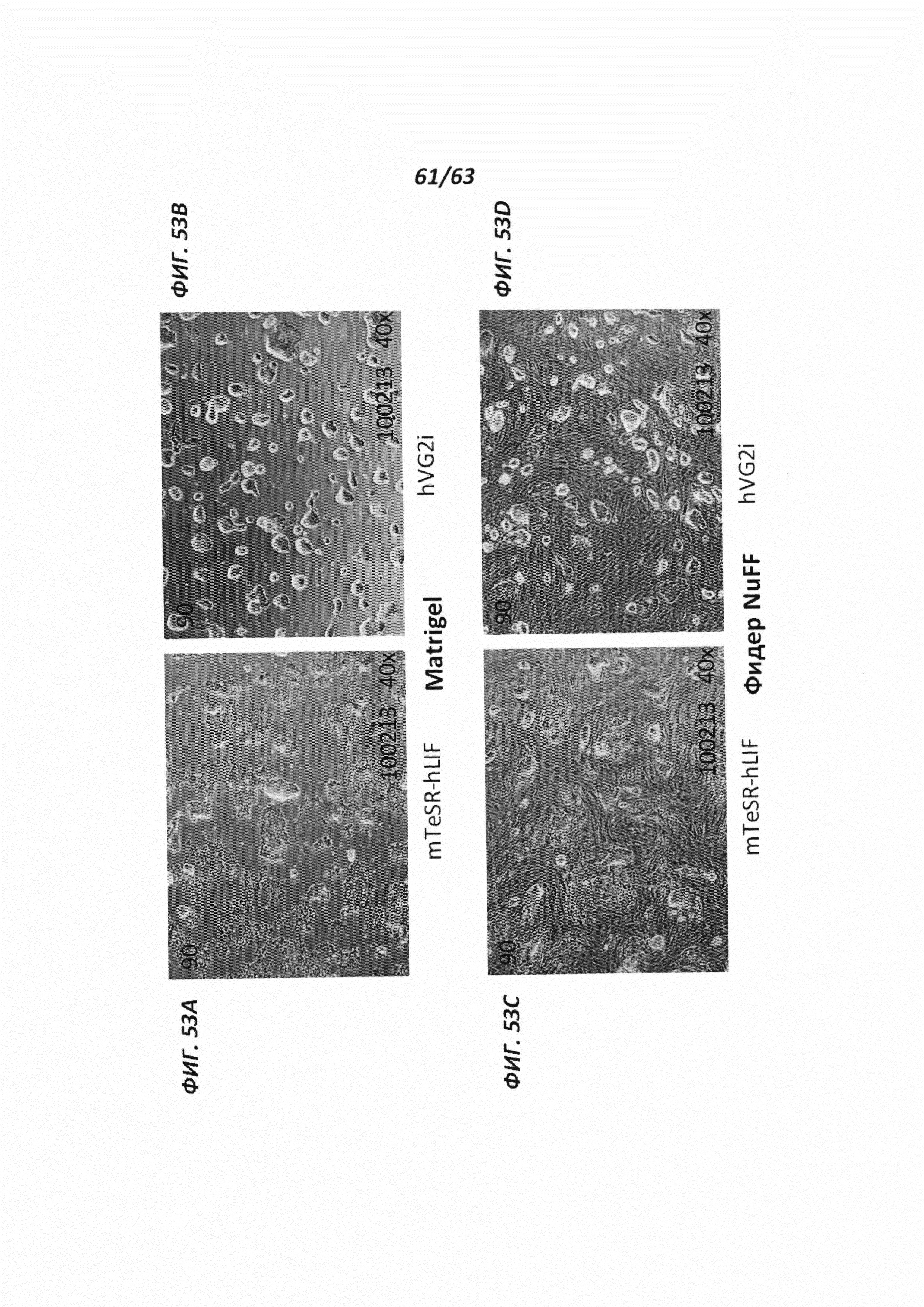
[00125] Фигуры 53A-53D иллюстрируют морфологию, наблюдаемую для человеческих иПС клеток, культивируемых в среде mTeSR™-hLIF или среде VG2i с низкой осмолярностью на протяжении 6 дней. Фигуры 53А и 53В иллюстрируют морфологию, наблюдаемую для человеческих иПС клеток, культивируемых в среде mTeSR™-hLIF (Фигура 3А) или среде VG2i (Фигура 53В) на протяжении 6 дней. Фигуры 53С и 53D иллюстрируют морфологию, наблюдаемую для человеческих иПС клеток, культивируемых на питающих клетках фибробластов крайней плоти новорожденного человека (NuFF) в среде mTeSR™-hLIF (Фигура 53С) или среде VG2i (Фигура 53D) на протяжении 6 дней.
[00126] Фигура 54А иллюстрирует перепрограммированные человеческие иПС клетки, культивируемые в среде VG2i, которые были окрашены в отношении щелочной фосфатазы. Фигуры 54В и 54С иллюстрирует перепрограммированные человеческие иПС клетки, культивируемые в среде VG2i, которые были иммуноокрашены в отношении экспрессии NANOG.
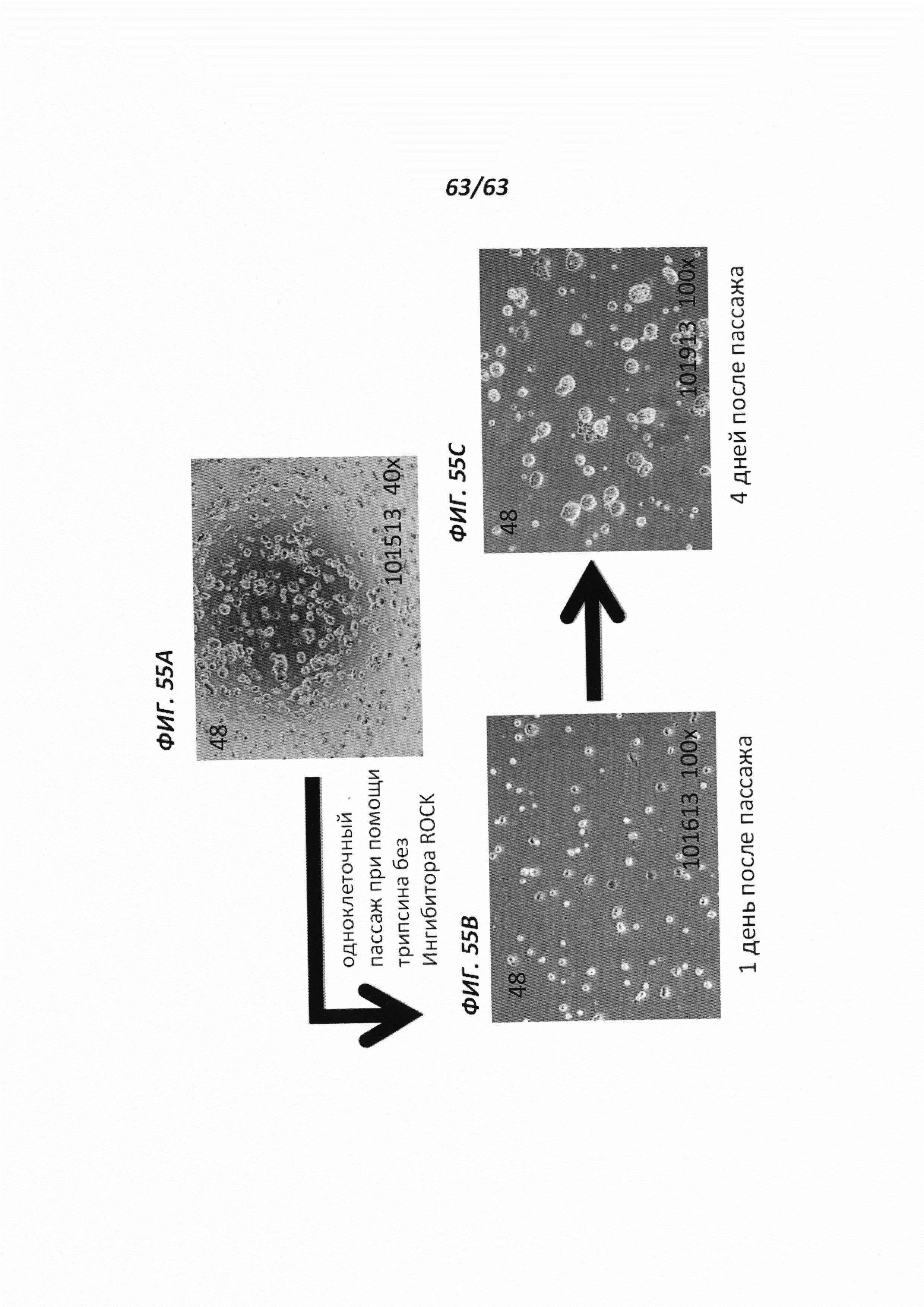
[00127] Фигуры 55А-55С иллюстрируют ферментативную диссоциацию и пересев перепрограммированных человеческих иПС клеток, культивируемых в среде VG2i. Фигура 55А иллюстрирует перепрограммированные человеческие иПС клетки, культивируемые в среде VG2i, до ферментативной диссоциации трипсином в отсутствие ингибитора ROCK. Фигура 55В иллюстрирует человеческие иПС клетки, культивируемые в среде VG2i на протяжении 1 дня после пересева. Фигура 55С иллюстрирует человеческие иПС клетки, культивируемые в среде VG2i на протяжении 4 дней после пересева.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[00128] Предложены композиции и способы для модификации представляющего интерес геномного локуса крысы, эукариотического организма, отличного от крысы эукариотического организма, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка путем бактериальной гомологичной рекомбинации (БГР) в прокариотической клетке. Также предложены композиции и способы для генетической модификации представляющего интерес геномного локуса, например, представляющего интерес геномного локуса крысы, эукариотического организма, отличного от крысы эукариотического организма, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна или мыши при помощи крупного направляющего вектора (LTVEC) в комбинации с эндонуклеазами. Также предложены композиции и способы для получения генетически модифицированного отличного от человека животного, например, крысы, мыши, грызуна, отличного от крысы грызуна, содержащего одну или более направленных генетических модификаций. Также предложены выделенные человеческие и нечеловеческие тотипотентные или плюрипотентные стволовые клетки, в частности, крысиные эмбриональные стволовые клетки, которые способны сохранять плюрипотентность после одной или более серийных генетических модификаций in vitro, и которые способны передавать направленные генетические модификации последующим поколениям через зародышевую линию.
Глоссарий
[00129] Употребляемый в данном документе термин «эмбриональная стволовая клетка» или «ЭС клетка» включает полученную из эмбриона тотипотентную или плюрипотентную клетку, которая способна развиться в любую ткань развивающегося эмбриона после внесения в эмбрион. Употребляемый в данном документе термин «плюрипотентная клетка» включает недифференцированную клетку, которая обладает способностью развиваться в более чем один тип дифференцированных клеток. Термин «неплюрипотентная клетка» включает клетки, которые не являются плюрипотентными клетками.
[00130] Употребляемый в данном документе термин «гомологичная нуклеиновая кислота» включает нуклеотидную последовательность, которая идентична или в значительной степени сходна с известной контрольной последовательностью. В одном варианте реализации изобретения термин «гомологичная нуклеиновая кислота» используют для характеристики последовательности, имеющей аминокислотную последовательность, которая по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или даже 100% идентична с известной контрольной последовательностью.
[00131] Употребляемый в данном документе термин «ортологичная нуклеиновая кислота» включает нуклеотидную последовательность одного вида, которая является функционально эквивалентной известной контрольной последовательности другого вида.
[00132] Употребляемый в данном документе термин «крупный направляющий вектор» или «LTVEC» (от англ. «large targeting vector») включает крупные направляющие векторы для эукариотических клеток, которые получены из фрагментов клонированной геномной ДНК, крупнее тех, которые обычно используются в других подходах для осуществления гомологичного таргетирования генов в эукариотических клетках. Примеры LTVEC включают, но не ограничиваются этим, бактериальную искусственную хромосому (БИХ) и дрожжевую искусственную хромосому (ДИХ).
[00133] Употребляемый в данном документе термин «модификация аллеля» (МОА) включает модификацию конкретной последовательности ДНК из одного аллеля гена(ов) или хромосомного локуса (локусов) в геноме. Описываемые в данном документе примеры «модификации аллеля (МОА)» включают, но не ограничиваются этим, удаления, замены или вставки как минимум одного нуклеотида или удаления многих тысяч пар оснований, составляющих представляющий интерес ген(ы) или хромосомный локус(ы), а также любые и всевозможные вариации между этими двумя крайними значениями.
[00134] Употребляемый в данном документе термин «участок рекомбинации» включает нуклеотидную последовательность, которая распознается сайт-специфической рекомбиназой и которая может служить субстратом для акта рекомбинации.
[00135] «Серийные» генетические модификации включают две или более модификаций, независимо проводимых с клеткой (например, эукариотической клеткой, некрысиной эукариотической клеткой, клеткой млекопитающего, человеческой клеткой, клеткой отличного от человека млекопитающего, плюрипотентной клеткой, неплюрипотентной клеткой, нечеловеческой плюрипотентной клеткой, человеческой плюрипотентной клеткой, человеческой ЭС клеткой, человеческой взрослой стволовой клеткой, человеческой клеткой-предшественником с ограниченным развитием, человеческой иПС клеткой, человеческой клеткой, клеткой грызуна, клеткой отличного от крысы грызуна, крысиной клеткой, мышиной клеткой, клеткой хомяка, фибробластом или клеткой яичников китайского хомяка (СНО)). Первая модификация может быть осуществлена путем электропорации или любым другим известным в данной области техники способом. Затем проводят вторую модификацию того же самого клеточного генома, применяя подходящую вторую нуклеотидную конструкцию. Вторая модификация может быть осуществлена путем второй электропорации или любым другим известным в данной области техники способом. В различных вариантах реализации изобретения после первой и второй генетических модификаций одной и той же клетки, третья, четвертая, пятая, шестая и т.д. серийные генетические модификации (одна за другой) могут быть осуществлены при помощи, например, серийной электропорации или любого другого известного в данной области техники подходящего способа (серийного).
[00136] Употребляемый в данном документе термин «сайт-специфическая рекомбиназа» включает группу ферментов, которые могут облегчать рекомбинацию между «участками рекомбинации», когда два участка рекомбинации физически разделены в пределах одной молекулы нуклеиновой кислоты или находятся на отдельных молекулах нуклеиновых кислот. Примеры «сайт-специфических рекомбиназ» включают, но не ограничиваются этим, рекомбиназы Cre, Flp и Dre.
[00137] Термин «зародышевая линия» в отношении нуклеотидной последовательности включает нуклеотидную последовательность, которая может передаваться потомству.
[00138] Выражение «тяжелая цепь» или «тяжелая цепь иммуноглобулина» включает последовательность тяжелой цепи иммуноглобулина, включая последовательность константной области тяжелой цепи иммуноглобулина, из любого организма. Вариабельные домены тяжелой цепи включают три CDR тяжелой цепи и четыре области FR, если не указано иное. Фрагменты тяжелых цепей включают CDR, CDR и PR и их комбинации. Типовая тяжелая цепь содержит следующие элементы: вариабельный домен (от N-конца до С-конца), домен CH1, шарнирную область, домен CH2 и домен CH3. Функциональный фрагмент тяжелой цепи включает фрагмент, который способен специфически распознавать эпитоп (например, распознавать эпитоп с KД в микромолярном, наномолярном или пикомолярном диапазоне), который способен экспрессироваться и секретироваться из клетки и который содержит по меньшей мере одну CDR. Вариабельные домены тяжелой цепи кодируются нуклеотидной последовательностью вариабельной области, которая в общем случае содержит сегменты VH, DH и JH, полученные из набора сегментов VH, DH и JH, присутствующих в зародышевой линии. Последовательности, местоположение и номенклатуру для сегментов тяжелой цепи V, D и J для различных организмов можно найти в базе данных IMGT, которая доступна через Интернет по адресу (www) с URL «imgt.org».
[00139] Выражение «легкая цепь» включает последовательность легкой цепи иммуноглобулина любого организма и, если не указано иное, включает человеческие каппа (κ) и лямбда (λ) легкие цепи и VpreB, а также суррогатные легкие цепи. Вариабельные домены легкой цепи, как правило, включают три CDR легкой цепи и четыре каркасные области (FR), если не указано иное. В общем случае полноразмерная легкая цепь включает, от амино-конца к карбокси-концу, вариабельный домен, который содержит FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4, и аминокислотную последовательность константной области легкой цепи. Вариабельные домены легкой цепи кодируются нуклеотидной последовательностью вариабельной области легкой цепи, которая в общем случае содержит генные сегменты легкой цепи VL и JL, полученные из набора генных сегментов легкой цепи V и J, присутствующих в зародышевой линии. Последовательности, местоположение и номенклатуру для генных сегментов легкой цепи V и J для различных организмов можно найти в базе данных IMGT, которая доступна через Интернет по адресу (www) с URL «imgt.org». Легкие цепи включают те, которые, например, избирательно не связываются с первым или вторым эпитопом, избирательно связываемым эпитопсвязывающим белком, в котором они находятся. Легкие цепи также включают те, которые связываются и распознают или помогают тяжелой цепи связывать и распознавать один или более эпитопов, избирательно связываемых эпитопсвязывающим белком, в котором они находятся.
[00140] Выражение «функционально связанный» отображает взаимосвязь, в которой функционально связанные компоненты функционируют надлежащим образом. В одном случае нуклеотидная последовательность, кодирующая белок, может быть функционально связана с регуляторными последовательностями (например, промотором, энхансером, последовательностью сайленсера и т.д.) таким образом, чтобы поддерживать надлежащую транскрипционную регуляцию. В одном случае нуклеотидная последовательность вариабельной области иммуноглобулина (или сегментов V(D)J) может быть функционально связана с нуклеотидной последовательностью константной области иммуноглобулина таким образом, чтобы создавать возможность надлежащей рекомбинации между последовательностями в последовательность тяжелой или легкой цепи иммуноглобулина.
1. Целевой локус, содержащий нуклеиновую кислоту
[00141] Предложены различные способы и композиции, которые позволяют осуществлять интеграцию по меньшей мере одной нуклеотидной вставки в целевой локус. В контексте данного документа «представляющий интерес геномный локус» содержит любой сегмент или участок ДНК в пределах генома, в который необходимо интегрировать нуклеотидную вставку. Термины «представляющий интерес геномный локус» и «представляющий интерес целевой геномный локус» можно применять взаимозаменяемо. Представляющий интерес геномный локус может быть нативным по отношению к клетке или, в альтернативном варианте, может содержать гетерологичный или экзогенный сегмент ДНК, который был интегрирован в геном клетки. Такие гетерологичные или экзогенные сегменты ДНК могут включать трансгены, экспрессионные кассеты, полинуклеотид, кодирующий селективные маркеры, или гетерологичные или экзогенные области геномной ДНК. Термин «локус» определен в данном документе как сегмент ДНК в пределах геномной ДНК. Описанные в данном документе генетические модификации могут включать одну или более делеций из представляющего интерес локуса, добавок в представляющий интерес локус, замещение представляющего интерес локуса и/или любые их комбинации. Представляющий интерес локус может содержать кодирующие области или некодирующие регуляторные области.
[00142] Представляющий интерес геномный локус может дополнительно содержать любой компонент системы направленной интеграции, включая, например, участок распознавания, селективный маркер, ранее интегрированную нуклеотидную вставку, полинуклеотиды, кодирующие нуклеазные агенты, промоторы и т.д. В альтернативном варианте представляющий интерес геномный локус может быть расположен во внехромосомной ДНК в пределах клетки, такой как дрожжевая искусственная хромосома (ДИХ), бактериальная искусственная хромосома (БИХ), человеческая искусственная хромосома или любая другая сконструированная геномная область, находящаяся в подходящей клетке-хозяине. В различных вариантах реализации изобретения целевой локус может содержать нативную, гетерологичную или экзогенную нуклеотидную последовательность прокариота, эукариота, отличного от крысы эукариота, дрожжей, бактерий, отличного от человека млекопитающего, нечеловеческой клетки, грызуна, отличного от крысы грызуна, человека, крысы, мыши, хомяка, кролика, свиньи, быка, оленя, овцы, козы, курицы, кошки, собаки, хорька, примата (например, мармозетки, макака-резуса), домашнего млекопитающего или сельскохозяйственного млекопитающего или любого другого представляющего интерес организма или их комбинаций. В некоторых вариантах реализации изобретения представляющий интерес геномный локус содержит нуклеотидную последовательность человека, мыши или их комбинацию.
[00143] В конкретных вариантах реализации изобретения целевой локус получен из, например, эукариотической клетки, некрысиной эукариотической клетки, клетки млекопитающего, человеческой клетки, клетки отличного от человека млекопитающего, плюрипотентной клетки, неплюрипотентной клетки, нечеловеческой плюрипотентной клетки, человеческой плюрипотентной клетки, человеческой ЭС клетки, человеческой взрослой стволовой клетки, человеческой клетки-предшественника с ограниченным развитием, человеческой иПС клетки, человеческой клетки, клетки грызуна, клетки отличного от крысы грызуна, крысиной клетки, мышиной клетки, клетки хомяка, фибробласта или клетки СНО.
[00144] В конкретных вариантах реализации изобретения представляющий интерес геномный локус содержит целевой локус «крысиной нуклеиновой кислоты». Такая область содержит нуклеиновую кислоту крысы, которая интегрирована в геном клетки. Неограничивающие примеры целевых локусов включают геномный локус, который кодирует белок, экспрессируемый в В-клетке, геномный локус, который экспрессирует полипептид в незрелой В-клетке, геномный локус, который экспрессирует полипептид в зрелой В-клетке, локусы иммуноглобулина (Ig) или локусы рецепторов Т-клеток, включая, например, локус альфа рецептора Т-клеток. Дополнительные примеры целевых геномных локусов включают локус Fcer1a, локус Tlr4, локус Prlr, локус Notch4, локус Accn2, локус Adamts5, локус Trpa1, локус Folh1, локус Lrp5, локус рецептора IL2, включая, например, локус рецептора IL2 гамма (Il2rg), локус АроЕ, локус Rag1, локус Rag2, локус Rag1/Rag2 и локус Erbb4. Любой такой целевой локус может быть получен из крысы или может быть получен из эукариотической клетки, некрысиной эукариотической клетки, клетки млекопитающего, человеческой клетки или клетки отличного от человека млекопитающего.
[00145] В одном варианте реализации изобретения целевой локус кодирует аминокислотную последовательность вариабельной области тяжелой цепи иммуноглобулина млекопитающего. В одном варианте реализации изобретения целевой локус кодирует аминокислотную последовательность вариабельной области тяжелой цепи иммуноглобулина крысы. В одном варианте реализации изобретения целевой локус содержит последовательность геномной ДНК, содержащую неперестроенную нуклеотидную последовательность вариабельной области тяжелой цепи иммуноглобулина крысы, мыши или человека, функционально связанную с нуклеотидной последовательностью константной области тяжелой цепи иммуноглобулина. В одном варианте реализации изобретения нуклеотидная последовательность константной области тяжелой цепи иммуноглобулина представляет собой нуклеотидную последовательность константной области тяжелой цепи иммуноглобулина крысы, мыши или человека, выбранную из СН1, шарнирной области, СН2, CH3 и их комбинации. В одном варианте реализации изобретения нуклеотидная последовательность константной области тяжелой цепи содержит СН1-шарнирную область-СН2-СН3. В одном варианте реализации изобретения целевой локус содержит перестроенную нуклеотидную последовательность вариабельной области тяжелой цепи иммуноглобулина крысы, мыши или человека, функционально связанную с нуклеотидной последовательностью константной области тяжелой цепи иммуноглобулина. В одном варианте реализации изобретения нуклеотидная последовательность константной области тяжелой цепи иммуноглобулина представляет собой нуклеотидную последовательность константной области тяжелой цепи иммуноглобулина крысы, мыши или человека, выбранную из СН1, шарнирной области, СН2, СН3 и их комбинации. В одном варианте реализации изобретения нуклеотидная последовательность константной области тяжелой цепи содержит СН1-шарнирную область-СН2-СН3.
[00146] В одном варианте реализации изобретения целевой локус содержит последовательность геномной ДНК, которая кодирует аминокислотную последовательность вариабельной области легкой цепи иммуноглобулина млекопитающего. В одном варианте реализации изобретения последовательность геномной ДНК содержит неперестроенную нуклеотидную последовательность вариабельной области λ и/или κ легкой цепи млекопитающего.
[00147] В одном варианте реализации изобретения последовательность геномной ДНК содержит перестроенную нуклеотидную последовательность вариабельной области λ и/или κ легкой цепи млекопитающего. В одном варианте реализации изобретения перестроенная нуклеотидная последовательность вариабельной области λ или κ легкой цепи функционально связана с нуклеотидной последовательностью константной области легкой цепи иммуноглобулина млекопитающего, выбранной из нуклеотидной последовательности константной области λ легкой цепи и нуклеотидной последовательности константной области κ легкой цепи. В одном варианте реализации изобретения нуклеотидная последовательность константной области легкой цепи иммуноглобулина млекопитающего представляет собой нуклеотидную последовательность константной области легкой цепи иммуноглобулина крысы. В одном варианте реализации изобретения нуклеотидная последовательность константной области легкой цепи иммуноглобулина млекопитающего представляет собой нуклеотидную последовательность константной области легкой цепи иммуноглобулина мыши. В одном варианте реализации изобретения нуклеотидная последовательность константной области легкой цепи иммуноглобулина млекопитающего представляет собой нуклеотидную последовательность константной области легкой цепи иммуноглобулина человека.
[00148] В контексте данного документе локус АроЕ, локус рецептора интерлейкина-2 гамма (Il2rg), локус Rag2, локус Rag1 и/или локус Rag2/Rag1 содержит соответствующие области генома (т.е. генома млекопитающего, генома человека или генома отличного от человека млекопитающего), в котором расположен каждый из этих генов или генных комбинаций. Модификация любого из локуса АроЕ, локуса рецептора интерлейкина-2 гамма (Il2rg), локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 (т.е. локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или комбинированного локуса Rag2/Rag1 млекопитающего, человека или отличного от человека млекопитающего) может включать любое необходимое изменение в заданном локусе. Неограничивающие примеры модификаций в заданном локусе (т.е. локусе млекопитающего, человека или отличного от человека млекопитающего) более подробно обсуждаются ниже.
[00149] Например, в конкретных вариантах реализации изобретения один или более из локуса АроЕ, локуса рецептора интерлейкина-2 гамма (Il2rg), локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 (локуса АроЕ млекопитающего, человека или отличного от человека млекопитающего, локуса рецептора интерлейкина-2 гамма млекопитающего, человека или отличного от человека млекопитающего, локуса Rag2 млекопитающего, человека или отличного от человека млекопитающего и/или локуса Rag2/Rag1) модифицируют так, чтобы активность и/или уровень кодируемого белка АроЕ или белка рецептора интерлейкина-2 гамма, или белка Rag1, или белка Rag2, или комбинации белков Rag1 и Rag2 снижались. В других вариантах реализации изобретения активность белка АроЕ, белка рецептора интерлейкина-2 гамма, белка Rag1 или белка Rag2, или комбинации белков Rag1 и Rag2 отсутствует.
[00150] Под «снижается» подразумевается любое снижение уровня или активности гена/белка, кодируемого в представляющем интерес локусе. Например, снижение активности может включать (1) статистически значимое снижение общего уровня или активности данного белка (т.е. АроЕ, рецептора интерлейкина-2 гамма, Rag2, Rag2 или комбинации Rag1 и Rag2), включая, например, снижение уровня или активности на 0,5%, 1%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 120% или более по сравнению с соответствующим контролем. Способы анализа снижения концентрации и/или активности любого из АроЕ, рецептора интерлейкина-2 гамма, Rag1 и Rag2 известны в данной области техники.
[00151] В других вариантах реализации изобретения один или более из локуса АроЕ млекопитающего, человека или отличного от человека млекопитающего, локуса рецептора интерлейкина-2 гамма млекопитающего, человека или отличного от человека млекопитающего, локуса Rag2 млекопитающего, человека или отличного от человека млекопитающего, локуса Rag1 млекопитающего, человека или отличного от человека млекопитающего и/или локуса Rag2/Rag1 млекопитающего, человека или отличного от человека млекопитающего содержат модификацию, которая приводит к тому, что активность и/или уровень кодируемого полипептида АроЕ, полипептида рецептора интерлейкина-2 гамма, полипептида Rag2, полипептида Rag1 или полипептида Rag1 и Rag2 повышается. Под «повышается» подразумевается любое повышение уровня или активности гена/белка, кодируемого в представляющем интерес локусе. Например, повышение активности может включать (1) статистически значимое повышение общего уровня или активности данного белка (т.е. АроЕ, рецептора интерлейкина-2 гамма, Rag1, Rag2 или Rag1 и Rag2), включая, например, повышение уровня или активности на 0,5%, 1%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 120% или более по сравнению с соответствующим контролем. Способы анализа повышения концентрации и/или активности любого из АроЕ, Rag1, Rag2 и рецептора интерлейкина-2 гамма известны в данной области техники.
[00152] Генетическая модификация локуса АроЕ млекопитающего, человека или отличного от человека млекопитающего, локуса рецептора интерлейкина-2 гамма млекопитающего, человека или отличного от человека млекопитающего, локуса Rag2 млекопитающего, человека или отличного от человека млекопитающего, локуса Rag1 млекопитающего, человека или отличного от человека млекопитающего и/или локуса Rag2/Rag1 млекопитающего, человека или отличного от человека млекопитающего может включать удаление эндогенной нуклеотидной последовательности в геномном локусе, вставку экзогенной нуклеиновой кислоты в геномный локус или их комбинацию. Удаление и/или вставка могут находиться в любом месте заданного локуса, как обсуждается в другом месте данного документа.
[00153] Дополнительные предложенные в данном документе варианты реализации изобретения включают модификацию одного или более из локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 млекопитающего, человека или отличного от человека млекопитающего путем замещения части локуса АроЕ, локуса рецептора интерлейкина-2 гамма (Il2rg), локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 соответствующей гомологичной или ортологичной частью локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 другого организма.
[00154] В других вариантах реализации изобретения модификацию одного или более из локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 осуществляют путем замещения части локуса АроЕ, локуса рецептора интерлейкина-2 гамма (Il2rg), локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 полинуклеотидной вставкой, обладающей по всей своей длине сходством по меньшей мере на 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% с частью локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1, которую она замещает.
[00155] Заданная полинуклеотидная вставка и/или соответствующая удаляемая область локуса может быть кодирующей областью, интроном, экзоном, нетранслируемой областью, регуляторной областью, промотором или энхансером или любой их комбинацией или частью. Кроме того, заданная полинуклеотидная вставка и/или удаляемая область локуса могут, например, быть любой необходимой длины, включая, например, 10-100 нуклеотидов в длину, 100-500 нуклеотидов в длину, 500-1 т.п.о. нуклеотидов в длину, от 1 т.п.о. до 1,5 т.п.о. нуклеотидов в длину, от 1,5 т.п.о. до 2 т.п.о. нуклеотидов в длину, от 2 т.п.о. до 2,5 т.п.о. нуклеотидов в длину, от 2,5 т.п.о. до 3 т.п.о. нуклеотидов в длину, от 3 т.п.о. до 5 т.п.о. нуклеотидов в длину, от 5 т.п.о. до 8 т.п.о. нуклеотидов в длину, от 8 т.п.о. до 10 т.п.о. нуклеотидов в длину или более. В других случаях размер вставки или замещения составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о., от около 350 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 800 т.п.о., от около 800 т.п.о. до 1 м.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о., от около 2,5 м.п.о. до около 2,8 м.п.о., от около 2,8 м.п.о. до около 3 м.п.о. В других вариантах реализации изобретения заданная полинуклеотидная вставка и/или удаляемая область локуса составляет по меньшей мере 100, 200, 300, 400, 500, 600, 700, 800 или 900 нуклеотидов или по меньшей мере 1 т.п.о., 2 т.п.о., 3 т.п.о., 4 т.п.о., 5 т.п.о., 6 т.п.о., 7 т.п.о., 8 т.п.о., 9 т.п.о., 10 т.п.о., 11 т.п.о., 12 т.п.о., 13 т.п.о., 14 т.п.о., 15 т.п.о., 16 т.п.о. или более. В других вариантах реализации изобретения заданная полинуклеотидная вставка и/или удаляемая область локуса составляет по меньшей мере 10 т.п.о., по меньшей 20 т.п.о., по меньшей 30 т.п.о., по меньшей 40 т.п.о., по меньшей 50 т.п.о., по меньшей 60 т.п.о., по меньшей 70 т.п.о., по меньшей 80 т.п.о., по меньшей 90 т.п.о., по меньшей 100 т.п.о., по меньшей 150 т.п.о., по меньшей 200 т.п.о., по меньшей 250 т.п.о. или по меньшей 300 т.п.о. или более.
[00156] Заданная полинуклеотидная вставка может принадлежать любому организму, включая, например, грызуна, отличного от крысы грызуна, крысу, мышь, хомяка, млекопитающее, отличное от человека млекопитающее, эукариота, отличного от крысы эукариота, человека, сельскохозяйственное животное или домашнее животное.
[00157] Как более подробно обсуждается в данном документе, предложены различные способы создания направленных модификаций любого представляющего интерес локуса, включая, например, направленные модификации локуса АроЕ, локуса рецептора интерлейкина-2 гамма (Il2rg), локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1. Дополнительно предложены генетически модифицированные отличные от человека животные, генетически модифицированные отличные от человека млекопитающие, генетически модифицированные отличные от крысы эукариоты, генетически модифицированные неплюрипотентные клетки или генетически модифицированные плюрипотентные клетки (например, плюрипотентная клетка, нечеловеческая плюрипотентная клетка, человеческая плюрипотентная клетка, человеческая ЭС клетка, человеческая взрослая стволовая клетка, человеческая клетка-предшественник с ограниченным развитием или человеческая иПС клетка), которые содержат удаление, вставку, замещение и/или любую их комбинацию в локусе рецептора интерлейкина-2 гамма, в локусе АроЕ, в локусе Rag2, в локусе Rag1 и/или в локусе Rag2/Rag1. Такие генетические модификации (включая те, которые приводят к отсутствию, снижению, повышению или модуляции активности целевого локуса) также способны передаваться через зародышевую линию. В конкретных вариантах реализации изобретения генетические модификации приводят к выключению необходимого целевого локуса. Такие отличные от человека животные находят применение, например, в различных экспериментальных системах, как обсуждается в другом месте данного документа.
[00158] Например, выключение АроЕ (аполипопротеин Е) позволяет получить животную модель для изучения эндотелиальной функции, включая, но не ограничиваясь этим, образование бляшек, транскрипционные изменения (секвенирование методом дробовика полного транскриптома (секвенирование РНК)), и ex vivo функции. АроЕ является важной транспортной молекулой и может переносить липиды, такие как холестерин, через кровоток. АроЕ также может функционировать в нервной системе, например, выводить β-амилоид из мозга. Модификации АроЕ вовлечены в различные патологические состояния, включая, например, атеросклероз, гиперлипидемию и болезнь Альцгеймера. Животные с выключенным АроЕ демонстрируют нарушение выведения липопротеинов из крови и подвержены развитию атеросклероза. Таким образом, животные с выключенным АроЕ обеспечивают животную модель для изучения патологических состояний и/или процессов, таких как, например, эндотелиальная функция, образование бляшек, транскрипционные изменения (секвенирование РНК), гиперлипидемия, атеросклероз и болезнь Альцгеймера. Методы анализа измерения активности АроЕ известны в данной области техники. Например, снижение активности АроЕ можно измерить путем анализа снижения уровней АроЕ в образце крови, полученном от субъекта, методом иммуноанализа, такого как ELISA или иммуноблоттинг. Кроме того, крупный размер крыс облегчает проведение таких анализов и улучшает качество данных.
[00159] RAG1 (активирующий рекомбинацию ген 1) и RAG2 (активирующий рекомбинацию ген 2) представляют собой ферменты, которые являются частью состоящего из многих субъединиц комплекса, обладающего VDJ рекомбинационной активностью, и играют важную роль в перестройке и рекомбинации генов иммуноглобулинов и рецепторов Т-клеток в лимфоцитах. RAG1 и RAG2 индуцируют расщепление двухцепочечной ДНК для облегчения рекомбинации и соединения сегментов генов рецепторов Т-клеток и рецепторов В-клеток (т.е. иммуноглобулинов). Выключение RAG1 и/или RAG2 приводит к потере В-клеток и Т-клеток в организме животного, результатом чего является тяжелый иммунодефицит. Животные с выключенными RAG1 и/или RAG2 находят применение, например, в изучении ксенотрансплантатов (т.е. ксенотрансплантатов человеческих клеток в организме крысы), рака, разработке вакцин, аутоиммунных заболеваний, инфекционных заболевания и болезни «трансплантат против хозяина» (БТПХ). Различные методы анализа измерения активности RAG1 и/или RAG2 известны в данной области техники и включают, например, измерение эффективности рекомбинации или анализ наличия или отсутствия В-клеток и/или Т-клеток в организме субъекта.
[00160] Рецептор IL-2 (IL-2R) экспрессируется на поверхности определенных иммунных клеток и связывается с цитокином интерлейкином-2 (IL-2). IL-2R представляет собой интегральный мембранный белок, содержащий по меньшей мере три отдельных субъединичных цепи, включая альфа-цепь (IL-2Ra, CD25), бета-цепь (IL-2Rb, CD122) и гамма-цепь (IL2-Rg, CD132). Цепь рецептора IL-2 гамма (также называемого IL2r-γ или IL2Rg) представляет собой обыкновенную гамма-цепь, общую для многих рецепторов цитокинов, включая, например, рецепторы IL-2, IL-4, IL-7, IL-9, IL-15 и IL-21. IL-2Rg содержит эктодомен на внешней поверхности клетки, который отвечает за связывание лиганда, трансмембранный домен и внутриклеточный домен, который может взаимодействовать с различными молекулами и индуцировать внутриклеточные пути передачи сигнала. Ген Il2rg находится у млекопитающих в Х-хромосоме, а некоторые мутации гена гамма-цепи у людей могут приводить к Х-сцепленному тяжелому комбинированному иммунодефициту человека (ХТКИД), который характеризуется сильным нарушением функционирования Т-клеток. Кроме того, экто домен гамма-цепи может отделяться от трансмембранного рецептора и высвобождаться в виде растворимого рецептора гамма-цепи. Растворимый рецептор гамма-цепи выявляется в крови субъекта и может выполнять функцию регуляции сигнализации цитокинов.
[00161] В некоторых вариантах реализации изобретения цепь нечеловеческого IL-2Rg замещают цепью человеческого IL2-Rg так, что генетически модифицированное животное экспрессирует цепь полностью человеческого IL-2Rg. В других случаях целесообразно замещать только эктодомен цепи нечеловеческого IL-2Rg эктодоменом цепи человеческого IL-2Rg. В таких случаях полученная в результате гуманизированная цепь IL-2Rg, экспрессируемая в отличном от человека организме, содержит человеческий эктодомен, а оставшаяся часть молекулы принадлежит нативному организму.
[00162] Полноразмерная гуманизация IL-2Rg является целесообразной, так как отличные от человека млекопитающие, содержащие такой модифицированный локус, будут вырабатывать человеческий IL-2Rg. Это даст возможность выявлять человеческий IL-2Rg у отличных от человека млекопитающих при помощи антител, специфических к человеческому IL-2Rg. Эктогуманизация (т.е. замещение эктодомена IL-2Rg отличного от человека млекопитающего эктодоменом человеческого IL-2Rg) приведет к получению полипептида IL-2Rg, который будет связывать лиганды человеческого IL2-Rg, но так как цитоплазматический домен принадлежит отличному от человека млекопитающему, эктогуманизированная форма IL-2Rg также будет взаимодействовать с сигнальным аппаратом отличного от человека млекопитающего.
2. Модификация целевого локуса
А. Направляющие векторы и нуклеотидные вставки
i. Нуклеотидная вставка
[00163] В контексте данного документа «нуклеотидная вставка» включает сегмент ДНК, который необходимо интегрировать в целевой локус. В одном варианте реализации изобретения нуклеотидная вставка содержит один или более представляющих интерес полинуклеотидов, В других вариантах реализации изобретения нуклеотидная вставка может содержать одну или более экспрессионных кассет. Данная экспрессионная кассета может содержать представляющий интерес полинуклеотид, полинуклеотид, кодирующий селективный маркер и/или репортерный ген, наряду с различными регуляторными компонентами, которые влияют на экспрессию. Неограничивающие примеры представляющих интерес полинуклеотидов, селективных маркеров и репортерных генов, которые могут быть включены в нуклеотидную вставку, более подробно обсуждаются в другом месте данного документа.
[00164] В конкретных вариантах реализации изобретения нуклеотидная вставка может содержать нуклеиновую кислоту крысы, которая может содержать сегмент геномной ДНК, кДНК, регуляторную область или любую их часть или комбинацию. В других вариантах реализации изобретения нуклеотидная вставка может содержать нуклеиновую кислоту эукариота, отличного от крысы эукариота, млекопитающего, человека, отличного от человека млекопитающего, грызуна, отличного от крысы грызуна, человека, крысы, мыши, хомяка, кролика, свиньи, быка, оленя, овцы, козы, курицы, кошки, собаки, хорька, примата (например, мармозетки, макака-резуса), домашнего млекопитающего или сельскохозяйственного млекопитающего или любого другого представляющего интерес организма. Как более детально указано в данном документе, нуклеотидная вставка, применяемая в различных способах и композициях, может приводить к «гуманизации» представляющего интерес целевого локуса.
[00165] В одном варианте реализации изобретения нуклеотидная вставка содержит включенный аллель по меньшей мере одного экзона эндогенного гена. В одном варианте реализации изобретения нуклеотидная вставка содержит включенный аллель целого эндогенного гена (т.е. «включенную генную замену»).
[00166] В одном варианте реализации изобретения нуклеотидная вставка содержит регуляторный элемент, включая, например, промотор, энхансер или транскрипционный репрессорсвязывающий элемент.
[00167] В дополнительных вариантах реализации изобретения нуклеотидная вставка содержит кондициональный аллель. В одном варианте реализации изобретения кондициональный аллель представляет собой мультифункциональный аллель, описанный в US 2011/0104799, которая в полном объеме включена посредством ссылки. В конкретных вариантах реализации изобретения кондициональный аллель содержит: (а) инициирующую последовательность в смысловой ориентации по отношению к транскрипции целевого гена и кассету отбора по чувствительности к лекарственному препарату в смысловой или антисмысловой ориентации; (b) представляющую интерес нуклеотидную последовательность (NSI) и кондициональный компонент, представленный инверсионным модулем (COIN, в котором используется разделяющий экзоны интрон и инвертируемый подобный генной ловушке модуль; смотрите, например, US 2011/0104799, которая в полном объеме включена посредством ссылки); и (с) рекомбинируемые единицы, которые рекомбинируют после воздействия первой рекомбиназой с образованием кондиционального аллеля, (i) в котором отсутствует инициирующая последовательность и DSC, и (ii) и который содержит NSI в смысловой ориентации и COIN в антисмысловой ориентации.
[00168] Диапазон нуклеотидной вставки составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.
[00169] В одном варианте реализации изобретения нуклеотидная вставка содержит удаление последовательности геномной ДНК, например, эукариотической клетки, некрысиной эукариотической клетки, клетки млекопитающего, человеческой клетки или клетки отличного от человека млекопитающего, в диапазоне от около 1 т.п.о. до около 200 т.п.о., от около 2 т.п.о. до около 20 т.п.о. или от около 0.5 т.п.о. до около 3 м.п.о. В одном варианте реализации изобретения размер удаления последовательности геномной ДНК превышает общую длину 5' плеча гомологии и 3' плеча гомологии. В одном варианте реализации изобретения размер удаления последовательности геномной ДНК соответствует диапазону от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 20 т.п.о. до около 30 т.п.о., от около 30 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 50 т.п.о., от около 50 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 70 т.п.о., от около 70 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 90 т.п.о., от около 90 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 110 т.п.о., от около 110 т.п.о. до около 120 т.п.о., от около 120 т.п.о. до около 130 т.п.о., от около 130 т.п.о. до около 140 т.п.о., от около 140 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 160 т.п.о., от около 160 т.п.о. до около 170 т.п.о., от около 170 т.п.о. до около 180 т.п.о., от около 180 т.п.о. до около 190 т.п.о., от около 190 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о., от около 350 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 800 т.п.о., от около 800 т.п.о. до 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о., до около 2,5 м.п.о., от около 2,5 м.п.о. до около 2,8 м.п.о., от около 2,8 м.п.о. до около 3 м.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.
[00170] В одном варианте реализации изобретения нуклеотидная вставка содержит вставку или замещение нуклеотидной последовательности эукариота, отличного от крысы эукариота, млекопитающего, человека или отличного от человека млекопитающего гомологичной или ортологичной человеческой нуклеотидной последовательностью. В одном варианте реализации изобретения нуклеотидная вставка содержит вставку или замещение последовательности ДНК гомологичной или ортологичной человеческой нуклеотидной последовательностью в эндогенном локусе, который содержит соответствующую последовательность ДНК.
[00171] В одном варианте реализации изобретения генетическая модификация представляет собой добавление нуклеотидной последовательности. В одном варианте реализации изобретения длина добавляемой нуклеотидной последовательности соответствует диапазону от 5 т.п.о. до 200 т.п.о.
[00172] В одном варианте реализации изобретения нуклеотидная вставка содержит генетическую модификацию в кодирующей последовательности. В одном варианте реализации изобретения генетическая модификация включает делеционную мутацию в кодирующей последовательности. В одном варианте реализации изобретения генетическая модификация включает слияние двух эндогенных кодирующих последовательностей.
В одном варианте реализации изобретения нуклеотидная вставка содержит вставку или замещение нуклеотидной последовательности эукариота, отличного от крысы эукариота, млекопитающего, человека или отличного от человека млекопитающего гомологичной или ортологичной человеческой нуклеотидной последовательностью. В одном варианте реализации изобретения нуклеотидная вставка содержит вставку или замещение последовательности ДНК гомологичной или ортологичной человеческой нуклеотидной последовательностью в эндогенном крысином локусе, который содержит соответствующую крысиную последовательность ДНК.
[00173] В одном варианте реализации изобретения генетическая модификация включает удаление не кодирующей белок последовательности, но не включает удаление кодирующей белок последовательности. В одном варианте реализации изобретения удаление не кодирующей белок последовательности включает удаление регуляторного элемента. В одном варианте реализации изобретения генетическая модификация включает удаление промотора. В одном варианте реализации изобретения генетическая модификация включает добавление промотора или регуляторного элемента. В одном варианте реализации изобретения генетическая модификация включает замещение промотора или регуляторного элемента.
[00174] В одном варианте реализации изобретения нуклеотидная последовательность направляющего вектора может содержать полинуклеотид, который после интеграции в геном будет обеспечивать генетическую модификацию области локуса АроЕ млекопитающего, человека или отличного от человека млекопитающего, при этом генетическая модификация в локусе АроЕ приводит к снижению активности АроЕ, повышению активности АроЕ или модуляции активности АроЕ. В одном варианте реализации изобретения происходит выключение АроЕ (создание «нулевого аллеля»).
[00175] В одном варианте реализации изобретения нуклеотидная последовательность направляющего вектора может содержать полинуклеотид, который после интеграции в геном будет обеспечивать генетическую модификацию области локуса рецептора интерлейкина-2 млекопитающего, человека или отличного от человека млекопитающего, при этом генетическая модификация в локусе рецептора интерлейкина-2 приводит к снижению активности рецептора интерлейкина-2. В одном варианте реализации изобретения происходит выключение рецептора интерлейкина-2 (создание «нулевого аллеля»).
[00176] В дополнительных вариантах реализации изобретения нуклеотидная вставка приводит к замещению части локуса АроЕ, локуса рецептора интерлейкина-2 гамма и/или локуса Rag2, и/или локуса Rag1, и/или локуса Rag2/Rag1 млекопитающего, человека или отличного от человека млекопитающего соответствующей гомологичной или ортологичной частью локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 другого организма.
[00177] В других вариантах реализации изобретения нуклеотидная вставка содержит полинуклеотид, обладающий по всей своей длине сходством по меньшей мере на 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% с частью локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1, которую он замещает.
[00178] Заданная пол и нуклеотидная вставка и соответствующая заменяемая область локуса млекопитающего, человека или отличного от человека млекопитающего может быть кодирующей областью, интроном, экзоном, нетранслируемой областью, регуляторной областью, промотором или энхансером или любой их комбинацией. Кроме того, заданная полинуклеотидная вставка и/или удаляемая область локуса млекопитающего, человека или отличного от человека млекопитающего могут быть любой необходимой длины, включая, например, 10-100 нуклеотидов в длину, 100-500 нуклеотидов в длину, 500-1 т.п.о. нуклеотидов в длину, от 1 т.п.о. до 1,5 т.п.о. нуклеотидов в длину, от 1,5 т.п.о, до 2 т.п.о. нуклеотидов в длину, от 2 т.п.о. до 2,5 т.п.о. нуклеотидов в длину, от 2,5 т.п.о. до 3 т.п.о. нуклеотидов в длину, от 3 т.п.о. до 5 т.п.о. нуклеотидов в длину, от 5 т.п.о. до 8 т.п.о. нуклеотидов в длину, от 8 т.п.о. до 10 т.п.о. нуклеотидов в длину или более. В других случаях размер вставки или замещения составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о., от около 350 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 800 т.п.о., от около 800 т.п.о. до 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о., до около 2,5 м.п.о., от около 2,5 м.п.о. до около 2,8 м.п.о., от около 2,8 м.п.о. до около 3 м.п.о. В других вариантах реализации изобретения заданная полинуклеотидная вставка и/или удаляемая область локуса млекопитающего, человека или отличного от человека млекопитающего составляет по меньшей мере 100, 200, 300, 400, 500, 600, 700, 800 или 900 нуклеотидов или по меньшей мере 1 т.п.о., 2 т.п.о., 3 т.п.о., 4 т.п.о., 5 т.п.о., 6 т.п.о., 7 т.п.о., 8 т.п.о., 9 т.п.о., 10 т.п.о., 11 т.п.о., 12 т.п.о., 13 т.п.о., 14 т.п.о., 15 т.п.о., 16 т.п.о. или более.
[00179] В одном варианте реализации изобретения промотор является конститутивно активным промотором.
[00180] В одном варианте реализации изобретения промотор является индуцибельным промотором. В одном варианте реализации изобретения индуцибельный промотор является химически регулируемым промотором. В одном варианте реализации изобретения химически регулируемый промотор является алкоголь-регулируемым промотором. В одном варианте реализации изобретения алкоголь-регулируемый промотор является промотором гена алкогольдегидрогеназы (alcA). В одном варианте реализации изобретения химически регулируемый промотор является тетрациклин-регулируемым промотором. В одном варианте реализации изобретения тетрациклин-регулируемый промотор является чувствительным к тетрациклину промотором. В одном варианте реализации изобретения тетрациклин-регулируемый промотор является последовательностью оператора тетрациклина (tetO). В одном варианте реализации изобретения тетрациклин-регулируемый промотор является промотором tet-On. В одном варианте реализации изобретения тетрациклин-регулируемый промотор является промотором tet-Off. В одном варианте реализации изобретения химически регулируемый промотор является стероид-регулируемым промотором. В одном варианте реализации изобретения стероид-регулируемый промотор является промотором крысиного глюкокортикоидного рецептора. В одном варианте реализации изобретения стероид-регулируемый промотор является промотором рецептора эстрогена. В одном варианте реализации изобретения стероид-регулируемый промотор является промотором рецептора экдизона. В одном варианте реализации изобретения химически регулируемый промотор является металл-регулируемым промотором. В одном варианте реализации изобретения металл-регулируемый промотор является промотором металлопротеина. В одном варианте реализации изобретения индуцибельный промотор является физически регулируемым промотором. В одном варианте реализации изобретения физически регулируемый промотор является температур но регулируемым промотором. В одном варианте реализации изобретения температурно регулируемый промотор является промотором теплового шока. В одном варианте реализации изобретения физически регулируемый промотор является фоторегулируемым промотором. В одном варианте реализации изобретения фоторегулируемый промотор является фотоиндуцибельным промотором. В одном варианте реализации изобретения фоторегулируемый промотор является фоторепрессируемым промотором.
[00181] В одном варианте реализации изобретения промотор является тканеспецифическим промотором. В одном варианте реализации изобретения промотор является нейрон-специфическим промотором. В одном варианте реализации изобретения промотор является нейроглия-специфическим промотором. В одном варианте реализации изобретения промотор является специфическим в отношении мышечных клеток промотором. В одном варианте реализации изобретения промотор является специфическим в отношении клеток сердца промотором. В одном варианте реализации изобретения промотор является специфическим в отношении клеток почек промотором. В одном варианте реализации изобретения промотор является специфическим в отношении костных клеток промотором. В одном варианте реализации изобретения промотор является специфическим в отношении эндотелиальных клеток промотором. В одном варианте реализации изобретения промотор является специфическим в отношении иммунных клеток промотором. В одном варианте реализации изобретения промотор иммунных клеток является промотором В-клеток. В одном варианте реализации изобретения промотор иммунных клеток является промотором Т-клеток.
[00182] В одном варианте реализации изобретения промотор является регулируемым уровнем развития промотором. В одном варианте реализации изобретения регулируемый уровнем развития промотор активен только во время эмбриональной стадии развития. В одном варианте реализации изобретения регулируемый уровнем развития промотор активен только во взрослой клетке.
[00183] В конкретных вариантах реализации изобретения промотор может быть выбран на основании типа клеток. Таким образом, различные промоторы находят применение в эукариотической клетке, некрысиной эукариотической клетке, клетке млекопитающего, клетке отличного от человека млекопитающего, плюрипотентной клетке, неплюрипотентной клетке, нечеловеческой плюрипотентной клетке, человеческой плюрипотентной клетке, человеческой ЭС клетке, человеческой взрослой стволовой клетке, человеческой клетке-предшественнике с ограниченным развитием, человеческой иПС клетке, человеческой клетке, клетке грызуна, клетке отличного от крысы грызуна, клетке крысы, клетке мыши, клетке хомяка, фибробласте или клетке СНО.
[00184] В некоторых вариантах реализации изобретения нуклеотидная вставка содержит нуклеиновую кислоту, фланкируемую целевыми последовательностями сайт-специфической рекомбинации. Следует понимать, что хотя целая нуклеотидная вставка может фланкироваться такими целевыми последовательностями сайт-специфической рекомбинации, любая область или отдельный представляющий интерес полинуклеотид в пределах нуклеотидной вставки также может фланкироваться такими участками. Сайт-специфическую рекомбиназу можно вносить в клетку любыми способами, включая внесение полипептида рекомбиназы в клетку или внесение полинуклеотида, кодирующего сайт-специфическую рекомбиназу, в клетку-хозяина. Полинуклеотид, кодирующий сайт-специфическую рекомбиназу, может быть расположен в пределах нуклеотидной вставки или в отдельном полинуклеотиде. Сайт-специфическая рекомбиназа может быть функционально связана с активным в клетке промотором, включая, например, индуцибельный промотор, эндогенный по отношению к клетке промотор, гетерологичный по отношению к клетке промотор, клеточно-специфический промотор, тканеспецифический промотор или специфический в отношении стадии развития промотор. Целевые последовательности сайт-специфической рекомбинации, которые могут фланкировать нуклеотидную вставку или любой представляющий интерес полинуклеотид в нуклеотидной вставке, могут включать, но не ограничиваются этим, loxP, lox511, lox2272, lox66, lox71, loxM2, lox5171, FRT, FRT11, FRT71, attp, att, FRT, rox и их комбинацию.
[00185] В некоторых вариантах реализации изобретения участки сайт-специфической рекомбинации фланкируют полинуклеотид, кодирующий селективный маркер и/или репортерный ген, который находится в нуклеотидной вставке. В таких случаях после интеграции нуклеотидной вставки в целевой локус последовательности между участками сайт-специфической рекомбинации можно удалять.
[00186] В одном варианте реализации изобретения нуклеотидная вставка содержит полинуклеотид, кодирующий селективный маркер. Селективный маркер может находиться в селекционной кассете. Такие селективные маркеры включают, но не ограничиваются этим, неомицин фосфотрансферазу (neor), гигромицин-В-фосфотрансферазу (hygr), пуромицин-N-ацетилтрансферазу (puror), бластицидин-S-дезаминазу (bsrr), ксантин/гуанин фосфорибозилтрансферазу (gpt) или тимидинкиназу вируса простого герпеса (HSV-k) или их комбинацию. В одном варианте реализации изобретения полинуклеотид, кодирующий селективный маркер, функционально связан с промотором, активным в клетке, крысиной клетке, плюрипотентной крысиной клетке, крысиной ЭС клетке, эукариотической клетке, некрысиной эукариотической клетке, плюрипотентной клетке, неплюрипотентной клетке, нечеловеческой плюрипотентной клетке, человеческой плюрипотентной клетке, человеческой ЭС клетке, человеческой взрослой стволовой клетке, человеческой клетке-предшественнике с ограниченным развитием, человеческой иПС клетке, клетке млекопитающего, клетке отличного от человека млекопитающего, человеческой клетке, клетке грызуна, клетке отличного от крысы грызуна, клетке мыши, клетке хомяка, фибробласте или клетке СНО. В случае серийного помещения представляющих интерес полинуклеотидов в целевой локус селективный маркер может содержать участок распознавания нуклеазного агента, как указано выше. В одном варианте реализации изобретения полинуклеотид, кодирующий селективный маркер, фланкируется целевыми последовательностями сайт-специфической рекомбинации.
[00187] Нуклеотидная вставка может дополнительно содержать репортерный ген, функционально связанный с промотором, при этом репортерный ген кодирует репортерный белок, выбранный из группы, состоящей из или включающей LacZ, mPlum, mCherry, tdTomato, mStrawberry, J-Red, DsRed, mOrange, mKO, mCitrine, Venus, YPet, усиленный желтый флуоресцентный белок (уЖФБ), Emerald, усиленный зеленый флуоресцентный белок (уЗФБ), CyPet, голубой флуоресцентный белок (ГФБ), Cerulean, T-Sapphire, люциферазу, щелочную фосфатазу и/или их комбинацию. Такие репортерные гены могут быть функционально связаны с активным в клетке промотором. Такие промоторы могут быть индуцибельными промоторами, промоторами, эндогенными по отношению к репортерному гену или клетке, промоторами, гетерологичными по отношению к репортерному гену или клетке, клеточно-специфическими промоторами, тканеспецифическими промоторами или промоторами, специфическими в отношении стадии развития.
[00188] В одном варианте реализации изобретения нуклеотидная вставка может содержать нуклеиновую кислоту млекопитающего, которая содержит геномный локус, который кодирует белок, экспрессируемый в нервной системе, костной системе, пищеварительной системе, системе кровообращения, мышечной системе, дыхательной системе, сердечнососудистой системе, лимфатической системе, эндокринной системе, мочевыделительной системе, репродуктивной системе или их комбинации. В одном варианте реализации изобретения нуклеиновая кислота млекопитающего содержит геномный локус, который кодирует белок, экспрессируемый в костном мозге или клетке костного мозга. В одном варианте реализации изобретения нуклеиновая кислота содержит геномный локус, который кодирует белок, экспрессируемый в клетке селезенки.
[00189] В одном варианте реализации изобретения нуклеиновая кислота млекопитающего содержит геномный локус, который кодирует белок, экспрессируемый в нервной системе, костной системе, пищеварительной системе, системе кровообращения, мышечной системе, дыхательной системе, сердечнососудистой системе, лимфатической системе, эндокринной системе, мочевыделительной системе, репродуктивной системе или их комбинации. В одном варианте реализации изобретения нуклеиновая кислота млекопитающего содержит геномный локус, который кодирует белок, экспрессируемый в костном мозге или клетке костного мозга. В одном варианте реализации изобретения нуклеиновая кислота содержит геномный локус, который кодирует белок, экспрессируемый в клетке селезенки. В одном варианте реализации изобретения геномный локус содержит мышиную последовательность геномной ДНК, крысиную последовательность геномной ДНК, последовательность геномной ДНК эукариота, последовательность геномной ДНК отличного от крысы эукариота, последовательность геномной ДНК млекопитающего, последовательность геномной ДНК человека или последовательность геномной ДНК отличного от человека млекопитающего или их комбинацию. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, крысиные и человеческие последовательности геномной ДНК. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, мышиные и человеческие последовательности геномной ДНК. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, мышиные и крысиные последовательности геномной ДНК. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, крысиные, мышиные и человеческие последовательности геномной ДНК.
[00190] В одном варианте реализации изобретения геномный локус содержит мышиную последовательность геномной ДНК, крысиную последовательность геномной ДНК, последовательность геномной ДНК хомяка, последовательность геномной ДНК человека, последовательность геномной ДНК эукариота, последовательность геномной ДНК отличного от крысы эукариота, последовательность геномной ДНК млекопитающего или последовательность геномной ДНК отличного от человека млекопитающего или их комбинацию. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, крысиные и человеческие последовательности геномной ДНК. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, мышиные и человеческие последовательности геномной ДНК. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, мышиные и крысиные последовательности геномной ДНК. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, крысиные, мышиные и человеческие последовательности геномной ДНК.
[00191] В одном варианте реализации изобретения генетическая модификация включает по меньшей мере один аллель заболевания человека из человеческого гена. В одном варианте реализации изобретения человеческое заболевание является неврологическим заболеванием. В одном варианте реализации изобретения человеческое заболевание является сердечнососудистым заболеванием. В одном варианте реализации изобретения человеческое заболевание является заболеванием почек. В одном варианте реализации изобретения человеческое заболевание является мышечным заболеванием. В одном варианте реализации изобретения человеческое заболевание является заболеванием крови. В одном варианте реализации изобретения человеческое заболевание является раком. В одном варианте реализации изобретения человеческое заболевание является заболеванием иммунной системы.
[00192] В одном варианте реализации изобретения аллель заболевания человека является доминантным аллелем. В одном варианте реализации изобретения аллель заболевания человека является рецессивным аллелем. В одном варианте реализации изобретения аллель заболевания человека включает аллель однонуклеотидного полиморфизма (ОНП).
[00193] В одном варианте реализации изобретения генетическая модификация приводит к получению мутантной формы белка с измененными характеристиками связывания, измененной локализацией, измененной экспрессией и/или измененным профилем экспрессии.
[00194] В одном варианте реализации изобретения нуклеотидная вставка содержит селекционную кассету. В одном варианте реализации изобретения селекционная кассета содержит нуклеотидную последовательность, кодирующую селективный маркер, при этом нуклеотидная последовательность функционально связана с промотором, активным в ЭС клетках. В одном варианте реализации изобретения селективный маркер выбран из или содержит ген устойчивости к гигромицину или ген устойчивости к неомицину.
[00195] В одном варианте реализации изобретения нуклеиновая кислота содержит геномный локус, который кодирует белок, экспрессируемый в В-клетке. В одном варианте реализации изобретения нуклеиновая кислота содержит геномный локус, который кодирует белок, экспрессируемый в незрелой В-клетке. В одном варианте реализации нуклеиновая кислота содержит геномный локус, который кодирует белок, экспрессируемый в зрелой В-клетке.
[00196] В одном варианте реализации изобретения нуклеотидная вставка содержит регуляторный элемент. В одном варианте реализации изобретения регуляторный элемент является промотором. В одном варианте реализации изобретения регуляторный элемент является энхансером. В одном варианте реализации изобретения регуляторный элемент является транскрипционным репрессорсвязывающим элементом.
[00197] В одном варианте реализации изобретения генетическая модификация включает удаление не кодирующей белок последовательности, но не включает удаление кодирующей белок последовательности. В одном варианте реализации изобретения удаление не кодирующей белок последовательности включает удаление регуляторного элемента. В одном варианте реализации изобретения удаление не кодирующей белок последовательности включает удаление регуляторного элемента. В одном варианте реализации изобретения генетическая модификация включает добавление промотора или регуляторного элемента. В одном варианте реализации изобретения генетическая модификация включает замещение промотора или регуляторного элемента.
ii. Экспрессионные кассеты
[00198] В данном документе предложены полинуклеотиды или молекулы нуклеиновых кислот, содержащие различные компоненты, применяемые в системе направленной геномной интеграции (т.е. любой из или любая комбинация нуклеазных агентов, участков распознавания, нуклеотидных вставок, представляющих интерес полинуклеотидов, направляющих векторов, селективных маркеров и других компонентов).
[00199] Термины «полинуклеотид», «полинуклеотидная последовательность», «нуклеотидная последовательность» и «фрагмент нуклеиновой кислоты» взаимозаменяемо употребляются в данном документе. Эти термины включают нуклеотидные последовательности и тому подобное. Полинуклеотид может представлять собой полимер РНК или ДНК, который является одно- или двухцепочечным, который, необязательно, содержит синтетические, неприродные или измененные нуклеотидные основания. Полинуклеотид в форме полимера ДНК может состоять из одного или более сегментов кДНК, геномной ДНК, синтетической ДНК или их комбинаций. Полинуклеотиды могут включать дезоксирибонуклеотиды и рибонуклеотиды, включая как молекулы природного происхождения, так и синтетические аналоги, и любые их комбинации. Предложенные в данном документе полинуклеотиды также включают формы последовательностей, включая, но не ограничиваясь этим, одноцепочечные формы, двухцепочечные формы, шпильки, структуры типа «петля на стебле» и тому подобное.
[00200] Дополнительно предложены рекомбинантные полинуклеотиды, содержащие различные компоненты системы направленной геномной интеграции. Термины «рекомбинантный полинуклеотид» и «рекомбинантная конструкция ДНК» взаимозаменяемо употребляются в данном документе. Рекомбинантная конструкция содержит искусственную или гетерологичную комбинацию нуклеотидных последовательностей, например, регуляторных и кодирующих последовательностей, которые нельзя обнаружить вместе в природном состоянии. В других вариантах реализации изобретения рекомбинантная конструкция может содержать регуляторные последовательности и кодирующие последовательности, полученные из разных источников, или регуляторные последовательности и кодирующие последовательности, полученные из одного источника, но упорядоченные таким образом, который не встречается в природе. Такую конструкцию можно применять саму по себе или применять в сочетании с вектором. В случае применения вектора, выбор вектора зависит от способа, применяемого для трансформации клеток-хозяев, как хорошо известно специалистам в данной области техники. Например, можно применять плазмидный вектор. Также предложены генетические элементы, необходимые для трансформации, отбора и размножения клеток-хозяев, содержащих любые из предложенных в данном документе выделенных фрагментов нуклеиновых кислот. Скрининг можно проводить, помимо прочего, методом Саузерн-блоттинга ДНК, Нозерн-блоттинга экспрессии мРНК, иммуноблоттинга белковой экспрессии или фенотипического анализа.
[00201] В конкретных вариантах реализации изобретения один или более компонентов описанной в данном документе системы направленной геномной интеграции могут находиться в экспрессионной кассете для экспрессии в прокариотической клетке, эукариотической клетке, некрысиной эукариотической клетке, бактериальной, дрожжевой клетке или клетке млекопитающего или другого представляющего интерес организма или типа клеток. Кассета может содержать 5' и 3' регуляторные последовательности, функционально связанные с предложенным в данном документе полинуклеотидом. «Функционально связанный» отображает взаимосвязь, в которой функционально связанные компоненты функционируют надлежащим образом. Например, функциональная связь между представляющим интерес полинуклеотидом и регуляторной последовательностью (т.е. промотором) представляет собой функциональную связь, которая делает возможной экспрессию представляющего интерес полинуклеотида. Функционально связанные элементы могут быть смежными или несмежными. При употреблении в отношении соединения двух кодирующих белок областей, функционально связанные означает, что кодирующие области находятся в одной рамке считывания. В другом случае нуклеотидная последовательность, кодирующая белок, может быть функционально связана с регуляторными последовательностями (например, промотором, энхансером, последовательностью сайленсера и т.д.) таким образом, чтобы поддерживать надлежащую транскрипционную регуляцию. В одном случае нуклеотидная последовательность вариабельной области иммуноглобулина (или сегментов V(D)J) может быть функционально связана с нуклеотидной последовательностью константной области иммуноглобулина таким образом, чтобы создавать возможность надлежащей рекомбинации между последовательностями в последовательность тяжелой или легкой цепи иммуноглобулина.
[00202] Кассета может дополнительно содержать по меньшей мере один представляющий интерес дополнительный полинуклеотид для совместного внесения в организм. В альтернативном варианте представляющий интерес дополнительный полинуклеотид может находиться на нескольких экспрессионных кассетах. Такая экспрессионная кассета содержит множество участков рестрикции и/или участков рекомбинации для того, чтобы вставка рекомбинантного полинуклеотида подлежала транскрипционной регуляции со стороны регуляторных областей. Экспрессионная кассета может дополнительно содержать гены селективных маркеров.
[00203] Экспрессионная кассета может содержать в 5'-3' направлении транскрипции участок инициации транскрипции и трансляции (т.е. промотор), предложенный в данном документе рекомбинантный полинуклеотид и участок терминации транскрипции и трансляции (т.е. терминирующий участок), функциональные в представляющей интерес клетке млекопитающего или клетке-хозяине. Регуляторные области (т.е. промоторы, транскрипционнае регуляторные области и трансляционные терминирующие области) и/или предложенный в данном документе полинуклеотид могут быть нативными/аналогичными в отношении клетки-хозяина или друг друга. В альтернативном варианте регуляторные области и/или предложенный в данном документе полинуклеотид могут быть гетерологичными в отношении клетки-хозяина или друг друга. Например, промотор, функционально связанный с гетерологичным полинуклеотидом, принадлежит виду, отличному от вида, от которого был получен полинуклеотид, или, в случае, если они принадлежат одному виду/аналогичным видам, один или оба элемента в значительной степени модифицированы по сравнению со своей оригинальной формой и/или геномным локусом, или промотор не является нативным промотором по отношению к функционально связанному с ним полинуклеотиду. В альтернативном варианте регуляторные области и/или предложенный в данном документе полинуклеотид могут быть полностью синтетическими.
[00204] Терминирующая область может быть нативной по отношению к области инициации транскрипции, может быть нативной по отношению к функционально связанному рекомбинантному полинуклеотиду, может быть нативной по отношению к клетке-хозяину или может быть получена из другого источника (т.е. чужеродного или гетерологичного), чем промотор, рекомбинантный полинуклеотид, клетка-хозяин, или соответствовать любой комбинации этих вариантов.
[00205] При получении экспрессионной кассеты можно проводить манипуляции с различными фрагментами ДНК, чтобы получить последовательности ДНК в надлежащей ориентации. С этой целью можно применять адаптеры или линкеры для соединения фрагментов ДНК или осуществлять другие манипуляции, чтобы обеспечить наличие удобных участков рестрикции, удаление избыточной ДНК, удаление участков рестрикции и тому подобное. С этой целью можно применять in vitro мутагенез, репарацию при помощи праймеров, рестрикцию, гибридизацию, повторные замены, например, транзиции и трансверсии.
[00206] В предложенных в данном документе экспрессионных кассетах можно применять большое количество промоторов. Промоторы можно выбирать на основании желаемого результата. Известно, что разные применения можно делать более эффективными, применяя в экспрессионных кассетах разные промоторы для модуляции времени, локализации и/или уровня экспрессии представляющего интерес полинуклеотида. Такие экспрессионные конструкции также могут содержать, в случае необходимости, промоторные регуляторные области (например, обеспечивающие индуцибельную, конститутивную, регулируемую внешней средой или уровнем развития, или клеточно- или тканеспецифическую/селективную экспрессию), участок инициации транскрипции, участок связывания рибосомы, сигнал процессинга РНК, участок терминации транскрипции и/или сигнал полиаденилирования.
[00207] Экспрессионная кассета, содержащая предложенные в данном документе полинуклеотиды, также может содержать ген селективного маркера для проведения отбора трансформированных клеток. Гены селективных маркеров применяют для отбора трансформированных клеток или тканей.
[00208] В случае целесообразности, последовательности, применяемые в способах и композициях (т.е. представляющий интерес полинуклеотид, нуклеазный агент и т.д.), можно оптимизировать для повышения экспрессии в клетке. Это означает, что можно синтезировать гены, используя кодоны, предпочтительные в данной представляющей интерес клетке, включая, например, кодоны, предпочтительные для млекопитающих, кодоны, предпочтительные для людей, кодоны, предпочтительные для грызунов, кодоны, предпочтительные для отличных от крысы грызунов, кодоны, предпочтительные для мышей, кодоны, предпочтительные для крыс, кодоны, предпочтительные для хомяков и т.д., для улучшения экспрессии.
[00209] В различных предложенных в данном документе способах и композициях можно применять селективные маркеры. В раскрытых в данном документе способах и композициях можно применять различные селективные маркеры. Такие селективные маркеры могут, например, придавать устойчивость к антибиотикам, таким как G418, гигромицин, бластицидин, неомицин или пуромицин. Такие селективные маркеры включают неомицин фосфотрансферазу (neor), гигромицин-В-фосфотрансферазу (hygr), пуромицин-N-ацетилтрансферазу (puror) и бластицидин-S-дезаминазу (bsrr). В других вариантах реализации изобретения селективный маркер функционально связан с индуцибельным промотором, а экспрессия селективного маркера является токсичной для клетки. Неограничивающие примеры таких селективных маркеров включают ксантин/гуанин фосфорибозилтрансферазу (gpt), гипоксантин-гуанин фосфорибозилтрансферазу (HGPRT) или тимидинкиназу вируса простого герпеса (HSV-TK). Полинуклеотиды, кодирующие селективные маркеры, функционально связаны с активным в клетке промотором.
iii. Направляющие векторы
[00210] Направляющие векторы применяют для внесения нуклеотидной вставки в целевой локус нуклеиновой кислоты крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка. Направляющий вектор содержит нуклеотидную вставку и дополнительно содержит 5' и 3' плечи гомологии, которые фланкируют нуклеотидную вставку. Плечи гомологии, которые фланкируют нуклеотидную вставку, соответствуют областям в целевом локусе нуклеиновой кислоты крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка. Для удобства, соответствующие когнатные геномные области в пределах целевого геномного локуса называются в данном документе «целевыми участками». Например, направляющий вектор может содержать первую нуклеотидную вставку, фланкируемую первым и вторым плечами гомологии, комплементарными первому и второму целевым участкам. Таким образом, направляющий вектор способствует интеграции нуклеотидной вставки в целевой локус нуклеиновой кислоты крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка посредством гомологичной рекомбинации, которая происходит между плечами гомологии и комплементарными целевыми участками в геноме клетки.
[00211] В одном варианте реализации изобретения целевой локус нуклеиновой кислоты крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка содержит первую нуклеотидную последовательность, которая комплементарна 5' плечу гомологии, и вторую нуклеотидную последовательность, которая комплементарна 3' плечу гомологии. В одном варианте реализации изобретения первая и вторая нуклеотидные последовательности разделены по меньшей мере 5 т.п.о. В другом варианте реализации изобретения первая и вторая нуклеотидные последовательности разделены по меньшей мере 5 т.п.о., но менее чем 200 т.п.о. В одном варианте реализации изобретения первая и вторая нуклеотидные последовательности разделены по меньшей мере 10 т.п.о. В одном варианте реализации изобретения первая и вторая нуклеотидные последовательности разделены по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 110 т.п.о., по меньшей мере 120 т.п.о., по меньшей мере 130 т.п.о., по меньшей мере 140 т.п.о., по меньшей мере 150 т.п.о., по меньшей мере 160 т.п.о., по меньшей мере 170 т.п.о., по меньшей мере 180 т.п.о., по меньшей мере 190 т.п.о. или по меньшей мере 200 т.п.о. В других вариантах реализации изобретения первая и вторая нуклеотидные последовательности разделены по меньшей мере 5 т.п.о., но менее чем 10 т.п.о., по меньшей мере 5 т.п.о., но менее чем 3 м.п.о., по меньшей мере 10 т.п.о., но менее чем 20 т.п.о., по меньшей мере 20 т.п.о., но менее чем 40 т.п.о., по меньшей мере 40 т.п.о., но менее чем 60 т.п.о., по меньшей мере 60 т.п.о., но менее чем 80 т.п.о., по меньшей мере около 80 т.п.о., но менее чем 100 т.п.о., по меньшей мере 100 т.п.о., но менее чем 150 т.п.о., или по меньшей мере 150 т.п.о., но менее чем 200 т.п.о., по меньшей мере около 200 т.п.о., но менее чем около 300 т.п.о., по меньшей мере около 300 т.п.о., но менее чем около 400 т.п.о., по меньшей мере около 400 т.п.о., но менее чем около 500 т.п.о., по меньшей мере около 500 т.п.о., но менее чем около 1 м.п.о., по меньшей мере около 1,5 м.п.о., но менее чем около 2 м.п.о., по меньшей мере около 1 м.п.о., но менее чем около 1,5 м.п.о., по меньшей мере около 2 м.п.о., но менее чем 2,5 м.п.о., по меньшей мере около 2,5 м.п.о., но менее чем 3 м.п.о., или по меньшей мере около 2 м.п.о., но менее чем около 3 м.п.о.
[00212] Плечо гомологии направляющего вектора может иметь любую длину, которой достаточно, чтобы стимулировать гомологичную рекомбинацию с соответствующим целевым участком, включая, например, длину, составляющую по меньшей мере 5-10 т.п.о., 5-15 т.п.о., 10-20 т.п.о., 20-30 т.п.о., 30-40 т.п.о., 40-50 т.п.о., 50-60 т.п.о., 60-70 т.п.о., 70-80 т.п.о., 80-90 т.п.о., 90-100 т.п.о., 100-110 т.п.о., 110-120 т.п.о., 120-130 т.п.о., 130-140 т.п.о., 140-150 т.п.о., 150-160 т.п.о., 160-170 т.п.о., 170-180 т.п.о., 180-190 т.п.о., 190-200 т.п.о. или более. Как более подробно описано ниже, в крупных направляющих векторах могут применяться направляющие плечи большей длины. В конкретном варианте реализации изобретения 5' плечо гомологии и 3' плечо гомологии в общей сумме составляют по меньшей мере 10 т.п.о. или 5' плечо гомологии и 3' плечо гомологии в общей сумме составляют по меньшей мере от около 16 т.п.о. до около 100 т.п.о. или от около 30 т.п.о. до около 100 т.п.о. В других вариантах реализации изобретения общий размер 5' и 3' плеч гомологии LTVEC составляет от около 10 т.п.о. до около 150 т.п.о., от около 10 т.п.о. до около 100 т.п.о., от около 10 т.п.о. до около 75 т.п.о., от около 20 т.п.о. до около 150 т.п.о., от около 20 т.п.о. до около 100 т.п.о., от около 20 т.п.о. до около 75 т.п.о., от около 30 т.п.о. до около 150 т.п.о., от около 30 т.п.о. до около 100 т.п.о., от около 30 т.п.о. до около 75 т.п.о., от около 40 т.п.о. до около 150 т.п.о., от около 40 т.п.о. до около 100 т.п.о., от около 40 т.п.о. до около 75 т.п.о., от около 50 т.п.о. до около 150 т.п.о., от около 50 т.п.о. до около 100 т.п.о. или от около 50 т.п.о. до около 75 т.п.о., от около 10 т.п.о. до около 30 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до около 150 т.п.о. В одном варианте реализации изобретения размер делеции одинаков или сходен с общим размером 5' и 3' плеч гомологии LTVEC.
[00213] В одном варианте реализации изобретения представляющий интерес геномный локус содержит (i) 5' целевую последовательность, которая гомологична 5' плечу гомологии; и (ii) 3' целевую последовательность, которая гомологична 3' плечу гомологии. В одном варианте реализации изобретения 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 3 м.п.о. В других вариантах реализации изобретения 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 10 т.п.о., по меньшей мере 5 т.п.о., но менее чем 3 м.п.о., по меньшей мере 10 т.п.о., но менее чем 20 т.п.о., по меньшей мере 20 т.п.о., но менее чем 40 т.п.о., по меньшей мере 40 т.п.о., но менее чем 60 т.п.о., по меньшей мере 60 т.п.о., но менее чем 80 т.п.о., по меньшей мере около 80 т.п.о., но менее чем 100 т.п.о., по меньшей мере 100 т.п.о., но менее чем 150 т.п.о. или по меньшей мере 150 т.п.о., но менее чем 200 т.п.о., по меньшей мере около 200 т.п.о., но менее чем около 300 т.п.о., по меньшей мере около 300 т.п.о., но менее чем около 400 т.п.о., по меньшей мере около 400 т.п.о., но менее чем около 500 т.п.о., по меньшей мере около 500 т.п.о., но менее чем около 1 м.п.о., по меньшей мере около 1,5 м.п.о., но менее чем около 2 м.п.о., по меньшей мере около 1 м.п.о., но менее чем около 1,5 м.п.о., по меньшей мере около 2 м.п.о., но менее чем 2,5 м.п.о., по меньшей мере около 2,5 м.п.о., но менее чем около 3 м.п.о., или по меньшей мере около 2 м.п.о., но менее чем около 3 м.п.о.
[00214] В случае применения нуклеазных агентов, когнатные геномные области, соответствующие 5' и 3' плечам гомологии направляющего вектора, «расположены достаточно близко» к нуклеазным целевым участкам, чтобы стимулировать гомологичную рекомбинацию между когнатными геномными областями и плечами гомологии после одноцепочечного или друхцепочечного разрыва в участке распознавания. Например, нуклеазные целевые участки могут располагаться в любом месте между когнатными геномными областями, соответствующими 5' и 3' плечам гомологии. В конкретных вариантах реализации изобретения участок распознавания непосредственно прилегает по меньшей мере к одной или обеим когнатным геномным областям.
[00215] В контексте данного документе плечо гомологии и целевой участок (т.е. когнатная геномная область) «дополняют» или «являются комплементарными» по отношению друг к другу, если две области обладают достаточной степенью идентичности последовательностей по отношению друг к другу, чтобы служить в качестве субстратов для реакции гомологичной рекомбинации. Под «гомологичными» подразумеваются последовательности ДНК, которые идентичны или обладают идентичностью последовательностей с соответствующей или «комплементарной» последовательностью. Идентичность последовательностей между заданным целевым участком и соответствующим плечом гомологии, находящимся в направляющем векторе, может характеризоваться любой степенью идентичности последовательностей, которая делает возможной гомологичную рекомбинацию. Например, степень идентичности последовательностей между плечом гомологии направляющего вектора (или его фрагмента) и целевым участком (или его фрагментом) может составлять по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%, так, что последовательности подлежат гомологичной рекомбинации. Кроме того, комплементарная область гомологии между плечом гомологии и комплементарным целевым участком может иметь любую длину, которой достаточно, чтобы стимулировать гомологичную рекомбинацию в расщепляемом участке распознавания. Заданные плечо гомологии и/или комплементарный целевой участок могут содержать комплементарные области гомологии, длина которых составляет по меньшей мере 5-10 т.п.о., 5-15 т.п.о., 10-20 т.п.о., 20-30 т.п.о., 30-40 т.п.о., 40-50 т.п.о., 50-60 т.п.о., 60-70 т.п.о., 70-80 т.п.о., 80-90 т.п.о., 90-100 т.п.о., 100-110 т.п.о., 110-120 т.п.о., 120-130 т.п.о., 130-140 т.п.о., 140-150 т.п.о., 150-160 т.п.о., 160-170 т.п.о., 170-180 т.п.о., 180-190 т.п.о., 190-200 т.п.о., 200 т.п.о. до 300 т.п.о. или более (так, как описано для векторов LTVEC, описанных в другом месте данного документа), так, что плечо гомологии обладает достаточной гомологией, чтобы подлежать гомологичной рекомбинации с соответствующими целевыми участками в пределах генома клетки. Для удобства плечи гомологии называются в данном документе 5' и 3' плечами гомологии. Эта терминология связана с относительным расположением плеч гомологии по отношению к нуклеотидной вставке в пределах направляющего вектора.
[00216] Следовательно, плечи гомологии направляющего вектора конструируют так, чтобы они были комплементарными целевому участку с таргетируемым локусом. Таким образом, плечи гомологии могут быть комплементарными локусу, который является нативным по отношению к клетке, или, в альтернативном варианте, они могут быть комплементарными области гетерологичного или экзогенного сегмента ДНК, который был интегрирован в геном клетки, включая, но не ограничиваясь этим, трансгены, экспрессионные кассеты или гетерологичные или экзогенные области геномной ДНК. В альтернативном варианте плечи гомологии направляющего вектора могут быть комплементарными области человеческой искусственной хромосомы или любой другой сконструированной геномной области, содержащейся в соответствующей клетке-хозяине. Кроме того, плечи гомологии направляющего вектора могут быть комплементарными или полученными из области библиотеки БИХ, библиотеки космид или фаговой библиотеки Р1. Таким образом, в конкретных вариантах реализации изобретения плечи гомологии направляющего вектора комплементарны геномному локусу крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка, который является нативным, гетерологичным или экзогенным для данной клетки. В дополнительных вариантах реализации изобретения плечи гомологии направляющего вектора комплементарны геномному локусу крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка, который нельзя таргетировать традиционным способом или который может быть таргетирован только неправильно или с очень низкой эффективностью в отсутствие одноцепочечного или двухцепочечного разрыва, индуцируемого нуклеазным агентом. В одном варианте реализации изобретения плечи гомологии получены из синтетической ДНК.
[00217] В других вариантах реализации изобретения 5' и 3' плечи гомологии комплементарны тому же геному, что и таргетируемый геном. В одном варианте реализации изобретения плечи гомологии получены из родственного генома, например, таргетируемый геном является геномом крысы из первого штамма, а плечи гомологии получены из генома крысы из второго штамма, при этом первый штамм и второй штамм отличаются. В других вариантах реализации изобретения плечи гомологии получены из генома одного животного или получены из генома одного штамма, например, таргетируемый геном является геномом крысы из первого штамма, а плечи гомологии получены из крысиного генома той же самой крысы или того же самого штамма.
[00218] Направляющий вектор (такой как крупный направляющий вектор) также может содержать селекционную кассету или репортерный ген, как обсуждается в другом месте данного документа. Селекционная кассета может содержать нуклеотидную последовательность, кодирующую селективный маркер, при этом нуклеотидная последовательность функционально связана с промотором. Промотор может быть активным в представляющей интерес прокариотической клетке и/или быть активным в представляющей интерес эукариотической клетке. Такие промоторы могут быть индуцибельными промоторами, промоторами, эндогенными по отношению к репортерному гену или к клетке, промоторами, гетерологичными по отношению к репортерному гену или к клетке, клеточно-специфическими промоторами, тканеспецифическими промоторами или промоторами, специфическими в отношении стадии развития. В одном варианте реализации изобретения селективный маркер выбран из или включает неомицин фосфотрансферазу (neor), гигромицин-В-фосфотрансферазу (hygr), пуромицин-N-ацетилтрансферазу (puror), бластицидин-S-дезаминазу (bsrr), ксантин/гуанин фосфорибозилтрансферазу (gpt) и тимидинкиназу вируса простого герпеса (HSV-R) и/или их комбинацию. Селективный маркер направляющего вектора может фланкироваться 5' and 3' плечами гомологии или быть расположенным 5' или 3' по отношению к плечам гомологии.
[00219] В одном варианте реализации изобретения направляющий вектор (такой как крупный направляющий вектор) содержит репортерный ген, функционально связанный с промотором, при этом репортерный ген кодирует репортерный белок, выбранный из группы, состоящей из или включающей LacZ, mPlum, mCherry, tdTomato, mStrawberry, J-Red, DsRed, mOrange, mKO, mCitrine, Venus, YPet, усиленный желтый флуоресцентный белок (уЖФБ), Emerald, усиленный зеленый флуоресцентный белок (уЗФБ), CyPet, голубой флуоресцентный белок (ГФБ), Cerulean, T-Sapphire, люциферазу, щелочную фосфатазу и/или их комбинацию. Такие репортерные гены могут быть функционально связаны с активным в клетке промотором. Такие промоторы могут быть индуцибельными промоторами, промоторами, эндогенными по отношению к репортерному гену или клетке, промоторами, гетерологичными по отношению к репортерному гену или клетке, клеточно-специфическими промоторами, тканеспецифическими промоторами или промоторами, специфическими в отношении стадии развития.
[00220] В одном варианте реализации изобретения комбинированное применение направляющего вектора (включая, например, крупный направляющий вектор) с нуклеазными агентами приводит к повышению эффективности таргетирования по сравнению с применением одного направляющего вектора. В одном варианте реализации изобретения, когда направляющий вектор применяют в сочетании с нуклеазным агентом, эффективность таргетирования направляющего вектора повышается по меньшей мере в два раза, по меньшей мере в три раза или по меньшей мере в 4 раза по сравнению с применением одного направляющего вектора.
[00221] При применении направляющего вектора конструкция вектора может быть такой, чтобы создавать возможность вставки заданной последовательности, составляющей от около 5 т.п.о. до около 200 т.п.о., как описано в данном документе. В одном варианте реализации изобретения вставка составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 30 т.п.о., от около 30 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 50 т.п.о., от около 50 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 70 т.п.о., от около 80 т.п.о. до около 90 т.п.о., от около 90 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 110 т.п.о., от около 110 т.п.о. до около 120 т.п.о., от около 120 т.п.о. до около 130 т.п.о., от около 130 т.п.о. до около 140 т.п.о., от около 140 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 160 т.п.о., от около 160 т.п.о. до около 170 т.п.о., от около 170 т.п.о. до около 180 т.п.о., от около 180 т.п.о. до около 190 т.п.о. или от около 190 т.п.о. до около 200 т.п.о., от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.
[00222] При применении направляющего вектора конструкция вектора может быть такой, чтобы создавать возможность замещения заданной последовательности, составляющей от около 5 т.п.о. до около 200 т.п.о. или от около 5 т.п.о. до около 3,0 м.п.о., как описано в данном документе. В одном варианте реализации изобретения замещение составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о, до около 20 т.п.о., от около 20 т.п.о. до около 30 т.п.о., от около 30 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 50 т.п.о., от около 50 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 70 т.п.о., от около 80 т.п.о. до около 90 т.п.о., от около 90 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 110 т.п.о., от около 110 т.п.о. до около 120 т.п.о., от около 120 т.п.о. до около 130 т.п.о., от около 130 т.п.о. до около 140 т.п.о., от около 140 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 160 т.п.о., от около 160 т.п.о. до около 170 т.п.о., от около 170 т.п.о. до около 180 т.п.о., от около 180 т.п.о. до около 190 т.п.о., от около 190 т.п.о. до около 200 т.п.о., от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.
[00223] В одном варианте реализации изобретения направляющий вектор содержит ген сайт-специфической рекомбиназы. В одном варианте реализации изобретения ген сайт-специфической рекомбиназы кодирует рекомбиназу Cre. В одном варианте реализации изобретения ген рекомбиназы Cre представляет собой Crei, в котором два экзона, кодирующие рекомбиназу Cre, разделены интроном для предотвращения ее экспрессии в прокариотической клетке.
[00224] В одном варианте реализации изобретения ген рекомбиназы Cre дополнительно содержит сигнал ядерной локализации для облегчения локализации Cre (или любой рекомбиназы или нуклеазного агента) относительно ядра (например, ген является геном NL-Cre). В конкретном варианте реализации изобретения ген рекомбиназы Cre дополнительно содержит сигнал ядерной локализации и интрон (например, NL-Crei).
[00225] В различных вариантах реализации изобретения подходящий для экспрессии нуклеазного агента (включая рекомбиназу Cre или Crei, обсуждаемую выше) промотор выбран из или включает Prm1, Blimp1, Gata6, Gata4, Igf2, Lhx2, Lhx5 и/или Рах3. В конкретном варианте реализации изобретения промотор представляет собой промотор Gata6 или Gata4. Различные промоторы могут быть получены из любого организма, включая, например, грызуна, такого как мышь или крыса, отличного от крысы грызуна, эукариота, отличного от крысы эукариота, отличного от человека млекопитающего, млекопитающего, человека или хомяка. В другом конкретном варианте реализации изобретения промотор представляет собой промотор Prm1. В другом конкретном варианте реализации изобретения промотор представляет собой промотор крысиного Prm1. В другом конкретном варианте реализации изобретения промотор представляет собой промотор мышиного Prm1. В другом конкретном варианте реализации изобретения промотор представляет собой промотор Blimp1 или его фрагмент, например, содержащий 1 т.п.о. или 2 т.п.о. фрагмент промотора Blimp1. Смотрите, например, патент США 8697851 и опубликованную заявку на патент США 2013-0312129, которые в полном объеме включены в данный документ посредством ссылки.
iv. Крупные направляющие векторы
[00226] Употребляемый в данном документе термин «крупный направляющий вектор» или «LTVEC» включает крупные направляющие векторы, которые содержат плечи гомологии, которые соответствуют или получены из нуклеотидных последовательностей, крупнее тех, которые обычно используются в других подходах для осуществления гомологичного таргетирования в клетках, и/или содержащие нуклеотидные вставки, содержащие нуклеотидные последовательности, крупнее тех, которые обычно используются в других подходах для осуществления гомологичного рекомбинационного таргетирования в клетках. Например, LTVEC позволяет осуществлять модификацию крупных локусов, которую невозможно осуществить при помощи традиционных основанных на плазмидах направляющих векторов из-за ограничений по размеру. В конкретных вариантах реализации изобретения плечи гомологии и/или нуклеотидная вставка LTVEC содержат геномную последовательность эукариотической клетки или некрысиной эукариотической клетки. Размер LTVEC слишком большой для проведения скрининга таргетирования традиционными методами анализа, например, Саузерн-блоттинга и ПЦР длинных фрагментов (например, 1 т.п.о. - 5 т.п.о.). Примеры LTVEC, включают, но не ограничиваются этим, векторы, полученные из бактериальной искусственной хромосомы (БИХ), человеческой искусственной хромосомы и дрожжевой искусственной хромосомы (ДИХ). Неограничивающие примеры LTVEC и способы их получения описаны, например, в патентах США №6586251, 6596541, 7105348 и WO 2002/036789 (PCT/US01/45375), и US 2013/0137101, которые все включены в данный документ посредством ссылки.
[00227] LTVEC может иметь любую длину, включая, но не ограничиваясь этим, от около 20 т.п.о. до около 400 т.п.о., от около 20 т.п.о. до около 30 т.п.о., от около 30 т.п.о. до 40 т.п.о., от около 40 т.п.о. до около 50 т.п.о., от около 50 т.п.о. до около 75 т.п.о., от около 75 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до 125 т.п.о., от около 125 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 175 т.п.о., от около 175 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 225 т.п.о., от около 225 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 275 т.п.о. или от около 275 т.п.о. до около 300 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о., от около 350 т.п.о. до около 400 т.п.о., от около 350 т.п.о. до около 550 т.п.о. В одном варианте реализации изобретения LTVEC составляет около 100 т.п.о.
[00228] В некоторых вариантах реализации изобретения LTVEC составляет по меньшей мере 10 т.п.о., по меньшей мере 15 т.п.о., по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
[00229] В некоторых вариантах реализации изобретения LTVEC содержит нуклеотидную последовательность, составляющую по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
[00230] В одном варианте реализации изобретения LTVEC содержит нуклеотидную вставку в диапазоне от около 5 т.п.о, до около 200 т.п.о., от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 30 т.п.о., от около 0.5 т.п.о. до около 30 т.п.о., от около 0.5 т.п.о. до около 40 т.п.о., от около 30 т.п.о. до около 150 т.п.о., от около 0.5 т.п.о. до около 150 т.п.о., от около 30 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 50 т.п.о., от около 60 т.п.о. до около 70 т.п.о., от около 80 т.п.о. до около 90 т.п.о., от около 90 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 110 т.п.о., от около 120 т.п.о. до около 130 т.п.о., от около 130 т.п.о. до около 140 т.п.о., от около 140 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 160 т.п.о., от около 160 т.п.о. до около 170 т.п.о., от около 170 т.п.о. до около 180 т.п.о., от около 180 т.п.о. до около 190 т.п.о. или от около 190 т.п.о. до около 200 т.п.о., от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.
[00231] В одном варианте реализации изобретения LTVEC содержит нуклеотидную последовательность, составляющую по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
[00232] При применении LTVEC конструкция вектора может быть такой, чтобы создавать возможность замещения заданной последовательности, составляющей от около 5 т.п.о. до около 200 т.п.о. или от около 5 т.п.о. до около 3 м.п.о., как описано в данном документе. В одном варианте реализации изобретения замещение составляет от около 5 т.п.о, до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 30 т.п.о., от около 30 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 50 т.п.о., от около 50 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 70 т.п.о., от около 80 т.п.о. до около 90 т.п.о., от около 90 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 110 т.п.о., от около 110 т.п.о. до около 120 т.п.о., от около 120 т.п.о. до около 130 т.п.о., от около 130 т.п.о. до около 140 т.п.о., от около 140 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 160 т.п.о., от около 160 т.п.о. до около 170 т.п.о., от около 170 т.п.о. до около 180 т.п.о., от около 180 т.п.о. до около 190 т.п.о., от около 190 т.п.о. до около 200 т.п.о., от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.
[00233] В одном варианте реализации изобретения плечи гомологии LTVEC получены из библиотеки БИХ, библиотеки космид или фаговой библиотеки Р1. В других вариантах реализации изобретения плечи гомологии получены из целевого геномного локуса клетки, а в некоторых случаях таргетирование целевого геномного локуса, на который нацелен LTVEC, невозможно осуществить традиционным способом. В других вариантах реализации изобретения плечи гомологии получены из синтетической ДНК.
[00234] В одном варианте реализации изобретения 5' плечо гомологии и 3' плечо гомологии в LTVEC в общей сумме составляют по меньшей мере 10 т.п.о. В других вариантах реализации изобретения 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.о. до около 30 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от 100 т.п.о. до около 120 т.п.о., от около 120 т.п.о. до около 140 т.п.о., от около 140 т.п.о. до около 160 т.п.о., от около 160 т.п.о. до около 180 т.п.о., от около 180 т.п.о. до около 200 т.п.о. В одном варианте реализации изобретения 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 30 т.п.о. до около 100 т.п.о. В других вариантах реализации изобретения общий размер 5' и 3' плеч гомологии LTVEC составляет от около 10 т.п.о. до около 150 т.п.о., от около 10 т.п.о. до около 100 т.п.о., от около 10 т.п.о. до около 75 т.п.о., от около 20 т.п.о. до около 150 т.п.о., от около 20 т.п.о. до около 100 т.п.о., от около 20 т.п.о. до около 75 т.п.о., от около 30 т.п.о. до около 150 т.п.о., от около 30 т.п.о. до около 100 т.п.о., от около 30 т.п.о. до около 75 т.п.о., от около 40 т.п.о. до около 150 т.п.о., от около 40 т.п.о. до около 100 т.п.о., от около 40 т.п.о. до около 75 т.п.о., от около 50 т.п.о. до около 150 т.п.о., от около 50 т.п.о. до около 100 т.п.о. или от около 50 т.п.о. до около 75 т.п.о., от около 10 т.п.о. до около 30 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до около 150 т.п.о. В одном варианте реализации изобретения размер делеции одинаков или сходен с общим размером 5' и 3' плеч гомологии LTVEC.
[00235] В других вариантах реализации изобретения диапазон 5' плеча гомологии составляет от около 5 т.п.о. до около 100 т.п.о. В одном варианте реализации изобретения диапазон 3' плеча гомологии составляет от около 5 т.п.о. до около 100 т.п.о. В других вариантах реализации изобретения 5' и 3' плечи гомологии в общей сумме составляют от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 30 т.п.о., от около 30 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 50 т.п.о., от около 50 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 70 т.п.о., от около 70 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 90 т.п.о., от около 90 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 110 т.п.о., от около 110 т.п.о. до около 120 т.п.о., от около 120 т.п.о. до около 130 т.п.о., от около 130 т.п.о. до около 140 т.п.о., от около 140 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 160 т.п.о., от около 160 т.п.о. до около 170 т.п.о., от около 170 т.п.о. до около 180 т.п.о., от около 180 т.п.о. до около 190 т.п.о., от около 190 т.п.о. до около 200 т.п.о. или от около 30 т.п.о. до около 100 т.п.о., от около 10 т.п.о. до около 30 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до около 150 т.п.о.
[00236] В одном варианте реализации изобретения LTVEC содержит нуклеотидную вставку, которая гомологична или ортологична крысиной нуклеотидной последовательности, фланкируемой плечами гомологии LTVEC. В одном варианте реализации изобретения последовательность нуклеотидной вставки получена от вида, отличного от крысы. В одном варианте реализации изобретения последовательность нуклеотидной вставки получена от эукариота. В одном варианте реализации изобретения нуклеотидная вставка, которая является гомологичной или ортологичной крысиной нуклеотидной последовательности, представляет собой нуклеиновую кислоту млекопитающего. В одном варианте реализации изобретения нуклеотидная вставка, которая является гомологичной или ортологичной крысиной нуклеотидной последовательности, представляет собой нуклеиновую кислоту отличного от человека млекопитающего. В одном варианте реализации изобретения нуклеиновая кислота млекопитающего представляет собой нуклеиновую кислоту мыши. В одном варианте реализации изобретения нуклеиновая кислота млекопитающего представляет собой нуклеиновую кислоту человека. В одном варианте реализации изобретения нуклеиновая кислота млекопитающего представляет собой нуклеиновую кислоту хомяка. В одном варианте реализации изобретения нуклеотидная вставка представляет собой геномную ДНК. В одном варианте реализации изобретения вставка составляет от 5 т.п.о. до 200 т.п.о., как описано выше.
[00237] В одном варианте реализации изобретения LTVEC содержит селекционную кассету или репортерный ген. Различные формы селекционных кассет или репортерных генов, которые могут применяться, обсуждаются в другом месте данного документа.
Как описано в другом месте данного документа, LTVEC также можно применять в предложенных в данном документе способах в комбинации с нуклеазным агентом, который стимулирует гомологичную рекомбинацию между направляющим вектором и целевым локусом нуклеиновой кислоты крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка в плюрипотентной или неплюрипотентной клетке крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка.
[00238] В одном варианте реализации изобретения крупный направляющий вектор (LTVEC) содержит ген сайт-специфической рекомбиназы. В одном варианте реализации изобретения ген сайт-специфической рекомбиназы кодирует рекомбиназу Cre. В одном варианте реализации изобретения ген рекомбиназы Cre представляет собой Crei, в котором два экзона, кодирующие рекомбиназу Cre, разделены интроном для предотвращения ее экспрессии в прокариотической клетке. В одном варианте реализации изобретения ген рекомбиназы Cre дополнительно содержит сигнал ядерной локализации для облегчения локализации Cre (или любой рекомбиназы или нуклеазного агента) относительно ядра (например, ген является геном NL-Cre). В конкретном варианте реализации изобретения ген рекомбиназы Cre дополнительно содержит сигнал ядерной локализации и интрон (например, NL-Crei).
[00239] В различных вариантах реализации изобретения подходящий для экспрессии нуклеазного агента (включая рекомбиназу Cre или Crei, обсуждаемую выше) промотор выбран из или включает Prm1, Blimp1, Gata6, Gata4, Igf2, Lhx2, Lhx5 и/или Рах3. В конкретном варианте реализации изобретения промотор представляет собой промотор Gata6 или Gata4. Различные промоторы могут быть получены из любого организма, включая, например, грызуна, такого как мышь или крыса, отличного от крысы грызуна, эукариота, отличного от крысы эукариота, отличного от человека млекопитающего, млекопитающего, человека или хомяка. В другом конкретном варианте реализации изобретения промотор представляет собой промотор Prm1. В другом конкретном варианте реализации изобретения промотор представляет собой промотор крысиного Prm1. В другом конкретном варианте реализации изобретения промотор представляет собой промотор мышиного Prm1. В другом конкретном варианте реализации изобретения промотор представляет собой промотор Blimp1 или его фрагмент, например, содержащий 1 т.п.о. или 2 т.п.о. фрагмент промотора Blimp1. Смотрите, например, патент США 8697851 и опубликованную заявку на патент США 2013-0312129, которые в полном объеме включены в данный документ посредством ссылки.
[00240] В одном варианте реализации изобретения LTVEC содержит нуклеотидную вставку, которая может обеспечить удаление, добавление, замещение или их комбинацию области локуса АроЕ, локуса Il2rg, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка, как более подробно обсуждается в другом месте данного документа. В конкретных вариантах реализации изобретения генетическая модификация в локусе АроЕ приводит к снижению, повышению или модуляции активности АроЕ, активности IL-2Rg, активности Rag2, активности Rag1 и/или активности Rag2 и Rag1. В одном варианте реализации изобретения происходит выключение АроЕ, выключение Il2rg, выключение Rag2, выключение Rag1, выключение Rag2/Rag1. Как обсуждается ниже, нуклеазные агенты можно применять с любой из направляющих систем LTVEC для нацеливания на любой представляющий интерес геномный локус.
[00241] В другом варианте реализации изобретения геном подвергают воздействию белка Cas и РНК CRISPR в присутствии крупного направляющего вектора (LTVEC), содержащего нуклеотидную последовательность по меньшей мере из 10 т.п.о. В таких случаях после воздействия белка Cas, РНК CRISPR и LTVEC происходит модификация генома так, чтобы он содержал по меньшей мере 10 т.п.о. нуклеотидной последовательности. В конкретных вариантах реализации изобретения LTVEC содержит нуклеотидную последовательность, составляющую по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
v. Нуклеазные агенты и участки распознавания нуклеазных агентов
[00242] Как подробно описано выше, нуклеазные агенты можно применять в раскрытых в данном документе способах и композициях для облегчения модификации целевого локуса как в прокариотической клетке, так и в плюрипотентной или неплюрипотентной клетке крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка. Такой нуклеазный агент может стимулировать гомологичную рекомбинацию между направляющим вектором и целевым локусом. В одном варианте реализации изобретения нуклеазный агент включает эндонуклеазный агент.
[00243] Употребляемый в данном документе термин «участок распознавания нуклеазного агента» включает последовательность ДНК, в которой нуклеазный агент индуцирует одноцепочечный или двухцепочечный разрыв. Участок распознавания нуклеазного агента может быть эндогенным (или нативным) по отношению к клетке или участок распознавания может быть экзогенным по отношению к клетке. В конкретных вариантах реализации изобретения участок распознавания является экзогенным по отношению к клетке и, следовательно, в природном состоянии не присутствует в геноме клетки. В дополнительных вариантах реализации изобретения участок распознавания является экзогенным по отношению к клетке и к представляющим интерес полинуклеотидам, которые необходимо поместить в целевой геномный локус. В дополнительных вариантах реализации изобретения экзогенный или эндогенный участок распознавания присутствует только в одной копии в геноме клетки-хозяина. В конкретных вариантах реализации изобретения выявляют эндогенный или нативный участок, который находится только в одной копии в геноме. Впоследствии такой участок можно применять для конструирования нуклеазных агентов, которые будут создавать одноцепочечный или двухцепочечный разрыв в эндогенном участке распознавания.
[00244] Длина участка распознавания может варьироваться и включает, например, участки распознавания, длина которых составляет по меньшей мере 4, 6, 8, 10, 12, 14, 16, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70 или более нуклеотидов. В одном варианте реализации изобретения каждый мономер нуклеазного агента распознает участок распознавания из по меньшей мере 9 нуклеотидов. В других вариантах реализации изобретения длина участка распознавания составляет от около 9 до около 12 нуклеотидов, от около 12 до около 15 нуклеотидов, от около 15 до около 18 нуклеотидов или от около 18 до около 21 нуклеотидов и любые комбинации таких поддиапазонов (например, 9-18 нуклеотидов). Участок распознавания может быть палиндромным, что означает, что последовательность одной цепи одинаково считывается с комплементарной цепью в противоположном направлении. Известно, что нуклеазный агент может связываться с участком распознавания и расщеплять этот участок связывания или, в альтернативном варианте, нуклеазный агент может связываться с последовательностью, которая отличается от участка распознавания. Кроме того, термин участок распознавания включает как участок связывания нуклеазного агента, так и участок одноцепочечного разрыва/расщепления, независимо от того, находится ли и участок одноцепочечного разрыва/расщепления в пределах или за пределами участка связывания нуклеазного агента. В другом варианте расщепление нуклеазным агентом может происходить в нуклеотидных позициях, непосредственно противоположных по отношению к друг другу, с получением тупого разреза или, в других случаях, надрезы могут быть сделаны со сдвигом с получением одноцепочечных выступов, также называемых «липкими концами», которые могут являться как 5' липкими концами, так и 3' липкими концами.
[00245] Любой нуклеазный агент, который индуцирует одноцепочечный или двухцепочечный разрыв в необходимом участке распознавания, можно применять в раскрытых в данном документе способах и композициях. Природный или нативный нуклеазный агент можно применять до тех пор, пока нуклеазный агент индуцирует одноцепочечный или двухцепочечный разрыв в необходимом участке распознавания. В альтернативном варианте можно применять модифицированный или сконструированный нуклеазный агент. «Сконструированный нуклеазный агент» включает нуклеазу, которая была сконструирована (модифицирована или получена) на основании своей нативной формы для специфического распознавания и индукции одноцепочечного или двухцепочечного разрыва в необходимом участке распознавания. Таким образом, сконструированный нуклеазный агент может быть получен из нативного нуклеазного агента природного происхождения или он может быть создан искусственно или синтезирован. Модификация нуклеазного агента может составлять минимум одну аминокислоту в белке расщепляющего агента или один нуклеотид в нуклеиновой кислоте расщепляющего агента. В некоторых вариантах реализации изобретения сконструированный нуклеазный агент индуцирует одноцепочечный или двухцепочечный разрыв в участке распознавания, при этом участок распознавания не является последовательностью, которую распознавал бы нативный (не сконструированный или немодифицированный) нуклеазный агент. Создание одноцепочечного или двухцепочечного разрыва в участке распознавания или другой ДНК может называться в данном документе «разрезанием» или «расщеплением» участка распознавания или другой ДНК.
[00246] Также предложены активные варианты и фрагменты типовых участков распознавания. Такие активные варианты могут обладать по меньшей мере 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательностей с заданным участком распознавания, при этом активные варианты сохраняют биологическую активность и, следовательно, могут распознаваться и расщепляться нуклеазным агентом специфическим в отношении последовательности образом. В данной области техники известны методы анализа для определения наличия двухцепочечного разрыва в участке распознавания вследствие действия нуклеазного агента, и в общем случае в них определяют способность нуклеазы разрезать участок распознавания.
[00247] Участок распознавания нуклеазного агента может быть расположен в любом месте или вблизи целевого локуса. Участок распознавания может быть расположен в пределах кодирующей области гена или в пределах регуляторных областей, которые влияют на экспрессию гена. Таким образом, участок распознавания нуклеазного агента может быть расположен в интроне, экзоне, промоторе, энхансере, регуляторной области или любой не кодирующей белок области.
[00248] В одном варианте реализации изобретения нуклеазный агент представляет собой подобную активатору транскрипции эффекторную нуклеазу (TALEN). TAL эффекторные нуклеазы представляют собой класс специфических в отношении последовательностей нуклеаз, которые можно применять для создания двухцепочечных разрывов в конкретных целевых последовательностях в геноме прокариотического или эукариотического организма. TAL эффекторные нуклеазы создают путем слияния нативного или сконструированного подобного активатору транскрипции (TAL) эффектора или его функциональной части с каталитическим доменом эндонуклеазы, таким как, например, FokI. Уникальный, модульный ДНК-связывающий домен TAL эффектора позволяет конструировать белки со специфичностью распознавания потенциально любой заданной ДНК. Таким образом, ДНК-связывающие домены TAL эффекторных нуклеаз можно сконструировать для распознавания конкретных целевых участков ДНК и, следовательно, применять для создания двухцепочечных разрывов в необходимых целевых последовательностях. Смотрите, WO 2010/079430; Morbitzer et al. (2010) PNAS 10.1073/pnas.1013133107; Scholze & Boch (2010) Virulence 1: 428-432; Christian et al. Genetics (2010) 186: 757-761; Li et al. (2010) Nuc. Acids Res. (2010) doi:10.1093/nar/gkq704; и Miller et al. (2011) Nature Biotechnology 29: 143-148; которые все включены в данный документ посредством ссылки.
[00249] Примеры подходящих TAL нуклеаз и способы получения подходящих TAL нуклеаз раскрыты, например, в заявках на патент США № 2011/0239315 A1, 2011/0269234 A1, 2011/0145940 A1, 2003/0232410 A1, 2005/0208489 A1, 2005/0026157 A1, 2005/0064474 A1, 2006/0188987 A1 и 2006/0063231 A1 (каждая из которых включена в данный документ посредством ссылки). В различных вариантах реализации изобретения конструируют TAL эффекторные нуклеазы, которые делают разрез в или вблизи целевой нуклеотидной последовательности, например, в представляющем интерес геномном локусе, при этом целевая нуклеотидная последовательность находится в или вблизи последовательности, предназначенной для модификации направляющим вектором. TAL нуклеазы, подходящие для применения в различных предложенных в данном документе способах и композициях, включают те, которые были сконструированы специально для связывания в или вблизи целевых нуклеотидных последовательностей, предназначенных для модификации направляющими векторами, как описано в данном документе.
[00250] В одном варианте реализации изобретения каждый мономер TALEN содержит 12-25 TAL повторов, при этом каждый TAL повтор связывает субсайт из 1 п.о. В одном варианте реализации изобретения нуклеазный агент представляет собой химерный белок, содержащий ДНК-связывающий домен на основе TAL повторов, функционально связанный с независимой нуклеазой. В одном варианте реализации изобретения независимая нуклеаза представляет собой эндонуклеазу FokI. В одном варианте реализации изобретения нуклеазный агент содержит первый ДНК-связывающий домен на основе TAL повторов и второй ДНК-связывающий домен на основе TAL повторов, при этом каждый из первого и второго ДНК-связывающих доменов на основе TAL повторов функционально связан с нуклеазой FokI, при этом первый и второй ДНК-связывающий домен на основе TAL повторов распознают две смежные целевые последовательности ДНК на каждой цепи целевой последовательности ДНК, разделенные участком расщепления из от около 6 п.о. до около 40 п.о., и при этом нуклеазы FokI димеризуются и создают двухцепочечный разрыв в целевой последовательности.
[00251] В одном варианте реализации изобретения нуклеазный агент содержит первый ДНК-связывающий домен на основе TAL повторов и второй ДНК-связывающий домен на основе TAL повторов, при этом каждый из первого и второго ДНК-связывающих доменов на основе TAL повторов функционально связан с нуклеазой FokI, при этом первый и второй ДНК-связывающий домен на основе TAL повторов распознают две смежные целевые последовательности ДНК на каждой цепи целевой последовательности ДНК, разделенные участком расщепления из от 5 п.о. до около 6 п.о., и при этом нуклеазы FokI димеризуются и создают двухцепочечный разрыв.
[00252] Нуклеазный агент, применяемый в различных описанных в данном документе способах и композициях, может дополнительно включать цинк-пальцевую нуклеазу (ZFN). В одном варианте реализации изобретения каждый мономер ZFN содержит 3 или более ДНК-связывающих доменов на основе на основе цинковых пальцев, при этом каждый ДНК-связывающий домен на основе цинковых пальцев связывается с субсайтом из 3 п.о. В других вариантах реализации изобретения ZFN представляет собой химерный белок, содержащий ДНК-связывающий домен на основе цинковых пальцев, функционально связанный с независимой нуклеазой. В одном варианте реализации изобретения независимая нуклеаза представляет собой эндонуклеазу FokI. В одном варианте реализации изобретения нуклеазный агент содержит первый ZFN и второй ZFN, при этом каждый из первого ZFN и второго ZFN функционально связан с нуклеазой FokI, при этом первый и второй ZFN распознают две смежные целевые последовательности ДНК на каждой цепи целевой последовательности ДНК, разделенные участком расщепления из от около 6 п.о. до около 40 п.о. или участком расщепления из от около 5 п.о. до около 6 п.о., и при этом нуклеазы FokI димеризуются и создают двухцепочечный разрыв. Смотрите, например, US 20060246567; US 20080182332; US 20020081614; US 20030021776; WO/2002/057308 A2; US 20130123484; US 20100291048; и WO/2011/017293 A2, каждая из которых включена в данный документ посредством ссылки.
[00253] В одном варианте реализации предложенных в данном документе способов нуклеазный агент содержит (а) химерный белок, содержащий ДНК-связывающий домен на основе цинковых пальцев, слитый с эндонуклеазой FokI; или (b) химерный белок, содержащий подобную активатору транскрипции эффекторную нуклеазу (TALEN), слитую с эндонуклеазой FokI.
[00254] В другом варианте реализации изобретения нуклеазный агент представляет собой мегануклеазу. Мегануклеазы были разделены на четыре семейства на основании консервативных мотивов последовательностей, и этими семействами являются семейства LAGLIDADG (SEQ ID №: 16), GIY-YIG, H-N-H и His-Cys бокс. Эти мотивы участвуют в координации ионов металлов и гидролизе фосфодиэфирных связей. НЕазы известны своими длинными участками распознавания и допустимостью некоторой степени полиморфизма последовательностей в своих ДНК-субстратах. Известны домены, структура и функция мегануклеаз, смотрите, например, Guhan and Muniyappa (2003) Crit Rev Biochem Mol Biol 38: 199-248; Lucas et al., (2001) Nucleic Acids Res 29: 960-9; Jurica and Stoddard, (1999) Cell Mol Life Sci 55: 1304-26; Stoddard, (2006) Q Rev Biophys 38: 49-95; и Moure et al., (2002) Nat Struct Biol 9: 764. В некоторых примерах применяют вариант природного происхождения и/или сконструированное производное мегануклеазы. Известны способы изменения кинетики, взаимодействия кофакторов, экспрессии, оптимальных условий и/или специфичности участков распознавания, а также скрининга активности, смотрите, например, Epinat et al., (2003) Nucleic Acids Res 31: 2952-62; Chevalier et al., (2002) Mol Cell 10: 895-905; Gimble et al., (2003) Mol Biol 334: 993-1008; Seligman et al., (2002) Nucleic Acids Res 30: 3870-9; Sussman et al., (2004) J Mol Biol 342: 31-41; Rosen et al., (2006) Nucleic Acids Res 34: 4791-800; Chames et al., (2005) Nucleic Acids Res 33: e178; Smith et al., (2006) Nucleic Acids Res 34: el49; Gruen et al., (2002) Nucleic Acids Res 30: e29; Chen and Zhao, (2005) Nucleic Acids Res 33: e154; WO 2005105989; WO 2003078619; WO 2006097854; WO 2006097853; WO 2006097784; и WO 2004031346.
[00255] В данном изобретении могут быть использованы любые мегануклеазы, включая, но не ограничиваясь этим, I-SceI, I-SceII, I-SceIII, I-SceIV, I-SceV, I-SceVI, I-SceVII, I-CeuI, I-CeuAIIP, I-CreI, I-CrepsbIP, I-CrepsbIIP, I-CrepsbIIIP, I-CrepsbIVP, I-TliI, I-PpoI, PI-PspI, F-SceI, F-SceII, F-SuvI, F-TevI, F-TevII, I-AmaI, I-AniI, I-ChuI, I-CmoeI, I-CpaI, I-CpaII, I-CsmI, I-CvuI, I-CvuAIP, I-DdiI, I-DdiII, I-DirI, I-DmoI, I-HmuI, I-HmuII, I-HsNIP, I-LlaI, I-MsoI, I-NaaI, I-NanI, I-NcIIP, I-NgrIP, I-NitI, I-NjaI, I-Nsp236IP, I-PakI, I-PboIP, I-PcuIP, I-PcuAI, I-PcuVI, I-PgrIP, I-PobIP, I-PorI, 1-PorIIP, I-PbpIP, I-SpBetaIP, I-ScaI, I-SexIP, I-SneIP, I-SpomI, I-SpomCP, I-SpomIP, I-SpomIIP, I-SquIP, I-Ssp6803I, I-SthPhiJP, I-SthPhiST3P, I-SthPhiSTe3bP, I-TdeIP, I-TevI, I-TevII, I-TevIII, I-UarAP, I-UarHGPAIP, I-UarHGPA13P, I-VinIP, I-ZbiIP, PI-MtuI, PI-MtuHIP PI-MtuHIIP, PI-PfuI, PI-PfuII, PI-PkoI, PI-PkoII, PI-Rma43812IP, PI-SpBetaIP, PI-SceI, PI-TfuI, PI-TfuII, PI-ThyI, PI-TliI, PI-TliII или любые их активные варианты или фрагменты.
[00256] В одном варианте реализации изобретения мегануклеаза распознает двухцепочечные последовательности ДНК от 12 до 40 пар оснований. В одном варианте реализации изобретения мегануклеаза распознает одну идеально совпадающую целевую последовательность в геноме. В одном варианте реализации изобретения мегануклеаза представляет собой хоуминг-нуклеазу. В одном варианте реализации изобретения хоуминг-нуклеаза принадлежит семейству LAGLIDADG (SEQ ID №16) хоуминг-нуклеаз. В одном варианте реализации изобретения семейство LAGLIDADG (SEQ ID №16) хоуминг-нуклеаз выбрано из I-SceI, I-CreI и I-Dmol.
[00257] Нуклеазные агенты могут дополнительно включать рестрикционные эндонуклеазы, которые включают эндонуклеазы типа I, типа II, типа III и типа IV. Рестрикционные эндонуклеазы типа I и типа III распознают специфические участки распознавания, но, как правило, расщепляют в произвольной позиции относительно участка связывания, которая может находиться за сотни пар оснований от участка расщепления (участка распознавания). В системах типа II рестрикционная активность не зависит от какой-либо метилазной активности, а расщепление, как правило, происходит в конкретных участках в пределах или вблизи участка связывания. Большинство ферментов типа II разрезают палиндромные последовательности, при этом ферменты типа IIa распознают непалиндромные участки распознавания и расщепляют за пределами участка распознавания, ферменты типа IIb разрезают последовательности дважды с двух сторон за пределами участка распознавания, а ферменты типа IIs распознают ассиметрический участок распознавания и расщепляют с одной стороны и на определенном расстоянии, составляющем около 1-20 нуклеотидов, от участка распознавания. Рестрикционные ферменты типа IV нацелены на метилированную ДНК. Рестрикционные ферменты дополнительно описаны и классифицированы, например, в базе данных REBASE (интернет-сайт на rebase.neb.com; Roberts et al., (2003) Nucleic Acids Res 31: 418-20), Roberts et al., (2003) Nucleic Acids Res 31: 1805-12, и Belfort et al., (2002) в Mobile DNA II, pp. 761-783, Eds. Craigie et al., (ASM Press, Washington, DC).
[00258] Нуклеазный агент, применяемый в различных способах и композициях, также может включать систему CRISPR/Cas. В таких системах может применяться, например, нуклеаза Cas9, которая в некоторых случаях является кодон-оптимизированной для необходимого типа клеток, в которых она должна экспрессироваться. В таких системах также может применяться направляющая РНК (нРНК), которая содержит две отдельные молекулы. Типовая нРНК из двух молекул содержит crРНК-подобную («РНК CRISPR» или «нацеливающая РНК», или «crРНК», или «crРНК повтор») молекулу и соответствующую tracrРНК-подобную («транс-действующую РНК CRISPR» или «активирующую РНК», «tracrРНК, или «скаффолд») молекулу. crРНК содержит как ДНК-нацеливающий сегмент (одноцепочечный) нРНК, так и группу нуклеотидов, которая формирует одну половину двухцепочечной спирали РНК (дцРНК) белоксвязывающего сегмента нРНК. Соответствующая tracrРНК (активирующая РНК) содержит группу нуклеотидов, которая формирует другую половину спирали дцРНК белоксвязывающего сегмента нРНК. Таким образом, группа нуклеотидов crРНК комплементарна и гибридизируется с группой нуклеотидов tracrРНК с образованием спирали дцРНК белоксвязывающего домена нРНК. Следовательно, можно сказать, что crРНК соответствует tracrРНК. crРНК дополнительно обеспечивает одноцепочечный ДНК-нацеливающий сегмент. Соответственно, нРНК содержит последовательность, которая гибридизируется с целевой последовательностью, и tracrРНК. Таким образом, crРНК и tracrРНК (как соответствующая пара) гибридизируются с образованием нРНК. В случае применения для модификации в клетке точную последовательность и/или длину заданной молекулы crРНК или tracrРНК можно подобрать так, чтобы они оказались специфическими по отношению к виду, к которому будут применять молекулы РНК.
[00259] Гены природного происхождения, кодирующие три элемента (Cas9, tracrРНК и crРНК), как правило, входят в состав оперона(ов). РНК CRISPR природного происхождения отличаются в зависимости от системы Cas9 и организма, но часто содержат нацеливающий сегмент длиной от 21 до 72 нуклеотидов, фланкируемый двумя прямыми повторами (ПП) длиной от 21 до 46 нуклеотидов (смотрите, например, WO 2014/131833). В случае S. pyogenes длина ПП составляет 36 нуклеотидов, а длина нацеливающего сегмента составляет 30 нуклеотидов. 3' расположенный ПП является комплементарным и гибридизируется с соответствующей tracrРНК, которая в свою очередь связывается с белком Cas9.
[00260] В альтернативном варианте в системе дополнительно применяется слитая конструкция crPHK-tracrРНК (т.е. один транскрипт), которая функционирует с кодон-оптимизированной Cas9. Эта РНК часто называется направляющей РНК или нРНК. В пределах нРНК часть crРНК определяется как «целевая последовательность» для данного участка распознавания, а tracrРНК часто называется «скаффолдом». Вкратце, короткий фрагмент ДНК, содержащий целевую последовательность, вносят в экспрессионную плазмиду направляющей РНК. Экспрессионная плазмида направляющей РНК содержит целевую последовательность (в некоторых вариантах реализации изобретения около 20 нуклеотидов), форму последовательности tracrРНК (скаффолд), а также подходящий активный в клетке промотор и необходимые элементы для надлежащего процессинга в эукариотических клетках. Многие из систем основаны на индивидуально подобранных комплементарных олиго, которые гибридизируют для образования двухцепочечной ДНК, а затем клонируют в экспрессионную плазмиду нРНК. Затем экспрессионную кассету нРНК и экспрессионную кассету Cas9 вносят в клетку. Смотрите, например, Mali P et al. (2013) Science 2013 Feb 15; 339(6121): 823-6; Jinek M et al. Science 2012 Aug 17; 337(6096): 816-21; Hwang WY et al. Nat Biotechnol 2013 Mar; 31(3): 227-9; Jiang W et al. Nat Biotechnol 2013 Mar; 31(3): 233-9; и Cong L et al. Science 2013 Feb 15; 339(6121): 819-23, каждая из которых включена в данный документ посредством ссылки. Также смотрите, например, WO/2013/176772 A1, WO/2014/065596 A1, WO/2014/089290 A1, WO/2014/093622 A2, WO/2014/099750 A2 и WO/2013142578 A1, каждая из которых включена в данный документ посредством ссылки.
[00261] В некоторых вариантах реализации изобретения нуклеаза Cas9 может находиться в форме белка. В некоторых вариантах реализации изобретения белок Cas9 может находиться в форме комплекса с нРНК. В других вариантах реализации изобретения нуклеаза Cas9 может находиться в форме нуклеиновой кислоты, кодирующей белок. Нуклеиновая кислота, кодирующая нуклеазу Cas9 может представлять собой РНК (например, матричную РНК (мРНК)) или ДНК.
[00262] В некоторых вариантах реализации изобретения нРНК может находиться в форме РНК. В других вариантах реализации изобретения нРНК может находиться в форме ДНК, кодирующей нРНК. В некоторых вариантах реализации изобретения нРНК может находиться в форме отдельных молекул crРНК и tracrРНК или отдельных молекул ДНК, кодирующих, соответственно, crРНК и tracrРНК.
[00263] В одном варианте реализации изобретения способ модификации представляющего интерес геномного локуса в клетке дополнительно включает внесение в клетку: (а) первой экспрессионной конструкции, содержащей первый промотор, функционально связанный с первой нуклеотидной последовательностью, кодирующей ассоциированный с короткими палиндромными повторами, регулярно расположенными группами (CRISPR), белок (Cas); (b) второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с целевой геномной последовательностью, связанной с направляющей РНК (нРНК), при этом целевая геномная последовательность фланкируется мотивом, прилегающим к протоспейсеру. Необязательно, целевая геномная последовательность фланкируется в 3' конце последовательностью мотива, прилегающего к протоспейсеру (РАМ). В одном варианте реализации изобретения клетка включает эукариотическую клетку, некрысиную эукариотическую клетку, клетку млекопитающего, человеческую клетку, клетку отличного от человека млекопитающего, плюрипотентную клетку, неплюрипотентную клетку, нечеловеческую плюрипотентную клетку, человеческую плюрипотентную клетку, человеческую ЭС клетку, человеческую взрослую стволовую клетку, человеческую клетку-предшественника с ограниченным развитием, человеческую иПС клетку, человеческую клетку, клетку грызуна, клетку отличного от крысы грызуна, крысиную клетку, мышиную клетку, клетку хомяка, фибробласт или клетку СНО.
[00264] В одном варианте реализации изобретения целевая геномная последовательность содержит нуклеотидную последовательность GNNNNNNNNNNNNNNNNNNNNGG (GN1-20GG; SEQ ID №1). В одном варианте реализации изобретения целевая геномная последовательность содержит SEQ ID №23, где длина N составляет от 1 до 20 нуклеотидов. В другом варианте реализации изобретения длина целевой геномной последовательности составляет от 14 до 20 нуклеотидов от SEQ ID №1.
[00265] В одном варианте реализации изобретения нРНК содержит третью нуклеотидную последовательность, кодирующую РНК коротких палиндромных повторов, регулярно расположенных группами (CRISPR) (crРНК), и транс-активирующую РНК CRISPR (tracrРНК). В конкретных вариантах реализации изобретения белок Cas представляет собой Cas9.
[00266] В некоторых вариантах реализации изобретения нРНК содержит (а) химерную РНК с нуклеотидной последовательностью 5'-GUUUUAGAGCUAGAAAUAGCAAGUUAAAAUAAGGCUAGUCCGUUAUCAACUUGAAAAAGUGGCACCGAGUCGGUGCUUUU-3' (SEQ ID №2); или (b) химерную РНК с нуклеотидной последовательностью 5'-GUUUUAGAGCUAGAAAUAGCAAGUUAAAAUAAGGCUAGUCCG-3' (SEQ ID №3).
[00267] В другом варианте реализации изобретения crРНК содержит 5'-GUUUUAGAGCUAGAAAUAGCAAGUUAAAAU-3' (SEQ ID №4); 5'-GUUUUAGAGCUAGAAAUAGCAAGUUAAAAUAAG (SEQ ID №5); или 5'-GAGUCCGAGCAGAAGAAGAAGUUUUA-3' (SEQ ID №6).
[00268] В других вариантах реализации изобретения tracrРНК содержит 5'-AAGGCUAGUCCG-3' (SEQ ID №7) или 5'-AAGGCUAGUCCGUUAUCAACUUGAAAAAGUGGCACCGAGUCGGUGCUUUU-3' (SEQ ID №8).
[00269] В одном варианте реализации изобретения белок Cas представляет собой белок Cas типа I. В одном варианте реализации изобретения белок Cas представляет собой белок Cas типа II. В одном варианте реализации изобретения белок Cas типа II представляет собой Cas9. В одном варианте реализации изобретения первая нуклеотидная последовательность кодирует кодон-оптимизированный белок Cas.
[00270] В определенных вариантах реализации изобретения белок Cas представляет собой «никазу», которая может создавать одноцепочечные разрывы (т.е. «ники») в целевом участке, не разрезая обе нити двухцепочечной ДНК (дцДНК). Cas9, например, содержит два нуклеазных домена - RuvC-подобный нуклеазный домен и НМН-подобный нуклеазный домен, - которые отвечают за расщепление противоположных цепей ДНК. Мутация в любом из этих доменов может привести к созданию никазы. Примеры мутаций, приводящих к созданию никаз, можно найти, например, в WO/2013/176772 A1 и WO/2013/142578 A1, каждая из которых включена в данный документ посредством ссылки.
[00271] В определенных вариантах реализации изобретения два отдельных белка Cas (например, никазы), специфические по отношению к целевому участку на каждой цепи дцДНК, могут создавать выступающие последовательности, комплементарные выступающим последовательностям другой нуклеиновой кислоты или отдельной области той же самой нуклеиновой кислоты. Выступающие концы, полученные вследствие контакта нуклеиновой кислоты с двумя никазами, специфическими в отношении целевых участков на обоих цепях дцДНК, могут быть как 5', так и 3' выступающими концами. Например, первая никаза может создавать одноцепочечный разрыв в первой цепи дцДНК, а вторая никаза может создавать одноцепочечный разрыв во второй цепи дцДНК, что приводит к созданию выступающих концов. Целевые участки каждой никазы, создающей одноцепочечный разрыв, могут быть выбраны так, чтобы полученные последовательности выступающих концов были комплементарны последовательностям выступающих концов другой молекулы нуклеиновой кислоты. Гибридизацию комплементарных выступающих концов двух разных молекул нуклеиновых кислот можно проводить раскрытыми в данном документе способами. В некоторых вариантах реализации изобретения целевой участок никазы на первой цепи отличается от целевого участка никазы на второй цепи.
[00272] В одном варианте реализации изобретения первая нуклеиновая кислота содержит мутацию, которая приводит к разрушению по меньшей мере одного аминокислотного остатка в активных участках нуклеаз в белке Cas, при этом мутантный белок Cas создает разрыв только в одной цепи целевой области ДНК, а мутация снижает вероятность негомологичной рекомбинации в целевой области ДНК.
[00273] В одном варианте реализации изобретения первая нуклеиновая кислота, которая кодирует белок Cas, дополнительно содержит сигнал ядерной локализации (NLS). В одном варианте реализации изобретения сигнал ядерной локализации представляет собой сигнал ядерной локализации SV40.
[00274] В одном варианте реализации изобретения второй промотор, который управляет экспрессией целевой геномной последовательности и направляющей РНК (нРНК) представляет собой промотор РНК-полимеразы III. В одном варианте реализации изобретения промотор РНК-полимеразы III представляет собой промотор U6 человека. В одном варианте реализации изобретения промотор РНК-полимеразы III представляет собой промотор полимеразы III U6 крысы. В одном варианте реализации изобретения промотор РНК-полимеразы III представляет собой промотор полимеразы III U6 мыши.
[00275] В одном варианте реализации изобретения нуклеотидные последовательности, кодирующие crРНК и tracrРНК, связаны посредством синтетической петли, при этом после экспрессии crРНК и tracrРНК образуют спираль crPHK: tracrРНК,
[00276] Описанную выше систему CRISPR/Cas можно применять в комбинации с крупными направляющими векторами с любым из следующих типов клеток: эукариотической клеткой, некрысиной эукариотической клеткой, клеткой млекопитающего, клеткой отличного от человека млекопитающего, плюрипотентной клеткой, неплюрипотентной клеткой, нечеловеческой плюрипотентной клеткой, человеческой плюрипотентной клеткой, человеческой ЭС клеткой, человеческой взрослой стволовой клеткой, человеческой клеткой-предшественником с ограниченным развитием, человеческой иПС клеткой, человеческой клеткой, клеткой грызуна, клеткой отличного от крысы грызуна, крысиной клеткой, мышиной клеткой, клеткой хомяка, фибробластом или клеткой СНО.
[00277] В одном варианте реализации изобретения первая экспрессионная конструкция и вторая экспрессионная конструкция экспрессируются из одной плазмиды.
[00278] В одном варианте реализации изобретения первую и вторую экспрессионные конструкции вносят вместе с LTVEC. В одном варианте реализации изобретения первую и вторую экспрессионные конструкции вносят отдельно от LTVEC в течение некоторого времени.
[00279] В одном варианте реализации изобретения способ включает внесение нескольких вторых конструкций и нескольких LTVEC для множественного редактирования разных целевых локусов, как описано в данном документе.
[00280] Также предложены активные варианты и фрагменты нуклеазных агентов (т.е. сконструированные нуклеазные агенты). Такие активные варианты могут обладать по меньшей мере 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательностей с нативным нуклеазным агентом, при этом активные варианты сохраняют способность разрезать необходимый участок распознавания и, следовательно, сохраняют индуцирующую одноцепочечный или двухцепочечный разрыв активность. Например, любые описанные в данном документе нуклеазные агенты могут быть модифицированы относительно последовательности нативной эндонуклеазы и сконструированы для распознавания и индукции одноцепочечного или двухцепочечного разрыва на участке распознавания, который не распознавался нативным нуклеазным агентом. Таким образом, в некоторых вариантах реализации изобретения сконструированная нуклеаза обладает специфичностью в отношении индукции одноцепочечного или двухцепочечного разрыва на участке распознавания, который отличается от соответствующего участка распознавания нативного нуклеазного агента. Известны методы анализа индуцирующей одноцепочечный или двухцепочечный разрыв активности, и в общем случае в них определяют общую активность и специфичность эндонуклеаз на ДНК-субстратах, содержащих участок распознавания.
[00281] Нуклеазный агент можно вносить в клетку любыми известными в данной области техники способами. В клетку можно вносить непосредственно полипептид, кодирующий нуклеазный агент. В альтернативном варианте в клетку можно вносить полинуклеотид, кодирующий нуклеазный агент. При внесении в клетку полинуклеотида, кодирующего нуклеазный агент, нуклеазный агент может временно, при определенных условиях или конститутивно экспрессироваться в клетке. Таким образом, полинуклеотид, кодирующий нуклеазный агент, может находиться в экспрессионной кассете и быть функционально связанным с кондициональным промотором, индуцибельным промотором, конститутивным промотором или тканеспецифическим промотором. Такие представляющие интерес промоторы более подробно обсуждаются в другом месте данного документа. В альтернативном варианте нуклеазный агент вносят в клетку в виде мРНК, кодирующей или содержащей нуклеазный агент.
[00282] В одном варианте реализации изобретения crРНК и tracrРНК экспрессируются как отдельные РНК-транскрипты.
[00283] В конкретных вариантах реализации изобретения полинуклеотид, кодирующий нуклеазный агент, стабильно интегрирован в геном клетки и функционально связан с активным в клетке промотором. В других вариантах реализации изобретения полинуклеотид, кодирующий нуклеазный агент, находится в одном направляющем векторе, содержащем нуклеотидную вставку, тогда как в других случаях полинуклеотид, кодирующий нуклеазный агент, находится в векторе или плазмиде, отличном от направляющего вектора, содержащего нуклеотидную вставку.
[00284] Если нуклеазный агент вносят в клетку путем внесения полинуклеотида, кодирующего нуклеазный агент, такой полинуклеотид, кодирующий нуклеазный агент, можно модифицировать с целью замещения кодонов, имеющих большую частоту использования в представляющей интерес клетке, по сравнению с природной полинуклеотидной последовательностью, кодирующей нуклеазный агент. Например, полинуклеотид, кодирующий нуклеазный агент, можно модифицировать с целью замещения кодонов, имеющих большую частоту использования в данной представляющей интерес прокариотической или эукариотической клетке, включая бактериальную клетку, дрожжевую клетку, человеческую клетку, нечеловеческую клетку, некрысиную эукариотическую клетку, клетку млекопитающего, клетку грызуна, клетку отличного от крысы грызуна, мышиную клетку, крысиную клетку, клетку хомяка или любую другую представляющую интерес клетку-хозяина, по сравнению с природной полинуклеотидной последовательностью.
[00285] В одном варианте реализации изобретения эндонуклеазный агент вносят вместе с LTVEC. В одном варианте реализации изобретения эндонуклеазный агент вносят отдельно от LTVEC в течение некоторого времени. В одном варианте реализации изобретения эндонуклеазный агент вносят до внесения LTVEC. В одном варианте реализации изобретения эндонуклеазный агент вносят в ЭС клетку крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка после внесения LTVEC.
[00286] В одном варианте реализации изобретения эндонуклеазный агент представляет собой экспрессионную конструкцию, содержащую нуклеотидную последовательность, кодирующую эндонуклеазу, при этом нуклеотидная последовательность функционально связана с промотором. В одном варианте реализации изобретения промотор представляет собой конститутивно активный промотор. В одном варианте реализации изобретения промотор является индуцибельным промотором. В одном варианте реализации изобретения промотор активен в плюрипотентной или неплюрипотентной клетке крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка. В одном варианте реализации изобретения эндонуклеазный агент представляет собой мРНК, кодирующую эндонуклеазу.
В. Способы интеграции представляющего интерес полинуклеотида в целевой локус
[00287] Предложены способы модификации представляющего интерес целевого локуса. В одном варианте реализации изобретения целевой локус в плюрипотентной или неплюрипотентной клетке крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка предназначен для генетической модификации. Такой способ включает: (а) внесение в плюрипотентную или неплюрипотентную клетку крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка направляющего вектора, содержащего нуклеотидную вставку, фланкируемую 5' плечом гомологии крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка и 3' плечом гомологии крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка; и (b) выявление генетически модифицированной плюрипотентной или неплюрипотентной клетки крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка, содержащей направленную генетическую модификацию в целевом локусе, при этом направленная генетическая модификация может передаваться через зародышевую линию. В конкретных вариантах реализации изобретения 5' плечо гомологии и 3' плечо гомологии в общей сумме составляют по меньшей мере 10 т.п.о. и/или применяют крупный направляющий вектор.
[00288] В других вариантах реализации изобретения общий размер 5' и 3' плеч гомологии LTVEC составляет от около 10 т.п.о. до около 150 т.п.о., от около 10 т.п.о. до около 100 т.п.о., от около 10 т.п.о. до около 75 т.п.о., от около 20 т.п.о. до около 150 т.п.о., от около 20 т.п.о. до около 100 т.п.о., от около 20 т.п.о. до около 75 т.п.о., от около 30 т.п.о. до около 150 т.п.о., от около 30 т.п.о. до около 100 т.п.о., от около 30 т.п.о. до около 75 т.п.о., от около 40 т.п.о. до около 150 т.п.о., от около 40 т.п.о. до около 100 т.п.о., от около 40 т.п.о. до около 75 т.п.о., от около 50 т.п.о. до около 150 т.п.о., от около 50 т.п.о. до около 100 т.п.о. или от около 50 т.п.о. до около 75 т.п.о., от около 10 т.п.о. до около 30 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до около 150 т.п.о. В одном варианте реализации изобретения размер делеции одинаков или сходен с общим размером 5' и 3' плеч гомологии LTVEC.
[00289] Плюрипотентная клетка, например, крысиная клетка, может являться эмбриональной стволовой клеткой, например, крысиной эмбриональной стволовой клеткой. В конкретном варианте реализации изобретения (а) крысиная ЭС клетка получена от штамма DA или штамма ACI; или (b) крысиная ЭС клетка характеризуется экспрессией маркера плюрипотентности, включая Oct-4, Sox-2, щелочную фосфатазу или их комбинации. В других случаях применяемая крысиная эмбриональная стволовая клетка включает крысиную ЭС клетку, описанную в заявке на патент США №14/185103, поданной 20 февраля 2014 г., в полном объеме включенной в данный документ посредством ссылки.
[00290] В предложенных в данном документе способах можно применять любую плюрипотентную или неплюрипотентную клетку. Например, плюрипотентная или неплюрипотентная клетка может быть получена от эукариота, отличного от крысы эукариота, отличного от человека млекопитающего, млекопитающего, грызуна, отличного от крысы грызуна, крысы, мыши, человека или хомяка.
[00291] Как описано в другом месте данного документа, нуклеотидная вставка может представлять собой любую нуклеотидную последовательность. В неограничивающих вариантах реализации изобретения (а) нуклеотидная вставка содержит замещение эндогенной нуклеотидной последовательности крысы, эукариота, отличного от крысы эукариота, млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка гомологичной или ортологичной нуклеотидной последовательностью млекопитающего; (b) нуклеотидная вставка содержит удаление эндогенной нуклеотидной последовательности крысы, эукариота, отличного от крысы эукариота, млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка; (с) нуклеотидная вставка содержит удаление эндогенной нуклеотидной последовательности крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка, при этом диапазон удаления составляет от 5 т.п.о. до 200 т.п.о. или от 5 т.п.о. до 3 м.п.о. (как подробно обсуждается в другом месте данного документа); (d) нуклеотидная вставка содержит добавление экзогенной нуклеотидной последовательности (включая, например, экзогенную нуклеотидную последовательность, диапазон которой составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.); (е) нуклеотидная вставка содержит экзогенную нуклеотидную последовательность, содержащую гомологичную или ортологичную нуклеотидную последовательность; (f) гомологичную или ортологичную нуклеотидную последовательность согласно (а), при этом нуклеотидная последовательность является человеческой нуклеотидной последовательностью; (g) нуклеотидная вставка содержит гомологичную или ортологичную нуклеотидную последовательность согласно (а), при этом нуклеотидная последовательность является химерной нуклеотидной последовательностью, содержащей человеческую и крысиную нуклеотидную последовательность; (h) нуклеотидная вставка содержит экзогенную нуклеотидную последовательность согласно (е), при этом диапазон нуклеотидной вставки составляет от около 5 т.п.о. до около 200 т.п.о.; (i) нуклеотидная вставка содержит кондициональный аллель, фланкируемый целевыми последовательностями сайт-специфической рекомбиназы; (j) нуклеотидная вставка содержит репортерный ген, функционально связанный с промотором; (k) нуклеотидная вставка содержит один или более неперестроенных генных сегментов VH тяжелой цепи иммуноглобулина человека, один или более неперестроенных генных сегментов D тяжелой цепи иммуноглобулина человека и один или более неперестроенных генных сегментов JH тяжелой цепи иммуноглобулина человека, которые функционально связаны с нуклеотидной последовательностью константной области тяжелой цепи грызуна; (l) нуклеотидная вставка содержит перестроенную нуклеотидную последовательность вариабельной области тяжелой цепи иммуноглобулина человека, функционально связанную с нуклеотидной последовательностью константной области тяжелой цепи грызуна; (m) нуклеотидная вставка содержит один или более неперестроенных генных сегментов Vκ или Vλ иммуноглобулина человека и один или более неперестроенных генных сегментов Jκ или Jλ иммуноглобулина человека, которые функционально связаны с нуклеотидной последовательностью константной области λ или κ легкой цепи иммуноглобулина млекопитающего; (n) нуклеотидная вставка содержит перестроенную нуклеотидную последовательность вариабельной области λ или κ легкой цепи иммуноглобулина человека, функционально связанную с нуклеотидной последовательностью константной области λ или κ легкой цепи иммуноглобулина млекопитающего; (о) нуклеотидная последовательность константной области тяжелой цепи млекопитающего согласно (k) и/или (l) включает нуклеотидную последовательность константной области крысы, нуклеотидную последовательность константной области человека или их комбинацию; или (р) нуклеиновая кислота константной области λ или κ легкой цепи иммуноглобулина млекопитающего согласно (m) и/или (n) включает нуклеотидную последовательность константной области крысы, нуклеотидную последовательность константной области человека или их комбинацию.
[00292] В одном варианте реализации изобретения нуклеотидная вставка содержит один или более функциональных человеческих генных сегментов VH, включающих VH1-2, VH1-3, VH1-8, VH1-18, VH1-24, VH1-45, VH1-46, VH1-58, VH1-69, VH2-5, VH2-26, VH2-70, VH3-7, VH3-9, VH3-11, VH3-13, VH3-15, VH3-16, VH3-20, VH3-21, VH3-23, VH3-30, VH3-30-3, VH3-30-5, VH3-33, VH3-35, VH3-38, VH3-43, VH3-48, VH3-49, VH3-53, VH3-64, VH3-66, VH3-72, VH3-73, VH3-74, VH4-4, VH4-28, VH4-30-1, VH4-30-2, VH4-30-4, VH4-31, VH4-34, VH4-39, VH4-59, VH4-61, VH5-51, VH6-1, VH7-4-1, VH7-81 или их комбинацию.
[00293] В одном варианте реализации изобретения нуклеотидная вставка содержит один или более функциональных человеческих генных сегментов D, включающих D1-1, D1-7, D1-14, D1-20, D1-26, D2-2, D2-8, D2-15, D2-21, D3-3, D3-9, D3-10, D3-16, D3-22, D4-4, D4-11, D4-17, D4-23, D5-12, D5-5, D5-18, D5-24, D6-6, D6-13, D6-19, D6-25, D7-27 или их комбинацию.
[00294] В одном варианте реализации изобретения нуклеотидная вставка содержит один или более функциональных генных сегментов JH, включая JH1, JH2, JH3, JH4, JH5, JH6 или их комбинацию. В одном варианте реализации изобретения нуклеотидная вставка содержит один или более человеческих генных сегментов Vκ, включающих Vκ4-1, Vκ5-2, Vκ7-3, Vκ2-4, Vκ1-5, Vκ1-6, Vκ3-7, Vκ1-8, Vκ1-9, Vκ2-10, Vκ3-11, Vκ1-12, Vκ1-13, Vκ2-14, Vκ3-15, Vκ1-16, Vκ1-17, Vκ2-18, Vκ2-19, Vκ3-20, Vκ6-21, Vκ1-22, Vκ1-23, Vκ2-24, Vκ3-25, Vκ2-26, Vκ1-27, Vκ2-28, Vκ2-29, Vκ2-30, Vκ3-31, Vκ1-32, Vκ1-33, Vκ3-34, Vκ1-35, Vκ2-36, Vκ1-37, Vκ2-38, Vκ1-39, Vκ2-40 или их комбинацию.
[00295] В одном варианте реализации изобретения нуклеотидная вставка содержит один или более человеческих генных сегментов Vλ, включающих Vλ3-1, Vλ4-3, Vλ2-8, Vλ3-9, Vλ3-10, Vλ2-11, Vλ3-12, Vλ2-14, Vλ3-16, Vλ2-18, Vλ3-19, Vλ3-21, Vλ3-22, Vλ2-23, Vλ3-25, Vλ3-27 или их комбинацию.
[00296] В одном варианте реализации изобретения нуклеотидная вставка содержит один или более человеческих генных сегментов Jκ, включающих Jκ1, Jκ2, Jκ3, Jκ4, Jκ5 или их комбинацию.
[00297] В конкретных вариантах реализации изобретения после модификации целевого локуса в плюрипотентной или неплюрипотентной клетке крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка генетическая модификация передается через зародышевую линию.
[00298] В одном варианте реализации изобретения вставленная нуклеотидная последовательность содержит полинуклеотид, который при интеграции в геном будет приводить к генетической модификации области локуса АроЕ крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка, при этом генетическая модификация в локусе АроЕ приводит к снижению активности АроЕ, повышению активности АроЕ или модуляции активности АроЕ. В одном варианте реализации изобретения происходит выключение АроЕ.
[00299] В одном варианте реализации изобретения вставленная нуклеотидная последовательность содержит полинуклеотид, который при интеграции в геном будет приводить к генетической модификации области локуса рецептора интерлейкина-2 гамма крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка, при этом генетическая модификация в локусе рецептора интерлейкина-2 гамма приводит к снижению активности рецептора интерлейкина-2, повышению активности рецептора интерлейкина-2 гамма или модуляции активности рецептора интерлейкина-2. В одном варианте реализации изобретения генерируют выключение рецептора интерлейкина-2.
[00300] В другом варианте реализации изобретения вставленная нуклеотидная последовательность содержит полинуклеотид, который при интеграции в геном будет приводить к генетической модификации области локуса Rag1 крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка, локуса Rag2 крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка и/или локуса Rag2/Rag1 крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка, при этом генетическая модификация в локусе Rag1, Rag2 и/или Rag2/Rag1 крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка приводит к снижению белковой активности Rag1, Rag2 или Rag1 и Rag2, повышению белковой активности Rag1, Rag2 или Rag1 и Rag2 или модуляции белковой активности Rag1, Rag2 или Rag1 и Rag2. В одном варианте реализации изобретения генерируют выключение Rag1, Rag2 или Rag2/Rag1.
[00301] В дополнительных вариантах реализации изобретения нуклеотидная вставка приводит к замещению части локуса АроЕ, локуса рецептора интерлейкина-2 гамма и/или локуса Rag2, и/или локуса Rag1, и/или локуса Rag2/Rag1 крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка соответствующей ортологичной частью локуса АроЕ, локуса рецептора интерлейкина-2 гамма и/или локуса Rag2, локуса Rag1, и/или локуса Rag2/Rag1 другого организма.
[00302] В других вариантах реализации изобретения нуклеотидная вставка содержит полинуклеотид, обладающий по всей своей длине сходством по меньшей мере на 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% с частью локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1, которую он замещает.
[00303] Заданная полинуклеотидная вставка и соответствующая замещаемая область крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка могут быть кодирующей областью, интроном, экзоном, нетранслируемой областью, регуляторной областью, промотором или энхансером или любой их комбинацией. Кроме того, заданная полинуклеотидная вставка и/или замещаемая область крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка могут иметь любую необходимую длину, включая, например, 10-100 нуклеотидов, 100-500 нуклеотидов, 500-1 т.п.о. нуклеотидов, от 1 т.п.о. до 1,5 т.п.о. нуклеотидов, от 1,5 т.п.о. до 2 т.п.о. нуклеотидов, от 2 т.п.о. до 2,5 т.п.о. нуклеотидов, от 2,5 т.п.о. до 3 т.п.о. нуклеотидов, от 3 т.п.о. до 5 т.п.о. нуклеотидов, от 5 т.п.о. до 8 т.п.о. нуклеотидов, от 8 т.п.о. до 10 т.п.о. нуклеотидов или более. В других случаях размер вставки или замещения составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о., от около 350 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 800 т.п.о., от около 800 т.п.о. до 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о., до около 2,5 м.п.о., от около 2,5 м.п.о. до около 2,8 м.п.о., от около 2,8 м.п.о. до около 3 м.п.о. В других вариантах реализации изобретения заданная полинуклеотидная вставка и/или замещаемая область крысы, эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка составляет по меньшей мере 100, 200, 300, 400, 500, 600, 700, 800 или 900 нуклеотидов или по меньшей мере 1 т.п.о., 2 т.п.о., 3 т.п.о., 4 т.п.о., 5 т.п.о., 6 т.п.о., 7 т.п.о., 8 т.п.о., 9 т.п.о., 10 т.п.о., 11 т.п.о., 12 т.п.о., 13 т.п.о., 14 т.п.о., 15 т.п.о., 16 т.п.о. или более.
i. Способы модификации целевого локуса нуклеиновой кислоты посредством бактериальной гомологичной рекомбинации (БГР)
[00304] Предложены способы и композиции для модификации целевого локуса нуклеиновой кислоты эукариота, отличного от крысы эукариота, млекопитающего, человека или отличного от человека млекопитающего посредством бактериальной гомологичной рекомбинации (БГР) в прокариотической клетке. Такие способы находят применение в использовании бактериальной гомологичной рекомбинации в прокариотической клетке для генетической модификации целевого локуса нуклеиновой кислоты эукариота, отличного от крысы эукариота, млекопитающего, человека или отличного от человека млекопитающего с целью создания направляющего вектора. Такой направляющий вектор, содержащий генетически модифицированный целевой локус, можно вносить в эукариотическую клетку, например, эукариотическую клетку, некрысиную эукариотическую клетку, клетку млекопитающего, человеческую клетку, клетку отличного от человека млекопитающего, плюрипотентную клетку, неплюрипотентную клетку, нечеловеческую плюрипотентную клетку, человеческую плюрипотентную клетку, человеческую ЭС клетку, человеческую взрослую стволовую клетку, человеческую клетку-предшественника с ограниченным развитием, человеческую иПС клетку, человеческую клетку, клетку грызуна, клетку отличного от крысы грызуна, крысиную клетку, мышиную клетку, клетку хомяка, фибробласт или клетку СНО. «Гомологическая рекомбинация» включает обмен ДНК-фрагментами между двумя молекулами ДНК в кроссоверных участках в пределах областей гомологии. Таким образом, «бактериальная гомологичная рекомбинация» или «БГР» включает гомологичную рекомбинацию, которая происходит в бактериях.
[00305] Предложены способы модификации целевого локуса нуклеиновой кислоты из эукариотической клетки, некрысиной эукариотической клетки, клетки млекопитающего, человеческой клетки, клетки отличного от человека млекопитающего, плюрипотентной клетки, неплюрипотентной клетки, нечеловеческой плюрипотентной клетки, человеческой плюрипотентной клетки, человеческой ЭС клетки, человеческой взрослой стволовой клетки, человеческой клетки-предшественника с ограниченным развитием, человеческой иПС клетки, человеческой клетки, клетки грызуна, клетки отличного от крысы грызуна, крысиной клетки, мышиной клетки, клетки хомяка, фибробласта или клетки СНО посредством бактериальной гомологичной рекомбинации (БГР). Способы включают внесение в прокариотическую клетку направляющего вектора, содержащего нуклеотидную вставку, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом прокариотическая клетка содержит целевой локус нуклеиновой кислоты и способна экспрессировать рекомбиназу, которая опосредует БГР в целевом локусе. Такие направляющие векторы могут включать любой из описанных в данном документе крупных направляющих векторов.
[00306] В одном варианте реализации изобретения способ включает внесение в прокариотическую клетку: (i) первой конструкции, содержащей нуклеиновую кислоту, имеющую представляющую интерес последовательность ДНК; (ii) второй направляющей конструкции, содержащей нуклеотидную вставку, фланкируемую 5' плечом гомологии и 3' плечом гомологии, и (iii) третьей конструкции, кодирующей рекомбиназу, которая опосредует бактериальную гомологичную рекомбинацию. В одном варианте реализации изобретения первую, вторую и третью конструкцию вносят в прокариотическую клетку отдельно в течение некоторого времени. В одном варианте реализации изобретения прокариотическая клетка содержит нуклеиновую кислоту, которая кодирует рекомбиназу, а способ не требует внесения третьей конструкции. В одном варианте реализации изобретения рекомбиназа экспрессируется под управлением индуцибельного промотора.
[00307] В одном варианте реализации изобретения первая конструкция, содержащая нуклеиновую кислоту, получена из бактериальной искусственной хромосомы (БИХ) или дрожжевой искусственной хромосомы (ДИХ). Можно выбрать прокариотическую клетку, содержащую нуклеотидную вставку в целевом геномном локусе. Этот способ можно серийно повторять, как описано в данном документе, чтобы осуществить внесение множественных нуклеотидных вставок в целевой локус в прокариотической клетке. После «встраивания» целевого локуса нуклеиновой кислоты в прокариотическую клетку направляющий вектор, содержащий модифицированный целевой локус, можно выделять из прокариотической клетки и вносить в целевой геномный локус в эукариотической клетке, некрысиной эукариотической клетке, клетке млекопитающего, клетке человека, клетке отличного от человека млекопитающего, плюрипотентной клетке, неплюрипотентной клетке, нечеловеческой плюрипотентной клетке, человеческой плюрипотентной клетке, человеческой ЭС клетке, человеческой взрослой стволовой клетке, человеческой клетке-предшественнике с ограниченным развитием, человеческой иПС клетке, человеческой клетке, клетке грызуна, клетке отличного от крысы грызуна, клетке крысы, клетке мыши, клетке хомяка, фибробласте или клетке СНО.
[00308] Предпочтительные крысиные клетки для получения направляющих векторов описаны в заявке на патент США 14/185703, поданной 20 февраля 2014 г., содержание которой кратко изложено в данном документе. Эти крысиные клетки являются плюрипотентными крысиными клетками, способными сохранять свою плюрипотентность после одной или более направленных генетических модификаций in vitro и способны передавать направленные генетические модификации через зародышевую линию.
[00309] Электропорированные плюрипотентные клетки, например, высевают с высокой плотностью для отбора устойчивых к лекарственному препарату клеток, содержащих направляющий вектор. Процесс отбора по чувствительности к лекарственному препарату приводит к удалению большинства высеянных клеток (~99%), оставляя отдельные колонии, каждая из которых является клоном, полученным от одной клетки. Среди оставшихся клеток большинство клеток (~80-100%) содержат направляющий вектор (содержащий кассету отбора по чувствительности к лекарственному препарату), интегрированный в случайный участок генома. Следовательно, колонии собирают по отдельности и проводят генотипирование для выявления ЭС клеток, содержащих направляющий вектор в правильном участке генома (например, применяя анализ модификации аллеля, описанный ниже).
[00310] Для генотипирования можно применять высокопроизводительный количественный анализ, а именно анализ модификации аллеля (МОА). Такой анализ позволяет проводить крупномасштабный скрининг модифицированного(ых) аллеля(ей) в родительской хромосоме после генетической модификации. Анализ МОА можно проводить при помощи различных аналитических методов, включая, но не ограничиваясь этим, количественную ПЦР, например, ПЦР в режиме реального времени (кПЦР). Например, ПЦР в режиме реального времени включает применение первой группы праймеров, которая распознает целевой локус, и второй группы праймеров, которая распознает нецелевой контрольный локус. Кроме того, группа праймеров содержит флуоресцентный зонд, который распознает амплифицированную последовательность. В одном варианте реализации изобретения количественный анализ проводят при помощи Invader Probes®. В одном варианте реализации изобретения количественный анализ проводят при помощи ММР assays®. В одном варианте реализации изобретения количественный анализ проводят при помощи TaqMan® Molecular Beacon. В одном варианте реализации изобретения количественный анализ проводят при помощи метода зондов Eclipse™. (Смотрите, например, US 2005/0144655, которая в полном объеме включена в данный документ посредством ссылки).
[00311] Затем отобранную плюрипотентную клетку (т.е. нечеловеческую плюрипотентную клетку, нечеловеческую ЭС клетку), содержащую направленную генетическую модификацию, можно вносить в эмбрион-хозяина, например, в эмбрион на стадии пре-морулы или на стадии бластоцисты, и имплантировать в матку суррогатной матери для получения животного-основателя (F0-животного). После этого животное-основателя можно скрещивать с животным дикого типа для получения потомства F1, гетерозиготного в отношении генетической модификации. Спаривание гетерозиготных животных F1 может дать потомство, гомозиготное в отношении генетической модификации. Спаривание гетерозиготных животных F1 может дать потомство, гомозиготное в отношении генетической модификации. В некоторых вариантах реализации изобретения можно осуществлять различные описанные в данном документе генетические модификации целевых локусов, применяя крупный направляющий вектор (LTVEC), как подробно описано в другом месте данного документа. Например, LTVEC может быть получен из ДНК бактериальной искусственной хромосомы (БИХ) при помощи метода генной инженерии VELOCIGENE® (смотрите, например, патент США №6586251 и Valenzuela, D.M. et al. (2003), High-throughput engineering of the mouse genome coupled with high-resolution expression analysis, Nature Biotechnology 21(6); 652-659, которые в полном объеме включены в данный документ посредством ссылки).
[00312] Применение бактериальной гомологичной рекомбинации (БГР) для получения крупного направляющего вектора (LTVEC) снимает ограничения, возникающие вследствие невозможности помещения крупных фрагментов геномной ДНК в плазмиды и связанной с этим низкой эффективностью внесения направленных модификаций в эндогенный локус в плюрипотентных или неплюрипотентных клетках. Путем получения LTVEC можно осуществить одну или более направленных генетических модификаций. Типовой LTVEC, получаемый в прокариотической клетке, может содержать нуклеотидную вставку, которая несет геномную последовательность с одной или более генетическими модификациями или экзогенную нуклеиновую кислоту (например, гомолог или ортолог крысиной нуклеиновой кислоты), которая фланкируется плечами гомологии, комплементарными к конкретным геномным областям.
[00313] Также предложены прокариотические клетки-хозяева, содержащие различные описанные в данном документе направляющие векторы. Такие прокариотические клетки включают, но не ограничиваются этим, бактерии, такие как Е.coli. В одном варианте реализации изобретения прокариотическая клетка-хозяин содержит направляющий вектор, содержащий нуклеотидную вставку, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом диапазон нуклеотидной вставки составляет от около 5 т.п.о. до около 200 т.п.о.
[00314] Прокариотическая клетка-хозяин может дополнительно содержать нуклеиновую кислоту, которая кодирует полипептид рекомбиназы, или нуклеиновая кислота, которая кодирует полипептид рекомбиназы, функционально связана с индуцибельным промотором.
[00315] Дополнительно предложены различные способы и композиции, в которых применяют описанный в данном документе LTVEC в комбинации с прокариотической клеткой с целью получения направленных генетических модификаций. Такие композиции и способы обсуждаются в другом месте данного документа.
[00316] Предложены способы модификации целевого локуса нуклеиновой кислоты посредством бактериальной гомологичной рекомбинации (БГР), которые включают внесение в прокариотическую клетку направляющего вектора, содержащего нуклеотидную вставку, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом прокариотическая клетка содержит нуклеиновые кислоты, соответствующие 5' и 3' плечам гомологии, и способна экспрессировать рекомбиназу, которая опосредует БГР в целевом локусе. Такие направляющие векторы могут включать любой из описанных в данном документе крупных направляющих векторов. В таких способах LTVEC можно применять так, как подробно обсуждается в данном документе, а также дополнительно применять систему CRISPR/Cas, как обсуждается в другом месте данного документа.
[00317] В одном варианте реализации изобретения система CRISPR/Cas может находиться под управлением промотора, активного в прокариотической клетке, такой как, например, E.coli.
ii. Способы модификации представляющего интерес целевого локуса в плюрипотентной клетке или неплюрипотентной клетке.
[00318] Дополнительно предложен способ модификации представляющего интерес целевого локуса в плюрипотентной клетке или неплюрипотентной клетке посредством направленной генетической модификации, включающий (а) внесение в плюрипотентную клетку или неплюрипотентную клетку направляющего вектора, содержащего нуклеотидную вставку, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом 5' плечо гомологии и 3' плечо гомологии в общей сумме составляют по меньшей мере 10 т.п.о.; и (b) выявление генетически модифицированной плюрипотентной или неплюрипотентной клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе. В одном варианте реализации изобретения 5' плечо гомологии и 3' плечо гомологии в общей сумме составляют по меньшей мере от около 16 т.п.о. до около 30 т.п.о. В конкретных вариантах реализации изобретения направленная генетическая модификация может передаваться через зародышевую линию. Такие направляющие векторы могут включать любой из описанных в данном документе крупных направляющих векторов.
[00319] Также в способах модификации предложенного в данном документе представляющего интерес целевого локуса можно применять различные клетки. В конкретных вариантах реализации изобретения клетка является эукариотической клеткой, некрысиной эукариотической клеткой, плюрипотентной клеткой, неплюрипотентной клеткой, нечеловеческой плюрипотентной клеткой, человеческой плюрипотентной клеткой, человеческой ЭС клеткой, человеческой взрослой стволовой клеткой, человеческой клеткой-предшественником с ограниченным развитием, человеческой индуцированной плюрипотентной клеткой (иПС), клеткой млекопитающего, человеческой клеткой, фибробластом, клеткой грызуна, клеткой отличного от крысы грызуна, мышиной клеткой, клеткой хомяка или клеткой СНО.
[00320] В одном аспекте предложен способ модификации представляющего интерес целевого локуса в плюрипотентной клетке посредством направленной генетической модификации, включающий: (а) получение плюрипотентной клетки, которая способна сохранять свою плюрипотентность после по меньшей мере одной направленной генетической модификации ее генома и способна передавать направленную модификацию зародышевой линии поколения F1; (b) внесение крупного направляющего вектора (LTVEC) в плюрипотентную клетку, при этом LTVEC содержит нуклеотидную вставку, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом 5' плечо гомологии и 3' плечо гомологии содержат фрагмент геномной ДНК; и (с) выявление генетически модифицированной плюрипотентной клетки, содержащей направленную генетическую модификацию.
[00321] Для выявления клеток, содержащих нуклеотидную вставку, интегрированную в представляющий интерес целевой локус, можно применять различные способы. Вставка нуклеиновой кислоты в представляющий интерес целевой локус приводит к «модификации аллеля». Термин «модификация аллеля» и способы выявления модифицированного аллеля более подробно обсуждаются в другом месте данного документа.
[00322] В одном аспекте предложен способ модификации представляющего интерес целевого локуса в неплюрипотентной клетке или плюрипотентной клетке посредством опосредованного эндонуклеазами направленного воздействия на гены, включающий: (а) получение выделенной неплюрипотентной клетки или выделенной плюрипотентной клетки, которая способна передавать генетически модифицированный геном зародышевой линии поколения F1; (b) внесение в неплюрипотентную клетку или плюрипотентную клетку эндонуклеазного агента; при этом эндонуклеазный агент создает одноцепочечный или двухцепочечный разрыв в целевой последовательности ДНК, расположенной в представляющем интерес геномном локусе, а одноцепочечный или двухцепочечный разрыв в целевой последовательности ДНК в неплюрипотентной клетке или плюрипотентной клетке индуцирует: (i) опосредованную негомологичным соединением концов (НГСК) репарацию ДНК в месте одноцепочечного или двухцепочечного разрыва, при этом НГСК-опосредованная репарация ДНК приводит к созданию мутантного аллеля, содержащего вставку или удаление нуклеотидной последовательности в целевой последовательности ДНК; или (ii) опосредованную гомологичной рекомбинацией репарацию ДНК, которая приводит к восстановлению нуклеотидной последовательности дикого типа; и (с) выявление представляющего интерес модифицированного геномного локуса.
[00323] В одном аспекте предложен способ модификации представляющего интерес целевого локуса в выделенной эмбриональной стволовой клетке (ЭС) при помощи нуклеазного агента, включающий: (а) получение выделенной ЭС клетки, которая способна передавать направленную модификацию зародышевой линии поколения F1; (b) внесение в ЭС клетку: (i) крупного направляющего вектора (LTVEC), содержащего нуклеотидную вставку, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом вставка представляет собой нуклеотидную последовательность по меньшей мере из 5 т.п.о.; и (ii) эндонуклеазного агента, при этом эндонуклеазный агент создает одноцепочечный или двухцепочечный разрыв в целевой последовательности ДНК, расположенной в представляющем интерес геномном локусе, а целевая последовательность не присутствует в нуклеотидной вставке; и (с) выявление направленной генетической модификации в эмбриональной стволовой (ЭС) клетке.
[00324] В одном аспекте предложен способ модификации представляющего интерес целевого локуса в неплюрипотентной клетке или плюрипотентной клетке посредством РНК-управляемой генной инженерии, включающий: (а) получение неплюрипотентной клетки или плюрипотентной клетки, которая способна передавать генетически модифицированный геном зародышевой линии поколения F1; (b) внесение в неплюрипотентную клетку или плюрипотентную клетку: (i) первой экспрессионной конструкции, содержащей первый промотор, функционально связанный с первой нуклеотидной последовательностью, кодирующей ассоциированный с короткими палиндромными повторами, регулярно расположенными группами (CRISPR), белок (Cas), (ii) второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с целевой геномной последовательностью, связанной с направляющей РНК (нРНК), при этом целевая геномная последовательность фланкируется последовательностью мотива, прилегающего к протоспейсеру (РАМ). Необязательно, целевая геномная последовательность фланкируется в 3' конце последовательностью мотива, прилегающего к протоспейсеру (РАМ). В одном варианте реализации изобретения белок Cas и РНК CRISPR и/или tracrРНК не встречаются вместе в природном состоянии (например, белок Cas и РНК CRISPR не встречаются вместе в природном состоянии). В одном варианте реализации изобретения целевая геномная последовательность содержит нуклеотидную последовательность GNNNNNNNNNNNNNNNNNNNNNGG (GN1-20GG; SEQ ID №1). В одном варианте реализации изобретения целевая геномная последовательность содержит SEQ ID №1, где длина N составляет от 14 до 20 нуклеотидов. В одном варианте реализации изобретения нРНК содержит третью нуклеотидную последовательность, кодирующую РНК коротких палиндромных повторов, регулярно расположенных группами (CRISPR) (crРНК), и четвертую нуклеотидную последовательность, кодирующую транс-активирующую РНК CRISPR (tracrРНК). В одном варианте реализации изобретения после экспрессии белок Cas образует комплекс CRISPR-Cas, содержащий crРНК и tracrРНК, a комплекс CRISPR-Cas создает одноцепочечный или двухцепочечный разрыв в целевой последовательности ДНК, расположенной в представляющем интерес геномном локусе, а одноцепочечный или двухцепочечный разрыв в целевой последовательности ДНК в неплюрипотентной клетке или плюрипотентной клетке индуцирует: (i) опосредованную негомологичным соединением концов (НГСК) репарацию ДНК в месте одноцепочечного или двухцепочечного разрыва, созданного комплексом CRISPR-Cas, при этом НГСК приводит к созданию мутантного аллеля, содержащего вставку или удаление нуклеотидной последовательности в целевой последовательности ДНК; или (ii) опосредованную гомологичной рекомбинацией репарацию ДНК, которая приводит к восстановлению нуклеотидной последовательности дикого типа; и (с) выявление представляющего интерес модифицированного геномного локуса.
[00325] В одном аспекте предложен способ модификации представляющего интерес целевого локуса в неплюрипотентной клетке или плюрипотентной клетке посредством РНК-управляемой генной инженерии, включающий внесение в неплюрипотентную клетку или плюрипотентную клетку, которая способна передавать генетически модифицированный геном через зародышевую линию: (i) ассоциированного с короткими палиндромными повторами, регулярно расположенными группами (CRISPR), белка (Cas) или нуклеиновой кислоты, кодирующей белок Cas; и (ii) нРНК или ДНК, кодирующей нРНК, при этом нРНК содержит нуклеотидную последовательность, которая гибридизируется с целевой геномной последовательностью, и тран-активирующей РНК CRISPR (tracrРНК); при этом целевая геномная последовательность фланкируется последовательностью мотива, прилегающего к протоспейсеру (РАМ).
[00326] В некоторых вариантах реализации изобретения белок Cas можно вносить в неплюрипотентную клетку или плюрипотентную клетку в виде выделенного белка. В некоторых вариантах реализации изобретения белок Cas дополнительно содержит домен, пенетрирующий клетку, который облегчает поглощение белка клеткой. В других вариантах реализации изобретения белок Cas можно вносить в клетку в виде молекулы матричной РНК (мРНК), кодирующей белок Cas. В других вариантах реализации изобретения белок Cas можно вносить в клетку в виде молекулы ДНК, кодирующей белок Cas. Например, молекула ДНК, кодирующая белок Cas, может находиться в конструкции и быть функционально связанной с промотором, способным экспрессировать в неплюрипотентной клетке или плюрипотентной клетке. В определенных вариантах реализации изобретения нуклеиновая кислота, кодирующая белок Cas, является кодон-оптимизированной для экспрессии в неплюрипотентной клетке или плюрипотентной клетке.
[00327] В некоторых вариантах реализации изобретения нРНК можно вносить в неплюрипотентную клетку или плюрипотентную клетку в виде молекулы РНК. Например, молекула нРНК может быть транскрибирована in vitro. В других вариантах реализации изобретения нРНК можно вносить в неплюрипотентную клетку или плюрипотентную клетку в виде молекулы ДНК, кодирующей нРНК. Например, молекула ДНК, кодирующая нРНК, может находиться в конструкции и быть функционально связанной с промотором, способным экспрессировать нРНК в неплюрипотентной клетке или плюрипотентной клетке. В других вариантах реализации изобретения нРНК можно синтезировать химическим путем.
[00328] В некоторых вариантах реализации изобретения нРНК можно вносить в неплюрипотентную клетку или плюрипотентную клетку в виде слитой молекулы crРНК-tracrРНК (т.е. одного транскрипта). В других вариантах реализации изобретения нРНК можно вносить в неплюрипотентную клетку или плюрипотентную клетку в виде отдельных молекул crРНК и tracrРНК (т.е. отдельных транскриптов). В других вариантах реализации изобретения нРНК можно вносить в неплюрипотентную клетку или плюрипотентную клетку в виде отдельных молекул ДНК, кодирующих, соответственно, crРНК и tracrРНК. Например, отдельные молекулы ДНК, кодирующие crРНК и tracrРНК, могут находиться в отдельных конструкциях и быть функционально связанными с промоторами, способными экспрессировать нРНК в неплюрипотентной клетке или плюрипотентной клетке. В любом из вышеописанных вариантов реализации изобретения любые комбинации конструкций могут находиться в отдельных молекулах нуклеиновых кислот или вместе в одной молекуле нуклеиновой кислоты.
[00329] В некоторых вариантах реализации изобретения белок Cas и нРНК можно вносить в неплюрипотентную клетку или плюрипотентную клетку одновременно или последовательно. Аналогично, crРНК и tracrРНК нРНК можно вносить в неплюрипотентную клетку или плюрипотентную клетку одновременно или последовательно. Соотношение между белком Cas (или кодирующей нуклеиновой кислотой) и нРНК (или кодирующей ДНК) и/или соотношение между crРНК и tracrРНК может быть приблизительно стехиометрическим, чтобы они могли образовать РНК-белковый комплекс.
[00330] В определенных вариантах реализации изобретения белок Cas можно вносить в неплюрипотентную клетку или плюрипотентную клетку в виде комплекса с нРНК.
[00331] В одном варианте реализации изобретения плюрипотентная клетка представляет собой индуцированную плюрипотентную клетку (иПС). В одном варианте реализации изобретения плюрипотентная клетка представляет собой клетку-предшественника с ограниченным развитием.
[00332] Наличие одноцепочечного или двухцепочечного разрыва в участке распознавания в пределах селективного маркера в различных вариантах реализации изобретения повышает эффективность и/или частоту рекомбинации между направляющим вектором (таким как LTVEC) и представляющим интерес целевым локусом. В одном варианте реализации изобретения рекомбинация является гомологичной рекомбинацией. В другом варианте реализации изобретения рекомбинация представляет собой вставку вследствие негомологичного соединения концов. В различных вариантах реализации изобретения в случае наличия одноцепочечного или двухцепочечного разрыва эффективность таргетирования направляющего вектора (такого как LTVEC) в целевом геномном локусе по меньшей мере в около 2 раз выше, по меньшей мере в около 3 раз выше, по меньшей мере в около 4 раз выше, чем в случае отсутствия одноцепочечного или двухцепочечного разрыва (при применении, например, одного и того же направляющего вектора и одних и тех же плеч гомологии и соответствующих целевых участков в представляющем интерес геномном локусе, но без добавляемого нуклеазного агента, который создает одноцепочечный или двухцепочечный разрыв).
[00333] В одном варианте реализации изобретения направленная генетическая модификация в целевом локусе является биаллельной. Под «биаллельной» подразумевается, что оба аллеля гена содержат направленную генетическую модификацию. В каждом аллеле направленная генетическая модификация может быть одинаковой или разной. Например, биаллельная модификация может быть результатом одной модификации, проведенной в соответствующих аллелях в соответствующих гомологичных хромосомах, или разных модификаций, проведенных в соответствующих аллелях в соответствующих гомологичных хромосомах. Таким образом, биаллельная модификация может приводить, например, к гомозиготности в отношении конкретной модификации в представляющем интерес геномном локусе (т.е. конкретной модификации в обоих аллелях), компаунд-гетерозиготности в представляющем интерес геномном локусе (т.е. конкретной модификации в одном аллеле и инактивации или нарушению другого аллеля) или гемизиготности в представляющем интерес геномном локусе (например, конкретной модификации в одном аллеле и потере другого аллеля). В определенных вариантах реализации изобретения комбинированное применение направляющего вектора (включая, например, LTVEC) с нуклеазным агентом приводит к биаллельной направленной генетической модификации в представляющем интерес геномном локусе в клетке по сравнению с применением одного направляющего вектора. Когда направляющий вектор применяют в сочетании с нуклеазным агентом эффективность биаллельного таргетирования возрастает по меньшей мере в два раза, по меньшей мере в три раза, по меньшей мере в 4 раза или более по сравнению с применением одного направляющего вектора. В дополнительных вариантах реализации изобретения эффективность биаллельного таргетирования составляет по меньшей мере 0,2%, 0,3%, 0,4%, 0,5%, 0,6%, 0,7%, 0,8%, 0,9%, 1%, 2%, 3%, 4% или 5% или более.
[00334] Биаллельная направленная генетическая модификация в целевом локусе может приводить к получению гомозиготной генетически модифицированной клетки. Под «гомозиготной» подразумевается, что оба аллеля целевого локуса (т.е. аллели в обеих гомологичных хромосомах) были модифицированы одинаково. В определенных вариантах реализации изобретения комбинированное применение направляющего вектора (включая, например, LTVEC) с нуклеазным агентом приводит к биаллельной гомозиготной направленной генетической модификации в представляющем интерес геномном локусе в клетке. В одном варианте реализации изобретения биаллельная генетическая модификация включает удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе в двух гомологичных хромосомах (т.е. паре из первой и второй гомологичных хромосом) и вставку нуклеиновой кислоты в представляющий интерес геномный локус в двух гомологичных хромосомах (т.е. паре из первой и второй гомологичных хромосом). В некоторых вариантах реализации изобретения нуклеотидная вставка замещает эндогенную нуклеотидную последовательность в представляющем интерес геномном локусе в обеих гомологичных хромосомах. В одном варианте реализации изобретения нуклеотидная вставка является гомологичной или ортологичной по отношению к удаленной эндогенной нуклеотидной последовательности.
[00335] В одном варианте реализации изобретения направленная генетическая модификация в целевом локусе приводит к получению гемизиготной генетически модифицированной клетки. Под «гемизиготной» подразумевается, что присутствует только один аллель (т.е. аллель в одной из двух гомологичных хромосом) целевого локуса или только один аллель может экспрессироваться и функционировать. В других вариантах реализации изобретения направленная генетическая модификация в более общем случае приводит к компаунд-гетерозиготности. Компаунд-гетерозиготность включает ситуации, в которых были модифицированы оба аллеля целевого локуса (т.е. аллели в обеих гомологичных хромосомах), но модифицированы разным образом (например, вставка в одном аллеле и инактивация или нарушение другого аллеля). В определенных вариантах реализации изобретения комбинированное применение направляющего вектора (включая, например, LTVEC) с нуклеазным агентом приводит к гемизтготной направленной генетической модификации в представляющем интерес геномном локусе в клетке. В определенных вариантах реализации изобретения комбинированное применение направляющего вектора (включая, например, LTVEC) с нуклеазным агентом приводит к направленным генетическим модификациям, которые создают компаунд-гетерозиготность в представляющем интерес геномном локусе в клетке. В одном варианте реализации изобретения направленная генетическая модификация в представляющем интерес геномном локусе в одной хромосоме включает удаление эндогенной нуклеотидной последовательности и вставку нуклеиновой кислоты. В других вариантах реализации изобретения направленная генетическая модификация включает: (1) удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе в двух гомологичных хромосомах; и (2) вставку нуклеиновой кислоты в представляющий интерес геномный локус в первой хромосоме и нарушение представляющего интерес геномного локуса во второй хромосоме. Первая хромосома может быть первой из двух гомологичных хромосом, а вторая хромосома может быть второй из двух гомологичных хромосом. В других вариантах реализации изобретения направленная модификация включает: (1) удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе и вставку нуклеиновой кислоты в представляющий интерес геномный локус в первой гомологичной хромосоме; и (2) нарушение представляющего интерес геномного локуса во второй гомологичной хромосоме. Нарушение эндогенной нуклеотидной последовательности может происходить, например, когда происходит репарация созданного нуклеазным агентом одноцепочечного или двухцепочечного разрыва в представляющем интерес геномном локусе путем опосредуемой негомологичным соединением концов (НГСК) репарации ДНК, что приводит к созданию мутантного аллеля, содержащего вставку или удаление нуклеотидной последовательности в представляющем интерес геномном локусе, и, следовательно, приводит к разрушению представляющего интерес геномного локуса. Примеры нарушений включают изменение регуляторного элемента (например, промотора или энхансера) в представляющем интерес геномном локусе, миссенс-мутацию, мутацию с усечением, нуль-мутацию или вставку или удаление небольшого количества нуклеотидов (например, приводящие к мутации со сдвигом рамки). Другим примером нарушения является нонсенс-мутация. Нарушение может приводить к инактивации (т.е. потере функции) или потере аллеля.
[00336] Гомозиготные и гемизиготные генетические модификации имеют преимущество, так как в случае применения генетически модифицированных клеток, содержащих эти мутации, для получения генетически модифицированных животных, как обсуждается ниже, процесс получения генетически модифицированных животных, которые являются негетерозиготными (т.е. гомозиготными или гемизиготными) в отношении предполагаемой направленной генетической модификации, является более эффективным и менее времязатратным, так как требуется меньшее количество этапов разведения. Направленные генетические модификации, приводящие к компаунд-гетерозиготности или гемизиготности (т.е. вставке в одном аллеле и инактивации, нарушению или потере другого аллеля), могут иметь преимущество по той же причине.
[00337] В любом из различных вышеописанных способов модификации геномного локуса при помощи нуклеазного агента также можно использовать различные типы клеток. В конкретных вариантах реализации изобретения клетка является эукариотической клеткой, некрысиной эукариотической клеткой, плюрипотентной клеткой, неплюрипотентной клеткой, нечеловеческой плюрипотентной клеткой, человеческой плюрипотентной клеткой, человеческой ЭС клеткой, человеческой взрослой стволовой клеткой, человеческой клеткой-предшественником с ограниченным развитием, человеческой индуцированной плюрипотентной клеткой (иПС), клеткой млекопитающего, человеческой клеткой, фибробластом, клеткой грызуна, клеткой отличного от крысы грызуна, мышиной клеткой, клеткой хомяка или клеткой СНО.
[00338] Предложены композиции, которые включают применение генетически модифицированного отличного от человека животного, имеющего генетическую модификацию в локусе рецептора интерлейкина-2 гамма или в локусе АроЕ. Различные предложенные в данном документе способы и композиции позволяют передавать эти модифицированные локусы через зародышевую линию.
[00339] В конкретных вариантах реализации изобретения генетически модифицированное отличное от человека животное или генетически модифицированная плюрипотентная или неплюрипотентная клетка содержит геномный локус, содержащий направленную генетическую модификацию в локусе рецептора интерлейкина-2 гамма или содержащий направленную генетическую модификацию в локусе АроЕ, при этом геномный локус рецептора интерлейкина-2 гамма или локус АроЕ содержит: (i) удаление по меньшей мере части локуса рецептора интерлейкина-2 гамма или по меньшей мере части локуса АроЕ; (ii) вставку гетерологичной нуклеотидной последовательности в локус АроЕ или в локус рецептора интерлейкина-2 гамма; или (iii) их комбинацию, при этом генетически модифицированный геномный локус может передаваться через зародышевую линию.
[00340] Дополнительно предложены способы, которые позволяют получать таких генетически модифицированных отличных от человека животных или такие генетически модифицированные плюрипотентные клетки. Такие способы включают способ модификации геномного локуса АроЕ или локуса рецептора интерлейкина-2 гамма в плюрипотентной клетке посредством направленной генетической модификации. Указанный способ включает (а) внесение в плюрипотентную клетку направляющего вектора, содержащего нуклеотидную вставку, фланкируемую 5' плечом гомологии в локус АроЕ и 3' плечом гомологии в локус АроЕ, (b) выявление генетически модифицированной плюрипотентной клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе АроЕ, при этом направленная генетическая модификация может передаваться через зародышевую линию.
[00341] Дополнительные способы включают (а) внесение в плюрипотентную клетку направляющего вектора, содержащего нуклеотидную вставку, фланкируемую 5' плечом гомологии в локус рецептора интерлейкина-2 гамма и 3' плечом гомологии в локус рецептора интерлейкина-2 гамма, (b) выявление генетически модифицированной плюрипотентной клетки, содержащей направленную генетическую модификацию в локусе рецептора интерлейкина-2 гамма, при этом направленная генетическая модификация может передаваться через зародышевую линию.
iii. Способы интеграции множественных представляющих интерес полинуклеотидов в целевой локус
[00342] Различные предложенные в данном документе способы и композиции позволяют осуществлять направленную интеграцию множественных представляющих интерес полинуклеотидов в заданный целевой локус. Можно осуществлять последовательный повтор различных приведенных выше способов, чтобы обеспечить направленную интеграцию любого количества нуклеотидных вставок в заданный целевой локус. Таким образом, различные способы предусматривают вставку по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более нуклеиновых кислот в целевой локус. В конкретных вариантах реализации изобретения такие способы последовательных изменений позволяют реконструировать крупные геномные области из эукариотической клетки, например, некрысиной эукариотической клетки, клетки млекопитающего (т.е. человека, не человека, грызуна, отличного от крысы грызуна, мыши, обезьяны, крысы, хомяка, домашнего млекопитающего или сельскохозяйственного животного) в целевом локусе. В таких случаях перенос и реконструкция геномных областей, которые содержат как кодирующие, так и некодирующие области, позволяют сохранить сложность заданной области путем по меньшей мере частичного сохранения кодирующих областей, некодирующих областей и вариаций числа копий, присущих нативной геномной области. Таким образом, в различных способах предложены, например, способы получения «гетерологичных» или «экзогенных» геномных областей в любой эукариотической клетке, любой некрысиной эукариотической клетке, любой клетке млекопитающего или представляющего интерес животного, в частности, в прокариотической клетке-хозяине или в неплюрипотентной клетке, плюрипотентной клетке или ЭС клетке. В одном неограничивающем примере получают «гуманизированную» геномную область в отличном от человека животном (т.е. в крысе). В данном документе предложены способы получения геномных областей в любой клетке. В конкретных вариантах реализации изобретения клетка является эукариотической клеткой, некрысиной эукариотической клеткой, плюрипотентной клеткой, неплюрипотентной клеткой, нечеловеческой плюрипотентной клеткой, человеческой плюрипотентной клеткой, человеческой ЭС клеткой, человеческой взрослой стволовой клеткой, человеческой клеткой-предшественником с ограниченным развитием, человеческой индуцированной плюрипотентной клеткой (иПС), клеткой млекопитающего, человеческой клеткой, фибробластом, клеткой грызуна, клеткой отличного от крысы грызуна, мышиной клеткой, клеткой хомяка или клеткой СНО.
3. Гуманизированный геномный локус
[00343] В данном документе предложены различные способы и композиции, включающие применение гуманизированного геномного локуса. В контексте данного документа под «гуманизированным» геномным локусом подразумевается область нечеловеческого генома, содержащая по меньшей мере одну человеческую нуклеотидную последовательность. Гуманизированный геномный локус может содержать область ДНК из любого организма, в которую вставлена человеческая последовательность ДНК. В конкретных вариантах реализации изобретения организм является эукариотом, отличным от крысы эукариотом, отличным от человека млекопитающим, млекопитающим, человеком, грызуном, отличным от крысы грызуном, крысой, мышью или хомяком. Например, «гуманизированный крысиный локус» содержит область крысиной ДНК, в которую вставлена человеческая последовательность ДНК.
[00344] Человеческая последовательность ДНК может быть человеческой последовательностью ДНК природного происхождения или может быть модифицирована относительно нативной формы. В конкретных вариантах реализации изобретения человеческая последовательность ДНК обладает по меньшей мере 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности последовательностей с нативной человеческой последовательностью. Если человеческая последовательность не является нативной человеческой последовательностью, она обладает большей идентичностью последовательностей с нативной человеческой последовательностью, чем с ортологичной нечеловеческой последовательностью. Кроме того, человеческая последовательность ДНК может содержать кДНК, область человеческой геномной ДНК, некодирующую регуляторную область или любую часть кодирующей, геномной или регуляторной области человеческой ДНК. Человеческая последовательность ДНК, вставленная в нечеловеческий локус, может содержать любую из полинуклеотидных вставок, как описано в другом месте данного документа. В конкретных вариантах реализации изобретения человеческая последовательность ДНК является ортологичной нечеловеческому целевому локусу, в то время как в других случаях человеческая последовательность ДНК является гомологичной нечеловеческому целевому локусу.
[00345] В одном варианте реализации изобретения направленная генетическая модификация представляет собой вставку или замещение эндогенной нуклеотидной последовательности гомологичной или ортологичной человеческой нуклеотидной последовательностью. В одном варианте реализации изобретения направленная генетическая модификация включает вставку или замещение эндогенной нуклеотидной последовательности гомологичной или ортологичной человеческой нуклеотидной последовательностью в эндогенном локусе, который содержит соответствующую нечеловеческую нуклеотидную последовательность.
[00346] Способы получения гуманизированного локуса включают внесение в целевой локус, содержащий нуклеиновую кислоту, человеческой нуклеотидной последовательности. В одном варианте реализации изобретения предложен способ получения гуманизированного отличного от человека животного. Такой способ включает (а) модификацию генома нечеловеческой плюрипотентной клетки или неплюрипотентной клетки направляющим вектором, содержащим нуклеотидную вставку, которая содержит человеческую нуклеотидную последовательность, для формирования донорной клетки; (b) внесение донорной клетки в эмбрион-хозяина; и (с) вынашивание эмбриона-хозяина суррогатной матерью; при этом суррогатная мать производит потомство, которое содержит человеческую нуклеотидную последовательность. В конкретных вариантах реализации изобретения гуманизированный локус может передаваться через зародышевую линию. В дополнительном варианте реализации изобретения направляющий вектор включает крупный направляющий вектор (LTVEC), а нуклеотидная вставка, которая содержит человеческую нуклеотидную последовательность, составляет по меньшей мере 5 т.п.о.
[00347] В других способах гуманизированный геномный локус получают путем модификации целевого локуса нуклеиновой кислоты посредством бактериальной гомологичной рекомбинации (БГР). Указанный способ включает внесение в прокариотическую клетку направляющего вектора, содержащего нуклеотидную вставку, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом нуклеотидная вставка содержит человеческую нуклеотидную последовательность, а прокариотическая клетка содержит нуклеиновую кислоту, которая способна экспрессировать рекомбиназу, которая опосредует БГР в целевом локусе.
[00348] Гуманизированный геномный локус может содержать (а) вставку гомологичной или ортологичной человеческой нуклеотидной последовательности; (b) замещение эндогенной нуклеотидной последовательности гомологичной или ортологичной человеческой нуклеотидной последовательностью; или (с) комбинацию вышеперечисленного. В конкретных вариантах реализации изобретения гуманизированный геномный локус может передаваться через зародышевую линию. В других вариантах реализации изобретения человеческая ортологичная последовательность замещает соответствующую последовательность, находящуюся в нечеловеческом локусе.
[00349] В предложенных в данном документе способах и композициях можно применять любую человеческую нуклеотидную последовательность. Неограничивающие примеры человеческих нуклеотидных последовательностей, которые можно применять в способах и композициях, подробно обсуждаются в другом месте данного документа.
[00350] Человеческая нуклеотидная последовательность, предназначенная для вставки в представляющий интерес локус, может быть любого размера. В одном варианте реализации изобретения человеческая нуклеотидная последовательность может составлять от около 500 нуклеотидов до около 200 т.п.о., от около 500 нуклеотидов до около 5 т.п.о., от около 5 т.п.о. до около 200 т.п.о., от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 30 т.п.о., от около 30 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 50 т.п.о., от около 60 т.п.о. до около 70 т.п.о., от около 80 т.п.о. до около 90 т.п.о., от около 90 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 110 т.п.о., от около 120 т.п.о. до около 130 т.п.о., от около 130 т.п.о. до около 140 т.п.о., от около 140 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 160 т.п.о., от около 160 т.п.о. до около 170 т.п.о., от около 170 т.п.о. до около 180 т.п.о., от около 180 т.п.о. до около 190 т.п.о. или от около 190 т.п.о. до около 200 т.п.о. В конкретном варианте реализации изобретения человеческая нуклеотидная последовательность составляет по меньшей мере 5 т.п.о.
[00351] В одном варианте реализации изобретения предложен геномный локус, в котором гомологичная или ортологичная человеческая нуклеотидная последовательность содержит (а) один или более неперестроенных генных сегментов VH тяжелой цепи иммуноглобулина человека, один или более неперестроенных генных сегментов D тяжелой цепи иммуноглобулина человека и один или более неперестроенных генных сегментов JH тяжелой цепи иммуноглобулина человека, которые функционально связаны с нуклеотидной последовательностью константной области тяжелой цепи млекопитающего; (b) перестроенную нуклеотидную последовательность вариабельной области тяжелой цепи иммуноглобулина человека, функционально связанную с нуклеотидной последовательностью константной области тяжелой цепи млекопитающего; (с) один или более неперестроенных генных сегментов Vκ или Vλ иммуноглобулина человека и один или более неперестроенных генных сегментов Jκ или Jλиммуноглобулина человека, которые функционально связаны с нуклеотидной последовательностью константной области λ или κ легкой цепи иммуноглобулина млекопитающего; или (d) перестроенную нуклеотидную последовательность вариабельной области λ или κ легкой цепи иммуноглобулина человека, функционально связанную с нуклеотидной последовательностью константной области λ или κ легкой цепи иммуноглобулина млекопитающего.
[00352] В другом варианте реализации изобретения предложен геномный локус, в котором (а) нуклеотидная последовательность константной области тяжелой цепи млекопитающего представляет собой нуклеотидную последовательность константной области крысы, нуклеотидную последовательность константной области человека или их комбинацию; или (b) нуклеотидная последовательность константной области λ или κ легкой цепи иммуноглобулина млекопитающего представляет собой нуклеотидную последовательность константной области крысы, нуклеотидную последовательность константной области человека или их комбинацию.
[00353] В конкретном варианте реализации изобретения предложен геномный локус, в котором нуклеотидная последовательность константной области тяжелой цепи иммуноглобулина выбрана из или содержит СН1, шарнирную область, СН2, СН3 и/или их комбинацию.
[00354] В одном варианте реализации изобретения геномный локус содержит один или более функциональных человеческих генных сегментов VH, включая VH1-2, VH1-3, VH1-8, VH1-18, VH1-24, VH1-45, VH1-46, VH1-58, VH1-69, VH2-5, VH2-26, VH2-70, VH3-7, VH3-9, VH3-11, VH3-13, VH3-15, VH3-16, VH3-20, VH3-21, VH3-23, VH3-30, VH3-30-3, VH3-30-5, VH3-33, VH3-35, VH3-38, VH3-43, VH3-48, VH3-49, VH3-53, VH3-64, VH3-66, VH3-72, VH3-73, VH3-74, VH4-4, VH4-28, VH4-30-1, VH4-30-2, VH4-30-4, VH4-31, VH4-34, VH4-39, VH4-59, VH4-61, VH5-51, VH6-1, VH7-4-1, VH7-81 или их комбинацию.
[00355] В одном варианте реализации изобретения геномный локус содержит один или более функциональных человеческих генных сегментов D, включая D1-1, D1-7, D1-14, D1-20, D1-26, D2-2, D2-8, D2-15, D2-21, D3-3, D3-9, D3-10, D3-16. D3-22, D4-4, D4-11, D4-17, D4-23, D5-12, D5-5, D5-18, D5-24, D6-6, D6-13, D6-19, D6-25, D7-27 или их комбинацию.
[00356] В одном варианте реализации изобретения геномный локус содержит один или более функциональных человеческих генных сегментов JH, включая JH1, JH2, JH3, JH4, JH5, JH6 и/или их комбинацию. В одном варианте реализации изобретения нуклеотидная вставка содержит один или более человеческих генных сегментов Vκ, включая Vκ4-1, Vκ5-2, Vκ7-3, Vκ2-4, Vκ1-5, Vκ1-6, Vκ3-7, Vκ1-8, Vκ1-9, Vκ2-10, Vκ3-11, Vκ1-12, Vκ1-13, Vκ2-14, Vκ3-15, Vκ1-16, Vκ1-17, Vκ2-18, Vκ2-19, Vκ3-20, Vκ6-21, Vκ1-22, Vκ1-23, Vκ2-24, Vκ3-25, Vκ2-26, Vκ1-27, Vκ2-28, Vκ2-29, Vκ2-30, Vκ3-31, Vκ1-32, Vκ1-33, Vκ3-34, Vκ1-35, Vκ2-36, Vκ1-37, Vκ2-38, Vκ1-39, Vκ2-40 или их комбинацию.
[00357] В одном варианте реализации изобретения геномный локус содержит один или более человеческих генных сегментов Vλ, включая Vλ3-1, Vλ4-3, Vλ2-8, Vλ3-9, Vλ3-10, Vλ2-11, Vλ3-12, Vλ2-14, Vλ3-16, Vλ2-18, Vλ3-19, Vλ3-21, Vλ3-22, Vλ2-23, Vλ3-25, Vλ3-27 или их комбинацию.
[00358] В одном варианте реализации изобретения геномный локус содержит один или более человеческих генных сегментов Jκ, включая Jκ1, Jκ2, Jκ3, Jκ4, Jκ5 или их комбинацию.
[00359] В другом варианте реализации изобретения предложен геномный локус, содержащий гуманизированный геномный локус, содержащий нуклеотидную последовательность человеческого рецептора интерлейкина-2 (IL2R) или ее вариант или фрагмент. В конкретных вариантах реализации изобретения нуклеотидная последовательность IL2R включает нуклеотидную последовательность рецептора интерлейкина-2 альфа, рецептора интерлейкина-2 бета или рецептора интерлейкина-2 гамма, или их варианты или фрагменты.
[00360] В дополнительных вариантах реализации изобретения геномный локус содержит гуманизированный геномный локус, состоящий из части локуса человеческого АроЕ, локуса человеческого рецептора интерлейкина-2 гамма, локуса человеческого Rag2, локуса человеческого Rag1 и/или локуса человеческого Rag2/Rag1, замещающую соответствующую гомологичную или ортологичную часть локуса нечеловеческого АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1. В одном варианте реализации изобретения эктодомен нечеловеческого IL-2Rg замещен эктодоменом человеческого IL-2Rg, а остаток молекулы принадлежит отличному от человека животному.
[00361] В другом варианте реализации изобретения предложено генетически модифицированное отличное от человека животное, содержащее гуманизированный геномный локус. Такие генетически модифицированные отличные от человека животные содержат (а) вставку гомологичной или ортологичной человеческой нуклеотидной последовательности; (b) замещение нуклеотидной последовательности гомологичной или ортологичной человеческой нуклеотидной последовательностью в эндогенном геномном локусе; или (с) комбинацию вышеперечисленного, при этом гуманизированный геномный локус может передаваться через зародышевую линию.
[00362] Также предложены генетически модифицированные животные, включая отличных от человека животных, содержащие любые из различных предложенных в данном документе и описанных выше гуманизированных геномных локусов.
4. Представляющие интерес полинуклеотиды
[00363] В различных нуклеотидных вставках может находиться любой представляющий интерес полинуклеотид и, следовательно, интегрироваться в целевой локус. В раскрытых в данном документе способах предложено по меньшей мере 1, 2, 3, 4, 5, 6 или более представляющих интерес полинуклеотидов для интеграции в целевой геномный локус.
[00364] Интеграция представляющего интерес полинуклеотида, находящегося в нуклеотидной вставке, в целевой геномный локус может вносить одну или более генетических модификаций в клетку. Генетическая модификация может включать удаление эндогенной нуклеотидной последовательности и/или добавление экзогенного или гетерологичного, или ортологичного полинуклеотида в целевом геномном локусе. В одном варианте реализации изобретения генетическая модификация включает замещение эндогенной нуклеотидной последовательности представляющим интерес экзогенным полинуклеотидом в целевом геномном локусе. Таким образом, предложенные в данном документе способы позволяют получить генетическую модификацию, включающую выключение, удаление, вставку, замещение («нокин»), точечную мутацию, замену домена, замену экзона, замену интрона, замену регуляторной последовательности, замену гена или их комбинацию. Такие модификации могут возникать после интеграции первой, второй, третьей, четвертой, пятой, шестой, седьмой или любой последующей нуклеотидной вставки в целевой геномный локус.
[00365] Представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, может содержать последовательность, которая является нативной по отношению к клетке, в которую его вносят; представляющий интерес полинуклеотид может быть гетерологичным по отношению к клетке, в которую его вносят; представляющий интерес полинуклеотид может быть экзогенным по отношению к клетке, в которую его вносят; представляющий интерес полинуклеотид может быть ортологичным по отношению к клетке, в которую его вносят; или представляющий интерес полинуклеотид может быть получен от другого вида, чем клетка, в которую его вносят. В контексте данного документа выражение «нативный», употребляемое в отношении последовательности, вставленной в целевой локус, означает последовательность, которая является нативной для клетки, содержащей целевой локус, или нативной для клетки, из которой был получен целевой локус (т.е. из клетки крысы). В контексте данного документа выражение «гетерологичный», употребляемое в отношении последовательности, включает последовательность, которая принадлежит чужеродному виду, или, если она принадлежит тому же виду, она существенно отличается или модифицирована по сравнению со своей нативной формой в композиции и/или геномном локусе вследствие преднамеренного вмешательства человека. В контексте данного документа выражение «экзогенный», употребляемое в отношении последовательности, относится к последовательности, которая принадлежит чужеродному виду. Представляющий интерес полинуклеотид может принадлежать любому представляющему интерес организму, включая, но не ограничиваясь этим, отличное от человека животное, грызуна, отличного от крысы грызуна, хомяка, мышь, крысу, человека, обезьяну, сельскохозяйственное млекопитающее или несельскохозяйственное млекопитающее. Представляющий интерес полинуклеотид может дополнительно содержать кодирующую область, некодирующую область, регуляторную область или геномную ДНК. Таким образом, 1-ая, 2-ая, 3-я, 4-ая, 5-ая, 6-ая, 7-ая и/или любая из последующих нуклеиновых кислот может содержать такие последовательности.
[00366] В одном варианте реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, является нативным для нуклеотидной последовательности мыши, человеческой нуклеиновой кислоты, нечеловеческой нуклеиновой кислоты, нуклеиновой кислоты эукариота, нуклеиновой кислоты отличного от крысы эукариота, нуклеиновой кислоты отличного от человека млекопитающего, нуклеиновой кислоты млекопитающего, нуклеиновой кислоты грызуна, нуклеиновой кислоты отличного от крысы грызуна, нуклеиновой кислоты крысы, нуклеиновой кислоты обезьяны, нуклеиновой кислоты сельскохозяйственного млекопитающего или нуклеиновой кислоты несельскохозяйственного млекопитающего. В дополнительных вариантах реализации изобретения представляющий интерес полинуклеотид, интегрированный в целевой локус, является фрагментом геномной нуклеиновой кислоты. В одном варианте реализации изобретения геномная нуклеиновая кислота представляет собой геномную нуклеиновую кислоту мыши, человеческую геномную нуклеиновую кислоту, нечеловеческую нуклеиновую кислоту, нуклеиновую кислоту эукариота, нуклеиновую кислоту отличного от крысы эукариота, нуклеиновую кислоту отличного от человека млекопитающего, нуклеиновую кислоту млекопитающего, нуклеиновую кислоту грызуна, нуклеиновую кислоту отличного от крысы грызуна, нуклеиновую кислоту крысы, нуклеиновую кислоту обезьяны, нуклеиновую кислоту сельскохозяйственного млекопитающего или нуклеиновую кислоту несельскохозяйственного млекопитающего или их комбинации.
[00367] В одном варианте реализации изобретения длина представляющего интерес полинуклеотида находится в диапазоне от около 500 нуклеотидов до около 200 т.п.о., как описано выше. Представляющий интерес полинуклеотид может составлять от около 500 нуклеотидов до около 5 т.п.о., от около 5 т.п.о. до около 200 т.п.о., от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 30 т.п.о., от около 30 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 50 т.п.о., от около 60 т.п.о. до около 70 т.п.о., от около 80 т.п.о. до около 90 т.п.о., от около 90 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 110 т.п.о., от около 120 т.п.о. до около 130 т.п.о., от около 130 т.п.о. до около 140 т.п.о., от около 140 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 160 т.п.о., от около 160 т.п.о. до около 170 т.п.о., от около 170 т.п.о. до около 180 т.п.о., от около 180 т.п.о. до около 190 т.п.о. или от около 190 т.п.о. до около 200 т.п.о., от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.
[00368] Представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или вставленный в целевой геномный локус, может кодировать полипептид, может кодировать миРНК или может содержать любые представляющие интерес регуляторные области или некодирующие области, включая, например, регуляторную последовательность, промоторную последовательность, энхансерную последовательность, транскрипционную репрессорсвязывающую последовательность или удаление не кодирующей белок последовательности, но не содержит удаление кодирующей белок последовательности. Кроме того, представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или вставленный в целевой геномный локус, может кодировать белок, экспрессируемый в нервной системе, костной системе, пищеварительной системе, системе кровообращения, мышечной системе, дыхательной системе, сердечнососудистой системе, лимфатической системе, эндокринной системе, мочевыделительной системе, репродуктивной системе или их комбинации. В одном варианте реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или вставленный в целевой геномный локус, кодирует белок, экспрессируемый в костном мозге или клетке костного мозга. В одном варианте реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или вставленный в целевой локус, кодирует белок, экспрессируемый в клетке селезенки. В дополнительных вариантах реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или вставленный в целевой локус, кодирует белок, экспрессируемый в В-клетке, кодирует белок, экспрессируемый в незрелой В-клетке или кодирует белок, экспрессируемый в зрелой В-клетке.
[00369] Представляющий интерес полинуклеотид, находящийся в полинуклеотидной вставке, может содержать часть локуса АроЕ, локуса Il2rg, локуса Rag1, локуса Rag2 и/или локуса Rag2/Rag1. Такие части данных локусов обсуждаются в другом месте данного документа, как и различные гомологичные и ортологичные области, принадлежащие любому представляющему интерес организму, которые можно применять.
[00370] В одном варианте реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или вставленный в целевой локус, содержит геномную нуклеотидную последовательность, которая кодирует аминокислотную последовательность вариабельной области тяжелой цепи иммуноглобулина. Выражения «тяжелая цепь» или «тяжелая цепь иммуноглобулина» описаны в другом месте данного документа.
[00371] В одном варианте реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, содержит геномную нуклеотидную последовательность, которая кодирует аминокислотную последовательность вариабельной области тяжелой цепи иммуноглобулина человека.
[00372] В одном варианте реализации изобретения геномная нуклеотидная последовательность содержит один или более неперестроенных генных сегментов VH тяжелой цепи иммуноглобулина человека, один или более неперестроенных генных сегментов D тяжелой цепи иммуноглобулина человека и один или более неперестроенных генных сегментов JH тяжелой цепи иммуноглобулина человека, которые функционально связаны с нуклеотидной последовательностью константной области тяжелой цепи млекопитающего. В одном варианте реализации изобретения геномная нуклеотидная последовательность содержит перестроенную нуклеотидную последовательность вариабельной области тяжелой цепи иммуноглобулина человека, функционально связанную с нуклеотидной последовательностью константной области тяжелой цепи млекопитающего. В одном варианте реализации изобретения геномная нуклеотидная последовательность содержит один или более неперестроенных генных сегментов Vκ или Vλ иммуноглобулина человека и один или более неперестроенных генных сегментов Jκ или Jλ иммуноглобулина человека, которые функционально связаны с нуклеотидной последовательностью константной области λ или κ легкой цепи иммуноглобулина млекопитающего. В одном варианте реализации изобретения геномная нуклеотидная последовательность содержит перестроенную нуклеотидную последовательность вариабельной области λ или κ легкой цепи иммуноглобулина человека, функционально связанную с нуклеотидной последовательностью константной области λ или κ легкой цепи иммуноглобулина млекопитающего. В одном варианте реализации изобретения нуклеотидная последовательность константной области тяжелой цепи включает нуклеотидную последовательность константной области крысы, нуклеотидную последовательность константной области человека или их комбинацию. В одном варианте реализации изобретения нуклеотидная последовательность константной области λ или κ легкой цепи иммуноглобулина включает нуклеотидную последовательность константной области крысы, нуклеотидную последовательность константной области человека или их комбинацию.
[00373] В одном варианте реализации изобретения нуклеотидная последовательность константной области тяжелой цепи иммуноглобулина выбрана из или содержит СН1, шарнирную область, СН2, СН3 и/или их комбинацию. В одном варианте реализации изобретения нуклеотидная последовательность константной области тяжелой цепи содержит СН1-шарнирную область-СН2-СН3.
[00374] В одном варианте реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, содержит геномную нуклеотидную последовательность, которая кодирует аминокислотную последовательность вариабельной области легкой цепи иммуноглобулина. Выражение «легкая цепь» включает последовательность легкой цепи иммуноглобулина, принадлежащую любому организму, и описана в другом месте данного документа.
[00375] В одном варианте реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой геномный локус, содержит геномную нуклеотидную последовательность, которая кодирует аминокислотную последовательность вариабельной области легкой цепи иммуноглобулина человека.
[00376] В одном варианте реализации изобретения геномная нуклеотидная последовательность содержит один или более неперестроенных генных сегментов Vκ или Vλ иммуноглобулина человека и один или более неперестроенных генных сегментов Jκ или Jλ иммуноглобулина человека, которые функционально связаны с нуклеотидной последовательностью константной области λ или κ легкой цепи иммуноглобулина грызуна. В одном варианте реализации изобретения геномная нуклеотидная последовательность содержит перестроенную нуклеотидную последовательность вариабельной области λ или κ легкой цепи иммуноглобулина человека, функционально связанную с нуклеотидной последовательностью константной области λ или κ легкой цепи иммуноглобулина грызуна. В одном варианте реализации изобретения нуклеотидная последовательность константной области легкой цепи включает нуклеотидную последовательность константной области крысы, нуклеотидную последовательность константной области человека или их комбинацию. В одном варианте реализации изобретения нуклеотидная последовательность константной области λ или κ легкой цепи иммуноглобулина включает нуклеотидную последовательность константной области крысы, нуклеотидную последовательность константной области человека или их комбинацию.
[00377] Представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, может кодировать внеклеточный белок или лиганд для рецептора. В конкретных вариантах реализации изобретения кодируемый лиганд представляет собой цитокин. Представляющие интерес цитокины включают хемокины, выбранные из или включающие CCL, CXCL, CX3CL и/или XCL. Цитокин также может включать фактор некроза опухоли (TNF). В других вариантах реализации изобретения цитокин представляет собой интерлейкин (IL). В одном варианте реализации изобретения интерлейкин выбран из или включает IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-19, IL-20, IL-21, IL-22, IL-23, IL-24, IL-25, IL-26, IL-27, IL-28, IL-29, IL-30, IL-31, IL-32, IL-33, IL-34, IL-35 и/или IL-36. В одном варианте реализации изобретения интерлейкин представляет собой IL-2. В конкретных вариантах реализации изобретения такие представляющие интерес полинуклеотиды, находящиеся в нуклеотидной вставке и/или интегрированные в целевой геномный локус, получены от человека и, в более конкретных вариантах реализации изобретения, могут содержать человеческую геномную последовательность.
[00378] Представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой геномный локус, может кодировать аполипопротеин Е (АроЕ).
[00379] Представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, может кодировать цитоплазматический белок или мембранный белок. В одном варианте реализации изобретения мембранный белок представляет собой рецептор, такой как рецептор цитокинов, рецептор интерлейкинов, рецептор интерлейкина-2 альфа, рецептор интерлейкина-2 бета, рецептор интерлейкина-2 гамма или рецептор тирозинкиназы. В других случаях представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, может содержать ортологичную или гомологичную область целевого локуса.
[00380] Представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, может содержать полинуклеотид, кодирующий по меньшей мере одну область рецептора Т-клеток, включая рецептор Т-клеток альфа. В конкретных способах каждая из нуклеотидных вставок содержит геномную область локуса рецептора Т-клеток (т.е. локуса рецептора Т-клеток альфа) так, что после завершения серийной интеграции часть или весь геномный локус рецептора Т-клеток интегрируется в целевой локус. Такие нуклеотидные вставки могут содержать один или более вариабельных сегментов или соединяющих сегментов локуса рецептора Т-клеток (т.е. локуса рецептора Т-клеток альфа). В дополнительных вариантах реализации изобретения представляющий интерес полинуклеотид, кодирующий область рецептора Т-клеток, может быть получен, например, из кодирующего мутантный белок полинуклеотида эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, грызуна, отличного от крысы грызуна, мыши, крысы, человека, обезьяны, хомяка, сельскохозяйственного млекопитающего или домашнего млекопитающего.
[00381] В других вариантах реализации изобретения представляющий интерес полинуклеотид, интегрированный в целевой локус, кодирует ядерный белок. В одном варианте реализации изобретения ядерный белок является ядерным рецептором. В конкретных вариантах реализации изобретения такие представляющие интерес полинуклеотиды, находящиеся в нуклеотидной вставке и/или интегрированные в целевой локус, получены от человека и, в более конкретных вариантах реализации изобретения, могут содержать человеческую геномную последовательность.
[00382] Представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой геномный локус, может содержать генетическую модификацию в кодирующей последовательности. Такие генетические модификации включают, но не ограничиваются этим, делеционную мутацию кодирующей последовательности или слияние двух кодирующих последовательностей.
[00383] Представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, может содержать полинуклеотид, кодирующий мутантный белок, включая, например, человеческий мутантный белок. В одном варианте реализации изобретения мутантный белок характеризуется измененными характеристиками связывания, измененной локализацией, измененной экспрессией и/или измененным профилем экспрессии. В одном варианте реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, содержит по меньшей мере один аллель заболевания, включая, например, аллель неврологического заболевания, аллель сердечнососудистого заболевания, аллель заболевания почек, аллель мышечного заболевания, аллель заболевания крови, аллель гена, приводящего к раку, или аллель заболевания иммунной систему. В таких случаях аллель заболевания может быть доминантным аллелем или аллель заболевания является рецессивным аллелем. Кроме того, аллель заболевания может содержать аллель однонуклеотидного полиморфизма (ОНП). Представляющий интерес полинуклеотид, кодирующий мутантный белок, может быть получен из любого организма, включая, но не ограничиваясь этим, кодирующий мутантный белок полинуклеотид эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, грызуна, отличного от крысы грызуна, мыши, крысы, человека, хомяка, обезьяны, сельскохозяйственного млекопитающего или домашнего млекопитающего.
[00384] В одном варианте реализации изобретения генетическая модификация приводит к получению мутантной формы белка с измененными характеристиками связывания, измененной локализацией, измененной экспрессией и/или измененным профилем экспрессии.
[00385] В одном варианте реализации изобретения результатом генетической модификации является удаление, добавление, замещение или их комбинация области локуса АроЕ, например, локуса крысиного АроЕ, при этом генетическая модификация в локусе АроЕ приводит к снижению активности АроЕ. В одном варианте реализации изобретения происходит выключение АроЕ.
[00386] В одном варианте реализации изобретения результатом генетической модификации является удаление, добавление, замещение или их комбинация области локуса Rag1, например, локуса крысиного Rag1, при этом генетическая модификация в локусе Rag1 приводит к снижению активности Rag1. В одном варианте реализации изобретения происходит выключение Rag1. В одном варианте реализации изобретения результатом генетической модификации является удаление, добавление, замещение или их комбинация области локуса Rag2, например, локуса крысиного Rag2, при этом генетическая модификация в локусе Rag2 приводит к снижению активности Rag2. В одном варианте реализации изобретения происходит выключение Rag2. В одном варианте реализации изобретения результатом генетической модификации является удаление, добавление, замещение или их комбинация области локуса Rag1/Rag2, например, локуса крысиного Rag1/Rag2, при этом генетическая модификация в локусе Rag1/Rag2 приводит к снижению активности Rag1 и снижению активности Rag2. В одном варианте реализации изобретения происходит выключение Rag1/Rag2.
[00387] В одном варианте реализации изобретения результатом генетической модификации является удаление, добавление, замещение или их комбинация области локуса рецептора интерлейкина-2 гамма, например, локуса крысиного рецептора интерлейкина-2 гамма, при этом генетическая модификация в локусе рецептора интерлейкина-2 гамма приводит к снижению активности рецептора интерлейкина-2 гамма. В одном варианте реализации изобретения происходит выключение рецептора интерлейкина-2 гамма.
[00388] Как обсуждается в другом месте данного документа дополнительные предложенные варианты реализации изобретения включают модификацию одного или более из локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1, например, локуса крысиного АроЕ, локуса крысиного рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 путем замещения части локуса крысиного АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 соответствующей ортологичной частью локуса АроЕ, локуса рецептора интерлейкина-2 гамма, локуса Rag2, локуса Rag1 и/или локуса Rag2/Rag1 из другого организма.
[00389] В одном варианте реализации изобретения создают множественные генетические модификации. В одном варианте реализации изобретения результатом генетической модификации является удаление, добавление, замещение или их комбинация области локуса рецептора интерлейкина-2 гамма, например, локуса крысиного рецептора интерлейкина-2 гамма, при этом генетическая модификация в локусе рецептора интерлейкина-2 гамма приводит к снижению активности рецептора интерлейкина-2 гамма, а результатом второй генетической модификации является удаление, добавление, замещение или их комбинация области локуса крысиного Rag2, при этом генетическая модификация в локусе Rag2 приводит к снижению активности Rag2. В одном варианте реализации изобретения происходит выключение рецептора интерлейкина-2 гамма/Rag2. Такая крыса имеет фенотип ТКИН.
[00390] В одном варианте реализации изобретения нуклеиновая кислота млекопитающего содержит геномный локус, который кодирует белок, экспрессируемый в нервной системе, костной системе, пищеварительной системе, системе кровообращения, мышечной системе, дыхательной системе, сердечнососудистой системе, лимфатической системе, эндокринной системе, мочевыделительной системе, репродуктивной системе или их комбинации. В одном варианте реализации изобретения нуклеиновая кислота млекопитающего содержит геномный локус, который кодирует белок, экспрессируемый в костном мозге или клетке костного мозга. В одном варианте реализации изобретения нуклеиновая кислота содержит геномный локус, который кодирует белок, экспрессируемый в клетке селезенки. В одном варианте реализации изобретения геномный локус содержит последовательность геномной ДНК мыши, последовательность геномной ДНК крысы, последовательность геномной ДНК человека или их комбинацию. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, крысиные и человеческие последовательности геномной ДНК. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, мышиные и человеческие последовательности геномной ДНК. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, мышиные и крысиные последовательности геномной ДНК. В одном варианте реализации изобретения геномный локус содержит, в любом порядке, крысиные, мышиные и человеческие последовательности геномной ДНК.
[00391] В одном варианте реализации изобретения нуклеотидная вставка содержит генетическую модификацию в кодирующей последовательности гена. В одном варианте реализации изобретения генетическая модификация включает делеционную мутацию в кодирующей последовательности. В одном варианте реализации изобретения генетическая модификация включает слияние двух эндогенных кодирующих последовательностей.
[00392] В одном варианте реализации изобретения генетическая модификация включает удаление не кодирующей белок последовательности, но не включает удаление кодирующей белок последовательности. В одном варианте реализации изобретения удаление не кодирующей белок последовательности включает удаление регуляторного элемента. В одном варианте реализации изобретения генетическая модификация включает добавление промотора. В одном варианте реализации изобретения генетическая модификация включает замещение промотора или регуляторного элемента. В одном варианте реализации изобретения регуляторный элемент является энхансером. В одном варианте реализации изобретения регуляторный элемент является транскрипционным репрессорсвязывающим элементом.
[00393] В одном варианте реализации изобретения генетическая модификация включает замещение человеческой нуклеотидной последовательности, кодирующей мутантный человеческий белок. В одном варианте реализации изобретения генетическая модификация включает по меньшей мере один аллель заболевания человека из человеческого гена. В одном варианте реализации изобретения человеческое заболевание является неврологическим заболеванием. В одном варианте реализации изобретения человеческое заболевание является сердечнососудистым заболеванием. В одном варианте реализации изобретения человеческое заболевание является заболеванием почек. В одном варианте реализации изобретения человеческое заболевание является мышечным заболеванием. В одном варианте реализации изобретения человеческое заболевание является заболеванием крови. В одном варианте реализации изобретения человеческое заболевание является раком. В одном варианте реализации изобретения человеческое заболевание является заболеванием иммунной системы. В одном варианте реализации изобретения аллель заболевания человека является доминантным аллелем. В одном варианте реализации изобретения аллель заболевания человека является рецессивным аллелем. В одном варианте реализации изобретения аллель заболевания человека включает аллель однонуклеотидного полиморфизма (ОНП).
[00394] Представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой локус, также может содержать регуляторную последовательность, включая, например, промоторную последовательность, энхансерную последовательность или транскрипционную репрессорсвязывающую последовательность. В конкретных вариантах реализации изобретения представляющий интерес полинуклеотид, находящийся в нуклеотидной вставке и/или интегрированный в целевой геномный локус, содержит полинуклеотид, содержащий удаление не кодирующей белок последовательности, но не содержит удаление кодирующей белок последовательности. В одном варианте реализации изобретения удаление не кодирующей белок последовательности включает удаление регуляторной последовательности. В другом варианте реализации изобретения удаление регуляторного элемента включает удаление промоторной последовательности. В одном варианте реализации изобретения удаление регуляторного элемента включает удаление энхансерной последовательности. Такой представляющий интерес полинуклеотид может быть получен из любого организма, включая, но не ограничиваясь этим, кодирующий мутантный белок полинуклеотид эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, грызуна, отличного от крысы грызуна, мыши, крысы, человека, обезьяны, сельскохозяйственного млекопитающего или домашнего млекопитающего.
5. Способы внесения последовательностей и получения трансгенных животных
[00395] Как указано выше, в данном документе предложены способы и композиции, позволяющие осуществлять направленную интеграцию одного или более представляющих интерес полинуклеотидов в целевой локус. В таких системах применяется множество компонентов и для удобства употребляемый в данном документе термин «система направленной интеграции» в общем случае включает все компоненты, необходимые для интеграции (т.е., как неограничивающие примеры, это различные нуклеазные агенты, участки распознавания, полинуклеотидные вставки ДНК, направляющие векторы, целевой геномный локус и/или представляющие интерес полинуклеотиды).
[00396] Предложенные в данном документе способы включают внесение в клетку одной или более полинуклеотидных или полипептидных конструкций, содержащих различные компоненты системы направленной геномной интеграции. «Внесение» означает передачу последовательности (полипептидной или полинуклеотидной) клетке таким образом, что последовательность получает доступ к внутренней части клетки. Предложенные в данном документе способы не зависят от конкретного способа внесения любого компонента системы направленной геномной интеграции в клетку, а значение имеет только то, что полинуклеотид получает доступ к внутренней части по меньшей мере одной клетки. Способы внесения полинуклеотидов в различные типы клеток известны в данной области техники и включают, но не ограничиваются этим, способы стабильной трансфекции, способы временной трансфекции и вирус-опосредованные способы.
[00397] В предложенных в данном документе способах можно применять любые клетки из любого организма. В конкретных вариантах реализации изобретения клетки получены от эукариота, отличного от крысы эукариота, млекопитающего, отличного от человека млекопитающего, человека, грызуна, отличного от крысы грызуна, мыши или хомяка. В конкретных вариантах реализации изобретения клетки представляют собой эукариотическую клетку, некрысиную эукариотическую клетку, плюрипотентную клетку, неплюрипотентную клетку, нечеловеческую плюрипотентную клетку, клетку отличного от человека млекопитающего, человеческую плюрипотентную клетку, человеческую ЭС клетку, человеческую взрослую стволовую клетку, человеческую клетку-предшественника с ограниченным развитием, человеческую индуцированную плюрипотентную (иПС) клетку, клетку млекопитающего, человеческую клетку, фибробласт, клетку грызуна, клетку отличного от крысы грызуна, крысиную клетку, мышиную клетку, клетку хомяка или клетку СНО.
[00398] В некоторых вариантах реализации изобретения клетки, применяемые в способах и композициях, содержат конструкцию ДНК, стабильно включенную в их геном. «Стабильно включенный» или «стабильно внесенный» означает внесение полинуклеотида в клетку таким образом, что нуклеотидная последовательность интегрируется в геном клетки и способна наследоваться ее потомством. Для стабильного внесения конструкций ДНК или различных компонентов системы направленной геномной интеграции можно применять любой протокол.
[00399] Протоколы трансфекции, как и протоколы внесения полипептидов или полинуклеотидных последовательностей, могут варьироваться. Неограничивающие способы трансфекции включают химические способы трансфекции, включая применение липосом; наночастиц; фосфата кальция (Graham et al. (1973). Virology 52 (2): 456-67, Bacchetti et al. (1977) Proc Natl Acad Sci USA 74 (4): 1590-4 и Kriegler, M (1991). Transfer and Expression: A Laboratory Manual. New York: W.H. Freeman and Company, pp. 96-97); дендримеров; или катионных полимеров, таких как ДЭАЭ-декстран или полиэтиленимин. Нехимические способы включают электропорацию; сонопорацию; и оптическую трансфекцию. Трансфекция на основании частиц включает применение генной пушки, магнитной трансфекции (Bertram, J. (2006) Current Pharmaceutical Biotechnology 7, 277-28). Также для трансфекции можно применять вирусные способы.
[00400] В одном варианте реализации изобретения внесение одного или более полинуклеотидов в клетку опосредуется электропорацией, интрацитоплазматической инъекцией, вирусным инфицированием, аденовирусом, лентивирусом, ретровирусом, трансфекцией, липид-опосредованной трансфекцией или опосредуется нуклеофекцией™.
[00401] В одном варианте реализации изобретения внесение одного или более полинуклеотидов в клетку дополнительно включает: внесение экспрессионной конструкции, содержащей представляющую интерес нуклеотидную последовательность, функционально связанную с промотором. В одном варианте реализации изобретения промотор является конститутивно-активным промотором. В одном варианте реализации изобретения промотор является индуцибельным промотором. В одном варианте реализации изобретения промотор активен в стволовой клетке, например, эмбриональной стволовой клетке.
[00402] В одном варианте реализации изобретения экспрессионную конструкцию вносят вместе с LTVEC. В одном варианте реализации изобретения экспрессионную конструкцию вносят отдельно от LTVEC в течение некоторого времени.
[00403] В одном варианте реализации изобретения внесение одного или более полинуклеотидов в клетку можно осуществлять много раз в течение некоторого времени. В одном варианте реализации изобретения внесение одного или более полинуклеотидов в клетку осуществляют по меньшей мере два раза в течение некоторого времени, по меньшей мере три раза в течение некоторого времени, по меньшей мере четыре раза в течение некоторого времени, по меньшей мере пять раз в течение некоторого времени, по меньшей мере шесть раз в течение некоторого времени, по меньшей мере семь раз в течение некоторого времени, по меньшей мере восемь раз в течение некоторого времени, по меньшей мере девять раз в течение некоторого времени, по меньшей мере десять раз в течение некоторого времени, по меньшей мере одиннадцать раз, по меньшей мере двенадцать раз в течение некоторого времени, по меньшей мере тринадцать раз в течение некоторого времени, по меньшей мере четырнадцать раз в течение некоторого времени, по меньшей мере пятнадцать раз в течение некоторого времени, по меньшей мере шестнадцать раз в течение некоторого времени, по меньшей мере семнадцать раз в течение некоторого времени, по меньшей мере восемнадцать раз в течение некоторого времени, по меньшей мере девятнадцать раз в течение некоторого времени или по меньшей мере двадцать раз в течение некоторого времени.
[00404] В одном варианте реализации изобретения нуклеазный агент вносят в клетку одновременно с направляющим вектором или крупным направляющим вектором (LTVEC). В альтернативном варианте нуклеазный агент вносят отдельно от направляющего вектора или LTVEC течение некоторого времени. В одном варианте реализации изобретения нуклеазный агент вносят до внесения направляющего вектора или LTVEC, в то время как в других вариантах реализации изобретения нуклеазный агент вносят после внесения направляющего вектора или LTVEC.
[00405] В одном варианте реализации изобретения этап скрининга включает количественный анализ для оценки модификации аллеля (МОА) родительской хромосомы. В одном варианте реализации изобретения количественный анализ проводят методом количественной ПЦР. В одном варианте реализации изобретения количественная ПЦР представляет собой ПЦР в режиме реального времени (кПЦР). В одном варианте реализации изобретения ПЦР в режиме реального времени включает применение первой группы праймеров, которая распознает целевой локус, и второй группы праймеров, которая распознает нецелевой контрольный локус. В одном варианте реализации изобретения группа праймеров содержит флуоресцентный зонд, который распознает амплифицированную последовательность. В одном варианте реализации изобретения количественный анализ проводят методом флуоресцентной гибридизации in situ (FISH). В одном варианте реализации изобретения количественный анализ проводят методом сравнительной геномной гибридизации. В одном варианте реализации изобретения количественный анализ проводят методом изотермической амплификации ДНК. В одном варианте реализации изобретения количественный анализ проводят методом изотермической амплификации ДНК. В одном варианте реализации изобретения количественный анализ проводят методом количественной гибридизации с иммобилизованным(и) зондом(ами). В одном варианте реализации изобретения количественный анализ проводят при помощи Invader Probes®. В одном варианте реализации изобретения количественный анализ проводят при помощи ММР assays®. В одном варианте реализации изобретения количественный анализ проводят при помощи TaqMan® Molecular Beacon. В одном варианте реализации изобретения количественный анализ проводят при помощи метода зондов Eclipse™. (Смотрите, например, US 2005/0144655, которая в полном объеме включена в данный документ посредством ссылки).
[00406] Дополнительно предложен способ получения гуманизированного отличного от человека животного, включающий: (а) модификацию генома плюрипотентной клетки направляющим вектором, содержащим нуклеотидную вставку, которая содержит человеческую нуклеотидную последовательность для формирования донорной клетки; (b) внесение донорной клетки в эмбрион-хозяина; и (с) вынашивание эмбриона-хозяина суррогатной матерью; при этом суррогатная мать производит потомство, которое содержит человеческую нуклеотидную последовательность. В одном варианте реализации изобретения донорную клетку вносят в эмбрион-хозяина, который находится на стадии бластоцисты или стадии пре-морулы (т.е. 4-клеточной стадии или 8-клеточной стадии). Кроме того, этап (а) также можно проводить с крупным направляющим вектором (LTVEC) и/или человеческой нуклеотидной последовательностью длиной по меньшей мере 5 т.п.о. В других вариантах реализации изобретения генетическая модификация может передаваться через зародышевую линию.
[00407] Генетически модифицированных отличных от человека животных можно получать, применяя различные раскрытые в данном документе способы. Такие способы включают (1) интеграцию одного или более представляющих интерес полинуклеотидов в целевом локусе плюрипотентной клетки для получения генетически модифицированной плюрипотентной клетки, содержащей нуклеотидную вставку в целевом геномном локусе, при помощи раскрытых в данном документе способов; (2) отбор генетически модифицированной плюрипотентной клетки, содержащей один или более представляющих интерес полинуклеотидов в целевом геномном локусе; (3) внесение генетически модифицированной плюрипотентной клетки в эмбрион-хозяина; и (4) имплантацию эмбриона-хозяина, содержащего генетически модифицированную плюрипотентную клетку, в организм суррогатной матери. Получают потомство от генетически модифицированной плюрипотентной клетки. В одном варианте реализации изобретения донорную клетку вносят в эмбрион-хозяина, который находится на стадии бластоцисты или стадии пре-морулы (т.е. 4-клеточной стадии или 8-клеточной стадии). Получают потомство, которое может передавать генетическую модификацию через зародышевую линию. Плюрипотентная клетка может быть ЭС клеткой, как обсуждается в другом месте данного документа.
[00408] Для получения генетически модифицированных отличных от человека животных также можно применять метод ядерной передачи. Вкратце, метод ядерной передачи включает этапы: (1) удаления ядра из ооцита; (2) выделения донорной клетки или ядра, предназначенных для внесения в ооцит; (3) внесения клетки или ядра в безъядерный ооцит для формирования восстановленной клетки; (4) имплантации восстановленной клетки в матку животного для формирования эмбриона; и (5) создания возможности развития эмбриона. В таких способах ооциты в общем случае получают от мертвых животных, хотя их также можно выделять из маточных труб и/или яичников живых животных. Перед удалением ядра ооциты могут созревать в различных средах, известных специалистам в данной области техники. Удаление ядра из ооцита можно проводить большим количеством способов, хорошо известных специалистам в данной области техники. Внесение донорной клетки или ядра в безъядерный ооцит для формирования восстановленной клетки обычно проводят путем микроинъекции донорной клетки под блестящую оболочку перед слиянием. Слияние можно индуцировать, пропуская постоянный электрический импульс через плоскость контакта/слияния (электрослияние), обрабатывая клетки стимулирующими слияние химическими веществами, такими как полиэтиленгликоль, или посредством инактивированного вируса, такого как вирус Сендай. Восстановленную клетку, как правило, активируют электрическим и/или неэлектрическим способом до, во время и/или после слияние донорного ядра и ооцита-реципиента. Способы активации включают электрические импульсы, химически индуцированный шок, проникновения сперматозоида, повышение уровней двухвалентных катионов в ооците и снижение фосфорилирования клеточных белков (например, посредством ингибиторов киназы) в ооците. Активированные восстановленные клетки или эмбрионы, как правило, культивируют в среде, хорошо известной специалистам в данной области техники, а затем переносят в матку животного. Смотрите, например, US 20080092249, WO/1999/005266 A2, US 20040177390, WO/2008/017234 A1, и патент США №7612250, которые все включены в данный документ посредством ссылки.
[00409] В одном аспекте предложен способ получения гуманизированного отличного от человека животного, включающий модификацию представляющего интерес геномного локуса в плюрипотентной клетке с применением опосредованного эндонуклеазами таргетирования генов для внесения модификации в представляющий интерес геномный локус для получения модифицированной плюрипотентной клетки, содержание модифицированной плюрипотентной клетки в условиях, достаточных для сохранения плюрипотентности, применение модифицированной плюрипотентной клетки в качестве донорной клетки в эмбрионе-хозяине и вынашивание эмбриона-хозяина, содержащего модифицированную плюрипотентную клетку, суррогатной матерью, при этом эмбрион-хозяин вынашивается суррогатной матерью и рождается генетически модифицированное потомство.
[00410] В одном варианте реализации изобретения целевая последовательность расположена в интроне. В одном варианте реализации изобретения целевая последовательность расположена в экзоне. В одном варианте реализации изобретения целевая последовательность расположена в промоторе. В одном варианте реализации изобретения целевая последовательность расположена в регуляторной области промотора. В одном варианте реализации изобретения целевая последовательность расположена в энхансерной области.
[00411] В одном варианте реализации изобретения этап внесения осуществляют много раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности. В одном варианте реализации изобретения этап осуществляют по меньшей мере два раза в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере три раза в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере четыре раза в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере пять раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере шесть раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере семь раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере восемь раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере девять раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере десять раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере одиннадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере двенадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере тринадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере четырнадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере пятнадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере шестнадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере семнадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере восемнадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности, по меньшей мере девятнадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности или по меньшей мере двадцать раз в течение периода времени, используя множество эндонуклеаз, которые распознают разные целевые последовательности.
[00412] В одном варианте реализации изобретения этап внесения опосредуется электропорацией, интрацитоплазматической инъекцией, аденовирусом, лентивирусом, ретровирусом, трансфекцией, липид-опосредованной трансфекцией или опосредуется нуклеофекцией™.
[00413] В одном варианте реализации изобретения способ дополнительно включает внесение экзогенной нуклеиновой кислоты в генетически модифицированную плюрипотентную клетку. В одном варианте реализации изобретения экзогенная нуклеиновая кислота является трансгеном. В одном варианте реализации изобретения экзогенную нуклеиновую кислоту вносят в эндогенный локус. В одном варианте реализации изобретения экзогенную нуклеиновую кислоту вносят эктопически (например, в локус, отличный от ее эндогенного локуса).
[00414] В одном аспекте предложен способ получения гуманизированного отличного от человека животного, включающий модификацию представляющего интерес геномного локуса в плюрипотентной клетке с применением РНК-управляемой генной инженерии для внесения модификации в представляющий интерес геномный локус для получения модифицированной плюрипотентной клетки, содержание модифицированной плюрипотентной клетки в условиях, достаточных для сохранения плюрипотентности, применение модифицированной плюрипотентной клетки в качестве донорной клетки в эмбрионе-хозяине и вынашивание эмбриона-хозяина, содержащего модифицированную плюрипотентную клетку, суррогатной матерью, при этом эмбрион-хозяин вынашивается суррогатной матерью и рождается генетически модифицированное потомство.
[00415] В одном варианте реализации изобретения уровень таргетирования для данного метода соответствует диапазону от около 2% до около 80%.
[00416] В одном варианте реализации изобретения способ включает совместное внесение множества вторых экспрессионных конструкций, содержащих разные целевые геномные последовательности, для множественного редактирования разных геномных локусов. В одном варианте реализации изобретения способ включает внесение множества вторых экспрессионных конструкций, содержащих разные целевые геномные последовательности, для множественного редактирования разных геномных локусов в течение периода времени.
[00417] В одном варианте реализации изобретения этап внесения осуществляют много раз в течение периода времени. В одном варианте реализации изобретения этап внесения (b) осуществляют по меньшей мере два раза в течение периода времени, по меньшей мере три раза в течение периода времени, по меньшей мере четыре раза в течение периода времени, по меньшей мере пять раз в течение периода времени, по меньшей мере шесть раз в течение периода времени, по меньшей мере семь раз в течение периода времени, по меньшей мере восемь раз в течение периода времени, по меньшей мере девять раз в течение периода времени, по меньшей мере десять раз в течение периода времени, по меньшей мере одиннадцать раз в течение периода времени, по меньшей мере двенадцать раз в течение периода времени, по меньшей мере тринадцать раз в течение периода времени, по меньшей мере четырнадцать раз в течение периода времени, по меньшей мере пятнадцать раз в течение периода времени, по меньшей мере шестнадцать раз в течение периода времени, по меньшей мере семнадцать раз в течение периода времени, по меньшей мере восемнадцать раз в течение периода времени, по меньшей мере девятнадцать раз в течение периода времени, по меньшей мере двадцать раз в течение периода времени.
[00418] В одном варианте реализации изобретения первая экспрессионная конструкция и вторая экспрессионная конструкция экспрессируются из одной плазмиды.
[00419] В одном варианте реализации изобретения этап внесения опосредуется электропорацией, интрацитоплазматической инъекцией, аденовирусом, лентивирусом, ретровирусом, трансфекцией, липид-опосредованной трансфекцией или опосредуется нуклеофекцией™.
[00420] В одном варианте реализации изобретения способ дополнительно включает внесение экзогенной нуклеиновой кислоты в плюрипотентную клетку, содержащую мутантный аллель.
[00421] В одном варианте реализации изобретения экзогенная нуклеиновая кислота является трансгеном. В одном варианте реализации изобретения экзогенную нуклеиновую кислоту вносят в эндогенный локус. В одном варианте реализации изобретения экзогенную нуклеиновую кислоту вносят эктопически (например, в локус, отличный от ее эндогенного локуса).
[00422] В одном варианте реализации изобретения способ дополнительно включает внесение экзогенной нуклеиновой кислоты в генетически модифицированную плюрипотентную клетку. В одном варианте реализации изобретения экзогенная нуклеиновая кислота является трансгеном. В одном варианте реализации изобретения экзогенную нуклеиновую кислоту вносят в эндогенный локус. В одном варианте реализации изобретения экзогенную нуклеиновую кислоту вносят эктопически (например, в локус, отличный от ее эндогенного локуса).
[00423] В одном аспекте предложен способ получения гуманизированного отличного от человека животного, включающий модификацию плюрипотентной клетки при помощи LTVEC, содержащего вставку, которая содержит человеческую последовательность из по меньшей мере 5 т.п.о., и применение плюрипотентной клетки в качестве донорной клетки, внесение донорной клетки в эмбрион-хозяина и вынашивание эмбриона-хозяина суррогатной матерью, при этом суррогатная мать производит потомство, которое содержит гуманизацию.
[00424] Предложены другие способы получения генетически модифицированного отличного от человека животного, содержащего в зародышевой линии одну или более описанных в данном документе генетических модификаций, включающие: (а) модификацию целевого локуса, содержащегося в прокариотической клетке, с применением различных описанных в данном документе способов; (b) отбор модифицированной прокариотической клетки, содержащей генетическую модификацию в целевом локусе; (с) выделение генетически модифицированного направляющего вектора из генома модифицированной прокариотической клетки; (d) внесение генетически модифицированного направляющего вектора в плюрипотентную клетку для получения генетически модифицированной плюрипотентной клетки, содержащей нуклеотидную вставку в целевом геномном локусе; (е) отбор генетически модифицированной плюрипотентной клетки; (f) внесение генетически модифицированной плюрипотентной клетки в эмбрион-хозяина на стадии пре-морулы; и (g) имплантацию эмбриона-хозяина, содержащего генетически модифицированную плюрипотентную клетку в организм суррогатной матери для получения поколения F0, полученного из генетически модифицированной плюрипотентной клетки. В таких способах направляющий вектор может включать крупный направляющий вектор. Плюрипотентная клетка может являться ЭС клеткой. В дополнительных способах этап выделения (с) дополнительно включает (с1) линеаризацию генетически модифицированного направляющего вектора (т.е. генетически модифицированного LTVEC). В дополнительных вариантах реализации изобретения этап внесения (d) дополнительно включает (d1) внесение описанного в данном документе нуклеазного агента в плюрипотентную клетку. В одном варианте реализации изобретения этапы отбора (b) и/или (е) проводят путем применения описанного в данном документе селективного агента к прокариотической клетке или плюрипотентной клетке. В одном варианте реализации изобретения этапы отбора (b) и/или (е) проводят методом анализа модификации аллеля (МОА), как описано в данном документе.
[00425] Предложены дополнительные способы модификации целевого геномного локуса клетки млекопитающего посредством бактериальной гомологичной рекомбинации (БГР) в прокариотической клетке, включающие: (а) получение прокариотической клетки, содержащей целевой локус, содержащий нуклеиновую кислоту, (b) внесение в прокариотическую клетку направляющего вектора, содержащего нуклеотидную вставку, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом нуклеотидная вставка содержит область млекопитающего (включая, например, вставку ДНК человека), и (с) отбор таргетированной прокариотической клетки, содержащей нуклеотидную вставку в целевом локусе, при этом прокариотическая клетка способна экспрессировать рекомбиназу, которая опосредует БГР. Этап (а1) может включать получение прокариотической клетки, содержащей целевой локус, содержащий нуклеиновую кислоту, содержащую первый полинуклеотид, содержащий первый участок распознавания для первого нуклеазного агента, а этап (b1) может дополнительно включать экспрессию в прокариотической клетке нуклеазного агента, который создает одноцепочечный или двухцепочечный разрыв в или вблизи первого участка распознавания. Этапы (а)-(с) можно повторять серийно, как описано в данном документе, чтобы сделать возможным внесение множества нуклеотидных вставок в целевой локус в прокариотической клетке. После «встраивания» целевого геномного локуса в прокариотическую клетку направляющий вектор, содержащий модифицированный целевой локус, можно выделять из прокариотической клетки и вносить в целевой геномный локус в плюрипотентной клетке. Затем плюрипотентные клетки (т.е. ЭС клетки), содержащие модифицированный геномный локус, можно превращать в генетически модифицированных отличных от человека животных.
[00426] В некоторых вариантах реализации изобретения различные описанные в данном документе генетические модификации целевых геномных локусов можно проводить при помощи серии реакций гомологичной рекомбинации (БГР) в бактериальных клетках, используя LTVEC, полученный из ДНК бактериальной гомологичной хромосомы (БГХ) при помощи метода генетической инженерии VELOCIGENE® (смотрите, например, патент США №6586251 и Valenzuela, D.M. et al. (2003), High-throughput engineering of the mouse genome coupled with high-resolution expression analysis, Nature Biotechnology 21(6): 652-659, которые в полном объеме включены в данный документ посредством ссылки).
[00427] В некоторых вариантах реализации изобретения таргетированные ЭС клетки, содержащие различные описанные в данном документе генетические модификации, применяют в качестве вставочных ЭС клеток и вносят в эмбрион на стадии пре-морулы соответствующего организма, например, мышиный эмбрион на 8-клеточной стадии, при помощи метода VELOCIMOUSE® (смотрите, например, US 7576259, US 7659442, US 7294754 и US 2008-0078000 A1, которые все в полном объеме включены в данный документ посредством ссылки). Эмбрион, содержащий генетически модифицированные ЭС клетки, инкубируют до стадии бластоцисты, а затем имплантируют в организм суррогатной матери для получения F0. Животных, несущих модифицированный геномный локус, можно определить при помощи анализа модификации аллеля (МОА), как описано в данном документе. Полученное в результате отличное от человека животное поколения F0, полученное из генетически модифицированных ЭС клеток, скрещивают с отличным от человека животным дикого типа для получения потомства поколения F1. После генотипирования при помощи специфических праймеров и/или зондов отличных от человека животных F1, которые являются гетерозиготными в отношении генетически модифицированного геномного локуса, скрещивают друг с другом для получения животных, которые являются гомозиготными в отношении генетически модифицированного геномного локуса. В альтернативном варианте можно проводить скрещивание между самкой F0 отличного от человека животного и самцом F0 отличного от человека животного, которые имеют генетическую модификацию, для получения отличного от человека животного F1, гомозиготного в отношении генетической модификации.
[00428] В одном аспекте предложен, например, генетически модифицированный крысиный геном, содержащий направленную модификацию эндогенной нуклеотидной последовательности гомологичной или ортологичной нуклеотидной последовательностью из другого организма.
[00429] В одном варианте реализации изобретения длина гомологичной или ортологичной нуклеотидной последовательности составляет от около 5 т.п.о. до около 200 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 5 т.п.о. до около 10 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 10 т.п.о. до около 20 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 20 т.п.о. до около 30 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 30 т.п.о. до около 40 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 40 т.п.о. до около 50 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 50 т.п.о. до около 60 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 60 т.п.о. до около 70 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 70 т.п.о. до около 80 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 80 т.п.о. до около 90 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 90 т.п.о. до около 100 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 100 т.п.о. до около 110 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 110 т.п.о. до около 120 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 120 т.п.о. до около 130 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 140 т.п.о. до около 150 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 150 т.п.о. до около 160 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 160 т.п.о. до около 170 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 170 т.п.о. до около 180 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 180 т.п.о. до около 190 т.п.о. В одном варианте реализации изобретения гомологичная или ортологичная некрысиная нуклеотидная последовательность соответствует диапазону от около 190 т.п.о. до около 200 т.п.о. Различные представляющие интерес полинуклеотиды, которые можно применять в нуклеотидной вставке, описаны в другом месте данного документа.
[00430] Предложены дополнительные способы направленной модификации генома отличного от человека животного. Такие способы могут включать (а) модификацию представляющего интерес геномного локуса в нечеловеческой плюрипотентной клетке в соответствии с любым из предложенных в данном документе способов модификации представляющего интерес геномного локуса с получением, таким образом, генетически модифицированной нечеловеческой плюрипотентной клетки, содержащей направленную модификацию генома; (b) внесение модифицированной нечеловеческой плюрипотентной клетки с этапа (а) в нечеловеческий эмбрион-хозяина; и (с) вынашивание нечеловеческого эмбриона-хозяина, содержащего модифицированную плюрипотентную клетку, суррогатной матерью, при этом суррогатная мать производит потомство F0, содержащее направленную модификацию генома, а направленная модификация генома может передаваться через зародышевую линию.
[00431] В некоторых вариантах реализации изобретения направленная модификация генома включает одновременное удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе и вставку экзогенной нуклеиновой кислоты в представляющий интерес геномный локус (т.е. удаление и вставку на одном этапе). В некоторых вариантах реализации изобретения направленная модификация генома включает биаллельную генетическую модификацию. Биаллельная генетическая модификация может включать удаление эндогенной нуклеотидной последовательности и вставку экзогенной нуклеиновой кислоты в представляющий интерес геномный локус в двух гомологичных хромосомах (т.е. в паре из первой и второй гомологичных хромосом).
[00432] В других вариантах реализации изобретения направленная модификация генома приводит к созданию модифицированной плюрипотентной клетки, которая является компаунд-гетерозиготной в представляющем интерес геномном локусе. В других вариантах реализации изобретения направленная модификация генома приводит к созданию модифицированной плюрипотентной клетки, которая является гемизиготной в представляющем интерес геномном локусе. В некоторых вариантах реализации изобретения направленная модификация генома в представляющем интерес геномном локусе в одной хромосоме включает удаление эндогенной нуклеотидной последовательности и вставку экзогенной нуклеиновой кислоты. Например, направленная модификация генома может включать: (1) удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе в двух гомологичных хромосомах; и (2) вставку экзогенной нуклеиновой кислоты в представляющий интерес геномный локус в первой хромосоме и разрушение представляющего интерес геномного локуса во второй хромосоме. Первая хромосома может быть первой из двух гомологичных хромосом, а вторая хромосома может быть второй из двух гомологичных хромосом.
6. Клетки
[00433] В различных описанных в данном документе способах и композициях применяют систему таргетирования геномного локуса в клетке. В одном варианте реализации изобретения клетка является плюрипотентной клеткой. В одном варианте реализации изобретения клетка является неплюрипотентной клеткой. В одном варианте реализации изобретения плюрипотентная клетка является нечеловеческой плюрипотентной клеткой. В одном варианте реализации изобретения нечеловеческая плюрипотентная клетка является плюрипотентной клеткой млекопитающего. В одном варианте реализации изобретения плюрипотентная клетка является человеческой индуцированной плюрипотентной стволовой (иПС) клеткой.
[00434] В других вариантах реализации изобретения клетка является эукариотической клеткой, некрысиной эукариотической клеткой, человеческой плюрипотентной клеткой, человеческой ЭС клеткой, человеческой взрослой стволовой клеткой, человеческой клеткой-предшественником с ограниченным развитием, клеткой отличного от человека млекопитающего, клеткой млекопитающего, человеческой клеткой, фибробластом, клеткой грызуна, клеткой отличного от крысы грызуна, крысиной клеткой, мышиной клеткой, клеткой хомяка или клеткой СНО.
[00435] В одном варианте реализации изобретения эукариотическая клетка является первичной клеткой. Первичные клетки включают клетки или культуры клеток, которые были выделены непосредственно из организма, органа или ткани. Первичные клетки включают клетки, которые не являются ни трансформированными, ни иммортальными. Они включают любую клетку, полученную из организма, органа или ткани, которую ранее не пассировали в тканевой культуре или которую ранее пассировали в тканевой культуре, но которую невозможно бесконечно пассировать в тканевой культуре. Такие клетки могут быть выделены традиционными методами и включают, например, гемопоэтические клетки, эндотелиальные клетки, эпителиальные клетки, фибробласты, мезенхимальные клетки, кератиноциты, меланоциты, моноциты, мононуклеарные клетки, адипоциты, преадипоциты, нейроны, глиальные клетки, гепатоциты, скелетные миобласты и клетки гладкой мускулатуры. В некоторых вариантах реализации изобретения первичные клетки получены из соединительной ткани, мышечной ткани, ткани нервной системы или эпителиальной ткани.
[00436] В другом варианте реализации изобретения эукариотическая клетка является иммортализованной клеткой. Иммортализованные клетки включают клетки из многоклеточного организма, которые в нормальном состоянии не могли бы пролиферировать бесконечно, но вследствие мутации или изменения избежали процесса клеточного старения и вместо этого продолжают делиться. Такие мутации или изменения могут возникать природным образом или могут быть индуцированы преднамеренно. Примеры иммортализованных клеток включают клетки яичников китайского хомяка (СНО), человеческие эмбриональные клетки почек (например, клетки HEK 293) и фибробласты эмбриона мыши (например, клетки 3Т3). В данной области техники известно множество типов иммортализованных клеток.
[00437] В некоторых вариантах реализации изобретения иммортализованные клетки получены из раковых клеток. В другом варианте реализации изобретения первичная или иммортализованная клетка - это та, которую, как правило, используют для культивирования или для экспрессии рекомбинантных генов или белков.
[00438] В других вариантах реализации изобретения плюрипотентная клетка способна сохранять свою плюрипотентность после по меньшей мере одной направленной генетической модификации ее генома и способна передавать направленную модификацию зародышевой линии поколения F1.
[00439] В одном варианте реализации изобретения плюрипотентная клетка является нечеловеческой оплодотворенной яйцеклеткой на одноклеточной стадии. В одном варианте реализации изобретения нечеловеческая оплодотворенная яйцеклетка является оплодотворенной яйцеклеткой млекопитающего. В одном варианте реализации изобретения оплодотворенная яйцеклетка млекопитающего является оплодотворенной яйцеклеткой грызуна на одноклеточной стадии. В одном варианте реализации изобретения оплодотворенная яйцеклетка млекопитающего является оплодотворенной яйцеклеткой мыши или крысы на одноклеточной стадии.
[00440] Различные клетки, применяемые в описанных в данном документе способах и композициях, также могут включать прокариотические клетки, такие как бактериальные клетки, включая E.coli. В конкретных вариантах реализации изобретения прокариотическая клетка представляет собой рекомбинационно-компетентный штамм E.coli. В одном варианте реализации изобретения прокариотическая клетка содержит нуклеиновую кислоту, которая кодирует рекомбиназу, в то время как в других случаях прокариотическая клетка не содержит нуклеиновую кислоту, которая кодирует рекомбиназу, и нуклеиновую кислоту, кодирующую рекомбиназу, вносят в прокариотическую клетку. В одном варианте реализации изобретения нуклеиновая кислота, кодирующая рекомбиназу, включает ДНК или мРНК. В некоторых вариантах реализации изобретения нуклеиновая кислота, кодирующая рекомбиназу, представляет собой pABG. В одном варианте реализации изобретения рекомбиназа экспрессируется под управлением индуцибельного промотора. В одном варианте реализации изобретения экспрессия рекомбиназы управляется арабинозой.
А. Среда с низкой осмолярностью для получения и поддержания человеческих индуцированных плюрипотентных клеток
[00441] Предложена среда для клеточного культивирования для применения в способах и композициях согласно изобретению. В одном варианте реализации изобретения среда подходит для создания популяции человеческих иПС клеток. В другом варианте реализации изобретения среда подходит для поддержания человеческих иПС клеток в культуре. В некоторых вариантах реализации изобретения человеческие иПС являются наивными или подобными наивным.
[00442] Предложенная в данном документе среда содержит по меньшей мере основную среду, полипептид фактора, ингибирующего лейкемию (LIF), ингибитор киназы гликогенсинтазы 3 (GSK3) и ингибитор MEK.
[00443] Данная среда является средой с низкой осмолярностью. В одном примере осмолярность составляет около 175-280 мОсм/кг. В дополнительных примерах осмолярность среды составляет около 180-270 мОсм/кг, около 200-250 мОсм/кг, около 220-240 мОсм/кг или около 225-235 мОсм. В конкретном варианте реализации изобретения осмолярность среды составляет около 233 мОсм/кг.
[00444] Основная среда, предложенная в изобретении, представляет собой основную среду с низкой осмолярностью, в которую добавляют дополнительные компоненты. Данная основная среда отличается от основных сред, как правило, применяемых для поддержания человеческих иПС клеток в культуре, которые включают модифицированную по способу Дульбекко среду Игла (DMEM) в разных формах (например, DMEM от Invitrogen, Кат. №1 1971-025) и DMEM с низким содержанием соли, коммерчески доступную под названием KO-DMEM™ (Invitrogen, Кат. №10829-018).
[00445] Основная среда, предложенная в изобретении, представляет собой основную среду с низкой осмолярностью, но имеет характеристики, которые не ограничиваются низкой осмолярностью. Например, состав DMEM, приведенный в Таблице А, можно сделать подходящим для целей изобретения путем изменения концентраций хлорида натрия и/или бикарбоната натрия, как предложено в данном документе, что приведет к изменению осмолярности по сравнению со стандартной основной средой DMEM или основной средой DMEM с низким содержанием соли (KO-DMEM), приведенными в Таблице А.
[00446]
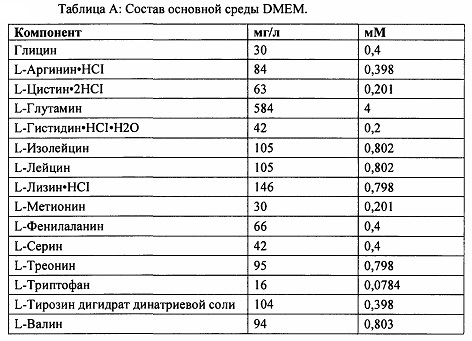
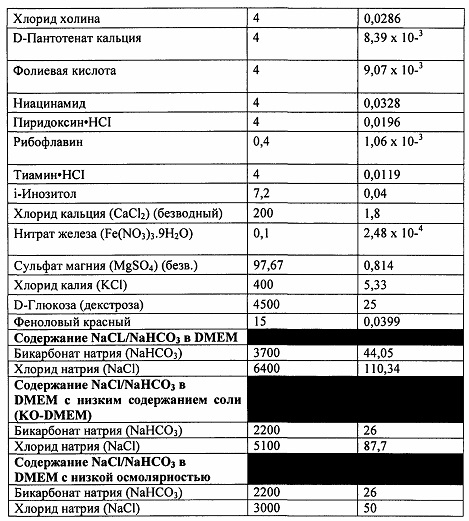
[00447] Данная основная среда может содержать соль щелочного металла и галид, такой как хлорид натрия (NaCl). Типовые концентрации NaCl в основной среде включают 50±5 мМ или около 3 мг/мл.
[00448] В другом варианте реализации изобретения в основной среде наблюдается некоторая концентрация углекислоты. Соль углекислоты может являться солью натрия. В таком примере соль натрия может являться бикарбонатом натрия. В конкретном варианте реализации изобретения бикарбонат натрия присутствует в основной среде в концентрации, составляющей около 26±5 мМ или около 2,2 мг/мл.
[00449] В другом варианте реализации изобретения основная среда представляет собой основную среду с низкой осмолярностью. Осмолярность основной среды может соответствовать диапазону около 175-280 мОсм/кг, около 180-250 мОсм/кг, около 190-225 мОсм/кг или около 195-205 мОсм/кг. Типовая осмолярность основной среды может составлять 200, 214, 216 или 218 мОсм/кг. В конкретном примере осмолярность основной среды составляет 200 мОсм/кг. Осмолярность можно определить, когда клетки культивируют с разными концентрациями CO2. В некоторых примерах клетки культивируют в 3% CO2 или 5% CO2.
[00450] В предпочтительном варианте реализации изобретения основная среда содержит NaCl в концентрации 3,0 мг/мл, бикарбонат натрия в концентрации около 2,2 мг/мл и обладает осмолярностью, составляющей 200 мОсм/кг.
[00451] Добавки, входящие в состав основной среды согласно изобретению, подходят для получения, поддержания или обогащения раскрытых в данном документе человеческих иПС клеток. В настоящем описании такие добавки обозначают как «добавки» или «+ добавки». Термин «добавки» или выражение «+ добавки» включает один или более дополнительных элементов, добавляемых к компонентам основной среды, приведенным в Таблице А. Например, добавки могут включать, без ограничений, среду F-12® (Gibco), добавку N2® (Gibco; 100X раствор), среду NEUROBASAL® (Gibco), добавку В-27® (Gibco; 50X раствор), L глутамин, глюкозу, 2 меркаптоэтанол, полипептид фактора, ингибирующего лейкемию (LIF), ингибитор киназы гликогенсинтазы 3 (GSK3), ингибитор MEK или любую их комбинацию.
[00452] В конкретном варианте реализации изобретения полипептид LIF является человеческим полипептидом LIF (hLIF). В некоторых примерах полипептид hLIF применяют в концентрации около 1-1000 единиц/мл, около 20-800 единиц/мл, около 50-500 единиц/мл, около 75-250 единиц/мл или около 100 единиц/мл.
[00453] В другом конкретном варианте реализации изобретения ингибитор GSK3 включает CHIR99021. В некоторых примерах CHIR99021 применяют в концентрации от около 0,1 до 10 мкМ, около 1-5 мкМ, около 2-4 мкМ или около 3 мкМ.
[00454] В другом конкретном варианте реализации изобретения ингибитор MEK включает PD0325901. В некоторых примерах PD0325901 применяют в концентрации около 0,1-5 мкМ, около 0,2-1 мкМ, около 0,3-0,7 мкМ или около 0,5 мкМ.
[00455] Типовая среда содержит около 24,75% (об/об) описанной в данном документе основной среды с низкой осмолярностью, около 24,75% (об/об) среды F-12, около 0,5% (об/об) добавки N2, около 49% (об/об) среды NEUROBASAL, около 1% (об/об) добавки В-27, около 2 мМ L-глутамина, около 0,1 мМ 2-меркаптоэтанола, около 100 единиц/мл hLIF, около 3 мкМ CHIR99021 и около 0,5 мкМ PD0325901.
[00456] В другом конкретном варианте реализации изобретения среда может содержать или не содержать основной фактор роста фибробластов (bFGF, также известный как FGF2 или FGF-β). Предпочтительно данная среда не содержит bFGF.
В. Человеческие индуцированные плюрипотентные стволовые клетки
[00457] В данном документе предложены способы и композиции для получения популяции человеческих иПС клеток. Дополнительно предложены способы и композиции для поддержания человеческих иПС клеток в культуре. Также предложены человеческие иПС клетки, которые получают или поддерживают в культуре.
[00458] Термин «плюрипотентная клетка» или «плюрипотентная стволовая клетка» включает недифференцированную клетку, которая обладает способностью развиваться в более чем один тип дифференцированных клеток. Такими плюрипотентными клетками могут быть, например, эмбриональные стволовые клетки (ЭС клетки) млекопитающих или индуцированные плюрипотентные стволовые клетки (иПС клетки) млекопитающих. Примеры плюрипотентных клеток включают человеческие иПС клетки.
[00459] Термин «эмбриональная стволовая клетка» или «ЭС клетка» означает полученную из эмбриона тотипотентную или плюрипотентную стволовую клетку, полученную из внутренней клеточной массы бластоцисты, которую можно поддерживать в in vitro культуре в подходящих условиях. ЭС клетки способны дифференцироваться в клетки любого из трех зародышевых листков позвоночных, например, энтодерму, эктодерму или мезодерму. ЭС клетки также характеризуются своей способностью к бесконечному размножению в подходящих in vitro культуральных условиях. Смотрите, например, Thomson et al. (Science (1998) Vol. 282 (5391), pp. 1145-1147).
[00460] Термин «индуцированная плюрипотентная стволовая клетка» или «иПС клетка» включает плюрипотентную стволовую клетку, которую можно получить непосредственно из дифференцированной взрослой клетки. Человеческие иПС клетки можно получать путем внесения специальных групп перепрограммирующих факторов в неплюрипотентную клетку, которые могут включать, например, Oct3/4, транскрипционные факторы семейства Sox (например, Sox1, Sox2, Sox3, Sox15), транскрипционные факторы семейства Myc (например, с-Myc, l-Myc, n-Myc), семейство Крюппель-подобных (KLF) транскрипционных факторов (например, KLF1, KLF2, KLF4, KLF5) и/или родственные транскрипционные факторы, такие как NANOG, LIN28 и/или Glis1. Человеческие иПС клетки также можно получать, например, путем применения миРНК, небольших молекул, которые имитируют действия транскрипционных факторов, или спецификаторов линии дифференцировки. Человеческие иПС клетки характеризуются своей способностью дифференцироваться в любые клетки трех зародышевых листков позвоночных, например, энтодерму, эктодерму или мезодерму. Человеческие иПС клетки также характеризуются своей способностью к бесконечному размножению в подходящих in vitro культуральных условиях. Смотрите, например, Takahashi and Yamanaka (Cell (2006) Vol. 126(4), pp. 663-676).
[00461] Термины «наивный» или «примированный» указывают на разное состояние плюрипотентности человеческих иПС клеток. Термин «подобный наивному» указывает на клетку, экспрессирующую плюрипотентное состояние, которая демонстрирует одну или более характеристик наивной плюрипотентной клетки. Подобные наивным человеческие иПС клетки также могут называться «условно наивными» человеческими иПС клетками. В некоторых вариантах реализации изобретения подобные наивным человеческие иПС клетки демонстрируют одну или более морфологических характеристик наивных человеческих иПС клеток, например, морфологию, характеризуемую компактными полусферическими колониями. В некоторых вариантах реализации изобретения подобные наивным человеческие иПС клетки экспрессируют один или более маркеров плюрипотентности, описанных в данном документе. В некоторых вариантах реализации изобретения наивные или подобные наивным человеческие иПС клетки представляют собой наивные человеческие иПС клетки. В других вариантах реализации изобретения наивные или подобные наивным человеческие иПС клетки представляют собой подобные наивным человеческие иПС клетки.
[00462] Характеристики наивных и примированных иПС клеток описаны в данной области техники. Смотрите, например, Nichols and Smith (Cell Stem Cell (2009) Vol. 4(6), pp. 487-492). Наивные человеческие иПС клетки демонстрируют состояние плюрипотентности, сходное с ЭС клетками внутренней клеточной массы предимплантационного эмбриона. Такие наивные клетки не являются примированными в отношении спецификации и детерминации дифференцировки. Женские наивные иПС клетки характеризуются наличием двух активных X-хромосом. Самообновление наивных человеческих иПС клеток в культуре зависит от фактора, ингибирующего лейкемию (LIF), и других ингибиторов. Культивируемые наивные человеческие иПС клетки демонстрируют клональную морфологию, характеризуемую полусферическими колониями и отсутствием апико-базальной полярности. Культивируемые наивные клетки также могут демонстрировать один или более маркеров плюрипотентности, описанных в другом месте данного документа. В подходящих условиях время удвоения наивных человеческих иПС клеток в культуре может составлять между 16 и 24 часами.
[00463] Примированные человеческие иПС клетки экспрессируют состояние плюрипотентности, сходное с постимплантационными клетками эпибласта. Такие клетки являются примированными в отношении спецификации и детерминации дифференцировки. Женские примированные иПС клетки характеризуются наличием одной активной Х-хромосомы и одной неактивной Х-хромосомы. Самообновление примированных человеческих иПС клеток в культуре зависит от фактора роста фибробластов (FGF) и активина. Культивируемые примированные человеческие иПС клетки демонстрируют клональную морфологию, характеризуемую эпителиальным монослоем и демонстрируют апико-базальную полярность. В подходящих условиях время удвоения примированных человеческих иПС клеток в культуре может составлять 24 часа или более.
[00464] В одном варианте реализации изобретения человеческие иПС клетки могут быть получены из неплюрипотентных клеток, трансформированных так, чтобы экспрессировать плюрипотентное состояние. Такие трансформированные клетки включают, например, клетки, которые были трансформированы так, чтобы экспрессировать перепрограммирующие гены, которые индуцируют плюрипотентность. Плюрипотентное состояние может включать, например, экспрессию одного или более маркеров плюрипотентности, описанных в данном документе. Такие клетки (такие как фибробласты крайней плоти человека) можно трансформировать так, чтобы они экспрессировали перепрограммирующие гены или любые дополнительные представляющие интерес гены, любыми известными в данной области техники способами. Смотрите, например, Takahashi and Yamanaka (Cell (2006) Vol. 126(4), pp. 663-676). Например, их можно вносить в клетки, используя один или более элемент из плазмид, лентивирусных векторов или ретровирусных векторов. В некоторых случаях векторы интегрируются в геном и могут быть удалены после завершения перепрограммирования. В конкретных вариантах реализации изобретения неплюрипотентные клетки трансформируют перепрограммирующими генами, включая Oct4, Sox2, Klf4, Myc или любую их комбинацию. В некоторых примерах трансформированные клетки включают примированные человеческие иПС клетки.
[00465] В некоторых вариантах реализации изобретения человеческие иПС клетки, культивируемые в описанной в данном документе среде с низкой осмолярностью, экспрессируют один или более фенотипов, профилей генной экспрессии или маркеров, характерных для наивного состояния. В одном примере человеческие иПС клетки экспрессируют один или более маркеров плюрипотентности, характерных для наивного состояния. Такие маркеры плюрипотентности могут включать щелочную фосфатазу, NANOG, 5T4, ABCG2, Activin RIB/ALK-4, Activin RIIB, Е-кадгерин, Cbx2, CD9, CD30/TNFRSF8, CD117/c-kit, CDX2, CHD1, Cripto, DNMT3B, DPPA2, DPPA4, DPPA5/ESG1, EpCAM/TROP1, ERR beta/NR3B2, ESGP, белок F-бокс 15/FBXO15, FGF-4, FGF-5, FoxD3, GBX2, GCNF/NR6A1, GDF-3, Gi24/VISTA/B7-H5, интегрин альфа 6/CD49f, интегрин альфа 6 бета 1, интегрин альфа 6 бета 4, интегрин бета 1/CD29, KLF4, KLF5, L1TD1, Lefty, Lefty-1, Lefty-A, LIN-28A, LIN-28B, LIN-41, cMaf, cMyc, Oct-3/4, Oct-4A, подокаликсин, Rex-1/ZFP42, Smad2, Smad2/3, SOX2, SSEA-1, SSEA-3, SSEA-4, STAT3, Stella/Dppa3, SUZ12, TBX2, ТВХ3, ТВХ5, TERT, TEX19, TEX19.1, THAP11, TRA-1-60(R), TROP-2, UTF1 и/или ZIC3. В конкретном примере экспрессируемым маркером плюрипотентности является щелочная фосфатаза, NANOG или оба.
[00466] В другом варианте реализации изобретения человеческие иПС клетки, культивируемые в описанной в данном документе среде с низкой осмолярностью, демонстрируют морфологические характеристики, характерные для наивного состояния. Типовая морфология характеризуется клетками, образующими компактные полусферические колонии в культуре.
[00467] В другом варианте реализации изобретения человеческие иПС клетки, культивируемые в описанной в данном документе среде с низкой осмолярностью, можно механически или ферментативно. разделить до одноклеточной суспензии, пассировать и/или субкультивировать. В одном примере ферментативное разделение можно проводить, используя трипсин. При культивировании в присутствии среды с низкой осмолярностью человеческие иПС клетки могут обеспечить большую эффективность трансформации вследствие улучшенной диссоциации в одноклеточную суспензию. В случае других типов сред (например, среды mTeSR™ или среды 2i), обычно применяемых для поддержания человеческих иПС клеток в культуре, разделение человеческих иПС клеток нужно проводить механически или при помощи ферментов, таких как коллагеназа, которые являются мене жесткими, чем трипсин. Соответственно, клетки не диссоциируют настолько эффективно или настолько полно. В противоположность этому, в присутствии среды с низкой осмолярностью для разделения клеток можно использовать трипсин, а улучшенная диссоциация приводит к повышению эффективность трансформации. Кроме того, в отличие от других типов сред, обычно применяемых для поддержания человеческих иПС клеток в культуре (например, среды mTeSR™ или среды 2i), ферментативное разделение человеческих иПС клеток, культивируемых в присутствии среды с низкой осмолярностью (предпочтительно среды с низкой осмолярностью, не содержащей bFGF), можно проводить в отсутствие одного или более ингибиторов, которые в общем случае необходимы для пассирования таких клеток. Типовой ингибитор, которым можно пренебречь, это ингибитор Rho-ассоциированной протеинкиназы (ROCK). Ингибитор ROCK в общем случае является необходимым при пассировании человеческих иПС клеток для ингибирования активации проапоптотических путей.
[00468] В дополнительном варианте реализации изобретения субкультивируемые человеческие иПС клетки, культивируемые в описанной в данном документе среде с низкой осмолярностью, могут сохранять наивное или подобное наивному состояние после ферментативного разделения и суб культивирования. В некоторых примерах субкультивируемые человеческие иПС клетки могут продолжать демонстрировать морфологию, характеризуемую компактными полусферическими колониями. Субкультивируемые человеческие иПС клетки также могут продолжать экспрессировать один или более маркеров плюрипотентности, описанных в данном документе.
С. Способы получения и поддержания популяции человеческих индуцированных плюрипотентных стволовых клеток
[00469] Предложены способы и композиции для получения человеческих иПС клеток в in vitro культуре. Дополнительно предложены способы и композиции для поддержания человеческих иПС клеток в in vitro культуре.
[00470] Термин «получение» включает культивирование неплюрипотентных клеток, трансформированных, чтобы экспрессировать один или более описанных в данном документе перепрограммирующих факторов, в подходящих условиях, чтобы индуцировать изменение клеточного фенотипа, генной экспрессии или их обоих, так, что клетки демонстрируют наивное или подобное наивному состояние, т.е. экспрессируют одну или более характеристик человеческих иПС клеток. Наивное или подобное наивному состояние может экспрессироваться в ответ на конкретные культуральне условия, например, культивирование в описанной в данном документе среде с низкой осмолярностью. В некоторых примерах доля клеток, экспрессирующих наивное или подобное наивному состояние, составляет по меньшей мере около 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% и до 100% клеток в культуре.
[00471] В одном варианте реализации изобретения способ обогащает in vitro культуру популяцией наивных или подобных наивным человеческих иПС клеток. В таком варианте реализации изобретения наивные или подобные наивным человеческие иПС клетки могут преимущественно размножаться в культуре по сравнению с клетками, которые не экспрессируют наивное или подобное наивному состояние. В другом варианте реализации изобретения наивные или подобные наивным человеческие иПС клетки можно отбирать из культуры, ферментативно разделять и субкультивировать для получения обогащенной популяции наивных или подобных наивным человеческих иПС клеток.
[00472] В одном варианте реализации изобретения неплюрипотентные клетки, трансформированные, чтобы экспрессировать плюрипотентое состояние, культивируют in vitro в предложенной в данном документе среде, которая подходит для индукции экспрессии наивного или подобного наивному состояния в течение периода, составляющего по меньшей мере 1, 2, 5, 7, 10, 14, 21 или 28 дней, или любого периода времени, достаточного, чтобы индуцировать экспрессию наивного или подобного наивному состояния в культуре. Трансформированные клетки можно культивировать в присутствии среды в течение по меньшей мере 1, 2, 3 или 4 недель. Иногда трансформированные клетки культивируют в течение 1-4 недель. Экспрессию наивного или подобного наивному состояния можно определить, наблюдая морфологические характеристики или экспрессию маркеров плюрипотентности, которые описаны в другом месте данного документа.
[00473] В одном варианте реализации изобретения неплюрипотентные клетки, трансформированные, чтобы экспрессировать плюрипотентое состояние, культивируют в присутствии среды с низкой осмолярностью до тех пор, пока они не начинают экспрессировать характеристики наивного или подобного наивному состояния. Затем клетки можно культивировать в среде для поддержания наивного или подобного наивному состояния. В другом варианте реализации изобретения неплюрипотентные клетки, трансформированные, чтобы экспрессировать плюрипотентое состояние, сначала культивируют в среде с высокой осмолярностью перед культивированием в присутствии среды с низкой осмолярностью. Такая среда с высокой осмолярностью имеет более высокую осмолярность, чем предложенная среда с низкой осмолярностью, и может содержать bFGF. Некоторая среда с высокой осмолярностью содержит один или более компонентов из бычьего сывороточного альбумина, bFGF, трансформирующего фактора роста β (TGFβ), хлорида лития, пипеколиновой кислоты и гамма-аминомасляной кислоты (GABA). Примеры сред с высокой осмолярностью включают среду mTeSR™ (Stemcell Technologies).
[00474] В некоторых вариантах реализации изобретения неплюрипотентные клетки, трансформированные, чтобы экспрессировать плюрипотентое состояние, можно сначала культивировать в среде с высокой осмолярностью, содержащей bFGF, до тех пор, пока они не начнут экспрессировать характеристики наивного или подобного наивному состояния, и с этого момента клетки культивируют в присутствии среды с низкой осмолярностью. В одном примере можно культивировать в среде с высокой осмолярностью, содержащей bFGF, в течение периода времени, составляющего по меньшей мере 1, 2, 5, 10, 30, 60 или 90 дней, периода, составляющего 1, 2, 4, 8 или 12 недель, или периода от 1 дня до 3 месяцев. Типовой период культивирования в среде с высокой осмолярностью, содержащей bFGF, составляет 2 месяца.
[00475] В других вариантах реализации изобретения неплюрипотентные клетки, трансформированные, чтобы экспрессировать плюрипотентое состояние, можно сначала культивировать в среде с высокой осмолярностью, содержащей bFGF, до тех пор, пока они не начнут демонстрировать морфологию, характеризуемую трехмерными скоплениями клеток, и с этого момента клетки культивируют в присутствии среды с низкой осмолярностью. В таких вариантах реализации изобретения клетки, демонстрирующие трехмерные скопления, можно отбирать, разделять (например, при помощи трипсина) и переносить в новую культуру в описанную в данном документе среду с низкой осмолярностью.
[00476] Термины «поддерживать» и «поддержание» включают сохранение по меньшей мере одной или более характеристик или фенотипов описанных в данном документе человеческих иПС клеток. Такие характеристики могут включать сохранение плюрипотентности, профилей генной экспрессии и/или функциональных характеристик наивных клеток. Термины «поддерживать» и «поддержание» также могут включать размножение клеток и/или повышение количества культивируемых наивных клеток. Данные термины включают культуральные условия, которые предотвращают преобразование клеток в примированное или неплюрипотентное состояние. Данные термины дополнительно включают культуральные условия, которые позволяют клеткам оставаться плюрипотентными и/или наивными, в то время как клетки могут продолжать или не продолжать делиться и увеличиваться в количестве.
[00477] В одном варианте реализации изобретения человеческие иПС клетки культивируют in vitro в предложенной в данном документе среде, которая подходит для поддержания таких клеток в наивном или подобном наивному состоянии. В конкретном примере человеческие иПС клетки можно культивировать в подходящей среде в течение периода, составляющего 1, 2, 5, 7, 10, 14, 21 или 28 дней, или периода, составляющего около 2 недель, около 3 недель, около 4 недель или более, пока культивируемые клетки остаются в наивном или подобном наивному состоянии. Клетки можно культивировать в течение по меньшей мере 1, 2, 3 или 4 недель. Иногда клетки культивируют в течение 1-4 недель. Человеческие иПС клетки можно поддерживать, например, в течение любого периода времени, достаточного для размножения клеток в культуре, генетической модификации клеток и/или субкультивирования клеток.
[00478] В другом варианте реализации изобретения человеческие иПС клетки или неплюрипотентные клетки, трансформированные, чтобы экспрессировать плюрипотентое состояние, можно культивировать на субстрате или слое питающих клеток, подходящем для in vitro культивирования. В конкретном примере клетки культивируют на MATRIGEL™ (BD Biosciences). В другом примере клетки культивируют на питающих клетках фибробластов крайней плоти новорожденного человека (NuFF). В другом примере клетки культивируют на GELTREX™ (Life Technologies).
[00479] В дополнительном варианте реализации изобретения время удвоения человеческих иПС клеток, культивируемых в присутствии среды с низкой осмолярностью, снижено по сравнению с примиро ванным и человеческими иПС клетками или неплюрипотентными клетками, трансформированными, чтобы экспрессировать плюрипотентое состояние. В конкретном примере время удвоения данных человеческих иПС клеток составляет около 16-24 часов.
7. Идентичность последовательностей
[00480] В предложенных в данном документе способах и композициях применяют множество разных компонентов системы направленной геномной интеграции (т.е. нуклеазных агентов, участков распознавания, нуклеотидных вставок, представляющих интерес полинуклеотидов, направляющих векторов, селективных маркеров и других компонентов). Из описания понятно, что некоторые компоненты системы направленной геномной интеграции могут иметь активные варианты и фрагменты. Такие компоненты включают, например, нуклеазные агенты (т.е. сконструированные нуклеазные агенты), участки распознавания нуклеазных агентов, представляющие интерес полинуклеотиды, целевые участки и соответствующие плечи гомологии направляющего вектора. Биологическая активность каждого из этих компонентов описана в другом месте данного документа.
[00481] В данном документе «идентичность последовательностей» или «идентичность» в контексте двух полинуклеотидов или полипептидных последовательностей относится к остаткам в двух последовательностях, одинаковым при выравнивании для максимального соответствия в конкретном окне сравнения. Когда в отношении белков используют процент идентичности последовательностей, следует понимать, что позиции остатков, которые являются не идентичными, часто отличаются консервативными аминокислотными заменами, когда аминокислотные остатки замещаются другими аминокислотными остатками со схожими химическими свойствами (например, зарядом или гидрофобностью) и, следовательно, не приводят к изменению функциональных свойств молекулы. Когда последовательности отличаются консервативными заменами, процент идентичности последовательностей может быть повышен, учитывая консервативную природу замены. Говорят, что последовательности, которые отличаются такими консервативными заменами, обладают «сходством последовательностей» или «сходством». Способы проведения такой корректировки хорошо известны специалистам в данной области техники. Как правило, консервативную замену учитывают как частичное, а не полное несовпадение, тем самым повышая процент идентичности последовательностей. Таким образом, например, если идентичной аминокислоте приписывается значение 1, а неконсервативной замене приписывается значение ноль, консервативной замене приписывается значение между нулем и 1. Производят подсчет значений консервативных замен, например, как в программе PC/GENE (Intelligenetics, Mountain View, California).
[00482] В контексте данного документа «процент идентичности последовательностей» означает величину, определяемую путем сравнения двух оптимально выровненных последовательностей в окне сравнения, при этом часть полинуклеотидной последовательности в окне сравнения может содержать добавки или делеции (т.е. гэпы) по сравнению с контрольной последовательностью (которая не содержит добавок или делеций) для оптимального выравнивания двух последовательностей. Процент рассчитывают, определяя количество позиций, в которых в обеих последовательностях содержатся идентичные нуклеотидные основания или аминокислотные остатки, чтобы получить количество совпадающих позиций, деля количество совпадающих позиций на общее количество позиций в окне сравнения и умножая результат на 100, чтобы получить процент идентичности последовательностей.
[00483] Если не указано иное, приведенные в данном документе значения идентичности/сходства последовательностей относятся к значениям, полученным при помощи GAP, версия 10, с применением следующих параметров: в случае % идентичности и % сходства для нуклеотидной последовательности с применением штрафа за гэп 50 и штрафа за продолжение 3, а также матрицы замен nwsgapdna.cmp; в случае % идентичности и % сходства для аминокислотной последовательности с применением штрафа за гэп 8 и штрафа за продолжение 2, а также матрицы замен BLOSUM62; или любой другой эквивалентной программы. «Эквивалентная программа» означает любую программу для сравнения последовательностей, которая в случае любых двух сравниваемых последовательностей создает выравнивание, дающее идентичное совпадение нуклеотидных или аминокислотных остатков, а так же такой же процент идентичности последовательностей, если сравнивать с соответствующим выравниванием, созданным GAP, версия 10.
[00484] Если не указано иное, все применяемые в данном документе технические и научные термины имеют те же значения, которые обычно подразумеваются специалистом в области техники, к которой принадлежит данное изобретение. Хотя для практической реализации или тестирования описанного изобретения также можно применять любые способы и материалы, сходные или эквивалентные описанным в данном документе, предпочтительные способы и материалы описаны в тексте. Все публикации, упоминаемые в данном документе, включены посредством ссылки для раскрытия и описания способов и/или материалов, в связи с которыми упоминаются эти публикации.
[00485] Следует отметить, что применяемая в тексте данного документа и прилагаемой формуле изобретения форма единственного числа включает множественное число, если иное четко не предусмотрено контекстом. Все применяемые в данном документе технические и научные термины имеют те же значения.
[00486] Обсуждаемые в данном документе публикации приведены исключительно в отношении их содержания до даты подачи настоящей заявки. Ничто в данном документе не следует рассматривать как признание того, что описываемое изобретение не дает права датировать такую публикацию задним числом на основании предыдущего изобретения. Кроме того, приведенные даты публикации могут отличаться от фактических дат публикации, которые могут требовать независимого подтверждения.
[00487] Реализацию описываемого изобретения можно осуществлять в других конкретных формах, не отступая от его сути или существенных признаков, и, соответственно, ссылаться следует не на вышеприведенное описание, а на прилагаемую формулу изобретения, как определяющую объем изобретения.
[00488] Неограничивающие варианты реализации изобретения включают:
[00489] 1. Способ направленной генетической модификации представляющего интерес геномного локуса в плюрипотентной крысиной клетке, включающий (а) внесение в плюрипотентную крысиную клетку крупного направляющего вектора (LTVEC), содержащего нуклеотидную вставку, фланкируемую 5' крысиным плечом гомологии и 3' крысиным плечом гомологии, при этом 5' и 3' плечи гомологии в общей сумме составляют по меньшей мере 10 т.п.о., но менее чем 150 т.п.о.; и (b) выявление генетически модифицированной плюрипотентной крысиной клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе, при этом направленная генетическая модификация может передаваться через зародышевую линию.
[00490] 2. Способ по варианту реализации изобретения 1, отличающийся тем, что направленная генетическая модификация является биаллельной.
[00491] 3. Способ по варианту реализации изобретения 1 или 2, отличающийся тем, что плюрипотентная крысиная клетка является крысиной эмбриональной стволовой (ЭС) клеткой.
[00492] 4. Способ по варианту реализации изобретения 1, 2 или 3, отличающийся тем, что плюрипотентная крысиная клетка получена от штамма DA или штамма ACI.
[00493] 5. Способ по любому из вариантов реализации изобретения 1-4, отличающийся тем, что плюрипотентная крысиная клетка характеризуется экспрессией по меньшей мере одного маркера плюрипотентности, включая Dnmt3L, Eras, Err-beta, Fbxo15, Fgf4, Gdf3, Klf4, Lef1, рецептор LIF, Lin28, Nanog, Oct4, Sox15, Sox2, Utf1 или их комбинацию.
[00494] 6. Способ по любому из вариантов реализации изобретения 1-4, отличающийся тем, что плюрипотентная крысиная клетка характеризуется одной или более из следующих характеристик:
(а) отсутствием экспрессии одного или более маркеров плюрипотентности, включая с-Myc, Ecat1 и/или Rexo1; (b) отсутствием экспрессии мезодермальных маркеров, включая брахиурию и/или Bmpr2; (с) отсутствием экспрессии одного или более энтодермальных маркеров, включая Gata6, Sox17 и/или Sox7; или (d) отсутствием экспрессии одного или более нейральных маркеров, включая Nestin и/или Рах6.
[00495] 7. Способ по любому из вариантов реализации изобретения 1-6, отличающийся тем, что 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.о. до около 30 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до 150 т.п.о.
[00496] 8. Способ по любому из вариантов реализации изобретения 1-6, отличающийся тем, что 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 16 т.п.о. до около 150 т.п.о.
[00497] 9. Способ по любому из вариантов реализации изобретения 1-8, отличающийся тем, что направленная генетическая модификация включает: (а) замещение эндогенной крысиной нуклеотидной последовательности гомологичной или ортологичной нуклеотидной последовательностью; (b) удаление эндогенной крысиной нуклеотидной последовательности; (с) удаление эндогенной крысиной нуклеотидной последовательности, при этом диапазон удаления составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.; (а) экзогенную нуклеотидную последовательность в диапазоне от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.; (е) экзогенную нуклеотидную последовательность, содержащую гомологичную или ортологичную нуклеотидную последовательность; (f) химерную нуклеотидную последовательность, содержащую человеческую и крысиную нуклеотидную последовательность; (g) кондициональный аллель, фланкируемый целевыми последовательностями сайт-специфической рекомбиназы; или (h) репортерный ген, функционально связанный с промотором, активным в крысиной клетке.
[00498] 10. Способ по любому из вариантов реализации изобретения 1-9, отличающийся тем, что представляющий интерес геномный локус содержит (i) первую нуклеотидную последовательность, которая комплементарна 5' крысиному плечу гомологии; и (ii) вторую нуклеотидную последовательность, которая комплементарна 3' крысиному плечу гомологии.
[00499] 11. Способ по варианту реализации изобретения 10, отличающийся тем, что первая и вторая нуклеотидные последовательности разделены по меньшей мере 5 т.п.о., но менее чем 3 м.п.о.
[00500] 12. Способ по варианту реализации изобретения 10, отличающийся тем, что первая и вторая нуклеотидные последовательности разделены по меньшей мере 5 т.п.о., но менее чем 10 т.п.о., по меньшей мере 10 т.п.о., но менее чем 20 т.п.о., по меньшей мере 20 т.п.о., но менее чем 40 т.п.о., по меньшей мере 40 т.п.о., но менее чем 60 т.п.о., по меньшей мере 60 т.п.о., но менее чем 80 т.п.о., по меньшей мере около 80 т.п.о., но менее чем 100 т.п.о., по меньшей мере 100 т.п.о., но менее чем 150 т.п.о., или по меньшей мере 150 т.п.о., но менее чем 200 т.п.о., по меньшей мере около 200 т.п.о., но менее чем около 300 т.п.о., по меньшей мере около 300 т.п.о., но менее чем около 400 т.п.о., по меньшей мере около 400 т.п.о., но менее чем около 500 т.п.о., по меньшей мере около 500 т.п.о., но менее чем около 1 м.п.о., по меньшей мере около 1 м.п.о., но менее чем около 1,5 м.п.о., по меньшей мере около 1,5 м.п.о., но менее чем около 2 м.п.о., по меньшей мере около 2 м.п.о., но менее чем около 2,5 м.п.о., или по меньшей мере около 2.5 м.п.о., но менее чем около 3 м.п.о.
[00501] 13. Способ по любому из вариантов реализации изобретения 1-12, отличающийся тем, что этап внесения (а) дополнительно включает внесение второй нуклеиновой кислоты, кодирующей нуклеазный агент, который стимулирует гомологичную рекомбинацию между направляющей конструкцией и представляющим интерес геномным локусом в плюрипотентной крысиной клетке.
[00502] 14. Способ по варианту реализации изобретения 13, отличающийся тем, что нуклеазный агент включает (а) химерный белок, содержащий цинк-пальцевый ДНК-связывающий домен, слитый с эндонуклеазой FokI; или (b) химерный белок, содержащий подобную активатору транскрипции эффекторную нуклеазу (TALEN), слитую с эндонуклеазой FokI.
[00503] 15. Способ по любому из вариантов реализации изобретения 1-12, отличающийся тем, что этап внесения (а) дополнительно включает внесение в плюрипотентную крысиную клетку: (i) первой экспрессионной конструкции, содержащей первый промотор, функционально связанный с первой нуклеотидной последовательностью, кодирующей ассоциированный с короткими палиндромными повторами, регулярно расположенными группами (CRISPR), белок (Cas), (ii) второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с целевой геномной последовательностью, связанной с направляющей РНК (нРНК), при этом целевая геномная последовательность непосредственно фланкируется в 3' конце последовательностью мотива, прилегающего к протоспейсеру (РАМ).
[00504] 16. Способ по варианту реализации изобретения 15, отличающийся тем, что представляющий интерес геномный локус содержит нуклеотидную последовательность SEQ ID №1.
[00505] 17. Способ по варианту реализации изобретения 15 или 16, отличающийся тем, что нРНК содержит третью нуклеотидную последовательность, кодирующую РНК коротких палиндромных повторов, регулярно расположенных группами (CRISPR) (crРНК), и транс-активирующую РНК CRISPR (tracrРНК).
[00506] 18. Способ по варианту реализации изобретения 15, 16 или 17, отличающийся тем, что белок Cas представляет собой Cas9.
[00507] 19. Способ по варианту реализации изобретения 15, 16, 17 или 18, отличающийся тем, что нРНК содержит: (а) химерную РНК из нуклеотидной последовательности SEQ ID №2; или (b) химерную РНК из нуклеотидной последовательности SEQ ID №3.
[00508] 20. Способ по варианту реализации изобретения 17, отличающийся тем, что crРНК содержит SEQ ID №4; SEQ ID №5; или SEQ ID №6.
[00509] 21. Способ по варианту реализации изобретения 17, отличающийся тем, что tracrРНК содержит SEQ ID №7 или SEQ ID №8.
[00510] 22. Модифицированный крысиный геномный локус, содержащий: (i) вставку гомологичной или ортологичной человеческой нуклеотидной последовательности; (ii) замещение эндогенной крысиной нуклеотидной последовательности гомологичной или ортологичной человеческой нуклеотидной последовательностью; или (iii) их комбинацию, при этом модифицированный крысиный геномный локус может передаваться через зародышевую линию.
[00511] 23. Модифицированный крысиный геномный локус по варианту реализации изобретения 22, отличающийся тем, что размер вставки или замещения составляет от около 5 т.п.о. до около 400 т.п.о.
[00512] 24. Крысиный геномный локус по варианту реализации изобретения 22, отличающийся тем, что размер вставки или замещения составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.
[00513] 25. Способ получения гуманизированной крысы, включающий: (а) таргетирование представляющего интерес геномного локуса в плюрипотентной крысиной клетке направляющей конструкцией, содержащей человеческую нуклеиновую кислоту, для формирования генетически модифицированной плюрипотентной крысиной клетки; (b) внесение генетически модифицированной плюрипотентной крысиной клетки в крысиный эмбрион-хозяина; и (с) вынашивание крысиного эмбриона-хозяина суррогатной матерью, при этом суррогатная мать дает крысиное потомство, содержащее модифицированный геномный локус, который содержит: (i) вставку человеческой нуклеотидной последовательности; (ii) замещение крысиной нуклеотидной последовательности в представляющем интерес геномном локусе гомологичной или ортологичной человеческой нуклеотидной последовательностью; (iii) химерную нуклеотидную последовательность, содержащую человеческую и крысиную нуклеотидную последовательность; или (iv) их комбинацию, при этом модифицированный геномный локус может передаваться через зародышевую линию.
[00514] 26. Способ по варианту реализации изобретения 25, отличающийся тем, что направляющая конструкция представляет собой крупный направляющий вектор (LTVEC), а 5' и 3' плечи гомологии LTVEC в общей сумме составляют по меньшей мере 10 т.п.о., но менее чем 150 т.п.о.
[00515] 27. Способ по варианту реализации изобретения 26, отличающийся тем, что 5' и 3' плечи гомологии направляющей конструкции в общей сумме составляют от около 10 т.п.о. до около 30 т.п.о., от около 20 т.п.о. to 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о. или от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до 150 т.п.о.
[00516] 28. Способ по варианту реализации изобретения 25, 26 или 27, отличающийся тем, что человеческая нуклеотидная последовательность составляет по меньшей мере 5 т.п.о., но менее чем 400 т.п.о.
[00517] 29. Способ по варианту реализации изобретения 25, 26 или 27, отличающийся тем, что человеческая нуклеотидная последовательность составляет по меньшей мере 5 т.п.о., но менее чем 10 т.п.о., по меньшей мере 10 т.п.о., но менее чем 20 т.п.о., по меньшей мере 20 т.п.о., но менее чем 40 т.п.о., по меньшей мере 40 т.п.о., но менее чем 60 т.п.о., по меньшей мере 60 т.п.о., но менее чем 80 т.п.о., по меньшей мере около 80 т.п.о., но менее чем 100 т.п.о., по меньшей мере 100 т.п.о., но менее чем 150 т.п.о., по меньшей мере 150 т.п.о., но менее чем 200 т.п.о., по меньшей мере 200 т.п.о., но менее чем 250 т.п.о., по меньшей мере 250 т.п.о., но менее чем 300 т.п.о., по меньшей мере 300 т.п.о., но менее чем 350 т.п.о., или по меньшей мере 350 т.п.о., но менее чем 400 т.п.о.
[00518] 30. Способ по любому из вариантов реализации изобретения 25-29, отличающийся тем, что плюрипотентная крысиная клетка представляет собой крысиную эмбриональную стволовую (ЭС) клетку.
[00519] 31. Способ по любому из вариантов реализации изобретения 25-30, отличающийся тем, что плюрипотентная крысиная клетка получена от штамма DA или штамма ACI.
[00520] 32. Способ по любому из вариантов реализации изобретения 25-31, отличающийся тем, что плюрипотентная крысиная клетка характеризуется экспрессией по меньшей мере одного маркера плюрипотентности, включая Dnmt3L, Eras, Err-beta, Fbxo15, Fgf4, Gdf3, Klf4, Lef1, рецептор LIF, Lin28, Nanog, Oct4, Sox15, Sox2, Utf1 или их комбинацию.
[00521] 33. Способ по любому из вариантов реализации изобретения 25-31, отличающийся тем, что плюрипотентная крысиная клетка характеризуется одной или более из следующих характеристик: (а) отсутствием экспрессии одного или более маркеров плюрипотентности, включая с-Myc, Ecat1 и/или Rexo1; (b) отсутствием экспрессии одного или более мезодермальных маркеров, включая брахиурию и/или Bmpr2; (с) отсутствием экспрессии одного или более энтодермальных маркеров, включая Gata6, Sox17 и/или Sox7; или (d) отсутствием экспрессии одного или более нейральных маркеров, включая Nestin и/или Рах6.
[00522] 34. Модифицированная крыса, содержащая гуманизированный геномный локус, при этом гуманизированный геномный локус содержит: (i) вставку гомологичной или ортологичной человеческой нуклеотидной последовательности; (ii) замещение крысиной нуклеотидной последовательности в эндогенном геномном локусе гомологичной или ортологичной человеческой нуклеотидной последовательностью; (iii) химерную нуклеотидную последовательность, содержащую человеческую и крысиную нуклеотидную последовательность, или (iv) их комбинацию, при этом модифицированный геномный локус может передаваться через зародышевую линию.
[00523] 35. Крыса или крысиная клетка, содержащая направленную генетическую модификацию в своем геномном локусе, при этом геномный локус представляет собой локус рецептора интерлейкина-2 гамма, локус АроЕ, локус Rag1, локус Rag2 или локус Rag2/Rag1, при этом направленная генетическая модификация включает: (а) удаление эндогенной крысиной нуклеотидной последовательности в геномном локусе; (b) вставку гомологичной нуклеиновой кислоты, ортологичной нуклеиновой кислоты или химерной нуклеиновой кислоты, содержащей человеческую и крысиную нуклеотидную последовательность, или (с) их комбинацию, при этом направленная генетическая модификация может передаваться через зародышевую линию крысы или крысы, выращенной из крысиной клетки.
[00524] 36. Крыса или крысиная клетка по варианту реализации изобретения 35, отличающаяся тем, что (а) удаление эндогенной крысиной нуклеиновой кислоты в геномном локусе составляет по меньшей мере около 10 т.п.о.; или (b) удаление эндогенной крысиной нуклеиновой кислоты в геномном локусе составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.; (с) вставка экзогенной нуклеотидной последовательности в геномном локусе составляет по меньшей мере около 5 т.п.о.; или (d) вставка экзогенной нуклеотидной последовательности в геномном локусе составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.
[00525] 37. Крыса или крысиная клетка по варианту реализации изобретения 35 или 36, отличающаяся тем, что (а) направленная генетическая модификация в локусе рецептора интерлейкина-2 гамма приводит к снижению или отсутствию белковой активности рецептора интерлейкина-2 гамма; (b) направленная генетическая модификация в локусе АроЕ приводит к снижению или отсутствию белковой активности АроЕ; (с) направленная генетическая модификация в локусе Rag1 приводит к снижению или отсутствию белковой активности Rag1; (d) направленная генетическая модификация в локусе Rag2 приводит к снижению или отсутствию белковой активности Rag2; или (е) направленная генетическая модификация в локусе Rag2/Rag1 приводит к снижению или отсутствию белковой активности Rag2 и активности Rag1.
[00526] 38. Крыса или крысиная клетка по варианту реализации изобретения 35, 36 или 37, отличающаяся тем, что направленная генетическая модификация локуса рецептора интерлейкина-2 гамма включает: (а) удаление полной кодирующей области крысиного рецептора интерлейкина-2 гамма или ее части; (b) замещение полной кодирующей области крысиного рецептора интерлейкина-2 гамма или ее части кодирующей областью человеческого рецептора интерлейкина-2 гамма или ее частью; (с) замещение эктодомена кодирующей области крысиного рецептора интерлейкина-2 гамма эктодоменом человеческого рецептора интерлейкина-2 гамма; или (d) удаление в локусе рецептора интерлейкина-2 гамма, составляющее по меньшей мере 3 т.п.о.
[00527] 39. Крыса или крысиная клетка по любому из вариантов реализации изобретения 35-37, отличающаяся тем, что направленная генетическая модификация локуса АроЕ включает: (а) удаление полной кодирующей области АроЕ или ее части; или (b) удаление в локусе АроЕ, содержащем кодирующую область АроЕ, составляющее по меньшей мере 1,8 т.п.о.
[00528] 40. Крыса или крысиная клетка по любому из вариантов реализации изобретения 35-37, отличающаяся тем, что направленная генетическая модификация локуса Rag2 включает: (а) удаление полной кодирующей области Rag2 или ее части; (b) удаление в локусе Rag2, содержащем кодирующую область Rag2, составляющее по меньшей мере 5,7 т.п.о.
[00529] 41. Крыса или крысиная клетка по любому из вариантов реализации изобретения 35-37, отличающаяся тем, что направленная генетическая модификация локуса Rag2/Rag1 включает: (а) удаление полной кодирующей области Rag2 или ее части и удаление полной кодирующей области Rag1 или ее части; или (b) удаление в локусе Rag2/Rag1, содержащем кодирующую область Rag2, составляющее по меньшей мере 16 т.п.о.
[00530] 42. Крыса или крысиная клетка по любому из вариантов реализации изобретения 35-41, отличающаяся тем, что направленная генетическая модификация включает вставку экспрессионной кассеты, содержащей селективный маркер в локусе рецептора интерлейкина-2 гамма, локусе АроЕ, локусе Rag1, локусе Rag2 или локусе Rag2/Rag1.
[00531] 43. Крыса или крысиная клетка по любому из вариантов реализации изобретения 42, отличающаяся тем, что экспрессионная кассета содержит ген lacZ, функционально связанный с эндогенным промотором в геномном локусе, и промотор человеческого убиквитина, функционально связанный с селективным маркером.
[00532] 44. Крыса или крысиная клетка по любому из вариантов реализации изобретения 35-43, отличающаяся тем, что направленная генетическая модификация в локусе рецептора интерлейкина-2 гамма, локусе АроЕ, локусе Rag1, локусе Rag2 или локусе Rag2/Rag1 включает вставку самоуничтожающейся селекционной кассеты.
[00533] 45. Крыса или крысиная клетка по варианту реализации изобретения 44. отличающаяся тем, что самоуничтожающаяся селекционная кассета содержит ген селективного маркера, функционально связанный с промотором, активным в крысиной клетке, и ген рекомбиназы, функционально связанный со специфическим в отношении мужских зародышевых клеток промотором, при этом самоуничтожающаяся кассета фланкируется рекомбинационными участками распознавания, распознаваемыми рекомбиназой.
[00534] 46. Крыса или крысиная клетка по варианту реализации изобретения 45. отличающаяся тем, что (а) специфический в отношении мужских зародышевых клеток промотор представляет собой промотор протамина-1; или (b) ген рекомбиназы кодирует Cre, а рекомбинационные участки распознавания представляют собой участки loxP.
[00535] 47. Крыса или крысиная клетка по любому из вариантов реализации изобретения 35-46, отличающаяся тем, что вставка экзогенной нуклеотидной последовательности в геномном локусе содержит репортерную нуклеиновую кислоту, функционально связанную с эндогенным промотором рецептора интерлейкина-2 гамма, эндогенным промотором АроЕ, эндогенным промотором Rag1 или эндогенным промотором Rag2.
[00536] 48. Крыса или крысиная клетка по варианту реализации изобретения 47, отличающаяся тем, что репортерная нуклеиновая кислота кодирует репортер, включая β-галактозидазу, mPlum, mCherry, tdTomato, mStrawberry, J-Red, DsRed, mOrange, mKO, mCitrine, Venus, YPet, усиленный желтый флуоресцентный белок (уЖФБ), Emerald, усиленный зеленый флуоресцентный белок (уЗФБ), CyPet, голубой флуоресцентный белок (ГФБ), Cerulean, T-Sapphire, люциферазу, щелочную фосфатазу или их комбинацию.
[00537] 49. Крысиная клетка по любому из вариантов реализации изобретения 35-48, отличающаяся тем, что крысиная клетка является плюрипотентной крысиной клеткой или крысиной эмбриональной стволовой (ЭС) клеткой.
[00538] 50. Крысиная клетка по варианту реализации изобретения 49, отличающаяся тем, что плюрипотентная крысиная клетка или крысиная эмбриональная стволовая (ЭС) клетка (а) получена от штамма DA или штамма ACI; (b) характеризуется экспрессией по меньшей мере одного маркера плюрипотентности, включая Dnmt3L, Eras, Err-beta, Fbxo15, Fgf4, Gdf3, Klf4, Lef1, рецептор LIF, Lin28, Nanog, Oct4, Sox15, Sox2, Utf1 или их комбинацию; или (с) характеризуется одной или более из следующих характеристик: (i) отсутствием экспрессии одного или более маркеров плюрипотентности, включая с-Myc, Ecat1 и/или Rexo1; (ii) отсутствием экспрессии мезодермальных маркеров, включая брахиурию и/или Bmpr2; (iii) отсутствием экспрессии одного или более энтодермальных маркеров, включая Gata6, Sox17 и/или Sox7; или (iv) отсутствием экспрессии одного или более нейральных маркеров, включая Nestin и/или Рах6.
[00539] 51. Способ модификации целевого геномного локуса в локусе рецептора интерлейкина-2 гамма, локусе АроЕ, локусе Rag1, локусе Rag2 или локусе Rag2/Rag1 в плюрипотентной крысиной клетке, включающий: (а) внесение в плюрипотентную крысиную клетку направляющего вектора, содержащего нуклеотидную вставку, фланкируемую 5' и 3' крысиными плечами гомологии, гомологичными целевому геномному локусу, (b) выявление генетически модифицированной плюрипотентной крысиной клетки, содержащей направленную генетическую модификацию в целевом геномном локусе, при этом направленная генетическая модификация может передаваться через зародышевую линию крысы, выращенной из плюрипотентной крысиной клетки.
[00540] 52. Способ по варианту реализации изобретения 51, отличающийся тем, что направляющий вектор представляет собой крупный направляющий вектор (LTVEC), при этом 5' и 3' крысиные плечи гомологии в общей сумме составляют по меньшей мере около 10 т.п.о., но менее чем около 150 т.п.о.
[00541] 53. Способ по варианту реализации изобретения 51 или 52, отличающийся тем, что внесение направляющего вектора в плюрипотентную крысиную клетку приводит к: (i) удалению эндогенной крысиной нуклеотидной последовательности в целевом геномном локусе; (ii) вставку экзогенной нуклеотидной последовательности в целевой геномный локус; или (iii) их комбинацию.
[00542] 54. Способ по варианту реализации изобретения 53, отличающийся тем, что (а) удаление эндогенной крысиной нуклеиновой кислоты в геномном локусе составляет по меньшей мере около 10 т.п.о.; или (b) удаление эндогенной крысиной нуклеиновой кислоты в геномном локусе составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.; (с) вставка экзогенной нуклеотидной последовательности в геномном локусе составляет по меньшей мере около 5 т.п.о.; или (d) вставка экзогенной нуклеотидной последовательности в геномном локусе составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.
[00543] 55. Способ по любому из вариантов реализации изобретения 51-54, отличающийся тем, что (а) направленная генетическая модификация в локусе рецептора интерлейкина-2 гамма приводит к снижению или отсутствию белковой активности рецептора интерлейкина-2 гамма; (b) направленная генетическая модификация в локусе АроЕ приводит к снижению или отсутствию белковой активности АроЕ; (с) направленная генетическая модификация в локусе Rag1 приводит к снижению или отсутствию белковой активности Rag1; (d) направленная генетическая модификация в локусе Rag2 приводит к снижению или отсутствию белковой активности Rag2; или (е) направленная генетическая модификация в локусе Rag2/Rag1 приводит к снижению или отсутствию белковой активности Rag2 и белковой активности Rag1.
[00544] 56. Способ по любому из вариантов реализации изобретения 51-54, отличающийся тем, что направленная генетическая модификация локуса рецептора интерлейкина-2 гамма включает: (а) удаление полной кодирующей области крысиного рецептора интерлейкина-2 гамма или ее части; (b) замещение полной кодирующей области крысиного рецептора интерлейкина-2 гамма или ее части кодирующей областью человеческого рецептора интерлейкина-2 гамма или ее частью; (с) замещение эктодомена кодирующей области крысиного рецептора интерлейкина-2 гамма эктодоменом человеческого рецептора интерлейкина-2 гамма; или (d) удаление в локусе рецептора интерлейкина-2 гамма, содержащем кодирующую область рецептора интерлейкина-2 гамма, составляющее по меньшей мере 3 т.п.о.
[00545] 57. Способ по любому из вариантов реализации изобретения 51-55, отличающийся тем, что направленная генетическая модификация локуса АроЕ включает: (а) удаление полной кодирующей области АроЕ или ее части; или (b) удаление в локусе АроЕ, содержащем кодирующую область АроЕ, составляющее по меньшей мере 1,8 т.п.о.
[00546] 58. Способ по любому из вариантов реализации изобретения 51-55, отличающийся тем, что направленная генетическая модификация локуса Rag2 включает: (а) удаление полной кодирующей области Rag2 или ее части; или (b) удаление в локусе Rag2, содержащем кодирующую область Rag2, составляющее по меньшей мере 5,7 т.п.о.
[00547] 59. Способ по любому из вариантов реализации изобретения 51-55, отличающийся тем, что направленная генетическая модификация локуса Rag1/Rag2 включает: (а) удаление полной кодирующей области Rag2 или ее части и удаление полной кодирующей области Rag1 или ее части; или (b) удаление в локусе Rag2/Rag1, содержащем кодирующие области Rag2 и Rag1, составляющее по меньшей мере 16 т.п.о.
[00548] 60. Способ по любому из вариантов реализации изобретения 51-59, отличающийся тем, что нуклеотидная вставка, содержит экспрессионную кассету, содержащую полинуклеотид, кодирующий селективный маркер.
[00549] 61. Способ по варианту реализации изобретения 60, отличающийся тем, что экспрессионная кассета содержит ген lacZ, функционально связанный с эндогенным промотором в геномном локусе, и промотор человеческого убиквитина, функционально связанный с селективным маркером.
[00550] 62. Способ по любому из вариантов реализации изобретения 51-60, отличающийся тем, что нуклеотидная вставка содержит самоуничтожающуюся селекционную кассету.
[00551] 63. Способ по варианту реализации изобретения 62, отличающийся тем, что самоуничтожающаяся селекционная кассета содержит селективный маркер, функционально связанный с промотором, активным в крысиной плюрипотентной клетке, и полинуклеотид, кодирующий рекомбиназу, функционально связанный со специфическим в отношении мужских зародышевых клеток промотором, при этом самоуничтожающаяся кассета фланкируется рекомбинационными участками распознавания, распознаваемыми рекомбиназой.
[00552] 64. Способ по варианту реализации изобретения 63, отличающийся тем, что (а) специфический в отношении мужских зародышевых клеток промотор представляет собой промотор протамина-1; или (b) ген рекомбиназы кодирует Cre, а рекомбинационные участки распознавания представляют собой участки loxP.
[00553] 65. Способ по варианту реализации изобретения 53, отличающийся тем, что вставка экзогенной нуклеотидной последовательности в геномном локусе содержит репортерную нуклеотидную последовательность, функционально связанную с эндогенным промотором рецептора интерлейкина-2 гамма, эндогенным промотором АроЕ, эндогенным промотором Rag1 или эндогенным промотором Rag2.
[00554] 66. Способ по варианту реализации изобретения 65, отличающийся тем, что репортерная нуклеотидная последовательность кодирует репортер, включая β-галактозидазу, mPlum, mCherry, tdTomato, mStrawberry, J-Red, DsRed, mOrange, mKO, mCitrine, Venus, YPet, усиленный желтый флуоресцентный белок (уЖФБ), Emerald, усиленный зеленый флуоресцентный белок (уЗФБ), CyPet, голубой флуоресцентный белок (ГФБ), Cerulean, T-Sapphire, люциферазу, щелочную фосфатазу или их комбинацию.
[00555] 67. Способ по любому из вариантов реализации изобретения 51-66, отличающийся тем, что пюрипотентная крысиная клетка является крысиной эмбриональной стволовой (ЭС) клеткой.
[00556] 68. Способ по любому из вариантов реализации изобретения 51-67, отличающийся тем, что плюрипотентная крысиная клетка (а) получена от штамма DA или штамма ACI; или (b) характеризуется экспрессией маркера плюрипотентности, включая Oct-4, Sox-2, щелочную фосфатазу или их комбинацию; или (с) характеризуется одной или более из следующих характеристик: (i) отсутствием экспрессии одного или более маркеров плюрипотентности, включая с-Myc, Ecat1 и/или Rexo1; (ii) отсутствием экспрессии мезодермальных маркеров, включая брахиурию и/или Bmpr2; (iii) отсутствием экспрессии одного или более энтодермальных маркеров, включая Gata6, Sox17 и/или Sox7; или (iv) отсутствием экспрессии одного или более нейральных маркеров, включая Nestin и/или Рах6.
[00557] 69. Способ по любому из вариантов реализации изобретения 51-68, дополнительно включающий выявление направленной генетической модификации в целевом геномном локусе, при этом на этапе выявления применяют количественный анализ для оценки модификации аллеля (МОА) в целевом геномном локусе.
[00558] 70. Способ по любому из вариантов реализации изобретения 51-69, отличающийся тем, что этап внесения (а) дополнительно включает внесение второй нуклеиновой кислоты, кодирующей нуклеазный агент, который стимулирует гомологичную рекомбинацию между направляющим вектором и целевым геномным локусом в плюрипотентной крысиной клетке.
[00559] 71. Способ по варианту реализации изобретения 70, отличающийся тем, что нуклеазный агент включает химерный белок, содержащий цинк-пальцевый ДНК-связывающий домен, слитый с эндонуклеазой FokI.
[00560] 72. Способ по варианту реализации изобретения 71, отличающийся тем, что указанный способ приводит к биаллельной модификации целевого геномного локуса.
[00561] 73. Способ по любому из вариантов реализации изобретения 51-70, отличающийся тем, что этап внесения (а) дополнительно включает внесение в плюрипотентную крысиную клетку: (i) первой экспрессионной конструкции, содержащей первый промотор, функционально связанный с первой нуклеотидной последовательностью, кодирующей ассоциированный с короткими палиндромными повторами, регулярно расположенными группами (CRISPR), белок (Cas), (ii) второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с целевой геномной последовательностью, связанной с направляющей РНК (нРНК), при этом целевая геномная последовательность непосредственно фланкируется в 3' конце последовательностью мотива, прилегающего к протоспейсеру (РАМ).
[00562] 74. Способ по варианту реализации изобретения 73, отличающийся тем, что представляющий интерес геномный локус содержит нуклеотидную последовательность SEQ ID №1.0
[00563] 75. Способ по варианту реализации изобретения 73 или 74, отличающийся тем, что нРНК содержит третью нуклеотидную последовательность, кодирующую РНК коротких палиндромных повторов, регулярно расположенных группами (CRISPR) (crРНК), и транс-активирующую РНК CRISPR (tracrРНК).
[00564] 76. Способ по варианту реализации изобретения 73, отличающийся тем, что белок Cas представляет собой Cas9.
[00565] 77. Способ по варианту реализации изобретения 73, 74 или 75, отличающийся тем, что нРНК содержит: (а) химерную РНК из нуклеотидной последовательности SEQ ID №2; или (b) химерную РНК из нуклеотидной последовательности SEQ ID №3.
[00566] 78. Способ по варианту реализации изобретения 75, отличающийся тем, что crРНК содержит SEQ ID №4; SEQ ID №5; или SEQ ID №6.
[00567] 79. Способ по варианту реализации изобретения 75, отличающийся тем, что tracrРНК содержит SEQ ID №7 или SEQ ID №8.
[00568] 80. Крыса или крысиная клетка по любому из вариантов реализации изобретения 35-50, отличающаяся тем, что крыса или крысиная клетка содержит направленные генетические модификации в локусе рецептора интерлейкина-2 гамма, локусе АроЕ, локусе Rag1, локусе Rag2 и/или локусе Rag2/Rag1.
[00569] 81. Крыса или крысиная клетка по варианту реализации изобретения 80, отличающаяся тем, что крыса или крысиная клетка содержит направленные генетические модификации в локусе рецептора интерлейкина-2 гамма и локусе Rag2/Rag1.
[00570] Дополнительные неограничивающие варианты реализации изобретения включают:
[00571] 1. Способ модификации представляющего интерес геномного локуса в эукариотической клетке, включающий: (а) внесение в эукариотическую клетку: (i) крупного направляющего вектора (LTVEC), содержащего первую нуклеиновую кислоту, фланкируемую 5' плечом гомологии и 3' плечом гомологии, при этом LTVEC содержит по меньшей мере 10 т.п.о.; (ii) первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas, (iii) второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей направляющую РНК (нРНК), содержащую нуклеотидную последовательность, которая гибридизируется с целевой последовательностью, и транс-активирующую РНК CRISPR (tracrРНК), при этом первый и второй промоторы активны в эукариотической клетке; и (b) выявление модифицированной эукариотической клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе.
[00572] 2. Способ по варианту реализации изобретения 1, отличающийся тем, что направленная генетическая модификация является биаллельной генетической модификацией.
[00573] 3. Способ по варианту реализации изобретения 1, отличающийся тем, что LTVEC составляет по меньшей мере 15 т.п.о., по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о. или по меньшей мере 90 т.п.о.
[00574] 4. Способ по варианту реализации изобретения 1, отличающийся тем, что LTVEC составляет по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
[00575] 5. Способ по варианту реализации изобретения 1, отличающийся тем, что эукариотическая клетка является клеткой млекопитающего.
[00576] 6. Способ по варианту реализации изобретения 5, отличающийся тем, что клетка млекопитающего является фибробластом.
[00577] 7. Способ по варианту реализации изобретения 1, отличающийся тем, что эукариотическая клетка является плюрипотентной клеткой.
[00578] 8. Способ по варианту реализации изобретения 7, отличающийся тем, что плюрипотентная клетка является человеческой плюрипотентной клеткой.
[00579] 9. Способ по варианту реализации изобретения 8, отличающийся тем, что человеческая плюрипотентная клетка является человеческой эмбриональной стволовой (ЭС) клеткой или человеческой взрослой стволовой клеткой.
[00580] 10. Способ по варианту реализации изобретения 8, отличающийся тем, что человеческая плюрипотентная клетка является человеческой клеткой-предшественником с ограниченным развитием.
[00581] 11. Способ по варианту реализации изобретения 8, отличающийся тем, что человеческая плюрипотентная клетка является человеческой индуцированной плюрипотентной стволовой (иПС) клеткой.
[00582] 12. Способ по варианту реализации изобретения 1, отличающийся тем, что белок Cas представляет собой Cas9.
[00583] 13. Способ по варианту реализации изобретения 1, отличающийся тем, что целевая последовательность непосредственно фланкируется в 3' конце последовательностью мотива, прилегающего к протоспейсеру (РАМ).
[00584] 14. Способ по варианту реализации изобретения 1, отличающийся тем, что 5' и 3' плечи гомологии в общей сумме составляют от около 10 т.п.о. до около 150 т.п.о.
[00585] 15. Способ по варианту реализации изобретения 1, отличающийся тем, что 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до 150 т.п.о.
[00586] 16. Способ по варианту реализации изобретения 1, отличающийся тем, что направленная генетическая модификация включает: (а) замещение эндогенной нуклеотидной последовательности гомологичной или ортологичной нуклеотидной последовательностью; (b) удаление эндогенной нуклеотидной последовательности; (с) удаление эндогенной нуклеотидной последовательности, при этом диапазон удаления составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.; (d) вставку экзогенной нуклеотидной последовательности; (е) вставку экзогенной нуклеотидной последовательности в диапазоне от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.; (f) вставку экзогенной нуклеотидной последовательности, содержащей гомологичную или ортологичную нуклеотидную последовательность; (g) вставку химерной нуклеотидной последовательности, содержащей человеческую и нечеловеческую нуклеотидную последовательность; (h) вставку кондиционального аллеля, фланкируемого целевыми последовательностями сайт-специфической рекомбиназы; (i) вставку селективного маркера или репортерного гена, функционально связанного с промотором, активным в плюрипотентной клетке; или (j) их комбинацию.
[00587] 17. Способ по варианту реализации изобретения 1, отличающийся тем, что представляющий интерес геномный локус содержит (i) 5' целевую последовательность, которая гомологична 5' плечу гомологии; и (ii) 3' целевую последовательность, которая гомологична 3' плечу гомологии.
[00588] 18. Способ по варианту реализации изобретения 17, отличающийся тем, что 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 3 м.п.о.
[00589] 19. Способ по варианту реализации изобретения 17, отличающийся тем, что 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 10 т.п.о., по меньшей мере 10 т.п.о., но менее чем 20 т.п.о., по меньшей мере 20 т.п.о., но менее чем 40 т.п.о., по меньшей мере 40 т.п.о., но менее чем 60 т.п.о., по меньшей мере 60 т.п.о., но менее чем 80 т.п.о., по меньшей мере около 80 т.п.о., но менее чем 100 т.п.о., по меньшей мере 100 т.п.о., но менее чем 150 т.п.о., или по меньшей мере 150 т.п.о., но менее чем 200 т.п.о., по меньшей мере около 200 т.п.о., но менее чем около 300 т.п.о., по меньшей мере около 300 т.п.о., но менее чем около 400 т.п.о., по меньшей мере около 400 т.п.о., но менее чем около 500 т.п.о., по меньшей мере около 500 т.п.о., но менее чем около 1 м.п.о., по меньшей мере около 1 м.п.о., но менее чем около 1,5 м.п.о., по меньшей мере около 1,5 м.п.о., но менее чем около 2 м.п.о., по меньшей мере около 2 м.п.о., но менее чем около 2,5 м.п.о., или по меньшей мере около 2,5 м.п.о., но менее чем около 3 м.п.о.
[00590] 20. Способ по варианту реализации изобретения 1, отличающийся тем, что представляющий интерес геномный локус содержит локус рецептора интерлейкина-2 гамма, локус АроЕ, локус Rag1, локус Rag2 или оба локуса Rag1 и Rag2.
[00591] 21. Способ по варианту реализации изобретения 1, отличающийся тем, что первая и вторая экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[00592] 22. Способ модификации генома, включающий воздействие на геном белком Cas и РНК CRISPR в присутствии крупного направляющего вектора (LTVEC), содержащего нуклеотидную последовательность по меньшей мере из 10 т.п.о., при этом после воздействия белка Cas, РНК CRISPR и LTVEC происходит модификация генома так, чтобы он содержал нуклеотидную последовательность по меньшей мере из 10 т.п.о.
[00593] 23. Способ по варианту реализации изобретения 22, отличающийся тем, что LTVEC содержит нуклеотидную последовательность из по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о. или по меньшей мере 90 т.п.о.
[00594] 24. Способ по варианту реализации изобретения 22, отличающийся тем, что LTVEC содержит нуклеотидную последовательность из по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
[00595] 25. Способ модификации генома, включающий приведение генома в контакт с белком Cas, РНК CRISPR, которая гибридизируется с целевой последовательностью, и tracrРНК в присутствии крупного направляющего вектора (LTVEC), при этом LTVEC составляет по меньшей мере 10 т.п.о. и содержит первую нуклеиновую кислоту, фланкируемую 5' плечом гомологии и 3' плечом гомологии, а после контакта с белком Cas, РНК CRISPR и tracrРНК в присутствии LTVEC, происходит модификация генома в представляющем интерес геномном локусе так, чтобы он содержат первую нуклеиновую кислоту.
[00596] 26. Способ по варианту реализации изобретения 25, отличающийся тем, что геном находится в эукариотической клетке, а белок Cas, РНК CRISPR, tracrРНК и LTVEC вносят в эукариотческую клетку.
[00597] 27. Способ по варианту реализации изобретения 26, дополнительно включающий выявление модифицированной эукариотической клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе.
[00598] 28. Способ по варианту реализации изобретения 26 или 27, отличающийся тем, что РНК CRISPR и tracrРНК вносят вместе в форме одной направляющей РНК (нРНК).
[00599] 29. Способ по варианту реализации изобретения 26 или 27, отличающийся тем, что РНК CRISPR и tracrРНК вносят отдельно.
[00600] 30. Способ по любому из вариантов реализации изобретения 26-29, отличающийся тем, что: (а) белок Cas вносят в эукариотическую клетку в форме белка, матричной РНК (мРНК), кодирующей белок Cas, или ДНК, кодирующей белок Cas; (b) РНК CRISPR вносят в эукариотическую клетку в форме РНК или ДНК, кодирующей РНК CRISPR; и (с) tracrРНК вносят в эукариотическую клетку в форме РНК или ДНК, кодирующей tracrРНК.
[00601] 31. Способ по варианту реализации изобретения 30, отличающийся тем, что белок Cas, РНК CRISPR и tracrРНК вносят в эукариотическую клетку в виде комплекса белок-РНК.
[00602] 32. Способ по варианту реализации изобретения 30, отличающийся тем, что: (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; (b) ДНК, кодирующая РНК CRISPR, находится в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей РНК CRISPR; и (с) ДНК, кодирующая tracrРНК, находится в форме третьей экспрессионной конструкции, содержащей третий промотор, функционально связанный с четвертой нуклеиновой кислотой, кодирующей tracrРНК, при этом первый, второй и третий промоторы активны в эукариотической клетке.
[00603] 33. Способ по варианту реализации изобретения 32, отличающийся тем, что первая, вторая и/или третья экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[00604] 34. Способ по варианту реализации изобретения 30, отличающийся тем, что: (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; и (b) ДНК, кодирующая РНК CRISPR, и ДНК, кодирующая tracrРНК, находятся в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей нРНК, содержащую РНК CRISPR и tracrРНК; при этом первый и второй промоторы активны в эукариотической клетке.
[00605] 35. Способ по варианту реализации изобретения 34, отличающийся тем, что первая и вторая экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[00606] 36. Способ по любому из вариантов реализации изобретения 27-35, отличающийся тем, что направленная генетическая модификация включает одновременное удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус.
[00607] 37. Способ по любому из вариантов реализации изобретения 27-36, отличающийся тем, что направленная генетическая модификация является биаллельной генетической модификацией.
[00608] 38. Способ по варианту реализации изобретения 37, отличающийся тем, что биаллельная генетическая модификация включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в двух гомологичных хромосомах.
[00609] 39. Способ по любому из вариантов реализации изобретения 27-36, отличающийся тем, что модифицированная эукариотическая клетка является гемизиготной в представляющем интерес геномном локусе.
[00610] 40. Способ по варианту реализации изобретения 39, отличающийся тем, что направленная генетическая модификация в представляющем интерес геномном локусе в одной хромосоме включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты.
[00611] 41. Способ по варианту реализации изобретения 39, отличающийся тем, что направленная генетическая модификация включает: (1) удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе в двух гомологичных хромосомах; и (2) вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в первой хромосоме и разрушение представляющего интерес геномного локуса во второй хромосоме.
[00612] 42. Способ по любому из вариантов реализации изобретения 25-41, отличающийся тем, что LTVEC составляет по меньшей мере 15 т.п.о., по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о. или по меньшей мере 90 т.п.о.
[00613] 43. Способ по любому из вариантов реализации изобретения 25-42, отличающийся тем, что LTVEC составляет по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о. или по меньшей мере 200 т.п.о.
[00614] 44. Способ по любому из вариантов реализации изобретения 25-43, отличающийся тем, что первая нуклеиновая кислота составляет по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 150 т.п.о., по меньшей мере 200 т.п.о., по меньшей мере 250 т.п.о. или по меньшей мере 300 т.п.о.
[00615] 45. Способ по любому из вариантов реализации изобретения 26-44, отличающийся тем, что эукариотическая клетка является клеткой млекопитающего.
[00616] 46. Способ по варианту реализации изобретения 45, отличающийся тем, что клетка млекопитающего является фибробластом.
[00617] 47. Способ по любому из вариантов реализации изобретения 26-43, отличающийся тем, что эукариотическая клетка является плюрипотентной клеткой.
[00618] 48. Способ по варианту реализации изобретения 47, отличающийся тем, что плюрипотентная клетка является нечеловеческой плюрипотентной клеткой.
[00619] 49. Способ по варианту реализации изобретения 48, отличающийся тем, что нечеловеческая плюрипотентная клетка является плюрипотентной клеткой грызуна.
[00620] 50. Способ по варианту реализации изобретения 49, отличающийся тем, что плюрипотентная клетка грызуна является мышиной или крысиной эмбриональной стволовой (ЭС) клеткой.
[00621] 51. Способ по варианту реализации изобретения 47, отличающийся тем, что плюрипотентная клетка является человеческой плюрипотентной клеткой.
[00622] 52. Способ по варианту реализации изобретения 51, отличающийся тем, что человеческая плюрипотентная клетка является человеческой эмбриональной стволовой (ЭС) клеткой или человеческой взрослой стволовой клеткой.
[00623] 53. Способ по варианту реализации изобретения 51, отличающийся тем, что человеческая плюрипотентная клетка является человеческой клеткой-предшественником с ограниченным развитием.
[00624] 54. Способ по варианту реализации изобретения 51, отличающийся тем, что человеческая плюрипотентная клетка является человеческой индуцированной плюрипотентной стволовой (иПС) клеткой.
[00625] 55. Способ по любому из вариантов реализации изобретения 25-54, отличающийся тем, что белок Cas представляет собой Cas9.
[00626] 56. Способ по любому из вариантов реализации изобретения 25-55, отличающийся тем, что целевая последовательность непосредственно фланкируется последовательностью мотива, прилегающего к протоспейсеру (РАМ).
[00627] 57. Способ по любому из вариантов реализации изобретения 25-56, отличающийся тем, что 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.о. до около 150 т.п.о.
[00628] 58. Способ по любому из вариантов реализации изобретения 25-57, отличающийся тем, что 5' и 3' плечи гомологии LTVEC в общей сумме составляют от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 120 т.п.о. или от около 120 т.п.о. до 150 т.п.о.
[00629] 59. Способ по любому из вариантов реализации изобретения 27-58, отличающийся тем, что направленная генетическая модификация включает: (а) замещение эндогенной нуклеотидной последовательности гомологичной или ортологичной нуклеотидной последовательностью; (b) удаление эндогенной нуклеотидной последовательности; (с) удаление эндогенной нуклеотидной последовательности, при этом диапазон удаления составляет от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о. или от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 400 т.п.о., от около 400 т.п.о. до около 500 т.п.о., от около 500 т.п.о. до около 1 м.п.о., от около 1 м.п.о. до около 1,5 м.п.о., от около 1,5 м.п.о. до около 2 м.п.о., от около 2 м.п.о. до около 2,5 м.п.о. или от около 2,5 м.п.о. до около 3 м.п.о.; (d) вставку экзогенной нуклеотидной последовательности; (е) вставку экзогенной нуклеотидной последовательности в диапазоне от около 5 т.п.о. до около 10 т.п.о., от около 10 т.п.о. до около 20 т.п.о., от около 20 т.п.о. до около 40 т.п.о., от около 40 т.п.о. до около 60 т.п.о., от около 60 т.п.о. до около 80 т.п.о., от около 80 т.п.о. до около 100 т.п.о., от около 100 т.п.о. до около 150 т.п.о., от около 150 т.п.о. до около 200 т.п.о., от около 200 т.п.о. до около 250 т.п.о., от около 250 т.п.о. до около 300 т.п.о., от около 300 т.п.о. до около 350 т.п.о. или от около 350 т.п.о. до около 400 т.п.о.; (f) вставку экзогенной нуклеотидной последовательности, содержащей гомологичную или ортологичную нуклеотидную последовательность; (g) вставку химерной нуклеотидной последовательности, содержащей человеческую и нечеловеческую нуклеотидную последовательность; (h) вставку кондиционального аллеля, фланкируемого целевыми последовательностями сайт-специфической рекомбиназы; (i) вставку селективного маркера или репортерного гена, функционально связанного с промотором, активным в плюрипотентной клетке; или (j) их комбинацию.
[00630] 60. Способ по любому из вариантов реализации изобретения 25-59, отличающийся тем, что представляющий интерес геномный локус содержит (i) 5' целевую последовательность, которая гомологична 5' плечу гомологии; и (ii) 3' целевую последовательность, которая гомологична 3' плечу гомологии.
[00631] 61. Способ по варианту реализации изобретения 60, отличающийся тем, что 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 3 м.п.о.
[00632] 62. Способ по варианту реализации изобретения 60, отличающийся тем, что 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 5 т.п.о., но менее чем 10 т.п.о., по меньшей мере 10 т.п.о., но менее чем 20 т.п.о., по меньшей мере 20 т.п.о., но менее чем 40 т.п.о., по меньшей мере 40 т.п.о., но менее чем 60 т.п.о., по меньшей мере 60 т.п.о., но менее чем 80 т.п.о., по меньшей мере около 80 т.п.о., но менее чем 100 т.п.о., по меньшей мере 100 т.п.о., но менее чем 150 т.п.о., или по меньшей мере 150 т.п.о., но менее чем 200 т.п.о., по меньшей мере около 200 т.п.о., но менее чем около 300 т.п.о., по меньшей мере около 300 т.п.о., но менее чем около 400 т.п.о., по меньшей мере около 400 т.п.о., но менее чем около 500 т.п.о., по меньшей мере около 500 т.п.о., но менее чем около 1 м.п.о., по меньшей мере около 1 м.п.о., но менее чем около 1,5 м.п.о., по меньшей мере около 1,5 м.п.о., но менее чем около 2 м.п.о., по меньшей мере около 2 м.п.о., но менее чем около 2,5 м.п.о., или по меньшей мере около 2,5 м.п.о., но менее чем около 3 м.п.о.
[00633] 63. Способ по варианту реализации изобретения 60, отличающийся тем, что 5' целевая последовательность и 3' целевая последовательность разделены по меньшей мере 20 т.п.о., по меньшей мере 30 т.п.о., по меньшей мере 40 т.п.о., по меньшей мере 50 т.п.о., по меньшей мере 60 т.п.о., по меньшей мере 70 т.п.о., по меньшей мере 80 т.п.о., по меньшей мере 90 т.п.о., по меньшей мере 100 т.п.о., по меньшей мере 110 т.п.о., по меньшей мере 120 т.п.о., по меньшей мере 130 т.п.о., по меньшей мере 140 т.п.о., по меньшей мере 150 т.п.о., по меньшей мере 160 т.п.о., по меньшей мере 170 т.п.о., по меньшей мере 180 т.п.о., по меньшей мере 190 т.п.о. или по меньшей мере 200 т.п.о.
[00634] 64. Способ по любому из вариантов реализации изобретения 25-63, отличающийся тем, что представляющий интерес геномный локус содержит локус рецептора интерлейкина-2 гамма, локус АроЕ, локус Rag1, локус Rag2 или оба локуса Rag1 и Rag2.
[00635] 65. Способ по любому из вариантов реализации изобретения 25-63, отличающийся тем, что представляющий интерес геномный локус содержит локус Adamts5, локус Trpa1, локус Folh1 или локус Erbb4.
[00636] 66. Способ по любому из вариантов реализации изобретения 25-63, отличающийся тем, что представляющий интерес геномный локус содержит локус Lrp5.
[00637] 67. Способ получения отличного от человека животного поколения F0, которое содержит направленную генетическую модификацию в представляющем интерес геномном локусе, включающий: (а) приведение в контакт генома в нечеловеческой ЭС клетке с белком Cas, РНК CRISPR и tracrРНК в присутствии крупного направляющего вектора (LTVEC) для формирования модифицированной нечеловеческой ЭС клетки, при этом LTVEC состоит по меньшей мере из 10 т.п.о. и содержит первую нуклеиновую кислоту, фланкируемую 5' плечом гомологии и 3' плечом гомологии; (b) выявление модифицированной нечеловеческой ЭС клетки, содержащей направленную генетическую модификацию в представляющем интерес геномном локусе; (с) внесение модифицированной нечеловеческой ЭС клетки в нечеловеческий эмбрион-хозяина; и (d) вынашивание нечеловеческого эмбриона-хозяина суррогатной матерью, при этом суррогатная мать производит отличное от человека животное поколения F0, которое содержит направленную генетическую модификацию в представляющем интерес геномном локусе.
[00638] 68. Способ по варианту реализации изобретения 67, отличающийся тем, что РНК CRISPR и tracrРНК вносят вместе в форме одной направляющей РНК (нРНК).
[00639] 69. Способ по варианту реализации изобретения 67, отличающийся тем, что РНК CRISPR и tracrРНК вносят отдельно.
[00640] 70. Способ по любому из вариантов реализации изобретения 67-69, отличающийся тем, что: (а) белок Cas вносят в нечеловеческую ЭС клетку в форме белка, матричной РНК (мРНК), кодирующей белок Cas, или ДНК, кодирующей белок Cas; (b) РНК CRISPR вносят в нечеловеческую ЭС клетку в форме РНК или ДНК, кодирующей РНК CRISPR; и (с) tracrРНК вносят в нечеловеческую ЭС клетку в форме РНК или ДНК, кодирующей tracrРНК.
[00641] 71. Способ по варианту реализации изобретения 70, отличающийся тем, что белок Cas, РНК CRISPR и tracrРНК вносят в нечеловеческую ЭС клетку в виде комплекса белок-РНК.
[00642] 72. Способ по варианту реализации изобретения 70, отличающийся тем, что: (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; (b) ДНК, кодирующая РНК CRISPR, находится в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей РНК CRISPR; и (с) ДНК, кодирующая tracrРНК, находится в форме третьей экспрессионной конструкции, содержащей третий промотор, функционально связанный с четвертой нуклеиновой кислотой, кодирующей tracrРНК, при этом первый, второй и третий промоторы активны в нечеловеческой ЭС клетке.
[00643] 73. Способ по варианту реализации изобретения 72, отличающийся тем, что первая, вторая и/или третья экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[00644] 74. Способ по варианту реализации изобретения 70, отличающийся тем, что: (а) ДНК, кодирующая белок Cas, находится в форме первой экспрессионной конструкции, содержащей первый промотор, функционально связанный со второй нуклеиновой кислотой, кодирующей белок Cas; и (b) ДНК, кодирующая РНК CRISPR, и ДНК, кодирующая tracrРНК, находятся в форме второй экспрессионной конструкции, содержащей второй промотор, функционально связанный с третьей нуклеиновой кислотой, кодирующей нРНК, содержащую РНК CRISPR и tracrРНК; при этом первый и второй промоторы активны в нечеловеческой ЭС клетке.
[00645] 75. Способ по варианту реализации изобретения 74, отличающийся тем, что первая и вторая экспрессионные конструкции находятся в одной молекуле нуклеиновой кислоты.
[00646] 76. Способ по любому из вариантов реализации изобретения 67-75, отличающийся тем, что направленная генетическая модификация включает одновременное удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус.
[00647] 77. Способ по любому из вариантов реализации изобретения 67-76, отличающийся тем, что направленная генетическая модификация является биаллельной генетической модификацией.
[00648] 78. Способ по варианту реализации изобретения 77, отличающийся тем, что биаллельная генетическая модификация включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в двух гомологичных хромосомах.
[00649] 79. Способ по любому из вариантов реализации изобретения 67-76, отличающийся тем, что модифицированная нечеловеческая ЭС клетка является гемизиготной в представляющем интерес геномном локусе.
[00650] 80. Способ по варианту реализации изобретения 79, отличающийся тем, что направленная генетическая модификация в представляющем интерес геномном локусе в одной хромосоме включает удаление эндогенной нуклеотидной последовательности и вставку первой нуклеиновой кислоты.
[00651] 81. Способ по варианту реализации изобретения 79, отличающийся тем, что направленная генетическая модификация включает: (1) удаление эндогенной нуклеотидной последовательности в представляющем интерес геномном локусе в двух гомологичных хромосомах; и (2) вставку первой нуклеиновой кислоты в представляющий интерес геномный локус в первой хромосоме и разрушение представляющего интерес геномного локуса во второй хромосоме.
[00652] 82. Способ по любому из вариантов реализации изобретения 67-81, отличающийся тем, что белок Cas представляет собой Cas9.
ПРИМЕРЫ
[00653] Следующие примеры приведены, чтобы предоставить специалистам в данной области техники полное раскрытие и описание реализации и применения настоящего изобретения, и не предназначены ни для ограничения объема того, что авторы заявляют как свое изобретение, ни для утверждения, что нижеприведенные эксперименты являются всеми или единственными проведенными экспериментами. Были приложены усилия, чтобы гарантировать точность в отношении применяемых чисел (например, количества, температуры и т.д.), но следует учитывать возможность некоторых экспериментальных погрешностей и отклонений. Если не указано иное, доли являются массовыми долями, молекулярная масса является средневесовой молекулярной массой, температура приведена в градусах Цельсия, а давление равно или приближается к атмосферному.
Пример 1. Получение и характеристики крысиных ЭС клеток
1.1. Характеристики крысиных ЭС клеток
[00654] Как показано на Фигуре 1, крысиные ЭСК растут в виде компактных сферических колоний, которые обычно отделяются и плавают в чашке (крупный план, Фигура 8). Крысиные ЭСК экспрессируют маркеры плюрипотентности, включая Oct-4 (Фигура 2А) и Sox2 (Фигура 2В), и экспрессирует высокие уровни щелочной фосфатазы (Фигура 3). Кариотипом для линии DA.2B является 42X,Y (Фигура 4). Крысиные ЭСК часто становятся тетраплоидными; поэтому проводили предварительный скрининг линий путем подсчета метафазных хромосомных препаратов; затем линии с большинством нормальных результатов формально кариотипировали.
[00655] От приобретенных на коммерческой основе суперовулированных самок получали бластоцисты ACI. Бластоцисты DA культивировали из замороженных 8-клеточных эмбрионов, приобретенных на коммерческой основе. Блестящую оболочку удаляли при помощи кислоты Тироде; а бластоцисты высевали на митотически инактивированные ФЭМ. Увеличившиеся в размере бластоцисты собирали и размножали стандартными способами. Все бластоцисты высевали, культивировали и размножали, используя среду 2i (Li et al. (2008) Germline competent embryonic stem cells derived from rat blastocysts, Cell 135: 1299-1310; в полном объеме включенную в данный документ посредством ссылки).

1.2.: Получение крыс
[00656] Химерных крыс получали путем инъекции в бластоцисты и переноса генома крысиных ЭСК. Химеры, полученные путем микроинъекции в бластоцисты с применением родительских ЭСК крыс ACI.G1, показаны на Фигуре 9. Детеныши агути F1 с однопометными детенышами-альбиносами, полученными от химеры ACI/SD, помеченной звездочкой (*) на Фигуре 9, показаны на Фигуре 10.
Трансмиссия зародышевой линии родительских крысиных ЭСК.
[00657] Три эуплоидные крысиные линии ЭСК оценивали в отношении плюрипотентности путем микроинъекции в бластоцисты альбиносов SD. Химеры определяли по цвету шкуры агути, который указывает на влияние крысиных ЭСК (смотрите Фигуру 10). В каждой линии для большинства химер наблюдали передачу генома кЭСК потомкам F1 (Таблица 2).
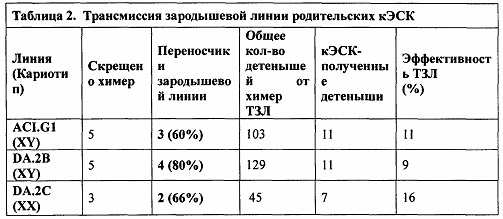
1.3.: Получение крысиных эмбриональных стволовых клеток.
[00658] Протокол суперовуляции, крысы
[00659] День 0: инъецировали сыворотку жеребой кобылы: ВБ, 20 Е (0,4 мл).
[00660] День 1: без действий
[00661] День 2: (через 46 ч): инъецировали hCG, ВБ, 50 Е (1 мл).
[00662] - спаривание одиночных самок.
[00663] День 3: проверяли копулятивные пробки. Пробки у самок присутствовали. Это соответствует дню 0,5.
[00664] День 6 (т.е. 3,5): Самок умерщвляли и вымывали эмбрионы.
[00665] Протокол получения ЭС клеток (суперовуляция)
[00666] День 0:
[00667] 1) Умерщвляли самку крысы при помощи СО2.
[00668] 2) Протирали брюшную полость 70% этанолом; при помощи ножниц вскрывали стенку брюшной полости, чтобы получить доступ к внутренним органам.
[00669] 3) Вырезали фаллопиевы трубы и рога матки и помещали их в чашку для тканевого культивирования, содержащую теплую среду N2B27. Насколько возможно, вымывали кровь и переносили в новую чашку с N2B27.
[00670] 4) При помощи 1 мл шприца и тупоконечной иглы 27g пропускали среду через рога матки и фаллопиевы трубы, чтобы извлечь бластоцисты в среду.
[00671] 5) Собирали бластоцисты при помощи пипетки и переносили в чашку для культивирования эмбрионов, содержащую KSOM + 2i (1 мкМ PD0325901, 3 мкМ CHIR99021). KSOM является культуральной средой, производимой Millipore. Номер в каталоге MR-106-D.
[00672] 6) Культивировали в течение ночи при 37°; 7,5% CO2.
[00673] Протокол получения ЭС клеток (замороженные эмбрионы)
[00674] День 0:
[00675] 1) Размораживали замороженные 8-клеточные эмбрионы (приобретенные на коммерческой основе) в среде М2. Культивировали 10 мин при комнатной температуре.
[00676] 2) Переносили в KSOM + 2i и культивировали в течение ночи.
[00677] Протокол получения ЭС клеток (одинаковый для обоих случаев)
[00678] День 1:
[00679] 1) Переносили кавитированные эмбрионы в среду 2i и культивировали в течение ночи.
[00680] 2) Продолжали культивирование некавитированных эмбрионов в KSOM + 2i
[00681] День 2:
[00682] 1) Переносили все оставшиеся эмбрионы в среду 2i (вне зависимости от того, являлись ли они кавитированными).
[00683] 2) Культивировали в течение ночи; продолжали культивирование более ранних эмбрионов в среде 2i.
[00684] День 3:
[00685] 1) Переносили эмбрионы на 30-60 секунд в кислоту Тироде, чтобы удалить блестящую оболочку.
[00686] 2) Промывали эмбрионы 3х в среде 2i, чтобы удалить кислоту Тироде.
[00687] 3) Помещали каждый эмбрион в отдельную лунку 96-луночного питающего планшета (лунки содержали монослой митотически инактивированных фибробластов эмбриона мыши (ФЭМ)).
[00688] 4) Культивировали в течение ночи в среде 2i.
[00689] День 4-5:
[00690] 1) Проводили мониторинг высеянных эмбрионов в отношении наличия зародышей (аморфной недифференцированной массы клеток). Зародыши готовы к переносу, когда их размер приблизительно вдвое превышает высеянный эмбрион.
[00691] 2) Каждый день: удаляли отработанную среду при помощи микропипетки и заменяли свежей средой 2i.
[00692] 3) Переносили зародыши в новые питающие лунки:
[00693] а. Удаляли отработанную среду и аккуратно промывали лунку ФСБ.
[00694] b. Удаляли ФСБ и добавляли 30 мкл 0,05% трипсина; инкубировали в течение 10 минут.
[00695] с. Останавливали реакцию трипсина, добавляя 30 мкл 2i + 10% ФБС.
[00696] d. Аккуратно разделяли клетки при помощи микропипеттора и переносили все содержимое лунки в новую лунку в 24-луночном питающем планшете. Это соответствовало пассажу 1 (P1).
[00697] е. Культивировали в течение ночи в среде 2i.
[00698] День 5-8: (время зависит от того, насколько быстро размножается каждая линия)
[00699] 1) Каждый день меняли среду (среда 2i) и проводили мониторинг в отношении наличия колоний с морфологией ЭСК.
[00700] 2) После появления колоний продолжили культивирование, пока колонии не достигли ~50% конфлюэнтности.
[00701] 3) Колонии обрабатывали трипсином и пассировали как и ранее; высевали на питающие слои, 1 лунка на линию, в 6-луночный планшет. Это соответствовало пассажу 2 (Р2).
[00702] Текущие действия:
[00703] 1) Продолжали подпитку и мониторинг каждой линии приблизительно до 50% конфлюэнтности.
[00704] 2) Обрабатывали трипсином как обычно.
[00705] 3) Останавливали реакцию трипсина при помощи 2i + 10% ФБС; осаждали клетки центрифугированием (5', 1200 об/мин в настольной центрифуге Beckman-Coulter).
[00706] 4) Отсасывали супернатант и аккуратно пересуспендировали клетки в 400 мкл среды для замораживания (70% 2i, 20% ФБС, 10% ДМСО).
[00707] 5) Распределяли клетки по двум пробиркам и замораживали при -80°. Это соответствовало пассажу 3 (Р3).
[00708] 6) Для длительного хранения помещали пробирки в жидкий N2.
[00709] Среду 2i готовили как приведено в Таблице 3.
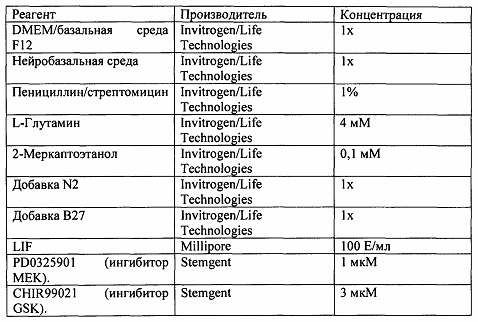
[00710] Материалы: Сывороточный гонадотропин жеребой кобылы (СГЖК)
[00711] Хорионический гонадотропин мочи беременной женщины (ХГЧ)
[00712] Самки крыс (в возрасте 5-12 недель)
[00713] Самцы крыс (в возрасте от 12 нед. до 8 мес.), один на клетку
[00714] Шприцы/иглы
[00715] Виварий с включенным светом 6:00-18:00
[00716] Процедура:
[00717] День 1: 8:00-10:00 до полудня
[00718] Инъецирование самок 20 ME СГЖК (0,4 мл), ВБ
[00719] Удаление неиспользованного СГЖК.
[00720] День 3: 8:00-10:00 до полудня (48 часов после инъекции СГЖК)
[00721] Инъецирование самок 50 ME ХГЧ (1 мл), ВБ
[00722] Размещение одна самка на самца в клетке для спаривания.
[00723] Удаление неиспользованного ХГЧ.
[00724] День 4: 8:00-10:00 до полудня (24 часов после инъекции ХГЧ)
[00725] Проверка самок на наличие копулятивных пробок.
[00726] Поставщики гормонов
[00727] СГЖК: Sigma #G-4877 (1000 ME). Пересуспендировали в ФСБ до конечной концентрации [] 50 МЕ/мл. Хранили при -20° в 1 мл аликвотах.
[00728] ХГЧ: Sigma #CG-5 (5000 ME). Пересуспендировали в ФСБ до конечной концентрации [] 50 МЕ/мл. Хранили при -20° в 1 мл аликвотах.
1.4.: Кариотипирование линий крысиных эмбриональных стволовых клеток
[00729] Кариотипировали полученные в данном документе линии крысиных ЭС клеток, а результаты обобщены в Таблицах 4-7.
[00730]

[00731]

[00732]

[00733]

1.5.: Электропорация вектора в крысиную эмбриональную стволовую клетку
[00734] 1. Крысиные ЭС клетки пассировали 24-48 ч перед электропорацией.
[00735] 2. Меняли среду на RVG2i + ROCKi (10 мкМ Y-27632) за 24 ч до электропорации
[00736] 3. Меняли среду за 30 мин до обработки трипсином.
[00737] 4. Аликвотировали ДНК для электропорации.
[00738] 5. Позволяли ДНК нагреваться при КТ в течение >10 мин.
[00739] 6. Нагревали ДНК 5 мин при 62°С. Помещали ДНК на лед.
[00740] 7. Обработанные трипсином клетки:
[00741] а. Собирали плавающие колонии. Промывали планшет, чтобы собрать как можно больше плавающих клеток.
[00742] b. Осаждали колонии: 3 мин при 750 об/мин.
[00743] с. Промывали осадок 1х 5-10 мл ФСБ и повторно центрифугировали/осаждали
[00744] d. Отсасывали супернатант; добавляли 500 мкл трипсина, 0,05% + 1% куриной сыворотки.
[00745] i. He набирали более 1 10 см планшета колоний в пробирку. Если во время обработки трипсином на дне пробирки будет находиться слишком много колоний, они будут агрегироваться, и большинство клеток будет потеряно.
[00746] е. 4 мин при 37°. Пипетировали колонии несколько раз для минимизации агрегации.
[00747] f. Повторяли этапы 1-2 X: 4 мин при 37°.
[00748] g. Останавливали реакцию трипсина при помощи 500 мкл RVG2i + 10% ФБС.
[00749] 8. Осаждали клетки: 5 мин при 1200 об/мин.
[00750] 9. Пересуспендировали клетки в 10 мл ФСБ. Отсчитывали две 20 мкл аликвоты, чтобы определить общее число клеток.
[00751] 10. Осаждали клетки (5 мин/1200 об/мин); подсчитывали общее число клеток и общий объем повторной суспензии, чтобы получить правильную концентрацию клеток (цель #/75 мкл буфера ЕР).
[00752] 11. Пересуспендировали в минимальном объеме буфера ЕР; определяли общий объем и доводили до целевого объема буфером ЕР. Буфер для электропорации продается Millipore. Номер в каталоге соответствует ЭС-003-D. Смотрите Valenzuela et al. (2003) Nature Biotechnology 21: 652-659, которая включена в данный документ посредством ссылки.
[00753] 12. Добавляли 75 мкл клеток в 50 мкл ДНК; переносили 125 мкл раствора клетки/ДНК в одну лунку 48-луночной кюветы ВТХ.
[00754] а. Заполняли пустые лунки в той же колонке 125 мкл буфера ЕР.
[00755] 13. Один раз облучали кювету в электропораторе ВТХ:
[00756] а. Настройки: 400 В; Ω; 100 мкФ (настройки могут варьироваться)
[00757] 14. Помещали кювету на лед на 15 мин для восстановления.
[00758] 15. Переносили клетки в 5 мл RVG2i + 10 мкМ ROCKi.
[00759] 16. Добавляли в 15 см планшет с 20 мл RVG2i + 10 мкМ ROCKi. Планшет содержал 2х neoR ФЭМ (или других ФЭМ в зависимости от проекта). Селективный маркер neoR представляет собой ген неомицин фосфотрансферазы (neo) согласно Beck et al. (1982) Gene, 19: 327-36 или патенту США №7205148 или 6596541, которые все включены в данный документ посредством ссылки..
[00760] 17. Инкубировали при 37°. Через 48 ч начинали отбор.
[00761] Ингибитор ROCK представлял собой Y-27632.
1.6: Отбор направленной генетической модификации в крысиной эмбриональной стволовой клетке.
[00762] 1. Пассировали клетки 24-48 ч перед электропорацией.
[00763] 2. Меняли среду на RVG2i + ROCKi (10 мкМ Y-27632) за 24 ч до электропорации
[00764] 3. Меняли среду за 30 мин до обработки трипсином.
[00765] 4. Аликвотировали ДНК для электропорации.
[00766] 5. Позволяли ДНК нагреваться при КТ в течение >10 мин.
[00767] 6. Нагревали ДНК 5 мин при 62°С. Помещали ДНК на лед.
[00768] 7. Обработанные трипсином клетки:
[00769] а. Собирали плавающие колонии. Промывали планшет, чтобы собрать как можно больше плавающих клеток.
[00770] b. Осаждали колонии: 3 мин при 750 об/мин.
[00771] с. Промывали осадок 1х 5-10 мл ФСБ и повторно центрифугировали/осаждали
[00772] d. Отсасывали супернатант; добавляли 500 мкл трипсина, 0,05% + 1% куриной сыворотки.
[00773] i. He набирали более 1 10 см планшета колоний в пробирку. Если во время обработки трипсином на дне пробирки будет находиться слишком много колоний, они будут агрегироваться, и большинство клеток будет потеряно.
[00774] е. 4 мин при 37°. Пипетировали колонии несколько раз для минимизации агрегации
[00775] f. Повторяли 1-2 X: 4 мин при 37°.
[00776] g. Останавливали реакцию трипсина при помощи 500 мкл RVG2i + 10% ФБС.
[00777] 8. Осаждали клетки: 5 мин при 1200 об/мин.
[00778] 9. Пересуспендировали клетки в 10 мл ФСБ. Отсчитывали две 20 мкл аликвоты, чтобы определить общее число клеток.
[00779] 10. Осаждали клетки (5 мин/1200 об/мин); подсчитывали общее число клеток и общий объем повторной суспензии, чтобы получить правильную концентрацию клеток (цель #/75 мкл буфера ЕР).
[00780] 11. Пересуспендировали в минимальном объеме буфера ЕР; определяли общий объем и доводили до целевого объема буфером ЕР.
[00781] 12. Добавляли 75 мкл клеток в 50 мкл ДНК; переносили 125 мкл раствора клетки/ДНК в одну лунку 48-луночной кюветы ВТХ.
[00782] а. Заполняли пустые лунки в той же колонке 125 мкл буфера ЕР.
[00783] 13. Один раз облучали кювету в электропораторе ВТХ:
[00784] а. Настройки: 400 В; 100 мкФ (настройки могут варьироваться)
[00785] 14. Помещали кювету на лед на 15 мин для восстановления.
[00786] 15. Переносили клетки в 5 мл RVG2i + 10 мкМ ROCKi.
[00787] 16. Добавляли в 15 см планшет с 20 мл RVG2i + 10 мкМ ROCKi.
Планшет содержал 2х neoR ФЭМ (или других ФЭМ в зависимости от проекта).
[00788] 17. Инкубировали при 37°. Через 48 ч начинали отбор.
[00789] 18. Протокол отбора G418 был следующим:
[00790] а. День 2 (2-й день после ЭП): инкубировали клетки в среде 2i + G418, 75 мкг/мл.
[00791] b. День 3: инкубировали клетки в среде 2i без G418
[00792] с. День 4: инкубировали клетки в среде 2i + G418, 75 мкг/мл.
[00793] d. День 5: инкубировали клетки в среде 2i без G418
[00794] е. День 6: инкубировали клетки в среде 2i + G418, 75 мкг/мл.
[00795] f. День 7: инкубировали клетки в среде 2i без G418
[00796] g. День 8: инкубировали клетки в среде 2i + G418, 75 мкг/мл.
[00797] h. День 9: инкубировали клетки в среде 2i без G418
[00798] i. День 10: инкубировали клетки в среде 2i + G418, 75 мкг/мл.
[00799] j. День 11: инкубировали клетки в среде 2i без G418
[00800] k. День 12: собирали колонии для размножения для проведения скрининга. Каждую колонию разделяли в 0,05% трипсине + 1% куриной сыворотки в течение 10 минут, а затем высевали в 1 лунку 96-луночного питающего планшета.
[00801] 19. Размножали колонии в течение 3 дней в среде 2i.
[00802] 20. Пассировали клоны 1:1 в новые 96-луночные питающие планшеты.
[00803] 21. Размножали клоны в течение 3 дней в среде 2i.
[00804] 22. Для каждого клона проводили разделение колоний в трипсине. Замораживали 2/3 каждого клона и хранили при -80°; высевали оставшуюся 1/3 в планшеты с ламинином (96-луночные планшеты, покрытые 10 мкг/мл ламинина).μ
[00805] 23. Когда планшеты с ламинином достигали конфлюэнтности, переносили их в лабораторию для скрининга для генотипирования клонов.
1.7. Молекулярный портрет крысиных эмбриональных стволовых клеток
[00806] Гены, перечисленные в Таблице 8, экспрессировались в 20 раз меньше в крысиных ЭС клетках, чем соответствующие гены в мышиных ЭС клетках. Гены, перечисленные в Таблице 9, экспрессировались на уровне в 20 раз большем в крысиных ЭС клетках, чем соответствующие гены в мышиных ЭС клетках.
[00807] Микроматричные данные в Таблицах 8 и 9 были получены следующим образом. Крысиные ЭС клетки (ACI.G2 и DA.2B) и мышиные ЭС клетки (F1H4) культивировали в среде 2i на протяжении 3 пассажей до достижения конфлюэнтности. Клетки F1H4 культивировали на покрытых желатином планшетах в отсутствие подпитки. ЭС клетки мышей F1H4 были получены из гетерозиготных эмбрионов 129S6/SvEvTac и C57BL/6NTac (смотрите, например, патент США №7294754 и Poueymirou, W.T., Auerbach, W., Frendewey, D., Hickey, J.F., Escaravage, J.M., Esau, L., Dore, A.T., Stevens, S., Adams, N.C., Dominguez, M.G., Gale, N.W., Yancopoulos, G.D., DeChiara, T.M., Valenzuela, D.M. (2007), в полном объеме включенные в данный документ посредством ссылки).
[00808] Следующий протокол использовали для приготовления образцов: На 1,5 мл пробирки Эппендорф наносили метки с ID образцов. Клетки, выращенные на планшете, промывали в 37°С фосфатно-солевом буфере (ФСБ). ФСБ удаляли и добавляли 300 мкл Trizol®. Для разрушения клеток в Trizol® (Life Technology) использовали скребок. Лизированные клетки собирали в Trizol® в 1,5 мл пробирку Эппендорф. Клетки, выращенные в суспензии, промывали в 37°С ФСБ и собирали в 1,5 мл пробирку. Клетки центрифугировали; ФСБ удаляли; и добавляли к клеткам 300 мкл Trizol®. Клеточные мембраны разрушали путем пипетирования. Проводили сортинг образцов методом FACS с от 10 до 105 клеток, объем уменьшали концентрированном до менее чем 100 мкл. Добавляли 4 объема буфера для лизиса РНК и смешивали путем пипетирования. Для получения образца добавляли 320 мкл буфера для лизиса РНК к 80 мкл образца. Образцы хранили при -20°С.
[00809] Для определения уровня экспрессии мышиных и крысиных генов применяли секвенирование РНК. Результаты секвенирования картировали на мышиный и крысиный контрольный геном при помощи Tophat и подсчитывали RPKM (число фрагментов на тысячу пар оснований экзона на миллион картированных фрагментов) для мышиных и крысиных генов. Гомологичные гены отбирали на основании символа гена, а затем применяли t-критерий, чтобы сравнить уровень экспрессии каждого гена для мышей и крыс. miR-32 входил в 10 наиболее экспрессируемых компонентов в крысиных ЭСК, но не экспрессировался в мышиных ЭС клетках. Хотя сравнительных данных по miR-632 не существует, на основании уровня его экспрессии по сравнению с другими генами, экспрессируемыми в крысиных ЭСК, и его известной функции в эмбриональном развитии miR-632 был выбран в качестве маркера для крысиных ЭС клеток.
[00810]
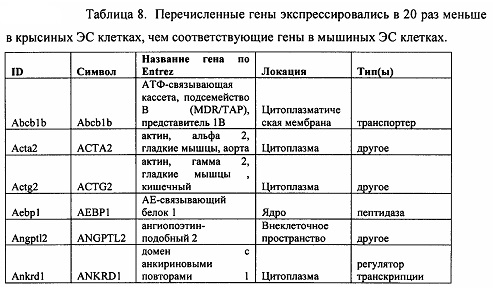
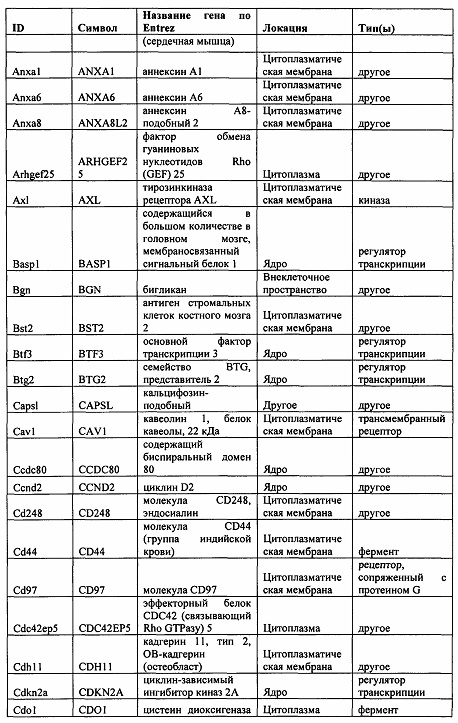

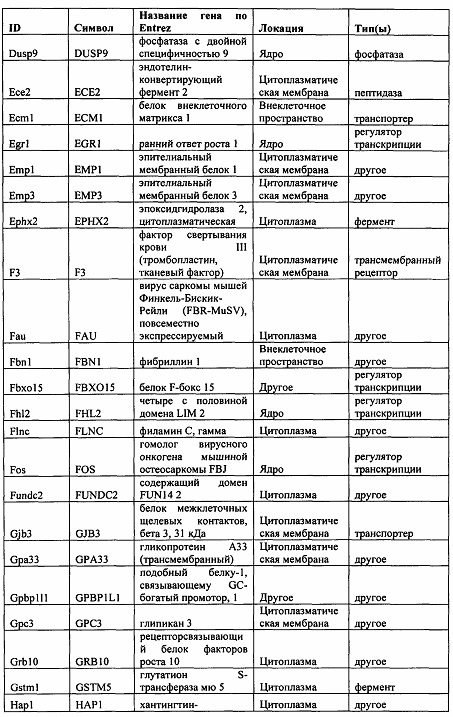



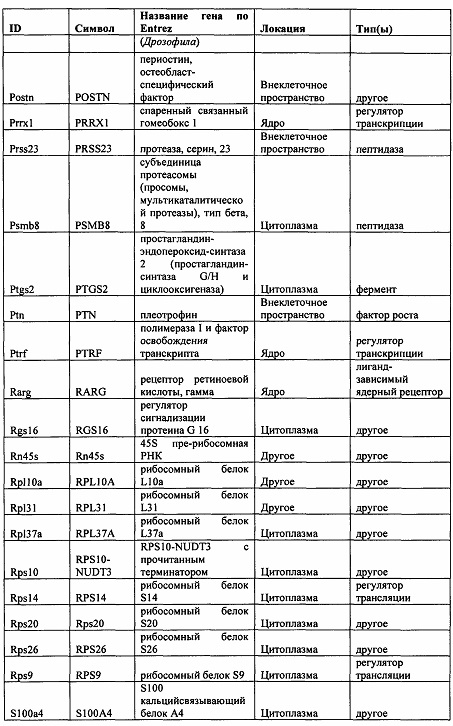



[00811]


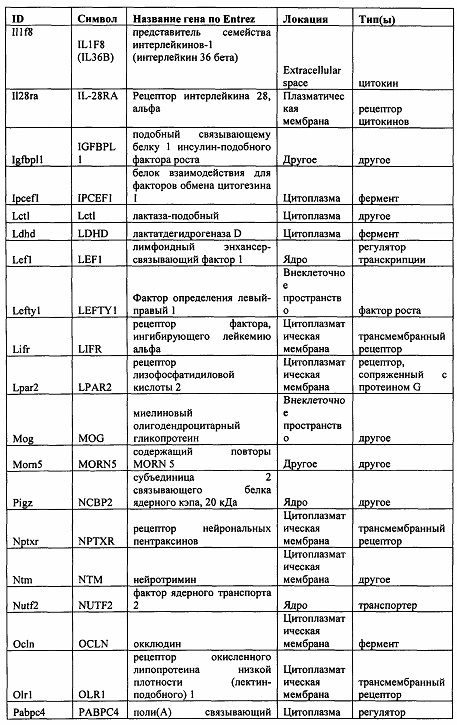

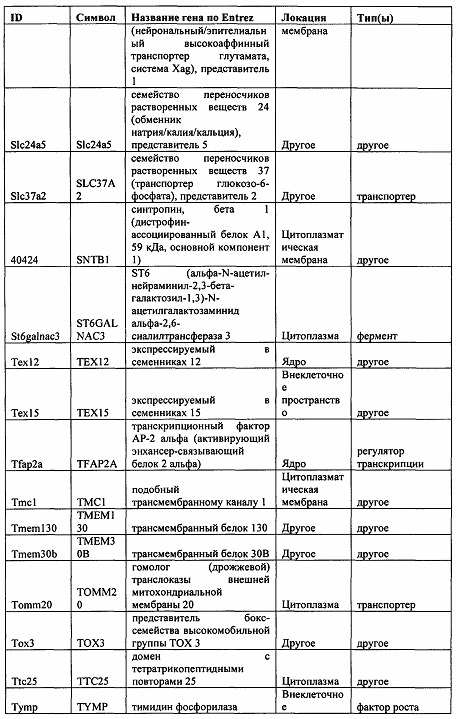
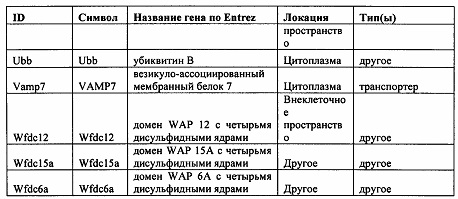
[00812]
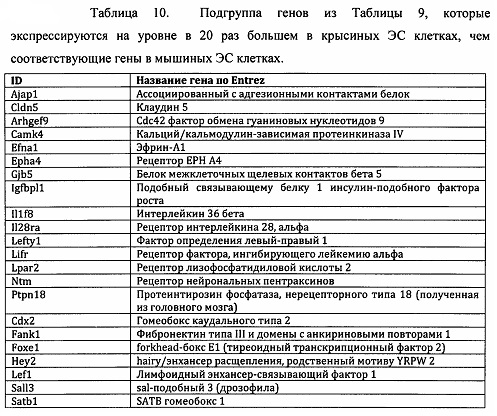
[00813] Также был разработан дополнительный молекулярный портрет с применением маркеров/генов плюрипотентности для крысиных ЭС клеток. В Таблице 11 приведен список геном и их степень экспрессии из данных профилирования РНК. мРНК выделяли из крысиных ЭС клеток и сравнивали уровни экспрессии различных маркеров по отношению друг к другу. Термин «степень» означает сравнительные уровни экспрессии отдельных генов: чем выше степень (наивысшей является 1-ая), тем выше экспрессия. Например, степень Oct4 13 означает, что среди всех анализируемых генов он экспрессировался на более высоком уровне, чем 12 генов. Фоновым значение в этом эксперименте было любое значение экспрессии ниже 30; 6107 генов имели уровень экспрессии 30 и выше.
[00814]
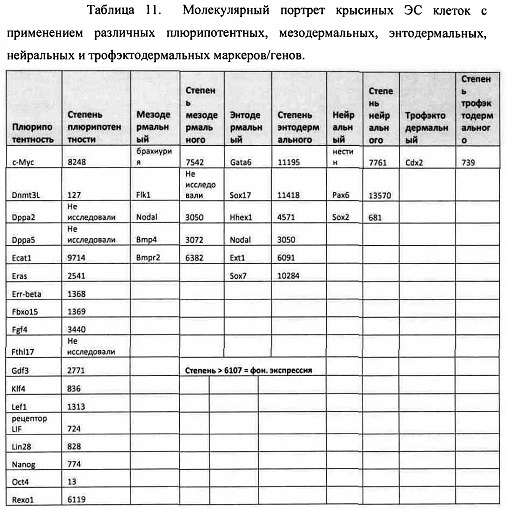
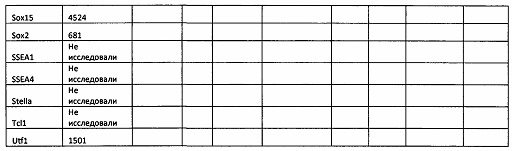
Пример 2: Инактивация геномных локусов у крыс
2.1: Инактивация эндогенных геномных локусов при помощи эндонуклеазного агента
[00815] Чтобы внести мутантный аллель в эндогенный крысиный геномный локус, описанные в данном документе крысиные ЭС клетки электропорируют экспрессионными векторами (или мРНК), которые экспрессируют ZFN 1 и 2 (или TALEN 1 и 2). Эти белки связывают свои целевые последовательности на противоположных цепях, разделенные от около 6 п.о. до около 40 п.о. В целевом локусе образуется двухцепочечный разрыв, который клетки пытаются починить посредством негомологичного соединения концов (НГСК). Во многих случаях НГСК приводит к созданию делеции, которая часто нарушает функционирование гена (наиболее часто вследствие создания мутации со сдвигом рамки). Чтобы выявить мутантный аллель, содержащий положительный клон, электропорированные клетки высевают при низкой плотности, так как отбор по чувствительности к лекарственному препарату не проводится. Колонии собирают и проводят анализ целевого участка, чтобы выяснить, была ли создана мутация (например, при помощи анализа модификации аллеля (МОА), описанного выше). Затем отобранные ЭС клетки, содержащие мутантный аллель, вносят в крысиный эмбрион-хозяина, например, находящийся на стадии пре-морулы или бластоцисты крысиный эмбрион, и имплантируют в матку суррогатной матери, чтобы получить крысу-основательницу (крысу F0). После этого крысу-основательницу скрещивают с крысой дикого типа для получения потомства F1, гетерозиготного в отношении мутантного аллеля. Путем спаривания гетерозиготных крыс F1 можно получить потомство, гомозиготное в отношении мутантного аллеля.
2.2.: Таргетирование крысиных ЭСК для инактивации гена крысиного аполипопротеина Е (АроЕ) при помощи цинк-пальцевых нуклеаз
[00816] Цинк-пальцевые нуклеазы используют специфические к последовательности модулярные ДНК-связывающие домены, чтобы направлять активность эндонуклеаз на определенную целевую последовательность в геноме. ZFN сконструированы в виде пары мономеров. Каждый мономер содержит неспецифический домен расщепления из эндонуклеазы FokI, слитый с 3 или более цинк-пальцевыми ДНК-связывающими доменами. Каждый цинковый палец связывает субсайт из 3 п.о., а специфичность достигается путем комбинирования целевых участков обоих мономеров. ZFN создают двухцепочечные разрывы (ДЦР) в ДНК, и во время негомологичного соединения концов (НГСК) часто возникают мутации (вставки или делеции). Фигура 15 иллюстрирует механизм, посредством которого редактирующие геном эндонуклеазы, такие как ZFN и TALEN, вносят двухцепочечные разрывы в целевую геномную последовательность и активируют в клетке НГСК. ДЦР часто стимулируют направляемую гомологией репарацию (НГР) путем гомологичной рекомбинации, если донорная последовательность содержит ZFN.
[00817] Такие ZFN применяли в комбинации с описанными в данном документе различными способами и композициями для улучшения эффективности таргетирования. Таргетирование крысиного локуса аполипопротеина Е (АроЕ) проводили так, как описано в Примере 3.2(a)(i), за исключением того, что экспрессионные векторы, которые экспрессируют ZFN 1 и 2, также вносили в крысиные ЭС клетки. Смотрите Фигуру 11, на которой приведена схема таргетирования АроЕ в комбинации с rTZFN1P и rTZFN2P. Эффективность таргетирования определяли так, как обсуждается ниже в Примере 5, а результаты приведены в Таблице 12. Для проведения скрининга в отношении гетерозиготного таргетирования, гомозиготного таргетирования и «смешанных» пар (например, компаунд-гетерозиготного таргетирования) применяли специфические праймеры и зонды для определения генотипа. Неожиданно, эффективность таргетирования возросла в 8-10 раз.
[00818]

[00819] Плазмидный направляющий вектор конструировали с самоуничтожающейся кассетой отбора по чувствительности к лекарственному препарату и геном lacZ в качестве репортерного гена (смотрите Фигуру 14, иллюстрирующую гомологичную и негомологичную рекомбинацию, которая может происходить после электропорации направляющего вектора, содержащего селекционную кассету). Была достигнута хорошая эффективность таргетирования и получены химеры с высоким %. Также исследовали цинк-пальцевые нуклеазы (ZFN) в комбинации с направляющими векторами, чтобы изучить их влияние на улучшение эффективности таргетирования (смотрите Фигуру 16, иллюстрирующую метод таргетирования генов с применением ZFN или TALEN для улучшения эффективности гомологичной рекомбинации направляющего вектора). Направляющий вектор коэкспрессировался с экспрессионными векторами для 2 пар ZFN, которые разрезают локус АроЕ. Клоны крысиных ЭСК, электропорированные как направляющим вектором, так и группой ZFN, демонстрировали эффективность таргетирования в 8-10 раз выше, чем клоны крысиных ЭСК, электропорированные только направляющим вектором. Кроме того, было выявлено биаллельное гомозиготное таргетирование приблизительно в 2% клонов. Из этих двух таргетированных клонов были получены химеры с высоким %.
[00820] Проводили микроинъекцию клонов крысиных ЭСК с таргетированным АроЕ (при помощи ZFN) в бластоцисты SD, которые затем переносили в организм псевдобеременных самок-реципиентов SD, используя стандартные методы. Химеры определяли по цвету шкуры (смотрите Фигуру 17, иллюстрирующую химер ApoE-ZFN-AB5 (т.е. химер АроЕ-/-); самцов химер F0 скрещивали с самками SD. Детенышей зародышевой линии F1 генотипировали в отношении наличия таргетированного аллеля АроЕ (Таблица 13). Из этих двух таргетированных клонов были получены химеры с высоким %.
[00821]

[00822] Крыса с выключенным АроЕ представляет собой средство изучения различных типов нарушений и заболеваний. У людей аполипопротеин находится в хиломикроне, ЛПВП, ЛПНП и ЛПОНП. АроЕ важен для нормального катаболизма триглицерид-богатых составляющих липопротеинов. Дефекты в АРОЕ приводят к многочисленным болезненным состояниям, включая, например, семейную гиперхолестеринемию, гиперлипидемию, беталипопротеинемию, семейную дисбеталипопротеинемию, гиперлипопротеинемию типа III (HLP III), риск заболевания коронарных артерий. Одна изоформа (АроЕ4) связана с семейной болезнью Альцгеймера с поздним началом и спорадической болезнью Альцгеймера, а также, возможно с PC (рассеянным склерозом).
[00823] У мышей АроЕ главным образом находится в ЛПВП; переносит холестерин, как и у людей. У мышей с отсутствующим АроЕ (2 независимых выключения) наблюдается в 5 раз превышающий нормальный уровень холестерина в крови; образование пенистых богатых клетками отложений в проксимальных аортах в возрасте 3 месяцев (сравнимо с человеческим синдромом).
[00824] Выключения АроЕ у крыс обеспечивают животную модель для изучения эндотелиальной функции, включая, но не ограничиваясь этим, образование бляшек, транскрипционные изменения (секвенирование РНК), ex vivo функцию. Кроме того, более крупные размеры крыс облегчают проведение этих анализов и потенциально улучшают качество данных секвенирования РНК.
2.3. Инактивация локуса крысиного рецептора интерлейкина-2 гамма (IL2r-γ) при помощи цинк-пальцевых нуклеаз
[00825] Таргетирование локуса крысиного рецептора интерлейкина-2 гамма (IL2r-γ или Il2rg) проводили как описано в Примере 3.3(а), за исключением того, что в крысиные ЭС клетки также вносили экспрессионные векторы, которые экспрессируют ZFN U (ZFN вышележащий) и ZFN D (ZFN нижележащий). На Фигуре 18 приведено схематическое изображение таргетирования IL2r-γ в комбинации с ZFN U и ZFN D. Последовательность локуса IL2r-γ, которую связывают эти цинковые пальцы, обозначена на Фигуре 18 в пределах SEQ ID №93. Эффективность таргетирования определяли, как описано ниже в Примере 3.3(а), а результаты приведены в Таблице 14. Вкратце, гомозиготно таргетированные клоны подтверждали при помощи ПЦР. Для пары ZFN1: 173 мутантных клона из 192 исследованных (90%), и для пары ZFN2: 162 клона из 192 исследованных (84%).
[00826]

[00827] Проводили микроинъекцию клонов крысиных ЭСК с таргетированным IL2r-γ (при помощи ZFN) в бластоцисты SD, которые затем переносили в организм псевдобеременных самок-реципиентов SD, используя стандартные методы. Химеры определяли по цвету шкуры; самцов химер F0 скрещивали с самками SD. Детенышей зародышевой линии F1 генотипировали в отношении наличия таргетированного аллеля IL2r-γ.
2.4.: Инактивация локуса крысиного рецептора интерлейкина-2 гамма (IL2r-γ) при помощи CRISPR/Cas9
[00828] Таргетирование локуса крысиного IL2r-γ проводили, как описано в Примере 3.3(а), за исключением того, что в крысиные ЭС клетки также вносили систему CRISPR/Cas9 для улучшения эффективности таргетирования. SBI: Применяли векторы «все-в-одном» System Biosciences Cas9 «SmartNuclease», a экспрессией Cas9 управлял промотор CAG, EF1a, PGK или CMV. Специальную нРНК лигировали в вектор и экспрессировали при помощи промотора HI. Было сконструировано 4 нРНК против Il2rg. Области локуса крысиного IL2r-γ, на которые нацелены нРНК 1-4, показаны на Фигуре 19. Для проведения скрининга в отношении таргетирования (например, гетерозиготного таргетирования, гомозиготного таргетирования и компаунд-гетерозиготного таргетирования) применяли специфические праймеры и зонды для определения генотипа. Результаты таргетирования при применении разных направляющих РНК показаны в Таблице 15. «Сильный» и «слабый» относятся к совокупности данных скрининга в отношении того, что колония имеет целевую модификацию.
[00829]

2.5.: Инактивация гена мышиной гипоксантин-гуанинфосфорибозилтрансферазы (Hprt) при помощи CRISPR/Cas9
[00830] Проводили таргетирование локуса мышиного Hprt в мышиных ЭС клетках при помощи одного LTVEC или в комбинации с CRISPR/Cas9. Проводили таргетирование полной кодирующей последовательности Hprt в 32,9 т.п.о. для создания делеции и замещения селекционной кассетой устойчивости к пуромицину pCAGG-Puro, которая также экспрессирует уЗФБ. Крайними точками делеции были стартовый и стоп-кодоны. Применяемая последовательность направляющей РНК соответствовала 5'-GACCCGCAGUCCCAGCGUCG-3' (SEQ ID №84) и была нацелена на экзон 1 гена мышиного Hprt. Прогнозируемый целевой участок расщепления соответствовал 22 парам оснований от 5' конца делеции. Эффективность расщепления Cas9/нРНК в целевом участке, наблюдаемая в ЭС клетках, составила ≥93%. Обобщенные результаты приведены в Таблице 16. Применение CRISPR/Cas9 для помощи при таргетировании полного локуса Hprt в 32,9 т.п.о. привела к пятикратному повышению таргетирования по сравнению с применением одного LTVEC.
[00831]

Пример 3: Направленная модификация крысиных геномных локусов
3.1: Таргетирование крысиных ЭСК: Локус крысиного Rosa26.
[00832] Локус крысиного Rosa26 находится между генами Setd5 и Thumpd3, как и у мышей, с такими же интервалами. Локус крысиного Rosa26 (Фигура 12, панель В) отличается от локуса мышиного Rosa26 (Фигура 12, панель А). Транскрипты мышиного Rosa26 состоят из 2 или 3 экзонов. Крысиный локус содержит 2-й экзон 1 (Ex1b) в добавок к гомологичному экзону к мышиному экзону 1 (Ex1a). У крыс не было выявлено 3-го экзона. Таргетирование аллеля крысиного Rosa26 проиллюстрировано на Фигуре 12С, где плечи гомологии по 5 т.п.о. каждое были клонированы посредством ПЦР с применением геномной ДНК из ЭСК крыс DA. Таргетированный аллель содержит кассету SA (акцептор сплайсинга)-lacZ-hUb-nео, замещающую делецию в 117 п.о. в интроне крысиного Rosa26.
[00833] Определяли эффективность таргетирования локуса крысиного Rosa26 (Таблица 17). Линеаризованный вектор электропорировали в ЭСК крыс DA или ACI, а трансфицированные колонии культивировали в среде 2i media + G418, используя стандартные методы. Собирали отдельные колонии и проводили скрининг методом анализа потерянного аллеля (LOA) (Valenzuela, D. et al. (2003) High-throughput engineering of the mouse genome coupled with high-resolution expression analysis, Nature Biotech. 21: 652-660, включенная в данный документ посредством ссылки).

[00834] Получение химер и трансмиссия зародышевой линии с применением Rosa26-таргетированных клонов крысиных ЭСК. Проводили микроинъекцию повторно подтвержденных Rosa26-таргетированных клонов крысиных ЭСК в бластоцисты SD, которые затем переносили в организм псевдобеременных самок-реципиентов SD, используя стандартные методы. Химеры определяли по цвету шкуры; самцов химер F0 скрещивали с самками SD. Детенышей (агути) зародышевой линии F1 генотипировали в отношении наличия таргетированного аллеля Rosa26; девять из 22 детенышей агути были генотипированы как гетерозиготные в отношении локуса Rosa26 (Таблица 18).

[00835] Чтобы подтвердить, что генетически модифицированный аллель в локусе Rosa26 передавался через зародышевую линию, проводили подтверждение экспрессии lacZ путем окрашивания X-gal у гетерозиготных крыс с таргетированным Rosa26. Окрашивание X-gal головного мозга, сердца, вилочковой железы и легких 14-недельных гетерозиготных крыс с таргетированным Rosa26 показало наличие экспрессии lacZ (Фигура 13В, D и F, соответственно), в то время как контрольные животные дикого типа того же возраста продемонстрировали низкий уровень фонового окрашивания X-gal (Фигура 13А, С и Е, соответственно). Окрашивание X-gal у Е12.5 и Е14.5 гетерозиготных крысиных эмбрионов с таргетированным Rosa26 продемонстрировало повсеместную экспрессию lacZ (Фигура 13G и I, соответственно), в то время как контрольные крысиные эмбрионы демонстрировали низкие уровни фонового окрашивания X-gal (Фигура 13Н и J, соответственно).
3.2.(a)(i): Таргетирование локуса крысиного аполипопротеина Е (АроЕ).
[00836] Проводили таргетирование локуса крысиного аполипопротеина Е (АроЕ), чтобы блокировать функцию АроЕ. Таргетирование локуса АроЕ осуществляли при помощи направляющего вектора, содержащего кассету lacZ-hUb-neo, фланкируемую 5' и 3' плечами гомологии, гомологичными локусу АроЕ. Фигура 20 иллюстрирует генетически модифицированный локус крысиного АроЕ, который был разрушен вследствие 1,8 т.п.о. делеции и вставки кассеты lacZ-hUb-neo, которая дополнительно содержит самоуничтожающуюся кассету Cre, содержащую ген Crei под управлением промотора протамина. Условия электропорации были следующими: 6 мкг ДНК; 2,05×106 клеток; 400 В; 200 мкФ: 342 В, 593 мкс; высеяно на 15 см с 2х плотностью neoR ФЭМ в 2i + 10 мкМ ROCKi.
[00837] Определяли эффективность таргетирования в локусе АроЕ, а результаты приведены в Таблице 19. Линеаризованный вектор электропорировали в ЭСК крыс DA.2B, полученные от штамма DA, и культивировали трансфицированные колонии, используя стандартные методы. Собирали отдельные колонии и проводили скрининг методом анализа потерянного аллеля (LOA).

[00838] Осуществляли получение химер и трансмиссию зародышевой линии с применением клонов крысиных ЭСК с таргетированным АроЕ. Проводили микроинъекцию клонов крысиных ЭСК с таргетированным АроЕ в бластоцисты SD, которые затем переносили в организм псевдобеременных самок-реципиентов SD, используя стандартные методы. Химеры определяли по цвету шкуры; самцов химер F0 скрещивали с самками SD. Была достигнута трансмиссия зародышевой линии. Детенышей F1 генотипировали в отношении наличия таргетированного аллеля АроЕ (Таблица 20).

[00839] Проводили подтверждение экспрессии LacZ под управлением эндогенного промотора АроЕ путем окрашивания X-gal головного мозга, кровеносных сосудов и печени 12-месячных самок крыс АроЕ+/- (Фигуры 43-45, соответственно). Фигуры 43-45 иллюстрируют профиль экспрессии lacZ, который повторяет профиль экспрессии эндогенного АроЕ. Контрольные животные дикого типа того же возраста демонстрировали низкий уровень фонового окрашивания X-gal.
[00840] Дополнительно изучали фенотипы крыс с удаленным АроЕ-. Проводили продолжительные химические исследования сыворотки для определения уровней холестерина, ЛПНП, ЛПВП и триглицеридов с трехнедельными интервалами. Фигура 46A-D иллюстрирует сывороточные уровни холестерина, ЛПНП, ЛПВП и триглицеридов у гомозиготно таргетированных, гетерозиготно таргетированных и дикого типа крыс в возрасте 6 недель, 9 недель, 12 недель и 15 недель. Забор крови из глаз осуществляли для соответствующей возрастной группы, состоящей из 2 крыс дикого типа, 7 гетерозиготных и 8 гомозиготных крыс. Между самцами и самками не наблюдали значительной разницы. Гомозиготные крысы с удаленным АроЕ демонстрировали повышенные уровни холестерина и ЛПНП и пониженные уровни ЛПВП. В отличие от мышей АроЕ-/-, у крыс с удаленным АроЕ не наблюдали значительного повышения уровня триглицеридов.
[00841] Проводимый дополнительный фенотипический анализ включал гистологическую/еx vivo визуализацию образования бляшек в дуге аорты, in vivo визуализацию образования бляшек в дуге аорты и транскрипционные изменения (секвенирование методом дробовика полного транскриптома (секвенирование РНК)) в эндотелии дуги аорты. Время проведения этих анализов зависит от продолжительности образования бляшек. Бляшки становятся выявляемыми у мышей АроЕ-/- в 24 недели.
[00842] Дополнительные данные по таргетированию АроЕ приведены в Таблице 22.
3.2.(a)(ii). Таргетирование АроЕ у крыс при помощи направляющего вектора
[00843] На Фигуре 20 приведено схематическое изображение локуса крысиного АроЕ и направляющей плазм иды. На верхней схеме на Фигуре 20 показана геномная структура локуса крысиного АроЕ и геномные области, соответствующие 5' и 3' плечам гомологии (5 т.п.о. и 5,4 т.п.о., соответственно; темно-серые прямоугольники). Экзон 1 АроЕ является некодирующим и показан в виде неокрашенного прямоугольника, расположенного наиболее близко к 5' плечу гомологии. Три интрона в гене АроЕ обозначены в виде линий, а экзоны 2 и 3 содержат кодирующие области и показаны в виде заштрихованных пунктиром серых прямоугольников. Экзон 4 содержит как кодирующие, так и некодирующие последовательности, обозначенные серым пунктиром и неокрашенным прямоугольником.
[00844] На нижней схеме на Фигуре 20 представлен направляющий вектор. 5' и 3' плечи гомологии (5 т.п.о. и 5,4 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. Направляющий вектор содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки). Самоуничтожающаяся кассета содержит ген Crei, функционально связанный с промотором мышиного Prm1, и селекционную кассету, содержащую ген устойчивости к неомицину, функционально связанный с промотором человеческого убиквитина.
[00845] Ген Crei содержит два экзона, кодирующих рекомбиназу Cre, которые разделены интроном (Crei) для предотвращения его экспрессии в прокариотической клетке. Смотрите, например, патент США 8697851 и опубликованную заявку на патент США 2013-0312129, в которых подробно описана самоуничтожающаяся кассета, и которые в полном объеме включены в данный документ посредством ссылки. Самоуничтожающуюся кассету можно удалять, применяя промотор Prm1, в частности, в мужских зародышевых клетках крыс F0. Направляющий вектор электропорировали в крысиные ЭС клетки, полученные в Примере 1, и высевали клетки на 15 см с 2х плотностью устойчивых к неомицину ФЭМ в 2i + 10 мкМ ROCKi. Трансформированные крысиные ЭС клетки культивировали, отбирали и поддерживали, как описано в Примере 1.
[00846] Как показано в Таблице 44, проводили скрининг 384 колоний и получили 23 таргетированных клона. Эффективность таргетирования составила 5,99%. Проводили инъекцию 3 клонов в бластоцисты как описано в Примере 1. Было получено 3 клона, продуцирующих химеры, и 1 из клонов передавал направленную модификацию через зародышевую линию.
3.2.(а)(iii). Таргетирование АроЕ у крыс при помощи направляющего вектора в комбинации с цинк-пальцевыми нуклеазами
[00847] Направляющий вектор, применяемый в Примере 3.2(а)(ii), использовали в комбинации с цинк-пальцевыми нуклеазами для таргетирования локуса крысиного АроЕ. В Таблице 21 приведены обобщенные данные по геномной структуре локуса крысиного АроЕ. Позиции, приведенные в Таблице 21, взяли из конструкции 5.0 стандартной последовательности крысиного генома (ENSMBL). АроЕ находится на хромосоме 1 на цепи (-).
[00848]

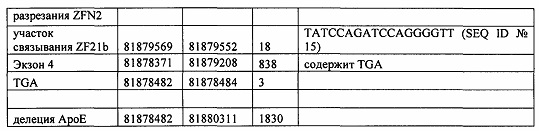
[00849] На Фигуре 11 приведено схематическое изображение локуса крысиного АроЕ, а серыми прямоугольниками обозначены участки разрезания ZFN1 и ZFN2. Участок разрезания ZFN1 находится в экзоне 3, а участок разрезания ZNF2 находится в интроне 3. Точные положения обоих участков ZFN приведены в Таблице 21. Геномные области, соответствующие 5' и 3' плечам гомологии (5 т.п.о. и 5,4 т.п.о., соответственно), обозначены темно-серыми прямоугольниками. Экзон 1 АроЕ является некодирующим и показан в виде неокрашенного прямоугольника, расположенного наиболее близко к 5' плечу гомологии. Три интрона в гене АроЕ обозначены в виде линий, а экзоны 2 и 3 содержат кодирующие области и показаны в виде заштрихованных пунктиром серых прямоугольников. Экзон 4 содержит как кодирующие, так и некодирующие последовательности, обозначенные серым пунктиром и неокрашенным прямоугольником.
[00850] Применяемый направляющий вектор был таким же, как и в Примере 3.2(а)(ii), и показан на Фигуре 20, а на Фигуре 21А приведена схема таргетирования локуса АроЕ в крысиных ЭС клетках при помощи цинк-пальцевых нуклеаз и направляющего вектора, проиллюстрированного на Фигуре 20. ZFN вносили в виде двух экспрессионных плазмид, по одной на каждую половинку пары ZFN. Использовали 20 мкг плазмид для ZFN1 и 20 мкг плазмид для ZFN2. ZFN были приобретены от Sigma. Экспрессией каждой ZFN управлял промотор CMV.
[00851] Направляющий вектор электропорировали в крысиные ЭС клетки, полученные в Примере 1, и высевали клетки на 15 см с 2х плотностью neoR ФЭМ в 2i + 10 мкМ ROCKi. Трансформированные крысиные ЭС клетки культивировали, отбирали и поддерживали, как описано в Примере 1.
[00852] Как показано в Таблице 22 и Таблице 44, проводили скрининг 384 колоний и получили 290 таргетированных клонов. Эффективность таргетирования составила 75,52%. Проводили инъекцию 2 клонов в бластоцисты, как описано в Примере 1. Было получено два клона, продуцирующих химеры, и один из клонов передавал направленную модификацию через зародышевую линию.
[00853] Кроме того, применение ZFN1 и ZFN2 привело к получению 8 биаллельных таргетированных клонов с эффективностью 2,08%.
[00854]

3.2.(b)(i): Направленная модификация локуса крысиного аполипопротеина Е (АроЕ) при помощи крупного направляющего вектора (LTC).
[00855] Таргетирование локуса АроЕ проводят при помощи крупного направляющего вектора (LTVEC), содержащего кассету lacZ-мышиный Prm1-Crei, фланкируемую 5' плечом гомологии к локусу АроЕ из около 45 т.п.о. и 3' плечом гомологии к локусу АроЕ из около 23 т.п.о. Фигура 22 иллюстрирует локус крысиного АроЕ, в котором локус АроЕ был разрушен вследствие 1,83 т.п.о. делеции и вставки гена lacZ и самоуничтожающейся кассеты, содержащей кассету mPrm1 1-Crei и селекционную кассету hUb-neo. Способы, применяемые в 3.2(a)(i), можно применять для внесения этого вектора в крысиные ЭС клетки.
Пример 3.2.(b)(ii). Таргетирование локуса крысиного АроЕ при помощи крупного направляющего вектора (LTVEC)
[00856] На Фигуре 22 приведено схематическое изображение локуса крысиного АроЕ и крупного направляющего вектора (LTVEC). На верхней схеме на Фигуре 22 показана геномная структура локуса крысиного АроЕ и геномные области, соответствующие 5' и 3' плечам гомологии (45 т.п.о. и 23 т.п.о., соответственно; темно-серые прямоугольники). Экзон 1 АроЕ является некодирующим и показан в виде неокрашенного прямоугольника, расположенного наиболее близко к 5' плечу гомологии. Три интрона в гене АроЕ обозначены в виде линий, а экзоны 2 и 3 содержат кодирующие области и показаны в виде заштрихованных пунктиром серых прямоугольников. Экзон 4 содержит как кодирующие, так и некодирующие последовательности, обозначенные серым пунктиром и неокрашенным прямоугольником.
[00857] На нижней схеме на Фигуре 22 показан LTVEC. 5' и 3' плечи гомологии (45 т.п.о. и 23 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. Направляющий вектор содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки), которая содержит ген Crei, функционально связанный с промотором мышиного Prm1, и кассету отбора по чувствительности к лекарственному препарату, содержащую ген устойчивости к неомицину, функционально связанный с промотором человеческого убиквитина. Crei содержит два экзона, кодирующих рекомбиназу Cre, которые разделены интроном (Crei) для предотвращения его экспрессии в прокариотической клетке. Смотрите, например, патент США 8697851 и опубликованную заявку на патент США 2013-0312129, в которых подробно описана самоуничтожающаяся кассета, и которые в полном объеме включены в данный документ посредством ссылки. Самоуничтожающуюся кассету можно удалять, применяя промотор мышиного Prm1, в частности, в мужских зародышевых клетках крыс F0.
[00858] LTVEC электропорировали в крысиные ЭС клетки, полученные в Примере 1, и высевали клетки на 15 см с 2х плотностью neoR ФЭМ в 2i + 10 мкМ ROCKi. Трансформированные крысиные ЭС клетки культивировали, отбирали и поддерживали, как описано в Примере 1.
[00859] Как показано в Таблице 44, проводили скрининг 288 колоний и получили 8 таргетированных клонов. Эффективность таргетирования составила 2,78%. Проводили инъекцию 3 клонов в эмбрион-хозяина на стадии бластоцисты, как описано в Примере 2, для получения химерных крыс (FO). Кроме того, был получен один биаллельный таргетированный клон с биаллельной эффективностью 0,35%.
3.2.(b)(iii). Таргетирование АроЕ у крыс при помощи крупного направляющего вектора (LTVEC) в комбинации с цинк-пальцевыми нуклеазами
[00860] LTVEC, применяемый в Примере 3.2.(b)(ii), применяли в комбинации с цинк-пальцевыми нуклеазами для таргетирования локуса крысиного АроЕ. В Таблице 21 приведены обобщенные данные по геномной структуре локуса крысиного АроЕ, а приведенные позиции были взяты из конструкции 5.0 стандартной последовательности крысиного генома (ENSMBL).
[00861] На Фигуре 23 приведено схематическое изображение локуса крысиного АроЕ и серыми прямоугольниками обозначены места разрезания ZFN1 и ZFN2. Участок разрезания ZFN1 находится в экзоне 3, а участок разрезания ZNF2 находится в интроне 3. Точные положения обоих участков ZFN приведены в Таблице 21. 5' и 3' плечи гомологии (45 т.п.о. и 23 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. Экзон 1 в гене АроЕ является некодирующим и показан в виде неокрашенного прямоугольника, расположенного наиболее близко к 5' плечу гомологии. Три интрона в гене АроЕ обозначены в виде линий. Экзоны 2 и 3 содержат кодирующие области и показаны в виде заштрихованных пунктиром серых прямоугольников. Экзон 4 содержит как кодирующие, так и некодирующие последовательности, обозначенные серым пунктиром и неокрашенным прямоугольником.
[00862] Применяемый LTVEC был таким же, как и в Примере 3.2(b)(ii), и показан на Фигуре 22. ZFN вносили в виде двух экспрессионных плазмид, по одной на каждую половинку пары ZFN. Использовали 20 мкг плазмид для ZFN1 и 20 мкг плазмид для ZFN2. ZFN были приобретены от Sigma. ZFN были приобретены от Sigma. Экспрессией каждой ZFN управлял промотор CMV.
[00863] Направляющий вектор электропорировали в крысиные ЭС клетки, полученные в Примере 1, и высевали клетки на 15 см с 2х плотностью neoR ФЭМ в 2i + 10 мкМ ROCKi. Трансформированные крысиные ЭС клетки культивировали, отбирали и поддерживали, как описано в Примере 1.
[00864] Как показано в Таблице 44, проводили скрининг 288 колоний и получили 16 таргетированных клонов. Эффективность таргетирования составила 5,56%. Проводили инъекцию одного клона в бластоцисты, как описано в Примере 2.
[00865] Кроме того, применение ZFN1 и ZFN2 привело к получению одного биаллельного таргетированного клона с эффективностью 0,35%.
3.2.(b)(iv). Таргетирование АроЕ у крыс при помощи крупного направляющего вектора (LTVEC) в комбинации с CRISPR/Cas9
[00866] LTVEC, применяемый в Примере 3.2.(b)(ii), применяли в комбинации с CRISPR/Cas9 для таргетирования локуса крысиного АроЕ. В Таблице 23 приведено сравнение результатов экспериментов, в которых АроЕ LTVEC применяли один для таргетирования локуса крысиного АроЕ или применяли в комбинации с CRISPR/Cas9 нуклеазой для таргетирования локуса крысиного АроЕ. В каждом эксперименте электропорированные клетки высевали при высокой плотности и подвергали отбору по чувствительности к лекарственному препарату, чтобы найти устойчивые к лекарственному препарату колонии. Устойчивые к лекарственному препарату колонии собирали и проводили скрининг в отношении направленной модификации методом анализа модификации аллеля (МОА), как описано в данном документе. В частности, 4×106 клеток электропорировали 2 мкг АроЕ LTVEC при напряжении 400 В, емкости 100 мкФ и сопротивлении 0. В последнем эксперименте также электропорировали 6 мкг экспрессионной плазмиды Cas9 и 3 мкг нРНК2 АроЕ или 3 мкг нРНК3 АроЕ. Отбор проводили, используя 75 мкг/мл G418. нРНК2 АроЕ имеет последовательность GCAGGCCCTGAACCGCTTCTTGG (SEQ ID №87) и нацелена на область из 67 п.о. 3' от начала экзона 3 крысиного АроЕ. нРНК3 АроЕ имеет последовательность CCTGCGCTGGGTGCAGACGCTTT (SEQ ID №88) и нацелена на область из 97 п.о. 3' от начала экзона 3 крысиного АроЕ (смотрите Фигуру 47). Как показано в Таблице 23, если в клетку вносили Cas9 и любую из нРНК вместе с АроЕ LTVEC, эффективность таргетирования возрастала (от 43% до 53% или 47%). Биаллельное таргетирование наблюдали в пяти колониях, таргетируемых АроЕ LTVEC в комбинации с нРНК2 или 3 АроЕ, но для одного АроЕ LTVEC биаллельной модификации не наблюдали.
[00867]
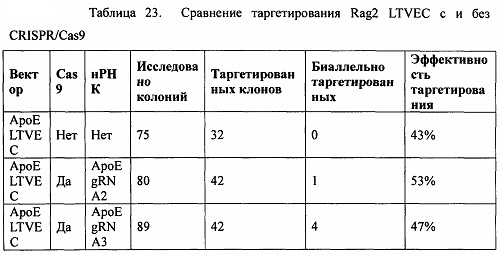
3.3(а): Таргетирование локуса крысиного рецептора интерлейкина-2 гамма (IL2r-γ)
[00868] Проводили таргетирование локуса крысиного рецептора интерлейкина-2 гамма (IL2r-γ или Il2rg), чтобы блокировать функцию IL2r-γ. IL2r-γ играет важную роль для сигнализации IL-2, IL-4, IL-7, IL-9, IL-15, IL-21, а мутации в IL2r-γ связаны с тяжелыми нарушениями в развитии Т-, В- и NK-клеток.
[00869] Таргетирование локуса IL2r-γ проводили при помощи направляющего вектора, содержащего кассету eGFP-hUb-neo, фланкируемую 5' и 3' плечами гомологии, гомологичными локусу IL2r-γ, как проиллюстрировано на Фигуре 24. Фигура 25 иллюстрирует геномную структуру локуса крысиного IL2r-γ, в которой локус IL2r-γ был разрушен вследствие 3,2 т.п.о. делеции. Таргетируемый локус IL2r-γ также содержит ген уЗФБ и самоуничтожающуюся кассету, содержащую Crei, функционально связанный с мышиным промотором протамина 1, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор hUb, функционально связанный с геном устойчивости к неомицину.
[00870] Определяли эффективность таргетирования в локусе IL2r-γ, a результаты приведены в Таблице 24. Линеаризованный вектор электропорировали в ЭСК крыс DA.2B и культивировали трансфицированные колонии, используя стандартные методы. Собирали отдельные колонии и проводили скрининг методом анализа потерянного аллеля (LOA).
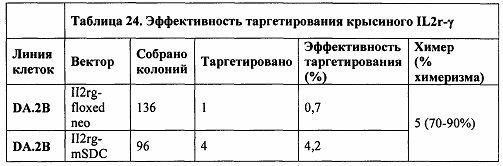
[00871] Осуществляли получение химер и трансмиссию зародышевой линии с применением клонов крысиных ЭСК с таргетированным IL2r-γ. Проводили микроинъекцию клонов крысиных ЭСК с таргетированным IL2r-γ в бластоцисты SD, которые затем переносили в организм псевдобеременных самок-реципиентов SD, используя стандартные методы. Химеры определяли по цвету шкуры; самцов химер F0 скрещивали с самками SD. Детенышей зародышевой линии F1 генотипировали в отношении наличия таргетированного аллеля IL2r-γ (Таблица 25). В другом эксперименте с микроинъецированием с клоном Il2rg-CG12 трансмиссию зародышевой линии также подтверждали по цвету шкуры и генотипированием.
[00872]
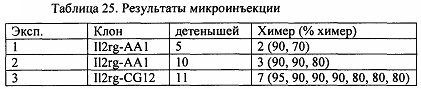
[00873] Дополнительно изучали фенотип химеры Il2rg-/Y #3. Мононуклеарные клетки периферической крови (МКПК) окрашивали антителами, которые распознают антигены в нескольких лимфоидных линиях дифференцировки. ЗФБ-положительные МКПК были выявлены у 2 химер, как показано на Фигуре 30. Кроме того, ЗФБ + клетки оказались негативными в отношении маркера Т-клеток CD3 (Фигура 29А) и в большинстве были негативными в отношении маркера В-клеток В220 и маркера NK-клеток CD161a (Фигура 29В и С, соответственно). МКПК, полученные от крысы дикого типа, использовали в качестве негативного контроля для экспрессии ЗФБ. Смотрите Фигуру 29D-F. Небольшие дважды положительные популяции согласуются с опубликованными данными по фенотипу мышей с выключенным Il2rg. Эти данные были получены от химерной крысы, которая содержит положительные в отношении рецептора IL2 гамма клетки, и это может усложнить анализ фенотипа. Также можно проводить анализ методом проточной цитометрии с популяциями клеток из костного мозга и селезенки для выявления соответствующих заболеваний в большом количестве лимфоцитов. Смотрите Mashimo et al. (2010) PLoS One 5(1): e8870.
3.3(b): Направленная модификация локуса крысиного рецептора интерлейкина-2 гамма (IL2r-γ)
[00874] Проводили таргетирование локуса крысиного рецептора интерлейкина-2 гамма (IL2r-γ), чтобы блокировать функцию IL2r-γ у крыс. Фигура 25 иллюстрирует геномную структуру локуса крысиного Il2rg (верхняя панель на Фигуре 25) и направляющий вектор, вносимый в локус (нижняя панель на Фигуре 25). В качестве репортера был выбран уЗФБ, чтобы иммунофенотип генетически модифицированных крыс можно было определять методом FACS. Самоуничтожающуюся кассету (hUb-Neo; Prm1-Cre) использовали для удаления кассеты отбора по чувствительности к лекарственному препарату и гена Cre, в частности, в мужских зародышевых клетках крысы F0. Кроме того, направляющий вектор был сконструирован так, чтобы удалять целую кодирующую область (около 3,2 т.п.о.) гена крысиного Il2rg.
[00875] Размер делеции в крысиных ЭСК подтверждали методом ПЦР с применением праймеров, специфических к локусу крысиного Il2rg. После микроинъекции таргетированных клонов в эмбрионы-хозяев на стадии бластоцист были получены химеры с высоким процентным содержанием. Эти химеры были отобраны для скрещивания. Чтобы определить, действует ли таргетирование так, как ожидалось, перед скрещиванием у химер брали периферическую кровь и анализировали фенотип иммунных клеток в периферической крови методом FACS. Как показано на Фигуре 30, ЗФБ-положительные клетки были выявлены в крови 2 из 3 исследуемых химер, а химерные крысы содержали менее 1% Т-клеток, менее 1% В-клеток и менее 1% NK-клеток, которые были положительными в отношении ЗФБ (т.е. KO-клетки Il2rg) (Фигура 29А-С).
3.4(a)(i). Таргетирование локуса Rag2 у крыс при помощи крупного направляющего вектора (LTVEC)
[00876] В Таблице 26 приведены обобщенные данные по геномной структуре локуса крысиного Rag2, а приведенные позиции были взяты из конструкции 5.0 стандартной последовательности крысиного генома (ENSMBL). Rag2 находится в хромосоме 3 на (+) цепи.
[00877]

На Фигуре 26 приведено схематическое изображение локуса крысиного Rag2 и крупного направляющего вектора (LTVEC). LTVEC составляет 140 т.п.о. и нацелен на приблизительно 5,7 т.п.о. часть локуса крысиного Rag2 для создания делеции. На верхней схеме на Фигуре 26 показана геномная структура локуса крысиного
[00878] и геномных областей, соответствующих 5' и 3' плечам гомологии (48 т.п.о. и 84 т.п.о., соответственно; темно-серые прямоугольники). Rag2 содержит один экзон, обозначенный пунктирной серой штриховкой.
[00879] На нижней схеме на Фигуре 26 представлен LTVEC. 5' и 3' плечи гомологии (48 т.п.о. и 84 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. LTVEC содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки). Самоуничтожающаяся кассета содержит промотор мышиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую промотор человеческого убиквитина, функционально связанный с геном устойчивости к неомицину. Была создана другая версия LTVEC, в которой ген устойчивости к неомицину был замещен геном устойчивости к гигромицину, чтобы сделать возможным повторное таргетирование крысиных ЭС клеток с таргетированным Il2rg. Crei содержит два экзона, кодирующих рекомбиназу Cre, которые разделены интроном (Crei) для предотвращения его экспрессии в прокариотической клетке. Смотрите, например, патент США 8697851 и опубликованную заявку на патент США 2013-0312129, в которых подробно описана самоуничтожающаяся кассета, и которые в полном объеме включены в данный документ посредством ссылки. Самоуничтожающуюся кассету можно удалять, применяя промотор мышиного Prm1, в частности, в мужских зародышевых клетках крыс F0.
[00880] LTVEC электропорировали в крысиные ЭС клетки, полученные в Примере 1, и высевали клетки на 15 см с 2х плотностью neoR ФЭМ в 2i + 10 мкМ ROCKi. Трансформированные крысиные ЭС клетки культивировали и поддерживали, как описано в Примере 1.
[00881] Проводили скрининг колоний, как описано в другом месте данного документа, и получали таргетированные клоны. Проводили инъекцию таргетированных клонов в эмбрион-хозяина, как описано в другом месте данного документа, для получения крыс F0.
3.4(a)(ii). Таргетирование локуса Rag2 у крыс при помощи крупного направляющего вектора (LTVEC) и CRISPR/Cas9
[00882] В Таблице 27 приведено сравнение результатов экспериментов, в которых Rag2 LTVEC, содержащий ген устойчивости к гигромицину (смотрите Фигуру 48), применяли один для таргетирования локуса крысиного Rag2 или применяли в комбинации с CRISPR/Cas9 нуклеазой для таргетирования локуса крысиного Rag2. В каждом эксперименте электропорированные клетки высевали при высокой плотности и подвергали отбору по чувствительности к лекарственному препарату, чтобы найти устойчивые к лекарственному препарату колонии. Устойчивые к лекарственному препарату колонии собирали и проводили скрининг в отношении направленной модификации методом анализа модификации аллеля (МОА), как описано в данном документе. В частности, 4×106 клеток электропорировали 2 мкг Rag2 LTVEC при напряжении 400 В, емкости 100 мкФ и сопротивлении 0. В последнем эксперименте также электропорировали 6 мкг экспрессионной плазмиды Cas9 и 3 мкг нРНК1 Rag2 или 3 мкг нРНК4 Rag2. Отбор проводили, используя 75 мкг/мл G418. нРНК1 Rag2 имеет последовательность CCAGCTACTTGCTCGTACAA (SEQ ID №89) и нацелена на область из 219 п.о. 3' от начала стартового кодона крысиного Rag2 (ATG). нРНК4 Rag2 имеет последовательность CCCCTCAGATTCACGTGCGT (SEQ ID №90) и нацелена на область из 12 п.о. 3' от стоп-кодона крысиного Rag2 (TAG) (смотрите Фигуру 48). Как показано в Таблице 27, если в клетку вносили Cas9 и любую из нРНК вместе с Rag2 LTVEC, эффективность таргетирования возрастала (от 0 до 10% или 38%). Биаллельное таргетирование наблюдали в одной колонии.
[00883]


3.4. (b)(i): Таргетирование локуса Rag1 и Rag 2 у крыс
[00884] На Фигуре 27 приведена геномная структура локуса крысиного Rag1/Rag2. CDS обозначает кодирующую последовательность, а серые прямоугольники представляют экзоны. Rag2 находится на «плюс»-цепи с правым направлением транскрипции. Rag1 находится на «минус»-цепи с левым направлением транскрипции. М.п.о. = миллион пар оснований.
[00885] В Таблице 28 приведены обобщенные данные по геномной структуре локуса крысиного Rag2 и локуса крысиного Rag1, а приведенные позиции были взяты из конструкции 5.0 стандартной последовательности крысиного генома (ENSMBL). Rag1 находится в хромосоме 3 на (-) цепи.
[00886]
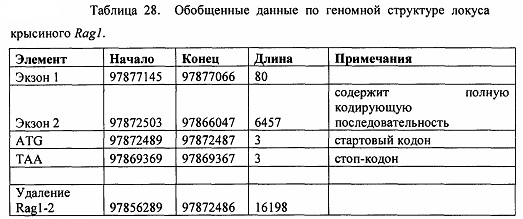
[00887] На Фигуре 28 приведено схематическое изображение локуса крысиного Rag2 и Rag1 и крупного направляющего вектора (LTVEC). LTVEC составляет около 70 т.п.о. и нацелен на приблизительно 16,6 т.п.о. крысиный геномный локус, содержащий локусы Rag1 и Rag2, для создания делеции. На верхней схеме на Фигуре 28 показана геномная структура локусов Rag1 и Rag2 и геномных областей, соответствующих 5' и 3' плечам гомологии (48 т.п.о. и 15 т.п.о., соответственно; темно-серые прямоугольники). Каждый из Rag1 и Rag2 содержит один экзон, обозначенный пунктирной серой штриховкой. На нижней схеме на Фигуре 28 представлен LTVEC. 5' и 3' плечи гомологии (48 т.п.о. и 15 т.п.о., соответственно) обозначены темно-серыми прямоугольниками. LTVEC содержит репортерный ген (lacZ) и самоуничтожающуюся кассету, фланкируемую участками loxP (неокрашенные стрелки). Самоуничтожающаяся кассета содержит промотор крысиного Prm1, функционально связанный с геном Crei, и кассету отбора по чувствительности к лекарственному препарату, содержащую человеческий промотор убиквитина, функционально связанный с геном устойчивости к неомицину. Была создана другая версия LTVEC, в которой ген устойчивости к неомицину был замещен геном устойчивости к гигромицину, чтобы сделать возможным повторное таргетирование крысиных ЭС клеток с таргетированным Il2rg. Crei содержит два экзона, кодирующих рекомбиназу Cre, которые разделены интроном (Crei) для предотвращения его экспрессии в прокариотической клетке. Смотрите, например, патент США 8697851 и опубликованную заявку на патент США 2013-0312129, в которых подробно описана самоуничтожающаяся кассета, и которые в полном объеме включены в данный документ посредством ссылки. Самоуничтожающуюся кассету можно удалять из мужских зародышевых клеток крыс F0, применяя промотор крысиного Prm1, который управляет экспрессией Crei, в частности, в мужских зародышевых клетках.
[00888] LTVEC электропорировали в крысиные ЭС клетки, полученные в Примере 1, и высевали клетки на 15 см с 2х плотностью neoR ФЭМ в 2i + 10 мкМ ROCKi. Трансформированные крысиные ЭС клетки культивировали и поддерживали, как описано в Примере 1.
[00889] Проводили скрининг колоний, как описано в другом месте данного документа, и получали таргетированные клоны. Проводили инъекцию таргетированных клонов в эмбрион-хозяина, как описано в другом месте данного документа, для получения крыс F0.
3.4.(b)(ii): Повторное таргетирование локуса Rag1 и Rag2 в крысиных ЭС клетках с уже таргетированным локусом Il2rg
[00890] Получали LTVEC согласно Фигуре 50 для таргетирования локусов Rag1 и Rag2 для создания делеции. Общая длина LTVEC составляла 72 т.п.о. LTVEC электропорировали в крысиные ЭС клетки, которые уже были таргетированы для удалений локуса Il2rg, как описано в Примере 3.3. В частности, крысиные ЭС клетки принадлежали клону Il2rg-CG12, для которого была подтверждена трансмиссия зародышевой линии в Примере 3.3(а). Трансформированные крысиные ЭС клетки культивировали и поддерживали, как описано в Примере 1. Проводили скрининг клонов с двойным таргетированием, как описано в другом месте данного документа, и получали таргетированные клоны. Проводили повторное таргетирование клеток Il2rg-CG12 с эффективностью 85%, при этом мутации Il2rg все еще присутствовали в таргетированных клонах. Электропорацию проводили, как описано в другом месте данного документа, а отбор по чувствительности к антибиотику проводили, используя 1,5 мкг/мл пуромицина. Затем проводили инъекцию таргетированных клонов в эмбрион-хозяина, как описано в другом месте данного документа, для получения крыс F0. Повторное таргетирование имеет преимущество, так как оно занимает меньше времени, чем скрещивание Rag1/Rag2-таргетированных крыс с Il2rg-таргетированными крысами.
Пример 4. Гуманизация
4.1. Гуманизация крысиных геномных локусов
[00891] Гуманизацию крысиных геномных локусов проводят, используя описанные в данном документе крысиные ЭС клетки, которые способны сохранять свою плюрипотентность после одной или более электропораций т vitro и способны передавать направленные генетические модификации последующим поколениям. Кроме того, чтобы преодолеть ограничения, связанные с неспособностью плазмид вмещать крупные фрагменты геномной ДНК, и преодолеть низкую эффективность внесения направленной генетической модификации в эндогенный локус в крысиных ЭС клетках, осуществляют одну или более направленных генетических модификаций в бактериях, например, Е.coli, посредством применения бактериальной гомологичной рекомбинации (БГР) и крупного направляющего вектора (LTVEC). Описанный в данном документе LTVEC, содержит, например, крупный фрагмент эндогенной крысиной геномной последовательности с одной или более модификациями или содержит экзогенную нуклеиновую кислоту (например, гомологичную или ортологичную человеческую нуклеиновую кислоту), фланкируемую крысиными плечами гомологии, комплементарными конкретным геномным областям.
4.2. Гуманизация локусов крысиного иммуноглобулина
[00892] Гуманизацию эндогенного крысиного локуса тяжелой цепи иммуноглобулина проводят путем удаления одной или более нуклеотидных последовательностей тяжелой цепи крысиного иммуноглобулина (например, одного или более эндогенных генных сегментов VH, одного или более человеческих генных сегментов D и одного или более человеческих генных сегментов JH); и внесения в модифицированный локус иммуноглобулина направляющего вектора, например, крупного направляющего вектора (LTVEC), содержащего: (i) одну или более неперестроенных нуклеотидных последовательностей человеческой вариабельной области (например, один или более человеческих генных сегментов VH, один или более человеческих генных сегментов D и один или более человеческих генных сегментов JH) или одну или более перестроенных нуклеотидных последовательностей человеческой вариабельной области (например, один или более перестроенных человеческих генных сегментов V-D-J); (ii) селекционную кассету (например, ген устойчивости к неомицину, фланкируемый участками loxP); и (iii) 5' и 3' крысиные плечи гомологии
[00893] Вкратце, один или более эндогенных генных сегментов вариабельной области тяжелой цепи крысиного иммуноглобулина (т.е. один или более генных сегментов VH, один или более человеческих генных сегментов D и один или более человеческих генных сегментов JH) в крысином БИХ клоне удаляют или инактивируют путем таргетирования эндогенного крысиного локуса тяжелой цепи иммуноглобулина при помощи селекционной кассеты, фланкируемой крысиными плечами гомологии. Конкретнее, конструируют направляющий вектор, содержащий селекционную кассету (например, ген устойчивости к неомицину, фланкируемый участками loxP), фланкируемую 5' и 3' крысиными плечами гомологии, которые комплементарны целевым крысиным геномным последовательностям (например, вышележащим и нижележащим крысиным последовательностям геномной ДНК, включающим один или более генных сегментов VH, один или более человеческих генных сегментов D и один или более человеческих генных сегментов JH).
[00894] После этого отбирают бактериальные клетки, содержащие крупный фрагмент крысиной геномной ДНК, содержащий крысиный локус, тяжелой цепи иммуноглобулина, и вносят с плазмидой (например, pABG), кодирующей рекомбиназу, функционально связанную с временно индуцибельным промотором. Затем направляющий вектор с вышеприведенной конструкцией вносят в рекомбинационно-компетентные бактериальные клетки. После электропорации бактериальные клетки обрабатывают индуктором (например, арабинозидом), чтобы инициировать гомологичную рекомбинацию между направляющим вектором и целевой крысиной геномной последовательностью в БИХ клоне. Трансформированные клетки высевают при высокой плотности и подвергают отбору по чувствительности к лекарственному препарату, чтобы найти устойчивые к лекарственному препарату колонии. Устойчивые к лекарственному препарату колонии собирают и проводят скрининг в отношении направленной модификации.
[00895] Чтобы облегчить выявление направленной генетической модификации, применяют высокопроизводительный количественный анализ, а именно анализ модификации аллеля (МОА), который позволяет проводить крупномасштабный скрининг модифицированного(ых) аллеля(ей) в родительской хромосоме после генетической модификации. Анализ МОА можно проводить при помощи различных аналитических методов, включая, но не ограничиваясь этим, количественную ПЦР, например, ПЦР в режиме реального времени (кПЦР). Например, ПЦР в режиме реального времени включает применение первой группы праймеров, которая распознает целевой локус, и второй группы праймеров, которая распознает нецелевой контрольный локус. Кроме того, группа праймеров может содержать флуоресцентный зонд, который распознает амплифицированную последовательность. В альтернативном варианте количественный анализ можно проводить при помощи различных аналитических методов, включая, но не ограничиваясь этим, флуоресцентную гибридизацию in situ (FISH), сравнительную геномную гибридизацию, изотермическую амплификацию ДНК, количественную гибридизацию с иммобилизованным(и) зондом(ами). Invader Probes®, MMP assays®, TaqMan® Molecular Beacon и методом зондов Eclipse™. (Смотрите, например, US 2005/0144655, которая в полном объеме включена в данный документ посредством ссылки).
[00896] Затем бактериальные клетки, содержащие модифицированный крысиный БИХ клон, т.е. БИХ клон, содержащий крысиную последовательность геномной ДНК, в которой один или более эндогенных генных сегментов вариабельной области тяжелой цепи (генных сегментов VH, D и/или JH) были удалены или инактивированы, электропорируют вместе с крупным направляющим вектором (LTVEC), содержащим: (i) одну или более неперестроенных нуклеотидных последовательностей человеческой вариабельной области (например, один или более неперестроенных человеческих генных сегментов VH, один или более человеческих генных сегментов D и один или более человеческих генных сегментов JH) или одну или более перестроенных нуклеотидных последовательностей человеческой вариабельной области (например, один или более перестроенных человеческих генных сегментов V-D-J).
[00897] Инициацию гомологичной рекомбинации в бактериальных клетках и отбор положительных клонов проводят так, как описано выше. Неперестроенные или перестроенные нуклеотидные последовательности вариабельной области тяжелой цепи человеческого иммуноглобулина при встраивании в эндогенный локус тяжелой цепи иммуноглобулина становятся функционально связанными с эндогенной нуклеотидной последовательностью константной области тяжелой цепи крысиного иммуноглобулина. В альтернативном варианте эндогенный крысиный локус константной области тяжелой цепи можно инактивировать, например, путем удаления одного или более генных сегментов крысиной константной области тяжелой цепи (СН) из эндогенного локуса константной области тяжелой цепи и замещения нуклеотидной последовательностью человеческой константной области тяжелой цепи.
[00898] Аналогично, гуманизацию эндогенного локуса κ или λ легкой цепи крысиного иммуноглобулина проводят путем удаления одной или более эндогенных крысиных нуклеотидных последовательностей вариабельной области κ и/или λ легкой цепи иммуноглобулина (например, одного или более эндогенных крысиных генных сегментов Vκ и одного или более эндогенных крысиных генных сегментов Jκ); и таргетирования модифицированного локуса легкой цепи иммуноглобулина при помощи направляющего вектора, например, крупного направляющего вектора (LTVEC), содержащего: (i) одну или более неперестроенных нуклеотидных последовательностей человеческой вариабельной области легкой цепи иммуноглобулина (например, один или более человеческих генных сегментов Vκ и один или более человеческих генных сегментов Jκ) или одну или более перестроенных нуклеотидных последовательностей человеческой вариабельной области (например, один или более перестроенных человеческих генных сегментов Vκ-Jκ); (ii) селекционную кассету (например, ген устойчивости к неомицину, фланкируемый участками loxP); и (iii) 5' и 3' крысиные плечи гомологии.
[00899] Неперестроенные или перестроенные нуклеотидные последовательности вариабельной области легкой цепи человеческого иммуноглобулина при встраивании в эндогенный локус легкой цепи иммуноглобулина становятся функционально связанными с эндогенной нуклеотидной последовательностью константной области легкой цепи крысиного иммуноглобулина.
[00900] LTVEC, получаемый, таким образом, в бактериальных клетках, содержит, например, нуклеотидную вставку, которая содержит гуманизированный локус тяжелой цепи или легкой цепи крысиного иммуноглобулина, в котором один или более эндогенных генных сегментов крысиной вариабельной области тяжелой или легкой цепи были замещены одним или более генными сегментами человеческой вариабельной области тяжелой или легкой цепи; и крысиные плечи гомологии (например, например, в диапазоне от 5 т.п.о. до 150 т.п.о.), комплементарные конкретным целевым геномным последовательностям. Затем LTVEC, содержащий вышеописанную генетическую модификацию, линеаризуют и электропорируют в крысиные ЭС клетки. Электропорированные крысиные ЭС клетки высевают при высокой плотности, чтобы выбрать устойчивые к лекарственному препарату ЭС клетки, содержащие направляющий вектор. Процесс отбора по чувствительности к лекарственному препарату приводит к удалению большинства высеянных клеток (~99%), оставляя отдельные колонии, каждая из которых является клоном, полученным от одной клетки. Среди оставшихся клеток большинство клеток (~80-100%) содержат направляющий вектор, интегрированный в случайный участок генома. Следовательно, колонии собирают по отдельности и проводят генотипирование для выявления крысиных ЭС клеток, содержащих направляющий вектор в правильном участке генома (например, применяя анализ модификации аллелей (МОА), описанный выше).
[00901] Чтобы повысить эффективность направленной генетической модификации, крысиные ЭС клетки электропорируют экспрессионными векторами (или мРНК), которые экспрессируют ZFN 1 и 2 (или TALEN 1 и 2) вместе с LTVEC. Плечи гомологии направляющего вектора находятся за пределами целевого участка ZFN, следовательно, направляющий вектор не расщепляется ZFN. Создаваемый ZFN двухцепочечный разрыв стимулирует направляемую гомологией репарацию (НГР), которая в ином случае обеспечивает очень небольшой процент репараций, обычно происходящих в клетках млекопитающих (по сравнению с негомологичным соединением концов; НГСК).
[00902] В альтернативном варианте CRISPR-ассоциированную нуклеазу типа II (например, Cas9), направляющую РНК (включая CRISPR-РНК (cr-РНК) и транс-активирующую РНК CRISPR (tracrРНК)), описанные в данном документе, можно вносить в бактериальные клетки вместе с LTVEC для повышения эффективности гомологичной рекомбинации в целевом геномном локусе. Электропорированные клетки высевают при высокой плотности и подвергают отбору по чувствительности к лекарственному препарату, чтобы найти устойчивые к лекарственному препарату колонии. Устойчивые к лекарственному препарату колонии собирают и проводят скрининг в отношении направленной модификации, применяя описанный в данном документе анализ модификации аллеля (МОА). После этих процедур можно достичь улучшения эффективности таргетирования. Например, величина улучшения может быть небольшой (например, улучшение от 10% до 15%) или большой (например, улучшение от 10% до 80%).
[00903] Затем отобранные крысиные ЭС клетки, содержащие направленную генетическую модификацию, вносят в крысиный эмбрион-хозяина, например, находящийся на стадии пре-морулы или бластоцисты крысиный эмбрион, и имплантируют в матку суррогатной матери, чтобы получить крысу-основательницу (крысу F0). После этого крысу-основательницу скрещивают с крысой дикого типа для получения потомства F1, гетерозиготного в отношении генетической модификации. Путем спаривания гетерозиготных крыс F1 можно получить потомство, гомозиготное в отношении генетической модификации.
4.3(а). Замещение крысиного IL2rg человеческим рецептором IL2 гамма
[00904] В Таблице 29 приведены обобщенные данные по геномной структуре локуса крысиного рецептора интерлейкина-2 гамма, а приведенные позиции были взяты из конструкции 5.0 стандартной последовательности крысиного генома (ENSMBL). Il2rg находится в Х-хромосоме на (-) цепи.
[00905]

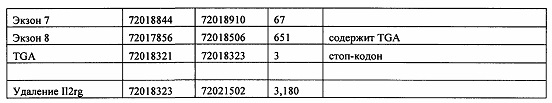
[00906] На нижней схеме на Фигуре 25 приведен направляющий вектор для создания 3,2 т.п.о. делеции в Il2rg. Направляющий вектор содержит репортерные ген (уЗФБ), функционально связанный с эндогенным промотором и самоуничтожающейся кассетой, фланкируемой участками loxP (неокрашенные стрелки). Самоуничтожающаяся кассета содержит ген Crei, функционально связанный с промотором мышиного Prm1, и селекционную кассету, содержащую ген устойчивости к неомицину, функционально связанный с промотором человеческого убиквитина.
[00907] Ген Crei содержит два экзона, кодирующих рекомбиназу Cre, которые разделены интроном (Crei) для предотвращения его экспрессии в прокариотической клетке. Смотрите, например, патент США 8697851 и опубликованную заявку на патент США 2013-0312129, в которых подробно описана самоуничтожающаяся кассета, и которые в полном объеме включены в данный документ посредством ссылки. Экспрессионную кассету Cre и самоуничтожающуюся кассету можно удалять, применяя промотор мышиного Prm1, в частности, в мужских зародышевых клетках крыс F0. Направляющий вектор электропорировали в крысиные ЭС клетки, полученные в Примере 1, и высевали клетки на 15 см с 2х плотностью устойчивых к неомицину ФЭМ в 2i + 10 мкМ ROCKi. Трансформированные крысиные ЭС клетки культивировали, отбирали и поддерживали, как описано в Примере 1.
[00908] Конструировали плазмидный направляющий вектор для замещения полноразмерной кодирующей области крысиного рецептора интерлейкина-2 гамма полноразмерной кодирующей областью человеческого рецептора интерлейкина-2 гамма, как показано на Фигуре 31. Направляющий вектор электропорировали в крысиные ЭС клетки, полученные в Примере 1, и высевали клетки на 15 см с 2х плотностью устойчивых к неомицину ФЭМ в 2i + 10 мкМ ROCKi. В частности, 4×106 клеток электропорировали 2 мкг полноразмерного вектора гуманизации Il2rg при напряжении 400 В, емкости 100 мкФ и сопротивлении 0. Отбор проводили, используя 75 мкг/мл G418. Трансформированные крысиные ЭС клетки культивировали, отбирали и поддерживали, как описано в Примере 1.
[00909] Как показано в Таблице 44, проводили скрининг 168 колоний и получили 6 таргетированных клонов. Эффективность таргетирования составила 3,57%. Проводили инъекцию одного клона в бластоцисты, как описано в Примере 1, и был получен один клон, продуцирующий химеры.
[00910] Клоны инъецировали в бластоцисты, как описано в данном документе в Примере 1. Получали клоны, продуцирующие химерных крыс F0. Бластоцисты переносили в организм псевдобеременных самок-реципиентов, используя стандартные методы, и получали химерных крыс F0. Получали крыс F0, которые передают направленную модификацию через зародышевую линию.
4.3(b)(i). Замещение крысиного эктодомена IL2rg человеческим эктодоменом IL2rg
[00911] Полноразмерная гуманизация рецептора IL 2 гамма имеет преимущество, так как крысы, имеющие такой модифицированный локус, будут вырабатывать человеческий Il2rg; и это позволит выявлять человеческий Il2rg у крыс при помощи антител, специфических к человеческому Il2rg.
[00912] Эктогуманизация (т.е. замещение крысиного эктодомена Il2rg человеческим эктодоменом Il2rg) приведет к получению полипептида Il2rg, который будет связывать человеческие лиганды Il2rg, но так как цитоплазматический домен остается крысиным, эктогуманизированная форма Il2rg будет также взаимодействовать с крысиным сигнальным аппаратом. На Фигуре 33 приведено выравнивание последовательностей белка человеческого IL-2rg (SEQ ID №20; NP_000197.1); белка крысиного IL-2rg (SEQ ID №21; NP_543165.1); и химерного белка IL-2rg (SEQ ID №22), содержащего эктодомен человеческого IL-2rg, слитый с остатком белка крысиного IL-2rg. Место соединения человеческого и крысиного IL-2rg обозначено вертикальной линией.
[00913] В Таблице 30 приведены обобщенные данные по геномной структуре локуса крысиного рецептора интерлейкина-2 гамма, а приведенные позиции были взяты из конструкции 5.0 стандартной последовательности крысиного генома (ENSMBL). Il2rg находится в Х-хромосоме на (-) цепи. Дополнительно обозначена позиция эктодомена Il2rg.
[00914]

[00915] Конструировали плазмидный направляющий вектор для замещения полноразмерной кодирующей области крысиного эктодомена рецептора интерлейкина-2 гамма человеческим эктодоменом, как показано на Фигуре 32. Направляющий вектор электропорировали в крысиные ЭС клетки, полученные в Примере 1, и высевали клетки на 15 см с 2х плотностью устойчивых к неомицину ФЭМ в 2i + 10 мкМ ROCKi. Трансформированные крысиные ЭС клетки культивировали, отбирали и поддерживали, как описано в Примере 1.
[00916] Как показано в Таблице 44, проводили скрининг 192 колоний и получили 13 таргетированных клонов. Эффективность таргетирования составила 6,77%.
[00917] Клоны инъецировали в бластоцисты, как описано в данном документе в Примере 1, и получили два клона, продуцирующие химерных крыс. Получали клоны, продуцирующие крыс F0. Получали крыс F0, которые передают направленную модификацию через зародышевую линию.
4.3(b)(ii). Замещение крысиного эктодомена IL2rg человеческим эктодоменом IL2rg при помощи плазмиды в комбинации с CRISPR/Cas9
[00918] В Таблице 31 приведено сравнение результатов экспериментов, в которых вектор с гуманизированным эктодоменом Il2rg, показанный на Фигуре 32, применяли один для таргетирования локуса крысиного Il2rg или применяли в комбинации с CRISPR/Cas9 нуклеазой для таргетирования локуса крысиного Il2rg. В каждом эксперименте электропорированные клетки высевали при высокой плотности и подвергали отбору по чувствительности к лекарственному препарату, чтобы найти устойчивые к лекарственному препарату колонии. Устойчивые к лекарственному препарату колонии собирали и проводили скрининг в отношении направленной модификации методом анализа модификации аллеля (МОА), как описано в данном документе. В частности, 4×106 клеток электропорировали 2 мкг вектора с гуманизированным эктодоменом Il2rg при напряжении 400 В, емкости 100 мкФ и сопротивлении 0. В последнем эксперименте также электропорировали 6 мкг экспрессионной плазмиды Cas9 и 3 мкг нРНК2 Il2rg или 3 мкг нРНК4 Il2rg. Отбор проводили, используя 75 мкг/мл G418. нРНК2 Il2rg имеет последовательность GAAGCTCTTTCTATACAATCTGG (SEQ ID №91) и нацелена на область из 190 п.о. 3' от экзона 1 крысиного Il2rg. нРНК4 Il2rg имеет последовательность CCCCCGAAAGGAGGAGCCCTAGG (SEQ ID №92) и нацелена на область из 80 п.о. 5' от стоп-кодона крысиного Il2rg (TGA) (смотрите Фигуру 49).
[00919]


4.4(а). Усиленное таргетирование эндонуклеазами CRISPR/Cas9 с большими делециями генов отличного от человека животного с одновременным замещением генами человека
[00920] Новые разработанные лекарственные препараты против человеческих заболеваний, такие как полностью человеческие антитела, часто являются высокоспецифическими в отношении своих мишеней в человеческих клетках и тканях и не распознают гомологичные мишени в организме грызунов. Такой высокий уровень избирательности делает невозможным исследование эффективности и механизма действия лекарственных препаратов на грызунах перед первым применением на людях.
[00921] Очень эффективным решением этой проблемы является создание генетически модифицированной мыши или крысы, у которой человеческий ген, кодирующий мишень лекарственного препарата, замещает гомолог грызуна. Одним из способов создания такого модифицированного аллеля у грызуна является удаление гена грызуна в эмбриональной стволовой (ЭС) клетке и вставка человеческого гена точно в удаленный локус на втором этапе модификации. Затем ЭС клетки инъецируют в эмбрион грызуна и имплантируют в матку суррогатной матери-грызуна, которая впоследствии производит генетически модифицированных детенышей, которые несут гуманизированный аллель.
[00922] Более эффективным способом создания гуманизированной генной модификации является применение крупного направляющего вектора (LTVEC), который управляет одновременным удалением гена грызуна и замещением его человеческим аналогом. При помощи методов генетической инженерии VELOCIGENE® можно осуществлять такую одноэтапную гуманизацию с относительно высокой эффективностью, если делеция гена грызуна и вставка гена человека не превышают около 20 тысяч пар оснований (т.п.о.). Более крупные одноэтапные гуманизации, приводящие к удалению и замещению более чем 100 т.п.о., возможны при помощи LTVEC и методов генетической инженерии, таких как методы генетической инженерии VELOCIGENE®, но вследствие снижения эффективности таргетирования, часто имеющих место при очень крупных модификациях, успешный результат часто требует скрининга от сотен до тысяч клонов ЭС клеток для обнаружения той, которая несет необходимую генетическую модификацию.
[00923] Для улучшения эффективности крупных гуманизации нами были разработаны способы, в которых комбинируется таргетирование генов при помощи LTVEC с направляемыми РНК коротких палиндромных повторов, регулярно расположенных группами, эндонуклеазами Cas9 (CRISPR/Cas9). CRISPR/Cas9 нуклеазы представляют собой рибонуклеопротеиновые ферменты, состоящие из бактериальной ДНК-эндонуклеазы Cas9, связанной с РНК CRISPR, которая направляет Cas9 для расщепления конкретной последовательности ДНК путем Уотсон-Криковского спаривания между направляющей РНК и одной нитью целевой ДНК. Вследствие простоты механизма нацеливания нетрудно конструировать эндонуклеазы CRISPR/Cas9, которые создают двухцепочечный разрыв вблизи любого геномного локуса. Двухцепочечные разрывы индуцируют клеточную геномную репарацию путем негомологичного соединения концов (НГСК), которое подвержено ошибкам и часто приводит к делециям и вставкам в участке двухцепочечного разрыва. Альтернативным механизмом репарации двухцепочечного разрыва является направляемая гомологией репарация (НГР), в которой эндогенный или экзогенный кусок ДНК, который обладает идентичностью или сходством последовательностей с поврежденным участком, органично чинит поврежденные концы посредством действия клеточного аппарата гомологичной рекомбинации. НГР может приводить к идеальной репарации, которая сохраняет оригинальную последовательность в участке повреждения, или ее можно применять для управления сконструированной модификацией, такой как удаление, вставка или замещение последовательности на участке двухцепочечного разрыва. CRISPR/Cas9 могут сильно повышать скорость предусмотренных актов НГР путем управления точными двухцепочечными расщеплениями в участках, предназначенных для генетических модификаций.
[00924] Для осуществления точного одноэтапного удаления всего или части гена грызуна и одновременного замещения всем или частью его человеческого гомолога мы вносили путем электропорации в ЭС клетки грызунов три молекулы нуклеиновой кислоты: (1) LTVEC; (2) плазмиду или мРНК, кодирующую эндонуклеазу Cas9; и (3) плазмиду, кодирующую одиночную направляющую РНК (онРНК) CRISPR, или саму онРНК. LTVEC, содержащий весь или часть человеческого гена, который кодирует генный продукт (белок или РНК), фланкируемый плечами гомологии ДНК грызуна, сконструирован для управления актом ГР, которая удаляет ген грызуна и вставляет человеческий ген. Гуманизирующий LTVEC также несет кассету отбора по чувствительности к лекарственному препарату, которая управляет экспрессией фермента (например, неомицин фосфотрансферазы), который придает устойчивость к антибиотику (например, G418). ЭС клетки, которые поглотили LTVEC и включили его в свой геном, были способны расти и формировать колонии в чашке Петри в среде для роста, содержащей антибиотик. Так как мы вносили в от 500 до 1000 раз больше CRISPR/Cas9-кодирующих нуклеиновых молекул, чем молекул LTVEC, большинство LTVEC-содержащих устойчивых к лекарственному препарату колоний также содержали, по меньшей мере временно, компоненты CRISPR/Cas9. Мы собирали устойчивые к лекарственному препарату колонии и проводили их скрининг методом потери аллеля (Valenzuela, D. et al. (2003) High-throughput engineering of the mouse genome coupled with high-resolution expression analysis, Nature Biotech. 21: 652-660; Frendewey, D. et al. (2010) The loss-of-allele assay for ES cell screening and mouse genotyping, Methods Enzymol. 476: 295-307; в полном объеме включенные в данный документ посредством ссылки) для выявления клонов, которые содержали правильно таргетированный гуманизированный аллель.
[00925] В одном конкретном эксперименте конструировали LTVEC для создания 68 т.п.о. удаления гена мышиного Lrp5 (родственный рецептору липопротеинов низкой плотности белок 5) и одновременного замещения 91 т.п.о. фрагментом гомологичного гена человеческого LRP5 (Фигура 34). LTVEC содержал 91 т.п.о. фрагмент гена человеческого LRP5, фланкируемый плечами гомологии, содержащими 7 т.п.о. и 33 т.п.о. геномной ДНК, полученной из частей локуса мышиного Lrp5, которые фланкируют 68 т.п.о. последовательность мышиного гена Lrp5, предназначенного для удаления. В отдельных экспериментах мы комбинировали предназначенный для гуманизации Lrp5 LTVEC с плазмидой, кодирующей Cas9, и второй плазмидой, кодирующей одну из восьми онРНК (gA, gB, gB2, gC, gD, gE2, gE, gF), сконструированных для создания двухцепочечных разрывов в области гена мышиного Lrp5, предназначенного для удаления. онРНК были сконструированы, чтобы избежать распознавания любой последовательности во вставленной части гена человеческого LRP5.
[00926] Результаты гуманизации гена Lrp5 при помощи CRISPR/Cas9 показаны в Таблице 32. Когда в ЭС клетки вносили только LTVEC, мы обнаружили, что 1,0% исследуемых устойчивых к лекарственному препарату клонов несли правильно таргетированный моноаллельный гетерозиготный гуманизированный аллель. В противоположность этому, комбинирование LTVEC с эндонуклеазами Cas9, направляемыми семью из восьми исследованных онРНК (онРНК-5'А, онРНК-5'В, онРНК-5B2, онРНК-С, онРНК-D, онРНК-3'Е2 и онРНК-3Т; последовательности приведены в Таблице 33), привело к получению правильно таргетированных моноаллельных гетерозиготных мутаций с эффективностью в диапазоне от 2,1 до 7,3%, что соответствует 2-9-кратному усилению одноэтапного таргетирования гуманизированных генов по сравнению с применением одного LTVEC. В случае Cas9-управляемого расщепления посредством онРНК-5'В2, кроме моноаллельного таргетирования, мы выявили биаллельную гомозиготную гуманизацию с частотой 1%. Гомозиготные в отношении Lrp5 гуманизированные ЭС клетки можно преобразовать методом генетической инженерии VELOCIMOUSE® (Poueymirou, W.Т. et al. (2007) F0 generation mice folly derived from gene-targeted embryonic stem cells allowing immediate phenotypic analyses, Nature Biotech. 25: 91-99, в полном объеме включенная в данный документ посредством ссылки) непосредственно в полностью полученных из ЭС клеток мышей, готовых для проведения исследований фенотипа и эффективности лекарственных препаратов.
[00927]
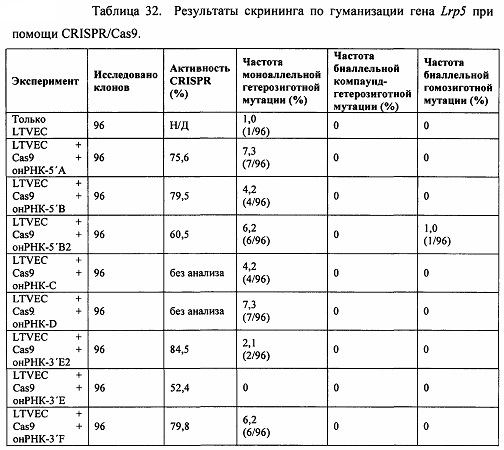
[00928]


[00929] Усиленное таргетирование при гуманизации крупного Lrp5 при помощи эндонуклеаз CRISPR/Cas9 существенно по сравнению с эквивалентными экспериментами, проводимыми с цинк-пальцевыми нуклеазами (ZFN). Мы получили четыре ZFN, сконструированных для создания двухцепочечных разрывов в области мышиного гена Lrp5, предназначенного для удаления (Фигура 34). ZFN была нацелена на последовательность вблизи 5'конца делеции (а), одна была нацелена на последовательность в середине делеции (b), а две были нацелены на последовательности вблизи 3' конца делеции (с, d). В отдельных экспериментах мы комбинировали гуманизирующий Lrp5 LTVEC с плазмидой, кодирующей одну из четырех ZFN (a-d), сконструированных для создания двухцепочечных разрывов в области мышиного гена Lrp5, которые были предназначены для удаления. Мы определили, что все ZFN были активны и способны индуцировать мутации НГСК в гене Lrp5 (данные не приведены), но в комбинации с LTVEC, ни одно усиленное НГР-опосредованное таргетинование генов не было сравнимо с одним LTVEC.
[00930] Повышение эффективности таргетирования при гуманизации крупного Lrp5 при помощи эндонуклеаз CRISPR/Cas9 также существенно по сравнению с серией экспериментов по гуманизации при помощи ZFN. В этих экспериментах проводили серию гуманизации при помощи ZFN, в которых увеличивали размер делеции целевого мышиного гена и вставки человеческого гена (Таблица 34; Фигура 35). Фигура 35А иллюстрирует процент эффективности таргетирования LTVEC, нацеленных на гены с возрастающим размером делеции. LTVEC применяли одни (серые квадраты) или в комбинации с ZFN (черные квадраты). Фигура 35В иллюстрирует процент эффективности таргетирования LTVEC с человеческими генными вставками возрастающего размера. Снова LTVEC применяли одни (серые треугольники) или в комбинации с ZFN (черные треугольники). Как показано в Таблице 34 и на Фигуре 35, способность ZFN-опосредованного расщепления ДНК повышать эффективность таргетирования LTVEC исчезла, когда размер делеции целевого мышиного гена превысил 24,7 т.п.о. и когда размер вставки человеческого гена превысил 22,2 т.п.о. (Таблица 34; Фигура 35А). В противоположность этому, CRISPR/Cas9 была способна повышать эффективность таргетирования LTVEC гена Lrp5, которое включало удаление мышиного гена из 68,3 т.п.о. и вставку человеческого гена из 91,0 т.п.о. (Таблица 32; Фигура 34). Это указывает на то, что эндонуклеазы CRISPR/Cas9 способны повышать эффективность таргетирования LTVEC в ситуациях, где другие нуклеазы (например, цинк-пальцевые нуклеазы) не могут.
[00931]
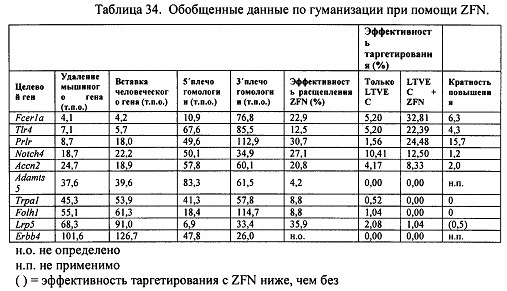
[00932] Проводили сопоставимые эксперименты по гуманизации других мышиных генов. В одном эксперименте конструировали LTVEC для создания 45 т.п.о. делеции мышиного гена Trpa1 (представитель 1 подсемейства катионных каналов с транзиторным рецепторным потенциалом) и одновременного замещения 55 т.п.о. фрагментом гомологичного человеческого гена TRPA1 (Фигура 36). LTVEC содержал 55 т.п.о. фрагмент человеческого гена TRPA1, фланкируемый плечами гомологии, содержащими 41 т.п.о. и 58 т.п.о. геномной ДНК, полученной из частей локуса мышиного Trpa1, который фланкирует 45 т.п.о. последовательность мышиного гена Trpa1, предназначенного для удаления. В отдельных экспериментах мы комбинировали предназначенный для гуманизации Trpa1 LTVEC с плазмидой, кодирующей Cas9, и второй плазмидой, кодирующей одну из восьми онРНК (gA, gB, gB2, gC, gD, gE2, gE, gF), сконструированных для создания двухцепочечных разрывов в области гена мышиного Trpa1, предназначенного для удаления. онРНК были сконструированы, чтобы избежать распознавания любой последовательности во вставленной части гена человеческого TRPA1.
[00933] Результаты проводимой при помощи CRISPR/Cas9 гуманизации гена Trpa1 приведены в Таблице 35. Когда в ЭС клетки вносили только LTVEC, мы обнаружили, что 1,0% исследуемых устойчивых к лекарственному препарату клонов несли правильно таргетированный моноаллельный гетерозиготный гуманизированный аллель. В противоположность этому, комбинирование LTVEC с эндонуклеазой Cas9, направляемой семью из восьми исследованных онРНК (А, А2, В, С, D и F; последовательности приведены в Таблице 43), привело к получению правильно таргетированных моноаллельных гетерозиготных мутаций или биаллельных компаунд-гетерозиготных или гомозиготных мутаций с эффективностью в диапазоне от 1,0 до 3,1%. В случае управляемого Cas9 расщепления посредством нРНК А и нРНК F мы выявили компаунд-гетерозиготные мутации с частотой 1,0%.
[00934]
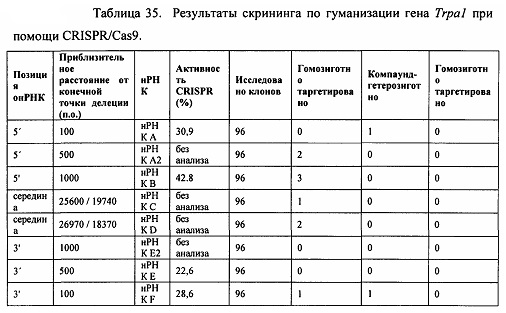

[00935] В другом эксперименте конструировали LTVEC для создания 55 т.п.о. делеции мышиного гена Folh1 (глутамат карбоксипептидаза 2) и одновременного замещения 61 т.п.о. фрагментом гомологичного человеческого гена FOLH1 (Фигура 37). LTVEC содержал 61 т.п.о. фрагмент человеческого гена FOLH1, фланкируемый плечами гомологии, содержащими 22 т.п.о. и 46 т.п.о. геномной ДНК, полученной из частей локуса мышиного Folh1, который фланкирует 55 т.п.о. последовательность мышиного гена Folh1, предназначенного для удаления. В отдельных экспериментах мы комбинировали предназначенный для гуманизации Folh1 LTVEC с плазмидой, кодирующей Cas9, и второй плазмидой, кодирующей одну из шести онРНК (gA, gA2, gC, gD, gE и gE2), сконструированных для создания двухцепочечных разрывов в области гена мышиного Folh1, предназначенного для удаления. онРНК были сконструированы, чтобы избежать распознавания любой последовательности во вставленной части гена человеческого FOLH1.
[00936] Результаты проводимой при помощи CRISPR/Cas9 гуманизации гена Folh1 приведены в Таблице 36. Когда в ЭС клетки вносили только LTVEC, мы обнаружили, что ни один из 96 исследуемых устойчивых к лекарственному препарату клонов не нес правильно таргетированный моноаллельный гетерозиготный гуманизированный аллель. В противоположность этому, комбинирование LTVEC с эндонуклеазой Cas9, направляемой тремя из шести исследованных онРНК (A, D и Е2; последовательности приведены в Таблице 43), привело к получению правильно таргетированных моноаллельных гетерозиготных мутаций с эффективностью в диапазоне от 1,0 до 3,1%.
[00937]

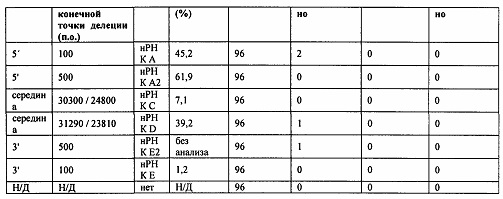
[00938] В другом эксперименте конструировали LTVEC для создания 76 т.п.о. делеции мышиного гена компонента комплемента 5 (С5 или Hc) и одновременного замещения 97 т.п.о. фрагментом гомологичного человеческого гена С5 (Фигура 38). LTVEC содержал 97 т.п.о. фрагмент человеческого гена С5, фланкируемый плечами гомологии, содержащими 34,1 т.п.о. и 31,2 т.п.о. геномной ДНК, полученной из частей локуса мышиного С5 (Hc), который фланкирует 76 т.п.о. последовательность мышиного гена С5 (Hc), предназначенного для удаления. В отдельных экспериментах мы комбинировали предназначенный для гуманизации С5 (Hc) LTVEC с плазмидой, кодирующей Cas9, и второй плазмидой, кодирующей одну из шести онРНК (gA, gB, gC, gD, gE и gE2), сконструированных для создания двухцепочечных разрывов в области гена мышиного С5 (Hc), предназначенного для удаления. онРНК были сконструированы, чтобы избежать распознавания любой последовательности во вставленной части гена человеческого С5.
[00939] Результаты проводимой при помощи CRISPR/Cas9 гуманизации гена С5 (Hc) приведены в Таблице 37. Когда в ЭС клетки вносили только LTVEC, мы обнаружили, что 1,0% исследуемых устойчивых к лекарственному препарату клонов несли правильно таргетированный моноаллельный гетерозиготный гуманизированный аллель. В противоположность этому, комбинирование LTVEC с эндонуклеазой Cas9, направляемой всеми шестью исследованными онРНК (А, В, С, D, Е и Е2; последовательности приведены в Таблице 43), привело к получению правильно таргетированных моноаллельных гетерозиготных мутаций или биаллельных компаунд-гетерозиготных или гомозиготных мутаций с эффективностью в диапазоне от 4,2 до 16,7%. В случае управляемого Cas9 расщепления посредством нРНК А и Е мы выявили компаунд-гетерозиготные мутации с частотой 5,2% и 4,2%, соответственно.
[00940]
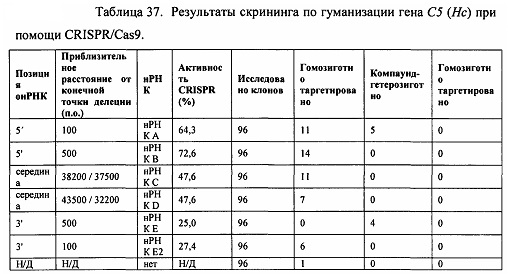
[00941] В другом эксперименте конструировали LTVEC для создания 38 т.п.о. делеции мышиного гена Adamts5 (дизинтегрин и металлопротеиназа с тромбоспондиновыми мотивами 5) и одновременного замещения 43 т.п.о. фрагментом гомологичного человеческого гена ADAMTS5 (Фигура 39). LTVEC содержал 43 т.п.о. фрагмент человеческого гена ADAMTS5, фланкируемый плечами гомологии, содержащими 22 т.п.о. и 46 т.п.о. геномной ДНК, полученной из частей локуса мышиного Adamts5, который фланкирует 38 т.п.о. последовательность мышиного гена Adamts5, предназначенного для удаления. В отдельных экспериментах мы комбинировали предназначенный для гуманизации Adamts5 LTVEC с плазмидой, кодирующей Cas9, и второй плазмидой, кодирующей одну из восьми онРНК (gA, gA2, gB, gC, gD, gE, gE2 и gF), сконструированных для создания двухцепочечных разрывов в области гена мышиного Adamts5, предназначенного для удаления. онРНК были сконструированы, чтобы избежать распознавания любой последовательности во вставленной части гена человеческого ADAMTS5.
[00942] Результаты проводимой при помощи CRISPR/Cas9 гуманизации гена Adamts5 приведены в Таблице 38. Когда в ЭС клетки вносили только LTVEC, мы обнаружили, что ни один из 96 исследуемых устойчивых к лекарственному препарату клонов не нес правильно таргетированный моноаллельный гетерозиготный гуманизированный аллель. В противоположность этому, комбинирование LTVEC с эндонуклеазой Cas9, направляемой двумя из восьми исследованных онРНК (В и F; последовательности приведены в Таблице 43), привело к получению правильно таргетированных моноаллельных гетерозиготных мутаций или биаллельных компаунд-гетерозиготных мутаций с эффективностью 1,0%. В случае управляемого Cas9 расщепления посредством нРНК Е2 мы выявили компаунд-гетерозиготные мутации с частотой 1,0%.
[00943]

[00944] В другом эксперименте конструировали LTVEC для создания 102 т.п.о. делеции мышиного гена Erbb4 (рецепторная тирозиновая протеинкиназа erbB-4) и одновременного замещения 127 т.п.о. фрагментом гомологичного человеческого гена ERBB4 (Фигура 40). LTVEC содержал 127 т.п.о. фрагмент человеческого гена ERBB4, фланкируемый плечами гомологии, содержащими 48 т.п.о. и 26 т.п.о. геномной ДНК, полученной из частей локуса мышиного Erbb4, который фланкирует 102 т.п.о. последовательность мышиного гена Erbb4, предназначенного для удаления. В отдельных экспериментах мы комбинировали предназначенный для гуманизации Erbb4 LTVEC с плазмидой, кодирующей Cas9, и второй плазмидой, кодирующей одну из восьми онРНК (gA, gB, gB2, gC, gD, gE, gE2 и gF), сконструированных для создания двухцепочечных разрывов в области гена мышиного Erbb4, предназначенного для удаления. онРНК были сконструированы, чтобы избежать распознавания любой последовательности во вставленной части гена человеческого ERBB4.
[00945] Результаты проводимой при помощи CRISPR/Cas9 гуманизации гена Erbb4 приведены в Таблице 39. Когда в ЭС клетки вносили только LTVEC, мы обнаружили, что ни один из 96 исследуемых устойчивых к лекарственному препарату клонов не нес правильно таргетированный моноаллельный гетерозиготный гуманизированный аллель. В противоположность этому, комбинирование LTVEC с эндонуклеазой Cas9, направляемой одной из восьми исследованных онРНК (D; последовательность приведена в Таблице 43), привело к получению правильно таргетированных моноаллельных гетерозиготных мутаций или биаллельных компаунд-гетерозиготных мутаций с эффективностью 1,0%. В случае управляемого Cas9 расщепления посредством нРНК D мы выявили компаунд-гетерозиготные мутации с частотой 1%.
[00946]
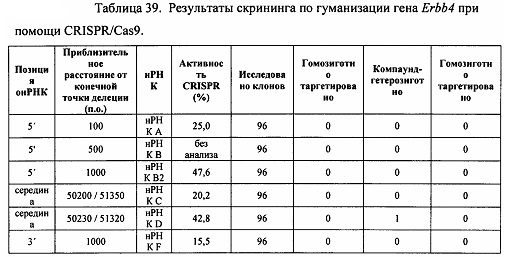

[00947] В другом эксперименте конструировали LTVEC для создания 110 т.п.о. делеции мышиного гена Ror1 (трансмембранный рецептор тирозиновой протеинкиназы ROR1) и одновременного замещения 134 т.п.о. фрагментом гомологичного человеческого гена ROR1 (Фигура 41). LTVEC содержал 134 т.п.о. фрагмент человеческого гена ROR1, фланкируемый плечами гомологии, содержащими 41,8 т.п.о. и 96,4 т.п.о. геномной ДНК, полученной из частей локуса мышиного Ror1, который фланкирует 110 т.п.о. последовательность мышиного гена Ror1, предназначенного для удаления. В отдельных экспериментах мы комбинировали предназначенный для гуманизации Ror1 LTVEC с плазмидой, кодирующей Cas9, и второй плазмидой, кодирующей одну из шести онРНК (gA, gB, gC, gD, gE и gF), сконструированных для создания двухцепочечных разрывов в области гена мышиного Ror1, предназначенного для удаления. онРНК были сконструированы, чтобы избежать распознавания любой последовательности во вставленной части гена человеческого ROR1.
[00948] Результаты проводимой при помощи CRISPR/Cas9 гуманизации гена Ror1 приведены в Таблице 40. Когда в ЭС клетки вносили только LTVEC, мы обнаружили, что ни один из 96 исследуемых устойчивых к лекарственному препарату клонов не нес правильно таргетированный моноаллельный гетерозиготный гуманизированный аллель. В противоположность этому, комбинирование LTVEC с эндонуклеазой Cas9, направляемой двумя из шести исследованных онРНК (D и F; последовательности приведены в Таблице 43), привело к получению правильно таргетированных моноаллельных гетерозиготных мутаций или биаллельных мутаций с эффективностью 1,0%. В случае управляемого Cas9 расщепления посредством нРНК F мы также выявили компаунд-гетерозиготные мутации с частотой 1%.
[00949]


[00950] В другом эксперименте конструировали LTVEC для создания 79 т.п.о. делеции мышиного гена Dpp4 (дипептидил пептидаза 4) и одновременного замещения 82 т.п.о. фрагментом гомологичного человеческого гена DPP4 (Фигура 42). LTVEC содержал 82 т.п.о. фрагмент человеческого гена DPP4, фланкируемый 5' и 3' плечами гомологии, содержащими по 46 т.п.о. геномной ДНК, полученной из частей локуса мышиного Dpp4, который фланкирует 79 т.п.о. последовательность мышиного гена Dpp4, предназначенного для удаления. В отдельных экспериментах мы комбинировали предназначенный для гуманизации Dpp4 LTVEC с плазмидой, кодирующей Cas9, и второй плазмидой, кодирующей одну из восьми онРНК (gA, gB, gB2, gC, gD, gE, gE2 и gF), сконструированных для создания двухцепочечных разрывов в области гена мышиного Dpp4, предназначенного для удаления. онРНК были сконструированы, чтобы избежать распознавания любой последовательности во вставленной части гена человеческого DPP4.
[00951] Результаты проводимой при помощи CRISPR/Cas9 гуманизации гена Dpp4 приведены в Таблице 41. Когда в ЭС клетки вносили только LTVEC, мы обнаружили, что 2,1% исследуемых устойчивых к лекарственному препарату клонов несли правильно таргетированный моноаллельный гетерозиготный гуманизированный аллель. В противоположность этому, комбинирование LTVEC с эндонуклеазой Cas9, направляемой любой из восьми исследованных онРНК (А, В, В2, С, D, Е, Е2 и F; последовательности приведены в Таблице 43), привело к получению правильно таргетированных моноаллельных гетерозиготных мутаций с эффективностью в диапазоне от 2,1 до 7,3%.
[00952]
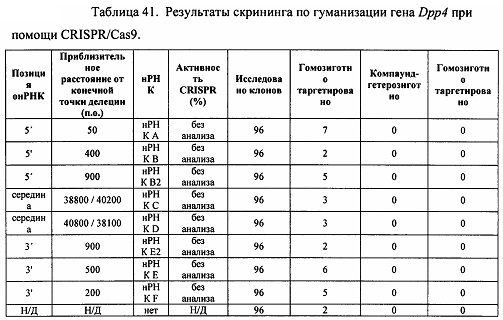
[00953] Обобщенные результаты по гуманизации различных мышиных генов при помощи CRISPR/Cas9 приведены в Таблице 42. В первом ряду указан таргетируемый генный локус. Во втором ряду указан размер делеции (Дел.) эндогенного мышиного локуса и размер вставки (Вст.) соответствующего человеческого локуса. В оставшихся колонках указано число колоний (из 96) для каждого условия, которое характеризовалось направленными моноаллельными гетерозиготными мутациями, биаллельными компаунд-гетерозиготными мутациями или биаллельными гомозиготными мутациями, «без нРНК» соответствует одному LTVEC, в то время как остальные ряды соответствуют LTVEC плюс соответствующие нРНК (указаны по относительной позиции в удаляемом локусе).
[00954]
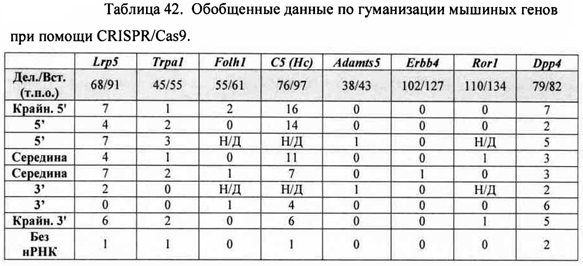
[00955]

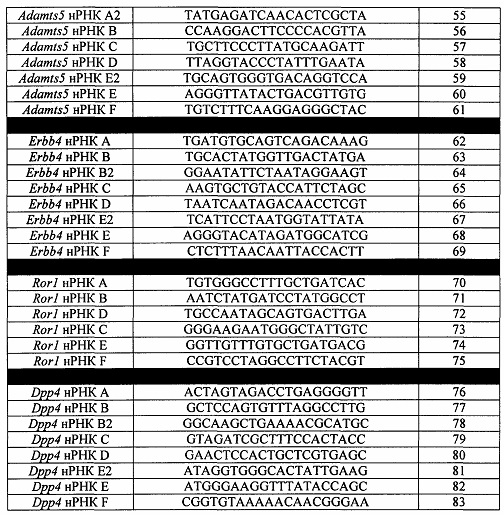
Пример 5. Обобщенные данные по направленной модификации крысиных геномных локусов
[00956] Таблица 44. Обобщенные данные по таргетированию крыс различными типами векторов и нуклеазными агентами, обсуждаемыми в Примерах 3 и 4.
[00957]


[00958] В Таблице 45 приведены обобщенные данные по таргетированию крысиных ЭС клеток плазмидами или LTVEC в комбинации с CRISPR/Cas9. Две нРНК исследовали отдельно для каждого целевого локуса: Rag2, ApoE и Il2rg. Эффективность расщепления CRISPR/Cas9 была >20% во всех трех локусах. Наблюдали повышение эффективности таргетирования и повышение биаллельного таргетирования при применении CRISPR/Cas9 в комбинации с направляющими плазмидами и LTVEC.
[00959]

[00960] В Таблице 46 приведены обобщенные данные по трансмиссии зародышевой линии для направленной модификации крысиных геномных локусов. Трансмиссия зародышевой линии была подтверждена для АроЕ-таргетированных крыс и Il2rg-таргетированных крыс. Крысиные ЭС клетки были XY (мужскими) и гетерозиготно таргетированными. Следовательно, когда таргетированные ЭС клетки вносят свой вклад в зародышевую линию, приблизительно 50% сперматозоидов, полученных из ЭС клеток, будут нести мутантный аллель и давать гетерозиготное потомство F1.
[00961]

Пример 6. Создание, поддержание и таргетирование человеческих индуцированных плюрипотентных стволовых клеток
6.1. Получение человеческих иПС клеток
[00962] В этом примере описано получение человеческих иПС клеток из неплюрипотентных человеческих клеток. Векторы PiggyBac (System Biosciences) (PB-600A_CAGGS Bst XI (0,64 мкг/мкл) и РВ-200 (0,99 мкг/мкл), содержащие гены, которые кодируют четыре перепрограммирующих фактора (hOct4, hSox2, hKLF-4, hMYC), функционально связанные с промоторомСМ7, вносили в неонатальные фибробласты крайней плоти человека, применяя трансфекционные реагенты RED и BLUE GeneIn™ (GlobalStem). Трансфицированные клетки инкубировали на питающих клетках NuFF1 в среде Е7 для встраивания векторов и экспрессии перепрограммирующих факторов. Среда Е7 содержала DMEM/F-12, NaHCO3, L-аскорбиновую кислоту, инсулин, трансферрин, селен и FGF-2.
[00963] Отбор по чувствительности к пуромицину начинали через 10 дней после трансфекции, используя 2 мкг/мл пуромицина в среде Е7. На 21 день колонии отбирали и культивировали в среде mTeSR™, которая содержала DMEM/F-12, NaHCO3, L-аскорбиновую кислоту, инсулин, трансферрин, селен, FGF-2, TGF-β1, глутатион, L-глутамин, определенные липиды, тиамин, следовые элементы В и С, β-меркаптоэтанол, бычий сывороточный альбумин, пипеколиновую кислоту, хлорид лития и GABA. В дни от 29 до 57 клетки размножали и пассировали в среде mTeSR™ до достижения ~50% конфлюэнтности в 6-луночных планшетах. В дни от 65 до 73 продолжали размножение и пассирование с применением среды mTeSR™ и реагента для аккуратного разделения клеток (Stem Cell Technologies). На 76 день среду меняли на среду с низкой осмолярностью VG2i для дополнительного размножения, пассирования и поддержания клеток, содержащих наивные или подобные наивным чиПСК.
6.2. LTVEC-таргетирование в человеческих иПС клетках
[00964] В этом примере описано применение LTVEC-таргетирования в человеческих иПС клетках. Как показано на Фигуре 51, мы вносили путем электропорации в человеческие иПС клетки, размноженные в среде VG2i, следующие молекулы нуклеиновых кислот: (1) LTVEC (0,67 мкг); (2) плазмиду, кодирующую эндонуклеазу Cas9 (5 мкг); и (3) плазмиду, кодирующую одиночную направляющую РНК CRISPR (нРНК) (10 мкг). В одной группе образцов были исключены Cas9 и нРНК. В частности, 3×106 клеток электропорировали при напряжении 700 В, емкости 25 мкФ и сопротивлении 400 Ом. LTVEC содержал 16,7 т.п.о. нуклеиновую кислоту, содержащую мышиные гены Adam6a и Adam6b, фланкируемые плечами гомологии, содержащими 34 т.п.о. и 105 т.п.о. геномной ДНК из геномных областей, которые фланкируют 4,1 т.п.о. последовательность локуса человеческого ADAM6, предназначенного для удаления. LTVEC также несет кассету отбора по чувствительности к лекарственному препарату, которая управляет экспрессией фермента, который придает устойчивость к антибиотику (гигромицину). Применяемая нРНК человеческого ADAM6 имела следующую последовательность: GTATAGCCCTGTTACACATT (SEQ ID №94).
[00965] Клетки, которые поглотили LTVEC и встроили его в свои геномы, были способны расти и формировать колонии в покрытой GELTREX™ чашке для культивирования в среде для роста, содержащей антибиотик. Так как мы вносили в от 500 до 1000 раз больше CRISPR/Cas9-кодирующих нуклеиновых молекул, чем молекул LTVEC, большинство LTVEC-содержащих устойчивых к лекарственному препарату колоний также содержали, по меньшей мере временно, компоненты CRISPR/Cas9. Мы собирали устойчивые к лекарственному препарату колонии и проводили их скрининг методом потери аллеля (Valenzuela et al. (2003) Nat. Biotech. 21: 652-660; Frendewey et al. (2010) Methods Enzymol. 476: 295-307; в полном объеме включенные в данный документ посредством ссылки) для выявления клонов, которые содержали правильно таргетированный аллель.
[00966] Результаты LTVEC-таргетирования при помощи CRISPR/Cas9 локуса ADAM6 приведены в Таблице 47.

[00967] Когда в человеческие иПС клетки вносили только LTVEC, наблюдаемая эффективность таргетирования составила 3,1%. В противоположность этому, комбинирование LTVEC с Cas9, направляемой нРНК ADAM6, привело к эффективности таргетирования 7,3%.
6.3. Влияние среды с низкой осмолярностью на морфологию человеческих иПС клеток
[00968] В этом примере описано влияние концентрации соли, ионной силы и/или осмолярности на состояние плюрипотентности человеческих иПС клеток в культуре. Человеческие иПС клетки культивировали на субстрате MATRIGEL™ или GELTREX™ в среде, описанной в Таблице 48, или в среде mTeSR™-hLIF.

[00969] Когда применяемой основной средой была DMEM, эту среду называли средой 2i. Когда применяемой основной средой была VG-DMEM, эту среду с низкой осмолярностью называли средой VG2i. Осмолярность среды VG2i (233 мОсм/кг) ниже, чем осмолярность традиционной среды 2i (261 мОсм/кг).
[00970] Как показано на Фигуре 52, человеческие иПС клетки, культивируемые на MATRIGEL™ в среде 2i в течение 8 дней (Фигура 52А) или 12 дней (Фигура 52В), демонстрировали морфологию, характерную для иПС клеток в примированном состоянии, в частности, рост в эпителиальном монослое и появление апико-базальной полярности.
[00971] Среду mTeSR-hLIF и среду VG2i дополнительно оценивали в отношении их влияния на морфологию и состояние плюрипотентности человеческих иПС клеток. В этом исследовании человеческие иПС клетки культивировали на MATRIGEL™ или питающих клетках NuFF в среде mTeSR™-hLIF (Фигуры 53А и 53С) или в среде VG2i (Фигуры 53В и 53D) в течение 6 дней. При культивировании в среде mTeSR™-hLIF на MATRIGEL™ или питающих клетках NuFF человеческие иПС клетки демонстрировали морфологию, характерную для примированного состояния плюрипотентности, в частности, рост в эпителиальном монослое и появление апико-базальной полярности. Некоторые клетки, культивируемые в среде mTeSR™-hLIF, начали демонстрировать морфологию, характерную для трехмерной агрегации. В противоположность этому, при культивировании в среде VG2i на MATRIGEL™ или питающих клетках NuFF человеческие иПС клетки демонстрировали морфологию, характерную для наивного состояния плюрипотентности, в частности, рост в круглых, полусферических колониях и отсутствие апико-базальной полярности.
[00972]
6.4. Влияние среды с низкой осмолярностью на экспрессию маркеров плюрипотентности в человеческих иПС клетках
[00973] В этом примере описано влияние концентрации соли, ионной силы и/или осмолярности на экспрессию маркеров плюрипотентности в человеческих иПС клетках, которые были перепрограммированы из примированного состояния в наивное состояние. Через 24 дня культивирования в среде VG2i на субстрате MATRIGEL™ перепрограммированные наивные человеческие иПС клетки окрашивали в отношении экспрессии щелочной фосфатазы или NANOG. Согласно наблюдениям, перепрограммированные клетки экспрессировали на высоком уровне как щелочную фосфатазу (Фигура 54А), так и NANOG (Фигуры 54В и 54С), которые указывают на наивное состояние плюрипотентности.
6.5. Влияние среды с низкой осмолярностью на ферментативное разделение и субкультивирование человеческих иПС клеток
[00974] В этом примере человеческие иПС клетки, которые было перепрограммированы до наивного состояния при помощи среды с низкой осмолярностью VG2i, ферментативно разделяли при помощи трипсина для получения одноклеточной суспензии (Фигура 55А). Клеточную суспензию пассировали на новых, покрытых GELTREX™ планшетах для субкультивирования в среде VG2i. Согласно наблюдениям, через 1 день (Фигура 55В) и 4 дня (Фигура 55С) субкультивируемые клетки продолжали демонстрировать морфологию, характерную для клеток в наивном состоянии плюрипотентности. В частности, клетки росли в виде в круглых, полусферических колоний и не демонстрировали апико-базальную полярность. Оказалось, что ферментативное разделение можно было проводить в отсутствие ингибитора ROCK, который обычно необходим для предотвращения активации проапоптотических путей. Это позволяет предположить, что проапоптотические пути не настолько сильно активируются во время ферментативного разделения и субкультивирования наивных человеческих иПС клеток в условиях, определенных в данном документе.
[00975] Все упоминаемые в описании публикации и патентные заявки соответствуют уровню специалистов в области техники, к которой относится данное изобретение. Все публикации и патентные заявки включены в данный документ посредством ссылки в той же степени, как если бы каждая отдельная публикация или патентная заявка была специально и отдельно включена посредством ссылки. Если иное не следует из контекста, любые вариант реализации, аспект, этап или признак изобретения можно применять в комбинации друг с другом. Указание на диапазон включает любые целые числа в пределах указанного диапазона, любой поддиапазон в пределах указанного диапазона. Указание на множественные диапазоны включает составляющие части таких диапазонов.
Реферат
Настоящее изобретение относится к генной инженерии. Предложен способ in vitro модификации генома в представляющем интерес геномном локусе в нечеловеческой плюрипотентной клетке млекопитающего, включающий внесение в клетку компонентов системы CRISPR/Cas9 в комбинации с крупным направляющим вектором (LTVEC), который составляет по меньшей мере 10 т.п.о. Данное изобретение позволяет осуществлять генетическую модификацию клетки путем делеции от около 30 т.п.о. до 200 т.п.о. и/или вставки от около 30 т.п.о. до около 200 т.п.о. 56 з.п. ф-лы, 55 ил., 48 табл., 6 пр.
Формула
Документы, цитированные в отчёте о поиске
Способ генетической модификации интересующего эндогенного гена или хромосомного локуса (варианты) иего использование

Комментарии