Применение рецептора edg2 на модели сердечно-сосудистой недостаточности у животных - RU2337963C2
Код документа: RU2337963C2
Чертежи


Описание
Данное изобретение относится к временно (транзиторно) трансформированному млекопитающему, которое может использоваться в качестве модели сердечно-сосудистой недостаточности у животных.
Рецепторы, сопряженные с G-белками (GPCR), играют основную роль в многочисленных физиологических процессах. Предполагается, что в геноме человека приблизительно 1000 генов кодируют это семейство рецепторов. Приблизительно 60% фармацевтических препаратов, назначаемых в настоящее время больным, действуют как агонисты или антагонисты GPCR. Это подчеркивает важность этого класса рецепторов для использования в фармацевтической промышленности. Благодаря большой численности и важности указанного семейства белков и в связи с тем фактом, что для многих GPCR до сих пор не известны физиологические лиганды (орфановые GPCR), можно предположить, что этот класс рецепторов будет одним из наиболее важных источников для подходящих мишеневых белков при поиске новых лекарственных веществ в будущем.
GPCR представляют собой семейство интегральных мембранных белков, которые расположены на поверхности клеток. Они получают сигналы от внеклеточных сигнальных веществ (например, гормонов, нейротрансмиттеров, пептидов, лихпидов) и передают эти сигналы во внутреннее пространство клетки посредством семейства гуанин-нуклеотид-связывающих белков, "G-белков". В зависимости от специфичности рецептора, активируемого G-белка и типа клеток, эти рецепторы индуцируют различные пути передачи сигналов.
Полипептидные цепи всех GPCR укладываются в семь α-спиралей, которые пронизывают фосфолипидный бислой клеточной мембраны. Это семикратное пронизывание приводит к образованию внеклеточных и внутриклеточных петель, которые позволяют связывать внеклеточный лиганд и делают возможным внутриклеточное взаимодействие G-белков. В связи с этим GPCR называют также seven-pass-трансмембранными рецепторами (рецепторами с семью проходами через мембрану).
Все рецепторы, сопряженные с G-белками, действуют в соответствии с общей основной картиной: связывание внеклеточного лиганда приводит к конформационному изменению белка рецептора, что позволяет этому белку рецептора взаимодействовать с G-белком. Опосредованные G-белком каскады трансдукции сигнала в клетке в конце концов приводят к биологическому ответу клетки. G-белки являются гетеротримерными белками, которые состоят из субъединиц α, β и γ. Они расположены на внутренней стороне клеточной мембраны посредством липидных якорей. Взаимодействие активированных GPCR с G-белками индуцирует обмен ГДФ/ГТФ на Gα-субъединице и диссоциацию гетеротримерного G-белка на α- и βγ-субъединицу. Как активированная α-субъединица, так и комплекс βγ способны взаимодействовать с внутриклеточными эффекторными белками.
Активация мембраносвязанной аденилатциклазы (АС) G-белками Gαs-типа, например, приводит к увеличению уровня внутриклеточного цАМФ или, в случае активации G-белками Gαi-типа, к уменьшению этого уровня. G-белки Gq-типа активируют фосфолипазу С (PLC), которая катализирует образование инозит-1,4,5-трифосфата (IP3) и диацилглицерина (DAG). Эти молекулы стимулируют высвобождение Са2+ из внутриклеточных депо или к активации протеинкиназы С (PKC).
Полинуклеотидная последовательность и аминокислотная последовательность ЕDG2 человека (ген 2 эндотелиальной дифференцировки) общедоступна. Эта последовательность доступна, например, от NCBI (Accession: NM_001401). Последовательность белка доступна от Swiss Prot (Accession: Q 92633). Клонирование рецептора из библиотеки кДНК легкого человека было опубликовано в "An et al., Biochem. Biophys. Res. Commun., 24, 231 (1997)".
Полноразмерная последовательность кодирует белок из 359 аминокислот, который принадлежит суперсемейству рецепторов гуанин-нуклеотид-связывающих белков (GPCR). мРНК EDG2 человека широко представлена в тканях человека и в наибольшей степени представлена в головном мозгу. Клетки НЕК293, экспрессирующие белок EDG2 человека, обнаружили усиленный ответ на лизофосфатидную кислоту (LPA) в анализе репортерного гена, чувствительного к сыворотке, который был зависим от концентрации LPA и специфичен в отношении LPA.
В качестве рецептора LPA также была идентифицирована мышиная копия белка EDG2.
Лизофосфатидная кислота (LPA) и сфингозин-1-фосфат (SlP) являются мощными фосфолипидными медиаторами с многообразным биологическим действием. По их виду и функциональным свойствам можно предположить о возможной роли в развитии, заживлении ран и регенерации тканей. Стимулирующую рост активность и другие системные биологические активности LPA и SlP отчасти относят к активации многочисленных внутриклеточных путей передачи сигналов, опосредуемых G-белками. Некоторые гетеротримерные G-белки, а также Ras- и Rho-зависимые пути, играют основную роль в клеточных ответах на LPA и SlP.
В объеме данного изобретения и во всех используемых случаях и без какого-либо исключения под термином «млекопитающее» не следует иметь в виду человека, как представителя биологического вида Homo sapiens, или часть тела человека.
Данное изобретение относится к клеткам миокарда млекопитающего, которые содержат вектор с аденовирусной последовательностью для одновременной экспрессии рецептора, сопряженного с G-белком EDG2 и GFP (зеленого флуоресцентного белка).
Вектор с аденовирусной последовательностью состоит, предпочтительно, из рекомбинантного аденовируса, дефектного по Е1/Е3-области, который экспрессирует рецептор, сопряженный с G-белком, EDG2 и GFP под контролем двух независимых промоторов. Такими промоторами могут быть два промотора CMV.
Миокардиальные клетки млекопитающих, которые содержат вектор с аденовирусной последовательностью, как указано выше, транспортируют рецептор, сопряженный с G-белком, EDG2 и GFP и содержат, следовательно, белок рецептора, сопряженного с G-белком, EDG2 и белок GFP.
Миокардиальные клетки, которые содержат вектор с аденовирусной последовательностью, являются предпочтительно клетками кролика, мыши или крысы.
Данное изобретение также относится к получению миокардиальных клеток, которые содержат вектор с аденовирусной последовательностью для одновременной экспрессии рецептора, сопряженного с G-белком рецептора, EDG2 и GFP, где
а] сердце млекопитающего удаляют оперативными способами ветеринарии,
b] сердце обрабатывают и подвергают расщеплению коллагеназой,
c] выделенные кардиомиоциты инфицируют аденовирусным вектором, состоящим из рекомбинантного аденовируса, дефектного по Е1/Е3-области, что обеспечивает экспрессию рецептора, сопряженного с G-белком, EDG2 и GFP под контролем двух независимых промоторов. Такими промоторами предпочтительно являются два промотора CMV.
Кроме того, данное изобретение относится к млекопитающему, имеющему миокард, который содержит аденовирусный вектор для одновременной экспрессии рецептора, сопряженного с G-белком, EDG2 и GFP. Этот вектор с аденовирусной последовательностью млекопитающих предпочтительно состоит из рекомбинантного аденовируса, дефектного по Е1/Е3-области, что обеспечивает экспрессию рецептора, сопряженного с G-белком, EDG2 и GFP под контролем двух независимых промоторов. Такими двумя независимыми промоторами являются предпочтительно два промотора CMV.
Данное изобретение также относится к млекопитающему, имеющему миокард, который содержит рецептор, сопряженный с G-белком, EDG2 и белок GFP. Таким млекопитающим, имеющим миокард с аденовирусным вектором для одновременной экспрессии рецептора, сопряженного с G-белком, EDG2 и GFP и/или имеющим миокард с белком рецептора, сопряженного с G-белком, EDG2 и белком GFP, предпочтительно является кролик, мышь или крыса. Кроме того, изобретение относится к получению млекопитающего, имеющего миокард с аденовирусным вектором для одновременной экспрессии рецептора, сопряженного с G-белком, EDG2 и GFP и/или имеющего миокард с белком рецептора, сопряженного с G-белком, EDG2 и белком GFP, в котором
a] представлен вектор с аденовирусной последовательностью для одновременной экспрессии рецептора, сопряженного с G-белком, EDG2 и GFP,
b] млекопитающее,
c] аденовирусная векторная система a], которую переносят в миокард млекопитающего b] при помощи катетера.
Данное изобретение также относится к применению млекопитающего, имеющего миокард с аденовирусным вектором для одновременной экспрессии рецептора, сопряженного с G-белком, EDG2 и GFP и/или имеющего миокард с белком рецептора, сопряженного с G-белком, EDG2 и белком GFP, для получения миокардиальных клеток, которые могут быть использованы в способе идентификации соединения, которое модифицирует активность рецептора EDG2, связанного с G-белком.
Данное изобретение относится к способу идентификации соединения, которое модифицирует активность рецептора EDG2, в котором
a] представлены трансформированные клетки сердечной мышцы, которые экспрессируют рецептор EDG2 или слитый белок, содержащий рецептор EDG2,
b] может быть осуществлена обработка клеток из a] с использованием изопротеренола и/или лизофосфатидной кислоты,
c] представлено химическое соединение,
d] происходит взаимодействие клеток a] или b] с химическим соединением c],
e] определяют сократимость клеток d] и сопоставляют с сократимостью клеток, которые имеют те же самые характеристики, что и клетки a], но которые не взаимодействовали с химическим соединением c],
и где относительное увеличение или уменьшение сократимости клеток, которые взаимодействовали с химическим соединением d], вызванное этим соединением, показывает способность этого соединения модифицировать активность рецептора EDG2.
Данное изобретение относится, кроме того, к способу идентификации соединения, которое модифицирует активность рецептора EDG2, в котором
a] представлены трансформированные клетки сердечной мышцы, которые экспрессируют рецептор EDG2 или слитый белок, содержащий рецептор EDG2,
b] может быть осуществлена обработка клеток a] с использованием изопротеренола и/или лизофосфатидной кислоты,
c] представлено химическое соединение,
d] происходит взаимодействие клеток a] или b] с химическим соединением c],
e] определяют сократимость клеток d] и сравнивают с сократимостью клеток того же клеточного типа, что и клетки a], но которые не экспрессируют рецептор EDG2 или слитый белок, содержащий рецептор EDG2,
где относительное увеличение или уменьшение сократимости клеток, которые экспрессируют рецептор EDG2 или слитый белок, содержащий рецептор EDG2, вызванное этим соединением, показывает способность этого соединения модифицировать активность рецептора EDG2.
Кроме того, данное изобретение относится к аденовирусному вектору, состоящему из одного полинуклеотида из следующих групп:
a] полинуклеотида, имеющего последовательность, показанную в SEQ ID NO:5,
b] полинуклеотида, который на 95% идентичен полинуклеотиду SEQ ID NO:5,
c] полинуклеотида, который имеет по меньшей мере ту же самую длину, что и полинуклеотид SEQ ID NO:5, и который гибридизуется с полинуклеотидом SEQ ID NO:5 при применении гибридизации с жесткими условиями.
Аденовирусная последовательность вектора предпочтительно включает в себя полинуклеотидную последовательность, которая кодирует белок SEQ ID NO:2.
Гибридизация обозначает сборку двух отдельных полинуклеотидных цепей, которые имеют комплементарные последовательности, в двойные цепи. Гибридизация может происходить между двумя ДНК-цепями, одной ДНК- и одной РНК-цепью, а также между двумя РНК-цепями. Образование гибридных полинуклеотидных цепей может начинаться в растворе, который содержит двухцепочечные полинуклеотидные молекулы, путем нагревания этого раствора для разделения двойных цепей на одноцепочечные полинуклеотиды. Стадия нагревания может включать кипячение на водяной бане в течение 10-20 минут. При медленном охлаждении раствора до комнатной температуры, после того как он был нагрет, будет происходить гибридизация с образованием двухцепочечных молекул. В экспериментальных условиях гибридизацию обычно проводили с помощью гибридизационых фильтров, на которые полинуклеотиды фиксировались, что было показано блоттингом или электрофорезом. Гибридизация может быть визуализирована с использованием комплементарных полинуклеотидных молекул, несущих радиоактивную или флуоресцентную метку. Жесткость условий связана со степенью соответствия при определенных условиях. Для большего соответствия требуются более жесткие условия. В условиях гибридизации нуклеиновых кислот жесткость условий корректируют в зависимости от участвующих нуклеиновых кислот, а также от цели и требования. Условиями гибридизации высокой жесткости условий являются такие условия, при которых способны гибридизоваться только максимально комплементарные молекулы. Максимально комплементарный полинуклеотид имеет, например, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99% степень идентичности в отношении комплементарной молекулы-партнера. При пониженных требованиях к условиям жесткости гибридизация также происходит между полинуклеотидными молекулами, которые комплементарны только в определенных сегментах этой молекулы или которые имеют большие участки с ошибочно спаренными или неспаренными парами оснований.
Гибридизацией в жестких условиях может быть гибридизация, при которой стадия гибридизации в присутствии меченого зонда будет проводиться в водном растворе 2ХSSC при 68°С в течение по меньшей мере 2 часов, а последующие стадии промывки включают первую промывку в 2ХSSC/0,1% SDS при комнатной температуре в течение 5 минут, вторую промывку в 1ХSSC/0,1% SDS при 68°С в течение 1 часа и третью промывку в 0,2ХSSC/0,1% SDS при 68°С в течение еще одного часа.
Растворы 2ХSSC, 1ХSSC или 0,2ХSSC получают путем разбавления раствора 20ХSSC. Раствор 20ХSSC состоит из 3 моль/л NaCl и 0,3 моль/л Na-цитрата. Специалисту в данной области хорошо известны другие стандартные способы гибридизации полинуклеотидов в жестких условиях. Рекомендации для специалистов приводятся, в частности, в таких руководствах, как "Current Protocols in Molecular Biology (Wiley Interscience; ISBN: 0-471-50338-X; eds.: F.M. Ausubel, R. Brant, R.R. Kingston, D.J. Moore, J.G. Seidmann, K. Struhl).
Данное изобретение также относится к применению аденовирусного вектора, включающего один полинуклеотид из нижеследующих групп:
a] полинуклеотид, имеющий последовательность, показанную в SEQ ID NO:5,
b] полинуклеотид, который на 95% идентичен полинуклеотиду SEQ ID NO:5,
c] полинуклеотид, который имеет по меньшей мере ту же самую длину, что и полинуклеотид SEQ ID NO:5, и который гибридизуется с полинуклеотидом SEQ ID NO:5 при проведении гибридизации в условиях повышенной жесткости,
для конструирования трансгенных млекопитающих, у которых рецептор, сопряженный с G-белком, EDG2 экспрессируется временно или постоянно, по меньшей мере, в одной ткани. Такой тканью является предпочтительно часть сердца млекопитающего. Этой тканью также может быть ткань головного мозга, печени, почки или других органов, мышечная или жировая ткань млекопитающего.
Общие технические аспекты данного изобретения будут более подробно объясняться в следующих далее разделах.
Аденовирусы могут инфицировать большое количество различных типов клеток и тканей, как делящихся, так и неделящихся клеток. Это свойство, а также относительная легкость их получения и очистки, является причиной их интенсивного применения в качестве векторов генов. В вирус может быть встроено только приблизительно 2 т.п.н. чужеродной ДНК без существенного влияния на его стабильность или инфицирующую способность. Следовательно, введение более длинных последовательностей требует удаления части или всех генов этого вируса. Существуют ряд способов конструирования рекомбинантных аденовирусов.
Векторы могут быть использованы (из числа прочих применений): (i) в терапии злокачественных опухолей для доставки генов, которые могут супрессировать и элиминировать опухоли; (ii) в генной терапии, то есть, для доставки генов в ткани для дополнения дефектных генов; (iii) в дополнительной терапии для доставки генов, экспрессия которых может подавлять развитие заболевания.
В векторах первого поколения удаляли кассеты генов Е1 и/или Е3, что позволяло вводить до 6,5 т.п.н. чужеродной ДНК, часто под контролем гетерологичного промотора. В случае делеций Е1, старались сохранить ITR и пакующие последовательности. Удаление области Е1 имело дополнительное преимущество повреждения транскрипции генов Е2 (которые являются Е1-зависимыми) и, следовательно, репликации ДНК вируса и синтеза белков капсида вируса.
Вирусы, дефектные по Е1-области, могли бы быть размножены инфицированием клеток 293, которые обеспечивают продукты гена Е1 in trans. Хотя большое количество предварительных исследований in vitro были многообещающими, вскоре стало очевидно, что экспрессия этого трансгена in vivo была лишь временной и подавлялась очень сильным иммунным ответом в основном против антигенов вирусного капсида, а также экспрессируемого трансгена. Наблюдения показали, что одной из причин этого ответа является тот факт, что большое количество клеток содержит Е1-подобные белки, которые делают возможным функционирование Е2-генов, хотя и при пониженных уровнях. В свою очередь, это облегчает репликацию ДНК и синтез поздних структурных антигенов и продукцию репликативно-компетентного аденовируса (RCA). Также очевидно, что, при более высокой множественности заражения (m.o.i.) могла бы элиминироваться Е1-зависимая транскрипция гена Е2.
Следующим подходом было конструирование векторов (используя подходящие комплементарные клеточные линии) с частично или полностью удаленными Е2-генами и, следовательно, неспособных к репликации вирусной ДНК и продукции RCA. Получение RCA могло бы также предотвращаться при конструировании клеточных линий, которые не содержат аденовирусных последовательностей, перекрывающих последовательности в векторе. Тем не менее, основное препятствие для достижения устойчивой экспрессии трансгена - иммунный ответ хозяина сохранялся и был особенно выражен при попытке повторных инфицирований. Ряд исследований подтвердил, что инфицирование самого рекомбинантного вируса было достаточным для индукции иммунного ответа, что, возможно, не является неожиданным в связи с ранней активацией каскадов передачи сигналов, указанных выше, и сильной антигенности компонентов капсида.
Другие, гораздо более сложные векторы (третье поколение) были сконструированы путем делетирования других вирусных генов (Amalfitano et al., 1988), и в самых поздних из них были удалены все или почти все вирусные гены. Эти так называемые "gutless" векторы (Hardy et al., 1997) первоначально сохраняли только ITR и пакующие последовательности и для их размножения требовался вспомогательный вирус и подходящие комплементарные клетки с последующей тщательной очисткой. Тем не менее, сохранялись трудности, связанные с этими способами, в основном в связи с контаминацией вспомогательным вирусом и нестабильностью вектора. Дальнейшая разработка, в которой предотвращалась упаковка вспомогательного вируса, включала в себя использование Cre-lox- системы, независимой от вспомогательного вируса.
Система AdEasy™ для получения рекомбинантных аденовирусов является коммерчески доступной от Qbiogene. Конструирование рекомбинантного аденовируса обычно является двухстадийным процессом, в котором желаемую экспрессионную кассету сначала собирают в вектор-переносчик, а затем переносят в аденовирусный геном гомологичной рекомбинацией. Встраивание ДНК путем гомологичной рекомбинации является наиболее эффективным путем введения гена в аденовирусный вектор по двум причинам: 1) аденовирусные ДНК являются большими линейными молекулами, которые содержат сайты почти всех ферментов рестрикции, и 2) этот геном является достаточно большим (36 т.п.н.) для легкого манипулирования им.
С векторной системой AdEasy™ этот основной вектор, содержащий большую часть аденовирусного генома, используют в форме суперспиральной плазмиды, а не в виде линейной ДНК. Стадию гомологичной рекомбинации проводят в Escherichia coli. В системе AdEasy™ представляющую интерес кДНК сначала клонируют в вектор-переносчик. Затем полученную плазмиду линеаризуют с помощью PmeI и котрансформируют в штамм E.coli BJ5183 вместе с pAdEasy-1, плазмидой из вирусной ДНК. В pAdEasy-1 делетированы Е1 и Е3; функции Е1 могут дополняться в клетках 293А. Рекомбинации селектируют с помощью канамицина и подвергают скринингу рестрикционным анализом. Затем рекомбинантную аденовирусную конструкцию расщепляют PacI для освобождения ее ITR (обращенного концевого повтора) и трансфицируют в клетки QDI-293А для получения вирусных частиц.
Стадия гомологичной рекомбинации осуществляется между линеаризованным вектором-переносчиком и интактной суперспиральной аденовирусной плазмидой. Ген устойчивости к канамицину, присутствующий в векторе-переносчике, делает возможным селекцию рекомбинантов. Так как расщепленные векторы-переносчики AdEasy™ дают только низкий фон устойчивых к канамицину колоний, эта система гомологичной рекомбинации имеет высокое отношение сигнала к шуму. Штамм E.coli BJ5183 не является recA, но является дефектным по другим ферментам, которые опосредуют рекомбинацию бактерий, и выбран благодаря своей высокой эффективности трансформации и способности к рекомбинации. После осуществления и подтверждения рекомбинации аденовирусная рекомбинантная ДНК может быть просто перенесена в обычный штамм recA, endA-штамм, такой как DH5α, для получения большего выхода ДНК. Вследствие его recA-статуса, штамм DH5α не может быть использован для получения аденовирусных рекомбинантов путем гомологичной рекомбинации.
Зеленый флуоресцентный белок (GFP) из Aequora victoria быстро стал стандартным репортерным белком многих биологических систем. GFP является уникальным среди светоизлучающих белков, так как он не требует присутствия кофакторов или субстратов для генерирования света. У медузы Aequora victoria GFP действует зависимым от кальция образом. При связывании Са2+ с другим биолюминесцентным белком экворином, переносящим энергию непосредственно к GFP, происходит испускание зеленого света. Этот перенос энергии может имитироваться экспериментально, подвергая GFP действию стандартного длинноволнового ультрафиолетового света. Доступными являются изоформы GFP, которые испускают синий или красный свет и которые являются стабильными при повышенных температурах. GFP сначала использовали для наблюдения за живыми клетками под флуоресцентным микроскопом для мониторинга локализации белка и для визуализации динамических клеточных событий. Слияние любого клонированного гена, представляющего интерес, и GFP может быть получено способами субклонирования, и слитый ген может быть введен в интересующий организм временной или стабильной экспрессией. Судьба полученного белка внутри живой клетки может затем отслеживаться с помощью обычной флуоресцентной микроскопии. Для обнаружения не требуется фиксация или увеличение проницаемости клеток. Подобным образом белок может быть исследован в ткани животного посредством одновременной экспрессии такого белка и GFP.
Получение клеток включает в себя получение клеточного материала, культивирование и дополнительную обработку. Клетки получают, например, извлечением подходящего клеточного материала из органов или тканей или размножением подходящих клеточных линий или микроорганизмов. Для культивирования могут быть использованы различные подходящие культуральные среды. Клетки поддерживают при оптимальной для конкретного организма температуре. По мере необходимости, в каждом случае к среде для роста добавляют консерванты, антибиотики, индикаторы рН, компоненты сыворотки крови, сыворотку крови, вспомогательные или другие вещества. Способы получения клеточного материала, культивирования и дополнительной обработки описаны в общепринятых справочниках (например: Basic Cell Culture; Ed. J.M.Davis; IRL Press; 1994).
Применение рекомбинантных способов дает конструкцию, экспрессируемую в клетке, присутствующую в форме полинуклеотидной последовательности, которая может быть получена специалистом в данной области обычным способом с применением его знаний. Специалист в области молекулярной биологии/биохимии может найти соответствующую информацию для специалистов, например, в F.M.Ausubel et al.; Current Protocols in Molecular Biology; John Wiley and Sons; New York. Векторную конструкцию получают путем включения полинуклеотида, кодирующего аминокислотную последовательность, например, GPCR, в вектор экспрессии. Вектором экспрессии является вектор, в котором полинуклеотидная последовательность может экспрессироваться в клетке-хозяине в белок. Векторы могут быть получены из плазмид, вирусов или космид и должны быть способны к автономной репликации. Обычно они содержат сайт инициации репликации, сайты расщепления рестриктаз и маркерные гены, такие как, например, гены устойчивости к антибиотикам. В экспрессирующем векторе полинуклеотидная последовательность, которая должна быть размножена или которая была введена извне, находится под функциональным контролем промотора. Промотором является функциональная полинуклеотидная последовательность различной длины, которая используется для регуляции транскрипции, то есть синтеза мРНК полинуклеотидной последовательности, расположенной непосредственно 3- от указанного промотора. Существуют промоторы, активные только у прокариот, такие как, например, промоторы lac, tac и trc, а также промоторы, которые активны только у эукариот, такие как, например, промоторы CMV или ADH. В предпочтительном варианте осуществления, рекомбинантная векторная конструкция содержит вектор экспрессии, применимый у эукариот и/или у прокариот. Вектор экспрессии содержит промотор, который может быть функционально связан с полинуклеотидной последовательностью таким образом, что белок, кодируемый указанной полинуклеотидной последовательностью, синтезировался в организме, например, бактерии, грибе или клеточной линии эукариотических клеток. Промотор может быть индуцибельным, например, триптофаном, или может быть конститутивно активным. Примерами экспрессирующих векторов являются pUC18, pUC19, pBlueScript, pcDNA3.1 и тому подобное.
Трансфекцией является введение чужеродных полинуклеотидных последовательностей в клетку-хозяина с помощью вектора и последующее увеличение количества указанной полинуклеотидной последовательности до любого числа идентичных копий.
Клеточную линию временно трансфицируют рекомбинантной конструкцией обычными способами, которые могут быть найдены специалистом в данной области в вышеупомянутых Current Protocols in Molecular Biology; John Wiley and Sons; New York или в Sambrook et al.: A Laboratory Manual, Cold Spring Harbor Laboratory, ISBN 0-87969-309-6. Примерами таких обычных способов являются электропорация, соосаждение Са2+-фосфатом и трансфекция с помощью липосом. Экспрессия трансфицированных генов в клетке-хозяине может быть обнаружена при Вестерн-блоттинге клеточных лизатов трансфицированных клеток в сочетании с иммунологическим способом обнаружения. В отношении этого необходимые лабораторные протоколы могут быть найдены специалистом в данной области в вышеупомянутых руководствах. Специфические антитела для иммунодетекции рецепторов GPCR, которые подходят для осуществления способа по данному изобретению, являются коммерчески доступными.
Химическое соединение получают, в частности, химическим синтезом и выделением химических веществ из биологического материала.
Специалист в данной области может применять стандартные способы для химического синтеза соединения или для выделения вещества из клеток. Такие способы доступны для специалиста из таких руководств, как Organic Synthesis Workbook; 1995; John Wiley and Sons; ISBN 3-527-30187-9, The Organic Chemistry of Drug Synthesis; 1998; John Wiley and Sons; ISBN 0-471-24510-0 или Bioactive Compounds from Natural Sources; 2001; Taylor and Francis; ISBN 0-7484-0890-8.
Соединения, полученные синтезом или выделением, могут быть растворены в подходящем растворителе. Подходящие растворители могут содержать воду, буферные вещества (например, Tris, HEPES, MOPS и тому подобное), моновалентные и/или двухвалентные ионы (например, К+, Na+, Mg2+, Ca2+и тому подобное), кислоты (например, HCl, H2SO4, муравьиную кислоту, уксусную кислоту и тому подобное), основания (например, NaOH и тому подобное), спирт (например, метанол, этанол, глицерин), детергенты (например, додецилсульфат натрия и тому подобное), органические растворители (например, формамид, ацетон, диметилсульфоксид и тому подобное) и другие компоненты, в частности солюбилизаторы и стабилизаторы.
Специалист в данной области может провести взаимодействие химического соединения и указанной клеточной линии с помощью обычных лабораторных способов. Взаимодействие может проводиться, например, в колбах Эрленмейера, пробирках, флаконах Эппендорфа или на микротитрационных планшетах. Для этого взаимодействия могут быть использованы терморегулируемые термостаты с установленной постоянной температурой, например 30°С или 37°С, или с установленными условиями СО2 или влажности. Взаимодействие также может, в частности, проводиться в лабораторных автоматических устройствах, обеспечивающих это взаимодействие (FLIPR). Взаимодействие может проводиться в течение различных периодов времени, от нескольких секунд до минут и до нескольких часов. Для каждого случая выбирают условия в зависимости от рецептора, клеточной линии и химического соединения.
Окончательная форма фармацевтического препарата относится к окончательной композиции, например, в форме таблетки, гранул, спрея, раствора, мази, настойки или других готовых форм.
Обработкой до готовой формы обычно называют получение конкретной композиции суточной дозы в диапазоне от 0,3 мг до 100 мг (обычно от 3 мг до 50 мг) в день и на 1 кг массы тела, например, 3-10 мг/кг/день. Внутривенная форма может быть, например, в диапазоне от 0,3 мг до 1,0 мг/кг, и ее можно вводить предпочтительно в виде инфузии от 10 нг до 100 нг на килограмм в минуту. Подходящие инфузионные растворы для этих целей могут содержать, например, от 0,1 нг до 10 мг, обычно от 1 нг до 10 мг на миллилитр. Единичные дозы могут содержать, например, от 1 мг до 10 г активного вещества. Таким образом ампулы для инъекций могут содержать, например, от 1 мг до 100 мг, и композиции в виде единичных доз, которые могут вводиться перорально, такие как, например, таблетки или капсулы, могут содержать, например, от 1,0 до 1000 мг, обычно от 10 до 600 мг.
Примеры
Нижеследующие примеры описывают данное изобретение, не ограничивая его объем этими примерами.
Описание экспериментальных животных
Используемые в этих исследованиях животные являются десятинедельными самками Новозеландских белых кроликов, поставляемыми Asamhof, Kissing (Germany). В начале исследования масса животных составляла от 2,7 до 3,3 кг.
Условия выращивания и содержания экспериментальных животных
Молодых животных отлучают от матери на 30-й день. Для минимизации стресса отлучения маток отделяют от молодняка, так чтобы приплод оставался вначале вместе. Через приблизительно 10-14 дней молодняк размещали по парам в клетки для откорма (длина × ширина × высота = 28,5×60×34 см) и затем через приблизительно две недели их размещали по отдельности. Систему кормления осуществляли в соответствии с системой «all-in/all-out" для облегчения чистки и дезинфекции.
Корм получали на собственном сельскохозяйственном производстве и давали кроликам ad libitum, как и питьевую воду.
Климат: Скорость вентиляции составляет 10000 м3/час летом и 3000 м3/час зимой. Особое внимание уделяется недопущению сквозняков. В холодную погоду температуру поддерживают при приблизительно 15°С; перегревание помещения для животных летом предотвращается настолько, насколько это возможно. Отлученный молодняк содержат при приблизительно 19°С. Аммиак в помещении для животных поддерживается ниже приблизительно 30 м.д., относительная влажность ниже 70%. Помещение для выкармливания освещается в течение 16 часов при интенсивности приблизительно 20 люксов.
Содержание тестируемых животных
Кроликов привозят в вентилируемом транспортном средстве в компанию, где их оставляют на адаптационный период 2-3 дня для акклиматизации к новому рациону питания и окружающей обстановке.
Кроликов содержат в обычных клетках. Клетка состоит из нержавеющей стали с PVC-вставками; площадь пола клетки составляет 4040 см2 и имеет форму перфорированного днища. Лотки для экскрементов ежедневно очищают, и клетки промывают и стерилизуют горячим воздухом один раз в неделю. Их поддерживают при постоянных условиях при комнатной температуре между 18°С и 21°С и относительной влажности 55±5%. Так как помещение для животных имеет окна, освещение соответствует природному циклу ночь/день при интенсивности по меньшей мере 100 люксов.
Анестезия и подготовка к хирургии
В первый день исследования до начала анестезии корм и вода кроликам доступны ad libitum. Затем предназначенное для исследования животное взвешивают и подвергают клиническому исследованию, в частности исследуют сердечно-сосудистую систему и дыхательную систему. У животных обеспечивают двойной внутривенный доступ через постоянные катетеры в левой и правой боковых ушных венах (Venflon™ 08×25 мм), через которые затем проводят анестезию 1% пропофолом (Disoprivan, Fresenius AG, Bad Homburg) в дозе 7 мг/кг массы тела в.в. На роговицу сразу после начала анестезии наносят глазную мазь (Vitamin A Dispersa, Ciba Vision®, Grossostheim). После исчезновения выпрямительного рефлекса кроликов выбривают вентрально на шее и на груди между локтевыми областями и последним ребром и затем интубируют продвижением трубки Magill c манжетой (внутренний диаметр 2,5-3,5 мм, Rüsch AG, Waiblingen) в трахею во время вдоха.
Для поддержания анестезии во время операции, животным вводят 2% пропофол (Disoprivan 2%, Zeneca, Italy) в.в. в дозе 12-14 мл/час через инфузионный аппарат (Perfusor®, ED1-300, B. Braun, Melsungen AG). В качестве аналгезирующего средства сразу же после интубации кроликам вводят фентанил (Fentanyl-Janssen 0,5 мг, Janssen-Cilag GmbH, Neuss) в дозе 0,01 мг/кг в.в. и затем, по мере необходимости, во время операции, приблизительно каждые 30 минут, для поддержания переносимости операции.
Используя аппарат для вентиляции легких для небольших животных (Anesthesia Workstation, Hallowell EMC, Volker GmbH, Kaltenkirchen), кроликов вентилируют 100% кислородом при давлении дыхания приблизительно 10 мм рт.ст., дыхательном объеме 8-12 мл/кг массы тела и частоте дыхания 29-32 вдохов в минуту, что дает парциальное давление СО2 приблизительно 35 мм рт.ст. выдыхаемого воздуха. Мониторинг деятельности сердечно-сосудистой системы осуществляют посредством ЭКГ (Medtronic®, 9790 Programmer, Vitatron Medical B.V., Dieren, Netherlands). Мониторинг дыхания и кровотока осуществляют пульсовой оксиметрией и капнометрией.
Пережатие аорты
Препарирование правой общей сонной артерии. Введение полиуретанового катетера (Cavafix®, 1,1·1,7 мм/16G, ссылка 4173589, B. Braun Melsungen AG, Melsungen, Germany) в артерию. После канюлирования правой общей сонной артерии грудную клетку открывают через третий межреберный промежуток. Вирус вводят в миокард по способу Sigscreen®, что обеспечивает, в частности, сохранение инфузируемого вектора этой области. Затем грудную клетку закрывают наложением лигатур (Nylon®, 2-0 USP) и зашивают (Vicryl® (3-0) и Nylon® (3-0)).
Аналгезия: после операции животные получают карпрофен (Rimadyl®, Pfizer, 4 мг/кг каждые 12 часов) и бупренофин (Temgesic®, Boehringer. 0,01 мг/кг каждые 12 часов) в течение 72 часов.
Эвтаназия животных
В последний день исследования животные подвергаются общей анестезии, как описано в Разделе 4. Эвтаназия происходит в глубоком наркозе, индуцированном пентобарбиталом 0,48 г/кг в.в. (Narcoren®, Rhone-Merieux GmbH, Laupheim).
Посмертная макропатологическая диагностика и взятие проб
Сразу же после смерти сердце удаляют так быстро, как это возможно, разделяя грудную стенку билатерально на уровне реберного края и полным вычленением грудины. Сердце отделяют от афферентных и эфферентных сосудов и промывают от крови холодным стерильным физиологическим раствором (изотонический раствор хлорида натрия, Delta-Pharm, Boehringer, Ingelheim), содержащим 5000 МЕ гепарина. После макроскопического патологического исследования и взвешивания сердце консервируют в интактном виде для последующего исследования. Сердца, предназначенные для выделения отдельных клеток, кратковременно хранят в стерильной пробирке холодного гепаринизированного физиологического раствора при приблизительно 4°С перед предстоящей срочной обработкой. Для определения флуоресценции GFP готовят замороженные срезы. Свежеудаленные сердца, предназначенные для клеточной микроскопии, промывают аналогичным образом стерильным физиологическим раствором, сушат с помощью целлюлозы и затем подвергают глубокому замораживанию в тест-пробирке с жидким азотом (-196°С) и хранят при -80°С перед последующей обработкой. Животных подвергают аутопсии в соответствии с руководствами колледжа ветеринаров, обращая особое внимание на оценку степени типичных симптомов сердечной недостаточности: асциты, плевральный выпот, масса сердца, форма сердца, печеночный застой и масса печени.
Удаление тушек
После сбора в камере для глубокого замораживания при -20°С тушки собирали для захоронения.
Конструирование и очистка рекомбинантного аденовируса
Рецептор EDG2 человека клонировали, используя подход, основанный на ПЦР, на основе кодирующей последовательности рецептора EDG2 человека. Получали рекомбинантные (дефектные по Е1/Е3-области) flag-меченые аденовирусы для этого рецептора (Ad-EDG2-GFP), экспрессирующие трансген и зеленый флуоресцентный белок (GFP) под контролем двух независимых промоторов CMV. В качестве контроля использовали Ad-GFP без дополнительных трансгенов. Получали большое количество исходных вирусных растворов и определяли титры аденовируса, используя титрование бляшек и титрование экспрессии GFP в неэкспрессирующих Е1 клетках.
Клонирование EDG2
ДНК рецептора EDG2 амплифицировали из кДНК из головного мозга человека с помощью ПЦР, используя прямой праймер 5'-gcggggggtaccaccatggctgccatctctacttccatcc-3' (SEQ ID NO:5) и обратный праймер 5'-gcggggctcgagtcacttgtcgtcgtcgtccttatagtcaaccacagagtgatcattgct-3' (SEQ ID NO:6).
Реакцию ПЦР проводили отжигом при 58°С в течение 1 минуты и при температуре амплификации 72°С в течение 1 минуты на протяжении 20 циклов с использованием Expand High Fidelity PCR System (Roche Molecular Biochemicals, Mannheim, Germany). В реакции ПЦР получали НА-tag-эпитоп из 9 аминокислот из гемаглютинина вируса гриппа А человека в рамке считывания на 3'-конце этого гена.
ПЦР-фрагмент клонировали в плазмиду pAD-Shuttle (Q Biogene, Htidelberg, Germany), используя сайты рестрикции для KpnI и XhoI, и последовательность полученной плазмиды pAD Track-CMV-EDG2 подтверждали секвенированием (MediGenomix, Martinsried, Germany).
SEQ ID NO:1 представляет полинуклеотидную последовательность EDG2, содержащую кодирующий регион НА-tag в 30 нуклеотидах 3'-конца.
SEQ ID NO:2 представляет аминокислотную последовательность EDG2, содержащую НА-tag из 9 аминокислот на С-конца.
SEQ ID NO:8 представляет полинуклеотидную последовательность EDG2, содержащую сайты 5'-HindIII и 3'-XhoI. Ген EDG2 клонирован в сайты HindIII/XbaI pcDNA 3.1 (Invitrogen). Такая векторная конструкция также подходит для амплификации гена EDG2.
Конструирование рекомбинантного flag-меченого аденовируса (pAD easy 1-EDG2-HA-GFP)
Плазмиду pADTrack-CMV-EDG2 с-НА линеаризовали при помощи PmeI (New England Biolabs, Beverly, MA) в течение ночи, дефосфорилировали и очищали (набор для очистки GFX DNA и Ge1; Amersham Pharmacia Biotech, Uppsala, Sweden). Для гомологичной рекомбинации электрокомпетентную E.coli BJ5183 (Stratagene, La Jolla, California) котрансформировали 1 мкг линеаризованной плазмиды pADTrack-CMV-EDG2 с-НА и 0,1 мкг pADeasyI при 2500 В, 200 Ватт и 25 мкФ (E.coli-генератор импульсов; Biorad, Heidelberg, Germany), высевали и инкубировали в течение ночи при 37°С. Полученный вектор, pAdEasyI-edg2-cHA-GFP, содержал полную рекомбинантную ДНК аденовируса для трансфекции. Эта полноразмерная последовательность ДНК представлена в SEQ ID NO:5.
Колонии проверяли после минипрепарирования плазмидной ДНК с использованием PacI и положительные клоны повторно трансформировали в E.coli DH5α.
Для трансфекции (Effectene Transfection reagent; Qiagen, Hilden, Germany) клеток 293 плазмидную ДНК расщепляли PacI. Клетки культивировали в течение 7 дней и собирали соскабливанием и центрифугированием. Осадок ресуспендировали в PBS Дульбекко и клетки лизировали четырьмя повторными циклами заморозки (-80°С) и оттаивания (37°С). Дебрис клеток удаляли центрифугированием и лизат хранили при -80°С. Для селекции бляшек рекомбинантного вируса клетки 293 инфицировали в PBS Дульбекко в течение 1 часа при комнатной температуре при осторожном перемешивании с различными серийными разведениями лизата, полученного при трансфекции. После инфицирования на клетки наслаивали среду для роста, содержащую 0,5% агарозу (смесь 1:1 модифицированной среды Игла 2x, Gibco Life Technologies #21935, дополненной 20% сывороткой, 2x пенициллин/стрептомицин, 2х L-глутамином, и агарозы в воде 1%, Seacam). Спустя 5-14 дней после инфицирования слой клеток подвергали мониторингу на образование бляшек, которые соскребали при помощи пастерки, ресуспендировали в 0,5 мл PBS Дульбекко и хранили при -80°С. Эти бляшки использовали для дополнительных циклов амплификации на клетках 293.
Модель сердечной недостаточности
Новозеландских белых кроликов подвергали кратковременной кардиостимуляции при 360 сердечных сокращениях в минуту после имплантации электрокардиостимулятора (пейсмекера). При этом способе индуцируемая тахикардией сердечная недостаточность (HF) развивается при повторении на протяжении двух недель. Средняя величина +dp/dt max (пика первой производной давления) в декомпенсированных сердцах составляла 2200±320 мм рт.ст./сек (против 3200±390 мм рт.ст./сек контроля со здоровым сердцем; р<0,05) и КДД (конечное диастолическое давление в левом желудочке) увеличивалось с 3,6±0,4 мм рт.ст. до 13±3,3 (р<0,05).
Перенос аденовирусного гена в миокард кроликов
Перед началом кратковременной кардиостимуляции все кролики получали через катетер аденовирусный ген (4×1010 бое) в миокард. Для хирургического вмешательства кроликов анестезировали фентанилом и пропофолом. После окончания экспериментов эффективность переноса гена оценивали во всех сердцах, исследуя поперечные срезы, полученные при замораживании, на экспрессию GFP при помощи флуоресцентной микроскопии. Морфологические изменения оценивали после фиксации 4% параформальдегидом. Перенос гена приводил к воспроизводимой экспрессии трансгена в ˜50% кардиомиоцитов.
Измерения укорочения в выделенных кардиомиоцитах
Сократительную способность инфицированных кардиомиоцитов измеряли с использованием электро-оптической системы мониторинга, подключенной к цифровому устройству оценки амплитуды и скорости укорочения и релаксации. Трансген-положительные кардиомиоциты идентифицировали по коэкспрессии GFP под флуоресцентным светом. После того как амплитуда сокращения становилась стабильной, использовали увеличивающиеся концентрации изопротеренола при константных концентрациях лизофосфатидной кислоты (LPA; 10-5 моль/л); или добавляли увеличивающиеся концентрации LPA к константным концентрациям изопротеренола (10-8 моль/л).
Сокращение отдельных клеток
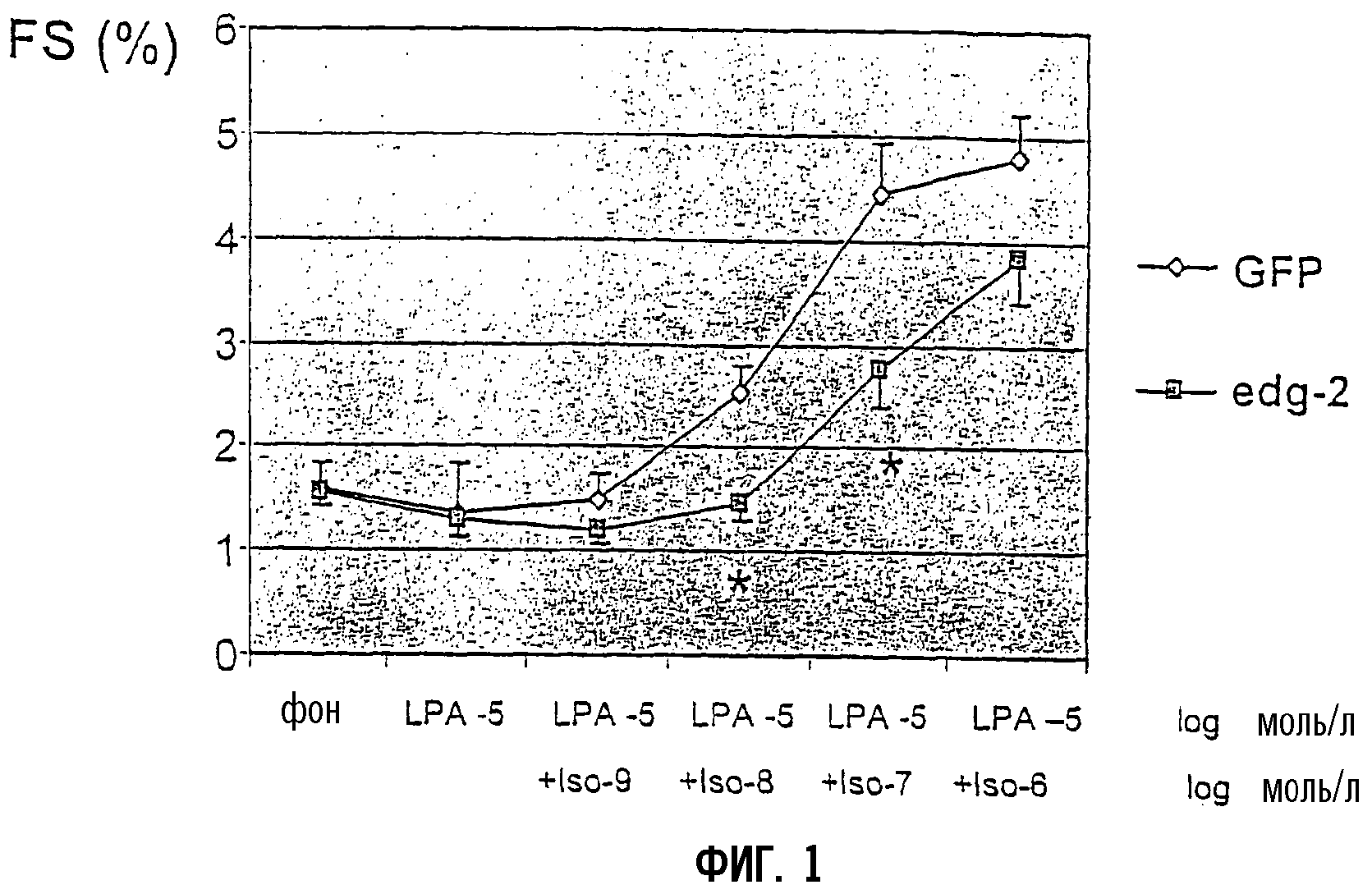
Для исследования эффекта EDG2 на сократимость кардиомиоцитов измеряли фракционное укорочение и скорость укорочения в отдельных, изолированных кардиомиоцитах декомпенсированных сердец после переноса гена ex vivo. При концентрации лизофосфатидной кислоты (LPA) 10-5 моль/л, которая не влияет на фоновую сократимость, увеличивающиеся концентрации изопротеренола имели значимо более низкое положительное миотропное действие в сверхэкспрессирующих EDG2 кардиомиоцитах (фиг.1). После предварительной стимуляции с помощью низкой концентрации изопротеренола (10-8 моль/л), увеличивающиеся концентрации LPA проявили значительное отрицательное миотропное действие в сверхэкспрессирующих EDG2 кардиомиоцитах, в то время как в контрольной GFP-группе не наблюдали никакого эффекта (фиг.2). В отсутствие предварительной стимуляции изопротеренолом LPA не влияла на сократительную способность кардиомиоцитов.
Вестерн-блот инфицированных кардиомиоцитов
Кардиомиоциты собирали через 48 часов после инфицирования аденовирусом. Клетки гомогенизировали и затем цитозольные экстракты использовали для вестерн-блоттинга с антителами против НА-метки или против EDG2. В качестве вторых антител использовали конъюгированные с пероксидазой хрена лошадиные антикроличьи антитела (Dianova, Germany).
Аденовирусная доставка трансгена in vivo в декомпенсированное сердце
Сверхэкспрессию всех трансгенов исследовали наблюдением коэкспрессии GFP в сердцах после переноса гена in vivo, так как все трансгены экспрессировались вместе с GFP. В макроскопическом срезе сердца кролика, инфицированного Ad-EDG2-GFP, была показана коэкспрессия, происходящая по всему левому желудочку, при окрашивании анти-GFP-антителами.
Экспрессия трансгена, оцениваемая при помощи Вестерн-блоттинга
На Вестерн-блоттинге регистрировалась экспрессия EDG2 с использованием антитела, направленного против НА-метки, или с использованием специфического антитела против EDG2 в кардиомиоцитах.
Получение и культивирование зрелых желудочковых кардиомиоцитов и инфицирование аденовирусом
Из декомпенсированных сердец Новозеландских белых кроликов выделяли отдельные кальций-толерантные желудочковые кардиомиоциты. Кратко, сердца обрабатывали и подвергали действию коллагеназы. Выделенные кардиомиоциты культивировали в модифицированной среде М199 на предварительно покрытых ламинином чашках (5-10 мкг/см2) при плотности 1,5×105 клеток на 1 см2 (при 5% СО2 и 37°С). Для экспериментов по сократимости эти клетки инфицировали аденовирусом (множественность заражения (moi) 1 бое на клетку) через 5 часов после высевания. В этом титре 50-60% инфицированных кардиомиоцитов экспрессировали этот трансген.
Измерения сократительной способности миокарда при помощи эхокардиографии и интравентрикулярного катетера (tip-катетера)
Сократимость левого желудочка изучали эхокардиографией перед началом кратковременной кардиостимуляции, через 1 неделю и через две недели после начала электрокардиостимуляции. Измерения с tip-катетером выполняли через 2 недели после кардиостимуляции. Кроликов анестезировали; постоянно выполняли мониторинг ECG.
Для эхокардиографии зонд 7,5 МГц фиксировали на треножнике. Стандартные срезы, которые были хорошо воспроизводимыми, регистрировали. Для измерений с tip-катетером tip-катетер Millar 3F, соединенный с дифференцирующим устройством, помещали в левый желудочек через трубку, помещенную в сонную артерию. После определения фона сократимости и давления в левом желудочке вводили инъекцией 200 мкл NaCl (0,9%) в качестве отрицательного контроля. Изопротеренол и лизофосфатидную кислоту (LPA) выделяли инфузией внутривенно при увеличивающихся дозах. После периода уравновешивания в течение 20 минут проводили измерения tip-катетера.
Ухудшение LV-дисфункции (дисфункции левого желудочка) в индуцированной электрокардиостимуляцией сердечной недостаточности
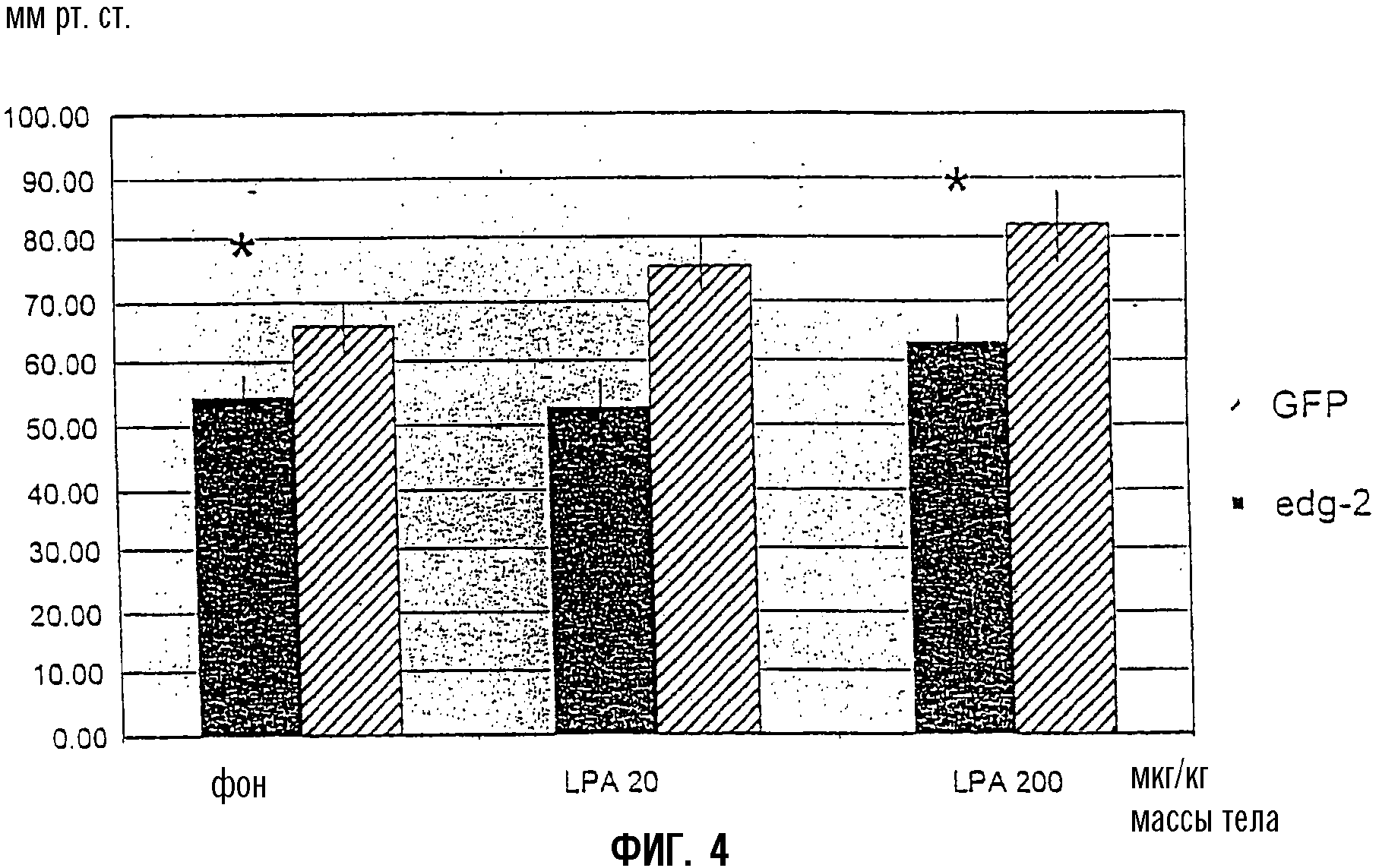
На Фиг.3 показано измерение с использованием tip-катетеризации через 2 недели кратковременной кардиостимуляции у кроликов, страдающих тяжелой сердечной недостаточностью (NYHA IV). В группе с экспрессией EDG2 первые производные LV-давления (dp/dt max) были значительно ниже, чем в инфицированной Ad-GFP контрольной группе при фоновых условиях и при увеличивающихся дозах LPA. То же самое наблюдали при увеличении систолического давления левого желудочка (LV) (фиг.4).
Эхокардиографией была показана явная гипертрофия миокарда через 2 недели в сверхэкспрессирующих EDG2 сердцах, которая также подтверждалась уменьшениями систолических и диастолических диаметров. Средняя толщина задней стенки и перегородки левого желудочка была значительно больше в сверхэкспрессирующих EDG2 сердцах по сравнению с GFP-контролями. Временной ход фракционного укорочения LV (FS) оценивали последовательной эхокардиографией на протяжении двухнедельного периода наблюдения. В обеих группах FS постепенно уменьшалось на протяжении периода времени быстрой электрокардиостимуляции.
Описание фигур:
Фиг.1:
Амплитуда сокращения отдельных кардиомиоцитов, выделенных из декомпенсированных сердец. Кардиомиоциты инфицировали ex vivo либо Ad-GFP, либо Ad-EDG2-GFP. Фракционное укорочение (FS) определяли в ответ на увеличивающиеся концентрации изопротеренола после предварительной стимуляции 10 мкМ LPA. Данные представляют средние значения ±SEM (стандартная ошибка среднего).
Фиг.2:
Амплитуда сокращения отдельных кардиомиоцитов, выделенных из декомпенсированных сердец. Подобно экспериментам, представленным на фиг.1, FS сравнивали в кардиомиоцитах после переноса гена либо с Ad-GFP, либо с Ad-EDG2-GFP in vitro. Фракционное укорочение определяли в ответ на увеличивающиеся концентрации LPA после предварительной стимуляции 10 мкМ изопротеренолом. Данные представляют средние значения ±SEM (стандартная ошибка среднего).
Фиг.3:
Пик первой производной левого вентрикулярного давления (LV dp/dt max) при базовой линии (фоне) и в ответ на увеличивающиеся дозы LPA, определенный tip-катетеризацией у кроликов с терминальной сердечной недостаточностью, обусловленной кратковременной кардиостимуляцией, и через две недели после переноса гена либо GFP, либо EDG2. Данные представляют средние значения ±SEM (стандартная ошибка среднего). Все измерения производили у 8 животных в трех повторностях, *р<0,05 в сравнении с GFP.
Фиг.4:
Систолическое давление левого желудочка при базовой линии (фоне) и в ответ на увеличивающиеся дозы LPA, определенное tip-катетеризацией у кроликов с терминальной сердечной недостаточностью, обусловленной кратковременной кардиостимуляцией, и через две недели после переноса гена либо GFP, либо EDG2. Данные представляют средние значения ±SEM (стандартная ошибка среднего). Все измерения производили у 8 животных в трех повторностях, *р<0,05 в сравнении с GFP.
Реферат
Изобретение относится к области генной инженерии и молекулярной биологии. Получен рекомбинантный аденовирусный вектор, экспрессирующий рецептор, сопряженный G-белком, EDG2 и GFP белок, а также трансфицированая миокардиальная клетка млекопитающего и трансгенное млекопитающее. Изобретение может быть использовано в экспериментальных целях в ветеринарии и медицине в качестве модели сердечной недостаточности. 7 н. и 10 з.п. ф-лы, 4 ил.

Комментарии