Лейколектины и их применение - RU2528860C2
Код документа: RU2528860C2
Чертежи

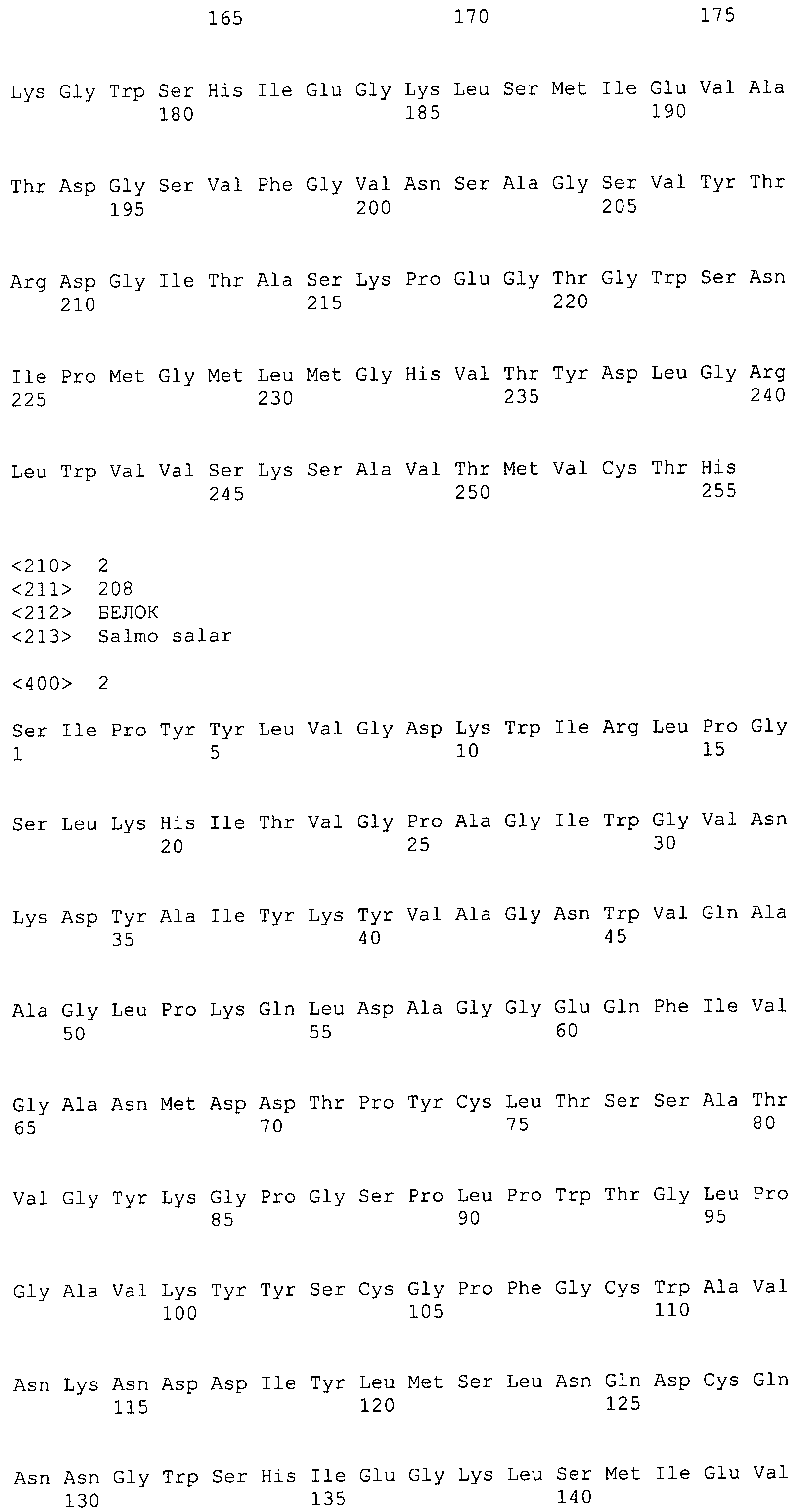
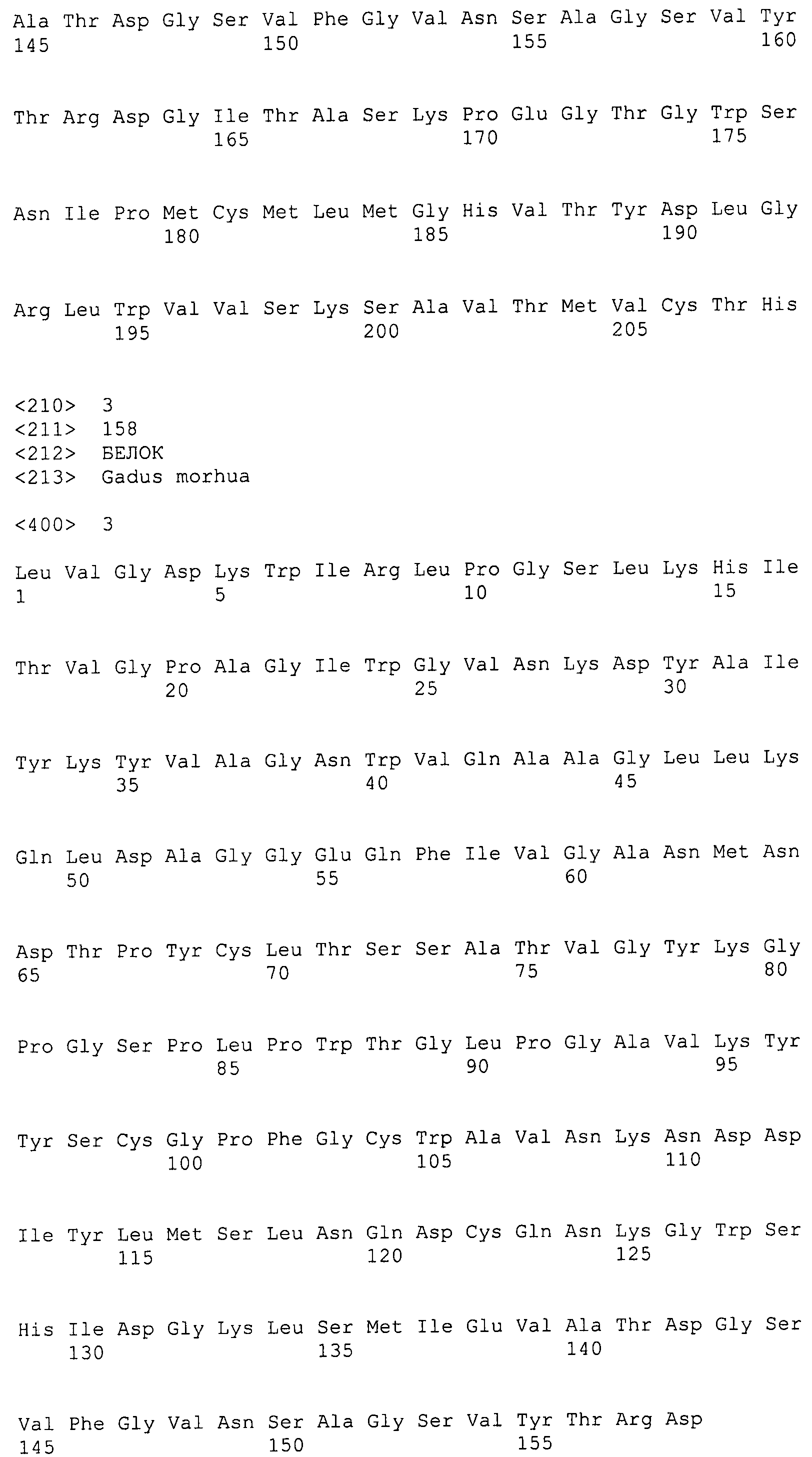
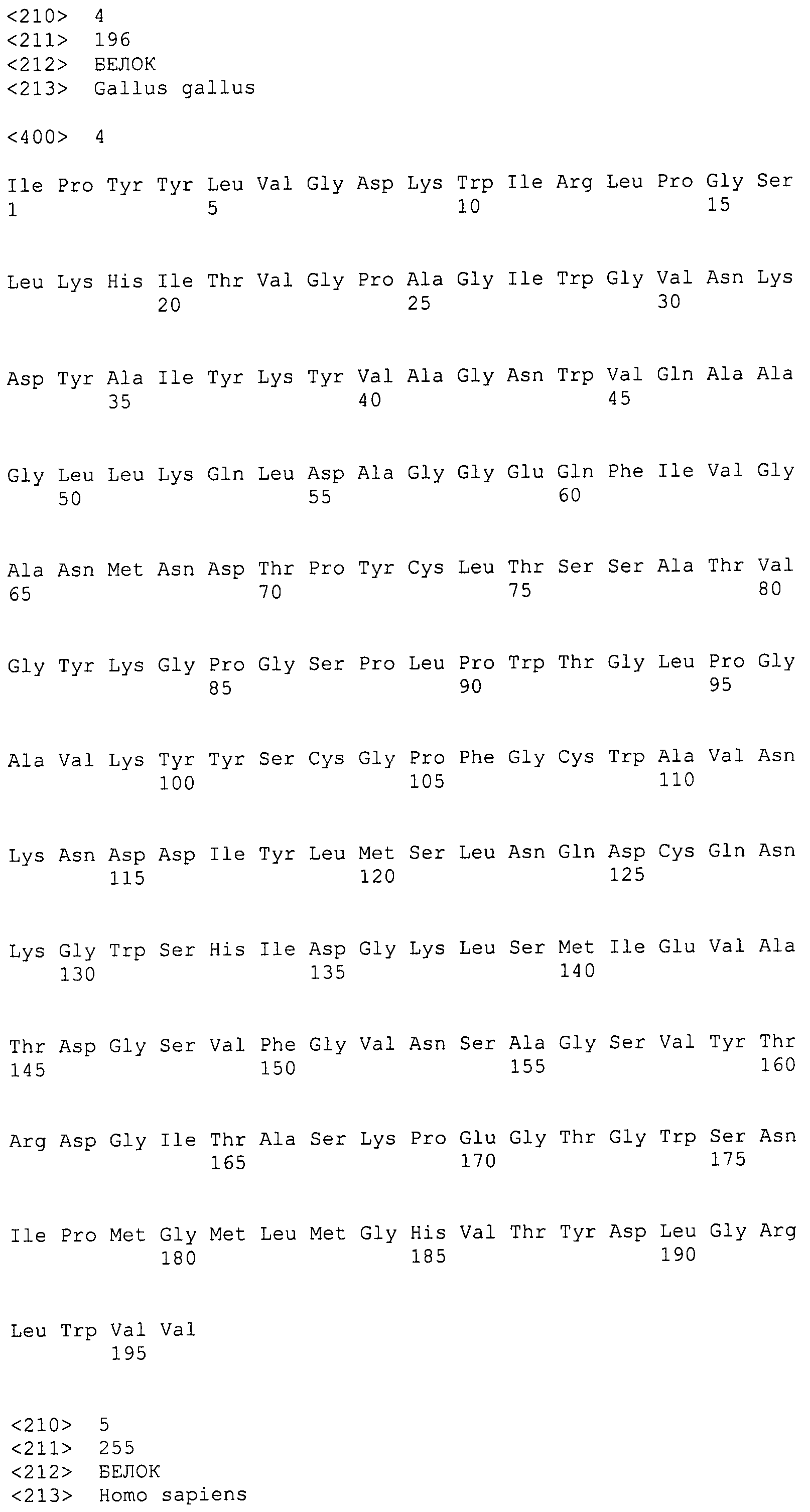
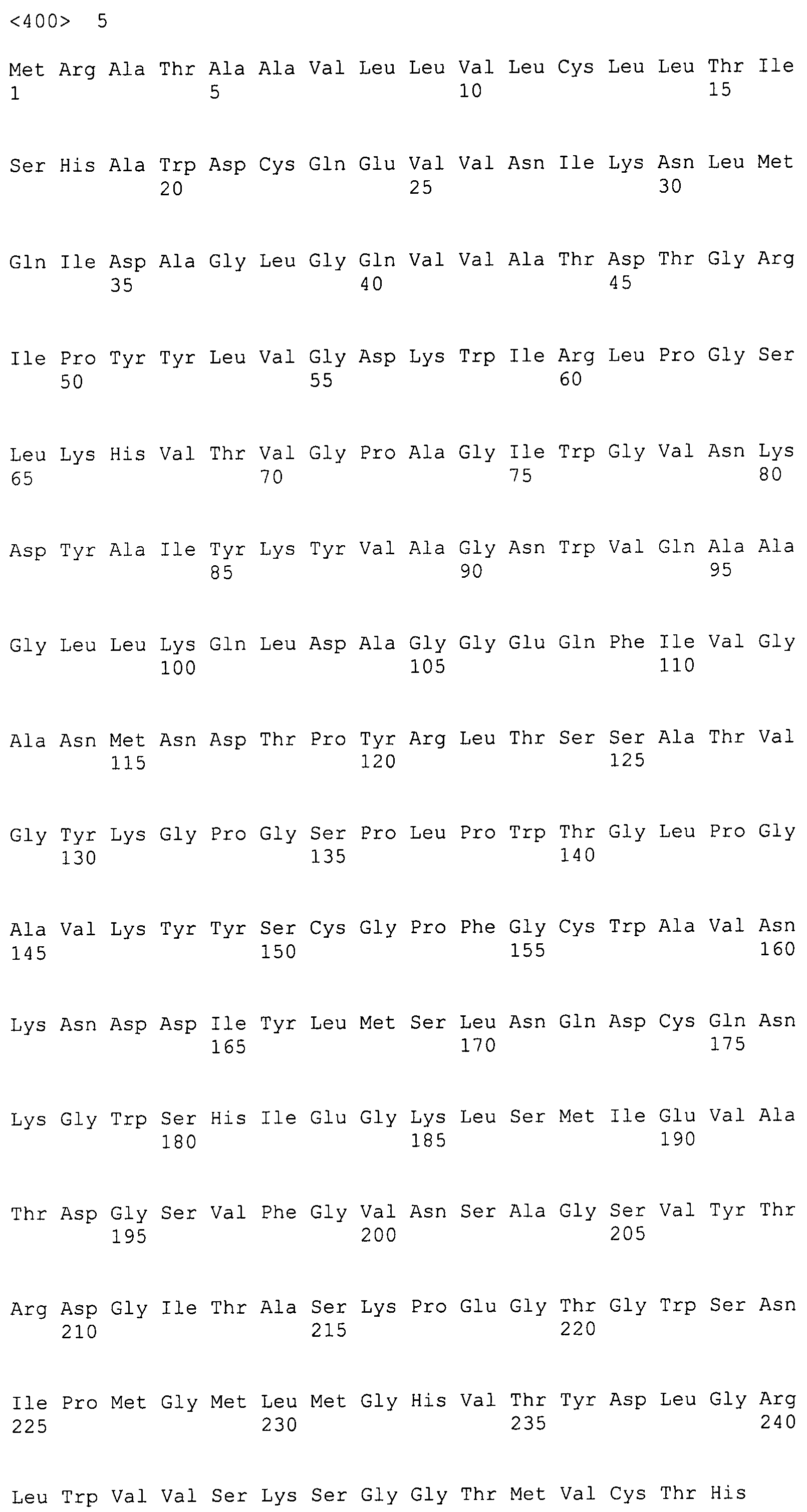
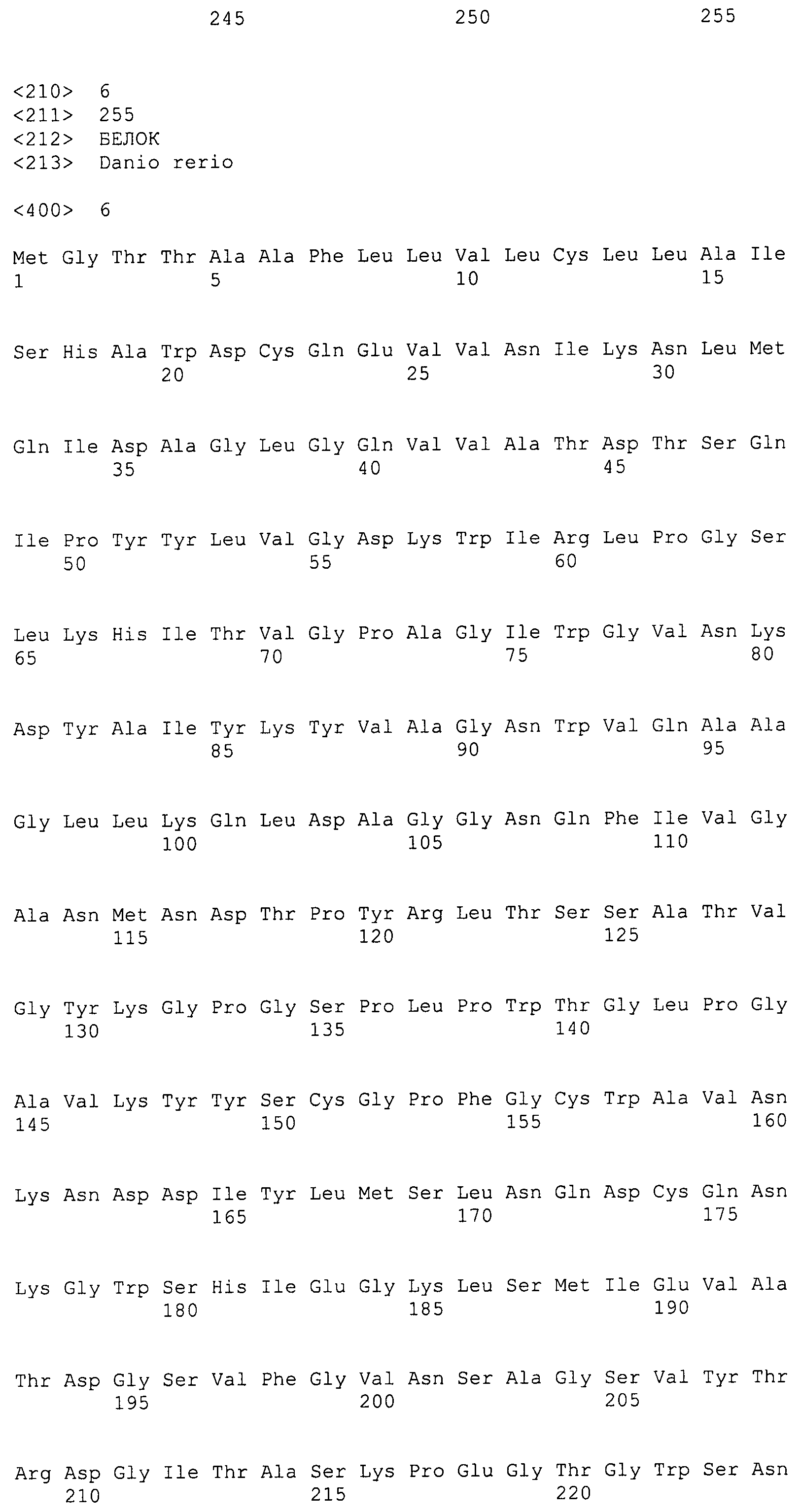
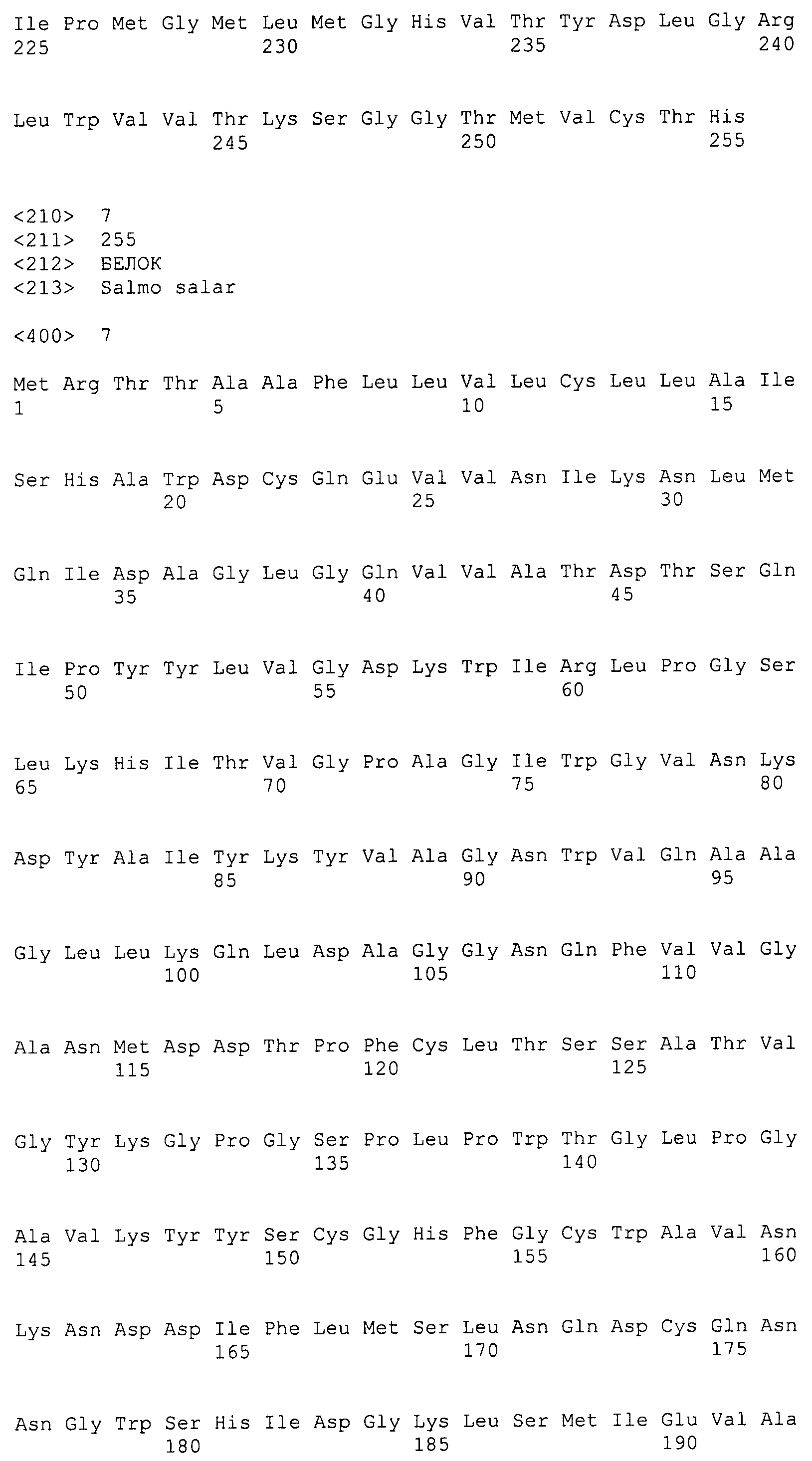
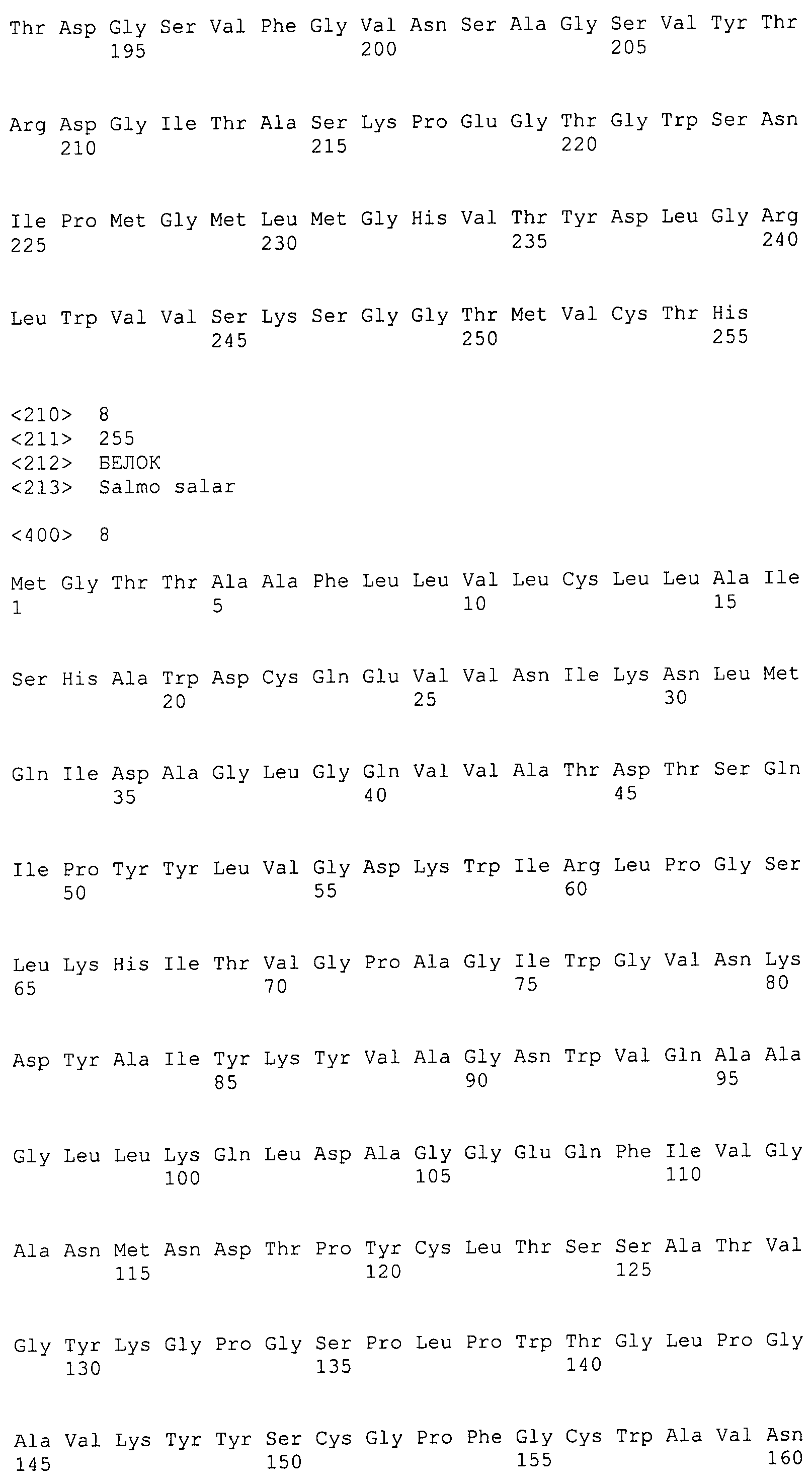










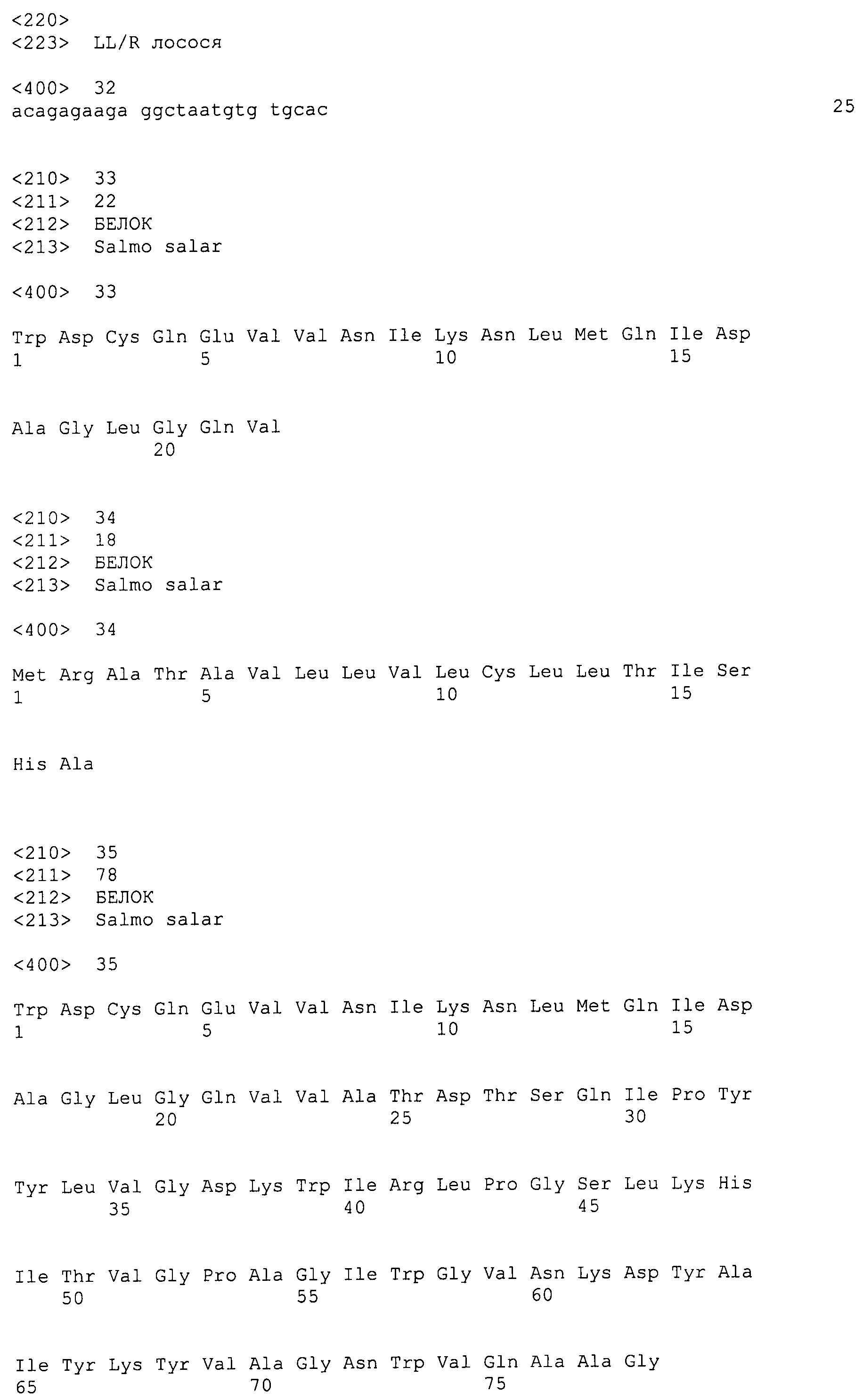






Описание
Настоящее изобретение относится к полипептиду, а именно к лектину, кодирующей его последовательности нуклеиновой кислоты и к антителам к этому полипептиду и их использованию в различных медицинских применениях.
Система клеточной иммунной защиты является основной для выживания при заражении микроорганизмами и паразитами. Эта система также является наиболее значимой для контроля над аномальными клетками при канцерогенезе, после вирусных инфекций и при аутоиммунных заболеваниях.
Межклеточное распознавание является основным для таких функций, но происхождение такого феномена само по себе недостаточно понятно. После миллиарда лет расхождения половых биотов гены должны были эволюционировать, чтобы обеспечить видоспецифичное распознавание половых клеток («фертилизация»). В противном случае, жизнеспособность половых видов находилась бы под угрозой. Эволюционировали некоторые молекулы клеточного распознавания. Когда в кембрийском периоде были показаны биоты, оккупировавшие наземные биотопы, такие безводные биотопы все больше и больше способствовали ограничению половой фертилизации к защищенной окружающей среде с меньшей вероятностью смешения видов. Следовательно, гены для видоспецифичного распознавания гамет имели бы тенденцию стать ненужными и таким образом освободиться для приобретения новой функциональности в развитии.
Одной очевидной новой функцией могла стать способность организмов к отличию его собственных (своих) клеток от чужеродных (не своих) клеток. Предполагается, что этот механизм представляет одно разумное объяснение происхождения клеточной иммунной системы, феномен, который иным образом плохо объясняется. Такое распознавание генетически детерминированным иммунитетом (Medzhitov & Janeway, 1997, Cell, 91(3), p. 295-298) является необходимым для многоклеточных организмов для предотвращения их каннибализации паразитами и микробами. Нарушение функции систем отличать «свое» от «не своего» может быть основой некоторых аутоиммунных заболеваний.
Неправильно направленные иммунные ответы, которые называются аутоиммунитетом, могут быть продемонстрированы присутствием аутоантител или Т-лимфоцитов, реактивных в отношении антигенов хозяина. Хотя это и безопасный и, вероятно, всеобщий феномен жизни позвоночного, аутоиммунитет может быть причиной широкого спектра заболеваний человека, известных как аутоиммунные заболевания. Эта концепция аутоиммунитета как причины заболеваний человека является сравнительно новой и не была принята в основное направление медицинского учения до 1950-х и 1960-х. Аутоиммунные заболевания определяются как заболевания, при которых происходит развитие от безвредного аутоиммунитета к патогенному аутоиммунитету. Это развитие определяется как генетическими влияниями, так и пусковыми механизмами окружающей среды.
Аутоиммунные заболевания представляют большую угрозу здоровью. Существует более восьмидесяти заболеваний, вызванных аутоиммунитетом. Они представляют особую угрозу для женщин; женщины составляют около 75% пациентов. Аутоиммунные заболевания находятся среди десяти лидирующих причин смерти среди женщин во всех возрастных группах до 65.
Аутоиммунные заболевания поражают многие различные части организма, в том числе кожу (например, очаговая алопеция, буллезный пемфигоид, врожденный буллезный эпидермолиз, слоистый пемфигоид, обыкновенная пузырчатка, витилиго, псориаз и акне), почки (например, IgA нефропатия), кровь (например, апластическая анемия, аутоиммунная гемолитическая анемия, идиопатическая тромбоцитопеническая пурпура и пернициозная анемия), суставы (например, анкилозирующий спондилит), мышцы (например, полимиозит/дерматомиозит), ухо (например, аутоиммунная потеря слуха и синдром Меньера), глаз (например, язва Мурена, синдром Рейтера и синдром Фогта-Коянаги-Харада), сердце (например, аутоиммунный миокардит, синдром Черджа-Строс, гигантоклеточный артериит, болезнь Кавасаки, узелковый полиартериит, синдром Такаясу и гранулематоз Вегенера), эндокринную систему (например, болезнь Аддисона, аутоиммунный гипопаратиреоз, аутоиммунный гипофизит, аутоиммунный оофорит, аутоиммунный орхит, болезнь Грейвса, тироидит Хашимото, полигландулярный аутоиммунный синдром 1 типа (PAS-1), полигландулярный аутоиммунный синдром 2 типа (PAS-2 полигландулярный аутоиммунный синдром 3 типа (PAS-3) и сахарный диабет 1 типа), гастроэнтеральную систему (например, аутоиммунный гепатит, глютеновая энтеропатия, воспалительное заболевание кишечника и первичный биллиарный цирроз), нервную систему (например, хроническая воспалительная демиелинизирующая полинейропатия, синдром Жиллиана-Барра, рассеянный склероз и миастения гравис), или может поражать организм системно (например, антифосфолипидный синдром, аутоиммунный лимфопролиферативный синдром, аутоиммунная полиэндокринопатия, болезнь Бехчета, синдром Гудпасчера, ревматоидный артрит, склеродермия, синдром Шегрена и системная красная волчанка).
Аутоиммунное заболевание может поражать любую часть организма, и, следовательно, симптомы варьируются в широких пределах, и диагноз и лечение зачастую вызывают трудности. Некоторые аутоиммунные заболевания могут быть опасными для жизни, если их не диагностировать должным образом и не лечить. Хронические аутоиммунные нарушения наподобие ревматоидного артрита калечат пациента, а также накладывают тяжкое бремя на семьи пациентов. Некоторые типы увеита могут вызывать слепоту. Для таких заболеваний как склеродермия, требуется умелое пожизненное лечение. Другие аутоиммунные заболевания, в том числе болезнь Грейвса и хронический тироидит, можно с успехом лечить, если правильно поставить диагноз, но их зачастую пропускают, вследствие их слабовыраженного проявления.
Воспаление представляет собой нормальный процесс, при котором лейкоциты организма и химические вещества защищают организм от инфекции и чужеродных веществ, таких как бактерии и вирусы. При некоторых заболеваниях, однако, иммунная система организма нецелесообразно запускает воспалительный ответ, когда отсутствуют чужеродные вещества, которые нужно побороть. Воспаление, следовательно, является типичным при аутоиммунных заболеваниях, но не все аутоиммунные нарушения представляют собой аутоиммунные реакции. Воспалительные заболевания также могут быть вызваны целым рядом агентов, которые непосредственно атакуют организм, такие как микроорганизмы (вирусы и грибы), бактериальные токсины, некоторые фармацевтические средства (антибиотики и противовоспалительные стероиды), и химические вещества (соли желчных кислот, токсичная бытовая химия). Заболевания, которые связаны с воспалением, включают артрит (который является общим термином, описывающим воспаление в суставах), воспаление сердечной мышцы (миокардит), воспаление мелких трахеол, которые переносят воздух в легкие (которое может вызывать асматический приступ), воспаление почек (нефрит) и воспаление толстого кишечника (колит).
Гастроинтестинальные воспалительные заболевания представляют собой особый интерес (например, воспалительные заболевания желудка (такие как язва желудка, язва двенадцатиперстной кишки и гастрит), и интестинальные воспалительные заболевания (в том числе болезнь Крона, воспалительное заболевание кишечника, тропические и нетропические спру, инфекционный энтерит, колит, язвенный колит, псевдомембранозный колит, дивертикулит и аллергические и лучевые воспалительные заболевания).
Гастроинтестинальные воспалительные заболевания характеризуются воспалением, в частности наличием отека, характерных воспалительных клеток (т.е. лейкоцитов, гистиоцитов и макрофагов) и в некоторых случаях, некрозом и изъязвлением поверхности эпителия. Известно, что эти воспалительные заболевания вызываются целым рядом агентов, находящихся в желудочно-кишечном тракте, которые, как известно, атакуют его поверхность, продуцируя реакцию воспалительного заболевания. Такие агенты включают микроорганизмы (вирусы и грибы), бактериальные токсины, некоторые фармацевтические средства (антибиотики и противовоспалительные стероиды) и химические вещества (соли желчных кислот, токсические средства бытовой химии). На самом деле, сам желудочный сок способен воздействовать на выстилку желудка и вызывать состояние воспаления.
Медицинские средства, используемые в настоящее время для лечения воспаления, включают нестероидные противовоспалительные лекарственные средства (NSAID - такие как аспирин, ибупрофен или напроксен), кортикостероиды (такие как преднизон), противомалярийные медицинские средства (такие как гидроксихлорохин) и другие медикаменты, такие как метотрексат, сульфасалазин, лефлуномид, средства против TNF, циклофосфамид и микофенолят. Некоторые гастроинтестинальные заболевания, в частности заболевания желудка, можно лечить путем ингибирования секреции желудочного сока, который вызывает воспаление, например, путем нейтрализации эффектов кислоты (например, введением антацида) или путем введения фармакологического средства, эффективного для ингибирования секреции желудочного сока.
Поврежденная кожа является чувствительной к инфекции и может быть неприглядной и/или вызывать боль или дискомфорт. Некоторые типы ран являются резистентными к заживлению в нормальных физиологических условиях, например, хронические язвы. Крайне желательными являются любые фармацевтические растворы для восстановления поврежденной кожи, особенно для заживления ран.
Существует необходимость в способах лечения, подходящих для лечения аутоиммунных и воспалительных нарушений и состояний или повреждения кожи с минимальными побочными эффектами.
После многих лет исследования процессов, потенциально вовлеченных в эволюцию эукариот, авторы настоящего изобретения идентифицировали новый белок (в настоящей заявке назван лейколектином) не только в гаметах и в зиготе, а также на ранней стадии эмбрионального развития (в особых клетках, названных лектоцитами) и во время онтогенеза клеток крови и, наконец, в лейкоцитах.
Первоначально этот белок был идентифицирован и очищен из рыб (см. Примеры). Этот белок содержит 255 аминокислот. Это пропептидная форма лектина, который содержит N-концевой пептид из 19 аминокислот, который, предположительно, направлен в лизосому для последующей секреции (т.е. в перивителлиновое пространство).
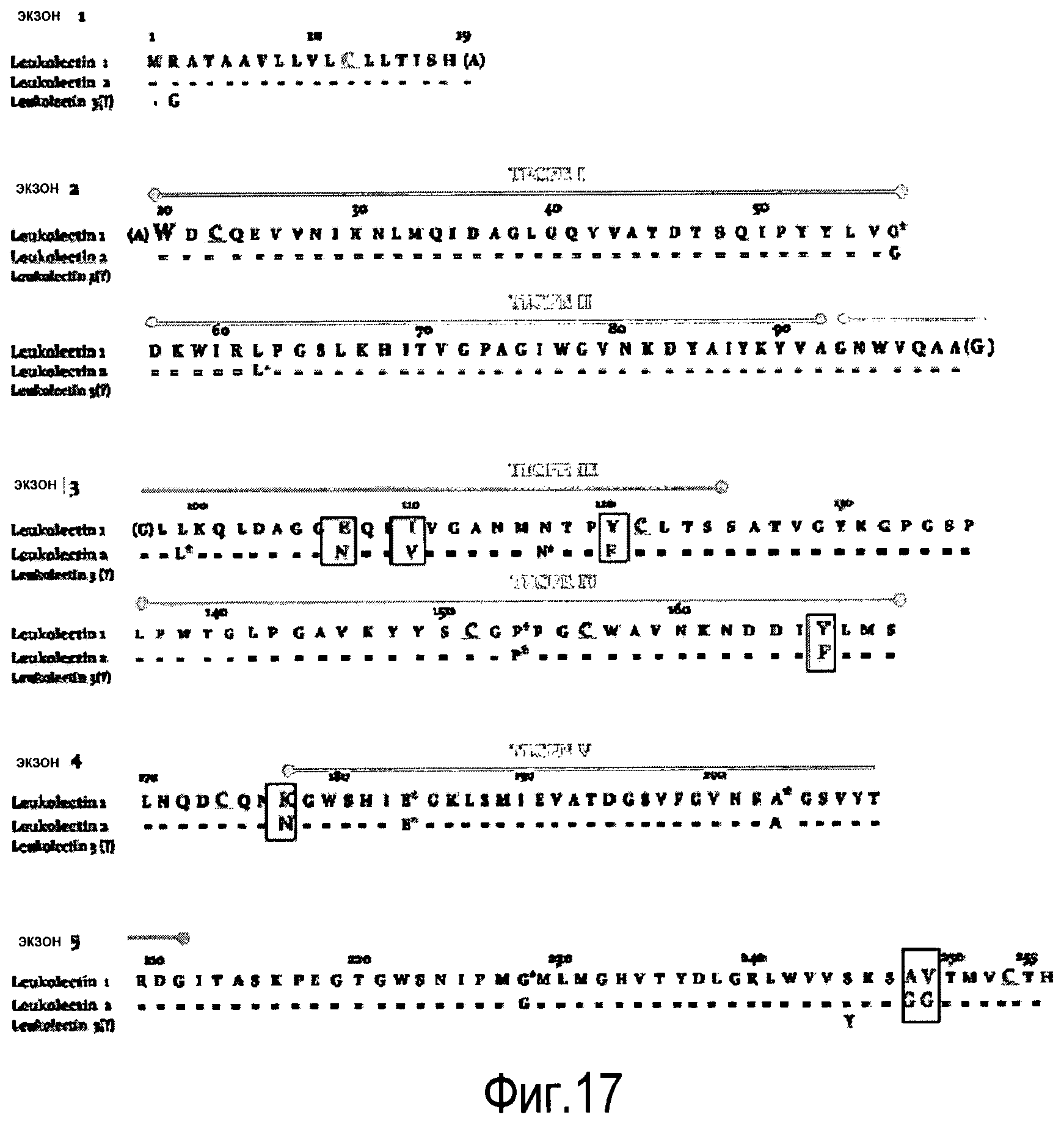
Аминокислотная последовательность лектина дает возможность развитию эпитоп-специфичных антител, которые, в свою очередь, способствуют идентификации многих (2-8) видимых изоформ этого белка (Фигура 5), в зависимости от анализируемой ткани. По меньшей мере две мРНК было выделено из лосося (см. пример 11), которые содержат минимальные различия последовательностей, которые в результате приводят только к 7 изменениям на уровне полипептида (Фигура 17). Усеченные формы этого белка также были идентифицированы из лейкоцитов лосося (см. SEQ ID NO: 2) и данио, в которых также была идентифицирована секретируемая форма (как описано выше, обозначенная sLL) и усеченная форма, которая лишена первых 32 аминокислот с N-конца, обозначенная tLL (см. Пример 9).
Этот белок мало похож на любой из известных белков, демонстрируя суммарное сходство менее чем 50% с любым известным белком. Некоторое сходство наблюдалось в небольших доменах с тахилолектинами.
У различных животных были идентифицированы родственные белки, в том числе данио, трески, радужной форели, Oikopleura dioica, а также у цыпленка и у людей. Их кДНК были идентифицированы (см. Примеры) и было обнаружено, что они являются чрезвычайно консервативными. Кодируемые белки у исследуемых видов, показали менее 4% вариабельность. Это указывает на жизненноважные функции этих белков.
До настоящего времени не сообщалось о генах с аналогичной последовательностью в каких-либо организмах. Используя зонды для индивидуальных экзонов или интронов, было установлено, что существует только редчайшее сходство одного экзона с частями двух других описанных белков, каждый из которых не имеет ничего общего с описанной в настоящей заявке молекулярной структурой.
Что важно, этот новый ген специфически экспрессируется в лейкоцитах человека, несмотря на тот факт, что этот ген не может быть обнаружен в опубликованных последовательностях генома человека. Могут быть обнаружены только очень короткие сегменты этого гена, но разбросанные по многочисленным хромосомам человека (см. примеры). Решение этой головоломки все еще не найдено.
Наконец, было обнаружено, что клетками секретируется эта молекулярная структура, которая соответствует про-пептидной форме этого белка. Была выделена как природная, так и рекомбинантная форма этого генного продукта.
Неожиданно было обнаружено, что эти белки обладают резко выраженным действием на аутоиммунитет и воспалительные нарушения, в частности кожи, и другие патологические состояния кожи. Не желая связываться теорией, считается, что лейколектин связывается со специфическими рецепторами, которые запускают нормальные и свойственные организму процессы заживления в организме человека. В результате наблюдаемых эффектов, авторы изобретения высказали предположение о том, что лейколектин принимает участие в нормальном процессе клеточного иммунитета. По-видимому, лейколектин отсутствует при многих патологических состояниях, так что его фармацевтическое введение запускает другие защитные реакции иммунной системы, чтобы нормально функционировать, несмотря на различные стимулы: присутствие чужеродных клеток (микроорганизмов, паразитов) и измененных клеток «своего», которые могут связывать лейколектин с этиологией аутоиммунных заболеваний, т.е. такие условия могут быть вызваны отсутствием достаточного лейколектина.
Лейкоциты человека содержат и экспрессируют чрезвычайно консервативные лейколектиновые белки. До настоящего времени эти белки представляли собой неизвестные белки в клетках крови. По-видимому, лейколектин является новым представителем семейства белков тахилолектинов.
В первом аспекте настоящее изобретение относится к полипептиду, содержащему аминокислотную последовательность, изложенную в одной из последовательностей No. 1-8, или последовательность, которая по меньшей мере на 50% идентична указанной последовательности или части любой из указанных последовательностей.
«Полипептиды» в контексте настоящего изобретения представляют собой молекулы предпочтительно более чем с 50, 100, 150, 200 или 250 остатками и/или менее чем 500, 400, 300, 200 или 100 остатками или выбранного из них диапазона. В контексте настоящего изобретения «часть» предпочтительно содержит по меньшей мере 30, 40, 50, 60, 70, 80, 90, 100, 150, 200 или более аминокислот последовательности, из которой они происходят. Указанная часть может быть получена из центральных или N-концевых или C-концевых частей последовательности. Предпочтительно, указанную часть получают из N-концевой области, например, из первых 50, 100 или 150 остатков этого полипептида. Предпочтительные аспекты включают усечения указанных полипептидов, например, для удаления сигнального пептида или части, отсутствующей в природных вариантах. Предпочтительные усечения встречаются на N-конце и представляют собой от 1 до 50, например от 1 до 10, 20, 30 или 40, или от 5 до 40, например от 10 до 35 остатков в длину.
Предпочтительно, указанная последовательность по меньшей мере на 55, 60, 65, 70, 75, 80, 85, 90, 95, 96, 97, 98 или 99% идентична последовательности, с которой ее сравнивают.
Идентичность последовательности может быть определена, например, путем использования базы данных последовательностей белков SWISS-PROT с использованием FASTA pep-cmp с вариабельным pamfactor и установлением штрафа за разрыв 12,0 и штрафа за удлинение разрыва 4,0 и промежуток из 2 аминокислот. Предпочтительно, указанное сравнение проводят по всей длине последовательности, но может быть проведено в меньшем окне сравнения, например, менее 200, 100 или 50 последовательных аминокислот.
Предпочтительно полипептиды, связанные такой идентичностью последовательностей, являются функционально эквивалентными полипептидам, которые изложены в последовательностях с цитируемыми номерами. Такие функционально эквивалентные полипептиды могут принимать форму производных, как изложено ниже. Аналогичным образом, полипептиды с последовательностями, изложенными в последовательностях «Sequence Nos.», могут быть модифицированы, не оказывая влияния на последовательность полипептида, как описано ниже.
Кроме того, «части», как описано в настоящей заявке, могут быть функциональными эквивалентами. Предпочтительно эти части удовлетворяют условиям идентичности (относительно сравниваемой области), упомянутым в настоящей заявке.
Как изложено в настоящей заявке, для достижения «функциональной эквивалентности» полипептид может демонстрировать несколько сниженную эффективность в осуществлении медицинской функции по сравнению с исходной молекулой (т.е. молекулой, из которой он был получен, например, путем аминокислотной замены), но предпочтительно является также эффективным или более эффективным. Таким образом, функциональная эквивалентность относится к полипептиду, который является эффективным для лечения заболевания, как изложено в настоящей заявке, т.е. для уменьшения одного или нескольких симптомов у пациента, например воспаления или кожных проявлений, как описано далее. Это может быть протестировано путем сравнения эффектов производного полипептида относительно полипептида, из которого он получен, качественным или количественным образом, например путем проведения анализов in vivo указанных в Примерах. В тех случаях, когда возможно получение количественных результатов, производное является эффективным по меньшей мере на 30, 50, 70 или 90% от эффективности исходного полипептида. Альтернативно, может быть проведено тестирование in vitro, например, путем анализа связывания дендритных клеток или эффектов на клеточные культуры in vitro.
Функционально эквивалентные белки, которые относятся к природному белку или происходят из природного белка, могут быть получены путем модификации нативной аминокислотной последовательности посредством одной или множества аминокислотных замен, добавлений и/или делеций (при условии, что они удовлетворяют указанным выше требованиям к идентичности последовательностей), но без разрушения функции молекулы. Предпочтительно нативная последовательность имеет менее 20 замен, добавлений или делеций, например менее 10, 5,4, 3, 2 или 1 таких модификаций. Такие белки кодируются «функционально эквивалентными молекулами нуклеиновой кислоты», которые получают путем соответствующей замены, добавления и/или делеции одного или нескольких оснований.
Предпочтительные функциональные эквиваленты представляют собой «добавочные» варианты, в которых получают амино- и/или карбокси-концевые слитые белки или полипептиды, содержащие дополнительный белок или полипептид, слитый с исходным полипептидом.
Особенно предпочтительными функционально-эквивалентными вариантами являются природные биологические варианты (например, аллельные варианты или географические варианты в пределах видов или, альтернативно, в различных родах, например, растений, животных или бактерий) и производные, полученные с использованием известных методик. Например, молекулы нуклеиновой кислоты, кодирующие функционально-эквивалентные белки, могут быть получены химическим синтезом или в рекомбинантной форме с использованием известных методик сайт-направленного мутагенеза, включая делецию, случайный мутагенез или ферментативное расщепление и/или лигирование нуклеиновых кислот.
Настоящее изобретение также относится к нуклеотидным последовательностям, кодирующим указанные полипептиды.
В предпочтительном аспекте, настоящее изобретение таким образом относится к молекуле нуклеиновой кислоты, как изложено в любой из последовательностей №№ 9-15, последовательности, которая по меньшей мере на 50% идентична указанной последовательности, или последовательности, которая гибридизируется с указанной последовательностью в нежестких условиях связывания 6×SSC/50% формамида при комнатной температуре и промывания в условиях высокой жесткости, например, 2×SSC, 65°C, где SSC=0,15M NaCl, 0,015M цитрата натрия, pH 7,2, или последовательности, комплементарной любой из указанных выше последовательностей, или их части. Предпочтительно, указанная молекула нуклеиновой кислоты кодирует полипептид, описанный ранее.
«Молекулы нуклеиновой кислоты» в контексте настоящего изобретения представляют собой молекулы, предпочтительно более чем с 150, 300, 450, 600 или 750 основаниями и/или менее чем 1500, 1200, 900, 600 или 300 основаниями или в интервале, выбранном из них. «Части», как указано выше, предпочтительно содержат по меньшей мере 90, 120, 150, 180, 210, 240, 270, 300, 450 или 600 нуклеотидных оснований последовательности, из которой они происходят. Предпочтительно указанные части кодируют N-концевые, центральные или C-концевые пептиды, как описано ранее в настоящей заявке. Как рассмотрено выше в отношении полипептидов, в предпочтительном аспекте рассматриваются усечения, приводящие в результате к удалению остатков с N-конца упомянутых полипептидов. В кодирующих нуклеотидных последовательностях, родственных последовательностям, представленным в настоящем изобретении, указанное усечение предпочтительно составляет от 1 до 150, например от 1 до 30, 60, 90 или 120, или от 13 до 120, например от 28 до 105 оснований в длину.
Предпочтительно указанная последовательность по меньшей мере на 55, 60, 65, 70, 75, 80, 85, 90, 95, 96, 97, 98 или 99% идентична последовательности, с которой проводят сравнение.
Идентичность последовательности может быть определена, например, с помощью FASTA Search, используя программное обеспечение GCG, со значениями по умолчанию и вариабельным pamfactor, и установлением штрафа за разрыв 12,0 и штраф за удлинение разрыва 4,0 с промежутком 6 нуклеотидов.
Предпочтительно такие молекулы нуклеиновой кислоты с родственной идентичностью последовательностей или гибридизирующиеся молекулы нуклеиновой кислоты являются функционально эквивалентными молекулам нуклеиновой кислоты, которые изложены в цитируемых последовательностях «Sequence Nos.» Такие функционально эквивалентные молекулы нуклеиновой кислоты могут принимать форму производных, как изложено ниже, и они считаются функционально эквивалентными, если они кодируют полипептиды, которые считались бы функциональными эквивалентами в соответствии с тестами, описанными ранее в настоящей заявке. Предпочтительными функциональными эквивалентами являются те, которые кодируют предпочтительные полипептиды, как изложено выше, например молекулы нуклеиновой кислоты, которые кодируют полипептиды, обнаруженные у разных родов или видов, чем специфические молекулы, упомянутые в настоящем описании.
Более того, «части», как описано в настоящей заявке, могут быть функциональными эквивалентами. Предпочтительно эти части удовлетворяют условиям идентичности (в отношении сравниваемой области) или гибридизации, упомянутым в настоящем описании.
Молекулы нуклеиновой кислоты по настоящему изобретению могут представлять собой одноцепочечную или двухцепочечную ДНК, кДНК или РНК, предпочтительно ДНК, и включают вырожденные, по существу идентичные и гибридизирующиеся последовательности, как описано выше. В идеале, однако, молекулы представляют собой ДНК или кДНК.
Полипептиды, как описано выше, включают те, которые модифицированы без воздействия на последовательность полипептида, например, химической модификацией, в том числе дегликозилированием или гликозилированием. Такие полипептиды могут быть получены модификацией после синтеза/выделения полипептида без воздействия на функциональность, например, определенным гликозилированием, метилированием и т.д. конкретных остатков.
Полипептиды по настоящему изобретению также могут принимать форму пептидомиметиков, которые могут рассматриваться производными, в которых функциональные особенности полипептида сохранены, но представлены в контексте другой, например, непептидной структуры. Такие пептидомиметики с успехом были разработаны и использованы для других, в особенности медицинских применений.
Пептидомиметики, в частности непептидные молекулы, могут быть получены посредством различных процессов, в том числе конформационным созданием лекарственных средств, скринингом, созданием направленной библиотеки и классической медицинской химией. Могут быть использованы не только олигомеры неприродных аминокислот или других органических структурных элементов, а также углеводы, гетероциклические или макроциклические соединения или любая органическая молекула, которая содержит структурные элементы и конформацию, которая предоставляет молекулярную электростатическую поверхность, которая имитирует такие же свойства 3-мерной конформации пептида, могут быть использованы с помощью способов, известных из уровня техники.
Таким образом, пептидомиметики могут совсем не иметь или иметь мало сходства с пептидным скелетом. Пептидомиметики могут содержать полностью синтетическую непептидную форму (например, основанную на углеводном скелете с соответствующими заместителями) или может сохранять один или несколько элементов пептида, на котором он основан, например, путем получения производных одной или нескольких аминокислот или замещения одной или нескольких аминокислот альтернативными непептидными компонентами. Пептидоподобные матрицы включают псевдопептиды и циклические пептиды. Структурные элементы, считающиеся излишними для функции этого пептида, могут быть минимизированы для сохранения только каркасной функции или удалены, при необходимости.
В тех случаях, когда пептидомиметики сохраняют один или более пептидных элементов, т.е. более одной аминокислоты, такие аминокислоты могут быть замещены их нестандартными или структурными аналогами. Аминокислоты, сохраненные в последовательностях, также могут образовывать производные или быть модифицированы (например, помечены, гликозилированы или метилированы), при условии, что сохраняются функциональные свойства полипептидов по изобретению. Эти пептидомиметики, называются в контексте настоящей заявке «производными от» определенной полипептидной последовательности. Под этим подразумевается, что этот пептидомиметик получен относительно определенной полипептидной последовательности таким образом, что он сохраняет структурные особенности полипептида, которые являются необходимыми для его функции. Это могут быть конкретные боковые цепи полипептида, или потенциал водородных связей этой структуры. Такие особенности могут быть представлены непептидными компонентами или одним или несколькими аминокислотными остатками или связи, соединяющие указанные аминокислотные остатки полипептида могут быть модифицированы таким образом, чтобы улучшить определенные функции полипептида, такие как стабильность или резистентность к протеазе, сохраняя структурные особенности полипептида, которые являются необходимыми для его функции.
Примеры нестандартных или структурных аналогов аминокислот, которые могут быть использованы, представляют собой D-аминокислоты, амидные изостеры (такие как N-метиламид, ретро-инвертированный амид, тиоамид, тиоэфир, фосфонат, кетометилен, гидроксиметилен, фторвинил, (E)-винил, метиленамин, метилентио или алкан), L-N метиламинокислоты, D-α метиламинокислоты, D-N-метиламинокислоты.
Примеры нетрадиционных аминокислот приведены в Таблице 1.
Нестандартные аминокислоты, которые могут быть использованы, включают конформационно ограниченные аналоги, например, такие как Tic (для замены F), Aib (для замены A) или пипеколиновая кислота (для замены Pro).
Полипептиды и молекулы нуклеиновой кислоты, описанные выше, также включают производные, которые были модифицированы, например, для облегчения их использования в фармацевтических применениях (рассмотренных ниже), например, путем добавления нацеливающих или функциональных групп, например, для улучшения липофильности, облегчения клеточного транспорта, растворимости и/или стабильности. Таким образом, олигосахариды, жирные кислоты, жирные спирты, аминокислоты, пептиды или полипептиды могут быть конъюгированы с указанными выше полипептидами или молекулами нуклеиновой кислоты. Молекулы нуклеиновой кислоты могут находиться в вирусном носителе, как описано далее в настоящей заявке.
Полипептиды также охватывают производные в форме «пролекарств» или «пропептидов» таким образом, что добавленный компонент может быть удален отщеплением при введении, например, путем отщепления заместителя, добавленного в процессе этерификации, который может быть удален под действием эстераз. Такие пролекарства включают природные предшественники природных белков, которые расщепляются, например, под действием протеолиза с высвобождением представляющего интерес полипептида. Такие предшественники могут быть неактивными в форме предшественника, но могут быть активированы путем протеолитического расщепления. Молекулы нуклеиновой кислоты по настоящему изобретению, следовательно, аналогичным образом охватывают молекулы, которые кодируют такие пролекарства или предшественники. Модифицированные полипептиды или молекулы нуклеиновой кислоты, как описано выше, могут быть протестированы для подтверждения, что они сохранили функциональную активность относительно немодифицированной молекулы путем определения, обладают ли они сходными медицинскими эффектами.
Молекулы нулеиновой кислоты, описанные выше, могут быть оперативно связаны с контрольной последовательностью экспрессии, или рекомбинантным клонирующим ДНК-носителем или вектором, содержащим такую рекомбинантную молекулу ДНК. Это дает возможность осуществлять внутриклеточную экспрессию полипептида по изобретению в виде генного продукта, экспрессия которого направляется геном (генами), введенным в клетки, представляющие интерес. Генная экспрессия направляется от промотора, активного в клетках, представляющих интерес, и может быть встроена в любой форме линейного или кольцевого ДНК вектора для включения в геном или для независимой репликации или транзиторной трансфекции/экспрессии. Подходящие методики трансформации или трансфекции подробно описаны в литературе. Альтернативно, молекула обнаженной ДНК может быть введена непосредственно в клетку для применений, описанных в настоящей заявке.
Подходящие векторы экспрессии включают соответствующие контрольные последовательности, например, такие как трансляционные (например, старт и стоп кодоны, сайты связывания рибосомы) и транскрипционные контрольные элементы (например, области промотор-оператор, стоп-последовательности терминации), включенные в соответствующую рамку считывания с молекулами нуклеиновой кислоты, необходимыми для осуществления способа по настоящему изобретению, как описано далее в настоящей заявке. Соответствующие векторы могут включать плазмиды и вирусы (включая как бактериофаги, так и эукариотические вирусы). Подходящие вирусные векторы включают бакуловирус, а также аденовирус, адено-ассоциированный вирус, вирусы герпеса и вирусы коровьей оспы/поксовирусы. Многие другие вирусные векторы описаны в уровне техники. Предпочтительные векторы включают бактериальные векторы экспрессии и векторы экспрессии млекопитающих pGEX-KG, pEF-neo и pEF-HA. Молекулу нуклеиновой кислоты можно удобно слить с ДНК, кодирующей дополнительный полипептид, например глутатион-S-трансферазу, для получения экспрессии слитого белка.
Таким образом, если смотреть со стороны дополнительного аспекта, настоящее изобретение относится к вектору, предпочтительно к вектору экспрессии, содержащему молекулу нуклеиновой кислоты, как описано выше.
Другие аспекты настоящего изобретения включают способы получения рекомбинантных молекул нуклеиновой кислоты в соответствии с изобретением, предусматривающим встраивание нуклеотидных последовательностей, кодирующих полипептиды по изобретению, в векторную нуклеиновую кислоту.
В способах, описанных далее в настоящей заявке, полипептиды можно вводить в клетку путем трансфекции клетки молекулой нуклеиновой кислоты по настоящему изобретению. Как упомянуто выше, настоящее изобретение, следовательно, распространяется на молекулы нуклеиновой кислоты, содержащие последовательность, которая кодирует полипептиды по настоящему изобретению, как описано в настоящей заявке, и к их применению в описанных в этой заявке способах. Предпочтительно, указанные молекулы нуклеиновой кислоты содержатся в векторе, например в векторе экспрессии.
Молекулы нуклеиновой кислоты по настоящему изобретению, предпочтительно, содержащиеся в векторе, могут быть введены в клетку любым подходящим способом. Подходящие методики трансформации или трасфекции подробно описаны в литературе. Известен целый ряд методик, и они могут быть использованы для введения таких векторов в прокариотические или эукариотические клетки для экспрессии. Предпочтительные клетки-хозяева для этой цели включают клеточные линии насекомых, линии эукариотических клеток или E. coli, например штамм BL21/DE3. Настоящее изобретение также распространяется на трансформированные или трансфектированые прокариотические или эукариотические клетки-хозяева, содержащие молекулу нуклеиновой кислоты, в частности вектор, описанный выше.
Дополнительный аспект настоящего изобретения относится к способу получения полипептида по изобретению, как определено ранее в настоящей заявке, который предусматривает культивирование клетки-хозяина, содержащей молекулу нуклеиновой кислоты, как определено выше, в условиях, в которых экспрессируется указанный полипептид, и выделение указанной молекулы, полученной таким образом. Экспрессированный полипептид образует дополнительный аспект настоящего изобретения.
Настоящее изобретение также распространяется на полипептид, кодируемый молекулой нуклеиновой кислоты, как описано ранее в настоящей заявке. Этот полипептид может быть получен путем экспрессии клетки-хозяина, как описано выше.
Клетки, содержащие полипептиды по настоящему изобретению, но которые не были модифицированы относительно нативных клеток путем прямого введения указанных полипептидов или путем экспрессии кодирующего материала нуклеиновой кислоты, образуют дополнительные аспекты настоящего изобретения. Предпочтительно указанные полипептиды или молекулы нуклеиновой кислоты не появляются в указанных клетках эндогенно, т.е. указанная клетка модифицирована таким образом, чтобы она содержала экзогенные полипептиды или материал нуклеиновой кислоты.
Настоящее изобретение также распространяется на антитела (моноклональные или поликлональные) и их антиген-связывающие фрагменты (например, фрагменты F(ab)2, Fab и Fv, т.е. фрагменты «вариабельной» области антитела, которые содержат антиген-связывающий сайт), специфически направленные на полипептиды, описанные ранее в настоящей заявке.
Такие антитела могут быть использованы в способах, описанных далее в настоящей заявке, в частности, в описанных терапевтических способах.
Антитела, описанные в настоящей заявке, могут быть использованы in vitro для идентификации наличия или количества полипептида по изобретению и могут быть использованы диагностически для идентификации нарушений или повреждений кожи, как описано в настоящей заявке, связанных с нарушенными уровнями указанного полипептида, т.е. колебанием относительно нормальных уровней, например повышенными или сниженными уровнями указанного полипептида.
Таким образом, в дополнительном аспекте настоящее изобретение относится к способу определения наличия или количества полипептида по изобретению или его части в образце, где антитело, как описано в настоящей заявке, приводят в контакт с указанным образцом и степень связывания антитела является показателем наличия или количества указанного полипептида или его части.
Исследуемый образец может представлять собой любой удобный образец, например кровь или образец ткани или небиологический образец. Предпочтительно, образец получен от животного, как описано в настоящей заявке, предпочтительно человека.
Настоящее изобретение дополнительно относится к способу диагностики нарушения или повреждения кожи, как описано в настоящей заявке, у животного, предусматривающему по меньшей мере стадии определения наличия или количества полипептида, как описано в настоящей заявке, в образце, полученном от указанного животного, где указанное наличие или количество является диагнозом указанного нарушения или повреждения кожи. Этот полипептид может быть обнаружен, например, путем использования антител, описанных ранее в настоящей заявке. Образец и животное предпочтительно описаны в настоящей заявке. Количество предпочтительно представляет собой снижение уровня указанного полипептида по сравнению с нормальными уровнями. Диагностирование может осуществляться путем сравнения стандартных таблиц здоровых пациентов с теми, кто проходит обследование по поводу нарушения или повреждения кожи.
Полипептиды или молекулы нуклеиновой кислоты, используемые в композициях и применениях настоящего изобретения, как описано далее в настоящей заявке, могут быть получены или могут происходить из природных источников или могут быть продуцированы синтетически полностью или частично.
Полипептиды и молекулы нуклеиновой кислоты удобно выделять в соответствии с протоколами, описанными в Примерах. Такие способы и продукты таких способов образуют дополнительные аспекты настоящего изобретения.
Таким образом, в дополнительном аспекте настоящее изобретение относится к способу выделения полипептида, как описано в настоящей заявке, из жидкости, образующейся при выклеве (например, лосося), предусматривающему по меньшей мере стадии:
a) суспендирования икринок в минимальном объеме воды (например, эквивалентном объему икринок или меньшем);
b) индукции синхронизированного быстрого выклева указанных икринок (предпочтительно, таким образом, чтобы выклев завершался в течение менее 2 часов для более чем 95% эмбрионов);
c) фильтрования икринок, из которых вышли мальки, для получения жидкости, образующейся при выклеве;
d) необязательно добавления твердой мочевины к указанной жидкости, образующейся при выклеве, для возможности осуществления диссоциации фрагментов оболочки яйца, и указанную жидкость подвергают центрифугированию на низких оборотах;
e) проведения первой стадии эксклюзионной хроматографии, например, используя колонку Superdex 16/60 или ультрафильтр Biotex 100;
f) необязательно проведения второй стадии эксклюзионной хроматографии, например, используя колонку Superdex 16/60, и
g) необязательно удаления контаминирующих белков, таких как зоназа, с помощью аффинной хроматографии, например, на колонке Бензамидин-Сефароза.
Настоящее изобретение дополнительно распространяется на полипептиды, полученные описанным выше способом.
В тех случаях, когда полипептид по настоящему изобретению получают из лейкоцитов, его получают в немодифицированной форме. Полипептиды, полученные из жидкости, образующейся при выклеве лосося, модифицируют (путем гликозилирования и/или фосфорилирования), но обе формы одинаково эффективны в описанных в настоящей заявке способах.
Полипептиды или молекулы нуклеиновой кислоты, описанные в настоящей заявке, предпочтительно являются по существу свободными от вещества источника или веществ, используемых в процедуре выделения или при их синтетическом получении. Особенно предпочтительно вещество очищают до степени чистоты более 50 или 60%, например >70, 80 или 90%, предпочтительно более 95 или 99% чистоты как определено мас./мас. (сухая масса). Такие уровни чистоты соответствуют специфической молекуле, представляющей интерес, но включает продукты ее разрушения. При необходимости, обогащенные препараты могут быть использованы, они имеют более низкую степень чистоты, например содержат более 1, 2, 5 или 10% молекулы, представляющей интерес, например более 20 или 30%. Полипептиды по настоящему изобретению могут быть очищены, например, с помощью хроматографии (например, HPLC, гель-фильтрационной, ион-обменной, аффинной, гидрофобного взаимодействия, с обращенной фазой) или капиллярного электрофореза.
Полипептиды по настоящему изобретению могут быть получены синтетическим путем, например путем лигирования синтетически полученных пептидов меньшего размера или более удобно путем рекомбинантной экспрессии молекулы нуклеиновой кислоты, кодирующей указанный полипептид, как описано ранее в настоящей заявке.
Молекулы нуклеиновой кислоты по настоящему изобретению могут быть получены синтетически, например, путем амплификации последовательности нуклеиновой кислоты, как описано в настоящей заявке, например, из соответствующей библиотеки кДНК.
Полипептиды, молекулы нуклеиновой кислоты или антитела, как описано в настоящей заявке, могут быть использованы in vitro, например, в клетке или культуре органа, чтобы воздействовать на иммунные функции в клетках.
Альтернативно, полипептиды, молекулы нуклеиновой кислоты или антитела могут быть использованы ex vivo, на частях животных или продуктах, например органах или собранной крови, клетках или тканях, в частности, когда предполагается, что они будут повторно введены в организм, из которого они получены.
Однако полипептиды, молекулы нуклеиновой кислоты и антитела получают для использования in vivo, как рассматривается ниже более подробно.
Полипептиды, молекулы нуклеиновой кислоты и антитела, как описано в настоящей заявке, применяются для лечения различных нарушений или состояний, как описано далее в настоящей заявке. Настоящее изобретение, следовательно, распространяется на фармацевтическую композицию, содержащую полипептид, молекулу нуклеиновой кислоты или антитело, как описано ранее в настоящей заявке, и один или более фармацевтически приемлемых эксципиентов и/или разбавителей.
Под «фармацевтически приемлемым» или «фармакологически приемлемым» подразумевается то, что ингредиент должен быть совместимым с другими ингредиентами в композиции, а также быть физиологически приемлемым для реципиента.
Активный ингредиент для введения может быть соответствующим образом модифицирован для использования в фармацевтической композиции. Например, соединения, используемые в соответствии с настоящим изобретением, могут быть стабилизированы против разрушения путем использования производных, как описано выше.
Активный ингредиент также может быть стабилизирован в композициях, например, путем использования соответствующих добавок, таких как соли или неэлектролиты, ацетат, SDS, EDTA, цитратный или ацетатный буферы, маннитол, глицин, HSA или полисорбат.
Молекула нуклеиновой кислоты, полипептид или антитело по настоящему изобретению могут находиться в указанных композициях в качестве единственного активного ингредиента, или могут быть объединены с другими ингредиентами, в частности с другими активными ингредиентами, например, для повышения терапевтического эффекта или для того, чтобы сделать композицию более привлекательной для потребителя.
Композиция, содержащая полипептид по настоящему изобретению, также может содержать зоназу или родственный фермент. В контексте настоящего изобретения зоназа представляет собой препарат, содержащий фермент, где указанный препарат демонстрирует одну белковую полосу в анализе SDS-PAGE с молекулярной массой около 28 кДа, получаемый способом, предусматривающим стадии:
a) суспендирования икринок лосося в минимальном объеме воды;
b) индукции синхронизированного быстрого выклева указанных икринок лосося;
c) фильтрования икринок, из которых вышли мальки лосося, для получения жидкости, образующейся при выклеве;
d) добавления твердой мочевины к указанной жидкости, образующейся при выклеве, для возможности осуществления диссоциации фрагментов оболочки яйца лосося и указанную жидкость подвергают центрифугированию на низких оборотах;
e) дополнительной очистки указанной зоназы путем центрифугирования супернатанта для гель-фильтрации; и
f) дополнительной очистки указанной зоназы с помощью аффинной хроматографии на колонке с модифицированной бензамидином сефарозой 6B®, где указанную аффинную хроматографию проводят промываниями концентрированными солями с последующей элюцией диоксаном, в концентрированном растворе солей, для экстракции зоназ, связанных с хроматографическим матриксом или с макромолекулярными структурами,
где указанная зоназа обладает следующими свойствами:
a) расщепляет хромозим X;
b) ингибируется под действием бензамидина;
c) расщепляет пептидные связи с аргинином;
d) остается активной в присутствии 8M мочевины, молярных концентраций соли, дистиллированной воды и органических растворителей, предпочтительно диоксана или пропанола; и
e) сохраняет ферментативную активность в растворе при комнатной температуре в течение 50 дней.
Зоназа может быть получена, как описано в примерах, и добавлена к композиции, или может представлять «примесь» после получения полипептида по изобретению из природных источников. В композициях, содержащих оба полипептида по изобретению и зоназу, полипептид может быть представлен в интервале 1-100% от их суммарной объединенной массы и зоназа может составлять от 0 до 99%. Предпочтительно полипептид представлен в интервале 50-100%, например >80, 90, 95, 96, 97, 98 или 99 и зоназа составляет от 0 до 50%, например <20, 10, 5, 4, 3, 2 или 1% объединенной массы.
В дополнительном аспекте настоящего изобретения, описанные в настоящей заявке композиции используют в терапии.
Как упомянуто выше, полипептиды, молекулы нуклеиновой кислоты и антитела по изобретению проявляют терапевтические свойства при лечении различных аутоиммунных и воспалительных нарушений, в частности, кожи, а также лечении поврежденной кожи, например, солнцем, холодом, излучением (например, рентгеновскими лучами, например, используемыми при лечении злокачественных опухолей) или как результат лечения ран.
В контексте настоящего изобретения «нарушение» относится к лежащему в основе патологическому расстройству в организме с симптоматикой или без симптоматики по сравнению с нормальным организмом, которое может быть результатом, например, инфекции или приобретенного или врожденного генетического нарушения.
Как изложено в Примерах, была проиллюстрирована пригодность лейколектина для лечения различных воспалительных, аутоиммунных и других состояний кожи. Аналогичная эффективность может ожидаться для лечения других состояний. Например, хроническое воспаление желудочно-кишечного тракта можно объяснить чрезмерной реакцией на (или, возможно, в некоторых случаях, как) недостаточность реакции дендритных клеток на токсические факторы. Можно ожидать, что введение лейколектина, например, перорально, следовательно, может лечить хроническое воспаление желудочно-кишечного тракта аналогичным образом, и что воспаленная кожа реагирует благоприятно на введение лейколектина.
Аутоиммунные заболевания могут быть обусловлены специфической соматической экспрессией мутантных вариантов нормальных антигенов клеточной поверхности. Не желая связываться теорией, лейколектины могут служить для защиты клеток-мишеней от агрессивного воздействия.
В контексте настоящего изобретения «воспалительное заболевание» представляет собой нарушение, при котором воспаление наблюдается в нескольких точках во время прогрессирования заболевания и может быть единственным симптомом или одним из нескольких симптомов. Воспалительное заболевание может быть острым или хроническим и может представлять собой заболевание, описанное ранее в настоящей заявке или далее. Воспалительные заболевания включают сердечно-сосудистое воспаление (например, атеросклероз, инсульт), воспаление желудочно-кишечного тракта (в том числе, язвы, например язвы желудка или язвы двенадцатиперстной кишки), воспалительные заболевания печени, легочное воспаление (например, астму, вентилятор-индуцированное повреждение легких), почечное воспаление, воспаление глаз (например, увеит), воспаление поджелудочной железы, урогенительное воспаление, нейровоспалительные нарушения (например, рассеянный склероз, болезнь Альцгеймера), аллергические реакции (например, аллергический ринит/синусит, кожные аллергические реакции и нарушения (например, аллергическая сыпь/крапивница, отек Квинке, атопический дерматит, контактный дерматит, псориаз), пищевые аллергические реакции, аллергические реакции на лекарственные средства, аллергические реакции на насекомых, мастоцитоз), воспаления скелета (например, артрит, остеоартрит, ревматоидный артрит, спондилоартропатии), инфекция (например, бактериальные или вирусные инфекции); воспалительные заболевания ротовой полости (т.е. пародонтоз, гингивит или стоматит); открытые поражения кожи на слизистых оболочках; и трасплантация (например, отторжение аллотрансплантата или ксенотрансплантата или внутриутробная толерантность).
Предпочтительные воспалительные нарушения для лечения в соответствии с настоящим изобретением представляют собой воспалительные заболевания кожи, такие как экзема, акне, розовые угри, псориаз и контактный дерматит, воспаление желудочно-кишечного тракта и патологические состояния слизистых мембран, такие как язвы и открытые поражения кожи.
В контексте настоящего изобретения «аутоиммунное нарушение» представляет собой нарушение, при котором не опасный аутоиммунитет развился до патологического аутоиммунитета и может представлять собой описанное ранее или далее в настоящей заявке. Аутоиммунные заболевания включают синдром приобретенного иммунодефицита (СПИД, который представляет собой вирусное заболевание с аутоиммунным компонентом), очаговую алопецию, анкилозирующий спондилит, антифосфолипидный синдром, аутоиммунную болезнь Аддисона, аутоиммунную гемолитическую анемию, аутоиммунный гепатит, аутоиммунное заболевание внутреннего уха (AIED), аутоиммунный лимфопролиферативный синдром (ALPS), аутоиммунную тромбоцитопеническую пурпуру (ATP), болезнь Бехчета, кардиомиопатию, целиакия-спру герпетиформный дерматит; синдром хронической усталости с иммунной дисфункцией (CFIDS), хроническую воспалительную демиелинизирующую полинейропатию (CIPD), рубцующийся пемфигоид, синдром холодовой агглютинации, CREST-синдром, болезнь Крона, синдром Дегоса, ювенильный дерматомиозит, дискоидную волчанку, идиопатическую криоглобулинемию смешанного типа, фибромиалгию-фибромиозит, болезнь Грейвса, синдром Жиллиана-Барра, тиреоидит Хашимото, идиопатический легочный фиброз, идиопатическую тромбоцитопеническую пурпуру (ITP), IgA нефропатию, инсулин-зависимый сахарный диабет, ювенильный хронический артрит (болезнь Стилла), ювенильный ревматоидный артрит, болезнь Меньера, смешанное заболевание соединительной ткани, рассеянный склероз, миастению гравис, пернациозную анемию, узелковый периартериит, воспаление нескольких хрящей, полигландулярные синдромы, ревматическую полимиалгию, полимиозит и дерматомиозит, первичную агаммаглобулинемию, первичный биллиарный цирроз, псориаз, псориатический артрит, синдром Рейно, синдром Рейтера, ревматическую лихорадку, ревматоидный артрит, саркоидоз, склеродермию (прогрессирующий системный склероз (PSS), также известный как системный склероз (SS)), синдром Шегрена, синдром мышечной скованности, системную красную волчанку, артериит Такаясу, височный артериит/гигантоклеточный артериит, язвенный колит, увеит, витилиго и грануломатоз Вегенера.
Термин «поврежденная кожа» в контексте настоящего изобретения включает кожу, которая была повреждена под действием внешних факторов, таких как тепло, излучение (светом различных длин волн, например, рентгеновскими лучами или УФ), холодом, трением или разрывом, или рану, например, в результате травмы или хирургического вмешательства. Альтернативно поврежденная кожа может быть результатом инфекции или заболевания или лежащей в основе генетической аномалии. Повреждение может проявляться в виде разрывов, покраснений, зуда, воспаления, ороговевшей кожи, чешуек, и так далее.
Настоящее изобретение таким образом относится к способу лечения или профилактики аутоиммунного нарушения, воспалительного заболевания или поврежденной кожи у животного, где полипептид, молекулу нуклеиновой кислоты, антитело или фармацевтическую композицию, как описано ранее в настоящей заявке, вводят указанному животному.
Кроме того, настоящее изобретение относится к применению полипептида, молекулы нуклеиновой кислоты, антитела или фармацевтической композиции, как описано в настоящей заявке, в получении лекарственного средства для лечения или профилактики аутоиммунного нарушения, воспалительного заболевания или поврежденной кожи у животного.
В дополнительном альтернативном утверждении, настоящее изобретение относится к полипептиду, молекуле нуклеиновой кислоты, антителу или фармацевтической композиции, как описано в настоящей заявке, для лечения или профилактики аутоиммунного нарушения, воспалительного заболевания или повреждения кожи у животного.
В предпочтительном аспекте настоящее изобретение относится к таким способам, применениям, полипептидам, молекулам нуклеиновой кислоты, антителам или фармацевтическим композициям для лечения или профилактики аутоиммунного заболевания кожи, воспалительного заболевания кожи или поврежденной кожи, где полипептид, молекулу нуклеиновой кислоты, антитело или фармацевтическую композицию, как описано ранее в настоящей заявке, предпочтительно местно наносят на кожу.
Предпочтительно, указанным заболеванием является экзема, акне, псориаз, воспаление желудочно-кишечного тракта (такое как болезнь Крона, язвенный колит и другое хроническое воспаление), гингивит и воспаление ротовой полости и пищевода, и указанная поврежденная кожа является раздраженной или воспаленной, потрескавшейся от холода, получившей солнечный ожог, поврежденной воздействием тепла или излучения, или является результатом ранения.
В контексте настоящего изобретения «лечение» относится к уменьшению, облегчению или устранению, предпочтительно до нормальных уровней, одного или нескольких симптомов или эффектов указанного нарушения или повреждения, например наличия или степени повреждения кожи, например, относительного размера раны, воспаления, покраснения, зуда, боли и так далее, по сравнению с симптомами или эффектами, имеющимися в другой части тела указанного индивидуума, не подвергавшихся указанному лечению, или у соответствующего индивидуума, не подвергавшемуся указанному лечению.
«Профилактика» относится к абсолютной профилактике, или к уменьшению или ослаблению степени или сроков (например, задержке) появления этого симптома или эффекта. Это может достигаться, например, методами генной терапии, например, используя анти-РНК или нонсенс последовательности.
Способ лечения или профилактики в соответствии с настоящим изобретением может преимущественно быть объединен с введением одного или нескольких активных ингредиентов, которые являются эффективными в лечении или профилактике нарушений или повреждений кожи. Таким образом, фармацевтические композиции по настоящему изобретению дополнительно могут содержать один или несколько таких активных ингредиентов.
В соответствии с еще одним аспектом настоящего изобретения представлены продукты, содержащие один или несколько полипептидов, молекул нуклеиновых кислот или антител, как определено в настоящей заявке, и один или несколько дополнительных активных ингредиентов в виде комбинированного препарата для одновременного, раздельного или последовательного использования при лечении человека или животного.
Композиции по изобретению могут быть получены общепринятым способом с одним или несколькими физиологически приемлемыми носителями, эксципиентами и/или разбавителями в соответствии с методиками, хорошо известными в данной области, используя легкодоступные ингредиенты.
Таким образом, активный ингредиент может быть включен, необязательно вместе с другими активными веществами в качестве комбинированного препарата с одним или несколькими общепринятыми носителями, разбавителями и/или эксципиентами, для получения общепринятых галеновых препаратов, таких как таблетки, пилюли, порошки, леденцы, саше, эликсиры, суспензии (в виде жидкостей для инъекций или инфузий), эмульсий, растворов, сиропов, аэрозолей (в виде твердого вещества или в жидкой среде), мазей, мягких и твердых желатиновых капсул, суппозиториев, стерильных инъецируемых растворов, стерильных фасованных порошков и подобного. Биоразлагаемые полимеры (такие как полиэфиры, полиангидриды, полимолочная кислота или полигликолевая кислота) также могут быть использованы для твердых имплантов. Эти композиции могут быть стабилизированы путем использования лиофилизации, недостаточного охлаждения или Permazyme.
Предпочтительными эксципиентами, носителями или разбавителями являются лактоза, декстроза, сахароза, сорбит, маннит, крахмалы, акациевая камедь, фосфат кальция, карбонат кальция, лактат кальция, кукурузный крахмал, альгинаты, трагакант, желатин, силикат кальция, микрокристаллическая целлюлоза, поливинилпирролидон, целлюлоза, водный сироп, вода, вода/этанол, вода/гликоль, вода/полиэтиленгликоль, пропиленгликоль, метилцеллюлоза, метилгидроксибензоаты, пропилгидроксибензоаты, тальк, стеарат магния, минеральное масло или жирные вещества, такие как твердый жир, или их подходящие смеси. Также могут быть использованы средства для получения составов замедленного высвобождения, такие как карбоксиполиметилен, карбоксиметилцеллюлоза, ацетатфталат целлюлозы или поливинилацетат.
Композиции дополнительно могут включать смазывающие вещества, увлажняющие вещества, эмульгирующие вещества, вещества, повышающие вязкость, гранулирующие вещества, дезинтегрирующие вещества, связующие вещества, осмотически активные вещества, суспендирующие вещества, консерванты, подсластители, вкусо-ароматические вещества, усилители адсорбции (например, вещества, смачивающие поверхность или для назальной доставки, например, соли желчных кислот, лецитины, поверхностно-активные вещества, жирные кислоты, хелаторы), агенты, вызывающие покоричневение, органический растворитель, антиоксидант, стабилизирующие агенты, смягчающие вещества, кремний-содержащие соединения, альфа-гидроксикислоту, средство, снимающее раздражение, противопенное средство, увлажняющее средство, витамины, ароматизаторы, ионные или неионные загустители, поверхностно-активные вещества, наполнители, ионные или неионные загустители, секвестранты, полимеры, пропелленты, подщелачивающие или подкисляющие средства, средства, придающие непрозрачность, красители и соединения жирного ряда и подобные.
Композиции по настоящему изобретению могут быть получены таким образом, чтобы обеспечивать быстрое, длительное или замедленное высвобождение активного ингредиента после введения в организм, используя методики, хорошо известные из уровня техники.
Композиция может находиться в любой подходящей лекарственной форме для возможности доставки или для наведения на конкретные клетки или ткани, например, в виде эмульсии, или в липосомах, ниосомах, микросферах, наночастицах или подобном, с которыми активный ингредиент может быть абсорбирован, адсорбирован, включен или связан. Это эффективно может превращать продукт в нерастворимую форму. Эти конкретные формы могут преодолевать как проблемы стабильности (например, разрушение), так и проблемы доставки.
Эти частицы могут нести соответствующие поверхностные молекулы для улучшения времени циркулирования (например, компоненты сыворотки, поверхностно-активные вещества, полиоксамин 908, ПЭГ и так далее) или группы сайт-специфичного нацеливания, такие как лиганды для конкретных клеточных рецепторов. Подходящие методики доставки лекарственных средств и для направленной доставки хорошо известны из уровня техники и описаны в WO99/62315.
Использование растворов, суспензий, гелей и эмульсий является предпочтительным, например активный ингредиент может быть введен в воду, водную жидкость, масло, гель, эмульсию, масло-в-воде или вода-в-масле, дисперсию или их смесь.
Композиции могут быть для местного (например, на кожу), перорального или парентерального введения, например путем инъекции. Как упоминалось ранее в настоящей заявке, лейколектин демонстрирует очень небольшую вариабельность между различными видами. Действительно, было обнаружено, что он является инвариантным в популяции здоровых людей, и это позволило бы использовать лейколектин, например, путем введения инъекционным путем пациентам без запуска гуморального антительного ответа, образом, аналогичным белку инсулину, который также является инвариантным в популяции людей. Следовательно, системная терапия путем введения лейколектина может быть использована для лечения состояний, описанных в настоящей заявке, в частности, аутоиммунных нарушений.
Однако предпочтительными являются местные композиции и применения и включают гели, кремы, мази, спреи, лосьоны, бальзамы, косметические карандаши, мыла, порошки, пленки, аэрозоли, капли, пены, растворы, эмульсии, суспензии, дисперсии, например неионные везикулярные дисперсии, молочко и любые другие фармацевтические формы, общепринятые в уровне техники.
Мази, гели и кремы могут, например, быть составлены в композицию с водной или масляной основой с добавлением подходящих загустителей и/или гелеобразующих веществ. Лосьоны могут быть составлены в композицию с водной или масляной основой и будут, в основном, также содержать один или несколько эмульгаторов, диспергирующих, суспендирующих агентов, загустителей или красителей. Порошки могут быть получены с помощью любой подходящей порошкообразной основы. Капли и растворы могут быть составлены в композицию с водной или неводной основой, также содержащей один или несколько диспергирующих, солюбилизирующих или суспендирующих агентов. Аэрозольные спреи удобно доставлять из контейнеров со сжатым воздухом с использованием подходящего пропеллента.
Альтернативно, композиции могут быть представлены в форме, адаптированной для перорального или парентерального введения. Альтернативные фармацевтические формы таким образом включают простые таблетки или таблетки, покрытые оболочкой, капсулы, суспензии и растворы, содержащие активный компонент, необязательно вместе с одним или несколькими инертными общепринятыми носителями и/или разбавителями, например, с кукурузным крахмалом, лактозой, сахарозой, микрокристаллической целлюлозой, стеаратом магния, поливинилпирролидоном, лимонной кислотой, винной кислотой, водой, водой/этанолом, водой/глицеролом, водой/сорбитом, водой/полиэтиленгликолем, пропиленгликолем, стеариловым спиртом, карбоксиметилыцеллюлозой или жировыми веществами, такими как твердый жир или их подходящими смесями.
Концентрация активного ингредиента в композициях по настоящему изобретению зависит от природы используемого соединения (т.е. полипептида, молекулы нуклеиновой кислоты или антитела), способа введения, курса лечения, возраста и массы тела пациента, медицинских показаний, организма или площади тела, подвергаемой лечению и может варьировать или устанавливаться в соответствии с выбором. В основном, однако, диапазоны концентраций для соединения, описанного в настоящей заявке, составляют 0,0001, 0,0005, 0,001 или от 0,01 до 25%, например 0,0005-15%, например от 0,01 до 10%, например от 0,1 до 5, например 1-5% (мас./мас. конечного препарата для введения, в частности для местного применения). Указанные концентрации определяют, основываясь на количестве самого соединения, и, следовательно, соответствующие величины поправки следует сделать, чтобы принять во внимание чистоту композиции. Эффективные однократные дозы могут находиться в интервале от 0,1-100 мг/день, предпочтительно 2-10 мг/день в зависимости от животного, подвергаемого лечению, взятые как однократная доза.
Введение может осуществляться любым подходящим способом, известным в области медицины, в том числе, например, пероральным, парентеральным (например, внутримышечным, подкожным, внутрибрюшинным или внутривенным) чрескожным, защечным, ректальным или местым введением или введением путем ингаляции. Предпочтительные формы введения будут введены перорально, или наиболее предпочтительно, местно. Понятно, что пероральное введение имеет свои ограничения, если активный ингредиент является расщепляемым. Для преодоления таких проблем ингредиенты могут быть стабилизированы, как упомянуто ранее.
Будет понятно, что поскольку активный ингредиент для осуществления настоящего изобретения принимает целый ряд форм, например, молекулы нуклеиновой кислоты (которая может находиться в векторе) или полипептида, форма композиции и путь доставки будет меняться. Предпочтительно, однако, будут использоваться жидкие растворы, кремы или суспензии, в частности, например, для пероральной доставки или местного применения.
Либо полипептид, либо молекулы нуклеиновой кислоты по изобретению могут быть использованы по указанным выше медицинским показаниям. В последних способах генной терапии молекулы нуклеиновой кислоты предпочтительно представлены в векторах, которые подходят для трансфекции/трансформации, как описано выше, например вирусных векторах, например аденовирусных, с использованием методов генной терапии, известных в уровне техники для медицинских применений.
Животные, у которых можно применять или которым можно вводить эти композиции, включают млекопитающих, рептилий, птиц, насекомых и рыб (например, лосось или треска). Предпочтительно животными, у которых применяют эти композиции, являются млекопитающие, в частности приматы, домашние животные, крупный рогатый скот и лабораторные животные. Таким образом, предпочтительные животные включают мышей, крыс, кроликов, морских свинок, кошек, собак, обезьян, свиней, коров, коз, овец и лошадей. Особенно предпочтительно композиции применяют у людей или вводят людям.
Следующие примеры даны только в качестве иллюстрации, в которых чертежи, на которые имеются ссылки, представляют собой следующее:
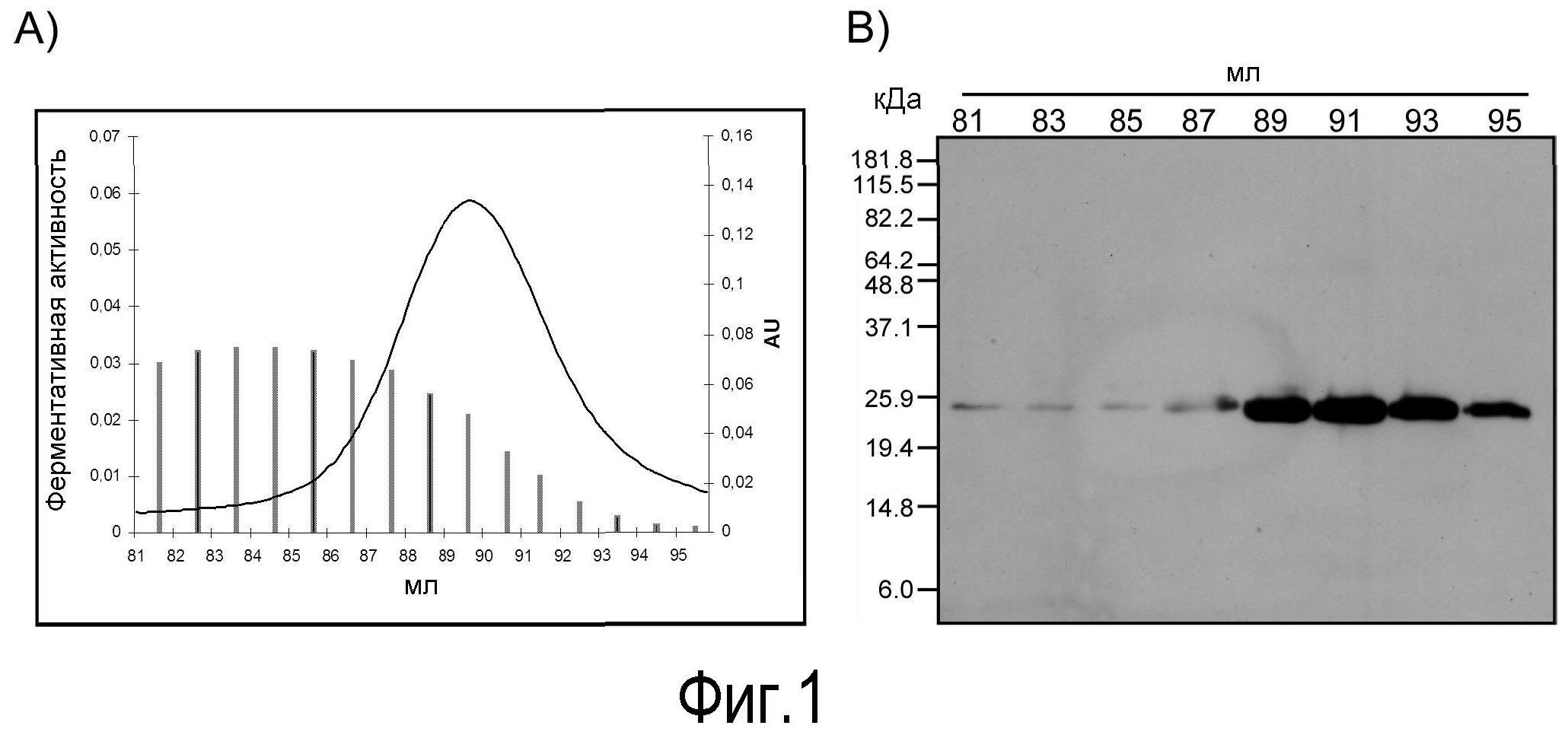
На Фигуре 1 показана (A) гель-фильтрация частично очищенной зоназы лосося с получением на выходе лейколектина. Колонку Superdex 16/60 (GE Healthcare) соединяли с системой FPLC и использовали с буферным потоком 1 мл/мин для 120 мл. Элюцию белков с колонки контролировали с использованием УФ 280 нм (правая ось y) и собирали в 1 мл фракции. Активность зоназы измеряли путем расщепления хромозима X при OD406. Нативная молекулярная масса зоназы перекрывает широкий диапазон с пиком около 50 кДа. Лектин MW=30 кДа, и (B) Идентификация (лейко-)лектина лосося путем иммуноблоттинга. Анализы иммуноблоттинга белков выбранных фракций, полученных в результате указанной выше гель-фильтрации с использованием антитела против (лейко-)лектина на основе эпитопа (см. Фиг. 3). Номера фракций показаны выше иммуноблотов. Маркеры молекулярной массы (кДа) указаны слева. Определенная молекулярная масса лектина соответствует молекулярной массе, полученной другими способами (см. Фиг. 3).
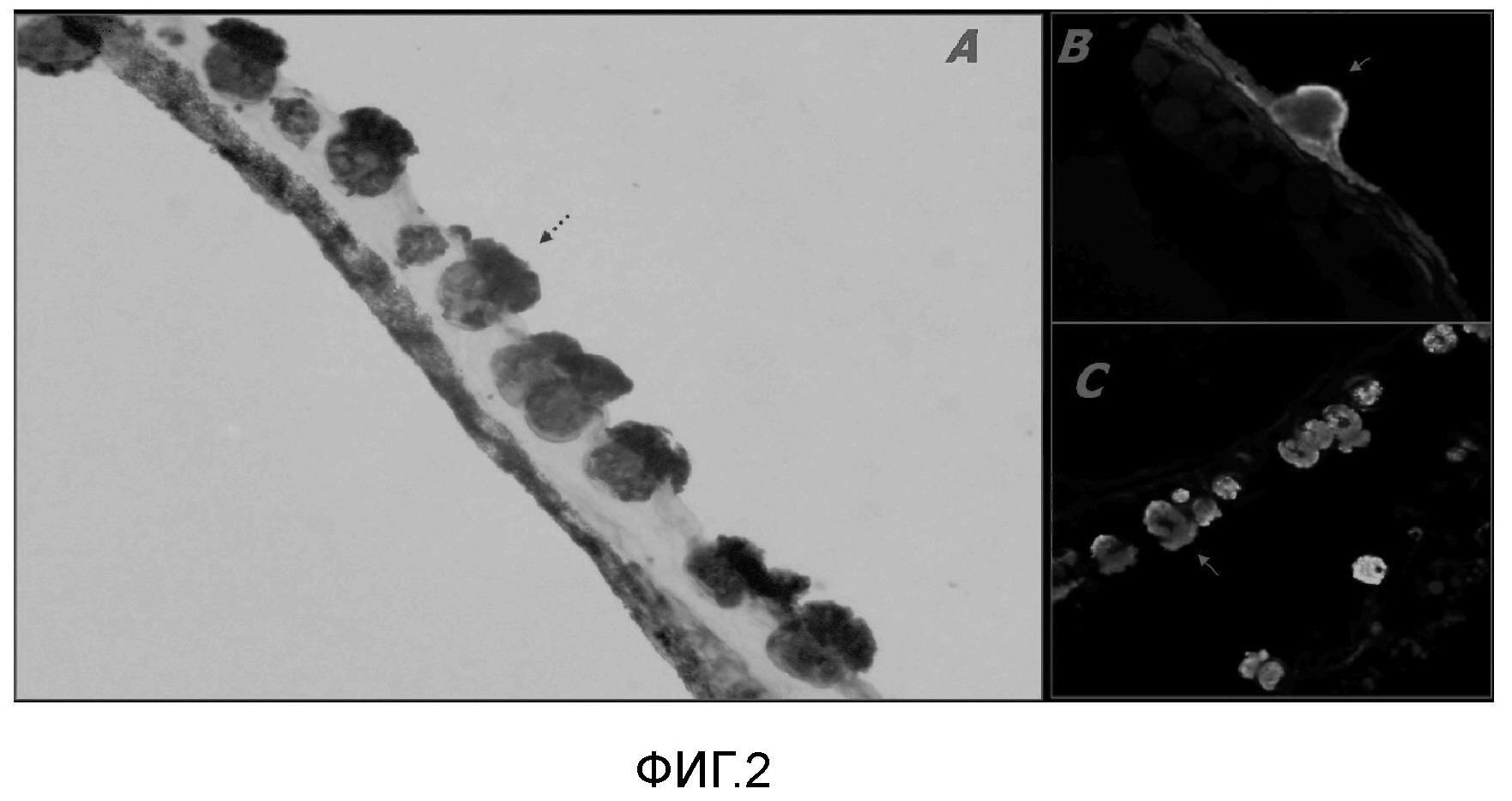
На Фигуре 2 показана идентификация лектин-продуцирующих клеток (лейкоцитов) в эмбрионах атлантического лосося, где на панелях А, В и С представлены поперечные срезы тел эмбрионов атлантического лосося, которые были фиксированы формалином и заключены в парафин. Присутствие лейколектина определяли с помощью поликлонального антитела кролика к LL, используя метод иммунопероксидазного окрашивания (A) или непрямой иммунофлуоресценции (B и C). Клетки, вступающие в реакцию с антителом против лектина, могут быть видны как темные (A), или светлые (B и C) по сравнению с фоном, соответственно. Многочисленные иммунологически реактивные единичные клетки со специфическими цитологическими особенностями видны в эпидермисе без пространственных ограничений вдоль переднезадней центральной оси эмбриона. Стрелки A и B указывают на сравнительно крупные клетки (лектоциты), легко отличимые от окружающих эпидермальных клеток. Их ядра являются базальными, тогда как цитоплазма заполнена лейколектином, так, что эти клетки выпячиваются как грибы в перивителлиновом пространстве. На панеле 2C показано их гранулярное содержимое.
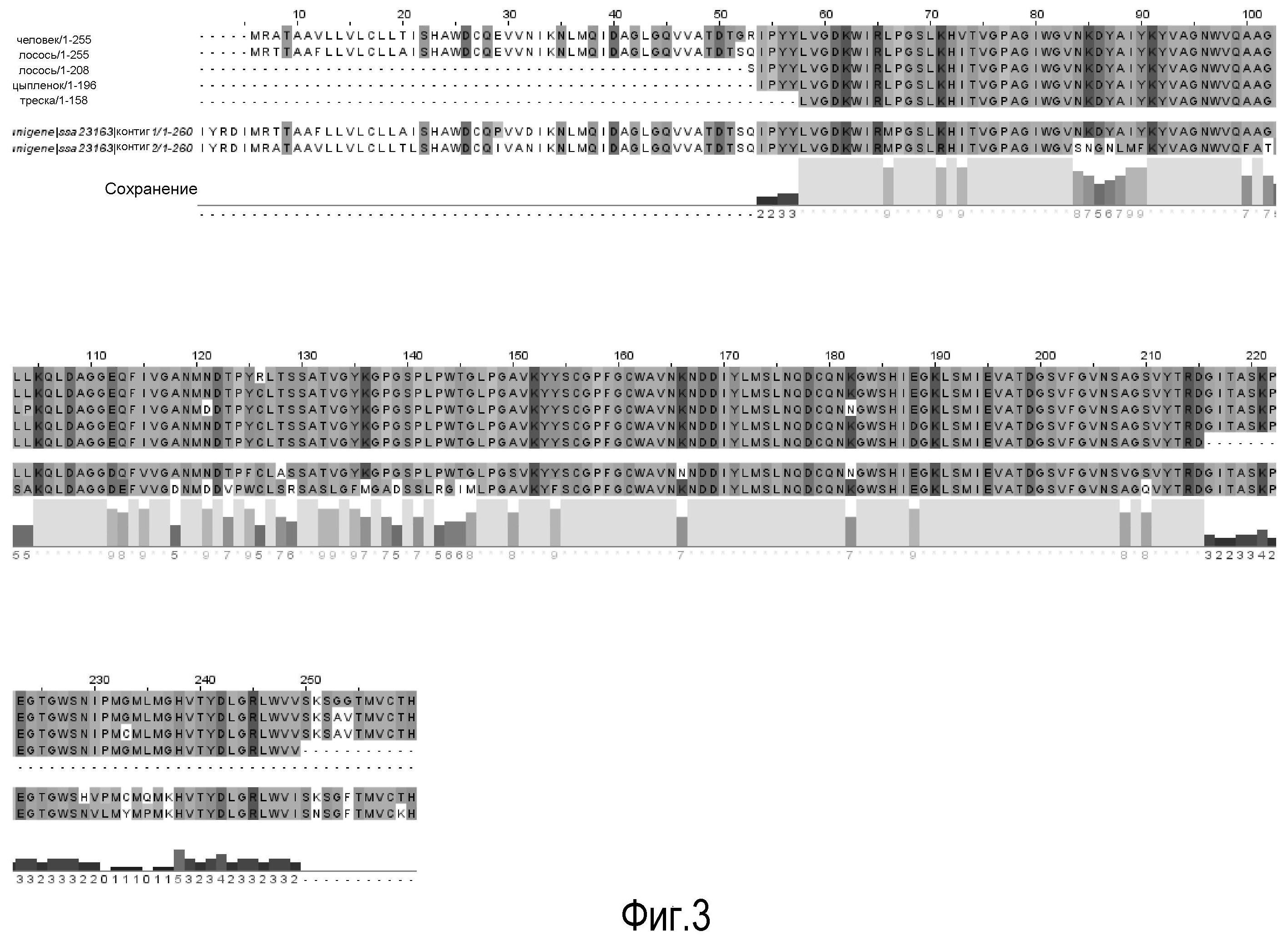
На Фигуре 3 показаны выравнивания лейколектинов человека, лосося, цыпленка, трески и две трансляции двух контигов, которые составляют семейство UniGene Family Ssa.23163, коллекция salmon EST. Из двух контигов контиг 1 представляет собой контиг, который имеет сходство с первичной структурой большинства лейколектинов. Однако различие между двумя контигами является небольшим, только около 80%.
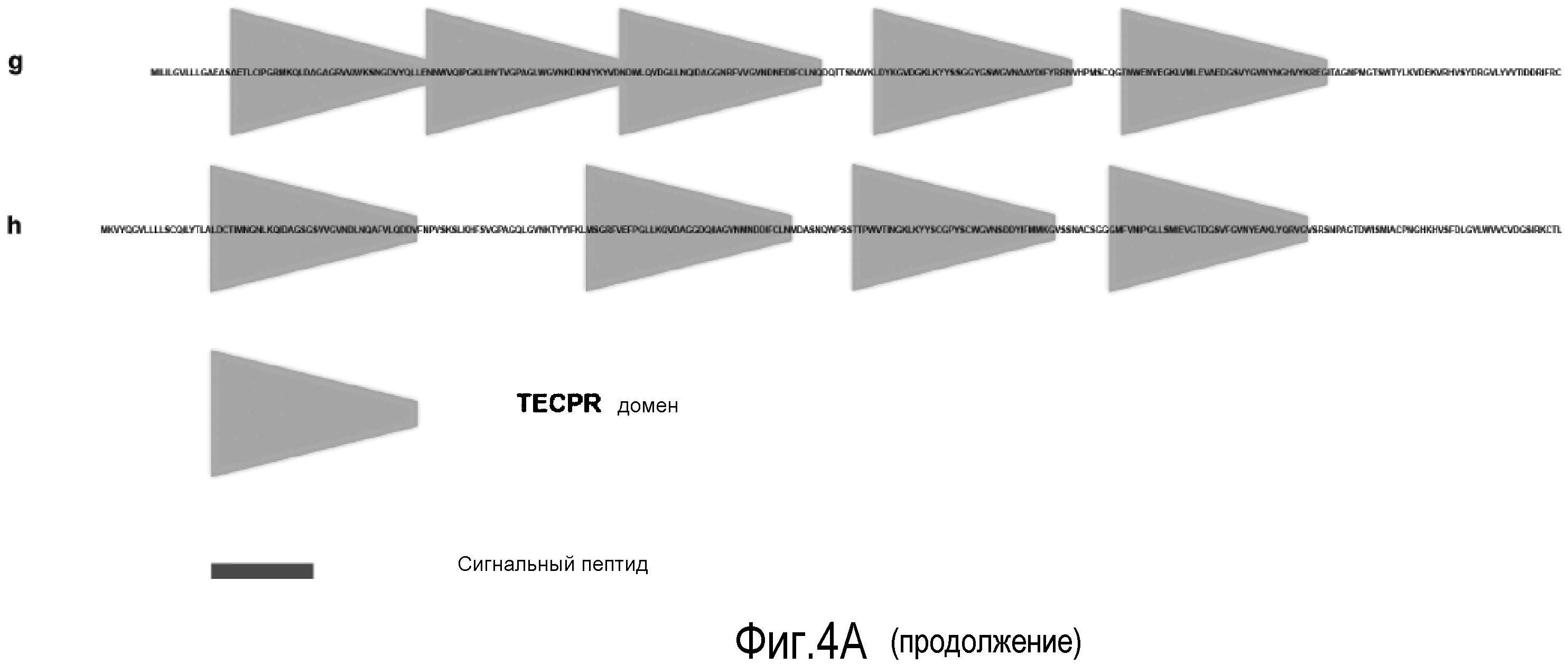
На Фигуре 4 показаны (A) SMART домены последовательностей, аналогичных лейколектину человека. Представлены наиболее высокие баллы для последовательности в результаре проведения поиска BLASTP с использованием WU-BLAST 2. Последовательности перечислены от более сходных к менее сходным. a - лейколектин человека, b - эмбриональный лейколектин лосося, с - лейкоцитарный лейколектин лосося (фрагмент), d - лейколектин цыпленка (фрагмент), e - лейколектин трески (фрагмент), f - лектин икринок карпа (Ac#-P68512), g - ранаспумин-6 лягушки tungara (Ac#:B5DCK6), h - данио Zgc: 173443 белок (Ac#: A8E4Z1). Следует отметить, что последовательности из лейкоцитарного лейколектина лосося, лейкоцитарного лейколектина цыпленка и лейкоциторного лейколектина трески представляют только частичные, а не полноразмерные последовательности. Полноразмерный вариант этих последовательностей, вероятно, будет иметь сходство с общей структурой, обнаруженной в лейколектине из лейкоцитов человека (a) и эмбрионов лосося (b). Далее лейколектиновый профиль с 5 следующими друг за другом TECPR-доменами все еще сохраняется для последовательности лягушки Tungara, но не для последовательности Данио, в которой обнаружено только 4 TECPR домена, и
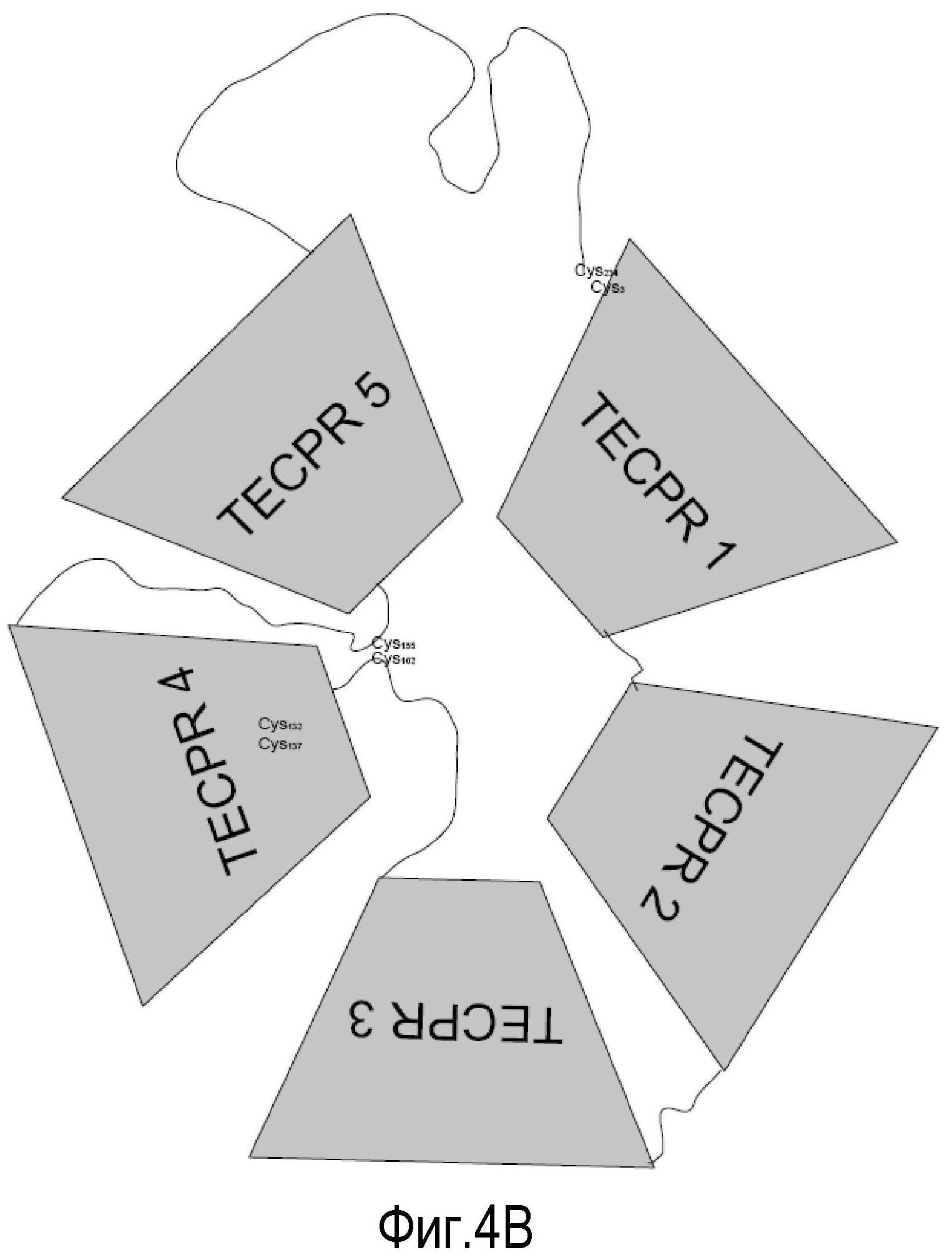
(B) графическое представление лейколектина с 5 TECPR-доменами. TECPR домены по всей вероятности состоят из 4 бета-спиралей, образуя 2 бета-складчатого слоя. Там имеется три дисульфидные связи: одна внутренняя в TECPR #4, две другие находятся в соединяющих петлях, как указано. В основном, сайты узнавания сахара находятся в таких лектинах в областях между TECPR-доменами. Лектин, наиболее близко родственный лейколектину, имеет известную специфичность к сахару главным образом в отношении N-ацетилглюкозамина. Предполагаемую специфичность распознавания сахара для лейколектина остается определить.
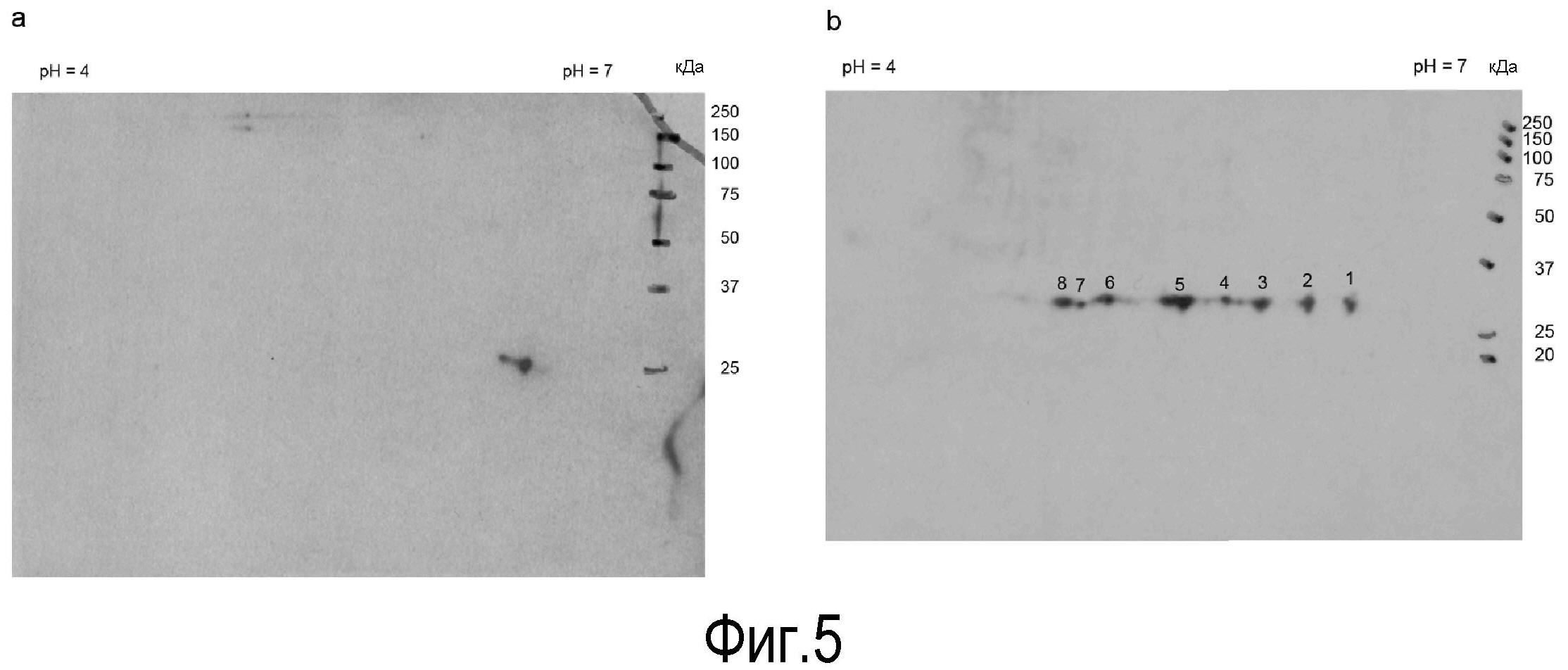
На Фигуре 5 показано присутствие перивителлинового лектина в лейкоцитах. IPG-полосу перекрывания pH-диапазона 4-7 использовали в первом измерении, тогда как 12,5% полиакриламидный гель использовали во время электрофореза второго измерения.
A: в лейкоцитах лосося было обнаружено только два пятна для положительного взаимодействия с поликлональным антителом против лектина. Их молекулярная масса составляла около 26 кДа, с pI около 6,5. Лейколектин также может быть идентфцирован в лейкоцитарных препаратах в других видах.
B: В препарате, полученном из лосося, был обнаружен ряд иммунологически реактивных пятен (под номерами 1-8) с молекулярной массой около 30 кДа, которые перекрывали pH диапазон pI от 4,9 до 6,5.
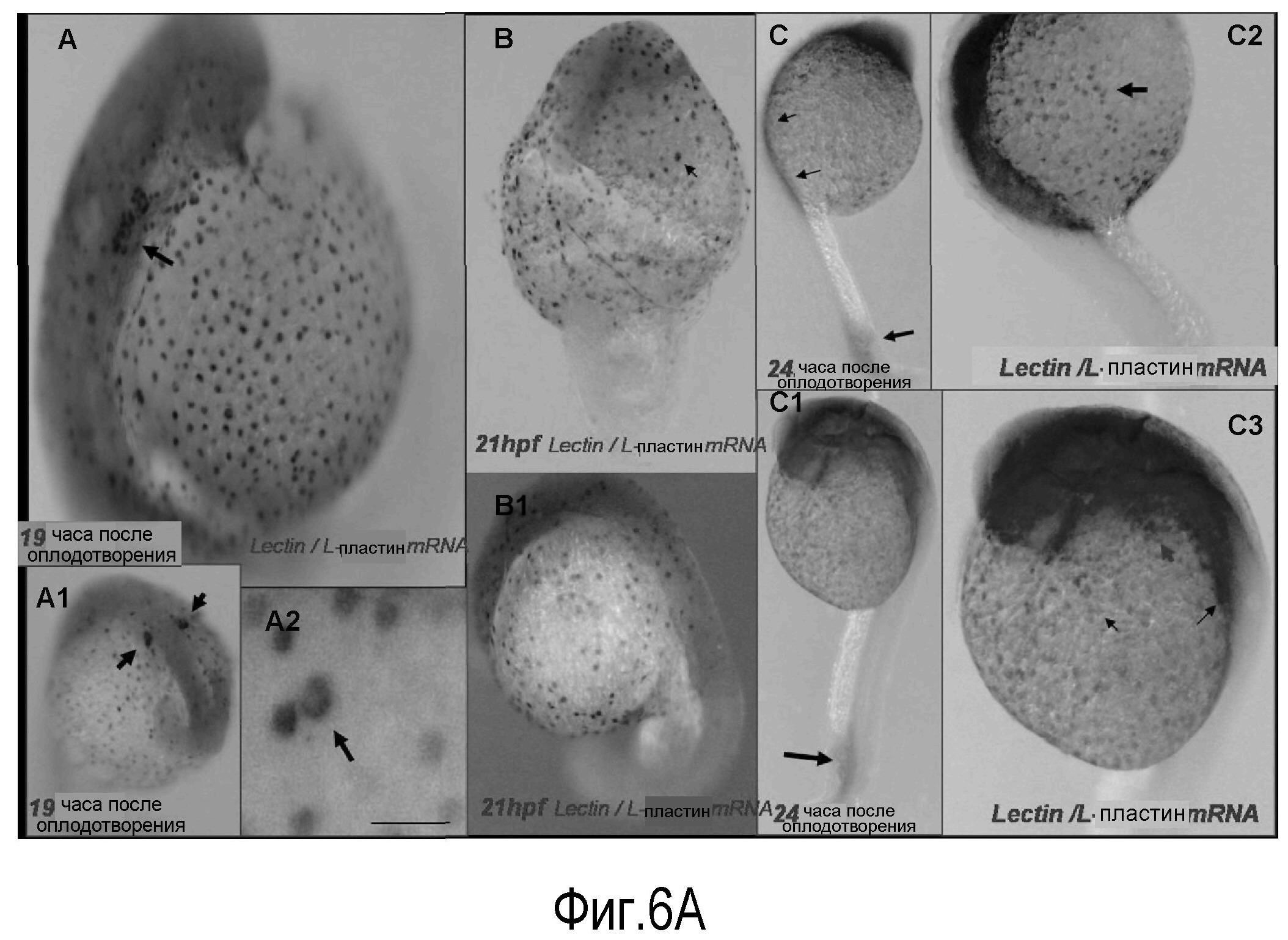
На Фигуре 6 показана ко-экспрессия лейколектина в миелоидной линии, в частности в моноцит-макрофагальной линии дифференцировки у данио. (A) профиль экспрессии генов лектина и L-пластина. Было обнаружено, что данио экспрессирует такой же лектин, который обнаружен у лосося. Меченный флуоресцеином зонд мРНК лектина использовали совместно с DIG-меченым зондом для зонда мРНК L-пластина, который является специфичным маркером моноцит-макрофагальной линии дифференцировки. С двойной меткой в гибридизации in situ выявляется ко-экспрессия мРНК лектина и L-пластина в одних и тех же клетках во время эмбриогенеза данио. Возраст эмбрионов в часах после оплодотворения (pf) представлен в нижнем левом углу. Светлые сигналы указывают на экспрессию гена L-пластина; более темные сигналы указывают на экспрессию лектина.
На панели A (вид сбоку) представлена ко-экспрессия мРНК лектина и L-пластина в одних и тех же клетках, которые образуют рассеянную аксиальную и параксиальную популяции на переднем и боковом желтках. Более сильное увеличение (A2) показывает характерную лейкоцитарную морфологию этих клеток. Данные в A1 демонстрируют экспрессию этих двух генов в билатеральных полосах клеток в передне-боковой пластинке мезодермы (стрелки). На Панели В показаны те же данные в 21 ч.
На Панели С (24 ч pf) показана ко-экспрессия генов L-пластина и лектина в задней промежуточной клеточной массе (две верхние стрелки), в области вентральной вены (нижняя стрелка), в значительном числе клеток, рассеянных вдоль тела и головы эмбриона. К 24 ч pf (C2) большинство клеток ко-экспрессируют эти два гена (см. стрелки), но многие клетки, по-видимому, экспрессируют только один или другой ген. Стрелки в C3 указывают на клетки, экспрессирующие только мРНК L-пластина, и
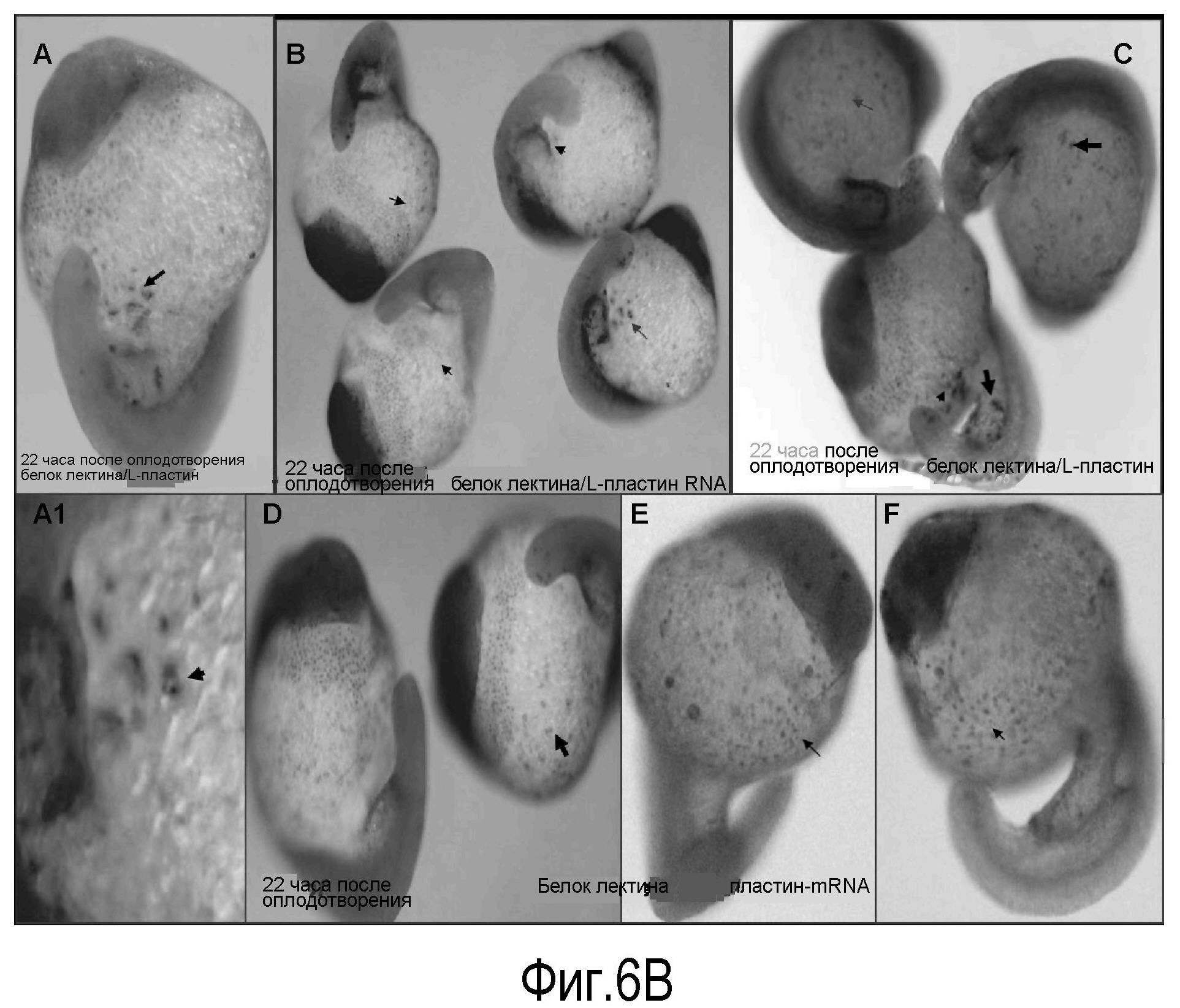
(B) совместная локализация в клетке мРНК белка лектина и L-пластина. Эмбрионы данио (22 ч pf) анализировали путем объединения иммуногистохимии с гибридизацией in situ на мРНК белка лектина (более темный сигнал) и мРНК L-пластина (более светлый сигнал). В гибридизации in situ использовали DIG-меченную кРНК, специфичную для гена L-пластина, объединенную иммуногистохимией с поликлональным антителом кролика против лектина.
На Панели A: представлен фронтальный вид эмбриона. Стрелки указывают на кластер клеток, характеризующихся общей экспрессией мРНК белка лектина и L-пластина. A1: большее увеличение кластера, демонстрирующее ко-экспрессию гена L-пластина и белка лектина в одной и той же клетке (черные стрелки). Следует отметить несколько клеток небольшого размера округлой формы, имеющих сходство со зрелыми лимфоцитами рядом с другой клеткой с сегментированным ядром, характерный морфологический признак зрелых нейтрофильных лейкоцитов. На панелях B, С, D, Е проиллюстрированы разбросанные популяции клеток по всему эмбриону данио, в которых совместно экспрессируется мРНК белка лектина и L-пластина (стрелка).
На Фигуре 7 показано семейство лейколектинов. Были собраны доступные лейколектиновые белки человека, лосося, цыпленка и трески (выравнивание weblogo). Полное соответствие аминокислотных остатков в одном положении представлено большими буквами, уменьшенный размер указывает на меньшую степень соответствия. Серия букв указывает на варианты.
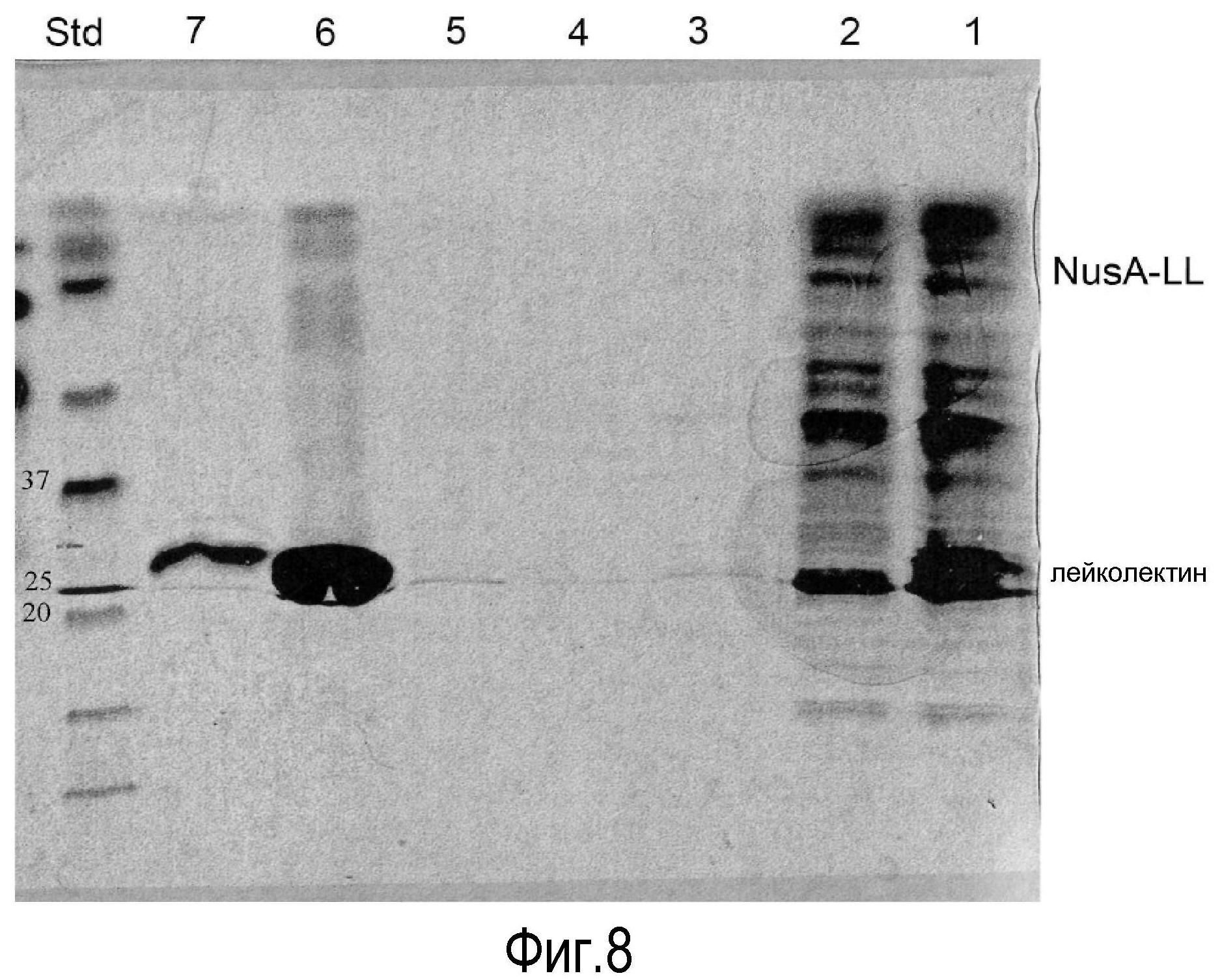
На Фигуре 8 показаны фракции, окрашенные кумасси, после очистки рекомбинантного лейколектина колоночной хроматографией. Дорожки представляют собой 1 - супернатант, 2 - проточную фракцию, 3 - промывку, 4 - F1, 5 - F2, 6- смесь F3, F4 и F5, 7- F6 и 8 - STD.
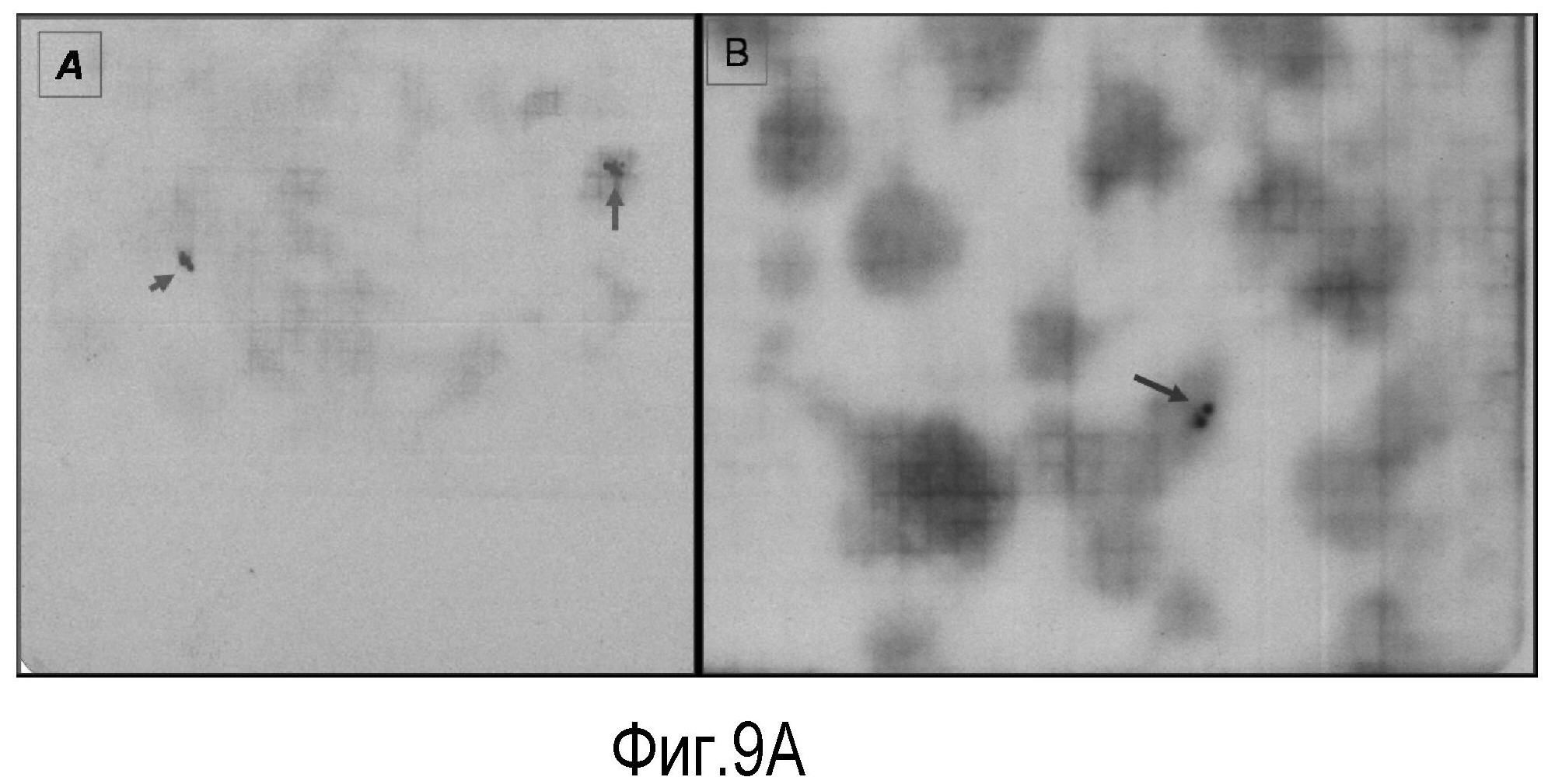
На Фигуре 9 показаны (A) эксперименты для идентификации и установления генной последовательности лейколектина лосося.
На панели A проиллюстрированы два положительных двойных пятна, идентифицированных в фильтре номер 6, панели #5 и 2, которые соответствуют точному номеру тарелок 257 и 176 и координатам лунок клона L-7 и F-7 соответственно.
На Панели В продемонстрировано одно положительное двойное пятно, идентифицированное в фильтре №3, панель #6, которое соответствует точному номеру тарелки 144 (на основании таблицы определителя координат тарелки) и координатам лунок клона A-12, и
(B) демонстрирует установленную геномную последовательность гена лейколектина (2323 пар оснований). Указано положение 5 экзонов и, следовательно, также интронов. Расположение начала транскрипции для этого гена (предопределение промотора, на основании BDGP Neural Network Promoter Prediction, "P", предопределенное начало транскрипции "ST", TATA box "T") и указаны последовательности, точно определяющие полиаденилирование ("PA") в генном продукте.
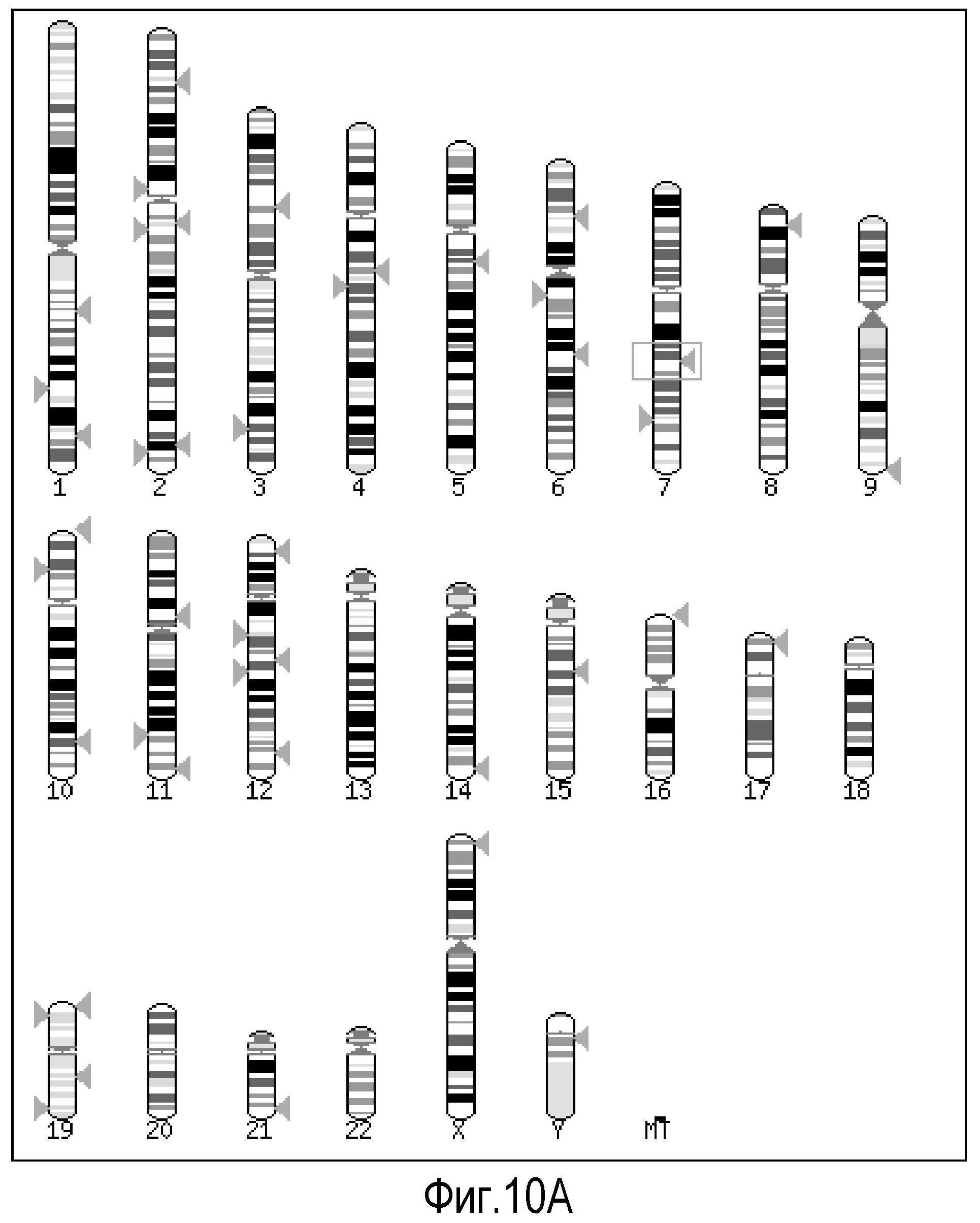
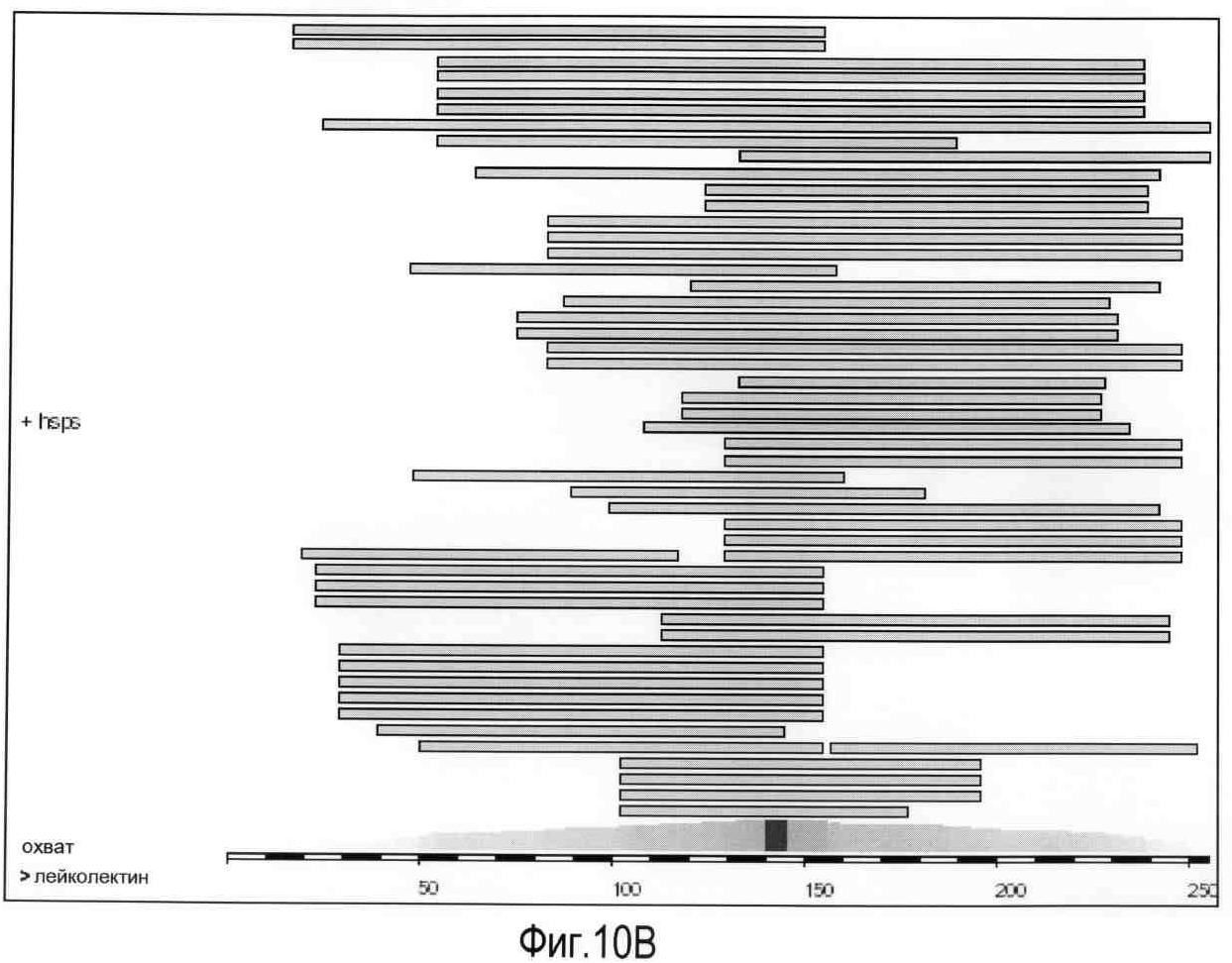
На Фигуре 10 показана (A) карта, на которой изображены хромосомы человека, положения совпадений BLASTP-hits (см. таблицу) указаны стрелками, (B) условные обозначения карты охвата:
Визуализация положения BLASTP совпадений (столбцы) и суммарный охват задаваемой последовательности (лейколектин человека). Очевидно, что найденная сумма последовательностей охватывает всю последовательность лейколектина, но эти данные явно не подразумевают, что это ген лейколектина, C) таблица, в которой представлены BLASTP совпадения и их положение в геноме человека с использованием лейколектина человека в качестве задаваемой последовательности.
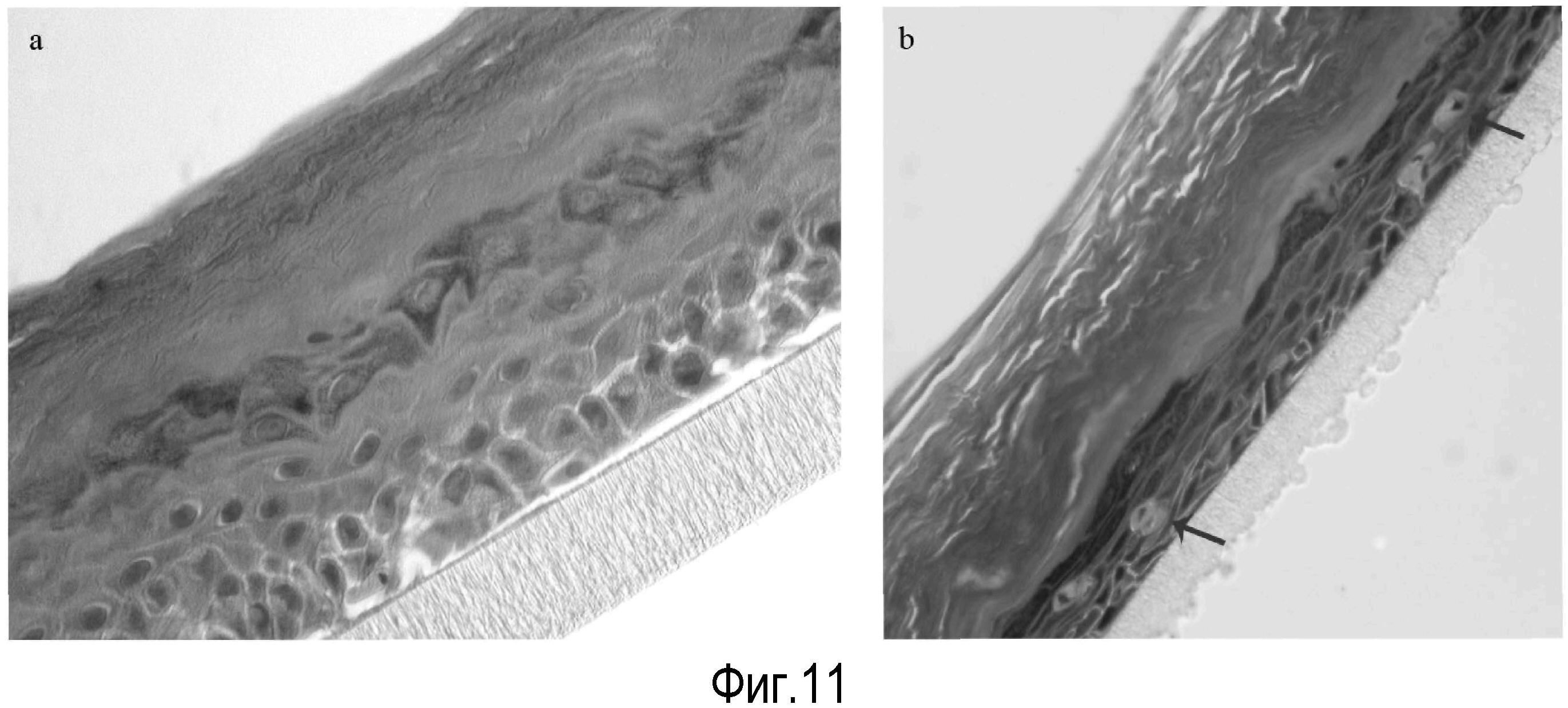
На Фигуре 11 показаны эффекты лейколектина на эпителий человека. Контрольная культура=A; Культура, подвергаемая действию лейколектина=B. Стрелки указывают на крупные клетки, появляющиеся в базальном слое только после воздействия лейколектина.
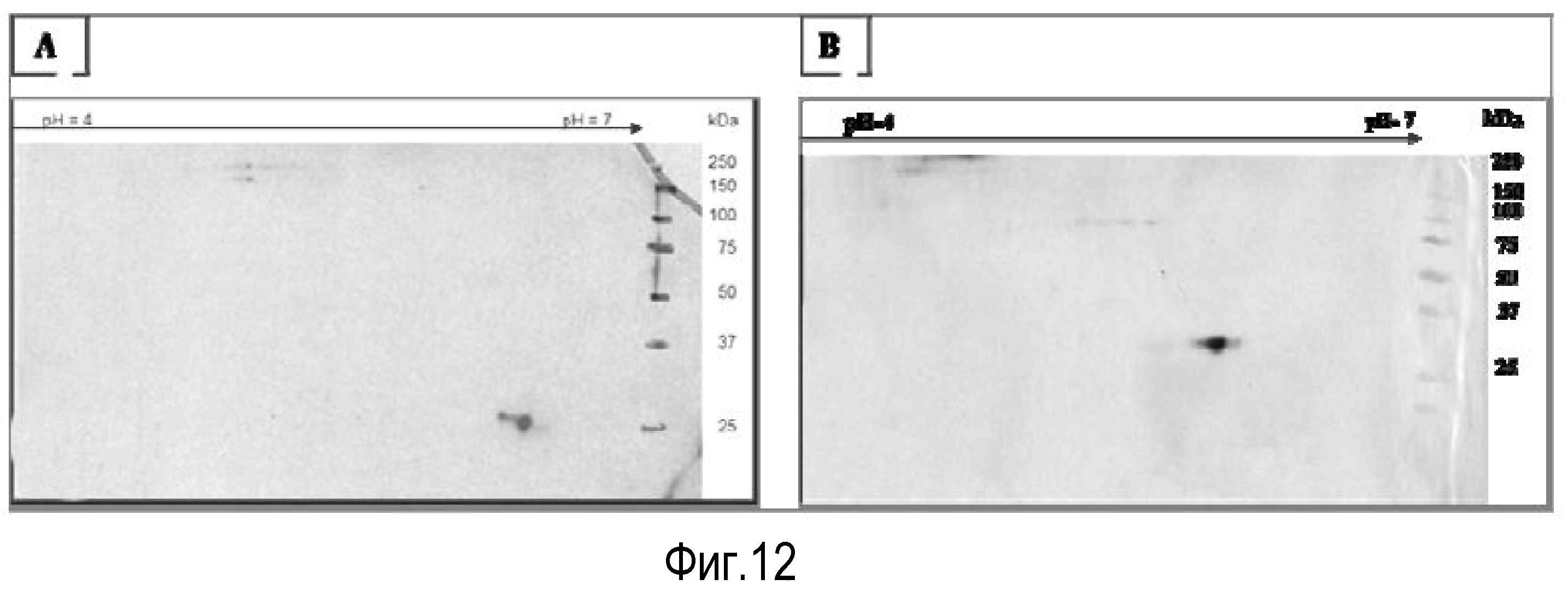
На Фигуре 12 показана экспрессия белка лейколектина в лейкоцитах. На Панели A показан 12% 2D PAGE очищенного белка, ~2 мкг, из лейкоцитов лосося. На Панели В показан 15% 2D PAGE очищенного белка, 0,8 мкг, из лейкоцитов человека от Lymphoprep™. Мембраны обрабатывали поликлональным первичным антителом к LL лосося, перед обработкой антителом козы против антитела кролика, и визуализировали с помощью системы детекции, усиленной ЭХЛ.
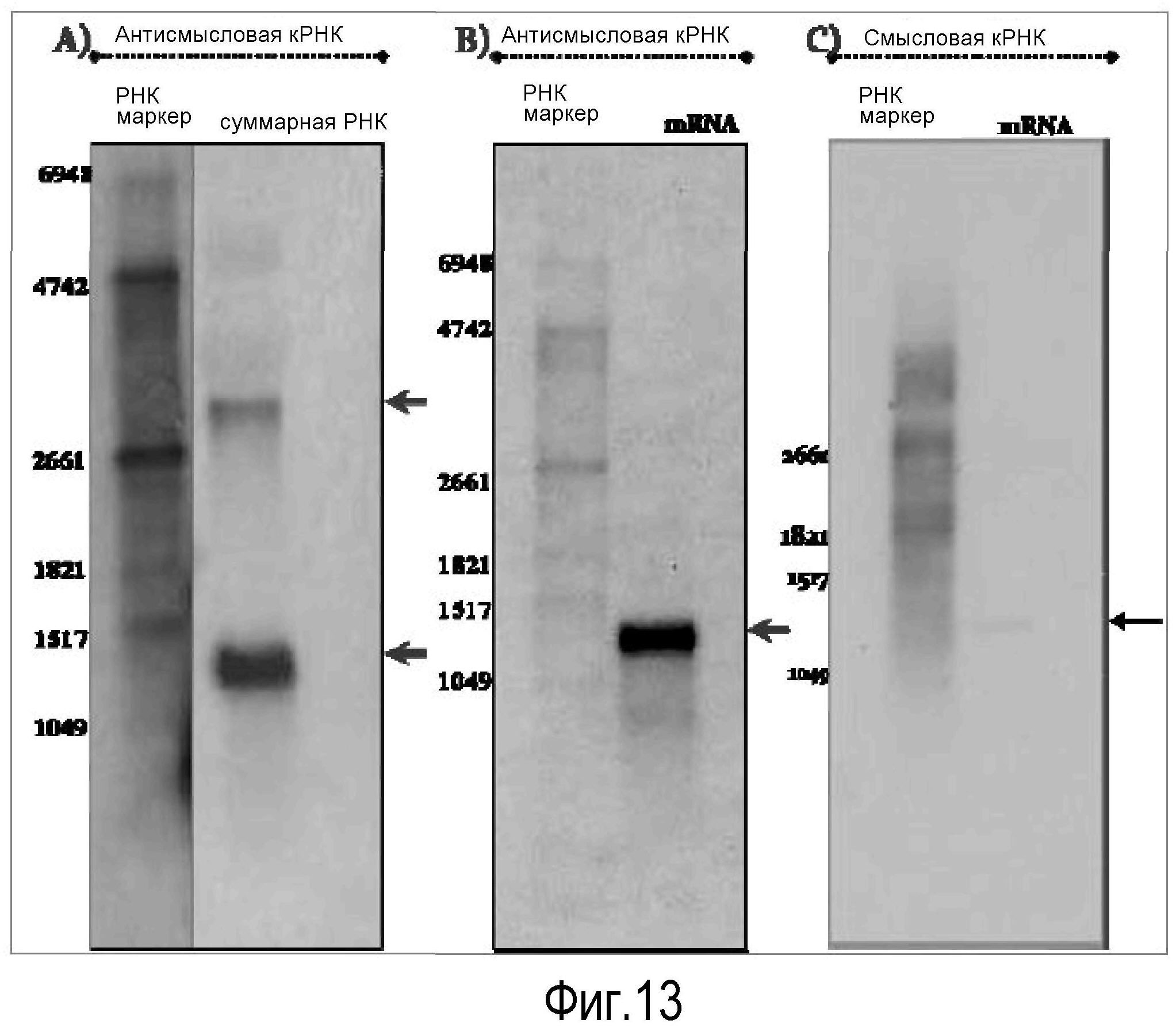
На Фигуре 13 показаны транскрипты лейколектина лосося, идентифицированные в Нозерн блотах. На Панели A показана суммарная РНК из эмбрионов атлантического лосося (370 dd), фракционированная в 1,2% агарозе в присутствии формальдегида и зондированная антисмысловым рибозондом, меченным DIG, специфичным в отношении LL (720 пар оснований). На Панели В показан Нозерн блот анализ мРНК (очищенной с помощью магнитных полиT-бус). При гибридизации использовали рибозонды, меченные DIG, полученные из частичной кодирующей последовательности LL. На Панели С показана нитроцеллюлозная мембрана (B), зондированная смысловым рибозондом, меченным DIG. Серые стрелки означают присутствие транскрипта; черная стрелка указывает на его отсутствие. Использовали DIG-РНК маркер I, 0,3-6,9 тыс. осн. (Roche).
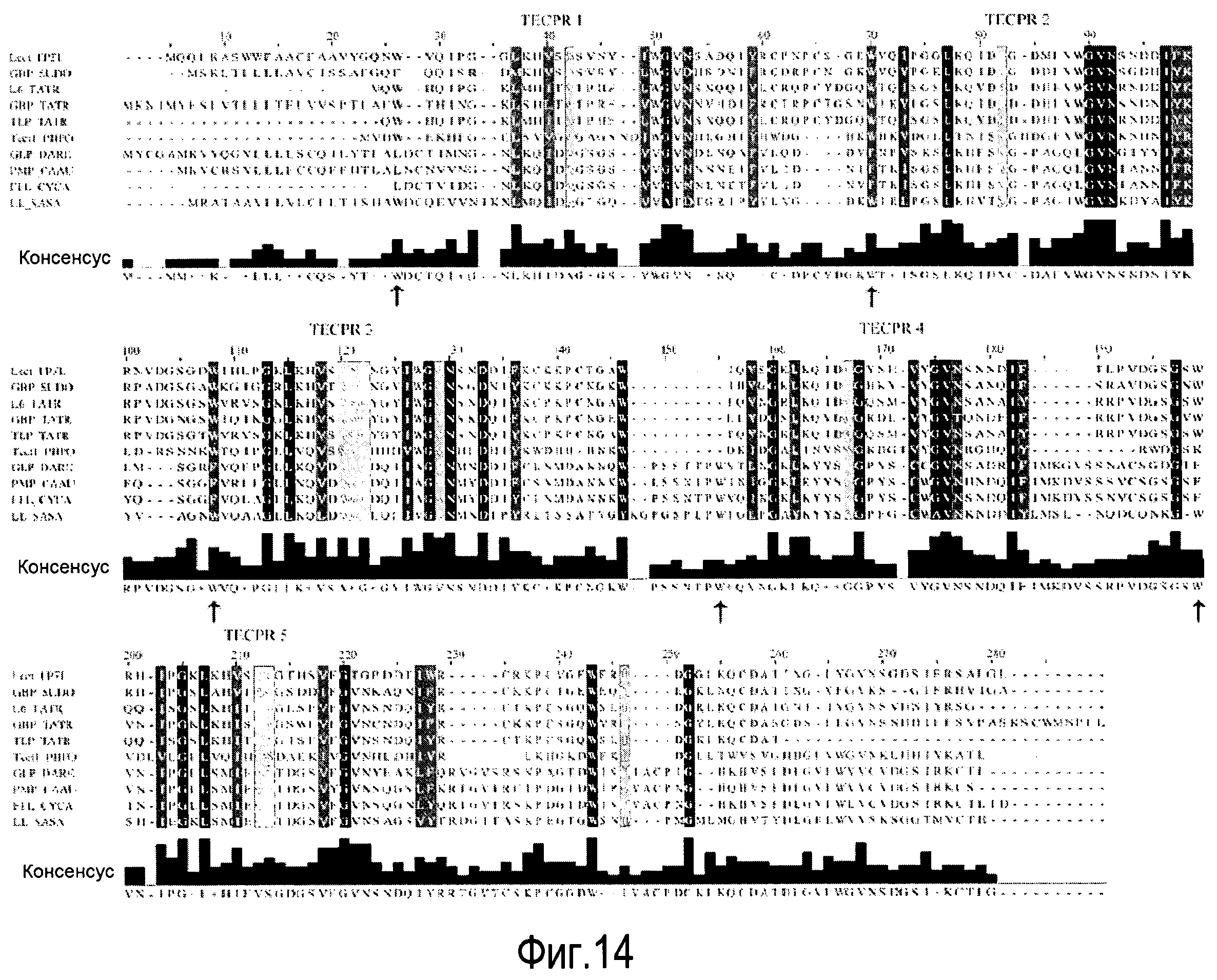
На Фигуре 14 показано выравнивание Clustal W LL с родственными β-пропеллерными белками.
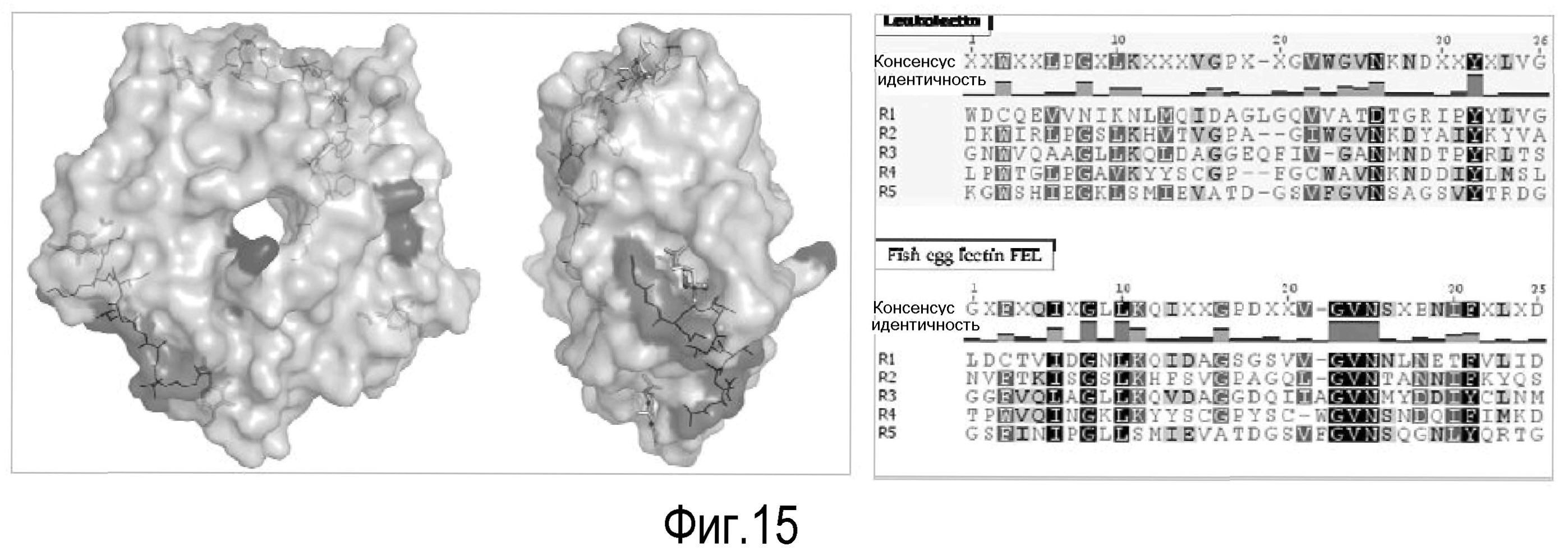
На Фигуре 15 показана 3-D модель LL. На левой панели представлено два вида 3D-представления 5 лопастного β-пропеллера 3D-модели лейколектина исходя из структуры тахилектина 1 из Tachypleus tridentatus (Biesel et al., 1999, EMBO J. 18, pp. 2313-2322). Эта модель получена с использованием программного обеспечения PyMol v 0.99. Остатки эпитопных белков изображены тонкими черными линиями в белковом теле.
Также положения 5 углевод-связывающих сайтов, предсказанные Biesel et al. (1999), показаны в виде неотчетливых, но плотных гексозных структур коричневого цвета. На правой панели представлены предсказанные пропеллерные домены в LL (верхняя) и в FEL (нижняя) по сравнению с консенсусным пропеллерным доменом.
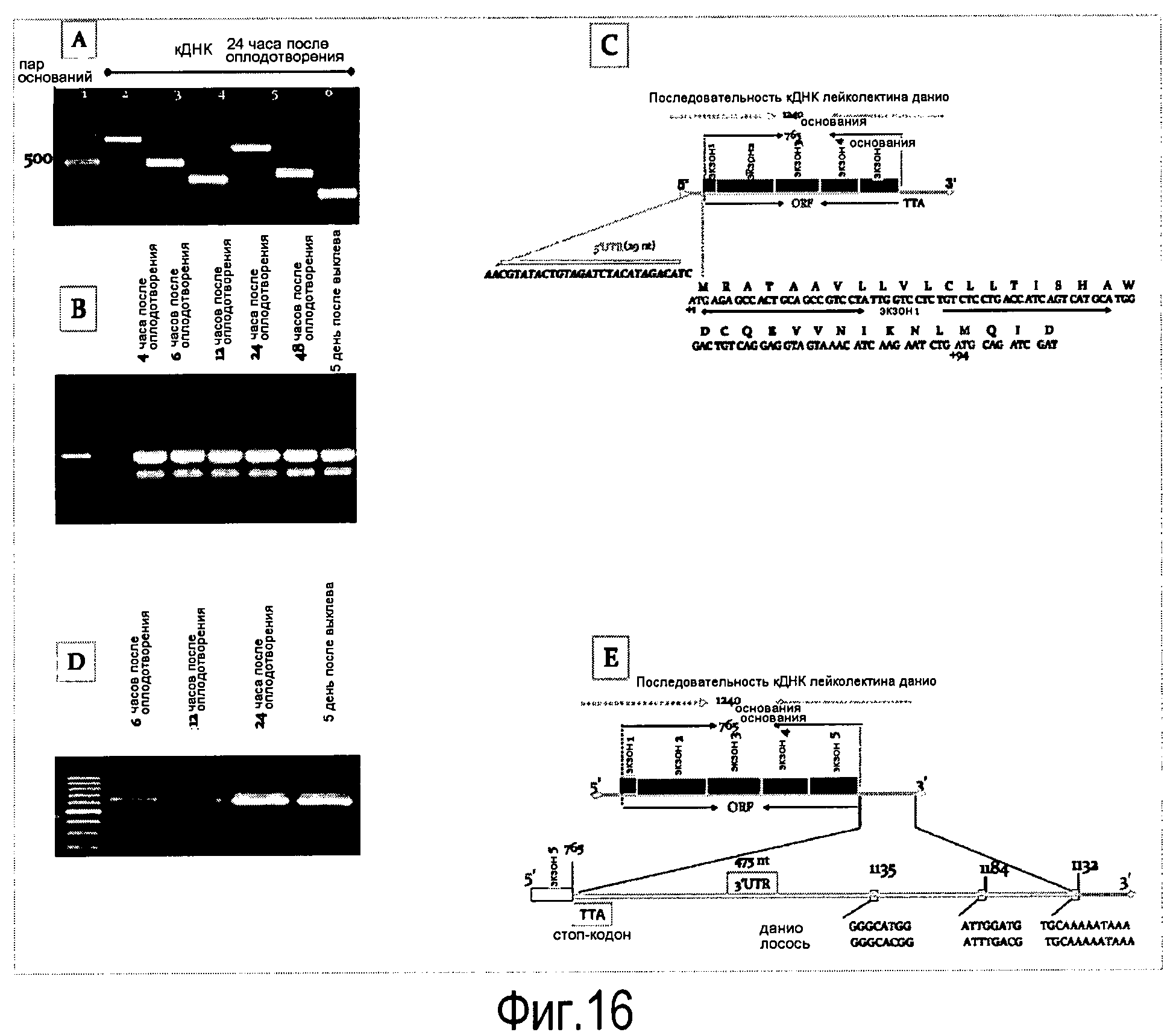
На Фигуре 16 показана амплификация полноразмерной последовательности кДНК лейколектина данио (LL). На панели A показаны ампликоны, которые были получены с использованием нескольких пар праймеров и клонированы с помощью ОТ-ПЦР. мРНК, используемую для обратной транскрипции, экстрагировали из эмбрионов на 24 ч pf. ДНК маркер: лесенка 100 пар оснований (New England Biolabs). На панели В показано, что 5'RACE ПЦР в результате приводит к амплификации двух различных продуктов, соответственно ~500 пар оснований и ~400 пар оснований (получены после второго раунда ПЦР амплификации с использованием ген-специфичного обратного праймера и прямого гнездового праймера GeneRacer). мРНК собирали на указанных стадиях развития. На панели С показано, что полноразмерная последовательность кДНК LL данио представляет собой 1240 нуклеотидов, включая открытую рамку считывания (ORF) из 765 нуклеотидов. ORF содержит пять экзонов, которые начерчены в масштабе и показаны в виде черных рамок. Область 5'UTR представлена в виде сплошной линии. Показана 5'UTR нуклеотидная последовательность. Место начала трансляции ATG в положении +1 и, возможно, второй ATG в положении +94 выделено. На панели D показана экспрессия усеченного LL на различных стадиях развития. На панели E показано, что последовательности лосося и данио являются высококонсервативными даже в 3'UTR.
На Фигуре 17 представлено краткое описание экзонов, доменов и вариабельности последовательностей лейколектинов из лосося. Данные о последовательности для различных лейколектинов показаны относительно положения вариабельных аминокислотных остатков, остатков цистеина (C) и TECPR-доменов (из базы данных SMART). Последовательности лейколектина отличаются только в семи положениях, отмеченных в рамках. Пять таких вариабельных остатков встречается в пределах TECPR-доменов, тогда как два найдено близко к С-концу. Варианты, несовместимые либо с лейколектином-1, либо с лейколектином-2, показаны ниже как лейколектин-3, где только два положения определены здесь (#2 и #245). Тогда как другие положения не отмечены, эти данные указывают на то, что большинство этих положений почти идентичны другим лейколектинам.
Как в случае лектина икринок (FEL), 3 дисульфидных мостика в LL предположительно соединяют, соответственно, первый и последний цистеины, тогда как второй и предпоследний цистеины образуют второй мостик, а два (средних) цистеина в пределах экзона 3 образуют последний дисульфидный мостик. Эти цистеина отмечены серым и подчеркнуты. Один цистеин в пропептиде, не вовлеченный в дисульфидные мостики, находится в экзоне 1. Следует отметить отсутствие соединяющих петель между первыми тремя доменами, и отсутствие вариабельности в двух петлях, которые соединяют два последних TECPR-домена. Три TECPR-домена кодируются одним экзоном (2 и 3), тогда как два домена перекрывают два экзона. Внимания заслуживает точная корреляция концов экзонов и доменов. В четырех из пяти доменов остаток Trp занимает третью аминокислоту AA домена, тогда как первый прогнозируемый домен TECPR, W является первым остатком. Наконец, звездочками отмечены остатки, в которых были найдены вариабельные аминокислоты либо в одном из лейколектана-1 или лейколектина-2 или в обоих.
На Фигуре 18 показан белок LL в жидкости, образующейся при выклеве эмбрионов радужной форели (Oncorhyncus mykiss), определенный в Вестерн блотах. Стандарты молекулярной массы (MW) показаны слева (BioRad 161-0373). Белки жидкости, образующейся при выклеве из радужной форели (дорожка 1), и белок лейколектина лосося, полученные с помощью аффинной хроматографии (дорожка 2), зондированы антителом против лейколектина. Белок ~26 кДа обнаружен в обоих случаях, соответствующий Mw лейколектина (LL).
На Фигуре 19 A, на левой панели показан лейколектин трески среди белков, найденных в жидкости, образующейся при выклеве трески. Жидкость, образующуюся при выклеве трески, анализировали с помощью 15% SDS PAGE, и составляющие ее белки визуализировали путем окрашивания серебром. Дорожка 1: белок маркер (BioRad's Dual color 161-0374). Дорожка 2: белки жидкости, образующейся при выклеве. На правой панели показана жидкость, образующаяся при выклеве трески, разделенная с помощью 15% SDS PAGE анализа, перенесенная на нитроцеллюлозную мембрану и зондированная соответствующими разведениями аффинно-очищенного поликлонального IgG антитела кролика против лейколектина. Дорожка 1: белок маркер (BioRad's Dual color 161-0374). Дорожка 2:
Аликвота жидкости, образующейся при выклеве. Локализация лейколектина была точно определена с использованием вторичного антитела козы, меченного пероксидазой хрена (HRP), против антитела кролика, усиленного ЭХЛ системой детекции. Был определен основной иммунологически реактивный белок около 26 кДа. В демонстрирует эквивалентный SDS PAGE и мембрану для белков жидкости, образующейся при выклеве из Oikopleura dioica.
Пример 1: идентификация и характеристика лейколектина
Выделение белка
В ходе анализа компонентов жидкости, образующейся при выклеве лосося, был идентифицирован новый белок, присутствующий в эмбринах.
Способ получения частично очищенной зоназы, которая может быть использована в качестве исходного вещества для выделения полипептида по изобретению, представлен в публикации WO99/29836, которая включена в настоящее описание в качестве ссылки (в частности, Пример 1 описанного способа, но, необязательно, без стадии мочевины).
Как зоназу, так и лейколектин очищали из жидкости, образующейся при выклеве лосося. Для увеличения концентрации белка в жидкости, образующейся при выклеве, икринки лосося переносили в минимальные объемы воды перед выклевом. Высокосинхронный выклев может быть индуцирован повышенными (комнатными) температурами или путем дезоксигенации (Oppen-Berntsen et al. 1990, Aquaculture, 86, pp. 417-430) с получением на выходе небольшого объема высококонцентрированного препарата неочищенной зоназы и связанных белков.
Начальная очистка зоназы включала фильтрацию икринок, из которых вышли мальки лосося, через марлю. Этот фильтрат может быть заморожен на годы без значительной деградации зоназы, до размораживания и использования для дальнейшей очистки белка. Этот факт существенно облегчает получение исходного материала для очистки зоназы лосося и связанных белков, в том числе лейколектина.
Следующая необязательная стадия включает доведение фильтрата белка до 4M мочевины, для диссоциации фрагментов яйцевой оболочки лосося, что позволяло их удалять наряду с лишним дебрисом путем низкоскоростного центрифугирования (15000g; 2×15 мин). В этом материале отсутствовали признаки забивания колонок, что является характерным для неочищенных веществ, полученных способом, отличным от описанного выше. Этот неочищенный препарат белка подходил для очистки с помощью общепринятых хроматографических методик, и зоназа может быть дополнительно очищена, как описано в Примере 7.
Лейколектин из жидкости, образующейся при выклеве, может быть выделен вместе с зоназой. Из частично очищенных препаратов зоназы (как описано выше) лейколектин может быть выделен путем эксклюзионной хроматографии в виде зоназы в ее нативной форме, по существу более крупной, чем лейколектин. Для первого разделения колонки Superdex 16/60 с условиями, описанными на подписях к Фигуре 1, является достаточным, после чего зоназа может быть удалена с помощью аффинной хроматографии на колонках Бензамидин-Сефароза.
Для получения препаратов в большом масштабе, применение ультрафильтрации также является подходящим, поскольку зоназа в своей нативной форме существенно не проникает через ультрафильтры с исключением размера 100 кДа, в отличие от лейколектина.
Используемыми буферами являются миллимолярный Tris (например, 10 мМ) при pH около нейтрального или слабощелочного (pH 7,5-8,5), содержащий 5 мМ NaCl.
Также предусматривается крупномасштабная экстракция лейкоцитов человека из продуктов, с истекшим сроком годности в банках крови, путем использования экстракции в органических растворителях (например, 80% ацетон), поскольку лейколектин остается в растворе во время этой процедуры, в которой осаждается большинство других белков. Конечная очистка методами хроматографии и фильтрации описана выше.
Также было обнаружено, что выделенный белок экспрессировался в гаметах и в зиготе, и более того также на ранней эмбриональной стадии (во время онтогенеза гемопоэтической системы) и, наконец, в лейкоцитах.
Было обнаружено, что ранее идентифицированный белок очищался вместе с зоназой. Размер этого нового белка по данным хроматографии в природных условиях составлял почти 30 кДа (Фиг. 1).
Экспрессия белка
Выделенный белок использовали для получения поликлонального антитела. Клетки анализировали на наличие белка с помощью поликлонального антитела кролика против LL, используя метод иммунопероксидазного окрашивания или непрямую иммунофлуоресценцию. Результаты показаны на Фигуре 2.
Путем использования антитела было обнаружено, что новый белок происходил из клеточного типа, отличного от клеток, которые продуцируют хориолизины (ферменты выклева). Морфология этих отдельных клеток (названных лектоцитами) показана на Фигуре и явно отличается от (отдельных) железистых клеток при выклеве, экспрессирующих хориолизины.
Анализ последовательности
Новый белок подвергали стандартной характеристике, например определению его триптических пептидов, с последующим частичным секвенированием по Edman. Из трудноразрешимых проблем пептидов, конструкции методом проб и ошибок вырожденных праймеров для обнаружения мРНК в эмбрионах рыб для получения кДНК, сначала были неудачными, пока не был установлен обратный праймер просто, чтобы совместить полиA-хвост. Этим способом и с использованием многочисленных новых наборов праймеров, по мере их идентифицирования, авторы изобретения смогли найти по меньшей мере две кДНК приблизительно 1200 нуклеотидов. Их последовательности оказались очень сходными, только с малым количеством вариантных аминокислотных остатков. Для обеих некоторые N-концевые последовательности были пропущены.
Используя методику N-RACE, авторы изобретения впоследствии установили, что указанные выше последовательности принадлежали белку из 255 аминокислот с полипептидом из 19 аминокислот и с необычным N-концевым остатком триптофана в процессированном белке. Этот последний результат объяснил бы большие трудности в получении N-концевой последовательности прямым анализом. Однако это было в конечном счете достигнуто для того, чтобы верифицировать фактические N-концевые остатки.
Используя N-концевую последовательность белка для исследования баз данных EST, авторы изобретения идентифицировали белковую последовательность белка, явно представляющую новый белок (Фиг. 3).
Исследование баз данных по белкам, подобных новому белку, идентифицировало только один несколько похожий подходящий вариант (Leren, неопубликовано). Это лектин икринок, выделенный из карпа (Galliano et al., 2003, Biochem., J., 376, p. 433-440), с суммарным сходством не более чем 48%, найденным путем выравнивая последовательностей вручную.
Биоинформационный анализ дал возможность предположить, что новый белок представлял собой лектин, родственный тектонинам (Leren, неопубликовано). При составлении списка всех белков с аналогичной структурой TECPR-домена, новый лектин, по-видимому, представляет новый тип лектина (Фигуры 4A и B). Фактическая аминокислотная последовательность нового лектина содержала пять TECPR-доменов, которые показали некоторое сходство с тахилолектинами у низших беспозвоночных (Shigenaga et al., 1993, J. Biochem (Tokyo), 114, p.307-316).
Пропептидная форма нового лектина содержит 19 аминокислотный пептид, который предполагал его нацеливание на лизосомы и для последующей возможной потенциальной секреции (т.е. в перивителлиновое пространство).
Фактическая аминокислотная последовательность нового лектина позволила разработать эпитоп-специфичные антитела, которые, в свою очередь, позволили авторам изобретения идентифицировать многие (2-8) видимые изоформы белка (Фиг. 5), в зависимости от анализируемой ткани.
Одной возможностью является то, что лектин, найденный в железистых клетках при выклеве (Фиг. 6B), секретируется в перивителлиновое пространство наряду с хориолизинами, и что они имеют просттрансляционные модификации, которые увеличивают их истинный размер и которые ниже их истинной pI.
Поскольку лосось является тетраплоидной рыбой, и как показывают данные, полученные авторами изобретения, более одного гена для лейколектина у лосося, матрица из 8 групп лейколектинов в частично очищенных препаратах зоназы может возникать из трех увеличивающихся модификаций двух несколько отличных белков лейколектина, в объеме 4×2, или 8 различных лейколектинов. Причина изменчивости нуждается в подтверждении эмпирическим путем.
По оценкам MW лейколектина составляет около 25-30 кДа. По оценкам pI для соответствующего лектина лосося равна примерно pH 6,5. Наблюдаемые pI (Riste, не опубликовано) находились от pH 6,5 до 4,9 в перивителлиновых лектинах лосося, и от pH 6,4 до 6,6 в лейкоцитарных лектинах лосося (лектин был идентифицирован методами Вестерн блоттинга).
Экспрессия во время эмбрионального развития
Используя нуклеотидные зонды для локализации экспрессии нового белка во время эмбрионального развития рыб, авторы изобретения обнаружили белок, находящийся в специфических типах эпидермальных клеток эмбрионов рыб. Кроме того, авторы изобретения обнаружили экспрессию белка в обеих гаметах, а также в зиготе. Более того, было показано, что белок отсутствует в большинстве клеток организмов, но экспрессируется в некоторых эмбриональных клетках, что дает возможность предположить, что белок мог быть связан с миелопоэзом (Фигуры 5 и 6). Такой профиль экспрессии является уникальным. Таким образом, авторы изобретения выбрали название «лейколектин» (сокращенно LL) для этого белка.
Экспрессия у различных видов
Исследование крови от рыб к цыплятам, от цыплят к людям показало, что лейколектины присутствуют в лейкоцитах по всей этой линии позвоночных. Их присутствие также могло быть выявлено в системе беспозвоночных с использованием поликлонального антитела по настоящему изобретению. Обнаружение лейколектинов в лейкоцитах (человека) сразу же подсказало возможные функции для лейколектинов. Лейколектины встречаются в клетках, выполняющих иммунные функции.
Наиболее неожиданной была чрезвычайная инвариантность последовательности лейколектинов на протяжении эволюции (Фиг. 7). Используя стандартную методику с использованием пары праймеров, авторы изобретения смогли обнаружить кДНК на протяжении всей линии позвоночных. Анализ показал крайне консервативную последовательность от рыб к цыплятам и к людям, что указывало бы на жизненно важные функции таких генов. Вариабельность между последовательностью рыб и людей составляет около 4% (10 вариабельных аминокислот) или 96% сходство, где половина из наблюдаемых вариантов представляли собой консервативные аминокислотные замены. Путем сравнения, один более или менее сходный известный белок представляет собой лектин икринки (FEL) карпа (менее 48% идентичности).
Краткий анализ варианта структуры LL (Фиг. 7) определяет новое LL-семейство белков. Видно около 2% неконсервативных изменений в аминокислотах от рыб до людей. Очевидно, что LL-гены кодируют белки, которые подвергаются чрезвычайному эволюционному отбору для сохранения инвариантности последовательностей. В свою очередь это указывает на важные, но еще неизвестные функции, которые не допускают случайные варианты в генных продуктах из возникающих и закрепляющихся во время эволюции видов.
Получение рекомбинантного лейколектина
кДНК лейколектина лосося клонировали из эмбрионов. ПЦР праймеры содержали сайт рестрикции Ncol (прямой) и ACC65 I (обратный). Вектор pETM-60 расщепляли с использованием NcoI/ACC65I и расщепленные продукты ПЦР лигировали путем лигирования в течение ночи. После амплификации и секвенирования плазмиды векторы экспрессии pETM-60, содержащие верифицированную секвенированием вставку лейколектина, трансформировали в BL21 (DE3)p Lys компетентные клетки и колонии использовали для инокуляции 5 мл LB (= Luria Broth) для получения бактериальных глицериновых маточных растворов.
Культура бактерий и очистка белка: новый бактериальный вектор pETM60-лейколектин обеспечивал экспрессию рекомбинантных белков, меченных His, слитых с C-концом NusA через последовательность распознавания TEV протеазой. Они были эффективно очищены посредством аффинной хроматографии с использованием металлов и выделяли в растворимой форме после удаления партнера слияния.
Материалы и методы
ПЦР верхний и нижний праймеры:
NWA15dPET(#23): Ncol
5-GCA.CCA.TGG.CCA.TGG.GCT.GGG.ACT.GTC.AGG.AGG.TAG.TA
CH.A15dPET(#13): ACC65I
5'-CCG.AAG.CTT.GGT.ACC.ATG.TGT.GCA.CAC.CAT.GGT.GAC
ПЦР смесь

Оба продукта ПЦР и плазмиду pETM-60 расщепляли рестриктазами Ncol и ACC65I и очищали из 1% агарозного геля для лигирования.
Лигирование вставки ДНК в вектор посредством ДНК лигазы T4
Лигазу T4 использовали для соединения 5' фосфата и 3'-гидроксильных групп двухспиральных молекул ДНК, используя следующую смесь:
200 нг векторной ДНК
500 нг ДНК вставки
10X лигазного буфера
1 мкл лигазы T4
Объем до 10 мкл
Инкубирование проводили при комнатной температуре в течение ночи, и тепловая инактивация лигазы достигалась путем помещения пробирки на водяную баню 65° на 10 минут.
Смесь для лигирования электропорировали в DH5α компетентные клетки и колонии использовали для инокуляции 5 мл LB.
Случайным образом выбирали 10 клонов для анализа. Анализ проводили путем расщепления рЕТМ6О-лейколектина под действием NcoI/ACC65I.
Последовательность лектиновой вставки верифицировали секвенированием pETM60-лейколектина с использованием праймеров #13 и #23.
In vitro трансляция лейколектина
BL21(DE3)pLysS содержит плазмиду (pLysS с резистентностью к хлорамфениколу), которая кодирует лизозим T7 для уменьшения фоновых уровней полимеразы T7 до индукции. BL21(DE3)pLysS обеспечивает более строгий контроль белковой экспрессии токсичных белков и является штаммом для высокого уровня экспрессии белка и легкой индукции.
Метка слияния, используемая в экспрессии рекомбинантного белка и в очистке, представляла собой NusA, который имеет размер 495 аминокислот (54,8 JcDa) и расположен на N-конце и используется для усиления растворения белков, которые гиперэкспрессируются.
NusA-лейколектин эффективно очищали аффинной хроматографией с использованием металлов и выделяли в растворимой форме после удаления партнера слияния.
Материалы для экспрессии и очистки NusA-лейколектина
Чашки с канамицином
Среда 2YTG
0,4 мМ IPTG (конечная концентрация 0,4 мкМ)
Колонка HisTrap HP (5 мл)
Индукцию проводили в течение 3 часов при 26°С.
Протокол очистки
Собственная ферментативная активность супернатанта NusA-лейколектин до очистки: 0,0060/мин.
Уравновешивание колонки с использованием 25 мл буфера В (IxPBS, 30 мМ имидазола, 0,4 M NaCl)
Нанесение образца
28 мл супернатанта фильтровали и дегазировали и 25 мл наносили на колонку.
Колонку промывали с использованием 75 мл буфера B. Элюцию проводили с использованием 25 мл буфера С (I×PBS, 0,5 M имидазола, 0,4 M NaCl), с одностадийной элюцией. Собирали 1 мл образцов.
Результаты
Свыше 98% протеазной активности из неочищенных рекомбинантных белков было обнаружено в проточной фракции и промывочном растворе. Только 1,6% протеазной активности было выделено в колоночных фракциях, включая фракции (F6 и F7) с рекомбинантным лейколектином, идентифицированным с помощью SDS-PAGE анализа (см. Фигуру 8). Эти фракции содержали 0,3% (фоновые уровни протеазной активности применимые относительно колонки).
Заключение
Рекомбинантный лейколектин лишен активности сериновой протеазы и, следовательно, является истинным лектином.
Следовые количества активности сериновой протеазы, найденные в некоторых препаратах лейколектина из природного источника (жидкость, образующаяся при выклеве), должны, следовательно, представлять следовые количества зоназы.
Лейколектин и зоназа существуют совместно в жидкости, образующейся при выклеве, и имеют тенденцию к совместной очистке во время большинства хроматографических методик, но могут быть разделены конечной ультрафильтрацией с использованием фильтров Biomax с исключением размера 100 кДа.
Анализ рекомбинантного белка
Рекомбинантный LL лосося, полученный как указано выше и очищенный с помощью SDS PAGE, анализировали с помощью методик MS/MS. Спектр пептидной карты массы пептидов LL анализировали в Mascot как в базах данных белков NCBI, так и EST для Actinopterygii без обнаружения каких-либо значительных совпадений (Riste, не опубликовано). Эти спектры тщательно сравнивали со спектрами LL, полученными из эмбриональных и лейкоцитарных групп LL, элюированных из 2D-гель анализа таких LLs, дополнительно подтверждая существование изоформ LL, наблюдаемых с использованием методов pH-градиента.
Геномная последовательность
У лосося была установлена геномная последовательность генов для этой структуры путем зондирования Bac-библиотки зондом 670 NT (полный протокол также подробно описан в Примере 10). Таким образом, полноразмерная последовательность кДНК для лейколектина была доступна в результате использования вырожденных праймеров, полученных на основании информации, происходящей из частичных аминокислотных последовательностей белка. ПЦР амплификации кДНК из эмбрионов 370 dd (суточных ступеней) (т.е. эмбрионы близки к выклеву, но все еще не выходят) давали ампликон 630 пар оснований, который очищали на геле и секвенировали.
Зонды, специфичные в отношении гена лектина, использовали для скрининга библиотеки ВАС (18× охват; средний размер вставки, 188 тыс. осн.), которые были предоставлены Salmon Genome Project (SGP) ассоциацией. Зонды (размер 630 пар оснований) получали путем встраивания дигоксигенин-11-dUTP (Roche), используя метод ПЦР. Скрининг библиотеки ВAC в результате привел к идентификации 7 позитивных клонов, охарактеризованных как A-12/144, L16/143, P6/76, B-5/70, О-20/85, L-7/257, F-7/176. Положительные реакции показаны на примерах на панелях А и В.
Специфические реакции выбранных клонов подтверждали с помощью ПЦР амплификации, используя те же праймеры, что и для ДНК-меченого зонда, используемого для скрининга библиотеки BAC. Размер вставки внутри векторной последовательности оценивали с помощью электрофореза в градиенте пульсирующего поля. Клоны секвенировали коммерчески (MWG-Biotech, Германия) с использованием метода дробовика.
Эта работа установила несколько близкородственных генов для лейколектинов в геноме (тетраплоидного) лосося (Фигуры 9A и B). Изменение в сегментных последовательностях казалось бы предположило существование по меньшей мере двух аналогичных генов. Структурно лейколектины представляются нормальными генами с 5 экзонами и 4 интронами, в гене около 2300 пар оснований от начала транскрипции до участка полиаденилирования, фактически стандартный размер.
Тем не менее, данные авторов настоящего изобретения позволили определить, что к настоящему времени не сообщалось о генах со сходной последовательностью в каких-либо организмах. Используя зонды для индивидуальных экзонов или интронов, авторы изобретения могли установить только редкое сходство одного экзона с частями двух других описанных белков, которые оба не имеют ничего общего с молекулярной структурой, которая была обнаружена авторами изобретения.
Исследование баз данных указывает на то, что не могут быть найдены гены, которые соответствуют белку LL, мРНК транскрипту LL или геномному гену лейколектина в хромосомах человека. По-видимому, ген лейколектина либо еще нигде не найден, либо его последовательность еще не депонирована, либо последовательность гена LL еще не обнаружена у людей. В дополнительных исследованиях авторы изобретения использовали отдельные небольшие структурные элементы, перечисленные в приведенной ниже Таблице 2, для расположения таких элементов в базах данных.
Эти результаты указывают на то, что некоторые известные белки демонстрируют некоторую степень сходства с частями лейколектина - приведены релевантные номера хромосом. Последовательности, не расположенные в хромосомах, указаны как «некоторое количество?».
Основным попаданием был трангелин человека, который представляет собой белок гладких мышц 22-альфа (SM22-альфа) (WS3-10). Трансгелин представляет собой актин-связывающий белок и является одним из наиболее ранних маркеров дифференцированных гладких мышц. Функция этого белка еще не определена.
Однако выравнивание белковых последовательностей трангелина и лейколектина показало минимальные консенсусные последовательности. В других случаях, некоторое небольшое сходство в частях структуры LL было обнаружено в отношении Т-клеточного рецептора и с неизвестным белком. Важно то, что этот новый ген специфически экспрессируется в лейкоцитах человека, несмотря на тот факт, что этот ген (еще) не может быть найден в опубликованных последовательностях генома человека. Некоторая экспрессия также видна в очищенных препаратах тромбоцитов человека. Только очень короткие сегменты этого гена могут быть обнаружены в геноме человека, но эти сегменты разбросаны в широких пределах по множеству хромосом человека (см. Фигуру 10).
Наблюдаемый профиль распределения на хромосомах является непонятным. Такие короткие последовательности могут не относиться к LL-гену, если сам LL-ген человека до настоящего времени не был секвенирован или локализован на конкретной хромосоме. Решение этой загадки пока недоступно.
Обсуждение
Новый LL-лектин был идентифицирован в лейкоцитах человека и является почти идентичным LL из рыб и цыплят. Ген LL у лосося представляет собой стандартную структуру, но еще не найден у людей.
Пример 2: медицинские применения лейколектина
Материалы и методы
Следующие исследования были проведены с использованием белка лейколектина лосося (обозначенного LL), полученного, как описано в Примере 1. Используемая концентрация LL составляла примерно 1-10 микрограмм/мл. Протеаза зоназа присутствовала в LL в соотношении 1:100 в воде и эмульсии кокосового масла (в которой присутствует свыше 30% кокосового масла). Лейколектин является стабильным в присутствии зоназы.
Результаты
A. ПОТРЕСКАВШАЯСЯ ОТ ХОЛОДА КОЖА
Многие люди испытывают сезонные потрескивания кожи, в частности, на руках.
Нанесение лейколектина на кожу во время наступления холодного времени года резко замедляет или во многих случаях предотвращает появление трещин от воздействия холода. Этот феномен был зарегистрирован в десятках случаев. Наблюдение эффектов LL на появившиеся трещины от воздействия холода меньше, но сообщалось о некотором закрытии появившихся холодовых ран.
B. ПОВРЕЖДЕНИЕ КОЖИ ОТ СОЛНЕЧНОГО ОЖОГА
Чрезмерное воздействие солнца на обнаженную кожу может вызывать солнечные ожоги и в результате ощущения жара, покраснение, зуд и возможное отшелушивание кожи, подвергавшейся воздействию.
Нанесение лейколектина приводило в результате к постепенному исчезанию красноты через минуты, к прекращению зуда и, возможно, к отсутствию появления шелушения кожи. Эти удивительные явления наблюдались повторно у многих пациентов.
С. ТЕРМИЧЕСКОЕ ПОВРЕЖДЕНИЕ КОЖИ
После прямого термического поражения кожи нанесение лейколектина лосося предотвращало характерные последствия такого поражения в значительной мере и до задержки поражения при нанесении через некоторое время после первоначального поражения, и до скорости полного восстановления.
D. АКНЕ
Субклинические случаи акне отмечались у многих подростков немедленным прекращением зуда и красноты. Улучшение состояния при акне само по себе было видно в небольшом пилотном исследовании примерно в половине случаев при нанесении LL в эмульсии кокосового масла.
E. ЛОКАЛЬНЫЙ ПСОРИАЗ
Крупные очаги пораженной псориазом кожи реагировали на нанесение лейколектина лосося ранним и почти немедленным уменьшением красноты с последующим существенным уменьшением чувства зуда. Избыток скоплений ороговевшей кожи уменьшался за первые несколько недель, но появлялся снова при уменьшении применения LL.
F. ОТКРЫТЫЕ РАНЫ КОЖИ
Наблюдения проводили у людей-добровольцев. Авторы изобретения изучали случаи хронических открытых и мокнущих ран кожи, которые являлись результатом компрессионных пяточных ран после хирургического вмешательства по поводу перелома бедра и которые безуспешно обрабатывал медицинский персонал в течение периода времени от месяцев до года. Видимые раны составляли от половины до двух см в диаметре.
При нанесении стерилизованных фильтрованием препаратов LL на хронические открытые раны на нижних конечностях (голенях) авторы изобретения наблюдали, что жидкость прекращала выделяться из ран после 2-3 дней с последующим быстрым сокращением площади раны, так что через 2-3 недели раны исчезали и заменялись нормальной кожей.
Учитывая природу пациентов с ранами, сначала появляющимися на дальнем конце конечностей, авторы изобретения заметили, что указанным выше образом сначала исчезнут раны, представляющие собой проксимальные раны. Авторы изобретения интерпретировали это как недавно появившиеся раны. Последними ранами, которые исчезнут, будут дистальные раны близкие к пятке, которые представляют собой наиболее поздно образованные раны. В конечном счете, все раны исчезли.
G. ИССЛЕДОВАНИЯ IN VITRO
Культуры дифференцированного эпителия кожи человека получали от SkinEthics (Nice, France) на 16 день после высевания на пластиковые ростовые субстраты с микропорами, позволяющими осуществлять доступ питательных веществ к эпителиальной ткани снизу. Такие культуры демонстрируют нормальную кожную морфологию после дифференцировки во время периода культивирования при 37°C. Эти культуры подращивали в течение еще двух дней in vitro так, чтобы верхний роговой слой подвергался воздействию воздуха, а базальный слой воздействию ростового субстрата. Аналогичные культуры перемещали в 30°C влажную атмосферу и предоставляли среду Ca, Mg-содержащего фосфатно-буферного солевого раствора в течение 6 часов с присутствием или отсутствием 10 мкг/мл лейколектина лосося. Культуры фиксировали в формалине и погружали в парафин в соответствии со стандартными процедурами, и окрашивали гематоксилином/эозином. Быстрая индукция крупных базальных клеток наблюдалась в эпидермисе с признаками клеточной пролиферации (Фиг. 11). Авторы изобретения интерпретируют такие результаты, как причинно связанные с эффектами заживления лейколектина на кожу, в которой сочетание пролиферации клеток и клеточной дифференцировки достаточно, чтобы закрыть рану и восстановить эпителиальную целостность кожи.
Обсуждение
Авторы изобретения не обнаружили экспрессии продуктов гена LL в клеточных культурах кератиноцитов. Также дендритные клетки являются единственными клетками в эпителии кожи, относящимися к лейкоцитам крови. Нормальный доступ лейкоцитов к эпителию кожи нарушается после некоторого механического или биологического повреждающего фактора вследствие плохого кровообращения, которое присутствует при компрессионных травмах, часто встречающихся в нормальной коже. Введение лейколектина корректирует эту недостаточность и запускает нормальные механизмы заживления в коже.
Пример 3: экспрессия белка лейколектина в лейкоцитах
Кровь лосося получали из Industrilab, Univ. of Bergen. Цельную кровь рыбы собирали в гепаринизированные пробирки (Riste, не опубликовано) и обрабатывали в соответствии с Miller et al. (1988, Nucleic Acids Research, 16(3) p. 1215). Образцы крови человека получали из банка крови в Haukeland University Hospital, Norway.
Цельную кровь человека собирали в 5 мл пробирки с цитратным буфером и обрабатывали в соответствии с Miller et al. (1988, указано выше) для получения лейкоцитов. Этот препарат дополнительно очищали путем обогащения с использованием Lymphoprep™ (Axis-Shield PoC, Norway). Lymphoprep™ использовали в соответствии с его протоколом для получения фракции лейкоцитов человека. Эту фракцию использовали для иммуноблоттинга, как описано у Miftari и Walther (не опубликовано). Анализ с использованием 2D PAGE проводили в соответствии с MacGillivray и Rickwood (1974, European Journal of Biochemistry, 41, pp. 181-190), с ~1 мкг белка. Белки LL из этих двух видов визуализировали с помощью 2D PAGE, используя иммуноблоты для специфического определения белков LL и их изоформ. Обработки с первичным поликлональным антителом к LL лосося с последующей обработкой антителом козы против антитела кролика позволили визуализировать LL-белки с помощью системы детекции, усиленной ЭХЛ. Специфичность иммунологической реакции тестировали в серии гелей, нанося от 0,5 до 5 мкг белка, с аналогичными результатами.
Лейкоциты лосося демонстрируют 2 LL-изоформы с MW ~26 кДа, c pI сходной с более основными формами 8 LL изоэлектрических форм, найденных в PVF лосося. Трудно точно оценить MW путем экстраполяции стандартов MW во втором измерении 2D PAGE. Лейкоциты человека содержат один основной LL-антиген с молекулярной массой ~30 кДа, которая по другим наблюдениям близка к 27 кДа. Кислая pI соответствует средней pI LL-изоформ лосося, найденных в PVF (Riste, указано выше) (см. Фигуру 12).
Пример 4: транскрипты лейколектина лосося, идентифицированные в Нозерн-блотах
Икринки лосося получали из разводимого на ферме маточного стада лосося в Bolaks (Fusa, Norway), сохраняемого для многократных воспроизведений потомства с 1975 путем фенотипической селекции, и в настоящее время часть лососей-производителей разводится Salmo Breed A/S, Норвегия.
Выделение суммарной РНК и полиаденилированной РНК
Суммарную РНК выделяли из эмбрионов лосося на поздних стадиях перед выходом мальков из икринок (около 370 dd), используя реактив тризол (Life Technologies) в соответствии с инструкциями производителя. Качество и количество суммарной РНК в отношении целостности и чистоты оценивали на основании формальдегидного агарозного геля, окрашенного этидия бромидом. Суммарную РНК количественно оценивали спектрофотометрически. Полиаденилированную фракцию РНК (мРНК) выделяли из 5-10 мкг суммарной РНК, используя набор для очистки мРНК Dynal beads mRNA purification kit (Invitrogen).
Конструирование зондов
Антисмысловой кРНК зонд, меченный дигоксигенином (DIG), получали путем транскрипции SP1 расщепленных матриц плазмидной ДНК с использованием РНК полимеразы T3. Смысловой DIG-меченый кРНК зонд получали путем транскрипции Xhol расщепленной матрицы плазмидной ДНК с использованием РНК полимеразы T7 (смысловой), используя набор «DIG RNA Labelling Kit» (SP6/T7) (Roche Diagnostics) в соответствии с протоколом производителя. Дигоксигенин (DIG)-меченые LL антисмысловые и смысловые кРНК зонды образовывали перекрывание ~650 пар оснований.
Анализ Нозерн-блоттинг
Аликвоты 0,5 мкг чистой мРНК и 1 мкг суммарной РНК подвергали электрофорезу и переносили на положительно заряженную нитроцеллюлозную мембрану (Amersham). Мембраны предварительно гибридизировали в буфере DIG Easy Hyb (Roche) при 55°C в течение 2 ч, а затем гибридизировали при 55°C в течение 16 ч с 1 мкг/мл LL рибозонда. Промывание проводили дважды в условиях низкой жесткости в 2×SSC с использованием 0,1% SDS при комнатной температуре в течение 15 мин каждое и дважды в условиях высокой жесткости в 0,1×SSC с использованием 0,1% SDS при 65°C в течение 20 мин каждое. Мембраны инкубировали в блокирующем растворе, содержащем малеиновый буфер (pH 7,5) и 1% блокирующий реагент (Roche), и в дальнейшем в блокирующем растворе с конъюгированным антителом против DIG-щелочной фосфатазы (AP) (Roche), разбавленном 1:10000 при комнатной температуре в течение 1 ч. После промывания 100 мМ малеиновым буфером (pH 7,5), содержащим 150 мМ NaCl и 0,5% Твина 20, мембрану уравновешивали 2 мин в детектирующем буфере (0,1 M TrisHCl, 0,1 M NaCl, pH 9,5 при комнатной температуре). Мишени гибридного зонда визуализировали с помощью хемилюминесцентного анализа, используя CSPD (Roche) в качестве субстрата, и подвергали блоты воздействию рентгеновской пленки (Kodak) в течение 5-30 мин. Использовали маркер молекулярной массы DIG-меченой РНК (Roche).
Антисмысловой рибозонд, меченный DIG и специфичный к LL, использовали для оценки размера зрелых транскриптов LL. Нозерн-блот анализ суммарной РНК (Фигура 13А) показал основной транскрипт с размером ~1250 пар оснований, а также наблюдалась более слабая полоса транскрипта (~3200 пар оснований). Доминирующая полоса соответствует транскрипту зрелого (безинтронного) и транслируемого транскрипта LL. Нозерн-блот анализ очищенной мРНК с использованием того же рибозонда обнаружил одну полосу ~1250 пар оснований (указывая на то, что амплифицированная кДНК была близка к полноразмерной кодирующей последовательности) (Фигура 13B). При инкубировании блотов из образцов суммарной РНК и мРНК со смысловым LL специфичным рибозондом наблюдалось отсутствие сигнала гибридизации, указывающее на то, что рибозонд, который использовался, был достаточно специфичным (Фигура 13C). Минорный транскрипт (~3200 пар оснований) больше полноразмерного LL-транскрипта для лосося. Задавая специфические условия для гибридизации, эта структура, возможно, не отражает структуру, содержащую информацию о последовательности LL. Положительные сигналы только от антисмысловых зондов, а не от смысловых зондов подчеркивает специфичность этих результатов. Размер полноразмерного транскрипта вмещает все LL-экзоны, описанные выше.
Пример 5: выравнивание LL с родственными β-пропеллерными белками
Биоинформационные анализы проводили в отношении последовательностей LL лосося в сравнении с информацией, размещенной в общедоступных базах данных последовательностей.
Анализ Clustal W (Фигура 14) показал, что полученная аминокислотная последовательность лейколектина лосося не имеет значительного сходства последовательностей ни с одним из описанных белков в базе данных. Однако BLAST показаывает сходства с более отдаленно родственными белками, в том числе FEL, лектином, происходящим из икринок карпа Cyprinus carpio (Gene bank Acc. Nr. P68512) с суммарным сходством только 48% (E величины 2,00 E-50). Кроме того, гипотетический белок из данио (HPZ; Acc. Nr. LOC678590) демонстрировал суммарное сходство 45% (E-величины 2,00 E-48). Сравнение последовательностей также показало, что лейколектин был на 38%, 28% и 26% идентичен TPL-1 (ранее лектин L6) из мечехвоста (Acc. Nr.P82151), тектонину I из Physarum polycephalum) (Acc. Nr. О61063) и тектонину II (О61064). По данным SwissProt, эти номера были на 49, 35, 32 и 29% идентичны, соответственно, и E-величина для FEL 1 e-51 и для L6, 1 e-40. Данные, полученные авторами изобретения, дают возможность предположить более высокое сходство LL с позвоночными, чем с беспозвоночными эквивалентами. Не включена 30% идентичность LL с тектонин β-пропеллерным, содержащим повторы, белком человека (KIAAO329_human).
Многочисленные выравнивания показали, что из четырех биохимически подтвержденных дисульфидных связей в FEL (Galliano et al., 2003, Biochem. J. 376, pp. 433-440) три, по-видимому, являются консервативными в лейколектине. Первый мостик соединяет N-конец с С-концом обоих белков. Этот мостик соединяет цистеины в положениях 3 и 234 в LL (или 238 в FEL). Второй и третий мостики соединяют Cys 102 с Cys 155 в LL (#157 в FEL) и Cys 132 и Cys 137 как в LL, так и FEL. Четвертая дисульфидная связь, обнаруженная в FEL карпа, содержащая Cys 208 (212) и Cys 226 (230), не обнаружена в лейколектине.
Пример 6: 3D-модель LL (лейколектин)
Белок лейколектина имеет высокую степень сходства в отношении архитектуры TECPR домена с L6 или тахилектином 1 (Tachypleus tridentaus), лектином, связывающим бактериальный липополисахарид, из гемоцитов мечехвоста и другими белками беспозвоночных, родственных тахилектину. Тем не менее, наблюдались отличия в отношении числа доменов, наряду с небольшим сдвигом β-пропеллерных доменов в направлении C-конца белка. Суммируя информацию из аналогичных исследований и SMART исследований, авторы изобретения сделали вывод о том, что суммарная 3-D структура лейколектина демонстрирует 5-лопастную β-пропеллерную белковую структуру. На основании этого авторы изобретения задействовали 3D модель (Biesel et al., 1999, EMBO J., 18, pp. 2313-2322) для получения рабочей модели, как может выглядеть белок лейколектина. Это только приближение, поскольку номера остатков одного белка полагаются равными остаткам в другом. Исследования в базе данных SMART указывают на главную структурную особенность в действительности транслированного белка лейколектина, который состоит из пяти тандемных повторов, каждый из которых содержит 35-36 аминокислот с 32-61% идентичностями внутренней последовательности (Фигура 15, правая панель). Удлинения внутренних повторов полученного белка лейколектина показали сходство среди них самих, составляя, главным образом, 13 аминокислот в длину. Две короткие консенсусные последовательности, XWXXLPGXLKXXXVGPX и GVNKNDXXYXLVG, являются высококонсервативными в каждом повторе. Помимо удлинения из 20 остатков в N-концевой области лейколектина, которая не найдена в FEL, оба белка показывают высокую степень сходства между количеством и суммарной доменной архитектуры TECPR доменов, имея только 48% идентичность последовательностей.
Пример 7: очистка зоназы из жидкости, образующейся при выклеве лосося
Жидкость, образующуюся при выклеве лосося, в примере 1, может быть дополнительно очищена для получения на выходе препарата чистой зоназы. Одного цикла гель-фильтрации было достаточно, чтобы отделить зоназу от более крупных молекулярных компонентов в фильтрате с 12-кратной очисткой с более чем 50% выходом. Используемая матрица может изменяться, но Sephacryl SR-200® представлял собой обычный выбор авторов изобретения. Буфер представлял собой Tris-HCl pH 8,0 или pH 8,5 (0,05 M) или Tris-ацетат (0,025 M, те же pH). Зоназу, полученную после процедур гель-фильтрации, оценивали в отношении преобладающих групп зоназы в жидкости, образующейся при выклеве.
Зоназу очищали до получения гомогенного белкового продукта аффинной хроматографией на коммерчески доступных колонках Benzamidine Sepharose 6B®. Используемые специфические условия (с колонками объемов 25 или 125 мл) снова представляли собой 0,05 M Tris-HCl буфер (pH 8 или 8,5), для удаления неспецифически связанного вещества на колонках, доводили до 1 M NaCl. Зоназа не удалялась на этой стадии, поскольку этот белок оставался прочно связанным с колонкой. Элюция зоназы с колонки достигалась путем использования 10-33% градиента диоксана в 1 M NaCl в том же Tris-HCl буфере. После аффинной очистки препарат зоназы демонстрировал одну полосу белка в SDS-PAGE анализе, с молекулярной массой около 28 кДа. В то же время, этот зоназный продукт не был чистым с высокой достоверностью, он был высокоочищенным.
Зоназу, очищенную гель-фильтрацией плюс очищенную аффинно, дополнительно очищали до высокой достоверности с помощью одной конечной хроматографической процедуры. В этой процедуре использовали колонку PBE94® с Tris-ацетатным буфером (10 мМ, pH 9,0), где последующую элюцию проводили с использованием градиента соли (вплоть до 1 M соли NaCl) в этом буфере. Сама эта стадия повышала каталитическую активность зоназы дополнительно в 7,6 раз, для суммарной очистки 714 раз, и с выходом 28% из исходного вещества. Эта стадия очистки оставляет белковую идентичность зоназы интактной в виде фрагмента 28 кДа.
Пример 8: получение и очистка антител к LL
Поликлональную кроличью антисыворотку против LL кролика против LL лосося получали следующим образом: белок лейколектина, очищенный с высокой достоверностью, из Примера 1, использовали для индукции поликлонального антитела у кроликов Chinchilla массой 4 кг, как описано Harlow и Lane (1988, Laboratory Manual, Cold Spring Harbor, NY). Три инъекции 80, 40 и 25 мг лейколектина высокой достоверности вводили в многочисленные участки под кожей. Первая была эмульгирована полным адъювантом Фрейнда, последние две неполным адъювантом через 3 и 6 недель. Через восемь дней после последней иммунизации брали кровь и получали сыворотку после центрифугирования при 3000 об/мин (ротор Sorvall SS-34) в течение 15 мин.
Аликвоты антисыворотки хранили при -80°C. Первичные антитела были аффино очищены с использованием колонок HiTrap 1 мл с белком G (Amersham Pharmacia Biotech) со скоростью потока 1 мл/мин. Цельную антисыворотку фильтровали через 45 мкм фильтрующий элемент перед нанесением на колонки один мл с белком G. Уравновешивание колонки проводили с использованием 5-10 объемов колонки связывающего буфера (20 мМ Na фосфат, pH 7,0) с последующими несколькими промываниями тем же буфером, пока белок не будет определяться УФ-поглощением при 280 нм. Фракцию IgG элюировали с использованием 5 мл буфера для элюции (0,1 M глицин HCl, pH 2,7) и делили на 10 пробирок, содержащих 25 мкл нейтрализирующего буфера (1 M TrisHCl, pH 9,0). Концентрацию определяли спектрофотометрически. Чистоту оценивали путем анализа аликвот очищенных фракций IgG в 12% SDS-PAGE с последующим окрашиванием серебром. Чувствительность определяли с помощью Вестерн-блот анализа, используя IgG козы против антитела кролика, вторичное антитело, конъюгированное с пероксидазой хрена.
Кроме того, поликлональные антитела предварительно адсорбировали путем инкубирования в ацетоновом порошке данио. Меченные изотиоцианатом флуоресцеина (FITC) антитела свиньи против F(ab')2 кролика получали из Dako (F-0054). Антитело козы против IgG кролика, меченное флуоресцентным агентом Alexa Fluor 647, получали из Molecular Probe, Eugene, US (Invitrogen, номер по каталогу A-21244) и биотинилированные поликлональные иммуноглобулины свиньи против иммуноглобулинов кролика были из Dako (номер по каталогу E0353). Оптимальные концентрации первичных и вторичных антител определяли перед экспериментами с разбавлением. Поликлональные антитела использовали в анализе экспрессии белка, описанном в Примере 1.
Пример 9: идентификация и характеристика LL из данио
Суммарную РНК выделяли из эмбриона данио в 4, 6, 12, 24, 48 часов после оплодотворения и 5 дней после оплодотворения, используя процедуру Trizol (Life Technologies) в соответствии с инструкциями производителя. Целостность и чистоту суммарной РНК оценивали на формальдегид-агарозном геле, окрашенном этидия бромидом. Использовали только образцы с соотношением 28S к 18S рРНК 2-2,4:1 и без определяемых примесей ДНК. РНК количественно анализировали спектрофотометрически. Полиаденилированные мРНК выделяли из 5-10 мкг РНК, используя наборы Dynal (Invitrogen).
Обратную транскрипцию проводили, используя 200 Ед/мкл TermoScript (Invitrogen). мРНК (0,5 мкг) нагревали до 72°C в течение 5 мин, охлаждали, осаждали центрифугированием и добавляли к 20 мкл реакционной смеси, содержащей 100 нг/мкл олиго dT, 10 мкМ DDT и 0,8 Ед/мкл ингибитора РНКазы в 2,0 мМ буфере для синтеза кДНК (Invitrogen). Инкубирование проводили при 50°C в течение 1 ч. Продукты очищали путем экстракции фенол/хлороформ/изоамиловым спиртом, пропускали через колонку MicroSpin S-200HR и осаждали этанолом. Ген-специфичные LL праймеры получали из последовательностей LL лосося (Таблица 3). ПЦР смесь (20 мкл) содержала 2 мкл матрицы кДНК, 0,4 мкМ праймеров (LLF1, LLF2, LLR1, LLR2, и LLR3), 1x ПЦР буфера, 0,5 Ед ДНК полимеразы Taq (Takara) и 0,2 мМ dNTP. В ПЦР амплификации использовали 32 цикла 94°C по 45 с /58°C по 45 с /72°C по 90 с и конечное удлинение при 72°C по 7 мин. Реакционную смесь анализировали с использованием 1,8% геля агароза-TBE с 0,5 мкг/мл этидия бромидом в 1× TBE буфере (pH 8,3) с лестничным маркером ДНК 100 пар оснований (New England Biolabs).
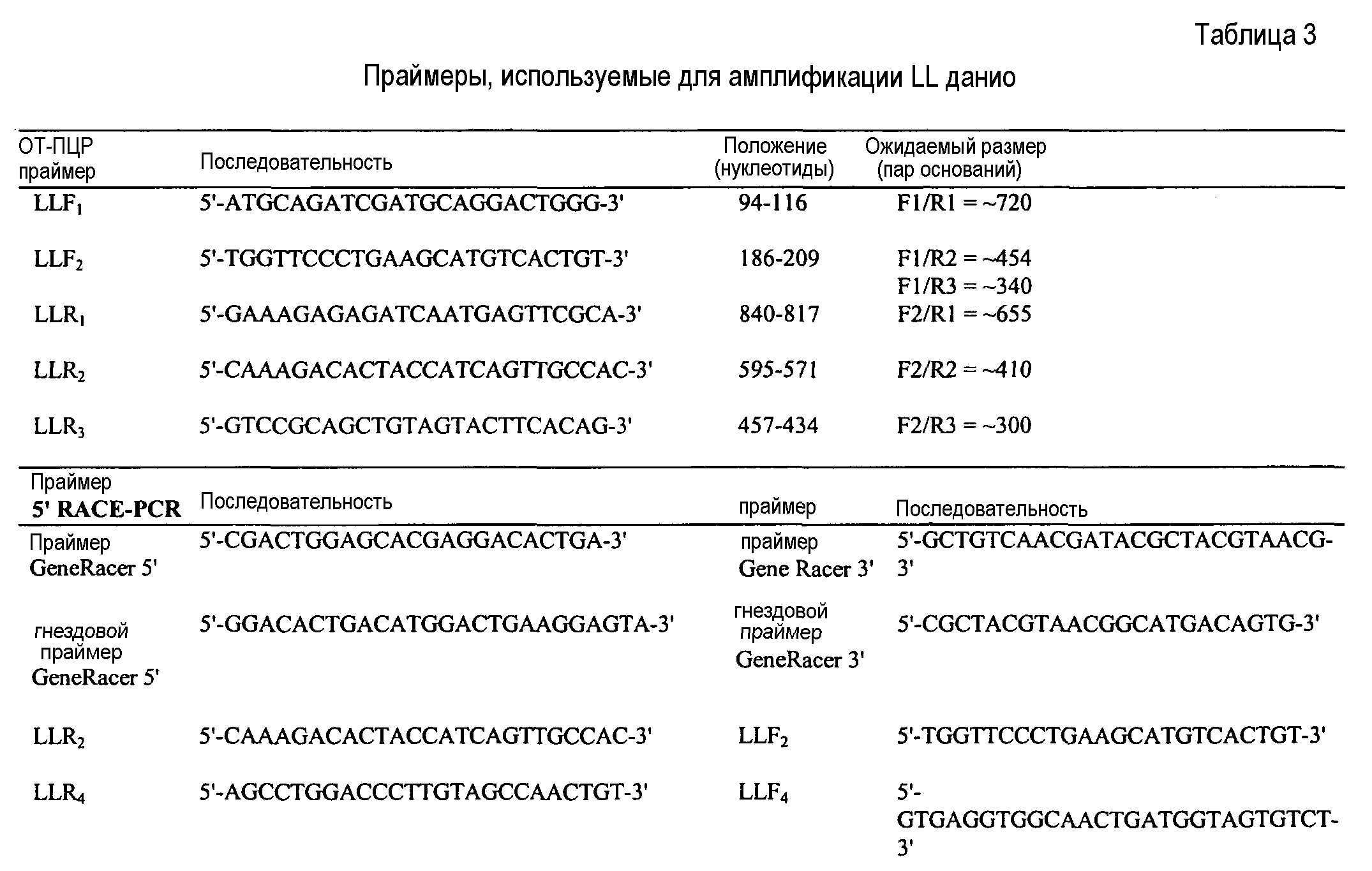
ПЦР фрагмент лигировали в векторную систему pGEM T-Easy Vector system 1 (Promega, Madison, WI) с использованием стандартных протоколов.
При электропорации использовали 40 мкл E. coli DH5α и 1 мкл лигированного фрагмента ПЦР в pGEM T-Easy Vector. Среду SOC (1 мл) добавляли перед инкубированием бактерий при 37°C в течение 1 ч. Рекомбинантные бактерии (200 мкл) высевали на стандартные LB/ампициллин, X-gal, IPTG агаровые чашки и инкубировали при 37°C в течение ночи для синего/белого скрининга. Десять белых клонов собирали и выращивали в 5 мл ночной культуры в среде LB с 100 мкг/мл ампициллина. Для очистки плазмиды использовали набор Plasmid Minipurification kit,(Qiagen, Chatsworth, CA). Плазмиды амплифицировали и секвенировали, используя стандартные протоколы (DNA Sequence Lab, Bergen).
5'- и 3'-RACE ПЦР LL проводили, используя набор GeneRacer core kit (Invitrogen cat. #45-0168) в соответствии с инструкциями. 2 мкг суммарной РНК использовали для синтеза первой цепи кДНК в ОТ, используя Superscript III (Invitrogen). Первый раунд 5'- и 3'-RACE ПЦР ампфликации проводили, используя 5'- или 3'-GeneRacer праймер и обратный или прямой ген-специфичный праймер LLR2 & LLF3 (Таблица 3). В гнездовой 5'- или 3'-RACE ПЦР амплификации использовали гнездовой праймер 5'- или 3'-RACE ПЦР GeneRacer и гнездовой обратный или прямой ген-специфичный праймер LLR4 и LLF4. Для 5'- и 3'-RACE ПЦР первая стадия пять циклов, 94°C в течение 30 сек и 72°C в течение 1 мин; следующие пять циклов при 94°C в течение 30 сек и 70°C в течение 1 мин; третья стадия 30 циклов с 94°C в течение 30 сек, и 68°C в течение 45 сек, и 72°C в течение 1 мин; конечная стадия удлинения 72°C в течение 7 мин. Гнездовая 5- или 3'-RACE ПЦР в три стадии: первая стадия 5 циклов при 94°C в течение 30 сек, 72°C в течение 2 мин; следующая стадия 5 циклов 94°C, 30 сек, 70°C 2 мин; 3 стадия 25 циклов 94°C в течение 30 сек, 65°C в течение 30 сек и 68°C в течение 1 мин; конечная стадия удлинения 72°C в течение 10 мин. Матрицы для гнездовой ПЦР использовали продукт ПЦР с первого раунда RACE ПЦР, разбавленный 1:25 в дистиллированной воде.
Праймеры для RACE ПЦР приведены в Таблице 3. Отдельные продукты ПЦР очищали с использованием набора для очистки «PCR purification kit» (Promega, Madison, WI, US) и лигировали в вектор PCR II Topo (Invitrogen) для трансформации JM109 высокоэффективной компетентной E. coli (Invitrogen). Рекомбинантные бактерии идентифицировали с помощью синего/белого скрининга на агаровых чашках Lucia Bertani. Плазмиды, содержащие вставки, очищали с использованием набора для очистки Promega и секвенировали с использованием праймеров M13. Последовательность мРНК LL анализировали, используя программы поиска Blastx и Blastp.
Путем объединения трех наборов праймеров (см. Таблицу 3) амплификация дала ампликоны с размерами (Фигура 16А), ожидаемыми исходя из LL лосося. Водная холостая проба без мРНК данио была отрицательной. Наиболее крупный продукт (720 пар оснований) был секвенирован, при условии, что LL присутствует у данио. Амплификацию продуктов ПЦР GWH различного размера (Фигура 16A) примировали специфическими олигонуклеотидами, фланкирующими экзоны лосося в различных положениях, дополнительно подтвержденными высокой гомологией между LL данио и лосося. В качестве положительного контроля для реакций амплификации использовали β-актин.
5'-RACE ПЦР прояснила последовательность 5'-нетранслируемой (5'-UTR) области LL данио. Авторы изобретения использовали мРНК (Фигура 16B) от 4 часов после оплодотворения (hpf) до 5 дней после выклева (dph). Первый раунд RACE ПЦР амплификации давал на выходе очень слабые продукты. Такие амплифицированные продукты со всех стадий использовали для второго раунда RACE ПЦР, используя высокую температуру отжига (65°C) для повышения специфичности реакции, используя разведения 1:20 первой реакции RACE ПЦР. Было получено два одинаковых продукта (520 и 420 пар оснований) на всех стадиях (Фигура 16B), даже на стадии 4 hpf. На этих стадиях развития была получена информация о LL-последовательности более чем 20 клонов. Все клоны содержали 29 нуклеотидов выше области (Фигура 16C), обнаруженной в LL лосося. 3'-конец также был секвенирован посредством многочисленных анализов и была выявлена структура, очень сходная (почти идентичная) структуре, обнаруженной в лейколектине лосося. Исходя из полной длины последовательности кДНК, обнаруженный LL-белок данио был депонирован в NCBI Gene Bank (Acc.nr. FJ 643620). Кодирующая последовательность состоит из 1213 нуклеотидов с открытой рамкой считывания из 765 нуклеотидов. Обнаруженная аминокислотная последовательность для LL данио предполагает белок из 255 аминокислот, заданный старт-кодон трансляции в положении нуклеотидов +1 (или нуклеотидов 30-32) (Фигура 16C). LL кДНК также имеет потенциальный старт-кодон на нуклеотиде +94 (Фигура 16C). В 4 из 20 клонов LL данио транскрипт содержал 29 нуклеотидов выше сайта +1, но не имел следующих 93 нуклеотидов (нуклеотидную последовательность правильно считывать вплоть до -1, за которым следует нуклеотид в положении +94: Фиг. 16C). Таким образом, эти данные дают возможность предположить, что могут быть транслированы два различных белка LL (Фигура 16C).
Сильная гомология между LL белками данио и лосося была очевидной. LL данио представляет собой гибридную структуру по сравнению с двумя LL лосося. Из семи установленных критериев классификации LL по 4 критериям LL данио находится в категории LL-1, тогда как по 2 критериям этот лейколектин находится в категории LL-2 (Фигура 16E). Седьмой критерий является уникальным для LL данио (Фигура 16E, область в рамке). Более того, один Cys отсутствует в экзоне 3 и заменен на Arg в последовательности «nmnTPYClts», который в данио считывается «nmnDTPRlts». Следовательно, данио LL имеет 5 цистеинов, где лосось имеет 6 цистеинов, все прогнозировали в дисульфидных мостиках.
В отношении различных экзонов, экзон 1 является идентичным, тогда как экзон 2 данио имеет три уникальные аминокислоты, не найденные у лосося (Gly-Arg вместо Ser-Gln в положениях № 57 и 58 и Val вместо Ile в положении № 78). Экзон 3 имеет 4 измененных остатка (или 21). В экзонах 4 и 5 отсутствуют различия кроме 3 классификационных сайтов. Таким образом, существует 5 (или 7) уникальных аминокислот в LL данио (всего 255 аминокислот), не считая классификационные сайты. LL данио является высококонсервативным по сравнению с LL лосося, отличаясь только на несколько процентных пунктов.
LL данио (Фигура 16D, E) имеет большое сходство с LL лосося. LL данио не имеет одного из шести Cys, видимых в LL лосося, и, следовательно, могут содержать только два дисульфидных мостика: один, соединяющий N- и C-концы, плюс внутренний мостик в экзоне 4. Сравнивая LL лосося и крупного LL данио (Фигура 16E), стереотипичные структурные варианты, видимые у лосося, усилены структурой LL данио. Наблюдается одно радикальное отличие (остаток № 131), но главным образом видны консервативные замены, где встречаются варианты в LL лосося. В PVF LL могут обладать иммунопротективными функциями. Рестриктированные варианты в структуре LL могут относиться к таким функциям. Усеченный лейколектин (tLL) лишен секреторного пептида, давая возможность предположить, что tLL (Фигура 16D) не секретируется, и tLL может представлять собой 4-лопастной β-пропеллерный белок. Различные LL-белки в теории могут выполнять различные клеточные функции. Функция tLL может осуществляться в клетках, отличных от лектоцитов.
Пример 10: выделение и характеристика гена LL лосося
Скрининг библиотеки ВАС
Для получения геномной структуры гена лейколектина авторы изобретения провели скрининг общедоступной геномной ВАС библиотеки лосося (18× покрытие, средний размер вставки около 188 тыс. оснований), предоставленной Salmon Genome Project (Осло, Норвегия). Библиотека бактериальной искусственной хромосомны (BAC) с высокой избыточностью, сконструированная из норвежской сельскохозяйственной породы самцов атлантического лосося (Salmo Salar), была подвергнута скринингу на LL позитивные клоны. Эта библиотека состоит из общего количества 305557 клонов. Средний размер вставки этой библиотеки составляет 188 тыс. пар оснований, представляя 18-кратный охват генома. Фильтры высокой плотности CHORI-214 Seg. 1 (набор фильтров-007193), каждый состоящий из 18432 клонов, определенных в двух повторах, были получены для гибридизационного скрининга.
Для скрининга библиотеки LL-специфичный кДНК зонд из 620 пар оснований был получен путем встраивания дигоксигенин-11-dUTP (Roche) методом ПЦР, используя прямые праймеры LL/F 5'-TACGGACACAGGTCGAATCCCCTACTACC-3' и обратный праймер LL/R 5'-ACAGAGAAGAGGCTAATGTGTGCAC-3'. DIG-меченый зонд кДНК инкубировали при 95°C в течение 10 мин и сразу же помещали на лед на 5 мин перед добавлением гибридизационного буфера (5×SSC, 50% формамид, 0,02% SDS, 2% блокирующий реагент (Roche), DEPC-обработанная вода).
Гибридизацию проводили в гибридизационных пробирках при 55°C в течение ночи. Стадию постгибридизационного промывания проводили дважды в условиях низкой жесткости в 2×SSC с 0,1% SDS при комнатной температуре в течение 15 мин каждую и дважды в условиях высокой жесткости в 0,1×SSC с 0,1% SDS при 65°C в течение 20 мин каждую. Фильтры инкубировали в блокирующем растворе, содержащем малеиновый буфер (pH 7,5) и 1% блокирующего реагента (Roche), и после этого в блокирующем растворе с конъюгированным антителом против Dig-щелочной фосфатазы (AP) (Roche) разбавленным 1:10000 в течение 1 ч при комнатной температуре. После промывания с использованием 0,1 M малеинового буфера (pH 7,5), содержащего 150 мМ NaCl и 0,5% Твина 20, мембрану уравновешивали в течение 2 мин в детектирующем буфере (0,1 M TrisHCl, 0,1M NaCl, pH 9,5 при комнатной температуре). Позитивные точки в двух повторах визуализировали с помощью хемилюминесцентного анализа, используя CSPD (Roche) в качестве субстрата. Идентификация положительных сигналов достигалась путем экспозиции фильтров на рентгеновской пленке (Kodak). Время экспозиции варьировалось от 3 до 15 мин. Два выбранных позитивных клона L-7/257 и A-12/144 высевали на агаровые чашки и инкубировали при 37°C в течение ночи. Три клона собирали, выращивали в течение ночи в 5 мл культуру при встряхивании при 37°C с 20 мкг/мл хлорамфеникола. Очистку плазмидной ДНК проводили на следующий день, используя набор для ультрачистой очистки ДНК (Qiagen). ДНК ВАС расщепляли с использованием Not I и анализировали с помощью электрофореза в пульсирующем поле (PFGE)(Osoegawa et al., 1998, Genomics, 52, pp. 1-8). Маркер Low Range PFG Marker (New England Biolabs) и фрагмент л-Hind III (Takara) использовали в качестве маркеров размера ДНК.
ПЦР верификация позитивных клонов
ПЦР реакции проводили с использованием очищенной ДНК ВАС в качестве матрицы и ген-специфичных праймеров. Реакционные смеси для ПЦР инкубировали при 95°C в течение 3 мин с последующими 35 циклами при 95°C в течение 30 с, проводя отжиг при 54°C в течение 30 с и удлинение при 72°C в течение 30 сек с конечным инкубированием при 72°C в течение 10 мин. После термоциклинга 2 мкл каждой реакционной смеси ПЦР анализировали на 1,5% агарозном геле.
Секвенирование лейколектина ВАС клонов методом «выстрела из дробовика»
Два клона секвенировали с помощью MRW, Берлин, Германия. Векторные вставки секвенировали для оценки избыточности в 2,4 раза. Риды очищали от вектора и элементов хозяина. Примерно из 180 ридов всего соответственно 33 и 22 контигов было установлено из двух клонов ВАС с использованием биоинформатики. Контиги исследовали как мРНК последовательностями, так и аминокислотными последовательностями. Анализ идентифицировал экзоны и интроны как с помощью программ поиска, так и путем проверки вручную. Полный ген LL был идентифицирован из перекрывающихся контигов.
Геномная структура
Результаты указанного выше скрининга идентифицировали 7 специфичных клонов, названных A-12/144, L-16/143, P-6/76, B-5/70, O-20/85, L-7/257 и F-7/176 в соответствии с номенклатурой ВАС библиотеки. Средний размер вставки геномных клонов ВАС оценивали по ДНК, очищенной из всех выбранных клонов ВАС, которую впоследствии расщепляли с использованием рестриктазы Not I. Продукты расщепления ДНК, содержащие вектор, разделяли с помощью гель-электрофореза в пульсирующем поле и визуализировали путем окрашивания этидия бромидом. Все клоны ВАС давали только две полосы, демонстрируя, что размер вектора (pTARBAC2.1) составил ~13 тыс. пар оснований (13397 пар оснований; Osoegawa et al., 1998, supra). Это дает возможность предположить, что размер вставки всех клонов составил ~25 тыс. пар оснований. Последовательности шести из 7 выбранных клонов ВАС верифицировали еще раз путем амплификации, используя в качестве матрицы ДНК, очищенную из клона ВАС, вместе с LL ген-специфичными праймерами. ПЦР амплификация давала продукт ~600 пар оснований из всех этих клонов. Их идентичность дополнительно была подтверждена прямым секвенированием.
Секвенирование методом «выстрела из дробовика» двух клонов ВАС
Программы сборки последовательностей BioEdit и Dna Baser использовали данные о всех последовательностях. Анализ показал, что как выделенные клоны ВАС 25 тыс. пар оснований содержали полную последовательность мРНК (после элиминации элементов векторной последовательности) при скрининге в отношении как последовательностей мРНК, так и белковых последовательностей. Данные по одному из клонов ВАС давали на выходе всего 80 ридов, которые собирали в 33 контига. Из них по меньшей мере 6 контигов содержали LL-последовательности, которые давали возможность реконструировать ген LL целиком. Помимо последовательностей LL, другие компоненты были часто идентифицированы в этих контигах с высокой степенью достоверности и включали обратную транскриптазу, ионную пептидазу и мобильный генетический элемент.
Особенности структуры геномного гена LL
В первом анализе только один из клонов (L7/247) позволил идентифицировать полный LL-ген, тогда как другой клон (A 12/144) показал большую часть геномной структуры (см. Фигуру 16). Данные по геномному клону L7/247 дали возможность предположить геномную организацию лейколектина, где этот ген состоит из 5 экзонов, прерывающихся 4 интронами, и перекрывает ~2,3 тыс. пар оснований, начиная с TATA-box. Геномные последовательности LL обнаружили TATA box, начиная с положения ~81 (TATAAAA) от ATG стартового кодона, указывания на 81 нуклеотидный 5'UTR (нетранслируемый элемент) мРНК. Стоп-кодон TAG расположен приблизительно 1850 нуклеотидом от ATG в геномной последовательности. Сигнал полиаденилирования длиной 6 нуклеотидов AATAAA начинается около положения 2250 от ATG. 3'UTR представляет последовательность длиной около 400 нуклеотидов, начинающуюся после стоп-кодона TAG. С 5'UTR, состоящей из 81 нуклеотида, размер гена LL оценивается по меньшей мере ~2,3 тыс. пар оснований путем обычных определений, с интронами, составляющими вдвое больше последовательности как экзоны. Для верификации границ сплайсинга гена лейколектина ПЦР праймеры получали из установленных геномных последовательностей интронов и использовали для амплификации каждого экзона из эмбриональной ДНК лосося. Эти 5 последовательностей экзонов получали прямым анализом последовательностей ампликонов, и все соответствовали установленным геномным последовательностям.
Размеры кодирующих экзонов оказались довольно однозначными и варьировали от 55 пар оснований (Экзон 1) до 234 пар оснований (Экзон 2). В частности, два интрона были относительно небольшими, так что точная длина могла быть получена в результате считывания данных вручную. Напротив, интрон 3 составляет около 250 нуклеотидов, тогда как интрон 4 перекрывает около 700 пар оснований. Точная длина интрона 4 не могла быть определена из доступных данных. Совокупность данных о последовательности экзона подтверждает прогнозированный продукт трансляции, а именно белок 255 аминокислот.
Более того, эти данные подтверждают геномную структуру гена LL с 5 экзонами и 4 интронами для одного из двух описанных вариантов лейколектина. Было установлено, что N-концевой аминокислотный остаток секретируемого белка LL представляет собой триптофан с помощью прямого расщепления по Edman очищенного LL. Этот Trp- остаток занимает положение 20 от N-концевого метионина в белке-предшественнике из 255 аминокислот, и ему предшествует аминокислоты 18 (His) и 19 (Ala). Сайт расщепления предполагается между Ala и Trp для процессирующей протеазы, для получения секретируемого белка LL. С помощью прямого расщепления по Edman установлена следующая последовательность этого секретируемого LL WDCQE VVNIK NLMQI DAGLG Q-V и также верифицирована с помощью многочисленных фактических белковых последовательностей. Экзоны не все находятся в рамке, но потенциально допускают пропуск некоторых экзонов без прерывания всех рамок считывания. Анализ геномной последовательности указывал последовательности границ экзон/интрон. Исключением является интрон 4, где возможно нестандартные нуклеотиды фланкируют последовательности интронов. В интронах 1, 2 и 3 авторы изобретения обнаружили общий GT//AG элемент, фланкирующий начало и конец многих интронов позвоночных (Shapiro and Senepathy, 1987, Nucleic Acids Research, 15, pp. 7155-7174).
Экзон 1 (19 аминокислот) в длину составляет 55 нуклеотидов с последовательностью MRATA-AVLLV-LCLLT-ISH(A) и заканчивается на первом G кодон для остатка Ala #19, предшествующим N-концевому триптофану секретируемого лейколектина. Большая R, выделенная жирным курсивом, означает вариант аминокислоты, в этом положении возможно связан с геном лейколектина-3 (см. Фигуру 17). Геномная последовательность гена продолжается с нуклеотидов GT до стартового интрона 1. Интрон 1 заканчивается нуклеотидами AG, за которыми следует экзон II, который содержит последние два основания (-CA) кодона #19 Ala, за которым следует кодон TGG для # 20 Тrp, N-конца лейколектина. Длина интрона 1 составляет 89 нуклеотидов.
Экзон 2 (234 нуклеотида) содержит 77 аминокислот (234 - 2 нуклеотида/3=77 аминокислот+1 нуклеотид). Здесь, геномная последовательность транслирует (ala) - WDCQEVVNIK - NLMQI DAGLG - QVVAT DTSQI - PYYLV G* DKWI - RL* PGS LKHIT - VGPAG IWGVN -KDYAI YKYVA - GNWVQ AA (G) (= 77 аминокислот+1 нуклеотид) до продолжения нуклеотидами GT (в интроне 2). Звездочка означает остаток, в котором альтернативные аминокислоты найдены либо в белке LL, либо в многочисленных последовательностях кДНК LL (см. Фигуру 17). G*, по-видимому, варьирует в лейколектине-1, тогда как L*, по-видимому, варьирует в лейколектине-2. Длина интрона 2 составляет 186 нуклеотидов, заканчиваясь в нуклеотидах AG.
Экзон 3 (72 аминокислоты) начинается после 2 нуклеотидов с GC (= Gly, остаток 78) и продолжается дополнительные 216 нуклеотидов (всего в объеме 218 нуклеотидов) или 72 аминокислоты. Аминокислотная последовательность ридов экзона 3: (G)LL* KQL DAGGE - QFIVG ANMN* D TPYCLTSSAT - VGYKG PGSPL - PWTGL PGAVK - YYSCG P* FGCW -AVNKN DDIYL - MS, где остаток 150 представляет собой S. Три большие буквы, выделенные жирным шрифтом и подчеркнутые, означают вариант аминокислот, которые служат для различия между лейколектином-1 и лейколектином-2. Буквы со звездочками тоже означают остатки с микроизменениями (N* в лейколектине-2; P* означает микроизменение как в лейколектине-1, так и в лейколектине-2) в таком положении (см. Фигуру 17). Интрон 3 идет, начиная с нуклеотидов GT, и продолжается еще ~250 нуклеотидов.
Экзон 4 (39 аминокислот) начинается с аминокислотного остатка 151= LNQDC QNKGW - SHIE* G KLSMI - EVATD GSVFG - VNSA* GSVYT, где T представляет собой остаток 189. Еще раз остаток, выделенный жирным шрифтом, служит для отличия лейколектина-1 от лейколектина-2, тогда как звездочка означает микроизменение в этом положении (видно либо в лейколектине в положении E*, и только в лейколектине -2 для положения A*). Интрон 4 возможно может не начинаться и заканчиваться стандартными нуклеотидными последовательностями для определения интрона. Данные, касающиеся интрона 4, таким образом, являются несколько предварительными, и, следовательно, длина интрона 4 является оценкой (~700 нуклеотидов).
Экзон 5 (47 аминокислот) начинается с кодона для R (= остаток 190) и продолжается до C-концевого гистидина (остаток 236), за которым следует стоп-кодон TAG, и 3'UTR. Эта последовательность ридов: RDGIT-ASKPE-GTGWS-NIPMG*-MLMGHVTYDL-GRLWV-VSKSAV-TMVCT-H, где звездочка указывает на микроизменение в этом положении в лейколектине-1. Буквы, выделенные жирным шрифтом, означают различия между лейколектином-1 и лейколектином-2. Буквы, выделенные жирным курсивом, означают возможность существования лейколектина-3. Эти данные суммированы на Фигуре 17.
Пример 11: сравнение геномной последовательности лейколектина-1 с последовательностями мРНК лейколектина
Используя более десятка отдельных экспериментов по клонированию и секвенированию кДНК лосося, выровненные последовательности показали, что только в 7 положениях находятся явные альтернативы различных размещенных аминокислотных остатков. Примечательным является малочисленность суммарной вариабельности последовательности и стереотипное ограничение таких вариантов.
Геномная последовательность из L-7/247 соответствует клонам лейколектина, классифицированным как лейколектин-1. Другие секвенированные кДНК, названные лейколектином-2, отличаются в семи указанных положениях. Помимо этих положений, существуют признаки некоторых дополнительных вариантов в аминокислотах. Это может наводить на мысль о дополнительной микрогетерогенности двух классифицированных кДНК, но эти данные могут наводить на мысль о существовании третьей категории кДНК LL, поскольку, например, в положении 226 авторы изобретения находят остаток тирозина в некоторых клонах, который никогда не наблюдался ни в кДНК лейколектина-1, ни лейколектина-2 (Фигура 17).
Краткое описание наблюдаемых вариантов показано на Фигуре 17. Два типа лейколектинов характеризуются соответственно (E, I, Y, Y, K, A, V) по сравнению с (N, V, F, F, N, G, G) в семи положениях (88, 91, 101, 147, 158, 229, 230) обнаруженной аминокислотной последовательности для зрелого лейколектина. Эти 7 положений однозначно классифицируют эти два лейколектина, которые, кроме того, могут демонстрировать микроварианты в стереотипичных положениях, показанных звездочками на Фигуре 17. Как указывают данные на Фигуре 17, некоторые последовательности мРНК указывают на уникальный Gly в положении 2 сигнального пептида LL, который не видно в лейколектинах-1 и 2 и который, следовательно, наводит на мысль о возможном лейколектине-3. Кроме того, авторы изобретения наблюдали Tyr в положении 226 в зрелом лейколектине, где только Ser наблюдается в лейколектинах 1 и 2. Авторы изобретения делают вывод о том, что геномная последовательность в L7/247 соответствует последовательностям лейколектина-1, найденным с помощью многократного секвенирования кДНК LL лосося. Дополнительное секвенирование клонов ВАС LL должно показать другую основную категорию лейколектина-2, и, возможно, также предполагается существование лейколектина-3, как определено указанными выше критериями в отношении остатков.
Пример 12: обнаружение белков лейколектина в других видах
Жидкость, образующаяся при выходе из икринок мальков радужной форели (Oncorhyncus mykiss), трески и Oikopleura dioica, была исследована на наличие белков лейколектина. Белок из жидкости, образующейся при выклеве, получали с помощью аффинной хроматографии и анализировали с помощью 15% SDS-PAGE. Гель либо окрашивали серебром, для того чтобы показать наличие целого ряда белков, либо переносили на мембрану и зондировали с использованием антитела к лейколектину лосося. В каждом случае был обнаружен один белок ~26 кДа, соответствующий молекулярной массе лейколектина (см. Фигуры 18 (радужная форель)), 19A (треска) и 19B (Oikopleura dioica).
Последовательности:
1: (полипептид лейколектина из эмбриона лосося):
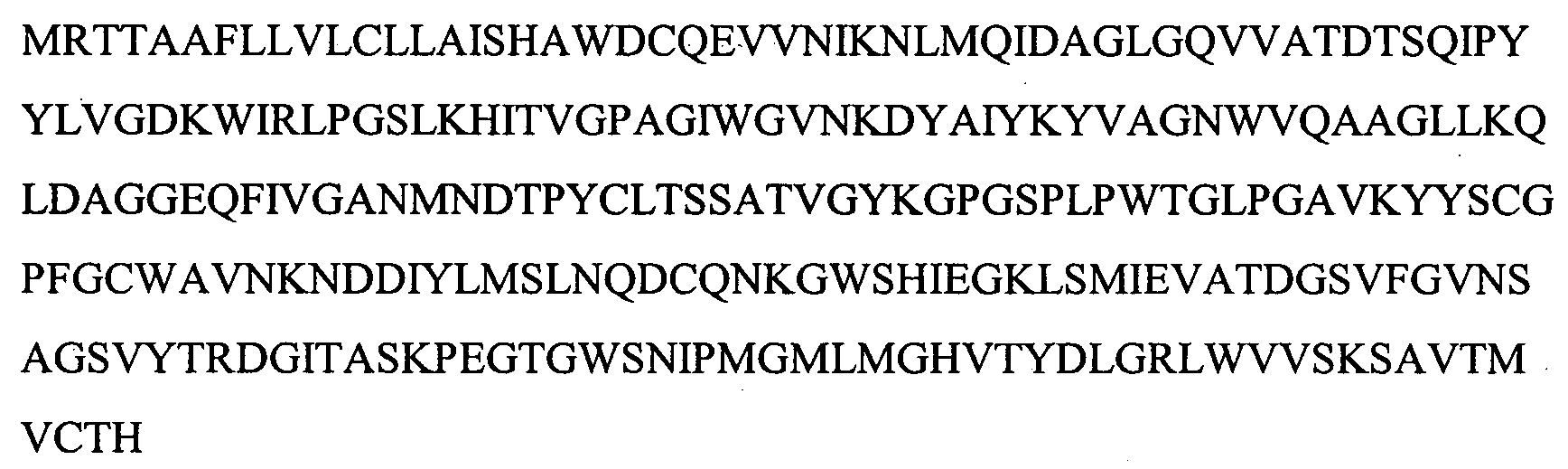
2: (полипептид лейколектина из лейкоцитов лосося):
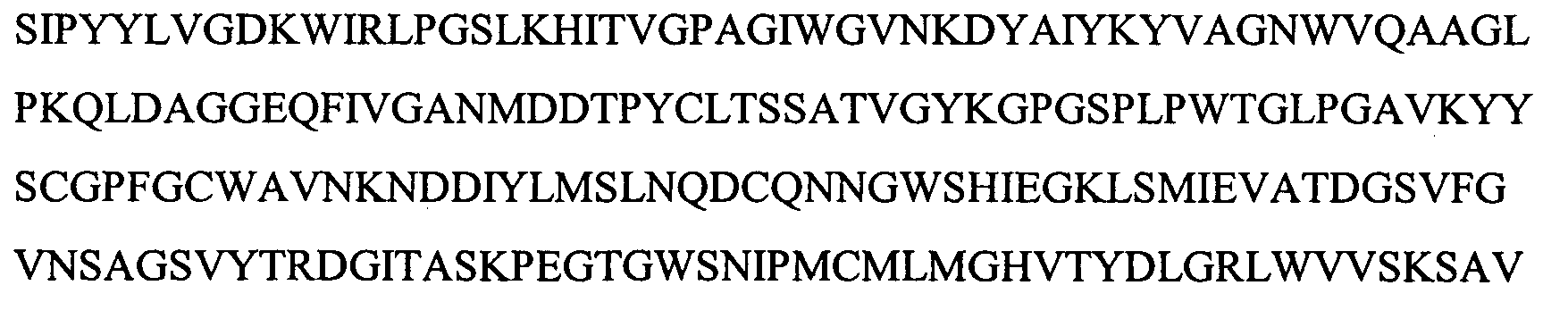
3: (полипептид лейколектина из лейкоцитов трески):
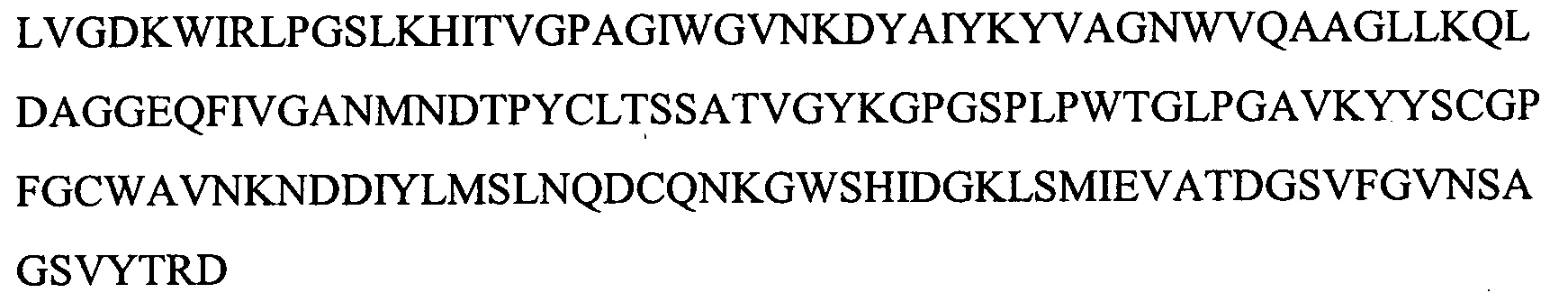
4: (полипептид лейколектина из лейкоцитов цыпленка):
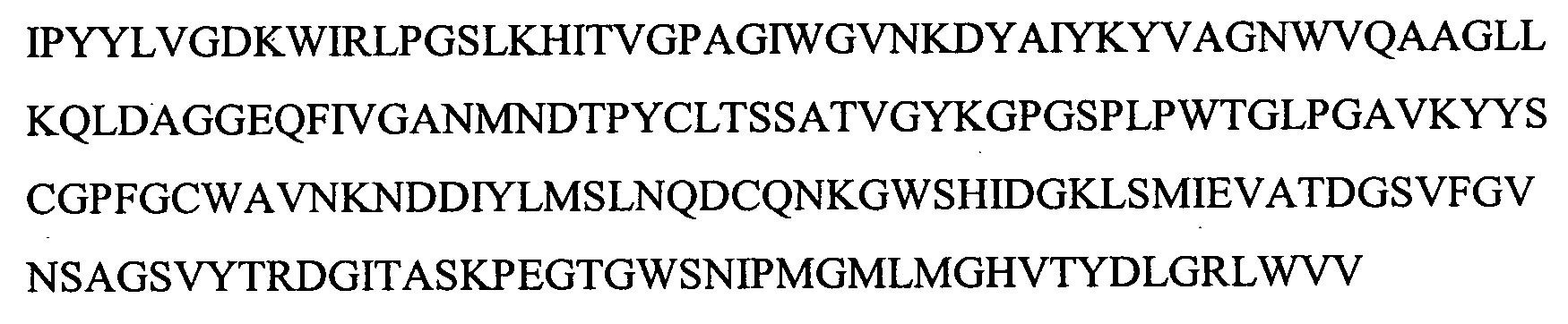
5: (полипептид лейколектина из лейкоцитов человека):
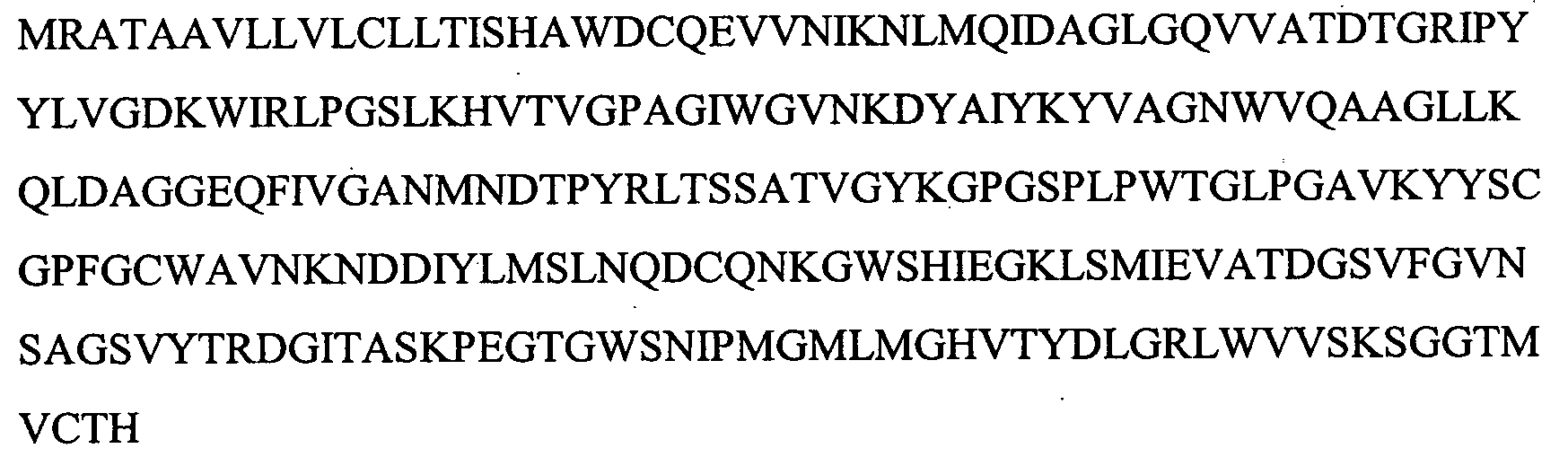
6: (полипептид лейколектина из данио):
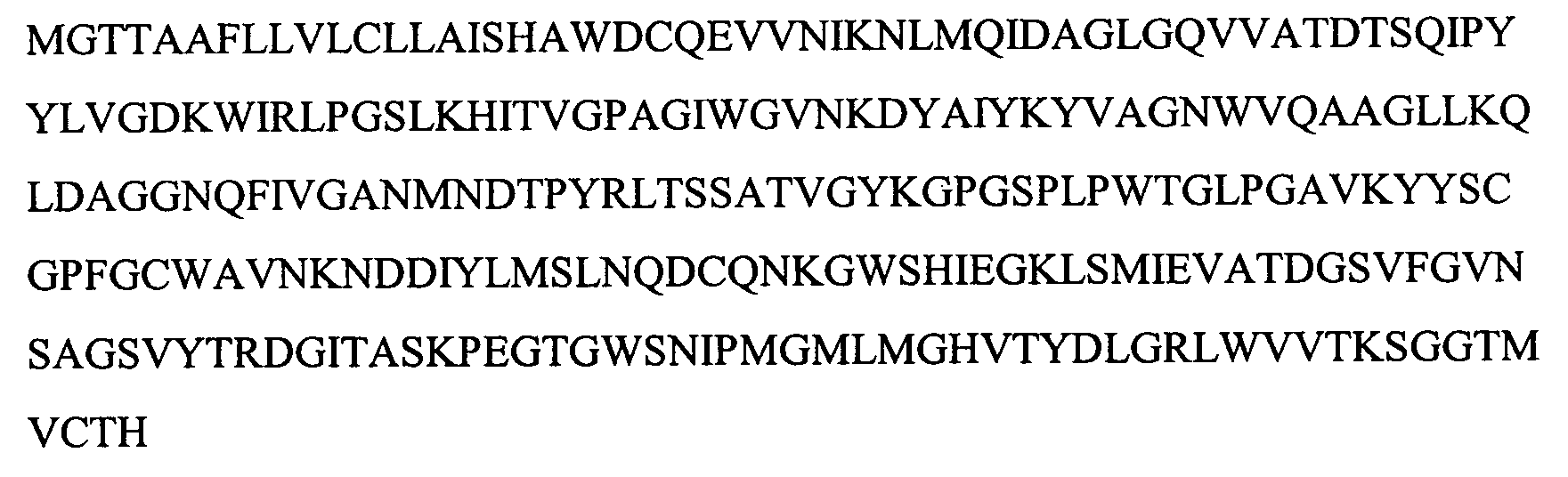
7: (полипептид лейколектина-2 из лосося):
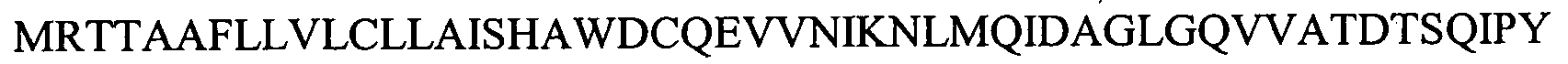
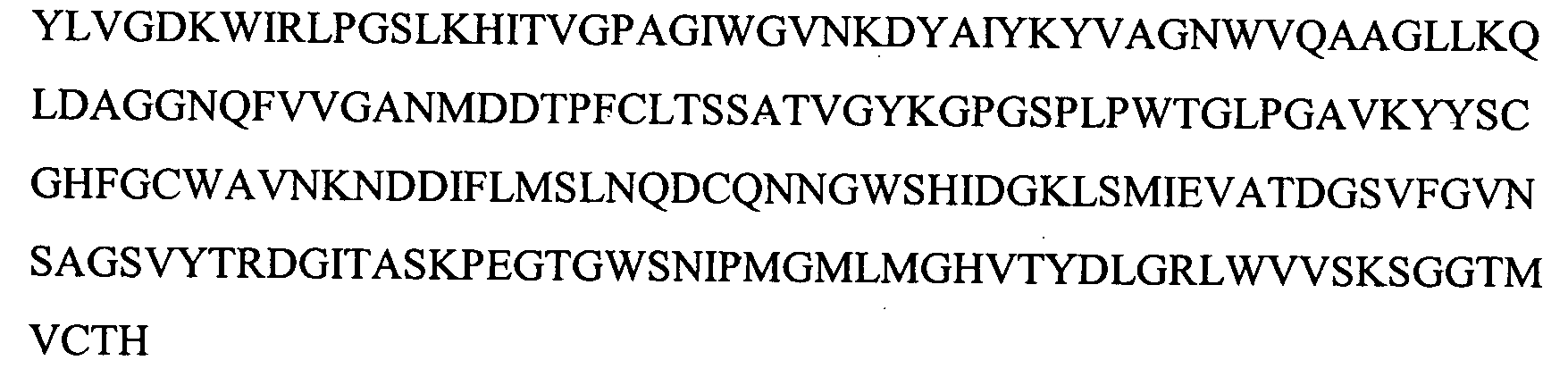
8: (полипептид лейколектина-3 из лосося):
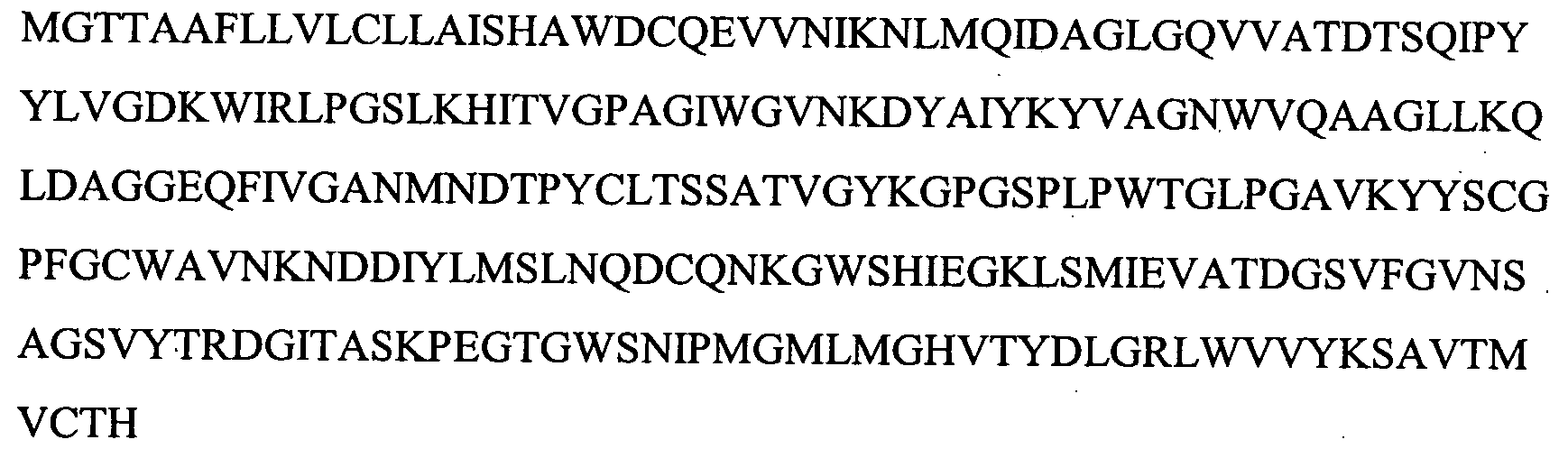
9: (последовательность кДНК лейколектина из крови человека):
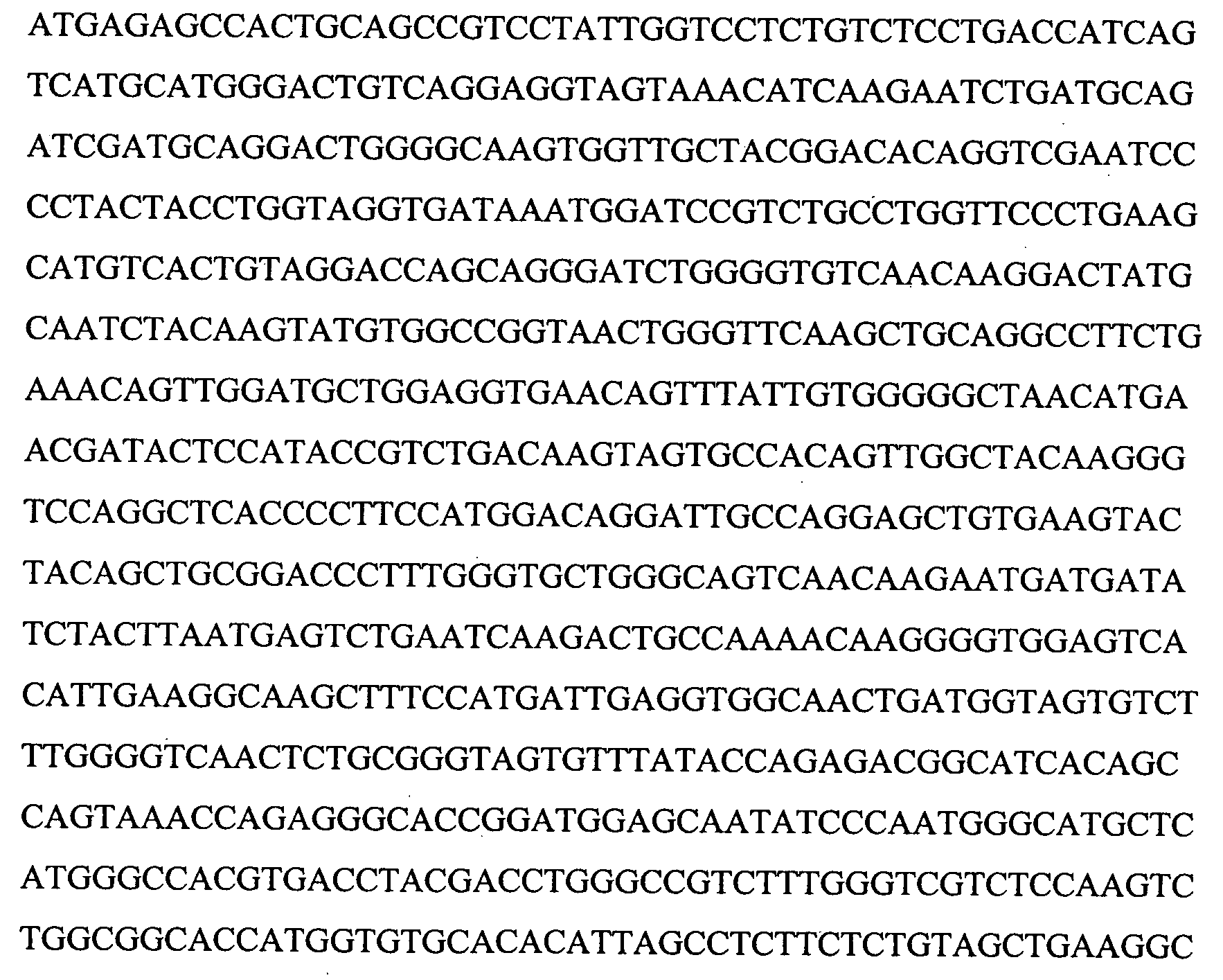
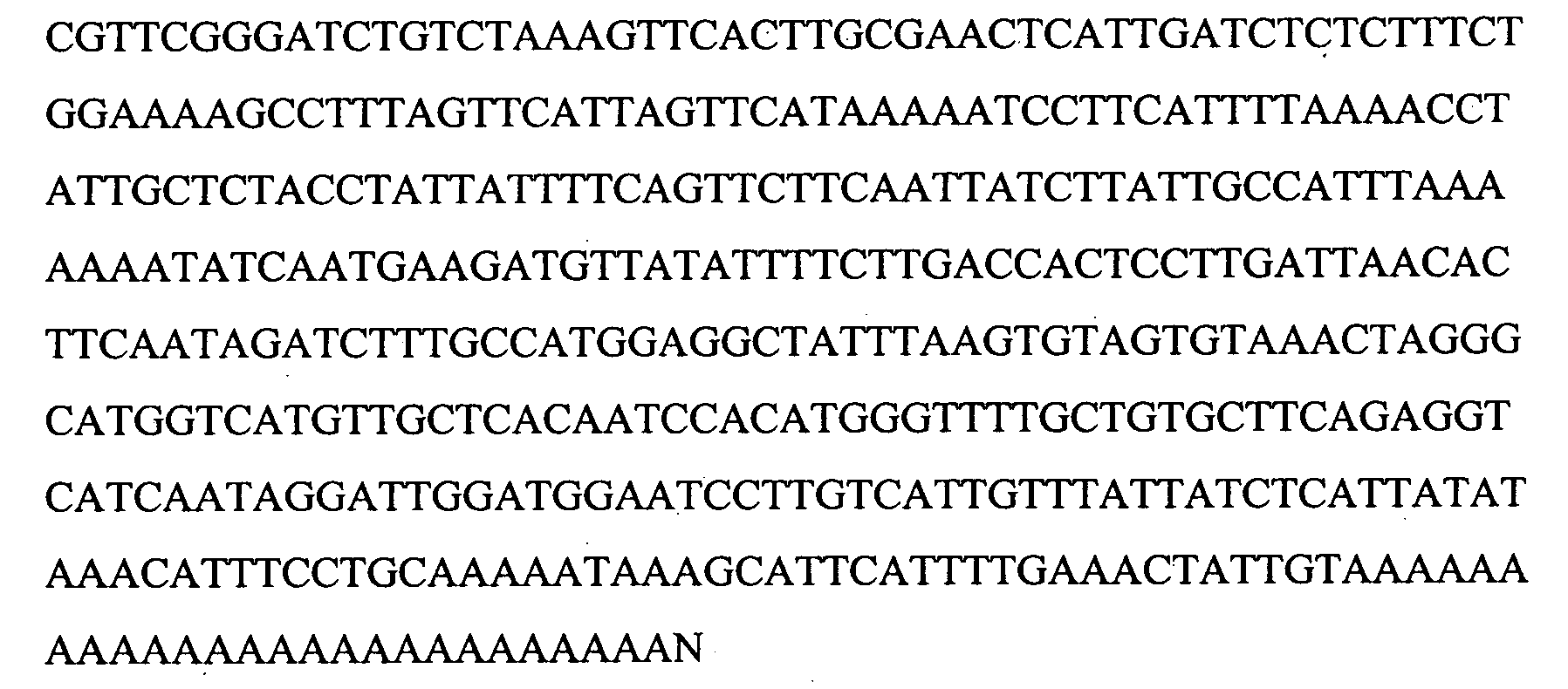
10: (последовательность гена лейколектина из лосося, из библиотеки геномной ДНК взрослого лосося):


11: (последовательность кДНК из эмбрионов лосося в возрасте 200-450 дней - только экзоны):

12: (последовательность гена лейколектина из лейкоцитов лосося):
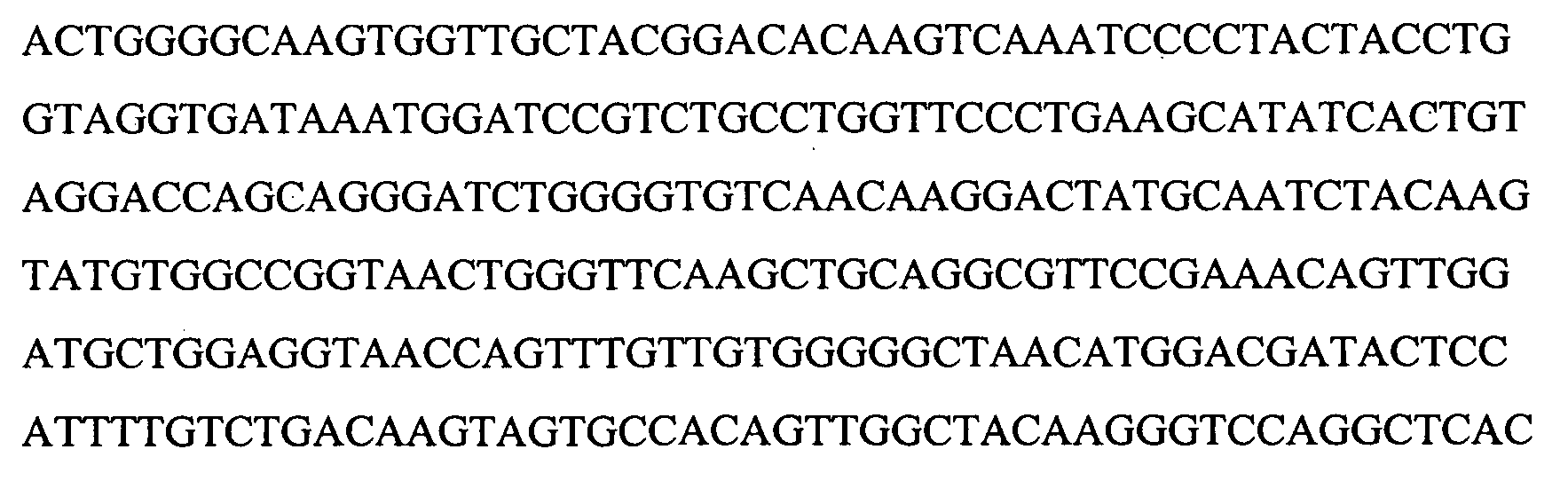
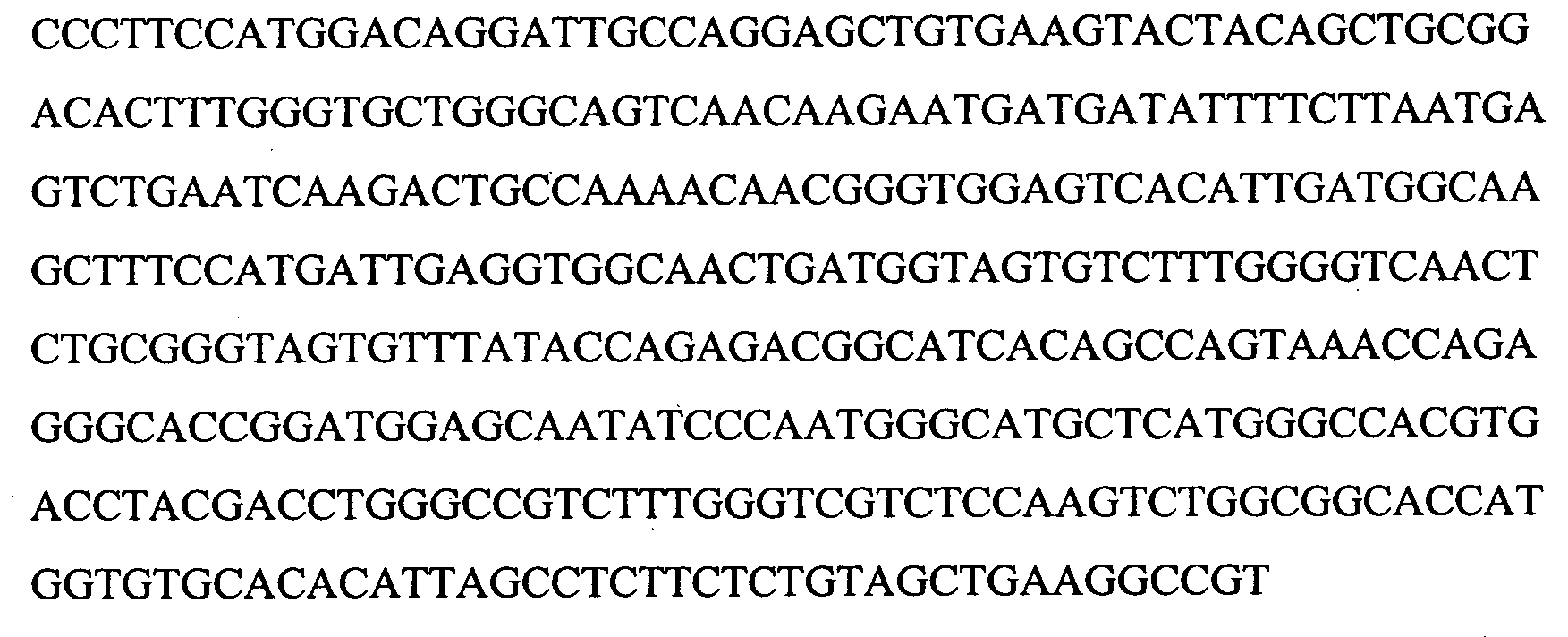
13: (последовательность гена лейколектина из трески):
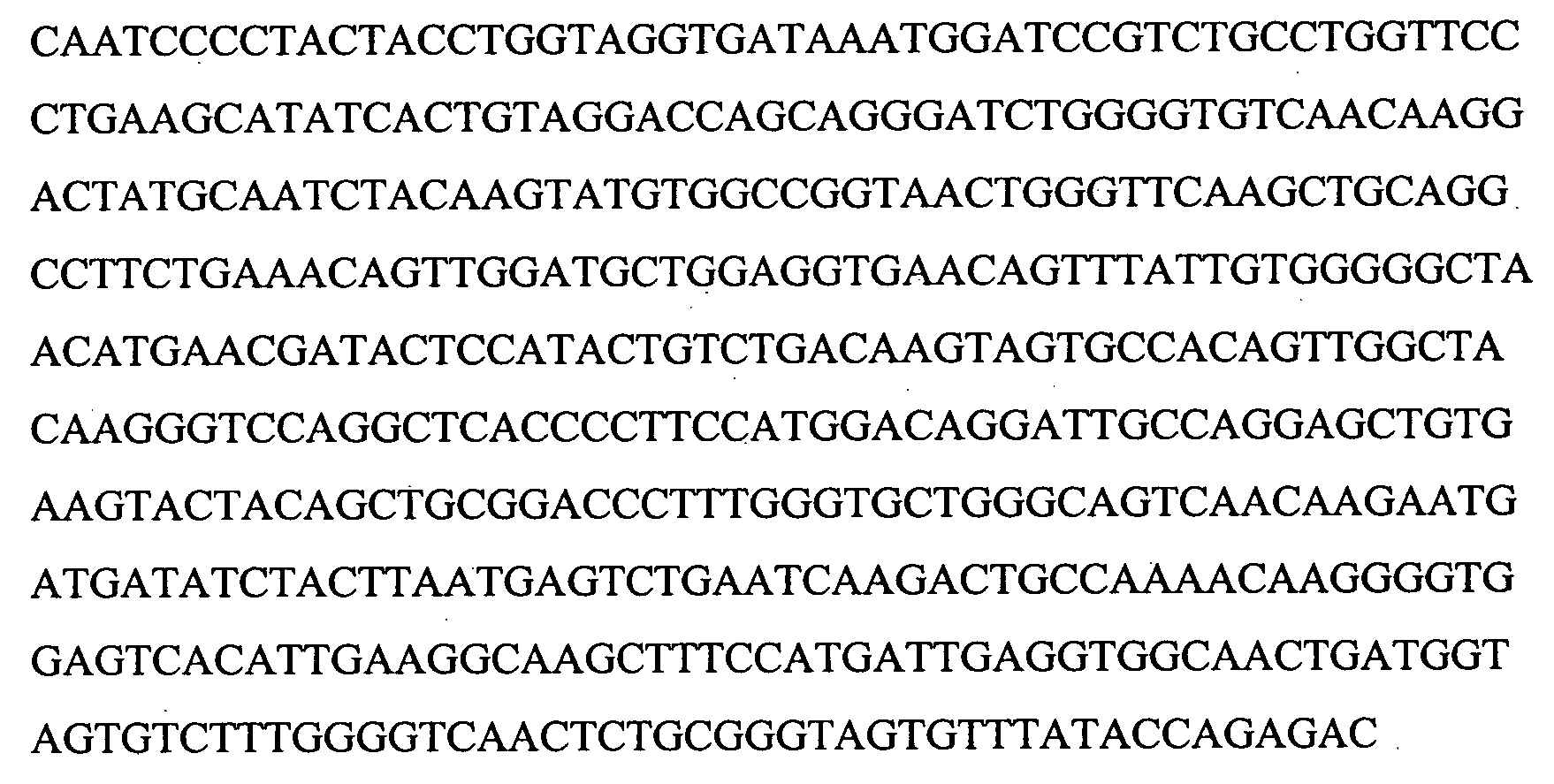
14: (последовательность гена лейколектина из цыпленка):
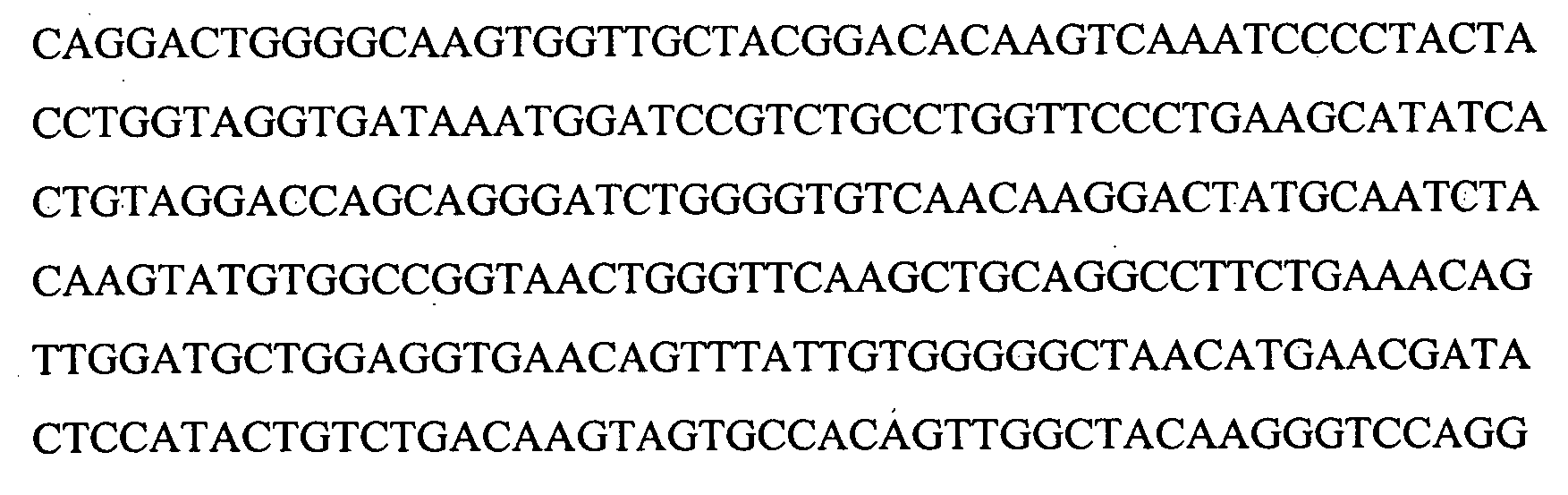
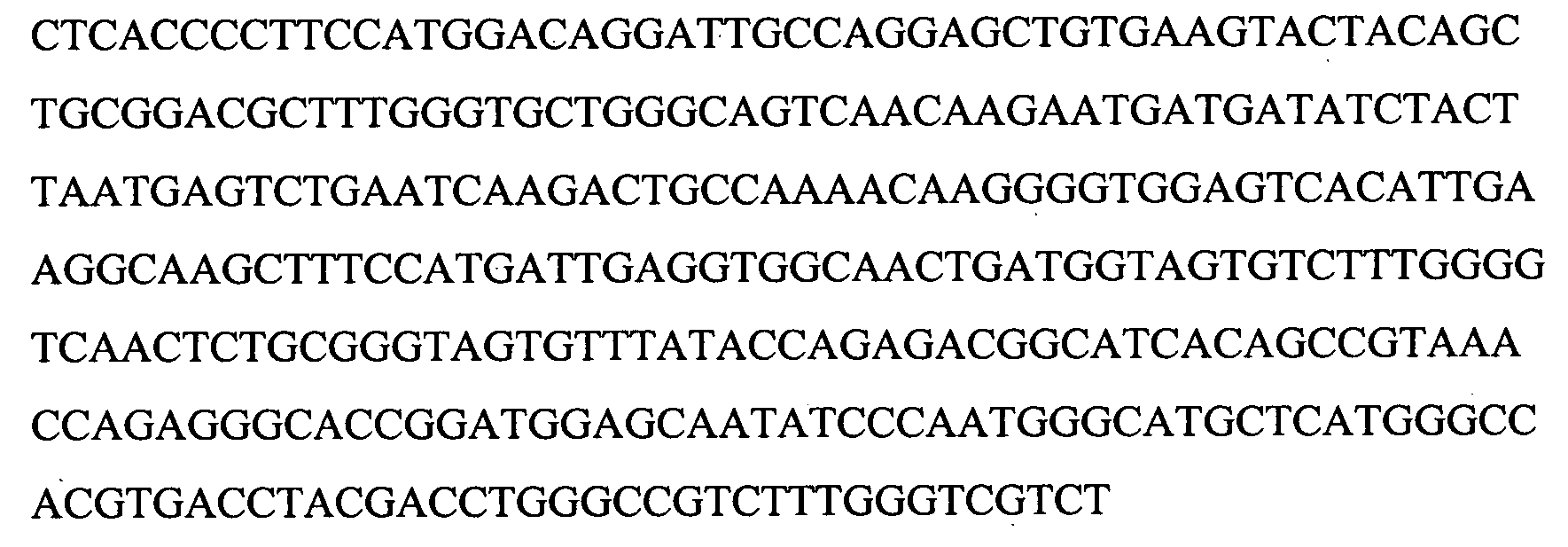
15: (частичная геномная последовательность лейколектина из данио):

Реферат
Изобретение относится к области биотехнологии, конкретно к лейколектинам, и может быть использовано в медицине. Получен полипептид лейколектин, характеризующийся SEQ ID NO:1-8. Для рекомбинантного получения лейколектина используют кодирующую его нуклеиновую кислоту, встроенную в вектор экспрессии, которым трансформируют клетку-хозяина. Для определения присутствия или определения количества полипептида лейколектина в образце используют антитело или антиген-связывающий фрагмент вариабельной области указанного антитела, которое специфически связывается с полипептидом лейколектином. Полипептид лейколектин или кодирующую его нуклеиновую кислоту используют в составе фармацевтической композиции в терапии патологических нарушений кожи и слизистых. Изобретение позволяет эффективно лечить или проводить профилактику аутоиммунных нарушений кожи, воспалительных заболеваний кожи или слизистой оболочки, или поврежденной кожи у животного. 11 н. и 5 з.п. ф-лы, 19 ил., 3 табл., 12 пр.

Комментарии