Композиции и способы лечения и предупреждения инфекций, вызванных staphylococcus aureus - RU2636780C1
Код документа: RU2636780C1
Чертежи


































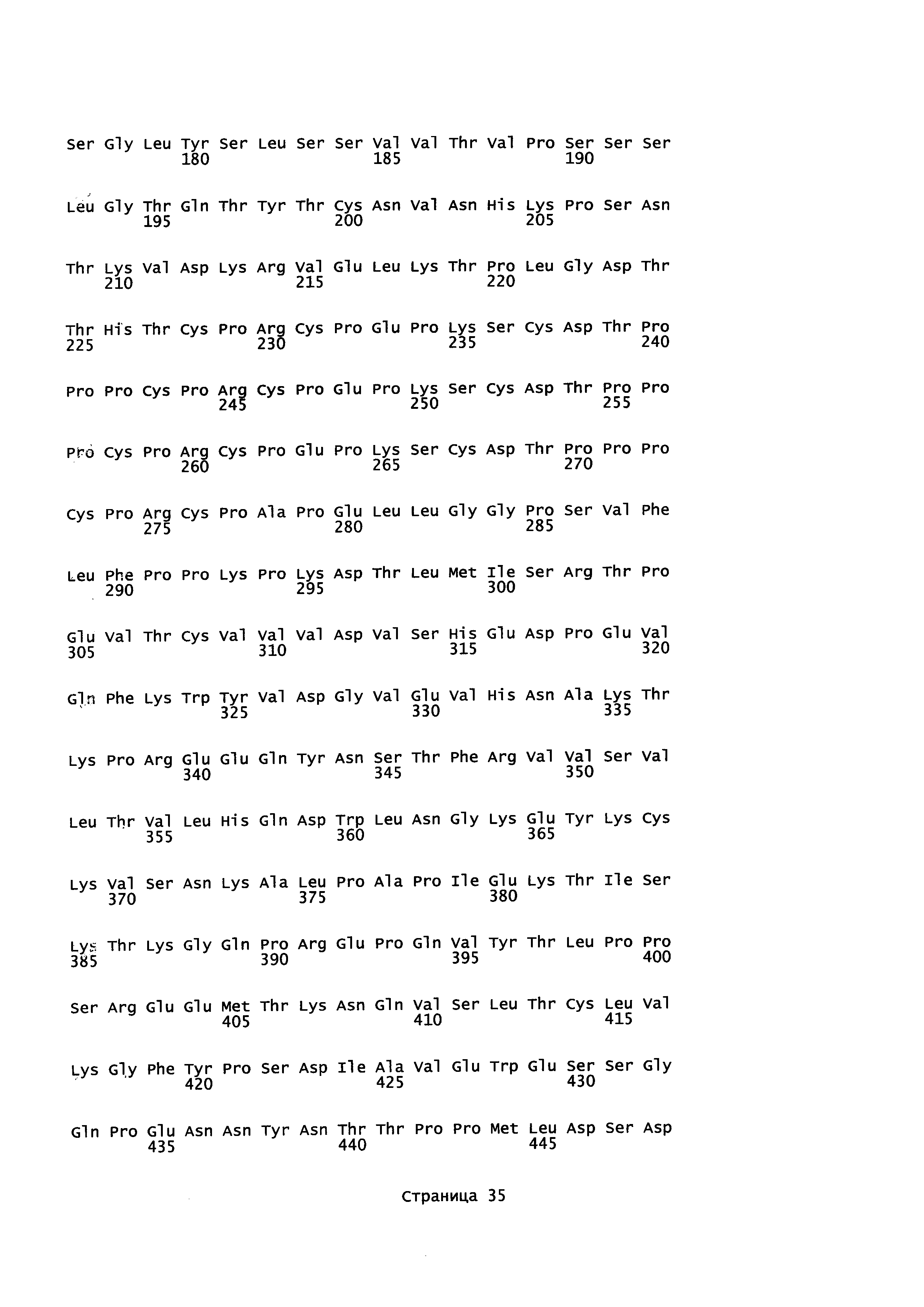















Описание
[0001] Данная заявка испрашивает приоритет предварительной заявки на патент США под номером 62/007242, поданной 3 июня 2014 года, предварительной заявки на патент США под номером 62/041423, поданной 25 августа 2014 года, и предварительной заявки на патент США под номером 62/115665, поданной 13 февраля 2015 года.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и, таким образом, включен в данный документ посредством ссылки в полном объеме. Вышеназванная копия в формате ASCII, созданная 28 мая 2015 года, названа 5407-0234_SL.txt и имеет размер 83036 байт.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0003] Настоящее изобретение, в общем, относится к способам терапевтического лечения, иммунологии и микробиологии. Более конкретно, настоящее изобретение относится к композициям и способам лечения и предупреждения инфекций, вызванных Staphylococcus aureus.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
[0004] Staphylococcus aureus (SA) является существенной причиной болезней и смертей, как среди людей, так и среди животных. Инфекция, вызванная данными грамположительными кокками, часто приводит к развитию поверхностного абсцесса. Другие случаи инфекции, вызванной SA, могут быть намного более серьезными. Например, попадание SA в лимфатическую систему и кровь может привести к системной инфекции, которая, в свою очередь, может привести к таким осложнениям, как эндокардит, артрит, остеомиелит, пневмония, септический шок и даже смерть. Внутрибольничная инфекция, вызываемая SA, является распространенной и особенно проблематичной в случае со SA, который является наиболее часто встречающейся причиной внутрибольничных инфекций в области хирургического вмешательства и пневмонии и второй, наиболее часто встречающейся причиной сердечно-сосудистых инфекций и инфекций кровотока. Введение антибиотиков было и остается стандартным лечением инфекций, вызванных SA. К сожалению, применение антибиотиков также способствовало развитию устойчивости к антибиотикам у SA. Причем метициллин-резистентный SA (MRSA) развил способность устойчивости к бета-лактамным антибиотикам, таким как пенициллин и цефалоспорины. Что более тревожно, недавно были выявлены SA, резистентные к антибиотикам «последней надежды», таким как ванкомицин и линезолид. Таким образом, необходим новый подход к предупреждению и лечению инфекций, вызванных SA.
КРАТКОЕ ОПИСАНИЕ
[0005] Было обнаружено, что определенные антитела (Ab) с паратопами Fab-фрагментов, которые специфично связываются с белком A SA (SpA), способны опосредовать опсонизацию бактерии SA несмотря на экспрессию SA SpA, нейтрализующего антитела (Ab). Предыдущие основанные на Ab стратегии лечения или предупреждения инфекций, вызываемых SA, продемонстрировали потенциал в доклинических испытаниях и клинических испытаниях на начальных этапах, но с ними не удалось достичь конечных точек в испытаниях фазы III. Вероятно, в качестве объяснения этих результатов, предыдущие стратегии не касались свойства SpA нейтрализовывать Ab. SpA представляет собой широко экспрессируемый белок, связанный с клеточной стенкой, который связывается с большинством иммуноглобулинов (Ig) посредством их Fс-(эффекторных) фрагментов. SpA связывается с антителами человека подклассов IgG1, IgG2 и IgG4 посредством их Fc-фрагмента с KD приблизительно 1×10-9 М и таким образом выступает в роли якоря Fc-фрагмента, который располагает эффекторную часть иммуноглобулина (Ig) в сторону, противоположную иммунным эффекторам, взаимодействующим с Fc-фрагментом, таким как фагоциты, несущие рецепторы для комплемента и рецепторы для Fc-фрагмента (FcR). Соответственно, большинство Ab, специфичных к антигенам SA, являются, таким образом, "изолированными" относительно иммунных эффекторов. В дополнение, поскольку SpA настолько широко распространен на клеточной стенке SA (предположительно 7% клеточной стенки), то он опосредует образование щита от Ig, покрывающих клеточную стенку. Данный щит стерически препятствует Ab, специфичным антигенам клеточной стенки, от связывания с их целями и опосредования опсоно-фагоцитозу бактерий. Образование щита от Ig ранее не рассматривали как фактор вирулентности. Таким образом, обнаружение, что Ab, связывающиеся с SA, имеющие Fab-фрагменты, которые специфично связываются с SpA, в тоже время позволяют продолжать взаимодействие их Fc-фрагментов с FcR на иммунных эффекторных клетках и/или активировать комплемент путем связывания C1q, несмотря на способность SpA нейтрализовывать Fc-фрагмент и на образование щита от Ig, являлось значительным шагом в сторону других основанных на Ab подходов против SA. Преимущественными вариантами этих Ab являются такие, которые способны к вытеснению Ig, уже связанных с SpA при помощи их Fc-фрагментов.
[0006] В качестве примеров вышеизложенного, в данном документе описаны выделенные или очищенные антитела (в частности, антитела IgG3 человека, которые имеют Fc-фрагменты с низкой или отсутствующей аффинностью к SpA, такие как фрагмент с аллотипом, содержащим аргинин в аминокислотной позиции 435; Stapleton et al., Nature Communications 2, Article number: 599, 2011), имеющие Fab-фрагменты, способные специфично связываться с целевым эпитопом SpA на бактерии SA, в то время как их Fc-фрагменты все еще способны взаимодействовать с FcR (например, растворимыми рекомбинантными или нативными на иммунных эффекторных клетках), несмотря на способность SpA к связыванию с Fc-фрагментом и стерический барьер целевого эпитопа путем связывания Ig с SpA посредством их Fc-фрагмента. В данном документе также предусмотрены фармацевтические композиции, которые содержат по меньшей мере одно из этих антител и фармацевтически приемлемый носитель (например, ненатуральный фармацевтически приемлемый носитель). Дополнительно предусмотрены способы лечения субъекта с инфекцией, вызванной SA, или снижения риска развития вызываемой SA инфекции у субъекта, которые включают введение терапевтически эффективного количества любой из фармацевтических композиций, описанных в данном документе, или любого из антител или антигенсвязывающих фрагментов, описанных в данном документе, нуждающемуся в этом субъекту.
[0007] Используемая в данном документе, форма единственного числа для существительного предусматривает "одно или несколько" данного существительного. Например, фраза "антитело" предусматривает "одно или несколько антител".
[0008] Термин "антитело" или "Ab" означает любой иммуноглобулин (например, антитела человека, хрящевых рыб или верблюда) или их конъюгат, который специфично связывается с антигеном (например, антигеном SpA, таким как SEQ ID NO: 1 или антигенным фрагментом под SEQ ID NO: 1). Специалисту в данной области известно огромное множество Ab. Неограничивающие примеры Ab включают моноклональные Ab (например, включая непроцессированные Ab), поликлональные Ab, мультиспецифические Ab (например, биспецифические Ab), Ab с двойным вариабельным доменом, одноцепочечные Ab (например, однодоменные Ab, Ab верблюдов и Ab хрящевых рыб), химерные Ab (например, гуманизированные, такие как гуманизированный IgG3) и Ab человека (например, Ab IgG3 человека). Термин антитело также включает конъюгаты Ab (например, Ab, конъюгированное со стабилизирующим белком, меткой или терапевтическим средством (например, любым из терапевтических средств, описанных в данном документе или известных из уровня техники)).
[0009] Термин "антигенсвязывающий фрагмент" означает любую часть непроцессированного Ab, которая содержит по меньшей мере один вариабельный домен ((например, вариабельный домен (например, человека, мыши, крысы, кролика или козы) тяжелой или легкой цепи иммуноглобулина млекопитающего), вариабельный антигенсвязывающий домен верблюда (VHH) или домен нового антигенного рецептора (Ig-NAR) иммуноглобулина хрящевых рыб), способный специфично связываться с антигеном. Например, антигенсвязывающий фрагмент, описанный в данном документе, может включать по меньшей мере часть Fc-фрагмента Ab, достаточную для того, чтобы опосредовать антитело-зависимую клеточно-опосредованную цитотоксичность (ADCC) и/или комплемент-зависимую цитотоксичность (CDC) у млекопитающих (например, человека), и/или коньюгирован с терапевтическим средством (например, любыми терапевтическими средствами, описанными в данном документе или известными из уровня техники). Неограничивающие примеры фрагментов Ab включают Fab-, Fab'-, F(ab')2-, Fv-фрагменты, диатела, линейные антитела, и мультиспецифические Ab, образованные из фрагментов Ab. Дополнительные фрагменты Ab, содержащие по меньшей мере один VHH домен верблюда или по меньшей мере один Ig-NAR домен хрящевых рыб, включают мини-тела, микро-антитела, субнано-антитела, и нано-антитела, и любые другие формы Ab, описанные в заявке на патент США №2010/0092470. Антигенсвязывающий фрагмент может являться, например, антигенсвязывающим фрагментом человека или гуманизированным IgG1, IgG2, IgG3 IgG4, IgD, IgA, IgE или IgM.
[0010] Термин "антитело человека" означает Ab, которое кодируется нуклеиновой кислотой (например, реаранжированный локус тяжелой или легкой цепи иммуноглобулина человека), которая присутствует в геноме человека. В некоторых вариантах осуществления Ab человека получают в культуре клеток млекопитающих (например, человека). В некоторых вариантах осуществления Ab человека получают в клетках, не относящийся к человеку (например, клеточной линии яичника китайского хомячка или клеточной линии мыши или хомячка). В некоторых вариантах осуществления Ab человека получают в клетках бактерий или дрожжей. Ab человека может включать конъюгированное терапевтическое средство (например, любые терапевтические средства, описанные в данном документе или известные из уровня техники). Ab человека может быть IgG1, IgG2, IgG4, IgD, IgA, IgE или IgM человека, и предпочтительно представляет собой IgG3 человека. Термин "истинное антитело человека" означает Ab с вариабельными участками тяжелой и легкой цепей, в норме присутствующие в сыворотке человека.
[0011] Термин "гуманизированное антитело" означает Ab, которое в основном содержит последовательности Ab человека, но также и включает немного последовательностей, полученных из Ig, отличного от Ig человека (например, мыши, крысы, кролика или козы). В неограничивающих примерах, гуманизированные Ab представляют собой Ab человека (Ab реципиента), в которых остатки гипервариабельного участка Ab реципиента заменены остатками гипервариабельного участка Ab видов, не являющихся человеком (Ab донора), например, Ab мыши, крысы, кролика или козы, имеющими необходимую специфичность, аффинность и емкость. В некоторых вариантах осуществления остатки каркасного участка Fv Ig человека заменены соответствующими остатками не от человека. В некоторых вариантах осуществления гуманизированные Ab могут содержать остатки, которые не присутствуют в Ab реципиента или в Ab донора. Данные модификации могут быть сделаны, чтобы дополнительно улучшить функциональные свойства Ab.
[0012] В некоторых вариантах осуществления гуманизированные Ab будут содержать существенную часть из по меньшей мере одного, а обычно двух вариабельных доменов, в которых все или существенная часть гипервариабельных петель (гипервариабельных участков) соответствуют таковым иммуноглобулина не от человека и все или существенная часть каркасных участков представляют собой последовательность иммуноглобулина человека. Гуманизированное антитело может также содержать по меньшей мере часть константного участка Ig (Fc-фрагмента), обычно, такового из Ig человека (например, IgG3 человека). Гуманизированные Ab можно получить с использованием способов молекулярной биологии, хорошо известных из уровня техники. В данном документе описаны неограничивающие примеры способов создания гуманизированных Ab. Гуманизированное антитело может включать конъюгированное терапевтическое средство (например, любые терапевтические средства, описанные в данном документе или известные из уровня техники).
[0013] Термин "одноцепочечное антитело" означает одиночный полипептид, который содержит по меньшей мере один вариабельный связывающий домен (например, вариабельный домен Ig млекопитающих тяжелой или легкой цепи, вариабельный антигенсвязывающий домен (VHH) верблюда или домен нового антигенного рецептора (Ig-NAR) иммуноглобулина хрящевых рыб (например, акулы)), способный специфично связываться с антигеном. Неограничивающие примеры одноцепочечных Ab описаны в данном документе, и известны из уровня техники (см., например, антитела, описанные в заявке на патент США №2010/0092470). Однодоменное антитело может включать конъюгированное терапевтическое средство (например, любые терапевтические средства, описанные в данном документе или известные из уровня техники).
[0014] Ab или его антигенсвязывающий фрагмент "специфично связывается" или "связывается специфично" с определенным антигеном, например, SpA (таким как эпитоп, содержащий SEQ ID NO: 1 или антигенным фрагментом под SEQ ID NO: 1), если оно связывается с данным антигеном, но распознает и связывается с другими молекулами в образце в меньшей степени (например, не распознает и не связывается). В некоторых вариантах осуществления Ab или его антигенсвязывающий фрагмент избирательно связывается с эпитопом с аффинностью (KD), равной или менее чем 1×10-10 М (например, менее чем 1×10-11 М или менее чем 1×10-12 М) в натрий-фосфатном буферном растворе (например, как определено при помощи поверхностного плазмонного резонанса). Способность Ab или антигенсвязывающего фрагмента специфично связываться с белковым эпитопом можно определить с использованием любых способов, известных из уровня техники или тех способов, что описаны в данном документе.
[0015] Термин "гипервариабельный участок" или "CDR" означает участок в Ig (тяжелой или легкой цепи Ig), который образует часть антигенсвязывающего участка (паратопа) в Ab или его антигенсвязывающем фрагменте. Как известно из уровня техники, тяжелая цепь Ig в норме содержит три CDR: CDR1, CDR2 и CDR3, соответственно, и легкая цепь Ig в норме содержит три CDR: CDR1, CDR2 и CDR3. В любом Ab или его антигенсвязывающем фрагменте три CDR из тяжелой цепи Ig и три CDR из легкой цепи Ig вместе образуют антигенсвязывающий участок в Ab или его антигенсвязывающий фрагмент. База данных Kabat является одной системой, применяемой в данной области для нумерации последовательностей CDR, присутствующих в легкой цепи Ig или тяжелой цепи Ig.
[0016] Если не указано иное, то все технические и научные термины, которые используются в данном документе, имеют то же значение, которое обычно понимается специалистом в той области техники, к которой относится настоящее изобретение. Способы и материалы описаны в данном документе для применения в настоящем изобретении; также можно применять другие, подходящие способы и материалы, известные из уровня техники. Материалы, способы и примеры являются только иллюстративными и не предназначены быть ограничивающими. Все публикации, патентные заявки, патенты, последовательности, значения в базах данных и другие ссылки, упомянутые здесь, включены в полном объеме путем ссылки на них. В случае возникновения конфликта, контрольным документом будет выступать настоящее описание, включая приведенные определения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
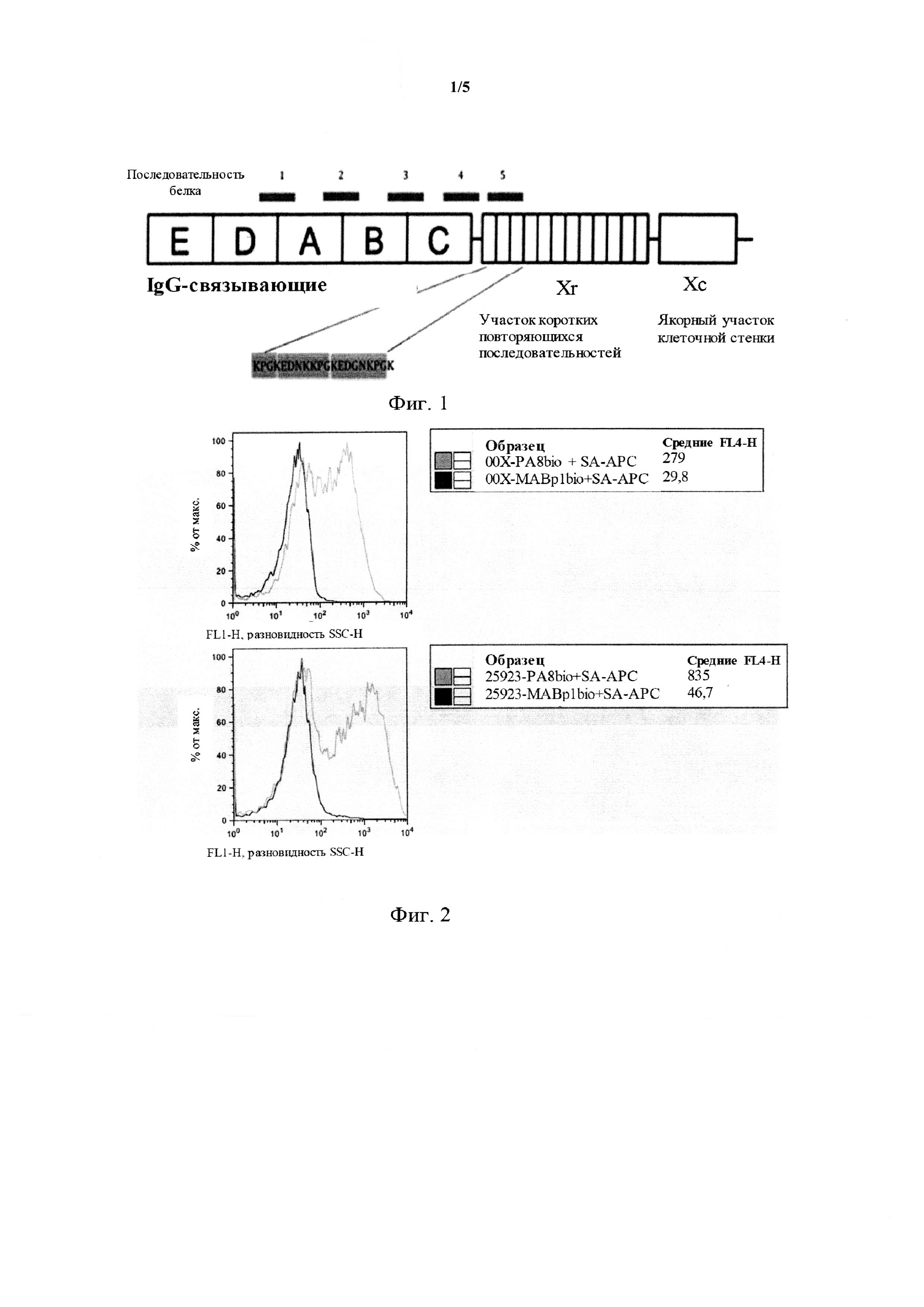
[0017] Фигура 1 представляет собой схематическое изображение SpA, демонстрирующее различные домены и расположение каждого из пяти антигенных пептидов. Показана последовательность антигенного пептида №5 (SEQ ID NO: 1).
[0018] Фигура 2 представляет собой серию из двух графических изображений, демонстрирующих гистограмму флуоресценции клинического штамма SA 00Х (верхняя часть) и штамма SA АТСС №25923 (нижняя часть), инкубированных с биотинилированными Ab PA8-G3 (светлая линия) или контрольных с биотинилированными Ab против интерлейкина-1 альфа (MABp1) (темная линия), а затем инкубированных со стрептавидином-АРС.
[0019] Фигура 3 представляет собой серию из двух графических изображений, демонстрирующая гистограмму флуоресценции клинического штамма 00Х (верхняя часть) и штамма АТСС №25923 (нижняя часть), инкубированных с немеченными Ab PA8-G3 (светлая линия) или немеченными Ab MABpl (темная линия), после чего следует биотинилированный рекомбинантный рецептор Fcγ 1, а затем инкубированных со стрептавидином-АРС.
[0020] Фигура 4 представляет собой графическое изображение среднего значения интенсивности флуоресценции дифференцированных клеток HL60 (с использованием сортировки клеток с флуоресценцией) после чего следует коинкубация с Ab PA8-G3, опсонизированных с меченным зеленым pHrodo штаммом АТСС №25923 или клиническим штаммом 00Х. Похожие образцы, инкубированные с контрольными Ab MABp1, вместо Ab PA8-G3, применяли в качестве отрицательного контроля.
[0021] Фигура 5 представляет собой серию из двух графических изображений, демонстрирующих интенсивность флуоресценции клинического штамма 00Х (верхняя часть) или АТСС №25923 (нижняя часть), предварительно инкубированного с сывороткой человека за 15 минут до добавления биотинилированных Ab PA8-G3 или Ab МАВР1 в качестве отрицательного контроля, а затем инкубированного со стрептавидином-АРС.
[0022] Фигура 6 представляет собой графическое изображение, демонстрирующее среднее значение интенсивности флуоресценции дифференцированных или недифференцированных клеток HL-60 после коинкубации с меченными зеленым pHrodo SA и одним из следующих немеченных Ab: PA7.2-G3, PA4-G3, PA8-G3, PA15-G3, PA21-G3, PA27-G3, PA32-G3, PA37-G3 или MABp1. Образцы Ab MABp1 применяли в качестве отрицательного контроля.
[0023] Фигуры 7A-D представляют собой графические изображения, демонстрирующие, что введение mAb РА8 повышает выживаемость субъектов-мышей, инфицированных S. aureus.
[0024] Фигуры 8А-С представляют собой графические изображения, демонстрирующие синергизм между PA8-G3 и ванкомицином.
ПОДРОБНОЕ ОПИСАНИЕ
[0025] В данном документе описаны способы и композиции для лечения субъекта с инфекцией, вызванной SA, или снижения риска развития инфекции у субъекта, вызываемой SA.
Антитела и их антигенсвязывающие фрагменты
[0026] В данном документе описаны очищенные или выделенные (например, по меньшей мере на 90%, 92%, 94%, 95%, 96%, 97%, 98% или 99% чистые по весу) Ab (например, предпочтительно "истинные" человеческие IgG3, IgG3 человека или гуманизированные IgG3), которые связываются с SpA и способны опосредовать опсонизацию бактерий SA, несмотря на экспрессию SA SpA, нейтрализирующего антитела (Ab). Предпочтительные указанные Ab связываются с пептидом под SEQ ID NO:1 с достаточной аффинностью связывания для вытеснения иммуноглобулинов IgG человека (например, одного или нескольких из IgG1, IgG2 и IgG4), связанных с SpA посредством их Fc-фрагмента. Предпочтительные Ab могут связываться с SpA посредством паратопов их Fab-фрагментов с KD менее чем 1×10-10 М (например, менее чем 1×10-11 М, менее чем 1×10-12 М, менее чем 0,5×10-12 М или менее чем 1×10-13 М) в физиологических условиях (например, в натрий-фосфатном буферном растворе) (например, как определено с использованием поверхностного плазмонного резонанса или био-слой интерферометрии с использованием рекомбинантного SpA). Например, описанные в данном документе Ab, которые связываются с SpA посредством их Fab-фрагментов с KD от 1×10-10 М до 0,5×10-12 М, от 1×10-11 М до 0,5×10-12 М, от 1×10-11 М до 0,2×10-12 М (например, в физиологических условиях, например, в натрий-фосфатном буферном растворе, например, как определено с использованием поверхностного плазмонного резонанса с использованием рекомбинантного SpA), являются предпочтительными. Такие Ab иди антигенсвязывающие фрагменты, описанные в данном документе, предпочтительно способны вытеснять Ab человека (например, один или несколько из IgG1, IgG2 и IgG4) связанные с SpA в клеточной стенке бактерии SA посредством их Fc-фрагментов. В данном документе также предусмотрены очищенные или выделенные (например, по меньшей мере на 90%, 92%, 94%, 95%, 96%, 97%, 98% или 99% чистые по весу) mAb (например, предпочтительно "истинные" человеческие IgG3, IgG3 человека или гуманизированные IgG3) которые специфично связываются с белком A (SpA) Staphylococcus aureus с KD менее чем 1×10-10 М посредством паратопов их Fab-фрагментов, где mAb способны опосредовать опсонизацию экспрессирующих SpA бактерий Staphylococcus aureus в присутствии по меньшей мере 1 мг/мл (например, по меньшей мере 1, 2, 3, 4, 5, 10, 25, 50 или 100 мг/мл или количества, в норме содержащегося в сыворотке человека) иммуноглобулинов IgG, которые связываются с SpA посредством их Fc-фрагментов.
[0027] Очищенные или выделенные предусмотренные в данном документе Ab могут связываться с эпитопом, присутствующим во внеклеточном домене (например, присутствующим в участке повторов XR и одном или нескольких IgG-связывающих доменах) SpA. Неограничивающие примеры антигена, который можно специфично распознать любым из Ab (или их антигенсвязывающих фрагментов), предусмотренные в данном документе, включают: 6, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 смежных аминокислот под SEQ ID NO: 1 (например, фрагмент, начинающийся с аминокислотной позиции 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 под SEQ ID NO: 1); 6, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или 21 смежных аминокислот под SEQ ID NO: 82 (например, фрагмент, начинающийся с аминокислотной позиции 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 под SEQ ID NO: 82); 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 смежных аминокислот под SEQ ID NO: 83 (например, фрагмент, начинающийся с аминокислотной позиции 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 под SEQ ID NO: 83); 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или 21 смежных аминокислот под SEQ ID NO: 84 (например, фрагмент, начинающийся с аминокислотной позиции 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 под SEQ ID NO: 84); 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 смежных аминокислот под SEQ ID NO: 85 (например, фрагмент, начинающийся с аминокислотной позиции 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 под SEQ ID NO: 85); или 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 смежных аминокислот из аминокислотных позиций от 1 до 20, от 10 до 30, от 20 до 40, от 30 до 50, от 40 до 60, от 50 до 70, от 60 до 80, от 70 до 90, от 80 до 100, от 90 до 110, от 100 до 120, от 110 до 130, от 120 до 140, от 130 до 150, от 140 до 160, от 150 до 170, от 160 до 180, от 170 до 190, от 180 до 200, от 190 до 210, от 200 до 220, от 210 до 230, от 220 до 240, от 230 до 250, от 240 до 260, от 250 до 270, от 260 до 280, от 270 до 290, от 280 до 300, от 290 до 310, от 300 до 320, от 310 до 330, от 320 до 340, от 330 до 350, от 340 до 360, от 350 до 370, от 360 до 380, 370 до 390, 380 до 400, 390 до 410, 400 до 420, 410 до 430, 420 до 440, или 430, или до 450 под SEQ ID NO: 86. Примеры других антигенов включают похожие фрагменты SpA, имеющие аминокислотные последовательности, отличающиеся от таковых под SEQ ID NO:86.
[0028] Способы определения способности Ab или его антигенсвязывающего фрагмента связываться с целевым белком (например, SpA или его частью) можно выполнять с использованием способов, известных из уровня техники. Неограничивающие примеры указанных способов включают конкурентно-связывающие анализы с использованием Ab с известным свойством связывания с целевым белком (например, SpA), иммуноферментные анализы, BioCoRE®, колонки для аффинной хроматографии, иммуноблот или технологию белкового микрочипа. В некоторых вариантах осуществления активность связывания Ab или его антигенсвязывающего фрагмента определяют путем приведения в контакт бактерии SA с Ab или его антигенсвязывающим фрагментом. Иллюстративные способы определения способности Ab или антигенсвязывающего фрагмента вытеснять Ab человека (например, один или несколько из IgG1, IgG2 и IgG4), связанных с SpA в клеточной стенке бактерии SA, описаны в разделе примеров ниже. Дополнительные способы определения способности Ab или антигенсвязывающего фрагмента вытеснять Ab человека (например, один или несколько из IgG1, IgG2 и IgG4), связанных с SpA в клеточной стенке бактерии SA, известны из уровня техники.
[0029] Ab может быть, например, mAb, мультиспецифическим Ab (например, биспицефическим Ab), химерным Ab (например, гуманизированным Ab, таким как гуманизированное Ab IgG), Ab человека или фрагментом любого из вышеназванного. Например, Ab может быть моноклональным Ab IgG3 человека или гуманизированным моноклональным Ab IgG3. Ab может также быть одноцепочечным Ab (например, однодоменным Ab), таким как одноцепочечное Ab верблюдов или хрящевых рыб (например, акулы) или одноцепочечное Ab, которое содержит по меньшей мере один вариабельный антигенсвязывающий домен (VHH) верблюда или по меньшей мере один домен нового антигенного рецептора (Ig-NAR) иммуноглобулина хрящевых рыб (например, акулы) (см, например, Ab, описанные в заявке на патент США №2010/0092470). Ab может быть молекулой целого Ab или мультимером Ab.
[0030] Термин Ab также включает конъюгаты Ab (например, Ab, конъюгированное со стабилизирующим белком, меткой или терапевтическим средством (например, любым из терапевтических средств, описанных в данном документе или известных из уровня техники)). Ab, предусмотренное в данном документе может, например, включать Fc-фрагмент или часть Fc-фрагмента, достаточную для того, чтобы опосредовать Ab-зависимую клеточно-опосредованную цитотоксичность (ADCC) и/или комплемент-зависимую цитотоксичность (CDC) у млекопитающих (например, человека), и/или конъюгировано с терапевтическим средством (например, любыми терапевтическими средствами, описанными в данном документе или известными из уровня техники). Ab может быть, например, IgG1, IgG2, IgG4, IgD, IgA, IgE или IgM человека или гуманизированным IgG1, IgG2, IgG4, IgD, IgA, IgE или IgM, и предпочтительно представляет собой IgG3 человека или гуманизированный IgG3.
[0031] Антигенсвязывающий фрагмент, описанный в данном документе, может, например, включать по меньшей мере часть Fc-фрагмента, достаточную для того, чтобы опосредовать Ab-зависимую клеточно-опосредованную цитотоксичность (ADCC) и/или комплемент-зависимую цитотоксичность (CDC) у млекопитающих (например, человека), и/или конъюгирован с терапевтическим средством (например, любыми терапевтическими средствами, описанными в данном документе или известными из уровня техники). Неограничивающие примеры Ab фрагментов включают Fab-, Fab'-, F(ab')2-, одноцепочечные Fv- (scFv-), Fv-фрагменты, фрагменты, содержащие либо вариабельный домен легкой, либо тяжелой, диатела, линейные Ab и мультиспецифические Ab, образованные из фрагментов Ab. Дополнительные фрагменты Ab, содержащие по меньшей мере один VHH домен верблюда или по меньшей мере один Ig- NAR домен хрящевых рыб, включают мини-тела, микро-Ab, субнано-Ab, и нано- Ab, и любые другие формы Ab, описанные в заявке на патент США №2010/0092470.
[0032] Ab или их антигенсвязывающие фрагменты могут быть любого типа (например, IgG, IgE, IgM, IgD, IgA, и IgY человека или гуманизированные IgG, IgE, IgM, IgD, IgA, и IgY), класса (например, IgG1 человека или гуманизированные IgG1 (например, IgG1a или IgG1b), IgG2 человека или гуманизированные IgG2 (например, IgG2a или IgG2b), IgG3 человека или гуманизированные IgG3 (например, IgG3a или IgG3b), IgG4 человека или гуманизированные IgG4 (например, IgG4a или IgG4b), IgA1 человека или гуманизированные IgA1, и IgA2 человека или гуманизированные IgA2) или подкласса, хотя предпочтительными являются те, у которых низкая аффинность связывания SpA с Fc-фрагментом (например, имеющим KD выше 1×10-7 М, 1×10-6 М, 1×10-5 М, 1×10-4 М или 1×10-3 М; или имеющим KD выше, чем для SpA и Fc-фрагментом IgG1 человека) в физиологических условиях (например, в натрий-фосфатном буферном растворе) (например, как определено с использованием поверхностного плазмонного резонанса с использованием рекомбинантного SpA). Антигенсвязывающий фрагмент может быть, например, антигенсвязывающим фрагментом IgG1 человека или гуманизированного IgG1 (например, IgG1a или IgG1b), IgG2 человека или гуманизированного IgG2 (например, IgG2a или IgG2b), IgG4 человека или гуманизированного IgG4 (например, IgG4a или IgG4b), IgD человека или гуманизированного IgD, IgA (например, IgA1 или IgA2), IgE человека или гуманизированного IgE или IgM человека или гуманизированного IgM, и предпочтительно представляет собой фрагмент IgG3 человека или гуманизированного IgG3 (например, IgG3a или IgG3b). Аминокислотные мутации можно вводить в константный участок данных подклассов IgG. Аминокислотные мутации, которые можно вводить, могут быть, например, такими, которые повышают связывание с рецепторами для Fc-фрагмента (как описано, например, в Proc. Natl Acad. Set U.S.A. 103(11): 4005-4010, 2006; MAb 1(6): 572-579, 2009; US 2010/0196362; US 2013/0108623; US 2014/0171623; US 2014/0093496; и US 2014/0093959) или повышают или снижают связывание с FcRn (как описано, например, в J. Biol Chem. 276(9): 6591-6604, 2001; Int Immunol. 18(12): 1759-1769, 2006; и J. Biol. Chem. 281(33): 23514-23524, 2006).
[0033] Два типа Н-цепей гетерологично соединены с получением биспецифичного Ab. Технология "выступы-во-впадины" (как описано, например, в J. Immunol Methods 248(1-2): 7-15, 2001; и J. Biol. Chem. 285(27): 20850-20859, 2010), технология электростатического отталкивания (как описано, например, в WO 06/106905), технология SEEDbody (как описано, например, в Protein Eng. Des. Sel. 23(4): 195-202, 2010), и подобные можно применять для гетерологичного соединения двух типов Н-цепей посредством СН3-домена. Любые антитела, описанные в данном документе, могут быть таковыми с модифицированной цепью или дефицитными по сахарной цепи. Примеры антител, содержащих модифицированные углеводные цепи, включают антитела, сконструированные посредством гликозилирования (как описано, например, в WO 99/54342), антитела с дефукозилированными углеводными цепями (как описано, например, в WO 00/61739, WO 02/31140, WO 06/067847 и WO 06/067913), и антитела, имеющие сахарную цепь с GlcNAc в точке ветвления (как описано, например, в WO 02/79255). Известные примеры способов получения антител IgG, дефицитных по сахарной цепи, включают способ введения в тяжелой цепи мутации в аспарагин в положении 297 нумерации EU (J. Clin. Pharmacol. 50(5): 494-506, 2010), и способ получения IgG с использованием Е. coli (J. Immunol. Methods 263(1-2): 133-147, 2002; и J. Biol. Chem. 285(27): 20850-20859, 2010). Кроме того, гетерогенность, сопутствующая делеции С-концевого лизина в IgG, и гетерогенность, сопутствующая нарушению комплементарности дисульфидных связей в шарнирном участке IgG2 можно снизить путем введения аминокислотных делеций/замен (как описано, например, в WO 09/041613). Любые из Ab или антигенсвязывающих фрагментов, описанных в данном документе, включают по меньшей мере одну (например, одну, две, три, четыре, пять или шесть) аминокислоту (например, добавленную, вставленную или замещенную аминокислоту, например, за пределами CDR), которая не присутствует в соответствующем Ab человека. Любые из Ab или антигенсвязывающих фрагментов, описанных в данном документе, могут также характеризоваться по меньшей мере одной удаленной аминокислотой (например, в сравнении с соответствующим Ab человека), например, N- или С-концевой делецией легкой или тяжелой цепи или делецией аминокислоты константного домена (например, Fc-фрагмента).
[0034] SpA или его фрагмент (например, по меньшей мере 7, 8, 9 или 10 смежных аминокислот под SEQ ID NO: 1 (например, начинающийся с аминокислотной позиции 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 под SEQ ID NO: 1) или все под SEQ ID NO: 1) можно применять в качестве иммуногенного вещества для создания Ab с использованием стандартных методик получения поликлональных и моноклональных Ab. Ab фрагменты можно создавать из моноклональных Ab с использованием способов, хорошо известных из уровня техники.
[0035] Иммуногенное вещество обычно применяют для получения Ab путем иммунизации подходящего субъекта (например, кролика, козы, мыши или другого млекопитающего). Подходящее получение иммуногенным путем может содержать, например, экспрессированный рекомбинантно или химически синтезированный полипептид. Получение может дополнительно включать вспомогательное вещество, такое как полный или неполный адъювант Фрейнда или похожее иммуностимулирующее средство.
[0036] В качестве альтернативы для получения моноклональных Ab-секретирующих гибридом, моноклональное Ab, направленное против полипептида, можно определить и выделить путем скрининга библиотеки рекомбинантных комбинаторных иммуноглобулинов (например, библиотеки фагового отображения Ab) на предмет полипептида, представляющего интерес. Наборы для создания и скрининга библиотек фагового отображения являются коммерчески доступными (например, набор Recombinant Phage Antibody System от Pharmacia, № по каталогу 27-9400-01; и набор SurfZAP* Phage Display от Stratagene, № по каталогу 240612). Дополнительно, примеры способов и реагентов, особенно пригодных для применения в создании и скрининге библиотеки отображения Ab, можно найти, например, в заявке на патент США №5223409; WO 92/18619; WO 91/17271; WO 92/2079; WO 92/15679; WO 93/01288; WO 92/01047; WO 92/09690; WO 90/02809; Fuchs et al., Bio/Technology 9:1370-1372, 1991; Hay et al., Hum. Antibod. Hybridomas 3:81-85, 1992; Huse et al., Science 246:1275-1281, 1989; Griffiths et al., EMBO J. 12:725-734, 1993.
[0037] Дополнительные способы выделения и секвенирования Ab человека (например, IgG3 человека), которое специфично связывается с эпитопом SpA (например, эпитопом, расположенным или определенным в пределах полипептида под SEQ ID NO: 1) описаны в разделе примеров ниже. Дополнительные общие способы создания Ab и антигенсвязывающих фрагментов описаны в заявке на патент США №2011/0059085.
[0038] В некоторых вариантах осуществления Ab или антигенсвязывающие фрагменты, предусмотренные в данном документе, представляют собой Ab человека или гуманизированные Ab (например, Ab IgG3 человека или гуманизированные Ab IgG3). В некоторых вариантах осуществления гуманизированное Ab представляет собой Ab человека, сконструированное так, чтобы содержать по меньшей мере один гипервариабельный участок (CDR), присутствующий в Ab не от человека (например, Ab крысы, мыши, кролика или козы). В некоторых вариантах осуществления гуманизированное Ab или его фрагмент может содержать все три CDR легкой цепи человека или Ab не от человека, которое специфично связывается с эпитопом SpA (например, эпитопом, расположенным или определенным в пределах полипептида под SEQ ID NO: 1). В некоторых вариантах осуществления гуманизированные Ab или его фрагмент может содержать все три CDR тяжелой цепи человека или Ab не от человека, которое специфично связывается с эпитопом SpA (например, эпитопом, расположенным или определенным в пределах полипептида под SEQ ID NO: 1). В некоторых вариантах осуществления гуманизированные Ab или его фрагмент может содержать все три CDR тяжелой цепи и все три CDR легкой Ab не от человека или моноклонального Ab человека, которое специфично связывается с эпитопом SpA (например, эпитопом, расположенным или определенным в пределах полипептида под SEQ ID NO: 1).
[0039] Ab по настоящему изобретению могут также включать мультимерные формы Ab. Например, Ab по настоящему изобретению могут принимать вид димеров, тримеров Ab или мультимеров молекул мономерного иммуноглобулина более высокого порядка. Димеры молекул целого иммуноглобулина или F(аb')2-фрагментов представляют собой тетраваленты, в то время как димеры Fab-фрагментов или молекул scFv представляют собой биваленты. Отдельные мономеры внутри мультимера Ab могут быть идентичными или различными, т.е., они могут быть гетеромерными или гомомерными мультимерами Ab. Например, отдельные Ab внутри мультимера могут обладать той же или иной специфичностью связывания.
[0040] Мультимеризацию Ab можно совершать путем естественной агрегации Ab или при помощи техник химического или рекомбинантного связывания, известных из уровня техники. Например, определенный процент очищенных продуктов Ab (например, очищенных молекул IgG1) самостоятельно образует белковые агрегаты, содержащие гомодимеры Ab и другие мультимеры Ab более высокого порядка. В качестве альтернативы, гомодимеры Ab можно образовывать при помощи техник химического связывания, известных из уровня техники. Например, гетеробифункциональные сшивающие агенты, включающие без ограничения SMCC (сукцинимидил-4-(малеимидометил)циклогексан-1-карбоксилат) и SATA (N-сукцинимидил-S-ацетилтио-ацетат) (доступные, например, от Pierce Biotechnology, Inc. (Рокфорд, Иллинойс)), можно применять для образования мультимеров Ab. Иллюстративный протокол образования гомодимеров Ab представлен Ghetie et al. (Proc. Natl. Acad. Sci. U.S.A. 94: 7509-7514, 1997). Гомодимеры Ab можно преобразовать до гомодимеров Fab'2-фрагментов путем ферментативного расщепления с пепсином. Другим путем получения гомодимеров Ab является путь при помощи применения аутофильного пептида Т15, описанного Zhao et al. (J. Immunol. 25:396-404, 2002).
[0041] В качестве альтернативы, можно подталкивать мультимеризацию Ab, используя методики рекомбинантных ДНК. IgM и IgA естественным образом образовывают мультимеры Ab путем взаимодействия с полипептидом зрелой J-цепи. Молекулы иммуноглобулинов, которые не являются IgA или IgM, такие как молекулы IgG, можно сконструировать так, чтобы они содержали домен взаимодействия J-цепи IgA или IgM, таким образом, придавая способность образовывать мультимеры более высокого порядка на молекулах иммуноглобулинов, которые не являются IgA или IgM (см., например, Chintalacharuvu et al., Clin. Immunol. 101:21-31, 2001, и Frigerio et al., Plant Physiol. 123:1483-1494, 2000). Димеры IgA естественным образом секретируют в полость органов, выстланных слизистой оболочкой. Данная секреция опосредована посредством взаимодействия J-цепи с полимерным рецептором IgA (p1gR) на эпителиальных клетках. Если секреция формы IgA Ab (или Ab, сконструированного так, чтобы он содержал домен взаимодействия J-цепи) является нежелательной, ее можно сильно понизить посредством экспрессии молекулы Ab совместно с мутантной J-цепью, которая не взаимодействует с p1gR должным образом (Johansen et al., J. Immunol, 167:5185-192, 2001). Димеры ScFv также можно образовывать при помощи рекомбинантных методик, известных из уровня техники; пример конструирования димеров scFv представлен Goel et al. (Cancer Res. 60:6964-71, 2000). Мультимеры Ab можно очищать с использованием любого подходящего способа, известного из уровня техники, включая без ограничения эксклюзионную хроматографию.
[0042] Любые из Ab или антигенсвязывающих фрагментов, описанных в данном документе, можно конъюгировать со стабилизирующими молекулами (например, молекулой, повышающей период полу-жизни Ab или его антигенсвязывающего фрагмента в кошке или в растворе). Неограничивающие примеры стабилизирующих молекул включают полимер (например, полиэтиленгликоль) или белок (например, сывороточный альбумин, такой как сывороточный альбумин кошек). Любые из Ab или антигенсвязывающих фрагментов, описанных в данном документе, можно конъюгировать с меткой (например, флуорофором, радиоизотопом или люминесцентной молекулой) или терапевтическим средством (например, цитотоксическим средством или радиоизотопом). Иллюстративные способы прикрепления метки или терапевтического средства к Ab описаны в заявке на патент США №2013/0224228. Неограничивающие примеры цитотоксических средств включают средства, которые, как известно, вызывают гибель микроба (например, грамположительной бактерии, такой как Staphylococcus aureus). Неограничивающие примеры цитотоксических средств, которых можно конъюгировать с любым Ab или антигенсвязывающим фрагментом, предусмотренным в данном документе, включают: линезолид, эритромицин, мупироцин, эртапенем, дорипенем, имипенем, циластатин, меропенем, цефадроксил, цефазолин, цефалотин, цефалексин, цефлакор, цефамандол, цефокситин, цефпрозил, цефуроксим, цефиксим, цефдинир, цефдиторен, цефоперазон, цефотаксим, цефподоксим, цефтазидим, цефтибутен, цефтизоксим, цефтриаксон, цефтаролина фосамил, цефтобипрол, тейкопланин, ванкомицин, телеванцин, клиндамицин, линкомицин, даптомицин, амоксициллин, ампициллин, азлоциллин, карбенициллин, клоксациллин, диклоксациллин, флуклоксациллин, мезлоциллин, метициллин, нафциллин, оксациллин, пенициллин G, пенициллин V, пиперациллин, пенициллин G, темоциллин, тикарциллин, бацитрацин, колистин, олимиксин В, ципрофлоксацин, эноксацин, гатифлоксацин, гемифлоксацин, левофлоксацин, ломефлоксацин, моксифлоксацин, налидиксовая кислота, норфлоксацин, офлоксацин, тровафлоксацин, грепафлоксацин, спарфлоксацин, темафлоксацин, мафенид, сульфацетамид, сульфадиазин, сульфадиазин серебра, сульфадиметоксин, сульфаметизол, сульфаметоксазол, сульфаниламид, сульфасалазин, сульфизоксазол, триметоприм-сульфаметаксозол, сульфонамидохризоидин, демеклоциклин, доксициклин, миноциклин, окситетрациклин и тетрациклин.
[0043] Например, предусмотренное в данном документе Ab (например, IgG3 человека или гуманизированный моноклональный IgG3) или его антигенсвязывающий фрагмент (например, фрагмент IgG3 человека или фрагмент гуманизированного моноклонального IgG3), которые специфично связываются с SpA, могут включать:
(i) тяжелую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 2, 3 и 4, соответственно, и/или легкую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 7, 8 и 9, соответственно;
(ii) тяжелую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 12, 13 и 14, соответственно, и/или легкую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 17, 18 и 19, соответственно;
(iii) тяжелую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 22, 23 и 24, соответственно, и/или легкую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 27, 28 и 29, соответственно;
(iv) тяжелую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 32, 33 и 34, соответственно, и/или легкую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 37, 38 и 39, соответственно;
(v) тяжелую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 42, 43 и 44, соответственно, и/или легкую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 47, 48 и 49, соответственно;
(vi) тяжелую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 52, 53 и 54, соответственно, и/или легкую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 57, 58 и 59, соответственно;
(vii) тяжелую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 62, 63 и 64, соответственно, и/или легкую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 67, 68 и 69, соответственно; или
(viii) тяжелую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 72, 73 и 74, соответственно, и/или легкую цепь, содержащую CDR1, CDR2 и CDR3 под SEQ ID NO: 77, 78 и 79, соответственно.
[0044] В некоторых примерах любое из Ab, предусмотренных в данном документе, содержит: тяжелую цепь Ab, включающую SEQ ID NO: 6, и/или легкую цепь Ab, включающую SEQ ID NO: 11; тяжелую цепь Ab, включающую SEQ ID NO: 16, и/или легкую цепь Ab, включающую SEQ ID NO: 21; тяжелую цепь Ab, включающую SEQ ID NO: 26, и/или легкую цепь Ab, включающую SEQ ID NO: 31; тяжелую цепь Ab, включающую SEQ ID NO: 36, и/или легкую цепь Ab, включающую SEQ ID NO: 41; тяжелую цепь Ab, включающую SEQ ID NO: 46, и/или легкую цепь Ab, включающую SEQ ID NO: 51; тяжелую цепь Ab, включающую SEQ ID NO: 56, и/или легкую цепь Ab, включающую SEQ ID NO: 61; тяжелую цепь Ab, включающую SEQ ID NO: 66, и/или легкую цепь Ab, включающую SEQ ID NO: 71; или тяжелую цепь Ab, включающую SEQ ID NO: 76, и/или легкую цепь Ab, включающую SEQ ID NO: 81.
[0045] В дополнительных примерах, любое из Ab (например, IgG3 человека или гуманизированного IgG3) или антигенсвязывающих фрагментов (например, антигенсвязывающего фрагмента IgG3 человека или гуманизированного IgG3), предусмотренных в данном документе, могут связываться с SpA с KD менее чем 1×10-10 М (например, менее чем 1×10-11 М или менее чем 1×10-12 М) и/или могут быть способными к вытеснению Ab человека (например, одного или нескольких из IgG1, IgG2, и IgG4), связанных с SpA, где антиген или антигенсвязывающий фрагмент, который содержит набор из шести CDR, всего имеет не более одной, двух, трех, четырех, пяти или шести аминокислотных замен (например, консервативных аминокислотных замен) в наборе (полном наборе) из шести CDR, выбранных из группы, состоящей из:
(i) SEQ ID NO: 2, 3, 4, 7, 8 и 9;
(ii) SEQ ID NO: 12, 13, 14, 17, 18 и 19;
(iii) SEQ ID NO: 22, 23, 24, 27, 28 и 29;
(iv) SEQ ID NO: 32, 33, 34, 37, 38 и 39;
(v) SEQ ID NO: 42, 43, 44, 47, 48 и 49;
(vi) SEQ ID NO: 52, 53, 54, 57, 58 и 59;
(vii) SEQ ID NO: 62, 63, 64, 67, 68 и 69; или
(viii) SEQ ID NO: 72, 73, 74, 77, 78 и 79.
[0046] Например, Ab (например, IgG3 человека или гуманизированный IgG3) или антигенсвязывающий фрагмент (например, антигенсвязывающий фрагмент IgG3 человека или гуманизированного IgG3), предусмотренные в данном документе, могут включать набор из шести CDR, которые всего имеют не более одной, двух, трех или четырех аминокислотных замен в наборе (целом наборе) из шести CDR под SEQ ID NO: 2, 3, 4, 7, 8 и 9. Например, Ab (например, IgG3 человека или гуманизированный IgG3) или антигенсвязывающий фрагмент (например, антигенсвязывающий фрагмент IgG3 человека или гуманизированного IgG3), предусмотренные в данном документе, могут содержать или состоять из:
(i) набора из шести CDR под SEQ ID NO: 2, 3, 4, 7, 8 и 9;
(ii) набора из шести CDR под SEQ ID NO: 12, 13, 14, 17, 18 и 19;
(iii) набора из шести CDR под SEQ ID NO: 22, 23, 24, 27, 28 и 29;
(iv) набора из шести CDR под SEQ ID NO: 32, 33, 34, 37, 38 и 39;
(v) набора из шести CDR под SEQ ID NO: 42, 43, 44, 47, 48 и 49;
(vi) набора из шести CDR под SEQ ID NO: 52, 53, 54, 57, 58 и 59;
(vii) набора из шести CDR под SEQ ID NO: 62, 63, 64, 67, 68 и 69; или
(viii) набора из шести CDR под SEQ ID NO: 72, 73, 74, 77, 78 и 79.
[0047] В дополнительных примерах, предусмотренные в данном документе Ab (например, IgG3 человека или гуманизированный моноклональный IgG3) или антигенсвязывающий фрагмент (например, антигенсвязывающий фрагмент IgG3 человека или гуманизированного IgG3), которые специфично связываются с SpA, включают вариабельный домен, выбранный из группы, состоящей из: (i) вариабельного домена, содержащего или состоящего из SEQ ID NO: 5; (ii) вариабельного домена, содержащего или состоящего из SEQ ID NO: 10; (iii) вариабельного домена, содержащего или состоящего из SEQ ID NO: 15; (iv) вариабельного домена, содержащего или состоящего из SEQ ID NO: 20; (v) вариабельного домена, содержащего или состоящего из SEQ ID NO: 25; (vi) вариабельного домена, содержащего или состоящего из SEQ ID NO: 30; (vii) вариабельного домена, содержащего или состоящего из SEQ ID NO: 35; (viii) вариабельного домена, содержащего или состоящего из SEQ ID NO: 40; (ix) вариабельного домена, содержащего или состоящего из SEQ ID NO: 45; (х) вариабельного домена, содержащего или состоящего из SEQ ID NO: 50; (xi) вариабельного домена, содержащего или состоящего из SEQ ID NO: 55; (xii) вариабельного домена, содержащего или состоящего из SEQ ID NO: 60; (xiii) вариабельного домена, содержащего или состоящего из SEQ ID NO: 65; (xiv) вариабельного домена, содержащего или состоящего из SEQ ID NO: 70; (xv) вариабельного домена, содержащего или состоящего из SEQ ID NO: 75; или (xvi) вариабельного домена, содержащего или состоящего из SEQ ID NO: 80. Например, Ab (например, IgG3 человека или гуманизированный моноклональный IgG3) или антигенсвязывающий фрагмент (например, антигенсвязывающий фрагмент IgG3 человека или гуманизированного IgG3), могут включать (i) вариабельный домен, содержащий или состоящий из SEQ ID NO: 5, и/или вариабельный домен, содержащий или состоящий из SEQ ID NO: 10; (ii) вариабельный домен, содержащий или состоящий из SEQ ID NO: 15, и/или вариабельный домен, содержащий или состоящий из SEQ ID NO: 20; (iii) вариабельный домен, содержащий или состоящий из SEQ ID NO: 25, и/или вариабельный домен, содержащий или состоящий из SEQ ID NO: 30; (iv) вариабельный домен, содержащий или состоящий из SEQ ID NO: 35, и/или вариабельный домен, содержащий или состоящий из SEQ ID NO: 40; (v) вариабельный домен, содержащий или состоящий из SEQ ID NO: 45, и/или вариабельный домен, содержащий или состоящий из SEQ ID NO: 50; (vi) вариабельный домен, содержащий или состоящий из SEQ ID NO: 55, и/или вариабельный домен, содержащий или состоящий из SEQ ID NO: 60; (vii) вариабельный домен, содержащий или состоящий из SEQ ID NO: 65, и/или вариабельный домен, содержащий или состоящий из SEQ ID NO: 70; или вариабельный домен, включающий или состоящий из SEQ ID NO: 75, и/или вариабельный домен, содержащий или состоящий из SEQ ID NO: 80.
[0048] Некоторые варианты осуществления любого из Ab (например, IgG3 человека или гуманизированного моноклонального IgG3) или антигенсвязывающих фрагментов (например, антигенсвязывающего фрагмента IgG3 человека или гуманизированного IgG3), описанные в данном документе, характеризуются одним или несколькими (например, одним, двумя, тремя или четырьмя) из следующих свойств: специфичного связывания с SpA в штамме MRSА; специфичного связывания с эпитопом, определенным SEQ ID NO: 1; связывания с SpA с KD менее чем 1×10-10 М (например, менее чем 1×10-11 М или менее чем 1×10-12); и вытеснения Ab человека, связанных с SpA в клеточной стенке бактерии Staphylococcus aureus (например, бактерии MRSА).
Фармацевтические композиции
[0049] Фармацевтические композиции, предусмотренные в данном документе, додержат по меньшей мере один фармацевтически приемлемый носитель (например, ненатуральный фармацевтически приемлемый носитель) и по меньшей мере одно (например, два, три или четыре) любое из Ab или антигенсвязывающих фрагментов, предусмотренных в данном документе. Неограничивающие примеры фармацевтически приемлемых носителей включают стерилизованную воду, физиологический солевой раствор, стабилизаторы, наполнители, антиоксиданты (например, аскорбиновая кислота), буферы (например, фосфатный, нитратный, гистидиновый и буфер других органический кислот), антисептики, поверхностно-активные вещества (например, PEG и Tween), хелатирующие средства (например, EDTA или EGTA) и связующие вещества. Дополнительные примеры фармацевтически приемлемых носителей также включают низкомолекулярные полипептиды, белки (например, сывороточный альбумин и желатин), аминокислоты (например, глицин, глутамин, аспарагин, глутаминовая кислота, аспарагиновая кислота, метионин, аргинин и лизин), сахара и углеводы (например, полисахариды и моносахариды), и сахарные спирты (например, маннит и сорбит). При приготовлении водных растворов для инъекций, можно применять физиологический солевой раствор и изотонические растворы, содержащие глюкозу и другие вспомогательные вещества, такие как D-сорбит, D-маннозу, D-маннит и хлорид натрия, и, при необходимости, в комбинации с подходящими растворителями, такими как спирт (например, этанол), многоатомные спирты (например, пропиленгликоль и PEG), и неионогенные поверхностно-активные вещества (например, полисорбат 80, полисорбат 20, полоксамер 188 и НСО-50). При добавлении в состав гиалуронидазы можно подкожно вводить больший объем жидкости (см., например, Expert. Opin. Drug. Deliv. 4(4): 427-440, 2007).
[0050] Ab и антигенсвязывающие фрагменты, предусмотренные в данном документе, можно, например, заключать в микрокапсулы (например, сделанные из гидроксиметилцеллюлозы, желатина и поли(метилметакрилата)) или включать в качестве компонентов коллоидных систем доставки лекарственного препарата (например, липосом, альбуминовых микросфер, микроэмульсии, наночастиц и нанокапсул) (см., например, "Remington's Pharmaceutical Science 16th edition", Oslo Ed. (1980)). Также хорошо известны способы приготовления фармацевтических композиций в виде фармацевтических средств с контролируемым высвобождением, и такие способы можно применять по отношению к Ab и антигенсвязывающим фрагментам по настоящему изобретению (см., например, Langer et al., J. Biomed. Mater. Res. 15: 267-277, 1981; Langer, Chemtech. 12: 98-105, 1982; патент США №3773919; европейская заявка на патент № ЕР 58481; Sidman et al., Biopolymers 22: 547-556, 1983; и ЕР 133988).
[0051] Фармацевтические композиции, предусмотренные в данном документе, можно составлять для внутривенного, внутриартериального, внутрикожного, подкожного, внутримышечного, внутрибрюшинного или перорального введения.
[0052] Дозу фармацевтической композиции по настоящему изобретению можно подходящим образом определить, принимая во внимание лекарственную форму, способ введения, возраст и вес тела пациента, симптомы пациента, степень тяжести инфекции, вызванной SA, или уровень риска инфекции, вызванной SA. В общем, суточная доза для взрослого может составлять, например, от 0,1 мг до 10000 мг за один раз или несколькими частями. Доза может составлять, например, от 0,2 до 10,000 мг/день (например, 1-10 г/день, 2-8 г/день, 1-5 г/день, от 0,5 до 2,5 г/день, от 0,5 до 500 мг/день, от 1 до 300 мг/день, от 3 до 100 мг/день или от 5 до 50 мг/день). Эти дозы можно варьировать, в зависимости от веса тела и возраста пациента и способа введения; однако, подбор подходящей дозы находится в компетенции специалиста в данной области. Похожим образом, период лечения можно подходящим образом определить в зависимости от терапевтического прогресса.
[0053] Любые фармацевтические композиции, предусмотренные в данном документе, могут дополнительно включать одно или несколько дополнительных противомикробных средств. Неограничивающие примеры таких противомикробных средств включают линезолид, эритромицин, мупироцин, эртапенем, дорипенем, имипенем, циластатин, меропенем, цефадроксил, цефазолин, цефалотин, цефалексин, цефлакор, цефамандол, цефокситин, цефпрозил, цефуроксим, цефиксим, цефдинир, цефдиторен, цефоперазон, цефотаксим, цефподоксим, цефтазидим, цефтибутен, цефтизоксим, цефтриаксон, цефтаролина фосамил, цефтобипрол, тейкопланин, ванкомицин, телеванцин, клиндамицин, линкомицин, даптомицин, амоксициллин, ампициллин, азлоциллин, карбенициллин, клоксациллин, диклоксациллин, флуклоксациллин, мезлоциллин, метициллин, нафциллин, оксациллин, пенициллин G, пенициллин V, пиперациллин, пенициллин G, темоциллин, тикарциллин, бацитрацин, колистин, олимиксин В, ципрофлоксацин, эноксацин, гатифлоксацин, гемифлоксацин, левофлоксацин, ломефлоксацин, моксифлоксацин, налидиксовая кислота, норфлоксацин, офлоксацин, тровафлоксацин, грепафлоксацин, спарфлоксацин, темафлоксацин, мафенид, сульфацетамид, сульфадиазин, сульфадиазин серебра, сульфадиметоксин, сульфаметизол, сульфаметоксазол, сульфаниламид, сульфасалазин, сульфизоксазол, триметоприм-сульфаметаксозол, сульфонамидохризоидин, демеклоциклин, доксициклин, миноциклин, окситетрациклин и тетрациклин.
Способы лечения субъекта с инфекцией, вызванной S. aureus, или снижения риска развития инфекции, вызванной S. aureus, у субъекта
[0054] Также предусмотрены способы лечения субъекта с инфекцией, вызванной SA (например, инфекцией вызванной MRSA, бактериемией SA, инфекцией кожи, вызванной SA, маститом, вызванным SA, флегмоной или фолликулитом, вызванными SA, или раневыми инфекциями, вызванными SA, нарывами, остеомиелитом, эндокардитом, пневмонией, септическим шоком, пищевым отравлением или токсическим шоком), которые включают введение нуждающемуся субъекту (например, человеку или другому млекопитающему, такому как представителю крупного рогатого скота, овечьих, собачьих, кошачьих, лошадиных, козьих, зайцевых, свиней, или птицам) терапевтически аффективного количества по меньшей мере одной любой из фармацевтических композиций, предусмотренных в данном документе, или по меньшей мере одного любого из Ab или антигенсвязывающих фрагментов, предусмотренных в данном документе. В некоторых примерах у субъекта диагностировали или идентифицировали инфекцию, вызванную SA (например, инфекцию, вызванную MRSA). Некоторые варианты осуществления дополнительно включают (до стадии введения) стадию диагностики, идентификации или отбора субъекта с инфекцией, вызванной SA, или с инфекцией, похожей на инфекцию, вызванную SA (например, инфекцией, вызванной MRSA или VRSA). В некоторых примерах инфекция, вызванная SA, является внутрибольничной инфекцией. В некоторых примерах субъекта ранее лечили с помощью антибактериального лечения, и предшествующее лечение не было успешным.
[0055] Также предусмотрены способы снижения риска развития инфекции, вызываемой SA, у субъекта (например, инфекции, вызываемой MRSA), которые включают введение субъекту эффективного количества по меньшей мере одной любой из фармацевтических композиций, предусмотренных в данном документе, или по меньшей мере одного любого из Ab или антигенсвязывающих фрагментов, предусмотренных в данном документе. В некоторых вариантах осуществления инфекция, вызванная SA, является внутрибольничной инфекцией. Некоторые варианты осуществления дополнительно включают перед введением отбор или идентификацию субъекта см повышенным риском развития инфекции, вызываемой SA (например, инфекции, вызываемой MRSA). Например, субъект может быть медицинским специалистом (например, врачом, медбратом или медсестрой, техником-лаборантом или помощником врача) (например, медицинским специалистом, вступающим в контакт с субъектом с инфекцией, вызванной SA (например, инфекцией, вызванной MRSA)). Субъектом в данных способах может также являться субъект, госпитализированный в больницу или центр стационарного лечения (например, в центре сестринского ухода), в котором содержится (госпитализирован) по меньшей мере один другой субъект с инфекцией, вызванной SA (например, инфекцией, вызванной MRSA). Субъект может быть госпитализированным пациентом, таким как пациент отделения интенсивной терапии и реанимации, пациент с нарушенным иммунитетом и пациент, перенесший или которому предстоит перенести операцию (например, операцию на сердце).
[0056] В любом из способов, предусмотренных в данном документе, субъектом может мужчина или женщина. Например, субъектом может быть младенец, ребенок ясельного возраста, адолесцент, подросток или взрослый человек (например, по меньшей мере 18 лет, по меньшей мере 20 лет, по меньшей мере 25 лет, по меньшей мере 30 лет, по меньшей мере 35 лет, по меньшей мере 40 лет, по меньшей мере 45 лет, по меньшей мере 50 лет, по меньшей мере 55 лет, по меньшей мере 60 лет, по меньшей мере 65 лет, по меньшей мере 70 лет, по меньшей мере 75 лет, по меньшей мере 80 лет, по меньшей мере 85 лет, по меньшей мере 90 лет, по меньшей мере 95 лет или по меньшей мере 100 лет). В некоторых примерах субъект имеет подавленную или ослабленную иммунную систему (например, гуморальную или клеточную иммунную систему).
[0057] В некоторых примерах по меньшей мере одна фармацевтическая композиция, предусмотренная в данном документе, или по меньшей мере одно Ab или антигенсвязывающий фрагмент, предусмотренные в данном документе, вводят при помощи внутривенного, внутриартериального, внутрикожного, подкожного, внутримышечного, внутрибрюшинного или перорального введения. Например, в способах снижения риска развития инфекции, вызываемой SA, субъекту вводят по меньшей мере одну из фармацевтических композиций, предусмотренных в данном документе, или по меньшей мере одно из Ab или антигенсвязывающих фрагментов, предусмотренных в данном документе, до или вскоре после вступления в физический контакт с субъектом, у которого идентифицировали, диагностировали, наличие или у которого подозревают наличие инфекции, вызываемой SA (например, инфекции, вызываемой MRSA).
[0058] В любом из способов, описанных в данном документе, субъекту вводят по меньшей мере одну (например, две, три, четыре, пять, шесть, семь, восемь, девять или десять) дозу(дозы) любой из фармацевтических композиций, предусмотренных в данном документе, или по меньшей мере одну (например, две, три, четыре, пять, шесть, семь, восемь, девять или десять) дозу(дозы) любого из Ab или антигенсвязывающих фрагментов, предусмотренных в данном документе. Субъекту можно ввести две или более доз любой из фармацевтических композиций или по меньшей мере две дозы любого из Ab или антигенсвязывающих фрагментов, предусмотренных в данном документе, с частотой по меньшей мере одна доза каждый месяц (например, по меньшей мере две дозы каждый месяц, по меньшей мере три дозы каждый месяц, по меньшей мере четыре дозы каждый месяц, по меньшей мере одна доза в неделю, по меньшей мере две дозы в неделю, по меньшей мере три дозы в неделю, по меньшей мере четыре дозы в неделю, по меньшей мере пять доз в неделю, по меньшей мере одна доза в день, по меньшей мере две дозы в день или по меньшей мере три дозы в день).
[0059] Некоторые варианты осуществления дополнительно включают совместное введение субъекту Ab, описанного в данном документе, и одного или нескольких дополнительных противомикробных средств. Неограничивающие примеры таких противомикробных средств включают линезолид, эритромицин, мупироцин, эртапенем, дорипенем, имипенем, циластатин, меропенем, цефадроксил, цефазолин, цефалотин, цефалексин, цефлакор, цефамандол, цефокситин, цефпрозил, цефуроксим, цефиксим, цефдинир, цефдиторен, цефоперазон, цефотаксим, цефподоксим, цефтазидим, цефтибутен, цефтизоксим, цефтриаксон, цефтаролина фосамил, цефтобипрол, тейкопланин, ванкомицин, телеванцин, клиндамицин, линкомицин, даптомицин, амоксициллин, ампициллин, азлоциллин, карбенициллин, клоксациллин, диклоксациллин, флуклоксациллин, мезлоциллин, метициллин, нафциллин, оксациллин, пенициллин G, пенициллин V, пиперациллин, пенициллин G, темоциллин, тикарциллин, бацитрацин, колистин, олимиксин В, ципрофлоксацин, эноксацин, гатифлоксацин, гемифлоксацин, левофлоксацин, ломефлоксацин, моксифлоксацин, налидиксовая кислота, норфлоксацин, офлоксацин, тровафлоксацин, грепафлоксацин, спарфлоксацин, темафлоксацин, мафенид, сульфацетамид, сульфадиазин, сульфадиазин серебра, сульфадиметоксин, сульфаметизол, сульфаметоксазол, сульфаниламид, сульфасалазин, йульфизоксазол, триметоприм-сульфаметаксозол, сульфонамидохризоидин, демеклоциклин, доксициклин, миноциклин, окситетрациклин и тетрациклин. Дополнительные примеры терапевтических средств, которые можно включить в любую из фармацевтических композиций, предусмотренных в данном документе, представляют собой одно или несколько Ab, описанных в заявке на патент США №2011/0059085.
Наборы
[0060] В данном документе также предусмотрены наборы, содержащие по меньшей мере одно (например, два, три, четыре или пять) из любых Ab или антигенсвязывающих фрагментов, предусмотренных в данном документе. В некоторых примерах наборы могут содержать рекомбинантный SpA или белок, содержащий или состоящий из SEQ ID NO: 1 или антигенным фрагментом под SEQ ID NO: 1 (например, по меньшей мере 7 смежных аминокислот под SEQ ID NO: 1 (например, начинающийся с аминокислотной позиции 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 под SEQ ID NO: 1)). В некоторых примерах по меньшей мере одно Ab или антигенсвязывающий фрагмент прикреплены к твердому субстрату (например, к лунке, чипу, пленке, шарику или хроматографической смоле). Указанные наборы могут включать серийную упаковку и/или напечатанную информацию об Ab и способах их применения.
ПРИМЕРЫ
Пример 1. Получение Ab человека, которые специфично связываются с SpA и вытесняют иммуноглобулины IgG человека, связанные с SpA посредством их Fc-фрагмента
[0061] Ab IgG3 человека, которые связываются с эпитопом SpA, получали так, как описано ниже. Пять синтезированных пептидов, охватывающих IgG-связывающие последовательности и последовательности Xr-повторов в SpA, применяли для скрининга в отношении присутствия Ab к пептидам в крови 311 здоровых взрослых добровольцев. Пять синтезированных пептидов SpA применяемых для скрининга, имели последовательности, обозначенные как: SEQ ID NO: 82, 83, 84, 85 и 1 (пептиды 1, 2, 3, 4 и 5, соответственно). У приблизительно 4% здоровых субъектов уровни Ab к пептидам (к SpA) относительно фона были увеличены в более чем 10 раз (с этого момента называемых "положительными донорами"), как определено с использованием иммуноферментного анализа (ELISA). От этих доноров получали плазму и ее применяли для выделения "истинных" человеческих Ab, которые связываются специфично с пептидом, покрывающим IgG-связывающие последовательности и последовательности Xr-повторов в SpA с использованием способов, описанных в заявке на патент США №2013/0018173. В итоге, выделяли Ab, представляющие интерес, с использованием хроматографии по сродству к антигену и секвенировали de novo с использованием масс-спектрометрии. Параллельно, Ab изотипировали с использованием набора для изотипирования человека.
[0062] Одно из выделенных Ab идентифицировали как относящееся к подсемейству VH3 и имеющее тяжелую цепь IgG2 и легкую цепь VK1. В-лимфоциты выделяли из крови доноров с использованием набора, полученного от STEMCELL Technologies, Inc. Их РНК выделяли с использованием протокола выделения с использованием Trizol и cDNA получали с использованием Superscript III. Праймеры, специфичные к мышиной лидерной последовательности, применяли для амплификации соответствующих тяжелых и легких цепей Ab и создавали "направленную" библиотеку ScFv. Библиотеку разделяли методом пэннинга против антигена SpA дикого типа на протяжении 7 циклов. Проводили скрининг клонов с использованием прямой ELISA и ELISA сэндвич-типа с SpA дикого типа. Отобранные клоны секвенировали, и тяжелые и легкие цепи клонировали в векторы с константным (Fc) участком IgG3 (того, у которого отсутствует сайт узнавания SpA в Fab-участках). Векторы трансфицировали в клеточные линии СНО и собирали высокопроизводительные клоны. Очищенные Ab тестировали в отношении активности к SpA. Количество клонов увеличивали в масштабе для производства в больших масштабах и полученные Ab очищали и применяли для дальнейших анализов. Примеры восьми подобных Ab описаны ниже:
Ab РА8 G3
Вариабельный домен тяжелой цепи под SEQ ID NO: 5.
CDR тяжелой цепи 1, 2 и 3 под SEQ ID NO: 2, 3 и 4, соответственно.
Тяжелая цепь под SEQ ID NO: 6.
Вариабельный домен легкой цепи под SEQ ID NO: 10.
CDR легкой цепи 1, 2 и 3 под SEQ ID NO: 7, 8 и 9, соответственно.
Легкая цепь под SEQ ID NO: 11.
Ab РА4 G3
Вариабельный домен тяжелой цепи под SEQ ID NO: 15.
CDR тяжелой цепи 1, 2 и 3 под SEQ ID NO: 12, 13 и 14, соответственно.
Тяжелая цепь под SEQ ID NO: 16.
Вариабельный домен легкой цепи под SEQ ID NO: 20.
CDR легкой цепи 1, 2 и 3 под SEQ ID NO: 17, 18 и 19, соответственно.
Легкая цепь под SEQ ID NO: 21.
Ab PA7.2-G3
Вариабельный домен тяжелой цепи под SEQ ID NO: 25.
CDR тяжелой цепи 1, 2 и 3 под SEQ ID NO: 22, 23 и 24, соответственно.
Тяжелая цепь под SEQ ID NO: 26.
Вариабельный домен легкой цепи под SEQ ID NO: 30.
CDR легкой цепи 1, 2 и 3 под SEQ ID NO: 27, 28 и 29, соответственно.
Легкая цепь под SEQ ID NO: 31.
Ab PA15-G3
Вариабельный домен тяжелой цепи под SEQ ID NO: 35.
CDR тяжелой цепи 1, 2 и 3 под SEQ ID NO: 32, 33 и 34, соответственно.
Тяжелая цепь под SEQ ID NO: 36.
Вариабельный домен легкой цепи под SEQ ID NO: 40.
CDR легкой цепи 1, 2 и 3 под SEQ ID NO: 37, 38 и 39, соответственно.
Легкая цепь под SEQ ID NO: 41.
Ab PA21G3
Вариабельный домен тяжелой цепи под SEQ ID NO: 45.
CDR тяжелой цепи 1, 2 и 3 под SEQ ID NO: 42, 43 и 44, соответственно.
Тяжелая цепь под SEQ ID NO: 46.
Вариабельный домен легкой цепи под SEQ ID NO: 50.
CDR легкой цепи 1, 2 и 3 под SEQ ID NO: 47, 48 и 49, соответственно.
Легкая цепь под SEQ ID NO: 51.
Ab РА27 G3
Вариабельный домен тяжелой цепи под SEQ ID NO: 55.
CDR тяжелой цепи 1, 2 и 3 под SEQ ID NO: 52, 53 и 54, соответственно.
Тяжелая цепь под SEQ ID NO: 56.
Вариабельный домен легкой цепи под SEQ ID NO: 60.
CDR легкой цепи 1, 2 и 3 под SEQ ID NO: 57, 58 и 59, соответственно.
Легкая цепь под SEQ ID NO: 61.
Ab РА32 G3
Вариабельный домен тяжелой цепи под SEQ ID NO: 65.
CDR тяжелой цепи 1, 2 и 3 под SEQ ID NO: 62, 63 и 64, соответственно.
Тяжелая цепь под SEQ ID NO: 66.
Вариабельный домен легкой цепи под SEQ ID NO: 70.
CDR легкой цепи 1, 2 и 3 под SEQ ID NO: 67, 68 и 69, соответственно.
Легкая цепь под SEQ ID NO: 71.
Ab РА37 G3
Вариабельный домен тяжелой цепи под SEQ ID NO: 75.
CDR тяжелой цепи 1, 2 и 3 под SEQ ID NO: 72, 73 и 74, соответственно.
Тяжелая цепь под SEQ ID NO: 76.
Вариабельный домен легкой цепи под SEQ ID NO: 80.
CDR легкой цепи 1, 2 и 3 под SEQ ID NO: 77, 78 и 79, соответственно.
Легкая цепь под SEQ ID NO: 81.
[0063] Проводили серию экспериментов для определения, способно ли Ab PA8-G3 связываться с SpA на клеточной стенке SA. В данных экспериментах штаммы SA АТСС №25923 или клинический штамм 00Х инкубировали либо с (i) биотинилированными PA8-G3, а затем со стрептавидином-АРС, чтобы при помощи флуоресценции подсчитать количество биотин-PA-G3, связанных с поверхностью SA (фигура 2), либо с (ii) очищенными немеченными Ab PA8-G3, после чего следует биотинилированный рекомбинантный рецептор Fсγ 1, а затем со стрептавидином-АРС, чтобы при помощи флуоресценции подсчитать количество PA8-G3, связанных с поверхностью SA, что приведет к фагоцитозу (т.е., в наличии будут свободные Fc-фрагменты, доступные для связывания с рекомбинантным рецептором Fсγ 1) (фигура 3). В данных экспериментах Ab к интерлейкину-1α (MABp1) применяли в качестве отрицательного контроля. Данные на фигуре 2 демонстрируют, что PA8-G3 связывается с SpA в клеточной стенке SA, и данные на фигуре 3 отмечают, что у связанного Ab PA8-G3 Fc-фрагменты были доступные для взаимодействия с FcR, что указывает на то, что Ab способно опосредовать опсоно-фагоцитоз SA у субъектов, являющихся людьми (не смотря на имеющиеся Fc-фрагменты, связанные с SpA и не способные контактировать с FcRs и, таким образом, опосредовать опсоно-фагоцитоз бактерий).
[0064] Дальнейшую серию экспериментов проводили для того чтобы исследовать, распознают ли рецепторы Fсγ на фагоцитах связывание Ab PA8-G3 с поверхностью SA. В данных экспериментах два разные меченные зеленым pHrodo штаммы S. aureus (клинический штамм 00Х или АТСС №25923) инкубировали либо с немеченными Ab PA8-G3, либо с контрольными Ab (MABp1), а затем инкубировали с дифференцированными клетками HL-60. Полученную в результате флуоресценцию клеток HL-60 определяли с использованием сортировки клеток с активированной флуоресценцией (FACS). Данные демонстрируют, что PA8-G3 связывается с клеточной стенкой обоих штаммов SA и опосредует фагоцитоз посредством рецепторов Fсγ на поверхности клеток HL-60 (фигура 4). Успешный фагоцитоз S. aureus,, связанной с PA8-G3, посредством дифференцированных клеток HL-60 также был очевидным из экспериментов с использованием флуоресцентной микроскопии.
[0065] Поверхностный плазмонный резонанс применяли для определения кинетики связывания PA8-G3 с SpA. В данных экспериментах Ab PA8-G3 иммобилизовали с использованием сенсора захвата белков человека, содержащих Fc-фрагмент, и доступного коммерчески SpA дикого типа. Эти данные показывают, что у PA8-G3 Ko составляет 5,38 рМ. Такая аффинность является примерно в 1000 выше, чем наномолярная аффинность IgG1, IgG2 и IgG4 сыворотки человека с SpA.
[0066] Дополнительную серию экспериментов проводили для того, чтобы определить способно ли Ab PA8-G3 успешно конкурировать за связывание с SpA с IgG человека, связанным с SpA посредством их рецептора для Fc-фрагмента. В данных экспериментах два различных штамма S. aureus предварительно инкубировали с сывороткой человека (которая содержит высокую концентрацию Ig, которые связываются с SpA посредством их Fc-фрагментов) за 15 минут до инкубации с биотинилированным Ab PA8-G3 Ab или биотинилированным Ab MABp1-IgG3 (родственным по изотипу негативным контролем), затем обрабатывали стрептавидином-АРС, а затем при помощи проточной цитометрии определяли флуоресценцию. Данные демонстрируют, что Ab PA8-G3 было способно связываться с SpA, при наличии Ab IgG человека, связанных с SpA посредством их Fc-фрагмента (фигура 5).
[0067] В другой серии экспериментов было продемонстрировано, что антитело PA8-G3 конкурировало с MABp1-IgG1 (который связывается с SpA посредством его Fc-фрагмента) за связывание на покрытых SpA шариках. Предварительное инкубирование шариков с SpA с PA8-G3 снизило связывание добавленных позже MABp1-IgG1 на 80,3%. В свою очередь, с шариками с SpA, предварительно инкубированными с MABp1-IgG1, добавленные позже PA8-G3 связывались с более чем >30% поверхности шариков с SpA в течение 15 минут, в то время как не наблюдалось значительное связывание добавленных позже MABp1-IgG3 (родственный по изотипу негативный контроль с Fab-фрагментом MABp1 и Fc-фрагментом IgG3 человека) с шариками с SpA, предварительно инкубированными с MABp1-IgG1.
[0068] Дополнительную серию экспериментов проводили для исследования способности дополнительных Ab к SpA способствовать фагоцитозу SA посредством дифференцированных клеток HL-60. В данных экспериментах дифференцированные клетки HL-60 совместно инкубировали с меченными зеленым pHrodo S. aureus и одним из следующих Ab: PA7.2-G3, PA4-G3, PA8-G3, PA15-G3, PA21-G3, PA27-G3, PA32-G3, PA37-G3 или MABpl. В данных экспериментах MABp1 применяли в качестве отрицательного контроля. Данные демонстрируют, что все исследованные Ab к SpA были способны способствовать опсонизации и фагоцитозу S. aureus посредством дифференцированных клеток HL-60 (фигура 6).
[0069] Дополнительно проводили эксперименты с использованием био-слой интерферометрии (проведенная с использованием прибора ForteBio Octet Red 96) для определения KD семи дополнительных Ab к SpA (проведенные с использованием 20 нМ антигена). Полученные в результате данные демонстрировали, что у PA7.2-G3 KD составляет менее 1×10-12 М, у PA4-G3 KD составляет 5,38×10-12 М, у PA15-G3 KD составляет менее 1×10-12 М, у PA21-G3 KD составляет менее 1×10-12 М, у PA27-G3 KD составляет менее 1×10-12 М, у PA32-G3 KD составляет менее 1×10-12 М и у PA37-G3 KD составляет менее 1×10-12 М.
[0070] В итоге, данные демонстрируют, что Ab, предусмотренные в данном документе, могут связываться с очень высокой аффинность с SpA в клеточной стенке SA, способствовать фагоцитозу посредством иммунных клеток и способны осуществлять это в присутствии IgG человека, связанных с SpA посредством их Fc-фрагмента.
[0071] Пример 2. Исследование выживаемости моноклонального антитела РА8 на модели с бактериемией/сепсисом у мышей. Исследовали выживаемость мышей с бактериемией S. aureus с использованием профилактических доз РА8 (моноклонального антитела, названного PA8-G3, что описано в примере 1).
[0081] Самок мышей BALB/c (возрастом 6-8 недель) приобретали в Charles River Laboratory, NIH, Мэриленд. По прибытии, мышей изучали, размещали по группам (10/клетку) в клетки с абсорбирующей подстилкой. Всех мышей помещали в условия, согласно необходимым стандартам содержания, описанным в руководстве по содержанию и использованию лабораторных животных NIH.
[0082] Профилактическую эффективность РА8 исследовали на модели с сепсисом SA, вызванным путем внутривенных инъекций (i.v.) 2×107 CFU штамма MRSA NR-46223. Мышей внутривенно обрабатывали РА8 в определенных дозах (5 мг или 10 мг) за 3 часа до инфицирования MRSA, или в двух дозах по 5 мг каждая в дни 0 и 3. Контрольных мышей обрабатывали только рецептурным буфером. За мышами следили на протяжении 10 дней (дважды в день), после чего умерщвляли всех оставшихся животных.
[0083] Через три часа после i.v. введения РА8/рецептурного буфера (0,1 мл), мышей заражали разовой внутривенной (IV) инъекцией штамма NR-46223 S. aureus (2×107 CFU в 0,1 мл). Одной группе мышей давали две дозы по 5 мг каждая в день 0 и 3. Между экспериментальными группами отмечали значительные отличия в относительной продолжительности выживаемости. Ссылаясь на фиг. 7A-D, пассивное введение разовой дозы mAb РА8 (внутривенно) в 5 мг (А) или 10 мг (В) или двух доз по 5 мг в день 0 и день 3 (С) значительно сильнее повышает выживаемость мышей BALB/c, по сравнению с обработкой с рецептурным буфером дозозависимо (10 мышей на группу), с сепсисом Staphylococcus aureus (вызванным путем внутривенных инъекций 2×107 колониеобразующих единиц метициллин-резистентного штамма S. Aureus NR-46223). Фигура (D) демонстрирует выживаемость с использованием всех различных обработок на одном графическом изображении. Выжило пятьдесят процентов (5/10) мышей, получавших 5 мг Mab РА8 (р=0,016), шестьдесят процентов, получавших две дозы по 5 мг каждая (р=0,09) и семьдесят процентов (7/10), получавших 10 мг mAb РА8 (р=0,003), по сравнению с 10% (1/10) мышей, выжившими в испытании с бактериальным заражением S. aureus NR-46223, получавших рецептурный буфер (1/10). Статистический анализ данных, полученных в ходе исследований на животных, проводили с использованием анализа выживаемости Каплана-Мейера и критерия Кокса-Мантеля (логранкового критерия). Данные результаты явно демонстрируют, что РА8 обеспечивает значительный уровень защиты от летальной инфекции со штаммом MRSA S. aureus.
[0084] Пример 3. Самкам мышей BALB/c (10 на группу) из Charles River Laboratory вводили инъекцию 0,5 мг ванкомицина посредством внутрибрюшинного пути введения вместе с различными суб-оптимальными дозами PA8-G3 (0 мг, 2,5 мг и 5 мг посредством внутривенного пути введения) за два часа до инфицирования MRSA (NR 46223 с 3×107 CFU i.v.). За мышами наблюдали на протяжении 14 дней. Ссылаясь на фигуры 8А-С, на 14 день выжило только 10% мышей, обработанных PBS, и 30% мышей, обработанных ванкомицином. Однако, когда проводили обработку инъекцией 2,5 мг PA8-G3 вместе с ванкомицином, выживало 60% животных (р=0,027), и когда вводили инъекцию 5 мг PA8-G3 с ванкомицином, выживало 60% животных, а те мыши, что умерли, проживали дольше, чем при более низких дозах (р=0,016). Эти данные демонстрируют, что суб-эффективные дозы PA8-G3 могут спасти животных от бактериемии, опосредованной SA, при совместной обработке с суб-оптимальной дозой ванкомицина. Статистический анализ данных, полученных в ходе исследований на животных, проводили с использованием анализа выживаемости Каплана-Мейера и критерия Кокса-Мантеля (логранкового критерия).
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
[0085] Следует понимать, что хотя настоящее изобретение было описано в связи с его подробным описанием, вышеуказанное описание предназначено для иллюстрации, а не для ограничения объема настоящего изобретения, который определяется объемом прилагаемой формулы изобретения. Другие аспекты, преимущества и модификации находятся в рамках объема следующей формулы изобретения.
Реферат
Изобретение относится к медицине и касается фармацевтической композиции для лечения и предупреждения инфекций, вызванных, содержащей фармацевтически приемлемый носитель и очищенное моноклональное антитело, содержащее вариабельный домен тяжелой цепи, содержащий CDR1, CDR2 и CDR3, и вариабельный домен легкой цепи, содержащий CDR1, CDR2 и CDR3, где моноклональное антитело специфично связывается с белком A (SpA)с Kменее чем 1×10М посредством паратопа его Fab-участка. Моноклональное антитело способно вытеснять иммуноглобулины IgG человека, связанные с SpA на поверхности бактерийпосредством их Fc-участков. Изобретение обеспечивает значительный уровень защиты от летальной инфекции со штаммом. 7 з.п. ф-лы, 3 пр.

Комментарии