Субстанция для получения средства, повышающего жизнеспособность и подвижность сперматозоидов млекопитающих - RU2725491C2
Код документа: RU2725491C2
Чертежи
Описание
Область техники, к которой относится изобретение
Изобретение относится к биотехнологии, в частности репродуктивной биологии.
Описан биологически активный белково-пептидный комплекс (ВПК), выделенный из ткани семенников млекопитающих, который в низких дозах, соответствующих диапазону концентраций 10-8-10-15 мг белка/мл, обладает стабильно выраженным эффектом повышения подвижности сперматозоидов в образцах эякулята. Выделенный и очищенный ВПК способствует повышению подвижности сперматозоидов в эякуляте. В то же время, действие данного ВПК характеризуется отсутствием негативных побочных эффектов, совместимостью с другими препаратами.
Изобретение относится к биологически активному ВПК, полученному из ткани семенников КРС, и может использоваться в медицине, фармакологии и ветеринарии в качестве субстанции для производства препарата для профилактики и лечения бесплодия, возникающего в результате астенозооспермии.
Уровень техники
Современная демографическая ситуация в России характеризуется резким падением рождаемости, и эта тенденция, по оценкам демографов, сохранится на протяжении многих лет. Причины такого положения разнообразны, в том числе довольно высокий уровень бесплодных браков. По данным ВОЗ частота бесплодных браков составляет в среднем 18% (10-20%) в разных регионах мира (Е.П. Келлэт, И.Е. Корнеева и др. Бесплодие неясного генеза. Проблемы репродукции, 2010, 1, 32-35). Многочисленные исследования в разных странах мира показали, что на протяжении последних десятилетий уровень мужской фертильности значительно снизился (Е.Ю. Пашкова, С.Ю. Калинченко. Мужское бесплодие в XXI веке - реалии и перспективы. Урология и нефрология, 2013, 1, 26-32). В настоящее время установлено, что одной из главных причин бесплодного брака является мужской фактор: более 50% среди всех возможных причин (И.В. Виноградов, М.Ю. Габлия. Роль мужского фактора при анализе неудач в протоколах ВРТ. Андрология и генит. хирургия, 2011, 2, 121). В последние несколько десятилетий в РФ по данным научного Центра акушерства, гинекологии и перинатологии им. Кулакова свыше 4 млн мужчин страдают бесплодием различной формы (В.И. Кулаков. Вспомогательные репродуктивные технологии - настоящее и будущее. М. 2005, 11-14) (И.А. Троицкий, А.А. Авдеева. Рождаемость и планирование семьи в России. История и перспективы. Демографические исследования. 2011, вып. 18, 177). Отмечается существенное падение подвижности сперматозоидов с одновременным повышением числа патологических форм сперматозоидов - такое патологическое состояние мужской половой системы называют астенотератозооспермией (М.В. Андреева, Л.Ф. Шилейко и др. Параметры спермограммы в период с июля по октябрь 2010 года по сравнению с таковыми в 2007-2009 гг. Андрология и генитальная хирургия 2013, 1, 11-14). Частным случаем астенотератозооспермии является астенозооспермия - малая подвижность сперматозоидов. Такая патология, как астенотератозооспермия занимает в структуре мужского бесплодия более 85% случаев (В.В. Евдокимов, Д.Т. Айбятов и др. Влияние факторов различной природы на фертильность эякулята человека. Андрология и генит. хирургия, 2015, 4, 41-45) (В.Л. Быков. Сперматогенез у мужчин в конце XX века. Проблемы репродукции, 2000, 1, 6-13). Сохранение фертильности самцов млекопитающих, в том числе человека, является сохранение параметров фертильности, в частности, поддержание жизнеспособности и подвижности сперматозоидов. Известно, что одной из причин низкой оплодотворяемости сперматозоидов выступает модификация ДНК свободными радикалами, образующимися при окислительном стрессе, возникающем при действии неблагоприятных факторов эндогенной и экзогенной природы. Развитие перекисного окисления липидов является универсальным. Причем окислительный стресс может приводить к гибели сперматозоидов путем апоптоза. Таким образом, актуальной задачей современной андрологии и репродукции человека является поиск агентов, способных повышать подвижность сперматозоидов, а также увеличивать их устойчивость к действию повреждающих факторов различной природы.
Известен ряд средств, в том числе белковой и пептидной природы, улучшающих репродуктивную функцию самцов млекопитающих, в частности человека, при астенозооспермии за счет повышения подвижности сперматозоидов.
Известен способ лечения бесплодия при астенозооспермии путем отбора живых неподвижных сперматозоидов с помощью гипоосмотического теста, при котором за счет воздействия на эякулят состава, содержащего фруктозу и цитрат натрия в соотношении 3:1, происходит набухание жгутиков живых сперматозоидов и, соответственно, возможность их выделения, например: Fertility and Sterility, 1997, №67, с. 1156-1158; матер. 23 межд. конф., Волгоград, 2013, с. 64-66. Данный способ обеспечивает возможность дифференцировки живых неподвижных сперматозоидов, пригодных для оплодотворения, однако процесс набухания жгутиков достаточно длительный: от 0,5 до 2 часов, трудоемкий и дорогостоящий.
Из литературных данных известны способы воздействия на подвижность сперматозоидов при помощи регуляторных пептидов (В.В. Евдокимов, С.В. Захариков, Л.А. Андреева, Н.Ф. Мясоедов, В.Б. Туровецкий. Влияние регуляторных пептидов на подвижность сперматозоидов человека in vitro. Экспериментальная и клиническая урология, 2016, 2, 67-69). Было исследовано влияние известных регуляторных пептидов семакс и селанк, а также целой группы синтезированных олигопептидов, на подвижность сперматозоидов при добавлении этих пептидов в раствор эякулята. Исследование показало, что только регуляторный пептид семакс обладал ярко выраженным действием, направленным на увеличение как активной, так и общей подвижности сперматозиодов.
Известен способ улучшения подвижности сперматозоидов путем воздействия на пробу раствором плацентарного α2-макроглобулина (Патент RU №2167675, МПК А61K 39/395, А61P 15/08, опубл. 10.11.1999, «Способ улучшения подвижности сперматозоидов»). Недостатками данного способа являются высокая стоимость получения препарата и, как следствие, его недоступность для всех нуждающихся пациентов.
Наиболее близким аналогом-прототипом является способ повышения подвижности сперматозоидов путем использования химического теста с введением в эякулят пентоксифиллина, при добавлении которого происходит кратковременное увеличение подвижности сперматозоидов за счет увеличения концентрации внутриклеточного цАМФ, например: Fertility and Sterility, 1992, №57, с. 2409-2416; Human Reproduction 1996, №11, с. 1655-1660. Однако известный способ для лечения бесплодия при астенозооспермии малоэффективен, так как довольно субъективен и требует наличия опытного лаборанта, а кроме того, при его использовании возможно возникновение побочных явлений.
Известен биорегулятор (М.С. Краснов, В.П. Ямскова, Б.Б. Березин, Н.В. Ямскова, И.А. Ямсков. Клеточные технологии в биологии и медицине, 2014, 1, 63-67), выделенный из семенников крыс, который в низких дозах оказывал протекторное действие на состояние ткани при роллерном органотипическом культивировании семенников крысы in vitro. В качестве протектора в данной работе выступает фракция супернатанта, выделенная из ткани семенников крысы. Однако в данной работе не была проведена дальнейшая очистка биорегулятора и его идентификация.
Задачей заявленного изобретения и достигаемым техническим результатом_ является получение биологически активного белково-пептидного комплекса (ВПК), обеспечивающего повышение подвижности сперматозоидов, позволяющий оперативно получить выраженный и стойкий клинический эффект при отсутствии побочных действий. Данный ВПК может быть использован как субстанция для разработки средства воздействия на самцов млекопитающих, в частности мужчин, страдающих бесплодием вследствие астенозооспермии, основанном на отборе пригодных для оплодотворения клеток путем проведения тестированного воздействия на эякулят.
Техническая задача решается получением ВПК из семенников млекопитающих, который проявляет активность в диапазоне концентраций от 10-8 до 10-15 мг/мл. Существенным отличием заявляемого изобретения является то, что в качестве активного компонента используется высокоочищенный ВПК, выделенный из семенников млекопитающих (быка), проявляющий биологическое действие в низких дозах, соответствующих диапазону концентраций 10-8-10-15 мг/мл, которое выражается в повышении подвижности и жизнеспособности сперматозоидов.
Техническим результатом при использовании изобретения является ярко выраженный эффект стабильного повышения подвижности сперматозоидов на 29-38%, в отдельных случаях на 70-100% вследствие добавления раствора заявляемого БПК к эякуляту. Эффект продолжается в течение 2-3 часов наблюдения. Этого временного интервала достаточно для проведения процедуры ИКСИ - интрацитоплазматической инъекции сперматозоида в яйцеклетку. Заявляемый БПК характеризуется отсутствием токсичности, совместимостью с другими препаратами и отсутствием негативных побочных эффектов.
Таким образом, задачей изобретения и техническим результатом является создание нетоксичного средства белково-пептидной природы, получаемого из доступного природного сырья, способствующего повышению подвижности и жизнеспособности сперматозоидов в эякуляте человека, которое является эффективным при использовании в низких дозах.
Существенным преимуществом заявляемого изобретения является то, что в качестве вещества, повышающего подвижность и жизнеспособность сперматозоидов в эякуляте человека, используется очищенный БПК, выделенный из семенников млекопитающих (быка), и проявляющий биологическое действие в низких дозах при разведении в водном фармацевтически приемлемом носителе и/или разбавителе до концентрации общего белка от 10-8 до 10-15 мг/мл. Заявляемый БПК содержит полученные из ткани семенников быков пептиды с молекулярными массами 1000-10000 Да и бычий сывороточный альбумин gi|1351907 с молекулярной массой 65712 Да, аминокислотная последовательность N-концевого мотива: DTHKSEIAHRFKDLGE. Соотношение пептидов и белка в составе выделенного БПК составляет от 1:1 до 1:7. Показано, что у заявляемого БПК отсутствуют аллергенные, сенсибилизирующие и иммунотоксические свойства, он также не обладает мутагенным действием и потенциальной канцерогенной активностью.
Изобретение иллюстрируется фигурами и следующими примерами:
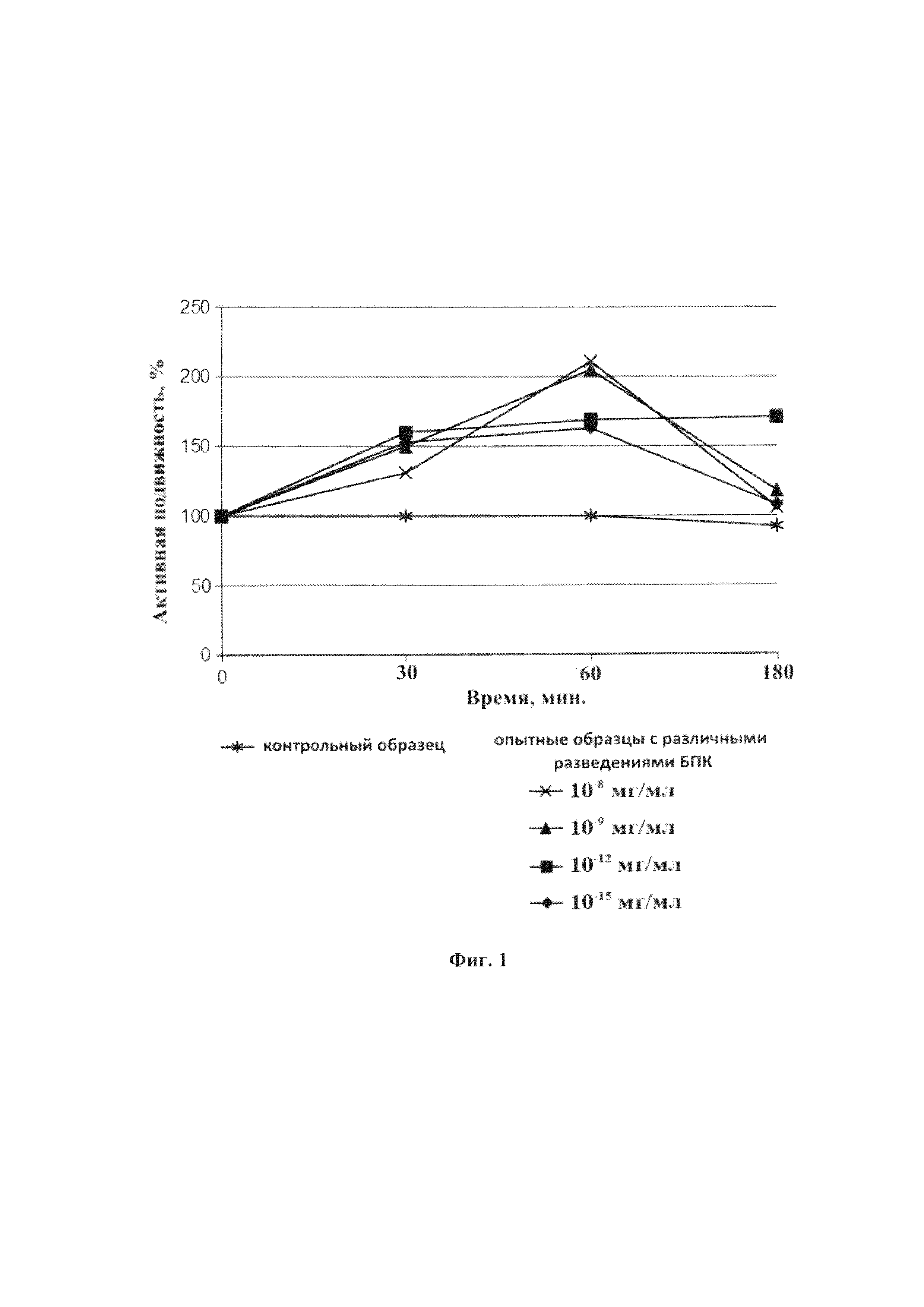
Фиг. 1. Диаграмма, отражающая дозовую зависимость действия белково-пептидного комплекса, выделенного из семенников быков (Bos Taurus), на активную подвижность (%) сперматозоидов в эякуляте человека in vitro в зависимости от времени инкубации эякулята без (контрольный образец) и с добавлением (опытные образцы). По оси абсцисс - время инкубации (мин), по оси ординат - активная подвижность сперматозоидов (%).
Пример 1. Способ получения белково-пептидного комплекса из семенников крупного рогатого скота. В работе используют семенники половозрелых быков (Bos Taurus), полученные при забое крупного рогатого скота (КРС) на мясокомбинатах Подмосковья. Ткани семенников нарезают на небольшие фрагменты, размером 1,5-2,0 см2, для экстракции помещают в раствор следующего состава: 0,15 М NaCl, 2,5×10-3 М KCl, 2×10-3 М CaCl2, 1×10-3 М HEPES. Экстракцию проводят в течение 3-х часов при температуре +4°С. Полученный экстракт фильтруют, центрифугируют при 3000 g в течение 30 мин. К охлажденному раствору тканевого экстракта постепенно добавляют сухой сернокислый аммоний при постоянном перемешивании до образования насыщенного раствора соли (на каждые 100 мл раствора экстракта добавляют 78 г соли). Суспензию белков оставляют на 72 час при +4°С, после чего центрифугированием при 12000g в течение 30 минут отделяют фракции супернатанта и осадка. Фракцию супернатанта в течение 7-8 суток диализуют против дистиллированной воды, а фракцию осадка - против буферного раствора (0,01 М Tris, рН 7,4) до полного удаления ионов сульфата аммония. Присутствие в растворе ионов аммония определяют качественной реакцией с реактивом Несслера. Полученные после диализа фракции супернатанта и осадка далее концентрируют, используя роторный вакуумный испаритель, при температуре не выше 40°С. Концентрацию белка во всех фракциях на отдельных стадиях очистки и исследования определяют спектрофотометрически (Р. Досон, Д. Эллиот, У. Эллиот, К. Джонс. Справочник биохимика М. Мир, 1991). Фракцию осадка семенников КРС разделяют методом обращенно-фазовой ВЭЖХ на колонке Kromasil С4 (4,6×250 мм) с использованием хроматографа высокого давления Agilent 1200 (США). Элюцию осуществляют в градиенте концентрации ацетонитрила (0-60%) в 0,1%-ной трифторуксусной кислоте (рН 2,2) со скоростью 1 мл/мин в течение 60 мин. Детекцию проводят при 280 и 214 нм. Собирают фракцию с временем удерживания 52,1 мин, из нее в вакуумном испарителе удаляют ацетонитрил и трифторуксусную кислоту и растворяют в физиологическом водно-солевом растворе.
Пример 2. Определение состава и структуры очищенного белково-пептидного комплекса. ВЭЖХ-фракцию с временем удерживания 52,1 мин, полученную из экстракта семенников КРС, исследуют методом MALDI TOF масс-спектрометрии на времяпролетном масс-анализаторе UltraFlex 2 (Bruker Daltonic, Германия) с использованием в качестве матрицы α-циано-4-гидроксикоричной кислоты. Получают масс-спектрометрический сигнал, соответствующий молекулярной массе 65712 Да. Также данную фракцию анализируют методом электрофореза в 15%-ном полиакриламидном геле в денатурирующих условиях (U.K. Laemmli. Cleavage of Structural Proteins during the Assembly of the Head of Bacteriophage T4. Nature, 1970, 227, 680-685). Из геля вырезают полосу, соответствующую молекулярной массе примерно в 65-66 кДа. Проведенный триптический гидролиз белка в геле с последующим масс-спектрометрическим исследованием продуктов гидролиза показывает, что выделенный белок с молекулярной массой около 65712 Да представляет собой белок семейства альбуминов млекопитающих под номером gi|1351907 в базе данных SwissProt. Методом Эдмана устанавливают частичную N-концевую аминокислотную последовательность этого белка (DTHKSEIAHRFKDLGE), которая имеет 100%-ную гомологию с N-концевой последовательностью зрелой молекулы БСА быка.
ВЭЖХ-фракцию со временем удерживания 52,1 минуты собирают и подвергают денатурации в буфере, содержащем 6 М GuHCl, 300 мМ NaCl, 3 мМ ЭДТА, для идентификации пептидных компонентов. Инкубация в данном буфере проводится в течение 24 часов при температуре 45°С. После завершения инкубации полученный раствор снова подвергают разделению с помощью метода обращенно-фазовой ВЭЖХ на колонке Kromasil С4 в условиях, аналогичным в примере 1. Полученные ВЭЖХ-фракции с малым временем удерживания анализируют MALDI TOF масс-спектрометрией в условиях, аналогичных для разделения ВЭЖХ-фракции со временем удерживания 52,1 минуты. При анализе данных фракций фиксируют масс-спектрометрические сигналы, соответствующие молекулярным массам от 1000 до 10000 Да.
Таким образом, в ткани семенников КРС был обнаружен БПК, который содержит пептиды с молекулярными массами от 1000 до 10000 Да и белок - представитель семейства альбуминов млекопитающих под номером gi|1351907 в базе данных SwissProt с молекулярной массой 65712 Да.
Пример 3. Способ получения белково-пептидного комплекса из семенников крупного рогатого скота методом изоэлектрофокусирования. Из тканевого экстракта семенников быков Bos Taurus получают фракцию супернатанта, как описано в примере 1. Сконцентрированный на роторном вакуумном испарителе супернатант далее разделяют методом изоэлектрофокусирования (ИЭФ) в градиенте плотности сахарозы на колонке LKB-440 («LKB», Швеция), используя амфолины диапазона рН 3,5-10,0 (Serva, Германия) (Остерман Л.А. Исследование биологических макромолекул электрофокусированием, иммуноэлектрофорезом и радиоизотопными методами. М.: Изд. "Наука", 1983, с. 304). Для разделения готовят следующие растворы: тяжелый электродный раствор - 60% сахарозы в 0,1%-ный р-р Н3РO4; легкий электродный раствор - 0,1%-ный NaOH; тяжелый градиентный раствор - 75 г. сахарозы, 100 мл супернатанта, доводят до 200 мл дистиллированной водой; легкий градиентный раствор - 15 г сахарозы, до 200 мл дистиллированной воды. В колонку наслаивают растворы в следующем порядке: тяжелый электродный раствор, тяжелый и легкий градиентные растворы, которые подают из градиентного смесителя, и затем легкий электродный раствор. ИЭФ проводят при +4°С в течение 96 часов при напряжении 500-1500 В. Собирают фракции объемом 10 мл. Детекцию белков осуществляют на любом спектрофотометре при 280 нм, для каждой фракции определяют значение рН с помощью рН-метра. Согласно полученной картине разделения собирают фракцию в интервале значений рН<3,0, которую далее диализуют против дистиллированной воды до удаления сахарозы в соотношении объемов 1:10 с пятикратной сменой воды. Проводят электрофорез в 15%-ном полиакриламидном геле в денатурирующих условиях ИЭФ-фракции, собранной в интервале значений рН<3,0. Из геля вырезают полосу, соответствующую молекулярной массе приблизительно в 66000 Да. Данную фракцию анализируют методом масс-спектрометрии на времяпролетном масс-анализаторе UltraFlex 2 (Bruker Daltonic, Германия) с использованием в качестве матрицы α-циано-4-гидроксикоричной кислоты, обнаруживают ряд пептидов с молекулярными массами в диапазоне 1000-10000 Да. Проведенный триптический гидролиз белка в геле с последующим масс-спектрометрическим исследованием продуктов гидролиза показывает, что выделенный белок с молекулярной массой 65712 Да представляет собой белок семейства альбуминов млекопитающих под номером gi|1351907 в базе данных SwissProt.
Проводят ИЭФ в градиенте плотности сахарозы на колонке LKB-110 («LKB», Швеция), используя амфолины диапазона рН 3,5-10,0 (Serva, Германия), определяют значение pI для белка, который предварительно был элюирован из полиакриламидного геля после электрофореза ИЭФ-фракции со значением рН<3,0. Значение pi данного белка находится в интервале рН 3,9-4,0.
Таким образом, ИЭФ-фракция, собранная в интервале значений рН<3,0 представляет собой БПК, состоящий из белка gi|1351907 - представителя семейства альбуминов сыворотки крови быка со значением pI в области рН 3,9-4,0 и смеси пептидов с молекулярной массой 1000-10000 Да.
Пример 4. Выделение белково-пептидного комплекса из ткани семенников крыс Wistar, определение его состава и структуры. Эксперимент проводят на крысах Wistar, самцы, весом 180-220 г. Крыс забивают эфирным наркозом, вырезают семенники, которые далее нарезают на небольшие фрагменты, размером 1,5-2,0 см2, для экстракции помещают в раствор следующего состава: 0,15 М NaCl, 2,5×10-3 М KCl, 2×10-3М CaCl2, 1×10-3 М HEPES. Экстракцию проводят в течение 3-х часов при температуре +4°С. Полученный экстракт фильтруют, центрифугируют при 3000 g в течение 30 мин. К охлажденному раствору тканевого экстракта постепенно добавляют сухой сернокислый аммоний при постоянном перемешивании до образования насыщенного раствора соли (на каждые 100 мл раствора экстракта добавляют 78 г соли). Суспензию белков оставляют на 72 час при +4°С, после чего центрифугированием при 12000 g в течение 30 минут отделяют фракции супернатанта и осадка. Фракции концентрируют, используя роторный вакуумный испаритель, при температуре ниже 40°С, далее разделяют с методом изоэлектрофокусирования (ИЭФ) в градиенте плотности сахарозы на колонке LKB-440 («LKB», Швеция), используя амфолины диапазона рН 3,5-10,0 (Serva, Германия). Для разделения готовят следующие растворы: тяжелый электродный раствор - 60% сахарозы в 0,1%-ный р-р Н3РO4; легкий электродный раствор - 0,1%-ный NaOH; тяжелый градиентный раствор - 75 г. сахарозы, 100 мл супернатанта, доводят до 200 мл дистиллированной водой; легкий градиентный раствор - 15 г сахарозы, до 200 мл дистиллированной воды. В колонку наслаивают растворы в следующем порядке: тяжелый электродный раствор, тяжелый и легкий градиентные растворы, которые подают из градиентного смесителя, и затем легкий электродный раствор. ИЭФ проводят при +4°С в течение 96 часов при напряжении 500-1500 В. Собирают фракции объемом 10 мл. Детекцию белков осуществляют на любом спектрофотометре при 280 нм, для каждой фракции определяют значение рН с помощью рН-метра. Согласно полученной картине разделения собирают фракцию в интервале значений рН<3,0, которую далее диализуют против дистиллированной воды до удаления сахарозы в соотношении объемов 1:10 с пятикратной сменой воды. Данную фракцию анализируют методом масс-спектрометрии на времяпролетном масс-анализаторе UltraFlex 2 (Bruker Daltonic, Германия) с использованием в качестве матрицы α-циано-4-гидроксикоричной кислоты, обнаруживают ряд пептидов с молекулярными массами в диапазоне 1000-10000 Да. Проводят электрофорез в 15%-ном полиакриламидном геле в денатурирующих условиях ИЭФ-фракции, собранной в интервале значений рН<3,0. Из геля вырезают полосу, соответствующую молекулярной массе приблизительно в 67000 Да. Проведенный триптический гидролиз белка в геле с последующим масс-спектрометрическим исследованием продуктов гидролиза показывает, что выделенный белок с молекулярной массой 66710 Да представляет собой белок семейства альбуминов млекопитающих под номером gi|124028612 в базе данных SwissProt.
Проводят ИЭФ в градиенте плотности сахарозы на колонке LKB-110 («LKB», Швеция), используя амфолины диапазона рН 3,5-10,0 (Serva, Германия), определяют значение pI для белка, который предварительно был элюирован из полиакриламидного геля после электрофореза ИЭФ-фракции со значением рН<3,0. Значение pI данного белка находится в интервале рН 4,0-4,1.
Таким образом, ИЭФ-фракция, собранная в интервале значений рН<3,0 представляет собой БПК, состоящий из белка gi|124028612 - представителя семейства альбуминов сыворотки крови крысы с молекулярной массой 66710 Да, значением pI в области рН 4,0-4,1 и смеси пептидов с молекулярной массой 1000-10000 Да.
Пример 5. Получение растворов различной концентрации высокоочищенного БПК, выделенного из семенников быков. В качестве раствора БПК используют ВЭЖХ-фракцию со временем удерживания 52,1 минуты, выделенную из ткани семенников КРС (описана в Примере 2) с концентрацией по белку 130±10 мкг/мл. Из данного раствора отбирают 100 мкл и вносят в 900 мкл дистиллированной воды, встряхивают полученный раствор 25 раз. Данную процедуру повторяют 15 раз, получая, таким образом, растворы БПК с 10-кратным последовательным разбавлением от 1 до 15 степени. В полученные растворы с различной концентрацией БПК добавляют хлорид кальция до его конечной концентрации 1 мМ. В экспериментах по изучению биологической активности раствора БПК, выделенного из семенников быков, были исследованы его разведения в концентрациях, соответствующих значениям 10-8-10-15 мг/мл.
Пример 6. Влияние БПК, выделенного из семенников быков, на подвижность сперматозоидов в эякуляте человека in vitro. Исследования биологического действия БПК проводят на сперматозоидах человека in vitro. Эякулят получают общепринятым способом по рекомендации ВОЗ, оценку подвижности сперматозоидов осуществляют согласно тем же стандартам рекомендаций ВОЗ (Рекомендации ВОЗ по исследованию и обработке эякулята человека. М., 2012, 5-е изд., 291). Эксперименты были проведены на образцах эякулята от 46 пациентов. Исследование проводят при комнатной температуре +20-22°С. Из полученного от каждого из пациентов образца эякулята отбирают по 1 мл для опыта и контроля. Согласно рекомендациям ВОЗ проводят процедуру разжижения образцов эякулята, инкубируя их при комнатной температуре в течение 30-40 минут. В контрольный образец не вносят ничего, в опытный образец к 1 мл эякулята добавляют 10 мкл водного раствора заявляемого БПК за два порядка до исследуемой концентрации (приготовленные, как описано в Примере 5), что отражено в таблице 1. Исследуют заявляемый БПК с конечными концентрациями общего белка 10-8, 10-9, 10-12 и 10-15 мг/мл в опытных образцах эякулята. После добавления заявляемого БПК к эякуляту, все образцы инкубируют в течение 3 часов при комнатной температуре +20-22°С.
После этого проводят микроскопическое исследование каждого образца на оптическом микроскопе («Amplival Karl Zeiss lena», Германия) при увеличении ×400. Образцы опытной и контрольной групп микроскопируют сразу после процедуры разжижения, а также спустя 30 минут, 1 час и 3 часа. Подвижность сперматозоидов рассчитывают как содержание в эякуляте подвижных клеток на 100 проанализированных клеток. Выделяют активную подвижность и общую подвижность, значение которой является суммой активной и малой подвижности. Полученные результаты представлены в виде средних арифметических значений исследованных параметров и их среднеквадратических ошибок, а графически отражены на фиг. 1.
Для удобства сравнения результатов вводят параметр ϕ, который рассчитывают по формуле: ϕх=Nx/100, где Nx - число подвижных сперматозоидов на каждые 100 подсчитанных клеток. При этом ϕк - значение параметра для образцов контрольной группы сразу после проведения разжижения и по прошествии 3 часов инкубации, а ϕ30, ϕ60, ϕ180 - значения параметра для образцов опытной группы по прошествии 30 минут, 1 часа и 3 часов, соответственно. Результаты экспериментов приведены в таблице 1. Данные обрабатывают методами вариационной статистики с использованием t-критерия Стьюдента. Различия между средними арифметическими значениями параметров считают достоверными при р<0,05.


Полученные данные показывают, что БПК, выделенный из семенников быков, оказывает влияние на подвижность сперматозоидов человека in vitro во всех изучаемых концентрациях. Следует отметить, что доза, соответствующая 10-12 мг/мл проявляла активность, как через 30 и 60 минут после начала инкубации, так и через 180 минут, в отличие от растворов других доз БПК. Наиболее эффективными по максимальной величине активной подвижности оказались дозы, соответствующие 10-8 и 10-9мг/мл белка. Можно предположить, что заявляемый БПК обладает выраженной мембранотропной активностью, то есть влияет на свойства клеточной мембраны, в данном случае, проявляет способность стабилизировать состояние мембраны сперматозоидов, что, в свою очередь, влияет на их подвижность.
Пример 7. Оценка жизнеспособности сперматозоидов в эякуляте человека in vitro. Как в нативной сперме, так и после различных воздействий in vitro: хранение при комнатной температуре, криоконсервация и обработка химическими агентами, часть сперматозоидов подвергается апоптозу, который на ранних стадиях характеризуется активацией эндонуклеаз, расщеплением ДНК, протеолитической деградацией ядерной оболочки, а на завершающей стадии процесса наблюдается нарушение проницаемости клеточной мембраны с последующей деструкцией клетки. Одним из главных критериев оценки качества эякулята, рекомендованных ВОЗ, является подсчет процента жизнеспособных сперматозоидов с сохраненной клеточной мембраной, непроницаемой для витальных красителей и проницаемой для некоторых флюоресцентных красителей (М.В. Плосконос, А.А. Николаев. Растворимые маркеры апоптоза в семенной плазме мужчин. Пробл. Репродукции, 2011, №3, 85-87).
Эксперименты были проведены на образцах эякулята от 27 пациентов, получение и разжижение эякулята было проведено согласно общепринятым рекомендациям ВОЗ, аналогично описанному в Примере 4. Из каждого полученного образца эякулята отбирают по 1 мл для опыта и контроля. Для исследования жизнеспособности спермы в проточном цитометре Coulter Epix XL («Вескглап Coulter», США) применяют метод последовательного двойного окрашивания с применением зеленого флюоресцентного красителя С-14 («Molecular Probes», США) и красного флюоресцентного красителя пропидий иодида (ПИ). Краситель С-14 проникает через неповрежденную мембрану, окрашивая нуклеиновые кислоты, таким образом, он способен окрашивать неповрежденные сперматозоиды в эякуляте. Пропидий иодид окрашивает ДНК только в клетках с поврежденной мембраной. При применении обоих красителей жизнеспособные сперматозоиды окрашиваются только С-14, а сперматозоиды с поврежденной мембраной (нежизнеспособные) и красителем С-14, и ПИ. Опытные и контрольные образцы эякулята после разжижения разводят солевым буфером HEPES в соотношении 1:1 и окрашивают С-14 в концентрации 0,02 мМ, инкубируя 10 минут при 37°С, после этого добавляют ПИ в концентрации 2,4 мМ с последующей инкубацией 10 минут. После этого в контрольный образец не вносят ничего, в опытный образец эякулята добавляют водный раствор заявляемого БПК (приготовлен, как описано в Примере 5) в объеме, необходимом для достижения исследуемой концентрации БПК в конечном растворе. Исследуют заявляемый БПК с конечными концентрациями общего белка 10-9 и 10-12 мг/мл в опытных образцах эякулята. Опытный и контрольный образцы эякулята инкубируют 48 часов при комнатной температуре. Производят подсчет жизнеспособных клеток на проточном цитометре в свежевыделенном эякуляте после его разжижения, подсчитывая % окрашенных клеток, а также подсчет жизнеспособных клеток в опытном и контрольном образцах после 24-часовой и 48-часовой инкубации при комнатной температуре. Результаты экспериментов обрабатывают методами вариационной статистики с использованием t-критерия Стьюдента, различия между средними арифметическими значениями параметров считают достоверными при р<0,05. Подсчет числа жизнеспособных сперматозоидов приведен в Таблице 2.
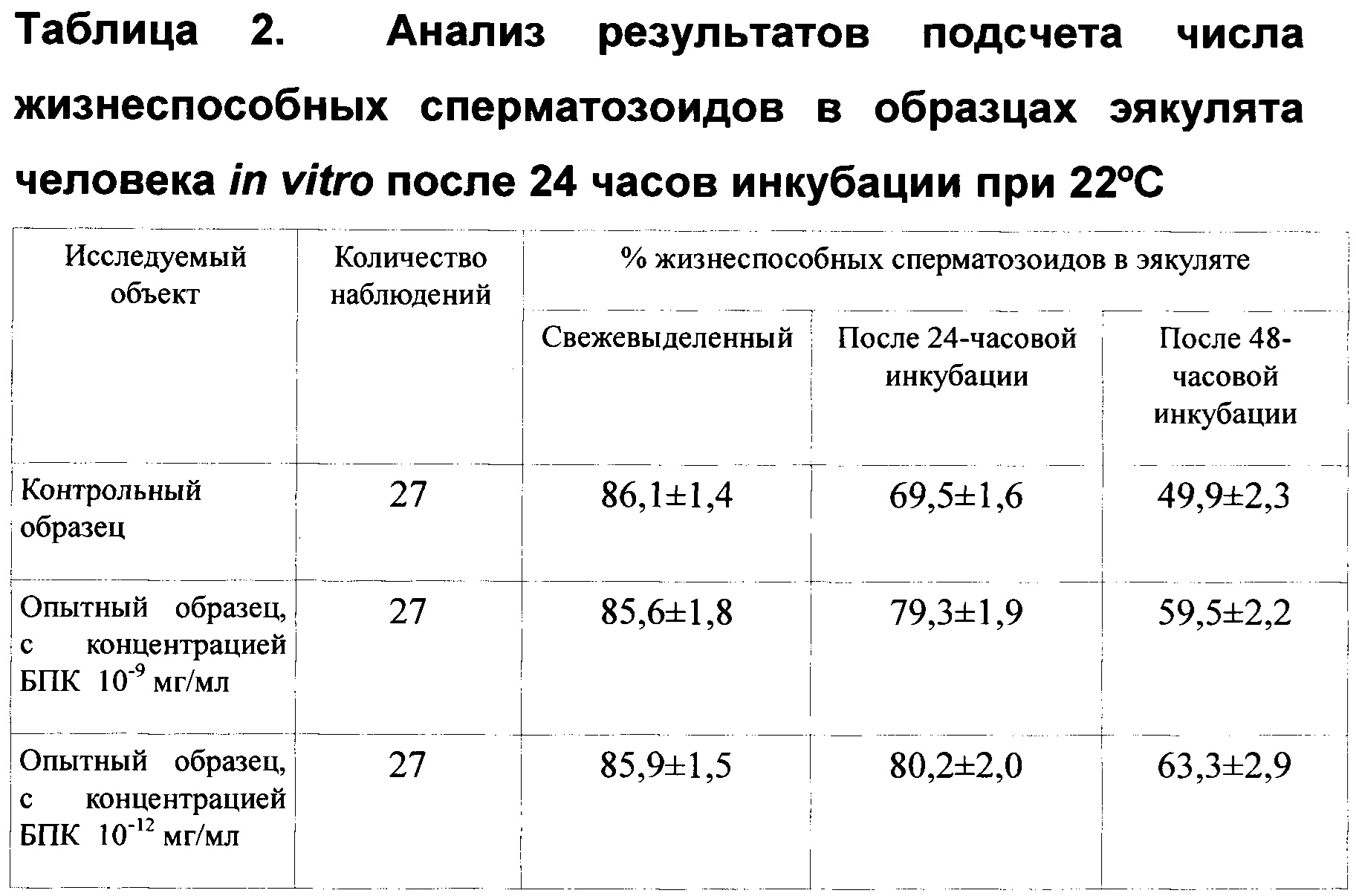
Таким образом, полученные результаты показывают, что заявляемый БПК способствует увеличению жизнеспособности сперматозоидов человека in vitro после 24 и 48 часов инкубации при комнатной температуре в дозах, соответствующих концентрациям 10-9 и 10-12 мг/мл. Можно отметить, что заявляемый БПК является основой биорегулятора, который относится к группе биорегуляторов, обнаруженных в тканях млекопитающих (В.П. Ямскова, М.С. Краснов, И.А. Ямсков. Saarbucken: Lambert Academic Publishing, 2012). Он представляет собой внеклеточно локализованный БПК, который в низких концентрациях оказывает влияние на основные биологические процессы. В условиях in vitro заявляемый БПК оказывает выраженное биологическое действие, направленное на поддержание жизнеспособности сперматозоидов. Такой характер биологического действия обусловлен способностью заявляемого БПК модулировать свойства плазматической мембраны и тем самым поддерживать внутриклеточный гомеостаз.
Пример 8. Получение растворов различных концентраций белково-пептидного комплекса, выделенного из семенников быков, для исследования его безопасности. В качестве раствора белково-пептидного комплекса используют ВЭЖХ-фракцию со временем удерживания 52,1 минуты, выделенную из ткани семенников быков (описана в Примере 2) с концентрацией по белку 130±10 мкг/мл. Во флакон, содержащий 0,1 мл водного раствора БПК, добавляют 0,9 мл 0,9%-ного раствора NaCl и интенсивно встряхивают 25 раз. Отбирают 0,1 мл образовавшегося раствора в следующий флакон и добавляют 0,9 мл 0,9%-ного раствора NaCl, встряхивают 25 раз. Данную процедуру повторяют 15 раз, получая таким образом растворы белково-пептидного комплекса с 10-кратным последовательным разбавлением от 1 до 15 степени. В экспериментах по изучению безопасности раствора БПК, выделенного из семенников быков, были исследованы его разведения в концентрациях, соответствующих значениям 10-3; 10-5-10-15 мг/мл. Растворы стерилизуют путем пропускания через стерильные мембранные фильтры GV с диаметром пор 0,22 мкм («Мillipore», США).
Исследования безопасности БПК, выделенного из семенников быков, проводят на кроликах породы «Шиншилла», морских свинках, крысах Wistar и белых беспородных мышах. Животные получены из питомника «Крюково», согласно паспорту молодые, половозрелые. Их содержат в стандартных металлических клетках по 5 особей (кролики содержатся индивидуально). Для кормления используют гранулированный комбинированный корм и свежие овощи. Доступ к воде и корму свободный. Освещение вивария искусственное, температура воздуха 18-22°С. До начала испытаний все животные проходят двухнедельный карантин. В целях стандартизации, перед началом опыта, животных не кормят в течение суток. Результаты эксперимента обрабатывают методами вариационной статистики по t-критерию Стьюдента.
Пример 9. Оценка местнораздражающего действия заявляемого БПК. Проведенные исследования показывают, что при подкожном, внутривенном и интраназальном введении биологически активного белково-пептидного комплекса в концентрациях 10-9 и 10-12 мг/мл (приготовление описано в примере 6) не оказывается местного раздражающего действия. Не обнаружено местного раздражающего действия на слизистую носа и горла при интраназальном введении БПК кроликам в течение 1 месяца.
Пример 10. Оценка способности заявляемого БПК вызывать активную кожную анафилаксию у морских свинок in vivo. Исследование проводят на морских свинках в количестве по 10 голов в каждой исследуемой группе, всего 2 группы. Сенсибилизируют животных по схеме: первая инъекция подкожно, две последующие внутримышечно через день в область бедра. На 14 день на выстриженных участках спины морским свинкам вводят внутрикожно раствор БПК в концентрации 10-9 мг/мл. Для контроля вводят физиологический раствор тому же животному на другой выстриженный участок кожи, контрольным животным вводят разрешающую инъекцию препарата (равную сенсибилизирующей дозе). Затем животным вводят внутривенно по 0,5 мл 1% раствора синего Эванса. Через 30 минут животных выводят из эксперимента эфирным наркозом и определяют размер синего пятна на внутренней стороне кожи в месте введения. Положительной считают реакцию при размере пятна выше 6 мм, не более 3 мм в контроле. При подсчете результатов эксперимента у обеих групп животных положительных реакций не наблюдалось. При статистической обработке полученных результатов не обнаружена достоверная разница между результатами опытных и контрольной групп (р>0,05).
Пример 11. Влияние заявляемого БПК на реакцию гиперчувствительности замедленного типа у мышей. Опыты проводили на нелинейных мышах массой 18-20 г, по 10 животных в группе. Общее количество животных в опыте -30. Животных однократно сенсибилизировали внутрикожно в основании хвоста эмульсией заявляемого БПК в неполном адъюванте Фрейда (НАФ) в соотношении 1:1. Доза введения составила 100 мкл. Контрольных животных сенсибилизировали эмульсией НАФ с раствором Хенкса в соотношении 1:1. Для выявления сенсибилизации через 5 суток мышам в подушечку задней лапы ввели 40 мкл раствора БПК в растворе Хенкса. Через 24 часа после тестирования измеряли величину отека с помощью инженерного микрометра МК-0-25. При статистической обработке полученных результатов не обнаружена достоверная разница в толщине лапок опытных и контрольной групп (р>0,05). Введение заявляемого БПК не вызывает реакции гиперчувствительности замедленного типа.
Пример 12. Влияние заявляемого БПК на реакцию дегрануляции тучных клеток у крыс in vitro. Эксперименты проводят на крысах Wistar, самки, весом 180-200 г, общее количество животных в опыте - 30. Вводят раствор БПК внутрибрюшинно, контролем служит интактная группа. Для получения взвеси тучных клеток животных декапитируют, в брюшную полость вводят буфер; после массажа передней брюшной стенки взвесь тучных клеток собирают центрифугированием в пробирки (3000 g, 30 мин). Препараты готовят на предметных стеклах, окрашенных 0,3%-ным спиртовым раствором нейтрального красного. К 0,03 мл взвеси тучных клеток добавляют 0,03 мл сыворотки опытного животного и 0,03 мл исследуемого раствора БПК в концентрации 10-9 мг/мл, в разведении 1:100. Препараты накрывают покровным стеклом, края герметизируют, инкубируют 15 минут в термостате при 37°С. Препараты исследуют микроскопически при увеличении ×40, подсчитывая тучные клетки, подвергшиеся дегрануляции и нормальные, сумму принимают за 100%. Реакцию считают положительной, если степень дегрануляции превышает 20%. В контроле дегрануляция не превышала 5%, значения параметра дегрануляции в опытной группе не отличаются от контроля и не превышают порогового значения 5%. Результаты контрольной и опытной групп статистически не имеют достоверных отличий (р>0,05).
Пример 13. Влияние заявляемого БПК на фагоцитарную активность макрофагов крысы in vitro. Эксперименты проводят на крысах Wistar, самки, весом 180-200 г, по 10 животных в каждой группе. Общее число животных в опыте 20. Метод основан на определении оптической плотности лизирующего раствора после разрушения фагоцитов, поглотивших частицы нейтрального красного. Крыс, подвергнутых воздействию исследуемого препарата, декапитируют. Асептически внутрибрюшинно вводят 5 мл среды 199, содержащей 20% эмбриональной телячьей сыворотки. После массажа брюшной полости среду отбирают шприцем. Порции клеточной суспензии, полученные от всей группы животных, объединяют в общий пул. Концентрацию живых клеток доводят до 1,5×103 клеток/мл. Суспензию клеток стерильно разливают по 2 мл в пластиковые чашки Петри диаметром 40 мм и инкубируют 2 часа при 37°С. Надосадочную фракцию, содержащую не адгезировавшие к пластику клетки, сливают, а фиксированный на пластике монослой дважды промывают средой 199. В слегка подсушенные чашки наливают раствор, содержащий нейтральный красный, и выдерживают при 37°С в течение 1 часа, затем раствор сливают, клетки промывают средой 199. В каждую чашку вносят по 3 мл лизирующего раствора, которым обрабатывают тщательно клетки, совершая вращательное движение чашки. Раствор сливают в пробирки и на спектрофотометре при длине волны 540 нм измеряют оптическую плотность. При внутрибрюшинном введении БПК в концентрации 10-9 мг/мл не было отмечено изменения фагоцитарной активности макрофагов по сравнению с животными контрольной группы. Статистически достоверных различий между показателями в опытной и контрольной группах нет (р>0,05).
Таким образом, при воздействии заявляемого БПК, выделенного из ткани семенников быков, наблюдается ярко выраженный эффект стабильного повышения подвижности и сперматозоидов человека in vitro на 29-38%, в отдельных случаях на 70-100% в течение 2-3 часов наблюдения, что достаточно для проведения процедуры ИКСИ -интрацитоплазматической инъекции сперматозоида в яйцеклетку. Также при действии заявляемого БПК наблюдается эффект увеличения жизнеспособности сперматозоидов человека in vitro. Решающим фактором действия заявляемого БПК является его мембранотропный эффект, то есть его способность модулировать свойства клеточных мембран.
Заявляемый белково-пептидный комплекс, выделенный из семенников быков, может быть использован как субстанция для разработки средств, повышающих жизнеспособность и подвижность сперматозоидов. Результаты проведенных исследований по безопасности заявляемого БПК, выделенного из семенников быков, позволяют сделать вывод об отсутствии у него аллергенных, сенсибилизирующих и иммунотоксических свойств и отсутствии его потенциальной канцерогенной активности. Таким образом, применение заявляемого БПК исключает развитие побочных негативных реакций со стороны как отдельных тканей и органов, так и со стороны организма в целом. Заявляемый БПК является нетоксичным веществом и может быть рекомендован для проведения клинических испытаний.
Реферат
Изобретение относится к области биотехнологии, конкретно к субстанции, выделенной из семенников быков, и может быть использовано в медицине. Субстанция может быть использована для разработки средств, повышающих жизнеспособность и подвижность сперматозоидов. 13 пр., 2 табл., 1 ил.

Комментарии