Способ экспансии клеток, способ получения кондиционной среды, популяция адгезивных мезенхимальных стромальных клеток плаценты или жировой ткани, фармацевтическая композиция и применение адгезивных мезенхимальных стромальных клеток плаценты или жировой тка - RU2433177C2
Код документа: RU2433177C2
Чертежи









Описание
ОБЛАСТЬ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ И ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам экспансии клеток, популяциям клеток, полученных таким образом, и их применениям. Конкретно, настоящее изобретение относится к способам размножения адгезивных клеток из плаценты или жировых тканей по всем РСТ и их терапевтическим применениям, например, для трансплантации гематопоэтических стволовых клеток.
В развивающемся мире медицины существует растущая потребность во взрослых стволовых клетках для целей приживления клеток и тканевой инженерии. Кроме того, способы лечения с использованием взрослых стволовых клеток непрерывно развиваются для лечения и лечебного воздействия на различные состояния, такие как гематопоэтические нарушения, заболевания сердца, болезнь Паркинсона, болезнь Альцгеймера, инсульт, ожоги, мышечная дистрофия, аутоиммунные нарушения, диабет и артрит.
Гематопоэтические стволовые клетки (HSC) представляют собой клетки-предшественники, которые дают начало всем типам клеток крови как миелоидного, так и лимфоидного ряда. Приживление и инициация гематопоэза трансплантированными HSC зависит от способности тех клеток к возвращению и пролиферации в костном мозге реципиента.
Является широко распространенным мнением, что стволовые клетки тесно связаны in vivo с дискретными нишами в костном мозге, которые предоставляют молекулярные сигналы, которые коллективно опосредуют их дифференцировку и самообновление, через контакты клетка-клетка или непосредственные взаимодействия. Эти ниши являются частью «гематопоэтического индуктивного микроокружения» (HIM), состоящего из клеток костного мозга, т.е. макрофагов, фибробластов, жировых клеток и эндотелиальных клеток. Клетки костного мозга поддерживают функциональную целостность HIM путем предоставления белков внеклеточного матрикса (ECM) и базальных компонентов мембраны, которые облегчают контакт клетка-клетка. Они также обеспечивают различные растворимые или резидентные цитокины, необходимые для контролируемой дифференцировки и пролиферации гематопоэтических клеток.
Взаимодействия между HSC и стромой требуются для сохранения жизнеспособности HSC и предотвращения их дифференцировки. После трансплантации HSC, трансплантированные HSC должны возвращаться обратно в микроокружение костного мозга (КМ) и размещаться в соответствующих нишах до их пролиферации и дифференцировки. Во время процесса хоуминга трансплантированные HSC покидают кровоток и перемещаются, следуя градиенту химокинов, через эндотелиальный клеточный барьер КМ для достижения специально предназначенных ниш. Донорские HSC затем должны возвращаться обратно в гематопоэтические ниши, где они встречаются с более благоприятным микроокружением для деления HSC, и где сплошная среда, физические и химические контакты могут быть установлены между HSC и мезенхимальными клетками, ECM и секретируемыми факторами роста. Все эти процессы включают сложный набор молекул, таких как цитокины, хемокины, гормоны, стероиды, белки внеклеточного матрикса, факторы роста, белки взаимодействия клетка-клетка, белки адгезии и матриксные белки.
Общее число клеток, прижившихся в специально предназначенных нишах костного мозга, лежит в основе успеха трансплантации HSC. Для достижения приживления донорские HSC, которые трансплантированы в кровоток, должны возвращаться в костный мозг реципиента, где они генерируют функциональные очаги гематопоэза. Количество таких очагов выводят как результат умножения общего количества HSC, введенных путем трансфузии, на эффективность их приживления.
Одной из основных проблем, затрагивающей трансплантацию HSC, является низкая выживаемость этих клеток в системе акцептора. Документально хорошо подтверждено, что HSC, трансплантированные внутривенно, выводятся из кровообращения и визуализируются в КМ в течение минут после их трансфузии. От трех до пяти часов после трансплантации HSC в периферической крови реципиентов донорские клетки не детектируются [Askenasy et al. 2002 Transplanted hematopoietic cells seed in clusters in recipient bone marrow in vivo. Stem Cells. 20:301-10]. Громадное большинство трансплантированных клеток разрушается вскоре после их трансфузии. Следовательно, колонизация костного мозга реципиента является низкоэффективной и только 1-5% трансфузированных клеток выявляется в КМ реципиента через 2-3 дня после трансплантации [Kerre et al. 2001 2001 Both CD34+38+ and CD34+38- cells home specifically to the bone marrow of NOD/LtSZ scid/scid mice but show different kinetics in expansion. J Immunol. 167:3692-8; Jetmore et al. 2002 2002 Homing efficiency, cell cycle kinetics, and survival of quiescent and cycling human CD34(+) cells transplanted into conditioned NOD/SCID recipients. Blood. 99:1585-93].
Мезенхимальные стромальные клетки (MSC) представляют собой гетерогенную популяцию клеток, способных к дифференцировке в различные типы зрелых мезенхимальных клеток. Дифференцировка этих клеток в ретикулярные эндотелиальные клетки, фибробласты, адипоциты и остеогенные клетки-предшественники зависит от влияний различных биологически активных факторов.
Из уровня техники известно использование MSC для поддержки приживления HSC. Несколько публикаций продемонстрировали более высокие эффективности приживления HSC при совместной трансплантации с мезенхимальными стволовыми клетками [Gurevitch et al. 1999 1999 Transplantation of allogeneic or xenogeneic bone marrow within the donor stromal microenvironment. Transplantation. 68:1362-8; Fan et al. 2001 2001 Successful allogeneic bone marrow transplantation (BMT) by injection of bone marrow cells via portal vein: stromal cells as BMT-facilitating cells. [Stem Cells. 19:144-50]. Также было показано, что совместная трансплантация мезенхимальных клеток человека в модели приживления человек-овца в результате приводила к увеличению долговременного приживления HSC человека химерного костного мозга у животных [Almeida-Porada et al. 2000]. Совместная трансплантация предшественников стромальных клеток человека преиммунным эмбрионам овцы в результате приводит к раннему появлению донорских клеток человека в циркуляции и повышает уровни клеток в костном мозге в более поздние моменты времени после трансплантации [Blood. 95:3620-7]. Было обнаружено, что одновременная инъекция HSC и мезенхимальных стволовых клеток ускоряла гематопоэз [Zhang et al. 2004. Stem Cells 22:1256-62]. Недавно эти сведения были распространены на более близкую животную модель - макаку Резус. Когда гапло-идентичные HSC и мезенхимальные стволовые клетки трансплантировали совместно, было показано более легкое приживление HSC [Liu et al. 2005 Zhonghua Xue Ye Xue Za Zhi. 26:385-8]. Также недавно сообщалось о применении мезенхимальных стволовых клеток для содействия приживлению HSC у людей [Koc ON, J Clin Oncol. 2000; 18:307-316; Lazarus HM, Biol Blood Marrow Transplant. 2005 May; 11(5):389-98].
По-видимому вклад MSC в гематопоэтическое приживление лежит в продукции цитокинов, поддерживающих HSC, которые помогают, опосредуя и уравновешивая хоуминг, самообновление и возможности детерминации трансплантированных HSC, в восстановлении нарушенного гематопоэтического микроокружения, необходимого для хоуминга и пролиферации HSC и в ингибировании донорских Т клеток, которые могут вызывать болезнь «трансплантат против хозяина» (GvHD), [Charbord P., и Moore, K., Ann. N.Y. Acad. Sci. 1044: 159-167 (2005); патенты США №6010696; 6555374]. Например, в исследовании, проведенном Maitra, [Maitra B, et al. Bone Marrow Transplant. 33(6):597-604. (2004)], было обнаружено, что мезенхимальные стволовые клетки человека поддерживали неродственные донорские гематопоэтические стволовые клетки и суппрессировали Т-клеточную активацию в мышиной модели NOD-SCID, показывая, что неродственные MSC, происходящие из костного мозга человека, могут улучшать исход аллогенной трансплантации.
Одним основным препятствием в использовании MSC является трудность выделения огромных количеств встречающихся в обычных условиях популяций этих клеток, что является технически сложным и дорогостоящим, частично вследствие ограниченного количества клеток. Наиболее очевидным источником MSC является костный мозг, но значительный дискомфорт, осложняющий получение аспиратов костного мозга, и риск биопсии являются недостатками этих способов. Широко распространено мнение, что эмбрион человека и плод образуют независимую жизнь, что делает эмбрион человека проблематичным источником стволовых клеток, добавляя религиозный и этический аспект к уже существующим материально-техническим трудностям.
Недавно были предприняты попытки найти альтернативные источники для получения стволовых клеток. Такими альтернативными источниками, например, является жировая ткань, волосяные фолликулы, тестикулы, обонятельная слизистая человека, желточный мешок эмбриона, плацента, юношеская кожа и кровь (например, пуповинная кровь и даже менструальная кровь). Однако получение стволовых клеток из альтернативных источников в адекватных количествах для терапевтических и исследовательских целей все еще ограничено и в основном трудоемко, включая, например, получение клеток или тканей от донора или пациента, культивирование и/или размножение клеток in vitro, препарирование и т.д.
Плацента рассматривается одним из наиболее доступных источников стволовых клеток, не вызывающих какой-либо дискомфорт или этические ограничения. Было обнаружено, что MSC, полученные из плаценты, имеют аналогичные свойства с MSC, полученными из КМ. Они адгезивны к пластику, экспрессируют мембранные маркеры CD105, CD73 и CD90 и недостаточно экспрессируют поверхностные молекулы CD45, CD34, CD14, CD19 HLA-DR. Однако в отличие от MSC из костного мозга (PD)-MSC из плаценты, обработанные интерфероном-γ, в очень незначительной степени активировали HLA-DR. Более того, PD-MSC клетки демонстрируют иммуносуппрессорные свойства, которые усиливаются в присутствии интерферона-γ. (Chang CJ, Yen ML, Chen YC, Chien CC, Huang HI, Bai CH, Yen BL. Placenta-derived Multipotent Cells exhibit immunosuppressive properties that are enhanced in the presence of interferon-gamma. Stem Cells. 2006 Nov;24(11):2466-77.)
Помимо MSC маркеров PD-MSC демонстрируют уникальные ESC клеточные маркеры SSEA-4, TRA-1-61 и TRA-1-80, что дает возможность предположить, что они могут быть очень примитивными клетками. (Yen BL, Huang HI, Chien CC, Jui HY, Ko BS, Yao M, Shun CT, Yen ML, Lee MC, Chen YC. Isolation of multipotent cells from human term placenta. Stem Cells. 2005; 23(1):3-9.) Более того, PD-MSC (эмбрионального происхожения), а не MSC костного мозга, являются позитивными в отношении межклеточного лимфоцитарного антигена-G человека (HLA). ? (Chang CJ, Yen ML, Chen YC, Chien CC, Huang HI, Bai CH, Yen BL. Placenta-derived multipotent cells exhibit immunosuppressive properties that are enhanced in the presence of interferon-gamma. Stem Cells. 2006 Nov; 24(11):2466-77.)
Исследования показали, что потенциал экспансии PD-MSC был значительно выше, чем потенциал взрослых MSC, полученных из костного мозга (Yen BL, Huang HI, Chien CC, Jui HY, Ko BS, Yao M, Shun CT, Yen ML, Lee MC, Chen YC. Isolation of Multipotent cells from Human Term Placenta. Stem Cells. 2005; 23(1):3-9; M.J.S. de Groot-Swings, Frans H.J. Claas, Willem E. Fibbe и Humphrey H.H. Pieternella S. в 't Anker, Sicco A. Scherjon, Carin Kleijburg-van der Keur, Godelieve. Placenta Isolation of Mesenchymal Stem Cells of Fetal or Maternal Origin from Human. Sem Cells, 2004;22;1338-1345). К тому же, полученные из плаценты адгезивные клетки могут дифференцироваться в остеобласты, адипоциты и хондробласты. Подобно MSC, полученным из костного мозга, было обнаружено, что планцентарные MSC супрессируют пролиферацию лимфоцитов пуповинной крови (UCB), что дает возможность предположить, что сочетанная трансплантация HSC и плацентарных (PD)-MSC может уменьшать возможную болезнь трансплантат-против-хозяина (GvHD) у реципиентов [Li CD, et al., Cell Res. Jul; 15(7): 539-47 (2005)] и может усиливать гематопоэтическую поддержку [Zhang Yi et al., Chinese Medical Journal 117(6): 882-15 887 (2004)]. Применение плаценты в качестве источника амниотических эпителиальных клеток представлено, например, в WO 00/73421, но получение этих клеток все еще остается трудоемким, а выход MSC очень низким.
Другим путем решения проблемы ограниченного количества MSC является ex-vivo экспансия этих клеток с использованием различных условий культивирования [например, патенты США №№6326198; 6030836; 6555374; 6335195; 6338942]. Однако недостатком таких способов остаются требующие много времени методики специфической селекции и выделения, что делает эти способы дорогостоящими и изощренными.
В нескольких исследованиях было обнаружено, что трехмерное (3D) культивирование клеток является более эффективным по выходу [Ma T, et al. Biotechnology Progress. Biotechnol Prog 15:715-24 (1999); Yubing Xie, Tissue Engineering 7(5): 585-598 (2001)]. Применение методик 3D культивирования, которые имитируют природное окружение MSC, основано на высевании этих клеток в перфузионный биореактор, содержащий полиактивные пены [Wendt, D. et al., Biotechnol Bioeng 84: 205-214, (2003)] tubular poly-L-lactic acid (PLLA) porous scaffolds in a Radial-flow perfusion bioreactor [Kitagawa et al., Biotechnology and Bioengineering 93(5): 947-954 (2006)], и поршневой проточный биореактор для роста и экспансии гематопоэтических стволовых клеток (патент США №6911201).
Трехмерный каркас, который присоединяет стромальные клетки, был предложен в патенте США №6022743, а губчатый коллаген был предложен в качестве 3D матрицы у Hosseinkhani, H et al., [Tissue Engineering 11(9-10): 1476-1488 (2005)]. Однако использование MSC, выращенных в этих условиях для поддержания in vivo приживления HSC после трансплантации HSC, никогда не предполагалось ни в одном из этих исследований. Также была необходима требующая много времени оптимизация различных условий, например условий перфузии, или различных методик выделения специфических клеточных типов.
Использование перфузированной послеродовой плаценты в качестве 3D реактора для культивирования MSC было предложено в патенте США №7045148 и в патентных заявках США №№20020123141, 20030032179 и 2005011871. Однако эта методика ограничена промежутком времени 24 часа после выделения плаценты и включает в себя перфузию, следовательно, нарастание массы клеток и их сохранение в течение продолжительных периодов времени невозможно.
Таким образом, существует общепризнанная необходимость, и было бы очень выгодно иметь новые способы экспансии клеток и применений клеток и кондиционной среды, продуцируемой при этом, для лечения, и которые лишены указанных выше ограничений.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В соответствии с одним аспектом настоящего изобретения предлагается способ экспансии клеток, этот способ включает культивирование адгезивных клеток из плаценты или жировой ткани в трехмерных условиях культивирования, которые обеспечивают экспансию клеток.
В соответствии с другим аспектом настоящего изобретения предлагается способ получения кондиционной среды, этот способ включает в себя: культивирование адгезивных клеток из плаценты или жировой ткани в трехмерных условиях культивирования, которые дают возможность для экспансии клеток; и сбор кондиционной среды разросшихся адгезивных клеток, тем самым получая кондиционную среду.
В соответствии с еще одним аспектом настоящего изобретения предлагается популяция клеток, полученная в соответствии с указанным выше способом.
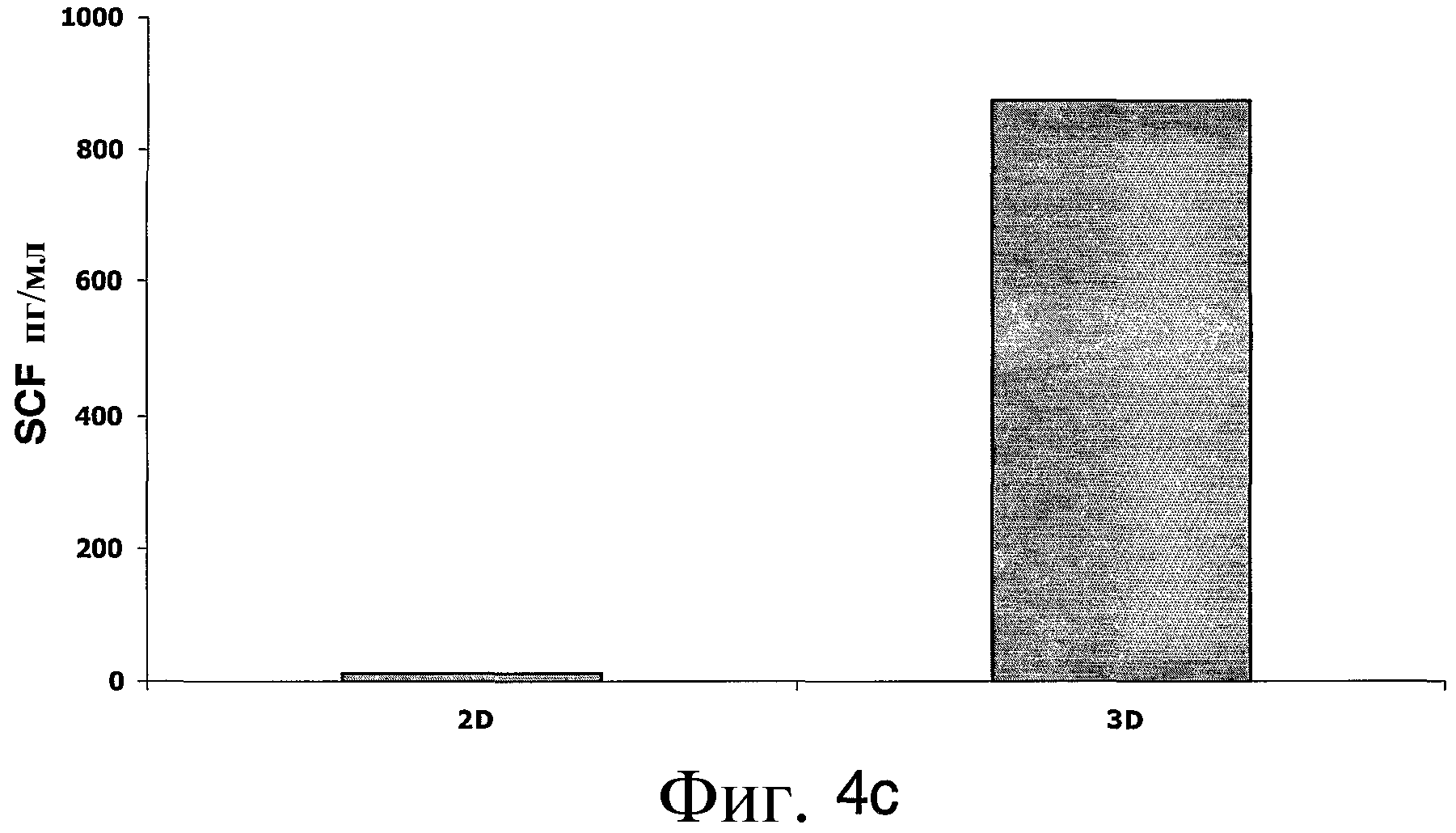
В соответствии с еще одним аспектом настоящего изобретения предлагается выделенная популяция клеток, содержащая адгезивные клетки плаценты или жировой ткани, в которой адгезивные клетки секретируют более высокий уровень по меньшей мере одного фактора, выбранного из группы, состоящей из SCF, IL-6 и Flt-3, чем уровень, секретируемый адгезивными клетками плаценты или жировой ткани, выращенными в 2D культуре.
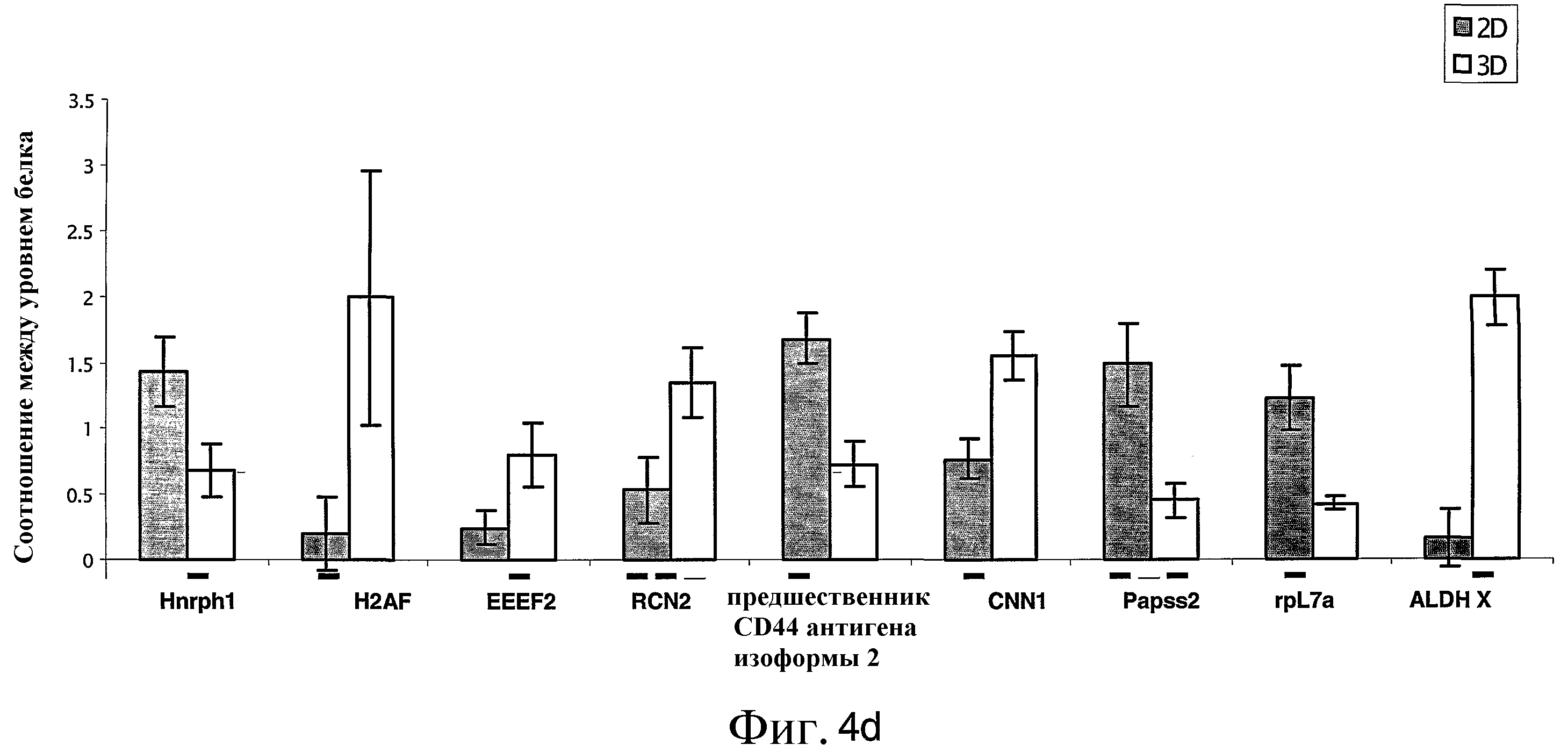
В соответствии с дополнительным аспектом настоящего изобретения предлагается выделенная популяция клеток, содержащая адгезивные клетки плаценты или жировой ткани, в которой адгезивные клетки экспрессируют более высокий уровень по меньшей мере одного белка, выбранного из группы, состоящей из семейства гистонов H2A (H2AF), альдегиддегидрогеназы X (ALDH X), эукариотического трансляционного фактора 2 элонгации (EEEF2), ретикулокальбина 3, кальций-связывающего домена “EF-рука” (RCN2) и кальпонина 1 щелочного гладкомышечного (CNN1), чем уровень, экспрессируемый адгезивными клетками плаценты или жировой ткани, выращенными в 2D культуре.
В соответствии с еще одним дополнительным аспектом настоящего изобретения предлагается выделенная популяция клеток, содержащая адгезивные клетки плаценты или жировой ткани, в которой адгезивные клетки экспрессируют более низкий уровень по меньшей мере одного белка, выбранного из группы, состоящего из гетерогенного ядерного рибонуклеопротеина H1 (Hnrph1), предшественника CD44 антигена изоформы 2, 3-фосфоаденозин-5-фосфосульфат-синтазы 2 изоформы a (Papss2) и рибосомального белка L7a (rpL7a), чем уровень, экспрессируемый адгезивными клетками плаценты или жировой ткани, выращенными в 2D культуре.
В соответствии с еще одним дополнительным аспектом настоящего изобретения предлагается выделенная популяция клеток, содержащая адгезивные клетки плаценты или жировой ткани, в которой адгезивные клетки характеризуются более высокой иммуносупрессирующей активностью, чем активность адгезивных клеток плаценты или жировой ткани, выращенных в 2D культуре.
В соответствии с дополнительными особенностями в предпочтительных вариантах осуществления изобретения описанных ниже, иммуносупрессирующая активность включает в себя снижение пролиферации Т клеток.
В соответствии с дополнительным аспектом настоящего изобретения предлагается фармацевтическая композиция, содержащая в качестве активного ингредиента популяцию клеток, полученных в соответствии с описанным выше способом.
В соответствии с дополнительным аспектом настоящего изобретения предлагается фармацевтическая композиция, содержащая в качестве активного ингредиента кондиционную среду, полученную в соответствии с описанным выше способом.
В соответствии с еще одним дополнительным аспектом настоящего изобретения предлагается фармацевтическая композиция, содержащая в качестве активного ингредиента выделенную популяцию клеток, в соответствии с описанным выше.
В соответствии с еще одним дополнительным аспектом настоящего изобретения предлагается способ лечения состояния, при котором трансплантация стромальных клеток пациенту, нуждающемуся в этом, может оказывать благоприятное воздействие, этот способ включает в себя введение пациенту терапевтически эффективного количества адгезивных клеток ткани, выбранной из группы, состоящей из плаценты и жировой ткани, тем самым осуществляя лечение состояния, при котором трансплантация стромальных клеток пациенту может оказывать благоприятное воздействие.
В соответствии с еще одним дополнительным аспектом настоящего изобретения предлагается способ лечения состояния, при котором трансплантация стромальных клеток пациенту, нуждающемуся в этом, может оказывать благоприятное воздействие, этот способ включает в себя введение пациенту терапевтически эффективного количества кондиционной среды адгезивных клеток, полученных из ткани, выбранной из группы, состоящей из плаценты и жировой ткани, тем самым осуществляя лечения состояния, при котором трансплантация стромальных клеток этому пациенту может оказывать благоприятное воздействие.
В соответствии с еще одним дополнительным аспектом настоящего изобретения предлагается способ снижения иммунного ответа у пациента, нуждающегося в этом, этот способ включает в себя введение пациенту терапевтически эффективного количества выделенной популяции клеток по пунктам 3, 4, 5, 6 или 7, таким образом, чтобы снизить иммунный ответ у пациента.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления пациента лечат с помощью клеточной терапии.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления способ дополнительно включает в себя введение стволовых клеток.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления стволовые клетки содержат гематопоэтические стволовые клетки.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления клетки вводят в сопровождении кондиционной среды или адгезивных клеток.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления клетки вводят после введения кондиционной среды или адгезивных клеток.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления адгезивные клетки получены из трехмерной культуры.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления адгезивные клетки получены из двухмерной культуры.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления состояние выбрано из группы, состоящей из дефицита стволовых клеток, заболевания сердца, болезни Паркинсона, злокачественного заболевания, болезни Альцгеймера, инсульта, ожогов, утраты ткани, потери крови, анемии, аутоиммунных заболеваний, диабета, артрита, рассеянного склероза, болезни трансплантат против хозяина (GvHD), нейродегенеративных заболеваний, аутомиммунного энцефаломиелита (EAE), системной красной волчанки (SLE), ревматоидного артрита, системного склероза, синдрома Шегрена, рассеянного склероза (MS), миастении гравис (MG), синдрома Гийена-Барре (GBS), тиреоидита Хашимото (HT), базедовой болезни, инсулинозависимого сахарного диабета (IDDM) и болезни воспаленного кишечника.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления трехмерная культура содержит 3D биореактор.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления биореактор выбран из группы, состоящей из поршневого проточного биореактора, биореактора с непрерывным механическим перемешиванием и биореактора с неподвижным слоем.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления культивирование клеток осуществляется в непрерывном потоке культуральной среды.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления трехмерная культура содержит адгезивный материал, выбранный из группы, состоящей из полиэфира, полиалкилена, полифторхлорэтилена, поливинилхлорида, полистирола, полисульфона, ацетата целлюлозы, стекловолокна, керамической частицы, матригеля, компонента внеклеточного матрикса, коллагена, поли L-молочной кислоты и инертного металлического волокна.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления культивирование осуществляют по меньшей мере в течение 3 дней.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления культивирование осуществляют по меньшей мере в течение 3 дней.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления культивирование осуществляют до достижения адгезивными клетками по меньшей мере 60% конфлюэнтности.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления для состояния может быть благоприятным облегчение приживления гематопоэтических стволовых клеток.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления адгезивные клетки содержат чип экспрессии позитивных маркеров выбранных из группы, состоящей из CD73, CD90, CD29 и CD105.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления адгезивные клетки содержат чип экспрессии негативных маркеров, выбранных из группы, состоящей из CD45, CD80, HLA-DR, CD11b, CD14, CD19, CD34 и CD79.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления адгезивные клетки секретируют более высокий уровень, по меньшей мере, одного фактора, выбранного из группы, состоящей из SCF, Flt-3 и IL-6 выше уровня, секретируемого адгезивными клетками из плаценты или жировой ткани, выращенными в 2D культуре.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления адгезивные клетки экспрессируют более высокий уровень по меньшей мере одного белка, выбранного из группы, состоящей из семейства гистонов H2A (H2AF), альдегиддегидрогеназы X (ALDH X), эукариотического трансляционного фактора 2 элонгации (EEEF2), ретикулокальбина 3, кальций-связывающего домена “EF-рука” (RCN2) и кальпонина 1 щелочного гладкомышечного (CNN1), чем уровень, секретируемый адгезивными клетками из плаценты или жировой ткани, выращенными в 2D культуре.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления адгезивные клетки экспрессируют более низкий уровень по меньшей мере одного белка, выбранного из группы, состоящей из гетерогенного ядерного рибонуклеопротеина H1 (Hnrph1), предшественника CD44 антигена изоформы 2, 3-фосфоаденозин-5-фосфосульфатсинтазы 2 изоформы a (Papss2) и рибосомального белка L7a (rpL7a), чем уровень, секретируемый адгезивными клетками из плаценты или жировой ткани, выращенными в 2D культуре.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления адгезивные клетки или среда характеризуются более высокой иммуносуппрессирующей активностью, чем активность адгезивных клеток плаценты или жировой ткани, выращенных в 2D культуре.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления иммуносуппрессирующая активность включает в себя уменьшение пролиферации Т клеток.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления клетки содержат клетки, имеющие фенотип стромальной стволовой клетки.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления фенотип стромальной стволовой клетки включает в себя суппрессирующую активность Т клеток.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления фенотип стромальной стволовой клетки включает в себя поддерживающую активность гематопоэтической стволовой клетки.
В соответствии с другими дополнительными особенностями в описанных предпочтительных вариантах осуществления применение популяции клеток, описанных выше, служит для производства лекарственного средства, идентифицированного для трансплантации.
Настоящее изобретение успешно решает недостатки известных в настоящее время конфигураций, предоставляя новые способы экспансии клеток и применений этих клеток и продуцируемой при этом кондиционной среды, для лечения.
Если не определено иное, все технические и научные термины, используемые в контексте настоящей заявки, имеют то же значение, которое обычно понимается специалистом в области, которой принадлежит это изобретение. Хотя все способы и материалы, аналогичные или эквивалентые описанным в настоящей заявке способам, могут быть использованы при практическом осуществлении или тестировании настоящего изобретения, подходящие способы и материалы описаны ниже. В случае конфликта патентное описание, в том числе определения будут контролироваться. Кроме того, материалы, способы и примеры являются только иллюстрирующими и не предназначены для ограничения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Изобретение описано только в качестве примера со ссылкой на сопровождающие чертежи. Теперь с конкретной ссылкой на чертежи подробно подчеркивается, что особенности показаны только в качестве примера и с целями иллюстративного рассмотрения предпочтительных вариантов осуществления изобретения, и представлены по соображениям обеспечения того, что считается наиболее подходящим и без труда понятным описанием принципов и концептуальных аспектов изобретения. В связи с этим не предпринято попыток показать структурные особенности изобретения более подробно, чем это необходимо для фундаментального понимания изобретения, описание, взятое вместе с чертежами, делает очевидным для специалистов в данной области то, как несколько форм изобретения могут быть осуществлены на практике.
На чертежах:
На ФИГ.1 a-g изображено микроокружение, подобное костному, созданное в системе биореактора, содержащей 3-D носители. На Фиг.1a-b представлены электронные микрографики, изображающие сравнение природной кости (Фиг.1a) и структуры PluriX™ 3D носителя через 7 дней после высевания адгезивных стромальных клеток (3D-ASC), имитируя костное микроокружение (Фиг.1b). На Фиг.1c-f представлены электронные микрографики, изображающие PluriX™ 3D матрицу, засеянную 3D-ASC, полученными из костного мозга, через 20 дней (Фиг.1c-d, увеличены X 150 и 250 соответственно) и через 40 дней (Фиг.1e-f, увеличены X 350 и 500 соответственно) после высевания. На Фиг.1g представлена диаграмма Plurix 3D поршневого проточного биореактора с отдельными частями, обозначенными под номерами: резервуар с культуральной средой (1), подача газовой смеси (2), фильтр (3), точка введения (4), колонка, в которой расположены 3D носители (5), индикатор потока (6), регулятор потока (6a), делительный контейнер (7), анализаторы клеточного роста (8), перистальтический насос (9), место отбора образцов (10), измерительный электрод растворенного O2 (11), измерительный электрод pH (12), контрольная система (13), свежая ростовая среда (14), использованная ростовая среда (15).
На ФИГ.2 представлен график, изображающий различные серии продукции адгезивных стромальных клеток (3D-ASC; серии 5-8), происходящих из плаценты, выращенных в 3D условиях роста в системах биореактора. ASC (2×106) высевали в биореактор с плотностью 10000-15000 клеток/носитель. После достижения 12-дневной культуры 3D-ASC плотности от 150000-250000 клеток/носитель или 22,5-37,5 × 106 в биореакторе, содержащем 150 носителей.
На ФИГ.3 a-b представлены столбчатые диаграммы, изображающие различные уровни экспрессии экспрессируемых мембранных маркеров в плацентарных 3D-ASC (темно-фиолетовый) по сравнению с мембранными маркерами в плацентарных клетках, культивируемых в обычных 2D условиях культивирования (светло-фиолетовый). Адгезивные клетки выращивали в течение 4-6 недель во флаконах (2D) или в течение 2-3 недель в системе биореактора, на полистирольных носителях (3D). После сбора либо из флаконов, либо с носителей клетки инкубировали и связывали с панелью моноклональных антител (MAb), которые распознают мембранные маркеры, характерные для MSC (Фиг.3a), или гематопоэтических клеток (Фиг.3b). Следует отметить более высокую экспрессию мембранных маркеров MSC в 2D культивируемых клетках, как показано для мембранных маркеров CD90, CD105, CD73 и CD29, по сравнению с мембранными маркерами MSC, экспрессируемыми в 3D-культивируемых адгезивных клетках, особенно CD105, который демонстрировал 56% экспрессию в 3D культивируемых клетках по сравнению с 87% в 2D культивируемых клетках (Фиг.3a). ASC обеих культур 2D и 3D не экспрессировали никаких гематопоэтических мембранных маркеров (Фиг.3b).
На ФИГ.4a-d представлены столбчатые диаграммы, изображающие сравнение уровней белков в ASC, полученных из плаценты, культивированных в условиях 2D и 3D, или в их кондиционной среде. На Фиг.4a-c изображены уровни лиганда Flt-3 (Фиг.4a), IL-6 (Фиг.4b) и SCF (Фиг.4c) в пг/мл, приведенные к 1×106 клеток/мл, по данным ELISA, в кондиционной среде 2D и 3D культивированных ASC. Результаты представляют один из трех независимых экспериментов. На Фиг.4d показаны уровни экспрессии различных клеточных белков, по данным масс-спектрометрии образцов белков, меченных реактивами iTRAQ, в сравнении. Образцы белка брали из ASC, выращенных в 2D (белые столбцы) и 3D (серые столбцы) условиях. На этой фигуре представлен один из двух повторов эксперимента. Следует отметить различие в уровне экспрессии некоторых белков в клетках и кондиционной среде 2D и 3D условиях культивирования.
На ФИГ.5a-d представлены микрографики, изображающие способность к дифференцировке in vitro плацентарных 3D-ASC в остеобласты. ASC из плаценты человека культивировали в остеогенной индукционной среде (DMEM, содержащей 10% FCS, 100 нМ дексаметазона, 0,05 мМ аскробиновой кислоты 2-фосфата, 10 мМ B-глицерофосфата) за период 3 недели. На Фиг.5a-b показаны клетки, экспрессирующие кальцифицированный матрикс, как показано окрашиванием с помощью ализарина красного С. На Фиг.5c-d показаны контрольные клетки, которые не были обработаны остеогенной индукционной средой и сохранили фибробластоподобный фенотип, и не демонстрирующие минерализацию.
На ФИГ.6 представлен график, изображающий процентное содержание CD45+ клеток человека, выявленных в костном мозге (КМ) мышей NOD-SOD, получавших химиотерапевтическое воздействие (внутрибрюшинные инъекции 25 мг/кг бусульфана в течение двух недель подряд) через 3,5 недели после трансплантации. Клетки CD34+ (100000), очищенные из мононуклеарных клеток пуповинной крови, трансплантировали отдельно (5 мышей, a) или трансплантировали совместно с 0,5×106 плацентарных адгезивных клеток, культивированных в 2D условиях (2D-ASC; 2 мыши, b), или плацентарными адгезивными клетками, культивированными в 3D условиях (3D-ASC), в биореакторе pluriX™ (5 мышей, c). Затем брали костный мозг из бедренных и большеберцовых костей мышей. Клетки человека в костном мозге выявляли с помощью проточной цитометрии. Процентное содержание клеток человека, экспрессирующих CD45, определяли путем инкубирования клеток с античеловеческими CD45-FITC. Следует отметить более высокое процентное содержание клеток человека (hCD45+) в костном мозге мышей при совместной трансплантации с 2D-ASC (b), а также с 3D-ASC (c) по сравнению с процентным содержанием клеток человека у мышей, получивших только HSC (a). Более высокая степень приживления наблюдаемая у мышей, получивших 3D-ASC культивированные клетки по сравнению с мышами, получившими 2D-ASC культивированные клетки, указывает на более высокое терапевтическое преимущество, уникальное для 3D культивированных ASC.
На ФИГ.7a-b представлены FACS анализы трансплантата CD45+ клеток человека у мышей, которым трансплантировали только CD34+ клетки (Фиг.7a) по сравнению с CD34+ клетками вместе с ASC, полученными из жировой ткани. (Фиг.7b). Следует отметить значительно более высокое процентное содержание гематопоэтической популяции человека (hCD45+) (7a-29%) у мыши, при совместной трансплантации с ASC, полученными из жировой ткани, по сравнению с мышью, получавшей только CD34+ человека (7b -12%).
На ФИГ.8 представлена столбчатая диаграмма, изображающая смешанную лимфоцитарную реакцию, проводимую между мононуклеарными клетками пуповинной крови человека (CB), и равными количествами облученных (3000 рад) клеток пуповинной крови (iCB), моноцитов периферической крови человека (PBMC), 2D культивированных (2D) или 3D культивированных (3D) плацентарных ASC, или сочетанием PBMC и 2D, и 3D культивированных плацентарных ASC (PBMC+2D и PBMC+3D). Размер CB клеточной популяции представлен захватом3H-тимидина (измеренным в CPM), который измеряли в течение последних 18 часов культивирования. Подъем стимулированной клеточной пролиферации CB указывает на иммунный ответ на более высоком уровне. Следует отметить более низкий уровень иммунного ответа, демонстрируемый клетками, инкубированными с адгезивными клетками, и, в частности, снижение CB иммунного ответа на PBMC при совместном инкубировании с адгезивными клетками. Для каждой реакции было сделано три повтора.
ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Настоящее изобретение представляет собой новые способы экспансии клеток и применения этих клеток и продуцируемой при этом кондиционной среды, для лечения, связанного со стволовыми клетками, приживления стволовых клеток и поддержки HSC.
Концепции и принципы действия настоящего изобретения могут быть лучше поняты со ссылкой на чертежи и сопровождающие описания.
Перед объяснением по меньшей мере одного варианта осуществления изобретения подробно, должно быть понятно, что изобретение не ограничено его применением с изложенными деталями в следующем описании, или проиллюстрированного Примерами. Изобретение может иметь другие варианты осуществления или оно может быть осуществлено на практике, или выполнено различными путями. Также, понятно, что фразеология и терминология, использованные в контексте настоящего изобретения, предназначены для описания и не должны рассматриваться как ограничение.
В развивающемся мире медицины существует растущая потребность в стволовых клетках, и более конкретно в стромальных стволовых клетках (также называемых «мезенхимальными стволовыми клетками»), для клинических и исследовательских целей. MSC используют для поддержки трансплантации HSC и приживления, а также для лечения растущего числа состояний, например заболеваний сердца, дефицита костного мозга, нейрональных заболеваний и состояний, при которых требуется трансплантация органа или ткани.
Препятствия использования стволовых клеток лежат в технической сложности выделения огромных количеств встречающихся в обычных условиях популяций стволовых клеток или клеток предшественников, вследствие ограниченного количества этих клеток в большинстве тканей, дискомфорт и риск, сопровождающие процедуры получения стволовых клеток, и сопутствующая утрата В клеток памяти и гематопоэтических стволовых клеток с наличием методик получения. Получение клеток из эмбриона человека добавляет религиозный и этический аспект к уже существующим техническим трудностям.
Альтернативные источники стволовых клеток, полученных из костного мозга, включают в себя жировые ткани и плацента. Однако в настоящее время отсутствуют способы эффективной экспансии стволовых клеток из таких тканей.
По мере доведения настоящего изобретения до практического осуществления авторы настоящего изобретения обнаружили, что адгезивные клетки из плаценты или жировой ткани могут эффективно размножаться в 3D условиях культивирования. Неожиданно авторы настоящего изобретения обнаружили, что такие клетки имеют функциональные свойства, сходные со свойствами MSC, и, следовательно, эти клетки и кондиционная среда, продуцируемая при этом, могут быть использованы для терапевтических целей, таких как трансплантация, регенерация тканей и in vivo поддержка HSC.
Как проиллюстрировано ниже и в разделе Примеры, который следует далее, авторы настоящего изобретения смогли вырастить жировые и плацентарные адгезивные клетки, имеющие свойства стромальных стволовых клеток, в 3D окружении. Было обнаружено, что клетки, разросшиеся соответствующим образом, были жизнеспособными после криоконсервирования, как подтверждено анализами адгезии и репопуляции (смотри Пример 1). Анализом проточной цитометрией плацентарных адгезивных клеток были обнаружены явно выраженные особенности экспрессии маркеров и (смотри Фиг.3a-b). Наиболее важно, жировые и плацентарные адгезивные клетки, размноженные в 2D или 3D окружении, были способны поддерживать приживление HSC (смотри Пример 2), обосновывая применение этих клеток в настоящем изобретении, в качестве стромальных стволовых клеток, в клинике.
Таким образом, в соответствии с одним аспектом настоящего изобретения предлагается способ экспансии клеток.
Этот способ включает в себя культивирование адгезивных клеток из плаценты или жировой ткани в трехмерных (3D) условиях культивирования, которые поддерживают экспансию клеток.
Используемые в контексте настоящего изобретения термины «разрастание» и «экспансия» относятся по существу к бездифференцировочному подращиванию клеток и в конечном счете клеточному росту, т.е. увеличению клеточной популяции (например, по меньшей мере в 2 раза) без дифференцировки, сопровождающей такое увеличение.
Используемые в контексте настоящего изобретения термины «сохранение» и «подращивание» относятся по существу к бездифференцировочному клеточному обновлению, т.е. по существу стационарной клеточной популяции без дифференцировки, сопровождающей такую стационарность.
Используемое в контексте настоящего изобретения выражение «адгезивные клетки» относится к гомогенной или гетерогенной популяции клеток, которые являются «заякоренными», т.е. для которых требуется прикрепление к поверхности для роста in vitro.
Используемое в контексте настоящего изобретения выражение «жировая ткань» относится к соединительной ткани, которая содержит жировые клетки (адипоциты).
Используемый в контексте настоящего изобретения термин «плацентарная ткань» относится к любой части органа самки млекопитающего, которая выстилает стенку матки и во время беременности окутывает плод, с которой он соединяется через пуповину. После рождения плацента выталкивается (и называется послеродовой плацентой).
Используемое в контексте настоящего изобретения выражение «трехмерные условия культивирования» относится к расположению клеток в условиях, которые совместимы с клеточным ростом, позволяющих клеткам расти более, чем в один слой. Хорошо понятно, что in situ окружение клетки в живом организме (или ткани) находится в виде трехмерной структуры. Клетки окружены другими клетками. Они удерживаются в сложной сети наномерных нитей внеклеточного матрикса, что дает возможность установить различные местные микроокружения. Их внеклеточные лиганды опосредуют не только прикрепление к базальной мембране, а также доступ к целому ряду (кровеносных) и лимфатических сосудов. Кислород, гормоны и питательные вещества переносятся к клеткам, а продукты жизнедеятельности выводятся. Трехмерные условия культивирования по настоящему изобретению предназначены для имитации такого окружения, как дополнительно проиллюстрировано примерами ниже.
Таким образом, адгезивные клетки этого аспекта настоящего изобретения извлекают из жировой или плацентарной ткани.
Плацентарные клетки могут быть получены из доношенной или недоношенной плаценты. Предпочтительно плаценту берут после обескровливания. Плаценту предпочтительно перфузируют в течение периода времени, достаточного для удаления оставшихся клеток. Термин «перфузировать» или «перфузия», используемый в контексте настоящего изобретения, относится к действию наливания или пропускания жидкости через орган или ткань. Плацентарная ткань может быть от любого млекопитающего; наиболее предпочтительно плацентарная ткань является тканью человека. Удобным источником плацентарной ткани является послеродовая плацента (например, 1-6 часов), однако источник плацентарной ткани или клеток или способ выделения плацентарной ткани не является важным для этого изобретения.
Плацентарные адгезивные клетки могут быть получены как из плодной (т.е. амниотической или внутренней частей плаценты, смотри Пример 1), так и материнской (т.е. базальной децидуальной оболочки и париетальной децидуальной оболочки) частей плаценты. Образцы ткани промывают в физиологическом буфере (например, фосфатно-солевом буфере (PBS) или буфере Хэнкса). Одноклеточные суспензии получают путем обработки ткани гидролизующим ферментом (смотри ниже) и/или измельчением и промывкой части ткани через нейлоновый фильтр, или осторожным пипетированием (Falcon, Becton, Dickinson, San Jose, CA) с промывочной средой.
Адгезивные клетки из жировой ткани могут быть выделены с помощью целого ряда способов, известных специалистам в данной области. Например, такие способы описаны в патенте США №6153432. Жировая ткань может быть получена из сальниковой висцеральной железы, молочной железы, половой железы или других участков жировой ткани. Предпочтительным источником жировой ткани является жир сальника. У людей жир обычно выделяют путем липосакции.
Выделенные адгезивные клетки из жировой ткани могут быть получены путем обработки ткани гидролизующим ферментом, таким как коллагеназа, трипсин и/или диспаза; и/или эффективными концентрациями гиалуронидазы или ДНКазы; и этилендиаминетерауксусной кислоты (EDTA); при температуре от 25 до 50°C, в течение периодов времени от 10 минут до 3 часов. Затем клетки можно пропустить через нейлоновый или марлевый сетчатый фильтр от 20 микрон до 800 микрон. Затем клетки подвергают дифференциальному центрифугированию непосредственно в среде или на градиенте Фиколла или Перколла, или другом градиенте частиц. Клетки центрифугируют со скоростью от 100 до 3000 × g в течение периодов времени от 1 минуты до 1 часа при температурах от 4 до 50°C (смотри патент США №7078230).
Помимо адгезивных клеток, полученных из плаценты или жировой ткани, в настоящем изобретении также предусматривается применение адгезивных клеток из других клеточных источников, которые характеризуются фенотипом стромальных стволовых клеток (как будет дополнительно описано ниже). Источники ткани, из которых могут быть извлечены адгезивные клетки, включают пуповинную кровь, волосяные фолликулы [например, как описано в патентной заявке США 20060172304], тестикулы [например, как описано у Guan K., et al., Nature. 2006 Apr 27; 440(7088): 1199-203], обонятельную слизистую человека [например, как описано у Marshall, CT., et al., Histol Histopathol. 2006 Jun; 21(6):633-43], эмбриональный желточный мешок [например, как описано у Geijsen N, Nature. 2004 Jan 8; 427(6970): 148-54] и амниотическую жидкость [Pieternella et al. (2004) Stem Cells 22:1338-1345], но не ограничиваются ими, все из которых, как известно, содержат мезенхимальные стволовые клетки. Адгезивные клетки из этих тканевых источников могут быть выделены путем культивирования этих клеток на адгезивной поверхности, таким образом, выделяя адгезивные клетки из других клеток в исходной популяции.
Независимо от происхождения (например, плацента или жировая ткань), извлечение клеток предпочтительно осуществляют в стерильных условиях. После получения выделенных клеток их оставляют для прилипания к адгезивному материалу (например, сформированному в виде поверхности) для выделения, таким образом, адгезивных клеток. Это можно осуществить до (смотри Пример 1) или одновременно с культивированием в 3D условиях.
Используемый в контексте настоящего изобретения «адгезивный материал» относится к синтетическому, природному или к их комбинации, нецитотоксическому (т.е. биологически совместимому) материалу, имеющему структуру (например, заряженные группы, расположенные на поверхности), которые могут удерживать клетки на поверхности.
Примеры адгезивных материалов, которые могут быть использованы в соответствии с этим аспектом настоящего изобретения, включают в себя, но не только, полиэфир, полиалкилен, полифторхлорэтилен, поливинилхлорид, полистирол, полисульфон, ацетат целлюлозы, стекловолокно, керамическую частицу, матригель, компонент внеклеточного матрикса (например, фибронектин, хондронектин, ламинин), коллаген, поли-L-молочную кислоту и инертное металлическое волокно.
Дополнительные стадии очистки или обогащения стромальных стволовых клеток могут осуществляться с использованием способов, хорошо известных в уровне техники (например, с помощью FACS, используя маркер экспрессии, как дополнительно описано ниже).
Неограничивающие примеры основной среды, используемой при культивировании в соответствии с настоящим изобретением, включают в себя минимальную среду Игла, ADC-1, LPM (без бычьего сывороточного альбумина), F10(HAM), F12 (HAM), DCCM1, DCCM2, RPMI1640, среду BGJ (с модификацией по Фиттону-Джексону или без модификации), основную среду Игла (BME-с добавлением солевого основания Эрла), модифицированную по Дульбекко среду Игла (DMEM-без сыворотки), Yamane, IMEM-20, Глазго модифицированную среду Игла (GMEM), среду L-15 Лейбовица, среду 5A МакКоя, среду M199 (M199E-с солевым основанием Эрла), среду M199 (M199H-с солевым основанием Хэнкса), минимальную среду Игла (MEM-E-с солевым основанием Эрла), минимальную среду Игла (MEM-H-с солевым основанием Хэнкса) и минимальную среду Игла (MEM-NAA с заменимыми аминокислотами), среди многочисленных других, в том числе среда 199, CMRL 1415, CMRL 1969, CMRL 1066, NCTC 135, MB 75261, MAB 8713, DM 145, Williams' G, Neuman & Tytell, Higuchi, MCDB 301, MCDB 202, MCDB 501, MCDB 401, MCDB 411, MDBC 153. Предпочтительной средой для использования в настоящем изобретении является DMEM. Эти и другие подходящие среды доступны от GIBCO, Grand Island, N.Y., USA и Biological Industries, Bet HaEmek, Israel, среди прочего. Многие из этих сред объединены в Methods in Enzymology, Volume LVIII, «Cell Culture», pp. 62 72, под редакцией William B. Jakoby и Ira H. Pastan, опубликовано Academic Press, Inc.
Среда может быть дополнена, например, сывороткой, такой как эмбриональная сыворотка теленка или других видов, и необязательно или альтернативно, факторами роста, цитокинами и гормонами (например, гормоном роста, эритропоэтином, тромбопоэтином, интерлейкином 3, интерлейкином 6, интерлейкином 7, макрофагальным колониестимулирующим фактором, c-kit лигандом/фактором стволовых клеток, лигандом остеопротегрина, инсулином, инсулиноподобными факторами роста, эпидермальным фактором роста, фактором роста фибробластов, фактором роста нервов, цилиарным нейротрофическим фактором, тромбоцитарным фактором роста и костным морфогенетическим белком в концентрациях от уровней пикограмм/мл до миллиграмм/мл).
Дополнительно отмечено, что к культуральной среде могут быть добавлены дополнительные компоненты. Такими компонентами могут быть антибиотики, противогрибковые средства, альбумин, аминокислоты и другие компоненты, известные в уровне техники для культивирования клеток. Соответственно, компоненты могут быть добавлены для усиления процесса дифференцировки, при необходимости (дополнительно смотри ниже).
После того, как адгезивные клетки готовы, их можно пассировать в трехмерное окружение (смотри Пример 1 раздела Примеры, который следует ниже). Тем не менее будет понятно, что клетки могут быть перенесены в матрицу с 3D-конфигурацией сразу же после выделения (как упомянуто выше).
Таким образом, адгезивный материал в соответствии с этим аспектом настоящего изобретения сформирован для 3D культивирования, тем самым обеспечивая ростовую матрицу, которая по существу увеличивает доступную поверхность присоединения для адгезии стромальных клеток, таким образом, чтобы имитировать инфраструктуру ткани (например, плаценты).
Например, для ростовой матрицы высотой 0,5 мм повышение составляет по меньшей мере от 5 до 30 раз, вычисленное путем проецирования на основание ростовой матрицы. Такое повышение примерно от 5 до 30 раз является повышением на единицу слоя, и при множестве таких слоев, либо сложенных, либо разделенных разделителями или подобным, повышение от 5 до 30 раз применяется для каждой такой структуры. В тех случаях, когда матрица используется в виде пласта, предпочтительно нетканых волокнистых поверхностей или пластов пенящихся полимеров с открытыми порами, предпочтительная толщина пласта составляет примерно от 50 до 1000 мкм или более, обеспечивая адекватную пористость для входа клеток, входа питательных веществ и для удаления продуктов жизнедеятельности из этого пласта. В соответствии с предпочтительным вариантом осуществления поры имеют эффективный диаметр от 10 мкм до 100 мкм. Такие пласты могут быть получены из волокон различной толщины, предпочтительная толщина волокна или диаметр волокна находится в интервале примерно от 0,5 мкм до 20 мкм, еще более предпочтительные волокна имеют диаметр 10 мкм до 15 мкм.
Структуры в соответствии с изобретением могут поддерживаться или даже лучше могут быть связаны с пористым поддерживающим пластом или экраном, обеспечивающим стабильность параметров и физическую силу.
Такие матриксные пласты также могут быть порезаны, перфорированы или измельчены с получением частиц с проекцией поверхности порядка примерно от 0,2 мм2 примерно до 10 мм2, с толщиной того же порядка (примерно от 50 до 1000 мкм).
Дополнительные подробности, относительно изготовления, применения и/или преимуществ ростовой матрицы, которая была использована для доведения настоящего изобретения до практического осуществления, описаны в патентах США №№5168085, и, в частности, 5266476, оба включены в качестве ссылки.
Адгезивная поверхность может иметь форму, выбранную из группы, состоящей из квадратов, колец, дисков или крестов.
Для получения в большом масштабе культивирование предпочтительно осуществляют в 3D биореакторе.
Примеры таких биореакторов включают в себя, но не ограничиваются, поршневой проточный биореактор, биореактор с непрерывным механическим перемешиванием и биореактор с неподвижным слоем.
Как показано в Примере 1 раздела Примеры, трехмерный (3D) поршневой проточный биореактор (как описано в патенте США №6911201) способен поддерживать рост и длительное сохранение стромальных клеток. В этом биореакторе стромальные клетки высевают на пористые носители, изготовленные из нетканого материала матрицы из полиэфира, упакованные в стеклянную колонку, тем самым, давая возможность для размножения огромного числа клеток в относительно небольшом объеме.
Матрица, используемая в поршневом проточном биореакторе, может быть в форме пласта, нетканых волокнистых поверхностей или пластов из пенящихся полимеров с открытыми порами, предпочтительная толщина пласта составляет примерно от 50 до 1000 мкм или больше, обеспечивая адекватную пористость для входа клеток, входа питательных веществ и для удаления продуктов жизнедеятельности из пласта.
Другие 3D биореакторы, которые могут быть использованы с настоящим изобретением, включают в себя, но не только, биореактор с непрерывным механическим перемешиванием, в котором культуральная среда непрерывно подается в биореактор и продукт непрерывно выводится, для поддержания постоянного во времени стационарного состояния в реакторе [Биореактор с механическим перемешиванием с волокнистой поддерживающей сеткой доступен, например, в New Brunswick Scientific Co., Edison, NJ], биореактор с неподвижным слоем, эрлифтный биореактор, в которых воздух обычно подается на дно центральной вытяжной трубы поднимающейся при образовании пузырьков газа, и высвобождающей отработанный газ в верхней части колонки], высевающий клетки перфузионный биореактор с полиактивными пенами [как описано у Wendt, D. et al., Biotechnol Bioeng 84: 205-214, (2003)] трубчатые пористые каркасы из поли-L-молочной кислоты (PLLA) в перфузионном биореакторе с радиальной фильтрацией [как описано у Kitagawa et al., Biotechnology and Bioengineering 93(5): 947-954 (2006)]. Другие биореакторы, которые могут быть использованы в соответствии с настоящим изобретением, описаны в патентах США №№6,277,151, 6,197,575, 6,139,578, 6,132,463, 5,902,741 и 5,629,186.
Высевание клеток предпочтительно осуществляется при 100000-1500000 клеток/мм высевания.
Клетки предпочтительно собирали после достижения по меньшей мере примерно 40% конфлюэнтности, 60% конфлюэнтности или 80% конфлюэнтности, предпочтительно избегая неконтролируемой дифференцировки и физиологического старения.
Культивирование осуществляют по меньшей мере примерно в течение 2 дней, 3 дней, 5 дней, 10 дней, 20 дней, месяца или даже больше. Будет понятно, что культивирование в биреакторе может продлить этот период. Также можно провести пассирование для увеличения числа клеток.
Адгезивные клетки по настоящему изобретению предпочтительно содержат по меньшей мере один «фенотип стромальной стволовой клетки».
Используемый в контексте настоящего изобретения «фенотип стромальной стволовой клетки» относится к структурному или функциональному фенотипу, характерному для стромальных (т.е. мезенхимальных) стволовых клеток, полученных из костного мозга.
Используемое в контексте настоящего изобретения выражение «стволовая клетка» относится к клетке, которая окончательно не дифференцировалась.
Таким образом, например, клетки могут иметь веретенообразную структуру. Альтернативно или дополнительно клетки могут экспрессировать маркер или набор маркеров (например, поверхностный маркер), характерный для стромальных стволовых клеток. Примеры поверхностных маркеров стромальных стволовых клеток (позитивных и негативных) включают в себя, но не только, CD105+, CD29+, CD44+, CD73+, CD90+, CD34-, CD45-, CD80-, CD19-, CD5-, CD20-, CD11B-, CD14-, CD19-, CD79-, HLA-DR- и FMC7-. Другие маркеры стромальных стволовых клеток включают в себя тирозингидроксилазу, нестин и H-NF, но не ограничиваются ими.
Примеры функциональных фенотипов, характерных для стромальных стволовых клеток, включают в себя суппрессирующую активность Т клеток (не стимулировать Т клетки, а наоборот, подавлять их), поддерживающую активность гематопоэтических стволовых клеток, а также адипогенную, гепатогенную, остеогенную и нейрогенную дифференцировку.
Любая из этих структурных или функциональных особенностей может быть использована для того, чтобы квалифицировать клетки по настоящему изобретению (смотри Примеры 1-2 в разделе Примера, который следует ниже).
Популяции клеток, генерированные в соответствии с настоящими наставлениями, характеризуются уникальным профилем экспрессии, как показано в Примере 1 в разделе Примеры. Таким образом, например, адгезивные клетки плаценты или жировой ткани, полученные в соответствии с настоящими наставлениями, способны экспрессировать и/или секретировать высокие уровни выбранных факторов. Например, такие клетки экспрессируют или секретируют SCF, Flt-3, H2AF или ALDH X по меньшей мере в 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или предпочтительно в 12 раз выше, чем экспрессируется или секретируется адгезивными клетками плаценты или жировой ткани, выращенными в 2D культуре. Дополнительно или альтернативно, популяция клеток по настоящему изобретению секретирует или экспрессирует IL-6, EEEF2, RCN2 или CNN1 на уровне по меньшей мере в 2, 3 или 5 раз выше, чем уровень, экспрессируемый или секретируемый адгезивными клетками плаценты или жировой ткани, выращенными в 2D культуре. Дополнительно или альтернативно, популяция клеток по настоящему изобретению характеризуется более низким уровнем экспрессии различных других белков, по сравнению с клетками, культивированными в 2D условиях. Таким образом, например, секретируется или экспрессируется менее 0,6, 0,5, 0,25 или 0,125 от уровня экспрессии Hnrph1, предшественника CD44 антигена изоформы 2, Papss2 или rpL7a, экспрессируемого или секретируемого адгезивными клетками плаценты или жировой ткани, выращенными в 2D культуре.
При дальнейшем приведении настоящего изобретения к практическому осуществлению, авторы настоящего изобретения поняли, что адгезивные стромальные клетки, и в частности 3D-ASC, демонстрировали иммуносупрессирующую активность. Как показано в Примере 3 раздела Примеры, который следует ниже, было обнаружено, что адгезивные стромальные клетки, и в частности 3D-ASC, супрессируют иммунную реакцию мононуклеарных клеток пуповинной крови человека в исследовании MLR. Таким образом, клетки по настоящему изобретению могут обладать биологическими активностями, которые предпочтительно могут быть использованы в клинике (например, Т клеточная суппрессирующая активность, поддерживающая активность гематопоэтических стволовых клеток).
При дальнейшем приведении настоящего изобретения к практическому осуществлению, авторы настоящего изобретения поняли, что кондиционная среда клеток по настоящему изобретению может обладать биологическими активностями, которые предпочтительно могут быть использованы в клинике (например, Т клеточная суппрессирующая активность, поддерживающая активность гематопоэтических стволовых клеток).
Таким образом, настоящее изобретение дополнительно предусматривает сбор кондиционной среды и ее применение как таковой или после дополнительных стадий концентрации, обогащения или фракционирования с использованием способов, которые хорошо известны в уровне техники. Предпочтительно кондиционную среду по настоящему изобретению получают из высокожизнеспособной культуры клеток в середине логарифмического роста.
Как упомянуто выше, клетки и кондиционная среда по настоящему изобретению характеризуются фенотипом стромальных стволовых клеток и по существу могут быть использованы в любом исследовании или клиническом применении, при котором может быть выгодным применение таких клеток.
Приживление и инициация гематопоэза трансплантированными HSC зависит от сложных процессов, которые включают хоуминг, движение по градиенту хемокинов через эндотелиальный клеточный барьер, к костному мозгу и заселение соответствующих ниш, устанавливая физические контакты между трансплантированными клетками, ECM и мезенхимальными клетками ниш. Все эти процессы вовлекают сложную совокупность молекул, таких как цитокины, гормоны, стероиды, белки внеклеточного матрикса, факторы роста, взаимодействие клетка-клетка и белки адгезии, и матриксные белки.
Известно, что только 1-5% трансфузированных HSC выявляется в костном мозге реципиента через 2-3 дня после трансплантации [Kerre et al., J Immunol. 167:3692-8. (2001); Jetmore et al., Blood. 99:1585-93 (2002)].
Вклад MSC в гематопоэтическое приживление частично осуществляется путем ингибирования продукции Т клеток донора, которые вызывают болезнь трансплантат против хозяина [GvHD, Charbord P., и Moore, K., Ann. N.Y. Acad. Set 1044: 159-167 (2005); Maitra B, et al., Bone Marrow Transplant. 33(6):597-604. (2004); патенты США №№6010696; 6555374]; и частично обеспечением поддержки гематопоэтическим стволовым клеткам (HSC) (т.е. поддержки и облегчения пролиферации, созревания и/или хоуминга гематопоэтических стволовых клеток).
Как показано в Примере 2 раздела Примеры, который следует ниже, неожиданно было обнаружено, что плацентарные адгезивные клетки и адгезивные клетки из жировой ткани поддерживают приживление HSC даже после химиотерапии.
Учитывая эти результаты, можно предположить, что клетки или среда по настоящему изобретению могут быть использованы в любом клиническом применении, при котором используется трансплантация стромальных стволовых клеток.
Таким образом, в соответствии с другим аспектом настоящего изобретения предлагается способ лечения медицинского состояния (например, патологии, заболевания, синдрома), при котором трансплантация стромальных стволовых клеток пациенту, нуждающемуся в этом, может оказывать благоприятное воздействие.
Используемый в контексте настоящего изобретения термин «лечение» относится к ингибированию или задержке развития патологии и/или уменьшению, ремиссии или регрессии патологии. Специалистам в данной области будет понятно, что различные методики и анализы могут быть использованы для оценки развития патологии, и подобным образом, различные методики и анализы могут быть использованы для оценки уменьшения, ремиссии или регрессии патологии. Предпочтительно, термин «лечение» относится к облегчению или уменьшению проявления симптома, связанного со злокачественным заболеванием. Предпочтительно, лечение излечивает, например, в значительной степени устраняет, симптомы, связанные с этим медицинским состоянием.
В контексте настоящего изобретения «медицинское состояние, при котором трансплантация стромальных стволовых клеток может оказывать благоприятное воздействие», относится к любому медицинскому состоянию, которое можно облегчить введением клеток/среды по настоящему изобретению.
Термин или выражение «трансплантация», «клеточная реплантация» или «пересадка» в контексте настоящего изобретения используются взаимозаменяемо и относятся к введению клеток по настоящему изобретению в ткань-мишень.
Используемый в контексте настоящего изобретения термин «пациент» относится к любому пациенту (например, млекопитающему), предпочтительно пациенту человеку.
Способ в соответствии с этим аспектом настоящего изобретения включает в себя введение пациенту терапевтически эффективного количества клеток или среды по настоящему изобретению (описанных выше), тем самым осуществляя лечение медицинского состояния, при котором трансплантация стромальных стволовых клеток этому пациенту может оказывать благоприятное воздействие.
Клетки, которые могут быть введены в соответствии с этим аспектом настоящего изобретения, включают в себя описанные выше адгезивные клетки, которые могут быть культивированы либо в двухмерном, либо в трехмерном окружении, а также их мезенхимальные и немезенхимальные частично или полностью дифференцированные производные.
Способы получения линиеспецифичных клеток из стромальных стволовых клеток по настоящему изобретению известны в уровне техники. См., например, патенты США №№5486359, 5942225, 5736396, 5908784 и 5902741.
Клетки могут быть нативными или генетически модифицированными, таким образом, чтобы получить линию, представляющую интерес (смотри патентную заявку США №20030219423).
Клетки и среда могут быть из аутологичного или неаутологичного источника (т.е. аллогенными или ксеногенными) свежих или замороженных (например, криоконсервированных) препаратов.
В зависимости от медицинского состояния, пациенту можно вводить дополнительные химические лекарственные средства (например, иммуномодулирующие, химиотерапевтические и т.д.) или клетки.
Таким образом, например, для улучшения приживления стволовых клеток (например, увеличивая число жизнеспособных HSC в костном мозге реципиента и оптимально улучшая уровень лейкоцитов в крови) клетки/среду по настоящему изобретению можно вводить до, одновременно или после трансплантации HSC.
Предпочтительно HSC и стромальные клетки имеют общие HLA антигены.
Предпочтительно, HSC и стромальные клетки представляют собой клетки от одного индивидуума. Альтернативно, HSC и стромальные клетки представляют собой клетки от разных индивидуумов.
Термин или выражение «трансплантация», «клеточная реплантация» или «пересадка» в контексте настоящего изобретения используются взаимозаменяемо и относятся к введению клеток по настоящему изобретению в ткань-мишень. Клетки могут быть получены от реципиента или от аллогенного или ксеногенного донора.
Поскольку неаутологичные клетки при введении в организм вероятно будут вызывать иммунную реакцию, было разработано несколько подходов для уменьшения вероятности отторжения неаутологичных клеток. Эти подходы включают либо суппрессию иммунной системы реципиента, либо инкапсулирование неаутологичных клеток в иммуноизолирующие, полупроницаемые мембраны перед трасплантацией.
Методики инкапсулирования обычно классифицируются как микроинкапсулирование, включающее мелкие сферические носители, и макроинкапсулирование, включающее более крупные плоскослойные мембраны и мембраны с полыми волокнами (Uludag, H. et al. Technology of mammalian cell encapsulation. Adv Drug Deliv Rev. 2000; 42:29-64).
Способы получения микрокапсул известны в уровне техники и включают в себя, например, способы, описанные Lu MZ, et al., Cell encapsulation with alginate and alpha-phenoxycinnamylidene-acetylated poly(allylamine). Biotechnol Bioeng. 2000, 70: 479-83, Chang TM и Prakash S. Procedures for microencapsulation of enzymes, cells and genetically engineered microorganisms. Mol Biotechnol. 2001, 17: 249-60, и Lu MZ, et al., A novel cell encapsulation method using photosensitive poly(allylamine alpha-cyanocinnamylideneacetate). J Microencapsul. 2000, 17: 245-51.
Например, микрокапсулы получают путем комплексообразования модифицированного коллагена с тер-полимерным каркасом 2-гидроксиэтилметилакрилата (HEMA), метакриловой кислоты (MAA) и метилметакрилата (MMA), в результате получая капсулу толщиной 2-5 мкм. Такие микрокапсулы могут быть дополнительно инкапсулированы дополнительными 2-5 мкм тер-полимерными каркасами для обеспечения отрицательно заряженной гладкой поверхности и минимизации абсорбции белков плазмы (Chia, S.M. et al. Multi-layered microcapsules for cell encapsulation Biomaterials. 2002 23: 849-56).
Другие микрокапсулы основаны на альгинате, морском полисахариде (Sambanis, A. Encapsulated islets in diabetes treatment. Diabetes Technol. Ther. 2003, 5: 665-8) или его производных. Например, микрокапсулы могут быть получены полиэлектролитным комплексообразованием между полианионами альгината натрия и сульфатом натриевой целлюлозы с поликатионом поли(метилен-ко-гуанидин) гидрохлорида в присутствии хлорида кальция.
Будет понятно, что инкапсулирование клеток улучшается, когда используются более мелкие капсулы. Следовательно, контроль качества, механическая стабильность, диффузионные свойства и активности in vitro инкапсулированных клеток улучшались, когда размер капсулы был уменьшен с 1 мм до 400 мкм (Canaple L. et al, Improving cell encapsulation through size control. J Biomater Sci Polym Ed. 2002; 13:783-96). Более того, было обнаружено, что нанопористые биокапсулы с хорошо контролируемым размером пор, величиной 7 нм, приспосабливающие химические свойства поверхности и уточняющие микроархитектуру, с успехом иммунологически изолировали микроокружения для клеток (Williams D. Small is beautiful: microparticle and nanoparticle technology in medical devices. Med Device Technol. 1999, 10: 6-9; Desai, T.A. Microfabrication technology for pancreatic cell encapsulation. Expert Opin Biol Ther. 2002,2: 633-46).
Примеры иммуносуппрессирующих средств включают метотрексат, циклофосфамид, циклоспорин, циклоспорин А, хлорохин, гидроксихлорохин, сульфасалазин (сульфасалазопирин), соли золота, D-пеницилламин, лефлуномид, азатиоприн, анакинру, инфликсимаб (REMICADE), этанерцепт, блокаторы TNFα, биологический агент, нацеливающий воспалительный цитокин и нестероидное противовоспалительное средство (НПВС), но не ограничиваются ими. Примеры НПВС включают ацетилсалициловую кислоту, салицилат холина магния, дифлунизал, салицилат магния, салсалат, салицилат натрия, диклофенак, этодолак, фенопрофен, флурбипрофен, индометацин, кетопрофен, кеторолак, меклофенамат, напроксен, набуметон, фенилбутазон, пироксикам, сулиндак, толметин, ацетаминофен, ибупрофен, ингибиторы Cox-2 и трамадол, но не ограничиваются ими.
В любом из описанных в настоящем изобретении способов клетки или среду можно вводить либо как таковые, либо предпочтительно как часть фармацевтической композиции, которая дополнительно содержит фармацевтически приемлемый носитель.
В контексте настоящего изобретения «фармацевтическая композиция» относится к препарату одного или нескольких химических конъюгатов, описанных в настоящем изобретении, с другими химическими компонентами, такими как фармацевтически пригодные носители и эксципиенты. Назначением фармацевтической композиции является облегчение введения соединения пациенту.
В дальнейшем, термин «фармацевтически приемлемый носитель» относится к носителю или разбавителю, который не вызывает у пациента значительного раздражения и не устраняет биологическую активность и свойства вводимого соединения. Примеры носителей, без ограничения, представляют собой пропиленгликоль, солевой раствор, эмульсии и смеси органических растворителей с водой.
В контексте настоящего изобретения термин «эксципиент» относится к инертному веществу, добавляемому в фармацевтическую композицию для дополнительного облегчения введения соединения. Примеры эксципиентов, без ограничения, включают в себя карбонат кальция, фосфат кальция, различные сахара и различные типы крахмала, производные целлюлозы, желатин, растительные масла и полиэтиленгликоли.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения фармацевтический носитель представляет собой водно-солевой раствор.
Технологии получения и введения лекарственных средств можно найти в «Remington's Pharmaceutical Sciences», Mack Publishing Co., Easton, PA, последнее издание, которое включено здесь в качестве ссылки.
Фармацевтическую композицию можно вводить системно (как подробно описано выше). Альтернативно, фармацевтическую композицию можно вводить местно, например, путем инъекции фармацевтической композиции непосредственно в участок ткани пациента.
Фармацевтические композиции по настоящему изобретению могут быть получены способами, хорошо известными в уровне техники, например способами обычного перемешивания, растворения, грануляции, изготовления драже, отмучивания, эмульгирования, инкапсулирования, включения или лиофилизацией.
Фармацевтические композиции для использования в соответствии с настоящим изобретением, таким образом, могут быть получены стандартным способом, с использованием одного или нескольких фармацевтически приемлемых носителей, содержащих эксципиенты и дополнительные вещества, которые облегчают обработку активных ингредиентов в препараты, которые могут быть использованы фармацевтически.
Подходящая технология получения лекарственного средства зависит от выбранного пути введения.
Для инъекции активные ингредиенты фармацевтической композиции могут быть получены в виде водных растворов, предпочтительно в виде физиологически совместимых буферов, таких как раствор Хэнкса, раствор Рингера, или физиологического солевого буфера. Для введения через слизистую оболочку в композиции используются диффундирующие вещества, соответствующие барьеру, через который проникает это вещество. Такие диффундирующие вещества в основном известны в уровне техники.
Для любого препарата, используемого в способах по изобретению, терапевтически эффективное количество или дозу исходно можно определить по данным in vitro анализов и анализов клеточных культур. Предпочтительно, доза составляется на животной модели для достижения желаемой концентрации или титра. Такая информация может быть использована для более точного определения подходящих доз у людей.
Токсичность и терапевтическая эффективность активных ингредиентов, описанных в настоящем изобретении, можно определить с помощью стандартных фармацевтических методик in vitro, в клеточных культурах или у экспериментальных животных.
Данные, полученных из этих in vitro анализов и анализов клеточных культур и изучения животных, могут быть использованы в составлении интервала доз для использования у людей. Эти дозы могут варьировать в зависимости от используемой лекарственной формы и используемого пути введения. Точный состав, путь введения и доза могут быть выбраны конкретным лечащим врачом с учетом состояния пациента (см., например, Fingl, et al., 1975, в «The Pharmacological Basis of Therapeutics», Ch. 1 p.1). Например, у пациентов с болезнью Паркинсона можно проводить симптоматические наблюдения на улучшение моторных функций, указывающее на положительный ответ на лечение.
Для инъекционного введения активные ингредиенты фармацевтической композиции могут быть получены в виде водных растворов, предпочтительно в виде физиологически совместимых буферов, таких как раствор Хэнкса, раствор Рингера или физиологического солевого буфера.
Величина дозы и интервал могут регулироваться индивидуально до уровней активного ингредиента, которые достаточны для эффективного регулирования синтеза нейтротрансмиттеров имплантированными клетками. Дозы, необходимые для достижения желаемого эффекта, будут зависеть от индивидуальных характеристик и пути введения. Для определения плазменных концентраций могут быть использованы детектирующие анализы.
В зависимости от тяжести и реакции состояния, подвергаемого лечению, введение дозы может быть однократным или многократным, с длительностью курса лечения от нескольких дней до нескольких недель или до достижения ослабления патологического состояния.
Количество вводимой композиции, разумеется, будет зависеть от индивидуума, которому проводят лечение, тяжести болезни, способа введения, мнения врача, назначающего лечение, и т.д. Доза и временной режим введения будут изменяться соответственно изменению состояния индивидуума, находящегося под внимательным и непрерывным контролем. Например, пациентам с болезнью Паркинсона, которым проводят лечение, будут вводить количество клеток, достаточное для облегчения симптомов этого заболевания исходя из показаний мониторинга.
После трансплантации клетки по настоящему изобретению предпочтительно продолжают существовать в патологическом очаге в течение периода времени (например, по меньшей мере 6 месяцев) так, чтобы наблюдался терапевтический эффект.
Композиции, содержащие препарат по настоящему изобретению, составленный в совместимом фармацевтически приемлемом носителе, также могут быть получены, помещены в соответствующий контейнер и отмечены этикеткой с указанием состояния, которое подвергают лечению.
Композиции по настоящему изобретению при необходимости можно поместить в контейнер или дозатор, такой как одобренный FDA набор, который может содержать одну или несколько лекарственных форм, содержащих активный ингредиент. Контейнер, например, может содержать металлическую или полимерную пленку, например блистерную упаковку. К контейнеру или дозатору могут прилагаться инструкции по применению. К контейнеру или дозатору также могут прилагаться памятка, относящаяся к контейнеру, в форме, предписанной правительственным органом, регулирующим производство, применение или продажу фармацевтических препаратов, указанная памятка отражает одобрение ведомством формы композиций, либо для применения у человека, либо у животных. Такой памятке, например, может быть присвоено обозначение, утвержденное Управлением по контролю за продуктами питания и лекарственными средствами США для назначения лекарственных средств или введения одобренного продукта.
ПРИМЕРЫ
Теперь ссылка дается на следующие примеры, которые вместе с приведенными выше описаниями иллюстрируют изобретение неограничивающим образом.
В основном, используемая в контексте настоящего изобретения номенклатура и лабораторные методики, использованные в настоящем изобретении, включают молекулярные, биохимические, микробиологические методики и технологии рекомбинантной ДНК. Такие методики подробно описаны в литературе. См., например, «Molecular Cloning: A laboratory Manual» Sambrook et al., (1989); «Current Protocols in Molecular Biology» Volumes I-III Ausubel, R. M., ed. (1994); Ausubel et al., «Current Protocols in Molecular Biology», John Wiley and Sons, Baltimore, Maryland (1989); Perbal, «A Practical Guide to Molecular Cloning», John Wiley & Sons, New York (1988); Watson et al., «Recombinant DNA», Scientific American Books, New York; Birren et al. (eds) «Genome Analysis: A Laboratory Manual Series», Vols. 1-4, Cold Spring Harbor Laboratory Press, New York (1998); методики, изложенные в патентах США №№4666828; 4683202; 4801531; 5192659 и 5272057; «Cell Biology: A Laboratory Handbook», том I-III Cellis, J. E., ed. (1994); «Current Protocols in Immunology» том I-III Coligan J. R, ed. (1994); Stites et al. (eds), «Basic and Clinical Immunology» (8-е издание), Appleton & Lange, Norwalk, CT (1994); Mishell и Shiigi (eds), «Selected Methods in Cellular Immunology», W. H. Freeman and Co., New York (1980); доступные иммунологические анализы подробно описаны в патентах и специальной литературе, см., например, патенты США №№3791932; 3839153; 3850752; 3850578; 3853987; 3867517; 3879262; 3901654; 3935074; 3984533; 3996345; 4034074; 4098876; 4879219; 5011771 и 5281521; «Oligonucleotide Synthesis» Gait, M. J., ed. (1984); «Nucleic Acid Hybridization» Hames, B. D., и Higgins S. J., eds. (1985); «Transcription and Translation» Hames, B. D., и Higgins S. J., Eds. (1984); «Animal Cell Culture» Freshney, R. I., ed. (1986); «Immobilized Cells and Enzymes» IRL Press, (1986); «A Practical Guide to Molecular Cloning» Perbal, B., (1984) и «Methods in Enzymology» Vol. 1-317, Academic Press; «PCR Protocols: A Guide To Methods And Applications», Academic Press, San Diego, CA (1990); Marshak et al., «Strategies for Protein Purification and Characterization - A Laboratory Course Manual» CSHL Press (1996); все они включены в качестве ссылки, как полностью изложенные здесь. Другие общие ссылки представлены по всему документу. Считается, что эти методики хорошо известны в уровне техники и представлены для удобства читателя. Вся информация, содержащаяся в них, включена здесь в качестве ссылки.
ПРИМЕР 1
Получение и культивирование адгезивных стромальных клеток (ASC) из костного мозга, плаценты и жировых тканей
Адгезивные клетки культивировали в системе биореактора, содержащей 3D носители для получения 3D-ASC клеток, характеризующихся специфическим профилем экспрессии клеточных маркеров.
Эффективность роста тестировали путем подсчета клеток. Способность к дифференцировке этих клеток тестировали путем культивирования в дифференцирующей среде.
МАТЕРИАЛЫ И ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДИКИ
Стромальные клетки костного мозга - стромальные клетки костного мозга получали из аспирированного костного мозга грудины гематологически здоровых пациентов, которым проводили операцию на открытом сердце или биопсию костного мозга. Аспираты костного мозга разводили в 3 раза в сбалансированном солевом растворе Хэнкса (HBSS; GIBCO BRL/Invitrogen, Gaithersburg MD) и подвергали центрифугированию в градиенте плотности Фиколл-Гипака (Robbins Scientific Corp. Sunnyvale, CA). После этого, мононуклеарные клетки костного мозга (<1,077 г/см3) собирали, промывали 3 раза в HBSS и ресуспендировали в ростовой среде [DMEM (Biological Industries, Beit Ha'emek, Israel) дополненной 10% FCS (GIBCO BRL), 10-4 M меркаптоэтанолом (Merck, White House Station, NJ), смесью пен-стреп-нистатин (100 Ед/мл:100 мкг/мл:1,25 мкг/мл; Beit Ha'Emek), 2 мМ L-глутамином (Beit Ha'Emek)]. Клетки от отдельных доноров инкубировали отдельно во флаконах для клеточных культур (Corning, Acton, MA) при 37°C (5% СО2) с еженедельной заменой культуральной среды. Клетки разделяли каждые 3-4 дня, используя 0,25% трипсин-EDTA (Beit Ha'Emek). После 2-40 пассажей, при достижении 60-80% конфлюэнтности клетки собирали для анализа или для культивирования в биореакторах.
Стромальные клетки, полученные из плаценты - внутренние части доношенной плаценты (Bnei Zion medical center, Haifa, Israel) нарезали в стерильных условиях, промывали 3 раза буфером Хэнкса и инкубировали в течение 3 часов при 37°C с 0,1% коллагеназой (1 мг/мл ткани; Sigma-Aldrich, St. Lewis, MO). Используя осторожное пипетирование, суспендированные клетки затем промывали с использованием DMEM дополненной 10% FCS, смесью пен-стреп-нистатин (100 Ед/мл:100 мкг/мл:1,25 ед./мл) и 2 мМ L-глутамина, высевали во флаконы площадью 75 см2и инкубировали при 37°C в термостате для тканевых культур в условиях увлажнения с 5% CO2. После этого, клетки оставляли для адгезии на пластиковой поверхности в течение 72 часов, после чего среду меняли каждые 3-4 дня. При достижении 60-80% конфлюэнтности (обычно 10-12 дней), клетки снимали с культуральных флаконов, используя 0,25% трипсин-EDTA, и высевали в новые флаконы. Культивированные клетки затем собирали для анализа или для культивирования в биореакторах.
Стромальные клетки, полученные из жировой ткани - стромальные клетки получали из жировой ткани человека процедурой липосакции (Rambam Haifa, Israel). Жировую ткань тщательно промывали равными объемами PBS и расщепляли при 37°C в течение 30 мин с помощью коллагеназы (20 мг/мл). Затем клетки промывали с использованием DMEM, содержащей 10% FCS, смесь пен-стреп-нистатин (100 Ед/мл:100 мкг/мл:1,25 ед./мл) и L-глутамин, и центрифугировали при 1200 об/мин в течение 10 мин при комнатной температуре, ресуспендировали лизирующим раствором (1:10; Biological Industries, Beit Ha'emek, Israel, чтобы отбросить эритроциты), центрифугировали и ресуспендировали с использованием DMEM, содержащей 10% FCS, смесь пен-стреп-нистатин (100 Ед/мл:100 мкг/мл:1,25 ед./мл) и L-глутамин. Промытые клетки затем высевали в стерильный флакон с тканевой культуральной средой при 3-10×107 клеток/флакон. На следующий день клетки промывали PBS для удаления оставшихся эритроцитов и мертвых клеток. Клетки держали при 37°C в термостате для клеточных культур в условиях увлажнения с 5% СО2. Среду меняли каждые 3-4 дня. При конфлюэнтности 60-80% клетки снимали с культурального флакона, используя 0,25% трипсин-EDTA и высевали в новые флаконы. После 2-40 пассажей, при достижении клетками 60-80% конфлюэнтности, клетки собирали для анализа или для культивирования в биореакторах.
PluriX™ Поршневой проточный биореактор - PluriX™ поршневой проточный биореактор (Pluristem, Haifa, Israel; изображенный на Фиг.1g, смотри также патент США №6911201), загружали 1-100 мл упакованных 3D пористых носителей (4 мм в диаметре), изготовленных из нетканой матрицы полиэфира. Эти носители обеспечивают размножение огромного числа клеток в сравнительно небольшом объеме. Стеклянные изделия были разработаны и произведены фирмой Pluristem. Биореактор держали в термостате при 37°C, с регулируемой скоростью потока и под контролем клапана (6a на Фиг.1g) и перистальтического насоса (9 на Фиг.1g). Биореактор содержит место отбора образцов и точку введения (4 на Фиг.1g), позволяя последовательно высевать клетки. Культуральную среду подавали при pH 6,7-7,4 из резервуара (1 на Фиг.1g). Резервуар был снабжен профильтрованной газовой смесью (2,3 на Фиг.1g), содержащей воздух/СО2/О2 в различных пропорциях, в зависимости от плотности клеток в биореакторе. Доля O2 соответствовала уровню растворенного O2 на выходе биореактора, определенного с помощью монитора (6 на Фиг.1g). Газовая смесь поступала в резервуар через силиконовые трубки или диффузор (Degania Bet, Emek Hayarden, Israel). Культуральную среду пропускали через делительный контейнер (7 на Фиг.1g), который обеспечивает сбор циркулирующих неадгезивных клеток. Циркулирование среды было получено с помощью перистальтического насоса (9 на Фиг.1g). Биореактор дополнительно был снабжен дополнительным местом отбора образцов (10 на Фиг.1g) и контейнерами для непрерывной замены среды.
Получение 3D-адгезивных стромальных клеток (3D-ASC) - неконфлюэнтные первичные адгезивные 2D клеточные культуры человека, выращенные, как указано выше, обрабатывали трипсином, промывали, ресуспендировали в DMEM, дополненной 10% FBS, смесью пен-стреп-нистатин (100 Ед/мл:100 мкг/мл:1,25 ед./мл) и 2 мМ L-глутамином, и высевали (103-105 клеток/мл) через точку введения на 3D носители в стерильный поршневой проточный биореактор (смотри Фиг.1g). Перед инокуляцией биореактор наполняли PBS-Ca-Mg (Biological Industries, Beit Ha'emek, Israel), автоклавировали (120°C, 30 мин) и промывали ростовой средой Дульбекко, содержащей 10% инактивированную нагреванием сыворотку теленка и смесь пен-стреп-нистатин (100 Ед/мл:100 мкг/мл:1,25 ед./мл). Скорость потока поддерживали при 0,1-5 мл/мин. Процесс высевания предусматривал прекращение циркуляции в течение 2-48 часов, тем самым давая клеткам возможность осесть на носителях. Биореактор держали при контролируемой температуре (37°C) и условиях pH (pH = 6,7-7,4); используя инкубатор, снабженный стерильным воздухом и CO2 при необходимости. Ростовую среду заменяли 2-3 раза в неделю. Циркулирующую среду заменяли свежей средой DMEM, каждые 4 часа - 7 дней. При плотности 1×106-1×107 клеток/мл (после 12-40 дней роста), общий объем среды удаляли из биореактора и биореактор и носители промывали 3-5 раз PBS. 3D-ASC клетки затем снимали с носителей с помощью трипсин-EDTA (Biological Industries, Beit Ha'emek, Israel; 3-15 минут осторожным встряхиванием, 1-5 раз) и ресуспендировали в DMEM и криоконсервировали.
3D-ASC качественные биологические анализы - криоконсервированные 3D-ASC клетки размораживали и подсчитывали. Для оценки жизнеспособности клеток 2×105 клетки высевали во флаконы 150 см2 для культивирования тканей, и их способность к адгезии и репопуляции оценивали в течение 7 дней после высевания. После этого, анализировали фенотип мембранных маркеров 3D-ASC, используя проточный цитометр с флуоресцирующими моноклональными антителами (Beckman Coulter, Fullerton, CA).
Сравнение профилей маркеров клеточной мембраны 3D и 2D культивированных адгезивных клеток, с использованием проточной цитометрии 100000 - 200000 адгезивных клеток из 2D культур и 3D культур проточной системы суспендировали в 0,1 мл культуральной среды в 5 мл пробирке и инкубировали (4°C, 30 мин в темноте) с насыщенными концентрациями каждого из следующих мАт: FITC-конъюгированного против CD90 человека (Chemicon International Inc. Temecula, CA), PE-конъюгированного против CD73 человека (Bactlab Diagnostic, Ceasarea, Israel), PE-конъюгированного против CD105 человека (eBioscience, San Diego, CA), FITC-конъюгированного против CD29 человека (eBioscience, San Diego, CA), Cy7-PE-конъюгированного против CD45 человека (eBiosience), PE-конъюгированного против CD19 человека (IQProducts, Groningen, The Netherlands), PE-конъюгированного против CD14 человека мАт (IQProducts), FITC-конъюгированного против CD11b человека (IQProducts) и PE-конъюгированного против CD34 человека (IQProducts) или с FITC-конъюгированным мАт против HLA-DR человека (IQProducts). После инкубирования клетки промывали дважды в ледяном PBS, содержащем 1% инактивированную нагреванием FCS, ресуспендировали в 500 мкл 0,5% формальдегида и анализировали, используя проточный цитометр FC-500 (Beckman Coulter, Fullerton, CA).
Сравнение профилей белков 3D и 2D культивированных адгезивных клеток, используя масс-спектрометрический анализ - ASC, полученные 2D и 3D методиками культивирования, получали из плаценты, как описано выше. Вкратце, 2D культуры получали культивированием 0,3-0,75×106 клеток во флаконах 175 см2 в течение 4 дней в увлажненной атмосфере с 5% СО2 при 37°C, до достижения 60 - 80% конфлюэнтности. 3D культуры получали высеванием 2-10×106 клеток/грамм в биореакторе, содержащем 2000 носителей, и культивированием в течение 18 дней. После сбора клетки промывали (X 3) для удаления всей сыворотки, осаждали и замораживали. Белки выделяли из осадка [используя набор Tri Reagent kit (Sigma, Saint Louis, USA) и расщепляли трипсином, и метили реактивом iTRAQ (Applied Biosciences, Foster City, CA)], в соответствии с инструкциями производителя. Вкратце, iTRAQ реактивы являются неполимерными реактивами для изобарного мечения. Пептиды в каждом образце метят одной из четырех изобарных кодированных изотопами меток через их N-концевые и/или лизиновые боковые цепи. Четыре меченных образца перемешивали, и пептиды анализировали с помощью масс-спектрометрии. После фрагментации пептидов каждая метка высвобождает различимый масс-репортерный ион; соотношение четырех репортеров, следовательно, дает относительную распространенность заданного пептида в образце (информация на: http://docs.appliedbiosystems.com/pebiodocs/00113379.pdf).
Протеомный анализ 2D культуры по сравнению с 3D культурой плацентарных ASC проводили в центре протеомных исследований Smoler proteomic center (биологический факультет, Technion, Haifa, Israel), используя LC-MS/MS на QTOF-Premier (Waters, San Francisco, CA), с идентификацией и анализом, сделанным с помощью программного обеспечения Pep-Miner [Beer, I., et al., Proteomics, 4, 950-60 (2004)] по сравнению с базой данных nr, в части, относящейся к человеку. Анализируемые белки представляли собой: гетерогенный ядерный рибонуклеопротеин H1 (Hnrph1 GeneBank Регистрационный № NP_005511), семейство гистонов H2A (H2AF, GeneBank Регистрационный № NP_034566.1), эукариотический фактор 2 элонгации трансляции (EEEF2, GeneBank Регистрационный № NP_031933.1), ретикулокальбин 3, кальций-связывающий EF-hand домен (RCN2, GeneBank Регистрационный № NP_065701), предшественник CD44 антигена изоформы 2 (GeneBank Регистрационный № NP_001001389, кальпонин 1 щелочной гладкомышечный (CNN1), GeneBank Регистрационный № NP_001290), изоформа а 3 фосфоаденозин 5 фосфосульфатсинтазы 2 (Papss2, GeneBank Регистрационный № NP_004661), рибосомальный белок L7a (rpL7a, GeneBank Регистрационный № NP_000963) и альдегиддегидрогеназу X (ALDH X, GeneBank Регистрационный №P47738). Каждый эксперимент был выполнен дважды. Вследствие особенности анализа каждый белок анализировали в соответствии с количеством пептидов, встречающихся в образце (2-20 появлений белка в каждом анализе).
Сравнение секретированных белков 3D и 2D культивированных адгезивных клеток с помощью ELISA - ASC, полученные 2D и 3D методиками культивирования, получают из плаценты, как описано выше, с 3D культурами в течение 24 дней. После этого собирали кондиционную среду и анализировали на Flt-3 лиганд, IL-6, тромбопоэтин (TPO) фактор стволовых клеток (SCF), используя ELISA (R&D Systems, Minneapolis, MN), в трех независимых экспериментах. Результаты были приведены к 1×106 клеток/мл.
Дифференцирующая среда остеобластов - остеогенную дифференцировку оценивали путем культивирования клеток в дифференцирующей среде для остеобластов, содержащей DMEM, дополненную 10% FCS, 100 нМ дексаметазона, 0,05 мМ 2-фосфат аскорбиновой кислоты, 10 мМ B-глицерофосфата, в течение 3-недельного периода. Кальцифицированный матрикс определялся окрашиванием ализарином красным С, а щелочную фосфатазу определяли с помощью набора для анализа щелочной фосфатазы Alkaline phosphatase assay kit (все реактивы от фирмы Sigma-Aldrich, St. Lewis, MO).
РЕЗУЛЬТАТЫ
Система биореактора PluriX™ создает физиологически подобное микроокружение
Чтобы воспроизвести эффективные условия культивирования для адгезивных клеток, было искусственно создано физиологически подобное микроокружение (изображенное на Фиг.1a), с использованием биореактора PluriX (Pluristem, Haifa, Israel; носитель проиллюстрирован на Фиг.1g и показан до высевания на Фиг.1b). Как показано на Фиг.1c-f, 3D-ASC клетки, продуцируемые костным мозгом, успешно культивировались и разрастались в 3D матрице, через 20 дней (Фиг.1b-c, увеличены X 150 и 250 соответственно) и 40 дней (Фиг.1c-d, увеличены X 350 и 500 соответственно) после высевания.
Клетки, выращенные в системе биореактора PluriX, значительно разрастались
Различные серии 3D-ASC клеток плаценты выращивали в системах биореактора PluriX. Плотность посева составляла 13300 клеток/носитель (до суммарной 2×106клеток). Через четырнадцать дней после высевания плотность клеток увеличилась в 15 раз, достигая приблизительно 200000 клеток/носитель (Фиг.2), или 30×106 в биореакторе со 150 носителями. В другом эксперименте клетки высевали в биореактор с плотностью 1,5×104 клеток/мл и через 30 дней после посева носители содержали более чем в 50 раз большее количество клеток, т.е. приблизительно 0,5×106 клеток/носитель, или 0,5×107 клеток/мл. Плотность клеток на носителях на различных уровнях ростовой колонки была постоянной, указывая на гомогенный перенос кислорода и питательных веществ к клеткам. Таким образом, было доказано, что 3D система культивирования обеспечивает поддерживающие условия для роста и длительного существования высокоплотных мезенхимальных клеточных культур, которые могут быть эффективно выращены до количества, достаточного для целей поддержания приживления и успешной трансплантации.
3D-ASC демонстрируют уникальные характеристики мембранных маркеров - чтобы определить различие профилей секреции растворимых молекул и продукции белка, под влиянием 3D методики культивирования, имитирующей костное окружение, был проведен FACS анализ. Как показано на Фиг.3a, FACS анализ клеточных маркеров показал, что 3D-ASC демонстрируют паттерн экспрессии маркеров, отличный от адгезивных клеток, выращенных в 2D условиях. 2D культивированные клетки экспрессировали более высокие уровни позитивных мембранных маркеров CD90, CD 105, CD73 и CD29 по сравнению с 3D культивированными клетками. Например, CD105 показывал 56% экспрессию в 3D культивированных клетках по сравнению с 87% в 2D культивированных клетках. ASC обеих 2D и 3D плацентарных культур не экспрессировали каких-либо гематопоэтических мембранных маркеров (Фиг.3b).
3D-ASC демонстрируют уникальный профиль растворимых факторов - гематопоэтическая ниша содержит поддерживающие клетки, которые продуцируют множество цитокинов, хемокинов и факторов роста. Для дальнейшего определения различия между 2D и 3D культивированными ASC, профиль четырех основных гематопоэтических секретируемых белков в кондиционной среде 2D и 3D культур ASC был получен с помощью ELISA. На Фиг.4a-c показано, что клетки, выращенные в 3D условиях, продуцировали кондиционную среду с более высокими уровнями Flt-3 лиганда (Фиг.4a), IL-60 (Фиг.4b) и SCF (Фиг.4c), тогда как низкие уровни IL-6 и близкий к нулю уровень Flt-3 лиганда и SCF определялись в кондиционной среде 2D культур. Продукция тромбопоэтина (TPO) была очень низкой и одинаковой в обеих культурах.
3D-ASC демонстрируют уникальный профиль белков в масс-спектрометрическом анализе - чтобы дополнительно определить различие между 2D и 3D культивированными ASC, был проанализирован белковый профиль этих клеток с помощью масс-спектрометрии. На Фиг.4d показано, что 2D и 3D культивированные ASC демонстрируют заметное различие профилей экспрессии белка. Как показано в приведенной ниже Таблице 1, 3D культивированные клетки демонстрируют значительно более высокий уровень экспрессии H2AF и ALDH X (более чем в 9 и 12 раз выше, соответственно) и более высокий уровень белков EEEF2, RCN2 и CNN1 (примерно в 3, 2,5 и 2 раза, соответственно). Кроме того, 3D культивированные клетки демонстрируют примерно половину от уровней экспрессии белков Hnrph1 и предшественника CD44 антигена изоформы 2 и примерно треть от уровней экспрессии Papss2 и rpL7a.
3D-ASC обладают способностью дифференцироваться в остеобласты - чтобы дополнительно охарактеризовать 3D-ASC, клетки культивировали в дифференцирующей среде для остеобластов в течение 3-недельного периода. После этого проводили осаждение кальция. Было показано, что дифференцированные клетки продуцировали кальций (показано красным на Фиг.5a-b), тогда как контрольные клетки сохраняли фибробластоподобный фенотип и не демонстрировали минерализации (Фиг.5c-d). Эти результаты показывают, что плацентарные 3D-ASC обладают способностью дифференцироваться in vitro в остеобласты.
ПРИМЕР 2
Оценка способности плацентарных 3D-ASC улучшать приживление HSC
3D-ASC поддержку приживления HSC оценивали по уровню гематопоэтических клеток человека (hCD45+) детектируемых у облученных сублетальной дозой или предварительно получивших химиотерапевтическое воздействие иммунологически дефицитных мышей NOD-SCID.
МАТЕРИАЛЫ И ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДИКИ
Выделение CD34+ клеток - образцы пуповинной крови брали в стерильных условиях во время родов (Bnei Zion Medical Center, Haifa, Israel) и мононуклеарные клетки фракционировали, с помощью центрифугирования в градиенте плотности Lymphoprep (Axis-Shield PoC As, Oslo, Norway) и криоконсервировали. Размороженные мононуклеарные клетки промывали и инкубировали с анти-CD34 антителами и выделяли, используя midi MACS (Miltenyl Biotech, Bergish Gladbach, Germany). Для достижения желаемого количества объединяли клетки более чем от одного образца (50000-100000 клеток).
Выявление трансплантированных клеток у облученных мышей - семинедельных самцов и самок мышей NOD-SCID (NOD-CB17-Prkdcscid/J; Harlan/Weizmann Inst., Rehovot Israel) содержали в стерильных клетках с открытой системой, на стерильной диете и автоклавированной подкисленной воде. Мышей облучали сублетальной дозой (350 сГр), и после этого (48 часов после облучения) им трансплантировали 50000-100000 hCD34+ клеток с дополнительными ASC (0,5×106-1×106) или без них, полученными из плаценты или жировой ткани (3-7 мышей в каждой группе), внутривенной инъекцией в боковую хвостовую вену. Через четыре - шесть недель после трансплантации мышей скарифицировали смещением, костный мозг брали путем промывания обеих бедренных и большеберцовых костей FACS буфером (50 мл PBS, 5 мл FBS, 0,5 мл 5% азида натрия). Клетки человека в костном мозге мышей выявляли методом проточной цитометрии, и процентное содержание клеток, экспрессирующих маркер гематопоэтических клеток CD45 человека и мышей, у получивших воздействие мышей NOD-SCID, осуществляли инкубированием клеток с античеловеческими CD45-FITC (IQ Products, Groningen, The Netherlands). Самый низкий порог для окончательного приживления клеток человека определялся на 0,5%.
Выявление трансплантированных клеток у мышей, получавших химиотерапевтическое воздействие - самцам мышей NOD-SCID в возрасте 6,5 недель (NOD.CB17/JhkiHsd-scid; Harlan, Rehovot Israel), содержавшихся, как описано выше для облученных мышей, вводили внутрибрюшинно бусульфан (25 мг/кг в течение 2 дней подряд). Через два дня после второй инъекции бусульфана мышам вводили CD34+ клетки отдельно или вместе с 0,5×106 ASC, полученными из плаценты. Через 3,5 недели после трансплантации мышей скарифицировали, и наличие гематопоэтических клеток человека определяли, как описано выше для облученных мышей.
РЕЗУЛЬТАТЫ
3D-ASC улучшали приживление HSC у облученных мышей - гематопоэтические клетки человека CD34+ и 3D-ASC, полученные из плаценты или жировой ткани, совместно трансплантировали облученным мышам NOD-SCID. Эффективность приживления оценивали через 4 недели после совместной трансплантации и сравнивали с мышами, которым трансплантировали только HSC. Как показано в Таблице 2 и на Фиг.6, совместная трансплантация 3D-ASC и CD34+ клеток пуповинной крови в результате приводили к гораздо более высоким показателям приживления и более высоким уровням клеток человека в костном мозге мышей-реципиентов по сравнению с мышами, которые получали только CD34+ клетки пуповинной крови.
3D-ASC улучшали приживление HSC у мышей, получавших химиотерапевтическое воздействие - гематопоэтические клетки человека CD34+ совместно трансплантировали с 500000 - 2D-ASC или 3D-ASC, полученными из плаценты, мышам NOD-SCID, предварительно получивших химиотерапевтическое воздействие. Эффективность приживления оценивали через 3,5 недели после совместной трансплантации и сравнивали с мышами, которым трансплантировали только HSC. Как показано в Таблице 3, совместная трансплантация ASC CD34+ клеток пуповинной крови в результате приводила к более высоким уровням приживления в костном мозге мышей-реципиентов по сравнению только CD34+ клетками пуповинной крови. Более того, как показано в Таблице 3, средний уровень приживления был выше у мышей, которым совместно трансплантировали плацентарные адгезивные клетки, выращенные в системе биореактора PluriX (3D-ASC), чем у мышей, которым совместно трансплантировали клетки того же донора, выращенные в обычных статичных 2D условиях культивирования (флакон).
Результаты FACS анализа, показанные на Фиг.7a-b, демонстрируют преимущество совместной трансплантации ASC с hHSC (Фиг.7b), и способность ASC улучшать восстановление гематопоэтической системы после трансплантации HSC.
Взятые вместе эти результаты показывают, что ASC могут служить в качестве поддерживающих клеток для улучшения гематопоэтического восстановления после трансплантации HSC (аутологичной или аллогенной). Способность 3D-ASC усиливать приживление гематопоэтических стволовых клеток и/или клеток-предшественников после трансплантации HSC может быть результатом способности 3D-ASC секретировать цитокины, поддерживающие HSC, которые могут улучшать хоуминг, самообновление и способность к пролиферации трансплантированных клеток, или быть результатом способности этих клеток восстанавливать поврежденное микроокружение, необходимое для хоуминга и пролиферации трансплантированных HSC.
ПРИМЕР 3
Суппрессия лимфоцитарного ответа под действием 2D и 3D культивированных ASC
Было обнаружено, что адгезивные стромальные клетки и, в частности, 3D-ASC, супрессируют иммунную реакцию мононуклеарных клеток пуповинной крови человека в MLR исследовании.
МАТЕРИАЛЫ И ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДИКИ
Анализ реакции смешанной культуры лимфоцитов (MLR) - иммуносупрессирующие и иммунологически привилегированные свойства 2D и 3D культивированных ASC, полученных из плаценты, проводились с помощью анализа MLR, в котором измеряют гистосовместимость по HLA локусу, под действием скорости пролиферации несовместимых лимфоцитов в смешанной культуре чувствительных (пролиферирующих) и стимулирующих (непролиферирующих) клеток. Мононуклеарные клетки пуповинной крови человека (CB) (2×105) были использованы в качестве чувствительных клеток и их стимулировали совместным культивированием с равными количествами (105) облученных (3000 рад) моноцитов периферической крови человека (PBMC), или с 2D или 3D культивированными адгезивными клетками, полученными из плаценты, или сочетанием адгезивных клеток и PBMC. Каждый анализ повторяли три раза. Клетки совместно культивировали в течение 4 дней в среде RPMI 1640 (содержащей 20% FBS в увлажненной атмосфере 5% СО2 при 37°C), в 96-луночном планшете. Планшеты сенсибилизировали 1мкС3H-тимидином в течение последних 18 часов культивирования. Затем клетки собирали на стекловолоконный фильтр и количественно определяли захват тимидина с помощью сцинтилляционного счетчика.
РЕЗУЛЬТАТЫ
На Фиг.8 показан иммунный ответ клеток CB, который представлен повышенной пролиферацией этих клеток при стимуляции PBMC, которые, не привязываясь к теории, вероятно связаны с Т клеточной пролиферацией в ответ на несовместимость по HLA. Однако гораздо более низкий уровень иммунного ответа был продемонстрирован этими клетками при инкубировании с адгезивными клетками по настоящему изобретению. Более того, иммунный ответ CB на PBMC был существенно снижен при совместном инкубировании с этими адгезивными клетками. Таким образом, было обнаружено, что подобно MSC, ASC обладают потенциальной способностью снижать Т клеточную пролиферацию донорских клеток, характерную для GvHD. Хотя обе культуры, 2D и 3D, снижали иммунный ответ лимфоцитов, и наряду с другими преимуществами 3D-ASC, описанными выше, 3D ASC были более иммуносуппрессирующими.
Понятно, что определенные особенности изобретения, которые для ясности описаны в контексте отдельных вариантов осуществления, также могут быть представлены в комбинации в одном варианте осуществления. Наоборот, различные особенности изобретения, которые для краткости описаны в контексте одного варианта осуществления, также могут быть представлены отдельно или в любой подходящей субкомбинации.
Хотя изобретение было описано в отношении конкретных вариантов его осуществления, ясно, что многие альтернативы, модификации и варианты будут очевидными для специалистов в данной области. Соответственно, предполагается охватить все такие альтернативы, модификации и варианты, которые подпадают под сущность и широкий объем прилагаемой формулы изобретения. Все публикации, патенты и патентные заявки, и регистрационные номера GenBank, упомянутые в этом описании, включены в качестве ссылки в полном объеме в это описание, в той же степени, как каждая отдельная публикация, патент или патентная заявка, или регистрационный номер GenBank были бы указаны отдельно для включения в качестве ссылки. Кроме того, цитирование или указание любой ссылки в этой заявке не должно интерпретироваться как признание того, что эта ссылка доступна в качестве предшествующего уровня техники настоящего изобретения.
Реферат
Изобретение относится к области биотехнологии, конкретно к получению мезенхимальных стромальных клеток плаценты или жировой ткани, и может быть использовано в медицине. Способ экспансии клеток включает культивирование адгезивных мезенхимальных стромальных клеток из плаценты или жировой ткани в трехмерных условиях культивирования, которые содействуют экспансии клеток. Изобретение позволяет получить адгезивные мезенхимальные стромальные клетки плаценты или жировой ткани, которые возможно использовать для поддержания гематопоэтических стволовых клеток, для иммуносупрессии, для получения кондиционных сред и в транспланталогии. 6 н. и 16 з.п. ф-лы, 22 ил., 3 табл.
Формула
(a) культивирование адгезивных мезенхимальных стромальных клеток из плаценты или жировой ткани в трехмерных условиях культивирования, которые дают возможность для экспансии клеток;
и
(b) сбор кондиционной среды указанных разросшихся адгезивных мезенхимальных стромальных клеток с получением тем самым кондиционной среды.
(i) секрецией более высокого уровня, по меньшей мере, одного фактора, выбранного из группы, состоящей из SCF, IL-6 и Flt-3, чем уровень, секретируемый адгезивными мезенхимальными стромальными клетками плаценты или жировой ткани, выращенными в 2D культуре;
(ii) экспрессией более высокого уровня, по меньшей мере, одного белка, выбранного из группы, состоящей из семейства гистонов Н2А (H2AF), альдегиддегидрогеназы Х (ALDH X), эукариотического фактора элонгации трансляции 2 (EEEF2), ретикулокальбина 3, кальций-связывающего домена "EF-рука" (RCN2) и кальпонина 1 щелочного гладкомышечного (CNN1), чем уровень, экспрессируемый адгезивными мезенхимальными стромальными клетками плаценты или жировой ткани, выращенными в 2D культуре;
(iii) экспрессией более низкого уровня, по меньшей мере, одного белка, выбранного из группы, состоящей из гетерогенного ядерного рибонуклеопротеина H1 (Hnrph1), предшественника CD44 антигена изоформы 2, 3-фосфоаденозин-5-фосфосульфатсинтазы 2 изоформы а (Papss2) и рибосомального белка L7a (rpL7a), чем уровень, экспрессируемый адгезивными мезенхимальными стромальными клетками плаценты или жировой ткани, выращенными в 2D культуре; и
(iiii) более высокой иммуносупрессирующей активностью, чем активность адгезивных мезенхимальных стромальных клеток плаценты или жировой ткани, выращенных в 2D культуре.
(i) секрецией более высокого уровня, по меньшей мере, одного фактора, выбранного из группы, состоящей из SCF, IL-6 и Flt-3, чем уровень, секретируемый адгезивными клетками плаценты или жировой ткани, выращенными в 2D культуре;
(ii) экспрессией более высокого уровня, по меньшей мере, одного белка, выбранного из группы, состоящей из семейства гистонов Н2А (H2AF), альдегиддегидрогеназы Х (ALDH X), эукариотического фактора элонгации трансляции 2 (EEEF2), ретикулокальбина 3, кальций-связывающего домена "EF-рука" (RCN2) и кальпонина 1 щелочного гладкомышечного (CNN1), чем уровень, экспрессируемый адгезивными клетками плаценты или жировой ткани, выращенными в 2D культуре;
(iii) экспрессией более низкого уровня, по меньшей мере, одного белка, выбранного из группы, состоящей из гетерогенного ядерного рибонуклеопротеина H1 (Hnrph1), предшественника CD44 антигена изоформы 2, 3-фосфоаденозин-5-фосфосульфатсинтазы 2 изоформы а (Papss2) и рибосомального белка L7a (rpL7a), чем уровень, экспрессируемый адгезивными клетками плаценты или жировой ткани, выращенными в 2D культуре; и
(iiii) более высокой иммуносупрессирующей активностью, чем активность адгезивных клеток плаценты или жировой ткани, выращенных в 2D культуре.
Документы, цитированные в отчёте о поиске
Композиции, содержащие кондиционированную клеточную культуральную среду, и способы их использования

Комментарии